Автор: Шел А.
Теги: биология микробиология
Текст
Алекс Шел
Микробушки. Взгляд в бесконечность,
полную жизни
(нескучный рассказ о микробах и всём,
что с ними связано)
Здравствуйте, уважаемые читатели!
Говорят, сейчас книгу не пишет только ленивый. Ну, или безрукий,
хотя Стивену Хоукингу – недавно скончавшемуся гениальному физику,
большую часть жизни полностью парализованному – даже это никак
не помешало.
Последнее время особенно много пишут о медицине и здоровье.
Пишут именитые учёные, начинающие аспиранты, простые врачи –
это и придаёт вес в профессиональном сообществе, и систематизирует
опыт, и помогает бороться с профессиональным выгоранием (очень
частое в работе врача состояние и страшная вещь, превратившая не
одного умницу и энтузиаста в злобного мизантропа). Так что скажу
вам по секрету: на самом деле я писал эту книгу для себя.
Шучу, конечно. Причем буду в меру скромных возможностей своего
чувства юмора делать это и дальше на страницах книги. Потому что
впереди нас ждут сложные, а порой и пугающие вопросы,
заковыристые определения и прочие совсем не развлекательные
моменты. И чтобы совсем не отпугнуть вас от чтения, я буду стараться
периодически давать такие передышки – «минутки смеха».
Ну а если серьёзно, то эта книга – «младшая сестра» сборника
лекций для моих студентов – будущих фельдшеров и медицинских
сестёр. И мне бы хотелось, чтобы и вы, читатели, и мои юные будущие
коллеги после прочтения получили ту базу знаний, которая поможет
лучше понять окружающую действительность. Не жить в плену
навязанных мнений, а понимать механизмы и принципы
функционирования мира микробов, рядом с которым мы живём
(именно так, а вовсе не наоборот): как он менял в прошлом и
продолжает менять сейчас планету и жизнь на ней, в том числе и нашу
собственную жизнь.
Кое-что из этого может войти в конфликт с уже имеющимися у вас
представлениями. Вы даже можете сказать, что я пытаюсь навязать вам
определённое мнение. Что ж, в этом случае советую, по крайней мере,
не отбрасывать книгу сразу – хотя бы потому, что вы заплатили за неё
свои деньги. Попробуйте для начала открыть содержание: вдруг среди
разделов, о которых вы бы со мной яростно поспорили, найдётся то, в
чём мы окажемся единомышленниками?
Если же вы нашли в книге неточности или даже досадные ошибки (к
сожалению, у меня не было научного редактора, и приходилось
рассчитывать лишь на собственные знания), либо хотите поспорить,
обсудить возникшие вопросы, а то и решите вдруг поблагодарить
автора за бессонные ночи и оторванные от семьи часы, то обратная
связь возможна через отзывы на Литрес, а также в соцсетях: на
Яндекс-Дзене у меня канал «ЛекцииPROинфекции», а канал в
Телеграме называется так же, как эта книга – «Микробушки».
Ну и, пожалуй, достаточно отвлекать ваше внимание, а то
микробушки заждались! Устраивайтесь поудобнее и извлеките
максимум удовольствия из чтения.
Глава 1. Знай врага в лицо! (и друга
тоже)
Начиная разговор о микробах, нужно сначала выяснить – а что же
это такое? Или, может быть, правильнее сказать: «Кто это?» То есть
встаёт принципиальный вопрос – являются ли микроорганизмы
живыми (на что вроде бы намекает само слово «организмы») или всё
же нет?
Что мы вообще знаем о мире микробов? Когда я читаю лекции в
медицинском колледже, чаще всего на вопрос: «Какие
микроорганизмы вы знаете?» студенты называют вирусы и бактерии.
И уже здесь мы сталкиваемся с нюансами и оговорками. Ведь вирус
представляет собой просто цепочку нуклеиновой кислоты в оболочке
из белковых молекул. Сам по себе он не в состоянии долго жить и
вообще не может размножаться. Для копирования генетической
информации и сборки новых вирусных частиц ему нужна клетка
живого организма. То есть вирус – абсолютный паразит. Его можно
сравнить с записанной на флеш-карту программой – пока не
подключишь к «порту»-рецептору и не запустишь на «компьютере»клетке, биологическая программа вируса воспроизводиться не будет, и
на другую «флешку» он себя не скопирует.
Так считать ли вирус в таком случае живым? А микроорганизмом?
Англоязычная школа микробиологов однозначно даёт ответ – нет.
Даже при чтении переводной научно-популярной литературы на эту
тему вы, скорее всего, столкнётесь с выражением «микробы и
вирусы». То есть последних вроде бы имеют в виду при обсуждении,
но всё же чётко выделяют в особую категорию.
В отечественной же микробиологии вирусы считают как бы
«преджизнью», выделяя эти микроорганизмы в особое надцарство
природы Vira («вира») – доклеточные формы жизни.
Бактерии – это уже клеточная форма жизни, способная к
автономному самовоспроизводству. Однако бактерии никогда не
объединяются в многоклеточные структуры, максимум они могут
образовывать колонии. Ещё одним отличительным свойством бактерий
является то, что у них нет выделенного ядра, поэтому они вместе с
археями (архебактериями) составляют группу прокариот (от лат.
«про» – перед, ранее, «карион» – ядро).
Поразмыслив, наряду с бактериями и вирусами, многие вспоминают
таких представителей микроорганизмов, как «грибки». И здесь есть
нюанс: грибы – это обширное царство живой природы, включающее и
какой-нибудь опёнок или мухомор, и пекарские дрожжи, и кандида
(причины «молочницы»), и аспергилл, знакомый вам по чёрному
налёту на стенах и потолках сырых помещений, а заодно вызывающий
у их обитателей аллергические реакции. Так вот, микробиология
занимается только микроскопическими представителями этого
разнообразия, то есть микромицетами (от греч. «микрос» – малый и
«микос/мицес» – гриб) – дрожжами и плесенями.
И да, терминологически правильно что микро-, что макромицеты
называть одинаково – грибами. Но у обычных людей это вызывает
путаницу, поэтому даже врачи в беседах с пациентами частенько
прибегают к разговорной форме «грибок», «грибковое поражение
кожи».
Грибы, в отличие от бактерий, уже являются эукариотами – у них
есть полноценное ядро, как в клетках растений и животных. К
растениям долгое время грибы и относили, хотя на деле они
формируют совершенно отдельное самостоятельное царство природы.
И здесь это не эпитет, а научный термин: царство грибов как
классификационная категория будет называться «микота» или
«фунги», смотря на какой язык вы переведёте слово «грибы» –
латинский или греческий. В такие же царства объединены бактерии
(название их царства Bacteria звучит сходно с русским вариантом),
растения (царство «планте» или «флора») и животные (царство
«анималия» или «зоа») с подцарством простейших («протозоа»).
Простейшие выделены в самостоятельную группу из большого
царства животных (к которому относится и человек) на том основании,
что, будучи полноценными эукариотами, они, как и прокариоты, всё
же не в состоянии слиться в многоклеточный организм. Их клетки
живут, питаются, дышат, охотятся или паразитируют, мигрируют к
источнику пищу или скрываются от опасности, но всегда остаются
одиночками. Максимум, на что способны простейшие, – объединяться
в колонии по типу вольвокса. Но никакой специализации клетки в
такой колонии не приобретают, оставаясь совершенно одинаковыми, в
отличие от гигантского разнообразия клеток и тканей в
многоклеточных организмах. По этой же причине одноклеточности
простейшие доступны для наблюдения и изучения в основном только с
использованием оптики.
Сами по себе водоросли, являющиеся частью царства растений,
тоже интересуют микробиологов лишь отчасти. К тому же ещё совсем
недавно считалось, что ни один вид водорослей не способен
инфицировать человека, и потому они не представляют интереса для
врачей и медицинских микробиологов.
Правда, в 1970-е годы сначала у животных, а затем и у человека
были описаны случаи прототекоза – инфекции кожи и центральной
нервной системы, вызванные нефотосинтезирующими водорослями
рода Prototheca («прототека»). Это ближайшие родственники
одноклеточных водорослей хлорелла, однако по своим свойствам в
организме больше напоминают грибы. Ранее считалось, что
прототекоз может поражать только особей с ослабленным
иммунитетом (например, ВИЧ-инфицированных лиц), то есть
является оппортунистической инфекцией. Однако в последние годы
выяснилось, что пусть редко, но болеть могут и люди с нормальным
иммунитетом. Из-за своей редкости и необычного возбудителя
прототекоз сложно диагностировать, но не запущенные случаи
успешно лечатся.
Но и помимо этого у микробиологии богатая история
взаимодействия с альгологией (наукой о водорослях, не путайте с
алгологией – разделом медицины о лечении болевых ощущений).
Например, микроорганизмы, вызывающие «цветение» водоёмов
жарким летом, до сих пор называют сине-зелёными водорослями, хотя
в действительности это бактерии (цианобактерии). Предполагается,
что именно у них первых на древней Земле появился процесс
фотосинтеза. А уже позже водоросли и простейшие устроили с ними
выгодный симбиоз, в результате которого (согласно одной из теорий)
свободноживущие цианобактерии деградировали до хлоропластов,
став органеллами в клетках своих более эволюционно продвинутых
соседей
Так же, как и поглощённые, но не переваренные предком эукариот
археи развились внутри него в митохондрии , положив начало
аэробным – дышащим кислородом – организмам.
А ещё водоросли образуют симбиоз с грибами, который вам всем
хорошо знаком и не раз встречался, например, на коре деревьев. Это
лишайники. Организм очень интересный, но медицинского значения,
в смысле патогенности для человека, не имеющий. Поэтому не нужно
путать лишайник с лишаём. Последним обозначают грибковое
поражение кожи и волос. Так, стригущий лишай – это микроспория
или трихофития, то есть заболевания, вызванные микроскопическими
грибами рода микроспориум или трихофитон соответственно.
Разноцветный (отрубевидный) лишай – тоже результат поражения
кожи грибом малассезией (Malassezia furfur).
Последняя, шестая, группа в классификации микроорганизмов –
прионы. Она самая новая (большинство вызываемых ими заболеваний
были описаны во второй половине XX века, как инфекционный агент
выделены в 1982 г.) и самая загадочная. Дело в том, что прионы вовсе
не содержат нуклеиновой кислоты, то есть не несут генетического
материала. Это просто особого рода белковые молекулы,
предшественники которых в норме имеются в организме животных
(недавно были открыты прионы у дрожжевых грибов и предполагается
их наличие у некоторых растений). Однако под действием до конца не
установленных факторов прионы в организме начинают менять свою
конформацию – способ укладки белковой молекулы в пространстве
или, попросту говоря, форму. Такие молекулы уже не могут нормально
нести свою функцию, и их накопление в клетках приводит к
заболеванию. У животных прионы доказанно вызывают губчатую
энцефалопатию (ГЭП) крупного и мелкого рогатого скота («коровье
бешенство», «скрэпи» у овец). У людей – фатальную семейную
бессонницу, болезнь «куру» и другие поражения центральной нервной
системы.
На роль причин, заставляющих «хорошие» прионы перерождаться в
патоген,
предполагают
наследственные,
внешние,
другие
перенесённые инфекции или сочетание всего перечисленного. А также
инфицирование «плохими» прионами извне: так, название болезни
«куру» происходит из языка племён каннибалов с островов ПапуаНовая Гвинея, у которых она и была впервые диагностирована. Нет,
они не охотятся на людей специально, но у них есть традиция съедать
некоторые органы своих умерших сородичей – особенно головной
мозг. А именно там у заболевших содержится наиболее высокая
концентрация злокачественных прионов. «Коровье бешенство»
и скрэпи тоже были ассоциированы со стадами, в корма которых для
ускоренной прибавки веса добавляли мясокостную муку – то есть они
были «каннибалами поневоле».
Конечно, прионы уже совсем нельзя назвать живыми. Однако пока
ими тоже занимаются микробиологи. Благо прионные инфекции
весьма редки.
Итого групп микроорганизмов шесть:
* вирусы
* бактерии
* микроскопические грибы (микромицеты)
* микроскопические водоросли
* простейшие
* прионы
Микроорганизмы чрезвычайно разнообразны и многочисленны. Их
даже сложно уложить в рамки одной классификации. Кроме того, они
очень малы, поэтому изучать их можно только с помощью микроскопа.
И далеко не всегда с помощью того оптического (светового)
микроскопа, которым вы, вероятно, пользовались на уроках биологии в
школе. Физический предел его способностей, определяемый длиной
волны видимого света – 0,2 микрона (это 2 десятитысячные доли
миллиметра). То есть кишечную палочку с диаметром клетки 0,4
микрона в нём видно, а вот вирусы, размеры которых измеряют уже в
нанометрах (тысячная доля микрона) – нет. Кроме разве что недавно
открытых гигантских РНК-вирусов диаметром до 1,5 микрона, но это
исключение. И ещё иногда получается подкрасить скопления вирусов
специальными светящимися пигментами, что используют, например, в
диагностике гриппа – однако такая хитрость работает, только если
вируса в исследуемом материале достаточно много.
Для изучения вирусов и тонкой структуры других микроорганизмов
через исследуемый образец направляют, например, поток электронов,
имеющих более короткую длину волны, чем свет. Поэтому такие
микроскопы называются электронными. Они позволяют заглянуть уже
не только в наномасштаб, но и «увидеть» структуры размером в
несколько ангстрем – то есть даже отдельные молекулы и атомы. Но
такие приборы очень сложны и дороги, поэтому их применяют в
научных целях, а для повседневной практики, например, диагностики
инфекций, ищут другие способы. Зачастую так гораздо проще и
удобнее. Но вот чтобы подтвердить открытие новых вирусов или
других мельчайших микроорганизмов, всё же нужно представить их
электронные микрофотографии.
Так размеры и относительно простое устройство «микробов»,
которое природа комбинирует во множество разнообразных вариантов,
сделали их реальными хозяевами нашего мира. Простота и
неприхотливость позволяют им приспосабливаться к почти любым
условиям среды. Именно по распространению микроорганизмов
определяют границы биосферы Земли. И они гораздо шире освоенных
любыми другими обитателями планеты.
Например, споры бактерий и грибов потоки воздуха заносят в
атмосферу на 15—20 км, куда даже не все самолёты залетают. Но
выше они пробраться не могут, так как без защиты находящегося на
этой высоте озонового слоя жёсткий ультрафиолет стерилизует всё
живое.
В
экспериментальных
сверхглубоких
скважинах
микроорганизмов находили до глубины 3,5—4 км. Некоторые виды
прекрасно чувствуют себя в термальных водах гейзеров и вулканов,
имеющих почти температуру кипятка. Даже в туннелях под 4-м
энергоблоком Чернобыльской электростанции, где произошло
разрушение ядерного реактора, обнаружили микрооорганизмы,
выживающие в условиях жесточайшей радиации.
Долгое время считалось, что полноценные экосистемы в океане
могут существовать только до той глубины, куда проникает свет, а
значит, есть фотосинтезирующие организмы как основа пищевой цепи.
А дальше, мол, идёт тёмная и холодная «мёртвая зона» с редкими
обитателями, поглощающими то, что падает из верхних слоёв воды.
Однако в середине XX века в центральных частях океанов, где
проходят стыки литосферных плит и постоянно поднимается магма из
недр планеты, открыли необычные образования, похожие на вулканы.
Они выбрасывают разогретую до 300—400 градусов Цельсия воду,
перенасыщенную минеральными солями и тяжёлыми металлами. Изза колоссального давления на глубине нескольких тысяч метров она не
кипит, и в свете прожекторов батискафов исходит со дна чёрными
вертикальными потоками, получившими за свой вид название
«курильщиков».
Каково же было удивление учёных, когда они обнаружили, что в
этом аду прекрасно чувствуют себя микроорганизмы, научившиеся в
отсутствие света извлекать энергию из химических связей тех
соединений, которые выбрасывали «курильщики». Они легли в основу
пищевой пирамиды, и вокруг «курильщиков» сформировались
настоящие оазисы жизни из моллюсков и рыб, никогда не видевших
солнечного света.
Микроорганизмы, способные выживать и размножаться при очень
высоких или очень низких показателях температуры, давления, в
агрессивной химической среде или других крайне неблагоприятных
условиях, называют экстремофильными. Их изучение помогает
узнавать пределы приспособляемости жизни. А гены этих
«экстремалов» и кодируемая ими биохимия, возможно, помогут не
только в будущем земным колонистам осваивать далёкие планеты, но
уже сейчас лечить некоторые заболевания.
Учитывая всё вышеприведённое, можно сказать, что в
отечественной микробиологии микроорганизмы – это искусственно
выделенная разнородная группа объектов микромира (живых
организмов и сложных органических молекул), объединенных
микроскопическими
размерами,
относительной
простотой
устройства и повсеместным распространением в биосфере.
Микробиология же изучает их строение, функционирование,
происходящие в них биохимические процессы, размножение и
передачу наследственного материала из поколения в поколение,
условия обитания и, наконец, изменение с течением времени
(эволюцию).
Однако сразу необходимо сказать, что почти никогда микробиология
не исследует свой объект – микроорганизмов – как «самих по себе». В
гораздо большей степени её интересуют их связь друг с другом и
влияние на макромир (мир, который мы ощущаем непосредственно с
помощью органов чувств, в первую очередь – зрения). Особенно это
важно для медицинской микробиологии, рассматривающей
взаимодействие микроорганизмов, в том числе патогенных, с
организмом человека.
Поэтому можно ввести такое определение: микробиология – это
наука о микроорганизмах, изучающая закономерности их жизни и
развития, а также изменения, вызываемые ими в организме
людей, животных, растений и в неживой природе.
Для того, чтобы упорядоченно заниматься изучением всего
перечисленного, в микробиологии выделяют ряд разделов. Во-первых,
микробиологи предпочитают глубоко заниматься только какой-то
одной группой микробов, в крайнем случае – несколькими смежными.
Поэтому среди них есть бактериологи, вирусологи, протозоологи.
Микология – это наука о вообще всех грибах, но некоторые микологи
предпочитают заниматься только микроскопическими их видами,
например, дрожжами. Так же, как и некоторые альгологи (вы ведь ещё
не забыли, что это учёные, занимающиеся водорослями?). И
микробиологи с удовольствием принимают их в свою «компанию».
Кроме того, разделы микробиологии выделяют ещё и по
прикладному их значению: по той области хозяйственной
деятельности, конкретные задачи которой призвана решать
микробиология, или по тому объекту интересов человека, где
требуется знание микробиологических аспектов. Это уже упомянутая
медицинская микробиология, а также санитарная, ветеринарная,
промышленная,
почвенная,
морская
и
даже
космическая
микробиология, изучающая вопросы возможного распространения
микробов с естественными (кометы, метеориты) и искусственными
(спутники, межпланетные станции) космическими телами, а также
решающая проблемы микробного загрязнения на орбитальных
станциях. Сюда же входит биотехнология – наука, разрабатывающая
способы получения нужных человеку веществ при помощи живых
организмов (чаще всего именно микроскопических).
Хотя на самом деле классификации разрабатывают скорее для
удобства и наглядности, и абсолютно всё в их рамки не уложить. Теми
же прионами из-за их необычности микробиологи вынуждены
заниматься совместно с биохимиками и другими учёными – первыми
белковую природу этого патогена предположили вообще радиобиолог
и биофизик. Впрочем, даже самые первые и самые «микробиологи из
микробиологов» Луи Пастер (чьё имя сейчас носит французский
институт микробиологии, и одно только перечисление заслуг и
открытий которого займёт целую страницу) и Роберт Кох
(первооткрыватель
возбудителя
туберкулёза
и
во
многом
основоположник бактериологии) внесли фундаментальный вклад в эту
науку, микробиологами в нынешнем понимании слова не являясь!
Первый был по образованию, как бы это сейчас сказали, «технологом
пищевой промышленности», а второй, тоже в современных
терминах, – санитарным врачом. Это лишний раз доказывает
условность всех классификаций и то, что крупные открытия всегда
совершаются людьми широкого кругозора и – на стыке наук.
Например, микробиология чрезвычайно тесно связана со
множеством наук и сфер деятельности человека: не только с
фундаментальными химией и биологией, но также с генетикой,
фармакологией, клинической медициной, химической и пищевой
промышленностью, обеззараживанием сточных вод и даже
производством материалов для электроники.
Ну а медицинская микробиология идёт рука об руку с
иммунологией. Их попросту сложно рассматривать отдельно друг от
друга.
Иммунитет, изучением которого занимается иммунология как
наука, – это способ защиты организма от антигенов экзогенного
(внешнего) и эндогенного (внутреннего) происхождения,
направленный на поддержание и сохранение гомеостаза,
структурной и функциональной целостности организма,
биологической индивидуальности каждого организма и, как
следствие, вида в целом.
Сейчас это определение кажется слишком сложным, но по мере
чтения книги вы разберётесь в терминах и поймёте, что иммунитет
оберегает организм от опасностей внешних (микробы, инородные
тела) и внутренних (опухолевые, отмершие и повреждённые клетки).
Таким способом он поддерживает постоянство внутренней среды
организма (гомеостаз), оберегает от повреждений его геном, что в
конечном счете позволяет живому существу выжить и передать свои
гены потомкам.
Ну а в заключение этой главы я хочу обратить внимание вот на что,
уважаемый читатель. Классификации и определения очень важны, они
– настоящие навигационные карты и маяки в мире микробиологии (да
и любой другой науки) и том безграничном «микрокосмосе», который
она изучает. Но чтобы по-настоящему понимать, и главное, любить
микробиологию, так важно за строгими терминами и сложными
взаимосвязями не терять живую и невероятно интересную связь науки
с нашей каждодневной окружающей жизнью. В самом деле: ведь без
микроскопических помощников-дрожжей у нас не было бы вкусного
хлеба, а без плесени он бы не портился, но зато мы не получили бы из
неё первые антибиотики. А если бы Александр Македонский не умер в
возрасте 32 лет от инфекции (за давностью лет мы точно не знаем,
какой именно, но по известным симптомам выбор лежит между
брюшным тифом, малярией и лихорадкой Западного Нила), то вся
история человечества могла пойти по совсем другому пути.
Глава 2. Мы были, есть и будем есть!
2.1. Экология микроорганизмов
Итак, мы бегло ознакомились с микроорганизмами и узнали, как
тесно, оказывается, мы сосуществуем с ними на нашей планете. Хотя
справедливее было бы сказать: «на их планете» – мало того, что
микробы забрались во все самые потаённые углоки Земли, так ещё
общая биомасса одних только бактерий превышает массу всех людей
планеты в 10 тысяч раз! А может и больше: учёные пока не могут
точно оченить биомассу микробных сообществ океана и геосферы
(населяющих различные пещеры, полости и просто поры горных
пород).
Тем, какие отношения складываются у микроскопических
обитателей планеты друг с другом, людьми и другими живыми
существами, а также со средой обитания, занимается наука экология.
Когда звучит слово «экология», обычно оно ассоциируется с
защитой природы, краснокнижных животных и с глобальным
потеплением. В действительности это гораздо более широкое
понятие: термин экология происходит от латинских слов «ойкос» –
дом, обиталище, и «логос» – наука, учение.
Если представить наше жилище, особенно частный сельский дом с
участком, то окажется, что вся наша жизнь будет тесно связана с
ним: здесь мы не просто находим безопасное убежище и место
отдыха, но и питаемся, общаемся друг с другом, развиваемся,
воспитываем потомство, а приусадебное хозяйство служит нам
средством воспроизводства пищи. То есть дом является местом
нашего глубокого взаимодействия с окружающим миром. В этом
смысле название «экология» хорошо отражает суть данной науки.
Одной из самых важных задач экологии является изучение
пищевых (трофических) цепочек, поскольку питание наряду с
дыханием считаются первыми и самыми важными признаками
живого. Питание и дыхание нужны не просто для нормального роста
организма, но и для самого его существования. Лишь немногие
организмы могут приостанавливать или существенно замедлять эти
процессы, да и то на ограниченное время (анабиоз, образование цист и
спор).
Вспомним, что такое питание. Упрощённо – это процесс поглощения
вещества и энергии. К энергии мы чуть позже вернёмся, а пока
разберёмся с веществом.
Жизнь на планете Земля – углеродная. То есть все органические
молекулы – белки, жиры, углеводы, нуклеиновые кислоты – так или
иначе имеют «скелет» из атомов углерода С. Поэтому в каком-то
смысле можно сказать, что питание – это поглощение источников
углерода и [источников] энергии. То есть живые клетки могут из
углеродных «кирпичиков» складывать собственные структуры. Для
этого они могут взять готовый углерод или разломать «на кирпичи»
другие клетки либо их отмершие остатки. Правда, поскольку углерод в
форме угля, графита или алмаза очень неудобен для использования в
биохимических процессах, то наиболее простым его источником для
живых существ является углекислый газ СО2. Плюс нужна вода как
универсальный растворитель и источник другого важного элемента –
водорода Н. Существа, которые могут из этих простых компонентов
синтезировать свои сложные молекулы – буквально «строить сами
себя», – называются автотрофами (от греч. «аутос» – сам,
самостоятельно). Те, которые разлагают органические субстраты,
чтобы затем собрать из них свои молекулы и клетки, обозначаются
термином гетеротрофы («гетерос» – другой, чуждый). Поскольку
автотрофам, в отличие от гетеротрофов, не нужно никого «разбирать
на запчасти», а вот их самих разбирают все, кому не лень, то именно
автотрофы являются первоосновой всех трофических (пищевых)
цепочек. На языке экологии – продуцентами.
Однако, чтобы соединить простые неорганические молекулы в
сложные органические, нужно затратить энергию, которая уходит на
образование химических связей. Здесь организмы (и микроорганизмы
в частности) тоже пошли разными путями. Одни научились
использовать энергию солнца. Их назвали фототрофами («фотос» –
свет) или фотосинтезирующими организмами. Поскольку только
фототрофы могут использовать солнечную энергию, поступающую на
нашу планету извне, из космоса, то именно они являются основными
продуцентами на планете.
Но не все умеют питаться от солнышка, некоторые предпочитают
что повкуснее: организмы, получающие энергию из расщеплённых
химических связей, называют хемотрофами. Причём последние
делятся на хемолитотрофных, которым достаточно энергии
неорганических молекул (аммиак, сероводород и др. – от «литос»,
камень), и хемоорганотрофных – которые меньше чем «бифштексом»
из органики не довольствуются.
Итак, имея две группы по два раздела в каждой, мы можем получить
2*2=4 типа живых существ (4 типа питания):
Фотоавтотрофы – синтезируют сложную органику из СО2 и воды
за счёт энергии солнца. Классический пример вы хорошо знаете – это
растения и водоросли. Некоторые простейшие (эвглена зелёная) и
бактерии, такие как цианобактерии (они же сине-зелёные водоросли,
которые, как мы узнали в предыдущей главе, вовсе не водоросли), тоже
фотоавтотрофы.
Хемоавтотрофы – образно говоря, играют в те же игрушки, только
запитывают их не от солнечных батарей, а используют дешёвые
батарейки: синтезируют сложную органику из простых молекул, но за
счёт энергии неорганических соединений. Если помните такие
необычные океанические образования из предыдущей главы, как
«чёрные курильщики», то вот там именно серные и
сульфатредуцирующие бактерии, а также археи, в отсутствие света, а
значит, и фотоавтотрофов, берут на себя роль продуцентов в этих
необычных экосистемах.
Фотогетеротрофы – редкий тип питания, когда энергию света
организмы направляют не на фотосинтез, а на расщепление чужих
органических молекул для синтеза собственных. Представлен,
например, пурпурными бактериями.
Наконец, хемогетеротрофы – самый распространённый тип
питания, когда органика служит одновременно источником и энергии,
и углерода. Мы, например, с вами типичные хемоорганогетеротрофы.
И большинство микроорганизмов – тоже. Хотя, как вы наверняка
заметили, бактерии успели захватить все типы питания, но
патогенными
для
человека
могут
быть
только
хемооргано(гетеро)трофные. Ещё бы: ведь мы их конкуренты за еду и
энергию!
Подробнее про типы питания вы можете прочесть в доступных
учебниках и Интернете. А что же дыхание? Если мы говорим не о
внешнем дыхании человека и других животных, а о дыхании как
биохимическом процессе, то, упрощённо, в его основе лежит
окисление – отрыв электрона от молекулы вещества. Электроны как
раз и есть та самая энергия. Поэтому про хемотрофов, например,
иначе говорят, что хемолитотрофы используют неорганические доноры
электронов, а хемоорганотрофы – органические. Стоп: так окисление –
это про дыхание или про питание? В том-то и дело, что эти два
процесса неразрывно связаны и составляют основу метаболизма –
обмена веществ. Так, растения в ходе фотосинтеза могут нарабатывать
глюкозу, чтобы потом полимеризовать её до целлюлозы и построить из
неё свои стебли, а могут запасти в виде других полисахаридов
(например, крахмала) в клубнях и семенах. И будущий росток станет,
наоборот, расщеплять этот запас на простые сахара для дальнейшего
создания уже собственных структур, а в процессе дыхания – на
углекислый газ и энергию, которой на рост требуется много, а листьев
для фотосинтеза пока ещё нет.
Так же могут поступать и органогетеротрофы, в том числе и мы с
вами. В процессах метаболизма мы можем расщеплять органические
полимеры пищи до составляющих их мономеров и синтезировать их
них собственные: из аминокислот – белки, из жирных кислот –
липиды, из моносахаридов – сложные углеводы, а уже из всего этого
набора – клетки, ткани и органы. Но на всё это требуется энергия.
Поэтому часть получаемых из пищи органических молекул (и даже
ставшие по какой-то причине ненужными свои) в цикле дыхания
расщепляется с образованием энергии. Так, один грамм белков и
углеводов может дать 4 килокалории энергии, а один грамм жиров –
целых 9.
Конечно, клетки не умеют поглощать энергию непосредственно в
виде электронов, мы всё-таки не кремниевые чипы, а углеродные
«анималькули» («зверушки» на латыни). Поэтому дыхание включает
не
просто
окисление,
а
длинный
цикл
окислительновосстановительных реакций, в итоге которых лежит универсальная
энергетическая «валюта» клетки – аденозинтрифосфат (АТФ) – она
может использоваться в любых реакциях биосинтеза. Для большинства
организмов, включая и нас с вами, окислителем в этих циклах служит
кислород. Для многих микроорганизмов – тоже, но… не для всех.
Например, ряд бактерий и дрожжевых грибов обходятся без него.
Вместо окислительного дыхания они используют брожение. В этом
процессе углеводы расщепляются не полностью до СО2 и воды –
остаются непереработанные соединения: спирты, органические
кислоты и др. Это менее выгодно в плане выхода энергии, но
биохимически проще и позволяет захватить такие экологические
ниши, где дышащие кислородом воздуха аэробы не выживают, а
значит, не создают конкуренции.
Такие микроорганизмы, которым не требуется кислород, называются
анаэробными или, коротко, анаэробами («аэрос» – воздух, приставка
«ан-» означает отсутствие). Самые хитрые из них приспособились
переключаться с одного режима на другой – их называют нестрогими
или факультативными анаэробами (как факультатив в школе – когда
посещение вроде как не обязательно, если, конечно, завуча не
боишься). Так ведут себя, например, коринебактерии – некоторые из
них в норме обитают на слизистой носоглотки человека, но вот
коринебактерия дифтерии может вызвать тяжёлую респираторную
инфекцию. В довакцинальную эпоху дифтерия была причиной смерти
множества детей (взрослые ей тоже болеют, но летальность у детей
выше по причине некоторых особенностей дыхательной системы:
например, у детей более узкий просвет воздухоносных путей, и они
быстрее перекрываются из-за специфического дифтерийного
воспаления).
Однако некоторые бактерии настолько «увлеклись» бескислородной
жизнью, что кислород начал оказывать на них губительное
воздействие. Они вообще не живут и не размножаются в его
присутствии. Типичным представителем таких облигатных
анаэробов являются бактерии-возбудители ботулизма. Их споры
переносят открытый воздух, но размножаться начинают только в
герметично укупоренных банках, домашних консервах и вакуумных
упаковках, в результате чего возможно сильнейшее пищевое
отравление – от ботулизма до сих пор бывают смертельные случаи.
Другие представители того же рода бактерий, клостридии столбняка и
газовой гангрены – возбудители раневых инфекции, при которых
споры бактерий прорастают в глубине раны и выделяют токсины.
Столбняк у непривитых людей легко может закончиться смертью от
паралича дыхательных мышц, а газовая гангрена – летальным исходом
от заражения крови, если раньше не произвести ампутацию
поражённой конечности.
Ну а некоторым микроорганизмам кислород всё же требуется, но в
очень небольшом количестве – они носят романтичное название
микроаэрофилы («микро» – мало, «филос» – любящий, ну а «аэрос»
вы уже должны были запомнить). К таковым относятся
кампилобактерии – возбудители кишечных инфекций – и
хеликобактерии (доказана роль хеликобактер пилори как одной из
причин воспаления слизистой желудка – гастрита, – с последующим
развитием у человека язвенной болезни желудка).
Справедливости ради нужно сказать, что наши клетки тоже умеют
функционировать в режиме анаэробиоза, правда, не все и недолго.
Например, когда вы в спортзале, кряхтя, не можете поднять штангу,
потому что «забились» мышцы, это в них «забилась» молочная
кислота – кровь не успевает снабжать кислородом миоциты,
мышечные клетки, и они временно переходят на молочнокислое
брожение. Нужно тренироваться постепенно, но систематически,
чтобы адаптировать кровеносное русло и биохимию мышц. Чем вы
хуже бактерий?!
Однако не все решают моральную дилемму «хуже—лучше»
честным путём – что в нашем мире, что в мире микробов. Зачем
упахиваться фотосинтезом, если можно расщепить готовое? Зачем
ждать, пока соседняя клетка «уйдёт на радугу», чтобы поживиться её
остатками, если можно ей «слегка помочь»? Среди микробов немало
таких же падальщиков и коварных хищников, как и в макромире.
Однако прежде чем начать «грабить к0р0ваны» живых клеток,
нужно чтобы было кого грабить. Говоря в терминах экологии, нужны
те, кто переведёт неорганический углерод и солнечную (чаще всего, но
– как мы только что видели – возможны другие варианты) энергию в
органические соединения и энергию их химических связей. Нужны
продуценты! Какие организмы ими являются, мы уже упомянули
выше.
Все живые существа не вечны, и даже если кто-то не «помог» им
закончить жизненный путь раньше времени, всё равно обычный цикл
рождения и роста закончится отмиранием. Но складывающие их
органические молекулы при этом не пропадают бесследно. Да, под
действием окружающей среды они будут деградировать: тот же
кислород является прекрасным окислителем и сам по себе, вне
биохимических циклов клеток. Но полный распад в обычных условиях
потребует много времени. Поэтому было бы странно, если бы не
нашлось охотников до такого количество дармовой органики. Хотя на
самом деле это не «охотники» вовсе, а «подбиратели» всего, что плохо
лежит. Однако не нужно с пренебрежением относиться к роли
организмов-редуцентов: только представьте, какие завалы отмершей
органики покрыли бы планету за миллиарды лет, если бы они не
помогали в её разложении. Микроорганизмов-редуцентов называют
сапрофитическими или сапротрофными (от «сапрос» – гниющий).
Причём некоторые сапротрофы могут произвольно менять свой
жизненный путь с сапрофитического на свободноживущий и обратно в
зависимости от условий среды.
Ну а самый большой интерес представляют, конечно, потребители
того, что дают продуценты, а частенько и самих продуцентов целиком.
Их называют консументами. И они вовсе не склонны соблюдать
последовательность продуцент – консумент – редуцент. Консумент
вполне может скушать консумента! Тогда они называются
консументами 1-го и 2-го порядка (как в известном анекдоте про
«завтрак туриста», где заблудившийся турист встретил медведя и
таким образом перешёл из 2-го порядка консументов в первый).
Консументы разнообразны и могут вести как свободный образ
жизни, самостоятельно расщепляя доступные им органические
субстраты, так и нахально «присоседиться» к другому организму,
полностью или частично переложив на того обязанность снабжать себя
любимого пищей и энергией (а в случае вирусов – и все остальные
функции вроде размножения). Иногда, правда, соседство получается
взаимовыгодным – один участник обменивается с другим чем-то
полезным или они оказывают друг другу взаимные услуги
(коралловые рыбки, например, очищают актинию от мусора и
паразитов, а сами в момент опасности прячутся среди её
стрекательных щупалец). Именно такой подход вам в школьном курсе
биологии и экологии преподносили как симбиоз. На самом деле
симбиоз – это любое тесное сосуществование двух организмов
разных биологических видов. И в зависимости от полученных при
нём вреда или выгоды для обоих участников оно делится на три типа:
Мутуализм – соотношение «польза/польза» – взаимовыгодное
сотрудничество организмов (бифидо-, лакто— и энтеробактерии
кишечной микрофлоры человека не только улучшают пищеварение, но
и синтезируют ряд необходимых нам витаминов, получая взамен
удобную среду обитания и обилие пищи);
Комменсализм (по-русски – «нахлебничество») – сочетание пользы
с пофигизмом – когда одному участнику (комменсалу)
сотрудничество выгодно, а другому (хозяину) нет, но он терпит и
относится с пониманием (пример: рыбы-прилипалы, путешествующие
на поверхности тела китообразных, а в мире микробов – многие
бактерии в составе микрофлоры человека);
Паразитизм – соотношение «польза/вред»: организм-хозяин терпит
убытки и лишения и всеми силами пытается от паразита (паратрофа
– конкурента за пищу) избавиться, для чего эволюция и придумала
иммунитет и другие защитные механизмы. Ну а для паразитов она
придумала гены факторов агрессии, защиту от антибиотиков, капсулы
против антител и много чего другого, чтобы тот самый иммунитет
обойти. Эволюция работает на приспособление всех участников
симбиоза.
Причём не всякое сосуществование можно с ходу отнести к той или
иной категории. Так, бактерии-комменсалы в составе микрофлоры
кожи человека получают подходящую среду обитания и питательный
субстрат, ничего вроде бы не давая хорошего. Даже слегка наоборот:
наш пот, к слову, почти не имеет собственного запаха – плохо пахнуть
после спортзала или пробежки мы начинаем из-за деятельности
бактерий и дрожжевых грибов, перерабатывающих пот и отмерший
эпителий с образованием летучих соединений. Но если посмотреть
шире, то эти бактерии так плотно заселяют наши покровы и настолько
полно используют доступные здесь ресурсы, что болезнетворным
микроорганизмам, попадающим на кожу, часто просто «негде
зацепиться», чтобы размножиться до угрожающих нашему здоровью
пределов. Да, иммунитет тоже работает, но бесполезные на первый
взгляд комменсалы тут играют роль своего рода «ополчения»,
вспомогательной силы в борьбе с инфекцией. Это явление называется
колонизационной резистентностью, и мы ещё вернёмся к нему в
теме микрофлоры человека.
Бывает и наоборот. Вам наверняка говорили в школе, что
лишайники – это взаимовыгодный симбиоз гриба и водоросли. Грибы
формируют каркас, тело лишайника, защищают от агрессивной
внешней среды, в частности от высыхания, доставляя через свои гифы
влагу непосредственно к клеткам водоросли. А те делятся с грибом
питательными веществами, получаемыми за счёт фотосинтеза. Данная
стратегия позволяет лишайникам заселять такие экологические ниши,
где ни грибы, ни водоросли по отдельности не выживают.
Однако сравнительно недавно учёные выяснили удивительное:
«мир, дружба, жвачка» между двумя компонентами лишайника длятся
только до тех пор, пока условия жизни приемлемые. Стоит начаться
засухе, или окажется исчерпанным питательный субстрат, как грибы
начинают обделять компаньонов водой и питательными веществами,
забирая больше, чем дают, а при крайне тяжёлых обстоятельствах и
вовсе выделяют пищеварительные ферменты, просто пожирая клетки
водоросли. Это уже не симбиоз – это рабовладение какое-то
получается!
2.2. Инфекционный процесс
Итак, теперь мы знаем: среди микроорганизмов немало таких, кто
предпочитает поживиться за чужой счёт, нежели в поте
цитоплазматической мембраны своей самостоятельно отыскивать
органические субстраты в окружающей среде.
Любой организм, который питается за счёт организма другого вида,
нанося ему при этом вред, с экологической точки зрения будет
называться паразитом. Теперь нам интересно выяснить, как связаны
паразитические микроорганизмы с явлением инфекции. И что вообще
под этим словом понимают врачи и учёные.
Нужно сказать, что люди всегда размышляли над причинами
явлений и процессов. Однако очень долгое время почти всё, что
происходило вокруг независимо от их воли, они объясняли действием
неких сверхъестественных сил: духов, богов и так далее. Можно
сказать, это был религиозный этап познания окружающего мира. Но
постепенно, по мере накопления знаний, стало возможным провести
между явлениями логические связи. Люди начали понимать, что одни
события являются следствием других, то есть они являются
детерминированными. А значит, сами эти события можно
предсказать, а некоторые – и предотвратить.
Так, если в древности любая заразная болезнь («мор», «поветрие»)
приписывалась гневу богов или проделкам духов, то постепенно люди
стали замечать, что в низменных и заболоченных местностях с
холодным климатом они болеют чаще, чем на открытых и солнечных,
что найденные тушки павших животных лучше не употреблять в пищу
и даже не охотиться в тех краях, где произошёл такой падёж. А если
мор всё-таки случился, то не нужно контактировать с заболевшими, а
тем более телами умерших, и вообще лучше на время уехать в другую
местность, где болезни нет. Эти принципы «защиты временем,
барьерами, расстоянием» остались непреложными и по сей день. И
они предполагали уже не влияние сверхъестественной силы, а некоего
физического начала: чего-то такого, что было невидимо, но реально
существовало, и от чего, в отличие от воли богов или козней духов,
можно было защититься путём определённых действий (сейчас бы мы
назвали это «неспецифической профилактикой»), а не мистических
ритуалов.
Конечно, огромный срок прошёл от первых представлений об этих
мельчайших первопричинах заразных болезней до момента, когда их
существование удалось подтвердить. Так, самые древние дошедшие до
нас в письменном виде рассуждения о заражении людей «миазмами»
оставил древнегреческий мыслитель Аристотель, живший в 5-м веке
до нашей эры. Правда, он считал их неживыми и
«самозарождающимися» в зловонных испарениях болот или смраде
разлагающихся тел животных и людей, уже погибших от заразного
заболевания.
Больше двух тысяч лет отделяет эти прозорливые измышления от
момента, когда на границе XVI и XVII веков нашей эры, совсем
недавно по историческим меркам, исследователям и учёным удалось
создать первые микроскопы и открыть с их помощью удивительный
мир «анималькулей» – живых микроскопических созданий. Это
событие стало возможным в результате настоящей «научной
коллаборации»: ведь успехам в оптике мы обязаны Галилео Галилею,
совершенствованием
микроскопов
были
заняты
множество
увлечённых людей из разных стран (даже наш знаменитый Михайло
Ломоносов), а самые подробные и многочисленные описания
«анималькулей» оставил Антуан ван Левенгук – голландский
любитель микроскопии, за 50 лет наблюдений направивший в
Лондонскую королевскую научную академию 300 писем-докладов с
множеством подробных рисунков.
Но ещё пара веков пройдёт, прежде чем станет окончательно
понятно, что заразные болезни не только человека, но и животных, и
растений вызываются некоторыми из этих самых «анималькулей». Что
они «виноваты» в порче продуктов питания и являются причиной
брожения. Работы Луи Пастера (1822—1895 гг.) и Роберта Коха (1843
—1910 гг.) пролили свет на многие из этих явлений: они помогли
научиться выделять зловредных микробов из окружающей среды и от
заболевших, а также дали точные критерии доказательства, что тот или
иной микроб действительно является причиной определённой
инфекции.
Пастер, Кох и плеяда их учеников открыли множество микробов,
доказав их роль в передаче инфекции людям: туберкулёза, дифтерии,
коклюша, малярии, бактериальных кишечных инфекций. Этот процесс
продолжается и поныне. Ведь мы постоянно находимся под угрозой
появления новых инфекций – пандемия COVID-19 тому примером.
Но мы несколько увлеклись историей. Хотя ничего удивительного в
этом и нет: история микробиологии невероятно насыщена
трагическими событиями, удивительными открытиями и яркими
именами. Если не верите, прочтите книгу Поля де Крюи «Охотники за
микробами». Хотя она и охватывает события лишь до момента своего
выхода в свет – 20-х годов XX века, – но это был полный историй
«золотой век» первооткрывателей мира микробов. Век «колумбов»
с микроскопами, «крузенштернов» с лабораторными животными и, к
сожалению, «куков», погибших от ими же открытых «аборигенов»
микромира. Ой-ой, снова увлёкся! Вернёмся к нашим микробам.
Когда микроорганизм атакует свою жертву (последняя по
отношению к нему будет называться хозяином, а если хозяин
многоклеточный, то ещё и макроорганизмом («макрос» – большой)),
он запускает специфический процесс взаимного противоборства. У
жертвы паразитов в ходе эволюции выработаны разные механизмы
защиты. Чем сложнее сам макроорганизм, тем более эти механизмы
многочисленны и совершенны (однако и нападает на него, как
правило, большее число видов разных паразитов). Поэтому в ряде
случаев паразит может не достичь цели и быть уничтоженным сразу –
то есть организм невосприимчив к нему. Но чаще, чтобы подавить
агрессора, нужно определённое время. Иногда этот процесс
затягивается надолго, вынуждая организм тратить на него
значительные силы и энергию. Если их резерв достаточно велик, то
противостояние с микробом может почти не сказываться на общем
состоянии – тогда говорят, что организм компенсировал процесс.
Однако в ряде случаев паразит при этом сохраняет способность
передаваться другим восприимчивым к нему организмам – заражать
их. Такое состояние, когда больной не испытывает симптомов, но
является источником инфекции, называется носительством.
Однако возможно и такое, что резервов не хватает, и тогда организм
начинает экономить на процессах своей жизнедеятельности –
замедляется рост, ухудшаются обновление и восстановление тканей,
нарушается функционирование всех систем последовательно от менее
важных к жизненно необходимым. Это называется декомпенсацией
процесса. Внешне она проявляется различными признаками болезни –
симптомами. То есть происходит манифестация болезни – переход от
компенсации к декомпенсации с проявлением симптомов. При крайнем
исходе начинают страдать и ухудшаться сами процессы защиты –
паразит побеждает. Если силы организма закончатся раньше, чем
удастся подавить паразита, то возможен летальный исход.
Любой процесс, который сопровождается напряжением сил
организма, проходя стадии компенсации, декомпенсации и исхода,
называется болезнью, заболеванием. Если причиной болезни служит
какой-то повреждающий фактор внешней среды, то его можно назвать
патогеном («патос» – болезнь, страдание, «генос» – порождение,
происхождение). Однако на практике термин патоген закрепился
именно за микроорганизмами, вызывающими заболевание. Такие
болезни называют инфекционными (от лат. «инфектум» – зараза), а
патогенные микроорганизмы – возбудителями инфекционных
болезней.
Ради точности определения стоит сказать, что патогеном может быть
не только сам возбудитель, но и выделяемые им токсины, а также –
помимо микроорганизмов – многоклеточные паразиты (например,
гельминты). Поскольку патоген-возбудитель является причиной
инфекционного заболевания, то о нём говорят как об этиологическом
факторе болезни (от «этиос» – причина).
Таким образом, инфекция – это процесс взаимодействия
возбудителя
и
хозяина
(восприимчивого
организма),
проявляющийся в зависимости от имеющихся условий либо
развитием клинически выраженного заболевания (манифестация),
либо бессимптомным носительством.
Для понимания этого определения нужно чётко представлять, что
инфекционный процесс является взаимодействием двух конкретных
организмов – возбудителя и восприимчивого организма-хозяина. И
характер его течения будет определяться особенностями каждого из
них в данном конкретном случае заболевания.
Попросту говоря, если два человека заразились даже одной и той же
ОРВИ, всё равно один может переболеть легче, другой тяжелее. А при
повторном заражении (такое часто возможно, поскольку корона- или
аденовирусы
имеют
множество
серотипов,
а
иммунитет
вырабатывается только на тот, которым человек переболел) всё может
протекать уже наоборот.
Понятие инфекции не привязано только к человеку, животным или
вообще какому-либо царству живой природы. Есть свои инфекции у
растений и грибов. Болеют бактерии, поражаемые вирусамибактериофагами. И даже некоторые вирусы могут паразитировать на
других вирусах!
Здесь же нужно упомянуть такие термины, как инвазия – состояние,
вызываемое простейшими и гельминтами (червями), и паразитоз –
заболевание,
вызываемое
многоклеточными
паразитарными
организмами (то есть теми же гельминтами, плюс членистоногими –
клещами, оводами и т. п.). Пока мы не будем на них останавливаться,
чтобы окончательно не запутаться.
Но ведь далеко не все окружающие нас микробы являются
возбудителями инфекции! Конечно, не зря ведь мы обсуждали, что
паразитизм – лишь одна из стратегий взаимососуществования видов
живых существ. Но почему одни микробы «плохие», а другие – нет?
Способность микроорганизма заражать те или иные биологические
виды «зашита» в его геноме и как-то кардинально измениться может
только под действием существенных мутаций. Поэтому говорят о
таком свойстве микроорганизма, как патогенность – генетически
детерминированная потенциальная способность микроорганизма
(возбудителя) вызывать инфекционный процесс у одного или
нескольких видов восприимчивых организмов.
Микроорганизм, вызывающий заболевание у одного вида живых
существ, может быть непатогенным для другого. Иногда, правда,
микроорганизмы в результате мутаций преодолевают межвидовые
барьеры: по одной из версий, именно так произошло с возбудителем
COVID-19, который «перепрыгнул» на людей с летучей мыши. Такой
же процесс неоднократно претерпевали вирусы гриппа с их «птичьим»
и «свиным» вариантами.
К счастью, микробные патогены не способны преодолевать барьеры
между царствами природы – поэтому, например, болезни растений не
передаются человеку или животным (хотя токсины ряда грибков,
поражающих зерновые и плодовые культуры, ядовиты для человека,
но это не является проявлением паразитизма по отношению к нему). У
животных и людей тоже не так много общих патогенов, и даже
родственные возбудители зачастую «нацелены» только на кого-то
одного. Например, ВИЧ не передаётся от человека к животным, хотя у
приматов существуют сходные ретровирусы, тоже вызывающие
иммунодефицит.
Чуму
собак
вызывает
парамиксовирус,
напоминающий возбудитель кори, но люди не болеют чумкой, а собаки
– корью.
Правда, по мере прочтения этой книги вы узнаете, что в живой
природе, а значит, и в микробиологии, не существует ничего
абсолютного. А в конце вы даже найдёте по меньшей мере один
экзотический фитопатоген, который от растений сумел перейти на
человека.
Хотя бывают у нас с братьями меньшими и общие заболевания:
например, бешенство, ГЛПС (геморрагическая лихорадка с почечным
синдромом, она же «мышиная лихорадка»), бруцеллёз и другие – их
называют зоонозными (от слова «зоо», животное) в противовес чисто
человеческим антропонозным. Для человека зоонозная инфекция –
это как бы «ошибка» возбудителя, потому для многих таких инфекций
заразившийся от животного человек становится «биологическим
тупиком», то есть не может заразить других людей.
Таким образом, патогенность – это качественная характеристика.
Она либо есть, либо её нет. И произвольно микроорганизм изменить её
не может. Почему же тогда одних инфекций мы боимся больше, чем
других, и даже применительно к какому-нибудь гриппу беспокоимся,
окажется ли очередной сезонный штамм более опасным, чем
предыдущие? Но ведь раз есть качественная характеристика
(патогенность), то, может быть, её можно как-то выразить и
количественно? Да, действительно, такая характеристика есть –
вирулентность. Её определение так и звучит – количественная мера
патогенности возбудителя. Соответственно, штаммы микроорганизма
могут быть высоковирулентными, умеренновирулентными и
слабовирулентными. А могут быть и авирулентными – то есть не
способными по какой-то причине проявить свои патогенные свойства.
Для некоторых микроорганизмов учёным удаётся управлять
вирулентностью, получая слабовирулентные и даже авирулентные
(совершенно не могущие вызвать заболевание) штаммы – например,
для производства вакцин. Такие препараты содержат живой
возбудитель, однако вероятность, что он вызовет инфекционный
процесс у привитого, исчезающе мала. Зато он гарантированно
вызовет иммунный ответ. По такому принципу создают вакцины от
бешенства, полиомиелита и других инфекций.
По этой причине не может существовать «высокопатогенного
гриппа», его правильно называть высоковирулентным – просто эта
ошибка журналистов настолько «завирусилась», что пришлось её
оставить в разговорном обиходе.
Помимо характеристик возбудителя, говорят о характеристиках
инфекционного процесса (хотя они тоже связаны со свойствами
микроорганизма):
специфичность
контагиозность
цикличность течения
Специфичность – способность каждого определённого
возбудителя вызывать специфическое заболевание в определённом
органе или ткани. Это свойство легко понять, если вы вспомните,
что, например, грипп в основном поражает дыхательную систему,
многочисленные кишечные инфекции потому так и называются, что
страдает от них ЖКТ, а стригущий лишай (микроспория) возникает на
коже (волосы тоже считаются придатком кожи). То есть, как правило,
возбудитель «заточен» под какой-то определённый орган или систему
органов.
Хотя специфичность инфекционного процесса может проявляться в
разной степени и зависеть от некоторых обстоятельств, например, от
условий заражения. Тот же вирус гриппа имеет тропность (сродство) в
основном к эпителию дыхательных путей, но в несколько меньшей
степени – к эндотелию кровеносных сосудов (эпителию их внутренней
выстилки). Поэтому при гриппе учащается вероятность кровотечений,
повышается свёртывание крови и тромбообразование, возможны
отсроченные сердечно-сосудистые осложнения. А при чуме форма
заболевания зависит от того, как чумная бактерия попала в организм:
в результате вдыхания разовьётся первично-лёгочная форма болезни
(одна из самых смертоносных), при заражении через укус
инфицированной блохи – бубонная.
Контагиозность – способность возбудителя передаваться от
заражённого организма-хозяина к незаражённому. Несмотря на то,
что инфекция ассоциируется с заразностью (и даже название
происходит от латинского эквивалента этого слова), однако выше мы
успели упомянуть, что инфекционные болезни не всегда передаются от
человека к человеку. Поэтому и говорят о высококонтагиозных и
малоконтагиозных инфекциях.
Например, при кори достаточно заразиться одному ребёнку, чтобы
заболел весь подъезд многоквартирного дома – контагиозность вируса
настолько высока, что он доберётся до всех непривитых малышей и
взрослых по системе общей вентиляции. Очень заразен и гепатит В –
достаточно невидимых следов инфицированной крови на поверхности
или предмете, которых коснулся человек с такими же незаметными
микроповреждениями на коже, чтобы произошло заражение. К
счастью, благодаря вакцинации эпидемия гепатита В, бушевавшая в
России в 90-е годы XX века, сошла до почти нулевого уровня. А вот
уже похожим на него гепатитом С (похожим по проявлениям –
генетически это другое семейство вирусов), так легко не заразиться –
здесь нужен массивный контакт «кровь в кровь»: переливание
некарантинизированной крови, инъекции нестерильными шприцами
(поэтому раньше гепатиты В, С и ВИЧ-инфекция были особенно
распространены среди наркоманов – у этих инфекций общие пути
передачи) или другие манипуляции нестерильными инструментами на
теле (непрофессиональный пирсинг, татуаж и прочее).
Наконец, инфекционный процесс характеризуется цикличностью –
последовательной сменой периодов:
инкубационный (латентный, скрытый)
продромальный (период «предвестников»)
период выраженных клинических проявлений («разгар»)
период реконвалесценции (выздоровления)
Запомнить последовательность легко. Инкубационный период
отсчитывается с момента проникновения возбудителя в организм и до
появления первых симптомов. То есть внешне он не проявляется и
потому крайне сложен для распознавания. В ряде случаев иммунитет
подавляет инфекцию уже на этой стадии, и клинически выраженное
заболевание не разовьётся. Такая форма называется абортивной
инфекцией.
В продромальный период отмечается уже появление симптомов,
однако по ним довольно трудно определить (диагностировать) болезнь,
потому что обычно они неспецифичны для конкретного заболевания:
повышение температуры, миалгия и артралгия (боль, ломота в мышцах
и суставах соответственно), быстрая утомляемость и астения
(слабость, упадок сил). «Продрома» (как её называют инфекционисты
на профессиональном сленге) может быть очень короткой, а может
растянуться почти на весь процесс, когда толком и симптомов
выраженных нет. Говорят: «переболел на ногах». Это так называемая
стёртая форма инфекции.
Наконец, в период разгара заболевания выраженность симптомов
достигает максимума, а кроме того, появляются специфические,
характерные только для данного заболевания – патогномоничные
симптомы. Например, корь можно распознать по появлению пятен
Бельского (также пятна Бельского-Филатова-Коплика) в виде мелких
белых точек на слизистой ротовой полости и мягкого нёба. К
большому сожалению клиницистов, патогномоничные симптомы есть
не у всех болезней и инфекций.
Период разгара заболевания заканчивается исходом – либо гибелью
больного,
либо
переходом
в
период
реконвалесценции
(выздоровления). Однако такая последовательность соответствует
только острой форме инфекции. А бывают и хронические, когда
возбудитель на определённый период времени снижает активность в
организме, например, будучи подавлен иммунитетом, но до конца не
удаляется из него (не элиминируется) и может развиться вновь. В
этом случае каждый цикл обострения инфекции будет проходить те же
периоды, только реконвалесценция предудыщего цикла и латентный
период нового объединяются в период ремиссии.
2.3. Эпидемический процесс
Что ж, мы рассмотрели процесс взаимодействия возбудителя
инфекционного заболевания с восприимчивым организмом. Но очень
редко когда в реальности происходит контакт инфекции с однимединственным человеком – не в пустыне живём. Гораздо чаще с
возбудителем контактирует группа лиц, причём некоторые из них
могли ранее уже перенести эту инфекцию, другие – быть привиты от
неё, а некоторые никогда ни с чем подобным не встречались. А если
возбудитель распространяется живыми переносчиками (клещами,
например, как вирусный энцефалит или крымская геморрагическая
лихорадка) или имеет природный резервуар (бешенство и др.), то речь
будет идти о взаимодействии популяции этих переносчиков с
неоднородной популяцией восприимчивых к данной инфекции людей
(и/или животных, которые в свою очередь могут стать популяцией
резервуаров). Поэтому теперь попробуем взглянуть на инфекции с
других – эпидемиологических – позиций.
Эпидемиология – это медицинская наука, изучающая причины
возникновения и особенности распространения инфекционных и
массовых неинфекционных заболеваний в обществе с целью
применения
полученных
знаний
для
решения
проблем
здравоохранения. За этим витиеватым определением скрывается
обширный комплекс специальных знаний, направленных, по большому
счёту, на профилактику массовых заболеваний. Прежде всего,
конечно, инфекционных, хотя примерно со второй половины XX века
активно развивается эпидемиология неинфекционных заболеваний:
гипертонической болезни, ишемической болезни сердца и других. Но
мы договоримся, что в дальнейшем будем подразумевать именно
эпидемиологию инфекций.
Эпидемиологию почему-то принято считать теоретической наукой.
Однако в реальности эпидемиологические знания проникают и
помогают в развитии вполне конкретных клинических дисциплин и
практических аспектов медицинской деятельности. Можно не
упоминать каждый раз эпидемиологию, но никуда не скроешь, что на
её базе построены весь санитарно-эпидемиологический режим
медицинского учреждения, гигиена рук медработников, вопросы
дезинфекции и стерилизации мединструментов, профилактика
хирургических осложнений, проблемы предупреждения заносов
инфекции в стационар, вакцинопрофилактика и многое-многое другое.
Так что польза эпидемиологии ясна, но хотелось бы понять, как она
работает и в чём её отличие от изучения собственно инфекционных
болезней.
Прежде всего, отличие состоит в задачах, решение которых мы
хотим получить в случае каждой из дисциплин. Так, учение об
инфекционных болезнях рассматривает конкретные заболевания
(инфекции) человека с точки зрения патогенеза, особенностей
клинического проявления, методов диагностики с целью их
своевременного выявления у больного и проведения лечения.
В то же время эпидемиология изучает инфекционные заболевания с
момента воздействия возбудителя на макроорганизм с целью
предотвращения их взаимодействия. То есть очень упрощённо
задача инфекциониста – выявить и вылечить, а задача эпидемиолога –
не дать никому заболеть (чтобы лишить инфекциониста работы –
шутка). Теперь о том, как этого добиться.
Мы уже сказали, что каждый случай возникновения инфекционного
процесса уникален из-за отличий характеристик его участников. А
потому для лечения лучше всего подходит правило «лечить не болезнь,
а больного», то есть требуется учёт индивидуальных особенностей.
Эпидемиологу этот подход поможет разве что в случае расследования
обстоятельств заражения определённого больного. Но для того, чтобы
предотвратить последующие случаи в масштабах города и шире,
нужно выявить общие закономерности. Проще всего это описать в
рамках «3D-модели», но не кинотеатра, конечно, а в трёх координатах:
«люди – время – территория». Нужно в целом понять: КТО больше
болеет – мужчины или женщины, дети или взрослые, а может, лица
определённых профессий, КОГДА болеют – есть ли сезонность
вообще, она весенне-летняя или это больше холодный период года,
ГДЕ болеют – какие климатические, географические, природные
факторы влияют на заражение. Затем требуется установить, какие
связи существуют между этими «координатами», и наконец, какие
особенности возбудителя обуславливают приоритет именно этих
связей.
Если инфектология оперирует понятием инфекционного процесса,
то объект изучения эпидемиологии – эпидемический процесс – это
процесс взаимодействия популяций возбудителя и организма-хозяина
при помощи устойчиво сложившихся механизмов и факторов
передачи, проявляющийся при определённых социальных и
природных
условиях
единичными
или
множественными
заболеваниями
(или
бессимптомными
формами
инфекции).
Рассматривая взаимодействие на популяционном уровне, мы жертвуем
частными особенностями возбудителя и восприимчивого организма,
чтобы выявить общие закономерности этого их взаимодействия.
В зависимости от числа заболевших в единицу времени
относительно всей популяции (населения) говорят либо о
спорадической заболеваемости (единичные, иногда даже не
связанные случаи), вспышке (связанные друг с другом случаи в
ограниченных пределах времени и/или пространства – например, одна
семья или подъезд многоквартирного дома, группа детского сада,
больничное отделение, район города и т. п.) или эпидемии.
Критерий, когда уровень заболеваемости засчитывает как
эпидемический, устанавливается специальным математическим
расчётом отдельно для каждой инфекции на каждой территории,
исходя из привычной заболеваемости на ней в предыдущие годы.
Потому что, например, 50 случаев туберкулёза в год на российский
город со стотысячным населением – это много, такая ситуация требует
проведения противоэпидемических мер, а 50 случаев ОРВИ в тех же
условиях – нереально малая величина. При этом в некоторых странах
Африки заболеваемость туберкулёзом привычно достигает 500—600
на 100 тыс. населения. Эпидемия, захватывающая большие массы
людей и распространяющаяся на несколько континентов, называется
пандемией. Причём массовой заболеваемости подвержены не только
люди, но и животные (тогда это называется эпизоотия), и растения
(эпифитотия).
Для реализации эпидемического процесса нужны 3 обязательных
звена или фактора эпидпроцесса (не путайте их с факторами
передачи инфекции, которые встретите в тексте позже), также
называемые «триадой Л.В. Громашевского»:
источник возбудителя
механизм передачи
восприимчивый организм
Эти звенья являются движущими силами эпидпроцесса. Потому с
установления каждого из звеньев начинается эпидемиологическое
расследование любой вспышки инфекции.
Источник инфекции (источник возбудителя) – это больной или
бессимптомный носитель, способный передать возбудитель
восприимчивым организмам в своём окружении.
Механизм передачи – эволюционно сложившийся способ
перемещения возбудителя из заражённого организма в незаражённый.
Для каждой конкретной инфекции он определяется основной
локализацией её возбудителя в заражённом организме. Как правило,
выделяют 4 таких локуса: желудочно-кишечный тракт (ЖКТ), кровь,
дыхательные пути, внешние покровы (кожа, слизистые, волосы).
Исходя
из
этого
и
складывается
эпидемиологическая
классификация инфекций:
Кишечные инфекции
Респираторные (или инфекции органов дыхания – от лат. «спиро»,
дышу)
Трансмиссивные (от «трансмиссия» – перенос)
Кожные и кровяно-контактные
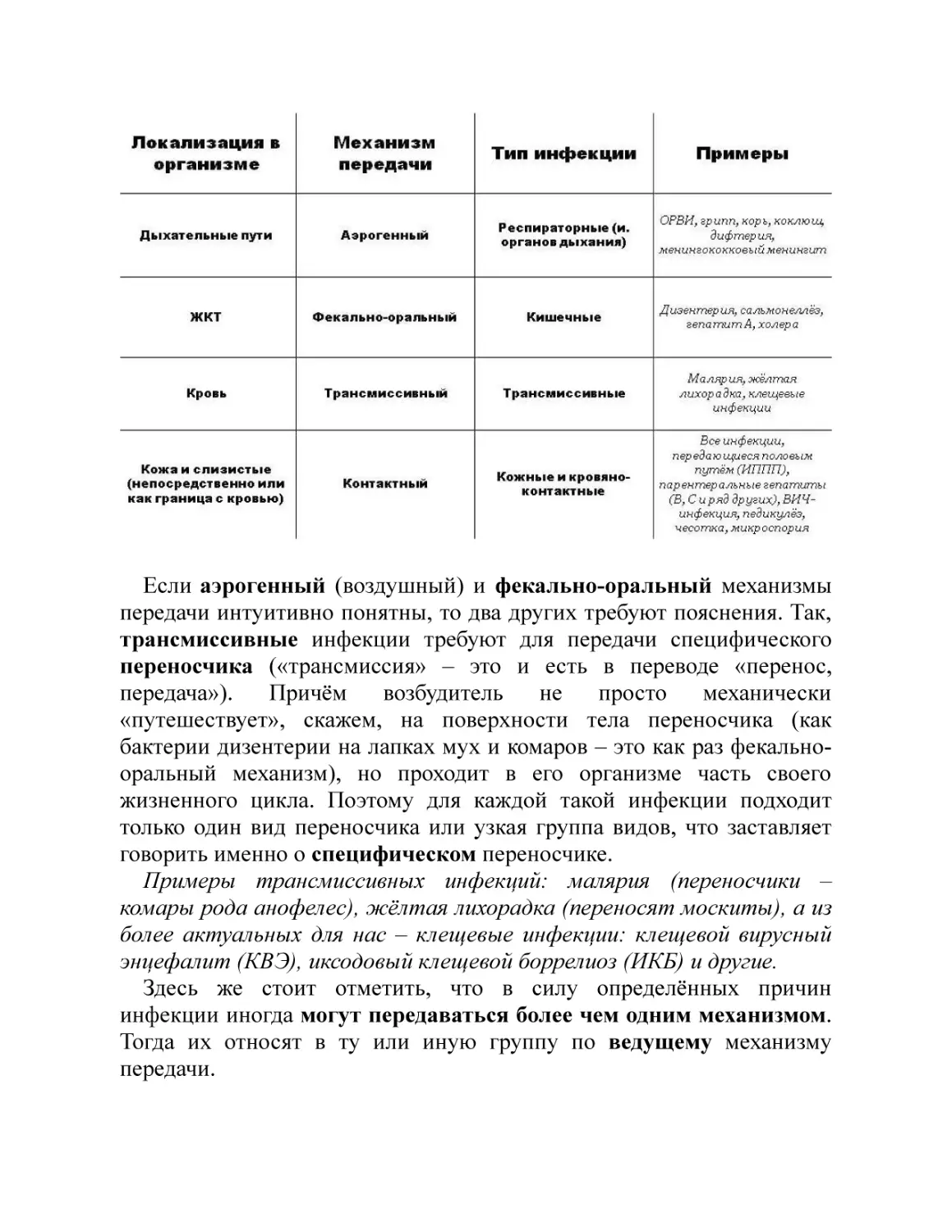
Каждой из них поставлен в соответствие свой механизм передачи
(см. таблицу):
Если аэрогенный (воздушный) и фекально-оральный механизмы
передачи интуитивно понятны, то два других требуют пояснения. Так,
трансмиссивные инфекции требуют для передачи специфического
переносчика («трансмиссия» – это и есть в переводе «перенос,
передача»).
Причём
возбудитель
не
просто
механически
«путешествует», скажем, на поверхности тела переносчика (как
бактерии дизентерии на лапках мух и комаров – это как раз фекальнооральный механизм), но проходит в его организме часть своего
жизненного цикла. Поэтому для каждой такой инфекции подходит
только один вид переносчика или узкая группа видов, что заставляет
говорить именно о специфическом переносчике.
Примеры трансмиссивных инфекций: малярия (переносчики –
комары рода анофелес), жёлтая лихорадка (переносят москиты), а из
более актуальных для нас – клещевые инфекции: клещевой вирусный
энцефалит (КВЭ), иксодовый клещевой боррелиоз (ИКБ) и другие.
Здесь же стоит отметить, что в силу определённых причин
инфекции иногда могут передаваться более чем одним механизмом.
Тогда их относят в ту или иную группу по ведущему механизму
передачи.
Выше мы уже упоминали чуму: обычно вспышки начинаются от
контакта с заражёнными грызунами, с которых на людей переходят
блохи, передающие чумных бактерий в результате укуса (если уж с
неаппетитными подробностями, то они попросту отрыгивают их в
ранку). Результатом такой трансмиссивной передачи обычно бывает
бубонная форма чумы. Но если чумной бубон (воспалённый лимфоузел)
вскрывается не наружу через свищ, а происходит прорыв бактерий в
кровоток, то развивается вторично-септическая форма с разносом
возбудителя во все органы, включая лёгкие. И больной становится
источником, заражая других уже через аэрогенный механизм лёгочной
формой болезни.
Несколько сложнее обстоит дело с 4-й группой инфекций. Если в
плане чесотки или стригущего лишая нам понятно, почему они
отнесены сюда, то, например, классификация сифилиса, ВИЧинфекции и гепатита В вызывает вопросы. Ведь они же не вызывают
кожных проявлений! Они вообще, как и трансмиссивные, в основном в
крови циркулируют.
Но если разобраться, противоречий здесь нет. Во-первых, общая
площадь кожи человека составляет порядка двух квадратных метров, а
со слизистыми – ещё больше, и они при этом активно
кровоснабжаются.
Во-вторых,
нет
никакого
эволюционно
сложившегося способа, при котором люди бы обменивались друг с
другом кровью (всякие «скрепления клятв» и братания – весьма редкие
культурные традиции), а хирургические операции и инъекции, даже
если отсчитывать их со времён Древней Индии и Китая, всё равно
слишком недавнее новшество, чтобы эволюция как-то учла его. Вот и
получается, что обитающим в крови микробам нужно либо искать
переносчика, становясь трансмиссивной инфекцией, либо как-то
пробиваться наружу в месте наиболее вероятного контакта крови с
окружающей средой, то есть через кожу и слизистые.
К чистым трансмиссивным инфекциям их тоже нельзя отнести,
потому что даже если кровососущие насекомые напиваются крови,
например, ВИЧ-инфицированного или больного гепатитом В, то они
не могут заразить другого укушенного. Во-первых, комары пьют
кровь, а не впрыскивают её, а того, что осталось на хоботке, просто
слишком мало для заражения. Во-вторых, в кишечнике комара под
действием пищеварительных ферментов и ультрафиолета солнечного
света указанные вирусы быстро инактивируются. Иначе говоря, они
эволюционно не приспособлены к передаче через подобный механизм,
а значит, никак не могут быть отнесены к трансмиссивным. Вот и
приходиться им «присоседиться» к чисто кожным инфекциям,
объединяясь с ними в одну группу.
От механизма передачи возбудителя следует отличать путь его
передачи. Это не одно и то же. Путь передачи возбудителя –
совокупность факторов передачи, обеспечивающих проникновение
возбудителя в восприимчивый организм в конкретных условиях места
и времени. У каждого механизма передачи свои определённые пути:
Респираторный может реализовываться как воздушно-капельным
путём (грипп и все ОРВИ), так и воздушно-пылевым. Это процесс,
когда в воздух попадают не капельки слизи из дыхательных путей
больного, а пылевые частицы с приставшим к ним возбудителем. Так
распространяется ГЛПС (геморрагическая лихорадка с почечным
синдромом), или в просторечии «мышиная лихорадка», потому что
источником её являются мышевидные грызуны, выделяющие вирус с
мочой и экскрементами. Поэтому уборку в сельскохозяйственных
постройках, подвалах и других местах, где есть такие «приживальцы»,
нужно проводить, защитив рот и нос маской или респиратором, а
после тщательно вымыть руки и принять душ. А ещё лучше заранее
озаботиться ловушками и «биологическим оружием» в лице кота (хотя
у него скорее – хитрая морда).
Фекально-оральный осуществляется пищевым, водным и контактнобытовым путями, которые в особом пояснении, думаю, не нуждаются.
Разве что стоит упомянуть роль мух, тараканов и других
синантропных насекомых в реализации этого механизма. В данном
случае они станут не специфическими переносчиками, как при
трансмиссии инфекции, а будут механическими – так как им всё
равно, что переносить на тельце и лапках: сальмонеллу,
дизентерийную шигеллу или вирус гепатита А. Да и конечный путь
может оказаться разным, смотря где они «наследят» возбудителем: на
продуктах питания, поручнях в санузле или рукоятке водопроводного
крана. Получается, что насекомые в этой ситуации – те самые
факторы передачи инфекции, которые упомянуты в определении
выше.
Иногда, правда, инфекции могут пользоваться «неродными» путями
передачи. Например, уже упомянутый клещевой вирусный энцефалит
(КВЭ), являясь трансмиссивной инфекцией, на эндемичных
территориях может распространяться и пищевым путём (и для этого
вовсе не нужно съедать заражённого человека). Эндемичные – это
такие территории, где циркуляция возбудителя постоянно сохраняется
в популяции переносчиков или заражённых животных. Так вот, в
эндемичных для КВЭ областях им болеют и люди, и животные (это
зоонозная инфекция), например, домашние козы и коровы. Так вот, при
употреблении некипячёного молока от них и можно заразиться
вирусным энцефалитом.
Все перечисленные пути описывают передачу инфекции между
ныне живущими поколениями людей. Но некоторые инфекции (ВИЧ,
гепатиты, корь, сифилис, токсоплазмоз) могут передаваться от матери
к плоду или новорождённому ребёнку. Это называется вертикальной
передачей инфекции. Среди учёных нет устоявшейся точки зрения на
то, механизм это или путь. Тем более что в одних случаях
инфицирование происходит при прохождении через родовые пути, а
другие возбудители способны проникать через гематоплацентарный
барьер в ходе беременности. Поэтому для простоты будем считать, что
это самостоятельный путь передачи.
Такую
же
самостоятельность
иногда
приписывают
артифициальному пути передачи инфекции («артис» – искусство) – это
искусственный перенос возбудителя в восприимчивый организм
при нестерильных медицинских (в том числе лабораторных) или
парамедицинских манипуляциях. Под последними понимаются
татуаж, пирсинг, а также инъекции нестерильными инструментами и
шприцами. Мы говорили о них выше, упоминая о заразности
гепатитов В и С (хотя иногда его считают подтипом гемоконтактного
пути передачи).
Стоит сказать, что в действующей версии Международной
классификации болезней (МКБ-10) приведено более 300 нозоформ
инфекционных болезней – а возбудителей их ещё больше (скажем, все
ОРВИ объединены под одним кодом J06.9, а ведь вызывают их сотни
разных вирусов). Инфекционистам в своей работе неизбежно
приходится искать какие-то общие подходы к их лечению, а
эпидемиологам – к профилактике. И несмотря на то, что коварные
микробы не желают полностью укладываться в рамки никаких
классификаций, эпидемиологический подход позволяет сузить поиск
общих решений, определить, на какие звенья эпидпроцесса и как
лучше воздействовать в первую очередь.
Воздействие может быть разным. Первым звеном является источник
инфекции. Значит, для начала нужно вовремя выявить всех возможных
заражённых – для этого существует множество методов клинической и
лабораторной диагностики. Зная, как распространяется та или иная
инфекция, уже принимают решение – нужно ли выявленных
заражённых изолировать. Так, грипп или дизентерия – острозаразные
инфекции, и таких больных нужно госпитализировать или хотя бы
ограничить их общение с окружающими. При этом одна инфекция
респираторная, а другая – кишечная, и меры предосторожности нужно
соблюдать несколько разные, так же как и использовать разные
средства защиты. А вот при вышеупомянутой «мышиной лихорадке»
(ГЛПС) человек не опасен для других людей – заражение происходит
только от контакта с выделениями больных грызунов.
Второе звено – механизм передачи инфекции. Чтобы эту передачу
разорвать, мы будем «охотиться» за возбудителем, который только в
этой фазе и находится в окружающей среде, а значит, и наиболее
доступен для внешнего воздействия. Здесь основную роль будут
играть дезинфекционные мероприятия, обеззараживание воздуха
различными способами (вы наверняка слышали об ультрафиолетовых
лампах, а возможно, и видели их характерный голубой свет в
медицинских учреждениях, а сейчас появились и новые методы с
использованием фильтрации или электростатического воздействия),
применение
кожных
антисептиков
и
т.
п.
Социальное
дистанцирование, отказ от посещения мест скопления людей в период
повышенной заболеваемости и ношение масок и респираторов – тоже
способы разрыва второго звена эпидпроцесса.
Ну а как воздействовать на восприимчивых к инфекции людей так,
чтобы они стали невосприимчивыми? В основном здесь речь идёт о
специфической профилактике – то есть вакцинации против
конкретных инфекций. Обычно каждое государство принимает свой
перечень инфекций, которые распространены на его территории, с
учётом наиболее уязвимых возрастов и социальных групп. Так, перед
коклюшем, например, наиболее беззащитны малыши до двух лет, а
медики и педагоги больше подвержены риску заражения
респираторными инфекциями, чем трудящийся в цеху работник завода.
Кроме того, в России нет жёлтой лихорадки, а во многих странах
Африки, Южной Америки и Карибского бассейна она распространена
– исходя из этого органы здравоохранения и составляют каждый свой
Национальный календарь прививок.
К сожалению, против многих инфекций нельзя (или пока не удаётся)
создать эффективные вакцины. И в рамках воздействия на 3-е звено
эпидпроцесса, то есть нас самих любимых, приходится укреплять
сопротивляемость инфекциям различными неспецифическими
способами – полноценным питанием, введением в него витаминных
добавок, здоровым образом жизни и т. п. Ведь общее состояние
организма неизбежно влияет на функциональность иммунитета. Плюс
в последнее время появились противовирусные препараты,
имеющие, помимо лечебной, ещё и профилактическую схему приёма.
Это подходит людям из группы риска, или если в ближайшем
окружении уже есть заболевший. Однако работает, как понятно из
названия, только против вирусных инфекций.
Ну, и напоследок несколько слов о правильном применении
терминов «эпидемический» и «эпидемиологический». Возможно, по
ходу
изучения
этой
главы
вы
уже
поняли,
что
«эпидемиоЛОГический» – это связанный с наукой («логос»)
эпидемиологией. В этом случае мы говорим «эпидемиологическое
расследование», «эпидемиологическая классификация» и так далее. А
вот «ЭПИДЕМический» – это уже как-то относящийся к процессу
распространения инфекции, к эпидемии. Поэтому процесс и уровень
заболеваемости у нас – эпидемические. Некоторые сложности
возникают с выбором правильного прилагательного для терминов
«обстановка» и «ситуация». Тут правомочны оба варианта:
и эпидемиологическая обстановка (у военных эпидемиологов,
например, в ходу именно такая формулировка), и эпидемическая
обстановка/ситуация (особенно употребима в журналистских
репортажах).
Глава 3. «Бить буду аккуратно, но
сильно!» – как работает иммунитет
В первой главе книги мы сказали, что иммунитет – это способ
защиты организма от повреждающих факторов внешнего и
внутреннего происхождения, направленный на поддержание и
сохранение наружной целостности и постоянства внутреннего состава
организма, его биологической индивидуальности и, в итоге,
способности передавать свои никем и ничем не повреждённые гены
потомству, а значит, обеспечивать выживание своего биологического
вида.
Фух, как ни старайся сформулировать простыми словами, всё равно
получается громоздко и сложно. И почему вообще нужно так
тщательно оберегать организм от проникновения чужеродных веществ
и тем более микроорганизмов? Какие молекулы, клетки, ткани и
органы обеспечивают иммунные функции в организме человека и как
они связаны с такими понятиями, как аллергия, воспаление,
заживление? Как организм понимает, что столкнулся с чем-то
чужеродным и опасным, и как он запоминает такие «встречи», чтобы
быть готовым к ним в будущем?
Как видите, целый ряд вопросов возникает при изучении
иммунитета, да ещё все они имеют свои особенности и нюансы на
разных уровнях организма – от биохимии молекул и клеточного
взаимодействия до повышения температуры тела в целом (лихорадка –
типичное внешнее проявление иммунного ответа и воспаления).
Попробуем хотя бы в общих чертах ответить на них.
3.1. Зачем нам иммунитет?
Прежде всего обратим внимание на понятие гомеостаза. Этот
термин происходит от сочетания греческих слов, дословно
означающих «постоянство состояния».
Чтобы понять, о чём идёт речь, представьте себя… на пляже! Светит
солнышко, тёплый песочек, с моря дует приятный бриз, а если станет
жарко, можно плюхнуться в море. Или забраться под зонтик и кушать
там персики. Благодать! Однако далеко не везде на планете
присутствуют курортные условия, а скорее даже наоборот. Почему же
нам гораздо приятнее валяться в сентябре на побережье Чёрного моря
где-нибудь в Сочи, чем на побережье Белого моря в Архангельске? Всё
дело в том, что мы воспринимаем как комфортные условия очень
узкий диапазон параметров внешней среды. В свою очередь, причиной
такой прихотливости является относительное постоянство параметров
среды внутри наших тел. Вспомните – нормальная температура нашего
тела около 36,60С. Всего на полградуса выше, и мы уже начинаем бить
тревогу – в организме что-то не в порядке! Какие-то 5—6 градусов
отделяют нас от гибели в результате гипертермии. А что такое для
погоды колебания на 5—6 градусов? В России в средней полосе по
весне можно одновременно видеть людей в шортах и людей в
пуховиках – смотря кто во сколько вышел из дома. А на плоскогорьях
Забайкалья с его сухим резкоконтинентальным климатом разница
дневных и ночных температур может перешкаливать и 40 градусов –
вот какие у нас «заколебания»! Организму приходится постоянно
напрягать механизмы терморегуляции, чтобы нивелировать эти
внешние изменения, держать внутреннюю температуру в пределах
допустимой. И это только один параметр гомеостаза.
А представьте, например, что вдруг у вас… вырос хобот! Да,
тянуться к верхней полке в шкафу станет проще, но всё-таки, в
отличие от слона, у нас есть руки, и мы к ним как-то больше
привыкли. Но хобот ещё куда ни шло, а если вместо хобота вырастет
пятачок? Вот это уже настоящий конфуз. Однако обычно ничего такого
«звероподобного» в облике человека не наблюдается (за исключением
редкого проявления так называемых атавизмов). Потому что,
например, группа так называемых box-генов определяет строение тела,
в том числе и чем мы будем отличаться от Слонёнка и Фунтика. Гены
кодируют синтез всех белков организма, полностью формируя наш
облик. И если поместить в наш организм гены другого существа, то не
факт, что это приведёт к чему-то хорошему. Правда, мы сами уже
довольно давно измываемся подобным образом над другими живыми
организмами. Скажем, генно-модифицированные дрожжи со
встроенным геном вируса гепатита В производят для нас белок, из
которого мы получаем вакцину против гепатита В, а дрожжи и
кишечные палочки с внедрённым геном человеческого инсулина
синтезируют этот важный гормон, необходимый для диабетиков. Но
такие хитрости мы придумали не сами – ими ежедневно занимаются
вирусы, заставляя в том числе и наши клетки синтезировать вирусные
белки, обеспечивая дальнейшее воспроизводство этих маленьких, но
зловредных биологических программ (помните, как в первой главе мы
сравнивали их с компьютерными вирусами?). Кстати, генномодифицированные кишечные палочки и дрожжи абсолютно не могут
выживать в обычных условиях среды. Их там забивают соседи, в том
числе «дикие» сородичи того же вида. Не потому, что у них
существует ксенофобия (в этом плане они лучше людей), а потому, что
изменённые человеком микроорганизмы тратят энергию и ресурсы на
выработку чуждого и абсолютно ненужного им белка, а потому
неизбежно проигрывают в конкуренции за «место под солнцем». То же
самое происходит и с человеком, заражённым вирусом. Даже
банальная ОРВИ способна настолько выбить нас из колеи, что все
намеченные планы идут прахом, а все желания сводятся к одному:
забраться под одеяло с пачкой носовых платков. А ведь респираторные
вирусы, включая даже коронавирусы и ужасный SARS-CoV2, не
встраиваются
в
геном.
Они
только
подчиняют
себе
белоксинтезирующий аппарат клетки. Стоит ли говорить, какие беды,
в отличие от них, несут человеку ВИЧ и гепатит С – их вообще
невозможно «вынуть» обратно, после того как они проникли и
затаились среди наших собственных генов. Единственный выход для
иммунитета в этом случае – уничтожить все заражённые клетки. Вот
только может выясниться, что, кроме заражённых, больше никаких
других клеток уже не осталось, а потому в результате войны вируса с
иммунитетом у человека «отвалилась» печень (цирроз – частый исход
хронических вирусных гепатитов) или полностью разрушился
иммунитет (итог заболевания ВИЧ-инфекцией).
Что-то похожее происходит и в том случае, если наши собственные
клетки «поломались». Ведь гены постоянно подвергаются
повреждающим влияниям: кванты ультрафиолетового и другого
электромагнитного излучения, молекулы свободных радикалов,
ошибки при репликации ДНК – всё это приводит к мутациям. Однако в
клетках человека есть специальные системы репарации, которые
выявляют и исправляют их. Но порой эти системы не справляются, и
клетка перерождается в настоящего «берсерка»: начинает
бесконтрольно делиться и поглощать питательные вещества, отравлять
организм продуктами метаболизма – вы, наверное, уже поняли, что так
происходит озлокачествление клеток с развитием онкологических
заболеваний (возможно, в литературе вам встретится термин
«малигнизация»). Вовремя найти и обезвредить переродившиеся
клетки – это тоже задача иммунитета. Конечно, с возрастом или под
влиянием неблагоприятных факторов – плохой экологии, воздействия
алкоголя, производственных вредностей, да тех же вирусов, в конце
концов, – системы репарации и иммунитета начинают «уставать»,
работают хуже. Поэтому онкологи справедливо говорят: «Рак (раковые
клетки) есть у каждого, но не каждый доживает до опухоли».
В отличие от вирусов и мутаций, болезнетворные бактерии и другие
паразиты не повреждают наш геном, но они всё равно нарушают
постоянство внутренней среды, отбирают ценные ресурсы и отравляют
организм отходами своей жизнедеятельности.
Поэтому организму необходимо строго соблюдать постоянство
своей внутренней среды, а уж собственные гены вообще нужно беречь
как зеницу ока, потому что без них (или с чужими и поломанными) мы
становимся уже не совсем людьми. И если для регуляции
температуры, газового и солевого баланса у нас есть специальные
врождённые механизмы и приобретённая «соображалка» (хотя глядя,
как некоторые мои студенты рассекают в лёгких «кроссах» без носков
в минус 20, я начинаю сомневаться в наличии у них последней), то
против целенаправленных атак патогенов эволюции пришлось
создавать целую отдельную систему организма – иммунную систему.
У человека она вобрала в себя весь предшествующий опыт (ведь даже
у некоторых вирусов есть механизмы восстановления повреждённых
мутациями генов), но всё равно нельзя назвать её абсолютно
совершенной – иначе бы инфекционные болезни не занимали 3-е
место среди основных причин смерти людей. Иногда нам приходится
ей помогать.
3.2. Такой разный иммунитет
Различают врождённый (видовой) и приобретённый (адаптивный)
иммунитет. Видовой иммунитет неспецифический – за годы
эволюции он сделал нас невосприимчивыми ко многим окружающим
микробам, например, к большинству инфекций животных (некоторые
представления об этом мы получили, обсуждая патогенность микробов
для разных биологических видов). Кроме того, он очень быстрый –
срабатывает моментально в ответ на проникновение антигенов в
организм. Однако он слишком консервативный – вот появился, скажем,
ранее незнакомый ему коронавирус, и врождённый иммунитет
спасовал. Но всё равно для иммунного ответа необходимо, чтобы
сначала сработал врождённый иммунитет – именно он даёт «команду
на запуск» адаптивного иммунитета.
Адаптивный иммунитет, в отличие от врождённого, требует много
времени на «запуск», но умеет опознавать совершенно любые
антигены, а главное – запоминать их на будущее. За счёт этой
иммунной памяти в следующий раз иммунитет срабатывает уже
гораздо расторопнее (формируется вторичный иммунный ответ), но
только если встреча произошла с тем же самым антигеном, который он
специфически опознаёт. Если антиген будет другой, процесс придётся
начинать заново – это снова будет первичный иммунный ответ. На
этом основана тактика ряда инфекционных возбудителей, особенно
вирусов – под влиянием мутаций они слегка меняют свою антигенную
структуру, ускользая от иммунитета или заставляя его каждый раз
бессмысленно проходить цикл формирования иммунной памяти.
Если представить оба эти вида иммунитета как две союзные армии,
то каждая из них должна иметь своё «оружие». У каждой армии оно
двух типов: клеточные иммунные механизмы и гуморальные. С
клетками всё понятно, а вот гуморальные («гумор» переводится с
латыни как «жидкость») – это все сигнальные и эффекторные
молекулы, циркулирующие в жидкой среде организма: сыворотке
крови, лимфе и межклеточной жидкости. Наиболее часто ими служат
белки: для врождённого иммунитета это будут дефензины, Среактивный белок и система комплемента. А клетками-«солдатами»
его являются нейтрофилы и макрофаги, нацеленные на уничтожение
всего чужеродного. Хотя мы и сказали, что врождённый иммунитет
«быстрый», но его армия – это что-то вроде неповоротливой пехоты
времён Первой мировой войны, которая может встать стеной на пути
патогена, но не всегда способна его стремительно одолеть.
Всё меняется, когда ей на помощь приходит «авиация и разведка»
в лице гуморальных белков адаптивного иммунитета – антител – и его
клеток лимфоцитов, способных безошибочно опознавать вражеские
образы патогенных микробов.
Логично предположить, что молекулы иммунной системы
синтезируются клетками, но сами клетки должны где-то
образовываться! Так мы приходим к необходимости наличия органов
иммунной системы. Но о них будет подробный рассказ чуть ниже,
чтобы сейчас не слишком перегружать вас информацией.
3.3. Как работает иммунная система
Антиген – это любая молекула, которую иммунная система
распознаёт как чужеродную и, следовательно, стремится как можно
скорее от неё избавиться. Чаще всего антигенами являются молекулы
белков и полисахаридов.
Иногда чужеродная молекула должна сначала соединиться с какимто собственным белком организма, чтобы стать полноценным
антигеном. Такой «предантиген» называется гаптеном. Но всё-таки
самую резкую реакцию вызывают белки – то есть они наиболее
иммуногенные. Поэтому аллергия чаще всего развивается именно на
белковые молекулы – белок куриного яйца, глютен пшеницы и т. п. И
да, аллергия – это одно из проявлений иммунитета, а вызывающий
аллергию антиген именуют аллергеном.
Болезнетворный микроорганизм целиком не является антигеном.
Даже вирусы слишком крупные для этого, и иммунной системе сложно
опознавать их «в лицо». Ей гораздо проще различать отдельные
молекулы на поверхности этих «лиц». Вирус окружён белковым
капсидом, а на бактериях присутствуют молекулы липополисахарида,
при этом то и другое – отличные, «сильные» антигены? Да и белковых
частиц у бактерий тоже хватает: например, в составе жгутиков. Вот эти
молекулы и опознаёт иммунная система. Только встаёт вопрос: как она
это делает? Ведь глаз-то на иммунных клетках нет!
Если пользоваться образными сравнениями, то «слепые» клетки
иммунной системы вынуждены в прямом смысле «нюхать» и
«ощупывать» окружающее пространство в поисках антигенов. В
помощь им существуют специальные молекулы, играющие роль
«собак-поводырей», которые облепляют чужеродные частицы, помечая
их для атакующих клеток и облегчая фагоцитоз.
Также это можно сравнить с пограничной службой, где клетки –
бойцы-пограничники, а молекулы гуморального звена – пограничные
собаки, которые помогают искать и задерживать нарушителей, а
если надо, могут и загрызть.
Такие молекулы-«поводыри» есть в системе как неспецифического
иммунитета, так и адаптивного. И они чётко придерживаются
«философии» своего звена: первые атакуют любые антигены подряд,
вторые (к ним относятся антитела) – только те, против которых были
специально синтезированы (продолжая аналогии с собачками, можно
сказать, что они взяли след нарушителя, и никакие шальные кошки их
на себя уже отвлечь не могут).
К группе молекул неспецифического иммунитета относятся:
дефензины – их выделяют кожа, лёгкие, слизистая ЖКТ,
лизоцим (мурамидаза) – фермент, расщепляющий пептидогликан
бактерий: содержится у человека в слюне, секретах слизистых,
грудном молоке; у птиц – в белке яиц, поэтому фармацевтический
лизоцим производят из белка куриного яйца,
О строении и функциях пептидогликана подробнее будет
рассказано в главе, посвящённой бактериям
и компоненты комплемента – циркулируют в кровотоке, где в
основном атакуют бактерии: могут делать это как самостоятельно, так
и совместно с антителами (альтернативный и классический пути
активации комплемента соответственно).
Не
путайте
комплЕмент
и
комплИмент
–
молекулы
неспецифического иммунитета не имеют ничего общего с приятными
словами,
которыми
вы
желаете
кого-то
похвалить.
«Комплементарность» означает соответствие чему-либо: молекулы
комплемента соответствуют друг другу, то есть подходят как детали
пазла. И при активации они действительно самособираются, только не
в красивую картинку, а в особую кольцевидную структуру – МАК
(мембраноатакующий комплекс). Это «колечко» имеет свойство
встраиваться во внешнюю и цитоплазматическую мембраны
бактериальных клеток, играя роль поры, канала для воды. Попросту
говоря, комплемент дырявит бактерии! Словно получившие заряд
дроби, они теряют цитоплазму, не успевают откачивать лишнюю воду
и в конце концов набухают и лопаются – лизируются.
Однако одни иммунные молекулы с защитой организма не
справятся. Чаще всего они только метят обнаруженный патоген –
опсонизируют его. Дальше в дело должны вступить клетки
иммунитета. А как клеткам «нащупать» молекулу антигена на
поверхности тех же бактерий и «услышать» антитела и компоненты
комплемента? Они делают это с помощью специальных молекул,
которые синтезируют на своей поверхности – чаще всего это опятьтаки белки. Такая структура опознаёт только определённую
отвечающую ей молекулу и не реагирует на другие. То есть они
специфичны друг к другу. Называется эта структура на поверхности
клетки рецептором. Само слово «рецептор» происходит от латинского
«реципе» – возьми. Потому что молекула рецептора как бы берёт
другую молекулу и опознаёт её форму как знакомую или незнакомую,
а знакома ей (специфична) только одна-единственная форма.
С этого же слова начинались старинные врачебные прописи
лекарственных препаратов, которые составлялись вручную из
нескольких компонентов. Древний врач писал древнему аптекарю:
возьми то-то и то-то в таком-то количестве, смешай, подпиши,
выдай больному. Со временем такие прописи стали называться
хорошо знакомым нам не только по медицине словом «рецепт».
И именно на специфическом связывании антигенов и сигнальных
молекул со своими рецепторами на поверхности клеток основан
запуск почти всех иммунных механизмов (да и практически любого
межклеточного взаимодействия в организме вообще).
Представим: человек получил глубокое ранение конечности
садовым инструментом. В земле обитает немало спорообразующих
бактерий, и, к несчастью, одна очень опасная – столбнячная палочка
(«клостридиум тетани») – попала несчастному в рану. В глубине раны
её споры оказались в подходящих условиях (клостридия – типичный
анаэроб, то есть не нуждается в кислороде) и начали превращаться в
делящиеся клетки. При этом они выделяют очень сильный токсин,
вызывающий паралич мышц. В месте ранения и бактериального
инфицирования часть клеток нашего организма погибла сразу, часть
ещё держится, но оказалось под «атакой» патогена. И все они
начинают, образно говоря, на разные голоса кричать об опасности:
одни радируют: «SOS», другие отправляют в эфир последнее:
«Умираю, но не сдаюсь». Только, естественно, делают они это не
голосом, а на языке сигнальных молекул. Всё для того, чтобы
предупредить соседние клетки и систему обороны организма о
нападении неприятеля.
«Под раздачу» в месте проникновения бактерий попали и тучные
клетки (тканевые базофилы) – эта группа лейкоцитов после
образования в красном костном мозге мигрирует по кровотоку в ткани.
Их цитоплазма набита гранулами таких веществ, как, например,
гистамин. При повреждении тучной клетки или под действием
сигналов SOS от клеток-соседей они выбрасывают содержимое гранул
наружу. Гистамин очень вазоактивное вещество, но цветочные вазы
здесь ни при чём: «ваза» с латыни – это сосуд. Под влиянием
гистамина кровеносные сосуды, окружающие место проникновения
патогена и повреждения тканей, резко расширяются. Спокойный ток
крови в них, когда форменные элементы в основном организованно
движутся по центру сосуда, нарушается – клетки крови, в том числе
лейкоциты, завихрениями потока откидывает к стенкам. Здесь их
рецепторы «чувствуют» сигнальные молекулы погибающих клеток, и
лейкоциты немедленно «вспоминают», что они не просто
расслабленные путешественники, а, на минуточку, грозные защитники
организма. И начинают цепляться за эндотелий сосудов, а
зацепившись – протискиваются сквозь него в ткани и мигрируют к
месту проникновения патогена.
Поскольку сосуды сильно расширены, то площадь контакта их
внутренней стенки с кровью и давление самой крови увеличены, а
стенка истончена: в результате в ткани просачивается больше
жидкости – начинается отёк, сдавливаются болевые нервные
рецепторы. Зато из плазмы теперь поступает гораздо больше защитных
молекул (сначала неспецифических, а позже и антител). Из-за
большого количества притекающей к очагу крови температура его
локально повышается (это плохо для здоровых тканей, зато усиливает
активность противомикробных ферментов). Естественно, что чем
интенсивнее идёт процесс, тем сложнее поражённой части тела
выполнять свои нормальные функции (попробуйте-ка сделать любое
привычное действие руками, когда у вас палец распухший и болит).
Итак, поражённый участок тела покрасневший, опухший, горячий,
болит и вообще мешает жить.
Соответствующее описание этой картины на латыни звучит как
заклинание из Хогвартса: «рубор, тумор, калор, долор эт функцио
леза».
Ничего не напоминает? Да, действительно – это признаки
воспаления. Воспаление является самостоятельным защитным
механизмом, включающимся в ответ на любое повреждение организма
– травматическое, термическое и т. п. Но проникший в ткани микроб –
тоже повреждающий фактор, поэтому воспаление здесь играет
совместную роль с иммунитетом, органично дополняя и помогая ему.
Ну а чем же, собственно, занят сам иммунитет? Да вон: вылезшие из
крови специализированные лейкоциты наконец добрались до
творящих беспредел клостридий и уже намыливают им шею. В
основном они представлены двумя группами клеток: нейтрофилами и
макрофагами.
Если
вы
играли
в
классические
RPG,
подразумевающие классы персонажей, то нейтрофилы здесь – класс
«вор», а макрофаги – «воины». Первые – тихие, но быстрые убийцы:
расставляют ловушки, выделяют токсичные для микроорганизма
вещества (в основном ферменты и активные формы кислорода –
свободные радикалы). Вторые идут на патоген в лобовую атаку,
обволакивают, словно амёбы, своими псевдоподиями, поглощают и
переваривают. Опять-таки: находят они своих жертв в тканях за счёт
рецепторов, опознающих патоген. Против бактерий, например, в
основном работают Toll-рецепторы. Против грибов – маннансвязывающий лектин. Только не путайтесь – рецепторы хоть и
опознают антигены специфически, но до сих пор в деле был
неспецифический, врождённый иммунитет – он работает против
патогенов вообще, не отличая, скажем золотистый стафилококк от
пиогенного стрептококка. Помимо уничтожения патогена, макрофаги
расчищают «поле битвы» от любого «мусора»: остатков погибших
клеток организма, обломков убитых комплементом бактерий и
прочего. Безжалостные чистюли, однако!
Нейтрофилы мигрируют в очаг воспаления по потребности, и
поскольку эта потребность при инфицировании увеличивается, мы
можем зафиксировать рост числа нейтрофилов в крови (об этом мы
расскажем в главе о лейкоформуле крови). Вместе с тем растёт и
число моноцитов – так они называются в крови, а оказавшись в
тканях, становятся теми самыми макрофагами. В отличие от
нейтрофилов, «дежурные» клетки моноцит-макрофагальной системы
присутствуют в тканях всегда: на «первой линии обороны» организма
– в коже, печени, лёгких, лимфоидной ткани и т. д. В ходе иммунной
реакции они только получают из «депо» и центральных иммунных
органов «подкрепление».
Особую группу клеток с макрофагальными способностями
составляют дендритные клетки. Эти не только кровожадные, но ещё
и крайне любопытные (маньяки, право слово!) – не просто пожирают
обнаруженный патоген, но, расщепив его в своих пищеварительных
вакуолях на составные части, начинают их «коллекционировать»
и даже хвастаться («лучшая и самая полная коллекция внутренностей
ужасного золотистого стафилококка»). А также путешествуют со
своими коллекциями на «выставки». Эти образные сравнения – далеко
не
шутка!
Дендритные
клетки
ещё
называют
антигенпрезентирующими, то есть представляющими обнаруженный
антиген другим клеткам. Для чего? Для запуска второго звена
иммунитета – адаптивного, до которого мы только сейчас добрались.
Расщепив патоген на отдельные антигены, дендритная клетка
выставляет их на своей мембране, но не просто так, а на «стенде» из
специальной молекулы – главного комплекса гистосовместимости 2го типа (ГКГ-II, в англоязычном варианте – MHC-II). Каким бы
зубодробительным вам не казалось это название, запомните его – оно
ещё понадобится.
Увешанная антигенами в комплексе с ГКГ-II дендритная клетка
(увешанный чужими внутренностями макрофаг – картинка, достойная
хоррора) немедленно отправляется по лимфатическим сосудам из
очага воспаления в ближайший лимфатический узел. Лимфоузлы
наполнены Т— и В-лимфоцитами. Именно Т-лимфоциты являются
теми «ценителями экзотики», которым антигенпрезентирующие
клетки стремятся показать комплекс антигена с ГКГ-II.
Созревание Т-лимфоцитов происходит в особом органе тимусе (о
нём чуть ниже), своего рода «академии», откуда обученные клетки
придут на «дежурство» в лимфоузлы. В-лимфоциты из красного
костного мозга (у новорождённых – ещё и из печени) тоже проходят
подобное «обучение». В результате один лимфоцит способен
специфически «узнавать» при помощи рецепторов на своей
поверхности только один какой-либо антиген. Но в целом вся
популяция лимфоцитов способна опознать абсолютно любой
антиген, даже такой, которого ещё нет в природе! Как это происходит,
мы сейчас обсуждать не будем, просто запомните, что в популяции
лимфоцитов вашего организма обязательно найдётся хотя бы
несколько клеток, способных опознать попавший в организм антиген –
как существующий, так и потенциальный.
Задача дендритных клеток – разыскать в лимфоузле такие Тлимфоциты, рецепторы которых подходят именно к обнаруженному
ими антигену. Для этого они раскидывают свои напоминающие ветки
дерева отростки (лат. «дендрит» – древовидный), стремясь
презентовать комплекс Аг-ГКГ-II как можно большему числу
потенциальных «зрителей».
В отличие от рецепторов к антигену, молекулы ГКГ как 1-го, так и
2-го типов одинаковые абсолютно во всём организме. Но при этом
уникальные – у каждого человека свои. Это обстоятельство, кстати,
мешает проводить трансплантацию органов и тканей: иммунитет
мгновенно опознаёт палец Миши, пришитый Васе на место
утраченного, по молекулам ГКГ 1-го типа, и начинает отторгать –
происходит
особая
иммунная
реакция
«хозяин
против
трансплантата».
Молекула ГКГ-II нужна антигенпрезентирующим клеткам, чтобы
взаимодействующие с ними лимфоциты чётко «понимали», на что
обращать внимание, а что игнорировать, не тратя попусту время и
энергию. У кого-то ГКГ-II лучше выполняет эту функцию, у кого-то
хуже. Образно можно сказать, что чем лучше дендритная или другая
презентирующая антигены клетка «оформила стенд» с ними, тем
быстрее на неё обратит внимание Т-лимфоцит, тем лучше и быстрее
произойдёт активация адаптивного иммунитета. Этим объясняется то
обстоятельство, что кто-то легко «хватает» те или иные инфекции, а
кто-то почти невосприимчив.
Как только нужное взаимодействие произошло, Т-лимфоцит
активируется и запускает несколько реакций. Во-первых, он начинает
размножаться (пролиферировать). Поскольку размножение идёт по
принципу клонирования, то есть получения точных копий, то весь
получившийся пул имеет аналогичные рецепторы к обнаруженному
антигену. Во-вторых, происходит дифференциация Т-лимфоцитов:
одни из них превращаются в цитотоксические клетки – образно
говоря, берут в руки оружие и мобилизуются для борьбы с микробом в
тканях;
вторые становятся Т-хэлперами – это условные «командиры»,
организующие и усиливающие действия других иммунных клеток, в
частности В-лимфоцитов и нейтрофилов,
третьи – Т-супрессорами, задача которых вовремя остановить
раздухарившихся нейтрофилов и макрофагов, когда с патогеном будет
покончено, чтобы они не натворили бед в и без того повреждённых
тканях;
ну а самые хитрые просто «засыпают», превращаясь в Т-клетки
памяти.
Именно активация В-лимфоцитов является одной из важнейших
функций Т-лимфоцитов в рамках адаптивного иммунного ответа. А
сами В-лимфоциты синтезируют ключевые молекулы иммунитета –
антитела. Те и другие заслуживают отдельного рассказа, который
ждёт вас дальше.
3.4. «Маска, я тебя знаю!»
В предыдущей части мы дошли до того момента, когда
антигенпрезентирующие клетки на своей мембране принесли в
лимфоузел «портрет врага» в виде комплекса «антиген – молекула
ГКГ-II». Т-лимфоциты опознали это «лицо» в своей самой
исчерпывающей во Вселенной «криминалистической картотеке»
и запустили адаптивный иммунный ответ уже против конкретного
«нарушителя». И помимо прочего, «разбудили» своих напарников – Влимфоциты.
В-лимфоциты точно так же, как их Т-«коллеги», узнают проникшие
в организм антигены. Причём для этого им не нужны
антигенпрезентирующие клетки – В-лимфоцит прекрасно справляется
самостоятельно. Хотя и от помощи не отказывается: если патоген
опсонизирован молекулами комплемента, это значительно облегчает
работу В-лимфоцита.
Рецептор В-лимфоцита к антигену похож на вилку или, скорее,
ухват (возможно, вы видели этот инструмент для русской печи, при
помощи которого в неё ставят и достают горшки и чугунки): из
«рукоятки» Fc-фрагмента выходят два «рожка» Fab-фрагментов,
каждый со своим участком связывания. Fab-фрагмент такого рецептора
специфически подходит к определённому антигену – то есть
опознаёт только его, по принципу «ключ – замОк».
Здесь нужно ещё сказать, что структура Fab-фрагмента, как и
любого белка, запрограммирована генетически, однако кодирующие
его участки гена являются вариабельными. Проще говоря, они могут
в определённых пределах меняться. В гене, кодирующем синтез
антител, это происходит не абы как, хаотично, а за счёт комбинации
нескольких вариантов генетических последовательностей. Чтобы не
ударяться в сложности генетики, можно представить такую аналогию:
в период созревания иммунной системы внутри её клеток словно
вращается калейдоскоп. Обычный детский калейдоскоп –
незамысловатый прибор: несколько осколков цветного стекла да
призма. Однако при каждом повороте в окуляре мы видим уникальную
картинку. Иммунная система заставляет несколько лимфоцитов
запомнить получившуюся картинку, затем поворачивает «генетический
калейдоскоп», и снова несколько клеток «запоминают» новый образ.
Так формируется гигантская библиотека, но это не просто картинки –
каждая из них словно слепок уникального «следа преступника»,
который ещё только собирается проникнуть в организм, а возможно, не
проникнет за всю жизнь. Фантастическая картина!
Конечно, это ещё не «шедевры», а скорее «наброски»: во-первых,
они не должны соответствовать молекулам нашего собственного
организма, чтобы не вызвать аутоагрессии в отношении своих органов
и тканей. Чуть ниже вы узнаете, какой жестокий отбор проходят Тлимфоциты в тимусе, чтобы такого не происходило. Во-вторых, когда
уже после распознавания антигенов проникшего в организм
возбудителя клетки начнут размножаться, преимущество получат те из
них, чьи рецепторы лучше всего подходят к этому антигену (имеют
высокую афинность).
Так и получается, что, хотя каждый лимфоцит имеет только один
«ключ» – к своему уникальному антигену – но лимфоцитарная система
в целом может подобрать «отмычку» к любому патогену.
Активированный сигналом своего рецептора и воздействием
лимфоцита из популяции Т-хэлперов, В-лимфоцит превращается в
плазматическую клетку, которая начинает не только экспрессировать
рецепторы к антигену на своей мембране, но и просто выделять их в
окружающее пространство. А для В-лимфоцита лимфоузла или
селезёнки это пространство – кровь и лимфа. Белковая молекула,
специфичная к антигену, циркулирующая в крови – вы ведь уже
догадались, что это? Да, конечно – антитело! Именно синтез антител
является основной функцией В-лимфоцитов, превратившихся при
активации
в
плазматические
клетки.
Это
настоящие
самоотверженные трудяги: срок их жизни после активации всего
несколько дней, но за это время они успеют произвести огромное
количество антител. Затем резервы работающей «на износ» клетки
истощатся, и она погибнет, но пока из тканей продолжают прибывать
дендритные клетки, «сигналя» антигенами Т-лимфоцитам, цикл будет
продолжаться вновь и вновь, поддерживая образование новых
продуцирующих антитела плазматических клеток. Так работает
первичный иммунный ответ.
Честно говоря, я сознательно опустил ряд нюансов жизненного
цикла наших иммунных клеток и их кооперации меж собой. Так, для
активации В-лимфоцита и его превращения в плазматическую клетку
на самом деле нужно, чтобы он провзаимодействовал с Тлимфоцитом, имеющим рецептор к тому же антигену! Без этого
срок жизни В-лимфоцита не продлится больше суток, а
синтезированные им за это время антитела будут иметь слабую
аффинность к антигену (то есть «ухват» антитела подойдёт к
«горшку» антигена, но так плохо, что тот вот-вот выпадет). Такой
механизм выработан, чтобы не продуцировать избыточное
количество антител, ведь они усиливают воспаление, а это не очень
хорошо для организма.
Однако, если бы после окончательной победы над микробом все Влимфоциты просто умерли, то большого смысла городить из них
целую подсистему иммунитета не было бы. Поэтому часть из них
вместо того, чтобы отдать жизнь в труде, просто «заснёт»,
превратившись в В-клетки памяти. Последние нужны на случай
повторного проникновения того же патогена. Тогда, опознав его
антигены, В-клетки спросонок кричат: «Хе-хей, старый знакомый!» – и
тут же начинают производить против него антитела. Поэтому при
вторичном иммунном ответе антител гораздо больше, а появляются
они раньше. Кроме того, это антитела другого класса.
У человека различают 5 классов антител. Все они являются белками
глобулиновой
фракции,
поэтому
антитела
ещё
называют
иммуноглобулинами (Ig): IgA, IgG, IgD, IgE, IgM.
Класс А в основном выделяется в составе секрета слизистых,
позволяя бороться с микробами на их поверхности, а также в
дыхательных путях и ЖКТ (он же выделяется с материнским молоком,
обеспечивая пассивный иммунитет грудных детей).
Класс D, как правило, связан на поверхности В-лимфоцита в составе
рецептора, а также участвует в активации некоторых иммунных
клеток.
Класс Е играет роль в защите от паразитов (гельминтов, например),
а также в запуске аллергических реакций.
Класс М образуется при первой встрече с патогеном и по строению
напоминает не «ухват», а скорее «ромашку» – у него вместо двух
участков связывания аж 10! Это нужно, чтобы малым числом антител
связать как можно больше антигена.
При повторной встрече с уже известным антигеном IgM тоже
синтезируется, но основная роль при вторичном иммунном ответе
принадлежит классу G. Поэтому если определить в крови антитела к
какому-либо микробу в разбивке на классы (распространённый способ
серологической диагностики заболеваний), то наличие только IgM
будет говорить о свежем инфицировании, IgM+IgG – о текущей
инфекции, а присутствие только IgG скорее всего говорит о давней
встрече с инфекцией, и если их уровень достаточно высок – о наличии
иммунитета к ней.
А ещё IgG способны проходить через гематоплацентарный барьер из
крови матери в кровь плода, и это ещё один механизм формирования
так называемого пассивного иммунитета новорождённого.
Антитела выполняют ряд универсальных функций. Например,
активируют систему комплемента по классическому пути (в основном
этим свойством обладают IgM и в меньшей степени IgG) и усиливают
выделение медиаторов воспаления тучными и другими клетками.
Однако большинство защитных свойств основано всё же на реакции
связывания антигенов специфически соответствующими (то есть
подходящими только к ним) антителами.
Так, за счёт взаимодействия участков связывания с патогеном
антитела облепляют его со всех сторон. Поскольку таких участков на
одной молекуле антитела минимум два, то она может одновременно
связать несколько микробных тел (вирусов или бактерий), склеивая
(агглютинируя) их друг с другом. Это лишает вирусы возможности
нормально взаимодействовать с клетками, а бактериям мешает
размножаться и двигаться.
А ещё эту реакцию агглютинации (от. англ. glue – клей) можно
использовать для диагностики: обработать биологический материал
от больного препаратом антител. Правда, вам заранее придётся
предположить, какой возбудитель может там находиться, и
выбрать именно подходящий против него иммуноглобулин. Если
предположение подтвердится, то в лунке реакционного планшета вы
увидите осадок из склеившихся вместе патогенов. Если нет, придётся
снова строить предположения и повторять реакцию с другими
иммуноглобулинами. В общем, иногда процесс диагностики инфекции
напоминает детскую игру «горячо-холодно».
Кстати, с отдельными молекулами антитела могут поступать так же.
Помните, мы говорили, что микробные и другие биологические
токсины тоже считаются патогенами? Как правило, они имеют
белковую природу, а значит, являются самостоятельными антигенами.
Помните, разбор действия иммунных механизмов мы начали с
примера инфицирования столбнячной бактерией, выделяющей очень
мощный экзотоксин. Заболевание, которое может развиться в
результате такого инфицирования, называется столбняк и
характеризуется прогрессирующим параличом мышц вплоть до тех,
которые обеспечивают дыхательные движения грудной клетки
человека. В случае их поражения столбнячным тетанотоксином
заболевший умирает от удушья. Однако микробные токсины (особенно
белковые молекулы, как при столбняке) сами являются антигенами, и
если в крови человека есть специфичные к такому токсину антитела,
они связывают его молекулы, обездвиживают их, не давая
распространяться по организму и отравлять клетки. Так же действует
иммунитет, например, против токсина дифтерийной палочки. Часто
даже в вакцины включают компоненты сразу против обоих этих
токсинов: в препаратах АКДС, АДС и АДС-М буквы Д и С как раз
указывают на дифтерийный и столбнячный компоненты соотественно
(и мы ещё вернёмся к ним в нашей книге чуть позже).
И в диагностике это схожее с агглютинацией явление связывания
молекул тоже используется. Только называется уже преципитацией.
Облепленный антителами патоген гораздо проще «нащупать»
клеткам иммунной системы, потому что большинство из них имеют
рецептор к Fc-фрагменту антител («рукоятке ухвата»). То есть они
словно «прозревают» и становятся способны специфически опознавать
антигены патогенов, даже если их собственные рецепторы на них не
срабатывают (вспомните сравнение с собакой-поводырём). После чего
макрофаги намного легче поглощают преципитированные токсины или
агглютинаты бактерий.
3.5. Органы иммунной системы
Для понимания работы иммунитета нужно прежде всего хорошо
представлять клеточные взаимодействия
всех
участников
иммунного ответа. Однако клеткам нужно где-то образовываться –
это происходит в органах иммунной системы. Давайте поговорим о
них.
Органы иммунной системы делят на центральные и
периферические: к первым относятся красный костный мозг (ККМ),
тимус, а у плода в период внутриутробного развития ещё и печень.
Периферические органы иммунитета – это лимфоузлы, селезёнка, а
также скопления лимфоидной ткани в разных органах и частях
организма, из которых вам лучше всего знакомы нёбные миндалины,
или в просторечье «гланды». Сообщение между центральными и
периферическими органами иммунитета осуществляется по сосудам
кровеносной и лимфатической систем.
Возможно, раньше вы уже слышали про красный костный мозг и
наверняка видели его, когда разламывали мозговую косточку из
бульона – у животных он выглядит и выполняет функции так же, как у
людей. Это основной орган, где происходит образование клеток крови:
тех же эритроцитов и тромбоцитов. Помимо них, здесь же рождаются
клетки так называемого «белого кровяного ростка» – лейкоциты. Их
нормальное содержание в крови значительно – на 3 порядка – ниже,
чем клеток «красной крови» – от 4 до 10*109 клеток в одном литре
крови. Однако само содержание лейкоцитов ещё ни о чём не говорит.
Если вы попробуете сдать кровь на общий анализ сразу после
интенсивной тренировки, то легко можете увидеть там и 12*109
клеток/л и больше. Это отражает лишь то, что ток крови усилился, а
для лучшего снабжения мышц кислородом организм выбросил из
своих «депо» ее резервный запас – в котором были не только
эритроциты, но, конечно, и лейкоциты тоже.
Поэтому гораздо важнее соотношение отдельных популяций
лейкоцитов, которых существует огромное множество. Раньше оно
отражалось в виде так называемой лейкоформулы – процентного
соотношения разных видов лейкоцитов в мазке крови. Сейчас
лаборатории всё чаще переходят к количественному подсчёту этих
видов в объёме крови.
Однако далеко не все и не всегда лейкоциты циркулируют в крови –
скорее даже наоборот. Чаще всего мы видим в мазке крови только их
часть, «путешествующую» из центральных органов иммунитета в
периферические, либо из этих органов в ткани, и обратно. Кроме того,
клетки и молекулы иммунной системы циркулируют не только по
кровеносному руслу. Важной «транспортной артерией» для них
служит лимфа.
В отличие от лимфатической системы, кровеносная вам уже
должна быть достаточно хорошо знакома. Вы знаете, что в
последней есть жидкая часть (сыворотка), в которой взвешены
форменные элементы: клетки крови и утратившие ядро зрелые
эритроциты и тромбоциты. В сыворотке содержится много белков,
в том числе необходимых для системы свёртывания крови:
фибриноген, протромбин и другие. Если отделённую от сгустка
прозрачную сыворотку крови некоторое время перемешивать в
пробирке стеклянной палочкой, то можно увидеть, как на ней
образуется белесоватый налёт – это нити белка фибрина, в который
полимеризуется фибриноген, создавая основу тромба и не давая нам
истечь кровью из-за незначительных ранений. Дефибринизированная
сыворотка называется плазмой. Однако она всё ещё содержит
множество белков (в частности компоненты комплемента и
антитела ), которые создают коллоидно-осмотическое давление в
капиллярах кровеносного русла. Не вдаваясь глубоко в физколлоидную
химию, просто поясним, что плазма за счёт белков тянет на себя
воду из межклеточного пространства. Но там есть своя жидкость
со своими белками, и они работают точно так же – «тянут одеяло
на себя». Однако главное давление в кровеносной системе создают,
конечно, не белки, а сердце, ритмично проталкивающее по ней кровь.
Гидростатическое давление крови достаточно велико, но нужно
помнить, что мы в целом весьма герметичны, ничего из нас с каждым
толчком сердца не выливается (а если выливается – это очень плохо, и
пора звать медиков). Но находимся мы не в вакууме – снаружи на нас
давит атмосфера, и давит очень сильно: более 1 кг на каждый
квадратный сантиметр тела (при 760 мм. рт. ст. нормального
атмосферного давления и общей площади поверхности тела взрослого
человека 1,5—2 м2 суммарно получается аж 15—20 тонн!). Через
поверхность кожи это давление передаётся на внутренние ткани,
клетки и межклеточную (интерстициальную) жидкость. Нас не
расплющивает только потому, что это давление уравновешивается
направленным изнутри давлением растворённых в крови и тканях
газов и гидростатическим давлением крови.
В итоге взаимного сложения противоборствующих сил образуется
очень небольшой – всего 3 мм. рт. ст. – градиент давления,
направленный из капиллярного русла в ткани. Из-за него некоторое
количество плазмы крови постоянно просачивается сквозь стенку
капилляров наружу. Если бы эта утечка не была ничем
скомпенсирована, то нас бы со временем раздуло до размеров слона:
болезненное нарушение оттока жидкости от конечностей с их
раздуванием так и называется – «слоновость». Этот же механизм
составляет часть патогенеза развития отёков: помимо него, там
задействовано нарушение венозного возврата.
Но в здоровом организме такого обычно не происходит или
происходит только временно. Потому что наряду с кровеносной
системой существует параллельная сеть капилляров и сосудов. За счёт
особых хитростей устройства в ней поддерживается небольшое
отрицательное давление, в результате вся «утёкшая» в ткани жидкость
дренируется через эту систему. Здесь она называется лимфой, а сама
система – лимфатической. Её сосуды постепенно сливаются друг с
другом во всё более крупные, пока наконец общий лимфатический
проток не вольётся в крупные вены в районе ключицы, вернув таким
образом все потери жидкости обратно в кровоток. Да ещё и с
«довеском», потому что лимфа, например, служит для переноса
всосавшихся в кишечнике жиров. В лимфатической системе они
формируют жировые шарики хиломикроны. Однако прежде чем
влиться в кровь, лимфа должна пройти через небольшие, чуть больше
горошины, но очень важные органы – лимфатические узлы.
Они расположены группами в подкожной жировой клетчатке в
районе паха, подмышек, на шее, в заушной области и под нижней
челюстью. Обычно их почти невозможно нащупать, пока в лимфоузле
не «поднимет кипиш» антигенпрезентирующая клетка, доставившая
туда антигены проникших в близлежащие ткани патогенов. Либо пока
в лимфоузел не попадёт сам возбудитель – например, чумная палочка
при бубонной форме этой инфекции мигрирует в ближайшие
лимфоузлы, вызывая в них гнойное воспаление – такой
увеличившийся в размерах лимфоузел и называют чумным бубоном.
Можно
сказать,
что
лимфоузлы
являются
своего
рода
«магистральными фильтрами» нашего организма, вылавливая все
оказавшиеся в тканях антигены.
Помимо лимфоузлов, существуют скопления очень похожей на них
по функциям лимфоидной ткани в разных органах и частях тела. Так,
в подслизистом слое тонкого кишечника (и начальном отделе толстого)
эти скопления носят названия пейеровых бляшек (по фамилии
описавшего их в XVII веке швейцарского анатома И. К. Пейера).
Особенно их много в червеобразном отростке слепой кишки (так что
пресловутый «аппендицит», который всё-таки, конечно, «аппендикс»,
тоже совсем не лишний орган). Здесь они стоят на страже барьера
между кишечным содержимым, полным чужеродной органики, и
собственными тканями организма.
Есть лимфоидные скопления, которые можно относительно просто
рассмотреть у человека – речь, конечно, идёт о нёбных миндалинах,
которые в просторечии называют «гландами». Они расположены по
обеим сторонам между дужками глотки. Неровная поверхность
миндалин с глубокими впадинами-«криптами» способствует задержке
частиц пищи, в которых содержащиеся здесь иммунные клетки
выискивают антигены опасных для человека микроорганизмов.
Нёбные миндалины, кстати, не единственные лимфоидные органы в
этой части тела. На задне-верхней поверхности глотки, позади
отверстий носовых хоан, в подслизистом слое находится непарная
глоточная миндалина. Обычно она не видна, но при воспалении
увеличивается в размерах, затрудняя свободный ток воздуха из
носовой полости в носоглотку. Иногда настолько, что приходится эту
миндалину, так же известную как аденоид, удалять. Аналогично
поступают и с патологически увеличенными гландами – их воспаление
называется тонзиллит, а операция удаления соответственно –
тонзилэктомия.
Если гланды и аденоиды более-менее выражены у всех людей, по
крайнем мере в детстве, то язычная (в корне языка) и две трубные (у
глоточного отверстия слуховых труб) миндалины могут быть совсем
небольшими скоплениями лимфоидных клеток. Все вместе эти
образования формируют внутреннее лимфоидное кольцо шеи (по
авторам – кольцо Пирогова-Вальдейра). Лимфатические сосуды
связывают их с лимфоузлами шеи, образующими внешнее
лимфоидное кольцо. Поэтому при ангине, например, увеличиваются не
только миндалины, но и набухают лимфоузлы в области шеи.
Селезёнка своим строением и функциями напоминает очень
крупный лимфоузел. Но хотя этот орган и не жизненно необходим
(селезёнка иногда разрывается при травмах брюшной полости, а это
чревато массивным внутренним кровотечением, и её приходится
удалять), он несёт целый ряд важных функций, в том числе связанных
с иммунной системой. Это одно из «депо крови», запасающее
резервный её объём на случай интенсивной физической нагрузки или
непредвиденных обстоятельств вроде ранения с кровопотерей. Как раз
для ликвидации последней пригодится и запасённая здесь же треть
всех наличных тромбоцитов организма.
Кроме того, селезёнка – это «кладбище эритроцитов». Красным
кровяным тельцам отмерено всего 4 месяца напряжённой «трудовой
жизни», в течение которой они обеспечивают газообмен между
лёгкими и тканями. По окончании этого срока эритроциты
задерживаются в селезёнке, разрушаются её макрофагами, а
оставшийся гемоглобин связывается в цикле синтеза желчных
пигментов и выводится кишечником.
Но самое главное – в селезёнке имеется специальная зона, где
происходит размножение и созревание особой группы лейкоцитов – Влимфоцитов. Их основная задача – синтез специальных молекул
иммунной системы, знаменитых антител. Впервые эта группа клеток
была открыта у птиц, где они образуются в птичьем аналоге селезёнки
– фабрициевой сумке. Сумка по латыни – «бурса» (bursa), отсюда и
название В-лимфоцитов. Когда при инфекционных заболеваниях
требуется повышенная продукция антител и В-лимфоциты начинают
активно размножаться, селезёнка увеличивается в размерах –
развивается так называемая спленомегалия (от лат. «сплен» –
селезёнка и греч. «мегас» – большой).
Во время внутриутробного развития плода многие функции
красного костного мозга и селезёнки несёт печень. После рождения
эти функции в ней угасают, но зато на полную включаются многие
другие: в частности, в печени происходит синтез множества белков
системы неспецифического иммунитета (С-реактивный белок,
молекулы системы комплемента). Она является ещё одним «депо»
крови. Кроме того, печень, кажущаяся такой однородной внешне,
имеет уникальное гистологическое строение – это настоящий
«зоопарк» разнообразных клеток, которые кооперируются друг с
другом, позволяя печени играть десятки важнейших ролей в нашем
организме: от эндокринных и иммунных до участия в пищеварении.
Печень является мощным «фильтром» для крови, обезвреживая
токсины и патогены, поступающие в первую очередь от ЖКТ по
системе воротной вены. Для этого она буквально набита
специализированными макрофагами – клетками Купфера. Печень, как
и селезёнка, тоже может значительно увеличиваться при
инфекционной
патологии.
Это
явление
носит
название
гепатомегалия,
а
когда
увеличиваются
оба
органа
–
гепатоспленомегалия.
Однако у В-лимфоцитов существуют друзья-приятели – Тлимфоциты. Они обозначены по названию другого важного органа
иммунной системы – тимуса. Тимус, или вилочковая железа,
представляет собой очень небольшое образование, помещающееся в
грудной клетке между грудиной и сердечной сумкой (перикардом).
Причём как функциональный орган он существует только у детей, а с
возрастом подвергается инволюции, постепенно замещаясь жировой и
соединительной тканью. Однако за столь непродолжительное время
жизни тимусу нужно провести очень ответственную работу – отобрать
из популяции лимфоцитов те, которые затем смогут опознавать
абсолютно любые попадающие в организм антигены, даже те их
конфигурации, которые природа ещё и создать не успела. При этом
лимфоциты ни в коем случае не должны возбуждаться в ответ на
молекулы собственного организма, иначе возникнет аутоиммунная
патология. По этой причине отбор лимфоцитов крайне жёсткий –
только одна из тысяч клеток-предшественников, мигрировавших из
красного костного мозга, успешно «сдаст экзамен» на право стать
защитником организма и отправится в «пункт постоянной
дислокации» в одном из лимфоузлов. Остальных немедленно
уничтожат макрофаги тимуса (надеюсь, вы не слишком живо
представили себя на месте Т-лимфоцита, для которого невыученный
билет равен расстрелу на месте?).
Т-лимфоциты, в отличие от В-лимфоцитов, антитела не
продуцируют. Но всё равно они играют важную роль для иммунитета –
особенно для связи неспецифического и специфического иммунитета,
для активации эффекторных клеток (макрофагов, нейтрофилов), а
иногда и для усмирения их излишней активности. Этим занимаются
две разные группы Т-лимфоцитов: Т-хелперы («помощники») и Тсупрессоры соответственно. Но не все Т-лимфоциты такие уж
раздумчивые
«миротворцы»
и
«дипломаты».
Когда
антигенпрезентирующая клетка активирует Т-лимфоцит, и тот
начинает делиться, то часть его клонов дифференцируется не в
хелперы или супрессоры, а «переходит на тёмную сторону»
и превращается в цитотоксический лимфоцит или Т-киллер. Эти
«киллеры» в организме предназначены в основном для уничтожения
раковых и заражённых вирусами клеток. Они опознают их по
изменившемуся ГКГ-I. Этот «родственник» ГКГ-II, экспрессируемого
дендритными клетками, имеется на всех клетках организма и служит
как бы опознающим сигналом: «Я свой!».
Важная поправка: ГКГ-I есть на всех клетках, имеющих ядро.
Эритроциты и тромбоциты поэтому лишены такого маркера. Чем и
пользуются, например, паразитические простейшие – малярийные
плазмодии. Из-за отсутствия ГКГ-I на мембране эритроцитов
иммунная система «не видит», что они заражены возбудителем
малярии, и долгое время позволяет плазмодиям безнаказанно
хозяйничать в нашей крови.
Под влиянием онкологического перерождения или атаки вирусов
ГКГ-I меняет свою структуру. В результате Т-лимфоциты-киллеры
слышат неправильный «пароль» на свои запросы и набрасываются на
такие клетки. Можно сказать, что они устраняют «предателей» и
«перебежчиков» среди клеток нашего организма. Так что, несмотря на
такое устрашающее название, Т-киллеры выполняют очень важную и
полезную для нас работу.
3.6. Лейкоформула крови
Разбираясь в механизмах иммунного ответа, строении и функциях
органов иммунитета, мы выяснили, что наши клетки-«бойцы»
и клетки-«разведчики» образуются в одних местах, а нести «боевое
дежурство» или идти «на подкрепление» вынуждены совсем в других.
И если человеческие солдаты для передислокации пользуются
автомобильными и железными дорогами, то для клеток иммунной
системы их роль играют лимфа и кровь. А это значит, что в период
инфекционного процесса там можно зафиксировать увеличенное
количество наших внутренних защитников «на марше».
Лимфу получить довольно сложно, а вот кровь обычно вполне
доступна для исследования. Общий анализ крови, при котором
подсчитываются содержание эритроцитов, лейкоцитов и тромбоцитов
в 1 литре крови, а также содержание гемоглобина и ещё ряд
показателей, является одним из самых распространённых в
клинической практике. По показаниям он дополняется подсчётом
лейкоформулы.
Естественно, что никто не откачивает у человека целый литр крови –
для исследования достаточно всего нескольких миллилитров. Раньше,
да и сейчас ещё зачастую тоже, подсчёт клеток проводился врачом или
лаборантом «глазами» при помощи микроскопа и специального
приспособления, называемого «камерой Горяева». Внесённый в неё
объём крови стандартный, а значит, полученное в нём содержание
форменных элементов крови можно легко пересчитать на любой
удельный объём решением простой пропорции. Для удобства
условились всегда считать на литр. Современные гематологические
анализаторы, конечно, делают это быстрее. Но пока они не могут
полностью заменить опытного специалиста.
Нормальные и патологические значения общего анализа крови
(ОАК) студенты изучают на клинических дисциплинах, а обычный
человек может попросить интерпретировать результат своего лечащего
либо участкового врача или сориентироваться на допустимые,
«референсные» значения, обычно тоже приведённые в бланке с
результатами. Правда, после такого самостоятельного «прочтения»,
обнаружив множество отклонений от нормы, человек, как правило,
начинает необоснованно подозревать, что дни его практически
сочтены, и в панике мчится в больницу. Где все его страхи частенько
оказываются последствиями нарушений подготовки к исследованию,
погрешностями диеты или индивидуальными особенностями (кроме
того, нужно учитывать пол и возраст – у взрослых и детей показатели
значительно отличаются, есть в картине крови и гендерные различия).
Для лейкоцитов, которые сейчас нас больше всего интересуют,
условно нормальным считается содержание от 4 до 10 на 109 клеток в
литре крови. Понижение этого значения называется лейкопения,
повышение – лейкоцитоз. Обычно о воспалении или наличии
инфекции судят по повышению числа лейкоцитов. Однако это не
всегда верно – вирусные инфекции, наоборот, могут приводить к его
снижению.
Лейкоформулой называется результат подсчёта отдельных
популяций лейкоцитов в крови. Для этого делается мазок крови на
предметном стекле, фиксируется, окрашивается красителем
Романовского-Гимзы, после чего клетки считают под микроскопом.
Современные
технологии
позволяют
облегчить
и
даже
автоматизировать этот процесс, однако и в этом случае часто
требуются глаза (и знания, конечно) человека.
Раньше общепринятым методом выражения лейкоформулы было
процентное соотношение: какую долю составляет каждая популяция
от всего числа просмотренных под микроскопом клеток. Сейчас это
исследование часто дополняется подсчётом абсолютного числа клеток
каждой популяции.
Каковы же составляющие лейкоформулы? Разумеется, в первую
очередь нас интересуют клетки, которые могут указать на развитие
иммунного и/или воспалительного ответа. Вы уже знаете, что это
нейтрофилы, макрофаги и лимфоциты.
Нейтрофил под микроскопом выглядит как крупная клетка с
выраженным ядром – отличительный признак высокой активности
(ведь нейтрофилу нужно синтезировать большое количество
антимикробных веществ). Чем более нейтрофил зрелый, тем сильнее у
него сегментировано ядро, чтобы обеспечить постоянную
транскрипцию информации с генома в белоксинтезирующий аппарат
клетки. Поэтому для лейкоформулы отдельно подсчитывают более
юные палочкоядерные и более зрелые сегментоядерные лейкоциты.
При ручном оформлении результатов анализа лейкоформулу для
краткости могут записывать сокращениями до одной буквы и
процентным содержанием в мазке. Получается запись вида п2 с60 э2
м6 л30 (сумма цифр, естественно, должна быть равна 100 – это же
проценты), где п и с – те самые палочкоядерные и сегментоядерные
нейтрофилы. Иногда в мазке могут находить так называемые юные
нейтрофилы (не более 1 процента) и миелоциты – предшественники
нейтрофилов, которые находятся в красном костном мозге и в норме в
кровь выходить не должны. Однако при инфекционных процессах в
организме, интоксикации, онкологических заболеваниях они
выявляются в мазке.
Эозинофилы названы так за характерное свойство содержащихся в
их цитоплазме гранул окрашиваться в красно-розовый цвет пигментом
азур-эозином (один из компонентов красителя Романовского-Гимзы).
Повышение их числа свидетельствует об аллергических реакциях
или глистной инвазии (заражение гельминтами – например,
аскаридой).
Помните, мы упоминали про тучные клетки при описании
воспалительного ответа на проникновение патогена? Именно они
запускали расширение сосудов в очаге поражения, облегчая
проникновение к нему клеткам и молекулам иммунитета. В крови их
содержится обычно не более 1 процента, так как в основном они сидят
в тканях, готовые известить организм о любом нарушении.
Содержащаяся в них аминокислота гистамин легко связывается с
имеющим щелочную реакцию метиленовым синим – вторым
компонентом краски Романовского-Гимзы. Из курса школьной химии
вы должны помнить, что другое название щелочей – основания (по
латыни – «базис»). Поэтому циркулирующие в крови, ещё не осевшие
в тканях, тучные клетки называют базофилами.
«Под псевдонимом» путешествуют в крови и будущие макрофаги –
здесь они ещё совсем не похожи на амёб, а выглядят как клетки с
крупным, занимающим значительную часть цитоплазмы, ядром, и
называются моноцитами.
Лимфоциты по сравнению с ними чуть мельче, но цитоплазмы в
них ещё меньше – клетку почти целиком занимает ядро. Часть из них
совсем скоро тоже сменит имя и начнёт активно синтезировать белки,
а именно – антитела. Речь, конечно, идёт о В-лимфоцитах, которые в
тканях именуются плазматическими клетками. Из-за округлого ядра,
чуть сдвинутого от центра клетки, лимфоциты в мазке имеют
характерный вид «перстня».
Если в крови увеличено относительное содержание нейтрофилов,
записываемых в левой части лейкоформулы, особенно палочкоядерных
и юных, а также появляются миелоциты, то говорят о сдвиге
лейкоформулы влево. Сильный сдвиг влево обычно характеризует
тяжёлую бактериальную инфекцию, гнойно-воспалительный процесс.
В большей степени он говорит об остром характере воспаления.
Увеличение содержания лимфоцитов, которые записывают в конце
лейкоформулы, называется сдвигом вправо. Оно больше характерно
для хронических инфекционных и воспалительных состояний, для
вирусных инфекций и интоксикаций.
Однако при любых колебаниях нормального процентного состава
как вверх, так и вниз нужно обращать внимание на абсолютное
содержание клеток – оно может оставаться нормальным, что указывает
на отсутствие патологии. Равно как и наоборот – в процентном
отношении лейкоформула в норме, а число клеток сокращается или
увеличивается (см. таблицу ниже).
Вообще всегда помните, что даже выраженные в виде интервалов
«нормальные значения» являются усреднёнными и должны
рассматриваться в связи друг с другом, с результатами клинического
обследования и других анализов.
Глава 4. На лицо ужасные, добрые
внутри
Теперь понемногу рассмотрим каждую группу микроорганизмов.
Начнём с бактерий. В отличие от тех же вирусов или прионов,
бактерии – это клеточная форма жизни, а значит, они способны к
автономному самовоспроизводству. Бактерии питаются, растут,
делятся, а также способны обмениваться друг с другом генами,
приспосабливаясь к меняющимся условиям среды. И так поколение за
поколением, за счёт закрепления наиболее подходящих для выживания
признаков, они меняются со временем – эволюционируют.
Однако клетки бактерий не могут объединиться в один
многоклеточный макроорганизм. Правда, и это утверждение несколько
спорно, поскольку бактерии могут образовывать колонии и
биоплёнки.
Первые обычно наблюдают бактериологи на поверхности
питательных сред в чашках Петри. Эти плоские стеклянные или
пластиковые сосуды, напоминающие тарелочки или скорее
пепельницы, состоят из собственно чашки и крышки к ней – такой же
формы, но чуть большего диаметра. В чашку разливают определённый
объём растопленной питательной среды – существует множество их
рецептур, предназначенных для выявления разных родов и видов
бактерий, но в целом все содержат набор питательных веществ и
солей, цветной индикатор, а основу составляет агар-агар, благодаря
которому остывшая среда образует упругий слой, напоминающий
застывший клейстер или очень плотное желе. На поверхность её
шпателем или чаще специальной бактериологической петлёй вносят
исследуемый биологический материал. Затем чашку Петри накрывают
крышкой и ставят в термостат, поддерживающий определённую
температуру: для бактерий – возбудителей инфекций человека это
обычно 37 градусов Цельсия.
Оставленные в этих условиях бактерии, если они были в
исследуемом материале, начинают размножаться. Из каждой
бактериальной клетки образуется огромное количество её клонов:
кишечная палочка, например, делится каждые несколько минут – в
итоге спустя сутки инкубации на поверхности среды в чашках Петри
их можно наблюдать как округлые капельки диаметром от менее
одного до нескольких миллиметров. Размер, цвет, форма колоний
отличаются у разных бактерий и, кроме того, зависят от среды, на
которой они выросли. А разработчики специально подбирают
рецептуру так, чтобы максимально точнее можно было отличать
колонии разных видов друг от друга. И при необходимости отобрать
нужные и перенести (пересеять) на свежую чашку для дальнейшего
изучения. В этом заключается бактериологический метод
диагностики – мы ещё будем говорить о нём подробнее в следующей
главе этой книги.
С биоплёнками всё ещё интереснее. Накопившиеся в последние
годы данные говорят, что лишь ничтожная часть бактерий (всего 3—
5% от всей планетарной популяции) проживает в виде свободно
взвешенных в среде (воздухе, водах океана и т. п.) отдельных клеток –
все остальные стремятся закрепиться на любом подходящем субстрате.
И здесь они образуют удивительную форму проживания – настоящий
микробный «город», в пределах которого бактерии (зачастую разных
родов и видов) устанавливают друг с другом симбиотические связи,
обмениваясь молекулярными сигналами, питательными веществами,
кислородом и т. п. Порой в биоплёнках на правах симбионтов могут
существовать и эукариоты – например, грибы. Получается уже
настоящий микробный «интернационал», который по многообразию
своих молекулярных и биохимических процессов, а также составу
участников приближается к настоящему многоклеточному организму.
Биоплёнки вы вполне могли наблюдать сами, если у вас есть
аквариум – в виде налёта на его стёклах, который ещё и чистить
регулярно приходится. Неприятный слизистый налёт, с которым вам,
возможно, приходилось сталкиваться при прочистке забившейся
канализации – это тоже биоплёнка. Чтобы закрепиться на какой-то
поверхности, бактерии выделяют клейкий слизистый матрикс, в
основном состоящий из полисахаридов – по сути, это крепкий кисель.
Он защищает бактерии от смывания или, наоборот, высыхания, так как
хорошо удерживает влагу. Со временем матрикс пропитывается солями
железа, кальция и других элементов, образуя уже нерастворимый
осадок, сужающий и забивающий просвет водопроводных и
канализационных труб. Зубной налёт – это тоже биоплёнка, в которой
идут схожие процессы. Поэтому образующийся зубной камень,
создающий определённые проблемы и заставляющий обращаться для
его удаления к стоматологам, тоже имеет непосредственное отношение
к деятельности микроорганизмов.
Так что бактерии не только живут разнообразной жизнью, заполняя
все уголки нашей планеты, но и на нашу жизнь очень заметно влияют.
Мы ещё вернёмся к бактериальным сообществам и биоплёнкам, когда
станем говорить о микрофлоре, а пока внимательнее рассмотрим
устройство бактерий.
Раньше бактерий делили на две группы – эубактерии, или истинные
бактерии, и архебактерии (археи). Сейчас подход несколько иной: все
прокариотческие организмы на основании структуры их генома
отнесены либо к бактериям (прежние «эубактерии»), либо к археям.
Последние медицинского значения не имеют – хотя вернее сказать, что
среди них пока не известно возбудителей заболеваний человека, а вот
значение для нашего здоровья они имеют, и ещё какое, и это мы тоже
обсудим в главе о нашей собственной микрофлоре.
Бактерии и археи являются прокариотами или предъядерными (от
«карион» – ядро – и приставки «про-», которая указывает на
нахождение чего-либо перед или раньше). Обычно говорят, что у
бактерий отсутствует ядро, хотя ниже мы скажем, что это не совсем
так. В качестве основного носителя генетической информации
бактерии имеют двойную спиральную молекулу ДНК, замкнутую в
кольцо. Вместе с поддерживающими белками она составляет
единственную «хромосому» бактериальной клетки. Именно так – в
кавычках, поскольку из-за отсутствия поддерживающих белковгистонов
бактериальная
ДНК
не
имеет
способности
суперспирализоваться и потому весьма некомпактно распределена в
цитоплазме, занимая до 20 процентов объёма клетки. Однако
функционально – это всё же аналог хромосомы эукариот. Данная
«консервативная» ДНК обеспечивает единообразие вида бактерий.
Помимо неё у бактерий могут быть 1—2 дополнительные линейные
молекулы ДНК и от одной до нескольких плазмид. Это небольшие
молекулы ДНК, кодирующие какие-либо дополнительные признаки,
отличающиеся у разных штаммов одного вида бактерий. Например,
есть плазмиды, несущие гены факторов устойчивости к
антибиотикам, агрессивным факторам среды, тяжёлым металлам и т.
д.
Штамм (название применимо как к бактериям, так и к вирусам) –
любой конкретный образец (изолят) данного вида, выделенный из
какого-либо объекта (в том числе и от человека).
Вариант – совокупность бактерий одного вида, различающихся по
антигенным характеристикам (сероварианты – сокращенно
серовары), по чувствительности к специфическим бактериофагам
(фаговары), биохимическим свойствам (хемовары) или биологическим
(биовары) и т. д.
Колония – видимая изолированная структура при размножении
бактерий на плотных питательных средах из одной (реже нескольких)
родительских клеток. Последние при этом называются КОЕ –
колониеобразующая единица , и именно в них чаще всего
указываются количественные результаты бактериологических
исследований.
Культура (чистая культура) – вся совокупность микроорганизмов
одного вида, выросших на плотной или жидкой питательной среде.
При всём этом хромосома бактерии не «размазана» по цитоплазме:
она образует скопление в центре бактериальной клетки – нуклеоид.
Нуклеоид, в отличие от истинного ядра эукариот, ничем не отграничен
(не компартментализирован) от цитоплазмы. Поэтому обычно
подчёркивают, что у бактерий нет выделенного ядра.
Организация генетического материала бактериальной клетки
влияет на то, что у них отсутствует половой обмен генами –
бактерии размножаются только путём неизменного копирования
своей ДНК с последующим разделением клетки. Поэтому колония
бактерий, выросшая на питательной среде из одной родительской
клетки, равнозначна понятию клон . Бесполое размножение
ограничивает изменчивость бактерий, однако они научились обходить
ограничения другими способами, в частности, той же передачей
плазмид.
Нуклеоид является одной из обязательных (облигатных) структур
бактериальной клетки. Наряду с ним к обязательным структурам
относятся:
цитоплазма;
клеточная мембрана (аналог цитоплазматической мембраны);
рибосомы;
клеточная стенка.
Дополнительными (необязательными) структурами бактерий
являются:
разного рода цитоплазматические включения (гранулы);
споры;
жгутики;
пили и фимбрии;
капсула.
Цитоплазма бактерии, как и любой живой клетки, представляет
собой коллоид (взвесь) белков, жировых глобул и твёрдых частиц в
водном растворе органических и неорганических солей.
В цитоплазме «плавают» и другие структуры (органеллы) бактерии,
например, рибосомы, служащие для синтеза белка. Рибосомы
бактериальной клетки отличаются от рибосом эукариот – они имеют
иное внутреннее строение и меньший размер (70S против 80S-рибосом
у эукариот, где S, «сведберг» – единица массы мельчайших структур,
для которых просто не существует весов, и поэтому их сравнивают по
скорости оседания в центрифуге под действием центробежной силы).
Это позволяет подобрать антибиотики, блокирующие синтез белка
только в бактериальных клетках и слабо воздействующие на клетки
эукариотического макроорганизма.
Однако такие антибиотики относятся к бактериостатическим –
способным только остановить рост и размножение бактерий, но не
убить их. Правда, иногда это даже хорошо. Ряд компонентов
бактериальной клетки способен провоцировать наш организм на
чрезмерно сильную иммунную реакцию, например, на резкое
повышение температуры тела и выброс медиаторов воспаления. В
случае массивной гибели бактерий под действием бактерицидных
антибиотиков такая реакция может оказаться запредельно сильной,
способной убить человека – возникает инфекционно-токсический
шок. Это ещё один аргумент в пользу рационального применения
антибиотиков – только по назначению врача.
Бактерии, в отличие от эукариот, не имеют таких органелл, как
митохондрии – эти структуры синтезируют АТФ, обеспечивая
клетку энергией. У бактерий данный процесс происходит в
цитоплазме. Впячивания цитоплазматической мембраны внутрь
бактериальной клетки – мезосомы – длительное время считались
аналогами как митохондрий, так и эндоплазматического ретикулума.
Однако к концу XX века было доказано, что подобные структуры
являются просто повреждениями клеточной мембраны бактерий при
подготовке препаратов для электронной микроскопии. И хотя ряд
учёных продолжает считать их самостоятельными органеллами,
однако в основном этот термин по отношению к прокариотам
больше не применяется.
Помимо органелл в цитоплазме могут быть взвешены гранулы
запасных питательных веществ или пигментов – так, золотистый
стафилококк при определённых условиях продуцирует золотистооранжевый пигмент, а синегнойная палочка – зеленовато-синий
пиоцианин.
Снаружи цитоплазму отграничивает от окружающей среды
клеточная мембрана. Она представляет собой двойной слой из
амфиполярных молекул – органических молекул, один конец которых
всегда ориентирован к водной среде, другой – от неё (соответственно
гидрофильный и гидрофобный концы, от «филос» – любящий, и
«фобос» – страх). В живых клетках такие молекулы обычно
представлены разного рода жирами (липидами), например
фосфолипидами. В двойном слое таких молекул их гидрофильные
«головы» во внутренней части разворачиваются в сторону жидкой
цитоплазмы, а в наружной – в сторону внешней (часто тоже жидкой)
среды. При этом их гидрофобные «хвосты» оказываются повёрнуты
друг к другу, в середину двойного слоя.
Иллюстрацией такой модели служит бутерброд, где гидрофильные
«головы» как булочка окружают гидрофобную «начинку». Она так и
называется – «сэндвич-модель». Правда, в чистом виде считается
устаревшей и уступила место «мозаичной модели», учитывающей
наличие
и
других
компонентов
мембраны.
Ведь
такая
самоупорядочивающаяся структура довольно стабильна, а главное –
непроницаема для воды, гидрофобных и крупных гидрофильных
молекул, ионов и т. п. Но без обмена веществами с окружающей
средой никакая клетка существовать не может. Поэтому она
вынуждена прокладывать сквозь свою мембрану «шоссе» для
перемещения различных веществ наружу или внутрь: для этого служат
различные ульраструктуры цитоплазматической мембраны – поры,
каналы, инвагинации (впячивания мембраны) и т. п., в образовании
которых участвуют прежде всего разного рода белки.
Клеточная мембрана не поддерживает форму клетки, она слишком
тонкая и непрочная для этого. Но с поддержанием внутреннего состава
клетки справляется достаточно хорошо. А этот состав значительно
отличается от внешней среды. Так, концентрация солей и других
осмотически активных веществ внутри бактериальной клетки
значительно выше, чем снаружи, а значит и так называемое
осмотическое давление в ней гораздо выше. Поэтому движущаяся по
законам химии в сторону большей «солёности» вода стремится
проникнуть в клетку, вызывая её набухание. Если бы бактерию
снаружи отграничивала только клеточная мембрана, то при большой
разнице концентраций солей внутри и снаружи клетки она бы не
выдерживала и разрывалась. Возможно, вы сами наблюдали или
читали описание такого опыта с эритроцитами человека, которые
сморщиваются в солёном (гипертоническом) растворе и лопаются
(подвергаются лизису) в дистиллированной воде.
Однако бактерии в нормальных условиях могут выдерживать
достаточно значительные колебания параметров внешней среды за
счёт уникальной структуры – клеточной стенки. Это весьма жёсткая
(ригидная) структура, выдерживающая на таких микромасштабах
давление до 40 атмосфер (для сравнения: в водопроводе, сорванный
кран на котором в считанные минуты фонтаном заливает и вас, и
соседей снизу, давление порядка 4 атмосфер). Достигается такое
свойство за счёт её необычного устройства.
Клеточная стенка бактерий в основном построена из комплекса
полисахарида и белка, называемого пептидогликан (пептид –
короткоцепочечный белок, «гликос» – сладкий, что указывает на
сладкий вкус сахаров, мономеров полисахарида). Он имеет очень
интересную структуру, в которой прочные цепочки полисахарида
располагаются параллельно и связаны «мостиками» пептидных
молекул. В результате бактерия под слоем пептидогликана выглядит
как арбуз в авоське. Казалось бы, одна «авоська» особой прочности не
даст, но бактерии напяливают на себя от 8—10 до 40 таких «авосек». А
это уже сродни применению композитных материалов в технике –
когда разные компоненты придают готовому изделию вроде бы
взаимоисключающие свойства. Например, крыло самолёта из
углеволокна одновременно прочное и гибкое. Как видите, многое из
технического прогресса мы повторяем за живой природой.
Ещё одним важным значением пептидогликана является то, что он –
мишень для действия ряда антибиотиков. Например, пенициллин и
его аналоги, а также цефалоспорины (так называемые бета-лактамные
антибиотики – из-за их химической структуры) нарушают синтез
пептидогликана и нормальное образование клеточной стенки. А
поскольку она, как мы уже сказали, обязательный компонент клетки,
то под действием этих групп антибиотиков бактерии погибают – это
бактерицидные препараты («цидос» – убивать). К сожалению, на
пенициллин и первые поколения цефалоспоринов почти у всех
болезнетворных бактерий уже выработалась устойчивость: они
научились
либо
продуцировать
ферменты
бета-лактамазы,
разрушающие молекулы антибиотиков, либо некоторое время
переживать «голыми», утрачивая клеточную стенку (сферопласты или
L-формы).
Клеточная стенка, в отличие от цитоплазматической мембраны,
настолько прочная, что сохраняет определённую форму бактерии.
Вообще этих форм достаточно много, но по большому счёту они
крутятся вокруг двух основных: шара и цилиндра. Первые называются
кокками (от «коккус» – зерно, ягода, орех; слово «кокос» вам ни о чём
не говорит?), для вторых решили не заморачиваться поиском
эквивалента и назвали просто палочками, потому что именно как
чёрточки-палочки они выглядят в микроскопе. Все остальные формы
сводят к этим двум: например, извитая в виде запятой холерная
бактерия (вибрион) считается палочковидной, а возбудитель гнойного
менингита, имеющий форму «кофейного зерна» диплококк –
кокковидным (не динозавр диплодок, а диплококк – располагающиеся
в мазках попарно круглые бактерии: от приставки «ди-», означающей
«двойной»).
Для бактериологов особенно важно, что форма клетки бактерии
присуща всему виду и даже роду и произвольно меняться не может,
пока не нарушена целостность клеточной стенки. То есть форму
можно использовать для идентификации бактерий.
Однако живые клетки под микроскопом довольно сложно
рассмотреть просто так, без дополнительной окраски. Чаще всего из
клинического материала или из колоний, выросших на питательной
среде, готовят мазок – тонко наносят бактериальную взвесь на
предметное стекло и подсушивают. Затем такой мазок окрашивают.
Методов окраски существует великое множество. Есть простые
методы – с применением одного красителя. Например, коринебактерии
(мы упоминали в предыдущих главах коринебактерию дифтерии –
возбудитель соответствующей инфекции) окрашивают синькой
Леффлера. Однако чаще всего применяют сложные, включающие два и
более красителя методы. Обычно окрашивается не вся бактериальная
клетка целиком, а определённые её структуры (клеточная стенка,
цитоплазма, споры и т. п.), что обусловлено физико-химическим
взаимодействием слагающих эти структуры молекул с молекулами
пигмента. Для окраски разных частей бактерии подбирают разные
пигменты (красители) и разные методы. Те из них, что основаны на
конкурентной окраске двумя пигментами разного цвета, называют
дихроматическими. Наиболее известный – окраска по Граму.
Правда, когда датский врач Ганс Христиан Грам в 1884 году
предложил свой метод окраски бактериальных мазков анилиновыми
красителями, он (метод, а не врач) ещё не был дихроматическим. Грам
использовал генциан-виолет или метил-виолет. Затем обрабатывал
мазки йодом для фиксации окраски и затем обесцвечивал спиртом.
Однако, если некоторые бактерии после такой обработки отлично
были видны в микроскоп как сине-фиолетовые шарики и палочки, то
другие – едва-едва.
Это был серьёзный шаг вперёд для специфической диагностики
инфекций, и потому в дальнейшем все бактерии были разделены по
тинкториальным свойствам (способности принимать окраску) на
Грам-положительные (грам«+» – хорошо окрашивались по методу
Грама) и Грам-отрицательные (грам«—» – соответственно
окрашивались плохо). Однако почему одни бактерии предпочитают
«цвет настроения синий», а другие воздерживаются – это тёзка и
земляк великого сказочника, как и другие учёные конца XIX века, мог
только предполагать.
Выяснилось всё много позже с изобретением электронного
микроскопа и других методов исследования. Оказалось, что красители,
используемые Грамом, задерживались не какими попало структурами
бактерии, а конкретно – клеточной стенкой. Ранее мы уже сказали, что
число слоёв пептидогликана у бактерий отличается. Следовательно, в
толстой стенке грамположительных бактерий сине-фиолетовый
краситель «запутывается» среди множества слоёв и при
обесцвечивании спиртом отмывается плохо. В то время как
грамотрицательные бактерии имеют тонкую клеточную стенку и не
могут удержать достаточное количество пигмента. В современных
модификациях метода Грама мазок после обработки генциан-виолетом
докрашивают другим – контрастным к нему, чаще всего ярко-красным
красителем фуксином. В результате грам«+» бактерии будут видны в
поле зрения микроскопа как сине-фиолетовые, а грам«-» – как розовые
или красные.
Для простоты запоминания студенты обычно пользуются
«правилом светофора»: красный сигнал – это «стоп», отрицание,
«минус». Значит, красные бактерии – грамотрицательные.
Однако и в этот раз коварные микробы не дали учёным создать
простую и понятную классификацию. Во-первых, оказалось, что
некоторые бактерии с толстой клеточной стенкой довольно плохо
воспринимают окраску по Граму и потому долгое время считались
грамотрицательными.
Во-вторых,
выяснилось,
что
есть
микроорганизмы, которые совсем не похожи на бактерии по
устройству клеточной стенки и даже могут вовсе её не иметь, и всё же
это именно бактерии.
Общее количество видов бактерий огромно. Все известные к
настоящему времени перечислены в одном общем международном
классификаторе. Впервые его составил американский исследователь
бактерий Девид Берджи почти 100 лет назад – в 1923 году (мы
упоминали его, когда вели разговор о морфологии бактерий и
строении их клеточной стенки). И хотя с тех пор этот труд постоянно
дополнялся и перерабатывался, из уважения к первому автору он
продолжает называться «Определителем бактерий Берджи».
Это в русском издании, а английское название – Bergey’s Manual of
Systematic Bacteriology, то есть «Справочник Берджи по
бактериологической систематике». Что поделать – специфика
перевода. Название фильма К. Нолана «Tenet» ведь тоже переводится
отнюдь не как «Довод», но кто поспорит, что русские переводчики
подобрали удачный эквивалент?
Д. Берджи в основном ориентировался на строение клеточной
стенки и другие фенотипические, то есть внешние, признаки бактерий
(ничего другого ему в начале XX века доступно и не было). На этом
основании он выделил 4 категории бактерий:
грациликуты – бактерии с тонкой клеточной стенкой (нетрудно
быть грациозным, когда ты тонкий) – их относят к грам«-» бактериям
независимо от того, как фактически они окрашиваются по Граму;
фирмикуты – бактерии с толстой клеточной стенкой (грам«+»
бактерии);
тенерикуты – бактерии, лишённые клеточной стенки (к ним
относятся микоплазмы, хламидии, риккетсии и актиномицеты);
мендозикуты – сюда относятся архебактерии, строение клеточной
стенки которых имеет значительные отличия от эубактерий.
Патогенных для человека мендозикут пока не обнаружено.
Со временем, правда, поменялся даже сам подход к классификации
бактерий: последние пересмотры классификации уже основаны на
молекулярно-генетическом методе. Он заключается в сравнении
последовательности нуклеотидов гена, кодирующего рибосомальную
16S-рРНК – компонент бактериальных 70S рибосом.
Хламидии, риккетсии и микоплазмы поверх цитоплазматической
мембраны имеют некий аналог клеточной стенки, но она состоит из
стеролов и других органических соединений, которые больше
присущи многоклеточным организмам. Возможно, это связано с тем,
что если микоплазмы ещё могут быть свободноживущими и давать
колониеобразование на плотных питательных средах, то риккетсии и
хламидии – это такие же облигатные внутриклеточные паразиты, как
вирусы. Размножаться они могут исключительно в цитоплазме клеток
организмов-хозяев и потому на питательных средах не растут. Однако
организация генетического материала (ДНК и РНК) и других органелл
однозначно заставляет отнести их к бактериям.
Многие тенерикуты имеют важное значение в инфекционной
патологии: определённые виды хламидий вызывают венерический
лимфогранулематоз, риккетсии – переносимые клещами инфекции
типа лихорадки Скалистых гор, микоплазмы – атипичные пневмонии и
инфекции мочеполовой сферы.
Актиномицеты долгое время считались грибами: их клетки
образуют длинные ветвящиеся нити, очень похожие на мицелий
плесневых грибов. К тому же актиномицеты размножаются
структурами, похожими на споры (конидии). Однако наличие
нуклеоида вместо оформленного ядра и отсутствие хитина в клеточной
стенке однозначно относят их к бактериям. К актиномицетам
принадлежат микобактерии, в том числе возбудители туберкулёза
человека (микобактерия туберкулёза – «палочка Коха») и животных.
Определитель Берджи в наше время включает 5 пухлых томов. К
нашему счастью, патогенных для человека бактерий среди них
сравнительно мало, но и этого количества хватает с лихвой.
Помимо деления на 4 категории (и внутри них – ещё более чем на 30
групп), определитель Берджи использует так называемую
филогенетическую классификацию бактерий, учитывающую степень
родства между отдельными видами. Согласно ей, домен эубактерий в
дальнейшем разделяется на филумы (у эукариот этот таксономический
уровень называется типом), те, в свою очередь, – на классы, классы на
порядки, затем следуют семейства, роды и наконец, виды.
На примере всё той же кишечной палочки это значит, что она
является протеобактерией (филум) из класса гамма-протеобактерий,
порядка энтеробактералес, который после внесения изменений в 2016
году включает одно-единственное семейство «энтеробактериацее»
(или, в русском варианте, энтеробактерии), разделённое на 26 родов.
В роду эшерихий как раз и описан вид «эшерихия толстокишечная»
(так дословно на русский язык переводится «эшерихия коли»), в
русской номенклатуре называемая кишечной палочкой.
Собственно, это та же биологическая классификация, в которую
вписываются и другие живые существа. Вспомните: вид человек
разумный относится к роду человек (люди) из семейства гоминид
отряда приматов класса млекопитающих типа хордовые царства
животных, входящего в домен эукариот.
Естественно, в обиходе никто не использует полные
классификационные наименования: их сокращают до двух последних
таксонов – названий рода и вида на русском или латинском языке. Это
называется бинарной классификацией.
Примерно то же самое, как прусская герцогиня София Августа
Фредерика Ангаль-Цербстская, выйдя в России замуж за наследника
престола Петра III, стала просто Екатериной Алексеевной, а чуть
позже Екатериной II.
Так, помимо кишечной палочки, появляются названия золотистый
стафилококк (S. aureus – стафилококкус аурес), туберкулёзная
микобактерия (M. tuberculosis – микобатерия туберкулёзис) и т.п. Для
некоторых (на самом деле для большинства) видов микроорганизмов
переводных названий на русский язык не существует: ацинетобактер
баумани (Ac. baumanii), стенотрофомонада мальтофилиа (St.
maltophilia). А у некоторых есть вненоменклатурные авторские или
«исторические» названия: палочка Гофмана (C. pseudodiphtheriticum),
палочка Фриша-Волковича (K. scleromae), вышеупомянутая M.
tuberculosis – это палочка Коха.
Поскольку бинарные названия стараются давать так, чтобы было
поменьше совпадений (например, есть золотистый стафилококк, но
нет золотистого стрептококка или стенотрофомонады), то
названия рода микроорганизма обычно можно без снижения
информативности сократить до одной или нескольких букв: так
кишечная палочка Escherichia coli обычно указывается просто как
E.coli.
Различие строения клеточной стенки грам«+» и грам«-» бактерий не
заканчивается только на её толщине. У грамотрицательных бактерий
тонкий слой пептидогликана прикрыт сверху ещё одной – наружной
мембраной, напоминающей по строению клеточную мембрану.
Пространство между ними называется периплазматическим или
периплазматической
щелью.
Внутренний
слой
наружной
бактериальной мембраны состоит из фосфолипидов, аналогичных
слагающим клеточную мембрану. А внешний – из молекул
липополисахарида (ЛПС), то есть комплекса из полисахарида и
липида (жира). Для нас ЛПС интересен тем, что он является
антигеном (молекулой, опознаваемой иммунной системой) и
эндотоксином грам-отрицательных бактерий (тем самым, который мы
упомянули ранее и из-за которого могут быть трагические последствия
при неправильной антибиотикотерапии).
Само предпочитаемое расположение бактериальных клеток в мазке
тоже является идентификационным признаком. Например, палочки
дифтерии часто располагаются под углом друг к другу, образуя в мазке
характерные «римские пятёрки» V и «десятки» Х.
Сферические кокки могут:
лежать поодиночке (микрококки – частые бактерии воздушной
среды),
образовывать группы по две клетки (диплококки – уже упомянутые
менингококки в форме «кофейного зерна» и ланцетовидные
пневмококки в форме «пламени свечи»),
по четыре (тетракокки – медицинского значения не имеют),
по восемь (форма «багажного тюка») – такой тип расположения и
одноимённый род непатогенных бактерий называется сарцины (не
путайте их с воинами-сарацинами)
или образовывать в мазке компактные скопления, отдалённо
напоминающие формой виноградную гроздь (по латыни она
называется «стафилос» – отсюда и термин).
Такая ориентация клеток не случайна и определяется характером их
деления и последующего расхождения: тетракокки делятся в двух
взаимно перпендикулярных плоскостях, сарцины – в трёх и т. д.
Иногда клетки делятся только в одной плоскости, образуя в результате
более или менее длинные цепочки. Для кокков их называют
стрептококками (частые возбудители гнойных заболеваний, а также
скарлатины), для палочек – стрептобациллами (от «стрепто» –
верёвка). Стрептобациллы сибирской язвы, например, имеют
утолщения на концах, что придаёт их цепочкам в мазке характерный
вид «бамбуковой трости».
Чтобы не усложнять себе жизнь, бактериологи вообще всё
многообразие форм бактерий считают вариациями сферической или
цилиндрической (палочковидной). Даже спиральные бактерии
(например, трепонемы, в том числе бледная трепонема – возбудитель
сифилиса) и бактерии в форме запятой (вибрионы, среди которых
есть холерный вибрион) относят к «изурлюченным», но палочкам.
Помимо формы и окраски бактериальной клетки, для их
«опознания» могут служить и другие внешние признаки: например,
наличие и расположение жгутиков. Жгутики, как правило, – атрибут
палочковидных бактерий. Они отличаются по белковому составу и
принципу действия от жгутиков простейших, но функция у них
сходная: чаще всего это орган движения. Жгутиков может быть один
(такой тип называют монотрихий от «трихос» – волос), два (полярно
расположенные на концах клетки – амфитрихий) или много. В
последнем случае они либо собраны в пучок на одном или на обоих
полюсах клетки (лофотрихий), либо более-менее равномерно
распределены по всей её поверхности – перитрихиальное
расположение. Кишечная палочка, например, – типичный перитрихий.
Пили и фимбрии – это специфические бактериальные структуры в
виде полых трубочек, обеспечивающие прикрепление к субстрату, а
также ряд специальных функций. Например, при помощи так
называемых F-пилей происходят конъюгация (соединение) бактерий и
передача плазмид, кодирующих различные признаки. Так бактерии
обходят ограничения бесполого способа размножения, имитируя
обмен генами при половом размножении у эукариот (F – сокращение
от fertile, половой).
Определённые роды бактерий могут образовывать споры. Почти все
они – палочки (пока известен только один род спорообразующих
кокков, но для человека он не патогенен). В отличие от спор грибов
или низших растений (папоротников и т. п.), у бактерий они не
являются средством размножения. Бактериальные споры образуются
при неблагоприятных внешних условиях и служат целям выживания,
поскольку выдерживают значительные интервалы температуры, от
низких до очень высоких, длительное высушивание и другие
губительные для вегетативных форм бактерий факторы.
В этом смысле они больше напоминают цисты простейших, хотя
тоже есть принципиальное отличие – простейшие «закукливаются»
целиком, выделяя на поверхности клетки непроницаемую оболочку. А
бактерии формируют спору внутри себя и держат там, как кенгуру –
детёныша. По этой причине крупные споры могут раздувать
клеточную стенку бактерий с образованием характерных форм,
видимых в микроскопе как «барабанные палочки» или «теннисные
ракетки» (терминальное, то есть на конце клетки, расположение
крупной споры). Такие спорообразующие палочки называют
клостридиями (их типовой род – клостридии, но есть и другие с
похожим строением). Среди них есть немало патогенных для человека:
клостридия перфрингенс вызывает газовую гангрену, клостридия
тетани – столбняк, а клостридия ботулини – тяжёлую пищевую
интоксикацию ботулизм. Если же спора «вписывается в габариты»
клетки, не вызывая существенного изменения её формы, то это –
бацилла (типовой род – бациллы – тоже включает патогенные виды,
например, бациллюс антрацис, вызывающий сибирскую язву).
Другая бацилла – бациллюс турингиензис – интересна тем, что
выделяет протоксин, который в пищеварительном тракте ряда
насекомых – вредителей сельского хозяйства превращается в токсин,
вызывая их гибель. В то же время он не ядовит для позвоночных
(включая человека) и полезных насекомых вроде пчёл и шмелей. Это
позволяет использовать его для защиты растений. Кроме того,
поскольку протоксин имеет белковую природу, то удалось установить
кодирующий его ген и получить с его использованием генномодифицированные растения, устойчивые к вредителям за счёт
продукции бактериального токсина.
Споры бактерий – очень плотные образования с низким
содержанием воды и прочной оболочкой. Поэтому многие методы
окраски, направленные на их выявление, предполагают обработку
мазка растворами кислот. Например, окраска по Цилю-Нильсену или
по Ожешко.
Ещё одна структура, которая присутствует у бактерий и которую
можно наблюдать при соответствующей окраске – это капсула.
Капсула состоит из экзополисахаридов, то есть выделяемых наружу
(«экзос» – внешний) полимеров из молекул сахара. Поэтому, если
угодно, это «кисель», окружающий бактерию поверх клеточной
стенки.
Капсулообразование – видовой признак. Он часто является одним из
так называемых «факторов агрессии» бактерий, поскольку помогает
избегать связывания с антителами и фагоцитоза макрофагами
иммунной системы. Правда, капсула может быть непостоянным
признаком – при некоторых условиях среды она отсутствует, при
других синтезируется вновь.
Капсулу можно выявить специальными методами окраски.
Например, если аккуратно окрасить мазок тушью, то на чёрном фоне
будут видны светлые «дырки» капсулированных бактериальных
клеток, потому что зёрна туши не проникают в этот «кисель». Такой
метод называется окраской по Бурри-Гинсу.
Даже некоторые гранулы-включения в цитоплазме бактерий можно
выявить окраской специальными методами. Например, уже
упоминавшаяся нами дифтерийная палочка запасает в цитоплазме
соединения фосфора в виде гранул волютина. С этим веществом
взаимодействует уксуснокислая синяя краска, что используется при
окраске мазков по методу Нейссера. При нём сами палочки в мазке
будут видны жёлтыми или светло-коричневыми, а зёрна волютина,
обычно расположенные на их концах, – тёмно-синими до черноты.
Такая характерная «гантель» или «штанга» с тёмными «блинами»
указывает на наличие в мазке возбудителя дифтерии.
Как видите, почти все методы окраски имеют авторские названия –
из уважения к тем микробиологам, врачам и химикам, которые
помогли раскрыть многие тайны мира бактерий.
В заключение обзора строения бактерий хотелось бы упомянуть ещё
одно важное свойство бактериальных структур, которое будет очень
интересовать нас в дальнейшем. Молекулы ряда из них являются
антигенами – опознаются иммунной системой организма-хозяина как
чужеродные структуры. Так, липополисахарид грам-отрицательных
бактерий обозначается как соматический или О-антиген, капсулы
содержат молекулы К-антигена, а жгутики – Н-антигена (аш-антиген –
используются латинские буквы). Все они могут немного отличаться
свойствами, чем и обусловлено существование упомянутых в начале
главы сероваров бактерий. Кроме того, это свойство можно
использовать для серологической диагностики (основанной на
взаимодействии антигенов бактерий и содержащих специфические к
ним антитела диагностических сывороток) и идентификации
бактерий.
Глава 5. Что посеял, то и культура
Разбирая в прошлых главах морфологию и устройство бактерий, мы
выяснили, что на их основании уже можно многое сказать о
принадлежности микроорганизма к тому или иному виду
(идентифицировать
или,
на
профессиональном
жаргоне,
«расшифровать» его). Однако чаще всего одних этих данных
недостаточно.
В настоящее время идентификация бактерий в основном полагается
на физиологические и биохимические свойства. Для их изучения
проводится посев исследуемого биологического материала на
питательные среды.
Питательные – это значит, что они предоставляют бактериям место
для роста и вещества для питания. О питании бактерий мы говорили в
дополнительном материале по экологии микроорганизмов и сегодня
тоже будем неоднократно к нему возвращаться.
Одним из наиболее подходящих питательных веществ являются
белки: да, они дают выход энергии меньше по сравнению с жирами,
но столько же, сколько углеводы, и при этом прекрасно обеспечивают
пластический обмен (синтез собственных структур клетки). Это
справедливо как для людей (вспомните, как больных выкармливают
нежирным бульоном), так и для бактерий.
Поэтому распространённым видом питательных сред являются
бульоны. Например, мясопептонный бульон (МПБ) и пептонная вода
(вы же помните, что пептиды – это коротенькие «недобелки», чьи
цепочки состоят из малого количества аминокислотных остатков?).
Бульоны – это один из видов жидких питательных сред,
применяемых в бактериологии. Для использования их обычно
разливают в прозрачные стеклянные или пластиковые пробирки. Но не
всегда удобно использовать для культивирования бактерий жидкость.
Ведь характер роста в них у разных бактерий отличается: одни дают
хорошо заметный осадок на дне, другие растут по всему объёму, и
попробуй на глаз определи – это действительно лёгкое помутнение в
результате диффузного роста или показалось. Кроме того, в жидкой
среде относительно мало кислорода, и требовательные к нему
микробы могут расти только в поверхностной плёнке. Поэтому
помимо жидких используют плотные питательные среды. Если вы
немного разбираетесь в кулинарии, то хорошо знаете, как можно из
жидкости – сока, бульона – получить желе или холодец. Для этого
нужно добавить, например, белок желатин. Желатиновые среды
успешно используют в бактериологии и по характеру их разжижения
судят о росте микроорганизма. Другой вариант желирующего агента –
полисахариды. Крахмал, например, с которым готовят кисель.
Бактериологи тоже начинали с крахмала – ещё Роберт Кох изучал рост
бактерий на богатых крахмалом картофельных пластинках. Но в
настоящее время подавляющее большинство плотных питательных
сред готовят с применением другого полисахарида – получаемого из
морских водорослей агара.
Причём именно готовят – почти как на кухне. В своё время учёные
потратили много сил и времени на разработку подходящих
питательных сред, буквально по граммам подбирая сочетание веществ,
которое бы удовлетворило прихотливые вкусы тех или иных видов
бактерий. Это закрепилось в авторских названиях многих из них –
среда Эндо, агар Клиглера, агар Плоскирева, среда Олькеницкого,
среда Вильсона-Блера, агар Сабуро и т. д. Но благодаря их стараниям
сейчас процесс приготовления питательных сред не сильно отличается
от того, как вы варите магазинный кисель из пакетика или
быстрорастворимое пюре. Нужно просто высыпать в кипяток сухой
готовый стерильный порошок, который уже содержит нужный набор
белков, сахаров, солей и других веществ, варить по инструкции, затем
процедить и разлить для застывания по пробиркам или в специальные
плоские ёмкости для микробиологических посевов – чашки Петри.
Даже помещение для этих работ в микробиологической лаборатории
так и называется – средоварочная или «средоварка». Только, конечно,
все компоненты здесь отмеряют с высокой точностью, а не в духе «две
столовых ложки без верха», а к средоварочной предъявляются
повышенные требования чистоты – примерно как к процедурному
кабинету. Чтобы облегчить процесс, иногда используют фабрично
изготовленные стерилизованные чашки Петри с уже готовой разлитой
средой – после культивирования и учёта результатов их просто
обеззараживают и утилизируют.
Кроме плотных и жидких питательных сред, иногда применяют
полужидкие – содержание агара в них таково, что среда не застывает
окончательно, а приобретает консистенцию крепкого киселя. Их
используют, например, для определения подвижности бактерий.
Мы уже сказали, что на жидких питательных средах разные виды
микроорганизмов могут расти по-разному: одни только в
поверхностной плёнке, другие выпадают на дно, третьи
распределяются по всему объёму. Ещё интереснее наблюдать рост
колоний бактерий на плотных питательных средах. Обычно колонии
бактерий округлые, диаметром от полумиллиметра до нескольких
миллиметров. Они могут быть полупрозрачными, белесоватыми,
окрашенными в цвет среды или продуцировать пигменты. А ещё
некоторые бактерии пахнут! Не всегда приятно, но бывают
удивительные исключения: возбудитель гнойных осложнений в
хирургических ранах – бактерия синегнойная палочка, выращенная в
чистой культуре, пахнет земляничным мылом! Форма колоний тоже
может быть необычной, отличаться от привычной круглой. Для их
описания бактериологи придумали множество образных поэтических
названий: форма цветка маргаритки, форма львиной гривы, колонии
типа «яичница-глазунья» и т. п. Ведь раньше у учёных не было
телефонов с фотоаппаратами, чтобы быстро показать коллегам, что
они увидели в посеве, и приходилось всё описывать словами, в
лучшем случае – делать рисунки.
Вся совокупность признаков, которыми характеризуется рост
бактерий на питательных средах (размер, форма, цвет, запах колоний,
изменение среды вокруг них и т. п.), называется культуральными
свойствами.
Каждая колония на питательной среде вырастает из одной
материнской клетки. Если очень тщательно отмерить исходное
количество биологического материала для посева, то, подсчитав затем
число колоний на чашке и решив несложную пропорцию, можно
сказать, сколько колоний содержится в одном грамме или одном
миллилитре исходного биологического материала. Такой метод учёта
результатов называется количественным и выражается в
колониеобразующих единицах (КОЕ/г, КОЕ/мл). Ведь нормальное
содержание бактерий разных видов, например, в кишечном
содержимом известно. Если одних вдруг стало меньше или они
исчезли, уступив место другим, можно говорить о дисбактериозе.
Но прежде чем начать «считать бактерии по головам», нам ещё
нужно «узнать их в лицо». Ведь не все из них дают характерный рост
на обычных средах, а некоторые привереды и вовсе не желают расти
на простых (универсальных) питательных средах вроде МПА, или их
в посеве забивают другие виды. Вот как раз тут учёные и практические
микробиологи вовсю начинают пользоваться изученными ранее
биохимическими
свойствами бактерий,
подбирая нужные
питательные среды для выделения именно тех видов, которые
наиболее интересуют в рамках конкретной диагностической ситуации.
Например, чтобы ингибировать рост посторонней микрофлоры,
которая станет мешать проведению исследования, в питательные
среды добавляют антибиотики и другие специальные вещества.
Например, желточно-солевой агар (среда ЖСА) имеет высокое
содержание соли, что крайне осложняет жизнь многим
микроорганизмам, но вот стафилококки на нём прекрасно растут.
Среда Эндо приготовлена так, чтобы, наоборот, ингибировать рост
грам«+» флоры, тех же кокков, для лучшего выделения
энтеробактерий. Такие среды называют селективными (селекция –
отбор).
В качестве удобного источника энергии бактерии, как и мы, с
удовольствием используют простые сахара. Представители обширного
семейства энтеробактерий, куда входит уже известная вам кишечная
палочка,
в
большинстве
своём
являются
нормальными
представителями кишечной микрофлоры, что отражено в их названии
(«энтерон» – кишечник). И почти все могут окислять как глюкозу, так
и лактозу (молочный сахар), образующиеся при гидролизе пищевых
сахаров. Но вот большинство патогенов из этого семейства лактозу «не
переваривает». Поэтому, если в скошенный в пробирке столбик агара
добавить глюкозо-лактозную смесь и провести посев изучаемой
культуры бактерий уколом в среду и одновременно по скошенной
поверхности среды (анаэробные и аэробные условия), то растущие
добропорядочные энтеробактерии «съедят» весь доступный сахар –
исходно малиново-красная среда в пробирке закислится продуктами
реакции, и содержащийся в ней пигмент-индикатор сменит окраску на
жёлтую. Но если в первичном посеве были возбудители кишечных
инфекций – сальмонеллы или шигеллы, не окисляющие лактозу, – то
оставшиеся
ярко-красными
«язычки»
скошенной
среды
просигнализируют бактериологу: «Внимание! Опасность!»
Такого рода питательные среды, помогающие отличать одни
бактерии от других, называют дифференциально-диагностическими.
Одновременно они могут быть и селективными по отношению к
определённым группам бактерий – такие среды называют
комбинированными. Не всегда они основаны только на
биохимическом отношении к углеводам: например, висмутсульфитный агар (среда ВСА) и ксилозо-лизин-дезоксихолатный агар
(вместо этого непроизносимого названия все пользуются торговым
наименованием XLD-агар) выявляют способность сальмонелл
продуцировать сероводород. Реагируя с компонентами этих сред, он
окрашивает колонии сальмонелл в чёрный цвет. Правда, сероводород
ещё выделяют бактерии рода протей. И их приходится
дифференцировать от сальмонелл другими тестами. Если же от
бактериолога требуется не просто отличить протей от сальмонеллы, а
сказать: это Proteus vulgaris или, скажем, Proteus mirabilis, то нужно
будет провести ряд дополнительных биохимических тестов.
Поскольку, как вы уже поняли, для лёгкого выявления биохимических
реакций используют цветные индикаторы, то ряд пробирок с
результатами этих тестов бактериологи называют «пёстрым рядом».
Более современные варианты метода предполагают использование
вместо пробирок с растворами специальных полимерных пластин с
лунками или бумажных полосок, на которые уже нанесены
отмеренные количества субстрата и требуется только добавить
бактериальную взвесь. Такие методы уже можно автоматизировать и
реализовать в виде «умного» аппарата – бактериологического
анализатора.
Есть ещё специальные среды, используемые при проведении
определённых видов исследований: например, агар ГивенталяВедьминой (среда АГВ) и Мюллера-Хинтон агар (МХА) используют
для определения чувствительности бактерий к антибиотикам дискодиффузионным методом.
В конечном итоге все направлено на то, чтобы, используя те или
иные наборы биохимических тестов и ключи для их расшифровки, с
уверенностью сказать – какую бактерию мы выделили из
клинического материала.
Однако если на ваших чашках Петри вовсе ничего не выросло, то
это ещё не значит, что в исследуемом материале не было бактерий.
Ведь пока мы дали им только кров и пищу (да и то в надежде, что
угадали их аппетиты). Да, посев будет инкубироваться 18—24 часа (а
иногда и больше) в термостате при температуре 370 Цельсия.
Большинству бактерий очень нравится температура человеческого
тела, хотя есть и такие, которым нужны 25 или 48 градусов. Но что
если бактериям не нравится… воздух?
Говоря об экологии микроорганизмов, мы уже упоминали, что ряд из
них не выживает в присутствии кислорода воздуха – это так
называемые облигатные анаэробы. Другие приспособились к смене
атмосферы – факультативно-анаэробные бактерии. В рамках
последней группы есть такие представители, которым кислород всётаки нужен, но в очень небольшой концентрации – микроаэрофилы, а
есть те, кому вынь да положь повышенное содержание углекислого
газа (капнофилы). В общем, бактерии те ещё привереды. И для
культивирования анаэробов бактериологам приходится прибегать к
самым разным ухищрениям. Иногда достаточно жидких сред, которые
и так плохо насыщаются кислородом, а если ещё добавить туда
подходящий пористый материал, поглощающий газы – например,
кусочки говяжьей печени, – то вполне можно растить некоторые
анаэробные бактерии. Описанным образом работает среда КиттаТароцци для культивирования возбудителя газовой гангрены и других
клостридий. Но чаще приходится использовать специальные
герметичные сосуды – эксикаторы и анаэростаты – где бескислородная
среда создаётся за счёт горящей свечи или в ходе химической реакции
карбонатов с сильной кислотой. Хотя наиболее удобным и
современным способом является использование газогенерирующих
пакетов «Газпак», которые за счёт всё тех же химических реакций
создают в герметичном объёме анаэростата атмосферу требуемого
химического состава.
Всё, о чём мы говорили выше, относилось к бактериям. Однако
похожие принципы можно использовать и для культивирования
грибов (но не груздей, естественно, а микроскопических: плесени
порой и так прорастают на чашках с бактериальными посевами, мешая
исследованию). Вирусы на питательных средах не растут, поскольку не
могут жить самостоятельно, но их можно вырастить на подходящей
культуре клеток (а бактериофаги – на бактериальном мате, хотя это
тоже своего рода культура клеток, только бактериальных). Однако есть
такие бактерии, которые либо совсем не растут на питательных средах
(в прошлой главе мы упоминали микоплазмы и риккетсии), либо
растут очень плохо и очень медленно (туберкулёзная микобактерия,
бактерия-возбудитель
лепры
и
другие).
Их
приходится
диагностировать либо по микроскопии образцов, либо определяя
реакцию на них иммунной системы (серодиагностка), либо призывая
на помощь учёных из других областей. Например, союз
микробиологов и физиков дал в руки первых не только электронный
микроскоп, но и масс-спектрометр – аппарат, позволяющий
определить химический состав образца по спектру излучения
входящих в него атомов.
Может быть, вся эта «кухня» покажется вам сложной, но примеры
этапов бактериологического исследования приведены здесь для того,
чтобы дать вам понимание общей сути и логики процесса. С
конкретными нюансами вы познакомитесь, если решите посвятить
себя миру микробов и придёте работать в микробиологическую
лабораторию. Сейчас мы скажем несколько слов о том, какие они
бывают и как устроены.
5.1. Организация микробиологической
лабораторной службы
В нашей стране гражданские микробиологические лаборатории в
основном входят в структуры здравоохранения, санитарноэпидемиологического надзора, научных и научно-образовательных
организаций (НИИ, ВУЗов и др.) или являются ведомственными
(специализированные лаборатории, выполняющие контрольные
исследования на водопроводных станциях, предприятиях пищевой
промышленности,
биотехнологических
и
фармацевтических
производствах). Для простоты дальше в тексте мы будем называть их
просто «лабораториями».
Лаборатории, действующие в интересах лечебных учреждений
(больниц, поликлиник), могут быть очень небольшими, работающими
на какую-то определённую медицинскую организацию. Иногда это
просто
специализированный
отдел
клинико-диагностической
лаборатории. Но бывает и наоборот – для всех больниц одного города,
скажем, строят одну централизованную лабораторию. Каждый вариант
имеет свои плюсы и минусы. В первом случае короче время получения
результата и лучше клиническое взаимодействие лечащего врача с
микробиологом, проще доставка биоматериала. Это важно для
стационаров, оказывающих экстренную помощь, отделений
реанимации и интенсивной терапии. Во втором – меньше затраты
труда и материалов на одно исследование, удобнее интерпретировать
результаты «в динамике» (анализы одного пациента, сделанные в
разное время), так как они будут выполнены на одном оборудовании, в
одной и той же размерности, а зачастую и одними и теми же
специалистами.
В любом случае основными задачами микробиологических
лабораторий лечебных организаций являются подтверждение/
опровержение инфекционного характера заболевания, диагностика
возбудителя (установление этиологии инфекции), подбор наиболее
эффективных в его отношении лечебных препаратов (установление
спектра чувствительности бактерий к антибиотикам, фагам и
прочее).
Микробиологические
лаборатории
Центров
гигиены
и
эпидемиологии заняты несколько иными задачами, которые в общем
можно назвать профилактическими. Они ведут мониторинг
циркуляции возбудителей инфекции в природе и среди людей,
оценивают коллективный иммунитет, расследуют вспышки пищевых
отравлений, определяют с санитарно-микробиологических позиций
доброкачественность воды, воздуха, пищевых продуктов. То есть в
рамках своей специфики заняты тем, что называется поддержанием
санитарно-эпидемиологического благополучия населения.
Разделение обязанностей между разными лабораториями не всегда
бывает таким строгим. Так, микробиологи больниц тоже выполняют
немало анализов с профилактической целью. Например, чтобы не
пропустить занос инфекции в стационар, когда она ещё в
инкубационном периоде, и у больного нет симптомов. Или в рамках
разного рода профилактических осмотров. На базе хорошо
оснащённых лабораторий крупных клиник могут выполняться
исследования, имеющие научное значение. В то же время лаборатории
научно-исследовательских институтов помогают медикам и
санитарным врачам делать сложные или редкие анализы.
Принципиальные различия между лабораториями, требования к их
оснащению и квалификации кадров определяются не ведомственными
различиями, а тем, с какими микроорганизмами они работают. Потому
что при диагностике банального гриппа, раневой микрофлоры и,
скажем, чумы подходы к выполнению работ во всех трёх случаях будут
совершенно разными, потому что искать микробиологи будут или
вирус, или бактерии и грибы (и да, не анализ показывает искомое, а
исследователю сначала нужно предположить, что он может найти, и
подтвердить это анализом… или опровергнуть).
А в случае с чумой (или высоковирулентными штаммами гриппа)
ещё нужно уделить особое внимание безопасности. Поэтому и в
отечественной классификации, и в понимании Всемирной организации
здравоохранения
(ВОЗ)
все
микроорганизмы,
вызывающие
заболевания у человека (патогенные для него), делятся на 4 группы в
зависимости от степени их опасности. А сама эта степень
определяется сочетанием двух свойств: насколько тяжёлые инфекции
микроб вызывает (насколько он опасен для конкретного больного –
«индивидуальная опасность») и насколько он склонен к
распространению среди неиммунных к нему людей («общественная
опасность»).
В классификации ВОЗ это называется «группами риска», и условно
можно сказать, что представители 1-й группы вызывают лёгкие
инфекции и не дают вспышек, а уж эпидемию точно вызвать не в
состоянии. В то время как микробы из 4-й группы легко выходят из
под контроля вследствие своей высокой вирулентности, и способны
убить значительное количество заразившихся.
В нашей стране нумерация групп (у нас они уже называются
«группами патогенности») обратная: самая опасная – 1-я, наименее
опасные микробы – в 4-й группе. Кроме того, несколько отличается
сам подход в отнесении патогенных биологических агентов (ПБА) к
той или иной группе патогенности. Мы под ПБА понимаем не только
самих микробов, но и выделяемые ими токсины, а также другие яды
биологического происхождения и паразитических многоклеточных
(клещей, гельминтов и т. п.):
1-я группа патогенности – возбудители чумы, лихорадки Марбург,
лихорадки Эбола;
2-я группа патогенности – ботулотоксин, столбнячный токсин,
возбудители
сибирской
язвы,
холеры,
конго-крымской
геморрагической лихорадки, ВИЧ, вирусы-возбудители гепатитов В, С
(однако для ВИЧ и вирусов парентеральных гепатитов есть оговорка,
что диагностировать эти инфекции можно и в лабораториях 3—4
групп патогенности, если при этом не происходит накопление
возбудителя);
3-я группа патогенности – возбудители гриппа, коклюша,
туберкулёза, токсины плесневых грибов (микотоксины);
4-я группа патогенности – вирусы-возбудители ОРВИ (аденовирусы,
риновирусы), золотистый стафилококк.
Микробиологические лаборатории всех ведомств Российской
Федерации лицензируют на работы либо с первой-второй группами
патогенности, либо с третьей-четвёртой. Первые обычно называют
«лабораториями особо опасных инфекций» – они оснащены
специальными боксами биологической безопасности, системами
очистки воздуха, обеззараживания сточных вод. А персонал здесь
работает в защитных комбинезонах и дышит через специальные
респираторы с высокой степенью защиты. А с особо заразными
(высококонтагиозными) возбудителями – в специальных костюмахскафандрах, куда воздух подаётся не только для дыхания, но и
надувает сам костюм, чтобы при его повреждении не произошёл
подсос инфекционного аэрозоля внутрь – к телу и органам дыхания
сотрудника.
Во втором типе лабораторий всё намного проще, но и здесь
существуют специальные меры безопасности, средства защиты и
осуществляется контроль безопасности работы, чтобы болезнетворные
культуры не могли попасть за пределы лаборатории даже случайно.
Глава 6. Руки! Мыл?! (про
бактериальные кишечные инфекции)
Большинство энтеробактерий обитает в кишечнике человека и
других животных, являясь комменсалами или мутуалистами, однако
некоторые их штаммы могут приводить к развитию инфекции. То есть
это условно-патогенные бактерии. Однако среди энтеробактерий есть и
типично патогенные роды, например, шигеллы (возбудители
бактериальной
дизентерии)
и
сальмонеллы
(возбудители
сальмонеллёзов, в том числе брюшного тифа и паратифов). Ранее в это
же семейство входил также род иерсиний, включавший не только
возбудителя чумы – бактерию иерсиния пестис, – но и ещё как
минимум пару возбудителей кишечных инфекций (иерсинию
псевдотуберкулёзис и иерсинию энтероколитика). Однако с 2016 года
он выделен в самостоятельное семейство.
Необычные названия родов и видов часто являются производными
от фамилии учёного, открывшего данные бактерии или внесшего
большой вклад в их изучение. Например, эшерихии – по фамилии
Теодора Эшериха, описавшего их в 1885 году, иерсинии названы в
честь Александра Иерсена, открывшего в 1894 году «чумную
палочку», а шигеллы – в честь открывшего возбудитель дизентерии в
1897 году японского врача Киёси Шига. В России шигеллу дизентериа
называют ещё палочкой Григорьева-Шиги, поскольку отечественный
микробиолог и судебный врач Алексей Григорьев на 6 лет раньше
Шиги высказал предположение об этиологической роли (то есть что
именно они и есть возбудитель) палочковидных бактерий,
обнаруженных им в трупах погибших от дизентерии людей.
Поскольку основной локализацией энтеробактерий является
кишечник,
то,
согласно
общим
принципам
реализации
эпидемического процесса, механизм передачи вызываемых ими
инфекций – фекально-оральный. В рамках него бактерии могут
передаваться любым из трёх возможных путей или предпочтительно
выбирать один преимущественный: например, шигелла дизентерия
предпочитает контактно-бытовой путь, шигелла Зонне – пищевой
(особенно с молочными продуктами), шигелла Флекснера – водный.
Хотя это и не мешает, скажем, флекснер-дизентерии передаться через
контаминированные продукты или грязные руки – всё зависит от
конкретных обстоятельств.
Клинически проявляющиеся формы энтеробактериальной инфекции
– это энтериты и гастроэнтериты (инфекционно-воспалительные
заболевания тонкого кишечника или желудка и тонкого кишечника
одновременно), вызванные нарушением пищеварения под действием
бактериальных токсинов. Однако есть исключения – шигеллёзная
дизентерия, например, характеризуется геморрагическим колитом.
Это воспаление нижних отделов толстого кишечника, когда бактерия
напрямую поражает клетки кишечной стенки, вызывая образование на
ней кровоточащих язв.
Как правило, такие инфекции имеют небольшой (от суток до
нескольких дней) инкубационный период и проявляются остро.
Поэтому их объединяют под аббревиатурой ОКИ (острые кишечные
инфекции). Тем не менее, те же шигеллы и сальмонеллы могут
длительно выделяться с калом после клинического излечения, что
рассматривается как носительство или хроническая инфекция.
Брюшнотифозная сальмонелла (Salmonella typhi) размножается в
лимфоидной ткани пейеровых бляшек и забрюшинных лимфоузлов
(это органы иммунной системы, о которых вы можете прочесть в
соответствующем разделе этой книги), вызывая их воспаление и
иногда прорыв гнойных масс в брюшную полость или просвет
кишечника. Это чревато потенциально смертельными осложнениями в
виде перфорации (разрыва) кишечника, кровотечения в брюшную
полость и перитонита (воспаление выстилающей изнутри брюшную
полость слизистой оболочки). Кроме того, при брюшном тифе сильное
воспаление бактериальной природы, вкупе с продуцируемыми
сальмонеллой токсинами, приводит к развитию сильнейшей лихорадки
(температура тела достигает 40—42 градусов Цельсия) и
интоксикации. В результате у тифозных больных нарушается сознание,
они могут бредить, галлюцинировать – отсюда и происходит название
болезни («тиф» по-гречески – туман, бред).
Помимо видовых характеристик, зачастую в задачи бактериолога
входит выяснение антигенных и других свойств конкретного штамма,
выделенного от пациента. Помните, мы говорили о строении бактерий:
что у всех них за рядом исключений (куда же без них в медицине) есть
клеточная стенка, что некоторые из них подвижны за счёт жгутиков, а
иные могут окружать себя полисахаридной капсулой? Так вот,
биомолекулы, входящие в состав этих образований, опознаются
иммунитетом как чужеродные – то есть они антигены. И мы тоже
можем их определять специальными методами иммунных реакций.
Например, сальмонеллы отличаются по строению О-антигена
клеточной стенки, но в пределах одного штамма все О-антигены
одинаковы. Значит, зная серовар (все бактерии, одинаковые по какомулибо антигену), выделенный от пострадавших из-за вспышки
кишечной инфекции, можно обследовать подозрительные пищевые
продукты и сотрудников предприятий, которых их производили,
упаковывали, доставляли. Обнаружение в продукте и у
сотрудников-«пищевиков» такого же серовара будет прямо указывать
на связь заражения с конкретным источником, что используется при
расшифровке вспышек кишечных инфекций.
К сожалению, в полном виде бактериологический метод занимает
достаточно много времени. Ведь он включает 3—4 этапа, большинство
которых сопровождается длительной (18—24 часа) инкубацией
бактериальных посевов (пересевов или «пассажей»). Поэтому при
необходимости быстрой первичной идентификации возбудителя у
пациентов с тяжёлой, в том числе жизнеугрожающей инфекцией
бактериологический метод дополняют экспресс-диагностикой:
агглютинацией чистой культуры из первичного посева, реакцией
пассивной гемагглютинации с сывороткой крови больного (при
подозрении на брюшной тиф) и другими. Либо используют
ускоренные аппаратные методы диагностики с применением
бактериологических анализаторов.
Глава 7. Эти необычные микобактерии
(про туберкулёз и не только)
Классический бактериологический метод с выделением возбудителя
на питательной среде не всегда удобен ещё и тем, что, помимо
временных затрат, бактериологи сталкиваются и с другими
трудностями. Далеко не все бактерии удаётся культивировать на
питательных средах. Одни очень требовательны к их составу
(прихотливые бактерии), как, например, гемофильные палочки или
возбудитель коклюша. Другие просто утратили в процессе эволюции
способность к свободному образу жизни и полностью перешли к
паразитированию на живых клетках, как группа тенерикут, а значит,
вообще не будут расти на питательных средах, как не растут на них,
скажем, вирусы. Третьи, такие как микобактерии, хоть и растут, но
крайне медленно – пока на плотных питательных средах можно будет
различить рост колоний, пройдёт больше 10 дней, а то и месяц.
Поэтому микобактерии хоть и исследуют бактериологическим методом
для окончательного подтверждения диагноза, но изначально ищут
другими способами – например, при помощи микроскопии.
Микобактерии – это семейство бактерий, включающее 74 вида.
Среди них есть и свободноживущие (сапрофитные), и паразитические
(условно-патогенные и патогенные) виды. Последние вызывают у
человека туберкулёз и лепру.
Оба возбудителя вызывают специфическое – гранулематозное, с
образованием бугорков и уплотнений – воспаление. Но туберкулёз
наиболее часто распространяется воздушно-капельным путём, и
туберкулёзные бугорки поэтому появляются в лёгких. Пути передачи
лепры и сейчас ещё не до конца понятны, но считается, что для
заражения необходим тесный контакт с заражённым. Лепроматозные
узелки образуются вначале на коже, непоправимо уродуя внешность
больного, из чего происходит русское название этой инфекции –
«проказа». А слово «прокажённый» и до сих пор является синонимом
человека, который отвержен обществом из-за каких-то безобразных
качеств личности или совершения отвратительного поступка.
Хотя лепра описана ещё в библейском Ветхом Завете, однако
наибольшее распространение она получила в средневековой Европе
(при том, что в Новом Свете и на островах Тихого Океана такой
болезни не существовало до открытия их европейцами). Реальных
прокажённых действительно изгоняли из общества, ссылая на
изолированные острова или в другие труднодоступные местности,
заключая в закрытые «лепрозории». Это было обусловлено не только
страхом заражения, но и бытовавшими в то время антинаучными
взглядами на природу инфекций, которые считались «печатью за
грехи». Хотя в исключительных случаях это не мешало некоторым
больным лепрой занимать высокое место в обществе: если вы
смотрели фильм «Царствие небесное» о временах крестовых походов,
то там король Иерусалима Балдуин IV (реальный исторический
персонаж) изображён постоянно носящим серебряную маску – именно
из-за кожных проявлений лепры, которой страдал.
Микобактерии отличаются очень высокой устойчивостью в
окружающей среде, уступающей разве что бактериальным и
грибковым спорам. Это представляет определённую проблему при
организации профилактики, лечения и дезинфекции в очагах
туберкулёза и других микобактериозов.
И с этим связано бытовавшее ранее заблуждение относительно
возбудителя туберкулёза о том, что такая устойчивость обусловлена
образованием спор. Поэтому считали, что он относится к группе
бацилл (про них, наряду с клостридиями, мы говорили в главе о
строении бактерий). В действительности микобактерии спор и капсул
не образуют, их устойчивость обусловлена содержащимися в составе
клеточной стенки необычными компонентами: воском и миколовыми
кислотами.
Однако возбудитель туберкулёза по-прежнему частенько называют
бациллой, и это даже закрепилось в профессиональном сленге
фтизиатров: больного туберкулёзом, выделяющего микобактерии с
мокротой, называют бациллярным или бациловыделителем.
Хотя формально микобактерии являются грам-положительными,
окрасить их по Граму сложно – из-за своих необычных компонентов
микобактериальная клеточная стенка не воспринимает окраску по
Граму, словно если бы вы пытались красить водорастворимой краской
кусочек масла. Поэтому их окрашивают по методу Циля-Нильсена,
сначала нанося на мазок мокроты красный раствор фуксина в феноле, а
затем нагревая полученный препарат в пламени горелки или
спиртовки, чтобы разрыхлить клеточную стенку. Окрашенный мазок
обесцвечивают спиртом или органической кислотой. Обычные
бактерии под действием таких агрессивных растворителей легко
отмываются от остатков краски, но возбудитель туберкулёза за счёт
своей особо прочной клеточной стенки удерживает в ней часть
красителя. При микроскопировании он будет виден как тонкие, чуть
изогнутые палочки красного или ярко-розового цвета. За свою форму,
а также потому, что был открыт Робертом Кохом (в 1882 г.), он получил
название «палочка Коха».
В клинической практике, чтобы не путать, особенно средний и
младший медперсонал, иностранными фамилиями, окраску мокроты
по методу Циля-Нильсена при подозрении на туберкулёз обычно
называют просто «анализом на КУМ» – кислотоустойчивые
микобактерии. А положительный результат анализа выражают как
«БК+» – бацилла (опять бацилла!) Коха плюс.
В действительности под словом «палочка Коха» понимается не один
вид – микобактерия туберкулёзис, – а целый ряд близкородственных
видов микобактерий. Туберкулёзная микобактерия вызывает
заболевание в основном только у человека, микобактерия бовис – у
человека и крупного рогатого скота (туберкулёз «бычьего типа»). Есть
ещё микобактерии африканум, микроти и другие. Но всё-таки при
заражении от человека к человеку основную роль играет
M.tuberculosis. А микобактерия авиум и вовсе вызывает туберкулёз
только у лиц со СПИДом и другими иммунодефицитами. Расшифровка
возбудителя до вида в данном случае имеет значение скорее для
установления источника, а также потому, что разные виды имеют
разные спектры устойчивости в лекарственным препаратам.
Путь передачи туберкулёзных микобактерий воздушно-капельный.
Несмотря на свою «бронированную» клеточную стенку, они не могут
слишком длительно выживать в окружающей среде, особенно если
частички инфицированной мокроты быстро высыхают под влиянием
тока воздуха и/или прямых солнечных лучей. А вот неинсолируемые
(лишённые солнечного света), плохо проветриваемые помещения с
большой скученностью людей – это, наоборот, идеальные условия для
распространения туберкулёза. Если ещё и люди имеют какие-то
проблемы со здоровьем или испытывают стресс и не получают
достаточного питания, то туберкулёз может косить их пачками. Из-за
таких особенностей туберкулёз может распространяться в лагерях
беженцев, поселениях мигрантов или «бомжатниках». А в период так
называемой промышленной революции, когда очень много народу
переселялось в города, и неквалифицированные работники часто
вынуждены были ютиться в убогих ночлежках, туберкулёз имел
просто эпидемическое распространение.
Что даже нашло отражение в культуре: действующие лица многих
английских романов страдают и умирают от туберкулёза, так же,
как и героиня итальянской оперы «Травиата»; у М. Горького
персонажи с туберкулёзом встречаются в романе «Юность» и пьесе
«На дне», а из более современных произведений можно вспомнить
аниме Х. Миадзаки «Ветер крепчает», где от этой инфекции умирает
невеста главного героя.
Основным поражаемым органом являются лёгкие, могут быть
поражены лимфоузлы средостения (внутригрудные лимфоузлы). Хотя
встречается и туберкулёз внелёгочной локализации – почек, костей и
др. Как правило, он связан с гематогенным диссеминированием
микобактерий (то есть распространением по току крови) из
первичного очага поражения, но туберкулёз кишечника может
возникнуть и вследствие заражения микобактериями бычьего типа
пищевым путём при употреблении молока больных животных.
Проникновение возбудителя туберкулёза в организм не всегда (даже
скорее наоборот – редко когда) приводит к развитию заболевания.
Сначала происходит лишь тубинфицирование. Помните, мы
говорили, что первыми в дело борьбы с инфекциями (особенно
бактериальными) вступают клетки неспецифического иммунитета:
макрофаги и нейтрофилы? Так вот, благодаря всё тем же
особенностям строения своей клеточной стенки микобактерии
обладают свойством сопротивляться макрофагам лёгких, которые
пытаются уничтожить их в месте проникновения. Даже будучи
поглощёнными, микобактерии выживают внутри макрофагов – это
называется незавершённый фагоцитоз. «Проглотив», словно удав, с
десяток микобактерий и будучи не в состоянии их переварить,
макрофаг гибнет, выбрасывая при этом большое количество
медиаторов воспаления. Те привлекают в первичный очаг ещё
больше иммунных клеток. Но, поскольку макрофаги не могут
справиться с возбудителем и гибнут, то основную роль в сдерживании
патогена играют нейтрофилы (полиморфноядерные лейкоциты),
которые плотно набиваются со всех сторон вокруг места
проникновения микобактерий. Вал нейтрофилов отгораживает,
изолирует первичный очаг от остального организма.
В это время иммунитет не оставляет попыток подавить патоген (как
и микобактерии – вырваться из окружения). Для этого макрофаги в
очаге настолько интенсивно пролиферируют (делятся), что в какой-то
момент перестают успевать расходиться на отдельные клетки и
начинают напоминать «сиамских близнецов», а со временем и вовсе
превращаются в гигантские многоядерные клетки (симпласты). На
этом этапе они отдают команду находящимся вокруг очага клеткам
соединительной ткани начать размножаться и продуцировать прочный
белок коллаген. Подобный процесс всегда происходит, когда
макрофаги сталкиваются с чем-то, что не могут полностью расщепить
и эвакуировать из тканей – инородными частицами вроде сажи из
сигаретного дыма или загрязнённого воздуха, микробами, которые не
удаётся фагоцитировать и т. п. За счёт этого достигается изоляция
попавшего внутрь или образовавшегося внутри организма инородного
тела, которое невозможно удалить – наш организм словно хоронит
чужое внутри себя, поместив в надёжный саркофаг.
Проросший соединительной тканью (склерозированный) очаг из
переродившихся макрофагов, периферического вала нейтрофилов и
«захороненных» в центре микобактерий настолько плотный, что при
патологоанатомическом исследовании напоминает мелкую опухоль и
прощупывается как узелок или бугорок в тканях лёгкого. От
латинского слова «туберкулум» (бугорок) и происходит название
болезни. При микроскопировании разреза такого очага в нём видна
зернистость от многоядерных клеток, поэтому он также получил
название гранулёмы («гранула» – зерно, суффикс -ома/-ёма указывает
на
опухолевидный
характер
образования).
Словосочетание
«туберкулёзная гранулёма» часто в литературе и практике сокращается
до «туберкулома».
Ещё в середине XIX века эти «гигантские клетки» в лёгких больных
туберкулёзом описал известный русский хирург и учёный Николай
Иванович Пирогов. Однако широкой известности этих работ
помешала занятость Пирогова в качестве оперирующего хирурга и
одновременно организатора здравоохранения на Крымской войне 1853
—1856 гг., а также негативное отношение ко всему русскому в тот
период в европейских странах (против Российской империи воевала
коалиция из Британской, Французской и Османской (будущая Турция)
империй). Поэтому спустя полтора десятка лет немецкий
патологоанатом Теодор Лангханс (Лангганс), не зная о работах Н. И.
Пирогова, заново описал патоморфологию туберкулёзной гранулёмы.
На Западе гигантские многоядерные клетки туберкулёзной гранулёмы
до сих пор называют клетками Лангханса, а у нас, по
справедливости, – клетками Пирогова-Лангханса.
Помимо
механизмов
неспецифического
иммунитета,
при
туберкулёзе задействуется и адаптивный иммунитет – как клеточное
звено с активацией Т-хэлперов и цитотоксических лимфоцитов, так и
гуморальное, с образованием молекул антител В-лимфоцитами.
Система
комплемента
участвует
в
противотуберкулёзном
иммунитете как по альтернативному пути активации (без участия
антител), так и по классическому, антителозависимому. Однако здесь
есть некоторые нюансы: во-первых, микобактерии способны выживать
внутри как макрофагов, так и дендритных клеток. В результате чего
последние – эти «разведчики иммунитета» – зачастую сами приводят
«врага» в лице микобактерий в лимфоузлы. Так происходит
лимфогенная диссеминация туберкулёзного возбудителя. Во-вторых,
запертые в гранулёмах и внутри макрофагов микобактерии почти
недоступны для воздействия антител. Таким образом, иммунный
ответ при туберкулёзе существенно отличается от обычного
антибактериального иммунного ответа.
Пользуясь военными аналогиями, можно сказать, что обычный
ответ антибактериального иммунитета напоминает оборону
против наступающей армии микробов – с артиллерийскими ударами
антител, танковыми контратаками макрофагов и авианалётами
нейтрофилов. Микобактерии в этом смысле напоминают
диверсантов,
неожиданно
высадившихся
прямо
в
окопы
обороняющегося иммунитета, клеткам которого приходится биться
против них врукопашную.
Фактически можно сказать, что иммунитет при микобактериозах,
включая туберкулёз, не может полностью подавить возбудитель,
балансируя на грани его сдерживания в очаге проникновения. Поэтому
такой иммунитет называют нестерильным.
Логичным следствием из этого является тот факт, что против
туберкулёза невозможно создать инактивированную (убитую) вакцину
классическими способами. И единственными существующими сейчас
вакцинами против туберкулёза являются живые вакцины на основе
ослабленных микобактерий бычьего типа (микобактерия бовис) –
БЦЖ и БЦЖ-М (последняя содержит уменьшенную дозировку
микробов). БЦЖ – это русифицированная аббревиатура BCG – bacillus
Calmette-Guerin (бацилла Кальмета и Герена). Здесь фигурируют опять
же ошибочное причисление микобактерии к бациллам и упоминание
авторов вакцины – французских учёных Альберта Кальмета и Камиля
Герена.
Важным следствием активации иммунитета в ответ на
проникновение
микобактерий
туберкулёза
в
организм
(тубинфицирование) является формирование так называемой
гиперчувствительности замедленного типа (ГЗТ). Немедленный
тип гиперчувствительности – это аллергия, о ней мы упоминали в
главе про иммунную систему. ГЗТ, как и аллергия, формируется в
ответ на повторное внедрение возбудителя или введение отдельных его
антигенов. Поэтому вакцину БЦЖ (равно и БЦЖ-М) нельзя вводить
тубинфицированным лицам!
Как же определить факт тубинфицирования, если клинически оно
никак не проявляется, а лёгкие у живого человека на предмет
туберкулом не прощупаешь? Для этого используются кожноаллергические пробы с туберкулином, а само обследование называют
туберкулинодиагностикой.
Туберкулин представляет собой очищенную смесь белков,
выделенных из убитых культур микобактерий трёх видов:
туберкулёзис (человеческого типа), бовис (бычьего типа) и авиум
(ранее – птичий тип). Пробу с туберкулином, используемую для
массовой туберкулинодиагностики у детей, упорно называют пробой
Манту, хотя это не совсем верно. Проба Манту может проводиться с
разным количеством туберкулина, в то время как у детей используют
строго 2 туберкулиновые единицы препарата ППД-Л (этого всего лишь
12 стомиллионных долей грамма!).
Вообще туберкулин впервые получил Роберт Кох – тот же учёный,
что открыл туберкулёзную палочку. На туберкулин он возлагал
большие надежды, планируя использовать его для лечения больных
туберкулёзом. Для Коха это был весьма личный вопрос, так как от
туберкулёза умирал его сын. Однако, вызывая на некоторое время
облегчение болезни за счёт реактивации иммунитета, в
действительности туберкулин ничего не лечил, а часто даже
провоцировал ускорение туберкулёзного процесса. Но разразившийся
скандал не умалил заслуг выдающегося учёного, а люди получили новый
диагностический препарат.
Правда, изначальный туберкулин Коха имел значительные колебания
состава и для использования в рутинной практике здравоохранения не
подходил. Фактически, туберкулин для массового применения
подарили медицине старания двух женщин: американки Флоренс
Барбары Зайберс, которая в 1934 году стандартизировала метод
получения белкового экстракта микобактерий со строго необходимым
содержанием нужного вещества (препарат был назван PPD-S, от
purified protein derivate – очищенный протеин, и первой буквы фамилии
автора – Saibers), и советского учёного Марии Линниковой из
Ленинградского института вакцин и сывороток, которая в 1939 году
получила усовершенствованный «туберкулин Линниковой». Именно его
под обозначением PPD-L (ППД-Л) в 1963 году ВОЗ признала эталоном
данного препарата.
В настоящее время для туберкулинодиагностики используется и
другой препарат – диаскин-тест (DST). Это уже синтетический белок,
а вернее, полученный при помощи генномодифицированных дрожжей,
которым внедрили ген, кодирующий этот белок у микобактерий
туберкулёзис (мы уже упоминали, что таким же способом получают,
например, белок HBsAg вируса гепатита В для создания вакцины от
этой инфекции). Это более чистый препарат, он не даёт
ложноположительных реакций у лиц, которые ранее были привиты
вакциной БЦЖ, и его можно использовать для контроля
эффективности лечения туберкулёза, но по понятным причинам
диаскин-тест выявляет только инфицирование микобактериями
человеческого типа.
Надеюсь, по прочтении этого текста вы уже поняли, что туберкулин
и диаскин-тест не являются вакцинами, поскольку не формируют
иммунитет, а лишь проверяют его состояние относительно реакции на
микобактерии – это диагностические препараты. У них, конечно,
есть свои медицинские противопоказания к применению, но ничего
общего с медотводами от прививок они не имеют. Равно как и живого
возбудителя ни туберкулин, ни тем более синтетический диаскин-тест,
не содержат, и опасаться по этому поводу не стóит. Как туберкулин,
так и DST вводят внутрикожно в объёме всего 0,1 мл (для этого
используются специальные шприцы с маленькими острыми иглами,
которые вводят почти параллельно коже на очень небольшую глубину).
При этом образуется возвышение на коже – папула. В течение
ближайших нескольких суток в ней разворачивается иммунная
реакция. Если ранее организм уже был инфицирован микобактериями,
то эта реакция идёт бурно, место введения наводняют клетки
иммунитета, и возникает местный воспалительный процесс – это и
есть проявление той самой гиперчувствительности замедленного типа
(ГЗТ). Поскольку в отличие от аллергии, которая проявляется почти
мгновенно (за минуты, максимум – часы), для развития ГЗТ нужно
время, то результат туберкулиновой пробы «читают» через 72 часа. По
величине папулы или инфильтрата реакцию оценивают как
положительную или отрицательную.
Проблема туберкулёза до сих пор имеет большое значение. Хотя в
течение XX века и было разработано немало препаратов для его
лечения, но и возбудитель успел к ним приспособиться. В результате
наибольшую опасность сейчас представляют МЛУ— и ШЛУ-формы
туберкулёза (с множественной лекарственной устойчивостью и
широкой лекарственной устойчивостью), плохо или совсем не
поддающиеся терапии. Поэтому вакцинопрофилактика туберкулёза
остаётся весьма актуальной.
Вакцинацию БЦЖ или БЦЖ-М (выбор зависит от уровня
заболеваемости в регионе страны) проводят детям уже в первые сутки
жизни, как правило, ещё в роддоме. Это связано с тем, что дети очень
подвержены инфицированию микобактериями, а антитела матери,
которые передаются плоду трансплацентарно, а новорождённым – с
грудным молоком, против микобактерий неэффективны (почему – см.
выше). Если прививается новорождённый или ребёнок до 2 месяцев
жизни, то туберкулинодиагностику ему не проводят. Вакцинацию
более старшим детям, а также ревакцинацию в 6—7 лет делают только
туберкулиноотрицательным детям.
Хотя мы и говорили ранее, что при туберкулёзе формируется
нестерильный иммунитет, но в отношении вакцины БЦЖ/БЦЖ-М
это не значит, что вакцинные микобактерии тоже будут долго
присутствовать в организме ребёнка. Ослабленные микобактерии
здоровый организм быстро подавит, а небольшое гранулематозное
воспаление на месте введения рассосется, оставив самое большее
небольшой рубчик. Но при повторной встрече с возбудителем
адаптивный иммунитет уже будет готов, и это повысит его шансы не
дать микобактериям распространиться из первичного очага.
Подавленные иммунитетом и проросшие соединительной тканью
первичные очаги спустя некоторое время пропитываются солями
кальция и обызвествляются – становятся плотными, как мел или
известняк. Их называют очагами Гона, и обнаружить их можно не
только при вскрытии умерших, но и при жизни – за счёт высокой
плотности они видны на флюорограмме или рентгенограмме. Эти же
методы лучевой диагностики (а также рентгеновскую томографию)
используют и для раннего выявления туберкулёза, так как
инфильтрированные иммунными клетками отёчные туберкулёзные
очаги видны как затемнения, а запущенные очаги с распадом лёгочной
ткани – как «пустоты».
Из-за опасности туберкулёза профилактическую флюорографию всё
население должно проходить не реже 1 раза в 2 года, но фактически
большая часть людей проходит её ежегодно: одни работают в
«декретированных» профессиях (медики, педагоги, соцработники и т.
п.), другие принадлежат к группам риска (страдают хроническими
заболеваниями дыхательной, эндокринной и других систем, негативно
сказывающимися на иммунитете). Те же, кто имел подтверждённый
контакт с больным туберкулёзом, и вовсе в течение некоторого
времени должны проходить флюорографию дважды в год.
Глава 8. Они такая малость…
В самом начале книги мы уже сказали, что вирусы занимают особое
место среди микроорганизмов, хотя, по сути, организмами не
являются. Ведь они почти ничего не могут самостоятельно – ни
питаться, ни размножаться, ни эволюционировать. Для всего этого им
нужна живая клетка «настоящего» организма: либо одноклеточного
(бактерии, простейшего), либо многоклеточного – растения, животного
или человека.
Правда, совсем недавно были открыты вирусы, которые
ухитряются паразитировать на других вирусах: точнее, они украдкой
записывают свой генетический материал в их геном, пока те заняты
ровно таким же «хулиганством» в клетках живых организмов. Жизнь
таких вирофагов напоминает поговорку о том, как «вор у вора
дубинку украл».
Но как мы уже упоминали в начале, отечественные микробиологи
относят вирусы, вироиды и нуклеопротеины в особое надцарство
природы Vira («вира») – владения доклеточных форм «преджизни».
Нужно пояснить, что вироид – это молекула вирусной РНК, не
имеющая белковой оболочки (капсида). Несмотря на свою
«раздетость», вироиды сохраняют инфекционные свойства. А
нуклеопротеин – комплекс из нуклеиновой кислоты (ДНК/РНК) и
поддерживающих её белков (протеинов), пока ещё не
сформировавший полноценный вирион. Вирионом же называют
полный вирус, как его привыкли изображать на всяких стилизованных
картинках – готовую к заражению вирусную частицу в составе
белковой оболочки-капсида, рецепторов на её поверхности и
генетического материала внутри (не путайте с бактерией рода
вибрион, и с эмбрионом тоже не путайте).
На этом вся замечательная простота и понятность вирусов
заканчивается. При всей примитивности устройства они могут
использовать в качестве носителя генома двухцепочечную ДНК (почти
как у нас), ДНК одноцепочечную, РНК вместо ДНК, РНК, свернутую в
кольцо, и так далее. Помните, мы сравнивали вирус с флешкой? Так
вот, знайте: кроме «флешек», с вашими клетками могут пытаться
коннектиться «лазерные диски», «флоппи-дискеты», «перфокарты» и
«грампластинки»!
А поскольку очень длинные молекулы нуклеиновых кислот в
милипусечные капсиды просто не помещаются, а кодировать белки
как-то нужно, то вирусы ещё и научились сверхплотно упаковывать
генетическую информацию. Начал считывание информации с одного
места – получай первую матричную РНК и один белок, сдвинул
«рамку считывания» – уже вторая РНК и совсем другой белок. В
наших клетках такие фокусы – летальная мутация, а вирусам профит и
оптимизация!
И самое удивительное – никто из учёных сегодня не знает, откуда
вообще вирусы появились! То есть теорий целых три: либо они когдато были автономными организмами, но выбрали «тёмную сторону»
паразитизма, и там их покорёжило в сторону максимального
упрощения, либо «сбежали» из живых клеток, превратившись из
просто части генома в обособленные структуры, либо – они потомки
далёкого прошлого планеты, когда на ней зарождались и
совершенствовались самоорганизующиеся молекулы (белки и
нуклеиновые кислоты). Только все нормальные молекулы стали
объединяться дальше в простейшие клетки, а вирусы на стадии
нуклеопротеинового междусобойчика сказали: «Нам и так норм!» А
возможно, что имели место все три пути в разной степени сочетания,
потому что ни один по отдельности не объясняет всё многообразие
существующих сегодня групп вирусов.
А многообразие это настолько велико, что трудно даже оценить. В
одном только нашем собственном кишечнике учёные «наловили» 140
тысяч видов вирусов. А ведь помимо наземной жизни есть ещё и
океан, и почти неизученная биота геосферы (всех этих пещер, шахт,
полостей и прочего) – и везде присутствуют вирусы. Ведь
«наездничают» они не только на клетках многоклеточных существ, но
и на нашей микрофлоре – есть даже группа специализированных
паразитов бактерий – вирусы-бактериофаги.
Кстати, бактериофагов ряда бактерий научились размножать в
искусственных условиях и использовать затем в качестве препарата
для лечения гнойно-воспалительных заболеваний и бактериальных
инфекций. В отличие от антибиотиков, к ним у бактерий
устойчивость разивается куда медленнее.
Однако бактерии не являются для специфичных к ним фагов совсем
уж беззащитными жертвами. У них тоже существует «иммунитет»,
сохраняющий постоянство их генетической информации. В частности,
ряд бактерий синтезирует ферменты, называемые рестриктазами; они
просто-напросто вырезают фрагменты бактериальной ДНК, в которые
встроился вирус. Сравните это с тем, как вы редактируете свои видео
для соцсетей: не понравился вам какой-то фрагмент – открыли
приложение и вырезали его из ролика, а потом программа склеит
половинки обратно.
Но клетки не умеют соединять ДНК конец-в-конец, как какиенибудь трубы, поэтому рестриктазам приходится работать очень
интересным образом: в месте разреза ДНК они оставляют на ней
«липкие концы». Сейчас поясню, что это значит.
Надеюсь, вы в общих чертах помните, как устроена двойная спираль
ДНК? Это две спиральные цепочки из нуклеотидов. Переплетаются
они друг с другом за счёт взаимодействия входящих в состав
нуклеотидов оснований, причём аденин на одной цепи
взаимодействует строго с тимином на другой, а гуанин – с цитозином.
Поэтому между цепочками получаются удерживающие их вместе
«мостики» вида А-Т, Г-Ц, Т-А, Ц-Г. Говорят, что эти пары оснований
комплементарны друг другу, а значит комплементарны и обе цепочки
двойной спирали ДНК.
Так вот, рестриктазы режут эту спираль не просто поперёк, а словно
буквой Z: так, что на каждом из получившихся фрагментов одна
цепочка чуть длиннее другой. А это значит, что на ней теперь есть
неспаренные нуклеотиды, которые только и ждут, чтобы поблизости
оказались такие же «одинокие» нуклеотиды, с которыми можно
«законнектиться». Очень похоже на застёжку-липучку. Только для
нормальной
работы
«липучки»
в
ДНК
нужно,
чтобы
последовательность «букв»-нуклеотидов на длинной цепи одного
фрагмента строго соответствовала (по принципу «А к Т, Г к Ц») их
последовательности на втором. То есть чтобы они опять-таки были
комплементарны. Тогда произойдёт самосборка, и фрагменты
«склеятся» обратно в нормальную молекулу ДНК.
Рестриктазы «знают» о необходимости соблюдения этого условия,
поэтому, когда «выпиливают» чужие вирусы из родной ДНК, то свои
«фигурные» разрезы наносят не где попало, а в таких местах, где
последовательности нуклеотидов совпадают – специальных сайтах
рестрикции. В результате после удаления заражённого вирусом
фрагмента на концах половинок ДНК получаются аккуратные,
соответствующие друг другу «липучки», которыми молекула
склеивается воедино. Ура! Победа! Вирус вышел из чата! Ощути
полноту здоровой ДНК!
Однако подходящие сайты рестрикции не всегда можно найти на
молекуле ДНК именно в нужных местах. Поэтому иногда получается
так, что рестриктазы удалили только регуляторные области гена,
принесённого
вирусом
(«включатель»
гена),
а
сама
последовательность, кодирующая чужеродный белок, осталась на
хромосоме. Бактерия не станет этот белок синтезировать, но,
размножаясь, будет исправно копировать ген вместе со всей ДНК. И
все потомки такой бактерии будут нести в геноме своеобразную «мину
с испорченным детонатором», которая неизвестно когда рванёт.
Мутация или очередная вирусная атака, покорёжившие ДНК, могут
«разбудить» ген и снова запустить на нём процессы «отжига»
матричных РНК. Те понесутся в рибосомы, где запустится синтез
белка. А уж последствия будут зависеть от того, какой именно белок
был зашифрован в «недобитом» чужом гене.
Иногда это не собственно вирусный белок, а имеющий
бактериальное происхождение. Откуда он взялся в геноме вируса?! А
вирус прихватил его случайно, когда в прошлые разы реплицировался
в заражённой бактерии. Из-за сбоя в ходе этого процесса он легко
может «вынести» из клетки больше генов, чем «принёс» в неё. А
потом, заражая следующих бактерий, такой «пополнившийся» штамм
вируса будет передавать им новый ген – не вирусный, но и не
«родной». И если бактерии переживут вирусную атаку, то могут
заполучить в свой геном неожиданный «подарок».
Так могут передаваться гены устойчивости к антибиотикам, а при
дифтерии (инфекции дыхательной системы человека) с этим
механизмом связан весь инфекционный процесс. Нетоксигенные
штаммы дифтерийной палочки могут спокойно жить на слизистой
нашей носоглотки в качестве комменсала, не причиняя вреда. Но как
только их инфицирует бактериофаг, приносящий в геном особый ген,
тут и начинается весь патогенез заболевания. Этот ген кодирует
структуру ядовитого белка – дифтерийного токсина. Под его
действием слизистая дыхательных путей воспаляется и начинает
покрываться корочками.
И если у взрослых людей просвет воздухоносных путей достаточно
широк, и они редко умирают от дифтерии, то тонкие дыхательне пути
маленьких детей просто забиваются дифтерийными плёнками,
вызывая смерть от удушья. До появления антибиотиков педиатры
лечили это заболевание, грушей или просто ртом отсасывая плёнки
через введённую в дыхательные пути трубку. Часто при этом
заражаясь сами. К счастью, дифтерию сначала научились лечить, а
затем появились вакцины (вы прочтёте о них подробнее в одной из
следующих глав), которые почти извели её.
Так что, если про нас в главе об иммунитете я говорил, что чужие
гены «нам не нать», то вот бактерии и другие одноклеточные совсем не
против горизонтального переноса генов (в пределах одного
поколения – мы-то можем передавать свои гены только потомкам, то
есть вертикально). И пугающая некоторых людей аббревиатура ГМО
(генно-модифицированные организмы) для них – обыденность. По
сути, все они – ГМО и продолжают «модифицироваться» каждую
минуту. Бояться этого – всё равно что бояться восхода солнца.
Мы даже научились этим пользоваться. Помните, я рассказывал
выше про рестриктазы? Так вот, умение разрезать ДНК
микроорганизмов в нужных, строго определённых местах порой
бывает очень важно. И для проведения ПЦР-диагностики (выявления в
пробе генетического материала того или иного организма), и для
«вклеивания» между «липкими концами» батериальной или
дрожжевой ДНК чужого гена. Такой ГМ-организм будет попутно со
своими продуцировать и белок, кодируемый «пересаженным» ему
геном. Этим занимается отрасль биотехнологии, и при помощи таких
«конструкторов» она синтезирует огромное количество различных
веществ, в том числе лекарств. Например, благодаря биотехнологии
производится столько гормональных
препаратов (инсулина,
соматотропина и других), сколько мы никогда бы не получили от
животных. К тому же бычий инсулин пусть немного, но отличается от
человеческого, да и вообще животных жалко. По этому же принципу
производят ряд вакцин – тех, где нужны очищенные антигены
патогенных микробов, а вот присутствие самих этих микробов опасно
и нежелательно.
Впрочем, о вирусах можно рассказывать долго и много – на эту тему
написано немало книг. Посоветовать могу А. Фомсгорд «Вирусы:
откуда они берутся» – из тех соображений, что она новая (2021 г.), а
потому туда попали все последние шумные инциденты с вирусными
инфекциями, включая пандемию COVID-19, а также открытие
пандоравиурсов (упомянутых выше вирофагов или «вирусов
вирусов»). Карин Мёллинг в книге «Вирусы. Скорее друзья, чем
враги» представляет «позитивную повестку» от вирусологии. Ну а
если хотите глубокий и всеобъемлющий взгляд, то найдите очень
редкую, к сожалению, книгу «История вирусологии от Д. И.
Ивановского до наших дней» – от российского вирусолога Феликса
Ершова. Он ученик другого корифея вирусологии и эпидемиологии –
академика Виктора Жданова, одного из авторов программы
ликвидации натуральной оспы, исследователя ВИЧ и автора
множества других открытий. Да и сам Феликс Иванович немало
сделал для изучения вирусов, а главное – поиска средств борьбы с
ними, в частности, препаратов интерферонов и индукторов выработки
последних в нашем организме. Сейчас это основные противовирусные
препараты непрямого действия (а прямого – можно буквально по
пальцам пересчитать). Первые редакции «Истории вирусологии…»
ученик и учитель писали вместе, а к моменту выхода нынешней – в
2020 году – Ершову уже 89 лет, но он по-прежнему сохраняет ясность
ума и знает о вирусах всё (настолько, насколько они позволили о себе
на сегодня узнать, конечно)!
Об инфекционных вирусных болезнях тоже написано немало, в том
числе и опытными врачами и большими учёными. Поэтому я решил
рассказать только об одной их группе – и больше с точки зрения
эпидемиолога. К тому же именно с интернатуры в лаборатории
вирусных гепатитов начался мой «вход» в мир микробов и вирусов.
8.1. Жизнь одна, и печень – тоже!
Проблема гепатитов – воспалительных заболеваний печени (от её
латинского названия hepar, «хепар»), особенно инфекционных форм,
очень актуальна. Ведь порядка 2 миллиардов всего населения планеты
были инфицированы в прошлом или заражены сейчас инфекционными
гепатитами. Каждый четвёртый! В каких-то странах соотношение
больше, в каких-то – меньше. В России, например, только от гепатита
С страдает более 4% населения, причём основная их часть – в самом
активном и трудоспособном возрасте, от 20 до 40 лет. А ведь печень в
нашем
организме
служит
«фильтром»,
самой
природой
приспособленным для инактивации токсинов и шлаков. Ещё в печени
протекает метаболизм целого ряда веществ, таких как холестерин,
некоторые гормоны, гемоглобин, а всего функций этого органа учёные
описывают несколько десятков. Поэтому болезни печени ведут к
резкому снижению качества жизни.
И всё равно даже у тех, кто «что-то слышал про желтуху»,
представления о болезни из-за разнообразия её форм расплывчаты. Да,
есть такой симптом – окрашивание кожи и слизистых у таких больных
от бледно-лимонного до зеленовато-оранжевого оттенков. Но это –
лишь внешнее проявление нарушения обмена желчных пигментов в
организме, и далеко не всегда оно связано с гепатитом. У
новорождённых первых 2–3 недель жизни вообще очень часто (у более
чем половины доношенных детей и у 80% недоношенных) бывает
физиологическая желтуха – и (голосом Малышевой) «это норма»! А
иногда наоборот – гепатит может протекать в безжелтушной или
субиктеричной (кожа на вид нормального цвета, но склеры глаз и
слизистые желтушные) форме.
Так что «мухи» в виде желтухи – отдельно, «котлеты» из гепатитной
печёнки продолжаем раскусывать дальше. Вызывать поражение
печени могут разные причины: гепатиты бывают аутоиммунные,
лекарственные, инфекционные и хренпоймические (по науке –
криптогенные, или «неизвестной этиологии»). Инфекционные
вызывают добрых два десятка микроорганизмов из совершенно
разных групп: бактерии (лептоспиры, бруцеллы), простейшие
(малярийные плазмодии). Но чаще всего виновны вирусы: Эпштейна-
Барр, Коксаки, ECHO (читаем «ЭКХО»), да тот же вирус кори. Но и
среди вирусов есть особенные «любители печёнки», выбирающие
именно её как основную мишень для поражения (при остальных
упомянутых инфекциях гепатит может не играть самостоятельной
роли). Их объединили под общим названием «вирусы гепатитов» (из
соображений практической медицины, так как друг другу они даже не
родственны) и присвоили обозначения по первым буквам латинского
алфавита – вирусы гепатита A, B, C, D, E. И это оказалось очень
дальновидно, потому что претендентов на пока не востребованные
буквы полно: за последнее десятилетие уже выделены вирусы F, G, Sen
и TT.
Весь этот «алфавит» можно разделить на две группы – по механизму
передачи инфекции. Так, у гепатитов А и Е он фекально-оральный. То
есть заразиться ими можно при употреблении инфицированной воды и
пищи, а также при несоблюдении мер гигиены: раньше всю группу
этих инфекций так и называли – «болезнями грязных рук». Все
остальные вирусы – B, C, D и их пока малоизученные компаньоны –
относятся к группе парентеральных инфекций. То есть они передаются
через кровь, и реализуется это контактно-бытовым и половым путями.
А также во время родов – от матери к ребёнку (вертикальный путь). И
при нарушении целостности кожи и слизистых загрязнённым
вирусами инструментом: иглой шприца или скальпелем, например (это
искусственный перенос, потому путь называется артифициальным).
Из всей большой и коварной компании фекально-оральные гепатиты
А и Е никогда не переходят в хроническую фазу, однако это не значит,
что они не опасны. Раньше гепатит А считался «детской инфекцией»,
однако с развитием гигиены и санитарии гораздо меньше детей стали
переносить «болезнь Боткина» (старое название недуга) и к взрослому
возрасту не имели иммунитета. При этом у взрослых гепатит А
протекает тяжелее, чем у детей. А изредка – менее чем в 1% случаев –
он протекает в молниеносной форме, грозящей смертью от тяжёлой
печёночной недостаточности.
Гепатит Е распространён в странах Восточной, Средней и Южной
Азии, но встречается и в России. Протекает менее злокачественно, чем
гепатит А, однако, по пока неизученным причинам, очень опасен для
беременных женщин. У них он вызывает молниеносные формы
болезни, до 25% которых заканчиваются летальным исходом.
Вирусы фекально-оральных гепатитов А и Е могут попадать вместе
с необеззараженными канализационными стоками в аварийный или
изношенный водопровод, при сбросе канализации в открытые
водоисточники. Часто вспышки фекально-оральных гепатитов
наблюдаются после паводков, когда содержимое выгребных ям
разносится
по
затапливаемой
территории,
а
источники
доброкачественной
воды
становятся
недоступны.
Поэтому
водопроводную воду для питья необходимо всегда кипятить, а в
путешествии или на отдыхе пользоваться бутилированной и не
доверять родникам и речкам (откуда вы знаете, не спускают ли парой
километров выше по течению канализационный сток – запаха при
таком разведении может не быть, а вот вирусов хватит для
инфицирования). Также необходимо тщательно мыть перед едой
овощи, фрукты, зелень, опять же используя для этого
доброкачественную воду. Так же тщательно нужно мыть руки, а при
невозможности – пользоваться кожным антисептиком или
бактерицидными салфетками. То есть соблюдать обычные правила
профилактики
кишечных
инфекций.
Кроме
того,
для
иммунопрофилактики гепатита А существует несколько вакцин
(«Альгавак», «Хаврикс» и их модификации). По эпидемическим
показаниям в России прививают педагогов, медиков, персонал
интернатов и пищевых производств, работников водопроводноканализационных сетей. В последние годы ряд регионов РФ
иммунизирует детей и подростков за счёт своих региональных
календарей прививок.
Обязательна прививка от гепатита А и при выезде в ряд зарубежных
стран, в том числе на модные южные курорты: в Египет, Турцию,
Грецию, Испанию, Кипр.
Хотя гепатиты с фекально-оральным механизмом нельзя назвать
неопасными, однако они редко дают эпидемическое распространение.
Разве что в специфических условиях перемещения больших масс
населения, лишённого доступа к нормальной питьевой (и вообще
любой) воде и продуктам питания. Вы уже, наверное, представили
себе беженцев, спасающихся от землетрясений и цунами. Да, а ещё
войн – гепатит А в своё время даже называли «окопной желтухой».
Но главную печальную славу гепатитам принесли другие их
«буквы» – возбудители парентеральных вирусных гепатитов (ПВГ).
Мало того, что они идут «рука об руку» с ВИЧ-инфекцией, поскольку
имеют с ней общий механизм передачи, так ещё и каждый обладает
своими коварными особенностями. Например, чтобы заразиться
гепатитом В, достаточно малейшего, практически незаметного глазом,
количества инфицированной крови, попавшей на слизистые или в
микротрещины кожи. Поэтому в быту можно легко заразиться
гепатитом В при пользовании общими с больным или носителем
инфекции гигиеническими принадлежностями (бритвой, полотенцем)
или косметикой – губной помадой, например. Это привело к тому, что
в 90-е годы XX века Россию едва не захлестнула эпидемия гепатита В.
Справиться с ростом заболеваемости тогда помогли только прививки.
Новорождённых детей начали прививать в первые часы жизни,
постепенно охватив и основную часть ранее не привитых детей и
взрослых. Выяснилось, что заодно вакцинация защищает и от гепатита
D, вызываемого «неполноценным» вирусом, который не может
размножаться в организме без «напарника» – вируса типа В. Однако в
последнее время с ростом «антипрививочных» настроений
увеличивается опасность повторного распространения гепатитов В и D
в эпидемических масштабах.
А вот от другого «ласкового убийцы» – вируса гепатита С – вакцины
пока не разработаны из-за большой изменчивости вируса в организме.
«Ласковым» гепатит С называют потому, что это медленная инфекция.
Да, это термин, но и на деле так – вирус поражает печень медленно, но
верно. А она, благодаря своим очень высоким компенсаторным
возможностям (человек может выжить, потеряв в результате ранения
или травмы 6 из 8 долей печени), долго не даёт знать о проблемах.
В итоге, переболев «на ногах» гриппоподобной инфекцией и не
обратив внимания на едва заметную желтизну слизистых, человек
может и вовсе не знать, что заразился, а в его печени уже запущен
необратимый механизм. Если гепатит В только в 10–15% случаев
переходит в хроническое течение, то гепатит С, наоборот,
хронизируется у 90–95% инфицированных, рано или поздно приводя к
циррозу печени – замещению здоровых клеток на бесполезную
рубцовую ткань. Печень буквально превращается в один большой
шрам. Одновременно вирус запускает раковое перерождение –
малигнизацию. Именно смерть от рака печени – гепатокарциномы –
как правило, становится печальным итогом заболевания гепатитом С.
Необходимая инфицирующая доза при гепатите С больше, чем у
ВИЧ, и многократно больше, чем у гепатита В, поэтому в его
распространении на первое место выходят половой путь и
инъекционное употребление наркотиков.
В своё время определённую роль в распространении ВИЧ и
«кровяных» гепатитов играли многоразовые шприцы, нестерильный
медицинский инструментарий и заражённая донорская кровь. Поэтому
сейчас цельную кровь не переливают, используя лишь отдельные
компоненты. При этом эритроцитарную массу прогоняют через
специальные фильтры, тромбоцитарную – особым образом
обрабатывают, чтобы избавиться от вирусов. Потенциально опасной
при таком подходе остаётся только донорская плазма. Чтобы
минимизировать и этот риск, полученную кровь тестируют на ВИЧ,
сифилис и гепатиты сразу после получения. А донора – дважды, сразу
после кровосдачи и через 3–6 месяцев, чтобы не пропустить «спящую»
инфекцию, или, по-научному, «период серонегативного окна». Всё это
время плазма не отправляется в больницы, а находится в специальном
хранилище в замороженном виде. Если донор не был обследован
дважды или у него выявили инфекцию, такая плазма отбраковывается
и уничтожается. В то же время шприцы повсеместно стали
одноразовыми, а методы обеззараживания медицинских инструментов
усовершенствовались.
Зато одновременно возросло количество так называемых
«парамедицинских» манипуляций – маникюр, педикюр, пирсинг и
татуаж доморощенные мастера нынче готовы проводить чуть ли не в
каждом подвале. Вообще-то врачи-эпидемиологи и инфекционисты
далеки от ханжества и принципиально не против даже тату, не говоря
уже о том, чтобы поддерживать свои «лапки и культяпки» в ухоженном
виде. Но только в одном случае – когда к инструментам для подобных
«художеств» предъявляются требования по безопасности как к
медицинским. То есть либо однократное использование, либо
стерилизация на сертифицированном оборудовании. Потому что от
выложенных в Ютуб роликов, где иглы для пирсинга
«дезинфицируют» водкой, у автора этих строк остатки волос встают
дыбом – по эпидемиологической значимости такое равносильно
пропаганде шприцевой наркомании!
Ещё парадоксальнее, что многих не пугает татуаж чуть ли не иглой
от циркуля, но при этом они могут панически бояться «комара,
насосавшегося инфицированной крови». Для сведения: комары сосут
кровь, а не впрыскивают её. Поэтому заразить гепатитом, ВИЧ или
сифилисом они никого не могут.
Ну и напоследок простая истина: презерватив не только избавляет от
нежелательной беременности, но и при правильном использовании
защищает от возбудителей половых инфекций, вирусов гепатитов и
ВИЧ.
К сожалению, о гепатитах – особенно парентеральных, с их
«интимными» путями передачи – до сих пор не принято говорить
широко и тем более держать в голове по ходу жизненных
обстоятельств. Один год даже эмблемой Всемирного дня борьбы с
гепатитом (отмечается ежегодно 28 июля) были выбраны три
обезьяны, символично зажимающие глаза, уши и рот – как знак
игнорирования проблемы обществом.
Глава 9. Я прививок не боюсь!
Когда в главах выше мы говорили об этапах иммунного ответа, то
предполагали, что в организм проник извне патогенный микроб, то
есть
привёл
к
инфицированию,
развитию
полноценного
инфекционного процесса. Если иммунитет быстро справится со своей
задачей, например, за счёт мощного вторичного иммунного ответа на
знакомый антиген, то мы даже и не узнаем об этом – в крайнем случае,
переболеем в стёртой форме. В противном случае разовьётся
инфекционное заболевание (если виновником стали условнопатогенные бактерии, вызвавшие, например, нагноение операционной
раны, то говорят о гнойно-воспалительном заболевании, но
иммунитет активируется в любом случае). Если организм справится с
инфекцией и не погибнет, то выработавшийся в результате иммунитет
будет считаться естественным и активным (инфекции существуют в
естественной природе, а для победы над заражением иммунитету
пришлось активно потрудиться).
Однако, когда люди узнали, как работает иммунитет (и даже
раньше), у наиболее пытливых из них возник вопрос: а можно ли както сделать так, чтобы иммунитет сработал – «познакомился»
с антигеном – а заболевание не возникло. А у наиболее пытливых из
вас, по-хорошему, должен был родиться не только такой вопрос, но и
ответ на него. Даже два ответа: раз в основе иммунитета лежит
реакция взаимодействия антиген–антитело, то для решения
поставленного вопроса нужны либо антиген отдельно от цельного
возбудителя, либо готовые антитела. Правда, тут же рождается
следующий вопрос: где то или другое взять?
С антигеном решение нашли быстро. Сначала Эдвард Дженнер ещё
в конце XVIII века из своих наблюдений предположил, что
близкородственные возбудители могут формировать перекрёстный
иммунитет. Правда, ни одного из этих терминов в то старинное время
Дженнер не знал – он просто обратил внимание, что доярки на фермах,
где распространена коровья оспа, почти не болеют человеческой
натуральной («чёрной») оспой. И, проведя эксперимент с заражением
девятилетнего ребёнка содержимым сначала оспенного пузырька с
вымени больной коровы, а спустя некоторое время – такого же
пузырька от больного натуральной оспой, Дженнер подтвердил свою
правоту: подопытный Джеймс Фиппс не заразился.
В наше время за такие «эксперименты по живому» Дженнеру бы не
поздоровилось, но напомню: на дворе стоял 1796 год, средняя
продолжительность жизни в Европе составляла всего 35–37 лет, а
«любовь и чёрная оспа миновали лишь немногих», – по выражению
одного из романистов того времени. Малолетний русский император
Пётр II – внук знаменитого Петра I – и вовсе скончался от натуральной
оспы в возрасте 14 лет, в результате чего род Романовых по прямой
мужской линии прервался, а история государства российского
изменилась, может, и не кардинально, но уж точно пошла по другой
колее. Может быть, в том числе и поэтому одна из следующих наших
правительниц – Екатерина II, именуемая также Великой, – была ярой
сторонницей вариоляции. Так тогда называлось оспопрививание (от
слова «вариола» – вздутие, оспенный пузырёк, образуемый действием
вируса на кожу). То есть до Дженнера тоже пытались бороться с оспой
посредством
«прививок»:
оспенные
пустулы
с
больного,
образовавшиеся после вскрытия вариол, собирали, сушили на солнце и
толкли в порошок, надеясь такими манипуляциями ослабить
возбудитель (хотя ещё даже самого представления о микробах не
существовало, и всё делалось почти интуитивно). А затем этот
порошок вдували в нос ещё не болевшим. Екатерина пользовалась уже
другим методом: когда через оспенный пузырёк больного
протягивалась нить, а затем её проводили через небольшой надрез на
коже здорового человека. Бррр! – само описание вызывает дрожь. А уж
каков был процент по-настоящему заболевших оспой после таких
процедур – ведь, в отличие от Дженнера, древние «вариоляторы»
использовали не слабовирулентный для человека близкородственный
штамм, а натуральный – «дикий».
Луи Пастер более чем полвека спустя после Дженнера подходил к
работе уже с более научных позиций. В ходе своей работы он заметил,
что ослабленная определёнными способами чистая культура
возбудителя инфекции либо перестаёт вызывать заболевание, либо
заболевшие переболевают легко (мы бы сказали, что у возбудителя
снижается вирулентность). Это позволило Пастеру создать сначала
вакцину против холеры цыплят, а затем против сибирской язвы – когда
последняя была успешно испытана на животных, восторженные
фермеры согласились подставить под прививку и собственные
конечности. Из уважения к работам Дженнера с коровьей оспой
Пастер оставил за всей этой группой препаратов название «вакцина» –
от лат. «вакка», корова.
Вакцины, приготовленные по такому типу, получили название
живых ослабленных (аттенуированных) – к сожалению, при их
использовании есть минимальная, но реальная вероятность, что у
ослабленного человека они вызовут полноценный инфекционный
процесс. Поэтому уже следующая вакцина Л. Пастера – против
бешенства – была, как бы мы сказали сегодня, инактивированной. Он
готовил её из подвергнутых высушиванию и обработке формалином
тканей мозга погибших от бешенства кроликов. Вирус-возбудитель
бешенства при этом погибал, однако белки вирусного капсида не
разрушались настолько, чтобы иммунитет переставал узнавать в них
характерные антигены. Хулигански выражаясь, Пастер начистил
возбудителю бешенства фейс, но не настолько, чтобы его мама родная
не узнала. По сути, это была первая «научно обоснованная»
цельновирионная инактивированная вакцина.
Вы, конечно, уже поняли, что риск заразиться инфекцией при
введении такого препарата отсутствует – ведь живого возбудителя
в нём нет. Хотя за соблюдением качества «убивки» возбудителя,
конечно, нужно следить. В нынешнее время этим заняты
производственные лаборатории самих производителей вакцин плюс
лаборатории контролирующих органов – Росздравнадзора и
Роспотребнадзора в нашей стране, FDA в США.
Дальше этот принцип начал совершенствоваться. Не будем
вдаваться глубоко в историю создания вакцин, скажем только, что со
временем учёные научились так ювелирно расщеплять микробные
тела возбудителей, чтобы получать отдельные очищенные антигены:
по такому принципу созданы современные инактивированные вакцины
против гриппа, например – так называемые сплит-вакцины, от англ.
split – «расщеплённый».
За счёт отсутствия в составе вакцины ненужных веществ и лишних
антигенов они дают меньший риск аллергических и других побочных
реакций. Например, отечественная детская вакцина АКДС помогла
победить такие детские болезни, как коклюш, дифтерию, столбняк.
Однако коклюшный компонент в ней готовился путём инактивации
культуры клеток возбудителя – бактерии бордетелла пертуссис
(дословно кашлевая бактерия Борде – бельгийский иммунолог Жюль
Борде совместо с О. Жангу выделил её в 1906 году, поэтому её ещё
называют
палочкой
Борде-Жангу).
Но
бордетеллы
–
грамотрицательные бактерии. А если вы внимательно читали главу о
строении бактерий, то помните, что у этой группы бактерий клеточная
стенка содержит липополисахарид (ЛПС), из-за которого даже убитые
бактерии могут вызывать в организме сильную реакцию с подъёмом
температуры. А у маленьких детей лихорадка чревата неприятными
сопутствующими симптомами вплоть до судорог. Благо, прививочная
доза вакцины содержит совсем мало бактериальных «трупиков»,
поэтому такие реакции весьма редки, и, пока не было альтернативы, с
этим мирились. Однако с появлением бесклеточных вакцин типа
«Пентаксим» и «Инфанрикс», приготовленных по сплит-технологии,
им стали отдавать предпочтение – по крайней мере, для иммунизации
детей с неврологическими нарушениями, у которых даже
минимальный риск фебрильных судорог нежелателен.
Правда, тут выплывает другой минус. Представьте, что вы пришли в
картинную галерею. Но картины тут какие-то странные. Вот на белом
фоне три медвежонка с матерью-медведицей, а здесь куда-то бегут
испуганные люди. И только увидев на размытом фоне третьей картины
улыбку Джоконды, которую сложно с чем-то перепутать, вы
догадываетесь, что и первые две – широко известные «Утро в
сосновом лесу» И. Шишкина и К. Савицкого и «Последний день
Помпеи» К. Брюллова. «Кто так над живописью поиздевался?!» –
возмущённо думаете вы и идёте требовать обратно деньги за билет.
Так же, как вы можете вспомнить хорошо знакомую картину по
отдельным элементам изображения, так и иммунитет может опознать
возбудитель
по
«чистым»
антигенам.
Не
зря
же
антигенпрезентирующие клетки сначала расщепляют патогенный
микроорганизм, чтобы выставить на мембране «для опознания»
другими иммунными клетками отдельные его компоненты. Но в
некоторых случаях оказывается, что иммунитет «плохо знает
живопись» – не может эффективно и быстро отвечать на очищенные
антигены. Те же низкореактогенные «Пентаксим» и «Инфанрикс»
дают чуть меньшую иммуногенность к коклюшу по сравнению с
«кондовой» АКДС. Как же быть? Неужели возвращаться к
цельноклеточным вакцинам?
Но учёные такие люди, что если чего-то очень сильно захотят, то
обязательно сделают. Хотите сплит-вакцину, но с нормальной
иммуногенностью? Да легко: вот, мы взяли вместо настоящей
бактерии, сочащейся опасным липополисахаридом, похожее по
размерам «пугало» из частицы гидроксида алюминия и осадили на
него нужный антиген. Соединение алюминия в данном случае
усиливает реакцию иммунных клеток – является в отношении них
адьювантом. И ещё – таким же сильным раздражающим фактором
для антипрививочников, ведь это «соли тяжёлых металлов»,
«сплошной яд», «трАвите детей своими вакцинами».
Открою вам этот «глобальный заговор бигфармы» до конца – в
вакцинах, помимо алюминия, ещё могут содержаться соединения
ртути, другие консерванты и даже антибиотики. Но чтобы этим
отравиться, вам придётся «заколоться» сотнями доз вакцины за раз.
Даже скандально известный тиомерсал (мертиолят) – соль ртути,
использовавшаяся в качестве консерванта, чтобы предотвратить
загрязнение вакцин посторонней микрофлорой, – это водорастворимое
соединение. В отличие от ртути металлической, оно легко и
беспроблемно выводится из организма почками. Кроме того, в одной
дозе вакцины содержится всего порядка 50 микрограммов этого
соединения. Для сравнения, в стограммовой баночке тунца этого же
тиомерсала 16,5 микрограмма, а в одном кило варёных креветок – 27.
И никто не орёт: «Отравили народ своими креветками!». В конечном
итоге в детских вакцинах от тиомерсала пришлось отказаться, но
только из соображений «народоуспокоения», а не токсикологической
опасности.
Опасность могут представлять лишь те компоненты вакцин, на
которые у людей развивается аллергия – поскольку аллергические
реакции не дозозависимы, развиваются в ответ на любое количество
аллергена. Скажем, людям с аллергией на белок куриного яйца нельзя
колоть некоторые вакцины от гриппа, так как вирус подращивается на
клетках куриных зародышей, и следовые количества белка могут
присутствовать в готовом препарате. Но, во-первых, эти компоненты
указываются в составе, а в инструкции обязательно прописывается
применение с осторожностью или полное противопоказание
использования у людей с соответствующей (а не любой, как некоторые
думают) аллергией. Во-вторых, от одной инфекции зачастую
разработаны несколько вакцин, производимых по разным технологиям,
и в ряде случаев можно подобрать безопасную замену.
Успокоившись, вернёмся к конструированию вакцин. На сплитвакцинах учёные не остановились и некоторые белковые антигены
начали синтезировать искусственно. Но не химическим путём,
соединяя последовательно нужные аминокислоты (это очень сложно и
дорого), а хитрее – используя природные «белковые фабрики». Для
этого сначала ген, кодирующий интересующий нас белок, вырезают из
генома возбудителя. Затем вместе с геном-регулятором специальными
методами вносят в геном организма-продуцента – чаще всего
определённых видов дрожжей или в бактерию кишечную палочку. И
такой генно-модифицированный организм начинает синтезировать
чужой белок как свой собственный. Остаётся выделить его из среды
биореактора, очистить и приготовить вакцину. Например, так делают
многие современные вакцины против гепатита В.
Наконец, совсем недавно в арсенале медиков появились особые –
векторные – вакцины. На этот раз кодирующий антиген участок генома
вводят не в организм-продуцент, а в вирус, который должен будет
заразить клетки прививаемого человека. Если вы помните, как
действуют вирусы в живой клетке – они подчиняют себе её
белоксинтезирующий аппарат и производят на нём собственные белки.
Но у вакцинного вируса из генома предварительно удаляют те участки,
которые отвечают за копирование его самого – то есть он не
размножается, а значит, и не вызывает заболевание. Вся его роль
сводится к тому, чтобы доставить в клетки ген, кодирующий нужный
нам антигенный белок. Таким образом, он просто проводник,
«вектор», если угодно, «извозчик» для такого гена. Вот его-то и начнёт
транскрибировать наша клетка, синтезируя затем в своих рибосомах.
Но наш иммунитет не проведёшь, он распознает и уничтожит
зараженную даже таким «дефектным» вирусом клетку, а среди её
«потрохов» антигенпрезентирующие клетки найдут тот самый
антиген, который был доставлен вирусом-вектором. И, естественно,
понесут Т-лимфоцитам, чтобы те запустили весь дальнейший
механизм по приобретению иммунной памяти. Первую такую
серийную вакцину создали и применили российские учёные против
смертельно опасной лихорадки Эбола (вакцина Гам-Эвак-Комби была
испытана в Гвинее во время вспышки инфекции 2015 года), затем –
против COVID-19, препарат Гам-КОВИД-Вак (коммерческое название
«Спутник-Ви») и его модификации.
Зачем такая сложная «многоходовочка», спросите вы? Ведь выше
перечислено столько других методов – попроще. Затем, что не всегда
получается ранее отработанными методами получить нужный антиген.
Иногда «измордованный» нашими манипуляциями по выделению и
очистке антиген становится слишком непохож на свой «боевой»
прототип в составе возбудителя. Это как если бы полицейские
пытались найти преступника по описанию единственного свидетеля,
столкнувшегося с ним мельком в глубоких сумерках. А антиген,
синтезированный клеткой из «подсаженного» гена, – это уже как
фотография в 4К разрешении, один в один соответствует искомому.
Есть особый вид вакцин, которые формируют иммунитет против
экзотоксинов бактерий. Возбудителей таких токсикоинфекций
довольно много: мы уже упоминали дифтерию, ботулизм и столбняк,
говоря о реакциях преципитации их токсинов антителами. Поскольку
токсины бактерий – тоже антигены, то, будучи обработаны
определённым способом для утраты ядовитых свойств и введены в
организм, они вызывают специфический иммунитет. Такие препараты
получили название анатоксинов.
Уже упомянутая широко распространённая вакцина для детского
возраста – АКДС – как раз и расшифровывается «анатоксин
коклюшно-дифтерийно-столбнячный». Взрослым же раз в 10 лет, а
также при травмах, вводят отдельный «анатоксин столбнячный»
либо комбинированный «анатоксин диферийно-столбнячный» – АС,
АДС. А ранее привитым – АДС-М, где «М» указывает, что это
модифицированный препарат с пониженным содержанием антигена.
Однако нужно помнить, что образование антител и вообще
адаптивного иммунного ответа – процесс небыстрый. При инфекциях
с довольно длительным инкубационным периодом мы можем
позволить себе даже экстренную вакцинопрофилактику – введение
вакцины уже после так называемой экспозиции возбудителя, то есть
после того, как произошло инфицирование (или мы предполагаем с
высокой вероятностью, что оно произошло). Это возможно при
профилактике бешенства, вирусного гепатита А, ряда других
инфекций. Но всё же наиболее часто вакцину или анатоксин вводят
заблаговременно (профилактическая вакцинация), чтобы к моменту
возможного инфицирования (заражения, травмы, укуса бешеным
животным или инфицированным переносчиком) организм уже
выработал иммунитет.
Но иногда совсем нет возможности ждать. Либо возбудитель
слишком заразен, либо обстоятельства заражения предрасполагают к
быстрому прогрессированию инфекции (например, опасная
локализация укусов бешеным животным: близко к центральной
нервной системе – голова, шея, места обильной иннервации или
прохождения крупных нервов), либо возбудитель активно выделяет
токсины (при том же столбняке, дифтерии, ботулизме). Тогда нужно
срочно ввести в организм какое-то супер-оружие, способное быстро
подавить возбудитель и если не уничтожить, то хотя бы задержать на
время выработки собственного иммунитета.
Если мыслить логически, нам нужны либо клетки иммунной
системы, либо готовые антитела, уже «обученные» против
соответствующего возбудителя. Где их брать, в определённом смысле
понятно – и те, и другие всегда присутствуют в крови переболевших и
выживших людей. Но на клетки чужого организма иммунитет, скорее
всего, ответит так же, как и на инфекцию – атакует и уничтожит. А вот
содержащая антитела гипериммунная плазма от переболевших
людей первоначально была (и даже в наше время остаётся) таким
«супер-оружием».
Однако сразу большое количество переболевших людей обычно
можно найти только во время вспышки или эпидемии. Да и не очень
гуманно забирать часть богатой белком плазмы у только что
перенёсших болезнь ослабленных людей. Пробовали использовать для
этого животных, которым вводили небольшие дозы токсинов, а затем
отбирали содержащие антитела сыворотку или плазму крови – так до
сих готовят антирабический иммуноглобулин против того же
бешенства (лат. «рабиес» – бешенство) или против ядов змей
(механизм инактивации всех белковых биологических ядов работает
более-менее одинаково).
Однако
настоящий
прорыв
произошёл
с
открытием
моноклональных антител. Обычно пролиферирующий (делящийся)
В-лимфоцит живёт недолго. Но если в искусственной среде
совместить его с клеткой раковой опухоли, обладающей способностью
к безудержному делению, то можно получить гибридому – культуру
клеток, которая будет постоянно делиться и постоянно вырабатывать
антитела. А поскольку один В-лимфоцит, равно как и происходящие от
него в процессе пролиферации клоны могут производить только одни
определённые антитела, то их назвали моноклональными. Сейчас это
важный препарат в лечении как инфекций, так и онкологических
заболеваний (мы уже упоминали, что иммунитет играет очень важную
роль в борьбе с онкологией).
Препараты на основе готовых антител называют сыворотками или
иммуноглобулинами (в зависимости от степени очистки от других
белков и примесей). Вам же нужно хорошо запомнить их основное
отличие от вакцин: готовые антитела сывороток и иммуноглобулинов
работают быстро, но так же быстро выводятся из организма, а главное
– не запускают в организме иммунизированного адаптивный
иммунный ответ и, следовательно, не формируют иммунную память
об инфекции на будущее. Это пассивный иммунитет.
В целом группа перечисленных лечебных и профилактических
препаратов называется ИЛП (иммунобиологические лекарственные
препараты), а в более ранних источниках вам встретится МИБП –
медицинские иммунобиологические препараты, что одно и то же.
Таким образом, их классификация следующая:
1. сыворотки
2. анатоксины
3. вакцины, в т.ч.
3.1 живые ослабленные (атеннуированные)
3.2 убитые (инактивированные)
3.3 сплит-вакцины, генноинженерные, векторные и др.
Иммунитет – это сложная система защиты со множеством
компонентов, связей, «регуляторов» и «предохранителей». Порой даже
кажется, будто такая сложность вовсе не должна работать. И тем не
менее работает! Да настолько эффективно, что некоторыми
инфекциями мы болеем лишь раз, после чего формируется
пожизненный иммунитет. Собственно говоря, даже одним и тем же
гриппом мы болеем лишь раз в жизни, а периодические эпидемии этот
вирус вызывает из-за мутаций, меняющих структуру его антигенов, а
не из-за несовершенства нашего иммунитета.
Тем более странными в свете сказанного кажутся заявления
отдельных «специалистов» и общественных деятелей, имеющих
«альтернативные»
взгляды
на
укрепление
иммунитета
и
вакцинопрофилактику инфекционных болезней. Чаще всего они ещё и
козыряют регалиями и званиями, пытаясь таким образом придать
дополнительный вес своей, мягко говоря, спорной точке зрения. Не
стоит забывать, что пресловутая «успешность» или профессорское
звание, если только оно получено не за исследования иммунитета,
никак не характеризуют уровень знаний человека в конкретной
области – в частности, в области иммунологии. Банально невозможно
знать всё – а в медицине невозможно в особенности. Порой мне
кажется, что между, скажем, физиками (ядерщиком и специалистом по
физике твёрдого тела, например) и то меньше разницы, чем между
двумя любыми медицинскими специальностями. Потому что законы
физики неизменны во всей Вселенной, а в медицине слово «закон»
применяется с большой осторожностью и множеством оговорок.
Банальных заблуждений даже среди сторонников прививок тоже
хватает. Недавно, например, довелось услышать весьма интересное
народное измышление (перед началом вакцинальной кампании против
гриппа): мол, вы колоться не торопитесь, а то до весны иммунитета не
хватит. То есть у некоторых обывателей бытует мнение, что прививка –
это такой защитный кокон, да ещё и с ограниченным сроком годности.
Села батарейка – и всё, аллес.
«Ноги» этого заблуждения, похоже, растут из иммунопрофилактики
ряда инфекций, которые действительно требуют ревакцинации –
периодического повторения прививки. Я уже упоминал, что против
дифтерии и столбняка взрослые должны ревакцинироваться каждые 10
лет (против гриппа, кстати, ежегодно проводится не ревакцинация, а
мы именно что вакцинируемся заново – ведь набор антигенов
противогриппозной вакцины меняется в зависимости от ожидаемых
штаммов вируса). Но, конечно же, прививка – это не защитный барьер.
Её компоненты не убивают вирусы и бактерии «на подлёте». Если
возбудитель инфекции добрался до человека, то инфекционный
процесс неизбежно запустится. А вот разовьётся ли он в заболевание,
зависит от того, кто победит в гонке внутри организма – размножение
возбудителя или активация иммунитета, который его подавит.
Прививка, как вы уже поняли из сказанного выше, предназначена
для того, чтобы «обучить» наш иммунитет, а ещё показать ему «образ
врага» заранее – до встречи с реальным возбудителем. Тогда активация
иммунитета происходит быстрее, а иммунный ответ будет более
мощным. Как мы теперь можем сказать в научных терминах:
у привитого человека встреча с возбудителем вызывает сразу
вторичный иммунный ответ. А значит, шансы победить инфекцию в
«гонке на выживание» внутри организма резко возрастают.
Стоп! Но мы же не ответили на вопрос: почему одни прививки
делают раз в жизни, а другие – с регулярной периодичностью? Здесь
как в жизни – «образ» микроба, который вакцина показала нашему
иммунитету, со временем может «забываться», да и сам микроб с
течением времени может всё меньше походить на свою «фотографию»
10-летней давности. Иначе говоря – возбудители могут мутировать и за
счёт этого ускользать от внимания ранее сформированного
иммунитета.
Это уже зависит от свойств конкретного возбудителя. Так, РНК-овые
вирусы обычно достаточно изменчивые, скорость мутаций у них
высока. Поэтому против COVID-19 приходилось делать ревакцинации
каждые полгода–год. В то же время вирус-возбудитель кори тоже
содержит в своей основе РНК, но он достаточно стабилен (вы,
наверное, уже поняли, что в медицине и биологии нет универсальных
правил – слишком велико разнообразие живого). Поэтому от кори
достаточно всего двух введений вакцины: основного и «бустера»
с интервалом не менее чем в 3 месяца (а бывает, что одна прививка
сделана в детстве, а вторую почему-то «забыли»; тогда достаточно
сделать второе введение – и всё, не нужно снова начинать полный
курс).
Кроме того, в разные периоды жизни человека риск некоторых
инфекций повышен, а к другим восприимчивы все возрастные группы.
Поэтому детей прививают препаратом АКДС, а взрослых
ревакцинируют уже АДС-М, лишённой коклюшного компонента,
поскольку к коклюшу взрослые маловосприимчивы. А вот против
бактерии пневмококка (которая не только пневмонии вызывает,
вопреки всеобщему мнению, но и воспаления среднего уха, и даже
оболочек головного мозга – менингит, в некоторых случаях) в
основном прививают детей и пожилых граждан, хотя и некоторые
другие категории подлежат вакцинации – либо потому, что у них
высокий риск инфицирования (медики, педагоги, соцработники), либо
из-за того, что, получив инфекцию, они с высокой вероятностью
перенесут её тяжело (например, страдающие бронхиальной астмой и
другими хроническими болезнями органов дыхания). А ещё против
пневмококка существуют два типа вакцин: конъюгированные (типа
«Превенар-13») и полисахаридные («Пневмо-23»). Для полноценного
иммунитета желательно иметь обе (они ещё охватывают и разное
число штаммов возбудителя – обозначено цифрами в названии
вакцины), но есть нюанс: дети раннего возраста практически не
отвечают выработкой иммунитета на введение полисахаридных
вакцин. Поэтому курс иммунизации им начинают с вакцин
конъюгированных.
К большому сожалению, расскать о нюансах применения всех
вакцинных препаратов в рамках этой книги нет возможности. Об этом
написаны
специальные
справочники,
предназначенные
для
медработников – чтобы их читать и применять, требуются достаточно
серьёзный базовый уровень знаний и определённый опыт работы. Да
ещё нормативная база и подходы к вакцинопрофилактике
периодически изменяются, уходят одни вакцины и появляются новые –
поэтому медработники, проводящие вакцинацию, регулярно проходят
дополнительное обучение, слушают семинары и лекции.
Но иногда возникают настолько сложные ситуации, что даже
фельдшер или врач (медсёстры не могут давать допуск к прививке,
только вводят препарат по уже сделанному назначению) понимает, что
его знаний недостаточно. На этот случай при каждой поликлинике (в
крайнем случае – при головном медицинском учреждении города или
района) формируется иммунологическая комиссия из наиболее
опытных специалистов. Их курирует региональная иммунологическая
комиссия, создаваемая обычно при детской республиканской больнице
или другом крупном клиническом учреждении здравоохранения. В
региональную комиссию уже входят не только врачи, но и юристы, и
организаторы здравоохранения. Поэтому со всеми сложными
вопросами относительно прививок нужно в первую очередь
обращаться именно туда.
Глава 10. Ах ты, плесень!
Я уже говорил в первой главе этой книги, что на вопрос о микробах
студенты обычно первыми называют бактерии и вирусы.
Действительно, они представляют серьёзный интерес, однако и грибы
не нужно сбрасывать со счетов. Прежде всего потому, что их значение
в жизни людей не исчерпывается только медицинским аспектом, а
медицинский – не заканчивается на их роли как патогена.
В подкрепление этих слов попробуем перечислить разнообразные
значения грибов в природе и жизни человека:
могут являться патогенами человека, причём спектр вызываемых
ими заболеваний далеко не исчерпывается одними поражениями кожи
и ногтей;
могут быть патогенами животных – самых разных животных, от
кошечек-собачек и вплоть до насекомых, включая сельхозвредителей, а
это свойство уже можно применять в народном хозяйстве;
могут быть патогенами растений (фитопатогенами), то есть уже
сами являться вредителями – и не просто повреждать урожай, но и
выделять ядовитые вещества, накапливающиеся в пищевом сырье
(микотоксины);
в то же время некоторые фитопатогены могут синтезировать и
полезные для человека вещества – например, уд, используемый в
парфюмерном производстве;
могут выделять особые вещества для защиты себя от бактерий –
большинство из них можно выделить и использовать в качестве
антибиотиков (типичный пример – пенициллин, изначально
полученный из культуры плесневого гриба рода пенициллиум);
являются важными продуцентами в области биотехнологии – генномодифицированные дрожжи, например, используют для создания
вакцин (мы не раз упоминали об этом раньше);
продукты биохимии грибов и даже сам их мицелий можно
использовать как материал для промышленности вместо пластиков и
синтетических тканей;
могут вызывать аллергии – споры плесеней являются одним из
распространённых и сильных аллергенов человека;
грибы используют в пищевом производстве – те же дрожжи, к
примеру, – они важный компонент в сыроварении, виноделии и т. п.
А ещё мы не упомянули о грибах как объекте «тихой охоты»
в осеннем лесу – возможно, скажете вы. Но не упомянули правильно –
ведь, говоря о грибах, мы фактически подразумевали лишь те из них,
которые в обиходе называют «грибками», то есть дрожжи или плесени.
Но микробиологи такого термина, как «грибки», не приемлют –
царство Fungi (лат.) или Mycota (греч.) в русском языке имеет
терминологический эквивалент «грибы» независимо от размеров и
числа клеток самого гриба. Просто они делятся на микроскопические
микромицеты и образующие плодовые тела макромицеты (те самые
опята, рыжики, мухоморы, трюфели и прочие съедобные и не очень
«дары леса»).
Но микробиологи себе такое могут позволить, поскольку объекты
их внимания весьма молчаливы, а вот клиническим медикам
приходится постоянно общаться с пациентами, и попробуй скажи,
что болезнь пациента вызвана грибом – тот жалобу в Минздрав тут
же накатает, мол, пришёл с лишаём, а в карточке написали, что
грибами отравился. Поэтому у дерматологов и инфекционистов
применимы такие термины, как «грибковое поражение кожи»,
«противогрибковый препарат» и т. п.
Справедливости ради нужно ещё упомянуть, что к царству грибов
относится и обширная группа «грибоподобных организмов», в
частности оомицеты, куда входит, например, возбудитель фитофтороза
картофеля, и миксомицеты (слизевики).
В
последнее
время
классификация
грибов
настолько
переусложнилась, что сами микологи теряются, кого куда относить.
А учитывая, что микология в целом до сих пор входит в группу
ботанических наук, так как изначально грибы считали растениями,
то можете представить, какая там царит путаница.
Мы же в дальнейшем будем говорить именно о микроскопических
грибах. И для начала бегло познакомимся с их строением.
Внешне клетки грибов напоминают бактериальные. Та же
цитоплазма, окружённая мембраной, та же клеточная стенка. Однако
сходство это обманчивое. Во-первых, грибы, в отличие от бактерий,
являются эукариотами – то есть в их клетках имеется ядро с
ядрышком. Генетический материал грибов уже собран в полноценные
хромосомы: геном разных видов грибов включает их от 2 до 28.
Благодаря этому многие грибы способны не только к бесполому
копированию себя из поколения в поколение, как бактерии, но и к
половому размножению с обменом генов, что резко повышает их
способности к приспособляемости в окружающей среде.
Состав органелл гриба тоже гораздо более богатый и напоминает
таковой у растительной клетки: они содержат эукариотические 80Sрибосомы, связанные с шероховатым эндоплазматическим
ретикулумом, аппарат Гольджи (пусть и слаборазвитый),
митохондрии.
Митохондрии в клетках эукариот выполняют функции выработки
АТФ – аденозинтрифосфата, который обеспечивает энергией все
биохимические процессы в клетке. Поэтому митохондрии часто
называют живыми электростанциями клетки. Интересно, что когда-то
эти органеллы были свободноживущими микроорганизмами. Но
будучи поглощены предками аэробных организмов, которые почемуто их не переварили, а вошли в симбиоз, стали обеспечивать
последних энергией. Происходило это за счёт окисления органических
субстратов молекулой кислорода. То есть симбиоз прокариот на заре
развития жизни привёл к появлению всех дышащих кислородом
существ, включая и нас с вами. А сами симбионты настолько
«привыкли» жить за счёт клеток-хозяев, что полностью отказались от
самостоятельного свободного проживания. Эту гипотеза подтверждает
то, что митохондрии имеют собственный геном в виде кольцевой
молекулы ДНК (так же организован геном бактерий) и рибосомы,
сходные с 70S-рибосомами прокариот.
А вот пластид, то есть хлоропластов, у грибов нет, поэтому они не
обладают способностью к фотосинтезу и вообще – к автотрофному
питанию. Грибы – типичные гетеротрофы (подробнее о типах
питания смотрите в материале по экологии микроорганизмов), однако
всасывают они органические вещества и воду всей поверхностью
клетки, как это делают бактерии и растения.
Гранулы запасных питательных веществ у грибов состоят не из
крахмала, как у растений, а в основном представлены гликогеном –
так же, как в клетках животных, например, в наших мышцах и печени.
А клеточная стенка грибов вместо пептидогликана зачастую сложена
из полимера хитина – такой же составляет основу жёсткого покрова
насекомых.
Наконец, грибы обладают ещё одним очень важным свойством. Если
бактерии способны образовывать сообщества и биоплёнки, но всё-таки
никогда не переходят рубеж к полноценному многоклеточному
существованию, то грибы – многоклеточные организмы. Да,
дрожжеподобные виды могут существовать в формате отдельных
клеток, но даже они склонны расти группами, образуя псевдомицелий
(см. ниже).
В то же время это не исключает того факта, что колонии многих
грибов по своей организации напоминают синцитий – одну огромную
многоядерную клетку с общей цитоплазмой.
Как видите, у грибов есть целый ряд признаков, которые роднят их
как с животными, так и с растениями и бактериями. Однако сочетание
этих свойств таково, что грибы слагают отдельное царство живой
природы. Поэтому, в частности, большинство антибиотиков на грибы
не действует: для них просто нет подходящих «мишеней» в клетке
гриба.
Также грибы образуют споры. Но если у бактерий это была
внутриклеточная структура, способствующая выживанию, то у грибов
она образуется в результате полового или бесполого деления клетки
(мейоза или митоза соответственно), однако не любой, а, как правило,
клеток специальных структур – спорангий и конидий. Отделяясь от
них, лёгкие споры грибов распространяются с потоком воды или по
воздуху. Таким образом, они служат половому размножению или
расселению грибов, или тому и другому одновременно. Споры грибов,
как и бактериальные, очень устойчивы к неблагоприятному внешнему
воздействию, включая высокие температуры. Это представляет
определённую проблему для дезинфекции при грибковых инфекциях
и для стерилизации медицинских инструментов и инвентаря.
Попадая в благоприятные условия среды, спора прорастает в клетку,
в результате деления которой образуется грибной мицелий. Эти
вытянутые клетки, похожие на тонкие ветвящиеся нити, грибы
формируют для колонизации максимально доступного количества
субстрата (среды обитания и питания), а также для увеличения
всасывательной поверхности.
Мицелий макромицетов (то есть «настоящих», «больших» грибов)
вам известен под названием грибницы. Наверняка опытные грибники
объясняли вам, что плодовые тела грибов нужно не вырывать, а
срезать ножом, чтобы не повреждать находящуюся в земле грибницу,
распространяющуюся порой на сотни квадратных метров. Так что,
обнаружив грибное место на лесной поляне, вы, вероятнее всего,
видите один единый организм, а точнее, пардон, его половые органы,
так как именно на пластинках шляпок и располагаются споры грибов.
Споры какого-нибудь опёнка без микроскопа не разглядеть, но если
вам приходилось встречать высохшие плодовые тела грибов
дождевиков, в обиходе называемых «дедушкин табак» за способность
при раздавливании давать характерное облако «дыма», то знайте – этот
«дым» и есть мельчайшие грибные споры.
Тонкие вытянутые клетки мицелия составляют гифы гриба. Клетки
гиф могут делиться по-разному. У так называемых высших грибов
они разделяются на полноценные самостоятельные клетки, оставаясь
связанными только в узком месте контакта, но и там их разделяют
перегородки клеточных стенок – такой мицелий называют
септированным (от лат. «септа» – перегородка). У некоторых видов,
правда, эти септы пронизаны каналами, через которые цитоплазма
одной клетки сообщается с другой. Однако другие – низшие — грибы
не озадачиваются такими условностями, и у них фактически делится
только ядро. То есть их мицелий, по сути, представляет собой одну
клетку со множеством ядер – синцитий. Можно сказать, что в этом
смысле грибы являются своеобразной переходной формой между
одноклеточными и многоклеточными организмами. А нас это
интересует прежде всего с точки зрения идентификации грибов, в
которой микроскопия имеет гораздо большее значение, чем при
идентификации бактерий. Там, если вы помните, мы полагались скорее
на биохимию и физиологию.
Мицелий, который вырастает из субстрата наружу, мы можем видеть
как налёт на поверхности. А у таких родов, как мукор, он и вовсе
образует выраженный «пушок». У одних видов он белый, у других
окрашен в жёлтый, зелёный цвета. В благородных видах сыров
плесень образует сине-зелёные прожилки. А аспергилл для защиты от
ультрафиолета вырабатывает чёрный пигмент меланин – пятна такого
чёрного налёта вы наверняка видели на стенах сырых помещений:
подвалов, санузлов и т. п. И возможно, не догадывались, что почти
такой же меланин предохраняет от солнечных ожогов клетки нашей
собственной кожи, образуя на ней красивый загар. Так что в известной
степени мы тоже «грибы».
Такой видимый мицелий, выступающий наружу, как раз и несёт на
концах гиф спорангии (специальный орган размножения с
образующимися внутри спорами) или конидии (специализированный
участок на конце гифа, где споры формируются за счёт его
септирования и свободно отделяются наружу). То есть он служит для
размножения и расселения гриба, поэтому называется генеративным
(от лат «генус» – род), а иногда ещё воздушным или репродуктивным.
Но иногда генеративный мицелий грибов приобретает весьма
специфический вид. Например, спорынья – гриб, паразитирующий на
колосьях злаков – формирует на них выросты (склероции),
напоминающие по форме рог или отросток-шпору на лапках
некоторых птиц. Пока не будем уходить от темы, но ниже мы к
спорынье обязательно вернёмся.
При этом совершенные грибы могут образовывать половые споры
в результате мейотического деления клеток – к этой группе относятся
такие отделы царства грибов, как аскомицеты, базидиомицеты и
зигомицеты. Дейтеромицеты так не могут и расселяются только за счёт
митотических спор, а потому относятся к несовершенным грибам.
Со строением гиф эта особенность не соотносится:
дейтеромицеты, скажем, несовершенные, но высшие грибы – у них
мицелий септированный, разделённый перегородками. В то время как
у размножающихся половыми спорами зигомицет септы
отсутствуют – они совершенные низшие грибы.
Органы спороношения устроены совершенно по-разному у разных
типов (отделов царства) грибов. У аскомицетов, например, спорангии
образуют компактные «аски» – от греч. «сумка». Конидии могут быть
собраны в характерные «метёлки» (род пенициллиум), словно
льющаяся из лейки вода, а могут напоминать детский рисунок
солнышка с лучами (род мукор). Все эти особенности тоже изучаются
при микроскопии и используются для идентификации грибов.
Помимо видимого на поверхности генеративного мицелия, та его
часть, которая скрыта в толще субстрата, называется мицелием
вегетативным (от лат «вегетатио» – расти). Он служит для
всасывания воды и питательных веществ, являясь аналогом корневой
системы растений (строго говоря, грибница макромицетов – это
именно вегетативный мицелий).
Однако способность образовывать гифы – нити мицелия – присуща
только мицелиальным (по-другому – плесневым или гифальным)
грибам. Другая группа грибов – дрожжи – являются одноклеточными
организмами: они делятся наподобие бактерий. И хотя их клетки не
отходят далеко друг от друга и даже могут иметь более или менее
вытянутую форму, но разрастания клеток дрожжей представляют
собой псевдомицелий.
Долгое время простое и понятное деление на дрожжевые и
мицелиальные (плесневые) грибы было общепризнанным в
микологии. Но всё-таки учёные подозревали, что в чём-то грибы нас
обманывают.
Так, ещё в конце XIX века был выделен дрожжевой гриб
питироспорум (типовой вид – питироспорум овале), который уверенно
связали с такой неприятной дерматологической проблемой, как
перхоть. Он же вызывал и себорею (собственно, перхоть и есть
начальная стадия себорейного дерматита). Но иногда его находили и
при разноцветном лишае. А иногда – у здоровых людей, не
страдающих кожными заболеваниями. В то же время учёным был
известен и другой патоген кожи – гифальный гриб малассезия,
который как раз и считали возбудителем разноцветного лишая. Но при
этом он встречался у страдающих себореей тоже. Уже тогда
находились такие исследователи, которые говорили: да это один и тот
же гриб! Им, мягко говоря, не очень верили, потому что под
микроскопом это морфологически совершенно разные организмы. А
на имевшихся тогда питательных средах эти грибы росли очень плохо,
если вообще росли. В общем, малассезия-питироспорум морочила
всем голову как те меняющие цвет осьминожки из мультика, пока не
были усовершенствованы методики культивирования грибов. Тогда и
было окончательно продемонстрировано: условно-патогенный гриб
малассезия (два основных вида – фурфур и глобоза) в дрожжевой
форме в норме живёт на коже волосистой части головы, а при
избыточном размножении может быть одним из факторов появления
перхоти и развития себорейного дерматита. Но если баланс факторов,
сдерживающих развитие грибов на поверхности кожи, меняется не в
пользу организма ещё сильнее (стресс, иммунодефицит и т. п.), то
малассезия словно оборотень меняет облик, переходит в патогенную
гифальную форму и запускает мицелий в кожу человека. В гифальной
форме она вызывает разноцветный лишай и малассезиозный
фолликулит. Вот и получается, что при описании одних и тех же
заболеваний встречается то название питироспорум овале, то – в
другом источнике – малассезия фурфур, и поди разберись, что это один
и тот же микроорганизм.
То есть среди грибов есть такие, которые в разных фазах
жизненного цикла могут существовать или в дрожжевой, или в
плесневой (гифальной) форме. За такую двойственность облика их
назвали диморфными грибами (лат. «ди» – два, двойной и
«морфос» – форма). Мало того, некоторые грибы настолько привыкли
проживать в какой-то одной форме, что, генетически являясь
диморфами, фактически никогда свой диморфизм не проявляют. Либо,
как вариант, в какой-то из этих фаз не растут на питательных средах, а
потому методом посева нельзя доказать их двойственную природу. Тут,
чтобы окончательно определиться, к какой группе отнести гриб, на
помощь микологам приходят генетики.
Таким образом, окончательная классификация микромицет
включает:
Дрожжевые грибы
Мицелиальные (плесневые или гифальные) грибы
Диморфные грибы
Сложно? А представьте, как от всего этого «грибозоопарка»
приходится обороняться нашему иммунитету! Мы ведь уже
упомянули, что грибы могут вызывать заболевания. Причём если
вспомнить, что разные виды лишая поражают не только человека, но и
животных, да ещё добавить сюда спорынью из начала главы, то
окажется, что грибы держат в страхе все другие царства живой
природы. Они, правда, не паразитируют на бактериях, но настолько
жёстко конкурируют с ними за сходные экологические ниши, что
практически никогда не уживаются друг с другом. Да ещё и не
гнушаются в этой борьбе никакими методами, включая и химическую
войну. Это к тому, что грибы выделяют антибиотики –
целенаправленное оружие против бактерий.
Инфекционные заболевания, вызываемые грибами, имеют общее
название микозы. Как вы, наверное, уже понимаете, применимо оно и
к людям, и к животным, и в какой-то степени даже к растениям. Во
всяком
случае,
сами
патогенные
грибы,
помимо
всех
вышеперечисленных классификаций, делят на:
антропопатогенные (другое название – антропофильные, от лат.
«антропос» – человек, и «филюс» – любовь), то есть патогены
человека;
зоопатогенные (зоофильные), вызывающие болезни животных
(греч. «зоа» – зверь), причём внутри группы зоопатогенные грибы
делятся конкретно на патогены теплокровных животных, патогены
насекомых (энтомопатогенные грибы) и т. п.;
фитопатогенные – патогены растений.
Ещё совсем недавно считалось, что фитопатогенные грибы не могут
поражать представителей других царств живой природы, но буквально
недавно один инцидент в Индии ещё раз доказал, что в медицине
«никогда не говори «никогда». Грибок хондостереум, вызывающий
заболевание растений «серебристый лист», вызвал заболевание
дыхательной системы у человека. Немного подробнее об этом я
расскажу в конце книги, в главе о редких и самых опасных инфекциях.
Но пока это единственный случай, и гораздо больше проблем
доставляют общие патогенные грибы человека и теплокровных
животных, называемые зооантропофильными. Много кому в детском
возрасте пришлось испытать это на себе, заработав стригущий лишай
(микроспорию).
А вот энтомопатогенные грибы для человека могут быть даже
полезны: например, они помогают бороться с опаснейшим вредителем
медоносных пчёл – клещом варроа. Этот мелкий (для нас, на пчелином
тельце он смотрится весьма крупным) паразит забирается в ульи,
переживает период спячки и размножения внутри ячеек с личинками
пчёл и может в короткие сроки выкосить целую пасеку. Но стоит
обработать ульи биопрепаратами, содержащими патогенные для
варроа микроскопические грибы, как уже сами клещи начинают
хиреть и вымирать.
Из другого фитопатогена – кордицепса – получают мощный
цитостатик циклоспорин, применяемый при пересадке органов.
Кордицепс же активно применяют в китайской народной медицине,
хотя приписываемое ему там тонизирующее и омолаживающее
действие научно не доказано. Но особенно интересен жизненный цикл
некоторых видов этого паразита: так, легчайшие споры кордицепса
однобокого прорастают, когда достигают своей жертвы – рабочего
муравья. Внутри его тела мицелий гриба за 2–3 недели создаёт
собственную параллельную нервную систему, перехватывая
управление поведением насекомого. Спустя этот «инкубационный
период» муравей покидает свою колонию, поднимается наверх по
растению и закрепляется здесь, вцепившись челюстями в центральную
жилку листа, после чего погибает. Гриб-паразит продолжает некоторое
время развиваться под защитой его покровов, а затем из них
прорастает спорангий, рассевающий споры, в том числе на других
муравьев этой же колонии. Такой способ превращения жертв в
управляемого паразитом «зомби» не мог оставить равнодушными
писателей-фантастов и сценаристов: кордицепс фигурирует как
причина зомби-апокалипсиса в играх серии The Last of Us, книге М.
Кэри «Дары Пандоры» и снятом по его мотивам фильме «Новая эра Z»
(Великобритания, 2016 г.).
Название микоза обычно образуется путём прибавления суффикса
-оз к родовому названию возбудителя. Так, кандида альбиканс
вызывает кандидоз, криптококкус неоформанс – криптококкоз, а уже
упомянутая малассезия – малассезиоз. Приведённый способ
образования номенклатуры заболеваний, вызванных грибами, является
универсальным. Однако бывают и «отклонения» от него: те же
микроспория и трихофития.
Кроме того, у клиницистов-дерматологов очень часто в ходу
традиционные названия микозов (возможно, потому, что они более
понятны и знакомы пациентам, а значит, не так пугают): например,
кандидоз слизистых известен под названием «молочница», проявления
малассезиоза будут расценивать как себорею или разноцветный лишай
(в зависимости от симптомов), а трихофития и микроспория
объединяются под общим названием «стригущий лишай».
Врачи-клиницисты и классификацию микозов предпочитают иную:
основанную не на эпидемиологической характеристике, а на глубине
поражения организма, которая будет определять симптоматику и
принципы лечения.
Так, кератомикозы поражают только ороговевающий слой кожи.
Здесь, на поверхности нашего тела присутствует так называемый
мантийный слой, состоящий из секрета потовых и сальных желёз,
слущенных клеток эпителия и т. п. Мантия кожи имеет кислую
реакцию, а кроме того, насыщена противомикробными веществами и
иммуноглобулинами класса А. Всё это задерживает рост основных
конкурентов грибов – бактерий. Помимо орогевевающего эпителия,
кератомикозы поражают и его производные – волосы и ногти.
Под слоем кератиновых чешуек, как вам, вероятно, известно,
находится собственно живой слой кожи – дерма. Это уже полигон для
атаки возбудителей дерматофитий. Кератомикозы и дерматофитии
объединяют под общим названием поверхностных микозов. Есть ещё
глубокие или системные микозы, которые часто являются маркером
иммунодефицитных состояний, поскольку безнаказано «разгуливать»
по здоровому организму грибы не могут. Генетические заболевания,
ВИЧ-инфекция, препараты, подавляющие иммунитет у людей с
пересаженными
органами
или
необходимость
принимать
гормональные противовоспалительные средства – всё это
предрасполагающие факторы для микозов, в том числе глубоких. И
кандидозов тоже – последние стоят как бы посередине, будучи
способными и вызывать поверхностные процессы вроде той же
«молочницы», и распространяться вглубь организма, если иммунитет
их по какой-то причине «проворонил».
Поверхностные микозы, как правило, распространяются через
контактный механизм передачи – либо непосредственно от
источника к заражаемому организму, либо опосредованно, через
предметы обихода и обстановки. Так, при зоонозной микроспории
источником являются домашние и бродячие животные: кошки, собаки
и т. п. Хотя микроспорией могут болеть и другие звери – только на
территории нашей страны известно около 30–40 возбудителей,
поражающих разных животных и человека.
Зоонозной микроспорией люди заражаются на протяжении всего
года, однако чёткие подъёмы заболеваемости характерны весной и
осенью. Это связано с появлением в эти периоды потомства у
животных, а детёныши более восприимчивы к заражению
возбудителями «стригущего лишая». У людей особенность та же самая
– дети, не обладающие ещё достаточным иммунитетом, заражаются от
котят и щеночков чаще взрослых.
Диагностика, как правило, основывается на клинической картине и
некоторых дополнительных методах исследования. Так, очаги
микроспории выглядят достаточно характерно: на гладкой коже это
округлые пятна 1–1,5 см в диаметре, с более бледным центром и
гиперемированной периферией (красно-розовой – вследствие прилива
крови через расширенные сосуды очага воспаления). Локализуются
они у детей старшего возраста и взрослых обычно на коже ладоней,
предплечий и голеней – проще говоря, там, где тёрся больной котик
или собачка (у них клинически заболевание выражено не всегда, но
при этом они остаются источником инфекции). У грудных детей,
ползающих по полу, очаги могут располагаться на ножках, животике,
ладошках и т. п., куда попадают заражённые частички волос и кожи
источника.
На волосистой части головы образуются такие же округлые пятна,
внутри которых обламываются волосы, оставляя участки, будто
состриженные под корень – отсюда и происходит название группы
заболеваний. При зоонозных микроспориях заразившийся человек
может передать стригущий лишай другому человеку точно так же, как
и при антропонозных. Поэтому независимо от вида возбудителя одной
из важных мер профилактики стригущего лишая является соблюдение
элементарной личной гигиены. Не следует одалживать кому-то свою
расчёску, одежду, головные уборы (шапки, косынки, банданы). В
особенности эти правила поведения нужно привить своим детям /
младшим братишкам или сестрёнкам, поскольку школьники и
садиковые дети очень любят примерять одежду друг друга.
Одни виды грибов, поражающие волосы, растут только внутри
стержня – эндотрихиально, другие образуют вокруг волоса чехол из
мицелия (перитрихиальное расположение). Это можно видеть при
микроскопии обломков волос и чешуек кожи. Для такого исследования
предметным стеклом делается соскоб с поражённого участка, затем на
полученный биоматериал капают раствором щёлочи, которая
растворяет остатки клеток кожи, но которой «не по зубам» клетки
гриба. Затем препарат рассматривают под микроскопом, отыскивая
характерные споры и мицелий.
Однако для постановки ориентировочного диагноза, а также когда
ещё нет видимых очагов поражения, используют иной метод – осмотр
кожи в ультрафиолетовом свете. Проводится такой осмотр в
помещении без окон и с минимальной подсветкой, так называемой
«тёмной комнате». Медработник направляет на кожные покровы и
волосистую часть головы пациента специальный прибор – так
называемую лампу «чёрного света» или «лампу Вуда». Несмотря на
загадочное название, к африканскому зомби-культу вуду она не имеет
ни малейшего отношения, разработал её американский физик Роберт
Вуд, а лампой «чёрного света» она называется потому, что покрыта
слоем чёрного люминофора, практически не пропускающего видимый
свет. Зато лампа Вуда излучает невидимый «мягкий» ультрафиолет (в
отличие
от
коротковолнового
«жёсткого»
ультрафиолета,
используемого в кварцевых и бактерицидных лампах).
Споры ряда грибов часто обладают свойством люминесцировать
под действием такого ультрафиолета (излучать свет в ответ на
освещение внешним источником излучения). Однако только споры
возбудителей стригущего лишая дают характерный люминесцентный
отсвет зелёного цвета. Чтобы не ошибиться, медицинские лампы Вуда
часто снабжены контрольным светодиодом того же оттенка.
Несколько слов о профилактике мы уже сказали, но как избежать
распространения инфекции в уже состоявшемся очаге, когда заболел
один из членов семьи, например? Так же, как и при всех других
инфекциях, следуя тактике воздействия на разные звенья
эпидпроцесса. К сожалению, против грибковых инфекций не
существует прививок, поэтому «третьему звену» в лице
контактирующих с заражённым можно порекомендовать только не
подрывать свой иммунитет стрессовыми и другими неблагополучными
воздействиями. Основные противоэпидемические мероприятия в
очаге микроспории будут направлены на источник инфекции и
механизм передачи возбудителя.
Источник нужно лечить, и при возможности на время лечения
изолировать. Либо в очаге, либо вообще удалить из очага. Больного
котика можно сослать в деревню или временно выселить на двор. С
детьми сложнее, но они, если не совсем маленькие, могут сами болееменее соблюдать меры гигиены. Хотя, если заболевает ребёнок в
интернате или приюте, всё равно придётся решать вопрос о
госпитализации, иначе велика вероятность вспышки микроспории в
этом учреждении. Детей, посещающих обычные школы и сады, на
время болезни отстраняют от занятий.
Для
лечения
существуют
противогрибковые
(иначе
–
антимикотические) препараты. Их не так много, в отличие от тех же
антибиотиков.
Обычно выделяют 6 групп препаратов по химическому строению:
1. Полиеновые антибиотики (нистатин, леворин, амфотерицин В и
др.) – они связываются с эргостеролом клеточной мембраны грибов,
нарушая её синтез и в конечном итоге приводя к лизису. Образно
говоря, содержимое грибковой клетки вываливается наружу из прорех
её внешней оболочки. Антибиотиками данную группу называют по
двум причинам: они имеют природное происхождение (их
синтезируют представители особых групп бактерий – актиномицеты и
стрептомицеты, удивительно, но эти бактерии сами по строению
напоминают грибы) и некоторые из них активны в отношении
бактерий (нистатин, например).
2. Производные имидазола (кетоконазол, клотримазол и др.).
3. Производные триазола (флуконазол и др.) – эти две группы
наиболее часто применяют для лечения поверхностных кандидозов
(«молочницы»).
4. Аллиламины (тербинафин, нафтифин и др.) – действующее
вещество препаратов «Микодерил» и «Экзодерил». Чаще всего против
стригущего лишая применяют как раз аллиламины и имидазолы.
5. Эхинокандины (каспофунгин).
6. Препараты разных химических групп (гризеофульвин и др.).
В клинической практике поступают проще: там антимикотики делят
на 3 группы. Одни для лечения глубоких микозов, другие – против
кандидозов, третья группа – для лечения дерматофитий.
Если вернуться к стригущему лишаю, то очаги поражения на голове
часто закрывают косынкой, чтобы уменьшить распространение по
помещению зараженных грибом обломков волос и чешуек кожи.
Ношеную косынку и другую одежду замачивают с раствором уксусной
кислоты или дезинфицирующего средства. После стирки (естественно,
отдельно от других вещей) ещё влажные вещи проглаживают горячим
утюгом. Так же с дезинфектантами нужно проводить частую влажную
уборку помещения. На период лечения из комнаты, где находится
больной, убирают ковры, паласы и мягкие игрушки. О том, что ему не
стоит во время болезни посиживать на одном мягком диване с другими
членами семьи, наверное, говорить не стóит?
Но как быть с той мягкой мебелью, которая всё же была в комнате
больного, с его верхней одеждой, постелью? Всё, что более-менее
укладывается по габаритам в объёме примерно с камеру большого
холодильника, можно обработать горячим паром. Именно такой размер
имеют паровые камеры на шасси автомобиля. Например, ДА-10,
размещаемая на шасси УАЗа-«буханки». Есть и камеры побольше,
устанавливаемые на грузовики: их используют, когда проводят
обработку большого объёма вещей в учреждениях с закрытым
режимом работы – пансионатов, приютов, интернатов, домов
престарелых и т. п.
В таких камерах можно обрабатывать ковры, одежду, постельные
принадлежности, мягкие игрушки. Всё, что в камеру не поместится,
придётся обрабатывать раствором дезинфицирующего средства в
противогрибковой (фунгицидной) концентрации, но нужно иметь в
виду, что некоторые вещи после этого могут быть испорчены.
Как вы уже поняли, эти меры направлены на профилактику передачи
инфекции по «второму звену» эпидпроцесса. То есть – на механизм
передачи. Но, конечно, в отличие от текущей уборки, каждый день
камерную и дезинфекционную обработку никто проводить не станет,
да этого и не требуется. Обычно такую обработку проводят по типу
заключительной дезинфекции – то есть когда источник инфекции
вылечился либо удалён из очага (госпитализирован). И делает такую
дезинфекцию
сотрудник
медицинского
учреждения
или
дезинфекционной станции, обученный работе с дезкамерой и
применению растворов дезинфектантов.
10.1. Микотоксикозы
Мы
уже
разобрали
строение
и
особенности
жизни
микроскопических грибов (микромицетов), узнали об их значении в
природе и медицине, выяснили, почему микологи не любят, когда
микромицетов называют грибками, и какие болезни (микозы) грибы
вызывают.
Но только возбудителями микозов роль грибов как источников
проблем здравоохранения не заканчивается. Иногда грибы могут не
являться патогенными для человека и животных, как упомянутые нами
фитопатогенные грибы, паразитирующие на растениях. Но при этом
последние продуцируют токсины, накапливающиеся в субстрате, на
котором они обитают, – микотоксины. А этим субстратом для
фитопатогенных
грибов
часто
являются
культурные
и
сельскохозяйственные растения: плоды фруктовых деревьев,
различные злаки, рис, кукуруза, бобовые, подсолнечник и другие
масличные культуры. И в результате употребления таких продуктов,
даже из переработанного и термически обработанного сырья,
возможно пищевое отравление – микотоксикоз. Причём имеется в
виду, что микотоксикозы вызваны именно токсинами микромицетов –
то есть. отравление употребляемыми в пищу грибами-макромицетами
микотоксикозом не является.
Микотоксины обычно относятся к группе алкалоидов –
органических соединений растительного происхождения, обладающих
чрезвычайно высокой биологической активностью. Несмотря на
созвучие названий, к алкоголю они отношения не имеют. Некоторые
алкалоиды в чистом виде используют в качестве лекарств (гликозиды
ландыша в качестве сердечного препарата, соединения из болиголова –
как противоопухолевые средства и т. д.), но в очень небольших и
строго контролируемых врачами дозировках, потому что они обладают
неприятным свойством накапливаться в организме человека. А
разница концентраций, отделяющая лекарство от превращения в яд,
для алкалоидов очень невелика.
Большинство микотоксинов, как и алкалоиды вообще, воздействуют
сначала на нервную систему, а уже опосредованно через неё – на
многие системы и органы. Поэтому клиника отравления
микотоксинами разнообразна и может включать как угнетение нервной
системы, так и повышенное возбуждение с развитием бреда,
галлюцинаций, чувства страха или повышенной агрессии. Вместе с
тем нарушение нервной регуляции ведёт к сбоям в работе сердца и
ЖКТ.
Микотоксины одинаково поражают не только человека, но и
животных, а потому представляют важную проблему как для
медицины, так и в ветеринарии.
Микотоксины различают в зависимости от того, каким родом грибов
они продуцированы: род фузариум выделяет фузариотоксины, гриб
аспергиллус флавус и другие виды аспергиллов – афлатоксин. Однако
некоторые классы микотоксинов могут продуцировать разные роды
грибов: например, патуллин – и аспергиллы, и пеницилл.
Помните, мы упоминали гриб спорынью, паразитирующую на
хлебных злаках – ржи и пшенице? Его мицелий образует на колосьях
подобие плодового тела макромицетов – в виде изогнутого на манер
птичьей шпоры отростка. Во французском языке петушиная шпора
называется «эргот», так же по-французски называется и сама
спорынья. Поэтому, когда люди выяснили, что именно алколоиды
спорыньи являются причиной тяжёлого пищевого отравления, они
назвали это заболевание эрготизм. Однако в средние века, когда
эрготизм вызывал массовые отравления в Европе, такого названия ещё
не существовало, да и сама роль спорыньи в его возникновении не
была известна (хотя о ядовитых свойствах «рожков» спорыньи уже
знали).
Между тем эрготизм крайне негативно отражался не только на
состоянии здоровья средневековых европейцев, но и на социальных
процессах того времени. Начать с того, что спорынья поражала посевы
злаков, особенно ржи, не абы когда, а преимущественно в холодные
влажные годы. В XVI–XVII веках наша планета переживала как раз
один из так называемых климатических минимумов, и в Центральной
и Западной Европе случались настоящие «годы без лета». Естественно,
что посевам это не шло на пользу, они были ослаблены и не могли
противостоять заражению вредителями, в том числе спорыньёй –
урожаи падали. Пшеница меньше поражается спорыньёй, но она менее
продуктивная, более капризная при выращивании, и её дефицит
проявлялся первым. Люди переходили на рожь, а она не только чаще
была заражена, но в тёмной ржаной муке ещё и трудно было различить
«рожки» спорыньи. Да и когда живот бурчит от голода, особо
привередничать не будешь – «всё, что попало в еду, тоже еда».
Выпеченный из такой муки хлеб содержал алкалоиды спорыньи,
которые довольно устойчивы к термическому воздействию. Спорынья
содержит их целый комплекс: прежде всего эрготамин, эргометрин и
лизергиновую кислоту. Последняя является родственной такому
наркотику, как ЛСД, а первые два вызывают нарушение нервной
проводимости и спазм гладких мышечных клеток (ГМК). ГМК, в
частности, находятся в составе стенок сосудов и дыхательных путей,
регулируя их просвет, а также многих внутренних органов – желудка,
кишечника, матки, обеспечивая их сокращение и расслабление в
процессе функционирования.
Сильное отравление спорыньёй приводило к мучительной смерти на
фоне судорог и нарушения жизненных функций организма. Но чаще
отравление было хроническим – яд гриба накапливался в организме
человека, поступая с некачественным хлебом (картошки в Европе
массово ещё не знали, и продукты из злаков и бобовых были основой
рациона). Комплексное действие нескольких алкалоидов приводило к
специфической клинической картине, называемой в то время
«антониевым огнём», а по современной классификации это была
гангренозная форма эрготизма.
Под действием эрготамина и эргометрина наступал длительный
спазм мышечной стенки кровеносных капилляров в коже, внутренних
органов и центральной нервной системы (ЦНС). Наступающее из-за
этого в тканях кислородное голодание в конце концов заканчивалось
отмиранием клеток (некрозом), развивалась гангрена. Сначала
наиболее дистальные отделы конечностей (периферические – пальцы
ног и рук, кисти, стопы) покрывались язвами, затем чернели и
отпадали, словно и впрямь сожженные огнём (отсюда и средневековое
название). Животные страдали наравне с людьми со схожими
симптомами и в прямом смысле слова «отбрасывали копыта».
Гангрена сопровождалась сначала сильнейшими болями, а по мере
интоксикации организма продуктами распада – эйфорией, снижением
критического отношения к своему состоянию, бредом. Вкупе с
поражением ЦНС это быстро приводило к умопомешательству.
Вчерашние нормальные люди на глазах превращались во что-то вроде
заживо гниющих тупых и агрессивных зомби.
Единственным лекарством тогда был… нормальный хлеб,
испеченный из незаражённой, чаще всего пшеничной, муки. А запасы
такого хлеба имелись в монастырях, и именно на церковь зачастую
уповали люди, для которых неурожайные годы оборачивались не
только голодом, но и превращением привычного мира в такой
«постап», который и не снился авторам современных хорроров. Тем
более что психотические симптомы, вызванные аналогом ЛСД из
спорыньи, вполне могли приобретать вид бреда и галлюцинаций на
религиозные мотивы.
Смотрели на церковь и власти, ища дополнительную опору в период
потрясений, когда трон под ними начинал заметно раскачиваться. Вот
только церковь в средневековой Европе не была единой – помимо
католичества, в ней существовало протестантство, которое само
разделялось на лютеранство, кальвинизм, англиканство и т. п. Плюс
несколько еретических течений вроде тех же альбигойцев. И всё это
ещё помножено на сложные отношения между странами. В итоге
центры религиозных течений и даже отдельные крупные монастыри
начали стремиться не только к религиозному, но и экономическому и
политическому влиянию. Как ни парадоксально, эпидемии, включая
вспышки «антониева огня», этому только способствовали. И как среди
любых «корпораций», между центрами религии довольно быстро
стала расти конкуренция, временами переходящая в «силовые акции».
Так называемые «религиозные войны» сотрясали Европу на
протяжении XVI–XVIII веков, периодически отмечаясь дикими
инцидентами вроде Варфоломеевской ночи, когда в течение
нескольких дней августа 1572 года католиками было уничтожено 30
тысяч гугенотов-протестантов. А всего с 1562 по 1598 годы выделяют
9 эпизодов гражданской войны между католиками и гугенотами,
общие потери населения в которых составили от 2 до 4 миллионов
человек – и это в одной только Франции! То есть в среднем эта
междоусобица уносила более 80 тысяч жизней в год – для сравнения,
столько же погибло солдат во время захвата Франции нацистской
Германией в 1940 году.
Нет, конечно, не спорынья была первопричиной «религиозных
войн». Однако отрицать её роль как одного из «отягощающих
факторов» не стóит. Тем более что эпидемии эрготизма сопровождали
голод и сопутствующие социальные проблемы и до, и после XVI века.
Так, порядка 100 тысяч участников первого Крестового похода (1096
г.) составляли крестьяне – его так и прозвали: «Крестовый поход
бедноты». Основная их масса была из восточных регионов Франции и
западных земель Германии. Что характерно – данные территории
незадолго до этого испытали эпидемию «антониева огня».
Религиозный экстаз, который ряд историков объясняет психотическим
влиянием алкалоидов спорыньи, помноженный на голод, нищету,
произвол феодалов и попустительство папской церкви, двинули
огромную массу этих людей на пресловутое «освобождение Святой
Земли», о которой абсолютное большинство из них даже не имели
реального представления.
Самое интересное, что ещё в 1670 году французский врач Луи Тулье,
сопоставив известные ему факты о массовых заболеваниях крестьян
«антониевым огнём» с картиной отравления некоторыми
лекарственными препаратами (экстракт спорыньи уже применялся в
медицине, например, в качестве абортивного средства), предположил,
что именно заражение ржи спорыньёй является причиной эпидемий.
Однако широкого распространения «теория Тулье» не получила, что
обернулось ещё сотнями тысяч пострадавших от эрготизма. Последняя
его вспышка в Европе зарегистрирована аж в 1954 году, и тогда тоже
были смертельные случаи.
В Российской Империи с начала XVIII до начала XX века
насчитывают 24 подобные европейским крупные вспышки. Впрочем,
есть мнение, что по крайней мере ряд из них был вызван вовсе не
спорыньёй. Тем не менее и испорченный хлеб, и предшествующий
событию голод, и паразитические грибы присутствовали и здесь.
Только грибы эти были уже из рода фузариум, следовательно,
вызывали фузариотоксикоз. Серьезные вспышки фузариотоксикоза
регистрировались в 1930–50 годы на Дальнем Востоке уже советской
России. Врачи описывали это заболевание под названием
некротической ангины или алиментарно-токсической алейкии, что
было связано с характерными симптомами заболевания: некрозом
ткани миндалин (мы разбирали эти органы иммунной системы ранее),
резким снижением в крови сначала лейкоцитов (лейкопения вплоть до
алейкии – когда последние вообще практически не обнаруживаются в
мазке), а затем общим угнетением кроветворения с одновременным
нарушением свёртываемости крови. Смерть наступала обычно от
внутренних кровотечений. Точно так же, как при отравлении
спорыньёй, страдали и сельскохозяйственные животные.
Виновника установили довольно быстро, связав воедино
предшествовавшие вспышкам неурожайные годы, когда крестьяне
были вынуждены употреблять в пищу хлеб из перезимовавшего в поле
и уже проросшего зерна (в отличие от спорыньи, это чаще были
пшеница и ячмень). Такой хлеб называли «пьяным» из-за характерной
картины острого отравления: человек становился излишне
возбуждённым, эйфоричным, нарушались речь, память и мышление.
Затем появлялись резь в животе, диарея, мелкие кровоизлияния на
коже и слизистых.
Однако установить конкретную причину, почему хлеб из
перезимовавшего зерна становился «пьяным», удалось только после
Великой Отечественной войны. В нём обнаружили споры и гифы
плесневых
грибов,
в
особенности
фузариума,
а
также
термостабильный (не разрушающийся при выпечке) токсин. Не
составило труда доказать, что последний является фузариотоксином –
продуктом выделения фузариума.
Только после этого удалось окончательно решить проблему
«болезни пьяного хлеба», как ещё называют фузариотоксикоз. Однако
не проблему микотоксикозов вообще – мы уже увидели, что грибковые
токсины достаточно стабильны и не разрушаются в окружающей среде
и
при
обработке.
Достаточно
нарушить
технологию
сельскохозяйственного производства, не убрать посевы в сухое время
или продержать сырьё во влажном хранилище, как на нём поселяются
плесени. Даже если потом такую сельхозпродукцию смешают с
доброкачественным сырьём или она попадёт туда случайно, то всё
равно может представлять опасность для человека и животных. То есть
микотоксины являются контаминантами кормов и пищевых
продуктов. И по-прежнему составляют серьёзную проблему для
современного мира, учитывая его глобализацию. Ведь если
средневековые крестьяне страдали от ими же выращенного хлеба, то
сегодня афлатоксин из заражённой бразильской кукурузы может
поразить индеек на английской ферме, а он же из африканского
арахиса – вызвать тяжёлое заболевание печени у жителя Франции.
Глава 11. Замори червячка
Почему мы отдельно говорим о паразитозах? Это то же самое, что
инфекции, или нет? На самом деле – не совсем. Вспомните, в главе об
экологии микробов мы сказали: если совместное существование двух
организмов разных видов приводит к тому, что один отбирает пищевые
ресурсы у другого и вообще наносит ему вред, то такой тип
взаимоотношений называется паразитизмом. И болезни, вызванные
паразитическими микроорганизмами (возбудителями), – это
инфекционные болезни.
Но что если организм по своему жизненному циклу является
типичным паразитом и при этом многократно мельче своего хозяина,
однако уже далеко выходит за рамки МИКРОорганизма? Как
поступать в таких случаях? Нет, конечно, есть такие исключения, как
непатогенная бактерия тиомаргарита магнифика, достигающая 2 см в
длину (это не опечатка, она действительно лишь чуть короче диаметра
пятирублёвой монеты), но она при этом остаётся одноклеточным
организмом и пусть не совсем типичным, но прокариотом. Потому,
закрыв глаза на неприличную длину, её считают микроорганизмом.
Чесоточный клещ с его размерами 0,2–0,3 мм гораздо меньше
тиомаргариты, но всё же он – многоклеточный эукариот (ровно так же,
как и человек, например). А потому никакими ухищрениями этого
паразита (во всех смыслах слова) под определение микроорганизма
уже не подгонишь. Так что же относить к паразитозам?
Отечественная классификация паразитозов выглядит так:
1. Гельминтозы (глистные инвазии) – инвазия паразитическими
организмами из рода червей.
2. Протозоозы (протозойные инвазии) – инвазии, вызванные
простейшими – среди них у человека наиболее распространены
лямблиоз (современное название – гиардиоз), токсоплазмоз, уже
упомянутая малярия и другие, вызванные всего примерно 50 видами
паразитических простейших.
3. Энтомонозы – паразитозы, вызванные насекомыми; характерным
примером является педикулёз – группа инвазий, вызванных вшами
различных видов (головной педикулёз, платяной, лобковый).
И наконец, 4. акариазы – паразитозы, вызванные клещами;
типичный пример – чесотка, возбудителем которой является
чесоточный клещ (зудень).
Получается, что паразитология одной ногой стоит в мире
микробиологии, а под другой имеет вполне самостоятельную основу.
Потому
что
эта
дисциплина
одновременно
занимается
паразитическими простейшими, являющимися одной из групп
микроорганизмов, но также гельминтами, клещами и прочими
«большими» паразитами. Да, такое деление выглядит несколько
неестественным, потому что в нём прослеживается чисто
практический подход – все объекты изучения паразитологии имеют
медицинское значение. С другой стороны, выделение паразитологии
как дисциплины, и паразитологов как отдельных специалистов,
позволяет этих самих специалистов готовить целенаправленно, не
«подсаживая их в телегу» к микробиологам или кому-либо ещё (это
важно, потому что в дальнейшем мы увидим – подходы к диагностике,
лечению, профилактике паразитозов свои – специфические).
И да, среди насекомых, паукообразных, червей и простейших лишь
небольшая часть видов является паразитами человека или других
животных. Поэтому не забывайте, что в целом каждой группой этих
живых существ занимаются учёные отдельных специальностей:
насекомыми – энтомологи, червями – зоологи с узкой специализацией
(нематологи, например), простейшими – протозоологи и т. д. А
паразитирующими на других видах – только паразитологи. Поэтому,
например, каждый паразитолог немножко протозоолог, но не
каждый протозоолог – паразитолог.
Таким образом, объектом изучения паразитологии являются
паразиты – организмы, живущие и питающиеся за счёт живых
существ другого вида и временно или постоянно пребывающие на
поверхности их тела (эктопаразиты) или внутри организма
(эндопаразиты).
Медицинская паразитология исследует паразитов и паразитарные
болезни человека, методы их диагностики, лечения и профилактики.
Не меньше от паразитов страдают и наши домашние питомцы, а
также сельскохозяйственные животные – их паразитозами
занимается ветеринарная паразитология.
Однако нападение на человека (и животных) блох, мух, оводов и
других насекомых также относится к энтомонозам (для
паразитирования двух последних, так называемых двукрылых, даже
имеется отдельное название – миазы ). Например, хорошо известно,
что оводы способны откладывать личинок в кожу животных и
человека. А у кошек, особенно в тропическом климате, миазы,
вызванные личинками оводов и мух, вообще распространены.
Вместо термина «инфекция» к паразитарным болезням больше
применимо понятие инвазия – внедрение паразитов в организмхозяин с последующим развитием у последнего комплекса
патологических, компенсаторных и защитных реакций, что
проявляется в формах:
паразитоносительства,
бессимптомной инвазии или
собственно паразитарной болезни (паразитоза).
То есть под инвазией у человека понимают внедрение не любых
организмов, ведущих паразитический образ жизни, а только
представителей царства Animalia (по-другому Zoa – животные,
включая и подцарство Protozoa – простейшие), с целью отличать их от
инфекций, вызванных микроорганизмами (кроме простейших).
Поэтому не следует путать, например, собственно акариазы и
энтомонозы с трансмиссивными инфекциями, передающимися
посредством, соответственно, клещей и вшей. Инвазия человека
вшами – педикулёз, а заражение человека переносимыми вшами
бактериями рода риккетсий – это уже трансмиссивная инфекция
сыпной тиф (другая связанная со вшами бактерия из той же группы
молликут – боррелия рекурентис – вызывает возвратный тиф).
Нападение на человека таёжных, лесных или пастбищных клещей –
это акариаз (паразитоз). Заражение при этом вирусом клещевого
энцефалита
или
крымской
геморрагической
лихорадки
–
трансмиссивная инфекция.
Лабораторная диагностика паразитозов тоже кардинально
отличается от рассмотренной нами при бактериальных, вирусных и
грибковых инфекциях. Гельминтов, как и простейших, практически
невозможно вырастить в посеве – для этого у них слишком сложные
жизненные циклы с наличием промежуточного хозяина (а иногда и
нескольких). Потому паразитологи больше полагаются на
микроскопию непосредственно биологического материала (иногда
специально концентрированного).
Кроме того, при лабораторной диагностике паразитозов нужно
учитывать ряд нюансов. Во-первых, на качество и точность
паразитологических исследований очень большое влияние оказывает
так называемая преаналитика . Это большой раздел знаний в
лабораторной диагностике, мы же для простоты понимания скажем
лишь, что на результат влияют правильность подготовки пациента,
сбора и доставки материала, выбор метода и реактивов. Дело в том,
что простейшие, для примера, по сравнению с бактериями гораздо
хуже выживают вне организма-хозяина. И в биологическом
материале вне организма, как правило, не размножаются. Иначе
говоря, чем больше времени проходит от момента взятия образца у
пациента, тем сильнее снижается в нём содержание доступных для
обнаружения
живых
паразитов.
Поэтому
однократный
отрицательный результат паразитологического анализа не всегда
свидетельствует об отсутствии инвазии, особенно при наличии
симптомов.
Во-вторых, обратная ситуация – однократная находка в
биоматериале единичных паразитов, их яиц или цист – тоже не
всегда однозначно указывает на заболевание. Так некоторые
паразитические амёбы могут пройти через наш кишечник
транзитом, поохотиться там на бактерии микрофлоры и, будучи
вполне
довольными
этим
приключением,
эвакуироваться
естественным путём обратно в окружающую среду – явление
транзиторного носительства.
При лечении паразитозов нужно учитывать, что большинство их
возбудителей – эукариоты, а значит, антибиотики автоматически
выпадают из арсенала борьбы с ними. Тут требуются совсем другие
препараты, и они будут оказывать немалое побочное действие на
организм-хозяин (человека или животное), потому что мы и наши
«братья меньшие» такие же эукариоты.
Наконец,
против
паразитов
практически
отсутствует
специфическая профилактика – попросту говоря, против них
сложно или вовсе нельзя разработать вакцины (правда, против
малярии пробуют). Это, с одной стороны, усложняет задачу борьбы с
ними, а с другой – целенаправленное применение достаточно простых
мер порой способно снизить заболеваемость некоторыми
паразитозами чуть ли не до нуля. Почему это возможно?
Тут нужно вспомнить кое-что из теории эпидемического процесса.
Мы говорили, что три звена эпидпроцесса – это источник инфекции,
восприимчивый к ней организм и связывающий их механизм передачи
[возбудителя] инфекции. Паразитозы в этом плане не исключение –
здесь тоже есть источник и заражаемый организм. Но если для
большинства бактериальных и вирусных инфекций между источником
и восприимчивым организмом находятся лишь абиогенные (неживые)
объекты и факторы внешней среды (воздух для воздушно-капельных
инфекций, пищевые продукты – для кишечных), то гельминт или
паразитарный простейший на разных стадиях своего развития могут
проживать в совершенно разных живых организмах. В дальнейшем вы
это увидите на примере конкретных инвазий. Малярийному
плазмодию, скажем, нужно сначала проникнуть в комара
определённого вида. А многие гельминты проводят часть своего
жизненного цикла в рыбах и моллюсках (описторхис), либо в
организмах зверей (аскарида, эхинококк, свиной цепень, трихинелла),
либо и в тех, и в других (бычий цепень).
Поэтому говорят, что биологической основой эпидемического
процесса при паразитозах является паразитарная система –
взаимодействие популяций различных биологических видов, из
которых один является паразитическим. И двухчленные паразитарные
системы, состоящие только из паразита и организма-хозяина, тут
скорее редкость (как пример, энтеробиоз – контактный гельминтоз,
передающийся непосредственно от человека к человеку контактнобытовым путём, или аскаридоз – геогельминтоз, при котором
созревание яиц происходит в почве). Чаще паразитарные системы
бывают трёхчленными или многочленными – с включением
нескольких промежуточных хозяев и одного или нескольких
окончательных.
И нужно ещё учитывать, что каждый из промежуточных хозяев
паразита существует в определённых условиях привычной ему
экосистемы. То есть, связываясь с окружающей средой через
промежуточных хозяев и механизм передачи, паразитарная система
становится эпидемической экосистемой, на состояние которой
оказывают влияние все входящие в неё природные (биогенные и
абиогенные) и социальные факторы.
Если перевести эти теоретические выкладки на понятный русский
язык – они неожиданно раскрывают важное практическое значение.
Связь паразитарной системы с окружающей средой (через абиогенные
– неживые – факторы среды) позволяет нам во многом управлять этой
системой, фактически не касаясь не только самого живого паразита, но
часто – вообще никаких живых её составляющих. Что зачастую
гораздо проще и эффективнее.
Поясним на примере малярии. Уничтожить малярийного плазмодия
в живой природе практически невозможно. Но можно в местах
поселения
людей
уничтожить
комаров-переносчиков
(это
определённые родá: анофелес, кулекс, ёдес). И это будет эффективно,
но сработает только на один сезон, а потом комары опять расплодятся.
К тому же неправильное или слишком массовое применение
инсектицидов может, помимо комаров, плохо сказаться на других
участниках экосистемы, включая самого человека (неправильное
«управление экосистемой» тоже больно бьёт по всем её участникам,
включая «управляющего»). Поэтому рациональнее использовать
«химию» ограниченно, но параллельно в населённых пунктах осушить
бесполезные водоёмы, вовремя устранять затопления подвалов и
низин, а бассейны и оросительные резервуары накрыть полотном или
крышками. Тогда в этих стоячих «водоёмах» не смогут развиваться
личинки комаров, что резко снизит численность переносчика на
территории. А в прудах применить «биологическое оружие» –
небольшая рыбка со смешным названием «гамбузия» (Gambusia
affinis) очень эффективно уничтожает комариных личинок.
Точно так же можно регулярно профилактически «пропаивать»
детские коллективы противоглистными препаратами. Но лучше не
пичкать детей таблетками, а учить их вовремя мыть руки и не
облизывать всё, до чего дотягивается язык (параллельно, конечно,
регулярно обследуя организованные коллективы на носительство
гельминтов, выявляя и пролечивая инвазированных детей).
11.1. А простейшие-то не так просты!
Почти наверняка из школьного курса биологии простейшие вам
знакомы в лице амёбы. Эта неторопливая микроскопическая
«осьминожка» запускает везде свои щупальца-ложноножки, а
обнаружив что-то «вкусненькое», обволакивает ими и поглощает,
образуя пищеварительную вакуоль. Как и лишенные скелета
осьминоги, амёба может протискивать своё податливое тельце в
любую самую узкую щель для укрытия или поиска пищи. Но если
осьминог всё же имеет постоянное число щупалец, то амёба может
отрастить столько псевдоподий (дословно «ненастоящая нога» –
ложноножка), сколько ей нужно. Причём в самом произвольном месте,
так как они являются просто выпячиваниями цитоплазматической
мембраны, подкреплёнными и управляемыми сократительным белком
актином. И если осьминог имеет множество специализированных
клеток: стрекательных, светочувствительных, нервных и т. д. – то
амёба, как и абсолютно все простейшие, является одноклеточным
живым организмом. Но что их при этом объединяет (и нас с ними,
кстати говоря), так это то, что оба – эукариоты и относятся к царству
животных (Zoa или Animalia), образуя в нём подцарство Protozoa.
Да, единственная клетка любого простейшего содержит
оформленное ядро с ядрышком, под двойной ядерной мембраной
которого заключен хроматин – молекулы ДНК с поддерживающими
белками. В этом смысле их клетки не сильно отличаются от наших.
Поэтому биоматериал для обнаружения простейших можно
окрашивать по методу Романовского–Гимзы, которым красят и мазки
крови (см. материал про лейкоформулу крови). У амёб и большинства
других простейших, окрашенных по Романовскому–Гимзе, под
микроскопом ядра будут красными, а цитоплазма – голубой (синей)
или светло-фиолетовой.
Простейшие могут размножаться обычным бинарным делением
(надвое, с предварительным удвоением генетического материала) – это
бесполый способ размножения (шизогония), характерный для
большинства из них. Либо же каждая клетка при делении получает
половину исходного генетического набора и для дальнейшего развития
должна встретиться и слиться с другой такой же «половинкой» – вот
такая мелодрама в мире микробов. Последний способ называется
спорогонией и служит половому размножению простейших, то есть
повышению их генетического разнообразия. Только не называйте
спорозоиты простейших спорами – это неграмотно. Споры образуют
бактерии внутри своих клеток, или грибы – обычно путём деления
специализированных клеток на концах гифов. А простейшие при
попадании в неблагоприятные условия среды образуют цисты. Клетка
простейшего как бы говорит: «Я в домике» – после чего целиком
покрывается толстой защитной оболочкой. Цисты простейших не
обладают той фантастической устойчивостью к высокой температуре и
другим неблагоприятным факторам, как грибные и бактериальные
споры – обычно они могут уберечь лишь от высыхания и помочь
пережить «голодный период».
Помимо ядра, в цитоплазме простейших содержатся и другие
органеллы, характерные для эукариот: 80S-рибосомы, митохондрии,
гладкий
и
шероховатый
эндоплазматические
ретикулумы.
Разнообразие внутреннего наполнения здесь побольше, чем в
бактериях. Да и размеры клетки обычно куда крупнее – типичные
простейшие от 2 до 100 микронов величиной. Микрон – он же
микромéтр – это 10-6 метра, одна миллионная его часть. Для
наглядности можно сравнить простейших с хорошо знакомой нам
бактерией кишечной палочкой: диаметр последней – 400–800 нм, то
есть 0,4–0,8 микрона, а длина – около 3 микронов. Простейшие по
сравнению с ней просто гиганты.
Причём есть «гиганты среди гигантов» – инфузория спиростомум
может вырастать до 4 мм. Это крупнее некоторых мелких
ракообразных типа дафний – то есть одноклеточный спиростомум
крупнее многоклеточного рачка! А фораминиферы, которые часто
встречаются в рифовых экосистемах, и вовсе достигают величины в
несколько сантиметров, оставаясь при этом одноклеточными. К
счастью, эти «монстры» не патогенны для человека.
Все простейшие по типу питания является гетеротрофами, то есть
вынуждены питательные вещества и энергию получать извне.
Чтобы как-то обойти данное ограничение, тот же спиростомум
бессовестно читерствует: он может поглощать, не переваривая, а
сохраняя в цитоплазме, одноклеточные водоросли рода хлорелла. В
«плену» хлорелла получает защиту (если спиростомума самого кто-
нибудь не скушает), а хозяин от неё – ряд питательных веществ
(явление эндосимбиоза ).
Окружает всё это великолепие аналог цитоплазматической
мембраны – пелликула. Она довольно тонкая и потому не определяет
форму клетки простейшего. Однако не все простейшие такие же
бесформенные, как амёбы. Упомянутые фораминиферы и солнечники
образуют подобие раковины (внешний скелет) из минеральных солей.
У радиолярий (лучевиков) – кристаллы минералов разрастаются
внутри клетки, формируя подобие внутреннего скелета. Да и другие
подгруппы простейших обычно имеют характерные внешние черты,
что используется в диагностике.
Классификация простейших включает минимум 6 групп, но из них
радиолярии и солнечники не имеют медицинского значения, так как на
людях не паразитируют. Остаются 4 группы, представляющие интерес
для паразитологов:
1. Саркодовые – они же корненожки, они же амёбы. Патогенный
представитель – дизентерийная амёба. Вызывает тяжёлое поражение
кишечника, сопровождающееся диареей и изъязвлением слизистой
оболочки кишки.
2. Жгутиконосцы (жгутиковые). Патогенный представитель –
гиардии (лямблии). Гиардиаз/лямблиоз – поражение желчевыводящих
протоков печени и желчного пузыря, тонкого кишечника –
сопровождается дискинезией желчных путей и энтеритом.
3. Споровики. Патогенны малярийные плазмодии (4 вида).
Малярия – поражение кровяных клеток, печени и селезёнки,
сопровождающееся периодическими регулярными приступами
лихорадки (резкое повышение температуры тела, озноб, профузный
пот).
4. Ресничные, они же инфузории. Патогенный представитель –
кишечный балантидий. Вызывает язвенно-некротическое (с
омертвением тканей) поражение кишечника.
Обратите внимание, что названия протозойных инвазий обычно
образуются путём добавления к названию возбудителя суффикса «аз», а не «-оз», как при инфекционных болезнях или гельминтозах.
Сравните бактериальный боррелиОЗ, грибковый кандидОЗ с
протозойными гиардиАЗом и балантидиАЗом (но: «лямблиОЗ», так
как это старое классификационное название)
Самым распространённым протозоозом на территории нашей
страны является гиардиаз. Это правильное современное его название,
однако чаще гиардиаз именуют по старинке – лямблиозом. Его
вызывают паразитические простейшие из группы жгутиковых
гиардия (лямблия) интестиналис (Giardia/Lamblia intestinalis). Их
клетки имеют характерную грушевидную форму с двумя
присасывательными дисками – на некоторых микрофотографиях
лямблии похожи на забавные глазастые рожицы. Однако
инвазирование этими «смайликами» не сулит ничего хорошего.
Гиардии поражают тонкий кишечник и гепатобилиарную систему
(печень, желчный пузырь и протоки). Однако это не единственный
кишечный протозооз.
Большинство кишечных протозойных инвазий, за исключением
балантидиаза и криптоспоридиоза, являются антропонозными. Хотя
лямблии и могут паразитировать в кишечнике котов, собак и грызунов,
но в подавляющем большинстве случаев для людей источником
инвазии кишечными простейшими лямблией и энтамёбой
хистолитика (Entamoeba histolytica – возбудитель амебиаза) является
именно
человек.
Наибольшую
эпидемическую
опасность
представляют больные хроническими формами протозоозов в
межрецидивный период и здоровые носители. Механизм передачи –
фекально-оральный, ведущий путь – контактно-бытовой, а также
пищевой. Инвазивной формой служат цисты. Последние могут
сохранять жизнеспособность во внешней среде в течение нескольких
недель, а иногда и нескольких месяцев.
На продукты цисты простейших попадают с загрязненных рук
цистовыделителей, переносятся мухами и тараканами, а также при
удобрении огородов и садов необеззараженными фекалиями человека,
свиней и крупного рогатого скота. Цистами могут быть загрязнены
предметы обихода, кухонная и столовая посуда, разделочные столы,
ножи и прочее оборудование пищевых производств и общепита,
дверные ручки и т. п.
Балантидиаз – зоонозная инвазия, основным источником заражения
которой являются свиньи. Возбудитель – инфузория кишечный
балантидиум
(Balantidium
coli).
Основным
источником
криптоспоридиоза (возбудитель криптоспоридиум парвум –
Criptosporidium parvum) является молодняк сельскохозяйственных
животных (телята, ягнята, поросята, козлята и другие), у которых
инвазия протекает как тяжелая острая, часто с летальным исходом для
животных, кишечная инфекция. Помимо пищевого и контактнобытового путей, при зоонозных протозоозах гораздо чаще реализуется
водный путь передачи возбудителя – особенно если источник воды
загрязнён стоками сельхозпредприятий, пастбищ и т. п.
Клинические проявления кишечных протозоозов чаще всего
сопровождаются диспептическими симптомами (тошнота, отрыжка,
изжога, тяжесть в животе, нарушение пищеварения, запор или,
наоборот, диарея) и варьируют от легких и бессимптомных форм
(лямблиоз, криптоспоридиоз) до тяжелого язвенно-некротического
поражения толстого кишечника (амебиаз, балантидиаз).
Что касается лямблий, то их цисты преодолевают кислотный барьер
желудка и достигают двенадцатиперстной и тонкой кишки, где
развиваются в вегетативные формы (те самые «смайлики»). Благодаря
наличию нескольких жгутиков они подвижны и легко могут проникать
в желчевыводящие пути и колонизировать желчный пузырь и
печёночные протоки. Присасывательные диски позволяют лямблиям
надежно прикрепляться к стенкам протоков изнутри так, что
перистальтика и ток желчи не могут их оттуда удалить.
Ввиду этого диагностика лямблиоза-гиардиаза может представлять
значительные трудности. Обычно для неё проводят микроскопию
нативных (сразу из биоматериала) или предварительно окрашенных
мазков фекалий. Но если количество лямблий не очень велико, и они
крепко «держатся» за стенки протоков высоко в гепатобилиарной
системе, то «на выходе» лаборант может ничего не обнаружить.
Плюс играет роль упомянутая в разделе общей паразитологии
преаналитика – для того чтобы протозоологический анализ
получился верным, нужно подвергать микроскопии ещё тёплый, то
есть практически только что собранный кал, так как вегетативные
формы при охлаждении быстро теряют подвижность, а в дальнейшем
подвергаются разрушению под действием содержащихся в фекалиях
протеолитических ферментов. В лучшем случае после этого можно
найти только цисты. Поэтому по правилам для любого
протозоологического анализа собирают кал после утренней дефекации
в стандартную посуду (стерильный стаканчик с вмонтированной в
крышку лопаточкой – продаётся в любой аптеке) и сразу же относят в
лабораторию, где их берут в работу в первую очередь.
Если же все подозрения на лямблиоз есть, а анализ кала упорно
отрицательный, иногда приходится проводить так называемое
дуоденальное
зондирование
–
тонкий
зонд
вводят
в
двенадцатиперстную кишку и получают несколько проб желчи,
которую подвергают микроскопическому исследованию.
Помимо простых методов копропротозооскопии (микроскопия
фекалий для обнаружения простейших), применяют методы с
обогащением биоматериала. Для этого фекалии эмульгируют с
дистиллированной водой или изотоническим раствором и фильтруют
для удаления крупных частиц. Далее фильтрат либо центрифугируют,
чтобы
осадить
цисты
и
клетки
простейших
на
дно
(седиментационные методы), либо в него добавляют насыщенный
раствор солей – поваренной или сульфата цинка. В последнем случае
плотность раствора повышается, и при центрифугировании крупные
фракции оседают, а вот более лёгкие цисты, наоборот, всплывают, как
яйцо в солёной воде – это флотационные методы. Соответственно,
при седиментационных способах исследуют под микроскопом осадок,
а при флотационных – собранную бактериальной петлёй или пипеткой
плёнку с поверхности. Запомнить легко по мнемоническому правилу –
если цисты оСЕДают – это СЕДиментация, если плавают как корабли
на флоте – флотация (хотя моряки всегда говорят, что на своих судах и
кораблях они «ходят»).
Для лечения протозоозов в настоящее время существует достаточно
большое количество антипротозойных препаратов. Но подбор
лечения должен осуществлять врач с учётом этиологии (возбудителя)
инвазии, локализации его в организме и особенностей заболевания –
например, против лямблиоза нужны препараты, хорошо проникающие
в желчь. Врач же должен определить дозировку, так как выше мы уже
упоминали, почему эти препараты достаточно токсичны для нашего
собственного организма.
В целом для лечения кишечных протозоозов можно упомянуть такие
препараты, как метронидазол, тинидазол, орнидазол. Есть
комбинированные препараты (метронидазол+фуразолидон). Для
уничтожения вегетативных форм амёб и балантидий в просвете
кишечника
могут
быть
эффективны
также
антибиотики
тетрациклинового ряда – угнетают синтез белка у простейших.
Но, как и всегда, лучше не доводить до необходимости лечения, а
предотвращать заболевания. В отношении кишечных протозоозов
профилактика в основном заключается в употреблении населением
качественной, то есть свободной от загрязнений простейшими и
другими микробами, питьевой воды. А уж чтобы обеспечить это,
нужен целый комплекс мер: тут и охрана водоёмов и артезианских
скважин от попадания поверхностных стоков, особенно с предприятий
животноводства и систем канализации населённых пунктов, и
предотвращение аварий на водопроводах, влекущих подсос в них
фекальных вод, и различные методы обеззараживания воды на
станциях водоподготовки (хлорирование, ультрафиолетовое облучение
и пр.). Если же вы оказались в местности, где с водой проблемы –
однозначно не стоит не только пить её из-под крана, хотя у себя дома
«я сто раз так делал», но даже использовать для полоскания после
чистки зубов. Помимо протозойной инвазии, это убережёт вас ещё и от
кучи вирусных и бактериальных зараз – типа той же холеры, которая
как раз и распространена в жарких регионах с дефицитом пресной
воды.
Глава 12. И микроб с микробом говорит
Прежде чем углубиться в тему о нашей с вами микрофлоре, вкратце
напомню содержание главы об экологии микроорганизмов. Итак,
микробы устанавливают разные виды связей друг с другом и с
окружающей средой. Одни ведут полностью свободный образ жизни,
самостоятельно синтезируя пищу и компоненты своей клетки за счёт
энергии солнца или доступных химических соединений (фото- и
хемоавтотрофы, соответственно), – но в мире микробов они
представлены только одноклеточными водорослями и некоторыми
архебактериями. Вторые – сапротрофы – предпочитают разлагать
мёртвые органические остатки. Третьим для существования нужны
другие живые существа – они не только питаются получаемыми от них
высокоэнергетическими соединениями, но зачастую ещё и используют
как среду обитания.
Далеко не всегда подобное сожительство вредит организму-хозяину.
Иногда микроорганизмы так приспосабливаются к нему, чтобы
максимально реже «напоминать о себе». На поверхности кожи они
могут питаться выделениями сальных и потовых желёз, отмершими
клетками эпидермиса – то есть, по сути, почти становятся
сапротрофами. А в кишечнике, например, научились разлагать
неперевариваемые нашим организмом соединения типа целлюлозы
(клетчатки).
То
есть
хоть
и
считаются
комменсалами
(«нахлебниками»), но особенно нас не объедают.
Некоторые микроорганизмы даже оплачивают «аренду» своего
проживания, выделяя различные полезные для нашего организма
вещества: витамины, углеводы и т. п. А, скажем, ряд кишечных
бактерий «отбывает общественные работы», участвуя в метаболизме
желчных кислот, обеспечивая нормальный процесс пищеварения.
Фактически это уже мутуализм – взаимовыгодное сожительство
организмов разных видов. В кишечнике, например, мутуалистами
являются бифидо- и лактобактерии, некоторые грибы. Можно сравнить
их с добропорядочными горожанами, которые честно трудятся,
заботятся о благоустройстве своего города и по возможности
пресекают хулиганства других микроскопических обитателей нашего
тела.
Правда, есть такие виды микроскопических сожителей, которые
иногда склонны чересчур увлекаться трапезой, переходя границы
«гостеприимства» нашего организма. Либо их становится слишком
много, либо они забывают о приличиях и ведут себя излишне
агрессивно, либо залезают туда, куда их «за стол» не приглашали.
Тогда они вызывают в организме патологический процесс –
инфекционно-воспалительное заболевание. Это может быть
гнойничковое поражение кожи, воспаление слизистой оболочки (глаза,
например
–
конъюнктивит)
или
нарушение
функции
пищеварительного тракта в верхних (гастроэнтерит) или нижних
(энтероколит, проктосигмоидит) отделах. Такое состояние даже не
всегда называют инфекцией, поскольку оно не отвечает классической
триаде критериев Коха (см. триада Генле–Коха): например,
большинство этих состояний не заразны для других людей, а если
микробы и передаются, то не всегда вызывают аналогичное
заболевание. А бывает так, что под действием лечения или других
внешних факторов микробы снова «берутся за ум», и сосуществование
микро- и макроорганизма возвращается в привычные рамки.
Таких слишком дерзких микробов, которые периодически
устраивают в организме разные «хулиганства», называют условнопатогенными. Потому что, по сути, они не плохие, просто детство у
них было тяжёлое, и воспитаны они дурно. Но в целом их как-то
можно терпеть. Особенно пока добропорядочных микробов в «городе»
большинство – тогда даже хулиганы стараются вести себя прилично,
работают на благо организма, а агрессию вымещают на «чужаках». Дада, они очень напоминают «пацанов на районе» ещё и тем, что
ревностно относятся к охране своей территории. Добропорядочные
«горожане» тоже обычно не в восторге от посторонней микрофлоры,
но борются с ней пассивно, создавая некомфортные для неё (и
комфортные для себя) условия – например, закисляют среду своего
обитания. Условно-патогенные же микробы побойчее и поактивнее –
они заселяют всё доступное место, занимают рецепторы клеток тела,
за которые могли бы «уцепиться» пришлые, они давно нашли
компромисс в отношениях и друг с другом, и с иммунитетом хозяина.
Это состояние, когда собственная микрофлора, размножаясь, не
пускает в организм «чужих» условно-патогенных и патогенных
микробов, называется колонизационной резистентностью (от слов
«колонизировать» и «сопротивляться» – можно считать за лозунг
условно-патогенной флоры).
Если же чужаки не понимают явных намёков в духе «вам здесь не
место», то в ход идут антибиотики (которые обычно продуцируют
грибы) и бактериоцины (особые вещества, выделяемые одними
бактериями против других). К сожалению, чужаки порой тоже не
полные хлюпики и пытаются провести «рейдерский захват», а если
сразу не получается, то постараются проникнуть скрытно или внести
смуту в ряды защитников. Ведь многим условно-патогенным
обитателям нашего организма они более или менее близкие
родственники. А значит, похожи внешне и «говорят» с ними на одном
языке. Поэтому иммунитет может вовремя не среагировать на
антигенный состав микробной армии вторжения, приняв их за
«своих». А умы «пацанов с района» могут совратить подброшенные
им чужаками плазмиды с факторами патогенности и генами
токсинообразования. Тогда у них произойдёт бунт, и они пойдут по
«городу»-организму жечь покрышки, бить витрины и сносить всё, что
не приколочено к базальной мембране. И устроить «революцию» тем
легче, чем сильнее осложнена нормальная жизнь микробного
мегаполиса – отголосками стресса организма-хозяина, неправильным
питанием, злоупотреблением антибиотиками и т. д.
Вот так образно можно представить каждодневную жизнь нашего
внутреннего
города,
населённого
микроорганизмами.
Добропорядочные граждане и «пацаны с района» составляют
нормальную микрофлору (нормофлору или нормальную
микробиóту) организма. Она включает порядка 500–1000 видов
микробов, связанных разными видами экологических отношений друг
с другом и с организмом-хозяином. Среди них есть грибы и археи, но
около 90% всей нормофлоры составляют бактерии, а раз есть
бактерии, то обязательно на них будут паразитировать вирусыбактериофаги. А бактерии с ними – бороться. Примерно как мы в
своих мегаполисах боремся с грызунами и вредными насекомыми. Но
друг с другом и с организмом человека микробный биоценоз
нормофлоры находится в состоянии равновесия, именуемого эубиозом
(дословно «хорошая жизнь»). Соответственно, нарушение этого
равновесия называется дисбиозом. А поскольку бактерий в
нормофлоре подавляющее большинство, то в качестве синонима
дисбиозу часто употребляют знакомый, вероятно, вам термин
дисбактериоз.
В норме микрофлорой колонизированы только кожа, видимые
слизистые и органы, сообщающиеся с окружающей средой. Однако в
отношении последних утверждение несколько условно. Скажем,
«трубка» желудочно-кишечного тракта сообщается с окружающей
средой на обоих своих концах и действительно колонизирована
микробами целиком. Из 1,5–2 кг микробных тел нормальной
микрофлоры (у некоторых людей в норме может быть и 3, и 5 кг – это
индивидуальная особенность) основная масса содержится именно в
кишечнике. Но это не одна и та же микрофлора – микробиоценозы
ротовой полости, тонкого и толстого кишечника заметно отличаются.
Как из-за разных условий в этих отделах, так и по причине того, что
разделяет их антисептический «барьер» содержимого желудка и
двенадцатиперстной кишки, преодолеть который могут далеко не все
микроорганизмы.
Но вот лёгкие тоже сообщаются с окружающей средой, да ещё как!
И при этом лёгкие в норме стерильны. Достигается это за счёт того,
что на пути к ним вдыхаемому воздуху нужно проделать долгий путь
по, простите за тавтологию, воздухоносным путям, выстланным
мерцательным эпителием и покрытым слизью. Частички пыли с
осевшими на них микроорганизмами турбулентным потоком
отбрасываются к стенкам дыхательных путей (почти как в воздушных
фильтрах системы «циклон»), где и прилипают к слою слизи. Затем
направленное движение ресничек медленно, но постоянно двигает
слизь в сторону носоглотки, где она вместе с налипшим «балластом»
и проглатывается. И дальше её ждёт «тартар» (не соус, конечно, а
древнегреческий аналог ада – глубокая тёмная бездна) в виде уже
упомянутого обеззараживающего кислотного барьера желудка. Та
небольшая часть микроорганизмов, которая всё-таки проникнет в
лёгкие, будет встречена иммунной системой в лице альвеолярных
макрофагов и сурфактантом, наполненным секреторными антителами
класса IgA. В слизи дыхательных путей их, кстати, тоже огромное
количество (подробнее о классах антител смотрите в главе про
иммунитет – им там посвящён целый раздел).
Аналогично и полость матки, и мочевой пузырь в известной степени
имеют сообщение с внешней средой, но эти органы тоже в норме
свободны от микроорганизмов. О крови, ликворе и спинномозговой
жидкости и говорить нечего – они стерильны априори. А если в
посеве данных биологических жидкостей обнаружен рост микробов,
то это повод бить тревогу!
Из-за того, что микрофлора разных мест на теле человека (и внутри
него) серьёзно отличается даже в пределах одной системы органов как
по количеству, так и по видовому составу, говорят о микрофлоре
разных локусов – мест её обитания:
микрофлора кишечника – около 40% всех видов микробов
нормальной микрофлоры и наибольшая биомасса из всех локусов;
микрофлора ротовой полости – около 20% видов;
слегка уступает ей микрофлора кожи, которая вместе с
микрофлорой конъюнктивы (слизистой оболочки глаза) составляет
18–20% видового состава нормофлоры;
на микрофлору верхних дыхательных путей приходится 15–16%
видов,
оставшиеся 4–7% видов населяют слизистую урогенитального
тракта – у мужчин видовой состав несколько беднее, у женщин за
счёт особой микрофлоры влагалища он может включать и до 10%
видов нормофлоры.
Хотя в среднем микрофлора у всех людей состоит из одних и тех же
микроорганизмов, но соотношение их в общем составе, а также
антигенный и генетический профили отличаются настолько, что
говорят об «отпечатках микрофлоры» по аналогии с отпечатками
пальцев – настолько картина микрофлоры уникальна у каждого
человека.
И всё же это разнообразие микрофлоры можно в общем разделить
на постоянную и транзиторную. Первая не даёт размножиться
последней
за
счёт
упомянутой
выше
колонизационной
резистентности. Поэтому долго транзиторная микрофлора в
организме присутствовать не может.
Постоянная микрофлора, в свою очередь, делится на облигатную
(обязательную) и факультативную. Облигатная микрофлора
составляет основу микробного биоценоза и задаёт условия его жизни.
В кишечнике это, например, бифидо- и лактобактерии, а также
нормальная кишечная палочка. Факультативная микрофлора может то
появляться, то почти совсем исчезать – это как будто в город на
спартакиаду приехала куча спортсменов и болельщиков, но через
некоторое время все они разъехались, и жители снова зажили обычной
жизнью. В устоявшемся микробиоценозе нормофлоры человека
процентное соотношение облигатной, факультативной и транзиторной
составляющих – около 90 : 9,5–10 : 0–0,5.
Итак, подытожим основные пункты того значения, которое несёт
нормальная микрофлора для человека:
является
фактором
неспецифической
резистентности
(сопротивляемости)
организма:
обладает
антагонистическим
свойством по отношению к патогенной и гнилостной микрофлоре за
счёт продукции кислых метаболитов и конкурентного преимущества
(та самая колонизационная резистентность);
участвует в метаболизме ряда важных веществ и соединений в
кишечнике: витаминов группы В и К, углеводов, жирных кислот,
желчных солей, стероидных гормонов;
поддерживает газовый состав и нормальную моторику
кишечника – кишечная трубка содержит слои гладкомышечных
волокон, которые позволяют ей сжиматься, но для расширения не
имеющей «скелета» кишке нужно, чтобы что-то раздувало её изнутри.
Эту функцию выполняют кишечные газы, большая часть которых
продуцируется бактериями (метанобразующими, например). Но если
значительную
часть
газогенерирующих
бактерий
занимают
продуценты сероводорода (протеи, например, или сальмонеллы в
случае заражения ими), то функция начинает дурно пахнуть в прямом
смысле слова;
оказывает значительное влияние на формирование и поддержание
местного (пейеровы бляшки кишечника) и системного иммунитета;
при
определённых
обстоятельствах
способна
вызывать
аутоинфекции (эндогенные инфекции) – микрофлора не зря
распределена по разным локусам, к условиям которых приспособилась
веками совместной с человеком эволюции; если происходит занос
микрофлоры в стерильные органы и ткани человека либо из одного
локуса в другой, то это чревато развитием гнойного воспаления. Так,
эпидермальный стафилококк с кожи часто колонизирует венозные
катетеры, откуда может попадать в кровеносное русло, что чревато
развитием сепсиса. Восходящий занос кишечной палочки по
мочевыводящим путям грозит воспалением почек – пиелонефритом, а
бактероиды, составляющие значительную часть нормофлоры,
особенно кишечной, при выходе за границы привычных локусов
(часто вследствие хирургических операций на внутренних органах)
могут вызывать абсцессы – локализованные гнойные очаги;
являются санитарно-показательными микроорганизмами: мы
уже говорили, что микрофлора каждого человека уникальна, а потому
контакт с чужой микрофлорой зачастую не слишком полезен (за
некоторыми исключениями – например, нормофлора новорождённого
во многом формируется за счёт микроорганизмов, занесённых от
матери). Кроме того, некоторые люди могут являться хроническими
или
транзиторными
(временными)
носителями
патогенных
микроорганизмов. Поэтому выявление микробного загрязнения
(контаминации) среды нашего обитания является важной задачей
санитарно-эпидемиологической службы страны. Но если у нас стоит
задача защитить, скажем, водоисточник от загрязнения шигеллами
(возбудитель дизентерии) или холерным вибрионом, то искать в
пробах конкретно их неэффективно – когда мы обнаружим патоген,
делать что-либо будет поздно, только запрещать брать воду из этой
скважины или колодца. С другой стороны, мы знаем, что холерный или
дизентерийный микробы просто так в воде не появятся – они должны
туда попасть от больного человека. А конкретно – из кишечника
больного человека, например, с содержимым повреждённой
канализации или по грунтовым водам из септика, уличного туалета и
т. п. Поэтому возле водоисточников и устраивают санитарно-защитные
зоны, а на всех этапах от скважины/водозабора до водоразборного
крана питьевую воду проверяют на маркеры фекального загрязнения –
химические и микробиологические. Последним очень часто является
наличие кишечной палочки – в норме сама она не вызывает
заражения, но её обнаружение выше допустимых норм позволяет
вовремя забить тревогу и начать искать причину ухудшения качества
воды, пока оно не привело к распространению уже настоящих
патогенов. В медицинских организациях в рамках производственного
контроля (когда клиника сама контролирует качество происходящих в
ней лечебных процессов) тоже ищут кишечную палочку в смывах с
поверхностей обстановки и оборудования. Положительная находка,
скорее всего, говорит о том, что персонал пренебрегает правилами
гигиены и дезинфекции, или плохо работает применяемое
дезсредство. А обнаружение золотистого стафилококка в смывах и
воздухе (особенно роддомов и отделений хирургического профиля)
указывает на то, что в отделении появился носитель этого условнопатогенного микроба, опасного для некоторых категорий пациентов, а
используемая система обеззараживания воздуха не справляется со
своими задачами.
А совсем недавно учёные выяснили, что даже на наши эмоции могут
иметь влияние живущие внутри нас микробы. Так, фраза: «Ты не ты,
когда голоден!» имеет куда более буквальный смысл, чем мы привыкли
считать. Как выяснилось, раздражительность и злость,
свойственные голодному человеку, в немалой степени обусловлены
метаболитами бактерий кишечной микрофлоры. Долгое время не
получая привычной порции питательных веществ, они начинают
выделять особые сигнальные молекулы, которые, всасываясь в кровь
хозяина-человека, вызывают негативные эмоции. Результаты этого
исследования не покажутся фантастичными, если мы вспомним о
других известных фактах влияния микробов на поведение
макроорганизмов-хозяев: в главе о грибах мы упоминали кордицепс,
превращающий муравьёв в зомби, и алкалоиды спорыньи,
подталкивавшие население средневековой Европы к жестоким
религиозным войнам. А ещё, возможно, вы слышали о том, как
токсоплазма, заражая грызунов, превращает их в безбашенных
отморозков, игнорирующих запахи своих врагов-кошек, в результате
чего мышки и крыски чаще становятся добычей последних, а
токсоплазма за счёт этого перескакивает на новых хозяев.
А много ли микробов в каждом из нас вовлечены в эту
увлекательную и почти недоступную нашему вниманию жизнь?
Естественно, никто не пересчитывал всех микробов в человеке. Но,
зная среднюю степень колонизации микроорганизмами каждого
локуса, площадь тела человека и примерный объём его внутренних
органов, прежде всего кишечника, можно сделать приблизительный
расчёт. Обычно говорят о 3–4*1013 микробных тел у каждого человека.
Иначе говоря – 30–40 триллионов. Собственных клеток у человека
примерно столько же – около 30 триллионов. Но! Это если считать
вместе с эритроцитами и тромбоцитами, которые как бы не совсем
клетки, поскольку в зрелом состоянии не имеют ядра, не растут и не
делятся. Если их исключить из подсчёта (а одних эритроцитов у
человека 4–5 на 1012 в каждом литре крови), то микробы резко
вырываются вперёд.
Если бы они могли выступать в суде и потребовать признать
людей скорее колонией микробов, чем человеческими организмами, то
они имели бы немалые шансы на успех. Это, конечно, шутка, как и
выражение микробиологов в отношении грубого, бестактного
коллеги: «Береги микробов – они в тебе единственная культура» (
чистой культурой , если забыли, называется совокупность
микроорганизмов одного вида, полученных из определённого
источника).
Довольно долго думали, что микробы в природе вообще и в наших
биологических жидкостях в частности так и живут – в виде отдельных
взвешенных клеток. И лишь в конце XX века выяснилось – подобных
«отшельников» в действительности лишь 5–10%, все остальные
предпочитают вести «осёдлый образ жизни» в компании себе
подобных. А иногда и не слишком подобных: так, некоторые виды
стрептококков (бактерий) в ротовой полости объединяются в
микробное сообщество с обитающими здесь же дрожжевыми грибами.
А в кишечнике «соседство» ещё разнообразнее. И поскольку
отдельным «кочующим» клеткам соседствовать сложно, то они
оседают на стенках того же кишечника в виде биоплёнки.
Биоплёнки являются настолько важными в жизни не только
микроорганизмов, но и нас с вами, и даже всей нашей планеты, что
заслуживают отдельного разговора. Пока же мы просто обратим
внимание на некоторые связанные с ними особенности кишечной
микрофлоры:
почти вся она существует в виде пристеночной биоплёнки;
в норме она находится в очень тесной сбалансированной
взаимосвязи своих компонентов друг с другом, с иммунитетом
человека и состоянием своего местообитания – очень чувствительно
реагируя на изменения любых условий;
общедоступные нам методы исследования кишечной микрофлоры
обычно не отражают истинный её состав.
Последний пункт нужно пояснить. Обычно о наличии или
отсутствии проблем с кишечной микрофлорой судят по результатам
микробиологического, в первую очередь бактериологического,
исследования кала. Для этого собирают его пробу в обязательно
стерильную ёмкость с плотно закрывающейся крышкой – такие
контейнеры продаются в аптеке, да и сама процедура наверняка вам
знакома. Даже если исключить проблемы с преаналитическим
влиянием на собранный биоматериал (мы немного говорили о
преаналитике в главе о простейших), то всё равно результаты посева
будут характеризовать только тот самый небольшой процент
«свободной» микрофлоры, которая периодически отправляется
«путешествовать», покидая родную биоплёнку. К тому же «ответ
всегда зависит от вопроса» – результат любого исследования призван
ответить на конкретный запрос врача, желающего диагностировать то
или иное состояние. Если речь идёт о диагностике инфекционного
гастроэнтерита, то здесь особенности распределения микрофлоры по
просвету кишечника особой роли не играют – патогенные
сальмонеллы, шигеллы и прочие диареегенные бактерии ещё не
успели колонизировать ЖКТ и вторгнуться в его нормальные
биоплёнки, а значит, мы «поймаем» их без особых проблем (если
только процесс не перешёл в хроническую стадию). Но если анализ на
«дизгруппу» (исследование на патогенные бактерии дизентерийной и
тифо-паратифозной группы) отрицательный, а проблема с ЖКТ
сохраняется, то тут микробиологу с инфекционистом приходится
немало поломать головы.
Можно провести исследование кала на условно-патогенную
флору. Тут уже обращают внимание на отклонения от обычного
нормального состава микрофлоры, а главное – результат выражается в
количественном виде. Например, золотистый стафилококк или грибы
рода кандида вполне могут присутствовать в кале в небольшом
количестве (см. выше таблицу состава микрофлоры разных локусов
организма), но если их содержание превышает 104 КОЕ в 1 грамме
фекалий – это повод заподозрить именно их как причину проблем с
ЖКТ.
Но в рутинной практике микробиологических лабораторий «анализ
кала на УПФ» обычно предполагает его посев только на 2–3 вида
питательных сред. Этого уже достаточно, чтобы многое сказать о
состоянии микрофлоры кишечника, однако «за кадром» тоже остаётся
немало. Поэтому существует более сложный метод – исследование на
дисбактериоз. Это уже не просто анализ, а целый комплекс анализов.
Для его проведения требуется засеять кал на несколько разных
питательных сред, причём часть посевов инкубировать в анаэростате
(в отсутствии или при пониженном содержании кислорода). Всё для
того, чтобы выяснить количество и соотношение между аэробным и
анаэробным звеньями микрофлоры, грибами и бактериями, а также
бактериями разных семейств.
На этом месте внимательный читатель может поймать нас на
противоречии и спросить: зачем так напрягаться в попытке вскрыть
соотношения между микроорганизмами в кале, если чуть выше мы
сказали, что оно всё равно не отражает истинного положения дел в
пристеночной микрофлоре? Да, действительно, биоплёнка с
микрофлорой цепко держится за стенки нашего кишечника, но всётаки часть её постоянно «ускользает» в его просвет и эвакуируется с
каловыми массами. Поэтому, зная нормальное распределение
(усреднённое из большой выборки здоровых людей) разных
компонентов микрофлоры в кале, можно судить и о состоянии её
«родины» в пристеночных зонах кишечника. Это как показатель
артериального давления, измеряемый «бескровным методом» при
помощи наложения манжеты тонометра – ничего не говорит нам о
реальном состоянии сердца, почек или сосудов человека. Но,
обнаружив его отклонение от нормального значения, мы можем
заподозрить, что с первым, вторыми или третьими что-то неладно. Так
и здесь.
Результат исследования на дисбактериоз может выглядеть примерно
следующим образом (отличается в зависимости от конкретной
лаборатории):
«Пролиферация» в данном случае означает размножение того или
иного представителя микрофлоры сверх нормы. Однако попытка
затормозить это размножение антибиотиками, как мы поступили бы в
случае типичной бактериальной инфекции, скорее всего, не приведёт к
нужному результату. Ведь антибиотики – препараты неизбирательного
действия, они «заглушат» все бактерии. И тогда на освободившееся
место придут, например, грибы рода кандида (Candida albicans или
другие). Кандидоз («молочница») – один из частых побочных
эффектов приёма антибиотиков. И вместо излечения дисбактериоза мы
получим лишь худший его вариант.
Поэтому чаще врачи заходят с другой стороны и заручаются
поддержкой «добропорядочных граждан» микробного «города». Но
поскольку разговаривать с микробами мы пока не умеем, приходится
пользоваться понятным всем в живой природе языком подарков.
Микробы не меньше людей любят вкусную еду и комфортные условия
жизни. Остаётся только дать им это!
Поэтому при явлениях дисбактериоза необходимо нормализовать
свою диету и режим питания, разобраться в причинах стрессов и
устранить их. Это должно положительно сказаться на общем
функционировании ЖКТ как среды обитания микробиоты. Хотя
одного этого, как правило, недостаточно. Дальше наступает время
«кормления» микробов! А значит, пора поговорить о пребиотиках и
метабиотиках.
Если коротко, то пребиотик – это лекарственный препарат (есть и
БАДы с пребиотическим эффектом), содержащий одно или несколько
веществ, положительно влияющих на нормофлору. Например,
углеводы (лактоза, мальтоза и т. п.), непосредственно усваиваемые
микрофлорой, или «факторы роста» для нормальной микрофлоры –
парааминобензойная кислота и т. п. Пищевые волокна (пектин,
клетчатка и т. п.), входящие в состав многих пребиотиков, не
расщепляются нашим организмом, но зато расщепляются бактериями
нормофлоры, а ещё увеличивают площадь для образования биоплёнки
и нормализуют пищеварение, что тоже важно для кишечной
микробиоты.
Чаще всего понятие пребиотиков применяют к кишечной
микрофлоре, хотя схожие по принципу действия средства используют
и при лечении дисбиозов других локусов организма – например, свечи с
аскорбиновой кислотой при бактериальном вагинозе.
Пребиотики могут быть натуральными или синтетическими, но это
вещества немикробного происхождения. В отличие от них
метабиотики являются метаболитами микробиоты – то есть
веществами, полученными от специально выращенных в
искусственной среде микроорганизмов.
Чем они лучше? Ведь янтарную или глутаминовую кислоту
(компоненты метабиотиков) можно получить и химическим путём.
Дело в том, что при химическом синтезе многих органических
веществ образуются их «рацематные смеси» из правовращающих Rмолекул и левовращающих L-молекул (имеется в виду вращение
плоскости поляризации света, проходящего через раствор такого
вещества – можете узнать подробности в Интернете или просто
примите как факт). Однако живые организмы зачастую могут
поглощать и использовать в метаболических путях только какую-то
одно форму молекул (чаще левовращающие), и синтезируют тоже
только их. Получение таких «оптически однородных» органических
соединений является важным разделом биотехнологии.
Входящие в состав метабиотиков L-аминокислоты и L-углеводы
будут лучше и полнее усваиваться нашей микробиотой, в то же время
меньше вмешиваясь в наш собственный метаболизм.
Но что делать, если в результате агрессивной антибиотикотерапии
или других обстоятельств наш «микробный город» вымер практически
целиком, в развалинах «партизанят» грибы, а жалкие остатки мирных
лактобактерий затаились по «подвалам»? Придётся заселять
микробиоту заново – и для этого служат пробиотики. Они содержат
один или несколько видов живых микроорганизмов, входящих в состав
кишечной нормофлоры: как правило, бифидо- и лактобактерии,
кишечную палочку. В качестве дополнительного компонента
пробиотики могут содержать и пребиотические вещества: углеводы,
пищевые волокна и т. п.
В последнее время пробиотики вместе с бактериофагами
позиционируют
близко
к
ИЛП
–
иммунобиологическим
лекарственным препаратам (о последних мы говорили в свете
вакцинопрофилактики инфекций). Резюмируем:
ПРЕбиотики
–
препараты
немикробного
происхождения,
улучшающие условия обитания нормофлоры, являющиеся для неё
«факторами роста» и/или питательными веществами;
МЕТАбиотики
–
препараты
микробного
происхождения
(МЕТАболиты микроБИОТы), улучшающие рост и развитие
нормофлоры;
ПРОбиотики – препараты, включающие живых представителей
нормофлоры: бифидобактерии, лактобактерии, кишечную палочку и
другие; часто в комплексе с пре- или метабиотическими
компонентами.
Ну, и стоит сказать пару слов о рационе питания, положительно
сказывающемся на состоянии кишечной микрофлоры. Во-первых,
опять-таки это должно быть правильное и сбалансирование питание,
полезное для организма в целом, потому что микробиота слишком
сильно связана с нами, чтобы нормально себя чувствовать в
недокормленном или больном организме. Во-вторых, нужно
ограничивать употребление «рафинированных продуктов» – с
повышенной питательной ценностью (за счёт жиров и легкоусвояемых
«быстрых» углеводов), но в целом обеднённым составом и почти не
содержащих пищевых волокон. В этом смысле овощи, фрукты и злаки
низкой степени переработки являются «природными пребиотиками».
И нет, этой фразой ваш покорный слуга не топит за модное нынче
веганство! Ещё раз – рацион должен быть сбалансированным, то есть в
том числе содержать животные жиры и белки как источник
незаменимых аминокислот и других биомолекул. Причём именно
«правильных» их оптических изомеров. Это важно в любом возрасте,
но особенно – для детей, подростков и молодёжи.
Наконец, практически все кухни мира включают так называемые
«ферментированные продукты» – в процессе заготовки или
приготовления подвергающиеся воздействию ферментов, изначально в
них содержащихся либо выделившихся из разрушенных клеток, или
же ферментов микроорганизмов. В последнем случае часто говорят о
брожении или сквашивании: по такому принципу образуются
простокваша и другие кисломолочные продукты, квашеная капуста,
солёные натуральным образом грибы и многие другие продукты. Если
перед употреблением они подвергаются пастеризации или другой
термической обработке, убивающей микроорганизмы, то их можно
считать продуктами с метабиотической активностью. Если же речь
идёт об употреблении, например, кисломолочных продуктов с живыми
бифидо- и лактобактериями – то это, по сути, пробиотики,
единственным недостатком которых является то, что при прохождении
кислого желудочного барьера подавляющее большинство бактерий
гибнет.
Глава 13. Эти опасные «неопасные»
инфекции
Очень часто, когда знакомые узнают, кем я работаю, то в первую
очередь просят: «Расскажи про какую-нибудь особенно злую заразу!
Про чуму там, про Эболу». В комментариях к постам на канале такое
тоже очень часто встречается.
С одной стороны, это вызывает улыбку (но не потому, что я такой
заносчивый), ведь совершенно не опасных инфекций не существует.
Даже риновирус, который у обычного человека вызовет лишь
небольшой насморк, может убить пациента с иммунодефицитом. Тут
всё зависит от стечения неблагополучных для больного обстоятельств.
А с другой стороны, интерес людей понятен. Всё, что пугает,
одновременно и привлекает. Смотрим же мы фильмы-катастрофы,
военное и криминальное кино. Да и об эпидемиях, как реальных, так и
вымышленных, написано и снято немало (некоторые произведения мы
упомянем ниже, а ещё на моём канале в Дзене «ЛекцииPROинфекции»
можно найти небольшую подборку). Я думаю, что мы просто
стараемся подсознательно подготовить себя к возможной встрече с
неприятностью, понять её причины и способы защиты. В конце
концов, со страхом можно справиться, только двигаясь ему навстречу.
И все же, дорогой читатель, должен просить прощения: в этой главе
про конкретные «чуму и Эбола» вы информацию не найдёте. Вопервых, ни с той, ни с другой мне работать не приходилось. В моём
активе лишь COVID-19, бруцеллёз да менингококковая инфекция. Ах
да, капелька крымской геморрагической лихорадки «для пикантности»
(чем не «Эбола»). И положа руку на сердце, не жалею, что у меня
такой «скромный» опыт. Во-вторых, если рассказывать обо всех особо
опасных инфекциях, получится отдельная книга – потолще этой раза в
два.
Но вот я произнёс этот термин – особо опасные инфекции – да ещё
и намекнул, что их немало. Но если, повторюсь, нет неопасных
инфекций, то какие из них всё же считаются самыми опасными, и
почему, и сколько их таких? В этой главе я постараюсь ответить на эти
вопросы, и таким образом дать представление в целом об этой
проблеме.
Говоря об особо опасных инфекциях (иногда в литературе
встречаются «особо-опасные» и даже «особоопасные» инфекции, а в
учебниках и рабочих документах – ещё аббревиатура ООИ), я бы
провёл аналогию с преступниками. Среди них есть карманники, есть
хулиганы, грабители-домушники, мошенники. Все они причиняют
своим жертвам вред. Иногда восполнимый, иногда очень серьёзный.
Например, когда в результате избиения человек остался инвалидом.
Самое ужасное преступление, конечно, это убийство – особенно
совершённое с умыслом и пренебрежением к жизни человека как
высшей ценности («с особым цинизмом» – пишут в полицейских
сводках). А бывают такие преступления, когда порча имущества или
даже убийство служат средством достижения более обширных целей –
например, запугивания населения, давления на власти и т. п. Я говорю
о терактах, конечно. Преступников, злодеяния которых вызывают у
нормальных людей оторопь и держат в страхе целые общества, пока
они разгуливают на свободе, называют «особо опасными».
Довольно несправедливо сравнивать возбудителей инфекций с
маньяками и убийцами – микроорганизмы не ведают о добре и зле, не
реализуют свою злую волю. И всё же есть такие инфекции, случаи
которых обязывают общество, власти и здравоохранение реагировать
немедленно и с максимальным напряжением сил – их ни в коем случае
нельзя оставить без внимания, даже если в это время происходят
какие-то другие серьёзные события или бедствия. Потому что данные
инфекции представляют исключительную эпидемическую опасность
из-за своей склонности к быстрому распространению в популяции или
тяжёлых последствий для заражённых (либо того и другого
одновременно) – собственно, именно так и звучит определение особо
опасных инфекций.
В начале этой книги, когда я рассказывал, как устроены
микробиологические лаборатории, то упомянул о четырёх группах
патогенности, выделенных в зависимости от склонности инфекции к
массовому распространению и способности вызывать тяжёлые формы
заболевания.
В 1-ю и 2-ю группу (самые «злые» по нашей, российской,
классификации) входит 15 бактериальных возбудителей, 4 грибка и
целых 13 групп вирусов. Это и есть исчерпывающий перечень особо
опасных инфекций (актуальную его версию можно найти в
Приложении № 1 к документу под названием СанПиН 3.3686-21
«Санитарно-противоэпидемические требования по профилактике
инфекционных болезней» – есть в свободном доступе в Интернете).
Далеко не все микробы из этого списка циркулируют на территории
нашей страны. Но нельзя забывать про такой фактор, как постоянное
перемещение людей и грузов по планете. Мы торгуем, путешествуем,
работаем в разных странах. Например, чтобы собрать один
пассажирский самолёт типа «Эйрбас», кооперируются специалисты и
производства из более чем 30 стран мира. Но, к сожалению, эти пути
сообщения создают лазейки для перемещения патогенов из одного
места планеты в другое с очень высокой скоростью. Самые разные
меры предотвращения этого собраны в обширное понятие «санитарная
охрана территории страны». И одним из условий её эффективности
является международный обмен информацией. Если у вас что-то
случилось, нельзя молчать, потому что завтра самолёты, корабли, да
хоть трэвел-блогеры на велосипедах разнесут инфекцию по всем
соседним государствам.
В нашей стране существует список из 26 инфекций, по отношению к
которым применяются меры санитарной защиты. Его можно считать
«сокращённым перечнем» особо опасных инфекций:
1. Натуральная оспа (она побеждена на планете благодаря
прививкам, но как минимум две лаборатории – в России и в США –
хранят культуру возбудителя).
2. Вирусный полиомиелит.
3. Высокопатогенный грипп человека.
4. Тяжелый острый респираторный синдром (ТОРС, англ. SARS) –
первый «предшественник» COVID-19, тяжёлая инфекция, вызванная
возбудителем из группы коронавирусов.
5. Холера.
6. Чума.
7. Желтая лихорадка.
8. Лихорадка Ласса.
9. Лихорадка Марбург.
10. Лихорадка Эбола.
11. Ближневосточный респираторный синдром (MERS) – второй
«подход к снаряду» со стороны коронавирусов в попытке вызвать
эпидемию тяжёлой инфекции.
12. Собственно коронавирусная инфекция COVID-19.
13. Малярия (вызванная любым из 4 видов плазмодия).
14. Лихорадка Западного Нила.
15. Крымская геморрагическая лихорадка (вызванная вирусом
Конго).
16. Лихорадка денге.
17. Лихорадка Рифт-Вали (долины Рифт).
18. Болезнь, вызванная вирусом Зика.
19. Менингококковая инфекция.
20. Сибирская язва.
21. Бруцеллез.
22. Сап.
23. Мелиоидоз («ложный сап»).
24. Эпидемический сыпной тиф.
25. Геморрагическая лихорадка Хунин.
26. Геморрагическая лихорадка Мачупо.
Двадцать седьмым пунктом в списке идут любые другие (в том
числе ранее неизвестные) инфекции, которые могут вызвать
чрезвычайную ситуацию в системе охраны здоровья в
международном масштабе. Такое понимание самых опасных инфекций
не противоречит нашему пониманию ООИ, а наоборот, дополняет его
в той части, когда мы сталкиваемся с чем-то новым и ранее не
известным: не хорошо знакомая чума, а какой-то новый возбудитель.
Ведь когда в январе 2020 года в далёком от нас китайском городе Ухань
стали регистрировать первые случаи тяжёлой пневмонии, никто и
предположить не мог, что следующие несколько лет «уханить» будет
весь мир. Поэтому на такие случаи и должны быть некие
универсальные правила, первоначально позволяющие локализовать
угрозу, а потом уже разбираться – достойна ли она пристального
внимания или «перебдели».
Тем более что с ранее не известными возбудителями (либо
известными, но не считавшимися серьёзными) мы сталкиваемся
ежегодно, иногда даже по несколько раз. Например, с 2020 по 2022
годы только навскидку автору этих строк в литературе и СМИ
встретились упоминания о распространении таких ранее
малоизвестных хворей, как вирус Даби, ювенильный гепатит, ну а про
оспу обезьян вы и без меня помните. Но в итоге «выстрелил» только
«ковид».
Причём если несколько расширить ретроспективу, то увидим, что
«пристреливался» он достаточно долго. Сначала в 2002 году всё в том
же
Китае
вспыхнула
«атипичная
пневмония»,
вызванная
короновирусом SARS-CoV, пока ещё без циферки 2. Спустя 10 лет на
Ближнем Востоке передающийся среди верблюдов через летучих
мышей коронавирус вызвал MERS – ближневосточный респираторный
синдром. Последний оказался слишком уж «отмороженным» – из
примерно 2,5 тысячи заболевших умерли от инфекции по разным
оценкам от 860 до чуть более 900 человек. Вирусы, имеющие такую
высокую летальность, как правило, глобальных вспышек не дают –
заражённые просто не успевают прожить достаточно долго, чтобы
проконтактировать с большим количеством народа. Правда, эта
«большая радость для человечества» служит слабым утешением тем,
до кого вирус всё же дотянулся.
Вирус SARS-CoV-2 нашёл «золотую середину»: вместо 35%
летальности у MERS он даже по первости убивал лишь 3% жёртв, а
около четверти заражённых вообще переносили его в стёртой форме,
что позволяло им протискиваться сквозь упорно (или не слишком
упорно) создаваемые карантинные барьеры и в конечном итоге
разнести инфекцию по всей планете.
И всё же многоликий ковидный возбудитель – это вирус. То есть
более или менее мы понимаем, с чем имеем дело (в отношении
вирусов менее, чем со всем остальным микромиром – наш
соотечественник Дм. Ивановский открыл, а скорее даже предсказал, их
в самом начале XX века). Но что если природа выкинет фортель и
покажет нам совсем неведомую «кузькину мать»?
Вы ведь не ожидаете, что на вас начнёт нападать ваша комнатная
герань? Вот и микробиологи всегда умилялись флоре в лице
одноклеточных водорослей – единственной группе микроорганизмов,
не пытавшихся заразить и сожрать человечество при каждом
неосторожном шаге. Правда, был известен прототекоз животных –
собак, кошек, крупного рогатого скота, – у которых несколько видов
водорослей из рода прототека (Prototheca) способны вызывать
воспаление молочных желёз, инфекцию кишечника и даже
центральной нервной системы (менингоэнцефалит). Однако недавно
были описаны случаи прототекоза у людей, в том числе закончившиеся
летальным исходом. Но в большинстве случаев это всё же пациенты с
серьёзно ослабленной по тем или иным причинам иммунной системой
– получающие системные глюкокортикостероиды, специфическое
противоопухолевое лечение, ВИЧ-инфицированные и др.
Ещё из экзотики можно упомянуть случай, когда заболевание у
человека вызвал необычный грибок. Да, грибы могут поражать
человека разными способами и на разную «глубину» – от грибка
ногтей до тяжёлых микозов внутренних органов. Однако чаще
тяжёлые инвазивные формы грибковой инфекции возникают опятьтаки как осложнение у иммунокомпрометированных пациентов. Но в
2023 году в Индии совершенно здоровый до этого человек попал в
больницу с абсцессом (локальное гнойное воспаление) в трахее. В
гное обнаружили характерные грибные клетки, однако вид
возбудителя врачам долго установить не удавалось. Когда же ответ
нашёлся, он немало удивил – в пробах присуствовал грибок
хондростереум пурпурный (Chondrostereum purpureum). Да, он
патогенный, но… для растений! У них он вызывает довольно тяжёлое
заболевание, известное как «серебряный лист». Заболевший индус
работал специалистом по защите растений и как раз имел постоянный
контакт с больными «серебряным листом» деревьями.
Можно, конечно, вспомнить, что многие возбудители инфекций
человека перешли на нас, преодолев межвидовые барьеры. Те же
новые штаммы человеческого гриппа частенько образуются в
результате мутаций и обмена генами между «животными» вирусами –
вспомним «свиной» и «птичий» грипп. Да и SARS-CoV-2 по одной из
версий возник в результате мутации одного из «звериных»
коронавирусов, до этого обитавшего в организме летучей мыши. Но
вместе со свиньями и рукокрылыми мы теплокровные
млекопитающие. То есть заведомо куда более сходны, чем со сливой
или черёмухой.
Но считать ли эти – единичные, а порой и единственные, – случаи
чрезвычайными ситуациями? Ведь даже в случае с хондростереумом
всё закончилось хорошо – мужчину полностью вылечили, да и вряд ли
подобный экзотический возбудитель получит эпидемическое
распространение среди людей. И всё же на этот вопрос нужно
ответить: «да». Ведь ранее неизвестный возбудитель на то и
неизвестный, что мы не знаем, как он себя поведёт. Кроме того, врачи
могут не располагать эффективным лекарством против него, а иногда
не иметь совсем никакого! Здесь опять приходится вспомнить COVID19 (нам ещё долго придётся часто вспоминать эту пандемию): вряд ли,
когда был выявлен первый случай ранее неизвестной инфекции, кто-то
предполагал, что очень скоро она проникнет во все уголки земного
шара, а мы будем то с отчаянием, то с надеждой ждать появления
противовирусных препаратов и вакцин.
Итак, чрезвычайные ситуации, связанные с микроорганизмами,
могут быть обусловлены следующими вариантами:
1. новые варианты привычных инфекций (высоковирулентные
штаммы гриппа, COVID-19, обезьянья оспа),
2. новые инфекции, вызванные привычными возбудителями (вирус
Даби, вирус Хабеки),
3. новые инфекции, вызванные атипичными возбудителями –
прототекоз, грибковые инфекции, протозойные инвазии, прионные
инфекции.
Прионы – белковые молекулы, которые ведут себя как
инфекционные частицы – мы упоминали в начале этой книги. К
сожалению, ввиду своей малой распространённости они остаются
недостаточно исследованными. И этот недостаток информации сам по
себе создаёт напряжённость. Врачи, учёные и чиновники
здравоохранения должны быть настороже: вдруг ситуация изменится,
прионы начнут атаковать людей, а мы не готовы!
Протозойные (вызванные простейшими) инвазии известны гораздо
лучше: да, малярия создаёт огромные проблемы, мало того – убивает
каждый год по миллиону человек. И при этом ареал её переносчиков
расширяется на север, захватывая новые территории, вплотную
подступая к Закавказью и даже нашим Тамани и Ставрополью. Но мы,
по крайней мере, знаем об этой проблеме. А вот патогенная амёба
неглерия Фоулера (Naegleria fowleri), обитающая в пресных водоёмах,
никогда раньше проблемой не рассматривалась. Пока опять-таки из-за
повышения температуры на планете не начала проявлять повышенную
активность, и случаи вызванного ею смертельно опасного
менингоэнцефалита (воспаления вещества и оболочек головного
мозга) не стали регистрироваться всё чаще и чаще.
Однако и хорошо известные инфеционные заболевания могут
создавать проблемы. Да, со многими из них успешно борются. Порой
даже удаётся полностью освободить от них целые регионы, а то и весь
земной шар. Почти наверняка вы слышали, как к 70-м годам XX века
благодаря массовой вакцинации удалось искоренить на планете
натуральную оспу. Гораздо меньше известно общественности, что из
трёх серотипов вируса, вызывающего полиомиелит (тяжёлое
заболевание, приводящее к параличу), второй и третий (PV-2 и PV-3)
также уже уничтожены благодаря прививкам. И это при том, что до
избретения вакцины в середине XX века «железные дети» (жертвы
полиовируса, которые могли дышать только благодаря искусственной
вентиляции лёгких) были настоящей приметой времени.
Но именно это «головокружение от успехов» частенько играет с
людьми злую шутку, реализуя четвёртый вариант чрезвычайных
ситуаций, связанных с микробами:
4. «возвращающиеся инфекции» – корь, туберкулёз.
Мы настолько привыкаем к тому, что инфекции перестали собирать
среди нас свою кровавую жатву, что расцениваем это не как тяжёлую
победу, плоды которой нужно сохранять, а как что-то самой собой
разумеещеся, непреложное. Отсюда проистекают отказы от прививок и
даже само абсурдное отрицание микробной природы ряда заболеваний
(мы сталкивались раньше с «ВИЧ-диссидентами», а теперь они
вернулись в виде «COVID-диссидентов»). К сожалению, подобные
веяния могут захватывать обширные массы людей и даже
поддерживаться на государственном уровне. Так, в 90-е годы в России
из-за того, что была ослаблена планомерная работа по вакцинации
населения, поднялась во весь рост практически забытая к тому
времени дифтерия. А в 2000-е годы многие страны Европы перестали
вакцинировать граждан против кори, считая её полностью
искоренённой в регионе. Однако «неиммунная прослойка» – вновь
родившиеся дети и непривитые взрослые, например, из числа
мигрантов, – со временем только растёт. А это настоящие «сухие
дрова», готовые моментально вспыхнуть, лишь только среди них
появится источник инфекции.
Так и произошло: вспышки кори преследуют Европейский регион
всё последнее десятилетие. В России из-за антиваксерских настроений
заболеваемость тоже увеличилась, хотя пока в основном она
проявляется локальными вспышками в непривитых общинах.
Дифтерия, корь, туберкулёз и другие, ранее считавшиеся
побеждёнными, инфекции могут вновь «поднять голову». Их называют
возвращающимися или «эмерджентными».
Всё вышеперечисленное было так или иначе связано с природными
процессами (хотя на примере вакцинопрофилактики хорошо видно,
как человек может влиять на них). Однако в ряде случаев человек
может быть главным фактором в распространении инфекционной
болезни. К сожалению, иногда – сознательно и злонамеренно. И это не
только
5. применение биологического оружия в военных целях, но и
6. биотерроризм (искусственные вспышки сальмонеллеза,
кокцидиоидоза). А ещё:
7. аварии на биотехнологических объектах или случайное
распространение боевых биологических рецептур.
Чем биотерроризм отличается от применения биологического
оружия? Примерно тем же, чем боевые действия регулярных армий
отличаются от подрыва в людном месте кустарно сделанной из
коммерческих химикатов бомбы. В первом случае военные сражаются
друг против друга в попытках вывести противника из строя: либо
непосредственно, либо совершая диверсии на его коммуникациях, тем
самым лишая снабжения. Мирное население при этом тоже страдает,
но попутно – оно не является целью удара, и ущерб ему обычно
стараются минимизировать обе стороны (по крайней мере, так должно
быть: об этом подписывают всяческие конвенции и за этим следят
международные организации). А вот теракты, как правило, направляют
именно на ничего не подозревающих беззащитных граждан, и цель тут
другая – посеять панику, страх, непреодолимое желание у общества
любой ценой избежать новых терактов.
Арсеналы биологического оружия в настоящее время почти во всех
странах ликвидированы – из всех видов ОМП (оружия массового
поражения) биологическое показало себя как самое потенциально
ужасное (ни ядерное оружие, ни химическое не распространяется из
первичного очага со всё возрастающей силой – наоборот, по мере
удаления от эпицентра разрушения и жертвы уменьшаются) и, по этой
же причине «самораспространения», как самое плохо управляемое.
Однако всякого рода террористы и фанатики вполне могут, заполучив
чистые культуры патогенных микробов, использовать их для создания
искусственной вспышки инфекции. Именно так они поступили в 1984
году в штате Орегон (США), заразив бактериями сальмонеллами
продукцию 10 ресторанов – от инфекции пострадал 751 человек, а
возможно, и больше, так как не все акции этой группы фанатиков были
доказаны. К счатью, никто не умер.
Однако использование биологического оружия и применение
патогенных микробов для терактов имеет явных исполнителей, а его
цели понятны. Но во второй половине XX века зародилась весьма
людоедская, надо сказать, концепция, когда противнику (не только
военному, но и политическому, или государству-конкуренту в торговле)
наносится ущерб так, что casus belli (повод к войне как ответу на
агрессию) при этом отсутствует – слишком уж события напоминают
природные стихийные бедствия. Но если целенаправленно вызвать
землетрясение или наслать ураган пока проблемно (хотя разного рода
геофизическое оружие и обсуждается), то вот микробы на эту роль
вполне подходят. Так что следующий пункт нашего печального списка:
8. применение биологических агентов в рамках экоцида.
Вообще под экоцидом (греч. «эко/ойко» – дом, «цидос» – убивать)
понимается целенаправленное разрушение экосистем на территории
противника, влекущее ущерб его сельскому хозяйству, среде обитания,
голод, эпидемии и другие последствия. А первым фактом экоцида
считается массовое применение американской армией гербицидов во
время войны во Вьетнаме (1955–1975 гг.). В густых тропических лесах
скрывались вьетнамские партизаны (и мирные жители, которых
военные не сильно горели желанием отличать от партизан), и чтобы
лишить их этой возможности, над лесами распыляли так называемый
«оранж агент» – химический состав, который не только вызывал
опадение листьев и гибель растений, но, как выяснилось позднее,
обладал тератогенным (вызывающим уродства у потомков) и
канцерогенным действием на людей и животных. В результате на
территории Вьетнама почти полностью погибла экосистема мангровых
лесов, вымерли многие виды птиц и животных, а здоровью людей на
много поколений вперёд был нанесён вред. Но поскольку этот эффект
от применения боевой химии был не запланированным, а
«сопутствующим», то появилась возможность объявить, что ничего
такого не замышлялось, а ущерб появился как бы «сам собой».
Учитывая, что Вьетнам в той войне проиграл, то ему даже извинений
до сих пор не принесли.
Сейчас, с появлением технологий манипулирования генами,
возможности использования природных патогенов для направленного
воздействия на страны и регионы «потенциальных противников»
только усилились. Путём модификации можно придать им
повышенную вирулентность или сделать «невидимыми» для обычных
диагностических тестов. Не хотелось бы мне в этой книге вдаваться в
политику и упоминать пресловутые «лаборатории Лугара» – скажу
лишь, что соблазн применить такое «тихое оружие» раньше, чем будут
оценены последствия его применения, несёт огромную опасность: не
только для жертв экоцида, но возможно, и в масштабах планеты.
– Клянусь, я этого не хотел, я не хотел! О, бедная моя страна, о
несчастный мой народ!
– Это мы бедные, а не твои! Это он нас сжигает и убивает!
– Ага! Сначала вас, а потом нас! Земля же круглая!
(киносказка «Раз, два – горе не беда», реж. М. Юзовский, СССР,
1988 г.)
Так, мы до сих пор довольно плохо представляем соэволюцию и
взаимодействие видов в паразитарных системах многих инфекций.
Например, арбовирусных – переносимых комарами, москитами и
другими подобного рода кровососущими «пискунами». Поэтому
9. незапланированный эффект от применения модифицированных
боевых патогенов
может привести к вспышкам ранее «тихого» возбудителя вследствие
спровоцированного эволюционного сдвига – не исключено, что
именно с этим была связана недавняя эпидемия вируса Зика в
Бразилии и других странах Южной и Латинской Америки.
Опасения, что микробиологические средства экоцида могут выйти
из-под контроля, не раз находили отражение в научной фантастике.
Поэтому, пока в качестве гипотетического, но выделим и такой
вариант, как
10. глобальная экологическая катастрофа по типу «серой слизи».
Сам термин «серая слизь» был предложен ещё в 1986 году Эриком
Дрекслером в книге «Машины создания» – и это была отнюдь не
фанастика, а вполне себе нон-фикшн, описывающий будущее
нанотехнологий и самовоспроизводящихся машин. Дрекслер – ученый
и инженер – описал сценарий конца света, когда наномашины,
создавая себе подобных из окружающей материи, уничтожат при этом
всю биосферу планеты. В литературу и кино данный сценарий перенёс
Майкл Крайтон – сначала в романе «Штамм «Андромеда», который
потом экранизировали в виде фильма и сериала. Но уже у Сергея
Лукьяненко в романе «Застава» «высокомолекулярная чума»
уничтожает всю нефть и пластмассу в вымышленном (и слава Богу)
мире – и это не наномашины, а микроорганизм. А собственно, чем
одни отличаются от других? Только лишь тем, что при слове «машина»
мы привыкли представлять что-то металлическое, на худой конец –
кремниевое? Но что мешает вам создать микроб с записанной в геноме
биологической программой на разрушение тех же полимеров или
выделение веществ, ускоряющих коррозию металлов? Вам даже не
придётся ничего изобретать – нужные ферменты уже существуют в
природе! Всего лишь и нужно: решить управленческую задачку
«время–специалисты–затраты», чтобы соединить нужные компоненты
в «готовом продукте». В другом фантастическом романе
(«Мутант-59» – К. Педлер, Дж. Дэвис) с этим вообще справился одинединственный учёный, который искал средство для борьбы с
пластиковым загрязнением (реальная проблема для современного
мира) и случайно упустил в городскую канализацию штамм бактерий,
разрушающих пластмассу. Так что последним «фантастическим»
вариантом чрезвычайной ситуации, вызванной микробами, назовём
11. выход из-под контроля небоевых биологических агентов с
последующей экологической и/или техногенной катастрофой.
Вы можете обвинить меня в том, что я начал с серьёзного, а
закончил фантастикой. Но считать научную фантастику несерьёзной –
почти то же самое, что легкомысленно относиться к экспериментам с
геномами микроорганизмов. Фантасты не просто описывают новые
технологии – они говорят о проблемах людей, которые рождаются при
появлении этих технологий (вспомните хотя бы классические
«Двадцать тысяч лье под водой» – да, там есть крутая подводная лодка,
но сюжет двигает не она, а конфликт одного инженера с
несправедливостью мирового порядка). И на эти, вроде
фантастические, вопросы лучше реально ответить уже сегодня.
бы
Глава 14. Неси, не расплескай!
И вот мы подошли к последней главе. А помните, в предисловии я
пошутил, что написал эту книгу, преследуя собственные цели? Открою
вам ещё одну такую «собственную цель». Есть у меня надежда, что
некоторые из моих юных читателей, ещё только определяющихся со
своим дальнейшим путём в жизни, проникнутся великолепной
сложностью микробного космоса, и захотят так или иначе связать свою
жизнь с его изучением. Из этой книги вы узнали, что микробиология
охватывает множество сфер нашей жизни, и в конечном итоге выбор
может занести вас и в геологию, и в растениеводство, и в поиск новых
лекарств, и много куда ещё. Но больше всего, конечно, я жду будущих
коллег – не только медицинских микробиологов, но и просто
медработников.
Но я был бы не я, если не решил заранее предупредить последних о
тех превратностях служения медицине, с которыми им так или иначе
придётся столкнуться. Разговор будет слегка шутливым, чтобы уж
совсем не отпугнуть от выбора медицинского будущего, и связан
только с одним аспектом – проведением анализов. Но и этого, думаю, с
лихвой хватит для впечатлений. Итак, начнём…
Стороннему наблюдателю может показаться, что нет ничего проще,
чем взять и принести в лабораторию биологический материал на
исследование. В действительности это не так.
Поскольку мы в основном говорим о медицинской микробиологии,
то здесь биологическим материалом, подлежащим исследованию,
будут являться биологические жидкости пациента, а иногда даже
небольшие фрагменты его тела (кусочки тканей, полученные при
биопсии, мазки-отпечатки с органов и т. п.).
Несколько реже в клинике исследуют объекты больничной среды
(смывы с поверхностей, рук медперсонала, пробы воздуха и другое), но
в 99% случаев этим занимаются специально обученные сотрудники
микробиологической
лаборатории
(в
целях
внутреннего
производственного контроля) или центра госсанэпиднадзора (при
проведении плановых комиссий или в рамках расследования случаев
внутрибольничного инфицирования).
А раз придётся контактировать с пациентом и получать от него
биологический материал, то это уже полноценная медицинская
процедура – одна из составляющих процесса оказания медицинской
помощи. А к этому процессу предъявляются два ключевых
требования: это соблюдение качества и безопасности.
Мы сознательно не будем здесь давать определение качества
оказания медицинской помощи, которое вы и так получите на курсе
основ организации здравоохранения. Применительно к нашей теме
лучше скажем, что качественно проведённый анализ означает
следующее:
врач
получит
ответ
на
интересующий
его
диагностический вопрос. Есть ли у больного та или иная инфекция,
какие препараты будут эффективны для лечения, правильно ли это
лечение продвигается и так далее. Что здесь может пойти не так? Да
что угодно на самом деле! Начать хотя бы с того, а у нужного ли
больного взят анализ. Каким бы курьёзным это ни казалось на
посторонний взгляд, а идентификация пациента представляет собой
очень важный вопрос, а иногда и проблему.
Представьте ситуацию: медицинская комиссия в военкомате.
Согласно действующему законодательству, призывники подлежат
обязательному обследованию на ВИЧ-инфекцию, гепатит В и С,
сифилис – для этого у них берут кровь на серологическую
диагностику. И именно вас «посадили на забор» (профессиональный
сленг медиков весьма забавен, это вы ещё «на посевах» не были). По
идее, у каждого парня в руках личное дело: смотри в него и
переписывай данные в направления и на пробирки с забираемой
кровью. А по факту вокруг вас будут галдящий вихрь подростков,
рыкающий бас военкома и куча других отвлекающих факторов. Если
позволите себе поддаться этому хаосу и утратите контроль, то можете
либо сами «по запарке» перепутать пробирки, либо кто-то сознательно
вам «поможет» ошибиться – сдаст кровь за другого человека,
например. Может, от желания что-то скрыть, а может и просто «в
шутку».
Моделируем ситуацию дальше: в лаборатории одна из проб
забранной вами крови покажет положительный результат на ВИЧ, её
отправят в референс-лабораторию, и если там результат подтвердится,
то начнут искать того, кто её сдал. В конечном итоге в региональном
Центре-СПИД у «плюсанувшего» повторно возьмут кровь и… ничего
в ней не найдут. Оставим за скобками самого несчастного призывника,
пережившего несколько неприятных дней в ожидании того, что у него
подтвердится / не подтвердится весьма неприятный диагноз. Но теперь
эпидемиологи вынуждены будут начать расследование – ведь у кого-то
из обследованной партии точно есть ВИЧ, и нужно выяснить, у кого
именно. А значит, нужно будет проследить в обратной
последовательности всю цепочку от лаборатории до всех пунктов, где
в тот день забирали кровь, отыскать всех сдававших и заново их
обследовать. А речь идёт о десятках, а то и сотнях людей со своими
делами и проблемами, не сидящих на месте в ожидании, когда за ними
придёт эпидемиолог. И каждому нужно будет объяснить, извиниться,
убедить повторить анализ. К тому моменту, когда удастся выйти на
ситуацию в военкомате, может быть потрачена уйма сил, средств и
человеко-часов труда. А когда ВИЧ-положительный призывник, к тому
времени уже военнослужащий, наконец отыщется, военное
руководство задаст резонный вопрос руководству здравоохранения: вы
кого в войска отправляете, трам-та-ра-рам, и кто теперь за это
ответит?! И раз уж ситуацию удалось отследить, то станет известно и
то, чьи дрожащие ручонки (спойлер: ваши) перепутали пробирки. И
хорошо если вы за это ответите только выговором и лишением премии,
а не сразу – диплома.
Может показаться, что в стационаре всё проще, ведь там
идентификация пациента происходит в начале госпитализации. И в
этом заблуждении вы можете пребывать ровно до того момента, пока
не зайдёте в реанимацию или ПИТ (палату интенсивной терапии), где
вашему взору предстанут 2, 4, а может и больше «загруженных»
седативными препаратами пациентов с трубкой ИВЛ в горле, которые
и «мама» сказать не могут, а не то что назвать вам свои паспортные
данные. Причём у дежурной медсестры могут быть гораздо более
важные дела, чем искать для вас среди них «больного Иванова». В
идеале это должно решаться наличием у таких пациентов
индивидуальных идентификационных браслетов. В крайнем случае –
табличкой на койке. Но в суровой реальности вместо браслета может
быть надпись фломастером по памперсу (сильно повезёт, если яркая и
разборчивая), а на кровати только что выписанного Иванова может
лежать минуту назад поступивший Сидоров.
Хорошо, допустим, что взятая кровь действительно принадлежит
искомому «пациенту Иванову». Частенько, если предусматривалась
выдача результатов анализа «на руки», то граждане так и спрашивают
в лаборатории: «Дайте мне результаты моей крови». Уточняющий
вопрос «А на что сдавали?» процентов 80 из них ставит глубоко в
тупик. Тот факт, что кровь может подлежать исследованию на
биохимические
параметры,
общему
анализу,
исследованию
серологическими методами и ещё куче всего, их особо не интересует –
«Врач разберётся!».
Хуже, если и медицинскому работнику не хватило времени (знаний,
желания – подставить свой вариант) уточнить, какой именно
биологический материал и как требуется получить сообразно с целями
будущего исследования. Простой пример – пациенту инфекционного
отделения с высокой температурой назначены общий анализ крови с
лейкоформулой и посев крови на стерильность. Если медработнику
хотя бы в общих чертах не понятно, как выполняется то и другое, то,
пожав плечами, он заберёт у пациента две одинаковые пробирки крови
из вены или ЦВК (катетера) – «А чотакова? И тут, и там кровь же».
Однако кровь, взятая в стандартную чистую пробирку, годится для
общего анализа, но для посева на стерильность пробирка должна быть,
на секундочку, стерильной, а условия отбора крови – асептическими,
то есть исключающими проникновение в пробу микрофлоры с
поверхности кожи пациента, рук медика, из воздуха и так далее.
Учитывая, что ожидание результатов посева крови на стерильность
стандартными методами и так достаточно долгое (до 10 суток), то
задержка на повторный отбор пробы для врача выльется в несколько
дополнительных дней неведения, то есть, вероятно, неправильного
лечения. А пациенту, соответственно, может стоить здоровья, а то и
жизни. Снова вспоминаем ту самую подкову, на которую не нашлось
гвоздя.
Такое длинное вступление понадобилось, чтобы наглядно показать:
при, казалось бы, простой процедуре медработника поджидает немало
подводных камней, и одновременно от неё зависит многое в
диагностическом процессе. Теперь давайте последовательно
пройдёмся по всем этапам подготовки и получения биологического
материала от пациента. Некоторые из них общие для любых видов
лабораторных исследований, но всё же мы будем акцентировать
внимание с учётом того, что готовим микробиологическое
исследование.
Наверняка, прежде чем вам в вену воткнут иглу, вам захочется
узнать, для чего в принципе это делается (и вообще, может, без этого
можно обойтись?). Как-то спокойнее, когда присутствует ощущение
контроля над ситуацией. Плюс можно отсечь некоторые ошибки
идентификации из разряда «так я ж не Иванов, его койка у окна». На
языке методической документации данный процесс называется
получением добровольного информированного согласия на
проведение
медицинской
манипуляции.
Согласие
пациент
подтверждает подписью в специальном документе с одноимённым
названием. При оказании стационарной помощи «согласие»
подписывают в момент госпитализации, в поликлинике – обычно один
раз в год, при первом в текущем году обращении за медицинской
помощью. Однако, во-первых, пациент может отозвать согласие в
любой момент, то есть никто не может заставить его (или вас, если вы
находитесь на месте пациента) сдавать какие-либо анализы, если он
того не желает. Если в результате этого дальнейшее оказание
медицинской помощи становится невозможным, то это уже повод
разрешать ситуацию с привлечением медицинского юриста. Вовторых, ряд процедур и манипуляций требует дополнительного
информирования – например, при взятии крови для исследования на
ВИЧ в обязательном порядке должно быть проведено так называемое
«предтестовое консультирование».
Ничего экстраординарного оно не предполагает – просто нужно
спокойно объяснить, что именно эта порция крови забрана для
определения ВИЧ, что это входит в стандарт оказания помощи при
данной болезни (практически для всех хирургических болезней, травм,
при переливании крови и множестве других), и что никаких
подозрений в отношении пациента у вас нет, и вообще – 30
процентов населения страны ежегодно обследуются в рамках так
называемых скрининговых (мониторинговых) показаний, и это обычно
и нормально.
При получении добровольного информированного согласия есть ряд
нюансов. Подростки могут давать его самостоятельно с 14 лет, за детей
младше этого возраста согласие выражают родители или законные
представители (бабушки, братья, дяди и тёти не могут выступать
законными представителями просто по факту своего родственного
отношения – это право должно быть закреплено за ними юридически
через назначение опеки). За недееспособных взрослых лиц согласие
дают их опекуны. Отдельная ситуация, когда пациент (взрослый или
ребёнок, неважно) находится без сознания и в жизнеугрожающем
состоянии (в результате ДТП, травмы, инсульта и т. п.) – формально,
без согласия оказывать ему помощь нельзя, но тогда он умрёт. В этом
случае согласие выражают близкие родственники, степень родства
которых можно подтвердить документально (не просто так в паспорт
ставят штамп о регистрации брака и пишут данные детей).
Кстати, поэтому неплохо бы носить в бумажнике или паспорте
записку «В случае непредвиденных обстоятельств прошу сообщить
обо мне по телефону такому-то маме Светлане Ивановне (жене
Надежде, адвокату Шнепперсону)», чтобы при наступлении этих
самых непредвиденных обстоятельств медикам и полицейским не
пришлось подбирать пароль к вашему заблокированному смартфону
(который к тому же может быть разряжен, разбит, потерян и
т. д.)
Если родственников нет рядом или от слова «вообще», то
необходимость оказания помощи (в том числе и взятия биологического
материала) обосновывается консилиумом врачей, в составе которого
присутствует не меньше чем заведующий отделением, а в идеале –
начмед или юрист больницы.
К слову, ещё более строго следует подходить к сообщению
результатов выполненных анализов. Они составляют часть
медицинской тайны пациента. Разглашение которой, как намеренное,
так и ненамеренное, может повлечь за собой даже уголовное
наказание. Многострадальный ВИЧ здесь снова как пример, хотя
сохранять в тайне нужно любые анализы. Например, работодатель
пациента не обрадуется, узнав о развитии у того болезни, которая в
скором времени приведёт к инвалидности. Медицинская тайна
предполагает личный характер, то есть из числа медработников её
должны знать только лечащий врач и те, кому она действительно
нужна для выполнения своих профессиональных обязанностей или в
ходе этого выполнения стала известна (врач или лаборант в
лаборатории). То есть даже другому медработнику отделения, если он
не занимается данным пациентом, сообщать эти данные запрещено.
Равно и пациент может решить не сообщать свой диагноз или
отдельные результаты анализов другим людям, в том числе и
родственникам, поэтому в общении с ними медработнику также нужно
контролировать свой язык, если доподлинно не известно, что они
посвящены в медицинскую тайну. Исключение – опять же
недееспособные пациенты, в том числе дети, и больные в
бессознательном состоянии.
Не обязан пациент и сообщать медработнику, что он заражён какойлибо инфекцией, тем же ВИЧ или гепатитом В либо С. Однако это не
лишает его права на оказание медицинской помощи. Поэтому к
любому пациенту по действующим санитарным нормам должны
применяться подходы, как если бы потенциально он был заражён –
отсюда следует необходимость использования медработником при
отборе биологических материалов спецодежды и средств
индивидуальной защиты (перчаток, маски, фартука, защитных очков
или экрана). К тому же пациент, вообще говоря, может и сам не знать,
что инфицирован. К вопросу безопасности мы ниже ещё вернёмся.
Помимо результатов анализа, неотчуждаемым является и сам
биологический материал пациента. В переводе с юридического на
разговорный это значит, что если человек не дал отдельного согласия,
то с его биологическим материалом нельзя проводить никаких других
исследований, кроме назначенных, даже в научных целях. То есть
остатки крови и сывороток подлежат обеззараживанию и правильной
утилизации – хотя в большей степени это делается с целью
недопущения
контакта
с
потенциально
инфицированным
биоматериалом других сотрудников больницы и лаборатории.
Есть,
правда,
некоторые
исключения.
Например,
в
микробиологических лабораториях зачастую поддерживается так
называемый «музей культур» – образцы микроорганизмов, выделенных
от пациентов или с объектов больничной среды. Они нужны для
мониторинга внутрибольничных инфекций или сравнения свойств
микробов в ходе работы. Так вот, если условная моча всецело
принадлежит «больному Иванову», то выделенная из неё синегнойная
палочка – уже нет. Кроме того, так называемые «утильные
сыворотки» и другой биоматериал иногда всё же допускается
изучать в научных целях при условии «обезличивания», то есть когда
это уже не «кровь Иванова», а «проба крови № 100500». Правда,
зачастую возможность восстановить принадлежность такой
зашифрованной пробы тем или иным способом сохраняется, и если в
ней найдут, скажем, неизвестный науке микроорганизм, то его даже
могут назвать именем пациента, как, например, вирус редкого
гепатита SenV или известная линия клеточной культуры HeLa ,
некогда полученная от пациентки Генриетты Лакс ( He nrietta La
cks).
Вопросы идентификации пациента и получения у него
добровольного информированного согласия на сбор биоматериала
относятся к так называемому преаналитическому этапу
исследования. Преаналитика включает в себя всё, что предшествует
собственно проведению анализа в лаборатории.
Например, одним из распространённых исследований является
общий анализ крови (ОАК). В ходе него определяется содержание
разных фракций форменных элементов, выраженное в пересчёте на 1
литр крови (подробнее см. раздел о лейкоформуле). Так вот, когда мы
совершаем какую-либо физическую нагрузку, бежим, например,
содержание эритроцитов и лейкоцитов в крови компенсаторно
увеличивается – они выбрасываются из так называемых «депо»
в селезёнке и печени (см. органы иммунной системы). Это
естественный и эволюционно выработавшийся процесс – когда-то
давно наши далёкие предки бежали вслед за добычей или удирали,
чтобы самим этой добычей не стать. В этой гонке выживали либо
быстроногие и выносливые, чья кровь приспособилась переносить
больше кислорода, либо сумевшие выжить после схватки со зверем,
что было сопряжено с получением травм и ран. А их залечивание в
отсутствие медицины всецело лежало на иммунной системе. Но сейчас
нам уже не нужно бегать за мамонтом или от саблезубого тигра, мы
скорее бегаем за маршруткой в час пик или для своего удовольствия и
пользы – на стадионе. Однако наши компенсаторные механизмы
продолжают работать, как и тысячи лет назад. И если сдать кровь на
ОАК после достаточно интенсивной нагрузки, то показатели довольно
сильно будут отличаться от нормальных, установленных для состояния
покоя. Интерпретировать такой анализ окажется крайне сложно.
Другой пример: все, кто когда-либо сталкивался со сдачей крови для
анализов, знают, что это нужно делать натощак. Применительно к
биохимическому
анализу
требование
интуитивно
кажется
обоснованным – как минимум содержание глюкозы и холестерина
зависит от приёма пищи. Но значит ли это, что для других
исследований требованием сдачи натощак можно пренебречь? В
подавляющем большинстве случаев нет. Дело в том, что через ЖКТ из
пищи в кровь всасываются не только водорастворимые соединения
(глюкоза и другие углеводы, аминокислоты и т. п.), но и
нерастворимые: в основном липиды – триглицериды, холестерин и т. д.
Чтобы не забить наши сосуды напрочь, они должны сначала
образовать
комплекс
с
определёнными
белками
(стать
липопротеинами) и сформировать мельчайшие капельки –
хиломикроны. В таком виде липиды уже могут транспортироваться в
лимфатической системе, откуда затем попадают в кровь. Поэтому
вскоре после приёма пищи хиломикрон в крови очень много. И если в
этот момент взять венозную кровь на анализ, то они попадут в пробу.
Проблема в том, что хиломикроны очень малы – самые крупные из них
чуть больше микрона (эритроцит, для сравнения, 6–8 мкм в диаметре)
– а следовательно, очень лёгкие и не оседают, как форменные
элементы, при центрифугировании. Полученная сыворотка крови
будет хилёзной – вместо светлой и прозрачной жидкости окажется
похожей на молоко (от греческого «хилос» – млечный сок растения –
происходит и термин, и название хиломикрон). Такая сыворотка плохо
подходит для серологических реакций, потому что хиломикроны будут
мешать образованию иммунных комплексов «антиген–антитело» и их
дальнейшему выявлению – в большинстве тест-систем для ИФА и
ИХА оно основано на цветной реакции. Мутная сыворотка помешает
считыванию такой реакции даже глазом, а уж оптику автоматических
приборов точно сведёт с ума. Для классических бактериологических
исследований хилёз крови тоже составляет проблему, поскольку
деградирующие под влиянием ферментов крови липиды не добавляют
точности анализу.
Очень часто за время лечения один и тот же анализ выполняют
несколько раз – в динамике – чтобы оценить эффективность лечебных
мероприятий. И здесь крайне важной характеристикой становится
воспроизводимость анализа – то есть на его результат не должны
влиять никакие посторонние факторы, кроме рассматриваемого
аспекта состояния организма: ни навыки лаборанта, ни модель
анализатора, ни что-либо ещё. Воспроизводимость – важный
показатель качества анализа. А преаналитика оказывает очень
большое влияние на воспроизводимость. Именно поэтому важно
анализы в динамике сдавать так, чтобы все преаналитические
параметры оставались неизменными: в одно и то же время суток, в
состоянии полного покоя, натощак, да и накануне лучше избегать
сильных отклонений от щадящей диеты, не говоря уже о возлияниях.
Даже положение тела пациента (сидя, лёжа) при взятии крови может
отразиться на ряде параметров! Очередной приём лекарственных
препаратов тоже откладывают до момента после сдачи анализов.
Особенно это важно в отношении микробиологических исследований
и антибиотиков.
Биологический материал для микробиологических исследований
отбирают до начала приёма антибиотиков (и противогрибковых
препаратов) либо через 3–4 дня после окончания курса их приёма. В
противном случае получить адекватные результаты становится почти
невозможным. И это, кстати, ещё один аргумент в пользу отказа от
«самоназначенного» приёма антибиотиков/антимикотиков.
Преаналитика предполагает и минимальность влияния на состояние
пробы методики её получения. Скажем, при взятии капиллярной крови
(из подушечки пальца) запрещается «доить» палец – активно
выжимать кровь из прокола. Это приводит к деформации её
форменных элементов, особенно эритроцитов. Аналогичное
требование существует и при взятии венозной крови. Раньше эта
процедура часто выполнялась при помощи иглы шприца с широким
просветом. Но и тогда предписывалось не использовать сам шприц, то
есть не насасывать кровь в его цилиндр активным движением поршня,
создавая ударные нагрузки на клетки крови. «Освоив вену», надлежало
отсоединить шприц от иглы и позволить крови самотёком заполнить
подставленную пробирку. Если всё же для отбора использовался
шприц, то по крайней мере сливать кровь в пробирку нужно,
предварительно сняв иглу. Во-первых, это позволяет избежать
повреждения форменных элементов крови, во-вторых, бывали случаи,
когда давлением сбрасывалась игла с канюли шприца, что чревато
разбрызгиванием крови.
Почему так важно щадить форменные элементы крови? Потому что
деформация мембраны спустя короткое время чаще всего приведёт к
полному её разрыву – лизису клетки. Состояние массивного
разрушения форменных элементов крови называется гемолизом. За
счёт того, что основную массу форменных элементов составляют
эритроциты,
то
полученная
после
центрифугирования
гемолизированной крови сыворотка содержит большое количество
выделившегося из них гемоглобина. На вид она вместо желтоватой
прозрачной жидкости выглядит мутно-красной. Такая сыворотка
непригодна для большинства общеклинических и серологических
исследований.
Сейчас процедура отбора венозной крови выглядит проще за счёт
вакуумированных пробирок – «вакутейнеров», «сарштедтов» и их
аналогов. В первых вакуум внутри создаётся на заводе путём
откачивания воздуха. У вторых медработник создаёт его сам, выдвигая
поршень как у обычного шприца – только в задней точке поршень
застопоривается, а вместо обычной канюли в таком «шприце»
находится клапан, блокирующий поступление внутрь воздуха. В
результате внутри герметичного цилиндра образуется разрежение. При
подсоединении вакуумированной пробирки к игле-переходнику кровь
активно засасывается внутрь, но это усилие дозировано
разработчиками пробирок так, чтобы минимально повреждать
форменные элементы. Кроме того, данные пробирки внутри
стерильны, а кровь при таком методе не контактирует с воздухом,
значит, создать асептические условия отбора становится намного
проще.
Асептика (предупреждение попадания любой микрофлоры)
особенно важна как раз для микробиологических исследований, о чём
мы выше уже упоминали. Вся посуда, все инструменты для отбора
проб в микробиологии должны быть либо продезинфицированы, либо
(и чаще всего) стерильны. Но и сама методика отбора должна
предполагать минимизацию контакта с микрофлорой.
Далее для исследования на стерильность или получения
гемокультуры кровь должна быть посеяна на питательные среды. То
есть микробиологам стерильную пробирку всё-таки придётся открыть
– как правило, это делается в условиях микробиологического бокса
(бокса биологической защиты). Посевы мокроты, мочи на содержание
микрофлоры обычно выполняют там же. Но для микробиологических
целей та же моча должна быть взята правильно – и совсем не так, как
на общий анализ. Снова понадобится стерильный флакон.
Предпочтительно использовать мочу, собранную после ночного сна.
Сбор мочи выполняют после туалета наружных половых органов,
которые обсушивают стерильной салфеткой. Первую порцию мочи,
априори содержащую микрофлору из уретры, спускают в унитаз или
судно.
Аналогично и с мокротой из лёгких – она должна быть как можно
меньше
контаминирована
слюной,
неизбежно
содержащей
микрофлору ротовой полости. То есть сначала чистим зубы и полощем
рот, потом – здравствуй стерильный флакончик.
Однако если вам требуется получить носоглоточный смыв или мазок
из носоглотки (стали широко известны в период пандемии COVID-19),
либо из ротоглотки (также известен как «мазок из зева»), то здесь
подход меняется на противоположный. Никаких чистки зубов и
полоскания рта за 2 часа до взятия анализа, и на это же время
исключить приём пищи и воды – иначе слизь с микроорганизмами
просто смоется, и анализ ничего не покажет.
Определённые требования предъявляются также к свойствам и
материалам зондов для отбора проб. Они должны обеспечивать
надёжное впитывание (абсорбцию) биоматериала, и в то же время
материал должен легко выделяться из них при посеве или погружении
в жидкую питательную среду. Материал тампона не должен оказывать
влияния на состояние пробы или жизнедеятельность микроорганизмов
в ней. Для каких-то анализов допустимы стерильные ватные тампоны
на деревянном стержне. Но, например, для ПЦР-исследований (тех же
«мазков» для определения SARS-CoV-2) натуральные материалы не
подходят: используют вискозные или синтетические тампоны на
пластиковых стержнях.
Иногда такой тампон является компонентом транспортной
системы для доставки биоматериала – «сваба». Сваб включает,
помимо зонда, стерильную пробирку, зачастую содержащую некоторое
количество транспортной питательной среды, в которую зонд с
отобранным биоматериалом погружается (обычно используют
полужидкие питательные среды, имеющие консистенцию густого
киселя – они практичнее по сравнению с жидкими, так как не
растекаются). Свабы широко используются в клинической
микробиологии. Они просты в применении и позволяют любому
обученному обращению с ними медработнику провести первичный
посев биоматериала прямо у постели больного. Их удобно
транспортировать, а за счёт наличия питательной среды свабы
увеличивают выживаемость микроорганизмов в биоматериале.
Вообще говоря, транспортировка биологического материала,
особенно для микробиологических целей, представляет отдельный
сложный вопрос. Для общеклинических исследований допускается
время транспортировки до 2 часов (например, от удалённого ФАПа до
центральной лаборатории), если нет показаний к срочному
выполнению (срочность определяет врач и делает на бланке
направления специальную пометку для лаборатории – cito! – «цИто!
срочно!»). Для микробиологии в идеале биоматериал должен
доставляться немедленно, так как любое пребывание вне тела человека
чревато либо гибелью микроорганизмов, либо их чрезмерным
размножением.
Удлинить время хранения и транспортировки можно за счёт
некоторых приёмов. Со свабами вы уже познакомились. Однако даже
на свабах с транспортной средой нужно соблюдать условия хранения,
зависящие от объекта исследования. Так, вы уже знаете, что вирусы не
могут размножаться самостоятельно. Поэтому вне тела человека
содержание вирусов в биологической жидкости с течением времени
может только уменьшаться. Чтобы сократить деградацию вирусных
частиц, пробы для вирусологических и ПЦР-исследований хранят в
холоде (иногда даже замораживают), а транспортируют в
термоизолирующих контейнерах с хладоэлементами или специальных
переносных холодильниках. В крайнем случае, используют
промаркированные знаками биологической опасности термосы со
льдом. В транспортную среду для вирусов добавляют буферный
раствор, стабилизирующий её pH (кислотно-щелочное состояние), и
консервант – чаще всего антибиотик широко спектра действия, чтобы
предотвратить бактериальный зарост пробы.
С пробами для бактериологических исследований всё с точностью
до наоборот – холод им противопоказан, большинство бактерий при
температуре ниже 370С начинают гибнуть. Поэтому в холодное время
года или если предполагается наличие особо «мерзлявой» бактерии –
менингококка, например, – пробы для исследований доставляют в
контейнере с грелкой. Транспортные среды применяют специальные,
содержащие ростовые факторы для поддержания бактерий в процессе
хранения и транспортировки. Некоторые транспортные среды
обладают селективными свойствами – ограничивают рост условнопатогенной флоры, которая может ингибировать развитие искомого
микроорганизма.
Если для транспортировки используют не свабы или другие
герметично закрываемые ёмкости, а стерильные микробиологические
пробирки с хлопковыми (для доступа воздуха к растущим
микроорганизмам) пробками, то доставлять их нужно в штативе в
вертикальном положении, избегая наклонов и переворачивания
транспортного контейнера. Даже если биоматериал не выльется при
таком неосторожном обращении, то жидкое содержимое пробирок
смочит пробки, и они перестанут быть преградой для внешней
микрофлоры.
Как видите, преаналитический этап содержит большое количество
разнообразных факторов и нюансов, влияющих на конечное качество
исследования:
идентификация пациента и правильное оформление направления на
исследование;
получение согласия пациента на исследование (юридический
аспект);
пробоподготовка пациента (соблюдение диеты, исключение высоких
физических нагрузок за день до исследования, отбор натощак, в
состоянии покоя, до приёма лекарственных препаратов);
подготовка места (локуса) отбора материала в зависимости от цели
исследования – асептически, после обработки либо наоборот,
исключая внешнее воздействие перед отбором (особенно актуально
для микробиологических исследований);
выбор оборудования и инструментов для отбора пробы в
зависимости от цели исследования (стерильные или чистые пробирки,
свабы со средой или без, тампоны нужной длины и из
соответствующего материала и т. п.);
соблюдение методики отбора пробы;
соблюдение допустимого времени и условий хранения пробы.
На качество оказывают влияние как человеческий фактор
(вспомните начало главы, где мы описывали ситуацию в военкомате),
так и другие факторы, условно говоря, «внешние» и «аппаратные».
Так, при помощи вакутейнеров за одно и то же время можно взять
больше проб, чем шприцами и пробирками, при этом условия отбора
будут стабильнее, а утомляемость медработника уменьшится. Кроме
того,
объём
выполненной
работы
в
единицу
времени
(производительность) будет выше в помещении с хорошим
освещением и комфортными температурным и влажностным
режимами. Наконец, делая небольшие перерывы через определённые
промежутки времени, можно сделать больше, а главное, с меньшим
числом ошибок, чем если «упахиваться без передыха».
Однако если вручить вакутейнер медработнику, который никогда
раньше с ним не работал, то никакие суперкомфортные условия и
отдых не помогут – первое время он всё равно будет работать
медленно и делать ошибки, пока не выработает навык. Но и этот
процесс можно сократить и облегчить, если существует чёткая
инструкция по данной методике (например, в клинике разработана
СОП – стандартная операционная процедура – по методике забора
венозной крови вакуумированными пробирками), а медработнику
помогает и страхует его наставник (более опытный сотрудник или
старшая медсестра отделения).
Ровно те же факторы влияют и на безопасность проведения
медицинских процедур, в том числе отбора биологического материала
на исследования:
человеческий фактор (степень подготовки сотрудника, степень его
усталости);
факторы окружающей среды или рабочего процесса (освещение,
температура, влажность на рабочем месте, приемлемый уровень шума,
приток свежего воздуха, отсутствие отвлекающих факторов, удобная
организация рабочего места, не вынуждающая тянуться или бегать по
кабинету за тем или иным предметом, принимать неудобную
вынужденную позу и т. п.);
оборудование и материалы, применяемые в работе (легко ли они
бьются с образованием острых осколков, имеют ли острые детали,
которые нельзя закрыть защитными кожухами, легко ли из них
проливается биоматериал и т.п.).
На последнее часто обращают больше внимания, потому что это
осязаемые и легко учитываемые вещи, однако в действительности для
улучшения качества и безопасности нужно учитывать все группы
факторов. Хотя никто не отрицает, что переход на лабораторный
пластик вместо хрупких стеклянных пробирок резко облегчает труд
медсестёр и лаборантов. Зачастую лабораторные анализаторы
полностью приспособлены под закрытый цикл работы с такой
пластиковой посудой: кровь или другой материал герметично
укупорены в них, их легко переносить даже просто навалом без
штатива, аппарат сам забирает из них дозированную порцию для
анализа, а использованную пробирку легко утилизировать (чаще всего
их «спекают» термическим путём с последующим измельчением –
обеззараженные таким образом, они становятся абсолютно безопасны,
и их можно утилизировать как обычные бытовые отходы).
Вообще, безопасность – это понятие, противоположное опасности,
то есть состоянию угрозы, когда объекту потенциально может быть
нанесён вред. Вероятность, с которой этот потенциал реализуется
(«Бахнет или не бахнет?!»), называется риск, и он, следовательно,
бывает высоким или низким. А при медицинском процессе рисков
создаётся достаточно много – мы, на минуточку, острым в пациента
тыкаем по несколько раз на дню и лекарства вводим, многие из
которых в определённой дозе токсичны.
«Всё есть яд, и всё есть лекарство. Одно от другого отличает
доза», – Парацельс, XV век.
Естественно, не все эти риски можно полностью устранить, но
уменьшить до низкого или приемлемого значения – реально.
Однако наибольшие риски для всех участников медицинского
процесса, бесспорно, создают микроорганизмы. Поэтому в целом мы
говорим о соблюдении инфекционной безопасности – системы мер,
направленных на защиту работающего медицинского персонала,
населения и окружающей среды от негативного воздействия
инфекционных (микробных) агентов.
И это, конечно, не всё, что можно было бы рассказать об
удивительном и почти безграничном «космосе» микроорганизмов, так
сильно влияющем не только на медицину, но и вообще на всю нашу
жизнь. Но когда-то нужно заканчивать, чтобы не стать автором вторых
«Войны и мира» (раз уж не по таланту, так хоть по объёму
написанного). Однако книга будет неполной, если я забуду в конце её
выразить…
Благодарности
Было бы большим тщеславием для меня считать, что книга в ваших
руках – это результат исключительно моего собственного труда. Да,
бесспорно, она написана мной, но знания, которые вы из неё, надеюсь,
почерпнули – результат усилий многих учёных, исследователей,
практических специалистов и врачей.
Кроме того, эта книга никогда бы не состоялась без тех людей, кто
вдохновлял, поддерживал и просто верил в меня всё время работы над
ней. Потому хочу выразить благодарность моей маме, моим друзьям и
коллегам, которые стали первыми «тестировщиками» и рецензентами.
Моим студентам, ради которых всё, собственно, и было затеяно.
И особенно людям, которые приняли деятельное участие в
написании и подготовке книги к публикации: редактору Ксении
Крутской-Баховец, врачам КЛД Ходосовой Е. М. (раздел
«Лейкоформула крови») и Каримовой А. Э., и всем друзьям,
подписчикам группы, которая сложилась вокруг моего телеграм-канала
«Микробушки».
Кстати, вы тоже можете в нём задать свои вопросы, высказать
замечания и предложения, возникшие после прочтения книги, или
обсудить выходящие там посты. А также приглашаю посетить мой
канал на Яндекс-Дзене «ЛекцииPROинфекции». Там я тоже публикую
статьи и лекции для студентов и всех, интересующихся
микробиологией, иммунитетом и инфекционными болезнями.