Автор: Каменщиков Ф.А. Черных Н.Л.
Теги: горное дело горные предприятия (рудники, шахты, карьеры) добыча нерудных ископаемых оборудование коррозия металлов нефтедобывающая промышленность
ISBN: 978-5-93972-621-4
Год: 2007
Текст
Ф. А. Каменщиков, Н. Л. Черных
БОРЬБА С СУЛ Ь ФАТ -
ВОССТАНАВЛИВАЮЩИМИ
БАКТЕРИЯМИ НА НЕФТЯНЫХ
МЕСТОРОЖДЕНИЯХ
Москва ♦ Ижевск
2007
F. A. Kamenshchikov, N. L. Chernykh
SULFATE-REDUCING BACTERIA
CONTROL OF OIL FIELDS
I
Moscow ♦ Izhevsk
2007
Ф. А. Каменщиков, Н. Л. Черных
БОРЬБА С СУЛЬФАТ-
ВОССТАНАВЛИВАЮЩИМИ
БАКТЕРИЯМИ НА НЕФТЯНЫХ
МЕСТОРОЖДЕНИЯХ
Москва ♦ Ижевск
2007
УДК 622
Каменщиков Ф. А., Черных Н. Л.
Борьба с сульфатвосстанавливающими бактериями на нефтяных месторо-
ждениях. — М,-Ижевск: НИЦ «Регулярная и хаотическая динамика», Ин-
ститут компьютерных исследований, 2007. — 412 с.
В книге рассмотрена коррозионная ситуация, сложившаяся на месторождениях
Удмуртии. Показаны причины высокой коррозионной агрессивности промысловых
сред.
Освещены вопросы физиологии, морфологии и систематики микроорганизмов,
участвующих в процессах биологической коррозии. Рассмотрены условия жизнеде-
ятельности бактерий и их взаимодействие с химическими реагентами, используе-
мыми в технологических процессах добычи нефти.
Значительное внимание уделено методологическим подходам к исследованию
СВБ, ингибиторов коррозии и бактерицидов. Описаны методы подавления жизне-
деятельности СВБ и способы поглощения сероводорода.
Книга предназначена для широкого круга специалистов нефтедобывающей
промышленности, занимающихся вопросами борьбы с биогенной коррозией. Будет
полезна студентам и аспирантам вузов нефтяного профиля и отраслевых институтов.
Kamenshchikov F. A., Chernykh N. L.
Sul fate-reducing bacteria control of oil fields. — Moscow-Izhevsk: SPC “Regular
& Chaotic Dynamics”, Institute of Computer Science, 2007. — 412 p.
The corrosion situation on oil fields of Udmurtia is considered in the book. Reasons
of high field-corrosiveness are explained.
The book dials with the questions of physiology, morphology and microorganism
systematics involved in biocorrosion processes. Living environment of bacteria and their
interaction with chemical agents used in technological processes of oil production arc also
considered.
Much attention is paid to methodological studies of sulfate-rcducing bacteria,
corrosion inhibitors and bactericides. Methods of bacterial inactivation and hydrogen
sulfide absorption are described.
The book is meant for a wide range of petroleum industry specialists engaged in
biogenic corrosion control. It will be useful for students and postgraduates of Petroleum
higher education establishments and industrial institutes.
ISBN 978-5-93972-621-4
© Ф. А. Каменщиков, H. Л. Черных, 2007
http://shop.rcd.ru
http://ics.org.ru
Оглавление
Введение............................................... 9
Глава 1. Анализ коррозионной ситуации на месторождениях
Удмуртии................................................ 18 •
1.1. Классификация нефтепромысловых сред по коррози-
онной агрессивности............................... 18
1.2. Влияние различных факторов на коррозионную агрес-
сивность промысловых сред......................... 25
1.3. Состояние трубопроводной системы............. 39
1.4. Распределение содержания сероводорода по место-
рождениям ......................................... 43
1.5. Методы защиты НКТ от коррозии................. 55
1.6. Эффективность ингибиторов коррозии ........... 58
Глава 2. Физиология, морфология и систематика микроор-
ганизмов ...........................................72
2.1. Термины и понятия............................ 72
2.2. Обмен веществ................................ 74
2.3. Литотрофные микроорганизмы................... 78
2.4. Тионовые бактерии ........................... 80
2.5. Бактерии, окисляющие углеводороды............ 89
6
Оглавление
2.6. Микроорганизмы, участвующие в восстановлении и
окислении соединений серы .......................... 94
2.7. Микроорганизмы, способствующие созданию на по-
верхности условий для действия концентрационных
элементов . ........................................101
2.8. Зараженность промысловых сред микроорганизмами 102
Глава 3. Условия жизнедеятельности сульфат восстанавли-
вающих бактерий .....................................113
3.1. Влияние физико-химической характеристики среды
на жизнедеятельность (?ВБ...........................113
3.2. Влияние свойств поверхности металла на развитие
СВБ и процессы биокоррозии .........................127
3.3. Жизнедеятельность СВБ в условиях осадкообразования 132
3.4. Особенности развития СВБ в условиях работы кор-
розионных макрогальванопар..........................133
3.5. Продуцирование СВБ сероводорода...............138
3.6. Скорость образования сероводорода в призабойной
зоне нагнетательных скважин.........................142
3.7. Продукты жизнедеятельности СВБ ...............146
3.8. Последствия жизнедеятельности микроорганизмов . 156
Глава 4. Взаимодействие сульфатвосстаиавливающих бакт е- .
рий и химических реагентов, используемых в нефтедобыче 181
4.1. Влияние химических реагентов на жизнедеятель-
ность СВБ ..............................................181
4.2. Влияние неионогенных поверхностно-активных ве-
ществ на жизнедеятельность СВБ.....................192
4.3. Влияние полимеров на жизнедеятельность СВБ ... 199
Оглавление
7
4.4. Адаптация СВБ к полиакриламидам..............209
Глава 5. Методологические подходы к исследованиям, свя-
занным с микроорганизмами..........................217
5.1. Оценка зараженности нефтепромысловых сред ми- 7
кроорганизмами....................................217
5.2. Исследование адаптационных свойств СВБ к реаген-
там-бактерицидам .................................235
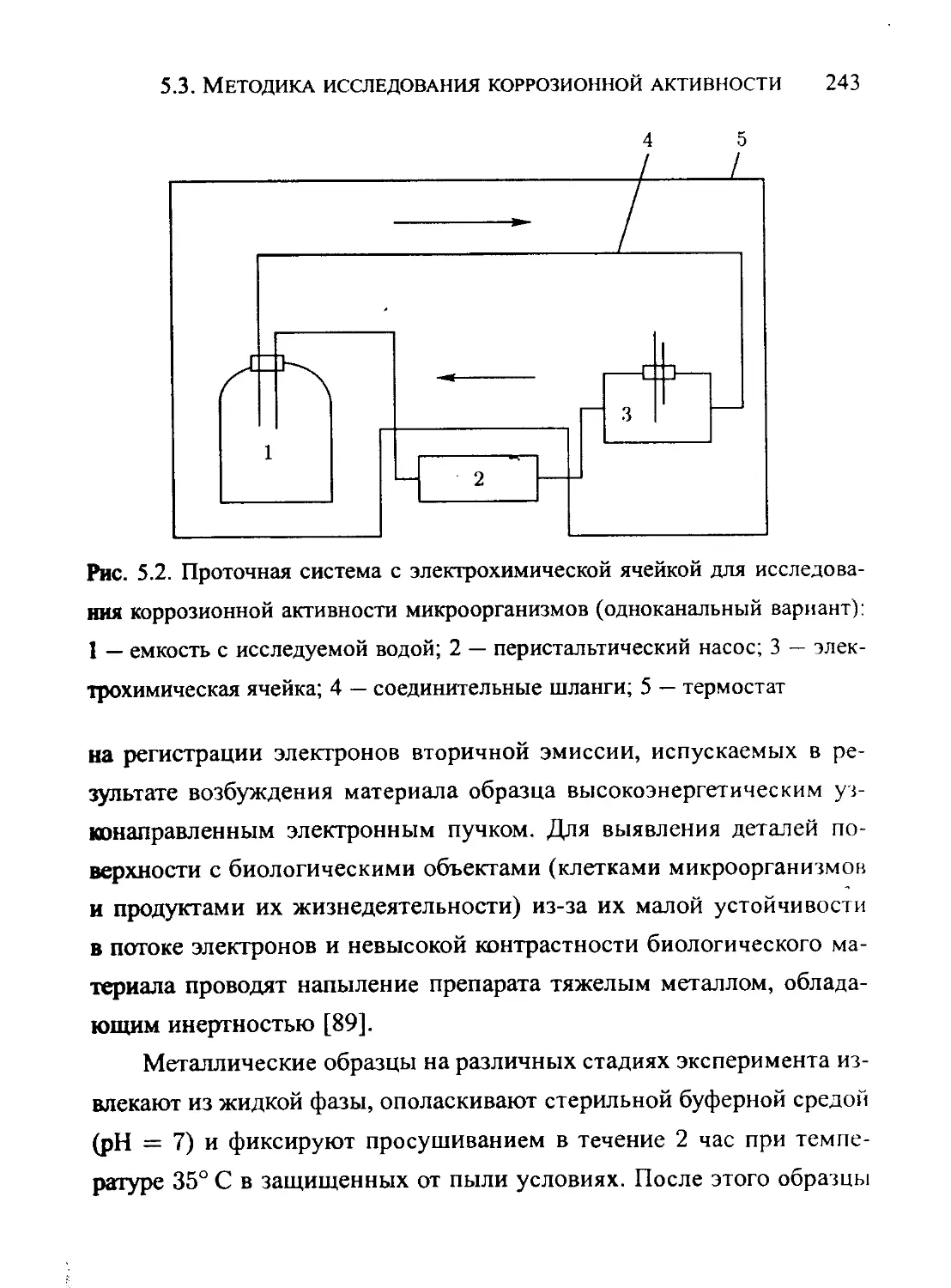
5.3. Методика исследования коррозионной активности
микрофлоры ........... . *......................241
5.4. Оценка эффективности ингибиторов коррозии .... 246
5.5. Оценка эффективности применения ингибиторов
коррозии в условиях микробиологической заражен-
ности нефтепромысловых сред.......................257
5.6. Приготовление питательных сред для микроорганизмов263
Глава 6. Подавление жизнедеятельности СВБ..............268
6.1. Физические методы............................269
6.2. Физико-химические методы.....................277
6.3. Химические методы............................284
Глава 7. Подавление сульфатредукции бактерицидами . . . 290
7.1. Тестирование бактерицидов....................293
7.2. Влияние физико-химических факторов на эффектив-
ность бактерицидов................................304
7.3. Биоцидная активность реагентов, используемых для по-
давления жизнедеятельности СВБ....................308
7.4. Промышленно выпускаемые бактерициды..........322
8 Оглавление
Глава 8. Поглотители сероводорода...........................335
8.1. Основы очистки промысловых сред от сероводорода 337
8.2. Методика оценки нейтрализующей способности по-
глотителей сероводорода .......................... 341
8.3. Удаление и нейтрализация сероводорода..............343
8.4. Надпакерные жидкости...............................359
8.5. Поглотители сероводорода для буровых растворов . . 363
Приложение..................................................379
Литература...................,..............................396
Введение
Коррозионное поражение металлической составляющей ин-
дустриально-промышленного комплекса многообразно и зависит
от технологических, физико-химических и микробиологических фак-
торов, которые нельзя рассматривать изолированно друг от друга без
совокупности всех признаков, в той или иной степени влияющих на
коррозионные процессы, и которые требуют выработки мероприятий
по их устранению. Главенствующая роль принадлежит микробиоло-
гической коррозии.
Естественная скорость коррозии углеродистых сталей в минера-
лизованных водных средах является незначительной величиной и до-
стигает порядка десятых долей миллиметра в год. В присутствии
сероводорода скорость коррозии увеличивается до 1... 1,5 мм/год,
что представляет уже реальную опасность для оборудования, за-
действованного в технологических процессах добычи, транспорта
и переработки нефтяного сырья. Если одновременно с сероводо-
родом в среде присутствуют углекислый газ, кислород или другие
компоненты, усиливающие агрессивность сероводорода, скорость
коррозии резко возрастает и достигает катастрофических значе-
ний — 6...8 мм/год. В средах, содержащих сероводород биоген-
ного происхождения, наряду с равномерной коррозией, часто на-
блюдают локальные поражения металла вследствие образования
10
Введение
на поверхности местных сульфидных отложений и колоний микро-
организмов. При этом скорость коррозии в отдельных случаях дости-
гает 10 мм/год и более [31].
В присутствии сероводорода даже дистиллированная вода при-
обретает агрессивные свойства, а соляная кислота резко их увеличи-
вает, табл. 1.
Таблица 1. Скорость коррозии малоуглеродистой стали (мм/год) в средах,
насыщенных сероводородом [42]
Среда । Температура, °C
20 50 90
Дистиллированная вода + H2S (нас) 0,448 0,518 — .
0,1 н НС1 0,560 8,000 143,0
0,1 н НС1 + H2S (нас) 13,20 65,00 171,0
Микроорганизмы, вызывающие биологическую коррозию, игра-
ют существенную роль в процессах коррозии подземных нефтепрово-
дов, газопроводов и водопроводов, коррозии судового и авиационного
оборудования, оборудования металлургической и металлообрабаты-
вающей, химической и пищевой промышленности. Микроорганизмы
действуют как коррозионные агенты главным образом за счет проду-
цирования агрессивных метаболитов и создания коррозионно-актив-
ных сред. В качестве агрессивных метаболитов выступают органиче-
ские и неорганические кислоты, ферменты, сероводород.
Во многих случаях факт микробиологического заражения оче-
виден, при этом видимыми признаками являются изменения цвета
среды, тягучесть, наличие слизи, шлама и других осадков. Менее
очевидные показатели — неэффективность пленкообразующих инги-
Введение
11
биторов коррозии и присутствие таких загрязнителей, как соли или
окислы железа.
Прокариоты (бактерии и археи) [37] имеют исключительное зна-
чение для жизни на Земле, поскольку им принадлежит основополага-
ющая роль в циклических превращениях основных элементов, необ-
ходимых для жизни, — углерода, кислорода, азота, серы, фосфора.
Циклические превращения элементов, из которых построены живые
организмы, в совокупности представляют круговорот веществ. В на-
стоящее время неоспоримо доказано^что определенные этапы циклов
осуществляют исключительно прокариоты, обеспечивая замкнутость
циклов основных биогенных элементов в биосфере [35].
Круговорот серы. Сера является биогенным элементом, необ-
ходимым компонентом живой материи. Содержится в белках в со-
ставе аминокислот. Объемное содержание серы в белках достигает
0,8... 2,4%. Сера входит в состав витаминов, гликозидов, кофермен-
тов, отмечена в растительных эфирных маслах. В изобилии присут-
ствует в земной коре, в углях, сланцах, нефтях, природных газах.
Сера относится к элементам с переменной валентностью. Это
обеспечивает ее подвижность. В виде неорганических соединений
известна в окисленной форме (сульфаты, политионаты), восстанов-
ленной форме (сульфиды) и молекулярной, осуществляя активный
окислительно-восстановительный цикл. В природе сера претерпевает
разнообразные химические и биологические превращения, переходя
из неорганических соединений в органические и обратно, меняя при
этом валентность в пределах от (—) 2 до (4-) 6.
Циклические превращения соединений серы, включающие окис-
лительные и восстановительные звенья, а также превращения серы
без изменения ее валентности, называют круговоротом серы.
12
Введение
Окислительная часть круговорота серы включает стадии от S2-
до SO4 , которые могут протекать в зависимости от условий как чисто
химически, так и с участием микроорганизмов — грибов, водорослей,
простейших и всех прокариот.
Восстановительная часть круговорота серы осуществляется пре-
имущественно биологическим путем с доминирующей ролью прока-
риот в этом процессе, при этом осуществляется восстановление атома
серы из состояния максимального окисления (+6) до максимального
восстановления (—2). Однако этот процесс не всегда происходит до
конца, и в среде нередко присутствуют не полностью окисленные
продукты: элементная сера, политионаты, сульфит.
Таким образом, цикл серы, так же как и круговорот веществ,
невозможен без участия прокариот, обеспечивающих замкнутость
цикла.
Восстановительная ветвь. Ассимиляция сульфата. Сульфат
используется в качестве источника серы почти всеми растениями
и микроорганизмами. При ассимиляции сульфат восстанавливается,
чтобы сера могла включиться в органические соединения, поскольку
в живых организмах сера встречается почти исключительно в восста-
новленной форме в виде сульфгидрильных (— SH) или дисульфидных
(— S — S —) групп. В обоих случаях ассимилируется ровно столько
питательных веществ, содержащих серу, сколько их необходимо для
роста организма, поэтому никакие восстановленные продукты мета-
болизма серы не выделяются в окружающую среду. В результате био-
синтеза сера включается в основном в состав серосодержащих ами-
нокислот: цистин, цистеин, метионин. Вовлечение сульфатов в состав
серосодержащих органических веществ носит название ассимиляци-
онной сульфатредукции.
Введение
13
Превращение органических соединений серы с образованием
H^S. Для живых организмов сера доступна в основном в форме рас-
творимых сульфатов или восстановленных органических соединений
серы.
При минерализации органических серосодержащих соединений
сера освобождается в неорганической восстановленной форме в ви-
де H2S. В освобождении серы из органических серосодержащих со-
единений (продукты метаболизма живых существ, отмершие расти-
тельные и животные остатки) принимают участие сапрофитные ми-
кроорганизмы, способные к аммонификации. При аммонификации
серосодержащие белки и нуклеиновые кислоты разлагаются с обра-
зованием СО2, мочевины, органических кислот, аминов и, что важно
для цикла серы, сероводорода и меркаптанов (тиоспирты). Меркап-
таны в аэробных условиях также окисляются с выделением H2S.
Разрушение белков микроорганизмами начинается как внекле-
точный процесс. При этом белки гидролизуются протеолитически-
ми экзоферментами до более мелких молекул, способных прони-
кать внутрь клетки и расщепляться внутриклеточными протеазами
до аминокислот, которые могут подвергаться дальнейшему расщеп-
лению.
Прямое образование H%S из сульфата и элементной серы.
Процессы образования в биосфере сероводорода связывают в основ-
ном с деятельностью сульфатредуцирующих бактерий, имеющих
большое значение для глобального круговорота серы. Сульфатреду-
цирующие бактерии осуществляют диссимиляционную сульфатре-
дукцию, представляющую собой анаэробное дыхание, при котором
сульфат служит конечным акцептором электронов (вместо кислорода)
при окислении органических веществ или молекулярного водорода.
14
Введение
Поэтому энергетический тип обмена у сульфатредуцирующих бакте-
рий часто называют сульфатным дыханием. Схематически процесс
восстановления сульфатов при диссимиляционной сульфатредукции
можно представить следующим образом:
so2~ -> so2~ -+ s3o2~ — S2O2~ S2~.
Ферментативная система, участвующая в восстановлении суль-
фата, состоит из двух частей: первая восстанавливает сульфат
в сульфит в АТФ-зависимом процессе (АТФ — аденозинтрифосфат),
а вторая восстанавливает сульфит сульфид путем шестиэлектронно-
го переноса. Именно последняя реакция, являясь диссимиляторной,
снабжает клетку энергией.
Сульфатредуцирующие бактерии преимущественно облигатные
анаэробные бактерии. Геохимическая роль сульфатредуцирующих
бактерий чрезвычайно велика, поскольку благодаря их деятельно-
сти инертное соединение — сульфат в анаэробной зоне в больших
масштабах вовлекается в биологический круговорот серы.
Сульфатредуцирующие бактерии — это физиологическая, а не
систематическая группа, так как к ним относятся бактерии из разных
таксономических групп, способных осуществлять один физиологиче-
ский процесс — анаэробное дыхание в присутствии сульфатов. Среди
сульфатредуцирующих организмов обнаружены и археи.
Сероводород может образовываться также при восстановлении
элементной серы. На сегодня известны два механизма образования
сероводорода из молекулярной серы. В первом случае бактерии и ар-
хеи используют молекулярную серу как акцептор электронов при
анаэробном дыхании (диссимиляционная сероредукция), в ходе ко-
торого синтезируется АТФ. Диссимиляционная сероредукция — это
Введение
15
ферментативный процесс, который осуществляют как мезофильные,
так и термофильные прокариоты. Во втором случае микроорганизмы
(дрожжи и прокариоты) используют серу лишь для сброса электро-
нов, освобождающихся при брожении (облегченное брожение).
Окислительная ветвь. Эта часть серного цикла может состоять
как целиком из реакций неорганических соединений серы
S2' -+ п • S2' -+ S° -+ S2o^~ SO2' so4 s2-,
так и включать реакции органических форм. Атом серы органических
сульфидов обычно окисляется после отделения в виде S2' по неор-
ганическому пути, хотя возможен и чисто органический путь окисле-
ния, когда атом серы окисляется, находясь в составе органических со-
единений, например цистеин — цистин. Большинство реакций окис-
ления серных соединений может протекать без участия микроорга-
низмов в присутствии сильных окислителей (Н2О2, О3, кислородных
радикалов), однако микробное окисление гораздо более эффективно,
особенно при низких концентрациях реагента.
Среди микроорганизмов, способных к окислению серных соеди-
нений, выделяют три основные физиологические группы: анаэроб-
ные фототрофные бактерии, аэробные и факультативно анаэробные
литотрофные бактерии, археи и различные гетеротрофные микроор-
ганизмы.
В последние десятилетия природный цикл серы подвергается
усиливающемуся антропогенному воздействию, приводя к накопле-
нию токсических соединений серы и нарушению баланса природного
цикла серы. В частности, в результате крупномасштабных выбросов
серных соединений образуются двуокись серы, выделяемая ТЭЦ при
сжигании органического топлива, сероводород и летучие органиче-
16
Введение
ские сульфиды, выделяемые целлюлозно-бумажными и металлурги-
ческими предприятиями, а также при разложении муниципальных и
сельскохозяйственных стоков. Эти соединения токсичны уже в ми-
крограммовых концентрациях. Они способны отравлять воздух, вли-
ять на атмосферную химию, вызывать дефицит растворенного в воде
кислорода.
Чрезвычайно высокая каталитическая активность микроорганиз-
мов является причиной того, что они играют главную роль в хими-
ческих превращениях, происходящих на поверхности Земли. Благо-
даря небольшим размерам микроорганизмы обладают по сравнению
।
с животными и высшими растениями высоким соотношением по-
верхности и объема, что и приводит к быстрому обмену субстратов
и продуктов выделения между клеткой и окружающей средой.
Важными факторами являются также высокая скорость их раз-
множения в благоприятных условиях и широкая распространенность
по всей биосфере. Однако, несмотря на исключительное значение
прокариот в трансформации биогенных элементов, до сих пор мас-
штабы деятельности прокариот в круговороте веществ, и в частности
в цикле серы, до конца не оценены.
В нефтедобывающей промышленности основными агентами
коррозионного процесса разрушения металлов являются сульфатвос-
станавливающис бактерии (СВБ). На их долю приходится не ме-
нее 90% сероводорода, поступающего в круговорот соединений се-
ры, около 80% всех коррозионных разрушений наземного и 50%
повреждений подземного оборудования [122].
Экономический ущерб от биоповреждений может достигать
до 3% от стоимости эксплуатирующихся металлических конструк-
ций [30].
Введение
17
Первыми учеными, описавшими сульфатредуцирующую бакте-
рию, были Н. Д. Зелинский — 1892 г. и Брусиловский — 1893 г. [106].
Затем исследования биогенной редукции сульфатов Beijerink (1895)
и Delden Van (1904) заложили основу всестороннего изучения это-
го процесса в природе. Одним из самых ранних исследований по
обнаружению микроорганизмов в нефтяных пластах являются ра-
боты В. Шейко (1901). Начало развития нефтяной микробиологии
относится к 1930-м годам и приурочивается к появлению работ
Т. Л. Гинзбург-Карагичевой (1926) и Е. Bastin (1926), обнаруживших
присутствие СВБ в нефтяных пластах. Большой вклад в изучение
распространения микроорганизмов в нефтяных месторождениях вне-
сли советские ученые Э. А. Рейнфельд (1933), В. Т. Малышек (1935),
А. А. Малиянц (1935). Как отмечал Б. Л. Исаченко (1945), в ряде при-
чин, изменяющих лик Земли, биологические факторы столь же зна-
чительны, как и геологические. Эта мысль, впервые высказанная
В. И. Вернадским (1934), получила широкое развитие в классических
трудах Б. Л. Исаченко и продолжена в работах Л. И. Рубенчика (1947),
С. И. Кузнецова (1962), Г. А. Заварзина (1972), Е. П. Розановой (1974),
Е. И.Андреюк (1974), И. А. Козловой (1977), М. В. Иванова (1983),
Вайнштейн (1996), Земской (2000) и других исследователей.
Авторы книги выражают огромную признательность и благодар-
ность всем ученым и исследователям, чьи публикации в той или иной
мере использованы при написании данной монографии.
Авторы благодарны всем за оказанную помощь и содействие
и выражают надежду, что книга окажется полезной и будет востре-
бована специалистами-нефтяниками.
Глава 1
Анализ коррозионной ситуации
на месторождениях Удмуртии
I
1.1. Классификация нефтепромысловых сред
по коррозионной агрессивности
Основным материалом для трубопроводных коммуникаций
и оборудования нефтегазодобывающих предприятий до сих пор оста-
ются углеродистые стали, как наиболее доступные, хотя в кор-
розионном отношении они относятся к малостойким средствам
нефтедобычи. Использование же коррозионно-стойких высоколеги-
рованных сталей допустимо только для особых условий и спе-
цифической промысловой техники — насосов, арматуры, валов
и т. п. В связи с этим к проблемам выбора оптимальных мето-
дологических решений защиты нефтепромыслового оборудования
и трубопроводов от коррозии следует подходят, как правило, все-
сторонне, взвешенно и комплексно, с использованием как тех-
нологических приемов, так и специальных мер защиты: защит-
ных покрытий, электрохимзащиты, ингибиторов коррозии, бакте-
рицидов.
1.1. Классификация нефтепромысловых сред
19
Определяющим фактором при выборе того или иного метода за-
щиты от коррозии является агрессивность нефтепромысловой среды
и прежде всего ее показатели, в качестве которых используют клас-
сификационные признаки.
Классификация нефтепромысловых сред месторождений Удмур-
тии по степени коррозионного воздействия на углеродистую сталь
может быть произведена в соответствии с работой [68], согласно ко-
торой нефтегазопромысловые жидкости по степени агрессивности
делятся на среды:
— неагрессивные, т. е. не вызывающие коррозионное растрескива-
ние и не изменяющие механические свойства металла;
— вызывающие коррозионное растрескивание и изменяющие ме-
ханические свойства металла;
— слабоагрессивные;
— среднеагрессивные;
— сильноагрессивные.
Степень агрессивного воздействия промысловых сред на нефте-
промысловое оборудование и трубопроводы из углеродистых сталей
зависит от наличия и концентрации в них агрессивных компонентов,
количества взвешенных частиц, скорости движения сред, темпера-
туры, минерализации воды, pH водной фазы, наличия коррозион-
но-опасных микроорганизмов [74, 107].
Степень агрессивного воздействия среды характеризуют пока-
зателем, определяемым как проникновение коррозии и рассчиты-
ваемым по данным потери массы металла после удаления с него
20
Глава 1
продуктов коррозии. Классификация нефтепромысловых жидкостей
по степени агрессивного воздействия среды в зависимости от глуби-
ны коррозионного проникновения [68] представлена в табл. 1.1.
Таблица 1.1. Степеньагрессивного воздействия среды в зависимости от глу-
бины коррозионного проникновения
№ п/п Коррозионное проникновение, мм/год Степень агрессивности среды
1 < 0,01 Неагрессивная
2 0,01... 0,1 Слабоагрессивная
3 0,1... 0,5 Среднсагрессивная
4 > 0,5 Сильноагрсссивная
5 Р (H2S) > 0,0003 МПа Вызывающая коррозионное разрушение
6 Р (СО2) > 0,05 МПа Вызывающая коррозионное разрушение
Для месторождений Удмуртии характерные скорости коррозии
углеродистой стали в сточных водах, классифицированные по степе-
ни агрессивности, отражены в табл. 1.2.
Результаты исследований показывают, что большинство промыс-
ловых сточных и пластовых вод месторождений Удмуртии по кор-
розионному воздействию могут быть классифицированы как слабо-
и среднеагрессивные. Однако необходимо учитывать и тот фактор,
что в большинстве своем они дополнительно содержат различные
химические реагенты, используемые в технологических процессах
1.1. Классификация нефтепромысловых сред
21
Таблица 1.2. Скорость коррозии углеродистой стали в сточных и пластовых
водах месторождений Удмуртии
Месторождение Участок Кор., мм/год Степень агрессивности среды
Гремихинское БКНС ДНС-27 ДНС-36 0,449 0,093 0,047 Среднеагрессивная Слабоагрессивная Слабоагрессивная
С.-Ижевское дне " 0,091 Слабоагрессивная
Киенгопская пл. КНС-1 0,076 Слабоагрессивная
Ю.-Киенгопское БКНС 0,068 Слабоагрессивная
Лудошурское дне УПС 0,043 0,165 Слабоагресси вная Среднеагрессивная
Бегешкинское дне 0,037 Слабоагресси вная
Чутырская пл. КНС-8 БКНС-7 0,044 0,094 Слабоагрессивная Слабоагресси вная
Красногорское БКНС-1 0,145 Среднеагрессивная
Сундурско- Нязинское ДНС-9 0,141 • Среднеагрессивная
Мишкинское БКНС КНС (ДНС-5) 0,128 0,045 Среднеагрессивная Слабоагрессивная
Архангельское БКНС 0,160 Среднеагрессивная
Ельникове кое БКНС-1 БКНС-3 ГС 0,089 0,144 0,058 Слабоагресси вн ая Среднеагрессивная Слабоагрессивная
22
Глава 1
добычи нефти, — деэмульгаторы, ингибиторы коррозии, бактерици-
ды, ингибиторы соле- и парафиноотложений, в той или иной сте-
пени влияющие на защитные свойства металлов. За счет этого ре-
альная, изначальная коррозионная агрессивность нефтепромысловых
вод может быть значительно выше. Правомерность данного утвер-
ждения подтверждают результаты коррозионных исследований, вы-
полненных в лабораторных условиях на пластовых средах Чутырской
площади, не содержащих реагентов. Помимо этого, проведение ис-
следований в лабораторных условиях исключает и биологическую
составляющую коррозии, вносящую значительный вклад в общий
процесс коррозионного разрушения металла.
Степень агрессивного воздействия нефтепромысловых сред
на конструкционные материалы трубопроводов и оборудования мо-
жет быть также определена исходя из вида и концентрации непо-
средственно самих агрессивных компонентов. Основные критерии
классификации по данному признаку приведены в табл. 1.3.
Следует отметить, что при наличии в коррозионной среде
нескольких агрессивных компонентов, концентрация которых нахо-
дится в пределах, указанных в таблице, степень агрессивного воздей-
ствия повышается на одну ступень.
Классификация агрессивности промысловых сточных вод ме-
сторождений Удмуртии с учетом находящихся в них сероводорода,
кислорода и углекислого газов представлена в табл. 1.4.
Исходя из состава коррозионно-активных компонентов пласто-
вые воды месторождений Удмуртии могут быть отнесены к силь-
ноагрессивным средам, безаварийная эксплуатация оборудования
в которых требует специальных средств и методов защиты от кор-
розии.
Таблица 1.3. Классификация агрессивности нефтепромысловых сред по содержанию в Ней агрессивных
компонентов
Среда pH Содержание агрессивных компонентов Степень агрессивности среды
Мине- рализация, г/л Наличие СВБ H2S, мг/л со2, мг/л о2, мг/л Взвешен- ные час- тицы, мг/л
Пластовые воды
Неаэриро- ванные г v v любая любая нет 4- нет нет > 1,0 нет нет нет > 20 АЛЛ о о р 100 100 100 Среднеагрессивная Сильноагрессивная Сильноагрессивная
Аэриро- ванные < 7 5» нет 4- нет нет > 1,0 нет нет нет > 20 > 0,1 > 0,1 > 0,1 > 100 100 100 Сильноагрессивная Сильноагрессивная Сильноагрессивная
Промысловые сточные воды
Неаэриро- ванные ~ 7 < 7 < 7 любая любая нет 4- нет нет > 1,0 нет нет нет > 20 АЛЛ р р р FeS Слабоагрессивн ая Сильноагрессивная Сильноагрессивная
Аэриро- ванные < 7 ** нет 4- нет нет > 1.0 нет нет нет > 20 > 0.1 > 0.1 > 0.1 FeS Сильноагрессивная Сильноагрессивная Сильноагрессивная
1.1. Классификация нефтепромысловых сред
Таблица 1.4. Классификация промысловых сточных вод месторождений Удмуртии с учетов растворенных
в них агрессивных компонентов
Месторождение pH Мине- рализа- ция, г/л Агрессивные компоненты 1 Степень агрессивного воздействия
H2S, мг/л со2, мг/л О2, мг/л
Архангельское 5,61 240,30 8.33 208...376 2,53... 4.55 Сильноагрессивная
Гремихинское 6,16 122,73 98,60 111...208 0,05... 0,45 Сильноагрессивная
Ельниковское 6,31 155.65 25,84 92...225 1,24... 2,39 Сильноагрессивная
Ижевское 6,23 172,32 3,04 203... 360 .2.88... 6.44 Сильноагрессивная
Киенгопская пл. 7,41 140.73 34,85 116... 166 0.14... 0.12 Сильноагрессивная
Красногорское 7,51 107,65 33,15 30... 90 0.23... 1,04 Сильноагрессивная
Лиственское 6,68 164.34 34,68 — — Силы^оагрессивная
Мишкин ское 7,28 144.58 31,45 127...158 0.79... 3.90 Силы|оагрессивная
Чутырское - БКНС-7 - КНС-8 7,28 6,91 92,70 70,05 66,30 112.20 136...166 0,51... 0,66 0,15 Сильноагрессивная Сильноагрессивная
Ю.-Киенгопское 6,76 182.47 54,40 — Сильноагрессивная
Глава 1
1.2. Влияние различных факторов на агрессивность 25 ,
1.2. Влияние различных факторов на коррозионную
агрессивность промысловых сред
Влияние опреснения пластовых вод на их коррозионную
активность
В системе поддержания пластового давления (ППД) в качестве
рабочего агента используют самые различные по своей характери-
стике воды:
— на начальном этапе разработки нефтяных месторождений под-
держание пластового давления осуществляют, как правило, закачкой
пресных вод;
— по мере роста обводненности разрабатываемых объектов воз-
никает необходимость утилизации отделяемой подтоварной воды
с установок подготовки нефти, в связи с чем ее целенаправленно
направляют в систему ППД;
— в ряде случаев из-за отставания строительства системы водо-
водов и нехватки подтоварной воды практикуют подкачивание в сточ-
ную воду пресной, обогащенной растворенным кислородом, или че-
редование закачки сточной воды с пресной.
Нередко в практике эксплуатации возникают случаи нарушения
герметизации запорной арматуры, сальниковых устройств, в резуль-
тате чего на насосных установках происходит подсос атмосфер ло-
го воздуха в трубопроводы и насыщение перекачиваемой жидкости
кислородом. Такая ситуация не может не сказываться на увеличе-
нии агрессивности перекачиваемых сред и росте количества порывов
в системе транспортных водоводов.
Оценочные исследования по влиянию добавления 10% пресной
воды к утилизируемой пластовой воде с установки предварительного
26
Глава 1
сброса Кузбаевского месторождения показали увеличение ее агрес-
сивности в среднем в 19,5 раз [94]. Утилизируемая пластовая во-
да плотностью 1110 кг/м3 была представлена следующим составом,
мг/л, табл. 1.5.
Таблица 1.5. Состав воды Кузбаевского месторождения
Катионы Мг/л Анионы Мг/л Показатели агрессивности
Fe2 + Fe3 14,7 НСО3 152 H2S 13,7 мг/л
Са2+ 9100 so2- , 775 СВБ 103 кл/мл
Mg2+ 2188 СГ 109 571 pH 6,4
К+ + Na+ 57947 •
В качестве инструмента для замера скорости коррозии был ис-
пользован коррозиметр «Корратер», производства США. Результаты
данных исследований показаны в табл. 1.6.
Влияние кислорода на скорость коррозии
Значительное влияние на коррозионную агрессивность промыс-
ловых сред оказывает кислород, поскольку принимает участие как
в анодных, так и в катодных процессах коррозии. При его попада-
нии в систему, содержащую углекислый газ и (или) сероводород,
происходит резкое увеличение скорости коррозии за счет проявления
синергетического эффеета. В связи с этим важным фактором проти-
вокоррозионных мероприятий является осуществление организаци-
онных и технологических мероприятий по предотвращению попада-
ния атмосферного кислорода в нефтепромысловые среды. Снижение
1.2. Влияние различных факторов на агрессивность
27
Таблица 1.6. Характер изменения скорости коррозии металла в пластовой
воде при добавлении пресной
Время с начала эксперимента, мин Скорость коррозии, мм/год Увеличение скорости коррозии, раз
До подачи пресной воды После подачи пресной воды
0 0,9 11,5 12,7
10 0,5 8,5 17,0
20 0,3 7,4 24,6
30 0,2 6,4 32,0
40 0,2 5,9 29,5
50 0,2 5,5 27,5
60 0,2 5,2 26,0
70 0,2 4,9 24,5
80 0,2 4,4 22,0
90 0,2 4,2 21,0
100 0,2 3,9 19,5
110 0,2 3,9 19,5
. 120 0,2 3,9 19,5
содержания кислорода до 0,05 мг/л практически устраняет его вли-
яние на коррозионную агрессивность пресных вод и большинство
рассолов.
Высокую коррозионную активность проявляет растворенный
в воде углекислый газ, который принимает непосредственное уча-
стие в коррозионных процессах и снижает pH раствора, тем самым
увеличивая коррозионную агрессивность среды.
28
Глава 1
Влияние содержания кислорода на скорость коррозии металла
в сероводородсодержащих средах исследовано в работах [28, 94].
Согласно этим исследованиям скорость коррозии металла в присут-
ствии кислорода в концентрации 1,0... 1,3 г/м3 возрастает в 40 раз.
Результаты данных исследований сведены в табл. 1.7.
Таблица 1.7. Характер изменения скорости коррозии металла в пластовой
воде при добавлении кислорода
Время с начала эксперимента, мин Скорость коррозии, мм/год Увеличение скорости коррозии, раз
До подачи воздуха После подачи воздуха
0 '0,8 9,3 11,6
10 0,8 9,3 7,8
20 0,6 9,1 8,8
30 0,5 8,9 18,2
40 0,5 8,8 16,8
50 0,5 8,7 17,4
60 0,5 8,7 17,4
70 0,4 8,6 22,0
80 0,2 8,4 43,0
90 0,2 8,2 41,0
100 0,2 8,0 40,0
110 0,2 8,0 40,0
120 0,2 8,0 40,0
Для месторождений, находящихся в разработке ОАО «Удмурт-
нефть», диапазон изменения содержания кислорода в добываемых
1.2. Влияние различных факторов на агрессивность
29
нефтепромысловых средах находится в пределах 0,05... 6,44 мг/л,
а углекислого газа — в интервале 30,6 ... 360,9 мг/л, табл. 1.8.
Таблица 1.8. Содержание кислорода и углекислого газа в сточных водах
месторождений ОАО «Удмуртнефть»
Месторождение Содержание коррозионно-активных компонентов, мг/л
о2 со2
Киенгопская площадь 0,14 -1,12 116,2- 166,5
Гремихинское 0,05 - 0,45 111,4 - 208,5
Чутырская площадь 0,51 - 0,66 136,0- 166,5
Красногорское 0,23- 1,04 30,6 - 90,2
Мишкинское 0,79 - 3,9 127,4 - 158,4
Архангельское 2,53 - 4,55 208,6 - 376,2
Ельникове кое 1,24 - 2,39 92,8- 225,1
Ижевское 2,88 - 6,44 203,5 - 360,9
Наибольшее содержание Ог наблюдается в сточных водах Ар-
хангельского и Ижевского месторождений. Однако низкая аварий-
ность водоводов сточных вод этих месторождений свидетельствует
и о низкой скорости коррозии. Это связано в первую очередь с низким
содержанием сероводорода (не более 10 мг/л).
Высокое содержание кислорода в сточной воде Ельниковского
месторождения в сочетании с сероводородом обуславливает ее высо-
кую коррозионную активность.
Исследование влияния кислорода на коррозионную активность
в настоящее время затруднено, поскольку нет соответствующего обо-
30
Глава 1
рудования для его замера в промысловых условиях. Лабораторными
исследованиями, проведенными в институте «УдмуртНИПИнефть»,
установлено, что содержание в воде кислорода в пределах 3 мг/л
снижает эффективность ингибиторов коррозии до 30 %.
Сероводородная коррозия сталей в присутствии углекислоты
Водная среда с растворенной в ней углекислотой считается кор-
розионно-активной, если содержание углекислоты выше, чем требу-
ется для поддержания растворимости карбоната кальция, поскольку
карбонатные отложения, формируясь на поверхности металла, об-
ладают защитными свойствами. Коррозионно-активными являются
среды, в которых парциальное давление углекислоты Рсо2 превы-
шает 2 МПа, и, наоборот, неактивными в коррозионном отношении,
если Рсо2 ниже 2 • 104 Па.
Скорость коррозии металла увеличивается с ростом парциаль-
ного давления углекислого газа, но снижается с увеличением Pn2s
от 0,1 до 1,5 МПа. При более широкой вариации Ph2s найдены две
области с высокой скоростью коррозии:
— 1 область — Рсо2 высокое, Ph2s меньше 0,01 МПа;
— 2 область — Рсо2 высокое, Ph2s в интервале 0,05... 0,1 МПа.
В сероводородной среде скорость общей коррозии составляет
0,05 мм/год и повышается до 0,2 мм/год в смеси сероводорода и уг-
лекислого газа, при содержании углекислого газа 50 % и более.
Влияние соединений железа на процессы коррозии
Значительную роль в сероводородной коррозии углеродистых
сталей отводят соединениям железа. В обедненной железом среде
1.2. Влияние различных факторов на агрессивность 31
коррозия стали значительно ниже благодаря образующейся на метал-
ле и прочно сцепленной с ним пленке сульфида железа состава Fej Sy
с заметно выраженными защитными свойствами. Сульфид железа об-
разуется даже при незначительном содержании сероводорода, поряд-
ка 2,0 мг/л.
При концентрации ионов железа, достаточной для осаждения
всего содержащегося в среде сероводорода, на металле образуется
рыхлый и объемный осадок сульфида, не обладающий защитным
свойством. Рыхлые отложения благодаря более высокому положи-
тельному потенциалу по сравнению со сталью способствуют пит-
тингообразованию и разрушению металла.
Установлено, что скорость коррозии металлов в средах, содержа-
щих СВБ, зависит от количества находящегося в них двухвалентного
железа [17].
Добавка в питательную среду Постгейта, зараженную СВБ, сер-
нокислого железа усиливает коррозию углеродистой стали в 2,5 раза
благодаря ускорению анодной реакции продуктами жизнедеятельно-
сти бактерий [47].
Влияние микроорганизмов на коррозию металлов
Биокоррозия — процесс коррозионного разрушения металла
при участии микроорганизмов. По механизму биокоррозию мож-
но характеризовать как электрохимический процесс, где, наряду
с известными факторами, в качестве значимого появляется новый,
не рассматриваемый ранее фактор, — биологический, учитываю-
щий влияние микроорганизмов. По характеру разрушения это мо-
жет быть как общая или сплошная (равномерная и неравномерная),
так и местная коррозия, в зависимости от особенностей воздействия
32
Глава 1
микроорганизмов, структуры металла и др. факторов. По услови-
ям протекания процесса в трех основных средах ее квалифициру-
ют как атмосферную, водную и почвенную (грунтовую) биокорро-
зию [44].
Ввиду специфики воздействия микроорганизмов, как самосто-
ятельного влияющего фактора, биокоррозию подразделяют на бак-
териальную и микромицетную при участии бактерий и грибов-тех-
нофилов соответственно. Предложенную классификацию [29] можно
условно представить в виде схемы, рис. 1.1.
Рис. 1.1. Виды биокоррозии
Исследование коррозионных процессов в сероводородсодержа-
щих средах [17] показало, что скорость коррозии во времени умень-
шается и стабилизируется примерно через 2 сут, что объясняется
образованием на поверхности металла прочной адгезионной пленки
сульфида железа, обладающей экранирующим действием и замедля-
1.2. Влияние различных факторов на агрессивность
33
ющей протекание анодного процесса. Графическое изменение скоро-
сти коррозии в стерильной среде Постгейта, содержащей 500 мг/л
Рис. 1.2. Скорость коррозии стали в среде Постгейта, содержащей серово-
дород
При введении в сероводородсодержащую среду СВБ скорость
коррозии заметно увеличивается, рис. 1.3. Данное явление обусловле-
но нарушением сплошности пленки сульфида железа под действием
продуктов метаболизма СВБ.
Продуктами метаболизма СВБ кроме сероводорода является так-
же углекислый газ. В среде Постгейта в результате жизнедеятельно-
сти СВБ образуется от 200 до 250 мг/л углекислого газа.
Влияние углекислого газа на целостность защитной пленки суль-
фида железа и скорость коррозии стали исследовано в работе [17].
В ходе исследований в стерильную среду Постгейта, содержащую
500 мг/л сероводорода, с момента стабилизации скорости коррозии
вводили 200 мг/л углекислого газа и измеряли скорость коррозии.
В результате исследований установлено, что после введения углекис-
34
Глава 1
Рис. 1.3. Скорость коррозии стали в среде Постгейта, содержащей серово-
дород, при введении СВБ (
лого газа скорость коррозии металла увеличилась в 3 раза, с 0,04
до 0,125 мм/год, рис. 1.4.
Рис. 1.4. Скорость коррозии стали в среде Постгейта, содержащей серово-
дород, при введении углекислого газа
На скорость коррозии стали в средах, содержащих сероводо-
род и СВБ, существенно влияет содержание двухвалентного железа.
1.2. Влияние различных факторов на агрессивность
35
При отсутствии ионов железа в исследуемых средах на поверхности
металла появляется адгезированный сульфид железа, а при их нали-
чии — хлопьевидный осадок, не обладающий защитным действием.
Скорость коррозии стали в среде Постгейта, содержащей сероводо-
род и СВБ, проиллюстрирована на рис. 1.5.
Рис. 1.5. Скорость коррозии стали в среде Постгейта, содержащей серо-
водород и СВБ: 1 — среда без железа; 2 — среда, обогащенная железом
FeSO4 • 7Н2О
Влияние концентрации двухвалентного железа на скорость кор-
розии металла в средах, содержащих СВБ, показано и в рабо-
тах [17, 145]. В них в качестве способа исследования принят метод
полунепрерывного культивирования бактерий при концентрациях же-
леза 25, 125, 525 и 1025 мкмоль.
Для коррозионных испытаний использовали образцы из горя-
чекатаной ленты толщиной 0,75 мм, размером 20 х 25 мм. После
6-, 8-, 12- и 14-недельной выдержки образцы визуально осматрива-
ли, а продукты коррозии подвергали рентгеновскому исследованию.
36
Глава 1
Наблюдения показали, что поверхность образцов металла покрылась
сульфидной пленкой почти сразу же с начала роста бактериальных
культур.
В среде, содержащей 25 мкмоль ионов железа, на поверхности
образцовнаходилась пленка сульфида железа, но видимых следов
коррозии на образцах не обнаружено. Рентгеновский анализ продук-
тов коррозии показал, что пленка состоит в основном из тетрагональ-
ного макинавита — FeSi_.
В среде, содержащей 125 мкмоль ионов железа, потеря защит-
ных свойств пленки сульфида железа наблюдалась после четырех-
недельной выдержки. На образцах’отмечено образование бугорков.
После восьминедельной выдержки структура пленки сульфида желе-
за состояла из макинавита и грейгита (кубического) — ЕезБд.
При концентрациях 525 и 1025 мкмоль отмечены значительные
разрушения сульфидной пленки. После чегырехнедсльной выдержки
на образцах обнаружено образование бугорков, а под продуктами
коррозии — язвы. После двенадцати недельной выдержки в пленке
сульфида железа обнаружены смитит (гексагональный) и пирротит
(кубический и тетрагональный).
Влияние двухвалентного железа на скорос ть коррозии малоугле-
родистой стали в диапазоне концентраций 0... 40 мкмоль приведено
на рис. 1.6.
Влияние СВБ на скорость коррозии металлов
На наличие СВБ указывает появление в среде сернистого же-
леза. Для установления факта микробиологической коррозии требу-
ется изучение состава ее продуктов. Так, питтинги, развивающиеся
под продуктами коррозии черного цвета, могут считаться следствием
1.2. Влияние различных факторов на агрессивность
37
Рис. 1.6. Зависимость скорости коррозии стали от концентрации железа
коррозии, вызываемой СВБ, если эти продукты представляют собой
сернистое железо. Чтобы отличить отложения сернистого железа от
накоплений черного магнетита, образующегося при недостаточном
поступлении в воду кислорода, можно использовать магнит. Серни-
стое железо немагнитно, и его легко отличить от магнетита. По дру-
гой методике черные отложения подвергают воздействию кислотой.
В случае появления запаха сероводорода отложения считают относя-
щимися к соединениям сернистого железа.
Проблеме изучения влияния СВБ на коррозию металлов посвя-
щено много работ [2, 17]. В них исследовалось влияние естествен-
ного биоценоза в природных пластовых водах и средах, зараженных
накопительной культурой на процессы коррозии.
Так, например, работа [2] посвящена изучению влияния нако-
пительной культуры СВБ рода Desulfovibrio, выделенной из пласто-
вых вод Азербайджана, на коррозию низколегированной стали Ст. 3.
Исследования проводили в средах, зараженных бактериями из рас-
чета 1 : 25 (одна часть инокулята на 25 частей питательной среды),
38
Глава 1
при температуре 32° С гравиметрическим методом с одновременной
регистрацией биогенного сероводорода. Использование в качестве
коррозионной среды питательной среды Постгейта В обусловлено
необходимостью создания для СВБ максимально оптимальных усло-
вий их жизнедеятельности, получения значимых результатов срав-
ниваемых величин и уменьшения времени исследований. Результаты
исследований проиллюстрированы на рис. 1.7.
Время, сут
Рис. 1.7. Потеря массы стали в питательной среде Постгсйта: 1 — стериль-
ная среда; 2 — стерильная среда + СВБ; 3 — концентрация биогенного
сероводорода
Влияние тионовых бактерий на коррозию стали
Результаты коррозионных и электрохимических исследова-
ний [105] показывают, что коррозия стали в присутствии тионовых
бактерий носит более сложный характер. В культуральной жидкости
коррозия стали, помимо серной кислоты, усиливается также неучтен-
1.3. Состояние трубопроводной системы
39
ными продуктами обмена веществ тионовых бактерий Т. thiooxidans,
несмотря на равенство pH среды, содержащей бактерии, и чистой
питательной среды, рис. 1.8.
Рис. 1.8. Коррозионные потери стали 10ХСНД в питательных средах: 1 —
стерильная среда; 2 — среда, подкисленная серной кислотой; 3 — среда
с бактериями
В роли таких соединений, заметно ускоряющих анодный про-
цесс электрохимической коррозии, могут выступать органические
кислоты, аминокислоты, сульфолипиды и др. [121, 123].
Скорость коррозии металла в грунте, содержащем ассоциацию
культур тионовых бактерий и СВБ, в 12 раз превышает аналогичный
показатель, полученный при исследовании стерильного грунта без
бактерий, и составляет 22,07 мг/(дм2- сут) [101].
1.3. Состояние трубопроводной системы
В соответствии с [97] срок службы трубопроводов для Вол-
го-Уральского региона составляет:
40
Глава 1
— для нефтепроводов сырой нефти — 10 лет;
— для водоводов сточных вод — 6 лет;
— для водоводов пресных вод — 15 лет.
В ОАО «Удмуртнефть» сроки службы примерно одной трети
нефтепроводов и водоводов сточных вод находятся внутри упомяну-
тых диапазонов, остальная же часть трубопроводов лежит за преде-
лами коррозионно-безопасной зоны. Распределение трубопроводов
по срокам службы в соответствии с градацией для Волге-Уральского
региона засвидетельствовано на рис. 1.9.
Старение трубопроводной системы неизбежно связано с корро-
зионными проявлениями и нарушением герметичности трубопровод-
ной системы. В результате растет количество протечек, виды и диапа-
зон проявления которых разнообразны как по характеру проявления,
так и по количеству пролитой промысловой жидкости, транспортиру-
емой этой системой. Количество протечек водоводов и нефтепрово-
дов по ОАО «Удмуртнефть» отражено в табл. 1.9, из которой видно,
что за 10 анализируемых лет количество протечек водоводов сточ-
ных вод сократилось почти в 10 раз, а нефтепроводов только на од-
ну треть. Количество протечек по причине коррозии трубопроводов
по основным месторождениям сведено в табл. 1.10.
В 2002 году наблюдается увеличение аварийности трубопрово-
дов по всем типам трубопроводных систем. Наибольшее увеличение
аварийности наблюдается на водоводах пресных вод — 34... 38 %.
Это связано с общим старением трубопроводов и недостатком ис-
пользования средств защиты от коррозии в этом году.
Аварийность водоводов сточных вод напрямую зависит от объ-
ема используемых ингибиторов коррозии. С уменьшением дозировки
ингибиторов ниже требуемой нормы количество порывов возрастает.
1.3. Состояние трубопроводной системы
41
Нефтепроводы
Более 20 лет
20%
10—15 лет
18%
Водоводы сточных вод
10—15 лет
6—10 лет
19%
18%
Водоводы пресных вод
15—20 лет
24%
Рис. 1.9. Распределение трубопроводов по срокам службы
42
Глава 1
Зависимость количества протечек от объема используемых реагентов
представлена на рис. 1.10.
Рис. 1.10. Количество протечек водоводов сточных вод в зависимости
от объема используемого ингибитора коррозии: 1 — количество протечек;
2 — объем ингибиторов
Большое влияние на увеличение количества протечек играет
непрерывность процесса дозирования ингибиторов коррозии. Так,
перерывы в дозировании ингибитора на 30... 40 дней вызывают рез-
кий скачок в росте количества протечек, поскольку эффект последей-
ствия большинства ингибиторов не превышает 7... 10 суток. Нагляд-
ным примером служит динамика протечек на Мишкинском место-
рождении в 2002 году, когда обработка нефтепроводов проводилась
не в полном необходимом объеме и со значительными перерывами,
рис. 1.11.
Наиболее информативным и объективным показателем надеж-
ности работы трубопроводов служит удельное количество протечек,
приходящееся на 1 км трубопровода. Данный показатель в ОАО «Уд-
1.4. Распределение содержания сероводорода
43
Рис. 1.11. Влияние периодичности и объема закачиваемого ингибитора на
аварийность нефтепроводов на Мишкинском месторождении в 2002 г.
муртнефть» за рассматриваемый период снизился пропорционально
физическому количеству протечек и отражен в табл. 1.11.
1.4. Распределение содержания сероводорода
по месторождениям
Разработка нефтяных месторождений, осуществляемых с под-
держанием пластового давления, предусматривает, как правило, на-
гнетание в продуктивные пласты пресной и опресненной пластовой
воды. В связи с этим возрастает содержание воды в продукции сква-
жин и сопровождается, как следствие этого процесса, повсеместным
ростом сероводорода в извлекаемой жидкости.
Рост содержания сероводорода в добываемой продукции сква-
жин отмечен для большинства месторождений ОАО «Удмуртнефть».
Так, за период с 1989 по 1996 годы среднее значение содержания
44
Глава 1
сероводорода в целом по ОАО «Удмуртнефть» увеличилось почти
в полтора раза. После 1996 года, благодаря активным применяе-
мым мерам по подавлению жизнедеятельности СВБ, была достиг-
нута стабилизация содержания сероводорода по одной части место-
рождений, по другой снижена до минимально возможных значений,
по третьей замедлены темпы его роста. К 2005 году прирост сред-
него содержания сероводорода по отношению к 1996 году составил
всего 3,5 %. Изменение содержания сероводорода в нефтепромысло-
вых средах основных месторождений ОАО «Удмуртнефть» за период
с 1989 по 2004 годы представлено в табл. 1.12. Как видно из таблицы,
по некоторым месторождениям все же наблюдается рост сероводо-
рода. Это объясняется недостаточностью принимаемых мер по по-
давлению жизнедеятельности сульфатвосстанавливающих бактерий
в промысловых средах, и прежде всего нехваткой бактерицидов.
По Ельниковскому месторождению и Чутырской площади мони-
торинг содержания сероводорода в промысловых средах представлен
данными начиная с 1981 года. Изменение содержания сероводорода
по этим месторождениям показано на рис. 1.12. Всплески и спады
характерны для периодов времени, когда на месторождениях велась
интенсивная закачка бактерицидов или снижалась до минимума.
Удельное количество протечек водоводов сточных вод и нефте-
проводов по Ельниковскому месторождению и Чутырской площади
представлено на рис. 1.13.
Сопоставляя кривые рис. 1.12 и 1.13, необходимо отметить весь-
ма эффективную борьбу с СВБ в 1987-89 годах и, как следствие этого,
снижение содержания сероводорода.
В 1998 году среднее содержание H2S по Чутырской площади
достигало 80 мг/л. На следующий год удельное количество про-
Таблица 1.9. Количество протечек водоводов и нефтепроводов в ОАО «Удмуртнефть» по годам, шт.
Тип трубопровода Года
1993 1994 1995 1996 1997 1998 1999 2000| 2001 2002
Водоводы сточных вод 1563 1184 937 749 826 622 290 150 151 176
в т.ч. от коррозии 1546 1172 923 722 761 550 285 146 138 166
Водоводы пресных вод 174 272 160 106 139 161 158 172 111 153
в т.ч. от коррозии 155 254 149 84 106 98 139 158 102 137
Водоводы, всего 1737 1456 1097 855 965 783 448 322 230 329
в т.ч. от коррозии 1701 1426 1072 806 867 648 424 304 209 303
Нефтепроводы, всего 696 714 632 737 682 602 539 500 421 462
в т.ч. от коррозии 663 674 604 703 661 568 501 463 388 443
ИТОГО порывов 2433 2170 1729 1592 1647 1385 987 822 683 791
в т.ч. от коррозии 2364 2100 1676 1509 1528 1216 925 767 628 746
1.4. Распределение содержания сероводорода
Таблица 1.11. Удельная аварийность трубопроводов, пор/км год
Тип трубопровода Года
1993 1994 1995 1996 1997 1998 1999 2000 2001 2002
Водоводы сточных вод 2.08 1.58 1.24 0,97 1,16 0.74 0.38 0,195 0,184 0.221
Нефтепроводы 0. 184 0. 187 0.168 0.195 0.184 0,158 0. 1'39 0.129 0.108 0.123
£
Таблица 1.10. Количество протечек по причине коррозии трубопроводов по основным месторождениям
Месторождение Назначение Года
трубопровода 1993 1994 1995 1996 1997 1998 1999 20( )0 2001 2002
Киенгопская площадь Водовод 172. 319 404 298 174 168 102 25 21 23
нефтепровод 232 206 192 288 242 167 160 108 119 132
Ю-Киенгопское Водовод — 8 3 8 63 20 2 0 1 1
нефтепровод — 71 55 35 78 51 26 26 15 8
Гремихинское Водовод 208 127 40 40 74 12 1 С 2 7
нефтепровод 16 11 30 33 22 39 26 3$ 38 44
Мишкинское Водовод 683 373 205 132 125 109 82 87 47 36
нефтепровод 87 60 80 73 29 45 39 36 32 122
Чутырская площадь Водовод 505 316 92 95 69 63 106 6$ 101 94
нефтепровод 155 214 138 129 155 142 113 139 76 46
Красногорское Водовод 54 99 68 28 45 51 24 15 18 29
нефтепровод 39 36 27 23 23 16 41 32 22 10
Ельниковское Водовод 78 152 286 191 245 198 67 15 23 51
Нефтепровод 46 56 40 60 46 60 40 18 22 16
Глава 1
Таблица 1.12. Содержание сероводорода в нефтепромысловых средах месторождений ОАО «Удмуртнефть»
Месторождение Года
1989 1990 1991 1992 1993 1994 1995 1996 1997 1998 1999 2000 2001 2002 2003 2004
Архангельское 6,6 4,08 4,45 3,9 6,8 10,7 5,0 2,0 5,1 2,4 5.8 6,2 4,3 3,5 2,45 6,4
Бегешкинское — — — 10,2 22,1 6,3 4,0 7,5 11,7 2,4 37,7 13,5 6,8 i 7,5 8,3 9,4
Гремихинское 91,1 91,77 147,5 112,2 91,9 108,4 118,0 120,0 119,2 91,2 123,3 111,4 111,5 95,7 111,7 78,8
Ельниковское 26,0 24,28 37,4 41,8 34,5 28,7 26,2 15,8 19,4 15,9 28,2 22,4 14,6 12,9 13,9 15,2
Ижевское 3,1 4,21 7,93 3,9 3,8 3,8 2,8 6,3 6,2 5,4 4,8 5,1 6,2 6,4 7,3 7,5
Киенгопская пл. 41,0 41,19 43,07 49,3 45,2 40,3 33,5 44,0 38,0 29,9 45,9 24,7 35,7 38,9 33,5 53,6
Красногорское 39,1 26,03 45,66 15,6 28,9 23,5 31,5 23,9 22,8 20,5 29,9 15,7 34,9 43,8 59,8 33,6
Кырыкмасское - - - 7,6 3,4 3,6 1,5 4,3 6,2 3,1 3,4 5,1 16,2 13,6 13,2 12,8
Лиственское — — — 16,8 18,7 39,4 32,7 30,1 28,4 30,2 31,2 23,0 25,1 25,5 46,5 45,2
Лудошурское - - — 27,2 14,0 22,6 28,9 31,3 22,8 18,2 38,1 28,5 42,1 35,3 37,7 38,1
Мишкинское 10,3 12,67 15,97 27,6 15,0 17,7 20,1 18,4 13,6 43,6 30,2 41,9 44,3 37,8 49,5 31,4
Сундурско- Нязинское — - — 27,5 25,5 44,1 42,3 61,2 54,5 58,5 88,8 86,4 75,4 57,8 91,2
Чутырская пл. 36,5 32,49 46,56 54,0 55,5 68,2 70,2 80.8 76,9 84,6 68.7 87.4 103,2 91,3 81,5 66,9
Ю.-Киенгопское башкир, ярус 12,7 18,4 28,9 35,7 34,4 50,5 64,3 80,7 75.1 38,4 47,3 34,2 54,4 46,6 48,9 54,2
1.4. Распределение содержания сероводорода
48
Глава 1
Рис. 1.12. Изменение содержания сероводорода в процессе разработки Чу-
тырской площади (1) и Ельниковского месторождения (2)
течек увеличилось с 0,6 до 0,8 на один километр трубопроводной
системы. После проведенных в 1999 году интенсивных обработок
продуктивных пластов среднее содержание H2S по месторождению
упало до 70 мг/л, а удельное количество протечек в 2000 году сни-
зилось до величины порядка 0,55 на 1 км. Масштабные обработки
в 2001 году привели к последующему снижению как содержания H2S,
так и количества протечек.
По Ельниковскому месторождению наблюдается примерно такая
же картина, однако периоды отклика пластовой и трубопроводной
системы на бактерицидное воздействие несколько затягиваются.
Как было отмечено, темп снижения количества протечек нефте-
проводов значительно отстает от темпов снижения количества проте-
чек водоводов сточных вод. Это объясняется более пристальным вни-
манием к водоводам и более регулярным обработкам их ингибитора-
ми коррозии. К нефтепроводам был несколько другой подход, объемы
1.4. Распределение содержания сероводорода
49
Рис. 1.13. Изменение удельного количества протечек водоводов сточных
вод (1) и нефтепроводов (2) на Ельниковском месторождении и Чутырской
площади
50
Глава 1
закачки для них выделялись по остаточному принципу, и к периоду
начала целенаправленной и постоянной их обработки возраст многих
нефтепроводов достиг критического значения. Действие ингибито-
ров коррозии оказалось не достаточно эффективным, а агрессивность
транспортируемой нефти достигла предельных значений.
Проведенный в 2001-2002 годах детальный анализ нефтепровод-
ной системы показал, что аварийность нефтепроводов зависит преж-
де всего от назначения нефтепровода. Вследствие этого, основная
и значительная доля протечек приходится на выкидные линии, дости-
гая 70... 80% всех регистрируемых протечек, причем с увеличением
срока службы выкидных линий количество протечек увеличивается.
Такая тенденция отмечена почти для всех месторождений. Относи-
тельное количество протбчек по типам трубопроводов для различных
групп месторождений в период 2001-2002 годов отражено в табл. 1.13
и 1.14. Наименьшее количество протечек зафиксировано для напор-
ных нефтепроводов.
Оценивая количество протечек нефтепроводов в 2000 и 2001 го-
дах, необходимо отметить, что по Игринской группе месторождений
доля протечек, приходящихся на выкидные линии, снизилась с 73,7
до 66,1 %, в то время как по остальным группам месторождений воз-
росла. Причиной такого неудовлетворительного состояния явилась
подача ингибиторов коррозии в нефтепроводы преимущественно на
ГЗУ и дне.
На месторождениях же Игринской группы ингибиторы коррозии
и ингибиторы-бактерициды подавались через затрубное простран-
ство непосредственно в скважину на прием насосных установок,
что, естественно, отразилось не только на изменении соотношений,
но и привело к значительному сокращению протечек в целом.
1.4. Распределение содержания сероводорода
51
Таблица 1.13. Распределение аварийности нефтепроводов по типам трубо-
проводных систем в 2000 году
Группы месторождений Относительное количество протечек нефтепроводов, %
Выкидные линии Нефтесборные коллекторы Напорные нефтепроводы
Ижевская 78,4 11,9 8,7
Игринская 73,7 25,8 0,5
Воткинская 87,0 - 8,7 4,3
Сарапульская 50,0 38,9 11,1
По всем месторождениям 77,1 17,9 5,0
Таблица 1.14. Распределение аварийности нефтепроводов по типам трубо-
проводных систем в 2001 году
Группы месторождений Относительное количество протечек нефтепроводов, %
Выкидные линии Нефтесборные коллекторы Напорные нефтепроводы
Ижевская 87,5 11,5 1,0
Игринская 66,1 26,8 7,1
Воткинская 89,4 6,4 4,3
Сарапульская 65,2 34,8 0,0
По всем месторождениям 80,3 16,7 3,1
52
Глава 1
Оценка наличия сероводорода в затрубном пространстве
скважин
Одним из показателей, характеризующих степень коррозионной
опасности промысловых сред, является наличие сероводорода в за-
трубном пространстве скважин и попутном газе.
В течение 1996-1998 годов институтом УдмуртНИПИнефть сов-
местно с промысловыми работниками был обследован практически
весь фонд эксплуатационных скважин, в результате которого опреде-
лена величина и классифицировано распределение содержания серо-
водорода в газовой фазе затрубного( пространства. Всего было произ-
ведено 3797 определений сероводорода. За счет этого была в целом
по объединению оценена ситуация с наличием и величиной содер-
жания сероводорода по месторождениям. Результаты исследований
помещены в табл. 1.15.
По результатам исследования распределения содержания серо-
водорода по месторождениям определены скважины с предельно-до-
пустимым содержанием сероводорода и среднее его значение по пло-
щади. Результаты приведены в табл. 1.16.
На двух месторождениях, Гремихинском и Киенгопской пло-
щади, только в 15% скважин количество сероводорода оказа-
лось в пределах нормы. На Гремихинском месторождении только
в 6,5 % скважин сероводород отсутствует полностью, а на Киенго-
пской площади — в 10,1% скважин. Это означает, что сероводород
на этих месторождениях распространился повсеместно и практиче-
ски по всему пласту.
Содержание сероводорода в попутном газе представлено
в табл. 1.17.
1.4. Распределение содержания сероводорода 53
Таблица 1.15. Распределение содержания сероводорода в затрубном про-
странстве скважин
Месторождение Год Количество обследованных скважин Количество замеров при содержании H2S в затрубном пространстве, мг/м3
0 0,1-3 3,1-10 > 10
Красногорское 1996 198 67 11 6 114
1997 179 72 10 8 89
1998 191 94 10 1 85
Сундурско-
Нязинское 1998 57 19 12 2 24
В. -Красногорское 1998 46 46 — — —
Чутырская пл. 1998 300 101 30 15 154
Лозолюкско-
Зуринское 1998 245 210 35 — —
Кезское 1998 100 99 1 — —
Ельниковское 1996 41 13 5 3 20
Мишкинское 1997 768 475 38 13 242
Лиственское 1997 181 86 7 4 84
Архангельское 1997 38 27 1 1 9
Киенгопская пл. 1997 535 54 30 23 428
Сев.-Ижевское 1997 28 24 4 — —
Бегешкинское 1997 160 137 23 — —
Лудошурское 1997 44 29 9 1 5
Юж.-Киенгопское 1997 46 31 15 — —
Гремихинское 1997 570 37 53 77 403
Ижевское 1997 37 23 9 2 3
Мещеряковское 1997 33 14 6 4 9.
54
Глава 1
Таблица 1.16. Предельно допустимое содержание H2S по месторождениям
Месторождение Среднее содержание сероводорода по месторождению, мг/л Количество скважин, % с содержанием сероводорода в пределах допустимого, < 3 мг
Красногорское 27,40 54,5
Сундурско-Нязинское 17,77 54,4
В.-Красногорское 0Д)0 1 100
Чутырская площадь 23,52 43,7
Лозолюкско-Зуринское 0,00 100
Кезское 0,10 99,0
Ельниковское 15,70 43,9
Мишкинское 14,78 66,8
Лиственское 22,18 51,4
Архангельское 7,82 73,7
Киенгопская площадь 24,03 15,7
С еверо-Ижевское 0,00 100
Бегешкинское 0,00 100
Лудошурское 3,90 86,4
Южно-Киенгопское 0,10 100
Гремихинское 29,68 15,8
Ижевское 3,18 86,5
Мещеряковское 7,12 60,6
1.5. Методы защиты НКТ от коррозии
55
Таблица 1.17. Содержание сероводорода в попутном газе месторождений
Месторождение Год исследования Содержание сероводорода, г/м3
Сундурско-Нязинское 96 2,49
Чутырская площадь 96 6,13
98 1,09
Лозолюкско-Зуринское 96 0,016
Кырыкмасское 98 0,029
Кстовское 98 3,01
Мишкинское 97 1,62
Ошворце-Дмитриевское 97 0,69
Киенгопская площадь 97 3,48
Северо-Ижевское 97 0,574
Бегешкинское 97 1,38
Лудошурское 97 4,589
Южно-Киенгопское 97 1,855
Гремихинское 97 8,45
1.5. Методы защиты НКТ от коррозии
Проблема коррозии НКТ в ОАО «Удмуртнефть» стоит довольно
остро. По причине коррозии, например, в 2001 году вышла из строя
181 колонна НКТ. Такое состояние обусловлено высоким содержани-
ем сероводорода, кислорода и наличием СВБ.
56
Глава 1
Защита от коррозии НКТ в нагнетательных скважинах
Защиту нагнетательных скважин от коррозии производят, как
правило, в двух направлениях:
1 — защита внутренней поверхности НКТ ингибиторами корро-
зии и бактерицидами. При этом ингибиторы коррозии подают по-
стоянно в поток закачиваемых вод через систему ППД, а закачку
бактерицида для подавления жизнедеятельности СВБ производят пе-
риодически через БКНС и КНС.
Помимо этого отдельные нагнетательные скважины обрабатыва-
ют бактерицидами по индивидуальным планам.
2 — защиту наружной поверхности НКТ и внутренней поверх-
ности обсадной колонны осуществляют закачкой защитного состава
в межтрубное пространство. Защитный состав разработан специали-
стами ОАО «Удмуртнефть». С 1996 по 2002 год защищено 310 на-
гнетательных скважин.
Защита от коррозии НКТ в добывающих скважинах
Защиту добывающих скважин от коррозии производят путем по-
дачи ингибитора коррозии на прием насосной установки через за-
трубное пространство с помощью дозировочных устройств различ-
ной конструкции и принципа действия. Объем обрабатываемых сква-
жин в 1999-2002 годах приведен в табл. 1.18.
Количество отказов НКТ по причине коррозии в 2001 году и ко-
личество защищаемых скважин в 2001-2002 годах по месторождени-
ям показаны в табл. 1.19.
Проведенный анализ обработок по Игринской группе месторо-
ждений показал, что за счет обработок добывающих скважин ингиби-
1.5. Методы защиты НКТ от коррозии 57
Таблица 1.18. Объемы защиты НКТ в добывающих скважинах
Группа месторождений Количество обрабатываемых скважин
1999 г. 2000 г. 2001 г. 2002 г.
Игринская 9 27 35 47
Киенгопская . ' 10 13 7 22
Воткинская — — 62 15
Таблица 1.19. Количество защищаемых скважин
Месторождение Количество отказов по причине коррозии в 2001 году Количество защищаемых скважин
2001 г. 2002 г.
Мишкинское 19 22 15
Гремихинское 10 — 10 ’
Лиственское 6 3 —
Красногорское 20 — 8
Сундурско-Нязинское 16 8 9
Чутырская площадь 110 27 34
Всего 181 60 76
торами коррозии и бактерицидами срок службы НКТ увеличивается
в среднем в 2 раза. Увеличение наработки на отказ за счет обработки
скважин ингибиторами коррозии и бактерицидами по месторожде-
ниям представлено в табл. 1.20.
Расчет потребности в ингибиторах коррозии для защиты НКТ
добывающих скважин показан в табл. 1.21.
58
Глава 1
Таблица 1.20. Увеличение наработки на отказ за счет применения ингиби-
торов коррозии
Месторождение Увеличение наработки на отказ, раз
Чутырская площадь 1,68
Красногорское 2
Сундурско-Нязинское 2,28
Таблица 1.21. Расчет потребности в ингибиторах коррозии для защиты
НКТ добывающих скважин
Месторождение Количество скважин Дебит по жидкости, м3/сут Расход ингибитора, г/м3 Расход ингибитора на год, т.
Мишкинское 19 15,6 50 5,1
Гремихинское 10 21.8 70 5,3
Лиственское 6 16.1 50 2,2
Красногорское 20 19.5 30 4,0
Сундурско- Нязинское 16 30.0 50 8,3
Чутырская пл. ПО 36,0 70 96,1
Всего 181 121
1.6. Эффективность ингибиторов коррозии
Различный состав и индивидуальная характеристика физико-хи-
мических свойств нефтепромысловых сред требуют индивидуально-
го подхода к каждому защищаемому объекту, т. е. для каждого кон-
1.6. Эффективность ингибиторов коррозии
59
кретного месторождения необходим свой ингибитор коррозии и тех-
нология его применения [131, 132, 148].
Подбор эффективных ингибиторов коррозии проводят, как пра-
вило, в несколько этапов:
1) Лабораторные исследования — выбор наиболее эффективных ин-
гибиторов коррозии.
2) Пилотные испытания — подбор для конкретного месторожде-
ния наиболее эффективного ингибитора коррозии и оптималь-
ной концентрации его применения.
3) Опытно-промысловые испытания — определение эффективности
и отработка технологии применения.
Наиболее распространенными и повсеместно принятыми в ла-
бораторной практике методами исследования эффективности инги-
биторов коррозии являются гравиметрический метод с использова-
нием U-образных ячеек и электрохимический метод с помощью ин-
дикатора скорости коррозии «Моникор-2». В качестве рабочих сред
используют как реальные пластовые и сточные воды, так и модель-
ную пластовую воду, приготовленную в соответствии с ГОСТ 9.506-
87 [119]. Дозировки реагентов выбирают исходя из рекомендаций по
их применению разработчиками реагентов. Испытания на сточной
воде проводят с целью подбора реагентов для системы водоводов
сточных вод, на пластовой воде — для защиты системы нефтесбора.
Результаты лабораторных испытаний ингибиторов коррозии,
проведенные с целью выбора наиболее приемлемого реагента для
условий месторождений Удмуртии, отражены в табл. 1.22, 1.23.
Результаты стендовых испытаний некоторых реагентов обобще-
ны в табл. 1.24, а пилотных испытаний — в табл. 1.25.
60
Глава 1
Таблица 1.22. Результаты лабораторных исследований ингибиторов корро-
зии на модельном растворе
Ингибитор Дозировка, мг/л Защитный эффект, % Метод испытаний
СНПХ-1004 25 ' 54,05 Гравиметрический
10 40,00 Гравиметрический
СНПХ-1004Р 15 95,30 Гравиметрический
25 96,60 Гравиметрический
СНПХ-6301 50 70,02 Гравиметрический
СНПХ-6302 50 66,88 Гравиметрический
Korrexit-7756 10 48,57 Гравиметрический
КРЦ-3 100 68,06 Гравиметрический
100 85,66 Электрохимический
Нефтсхим-3 50 63,03 Гравиметрический
50 53,43 Электрохимический
100 91,09 Гравиметрический
100 80,84 Электрохимический
Реапон-ИП 50 75,36 Электрохимический
100 91,63 Электрохимический
Реапон-ИФ 25 92,00 Электрохимический
75 96,00 Электрохимический
Рсапон-ИК 25 88,60 Электрохимический
75 95,40 Электрохимический
ТН-10Д 50 34,78 Гравиметрический
Амфикор 25 47,08 Гравиметрический
АМ-7МБ 50 35,30 Гравиметрический
ИКМ-1 50 15,20 Гравиметрический
ИКМ-2 50 31,80 Гравиметрический
100 58,50 Гравиметрический
Сонкор 4-9701 50 57,78 Гравиметрический
Таблица 1.23. Результаты лабораторных исследований ингибиторов коррозии на сточной воде
Месторождение Ингибитор Дозировка, мг/л Защитный эффект, % Метод испытаний
Ельниковское Реапон-ИФ 50 56,35 Электрохимический
KPN-268 15 42,71 Электрохимический
25 99,56 Электрохимический
KPN-268 15 53,23 Электрохимический
Чутырская пл. 25 77,55 Электрохимический
БКНС-6 50 84,16 Электрохимический
БКНС-7 Нефтехим-3 50 80,09 Электрохимический
Ю-Киенгопское Нефтехим-3 50 54,92 Электрохимический
100 80,20 Электрохимический
СНПХ-63026 50 36,58 Электрохимический
СНПХ-6014 М 50 30,91 Электрохимический
100 35,65 Электрохимический
Киенгопская пл. KPN-268 20 89.90 Электрохимический
1.6. Эффективность ингибиторов коррозии
Месторождение Ингибитор Дозировка, мг/л
Гремихинское, Реапон-ИФ 30
скв, 603 Реапон-ИК 30
СНПХ-1004Р 25
Мишкинское, 1 Реапон-ИФ 30
ДНС-3 Korrexit SXT-1003 30
Киенгопская пл. Korrexit SXT-1003 15
скв, 310 30
Киенгопская пл. Korrexit SXT-1003 15
ДНС-7 30
Ошворце- Нефтехим-3 50
Дмитриевское Нефтехим-3 100
Продолжение табл. 1.23
Защитный эффект, % Метод испытаний
85,5 80 93,4 Электрс|химический Электрс|химический Электрохим ический
80 85,2 Электрохимический Электрохимический
- Электрс|химический Электрохимический
Электрохимический Электрохимический
54,5 80,2 Гравиметрический Электрохимический
Глава 1
1.6. Эффективность ингибиторов коррозии
63 '
Таблица 1.24. Результаты стендовых испытаний ингибиторов коррозии для
защиты водоводов сточных вод
Место проведения испытаний Наименование реагента Дозировка, мг/л Защитный эффект, %
Чутырская площадь
- БКНС-6 Нефтехим-3 22 94,0
- БКНС-7 Нефтехим-3 30 54,6
50 80,1
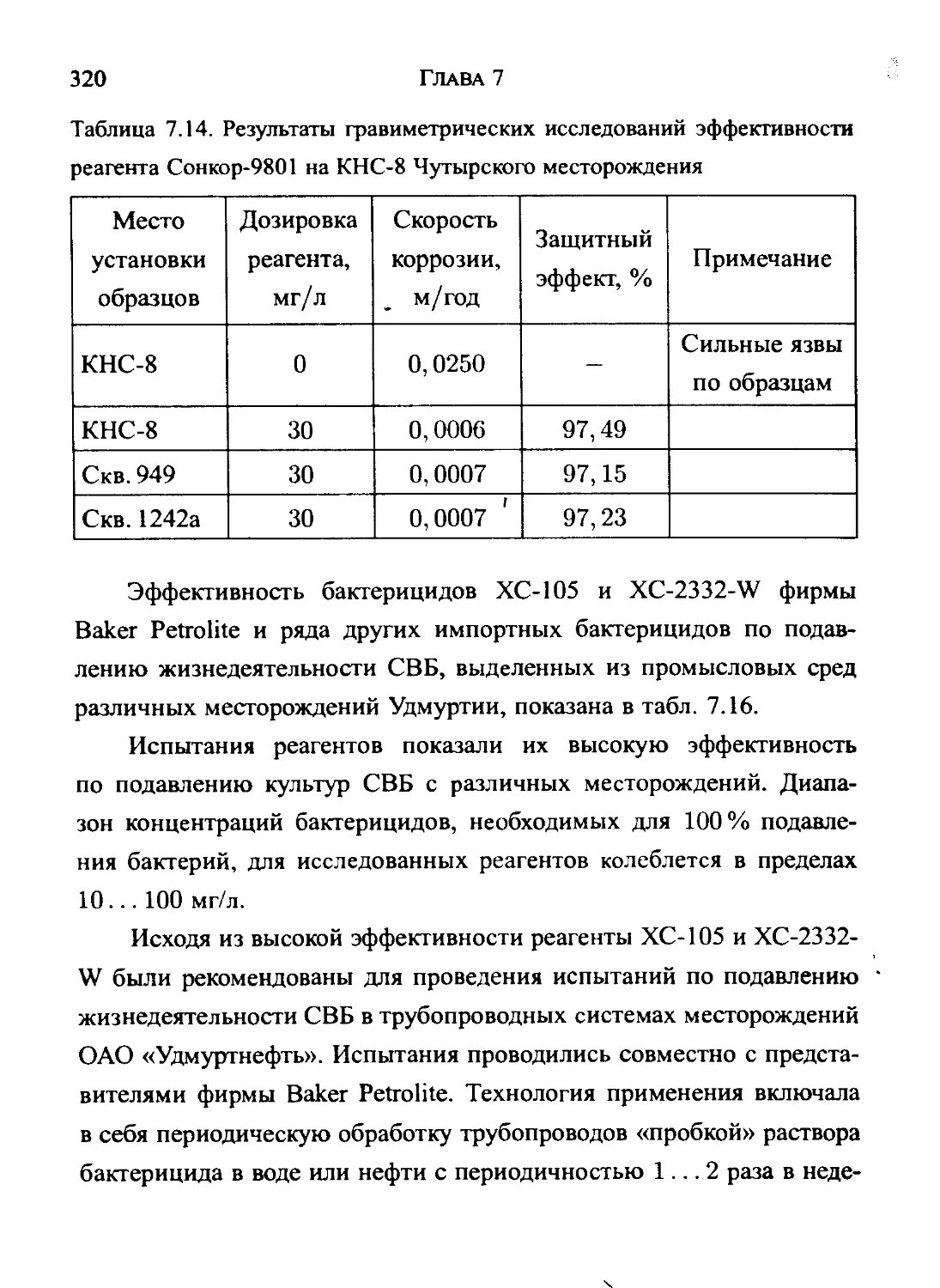
- КНС-8 Сонкор-9801 30 97,49
Гремихинское Нефтехим-1 50 92,0
месторождение Нефтехим-3 20 98,0
Нефтехим 4-9701 25 95,0
Ю.-Киенгопское СНПХ-6301 50 89,0
месторождение Нефтехим 4-9701 25 92,0
Ельниковское Нефтехим-1 30 95,6
месторождение, Нефтехим-3 20 93,3
БКНС-3 Азимут-14Б 30 89,23
Киенгопская площадь, Азимут-14Б 30 38,5
КНС-1 Гекор-3090 30 91,3
Рекод-608 30 88,0
Альтосон 25 81,0
Катасол-28-2 25 93,0
Нефтехим 4-9701 20 94,0
Киенгопская площадь, Korrexit-SXT-ЮОЗМ 20 94,0
КНС-1 Cortron KRN-214 20 90,0
25 93,3
Cortron KRN-301 25 66,6
30 66,6
К-143 20 97,0
64
Глава 1
Продолжение табл. 1.24
Место проведения испытаний Наименование реагента Дозировка, мг/л Защитный эффект, %
Киенгопская площадь, Сонкор-9510 20 88.7
КНС-1 25 92,8
Сонкор-9601 23,8 74,5
30 83,7
Сонкор-9701 22 81,0
25 82,6
Сонкор-9920( 30 86,9
35 94,0
Красногорское Сонкор-9801 30 93,0
месторождение, Сонкор-9701 30 95,2
БКНС-1 Сонкор-9601 30 97,5
Азимут-14Б 30 94,16
Альпан 54 88,70
Мишкинское Сонкор-9020А 35 86,34
месторождение Сонкор-9020Б 20 99,03
Сонкор-9510А 15 98,94
Сонкор-9510Б 20 95,75
На основании пилотных испытаний реагенты Danox CI-101,
Нефтехим-1, Нефтехим-6, Сонкор-9701, Сонкор-9601 и Азимут-
14Б были рекомендованы к проведению опытно-промышленных ис-
пытаний на месторождениях ОАО «Удмуртнефть» с дозировками
20... 30 г/м3. Реагенты Нефтехим-6, Danox CI-101 и Сонкор-9701
рекомендованы к проведению испытаний для защиты как водоводов
сточных вод, так и нефтепроводов.
1.6. Эффективность ингибиторов коррозии
65
Таблица 1.25. Результаты пилотных испытаний ингибиторов коррозии
Место проведения Реагент Дозировка, мг/л Степень защиты, %
Киенгопская Danox CI-101 22 84,1
площадь, НФС Нёфтехим-1 30 91,8
Нефтехим-6 30 95,9
Сонкор-9701 30 90,0
Сон кор-9601 * 30 90,0
Ижевское Нефтехим-1 30 90,9
месторождение, УПН Нефтехим-6 30 92,0
Сонкор-9701 30 88,0
Сон кор-9601 30 95,2
Архангельское СНПХ-6301 50 74,7
месторождение, Нефтехим-1 30 91,3
БКНС Сонкор-9701 30 89,3
Сон кор-9601 30 93,0
Чутырская площадь, БКНС-7 Азимут -14Б 20 92,1
Красногорское Danox CI-101 30 97,8
месторождение, Нефтехим-1 30 95,1
БКНС-1 Нефтехим-6 30 93,0
Сонкор-9701 30 95,2
Сонкор-9601 30 97,5
66
Глава 1
Обращает на себя внимание серия ингибиторов Азимут. Данный
реагент является новым поколением ингибиторов коррозии, имею-
щих полимерное строение. Основой реагента является полиэтилен-
полиамин (ПЭПА). Наличие в полимерной молекуле четвертичных
атомов -азота предопределяет создание на границе металл рас--
твор трехслойной адсорбционной структуры, полностью блокиру-
ющей поверхность металла от воздействия агрессивных нефтепро-
мысловых сред [131]. Высокая эффективность ингибитора Азимут
при дозировках всего 15... 20 мг/л подтверждает его высокую ад-
сорбционную способность.
Определенный вклад в исследование и подбор новых реаген-
тов для защиты скважинного оборудования добывающих скважин
и системы нефтесбора на Чутырской площади внесли представители
фирмы «Champion Technologies Inc» совместно с ОАО «ОЗ Нефте-
хим». Представители этих фирм в полевых условиях провели иссле-
дования новых перспективных марок ингибиторов коррозии электро-
химическим методом с помощью коррозиметра «Korrater 9000 Plas»
на водоводе сточной воды БКНС-7, на нефтепроводе на приеме ДНС-
2 и на добывающих скважинах, имеющих высокую степень обвод-
нения продукции. Проведение пилотных испытаний осуществлено
в проточных ячейках как гравиметрическим, так и электрохимиче-
ским методом. Преимуществом данного вида испытаний явилось то,
что исследования проведены в промысловых условиях в реальных
потоках коррозионных сред. Результаты исследований сгруппирова-
ны в табл. 1.26.
Лабораторные испытания новых ингибиторов коррозии серии
Лукойл представлены в табл. 1.27.
Таблица 1.26. Результаты пилотных испытаний ингибиторов коррозии фирмы «Champion Technologies Inc»
Место испытаний Реагент Концентрация ингибитора, мг/л Скорость коррозии, мм/год Защитный эффект, %
Без ингибитора С ингибитором
БКНС-7 KRN-192 30 0,019 0.002 89,5
KRN-192 45 0,033 0,005 84,8
KRN-214 30 0,026 0,001 96,2
KRN-264 30 0,019 0.006 68,4
KRN-301 20 0,034 0,002 94,1
KRU-263 20 0,073 0,001 98,6
Нефтехим-1 30 0,015 * 0,003 80,0
Нефтехим-1 45 0,025 0,010 60,0
ДНС-2 KRN-192 20 0,025 0,003 88,0
KRN-192 20 0,027 0.001 96,3
KRN-192 20 0,069 0.002 97,1
KRN-214 20 0,066 0.001 98,5
KRN-264 20 0,092 0.085 7,6
KRU-263 30 0,091 0.005 94,5
Сонкор-9801 20 0,025 0.003 88,0
ConKop-9801 30 0.031 0.024 22,6
1.6. Эффективность ингибиторов коррозии
Место испытаний Реагент Концентрация ингибитора, мг/л
Скв. 1083 KRN-192 10
KRN-192 10
KRN-214 10
KRN-264 50
KRN-301 20
KRN-317 20
KRN-317 30
Скв. 1287 KRN-214 30... 40
KRN-214 30... 40
KRN-301 30
KRN-317 40
KRN-66 40
KRU-263 30
Скв. 1292 KRN-192 10
KRN-214 10
Продолжение табл. 1.26
00
Скорость коррозии, мм/год Защитный эффект, %
Без ингибитора С ингибитор ом
0,007 0,001 85,7
0,025 0,001 96,0
0,028 0,002 92,9
0,039 0,010 74,4
0,019 0,002 89,5
0,007 0.001 85,7
0.02? 0.002 92.6
0,177 0.002 98,9
0,041 0,001 97,6
0,069 0.015 ' 78,3
0,039 0.004 89,7
0,183 0,010 94,5
0,080 0,006 92,5
0,045 0 100
0,013 0 100
Глава 1
Продолжение табл. 1.26
Место испытаний Реагент Концентрация ингибитора, мг/л Скорость коррозии, мм/год Защитный эффект, %
Без ингибитора С ингибитором
Скв. 1292 KRN-214 10 0.036 0 100
KRN-264 30 0,092 0,002 97,8
KRN-301 20 0,028 0,001 , 96,4
KRN-317 25 0,044 0 ' 100
Сонкор-9701 25 0,026 0,001 96,2
Сонкор-9801 20 0,100 0,002 98,0
Скв. 838 KRN-192 20 0,025 • 0,001 96,0
KRN-192 25 0,072 0,001 98,6
KRN-214 30 0,029 0,006 79,3
KRU-263 40 0,036 0,034 5,6
KRN-301 25 0,027 0,001 96,3
KRN-317 40 0,022 0,001 95,5
KRN-66 40 0.057 0,033 42,1
1.6. Эффективность ингибиторов коррозии
70
Глава 1
Таблица 1.27. Результаты лабораторных испытаний ингибиторов коррозии
на модельных средах
Ингибитор Защитный эффект, % при дозировке
15 мг/л 25 мг/л 35 мг/л 50 мг/л 75 мг/л
Лукойл-1280И — — 76,1 77,2 —
Лукойл-1240И — — 67,1 79,0 —
Лукойл-1250И — — 54,1 58,3 —
Лукойл-1251И — 76,7 80,8 90,9 —
Лукойл-1211И — 57,6 84,1 86,1 —
Лукойл-1211И — _ 1 — 28,9 32,7
Лукойл-1251И — — — 61,8 73,0
Cortron KRN-192 80,3 80,6 81,6 — —
Cortron KRN-301 81,4 82,2 83,1 — —
Cortron KRU-263 76,7 78,8 80,8 — —
Cortron KRN-214 82,0 83,7 85,2 — —
Cortron KRN-264 85,1 87,8 88,7 — —
Реапон-ИФ — 92 85,5* — 96
Реапон-ИК — 88,6 80,0* — 85,4
СНПХ-1004Р 95,3 96,6 93,4* — —
Примечание * — испытания проведены на пластовой воде скв. №603
Гремихинского месторождения с содержанием сероводорода 96 мг/л.
Результаты лабораторных испытаний показали, что реаген-
ты серии Cortron и реагенты Лукойл-1211 И и Лукойл-1251И мо-
гут быть рекомендованы для проведения пилотных и промышлен-
ных испытаний. Кроме того, реагенты Cortron KRN-301, Cortron
KRN-214 и Лукойл-1251 являются эффективными ингибиторами-
1.6. Эффективность ингибиторов коррозии 71
бактерицидами, поэтому они могут быть эффективны на участках,
характеризующихся высокой зараженностью СВБ.
Особо хочется отметить реагенты ОАО «Напор»: Реапон-ИК,
Реапон-ИФ и СНПХ-1004Р. Реагенты серии Реапон являются де-
эмульгаторами, проявляющими хорошие ингибиторные и бактери-
цидные свойства. Реагент СНПХ-1004Р — ингибитор-бактерицид, за-
рекомендовавший себя на многих нефтегазодобывающих предприя-
тиях Урала, Поволжья и Западной Сибири.
Глава 2
Физиология, морфология и систематика
микроорганизмов
2.1. Термины и понятия ।
Среди многообразия микроорганизмов, составляющих основу
микрофауны нефтяных месторождений, выделяют несколько физио-
логических групп различных бактерий, в той или иной степени вза-
имодействующих с нефтепромысловым оборудованием и водонеф-
тяными средами. Классификационные признаки, характеризующие
принадлежность того или иного микроорганизма к соответствую-
щей группе (порядку, семейству, роду, виду) многообразны, к глав-
ным из которых следует отнести тип питания и способ получения
энергии.
Микроорганизмы, получающие энергию за счет химического
окисления, называют хемосинтезирующими, за счет энергии света —
фотосинтезирующими. В свою очередь хемосинтезирующие организ-
мы могут использовать в качестве донора электронов органическое
вещество, и тогда они являются органотрофами, в случае исполь-
зования неорганического вещества — литотрофами. По отношению
к источнику углерода микроорганизмы делят на автотрофы, получа-
2.1. Термины и понятия
73
ющие углерод из углекислоты, и гетеротофы, получающие углерод
из органических соединений.
Термин «автотроф», означающий как сам себя питающий, опре-
деляет организм, который может жить, расти и размножаться в среде,
свободной от других организмов и продуктов их жизнедеятель-
ности, т. е. в такой среде, где единственным источником углеро-
да, необходимым для построения клеток организма, является угле-
кислота.
Доказательство автотрофной ассимиляции углекислоты при
окислении неорганического вещества было получено академиком
С. Н. Виноградовым при исследовании процесса нитрификации. Раз-
витие нитрификаторов происходило в минеральной среде без вне-
сения органического вещества, т. е. за счет ассимиляции углерода
углекислоты при использовании химической энергии окисления ам-
миака и азотистой кислоты. Открытие группы бесхлорофилльных ор-
ганизмов, способных, подобно зеленым организмам, ассимилировать
углерод углекислоты и обходиться при этом без света в абсолютной
темноте, отнесено к крупнейшим достижениям в области физиоло-
гии. Данный тип питания получил название «хемосинтез», или «анор-
гоксидация». Виды способов питания микроорганизмов перечислены
в табл. 2.1.
Комбинации терминов позволяют описать большинство типов
питания микроорганизмов. Так, тионовые бактерии, окисляющие
только неорганические соединения серы и использующие углекисло-
ту для построения своего тела, являются хемолитотрофами. Сульфат-
редуцирующие бактерии, осуществляющие диссимиляторное восста-
новление сульфатов, — хемолитогетеротрофами, поскольку использу-
74
Глава 2
Таблица 2.1. Терминология способов питания микроорганизмов
Признак Терминология Синоним
Источник энергии: живой организм химическая реакция фотохимическая реакция Паратрофия Хемотрофия Фототроф ИЯ Внутриклеточный паразитизм Фотосинтез
Донор электрона: неорганический органический Литотрофия 1 Органотрофия Аноргоксидация Хемосинтез Фотосинтез Гетеротрофия
Источник углерода для построения клеток: углекислота органическое вещество Автотрофия Гетеротроф ия Автотрофия Гетеротрофия
ют сульфат в качестве акцептора электрона в анаэробных условиях
для окисления органических соединений или водорода.
2.2. Обмен веществ
Обмен веществ (метаболизм) — совокупность химических про-
цессов, обеспечивающих жизнедеятельность организма. Химические
превращения в организме происходят в двух противоположных на-
правлениях — синтез сложных соединений из более простых (анабо-
2.2. Обмен веществ
75
лизм, или ассимиляция) и расщепление сложных соединений до бо-
лее простых (катаболизм, или диссимиляция).
Первоначально представления об обмене веществ возникли
в связи с изучением процессов обмена между организмами и внешней
средой, так называемый внешний или общий обмен веществ. Иссле-
дования превращений веществ внутри организма привели к пред-
ставлениям о внутреннем обмене веществ.
Во внутреннем и внешнем обмене принято различать структур-
ный (пластический) и энергетический обмены. В структурном об-
мене рассматривают превращения различных соединений в организ-
ме, их перенос (транспорт) внутри организма и между организмом
и средой. В энергетическом обмене рассматривают превращения хи-
мической энергии, образующейся в обмене веществ, в тепло, мы-
шечную ее работу, а также механизмы ее использования в активном
транспорте, биосинтезе и др.
В соответствии с природой участвующих в обмене веществ со-
единений, различают органический обмен (обмен углеводов, липи-
дов, азотсодержащих соединений и др.) и минеральный обмен (вод-
но-солевой обмен и обмен микроэлементов). Обмен веществ с уча-
стием свободного Ог называют аэробным, без участия О2 — анаэроб-
ным. Ввиду различий обмена веществ у организмов, принадлежащих
к различным таксономическим группам, выделяют обмен веществ
растений, животных, микроорганизмов.
Структурный обмен
В зависимости от того, в какой химической форме живые ор-
ганизмы способны усваивать из внешней среды углерод, их делят
76
Глава 2
на две большие группы — автотрофы и гетеротрофы. Для первых
основным источником углерода служит СО2, для вторых — различ-
ные органические соединения. Автотрофное питание осуществля-
ют зеленые растения и фотосинтезирующие бактерии, гетеротроф-
ное — животные и грибы. У микроорганизмов отмечен тот и дру-
гой типы питания. Обмен веществ автотрофных организмов является
по преимуществу анаболическим, гетеротрофных — катаболическим.
Основу пластического обмена составляет органический обмен. Тра-
диционное разделение его на углеводный обмен, липидный обмен
и обмен азотсодержащих соединений обусловлено большой распро-
страненностью в живой природе соединений этих классов и разли-
чием их свойств.
Энергетический обмен
Движущей силой обмена веществ служит разность термодина-
мических потенциалов участвующих в реакциях соединений. По ис-
точникам используемой при обмене веществ энергии организмы де-
лят на фототрофы и хемотрофы. У первых роль богатых энергией
субстратов выполняют эндогенные продукты начального этапа фо-
тосинтеза, у вторых — различные соединения экзогенной природы.
Если в качестве субстратов окисления хемотрофы используют орга-
нические соединения, то их относят к хемоорганотрофам, если неор-
ганические, например Н2, NH3, СО, H2S, — литотрофам.
В рамках общего обмена веществ изучение энергетического об-
мена у фототрофов состоит в определении энергетических парамет-
ров фотосинтеза, у хемотрофов — в исследовании баланса между
энергией, расходуемой на биосинтез конечных продуктов обмена ве-
2.2. Обмен веществ
77
ществ, на совершение механической работы, а также рассеиваемой
в виде тепла.
Гетеротрофные организмы получают энергию путем разложения
органических веществ, т. е. в процессе окисления глюкозы до угле-
кислоты и воды:
г*
СбЩгОб + 6O2 = 6СО2 + 6Н2О + 690 ккал.
Гетеротрофы также обладают способностью включать углекис-
лоту в состав клеточного материала, однако у этих организмов источ-
ником восстановителя может быть только органическое вещество.
Сульфатвосстанавливающие бактерии характеризуются разнооб-
разием типов энергетического обмена. Можно выделить следующие
типы обмена [104]: анаэробное дыхание и анаэробное сбраживание
органических субстратов в отсутствие SO^-. В процессы анаэробно-
го дыхания вовлекаются неорганический субстрат — водород и ор-
ганические субстраты. Акцептором электронов в этих процессах яв-
ляется сульфат. В некоторых случаях акцепторами могут служить
фумаровая кислота и ацетилен. Из органических веществ донора-
ми электронов в процессах сульфатредукции могут служить кисло-
ты — молочная, пировиноградная, яблочная, муравьиная, щавелевая
и некоторые спирты — этанол, бутанол. Упоминаемые в тексте угле-
водороды и их принадлежность к той или иной кислоте отражены
в табл. 2.2.
В промысловых средах месторождений, находящихся во 2 и 3
стадиях разработки, функционирует множество различных микроор-
ганизмов, так или иначе влияющих на эксплуатационную надежность
и долговечность нефтепромыслового оборудования.
78
Глава 2
Таблица 2.2. Упоминаемые в тексте углеводороды
Название углеводорода Название кислоты, соединения Формула
Лактат Молочная СН3СН(ОН)СООН
Малат Яблочная НООССН(ОН)СН2СООН
Пируват Пировиноградная СН3С(О)СООН
Формиат Муравьиная нсоон
Фумарат Фумаровая НООССН=СНС(О)ООН
Холин Гидроксид ( 2-гидроксиэтил (три-метил) аммония [HOCH2CH2N+(CH3)]OH-
К таким организмам прежде всего относят:
— литотрофные микроорганизмы;
— бактерии, окисляющие углеводороды;
— микроорганизмы, участвующие в восстановлении и окислении
соединений серы.
2.3. Литотрофные микроорганизмы
Известны литотрофные микроорганизмы, способные развивать-
ся за счет окисления неорганических соединений.
1. Водородные бактерии, осуществляющие окисление водорода
с образованием воды:
Нг + У2О2 —* Н2О + 56 ккал.
2.3. ЛИТОТРОФНЫЕ МИКРООРГАНИЗМЫ
79
2. Метанокисляющие бактерии:
СЩ + 2О2 -> СО2 + 2Н2О + 195 ккал.
3. Нитрифицирующие бактерии, окисляющие аммиак в две фа-
зы. В первой фазе происходит окисление аммиака до азотистой кис-
лоты: - '
NH3 + 3/2О2 HNO3 + Н2О + 73 ккал.
Возбудителем этой фазы нитрификации являются виды Nitroso-
monas, Nitrosocystis и др.
Вторая фаза нитрификации сопровождается окислением азоти-
стой кислоты до азотной и вызывается Nitrobacter vinogradskyi:
HNO2 + l/2O2 —> HNO3 + 17 ккал.
4. Серобактерии, окисляющие сероводород до элементарной се-
ры, которая откладывается внутриклеточно:
H2s -I- У2О2 —> S + Н2О + 41 ккал.
5. Thiobacillus thiooxidans, окисляющий элементарную серу
до серной кислоты:
S + Н2О + 3/2О2 —» H2SO4 + 118 ккал.
6. Thiobacillus ferrooxidans, окисляющий серно-кислое железо
до окисного в кислой среде:
2FeSO4 + H2SO4 + У2О2 -> Fe(SO4) + Н2О + 19 ккал.
7. Железобактерии, окисляющие закисное железо до окисного
в слабокислой среде:
4FeCO3 + О2 + 6Н2О —> 4Fe(OH)3 + 4СО2 + 40 ккал.
80
Глава 2
8. Метанобразующие бактерии, анаэробно окисляющие водород:
4Нз + СО2 —> СН.1 + 2Н2О + 62 ккал.
2.4. Тионовые бактерии
Тионовые бактерии играют основную роль в окислении боль-
шинства неорганических соединений серы в природе. Они являют-
ся автотрофными бактериями, использующими серу и не полностью
окисленные ее соединения как доноры электродов для ассимиляции
СО2, удовлетворяющего все углеродные потребности данной группы
бактерий. В 1902 г. Natanson из морской воды Неаполитанского зали-
ва выделил нефотосинтезирующую бактерию, способную окислять
тиосульфат с образованием внеклеточной элементарной серы [115].
Этим она отличалась от известных серобактерий, окисляющих со-
единения серы с откладыванием ее внутри клеток, и была названа
тионовой бактерией.
Семейство тионовых бактерий относят к порядку Pseudomonada-
les. Родовое название Thiobacillus является формальным, посколь-
ку это мелкие неспорообразующие грамотрицательные подвижные
палочки с закругленными концами, обладающие полярным жгути-
ком или пучком жгутиков [34]. К истинным бациллам тионовые
бактерии никакого отношения не имеют. Размеры клеток 0,5 ... 0,8
на 0,9... 1,5 мкм. Располагаются большей частью поодиночке, редко
образуют короткие цепочки.
Разделение на виды основано на различном отношении к источ-
никам питания и кислотности среды. Окисляя соединения серы, они
используют выделяющуюся энергию для синтетических процессов
и роста организма.
2.4. Тионовые бактерии
81
Рассматриваемые виды Thiobacillus являются аэробами, обли-
гатными автотрофами, т. е. все сложные органические соединения
(белки, углеводы и и т. п.) они синтезируют из неорганических ма-
териалов как источников питания. Клеточный углерод образуют из
углерода СО2, азот — из соединений аммония и т. д.
Среди тионовых бактерий преобладают сероокисляющие и же-
лезоокисляющие бактерии.
Сероокисляющие бактерии
Сероокисляющие бактерии [124] способны использовать энер-
гию окисления восстановленных соединений серы в серную кисло-
ту. С точки зрения коррозионной опасности наиболее важны виды
Т. thioparus, Т. thiooxidans и Т. novellus, которые существенно пони-
жают pH среды.
Типичными представителями сероокисляющих бактерий явля-
ются бактерии вида Т. thioparus. Свое название получили благодаря
способности образовывать серу на среде с тиосульфатом (thio — сера,
раго — рождать):
5Na2S2O3 + Н2О + 4О2 -> 5Na2SO4 + H2SO4 + 4S.
Эта реакция — главная реакция, дающая энергию.
Бактерии Т. thioparus в своей жизнедеятельности могут исполь-
зовать следующие восстановленные соединения серы: сероводород,
сульфид кальция, молекулярную серу, тиосульфат, тетратионат, гид-
росульфид и слабее — ди- и тритионаты. Развиваются в щелоч-
ной и нейтральных средах. Оптимальное значение pH для роста
Т. thioparus сдвинуто в щелочную сторону, а отдельные виды спо-
82
Глава 2
собны развиваться даже при pH 9,8. При pH, равной 5, развитие пре-
кращается, а при pH, меньшей 3,5, они погибают. При этом процесс
окисления сопровождается отложением серы и образованием суль-
фата. Эти бактерии окисляют также серу в сульфат. Но этот процесс
по сравнению сопроцессом окисления тиосульфата протекает крайне
медленно. Скорость образования серной кислоты зависит от степени
аэрации среды. Строго автотрофная природа этих бактерий тем не
менее не лишает их способности развиваться в присутствии орга-
нических пищевых веществ. Бактерии могут развиваться при очень
малом количестве кислорода, окисляя сероводород до элементарной
I
серы, отложения которой на поверхности металла являются активны-
ми катодами, что резко увеличивает скорость коррозии. Повышенная
аэрация подавляет их развитие. Бактерии встречаются в воде и поч-
ве. Геохимическая деятельность T.thioparus приводит к образованию
и накоплению серы в природе.
Бактерии Tthiooxidans являются ацидофильными бактериями,
встречаются в кислых средах, содержащих свободную серу и фосфо-
рит. Они являются облигатными автотрофами и строгими аэробами.
Источником углерода служит СО-2, в нейтральной среде бактерии не
развиваются и удовлетворяют свою потребность в энергии исключи-
тельно за счет серы, которую окисляют непосредственно в сульфат,
не вызывая ни отложений серы, ни полионатов:
S + 1,5О2 + Н2О -> H2SO4 + 141800 кал.
Значительные трудности для объяснения физиологии Т. thiooxi-
dans представляет то обстоятельство, что сера нерастворима в воде.
Потребление серы обусловлено наличием на каждом конце клетки
2.4. Тионовые бактерии
83
T.thiooxidans маслянистой капли, в которой растворяются прилипшие
к ней частицы серы.
Бактерии T.thiooxidans не могут использовать сероводород, суль-
фиды и тиосульфат, так как эти соединения в кислой среде при pH
менее 4 неустойчивы.
/*
Установлено, что в отличие от традиционных представлений
о доминирующей роли серной кислоты в интенсификации процес-
са коррозии в средах, содержащих тионовые бактерии, высокие ско-
рости растворения стали 10ХСНД обусловлены появлением в сре-
де липидов [29]. Липидная фракция тионовых бактерий содержит
насыщенные и жирные ненасыщенные кислоты, фосфо- и суль-
фолипиды. При наличии серной кислоты они переходят в поляр-
ную форму, повышая скорость коррозии стали 10ХСНД на поря-
док. В аналогичной среде, но без липидной фракции скорость кор-
розии с ростом концентрации серной кислоты увеличивается лишь
в 2... 3 раза.
Биологическая активность бактерий T.thiooxidans и скорость
коррозии металла в средах, их содержащих, непосредственно зависит
от химического состава металла. Например, коррозионная стойкость
стали 10ХСНД в культуральных средах Т. thiooxidans в 6 ... 7 раз ни-
же, чем Ст. 3, табл. 2.3 [29].
Более низкая коррозионная стойкость легированных сталей
в средах с тионовыми бактериями обусловлена присутствием в них
никеля, а биохимической среде — липидов. Никельсодержащая леги-
рованная сталь непригодна для эксплуатации в средах, где возможна
жизнедеятельность тионовых бактерий.
Кроме строгих автотрофных тионовых бактерий, в природе ши-
роко распространены миксотрофные бактерии — Т novellus, способ-
84
Глава 2
Таблица 2.3. Скорость коррозии металлов в биологически активной и мо-
дельной средах
Металл Скорость коррозии, г/(м сут)2 в среде
Содержащей тионовые бактерии Модельной
Ст. 3 19,3 41,5
10 хснд 132,7 16,2
Fe 16,5 19,3
Fe - 0,2Cr ' 25,6 31,8
Fe - 0,7Cr 41,4 58,5
Fe - 0,2Cu 11,6 8,5
Fe - 0,7Cu 9,1 7,8
Fe - 0,2Ni 24,8 16,0
Fe - 0,7Ni 89,6 15,8
Fe - 0,7Cr - 0,7Cu 17,7 10,1
Fe - 0,7Cr - 0,7Ni 147,4 29,3
Fe—0,7Cr—0,7Cu—0,7Ni 129,5 17,1
ные к автотрофному и гетеротрофному способу питания. Эти бакте-
рии распространены в основном в почвах и минеральных источниках.
Окисляют тиосульфат до сульфата при реакции, близкой к нейтраль-
ной, но не окисляют элементарную серу, хорошо растут на органи-
ческих средах.
2.4. Тионовые бактерии
85
Оптимум роста большинства миксотрофных видов тионовых
бактерий лежит в нейтральных или слабощелочных пределах. Осу-
ществляют реакции:
КагВзОз + 20г + Н2О —> Na2SO4 4- H2SO4,
2Na2S4O6 + 702 + 6Н2О -> 2Na2SO4 + 6H2SO4.
Железоокисляющие бактерии
Железоокисляющие бактерии [124] Thiobacillus ferrooxidans (си-
ноним Ferrobacillus ferrooxidans) занимают особое положение среди
тионовых бактерий, поскольку, помимо способности к автотрофно-
му росту за счет окисления соединений серы, они могут использо-
вать энергию окисления закисного железа в окисное. Оптимальное
количество железа для их существования составляет около 9 г/л. Уг-
леродное питание обеспечивают за счет использования углекислоты.
Оптимальным значением pH для их развития является 1,7... 2.5.
Вне этих пределов скорость окисления резко уменьшается. Макси-
мальную кислотность наблюдают при pH = 0,6.
Т. ferrooxidans устойчивы к действию тяжелых металлов и раз-
виваются в среде даже при наличии 6% CUSO4.
Для развития бактериям необходимо наличие соединений азота,
фосфора и минеральных солей. Концентрация кислорода в среде не
влияет существенно на развитие этих организмов. Окисление железа
бактерии осуществляют в соответствии с реакцией
4Fe2+ + 4Н+ + 6SO2' + О2 = 2Fe2(SO4)3 + Н2О.
Следствием этой реакции является некоторое подщелачивание
среды и гидролиз соли с образованием гидрата окиси железа и серной
86
Глава 2
кислоты:
Fe2(SO4)3 + 6Н2О = 2Fe(OH)3 + 6Н+ + 380^,
благодаря которыми обеспечивается оптимальная для бактерий реак-
ция среды. Максимальная скорость роста этих бактерий наблюдается
при 35°С, при температуре 50°С они погибают.
Т. ferrooxidans развиваются за счет относительно небольших ко-
личеств железа (если существует механизм регенерации восстанов-
ленного железа) [39]:
t
2MeS + 2Fe2(SO4)3 + ЗО2 + 2Н2О = FeSO4 + 2MeSO4.
Образующееся при реакции закисное железо может быть окисле-
но микроорганизмами с образованием серной кислоты и окисленного
железа, которые снова вступают в реакцию. Окисляемым веществом
оказывается сера сульфида, а железо служит посредником. В отличие
от других тионовых бактерий Т. ferrooxidans воздействуют на широ-
кий набор сульфидных материалов.
Т. ferrooxidans встречают в ассоциации с другими представите-
лями этого рода, чаще всего с Т. thiooxidans. Эти два организма яв-
ляются причиной создания кислых шахтных вод и загрязнения рек
серной кислотой.
Таким образом, тионовые бактерии вызывают существенное
подкисление среды обитания, что активизирует процесс коррозии
железа с водородной деполяризацией. При этом если в среде жиз-
недеятельности тионовых бактерий имеется сероводород и сульфид
железа, то скорость коррозии железа сильно возрастает.
2.4. Тионовые бактерии
87
Тионовые бактерии способны окислять соединения серы по ре-
акциям [9]:
2S + ЗО2 + 2Н2О 2H2SO4, (1)
Na2S + 2О2 4- Н2О —► Na2SO4 + H2SO4, (2)
2Na2S4Og 4- 7О2 4~ 6Н2О —> 2Na2SO4 4- 6H2SO4, (3)
2KSCN 4- 4О2 4- 2Н2О -» (NH4)2SO4 + K2SO4 4- 2СО2, (4)
5S + 6KNO3 4- Н2О -> 3K2SO4 + 2H2SO4 4- 3N2, (5)
5Na2S2O3 4- 8NaNO3 4- 2H2O -» 9Na2SO4 4- H2SO4 4- 4N2, (6)
12FeSO4 + 3O2 + 6H2O -» 4Fe2(SO4)3 + 4Fe(OH)3. (7)
Реакции (1-4) типичны для T.thioparus, (1-6) для T. denitrificans,
(1-3) для Т. thiooxidans, (1, 2, 7) для Т. ferrooxidans, (1-3) для
Т. novel ius.
Продуктом всех реакций является серная кислота, вызывающая
разрушение металлических сооружений.
Биогенная серная кислота, видимо, не является единственным
агентом, обуславливающим коррозию.
Железобактерии
Железобактерии относят к группе аэробных бактерий. Коррози-
онную активность проявляют преимущественно в водных средах.
Железобактерии способствуют созданию отложений и осадков
гидроокиси железа в виде морфологически оформленных структур,
путем ассимиляции или экстрагирования ионов железа из раство-
ра в результате своего метаболизма, что приводит к нарушению
ионного равновесия окисления и восстановления в системе и со-
88
Глава 2
зданию элементов дифференциальной аэрации и локальной корро-
зии.
Наиболее распространенными видами железобактерий являются
Gallionella, Leptothrix, Crenothrix [9], [39].
Бактерии рода Leptothrix, являлись пресноводными микроор-
ганизмами, представляют собой палочковидные клетки, собранные
в цепочки, окруженные трубчатым влагалищем, пропитанным окис-
лами железа. Клетки могут выскальзывать из влагалища и тогда
становятся подвижными благодаря наличию полярных жгутиков.
Данный род состоит из трех основных групп микроорганизмов:
L. ochracea, L. discorhora и L. sideropuls.
Crenothrix — нитчатые, прикрепленные формы с выраженным
влагалищем. Клетки дисковидные или цилиндрические.
Представителей Gallionella встречают в проточной воде ручьев,
где замедленное течение, в" водопроводных трубах.
Для нормального развития железобактерий необходимы следу-
ющие условия: pH среды близкая к нейтральной, наличие солей за-
кисного железа, кислород, температура от +6 до +25°С и источник
углерода, в качестве которого может быть использована растворенная
в воде углекислота.
Железобактерии не могут существовать в достаточно раскис-
ленной среде, поскольку в ней мало кислорода. В то же время эти
бактерии не могут развиваться и в среде с повышенным содержанием
кислорода вследствие нехватки двухвалентного железа. Источником
энергии является реакция окисления двухвалентного железа в трех-
валентное:
2FeCO3 + У2°2 + ЗН2О 2Fe(OH)3 + СО2.
2.5. Бактерии, окисляющие углеводороды 89
Образующиеся осадки в виде гидроокиси железа окрашены в яр-
кий желтый цвет, вследствие чего бактерии относят к группе образо-
вателей охры.
Возможны следующие пути участия железобактерий в коррози-
онном процессе [17]:
— первичное образование пары дифференциальной аэрации
вследствие изменения концентрации кислорода в инфицированном
месте и дальнейшее функционирование этой коррозионной пары при
участии бактерий или без них;
— механическое укрепление каверны благодаря волокнистой
структуре нитчатых железобактерий;
— каталитическое окисление ионов двухвалентного железа и бы-
строе осаждение гидроокиси железа, которое далее усиливает анаэ-
робные условия на анодном участке.
Это приводит к увеличению разности потенциалов между по-
верхностью железа под каверной и вне ее и соответственно к значи-
тельному росту скорости коррозии в каверне.
Гидроокись железа, осаждаемая железобактериями, образует на
стенках труб бугорки, наросты с анаэробными участками, характери-
зующимися высокой механической прочностью и недоступными для
кислорода.
2.5. Бактерии, окисляющие углеводороды
В окислении углеводородов принимают участие многие бакте-
рии, к числу которых относят микроорганизмы порядков Pseudomo-
nadales, Eubacteriales, Actinomycetales класса шизомицетов, среди ко-
торых распространены представители семейств Pseudomonadaceae,
90
Глава 2
Achromobacteriaceae, Micrococcaceae, Brevibacteriaceae, Corynebacte-
riaceae, Bacillaceae, Mycobacteriaceae, Actinomycetaceae. Перечень
микроорганизмов [104], использующих углеводороды, выделенные
из разных природных образцов, приведен в табл. 2.4.
Оптимальнаятемпература для жизнедеятельности бактерий,
окисляющих углеводороды, находится в пределах 30... 55°С. Од-
нако высокая температура не является препятствием для развития
углеводородокисляющих бактерий. Данный вид бактерий обнаружен
в термальных водах с температурой 55 ... 89°С. Термотолерантные
и термофильные штаммы микобактерий и псевдомонад, окисляющие
н-алканы Ci — Сю, выделены из пластов Краснодарского края и Став-
рополья с температурой 50... 80°С.
Особый интерес представляет постановка вопроса о широте
спектра используемых углеводородов. По-видимому, способность
микроорганизмов использовать тот или иной набор углеводородов
зависит от характера распределения последних в водных средах и от
механизма их проникновения в клетку.
Например, проникновение парафинов в клетки дрожжей проте-
кает по следующей схеме. На начальном этапе проникновения про-
исходит молекулярная сорбция углеводорода на поверхности клетки,
затем следует диффузия его через клеточную стенку и растворение
в липидах цитоплазменной мембраны. Полагают, что ферментативная
система окисления углеводорода не связана с оболочкой и локализо-
вана в цитоплазматической мембране, цитоплазме или иных органах
протопласта.
Приуроченность организмов рода Pseudomonas к нефтяным пла-
стам не случайна. Эти организмы в большей степени приспособлены
к использованию жидких легкокипящих н-алканов С5 — Сю и аро-
2.5. Бактерии, окисляющие углеводороды
91
Таблица 2.4. Микроорганизмы, использующие в своей жизнедеятельности
углеводороды
Среда обитания микроорганизмов
Воды и породы над залежами нефти и газа Битуминозные и озокеритовые породы и воды Пластовые водонефтяные залежи
Pseudomonas methanica Pseudomonas fluorescens Pseudomonas putida
Bacterium methanica Ps. rathonis Ps. dacunae
Pseudomonas fluorescens Ps. desmolytica Ps. Fluorescens
Ps. liquefaciens Ps. aeruginoSa Ps. aeruginosa
Ps. pantotropha Achromobacter parvulus Ps. desmolytica
Ps. gentrifugans Mycobacterium mucosum Ps. mycophaga
Ps. scissa M. globiforme Ps. radiobacter
Ps. pelliculosa M. coeliacum Ps. turcosa
Ps. boreophilus M. lacticolum Ps. denitrificans
Ps. arvilla M. convolutum Ps. scissa
Bacterium aliphaticum Mycococcus rubber Ps. longa
Mycobacterium rubrum var. propanicum Mycoc. albus Ps. pelliculosa
M. luteum Proactinomyces corallinus Ps. azotovorans
M. flavum Proact. paraffinae Ps. schuylkilliensis
M. lacticolum Brevibacterium maris Ps. nitroreduccns
M. equi Arthrobacter sp. Brevibacterium pussilum
Methanomanas methanica Candida lipolytica Brebibact.helvolum
Proactinomyces actinomorphus Penicillium notatum Arthrobacter tumescens
Pseudobacterium subluteum Penic. chrizogenum Micrococcus luteus
Penic. miczynki M. varians
Achromobacter deliatulus
92
Глава 2
магических углеводородов, чем дрожжи и микобактерии. Отсутствие
роста последних на легких бензиновых фракциях объясняют вред-
ным воздействием этих фракций как растворителей на обогащенные
липидами клетки. Вероятно, бензиновые фракции, постоянно при-
сутствующиев нефтях, препятствуют распространению в нефтяных----
пластах организмов семейства Mycobacteriaceae.
Другой причиной преимущественного распространения псевдо-
монад в нефтяных пластах может быть способность их к существо-
ванию в микроаэрофильных и анаэробных условиях.
Установлено [104], что газообразные углеводороды чаще потреб-
_ ।
ляют микобактерии, а жидкие, легкокипящие — псевдомонады.
Помимо псевдомонад алифатические углеводороды окисляют
многочисленные представители совершенных и несовершенных гри-
бов и дрожжевые организмы.
Парафины различной длины цепи потребляются микроорганиз-
мами в разном состоянии. Жидкие парафины средней длины цепи,
содержащие до 10 атомов углерода, используются в состоянии ис-
тинной растворимости. Парафины с длиной цепи более 10 атомов
углерода весьма слабо растворимы в воде, поэтому потребляются
в прямом контакте с клеткой. Эти различия оказывают влияние на
возможность использования парафинов микроорганизмами. Потреб-
ление трудно растворимых парафинов в капельно-жидком состоянии
предпочтительно, что подтверждается ускорением темпа роста дрож-
жей при увеличении площади поверхности эмульгированных капель.
Исследование воздействия микроорганизмов на изоалканы и уг-
леводороды гибридного строения показало, что длина углеводород-
ной цепи и количество ответвленных метильных групп напрямую
влияют на доступность углеводорода микробиологическому воздей-
2.5. Бактерии, окисляющие углеводороды
93
ствию. При этом огромное значение играет расположение этих групп
на молекуле алкана. Увеличение числа последовательно ответвляю-
щихся метильных групп уменьшает доступность, а увеличение длины
цепи — увеличивает.
Микобактерии и нокардия более активны в отношении разветв-
ленных парафинов и углеводородов сложного строения, чем бактерии
рода Pseudomonas.
Ароматические углеводороды, бензол, толуол, ксилол использу-
ют в своей жизнедеятельности бактерии различных родов — микобак-
терии, нокардия, псевдомонады. Среди ароматических углеводородов
наиболее легко подвергаются окислению соединения с боковыми це-
пями и полимеризованные структуры. Скелет бензольных ядер мало
изменяется. Процесс окисления идет в основном по боковым цепям
или по соединительному звену и приводит к различным продуктам
уплотнения. Возникают полимеризованные и конденсированные си-
стемы со сложноэфирными связями, кроме того, образуются структу-
ры с гидроксильными, карбоксильными и карбонильными группами.
Именно ароматические углеводороды и среди них бициклические
структуры являются основным источником смолообразования при
окислении нефтей.
Нафтеновые углеводороды легче окисляются, чем ароматиче-
ские. Основным продуктом окисления являются кислоты и оксикис-
лоты. Количество продуктов окислительной конденсации типа смол
невелико, и они образуются в результате вторичных продуктов.
Наиболее часто отмечают использование полициклических уг-
леводородов (нафталина, антрацена, фенантрена), как единственного
источника углерода и энергии, представителями рода Pseudomonas.
Замечено использование нафталина, антрацена, фенантрена дрожжа-
94
Глава 2
ми рода Trichosporon. По-видимому, дрожжи и грибы принимают
меньшее участие в разрушении ароматических углеводородов, чем
бактерии. В то же время дрожжи различных видов и грибы активно
расщепляют ароматические кислоты и спирты.
2.6. Микроорганизмы, участвующие в восстановлении
и окислении соединений серы
Большинство разрабатываемых месторождений имеет благопри-
ятные условия для развития и деятельности микроорганизмов, свя-
занных с круговоротом серы, поскольку нефти содержат до 5% серы,
а пластовые воды богаты соединениями сульфатов.
В процессах, связанных с восстановлением и окислением соеди-
нений серы, участвуют три основные группы микроорганизмов:
— бактерии, восстанавливающие сульфаты;
— фотосинтезирующие пурпурные бактерии;
— тионовые бактерии.
Сульфатвосстанавливающие бактерии
Процесс восстановления сульфатов, обеспечивающий организм
внутриклеточным материалом (ассимиляторная сульфатредукция),
встречается у значительного количества микробов, в частности,
у представителей родов Achromobacter и Pseudomonas, которые яв-
ляются факультативными анаэробами. Использование сульфата как
конечного акцептора электронов с образованием больших количеств
сероводорода (диссимиляторная сульфатредукция) присуще лишь
высоко специализированной группе микроорганизмов — облигатно
анаэробным бактериям, которые осуществляют энергообразующие
2.6. Микроорганизмы, участвующие в восстановлении среды 95
реакции:
SO^~ + 8е + 10Н+ H2S + 4Н2О.
Известно более 20 видов сульфатвосстанавливающих бактерий,
относящихся к родам: Desulfo vibrio, Desulfotomaculum, Desulfomonas.
Desulforomonas, Desulfobacter, Desulfofomicrobium, Desulfobulbus,
Thermodesulfobacterium, Desulfococcus, Desulfonema, Desulfosarcina
и др. Хотя они отличаются таксономически, но физиологически и эко-
логически они весьма похожи. К основным родам относят четыре:
Desulfovibrio, Desulfotomaculum, Desulfomonas и Desulforomonas [99].
Известны также термофильные архебакгерии, осуществляющие
сульфатредукцию, — Archaeoglubus fulgidus и A. profundus.
К роду Desulfovibrio относят неспороносные, грамотрицатель-
ные изогнутые палочки, иногда S-образные или спиральные, имею-
щие полярный жгутик, который обеспечивает быстрое поступатель-
ное движение бактериальной клетки [7].
Бактерии из родов Desulfovibrio способны восстанавливать эле-
ментарную серу. Все представители данного рода строгие анаэробы,
растущие при Eh от +115 до —450 мВ, при температуре 25 ... 44°С
и pH = 5,5 ... 9,0 (оптимум pH — 7,2), т. е. в условиях, соответству-
ющих зоне устойчивости сероводорода.
Известно шесть основных видов бактерий рода Desulfovibrio, че-
тыре из которых, D. desulfuricans, D. vulgaris, D. salexigenes, D. africans,
вызывают коррозию металлов [9].
D. desulfuricans — изогнутые вибриоидные, сигмоидные или пря-
мые палочки, размером 0,5... 1,0 х 3... 5 мкм, активно поступатель-
но двигающиеся с помощью полярного жгутика. Облигатные анаэ-
робы растут при Eh — 100 мВ, pH = 7,2 и температуре 28... 44°С.
96
Глава 2
Используют соединения углерода: лактат, малат, пируват и холин.
Желатину не разжижают, нитраты не восстанавливают.
D. vulgaris по морфологии и величине сходен с D. Desulfuricans,
но отличается по отношению к источникам углерода.
D. salexigenes по морфологии, величине и отношению к углероду
аналогичен D. desulfuricans, но отличается галофилией.
D.gigas имеет вид больших изогнутых палочек, 1,2...1,5х
х 5... 10 мкм, часто соединенных в цепочки, движение медленное,
поступательное, лофотрих.
D. africans — сигмовидная длинная палочка, 5... 10 мкм, лофо-
трих, обладающая быстрым поступательным движением и широкой
галотолерантностью.
D. thermophilus, выделенный из воды нефтяного пласта на Ап-
шероне, представляет собой подвижные палочки разной длины
(0,5 .. . 0,6 х 1,4... 2,4 мкм). Попадаются клетки почти округлой фор-
мы, часто сдвоенные. Встречаются цепочки, в которых обнаружива-
ются клетки разной длины, монотрихи. Культура развивается при
температуре 50... 80°С. Оптимальной является температура 65°С,
медленно растет при 45°С. При добавлении к среде 3... 5 мл пла-
стовой воды или 0,5 ... 1,0% NaCl рост ускоряется. Восстанавливает
сульфаты в присутствии лактата, пирувата, формиата и водорода.
Род Desulfotomaculum объединяет грамотрицательные прямые
или изогнутые одиночные палочки, иногда соединенные в цепоч-
ки. Спорообразование конечное или субтерминальное, вызывающее
слабое раздувание клетки. Характер движения обусловлен перитри-
хиальным жгутиком и напоминает кувырки. Облигатные анаэробы
восстанавливают сульфаты в сульфид. В процессах коррозии метал-
лов принимают участие виды Dtm. nigrificans и Dtm. orientis [9].
2.6. Микроорганизмы, участвующие в восстановлении среды 97
Dtm. nigrificans, обычно называемый Clostridium, размером около
0,3 ... 0,5 х 3 ... 6 мкм, имеет вид палочки с закругленными конца-
ми, иногда спаренные. Термофил растет при температуре 65 ... 70°С,
оптимум 55°С, может поддерживать рост при 30 ... 37°С. Растет на
среде с лактатом или пируватом, из сульфатов образует сероводо-
род. Обитают в почвах, компостах, термальных источниках. Термо-
фильные свойства Dtm. Nigrificans позволяют развиваться этому ор-
ганизму в системах центрального отопления, теплообменниках, где
он вызывает интенсивную коррозию.
Dtm. ruminis — грамотрицательные палочки, размером 0.5 х
хЗ... 6 мкм, с закругленными концами, одиночные, иногда в парах;
перитрихи, легко подвижные. Мезофиллы, температурный оптимум
роста 37°С, верхний предел — 48°С. Растут на среде с лактатом,
пируватом или формиатом. В присутствии сульфата образуют се-
роводород. На ацетате не растут, на пирувате растут без сульфата,
непатогенны.
Dtm. orientis — грамотрицательные толстые изогнутые палочки
размером 1,5 х 5 мкм, одиночные или парные, подвижные, жгутико-
вание перитрихиальное. Мезофиллы, температурный оптимум роста
30 ... 37°С, верхний предел — 42°С. Желатину не разжижают, нитрат
не восстанавливают. Растут в присутствии лактата или пирувата и
сульфата или тиогликолата с образованием сероводорода. Не растут
на среде с формиатом или ацетатом в присутствии сульфата. Без суль-
фата не растут даже в присутствии пирувата. Непатогенны.
Dtm. antarcticum nov. sp. — грамотрицательные толстые палочки
с закругленными концами, иногда соединенные попарно или в корот-
кие цепочки размером 1,0 ... 1,2 х 4... 6 мкм. Споры овальные, цен-
тральные или полярные, слегка раздувающие клетку. Подвижность
98
Глава 2
обусловлена перитрихиальным жгутикованием. Облигатные анаэро-
бы. Оптимальная температура роста 2О...ЗО°С, т.е. оптимум ни-
же, чем для известных видов этого рода. Хорошо растут на средах
с добавлением дрожжевого экстракта. Восстанавливают сульфаты до
сульфидов. Содержат цитохром 1), не имеют десульфовиридина. Со-
леустойчив, но при содержании в среде 10% NaCl рост прекращает-
ся. Этот вид отличается от известных видов рода Desulfotomaculum
и тем, что не образует кислоты из фруктозы, сахарозы, ксилозы и ара-
бинозы, а образует только из глюкозы. Разжижает желатину.
Обзор видовых признаков представителей родов Desulfovibrio
I
и Desulfotomaculum свидетельствует о том, что морфилогическая ха-
рактеристика уже не может быть основой для определения видов
сульфатредуцирующих бактерий. Выделение палочковидных форм
СВБ наряду с искривленными формами говорит о необходимости
более глубоких исследований, позволяющих выявить новые виды
бактерий этой группа. Изучение закономерностей распределения от-
дельных видов СВБ в различных экологических нишах показывает
следующее: в воде и илах морей и пресных водоемов распростране-
ны главным образом представители рода Desulfovibrio, представите-
ли рода Desulfotomaculum обнаруживают преимущественно в почве.
Коррозионная активность различных видов бактерий различна.
Так, наибольшая скорость коррозии характерна для культур, обла-
дающих максимальной гидрогеназной активностью [104]. Скорость
коррозии под действием D. desulfuricans шт. Llanelly, Hildenborough
и Dtm. orientis шт. Singapore достигает соответственно 8,7; 7,3;
3,3 мг/дм2-сут, рис. 2.1. Два штамма D. desulfuricans (Llanelly,
Hildenborough), вызывающие самую высокую скорость коррозии, вы-
2.6. Микроорганизмы, участвующие в восстановлении среды 99
делены из почвы, отобранной в непосредственной близости от кор-
родированных труб, обладают высокой гидрогеназной активностью.
Время, сут
Рис. 2.1. Потеря в весе стальных образцов под действием различных штам-
мов СВБ: 1 — Llanelly; 2 — Hildenborough; 3 — TeddingtonR; 4 — America;
5 — Benghazi; 6 — Singapore; 7 — стерильная среда.
В нефтепромысловых средах существуют планктонные (свобод-
но плавающие) и адгезированные (закрепленные на поверхности)
клетки СВБ.
Адгезированные клетки СВБ образуют довольно плотные при-
легающие к поверхности слои колоний. В результате жизнедеятель-
ности сообщества микроорганизмов в водной среде на поверхно-
сти клеток образуется плотная биопленка, обеспечивающая их внеш-
нюю защиту от проникновения внутрь химических реагентов. Обыч-
но эта пленка состоит из аэробных бактерий. Под прикрытием этой
100
Глава 2
биопленки, препятствующей проникновению кислорода, развивают-
ся анаэробные микроорганизмы, в частности СВБ, которые и обу-
славливают биологическую коррозию. В результате операция по-
давления жизнедеятельности адгезированных клеток СВБ является
более трудоемкой и требует более высоких концентраций бактери-
цидов.
Пурпурные бактерии
Из фотосинтезирующих микроорганизмов в нефтяных пластах
могут быть распространены только те формы организмов, которые
способны развиваться в темноте. Такими свойствами обладают пред-
ставители несерных пурпурных бактерий. Представители несерных
бактерий Rhodopseudomonas capsulate, Rh. sphaeroides, Rh. palustris,
Rhodospirillum rubrum способны окислять сульфиды, однако в зна-
чительно меньших концентрациях, чем серные пурпурные организ-
мы. При этом выше перечисленные организмы, кроме Rh. palustris,
окисляют сульфид до внеклеточной элементарной серы, а послед-
ний — до серной кислоты без промежуточного образования серы.
Сульфид используется как донор электронов при фотосинтезе. Окис-
ление тиосульфата Rh. palustris было известно ранее. Помимо этого,
использование органических соединений как доноров восстановите-
ля, а также в качестве источников углерода свойственно многим так
называемым серным пурпурным бактериям. Таким образом, основ-
ные качественные различия между серными и несерными бактериями
исчезают.
Пурпурные бактерии относят к подпорядку Rhodospirillinae
и разделяют на два семейства — Rhodospirillaceae и Chromatiaceae,
включающие в качестве типовых родов Rhodospirillum и Chromatium.
2.7. Микроорганизмы, способствующие созданию условий 101
Ряд пурпурных бактерий, которые ранее рассматривали как
несерные, способны использовать органические вещества в темно-
те, окисляя их молекулярным кислородом для извлечения энергии.
Таким образом, в темноте они переключаются на процессы дыха-
ния. К числу таких факультативных аэробов относят Rhodospirillum
rubrum, RhodopseudomonSis palustris, Rh. capsulate, Rh. sphaeroides,
Rh. acidophila и некоторые другие организмы. При этом разные ви-
ды развиваются при различных концентрациях кислорода — от 0,3
до 3 мг/л.
Ectothiorhodospira shaposhnikovif'— организм, относящийся к сер-
ным пурпурным бактериям, способный переключаться на органиче-
ские вещества, может также расти в темноте в микроаэрофильных
условиях. Кроме того, некоторые пурпурные бактерии могут разви-
ваться в темноте в анаэробных условиях.
Разнообразие путей обмена у пурпурных фотосинтезирующих
бактерий позволяет предположить возможность переключения их на
процессы дыхания в темноте при окислении восстановленных соеди-
нений серы.
2.7. Микроорганизмы, способствующие созданию
на поверхности условий для действия
концентрационных элементов
Бактерии, образующие отложения. К ним относят бактерии,
развивающиеся на стенках резервуаров, внутренней поверхности во-
доводов, использующие в процессе обмена веществ кислород и обра-
зующие плотные массы отложений. Проникающий в эту массу кисло-
род полностью потребляется. Образующиеся слои отложений служат
102
Глава 2
отличной защитой для СВБ, которые растут под ними. Характер-
ной особенностью развития рассматриваемых организмов является
их способность двигаться во всех направлениях, и даже против тече-
ния. Последнее в ряде случаев приводит к загрязнению даже артези-
<|ПАг1\*1А. HVlVTnrllMjD. Jl И VdI41 VjJrlrl 11|_7г1Г1<1ДЛ&ЛКС11 lx I ovttWlitVildO,-
Flavobacterium, Aerobacter и Bacillus и могут встречаться как в прес-
ной, так и в соленой воде.
Железобактерии. К бактериям, образующим отложения гидро-
окиси железа, относят железобактерии, которые образуют слизи-
стые колонии. Волокнистая структура образуемой ими гидрооки-
си железа обладает высокой прочностью и устойчивостью к току
воды.
Водоросли. Водоросли развиваются только в присутствии воз-
духа и в тепле. Их обнаруживают в речной воде, резервуарах и дру-
гих емкостях. Они преобразуют, катализируя реакцию фотосинтеза,
двуокись углерода и воду в кислород и глюциды. В водопроводах
пресной воды они иногда образуют вязкие массы на ее поверхности.
Унесенная часть водорослей представляет питательную среду для
бактерий и создает идеальные условия для развития СВБ на стенках
трубопроводов, емкостей и дне водоемов.
2.8. Зараженность промысловых сред микроорганизмами
Зараженность промысловых сред микроорганизмами зависит от
стадии разработки месторождения и изменяется во времени. На пер-
вой стадии разработки месторождений, после их обустройства и вво-
да в эксплуатацию системы поддержания пластового давления, вме-
сте с нагнетаемой в продуктивные пласты пресной водой поступают
2.8. Зараженность промысловых сред микроорганизмами 103
различные микроорганизмы и растворенный в водной среде кисло-
род.
Помимо СВБ, с закачиваемой водой в продуктивные пласты неф-
тяных месторождений попадают и другие виды микроорганизмов.
----Среди них наибольшую опасность представляют аэробные тионо-
вые (ТБ), нитрифицирующие (НФ) и углеводородокисляющие бак-
терии (УОБ), продуктами метаболизма которых являются различные
кислоты (серная, азотная и органические кислоты), которые, пони-
жая pH среды, создают благоприятные условия для развития бакте-
рий, существующих в анаэробных условиях.
Сульфатвосстанавливающие бактерии почти всегда находятся
в ассоциации с аэробными слизеобразующими микроорганизмами.
Образователи слизи запасают питательные вещества и создают необ-
ходимые для этой группы бактерий анаэробные условия.
Обычно развитию СВБ предшествует биоценоз углеводород-
окисляющих бактерий, использующих содержащийся в нагнетаемых
водах молекулярный кислород. Эти бактерии в ограниченных аэроб-
ных условиях образуют промежуточные продукты неполного окисле-
ния типа спиртов, альдегидов и кислот — доступные СВБ органиче-
ские субстраты, по мере накопления которых и развивается биоценоз
бактерий.
Основным фактором, влияющим на биогенную сульфатредук-'
цию, является наличие в среде растворенного окисленного органи-
ческого вещества, в генерации которого активно участвуют углево-
дородокисляющие бактерии. В зоне распространения таких веществ
наблюдают активную сульфатредукцию, зависящую от скорости об-
разования необходимого для развития СВБ питательного субстрата.
Помимо этого, использование молекулярного водорода УОБ способ-
104
Глава 2
ствует развитию сульфатредукции в пластах за счет снижения окис-
лительно-восстановительного потенциала.
На начальных стадиях разработки месторождений в промысло-
вых средах превалируют УОБ, табл. 2.5. В альбской воде место-
риЖДСНИл—I\.dJld MudU WriapyA\vrlbl—1 pyillibl—UdMUpilll 1 J,
табл. 2.6.
В промысловых средах большинства месторождений, вступив-
ших в третью стадию разработки, наблюдают активную жизнеде-
ятельность ряда физиологических групп микроорганизмов. Так, на-
пример, в нефтепромысловых водах Усть-Балыкского месторождения
помимо сульфатвосстанавливающих ’бактерий присутствуют гетеро-
трофные (ГТБ) микроорганизмы, в т. ч. динитрофицирующие (ДНФ),
УОБ. Однако соотношение групп бактерий резко меняется в сторо-
ну увеличения СВБ и снижения УОБ. Указанные группы бактерий
обнаружены в пробах закачиваемых вод и пробах изливаемых вод
с нагнетательных скважин месторождения Каламкас, табл. 2.7.
Наибольшая численность бактерий характерна непосредственно
для призабойной зоны нагнетательных скважин, поскольку именно
в них создаются исключительно благоприятные условия для жизне-
деятельности микроорганизмов: оптимальная минерализация воды,
наличие остаточной нефти, оптимальная температура 25... 35°С.
Для месторождений Удмуртии характерно следующее соотно-
шение микроорганизмов, табл. 2.8.
Как видно из представленной таблицы, количество ТБ и УОБ
в пробах воды с месторождений не так высоко в сравнении с суль-
фатвосстанавливающими бактериями. Причиной такого соотношения
следует считать незначительное количество кислорода в пластовой
воде.
Таблица 2.5. Распространенность микроорганизмов
Среда обитания микроорганизмов СВБ ГТБ Т1 Источник
ДНБ УОБ £
Сточная вода Алехин- ского месторождения 2,5.. .6,0-Ю3 2,5-Ю3.. .2,5-Ю4 2,5...6,0-102 2,5-103.. .1,3-10® 92
Воды Южно- Балыкского месторождения 7,0-Ю4 > 1,1-Ю7 112
Пластовые воды Восточно-Сулеевской площади 0...3101 1О2...1О4 ЗЮ2..ЛЮ3 60
Подтоварные воды Альметьевской площади ОДЮ'.-.Ю2 о.б-юТ-.ю4 0,5. ..З Ю1 60
Подтоварные воды Талинского месторождения 103 10s...10®
2.8. Зараженность промысловых сред микроорганизмами
106
Глава 2
Таблица 2.6. Микрофлора вод месторождения Каламкас
Год Микрофлора, клеток/мл
СВБ ДНБ УОБ Тионовые
Th. denitrificans Th. thioparus
1981 Единицы Нет Единицы Единицы Нет
1982 Единицы Нет До 102 До 103 До 103
1983 Единицы Единицы Единицы Единицы Единицы
1984 До 102 До ю2 До 102 До ю2 102 ... 103
В коррозионных процессах принимают участие различные ми-
кроорганизмы, среди которых наиболее опасны литотрофные бакте-
рии, участвующие в трансформации серы в природе и способствую-
щие созданию агрессивных сред.
В процессе жизнедеятельности бактерий в почве и природных
водах возможно протекание трех основных типов биологических ре-
акций превращения серы: ассимиляция, окисление серы и серосодер-
жащих соединений, восстановление сульфатов в сульфиды.
Одни микроорганизмы ответственны за окислительные процес-
сы в биохимических реакциях серы с конечным образованием суль-
фатов и минеральных кислот; другие, напротив, — за восстановитель-
ные, с образованием из сульфатов сероводорода и сульфидов.
В процессах окисления серы превалирующую роль отводят тио-
новым бактериям, а восстановительную стадию реакций в основном
выполняют СВБ. Деятельность тионовых бактерий и СВБ и их от-
ношения в определенной степени носят синтрофный характер, когда
продукты жизнедеятельности одних микроорганизмов служат необ-
ходимым энергетическим субстратом, пищей для активного роста
2.8. Зараженность промысловых сред микроорганизмами 107
Таблица 2.7. Зараженность промысловых сред микроорганизмами [95]
Место отбора проб Количество бактерий, кл/см3
-евв— ГТБ
S В том числе
ДНБ УОБ
КНС-1 6,0 ю2 5,0 • 104 2,5 • 102 2,5 • 10’
КНС-2 2,5 101 6,0 • 103 0,6 • 101 —
КНС-3 6,0 102- 1,3 - 105 2,5 • 102 6,0 • 101
К НС-4 2,5 • 103 6,0 105 6,0 • 103 6,0 • ю1
КНС-5 6,0 • 105 1,3 - 106 2,5 104 1,3 103
При изливе скв.7071
Начало излива 2,5 • 103 2,5 • 106 6,0 102 2,5 102
Излив в объеме колонны 2,5 • 104 6,0 • 107 6,0 104 2,5 • 104
Конец излива +15 м3 6,0 • 103 2,5 • 107 2,5 • 104 6,0 103
При изливе скв.7092
Начало излива 2,5 • 103 2,5 • 106 6,0 • 102 2,5 102
Излив в объеме колонны 2,5 • 104 2,5 107 2,5 103 6,0 • 102
Конец излива +25 м3 2,5 • 103 2,5 105 6,0 • 102 2,5 • 102
других, несмотря на то что тионовые бактерии по природе аэробы,
а СВБ — анаэробы.
Следует отметить, что численность аэробных тионовых бакте-
рий в пластах превосходит количество анаэробных сульфатвосста-
навливающих бактерий, связанных с ними единым циклом превра-
щения соединений серы. Это указывает на присутствие растворен-
108
Глава 2
Таблица 2.8. Результаты тестирования по определению ТБ, УОБ и СВБ
в промысловых средах месторождений Удмуртии
Месторождение Участок Вид бактерий Количество клеток, кл./мл
БКНС УОБ 24
Архангельское БАС - УОБ 24
скв. 177 УОБ 102
Мишкинское ДНС-1 ТБ 24
УОБ 24
УПН ТБ 24
УОБ 102
СВБ 103
Лиственское 1 поток УОБ 102
2 поток УОБ 102
3 поток УОБ 24
ДНС-5 УОБ 24
СВБ 102
Красногорское КСП ТБ 103
Скв. 2408 ТБ 103
Скв. 2424 ТБ 103
Чутырское КНС-8 ТБ 2
УОБ 2
СВБ 102
Южно- УПС ТБ 24
Киенгопское УОБ 24
2.8. Зараженность промысловых сред микроорганизмами 109
ного кислорода в пластовых водах, что связано, вероятно, с высокой
кратностью водообмена.
Еще в 1953 г. Kulman [9] отметил, что ни одна из групп микро-
организмов, участвующих в коррозионных процессах, не является
единственным потенциальным агентом, ответственным за протека-
ние коррозионных процессов на поврежденных участках трубопро-
водов. Везде совместно существуют аэробы и анаэробы, ответствен-
ные за различные реакции в цепи превращений соединений серы.
Автор считает, что микробная коррозия не может быть процессом,
вызываемым одним видом бактерий, а является скорее механизмом,
в котором причинными агентами может быть несколько видов, уси-
ливающих свой рост и активность в зависимости от окружающих
условий. Более того, смена аэробных и анаэробных условий способ-
ствует более активной коррозии железных сооружений по сравне-
нию с постоянным анаэробиозом. В промысловой практике в силу
тех или иных обстоятельств данным фактором, как правило, прене-
брегают.
Зараженность почвенных сред микроорганизмами
При исследовании трансконтинентальных газопроводов было
установлено [10], что в грунте, прилегающем к поверхности газо-
провода, численность СВБ превышает количество этих микроорга-
низмов вне массива трубы, причем в плотных глинистых грунтах
количество СВБ вблизи газопровода на 3... 4 порядка превышает
их численность вне газопровода, что в свою очередь обуславливает
наибольшую интенсивность коррозионных процессов в этой зоне.
В условиях модельного лабораторного опыта было показано, что
максимальное количество клеток СВБ распределено в зоне грунта,
по
Глава 2
непосредственно прилегающего к поверхности металла. Численность
СВБ в этой зоне на 1... 3 порядка выше, чем в зоне, удаленной от
поверхности металла, на 1 см. Это объясняется миграцией бактерий
в грунте от зон с меньшим содержанием ионов растворенного железа
к зонам с повышенной концентрацией Fe2+ [7].
Степень агрессивности грунтов предложено [10] оценивать по
интегральному критерию, учитывающему в совокупности микробио-
логические и физико-химические показатели:
К — lg[TCB6 • • Fe06uj • Бобщ р ],
i
где Тсвб — количество клеток СВБ в 1 г грунта (титр); Т-^ — титр
тионовых бактерий; РеОбщ — общее содержание железа в грунте, %;
So6m — общее содержание серы в грунте, %; р — удельное электри-
ческое сопротивление грунта, Ом.м.
Для классификации грунтов предложены следующие критерии
агрессивности, табл. 2.9.
Практическая полезность классификации в том, что благодаря ее
информационной полноте возможно более точное прогнозирование
ущерба в результате подземной коррозии и определение объема ме-
роприятий по его предотвращению. С учетом этого показателя может
быть рассчитан интегральный критерий К.
[7-1012-ехр(—0,18/>)] р * 1
[ехр(-0,06/>)(3-10п — 8-108/>)] /Г1
K = lg [3,1-107 ехр(—0,04/>)(20/>2 —4/>—1,2 —103)] р~1
[1О7ехр(-О,ОЗ/>)(-8,1-1(Г1/>3+69/>2-
-11/>+3,1-10/>)] р~1 /><100.
При
0 </>< 40,
40 </><80,
80 </><100,
Таблица 2.9. Классификация грунтов по критерию агрессивности
Степень агрессивности грунта Повреждения поверхности металла р, Ом.м. Средние значения показа! гелей К
Титр клеток % в гр >унте
СВБ ТБ Ббобщ Зобщ
Неагрессивные Практически отсутствуют 100 - 400 10 10 2,2Ч 0,6 i 1,5
Потенциально агрессивные Незначительные (язвы до 1... 2 мм) 40 - 100 100 10 к 2,3 i 0,9 1,5-4
Умеренно агрессивные Умеренные (язвы до 5 мм) 20-40 103 100 2,7 j 1,7 1 4-7
Агрессивные Значительные (язвы до 8 мм) 5-20 ю4 - ю5 103 5,6 2,0 7-10
Весьма агрессивные Весьма значительные (язвы до 1... 12 мм) 2-5 103 6,8 2,5 10
I
2.8. Зараженность промысловых сред микроорганизмами
112
Глава 2
Адсорбции микроорганизмов на металлах предшествует стадия
модификации поверхности. Этот процесс выражается либо в накоп-
лении на твердой поверхности гликопротеинов, либо в образовании
слоя, состоящего из других органических и неорганических веществ,
имеющего толщину 200... 800 А. Он изменяет гидрофобные свой-
ства поверхности, стимулируя адгезию микроорганизмов [141].
Наиболее опасные повреждения трубопроводов происходят
в низкоомных грунтах. Такие грунты представляют собой глины с же-
лезистыми и марганцевыми отложениями и содержат значительное
количество серы, железа и органических веществ. Это благоприятная
экологическая ниша для развития анаэробной коррозии.
Невысокое содержание СВБ и тионовых бактерий (104 и 102 кле-
ток на 1 г грунта) содержат высокоомные грунты, где практически
отсутствуют повреждения трубопроводов.
Глава 3
--------^Условия жизнедеятельности
сульфатвосстанавливающих бактерий
На характер жизнедеятельности сульфатвосстанавливающих
бактерий оказывает влияние огромное количество физико-химиче-
ских, энергетических и других показателей.
К наиболее значимым факторам относят условия обитания ми-
кроорганизмов :
— минерализацию среды;
— температуру среды;
— pH среды.
3.1. Влияние физико-химической характеристики среды
на жизнедеятельность СВБ
Влияние минерализации среды на жизнедеятельность СВБ
Минерализация среды оказывает существенное влияние на жиз-
недеятельность СВБ. Существует некоторый оптимальный интервал
минерализации, в котором процессы жизнедеятельности СВБ про-
текают наиболее активно. Исследования, проведенные на культуре,
выделенной из промысловых сред башкирского яруса месторожде-
ний Пермской области, показывают [104], что в среде с лактатом
114
Глава 3
натрия максимальная величина выделяемого СВБ сероводорода фик-
сируется при содержании 120 г/л NaCl, рис. 3.1. С увеличением со-
держания минеральных солей или их уменьшением активность ми-
кроорганизмов значительно снижается. Тождественные результаты
получены как на раетворах, приготовленных из чистых галитов, так
и из комплексных солей, выделенных из рассолов.
Рис. 3.1. Влияние минерализации на развитие галофильной культуры в среде
с лактатом натрия: 1 — соли, выделенные из рассола; 2 — соль NaCl
Оптимальная объемная доля хлористого натрия для роста СВБ
составляет от 2 до 6%. На питательных средах, максимальная ве-
личина содержания NaCl, допускающая развитие СВБ, достигает
18 ... 20%. Высокоминерализованные (220... 270г/л) пластовые во-
ды нефтяных месторождений не способствуют развитию бактерий.
Пластовые рассолы оказывают отрицательное влияние на разви-
тие СВБ не только вследствие высокой величины общей минерализа-
ции, но также в результате ее компонентного состава. Катионы метал-
лов, вступая во взаимодействие с белковыми молекулами, нарушают
3.1. Влияние физико-химической характеристики среды 115
процесс жизнедеятельности бактерий. По способности вступать во
взаимодействие с белками катионы можно расположить в следую-
щий ряд приоритетности:
Cd24 > Zn2+ > NH+ > Li+ > Sr2+ > Mn2+> Ca2+ > Mg2+ > К r > Na ‘ .
Наиболее токсичны для микроорганизмов катионы кадмия
и цинка. При достаточно высокой концентрации в воде токсичность
свойственна и катионам кальция и магния.
Вредное лизирующее воздействие на микроорганизмы оказыва-
ют и анионы, располагаясь при этом в следующей последовательно-
сти:
CCI3 > CNS- > CIO7 > Br“ > NO3 > SO2~ > СН3СОО > СГ.
СВБ не развиваются в водах, где катионный коэффициент пла-
стовой воды более 0,4 [61], [96]. Для расчета катионного коэффици-
ента минеральный состав воды выражают в мг-экв/дм3,
Mg2+ + Са2+ >04
K++Na+
Согласно [61] при значении катионного коэффициента > 0,52
в пластовых водах Восточно-Сулеевской площади не отмечено раз-
вития СВБ. Снижение же содержания катионов кальция и магния
приводит к увеличению численности СВБ, табл. 3.1.
В этой связи следует отметить, что использование для завод-
нения пресных вод значения катионного коэффициента значительно
ниже 0,40 может привести в дальнейшем к росту численности СВБ
в пласте и связанных с этим негативных последствий.
116
Глава 3
Таблица 3.1. Взаимосвязь зараженности СВБ с катионным коэффициентом
попугно-добываемых вод эксплуатационных скважин [61]
Номер скважины Количество СВБ, кл/см3 Плотность ВОДЫ, кг/м3 Катионный коэффициент
1455 Отсутствуют 1103 0,52
1456 Отсутствуют 1140 0,55
11675 Отсутствуют 1129 0,52
11573 Единицы 1105 0,40
11564 Десятки 1043 0,48
11565 Десятки ' 1023 0,48
1479 Сотни 1026 0,41
В. А. Кузнецова [104], изучавшая палеозойские отложения Куй-
бышевской области, пришла к выводу, что при высокой минерали-
зации распространение бактерий в пластовых водах ограничивается
высоким содержанием Са2+ и Mg2+. По ее данным, СВБ развивают-
ся в тех водах, где значения катионного коэффициента не превышают
значения 0,36... 0,40. Полученные данные подтверждены результа-
тами лабораторных исследований по развитию культур в средах раз-
личного состава, рис. 3.2.
Влияние температуры на жизнедеятельность СВБ
Действие температуры испытывают все живые организмы, в том
числе и микроскопические. По отношению к температуре микроор-
ганизмы делят на мезофилы, психрофилы и термофилы.
Мезофилы (мезо — средний) лучше всего приспособлены к су-
ществованию в интервале средних температур. Они могут нормально
3.1. Влияние физико-химической характеристики среды
117
ч 400
V 350
'л 300
250
= 200
1 150
| 100
а 50
с о
0 5 10 15 20 25
Время, сут
Рис. 3.2. Влияние катионного состава воды на продуцирование H2S суль-
фатвосстанавливающими бактериями: 1-3 содержание хлора, %-экв, соот-
ветственно — 5,5; 6,1; 6,7.
размножаться в пределах от 20 до 40°С. В этой группе, как и в других,
есть организмы, развивающиеся в более широком или более узком
диапазоне температур, и указанный интервал нельзя считать строго
ограниченным. К мезофилам относят большую часть микроорганиз-
мов.
Психрофилы (психрос — холод) приспособлены к существова-
нию при пониженных температурах. Они нормально живут и размно-
жаются при температуре от —8 до +10°С. Большинство психрофи-
лов способно расти и при температурах, характерных для мезофил-
лов, поэтому их называют факультативными, т. е. необязательными
психрофилами. В отличие от факультативных облигатные (т. е. обя-
зательные) психрофилы погибают при температурах, близких к 30°С.
К психрофилам относят некоторые почвенные и морские бактерии,
а также виды, патогенные для морских животных и растений.
118
Глава 3
Термофилы (термо — тепло) способны нормально существовать
при температурах от 50 до 75°С. Некоторые из них выдерживают
10-минутное нагревание при температуре 80... 90°С.
Следует отличать выживаемость при какой-либо температуре
----и оптимальное значение температуры для жизнедеятельности ми-
кроорганизмов. Оптимум обычно лежит ближе к верхней границе
температурного диапазона. При более высоких температурах про-
цессы жизнедеятельности активизируются, организмы быстрее рас-
тут и размножаются. Это связано с активацией работы фермен-
тов при повышении температуры. Повышение границы температур-
I ,
ного интервала, как правило, приводит к разрушению ферментов
и к гибели вегетативных клеток. При температуре 70°С большин-
ство вегетативных клеток мезофилов погибает в течение 1... 5 мин,
при температуре 63°С — в течение 30 мин, термофилы при такой
температуре способны расти и размножаться. Причина повышен-
ной термостабильности термофилов заключается, во-первых, в ка-
чественном и количественном своеобразии отдельных компонен-
тов клеток (мембран, рибосом и особенно оболочек) и, во-вто-
рых, в более быстром синтезе клеточных элементов. Адаптация
микроорганизмов к повышенным температурам очень затруднена.
При кипячении все вегетативные клетки погибают за несколько
секунд.
Понижение температуры переносится микроорганизмами гораз-
до лучше, чем нагревание. У многих видов вегетативные клетки спо-
собны выдерживать однократное замораживание. Причину гибели
клеток при замораживании многие исследователи видят в разруша-
ющем действии кристаллов льда, образующихся в клетках. В слу-
чае быстрого замораживания (1... 10 сек), когда вместо кристаллов
3.1. Влияние физико-химической характеристики среды 119
в клетках образуется ледяная стекловидная масса, процент погибших
клеток значительно снижается.
Высокая температура в нефтяных пластах не является препят-
ствием для распространения СВБ. Так, СВБ обнаружены в нефтяных
пластах продукт иной толщи Аггшерона, где температура достига-
ет 85... 91°С. Поэтому отсутствие их в пластах ряда месторождений
с высокой температурой объясняется другими причинами.
Термофильные СВБ, выделенные из нефтяных пластов место-
рождений острова Песчаного на Апшероне, имеющих температуру
—I
80... 90°С, при низкой температуре за семь суток показали низкую
степень развития, в то время как галофильная культура интенсивно
развивалась в интервале температур 60 ... 70°С [9], рис. 3.3.
Рис. 3.3. Влияние температуры на развитие культур СВБ: 1 — термофильная
в среде с лактатом натрия и 0,5% NaCl; 2 — галофильная в среде с лактатом
натрия и 12% солей рассола
Ряд месторождений Удмуртии разрабатывают с использовани-
ем термических методов. Так, например, разработку Гремихинского
месторождения осуществляют с использованием импульсно-дозиро-
120
Глава 3
ванного теплового воздействия, Черепетскую залежь Мишкинского
месторождения — с помощью термополимерного заводнения. Вне-
дрение тепловых методов планируют и на других месторождениях.
В связи с этим исследование влияния температуры на жизнедеятель-
ность СВБ весьма актуально.
Существует несколько методик оценки влияния температуры на
жизнедеятельность микроорганизмов. Наиболее приемлемые из них:
— электрохимический метод — по изменению тока коррозии;
— объемный — по количеству вырабатываемого сероводорода.
По первому способу исследования проводят с помощью двухка-
нального варианта проточной системы с объемом канала 250 дм3.
В качестве исследуемой среды принимают, как правило, нефте-
промысловые среды. Так, при исследовании воды НГДУ Альме-
тьевскнефть [41], содержащей микроорганизмы основных физио-
логических групп окислительно-восстановительного цикла серы:
СВБ — 1()2 кл/дм3, тионовые — 101 кл/дм3, углеводородокисля-
ющие — 104 кл/дм3, получены следующие кинетические кривые,
рис. 3.4.
Кинетические кривые, приведенные на рис. 3.4, имеют типич-
ный для топохимических реакций S-образный вид, поскольку с точ-
ки зрения химической теории твердого состояния (топохимии) воз-
никновение пленки микроорганизмов на поверхности металла может
рассматриваться как образование новой фазы и подчиняться уравне-
нию [41]
I = Iq ехр(±А: • £п),
где I, 10 — текущее и фоновое значения токов коррозии; к — эф-
фективная константа скорости процесса; t — время; п — показатель,
3.1. Влияние физико-химической характеристики среды
121
Рис. 3.4. Кинетика развития коррозионного процесса в среде, содержащей
микроорганизмы, при различной температуре: 1-4 — соответственно 10, 20,
30 и 40°С
зависящий от поверхностной геометрии (или фрактальной размерно-
сти) образующейся фазы.
Знак (+) характеризует процесс увеличения скорости коррозии
под действием пленки биофазы. Знак (—) — снижение скорости кор-
розии при уничтожении биофазы реагентом-бактерицидом.
Результаты исследований показывают, что в области низких тем-
ператур процессы жизнедеятельности микроорганизмов замедлен-
ны, в области температур, соответствующих оптимальным усло-
виям их развития (32°С), максимально высокие. Так, с повыше-
нием температуры с 10°С до 20°С время выхода тока коррозии
на максимальный уровень сокращается в 1,7 раза, а до 30°С —
в 3,8 раза.
По второму способу исследование влияния температуры на жиз-
недеятельность СВБ проводят по следующей методике.
122
Глава 3
Из отобранных проб воды скважины №3223 Северо-Ижевского
месторождения и сточной воды Гремихинской УПН методом двойно-
го пересева выделяют и очищают бактерии СВБ, на которых и про-
водят все последующие исследования.
Пробы СВБ, содержащиеся в водной фазе, нагревают на водя-
ной бане до исследуемой температуры в диапазоне от 20 до 100°С,
выдерживают 30 минут и затем рассевают в посевные склянки с пи-
тательной средой, которые инкубируют при температуре 32°С в те-
чение 15 суток. За контрольную пробу принимают посев СВБ при
комнатной температуре в 20 градусов.
Через 15 суток во всех пробах методом йодометрического тит-
рования определяют количество сероводорода, выработанного бакте-
риями СВБ.
Результаты исследований на культурах, выделенных из вод
Гремихинского и Северо-Ижевского месторождений, отражены
в табл. 3.2.
Следует отметить, что в промысловой практике известны слу-
чаи [26] существования микрофлоры в высокотемпературных об-
ластях призабойной зоны и продуктивного пласта. Ярким приме-
ром является биоценоз нефтепромысловой микрофлоры Талинского
месторождения, характеризующегося высокой температурой продук-
тивного пласта, лежащей в области 100°С.
Согласно проведенным исследованиям, технологическая схема
нефтедобычи Талинского месторождения включает три зоны актив-
ной жизнедеятельности микроорганизмов, различающихся темпера-
турными режимами. К первой зоне относят прежде всего призабой-
ную зону нагнетательных скважин, характеризующихся высокими
зараженностью и активностью микрофлоры. Вторым участком явля-
3.1. Влияние физико-химической характеристики среды 123
Таблица 3.2. Влияние температуры на количество вырабатываемого СВБ
сероводорода
Температура нагрева культуры СВБ, °C Количество сероводорода, мг/л вырабатываемого СВБ, выделенных из культур месторождений
Гремихинского Сев.-Ижевского
20 292,7 438,6
30 — 414,8
40 306,8 " —
60 306,7 414,8
75 — 279,9
80 117,8 —
90 — 116,7
100 37,8 —
ются сырьевые резервуары, где осуществляется предварительное раз-
деление добываемой обводненной нефти. Характер отношения ми-
крофлоры к температуре можно отнести как мезофильный, т. е. бак-
терии активны при средних температурах. Третьим участком, содер-
жащим значительное количество активной микрофлоры, является то-
варный парк. Здесь микрофлора развивается также по мезофильному
типу.
Разнообразие температурных режимов в условиях Талинского
месторождения определяет «разорванный» тип жизнедеятельности
нефтепромыслового биоциноза. Биоциноз имеет три своеобразных
«ареала», включающих высокотемпературный биотип в призабой-
ной зоне и продуктивном пласте, а также два участка, образующих
124
Глава 3
единый биотоп системы ППД с относительно низкой температурой.
Между указанными биотопами осуществляется непрерывная связь
путем оборота закачиваемых и добываемых вод.
В анализируемых пробах вод Талинского месторождения об-
наружено наличие трех физиологических групп коррозионно-опас-
ных бактерий: сероокисляющих, сульфатвосстанавливающих, гете-
ротрофных (ГТБ), а также подгрупп гетеротрофов: динитрифициру-
ющих бактерий и углеводородокисляющих бактерий.
Интересна оценка показателей роста бактериальных культур
и зависимости активности микрофлоры от температуры культиви-
рования. Так, для микроорганизмов, выделенных из низкотемпе-
ратурных зон системы нефтедобычи характерна высокая скорость
роста при стандартных условиях культивирования (32°С): индекс
активности ГТБ составляет 100 ед, а СВБ — 50. При культи-
вировании этих микроорганизмов при повышенной температуре
(42°С) индекс активности ГТБ снижается до 30... 50 ед, а СВБ —
до 20... 25 ед. •
В то же время различие температур культивирования существен-
но влияет на показатели роста мезофильных штаммов СВБ и ГТБ.
При температуре 32°С индекс активности ГТБ снижался до 25 ед,
а СВБ до 20 ед. При культивировании в условиях повышенной тем-
пературы (42°С) активность ГТБ повышалась до 100 ед, а СВБ —
до 50 ед.
Рост числа микроорганизмов, выделенных из высокотемпера-
турных зон, был затруднен как при температуре 32°С, так и при
температуре 42°С.
Исследованиями [26] показано, что процесс жизнедеятельности
микроорганизмов протекает по следующей схеме. Микроорганизмы
3.1. Влияние физико-химической характеристики среды 125
вместе с закачиваемой водой попадают в призабойную зону нагне-
тательных скважин. Здесь происходит активное развитие внесенной
микрофлоры, которая в процессе температурной адаптации форми-
рует специфический термофильный биоценоз. При этом заражение
распространяется в продуктивном пласте. Далее часть микрофлоры
фильтруется через высокотемпературный пласт, при этом значитель-
ная доля ее погибает, другая же в малоактивной форме доставляется
с попутно-добываемой водой в товарный парк, где ее жизнедеятель-
ность реактивируется по мезофильному температурному типу. Отде-
ленная вода, смешиваясь с пресной водой, поступает снова в систему
ППД.
Влияние pH среды на жизнедеятельность СВБ
Существование того или иного микроорганизма, помимо все-
го прочего, предопределяет кислотность среды обитания организма.
Так, некоторые организмы благоприятно себя чувствуют в довольно
широком диапазоне pH, характеризующие как кислую, так и щелоч-
ную среду. При этом диапазоны изменения pH могут быть довольно
значительными, табл. 3.3.
Таблица 3.3. Диапазон pH существования микроорганизмов
Организмы Пределы pH Размер диапазона pH
Десульфурирующие 4,15... 9,92 5,77
Денитрифицирующие 6,20...10,2 4,00
Метанобразующие 7,00... 7,80 0,80
126
Глава 3
В работе [9] авторы приводят данные, полученные на основе
экспериментальных исследований зависимости pH среды от измене-
ния титра ацидофильных тионовых бактерий, табл. 3.4. Ординаты
кривой определялись усреднением pH по признаку равных значений
титра Тионовых бактерий;
Таблица 3.4. Изменение pH среды от количества бактерий
Количество бактерий, кл/мл pH среды Количество бактерий, кл/мл pH среды
0 7,05 104 5,56
101 6,65 105 5,12
102 6,06 106 4,82
103 5,79
Полученные данные позволяют оперировать промежуточными
значениями титра тионовых бактерий и pH, а также определять ве-
личины pH при заданных значениях титра и наоборот.
СВБ лучше развиваются в кислых средах и количество выраба-
тываемого при этом в них сероводорода выше.
Влияние pH среды на развитие СВБ в течение семи суток при
температуре 25° С показано в табл. 3.5.
Таблица 3.5. Влияние pH среды на развитие СВБ
Содержание в средах воды, % Образование сероводорода, мг/л
Пластовой Пресной при pH 5,75 при pH 7,2
89 11 224 160
66 34 42 7
3.2. Влияние свойств поверхности металла на развитие СВБ 127
3.2. Влияние свойств поверхности металла на развитие
СВБ и процессы биокоррозии
Особенностью динамики развития микробиологических процес-
сов коррозии является ее функциональная зависимость от структуры
и природы твердой поверхности, т. е. они являются в своей основе
топохимическими [41].
Макроскопические токи, алгебраическая сумма которых и опре-
деляет конечный результативный ток коррозии, характеризующий пе-
реход атомов решетки металла в раствор в виде ионов, весьма зави-
сит от состояния поверхности металла, ее свойств и энергетических
характеристик взаимодействия с жидкой фазой.
В связи с этим исследования [71] влияния свойств поверхности
металла с измененной механической структурой на особенности раз-
вития и протекания коррозионных процессов в присутствии микро-
организмов представляют как теоретический, так и практический ин-
терес. В качестве источника микроорганизмов использована сточная
вода Южно-Сергеевского месторождения (Башкирия), содержащая
СВБ и УОБ, в качестве электродов образцы из низкоуглеродистаой
стали с размерами 4 х 4 х 100 мм.
Поверхностная структура трех образцов изменена путем меха-
нического воздействия:
— 1 — контрольный — без механических повреждений;
— 2 — нанесением царапин глубиной до 1 мм по всей длине
образца;
— 3 — нанесением симметрично расположенных лунок на одной
из граней образца (кернение);
— 4 — сварным соединением посередине.
128
Глава 3
Исследования проводили с помощью проточной системы по сле-
дующей схеме. Подготовленные образцы металла помещали в емко-
сти, после чего систему заполняли нефтепромысловой водой, герме-
тизировали при отсутствии видимых пузырей воздуха и проводили
измерения величины коррозионных токов в установочном режиме.
Одновременно измеряли электродный потенциал для оценки стацио-
нарности электрохимической системы. После стабилизации потенци-
ала и тока определяли фоновую составляющую коррозионного про-
цесса, флуктуационные характеристики тока в импульсном (балли-
стическом) режиме подключения к измерительной схеме.
Количественные зависимости фонового макроскопического тока
от состояния поверхности контрольного образца и образцов с изме-
ненной структурой определяли как квадрат амплитуды токовых флук-
туаций при установившемся стационарном коррозионном потенциа-
ле. В табл. 3.6 представлены величины потенциалов, фоновых токов
и их флуктуаций для исследуемых образцов металла.
Таблица 3.6. Параметры электрохимической системы до начала развития
биокоррозии [71]
Параметры Вид повреждения образца
Контрольный С царапиной С лунками Со сваркой
Е, ИГ3 В -671 -627 -686 -698
Ik, Ю~6 А 68,4 73,8 77,5 84,4
(г2), 10“9 1,5 9,0 21,0 28,0
Просматривается четко выраженная связь между этими показа-
телями и изменением структурно-механических свойств поверхно-
3.2. Влияние свойств поверхности металла на развитие СВБ 129
сти металла. В частности, удаление металла с образованием щели
(царапина) приводит к смещению электродного потенциала в сто-
рону более отрицательных значений, возрастанию тока коррозии по
сравнению с неповрежденным образцом. Еще более выражены из-
—мененияэтихдвух параметров у образцов с кернением и сварным
швом. Полученные результаты могут быть объяснены изменением
энергетического состояния металлической поверхности и ее боль-
шей склонностью корродировать при деформациях. Такое истолко-
вание достаточно тривиально и не дает существенной информации
о развитии коррозионного процесса даже в безмикробной среде. Зна-
чительно больший интерес представляют данные по изменению квад-
рата флуктуаций стационарного тока коррозии для всех исследован-
ных образцов. Формально подтверждая обнаруженную в этом ряпу
тенденцию, т. е. возрастание «готовности корродировать» при меха-
нических повреждениях, квадрат амплитуды флуктуационных токов
позволяет выделить две особенности коррозионного электрохимиче-
ского поведения металла:
— определить интенсивность микроскопических токов обмена
на границе «электрод — раствор»;
— оценить стабильность их во времени, что дает представление
об устойчивости стационарности процесса растворения металла.
Следует отметить, что эта микровеличина, по сравнению с ма-
кроскопическими стационарными величинами электродного потен-
циала и тока коррозии имеет значительно большие разности ря-
дом стоящих значений и наглядно демонстрирует отличие процессов
с близкими параметрами Е и Ik- Так, в ряду изученных образцов
низкоуглеродистой стали имеет место увеличение квадрата флукту-
ационного тока, показывающего возрастание интенсивности обмена
130
Глава 3
ионами между металлом и жидкой фазой, а также понижение устой-
чивости стационарного состояния на границе раздела фаз.
Влияние микробиологического фактора при контакте образцов,
с нефтепромысловой водой определяли уже в первые часы экспе-
римента именно по возрастанию квадрата амплитуды микрокорро-
зионных токов, в то время как макровеличины Е и 1к проявляли
тенденцию к изменению лишь через 12 ... 18 час. Изменение микро-
скопических флуктуационных токов (квадрата их амплитуды) в ходе
Время, час
Рис. 3.5. Изменение среднего квадрата тока обмена в электрохимической
системе с водой, содержащей микроорганизмы.
Полученные результаты дают возможность сравнить особенно-
сти развития процессов биокоррозии в зависимости от энергетиче-
ского состояния поверхности металла. Образец без видимых механи-
ческих повреждений (1) характеризуется наименьшим макроскопиче-
ским фоновым током коррозии и наименьшим квадратом амплитуды
микротоков и после начала развития микробиологической состав-
ляющей. В соответствии с закономерностью изменения электрохи-
3.2. Влияние свойств поверхности металла на развитие СВБ 131
мических параметров ведут себя и остальные образцы — создается
впечатление, что термодинамическая нестабильность, выражающая-
ся в «усилении» коррозионной активности, привлекает к поверхности
металла микроорганизмы, еще более «усиливающие» коррозионный
___________процесс. Так, наиболее «привлекательным» для микроорганизмов яв-
ляется образец со сварным швом (4) и «царапинами» (2). Наличие
плато указывает на насыщение металлической поверхности клетка-
ми микроорганизмов, образующих устойчивую биопленку. С учетом
того обстоятельства, что в батарее емкостей циркулирует одна и та же
вода, исходно содержащая одинаковое количество микроорганизмов,
полученные результаты можно объяснить лишь влиянием свойств
металлической поверхности на развитие бактерий.
О характере коррозионных процессов в упомянутых экспери-
ментах можно судить по изменению цвета продуктов коррозии в ем-
костях с образцами, в том числе и на самих образцах. Наиболее
наглядно такие изменения отмечены именно в емкостях с механи-
ческими поврежденными образцами. Так, для образца с царапиной
характерны отложения продуктов коррозии черно-серого цвета, ло-
кализующиеся в щели, и темно-серый осадок на дне сосуда. Образец
с кернением покрыт выраженными отложениями интенсивно-черного
цвета, в сосуде на дне содержится большое количество черного осад-
ка. Образец со сварным швом покрыт продуктами коррозии ржавого
цвета, причем сам сварной шов свободен от каких-либо покрытий.
Осадок на дне емкости интенсивно ржавого цвета. Такие результаты
можно объяснить различными типами закрепленных микробиоцено-
зов, с преобладающим количеством сульфатвосстанавливающих бак-
терий в первом и втором случаях, и с преобладанием гетеротрофных
микроорганизмов в третьем.
132
Глава 3
3.3. Жизнедеятельность СВБ в условиях
осадкообразования
При транспорте нефтепромысловых сред, в силу своей специфи-
ки, на внутренней поверхности трубопроводов нередко наблюдают
наличие осадков, состоящих в основном из кальцита, гипса, крем-
незема, асфальтосмолопарафиновых веществ и продуктов коррозии.
В условиях отложения осадков аварийность трубопроводных комму-
никаций резко усиливается, что связано прежде всего с активизацией
жизнедеятельности СВБ, микролокализацией коррозионных процес-
сов и образованием макрогальванопдр, когда поверхность металла
под осадком становится анодной по отношению к остальной поверх-
ности.
Исследование активности СВБ, характера протекания коррози-
онных процессов в условиях отложения осадков и зараженности сре-
ды микроорганизмами может быть осуществлено на установке, мо-
делирующей состояние внутренней поверхности трубопровода с от-
ложениями [38].
Установка представляет собой ячейку с коррозионно-агрессив-
ной средой, в которую вставлен шток с насаженными на него коль-
цеобразными образцами и закрепленным в нижней части пеналом
с осадком. Шток с образцами имитирует участок внутренней поверх-
ности трубопровода от верхней образующей до нижней в его попе-
речном сечении. В качестве модели осадка, как наиболее простого,
используют кварцевый песок.
В качестве коррозионной среды используют 3% раствор хлори-
да натрия с последующей продувкой через него диоксида углерода
в течение 20 мин, добавлением гидроксида натрия до pH = 7 и до-
3.4. Особенности развития СВБ в условиях работы
133
зировкой 50 мг/дм3 сероводорода. Для исследования влияния СВБ
на процессы коррозии в условиях осадкообразования в коррозионную
среду вводят накопительную культуру, выделенную из сточной воды
и содержащую 106 кл/см3 СВБ, в объеме 2% от объема коррозионной
среды.
Время экспозиции образцов в коррозионной среде в статических
условиях — 480 час.
Результаты исследований отражают повсеместную активизацию
процессов жизнедеятельности СВБ, о чем свидетельствует резкое
возрастание скорости коррозии образцов по сравнению с контроль-
ными образцами. Причем если для образцов, находящихся в жидкой
фазе, это увеличение составляет 20... 50%, то для образцов, распо-
ложенных под осадком, оно составляет 100... 200%. Данные иссле-
дований [38] отражены на рис. 3.6.
Визуальный осмотр образцов после эксперимента показал, что
образцы из контрольных ячеек, находившихся в жидкой среде, по-
крыты тонкой, но плотной пленкой сульфида железа. Аналогичные
образцы из ячеек с добавлением СВБ покрыты более толстым и рых-
лым слоем сульфида железа.
3.4. Особенности развития СВБ в условиях работы
коррозионных макрогальванопар
Локальные коррозионные поражения нефтепромысловых тру-
бопроводов обусловлены образованием на внутренней поверхности
труб коррозионных макрогальванопар. При работе коррозионных ма-
крогальванопар происходит пространственное разделение катодных
и анодных зон, что в свою очередь приводит к увеличению pH при-
134
Глава 3
Рис. 3.6. Зависимость скорости коррозир образцов от их местонахождения
в системе осадок-жидкая среда: 1 — контрольная, без СВБ, среда; 2 — среда
с добавкой СВБ
электродного слоя электролита на катоде до 10... 12 и снижению
на аноде до 3... 4 [68].
В связи с этим исследование особенностей роста и развития
СВБ на электрохимически гетерогенной поверхности металла в усло-
виях работы макрогальванопар представляется важным и необходи-
мым. В институте ВНИИСПТнефть такие исследования выполнялись
на накопительных культурах СВБ, выделенных из сточных вод Ар-
ланского месторождения [74].
Методика исследований заключалась в следующем. Для моде-
лирования работы коррозионной макрогальванопары использованы
образцы-пластины (75 х 25 мм) из малоуглеродистой стали. От-
шлифованные и обезжиренные стерильные образцы помещали в со-
суд так, чтобы нижняя часть пластин (10 мм) была погружена
в песок, находящийся на дне сосуда. Сосуд заполняли питатель-
ной средой Постгейт В и инокулировали в нее двухсуточную куль-
3.4. Особенности развития СВБ в условиях работы 135
туру СВБ. Сосуд выдерживали в термостате при 32°С в течение
7 дней.
Фиксацию адгезированных СВБ пластинок осуществляли в 3%
растворе глутарового альдегида в 0,08 М фосфатном буфере pH =
"== 7,2. Для подсчета количсстваадгезированных клеток исполь-
зован метод мембранных фильтров с некоторыми модификация-
ми [107].
При извлечении пластин из культуральной среды визуально об-
наружено, что катодная часть пластин покрыта сульфидной пленкой
с хорошей адгезией к поверхности металла, а анодная часть, нахо-
дящаяся в песке, — светлая, чистая. Выявлены различия в числен-
ности адгезированных СВБ на анодном и катодном участках. Ми-
кроскопия катодного участка пластин показала, что на поверхности
металла адгезировано большое количество СВБ в основном палоч-
кообразной формы. Основная масса клеток образует микроколонии,
реже встречаются единичные клетки. На анодном участке отмечены
от 1 до 5 обособленных клеток. Образование колоний на аноде не
обнаружено. Подсчет количества клеток показал, что число адгези-
рованных на катоде клеток СВБ на три порядка выше, чем на аноде.
Результаты подсчетов СВБ по отдельным участкам образцов сведены
в табл. 3.7.
Большое количество бактерий, образующих многослойные коло-
нии в катодной зоне, свидетельствует об активном росте СВБ на като-
де, а небольшое количество обособленных бактерий в анодной зоне —
о подавлении развития СВБ. Рост и развитие СВБ на поверхности ме-
талла, являющегося катодной зоной, обусловлен способностью бак-
терий СВБ к саморегуляции pH среды вследствие их специфическо-
го метаболизма. При диссимиляторном восстановлении сульфатов,
136
Глава 3
Таблица 3.7. Количество клеток СВБ на поверхности анодного и катодного
участков металлической пластины
Зона Участок образца Количество клеток, тыс. на 1 см2 поверхности металла
Анодная 1 21,0
2 10,0
3 8,3
4 6,2
5 20,0
6 ' 9,4
Среднее по зоне 12,5
Катодная 1 18000
2 13000
3 7300
4 11000
5 10000
6 12000
Среднее по зоне 11880
осуществляемых СВБ, происходит образование больших количеств
сероводорода, а также конечных продуктов окисления органических
субстратов — ацетата и СОг- За счет накопления бактериальных про-
дуктов метаболизма, имеющих кислый характер, происходит смеще-
ние значений pH приэлектродного слоя электролита у катода к обла-
сти, близкой к нейтральной [74]. При этом условия становятся более
благоприятными для роста и развития адгезированных СВБ.
3.4. Особенности развития СВБ в условиях работы
137
Способность накопительной культуры к саморегуляции подтвер-
ждена исследованиями по выращиванию бактерий в среде Постгейта
при начальных значениях pH среды от 3,11 до 11,07. Установле-
но [74], что наиболее сильно способность к саморегуляции внешнего
pH среды выражена при исходном значении pH = 9,11. Через 18 ча-
сов наблюдалось выравнивание pH до значения 7,55. В данном случае
получено и наибольшее нарастание биомассы бактерий, превышаю-
щее достигнутое при контрольном значении pH = 7,05. При низких
значениях pH прирост биомассы незначителен.
Полученные результаты свидетельствуют о том, что СВБ способ-
ны уменьшать щелочность среды в процессе своего роста к области,
близкой к нейтральной.
Особенности развития СВБ на электрохимически гетерогенной
поверхности металла позволяют уточнить механизм стимулирования
коррозионного процессе при их участии. Роль СВБ сводится к сле-
дующему. Активная жизнедеятельность адгезированных на катодной
поверхности СВБ обуславливает интенсивное образование вторич-
ных продуктов сероводородной коррозии — сульфидов железа, накоп-
ление которых на внутренней поверхности труб приводит к образо-
ванию мощной макрогальванопары железо — сульфид железа. Имея
более положительный, в сравнении с железом, потенциал и разви-
тую поверхность, сульфиды железа усиливают работу макрогальва-
нопар в десятки и сотни раз (в зависимости от количества сульфидов
железа), чем и определяют аномально высокие скорости локальных
коррозионных поражений труб.
Пределы параметров окислительно-восстановительных условий
и диапазон их колебаний в средах местообитания микроорганизмов
составляют [100], [115], табл. 3.8.
138 Глава 3
Таблица 3.8. Диапазон параметров окислительно-восстановительных усло-
вий существования микроорганизмов
Организмы Пределы Eh, мв Диапазон Eh, мв
Десульфурирующие + 115. .450 565
Денитрифицирующие +665. .205 870
Метанобразующие + 100. .300 400
3.5. Продуцирование СВБ сероводорода
Объем вырабатываемого сульф^твосстанавливающими бактери-
ями в промысловой среде сероводорода напрямую зависит от коли-
чества микроорганизмов в среде и индекса их активности. Все эти
параметры связаны зависимостью
Vh2s I),
где N — количество клеток СВБ; I — индекс активности СВБ.
Индекс активности СВБ представляет собой параметр, харак-
теризующий скорость роста бактерий. Определяется визуально по
моменту появления сульфида железа в посевном флаконе и выра-
жается в частичном или полном окрашивании осадка питательной
среды в черный цвет. При появлении сульфида в течение одних су-
ток индекс активности СВБ принимают за 100 единиц, за 2 сут —
50 единиц и т. д. Расчет индекса активности производят по формуле
I = 100/а,
где а — время появления черного осадка, сут.
При отсутствии осадка сульфида железа за время инкубации-
в течение 15 суток считают, что в исследуемой пробе СВБ отсутству-
ют.
3.5. Продуцирование СВБ сероводорода
139
В лабораторных условиях установлена тесная связь между ин-
дексом активности СВБ и их количеством, причем чем активнее клет-
ки СВБ, тем их больше. Исследования проведены в среде Постгей-
та В исходя из возможности создания идеальных условий развития
СВБ. При этих благоприятных условиях развития СВБ может быть-----
получено максимально возможное количество сероводорода, кото-
рое может быть принято за предельное. В реальных условиях ме-
сторождений количество растворенного в воде сероводорода бу;гет
значительно меньше, хотя и не исключено, что при благоприятных
условиях биогенные процессы образования сероводорода могут идти
по приведенным зависимостям. Зависимость количества клеток СВБ
от индекса их активности показана на рис. 3.7, а количество выра-
батываемого СВБ сероводорода в зависимости от количества клеток
и индекса их активности проиллюстрировано на рис. 3.8. Исследова-
ния отражают характер жизнедеятельности накопительной культуры
СВБ, выделенной из промысловых сред Чутырско-Киенгопского ме-
сторождения Удмуртии.
Анализ промысловых данных и лабораторных исследований по-
путно-добываемых вод позволил установить зависимость количества
выделяющегося сероводорода в результате жизнедеятельности СВБ
Чутырской площади от индекса их активности. Зависимость можно
описать уравнением
У = а-10в/х,
где У — содержание сероводорода, мг/л; х — индекс активности;
а и в — коэффициенты, равные соответственно 162,82 и 11,3.
Полученные зависимости (рис. 3.8) дают возможность прогно-
зировать объем продуцирования сероводорода клетками СВБ.
140
Глава 3
Рис. 3.7. Зависимость количества клеток СВБ от индекса их активности
Рис. 3.8. Зависимость количества вырабатываемого СВБ сероводорода от
индекса их активности: 1—4 количество клеток соответственно 1, 10, 100,
1000 в 1 мл питательной среды Постгейта В
Продуцирование сероводорода зависит от состава среды, в кото-
рой они находятся. Естественно, что максимальное количество серо-
3.5. Продуцирование СВБ сероводорода
141
водорода может быть выработано бактериями, находящимися в спе-
циально приготовленной питательной среде, идеальным вариантом
которой является среда Постгейта. Кинетика продуцирования био-
генного сероводорода в среде Постгейта В в виде кривой изображена
на рис. 3.9.-------------------------------------------------
Время, сут
Рис. 3.9. Продуцирование сероводорода сульфатвосстанавливающими бак-
териями в среде Постгейта В
Полученная графическая зависимость [114] характеризует три
этапа жизнедеятельности СВБ, выражающиеся тремя участками
на экспериментальной кривой:
1) Адаптация очищенной накопительной культуры СВБ к пита-
тельной среде. Участок характеризуется невысоким значением кон-
центрации сероводорода.
2) Интенсивный рост СВБ. Для участка (интервал 3 ... 6 сут) ха-
рактерно заметное увеличение скорости образования сероводорода за
счет интенсивного роста СВБ. Концентрация сероводорода возраста-
ет до 280 мг/л.
142
Глава 3
3) Прекращение роста СВБ. Через 7 сут развитие бактерий пре-
кращается и содержание сероводорода в среде стабилизируется, хотя
отдельные клетки бактерий сохраняют свою первоначальную актив-
ность.
----После пересева на свежую питательную среду цикл развития
СВБ и генерацию биогенного сероводорода повторяют.
Скорость продуцирования сероводорода одной сульфатвосста-
навливающей бактерией составляет 10... 8G мгк Б2-/(дм3 • сут).
При общей средней зараженности месторождения (например, Куш-
кульского 102 ... 104 клеток в 1 см3) прирост сероводорода за год
составляет 0,3... 5,1 мг/дм3, или 4,2 ... 71,4 т в год [136]. Ежегод-
ный прирост сероводорода по всем месторождениям, подвергнутым
заводнению без антибактериальной обработки закачиваемых вод, мо-
жет достигать тысяч тонн в год. Некоторые виды СВБ могут образо-
вывать до 3100 мг/л сероводорода [9].
3.6. Скорость образования сероводорода в призабойной
зоне нагнетательных скважин
Из промысловой практики известно, что на ряде скважин, на-
ходящихся долгое время в простое, в процессе проведения подзем-
ных и капитальных ремонтов наблюдаются выбросы сероводорода.
При этом концентрация сероводорода в некоторых случаях превыша-
ет предельно допустимую в десятки и сотни раз, причем чем сква-
жина дольше находится в простое, тем выше концентрация серово-
дорода. С целью установления влияния времени нахождения нагне-
тательной скважины в простое на характер и величину образования
сероводорода [52], в объединении «Удмуртнефть» проведен крупно-
3.6. Скорость образования сероводорода в призабойной зоне 143
масштабный промысловый эксперимент на 7 месторождениях. Всего
в ходе проведения эксперимента было задействовано 75 скважин,
с которых отобрано 222 пробы воды. Распределение количества проб
по месторождениям отражено в табл. 3.9.
Таблица 3.9. Количество исследованных скважин и отобранных проб
Месторождение Количество исследованных скважин „ Количество отобранных проб
Из пласта Из затрубного пространства
Чутырская площадь 10 12 12
Красногорское 25 18 26
Лозолюкско-Зуринское 6 5 4
Сундурско-Нязинское 2 2 1
Мишкинское 12 37 42
Лиственское 2 9 8
Ельниковское 22 19 23
Необходимо отметить, что на Мишкинском и Лиственском ме-
сторождениях эксперимент проводился в период остановки закач-
ки в системе поддержания пластового давления в течение 30 суток,
на Ельниковском месторождении скважины находились в простое
до 30 суток. В Игринском нефтедобывающем районе для проведе-
ния эксперимента были выбраны находящиеся в простое скважины
продолжительностью до 200 суток.
Проведенный анализ позволил установить, что в простаиваю-
щих нагнетательных скважинах в призабойной зоне пласта происхо-
144
Глава 3
дит рост СВБ и накопление продукта их жизнедеятельности — серо-
водорода.
С увеличением продолжительности нахождения скважины в про-
стое отмечен рост содержания в призабойной зоне пласта сероводо-
рода. Наиболее показательным примером может служить скважина
№ 1142 на Чутырской площади, рис. 3.10. За 35 суток в этой скважине
образовалось 108,12 мг/л сероводорода. Это очень высокое значе-
ние, которое могло бы привести к нежелательным последствиям при
проведении последующих ремонтных работ на скважине. Скважина
№ 1142 не единичная. На скважине № 1134 за 106 суток простоя
образовалось 174,4 мг/л сероводорода.
Рис. 3.10. Динамика образования сероводорода в призабойной зоне скважи-
ны № 1142 Чутырской площади
Если по всем максимально полученным значениям сероводорода
построить обобщенную кривую, то она примет вид кривой, отражен-
ной на рис. 3.11.
Необходимо отметить, что на Ельниковском месторождении се-
роводород обнаружен на небольшом количестве скважин и в незна-
3.6. Скорость образования сероводорода в призабойной зоне 145
чительных количествах. Однако отбор пробы воды из призабойной
зоны пласта со скважины № 3992, находящейся в длительном про-
стое (803 дня), показал возможность генерирования значительного
количества сероводорода — 50 мг/л.
Рис. 3.11. Динамика образования сероводорода в призабойной зоне скважин
Чутырской площади
Проведенный анализ позволил в обобщенном виде определить
скорость вырабатывания сероводорода сульфатвосстанавливающими
бактериями в призабойной зоне нагнетательных скважин различ-
ных месторождений, табл. 3.10. Полученные значения, с определен-
ной долей погрешности, можно использовать в качестве прогнозных
данных, характеризующих протекание процесса жизнедеятельности
СВБ в остановленной на длительное время нагнетательной скважине
и скорость вырабатывания сероводорода в зависимости от времени
простоя скважины.
Наиболее опасным месторождением по интенсивности образо-
вания сероводорода является Чутырская площадь.
146
Глава 3
Таблица 3.10. Скорость образования сероводорода в призабойной зоне на-
гнетательных скважинах
Месторождение Усредненное содержание H2S Среднее время простоя Скорость вырабатывания
в призабойной зоне, мг/л скважины, сут H2S, мг/л-сут
Чутырская площадь 73,9 45 1,642
Мишкинское 7,6 11 0,691
Красногорское 16,4 ' 57 0,287
Ельниковское 3,06 13 0,235
Лиственское 1,6 10 0,16
3.7. Продукты жизнедеятельности СВБ
Сульфиды железа
Состав и структура сульфидных слоев в кинетике коррозионных
процессов играют весьма важное значение. Однако решение этих
задач затруднено тем, что на поверхности железа в водных сероводо-
родсодержащих средах формируется одновременно несколько моди-
фикаций сульфидов железа, отличающихся соотношением S2~/Fe2+
и структурой. С течением времени при изменении внешних усло-
вий: температуры, концентрации в растворе или давления Ph2s над
раствором, pH, минерализации и др. факторов — комбинации моди-
фикаций, их количественные соотношения в слое на поверхности
металла меняются [31].
3.7. Продукты жизнедеятельности СВБ
147
Содержание тех или иных форм сульфида железа в среде зависит
от концентрации сероводорода. При низких концентрациях серово-
дорода (порядка 2 мг/л) первичным продуктом коррозии считают
макинавит (Fei+xS, при х = 0,057... 0,064), который в зависимо-
сти от внешних условий трансформируется в другие фазы: трои---------
лит (FeS), пирротит (Fei_xS гексагональный и моноклинный) и пи-
рит (FeS2). Масса первичных продуктов коррозии достигает порядка
1 • 10-4 г/см2. Начальные скорости коррозии практически не зависят
от концентрации сероводорода [31].
Пирротит представляет собой сульфид железа с составом от
FeySg до стехиометрического FeS (троилита).
Моноклинный пирротит FeySg имеет упорядоченную дефектную
структуру с одной вакансией на каждом четвертом катионе в каж-
дом втором слое и для электронейтральности в этой же подрешетке
содержит Fe3+ (с составом от Feo,90S до Feo,94S), является полупро-
водником p-типа и дополнительно к катионным вакансиям содержит
электронные дырки. При взаимодействии с серой макинавит превра-
щается в грейгит, пирит или марказит.
Грейгит — это тиошпинель железа FeoS^ содержащая серу
в плотной кубической упаковке с 8 Fe2+ в тетраэдрической коор-
динации и 16 Fe2+ в октаэдрической координации. Грейгит так-
же термодинамически неустойчив по сравнению с троилитом и пи-
ритом.
Марказит представляет собой орторомбический дисульфид же-
леза, где сера находится в виде полисульфида S^-, а вариация сте-
хиометрии обусловлена недостатком серы.
Пирит обладает кубической кристаллической структурой, в ко-
торой сера находится также в виде Sj-, как и в марказите. Однако
148
Глава 3
связь Fe-S в пирите сильнее, недостаток Fe2+ или S2- приводит
к проводимости р- или п-типа.
По мнению ряда исследователей, первоначальный тонкий слой
макинавита постепенно утолщается и затем покрывается толстыми
защитными слоями пирротита и ттирита.
Содержание тех или иных форм сульфида железа в среде зави-
сит от концентрации сероводорода. При низких концентрациях серо-
водорода, порядка 2 мг/л, продукты коррозии состоят из троилита
и пирита.
В области концентраций сероводорода 2... 20 мг/л в продук-
тах коррозии дополнительно содержится канзит. При концентрациях
20... 600 мг/л сульфид железа присутствует в основном в виде кан-
зита [32]. Согласно данным Мильтона [31], канзит FegSs, первичный
и наименее защищающий продукт коррозии стальных труб, является
в действительности тетрагональным макинавитом FeS.
Состав пленок на поверхности железа зависит главным образом
от парциального давления сероводорода в растворе. При изменении
парциального давления от 65 Па до 22 кПа состав пленки изменяется
от FeS до FeS2 и FegSs [55]. При этом максимальными защитными
свойствами обладают пленки троилита (FeS) и пирита или марказита
(FeS2).
Сульфид железа по отношению к железу и стали является эффек-
тивным катодом. Разница в потенциалах между сталью и сульфидом
железа может составлять 0,2 ... 0,4 в.
Сульфиды железа обладают различной степенью экранирования
металлической поверхности. Сульфиды железа, состоящие из трои-
лита и пирита, обладая почти совершенной кристаллической решет-
кой с относительно небольшим количеством дефектов, имеют вы-
3.7. Продукты жизнедеятельности СВБ 149
сокие защитные свойства. Для канзита характерна несовершенная
кристаллическая решетка и, следовательно, незначительная степень
экранирования поверхности.
г В нейтральных средах, характерных для сточных вод промыс-
лов, на поверхности металла преобладают сульфиды железа в виде_____
канзита, обладающие наименьшими защитными свойствами.
Биогенные сульфиды при взаимодействии с атомарным желе-
зом или ионами железа образуют твердые сульфиды железа. Процесс
ионообмена с образованием сульфидов согласно [146] засвидетель-
ствован на рис. 3.12.
Рис. 3.12. Процесс ионообмена с образованием сульфидов железа: М = рав-
новесие металлических ионов; Sn — полисульфиды; So — молекулярная
сера; (—) — химические реакции; (-) — биологические реакции
На данной схеме показаны основные виды сульфида железа, ко-
торые могут образоваться. Переход сульфидов из одной формы в дру-
150
Глава 3
гую определяют температура, pH, окислительно-восстановительный
потенциал и относительная концентрация самих сульфидов.
В результате прямой реакции растворимых сульфидов с иона-
ми железа образуются пленки с хорошей адгезией к поверхности
металла, которые замедляют, но не предотвращают коррозию. Рост
сульфидной пленки приводит к ее уплотнению. Этот процесс яв-
ляется диффузионно контролируемым. В дальнейшем пленки раз-
рушаются и отделяются от металлической поверхности, которая
становится анодной по отношению к оставшимся катодным суль-
фидным пленкам. На этих участках оголенного металла наблюда-
ется интенсивное питтингообразование. Сульфидные пленки вновь
не образуются.
Природу и состав сульфидных пленок, скорость их роста и ска-
лывания определяет в основном pH среды. Первоначально выраба-
тываемый сульфид — это макинавит, который переходит в грейгит.
После продолжительного контакта металла с сульфидными раство-
рами образуется некоторое количество пирротита. Предполагают, что
переход FeSi-x в FeaS4 связан с разрушением пленки. Скорость кор-
розии приблизительно описывается кинетическим уравнением пер-
вого порядка. Различные формы сульфида железа обладают различ-
ной коррозионной активностью. Коррозия железа, вызванная СВБ,
проявляется обычно в виде питтинговой коррозии.
Сероводород
Сероводород при нормальном давлении и температуре представ-
ляет собой бесцветный газ со специфическим запахом. При объемной
доле 4,3... 45,5% образует с воздухом взрывоопасные смеси.
3.7. Продукты жизнедеятельности СВБ 151
Является сильным нервным ядом. Опасность отравления усу-
губляется тем, что при массовой концентрации 11 • 10~6 кг/м3
и выше специфический запах сероводорода становится менее ощу-
тимым. Физико-химические свойства сероводорода представлены
Таблица 3.11. Физико-химическая характеристика сероводорода
Показатель Значение
Состояние Бесцветный газ
Плотность, кг/м3 1,538
Относительная плотность жидкого H2S (по воде) 0,94
Давление насыщенного пара при 20° С, атм 18,5
Теплотворная способность, ккал/м3 6070
Теплота растворения в воде, кал/моль 4500
Температура самовоспламенения, °C 290
ПДК в воздухе, кг/м3 1•10~5
ПДК в углеводородной среде, кг/м3 3- ИГ6
Сероводород растворим как в водной, так и в углеводородной
фазе, причем с увеличением температуры растворимость в водной
фазе уменьшается, поскольку растворение газов в воде представляет
собой экзотермический процесс, табл. 3.12.
При растворении в воде сероводород диссоциирует в две ступени
по формуле
H2S Н+ + HS 2Н+ 4- S2-.
152
Глава 3
Таблица 3.12. Растворимость сероводорода в воде при 760 мм рт. ст. [117]
Температура, °C Растворимость Температура, °C Растворимость
м3/м3 мг/л м3/м3 мг/л
0 4,670 7066 40 1,660 2361
5 3,977 6001 45 1,516 2110
10 3,399 5112 50 1,392 1883
15 2,945 4411 60 1,190 1480
20 2,582 3846 70 1,022 1101
25 2,282 3375 80 0,917 765
30 2,037 2983 90 0,840 41
35 1,831 2661 100 0,810 40
Константа диссоциации первой ступени:
[н+] • [HS-] s
L J L J = 9,5 • 10“8; - 1g A'l = pl<! = 7.
[H2S]
Константа диссоциации второй ступени:
[H+] • [hs2-]
A2 = 1H2S] = 13'10
- 1g 1<2 = = 12,9.
При pH, меньших рК\, сероводород в растворе находится пре-
имущественно в молекулярной форме, при рКi < pH < рК‘2 — в виде
гидросульфид-ионов и при pH > рК? — в виде S2--ионов.
Насыщенный раствор сероводорода в воде (3000 мг/л при 30° С
и парциальном давлении Fh2s, равном 0,1 МПа) представляет собой
слабокислую среду с pH = 4.
3.7. Продукты жизнедеятельности СВБ
153
' В углеводородах сероводород растворяется гораздо лучше, чем
в воде. Для примера в табл. 3.13 приведена растворимость серово-
дорода и некоторых других газов при нормальных условиях (20° С
и давлении 0,1 МПа) в углеводородных растворителях.
Таблица 3.13. Растворимость газов в углеводородных растворителях, м !/м
жидкости
Газ Растворитель
Цикло- гексан Четырех- хлористый углерод Этанол Гексан Бензол Вода
Сероводород 6,50 9,300 7,420 5,430 13,10 2,420
Азот 0,17 0,210 0,120 0,206 0,116 0.015
Кислород 0,28 0,278 0,220 — 0,220 0,031
Метан 0,89 0,720 0,505 0,560 0,532 0.03 4
Диоксид углерода 1,71 2,340 2,670 — 2,300 0,878
В качестве показателя растворимости может быть принят коэф-
фициент распределения сероводорода между жидкими углеводоро-
дами и водой [117, 150]. Согласно закону распределения вещество,
способное растворяться в двух несмешивающихся растворителях,
распределяется между ними так, что отношение его концентраций
в этих растворителях при постоянной температуре остается постоян-
ным, независимо от общего количества растворенного вещества [33]:
154
Глава 3
где Ci и Сг — концентрации растворенного вещества в первом и вто-
ром растворителях.
Для нефтепромысловой жидкости, содержащей сероводород,
уравнение принимает вид
Содержание H2S в углеводородах
Содержание H2S в воде
Коэффициенты распределения сероводорода между водой и бен-
зином, водой и керосином [150] приведены в табл. 3.14. В более
легком углеводороде — бензине сероводород растворяется лучше.
।
Таблица 3.14. Коэффициент распределения H2S между жидкими углеводо-
родами и водой
Температура, °C Коэффициент распределения
Для бензина Для керосина
15 5,65 3,70
25 - 6,30 3,20
35 7,00 3,20
Коэффициент распределения между водой и легкой нефтью ле-
жит в пределах 1,5... 1,75.
Свойство изменения растворимости сероводорода в водной и уг-
леводородной фазах в зависимости от температуры можно исполь-
зовать для регулирования величины его содержания в воде и неф-
ти в ходе технологического процесса разделения эмульсии на нефть
и воду, например перед предварительным сбросом воды и т. п. Если
водонефтяные потоки после разделения на фазы в концевом делите-
ле фаз охладить, то содержание сероводорода в водной фазе можно
3.7. Продукты жизнедеятельности СВБ 155
увеличить, а в нефтяной фазе уменьшить. Все будет зависеть от по-
ставленной цели и используемой технологии.
В электролите сероводород в зависимости от pH среды может
находиться при различном соотношении диссоциированной и недос-
социированной форм. Так, при pH — 7 соотношение этих форм, %,
выражается как 53 к 47.
Сероводород является химически активным сернистым компо-
нентом. В присутствии воды легко вступает в реакции
с металлами Fe + H2S —► FeS + Н2
с кислородом H2S + О? —» Н2О + S.
Эти реакции протекают при обычной температуре.
На воздухе горит синеватым пламенем, образуя диоксид серы
(при избытке кислорода) или серу (при недостатке кислорода):
H2S + 3/2O2 H2O + SO2;
H2S + у2о2 Н2О + S.
Как слабая кислота, раствор сероводорода взаимодействует
со щелочами с образованием гидросульфида и сульфида:
H2S + NaOH NaHS + Н2О;
H2S + 2NaOH Na2S + H2O.
Эти реакции лежат в основе процессов очистки как газовых,
так и жидких продуктов.
При совместном нахождении в растворе с кислородом серово-
дород вступает с ним в химическое взаимодействие, окисляясь до
элементарной серы, 80з+, SO^-, SO^- и некоторых других про-
межуточных форм. Скорость взаимодействия реагирующих между
собой молекул сероводорода и кислорода подчиняется законам хи-
мической кинетики и зависит от концентрации исходных и конечных
156
Глава 3
продуктов. На рис. 3.13 показана скорость взаимодействия кислорода
и сероводорода в зависимости от pH среды в условиях ограниченного
доступа кислорода [42]. За 6 часов при pH — 6 расходуется до 50%
первоначального содержания кислорода, а при pH = 10 — уже 77 %.
Поскольку величина pH сточных вод находится впределах С...7,5,
то очевидно, что кислород и сероводород в течение практически все-
го времени транспортирования сточных вод по системе водоводов
сосуществуют, что и обуславливает высокую скорость коррозии ме-
таллов в таких средах.
Время, час
Рис. 3.13. Взаимодействие кислорода с сероводородом при температуре
20° С и различных pH среды: 1 — 10,0; 2 — 6,0; 3 — 3,0
3.8. Последствия жизнедеятельности микроорганизмов
Влияние микроорганизмов на проницаемость продуктивных
пластов
Влияние микроорганизмов на проницаемость продуктивных
пластов установлено многими исследователями [95, 127].
3.8. Последствия жизнедеятельности микроорганизмов 157
Коллекторские свойства продуктивного пласта зависят от сте-
пени зараженности пластовых флюидов микроорганизмами. С це-
лью выявления степени их влияния на проницаемость пласта ав-
торами [95] проведен лабораторный эксперимент по фильтрации
накопительных культур, выделенных из промысловых сред Усть-Ба-
лыкского месторождения, на насыпной песчаной модели. Пористая
среда с проницаемостью 0,75 мкм2 представлена смесью кварце-
вого песка и дезинтегрированной породы пласта. Модельное со-
общество микроорганизмов создано ^при смешивании в равном со-
отношении накопительных культур УОБ, СВБ, а также коллек-
ционных культур гетеротрофных микроорганизмов. Общее число
микроорганизмов в полученном модельном сообществе достигало
1 • 107 ... 1 • 1()8 клеток/см3.
Эксперимент по фильтрации культуральной жидкости выполнен
на установке, имеющей постоянные перепады давления, в качестве
контролируемого параметра определен расход жидкости. Установив-
шийся расход пресной воды без микроорганизмов принят за единицу.
Удельный расход жидкости рассчитывался по формуле
где Qt — расход жидкости к моменту времени t; Q — расход жид-
кости без микроорганизмов. Результаты эксперимента представлены
на рис. 3.14.
Как видно из рис. 3.14, фильтрация культуральной жидкости
сопровождается уменьшением проницаемости пористой среды. Так,
при закачке 3 поровых объемов культуральной жидкости удельный
расход равен 0,9, а после фильтрации 6 объемов расход снизился
до 0,47. Микробиологическое исследование культуральной жидкости
158
Глава 3
Рис. 3.14. Динамика фильтрации культуральной жидкости через модель пла-
ста: 1 — воздействие этанолом; 2 — ЛПЭ-11
и фильтрата, отобранного в период снижения проницаемости пори-
стой среды, после закачки 5 поровых объемов показал, что числен-
ность микроорганизмов в фильтрате значительно ниже, чем в исход-
ной культуральной жидкости, т. е. в период снижения проницаемости
наблюдается иммобилизация микроорганизмов в пористой среде.
После воздействия этанолом и бактерицидом ЛПЭ-11 проис-
ходит незначительное снижение расхода жидкости за счет гибе-
ли микроорганизмов и уменьшения проницаемости при фильтра-
ции дисперсной фазы биомассы и мертвых клеток микроорганиз-'
мов. Дальнейшее нагнетание воды приводит к увеличению расхода
фильтруемой жидкости и восстановлению проницаемости пористой
среды. Действие бактерицида заканчивается, наблюдается адаптация
микроорганизмов и рост их биомассы.
В промысловой практике прокачка жидкости в количестве
5... 10 объемов порового пространства реальна на отдельных участ-
ках, что подтверждено исследованиями методом закачки меченых
жидкостей. При этом полученные расчетные значения скорости дви-
3.8. Последствия жизнедеятельности микроорганизмов 159
жения жидкости от нагнетательных до добывающих скважин дости-
гали величин порядка 2 км/сут.
Прогнозирование процессов поведения технологической си-
стемы добычи нефти от бесконтрольно циркулирующих в ней хи-
мических реагентов или отдельных категорий загрязнителей пласта
и системы является сегодня крайне актуальной задачей, в особен-
ности для случаев, когда загрязнение происходит в многопластовом
объекте за счет биологического заражения.
Оценка влияния бактериального заражения на технологические
показатели месторождения основана на том факторе, что процесс
затухания фильтрации, связанный с загрязнением пласта вносимыми
дисперсиями, может быть описан функцией Кольрауша [27]:
w = wo • exp atb^, (3.1)
где wo — начальная скорость фильтрации; t — время; а, b — коэф-
фициенты, зависящие от природы и структуры дисперсной фазы,
дисперсной среды и порового пространства, при этом бактериаль-
ная биомасса рассматривается как некая дисперсная среда.
Однако для биосистемы характерны свои законы развития, от-
личные от поведения неорганических дисперсий. В связи с этим
рассмотрение задачи о модели развития бактериальной микрофло-
ры в среде с ограниченными жизненными ресурсами и о влия-
нии бактериального заражения на проницаемость пластов представ-
ляется крайне важным. Уравнение, описывающее рост числа бак-
терий в экосистеме с ограниченными пищевыми запасами, имеет
вид [127]
= aN - с№,
dt
(3.2)
160
Глава 3
где N — число бактерий; а, с — некоторые положительные постоян-
ные, в общем случае зависящие от нефтенасыщенности, пористости
и других параметров пласта.
Физический смысл постоянных:
а — определяет скорость роста числа бактерий;
с — скорость уменьшения числа бактерий в результате естествен-
ной гибели и конкуренции за жизненные ресурсы;
отношение а/с дает предел роста числа бактерий.
Решение уравнения имеет вид
с + ехр(—at) ’
и может быть аппроксимировано кривыми, помещенными на
рис. 3.15.
Из рисунка видно, что через некоторое время t число бактерий
достигает своего предельного значения. Скорость роста числа бакте-
рий имеет максимум в некоторый момент времени.
Полуэмпирическая модель кинетики загрязнения объекта, с уче-
том релаксационного понижения проницаемости при фильтрации
жидкости с примесями, имеет вид
§ = Q - « • S, (3.4)
at
где S — массовое содержание загрязняющих частиц, осевших на по-
верхностях пор; q — скорость увеличения концентрации загрязня-
ющих частиц; а — коэффициент, определяющий скорость выноса
загрязняющих частиц.
С учетом предположения, что объем загрязнения пропорциона-
лен числу бактерий, а скорость q пропорциональна dN/dt, уместно,
3.8. Последствия жизнедеятельности микроорганизмов 161
Время, о(гн. ед.
Рис. 3.15. Изменение относительного числа и скорости роста числа бактерий
во времени: 1 — число бактерий при а/с = 3; 2 — скорость роста бактерий
при а/с = 3; 3 — число бактерий при а/с = 1; 4 — скорость роста бактерий
при а/с = 1
где 7 — коэффициент пропорциональности.
Массовое содержание загрязняющих частиц, осевших на поверх-
ностях пор, связано с проницаемостью выражением
К = Ко - /35, (3.6)
где (3 — коэффициент пропорциональности; Kq — проницаемость
незагрязненной пористой среды.
Подставляя все выражения в уравнение для S, можно получить
уравнение проницаемости
^+£-K + f(t) = r], (3.7)
где С = а/0,7] = а//3 Ко, f(t) = 7 -^ ех^ aQ
(с + ехр(—at)Y
162
Глава 3
Предполагается, что все сказанное выше относится к одному
пласту. Для многослойной же системы уравнение будет иметь вид
л rs
^+£г/<г + Л(0 = ^ (3.8)
где i — индекс пласта.
Используя уравнение (3.8), при допущениях для уравнений (3.6),
(3.7) можно произвести их численное исследование по конкретной
геологической характеристике нагнетательных скважин, закачиваю-
щих загрязненную микроорганизмами сточную воду.
Зависимости изменения средневзвешенной проницаемости си-
стемы, при закачке в нее загрязненной сточной воды Абдрахманов-
ской площади [127], во времени и для конкретных скважин приведе-
ны на рис. 3.16.
Время, отн. ед.
Рис. 3.16. Зависимость средневзвешенной проницаемости от времени после
закачки сточной воды, содержащей микроорганизмы [127]: 1 — скв. 279; 2 —
скв. 312; 3 — скв. 278; 4 — скв. 276
Эти зависимости имеют различные значения уменьшения прони-
цаемости, что обусловлено отключением низкопроницаемых пластов.
I 3.8. Последствия жизнедеятельности микроорганизмов 163
Отключение низкопроницаемых пластов связано с более быстрым по-
нижением практически до нуля коэффициента проницаемости пласта
при росте числа бактерий.
Воздействие бактерицида приводит к подавлению жизнедеятель-
ностибактерий и, как следствие этого, — к увеличению выноса от-
мерших бактериальных образований из пласта. В рассматриваемой
модели воздействие бактерицида описывается увеличением скорости
уменьшения числа бактерий (с) и скорости выноса бактериальной
пленки (а).
Результаты исследований воздействия бактерицида на проница-
емость применительно к низкопроницаемым пластам отражены на
рис. 3.17.
Рис. 3.17. Изменение проницаемости после закачки загрязнителя (t = 0)
и бактерицида (t = Т): 1 — t = 0,5; 2 — t = 1; 3 — t = 2; 4 — t = 3; 5 —
t = 4
Предполагая, что начиная с времени t = 0 в пласте происхо-
дит рост биомассы и, как следствие этого, — понижение прони-
164
Глава 3
цаемости пласта. В момент времени t = Т в пласт закачивается
бактерицид. В течение времени t > Т происходит восстановление
проницаемости пласта. Как показано на рис. 3.17, в зависимости
от момента времени закачки бактерицида кривые восстановления
проницаемости имеют различный характер скорости восстановле-
ния проницаемости. Чем раньше после заражения пласта закачива-
ется бактерицид (Г = 0,5), тем на большую абсолютную величи-
ну восстанавливается проницаемость. Однако скорость восстановле-
ния проницаемости мала. При более поздней закачке бактерицида
в пласт (Т — 2,3,4) скорость восстановления увеличивается, но аб-
солютная величина проницаемости 'будет значительно меньше, чем
при Т = 0,5.
Роль микроорганизмов в формировании солеотломсений
О целесообразности комплексного подхода к исследованию под-
земных вод как к химически и физически чрезвычайно активному те-
лу, меняющемуся при соприкосновении с окружающей средой, под-
черкивал еще в 1933 г. В. И. Вернадский. В связи с этим был про-
возглашен принцип возможности и необходимости широкого изуче-
ния подземных вод как с точки зрения химии, физики, геологии, так
и биохимии и микробиологии.
В результате в ходе проведенных последующих исследований
плеядой выдающихся российских и зарубежных исследователей был
наработан значительный фактический материал, позволивший сде-
лать ряд принципиально новых обобщенных выводов. Оказалось,
что большую роль в преобразовании состава подземных вод играют
биохимические реакции окисления и восстановления, приводящие
к частичной перегруппировке атомов, к появлению новых соедине-
3.8. Последствия жизнедеятельности микроорганизмов 165
ний. Так, например, широко распространенным процессом оказалось
явление восстановления сульфатов, за счет которого образуется серо-
водород. Генезис сероводорода в нефтяных месторождениях до по-
следнего времени оставался спорным. Многие из геологов допускали
возможность химических процессов восстановления сульфатов пла-
стовых вод путем их взаимодействия с органическими веществами
нефти. Однако известно, что химическое восстановление сульфатов
возможно только при условиях, значительно превышающих темпе-
ратуру 100° С, а такая температура в нефтяных пластах встречается
довольно редко.
Вопрос основного происхождения сероводорода был оконча-
тельно сформулирован М. В. Ивановым (1964) в пользу биологиче-
ского восстановления сульфата. При его обосновании в исследуе-
мую пластовую воду вносили меченный по сере сульфат натрия
Na^5SO4, воду инкубировали в замкнутом объеме при температуре
пласта от одних до нескольких суток и по радиоактивности обра-
зовавшегося сульфида определяли интенсивность процесса редук-
ции сульфатов за счет естественной микрофлоры самого месторож-
дения.
Опыты М. В. Иванова и В. М. Горленко в 1966 г. с внесением
антисептика подтвердили, что химического восстановления сульфата
в пластовой воде не происходит.
В процессе образования сероводорода, по мере использования
растворенных сульфат-ионов, в раствор переходят все новые их
порции из сульфатсодержащих пород, например сульфата кальция,
за счет чего количество сульфатных минералов неизбежно уменьша-
ется, содержание сероводорода увеличивается, а содержание сульфат-
ионов в воде неуклонно снижается, рис. 3.18.
166
Глава 3
Рис. 3.18. Изменение содержания сероводорода и сульфатов в воде излива-
ющей скважины: 1 — сероводород; 2 — сульфат-ион
г
Сульфатвосстанавливающие бактерии участвуют в преобразова-
нии самых разнообразных сульфатсодержащих минералов, участву-
ют в преобразовании гипса, целестина, барита, потребляют сульфаты
железа, цинка, меди. Если в пластовой воде имеются ионы тяжелых
металлов, то они осаждаются с образованием соответствующих суль-
фидов. Черный осадок сульфидов железа повсеместно отмечается
в пробах, отобранных в зонах смешения закачиваемых вод с пласто-
вой, обогащенной железом. На начальной стадии развития процес-
са сульфатредукции отмечают аморфный сульфид железа, представ-
ленный, как правило, гидротроиллитом, постепенно уплотняющимся
и кристаллизующимся до пирита и отлагающимся в продуктивных
породах. В случаях когда в пластах активно присутствуют тионовые
бактерии, содержание сульфатов в пластовой воде может и повы-
шаться.
Таким образом, сульфатредукция приводит к преобразованию
вмещающих продуктивных пород, растворяя сульфатные минералы
и осаждая сульфиды.
3.8. Последствия жизнедеятельности микроорганизмов 167
В ОАО «Удмуртнефть» в 2005-2006 годах было исследовано
184 пробы отложений солей, из которых в 160 пробах (87%) обна-
ружен сульфид железа. Наибольшее содержание сульфида отмече-
но на Гремихинском, Кезском, Чутырско-Киенгопском, Красногор-
ском, Лозолюкско-Зуринском, Лиственском, Мишкинском, Лудошур-
ском месторождениях. Количественное содержание сульфида железа
в анализируемых пробах достигает 95%, однако доля таких скважин
в настоящее время не велика, рис. 3.19.
Рис. 3.19. Содержание сульфида железа в пробах, отобранных с глубинно-
насосного оборудования
Характерно, что доля сульфидов железа в осадках увеличивается
год от года, рис. 3.20.
В процессах биогенного окисления углеводородов происходит
их разрушение до углекислоты и воды или промежуточных продук-
тов, с последующим превращением в вещества микробной биомас-
сы. Промежуточные продукты окисления, используемые в процессах
восстановления сульфатов, в свою очередь окисляются до углекис-
168
Глава 3
Рис. 3.20. Изменение содержания сульфида железа в пробах, отобранных
в разные годы '
лоты. Таким образом, бактериальная жизнедеятельность в нефтяных
пластах приводит к увеличению ионов хлора и карбонатов, рис. 3.21.'
Накопление бикарбонатов было отмечено А. Д. Ли и В. А. Кузнецовой
(1963) в призабойной зоне нагнетательной скважины, где развивал-
ся биоценоз углеводородокисляющих и сульфатвосстанавливающих
бактерий [104].
В Удмуртии в последнее десятилетие заметно увеличилось ко-
личество карбонатных и хлоридных солей в составе осадков, обра-
зующихся на поверхности нефтепромыслового оборудования. Стати-
стические данные отражены на рис. 3.22.
Если пластовые воды богаты сульфатами кальция, то использо-
вание этих сульфатов в процессе редукции протекает согласно сле-
дующему упрощенному уравнению:
CaSO4 + 2«С» CaS + 2СО2,
где «С» условно обозначает органическое вещество нефти. При
этом CaS, реагируя с более сильной угольной кислотой, может вы-
3.8. Последствия жизнедеятельности микроорганизмов 169
Рис. 3.21. Изменение бикарбонатов и хлоридов в воде изливающей скважи-
ны: 1 — хлориды; 2 — бикарбонаты
падать в виде вторичного кальцита, который запечатывает нефтяную
залежь:
CaS + СО2 + Н2О СаСОз + H2S.
Направление реакции в сторону осаждения или растворения
карбоната кальция может быть определено на основании уравнения
Колтгофа (I.Kolthoff, 1922), которое имеет следующий вид:
а [Са2+] • [НСО7]2
= К = 1,13 - 10~4,
где концентрации [Са2+] и [НСО3] выражены в г-экв, а [СО2] —
в г-мол.; а — степень диссоциации, близкая к единице. Если для ис-
следуемых пластовых вод константа К^ксп меньше константы Кольт -
гофа К = 1,13 • 10~4, то раствор содержит агрессивную углекислоту
и при соприкосновении с кальцитом будет его растворять. Если же
Кэксп больше константы Кольтгофа, то данный раствор пересыщен
карбонатом кальция и склонен к осаждению вторичного кальцита.
170
Глава 3
Хлористый кальций
Года
Года
Рис. 3.22. Изменение содержания хлористых солей и карбонатов в отложе-
ниях по годам
В данном случае поступление в раствор углекислоты за счет био-
генных процессов при активной реакции пластовых вод, близкой
к pH — 7, только повышает концентрацию НСО:7 и способствует
осаждению вторичного кальцита. Особенно энергично этот процесс
происходит, если пластовые воды богаты сульфатами или хлоридами
кальция. Например в нефтяных водах Шор-Су и Гаурдака соотноше-
ния таковы, что благоприятствуют выпадению вторичного кальцита,
табл. 3.15.
3.8. Последствия жизнедеятельности микроорганизмов 171
Таблица 3.15. Условия карбонатного равновесия в пластовых водах Шор-Су
и Гаурдака
Место отбора проб и степень Компонентный состав, мг-экв/л ^эксп / ^кольтг
минерализации воды СО2 НСО3 Сумма
Шор-Су
слабоминерализованная 1,0 5,4 218,8 6,5 • ИГ4 5,75
сильноминерализованная 2,37 7,0 2298,2 16,82- 10-4 14,9
Гаурдак
сильноминерализованная 2,5 3,2 7789,8 62,81 • IO"4 55,6
Подтверждение биогенной природы вторичного кальцита
К. Б. Ашировым и И. В. Сазоновой (1961-62) получено в ходе про-
ведения лабораторных исследований на модели, схематично пред-
ставленной на рис. 3.23. Модель выполнена в виде стеклянной труб-
ки диаметром 4 см, с обеих сторон закрытой пробками с отводны-
ми стеклянными трубками. В середину трубки впаивалась дырчатая
стеклянная пластинка, на которую помещался керн песчаника, обра-
ботанный 10 %-ной соляной кислотой, промытый водой до нейтраль-
ной реакции и насыщенный нефтью. Трубки заливались минераль-
ной средой Таусона для сульфатредуцирующих бактерий с добавкой
сульфатов кальция и бикарбоната натрия. В ряд опытных трубок вно-
силась культура сульфатредуцирующих бактерий. Температура опыта
поддерживалась в пределах 25 ... 27° С, продолжительность экспери-
мента достигала 80 суток. В остальных опытах в качестве донаторов
водорода в среду Таусона добавлялся лактат или над нефтью созда-
валась атмосфера из молекулярного водорода.
172
Глава 3
МШШ
1
CaSO4 + NaHCO,:
* D.desulfuricans
CaSO, + NaHCOK;
з
I
4
5
Рис. 3.23. Модель для лабораторного исследования образования вторичного
кальцита в процессе сульфатредукции: 1 — нефть; 2 — кристаллы кальцита;
3 — песок; 4 — кварцевая проницаемая перегородка; 5 — жидкая минеральная
среда
Просмотр под микроскопом выпавшего осадка (табл. 3.16) пока-
зал, что он состоит из мелких призматических кристаллов кальцита
с размерами частиц 0,001 мм и меньше. Кристаллы идентичны тем,
которые обнаруживаются в подошве нефтяных залежей с карбонат-
ными коллекторами.
3.8. Последствия жизнедеятельности микроорганизмов 173
Таблица 3.16. Бактериальное образование карбоната кальция культурой СВБ
Вариант опыта (донатор При поста- новке опыта При снятии опыта Вес образовав- шегося СаСОз, г
пН Внесение Наличие СВБ
Р*1 культуры
Газообразный водород 7,0 + 7,75 Ч—h 0,5043
8,35 — 8,3 — 0,0788
Нефть 8,09 + - 7,83 + + + 0,4665
8,19 — 8,09 — 0,0889
Лактат и ацетат Са 7,29 + 7,32 Ч—h 0,4253
7,62 — 7,4 — 0,0
Опыты К. Б. Аширова и И. В. Сазоновой показали, что выпаде-
ние вторичного кальцита является следствием процесса восстанов-
ления сульфатов в среде в присутствии нефти. Отложение вторично-
го кальцита на фильтрах скважины в заводняемом нефтяном пласте
Апшерона отмечено в тех зонах, где активно начинала развиваться
сульфатредукция и появлялся сероводород, связывающийся ионами
железа с образованием сульфида. Таким образом, удалось наблюдать
реальное проявление процесса выпадения кальцита в нефтяном пла-
сте в связи с биогенным восстановлением сульфатов.
Преобразование вмещающих пород под влиянием биогенных
процессов сопровождается изменением состава пластовых вод.
Последовательность протекающих при этом процессов пред-
ставлена В. А. Сулиным (1948). Сульфаты натрия при участии
174
Глава 3
Desulfovibrio или другого вида сульфатредуцирующих бактерий вос-
станавливаются до сульфидов. При этом образуется бикарбонат на-
трия:
N2SO4 + 2«C»opr + 2Н2О —► 2NaHCO3 H2S.
Бикарбонаты натрия взаимодействуют со щелочноземельными
солями сильных кислот. При этом карбонаты кальция и магния вы-
падают из воды и обогащают породы, а хлорид натрия накапливается
в воде:
2NaHCO3 + СаС12 2NaCl + СаСО3 + Н2СО3.
I
Тип воды из сульфатно-хл ори дно-кал ьциевого превращается
в гидрокарбонатно-хлоридно-натриевый. Подобные реакции будут
продолжаться до тех пор, пока не будут израсходованы сульфаты
и хлориды щелочных земель. В случае вод хлоридно-магниевого ти-
па морского происхождения, содержащих хлориды натрия и магния
и сульфаты магния и кальция, в процессе редукции сульфатов по-
следние выпадают в виде карбонатов кальция и магния, и эти воды
переходят в тип хлоридно-натриевых.
О влиянии бактериального восстановления сульфатов на измене-
ние химического состава подземных вод в геосистеме «вода-порода»'
упоминается и в работе [23], в которой, на основе проведенных тер-
модинамических расчетов развития процессов биогенной сульфатре-
дукции, делается заключение о неизбежном повышении в подземных
водах содержания ионов кальция и гидрокарбоната.
В результате биогенной сульфатредукции, помимо исчезновения
ионов кальция и сульфатов, из раствора удаляются и тяжелые метал-
лы, связывающиеся сероводородом. Ионы закисного железа в зна-
чительных количествах присутствуют в воде терригенных нефтяных
3.8. Последствия жизнедеятельности микроорганизмов 175
коллекторов, свободных от сероводорода. По мере заводнения этих
коллекторов и образования сероводорода железо исчезает из воды-
Эта закономерность прослежена для заводняемого пласта Бинагадин-
ской складки Апшерона, Бураевского и Игровского месторождений
Башкирии [28, 104]. Несомненно, биохимические процессы должны-----
оказывать влияние на содержание биогенных элементов в пластовых
водах.
Данные об образовании сероводорода, содержании растворенно-
го железа и величине окислительно-восстановительного потенциала
•л,
в воде разных зон заводняемого нефтяного пласта Бинагадинской
складки отражены в табл. 3.17.
Таблица 3.17. Влияние сероводорода на изменение содержания закисного
железа и величину окислительно-восстановительного потенциала
Сероводород, мг/л F ^общ Eh., мв
0 37,69 —
9 8,14 -10
17 11,61 -50
37 5,56 -90
680 1,16 -120
Полученные данные по изменению содержания сероводорода,
фосфатов, аммонийного азота, углекислоты в заводняемом карбо-
натном коллекторе, где протекают биогенные процессы восстановле-
ния сульфатов, дают представление об изменении состава биогенов,
табл. 3.18.
176
Глава 3
Таблица 3.18. Изменение гидрохимических параметров вод Полазненского
месторождения по мере их разбавления закачиваемой пресной водой
Вид Минера- лиза- Содержание компонентов, мг/л Количество СПС Г» 1 ЧП
ция, г/л H2S so^- HPCTj- NHf СО2, своб. Udd в ± мл
Закачиваемая 0,3 0,0 108 0,16 0,32 45,9 Единицы
Пластовая 10,0 1,5 816 0,24 18,0 — Десятки
Скв. 66 19,4 26,0 1136 0.21 14,4 60,5 Десятки тысяч
Скв. 64 45.4 147,1 1732 0,35 36,0 193,1 Сотни
Скв. 74 53.9 62,7 473 0,48 । 43,2 73,0 Десятки
Скв. 25 G2.4 195,6 1763 0,47 32,4 197,7 —
Фосфаты по мере заводнения и увеличения водообмена, по-ви-
димому, так же как и сульфаты, вымываются из пород коллектора
и далее используются в биогенных процессах.
Роль микроорганизмов в самовозгорании осадочных пород
Проблема предотвращения самовозгорания осадочных горных
пород и тушения пожаров является одной из наиболее крупных и ак-
туальных в жизни и производственной деятельности густонаселен-
ных углепромышленных районов Донецкого региона. Решение этой
проблемы обеспечивает повышение безопасности труда подземных
горнорабочих, существенно уменьшает количество сложных и опас-
ных аварий на угольных шахтах, предотвращает большие материаль-
ные убытки и резко уменьшает загрязнение окружающей техноген-
ной и природной среды. За последнее десятилетие в угольных шахтах
ежегодно происходило от 15 до 40 эндогенных пожаров (вследствие
3.8. Последствия жизнедеятельности микроорганизмов 177
самовозгорания угля или углисто-глинистых пород). На территории
Украинского Донбасса имеется около 1100 породных отвалов, в ко-
торых заскладировано более 1 млрд м3 породы, занимающей пло-
щадь 5526 гектаров. С отвалов (терриконов) ветер сдувает сотни
тысяч тонн пыли, примерно третья часть их (около 360) являются
горящими. При сгорании 1 кг породы происходит загрязнение до
опасного предела от 6,7 до 8,7 млн м3 атмосферного воздуха. Из го-
рящих отвалов в атмосферу выделяется около двух десятков вредных
веществ: оксид углерода, углекислый газ, сернистый газ, серный ан-
гидрид, сероводород, сероуглерод, серооксид углерода, оксиды азота,
серная кислота, цианводород, аммиак, цианиды, тиоцианаты и др.
Согласно [45] причиной самонагревания и самовозгорания пород
являются тионовые бактерии (Th. ferrooxidans). При самонагревании
породы происходит изменение морфологии (формы существования)
тионовых бактерий в поровом растворе в зависимости от измене-
ния его параметров (температуры, кислотности, наличия питатель-
ных субстратов и источников энергии). Суть этого ранее неизвестно-
го природного явления в том, что по мере роста температуры бак-
терии последовательно приобретают следующие формы: подвижные
палочки средних размеров, переходные (раздутые) формы и длин-
ные палочки, нитчатые структуры, сферические формы. Тионовые
бактерии таких форм подобны аэробным хемолитотрофным бакте-
риям, которые способны окислять в гидротермах восстановленные
соединения серы и железа при температурах от 30 до 99... 100° С
и pH от 1 до 6,5... 7. Установлено также и явление выделения из
пиритсодержащей горной породы элементной серы под действием
тионовых бактерий, заключающееся в том, что в естественных водно-
воздушных условиях тионовые бактерии разлагают в порах породы
178
Глава 3
микрокристаллы пирита по их внешней поверхности на элементную
серу и сопутствующие компоненты (серную кислоту, сульфаты, гид-
роксид железа и др.). В целом процесс бактериального окислительно-
го выщелачивания пирита (сульфидных минералов) включает две тес-
но связанные и параллельно протекающие стадии: непосредственное
окисление минерала и деструкция кристаллической решетки; окисле-
ние образующихся при этом новых веществ (двухвалентного железа
и серы). При этом вследствие выделения серной кислоты образуются
сернокислотные поровые растворы. Часть неокисленной серы обра-,
зует с ионами трехвалентного железа и сульфат-ионами коллоидный
।
раствор. Все реакции, связанные с окислительным выщелачивани-
ем пирита, протекают самопроизвольно и являются экзотермически-
ми. В процессах самонагревания пород роль бактерий заключается
в следующем: расчленение поверхности пирита и увеличение его ре-
акционноспособной поверхности; окисление серы и двухвалентного
железа (в условиях невозможного их чисто химического окисления);
предотвращение отложения веществ новообразования на поверхно-
сти минерала; непосредственное участие в экзотермических реакци-
ях. Тионовые бактерии, образно говоря, запускают экзотермические
процессы окислительного выщелачивания пирита, без участия бак-
терий такие процессы не протекают. Следует отметить, что в кислой
среде чисто химическое окисление двухвалентного железа протекает
очень медленно. При воздействии же бактерий окисление двухва-
лентного железа до трехвалентного протекает со скоростью, пример-
но в 500 тыс. раз большей скорости чисто химического окисления.
Вместе с тем биохимические процессы, увеличивая реакционную
способность поверхности пирита и повышая температуру, интен-
сифицируют чисто химические процессы окислительного выщела-
3.8. Последствия жизнедеятельности микроорганизмов 179
чивания этого минерала, которые способствуют дальнейшему росту
температуры и выделению веществ новообразования (серы, серной
кислоты и соединений железа).
В естественных условиях самонагревающаяся порода представ-
ляет собой биохимический реактор, который затем при температуре
более 100° С становится чисто химическим реактором. В нем про-
текает автоклавный процесс окислительного выщелачивания пирита
и роста температуры породы. При дальнейшем нагревании пород эле-
ментная сера испаряется. Когда породы прогреются до 248 ... 261 ° С,
пары серы воспламеняются на воздухе. От пламени серы воспламе-
няется десорбирующийся из породы метан, самонагревание породы
переходит в ее возгорание. При температуре горения около 300°С
и более из углей и углеглинистых пород выделяется большое коли-
чество весьма опасных и вредных веществ.
Последствия жизнедеятельности микроорганизмов
в пиритсодержащих средах
В грунтах, содержащих значительное количество пирита и дру-
гих соединений серы, в результате окислительной деятельности ти-
оновых бактерий [17, 66] могут образовываться агрессивные кис-
лотные среды. Например, при строительстве одного из участков
Киевского метрополитена, в результате деятельности ацидофиль-
ных тионовых бактерий, величина pH среды резко снизилась с 7
до 1... 0,5 и началась сильная коррозия болтовых креплений. Про-
цесс коррозии протекал весьма активно и за три-четыре месяца
площадь поперечного сечения стальных болтов, используемых при
строительстве метрополитена, в ряде случаев была скорродирована
до 40 % [9].
180
Глава 3
Лабораторные и натурные исследования подтвердили, что при-
чиной создания агрессивной среды в харьковских отложениях Па-
леогена при использовании кессонного метода проходки являются
тионовые бактерии, использующие в качестве источника энергии ди-
сульфид железа в форме пирита/ кбторый содержится в песке этих
отложений, а также закисное железо, которое накопилось в процессе
окисления пирита.
Окисление закисного железа до окисного бактериями Т. ferroo-
xidans протекает по реакции
2FeSO4 + ^/2^2 + H2SO4'—> Рег(5О4)з + Н2О.
Снижение pH обусловлено реакцией гидролиза окисного железа
до гидрата окиси железа и серной кислоты:
2Fe2(SO4)3 + 6Н2О 2Fe(OH)3 + 3H2SO4.
и превращения, в условиях наличия энергетического материала и по-
вышенной аэрации, безобидной нейтральной среды в агрессивную.
Глава 4
сульфатвосстанавливающих бактерий
и химических реагентов, используемых
в нефтедобыче
4.1. Влияние химических реагентов на жизнедеятельность
СВБ
,г
В настоящее время в промысловой практике задействован до-
вольно широкий ассортимент химических реагентов, используемых
на различных этапах технологического процесса добычи нефти.
На некоторых стадиях процесса одновременно применяют до 5-6 раз-
личных по функциональному назначению и составу химических ре-
агентов. Комплексное действие механически соединенных реаген-
тов может оказаться непредсказуемым не только по отношению друг
к другу, но и к транспортируемой среде и нефтепромысловому обо-
рудованию.
Исследованиями, проведенными в НПО «Союзнефтеотдача»,
установлено, что химические реагенты, взаимодействующие с СВБ,
усиливают или снижают количество вырабатываемого ими сероводо-
рода, а в ряде случаев остаются инертными и не влияют на них [131].
182
Глава 4
В связи с этим представляется чрезвычайно важным установление
степени влияния применяемых на месторождениях химических реа-
гентов на жизнедеятельность СВБ и продуцирование ими сероводо-
рода.
Всемногообразие химических реагентов, задействованных в тех-
нологической системе добычи, транспорта и подготовки нефти, в за-
висимости от их функционального назначения и способа примене-
ния, может быть подразделено на шесть основных групп:
1. Ингибиторы солеотложения.
2. Ингибиторы асфальтосмолопарафиновых отложений.
3. Растворители асфальтосмолопарафиновых отложений.
4. Деэмульгаторы и эмульгаторы.
5. Ингибиторы коррозии.
6. Полимеры и ПАВ различного назначения.
Таблица 4.1. Влияние ингибиторов парафиноотложений на рост СВБ [132]
Исследуемый реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатредукцию, %
50 +3,3
СНПХ-7401М 100 +0,8
200 -3,6
50 +2,4
СНПХ-7212 100 +5,4
200 +8,1
СНПХ-7215 100 0
СНПХ-7401 100 0
СНПХ-7410 100 0
4.1. Влияние химических реагентов на СВБ
183
Таблица 4.2. Влияние растворителей парафиноотложений на рост СВБ
Исследуемый реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатредукцию, %
Легкая пиролизная смола 5000...20000 -100
Гексановая фракция 5000 -39,1
Нефрас 200 + 10
Бутил-бензольная
1000... 5000 -21,4... 100
фракция
100- +8,0
Бензиновая смесь -
5000...20000 -4,6
500 5,4
Метилметановая фракция 1000
17,3
(ММФ)
2000 33,4
500 4,0
Диметилдиоксан (ДМД) 1000 6,7
2000 23,9
500 18,7
Масло зеленое 1000 34,6
2000 93,3
Оксоль 500 3,9
(спирты диоксановые) 1000 12,2
2000 12,2
500 22,7
Пирановая фракция (ПФ) 1000 25,3
2000 71,9
184
Глава 4
Результаты исследований влияния химических реагентов на жиз-
недеятельность СВБ, выделенных из промысловых сред месторожде-
ний Удмуртии, приведены в табл. 4.1^4.5. За показатель жизнеде-
ятельности микроорганизмов принята способность СВБ продуциро-
пл 1 г> ссрмоидирид,. cpiljyCl vГпмулприваппи) эпал
подавление жизнедеятельности СВБ.
Влияние ингибиторов парафиноотложений на продуцирование
микроорганизмами сероводорода показано в табл. 4.1
Влияние растворителей асфальтосмолопарафиновых отложений
на жизнедеятельность СВБ отражено в табл. 4.2.
Таблица 4.3. Влияние ингибиторов солеотложения на рост СВБ
Исследуемый реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатредукцию, %
ДПФ 20 500 -6 -100
ПАФ-13А 50.. .200 0
Инкредол 50... 200 2000 +8 -25
СНПХ-5301 10. 2000. ..50 ..4000 + 15 -60... 100
50 -65
ОЭДФ 100 -100
200 -100
ИСБ-1 50 ... 200 2000 +10 -10
ФТЭА 50.. .200 0
4.1. Влияние химических реагентов на СВБ
185
Влияние ингибиторов солеотложений на продуцирование микро-
организмами сероводорода представлено в табл. 4.3.
Влияние деэмульгаторов и эмульгаторов на продуцирование се-
роводорода СВБ приведено в табл. 4.4.
Таблица 4.4. Влияние деэмульгаторов и эмульгаторов на рост СВБ
Исследуемый реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатредукцию, %
Дипроксамин 157-65М 500 1000 2000 + 10 -2,6 -10,1
ЭС-2 100 -100
Прогалит ДМ 43/43* 30 -11
Прогалит ГМ 20/40* 30 -12
Сепарол WF-34* 30 -13
Сепарол WF-41* 30 -19
Диссолван 4411 200 0
R-11 200 0
Прогалит ДЕМ 34/68* 30 +8
Х-2647 30 + 14
НОЕ 1877-4* 30 + 14
Сепарол 25 30 + 19
Прохинор ЖР-77 30 +21
Доуфакс 5 30 +27
Прогалит ДЕМ 15/100 30 +27
* — по данным [131]
186
Глава 4
Результаты исследования влияния ингибиторов коррозии на про-
дуцирование микроорганизмами сероводорода сведены в табл. 4.5.
Степень влияния ингибиторов коррозии, исследованных при
концентрации 100 мг/л, на характер продуцирования микроорганиз-
Реагенты
Рис. 4.1. Влияние ингибиторов коррозии на жизнедеятельность СВБ [6]: 1 —
Икар-1; 2 — ИКБ-4В; 3 — Korrexit 7798; 4 — Виско-938; 5 — Север-1; 6 —
Урал-1; 7 - СНПХ-6003; 8 - Урал-1М; 9 - Тарин; 10 - СК-378; 11 - Т-80
Полученные данные* свидетельствуют о существующей воз-
можности стимулирования образования сероводорода в нефтепро-
мысловых водах систем сбора, подготовки нефти и поддержания
пластового давления некоторыми химическими реагентами. При-
менение традиционных ингибиторов для снижения сероводородной
коррозии может оказаться недостаточно эффективным из-за уча-
стия самих ингибиторов в процессах биокоррозии. Целесообраз-
но в каждом конкретном случае проверять наличие в нефтепро-
4.1. Влияние химических реагентов на СВБ
187
Таблица 4.5. Влияние ингибиторов коррозии на рост СВБ
Исследуемый реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатредукцию, %
10 0
20 ^2,0...2,4 --
Нефтехим-101 ' ' 30 +3,7
50 +3,7... 5,7
100 +6,1 ...7,2
Север-1 50 ...4000 -8,3 ... 100
50 +50
100 +25
СНПХ-6011 200 + 10
500 -0,25
1000...2000 -0,3
10 0... - 1,1
20 0
СНПХ-6014 30 -0,4...+ 2,0
50 -1,3... 9,2
100 0... - 11,8
50 -10,3
СНПХ-6311
100 -11,5
200 -50
ЖСМ-1 500 -96
1000 -98
Каталин 50...100 -53,7... 100
Норуст А-23/Д 200...400 -3... 98
150 -21,1
НИИФОХ-3
500 -95,4
188
Глава 4
мысловых трубопроводах и оборудовании микроорганизмов, способ-
ствующих усилению коррозионных процессов, и оценивать влия-
ние на них химических реагентов, применяемых при добыче неф-
ти. Предпочтение должно быть отдано реагенту, не оказывающе-
му стимулирующего действия на бактерии. В пртивном случае"
необходимо всю транспортную систему подвергать бактерицидной
обработке для полного подавления жизнедеятельности микроорга-
низмов.
Проблему активизации СВБ в призабойной зоне и пласте следует,
рассматривать применительно к конкретным нефтяным месторожде-
ниям, поскольку влияние реагентов нЬ накопительные культуры СВБ,
выделенных из нефтепромысловых вод различных нефтяных площа-
дей, различно. Результаты влияния некоторых реагентов на жизнеде-
ятельность СВБ, выделенных из промысловых сред Талинского, Пав-
ловского и Кокуйского месторождений [132], рассмотрены в табл. 4.6
и табл. 4.7. Для сопоставимости результатов параллельно исследова-
ли влияние этих реагентов и на музейную культуру СВБ ВКМВ-1388,
принятую в качестве эталона.
Экспериментальные данные свидетельствуют и о том, что ис-
следованные накопительные культуры СВБ обладают более высокой
активностью, чем музейные. На полной питательной среде, наиболее
благоприятной для развития СВБ, музейная культура продуцирует
в среднем 700 мг/л сероводорода, а накопительные культуры Та-
линского и Павловского месторождений до 755 мг/л, Кокуйского —
853 мг/л.
Неоднозначность реакций бактерий различных месторождений
на химические реагенты обусловлена видовой специфичностью куль-
тур и возникает в результате адаптации бактерий к используемому хи-
4.1. Влияние химических реагентов на СВБ
189
Таблица 4.6. Влияние химических реагентов на музейную и накопительную
культуру СВБ Талинского месторождения
Химический Концентрация Степень влияния реагента на сульфатредукцию, %
реагент реагента, мг/л СВБ Талинского месторождения Музейная ВКМВ-1388
10 +0,4 +0,6
20 +2,2 + 12,4
Прогалит Н 20/40 30 +5,3 +16,8
50 + 13,1 +20,4
100 +11,2 +20,4
10 +12,6 +2,1
20 +18,5 +5,3
Дипроксамин 157-65М 30 +25,1 +7,0
50 +26,4 +8,2
100 +26,4 +8,2
1000 +4,9 -3,4
3000 -5,7 -6,2
КМЦ 5000 -9,7 -13,9
7000 -12,3 -15,2
10000 -15,4 -18,5
50 -1,9 -4,7
100 -3,7 -5,0
Сульфонол 500 -6,2 -5,1
1000 -8,2 -4,7
10000 -7,6 -7,0
50000 -100,0 -100,0
190
Глава 4
Продолжение табл. 4.6
Химический реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатредукцию, %
СВБ Талинского Музейная
месторождения ВКМВ-1388
25 +7,8 +13,0
50 +24,3 +27,0
75 + 11,3 +15,0
СНПХ-1002М * 100 + 10,4 + 13,0
200 ' +10,0 -92,0
450 +1,2 -100,0
500 -92,4 -100,0
1000 -100,0 -100,0
мическому продукту. Адаптация микроорганизмов зависит от вида,
технологического режима и продолжительности применения реаген-
та на нефтяном промысле.
Особо следует обратить внимание на использование бакте-
рицида СНПХ-1002М. Химический продукт СНПХ-1002М имеет
некоторые особенности. В области низких концентраций поряд-
ка 25... 200 мг/л он стимулирует сульфатредукцию накопитель-
ной культуры в среднем на 10 ... 24 %. Подавление сульфатредукции
на 100% достигается при дозировке реагента в концентрации бо-
лее 1000 мг/л обрабатываемой среды. Требуется строгое соблюдение
технологии применения бактерицида для избежания стимулирования
сульфатредукции при низких его концентрациях в результате разбав-
ления в продуктивном пласте.
Таблица 4.7. Влияние химических реагентов на музейную и накопительную культуру СВБ Кокуйского
и Павловского месторождений
Химический реагент Концентрация реагента, мг/л Степень влияния реагента на сульфатре,1укцию, %
СВБ Кокуйского месторождения СВБ Павловского месторождения Музейная ВКМВ-1388
25 +1,5 +1,1 +1,6
50 +3,2 +3,4 +3,1
75 +2,8 +1,9 +3,5
СНПХ-7401 М 100 + 1,5 0 +6,0
150 0 -0,8 -29,2
200 -6,3 ' -0,9 -j -59,5
25 -0,5 > +1’3 +1,2
50 +2,3 +2,4 +2,4
75 +5,0 +5,3 +4,9
СНПХ-7212 100 +5,0 +5,8 +7,4
150 +6,2 +7,0 +9,0
200 +6,7 +9,4 + 14,3
10 +3,5 +1,7 +2,1
20 +3,8 +3,7 +5,3
Дипроксамин 30 +2,4 +5,6 +7,0
157-65 М 50 +0,6 +5,6 +8,2
100 +0Д + з,3 +8,2
4.1. Влияние химических реагентов на СВБ
192
Глава 4
4.2. Влияние неионогенных поверхностно-активных
веществ на жизнедеятельность СВБ
В связи с широким применением неионогенных поверхностно-
активных веществ (НПАВ) во многих технологических процессах
нефтедобычи огромное значение приобретает необходимость уста-
новления степени влияния этих веществ на микробное сообщество
нефтяных месторождений, в частности на СВБ, которым принадле-
жит доминирующая роль среди микроорганизмов, инициирующих
процесс коррозии нефтепромыслового оборудования [46].
В литературе накоплен обширный материал по исследованию
влияния НПАВ на жизнедеятельность микроорганизмов. В ряде ра-
бот отмечают подавляющее воздействие НПАВ на физиологиче-
скую активность клеток бактерий [119]. Имеются сведения и о том,
что в присутствии НПАВ происходит дезорганизация структуры
бактериальных клеток, изменение проницаемости клеточных мем-
бран [76, 120]. Некоторые авторы допускают возможность стиму-
лирующего влияния НПАВ на сульфатредуцирующую способность
СВБ [129, 133]. Однако в этих работах авторы ограничиваются опре-
делением одного из физиологических параметров состояния клеток
СВБ.
Для обоснованного суждения о влиянии химических реагентов
на жизнедеятельность СВБ авторами работы [46] подробно были ис-
следованы некоторые физиологические и биохимические парамет-
ры развития СВБ, к числу которых отнесены объемы накопления
биомассы (белка) и продуктов метаболизма. Параллельно данным
исследованиям проведено'сравнительное электронно-микроскопиче-
ское изучение ультраструктуры бактериальных клеток.
4.2. Влияние неионогенных веществ на СВБ 193
В ходе исследований были использованы следующие виды
НПАВ: дипроксамин 157-65 М (блоксополимер этилен- и пропилен-
оксидов на основе этиленди амина), ОП-10 (алкилфенол на основе
тетрамеров пропилена), неонол АФ-9-12 (оксиэтилированный моно-
алкилфенол на основе "триммеров" гТрбпйлена-изинонена). Установ-
лено, что накопительная культура СВБ может расти в присутствии
всех испытываемых ПАВ. Количество белка в средах с НПАВ оста-
ется практически на одном уровне с контрольными пробами. Иссле-
дованные реагенты не оказывают влияния на накопление одного из
продуктов метаболизма — сероводород. Изменение содержания белка
(биомассы) и сероводорода при росте СВБ в присутствии дипрокса-
мина 157-65 М отмечено в табл. 4.8.
Таблица 4.8. Влияние дипроксамина 157-65 М на содержание белка и серо-
водорода при росте СВБ
Концентрация дипроксамина 157, мг/л Содержание
Белка, мкг/мл Сероводорода, мг/л
50 96 353
100 92 345
500 94 338
1000 92 345
5000 92 338
Без реагента 96 360
Результаты испытания НПАВ, в качестве реагентов подавляю-
щих жизнедеятельность СВБ, помещены в табл. 4.9.
194
Глава 4
Таблица 4.9. Бактерицидная активность НПАВ [108]
Наименование НПАВ Эффективность НПАВ по подавлению СВБ при концентрации, мг/л
100 500 1000 5000
Неонол АФ-9-12 + + + +
ОП-Ю + + + +
Дипроксамин 157-65 М + + + +
Примечание: «+» — означает наличие роста бактерий. При росте СВБ
в среде накапливается до 100... 150 м^/л сероводорода
Таким образом, было установлено, что НПАВ непосредственно
не оказывают стимулирующего влияния на рост и развитие СВБ и не
обладают бактерицидным действием.
Электронно-микроскопические исследования [108] показали,
что ультраструктура клеток СВБ, бывших в контакте с НПАВ, су-
щественно отличается от контрольных.
Контуры стенок бактериальных клеток из контрольной серии
опытов четкие, цитоплазматическая мембрана выявляется как од-
нородное образование, плотно прилегающее к клеточной стенке.
Во внутренней полости клеток отчетливо выявлены структурные эле-
менты, которые представлены в виде отдельных компонентов, огра-
ниченных мембранной оболочкой.
Под действием НПАВ в структуре клеток обнаружены значи-
тельные изменения: их стенки разрыхляются, утрачивается контур-
ность, внутренний электронно-плотный слой едва прослеживается,
изменяется структура цитоплазмы, которая становится глыбчатой,
4.2. Влияние неионогенных веществ на СВБ
195
ядерное вещество не определяется, местами цитоплазма отделяется
от клеточной стенки.
Таким образом, проведенные электронно-микроскопические ис-
следования показали, что под действием испытанных НПАВ про-
исходит повреждение клеточных'стенок бактерий. Основным"в-мхг-
ханизме действия НПАВ на структуру клеток является растворение
липидов, большая часть которых входит в состав клеточных стенок
бактерий. Нарушение клеточных стенок приводит к увеличению их
проницаемости, что в свою очередь обеспечивает снижение устойчи-
вости микроорганизмов к действию бактерицидов.
Выше отмечалось, что НПАВ, обладая специфическим действи-
ем на стенки клеток СВБ, способствуют повышению проницаемости
бактериальных клеток, обеспечивая тем самым снижение их устой-
чивости к бактерицидам. Исследование этого явления подробно опи-
сано в [108].
Методология эксперимента заключалась в следующем. Модель
пластовой воды заражали культурой СВБ, выделенной из нефтепро-
мысловых вод Арланского месторождения. Часть воды обрабатывали
НПАВ различной концентрации в диапазоне 80... 250 мг/л и выдер-
живали в течение 24 часов. Другая часть воды служила в качестве
контрольной.
В выдержанные пробы дозировали исследуемые бактерициды,
СНПХ-1002, СНПХ-1003, глутаровый альдегид (25% водный рас-
твор фирмы «Reanal») и выдерживали при комнатной температуре.
Через 6, 12, 24 часа контакта СВБ с бактерицидом отбирали часть
пробы и помещали в питательную среду Постгейта В для выявления
количества жизнеспособных клеток стандартным методом предель-
ных разведений, при этом определяли минимальную подавляющую
196
Глава 4
концентрацию (МПК), при которой достигалось прекращение роста
СВБ. В табл. 4.10 показаны результаты исследований выявленного
количества жизнеспособных клеток СВБ после воздействия глута-
рового альдегида на СВБ, предварительно обработанных неонолом
АФ-9-Ь2"концентрацией 100 мг/л в течение 24 часов"
Полная гибель клеток, не имевших предварительного контак-
та с неонолом, наступает при концентрации бактерицида 150 мг/л,
а клеток, имевших контакт с неонолом, уже при 20 мг/л.
Следует отметить, что после контакта с неонолом некоторая
часть бактерий становится нежизнеспособной. В связи с этим ко-
I
личество клеток в контрольном опыте с неонолом уменьшилось
с 105 кл/мл до 103 кл/мл. Это объясняется тем, что под действи-
ем НПАВ, обладающих повреждающим эффектом, стенки клеток
наиболее чувствительных бактерий (любая популяция бактерий не
гомогенна по составу) лизируются до степени, вызывающей их ги-
бель. Значительная же часть популяции микроорганизмов остается
жизнеспособной и при создании подходящих условий, например при
последующем пересеве в питательную среду, активно развивается.
Те же закономерности наблюдаются и при воздействии других бак-
терицидов на клетки, обработанные и не обработанные НПАВ. Сни-
жение устойчивости СВБ к бактерицидам и повышение активности
бактерицидов отмечено во всех случаях, когда клетки обрабатывали
НПАВ [108].
В табл. 4.11 освещены сводные данные о величинах минималь-
но подавляющей концентрации (МПК) бактерицидов по отношению
к СВБ, имевших контакт с НПАВ с концентрацией 100 г/л.
Таким образом, совокупность полученных данных свидетель-
ствует о том, что снижение величин МПК бактерицидов по отноше-
4.2. Влияние неионогенных веществ на СВБ
197
Таблица 4.10. Количество жизнеспособных клеток СВБ после воздействия
бактерицидом
Концентрация Время контакта Количество жизнеспособных клеток СВБ, кл/мл
бактерицида, мг/л СВБ с бакте- рицидом, час не имевших контакт с неонолом имевших контакт с неонолом
20 6 104 102
12 ю3 10
24 102 0
25 6 104 10
12 103 0
24 102 0
30 6 103 10
12 ю2 0
24 10 0
50 6 ю4 10
12 103 0
24 ю2 0
100 6 103 0
12 ю2 0
24 10 0
150 6 103 0
12 ю2 0
24 10 0
Контрольный 6 ю5 103
12 ю5 103
24 ю5 103
198
Глава 4
Таблица 4.11. Минимальная подавляющая концентрация, мг/л, бактерици-
дов по отношению к СВБ, предварительно обработанных НПАВ
Минимальная подавляющая концентрация бактерицидов, мг/л
бактерицида Без контакта с НПАВ После контакта СВБ с НПАВ
Неонол АФ-9-12 оп-ю Дипроксамин
Глутаровый альдегид 150 20 40 45
СНПХ-1002 700 100 200 220
СНПХ-1003 200 70 100 100
нию к СВБ, имевших предварительный контакт с НПАВ, является
результатом воздействия последних.
Надо полагать, что повреждение мембранного барьера клеток
лежит в основе эффекта НПАВ как веществ, усиливающих дей-
ствие бактерицидов. По-видимому, нарушения целостности клеточ-
ной стенки бактерий способствуют дальнейшему повышению прони-
цаемости мембран клеток, что в свою очередь облегчает проникно-
вение в микробную клетку бактерицидов, т. е. усиливается действие
последних. Следовательно, предварительная обработка бактериаль-
ных клеток НПАВ не только позволяет повысить эффективность по-
следующего действия бактерицидов, но, что особенно важно, обес-
печивает достижение требуемого технологического эффекта при ми-
нимальной концентрации бактерицида и сроков полного подавления
роста бактерий. Информация такого плана важна и с экологических
позиций. Интенсивное применение для подавления СВБ бактерици-
4.3. Влияние полимеров на жизнедеятельность СВБ
199
дов, являющихся высокоактивными соединениями общетоксическо-
го действия, расширяет вероятность загрязнения окружающей среды
и прежде всего подземных вод и поверхностных водоемов, создавая
реальные предпосылки неблагоприятного воздействия на экосистему
района месторождения. ~Нет необходимости доказывать, чте-одной-
из важнейших проблем, требующих своего решения при разработ-
ке и осуществлении технологического процесса, является обеспече-
ние высокой эффективности бактерицидов по отношению к СВБ при
сокращении объемов их применения, что позволяет до минимума
свести отрицательное воздействие этих реагентов на окружающую
среду [108].
Данные этих исследований могут быть положены в основу но-
вых технологических разработок, направленных на подавление роста
и развития СВБ в нефтепромысловых средах.
4.3. Влияние полимеров на жизнедеятельность СВБ
Взаимодействие полиакриламида с аборигенными микроорга-
низмами, обитающими в пласте или привнесенными с закачиваемой
водой, в ряде случаев вызывает нежелательные последствия. Так,
например, на нефтяном месторождении в Техасе после закачивания
в пласт воды, содержащей полимерные субстраты, скорость коррозии
промыслового оборудования резко возросла [148]. Микробиологиче-
ские исследования показали, что коррозия обусловлена активизацией
роста СВБ, расщепляющих полимер. В результате трубы забивались
отложениями, состоящими из микробной биомассы, слизи, сульфи-
дов и капелек нефти. Восстановить нормальную работу оборудования
удалось путем введения в пласт двух биоцидных соединений [148].
200
Глава 4
В Удмуртии исследование влияния полимеров на жизнедеятель-
ность СВБ проводилось на четырех специально отобранных для этих
целей химических реагентах: полиакриламидах PDA-1041, DKS ORP
F-40 NT и полимерах DK-DRILL А-1 и DK-DRILL S-1 японской фир-
мы «Иточу», приготовленных на селективных средах Постгейта В.
В качестве посевного материала использовалась четырехсуточная на-
копительная культура, выделенная из пластовой воды Лиственского
месторождения.
Методика исследований. Приготовленные растворы полимеров
с концентрацией 0,025 вес.% разливали в пенициллиновые пузырьки
по 3 параллельные пробы. Для сравнения и контроля в 3 пузырька
помещали чистую питательную среду без добавления полимера. Со-
здание анаэробных условий в пузырьках достигалось за счет герме-
тизации, исключающей возможность нахождения в них воздушного
пространства.
В разлитую в пузырьки питательную среду с полимерами вводи-
ли шприцем по 0,3 мл культуры СВБ. Введенную культуру инкуби-
ровали в суховоздушном термостате 15 суток при температуре плюс
32° С.
Результаты влияния полимеров на жизнедеятельность СВБ каче-
ственно оценивали по появлению сульфида железа, количественно —
по объему выделенного сероводорода.
Полученные в ходе исследований данные позволили утверждать,
что наличие полимеров в приготовленной питательной среде практи-
чески не влияет на количество выработанного бактериями сероводо-
рода. Результаты данных исследований приведены в табл. 4.12.
Общеизвестно, что синтетические полимерные материалы, при-
меняющиеся в технологических процессах бурения, промысловой
4.3. Влияние полимеров на жизнедеятельность СВБ 201
Таблица 4.12. Влияние полимеров на количество вырабатываемого СВБ
сероводорода
Марка полимера Количество выработанного Величина отклонения, %
сероводорода, мг/л
Контрольная проба без полимера 385,5
PDA - 1041 381 -1,1
DKS ORP F - 40 NT 37G;3 -3,9
DK - DRILL A - 1 381,6 -1,0
DK - DRILL S - 1 400,6 +3,9
практике повышения нефтеотдачи пластов, подвержены механиче-
ской, окислительной и биологической деструкции [141]. Так, напри-
мер, установленная величина биодеструкции полиакриламида, ис-
пользовавшегося при полимерном заводнении на месторождении Ка-
ламкас, под действием биоциноза вод альбских горизонтов лежит
в пределах 10...20% от общей его массы [90, 91]. Проведенными
в институте ВНИИнефтеотдача исследованиями подтверждено [100],
что степень деструкции полиакриламида марки DK.S ORP F-40 NT
может достигать более высоких значений и находиться в более ши-
роком диапазоне, порядка 20... 80 %. Численные показатели величи-
ны механической и термоокислительной деструкции представлены
в табл. 4.13, а биологической деструкции — в табл. 4.14.
Степень механической и термоокислительной деструкции рас-
творов ПАА зависит от конструкции узла приготовления реагентов
и его технологических параметров работы. Воздействуя на эти два
202
Глава 4
Таблица 4.13. Механическая и термоокислительная деструкции полиакрил-
амида
Исследуемый вид Раствор ПАА Скрин-фактор Степень деструк-
Растворитель Концент- До испы- После ис-
деструкции рация, % тания пытания ции, %
Механическая Пресная вода 0,06 88 50 43,2
Минера- лизован- ная, г/л 83,5 0,06 69 16 76,8
166,8 0,03 47 26 44,7
Термо- окислительная 111,1 0,03 47 26 44,7
111,1 0,06 '—1 69 39 43,5
Таблица 4.14. Биологическая деструкция полиакриламида
Раствор ПАА Вязкость, мПа с Степень деструкции, %
Растворитель Концент- рация, % В начале опыта Через 30 суток
Минерализован- ная, 111,1 г/л 0,03 2,95 2,05 30,5
Водопроводная 0,01 1,46 1,05 28,1
параметра, можно регулировать величину деструкции, снижая ее или
повышая, в зависимости от конкретных условий.
Биологическая деструкция растворов ПАА является результа-
том жизнедеятельности микробного сообщества в промысловых во-
дах месторождений, разрабатываемых с поддержанием пластового
давления.
В промысловых водах Удмуртии обнаружен широкий спектр
микроорганизмов, среди которых превалируют сульфатвосстанавли-
4.3. Влияние полимеров на жизнедеятельность СВБ 203
вающие бактерии (СВБ), денитрифицирующие (ДНБ), углеводород-
окисляющие (УОБ) и тионовые бактерии. Комплексные лаборатор-
ные исследования влияния микроорганизмов на биологическую де-
струкцию ПАА проводились на бактериях, выделенных из попутно-
добываемых вод и культивированных в селективных питательных
средах Гильтая, Раймонда, Постгейта.
Оценка глубины биодеструкции произведена по следующим па-
раметрам:
— росту количества клеток бактерий;
< — появлению продуктов жизнедеятельности бактерий;
— изменению вязкости растворов ПАА;
— скрин-фактору, характеризующему вязко упругие свойства рас-
творов ПАА.
Все перечисленные параметры измерялись в начале и через
30 дней после экспозиции, необходимой для развития биопроцессов.
Величина деструкции рассчитывалась по изменению скрин-фактора
и вязкости растворов ПАА до и после экспозиции. Результаты иссле-
дований [90] биодеструкции 0,05 % раствора ПАА под воздействием
микрофлоры показаны в табл. 4.15.
Полученные значения указывают на незначительную величину
биодеструкции под влияние ДНБ и УОБ. Присутствие же бактерлй
СВБ усиливает процесс биодеструкции.
Следует отметить, что увеличение количества клеток СВБ в ис-
следуемой среде приводит к интенсификации процесса деструкции
ПАА и росту количества выделяемого ими сероводорода.
В промысловой практике наличие в попутно-добываемых водах
микроорганизмов одного какого-либо типа практически не отмече-
но. Обычно в коррозионных процессах участвуют бактерии многих
204
Глава 4
Таблица 4.15. Степень биодеструкции растворов ПАА под действием бак-
терий
Вид Количество клеток/мл ло Признак Величина биодеструкции,
бактерий и после опыта Ьиодеструкции %
ДНБ ю7/ю9 Наличие газа 2,6
УОБ 105/106 Помутнение среды 4,7
СВБ 102/102 Не обнаружено 2,9
1/10 Следы H2S 7,6
1/102 H2S 10,7
видов, связанных между собой сложными энергетическими и до-
норскими связями. Так, анаэробные условия в среде, содержащей
кислород, могут быть созданы деятельностью аэробных бактерий,
поглощающих кислород. Сульфатвосстанавливающие бактерии по-
чти всегда находятся в ассоциации с аэробными слизеобразующими
микроорганизмами, поскольку последние запасают питательные ве-
щества и создают для СВБ анаэробные условия.
Полагают, что чистые культуры СВБ не способны использовать
нефть в качестве источника углерода, но в комплексе с углеводород-
окисляющими бактериями процесс сульфатредукции протекает весь-
ма активно за счет усвоения СВБ, окисленных УОБ, простых орга-
нических соединений.
Исследование влияния ассоциированного сообщества клеток
бактерий ДНБ, УОБ и СВБ на процессы биодеструкции показало,
4.3. Влияние полимеров на жизнедеятельность СВБ
205
что их совместное присутствие в испытываемых средах увеличивает
степень биодеструкции ПАА [90, 91], табл. 4.16.
Таблица 4.16. Влияние микрофлоры на степень биодеструкции ПАА
Концент- рация ПАА, % Содержание микрмф,лоры, ~ клеток/мл, до и после испытания Степень биодеструкции, %
СВБ УОБ ДНБ
0,15 един/10 102/10 " 102/104 10
0,1 един/1О2 102/102 102/104 20
0,05 един/104 10/103 102/107 48
Анализ полученных данных позволяет сделать вывод о доми-
нирующей роли СВБ в процессах биодеструкции ПАА, причем ее
величину определяет в первую очередь концентрация СВБ в раство-
ре в конце экспозиции.
Влияние ПАА и температуры на жизнедеятельность СВБ
В связи с использованием вторичных термополимерных методов
повышения нефтеотдачи на ряде месторождений России и Удмуртии
(Мишкинское, Северо-Ижевское) вопрос о необходимости исследова-
ния поведения СВБ в условиях повышенной температуры и наличия
полиакриламида (ПАА) становится значимым, поскольку от его по-
нимания зависят в первую очередь показатели текущей нефтеотдачи,
управляемость процессами разработки месторождений и их экологи-
ческая безопасность.
206
Глава 4
Результаты исследований, проведенных в средах, содержащих
ПАА, на культурах СВБ, выделенных из попутно-добываемых вод
Северо-Ижевского месторождения Удмуртии, отражены в табл. 4.17.
Таблица 4.17. Количество сероводорода, выработанного СВБ Северо-Ижев-
ского месторождения
Температура нагрева, °C Количество сероводорода, мг/л вырабатываемого СВБ
в средах без ПАА в средах с ПАА
20 438,6 438,6
30 . 414,8' 430,0
60 414,8 433,7
75 279,9 326,8
90 116,7 162,2
Из приведенных в таблице результатов исследований видно, что
увеличение температуры в интервале 75 ... 90° С существенно вли-
яет на количество вырабатываемого СВБ сероводорода как в сре-
дах, содержащих полиакриламид, так и без него. Однако остаточное
содержание сероводорода в растворах с полиакриламидом выше во
всем диапазоне исследованных температур 30... 90° С. Изменение
температуры от 20 до 60° С практически не влияет на изменение
содержания сероводорода.
Полученные результаты показывают, что при нагреве СВБ
до температуры 90 градусов активность бактерий снижается и ко-
личество вырабатываемого ими сероводорода уменьшается, однако
полного подавления их жизнедеятельности не достигается.
4.3. Влияние полимеров на жизнедеятельность СВБ 207
Влияние СВБ на нитроцеллюлозу
В связи с использованием в нефтедобывающей промышленности
препаратов на основе целлюлозных материалов, понимание процес-
сов взаимодействия СВБ с этими материалами представляется необ-
ходимым.
Новейшие технологии переработки отходов промышленности
основаны на использовании каталитических способностей микро-
организмов. Например, нитроцеллюлоза (НЦ), входящая в состав
отходов ряда производств взрывоопасных веществ, лаков, пласт-
масс и др., с трудом поддается биоразрушению и длительное
время присутствует в окружающей среде. Устойчивость НЦ для
разложения целлюлолитическими микроорганизмами обусловлена
введением в структуру целлюлозы NOa-rpynn. Предварительная хи-
мическая обработка отходов, связанная с удалением азота из мо-
лекулы целлюлозы, является энергоемким и неэкологичным про-
цессом.
Представляется перспективным использование для утилизации
и переработки НЦ накопительных культур анаэробных сульфатвос-
станавливающих микроорганизмов. Все изученные виды сульфатре-
дуцирующих бактерий рода Desulfovibrio способны к трансформации
НЦ [125]. Эффективность процесса зависит от условий его проведе-
ния и максимальна при наличии углеродного и азотного питания для
бактерий. Бактерии содержат активную нитратредуктазу.
Использование СВБ обеспечивает снижение концентрации НЦ
за 14 дней от 5 до 9 %; удельная скорость процесса при этом состав-
ляет 46... 73 мг НЦ на 1 мг белка, рис. 4.2. Особенно эффективен
оказался штамм Desulfovibrio desulfuricans 1388.
208
Глава 4
Время, сут
Рис. 4.2. Кривые роста D. desulfuricans в среде Постгейта Б (1) и в той же
среде с добавлением нитроцеллюлозы (2)
Заметное снижение концентрации НЦ в среде происходит на
восьмые сутки культивирования бактерий, через 14 дней ее убыль
достигает 10%. Процентное содержание азота в оставшейся нит-
роцеллюлозе снижается на 13%. При трансформации НЦ клетками
D. desulfuricans наблюдают появление в культуральной среде ионов
нитратов. Их количество достигает максимума значения на восьмые
сутки.
Таким образом, снижение концентрации НЦ свидетельствует
о том, что D. desulfuricans обладает биохимическим потенциалом для
ведения процесса трансформации нитроцеллюлозы. Использование
для микробной денитрификации НЦ сульфатредуцирующих бакте-
рий может оказаться перспективным для создания биотехнологии
минерализации НЦ.
4.4. Адаптация СВБ к полиакриламидам
209
4.4. Адаптация СВБ к полиакриламидам
Ранее проведенными исследованиями показано, что бактерии
СВБ могут адаптироваться к какому-либо химическому реагенту.
R связи с этим и на основании того, что объемы вырабатываемо-
го бактериями сероводорода в средах, содержащих различные мар-
ки полимеров, получены примерно одинаковые, все дальнейшие ис-
следования по выявлению адаптационных свойств микроорганизмов
проведены на одном широко используемом в практике полимерного
заводнения полиакриламиде марки PDA-1041.
Степень адаптации бактерий к исследуемому реагенту оцени-
валась по результатам повторного пересева культуры СВБ. Для это-
го, после первой 15-суточной инкубации микроорганизмов в среде
Постгейта В с добавлением полимера PDA-1041, выросшую куль-
туру переносили в аналогично приготовленные растворы PDA-1041
и культивировали еще 15 суток при температуре 32° С. В первой
и второй сериях опытов определение содержания сероводорода про-
изводили йодометрическим титрованием. Результаты замеров серо-
водорода сведены в табл. 4.18.
В первой серии экспериментов бактерии СВБ испытывают неко-
торое угнетение со стороны полиакриламида. Затем происходит адап-
тация микроорганизмов и они начинают расщеплять ПАА и исполь-
зовать его в своей жизнедеятельности.
Принимая во внимание, что количество вырабатываемого се-
роводорода в средах, содержащих полимеры PDA-1041, DKS ORP
F-40 NT, DK-DRILL S-1 и DK-DRILL A-l, и в контрольном опыте
было приблизительно одинаковое (табл. 4.12), можно предположить,
что и адаптация СВБ ко всем перечисленным реагентам будет тоже
хорошая.
210
Глава 4
Таблица 4.18. Влияние PDA-1041 на количество вырабатываемого СВБ се-
роводорода
Марка Концентра- Количество выработанного Степень влияния
полимера ция, вес. % сероводорода, мг/л реагента на суль- фатредукцию, %
PDA-1041 Первый посев 0,0003 390,0 +1,1
0,001 382,1 -0,9
0,0025 381,0 -1,1
0,005 ' 378,7 -1,7
0,01 359,9 -6,6
PDA-1041 Второй посев 0,0003 547,0 +42
0,001 972,0 +115,2
0,005 1294,0 +236
0,01 1407,0 +265
Таким образом, проведенными исследованиями установлено,
что полимеры типа полиакриламида стимулируют жизнедеятель-
ность СВБ. В связи с этим борьба с ними возможна только с приме-
нением бактерицидов.
Согласно техническим условиям в области повышенных тем-
ператур, высоким бактерицидным эффектом, хорошей стойкостью
к термоокислительному разложению обладает биоцид ЛПЭ-11, кото-
рый и может быть рекомендован для борьбы с СВБ в условиях термо-
и термополимерного заводнения.
4.4. Адаптация СВБ к полиакриламидам
211
Бактерицид марки ЛПЭ-11 представляет собой продукт взаимо-
действия гексаметилентетрамина с хлорпроизводными ненасыщен-
ных углеводородов и производится на основе уротропиновых осно-
ваний.
ЛПЭ-11 способен снижать механическую, термоокислительную
и биологическую деструкцию ПАА. Степень снижения величины де-
струкции ПАА в присутствии биоцида отмечена в табл. 4.19.
Лабораторные исследования эффективности бактерицида ЛПЭ-
11 на культурах СВБ, выделенных из нефтепромысловых сред место-
рождений Удмуртии, показали, что полное подавление жизнедеятель-
ности СВБ может быть достигнуто при концентрациях бактерици-
да, равных 150... 500 г/т воды. Установлено также, что содержание
ПАА в промысловых водах не оказывает влияния на эффективность
действия реагента ЛПЭ-11.
Результаты оценки эффективности действия ЛПЭ-11 по подав-
лению жизнедеятельности СВБ помещены в табл. 4.20.
Адаптация СВБ к бактерициду ЛПЭ-11
Стабилизацию растворов полиакриламида от биологической де-
струкции, путем введения в них бактерицида ЛПЭ-11 на основе уро-
тропиновых соединений, осуществляют преимущественно на место-
рождениях, пластовые флюиды которых уже достаточно заражены
микроорганизмами.
Технологический процесс стабилизации полиакриламида осу-
ществляют путем непрерывной дозированной подачи бактерицида
ЛПЭ-11 в состоянии поставки с массовой долей 0,02... 0,04 % на ко-
Таблица 4.19. Влияние ЛПЭ-11 на снижение деструкции ПАА
Вид деструкции Исследуемый раствор ПАА Модификация бактерицида, % Концентрация бактерицида, % Степень снижения деструкции, раз
Растворитель Концентрация, %
Механи- ческая Пресная вода 0,06 ЛПЭ-11В 0,02 2,1
Минерализо- ванная — 83,5 г/л 0,06 ЛПЭ-11 0,02 1,18
0,06 ЛПЭ-11 0,04 1,27
Минерализо- ванная — 166,8 г/л — 111,1 г/л - 111,1 г/л — 111,1 г/л - 111,1 г/л — 111,1 г/л 0,03 ЛПЭ-11В 0,02 1,37
Термоокис- лительная 0,03 ЛПЭ-11 0,02 1,26
0,06 ЛПЭ-11 0,02 1,55
0,06 ЛПЭ-11 0,04 2,05
Биологи- ческая 0,03 ЛПЭ-11 0,01 5,08
0,03 ЛПЭ-11В 0,01 5,08
212 Глава 4
4.4. Адаптация СВБ к полиакриламидам
213
•' Таблица 4.20. Эффективность ЛПЭ-11 по подавлению жизнедеятельности
СВБ
4 А • Месторождение Эффективность ЛПЭ-11, %, при концентрации, г/т
50 150 500
!l Воды без ПАА
Мишкинское 100 100 100
Гремихинское 95 100 100
Прикамский участок 75 100 100
Воды, содержащие ПАА
Мишкинское 100 100 100
Гремихинское — 100 —
личество закачиваемой в нагнетательные скважины воды. Подачу
бактерицида осуществляют либо непосредственно на узле дозиро-
ванной подачи полимера одновременно с полиакриламидом, либо
до растворения полимера.
Основными критериями соблюдения технологического режима
являются поддержание заданной, с учетом конкретных условий, кон-
центрации бактерицида и обеспечение полного смешения реагента
с закачиваемым раствором полимера.
На Лиственском месторождении Удмуртии промышленные ис-
пытания бактерицида ЛПЭ-11 для предотвращения биодеструкции
полиакриламида и подавления жизнедеятельности СВБ проводились
начиная с конца 1993 года. Технология обработки была принята пре-
дельно простой и включала цикл непрерывного дозирования реагента
в поток смеси полимера с водой в концентрации 100 г/м3.
214
Глава 4
Для определения периода адаптации СВБ к реагенту были уста-
новлены реперные концентрации биоцида, при которых зафикси-
ровано начальное и полное подавление жизнедеятельности СВБ.
Необходимо отметить, что на момент исследования используемые
культуры СВБ уже в течение трех лет подвергались промыслово-
му воздействию полиакриламидом и бактерицидом ЛПЭ-11. Резуль-,
таты исследования эффективности бактерицида ЛПЭ-11 по подав-
лению жизнедеятельности культур СВБ, выделенных из промысло-
вых сред Лиственского месторождения в 1997 году, представлены
в табл. 4.21.
Таблица 4.21. Эффективность биоцида ЛПЭ-11 по подавлению жизнедея-
тельности культур СВБ Лиственского месторождения
Концентрация ЛПЭ-11, мг/л 50 100 250 500 750
Степень подавления СВБ, % 4 5,4 25,4 86,2 100
Характерно, что полное подавление жизнедеятельности культу-
ры СВБ Лиственского месторождения, отобранной в 1997 году, до-
стигнуто при очень высокой концентрации бактерицида — 750 мг/л,
тогда как в 1993 году для 100% подавления СВБ требовалось всего
100 мг/л [133].
Для предупреждения адаптации микроорганизмов к реаген-
там-бактерицидам необходима их периодическая замена на другие,
созданные на принципиально новой основе биоциды.
Для условий Лиственского месторождения было предложено,
а затем и исследовано несколько новых перспективных реагентов
с целью выявления из них наиболее эффективного. Результаты испы-
таний показаны в табл. 4.22.
4.4. Адаптация СВБ к полиакриламидам
215
Таблица 4.22. Степень подавления бактерицидами культуры СВБ Листвен-
ского месторождения
Реагент Степень подавления жизнедеятельности СВБ, %, при дозировке бактерицида, мг/л
50 100 ' 7250
ЛПЭ-11В 4,0 5,4 25,4
ЛПЭ-11У 28,3 86,2 100
СНПХ-1004 92,0 96,0 100
Korrexit-6350 94,8 97,4 100
МБ-1 97,4 100 100
KRU-169 93,6 100 100
SURFLO-6552 82,6 89,2 100
Все исследованные новые реагенты проявляют высокую ак-
тивность по подавлению СВБ Лиственского месторождения. Наи-
большую эффективность проявляют МБ-1, KRU-169, Korrexit-6350.
Из Российских реагентов высокую эффективность обеспечивает био-
цид СНПХ-1004. Данные реагенты могут быть рекомендованы в ка-
честве замены бактерицида ЛПЭ-11 для подавления сульфатвосста-
навливающих бактерий, вызывающих биодеструкцию ПАА на Лист-
венском месторождении.
Таким образом, в ходе проведенных исследований было уста-
новлено:
1) Полиакриламид в растворах подвержен механической, термо-
окислительной и биологической деструкции.
2) Биологическую деструкцию вызывают углеводородокисляющие,
денитрифицирующие и особенно сульфатвосстанавливающие
бактерии.
216 Глава 4
3) Бактерии СВБ хорошо адаптируются к ПАА, а ПАА стимулирует
их жизнедеятельность.
4) Биоциды снижают все виды деструкции ПАА и подавляют жиз-
недеятельность СВБ.
F
Ь*-4
Глава 5
Методологические подходы
к исследованиям, связанным
с микроорганизмами
5.1. Оценка зараженности нефтепромысловых сред
микроорганизмами
Согласно [77, 151] известно 6 способов тестирования промысло-
вых сред на присутствие СВБ, три из которых основаны на методах
культивирования, а три — на прямом определении наличия СВБ.
Способ, оговоренный документом RP-38 Американского нефтя-
ного института (АНИ), предполагает использовать лактат в качестве
среды для культивирования СВБ. В культивационную среду в каче-
стве образца вносят определенное количество рабочей среды, в ко-
торой могут содержаться микроорганизмы. На погруженном в лактат
образце в случае присутствия СВБ происходит восстановление суль-
фата до сульфида, который реагирует с железом, находящимся в рас-
творе, образуя темное сульфидное железо. В этом случае потемнение
раствора после 28 сут испытаний указывает на наличие СВБ. При
этом считают, что для потемнения раствора достаточно присутствие
одного микроорганизма. Для того чтобы определить количество ми-
кроорганизмов в растворе, испытание проводят в 10 —12 сосудах. Ес-
218
Глава 5
ли потемнение обнаруживается в двух сосудах, принято считать, что
в наличии имеется 10 микроорганизмов, в трех сосудах — 100 и т. д.
Таким образом, потемнение в четырех сосудах дает основание
считать, что в исследуемой пробе присутствует 103 ... 104 микроор-
ганизмов на 1 мл.
Аналогичные испытания проводят в той же среде с добавлением
сульфита натрия для связывания кислорода. В этом случае количе-
ство СВБ характеризуется скоростью, с которой возникает потем-
нение. Трубку с испытываемой средой и среду для культивирования
СВБ помещают в сосуд, заполненный мягким агаром. После добавле-
ния таблетки, образующей СО2, который способствует вытеснению
воздуха, сосуд закупоривают на 5 сут, после чего в течение одного
дня проверяют интенсивность потемнения.
Третий метод, основанный на культивировании бактерий, пред-
полагает использование нескольких трубок, помещенных в расплав
агара, при этом культивируемая среда располагается в данном слу-
чае на дне трубок. При использовании данного метода количество
трубок, в которых обнаруживается потемнение среды, указывает на
число колоний СВБ, приходящихся на 1 мл.
Для прямого определения количества СВБ используют три ме-
тода. Один из них позволяет определить общее число всех микро-
организмов путем замера фотометром результатов фотохимической
реакции.
Два других метода основаны на использовании флуоресцирую-
щих и окрашивающих добавок, которые также позволяют определить
количество СВБ прямым счетом.
Все рассмотренные методы определения количества СВБ могут
быть сравнены между собой.
5.1. Оценка зараженности нефтепромысловых сред 219
Критериями оценки пригодности того или иного метода считают
следующие характеристики:
— точность, соответствие условиям работы системы, относитель-
ная легкость или сложность использования;
— время, необходимое для получения результата;
— пригодность для лабораторных или промышленных исследова-
ний;
— имеющиеся ограничения в части„использования.
Оценки, полученные в соответствии с этими критериями [151],
указывают на следующее:
1. При культивировании СВБ обнаруживается меньшее количе-
ство микроорганизмов.
2. Культивирование в сосудах согласно спецификации API RP-38
лучше проводить в течение 28 сут. Это дает лучшие результаты, чем
при обычно применяемых сроках культивирования (14 или 21 сут).
3. Погружение в агар культивационных сред — способ наибо-
лее простой, что делает его доступным для использования в полевых
условиях. Недостаток этого метода — сложность сопоставления с ре-
зультатами других испытаний.
4. Использование мягкого или расплавленного агара не обеспе-
чивает достаточной чувствительности при малом количестве СВБ,
а при большом их количестве — точности оценки.
5. Определение количества СВБ по результатам фотохимической
реакции проводят в течение 1 ч. Однако этот метод применим только
для оценки общего количество микроорганизмов, так как выделить
отдельные СВБ не представляется возможным.
220
Глава 5
6. Применение флуоресцирующих добавок для определения ко-
личества СВБ требует от 2 до 3 ч, а также использования дорогого
специального микроскопа. При этом наличие в испытываемых об-
разцах взвешенных твердых частиц снижает точность результатов.
Этот способ применим для сред, содержащих до 104 микроорга-
низмов/мл.
7. Окрашивание — наиболее быстрый (15 мин) и простой способ
обнаружения и подсчета СВБ, который может быть применен в поле-
вых условиях и не требует применения лабораторного оборудования.
Его точность соответствует точности результатов, полученных при
культивировании СВБ в лактатной срёде, но ограничивается уровнем
103 кл/мл.
Ввиду того что ни один из рассмотренных методов не обеспе-
чивает высокой надежности при быстроте и доступности в промыш-
ленных условиях, рекомендуют применять их в сочетании, обеспе-
чивающем наибольшую достоверность.
Оценка зараженности нефтепромысловых сред
Места отбора проб
Пробы воды для микробиологического контроля и химического
анализа отбирают:
— из водозаборов всех источников водоснабжения;
— из нагнетательных скважин;
— из эксплуатационных скважин;
— в различных точках систем подготовки нефти и утилизации сточ-
ных вод.
5.1. Оценка зараженности нефтепромысловых сред
221
Отбор проб на водозаборах производят из нагнетательных тру-
бопроводов насосов.
Отбор проб из нагнетательных скважин производят при их са-
моизливе с периодичностью отбора проб через каждые 20... 30 м3.
Нагнетательные скважины, выбранные для контроля, должны соот-
ветствовать следующим требованиям:
— иметь избыточное буферное давление на устье при остановке
скважины;
— продолжительность закачки водьГ должна быть не менее 2 лет;
— схема обвязки и подсоединения скважины к кустовой насосной
станции должна позволять проводить исследования без опасно-
сти загрязнения окружающей среды;
— устье скважины должно быть оборудовано пробоотборным кра-
ном.
Эксплуатационные скважины, выбранные для контроля, должны
соответствовать следующим требованиям:
— гидродинамически должны быть связаны с контролируемыми
нагнетательными скважинами;
— массовая доля воды в добываемой нефти должна быть не менее
60%.
Пробы для контроля сточной воды отбирают:
— из резервуаров предварительного сброса;
— после очистных сооружений из всасывающих трубопроводов на-
сосов откачки воды;
— из всасывающих трубопроводов насосов кустовых насосных
станций.
222
Глава 5
При отборе проб из эксплуатационных скважин, магистральных
нефтепроводов или других систем, где вода не отделяется в виде
свободной фазы, эмульсию наливают в стерильную делительную во-
ронку и оставляют до отделения водного слоя. Сливают воду в сте-
рильный сосуд, быстро отбирают стерильным шприцем пробу воды
и вводят в склянку с питательной средой.
Для химического анализа воду отбирают в колбы объемом
500 см3. В каждой пробе воды определяют: pH, температуру, со-
держание сероводорода, сульфатов.
।
Обнаружение планктонной популяции бактерий
Сущность метода заключается в посеве определенного объема
анализируемой воды в питательные среды, разлитые в пеницилли-
новые флаконы, с последующим наблюдением за ростом изучаемых
бактерий и определением наиболее вероятного числа бактерий в 1 см3
воды.
При проведении микробиологических исследований нефтепро-
мысловых систем решающим фактором является время посева ото-
бранных проб на питательные среды. Сразу же после отбора проб
из системы начинаются структурные изменения сообщества бакте-
рий. Поэтому с целью улучшения качества проводимых исследований
и повышения точности полученных результатов необходимо прово-
дить посев отобранной пробы на месте ее отбора.
Обнаружение планктонной популяции бактерий производят
в следующей последовательности:
— пробу воды отбирают стерильным шприцем в объеме 2 см3
после спуска воды в течение 10... 15 минут при полностью открытом
пробоотборном кране;
5.1. Оценка зараженности нефтепромысловых сред 223
Ц’г — поверхность пробки промаркированного пенициллинового
флакона с питательной средой протирают ватным тампоном, смо-
ченным этиловым спиртом;
у — по 1 см3 пробы вносят в питательную среду Постгейта В для
обнаружения СВБ и в пептон-дрожжевую питательную среду для
выявления аэробных бактерий.
При невозможности выполнения посевов в питательные сре-
ды сразу же после отбора проба должна быть отобрана в сте-
рильные склянки. Наполненные склянки закрывают притертыми
или резиновыми пробками. Каждая проба сопровождается доку-
ментом, содержащим сведения о месте отбора проб и дате отбо-
ра (с указанием числа и часа). Посев проб в питательные сре-
ды должен быть осуществлен не позже чем через 2 часа после
ее отбора.
Допускается проводить микробиологические посевы проб не поз-
же чем через 6 часов после отбора, при условии хранения пробы при
температуре от 1 до 4° С.
После рассева проб воды в соответствующие питательные среды
пенициллиновые флаконы инкубируют при температуре 32° С в те-
чение 15 дней. Одновременно в термостат ставят флакон со средой
для контроля ее стерильности. При работе с термофильными бак-
териями режим термостата устанавливают до значения температуры
40... 70° С.
Все посевы проб проводят в 2... 3-кратной повторности.
Присутствие СВБ устанавливают по развитию процесса суль-
фатредукции в посевных флаконах. Развитие сульфатредукции фик-
сируют визуально по помутнению среды, появлению черного осадка
сульфида железа в питательной среде и наличию сероводорода. Об-
224
Глава 5
разование равномерной и не оседающей мути характеризует накоп-
ление бактериальных клеток во всем объеме питательной среды.
При наиболее интенсивном росте и развитии СВБ черный суль-
фид железа с легким металлическим блеском адгезируется на стенках
флакона.
Количественно сульфатредукцию оценивают по приросту в по-
севных флаконах сероводорода, который определяют методом йодо-
метрического титрования.
Обнаружение адгезированной популяции бактерий
1
При микробиологическом контроле нефтепромысловых систем
традиционным методом высева извлекаемых на поверхность проб
жидкости на питательные среды не учитывается большая часть бак-
терий, находящихся в адгезированном состоянии [138, 144, 147].
Для устранения этого недостатка и обеспечения учета адгези-
рованных клеток СВБ предложен следующий метод. Сущность ме-
тода заключается в том, что в действующий трубопровод помещают
при помощи специального устройства металлические образцы, слу-
жащие объектами для колонизации (обрастания) микроорганизмов
из окружающей образцы среды. Это дает возможность исследовать
количественное развитие микроорганизмов на поверхности метал-
ла, оценить степень воздействия различных реагентов на популяцию
бактерий.
Оценка уровня колонизации СВБ внутренней поверхности
трубопроводов
Уровень колонизации металла микроорганизмами из окружаю-
щей нефтепромысловой среды оценивают по образцам, которые экс-
5.1. Оценка зараженности нефтепромысловых сред 225
понируют в действующем трубопроводе. Схема ввода образцов в тру-
бопровод показана на рис. 5.1.
Образец (11) представляет собой цилиндр диаметром 11,3 мм;
длиной 12 мм с кольцевой проточкой посередине глубиной 1,25 мм
и торцевыми рабочими поверхностями. Образцы изготавливают
из материала, тождественного металлу трубопровода. Допускается
использование образцов, изготовленных из малоуглеродистой стали.
Перед установкой в трубопровод образцы тщательно обезжи-
ривают ацетоном, промывают дистиллированной водой и опускают
на 5 минут в 50% водный раствор соляной кислоты, затем снова
промывают водой.
Подготовленные таким образом образцы вставляют в кассеты,
закрепляют фиксаторами, помещают в герметичный сосуд с 70%
раствором этанола для доставки их в асептических условиях к месту
установки.
Кассету с образцами (10) при помощи устройства ввода образ-
цов устанавливают в трубопроводе, предварительно удалив из узла
врезки скопившуюся нефть.
Скорость колонизации образцов зависит от физиологического
состояния микроорганизмов и их количественного содержания в неф-
тепромысловых средах, вследствие чего оптимальное время экспози-
ции должно быть выбрано особо в каждом случае [28].
Как правило, активное заселение образцов происходит в первую
неделю экспозиции. В дальнейшем увеличение численности микро-
организмов на образцах происходит преимущественно за счет разви-
тия уже поселившихся бактерий.
Для сформировавшейся биопленки, с численностью микроор-
ганизмов в диапазоне естественных уровней обитания, характер-
226
Глава 5
Рис. 5.1. Схема ввода образцов-субстратов в трубопровод: 1 — трубопровод;
2 — штуцер; 3 — задвижка; 4 — корпус; 5 — струбцина; 6 — нажимная втулка;
7 — штанга узла ввода образцов-субстратов; 8 — упор; 9 — держатель; 10 —
кассеты; 11 — образцы-субстраты; 12 — фиксатор образцов
5.1. Оценка зараженности нефтепромысловых сред 227
во относительно стабильное количество клеток, достигаемое дина-
мическим равновесием процессов размножения и отмирания кле-
ток.
: Время экспозиции образцов, обеспечивающее формирование
на них стабильной по численности микроорганизмов биопленки, со-
ставляет 2... 4 недели.
Для выяснения скорости и интенсивности колонизации при на-
личии на трубопроводе нескольких узлов врезки (например, трех)
целесообразно установить образцы в каждый из них. Это позволя-
ет проводить количественное определение адгезированных СВБ при
извлечении образцов поочередно через 10, 20, 30 суток.
При наличии на трубопроводе только одного узла врезки для
определения уровня колонизации образцы устанавливают на 30 дней.
По истечении времени экспозиции кассеты извлекают из трубо-
провода и производят количественную оценку интенсивности коло-
низации образцов СВБ методом предельных разведений, предвари-
тельно осуществив «извлечение» клеток бактерий с поверхности ме-
талла. Для этого в небольшую стерильную фарфоровую чашку нали-
вают определенное количество (например, 10 см3) стерильной воды
и, придерживая образец-свидетель стерильным пинцетом, тщательно
очищают его поверхность кусочком (~ 1 см2) предварительно стери-
лизованной кипячением губки типа «Эффект» (делают соскоб). Затем
воду с губкой переносят в пенициллиновый флакон. Соскоб можно
проводить стерильным скальпелем. Для десорбции клеток с губки
и дезагрегирования колоний бактерий флакон обрабатывают в уль-
тразвуковой ванне, например, модели U-300 фирмы Ultrawave Limited
(Великобритания). Из обработанного ультразвуком флакона отбира-
ют стерильным шприцем 1 см3 воды и далее определяют количество
228
Глава 5
бактерий методом предельных разведений. Количество разведений
в пределах 6... 8.
Полученные данные выражают в количестве бактерий на 1 см2
площади образца, учитывая тот объем воды, в который был перенесен
соскоб.
При отсутствии специальных образцов-субстратов для оцен-
ки уровня колонизации бактериями трубопроводов допускается
использование устанавливаемых в трубопровод гравиметрических
образцов-свидетелей. В этом случае соскоб делают по всей площади
образца.
I
Оценка уровня колонизации СВБ в осадках
Для определения наличия клеток СВБ в осадках пробу осадка
отбирают в стерильную, герметично закрывающуюся склянку.
Осадок должен быть обработан не позднее чем через 2 часа
после отбора. Допускается обработка осадка не позднее чем через
6 часов после отбора, сохраняя его при этом в герметично закрытом
сосуде при температуре от 1 до 4° С.
Необходимо избегать высыхания осадка, так как при этом проис-
ходит гибель большей части содержащихся в нем микроорганизмов.
Как правило, при этом в осадке остаются лишь спорообразующие
формы бактерий, составляющие небольшую часть микробного насе-
ления.
Определение количества СВБ в осадке проводят методом пре-
дельных разведений. В стерильный пенициллиновый флакон отвеши-
вают 1 г осадка и приливают 10 см3 стерильной воды. Для десорбции
клеток бактерий и дезагрегирования их колоний флакон обрабатыва-
ют ультразвуком в ультразвуковой ванне. Затем из флакона отбирают
5.1. Оценка зараженности нефтепромысловых сред 229
стерильным шприцем 1 см3 воды и далее определяют количество
бактерий методом предельных разведений. Количество разведений
в пределах 6... 8.
Расчет количества бактерий ведут на 1 г осадка, учитывая тот
объем воды, который использовался при десорбции клеток.
Методика подсчета количества планктонных
бактериальных клеток в исследуемой среде
Существующая методика количественной оценки наличия бак-
териальных клеток в исследуемой среде (РД 39-3-973-83) имеет су-
щественные недостатки:
— не обеспечивает достоверного усреднения n-количества па-
раллельных проб с различным кратно отличающимся количеством
бактерий;
— отсутствуют формулы и готовые расчетные таблицы для нахо-
ждения достоверного числа клеток в 3, 5, 10 параллельных пробах.
В связи с этим для количественной оценки наличия клеток бак-
терий при любом их количестве в каждой параллельной пробе пред-
ложена методика, в основу которой положены работы [51, 64].
Принцип метода. Оценка количества бактерий в нефтепромыс-
ловых средах основана на методе предельных разведений, заключа-
ющемся в определении минимального количества посевного матери-
ала, содержащего одну бактериальную клетку.
Подготовительные работы. Приготовление питательных сред
для культивирования бактерий производят согласно [99].
Ход лабораторного анализа. Из анализируемой нефтепромыс-
ловой среды стерильным шприцем отбирают 1 мл жидкости и вводят
230
Глава 5
в 10-миллилитровый пенициллиновый флакончик с питательной сре-
дой, соответствующей культивируемым бактериям.
Содержимое перемешивают и новым стерильным шприцем от-
бирают из этого пузырька 1 мл пробы и вводят во второй сте-
рильный флакончик с питательной средой (содержание исходной
среды 0,1 мл). Затем из второго флакончика отбирают 1 мл жид-
кости, вводят в третий флакончик и перемешивают (содержание
исходной среды 0,01 мл). Таким образом готовят и последующие
разведения для получения содержания исходной среды во флаконах
1О-3,10~4...1О'П мл.
После посева все флакончики инкубируют в суховоздушном тер-
мостате при температуре 32° С и наблюдают в течение 15 суток. Рост
бактерий оценивают согласно [99].
Обработка результатов. Обработка результатов основана на
использовании метода наиболее вероятного числа (НВЧ), заключаю-
щегося в математической оценке вероятности присутствия жизнеспо-
собных клеток в трех последних серийных 10-кратных разведениях
для любого количества параллельных проб. Считают, что в выросшем
посеве, где использовано максимальное разведение, присутствует од-
на клетка.
Расчет количества бактерий производят по формуле
М = К- 10("“2),
где М — количество бактериальных клеток в 1 мл исходной во-
ды; 10^п“2^ — концентрация бактерий в исходной среде во флаконе
(п — 1) разведения, т. е. среднее значение концентрации в последних
трех разведениях; К — наиболее вероятное число клеток при разве-
5.1. Оценка зараженности нефтепромысловых сред 231
дении (п — 1); п — порядковый номер разведения; 10 — коэффициент
разведения.
Наиболее вероятное число клеток для 3-х параллельных проб
определяют по табл. 5.1 на основании числа определений, в которых
наблюдают рост бактерий (код роста).
Для 5-ти и 10-ти параллельных проб НВЧ берутся из табл. П1
и П2.
Код роста соответствует количеству флаконов, в которых отме-
чен рост в каждом из последних трех разведений. Например, код 324
установлен следующим образом, табл. 5.2.
Определение наиболее вероятного числа бактерий в исследуе-
мой среде по последним трем разведениям производят по формуле
п п
E<*i * Pi
——=
i=0 1 e t=0
где К — наиболее вероятное число клеток бактерий; at — исследу-
емый объем среды; гр — количество параллельных проб; pi — число
определений, в которых наблюдается рост бактерий.
Пример, проверка и сравнение полученных результатов
В серии трех параллельных разведений обнаружены признаки
роста бактерий во флаконах, отмеченных в табл. 5.3 знаком (+).
Код роста бактерий (1 вариант) по трем последним разведени-
ям (5,6,7) составляет 210. Соответственно данному коду значение
«К» по табл. 5.1 составляет 0,1467. Это означает, что НВЧ клеток
во флаконе с содержанием исходной культуры 10~5 мл составляет
0,1467 клеток в 1 мл, а НВЧ в 1 мл исходной культуры равно М =
= 0,1467 • 10(7-2> = 14670.
232
Глава 5
Таблица 5.1. Код роста и вероятность НВЧ для 3 параллельных проб
Код роста Значение НВЧ Код роста Значение НВЧ
333 100 133 0,288
332 10,966 132 0,241
331 4,050 131 0,1977
330 2,397 130 0,157
323 2,920 123 0,237
322 2,100 122 0,1958
321 1,494 121 0,1549
320 0,931 120 0,1137
313 1,580 113 0,190
312 1,140 112 0,151
311 0,740 111 0,1125
310 0,361 110 0,0735
303 0,950 103 0,1485
302 0,635 102 0,108
301 0,383 101 0,0745
300 0,230 100 0,0357
233 0,525 033 0,1899
232 0,440 032 0,158
231 0,360 031 0,1262
230 0,285 030 0,0943
223 0,4234 023 0,1556
222 0,348 022 0,124
221 0,277 021 0,093
220 0,2105 020 0,0619
5.1. Оценка зараженности нефтепромысловых сред
233
Продолжение табл. 5.1
Код роста Значение НВЧ Код роста Значение НВЧ
213 0,334 013 0,1222
212 0,267 012 0,094
211 0,20595 011 0,0621
210 0,1467 010 0,0304
203 0,2595 003 0,0904
202 0,1985 002 0,0602
201 0,1445 001 0,030
200 0,0917
Таблица 5.2. Определение кода роста бактерий
Порядковый номер разведения Флаконы, в которых отмечен рост бактерий Код роста
Номера параллельных проб
1 2 3
п — 2 + + + 3
п — 1 + + 2
п + 1 + 1
Если отбросить последнее разведение и заново составить код
роста, то он будет равен — 321. Количество НВЧ по табл. 5.1 со-
ставит 1,494, а = 1,494 • 10^6-2^ = 14940. Разница в полученных
значениях не превышает 2 %.
Вычисление НВЧ по формуле отражено в табл. 5.4 и дает тот же
результат.
234
Глава 5
Таблица 5.3. Пример расчета кода роста бактерий с учетом номера разведе-
ния
Номер па- раллельной пробы Рост бактерий
№ разведения / количество посевного материала, мл
1/1 2-101 3-Ю'2 4-10-3 510-4 ею-5 7-10“6
1 + + + + + +
2 + + + + +
3 + + + +
Код роста 1 вариант 1
2 1 0
Код роста 2 вариант
3 2 1
Таблица 5.4. Определение НВЧ по формуле
Символ Значения в примере
СТ, 10 1 0,1
Чг 3 3 3
12 а1г Vi 10 • 3 1-3 0,1-3
Pi 3 2 1
Qi ТЦ 30 2 0,1
i 'Pi ^177 + Чк + =33’3 1~Г-1ОА 1-е~1К i-e-O’iА
Решая уравнение, составленное в табл. 5.4, относительно К,
получим значение К = 1,494, что соответствует М = 14940.
5.2. Исследование адаптационных свойств СВБ
235
Расчет количества СВБ согласно РД 39-3-973-83
Поскольку в седьмом разведении (см. табл. 5.3) не наблюдается
роста клеток СВБ, то принимаем, что в предыдущем шестом разве-
дении присутствует 1 клетка. Тогда в 5 разведении будет 10 клеток,
в 4 — 100 и в 1 — 100 000 клеток.
В трех параллельных пробах количество бактерий составляет
1 — 100000 клеток (рост в шестом разведении);
2 — 10000 клеток (рост в пятом разведении);
3 — 1 000 клеток (рост в четвертом разведении)
при среднем значении 37 000 клеток.
Полученное значение М существенно отличается от рассчитан-
ного по методу НВЧ и дает искаженную картину.
5.2. Исследование адаптационных свойств СВБ
к реагентам-бактерицидам
Получение накопительной культуры
Из нефтепромысловых сред, где предполагается использова-
ние реагентов, выделяется накопительная культура микроорганизмов.
Сущность метода выделения накопительных культур заключается
в создании элективных условий, которые обеспечивают преимуще-
ственное развитие определенной группы микроорганизмов и препят-
ствуют росту посторонних. Для СВБ такой элективной средой явля-
ется среда Постгейта В, для аэробных бактерий — пептон-дрожжевая
среда.
Для получения накопительной культуры вносят нефтепромысло-
вую воду в количестве 1... 2 см3 в пенициллиновые флаконы с пи-
236
Глава 5
тательной средой. Засеянные флаконы помещают в термостат и вы-
держивают при температуре 34 ... 35° С в течение семи суток.
Очистку полученной накопительной культуры производят путем
ее рассева в новые флаконы с питательной средой и после термоста-
тирования в течение семи суток производят новый пересев. Получен-
ная накопительная культура практически свободна от сопутствующих
микроорганизмов. Для сохранения жизнеспособности клеток каждые
7 дней производят пересев накопительной культуры на свежую пи-
тательную среду.
Для оценки бактерицидной эффективности реагентов рекомен-
дуется использовать двух- трехсуточную накопительную культуру,
получаемую пересевом полученной накопительной культуры на све-
жую питательную среду с последующим термостатированием в тече-
ние двух-трех суток. За этот период клетки достигают максимального
роста и развития.
Исследование адаптационных свойств СВБ
к реагентам-бактерицидам
Определение понятия. Адаптацией СВБ к реагенту-бактерици-
ду называется снижение эффективности действия бактерицида на
микрофлору обрабатываемой жидкости в условиях длительного при-
менения бактерицида.
Принцип подхода. Метод основан на сравнении необходимой
концентрации бактерицида для 100 % подавления роста СВБ с кон-
центрацией бактерицида, достаточной для подавления роста выжив-
ших и культивированных до восстановления первоначального индек-
са активности жизнеспособных клеток, после воздействия на них
5.2. Исследование адаптационных свойств СВБ
237
минимальной концентрацией бактерицида, при которой отмечается
начало подавления роста бактерий при трех-, пятикратной повторно-
сти воздействия минимальной концентрацией [53].
Подготовительные работы
Подготовка СВБ. Исследования проводят на накопительной
культуре бактерий, выделенных из промысловой жидкости то-
го месторождения, где предполагается использование бактерици-
да. Для испытаний реагентов испрльзуют двухсуточную куль-
туру.
Выбор концентрации бактерицида для исследований. По ре-
зультатам предварительных испытаний выбирают минимальную кон-
центрацию бактерицида, при которой отмечается начало подавленья
роста СВБ (7Снпр), и минимальную концентрацию реагента, обеспе-
чивающую 100 % подавление роста СВБ (7Спр).
Возможность адаптации СВБ к выбранному бактерициду опре-
деляют при исследовании степени подавления СВБ при заданных
пределах концентраций бактерицидов — (/Grip — 25% от К,ф):
(-Кипр + 25 % от Кпр); т. е. таких концентрациях, при которых
степень подавления роста СВБ составляет величину, приведенную
в табл. 5.5.
При соответствии выбранной концентрации /Gnp и А"Пр число-
вым значениям, приведенным в табл. 5.5, дальнейшие исследования
проводят с теми же концентрациями. Если полученные значения сте-
пени роста СВБ не соответствуют табличным, то концентрации бак-
терицида Кипр и /СПр корректируют в соответствии с табличными
данными.
238
Глава 5
Таблица 5.5. Задаваемые параметры подавления роста СВБ при исследова-
ниях
Концентрация бактерицида, мг/л Степень подавления роста СВБ, %, на накопительных культурах месторождений
Чутырская пл. Киенгопская пл. Ельниковское
Кнпр — 25 % от А Пр 0 0 0
А нпр 5...15 5...15 5...15
нпр “Ь 25 % от А Пр 30... 80 30... 80 30... 80
А нпр 100 100 100
г
Ход определения
а) В ряд маркированных стерильных пробирок (не менее 3) объ-
емом 20 ... 25 мл наливают по 10 мл предварительно прокипяченной
и охлажденной пресной или минерализованной воды.
б) Предварительно заготовленную накопительную культуру СВБ
перемешивают, выдерживают до осаждения осадка сульфидов, от-
бирают стерильной пипеткой или шприцем жидкость над осадком
и вводят по 0,5 мл в каждую пробирку с водой.
в) Во все пробирки дозируют испытываемый реагент в концен-
трации А'н„р, затем тщательно перемешивают.
г) Пробирки доливают такой же водой без пузырьков воздуха,
закрывают пробкой, перемешивают и выдерживают в течение су-
ток.
д) После выдержки отбирают из пробирок по 5 мл жидкости,
переносят в новые стерильные маркированные пробирки объемом
22 ... 25 мл, доливают питательной средой до верха, закрывают проб-
5.2. Исследование адаптационных свойств СВБ
239
кой, перемешивают и термостатируют при 32° С в течение 15 суток.
е) Жизнеспособные клетки после воздействия концентрацией
Кипр вновь многократными пересевами в среде Постгейта доводят
до первоначального индекса активности и подвергают обработке кон-
центрациями Кнпр и Кпр (№ 2).
Если при воздействии концентрацией Кпр (№2) получено по-
давление роста СВБ менее 100%, ее последовательно увеличивают
до полного подавления роста СВБ (Кпр + 25 %; Кпр + 50 %).
ж) Жизнеспособные клетки после повторного воздействия кон-
центрации Кипр вновь многократными пересевами доводят до перво-
начального индекса активности и подвергают обработке концентра-
циями Кипр и Кпр (№ 3).
з) При трех- и пятикратной повторности эксперимента, по сте-
пени увеличения первоначально установленной минимальной кон-
центрации (Кнпр), подавляющей на 100% развитие СВБ, оценивают
возможность адаптации СВБ к данному бактерициду.
Обработка результатов. Расчет коэффициента адаптации про-
изводят по формуле
=
\ , .пр 100%,
пр (№)
где -Ах» — коэффициент адаптации при №-кратной повторности
эксперимента; Кнпр(№) — концентрация реагента, подавляющая на
100% развитие СВБ при №-кратной повторности эксперимента,
мг/л; Кипр — первоначальная концентрация реагента, подавляющая
на 100% жизнедеятельность СВБ, мг/л; № — повторность экспери-
мента, 1, 2, 3, 4, 5.
240
Глава 5
Пример. Определить период адаптации СВБ к бактерициду ЛПЭ-11.
Определение. Результаты исследования согласно методике приведены
в табл. 5.6.
Таблица 5.6. Определение периода адаптации к ЛПЭ-11 культуры СВБ Лисг-
венского месторождения
№ воздействия Концентрация ЛПЭ-11, мг/л Степень подавления, %
1 250 750 ' 25 100
2 250 1000 25 100
3 400 1000 25 100
4 500 1250 25 100
Расчет коэффициента адаптации осуществляют по формуле:
А'пр(№) - А11р 1250(№4) — 750
Ако = ---—-------- • 100 Л — ------------ = 16,7%.
А„р№ 750(№1)-4
Таким образом, коэффициент адаптации культуры СВБ Лиственского
месторождения равен 16,7%. Это означает, что при проведении одной обра-
ботки эффективность бактерицида снижается на 16,7%, а через шесть об-
работок эффективность достигнет нулевого результата (100 %/16,7 % = 6).
5.3. Методика исследования коррозионной активности 24]
53. Методика исследования коррозионной активности
микрофлоры
:;Л.
Исследования с помощью проточной системы
Влияние микроорганизмов на коррозию металлов определяют
следующие основные факторы [57]:
— модификация среды в результате выделения в нее продуктов
микробного обмена с повышенной агрессивностью и деполяризую-
щей способностью;
— адгезия отдельных клеток и колоний на поверхности метал-
ла, создание микрогальванических коррозионных элементов, работа
которых приводит к точечным разрушениям (питтингам);
— развитие на металле слоя биообразований, первичным этапом
которого является формирование биопленки, выполняющей функцию
барьера, защищающего клетки от неблагоприятных условий среды
и регулирующего потоки вещества и энергии.
На отдельных стадиях взаимодействия микроорганизмов с ме-
таллами указанные факторы проявляются по-разному. В условиях
длительной эксплуатации нефтепромыслового оборудования с ис-
пользованием для технологических целей необеззараженной воды
основной определяющей причиной интенсивной коррозии становит-
ся реальное наличие на металле биопленок [142]. При этом процессы
коррозии локализуются в местах скопления колоний микроорганиз-
мов, экранирующих металлическую поверхность от защитного дей-
ствия ингибиторов. Под толщей биообразований продолжают рабо-
тать как микрогальванопары, так и деполяризаторы, имеющие низ-
комолекулярную природу.
242
Глава 5
В связи с изложенным, практическую значимость приобретают
исследования особенностей развития процессов коррозии в средах,
содержащих микроорганизмы различных физиологических групп,
и изучение влияния совместного действия ингибитора и бактерицида
для разработки эффективных технологий защиты.
Для исследований коррозионной активности микроорганизмов
предложена схема проточной лабораторной системы [57], представ-
ляющей собой микровариант модели тубулярной культуры полного
вытеснения с возвратом. Параметры ее хорошо соответствуют па-
раметрам реальных потоков в системах водоводов. Время удержа-
।
ния произвольного объема жидкости распределяется около среднего
значения по закону Гаусса [88]. Принципиальная схема проточной
лабораторной системы представлена на рис. 5.2.
Для определения способности микроорганизмов адгезироваться
на поверхности металла и образовывать биопленки применяют ме-
тод смешанной культуры, выращиваемой чашечным способом. Ме-
тодика заключается в следующем. Предварительно подготовленные
образцы стали, диаметром 15 мм, помещают в чашки Петри по три
в каждую, затем чашки заполняют исследуемой натуральной неф-
тепромысловой водой с внесением 10% питательных сред (пептона
и среды Постгейта). В чашки вносят по 2 см3 смеси культур ге-
теротрофов и СВБ, выделенных из места отбора проб. Обогащен-
ные таким образом культуры термостатируют в вакуум-эксикато-
ре при температуре 30° С. Длительность эксперимента составляет
20 суток.
Исследование адгезии микроорганизмов на поверхности металла
возможно методом сканирующей электронной микроскопии, позво-
ляющей определять фазы развития биообразований. Метод основан
5.3. Методика исследования коррозионной активности 243
Рис. 5.2. Проточная система с электрохимической ячейкой для исследова-
ния коррозионной активности микроорганизмов (одноканальный вариант):
1 — емкость с исследуемой водой; 2 — перистальтический насос; 3 — элек-
трохимическая ячейка; 4 — соединительные шланги; 5 — термостат
на регистрации электронов вторичной эмиссии, испускаемых в ре-
зультате возбуждения материала образца высокоэнергетическим уз-
монаправленным электронным пучком. Для выявления деталей по-
верхности с биологическими объектами (клетками микроорганизмов
и продуктами их жизнедеятельности) из-за их малой устойчивости
в потоке электронов и невысокой контрастности биологического ма-
териала проводят напыление препарата тяжелым металлом, облада-
ющим инертностью [89].
Металлические образцы на различных стадиях эксперимента из-
влекают из жидкой фазы, ополаскивают стерильной буферной средой
(pH = 7) и фиксируют просушиванием в течение 2 час при темпе-
ратуре 35° С в защищенных от пыли условиях. После этого образцы
244
Глава 5
помещают на 15 мин в стерильную дистиллированную воду и вы-
держивают при периодическом перемешивании. После трехкратной
смены воды (объемом по 20 см3) образцы размещают на фильтрах и
сушат в тех же условиях при указанной температуре в течение 2 сут.
Подготовленный таким образом препарат напыляют слоем золота
и платины путем ионной эмиссии в высоком вакууме. Для напыления
используют прибор, входящий в комплект электронного сканирующе-
го микроскопа. Сканирование осуществляют на микроскопе с золо-
топлатиновым катодом. После общего просмотра участков поверх-
ности металла при малом увеличении отмечают элементы структуры
।
образца, наиболее оптимальные по качеству получаемого изображе-
ния. Указанные участки сканируют при высоком разрешении и интен-
сивности электронного пучка, что позволяет достигать значительных
увеличений. Документирование участков препарата проводят фото-
камерой. В дальнейшем фотоматериалы обрабатывают стандартными
методами.
Разработан и двухканальный вариант проточной системы с при-
менением двух одинаковых емкостей вместимостью 250 см3 и иден-
тичных ячеек-реакторов вместимостью 10 см3. Пропуск жидкости
через систему осуществляют многоканальным перистальтическим
насосом. Систему термостатируют в суховоздушном термостате.
Коррозионные электрохимические исследования проводят в про-
точном режиме системы, электрохимическими ячейками которой слу-
жат ячейки-реакторы, с установленными в них игольчатыми электро-
дами из низкоуглеродистой стали.
Для измерения тока коррозии используют высокопрецизион-
ный микроамперметр класса точности 0,2, связанный с транзистор-
ным преобразователем прибора, имеющим выход на автоматиче-
5.3. Методика исследования коррозионной активности 245
ский самопишущий потенциометр. Измерительная схема сблокиро-
вана с электромеханическим реле времени, управляющим шаговым
искателем на шесть коммутирующих контактов по числу рабочих
электродов. Время экспозиции каналов — 10 сек. Блок-схема измери-
тельной и управляющей цепей представлена на рис. 5.3.
Р-
к ионным мостикам
электрохимических ячеек
Рис. 5.3. Блок-схема измерительной и управляющей цепей проточной си-
стемы (двухканальный вариант): 1 — электрод сравнения с тройником; 2
микроамперметр; 3 — транзисторный преобразователь; 4 — самописец; 5 -
шаговый искатель; 6 — реле времени
Подготовка игольчатых рабочих электродов включает зачистку
и обезжиривание электродов спиртово-ацетоновой смесью, сборку
электрохимических ячеек-реакторов и подключение их к проточной
системе. Заполнение системы исследуемой водой проводят с помо-
щью перистальтического насоса с дальнейшей герметизацией. Режим
работы насоса определяют из расчета полного оборота жидкости в те-
чение 7 суток.
246
Глава 5
В зависимости от задач исследования в исходную воду вводят
бактерицид и ингибитор коррозии исследуемых концентраций. Про-
точную систему термостатируют при температуре 32° С. Измеритель-
ную и управляющую цепи подключают к рабочим электродам и элек-
троду сравнения, измеряют ток коррозии ручным способом в тече-
ние первых 2 часов с интервалом 5... 10 мин, регистрируют время
установления и выхода на стационарный уровень. После достиже-
ния устойчивых значений тока систему переводят на автоматический
режим, который контролируют с помощью управляющей цепи.
Результаты обрабатывают, строя зависимость тока коррозии от
времени. Опытным путем устанавливают эмпирический коэффици-
ент связи потери массы металла с током коррозии, генерируемым
электрохимической ячейкой. Скорость коррозии определяют путем
пересчета токовых единиц в массовые.
5.4. Оценка эффективности ингибиторов коррозии
Эффективность ингибиторов коррозии зависит от множества
факторов, в обобщенном виде которые можно представить в виде
двух основных — внешних и внутренних.
Внешние факторы:
— физико-химические свойства транспортируемой среды;
— термодинамические условия движения жидкости;
— наличие микроорганизмов.
Внутренние факторы:
— состав и свойства основы ингибитора;
— растворимость ингибитора в водной фазе;
— состав и свойства растворителя, входящего в состав ингибитора;
5.4. Оценка эффективности ингибиторов коррозии
247
энергия адгезии водных растворов ингибиторов коррозии к по-
верхности стали.
Все упомянутые факторы в той или иной степени влияют на эф-
фективность ингибиторов и заслуживают пристального внимания,
однако нам представляется целесообразным остановиться на послед-
них трех внутренних факторах, как наименее затрагиваемых в науч-
ной литературе.
Влияние растворимости ингибиторов в водной фазе
на их эффективность
Влияние фактора растворимости на обеспечение достиже-
ния максимальной эффективности ингибиторов коррозии может
быть установлено по их растворимости в воде. Для этого авто-
ры [ПО] предлагают ввести систематизацию выпускаемых реаген-
тов по характеру растворимости и разделить их на три основные
группы.
Группа 1 — хорошо растворимые в воде реагенты, образующие
в ней истинные молекулярные растворы и вследствие этого имею-
щие оптическую плотность их водных растворов, близкую к нулю,
вплоть до концентрации порядка 1 г/л. Примерами таких реагентов
являются Rocor С410, K.emelix-1117Х.
Группа 2 — ограниченно растворимые в воде реагенты и способ-
ные к мицеллообразованию в ней критической концентрации мицел-
лообразования (ККМ) менее 1 г/л, например СНПХ 6301, «Ивкор-5».
Kemelix-1116Х, Kemelix-C856.
Группа 3 — нерастворимые в воде реагенты и образующие в ней
микроэмульсии. Типичными реагентами данной группы являются ин-
гибиторы «Нефтехим», «Щит».
248
Глава 5
Влияние растворимости ингибиторов в воде на их эффектив-
ность было установлено при исследовании воздействия переменных
магнитных полей на ПАВ [109]. Как оказалось, эффективность маг-
нитной обработки для реагентов группы 1 мала, а для групп 2 — 3 за-
щитный эффект повышается лишь в том случае, если увеличивается
оптическая плотность D их водных растворов концентрацией более
100 мг/л (табл. 5.7).
Таблица 5.7. Влияние растворимости ингибиторов коррозии в воде на их
эффективность
Реагент, группа растворимости D при концент- рации 200 мг/л Защитный эффект, %, при дозировке, г/м3
25 50 100 150
СНПХ-6301 — исходный, 2 0,26 -20 — — 79
СНПХ-6301 — обработанный, 2 0,48 -6,3 4 72 91
«Щит» — исходный, 3 0,08 4,1 15 20 —
«Щит» — обработанный, 2 0,40 -2,7 31 50 —
Повышение оптической плотности обусловлено повышением
мицеллообразующей способности молекул ингибитора в водной сре-
де, причем у реагентов группы 2 это эквивалентно снижению рас-
творимости в воде, а у реагентов группы 3, наоборот, — повы-
шению.
Реагенты группы 2 характеризует более высокий защитный эф-
фект. Повышение эффективности реагентов группы 3 после магнит-
ной обработки сопровождается их переходом в группу 2, так как
5.4. Оценка эффективности ингибиторов коррозии 249
оптическая плотность их растворов увеличивается до уровня, свой-
ственного реагентам группы 2.
Таким образом, защитный эффект ингибитора усиливается, если
он находится в воде не в дисперсном, а мицеллярном состоянии, ко-
гда размеры частиц масляной фазы снижаются до размеров мицелл
(0,1... 0,5 мкм). Слишком крупные частицы размером 1... 10 мкм
нерастворимых в воде ингибиторов группы 3 образуют на поверх-
ности металла неоднородную пленку, в местах разрыва которой ско-
рость коррозии может увеличиваться.
Поскольку индикатором появления мицелл в растворе являет-
ся увеличение его плотности, существует взаимосвязь между за-
щитным эффектом ингибитора коррозии и оптической плотностью
его водных растворов. Зависимость защитного эффекта ингибито-
ров коррозии от оптической плотности их водных растворов по-
казана на рис. 5.4. Защитный эффект определен гравиметрическим
методом.
Результаты, отраженные на рис. 5.4, показывают, что защитный
эффект хороших как молекулярных, так и мицеллярных ингибито-
ров примерно одинаков. Однако повысить эффективность реагентов
группы 1 можно лишь путем создания новых реагентов, а реагентов
группы 2 более простым способом — улучшением их мицеллообра-
зующей способности в водной среде.
Влияние растворителя, входящего в состав ингибитора, на его
эффективность
При изготовлении товарных форм ингибиторов коррозии зача-
стую совершенно не уделяют внимание растворителю основы инги-
битора. Между тем растворитель занимает довольно существенную
250
Глава 5
i
Оптическая плотность, D
Рис. 5.4. Зависимость защитного эффекта ингибиторов коррозии от опти-
ческой плотности их водных растворов: 1 — для молекулярных реагентов
группы 1; 2 — для мицеллярных реагентов группы 2
долю в общей эффективности ингибитора и пренебрегать ею нельзя.
Например, замена растворителя в товарной форме реагента «Викор-
8» на другой позволяет повысить эффективность ингибитора корро-
зии почти на 20%. Замену растворителя осуществляют следующим
образом. Исходную товарную форму реагента выдерживают под ва-
куумом, а испарившийся при этом растворитель заменяют таким же
объемом другого растворителя, усиливающего мицеллообразование
реагента «Ивкор-8» в воде. Результаты данных исследований показа-
ны в табл. 5.8.
После проведения модифицирования возросла оптическая плот-
ность водных растворов ингибитора, а его защитный эффект повы-
сился до уровня лучших импортных реагентов, особенно после до-
полнительной обработки магнитным полем [ПО].
5.4. Оценка эффективности ингибиторов коррозии
251
Таблица 5.8. Влияние замены растворителя на эффективность ингибитора
«Ивкор-8»
Форма реагента «Ивкор-8» D при кон- центрации 200 мг/л Защитный эффект, %, на пластовой воде
содержащей 5 мг/л О2. Дозировка 50 мг/л в отсутствие о2. Дозировка 25 мг/л
Исходная 0,28 - 53,5 78,8
Модифицированная 0,80 73,0 90,0
Исходная после магнитной обработки 0,77 71,5 89,0
Модифицированная после магнитной обработки 1,12 79,0 95,0
Влияние адгезии водных растворов ингибиторов коррозии
к поверхности стали на величину защитного эффекта
Предпосылка. Если ввод ингибитора коррозии в воду снижает ее
взаимодействие со сталью, то этот процесс должен сопровождаться
снижением энергии адгезии воды к поверхности стали И'’ас/, причем
чем эффективнее реагент, тем ниже должна быть величина Wad [111]:
Wad = <г(1 + COS0),
252
Глава 5
где а — поверхностное натяжение водного раствора ингибитора кор-
розии на границе с воздухом; в — краевой угол смачивания раствором
ингибитора поверхности стали.
Очевидно, что снижение Wad будет иметь место при уменьше-
нии величины ст и увеличении в. Для большинства ингибиторов кор-
розии при дозировках 20... 40 мг/л диапазон изменения а не пре-
вышает 5... 10% [111] и регулирование величины Wad их растворов
к стали определяет в основном изменение величины в.
Наиболее эффективный реагент и оптимальную концентрацию
его дозировки определяет максимум концентрационной зависимости
I
Д0(С) = 0 - 0О,
где 0 и 0о — краевые углы смачивания поверхности стали раствором
ингибитора и одним растворителем, на котором приготовлен рас-
твор ингибитора; С — концентрация вводимого реагента. На рис. 5.5
на примере двух реагентов, отличающихся между собой лишь рас-
творителем, показан вид получающихся зависимостей.
Согласно приведенным зависимостям ингибитор, приготовлен-
ный с использованием в качестве растворителя метанола, будет
подавлять коррозионные процессы лишь при концентрациях вы-
ше 100 мг/л, при меньших дозировках он даже ускоряет коррозию.
Гораздо более эффективным является ингибитор, приготовленный
на основе бинарного растворителя. Данные убедительно демонстри-
руют, в какой степени можно изменить эффективность ингибито-
ров коррозии путем изменения растворителя, который используют
для приготовления его товарной формы. Оптимальный растворитель
достаточно легко может быть подобран из анализа зависимостей
5.4. Оценка эффективности ингибиторов коррозии
253
Рис. 5.5. Изменение краевого угла смачивания поверхности стали от концен-
трации ингибитора: 1 — растворитель метанол; 2 — бинарный растворитель
Д0 = f(C) товарных форм одного и того же реагента на различ-
ных растворителях.
По результатам исследований ингибиторов коррозии по изме-
нению Wad [НО] выявлено принципиальное отличие ингибитор-эв
групп 1 и 2. Ввод ингибиторов группы 2 с высокой мицеллообразую-
щей способностью в воду приводит к снижению Wad, з следователь-
но, и скорости коррозии. Противоположные знаки изменения Wri,i
и Z наблюдаются лишь при малых концентрациях малоэффективных
реагентов с КММ порядка 100 мг/л, например СНПХ-6301.
Отличительной особенностью ингибиторов коррозии группы 1
является способность менять Wad в двух противоположных направ-
лениях примерно в равной степени. При малых концентрациях эти
ингибиторы снижают Wad, что сопровождается снижением скоро-
сти коррозии, а при более высоких — увеличивают Wad и скорость
коррозии. Подтверждением этому служат результаты лабораторных
и промысловых испытаний реагента Danox-1.
254
Глава 5
Результаты лабораторных исследований зависимости изменения
Wad водных растворов ингибитора Danox-1 от концентрации, а также
других ингибиторов коррозии группы 1 и 2 представлены на рис. 5.6.
Рис. 5.6. Зависимость изменения Wa,i водных растворов ингибиторов кор-
розии от концентрации. Реагенты группы I: 1 — Danox-1; 2 — Kemelix 1117.
Реагенты группы II: 3 — СНПХ-6301; 4 — Kemilix 1026
Результаты промысловых исследований эффективности приме-
нения ингибитора Danox-1 на месторождении ОАО «Когалымнеф-
тегаз» с дозировкой, рекомендуемой представителями французской
фирмы, равной 25 мг/л, показали увеличение, а не замедление ско-
рости коррозии в водоводах данного месторождения.
Результаты промысловых испытаний прекрасно согласуются
с данными лабораторных исследований, представленных на рис. 5.5.
Минимум Wad, а следовательно, и максимум защитного эффекта
у Danox-1 наблюдают при концентрации 10 мг/л, а при 25 мг/л —
Wad, наоборот, максимум. Исходя из этого, при концентрации
5.4. Оценка эффективности ингибиторов коррозии 255
25 мг/л, из-за увеличения энергии адгезии воды к поверхности стали
скорость коррозии должна увеличиваться, что и объясняет неудовле-
творительные результаты промысловых испытаний.
Все рассмотренные факторы в комплексе могут быть проиллю-
стрированы примером оценки эффективности ингибитора коррозии
СНПХ-6301, рис. 5.7.
Из рисунка видно, что увеличение защитного эффекта ингиби-
тора сопровождается уменьшением энергии адгезии (И^)- При ма-
лой дозировке данного реагента меняется знак защитного эффекта
и Wad- Помимо этого, для мицеллярного реагента СНПХ-6301 мини-
мум Wad И максимум защитного эффекта достигаются при концен-
трации, близкой к КЕМ, определяемой по точке перегиба зависимо-
сти оптической плотности от концентрации.
Рис. 5.7. Зависимость защитного эффекта Z (1), изменения оптической плот-
ности ДО (2) и энергии адгезии к стали &.Wad (3) водных растворов СН-
ПХ-6301 от его концентрации
Проведенными исследованиями установлено [ПО], что адгезия
водных растворов реагентов группы 1 по мере формирования корро-
256
Глава 5
зионной пленки увеличивается, а следовательно, их эффективность
снижается. В то же время адгезия водных растворов реагентов груп-
пы 2 к покрытому коррозионной пленкой металлу, наоборот, оказы-
вается ниже, чем к чистой поверхности. Поэтому на чистой поверх-
ности металла выше эффективность ингибиторов коррозии группы 1,
а на поверхности металла, покрытого коррозионной пленкой, наобо-
рот, — ингибиторов группы 2. Поскольку поверхность всех водоводов
уже покрыта коррозионной пленкой, преимущество мицеллярных ин-
гибиторов становится очевидным.
Все рассмотренные методологические аспекты показывают прак-
тическую значимость метода оценки эффективности ингибиторов
коррозии по изменению параметра Wad- Преимуществом способа
является и высокая скорость получения информации: за 2... 3 ча-
са с высокой точностью можно получить полную концентраци-
онную зависимость эффективности реагента, по которой оцени-
вается его оптимальная дозировка. Кроме того, по имеющимся
контрационным зависимостям нескольких реагентов можно
отобрать наиболее эффективные ингибиторы при меньшем числе
коррозионных испытаний, необходимых лишь на заключительном
этапе.
Для того чтобы полностью исключить неудачи промысловых ис-
пытаний, исследования свойств растворов ингибиторов необходимо
проводить в той воде, в которой планируется их применение, по-
скольку параметры растворов очень чувствительны к составу воды.
Например, упомянутый ингибитор Danox-1 в сравнительно чистой
технической водопроводной воде ведет себя уже как мицеллярный
реагент группы 2, причем максимальный защитный эффект его на-
блюдается при дозировке 25 мг/л, которая ошибочна и была реко-
5.5. Оценка эффективности применения ингибиторов
257
мендована фирмой, производящей этот реагент, для промысловых
испытаний в минерализованной пластовой воде [110].
5.5. Оценка эффективности применения ингибиторов
коррозии в условиях микробиологической
зараженности нефтепромысловых сред
Микробиологическая зараженность нефтепромысловых сред
и связанное с ней формирование закрепленных биоценозов требует
обоснованного выбора критериев оценки эффективности применяе-
мых реагентов для обеспечения защиты от общей и микробиологи-
ческой коррозии.
Определить вклад микробиологического фактора в общую кор-
розионную агрессивность традиционно используемыми гравимет-
рическими методами затруднительно [57]. В связи с этим пред-
лагается [56] руководствоваться тремя основными критериями,
обеспечивающими получение объективной и достоверной инфор-
мации.
Первым из критериев является полное подавление микроорга-
низмов и удаление с поверхности металла как отмерших колоний,
так и продуктов их жизнедеятельности. Осуществить это возмож-
но как повышением ударной дозировки применяемого бактерицида,
так и увеличением времени его подачи. В лабораторных эксперимен-
тах первичная эффективность бактерицида однозначно может быть
установлена по выходу коррозионного тока на уровень фоновых зна-
чений, что, однако, свидетельствует лишь о подавлении жизнедея-
тельности микробов и связанной с ней биологической составляющей
общей коррозии.
258
Глава 5
Вторым критерием эффективности антикоррозионной защиты
служит степень ингибирующего действия традиционно применяемых
реагентов с хорошо изученной функцией на фоне подачи бактерици-
да.
Третьим объективным критерием оценки эффективности хими-
ческих реагентов в процессах подавления всех видов коррозии яв-
ляется общий вид кинетической токовой кривой. В зависимости
от достигнутых результатов, такая кривая наиболее объективно ха-
рактеризует как вклад всех возможных составляющих в коррози-
онное разрушение металла, так и все защитные эффекты, реали-
зуемые в результате применения бактерицидов и ингибиторов кор-
розии.
Исследования проводят с использованием высокочувствитель-
ных электрохимических методов в условиях проточной лабораторной
системы. По результатам исследований строят кинетическую кривую
изменения тока коррозии во времени, рис. 5.8.
Левый склон кинетической кривой изменения тока коррозии
характеризует особенности коррозионной активности микрофлоры
исследуемой нефтепромысловой воды конкретного месторождения
и является индивидуальным показателем вклада микроорганизмов
в общий коррозионный процесс.
Начало склона с t = 0 сут характеризует фоновую коррозионную
агрессивность воды (1), значение Ik составляет 87,3 • 10~6 А. Начало
выхода токовой кривой на плато характеризует завершение форми-
рования биопленки, а значения на оси абсцисс (3 сут) — время фор-
мирования биопленки, на оси ординат (123,1 • 1(Г 6 А) — суммарную
агрессивность среды. Разница между максимальным значением тока
коррозии и фоновым значением характеризует микробную состав-
5.5. Оценка эффективности применения ингибиторов
259
Время, сут
Рис. 5.8. Развитие и подавление коррозионных процессов в воде, заражен-
ной микроорганизмами [56]: 1 — коррозионный фон; 2 — развитие ми-
кробной коррозии; 3 — подавление микробной коррозии бактерицидом: 4 -
подавление фоновой коррозии ингибитором
ляющую коррозии (2), величина которой в нашем рассматриваемом
случае составляет 35,8 • 10-6 А.
Правый склон кинетической кривой отражает особенности из-
менения тока коррозии в условиях воздействия на систему бактери-
цидами и ингибиторами коррозии.
Введение бактерицида с концентрацией 500 мг/дм3 позволяет
подавить биологическую составляющую коррозии (3) и жизнедея-
тельность закрепленного биоциноза. Ток коррозии при этом падает
260
Глава 5
до величины 88 -10~6 А, что практически соответствует фоновым зна-
чениям коррозии, существовавшим до подключения биологической
составляющей.
Полученные результаты показывают, что применение бактери-
цида позволяет значительно снизить величину тока коррозии, однако
при наличии высокого коррозионного фона задача эффективной за-
щиты от всех видов коррозии оказывается нерешенной и требуется
ингибирование.
Участок правого склона кинетической кривой ниже пунктирной
линии (4) отражает процесс ингибирования фоновой (абиогенной)
компоненты ингибиторами коррозии/т. е. защиту от электрохимиче-
ской составляющей общей коррозии. Заданная степень защиты 98%
достигается при введении ингибитора с концентрацией 300 мг/дм3.
При этом достигаемая степень защиты от коррозии при меньших
концентрациях ингибитора отражена на правом склоне кривой.
В качестве иллюстрации предложенного методологического под-
хода исследований приводим характеристику изменения тока корро-
зии в присутствии ингибитора коррозии Нефтехим-3 и бактерици-
да ЛПЭ-11в в условиях микробиологической зараженности сточной
воды с БКНС Сухой бор [57], рис. 5.9. Левая ветвь кинетической
кривой, характеризующая развитие биоценозов, на данном рисунке
упущена.
Микробное сообщество в исследуемой сточной воде представле-
но СВБ в концентрации 102 ... 103 кл/см3 и гетеротрофными бакте-
риями — 105 кл/см3 с высокой начальной активностью (проявление
признаков роста 1 — 2 сут). Исследование адгезионной способности
микрофлоры показало, что микроорганизмы, выделенные в накопи-
тельные культуры, обладают выраженной способностью к прикреп-
5.5. Оценка эффективности применения ингибиторов
261
Время, сут
Рис. 5.9. Изменение тока коррозии в электрохимической системе в про-
точном режиме в присутствии ингибитора и бактерицида: 1 — содержание
Нефтехима-3 — 50 мг/дм3; 2-4 содержание бактерицида ЛПЭ-11 соответ-
ственно 150, 250 и 500 мг/дм3
лению к поверхности металла с образованием биопленки. Исходя
из полученных данных можно предположить, что в течение экспе-
римента в проточной системе большая часть бактерий оказывается
прикрепленной.
В условиях бактериального заражения ухудшаются свойства ин-
гибиторов коррозии, традиционно применяемых для защиты нефте-
промыслового оборудования.
Полученные в ходе исследований данные свидетельствуют
о том, что изменение тока коррозии во времени в системах без
бактерицида (кривая 1) характеризуется наличием четырех основ-
ных участков кинетической кривой. В короткий период време-
ни (1... 2 сут) происходит падение тока коррозии, затем кривые
ненадолго стабилизируются, после чего происходит ускоренное на-
растание тока, переходящее в фазу плато.
262
Глава 5
В отсутствие бактерицида усиление тока коррозии и ее общей
скорости можно объяснить наличием микроорганизмов в исследу-
емой воде. В этой связи различные участки кинетических кривых
могут быть обусловлены следующим. На первом участке ток корро-
зии снижается, поскольку коррозионная активность микроорганиз-
мов в жидкой фазе системы невысока. По мере нарастания концентра-
ции бактерий из потока движущейся жидкости в слое, прилегающем
к металлу, скорость коррозионного процесса стабилизируется. В ре-
зультате прекращается снижение тока коррозии и некоторое время
он практически не меняется. Последующее нарастание тока связано
с началом адгезии микроорганизмов на поверхности металла, в ре-
зультате которой ускоряются токообразующие реакции. Достижение
током максимального значения с дальнейшей стабилизацией на этом
уровне, вероятнее всего, связано с формированием первичной био-
пленки, покрывающей все большую площадь поверхности металла.
Конечные скорости коррозии, полученные токовым методом, за вре-
мя эксперимента различаются более чем в 4 раза, что, очевидно,
соответствует реальному «вкладу» микроорганизмов в общую кор-
розионную агрессивность среды.
Полученные данные дают возможность утверждать, что в сре-
дах, зараженных микроорганизмами, защитный эффект ингибито-
ра резко падает. По истечении первых суток эффективность защи-
ты, составляющая около 91 %, снижается на третьи-четвертые сутки
до 27%.
Введение в систему ингибитора коррозии и бактерицида
ЛПЭ-11 в в соотношениях 1 : 5 и 1 : 10 позволяет достичь защит-
ного эффекта, приблизительно равного 94 %. Соотношение 1:3 обес-
печивает эффективность около 55 %, что связано с недостаточным
5.6. Приготовление питательных сред для микроорганизмов 263
подавлением микроорганизмов в водной фазе. Неэффективность ин-
гибитора в зараженной воде может быть объяснена концентрацией
бактерий в приэлектродном пространстве с последующей адгезией
их к металлу, которая заканчивается созданием пленки, экранирую-
щей металл от контакта с ингибитором. Бактерицид, подавляя жиз-
недеятельность микроорганизмов, способствует более эффективной
защите. Для сравнения следует отметить, что собственный защитный
эффект бактерицида ЛПЭ-11 в составляет около 75% за счет устра-
нения микробиологического фактора.
5.6. Приготовление питательных сред
для микроорганизмов
1. Среда Постгейта В [149]. Используют для обнаружения
СВБ и поддержания культуры с целью сохранения жизнеспособности
клетки, а также таксономических свойств бактерий.
Основная среда:
— калий фосфорно-кислый однозамещенный — аммоний хлористый — кальций сернокислый — магний сернокислый 7-водный — натрий молочно-кислый — натрий хлористый КН2РО4 - 0,5 г - по ГОСТ 4198-75 NH4C1 - 1,0 г - по ГОСТ 3773-72 CaSO4 - 1,0 г - по ГОСТ 3210-77 MgSO4 • 7Н2О - 2,0 г - по ГОСТ 4523-77 C2H5O3Na - 3,5 г - ТУ 6-09-3664-74 NaCl - 5,0 г - по ГОСТ 4233-77
Для приготовления питательной среды, предназначенной для об-
наружения галофильных или солетолерантных СВБ, количество хло-
ристого натрия увеличивают до 60 г и более.
264
Глава 5
Добавки:
— дрожжевой экстракт
(5 % водный экстракт)
— железо серно-кислое
закисное 7-водное
— натрий углекислый
кислый
— натрий сернистый
1,0 г - ТУ 6-09-3979-75
FeSO4 • 7Н2О - 0,5 г - по ГОСТ 4148-78
NaHCO3 - 2,0 г - по ГОСТ 4201-79
Na2S-9H2O - 0,2 г - по ГОСТ 2053-77
В качестве восстановителей для питательных сред можно ис-
пользовать сульфид натрия, аскорбиновую кислоту и другие.
Все реактивы основной среды по'следовательно растворяют в 1 л
водопроводной воды. Добавки готовят каждую в отдельности.
Приготовление добавок
Добавки к основной среде готовят отдельно на дистиллирован-
ной воде:
— дрожжевой экстракт (5% водный раствор) — 1,0 г. Растворен-
ную в дистиллированной воде навеску дрожжевого экстракта тща-
тельно перемешивают, кипятят 20 минут и фильтруют через бумаж-
ный фильтр. Фильтрат вновь кипятят 20 минут и фильтруют через
мелкопористый бумажный фильтр;
— железо серно-кислое закисное — 0,5 г (готовят в виде 5%
раствора в 2 % растворе соляной кислоты);
— натрий сернистый (готовят 5% раствор в 5% растворе на-
трия углекислого кислого), после стерилизации используется не бо-
лее 7 дней.
Питательную среду и добавки разливают в колбы (добавки —
каждую в отдельности) не выше, чем на половину объема колбы,
5. 6. Приготовление питательных сред для микроорганизмов 265
закрывают ватными пробками и бумажными колпачками. Стерили-
зацию проводят в стерилизаторе паровом. Визуальный контроль ка-
чества паровой стерилизации проводят с использованием индикатор-
ной ленты, например «Комплайн 1222», для паровых стерилизаторов.
Появление окрашенных полосок на ленте свидетельствует, что сте-
рилизация проведена правильно.
С соблюдением приемов стерильности добавки вносят в основ-
ную среду непосредственно перед использованием питательной сре-
ды в следующем порядке: дрожжевой экстракт, затем железо серно-
кислое закисное, далее доводят pH среды до величины 7,3 с помощью
раствора бикарбоната натрия и затем вносят по каплям натрий сер-
нистый до образования темно-серой окраски среды. В готовом виде
среда Постгейта В содержит осадок.
2. Среда Постгейта С. Используют для накопления клеток СВБ
в лабораторной практике для исследовательских целей:
— калий фосфорно-кислый
однозамещенный КН2РО4 - 0,5 г - по ГОСТ 4198-75
— аммоний хлористый NH4CI - 1,0 г - по ГОСТ 3773-72
— натрий серно-кислый Na2SO4 - 4,5 г - по ГОСТ 6053-77
— кальций хлористый
6-водный СаС<2 • 6Н2О - 0,06 г - по ГОСТ 4209-77
— магний серно-кислый
7-водный MgSC>4 • 7НгО - 0,06 г - по ГОСТ 4523-77
— натрий молочно-кислый СгЩОзМа - 6,0 г - ТУ 6-09-3664-74
— натрий лимонно-кислый CgHaOyNa - 0,3 г - ГОСТ 22280-77
— дрожжевой экстракт 0,1 г - ТУ 6-09-3979-75
— железо серно-кислое
7-водное FeSO4 • 7НгО - 0,004 г - по ГОСТ 4148-78
266
Глава 5
— дистиллированная вода 1 л
— натрий хлористый NaCl — по мере надобности
3. Пептон-дрожжевая питательная среда. Для обнаружения
и количественного подсчета общего числа аэробных бактерий ис-
пользуют пептон-дрожжевую питательную среду, состоящую из сле-
дующих реактивов [64]:
— дрожжевой экстракт — 3,0 г;
— пептон — 5,0 г;
— дистиллированная вода — 1 дм3. (
— pH среды должен быть 7,2. При отклонении от заданного зна-
чения pH повышают добавлением стерильного раствора щело-
чи (NaOH).
Приготовленную среду нагревают на водяной бане до полного
растворения дрожжевого экстракта и пептона, фильтруют и устанав-
ливают pH.
Среду разливают в колбы не выше чем на половину объема кол-
бы, закрывают ватными пробками и бумажными колпачками. Стери-
лизацию проводят в стерилизаторе паровом в течение 15 минут.
Хранят питательные среды в холодильнике. Срок хранения
не более двух недель. Каждый сосуд должен иметь этикетку с обо-
значением состава, названия среды и времени ее приготовления.
4. Питательные среды для тионовых бактерий
Для Т. ferrooxidans. Среда Сильвермана и Лундгрена
(NH4)2SO4 - 3,00 г. MgSO4 - 0,50 г;
КС1 - 0,10 г. Ca(NO3)2 - 0,01 г;
5.6. Приготовление питательных сред для микроорганизмов 267
К2НРО4 - 0,50 г. FeSO4 - 30,00 г;
Дистиллированная вода — 1 л pH — 3,5.
Среда Летена
(NH4)2SO4 - 0,15 г. MgSO4 - 0,50 г;
КС1 0,05 г. Ca(NO3)2 - 0,01 г;
К2НРО4 - 0,05 г. FeSO4 - 1,00 г;
Водопроводная вода — 1 л pH — 3,5.
Для Т. thiooxidans. Среда Ваксмана и Иоффе
(NH4)2SO4 - 0,20 MgSO4 - 0,50
СаС12 - 0,25 К2НРО4 - 3,00
Fe2(SO4)3 - 0,001
Глава 6
Подавление жизнедеятельности СВБ
Достоинства и преимущества того или иного метода защиты ме-
талла от биологической коррозии зависят от огромного количества
факторов, главными из которых, на йаш взгляд, являются неорди-
нарные природные факторы. Об одном из таких природных факто-
ров упоминает G. Н. Booth (1971 г.). В 1950 г. при археологических
раскопках в Йорке были найдены многочисленные хорошо сохранив-
шиеся железные предметы, относящиеся к эпохе Римской Империи.
Все предметы были извлечены из почвы, в которой могли бы про-
текать очень интенсивные коррозионные процессы. В Лондонском
Гвилдхолл-музее также имеются археологические железные экспо-
наты, которые хорошо сохранились. Почвы, в которых были обна-
ружены хорошо сохранившиеся железные предметы, были черные,
болотистые, глинистые и иловые, т. е. представляли классическую
среду для активной анаэробной коррозии. Специальными методами
исследования удалось выяснить, что извлеченные железные предме-
ты покрыты тонкой, черной, компактной, плотно прилегающей к ме-
таллу пленкой, состоящей в основном из фосфата закиси железа —
ЗРеО РгОз -вНгО. Эта пленка и была тем защитным элементом, кото-
рый предохранял предметы от коррозии как в аэробных, так и в ана-
эробных условиях.
6.1. Физические методы
269
В настоящее время механизм образования этой высоко эффек-
тивной природной пленки не известен. Не известно также, может
ли быть искусственно воссоздан ее эквивалент. Очевидно, условия,
в которых она была создана, существенно отличаются от тех, в ко-
торых в настоящее время применяют промышленные «фосфатные»
покрытия, и от тех, при Которых обычно используют железные пред-
меты.
6.1. Физические методы
К физическим методам подавления жизнедеятельности СВБ от-
носят рентгеновское и ультрафиолетовое облучение, воздействие уль-
тразвуком, термическое воздействие, радиационное излучение, токи
высокой частоты и др. [28], [114], [135].
Ультрафиолетовое облучение. Обеззараживание воды ультра-
фиолетовыми лучами происходит в результате воздействия на микро-
организмы биологически активной части спектра. В качестве источ-
ника излучения могут быть использованы ртутно-кварцевые лампы.
На практике для стерилизации питьевых вод используют уста-
новки двух типов: с погружными и непогружными источниками бак-
терицидного излучения.
Установки первого типа имеют ряд преимуществ: возможность
размещения источников излучения над свободной поверхностью во-
ды, простота их изготовления и эксплуатации. Недостатком этих
установок является низкий коэффициент использования потока бак-
терицидного излучения.
Установки второго типа обеспечивают более высокое исполь-
зование бактерицидного излучения. Лампы в них помещают в спе-
270
Глава 6
циальных кварцевых чехлах, прозрачных для бактерицидных лучей.
К недостаткам данного метода стерилизации воды следует отнести
предъявление специальных требований к качеству обеззараживаемой
воды (отсутствие механических примесей, нефти, отложения солей
и т. п.).
Стерилизация водных сред наиболее эффективна при ультрафи- ‘
олетовом излучении с длиной волны 254 ... 257 нм [114]. Скорость
коррозии стали в облученных водах на 25... 50% ниже, чем в необ-
лученных благодаря подавлению жизнедеятельности СВБ, тионовых
и железобактерий [3], [28].
Ионизирующее излучение. Ионизирующее излучение обладает
высокой проникающей способностью, при этом эффект воздействия
зависит от дозы облучения. Нередки случаи, когда излучение в ма-
лых дозах стимулирует интенсивность жизненных процессов. Одна-
ко с возрастанием дозы излучения все резче проявляется угнетаю-
щее действие лучей, при котором изменяются морфологические и
физиологические свойства бактерий, задерживается их рост и раз-
множение. Дальнейшее увеличение дозы лучистой энергии вызывает
гибель бактериальной клетки.
Ультразвук. Бактерицидное действие ультразвука основано на
механическом разрушении бактерий в ультразвуковом поле. Действие
ультразвука распространяется в равной мере как на вегетативные, так
и на споровые формы микроорганизмов.
Эффективность действия ультразвука [135] определяет время
экспозиции и толщина водного слоя. Если при толщине слоя жид-
кости в 1 см за 1 мин погибает до 80% бактерий, то при увеличении
слоя до 8 см в тех же условиях погибает только 20% бактерий.
6.1. Физические методы
271
В институте УдмуртНИПИнефть исследования по подавлению
жизнедеятельности СВБ с помощью ультразвука проводились на уль-
тразвуковом диспергаторе мощностью 400 вт при частоте 22 и 44 кгц.
В первой серии исследования проводились на накопительной
культуре СВБ, выделенной из промысловых сред Чутырской площа-
ди, при ее введении в дистиллированную воду. Этим обеспечивалась
чистота эксперимента и отметались все побочные факторы, способ-
ные оказать какое-либо влияние на результаты эксперимента. Вторая
серия проводилась на сточной воде, отобранной с резервуара РВС-3
Гремихинского месторождения. Обработке подвергалась непосред-
ственно и сама вода, содержащая клетки СВБ. Результаты обработки
представлены в табл. 6.1.
Таблица 6.1. Влияние ультразвука на степень подавления СВБ
Частота обработки, кГц Культура СВБ Степень подавления СВБ, %, при времени воздействия, мин.
2 5
22 Накопительная культура 95 99
44 СВБ Чутырской площади 30 33,0
22 Сточная вода с РВС-3 23 25,6
Гремихинского
44 месторождения 0 7
Как видно из табл. 6.1, наиболее эффективное подавление жизне-
деятельности СВБ достигается при воздействии на них ультразвуком
с частотой 22 кгц.
272
Глава 6
Данный метод в настоящее время в нефтепромысловой практике
не применяется ввиду большой энергоемкости и малого КПД.
Гидродинамические вибраторы. Технология подавления жиз-
недеятельности СВБ с помощью гидродинамических вибраторов раз-
работана в ООО «ПермНИПИнефть» [69]. Схематическое изображе-
ние вибратора приведено на рис. 6.1.
Рис. 6.1. Гидродинамический вибратор: 1 — корпус; 2 - входная решетка;
3 — шелевое сопло; 4 — резонансная пластина; 5 — выходная решетка; 6 —
выходные отверстия
Устройство работает следующим образом. В натекающей на пла-
стину струе жидкости возникают автоколебания. Одновременно
с этим струя жидкости возбуждает в пластине ее собственные ко-
лебания. При совпадении частот этих колебаний наступает явление
резонанса, в результате чего амплитуда колебаний пластины резко
возрастает. Колебания пластины сопровождают излучения звука с ча-
стотой, равной собственной частоте колебаний пластины.
Излучение звука, при наличии острых кромок на входных от-
верстиях и резонансных пластинах, ведет к развитию кавитации.
6.1. Физические методы
273
Звук и кавитация стимулируют, в обрабатываемой гидродинамиче-
ским вибратором жидкости, протекание звуко-химических реакций,
в результате которых происходит расщепление молекул воды на сво-
бодные радикалы:
Н2О Н+ + ОН-.
Эксперименты показали [21], что в звуковом поле вибратора на-
блюдается уменьшение концентрации сероводорода. Это, вероятно,
обусловлено образованием в результате звуко-химических реакций
пероксида водорода Н2О2.
Подавление жизнедеятельности СВБ с помощью вибратора ис-
следовано в промысловых условиях путем сравнения микробиологи-
ческой зараженности проб воды, отобранных до и после аппарата,
установленного в систему водозабора.
Эффективность действия вибратора оценивалась в два эта-
па. На первом этапе скорость прохождения жидкости через вход-
ные отверстия гидродинамического вибратора задавалась в пределах
2,5... 2,6 м/с. На втором этапе скорость прохождения жидкости через
отверстия входной решетки увеличивалась до 3,9 ... 4,1 м/с за счет
отключения части входных отверстий. Результаты исследований [69]
отражены в табл. 6.2.
На первом этапе при низких скоростях натекания жидкости по-
ложительные результаты не были достигнуты. При увеличении ско-
рости жидкости на резонансных пластинах бактерии в пробах воды
после вибратора обнаружены не были. Учитывая вероятностный ха-
рактер определения СВБ в пробах воды, следует констатировать, что
вибратор если и не полностью уничтожает СВБ, то, по крайней мере,
подавляет их жизнедеятельность.
Глава 6
274
Таблица 6.2. Количественная характеристика бактериальной зараженности
проб в процессе воздействия вибратором
Номер серии Количество клеток в 1 мл жидкости
До вибратора После вибратора
Сразу после вибратора 0,25 протя- женности водовода В конце водовода
Скорость натекания жидкости на резонансные пластины 2,5 ..,. 2,6 м/с
1 9 Отс. — 45
2 45 25 — 25
Скорость натекания жидкости на резонансные пластины 3,9 ... 4,1 м/с
1 9 Отс. Отс. Отс.
2 9 Отс. Отс. Отс.
3 25 Отс. Отс. Отс.
Возможный механизм бактерицидного действия вибратора [69]
обусловлен тем, что при воздейсгвии звука на воду в присутствии
воздуха образуются пероксид водорода, азотистая и азотная кислоты.
Для биологических объектов образование даже небольшого количе-
ства этих реакционноспособных соединений может привести к за-
метным последствиям.
Схлопывание кавитационных пузырьков приводит к возник-
новению ударных волн с амплитудой до сотен МПа и к резко-
6.1. Физические методы
275
му, хотя и локальному, повышению температуры до 103 ... 104 ° К.
Вследствие акустической прозрачности клеточной оболочки кави-
тационные явления, обусловленные бегущей звуковой волной, мо-
гут происходить и внутри самой клетки. Исследованиями, проведен-
ными на растительных клетках, установлено [21], что ультразвуко-
вая обработка вызывает почти мгновенный разрыв объектов в поле
ультразвука за счет заключенных внутри этих организмов пузырь-
ков воздуха или находящихся в растительных клетках углекисло-
го газа.
Электрогидравлический эффект. Известен метод стерилиза-
ции воды путем применения электрогидравлического эффекта, со-
здаваемого высоковольтным импульсным разрядом в обрабатывае-
мой среде, сопровождающегося резким повышением температуры
гидравлического давления в канале разряда. Исследованиями уста-
новлено [17], что для обеззараживания пресной воды, зараженной
СВБ в концентрации 1012 клеток на 1 мл, достаточно 0,3 импульса
на 1 мл, а для зараженной модели пластовой воды с той же концен-
трацией СВБ — 3 импульса на 1 мл жидкости.
Радиационное излучение. Известны методы обеззараживания
питьевой воды гамма-излучениями. В качестве источника гамма-из-
лучения в установках используют радиоактивный кобальт (Сэ-
60) с периодом полураспада 5,3 года. Основная масса бактерий
(90%) погибает при относительно невысоких дозах облучения
(10000... 15000 Р).
В нефтепромысловой практике может быть использован метод
подавления жизнедеятельности СВБ радиационным облучением [93].
Для этих целей в скважину спускают контейнер, содержащий радио-
Глава 6
276
активный изотоп (Со-60 либо Zn-65). Метод позволяет уничтожать
бактерии, находящиеся в затрубном пространстве и окружающем
грунте.
Радиационное излучение а-, (3-, 7-лучами вызывает ионизацию
атомов и молекул, приводящих к патологическим изменениям в клет-
ках и отмиранию микроорганизмов. Так, например, 7-лучи эффек-
тивно подавляют жизнедеятельность СВБ при дозах 40... 80 крад,
причем действие их проявляется неодинаково в зависимости от пе-
риода инкубационного развития бактерий [1]. Наиболее устойчивой
к воздействию 7-лучей дозой 40 крад в среде Постгейта В является
семисуточная культура бактерий СВЕ>.
Рассматривая возможности применения физических методов по-
давления жизнедеятельности микроорганизмов в нефтепромысловых
средах, следует отметить следующие моменты.
При использовании методов радиационного и ультрафиолетово-
го облучения, ультразвукового воздействия и электрогидравлическо-
го эффекта стерилизация воды происходит только в пределах самой
установки. Данные способы не оказывают существенного влияния
на внутреннюю поверхность трубопроводов и тем более на пласт,
где происходит генерация сероводорода.
На зараженных СВБ и сероводородом месторождениях примене-
ние вышеперечисленных физических методов не приводит к стерили-
зации всей системы. Полная стерилизация системы в этих условиях
может быть достигнута только при сочетании физических и хими-
ческих методов, т. е. сначала химическими реагентами необходимо
стерилизовать внутреннюю поверхность трубопроводов и продук-
тивного пласта, а затем перейти к стерилизации закачиваемой воды
физическими методами. Ввиду отсутствия гарантий бесперебойной
6.2. Физико-химические методы
277
работы любой установки стерилизацию химреагентами необходимо
производить периодически.
6.2. Физико-химические методы
Исследование возможности использования
электрохимически активированных водных растворов
в качестве бактерицидов
В последние годы внимание ученых и специалистов различных
отраслей промышленности вновь привлечено к технологии электро-
химической активации воды (ЭХА) и водных растворов [4, 5, 19.
20, 48, 75, 116, 137], позволяющей управлять кислотно-щелочны-
ми и окислительно-восстановительными свойствами водных систем
и растворов различной степени минерализации и состава. В ре-
зультате такого воздействия водные растворы превращают в функ-
ционально новый продукт для различных технологических процес-
сов. В первую очередь это связано с тем, что высокая реакционная
способность электрохимически обработанной воды обуславливается
непосредственно высокой активностью действующих основ в соста-
ве воды при малой их концентрации и длительно существующими
структурно-энергетическими возбуждениями; во вторую — данная
технология является экологически чистой и безопасной.
Факторы реакционной способности электрохимически
активированных растворов
Электрохимически активированные растворы получают путем
обработки исходных водных разбавленных растворов минеральных
278
Глава 6
солей или воды в катодной или анодной камерах проточного диа-
фрагменного электрохимического реактора. Метод обработки водных
систем только в анодной или только в катодной камере реактора при-
нято называть электрохимической активацией, а получаемую воду
после такой обработки именовать либо анолитом, либо католитом,
переходящую в метастабильное состояние с повышенной реакцион-
ной способностью.
Термины «вода» и «растворы» здесь тождественны. В природе
не бывает совершенно чистой воды, поэтому даже дистиллят можно
считать очень разбавленным раствором.
Воду любого минерального состава и концентрации можно под-
вергнуть анодной или катодной электрохимической обработке и по-
лучить электрохимически модифицированный раствор — анолит или
католит соответственно.
Изменение физико-химических свойств и биологической актив-
ности воды в результате электрохимической обработки происходит
под воздействием электрического тока, который в проводниках пер-
вого рода (металлических проводах, электродах) переносится элек-
тронами, а в проводниках второго рода (растворах электролитов,
в т. ч. воде) — ионами.
Поступление электронов из катода в воду, так же как и удаление
электронов из воды в анод сопровождается целой серией электрохи-
мических реакций на поверхности катода и анода.
В результате этих реакций образуются новые вещества, изме-
няется вся система межмолекулярных взаимодействий, в том числе
изменяется и структура воды как растворителя.
Свойства воды, подвергнутой электрохимической обработке, ‘
определяет состав минеральных солей в исходной воде, а также вид
6.2. Физико-химические методы
279
и режим электрохимического воздействия. Обычно в результате ка-
тодной обработки любая вода, даже дистиллированная, которая со-
держит растворенные минеральные вещества, приобретает щелоч-
ную реакцию (от исходного pH - 7,5 до 12) за счет превращения
некоторой части растворенных солей в гидроксиды. В результате об-
работки воды изменяются физико-химические свойства:
— резко понижается окислительно-восстановительный потенци-
ал (ОВП) от исходного (+) 300 мВ до (—) 300... 800 мВ по шка-
ле индикаторного платинового -электрода относительно хлор-
серебряного электрода сравнения;
— уменьшается поверхностное натяжение;
— снижается содержание растворенных в воде кислорода, хлора,
азота;
— возрастает концентрация водорода, свободных гидроксильных
групп;
— уменьшается электропроводность;
— изменяется структура не только гидратных оболочек ионов,
но и свободного объема воды.
В результате образования хорошо растворимых гидроксидов на-
трия и калия и повышения вследствие этого pH, происходит сдвиг
углекислого равновесия с образованием трудно растворимых карбо-
натов кальция и магния из находящихся обычно в исходной воде рас-
творимых соединений этих металлов (гидрокарбонатов, хлоридов,
сульфатов).
Ионы тяжелых металлов и железа практически полностью вы-
падают в осадок в виде нерастворимых гидроксидов. При взаимо-
280
Глава 6
действии гидроксидов натрия и калия с углекислым газом воздуха
образуются растворимые карбонаты и гидрокарбонаты.
При анодной электрохимической обработке кислотность воды
увеличивается от исходного pH = 7 до pH = 2... 6, ОВП возрастает
от (4-) 300 мВ до (+) 400... 1200 мВ за счет образования устойчи-
вых и нестабильных кислот: серной, соляной, хлорноватистой, хло-
ристой, хлорноватой, хлорной, надсерных кислот, а также пероксида
водорода, пероксосульфатов, пероксокарбонатов, перхлоратов натрия
и калия, оксидов хлора и различных промежуточных соединений,
возникающих в процессе самопроизвольного распада и взаимодей-
ствия названных веществ. Также в результате анодной электрохими-
ческой обработки несколько уменьшается поверхностное натяжение,
увеличивается электропроводность, увеличивается содержание рас-
творенного хлора, кислорода, уменьшается концентрация водорода,
азота, изменяется структура воды.
Известны три фактора, ответственные за свойства электрохими-
чески активированных растворов.
Первый, обозначенный Ф1, указывает на наличие в католите ще-
лочей, а в анолите кислот, образовавшихся при электрохимической
обработке из растворенных в исходной воде солей. Чем больше ис-
ходное солесодержание воды и чем больше расход тока, тем выше
концентрация кислот в анолите и щелочей в католите. Кислоты и ще-
лочи являются стабильными продуктами электролиза.
Второй фактор (Ф2) — существование суперактивных соедине-
ний с высокой окислительной (в анолите) или восстановительной
(в католите) способностью. Эти соединения присутствуют в течение
нескольких десятков часов, после чего распадаются. Они обеспечи-
вают высокую окислительную биоцидную способность анолита, мо-
6.2. Физико-химические методы 281
ющие, экстрагирующие, пептизирующие, регенерационные (в биохи-
мических процессах), антиоксидантные свойства католита.
Третьим фактором (ФЗ) является нестабильная структура воды
и водных растворов, которая возникает под влиянием электрического
поля высокой напряженности (по 10 млн. вольт на сантиметр) у по-
верхности электрода. Этот фактор оказывает большое влияние на
тонкие физико-биологические реакции, такие как образование и рост
кристаллов, эпитаксиальных пленок, активация катализаторов и фер-
ментов. Структурные аномалии электрохимически активированного
раствора являются самыми нестойкими и релаксируются в течение
нескольких часов.
Для каждого из названных факторов активность электрохимиче-
ски обработанного раствора может существенно различаться в зави-
симости от физико-химических параметров исходной воды (раствора)
и условий электрохимической обработки.
Вклад каждого из факторов активности в общую реакционную
способность электрохимически активированных растворов показан
в табл. 6.3.
Свойства анолита. Анолит имеет очень высокую окислитель-
ную активность, достигающую значений ОВП порядка 1200 мВ. Ре-
жим анодной обработки исходной воды в электрохимическом реакто-
ре обеспечивают оптимальные условия образования диоксида хлора
(CIO2), который при ОВП +800 мВ превосходит по биоцидной ак-
тивности гипохлорит натрия (NaClO) более чем в 300 и более чем
в 2 раза — хлорноватистую кислоту (НС1О). Диоксид хлора в от-
личие от других соединений активного хлора (CI2, NaClO, Са(СЮ)о
и др.) не образует хлорорганических веществ при растворении в воде
и не увеличивает вследствие этого токсичность анолита.
282
Глава 6
Таблица 6.3. Соотношение факторов активности электрохимически активи-
рованных растворов
Тип исходного раствора воды в зависимости от минерализации Соотношение факторов активности электроактивированного раствора при 7<э. п. — 1
Номер группы минерализации Минерализация, г/л
1 Менее 3 ФЗ » Ф2 » Ф1
2 0,3. .. 1 ФЗ > Ф2 » Ф1
3 1.. .3 ФЗ = Ф2 > Ф1
4 3... 10 ' ФЗ < Ф2 < Ф1
5 10.. .35 ФЗ <S Ф2 <g Ф1
б 35... 100 Ф «С Ф2 С Ф1
7 100.. . 140 ФЗ «С Ф2 «С Ф1
8 140.. .340 ФЗ <S Ф2 <g Ф1
9 340 и выше ФЗ «С Ф2 С Ф1
Основными биоцидными агентами анолита являются двуокись
хлора, хлорноватистая кислота и неустойчивые суперактивные ча-
стицы:
С1’, О’, О3, ОН*,НО£, Н2О’, Н3О+, Н3О’.
В анолите нарушена система водородных связей. Молекулы во-
ды в объеме и в окружении сильно заряженных оксидатных ионов
имеют высокую подвижность. Это придает анолиту биологически ак-
тивные свойства. Прогнозирование биоцидных свойств анолита мо-
жет быть осуществлено посредством измерения содержания актив-
ного хлора (Са.х.)- Чем больше концентрация активного хлора, тем
6.2. Физико-химические методы 283
выше его биоцидная активность. Анолит с содержанием активного
хлора от 220 до 400 мг/л является дезинфицирующим и стерилизу-
ющим раствором. Оптимальным содержанием активного хлора, при-
дающим анолиту эффективные стерилизующие и дезинфицирующие
свойства, является 300 ± 50 мг/л.
Исследование эффективности использования электрохимически
активированных водных растворов в качестве бактерицидов прово-
дилось с нейтральным и кислым анолитом. Нейтральный и кислый
анолиты получены из водопроводной воды с использованием соот-
ветственно хлористого натрия и натриевых солей из пластовой воды.
Характеристика анолитов приведена в табл. 6.4.
Таблица 6.4. Характеристика анолитов
Показатели Значения
Нейтральный анолит Кислый анолит
Концентрация активного хлора, мг/л 400 200
Окислительно-восстано- вительный потенциал, мВ +845 +979
рн 6,9 1,5
Плотность, кг/м3 1008 1012
Минерализация, г/л 5,94 12,88
Проведенные согласно РД 39-3-973-83 оценочные исследования
эффективности анолитов-бактерицидов показали, что анолит, вве-
денный в пресную воду даже при малых концентрациях (1... 5%).
подавляет жизнедеятельность чистой культуры СВБ, выделенной
284
Глава 6
из промысловой среды, табл. 6.5. Установлено также, что эффек-
тивность анолита зависит от времени его контакта с культурой СВБ.
С увеличением времени воздействия анолита на СВБ повышают-
ся его бактерицидные свойства. Однако тот же анолит, введенный
в сточную воду при концентрациях до 10 %, недостаточно эффектив-
но подавляет жизнедеятельность содержащихся в ней клеток СВБ.
Промысловые испытания, проведенные на Чутырской площади,
позволили установить, что вводимый анолит поглощает находящийся
в сточной воде сероводород и подавляет жизнедеятельность СВБ.
Анолит нейтрализует сероводород и связывает его в комплексные
соединения, выпадающие в осадок. Результаты испытаний анолита
сведены в табл. 6.6.
6.3. Химические методы
Наиболее распространенным методом подавления жизнедея-
тельности микроорганизмов в нефтяных пластах является исполь-
зование химических реагентов.
По принципу действия химические реагенты, предназначенные
для подавления жизнедеятельности микроорганизмов, подразделяют
на окисляющие бактерициды, биодиспергенты и неокисляющие бак-
терициды [7].
Окисляющие бактерициды. Действие реагентов этой группы
основано на способности бактерицидов необратимо окислять груп-
пы протеинов, что приводит к утрате нормальной активности энзимов
и гибели клеток бактерий. Для этих целей используют технологиче-
ские процессы хлорирования и бромирования зараженных водных
сред и поверхностей.
Таблица 6.5. Влияние анолита на степень подавления жизнедеятельности сульфатвосстанавливающих
бактерий
Условия обработки Вид анолита Культура СВБ Содер- жание H2S, мг/л Степень подавления СВБ, %, при дозировке анолита, %
0,1 1 5 10 25 50 75 100
СВБ выдержаны с анолитом 4 часа Нейтральный Выделенная куль- тура СВБ с Чу- тырской площади 0 5 27 77 87 100 100 100 100
СВБ выдержаны с анолитом 24 часа Нейтральный 0 0 97 99 100 — — — 100
СВБ выдержаны с анолитом 24 часа Нейтральный Сточная вода с Гремихинского месторождения — 0 5 15 38 — — — —
СВБ выдержаны с анолитом 24 часа Кислый Сточная вода с Чутырской пло- щади 68 13 16,7 22,2 22 — — 88 100
СВБ выдержаны с анолитом 21 часа Кислый № 3 68 3,7 5,6 7,4 Н,4 — — 86 100
6.3. Химические методы 285
286
Глава 6
Таблица 6.6. Результаты промысловых испытаний анолита
Участок Количество СВБ, кл/мл Степень подавления СВБ, %
До обработки анолитом После обработки анолитом
Нагнетательная скв. 1103 1000 6,3 99,4
Нагнетательная скв. 1242 17 3,6 78,8
Хлорирование, по мнению специалистов фирмы Nalco Chemi-
kal Со., обязательно необходимо для контроля микробиологическо-
го роста. Рекомендуется применение хлорированных вод или гипо-
хлорита натрия. Выбор непрерывной или ударной обработки дела-
ют в зависимости от специфических условий каждого конкретного
случая.
Бромирование: из-за некоторых недостатков хлорирования фир-
ма Nalco Chemikal Со. предлагает использовать Акти-бром на базе
солей брома. Продукт применяют вместе с хлором, обеспечивая тем
самым уменьшение расхода хлора и увеличивая в то же время бакте-
рицидную эффективность реагента.
Биодиспергенты. Применяемые бактерициды обычно воздей-
ствуют на верхние слои биомассы. Для эффективного подавления ро-
ста микроорганизмов большое значение имеет способность биодис-
пергентов к проникновению через образовавшиеся отложения с це-
лью уничтожения анаэробных бактерий, например СВБ.
Неокисляющие бактерициды. Для улучшения эффекта бакте-
рицидной обработки фирма предусматривает дополнительное при-
6.3. Химические методы
287
менение неокисляющих бактерицидов, в качестве которых обычно
применяют:
— органические соединения брома для селективного удаления спе-
цифичных микроорганизмов;
— органические соединения олова для удаления аэробных бакте-
рий. Соединения инициируют образование комплексов протеи-
нов с группами аминокислот и карбоновой кислоты, блокируя
метаболизм клетки;
— органические соединения серы эффективны против водорослей
и плесени. Соединения характеризует низкая токсичность по от-
ношению к животным;
— четвертичные амины эффективны против анаэробных бакте-
рий.
Подавление жизнедеятельности бактерий может быть осу-
ществлено как органическими, так и неорганическими соедине-
ниями.
Неорганические соединения. Из неорганических соединений
наиболее известны соляная и серная кислоты, кислород, озон,
хроматы, медный купорос, бура, каустическая сода, хлорная из-
весть [59]. Реагенты CuSC>4, СгС1г, ZnCh, К2СЮ4, К2СЮ7 эф-
фективно подавляют жизнедеятельность СВБ при концентраци-
ях 0,005...0,02 г/л [114]. Однако применение кислот, кислорода,
озона, медного купороса для подавления жизнедеятельности СВБ со-
провождается повышением коррозионной агрессивности вод, поэто-
му эти соединения могут быть использованы только в сочетании с ме-
рами, обеспечивающими снижение коррозионной активности водных
сред.
288
Глава 6
Хроматы угнетают СВБ и являются также ингибиторами корро-
зии, но они действуют и на человека, вызывая дерматиты, что делает
нежелательным их применение.
Ионы тяжелых металлов (Hg, Си) благодаря большому сродству
к SH-группам активных центров ферментов обладают заметно выра-
женными бактерицидными свойствами [103].
Известен способ подавления СВБ с использованием хлора, ко-
торый генерируют непосредственно в призабойной зоне пласта на-
гнетательной скважины методом электролиза [128]. За счет этого ис-
ключают непосредственный контакт хлора с металлом и процесс его
коррозии. '
Органические соединения. В нефтепромысловой практике в 80-е
годы на месторождениях Калиновско-Новостепановском, Узень, объ-
единениях «Татнефть» и «Башнефть» широко использовался в каче-
стве реагента для подавления СВБ формалин [17, 59, 102]. Данный
реагент в виде 0,1... 0,2 % раствора закачивался в призабойную зону
нагнетательных скважин. Продолжительность эффекта по подавле-
нию биоценоза составляла от 2 до 12 мес. При этом после обработок
было отмечено увеличение приемистости скважин от 4 до 70 %.
Для подавления жизнедеятельности широко используют реаген- *
ты на основе четвертичных солей аммония, например, алкилтриме-
тиламмонийхлорид, алкилбензилдиметиламмонийхлорид, алкилбен-
золпиридинийхлорид и др. Эффективность действия реагентов этой
группы может быть объяснена катионной структурой соединений
и способностью их растворения в фосфолипидных слоях клеточной
оболочки, вызывая при этом их разрушение [114]. Более подробно
использование химических реагентов для борьбы с СВБ будет рас-
смотрено в следующей главе.
6.3. Химические методы
289
Увеличение стойкости конструкционных сталей
Одним из превентивных методов борьбы с СВБ является замена
материалов нефтепромыслового оборудования на материалы, стойкие
к сероводородной коррозии и сульфидному растрескиванию метал-
лов.
Сульфидное растрескивание имеет электрохимическую природу
и при этом степень локального или селективного растворения или во-
дородного охрупчивания контролируется электрохимическими пара-
метрами системы, прежде всего pH. В большинстве случаев сульфид-
ного растрескивания трубных сталей микротрещины инициируются
неметаллическими включениями и аномальной структурой — продук-
том низкотемпературного преобразования (мартенситом и бейнитом),
который обогащен марганцем и фосфором.
Увеличение стойкости конструкционных сталей к сульфидному
растрескиванию возможно путем их легирования, однако возможно-
сти довольно ограничены. Легирование обеспечивает их долговре-
менную коррозионную прочность лишь при критических пороговых
напряжениях не более 690... 700 МПа [55].
Глава 7
Подавление сульфатредукции
бактерицидами
Защита от микробиологической коррозии не предполагает ис-
пользования каких-либо особых специальных средств. Самым про-
стым и надежным способом борьбы с биологической коррозией
является создание таких условий, при которых достигается полная
ликвидация первоисточника, т. е. устранение микроорганизмов, ее
вызывающих, но это чаще всего практически не выполнимо. Ис-
ключение составляют закрытые системы в виде баков, цистерн для
хранения горючего, холодильные установки, теплообменники и т. п.
Однако и в этих случаях требуется тщательная предварительная ме-
ханическая или химическая очистка внутренней поверхности с по-
следующим использованием эффективных бактерицидов.
Ингибиторы микробиологической коррозии по характеру воз-
действия на СВБ можно подразделить на два типа. Первый относит-
ся к «биоцидам», которые убивают организмы, второй — к «биоста-
там», которые угнетают рост и инактивируют процессы жизнедея-
тельности. Различие между этими двумя типами довольно условное
и заключается прежде всего в выборе концентрации применяемо-
го реагента: вещество может быть бактериостатическим при низкой
Подавление сульфатредукции бактерицидами 291
концентрации и бактерицидным — при более высокой. Эффективный
«бактериостат» может никогда не стать «бактерицидом».
К бактерицидам и ингибиторам микроорганизмов, вызывающих
коррозию, должны быть предъявлены следующие требования:
1. Реагенты должны прочно соприкасаться с микроорганизма-
ми. При использовании ингибиторов должна быть учтена его специ-
фичность к организму, против которого направлено действие реаген-
тов.
2. Бактерициды должны сохранясь свои ингибирующие и бакте-
рицидные свойства, т. е. они не должны инактивироваться другими
веществами. Реагенты должны быть устойчивыми к заданной темпе-
ратуре системы и должны быть веществами, к которым микроорга-
низм не развивает устойчивости и привыкания.
3. Бактерицид не должен сам оказывать какое-либо коррозион-
ное действие на систему, в которой применяется.
В каждом конкретном случае при выборе бактерицида и оп-
тимальной концентрации его применения должен быть индиви-
дуальный подход. Например, на спорообразующие термофильные
сульфатвосстанавливающие бактерии Dtm. nigrificans будет оказы-
вать достаточное бактериостатическое действие 0,25 мг/л глюкона-
та хлоргексидина, на мезофильный штамм D. vulgaris — 2,5 мг/л,
на D. desulfuricans 10 ... 25 мг/л, а облигатный галофил D. salexigenes
будет устойчивым к 1000 мг/л [140].
Исследование характера подавления жизнедеятельности микро-
организмов различных физиологических групп показало, что для
каждой группы микроорганизмов характерна своя строго определен-
ная эффективная концентрация [95]. Наибольшая массовая концен-
трация требуется для гетеротрофных бактерий, табл. 7.1.
292
Глава 7
Таблица 7.1. Эффективная концентрация подавления жизнедеятельности
бактерий
Реагент Массовая концентрация реагентов, %, при которой полностью подавляется жизнедеятельность
СВБ ДНБ ГТБ
Глутаровый альдегид 0,0025 0,02 0,1
СНПХ-1002м ОД 0,1 0,3
ЛПЭ-11 в 0,02 0,05 0,3
Азин-6 0,02 0,05 0,3
Соляная кислота, 12 % 1,0 1,0 2,0
Полученные результаты свидетельствуют об избирательном ха-
рактере подавления жизнедеятельности бактерий, среди которых
наиболее трудно удаляемыми бактериями являются ГТБ. Для их
подавления требуются более высокие концентрации биоцидов. Сле-
дует также отметить возможность подавления бактерий соляной кис-
лотой при массовой концентрации 2% и суточном с ними кон-
такте.
Большинство сульфатредуцирующих бактерий угнетается 20...
50 мг/л Си2+, но это свойство не может служить основанием для со-
здания защитных структур железных конструкций, поскольку в сре-
дах, содержащих до 200 000 мг/л Си2+, интенсивно развиваются тио-
бациллы.
Подбор возможных эффективных бактерицидов предварительно
осуществляют в лабораторных условиях, но поскольку их резуль-
таты не могут быть напрямую перенесены в промысловые условия,
7.1. Тестирование бактерицидов
293
то проводят и пилотные испытания, являющиеся необходимым и обя-
зательным дополнением к лабораторным исследованиям.
7.1. Тестирование бактерицидов
Оценка бактерицидной зффективности реагентов
относительно планктонных клеток СВБ
Оценку бактерицидной эффективности реагентов относительно
планктонных клеток СВБ проводят по следующей методике.
В ряд маркированных, герметически закрывающихся пробирок
вместимостью 25... 30 см3 дозируют исследуемый реагент в задан-
ной концентрации (например, 100,200,... ,500 мг/дм3). Приливают
стерильную минерализованную воду, состав которой соответствует
сточной воде месторождения, где предполагается испытание реаген-
та. Двух- трехсуточную накопительную культуру СВБ тщательно пе-
ремешивают, отбирают стерильной пипеткой и вносят в каждую про-
бирку в количестве 5... 10% по отношению к объему пробирки.
После этого пробирки доливают доверху минерализованной водой,
герметично закрывают резиновой пробкой, перемешивают и выдер-
живают при комнатной температуре от 1 до 24 часов. Для выбора
оптимальных параметров технологического режима использования
биоцида концентрацию реагента и время контакта бактерий с ним
варьируют. После заданной выдержки из каждой пробирки стериль-
ной пипеткой отбирают по 5 см3 жидкости и высевают в пробирки
с питательной средой Постгейта В (допускается использование пе-
нициллиновых флаконов с питательной средой, но тогда высев СВБ
производят стерильным шприцем по 1 см3), герметично закрывая
их резиновыми пробками. Пробирки инкубируют при температуре
294
Глава 7
32° С в течение 15 дней. О росте и развитии СВБ судят визуально по
помутнению среды и образованию черного осадка сульфида железа.
Отсутствие мути и черного осадка свидетельствует о полном подав-
лении роста популяции. Реагент, обеспечивающий подавление роста
микроорганизмов, проявляет бактерицидную эффективность (явля-
ется бактерицидом). Самая низкая концентрация бактерицида, при
которой прекращается рост и развитие популяции, обозначается как
минимальная подавляющая концентрация (МПК).
Для каждой концентрации проводят три параллельных исследо-
вания. Три пробирки без добавления реагента служат контрольной
пробой. '
Одновременно в качестве стандартного реагента сравнения, яв-
ляющегося бактерицидом, исследуют двухромовокислый калий (или
фенол). Контролем стерильности среды являются три пробирки с пи-
тательной средой, не инокулированной бактериями.
Оценка бактерицидной эффективности реагентов
относительно планктонных клеток аэробных бактерий
Испытание реагентов относительно накопительной культуры
аэробных бактерий проводят в той же последовательности, как и от-
носительно СВБ, с той лишь разницей, что высев аэробных бактерий
проводят на пептон-дрожжевой среде.
О росте и развитии аэробных бактерий судят по помутнению
питательной среды. Прозрачность среды свидетельствует о полном
подавлении роста популяции. Реагент, обеспечивающий подавление
роста популяции, проявляет бактерицидную эффективность. Самая
низкая концентрация бактерицида, при которой прекращаются рост
и развитие популяции, обозначается как МПК.
7.1. Тестирование бактерицидов
295
Оценка бактерицидной эффективности реагентов
относительно адгезированных клеток
Оценку бактерицидной эффективности реагентов относительно
адгезированных клеток СВБ проводят согласно методологическим
подходам, изложенным в РД 30-0147103-350-89. Методика разрабо-
тана для скрининга реагентов относительно адгезированных на ме-
таллической поверхности СВБ в лабораторных условиях.
Адгезия бактериальных клеток СВБ на поверхности нефте-
промыслового оборудования осуществляется с помощью продуци-
руемых ими внеклеточных биополимеров — полисахаридов, кото-
рые играют роль барьера, предохраняющего клетки от воздействия
неблагоприятных факторов внешней среды, в том числе и бактери-
цидов.
Сущность метода заключается в следующем. Образцы в виде
дисков диаметром 10 мм и толщиной 2 мм, выполненных из ма-
лоуглеродистой стали, для колонизации бактериями выдерживают
в активной культуре СВБ. Затем адгезированные СВБ в течение опре-
деленного времени подвергают действию испытуемого реагента в за-
данной концентрации. Далее, с целью выявления жизнеспособности
адгезированных СВБ, образцы помещают в питательную среду Пост-
гейта В.
Металлические образцы тщательно обезжиривают, промывают
водой, опускают на 5 минут в водный раствор соляной кислоты (раз-
бавление 1 :1), снова промывают водой и затем обрабатывают 70%
раствором этанола. Подготовленные образцы помещают на дно сте-
рильной колбы объемом 250... 300 см3, куда последовательно вно-
сят среду Постгейта В и накопительную двух-трехсуточную куль-
туру СВБ в количестве 5... 10 % от объема среды, закрывают гер-
296
Глава 7
метично пробкой и помещают в термостат при температуре 32° С
на 5... 7 дней. За этот период инкубации на металле формируется
биопленка, представляющая собой колонию клеток СВБ, «фиксиро-
ванную» на поверхности выделяемыми ими биополимерами.
Количество металлических образцов определяют исходя из чис-
ла испытуемых реагентов, задаваемых концентраций, времени вы-
держки, параллельности испытаний.
Для определения биоцидной активности реагентов в ряд марки-
рованных стерильных пробирок объемом 20... 25 см3 вводят опреде-
ленное количество испытуемого бактерицида (например, 100,200,...,
500 мг/дм3) и приливают стерильную минерализованную воду, со-
став которой соответствует сточной воде месторождения, где пред-
полагается дальнейшее испытание реагента.
Образцы со сформировавшейся на них биопленкой по одному
достают из пробирок стерильным пинцетом и помещают в пробир-
ки с реагентом, герметично закрывая их резиновой пробкой. Пробы
выдерживают при комнатной температуре от 1 до 24 часов.
Выдержанные в реагенте образцы с адгезированными клетками
помещают в пробирки с питательной средой Постгейта В и инкуби-
руют в термостате в течение 15 суток при температуре 32° С.
О росте и развитии СВБ судят визуально по образованию черно-
го осадка сульфида железа, распространяющегося от образца вверх
по объему среды. Отсутствие черного осадка свидетельствует о пол-
ном подавлении роста адгезированных СВБ. Самая низкая концен-
трация, при которой прекращается рост и развитие адгезированных
СВБ, обозначается как МПК.
Для каждой концентрации проводят три параллельных опре-
деления. Три образца, не бывшие в контакте с реагентом, служат
7.1. Тестирование бактерицидов
297
для контроля роста бактерий. Три пробирки с питательной сре-
дой служат для контроля стерильности. Одновременно в качестве
стандартного бактерицида сравнения испытывают двухромовокис-
лый калий.
В качестве примера приводим результаты испытаний бактери-
цидов на накопительной культуре СВБ, выделенной из промысловой
среды Чутырской площади.
Испытания осуществлялись в соответствии с [98]. Методика экс-
перимента заключалась в следующем:
1 этап — выращивание адгезированных к поверхности металла
клеток СВБ в течение 7... 10 суток;
2 этап — обработка пластин металла с адгезированными клетка-
ми СВБ бактерицидами заданной концентрацией в течение 2... 24 ча-
сов;
3 этап — культивирование адгезированных СВБ в питательной
среде в течение 15 суток.
Каждая концентрация реагента испытана в трехкратной повтор-
ности. Результаты исследований представлены в табл. 7.2.
Из представленных результатов видно, что наиболее эффек-
тивными реагентами по подавлению адгезированной культуры СВБ
являются бактерициды Сонцид-8102 и СНПХ-1050 с дозировками
1000 и 3000 мг/л соответственно. Низкая бактерицидная активность
Сонцид-8101 обусловлена, очевидно, тем, что в результате его дли-
тельного применения на Чутырском месторождении произошла неко-
торая адаптация микроорганизмов к реагенту.
Интересно отметить, что реагент Азимут-14Б, который является
ингибитором коррозии, также проявляет некоторую бактерицидную
активность по отношению к адгезированным клеткам СВБ.
298
Глава 7
Таблица 7.2. Влияние реагентов на адгезированные клетки СВБ
Реагент Время культиви- рования, сут. Холостая проба Концентрация реагента, мг/л
100 250 500 1000 3000
СНПХ-1050 5 + + + — — —
10 + + + + + —
15 + + + + + —
Сонцид-8101 5 + + + + +/— —
10 + + + + + +
15 + ' + + + + +
Сонцид-8102 5 + + + — — —
10 + + + +/“ — —
15 + + + + — —
Азимут-14Б 5 + + + — — —
10 + + + + + +
15 + + + + + +
Примечание: «—» — отсутствие роста бактерий
«+» — наличие роста бактерий
Оценка эффективности бактерицидов по подавлению СВБ
в призабойной зоне нагнетательной скважины по содержанию
сероводорода и сульфатов
Оценку эффективности применения бактерицида по подавлению
СВБ в призабойной зоне нагнетательных скважин производят при
сопоставлении результатов химического анализа воды при изливе
нагнетательных скважин до и после закачки реагентов.
7.1. Тестирование бактерицидов
299
Для этого в отобранных пробах воды определяют содержание се-
роводорода и сульфат-иона. Результаты представляют в виде графика
зависимости концентрации сероводорода и сульфат-иона от количе-
ства излившейся воды (C-Q). Из графика, по разности содержания се-
роводорода и сульфат-иона до и после закачки реагента, определяют
степень эффективности бактерицидной обработки Z(h2s) и ^(so2'):
Z(H2S) = • 100%,
где С, Ci — установившиеся значения концентрации сероводоро-
да в воде при изливе нагнетательной скважины до и после закачки
реагента, мг/дм3; Сд — концентрация сероводорода в закачиваемой
воде, мг/дм3;
Qi _ (ji
Z(v.2-x = -4----: • 100%;
(s°4 ) сг2-Сг
С1, С1} — установившиеся значения концентрации сульфат-иона в во-
де при изливе нагнетательной скважины до и после закачки реаген-
та, мг/дм3; С2 — концентрация сульфат-иона в закачиваемой воде,
мг/дм3.
Определение эффективности бактерицидов электрохимическим
методом
Несмотря на широкую гамму промышленно выпускаемых бакте-
рицидов, эффективность их зачастую достаточна низка, что связано,
с одной стороны, с высокой устойчивостью закрепленных форм ми-
кроорганизмов к воздействию химических реагентов вообще, с дру-
гой, — с особенностью методик испытания ингибиторов и бактери-
цидов, не учитывающих существования биообразований и исполь-
300
Глава 7
зующих свободноплавающие планктонные формы микроорганизмов
для определения эффективности их подавления [25]. Что касается
микробиологической составляющей коррозии, то существующими
методами, описываемыми в РД, ТУ, СТО, определить вклад микро-
организмов в суммарный процесс коррозии вообще затруднительно.
Защитный эффект ингибиторов в условиях краткосрочного экспери-
мента, длящегося 6 часов, дает представление о подавлении лишь
фоновой, а не биологической коррозии. В длительных эксперимен-
тах гравиметрические методы дают искаженные результаты из-за
невоспроизводимости, что связано с невозможностью стандартиза-
ции удаления биообразований и продуктов коррозии в процессе экс-
периментов [65]. Наиболее приемлемые методы исследований бази-
руются на использовании высокочувствительных электрохимических
методов, позволяющих изучить макрокинетику растворения металла
в коррозионных средах.
В качестве основной измеряемой величины, характеризующей
скорость процессов в системе, определяют ток коррозии (/к) в сте-
рильных и зараженных образцах исследуемой воды.
Наглядным примером эффективности данного метода исследо-
ваний являются результаты электрохимических замеров, полученных
при оценке эффективности подавления микроорганизмов бактери-
цидами ЛПЭ-11, Сонцид, Бактирам 401, СНПХ-1001, СНПХ-1002
и СНПХ-1004 в сточной воде Южно-Сергеевского месторождения
Башкирии, содержащей сульфатвосстанавливающие, гетеротрофные
и углеводородокисляющие бактерии в концентрациях, соответству-
ющих 101, 102, 104 клеток в см3. Результаты исследований соглас-
но [65] отражены на рис. 7.1, а численные значения тока коррозии
сведены в табл. 7.3.
7.1. Тестирование бактерицидов
301
Таблица 7.3. Изменение тока коррозии в электрохимической системе с водой
во времени
Время, час Концент- рация, мг/дм3 Ток коррозии, 1к, 10 6
ЛПЭ-11 Сонцид Бакти- рам 401 снпх
1001 1004 1002 1005
126 100 129,Г 135,5 135,2 134,8 134,6 134,2 134
132 126,7 133,7 133,6 133,5 133,4 132,7 132,2
138 126,7 133,7 133,6 133,5 133,4 132,7 132.2
144 126,7 133,7 133,6 133,5 133,4 132,7 132,2
150 200 110,7 133,1 132,2 130,8 130,4 128,6 128.2
156 106,3 132,3 131,2 130,2 129,8 128 127.9
162 105,8 132,3 131,8 130,2 129,8 128 127.9
168 105,8 132,3 131,8 130,2 129,8 128 127.9
174 300 87,1 131,8 131,2 129,1 128,7 126,7 126.3
180 80,3 131,1 130,8 128,6 128,1 126 125,8
186 78,6 131,1 130,8 128,6 128,1 126 125.8
192 78,6 131,1 130,8 128,6 128,1 126 125.8
198 400 71,3 130,3 129 127,8 127,1 125,2 124,5
204 68,8 129,2 128,8 126,1 125,8 123,2 122.8
210 68,8 129,2 128,8 126,1 125,8 122,5 121.9
216 68,8 129,2 128,8 126,1 125,8 122,5 121.9
222 500 62,3 128,1 127,6 125,2 124,9 118,3 117.8
228 61,4 127,3 125,1 121,9 121,1 116,9 116.2
234 61,4 127,3 125,1 121,9 121,1 116,9 116.2
246 600 61,4 118,4 116,3 114,1 113,9 112,3 110.7
252 61,4 116,1 114 112,1 111,2 108,1 106.5
258 61,4 116,1 114 109,2 108,6 106.5 104.3
264 61,4 116,1 114 109,2 108,6 106.5 104.3
302
Глава 7
Продолжение табл. 7.3
Время, час Концент- рация, мг/дм3 Ток коррозии, 1к, 10 6
ЛПЭ-11 Сонцид Бакти- рам 401 СНПХ
1001 1004 1002 1005
270 700 61,4 108,2 106,1 104,1 102,8 96,7 94,8
276 61,4 106,3 104,2 100,1 98,7 90,3 88,4
282 61,4 104,2 102,1 98,1 96,7 90,3 88,4
288 61,4 104,2 102,1 98,1 96,7 90,3 88,4
294 800 61,4 93,3 91,2 86,3 84,7 82,7 80,9
300 61,4 92,1 90 84,6 83,2 78,1 76,2
306 61,4 91,7 ' 89,6 83,2 81,7 77,6 75,9
312 61,4 91,7 89,6 83,2 81,7 77,6 75,9
318 900 61,4 84,8 82,7 78,8 76,5 69,2 67,4
324 61,4 76,2 74,1 72,2 70,5 64,3 62,5
330 61,4 74,5 72,3 64,8 63,8 63,5 61,3
336 61,4 74,5 64,6 64,6 63,8 63,5 61,3
342 1000 61,4 66,2 62,7 62,7 62,6 62 61,3
348 61,4 63,9 61,3 61,3 61,3 61,9 61,3
354 61,4 62,1 61,3 61,3 61,3 61,9 61,3
Исследование кинетики развития коррозионного процесса поз-
воляет решать две задачи.
Первая — оценка влияния микроорганизмов на кинетику раз-
вития коррозионного процесса. В стерильной среде, не содержащей
микроорганизмы, (8) наблюдается стабильная величина тока корро-
зии, /к — 60 мкА. Относительно высокая агрессивность химической
составляющей коррозии не идет в сравнение с таковой для среды
с активными микроорганизмами. Так, за 72 ч развития коррозионного
7.1. Тестирование бактерицидов
303
Рис. 7.1. Кинетика развития коррозионного процесса в среде, содержа-
щей микроорганизмы и бактерициды: 1 — ЛПЭ-11; 2 — СНПХ-1004; 3 —
СНПХ-1005; 4 — Сонцид; 5 — Бактерицид 401; 6 — СНПХ-1002; 7 —
СНПХ-1001; 8 — стерильная среда, 1К = 60 мкА
процесса и выхода тока на стационарный уровень (плато) ток возрас-
тает более чем в два раза, т. е. вклад биологической составляющей
становится весьма существенным. Нарастание тока в течение 3 сут
происходит практически непрерывно, с незначительным начальным
стабилизационным периодом (1... 3 часа). Такая особенность элек-
трохимического поведения стали Ст. 20 нехарактерна для обычных,
не содержащих микроорганизмы, высокоагрессивных сред, где выход
на плато определяется интенсивным расходом компонентов повы-
шенной агрессивности, таких как растворенные газы, кислоты и т. п.,
после чего устанавливается стационарный режим растворения метал-
ла. Для случая с введенными микроорганизмами кинетика электрохи-
304
Глава 7
мического поведения металла имеет вид химической реакции, разви-
тие которой определяет скорость формирования биопленки. По окон-
чании роста биообразований устанавливается новый стационарный
режим процесса, длительность которого неопределенно долгая.
Вторая — эффективность подавления процесса коррозии хими-
ческими реагентами. Изменение тока коррозии исследуемых хими-
ческих реагентов отражено на правом склоне коррозионных кривых.
Полученные результаты позволяют по степени снижения значе-
ния тока коррозии оценить эффективность подавления коррозионных
процессов. Так, установлено, что бактерицид ЛПЭ-11 при концен-
I
трациях 500 мг/л полностью подавляет микробную составляющую
процесса. Значительно ниже эффективность других химических реа-
гентов — от 800... 900 мг/л и выше.
Кинетические кривые тока коррозии позволяют оценить величи-
ну дополнительного расхода реагентов бактерицидов на преодоление
явления своеобразного «последействия» биообразований — поверх-
ность металла с «подавленными» биоценозами оказывается невос-
приимчивой к дальнейшему ингибированию. В результате этого кор-
розионный ток с увеличением концентрации реагентов не снижается,
что обуславливает появление полочек (ступенек) на правых ветвях
кинетических кривых.
7.2. Влияние физико-химических факторов
на эффективность бактерицидов
Влияние адсорбции бактерицидов на их эффективность
Максимальная эффективность подавления бактерицидами суль-
фатредукции в продуктивном пласте зависит от множества факторов
7.2. Влияние физико-химических факторов
305
и, прежде всего, от характера взаимодействия реагентов с породой
пласта и нефтепромысловым оборудованием. Наивысшую степень
подавления закрепленных и планктонных форм бактерий обеспечат
лишь оптимальные дозировки бактерицидов в местах развития ми-
кроорганизмов. При этом необходимо учитывать их адсорбционную
способность, поскольку реагенты с высокой адсорбционной способ-
ностью могут потерять свою активность уже на первом этапе после
закачки в призабойную зону скважины в результате сорбции породой
пласта.
Судить о степени адсорбции на практике по изменению их кон-
центрации не всегда удается из-за сложности и трудоемкости методик
и многокомпонентности составов промышленных бактерицидов.
В связи с этим адсорбционную способность реагентов-бактери-
цидов можно оценивать по изменению их активности в водной фазе
до и после контакта с породой пласта. Исследования, например, для
терригенных коллекторов проводят по следующей методике. В ряд
конических колб вместимостью 100 см3 вносят по 10 г кварцевого
песка и 30 см3 водного раствора исследуемого бактерицида, интен-
сивно перемешивают на встряхивателе в течение 2 час и центрифуги-
руют. Бактерицидную активность водного раствора реагентов опре-
деляют до и после его контакта с песком известным методом. Степень
подавления СВБ рассчитывают по содержанию сероводорода в кон-
трольных и опытных пробах. Результаты степени подавления культу-
ры СВБ на примере штамма DY-2198 ВКМ [130] показаны в табл. 7.4.
Из представленных результатов видно, что после контакта
с кварцевым песком активность водных растворов бактерицидов по
сравнению с первоначальной изменяется. Так, заметно снижается
степень подавления СВБ водными растворами АНП-2, СНПХ-1002,
306
Глава 7
Таблица 7.4. Степень подавления СВБ бактерицидами до и после адсорбции
биоцида на кварцевом песке
Бактерицид Степень подавления СВБ, %, до/после адсорбции при исходной массовой концентрации бактерицида, кг/м3
од 0,25 0,5 1,о 5,0
Формалин 51/38 100/100 100/100 — —
АНП-2 87/32 100/38 100/38 — —
СНПХ-1002 — 85/30 92/43 100/57 100/82
Дон-2 — — / 100/78 100/94 100/98
Дон-52 100/70 100/90 100/100 — —
СК-492 100/55 100/100 100/100 — —
Ск-601 100/100 100/100 100/100 — —
Корексит-7670 100/72 100/100 100/100 — —
Корексит-7671 100/100 100/100 100/100 — —
ЛПЭ-6 — — 100/94 100/100 —
ЛПЭ-9 37/35 100/83 100/100 100/100 —
ЛПЭ-11 100/100 100/100 100/100 100/100 —
Дон-2. Реагенты СК-601, ЛПЭ-11, Корексит-7671 практически не
снижают свою активность и могут быть рекомендованы для борь-
бы с СВБ.
Влияние времени контакта бактерицида с СВБ
на их жизнедеятельность
Влияние времени контакта бактерицида с СВБ на их жизнеде-
ятельность исследовано в работе [43]. Методология этих исследова-
7.2. Влияние физико-химических факторов 307
ний заключалась в следующем. В пенициллиновые флаконы, запол-
ненные пресной водой, добавляли растворы тестируемых реагентов
в различной концентрации и вносили СВБ, концентрация клеток ко-
торых в 1 мл достигала 105. В контрольные флаконы реагенты не
вводили. Через 3... 10 сут проводили посев в питательную среду
Постгейта. Поскольку при проведении исследований СВБ развива-
лись в ограниченном объеме среды, к которой не добавляли пита-
тельных веществ и из которой не выводили продуктов метаболизма,
то часть клеток отмирала естественным путем. В связи с этим в ходе
эксперимента вели наблюдение и за количеством жизнеспособных
клеток в контрольных флаконах.
Результаты показали, что с увеличением времени контакта бак-
терицида СНПХ-1004 с СВБ степень подавления роста бактерий зна-
чительно возрастает, табл. 7.5. Так, добавление 15 мг/л бактерицида
приводит к 100%-ному подавлению жизнедеятельности СВБ через
4 суток выдержки реагента с бактериями. При увеличении времени
реагирования СНПХ-1004 с СВБ до б сут биоцидный эффект прояв-
ляется при концентрации 10 мг/л, до 8 сут — 5 мг/л. Причем сни-
жение биоцидной концентрации реагента в процессе эксперимента
не коррелирует с естественным изменением количества клеток бак-
терий.
Результаты исследований показывают также, что время подав-
ления жизнедеятельности СВБ напрямую зависит от концентрации
используемого бактерицида, рис. 7.2.
Изменение бактерицидных концентраций ингибиторов корро-
зии — бактерицидов СНПХ-1003 и НАПОР-1007 в зависимости от
времени реагирования приведено на рис. 7.3. Из него видно, что
при воздействии, например, реагентом НАПОР-1007 бактерицидный
308
Глава 7
Таблица 7.5. Влияние времени контакта СНПХ-1004 с СВБ на степень по-
давления роста микроорганизмов
Время контакта реагента с СВБ, сут Количество СВБ в контрольных флаконах (без добавления реагента), кл/мл Степень подавления СВБ при концентрации СПНП-1004, мг/л
5 10 15
3 105 + + +
4 105 + + —
5 104 + + —
6 104 + — —
7 104 + — —
8 104 — — —
9 103 — — —
10 103 — — —
Примечание: «+»,. «—» — соответственно рост и отсутствие роста СВБ
не менее чем в 75% вариантов опытов
эффект при концентрации 15 мг/л достигается через 9 суток, СНПХ-
1003 при концентрации 5 мг/л — через 7 суток.
7.3. Биоцидная активность реагентов, используемых
для подавления жизнедеятельности СВБ
Биоцидная активность ингибиторов коррозии
Некоторые ингибиторы коррозии обладают свойством подавлять
жизнедеятельность бактерий, т. е являются бактерицидами.
7.3. Биоцидная активность реагентов
309
Концентрация СНПХ-1004, мг/л
Рис. 7.2. Влияние концентрации СНПХ-1004 на время подавления СВБ
Рис. 7.3. Жизнеспособность СВБ при действии СНПХ-1003 (1) и НА-
ПОР-1007 (2) в различных концентрациях в течение 10 суток
Исследование бактерицидной активности части ингибиторов
коррозии показало, что минимальная концентрация, при которой по-
давляется жизнедеятельность бактерий, зависит от физиологической
группы микроорганизмов [63] и колеблется довольно в широком диа-
пазоне, табл. 7.6.
310
Глава 7
Таблица 7.6. Эффективная концентрация подавления бактерий ингибитора-
ми коррозии
Ингибитор коррозии Эффективная концентрация подавления бактерий, мг/л
СВБ Thiobacillus thioparus Thiobacillus thiooxidans Thiobacillus thioparus УОБ
Виказол 800 — — — —
Газохим > 1000 > 1000 800 200 1000
Корексит-7798 500 1000 > 1000 > 1000 200
Нефтехим-1 > 1000 >•1000 (> 1000 > 1000 > 1000
Олазол 100 800 200 > 1000 > 1000
СНПХ-1002Б 800 800 800 > 1000 800
СНПХ-1003 200 800 800 200 200
СНПХ-4301 400 800 1000 > 1000 800
СНПХ-4302 800 1000 1000 > 1000 800
СНПХ-4540 200 > 1000 > 1000 > 1000 > 1000
СНПХ-4570 200 > 1000 > 1000 > 1000 > 1000
СНПХ-6011Б > 1000 > 1000 800 > 1000 400
СНПХ-6013 1000 > 1000 > 1000 > 1000 > 1000
СНПХ-6210 200 1000 400 200 400
СНПХ-6301 А 600 > 1000 800 1000 > 1000
СНПХ-6302А 400 > 1000 200 > 1000 > 1000
СНПХ-6302Б 400 > 1000 1000 > 1000 > 1000
ФОМ-9-12 1000 1000 1000 600 1000
Большинство ингибиторов, за исключением Газохим, Нефте-
хим-1, СНПХ-6011Б и СНПХ-6013, подавляют рост СВБ.
7.3. Биоцидная активность реагентов 311
Реагенты СНПХ-1003 и СНПХ-6210 эффективно подавляют все
упомянутые в таблице микроорганизмы, менее эффективны Олазол,
СНПХ-4301 и СНПХ-1002Б. Последние пять ингибиторов корро-
зии могут успешно применяться для подавления биоценоза реаль-
ных нефтепромысловых систем. Такие реагенты, как СНПХ-6301А,
СНПХ-6302А-Б, СНПХ-4540, СНПХ-4570 и Корексит-7798, будут по-
давлять микробиологическую коррозию в основном за счет активно-
сти по отношению к СВБ и нарушения единства цепи микробиоло-
гических процессов.
Некоторые ингибиторы коррозии серии Лукойл также облада-
ют свойствами бактерицидов и могут подавлять жизнедеятельность
СВБ, табл. 7.7.
Таблица 7.7. Эффективность ингибиторов коррозии Лукойл в качестве бак-
терицидов [72]
Наименование реагента Степень подавления СВБ, %, при дозировке, мг/л
25 50 100 250
Лукойл-1280И 0 18 100 100
Лукойл-1240И 0 0 59 100
Лукойл-1250И — — — 9
Лукойл-1251И 100 100 100 100
Лукойл-1211И — 5 11 34
Биоцидная активность ингибиторов коррозии-бактерицидов
Существует определенный класс реагентов комплексного дей-
ствия, обладающих свойствами ингибитора коррозии и бактерицида.
312
Глава 7
Лабораторные исследования. Эффективность реагентов в каче-
стве ингибиторов коррозии на модельной воде, а бактерицидов на
накопительной культуре СВБ приведена в табл. 7.8.
Таблица 7.8. Эффективность реагентов ингибиторов коррозии — бактери-
цидов
Реагент Дозировка, г/т Антикоррозионные свойства Бактерицидное действие, степень подавления СВБ, %
Скорость коррозии в модельном растворе, м/год Степень защиты, %
DodigenWS 180 10 — — 82,5
25 — — 90,5
50 0,081 37,04 100
100 — — 100
Danox CI-101 25 — — 89,0
31,5 0,001 86,73 —
50 — — 100
100 — — 100
Корексит 20 0,00865 98,06 —
SXT-1003 30 0,00517 98,36 95,0
ТН-10Д 10 — — 62,9
25 — — 74,6
50 0,0833 34,78 80,9
100 — — 90,5
АМ-7МБ 10 — — 4,8
25 — — 7,95
50 0,088 35,3 100
100 — — 100
7.3. Биоцидная активность реагентов
313
Продолжение табл. 7.8
Реагент Дозировка, г/т Антикоррозионные свойства Бактерицидное действие, степень подавления СВБ, %
Скорость коррозии в модельном растворе, м/год Степень защиты, %
Диссолван-4316 10 — — 0
25 — — 1,6
50 — стимул.
100 - 0,1889 29,2 стимул.
ИКМ-1 50 0,2167 15,2 64,9
(модификатор-1) 100 — — 66,4
250 — — 66,4
500 — — 69,3
ИКМ-2 50 0,1667 31,8 61,8
(модификатор-2) 100 0,1222 58,5 63,5
250 — — 64,9
500 — — 70,8
Нефтехим-3 50 0,0542 63,03 61,8
100 0,0163 91,09 64,9
250 — — 64,9
500 — — 70,8
Сонкор-9801 50 0,1056 57,78 90
100 — — 95,6
250 — — 99
500 — — 99
СНПХ-6301 50 0,0722 56,67 32
100 0,0677 65,7 36 .
250 — — 44
500 — 94
314
Глава 7
Эффективность некоторых реагентов по подавлению жизнедея-
тельности культур СВБ, выделенных из промысловых сред ряда ме-
сторождений, освещена в табл. 7.9.
Промысловые испытания. Промысловые испытания эффектив-
ности реагента комплексного действия Корексит SXT-1003 фирмы
Nalko Ехсоп для защиты от коррозии и биокоррозии водоводов сточ-
ных вод проводились на Ельниковском месторождении.
Контроль за эффективностью осуществлялся по скорости корро-
зии образцов-свидетелей, установленных в трубопроводы до и после
подачи реагента с концентрацией 30 уг/л. Образцы-свидетели из ма-
териала Ст. 3 устанавливались на 15 ... 36 дней в четырех точках:
— на скважине №3934 куста №4 — расстояние от точки подачи
реагента 6 км.;
— на приеме насосов БКНС-3 — расстояние от точки подачи реа-
гента 3 км.;
— на скв. 3987 куста 36 — расстояние от точки подачи регента 3 км.;
— на скв. 3913 куста 13 — расстояние от точки подачи реагента
3 км.
Величина скоростей коррозии, установленная по образцам-сви-
детелям при дозировке реагента 30 г/м3, продемонстрирована
в табл. 7.10.
Промысловые испытания ингибитора коррозии-бактерицида Da-
nox CI-101 фирмы Cao Corporation проводились на Красногор-
ском месторождении. Исследования носили комплексный харак-
тер.
1. Определение защитного эффекта ингибитора коррозии прово-
дилось гравиметрическим методом по изменению веса образцов-сви-
7.3. Биоцидная активность реагентов
315
Таблица 7.9. Эффективность реагентов по подавлению СВБ ингибиторами
коррозии — бактерицидами
Месторождение, из которого выделена культура СВБ Наименование реагента Степень подавления СВБ, %, при дозировке, мг/л
10 25 50 100 250
Красногорское Danox CI-101 — 92,4 100 100 100
Азимут-14Б — 68,1 100 100 100
Азимут-14Г — 86,1 100 100 100
Чутырская пл. Корексит SXT-1003 3,2 66,2 100 100 —
Dodigen WS 180 41,2 70,6 94,7
909 («Нефтехим») — 0 98,4 100 100
06-6 («Нефтехим») — 94,5 100 100 100
06-27(«Нефтехим») — 94 96,5 100 100
Гремихинское СНПХ-1050М — 0,9 39,5 92.1 100
1052 («Нефтехим») — 0 14,0 44,2 —
1087 («Нефтехим») — 7,0 95,4 100 —
Dodigen WS-180 82,5 90,5 100 100 —
Мишкинское CI-120 EG — 15,8 100 100 —
CI-101 — 100 100 100 —
Dodigen WS-180 — 38,6 100 100 100
Мещерякове кое CI-102 76,0 86,0 100 100 —
Dodigen WS-180 86,0 100 100 100 —
Лиственское Dodigen WS-180 — 9,1 39,4 100 100
Киенгопская пл. Dodigen WS-180 — — 100 100 —
Ельниковское Dodigen WS-180 — — 98,1 100 —
им
Таблица 7.10. Результаты гравиметрических испытаний
Место установки образцов Время испытаний, сут. Дозировка, мг/л Скорость коррозии, мм/год Защитный эффект, % Примечание
УПН 21 0,0325 Контрольная (без реагента)
Скв. 3934 (куст 4) 14 30 30 . 0,0047 0,0162 98,5 95,0 Язва под втулкой
14 30 20 0,0165 0,1602 94,9 50,7 Глубокие язвы по телу
Скв. 3987 (куст 36) 14 30 30 0,0020 0,0019 99,3 99,4
14 30 20 0,0010 0,0009 99,6 99,7
Скв. 3913 (куст 13) 14 30 30 0,0025 0,0037 99,2 98,8
14 30 20 0,0009 0,0012 99,7 99,6
Глава 7
7.3. Биоцидная активность реагентов
317
детелей (купонов), установленных в трубопровод на две недели
и на месяц в трех точках:
— на приеме насосов БКНС-1 (до подачи реагента);
— на выкиде насосов БКНС-1 в БНГ (с реагентом);
— на приемной линии нагнетательной скважины № 2612 на рассто-
янии 10 км от БКНС-1.
Дозирование реагента осуществлялось с помощью БР-2,5 по сле-
дующей схеме:
— ударная дозировка 75 г/м3 в течение суток;
— рабочая дозировка 30... 33 г/м3 в течение двух недель;
— рабочая дозировка 28 г/м3 в течение месяца.
Результаты испытаний представлены в табл. 7.11.
Точечные язвы на образцах обусловлены интенсивной серово-
дородной коррозией, протекающей в присутствии СВБ. На образцах,
находившихся в ингибированной среде, язв не наблюдалось. Более
высокая степень защиты при дозировке 28 г/м3 объясняется боль-
шей продолжительностью испытаний, чем при дозировке 31 г/м3.
2. Определение эффективности реагента как бактерицида про-
водилось на культурах СВБ, отобранных непосредственно с образ-
цов свидетелей. Для этого с поверхности образцов производили
соскоб отложений и по 1 см3 переносили в пенициллиновый фла-
кончик и приливали 10 мл кипяченой воды. Флакончик интенсив-
но встряхивали и после отстоя нефтепродуктов отбирали пробу во-
ды для посева в питательную среду и определения эффективности
бактерицида в соответствии с РД. Результаты испытаний отражены
в табл. 7.12.
318
Глава 7
Таблица 7.11. Результаты опытно-промышленных испытаний реагента
Danox CI-101 в качестве ингибитора коррозии на Красногорском место-
рождении
Место установки купонов Продолжи- тельность испытаний, сут Скорость коррозии, мм/год Дозировка реагента, г/м3 Защитный эффект, % Примечание
БКНС 14 0,0077 0 — Точечные язвы на образцах
БИТ 14 0,0010 31,5 86,73
Скв. 2612 14 0,0011 31,5 85,38
БКНС 32 0,1446 0 — Точечные язвы на образцах
БНГ 32 0,0008 28,2 99,44
Скв. 2612 32 0,0005 28,2 00,67
Таблица 7.12. Результаты лабораторных испытаний Danox CI-101 в качестве
бактерицида
Дозировка реагента, мг/л 25 50 100 250
Степень подавления, % 89 100 100 100
3. Промышленные испытания проводились на Красногорском
месторождении в течение 3 месяцев. Результаты испытаний приве-
дены в табл. 7.13.
Реагент ингибитор коррозии-бактерицид Danox CI-101 в ходе
исследований показал себя и как эффективный ингибитор корро-
зии, и как бактерицид, эффективно подавляя жизнедеятельность как
планктонной, так и адгезированной форм СВБ.
7.3. Биоцидная активность реагентов 319
Таблица 7.13. Результаты промышленных испытаний Danox CI-101
Точка отбора пробы Исследуемая среда Дозировка реагента, г/м3 Количество СВБ, кл/мл
без реагента с реагентом
БКНС-1 Вода 32 1000 41
скв. №2612 Вода 32 1000 16
Вода 28 1000 0
БКНС Отложения 0 > 10000 —
Скв. №2612 Отложения 28 > 10000 0
Опытно-промышленные испытания ингибитора-бактерицида
Сонкор-9801 были начаты в мае-июне 2001 на Чутырском и Крас-
ногорском месторождениях нефти. Подача реагента осуществля-
лась в водоводы сточных вод на КНС-8 Чутырского месторожде-
ния и на БКНС-1 Красногорского месторождения. Контроль за эф-
фективностью реагента по снижению коррозионного разрушения
нефтепромыслового оборудования осуществлялся гравиметрическим
и электрохимическим методами. Результаты испытаний сведены
в табл. 7.14.
Представленные данные показывают, что при дозировке 30 мг/л
ингибитор-бактерицид Сонкор-9801 проявляет защитный эффект бо-
лее 97 %.
Эффективность бактерицидов
Эффективность российских бактерицидов по подавлению жиз-
недеятельности СВБ, выделенных из промысловых сред различных
месторождений Удмуртии, продемонстрирована в табл. 7.15.
320
Глава 7
Таблица 7.14. Результаты гравиметрических исследований эффективности
реагента Сонкор-9801 на КНС-8 Чутырского месторождения
Место установки образцов Дозировка реагента, мг/л Скорость коррозии, м/год Защитный эффект, % Примечание
КНС-8 0 0,0250 — Сильные язвы по образцам
КНС-8 30 0,0006 97,49
Скв. 949 30 0,0007 97,15
Скв. 1242а 30 0,0007 97,23
Эффективность бактерицидов ХС-105 и XC-2332-W фирмы
Baker Petrolite и ряда других импортных бактерицидов по подав-
лению жизнедеятельности СВБ, выделенных из промысловых сред
различных месторождений Удмуртии, показана в табл. 7.16.
Испытания реагентов показали их высокую эффективность
по подавлению культур СВБ с различных месторождений. Диапа-
зон концентраций бактерицидов, необходимых для 100% подавле-
ния бактерий, для исследованных реагентов колеблется в пределах
10... 100 мг/л.
Исходя из высокой эффективности реагенты ХС-105 и ХС-2332-
W были рекомендованы для проведения испытаний по подавлению
жизнедеятельности СВБ в трубопроводных системах месторождений
ОАО «Удмуртнефть». Испытания проводились совместно с предста-
вителями фирмы Baker Petrolite. Технология применения включала
в себя периодическую обработку трубопроводов «пробкой» раствора
бактерицида в воде или нефти с периодичностью 1... 2 раза в неде-
7.3. Биоцидная активность реагентов 321
Таблица 7.15. Эффективность российских реагентов по подавлению СВБ
Наименование реагента Месторождение, из которого выделена культура СВБ Степень подавления СВБ, %, при дозировке, мг/л
10 25 50 100 150 250 500
Сульфан Киенгопская пл. — — 89,5 100 — 100 —
Сонцид 8102 Мишкинское — 100 100 100 — — —
Киенгопская пл. — 80 100 100 — — —
Мишкинское — 0 0 31,6 — 100 —
Лиственское — 9,1 13,7 88,4 — 100 —
СНПХ-1002 СНПХ-1002 Лиственское — — стимул 6,9 — 83,2 —
Киенгопская пл. — — — — 35,0 __ 39.5
СНПХ-1002Б Киенгопская пл. — — 18,2 — 49.1 — 72,7
Чутырская пл. — — 38,2 — 49,1 — 72,7
СНПХ-1002М Киенгопская пл. — — — — 57,5 — 85,3
С.-Нязинское — — — — 57,5 — 85. 3
СНПХ-1004 Мишкинское — — 82,1 100 — — —
Красногорское — 97,6 — — — — —
Лиственское — — • 95,3 97,3 — 100 —
СНПХ 1050М СНПХ 1050 Киенгопская пл. — — 100 100 — 100 —
Киенгопская пл. — — 87,7 100 — 100 —
МБ-1 Мишкинское — — 76,9 97,6 — 100 —
Лиственское — — 97,4 100 — 100 —
Киенгопская пл. — — 100 100 — — —
Чутырская пл. 0 0 17,6 100 — — —
ЛПЭ-11 Прикамский уч. — — 75,0 100 — — —
Мишкинское — — 100 — — — —
Гремихинское - — 96,0 100 — — —
322
Глава 7
Продолжение табл. 7.15
Наименование реагента Месторождение, из которого выделена культура СВБ Степень подавления СВБ, %, при дозировке, мг/л
10 25 50 100 150 250 500
ЛПЭ-11 В Лиственское — — 4,0 5,4 — 25,4 —
Чутырская пл. — — — 96,5 — 100 —
Красногорское — — — 81,2 — 86,4 100
Мишкинское — — 36,1 82,0 — 96,1 100
Ельниковское — — 24,6 86,2 100 —
ЛПЭ-11 У Лиственское — 1 28,3 86,2 __ 100 —
Мишкинское — — 24,8 64,2 — 81,6 100
Красногорское — — — 80,0 — 88,5 100
Ельниковское — — — 18,2 — 49,6 100
ЛПЭ-321 Мишкинское — 43 100 100 — — —
Киенгопская пл. — 15 30 50 — — —
БН-1 Мишкинское — — 64,1 — 95,4 — 97,7
Чутырская пл. — — 24,1 — 95,4 — 97,7
лю. Продолжительность закачки и количество реагента определя-
ли исходя из протяженности трубопровода и уровня зараженности
СВБ. В результате испытаний установлена их высокая эффективность
по подавлению СВБ в промысловых средах Чутырской площади.
7.4. Промышленно выпускаемые бактерициды
В РФ промышленно выпускаемые и разрешенные к исполь-
зованию бактерициды публикуются в отраслевом реестре «Пере-
7.4. Промышленно выпускаемые бактерициды
323
Таблица 7.16. Эффективность импортных реагентов по подавлению СВБ
Наименование реагента Месторождение, из которого выделена культура СВБ Степень подавления СВБ, %, при дозировке бактерицида, мг/л
50 100 250
Бактирам 607 Чутырская пл. 70,6 85,6 96,0
Корексит-6350 Лиственское 94,8 97,4 100
KRU-169 Лиственское Мишкинское 93,6 98,5 100 100 100
Surflo-6552 Лиственское Мишкинское 82,6 92,4 89,2 100 100
XC-2332-W Киенгопская пл. 99,9 100 —
ХС-105 Киенгопская пл. 99,9 100 —
чень химпродуктов, согласованных и допущенных к применению
в нефтяной отрасли». Помимо самого перечня в реестре приводит-
ся номер технических условий и организация-заявитель реагента,
табл. 7.17.
Характеристика некоторых бактерицидов приведена ниже.
СНПХ-1004
Ингибитор коррозии-бактерицид СНПХ-1004 предназначен для
защиты от коррозии нефтепромыслового оборудования, работающего
в средах, содержащих двуокись углерода и сероводород, в том числе
и зараженных СВБ.
324
Глава 7
Таблица 7.17. Перечень промышленно выпускаемых бактерицидов в РФ
Наименование реагента № технических условий Предприятие-заявитель
Ингибитор коррозии- бактерицид СНПХ-1003 ТУ 39-1192-87, изм. №1-4 ОАО «НАПОР» г. Казань
Ингибитор коррозии- бактерицид СНПХ-1004 ТУ 2458-011-12966038-2001 ОАО «НАПОР» г. Казань
Бактерицид СНПХ-1050 ТУ 2458-256-05765670-99, изм. №№ 1-7 ОАО «НИИнефтепром- хим» г. Казань
Нейтрализатор серово- дорода-бактерицид Десульфон-СНПХ-1100 ТУ 2458-293-05765670-2003 изм. № 1 ОАО «НИИнефтепром- хим» г. Казань
Ингибитор коррозии- бактерицид СНПХ-6418, марка А ТУ 2458-279-05765670-2001 изм. №1,2 ОАО «НИИнефтепром- хим» г. Казань
Бактерициды «Сульфо- цид-10» и «Сульфоцид- 20» ТУ 2458-285-00204197-2003 ОАО «Бератон» г. Берез- ники Пермской обл.
Ингибитор коррозии- бактерицид НАПОР-- 1007 и НАПОР-1007А ТУ 2458-015-12966038-2001 изм. № 1 ОАО «НАПОР» г. Казань
Ингибитор коррозии- бактерицид НАПОР- 1010 ТУ 2458-021-12966038-2006 ОАО «НАПОР» г. Казань
Бактерицид СОНЦИД- 8104 ТУ 2458-027-00151816-2003 ЗАО «Опытный завод Нефтехим» г. Уфа
Нейтрализатор серово- дорода-биоцид «КАЛАН» ТУ 2458-001-50771613-99 ООО «АНК» г. Уфа
Бактерицид Сульфан ТУ 2458-003-42147065-ОП- 99, изм. №№ 1, 2 ООО «ИНИШ» с. Ново- троицкое Тукаевского района Республики Татарстан
7.4. Промышленно выпускаемые бактерициды
325
Продолжение табл. 7.17
Наименование реагента № технических условий Предприятие-заявитель
Препарат «Бактерицид Л ПЭ» марки «ЛПЭ-11», «ЛПЭ-12», «ЛПЭ-НОЛ», «ЛПЭ-33», «ЛПЭ-32», «ЛПЭ-321» ТУ 2458-039-00209295-02, изм. № 1 ОАО НПО «Технолог» г. Стерлитамак
Ингибиторы коррозии- бактерициды СОНКОР- 9801, СОНКОР-9802 ТУ 2458-015-00151816-2001 изм. №№ 1, 2 ЗАО «Опытный завод Нефтехим» г. Уфа
Ингибитор коррозии- бактерицид СОНКОР- 9920 ТУ 2458-030-00151816-2004 ЗАО «Опытный завод Нефтехим» г. Уфа
Бактерицид ХПБ-002, марки ХПБ-002(Л), ХПБ-002(3) ТУ 2491-033-43122541-00, изм. №№ 1-3 ОАО «РДН Групп» филиал «Когалымский завод химреагентов» г. Самара
Бактерицид «Petrolen 6004» ТУ 2458-007-58654953-2006 ООО «Петролен» г. Ка- зань
Бактерицид многофункцио- нальный «ATREN-bio» ТУ 2458-002-57258729-2004 изм. №№ 1, 2 ЗАО «Гамма-Хим» г. Ка- зань
Бактерицид марки БиоМастер 6010 ТУ 2458-009-50622652-2006 ЗАО «Мастер Кемикалз» г. Казань
СНПХ-1004 представляет собой катионоактивное фосфорсодер-
жащее ПАВ в смеси органических растворителей.
В зависимости от соотношения исходных компонентов и области
применения реагент выпускают двух марок: Б и Р.
326
Глава 7
Техническая характеристика бактерицида
Наименование показателя Норма Метод анализа
Марка Б Марка Р
Внешний вид От светло-желтого до светло-коричневого цвета По 5.3 ТУ
Температура застывания, °C, не выше -50 -50 По 5.8 ТУ
Плотность при 20°, кг/м3 По ГОСТ 18995.1
Концентрация водородных ионов (pH) 5,5... 8,5 г 5,5... 8,5 По 5.5 ТУ
Массовая доля фосфора, % 4...5 2,9... 3,5 По 5.6 ТУ
Аминное число несвязанных аминов, мг НС1 /г, не более 5,0 3,0 По 5.5 ТУ
Аминное число, мг НСЮд/г 145...165 100... ПО По 5.4 ТУ
Удельный расход, обеспечива- ющий защитное действие не менее 90 % в стандартном рас- творе минерализованной во- ды, не более, мг/л 25 25 По 5.9 ТУ
Удельный расход СНПХ-1004, обеспечивающий подавление СВБ на 100 %, мг/л, не более 100 100
Технические условия ТУ 2458-011-12966038-2001
Разработчик НИИнефтепромхим, г. Казань
СНПХ-1050
Бактерицид СНПХ-1050 предназначен для подавления роста -
сульфатвосстанавливающих бактерий, вызывающих микробиологи-
ТА. Промышленно выпускаемые бактерициды 327
вескую коррозию нефтепромыслового оборудования; для защиты от
сероводородной и углекислотной коррозии нефтепромыслового обо-
рудования, в качестве поглотителя сероводорода.
СНПХ-1050 представляет собой композиционную смесь третич-
ных аминов и серосодержащей органической соли.
Техническая характеристика бактерицида
Наименование показателя Норма Метод анализа
Внешний вид Жидкость от свет- ло-желтого до ко- ричневого цвета По 5.3 ТУ -
Температура застывания, °C, не выше Минус 25 По 5.4 ТУ
Плотность при 20°С, кг/м3 1110-1140 ПоГОСТ 18995.1, разд. 1
Концентрация водородных ионов (pH) 9-10 По 5.5 ТУ
Удельный расход СНПХ-1050, обеспечивающий подавление СВБ на 100 %, мг/дм3, не более 150
Технические условия ТУ 2458-256-05765670-99
Разработчик НИИнефтепромхим, г. Казань
ДЕСУЛЬФОН СНПХ-1100
Нейтрализатор сероводорода-бактерицид Десульфон СНПХ-
1100 предназначен для нейтрализации сероводорода в пластовой во-
де, используемой для глушения скважин, в товарной нефти, в си-
стемах сбора и подготовки нефти, системе поддержания пластового
328
Глава 7
давления. Реагент проявляет свойства бактерицида для подавления
роста сульфатвосстанавливающих бактерий, вызывающих микробио-
логическую коррозию нефтепромыслового оборудования, обладает
защитным антикоррозионным эффектом в сероводородсодержащей
среде.
Десульфон-СНПХ-1100 представляет собой композиционную
смесь.
Техническая характеристика бактерицида
Наименование показателя Норма Метод анализа
Внешний вид Жидкость от светло- желтого до темно-ко- ричневого цвета По 5.3 ТУ
Температура застывания, °C, не выше минус 40 По 5.4 ТУ
Плотность при 20° С, кг/м3, в пределах 1050 - 1200 По ГОСТ 18995
Концентрация водородных ионов (pH), не менее 8,0 По 5.5
Массовая доля связанного фор- мальдегида, %, не менее 15,0 По 5.6
Технические условия ТУ 2458-293-0576570- 2003
Разработчик НИИнефтепромхим, г. Казань
СОНЦИД-8104
Бактерицид СОНЦИД-8104 предназначен для защиты системы
сбора и подготовки нефтепромысловой пластовой воды, трубопрово-
дов и системы ППД от биологической коррозии.
7 А. Промышленно выпускаемые бактерициды
329
Техническая характеристика бактерицида
Наименование показателя Норма Метод испытаний
Внешний вид Однородная жид- кость от желтого до коричневого цвета По п. 5.2 ТУ
Плотность при 20° С, г/см3, не менее 1,000 По ГОСТ 18995.1, раздел 1
Показатель активности ионов водорода (pH) 10%, масс, водного раствора, не менее ЗД По п.5.3 ТУ
Температура вспышки в за- крытом тигле, °C 38
Температура застывания, °C, не выше минус 40 По ГОСТ 20287 и по п. 5.4 ТУ
Концентрация бактерицида, при которой наблюдается 100 % подавление клеток СВБ, мг/дм3: — планктонная форма — адгезированная форма 30 - 100 500 - 700 По РД 03-00147275- 067-2001 и по п.5.5 ТУ
ПДК, мг/мЗ по метанолу по формальдегиду 5,0 0,5
Класс опасности 4
Технические условия ТУ 2458-027-00151816-2003
Разработчик и изготовитель ЗАО «Опытный завод Нефтехим»
330
Глава 7
Бактерицид СОНЦИД-8104 представляет собой смесь четвер-
тично-аммониевых солей, альдегидов и органических растворителей.
В качестве исходного сырья для получения бактерицида СОН-
ЦИД-8104 используют:
— алкилдиметиламмоний хлорид по импорту;
— формалин технический по ГОСТ 1625;
— метанол технический по ГОСТ 2222.
НАПОР-1007
Ингибитор коррозии-бактерицид НАПОР-1007 предназначен
для защиты от коррозии нефтепромыслового оборудования, рабо-
Техническая характеристика бактерицида
Наименование показателя Норма Метод анализа
Внешний вид Однородная жидкость от светло-желтого до коричневого цвета по 5.3 ТУ
Аминное число, мг HCL/r 30... 32 по 5.4 ТУ
Кислотное число, мг КОН/г 48... 56 поГОСТ 28351 и по 5.5 ТУ
Температура застывания, °C, не выше минус 40 по ГОСТ 20287 и по 5.6 ТУ
Удельный расход, обеспечиваю- щий защитное действие не ме- нее 90% в стандартном раство- ре, мг/дм3, не более 30 по ОСТ 39-099 и по 5.7 ТУ
ТУ ТУ 2458-015-12966038-2001
Разработчик ООО «Напор»
7.4. Промышленно выпускаемые бактерициды
331
тающего в средах, содержащих сероводород и двуокись углерода,
в том числе и зараженных сульфатвосстанавливающими бактериями
(СВБ).
НАПОР-1007 представляет собой смесь четвертичной аммони-
евой соли синтетической жирной кислоты и катионоактивного ПАВ
в органическом растворителе.
Степень подавления СВБ при концентрации реагента не более
150 мг/дм3 составляет 100%.
БАКТЕРИЦИДЫ СЕРИИ ЛПЭ
Предназначены для защиты от биокоррозии, подавления СВБ,
анаэробных бактерий, сине-зеленых водорослей и микроскопических
грибов в нефтепромысловых средах, увеличения нефтеотдачи.
Техническая характеристика бактерицида
Наименование показателя Норма
ЛПЭ-11 ЛПЭ-12 ЛПЭ-32 ЛПЭ-321
Массовая доля основного веще- ства, не менее, % 50
Температура застывания, °C -25
Пожароопасность Не горючи и не взрывоопасны
Степень защиты от коррозии, % 67
Биоцидная активность по полно- му подавлению СВБ, мг/л 400 250 75...100 50...75
Поглощение H2S, мг/г 130 102 252 130
Условная вязкость (ВЗ-246, d — — 4 мм), сек 14,8 14 65 118
Технические условия ТУ 2458-039-00209295-02
Изготовитель ОАО НПО «Технолог» г. Стерлитамак
Класс опасности 4 4 4 4
332
Глава 7
Реагенты серии ЛПЭ представляют собой продукты взаимодей-
ствия гексаметилентетраамина с хлорпроизводными ненасыщенных
углеводородов С, — С.
БД-2
Ингибитор-бактерицид БД-2 предназначен для борьбы с:
— микробиологическим заражением различных технологических
жидкостей (буровых и тампонажных растворов, надпакерных
Техническая характеристика бактерицида
Наименование показателя Норма Метод анализа
Внешний вид Жидкость от светло- до темно-коричневого цвета По 5.3 ТУ
Температура застывания, °C, не выше Минус 25 По 5.4 ТУ
Плотность, р20, кг/м3 - 1050- 1100 По ГОСТ 18995.1, разд.1
Рабочая концентрация бактерицида 0,05... 0,5 % от объема обрабатываемой жидкости
Пожароопасность Взрывобезопасен
Влияние на переработку нефти Не оказывает отрицательного влияния
Технические условия ТУ 39-1596-93
Разработчик ООО «Научно-производственная компания «ЭКСБУР Ко»
Токсичность Умеренно-опасное вещество
Класс опасности III класс ПоГост 12.1.007-76
Санитарно-эпидемиологи- ческое заключение №61 РЦ.03.260. П.001015.09.02 от 30.09.2002 г.
1А. Промышленно выпускаемые бактерициды
333
жидкостей, систем подготовки воды и нефти, систем оборотного
водоснабжения);
— микробиологической и химической коррозией оборудования,
в том числе сероводородной агрессией;
— биоценозом сульфатвцсстанавливающих бактерий в продуктив-
ных нефтяных пластах.
По физико-химическим показателям БД-2 относится к классу
гетероциклических аминов.
СУЛЬФОЦИДЫ
Техническая характеристика бактерицида
Наименование показателей Норма
Сульфоцид-10 Сульфоцид - 20
Марка А Марка Б Марка А Марка Б
Внешний вид жидкости от зеленовато-желтого до темно-коричневого цвета
Плотность при 20°С, г/см3 1,143. ..1,153 1,133...1,143 1,129. ..1,139 1,144.-.1,154
Аминное число, мг НС1/г, не менее 200 180 160 180
Температура застыва- ния, °C, ие более -40 -40 -30 -30
pH раствора с массовой долей основного веще- ства 1 % 10,0. ..10,6 10,0...10,6 10,4.. .11,0 10,5.. .11.1
Класс опасности 3 3 3 3
Технические условия ТУ 2458-285-00204197-2003
Производитель ОАО «Бератон» г. Березники
334 Глава 7
Бактерициды предназначены для:
— подавления роста СВБ и защиты систем поддерживания пласто-
вого давления и нефтесбора от биокоррозии;
— подавления роста углеводородокисляющих бактерий и грибов
в системах циркуляционного охлаждения;
— предупреждения микробиологического поражения буровых рас-
творов на основе полисахаридов.
Сульфоциды обладают защитным антикоррозионным эффектом
в средах, содержащих сероводород, являются нейтрализаторами се-
роводорода. '
Глава 8
Поглотители сероводорода
>
В нефтепромысловой практике к решению вопросов удаления
сероводорода из нефтепромысловых сред и технологических объек-
тов, содержащих эти среды, подходят, как правило, не однозначно.
К работам, выполняемым на технологическом наземном и под-
земном оборудовании эксплуатационного фонда скважин, в продук-
ции которых содержится сероводород, подходят с оперативным вни-
манием и тщательностью, поскольку они обусловлены необходимо-
стью соблюдения правил промышленной безопасности и связаны
со здоровьем обслуживающего персонала. Безотлагательное приня-
тие мер по нейтрализации сероводорода является основой успешного
проведения ремонтных работ.
Реализация мероприятий по борьбе с сероводородом на разра-
батываемых объектах, связанных с поддержанием пластового давле-
ния и повышения нефтеотдачи пластов, сопряжена со значительными
трудностями решения поставленных задач, поскольку объемы раство-
ренного в пластовой воде сероводорода достаточно велики. Эффек-
тивность воздействия на пласт через систему поддержания пластово-
го давления зависит от длительности и непрерывности осуществле-
ния процесса, поэтому неадекватность подхода к принятию решений
по проблемам нейтрализации сероводорода в разрабатываемых объ-
ектах только усугубляет саму проблему.
336
Глава 8
Работы местного характера — текущие плановые работы
1. Остановка технологического оборудования и предполагае-
мые на нем ремонтные работы, в том числе и огневые, предпо-
лагают продувку его инертным газом, с целью удаления горючих
и взрывоопасных газов, и промывку, при необходимости, раствора-
ми, содержащими поглотители сероводорода, для нейтрализации се-
роводородсодержащих жидкостей и удаления углеводородной состав-
ляющей.
2. Проведение подземных и капитальных ремонтов скважин,
в продукции которых содержится газообразный или растворенный
сероводород, требует выполнения предварительной операции глуше-
ния скважин жидкостями, содержащими поглотители сероводорода.
Только в этом случае можно считать скважину готовой к проведению
на ней геолого-технических мероприятий и выходу на площадку ра-
бочей бригады.
3. Защита эксплуатационных колонн нагнетательных скважин
нейтральными жидкостями, так называемыми «надпакерными» жид-
костями.
4. Консервация и ликвидация скважин.
5. Нейтрализация буровых растворов.
Масштабные проблемы месторождений, вступающих
в заключительную стадию разработки
Первой составляющей поистине масштабной проблемы являет-
ся необходимость повсеместного устранения сероводорода в добы-
ваемой продукции по всей технологической цепочке добычи, сбора,
транспорта и подготовки нефти.
8.1. Основы ОЧИСТКИ ПРОМЫСЛОВЫХ СРЕД ОТ СЕРОВОДОРОДА 337
Вторая составляющая проблемы заключается в наличии той
огромной, насыщенной сероводородом, массе водной фазы, отде-
ляемой на узлах предварительного сброса и установках подготов-
ки нефти. Проблема усугубляется тем, что вся подтоварная вода,
как правило, не подвергается обработке бактерицидами и закачи-
вается непосредственно в продуктивные пласты, при этом толь-
ко незначительная часть воды утилизируется в поглощающих сква-
жинах.
Во всех перечисленных случаях требуется повсеместное удале-
ние сероводорода или его поглощение (связывание, нейтрализация).
8.1. Основы очистки промысловых сред от сероводорода
Основы процесса абсорбции
Абсорбция — процесс объемного поглощения газов и паров жид-
кими поглотителями. Абсорбция (absorption) происходит от латин-
ского слова — absorbeo (поглощаю). Поглощаемый газ называют аб-
сорбатом, жидкий поглотитель — абсорбентом. Процесс, обратный
абсорбции, называют десорбцией. Его используют для выделения
из раствора поглощенного газа и регенерации абсорбента.
Различают физическую и химическую абсорбцию, или хемо-
сорбцию. При физической абсорбции энергия взаимодействия мо-
лекул газа и абсорбента в растворе не превышает 20 кДж/моль. При
химической абсорбции молекулы растворенного газа реагируют с ак-
тивным компонентом абсорбента при энергии взаимодействия моле-
кул более 25 кДж/моль, либо в растворе происходит диссоциация или
ассоциация молекул газа. Промежуточные варианты абсорбции ха-
рактеризуются энергией взаимодействия молекул 20... 30 кДж/моль.
338
Глава 8
К таким процессам относится растворение с образованием водород-
ной связи, например, абсорбция ацетилена диметил формамид ом.
Схематический процесс абсорбции можно записать в виде
1
А + В М + q,
2
где А — поглощенный газ; В — абсорбент; М — продукты физическо-
го или химического взаимодействия газа и абсорбента; q — тепловой
эффект абсорбции.
Стадия (1) соответствует абсорбции, (2) — десорбции. Если про-
цессу свойственны обе стадии, то говорят об обратимой абсорбции.
Процесс, протекающий только в направлении (1), является необрати-
мым.
Физические абсорбенты, по сравнению с хемосорбентами, тре-
буют пониженных температур для увеличения сорбционной емкости
и хорошо растворяют углеводородные компоненты газа, поэтому при-
ходится применять специальные меры для уменьшения содержания
углеводородов в кислых газах, что усложняет технологию очистки.
Из физических абсорбентов промышленное применение для очист-
ки газов нашли такие, как метанол, метил-пирролидон, пропилен-
карбонат, эфиры полиэтиленгликоля [67] и др. Физико-химические
свойства некоторых физических абсорбентов приведены в табл. 8.1.
Химическая абсорбция может быть обратимой и необратимой.
Например, поглощение сероводорода этаноламинами — обратимый
процесс, а едкими щелочами — необратимый.
Процесс абсорбции всегда сопровождается уменьшением объема
системы газ-жидкость за счет растворения газа и выделения тепла
абсорбции. Поэтому повышение давления абсорбции и понижение
Таблица 8.1. Физико-химические свойства физических абсорбентов
Абсорбент Молекулярная масса Плотность при 20°С, г/см3 Температура кипения при 1 0,1 МПа, °C Температура застывания, °C Вязкость кинематическая, •106 м2/с Температура, °C
Пропиленкарбонат Н2СОСООСНСН3 102 1,204 240 V -55,2 2,1 25
Диметиловый эфир полиэтиленгликоля 280...310 1,035 — *—22... - 29 6,8 25
Метилизопропиловый эфир полиэтиленгликоля 316 1,002 — -25 7,2 25
N-метил-пирроли дон 99 1,027 202 -24 — —
Трибутилфосфат (С4Н9О)РО 282 0,976 161* -80 3,9 20
Сульфолан 120,1 1,265 283 28,9 8,2 30
Метанол СН3ОН 32 0,791 64,7 -97,8 0,55 25
* — при давлении 0,002 МПа
8.1. Основы ОЧИСТКИ ПРОМЫСЛОВЫХ СРЕД ОТ СЕРОВОДОРОДА 339
340
Глава 8
температуры благоприятствуют протеканию абсорбции и, наоборот,
понижение давления и повышение температуры способствуют де-
сорбции.
Процесс абсорбции продолжается до тех пор, пока не устано-
вится равновесие между газовой и жидкой фазами. Условие равно-
весия — равенство температур сосуществующих жидкой и газовой
фаз (Тж — Тг) и парциальных давлений абсорбируемого компонента
в обеих фазах:
Рж = Рг-
Парциальное давление газа в ауеси газов находят по закону
Дж. Дальтона, согласно которому общее давление смеси газов (паров)
равно сумме парциальных давлений газов, составляющих смесь. Об-
щее число молей газа в смеси равно сумме молей отдельных газов,
т. е.
Робш = Pi + Р2 + • • • + Pi-
При этом под парциальным давлением понимают то давление,
которым обладал бы каждый отдельно взятый газ, если бы он один
при той же температуре занимал тот же объем, который занимает вся
смесь. Из закона Дальтона следует, что парциальное давление газа
(Pi) пропорционально его молярной доле (уг) в газовой смеси:
Pi = Робщ ’ Pi-
Второй закон Дж. Дальтона гласит, что растворимость компо-
нента газовой смеси в данной жидкости при постоянной температу-
ре пропорциональна парциальному давлению этого компонента и не
зависит от давления смеси и природы других компонентов.
8.2. Методика оценки нейтрализующей способности 341
Оба закона справедливы лишь в том случае, если между ком-
понентами смеси отсутствует какое-либо взаимодействие и каждый
из компонентов, равно как и смесь, ведет себя как идеальный газ.
Растворимость сероводорода в зависимости от парциального
давления для физического и химического абсорбентов [67] представ-
лены на рис. 8.1
Рис. 8.1. Зависимость растворимости сероводорода от давления в физиче-
ском (1) и химическом (2) абсорбентах: 1 — диметиловый эфир полиэтилен-
гликоля; 2 — диэтаноламин
8.2. Методика оценки нейтрализующей способности
поглотителей сероводорода
Для оценки нейтрализующей способности реагентов предложе-
на методика [8], позволяющая определять поглощающую способ-
ность реагентов в условиях наличия кислорода воздуха, углекислого
газа и других побочных компонентов. Схема установки для исследо-
вания нейтрализующих свойств реагентов приведена на рис. 8.2.
342
Глава 8
Рис. 8.2. Схема установки для изучения нейтрализующих свойств реагентов:
1 — аппарат Киппа; 2 —пустая промежуточная склянка; 3, 4 — ёмкости
с раствором соляной кислоты; 5 — склянка с раствором хлорида хрома; 6 —
ёмкость с известковой водой; 7 — склянйа с дистиллированной водой; 8 —
U-образная трубка с хлористым кальцием; 9 — склянки Дрекселя с навеской
нейтрализатора; 10 — поглотительный сосуд со щелочным раствором
Основным узлом установки является батарея последовательно
соединенных промывных склянок Дрекселя, содержащих по 100 мл
дистиллированной воды и проб исследуемых реагентов-нейтрализа-
торов, взвешенных с точностью до 0,001 г. Промывные склянки перед
началом проведения исследований продувают азотом, а в процессе
эксперимента — термостатируют.
Сероводород, получаемый при взаимодействии пирита с соля-
ной кислотой в аппарате Кипа (I), предварительно проходит через
буферную емкость (2) и склянки (3, 4) с соляной кислотой для очист-
ки от возможных примесей, затем последовательно через склянки
с раствором СгС1г (5) и известковой водой (6) для очистки от кисло-
рода и углекислого газа. Из склянки с дистиллированной водой (7)
через U-образную трубку с СаС1г сероводород, очищенный от при- *,
месей и влаги, поступает в систему склянок Дрекселя (9), в которых
происходит его поглощение исследуемыми нейтрализаторами.
8.3. Удаление и нейтрализация сероводорода
343
Для связывания остаточного сероводорода предназначен послед-
ний сосуд (10) со щелочным раствором любого активного поглотите-
ля H2S, например, двуокиси марганца.
В процессе исследований каждую из промывных склянок Дрек-
селя взвешивают до и после эксперимента и по увеличению массы
определяют количество Н2 S, связанного реагентом, принятым к ис-
следованию. После этого склянки охлаждают в холодильнике до 0°С
и из осветленной части пипеткой отбирают по 5 мл для определения
остаточной концентрации H2S методом йодометрического титрова-
ния. "
Поглотительную способность реагента (мг/г) оценивают по фор-
муле
П=Т(,-0,1С),
где т — навеска реагента-нейтрализатора, г; q — привес склянки, мг;
С — остаточная концентрация H2S, мг.
Использование данной методики повышает достоверность ре-
зультатов экспериментов благодаря устранению влияния на процесс
окисления H2S кислорода воздуха и других примесей, возможности
одновременного определения поглотительной способности до десяти
проб нейтрализаторов и исключения получения случайного резуль-
тата.
8.3. Удаление и нейтрализация сероводорода
Существующие методы нейтрализации сероводорода в нефти
можно разделить на физические и химические.
К физическим методам удаления сероводорода относят:
— сепарацию нефти, включая вакуумную;
344
Глава 8
— отдувку сероводорода из нефтей углеводородным газом, не со-
держащим сероводорода;
— ректификацию (включая вакуумную);
— удаление сероводорода из нефтей в аппаратах, интенсифициру-
ющих процессы сепарации и массообмена — эжекторах, гидро-
циклонах, аппаратах Вентури.
Сепарация, отдувка и ректификация являются массообменными
процессами дегазации нефти, и очистка ее от сероводорода в этих
процессах происходит в силу того, что сероводород является га-
зом с высокой летучестью. Сероводород при использовании физи-
ческих методов выводится из нефти в химически неизменном виде
в составе газов, требующих последующей утилизации или нейтрали-
зации.
Эффективным методом удаления сероводорода из продукции
нефтяных скважин является дегазация нефти и воздействие на нее
химическими реагентами. На предприятиях АНК «Башнефть» при-
меняют дегазацию нефти путем отдувки и сепарации с последующей
очисткой газа от сероводорода. При этом наиболее перспективным
методом считают моноэтаноламиновую очистку газа от сероводоро-
да [113]. В данном процессе сероводородсодержащий газ направля-
ют в реакционную колонну с реагентом-нейтрализатором, который
в последующем поступает на регенерацию. Выделенный на ступени
регенерации сероводород направляют в печь для получения элемен-
тарной серы, а очищенный газ — потребителю.
В ОАО «Татнефть» для удаления из нефти основного количества
сероводорода предложено использовать технологию отдувки нефти
бессероводородным газом и метод вакуумирования.
8.3. Удаление и нейтрализация сероводорода
345
Технологию отдувки осуществляют, как правило, в колонном ап-
парате после концевой ступени сепарации при противотоке поступа-
ющего снизу газа и подаваемой сверху нефти. Испытания технологии
отдувки сероводорода проведены на Альметьевской ТХУ, в ходе ко-
торых установлена возможность снижения его содержания в нефти
с 550 мг/л до 87 мг/л прй температуре нефти 40°С и расходе отду-
вочного газа не менее 5 м3 на тонну нефти.
Сущность метода вакуумирования заключается в удалении серо-
водорода из нефти в эжекторной установке с последующей подачей
смеси нефть-газ в сепаратор, из которого газ с высоким содержани-
ем сероводорода поступает на установку сероочистки. Данная уста-
новка смонтирована на Кама-Исмагиловской УПВСН и позволяет
извлечь из нефти до 80... 90% сероводорода от исходного содер-
жания.
К химическим методам следует отнести нейтрализацию серо-
водорода, его окисление или связывание с помощью химических ре-
агентов [8], [13], [67], [85]. Возможно совместное применение физи-
ческих и химических способов.
Использование щелочей, едкого натра и едкого калия, углекис-
лотных солей щелочных металлов, карбонатов натрия и калия для
удаления сероводорода из нефтей общеизвестно [67], [134]. При про-
мывке нефти водным раствором щелочи нефтяные кислоты, фено-
лы, сероводород образуют с ней водорастворимые соли и выводятся
с промывочной водой.
Технология очистки нефти от сероводорода путем окисления
предусматривает введение 20... 50% водного раствора перекиси во-
дорода при температуре от 0 до 60°С и давлении от 0,5 до 2 МПа.
При этом водный раствор пероксида водорода берут из расчета не ме-
346
Глава 8
нее 20 л на 1 кг сероводорода [87]. Процесс проводят непосредствен-
но в трубопроводе.
Недостатком способа являются длительность проведения про-
цесса, недостаточно высокая степень очистки нефти из-за низкой
скорости окисления сероводорода при низких температурах и высо-
кий расход используемого реагента.
Известен способ окислительной очистки нефти от сероводорода
и меркаптанов, заключающийся в обработке нефти смесью азотной
кислоты с железом, взятым в количестве 0,1... 1,0% от общей мас-
сы смеси. Смесь вводят в нефть в количестве 0,01... 0,5% от об-
щей массы. Перед обработкой химичёским реагентом исходное сы-
рье нагревают до 30... 100°С с последующим выдерживанием в те-
чение 10... 180 мин. Азотную кислоту используют концентрацией
50... 100%.
К достоинствам способа следует отнести повышенную эффек-
тивность за счет интенсификации процесса и использования доступ- •
ных компонентов для окислительной смеси; к недостаткам — корро-
зию оборудования и трубопроводов вследствие проведения процесса
непосредственно в транспортируемой кислой среде.
Предложен способ очистки сырой нефти от сероводорода пу-
тем окисления ее кислородсодержащим газом (воздухом) в присут-
ствии эффективного количества аммиака, взятых при соотношениях
0,5... 7,0 моль кислорода и 0,2... 2,0 моль аммиака на 1 моль се-
роводорода [86]. Аммиак вводят в исходное сырье в жидком или га-
зообразном виде вместе с воздухом. Процесс очистки проводят при
обычных или повышенных температурах и давлениях, а в качестве
реактора окисления используют насадочную, тарельчатую колонну,
емкостное оборудование и/или трубопровод.
8.3. Удаление и нейтрализация сероводорода 347
Поглотители сероводорода на основе органических соединений
К нейтрализаторам сероводорода на основе аминов относят реа-
генты типа БН, Урал-ЗМ, Сонцид, Калан, реагент SC 6408 компании
«Эксон Кемикал Лтд» [70], [113].
Свойствами нейтрализаторов сероводорода обладают производ-
ные гексаметилентетрамина [101].
В качестве нейтрализатора сероводорода авторами [8], [85] пред-
ложен реагент Т-66, являющийся побочным продуктом производства
изопрена из изобутилена и формальдегида. Данный реагент выпус-
кается рядом заводов синтетического каучука в виде маслянистой
жидкости желто-зеленого цвета плотностью 1030... 1080 кг/м3. Тер-
мостойкость составляет 250°С, а температура замерзания — минус
25°С. Продукт хорошо эмульгируется в растворах с различной сте-
пенью минерализации, растворимость в воде до 90%.
Реагент может быть использован в качестве добавки как к поли-
дисперсным буровым растворам, так и к технической воде. Основ-
ными компонентами, поглощающими H2S, являются 4,4-диметилди-
оксан и диоксановые спирты.
При взаимодействии диоксанов и их производных с H2S проис-
ходит разрыв связей кольца 1-2 и 2-3 с замещением атомов кислорода
атомами серы, в результате чего образуются серосодержащие диок-
саны и их производные. Количество связанного H2S колеблется от 25
до 100 мг на 1 г реагента в зависимости от температуры и pH среды.
С увеличением температуры при pH = 6... 7 процесс нейтрализации
H2S ускоряется, а при достижении температуры 200°С протекает по-
чти мгновенно. Образующиеся в результате реакции Т-66 с H2S про-
дукты являются ингибиторами коррозии, обеспечивающими степень
защиты в пределах 70... 85%.
348
Глава 8
Фурфурол [13] представляет собой маслянистую желтоватую
жидкость плотностью 1149... 1156 кг/м3 со специфическим запа-
хом. Растворимость в воде — 8,3 г на 100 г НгО. Фурфурол является
альдегидом фуранового ряда и относится к классу пятичленных гете-
роциклических соединений. Структурная формула фурфурола имеет
вид
НС— СН
II II
нс с — СН
\/ II
о о
Технический продукт в зависимости от исходного сырья содер-
жит от 96,3 до 99,5% фурфурола.
Максимальная поглотительная способность реагента по отноше-
нию к сероводороду составляет 239 мг H2S на 1 г фурфурола в кислой
среде (pH = 4,5) и 172 мг ЩБ/г фурфурола в щелочной среде (pH =
= 10).
Поглотительная способность реагентов-нейтрализаторов в при-
сутствии дисперсной фазы существенно снижается [13]. Исследо-
вания показали, что снижение поглотительной способности в этих
условиях для фурфурола составляет 29%, а для Т-66 — 43%.
Хлорамин Б. Для глушения скважин при текущем и капитальном
ремонте скважин в качестве нейтрализатора H2S предложен хлора-
мин Б [18, 85]. Структурная формула хлорамина имеет вид
( \ - SO2NClNa-3H2O,
а эмпирическая — C6HsSO2N(Na)Cl • ЗН2О.
8.3. Удаление и нейтрализация сероводорода 349
Хлорамин Б (N-хлорбензолсульфамид натрия) представляет со-
бой порошкообразное вещество белого или желтоватого цвета, рас-
творимое в пресной и минерализованной воде. Продукт содержит
до 25... 30% активного хлора, термостоек до 150°С, а при нагрева-
нии выше этой температуры разлагается с выделением хлора и хло-
ристого водорода. Хлорамин Б проявляет окислительные свойства
как в кислой, так и в щелочной средах.
Механизм нейтрализации сероводорода техническим хлорами-
ном Б заключается в следующем. При растворении в воде хлорамин
Б подвергается гидролизу с образованием гипохлорита натрия [22]:
C6H5SO2NClNa + Н2О = C6H5SO2NH2 + NaClO.
При взаимодействии гипохлорита натрия с сероводородом про-
текает реакция
NaClO + H2S = NaCl + S + H2O.
Продуктами реакции являются хлористый натрий, растворяю-
щийся в воде, и элементарная сера, всплывающая на поверхность
воды. Реакция хлорамина Б протекает мгновенно, а полная нейтра-
лизация сероводорода происходит в течение 1 минуты.
К преимуществам хлорамина Б следует отнести необратимость
его реакции с H2S, возможность использования как в структури-
рованных, так и в неструктурированных промывочных жидкостях.
К недостаткам хлорамина Б — сравнительно невысокую сероводород
нейтрализующую способность (100 мг H2S/r), коррозионную актив-
ность вследствие содержания большого количества хлора и высо-
кую стоимость продукта. Кроме того, хлорамин Б является сильным
350
Глава 8
аллергеном: при содержании его 4 • 10~9... 83 • 10”7 кг/м3 может
наблюдаться развитие аллергических заболеваний.
Металлилсульфонат натрия [15] (эмпирическая формула
C^ySOaNa) представляет собой негорючий тонкодисперсный по-
рошок бело-желтого цвета плотностью 980... 1000 кг/м3, хорошо
растворимый в пресной и минерализованной воде. Реагент является
малотоксичным веществом, относится к четвертому классу опасно-
сти.
Поглотители на основе арилсулъфиновых кислот известны
в виде парахлорбензолсульфиновой и метанитробензолсульфиновой
кислот [8,16,114], относящихся к классу ароматических арилсульфи-
новых кислот и представляющих собой кристаллические соединения
беловато-желтого цвета, хорошо растворимые в пресной и минера-
лизованной воде. Данные соединения широко используются в орга-
ническом синтезе как промежуточные продукты для получения суль-
фонов.
Структурная формула арилсульфиновых кислот имеет вид
О
! У? xS. II (I) R1 = C1, R2 = H,
R У~~ S — OH j 2
(II) R = H, R = NO2.
R2
Оба продукта относятся к классу слабых кислот и малотоксичны.
Натриевые соли п-хлорбензолсулъфиновой и т-нитробензол-
сульфиновой кислот представляют собой кристаллические вещества
белого цвета, хорошо растворимые в пресной и минерализованной
воде. Отличаются повышенной устойчивостью при длительном хра-
нении, не пожароопасны, коррозионно не активны.
8.3. Удаление и нейтрализация сероводорода 351
Для получения солей в качестве исходного сырья используют
хлорбензол и хлорсульфоновую кислоту.
Взаимодействие H2S с п-хлорбензолсульфинатом натрия или
с m-нитробензолсульфинатом натрия происходит согласно уравне-
нию
2С1—<^~o~>-S02Na + H2S
S + Cl^b~^SO2 S-<b^Cl + 2NaOH.
Поглотительная способность нейтрализаторов сероводорода
на основе арилсульфиновых кислот показана в табл. 8.2.
Таблица 8.2. Поглотительная способность арилсульфиновых кислот и их
солей [8]
Тип нейтрализатора Поглотительная способность, мг H2S/r, нейтрализатора
Без кислорода В присутствии кислорода
Металлилсульфонат натрия 235 480
Натриевая соль парахлорбен- золсульфиновой кислоты 210 380
Натриевая соль п-метанитро- бензолсульфиновой кислоты 205 382
Парахлорбензолсульфиновая кислота 296 706
Метанитрохлорбензолсуль- финовая кислота 273 697
352
Глава 8
Нейтрализующая способность пара- и метанитрохлорбензол-
сульфиновой кислот выше, чем у их натриевых солей, а метал-
лилсульфонат натрия занимает между указанными парами реагентов
промежуточное положение. Полученные результаты свидетельству-
ют и о том, что в присутствии кислорода воздуха нейтрализующая
способность исследуемых реагентов значительно возрастает, особен-
но паро- и метанитрохлорбензолсульфиновых кислот.
Установлено, что наряду с сероводороднейтрализующими свой-
ствами арилсульфиновые кислоты проявляют бактерицидную актив-
ность по отношению к СВБ [14].
Таблица 8.3. Бактерицидная активность п-хлорбензолсульфиновой и т-нит-
робензолсульфиновых кислот
Вещество Массовая доля, % Степень подавления СВБ, %
п-хлорбензолсульфиновая кислота 0,01 23,0
0,02 44,0
0,04 62,0
0,06 85,0
0,08 96,0
0,10 100,0
т-нитробензолсульфино- вая кислота 0,01 19,0
0,02 41,0
0,04 60,0
0,06 81,0
0,08 92,0
0,10 100,0
8.3. Удаление и нейтрализация сероводорода
353
Результаты испытаний (табл. 8.3 и 8.4) показали, что п-хлорбен-
золсульфиновая и т-нитробензолсульфиновая кислоты при массовой
доле 0,06... 0,08 % обеспечивают полное подавление жизнедеятель-
ности СВБ.
Таблица 8.4. Степень подавления СВБ пластовых вод Сергеевской площади
Испытываемая среда Количество СВБ в 1 мл пластовой воды Степень подавления СВБ, %
Пластовая вода (конт- роль) 1300 —
Пластовая вода +0,04% п-хлорбензолсульфино- вой кислоты 474 63,6
Пластовая вода +0,06% п-хлорбензолсульфино- вой кислоты 217 83,3
Пластовая вода +0,04% т-нитробензолсульфи- новой кислоты 519 60,1
Пластовая вода +0,06% т-нитробензолсульфи- новой кислоты 242 81,4
1-гидрокси-2-{1, 3-оксазетидин-3-ил)этан предложен для уда-
ления сероводорода из газа, нефти, пластовых вод и буровых раство-
ров [85]. Реагент представляет собой 70% водный раствор 1-гидрок-
си-2-(1, 3-оксазетидин-3-ил)этана общей формулы C4H9NO2.
354
Глава 8
Реагент получают взаимодействием формальдегида и моноэта-
ноламина при температуре 0... 40° С в течение 20 ... 24 часов в при-
сутствии катализатора щелочной природы. Реагент обладает серово-
дороднейтрализующей способностью в пределах 150 мг H2S на 1 г
средства, хорошей совместимостью с пластовыми водами и не вызы-
вает коррозии. Может быть использован для поглощения сероводо-
рода в буровых растворах.
Для нейтрализации сероводорода в нефтяных скважинах пред-
ложены композиции на основе полиглицеринов — продуктов отхода
производства глицерина [82]. В состав композиции входят, об. %:
полиглицерины — 60 ... 90 и водный раствор хлористого натрия в ко-
личестве 10... 40. Обработку осуществляют, закачивая нейтрализую-
щий состав в скважину с последующей его продавкой в призабойную
зону пластовой или сточной водой.
Технологические процессы нейтрализации сероводорода
Для дезодорирующей очистки нефти и газоконденсата от серово-
дорода и меркаптанов ГУП ВНИИУС (г. Казань) рекомендует способ
обработки их водным раствором, содержащим формальдегид, азотсо-
держащие органические основания, в качестве которых могут быть
использованы первичные и вторичные амины, алканоламины и мо-
чевина, аммиак и едкий натр и/или карбонат натрия [84]. Реагенты
вводят в виде водных растворов или в виде предварительно приго-
товленной смеси при температуре 0... 60° С. Реагенты известны под
названием НСМ.
Регенты НСМ — негорючие при обычных условиях жидкости
с запахом формальдегида и аминов, смешиваются с водой в любых
8.3. Удаление и нейтрализация сероводорода
355
соотношениях. При повышенных температурах концентрация фор-
мальдегида в парах реагента может достигнуть взрывоопасной.
Реагент готовится смешением в определенном порядке формали-
на, моноэтаноламина и катализатора — NaHCO.3, КагСОз или NaOH.
При этом моноэтаноламин вступает в экзотермическую реакцию
с формальдегидом с образованием смеси нелетучих метанолэтанола-
минов и оксазолидина. Полученный реагент, в отличие от формалина,
не замерзает и не полимеризуется при низких температурах и явля-
ется менее токсичным и летучим реагентом, чем формалин. Разрабо-
тано несколько модификаций реагентов НСМ: НСМ-3-1-Б, НСМ-3,5-
2Е, НСМ-4-2К, НСМ-5-2Б, НСМ-6-ЗК, отличающихся между собой
массовой долей несвязанного формальдегида. Характеристика одно-
го из них, реагента НСМ-4, приведена в табл. 8.5.
Технология нейтрализации сероводорода и легких меркаптанов
ДМС-1М разработана ГУП ВНИИУС. По данной технологии нейтра-
лизацию проводят водным раствором едкого натра с одновременным
окислением образующихся Na2S и RSNa кислородом воздуха при
температуре 20... 60° С и давлении 0,5... 1,5 МПа в присутствии го-
могенного катализатора «Ивказ» с последующей регенерацией и воз-
вратом в технологический процесс очистки большей части едкого
натра. Катализатор «Ивказ» производит и поставляет ГУП ВНИИУС.
Дозировка катализаторного комплекса составляет 1... 5 литров
на тонну нефти, при удельном расходе едкого натра 300 г/т и ката-
лизатора 0,8 г/т нефти.
Удельный расход воздуха составляет 1 м3 на тонну очищаемой
нефти. Отработанный воздух состоит на 30... 60 % из азота и по-
ступает с нефтью в товарные резервуары, создавая в них азотную
подушку.
356
Глава 8
Таблица 8.5. Характеристика реагента НСМ-4
Наименование параметра Значение
Эмпирическая формула Исходная смесь: Н2О + СН2О + + RNH2 + R2NH2 + СН3ОН
Состав, масс, доли, % Формальдегид — 15 ... 25 Амины — 20 ... 35 Вода — 43... 50 Метанол — 3 ... 5
Температура кипения, °C (при давлении 101 кПа) Начало - 100° С. 50% выкипает при 100... 102° С
Плотность, кг/м3 1100
Запах Формальдегида и аминов
Температура вспышки, °C 75
Пределы взрываемости в смеси с воздухом, об. доли 7... 73
Класс опасности 2
ПДК в воздухе рабочей зоны 0,5 мг/м3
ПДК в атмосферном воздухе 0,035 мг/м3
Разработанные процессы ДМС-1, ДМС-1м ДМС-3 успешно ис-
пользуются на промыслах Тенгизского месторождения, Казахстана
и на Оренбургском ГПЗ [79].
Достоинства процесса: технология прошла апробацию в про-
мышленности, недефицитность реагентов. Небольшая часть щелоч-
ного раствора остается в нефти и служит ингибитором коррозии
магистральных трубопроводов и оборудования НПЗ. К недостатку
8.3. Удаление и нейтрализация сероводорода 357
процесса следует отнести возрастающие потери углеводородов из-за
насыщения ими отработанного воздуха.
Технологический процесс нейтрализации сероводорода и мер-
каптанов, разработанный ООО «Башстройиндустрия», г. Уфа, преду-
сматривает использование реагента-нейтрализатора «Калан» на осно-
ве аминов и формальдегида. Сернистые соединения переводят в вод-
ную фазу вместе с отработанным нейтрализатором. Поглотительная
способность реагента «Калан» составляет 83,3 мг H2S на 1 г нейтра-
лизатора. „
Научно-производственная фирма «Инкорсервис», г. Уфа, пред-
лагает нейтрализатор сероводорода в водно-нефтяных средах, содер-
жащий амин, производное формальдегида и водорастворимый спирт.
Нейтрализатор готовится смешиванием в оптимальных соотношени-
ях упомянутых реагентов, выпускаемых в крупнотоннажном произ-
водстве.
ООО «Фирма Спецгазавтоматика» (г. Казань) предлагает раз-
личные технологические процессы очистки нефти от сероводорода
и меркаптанов — «Форминокс», ДСН-2, ДСН-3 и др., где использу-
ются в различной комбинации методы отдувки, окисления и нейтра-
лизации. В процессе «Форминокс» используют метод очистки нефти
от сероводородов и легких меркаптанов с применением нейтрали-
затора сероводорода — бактерицида НСМБ-1. Сущность метода за-
ключается в их нейтрализации с образованием нелетучих, стабиль-
ных и некоррозионных сероорганических соединений, растворимых
в углеводородах и остающихся в составе очищенной нефти. Нейтра-
лизатор сероводорода — бактерицид НСМБ-1 готовится смешением
в оптимальных соотношениях формалина и моноэтаноламина. В со-
став реагента может входить антифриз.
358
Глава 8
Процесс очистки проводят при обычных или повышенных тем-
пературах 10... 80° С, при атмосферном (и выше) давлении пу-
тем смешения исходного сырья с расчетным количеством реагента-
нейтрализатора в типовых смесительных устройствах или проточных
роторных смесителях типа ПРГ, ГАРТ и т. п.
Удельный расход НСМБ-1 на нейтрализацию содержащегося
в нефти сероводорода составляет 5,5 кг на 1 кг H2S, а на нейтра-
лизацию этилмеркаптана — 3,0 кг на 1 кг C2H5SH.
Предлагается способ очистки нефти от сероводорода и меркап-
танов алифатическим или циклическим альдегидом и дополнительно
первичным и/или вторичным органическим амином и/или аммиа-
ком. При этом используют моно-, диалкиламины Ci — С9, моноэта-
ноламин, моноизопропиламин, морфолин, циклогексиламин, бензиа-
мин, N, N-диметилпропилендиамин или их смеси. Альдегиды берут
в количестве 0,3... 3,0 моль на 1 моль меркаптановой и сероводо-
родной серы [81].
Достоинствами большинства из рассмотренных процессов с ис-
пользованием реагентов на основе аминоформальдегидных смесей
являются простота технологии и доступность сырья. К недостаткам
процессов следует отнести токсичность формальдегида и значитель-
ные эксплуатационные затраты за счет высокой стоимости и повы-
шенных удельных расходов некоторых реагентов.
При выборе методов извлечения сероводорода и меркаптанов
применительно к нефти и существующей технологии ее подго-
товки необходимо подходить индивидуально. Так, например, мето-
ды с использованием реагентов на основе аминоформальдегидных
смесей идеально подходят для технологий с дозированной пода-
чей реагентов непосредственно в нефтепровод, поскольку обеспе-
8.4. Надпакерные жидкости
359
чивают эффективность перемешивания и необходимое время кон-
такта.
Применение способа очистки нефти путем промывки ее щелоч-
ными растворами нежелательно для очистки тяжелых нефтей из-за
возможности образования трудно разделяющихся эмульсий и нару-
шения карбонатного равновесия сточных вод.
При наличии достаточного объема попутного газа применение
метода отдувки сероводорода из нефти в реакционных колоннах поз-
воляет при относительно низких эксплуатационных затратах добгть-
ся высокой эффективности процесса.
8.4. Надпакерные жидкости
В системе разработки нефтяных месторождений с поддержани-
ем пластового давления нагнетательные скважины играют ведущую
роль, поскольку через них идет восполнение энергии пласта. В свя-
зи с этим к надежности и долговечности нагнетательных скважин
предъявляются особые требования.
Потеря герметичности обсадных колонн нагнетательных сква-
жин вызывает такие нежелательные явления, как утечки продук-
ции скважин, загрязнение недр и окружающей среды. Ремонтно-
восстановительные работы в таких скважинах связаны с большими
затратами средств и времени и не всегда обеспечивают восстановле-
ние первоначальной надежности.
Для защиты нефтепромыслового оборудования от коррозии су-
ществует несколько способов защиты эксплуатационной колонны,
самым простым из которых является заполнение межтрубного про-
странства нейтральными (надпакерными) жидкостями. В качестве
360
Глава 8
надпакерной жидкости в основном рекомендуют пресную воду или
обезвоженную нефть.
Наиболее полно этим требованиям отвечает пресная техническая
вода. Однако ее применение приводит к развитию язвенной коррозии
из-за наличия в ней растворенного кислорода и вероятности обра-
зования сероводорода за счет жизнедеятельности сульфатвосстанав-
ливающих бактерий в обескислороженной среде после его расхода
на коррозию.
Удаление растворенного кислорода и подавление развития СВБ
путем химической обработки пресных вод позволяет их реко-
мендовать в качестве наиболее универсальных надпакерных жид-
костей.
Для удаления кислорода авторы [40] предлагают использовать
кислородоудаляющие реагенты — гидразин и сульфит натрия.
Нефть также является нейтральной средой, в которой металлы
практически не корродируют, однако при ее использовании в качестве
надпакерной жидкости возможна опасность развития СВБ.
Требования, предъявляемые к надпакерным жидкостям. Над-
пакерные жидкости должны обладать [40]:
— инертностью к металлу обсадных колонн и колонн НКТ и/или
наличием ингибирующего эффекта;
— постоянством физико-химических свойств в течение длительно-
го времени;
— способностью не образовывать нерастворимых продуктов реак-
ции в контакте с заколонными водами и не ухудшать состояние
призабойной зоны при закачке в пласт;
— технологичностью при использовании;
8.4. Надпакерные жидкости
361
— нетоксичностью (не должны содержать вредных веществ);
— отвечать требованиям охраны недр и окружающей среды.
Надпакерная жидкость на основе гидразина и формалина
Реакция связывания растворенного кислорода гидрат-гидрази-
ном происходит по уравнению N2H4 Н2О + О2 N2 + ЗН2О.
При взаимодействии гидрат-гидразина с кислородом образуются
нетоксичные продукты реакции — нейтральный газообразный азот
и вода.
Для подавления возможной деятельности СВБ в пресную во-
ду добавляют формалин в количестве 35 мг/л. Расчетное количе-
ство смеси определяют исходя из объема межтрубного пространства.
Необходимое количество формалина для обработки 1 м3 пресной во-
ды для всех концентраций гидразина составляет 35 г. Дозировка гид-
рат-гидразина в зависимости от исходной концентрации гидразина
приведена в табл. 8.6.
Таблица 8.6. Дозировка гидрат-гидразина на 1 м3 пресной воды
Концентрация гидразина, % 100 90 80 70 60 50 40 30 20
Дозировка гидрат- гидразина, мл/м3 воды 100 110 125 143 166 200 250 333 500
Время реакции определяют исходя из избытка гидразина, на-
чальной концентрации растворенного кислорода, температуры, зна-
чения pH среды. Исходя из оптимального времени реакции в пре-
делах 40... 60 мин процесс поглощения может быть осуществлен
непосредственно во время закачки надпакерной жидкости. Время пе-
ремешивания гидразина, технической воды и формалина составля-
362
Глава 8
ет 10... 15 мин, что обеспечивает равномерное распределение реа-
гентов в объеме воды.
Надпакерные жидкости на основе алюминиевой пудры
Авторами [83] предложен скважинный защитный состав, вклю-
чающий кальцинированную соду или хлорамин-Б, алюминиевую
пудру, неонол-6 и воду. В композиционный состав ингредиенты вве-
дены из следующих соображений:
— хлорамин-Б выступает в качестве поглотителя сероводорода
и биоцида СВБ, проявление жизнедеятельности которых возможно
i
при поступлении пластовой воды в межтрубное пространство;
— кальцинированная сода обеспечивает снижение скорости кор-
розии оборудования за счет создания щелочной среды;
— добавки алюминиевой пудры обеспечивают обескислорожива-
ние раствора на этапе приготовления и протекторную защиту колонн .
труб за счет пленочной адсорбции алюминиевого порошка на поверх-
ности металла;
— неонол-6 обеспечивает объемное диспергирование алюмини-
евой пудры в воде и ингибитора коррозии пленочного типа.
Полное удаление кислорода алюминиевой пудрой из пресной
воды может быть достигнуто при ее концентрации 0,1 г/л и времени
контакта 4... 5 часов, табл. 8.7.
В качестве надпакерной жидкости предложен состав при следу-
ющем соотношении компонентов, масс. %:
— кальцинированная сода или хлорамин-Б — 0,35 ... 1,2
— алюминиевая пудра — 0,008... 0,012
— неонол-6 — 0,09... 0,11
— вода пресная — остальное.
8.5. Поглотители сероводорода для буровых растворов 363
Таблица 8.7. Содержание кислорода в воде при дозировании в нее алюми-
ниевой пудры
Время контакта, час Содержание кислорода, мг/л, при дозировке алюминиевой пудры, г/л
0 - 0,04 0,06 0,08 0,1
0 7,4 — — — —
1 — 6,8 4,9 2,9 1,2
2 — 3,5 - 3,0 1,0 0,3
3 — 2,3 1,9 0,5 0,05
4 — 1,5 1,0 0,3 0
5 — 1,0 0,4 0,1 0
6 — 0,5 0,3 0,01 0
Эффективность оптимального состава подтверждена результата-
ми лабораторных исследований, табл. 8.8.
Объемы использования разработанных в ОАО «Удмуртнефть»
скважинных защитных составов (СЗС) приведены в табл. 8.9.
8.5. Поглотители сероводорода для буровых растворов
Нейтрализаторы на основе соединений железа
Разработанный в 80 годы в ВолгоградНИПИнефть реагент ЖС-7
представляет собой тонкодисперсный порошок плотностью 4100...
4300 кг/м3, в котором до 98% его состава приходится на окислы
железа (РегОз) и 1,5... 2 % на хлорное железо (РеС1з).
364
Глава 8
Таблица 8.8. Коррозионная активность защитного состава во времени
Время, сут Скорость коррозии металла, мм/год Защитный эффект, %
В сточной воде В защитном составе
1 0,34 0,038 88,82
6 0,32 0,029 90,93
24 0,31 0,022 92,90
35 0,31 0,021 93,22
54 0,34 0,020 94,11
73 0,33 0,033 90,00
87 0,32 ' 0,048 85,00
103 0,31 0,067 78,38
112 0,33 0,074 77,57
122 0,35 0,087 75,14
215 0,33 0,075 77,27
Таблица 8.9. Количество скважин, защищенных СЗС
Состав Года
1996 1997 1998 1999 2000 2001 2002
На нефтяной основе 22 8 35 28 24 — —
СЗС — — 1 49 47 80 36
Всего 22 8 36 77 71 80 36
Нейтрализация H2S обеспечивается за счет реакций
Fe2O3 + 3H2S 2FeS + S + ЗН2О
FeS + S FeS2
FeCl3 + 3H2S 2Fe2S3 + 6HC1.
8.5. Поглотители сероводорода для буровых растворов 365
Реакции носят обратимый характер и для устойчивости получа-
емых продуктов необходима щелочная среда, поэтому для поддержа-
ния pH в пределах 9... 10 на каждые 50 кг реагента ЖС-7 в буро-
вой раствор добавляют 0,7... 0,8 кг извести или 0,3... 0,4 кг едкого
натра.
На основании анализа экспериментального материала была вы-
ведена математическая зависимость количества поглощенного H2S от
его начальной концентрации [24], которую с достаточной точностью
описывает формула
у = 0 хп,
где у — ——; х = \ Со и С\ — начальная и конечная
концентрации H2S в воде, мг/мл; Vb — объем раствора, мл; т —
навеска нейтрализатора, мг; 0, п — постоянные, характеризующие
нейтрализатор.
Коэффициент 0 зависит от соотношения размеров молекул ад-
сорбируемого вещества и пор адсорбента. При адсорбции одного
и того же вещества на различных адсорбентах 0 становится характе-
ристикой адсорбционной поверхности, а при ограничении времени
может характеризовать активность реагента. Показатель степени п
зависит от концентрации адсорбируемого вещества и характеризует
потенциальные возможности адсорбента. Постоянные 0 и п могут
быть использованы для сравнительной оценки реагентов и кинетики
их взаимодействия с H2S.
Максимальная поглотительная способность ЖС-7 по H2S —
640 мг/г. Однако из-за неоднородности реагента, являющегося от-
ходом производства, возможны значительные колебания этого значе-
ния.
366
Глава 8
Магнетит (РегОз), используемый в практике бурения скважин
как утяжелитель, является наиболее перспективным нейтрализато-
ром H2S в буровых растворах из природных окислов железа. Однако
поглотительная способность этой руды сравнительно невелика. Даже
обогащенный магнетитовый концентрат значительно уступает ЖС-7.
Увеличение удельной поверхности реагента является эффек-
тивным средством ускорения реакции взаимодействия с H2S. Ис-
следования показали, что при увеличении удельной поверхности
до 3500 см2/г сероводороднейтрализующая способность концентра-
та магнетита становится значительно выше. На основании этого была
разработана технология [8], предусматривающая измельчение и ще-
лочную обработку магнетитового концентрата. Полученный продукт
имеет удельную поверхность 3174 см2/г и по поглотительной спо-
собности в 4 раза превосходит концентрат магнетита [6, 118]. Опти-
мальная концентрация применения составляет 5%.
Хлорное железо (РеС1з) представляет собой темно-коричне-
вое кристаллическое, очень гигроскопичное вещество плотностью
2800 кг/м3. Хлорное железо способно быстро реагировать с H2S,
но ухудшает технологические свойства буровых суспензий, поэтому
его используют только для нейтрализации H2S в технической воде,
применяемой в качестве промывочной жидкости.
Недостатком хлорного железа является также высокая коррози-
онная активность. При взаимодействии РеС1з с H2S образуется соля-
ная кислота, для нейтрализации которой в техническую воду вместе
с реагентом вводят щелочь.
Хелатные соединения железа. Для нейтрализации H2S может
быть использована композиционная смесь, основными компонентами
которой являются соли железа (FeSC>4 или РеС1з 6Н2О) и двунатрие-
8.5. Поглотители сероводорода для буровых растворов 367
вая соль этилендиаминтетрауксусной кислоты (трилон Б). При pH =
= 7... 8 в растворе образуются хорошо растворимые хелатные ком-
плексы железа. Последние, будучи малодиссоциируемыми соедине-
ниями, регулируют концентрацию ионов железа в растворе, устраняя
их отрицательное воздействие на буровые суспензии и снижая кор-
розию оборудования. В то же время количество ионов железа, всту-
пивших в реакцию с сероводородом, мгновенно пополняется за счет
хелатного комплекса, и нейтрализация H2S осуществляется очень эф-
фективно.
К недостаткам хелатных комплексов следует отнести сравни-
тельно большой расход трилона Б. Помймо этого, необходимо вво-
дить еще и щелочь для поддержания pH > 7, иначе хелатные ком-
плексы будут образовываться не с ионами железа, а с другими иона-
ми, присутствующими в буровом растворе.
Сидерит, представляющий собой карбонат железа (БеСОз),
встречается в природе в значительных количествах. Практически
нерастворимый в чистой воде, он растворяется в воде, содержащей
СО2, образуя растворимый бикарбонат Бе(НСО.з)2. Для нейтрализа-
ции H2S в буровом растворе применяют тонкодисперсный порошок
сидерита с удельной поверхностью 1500 ... 2500 см2/г [11].
Нейтрализаторы на основе соединений меди
Использование соединений меди для нейтрализации сероводоро-
да основано на образовании в результате их взаимодействия с серово-
дородом соединений, не диссоциируемых в воде и водных кислотных
растворах.
Медный купорос (C11SO4 -5^0) вводят в буровой раствор в объ-
еме 0,01... 0,2% в виде 2 ... 10%-ного водного раствора. Такие до-
368
Глава 8
бавки практически не влияют на технологические параметры буро-
вого раствора. Однако увеличение концентрации реагента приводит
к повышению показателя фильтрации и снижению pH. В связи с этим
следует использовать медный купорос для нейтрализации H2S пре-
имущественно в технической воде, применяемой для промывки сква-
жин.
Применение растворов сульфата меди целесообразно и для глу-
шения сероводородсодержащих коллекторов, представленных песча-
никами.
Трудно растворимый основной карбонат меди [СиСОз -Си(ОН)2]
используют в структурированных промывочных жидкостях. В отли-
чие от медного купороса, он не оказывает отрицательного воздей-
ствия на параметры бурового раствора и не образует агрессивных
побочных продуктов.
Для поглощения сероводорода может быть использовано ком-
плексное соединение меди, являющееся отходом производства вис-
козного волокна [12] — тетрааминкупрогидроксид или тетраамин-
медь (П) гидроксид [Си(МНз)4](ОН)2. Готовой формой нейтрали-
затора служат водные растворы, содержащие 0,1...0,5% реагента.
Высвобождающийся в результате реакции с H2S аммиак является
нейтрализатором и усиливает положительный эффект.
Нейтрализаторы, содержащие двуокись марганца
Реагенты, содержащие двуокись марганца, могут быть исполь-
зованы для нейтрализации сероводорода. Например, пастообразный
реагент на основе двуокиси марганца, являющийся отходом про-
изводства аскорбиновой и никотиновой кислот, содержит до 65%
8.5. Поглотители сероводорода для буровых растворов 369
двуокиси марганца и 5 % щелочи (в пересчете на КОН). Для
предотвращения его промерзания при минусовых температурах ре-
комендуют вводить хлористый кальций. Водная суспензия реаген-
та с 20... 30 % хлористого кальция не замерзает при температуре
минус 50° С.
Экспериментально установлено, что для нейтрализации H2S
в буровом растворе, при его объемном содержании от 1 до 45 %,
достаточно ввести в раствор 0,045... 2,0 кг/м3 реагента. При этом
полная нейтрализация сероводорода наступает через 3... 5 мин.
При взаимодействии H2S с двуокисью марганца выделяется
сульфид марганца и элементарная сера. Щелочь выполняет в этом
процессе роль катализатора:
2МпО2 + 3H2S MnS + MnO + 3S + 3H2O
2KOH + H2S <=* K2S + 2H2O.
Исследование поглотителей сероводорода в жидкой фазе
В качестве реагентов-поглотителей сероводорода были иссле-
дованы следующие виды реагентов: уксусно-кислый кадмий, как
классический поглотитель сероводорода, используемый в лаборатор-
ной практике, двуокись марганца, марганцово-кислый калий, хло-
рамин Б, флотореагент Т-80 и электроактивированная вода — ано-
лит [49, 129]. Результаты исследований поглощающей способности
реагентов из водной фазы представлены в табл. 8.10.
Кроме поглотительной способности указанных реагентов были
исследованы их продукты взаимодействия с сероводородом. Иссле-
дования проводились на коррозиметре «Korrater», предназначенном
для измерения скорости коррозии стали в электрически проводимых
370
Глава 8
Таблица 8.10. Поглощающая способность реагентов и коррозионная актив-
ность продуктов взаимодействия поглотителей с сероводородом
Реагент Поглощающая способность, мг H2S на г поглотителя Продукт связывания с сероводо- родом Скорость коррозии в модельном растворе с осадком, мм/год
Уксусно-кислый кадмий 147,5 CdS (осадок) 0,018
Двуокись марганца 845,0 MnS (осадок) 1 0,025
Марганцово- кислый калий 629,0 MnS (осадок) 0,088
Хлорамин Б 170,0 S (взвесь) 0,145
Электро- активированная вода (анолит) 413,0 S (взвесь) 0,148
растворах. Измерения скорости коррозии стальных образцов из стали
Ст. 3 проводились в модельном растворе с добавлением соответству-
ющих продуктов реакции поглощения сероводорода.
Полученные результаты показывают, что наилучшими погло-
тителями сероводорода являются двуокись марганца, марганцово-
кислый калий и электроактивированная вода — анолит. Анолит, к то-
му же, является перспективным материалом, поскольку исходная сре-
да для его получения неограниченна. Продукты реакции (CdS, MnS,
S) замедляют коррозионный процесс.
8.5. Поглотители сероводорода для буровых растворов 371
Пилотные испытания ряда реагентов, показавших высокую по-
глощающую способность при лабораторных испытаниях, проводи-
лись на скв. 102Г Патраковского месторождения.
Методика испытаний заключалась в том, что в пробоотборник
известного объема вводился исследуемый реагент, а затем туда же
непосредственно с устья скважины отбиралась проба водонефтяной
эмульсии. После этого в лабораторных условиях проводилось опре-
деление содержания сероводорода в полученных пробах. Результаты
испытаний представлены в табл. 8.11.
Таблица 8.11. Результаты лабораторных и пилотных испытаний поглотите-
лей сероводорода из водонефтяной эмульсии
Реагент Поглощающая способность реагента, мг H2S на 1 г поглотителя Расход реагента, кг/т нефти при C(H2S) = = 290 мг/л
Лабораторные испытания Пилотные испытания
МпО2 495 402 0,72
КМпО4 413 290 1,00
К-117 122 122 2,38
Хлорамин Б 67,5 — 4,29
Анолит Ссг = 1255 мг/л 0,57 активного СГ 0,18 активного СГ 41,5 л
Как видно из полученных данных, наибольшую поглотительную
способность проявляют двуокись марганца (МпО2) и перманганат
калия.
372
Глава 8
Хлорамин Б в настоящее время успешно используют для погло-
щения сероводорода при глушении скважин. Лабораторные исследо-
вания показывают, что он также может эффективно использоваться
для поглощения сероводорода из нефти и водонефтяных эмульсий.
Особо следует отметить анолит — электрохимически активиро-
ванную воду. Методика получения анолита проста и экологически
безопасна, что дает широкие перспективы в его использовании для
снижения биокоррозии. Результаты промысловых испытаний анолита
на Чутырской площади приведены в табл. 8.12. В качестве источни-
ка получения анолита использована установка СТЭЛ-1000, обеспе-
t
чившая достижение средней концентрации активного хлора в преде-
лах 245 мг/л.
Таблица 8.12. Результаты промысловых испытаний анолита
Содержание H2S до об- работки анолитом, мг/л Содержание H2S после обработки анолитом, мг/л % нейтра- лизации H2S
Участок - H2S Участок H2S
КНС-8 95,20 КНС-8 88,4 7,10
КНС-8 103,7 скв. 948 66,3 36,1
КНС-8 103,7 СКВ. 1166 78,2 24,6
Скв. 1103 125,5 скв. 1103 43,5 65,3
Скв. 948, 1166, 1172, 1242 90,7 Скв. 1242 40,8 55,0
Постоянное дозирование анолита в сточную воду в объеме
5 л/м3 обеспечило снижение содержания растворенного в воде серо-
водорода на 24... 65 %. Более полную нейтрализацию сероводорода
8.5. Поглотители сероводорода для буровых растворов 373
достичь не удалось из-за недостаточной мощности установки по про-
изводству анолита.
Поглотительная способность некоторых реагентов в водной фазе
приведена в табл. 8.13.
Таблица 8.13. Поглотительная способность реагентов в водной фазе
Наименование реагента Количество связанного H2S, мг H2S/I г реагента Степень подавления СВБ, %
Нефтехим-1 29,3 2.. .89
СНПХ-1002 42,1 14,9 ..93
Бактирам 607 9,9 70,6. ..100
ЖСМ-1 10,7 50. .98
Высококипящий побочный продукт производства син- тетического каучука 26,0 5.. .25
Диметилдиоксан 26,0 4... 17,1
Поглощающая способность сероводорода из углеводородной фа-
зы показана в табл. 8.14.
Промышленностью выпускается значительное количество реа-
гентов, в той или иной степени связывающих или поглощающих се-
роводород. Перечень некоторых из них приведен в табл. 8.15.
Поглотители сероводорода в значительной мере востребованы
в технологических процессах проведения подземных и капиталь-
ных ремонтов скважин для обеспечения промышленной безопасно-
сти персонала бригад, работающих на скважинах. Поглотители се-.
374
Глава 8
Таблица 8.14. Поглощение реагентами сероводорода из углеводородной фа-
зы
Реагент Поглощающая способность, мг H2S на 1 г реагента
По результатам лабораторных исследований По результатам промысловых испытаний
В нефти В газе В нефти
К-117 (товарная форма) 63,9 250
К-117 (растворенный в нефти) 152,
К-117 (в эмульсии) 122 249 76...122
Двуокись марганца МпОг 495 173...401
Перманганат калия КМпОд 413 291
Диметилдиоксан 4,8
Т-80 4,3
Sulfa-Clear 1323-291 75,1 153
Политлицерины 178
Полиглицерины + 0,8% КОН 89
Анолит (концентрация актив- ного хлора 1255 мг/л) 500 625
Хлорамин-Б (10 % водный р-р) 67,5
роводорода используются в качестве добавки в жидкость глушения.
Реагенты должны обладать следующими критериями:
— обеспечивать быстрое (в течение 1 часа) поглощение сероводо-
рода до 20 мг/л;
— обеспечивать полное удаление сероводорода в течение 24 часов.
8.5. Поглотители сероводорода для буровых растворов 375
Таблица 8.15. Перечень промышленно выпускаемых реагентов, нейтрали-
зующих H2S
Наименование реагента № технических условий Предприятие-заявитель реагента
Нейтрализатор серово- дорода и меркаптанов, марка НСМ ТУ 2456-057-00151638-2003 изм. № 1 ОАО «Татнефть». Управ- ление «Нефтехим-сер- вис» г. Альметьевск
Нейтрализатор серово- дорода — ингибитор коррозии «Урал-ЗМ» ТУ 2458-006-04683467-2004 ООО НПФ «Инкорсер- вис», г. Уфа
Бактерицид-нейтрали- затор сероводорода СНПХ-1050 ТУ 2458-256-05765670-1999 изм. № 1-5 ОАО «НИИнефтепром- хим», г. Казань
Нейтрализатор серово- дорода — бактерицид Десульфон-СНПХ-1100 ТУ 2458-293-05765670-2003 изм. № 1 ОАО «НИИнефтепром- хим», г. Казань
Нейтрализатор метил-, этилмеркаптанов и се- роводорода Десульфон- СНПХ-1200 ТУ 2458-294-05765670-2003 изм №№ 1,2 ОАО «НИИнефтепром- хим», г. Казань
Нейтрализатор серово- дорода-биоцид «Калан» ТУ 2458-001-50771613-99 ООО «АНК», г. Уфа
Поглотитель сероводо- рода ПСВ-3401 (марка А, Б) ТУ 2458-032-00151816-2005 ЗАО «Опытный завод Нефтехим», г. Уфа
Нейтрализатор серово- дорода и меркаптанов «НСМ-2» ТУ 2458-002-27815380-2003 ООО «Фирма Спецгазав- томатика», г. Казань
Компоненты нейтрализа- тора сероводорода уни- версального (НСВУ-1) ТУ 2458-001-50801389-2006 ООО УфНИПИцентр «Нефтегаз-2», г. Уфа
Компоненты нейтрализа- тора сероводорода уни- версального (НСВУ-2) ТУ 2458-002-50801389-2006 ООО УфНИПИцентр «Нефтегаз-2», г. Уфа
376
Глава 8
Наилучшими показателями по этим критериям обладают реа-
генты из серии Десульфон СНПХ-1200. При дозировке 400 г/м3
жидкости они поглощают до 100 мг/л сероводорода. Поглощающая
способность реагента составляет 4 мг реагента на 1 мг сероводорода.
Результаты исследования поглощающей способности реагентов,
проведенные на попутно-добываемой воде со скважины № 977 Гре-
михинского месторождения, при дозировке реагента 250 мг/л, пред-
Таблица 8.16. Поглотительная способность промышленно выпускаемых ре-
агентов в воде при дозировке 250 мг/л
Реагент Количество поглощенного сероводорода, мг, за время
1 час 3 часа 24 часа
Десульфон СНПХ-1200 90 106 112
GAS TREAT К-131 88 107 118
Десульфон СНПХ-1100 86 98 105
НСМБ «А» 75 92 94
Сонцид 8102 74 95 106
НСМБ «Б» 71 83 85
ЛПЭ-32 66 85 88
Сондем 4403-183 66 75 83
Сульфачек 63 72 75
НСК-5 60 70 76
Сода 59 66 72
Сонцид 8101 58 63 75
ПАК 50 57 —
НСК-3 50 58 66
8.5. Поглотители сероводорода для буровых растворов 377
ставлены в табл. 8.16. Начальное содержание сероводорода в исход-
ной воде определено в пределах 139 мг/л при плотности жидко-
сти 1180 кг/м3.
Эффективность поглощения сероводорода нейтрализаторами
из товарной нефти Гремихинского месторождения приведена
_ >
в табл. 8.17. Содержание сероводорода контролировалось экспресс-
методом по СТП 03-152-96 «Технологический регламент по нейтра-
лизации сероводорода в продукции скважин при проведении подзем-
ного и капитального ремонта».
Таблица 8.17. Поглотительная способность промышленно выпускаемых ре-
агентов в нефти при дозировке 500 мг/л
Реагент Темпера- тура, °C Содержание сероводорода, ppm Эффектив- ность поглощения, %
До После
Десульфон СНПХ-1200 6 245 135,8 44,6
Сонцид 8101 245 169 31,0
Десульфон СНПХ-1200 16 216,5 75,3 65,2
Сонцид 8101 216,5 117,5 45,7
Десульфон СНПХ-1200 22 202 16,9 91,6
ПСВ-3401 Б 202 50,0 75,2
Десульфон СНПХ-1200 22 196,3 60,5 69,2
ПСВ-3401 Б 196,3 102,0 48,0
Десульфон СНПХ-1200 22 133,5 87,5 34,4
ПСВ-3401 Б 133,5 84,1 37,0
378
Глава 8
Полученные экспериментальные данные свидетельствуют:
— с понижением температуры процесс поглощения сероводорода
реагентами ухудшается. Поглощающая способность СНПХ-1200
при 22° С - 91,6 %; 16° С - 65,2 %; 6° С - 44,6 %;
— при постоянной температуре поглощающая способность реаген-
тов тем выше, чем выше исходная концентрация сероводорода
в пробе нефти.
Отмечено увеличение поглощающей способности реагентов
от исходной концентрации сероводорода и в процессе его нейтра-
лизации в попутно-добываемой воде, рис. 8.3. Увеличение дозировки
нейтрализатора не приводит к существенному увеличению объема
поглощаемого сероводорода.
Рис. 8.3. Зависимость поглощенного сероводорода от объема нейтрализа-
тора Сонцид 8102. Исходное содержание сероводорода: 1 — 106 мг/л; 2 —
139 мг/л; 3 — 200 мг/л
Приложение
Таблица П. 1. Код роста и вероятность НВЧ для 5 параллельных проб
Код роста Значение НВЧ Код роста Значение НВЧ
5 5 5 100 442 0,4664
5 5 4 16,0 4 4 1 0,3980
5 5 3 9,00 4 4 0 0,3350
5 5 2 5,00 4 3 5 0,5927
5 5 1 3,470 4 34 0,5204
5 5 0 2,397 4 3 3 0,4513
5 4 5 4,250 4 3 2 0,3862
5 4 4 3,450 4 3 1 0,3259
5 4 3 2,780 4 2 0 0,2708
5 4 2 2,210 4 2 5 0,5034
5 4 1 1,720 4 2 4 0,4374
5 4 0 1,299 4 2 3 0,3751
5 3 5 2,520 4 2 2 0,3173
5 34 2,120 4 2 1 0,2643
5 33 1,748 4 2 0 0,2160
5 3 2 1,3999 4 1 5 0,4245
5 3 1 1,0832 4 1 4 0,3648
5 3 0 0,7921 4 1 3 0,3094
380
Приложение
Продолжение табл. П.1
Код роста Значение НВЧ Код роста Значение НВЧ
5 2 5 1,7650 4 1 2 0,2582
5 2 4 1,4775 4 1 1 0,2115
5 2 3 1,2020 4 1 0 0,1688
5 2 2 0,9435 4 0 5 0,3553
5 2 1 0,6983 404 0,3029
5 2 0 0,4929 4 0 3 0,2525
5 15 1,2920 4 0 2 0,2072
5 14 1,0600 t 40 1 0,1657
5 13 0,8400 4 0 0 0,1275
5 1 2 0,6300 3 5 5 0,4498
5 1 1 0,4560 3 5 4 0,4069
5 1 0 0,3290 3 5 3 0,3652
505 0,9526 35 2 0,3247
5 0 4 0,7586 3 5 1 0,2856
5 0 3 0,5770 3 5 0 0,2479
5 0 2 0,4265 3 4 5 0,3989
5 0 1 0,3137 3 4 4 0,3583
5 0 0 0,2311 3 4 3 0,3188
4 5 5 0,8063 3 4 2 0,2806
4 5 4 0,7217 34 1 0,2438
4 5 3 0,6391 340 0,2085
4 5 2 0,5592 3 3 5 0,3516
4 5 1 0,4825 3 34 0,3131
4 5 0 0,4109 3 3 3 0,2758
4 4 5 0,6930 3 3 2 0,2398
Приложение
381
Продолжение табл. П.1
Код роста Значение НВЧ Код роста Значение НВЧ
4 4 4 0,6148 33 1 0,2052
443 0,5390 330 0,1721
3 2 5 0,3077 ' 2 12 0,1162
3 2 4 0,2712 2 11 0,0921
3 2 3 0,2360 2 10 0,0683
3 2 2 0,2021 2 0 5 0,1641
3 2 1 0,1696 - 2 0 4 0,1393
320 0,1384 203 0,1150
3 1 5 0,2667 202 0,0910
3 1 4 0,2322 , 2 0 1 0,0676
3 13 0,1991 200 0,0446
3 12 0,1671 1 5 5 0,2400
3 11 0,1365 1 5 4 0,2172
3 10 0,1070 15 3 0,1946
305 0,2287 15 2 0,1721
304 0,1965 1 5 1 0,1499
303 0,1647 15 0 0,1279
30 2 0,1346 14 5 0,2149
3 0 1 0,1056 14 4 0,1926
300 0,0777 143 0,1704 -
255 0,3152 14 2 0,1484
2 5 4 0,2860 14 1 0,1266
2 5 3 0,2573 14 0 0,1050
2 5 2 0,2290 1 3 5 0,1906
2 5 1 0,2014 1 3 4 0,1687
382
Приложение
Продолжение табл. П. 1
Код роста Значение НВЧ Код роста Значение НВЧ
2 5 0 0,1743 1 3 3 0,1469
2 4 5 0,2822 13 2 0,1253
2 4 4 0,2539 1 3 1 0,1039
2 4 3 0,2261 1 3 0 0,0828
2 4 2 0,1989 1 2 5 0,1670
2 4 1 0,1721 1 24 0,1455
2 4 0 0,1459 1 2 3 0,1241
2 3 5 0,2506 , 12 2 0,1030
2 3 4 0,2232 1 2 1 0,0820
2 3 3 0,1964 1 2 0 0,0612
2 3 2 0,1700 1 1 5 0,1441
2 3 1 0,1442 1 1 4 0,1239
230 0,1189 1 1 3 0,1020
2 2 5 0,2205 1 1 2 0,0812
224 0,1940 1 1 1 0,0606
223 0,1680 1 1 0 0,0402
2 2 2 0,1425 1 0 5 0,1217
2 2 1 0,1176 1 0 4 0,1010
220 0,0931 1 0 3 0,0804
2 15 0,1917 102 0,0601
2 1 4 0,1661 1 0 1 0,0398
2 1 3 0,1409 1 0 0 0,0198
055 0,1898 0 2 5 0,1290
054 0,1706 0 2 4 0,1105
053 0,1515 023 0,0920
Приложение
383
Продолжение табл. П. 1
Код роста Значение НВЧ Код роста Значение НВЧ
05 2 0,1324 022 0,0735
0 5 1 0,1133 02 1 0,0551
0 5 0 0,0944 020 0,0367
0 4 5 0,1691 0 1 5 0,1096
044 0,1502 0 1 4 0,0912
043 0,1313 0 1 3 0,0729
0 4 2 0,1124 ” 0 12 0,0546
0 4 1 0,0935 0 1 1 0,0363
0 4 0 0,0747 0 1 0 0,0181
0 3 5 0,1489 0 0 5 0,0904
034 0,1301 004 0,0723
033 0,1114 003 0,0541
0 3 2 0,0928 002 0,0361
0 3 1 0,0741 00 1 0,0180
0 3 0 0,0555
384
Приложение
Таблица П.2. Код роста и вероятность НВЧ для 10 параллельных проб
Код роста Значение НВЧ Код роста Значение НВЧ
10 10 10 100 10 5 3 1,02
10 10 9 23,0 10 5 2 0,872
10 10 8 16,2 10 5 1 0,742
10 10 7 12,0 10 5 0 0,622
10 10 6 9,18 10 4 5 1,073
10 10 5 7,02 10 4 4 0,943
10 10 4 5,42 10 4 3 0,818
10 10 3 4,28 , 10 4 2 0,700
10 10 2 3,49 10 4 1 0,589
10 10 1 2,75 10 4 0 0,493
10 10 0 2,40 10 3 4 0,773
10 9 9 6,07 10 3 3 0,662
10 9 8 5,26 10 3 2 0,561
10 9 7 4,58 10 3 1 0,474
10 9 6 3,98 10 3 0 0,399
10 9 5 3,46 10 2 4 0,631
10 9 4 2,98 10 2 3 0,534
10 9 3 2,63 10 2 2 0,456
10 9 2 2,28 10 2 1 0,388
109 1 1,97 10 2 0 0,329
10 9 0 1,70 10 1 3 0,442
10 8 7 3,10 10 1 2 0,376
10 8 6 2,78 10 1 1 0,317
10 8 5 2,49 10 1 0 0,275
10 8 4 2,21 10 0 2 0,314
Приложение
385
Продолжение табл. П.2
Код роста Значение НВЧ Код роста Значение НВЧ
10 8 3 1,96 10 0 1 0,268
10 8 2 1J1 10 0 0 0,231
10 8 1 1,50 980 0,499
10 8 0 1,30 9 7 1 0,488
10 7 6 2,19 9 70 0,435
10 7 5 1,95 962 0,474
10 7 4 1,74 « 9 6 1 0,425
10 7 3 1,53 960 0,381
10 7 2 1,33 9 5 2 0,416
10 7 1 1,16 9 5 1 0,372
10 7 0 1,01 9 5 0 0,334 ~
10 6 6 1,75 943 0,408
10 6 5 1,57 942 0,365
10 6 4 1,41 94 1 0,324
10 6 3 1,25 940 0,290
10 6 2 1,09 933 0,362
10 6 1 0,933 9 3 2 0,324
10 6 0 0,792 9 3 1 0,288
10 5 5 1,30 930 0,255
10 5 4 1,15 9 2 3 0,316
9 2 2 0,284 642 0,171
9 2 1 0,253 64 1 0,155
92 0 0,223 640 0,139
9 1 2 0,249 6 3 2 0,153
9 1 1 0,221 6 3 1 0,138
386
Приложение
Продолжение табл. П.2
Код роста Значение НВЧ Код роста Значение НВЧ
9 1 0 0,193 6 3 0 0,123
9 0 2 0,217 6 2 2 0,137
9 0 1 0,191 6 2 1 0,122
900 0,164 6 2 0 0,107
860 0,270 6 1 2 0,121
85 1 0,267 6 1 1 0,106
850 0,242 6 1 0 0,092
842 0,266 , 602 0,106
8 4 1 0,240 6 6 1 0,092
840 0,217 6 0 0 0,078
83 2 0,239 5 5 0 0,128
8 3 1 0,214 5 4 1 0,127
830 0,193 5 4 0 0,114
823 0,233 5 3 1 0,113
8 2 2 0,210 5 3 0 0,100
8 2 1 0,188 5 2 2 0,113
8 2 0 0,169 5 2 1 0,099
8 1 2 0,187 5 2 0 0,086
8 1 1 0,166 5 1 2 0,099
8 1 0 0,147 5 1 0 0,073
802 0,166 5 0 2 0,085
80 1 0,146 5 0 1 0,072
800 0,128 5 0 0 0,060
76 0 0,212 4 5 0 0,106
75 1 0,209 4 4 0 0,093
Приложение
387
Продолжение табл. П.2
Код роста Значение НВЧ Код роста Значение НВЧ
7 5 0 0,191 43 1 0,092
74 2 0,208 43 0 0,080
74 1 0,188 42 1 0,080
740 0,171 4 2 0 0,068
73 2 0,188 4 12 0,080
73 1 0,169 4 1 1 0,068
730 0,152 4 10 0,056
722 0,167 402 0,067
72 1 0,150 40 1 0,056
720 0,133 400 0,045
7 1 2 0,149 340 0,076
7 1 1 0,132 33 2 0,086
7 1 0 0,116 3 3 1 0,075
702 0,132 3 3 0 0,064
7 0 1 0,116 3 2 1 0,064
700 0,101 3 2 0 0,053
6 50 0,155 3 1 2 0,064
3 1 1 0,053 200 0,020
3 1 0 0,043 1 3 0 0,038
302 0,052 1 2 1 0,038
3 0 1 0,042 12 0 0,029
300 0,032 1 1 1 0,028
2 4 0 0,062 1 1 0 0,019
2 3 0 0,051 1 0 1 0,019
2 2 0 0,041 100 0,011
388 Приложение
Продолжение табл. П.2
Код роста Значение НВЧ Код роста Значение НВЧ
2 1 1 0,040 0 2 0 0,018
2 10 0,030 0 1 1 0,018
2 0 2 0,040 0 1 0 0,009
2 0 1 0,030 0 0 1 0,009
Взаимодействие сероводорода
с компонентами окружающей среды
_ г
Влияние сероводорода на растения. В зонах с загазованно-
стью 0,002... 0,06 мг/м3 сероводорода в растениях происходит на-
копление серы. В течение вегетационного периода накопление се-
ры составляет, г/кг сухого вещества: для тополя бальзамическо-
го 2,3... 6,7; для ясеня зеленого 2,2... 6,2; для сирени обыкновенной
2,2... 3,3; для жимолости татарской 2,0... 5,5; для липы мелколист-
ной 2,8... 3,1; для вяза гладкого 1,0... 5,3; для черемухи обыкновен-
ной 0,7... 1,1; для клена 1,0... 4,4.
Гидробионты. При наличии в водоеме избытка H2S возни-
кает резкий дефицит кислорода. При концентрации H2S 1,0 мг/л
у рыб снижается частота дыхания, дыхательные движения нерит-
мичны, глубина их варьирует. Сероводород угнетает у рыб способ-
ность тканей утилизировать кислород. Он легко проникает в клетку
при pH < 6, но с увеличением pH воды его токсичность снижается.
К собственной токсичности яда прибавляется его способность сни-
жать содержание кислорода в водной среде.
Личинки мух-поденок и дафнии гибнут при концентрации
1,0 мг/л. Циклопы к H2S устойчивы.
Токсическое действие сероводорода через 24 часа проявляется
на форель уже при концентрации 0,86... 1,0 мг/л, на гольяна, ле-
ща, чавычу, лосося — при 1,0 мг/л, карпа — при 3,3, чукчана —
390
Приложение
при 3,8 мг/л. Гольян гибнет через 48 ч при концентрации 1,35 мг/л,
карась — через 36 ч при 10,0 мг/л.
Общий характер действия на теплокровных. Раздражающий
и удушающий газ вызывает поражения нервной системы, дыхатель-
ных путей и глаз. Может вызывать острые и хронические отравле-
ния с разного рода отдаленными последствиями. Острая интокси-
кация часто является тяжелым поражением, иногда со смертельным
исходом. Высокие дозы HjS оказывают действие, сходное с эффек-
том цианидов, ингибируя цитохромоксидазу, сукцинатдегидрогеназу
и нарушая тем самым процессы тканевого дыхания; возможно пря-
мое поражение ЦНС с параличом дыхательного центра. Длительное
и систематическое воздействие приводит к снижению иммунобио-
логической реактивности организма, увеличению общей неспецифи-
ческой заболеваемости, в том числе катарам верхних дыхательных
путей, ангинам, пневмониям, неврозам и др. Обладает также кож-
но-резорбтивным и эмбриотропным эффектами.
Острое отравление. Животные. Порог острого ингаляционно-
го действия для крыс 48,2 мг/м3. Для кроликов подпороговая концен-
трация при 40-минутной ингаляции составляет 60 мг/м3. Для мышей
при 2-часовой ингаляции 1080... 1300 мг/м3. У крыс, морских сви-
нок, кошек, кроликов и собак острое ингаляционное воздействие H2S
вначале вызывает возбуждение, гипервентиляцию, артериальную ги-
пертензию, затем паралич нервных центров, мидриаз, снижение ле-
гочной вентиляции, угнетение дыхания и гибель.
После нескольких часов вдыхания H2S в концентрациях 150...
225 мг/м3 появляются признаки раздражения слизистых глаз и глот-
ки, при 300... 400 мг/м3 раздражение глаз и слизистых оболочек
отмечается через 1 час, а после более длительного воздействия появ-
Приложение
391
ляются и слабо выраженные общие симптомы; при 750... 1050 мг/м3
локальное раздражение и нерезкие общие проявления интоксика-
ции развиваются менее чем через 1 час, а при воздействии в те-
чение нескольких часов возможна гибель животного. При концен-
трации 1350 мг/м3 через 30 мин развиваются тяжелые общие симп-
томы и менее чем через' 1 час наступает смерть; при 2250 мг/м3
коллапс и гибель наступают в течение первых 15... 30 мин;
при 2700... 3000 мг/м3 коллапс, паралич дыхания, судороги и гибель
наступают немедленно, через 1 — 2 вдоха. Видовые различия в чув-
ствительности к действию H2S невелики; наиболее чувствительны
канарейки, наиболее устойчивы козы.
Человек. Концентрация 0,0094 мг/м3 является подпорого-
вой. Максимально недействующая концентрация по рефлекторно-
му признаку 0,01 мг/м3. Порог обонятельного ощущения 0,014...
0,03 мг/м3. Порог влияния на световую чувствительность гла-
за 0,012 мг/м3, недействующая концентрация 0,01 мг/м3; при ком-
бинированном воздействии H2S и сероуглерода в пороговых концен-
трациях отмечается эффект простого суммирования.
При концентрации 0,0011 мг/л и более сероводород придает
воде запах тухлых яиц, концентрация в питьевой воде 0,07 мкг/л
может изменить ее вкус, но колебания индивидуальной чувствитель-
ности довольно значительны. Специфический запах не всегда мо-
жет служить предупреждающим об опасности отравления сигналом,
так как в концентрациях более 225 мг/м3 H2S оказывает парализу-
ющее действие на обонятельный аппарат, что снижает сигнальное
значение его запаха. Известен случай, когда большинство из 42 ра-
бочих, впавших в бессознательное состояние в результате острого
ингаляционного воздействия H2S, не ощущали характерного запа-
392
Приложение
ха но отметили ощущение слабого приятного запаха, перед потерей
сознания.
Под острым отравлением обычно подразумеваются эффекты ин-
галяционного воздействия (секунды — минуты) H2S в концентрациях
около 1400 мг/мз, быстро вызывающего дыхательные расстройства.
Подострое отравление — более длительное (до нескольких часов)
воздействие H2S в концентрациях от 140 до 1400 мг/м3. Наибо-
лее выраженной симптоматикой при подостром отравлении являет-
ся поражение глаз, хотя раздражение глаз может наблюдаться через
несколько часов или дней после воздействия малых концентраций
порядка 16... 32 мг/м3. '
При остром отравлении в легкой форме наблюдается раздра-
жение слизистой оболочки глаз, носа и глотки, боли и резь в гла-
зах, слезотечение, светобоязнь, блефароспазм, боли за грудиной, ка-
шель. Отравления средней тяжести характеризуются выраженными
признаками резорбтивного действия: головная боль, головокруже-
ние, неустойчивая походка, тошнота, рвота, коликообразные боли
в животе, понос, состояние оглушения или возбуждения, обмороки.
Быстро развиваются бронхит, бронхопневмония, отек легких, рас-
стройства сердечной деятельности с падением артериального кро-
вяного давления. Тяжелые поражения протекают по типу судорож-
ной комы: быстрая и глубокая потеря сознания, судороги, угнете-
ние рефлексов, галлюцинация, расстройства сердечной деятельности
и дыхания, отек легких. Коматозное состояние может завершиться
смертельным исходом или сменяется двигательным возбуждением
с последующим глубоким сном. Из поздних осложнений отмечаются
пневмония, астенический синдром, нередко осложненный энцефало-
патией.
Приложение
393
При воздействии очень высоких концентраций может возник-
нуть молниеносная (апоплектическая) форма отравления, которая
приводит к почти мгновенной смерти от паралича дыхательного цен-
тра. При аутопсии обнаруживается картина смерти от асфиксии, за-
пах тухлых яиц от вскрытых полостей, внутренних органов, особенно
легких; кровь и внутренние органы вишнево-красного цвета.
В промышленных условиях, например при перегонке нефти,
производстве вискозного шелка, в дубильном производстве, при кана-
лизационных работах, на предприятиях химической промышленно-
сти, при работах, связанных с освоением и использованием геотер-
мальных ресурсов и т.п., воздействие образующихся высоких кон-
центраций H2S может приводить к тяжелым и смертельным пораже-
ниям. Известен случай, когда три человека попали в облако H2S, вы-
рвавшегося из баллона высокого давления, у всех наступила останов-
ка дыхания, бессознательное состояние. Пострадавшие были спасены
благодаря немедленным реанимационным мероприятиям, при этом
у двоих отмечались тяжелые судороги, сознание не возвращалось
в течение 30 мин. Никто из них не вспомнил, что ощущал характер-
ный запах H2S, концентрация которого была оценена в 2800 мг/м3.
На предприятиях нефтедобывающей, газодобывающей и нефте-
химической промышленности Канады из 221 случая отравлений H2S
общая смертность составила 6%, в 75% случаев у пострадавших
отмечалась потеря сознания, у 124 развилась кома. У большинства
отравленных наблюдались различные симптомы поражения нервной
системы, в том числе нарушения поведения, головокружение, спутан-
ность сознания, ажитация или сомноленция. В 40% случаев отмеча-
лись респираторные нарушения, потребовавшие применения вспо-
могательного дыхания, у 15% пострадавших развился отек легких.
394
Приложение
При более легких поражениях отмечались жалобы на головную боль,
ощущение «песка в глазах», расстройства со стороны желудочно-ки-
шечного тракта.
Хронические отравления. Лица, подвергающиеся длительно-
му воздействию сравнительно небольших концентраций H2S, в част-
ности на нефтеперерабатывающих заводах, жалуются на головные
боли, головокружения, общую слабость, быструю утомляемость, пот-
ливость, сладкий вкус во рту, тошноту, кашель, боли в области серд-
ца. Объективно: бледность кожных покровов, упадок питания, брон-
хит, расстройство функции кишечника со склонностью к поносу, рез-
ко выраженная влажность ладоней, стойкий красный дермографизм,
дрожание пальцев, век, языка, болезненность в мышцах и иногда
по ходу нервных стволов, сужение полей зрения, гиперемия глазно-
го дна, иногда побледнения сосков с переходом в атрофию. Может
снижаться уровень эритроцитов в периферической крови.
При хронических отравлениях H2S возможно развитие цереб-
растенического синдрома, нередко сочетающегося с отдельными ор-
ганическими симптомами. У лиц, работающих на перегонке нефти,
иногда к концу рабочего дня снижается активность ацстилхолинэсте-
разы, причем степень снижения ее находится в определенной зави-
симости от содержания H2S в нефтяном газе.
Поступление, распределение и выведение H2S из организма.
Сероводород поступает в организм главным образом ингаляцион-
ным путем, редко через кожные покровы. После поступления быстро
окисляется и выводится с мочой в виде полисульфидов, сульфата,
тиосульфата. Детоксикация происходит в печени под воздействием
сульфоксидазы либо путем образования дисульфидных связей с глу-
Приложение
395
татионом. Часть H2S, особенно поступившего через кожу и не под-
вергшегося метаболизму, выделяется через легкие (7 %), кожу.
Неотложная помощь. Прежде всего, пострадавший должен
быть удален из опасной зоны и вынесен на свежий воздух. За-
тем — кислород (осторожно), искусственное дыхание по показани-
ям, в/венно 0,25...0,5% раствор метиленового синего по 10 ,мл
с глюкозой; лобелии, цититон и другие средства, возбуждающие ды-
хательный центр, сердечно-сосудистые средства. При токсической
коме с обильной ротоносовой секрецией — положение на спине,
гиперэкстензия головы, рото- или носоглоточная искусственная ас-
пирация отделяемого с выдвижением нижней челюсти вперед, фик-
сация западающего языка (восстановление ротоглоточной проходи-
мости). При отеке легких — хлорид кальция (10 мл 10% раствора
внутривенно) или глюконат кальция (10 мл 10% раствора в/венно
или в/мышечно). В случае приема внутрь — промывание желудка
насыщенным раствором гидрокарбоната натрия, затем солевое сла-
бительное. При поражении глаз — промывание водой, затем в конъ-
юнктивальный мешок 3 — 4 капли адреналина 1:1000 повторно, за ве-
ки вазелиновое масло или индифферентную глазную мазь. При бо-
лях — местное обезболивающее: 1 — 2 % раствора кокаина, новокаина,
на глаза — прохладные примочки.
Литература
[1] Агаев Н. М., Смородин А. Е., Гусейнов М.М. Влияние 7-облучения
на жизнедеятельность сульфатвосстанавливающих бактерий // За-
щита металлов. — 1985. — № 1. — С. 127.
[2] Агаев Н. М., Смородин А. Е., Гусейнов М. М. О влиянии суль-
фатвосстанавливающих бактерий на коррозию стали // Эксп.-инф:
Сер. Коррозия и защита окружающей среды. — М.: ВНИИОЭНГ,
1984,-№7.-С.4-9.
[3] Акользин А. П„ Новичихина А. В. Микробиологическая коррозия
стали в исходных водах теплоэнергетических объектов // Теплоэнер-
гетика. — 1981. — № 11. — С. 65-67.
[4] Активация в биологии / В. М.Бахир, Л. Е. Спектор, Г. Р. Мирзака-
римова и др. // М.: Профиздат. Техника и Наука, 1982. — № 12.
[5] Активированные вещества. Некоторые вопросы теории и практики /
В.М.Бахир, А.Р. Атаджанов, У.Д.Мамаджанов и др. // Изв. АН Уз-
ССР: Сер. техн. наук. — 1981. — №5.
[6] Александров В. П., Кайнаш В. В., Рябоконь С. А. Промышленное про-
изводство утяжеляющей добавки к буровым растворам, нейтрали-
зующей сероводород // М.: ВНИИОЭНГ, РНТС Бурение, 1981. —
№1.-С. 19-21.
[7] Андресон Р. К., Эфенди-заде С. М. Бактерициды для борьбы с био-
коррозией в нефтегазовой промышленности // Обзорн. инф: Сер.
Борьба с. коррозией и защита окружающей среды — М.: ВНИИОНГ,
1989.-Вып. 8 (92).-52 с.
Литература
397
[8] Андресон Б. А., Андресон Р. К., Огаркова Э. И. Нейтрализация се-
роводорода и борьба с сульфатредукцией в нефтедобывающей про-
мышленности // Обзорн. инф: Сер. Коррозия и защита в нефтега-
зовой промышленности — М.: ВНИИОЭНГ, 1985. — Вып. 5 (49). —
33 с.
[9] Андреюк Е. И., Козлова И. А. Литотрофные бактерии и микробиоло-
гическая коррозия. — Киев: Наукова думка, 1977. — 163 с.
[10] Антоновская Н. С., Козлова И. А., Андреюк Е. И. Распределение СРБ
в грунте вблизи газопровода // Микробиол. журн. — 1985. — Т. 47,
№2.-С.93-94.
[11] А. с. 914611 СССР, МКИ С 09 К 7/00. Способ обработки бурового рас-
твора для нейтрализации сероводорода / А. И. Булатов, А. П. Крезуб,
В. А. Мосин (СССР). - №2917096/22-03. Заявлено 25.04. 1980.
Опубл. 23.03.1982. Бюл. № 11.
[12] А. с. 1030535 СССР, МКИ Е 21 В 33/138. Способ борьбы с перетоком
пластовых сероводородных вод в затрубное пространство скважин /
В. Н. Дядечко, И. И. Нестеров, Т. А. Панова (СССР). — № 3366634/22-
03. Заявлено 17.12.1981. Опубл. 23.07.1983. Бюл. №27.
[13] А. с. 1049516 СССР, МКИ С 09 К 7/02. Способ поглощения серово-
дорода и водорастворимых сульфидов в буровых растворах на вод-
ной основе / А. А. Русаев, К. В. Бибиков, К. И. Суркова (СССР). --
№3473808/23-03. Заявлено 08.04.1982. Опубл. 23.10.1983. Бюл.
№39.
[14] А. с. 1099966 СССР, МКИ А 61 L 2/16. Бактерицидное средство /
Г. А. Толстиков, У. М. Джемилев, Р. К. Андресон и др. (СССР). —
№3353122/28-13. Заявлено 27.10.1981. Опубл. 30.06.1984. Бюл.
№24.
[15] А. с. 1127893 СССР, МКИ С 09 К 7/06. Смазочная, противоизносная
и сероводороднейтрализующая добавка к буровым растворам на вод-
ной основе / Б. А. Андресон, Г. П. Бочкарев, Э. И. Огаркова и др.
398
Литература
(СССР). - № 3562221/23-03. Заявлено 03.03.1983. Опубл. 07.12.1984.
Бюл. №45.
[16] А. с. 1138402 СССР, МКИ С 09 К 7/02. Промывочная жидкость
для бурения скважин / Е. В. Столяров, Б. А. Андресон, У. М. Дже-
милев и др. (СССР). — №3540423/23-03. Заявлено 07.12.1982.
Опубл. 07.02.1985. Бюл. №5.
[ 17] Асфандияров Ф. А., Кильдибеков И. Г., Низамов К. Р. Методы борьбы
с сульфатвосстанавливающими бактериями и вызываемой ими кор-
розией стали // Обзорн. инф: Сер. Коррозия и защита в нефтегазовой
промышленности — М.: ВНИИОЭНГ, 1983. — Вып.6 (30). — 33 с.
[18] Атаджанян Б. П., Всзиров Ч. Б., Алиев М. Р. Способ нейтрализации
сероводорода в пластовой воде // Нефтяное хозяйство. — 1984. —
№9. - С. 48-51
[19] Бахир В. М. Химический состав и свойства электрохимических ак-
тивированных растворов. — М.: Гиперокс, 1990. — 345 с.
[20] Бахир В. М. Электрохимическая активация. — М.: ВНИИИМТ,
1992.-675 с.
[21] Бергман Л. Ультразвук и его применение в науке и технике. — М.:
ИЛ, 1956.-272 с.
[22] Берк А., Вултерин Я., Зык Я. Новые редокс-методы в аналитической
химии. — М.: Химия, 1968.
[23] Борзенков И. А. Формирование химического состава подземных вод
в результате бактериальной сульфатредукции // Тр. ВНИИгидрогео-
логия и инженерная геология. — М., 1982. — № 146. — С. 15-19.
[24] Бурение глубоких скважин в условиях сероводородной агрессии /
А. Г. Потапов, А. Н. Ананьев и др. // Обзорн. инф: Сер. Бурение. —
М.: ВНИИОЭНГ, 1981. - 60 с.
[25] Влияние биологического фактора на процессы коррозии в нефтепро-
мысловых водах Уршакского месторождения / В. В. Леонов и др. //
НТЖ. Сер. Защита от коррозии и охрана окружающей среды. — М.:
ВНИИОЭНГ, 1994. -№3. - С. 11-14.
Литература
399
[26] Влияние температурных условий продуктивного пласта на особен-
ности формирования биоценоза нефтепромысловой микрофлоры /
Р. X. Хазипов, Н. Н.Силищев, В. В. Леонов и др. // Нефтяное хозяй-
ство. - 1991. - № 7. - С. 3 7-39.
[27] Влияние технологических факторов на физико-гидродинамические
характеристики и. технологические процессы добычи нефти /
Н. И. Хисамутдинов, М. М. Хасанов, Р. Ш. Тахаутдинов и др. // Неф-
тепромысловое дело. — 1977. — № 12. — С. 2-10.
[28] Гарифуллин Ф. С. Предупреждение образования комплексных суль-
фидсодержащих осадков в добыче обводненной нефти. — Уфа: Изд-
во УГНТУ, 2002. - 267 с.
[29] Герасименко А. А. Биокоррозия и защита металлоконструкций.
1. Особенности процесса биокоррозии. Микробная коррозия в при-
родных средах // Практика противокоррозионной защиты. — 1998. —
№4(10).-С. 14-26.
[30] Герасименко А. А. Защита машин от биоповреждений. — М: Маши-
ностроение, 1984. — 112 с.
[31] Гетманский М.Д., Еникеев Э. X. Современное состояние и перспек-
тивы ингибирования нефтепромыслового оборудования в средах, со-
держащих сероводород и двуокись углерода // Обзорн. инф: Сер.
Коррозия и защита в нефтегазовой промышленности. — М.: ВНИ-
ИОЭНГ, 1985.-60 с.
[32] Гетманский М.Д., Рождественский Ю. Г., Калимуллин А. А. Преду-
преждение локальной коррозии нефтепромыслового оборудования //
Обзорн. инф: Сер. Коррозия и защита в нефтегазовой промышлен-
ности. - М.: ВНИИОЭНГ, 1981. - 57 с.
[33] Глинка Н. Л. Общая химия. Изд. 18, испр. — Л.: Химия, 1976.— 728 с.
[34] Голубовская Э. К. Биологические основы очистки воды. — М.: Выс-
шая школа, 1978. — 268 с.
[35] Грабович М.Ю. Участие прокариот в круговороте серы // Соросов-
ский образовательный журнал. — 1999. — № 12. — С. 16-20.
400
Литература
[36] Громов Б. В., Павленко Г. В. Экология бактерий. — Л.: Изд-во ЛГУ,
1989. - 248 с.
[37] Громов Б. В. Удивительный мир архей // Соросовский образователь-
ный журнал. — 1997. — №4. — С. 23-26.
[38] Даминов А. А., Кольчугин И. С. Некоторые особенности коррозион-
ных процессов в условиях отложения осадков // Нефтепромысловое
дело. - 1998. - №6. - С. 37-38.
[39] Заварзин Г. А. Литотрофные микроорганизмы. — М.: Наука, 1972. —
329 с.
[40] Загиров М. М., Перов А. В. Защита обсадных колонн нагнетатель-
ных скважин от коррозии //Обзорн. инф: Сер. Коррозия и защита
в нефтегазовой промышленности. — М.: ВНИИОЭНГ, 1978. — 40 с.
[41] Закономерности топохимической ^инетики развития и подавления
процессов биокоррозии в нефтепромысловых водах / М.Ю. Доло-
матов, А. Г. Телин, В. В. Леонов и др. // Нефтепромысловое дело. —
1999.-№12.-С.37-39.
[42] Защита нефтепромыслового оборудования от коррозии. Учебное по-
собие для рабочих / Э."М. Гутман, К. Р. Низамов, М. Д. Гетманский
и др. // М., Недра, 1983. — 152 с.
[43] Защита от коррозии реагентами комплексного действия в условиях
зараженности нефтепромысловых систем сульфатвосстанавливаю-
щими бактериями / А. Р. Пантелеева, С. В. Улахович, Р. Ф. Тишанкина
и др. // Нефтяное хозяйство. — 2004. — №8. — С. 106-107.
[44] Защита от коррозии, старения, биоповреждений машин, оборудова-
ния, сооружений. Справочник в 2-х томах. Под редакцией А. А. Ге-
расименко. — М: Машиностроение. — 1987. — Т. 1. — 688 с., Т. 2. —
784 с.
[45] Зборщик М. П., Осокин В. В. Явление выделения из пиритсодержа-
щей горной породы элементной серы под действием тионовых бак-
терий / Международная ассоциация авторов научных открытий. —
Диплом №79 на открытие. — 1998.
Литература
401
[46] Изучение влияния используемых в нефтяной промышленности
НПАВ на сульфатвосстанавливающие бактерии / А. X. Сабирова,
3. Г. Мурзагильдин, Е. Г. Юдина и др. // Сб. научных трудов. — Уфа,
ВНИИСПТнефть, 1990. - С. 78-82.
[47] Изучение кинетики коррозионного процесса Ст. 3 в средах, содер-
жащих СВБ и сероводород / В. Г. Кильдибеков, Ф. А. Асфандияров.
К. Р. Низамов и др. // Тезисы докл. II Всесоюз. конф, по биоповре-
ждениям. — Горький, 1981. — Ч. 1 — С. 100.
[48] Использование анолита в качестве бактерицида для подавления
жизнедеятельности сульфатвосстанавливающих бактерий (СВБ) /
Ф. А. Каменщиков, Н. Л. Черных, В. В. Минаков и др. // Тезисы до-
кладов 4-й Российской университетско-академической научно-прак-
тической конференции. 4.6. — Ижевск: Изд-во Удм. ун-та, 1999. —
С. 118-120.
[49] Исследование поглотителей сероводорода в жидкой фазе /
Л. Л. Макарова, Т. В. Поторочина, Каменщиков Ф. А. и др. // Те-
зисы докладов 4-й Российской университетско-академической на-
учно-практической конференции. 4.2. — Ижевск: Изд-во Удм. ун-
та, 1999.-С. 139-140.
[50] Кальдерные микроорганизмы / Под ред. Г. А. Заварзина. — М.: Наука,
1972. - 120 с.
[51] Каменщиков Ф. А. Методика количественной оценки микробиологи-
ческой зараженности нефтепромысловых сред // Инфор. листок /
Удм. ЦНТИ. - 1990. - №48-90. - С. 1-3.
[52] Каменщиков Ф. А. Причины образования сероводорода в нагнета-
тельных скважинах / Тезисы докладов 4-й Российской универ-
ситетско-академической научно-практической конференции. 4.6. —
Ижевск: Изд-во Удм. ун-та, 1999. — С. 126-127.
[53] Каменщиков Ф. А., Тощевиков Л. Г., Григорьева Т. М. Определение
периода адаптации СВБ к бактерициду ЛПЭ-11 / Тезисы докладов
402
Литература
4-й Российской университетско-академической научно-практической
конференции. Ч. 6. — Ижевск: Изд-во Удм. ун-та, 1999. — С. 121-122.
[54] Кондратьева Е. Н. Хемолитотрофы и метилотрофы. — М: Изд-во
МГУ, 1983.- 172 с.
[55] Коррозионное разрушение внутрискважинного оборудования и про-
мысловых трубопроводов на нефтяных месторождениях Западной
Сибири / Н. П. Кузнецов, В. Д. Макаренко, В. В. Объедкова и др. //
Нефтяное хозяйство. — 2004. — № 12. — С. 69-71.
[56] К оценке эффективности применения ингибиторов в условиях ми-
кробиологической зараженности нефтепромысловых вод Миниба-
евской площади Ромашкинскога месторождения / В. В. Леонов,
А. Ф. Закиров, А. А. Магалимов и др. // Нефтепромысловое дело. —
2000,-№11. - С. 55-56.
[57] Коррозионная активность микрофлоры нефтепромысловых вод и ин-
гибиторная защита от нее / В. В. Леонов, Р. X. Хазипов, Н. С. Сатта-
ров и др. // Нефтяное хозяйство. — 1994. — № 8. — С. 53-56.
[58] Кудрявцева Е. И., Свечина Р. М. Микробиологическая характеристи-
ка подземных вод Камчатки в связи с нефтегазоносностью. В кн.:
Гидрогеологическое составление прогноза нефтегазоносности. — Л.,
1983.-С.78-85.
[59] Ли А. Д., Полюбай П. И. Борьба с образованием сероводорода в неф-
тяных пластах при их заводнении. — М.: ВНИИОЭНГ, 1974.
[60] Магалимов А. А. Опыт разработки и реализации технологий подавле-
ния биоценоза нефтепромыслового оборудования // Нефтепромыс-
ловое дело. — 1999. — № 11. — С. 40-44.
[61] Магалимов А. А. Опыт текущей оценки биоценоза нефтяных пластов
и разработка мероприятий по его подавлению // Нефтепромысловое
дело.- 1999, —№11.-С.27-31.
[62] Малахов В. В. Вестиментиферы — автотрофные животные // Соро-
еовский образовательный журнал. — 1997. — №9. — С. 18-26.
Литература
403
[63] Маркин А. Н., Шаманина А. Н., Вавер В. И. Биоцидная активность
ингибиторов коррозии // Нефтяное хозяйство. — 1994. — №1. -
С. 65-66.
[64] Методы общей бактериологии: Пер. с англ./Под ред. Ф. Гархарда
и др. — М.: Мир, 1983. — 536 с.
[65] Микробная коррозия в нефтепромысловых водах и ее подавление
химреагентами / В. В. Леонов, Т.М. Вахитов, К. Р.Уразаков и др. //
Нефтепромысловое дело. — 2000. — №7. — С. 37-39.
[66] Микробная коррозия и ее возбудители // Е. И. Андреюк, В. И. Билай '
и др. — Киев: Наукова думка, 1980.
[67] Мишин В. М., Афанасьев А. И. Оператор по переработке сернистого
природного газа. — М.: Недра, 1987. — 132 с.
[68] Мурзагильдин 3. Г. Разработка и совершенствование методов сниже-
ния аварийности нефтесборных трубопроводных систем: Автореф.
дис. канд. техн, наук / Уфимский нефт. ин-т. — Уфа, 1989. — 23 с.
[69] Неволин В. Г., Шарова Г. А. Использование вибратора ЗАО «Инокар»
для борьбы с коррозией и СВБ // Нефтепромысловое дело. — 2003. —
№3.-С. 18-20.
[70] Новые нейтрализаторы сероводорода и их биоцидные свойства /
Р. Р. Гафиатуллин, Р. С. Алеев, Ю. С. Дальнова и др. // Нефтяное хо-
зяйство. — 2000. — № 1. — С. 61-62.
[71] О влиянии свойств поверхности металла на процессы биокор-
розии в нефтепромысловых водах / В. В. Леонов, Т. М. Вахитов,
К.Р.Уразаков и др. // Нефтепромысловое дело. — 2000. — №7. —
С. 34-37.
[72] Определение бактерицидных свойств некоторых ингибиторов /
Л. Л. Макарова, Т. В. Поторочина, Ф. А. Каменщиков и др. // Тези-
сы докладов 4-й Российской университетско-академической научно-
практической конференции. 4.2. — Ижевск: Изд-во Удм. ун-
та, 1999.-С. 140-141.
404
Литература
[73] Особенности концентрационно-температурной кинетики подавле-
ния биокоррозии реагентами-бактерицидами / М. Ю. Доломатов,
В. В. Леонов, А. А. Магалимов и др. // Нефтепромысловое дело. —
2000.-№5.-С.32-34.
[74] Особенности развития СВБ в условиях работы коррозионных ма-
крогальванопар / З.Г. Мурзагильдин, А. X. Сабирова, К. Р. Низамов
и др. // Сб. трудов. Методы и средства эффективной эксплуатации
нефтепромыслового оборудования и трубопроводов. — Уфа: ВНИ-
ИСПТнефть, 1990. - С. 73-77.
[75] О природе электрохимической активации сред / П. А. Кирпичников,
В. М. Бахир, П. У. Гамер и др. // Докл. АН СССР. — 1986. — Т. 286. —
№3,-С. 663-666. '
[76] Островский Д. Н., Капрелянц А. С., Лукоянова М. А. Прикладные ас-
пекты биохимии мембран // Обзор. Прикладная биохимия и микро-
биология. — 1983. — Т. 19. — Вып. 1. — С. 60.
[77] Пастернак В. И. Испытание на присутствие сульфатвосстанавливаю-
щих бактерий / Экспресс инф., зарубежный опыт: Сер. Борьба с кор-
розией и защита окружающей среды. — М.: ВНИИОЭНГ. — 1989. —
№17.-С. 12-15.
[78] Пат. 2107085 РФ, МКИ С 10 G 29/24. Способ очистки жидких углево-
дородных фракций от сероводорода и меркаптанов / А. М. Фахриев,
Р. А. Фахриев, М. М. Белкина (РФ). — Опубл. 20.03.1998. Бюл. № 8.
[79] Пат. 2109033 РФ, МКИ С 10 G 27/10. Способ очистки нефти
и газоконденсата от сероводорода / Ф. Г. Шакиров, А. М. Мазгаров,
А. Ф. Вильданов и др. (РФ). — Опубл. 20.04.1998. Бюл. № 11.
[80] Пат. 2118649 РФ, МКИ С 10 G 29/20. Способ очистки нефти и газо-
конденсата от сероводорода / А. М. Фахриев, Р. А. Фахриев (РФ). —
Опубл. 10.09.1998. Бюл. №25.
[81] Пат. 2121492 РФ, МКИ С 10 G 29/20. Способ очистки нефти, газо-
конденсата и их фракций от меркаптанов и сероводорода / А. М. Фах-
риев, Р. А. Фахриев (РФ). — Опубл. 10.11.1998. Бюл. №31.
Литература
405
[82] Патент 2136864 РФ, МКИ Е 21 В 43/22. Способ нейтрализа-
ции сероводорода в нефтяной скважине / М. К. Рогачев, Ю. В. Зейг-
ман, М. М. Мухаметшин и др. (РФ). — №98106004/03. Заявле-
но 30.03.1998. Опубл. 10.09.1999. Бюл. №25.
[83] Пат. 2143055 РФ, МКИ Е 21 В 41/02. Скважинный защитный со-
став от коррозии /-Е'. И. Богомольный, А. М. Насыров, С. Д. Бирюков
и др. (РФ). - № 99110836/03. Заявлено 01.06.1999. Опубл. 20.12.1999.
Бюл. №35.
[84] Пат. 2160761 РФ, МКИ С 10 G 29/20. Способ дезодорирую-
щей очистки нефти и газоконденсата от сероводорода и меркапта-
нов / Ф. Г. Шакиров, А. М. Мазгаров, А. Ф. Вильданов и др. (РФ). —
Опубл. 20.12.2000. Бюл. №35.
[85] Пат. 2241684 РФ, МКИ С 02 F 1/58. Средство для удаления серо-
водорода и меркаптанов из газов, нефти, нефтепродуктов, пласто-
вых вод и буровых растворов / В. М. Андрианов, Ю. С. Дальнова,
К. Р. Низамов и др. (РФ). — №2003117325/15. Заявлено 09.06.2003.
Опубл. 10.12.2004. Бюл. №34.
[86] Пат. США №3250697, 1966.
[87] Пат. ФРГ №3151133, МКИ С 10G 27/12, 1983.
[88] Перт С. Дж. Основы культивирования микроорганизмов и клеток. —
М.: Мир, 1978.- 331 с.
[89] Пиз Д. Гистологическая техника в электронной микроскопии. — М.:
Изд-во Иностранной литературы. — 1963. — 164 с.
[90] Праздникова 3. Ф., Филатова Л. А. Исследование биодеструкции
полиакриламидов, применяемых на месторождении Каламкас //
Тр. Каз-НИПИнефть. — 1984. — Вып. 11. — С. 54-56.
[91] Праздникова 3. Ф., Вебер В. И., Костюк Т. В. Предупреждение био-
деструкции полиакриламидов при полимерном заводнении место-
рождения Каламкас // М.: ВНИИОЭНГ, НТИС Нефтепромысловое
дело и транспорт нефти, 1985. — №6. — С.61-63.
406
Литература
[92] Применение технологии биоцидного воздействия на Алехинском ме-
сторождении / 3. М. Хусаинов, О. Р. Коробовкин, В. Л. Чирков и др. //
Нефтепромысловое дело. — 1999. — №8. — С. 10-11.
[93] Пригула В. В., Лупулов В. В. Применение радиоактивных изотопов
в практике борьбы с коррозией. — М.: ВНИИОЭНГ, 1974.
[94] Промысловые исследования влияния кислорода на усиление корро-
зии трубопроводов / Р. М. Саматов, Ф. Г. Арсланов, Ф. С. Гарифуллин
и др. // Нефтяное хозяйство. — 2003. — № 1. — С. 71-73.
[95] Разработка и испытание технологии удаления и предупреждения
биообразований в призабойной зоне и пласте / В. И. Соловых,
А. М. Потапов, Н. И. Хисамутдинов и др. // Нефтяное хозяйство. —
1994. — №2. — С. 69-73.
[96] Разработка технологии защиты ПАА от бидеструкции / Р. X. Хази-
пов, Т. А. Исмагилов, Б. М. Шарафутдинов и др. // Нефтяное хозяй-
ство. - 1992. - №8. - С. 17-20.
[97] РД 39-132-94. Правила по эксплуатации, ревизии, ремонту и отбра-
ковке нефтепромысловых трубопроводов / НПО ОБТ. — Москва,
1994.
[98] РД 39-0147103-350-89. Оценка бактерицидной эффективности реа-
гентов относительно адгезированных клеток сульфатвосстанавлива-
ющих бактерий при лабораторных испытаниях / ВНИИСПТнефть. —
Уфа, 1989,- 12 с.
[99] РД 39-3-973-83. Методика контроля микробиологической заражен-
ности нефтепромысловых вод и оценка защитного и бактерицидного
действия реагентов / ВНИИСПТнефть. — Уфа, 1984. — 38 с.
[100] РД 39-5794688-288-89Р. Инструкция по применению уротропиновых
оснований для стабилизации водного раствора полиакриламида /
НПО Союзнефтеотдача. — Уфа, 1989.
[101] Реагенты для борьбы с сульфатредуцирующими бактериями и ней-
трализации сероводорода / Б. А. Андресон, А. Г. Телин, В. М. Шара-
Литература
407
футдинов и др. // Экспресс-инф: Сер. Борьба с коррозией и защита
окружающей среды. - М.: ВНИИОЭНГ. - 1988. - № 1. - С. 1-5.
[102] Результаты применения бактерицидов на месторождениях Узень
и Жетыбай / 3. Ф. Праздникова, Л. А. Филатова и др. — Материа-
лы Всесоюзного научно-технического семинара «Особенности зара-
жения нефтяных пластов микроорганизмами, совершенствование си-
стем подготовки вод для закачки их в продуктивные пласты и методы
борьбы с микробиологической коррозией. — М.: ВНИИОЭНГ, 1980.
[103] Розанова Е. П., Балдина А. Л. Сульфатредукция в заводняемых неф-
тяных карбонатных пластах ft Нефтяное хозяйство. — 1978. — №4. —
С.43-Л5.
[104] Розанова Е. П., Кузнецов С. И. Микрофлора нефтяных месторожде-
ний. — М.: Наука, 1974. — 197 с.
[105] Роль продуктов жизнедеятельности бактерий Thiobacillus Thiooxi-
dans в коррозии стали 10ХСНД / Р. Л. Бару, А. М. Зиневич, Г. М. Мо-
гильницкий и др. // Защита металлов. — 1982. — Т. 18. — №5. —
С. 761.
[106] Рубенчик Л. И. Сульфатредуцирующие бактерии. — М.-Л.: Изд-во
АН СССР, 1947. - 96 с.
[107] Руководство к практическим занятиям по микробиологии / Под ред.
Егорова Н. С. — М.: МГУ, 1983. — 136 с.
[108] Сабирова А. X., Мурзагильдин 3. Г., Юмагужин. Влияние неионо-
генных поверхностно-активных веществ на чувствительность суль-
фатвосстанавливающих бактерий к бактерицидам / Труды ВНИИС-
ПТнефть. Сбор и подготовка транспорта нефти и нефтепродуктов. —
Уфа, 1991.-С.63-67.
[109] Семенихина Л. П., Перекупка А. Г. Повышение эффективности
поверхностно-активных веществ, применяемых в нефтедобыче, с по-
мощью магнитных полей // Материалы 8-й международной Плес-
ской конференции по магнитным жидкостям. — 1988.
408
Литература
[ПО] Семихина Л. П., Перекупка А. Г., Семихин Д. В. Повышение эффек-
тивности ингибиторов коррозии // Нефтяное хозяйство. — 2003. —
№1,-С. 62-65.
[111] Семихина Л. П., Перекупка А. Г., Семихин Д. В. Способы повыше-
ния эффективности ингибиторов коррозии // Материалы Всероссий-
ской научно-практической конференции: «Разработка, производство
и применение химических реагентов для нефтяной и газовой про-
мышленности». — 2001. — С. 151-153.
[112] Совершенствование биоцидной технологии удаления и предупре-
ждения биообразований и повышения нефтеотдачи для условий ме-
сторождений Западной Сибири / Т. А. Исмагилов, М. 3. Игдавлетова,
О. И. Воротилин и др. // Нефтепромысловое дело. — 1999. — №5. —
С. 32-35.
[113] Современное состояние и перспективы применения методов борь-
бы с сероводородом / М. М. Мухаметшин, М. К. Баймухаметов,
И. Ш. Гарифуллин и др. // Нефтяное хозяйство. — 2002. — №4. —
с. 65-67.
[114] Современное состояние проблемы предотвращения бактериальной
коррозии в нефтяной промышленности / Н. М. Агаев, А. Е. Сморо-
дин, А. В. Аллахвердова и др. // Обзорн. инф: Сер. Борьба с кор-
розией и защита окружающей среды — М.: ВНИИОЭНГ, 1986. —
Вып.7 (59).- 64 с.
[115] Соколова Г. А., Каравайко Г. И. Физиология и геохимическая деятель-
ность тионовых бактерий. — М.: Наука, 1964. — 333 с.
[116] Спектор Л. Е., Мамаджанов У. Д. Физическая природа явлений акти-
вации веществ // Изв. АН УзССР: Сер. техн. наук. — 1983. — № 1.
[117] Справочник азотчика / Н. А. Симулин, Е. Я. Мельников, М. С. Фур-
ман и др. Под ред. Е. Я. Мельникова. — М.: Химия, 1967. — Т. 1. —
492 с.
Литература
409
[118] Сравнительные исследования эффективности реагентов-нейтрализа-
торов сероводорода / В. В. Кайнаш и др. В кн.: Выбор оптимальной
технологии промывки скважин. — Краснодар, 1981. — С. 71-75.
[119] Ставская С. С. Биологическое разрушение анионных ПАВ // Киев,
Наукова думка, 1981.
[120] Ставская С. С., Григорьева Т. Ю., Гаибова Н. Д., Ротмистров М. Н.
Бактериальная деструкция анионных поверхностно-активных ве-
ществ сульфоэтоксилатов / Микробиология, 1987. — Т. 56. —
Вып.4. — С. 698.
[121] Старосветская Ж. О., Бару Р. Л.,-Тимонин В. А. Влияние тионовых
бактерий на коррозионную стойкость низколегированных сталей //
Противокоррозионная защита в химической промышленности. — М.,
1983.-С. 7-11.
[122] Старосветская Ж. О. Закономерности биокоррозионного разрушения .
низколегированной стали 10ХСНД в средах тионовых бактерий. Ав-
тораф. дис. ктн. — М: ВНИИК, МИНГ. — 1987. — 26 с.
[ 123] Старосветская Ж. О., Могильницкий Г. М., Сапожникова Г. А. Микро-
биологическая коррозия стали ЮОХСНД в присутствии бактерий //
Тезисы докл. II Всесоюз. конф, по биоповреждениям. — Горький,
1981.-Ч. 1.-С.97.
[124] Стрижевский И. В. Некоторые аспекты борьбы с микробиологиче-
ской коррозией нефтепромыслового оборудования и трубопрово-
дов // Обзорн. инф: Сер. Коррозия и защита в нефтегазовой про-
мышленности — М.: ВНИИОЭНГ, 1979. — 56 с.
[125] Сульфатредуцирующие бактерии в биологической переработке про-
мышленных отходов, содержащих нитроцеллюлюзу / О. Е. Петрова.
М.Н. Давыдова, Н. Б. Тарасова и др. // Вестник Московского ун-та.
Сер. 2. Химия. - 2003. - Т. 44, № 1. - С. 43-45.
[126] Сульфатвосстанавливающие бактерии в нефтяных пластах Ро-
машкинского месторождения / Ф. Г. Студеникина, И. Н. Рязанцева,
Ф. К. Мухитова и др. // Изв. АН СССР, Сер. Биология. — 1983. —
№3.-С.454.
[127] Тахаутдииов Р. Ш. Метод расчета загрязнения нефтяного многослой-
ного пласта биозаражением и прогнозирование времени его подав-
ления // Нефтепромысловое дело. — 1999. — № 11. — С. 31-35.
[128] Усов В. Л., Вавер В. И., Смирнов В. И. Влияние продуктов электро-
лиза минерализованных подтоварных вод на рост СВБ // Матери-
алы Всесоюзного научно-технического семинара «Особенности за-
ражения нефтяных пластов микроорганизмами, совершенствование
систем подготовки вод для закачки их в продуктивные пласты и ме-
тоды борьбы с микробиологической коррозией». — М.: ВНИИОЭНГ,
1980.
[129] Фаткуллина Л. Г. Ягофарова Г. Г. Оценка влияния ПАВ на активность
клеток сульфатвосстанавливающих бактерий // Проблемы нефти
и газа Тюмени, 1979. — Вып. 42. — С. 44.
[130] Хазипов Р. X., Вахитова Р. Г. Влияние адсорбции на активность бак-
терицидов // Экспресс-инф: Сер. Коррозия и защита окружающей
среды. - М.: ВНИИОЭНГ. - 1985. - № 10. - С. 10-12.
[131] Хазипов Р.Х., Резяпова И,Б. Влияние ингибиторов коррозии и де-
эмульгаторов на процесс сульфатредукции // Нефтяное хозяйство. —
1985.-№12. -С.46—47.
[132] Хазипов Р. X., Резяпова И. Б., Силищев Н. Н. Особенности сульфатре-
дукции при применении химических продуктов в процессах добычи
нефти // Нефтяное хозяйство. — 1991. — № 6. — С. 36-38.
[133] Хазипов Р. X., Резяпова И. Б. Влияние неионогенных поверхност-
но-активных веществ на сульфатредукцию // Микробиология,
1985. - Т. 54, Вып. 4. - 563 с.
[134] Химия нефти и газа. Под. рсд. Проскурякова В. А. / Л.: Химия,
1981.- 358 с.
[135] Черкинский С. Н. Руководство по гигиене водоснабжения. — М.: Ме-‘
дицина, 1975.
[136] Экологические последствия биогенной сульфатредукции на неф-
тяных месторождениях республики Башкортостан / Р. X. Хазипов,
Р. Я. Нугаев, Н. Н. Силищев и др. // Нефтепромысловое дело. —
2005,- №4. - С. 47-48.
[137] Электрохимическая активация химических реагентов и буровых
растворов / У. Д.Мамаджанов, В.М.Бахир, Н. А. Мариампольский
и др. // Газовая промышленность. — М.: Недра. — 1981. — № 10.
[138] Battersby N.C., Stewart D.J., Sharma А. Р. Microbiological problems
in the offshore oil and.
[139] Bock Eberhard. Beductung der Mikroorganismus bei der corrosion von
Nowasserkanalen // Tiefban-Ingenieurban-Stassenban. — 1983. — Bd 25,
№ 17. — S. 437-439.
[140] Booth G.H. Microbiological corrosion. Mills and Boon Limited. —
London. — 1971.
[141] Brankevich G., Mele M., De Videla H. / Pev. iberoam. corros. у prot. —
1987, Vol. 17, №5,-P. 335.
[142] Costerton J. W., Lashen E. S. Influence of Biofilm on Efficacy of Biocides
on Corrosion-Causing Bacteria // National Association of Corrosion
Engineers. — 1984. — 23. — №2. — P. 13-17.
[143] I. Chanterean. La Corrosion bacterienne. Aout-Septembre. — 1978. —
P.417-418, 311-315.
[144] Fletcher M. and Marshall К. C. Are solid surfaces of ecological signifi-
cance to aquatic bacteria? // Adv. Microb. Ecol. — New-York, London,
1982,-Vol. 6,-P. 199-236.
[145] King R. A., Dittmem С. K., Miller J. D. A. Effect of Ferrous Ion Con-
sentration on the Corrosion of Iron in Semicontinuous Cultures of sul-
phate-reducing Bacteria. — Br. Corrosion J., 1976. — Vol. 11, №2. —
P. 105, consentration during growth. — Br. Corrosion J., 1973. — Vol. 8,
№2.
[146] King R. A., Miller J. D. A., Biol F.J. Corrosion of ferrous metals
by bacterially produced iron sulphides and its control by cathodis
protection. Anti -Corrosion Methods and Materials. — 1977. — Vol. 24,
№8.-P.9-11.
[147] Hamilton W. A. Sulphate-reducing bacteria and anaerobic corrosion //
Ann. Rev. Microbiol. — 1985. — Vol. 39. — P. 195-217.
[148] Microbiologically influenced corrosion of oilfield producing well
equipment: Corrosion 87, San Francisko, Calif., March — 9-13. —
P. 372 / E. S. Liftman. - Houston, Tex: NACE, 1987. -9 c.
[149] Postgate J. R. The sulphate-reducing bacteria. — Cambridge, Cambridge
University Press, 1979.
[150] Rorchach R., Garder F„ Ind. Eng. Chem. - Vol. 41, № 7. - P. 1380 (1949).
[151] Tatnall R., Stanton K., Ebersole R. Testing for the presence of sulfa-
te-reducing bacterria // Materials Performance. — 1988, VIII. — Vol. 27,
№8.-P. 71-80.
Каменщиков Феликс Анатольевич, Черных Нина Леонидовна
Борьба с сульфатвосстанавливающими
БАКТЕРИЯМИ НА НЕФТЯНЫХ МЕСТОРОЖДЕНИЯХ
Дизайнер М. В. Ботя
Технический редактор А. В. Широбоков
Компьютерная верстка Д. 77. Вакуленко
Корректор Г. Г. Тетерина
Подписано в печать 11.09.2007. Формат 60 х 84
Печать офсетная. Усл. печ.л. 23,95. Уч. изд. л. 19,95.
Гарнитура Таймс. Бумага офсетная №1. Заказ № 00170.
Научно-издательский центр «Регулярная и хаотическая динамика»
426034, г. Ижевск, ул. Университетская, 1.
http://shop.rcd.ru E-mail: mail@rcd.ru Тел./факс: (+73412) 500-295
Отпечатано в ГУП УР «Ижевский полиграфический комбинат»
426039, г. Ижевск, Воткинское шоссе, 180.