Текст
СПРАВОЧНИК ХИМИКА
ВТОРОЕ ИЗДАНИЕ
ПЕРЕРАБОТАННОЕ И ДОПОЛНЕННОЕ
ТОМ ЧЕТВЕРТЫЙ
АНАЛИТИЧЕСКАЯ ХИМ.МЯ
СПЕКТРАЛЬНЫЙ АНАЛИЗ ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ
ИЗДАТЕЛЬСТВО „ХИМИЯ" „ ЛЕНИНГРАДСКОЕ ОТДЕЛЕНИЕ 1967
УДК 54/083
Никол 64
Четвертый том справочника содержит сведения по аналитической химии (методы разделения; весовой, объемный и газовый анализ; потенциометрический, полярографический, колориметрический и другие методы анализа), по атомному эмиссионному и абсорбционному спектральному анализу, спектрам поглощения неорганических и органических соединений. Приводятся также дацныё о показателях преломления жидкостейоптической активности органических соединений.
Справочник предназначен для химиков всех специальностей — сотрудников научно-исследовательских институтов и лаборатории, инженерно-технических работников химической и других отраслей промышленности, преподавателей и учащихся вузов и техникумов.
РЕДАКЦИОННАЯ КОЛЛЕГИЯ
Чл.-корр. АН СССР Б. П. НИКОЛЬСКИЙ — главный редактор, О. Н. ГРИГОРОВ, М. Е. ПОЗИН, Б. А. ПОРАЙ-КОШИЦ, В. А. РАБИНОВИЧ (зам. главного редактора), Ф. Ю. РАЧИНСКИЙ, П. Г. РОМАНКОВ, Д. А. ФРИДРИХСБЕРГ
К ЧИТАТЕЛЮ
Издательство просит присылать Ваши замечания и отзывы об этой книге по адресам:
Москва, Новая площадь, 10, подъезд 11, Издательство «Химия», Ленинград, Невский пр., 28, Издательство «Химия» Ленинградское 'отделение
3-14-1
РЕДАКТОРЫ РАЗДЕЛОВ «СПРАВОЧНИКА ХИМИКА»
Докт. хим. наук О. Н. Григоров (физические свойства важнейших веществ, электродные процессы)
Докт. физ.-мат. наук А. Н. Зайдель (атомный спектральный анализ) Канд. хим. наук А. И. Заславский (структура кристаллических тел) Проф. Ю. В. Морачевский, канд. хим. наук Ф. Ю. Рачинский (аналитическая химия)
Докт. техн, наук М. Е. Позин (неорганическая технология)
Докт. хим. наук Б. А. Порай-Кошиц (органическая химия)
Канд. хим. наук В. А. Рабинович (общие сведения, гомогенное равновесие, свойства растворов)
Канд. хим. наук Ф. Ю. Рачинский (неорганическая химия)
Чл.-корр. АН СССР П. Г. Романков (процессы и аппараты, коррозионностойкие материалы)
Докт. хим. наук Д. А. Фридрихсберг (гетерогенное равновесие, химические справочники и периодические издания)
1*
ТОМ IV
СОДЕРЖАНИЕ
Аналитическая химия
Основные справочные руководства по неорганическому анализу . . • 15
Принятые сокращения...............................................16
Приготовление растворов..................................... . . 17
Методы разделения и качественного анализа ....... .............30
Аналитические группы ионов ................... - • -30
Аналитические реакции разделения ионов . . ................. .36
Групповые реактивы ... .... 36
pH осаждения гидроокисей......................................... 56
Последовательный ряд осаждения гидроокисей из кислого раствора 56
Последовательный ряд осаждения лантанидов ......................57
Последовательный ряд осаждения гидроокисей из щелочного раствора ................................................... 57
pH полного осаждения гидроокисей . ...... 57
Реактивы для осаждения гидроокисей . • . 58
Некоторые частные методы разделения ионов . .59
Экстракционные методы разделения ..................................... 72
Экстракция фторидов . . . 72
Экстракция хлоридов .73
Экстракция бромидов 75
Экстракция иодпдов . 76
Экстракция роданидов . ; .76
Экстракция оксихинолинатов 78
Экстракция купферонатов . 79
Экстракция днэтилдитиокарбаматов 80
Экстракция ацетилацетонатов ..................................... 82
Экстракция тиофепкарбонилтрифторацетоиатов • 83
Экстракция анионов в виде солей тетрафениларсония 84
Экстракция кислот метилдиоктиламином ............................ 85
Экстракция элементов растворами алифатических аминов 85
Экстракция элементов растворами солей тетраалкпламмоипя . . 87
Экстракция- элементов фосфорорганическими соединениями ... 93
Экстракция редкоземельных элементов ..................... • 98
Некоторые экстракционные системы, применяемые для разделения элементов...................................................... 101
4
Константы распределения некоторых комплексов металлов с органи-ческими аддендами .................................... . ПО
Константы распределения оксихинолинатов ........ .110
Константы распределения купферонатов ......................... 111
Константы распределения дитизонатов ... 112
Константы распределения ацетилацетонатов ... 113
Константы распределения тиофенкарбонилтрифторацетонатов . .114
Константы распределения бензоилацетонатов ... 116
Константы распределения дибензоилметанатов . 117
Коэффициенты распределения органических соединений в системах ор ганический растворитель—вода ..............118
Коэффициенты распределения органических соединений в системах изобутиловый спирт — вода и диэтиловый эфир — вода............118
Коэффициенты распределения некоторых карбоновых кислот .... 122
Коэффициенты распределения некоторых- фенолов в системе циклогексан — вода ............................................. ... 122
Хроматографические методы разделения . - • • - - 123
Хроматография неорганических веществ на бумаге ... • 123
Значения Ri некоторых ионов в системах с комплексообразова-телями . ................/............................... 123
Значения Rf катионов для различных растворителей, содержащих HCI 124
Значения R, некоторых катионов на бумаге, пропитанной 8-окси-хииолином .................................................124
Зависимость Rt некоторых катионов от природы аниона .... 125
Системы для хроматографического разделения смесей ионов .... 125
Окраска зон неорганических катионов при проявлении некоторыми реактивами ................................................ 132
Систематический хроматографический анализ смеси катионов • - 133
Проявление хроматограмм при систематическом анализе смеси катионов ................................................... 133
Хроматография органических веществ на бумаге ... 135
Значения Rf для различных групп органических соединении . . 135
Проявляющие реагенты......................................... 142
Газовая хроматография органических веществ .....................144
Коэффициенты селективности некоторых стационарных фаз для разделения гомологических рядов углеводородов ............144
Коэффициенты селективности некоторых стационарных фаз для разделения гомологических рядов кислородсодержащих органических соединений.................................................. 146
Максимальные рабочие температуры некоторых стационарных фаз - 147
Ионообменные методы разделения ... .............148
Свойства ионитов ..... ... 148
Иониты заводского и полузаводского изготовления отечественных марок......................................................... .148
Иониты лабораторного изготовления отечественных марок ... 152
Попиты иностранных марок ... ........................157
Зависимость свойств катионита КУ-2 от содержания дивииилбензола и сульфогрупп в сополимере ... . . 166
Зависимость свойств катионита КБ-4 от содержания дивииилбензола в сополимере ...... . ... ... 166
Свойства ионитовых мембран .... . . 167
Ионитовые мембраны отечественных марок 167
Ионитовые мембраны иностранных марок . . . .........168
Сравнительная характеристика ионитовых мембран некоторых отечественных и иностранных марок................................... 170
Коэффициенты распределения ионов в ионообменной хроматографии . 172
Коэффициенты распределения щелочных металлов ..................190
Коэффициенты распределения щелочноземельных элементов .... 190
5
Индивидуальные реакции ионов..........................................191
Микрохимический анализ ............................................ 235
Микрокристаллоскопия ............................................235
Абсорбциометрия ................................................ 268
Люминесцентные методы открытия элементов.............(................271
Реакции открытия ионов (элементов) по образованию люминесцнрую-щих осадков и растворов.......................................' • 271
Реакция открытия ионов (элементов) по гашению люминесценции реактива • ........................................277
Люминесценция некоторых индивидуальных химических соединений .... 278
Методы весдвого и объемного определения элементов . ................ 279
Весовой анализ.................................................. .... 279
Объемный анализ..................................................... 303
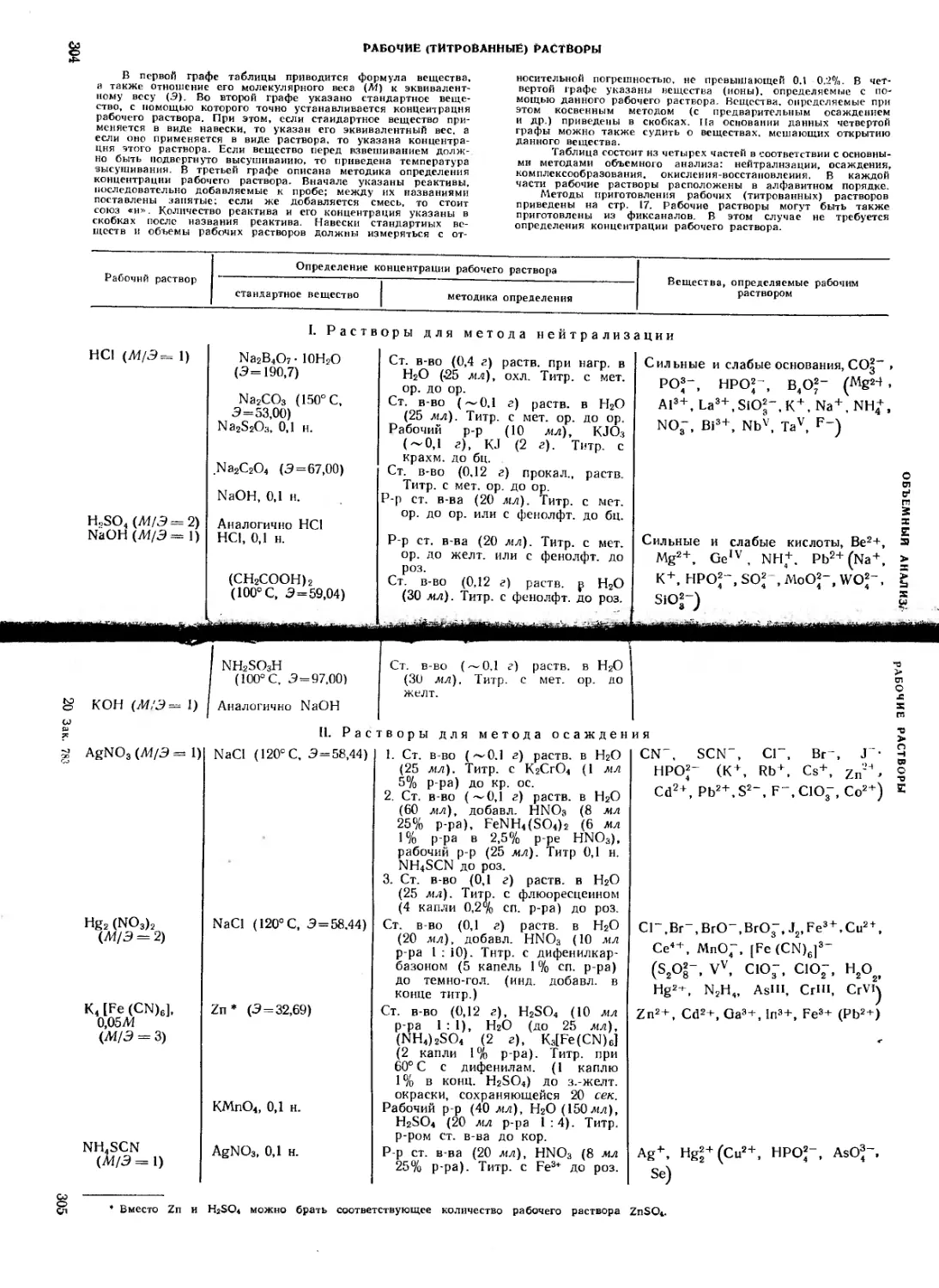
Рабочие (титрованные) растворы...................................304
Объемные методы определения неорганических веществ ....... 315
Кислотно-основные индикаторы.........................................352
I. Индивидуальные кислотно-основные индикаторы ................357
II. Смешанные индикаторы........................................367
III. Универсальные индикаторы •................................370
Окислительно-восстановительные индикаторы ............................372
I. Индикаторы, окраска которых мало зависит от pH и ионной силы раствора .... ............... .................... . 373
II. Индикаторы, чувствительные к изменению pH и ионной силы раствора..................................................... . 375
Адсорбционные индикаторы.......................................... . 380
Люминесцентные индикаторы....................................... .... 381
Индикаторные и реактивные бумаги........... 386
Универсальные индикаторные бумаги ............................. 386
Реактивные бумаги .............................................. 386
Индикаторные бумаги РИФАН .......................................387
Комплексометрические методы анализа ... . •................. 388
Комплексометрическое титрование неорганических ионов раствором Na-ЭДТА...........................................................388
Комплексометрическое титрование неорганических ионов различными комплексонами ....................... ... .... 397
Комплексометрические индикаторы .................................400
Объемный анализ с применением неводных растворителей............409
Важнейшие неводные растворители, применяемые в аналитической химии ........................................................... 415
Диэлектрическая проницаемость некоторых растворителей......418
Константы аутопротолиза некоторых растворителей .............. . 419
Протонное сродство анионов...................... • -............419
Важнейшие стандартные вещества, применяемые при кислотно-основном титровании в неводных растворах.............................. 420
Методы титрования соединений основного характера в неводных растворах ....................................................... 421
Методы титрования соединений кислотного характера в неводных растворах . ...... ......... . 425
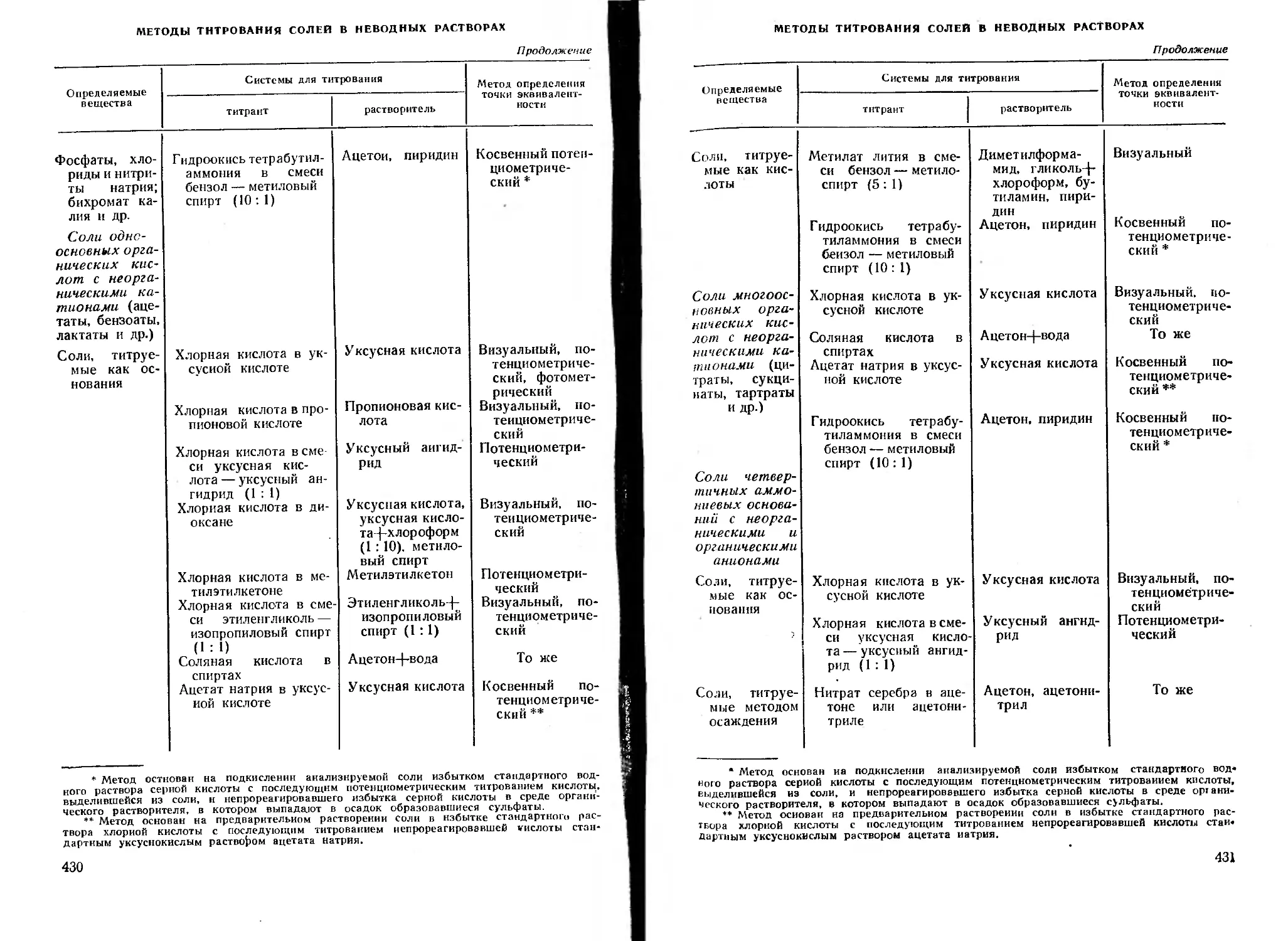
Методы титрования солей в неводных растворах . 429
Методы титрования смесей электролитов в неводных растворах . . • 433
6
Методы окислительно-восстановительного титрования в неводных рас-творах .... ..................................... • 437
Методы спектрофотометрического титрования в неводных растворах . 439
Важнейшие индикаторы, применяемые для кислотно-основного титро-
вания в неводных растворах ..................................... 441
Важнейшие индикаторы, применяемые для окислительно-восстановительного титрования в неводных растворах...........................442
Колориметрические и спектрофотометрические методы определения .... 443
Колориметрическое и спектрофотометрическое определение элементов в видимой (и ближней инфракрасной) области спектра ...... 443
Определение элементов методом ультрафиолетовой спектрофотометрии 454
Флуорометрическое определение элементов (ионов) ................ 461
Электрохимические методы анализа..................................... 465
Кондуктометрическое титрование ................................... 465
Высокочастотное титрование в водной среде . .................... 469
Амперометрическое (полярометрическое) титрование ......... 473
Потенциометрическое титрование .......................481
Рабочие (титрованные) растворы • ... ... 481
Методы определения неорганических ионов ..................... . 486
Полярографические методы определения.............................494
Потенциалы полярографических полуволн неорганических веществ . 499
Потенциалы полярографических полуволн органических веществ . 515
Магнитные и ядерные методы анализа
........... ..................... . 521
Масс-спектрометрия.........................................521
Относительные атомные массы изотопов...................522
Относительные атомные массы изотопов по углеродной шкале . . 522
Относительные атомные массы изотопов по кислородной (физической) шкале ............................................... 522
Сводная таблица спектров масс органических и некоторых неорганических соединений ..................................... . 526
Радиоактивационный анализ ................................ . 542
Газовый анализ ... ..... ........................ 572
Единицы измерения концентраций газов и паров и их взаимный пересчет 572
Таблица для пересчета концентраций газов и паров ..... 572
Номограмма для пересчета концентраций газов и паров • . • 574
Некоторые физические свойства газов и паров ....................... 576
Коэффициенты теплопроводности некоторых газов и паров при различных температурах ... ............. .................576
Магнитная восприимчивость газов и паров.........................580
Скорость звука в газах и парах ................................ 581
Расчет результатов газовых и газометрических анализов...............582
Значения коэффициента F при различных температурах и давлениях . 583
Номограмма для приведения объема газа к 0° С и 760 мм рт. ст. . 588
7
Соотношения между значениями давления, выраженными в различных единицах ..................................................... 589
Значения коэффициента / при 0° С и 760 мм рт. ст. . . • 589
Расчет результатов газометрического определения углерода .... 589
Избирательная осушка и очистка газовых смесей А. .... . . 590
Затворные жидкости, применяемые в газовом анализе . ...............594
Затворные жидкости ...........................................594
Давление паров воды над насыщенными растворами хлорида и сульфата натрия .................................... ... ... 594
Давление паров некоторых смазочных масел ... . . - . 595
Растворимость газов в концентрированных растворах хлорида натрия 595
Растворимость газов в водном растворе сульфата натрия при 25° С . • 595
Растворимость двуокиси углерода в некоторых затворных жидкостях при 25° С . . ........................................ • 596
Поглотительные растворы......................... . - • • 596
Поглотители для абсорбционного анализа газов ................. 596
Абсорбционная способность некоторых поглотительных растворов по отношению к газам . ............................ • 597
Методы анализа газов и паров ..... ... ... 598
Лабораторные методы анализа................................... 598
Автоматический анализ газов................................... 601
Типичные случаи применения промышленных автоматических газоанализаторов ......................................................613
Приготовление контрольных газовых смесей для градуировки и поверки газоаналитическпх приборов .................................... .... 614
Состав исходных газов, применяемых для приготовления контрольных смесей .........................................................614
Очистка и осушка исходных газов при повышенном давлении . • 615
Очистка и осушка исходных газов при атмосферном давлении . • - 616
Приготовление газовых смесей ................................ ... 617
Идентификация органических соединений по температурам плавления их производных ......................... . . 622
Спектральный анализ
Атомный эмиссионный и абсорбционный спектральный анализ ..............637
Аналитические линии элементов, используемые при эмиссионном спектральном анализе '...........................................637
Совпадения спектральных линий элементов ....................... 648
Абсолютная чувствительность эмиссионного спектрального анализа . 720
Температуры некоторых пламен, используемых в качестве источников возбуждения ....................................720
Наиболее интенсивные аналитические линии, возбуждаемые в воздушио-ацетиленовом пламени ...........................................720
Аналитические линии атомов и канты молекулярных полос, возбуждаемые в пламени . . .............. . . 721
Длины волн спектральных линий и кантов молекулярных полос, возбуждаемых в пламени (в порядке возрастания) . ...................730
Чувствительность обнаружения элементов методом атомно-абсорб-цнонного анализа в пламени ..................................... 733
Абсолютная чувствительность метода атомно-абсорбционного анализа в пламени при применении графитовой кюветы.......................733
8
Спектры поглощения . .................................. ..... 734
Таблица для пересчета lev. . . 734
Таблица для пересчета 7 в D ............................... 736
Спектры поглощения неорганических ионов и комплексных соединений в ультрафиолетовой и видимой области ......................... 738
Спектры поглощения органических соединений в ультрафиолетовой области • • ..... .............. . . 781
Показатели преломления и оптическая активность
Показатели преломления жидкостей...............................821
Оптическая активность органических соединений ................ 895
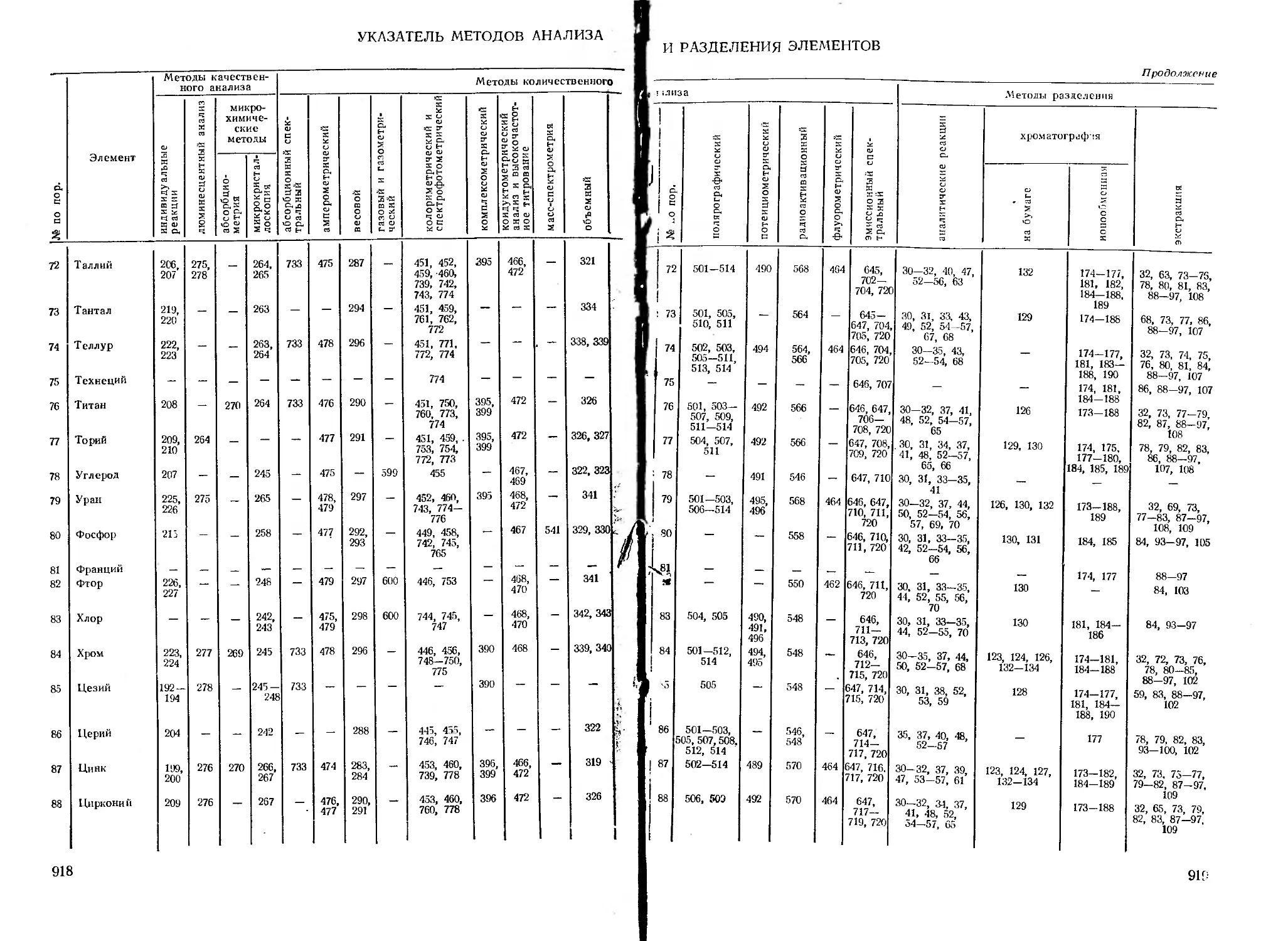
Указатель методов анализа й разделения элементов ................... 910
КРАТКОЕ СОДЕРЖАНИЕ ОСТАЛЬНЫХ ТОМОВ «СПРАВОЧНИКА ХИМИКА»
ТОМ I
Общие сведения
Атомные веса и распространенность элементов
Универсальные физические константы
Единицы измерения физических величин
Соотношения между единицами измерения величин
Измерение температуры и давления
Математические таблицы и формулы
Важнейшие химические справочники и периодические издания
Строение вещества и структура кристаллов
Строение вещества
Структура кристаллических тел
Физические свойства важнейших веществ
Плотность и сжимаемость жидкостей и газов
Термическое расширение твердых тел, жидкостей и газов
Равновесные температуры и давления (гетерогенные равновесия)
Критические величины и константы Ван-дер-Ваальса
Энергетические свойства важнейших веществ
Теплопроводность
Электропроводность и числа переноса
Диэлектрическая проницаемость
Дипольные моменты
Вязкость
Поверхностное натяжение
Показатели преломления химических соединений
Краткие сведения по лабораторной технике
Предметный указатель
ТОМ II
Свойства неорганических соединений
Основы классификации и номенклатуры органических соединений
Свойства органических соединений
ТОМ III
Гомогенное химическое равновесие
Химическое равновесие в газовой-фазе
Химическое равновесие в жидкой фазе
10
Гетерогенное химическое равновесие (растворимость, температуры замерзания и кипения растворов, давление пара и состав равновесных фаз, давление диссоциации)
Равновесие жидкость — твердое
Равновесие газ — жидкость
Равновесие твердое — газ
Равновесие жидкость — жидкость
Криоскопические и эбуллиоскопические константы
Свойства гомогенных жидких растворов
Плотность растворов
Коэффициенты активности
Энергетические свойства растворов
Теплопроводность растворов
Электропроводность растворов и числа переноса
Вязкость растворов
Поверхностное натяжение растворов
Показатели преломления растворов
Электродные процессы
Электродные процессы в растворах
Электродные процессы в расплавах
Химическая кинетика и диффузия
Кинетика химических реакций
Диффузия
Реакционная способность органических соединений
Предметный указатель
ТОМ V
Процессы и аппараты химической технологии
Характеристика сырья и продуктов производства неорганической технологии
ТОМ V/
Характеристика сырья и продуктов производства органической технологии Техника безопасности и промышленная санитария
В СОСТАВЛЕНИИ ЧЕТВЕРТОГО ТОМА ПРИНИМАЛИ УЧАСТИЕ:
Канд. хим. наук Н. Ш. А л д а р о в а
Канд. хим. наук Л. Н. Быкова
Ассист. В. И. Васильев
Канд. хим. наук Е. Г. Власова
Канд. хим. наук И. В. Вольф
Научный сотрудник Л. Н. Воробьев
Канд. хим. наук В. А. Дроздов
Ассист. И. Я. Зельманова
Канд, физ.-мат. наук Е. И. Зильберштейи
Научный сотрудник Д. В. Иоффе
Канд. хим. наук Н. А. Казарян
Ассист. О. Ф. Кириллова
Докт. хим. наук А. П. К р е ш к о в
Канд, физ.-мат. наук Л. М. К р и ж а н с к и й
Канд. хим. наук Л. Н. Лазарев
Канд, физ.-мат. наук А. А. Липовский
Канд. хим. наук А. П. М у с а к и н
Инж. М. К. Никитин
Инж. Д. Л. Оршанский
Ассист. И. Д. Певзнер
Научный сотрудник И. А. Полетаева
Инж. М. Б. Рабинов и ч
Докт. хим. наук Я. М. Слободин.
Канд. хим. наук Н. Т. Смолова
Научный сотрудник С. П. С п и в а к
Канд. хим. наук К. П. Столяров
Ассист. Р. Р. Тарасянц
Научный сотрудник В. В. Уточкин
Научный сотрудник Г. А. Шейн н и а
Инж. Н. Ф. Я б л о и с к а я •
Канд. хим. науд А. Н. Я р.о в е п к о
АНАЛИТИЧЕСКАЯ ХИМИЯ
ОСНОВНЫЕ СПРАВОЧНЫЕ РУКОВОДСТВА ПО НЕОРГАНИЧЕСКОМУ АНАЛИЗУ
1. Аналитическая химия элементов. Серия монографий, Изд. АН СССР, I960—.*
2. В. Ф. Г и л л е б р а и д т, Г. Э. Л е и д е л ь, Г. А. Б р а й т, Д. И. Г о ф м а н, Практическое руководство по неорганическому анализу, перев. с англ., 2-е изд., Госхимиздат, 1960.
3. Г. Ш а р л о, Методы аналитической химии. Количественный анализ неорганических соединений, перев. с франц., Изд. «Химия», 1965.
4. Анализ минерального сырья, ред. Ю. Н. Книпович, Ю. В. о р а ч е в-ский, 3-е изд., Госхимиздат, 1959.
5. В. Р. Шеллер, А. Р. П о у э л л, Анализ минералов и руд редких элементов, перев. с англ., Госгеолтехиздат, 1962.
6. Методы определения и анализа редких элементов, ред. А. П. Рябчиков, Изд. АН СССР, 1961.
7. Chemical Analysis. A Series of Monographs on Analytical Chemistry and its Applications, B. L. Clarke, J. M. Koi th of (Ed.), Нью-Йорк, 1944—.
8. Handbuch der analytischen Chemie, W. Fresenius, G. Jander (Ed.), Берлин, 1940—.
9. International Series Monographs on Analytical Chemistry, R. Belcher, L. Gordon (Ed.), Оксфорд, 1960—.
10. Physical Methods in Chemical Analysis, W. Berl (Ed.), Лондон—Нью-Йорк, 1950—.
11. Handbook of Analytical Chemistry, L. Meites (Ed.), Нью-Йорк—Торонто— Лондон, 1963.
12. Standard Methods of Chemical Analysis, Нью-Йорк—Торонто—Лондон, т. I, 1962; т. II, 1963.
13. Comprehensive Analytical Chemistry, C. Z, Wilson, D. W. Wilson (Ed.), Амстердам—Лондон—Нью-Йорк, 1959—.
Таким образом здесь и ниже обозначается год начала издания.
ПРИНЯТЫЕ СОКРАЩЕНИЯ
амил. сп. — амиловый спнр-анал. — анализируемый атм. — атмосфера
бел. — белый
бл. — бледный бур. — бурый бутил, сп. — бутиловый спирт буф. — буферный раствор бц. — бесцветный
в-во — вещество
взбалт. — взбалтывают водн. — водный
возг. — возгонка, возгоняют
восст. — восстановленный, восстанавливают
выпар. — выпаривают р-р досуха (см. упар.)
высуш. — высушивают
гор. — горячий
добавл. —добавляют
желт. — желтый
з. — зеленый
зол. — золотистый
изб. — избыток
кип. — кипятят, кипящий
кисл. — кислая
конц. — концентрация, концентрированный
кор. — коричневый кр. — красный
крист. — кристаллический к-та — кислота
лед. — ледяная
маек. — маскируют
мет. сп. — метиловый спирт меш. — мешают
иагр. — нагревают
нас. — насыщенным, насыщают
нейтр. — нейтральный, нейтрализуют образ. — образуются
окисл. — окисляют
опр. — определение, определяют ор. — оранжевый
ос. — осадок
осажд. — осаждают, осаждение
охл. — охлаждают
перемеш. — перемешивают переос. — переосаждают прокал. — прокаленный промыв. — промывают
пурп. — пурпурный
разб. — разбавленный, разбавляют раств. — растворяют
р-в — реактив
Р. 3. — редкоземельные элементы роз. — розовый р-р — раствор
св---светло-
син. — синий СП. — этиловый спирт
, тв. — твердый
титр. — титрование, титруют тм.— темно-
упар. — упаривают р-р до небольшого объема
фенолфт. — фенолфталеин
фильтр. — фильтруют фиол. — фиолетовый ф-т — фильтрат
хол. — холодный
черн.— черный
шел. — щелочной
экстр. — экстракция, экстрагируют эмпир — эмпирический эф. — днэтиловый эфир
Na-ЭДТА — этилендиаминтетраацетат натрия, трилон Б, комплексон 1П
16
Приготовление растворов
В таблицах приведены сведения, необходимые для приготовления в лабораторных уело* растворов, наиболее часто используемых при анализе неорганических веществ; в по-рПсд11ей таблице описаны способы приготовления металлов, применяемых в редукторах. Hei спорые специальные реактивы размещены в таблице по фамилии автора (например: Фишера реактив). В конце раздела приведены формулы, по которым можно проводить пасчсты при приготовлении растворов.
1 Погрешность, допустимая при взятии навесок и при измерении объемов, должна соот-етствовать той точности, с которой задается концентрация раствора. Так. при приготовлении растворов, концентрации которых указаны с точностью до одной или двух значащих цифр допустима относительная погрешность, равная 5%. Для рабочих (титрованных) растворов (их концентрация указана в таблицах с точностью до трех или четырех значащих цифр) относительная погрешность не должна превышать 0.1%.
Реактивы, применяемые для приготовления растворов, в большинстве случаев следует брать марки ч.д.а.. вода должна быть перегнанной или деминерализованной.
Приготовление растворов по фиксаналам не включено в таблицы. Фиксаналы. выпускаемые отечественной промышленностью, приведены в разделе «Объемный анализ» (стр. 304). Приготовление буферных растворов см. «Справочник химика». 2-е изд., т. Ш. стр. 168.
Более подробные сведения о приготовлении растворов и реактивов и об нх очистке содержатся в книгах: 1. П, П. Коростылев. Приготовление растворов для химико-аналитических работ, 2-е изд.. Изд. АН СССР. 1964.-2. В. М. С У с л е и и и к о в а. Е. К. Киселева. Руководство по приготовлению титрованных растворов. 3-е изд.. Изд. «Химия», 1965—3. ю. В. Карякин, И И. Ангелов. Чистые химические реактивы. Госхимнздат, (953.—4* Руководство по препаративной неорганической химии, ред. Г. Б р а у е р, перев. с нём., ИЛ. 1956.—5. Химические реактивы и препараты, справочник под ред. В. И. К у з-п е ц о в а, Госхимнздат. 1953.—6. Сборник технических условий на реактивы н препараты для лабораторных работ. Госхимнздат, 1961; Изд. «Химия», 1965.
В таблице приняты следующие сокращения: абс. — абсолютный: встрях. — встряхивают; выдерж. — выдерживают; сплавл. — сплавляют.
Остальные сокращения см. стр. 16.
Растворы неорганических кислот
Кислота Концентрация Плотность, г/с.и3 Способ приготовления
г-экв[л вес. ?я
^Азотная
КОНЦ. 15,7 69,8 1,42
разб. 6 31,6 1,195 385 лм HNO.i (конц.) разб. до 1 л
9 11,8 1.067 128 мл HNO3 (копи.) разб. до 1 л
0,1 0.36 1,00 6,5 лгл перегнанной HNO3 (конц.) разб. до 1 л
Серная
КОНЦ. 35.9 95,6 1,84
разб. 4 17,5 1,123 112 мл H2SO4 (кони.) вливают в 0,5 л воды, о.хл., разб. до 1 л
Сернистая, конц. 0,1 0,49 1,00 а) 2,8 мл H2SO4 (конц.) вливают в 0,5 л воды, охл.. разб. до 1 л б) 25 мл H2SO( (4 и ) разб. до 1 л
3,0 • 10 1,05 Через воду пропускают SO2 до нас.
Соляная,
КОНЦ. 12,14 37,23 1,19
разб. 6 20,0 1,100 494 мл HCI (конц.) разб. до 1 л
2 7.05 1.034 164 ли НО (конц.) разб. до 1 л
0.1 0,36 1.00 8,23 .«л -HCI . (конц.) разб. до 1 л
2 Зак. 783
17
Приготовление растворов
П родолжение
Кислота Концентрация Плотность, г {см3 -Способ приготовления
2-ЭКВ/Л вес. %
Соляная, разб. Фосфорная (орто). 0.1000 0,36 1,00 а г азеотрог лученной при рт. ст., разб. j р 680 720 760 780 шой смеси, подавлении Р мм, ю 1 л а 17,85 17,94 18,02 18,06
КОНЦ. 44,4 (14.8 М) 85 1,70
разб. 3 9,5 .... 67,5 мл НзРО4 (конц.) разб. до I л
Фтористоводородная Хлорная 27,4 48,0 1,15
КОНЦ. 3,6—11,7 30—70 1,21—1,67
уксуснокислый р-р 0,1 0,95 1,05 Измеренный объем конц. хлорной кислоты, содержащий 10 г НСЮ4, раств. при непрерывном перемеш. в 800 мл безводной СНзСООН, добавл. уксусный ангидрид в количестве, соответствующем содержанию Н2О во взятых к-тах. Тщательно перемеш., разб. лед. СНзСООН до 1 л и оставляют на 1 сутки.
Растворы неорганических оснований
Основание Концентрация Плотность, Способ приготовления
г-эке (л вес. %
Аммиак КОНЦ. 13,4 25,0 0,91
конц., без СО2 13,4 25,0 0,91 а) Нас. свежепрокипячен-
разб. 6 10,7 0,957 ную воду аммиаком из баллона; б) К 500 мл NH4OH (конц.) добавл. 10 г свежегашенной извести, нагр. и отгоняют NH3 в 500 мл воды 450 мл NH4OH (конц.)
2 3,5 0,985 разб. до 1 л 150 мл NH4OH (конц.)
Барий, гидроокись — 0,35 — 5,5 — 1,0 разб. до 1 л 70 г Ва(ОН)г-8Н2О встрях.
(баритовая вода) (нас. р-р) с 1 л Н2О, отстаивают и сливают прозрачный р-р
18
Приготовление растворов
Продолжение
Концентра цияЗ Плотность, Способ приготовления
Основание г-экв/л вес. % г/см3
_ Калий гидроокись 6 26,9 1.26 340 г КОН раств. в Н2О и разб. до 1 л
2 10,3 1,09 112 г КОН раств. в Н2О и разб. до 1 л
0,1 0,56 1,00 5,6 г КОН раств. в Н2О и разб. до 1 л
гидроокись, 0,1 0,56 1,00 К 100 мл 1,0 и. р-ра КОН
без СО2 добавл. 8 мл р-ра Са(ОН)2. После отстаивания декантируют и разб. до 1 л
Кальций, гидро- 0,04 1,7 — 1,0 17 г Са(ОН)2 встрях. с 1 л
окись (известковое молоко) (нас. р-р) Н2О
Натрий гидроокись 6 19,7 1,22 240 г NaOH раств. в Н2О, охл. и разб. до 1 л
2 7,4 1,08 80 г NaOH раств. в Н2О, охл. и разб. до 1 л
гидроокись, 0,1 0,4 1.00 а) Смешивают (в термо-
без СО2 стойком сосуде) NaOH и Н2О (1:1 вес. ч.). После от-
стаивания декантируют и разб. р-р до 0,1 н. (~ в 190 раз)
б) 5 г NaOH раств. в 300 мл Н2О, добавл. 20 мл 0,5 и. р ра Ва(ОН)2. После
отстаивания декантируют и разб. до 1 л в) К 50 лл 2 и. р-ра NaOH добавл. 8 мл известкового молока. После отстаивания декантируют и разб. до I л
Растворы солей
и других неорганических реактивов
Вещество Концентрация Способ приготовления
Аммоний азотнокислый ванадиевокислый многосернистый молибденовокислый 1 н. 0,1 н. (0,1 Af) — 6% 80 г NH4NO3 раств. в Н2О. разб. до 1 л К 11,7 г NH4VO.3 добавл. 200 мл Н2О, 150 мл H2SO4 (конц.). Охл., разб. до 1 л Настаивают в течение суток 1 л конц. р-ра (NH4)2§ с 12 г измельченной серы, затем декантируют 150 г (NH4)6Mo7O24-4H2O раств. в 1 л гор. Н2О, добавл. NH4OH до просветления; охл., вливают в 1 л HNO3 (33%); через несколько дней декантируют и хранят в бутыли, закрытой стаканом
2*
19
Приготовление растворов
Продолжение
Вещество Концентрация Способ приготовления
Аммоний
роданистый 0.1000 и. 7,612 г NH4SCN раств. в Н2О; разб. до 1 л
сернистый КОНЦ. 200 лтл NH4OH (кони.), H2S (до нас.), 200 мл NH4OH (конц.) разб. до 1 л
сернокислый ~8 н. 5и г (NH4)2S(-)4 раств. в 100 мл гор. Н2О, охл., фильтр.
тетра рода но мерку- . . . . . К 32 г NH4SCN добавл. 200 мл Н2О,
риат 27 г HgCl2; разб. до 1 л. Через 2 суток фильтр.
углекислый 2 н. 115 г (NH4)2CO3• Н2О раств. в Н2О] разб. до 1 л
уксуснокислый 1 и. К 1 объему СНзСООН (2 и.) добавл. 1 объем NH4OH (2 н.)
фосфорнокислый, двузамещенный 10% 10 г (NH4)2HPO4 раств. в 90 мл Н2О
хлористый Барий 6 и. 320 г NH4CI раств. в Н2О; разб. до 1 л
уксуснокислый 2,5 н. 386 г (СН3СОО)2Ва • ЗН2О раств. в Н2О; разб. до 1 л
хлористый 10 % 117 г ВаС12-2Н2О расгв. в Н2О; разб. до 1 л. Через 1 сутки фильтр.
Бром (водный рас- 0,1 н. 3 мл брома и 3 г NaBr раств. в Н2О;
твор—«бромная вода») разб. до 1 л
раствор в уксусной кислоте 0,1 и. 8 г брома раств. в 1 л СНзСООН (конц.)
Ванадий. сернокислый 0,1 н. 12 г NH4VO3 раств. в 1 л 1 н. H2SC>4,
(II) 0,1 н. добавл. Zn-амалыаму (или 8 г Zn), встрях. в атм. СО2 (или N2) до фиол. окраски р-ра. Фильтр, в бутыль, соединенную с бюреткой и заполненную СО2
Ванадил, сернокислый 12 г NH4VO3 раств. в 1 л H2SC>4 (2 н.),
(IV) нагр. до 70° С и пропускают SO2 (2—3 ч). Изб. SO2 удаляют током СО2. Охл., разб. до 1 л
Вольфрамат (V) соля- 0,1 н. 29,4 г Na2WO4 раств. в 1 л НС1 (10 в.).
ио к целый Восст. электролитически (Pt-электроды, разделенные диафрагмой, 0,02 а! см2). Применяют и хранят в атм. СО2 (устойчив до 14 дней)
Гидразин сернокислый Железо 0.1000 н. 13,01 г N2H4 • H2SO4 раств. в Н2О; разб. до 1 л
аммоний сернокпс- ~ 10% В р-р 50—70 мл H2S©4 (конц.) в 500 мл
лое (II). (Мора Н2О вносят 100 г Fe(NH4)2(SO4)2 • 6Н2О;
соль) после раств. разб. до 1 л
~3,5% В р-р 50 мл H2SO4 (конц.) в 200 мл Н2О вносят 40 г Fe(NH4)2(SC>4)2• 6Н2О; после раств. разб. до 1 л
сернокисл2е (Ill) 0,1 /И 48 г FeNH4(SO4)2-12Н2О раств. в 200 .чл р-ра, содержащего 10 мл конц. H2SO4; фильтр., разб. до 1 л
20
Приготовление растворов
Продолжение
Вещество (онцентрация Способ приготовления
Железо, сернокислое (II) 0,5 н. 139 г FeSO, 6Н2О раств. в 50 мл 5 н. H2SO4; разб. до 1 л
Под 0,04 н. 5,1 г иода раств. в конц. р-ре KJ (~ 15 г) и разб. до 1 л
0,1 н. 12,7 г иода (возогнанпого) раств. в 300 мл KJ (10% р-р); разб. до 1 л
Иод, хлористый (JC1) 0,1000 М Раств. 11,07 г KJ в 50 мл Н2О, добавл. р-р 7,134 г KJO3 в 250 мл Н2О, 200 мл НС1 (конц.); разб. до 1 л. Пробу
взбалт. с СНСЬ; в случае окрашивания последнего в фиол. цвет добавл. к приготовленному р-ру 0,1 М KJO3 до прекра-
щения окрашивания; если окрашивания нет, добавл. KJ до появления фиол. окрашивания СНС]3
Калин бромноватокислый 0,1000 п. 2,784 г КВгОз раств. в Н2О н разб. до 1 л
бромноватокислый- 0,1000 н. 2,784 г КВгОз и 10 г КВг раств. в Н2О
бромистый (0,017 М) и разб. до 1 л
гексацианоферриат 0,05 и. 16,5 г Кз[Ре(СМ)6] раств. в Н2О и разб.
(0,033 М) до 1 л
гексацианоферраат 0,1000 и. 14,08 г К.4|Ре(СЛ1)б] • ЗН2О раств. в Н2О,.
(0,017 Л4) добавл. 0,2 г Na2CO3 и разб. до 1 л
двухромовокислый 0,1000 и. 4,904 г КгСггО? (высушенного при 110° С,
(0,017 А1) а затем при 200° С) раств. в Н2О и разб.
до 1 л
ио диеты и 0,2 и. 33 г KJ раств. в Н2О н разб. до 1 л
и о ди о в а ток и сл ы й 0,1000 и. 5,350 г KJO3 раств. в Н2О и разб.
марганцовокислый (0,025 М) до 1 л
0,1 и. 3,16 г КМпО4 раств. в 1 л прокипячен-
(0,02 М) ной воды, кип. 1 мин, через 2 ч фильтр, через стеклянный фильтр
роданистый 0,1 и. 9,7 г NH4SCN раств. в Н2О и разб.
до I л
0,5 и. 49 г NH4SCN раств. в Н2О н разб.
до I л
хромовокислый 1 и. 97 г К2С1О4 раств. в Н2О и разб.
(0,5 М) до 1 л
цианистый 1 и. 65 г KCN раств. в Н2О н разб. до 1 л
Кальцин
хлористый 0,1000 и. 0,1 н. 5,005 г СаСОз (высуш. при 105° С) раств. в кони. НС1 (20 лл), разб. до 1 л
хлорноватистокис- а) 4,5 г Са(ОС1)2-2Н2О взбалт. с
лый (0,025 Ж) 250 мл Н2О, фильтр, и разб. до 1 л б) ~ 14 г хлорной извести (25% активного хлора) растирают в чашке с Н2О, переливают в цилиндр, оставляют до отстаивания, после чего декантируют через стеклянный фильтр в мерную колбу и разб. до 1 л
21
Приготовление растворов
Продолжение
Вещество Концентрация Способ приготовления
Кобальт, сернокислый (Ш) 0.01 м 7,3 г Co2(SO4)3- 18Н2О * раств. в H2SO4 (18 н.) и разб. ею до I л. При —7° С р-р устойчив до 2 месяцев
Магнезиальная смесь ~0,7 Л4 (по Mg2+) ~0,25 М (по Mg2+) а) К 240 г NH4NO3 добавл. 130 г Mg(NO3)2 • 2Н2О, 150 мл NH4OH (конц.), разб. до 1 л б) К 100 г MgCl2 • 6Н2О добавл. 125 г NH4CI, 150 мл Н2О, 500 мл NH4OH (конц.) К 55 г MgCl2 • 6Н2О добавл. 105 г NH4CI, 200 мл Н2О, 350 мл NH4OH (конц.), разб. до 1 л Через 3—4 дня фильтр.
Марганец (III), фосфатный комплекс КН2[Мп(РО4)2] 0.05 н. а) Р-р MnSO4 (5 мл 0,5 М), Н3РО4 (15 мл 80%), К2СО3 (1—2 г). Harp, добавл. КВгОз (0,1 г), удаляют кипячением Вг2, добавл. Н2О до 50 мл. Устойчив 10 дней б) КМпО4, Н,О2
Медь (III), перйодатный комплекс (калиевая соль) Кт[Си(ЛОб)г] 0.1 М 12,49 г CuSO4-5H2O и 23,00 г KJO4 раств. в 400 мл кип. Н2О. К суспензии медленно добавл. при кип. нас. р-р КОН (56 г) и затем небольшими порциями 20 г K2S2O8. Прозрачный р-р кип. 30 мин, охл., отделяют K2SO4 и разб до 500 мл
Медь, хлористая (I) 0,1 н. 24,97 г CuSO4-5H2O (или 17,05 г СцС12 • 2Н2О) раств. в 1 л 2 н. НС1. Восст. на серебряном редукторе (стр. 28) со скоростью 7 мл/мин. Р-р используют сразу для титр., поэтому редуктор удобно соединить с бюреткой.
Молибден (V) солянокислый 0.1 н. 178 г (NH4)6Mo7O24-4H2O раств. в 1 л НС1 (8 и.). Восст. электролизом (Pt-электроды, 0,008 а/см2) и разб. в 4 раза. Хранят в атм. СОг
Мора соль ~ Ю% См. Железо-аммоний сернокислое (II)
Мышьяковистая кислота Натрий 0,1000 н. 4,945 г чистого высуш. As2O3 раств. в 60 мл NaOH (1 н.), добавл 50—60 мл НС1 или H2SO4 (1 н.); разб. до 1 л. Р-р должен быть нейтр. по лакмусу; в этом случае р-р устойчив много месяцев
азотистокислый 0,1 м 6,9 г NaNO2 раств. в' 1 л Н2О
бромноватисто- 0.1 н. 24 г NaOH раств. в 1 л Н2О, охл. до
КИСЛЫЙ (0.05 М) —4° С, осторожно добавл. 8 г брома и выдерж. при охл. 2 ч (титр. опр. через 12 ч)
* Cog (SO4)3-18H2O получают анодным окислением CoSO4-7H2O в 8 н. H2SO4 при 0° С (см. «Руководство по препаративной неорганической химии», под ред. Г. Брауера, ИЛ, 1956).
22
Приготовление растворов
Продолжение
Вещество Концентрация Способ приготовления
Натрий гексанитрокооаль- 0,6 м К р-ру 30 г Co(NO3)2• 6Н2О (или 25 г
тиат СоС12 • 6Н2О) в 60 мл Н2О добавл. р-р 50 г NaNO2 в 100 мл Н2О, 10 мл лед. СНзСООН. Через сутки продувают воздух 5 мин и фильтр. Хранят в темноте (годен I—2 недели)
иоднокислый 0,05 М 10,70 г NaJO< раств. в Н2О и разб. до 1 л
мышьяковистокис- 0,0500 и. К кип. р-ру 5 г Na2CO3 (безводн.)
лый в 100 мл Н2О добавл. при перемешивании 2,5 г As2O3, охл., разб. до 300 мл, фильтр, и разб. до 1 л
0,1000 и. См. Мышьяковистая кислота
мышьяковисто- 0,05 н. 1,3 г As2O3 раств. при нагр. в 2,5 мл
азотистокислый NaOH (4 н.), добавл. 200 мл Н2О, H2SO4 (40%) до красного цвета лакмуса и еще 1 мл H2SO4, NaHCOa до нейтр. реакции, 0,85 г NaNO2 в 5 мл Н2О и разб. до 1 л
тиосернокислый 0,1 и. 25 г Na2S2O3-5H2O раств. в 1 л свеже-прокипяченной и охл. Н2О, добавл. 0,1 г Na2CO3. Оставляют на 1—2 дня. Хранят в темной бутыли. Концентрация не меняется 2—3 месяца
Несслера реактив 0,08 М К 50 г KJ в 50 мл Н2О добавл. нас. р-р HgCls до появления ос., 200 мл NaOH (6 н.); разб. до 500 мл. Хранят в темноте
0,1 М К 45,5 г HgJ2 добавл. 34,9 г KJ (в небольшом количестве Н2О), 146 мл КОН (50%), разб. до 1 л. Хранят в темноте
Олово, хлористое (II) 0,08 М К 13 г KJ в 25 мл Н2О добавл. HgCl2 (нас. р-р) до помутнения, р-р 55 г КОН в 150 мл Н2О, Н2О до 250 мл, нас. р-р HgCI2 до появления едва заметного не исчезающего осадка. Хранят в темноте
10% а) 57 г олова раств. в 300 мл НС1 (конц.), фильтр, через, стеклянную вату, разб. до 1 л, добавл. немного Sn
0,1 М б) К 100 г SnCl2-2H2O добавл. 100 мл НС1 (конц ), разб. до 1 л
12 г SnCl2 • 2Н2О вносят в 80 мл НС!
Перекись водорода (конц.), предварительно обработанной 4—6 г СаСОз (для вытеснения воздуха, выделяющейся СОг); разб. до 1 л
3% 10 мл Н2О2 (30%) разб. до 100 мл. Хранят в темноте
Рейнеке соль 0,1 н. 5,7 мл Н2О2 (30%) разб. до 1 л
1% 1 г NH4[Cr(NH3)2- (SCN)4]-H2O раств. при 50еС в 100 мл НС1 (5%), фильтр.
23
Приготовление растворов
Продолжение
Вещество Концентрация Способ приготовления
Ртуть азотнокислая (I) 0,1 и. (0,05 Л1)
азотнокислая (II) 0.1 и.
хлорнокислая (I) 0,1 н.
Свинец уксуснокислый (II) 0,1 и.
уксуснокислый (IV) 0.1 и.
Серебро, азотнокислое Сероводородная вода 0,05 и. — 0,5%
Сурьма, хлористая (V) 0.5%
Титан сернокислый (III) 0,1 и.
хлористый (III) 0,1 и. (0,1 М)
Торий, азотнокислый Уран, хлористый (IV) 0,05 п. 0.1 и.
а) 28,1 г Hg2(NO3)2 2Н2О расти в 300—400 мл теплой Н2О, подкисленной 10 мл HNOa (конц ), добавл. Hg (2—3 капли), хорошо перемет. Через I сутки фильтр, в склянку из темного стекла, разб. до 1 л
б) К 30—40 г Hg добавл. 20 мл 25% р-ра мочевины, 40 мл HNOj (конц.). После окончания реакции охл., добавл. 33,5 мл HNO3 (6 и.), разб. до 1 л
17 г Hg(NO3)2 • 0,5Н2О раств. в Н2О, содержащей 20 мл HNO3 (6 н.), разб. до 1 л
10,9 г HgO (красная модификация) раств. в 10 г НСЮ4 (конц ), нагр. 3 ч на водяной бане с Hg. разб. до 1 л
20 г (СНдСОСОгРЬ-ЗНзО раств. в Н2О и разб. до 1 л
а) 34 г РЬ3О4 раств. в 1 л лед. СНзСООН *
б) 22,17 г (СН3СОО)4РЬ раств. в 1 л лед. СНзСООН
8, 5 г AgNO3 раств. в 1 л Н2О
Нас. Н2О сероводородом из расчета 3 л H2S на 1 л Н2О **
К гор. р-ру SbCl3 (0,5%) в НС1 (4 н.) добавл. нас. р-р КВгО3 до желт, окраски
а ) 100 мл продажного 15% р-ра Ti2(SO4)3 (р=1,4 г,'см3) разб до 1 л H2SO4 (4 и.)
б ) 1,5 г ТЮг сплавл. с 10 г KHSO4 (или K2S2O7), сплав выщелачивают 80 мл р-ра H2SO4 (1:5) и разб. до 200 мл. Фильтр, и встрях. с амальгамой цинка
25 мл продажного р-ра TiCl3 кип. 1 мин с 50 мл НС1 (25%), охл., разб. до I л. Хранят в темноте в атм. Н2 или СО2. Для восст. частично окисленного Т1 встрях. р-р с Na-амальгамой
7 г Th(NO3)4 раств. в Н2О и разб. до 1 л UO2CI2 (17 г) или уранилацетат (21,5 г) раств в HCi (I и ), восст. (на Ag-редук-торе или цинком, или электролитически). Разб. HCI (1 н.) до 1 л
* При этом получается раствор, содержащий РЬ^ и РЬ2' .
** Газообразный сероводород получают одним из следующих способов:
1. Сернистое железо (кусочки 1 — 2 г.и) в аппарате Киппа обрабатывают серной (1:4) или соляной (1:1) цислотой.
2. К Na2S в двугорлой'колбе добавляют медленно из капельной воронки 5 — 10%-пую HCi.
3. К AlgS3 приливают медленно из капельной воронки воду.
4. Смесь I вес. ч. серы и 1 вес. ч. парафина с добавкой асбеста нагревают до 300° С.
24
Приготовление растворов
Продолжение
Вещество Концентрация] 1 Способ приготовления
Фишера реактив * Хром сернокислый (11) Реактив готовится в сухой посуде с
0,1 н. высуш. (обезвоженными) веществами 85 г иода раств. в 270 ли пиридина и добавл. 670 мл СН;(ОН (полученный р-р сохраняется долго). К этому р-ру, охлажденному в лед. Н2О, добавл. осторожно 45 мл высушенного жидкого SO2 (мерный цилиндр охл. сухим СО2 с ацетоном). Перед определением титра оставляют на несколько дней Через р-р 40 г КгСг2От в 200 мл Н2О,
хлористый (II) 0.1 и. содержащей 15 мл H2SO4 (конц.), пропускают SO2, затем изб. SO2 удаляют продуванием воздуха. Разб. до 250 мл н восст. электролизом (16 в, 0,02 а/см2, 7—12 ч). Сохраняют в атм. СО2 Восст солянокислый (0,1 .14) р-р СгС]3
Циммермана—Рейпгар- (0,1 М) гранулированным цинком при взбалт в сосуде с клапаном Бунзена до чисто гол. окраски. Хранят в инертной атм. (под слоем бензина) 70 г MnSO4 • 7НгО раств. в 400 мл НаО,
та смесь Церий, сернокислый (IV) 0,1 н. содержащей 130 ли H2SO< (конц ), охл., добавл. 140 мл Н.4РО4 (р=1.70 а/сл<3) и разб. до 1 л а) 64 г Ce(SO4)2-2(NH4)2SO4-2H2O
Цинк сернокислый 0.1000 и. или 41 г Ce(SO.i)2 • 4Н2О раств. в 500 мл Н2О, содержащей 30 мл H2SO4 (конц.), охл., фильтр, и разб. до 1 л б) К 20 г СеОг добавл. 500 ли H2SO4 (1 : I), натр, до раств. (3 ч), разб. до 600 мл, охл., фильтр., разб. до 1 л 14,38 г ZnSO4 • 7Н2О раств. в Н2О и
хлористый 0,1000 н. разб. до 1 л 3,269 г Zn раств. в 50 мл НС1 (1:1) и
Цинк-уранил, уксусно- . .... разб. до 1 л Раствор 1. 10 г (СН3СОО)2• UO2• 2Н2О
КИСЛЫЙ раств. при натр, в 6 мл 30% СНзСООН и разб. Н2О до 50 ли Раствор II. 30 г (CH3COO)2Zn • 2Н2О растирают с 3 ли СНЗСООН (30%); добавл. 50 ли НгО К смеси равных объемов растворов I н 11 добавл. NaCl (1 каплю 0,1% р-ра) и через 24 ч фильтр.
растворов М 1 и 2, которые перед употребление м
* Выпускается промышленностью в виде смешивают.
25
П родолэкение
Приготовление растворов
Растворы органических реактивов
Реактив Концентрация Способ приготовления
Ализариновый красный 0,25%
S (ализарин сульфонат натрия) Алюминон (ауринтри- 0,08 мг/мл
карбоновая кислота, аммонийная соль) 1 мг/мл
Антраниловая кислота 5%
Антраниловая кислота, 3%
натриевая соль Арсеназо (бензол-2-ар- 0,005%
соновая кислота-(1 -азо 2) -1,8-диоксннаф-талин-3, 6-дисульфокислота. динатриевая соль) 0,1 н.
Аскорбиновая кислота
Бензидин 2%
0,25%
Бензоат аммония 10%
Вариаминовый синий 1%
(4-амино-4'-метокси-дифениламин)
Винная кислота 2 н.
Г идрохинон 0,1 н.
5%
1%
Грисса реактив
Дим етилгл иоксц м 1.2%
0,25 г р-ва раств. в 100 ил Н2О
К 7,8 г СНзСООМНч добавл. 5,4 г NH4CI, 8,0 тил алюминона (0,1 % р-ра) и 60 Л1л НС1 (1 : 1), разб. Н2О до 100 тил
К 10 мл алюминона (1%) добавл. 10 мл р-ра, содержащего 7,5 г CH3COONH4 и нейтрализованного по лакмусу, 5 мл нас. р-ра SO2, NH4OH до нейтр. реакции, разб. Н2О до 100 мл. Хранят закрытым. Периодически добавл. свежеприготовленный р-р SO2
5 г р-ва раств. в 100 мл Н2О или спирта
3 г антраниловой к-ты раств. в 22 мл NaOH (1 н.), нейтр. по лакмусу до слабокислой реакции, фильтр, и разб. НгО до 100 мл
0,005 г р-ва раств. в 100 мл Н2О (дважды перегнанной)
К р-ру 8,806 г р-ва в 1 л Н2О, перегнанной в стеклянном аппарате, добавл 0,1 г Na-ЭДТА и 4 мл НСООН. Хранят в темной бутыли в атм. СО2
2 г р-ва раств. в 100 мл 95% сп.
0,25 г р ва раств. в 10 мл лед. СНзСООН и разб. Н2О до 100 мл
10 г р-ва раств. в 90 мл Н2О
1 г р-ва растирают с небольшим количеством Н2О, разб. I1C1 (0,1 н.) до 100 мл и фильтр.
150 г р-ва раств. в Н2О и разб. до 1 л
5,50 г р-ва раств. в 1 л гор. НС1 или H2SO4 (1%)
10 г р-ва раств. в 100 мл H2SO4 (конц.). Хранят не более 2 дней
1 г р-ва раств. в 100 мл ацетатн. буф. (pH ~ 4,5). Готовят перед употреблением
Смешивают два р-ра:
а) 0,5 г сульфаниловой к-ты раств. в 150 мл 2 н. СНзСООН
б) 0,22 г а-нафтиламина раств. в 200 мл воды, добавл. 150 мл СНзСООН
1, 2 г р-ва раств, в 100 мл 95% сп.
26
Приготовление растворов
Продолжение
Реактив Концентрация Способ приготовления
.——— 0,005% 0,005 а р-ва раств. в 100 мл СС14 или
Дитизон СНС1з. Р-р годен 3—4 дня
0,5% Смесь 0,5 г р-ва с 3 мл Н2О раств. в
Дифениламин 100 мл конц. H2SO4 (или в 100 мл конц. НзРО4)
Дифенилкарбазид 0,1% 0,1 г р-ва раств. в 10 мл лед. СНзСООН, добавл. 90 мл сп. Хранят в
темноте
Дифенилкарбазон Ильинского реактив Крахмал, растворимый 0,5% 0,25% 0,5 г р-ва раств. в 100 мл 95% сп. См. а-Нитрозо-Р-нафтол К 2,5 г р-ва добавл. 0,01 г HgJ2, взбалт. с 5 мл Н2О; кашицу вливают в 1 л кип.
Н2О и кип. 2 мин (после охл. добавл. 5 мл толуола)
Купферон ** (аммонийная соль нитрозофе- 6% 6 г р-ва раств. в 100 мл хол. Н2О и фильтр. Применяют свежеприготовленный
нилгидроксиламина) 5% р-р
2-Меркаптобензтиазол 5 г р-ва раств. в 100 мл 95% сгк
Мочевина 20% 25 г р-ва раств. в 100 мл 5 н. НС1
а-Нитрозо-₽-нафтол 2% 2 г р-ва раств. в 50 мл лед. СНзСООН,
(Ильинского реактив) добавл. 50 мл гор. Н2О, фильтр.
8-Оксихинолин 5% 5 г р-ва растирают с небольшим количеством 2 н. СНзСООН. Затем раств. в этой к-те и разб. ею до 100 мл. Слегка натр., фильтр. Хранят в темном сосуде
Родамин С (диэтил- 0,01 % 0,01 г р-ва раств. в 100 мл Н2О
л-аминофенол фталеин)
Рубеановодородная кис- 0,5% 0,5 г р-ва раств. в 100 мл 95% сп.
лота (дитиооксамид) Сульфосалициловая кис- 10% 10 г р-ва раств. в 90 мл Н2О (добавл.
лота р-р NaOH до рН=4,5-—7)
'Ганнин 1% 1 г р-ва раств. в 100 мл 5% СНзСООН.
Тетраэтиламмоний, гид- Применяют свежеприготовленный р-р
0,1 н. К 30 г (C2HS)4NJ добавл. 300 мл СН3ОН (абс.), свежеосажденную Ag2O (до отрицательной реакции р-ра на J-). Фильтр, и разб. бензолом до I л
роокись Тионалид (Р-нафталид
1% 1 г р-ва раств. в 100 мл 95% сп. или
тиогликолевой кисло- лед. СНзСООН
Уксусная кислота 6 н. 345 мл копц. СНзСООН (р= 1,05 г/см3) раств. в Н2О и разб. до 1 л
2 н. 115 мл конц. СНзСООН раств. в Н2О и
Уротропин о-Фенантролин Фенилантраниловая кис- 10% разб. до 1 л 10 г р-ва раств. в 90 мл Н2О
0,25% 0,25 г р-ва раств в 100 мл Н2О
0,33% 0,1 г р-ва раств. в 30 мл 0,6% р-ра
Na2CO3; фильтр. Хранят в темноте
** Сухой следУет хранить в темноте в эксикаторе над 1% H2SO4.
> упферон хранят в темноте в присутствии твердого углекислого аммония.
27
Приготовление растворов
П родолжение
Реактив Концентрация' Способ приготовления
Феииларсоиовая кислота 2,5% 2,5 г р-ва раств. в 100 мл Н2О
Формиатный буфер 2.8 г HCOONa раств. в 100 мл 98%
(рН~2) 2%- НСООН
Ферроин 1,49 г о-фенантролина и 0,7 г FeSO4
о-Фталевая кислота 2% раств. в 100 мл НгО 2 г р-ва раств. в 100 мл НгО
Хинализарин 0.05% 5 мг р-ва раств. в 10 мл КОН или
0,01% NaOH (0,25 и.) 1 мг р-ва раств. в 10 мл абс. сп.
Хинальдиновая кислота 1% 1 г р-ва раств. в 100 мл Н2О нейтр.
Хлорамин Т (N-хлор- 0.1 н. NaOH, затем добавл. 0,2 мл лед. СНзСООН 14 г р-ва раств в 1 л НгО
и- толуолсульфа МИД, Na-соль)
Щавелевая кислота 1 М 126 г Н2С2О4 • 2НгО раств. в гор. Н2О,
0,1000 н. охл., разб. до 1 л 6,304 г Н2С2О4 2Н2О раств. в 300 мл
Этплеидиаминтетрааце- 0,1000 н. H2SO4 (1:5) и разб. НгО до 1 л 18,61 г Na-ЭДТА, высушенного при
тат натрия (Na-ЭДТА, 20° С, раств. в НгО и разб. до 1 л
трилон Б, комплексон Ш) 0,1000 н.
Этплеидиаминтетрааце- Смешивают равные объемы 0,2000 н.
тат магния р-ров MgCl2 и Na-ЭДТА
Металлы, применяемые в редукторах
Металл Способ приготовления
Кадмий
Висмут
Серебро
Цинк амальгамированный
В нас. р-р CdSOj (750 г/л) помещают палочку металлического Cd (анод) и Pt-проволоку или пластинку (катод), добавл. несколько капель H2SO4 (конц.). Электролиз проводят при перемеш.. катодной плотности тока 0.01 а1см2 и при напряжении 3—4 в. Выделенный кадмий промывают. Сохраняют под водой
Металлический висмут дробят, а затем измельчают до кусочков 0,3—0,6 мм (остатки пыли и мелочи сплавл. под слоем буры и снова измельчают). Хранят под слоем НС1 ИЛИ H2SO4 (1 и.).
30 г AgNO3'раств. в 400 мл НгО с несколькими каплями HNO3. Погружают в р-р ленту меди (10 см2). Перемеш. до полного выделения серебра. Полученный порошок переносят в редуктор и промывают H2SO4 (I : 200) до удаления меди. Заливают редуктор НС1 (1:9). Для регенерации серебра (при его‘почернении) наливают, в редуктор H2SO4 (1:200) и сверху помещают цинковую палочку. Оставляют ее до полного восст. темного AgCl. Промыв. H2SO4 (1 : 200) до удаления цинка и затем НС1 (1:9).
Harp, цинк при 200° С до расплавления, растирают (в стальной ступке). Просеивают, отбирая фракцию 0,6—0,8 мм. Всыпают Zn в р-р HgCl, (100 мл р-ра, содержащего 2,7 г HgCl2, на 100 г Zn). Перемеш. 5 мин. Промывают Н2О. Хранят под водой.
28
Приготовление растворов
Продолжение
Расчетные формулы для приготовления растворов
Принятые обозначения:
д —концентрация приготовленного раствора, вес. %;
д'—нормальность приготовленного раствора, г-экв'л-, д — нормальность исходного раствора, г-экв!л‘, р —весовое количество вещества, г;
у — объем исходного раствора, мл;
р —содержание данного вещества в исходном веществе, вес. %;
а — содержание данного вещества в исходном растворе, вес. %;
^ — эквивалентный вес вещества;
— плотность растворителя;
—плотность получаемого раствора;
(Ц —плотность исходного раствора;
(/ — количество добавляемого растворителя.
Формулы для пересчета концентраций раствора из одних единиц измерения в другие см. „Справочник химика“, т. III, стр. 494.
Приготовление раствора заданной процентной концентрации
а) Количество вещества пли объем исходного раствора на I л растворителя:
1.--Л 100М° _ Л 10W° (2,
(а —Л)</| О,Ь¥|Э-Д</, (’
б) Количество вещества или объем исходного раствора на 1 л раствора;
<Э = Л IOd (3)
„ А IOOOJ 10000J
r= -ad— =А-^Г «>
Приготовление раствора заданной нормальности
а) Количество вещества или объем исходного раствора на 1 л растворителя:
7V5 • ЮОО^о l000d-N3 (5>
ЛЭ lOOOdo N WOOJo
~ (I0da-M9)d, ~ (ЛГ|</-ЛГ</|)- (Ъ>
и) Количество вещества или объем исходного раствора на 1 л раствора:
Г = Л • аа\
17 = -—— . /V1
(7*
(8)
(9)
Разбавление растворов
Для вычисления количества растворителя (q мл), которое следует добавить к раствору (К мл) для разбавления его от одной концентрации до другой, следует пользоваться формулами:
Г (a V (0.17V.3 - 4J.) V(10da-N3) dt V(Nid-Ndi)
V~ Ad<> ~ Ad„ N3d„ ~ Nd0
Д «я вычисления объема раствора (V мл), которое следует взять для разбавления До объема 1 л, следует пользоваться формулами (4), (8) и (9).
МЕТОДЫ РАЗДЕЛЕНИЯ И КАЧЕСТВЕННОГО АНАЛИЗА
Аналитические группы ионов
В таблицах приведены схемы анализа смеси неорганических веществ, основанные на последовательном выделении групп катионов и анионов действием групповых реактивов. Перед систематическим анализом обычно проводят предварительное испытание анализируемого вещества дробными реакциями, что позволяет выбрать ту или иную схему.
В конце раздела указаны реактивы для определения групп окислителей или восстановителей.
Катионы
Сероводородиая схема анализа
Цифры в скобках означают номера примечаний.
Исследуемое вещество 0,3 н. НС1 (1)
Нерастворимый остаток (7) Раствор -р H2S (2)
осадок + (МН4)2 S,, (3) раствор 4-(NH4)2 S (4)
раствор осадок осадок раствор -f- (МН4)2 СО3 (5)
V Аналит .V ические труп 111 осадок пы (6): раствор 1
Примечания к схеме:
I. Часто предварительно выделяют из анализируемого вещества группу «летучих» соединений с помощью реактивов, . указанных в скобках: Si(HF), Se, As, Ge (НВгЧ-Вг2), Os (HNO3), Ru (HCIO4). Re (H2SO4),.a также группу благородных металлов: Au, Ag, Pt, Pd (Ir, Rh, Hg выделяются неполно)-’
2. Солянокислый раствор (0,3—1 н. HCI) доводят до кипения, насыщают H2S н выдерживают при 70—90° С 10—15 мин; охлаждают, разбавляют водой и снова насыщают H2S; закрывают колбу, встряхивают и оставляют на 15 мин.
Если в растворе присутствуют соединения молибдена, то после пропускания H2S добавляют немного Н2О2 и вновь насыщают H2S.
Вместо газообразного H2S можно иепользовать раствор H2S в ацетоие; применяют также другие групповые реактивы, образующие сульфиды.
3. Осадок от H2S обрабатывают избытком (NH4)2Sn при слабом нагревании.
4. Для осаждения III группы кислый раствор нейтрализуют NH<OH (не содержащим СО2), добавляют избыток его, насыщают H2S и снова добавляют NH4OH.
В присутствии РО4~, ^2^4 * ^^2 (V°3 ’ СгО^ , С4Н4Og , F , МоО4 ) вместе с III группой осаждается также и II группа. Поэтому перечисленные анноны необходимо предварительно удалить. Все они могут быть удалены при помощи анионитов (стр. 148 и сл.); кроме того, РО3” осаждают ионами Fe3"*" (в уксуснокислом растворе в присутствии CHsCOONa), а также ионами Zr4+ или Т14+ (в солянокислом растворе).
30
Аналитические группы ионов
Продолжение
При осаждении нонов III группы аммиаком (вместо (NH4)2S) не осаждаются Со2 + , ni2+, Zn2+, Мп2+.
5. Осаждение II группы карбонатом аммония проводится при нагревании в присутствии NH4CI и NH4OH.
6. Состав аналитических групп:
V аналитическая группа: As1^. As^, Ge^t Мо^®, Re^II, Sb^, Sb , SelV f Sn^V, SiJI, (частично W^, V^, Au^1, 1гШ, Ir^, Pt^).
IV аналитическая группа: Au111, Ag+, Bi3 + , Cd2 + , Cu2 + , Сц+, Hg2 + , Pb2 + , Pd^, Pd^V, RlJH, RiJH (частично осаждаются In3+, Zn2+); ионы Ag+ и Hg2 + обычно не попадают в эту группу, так как остаются в виде хлоридов в нерастворимом остатке.
III аналитическая группа: Ве2 + , Zn2+, Al3 + , Y3 + , Sc3 + , лантаниды, актиниды, Ga3 + , In3 + , TI3+, TpV, Zr4 + . Hf4 + , Th4 + , VV. Nbv, TaV, Cr3 + , UVI, UIV, Mn2+, Fe2+, Fe3+, Co2+, Nl2+.
II аналитическая группа: Ca2 + , Sr24-, Ba2+, Ra2+.
I аналитическая группа: Li4-, Na + , NH4+, K + , Rb + , Cs+, Mg2+.
Иногда применяют обратную нумерацию групп: пятая группа называется первой и т. д.
7. В нерастворимом остатке могут содержаться следующие вещества.
Окисльг. А12О3, S1O2, TiO2, ZrO2, HfO2, ThO2, SnO2, PbO, Nb2O5, Ta2O5, Sb2O5, Sb2O3, Sb2O4, Cr2O3, WO3, U3O8, UO2, Fe3O4, Fe2O3.
Кислоты: кремневая, ниобиевая, танталовая, (3-оловянная, вольфрамовая.
Силикаты: большинство (при большом отношении содержания SlO2 к содержанию основ* кого окисла).
Сульфаты: BaSO4, SrSO4, CaSO4, RaSO4, PbSO4, Hg2SO4, Fe2(SO4)3.
Сульфиды и тиоангидриды: CuS, Ag2S, Au2S, Au2S3, CdS, HgS, Hg2S, GeS2, SnS, SnS2, PbS, As2S3, As2S5, Sb2S3, Sb2s5, Bi2S3, M0S3, ReS2, Re2S7, RuS2, RhS, PdS, PdS2, OsS2, OsS4, IrS2, Ir2S3, IrS, PtS, Pt2S3, PtS2.
Фосфаты и пирофосфаты: Ti3(PO4)2, TiP2O7, Zr(HPO4)2, ZrP2O7, Hf(HPO4)2> HfP2O7, Th3(PO4)4, ThP2O7, Sn3(PO4)4, SnP2O7, BiPO4.
Хлориды, бромиды, иодиды, цианиды, роданиды: AgCI, AgBr, AgJ, AgCN, AgSCN, CuCL CuBr, CuJ, CuCN, CuSCN, AnCI, AuBr, AuJ, Hg2CI2, Hg2Br2, Hg2J2, Hg2(SCN)2, TIC I, TiBr, TlJ, T1SCN, PbCi2, PbBr2, PbJ2, BIJ3, PtCl2, PtJ2, PdJ2, Pd(CN)2.
Фториды: лантанидов, ThF4, ScF3, YF3, CaF2, UF4, PbF2.
Оксалаты: лантанидов, Th(C2O4)2, Sc2(C2O4)3, V2(C2O4)3, U(C2O4)2.
Металлы: Cu, Ag, An, Hg, Zr, Hf, Nb, V, Ta, Pb, Sb, Bl, Mo, W, Ru, Rh, Pd, Os, Ir, Pt.
Неметаллы: В, C, Si, P, As, S, Se, Те, J.
Бессероводородные схемы анализа
Во всех схемах указано последовательное действие реактивов, осаждающих некоторые группы ионов. Ионы, которые в данной схеме анализа не осаждаются, указаны в примечаниях.
I схема
Реактив Осаждаемые ионы Примечание
НС1 HNO3 Ка25О4-|-этиловый спирт nh4ci + nh4oh Ag+, Hg2+, Pb2+, WVI SnIV (Sn2+), Sbv, Sb111, TiIV, Movl Ca2+, Sr2+, Ba2+, Pb2+ Fe3+, Al3+, Cr3+, Mn2+. Bi3+, Zr4+ He осаждаются: Cu2+, Cd2+, Ni2+, Co2+, Hg2+, Zn2+, Mg2+
31
Аналитические группы ионов
Продолжений
П схема
Реактив Осаждаемые ионы Примечание
НС1 Н25О4-|-этиловый спирт КОН 4- Na2O2 (кипящий раствор) Ag+, Pb2+, Hg2 1 , WV1 Са2+, Sr2+, Ва2+, Pb2 + Мп2+, Fe3+, Fe2+, Bl3 + , Mg24-, Cu2+, Hg2+, Co2+, Cd2+ (эти ионы могут быть разделены после растворения осадка действием NH4OH 4- Na2HPO4; при этом осаждаются Bi3+, Fe3+, Mg2+, Mn2+) III схема He осаждаются: Sn2+, Snlv, Al3+,Sbv, Sb111. Zn2+, Cr3+, Cs‘
Реактив Осаждаемые ионы Примечание
НС1 Бензоат аммония (при рН=4) NH4F NaOH В таблице дана схема содержащего тот или другой Ag+, Hg2+, Pb2+, WVI Snlv. Bi3+, Sbv, Fe3+, Al3+, Cr3+ Pb2+, Mg2+, Ba2+, Sr2+, Ca2+ Mn2+, Co2+, Hg2+. Cu2+, Ni2+, Cd2+, Fe2+ Экстракционная схема анализа последовательного экстрагирования реагент. He осаждаются: Sn2+, Asv, As111, Zn2+ иолов из водного раствора,
Реагент-]- экстрагент Экстрагируемые ионы Примечание
НС1 (конц.) смесь метилизобутилкетона с амилацетатом NH4SCN -|- днэтиловый эфир Ацетилацетон Диэтилдитиокарбамат натрия 4* диэтиловый эфир Sbv, Ап111, Fe3+, Vv, MoVI, Ga3+, As111. Gelv, TeIV Co2+, Zn2'+, Be2+. SnIV Al3+, Cr3+, Cu2+, UO2+, Zr4+, Ti4+ Ni2-U. Co2+, Bi3+, Pb2+, Hg2+. T1+, WVI, Mn2+ , SeIV, In3+ Не экстрагируются: Ва2+, Sr2+, Са2+, Mg2+, Се3+, Th4+
32
Аналитические группы ионов
П родолжечие
Анионы
Осаждение анионов групповыми реагентами
Действием групповых реагентов можно разделить следующие группы анионов (ионы, осаждаемые неполно, заключены в скобки).
1. Осаждаемые BaCl2 или BaCi2-rCaCl2
а) в нейтральной или а м м и а ч н о й с р е д е: В4О?“, ВО|~, ВО“, СО^" , СО?", С НО?-, С Н О?- SIF?-, РО?-, РО", ро;-, РО?~, VO-, AsO~, А,О?~ , 24 446 657 о 4 d 2 / 2 о 3 2 4
AsO?”, SO?-, SO?', S2O?~, S2O?-, SeO?-, SeO?”, TeO?-, TeO?-. CrO?-, MoO?-, F” , JO”, JO- (из концентрированных растворов осаждаются также ВгО~ и 510?“);
6) в уксуснокислой среде (действием (CH COO) Ba): Р~, SO?-, J0“ CrO?~ , (Fe <CN)6]3-, (Fe (CNIJ^, SlF?" (s2*, S^J, SO?-);
в)в co лянокислой epe де: F", S04 , SiFg .
2. Осаждаемые AgNO3
а) в азотнокислой среде: CI“, Br~, J“, CN“, SON"”, CIO~, CIO~, {Fe (CN)6]S f [He 'CN)(.f-, (Co(CN)e]3-.S2O?-, JO’, CrO?" (SO?", SO?-, SlO?", BrO");
6) в нейтральной среде: те же ионы, что и в азотнокислой среде, и кроме того NO- S2-, Se2-, Те2-, CNO", НСОО-, РО?-, N~ SO?-, SeO?-, SeO?-, Те0?“, TeO?- , 2 ’ £ А А А 4 А 4
s2°r- s2°r> А8°Г- Аз°Г соГ- с2°Г- в<°Г- во2_- воГ- ВОз" С2°Г- С<Н4°Г • С Н О?-, РО- P.O?-, P,O1-,JO- VO-, CrO?-, J0~ РО?-,РО?-, MoO?— (сн СОО-);
557 А 4 I 2 0 А А 4 Ч Ч A “ \ о /
из них окрашенные осадки образуют: РО** , Р О* , S Oj , РО^ , S С? , AsO^ , AsO^ ,
* 4 20 20 «3 24 It о
CrO?-, VO-, JO-.
3. Неосаждаемые BaCI CaCI и AgNO : NO , CIO , CIO , S O* , SO?? , MnO „ z 2 Oo A xzo О y
MnO*~ (ch3coo~).
4. Осаждаемые кислотами из щелочного раствора: SiO^-, WO^~, Nb\ Ta^.
Некоторые схемы систематического анализа анионов
В таблицах приведены схемы последовательного выделения анионов действием групповых реактивов (осаждением или экстрагированием). В скобках указаны ионы, осаждав-* мые неполно.
I схема
Предварительно разрушают CN , S2O| и МпО4 и делают содовую вытяжку.
Реактив Осаждаемые или экстрагируемые ионы Примечание
AgNO3, NH,OH и СГ, Br~, J-, SCN-. [Fe(CN)6]3-, [Fe(CN)6]<-, S2-, AsO|-, JOf He осаждаются:
(NH4)2 со3 C.H.O?-, BO?- 6 5 7 3
HNO3 бензол sio?-, JO;, Bro; Экстрагируются бензоат- и салицилат-ионы
NH4OH4-CaCI2 Ва (N°3)2 F-, C2O?-, C4H4O62-, AsO?~, PO?-, (SiO?“) CrO?-, SO?* 4 4 Осадки, образуемые анионами С,Н„О?- , F“ и С2О?-, растворимы в СН3СООН
3 Зак. 7S3
33
Аналитические группы ионов
Продо жжение
II схема
Реактив Осаждаемые ионы Примечание
(СН3СОО)2 Са (СН3СОО)2 Ва -|- ацетон (СН3СОО)2 Cd Ni (NO3)2 AgNO34-HNO3 СО2", F-. PO3~(SO2-, ' [Fe(CN)6]4-. JO;. SO2-, во;) SO2 Л SO2', CrO2~, SO23-(S2O2- . BrO;,[Fe(CN)6j)4“ [Fe(CN)e]3~, [Fe (CN)e]4-, S2' (CN~ BO;) CN~ C1-, Br~-J-, scn-,s2o2-* He осаждаются: CIO”, cio;, cio;- BrO;-no;, no;
III схема
Реактив Осаждаемые ноны Примечание
ca(№3)2+Na°H BacNO^ Zn(NO3)2 AgNO3 CO2-. F-. C2O2-, AsO3- , AsO3“, PO3-, C4H4O2-, so2- SO2-. CrO2- CN“, BO?", [Fe(CN)„13-, [Fe(CN)6]’-, S2“ cr,Br-, j-, scn-,s2o2-* He осаждаются: CIO; , no;, no;, ch3coo'
IV схема
Реактив .Осаждаемые ионы Примечания
PbCO3 Zn (NO3)3 S2". VO3- a) [Fe(CN)6f-, JO;, TeO2", PO3-, A1O;, BeO2-, комплексные анионы Th, комплексные анионы Zr 1. Анионы подгрупп а—г разделяются последовательным действием следующих реактивов: а) осаждением NH4OH б) осаждением MgCl2 в) осаждением Ca(NO3)24-Ba (NO3)2
* При действии реактива образуются Ag2S н S.
34
Аналитические группы ионов
Продолжение
Реактив Осаждаемые иолы Примечания
.— Zn (ХО3)2 б) РО3', РО3~, AsO2', AsO3', ТеО’“, SiO’" . AIO;, BeO’-. SnO’", SnO’-, SeO’“, SbO’-(F-) в) MoO’", CrO’-, C2O’' , WO’“, SO?-. TeOg- . 2. He осаждаются: сю-, CIO;, BrO; po2", Mno; 3. Отдельно определяют CH,COO-, NO, NO,", CO’"
во- (SeO’-, jo; r) [Fe(CN)6]3-. ) SeO2 ,
BO3-
Cd(NO3)2 CO’-, MoO’-,JO3-CrO’~ SeO’- .
Са (NOg)2 B;i(NO3)2 F" SO’-, CrO’- 4 4
AgNO, Cl". Br-, J-, JO3’ CN-, S’- SCN' ,
Восстановители и окислители
Наличие окислителей и восстановителей обнаруживается по изменению окраски раствора с помощью приведенных в таблице реактивов. В скобках указаны ноны, которые с данными реактивами реагируют медленно.
Реактив Восстановители
KMnO4 (+ H2so4) J2 (+ CH3COOH) Br-, J-,S’-, S2O’-, SO’-, NO", SCN", C2O’“, СЛОГ- H2O2. S2O’- [Fe(CN),p-. AsO3- , N2H4. NH2OH, Sri2 ' , Fe’+ S’-, S2O’-, SO|- (CN~. SCN-, [Fe (CN)6p“ , AsO33~, N2H4, NH2OH)
Реактив Окислители
kj ch3cooh) Бензидин или дифениламин CIO- (C1O3-), NO- HO, BrO- JO- S2O’-, \O/ Z ZZ 0 3 ZD MnO7, Ce44-, Fe3+, Cu2+ (CrO’-. AsO3-, [Fe (CN)6]3-) См. табл, на стр. 46 и сл.
3*
35
Аналитические реакции разделения ионов
ГРУППОВЫЕ РЕАКТИВЫ
Раздел групповых реактивов состоит из трех таблиц: 1) неорганические групповые реактивы; 2) органические групповые реактивы; 3) реактивы для отдельных групп ионов.
В первой таблице в горизонтальных рядах вначале даны окраски раствора и окрашивание пламени, вызываемое данными нонами. Затем приведены результаты действия соответствующих групповых реактивов, которые расположены в следующем порядке:
I—12 — реактивы для осаждения катионов или для образования с ними комплексных анионов в целях маскировки катионов;
13 н 14 — реактивы для осаждения анионов;
15—18 — окислители и восстановители, вызывающие изменение окраски раствора.
Ионы в таблице расположены в порядке групп элементов периодической системы.
Во второй таблице реактивы расположены в алфавитном порядке. Ионы размещены так же как и в первой таблице, в порядке групп периодической системы
В третьей таблице приведен ряд неорганических и органических реактивов, не вошедших в первые две таблицы, и перечисляются ионы, которые могут этими реактивами определяться (см. также таблицу «Индивидуальные реактивы», стр. 191 и сл.).
В квадратных скобках даны пояснения или номера примечаний.
Принятые обозначения
4- образуется осадок
(+) образование осадка идет с трудом
4-4- образуется осадок, нерастворимый в разбавленных сильных кислотах (0,3 н. HCI)
(4- +) образование осадка, нерастворимого в разбавленных сильных кислотах, идет с трудом
-4 (44 образуется осадок, нерастворимый в слабых кислотах (в уксусной кислоте)
4— образуется осадок, растворимый в избытке реактива
4- ) образуется осадок, с трудом раство-
римый в избытке реактива
— осадок не образуется
----образуется растворимое комплексное соединение
(----) образуется растворимое непрочное
комплексное соединение, разрушаемое, например, NH4OH или Na2HPO4
-> Получается, становится
(->) образование соединения или изменение цвета идет с трудом
ф выделяется летучее соединение без нагревания
(ф) выделяется летучее соединение при нагревании или при выпаривании раствора
а осаждается лишь совместно с многовалентными анионами
к осаждается лишь совместно с многовалентными катионами
Н4* кислая среда
ОН" щелочная среда
э соединение экстрагируется .органическими растворителями
(э) экстрагирование соединения идет неполно или с трудом
Остальные сокращения см. стр. 16.
Бледные (слабые) окраски растворов и
пламени (или их оттенки)
приведены в скоб-
Примечания к таблице «Неорганические групповые реактивы»
1. Из растворов, содержащих цитрат- или тартрат-ионы, в щелочной среде Na2HPO4
осаждает следующие катионы: Ац1 * 3 1", Be24-, Mg24", Са24-, Sr24-, Ba24", Hg24", лантаниды (III),
In3+, Zr4+, Hf4+, Th4+, Pb2+, UO2+, Mn2+.
36
ГРУППОВЫЕ РЕАКТИВЫ
2. В случае, если для реакции берут раствор иода в иодиде калия, реактив реаги* рует не только как окислитель, но и как осадитель за счет ионов J-(см. реактив 16).
3. Осадок образуется за счет галогенид-ионов комплексного аниона.
I. Окрашены в растворе следующие иоиы: Се4+ (желт.-ор.), Рг3 + (з.\ Nd3 + (от роз. до кр.-фиол.), Stn2+ (кр.-бур.), Sm3+ (желт.), Еи3+ (роз.), Dy3 + (желт.-з.), Но3+ (желт.), Ег3+ (роз.), ТцЗ-Ь (з.), Yb2+ (з.). Ионы La3 + , Се3 + , Eu2 + , Gd3"’, Tb3'1', Yb3+, Lu3+ бесцветны.
5. Осадок нерастворим в избытке реактива, но растворим в растворе ДОН^л.
6. В щелочной среде NO~восстанавливается до NH3, а в кислой— до N2, NO или NO2.
7. При рН=2 при нагревании выпадает осадок V2O5.
8. Пятивалентный ванадий образует в растворах разнообразные ноны: в кислой среде VOj', VO3 + , H.V„Or; в щелочной VO“ V.O3”, V_O4“ Н V07, а также и другие ионы 2 3 2 / 33jvi»24
(см. «Справочник химика», т. III. стр. 764).
9. Обычно образуются сложные анионы поликислот. Часто Nb и Та в растворе образуют фторидные и оксалатные комплексные анионы, которые разрушаются щелочами или кислотами с образованием осадков.
10. Может выпасть осадок калиевой соли рениевой кислоты.
Примечания к таблице «Органические групповые реактивы»
1. Ализариновый красный S при увеличении pH до ~ 6 изменяет окраску (желтую на фиолетовую). Окрашенные соединения получаются в слабощелочной среде (СНзСОСШа) с последующим подкислением СН3СООН.
2. Слабое органическое основание, осаждает гидроокиси (стр. 58).
3. Дитизон дает окрашенные и экстрагируемые соединения. Спектры поглощения и условия колориметрического определения дитизонатов см стр. 734 и 443.
4. Значения pH осаждения оксихинолинатов:
Си2 +...............................5,3-14,6
Mg2 +...............................9,4-12,7
Zn2 + ..............................4,6-13,4
Cd2 +.............................. 5.4-14,6
Са2+..............................(среда NH3)
Sr2+............................... »
Ва2+............................... »
А|3+................................4,2—9,8
Оа3+................................6,0-8,0
La8+.................................6
Tl'V................................4,8-8,5
Sn2+.............................(среда NH3)
Pb2+ ...............................8,4—12,3
Th4+................................4,4—8,8
VV...................................~5
Zr4 +............................ . . ~5
Sb11'................................>1,5
B|3+................................4,5—10,5
MoVI.................................3,6-7,3
WVI ..................................5,0-5,7
Cr3 +.............................(среда NH3)
Mn2+................................. 5.9-10
UO2+.................................4.1-8.8
Fe3+ ...............................-2,8—11,2
Co2+ ................................4,4-11,6
Ni2+................................4,3-14,6
Pd2+.......................(среда разб. HCI)
Большинство осадков растворимо в СНС13 с образованием окрашенных растворов.
5. Константы нестойкости комплексных соединений ионов металлов с ЭДТА см. «Справочник химика», 2-е изд-. т. III, стр. 162.
37
Неорганические труп
№ реактива Окраска раствора I группа
Ll + Na + к+ Rb + Cs + Cu2h Ag + Au"1
. . . СИН. желт.
Окрашивание пламени кр. желт. фнол. фиол. CHH . 3. [СИН.)
1 Н2О (разбавление р-ра) — / — — — — — —
2 nh4oh + nh4ci (pH «г 9) — — — — — + — СИН. +- + желт.
3 NaOH — __ — — — + (-) СИН. бур. (+)-кр.-бур.
4 H2S — — — — __ + + черн. черн. + + бур., черн.
5 (NH4)2S — — — — — + (-) черн. + + черн. бур., черн.
6 (NH4)2CO3 (+) — — — — _| СИН. +- желт. +
7 Na2HPO4|l] H) — — — — + СИН. Ч-желт. +
8 HF (+) — — — — (+) СИН. —
9 HCI — — — — — — + + —
10 H2SO4 — — — — — — (+) —
11 K4 [Fe (CN)6J — — — — — кр.-бур. ++ (+) • ->з.
12 KCN — — — — — +- —
13 BaCl2 — —7 — — — — + (+)
14 AgNO3 — — — — — — + [3]
15 Zn — — — — — + + кр. ++ черн. черн., кр.
16 KJ+CH3COOH — — — — ++ бур. [->J2] + + желт. + - 3.
17 J2 [2] — — — — — — “1
18 KMnO4 4- H2SO4 — — - - —
38
Повые реактивы
II группа № реактива
_—-—-— Ве2+ —— Mg2+ Са2 + Sr2 + Ва2 + Ка2 + Zn2 + Cd24 Hg2 +
кр. (желт.) кр. з. (желт.) бел.-з.
— — — — — __ — — — 1
+ а а а а а +- 4-- + черн. 4- 2
+(-) + (+)а а а а 4— 4- 4-черн. 4* (желт.) 3
— — — — — — 4- (4*) желт. черн. черк 4
+ а а а а а 4-(4-) желт. черн. + + черн. 5
+(-) — 4- 4- + + 4— + (серый) 4-(желт.) 6
4- 4- 4- + 4- 4- 4- 4* 4- + желт. 7
— (4~) + (+) (+) (+) (+) — (4-) — — 8
— — — — — — — — + + — 9
— — (4-4-) 4-4- Н—h + + — — _|—р — 10
— (+) + желт. (+) желт. (+) желт. + + + 4* 4- + 11
•— — — — — — 4-- 4-- + черн. — 12
— — — — — — — — — — 13
— — — — — — — — — 14
— — — — — — — 4- черн. черн. 15
— — — — — — — —_ 4- (—) з.; черн. 4— кр. 16
— — — — — — — — — — 17
— — — ->бц. — 18
39
Неорганические труп
№ реактива 1 Окраска раствора HI группа
ВОГ В4ОГ А13 + Sc3 + уЗ-f- La3 + лантаниды Се4 + Ga3+ 1п3+ Т1 +
HI желт.
Окрашивание пламени (СИН.-3.) f । • • - фиол. фиол,-СИН. 3.
1 Н2О (разбавление р-ра) — — — — — (+) pH^l — — —
2 nh4ohh-nh4ci (pH « 9) К + + + + + желт. +- + —
3 NaOH к +- + + + + желт. +- +(-) —
4 H2S — — — — — — к +(+) желт. (+) черн.
5 (NH4)2 s к + + + + + желт. (+)к + (+) желт. + (+) черн.
6 (NH4)2 co3 к + +- +- + + бур- +- + ( ) желт. —
7 Na2HPO4 [1] — + (+) + (+) +(+) +(+) + (+) желт. + (+) +(+) —
8 HF — сн ++ (—) ++ ++ ++ — — — *
9 HC1 — + +
10 H2SO4 — — — — (++) (++) — — —
11 K4 [Fe (CN)e] (+) (+) + (+) ++ + + [->Се3+] ++ ~1—н (+)
12 KCN — + + (+) (+) (+) — + —
13 BaCl2 + —
14 AgNO3 (+) —
15 Zn — — — —• — -> бц. + +(+) +(+)
16 KJ + CH3COOH — — — — — — — — + желт.
17| J2 [2] ->бц. — —. - 1 — 1 - 1 - 1 - 1 —
1в| КМпО4 + H2SO4 1 1 бц.
40
новые реактивы
Продолжение
с0Г — CH3COO~ С2°Г SI0l~ IV группа TIIV Zr4 + Hf4+ Т114 + GelV № реактива *
— — — (+) (44 pH < 2 (+) pH и 2 (4-) pH да 2 — (4-) pH < 0 1
— — к к + (+) + (+) + (+) + (4-) 2
— — к к + (+) + (+) + (44 + + - 3
— — — — — — — — + + бел. 4
— — к к 4- (44 +(+) + (+) + 4-- 5
— — к к 4- (44 4— 4— 4— (4-) 6
— — — — + (+) + + 4- 4- 4- + 4- 7
-t — — -4 — G44 — 4~ 4~ — 8
—4 — 4-4- — — — — -4 9
-4 — — + 4- — — — (4-) — 10
— — — — 4-4-бур- ++ 4—Ь 4-4- 4- 11
— — — — 4- 4- 4- + 4- 12
+ — +(+) (44 — — — — (44 [ОН] 13
4- — 4- (+) желт. — — — — -[3] 14
— — — + -> фиол. (3.) — — — 4- 15
-4 — — — — — — — 16
.(->) бц. - — - — — - 17
-4 - —> бц. - - - 18
41
Неорганические труп
№ реактива । Окраска раствора IV группа V группа
Sn2+ Sn'V Ро2+ nh+ NO; pO4' As°r AsO3“
. . .
Окрашивание пламени (СИН.) (СИН.) (си».)
1 Н2О (разбавление р-ра) (-H pH и 2 4-рН~0 — — — — — —
2 NH4OH 4- NH4C1 (pH « 9) + 4- + — — к — к
3 NaOH + - 4-- +- (t) — к — к
4 H.S + + бур. + + желт. черн. — (++) I-*S] — ++ желт. + + желт.
5 (NH4)2 s 4-бур. [5] 4— 4- + (++) l->s] к +- —
6 (NH4)2 co3 + 4-- b к
7 Na2HPO4 [1] + + + (+) — — —
8 HF — — + (+) — — — —
9 HC1 — -(П ++ — — — -(t) — .
10 H2SO4 — — + + — — — — —
11 K4 [Fe (CN)6] + + ++ + (4~) — — — — —
12 KCN + 4- + - (f) __ — — —
13 BaCl2 — — + — — + т +
14 AgNO3 + + черн. -13] — — — + желт. + желт. + кор.
15 Zn + черн. + черн. бур? — -[6] — 4 (4 +) черн. t(++) черн.
16 KJ + CH3COOH — — ++(—) желт. — — — __ + [Js]
17 J2 [2] > бц. — . — — — — -> бц. —
18 KMnO4 + H2SO4 -»бц. - — —> бц. —
42
повые реактивы
Продолжение
V группа VI группа m X X
Sb34 SbV [Н'1 BI3* W (8| Nbv(9| [он-] Tav |9| [он-] so- Sc°r ТеОГ
И'* ->желт. rt О» Сц
icim.-зЛ (син.-з.) <3.1 (син.) (син.-з.)
pH~t 0 4 pH эд 0 4 рН эд 1 — (4) pH эд 13 (4) pH эд 13 — — — (4-) 1
4 + 4- к К' к — — к к 2
-1- — +(-) + (-) к — к к — — к к 3
44 кр. 4 4 бур- -4-СИН. (+) бур. — — — (4-4-) l-*sj 44 ор. 4- 4 бур- 4
(-+)-кр. (44)-кр. 4-4-бур- (4)х -> кр. к — к — (44) l->sj — — 5
4 4- + к к к — — It h 6
4 — 4-4- — — — - 4- 7
— — — — 4— 4 — — - f — (4-) 8
-(f) — 4 -> желт. 17] 4-4- — - f __ <4) 9
— — — -> желт. (7] + 4- 4-4- — - f — (4) 10
— 4-желт. 4-4- + + 3. 4 (желт.) — — — — — 11
4- 4- 4- — — — — — — — 12
— — — 4 (желт.) 4- 4~ + 4- 4- 4- 4 4- 4 13
— -[31 — 4 (желт.) + + 4-4- (4-) — 4- 4 14
+ + (П черн. 44(f) черн. черьЁ -> СИН. ->бур. -> желт. — -(f) 4- 4 ор. + + черн. 15
-- ->J2 + черн. желт. ->4 — — —- —- 4 кр. кр.-бур. 16
— — — — — — — -> бц. — — 17
->бц. — — — -> бц. ->бц. ->бц. 18
43
Неорганические труп
№ реактива 1 Окраска раствора VI группа VII группа
Cr3+ Cro2- MoO21 wo2+ [он-] ио2+ F” С!~ Вг“ J —
3. желт. желт.
Окрашивание пламени (3.) . . .
1 Н2О (разбавление р-ра) —
2 NH4OH-f-NH4Cl (pH и 9) +(-) 3. — к к + желт. — — — —
3 NaOH +-3. — к к + желт. — — —
4 H2S — ->S + + бур- — — — — —
5 (NH4)2s + 3. (+) 3. к к бур. — — — —
6 (NH4)2 CO3 + 3. — к к +- — — — —
7 Na2HPO4 [1] + 3. — + + желт. +- + — — — —
8 HF — <+)- + — — - - —
9 HCI — — (+)- желт. — •— — — —
10 H2SO4 — — (+)- + + желт. — —. — — —
И K4 [Fe (CN)6] — кор. 4урГ кор. — — — —
12 KCN + — — — (+) - — — —
13 BaCl2 — -(+) • + ++ [ой-] +(+) — — •—
14 AgNO3 — + кр. + + lot-] — ++ + + желт.
15 Zn — -> 3. + 4~ ->син. ->син. -> 3. — — — —
16 KJ 4- СНзСООН — ->J2 (-*)J2 — — — — — —
17 J2 [2] - — -> бц. — — — - -
'“1 KMnO4 4- H2SO4 (->)желт. — “7- *— — — — ->бур. ->бур.
44
ппвые реактивы
П родолжение
VII группа VIII группа
Мп2 + R(<o4 с 3 + Fe Ре2+ Со2+ Nl2 + Rul".VI Rh111 Rd11 Os’V Irlll IV PfIV св X
желт, бур- роз. 3. бур. кр. бур. кр. бур. (3.) желт. св OJ О.
. . .
— — (+) pH »2 — — — — — — 4-pH» 2 — — 1
(+) бур. ->син. 4~ бур. 4-3. (+)-к роз. (+) — 3.-СНН. + (~) черн. (+ +) желт. кр.->бц. 4~ бур. 4- (+) желт. 2
бур. — 4“ бур- + 3. + роз. 4-3. + черн. 4— желт, тм.-бур. (44-бур- (4-) кр.-бур. -»син.-з. (+) бур- -> бц. (4-) 3
— черн. (+) [-^S] — (+) черн. (+) черн. (++)бур- СИН. ч!рн. + (+) черн. черк -> 3. + 4- бур. (4-+) бур- 4
+ роз. (4-4-) черн. + черн. + черн. + (+) черн. +(+) черн. +(-) бур. СИН. черн. 4-(+) черн. + + черн. 4— бур- 44—) бур- 5
+ — + бур- + роз. + -3. 4- — 4-(—) бур- 4-бур- (4-) — 6
+ — +(+) кор. т 4-(4-) + 3. — — — — — — 7
(+) — — — (+) - — — — 8
9
-(f) 10
4-4- 4—Ь кр.-бур. |Ю) + + СИН. + + ->(син.) + + 3. 4-4- — желт.-бур. 4- — — (4-) 11
4-- -{Ю] 4-- 4— 4—-кр. 4- — — — 4-- — — бц. 12
— (+) — — — — + — — — (4-) (4-) 13
— + — — — — 4-кр. 4- 4-[3] 4- (4-) (4-) 14
— и—и —> бц. — <44 (4-) + + черн. + + черн. + + черн. + + черн. + + черн. бур- 15
— > J. [10]' -> J2 — — — + черн. ->кр. (+) черн. — бур.->кр. ->кр. 16
—- — — — — -> бц. 1 - 1^ бц. + — — 7
бур. -[10] — -> бц. — — |з.-черн. — — — 3.->бур — Р
45
Органические труп
е 1 грунт
№ рсачт Реактив Ха-*" к" Си2 + Ла + Аи3 +
I Ализариновый красный S [1] — кр.-фиол. ->бур. -> (бур)
9 Антраниловая кислота — — -+-(+) 3. 4- (желт.)
3 | Бензидин 1 i — — -> СИН. | -> СИН. -> СИН.
4 1 Бензоат аммония [2] | — 1 (+-) 1 1 1 —
5 Винная кислота
6 Дитизон [3] — -> фиол.-кр. до желт.-бур.; э -> желт. до фиол.-кр.; э -> желт.; э
7 Диэтиловый эфир + + НС1 (6 н.) — — -0) __ э
8 Купферон — — + (+) (з.); э э
9 Лимонная кислота —
10 Меркаптобензтназол — — 4" (ор.-желт.) 4- 4-(желт.)
11 Мочевина — —
12 8-Оксихинолйн [4] — — + (+) з.; э -НН э + ®
13 Пиридин [2] — — (+) +
14 Рубеановодородная кислота — — син. (з.-черн.) бур- 4-
15 Таннин — — — —
16 Тионалид — - + + желт. + + желт. 1 4-4-желт.-бур.
17 Тиоацетат аммония — — + + черн. + + черн. + + черн.
18 Уротропин [2] — (+) 1 1
19 Фениларсоновая кислота —
20 Фенилгидразин [2] — 1
21 Хинальдиновая кислота — 1 1 1 — 4-4- 1 4-
22 Щавелевая кислота + + NH4OH — — 4-( ) 4(+) 4 4-6v;>.
23 46 Этилендиаминтетра-ацетат натрия [5] 1 1 1
новые реактивы
——— II группа in группа я яз X
He2 ’ Mg2- Са2 + Sr2 — Ва2+ Zn2+ Cd2+ Hg2+ А|3 + Оа3— TI- и сЗ
_к'р_ (+) (кр.) ->кр. *(кр.) ->(кр.) -> роз. 4“ op. + кр. +(+) ор.-кр. + Ж кр. + СИН. 1
. . . +(+) +(+) +ж 2
- — — -> син. — 3
Z+ — — - — -f— 4- 4
' 1 — —1 — — — — 5
— — — — — -> пурп. до кр.; э ->кр.; э -> ор.-желт. до кр.; э — — -> кр.; э 6
— — — — — -(Э) — (э) — э — 7
— — — — — (+) э “h (+) э + желт.; э — 4-4-э + э 8
— — 9
. . . 4" бц. + бц. 4-(желт.) (желт.) 10
— — — — — — — + 4- + — 11
э + э (+) э ж э (+) э +(-!-) желт.; э +ж э + (+) э + + 'з.-желт.); э 4-ж э э 12
• — (+) — 4- + + 13
— 4- + бур. — — 14
4- — — - — — 4-ж 4-ж — 15
— — — — — — + ++ бц. — — + 16
(+) + + желт. черн. .... + 17
.— — — -• — - — + 4- 4- 18
— — — — (+) Ч- . . . 19
— — — — — - — + 4- 4- 20
+ + (+) + (+) + . . . 21
— (+) (—) + (+) + (+) + (+) 4-ж (—) 4-ж (—) 4- — +- — 22
(—-) — 23
47
Органические гр;
№ реактива 1 Реактив III группа IV группа
La3 + лантаниды Се4 + Т14 + Zr4 ! ш4+ Th4 +
1 Ализариновый красный S [1] + <+) фиол.-кр. ++ фиол.-кр. фиол.-кр. + + фиол.-кр.
2 Антраниловая кислота + + син.-черн. -> бур.
3 Бензидин -> СИН. — — —
4 Бензоат аммония [2] —- + + + 4-
5 Винная кислота — — — —
6 Дитизон [3] —- •— — —
7 Диэтиловый эфир + + НС1 (6 н.) -— — — —
8 Купферон +(+) э ++ э ++ э ++ э +(+) э
9 Лимонная кислота — — —
16“ Меркаптобензтиазол +
11 Мочевина — -4- + +
12 8-Оксихинолин [4] + (+) э + СТ) бур-; э + (+) ор.-кр.; э + (+) э +(+) э
13 Пиридин [2] — 4- 4- +
14 Рубеановодородная кислота ....
15 Таннин + + + (+) + (+) +(+)
16 Тионалид — — — •—
17 Тиоацетат аммония
18 Уротропин [2] — + + 4- +
19 Фениларсоновая кислота -— + + ++ 4-4- + (+)
20 Фенилгидразии [2] —• + 4- 4- 4-
21 Хинальдиновая кисло-та
22 Щавелевая кислота + + NH4OH ++ ++ —. — —..—. (--)
23 Этилендиаминтетра- ацетат натрия [5] 1 - (—)
48
новые реактивы
Продолжение
IV группа V группа № реактива 1
- IV Ос1 * Sn2 + (Sn'V) Pb2 + Vv Nbv TaV АзШ Sb3 + В13 +
ор. + op. 4-кр. >( желт.-op.) .... —кр. 4" кр. 1
.... 4-4- 2
— — -> СИН. •—• — — 3
4- 4- — .... 4- 4- 4
— — — .... — — — 5
-> кр.; э -> кр.; э — — > ор.-желт. до ор.-кр.; э 6
э э — — (э) э э — ~7
4- 4" э [Sniv] 4-(4-) э + + кр.; желт.; э 4-4-э — + + э 8
_ .—. — — •— — — 9
.... 4-желт. .... + желт. 10
4- 4- 4- 4- 11
-ь(+) э (+) э 4-(4-) э _|_ (Ц_) > син.-черн. 4-(4-) э — + (+) э 4-(4-) ор.-желт. э 12
4- 4- 4- 4- 4* 13
.... ор.-желт. 14
+4- +4- — 4-(4-) син.-черн. 4- 4-Та желт. Nb кр. — (4-4-) 4-4- 15
4-4-бц. 4- (4-) '— 4-4-бц. V + + желт. 16
4-4-[Snivj + + кр.(->)черн. 4- 4-4-желт. 4-4-кр. 4-4-бур- 17
+ 4- 4- 4- 18
(+4-) [Snivj 4-4- .... 4-(4-) 19
4- 4- 4- 4- 20
4- .... 21
— + + 4- (4-) -> СИН. [Н + ] — + (4-) 4-(4-) 22
— .... .... - — 23
4 Зак. 78 3
49
Органические труп
m s V группа VII группа
м rt а> Si Реактив Сг3 + МоО2-4 WO2- и0Г Мп2+
1 Ализариновый красный S [1] 4 (желт.) ->(желт.-ор.) ->(желт.-ор.) ф:юл. __
2 Антраниловая кислота 4- (4) + бц. 4
3 Бензидин — — -> СИН. [ОН-]
4 Бензоат аммония [2] + 4 4 4 желт. —
5 Винная кислота — — — — —
6 Дитизон [3] — >фиол.-бур. э
л Диэтиловый эфир + + НС1 (6 н.) — э — — —
8 Купферон + з.; э 44 э 44 э [UIV44] 4(4) роз.; э
9 Лимонная кислота — -— -- - — — —
>0 Меркаптобензтиазол 4
11 Мочевина’ 4 ч- 4 (4) —
12 8-Оксихинолии [4] 4(4) э 4(4) э + желт.; э 4 (4) кр.-бур.; э 4(4) желт.; э
13 Пиридин [2] 4 4 4
14 Рубеановодородная кислота
15 Таинин 3. (4 4) бур. ’ 4 бур. 4(4)
16 Тионалид .— — —
17 Тиоацетат аммония 44 бур. 4 4 бур.
18 Уротропин [2] Д- 4 4 4 —
19 Фениларсоновая кислота 44 4- (4)
20 Фенилгидразин [2] 4 4 4- — —
21 Хинальдиновая кислота 4 -Г-+-желт. 4
22 Щавелевая кислота + H-nh4oh — .— — — — 4(4)
23 Этилендиаминтетра-ацетат натрия [5] — —
50
новые реактивы
П родолжение
VII [ группа № реактива
Ре3 3 Со2 + Ni2 + Pd2+ 1г”' Pt'V
-> бур.-кр. + (фиол.-черн.) ->ор. + кр. 1
—L + (+) (кр.) 444) (3.) + (желт.) — — 2
-> СИН. -> СИН. -> СИН. 3
4-ор. — — 4
— — — — — — 5
-> черн. э ->ф иол.-бур. э -> кр.-бур. э -> бур.-з. до бур.-кр.; э — з.; э 6
э — — э (э) 7
++ бур.; э + (+) бур; э 444) з.; э ++ э 8
— — — — — 9
+ 3. + бур. + + 10
-1- — — + + 11
4 (~Ь) черн.; э + (+) (кр.); э 4- (Ч-) з.; э 4- + э 12
+ с-н (+j + 13
д. (4-) бур- (+) фиол. + + + фиол.-кр. 14
фиол.-черм. — — — 15
4- 4- + 4-желт. бур- + + бур- 18
СИН. ++ черн. + + бур- + + бур- 17
+ — — 4- -4- 18
+ 19
+ — — + 4 20
син.-з. + 4 21
желт. + (+) (—) 44+) (—) + кр. -> 3. + желт. 22
— — — 23
51
Реактивы для отдельных групп ионов Металлы и амальгамы
Металлы или их амальгамы применяются для восстановления ионов перед их определением. Приготовление металлов см. стр. 28*.
В таблице указана валентность, до которой восстанавливаются элементы
Металлы расположены в порядке увеличения их восстановительного потенциала.
Металлы ** Fe^l T|1V VV uvi wVI MoVI Cr'H Cull SnIV
Ag 2 .—. 4 4 5(3) 1
Hg 2 — 4 4 ... 5
Си 2 — ...
Bl 2 3 4 4 3 5 и 3 — 1 2
Cd 2 3 2 4 3 и 4 3 — . . . . . .
Pb 2 3 2 4- 3 3 2 . . . ...
Sn 2 3 2 3 3 1 и 0 2
Zn*** 2 3 2 4 и 3 3 3 2 0 2
* При восстановлении элементов в редукторе последний предварительно промывается кислотой. Скорость пропускания раствора через редуктор 50 лицмин. Уровень жидкости не должен опускаться ниже уровня металла.
* * Кроме указанных в таблице металлов применяются также алюминий для восстановления Eu3 + , Hg2 + , Hg2 + , Sn1V, NO", AsV, MoV1, CIO", PtIV, Cu2+ и магний для восстановления Eu^+, NO" и Pt1^ .
* ** Цинковая амальгама получается нагреванием смеси ртути н цинка (100:3) при 100е С с разб H2SO4.
Неорганические реактивы
Реактив Действие реактива Определяемые ионы (вещества)
ВаСО3 (суспензия) Осаждение Fe3+, А13+; Ti'v, Zr4+, Crs+, (JO2+ (PG3’ и VO” в при-сутствии перечисленных катионов)
FeSO, Восстановление Au111, NO~, Sevl, Crvl, C1O~, CIO-, Vv, S2O2~, Mnlv,vl,
RhIV, Pdlv
нсю4 Осаждение K+, Rb+, Cs+, Cd2+
н3РО2 Восстановление, осаждение As!ii,v, Nbv, Tav, Cu2+, Telv, Ag+, AuIH, Hg2+, Bi3+, Sb111, Sc3+, Zr4+, Th4+
Н2о2 Окрашивание, осаждение Au111, Ce3+, Ti4+, Zr4+, Hf4+, Th4+, Nbv, Crvl, Movl, UO?+, F“, T1
н, [Р (Мо3О1с)4) Окисление, окрашивание Ce3T, Tl+
52
Реактивы для отдельных групп ионов
Продолжение
Реактив Действие реактива Определяемые ионы (вещества)
IL [PtCle] Осаждение K k, Rb+. Cs+, NH+ Т1+, Cd2+
Hg2 (NO3)2 Восстановление Au111, Crvl, Movl, Vv, WV1, Fe3+ , Ce4+, Br2, BrO-, BrO-, Cu2+, MnO;, s2o2-, cio-
JC1 + CC14 Окисление As111, Sb1", Fe2+, SCN-, CN-, [Fe (CN)6[4-, J-, SO2-, N2H4, NH2OH, H2O2, Sn2+, Tl+, Selv
KBrO3 + KBr Окисление (бромирование), осаждение Ионы, осаждаемые оксихинолином; ионы, осаждаемые при pH < 2,7; А13+, Сг3+, Со2+ , Ni2+, Pd11, Rh111, Ir111
K2CrO4 (или К;.Сг2О7) Осаждение Ba2+, Sr2+, Ra2+, T1+, Pb2+
К3 [Fe (CN)eJ Окисление Tl\ Sn2+, Vlv, H2O2, Mov, Mn2+ , Fe2+, S2-. As1'1, N2H4, NH2OH
kjo3 + kj Осаждение Al3+, Cr3+, Fe3+, Co2+, Ni2+, Sn2+
MgCl2 » PO3", AsO3-
NaJO4 Окисление Hg2+, Sn2+, N2H4, SCN-, As"1, Sb"1, S2-, Telv. J-, Fe2+
nh4scn Окрашивание Fe3+, Co2+, UO2+, Rev", Ru"1-OsIV, Mov, WVI
(NH4)2[Hg (SCN)4J Осаждение (для микрохимических определений) Zn2+, Cd2+, Tl+, Co2+
(NH4)[Cr(NH3)2(SCN)4.H2O (соль Рейнеке) То же Cu2+, Hg2+> T1+, Ag+
(NH4)2 S2O8 Окисление Ce3+, Cr3+, Mn2+
.(NH4)2 Mo04 Осаждение Th4+, Gelv, Snlv, Pb2+, PO3-, AsO3-
n2h4 • H2SO4 Восстановление Cl2, Br , J2, BrO- JO,-, JO-, [Fe(CN)6]3-, Cr2O2-, VO-, Fe3+, Ag+, Au"1, Cu2+, Hg1,11, Selv, Telv, Cl4+, Pt-металлы, Rev"
Na3 [Co (NO2)6[ Осаждение K+, Rb+> Cs+, Tl+, NH/ 4
53
Реактивы для отдельных групп ионов
П родолжение
Реактив Действие реактива Определяемые ионы (вещества)
Na2HAsO4 NaN3 Na;S2O3 (CH3COO)2Pb PbO2 или Pb3O4 SnCl2 T1NO3 ZnO Осаждение Восстановление Осаждение Окисление Восстановление Осаждение (для микрохимических определений) Осаждение Органические реак Ti41, Th4+, Zr4 \ Hf4+ S2”, Se2~, Te2“, SCN-, S2O2 ' Ag+, Snlv, Sb111, Al3+, Fe3", Cr3+, H2S CrVI, MoVI, Vv Ce3+, Mn2+, Au111, Ag+ Au111, Pb24, Hg1’11, Asv, Bi34, Nbv, Selv'vl, Teiv,vl, Movl, yyVI, Pt-металлы Cl-, Br-, J-. Au111, Ptlv, карбонатные комплексные анионы, UO2+ и Th4+, Crvl, Vv, Movl, WVI Fe3', Cr3+, WVI, Vv, Movl, TiIV, Al3+, Cu2+, Tav, Nbv, Zrlv, SiO2~, PO3~ J 4 ТИВЫ
Реактив Действие реактива Определяемые нли маскируемые ионы
Алюминон Арсеиазо Бриллиантовый зеленый 2,3-Димеркаптопропа- нол п-Диметиламинобен-зилиденродамин Диметилглиоксим Дитиол Дифенилкарбазид Дифенилкарбазон Диэтилдитиокарбамат натрия Кристаллический фиолетовый Малоновая кислота * Ион F определяется Окрашивание » » Маскировка Окрашивание » » » » » » Маскировка по обесцвечиванию лака алю А13+ и F- * AI3+, Sc3+, P.3., Zr4+, HF+, In3+, Th4+, U4+ Sbv, Tl34 , Zn2+ (Ba2+, Hg2+) Al3+, As111, Bi3+, Cd2", Co2+, Cu2+, Fe3+, Hg2+, Mn2+, Pb2+, Sb1”, SnIV Ag+, Au + , Hg2+, Pd2+, Cu+, Pt4 + Ni2+, Pd2 + , Fe2+, Co2 + Snlv, WVI, Movl, Bi3" CrVI,Hg2+,pb2 + ,Cd24,Cu2+ Hg2+, Ag+ Cu2+, UO2+, Ni2 + Sbv, Zn2+, Tl3+, Cd2+, Hg2+ Al3+, Cd2+, Co2+, Fe, Ni2+ минона c Al3+.
«54
Реактивы для отдельных групп ионов
Продолжение
Реактив Действие реактива Определяемые или маскируемые ионы
Метиленовый синий Обесцвечивание с вое- Се3+, С1О3-, Сг3+, Со2+,
становителями или с Cu2+, CN~, [Fe(CN)6]3~,
сильными окислителями; восстановленный Fe3+, Mn2+, Hg1- n, MoVI.
реактив при действии O2, CIO;, MnO~, s2o2~,
слабых окислителей Revn- H2O2, Ag+, Sn2+»
становится синим Vv
Метиловый фиолетовый Окрашивание Sbv, Zn2+, Cd2+, Tl3+, Hg2+
Морин Флуоресценция Al3+, Ga3+, Zr4+, Th4+
(менее чувств, опр. Be2+. Cd2+, ln3+, Pb2+, MoVI,
Sc3+, Zn2+)
Муравьиная кислота Маскировка SO2-, NH+, CN~
а-Нитрозо-Р-нафтол Окрашивание Co2+, Fe3+, Pd2+, Cu2 +
(Ag+, Au111, B1», Cr3+, MoVI, Ti4 , Vv, WVI, Zr4+)
Нитрон Осаждение ReO- NOT, CIO", CIO, ,
WVI, Bin
Пикролоновая кислота » Pb2+, Ca2+, Sr2+, Mg2+, Th4+
Пирогаллол » Bi3 1 Sb3+, B111, Tav, Nbv
Родамин С Окрашивание Sbv, Zn2+, Ga3+, T13+,WVI,
Movl, Bi3 ’, Co2+, Nbv, Tav, Au111, Mn2+, Hg"
Салициловая кислота Маскировка Al3 +
Салициловая кислота, Окрашивание Fe3+, Cu2+, Pd2+ Be2+,
салицилальдоксим Ce4+ Zr4+ Al3+, Be2+, Cr3+, Cu2+, Fe3+, Mn2+, Ni2 +
Сульфосалициловая кислота Маскировка
Тиогликолевая кислота » Fe2+, Wvl, Sn2 r, Cu2+
Тиомочевина Окрашивание, маски- Asv, Bi3+, Fe3+, Sb1”’ v
ровка IrIV, OsIV, Rhin, Ru111, Revn
Триэтаноламин Маскировка Al3+, Bi3+, Cr3+, Fe3+, Hg,
Mg2+, Mn2+, Pd2+, Sn2+
Тирон (4,5-дигидрокси- » Al3+, Ce3+, Cr3+, Fe3+,
л-бензолдисульфоно-вая кислота, дина- Mn2+,MoVI, Ti4+, Vv, WVI
триевая соль) Торон Окрашивание Th4+, F" (->бц.) Al3+, Сг3П Pb2 +
Уксусная кислота Маскировка
Фурилдиоксим Окрашивание Ni2+, Pd2+, Pt44-
5&-
Реактивы для отдельных групп ионов
П родолжсние
Реактив Действие реактива Определяемые или маскируемые ионы
Хинализарин Окрашивание Ве2+, В111, Mg2+, А13+, Ga3+, Са2+, Се3+, GeIV , In3+, La3+, Nd34-, PO3", Sc3+, T1+, Th4+, Sn4+, Zr4+, F~, HI”
Хромоген черный ЕТОО » См. стр. 407
Хромотроповая кислота, динатриевая соль » Ti4+, CrVI
Цинхонин Осаждение Ir, Movl, Pt, WVI
Цнклогексаидионди-оксим-1, 2 Окрашивание Ni2+, Fe2+, Pd2+
pH ОСАЖДЕНИЯ ГИДРООКИСЕЙ
Многие ионы могут быть разделены на основании различия значений pH осаждения их гидроокисей. В таблице приведены ориентировочные значения pH осаждения различных ионов в виде гидроокисей, а также реактивы, позволяющие отделять группу элементов, осаждаемых при данном (указанном в таблице) или меньшем значении pH, от элементов, осаждаемых лишь при больших значениях pH. В некоторых случаях в скобках приведены более точные значения pH осаждения данного иона. pH осаждения гидроокиси зависит от концентрации иона (см. «Справочник химика», т. III. стр. 755 и сл.).
Принятые сокращения см. стр. 16.
Последовательный ряд осаждения гидроокисей из кислого раствора
pH pH
начала осажде- Осаждаемые иоиы начала осажде- Осаждаемые ионы
НИЯ НИЯ
~0 Sb'11, Sbv, Sn4+, Movl, WVI, ~6 Cu2+(5,5), Be2+, Sc3+(5, 9),
Gelv, Ti4+ Zn2+, Ru'“, Rh"1 и Pd"
~ 1 Nbv, Tav(0,6), Ce4+(1,2), TJ3 + (из Cl-комплексов; Pt при этом не осаждается)
~2 Oslv, Zr4+, Hf4+, Sn2+ , ~7 у!+ (6,8), Sm3+, Fe2+,Ni2+,
Fe3+(2,3), Hg2+, Bi3+ (из хлоридов) Co2+, Ce3+(7,4), Pb2+(7,8) Ag+ (8,0), Cd2+, La3 + Mn2+ (8, 7)
~3 Hg2+, Ga3+, In3+, Th4+ (3,5) — 8 ~9
Al3+, U4+, IrVI, Ti3+ ~ 10 Mg2 +
~4 > 12 Ca2+ (12), Sr2+ (14), Ba2+ (14;
~5 Cr3+, MnIV, Bi3+, UVI при большой концентрации бария)
-56
pH ОСАЖДЕНИЯ ГИДРООКИСЕЙ
П родолжение-
Последовательный ряд осаждения лантанидов
pH начала осаждения Осаждаемый ион pH начала осаждения Осаждаемый ион pH начала осаждения Осаждаемый ион
6,1 Lu3+ 6,8 Gd3+ 7,4 Рг3+
6,3 Yb3+ 6,8 Eu3+ 7,6 Се3+
6,4 Tu3+ 6,8 Sm3+ 7,8 La3+
6,8 Ег3+ 7,3 Nd3+
Последовательный ряд осаждения
гидроокисей
из щелочного раствора
pH начала осаждения Осаждаемые ионы pH начала осаждения Осаждаемые ионы
> 12 Nbv, Tav (12,6), Pb2h (13,0) ~ 10 Ga3+ (9,7)
~12 Zn2+, Be2+ (12,0) ~9 MoVI, Wvl (9)
~ 11 Al3+, Sb3+ (11), Sn2+ nSn4+,
Cr3+ (11,5)
pH полного осаждения гидроокисей
Ион pH Ион pH Ион pH Ион pH
Ag+ 11 —13 Co2+ 9 —14 In3 + 6 —10 TaV 6—5 > 10!
Al3+ 5 —7,5 Cr3+ 6 —11 La3+ ~ 14 Th4+ 4 — 5 > 10.
Be2 + 7 —10 Cu2+ 8 — > 10 Mg2+ > 11 Ti<+ > 2
Bi3+ 7 —8 Pe3+ • 4 —14 Mn2 + 10 —14 uo*+ ~8
Ca2i- >14 Fe2+ 9 —14 Ni2 + 9 — > 10 Zn2+ 8 —10
Celr Ce3 p Cd2 - 3 — > 10 8 — > 10 >9 Ga3+ Hf4+ Hg2+ 4 —10 4 — > 10 5 —12 Pb2+ SnlV Sn2+ 9 —10 1 —13 4 —10 Zr4+ 4 — ; > 10»
57/
pH ОСАЖДЕНИЯ ГИДРООКИСЕЙ
Продолжение
Реактивы для осаждения гидроокисей
Реактив Методика осаждения рн осаждения
NH4OH + NH4C1 Анал. р-р (солянокислый) натр., добавл. NH4OH до изменения окраски мет. ор. или мет. кр. 7—9*
CH3COONa + + СНзСООН Анал. р-р (слабокисл.), CH3COONa, иагр. до 70° С 4—6*
NaHCO3 Анал. р-р (слабокисл.), р-в до изменения окраски бромфенолового синего, кип. 4
Пиридин Анал. р-р (нейтр.) NH4C1. Harp, до кип., добавл. р-в до изменения окраски мет. кр., р-в (изб.) нагр. 5 — 6,5
Уротропин Анал. р-р (pH=2-ч-4) нагр. до 30° С, добавл. NH4CI, p-в (изб.) 5-5,8
<>eHHarHflpa3HH Анал. р-р (слабокисл.) нагр., добавл. р-в ~5
Бензоат аммония Анал. р-р нейтр. по мет. .ор., добавл. СНзСООН, p-в. Нагр. и кип. ~6
ВаСОз К анал. р-ру добавл. суспензию свежеприготовленного р-ва, взбалт. иа хол. или при нагр. 7,3
•CdCO3 Осажд. как с ВаСОз 65
СаСОз » » » » 7,5
РЬСОз » » » » 6,2
2пО Взбалт. с суспензией ZnO 5,5
MgO Взбалт. с суспензией MgO 10,5
HgO » • » » HgO 7.4
К анал. р-ру (слабокисл.) добавл. р-в; нагр. ~6
КВгОз + НВг Анал. р-р, p-вы. Кип. до удаления брома 2,7
КВгОз + HCI То же 1.3
* pH зависит от соотношения концентраций реактивов-
58
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
В таблице приведены некоторые методы разделения ионов, не разделяемых обычными групповыми реактивами.
Выделяемые ионы расположены в первой графе таблицы в соответствии с периодически ii системой элементов.
Методы разделения данной группы ионов следует находить по первой графе для-каждого из разделяемых ионов. Например, методы отделения алюминия от бериллия следует находить по первой графе таблицы не только при алюминии (III группа), но и при бериллии (II группа). Ионы отнесены к выделяемым или к отделяемым условно^ в соответствии с методом выделения данного иона, указанным в третьей графе.
В четвертой графе приводятся реактивы в порядке последовательного прибавления их к анализируемому раствору (в случае добавления смеси между составляющими ее реактивами стоит знак «+»). После формулы реактива во многих случаях указывается его концентрация, получающаяся в анализируемом растворе.
Сведения об экстракционных, хроматографических и ионообменных методах разделения приводятся в специальных таблицах.
Принятые
ац. — ацетон
ацетац. — ацетилацетон
вак. — вакуум
выщелач. — выщелачивание, выщелачивают
диет. — выделяемый ион в дистнллате
ос. — выделяемый ион в осадке
сплавл. — сплавление, сплавляют
Остальные сокращения см. стр. 16.
сокращения
ф-т — выделяемый ион в фильтрате
хлф. — хлороформ
экстр. — выделяемый ион экстрагируется органическим растворителем
эл-лиз — электролиз (выделяемый ион на< электроде)
этац. — этилацетат
Выделяемый ион Отделяемые ионы Метод Реактивы
1.Г Na+, Li+ Na K+, Rb+, Cs+ Rb h, Cs + Rb K + Cs+ Cu2 + 1 группа периоди Na+, К+, Rb+, Cs+ (не отд. Mg2+) Na+, K+, Ba2+, Sr2+, (плохо отд. Rb+, Cs+, Mg2+; не отд. Ca2+) Na+, K+, Rb+, Cs+ K+, Rb+, Cs+ Li+ Na+ ,Li+ K+ K+ Cs+ Rb + K+, Rb+, L1+, Na+, Mg2+, Ca2+, Al3+ Bi3+, Cd2+ и др. GelV, SniV Cd2+, Zn2+ и др. Fe3+, MoO2- (не отд. Cd2+, Sb111, Sbv, Sn2+) ческой си ф-т экстр, (из сухих хлоридов) ос. экстр, (из сухих перхлоратов) ос. ОС. экстр, (из сухих хлоридов) ос. ос. ос. ОС. ф-т ОС. эл-лиз ОС. с т е м ы НС1 (конц.), эт. сп.-Ь -гэф. НО + ац. уротропин, Ka[Fe(CN)61 НСЮ^, бут. сп. 4-этац. нас. р-р НО в эт. сп.+ +бут. СП. H2PtCI6 (упар.), эт. сп.. (Pt выделяют из ос. и ф-та НСООН)- нас. p-р НО в эт. сп. фосфорномолпбдено-вая к-та р-р (NH4)2SO4 в эт. СП. H3SbCl6 или кремпе-вольфрамовая к-та 3KJ • 2BiJ3, лед. СНзСООН КОН, KCN, H2S HF или Н2С2О4, H2S HNO3 Al или Zn, H2SO* (разб.)
59
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Си2+ Cd2+, Pb2+, Hg2+, Hg2+, Mn2+, Zn2+,N12+, Mg2 + Co2+, Ni2+, Mn2+, Zn2+ ОС. а-нитрозо-Р-нафтол, HCI
ОС. винная к-та, H2SO4, SO|-, SCN"
AsO’-, Sn2+, Bi3+, Sb111, MoO2~, VO“, WO2- ОС. NaOH
Ag+ Большинство (не отд. Hg2+. Pb2+, Cu+, T1+, Pd2+) ос. HCI
- II группа периодической системы
Ве2+ Большинство (не отд. ТР+, UO|+) ос. Na-ЭДТА, NH4OH
То же ОС. Na-ЭДТА, (NH4)2HPO4 или (NH4)2HAsO4, ацетатн. буф. (pH=5)
А13+ и др. экстр, (из сухих хлоридов) HCI (конц.; выпар.), эф. или смесь аиетац.+ + СС14
А13+, Fe3+ и др. возг. вак. (200° С) -НСООН
Al3+, Fe3+ и др. (меш. TF+, SiO2) ф-т 8-оксихинолнн (уксуснокисл. р-р), ацетатн. буф. (рН = 7)
• То же экстр. ОТД. ИОНОВ 8-оксихинолнн (уксуснокисл. р-р), ацетатн. буф. (pH =7), хлф.
Fe3+. Zr4+, Ti4 + (не отд. А13+, Оа3+) ф-т NaOH
А13+ выщелач. А13 + Na2CO3 (сплавл. окис-лов),Н20 (выщелач.)
А13+ (малые кол-ва) ф-т CH3COONH4, NH4CI, таннин
Mg2+ Al3+, Fe3+, Са2+, Mg2+ ф-т NaF
Са2+ ф-т (NH4)2C2O4
Li+ Na+, К+, Rb+, Cs+ ОС. HgO. или (NH4)2CO3, или СаО, эт. сп.
<а2+, Sr2+, Na+, K+. Rb+, Cs+ (не отд. LI+) ф-т НС1, эт. сп. 4- эф. или амил. сп.
LI+, Na+, K+, Rb+, Cs+, ОС. (NH4)2CO3 или
Ва2 + Mg2+ (NH4)2C2O4
Са2+, Sr2+, Ва2+ Mg2+ (не отд. Pb2+) ОС. H2SO4, эт. сп.
Са2+ Mg2+ ОС. (NH4)2MoO4
Sr2+, Ba2+ экстр, (из HNO3 (выпар.), эт. сп.+,
сухих нитратов) +эф.
«о
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Са2+ Sr2+, Ba24 ф-т (NH4)2CO3, Na-ЭДТА
Большинство (не отд. Sn • V) ОС. ацетатн. буф. (рН=4), Na-ЭДТА, (NH4)2C2O4
Большинство (не отд. экстр- отд. 8-оксихинолин
Sr2+. Ва2+ Мп2+) ионов (рН = 4,9-=-5,1)
Са2+, Mg2+, Ве2+, нитраты (не отд. РЬ2+) ОС. IINO3 (до 8%)
Са2+ и др. ОС. ацетатн. буф. (pH = 4,5), Na-ЭДТА, (NH4)2SO4
Са2+ и др. ОС. диметилсульфат + глицерин
Ва2+ Са2+ и др. ф-т (NH4)2CO3+ СНзСООН (на ос.)
Sr2Л Са2+ ос. ацетатн. буф. (pH=4,5), СгО
Sr2+, Са2+ ОС. мочевина (рН = 5,7), СгО2'
Sr2+, Са2+ ос. NH4CI + NH4OH (pH=8), Na-ЭДТА, SO2'
Sr2+, Са2+, Mg2+ ОС. ацетатн. буф. (рН = 5), Na-ЭДТА , СгО2'
Sr2+, Са2+ ОС. HCI (~ 11 н.), бут. сп. или эф.
Sr24, Са2 + ОС. (NH4)2C2O4+(NH4)2SO4 (ос. прокал.). HCI
Zn2+ Fe8+, Мп24-, Cr34, AI34-, Ni2+, Ti4+, Zr44 ОС. Na2SO4+NaHSO4 (pH = 1,65), H2S
To же ос. С1СН2СООН + 4-СНзСООН (рН = =2,8), H2S
Fe3+, Ti4+. Zr4+, VO34-, Still, Sniv ф-т купферон, H2SO4
Oa3+ ОС. K2[Hg(SCN)4]
Cd2+ Zn24- ОС. H2SO4 (3 н.), H2S
Zn2+ эл-лиз Н2С2О4 или смесь KOH + KCN
Cu+, Hg24-» Ag4 экстр. NH4SCN, пиридин, хлф.
Hg2+ Cd24-, Zn2+, Bl3+, Cu2+ ОС. HCI, H2S, ос.+33°/о-ная HNO3
Bi3+ ОС. HCI, SnCI2
Cd24-, Cu24-, Zn2+ (плохо отд. Bi3+, Sb111, SeIV, TeIV) ос. HCi, Н3РО3
61
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
П родолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
ВО3~
А1з+
Ga3h
III группа периодической системы
Большинство » ДИСТ. ДИСТ. мет. сп., H2SO4 HF + H2SO4
Fe3+, TF+, Zr4+, Р. 3., ф-т NaOH или KNaCOs
Мп2+ (меш. Mg21-, Ni2+; (сплавл.)
не отд. РО’ и др. анионы) купферон, HCI или H2SO4
3- и 4-валентные катионы ф-т
То же экстр, отд. ионов купферон, HCI, хлф.
Fe3+, Ni2+, Со2+, Сг3+, ЭЛ-л из (отд. H2SO4 « 0,5%)
Zn2+, Оа3+, Cu2+, Sn2 + ионы на Hg-
и др. катоде; А13 + не ос.)
Fe3+ экстр. Fe3 + HCI (d= 1,14-1,115), эф.
Со2+, Zn2+, Ni2+. Cr2+, ос. НН4-бензоат (рН-=4);
Fe2 + ион Fe3+ восст. тио-гликолевой к-той
Be2+, Mg2+, BO|~ ос. 8.-ОКСИХИНОЛИН + аце-татн. буф. (рН = 5)
Be2+, Mg2+, ВО|- экстр. 8-оксихшюлин + ацетата. буф., хлф.
РО»-, AsO3-, ВО’-, ос. 8-ОКСИХИНОЛИН, NH4OH
CrO2-- WO2- 4 4
МоО2“, VO-, Ti4+ ос. 8-ОКСИХИНОЛИН + + NH4OH + H2O2
Fe3+, Ti4+, P. 3., Be2+, ос. (из НС1 (конц.), эф., НС1
Zn2+, Cu2+, Hg2+. конц. р-ра) (газ)
Hg2+, Oa3+, Bi3+, PO3-(меш. Na+, K+, Rb+, Cs+) Fe2 +
ос. фенилгидразин
2-валентные катионы ос. смесь KJ + KJO3, или NH4NO2, или янтарная к-та + мочевина . (pH»7,5)
Al3+, Be2+, Th4+, Zr4+, экстр. НС1 (6 н.), эф. или бу-
ln3+, P. 3., Fe2+ и др. тилацетат
(не отд. Fe3+, MoVI, Tl3+, Sbv, Sn", SnIV, Pt", Auin, OeIV, Asln, TeIV)
In3+, Zn2+. диет. (220е С) НС1
62
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Ga3+ 2-валентные катионы ОС. NH4OH, или пиридин, или тапнин
1п3+, Fe34-, Т14+ (не отд. А13+, Ве2г) ф-т NaOH
А13+, Сг3+, Mn2+, Cd2+, Pb2+, Bi3+, ТГ, Hg2 + (не отд. Zn2+, Zr4+, In) ОС. K4[Fe(CN)6], HCI
AI34-, ln3+, Zn2+ и др. (не отд. SnIV, TiIV, Zr4+, Vv, Fe3'1') ос. купферон
Ti4+, Zr4+, Th4+ и др. ОС. купферон, Н2С2О4
Vv. Movl, WVI ОС. 8-ОКСИХИНОЛИН+ NH4OH
1п3+ 2-валентные катионы ОС. ВаСОз или пиридин
Oa34-, Al3+, Zr*+ ОС. H2SO4, Zn
Al3+, Fe2+, Be24-, Ga3+ Большинство экстр. Ш (0,5—2,5 н.), эф.
ТГ ос. тионалид, тартрат-ион и KCN
Большинство (не отд. Cu2+, Ag4-) ОС. HCI; ион Т134 восст. SO2
Ag+ ф-т HCI + HNO3
Ga3+, In3+, Mn2+, Pb2+, Fe3+, Al3+, Cr3+ и др. ф-т NH4OH+НН4-сульфо-салицилат, НагНРО4
Oa3+, In3+, Fe3+, Al34-, Cr3 + ос. К2СГО4, NH4OH, сульфосалициловая к-та
Zn24-, Cd2+, Ni2+, Co2+, SeVI ос. К2СГО4, NH4OH
Т13+ Ga3 + ф-т SO2, NH4OH
Большинство (не отд. Au111-Fe3+, Sbv, SnIV, Ga3+, OeIV, Hg2+,MoVI, As111, Pt", TeIV) экстр. HCI (4 н.), эф.
Большинство (не отд. Auln> Sb111, Hg2 + ) экстр. НВт (1 н.), эф.
Sc3+ Большинство (не отд. часть Р. 3. и Th4+) ОС. Na2[SiF6]
Р. 3., Fe?+, Mn2+, UO^+, Zn2+ и др. ОС. NasSgOa
Р. 3. ос. пиридин (pH=5,4)
Th44-. Р. 3., Zr4+, Ti4+, Be24- и 3-валентные катионы (не отд. Y3+) ОС. винная к-та, NH4OH, Na2CO3
Th4+, Zr4+, Hf4+, Ti44-, Р. 3., Mn2+, Са2+, Mg24-(не отд. Со2+, MoVI, Revn) экстр. SCN”, НС1, эф.
La3+, Be24-, Al3+, Cr3+, Ti4+ (не отд. U44- иТЬ4+) экстр. трибутилфосфат, HCf
63
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Р. 3. Большинство (не отд. Th4+, Sc3+) ОС. Н2С2О4 (нас.), HCI (0,3 н.)
То же ОС. метилоксалат + НС1
Nbv, Tav, Ti4+, UO2+, Zr4 + и др. (не отд. Th4+, Sc3+) ОС. HF
Р. 3., подгруппа Се (3-валентные катионы) Sc34- ос. Na2SO4 (нас.)
Се3 + La3+, Movl, Y3+, Ho3+, Er3+, Dy3+ и др. (не отд. Th4+, Zr4+) ос. КВгОз, KJO3, HNO3
Остальные P. 3. ос. (NH4)2S2O8, ZnO
Еп3+ Остальные P. 3. экстр, амальгамой CHgCOONa, К-питрат, амальгама К
Остальные P. 3. эл-лиз (Hg-катод) H2SO4 «0,5%)
IV группа периодическом системы
SiO23- Большинство
Большинство (не отд. ВО~) ВО- Fes + (большое к-во)
Oeiv Большинство
Sn2+, SnIV Pb2+ » Большинство (не отд. As111, OsVI) As111- Asv, Sb111, Sbv Большинство Cu21 , MoVI и др. (не отд. As111, Asv, Sb111, Sbv) Большинство (не отд. WVI) Cd2+, Cu2+, Bi3+ и др. To же » »
Mn2+, Zn2+, NF+-, Co24-, Cu2+, Bi3+, Fe3+, Cr3+, Al34-, Ba2 +
ДИСТ. NaF+H2SC>4 (газ про-
ОС. И ДИСТ. пускают через р р NaOH) HCI (упар.), HF, H2SO4
дист. ВО' мет. сп.
диет. FeCl3 НС1 (упар.), НС1 (газ, 400—700° С) HCI; ионы As111 и Sb111
дист.
ос. предварительно окисл. таннип, . H2SO4 (0,5—
экстр. I н.), (NH4)2SO4 HCI (8—9 н.), СС14
ос. Н2С2О4 (или HF)+H2S
ос. Snlv буф. р-р (pH =1,5):
дист. НС1 или НВг (газ,
ос. 200' С) HNO3 (упар.)
ОС. H2SO4 (выпар.)
ОС. К2СгО4
ОС. NaOH (рН=7+10),
ОС. КВгОз тиомочевина
64
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ИО 1 Отделяемые ионы Метод Реактивы
Ti” Большинство (не отд. Be2’, Sn2’, РО2", U4') ОС. купферон, Na-ЭДТА (рН = 4,3-7)
То же ОС. купферон, винная к-та, НС1
Большинство (иеотд. SbIH, Bi3’) ОС. HCOOH+HCOONH4 (рН=2)
Большинство (плохо отд. Мп2’, Ст3’) ОС. Na-ЭДТА, NH4CI, NH4OH; ионы Be2’ и О4’ маек. (NH4)2CO8
Fe3’, Со2’, Ni2’, Zn2’ (плохо отд. Мп2’) ф-т винная к-та, NH4OH, H2S
Zr4’, Th4’ MoVI, Vv. РО2-, А13т, Be2’ ф-т Na-салицилат
ОС. NaOH
Ni2’, Co2’, Мп2’, P. 3., Fe2’ ОС. уротропин, NH4CI
Al3’, Zr4’, Hf4’, Th4’, Cr3’, Fe3+, UO2 \ Vv, Mn2+, Be2’ ОС. таннин, Н2С2О4, NH4CI
Zr”, Hf4 + Большинство (плохо отд. Nbv, Tav, Th4’, Fe3’; не отд. SnIV, Ce4’) ОС. Na2HPO4 или Na2HAsO4, H2SO4 (3,5—7 н.) или HCI (1—2 и.); ионы Ti4’, Nbv, Tav маек. Н2О2
To же ОС. C6HEAsO (ОН) 2, H2SO4; ионы Ti4’ и Nbv маек. Н2О2
Ti4’, Nbv, Tav ОС. NH4CI, НС1 (0,25 н.), таннин
Большинство (не отд. 4-валентные катионы) ОС. купферон+H2SO4 или НС1 (10 объемн. %)
То же экстр. купферон -f- H2SO4 (< I н.), хлф.
» » ОС. НС1 «0,6 н.), H2SeO3
Th4’, Fe3’, Р. 3. (подгруппа Се, 3-валентные катионы) ОС. фталевая к-та, НС1 (0,3 н.)
Th4’, Fe3’, Cr3’, Се3’, Ti4’, Sbv, Bi3’, P. 3. И др. ОС. миндальная к-та
Al3’, Fe3’, P. 3. ф-т (NbhJaCOg
Th44 РО2-, WO2” ОС. Na2CO3 или Na2O2 (сплавл.), Н2О
Fe3’, Zr4’ и др. (не отд. Р. 3., Sc3’, Y3’) ОС. HF
То же ОС. Н2С2О4, НС1 (0,3 и.)
Р. 3. (не отд. Zr4’, Ti4’) ОС. NH4NO3, Н2О2
5 Зак. 783
65
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Th<+ Р. 3., РО3-, Sc3+ (не отд. 4-валентные катионы) Р. 3., А13+ и др. Sc3+ Р. 3. и др. (не отд. Zr4+) Р. 3. Fe34-, А13+, Р. 3. (не отд. Zr4+) Большинство ОС. ОС. ОС. ОС. ОС. ф-т ОС. HNO3 (0,5—1 н.), KJO3 На28гО3, или уротропин, или пиридин NH4F H2SO4 (1:9), СбН5АзО(ОН)2 Na4P2O7+HCl (0,3 н.) (NH4)2CO3 8-оксихинолин, Na-ЭДТА
V группа периодической системы
nh4+ K+, NaT, Mg24-, Ca2+, Sr2+, Ba2 + и др. K+, Na+, Mg2+, Ca2+, Sr2+, Ba2+ и др. ВОЗГ. ДИСТ. НС1 NaOH, или КОН, или HC1 + HNO3
NO- No- ДИСТ. CO(NH2)2, или NaN3, или NH4C1
РО3~ Большинство (не отд. AsO3-, WO3-, VO"; меш. F-) ОС. (NH4)2MoO4 (избыток), HNO3
MoO2-, большинство катионов ос. MgCI2, nh4oh, nh4ci, лимонная к-та или Na-ЭДТА
MoVI, Wvl, Vv и др. ос. MgCl2+ винная к-та
Все катионы ф-т катионит
» » ОС. анионит
» » ОС. Zr4+, НС1 или H2SO4 (Юобъемн. %)
Все катионы, кроме ионов амфотерных элементов ф-т NaOH
1- и 2-валентные ионы ОС. FeCl3, ацетатн. буф. (рН=4 4-5)
As111, AsO3-4 РО3“ и др. (не отд. OeIV; меш. Wvl) ДИСТ. НС1 «108° С)
Sb111. Sbv- Sn11, SnIV и др. (не отд. OeIV, Mov', Hg2+, Hg3+, Cu3+) ОС. НС1 (10 н.), H2S
Fe3+. Cu2+, Pb2+. Cr3+, Vv, MoVI, Ni2+, Co2+, Sn2+, Sb111 ОС. Н3РО2
Большинство ДИСТ. * Zn
* Микрометод для малых (меньше 0,1 мг) количеств As.
6b
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Asin AsO’- Sbni Bl3+ Vv Nbv, Tav Sn'v. OeIV OeIV Sb'», Sbv. Sn2+, SnIV и др. (не отд. РО3-) Cu2+, Pb2+, MoVI Большинство (не отд. Cu2+, Ag+, Hg2+, Hg2+, Pb2+, Bi3+, Asln, Asv. Sb111. Sbv) Большинство (не отд. Bi34-, А.Ч1 AqV) Pb2+, Cu2+, Zn2+, Cd2+ Cd2+ Cu2, Hg2 + Pb2+, Cd2+, Cu2+, Zn2+, Al3+, Cr3+, Fe3+, Ni2+, Co2+, Ba2+, Ca2+, K4-, Na + Na4-, K+, Mg2+, Ca2+, Sr2+, Zn2+, Cd2+, Cu2+, Pb2+, Hg2+, Co2+, Ni2 + Большинство (не отд. 4-валентные катионы) Pb2+, Sb"1. SnIV ио2+ UO2+(не отд. СгО2-, МоО2-, РО3-, WO2-, AsO3-) Fe34-, Ti4+, Zr44- (не отд. РО’-, AsO’, МоО2-, СгО2-, UO2+, АР+-, sior) ио2+ Zr4+, Hf4+, Ве2+, А13+, Fe’+, Th4+, 1Ю2+ ОС. ОС. ОС. ДИСТ. (200° С) ос. ос. (100° С) * ос. ос. ос. ос. • ос. ос. ЭЛ-ЛИЗ ос. ОС. ф-т ф-т ОС. HCI, HF, H2S H2SO4 (0,05 н.), (NH4)2SO4 (1%). H2s винная или лимонная к-та, Mg2++NH4OHp + NH4C1 H2SO4> S, Cl2 NaOH, Na2S2O4 медная пластинка, HCI (1:4) HCI или HBr, H2O H2SO4 (1:3), H2S (NH4)2CO3+NH4OH галловая к-та, HNOg (3%) пиридин (pH=4,2) купферон, HCI (1 н.) тартрат-ион+HCI или Н2С2О4 СНзСООН (после упар. р-ра) Hg(NO3)2 илиРЬ(1\Ю3)2 Na2O2 или Na2COs+ +KNO3 (сплавл.), Н2О (выщелач.) Na2HPO4, NH4OH K2S2O7 сплавл., раств. в винной к-те или Н2С2О4 (pH > 4 н-4,5), таннин или пирогаллол, NH4C1
* Микрометод для небольших (1—2 мг) количеств Sb.
5*
67
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Nbv, Tav Nbv Zr4 + Большинство Tav, Sb111, SnIV (плохо отд. Ti4+) ф-т экстр. ОС. К2СО3 (сплавл.), Н2О (выщелач.) H2SO4(3 Al), HF (ЮМ), метилпзобутнлкетон впивая к-та (рН = 6,5), 8-оксихинолпн
VI группа периодической системы
s2- s2or ОС. CdCOa
SeO2-, Большинство (не отд. Au111) ОС. SO2, HCI (2—2,5 н.)
Те°2~ То же ОС. SnCl2, HCI (2—2,5 н.)
» » ОС. N2H4. HCI (0,6—1,2 и.)
» » ОС. гипофосфит, HCI (6 н.)
Большинство (не отд. дйст. НВг + Вг2 или НС1 + С12
As111, Sb111, OeIV)
ТеО2' Se°r ос. Na2SC>3
SeO2~ ТеО2" ДИСТ. H2SO4 (конц.), HCI (газ,
300° С) или НВг
ТеОГ ОС. (200° С) NH2OH, HCI (5 н.)
ТеО2~ ОС. N2H4, HCI (5,5 н.)
Сг3+ Fe3+, Ti4+, Zr4+, Ni2+, ф-т NaOH или смесь
Co24-, Сп2+ и др. (не отд. Na2CO.4+KNO3
Al3+, AsO3", МоО2~, (сплавл.), Н2О (вы-
шелач.)
WO2- VO- и др.)
Большинство ДИСТ. HCI, НСЮ4
МоО2" Большинство (не отд. Wvl, ОС. Na-ЭДТА, ацетатн. буф.
Vv, Ti4+, LTVI) (рН=3,6->7,3), 8-ок-
сихинолнн
Nbv, Zr4+, UO2+, Cr3+, Cu2+, Ni2+, Tl4+, Fe3+, ОС. (NH4)2C2O4. H2SO4
(pH =2 4-З), 8-окси-
WVI, Revn хинолин
Большинство (не отд. WVI, Nbv, Tav, Pav) ОС. а-бензоиноксим, H2SO4 (20%); ионы CrVI и Vv предварительно
восст.
To же экстр. а-бензоиноксим, H2SO4
Cn2b, Mn2+, Ni2+, Co2+, (20%), хлф. НО (6 н.) или H2SO4
экстр.
Cr3+, Al3+ (не отд. Fe3+, WVI, VV, ReVII) (6 н.), ацетац.+хлф.
Большинство ДИСТ. НО (газ, 250—300° С)
68
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
МоО2-1 VO-, WO2- ос. винная к-та, NH4OH, H2S, H2SO4, H2S
Сп2+ и др. (не отд. Vv, WVI, Crvi, Asv) ОС. Pb(CH3COO)2, CH3COONH4, CH3COOH
Sbln, Sbv (большие кол-ва) и др. ф-т Pb, HCI
Малые кол-ва WO2~, VO3~, РО3~, AsO3’, Sbni, Sbv, Fe3 + (меш. Pb2+) ф-т Fe3+, NH4OH
WO?" 4 PO3' и др. (не отд. SiIV, Nbv, Tav) ОС. HNO3, цинхонин или таннин
Si°|~ дист. SiF4 HF
Большинство ОС. а-бензоиноксим
» экстр. а-беизоиноксим, хлф.
Большинство (не отд. MoVI, CrVI, Vv,) ф-т Na2CO3 (сплавл.), Н2О (выщелач.), MgSO4 + + NH4OH+NH4CI
Nbv. Tav ф-т таннин
Большинство (не отд. MoVI, Ti4+, Vv) ОС. СНзСООН (рН=3.6), Na-ЭДТА, 8-оксихи-нолин
UQ2+ Fe3 + , Al3+, Ti4 + и др. (не ф-т (NH4)2CO3, или
2 отд. Zr4+, Th44-) (NH4)2S+(NH4)2CO3, или (NH4)2S+Tap трат-ион
Ca2+ и др. ОС. уротропин, H2S
Th4+, P. 3., AF+, Fe3+, ZrIV, Vlv, Bi3+, PO3“, 2-валентные катионы и др. (не отд. Be24-, Ti4+) ОС. СНзСООН, Na-ЭДТА, CH3COONH4 (рН= =5,3), 8-оксихинолин
Vv, Fe3+, Ti4+, Zr4+, U4+ ф-т H2SO4, купферон
Большинство (меш. SO2-, СГ, PO3-) экстр. HNO3, эф.
Большинство (не отд. Auln,-Celv, Th4+, Asv, Bi3~, Ti3+. Zr4+, Hg24-, CrVI) экстр. HNO3, метилизобутил-кетон
и4+ Большинство (не отд. Th44-, P. 3.). ОС. HF
Большинство (не отд. Th44-, Zr'+) ОС. н4р2о7, HNO3
69
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
U4+ А13+, Сг3+, Мп2+, РО3', ио*+ ОС. H2SO4, купферон
VII группа периодической системы
F“ Cl , Вг , J и др. (не ОС. Са2+
отд. РО3", CrO2', SO2') Большинство дист. SiOa, H2SO4 или НСЮ4 AgNO3, HNO3
СГ, ВГ Большинство (не отд. ОС.
Вг-, J- CN~, SCN“; меш. SbIn, Sn2+, PtIV, Cr3+, Hg2+) cr ОС. Ag4[Fe(CN)6]
J- СГ, Br- ДИСТ. NO2 , илн Fe3+, или
er, ВГ ОС. смесь Fe2+ + CrO2-Pd2+
Вг“ cr дист. H2TeO4 (или KMnO4) 4-
cr дист. + СНзСООН КН(ЗОз)г + ННОз
Вг2 •I2 восст. НСООН
Мп2+ Большинство ОС. HNO3, КСЮз NH4OH, NH4C1
Fe3+, Al3+ ф-т
Zn2 + ф-т СНзСООН или НСООН,
VO-, MoO2- ОС. H2S NaOH, НагО2
Cr3+ ОС. NaOH, K2S2OB
ReO~, Re3+ Большинство . дист. H2SO4, HNO3 ИЛИ Н3РО4
Большинство (не отд. (200° С) экстр. метилэтилкетон, NaOH
SeO2-, OeIV, AsO?“) 3 4 J MoO2" 4 экстр. (3,5 и.) или ИагСО» (3,5 н.) тетрафениларсоний.
VIII группа период ической с хлф. и с т е м ы
Fe3+ Al3+, Be24-, Ti4+, Zr4+, ОС. НН4-тартрат, (NH4)2S
Nbv, Tav, UO2+, Vv, РО3' и др. VO- WO2-, MoO2-, ОС. NaOH
AsO3“, Al3+, PO3' Ti4+, Zr4+, Al3+, Cr3+, экстр. HCI (6 н.), эф.
Ве2+(не отд. Oa3+, Au111, OeIV, As111, TeIV, Pt", MoVI, Tl3+, Sbv, Sn2+, SnIV)
70
НЕКОТОРЫЕ ЧАСТНЫЕ МЕТОДЫ РАЗДЕЛЕНИЯ ИОНОВ
Продолжение
Выделяемый ион Отделяемые ионы Метод Реактивы
Fe3+ Zn2+, Mn2+, Ni2+, Co2+ ос. ВаСОз, или СНзСООЫа, или мочевина
Со2+ Ni2+, Zn2+, Mn2 + ОС. KNO2,CH3COOH(pH=3)
Fe3+, Tl4+, Zr4+, Hf4 + ф-т Na2HPO4 (рН=3,5)
Большинство ОС. а-нитрозо- Р- на фтол
Ni2+ Большинство (не отд. Pd", Fe2+. PtIv. Au111) ОС. диметилглиоксим
3- и 4-валентные катионы ф-т nh4oh
Мп24- эл-лиз NH4OH, (NH4)2SO4
Pt-металлы In3+, Cu2+, Zn2+, Ni24-, Co24-, Cr3+, Fe8+ н др. (не отд. Pd11) ф-т NaNO2, NaOH или Na2CO3 (pH=10)
Au111 ф-т NaNO2 (pH = 8), илн SO2, или N2H4 • HCI, или H2C2O4, или гидрохинон-!-HCI (1,2н.)
Au'» Последовательно выделяются: экстр. АиШ эф. или этац., HCI
Os дист. OsO4 HNO3
Ru дист. RuO4 КВгОз
Pd, Rh, Ir или ос. КВгОз (рН=8)
Pd ос. диметилглиоксим
Rh ос. ЛС1з
Pt, Ir ос. nh4ci
Pt'v, Pd" Ионы неблагородных металлов ос. Н2С2О4, H2SO4
Pt'v, Ir'v Rh»1, Pd» (хуже отд. Os'v, Rulv, Ru1», Ir»1) ос. NH4C1
Ir'V Pt'v, Pd", Rh'» (не отд. ионы благородных металлов) ф-т HCI, NaHzPOz, Hg2+
То же ф-т TiCIs
71
Экстракционные методы разделения
Для описания распределения вещества между водной фазой и не смешивающейся с ней органической фазой используется коэффициент распределения D, который представляет собой отношение концентрации вещества в органической фазе к концентрации его в водной фазе. Степень извлечения Е выражается в процентах. С коэффициентом D эта величина связана следующим соотношением;
р , 100 D
V
Г, . водн ——
орг
где ^ВОдН н %рг— соответственно объемы волной н органической фаз.
Приведенные данные всюду, где это специально не оговорено, относятся к случаю, когда = 1'0рГ и £—100%. Концентрация экстрагента выражается в моль!л (М) или в объемн. %.
ЭКСТРАКЦИЯ ФТОРИДОВ
Экстрагируемый элемент Водная фаза Органическая фаза Е, %
Ag 20 M HF Диэтиловый эфир 0,05
Al 20 M HF » » 0,2
Asni 20 M HF » » 37,7
4,6 Л1 HF * » » 62
AsV 20 M HF » » 13,6
Be 20 M HF » » 4,0
Cd 20 M HF » » 1,4
Co 20 M HF » » 1,7
Cr hi 20 M HF » » <0,1
Cun 20 M HF » » 1,3
Fell 20 M HF » » <0,1
Fel" 20 M HF » » < 0,1
Oa 20 M HF » » < 0,05
OeIV 20 M HF » » 6,7
HgU 20 M HF » » 2,7
In 20 M HF » » <0,05
Mnll 20 M HF » » 1,3
MoVI 10 M HF+ 6 M H2SO4 + Метилизобутилкетон 9,7
+ 2,2 Л/ NH4F *»
3,5 M HF * Днэтиловый эфир 9,1
20 M HF 9,3
Nbv 6 M HF + 6 M H2SO4 ** Дииэобутилкарбинол 98
10 M HF + 6 M H2SO4 + Метилизобутилкетон 96
+ 2,2 M NH4F.**
20 M HF Диэтиловый эфир 65,8
Ni 20 M HF » » 0,7
ReVH 20 M HF » » 61,8
Sb111 20 M HF » » 6,3
Sbv 20 M HF » » 0,1
Seiv 4,6 M HF * » >> 3,1
20 M HF » » 12,9
Snii 4.6 Л1 HF* » » 100
20 M HF » » 4,9
Sniv 1.2—4,6 M HF* » » 100
20 M HF » » 5,2
с указанным видным
* Органическая фаза предварительно приведена в равновесие раствором HF, не содержащим экстрагируемого элемента.
** Соотношение объемов водной н органической фаз 1 ; 4.
72
ЭКСТРАКЦИЯ ФТОРИДОВ
Продолжение
Экстрагируемый элемент Водная фаза Органическая фаза Е, %
TaV 10 M HF + 6 M H2SO4 + Метилизобутилкетон 99,6
+ 2,2 M NH4F *
0,4 M HF + 3,7 M HCI * Динзопропилкетон 81
0,4 M HF + 3,9 M HNO3 * » 79
0,4 M HF + 4,5 M H2SO4 * » 95
0,4 M HF+ 4,6 Al HCIO4* » 90
20 M HF Диэтиловый эфир 79,3
Teiv 20 M HF » » 23
Tiiv 20 M HF » » < 0,05
Tl1 20 M HF » » < 0,05
Uvi 20 M HF » » М
vin 20 M HF » » 12
Vv 20 M HF » » 8,5
WVI 10 M HF + 6 M H2SO4 + Метилизобутилкетон ~26
+ 2,2 M NH4F *
20 M HF Диэтиловый эфир 0,5
Zn 20 M HF » » 0,9
Zr 20 M HF » » 2,9
* Соотношение объемов водной и органической фаз 1:4.
ЭКСТРАКЦИЯ ХЛОРИДОВ
Экстрагируемый элемент Водная фаза Органическая фаза Е, %
Asin 11,4 Al HCI Днизоамиловый эфир 79,1
11 M HCI Бензол 94
6 M HCI Диэтпловый эфир 6S
AsV 6 M HCI » » 2—4
6 M HCI Этилацетат 87,5
6,5—8,5 M HCI Динзопропиловый эфир 99,5
Auin 10% HCI Этилацетат 100
6 Al HCI Диэтпловый эфир 95
Насыщ. KCI; pH = 2-+6 Бутиловый спирт Следы
Со 4,5 M HCI 2-Октанол 9,1
0,85 M CaCI2 » 9,1
CrVi 3 M HCi * Метилизобутилкетон 100
1—3 M HCI Метплпропилкетон > 95
Fein 8—11 A'l HO Метилбутилкетон + бензол 99
(2: 1)
6 Al HCI Диэтпловый эфир 99
7,75—8,0 M HCI Динзопропиловый эфир 99,9
9 M HCI ₽, р'-Дихлордиэтиловый 99
эфир
• Соотношение объемов водной и органической фаз 1 ; 2,5.
73
ЭКСТРАКЦИЯ ХЛОРИДОВ
Продолжение
Экстрагируемый элемент Водная фаза Органическая фаза Е,
Petit 8 M HCI Метила милкетон 100
Оа 4 M HCI Диэтиловый эфир 71
8 M HCI » » 97
8 M HCI Диизопропиловый эфир 82
8 M HCI Дибутиловый эфир 65
9,0 M HCI Диизоамиловый эфир 77,7
12,1 M HCI » » 1С0
3 M HCI Трибутилфосфат 99,9
OeIV 6 M HCI Диэтнловый эфир 40—60
10,5 M HCI Четыреххлористый углерод 99,5
11 M HCI Бензол 99,6
HgU 0,125 M HCI Этплацетат 80
0,1 M HCI Трихлоруксусная кислота (3 А1) в бутилацетате) 82—89
6 Al HCI Диэтиловый эфир 0,2
In 8 M HCI » » 23
8 M HCI Диизопропиловый эфир 8
8 M HCI Дибутиловый эфир 1
Movt 6 M HCI Диэтиловый эфир 80—90
7,75 M HCI Диизопропиловын эфир 21
5 Al HCI Амилацетат 99
Nbv 11 M HCI* Диизопропилкетои 90
Ni 4,5 M HCI 2-Октанол 0,14
0,85 M CaCh г» 0,99
PaV 6 M HCI+ 8 M MgCl2 р, Р'-Дихлордиэтиловый эфир 90
6 M HCI * Диизопропилкарбинол 99,9
Pt” 3 M HCI Диэтиловый эфир >95
SbIl[ 6 M HCI » » 6
6,5—8,5 M HCI Диизопропиловый эфир 1,6
Sbv 11,9 Al HCI Диизоамиловый эфир 0
11,1 M HCI » » 99
6 Al HCI Диэтиловый эфир 81
6,5—8,5 M HCI Диизопропиловый эфир 99,5
Snii 6 Al HCI Диэтиловый эфир 15—30
SnIV 6 Al HCI » » 17
TeiV 6 Al HCI » » 34
Tl111 6 Al HCI » » 90—95
Vv 7,75 Al HCI Диизопропиловын эфир 22
* Органическая фаза предварительно приведена в равновесие с водной фазой, не содержащей экстрагируемого элемента.
74
ЭКСТРАКЦИЯ БРОМИДОВ
Экстракция диэтиловым эфиром из водных растворов бромистоводородной кислоты
В таблице приводится степень извлечения Е в 7о. Исходная концентрация нзвлекае-мых элементов 0.1 моль!л.
Экстрагируемый элемент Концентрация НВг, моль/л
1 2 3 4 5 6
Asin 3,0 6,7 22,8 63,1 72,9
Auin 99,5 99,9
Cd 0,4 6,9
Со 0,01 0,08
CuU 0,5 1,5 4,2 6,2
Fe”l 0,1 1,4 55,0 97,1 97,1 96,6
(та 0.9 1,5 54,8 96,7 95
HgH* 3,4 2,3 1,5
In 15 85,2 98,6 99,9 99,4 93,5
MoVI 0,16 28 25,0 54,1
MoVI ** 8,8 32,6 -
Ni >0,03 . . . > 6,03
Sb111 37,9 22,3 14,9 9,0 6,1
Sbv - 95,4 79,6
Seiv 0,3 3,5 18,3 31
Snii 32 64 79 84 78 36
Sniv 11,5 45,2 73,6 85,4 77,4 45,1
T|IH > 99,9 >99,9 > 99,9 99,0
TelV 0,7 . . • 2,2
Viv ~ 0,001 — 0.001
wvi *** 68,0 50,0
Zn 1,3 5,0 4,9 3,6
* При концентрации НВг 0.1 моль!л £'=58,3°/о-
** Исходная концентрация Мо^в водном растворе 2,1 • 10 молъ!л.
*** Исходная концентрация W^b водном растворе 1,2 • Ю”4 молъ!л.
Экстракция метилпропилкетоном из водных растворов бромистоводородной кислоты
Приведенные данные относятся к экстракции мнкроколнчеств элементов прн концентрации НВг 4,5 молъ!л.
Экстрагируемый элемент E. % Экстрагируемый элемент E, % Экстрагируемый элемент E, % Экстрагируемый элемент E, %
Ag 3,3 Crin 5,0 1 ln 100 Sniv 75
Ca < 1 CuU 5,8 1 Ni 3,0 Три 100
Cd 36,6 Fein 39,2 Pb 14.8 Zn 18,4
75
экстракция иодидов
Соотношение объемов водной и органической фаз для диэтилового эфира равно 1 : 4, для остальных органических растворителей 1:1.
Экстрагируемый элемент Водная фаза Органическая фаза Е, и
AsHi 6,9 M HJ Диэтиловый эфир 62
Аиш 6,9 M HJ » » 100
Bi 6,9 M HJ » » 34,2
1,5 Л1 KJ, 1,5 h. H2SO4 » » < 10
Cd 1,5 M KJ, 1,5 u. H2SO4 » » 100
6,9 M HJ » » 100
Си» 1,5 M KJ, 1,5 h. H2SO4 » » < 10
HgU 6,9 M HJ » » 100
1,5 Л1 KJ, 1,5 h. H2SO4 » » 33
In 1,5 M KJ, 1,5 h. H2SO4 » » 100
6,9 M HJ » » 7,8
MoVI 6,9 M HJ » » 6,5
Pb Избыток KJ в 5% HCI Метилизопропилкетон 97
Pd11 Четырехкратный избы- Метилизобутилкетон 100
ток KJ в 20% H2SO4
TeiV 6,9 M HJ Диэтиловый эфир 5,5
TI1 0,51 М HJ » » 99,9
HUI 0,51 М HJ » » 100
Zn 6,9 М HJ » » 10,6
1,5 М KJ, 1.5 н. H2SO4 » » 33
ЭКСТРАКЦИЯ РОДАНИДОВ
Экстракция диэтиловым эфиром из водных растворов роданистого аммония
В таблице приводится степень извлечения Е в - %. Исходные водные растворы содер* жали 0,1 молъ}л извлекаемого элемента и 0,5 моль[л HCL
Экстрагируемый элемент Концентрация NH4SCN, моль’л
0,5 1,0 2,0 3,0 5,0 6,0 7,0
А1 1,1 9,0 19,5
Asin 0,4* 0,4*
AsV 0,1 0,03
Be 3,8 24,3 49,7 84,1 92,2
Bi 0,3 • 0,1
Cd 0,1 ** 0,2 ***
Co 3,6 37,7 58,2 74,9 75,2
Crin 0,06 ** 3,4 **
Cui 2,9 0,4
Fein . . . 88,9 . . . 83,7 75,5 53.3
* Концентрация НС1 0,8 моль!л.
** Соотношение объемов водного
*** Соотношение объемов водного
раствора и диэтилового эфира 1 : Ю. раствора и диэтилового эфира 1 : 6.
76
ЭКСТРАКЦИЯ РОДАНИДОВ
Продолжение
Экстрагируемый элемент Концентрация NH4SCN, моль!л
0,5 1,0 2,0 3,0 5,0 6,0 7,0
Оа 18,3 65,4 90,5 99,3
Oeiv < 0,3 . . . < 0,5
Inin 26,0 51,5 75,1 75,3 68,3 47,6
MoV 99,3 97,2 97,3
Pd11 1,7 <0,1
Sb1» Г ндролиз Гидролиз Г идролиз 2,2
Sc 12,7 55,4 79,8 . . . 89,0
Sniv 99,3 99,9 > 99,9 >99,9
Ti"1 14,7 58.8 80,5 84,0 79,8 76,3
T1iv 13,0
pjV! 45,1 41,4 29,4 13,8 6,7
Viv 10,7 15,0 13,1 8,7 2,2
Zn 96,0 . . . 97,4 94,8 92,8
Экстракция различными растворителями
Экстрагируемый элемент Водная фаза Органическая фаза Е, %
А1 3 Al NH,SCN; pH = 3 Амиловый спирт 41,2
Be 3 Al NH4SCN; pH =3 » » 81
Со 0,16 Al NaSCN, 0.5 M HCIO, Циклогексанон 99,3
1 Al NaClO4
0,16 Al NaSCN, 0.5А1НСЮ, Метилизопропилкетон 97,9
1 Al NaClO4
ГеШ NaSCN; pH = 2,1 Трибутилфосфат 97
0.1 Al KSCN Нзоамиловый спирт 85
IrIV [SCN'];[lriV] = 10:l; pH = 1 Трибутилфосфат 8,2
Nbv 1 Al NH4SCN, 1 Al H2SO4 Этилацетат 97,8
2 Al SCN', 1 Al H2S34 Нзоамиловый спирт 99
2 Al SCN , 1 Al H2SO4 Метилизобутилкетон 95
Pd" [SCN'l: [Pd"l = 10: 1; pH = 1 Трибутилфосфат 99,3
Pt" fSCN-]jPt"J = 10:1; pH = 1 » 98,4
Rh1" [SCN_l:[RhI"]= 10: 1; pH -= 1 » 16
Tav 4 Al SCN . 0,5 Al H.,SO4 Нзоамиловый спирт 99,5
2 Al SCN ', 1 Al H.,SO4 Этилацетат 99
Ti,v 5 Al SCN-, 2 Al H,SO,+ » 89,5
3 Al HCI
5 Al SCN , 2 Al H2SO4 ^Метилизобутилкетон 41,7
3 Al HCI
77
ЭКСТРАКЦИЯ ОКСИХИНОЛИНАТОВ
Звездочка означает, что соотношение объемов водной и органической фаз равно 5:1. Во всех случаях, кроме специально оговоренных,
Экстрагируемый элемент pH водного раствора Органическая фаза Примечания
растворитель концентрация 8-оксихино-лина, моль/л
А1 5—11,5 5,2—5,5 Хлороформ Четыреххлористый углерод 0,02 0,013
Ба 11,5 Хлороформ 1,4 £ = 90%
Be > ю Бутиламин (0,2 М) в хлороформе 1.0 £ = 100$о при экстракции > 1ч
Са 11,5 11,5 Хлороформ Бутиламин (0,2 Л1) в хлороформе 1,0 0,14
Cd 10,5—12 То же 0,001
9—11 Хлороформ 0,001 £ = 80%
СеШ 9,9—10,5 * » 0,07
Со 7—9 » 0,001
СгШ 6—8* » 0,02
СиИ 2,8—14 * 0,07
Fein 2—12,5* » 0,02
Оа 4—11,5 » 0,02
HgH 8—12 » 0,001
In > 4 0,02
Mg 11—13,5 Бутиламин (0,2 М) в хлороформе 0,007
Mnli 11—12 Хлороформ 0,001 Водный раствор содержит Na2SO3 (0.1 н.)
MniH 9—12 0,001 Водный раствор содержит тартрат натрия (0,1 н.) и K3[Fe(CN)6] (2- 10~4М)
MoVI 2—5 1,6—5,6 0,001 0,07
Nbv 3—10 * 0,02
Ni 8,7 8,7—12,5 » Бутиламин (0,2 М) в хлороформе 0,001 0,001
Pb 8,5—12.5 Хлороформ 0.01
Pd11 3,5 » 0,001 £« 7596
Sc 9,5—10,5 Бензол 0,002
Snii 7,5—9,5 Хлороформ 0,001
Sniv 2.5—5,5 0,07
Sr 11,3 11,4 Бутиламин (0,4 41) в хлороформе Хлороформ 0,35 1,0
TiIV 4—9* 0,02
Tflll 4—9* » 0,02
Th 7—10* » 0,02
rjvi 7—9,5 * 6,5—9,0 » » 0,02 0,002
78
ЭКСТРАКЦИЯ ОКСИХИНОЛ ИНАТОВ
Продолжение
Экстрагируемый элемент pH водного раствора Органическая фаза Примечания
растворитель концентрация 8-оксихнно-лина, моль!л
Vv WVI Y Zn 3,5—4 2 4,5* 7—8 8—12,5 4,6—13,4 Хлороформ » » » Бутиламин (0,008 н.) в хлороформе Хлороформ 0,001 0,01 0,02 0,2 0,02 0,027
ЭКСТРАКЦИЯ КУПФЕРОНАТОВ
Экстрагируемый элемент Водная фаза Органическая фаза
А1 Bi Cd Ceiv Со СиП Fein HgH In Mnll MoVI Nbv PaV Sb"1 Snil Sniv TiII Th UIV Vlv Vv WVI* Zn* Zr pH=2^-5 HCI или H2SO4 Нейтральный раствор pH = 2 Разбавленная уксусная кислота HCI (1 : 10) H2SO4 (1 : 10) Нейтральный раствор Разбавленная кислота Нейтральный раствор HCI (2:11) Кислый раствор 0,1—4 н. кислота H2SO4 (1 : 10) 1,5 н. HCI HCI (1 : 10) HCI (1 : 10) HCI (1 . 10) H2SO4 (1 : 10) 0,5 н. НС1 HCI или H2SO4 (1 : 10) HCI (1 . 10) Нейтральный раствор H2SO4 (1 : 10) Хлороформ Толуол, метилэтилкетон Диэтиловый эфир (при т. кип.) Бутилацетат Этилацетат, диэтиловый эфир Хлороформ Хлороформ, этилацетат, диэтнло-вый эфир Бензол, хлороформ » » Диэтпловый эфир Этилацетат, хлороформ Хлороформ Бензол, хлороформ, диэтпловый эфир Хлороформ Бензол, хлороформ Этилацетат Хлороформ, этилацетат, диэтиловый эфир Этилацетат, бутилацетат Диэтиловый эфир Этилацетат Диэтиловый эфир, этилацетат Этилацетат Диэтиловый эфир Этилацетат
* Извлечение неполное.
79
ЭКСТРАКЦИЯ ДИЭТИЛДИТИОКАРБАМАТОВ
Экстрагируемый элемент pH водного раствора Органическая фаза
Ag 3 Этилацетат
4—11 Четыреххлористый углерод
AsIH 4—5,8 » »
АцШ 4-11 » »
Bi 4—11 » »
1—10 Хлороформ, диэтиловый эфир
Cd 4-11 Четыреххлористый углерод
3 Этилацетат
Co 4-11 Четыреххлористый углерод
Crvi 0—6 Хлороформ
CuU 1—3,5 »
4-11 Четыреххлористый углерод
Feu 4-11 » »
Fein 4—9,8 » »
0-10 Хлороформ
Ga* 5,5 Четыреххлористый углерод
3 Этилацетат
HgU 3 »
4-11 Четыреххлористый углерод
in 4—10 » »
3 Этилацетат
Mull 6—9 Четыреххлористый углерод
6,5 Этилацетат
MoVI 3 »
Nbv 4—5,5 Четыреххлористый углерод
Ni 0—10 Хлороформ
4-П Четыреххлористый углерод
Os’ 7—9 » »
Pb 4-11 » »
—0,2 Этилацетат
Pd11 4-H Четыреххлористый углерод
ptIV* 4-11 » »
PuVI 3 Амилацетат, амиловыи спирт
Re Конц. HCI Этилацетат
Sb111 4—9.5 Четыреххлористый углерод
Seiv 4—6,2 » »
3 Этилацетат
Sniv 5—6 Четыреххлористый углерод
Те iv 4—8,8 » »
0,001—5,0 н. сильная Хлороформ, бензол
кислота
Tl1 4—11 Четыреххлористый углерод
Tl111 4—11 » »
(JV! 1—5 Бензол
4—8 Четыреххлористый углерод
6,5—8,5 Хлороформ, амилацетат, диэтиловый эфир
Vv 4—5,9 Четыреххлористый углерод
VV 1—1.5 Этилацетат
Zn 3 »
4—11 Четыреххлористый углерод
* Извлечение неполное.
80
ЭКСТРАКЦИЯ ДИЭТИЛДИТИОКАРБАМАТОВ
Продолжение
Приведенные данные относятся к экстракции 0,04% раствором диэтилдитиокароамата диэтиламмоння в четыреххлористом углероде, для MoVI — в смеси четыреххлористого углерода и аллилового спирта (4 : 1), Для UVI - в хлороформе., Штриховка означает экстрак-цию только из растворов серной кислоты, а в случае Sn^* и Fe — только из
растворов соляной кислоты; черным цветом показана экстракция из растворов как соляной, так н серной кислот. Высота каждой клетки соответствует 100%-ному извлечению.
6 Зак. 783'
81
ЭКСТРАКЦИЯ АЦЕТИЛАЦЕТОНАТОВ
Экстрагируемый элемент pH водного раствора Органическа! фаза Е, %
А1 4—6 Ацетиладетон (50%) в хлороформе 90
1—4,4 Ацетилацетон 10—90
Be 1,0 » ~ 100
Bi 1,0 » ~ 100
СеШ >4 » ~ 100
Со111 1 Ацетилацетон (50%) в хлороформе ~ 100
0,0—2,0 Ацетилацетон 95—99,5
Crin 0,0—2,0 » ~ 100
Си» 2,5—6,0 » 85
Dy 5,3 » 45,8
Er 5,5 » 65,5
Fell I 1,5 » ~ 100
1,0 Ацетилацетон (50%) в хлороформе 96
Ga 3,0 Ацетилацетон 83
3,0 Ацетилацетон (50%) в хлороформе 95
Gd 5,8 Ацетилацетон 39,3
Hf 2,3 » >95
HgH 3,0 » 48
Ho 5,75 » 57,5
In 3,0 » 94
Mnll 4—6,5 » ~ 100
MoVI 0,01-6,0 н. H2SO4 Ацетилацетон (50%) в хлороформе 96—98
Nbv 2—5 Ацетилацетон (20%) в хлороформе 90
Nd 5,6 Ацетилацетон 30,0
Pb 5—7 » 80—98,5
Puiv 2—10 Ацетилацетон (0,1 М) в бензоле . ~ 100
Ruin 4—6 Ацетилацетон (33%) з хлороформе * 90
S n 5,55 Ацетилацетон 32,0
Tb 5,7 » 48,0
Th > 4 » ~ 100
TiIV 0,0—1,6 Ацетилацетон (50%) в хлороформе 10—76
U‘V 2,5 Ацетилацетон 73
UVi 4—6 ~ 100
v111 2,0 Ацетилацетон (50%) в хлороформе 93
Viv >2,3 То же 80
Vv 2,15 » » 68
Y 5,7 Ацетилацетон 52,9
Yb 5,8 » 84,6
Zn 5,5—7 » 70
Zr 2—3 » 73
3-8 Ацетилацетон (20%) в .хлороформе 98
* Соотношение объемов водной и органической фаз 25 : 1.
82
ЭКСТРАКЦИЯ ТИОФЕН КАРБОН ИЛТРИФТОРАЦЕТОНАТОВ
Экстрагируемый элемент pH водного раствора Органическая фаза
растворитель концентрация тиофенкарбо-нилтрифтор-ацетона, мо ль!л
Ас > 5,5 Бензол 0,25
AI 5,5 » 0,02
5,5—6,0 Метилизобутилкетон 0,1
Агаш >3,5 Бензол 0,2
Be 6—7 » 0,02
Bi 2,0 » 0,25
Bk >2,5 » 0.2
Ca 8,2 » 0,5
Celli * 1 и. H2SO4 Ксилол 0,5 •
Celli** 2,9 Трибутилфосфат (0,5 АТ) в бензоле 0,2
Cf 3,0 Бензол 0,2
Cm 3,5 » 0,2
CoH 5,1—6,8 Ацетон + бензол (3:1) 0,15
Crin 5,75 Бензол 0,15
Cs 8,7 Нитрометан, нитробензол 0,5
Cull 2,4—6,0 Бензол 0,15
Es — 3,0 » 0,2
Eu >3,4 Толуол 0,2
Fe4l 2—3 Бензол 0,02
Fm — 3,0 » 0.2
Hf 2 и. HC1CX, » 0,1
In 2,5—4 » 0,5
La > 4,5 » 0,2
MnH 6,7—8,0 Ацетон + бензол (3:1) 0,15
Na *** 8,7 Нитрометан, нитробензол 0,5
Ni 6 Ацетон + бензол (3:1) 0,15
NplV 1,0h. HCI или HNO3 Ксилол 0,5
Pa 4 h. HNO3 Бензол 0,4
ря m* 2—6 и. HCI » 0,5
Pb 4 » 0,25
Poiv 1,5—2,0 » 0,25
puiv 0,5н. HCI iuihHNO2 » 0,15
Sc 2.5—6 Ксилол 0,2
Sr > 10 Бензол 0,02
Th 0,8 » 0,25
2,0 Четыреххлористый углерод 0,5
Tl1 > 6,5 Бензол 0,25
TjHi >3,5 » 0,25
Ljvi >3 » 0,2
Vv 2,5—4,1 Бутиловый спирт 0,3
Y > 6 Бензол 0,02
4,2—10 Метилизобутилкетон 0,1
Yb > 3,4 Толуол 0,2
Zr 6 и. HCI Ксилол 0,5
2—10 h. HNO3 0,5
• E 80%.
E c= 91%.
♦** E 45%.
£ — 90%,
6*
83
ЭКСТРАКЦИЯ АНИОНОВ В ВИДЕ СОЛЕЙ ТЕТРАФЕНИЛАРСОНИЯ
Органическая фаза представляет собой раствор (C6H5)4AsOH (0,0133 моль!л) в хлороформе. Концентрация анионов в водном растворе 0,066 моль!л.
Экстрагируемый анион pH водного раствора (после экстракции) Е, % Экстрагируемый аннон pH водного раствора (после экстракции) Е, %
F" 1,5 < 1 no; 10,8 15,9
11,6 < 1 12,0 18,0
СГ 1,4 7,8 17,8 15,5 SOJ" 1,5 9,0 <0,1 <0,1
-• 12,1 15,4 12,0 <0,1
Вг” 1,4 82,0 8,1 4,7
4,5 83,2 so;
12,3 82,6 so; 12,0 1,5
J 1,4 >99,7 73 1 6
5,1 >99,7 s2or 11,8 1.7
12,2 >99,7
SCN” 0,7 4,4 97,2 97.2 рог 4 2,0 11,5 ~1 ~1
11,7 97,0 3,3 0,4
С1О~ 2,0 > 99.3 *2 11,6 0,3
BrO- 12,0 2,0 >99,3 47,8 СгОГ^Сг2ОГ 1,2 5,9 98,6 92,5
12,0 45,5 6,9 37,4
JO," 2,0 < 0,4 7,9 6,4
10,8 2,4
JO8- 12,0 < 0,4 MoO*" 10,3 <05
C1O4“ 1,5 > 99,5 10,5 <0,5
4,0 >99,5 wor
12,0 > 99,5 VO; 9,0 <0,5
MnO4" 1,4 >99,7 вог 1.5 <0,5
3,0 >99,7 11,9 <0,5
12,0 >99,7 AsO?~ 1,7 0,6
ReO; 2,0 >99,5 Н,4 4,5
12,0 > 99,5 АзОГ 1,8 < 1
jo; 12,0 2 10,4 < 1
NO" 1,4 95,3 Scor 2,5 < 1
3,5 98,4 8,5 8,0
12,1 97,7 ТеОГ 1,6 < 1
11.7 8,0
84
ЭКСТРАКЦИЯ КИСЛОТ МЕТИЛДИОКТИЛАМИ ном
Экстракция производилась 5% раствором метилдиоктил амии а в хлороформе.
Кислота Е, % Кислота Е, % Кислота 5о
Азотная 98,0 Муравьиная 89,9 Фтористоводородная
Аминоуксусная 0,0 Пикриновая 96,0 (плавиковая) 87,1
Аспарагиновая 0,0 Серная 98,0 Фумаровая 95,9
Глутаминовая 0,0 п-Т олу олсульфонов ая 97,0 Хлористоводородная
Глутаровая 86,9 Трихлоруксусная 98,7 (соляная) 98,0
Глюконовая 0,0 Уксусная 75,8 Щавелевая 98,9
Малеиновая 97,5 Фосфорная 76,5 Яблочная 90,8
Молочная 92,0 Янтарная 90,0
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ АЛИФАТИЧЕСКИХ АМИНОВ
В большинстве случаев, представленных в таблице, степень извлечения £>80 %.
Экстрагируемый элемент Водная фаза Органическая фаза
Ag 1 н. LiCl + HCI Метилдиоктнламин (10%) в трихлорэтилене
Ami" 12 M LiCl + 0,1 M HCI Триизооктиламин (20%) в ксилоле
As1" 8—11 M HCI Додецил-(триалкилметил)-амнн * (10%) в ксилоле
Be 0,1 M H2C2O4; pH=3-M Триизооктиламин (0,1 М) в хлороформе
Bi 0,5—2 M HCI Октиламин (0,1 М) в хлороформе
Cd 5—6 M HCI Трибензиламин (0,1 М) в бензоле
Co 6—10 M HCI > 6 M HCI Метилдиоктнламин (8%) в трихлорэтилене Триизооктиламин (0,1 А1) в керосине
Crvi Слабощелочная Метилдиоктнламин (5%) в хлороформе
Раствор НгСггО? в 6 М НС1 Трибензиламин (5%) в хлороформе, три-нзооктиламин (5%) в ксилоле
Cu" > 6 М HCI 6,5 Л-1 НС1 Метилдиоктнламин (8%) в трихлорэтилене Триоктиламнн (0,1 А1) в ксилоле
Fe"1 > 2 /VI HCI 5 М HCI Метилдиоктнламин (8%) в трихлорэтилене, триизооктиламин (10%) в ксилоле Трибензиламин (0,2 Л1) в хлороформе
Ga 7 М HCI Дециламин в хлороформе
Geiv 8—11 М HCI Додецил- (триалкилметил) -амин * (10%) в ксилоле
Hf > 8 М НС1 8 М НС1 0,1—1,0 М H2SO4 Метилдиоктнламин (5%) в ксилоле, три-нзооктиламин (5%) в ксилоле Триизооктиламин (0,2 AI) в циклогексане Метилдиоктнламин (5%) в ксилоле, три-октиламин или триизооктиламин (0,1 М) в смеси керосина (97%) и трпдека-нола (3%)
Hg" 1—8 М НС1 Додецил-(триалкилметил)-амин * (10%) в ксилоле
Общее число углеродных атомов в алкилах триалкилметильиой группы равно II —14.
85.
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ АЛИФАТИЧЕСКИХ АМИНОВ
Продолжение
Экстрагируемый элемент Водная фаза Органическая фаза
In 6—7 M HCI Додецил-(триалкилметил)-амин * (10%) в ксилоле
МпП 8 Al HCI Триоктиламин (0,1 AI) в ксилоле
MoVI 1 M SO2-; pH= 1ч-2 Метилдидециламин (0,1 М) в ароматическом углеводороде
Nbv > 8 M HCI Метилдиоктиламин (5%) в ксилоле, триизооктиламин (5%) в ксилоле
11 M HCI Трибензиламин (8%) в хлороформе или метиленхлориде
~2 M H3PO4 Метилдиоктиламин (5%) в трихлорэтилене
4—4,8 Al H2SO4 Трибензиламин (8°/о) в метиленхлориде
1,5 M H2SO4 Метилдиоктиламин (5%) в трихлорэтилене
Npiv 4—6 Al HNO., Триоктиламин (1О°/о) в ксилоле
~8 Al HCI То же
NpVl 5—7 M HNO3 » »
~ 6,3 Al HCI » »
PaV > 6 M HCI Метилдиоктиламин (5%) в ксилоле или хлороформе
1,8 M H3PO4 Метилдиоктиламин (5%) в трихлорэтилене
0,5 Al H2SO4 То же
Poiv 6 M HCI Трибензиламин (5°/о) в хлороформе, метилдиоктиламин (5%) в ксилоле
Ptiv 0,1—0,5 M HCI Триоктиламин (0,05 А1) в толуоле
Puiv 4—6 Al HNO3 Триоктиламин (10%) в ксилоле
>6 M HCI То же
pu VI 6—8 Al HNO3 » »
6—8 Al HCI Триоктиламин (10%) в ксилоле, триизо-октиламин (5%) в ксилоле, трибензиламин (5°/о) в хлороформе
1 M CH3COOH Триизооктиламин (20%) в ксилоле
Ruiv 0,1 M HCI Триизооктиламин (5%) в ксилоле
SbiH 1—4 Al HCI Додецил-(триалкилметил)-амин * (10%) в
» ксилоле
Sbv > 6 M HCI То же
Seiv 9 Al HCI » »
Sniv 5—6 M HCI » »
TaV > 4,8 M H2SO4 Трибензиламин (8%) в метиленхлориде
Tcvil 6 M A1(NO3)3 Тридодеци ламин (0,3 М) в ароматическом углеводороде
Teiv 4—6 Al HCI Додецил-(триалкнлметил)-амин * (10%) в ксилоле
Th 0,5 Al so4_; pH=l Октиламин (0,1 А1) в ароматическом угле-
водороде
’ Общее число углеродных атомов
в алкилах трналкилметильной группы равно 11—14.
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ АЛИФАТИЧЕСКИХ АМИНОВ
Продолжение
Экстрагируемый элемент Водная фаза Органическая фаза
Th 12 M LiCl + 0,1 M HCI ~6 M HNO3 Триизооктиламин (20%) в ксилоле Триоктиламин или триизооктиламин (0,4 М) в бензоле или толуоле
THV 1 M SO4-; pH=l,4-4-3 1-(3-Этилпентил)-этилоктиламин в керосине
UIV 9 M HCI 0,5 м so4~; pH=i Триоктиламин (10%) в ксилоле Октиламин (0,1 М) в ароматическом углеводороде
LTV1 0,1—1 M H2SO4 ~6,5 M HCI 1—2 M HF 0,1—1 M H3PO4 0.5—2 M СНзСООН 6—7 M HNO3 Метилдиоктиламин (5%) в ксилоле Триоктиламин или триизооктиламин (10%) в ксилоле Метилдиоктиламин (5%) в ксилоле Триоктиламин (0,1 М) в керосине Триизооктиламин или тридодециламин (10%) в ксилоле или метилизобутилкетоне, метилдиоктиламин (5%>) в ксилоле Триоктиламин (10%) в ксилоле
Vv SO*- pH=2 6—7 M HCI Метилдидециламин (0,1 М) в ароматическом углеводороде Додецил-(триалкилметил)-амин * (10%) в ксилоле
Zn > 2 M HCI Метилдиоктиламин (8%) в трихлорэтилене или ксилоле, трибензиламин (5%) в хлороформе, триизооктиламин (5%) в метилизобутилкетоне
Zr 0,1—1,0 M H2SO4 > 8 M HCI Метилдиоктиламин (5%) в ксилоле, триоктиламин или триизооктиламин (0,1 А1) в смеси керосина (97%) и тридеканола (3%) Триоктиламин (0,2 М) в циклогексаноне или ксилоле, триизооктиламин (5%) в ксилоле
* Общее число углеродных атомов
в алкилах триалкилметильной группы равно 11—14.
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ СОЛЕЙ ТЕТРААЛ КИЛАММОН ИЯ
Приведенные иа рис. 1—5 данные относятся к экстракции элементов 0,2 М растворами иодидов тетрапропил-, тетрабутил- и тет-рагексиламмония в метилизобутилкетоне. Исходная концентрация экстрагируемого элемента в водном растворе 2 • Ю~3 моль!л.
Обозначения:..........экстракция раствором (CaHy^NJ;
—----экстракция раствором ---экстракция раствором
(СбН1з)4Ш; минус означает, что £<1%, плюс — что £>98%.
Е.%
100\-----
75-
50-
25-
о 12345 концентрация ' щелочи или кислоты, г-экб/л
87
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ СОЛЕЙ ТЕТ РА АЛ КИЛ AMMO Н ИЯ
Рис. 1. Экстракция из растворов едкого натра.
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ СОЛЕИ ТЕТРААЛКИЛАММОНИЯ
8<Ь
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ СОЛЕИ ТЕТРААЛКИЛАММОНИЯ
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ СОЛЕЯ ТЕТРААЛКИЛАММОНИЯ
Рис. 3. Экстракция из растворов серной кислоты.
Рис. 4. Экстракция из растворов фтористого водорода.
91
90
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ РАСТВОРАМИ СОЛЕИ ТЕТРААЛ КИЛ АММОН ИЯ I ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ
Рис. 1. Экстракция трибутилфосфатом из растворов азотной кислоты (недостаточно надежные данные показаны штриховой кривой).
ю
036912
Концентрацъй
Mg
А1
Si Р S
К са Sc Ti V Сг"1 Мп" Fe1" Co Г* Ni -— Cu" Zn " Ca Ge Asv Se Br
Rh Sr Y Zr о Nb MOVI Tcv" Ru,v Rb Pd Ag Cd In Sn Sbv Tevi J
CS : Ва Лантаниды. Hf та WVI Rev" OsVI Mr Pt xAu’" Hg" Tl"’ Pb Bi Po At
Fr
La Ce,n Pr Nd Pm
Ac Pa UV1 Np ViL.
Puvl
Am111
Na Mg
А1 Si Р S С1
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ 1 ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ
£
Hg"
Cs
-Sm
:UV1
Рис. 4. Экстракция 5% раствором окиси триоктилфосфина в толуоле из растворов азотной кислоты.
ю
to'
Об 12 16
Концентрация
НМО3,г-э*ф>7
Na Mg Al Si P s Cl L—J
К Са Sc Т1 •V Сгш Мп" Fe,n Со -****-**' Ni Си" .—- Zn > , Ca Ce Asv Se™ A 1 Br
1 J
Rb Зг Y Zr Nb MOVI Тс Ru Rti Pd Ag Cd In Sn Sbv -Те —1—1— J ——*“ —1—1—
Osv'
Ba - Hf та WVI
I
- -1.
Re™
Fr Ra - - §
Ce17
Au111
Т-.ш
Зак. 783
ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ 1 ЭКСТРАКЦИЯ ЭЛЕМЕНТОВ ФОСФОРОРГАНИЧЕСКИМИ СОЕДИНЕНИЯМИ
кислоты.
При экстракции железа время контакта водного и органического растворов: 1 — 2 мин; 2 — 30 ч.
ЭКСТРАКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ
Обозначения: инд. конц. — индикаторная концентрация; Ln или Р. 3. — редкоземельные элементы.
Экстрагируемый элемент Экстрагент Водная фаза Коэффициент распределения D
La Ceiv Y Диэтиловый эфир » » » » » » Нитрометан Изоамиловый спирт 0.1 AlLa(NO3)3,1.0А1 HNO3, нас. р-р LiNO3 0,1 Al Се (NO3)4,1,0 М HNO3, нас. р-р LiNO3 0.1 А4 Се (NO3)4> 1,0 Al HNO3, нас. р-р NH4NO3, 0,1 Al Се (NO3)4,3,0 Al HNO3, нас. p-p NH4NO3 Инд. конц. Се (NO3)4,4,0 Al Ca(NO3)2, 3.0 Al HNO3 0,055 Al У-салицилат, 100 г/л салициловой кислоты 1.4 • 10-4 0,31 0.10 5,37 7.10
pH | 3.5 4,0 1.0 E x 100%
La » » 0,036 Al La-салицилат. 100 г/л салициловой кислоты
pH 4.15 4,5 1.0 E x 100%
Се111 » » 0.036 AI Се-салицилат. 100 г/л салициловой кислоты
pH 4,6 5.0 1.0 E x 100%
Nd 5,7-Д ихлор-8-оксихи-нолин (0,02 М) в хлороформе 10"3 pH Al Nd3+ 6.8 >9,4 1,0 E x 100%
Er То же ~10 -3 Al Er3+
pH 1 6.7 >8.3 1.0 E x 100%
La » » ~10” 5 Al La3+,0,l Al NaClO4
pH 5.15 5.35 5.46 6.12 6.51 6.61 9.77 • 10-3 3,54 • 10“2 1.74- KT1 3,24 26,9 229.0
Ce111 Триоктиламин (10%) в ксилоле Инд. конц, Се (NO3)3, 1.0—6.0 М HNO3 <10-3-—2-10-3
98
ЭКСТРАКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Экстрагент Водная фаза Коэффициент распределения D
Y, La, Трибутилфосфат Ln (NO3)3 HNO3 Y La Се111 Рг
Се111, Рг Nd, Pm, » Инд. конц. 0,7 М » » 3,0 М » » 5,0 М » » 8.0 М » » 12,0 М » » 15,0 М Ln (NO3)3 HNO3 0,04 0,08 0,10 0,06 0,24 0,12 0,17 0,22 0,69 0,09 0,14 0,20 2,4 0.06 0,09 0,15 27 0,09 0,14 0,30 220 0,22 0,42 0,81 Nd Pm Sm Eu
Smj Ей Gd, Tb, » Инд. конц. 0,5 М » » 3,0 М » х 5,0 М » » 8,0 М » » 12,0 М » » 15,0 М » » 18,4 М Ln(NO3)3 HNO3 0,05 0,08 0.06 ... 0,34 0,36 0,41 0.43 0,30 0,36 0,46 0,52 0,23 0,33 0,50 0,67 0,50 1,03 1,70 2,7 1,65 2,9 6,6 12,6 ... 13,2 ... 59 Gd Tb Dy Ho
Dy, Но Ег, Tu, » Инд. конц. 0,7 М » » 3,0 М » » 5.0 Л4 » » 12,0 М » » 15,0 М 0,10 ... 0,07 0.07 0,37 0,43 0,45 0,38 0,50 0,70 0,69 0,71 4,3 7,30 10,5 16,7 22,6 46,3 65,6 94,0 Er Tu Yb Lu
Yb, Lu La, Pr, » Инд. конц. 0,6 Л4 » » 3,0 М » » 5,0 М » » 8,0 М » » 12,0 М » » 15,0 Л! » » 17,0 М 0,05—0,1 М Ln (N О3)3,8,0 М 0,04 0,03 0,02 0,02 0,48 0,28 0,41 0,17 0,85 0,78 1,15 0,74 2,20 2,8 3,6 5,2 23,2 32 43 56 108 179 220 370 505 ... 796 ... La Pr Nd Sm
Nd, Sm, Eu, Gd, Dy, Y, Ho, Er, Tu, Yb Ce111 Трибутилфосфат (48%) в керосине NH4NO3; рН=4,5 Се (NO3)3 HNO3 NaNO3 Инд. конц. 4,00 Л4 2.00 М » » 1,50 М 4.50 М » » 0,50 Л1 5,50 Л4 » » 0,20 М 5,80 М » » 0,05 М 5,95 М » » 0,005 М 6,00 М 58 102 157 305 Eu Gd Dy Y 454 397 415 522 Ho Er Tu Yb 700 509 485 317 0,030 0,113 0,56 1,90 8,6 17,6
7*
99
ЭКСТРАКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Экстрагент Водная фаза Коэффициент распределения D
Y, La, Трибутилфос- Еп(ЫОз)3 HNO3 Y La Ce Pm Eu
СеШ, фат (48%) Инд. конц. 0,5 М 0,01 ... 0,02 0,03 0,04
Pm, Ей в керосине » » 3,0 М 0,07 ... 0,05 0,11 0,16
» » 5,0 М 0,11 0,02 0,02 0,08 0,16
» » 8.0 М 0,25 0,01 0,02 0,06 0,14
» » 12,0 М 3,4 0,01 0,03 0,22 0,47
La, Celli, Дибутилфос- Инд. конц. Ln (СЮ4)3,0,1 М La Ce Pr Pm Sm
Pr, Pm, Sm, форная кислота (0,1 М) НСЮ4 2,6 10,0 8,1 27,8 48
Eu, в дибутило- Eu Gd Tb
Od, Tb вом эфире 94 110 533
Tb, Ho, Y, Дибутилфос- Инд. конц. Ln (СЮ4)3, 0.1 М
Tu, Lu форная кислота в дн-бутиловом эфире НС1О4 Tb Ho Y Tu Lu
0,001 М р-р 0,002 0,010 0,015 0,10 0,81
0,01 М р-р 1.2 10 12 81 480
СеШ, Y, Дибутилфос- Ln (NO3)3 HNO3 Ce Y Eu
Eu форная кислота (0,1 Л1) в бензоле Инд. конц. » » 0,1 М 0,5 М 6,1-10-1 2,2-10-2 410-1 1,5-IO-2 9,5 9 10-2
СеШ, Диамилфос- Инд. конц. Ln (NO3)3, Ce Pm Eu Y Tu
Pm, Eu, форная 2,5 Л4 HNO. 0,0017 0,019 0,096 1,80 11,5
Y, Tu кислота
(0,98 М) в бензоле
Y, La Ди-(2-этилгек- LnCl3 hci Y La
сил)-фос-форная кислота (1,5 М) в толуоле Инд. конц. » » » » 0,05 Al 0.1 M 0.5 M > 105 50 > 104 6 1,7 • 102 LIO"2
Pm, Y, Ди-(2-этилгек- ЬпС1з HCI Pm Y Tu
Tu сил)-фос-форная кислота (0,75 М) в толуоле Инд. конц. » » 0,15 Al 0,55 Al 1,2 5,9-102 2,4-103 2,4 -10-2 10 50
CeIV, Ди-(2-этилгек- Инд. конц. Ln (NO3)3, или „10,0 Al HNO3 Cetv СеШ La Pr
Ce111, La, Pr, сил)-фос-форная Се (NO3) 4- 103l-10“33.10_45.10-4
Pm кислота Pm Eu Tu
Eu, Tu (0,30 М) в 1-10-3 5-IO-3 0,12
La, СеШ, Моно-(2-этил- LnCl3 HCI La Ce Pm Eu Y
Pm, Eu, Y гексил)-фос-форная Инд. конц. 2,0 Al 0,32 0,46 0,79 1,09 0,79
» » 6,0 Al 0,03 0,05 0,10 0,14 0,14
(048 7И) в толуоле » » 12,0 Al 0,17 0,30 0,56 0,92 2,4
100
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, применяемые для разделения элементов
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
Ag Си ЭДТА; pH=2 Диэтилдитиокарбамат натрия, ЭДТА; рН=11 Дитизон в четырех хлористом углероде Четыреххлористый углерод
Ai Be, Са, Cr, Mg, Мп, P.3., Th, W Fe, Ni, Ti, V 4-Сульфобензойная кислота; рН = 5-^6,6 или pH = 8,5 -= 11,5 8-Оксихинолин; рН = =5,04-9,0 Масляная кислота, NaCl; pH = 9,3 4- 9,5 Мории, кислая среда 8-Оксихинолин (1%) в хлороформе Бензол, хлороформ Хлороформ Амиловый спирт
Asm Си Ge, P, Si Asv (NH4)2MoO4, 1,8 М HNOs Диэтилдитиокарбамат натрия; pH =4 :- 5,8 (NH4)2Mo04, H2SO4 Бутиловый спйрт+хлоро-форм Четыреххлористый углерод Изобутиловый спирт
Au”1 8 М HNO3 Метиловый фиолетовый; рН=1 Диэтиловый эфир Трихлорэтилен
В F- Si А!С13, HCI NH4HF2, HF, Н2О2 Метиленовый синий, HF Метиловый фиолетовый, HF, pH = 3,4 Диэтиловый эфир (C6H6)4AsC1 (0,01 М) в хлороформе Дихлорэтан Бензол
Be Ai Al, Си, Fe Смесь продуктов деления и 2-Мет ил-8-оксихинолин; pH = 8,0 Масляная кислота, ЭДТА, КС1; рН=9,3<-9,5 Ацетилацетон, ЭДТА; pH = 6,0 4-9,0 ЭДТА; рН=5ч-7 Бензоат натрия; pH = 7 8-Оксихинальдин; рН = 8,1 Хлороформ » » Ацетилацетон в бензоле Этилацетат, бутиловый или амиловый спирт Хлороформ
Binl As1”, Со, Cr, Hg, Ni, Sb, SnIV, Zn' Nb, V Nd, Pr Pb, Sn Антипирин Диэтилдитиокарбамат нат: рия, тартраты, цианиды; рН= 114-12 1 М HNO3 0,1 М HNO3 » » Диэтилдитиокарбамат ди-этиламмония в хлороформе Тиомочевина в хлороформе
101
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
Bi111 и Ацетаты; рН = 5,54-6,0 Диэтилдитиокарбамаг ди-этиламмония в хлороформе
Все металлы, кроме РЬ, Sn11, Т11 KCN, щелочной раствор Дитизон в хлороформе
Вг- Cl КВгОз, H2SO4, диизобутилен Петролейный эфир
CI , и KMnO4. HNO3 Перфтороктановая кислота Четыреххлористый углерод
Са Одновалентные катионы Диэтиловый эфир
Cd In, Th KSCN, тартраты, ацетаты; рН = 5 Пиридин (5%) в хлороформе
Ni 2-А'1еркаптобензотиазол, аммиачный раствор Хлороформ
Pb, Zn Цитрат натрия, 1 М NaOH Дитизон в четыреххлористом углероде
Се Fe KCN; рН = 9,94-10,5 8-Оксихинолин (3%) в хлороформе
Продукты деления и 9 М HNO3 Метилизобутилкетон
Со Bl, be, Mo, U, V, W (C4H9)3N, KSCN, NaF, H2SO4 Амиловый спирт
Cu, Fe, Ni 3 Метокси-5-нитрозофенол-рН = б4-8 Бензол
Си, Fe, U 0,05 M (C6H5)„AsCl, KSCN, nh4f Хлороформ
Ni 1 Нитрозо 2-нафтол; pH = = 34-4 »
Th 1 - (2-Пиридилазо) -2‘наф-тол; pH = 34-6 »
2-Нитрозо-1-нафтол, цит- Изоамилацетат
Боратный буферный раствор; pH = 6,3 4-7,6 5,8-Хинолиндиондиоксим в изоамиловом спирте
Сг111 Cu. Fe, Ni. LT 1 Al НС1 Метилизобутилкетон
V Н2О2, H2SO4; pH =1,7 Этилацетат
Дифенилкзрбазид, 0,2 М H2SO4, NaCl 1-Нафтиламин, винная кислота Изоамиловый спирт
» »
Cs ’з Нитрометан + бензол
0,4 М KPF6 Нитрометан
0,001 М NaB(C6H5)4; pH=6,6 Нитробензол
Си11 Al, Co, Fe, Mn. Ni Са-ЭДТА; рН = 6,5 8-Оксихинолин (1%) в хлороформе
Bi, Cd, Co, Са-ЭДТА; рН = 9 Дитизон в четыреххлори-
Ni, Pb стом углероде
102
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
Си11 Tl, Zn, Fe Все металлы KH2PO4 Неокупроин, цитрат нат- рия; рН = 6 рН = 6,3-^10,3 Пиридин, КВг, NH2OH 8-Мерка птохинолин Дифенилкарбазон в бензоле Хлороформ Масляная кислота в бензоле Хлороформ Хлорбензол, хлороформ, амилацетат
F" SO*' [(C6H5)4Sb]2SO4, разб. H2SO4 Четыреххлористый углерод, хлороформ
Fe111 Al Al, Co, Cr, Cu, Mn, Ni, Tl, Vlv, Zn Al, Mg, Pb, Zn Al, Ti KSCN, (NH4)2SO4 7,75—8,0 Al HCI Антипирин, KSCN, HCI 8-Оксихинальдин; pH = 5,3 Батофенантролин, NH2OH; рН = 4 1, 10-Фенантролин, NH2OH; рН=4 NH4SCN, (C4H9)3N Бензоат натрия; рН = 7 Трибутилфосфат Динзопропиловый эфир Этилацетат Хлороформ Гексиловый спирт Нитробензол Амилацетат Этилацетат, бутиловый или амиловый спирт
Ga Al, In, Sb, Tl, W и др. Fe Силикаты » Родамин В, 6 Al НС1 6,5 М HCI, TiCI3 8-Оксихинальдин, NH2OH, ацетаты; pH = 3,9 Бензоат натрия: рН = 7 Бензол Динзопропиловый эфир Хлороформ Этилацетат, бутиловый или амиловый спирт
Ge As, Hg, Sb НС1 Бензол, четыреххлористый углерод
Hf Роданиды Диэтиловый эфир или метилизобутилкетон
Hg11 Ag, Cu Все металлы, кроме Ag, Bl, Cu, Pb и Tl111 NaCl, ЭДТА; pH =1,5 Диэтилдитиокарбамат натрия, ЭДТА; рН=11 Антипирин, KJ, НО, Дитизон в четыреххлористом углероде Четыреххлористый углерод Хлороформ
.г Те Н2О2, 0,2 М HCI Трибутилфосфат
In Be Cu Cu, Fe Fe 8-Оксихинальдин; рН = 5,5 Цианиды, аммиачный раствор Диэтилдитиокарбамат натрия, .NaCN, рН=9,0 НВт, TiCls Хлороформ Дитизон в хлороформе Четыреххлористый углерод Диэтиловый эфир
103
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
In Оа 5 М НВг Бутилацетат
Оа 0,25 М KJ, 0,05 М H2SO4 Циклогексанон
Th 0,5 М NaJ, IM НС1О4 Метилизобутилкетон
Бензоат натрия; pH = 7 Этилацетат, бутиловый или амиловый спирт
Th Родамин В, 2,5 М НВг Бензол
К J3 Нитрометан + бензол
La Фенилкарбоновые кислоты (салициловая, коричная или 3, 5-динитро-бензойная) Хлороформ, метилизобутилкетон
рН=7 0.1 М N-бензоилфенилгид-роксиламин в хлороформе
Li -’з Нитрометан+бензол
Mg Ba, Са, Sr Бутиламин; рН= 10,5-4- 13,6 8-Оксихинолин (0,1%) в хлороформе
Одновалентные катионы Перфтороктановая кислота Диэтиловый эфир
Мп11 Се, U Диэтилдитиокарбамат натрия, цитраты; рН = 7,54-8,0 Хлороформ
MoVI 4 М NaOH (CeH'JiAsCl, щелочной раствор Пиридин Хлороформ
Ag, Al, As, Cr, Cu, Fe, Hg, Pb, Pu, Ti, Ti, U, Zn. Zr 6AJ НС1, 0,4 М HF Метилизобутил кетон
Re KSCN, Hg2(NO3)2 Диэтиловый эфир
Ti, W KSCN, ЭДТА, NaF, HCI Амиловый спирт + четыреххлористый углерод
U KSCN, NaNO2, SnCh Диэтиловый эфир + керосин (2:1)
U Толуол-3, 4-дитиол, N2H4 • H2SO4 Четыреххлористый углерод
w H3PO4, HCI Диэтиловый эфир
w Тиогликолевая кислота, KSCN, H2SO4 Бутилацетат
w KSCN, NaF, SnCI2 Бутилацетат
w Толуол-3,4-дитиол, ли- монная кислота, Н3РО4 Керосин
Zr KSCN, кислый раствор Бутилацетат
Все металлы, Кислый раствор а-Бензоиноксим в хлоро-
кроме VV форме
Сплавы же- ЭДТА, pH =1,5 8-Оксихинолин (1%) в
леза хлороформе
104
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
MoVI Na Nb Ni Np,v и Npvl Os pv Pa Pb Pd Силикаты Продукты деления и Со Со Си Nb, Та Все металлы, кроме Со Pt, Rh Ru As, Cr, Cu, Mn, Si, V Отделение PaiV от Pav Все металлы, кроме Bi, Cd, Ti Одновалентные катионы Co, Cu, Fe, IrIV, Ni. Pt,v Все металлы » » а-Бензоиноксим, -С 1,8 Al HCI NaF или ЭДТА, 0,1—0,5 А! на Щавелевая кислота, 1 А1 H2SO4, 2,5 М (NH4)2SO4 Фториды; рН=1 Пиридин, KSCN; рН = 4,6 Диметилглиоксим, KCN, щелочной раствор Циклогександиондиоксим (ниоксим), аммиачный раствор Пирокатехин а-Бензоиноксим, аммиачный раствор а-Фурилдиоксим, аммиачный раствор 6—9 М HNO3 Эфедрин, NaOH (CeHsHAsCl, конц. НС1 Раствор OsO4 в кислоте Тиокарбанилнд Na2MoO4 или (NH4)2MoO4, HNO3 6 Af НС1 Диэтилдитиокарбамат натрия, NaCN; рН=11 Родизонат натрия, NH4F, НС1 Перфтороктановая кислота Салицилальдегид, NH2OH, слабокислый раствор Диметилглиоксим, 1 А1 H2SO4 2-Нитрозо-1-нафтол, ЭДТА, аммиачный раствор Диэтилдитнокарбамат натрия, ЭДТА; рН=11 Хлороформ Морин в бутиловом спирте Нитрометан + бензол Дибутилфосфорная кислота (0,6 Af) в дибутиловом эфире N-Бензоилфенилгидроксил-амин в хлороформе Хлороформ Хлороформ, четыреххлористый углерод Бензол Бутиловый спирт Хлороформ » Диэтиловый эфир, метил-изобутилкетон Четыреххлористый углерод Хлороформ Четыреххлористый углерод Диэтиловый эфир Бутиловый спирт + хлоро-форм Метилизобутилкетон или трибутилфосфат в бензоле Четыреххлористый углерод Хлороформ, четыреххлористый углерод, хлорбензол Диэтиловый эфир Бензол Хлороформ Толуол Четыреххлористый углерод
105
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
Pd Ро Ptn Pu Rb Re Rh Ru Sb Ir Mo Mo Mo, W Ag, Cd, Ce, In, La, Nb, Sb. Sn, Те, U, Zr As111, Bi, Co, Cr, Hg, Ni, Sniv, Zn Cd, Cu, Fe, Ge, Pb, Sn, Те Pb Pb, Sn 1,2-Нафтохинон, NHjOH H2O2, 8Af HNO3 SnCl2, 3AJ HCI SnCl2, бромиды pH=2,5 4-4,5 HNO3, нас. раствор NH4NO3 pH=4h-8 ^3 NaB (C6H5)4 Бензилдиоксим, 6 M H2SO4 4-Окси-З-меркаптотолуол, 6 M HCI (CeH6)4AsCl; pH = 9 Диэтилдитиокарбамат натрия, конц. HCI 4 M NaOH KSCN, HCI, SnCl2 Толуол-3,4-дитнол, кислый раствор NaOH 1-Нитрозо-2-нафтол, слабокислый раствор Тиокарбанилид, кислый раствор Антипирин Щавелевая кислота, лимонная кислота, 1—2 М НС1 Кристаллический фиолетовый, мочевина, 5пС1г, NaNO2, HCI Родамин В KJ, H2SO4 Фуксин, цитрат натрия; рН = 1,04-1,2 Малахитовый зеленый, цитрат натрия; рН = =0,6-i-l,2 Хлороформ Диэтиловый эфир, диизопропиловый эфир, метил-изобутилкетон, амиловый или изоамиловый спирт Этилацетат, амиловый спирт Диэтиловый эфир Коричная кислота в амилацетате Диэтиловый эфир 8-Оксихинолин в амилацетате Нитрометан + бензол Нитробензол Бензиловый спирт Хлороформ + изобутиловый спирт Хлороформ Этилацетат Пиридин Бутиловый спир г Хлороформ, амилацетат Пиридин Бензол Диэтиловый эфир Хлороформ Этилацетат Толуол Диизопропнловый эфир Бензол Амилацетат »
106
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
Sc ...... Бензоат натрия; рН = 7 Этилацетат, бутиловый или амиловый спирт
Морин, кислый раствор Бутиловый, амиловый или циклогексиловый спирт
Хинализарин, щелочной раствор Изоамиловый спирт
Se Си, Fe, Те 3, З-Диаминобензидин, ЭДТА; рН = 6ч-7 Толуол
Диэтилдитиокарбамат натрия, ЭДТА; pH =5-4-6 Четыреххлористый углерод
Si,v Ni (NH4)2MoO4, разб. HNO3 Амиловый спирт
Sn,v As, Sb Н2О2, 1 М HNO3 Дибутилфосфорная кислота (0,6 М) в дибутиловом эфире
5, 7-Дибром-8-оксихино-лин; pH =1,0 Изобутиловый спирт
Та Nb, Ti Пирокатехин (20%), оксалат аммония; рН = 3 Бутиловый спирт
Все элементы, кроме Nb. Se, Те 0,4 Л1 HF, 6/И H2SO4 Диизопропилкетон
Фториды; pH—1 N-Бензоилфенилгидроксил-амнп в хлороформе
1 М HNO3 Дпбутилфосфорпая кислота (0,6 М) в дибутиловом эфире
Метиловый фиолетовый; рН = 2,3 Бензол
TcV11 Mo, U (CcH5)4AsCl; pH =104-11 Хлороформ
4 М NaOH Пиридин
Те Bi, Cd, Си HCI. SnCl2 Этилацетат
Se Диэтилдитиокарбамат натрия, NaCN, ЭДТА; рН = 8,5-=-8,8 Четыреххлористый углерод
Отделение Te,v от TeVI 2—10 Л/ НС! Трибутил фосфат
Th Ce, V. Y A1(NO3)3 Окись мезитила
La, LTVI рН = 2 N-Бензоилфенилгидроксил-амин (0,1 Л/) в хлороформе
507
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
для РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
Th Р. 3. nh4scn Амиловый спирт
Т1 Си Салицилальдоксим, тиомочевина; pH=5,3 Изобутиловый спирт
Nb Пирокатехин (20%), оксалаты; рН = 3 Бутиловый спирт
Nb, Та Купферон, тартрат аммония; рН = 5 Изоамиловый спирт
Морин, кислый раствор Амиловый спирт
Сульфосалициловая кислота, ацетат трибутил-аммония; рН = 2,4ч-4 Хлороформ
Т1 Ag, Аи, Си, Fe, Hg, Pd, Sb, W, Zn NaCN; рН=9-=-12 Дитизон в хлороформе
Все металлы, кроме Bl Диэтилдитиокарбамат натрия, NaCN, ЭДТА; рН=11 Четыреххлористый углерод
Сульфосалициловая кислота, метиловый фиолетовый, НС1 Бензол
и Bi, Th Родамин С, бромная вода ЭДТА; рН = 7 » 8-Оксихинолин в метилизобутилкетоне
Co. Cr, Cu, Fe, Mn, Mo, Ni, Pb, Th A|(NO3)3; рН = 0,3 Метилизобутилкетон
Fe, V La 1-Нитрозо-2-нафтол рН=3,5 Изоамиловый спирт N- Бензоилфенилгидроксил-амин (0,1 Af) в хлороформе
Nd, Pr Ацетаты; р.Н=5,5-=-6 Диэтилдитиокарбамат ди-этиламмония в хлороформе
Th 1 - (2- Пиридилазо) -2-наф-тол, ЭДТА о-Дихлорбензол
Все металлы, кроме Be Ca(NO3)2, ЭДТА; рН = 7 Дибензоилметан в этилацетате
- HNO.3, высаливатели: AI(NO3)2, NH4NO3, NaNO3 и др. Диэтиловый эфир, этилацетат, метилизобутилкетон; трибутилфосфат в четыреххлористом углероде, бензоле или октане
108
НЕКОТОРЫЕ ЭКСТРАКЦИОННЫЕ СИСТЕМЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
Продолжение
Экстрагируемый элемент Отделяемые элементы Водная фаза Органическая фаза
и Фенилкарбоновые кислоты (салициловая,коричная. 3, 5-динитробензойная) Хлороформ, метилизобутилкетон
V А1, Со, Сг, Fe, Мп, N1 NaF; pH = 3,8 ч-4,5 8-Оксихинолин (0,3%) в изобутиловом спирте
Mo, U Салицилгидроксамовая кислота; рН=3,0-;-3,5 Этилацетат
и Диэтилдитиокарбамат натрия, тартраты; pH = 0,40,5 Амилацетат
Бензогидроксамовая кислота, кислый раствор Гексиловый спирт
N-Бензоилфенилгидроксил-амин, кислый раствор Бензол
KSCN. SnCI2 Этилацетат
W А1, Сг, Мп, Nb, Ni. Та, Tl, V Толуол-3, 4-дитиол, (NH2OH)2-H2SO4, НС1 Амилацетат
Mo HCI, SnC)2 Толуол-3,4-дитиол в амилацетате
Все металлы, кроме Мо а-Бензоиноксим, кислый раствор Хлороформ
• Н3РО4. ЗМ H2SO4 Амиловый спирт
Роданиды, SnCl2, HCI Диэтиловый эфир, диизопропиловый эфир
0.1 М HNO3 Дибутилфосфорная кислота в хлороформе
Zn Bi, Ga, In, Pb, Sb, Sn, Ti. U NH4SCN, пиридин Хлороформ
Cd KJ Циклогексанон
Все металлы, кроме Sn*' Тиосульфаты, цианиды; рН = 44-5 Дитизон в четыреххлористом углероде или хлороформе
Zr Се, V, Y A1(NO3)3 Окись мезитила
Nb и другие продукты деления (J Щавелевая кислота, Н2О2, IM H2SO4, 2,5М (NH4) 2SO4 Дибутилфосфорная кислота (0,06 М) в дибутиловом эфире
109
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Экстракция комплексов металлов органическим растворителем, содержащим комплексообразующее вещество HR. описывается уравнением реакции:
Ме'води+<" + г)(Н«'орг 7=* [М^л<Н^]орг+«Нв+одн
Константа равновесия реакции Ко называется в этом случае коистаитой распределения:
к [М^<НЧ]орг[нХД„ D ЕН+1вод..
Гме" + 1 [HR]',+r IHR]"+r
I Jboah ‘ морг 1 морг
Концентрация ноиов Мея+ совпадает с общей концентрацией металла в водном растворе при отсутствии гидролиза или комплексообразования.
Величина pH, при которой 0 = 1. обозначается как рНп и часто используется для характеристики равновесия экстракции. Чем больше разность величин pHiyt для двух ионов металлов, тем лучше оии разделяются при экстракции.
Константы распределения оксихинолииатов
Реагент:
(рК-9,71)
1 II 1 , + 1 11 11 h+
OH 0
(HR) (R>
Исходная концентрация элементов в водном растворе 1,0*10 4—2,0-10 4 моль!л\
ионная сила раствора 0,1 (HCIO4, NaCIO4, NaOH); температура, при которой проводилась
экстракция, 20 С. Растворитель — хлороформ.
рНу при концентрации
Элемент Экстрагируемый комплекс Ко 8-оксихиполина
0,10 Л1 0,01 м
Ag AgR HR 3,1 • 10“5 6,51 8.51
Al A1R3 6,0 10“6 2,87 3,77
Ba BaR2 2HR 1,3 • 10“21
Be BeR2 2,4-10“10 5,81 6,81
Bi111 BIR3 6,3- 10“2 2.13
Ca CaR2 HR 1,3-10'18 10,38
Cd CdR22HR • 5,1 • 10“6 4,65 6,65
Co CoR2 • 2HR 6,9 • 10“3 3,21 5,08
Cu11 CuR2 5,9 • 10* 1.37 1,77
Fein FeR3 1,3- 104 1,00 1,50
Ga QaR3 5,2- 103 1,07 1,57
In InR3 7,8 1,54' 2,13
La LaRs 4,3-10“17 6,46 7,46
Mg MgR2 7,4-10“16 8,57 9,57
Movl MoO2R2 7,6 • 109 — 0,5
Mn“ MnR2 4,8 • 1О“10 5,66 6,66
Ni NiR2 . 6,6- 10“ 3 2,38 3,16
110
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Элемент Экстрагируемый комплекс K0 pHi/ при концентрации 8-окснхинолнна
0,10 Л1 0,01 м
РЬ PbR2 9,1 • 10~9 5,04 6,04
Pd11 PdR2 ~ 1016 <0 <0
Sc ScR3 • HR 2,3- I(T7 3,57 4,87
Sr SrR2 • 2HR 2,0. KT 20 12,06 ...
Th ThR. 1,5- IO-8 , 2,91 3,80
TiIV TiOR2 7,9 1,45
Т11П TIR3 ~ 106 • . . 2,05
UV1 UO2R2 • HR 2,5-IO”2 2,60 3,81
Vv VO2R 4,7 • 10' 0,88 1,33
Zn ZnR2-2HR 3,9 - 10" 3 3,30 5,20
Zr ZrOR2 5,9- 102 1,01 1,50
Константы распределения Купферонатов
Реагент:
O=N ч I
H.NO-N-1^/1
(NH.R)
Исходная концентрация в водном растворе одно- и двухвалентных экстрагируемых элементов 10 моль!л\ концентрация элементов другой валентности 10“4 моль/л-. ионная сила раствора ОД (НС1О«, NaClO< и NaOH); температура, при которой проводилась экстракция. 20° С. Растворитель — хлороформ.
Величины pHi/2 соответствуют концентрации купферона 0,05 моль!л.
Элемент Экстрагируемый комплекс Ko PH1/2 Элемент Экстрагируемый комплекс Ko pH./.
А1 A1R3 3,2-10“5 3,51 Nbv <0
Be BeR2 2,9 -10~2 2,07 Pb PbR2 2,9- 10-2 2,06
Bi1" BiR3 . 1,2- 105 —0,4 Pd11 PdR2 <0
Со CoR2 2,75-IO-4 3,18 Sb1" SbR3 . • . <0
Сип CuR2 4,6 • 102 0,03 Th ThR. 2,75.10’ 0,2
Fein FeR3 . . . < 0 Tilv TiR„ < 0
Оа HgH OaR3 HgR2 8,3 • 10’ 8,1 -0,3 0,85 TI"1 T1R3 ~ 103
In InR3 2,6 • 10? 0,5 Vv V OgR * • . <0
La LaR, 6,0- 10-7 3,4 Y YR3 1,8- IO-6 2,9
MoVi < 0 Zn ZnR2 7,4
Zr ZrR4 . . . <0
Ill
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Константы распределения дитизонатов
Реагент:
(рК»4,7)
f Y-nh-n,
о—n=n/
C-S--hH +
о—N=N
(H2R)
(HR-)
Элемент Экстрагируемый комплекс Водная фаза Ко
СС14 СНС13
Ag AgHR 6 H. H2SO4 1,5 • 107 1,0-106
Bi111 Bi (HR)3 Ацетат аммония 0,1 М KCN 0,1 М NaCI 0,1 AI лимоннокислый натрий 0,1 А/ виннокислый калий-натрий 5,6 • Ю9 3,5 Ю9 8,3 104 3,9 • 10-6 2,5-10'6 2,3 -10 6 1,6 • 105 3,4 102 2,7- 10"“ 8,3- 10~'2
Cd Cd (HR)2 Ацетат аммония 1 М NaCI 0,2 Al лимоннокислый натрий 0,2 М виннокислый калий-натрий 38,5 0,27 1,2-10-2 0,38 3,4 2,6 • 10~2 1,4 -10~5 3,0 - 10~2
Co Co (HR)2 Ацетат аммония 1 М NaCI 0,2 AI лимоннокислый натрий 0,05 М виннокислый аммоний 39 12 4,6 • КГ4 3,2-10 2 7,9 - 10-3 3,0 10~7 3,07-10~7
Си» Cu (HR)2 0,1 М NaClO4 0,1 н. H2SO4 0,1 AI NaCI 0,5 AI KB г 0,5 M KJ 3,0-1010 3,4- 10’° 1,0- 10‘° 3,4- 101с 3,4-1010 3,2-106
HgH Hg (HR)2 NaClO4+HClO4 7,1 1026 . . .
In In (HR)3 Ацетат аммония 6,9 10‘ . . .
Ni N1(HR)2 Ацетат аммония 0,05 AI виннокислый аммоний 6,4-10-2 1,2-10 3 1,06-10"8
Pb Pb (HR)2 Ацетат аммония 1 AI NaCI 2,4 0,12 0,13 9,6 10~3
0,1 М KCN 0,2 А1 виннокислый калий-натрий 0,2 А1 лимоннокислый натрий 4,5 2,0-10-3 5,4-10~5 0,88 2,3 Ю-4 6,6 10~ 6
112
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Элемент Экстрагируемый комплекс Водная фаза *0
СС14 СНС13
РЬ Pb (HR)2 0,2 М лимоннокислый натрий, 0,1 М KCN 4,5 10"5 5,0 • 10“6
Т11 T1HR 4,6- 10“4
Zn Zn (HR)2 Ацетат аммония 0.1 М NaCI 0.1 М KCN 0,1 М Na2S2O3 . 0,05 М виннокислый аммоний 2,0-102 1,0- 102 2,2 • Ю2 0,2 102 4,4 2,0 4,4 1,2 5,4 • 10-5
Реагент: (рА-8.82)
Константы распределения ацетилацетонатов
i
Сн3 —С —СН = С—сн3 сн.-с-сн=с-сн3+н +
« I II I
° ОН о О
<HR> (R)
Исходная концентрация металла в водном растворе 10~ —10~~4 моль/л; ионная сила раствора 0.1 (HCIO4, NaClO4, NaOH); температура, при которой проводилась экстракция, 20° С. Растворитель — бензол. Концентрация реагента 0,1 моль(л.
Элемент Экстрагируе мый комплекс Ko PH./2
А1 A1R3 3,3- 10'6 3,30
Be BeR2 1,62 10-2 2,45
Си11 CuR2 1.17.10-3 2,90
Fe111 FeR3 4,07-Ю-1 1,60
Оа OaR3 3,09-IO-5 2.90
Mg ’ MgR2 . . . 9,4
In lnR3 6,3 • 10-7 3,40
Pb PbR2 7,08-10-‘° 6,2
Sc ScR2 1,48 - 10-5 2,95
Sn11 SnR2 • • . ~5
Th ThR4 6,92-10-12 4,10
8 Зак. 783
113
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Константы распределения тиофен карбонил трифторацето патов
Реагент:
(рК=6.38)
СН—СН О ОН СН—СН О О-
II II II I II И II I
СН С С-СН=С-CF, СН С-----------------C-CH-C-CFS + Н '
(HR1 Ч' <Rl
Величина Ко приведена с учетом зависимости коэффициента активности реагента от его концентрации при температуре 25° С. Эта зависимость для тиофенкарбонилтрифтор-ацетона описывается уравнением:
/HR=1 -0,24 [HR]0-48
Растворитель — бензол. Концентрация тиофеикарбонилтрифторацетона в бензоле 0.2 М. ц — ионная сила.
Элемент Экстрагируемый комплекс Водная фаза А-о рН|/,
А1 A1R3 5,9- 10’6 248
Ат AmR3 Разб. кислота 3,5- 10’8 3,22
Ва BaR2 ~ 2,3- 10”16 8,0
Вк BkR3 0,1 .41 CH2C1COONH4 ~ 1,5-10-7 3,0
Be BeR2 6,3-10“4 2,33
Bi“’ BiR3 Разб. NaCl 6,2- 10’" 1,80
Са CaR2 Разб. NaCl 1 • 10’12 6,7
Cd CdR2 . . . > 8
CeHl CeR3 HCi +KCI; и = 0,1 3,7- 10“10 3,88
Cm CmR3 0,1 M CH2C1COONH4 I 10’8 3,4
Co CoR2 ~2- 10-7 4,1
Cull CuR2 4,8 10’8 1,38
Dy DyR3 НС1 + КС1; Ц = 0,1 9,3 • 10~8 . 3,08
Es EsR3 0,1 M CH2C1COONH4 6-10”8 3,1
Eu EuR3 НС1-+- КС1; ii = 0,l 2,2-10~8 3,29
Fe HCi, 0,1 M Na2Cr2O7 2-103 —0,24
Fm FmR3 0,1 M CH2C1COONH4 8-10’8 3,1
Od GdR3 HCI4-KC1; ц = 0,1 2,7 10~8 3,26
Hf . . • 2—4 M HC1O4 3,7 • 107 —1,54
Ho H0R3 HCI + KCI; ]t = 0,l 5,6- 10’ 8 3,15
In lnR3 Бифталат калия -|- HCI 4,6- 10’5 2,18
La LaR3 HCI + KC1; [i = 0,l 3,1 • 10’“ 4.24
Разб. кислота 1,7- 10’10 3.99
114
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Элемент Экстрагируемый комплекс Водная фаза pH.,,
Li LiR 0,1 M LiCl >8
Lu LuR3 HCl + KCl; Ц = 0,1 1,7- 10“ 7 2,99
Nd NdR3 HCl + KCl; и = 0,1 2,7 • 10“9 3,59
NpIV NpR4 HCI HCIO4 + NaCIO4; p = 2 3,6 • 103 3,8 • 105 —0,34 —0,66
Ni HNO3 >5
Pb PbR2 Разб. NaCl 5,8 • 10 6 3,34
PalV PaR4 6 M HCI в присутствии Cr2+ 5,2 • 106 —0,94
PaV —0,73
Pm PmR3 HCI -f- KC1; Ц = 0,1 8,8 • 10~9 3,42
Po . . . Разб. NaCl 4,6 - IO-1 0,89
Pr PrR3 HCl + KCl; p = 0,1 1,4- 10“9 3,68
Puiil PuR3 0,005 M FeH + LiNO3; p = 0,1 3,6- I0“5 2,21
Puiv PuR4 1 M HCIO4 7,0- 106 —0,97
PuVi PuO2R2 0,05 M HNO3 1.5-10"2 1,64
Ra RaR2 Разб. NaCl > 7
Sm SmR3 HCl + KCl; p = 0,1 2,1 • IO'8 3,29
Sc ScR3 HCl + KCl; p = 0,l 1,7- IO-1 0,99
Sr SrR2 ~ 7,5- 10“15 7,8
Tb TbR3 HCl + KCl; p = 0,1 3,1 • IO-8 3,24
Th ThR4 Разб. NaCl 0,1 M HC1O, + L1CIO4; p = 3 10 7,5 0,48 0,52
Tl1 TIR Разб. NaCl 2,2-10“5 5,35
Tl’11 Разб. NaCl 1,1 IO-2 2,78
Tu TuR3 HCl + KCl; p = 0,l 1,1 • 10~7 3,05
U'V ur4 HCIO4 + NaClO4; p = 2 1,9 • 105 —0,58
UVI uo2r2- hr HClO4 + NaClO4; p = 2 5,5 • 10“3 1,79
Yb YbR3 HCl + KCl; p = 0,l 1,9 - 10-7 2,97
Y YR3 HCl + KCl; p = 0,l 4,1 • 10“8 3,20
Zr ZrR4 HCI 1,8-10' —1,08
8*
115
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Константы распределения бензоилацетонатов
Реагент: (рК-8,73)
^-С—СН=С—СН3 -7~> € \-С-СН=С-СН3 + Н +
X=Z II I Х=/ II I
о он о о-
(HR) (R)
Исходная концентрация металла в водном растворе 10 —10 4 моль {л:, ионная сила
раствора 0,1 (HCIO«, NaCIO4, NaOH); температура, при которой проводилась экстракция» 20° С. Растворитель — бензол. Концентрация реагента 0,1 моль(л.
Элемент Экстрагируемый комплекс Ko рН./2
Ag AgR 1.5-10-7 8,9
Al A1R3 2,5-10-7 3,60
Be BeR2 1,3 -10-3 2,94
Bi"1 BiR3 9,2
Ca CaR2 5,9-10"18 10,1
Cd CdR2 7,7 - IO-15 8,10
Co CoR2 7,7- I0-11 6,60
Cu” CuR2 6,6 • 10-6 3,00
Fe1” FeR3 3,16 1,2
Ga GaR3 4,5-10-6 3,10
Hg” HgR2 . . . 3,7
In InR3 5-10-9 4,10
La LaR3 3,5-10"19 7,89
Mg MgR2 2,2 - IO-'6 9,38
Mn” MnR2 2,3-10"14 8,30
Ni NiR2 7,6-10-12 6,90
Pb PbR2 2,45 • 10-8 5,7
Pd” PdR2. 15,85 0,4
Sc ScR3 1•10-5 3,10
Sn” SnR2 ~5
Sr SrR2 ~ 10-2° 11,5
Th ThR, 2,1 -10-7 2,90
Tl” TiOR2 . . . 2,4
Tl1” T1R3 . . . 4,0
(JVI UO2R2 • HR 2,1 - 10-4 3,82
Zn ZnR2 1,6-Ю-10 6,50
Zr ZrOR2 1,6-Ю-10 3,4
НО
КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ НЕКОТОРЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
С ОРГАНИЧЕСКИМИ АДДЕНДАМИ
Продолжение
Константы распределения дибензоилметанатов
Реагент: (РК=9,35)
? V-C-CH=C-Z \ -J—» ^-с-сн=с-^^+ н+
\=Z || | Х=/ || I \=/
о он о о-
(HR) (R)
Исходная концентрация металла в водном растворе 10 3 —10“4л«с>ль/л; ионная сила-раствора 0,1 (НС1О4, NaClO^ NaOH); температура, при которой проводилась экстракция, 20° С. Растворитель — бензол. Концентрация реагента 0,1 моль!л.
Элемент Экстрагируемый комплекс K0 рН>/2
Ag AgR 2,63 • 10-8 9,9
Al A1R3 1,2-W-8 4,00
Ba BaR2 . . . ~ 12
Be BeR2 3,47-Ю-8 2,73
Bi111 BiR3 ... 10,5
Ca CaR2 1-ю-18 9,9
Cd CdR2 1,05- Ю-13 8,00
Co CoRj 1,66- Ю-,° 6,40
Cu11 CuR2 1,6-Ю-3 2,90
Fe1” FeR3 1,17-Ю-1 1,70
Oa GaR3 1,74-10-8 2,90
Hg” HgR2 . . 3,9
In InR2 2,45- Ю-7 3,60
La LaR3 3,47-10"19 7,42
Mg MgR2 1,9- Ю-14 8,50
Mn” MnR2 1,95 - Ю-13 7,80
NI N1R2 9,55- Ю-11 6,40
Pb PbR2 3,55 -10-9 5,6
Pd” PdR2 ... 1,8
Sc ’ ScR3 9,12- Ю-8 3,05
Sr SrR2 ~1,26-1О-20 11,1
Th ThR, 4,17-Ю-8 2,60
Tl” . T1OR2 2,5
Tl1" T1R3 3,8
UVI UO2R2 • HR 7,6 10-4 3,56
Zn ZnR2 2,14-10-1° 6,40
Zr ZrOR2 . . . 3,3
117'
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В СИСТЕМАХ ОРГАНИЧЕСКИЙ РАСТВОРИТЕЛЬ — вода
Сведения о коэффициентах распределения органических соединений см. также «Справочник химика». 2-е изд., т. Ill. стр. 474.
Коэффициенты распределения органических соединений в системах изобутиловый спирт — вода и диэтиловый эфир — вода
В скобках приведены недостаточно надежные данные.
Соединенис Температура, °C Концентрация в воде, ММОЛЪ[Л Коэффициенты распределения в системах
изобутиловый спирт — вода ДИЭТИЛОВЫЙ эфир — вода
С!
Метиламин .... 20 670 0,62 0,023
Метиловый спирт . . 20 1920 0,14
Мочевина 19 3090 0,13 0,00047
Муравьиная кислота 18 47,6—836 0,37—0,42
Синильная кислота 2,4
Формальдегид . 20 58,2 0,11
Формамид . . 19 1738 0,22 0,0014
Цианамид . . 50 . . 0,11
С2
Ацетамид 19 1750 0,33 0,0025
Ацетонитрил . . • 20 624 0,60
Гликолевая кислота 21 78,3—748 0,35—0,33 0,028
Диметиламин 21 47,9 1,2 0,055
Дициандиамид 19 170 0,43 0,0029
Иодуксусная кислота .... 20 84,5 7,2
Метиловый эфир карбамино-
вой кислоты . 23 400 0,14
Метплмочевина . . 19 982 0,24 0,0012
Трихлоруксусная кислота 18,8—105 4,2—10
Хлоруксусная кислота 18 26,0—290 2,2—2,7
Щавелевая кислота 23 71,4—581 0,39—0,61 0,1
Этаноламин 20 165 0,24 0,0013
Этиламин . . 18 44,0 1,2 0,060
Этилендиамин . 22 85,6 0,23 0,0033
Этиловый спирт .19 1050 0,26
с3
Амид малоновой кислоты • . 19 911 0,086 0,0003
Амид пропионовой кислоты 19 1020 0,69 0,013
Аминопропионовая кислота 19 2080 0,0069 0,0001
Ацетон ... 20 617 0,062
Бромпропионовая кислота 19 65 13
1, З-Диаминопропапол-2 21 820 0,12 0,0002
Глицерин 19 2170 0,10 0,00066
Глицериновая кислота 20 87,0—697 0,18—0,22 0,009
Изопропаноламин 21 385 0,43 0,0043
Малоновая кислота ... 21 60,6—613 0,69—0.70 0,1
Соединение Температура, СС Концентрация в воде, ММОЛь!Л Коэффициенты распределений в системах
изобутиловый спирт— вода диэтиловый эфир — вода
Метиловый эфир гликолевой кислоты (простой) .... Метиловый эфир уксусной 18 (1900) . . . (0,15)
кислоты 20 177 2,7
Молочная кислота . . 21 60,5—612 0,66—0,72 0,091
Пропил амин 21 194 0,29
1, 2-Пропилендиамин 20 590 0,34 0,0011
Пропиловый спирт 22 935 1,9
Пропионовая кислота . • 22 15,0—67 1,7—1,8
Пропионовый альдегид 19 360 2,0
Триметиламин ... 21 183 0,46
Триметилендиамин ... 22 76,1 0,36 0,0007
Уретан 22 (500) (0,64).
Цианоуксусная кислота . . • 21 8,3 0,36
с4
Амид масляной кислоты . 18 690 1,5 0,058
Аминомасляпая кислота . 20 1286 0,016 0,00001
Бромянтарная кислота 25 5,6-87,9 1,5—2,4
Бутиловый спирт .... 18 242 7,7
втор-Бутиловый спирт . 20 390 4,5
трет-Бутиловый спирт .... 20 634 2,2
Винная кислота 21 79,7—792 0,15—6,17 0,0034
1, 2-Дибромянтарная кислота 25 30,2 17
Дигликолевая кислота 20 345 0,49 0,03
Диэтилендиамин 18 77,8 0,24 0,00052
Изобутиловый спирт . 20 259 6,9
Малеиновая кислота . 19 54,7—247 0,88—6,98 0,15
Масляная кислота . . . . • Метиловый эфир молочной 21 12,1—26,4 6,1—6,5
кислоты 19 (1400) (0,37)
Нитрил масляной кислоты 21 (65) (Ю)
а-Оксиизомасляная кислота 20 46,0—452 1,2 0,26
Тетраметилендиамин . • 22 62,8 0,69 0,0013
Фумаровая кислота . 20 18,4 4.6 1,5
Эритрит . . . 20 (2300) (0,037) (0,00611)
Этиленцианпд Этиловый эфир уксусной кис- 18 23,2 0,32
лоты 20 78 8,5
Яблочная кислота . . • 22 75,4—746 0,35—6,37 0,015
Янтарная кислота 23 50,8 0,96 0,15
с6
Амид изовалериановой кис-
лоты ..... 24 (250—500) (0.17)
Аминопиридин 21 34,2 0,77
Арабиноза 20 (2000) (0,019) (0,0004)
Глутаровая кислота ..... 19 34,4 2,0 0,27
11&-
118
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Соединение Температура, °C Концентрация в воде, ММ0ЛЬ[Л Коэффициенты распределения в системах
изобутиловый спирт — вода диэтиловый эфир— вода
Диметилмалоновая кислота . 25 26,2—268 1,3—1,6
Изоамиламин 19 34,2 2,0
Итаконовая кислота . . 22 34,4 1,8 0,3
Левулиновая кислота .... 20 287 1,2 0,26
Пентаметилендиамин .... 22 42,1 1,5 0,0025
Пентаэритрит 19 411 0,14 0,0003
Пиперидин 18 62,6 . . . 0,57
Пиридин 18 302 . . . 1,2
с6
Адипиновая кислота 22 22,9 3,5 0,54
Аконитовая кислота 24,3—236 0,33—0,47
Беизолдисульфоновая кислота 19 73,0 0,4 0,0013
Диизопропаноламин 21 515 0,7 0,0059
Дипропиламин 17 14,3 6,8
Диэтиламинэтанол 23 23,3 3,1 0,35
Гексаметилентетрамин . . . 18 525 0,067 0,00026
Гидрохинон . 15 . 2,2—3,7
Глюкоза 18 1991 0,011 0,00001
Глюконовая кислота 20 950 0,034 (0,032)
Капроновая кислота 1,66—13,5 90—93
Лимонная кислота 21 79,6—788 0,28—0,32 0,0086
л-Нитрофенол . . . ... 160
о-Нитрофенол . . . 150
л-Нитрофенол ... ПО
Пикриновая кислота .... 15 60 3,7
Пирогаллол 20 380 1,7
Пирокатехин 20 81,8 11
Рамноза 20 (1000) (0,057) (0,00019)
Резорцин 4,2
Триэтаноламин . 23 176 0,26 0,0011
Триэтилентетрамин 20 735 0,15 0,00007
Фенол 19 13,5 44
Флороглюцин 21 188 0,45
Хинон 19 2,92—8,41 . . . 0,33—0,31
с7 •
Амид диэтилмалоновой кисло-
ты ............ . . • (50) (0,012)
л-Аминобензойная кислота 18 31,4 1,5
о-Аминобензойная кислота 19 31,4 27
п-Аминобензойная кислота 19 55,0 7,6
Бензиламин 18 35,9 1,9
Бензойная кислота 1,9—14,2 70—78
Диацетин 20 (500) (0,22)
Галловая кислота 21 140 0,50
л-Оксибензойная кислота . . о-Оксибензойная (салицило- 19 17.0 21
вая) кислота 20 2,8 . . . 127
120
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Соединение Температура, *С Концентрация в воде, ммоль! л Коэффициенты распределения в системах
изобутиловый спирт — вода диэтиловый эфир —вода
п-Оксибензойная кислота . • 20 36,4 26
Пимелиновая кислота . . . • 25 2,84—10,0 1,3—1,4
Хинная кислота 21 89,9—378 0,081—0,84 0,00031
с8 Диэтнловый эфир винной кис-лоты 18 1087 0,65
Кофеин 17,8 1,2 0,06
Миндальная кислота .... . . . 33,2—231 . . . 2,2—3,2
Пробковая кислота ..... 25 0,49—9,86 . . • 3,6—4,7
Тетраэтиламмоний, гидрат окиси 19 129 0,015 0,00001
Тетраэтиленгликоль 19 732 0,24 0,0024
Тропин 19 19,2 3,1 0,053
Фенилуксусная кислота . . . 28,6 * 37
л-Фталевая кислота ..... 25 0,25—0,4 10—12
о-Фталевая кислота ..... 25 8,5—26,1 1,1—1,2
с9 Азелаиновая кислота .... 25 0,96—3,10 13—15
2-Амино-5- диэтиламинопентан 20 241 0,58
Гиппуровая кислота 17 23,7 . . . 0,39
Гомофталевая кислота . . • 25 3,95—13,8 2,0—2,2
Тетраэтилмочевина 18 25,6 11
Триацетин 18 (100) . . . (1.4)
Тримезиновая кислота ... 20 5,37 11
Триметиловый эфир лимонной кислоты 22 (100) . . . (0,43)
Сю Бензилмалоновая кислота 7,2 15
Камфорная кислота 25 1,48—2,29 . . . 25—26
а-Нафталинсульфоновая кис- лота 23 46,2 1,4 0,0051
Себациновая кислота .... 25 0,36—0,62 - 43—47
Эфедрин 22 34,5 2,0
Си—С23 Антипирин . ... 22 (100) (0,073)
Арбутин 22 201 0,28 0,00074
Атропин . 19 5,52 4,1
Бруцин . . 18 5,58 0,18
Кодеин 12,7 - 0,8
Кокаин 18 0,95 - 138
Морфин 18 (1) . . . (0,81)
Пентаацетилглюкоза .... 20 55,2 16
Пирамидон 20 205 0,63
Сахароза 18 1300 6,0056 0,00001
Стрихнин . . . 20 0.51 2,2
Хинин 20 0,82 44
12 F.
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
П родолжение
Коэффициенты распределения некоторых карбоновых кислот
Концентрация кислот в водном растворе 0.1—0,16%.
Кислота Коэффициенты распределения в системах
бутиловый спирт —вода этилацетат — вода ДИЭТИЛОВЫЙ эфир —вода вода — хлороформ петролей-ный эфир— вода
Адипиновая ..... 3,2 1,1 0,45 > ю <0,1
Азелаиновая > ю > 10 9,1 3,8 < 0,1
Глутаровая 1,7 0,66 0,24 > ю <0,1
{З-Карбоксиадипиновая 1,2 0,31 <0,1 > 10 <0,1
Лимонная 0,28 < 0,1 <0,1 > 10 <0,1
Малоновая 0,67 0,25 0,124 > 10 <0,1
Пимелиновая 6,7 2,63 1,1 > ю < 0,1
Пробковая ..... 8,3 6,25 2,94 > ю <0,1
Себациновая > ю > 10 > ю 0,63 0,154
а-Фениладипиновая . . > Ю > 10 > ю 4,0 <0,1
Фумаровая 3,3 1,7 0,91 > ю <0,1
Щавелевая 0,217 <0,1 < 0,1 > 10 <0,1
Янтарная ...... 1,21 0,37 0,125 > ю <0,1
Коэффициенты распределения некоторых фенолов в системе циклогексан — вода
Вещество Коэффициенты распределения при pH водного раствора Вещество Коэффициенты распределения при pH водного раствора
6,65 11,08 6,65 11,03
Фенол 0,22 0,02 2,6-Ксиленол . . . 21,7 3,57
о-Крезол .... 1,96 0,24 3,5-Ксиленол . . . 4,02 0,33
.м-Крезол 1,01 0,09 о-Этилфенол . . . 10,4 1,45
п-Крезол 1,14 0,11 .м-Этилфеиол . . . 4,31 0,31
2, 4-Ксиленол . . . 7,06 1,63 м-Этилфенол . . . 4,43 0,40
2,5-Ксиленол . • . 7,46 1,16 З-Метил-5-этилфенол 14,6 1,49
122
Хроматографические методы разделения
В настоящем разделе приводятся сведения по хроматографии неорганических и органических веществ на бумаге, а также по газовой хроматографии органических веществ.
Данные по ионообменной хроматографии см. стр. 172.
Более подробно см.: 1. Хроматография на бумаге, ред. И. М. Хайе, К. Мацек, перев. с чешек., ИЛ. 1962. — 2. А Кем ле м а нс, Хроматография газов, перев с англ.’ ИЛ, 1959. — 3. М. Ши и гл яр. Газовая хроматография в практике, перев. со словацк., Изд. «Химия», 1964. — 4. Э. Байер, Хроматография газов, перев с нем.. ИЛ, 1961 — 5- А. А. Жуховицкий. Н. М Туркельтауб, Газовая хроматография. Гостоптех-издат, 1962.—6. R. Block, A Manual of Paper Cromatography and Paper Electrophoresis. Нью-Йорк, 1958
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
В таблицах приведены значения относительной скорости передвижения веществ на бумаге:
J hp
где h — расстояние, пройденное веществом от старта до точки максимальной концентрации; Zip — расстояние, пройденное растворителем от старта до фронта.
Проявление зон, образуемых неорганическими ионами, проводится обычными групповыми или индивидуальными аналитическими реактивами (стр. 36 и 191). Некоторые системы проявителей приведены на стр. 132.
Принятые сокращения см. стр. 16.
Значения некоторых ионов в системах с комплексообразователями
Растворители:
1. Бутанол, нас. 0.1 н. HNO*, — бензоил ацетон (100 : 0,5).
2. Бута иол, нас. 2 и. HNO3, — ацетилацетон (100 : 1).
3. Бутанол, нас. 1 н. HNO3. - ацетоуксусный эфир (20 : I).
4. Бутанол, иас. 1 в. HNO3. “ антипирин (100 : 1).
5. Диоксан — Н2О—HNO3, — антипирин (100 : 2,5 : 1 : 1).
6. сшити-Коллидин — 0,4 и. HNO.< (1 : 1).
Пон Растворитель
I 2 3 4 5 6
Ag+ 0,10 0,15 0,18 0,19 0,08 0,78
А13+ 0,03 0,08 0,10 0,08 0,02 0,00
As^ 0,43 0,45 0,45 0,49 0,28 0,64
Ва2 + 0,02 0,07 0,06 0,03 0,01 0,27
Bi3 + 0,02 0,23 0,20 0,21 0,63 0.00
Са2 + 0,05 0,07 0,13 0,08 0,12 0,52
Cd2+ 0,05 0,13 0,15 0,15 0,28 0,76
Со2+ . . . . . 0,00 0,10 0,13 0,12 0,04 0,73
Сг3 + 0,03 0,08 0,10 0,08 0,01 0,00
Си2+ 0,22 0,13 0,15 0,18 0,24 0,76
Fe3+ 0,96 0,45 0,14 0,16 0,12 0,00
Н^+ 0,24 0,44 0,50 0,00 0,43 0,00
Hg2+ 0,32 0,44 0,50 0,00 0,42 0,00
к+ . . . 0,05 0,10 0,11 0,06 0,02 0,32
Mg2+ 0,06 0,10 0,14 0,10 0,03 0,64
Мп2+ 0,07 0,11 0,14 0.13 0,10 0,71
Na+ . . 0,06 0,10 0,11 0,06 0,03 0,43
Nl2+ . . 0,03 0,08 0,13 0,08 0,05 0,76
Pb2 + .... 0,03 0,08 0,08 0,10 0,18 0,00
Sb111 ... . . 0,00 0,02 0,00 U,00 0,65 0,38
Sn2+ 0,59 0,82 0,70 0,73 0,78 0,00
SnJV 0,55 0,80 0,65 0,68 0,58 0,00
Sr2 + . . 0,04 0,05 0,07 0,05 0,03 0,40
Zn2+ 0,05 0,10 0.13 0,10 0,08 0,75
123
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Значения Rj, катионов для различных растворителей, содержащих HCI
Ион Растворители
бутанол, насыщенный метилпропнлкетон — 8 н. НС1 ацетон — 6 н. НС1
1 и. HCI 2 н. HCI 3 н. HCI 20:3 4:1 10: 1
Ag+ 0,00 0,00 0,00 0,35 0,62
А13г 0,07 0,07 0,22 0,03 0,05 0,00
As111, Asv 0,43 0,52 0,63 0,57 . . . • 0,68
Ва2+ 0,02 0,02 0,08 0,02 0,05
Bi3+ 0,43 0,54 0,68 0,62 0,52 0,92
Hg2/ 0,98 0,93 0,94 0,79 0,90 0,99
Hg2 + 0,75 0,74 0,83 0,74 0,85 0,99
Ca2+ 0,04 0,04 0,12 0,03 0,05 0,00
Cd2+ 0,33 0,60 0,48 0,86 0,87
Co2 + 0,07 0,10 6,27 0,27 0,75 0,39
Cr3+ 0,08 0,24 0,03 0,05 0,00
Cu2+ 0,08 0,17 0,30 0,32 0,62 0,62
Fe3+ 0,08 0,18 0,45 0,93 0,94 0,78
Mg2+ 0,08 . * . •
Mn2+ 0,07 0,11 0,28 0,11 6,28 0,24
Ni2+ 0,07 0,08 0,27 0,07 0,05 0,15
Pb2+ 0,00 0,00 0,00 0,20 0,22 0,62
Sb111, Sbv ... 0,59 0,61 0,77 0,85 0,91 0,87
Sn2 + 0,65 0,67 0,82 0,87 0,88 0,92
Snlv 0,62 0,67 0,82 0,00 0,00 0,92
Sr2+ 0,03 0,04 0,10 0,00
Zn2+ ....... 0,53 0,61 0,76 0,47 0,83 0,83
бумаге, пропитанной 8-оксихинолином
Значения Rj некоторых катионов на
Катион Растворитель
Диоксан пиридин метанол этанол
А13+ 0,79 0,96 0,65 0,97
Ва2+ 0,68 0,00 0,46 0,06
Са2+ 0,11 0,42 0,08
Cd2+ 0,00 0,91 0,14 0,00
Со2+ 0,94 0,87 0,86 1,00
Си2+ 0,81 0,91 0,65 0,00
Ге3+ 0,99 0,92
Mg2+ 0,53 0,60 0,10
Ni2+ .... 0,79 0,93 0,79 0,75
Pb2+ . 0,69 0,83
Sb111 0,00 0,90 0,69 0,57
124
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Зависимость Rf некоторых катионов от природы аниона
Восходящая хроматография; растворитель — бутанол, нас. 4 н. СНзСООН.
Аннон Kf
Pb2 + Hg2 + Bl3 + Cu2 + Cd2+
SO2- 0,57 0,27 0,21
сг 0,84 0,61 0,40 0,42
NO- 0,46 0,69 0,62 0,54 0.52
сн3соо_ 0,51 0,82 0,57 0,54
Системы для хроматографического разделения смесей иоиов
В таблицах приведены данные для хроматографического разделения смесей нонов: растворители и их соотношения (большей частью объемные), тнп хроматограммы и значения R f.
Перечень таблиц
1. Ионы Ag+, Hg2+. Pb2 +
2. Ионы Cu2+, Pb2 + , Bi3+, Cd2+, Hg2+
3. Ионы As"', Sb111, Sn2+
4. Ионы Ft3 + , Cr3+, Al3+, T1IV, VV, UO2+
5. Ионы Co2+, Ni2+, Mn!+, Zn2+, Movl
6. Ионы Mg2+, Ca2+, Sr2+, Ba2+
7. Ионы щелочных металлов и аммония
ом л П1 dJV D .II „.III т Ill „ III Л IV
8. Ионы Au , Pt , Pd , Rh , Ir , Ru , Os
9. Некоторые смесн катионов
10. Галогенид- и роданид-ионы
11. Различные фосфат-ноны
12. Анионы различных кислот фосфора
13. Некоторые смеси анионов
Систематический хроматографический анализ смеси катионов различных аналитических групп приведен в отдельной таблице (стр. 133).
№ 1 Ионы Ag4', Hg24-, Pb24~
Растворитель Тип хроматограммы Rf
Ag+ Pb2+
Бутанол, нас. 1 н. HNO3, — бензоил-ацетон (200 : 1) Нисходящая 0,10 0,03 0,25
Бутанол — пиридин — Н2О (5:1 : 1) Радиальная 0,86 0,62 0,34
Бутанол — пиридин — Н2О (15:1 : 9) Восходящая 0,52 0,92 0,06
трет-Бутанол — ацетон — Н2О — конц. HNO3 (10:10:3:2) Радиальная 0,25 0,00 0.50
Метилпропнлкетон — 10 н. HCI (20: 3) Восходящая 0,59 0,84 0,19
125
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Предо гжение
№ 2 Ионы Cu2’*’, Pb2 h, Bi3+, Cd2+, Hg2+
Растворитель Тип хроматограммы Rf
Си24 РЬ2 + В13 + Cd2+ Hg2+
Бутанол — Н2О — ацетоуксусный эфир — СНзСООН (10:7: 1 : 2) Нисходящая 0,63 0,18 0,34 0,28 0,83
Бутанол, нас. 3 н. НС1 » 0,20 0,27 0,60 0,77 0,81
Бутанол — изопропанол — 5 н. НС1 (9:9:2) Восходящая 0,12 0,03 0,65 0,73 0,85
трет-Бутанол — ацетон — Н2О — 6 н. HNO3 — ацетил-ацетон (80 : 80 : 22 : 9 : 9) Радиальная 0,40 0,15 0,76 0,32 0,90
Метнлпропилкетон—10 н. НС1 (20 : 3) Восходящая 0,60 0,19 0,40 0,75 0,80
Изопропанол — СНзСООН — Н2О (10: 1 : 1) Радиальная 0,44 0,24 0,51 0,39 0,69
№ 3 Ионы As^I, Sb*”, Sn2 +
Растворитель Тип хроматограммы Rf
As41 Sb’" Sn2 +
трет-Бутанол — хлороформ — 8 н. Радиальная 0,64 0,85 1,0
НС1 — ацетилацетон (45 : 45 : 8 : 2) Ацетилацетон, нас. смесью Н2О + Нисходящая 0,20 0,50 1,0
+ конц. НС1 + ацетон (150:1:50) Бутанол — Н2О — винная к-та » 0.61 0,39 0,75
(20 мл : 20 мл : 4 г)
№ 4 Ионы Fe3+, Сг3+ Al3+, T11V, VV, Uo|+
Растворитель Тип хроматограммы К, J
Fe3 + Сг3+ А13 + TjIV vv ио2+
Ацетон — H2O — конц. HCI (20 : 1 : 1) Нисходящая 0,97 0,64 0,18 0,64
Бутанол— СНзСООН -ацетилацетон — Н2О (100 : 20 : 10 : 7) » 0,73 0,17
Этанол — 5 н. НС1 (Ю: 1) Восходящая 0,56 0,47 0,37 . • • • 0,38 0,57
Ацетон — конц. НС1 (20: 1)* Нисходящая 0,96 0,12 0,50
Амиловый спирт — бензол— HCI (6:1:3)** » 0,95 0,13 0,35
* Камера насыщена пйрамн бензола.
** Разделение хлоридов, растворенных в смесн 15%-ной HCI и 10%-иой лимонной кислоты.
126
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
№ 5 Ионы Со2+, М12ЛМп2+, Zn2*, Movl
Растворитель Тип хроматограммы Kf
Со2+ Ni2+ Мп2 + Zn2+ MOV1
Ацетон — H2O — HCI (100 : 5 : 8) Нисходящая 0,60 0,07 0,30 0,90 . . .
Ацетон — 6 н. HCI (20 : 3) Восходящая 0,51 0,03 0,26 0,82
Метилизобутилкетон — 10 н. HCI (20:3) Нисходящая 0,52 0,04 0,13 0,58 0,90
сплл-Коллидин — Н2О (1 •• В Восходящая 0,48 0,55 0,28 . . .
Тетрагидрофуран — конц. HCI (10:3)* » 0,78 0,27 0,50 1.0 1,0
* Отделяются также ионы Fe3 + , Cd2+(J?y= 1,0), UO!;+(/?^= 0,98), Cu2+(7?^= 0,91) и Vv (Ay = 0,56).
№ 6 Ионы M»2+, Ca2+, Sr2+, Ba2+
Растворитель Тип хроматограммы Rf
Mg2 + Са2 + Sr2* Ba2*
Метанол—этанол (1:1) Радиальная 0,80 0,62 0,49 0,28
Метанол—изобутанол— СНзСООН — Н2О — HCOONa (51 : 30 : 2 : : 15: 2) Восходящая 0,75 0,60 0,45 0,30
Метанол — конц. HCI — NH4SCN (189:10:1) » . . . 0,77 0,52 0,26
Метанол — СНзСООН (49: 1) » 0,74 0,66 0,52 0,39
Этанол — Н2О — пропионовая к-та — конц. NH4OH (21 :2: 1 : [)' » 0,93 0,82 0,56 0,23
Этанол — Н2О — LiCl (40 мл : 10 мл : 1 г) » 0,73 0,50 0,26 0,12
Метанол— конц. НС1 — . Н2О (8:1:1) » 0,85 0,69 0,51 0,23
Метанол — бутанол — силш-коллиднн — 6 н. СНзСООН (2 : 1 : 1 : 1) » 0,81 0,71 0,47 0,26
трет-Бутанол— 6 н. НС1 (1:1) Радиальная 0,60 0,50 0,20 0,10
127
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Растворитель 1 Тип хроматограммы Rf
Mg2 + Са2 + Sr2 + Ва2+
Изопропанол— пиридин— Н2О—СНзСООН (8:8:4: 1) Восходящая 0,53 0,35 0,19 0,09
стмсм-Коллидин — 0,4 н. HNO3 (1 : 1) Нисходящая 0,65 0,52 0,40 0,26
Метанол — НСООН — —Н2О—HCOONH4— изопропанол (50 мл : : 2 мл : 15 мл : 2,5 а: : 30 мл) » 0,75 0,60 0,45 0,30
Фенол, нас. Н2О Восходящая 0,09 0,08 0,80 0,07
Ионы щелочных металлов и аммония
№ 7
Растворитель Тип хроматограммы Rf
Ll + Na + к + NH+ 4 Rb + Cs+
силл-Коллидин — 0,4 н. HNO3 (1 • О Восходящая 0,54 0,45 0,3 . . .
Метанол — Н2О (9: 1)* » 0,72 0,62 0,0
Метанол — СНзСООН (49:1) » 0,66 0,48 0,32
Фенол — мет анол — конц. НС1 (115 : 45 : 40) » 0,27 0,09 0,08 0,15 0,33
Нитробензол, нас. Н2О** » 0,07 0,05 0,11 0,2
Метанол — этанол (1:1) Радиальная 0,68 0,42 0,20 . . .
Фенол, нас. Н2О *** Восходящая 0,17 0,14 0,19 0,25 0,26 0,40
Фенол, нас. 20%-ной НС1 » 0,19 0,11 0,27 0,43
Этанол — Н2О (4:1) » 0,61 0,37 0,25
Этанол — метанол (1:1) » 0,65 0,23 0,08 • 0,32 . . .
Бутанол—метанол (3:7) Радиальная 0,78 0,48 0,31 0,57
* Разделение сульфатов.
*♦ Разделение пикратов.
*** Разделение хлоридов. Проявляющий реагент — 10% раствор Na[Co(NO2)e] в 5%-ной СНзСООН.
128
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
№ 8
Ионы А|дШ, Pt^V, Pd4, Rh^l, 1гШ, RiJH, Os^
Продолжение
Растворитель Тип хроматограммы Kf
AuIH ptIV Pd" Rh’l’ Iri" R.1HI Osiv
Эфир — бутанол — конц. НС1 (1:2: 1) Восходящая 0,98 0,76 0,53 0,09 . . .
Бутанол, нас. 10 %-ной НС1 и 10%-ной HNO3 То же 1.0 0,71 0,55 0,17 0,70 0,13
Метилпропнлкетон —• конц. НС1 (10:3) Нисходящая 0,96 0,81 0,56 0,11 0,11 0,07 0,89
Некоторые смеси катионов
Разделяемые ионы Растворитель Kf Примечания
P. З.111 (нитраты) 100 мл 1%-ного р-ра NH4SCN в метилэтил-кетоне+ 3 мл 16%-ной НС1; фильтруют Определяются по смеси известного состава. Увеличиваются в порядке возрастания атомных номеров Бумага, пропитанная NH4NO3. Фронт хроматограммы 50—55 см. Проявитель 0,1 %-ный спиртовый р-р арсеназо. Чувствительность 0,3% от суммы Р. 3.
Sc3+ и Th4+ от P. 3.'" Тетрагидрофуран — Н2О —72%-ная HNOa (17:2: 1) Определяются по смеси известного состава Чувствительность ~ 1 мкг Sc в 1000 мкг Р. 3.
Zr4+ и Hf4+ (нитраты) Эфир — HNO3 (7:1) То же Проявитель — ализарин (нас. р-р в этаноле, содержащем 5 объемн. % 2 н. НС1).
Nbv и Tav (оксалатный раствор) Ацетон — 8 н. НС1 — 10% Н2С2О4 (8:1: 1) 0,85 и 0,46 Проявитель — таннин или пирогаллол
9 Зак. 783
129
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Разделяемые ноны Растворитель Примечания
ио|+ и Th4+ Oeiv, AsV, Asin Be2+, ln3+, Oeiv и Ga3+ Метанол—пиридин — толуол (7:2:1) Бутанол, нас. 1 н. НС1 Бутанол—3 н. НС1— Н2О (10:3:7) 0,86 и 0,16 0,26, 0,84 и 0,52 0,30, 0,40, 0,54 и 0,70
№ 10
Галогенид- и роданид- ионы
Растворитель Тип хроматограммы *f
F“ Cl“ Br“ J” SCN"
Бутанол— 1,5 н. NH4OH (1:1) Восходящая 0,0 0,10 0,16 0,30 0,45
Бутанол — пиридин — 1,5 н. NH4OH (2:1:2) Нисходящая . . . 0,24 0,36 0,47 0,56
Ацетон — Н2О (4:1) То же 0,25 0,50 0,61 0,77
Бутанол — пиридин — Н2О — NH4OH (16:8: 16: 1) » » 0,12 0,15 0,28 0,50 0,55
№ И
Различные фосфат-ионы
Восходящая хроматография; проявляющий реагент — 5% р-р молибдата аммония в 1 н. H2SO4. затем SnCh или H2S.
Растворитель Kf
ортофосфат пирофосфат трифосфат три-метафосфат тетрамета фосфат соль Грехема
Изопропанол — изобутанол — H2O — NH4OH (40:20:39: 1) 0,36 0,31 0,29 0,52 0,41 0,0
Изопропанол — Н2О — CClsCOOH — NH4OH (75 мл : 25 мл : 5 г : 0,3 мл) 0,71 0,53 0,35 0,22 0,16 0,0
130
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
П родолжение
№ 12
Анионы различных кислот фосфора
Восходящая хроматография.
Растворитель
н рсг 2 2 н„р„о2~ 2 2 5 н„р„о2-2 2 6 НРО2- Р2°Г
Этанол — Н2О — CCI3COOH — NH4OH (80 мл : 20 мл : 5 г : : 0,3 мл) 0,84 0,86 0,86 0,48 0,82 0,61
Этанол — изобутанол — н2о — nh4oh (30 : 30 : 39: 1) 0,75 0,49 0,66 0,39 0,21 0,29
Х-> 13
Некоторые смеси анионов
Восходящая хроматография.
Растворитель
Бутанол — этанол — Н2О (2:2:1) [Fe (CN)B]3- 0,12 [Fe (CN)6]4~ 0,15 s2— 0,16 As°r 0,26 PO3- 4 0,37 0,92
Бутанол, нас. 20%-ной СН3СООН [Fe (CN),p-0,03 AsO3-4 0,15 CrO2-4 0,24 As°r 0,41
Ацетон — конц. НС1 (20: 1) sio2-0,0 ВОГ ~0,6 MoO2- ~l,0
д*
131
ХРОМАТОГРАФИЯ неорганических веществ на бумаге
132
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Систематический хроматографический анализ смеси катионов
Приготовляются три хроматограммы (для трех проб анализируемого вещества):
1. Анализируемое вещество растворяют в 2 н. HNO3.
2. Анализируемое вещество растворяют в 2 и. НС1.
3» Анализируемое вещество растворяют в 2 и. HCI, затем бумажную полосу дважды опрыскивают щелочным раствором NaBrO, каждый раз высушивая, после этого тоже дважды опрыскивают бумагу СНзСООН и высушивают.
Восходящая хроматография; растворитель: бутанол, нас. 0,1 н. HNO3, — бензоилацетон (200 : 1); проявляющие реагенты см. ниже.
Rf Хроматограмма
1 2 3
0,0 Na+, K+ Mn2+, Ni2+, Co2+
РЬ2 + Al3+, Ca2+, Bi3+, Sr2+, Ba2+ Al3+, Ca2 +
0,1 Sb"1 Mg2+, Mn2 + Co2+,Sbin Sr2+, Ba2+, Mg2+
Мп2+, Со2+, Ni2+ Ni2+Cr3 +
0,2 Ag+ Zn2+, Cd2 + Zn2+, Cd2 +
Cu2+, Cd2+ Сц2+
0,35 Hg2/ Hg2+
0,5 Hg2+, As1" As"1, Hg2 +
0,65 Fe3+ Fe3+
0,7 Sn2+ Sn2+
Проявление хроматограмм при систематическом анализе смеси катионов
Для каждой из хроматограмм (см. предыдущую таблицу) предлагается несколько вариантов проявления, причем вначале проявляют хроматограмму реагентом «а», а затем— реагентом «б». Если реагенты «а» и «б» состоят из нескольких компонентов, которыми действуют на хроматограммы раздельно, они перечислены в нужной последовательности, если же реагенты «а» и «б» представляют собой смеси, то между компонентами стоит знак «+». Окраска зон указана раздельно для реагентов «а» и «б».
Хроматограмма Проявляющий реагент Окраска зон
1 а) 1%-ный води, р-р К2С1О4 б) NH3 (газ) РЬ2 + — желт., Ag+ — кр., Hg2+—ор.-кр., Hg2+ —ор. РЬ2 + — op., Ag+ — желт., Си2 + — син., Hg/ — черн., Fe3+ — кор.
1 а) 2 н. НС1, конц. р-р (NH«)2S + H2O (1:1) б) 2 н. 1ЧаОН+20%-ная Н2О2 (1 : 1), SO2 (газ) Sb1", Sbv — op., Pb2+, Mn2+, Co2+, Ni2+, Ag+ — кор., Cd2+, As1", Asv — желт., Hg^+, Hg2+ — черн. Ni, Hg|+, Hg2+ — черн.
133
ХРОМАТОГРАФИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Хроматограмма Проявляющий реагент Окраска зон
2 2 2 2 2 2 2 2 2 или 3 2 или 3 a) (NH4)2S, конц. НС], 5% води, р-р NaH2PO2-H2O б) 5% води, р-р фосфорномо-либденовой к-ты а) 2 и. NaOH, нас. Вг2+2н. NaOH (2:1) б) 2н. Н28О4+20%-ная Н2О2 (1:1) а) 2 н. NaOH, нас. Вг2+2н. NaOH (2:1), SO2 (газ), 0,05% р-р бензидина в 10%-ной СНзСООН, NH3 (газ) б) 0,1% р-р рубеановодородной к-ты в метаноле, NHs (газ) а) нас. водн. р-р KSCN + ацетон (1:1) б) NH3 (газ), 1% р-р диметил-глиокснма в этаноле, 0,1% р-р рубеановодородной кислоты в метаноле a) NHa (газ), 0,1% р-р родизо-ната натрия (свежеприготовленный) б) 2 н. НС1+2 н. СНзСООН (1 : 1) а) 0,02% р-р хинализарина в метаноле б) 2 н. К'аОН+20%-ная Н2О2 (1:1) 1% р-р галлацетофенона в 2 н. NI-UOH а) нас. р-р ацетата цинкурани-ла в 1 н. СНзСООН, УФ б) 5 г Co(NO3)2 • 6Н2О и 5 г Pb(NO3)2 раств. в 100 мл НгО, содержащей следы HNO3; затем прлбавл. НС1 (разб.) до появления осадка РЬС12 0,1% водн. р-р CuSO4-5H2O + +2 н. H2SO4 (10:1), HgCl2+ + NH4SCN+H2O (2,7 г : 3 г : 100 мл) а) 0,5% р-р 8-оксихинолина в 60%-ном этаноле, NH.j (газ), УФ б) лед. СНзСООН (слабое опрыскивание) Мп2+, Со2+, Ni2+, Asin, Asv—-кор., Hg2+— черн., Hg2+—снн. Sb111 — снн. Mn2+, Co2+, Ni2+ — кор., Cr3+ — желт., Cu2+ — син., Fe3+ — ор.-кор. Cr3+—син. (исчезает), Cu2+—кор. Mn2+ — син. Co2+ — желт.-кр., Nl2+ — син., Cu2+ — желт.-з. Bi3+—желт., Co2+—син., Cu2+ — черн., Fe3+ — кр.-кор. Ni2 + — кр. Ba2+, Sr2 + — кр. Ba2 + — кр. Al3 +—фиол., Zn2 + — фиол. или фиол.-кр. Mg2+ — снн. Ba2+, Sr2+, Ca2+—фиол. Флуоресценция: Na+ — син.-з. K+ — сер.-бур. Zn2+ — син.-фиол. Флуоресценция: Al3 +, Са2 + — з., Sr2+, Ba2 + , Mg2+—син.-з., Zn2+, Cd2 +, Sn2 + — желт. А13+—з., Zn2+, Sn2 + — желт.
134
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ ИА БУМАГЕ
В таблицах приведены значения относительной скорости передвижения веществ на бумаге: ’ h
где Л — расстояние, пройденное от старта до точки максимальной концентрации; ftp — расстояние, пройденное растворителем от старта до фронта.
Абсолютно точно значения /^совпадают с приведенными в таблицах только при идеальном соблюдении тех условий, в которых онн были получены исследователями. Однако соотношение значений Ryr для разных веществ при изменении условий меняется незначительно.
Для каждой системы указан тип хроматографии, растворители и нх соотношения (объемные).
Общие проявляющие реагенты даны перед каждой таблицей. В случае применения специальных проявителей они указаны в последней графе. Там же приводится окраска для специального (а также для общего) реагента, если она характерна для данного соединения. Если же окраска для всей группы соединений одинакова, оиа не приводится, и указание на тот нли иной реагент означает положительную реакцию.
Способы получения и применения проявляющих реагентов приведены на стр. 142—143.
Значения Rf для различных групп органических соединений
Перечень таблиц
Алкалоиды Ароматические кислоты
Аминокислоты Производные нафталина
Амнны Пурины, пиримидины и их производные
Алифатические кислоты Углеводы
Некоторые алифатические кислоты н их Фенолы галогенпронзводные Индикаторы
Алкалоиды
Восходящая хроматография.
Растворители:
Система 1. Бутанол — лед. уксусная к-та (25: 1) — Н2О (до нас.).
Система 2. Бутанол — лед. уксусная к-та (10 : 1) — Н2О (до нас.).
Система 3. Бутанол — конц. НС1 (50 : 1).
Общий проявляющий реагент — реактив Драгендорфа (ДР), окраска красная илн оранжевая.
Соединение Система Соединение Система
1 2 3 1 2 3
Ареколин 0,41 Никотин 0,44 0,50 0,06
Атропин ....... 0,63 0,63 0,88 Папаверин 0,80 0,72 0,94
Берберин ... ... 0,30 0,35 Пилокарпин 0,40 0,47 0,44
Бруцин .... 0,49 0,52 0,69 Скополамин 0,66
Вератрин 0,89 0,85 Стрихнин 0,73 0,69 0,78
Героин ... . . ". 0,84 Теобромин ..... 0,41 0,42
Гидрастинин .... 0,24 0,40 0,46 Теофиллин 0,64 0,59
Гоматропин 0,76 Тропин . 0,32
Дельфинин 0,84 0,88 Хинидин 0,91 0,80 0,94
Йохимбин 0,67 0,72 Хинин 0,87 0,80 0,94
Кодеин 0,46 0,51 0,61 Цинхонамин ..... 0,81 0,84
а-Кокаин 0,88 Цинхонидин 0,78 0,81 6,94
Котарнин 0.70 Цинхонин 0,90 0,79 0,94
Кофеин 0,69 0,67 Эзерин ... 0,78 0,72
Морфин 0,04 0,07 0,49 Эфедрин 0,70 0,66 • •
135
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Аминокислоты Продолжение
Восходящая хроматография.
Растворители:
Система 1. Бутанол — уксусная к-та — Н2О (12 : 3 : 5).
Система 2. Феиол — Н2О <4 : 1).
Система 3. Бутанол — пиридин — Н2О (1:1: 1).
Общие проявляющие реагенты: нингидрин >—пиридин (НП); специальные: нзатни (ИЗ), реактив Эрлиха (ЭР), диазотированная сульфаниловая кислота (СД), анизидин (А), нитрозонафтол (НН), реактив Сакагучи (СР).
Аминокислота 1 Системг 2 3 Примечания
0,30 0,58 0,37 ИЗ (сер.-син.)
Р-Аланин 0,33 0,64 0,28 ИЗ (син.)
0,30 0,40 0,18
cfZ-a-Аминовалериановая 0,56 0,77 0,50
6-Аминовалериановая 0,50 0,84 0,31
£>/.-а-Аминокапроновая 0,67 0,80 0,60
е-Аминокапроновая 0,53 0,80 0,45
6-Амннолевулиновая 0,37 0,23 НП (желт.)
а-Аминомасляная 0,40 0,68' 0,41 ИЗ (син.)
р-Аминомасляная 0,42 0,84 0,36
у-Аминомасляная 0,40 0,78 0,26
1-Аргинин 0,15 0,83 0,50 СР (ор.-кр.)
£ Аспарагин 0,12 0,40 0,20 НП (кор.)
/.-Аспарагиновая 0,23 0,20 0,20 из (син.)
£-Валин 0,51 0,78 0,48
£-Гистидин . 0,11 0,65 0,24 СД (кр.); А (кр.)
Глицин . . 0,23 0,42 0,29
/.-Глутамин 0,17 0,27 0,23 из (кр.)
/.-Глутаминовая 0,28 0,33 0,20 из (кор.)
Гомосерин 0,26 0,47 0,30
а, у-Диаминоглутаровая 0,08 0,21 0,17
Р, е-Диаминокапроновая 0,17 0,47 0,11
а, у-Диаминомасляная 0,13 0,17 0,20
/.-Изолейнин 0,67 0,85 0,56
/.-Лейцин 0,70 0,85 0,60
/.-Лизин 0,12 0,42 0,13 из (сер.-син.)
а-Метилсерин 0,26 0,51 0,36
/.-Метионин 0,50 0,82 0,53
£)£-[3-Оксивалин 0,35 0,58 0,40
Оксилейциь 0,18 0,68 0,49
4-Оксилизин '• • . 0,11 0,28 0,09
4-Оксипролин ’• • • 0,22 0,67 0,30 из (син.-з); ЭР (кр.)
£-Орнитин 0,12 0,17 0,11
2-Пиперидинкарбоновая 0,44 0,93 0,45 НП (син.-пурп.)
3-Пиперидинкарбоновая 0,45 0,96 0,33 НП (син.-пурп.)
4-Пиперидинкарбоновая 0,45 0,90 0,28 НП (син.-пурп.)
/.-Пролин 0,34 0,90 0,34 из (син.)
0,22 0,35 0,38
Таурин . 0,20 0,35 0,38
/.-Тирозин 0,45 0,60 0,60
/.-Триптофан 0,50 0,77 0,62 ЭР (пурп.-кр.)
Р-Фенил-Д£-аланнн 0,60 0,84 0,63 из (син.)
М-Фенилглицин 0,48 0,72 0,57
/.-Цистеин . • • 0,08 0,22 0,14 СР (роз.-кор.)
Цитруллин 0,18 0,63 0,23 ЭР (желт.)
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Амины
Система 1. Нисходящая хроматография; растворитель; Н2О. нас. бутанолом.
Система 2. Нисходящая хроматография; растворитель; бутанол — уксусная к-та — Н2О 1:5).
Система 3. Восходящая хроматография; растворитель: 2-бута нон — пропионовая к-та— (15:5:6).
Общий проявляющий реагент — нингидрин (Н); окраска пурпурная.
Соединение Система Соединение Система
1 2 3 1 2 3
Адреналин 0,14 0,45 0,54 Изоамиламин 0,52 0,77
Аллиламнн 0,03 0,50 Изопропиламин .... 0,27 0,57
Амиламин 0,53 0,77 Кадаверин 0,02 0,17 6,39
Бензиламин 0,38 0,68 Метиламин 0,10 0,37
Бутиламин 1, 6-Гексаметиленди- 0,31 0,70 • • Пропиламин Путресцин ...... 0,28 0,02 0,58 0,16 6,32
амин 0,03 0,20 1, З-Триметилендиамин 0,02 0,15
Гептиламин 0,58 0,85 Этаноламии 0,09 0,33
Гистамин 0,03 0,19 0,43 Этиламин 0,18 0,45
Диметиламин 0,12 0,43 • • 1,2-Этилендиамин . • . 0,02 0,14 • •
Алифатические кислоты
Система 1. Нисходящая хроматография; растворитель: бутанон-ацетон — Н2О — возводи. мупавьнная к-та (40 : 2 : 6 : 1).
Система 2. Восходящая хроматография; растворитель: этанол — конц. NH«OH (19:1), Приведены относительные значения R? (по сравнению с Rf гликолевой к-ты, принятым за единицу).
Система 3. Восходящая хроматография; растворитель: бутанов—лед. уксусная к-та — Н2О (12: 3 : 5).
Общие проявители: анилин — ксилоза (АК). иоднд — йодат — крахмал (ИИК). бромфеноловый синий (БФС); специальные: хлорное железо (ХЖ), 2,4-дннитрофеннлгидразин (ДНФГ), ультрафиолетовый свет (УФ), перманганат (ПМ). фосфорномолибдеиовая к-та (Ф)„
Кислота
Система
1 2 3
Примечания
Адипиновая ............................
Азелаиновая ...........................
Аконитовая ............................
Ацетилендикарбоновая ..................
Винная ............................. -
Гликолевая .............'..............
Глиоксиловая ..........................
Глицериновая ..........................
Глутаровая ....................... . •
Глутаконовая ..........................
₽. 0-Диметилакрнловая .................
Диметнлмалоновая ......................
«, а-Ди.метилянтарная .................
Диоксималеиновая ......................
0,79
0,88
0,82
0,32
0,51
0,35 0,78 0,79 0,91
0,81 0,86
0,80
0,20
0,79
УФ
0,30 0,39 (1,00) 0,70 . . . 0,66
0,90 0,17
ПМ
ХЖ (кр.-пурп.)
ПМ
137
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Кислота Система Примечания
1 2 3
Диоксивинная 0,47 'о,55 0,81’ ХЖ (желт.)
0,79 ХЖ (кр.-пурп.)
d-Камфорная 0,93 0,55 ДНФГ (зол.); ХЖ (кор.)
а-Кетоглутаровая • 0,65 . . .
Кротоновая 0,93 пм
Левулиновая - 0,78 ДНФГ (зол.)
Лимонная 0,48 0,15 0,49 ХЖ (желт.)
0,70 0,45 0,54
Малоновая 0,69 0,30 0,65
Молочная 0,68 1,45 0,78 ПМ; ХЖ (желт.)
Пимелиновая ... 0,84
Пировиноградная 0,92 . • . 0,65 ДНФГ (зол.);
ХЖ (желт.)
Пробковая Себациновая 0,92 1,30
Фумаровая 0,85 0,60 0,83 ХЖ (желт.); УФ
0,71 0,55 ПМ
Щавелевая 0,66 0,26 пм
Яблочная 0,48 0,40 0,55 ХЖ (зол.); УФ
Янтарная . 0,72 0,50 0,82
Некоторые алифатические кислоты и их галогеипроизводные
Система 1. Нисходящая хроматография; растворитель: пропанол — 2 М NH4OH (7:3).
Система 2, Восходящая хроматография; растворитель: бутанол, нас. NHS.
Общие проявляющие реагенты: бромфеноловый синий (БФС). бромкрезоловый пурпурный (БКП).
Кислота Система Кислота Система
1 2 1 2
а-Бромпропионовая . . 0,25 Муравьиная 0,47
P-Бром пропионовая . . . . . 0,20 Пропионовая .... 0,56 0,45'
Бромуксусная .... 0,02 Трихлоруксусная . . • . . .
Валериановая 0,67 Уксусная 0,48 0,08
Дихлоруксусиая .... 0,27 а-Хлорпропионовая 0,23
Изовалериановая . . . 0,66 . > . р-Хлорпропионовая . . . 0,19
Изомасляная Масляная 0,61 0,62 Хлоруксусная .... 0,14
138
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Ароматические кислоты
Нисходящая хроматография.
Растворители:
Система 1. Бутанон — Н2О — днэтнламии (921 : 77 : 2).
Система 2. Бензол — бутанон — 2% р-р уксусной к-ты (9:1: 1).
Общий проявитель — бромфеноловый синий (БФС); специальные — ультрафиолетовый свет (УФ); хлорное железо (ХЖ), перманганат (ПМ), фосфорномолибденовая кислота (Ф). 2. 6-днбромхннон-4-хлоримнд (ДБХ), диазотированная сульфаниловая кислота (СД).
Кислота Система Примечания
1 2
ти-Аминобензойная . . 0,00 о.н УФ, ПМ, ДБХ (з.)
п-Аминобензойная . . 0,00 0,27 ПМ, ХЖ (желт.-кор.)
п-Аминокоричная . . • 0,00 0,32 УФ, ПМ, СД (желт.)
Антраниловая .... 0,10 0,72 ХЖ (желт.-син.); ПМ, ДБХ (з.)
Бензойная 0,20 0,87
Гексаги дробензойная 0,93 0,93
Гидрокоричная .... 0,12 0,84
транс-Коричная .... 0,27 0,89 ХЖ (зол.); ПМ
о-Нитробензойная . . 0,16 0,89 УФ
л-Нитробензойная . . 0,45 0,85 УФ
п-Нитробензойная . . 0,22 0,88 УФ
п-Нитрокоричная . . . 0,13 0,90 УФ
о-Толуиловая 0,18 0,83
.и-Толуиловая 0,25 0,78
п-Толуиловая 0,34 0,83
о-Хлорбензойная . . . 0,28 0,86
.и-Хлорбензойная . . . 0,39 0,92
п-Хлорбензойная - 0,37 0,89
Производные нафталина
Нисходящая хроматография на бумаге, нмпрегнированной погружением в 30% раствор формалина в метаноле.
Растворители:
Система 1. Бензол, нас. формамидом, — этилацетат (8:2).
Система 2. Хлороформ, нас. формамидом, — этилацетат (8:2).
Общие проявители: диазотированный п-ннтроаинлин (НД), ультрафиолетовый свет в атмосфере NH3 (УФ).
Соединение Система Окраска
I 2 в УФ с НД
6-Аминонафтол-1 7-Аминонафтол-1 а, а'-Динафтол . . . ₽, ₽'-Динафтол 1,3- Дноксннафталин 1,5- Диоксннафталин 1,6- Диоксннафталии 1, 7-Диоксинафталин 1, 8-Диоксинафталин 0,32 0,33 0,95 0,96 0,30 0,32 0,27 0,27 0,80 0,31 0,33 0,95 0,96 0,21 0,23 0,22 0,22 0,81 СИН. » » СИН. » » » » фиол.-кр. син.-фиол. кр.-фиол. желт. кр.-ор. ор. » »
139
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Соединение Система Окраска
1 2 в УФ с НД
2, 3-Диоксинафталин 0,40 0,37 фиол. фиол.-кр.
2, 6-Диоксинафталин 0,18 0,18 » роз.-фиол.
2,7-Диоксинафталин 0,20 0,19 » ор.-кр.
1, 5-Нафтилендиамин 0,46 0,54 » син.-з.
1,8-Нафтилендиамин 0,87 0,88 син.-фиол. фиол.-син.
а-Нафтол 0,90 0,89 желт.-з. желт.
р-Нафтол 0,87 0,87 син. ор.
а-Нафтиламин 0,92 0,93 » фиол.-син.
р-Нафтиламин 0,89 0,92 фиол.-син. » »
N-Фенил-а-нафтиламин 0,96 0,96 син. син.-фиол.
N-Фенил-р-нафтиламин 0,95 0,95 » » »
Пурины, пиримидины и их производные
Восходящая хроматография.
Растворители:
Система I. Бутанол — уксусная к-та — Н2О (12:5:5).
Система 2. Бутанон — пиридин — Н2О (1:1:1).
Общие проявители: интрат серебра — бромфеноловый синий (НСБ); ультрафиолетовый свет; окраска синяя.
Соединение Система Соединение Система
1 2 1 2
Адениловая кислота-5 . 0,21 0,28 Инозиновая кислота . . 0,13 0,20
Адениловая кислота-3 . 0,18 0,25 Ксантин 0,43 0,70
Аденин 0,60 0,69 Ксантозин 0,33 0,43
Аденозин 0,49 0,69 Мочевая кислота . . . 0,32 0,32
Аденозин дифосфат . • 0,02 0,13 Тимин . 0,67 0,77
Гипоксантин 0,48 0,66 Урацил 0,52 0,71
Гуаниловая кислота . . 0,16 0,22 Уридин 0,41 0,79
Гуанин 0,38 0,60 Цитидин 0,38 0,66
Гуанозин 0,38 0,68 Цитозин 0,46 0,58
Инозин . 0,36 0,62
Углеводы
Система I. Нисходящая хроматография; растворитель: бутанол — этанол — Н2О — NH4OH (40:10:49:1). Приведены относительные значения R j (по сравнению с Rj 2, 3, 4, 6-тетраметилглюкозы» принятым за единицу).
Система 2. Нисходящая хроматография; растворитель: фенол, нас. Н2О.
Система 3. Восходящая хроматография; растворитель: изопропанол — Н2О (4:1). Приведены относительные значения (по сравнению с глюкозы, принятым за единицу).
Общие проявляющие реагенты: аммиачный раствор нитрата серебра (НСА); анилин — дифениламин (АД).
Соединение Система Соединение Система
1 2 3 1 2 3
Арабиноза Глюкоза 2-Дезоксиаллоза . . . 0,14 0,09 0,33 0,59 0,39 .1,12 (1,00) 2-Дезоксирамноза . . . 2-Дезоксирибоза . . • Дульцит 0,61 6,73 i,50 1,05
140
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Соединение Система Соединение Система
1 2 3 1 2 3
лезо-Инозит 0,35 О-Рибоза 0,21 0,59 1,37
D-Ксилоза 0,15 0,44 1,30 Рибокетоза 0,25
Лактоза (молочный са- Рибулоза 1,42
хар) 0,38 0,32 Сахароза 0,04 0,39 0,80
О-Ликсоза 0,19 О-Сорбоза 0,11 0,42 1,02
Мальтоза 0,36 6,47 О-Талоза 0,19
D-Маннит 1,10 О.-Фруктоза 0,13 6,51 i,05
Мелибиоза 0,35 О-Фукоза 0,21 0,63 1,35
Д-Рамноза 0,30 0,59 1,Ь2 Целлобиоза 0,45
Раффиноза 0,00 0,27 0,20 Цимароза 0,87 • .
Фенолы
Нисходящая хроматография.
Система 1. Бумага импрегнироваиа 20% р-ром формамида в метаноле и промыта циклогексаном, насыщенным формамидом.
Система 2. То же, но промывание производится циклогексаном, насыщенным смесью формамида н пиридина (25 : 1).
Общий проявляющий реагент — диазотированная сульфаниловая кислота (СД); спе-циальные — фосфорномолнбдеиовая кислота (Ф). перманганат (ПМ).
Соединение Система Окраска с СД Специальные проявляющие реагенты
2
2, 3-Диметилфенол 0,40 0,68 кор. ПМ, Ф
2, 4-Диметилфенол 0,40 0,69 кр.-фиол. ПМ, Ф
2, 5-Диметилфенол 0,42 0,69 кор. ПМ, Ф
3,4-Диметилфенол 0,25 0,49 ор.-фиол. Ф
3,5-Диметилфенол 0,30 0,58 ор.-кор. ПМ
о-Крезол 0,30 0,58 желт. ПМ
л<-Крезол 0,19 0,46 ор. ПМ
п-Крезол 0,19 0,44 фиол. ПМ
Фенол 0,12 0,32 желт.
о-Этилфенол (фролол) 0,55 0,76 ор.
М-Этилфенол 0,37 0,63 »
п-Этилфенол 0,35 0,61 фиол.
Индикаторы
Восходящая хроматография.
Растворители:
Система 1. Бутанол, нас. 1,5 Af NH4OH.
Система 2. Амиловый спирт, нас. 1,5 М 1ЧН4ОН.
Соединение Система Соединение Система
1 2 1 2
Бромкрезоловый пур- 0,43 0,10 Метиловый оранжевый 0,55 0,26
пурный ....... Метиловый фиолетовый 0,88 0,86
Бромкрезоловый синий 0,47 0,24 Нейтральный красный • 0,66 0,53
Бромтимоловый синий • 0,70 0,63 Тимоловый синий - • 0,90 0,75
Бромфеноловый синий . 0,55 0,19 Тимолфталеин * ... 0,92 0,92
Индиго кармин .... 0,00 0,00 Фенолфталеин * . . . . 0,92 0,89
Конго красный .... 0,00 0,00 Хлорфеноловый крас-
Крезоловый красный . 0,41 0,12 ный 0,17 0,01
Метиловый красный . 0,59 0,33
* Окраска проявляется после обработки щелочью.
141
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Проявляющие реагенты Продолжение
(состав, приготовление, способы применения)
Название проявителя Состав и приготовление Способ применения
сокращенное полное
А Анизидин а) n-анизидин, конц. НС1, этанол (1: 1 : 100) б) 2% р-р амилнитрата в этаноле в) 0,1 М р-р NaOH Смешивают «а» и «б» (1 : 1), погружают бумагу в р-р, сушат 5 мин при 20° С, погружают в р-р «в»
АД Анилин —дифениламин а) свежеперегнанный анилин, дифениламин, ацетон (1:1: 100) б) 85%-ная Н3РО4 Смешивают «а» и «б» (10: 1), погружают бумагу в р р, сушат несколько минут при 100° С
АК Анилин — ксилоза Ксилоза, Н2О, свежеперегнанный анилин (1 г: : 3 мл : 1 мл), разб. метанолом до 100 ли Погружают бумагу в р-р, сушат 5—10 мин при 20° С, нагревают 10 мин при 105—110° С
БКП Бромкрезоловый пурпурный Бромкрезоловый пурпурный, формалин, этанол (0,04 : 20 : 100) Смачивают бумагу, затем помещают в атмосферу NH3
БФС Бромфеиоло-вый синий а) 0,06% р-р бромфенолового синего в этаноле б) 30% р-р NaOH К «а» добавляют «б» (2 000 : 1) до изменения окраски от красной к синей и смачивают бумагу
ДБХ 2, 6-Дибром-хинои-4-хлори-мид 2, 6-дибромхинон-4-хло-римид, сухой диоксан, сухой ацетон (50 мг: : 12 мл : 3 лл), фильтр. Смачивают бумагу свежеприготовленным реагентом
ДНФГ 2, 4-Динитро-фенилгидразин 0,05% р-р в 1 М НС1 Смачивают бумагу
ДР Драгендорфа реактив a) BiNO3- 5НгО, лед. уксусная к-та, Н2О (0,8 г : : 10 мл : 40 лг.4) б) 40% р-р KJ в) уксусная к-та г) HSO Смешивают все компоненты (1:1:4: 20) и смачивают бумагу
ИЗ Изатин 0,2% р-р в ацетоне Погружают бумагу в р-р и сушат 2—3 мин при 105° С
иик Иодид — йодат — крахмал a) KJ, KJO3, Н2О (1: 2: 50) б) 2% р-р крахмала Смешивают «а» и «б» (1:1) и смачивают бумагу
н Нингидрин 0,2% р-р в ацетоне Смачивают бумагу и сушат при 100° С
нд п-Нитроани-лин диазотированный а) п-нитроанилин, конц. НС1, Н2О (1,5 а: 45 мл: : 950 лл) б) 5% р-р NaNO2 в) 10% р-р ИагСОз Смешивают «а» и «б», добавляют «в» (50: 1 :50). Смачивают бумагу н высушивают при 20° С
142
ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ НА БУМАГЕ
Продолжение
Название проявителя Состав и приготовление Способ применения
сокращенное полное
НН Нитрозонафтол а) 0,1% р-р а-ннтрозо-р-нафтола в этаноле б) КОНЦ. HNO3 Непосредственно перед употреблением смешивают «а» и «б» (9' 1). Смачивают бумагу и сушат несколько минут при 20° С. затем 3 мин при 100° С
НП Нингидрин — пиридин а) 0,2% р-р нингидрина в ацетоне б) пиридин Непосредственно перед употреблением смешивают «а» и «б» (49: 1). Смачивают бумагу и сушат несколько минут при 100° С
НСА Нитрат серебра, аммиачный р-р 0,1 М AgNOs, 5 М NH4OH (1 : 1) Смачивают бумагу и сушат несколько минут при 105° С
НСБ Нитрат серебра — бромфеноловый синий а) 0,4% р-р бромфенолового синего в ацетоне б) 0,2% р-р AgNOa Смешивают «а» и «б» (1 : 1), погружают бумагу на 10 мин, затем помещают ее в дистиллированную воду, декантируют. Операцию повторяют до появления хорошо видимых пятен
ПМ Перманганат 1% води, р-р КМпО4 Смачивают бумагу
СД Сульфаниловая к-та диазотированная а) сульфаниловая к-та, конц. НС1, Н2О (9 г: : 90 лм : 900 мл) б) 5% р-р NaNO2 в) 10% р-р Na2CO3 Непосредственно перед употреблением смешивают компоненты (10 мл: 10 капель : 5 мл), быстро погружают бумагу
СР Сакагучи реактив а) 0,1% р-р 8-оксихи-полипа в ацетоне б) 50% р-р мочевины в) Вг2, 0,5 М NaOH (3 : 1 000) Смешивают «а» и «б» (500:1). погружают бумагу в р-р, высушивают при 20° С, погружают в «в»
ф Фосфорномо-лнбденовая к-та а) 2% р-р фосфорно-молибденовой к-ты б) КОНЦ. NH4OH Бумагу смачивают «а», сушат при 20° С и смачивают «б»
хж Хлорное железо 2% р-р FeCl3-6H2O Смачивают бумагу
ЭР Эрлиха реактив а) 10% р-р п-диметил-аминобензальдегида в конц. НС1 б) ацетон Непосредственно перед употреблением смешивают «а» и «б» (1:4) и смачивают бумагу
143
ГАЗОВАЯ ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ
В таблицах даны коэффициенты селективности и максимальные рабочие температуры некоторых стационарных фаз.
Под коэффициентом селективности С стационарной фазы понимают отношение удерживаемых объемов V п (действительных, корригированных, удельных или относительных) двух веществ, принадлежащих к различным гомологическим рядам (А и Б), но имеющих одинаковую температуру кипения:
В таблицах приняты следующие сокращенные обозначения стационарных фаз:
ПМ —парафиновое масло
ОДП —р, Р'-окснднпропионнтрнловый эфир (р, р'-дицнанодиэтиловый эфир)
ПГ4 —полиэтиленгликоль (мол. вес 400)
ТКФ — трикрезнлфосфат
СМ —силиконовое масло ДЦ 703
ДФФ —дифенилформамид
ЭГС — этилгексилсебацинат
Все стационарные фазы нанесены на шамотную муку.
Коэффициенты селективности некоторых стационарных фаз для разделения гомологических рядов углеводородов в интервале температур кипения 50—160° С
Разделяемые гомологические ряды Стационарная фаза
А Б ПМ ОДП ПГ4 ТКФ СМ ДФФ ЭГС
я-Парафины Метил парафины 1,0 1,0 1,2 1,1 1,0 1,1 1,0
н-Олефины 1,0 1,9 1,2 1,3 1,2 1,5 1,2
н-Олефины Метилпарафины 1,1 2,1 1,3 1,4 1,2 1,7 1,2
Днолефины н-Парафины 3,3 1,3 1,5 1,3 2,0 1,4
Метилпарафины' 3,8 1,4 1,6 1,4 3,6 1,4
н-Олефины 1,7 1,1 1,2 1,1 1,3 1,3
Метилолефины 1,6 1,1 1,1 1,1 • . 1,2
Циклопентаны 1,8 1,0 1,2 1,0 1,2 1,3
Циклогексаны 1,7 1,о 1,0 1,0 1,2 1,2
Метилол ефины н-Парафины 1,0 2,3 1,2 1,4 1,2 1,2
Метилпарафины 1,1 2,4 1,3 1,4 1,2 1,2
н-Олефины 1,0 1,1 1,0 1,1 1,0 • • 1,0
144
ГАЗОВАЯ ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Разделяемые гомологические ряды Стационарная фаза
А Б пм ОДП ПГ4 ТКФ см ДФФ ЭГС
Циклоолефины н-Парафины 1,3 3,9 1,6 2,0 1,5 2,5 1,4
Метилпарафины 1,3 4,6 1,7 2,2 1.8 2,9 1,4
н-Олефины 1,3 2,1 1,4 1,6 1,4 1,7 0.9
Метилолефины 1,3 1,9 1,4 1,6 1,4 0,9
Циклопентаны 1,1 2,2 1,2 1,6 1.2 1,5 1,0
Циклогексаны 1,о 2,1 1,2 1.4 1,2 1,4 0,9
Циклодиолефины Циклоолефины - • 1,2 1,2 1,4 1,2 1.3 1,3
Циклопентаны н-Парафины 1,2 1,9 1,3 1,3 1,4 1,7 1,9
Метилпарафины 1,3 2,1 1,4 1,4 1,5 2,0 1,9
н-Олефины 1,2 1,0 1,2 1.0 1,2 1,2 0,9
Метилолефины 1,2 0,9 1,1 1,0 1,2 • • 0,9
Циклогексаны н-Парафины 1,2 1,8 1,3 1,4 1,3 1,7 1.2
Метилпарафины 1,3 2,1 1.4 1,6 1,4 2,0 1.2
н-Олефины 1,2 1,0 1,1 1,1 1,1 1,2 1.0
Циклопентаны 1,0 1,1 1,0 1.2 1.0 1,0 1.1
Ацетилены н-Парафины 0,8 7,6 1,9 2,1 1,4 3,2 1,6
Метилпарафины 0,9 8,5 2,1 2,3 1,4 3,5 1.6
н-Олефины 0,8 4,0 1,6 1,7 1,2 2,1 1.3
Диолефины 2,3 1,2 1.4 1,1 1.6 1.2
Метилолефины 0,8 3,6 1,6 1,6 1,2 1,4
Циклоолефины 0,7 1,9 1,2 1,1 1.0 1,2 1,6
Циклопентаны 0,7 4,2 1,4 1,7 1,0 1.8 1.5
Циклогексаны 0,7 4,1 1,5 1,5 1,1 1,9 1.4
Алкилбензолы н-Парафины 1,2 16,1 2,4 3,4 1.8 5.4 1,8
Метилпарафины 1,2 19,0 2,6 3,8 1,9 6,0 1,8
н-Олефины 1,2 9,0 2,1 2,7 1,5 3,6 1.5
Диолефины • . 5,3 1.9 2,3 1,4 2,7 1.3
Метилолефины 1,2 8,3 2,1 2,9 1,5 1,5
Циклоолефины 1,0 4,2 1,6 1,7 1,2 2,2 1.8
Циклопентаны 1,0 9,9 1,9 2,8 1,4 3,2 1,7
Циклогексаны 1,0 9,2 1,9 2,4 1,4 3,1 1.5
Ацетилены 1,4 2,2 1,3 1,6 1,2 1.6 1.2
Ю Зак. 783
145
ГАЗОВАЯ ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Коэффициенты селективности некоторых стационарных фаз для разделения гомологических рядов кислородсодержащих органических соединений в интервале температур кипения 50—150° С
Разделяемые гомологические ряды Стационарная фаза
А Б ПМ ОДП ПГ4 ТКФ СМ ДФФ эгс
Первичные спирты Вторичные спирты 1,1 1,4 1,2 1,3 0,9 1,0 1,5
Третичные спирты 0,8 1,5 1,2 1,3 0,7 1,о 1,3
Простые эфиры 0,3 6,0 1,8 0,4 1,8 0,6
Ацетали 2,2 1,2 0,47
Вторичные спирты Третичные спирты 0,7 1,2 1,1 1,0 0,8 1,0 0,9
Простые эфиры 0,3 4,4 1,6 • . 0,5 0,5
Ацетали - . 1,6 1,3 0,3
Третичные спирты Простые эфиры 0,3 3,9 1,5 0,6 1,8 0,42
Ацетали 1,4 1,3 0,2
Альдегиды Первичные спирты 1,3 1,0 1,5 2,7 1,3 1,9
Вторичные спирты 3,4 1,4 1,9 2,1 1,4 2,5
Третичные спирты 2,4 1,6 1,9 1,7 1.4 4,8
Простые эфиры 0,6 5,8 1,0 2,3 1,0
Кетоны 1.2 0,7 1,1 1,0 1,0 1,1
Эфиры муравьиной кислоты 1,0 1,2 • • 1,2 1,0 1,1 1,1
Эфиры уксусной кислоты 1,0 1,2 * - 1,2 0,9 1,1 1,0
Ацетали 2,1 1,5 0,9
Кетоны Первичные спирты 2,3 1,2 0,9 1,3 2,4 1,2 1,3
Вторичные спирты 2,2 1,9 1,0 1,7 2,0 1,3 2,2
Третичные спирты 1,9 2,1 1,2 1,7 1,7 1,3 3,7
Простые эфиры 0,6 8,0 1,7 1,0 2,4 0,92
Эфиры муравьиной кислоты 0,8 1,5 1,0 1,0 1,1 0,8
Эфиры уксусной кислоты 0,8 1,5 • • 1,0 0,8 1,2 0,9
Ацетали 3,2 1,4 0,8
Эфиры муравьиной кислоты Первичные спирты 2,3 0,8 • • 1,2 2,5 1,1 1,8
146
ГАЗОВАЯ ХРОМАТОГРАФИЯ ОРГАНИЧЕСКИХ ВЕЩЕСТВ
П родолжение
Разделяемые гомологические ряды Стационарная фаза
А Б ПМ ОДП ПГ4 ТКФ см ДФФ эгс
Эфиры муравьи- Вторичные спирты 3,7 1,2 1,6 2,1 1,1 2,4
НОЙ кислоты Третичные спирты 2,4 1,4 - • 1,6 1,7 1,1 3,8
Простые эфиры 0,6 5,5 • • • • 1,0 2,0 1,0
Ацетали 2,2 - • 1,3 0,9
Эфиры уксусной Первичные спирты 2,3 0,8 1,2 2,8 1,1 1,8
кислоты Вторичные спирты 3,7 1,2 • • 1,6 2,3 1,1 2,3
Третичные спирты 2,4 1,4 • • 1,6 1,9 1,1 3,8
Простые эфиры 0,6 5,5 • • • 1,2 2,0 1,1
Эфиры муравьиной кислоты 1,0 1,0 • • 1,0 1,1 1,0 1,0
Ацетали 1,4 0,9
Ацетали Простые эфиры . . 2,6 1,4 1,1
Максимальные рабочие температуры н?которых стационарных фаз, °C
Днметилформамид.................................. 20
Этиленгликоль, содержащий 10% AgNO3................ 40
Диметилсульфолан ................................. 40
Гексадекан .................... ...... ............ 50
(3, Р'-Оксидипропионнтриловый эфир................. 70
Полиэтиленгликоль (мол. вес 400).................. 100
Парафиновое масло ................................ 120
Бензилдифенил......................................120
Диноннлфталат................................ 130
Сквалан ................ 140
Трикрезилфосфат .................................. 140 (?)
Этнлгексилсебацннат............................... 140 (?)
Диглицерол,................................. . 150
Силиконовые масла ............................... 160
Полиэтилен гликоль (мол. вес 2000)................ 220
Полиэтиленгликольаднпинат ... . ................ 250
Силиконовая высоковакуумная смазка ............. . 300
Апиезон • • . •....................................300
10*
147
Ионообменные ме
Свойства
Статическая обменная емкость (СОЕ) характеризуется в таблицах числом миллиграмм-эквивалентов ионов, поглощенных 1 г сухого ионита при его равновесии с указанным раствором электролита.
Динамическая обменная емкость (ДОЕ) характеризуется числом миллиграмм-эквивалентов ионов, поглощенных 1 л набухшего нонита до момента проскока ионов соответствующего электролита в фильтрат.
Насыпная масса ионнта (в кг!л) представляет собой массу (в кг} единицы объема (1 л> воздушно-сухого ионита.
Удельный объем ионнта (в мл[г) отвечает объему, занимаемому I г сухого нонита после его набухания в воде.
Помещенные в таблицах сведения о свойствах ионнтов в ряде случаев несколько отличаются от показателей, приводимых в технических условиях, вследствие различных методов
иониты ЗАВОДСКОГО и ПОЛУЗАВОДСКОГО
Катио
1 № по пор. I Марка Сырьевая основа Активные группы Насыпная масса, кг/л Удельный объем, мл/ г Влажность, %
1 Сульфоуголь Каменный уголь —SO3H, —соон, —ОН 0,65—0,7 2,3—2,6 20—40
2 3 КУ-1 КУ-2 п-Фенолсульфокислота, формальдегид Стирол, дивинилбензол —SO3H, —он —SO3H 0,7—0,75 0,7—0,75 2,75—3,0 2,8—3,0 30—50 50
4 КУ-5 Нафталинсульфокислота, формальдегид —SO3H 0,55—0,6 5,7 . 50
5 КУ-11 Кокс сланцевой смолы —SO3H, —соон, —он 0,6 2,5—2,8 18—20
6 7 СБС КБ-2 Стирол, бутадиен Метиловый эфир акриловой кислоты, дивинилбензол —SO3H —соон 0,75 0,7 2,0—2,5 • • • • 20—40 30
8 КБ-4 Метиловый эфир метакриловой кислоты, дивинилбензол —соон 0,5—0,6 2,5—4,0 50
* Катионит модификации КУ-1г имеет зерна сферической формы размером 0,3—0,1 мм.
** Приведенная величина относится к Na-катиониту, Обменная емкость Н-катионита по CaCfe
148
тоды разделения
ионитов
определения этих свойств, а также из-за возможных расхождений в свойствах разных партий ионитов одной и той же марки.
Более полные сведения о ионнтах можно найтн в следующих книгах: I. К. М. С а л-д а д з е, А. Б. Пашков, В. С. Титов, Ионообменные высокомолекулярные соединения,. Госхимиздат, 1960.—2. Г. О с б о р и, Синтетические ионообменннки, перев. с англ.. Изд. «Мир», 1964. — 3. О. Samuelson. Ion Exchange Separations in Analytical Chemistry, Нью-Йорк — Лондой, 1963. — 4. Зарубежные промышленные полимерные материалы н их компоненты. Толковый словарь — справочник под ред. А. И. Семенова и К. К. Поляковой,. Изд. АН СССР, 1963.— 5. Ф. Гельферих, Поннты. Основы нониого обмена, перев. с нем., ИЛ, 1962. — 6. Р. Г р н с с б а х. Теория и практика ионного обмена, перев. с нем.. ИЛ, 1963. — 7. Jaderne chemicke tabylky (справочник), Прага, 1964.
ИЗГОТОВЛЕНИЯ ОТЕЧЕСТВЕННЫХ МАРОК
НИТЫ
СОЕ, мг-экв/г ДОЕ по 0,007 н. раствору СаС12, мг-экв!л Стойкость Максимальная рабочая температура, сС Внешний внд Размер зерен, мм
по 0,1 н. раствору СаС12 по 0,1 н. раствору JNaOH к кислотам к щелочам
№ по пор.
0,8—1,1 1,5—1,8 2,5—3,6 4,5—5,1 250—300 550—700 Стойкий То же Малостойкий То же 60 90 Черные зерна неправильной формы То же* 0,25—1,0 и 0,25—0,7 0,3—2,0 * 1 2
4,3—4,9 4,9—5,1 1100—1300 » » Стойкий 120—130 Светло-коричневые зерна сферической формы 0,3—1,0 з.
2,5 3,0 400—500 » » Малостойкий ПО Черные зерна неправильной формы 0,3—2,0 4
1,0—1,2 3,0—3,6 350—450 » » То же ~95 То же 0,5—2,0 5
2,3—2,7 2,8—3,0 800 » » Стойкий » » 0,3—1,5 6
10—11 Белые с желтоватым оттенком зерна сферической формы 0,3—1,0 7
0,1 8,5-9,5 2000** Стойкий Стойкий 150—180 Бесцветные зерна сферической формы 0,3—0,8 8
незначительна.
149
ИОНИТЫ ЗАВОДСКОГО И ПОЛУЗАВОДСКОГО
| № по пор. 1 Марка Сырьевая основа Активные группы Насыпная масса, кг!л Удельный объем, мл! г Влажность, %
9 СГ-1 —соон 0,45—0,65 2,0—2,5 . . .
10 кФУ Хлоруксусная кислота, фенол, формальдегид —СООН, —ОН 0,6 3,0—4,0 15
Анио
1 М по пор. I Марка Сырьевая основа Активные группы Насыпная масса, кг[л Удельный объем, мл/г Влажность, % СОЕ по 0,1 н. раствору H2SO4, мг-экв[г
1 АН-1 Меламин, формальдегид =NH, =N 0,7—0,9 2,2—2,3 50—60 4,0—4,5
2 АН-2Ф Полиэтиленполиамины, фенол =NH, =N 0,7—0,8 2,5—2,8 25 9,0—10,5
3 АН-9 Фенол, формальдегид, аммонийные соли =NH, =N 0,45 3,0 50 4,5
4 АН-18 Стирол, днвинилбензол e=N 0,7 3,0 4,0
5 ММГ-1 Мочевина, гуанидин, формальдегид =NH. =N 0,75—0,8 1,6—2,0 30—40 4,2
€ ЭДЭ-10П Полиэтиленполиамины, эпихлоргидрин =NH.=N, -N(R)3 0,6—0,72 2,8—3,5 15 9,0—9,5
7 АВ-16 Полиэтиленполиамины, пиридин,эпихлоргидрин и t+ ; II 1 0,69 4—5 . . . 9,8—10,5
8 АВ-17 Стирол, днвинилбензол -N (CH3), 0,74 . . . • . . 4,8
* Анионит модификации АН-2Фг имеет зёрна сферической формы.
** Ввиду амфотерности ионита регенерация должна производиться слабыми основаниями.
*** При длительной эксплуатации —не выше 35—40“ С.
150
ИЗГОТОВЛЕНИЯ ОТЕЧЕСТВЕННЫХ "МАРОК
Продолжение
СОЕ, мг-экб!г ДОЕ по 0,007 н. раствору СаС12, м г-эке! л Стойкость Максимальная рабочая температура, Внешний вид Размер зерен, мм 1 № по пор. 1
по 0,1 и. раствору CaClj по 0,1 н. раствору к кислотам к щелочам
.... 8,9 Стойкий Малостойкий .... Гранулы белого или желтоватого цвета 0,8—2,0 9
4,8—6,0 То же То же Светло- или темно-коричневые зерна сферической формы 0,24—0,8 10
НИТЫ
ДОЕ, мг-экв/л Стойкость Максимальная рабочая температура, Внешний вид Размер зерен, мм № по пор. |
по 0,01 и. раствору НС! по 0,005 н. раствору NaCI к кислотам к щелочам
300—400 .... Стоек к разбавленным растворам Стоек к разбавленным растворам 30 Белые или светло-серые зерна неправильной формы 0,3—2,0 1
440—850 .... Стойкий Стойкий 40 Коричневые стекловидные зерна неправильной формы * 0,3—2,0 2
400 .... ** . . . Коричневые зерна неправильной формы 0,3—2,0 3
Коричневые зерна 0,3—1,5 ’4
400 .... Малостойкий Малостойкий . • . Белые или светло-желтые зерна неправильной формы 0,3—2,5 5
1000 70 Стойкий Стойкий 60*** Светло-коричневые зерна неправильной формы 0,4—1,7 6
850—950 300 .... Темно-коричневые зерна неправильной или сферической формы 0,4—2,0 7
.... 620—760 Стойкий Стойкий 60*** Прозрачные зерна сферической формы 0,4—1,2 8
151
ЙОНИТЫ ЛАБОРАТОРНОГО ИЗГОТОВЛЕНИЯ ОТЕЧЕСТВЕННЫХ МАРОЙ
Катиониты
Марка Сырьевая основа Активные группы Насыпная масса, кг/л Удельный объем, мл! г СОЕ, мг-экв1г Внешний вид Размер зерен, мм
по 0,1 н. раствору NaOH по 0,1 н. раствору CaClg
Су л ь фо кис л о т и ые катиониты
МСФ-3 п-Хлорбензолсульфоновая кислота, формальдегид —SO3H, —он 0,65 2,8 4,3 1,8 Черны е зерна 0,3—2,0
НСФ Нафталин, формальде- —SO3H 0,45 5,0—7,0 3,0 2,4 » » 0,3—1,5
сдв гид
Стирол, дивинилбензол —SO3H 0,6 3,2 4,2 4,0 Коричневые 0,35—1,5
СМ-12 Стирол, малеиновый —SO3H, —COOH 0,35 . . _ - 4,5 зерна To же 0,35—1,5
ангидрид, дивинилбензол
КУ-3 Вииилпафталии, диви- —SO3H 0,65 2,5—3,0 5,5 5,2 » » 0,35—1,5
нилбепзол
КУ-4 Аценафтилен, дивинилбензол —SO3H 0,65 3,0 5,6 5,4 » » 0,35—1,5
КУ-6 Аценафтен, формаль- —SO3H, —COOH 0,75 2,7 5,5 3.4 Черные зерна 0,3—1,5
дегид
КУ-6Ф Аценафтен, фенол, фор- —SO3H, —COOH 0,8 3,0 5,6 3,8 » » 0,3—1,5
КУ-7 мальдегид
Фенол, бензальдегид, —SO3H, —OH 0,75 3,0 5,5 3,2 » » 0,3—1,5
КУ-8 2, 4-дисульфокислота, формальдегид
Фенол, сульфокислоты —SO3H, —OH 0.65 5,0 6,0 4,0 » » 0,3—1,5
алифатических альдегидов, формальдегид
КУ-9 Фенол, сульфокислоты —SO3H, —он 0,60 5,0 6,0 3,5 » » 0,3—1,5
кетонов, формальде-
КУ-21 гид Нафталинсульфокисло- —SO3H 0,55 4,0 5,5 4,5 » » 0,3—1.5
ты, формальдегид ~0,6 1,9—2,1 3,70 2,12
СБР-4 Бутадиеновая резина —SO3H, —COOH, —он
СКВ СН (с 4% серы) Бутадиеновый каучук Фенольные новолаки —SOsH, —COOH, —он —SO3H, —ОН —0,6 0,65 1,9—2,1 3,0 3,35 6,5 2,51 3,9 Черные зерна 0,3—1,5
СНФ Фенольные новолаки, —SO3H, —ОН 0,65 4,0 6.1 3,1 » » 0,3—1,5
ССФ формальдегид Полистирол, формаль- —SO3H 0,6 3,7 . . . . 3,9—4,2 » » 0,3—1,5
СХВ дегид • Поливинилхлорид —SO3H, —COOH 0,55 1,9—3,0 6,8 3,5—4,2 » » 0,3—1,5
СЭ Полиэтилен —SO3H, —COOH 0,55 .... 4,9 3,9 » » . . . .
Карбоксильные катиониты
КБ-1 Метакриловая кислота, —COOH 0,6 2,7 10,0 0 Белые сфери- 0,3—1,5
КБ-3 дивинилбензол Акрилонитрил, диви- —COOH 0,6 2,8 6,7 0,1 ческие зерна То же 0,3—1,5
нилбензол 0,3—1,5
КС-1 Малеиновый ангидрид, —COOH 0,7 2,8 10,0 1,0 Желтые зерна
метилакрилат, диви-
КБ-5 нилбензол Резорцин, монохлор- —COOH, —OH 0,6 6.0 7,5 0 Черные зерна 0,25—1,5
уксусная кислота,
КН формальдегид Акрилонитрил, диви- —COOH 0,6 .... 6,0 0 » » 0,25—1,5
КМ нилбензол Метакриловая кислота —COOH 0,3 .... 7,4—7,6 0 Белые зерна 0,25—1,5 0,25—1,5
кмд » » —COOH 0,35 . . . • 7.8—8,8 0 » »
кмг » » —COOH 0,35 . . . . 7,6—7,8 0 » » 0,25—1,5
КР Метакриловая кислота, —COOH 0,7 .... 6,4—6,8 0 » » 0,25— 1,5
кмт резорцин Метакриловая кислота, —COOH 0,55 3,5 10,1 0.4 Бесцветные или белые зерна сфери- 0,25-1,5
производные акриламида
ческой формы 0,25—0.8
К МДА То же —COOH 0,55 3,5 10,1 0,4 То же
Си КМТб $ * —COOH 0,55 3,5 10,1 0,4 » » 0.25—0,8
ИОНИТЫ ЛАБОРАТОРНОГО ИЗГОТОВЛЕНИЯ I ОТЕЧЕСТВЕННЫХ МАРОК
Продолжение
Марка Сырьевая основа Активные группы Насыпная масса, кг!л Удельный объем, мл1г СОЕ, мг-экв!г Внешний вид Размер зерен, мм
по 0,1 н. раствору NaOH по 0,1 н. раствору СаС12
КРФУ, КФФУ, КРФФУ Феноксиуксусная кислота, резорцин, фенол —СООН, —ОН 0,4—0,45 2,5—3,2 2,5—4,0 0 Коричневые зерна 0,25—1,5
КФУА Феноксиуксусная кислота, анизол, формальдегид —соон 0,4—0,45 2,2—2,5 3,0—3.3 .... Желтые зерна 0,25—1,5
КФУХ Феноксиуксусная кислота, п-хлорфенол, формальдегид Фосфорнок —соон, —он ислотные и м ы п 0,45—0,5 I Ь Я К О В ( 2,5—2,7 )КИСЛ 3,0—3,5 0 т н ы е к а т и о I Темно-коричневые зерна и т ы 0,25—1,5
КФ-1 Стирол, дивинилбензол -РО3Н, 0.7 2,7 5,0 0,5
КФ-2' » » -РОЭН2, —СН2РО3Н2 0,7 2,7 7,0 1,0
КФ-3 Виннлнафталин, дивинилбензол -РО3Н2 0,65 3.0 3,5 0,5
КФ-4 То же —СН2РО3Н2 0,65 3,0 5,5 1.0
РФ Моно- и дирезорцинфосфат —РО3Н2, —ОН 0,5 1,5 5,0
ВФ Поливиниловый спирт -РО3Н2 0,4 3,0—3,5 4,5
АР п-Оксифенилкрезоло-вая кислота —AsO3H2, —ОН Неорганичес 0,65 кие к а 1,5—1,6 ТИОН1 3,0 т ы
ФЦ Фосфат циркония —РО3Н2, =РО2Н .... 3,0-5,5* .... Белые зерна неправильной формы 1—1,5
ФТФЦ Фталофосфат циркония —РО3Н2, =РОгН, —СООН 3,4* . . . . То же 1—1,5
Ф,Ц Фталат циркония —СООН .... 2,0* х> » 1—1,5
ЦФЦ Цитрато-фосфат циркония —РОзНг, =РО2Н, —СООН 2,1* .... » > 1—1,5
оц Окись циркония —ОН 0,5* . ... 1—1,5
СОЕ определена по 0,2 н. раствору NaOH.
Аниониты
Марка Сырьевая основа Активные группы Насыпная масса, к г/л Удельный объем, мл/г СОЕ, мг-зкв1г Внешний вид Размер зерен, мм
по 0,1 н. раствору-НС! по 0,1 н. раствору
ИОНИТЫ ЛАБОРАТОРНОГО ИЗГОТОВЛЕНИЯ I ОТЕЧЕСТВЕННЫХ МАРОК
Сильноосновные аниониты
АВ-15 Стирол, дивинилбензол, триметиламин -N (СН3)з 0,59 2,9 3,8 1,62 Темно-корнч-невые зерна сферической формы 0,3—1,0
АВ-18 Стирол. дивинилбензол, пиридин -«О 0,7 3,0 3,0 1,5 Светло-желтые зерна сферн- 0,3—1,0
ческой формы
АВ-19 Виннлнафталин, диви- -N (СН3)3 0,6 3,2 3,0 2,5 То же 0,3—1,0
нилбензол, триметил-
амин
АВ-20 Винилпиридин, дивинилбензол Л +Z 1 0,5 4,5 6,0 1,5 » > 0,3—1,0
АВ-27 Стирол, дивинилбен —N—СН2СН2ОН 0,6 2,6 4,0 3,7 Светлые зерна 0,3—1,0
зол, диметиламин, оксиэтилен |\
сн3 сн3
ПЭК Полиэтиленполиамины, =N, =NH, —N (R)3 0,65 3,5 6,0 1,88 Коричневые 0,3—1,0
эпихлоргидрин зерна
АДВ-1 -N(R)3 2,8 2,2
АСД-2 Стирол, триметилдиамин -N (R)3 1,94
МТ Глицидилметакрилат, -N (R)3 0,6—0,7 3,1—4,4 2,9—3,0 Светло-желтые
триметиламин зерна сферической формы
МТП Глицидилметакрилат, -N (R)3 0,7 2,6—3,5 3,0—3,1 Зерна сфери-
пиридин ческой формы
на Си . . - . - • - Продолжение
Марка Сырьевая основа Активные группы Насыпная масса, кг!л Удельный объем, мл] г СОЕ, мг-экв/г Внешний вид Размер зерен, мм
по 0,1 н. раствору HCI по 0,1 н. раствору
АН-4К Поливинилхлорид, ам- Слабооснов =N, =NH н ы e а 0,35 1 и о н и 4,0 т ы 6,5 Коричневые 0,3—1,5
АН-7К миак Поливинилхлорид =N, =NH 0,42 3,5 7,4 . . . . зерна То же 0,3-1,5
АН-10 Аллиламин —nh2 0,6 4,0 10,0 . . . . » » 0,3—1,5
АН-15 Стирол, днвинилбензол —nh2 0,6 2,0 5,5 .... » » 0,3—1,5
АН-17 » » =NH 0,6 2,5 4,5 .... » » 0,3—1,5
АН-19 » » —nh2, =nh, ==n 0,6 2,5 6,0 . ... » » 0,3—1,5
АН-20 » » —nh2, =nh 0,6 2,2 3,0 . . . '. » » 0,3—1,5
АН-21 » » —nh2, =nh 0,6 2,8 6,0 . . . . » » 0,3—1,5
АН-22 » » —nh2, =nh 0,6 2,8 7,0 . . . . » » 0,3—1,5
АН-23 Винилпиридин, диви- 0,6 5,0 6,5 .... » » 0,3—1,5
АН-25 нилбензол 2,5-Метилвиннлпири- 0,6 . . . 6,2 . ... Коричневые 0,3—1,5
НО дин, днвинилбензол Мочевина, меламин, —/ sN, =NH 0,63 3,9 зерна сферической формы Светлые зерна 0,3—2,5
н гуанидин То же =N, =NH 0,53 4,4 Светло-жел- 0,3—2,0
мн » » =N, =NH 0,63 . . . 4,1 .... тые зерна Светлые зерна 0,3—2,0
АДВ-3 —nh2 .... 3,8
Указатель упоминаемых в таблицах
1. Bio-Rad Laboratories (США).
2. Chemical Process (США).
3. Cochrane Corporation (США).
4. Со-Fa Sozieta perazioni (Италия).
5. Dow Chemical (США).
6 E. Merck, A. G. (ФРГ).
7. Farbenfabriken Bayer, A. G. (ФРГ).
8. Farbenfabriken Wolfen, VEB (ГДР).
9. Fibre Fessili Artificial! (Италия).
10. Filmfabrlk und Kunstfaserwerk Agfa-Wolfen, VEB (ГДР).
II. Hoganas Billesholms (Швеция).
12. Hrusorske Chemicke Zavody (ЧССР).
13. Illinois Water Treatment (США).
14. Industrielle Maatschapij Activit N. V. (Imati) (Голландия).
15. Infilco Inc. (США).
16. lonac Co, Ltd (США).
17. Ionics Inc. (США).
18. Japan Organo (Япония).
В графе «Тип ионита» римские цифры указывают иа принадлежность ионитов к одной из следующих групп (марка наиболее характерного для данной группы отечественного ионнта приведена в скобках):
I. Сульфокнслотные катноннты конденсационного типа (КУ-1).
ИОНИТЫ ИНОСТРАННЫХ МАРОК
фирм
и предприятий, изготовляющих иониты
19. Liquid Conditioning Corporation (США).
20. Luis Kelly and Co (Аргентина).
21. Mitsubischi Kasel Co (Япония).
22. Montecatini S. А. (Италия).
23. MUKI (ВНР).
24. National Aluminate Corporation (США).
25. Norks Hydro Elektrisk Kvaelstof A. S. (Норвегия).
26. Permutit A. G. (Западный Берлин).
27. Permutit Co, Ltd (Англия).
28. Permutit Co (США).
29. Phillips et Pain (Франция).,
30. Research Products (США).
31. Rohm and Haas (США).
32. Spolek Usti n. L. (ЧССР).
33. United Water Softeners (Англия).
34. VUSPL (ЧССР).
35. Zavody Zaluzi u Mostu (ЧССР).
36. Zerhyd Departement de 1’Auxiliare des Chemins de Fer et de Vlndustrie S. А. (Франция).
II. Сульфокнслотные катноннты полимеризационного типа (КУ-2).
III. Слабокислотные карбоксильные катиониты (КБ-4).
IV. Сильноосновные аниониты (АВ-17).
V. Слабоосновные анноннты (АН-2Ф).
VI. Сульфоугли, фосфорнокислотные катиониты, неорганические ноннты н т. п.
Катноннты
Марка Сырьевая основа Активные группы Тип нонита СОЕ, мг-экв[г ДОЕ, мг-экв1л Максимальная рабочая температура, Фирма или предприятие
Amberlite IR-1 Пирокатехин, формальдегид -SOaH, -соон. -он I 2,0 700 31
Amberlite IR-100 Фенол, формальдегид -SO3H, -он -CH2SO3H, -ОН I 1.75 650 31
Amberlite IR-105 I 2,7 1000 31
Amberlite XE-100 (бывший IR-112) Полистирол -SO3H II 4,5 1400 120 31
Amberlite IR-112H —SO3H п 4,5 1200-1500 120 31
Amberlite IR-120 СЛ Стирол, дивиннлбензол -SO3H II 4,58 2150 129 31
ИОНИТЫ ЛАБОРАТОРНОГО ИЗГОТОВЛЕНИЯ ОТЕЧЕСТВЕННЫХ МАРОК ИОНИТЫ ИНОСТРАННЫХ МАРОК
£ Продолжение
оо Марка Сырьевая основа Активные группы Тип ионнта COE, мг-экв!г ДОЕ, мг-экв/л Максимальная рабочая температура, °C Фирма или предприятие
Amberlite IR-200 Amberlite IRQ Amberlite IR-105G Amberlite IRXE-69 Amberlite IRC-50 Alcalex Aliasion * Bio-Rad AMP-1 Вю-Rad HZO-1 Bio-Rad ZM-l Bio-Rad ZM-l Bio-Rad ZT-1 Catex-55 * Chempro C-20, C-21, C-25 Decaiso ** Dorollt KF Dowex-30 Dowex-50, 50W*** Dowex-50Q Duollte C-l, C-3 Duollte C-10 Duollte C-20, C-25 Duollte C-60 Duollte C-61 Duollte C-62, C-65 Duollte CS-100 Duollte CS Duollte CS-101 Duollte C-10H Hydrafln ZV * I mac C-18* lonac C-200 (Zeo-Rex) lonac C-240 lonac C-270 lonenaustauscher I lonenaustauscher IV Katex FN К at ex FK Katex F-extra Katex S Katex ROA Lewatlt PN Lewatlt KS-32 Lewatlt KS Lewatlt KSN Lewatlt CNS Lewatlt S-100 Lewatlt C Lewatlt CNO Lewatlt CNS-20, CNS-30 Llquonex CRM, CRP, CPQ Mtiklon P Mtiklon FO Mtiklon PS Стирол, дивинилбензол Пирокатехин, формальдегид Ьеиол, формальдегид Четакриловая кислота, дивинилбензол Окисленный уголь "идрофзсфоромолибдат аммония ^идроокись циркония Молибдат циркония >осфат циркония Зольфрамат циркония Стирол >енол, формальдегид » » Стирол, дивинилбензол » » >енол, формальдегид Нафталин, фенол, формальдегид Стирол, дивинилбензол Зенол 1, 3, 5-Резорциловая кислота, фенол, формальдегид Акриловая кислота, дивнии бензол Фенол, формальдегид Стирол Акриловая кислота, дивиин бензол Стирол, дивинилбензол Метакриловая кислота, ди виннлбеизол Фенол, формальдегид, нафталин Фенол » Стирол Резорцин, хлоруксусиая кислота Фенол, формальдегид » » Фенол, резорцин, бензаль дегнддисульфокислота Фенол, резорцин Стирол, дивинилбензол Фенол Резорциловая кислота, фе нол, формальдегид Фенол, формальдегид » » » » Стирол -SO3H -SO3H, — СООН, —ОН -SO3H, -он —SO3H -СООН -СООН -SO3H, -СООН, —ОН -ОН -РО3Н2, =РО2Н -SO3H, -СООН, -ОН -SO3H —SO3H, -ОН -CH2SO3H, -ОН —SO3H -SO3H -CH2SO3H, -ОН -SO3H, -ОН -SO3H —РО3Н2 -РО3Н2 -РО3Н2, —РО2Н2 -СООН -СООН п- -СООН . —СООН . -SO3H, -СООН, —ОН . -SO3H, -СООН, -он -СООН -SO3H п- -СООН -SO3H -СООН -SO3H, -ОН -SO3H, -ОН -SO3H -SO3H -СООН, -он —CH2SO3H, —он -SO3H -CH2SO3H -SO3H, —он —SO3H —COOH -СООН . -СООН -SO3H, -ОН -CH2SO3H, —ОН —SO3H, -он -SO3H II I I II III VI VI VI VI VI VI VI VI II VI I I 11 II I I II VI VI VI III III III HI VI VI III II III 11 III I 1 I II III I I I 1 II III III III I I I II 5,0 2,0 2,7 4,2 10,0 4,98 4.3—4,7 1,4 2,7 4,0 4,8 5,0 3,2 3,0 4,9 7Л 6,0 3,8 3,85 2,7 4,9 8,2 4,5 10,0 0,54 4,9-5,0 5,0-7,0 2,25 3,0 2,7-3,4 5,0 4,75 5,0 4,2 2,2 2,8 4,0 700 1000 2000 4200 180 300 1300-1500 800 600 1300 1900 1000 800 1700-2200 1400 2500 1100 1110 3500 810 2300 3700 430-500 390-460 19Э0 1700 900 1200 1100 2260 1500-1600 1000 1250 650 900 1570 120 125 65 150 80 100 100 100 80 100 80 120 40 ПО по 95 120 40 95 60 30 40 100 30 40 40 31 31 31 31 31 30 36 1 1 1 1 1 15 2 27 23 5 5 5 2 2 2 2 2 2 2 2 2 2 12 14 16 16 16 6 6 32 32 35 32 35 7 7 7 7 7 7 7 7 7 19 23 23 23
ИОНИТЫ ИНОСТРАННЫХ Я МАРОК
* Сульфоуголь.
** Синтетический алюмосиликат.
*-*-* Dowex 50W отличается высокой механической прочностью и очень малым содержанием тяжелых металлов.
8
Продолжение
Марка
Сырьевая основа
Активные группы
Тип
ионита
СОЕ, мг~экв!г
ДОЕ, мг-экв1л
Максимальная рабочая температура, °C
Фирма или предприятие
11 Зак. 783
Miiklon PSM Стирол -SO3H II 4,0 1000 23
Miiklon СР Метакриловая кислота, ди- -соон III 8,0 2800 23
винилбензол
Miiklon МКМ То же -соон III 8,6 1200 23
Nalcite MX Фенол, формальдегид -CH2SO3H, -он I • 3,0 1150 24
Nalcite HDR Стирол -SO3H II 40 27
Nalcite HCR » -SO3H II 4,5 2100 27
Nalcite X-219 »“ -РО3Н2 VI 8,8 24
Nakollte * VI 24
Permutit Q Стирол -SO3H II 4,3 2000 120 28
Permutit RS » -SO3H II 5,2 2200 26
Permutit S-53** . ......... -SO3H, -СООН, —ОН VI 800 100 26
Permutlt-215, 315 Фенол -SO3H, -он I 27, 28
Permutit-225 Стирол -SO3H li 4,3 27
Permutit-226 Метакриловая кислота -соон III 5,3 1700 27
Permutit H-70 » » -соон III 8,2 3700 28
Permutit C Акриловая кислота, диви- -соон III 9,0 4000 80 26
нилбензол
Permutit H Метакриловая кислота -соон III 5,3 1700 28
Permutit XP -РО2Н2 VI 28
Selektor CS-100 Резорцин, фенол —соон, —он III 2
Wofatlt F Фенол, формальдегид -SO3H, -он I 2,5 700 30-50 8
Wofatlt D Фенол, формальдегид, -SO3H, -он I 3,2 900 8
крезол .
Wofatlt KS Фенол, резорцин, беизаль- -SO3H, -ОН I 2,5 900 97 8
дегид, формальдегид
Wofatlt К Резорцин, бензальдегид, —SO3H, -ОН I 2,5 1000 8
формальдегид
Wofatlt P Фенол, формальдегид -CH2SO3H, -он I 1,9 300 97 8
Wofatit K-51-T -SO3H, -он I 3,2 900 8
Wofatlt KPS-200 Стирол -SO3H II 4,5 2000 115 8
Wofatit C Резорцнловая кислота -соон III 7,0 2500 8
Wofatit CN Резорцнловая кислота, фе- -соон III 2,0 800 30 8
нол, формальдегид 30 8
Wofatit CP-300 -соон III 2,6 2,2 4,9 1,6 40
Zeocarb-215 Феиол, формальдегид —GH2SO3H, —он 95 27
Zeocarb-315 Z cocarb-225 » » Стирол —CH2SO3H, —он —SO3H -SO3H, -соон, -он -СООН, —ОН 11 VI 2400 600 103 30 27 27
Zcocarb HI** III 5,3 1700 30 27
Zeocarb-216 9,0 2000 100 27
Zeocarb-226 Метакриловая кислота, ди- —СООН
винилбензол 1,7 28
Zeocarb ** Zeodur Стабилизированный глау- —SO3H, -СООН, —ОН VI VI 27
Zeo Rex копит Фенол, формальдегид -CH2SO3H, -ОН I 2,7 2,6 2,6 800 1000 30 27 33
Zerolit-215 Zcrolit-315 » » » » —CH3SO3H, —ОН -CH2SO3H, -ОН I 1000 95 33
ИОНИТЫ ИНОСТРАННЫХ МАРОК
Аниониты
Aiiasion —N (Юз
Aiiasion AW s=N
Amberlite IRA-400 Стирол, дивииилбензол —N (Юз
Amberlite IRA-401 » » —N (Юз
Amberlite IRA-402 » » —N (R)3
Amberlite IRA-410 » » -N (Юз 4-
Amberlite Amberlite IRA-411 IR-4B » » Полиэтиленполиамины, -N (R)3 eN. =nh, -nh2
фенол, формальдегид
Amberlite iR-45 Стирол, дивииилбензол •=N
Лутидин, формальдегид =N. —N (R)3
Anex L Ароматические амины, форм- sN, --Ml, —NH2
Anex MFD
альдегид
|— * Синтетический алюмосиликат.
О ** Сульфоуголь.
IV 2,2 750 50 36
V 7,8 1700 36
IV 2,5—3,9 1000—1200 50 31
IV 3,0—4,0 1800 50 31
IV 4,4 1350 50 31
IV 3,9 1250 40 31
IV 3,0 800—900 40 31
V 9,2 2500 40 31
V 5,5 1200 100 31
V 2,6 800 40 32
V 1300 34
О to -. .. Продолжение
Марка Сырьевая основа Активные группы Тип ионита СОЕ, мг-экв!г ДОЕ, мг-экв/л Максимальная рабочая температура, °C Фирма или предприятие
Anex OAL Пиридин, алифатические —N (R)3, =N, =NH V 1300 34
амииы
Anex S-8-TM Стирол, дивинилбензол -N (Юз IV 3,7—3,9 1400-1500 40 34
Anex S-8-D » » -N (Юз IV 3,4—3,5 1300—1400 40 34
Anex РА =N, =NH, -NH2 V 8,0 50 34
Ап1»ж Fart А-310 4,3 1100 30 3
Deacldlte Е Фенол, алифатические =N. =NH, —MH2 V 7,0 190) 9, 10
амины, формальдегид
Deacldite FF Полистирол -N (R), IV 3,5 1500 60 9, 10
Deacldlte G Стирол, дивинилбензол. ди- 1500 60 27
этиламин
Deacldlte H Полистирол sM, =nh, -nh2 V 27
Dialon SA # 100 Стирол, дивинилбензол -N (R)3 IV 21
Dowex-1 (Nalcite SBR) » » —N (Юз IV 2,5—3,5 1100—1300 50 5, 27
Dowex-2 (Nalcite SAR) » » -N (Юз IV 2,5-3,6 поэ 30 5, 27 5, 27
Dowex-3 (Nalcite WBR) » » sN, - Nil, —NH2 V 5,5-6,0 2500—2700 65
Dowex 21-K » » -N (Юз IV 4,5 1250 50 5
Duoiite A-l, Д-2, A-3, A-5, A-7 Фенол, поЛиэтиленполи- —N, =NH, -NH2 V 5,4-7,0 1100—1200 35 2
амииы
Duollte A-14 Стирол, дивинилбензол 5,9 1800 2
Duo lite A-33 —N (R)3, rfM IV 8,7 700 2
Duoiite A-40, A-42 -N(R)3 IV 2
Duollte A-41, A-43 Полиэтилеиполиамины. -N (Юз IV
эпихлоргидрин
*п Duoiite A-47 Винилпиридин —N (Юз, sN IV 1
Duollte A-102 —N (Юз IV 3,3 900
Imac A-21, S-3 Стирол —N (Юз; IV 14
lonac A-243, A-300 Полиэтилеиполиамины, мо- -N (Юз, =NH, -NH2 V 7,4 1500-1900 45 16
чевина, гуанидин 7,0 1900 40 16
lonac A-260 Полиэтилеиполиамины
—N —NH V 6,0 1900 16
lonac 293-M
lonac A-540, A-550 Стирол -N (R)3 IV 3,0—3,2 1100 100 16
lonenaustauscher II Алифатические амины =NH, —NH2 V 5,0
lonenaustauscher III Стирол, дивинилбензол -N (Юз IV 1700 40 6
Lewatlt M Амииофенол, формальдегид =N, =NH. -NH2 V 3,5
Lewatlt M-l -N(R)3, =N, =NH V 10,2 2700 7
Lewatlt MN —N (Юз IV 2,4 700 30 7
Lewatlt MJN jw-Фенилеидиамин, форм аль- 5,5—6,0 1900 30 7
дегид
LIquonex AD Алифатические амины -N(R)3 IV 19
Liquonex AF Miikion G Полиалкиленполиамины Гуанидин, формальдегид —N (Юз, =N IV V 4,6 1250 19 23
Miikion PA -N (Юз IV 3,2 1300 23
Miikion PAF —N (Юз IV 3,2 1100 80 23
Permutit E - N -NH V 9,0 3000 28
10SO 28
5,0
Permutit G
Permutit ES Стирол, дивинилбензол -N (Юз V, 5,0 1200 40 30
Permutit S-2 —N (Юз V 3,3-3,7 1100 30
> а
£
ИОНИТЫ ИНОСТРАННЫХ» МАРОК
£ Продолжение
Марка Сырьевая основа Активные группы Тип ионита СОЕ, мг-экв[г ДОЕ, м г-экв! л Максимальная рабочая температура, °C Фирма или предприятие
Permutit W Wofatit L, L-150, L-160 Wofatit L-165 Wofatit M Wofatit MD Wofatit N Zeroiit E Zeroiit G Алифатические амины Полиэтиленполиамииы, эпихлоргидрин То же лс-Ф е ни л е нд и амии, формальдегид -и-Фе ни л с и д и ам и и Ароматические амины, формальдегид Алифатические амины Стирол, дивинилбензол, днметиламин sN, =NH =sN, =NH, -NH; -N(R)S, =NH, -NH2 V V V 4,5 10,0 8,0 7,0 5,7 4,3 9,3 3,5 1300 1200 1200 2500 50 50 30 30 30 40 100 28 8 8 8 8 8 33 33
Zerofil FF Стирол, дивинилбензол -N (R), IV 3,5 1500 60 33
Жидкие аниониты
Жидкие иониты приведенных ниже марок представляют собой в воде и хорошо растворимые в углеводородных средах. высокомолекулярные вторичные амины, практически нерастворимые
Марка Молекулярный Нейтрализационный Обменная емкость Динамическая Фирма
вес эквивалент мг-экв!г мг-жв!мл вязкость при 2э спз с, г[смА
Amberlite LA-1 Amberlite LA-2 351-393 353—395 370— 360- 400 380 2,5—2,7 2,6-2,8 2,1-2,3 2,2-2,3 72 18 0,84 0,83 31 31
Иониты так называемого ядерного класса, содержат < 200 мг/л железа, < 100 мг(л меди, указанных в таблице, также иониты Bio-Rad А. Иониты для ядерной технологии изготовляемые по специальной технологии, характеризуются высокой степенью чистоты и < 100 мг[л свинца и других тяжелых металлов. К ионитам этого класса относятся, помимо G. и Bio-Rex, изготовляемые фирмой 1 для нужд лабораторий.
Марка Активные группы Тип ионита Поставляемая форма СОЕ, м г-экв! г Разм ср зерен, мм Фирма
Amberlite ХЕ-77 Amberlite ХЕ-151 -SO3H -SO,H II II 95% Н + , 5% Na + 99% К+, 1% Na + 4,7 4,0 0,45—0,60 0,45-0,60 3! 31
Amberlite ХЕ-163 Amberlite XE-I69 -SO3H -SOsH 11 II 99% LI+, 1% Na + 99% NH+, 1% Na + 4,6 4,4 0,45-0,60 0,45-0,60 31 31
Amberlite ХЕ-78 -N (R)« IV 80% OH , < 15% СО|“ 5 % Ci , 1 1 5 0,38-0,45 31
ИОНИТЫ ИНОСТРАННЫХ | МАРОК
Марка смешанного ионита К а тио китовый компонент Анионитовый компонент Продукт, получаемый в фильтрате Фирма
Amberlite ХЕ-149 Amberlite ХЕ-151 Amberlite ХЕ-78 Раствор КОН 31
Amberlite ХЕ-150 Amberlite ХЕ-77 Amberlite ХЕ-78 Вода 31
Amberlite ХЕ-154 - Amberlite ХЕ-163 Amberlite ХЕ-78 Раствор L1OH 31
Amberlite ХЕ-170 Amberlite ХЕ-169 Amberlite ХЕ-78 Раствор NH4OH 31
Готовые смеси ионитов для фильтров смешанного действия
Марка Катионитовый компонент Анионитовый компонент Объемное соотношение катионит : анионит ДОЕ, м г-ж в!л Фирма или предприятие
Amberlite МВ-1 Amberlite МВ-2, МВ-3 * Amberlite МВ-4 Amberlite МВ-5 Amberlite МВ-6 Bio-Dcmlnrollt lonenaustauscher V Wofatit MBR Amberlite IR-120 Amberlite IR-120 Amberlite IR-120 Amberlite IRC-50 Amberlite IRC-50 Zeocarb-225 lonenaustauscher I Wofatit KPS-200 Amberlite IRA-400 Amberlite IRA-410 Amberlite IR-45 Amberlite IRA-410 Amberlite IR-45 Deacldite FF lonenaustauscher III Wofatit SBV 1 : 1,5 1 : 1,5 I : 1 1 : 1,5 1 : 1 1 :2 1:2 * 460 550 31 31 31 31 31 27 6 8
* Amberlite МВ-3 отличается от Amberlite МВ-2 присутствием индикатора.
Ионообменные бумаги
Марка Содержащийся ионит Ионная форма Обменная емкость Фирма
м г-экв} г мг-экв/см2
Amberlite SA-2 Amberlite IR-120 Na + ~ 1,9 ~0,03 31
Amberlite WA-2 Amberlite IRC-50 H + ~ 4,6 ~ 0,06 31
a Amberlite SB-2 Amberlite IRA-400 CI ~ 1,5 ~ 0,02 31
gj Amberlite WB-2 Amberlite IR-4B OH* ~3,0 ~0,04 31
ЗАВИСИМОСТЬ СВОЙСТВ КАТИОНИТА КУ-2 ОТ СОДЕРЖАНИЯ ДИВИИИЛБЕНЗОЛА
И СУЛЬФОГРУПП В СОПОЛИМЕРЕ
Приводимые в таблице значения СОЕ и удельного объема ионита при одном и то» же содержании дивииилбензола расположены по возрастанию степени сульфирования.
Содержание дивииилбензола (номинальное), вес. % СОЕ, мг-экв1г Удельный объе м Н-формы набухшего катионита, мл/г Содержание дивииилбензола (номинальное), вес. % СОЕ, мг-экв/г Удельный объем Н-формы набухшего катионита, мл{г
по 0,1 н. раствору СаС12 ПО 0,1 н. PNaT0T по 0,1 н. раствору СаС12 по 0,1 н. раствору NaOH
2 1,2 1,2 3,2 12 1,0 1,4 2,8
2,0 2,0 4,5 1,9 2,1 3,0
4,2 4,4 5,7 4,8 5,2 3,0
5,2 5,8 5,8 5,1 5,3 3,0
8 1,2 1,5 2,6 16 0,9 1,3 1.8
2,5 3,0 4,0 2,3 2,8 2,3
4,8 4,9 4,4 3,0 3,6 2,4
5,0 5,3 4,6 5,3 5,4 2,8
ЗАВИСИМОСТЬ СВОЙСТВ КАТИОНИТА КБ-4 ОТ СОДЕРЖАНИЯ ДИВИИИЛБЕНЗОЛА В СОПОЛИМЕРЕ
Содержание дивииилбензола (номинальное), вес. % СОЕ по 0,1 н. раствору NaOH, мг-экв/г л Удельный объем набухшего катионита, мл)г Окисляемость 1 г катионита в Н-форме, мг Ог
N а-форма Н-форма
1 10,44 7,34 3,29 1,49
2 10,28 4,85 2,63 0,3
3 10,36 4,75 2,42 0,3
5 9,74 3,47 2,53 0,4
8 9,35 2,83 1,96 0,4
12 8,12 2,52 2,02 ’ 0,4
15 6,99 2,03 2,0 0,4
18 5,86 2,1 2,1 0,4
24 .4,52 2,1 1,94 0,5
166
Свойства ионитовых мембран
Мембраны, не содержащие связующего, называются гомогенными. Для повышения ппочиости в мембраны типов Nepton, МК-40 и МА-40 вводится армирующая ткань. Мембраны. содержащие обычно 60—65 вес. % иоинта и 35—40 вес. % связующего, называются гетерогенными.
Более подробные сведения по ионитовым мембранам можно найти в следующих источниках: L Деминерализация методом электродиализа. Ионитовые мембраны, перев. с аигл под ред. Б. Н. Л аскорина и Ф. В. Раузен, Госатомнздат, 1963. — 2. Б. Н. Л а-с к о Р и н, Н. М. Смирнова, М. Н. Г а н т м а и, Ионообменные мембраны и их применение, Госатомнздат, 1961, —3. Б. Н. Л аскорин, Н. М. Смирнова, ЖПХ, XXX|V, еып. 8 (1961)-
ИОНИТОВЫЕ МЕМБРАНЫ ОТЕЧЕСТВЕННЫХ МАРОК
Марка Ионитовая основа Связующее Толщина, мм Степень набухания, % Полная обменная емкость влажной мембраны, мг-экв/г Прочность на разрыв, кг[см2 Удельиое электрическое сопротивление в 2 н. растворе KCI, ом-см
ДКУ КУ-2 К а т и о н и Поливинил- т о в ы е 0,5—0,6 м е м б 25 эаны 2,0 25 200—300
ДКБ КБ-4 хлорид То же 0,5—0,6 20 3,3 30 70—120
ДПУ КУ-2 Полиэтилен 0,5—9,6 25 2.1 35 200—300
ДПБ КБ-4 » 0,5—0,6 20 3,5 30 70—120
МК-1 Сульфо- Отсутствует 0,2—0,6 До 5 3,2 . . . 20—50
МК-40 фенольная смола КУ-2 Полиэтилен 0,45—0,55 6—8 2,0 180—200
П-СБС СБС Синтети- 0,5—1,0 25 1,8 30 500
п-сдв сдв-з ческий каучук То же 0,5—1,0 85 2,3 25 200—300
П-КМД кмд » » 0,5—1,0 350 4,0 25 70—120
П-РФ РФ » » 0,5—1,0 65 3,6 10 100—200
ДАН ЭДЭ-Юп А и и о н и Поливинил- т о в ы е 0,5—0,6 м е м б ] 30 а н ы 2,0 20 180—250
ДАВ АВ-16 хлорид То же 0,5—0,6 35 2,0 20 150—200
ДАВ-17 АВ-17 » » 0,5—0,6 20 1,4 35 250—400
дпн ЭДЭ-Юп Полиэтилен 0,5—0,6 30 2,0 22 180—250
дпв АВ-16 » 0,5—0,6 35 2,0 22 150—200
ДПВ-17 АВ-17 » 0,-5—0,6 15 1,4 40 250—300
МА-40 ЭДЭ-Юп » 0,45—0,55 8—10 > 3,0 . . . 200—220
Л-ЭДЭ ЭДЭ-Юп Синтети- 0,5—1,0 46 3,0 20 100—200
Л-ММ Г ММГ-1 ческий каучук То же 0,5—1,0 20 2,5 18 150—130
167
ИОНИТОВЫЕ
В таблице приведена селективная ионопроиицаемость Р =
t-t„
где i и tj—числа переноса
Марка Тип мембраны Толщина, мм Полная обменная емкость влажной мембраны, мг-экв(г Влажность, % Удельная электропроводность х-103, о.и-|гл-1
В ди-с тил лированной воде в растворе КаС]
0,01 и. 0,1 н. 1,0 н.
Г е т е р о г е н н ы
Amberplex А-1 Анионитовая 0,5—0,75 1,1 25—35 0,45 0,51 0,84 1,90
Amberplex С-1 Катионитовая 0,5—0,75 2,0 30-40 0,46 0,54 1,06 3,32
Permaplex А-10 Анионитовая 0,5—0,6 1,3 30—40 0,8 2,06
Permaplex С-10 Катионитовая 0,5—0,6 2,0 30—40 . . . 2,0 2,33
Permutit А-1374 Анионитовая 0,2 . . . . 20 . • . . • . 2,5—3,1 . . •
Permutit С-1373 Катионитовая 0,2 .... 20 . . . г 2,5—3,1 о м о г е н н ы е
Nepton AR-111 Анионитовая 0,5—0,6 1,6 47 4,0 4,0 5,0 9,0
Nepton CR-51 Катионитовая 1,0 0,76 43 7,0 7,3 8,0 14,0
Nepton CR-61 » 0,5—0,6 3,0 42 8,0 8,0 9,0 15,0
* Указатель фирм и предприятий см. стр. 157.
168
ИНОСТРАННЫХ МАРОК
I го лона соответственно в фазе мембраны и во внешнем растворе электролита.
Селективная ионопроиицаемость Р в растворе NaCi Максимальная рабочая температура для Na- или С 1-форм. 'С Влияние высушивания и обезвоживания Устойчивость к растворителям Фирма или предприятие *
0,03 н. 0,1 н. 1,0 и.
мембраны
0,99 0,96 0,76 95 (50 — для щелочных растворов) Не разрушается, если мембрана не зажата в жесткую раму Удовлетворительная к большинству растворителей, кроме алифатических и ароматических углеводородов 31
0,97 0,95 0,78 95 То же То же 31
. . . 0,90 0,81 60 » » Удовлетворительная к большинству растворителей, кроме некоторых углеводородов 27
0,90 0,86 60 » х> То же 27
0,93 0,88 0,49 60 Разрушается при быстром неравномерном высушивании Устойчива к неорганическим кислотам, неустойчива к органическим растворителям 28
0,98 м е м б 0,96 рань 0,84 60 То же То же 28
0,98 0,95 0,81 .... Разрушается при высушивании Устойчива к большинству окислителей и восстановителей и к органическим растворителям 17
0,95 0,92 0,52 • • • • То же Устойчива к водным растворителям при pH <10, малоустойчива к окислителям 17
0,99 0,98 0,90 » » Устойчива к большинству окислителей и восстановителей и к органическим растворителям 17
169
СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА ИОНИТОВЫХ МЕМБРАЦ /н би ? Коэффициенты набухаемости -у— и —— (где индексы «н» и «с» относятся к набухшей и сухо! 1с °C мембранам) выражают степень набухания мембран в воде по длине 1 н толщине 6. Влагоемкость со определена по формуле:
где тк и г«с~масса, соответственно, набухшей браны, см^; р—плотность воды, равная 1 г/см^. -.100% иР и сухой мембраны, г; Ун —объем набухшей мем-
Марка Ионитовая основа Связующее Активные группы-.
ПВС + ПМАК Карбоксильный катио- Катионитов! Отсутствует >i е мембраны —СООН
дпу нит на основе поливинилового спирта и п о л и м ет а к р и л ово и кислоты КУ-2 (60%) Полиэтилен —SO3H
СДВ-3(1) СДВ-З (70%) Наирит —SO3H
СДВ-3(2) СДВ-3 (70%) Хлорсульфироваиный —SO3H
Permaple.x С-10 Сильнокислотный ка- полистирол Катионитовь i е мембраны —SO3H
Amherplcx С-1 ТИОНИТ То же —SO3H
Nepton CR-51 » » Отсутствует —SO3H
АП-1 Анионит на основе по- А н н о и и т о в ь Отсутствует le мембраны —nh2, =nh.
дпв лнэтиленполиамина и перхлорвиниловой смолы АВ-16 (60%) Полиэтилен -N (R)s —nh2, =nh,
П-ЭДЭ ЭДЭ-Юп (65%) Наирит -N (R)3 —nh2, =nh,
Permaplex А-10 Сильноосновной анио- А н и о н и т о в ь -N (R)3 e м e м б p а н ы -N (R)3
Amherplex А-1 ПИТ То же -N (R)3
170
НЕКОТОРЫХ ОТЕЧЕСТВЕННЫХ И ИНОСТРАННЫХ МАРОК
Коэффициент протекаемости D рассчитан по формуле:
Q
ч 2
D————см -сек-г Atp-13,55- 980,7
д —площадь мембраны, см2-, / — время, сек, необходимое для протекания q см^ жидкости; /—давление, см рт. ст.-, 13,55 —плотность ртути, г!см^-, 980,7 — ускорение силы тяжести, см]сек^. р ‘ Статическая обменная емкость (СОЕ) влажной мембраны определялась для катионитовых мембран по иону водорода, для аииоиитовых — по иону хлора.
Значения чисел переноса через катионитовые мембраны приведены для иона натрия, через амионятозые —для иона хлора.
Коэффициенты иабу-хаемости Влаго-емкость со, % Коэффициент протекаемости D, 2 — 1 см -сек-г СОЕ, мг-экв/г Числа переноса в растворе NaCI
по длине '.„"с по толщине 6н/6с 0,1 н. 0,5 н. 1 н. Зн.
отечественных марок
1,05 1,1 - • • - 1 • 10“" 3,18 0,98 0,63 0,57 0,40
1,31 1,14 55 0,8- 10“9 1,40 0,95 0,89 0,62
1,5 1,8—2,0 1,79 0,92 0,78 0,60
.... 0,92 . . . 0,76 . . .
иностранных чарок 54 44 0,3- 10“9 1,90 1,90 0,98 0,925 0,95 0,96 0,92 0,94 0,95 0,90 0,90 0,94 0,85 0,85 0,85
1,1 1,1 1,18 1,03
о т е ч е с 1,1 т в е н н ы 1Д х марс К 1,55 0,96 0,94 . . . 0,86
1,19 1,25 67 0,5- 10“9 1,57 0,96 . . . 0,88 . . .
1,22 1,2—2,45 56 1,52 . . . . . .
иностр а н н ы х марок
1.1 1,07 48 1- Ю-10 1.18 0,96 0,94 0,92 0,87
1,09 1,5 35 0,5- 10“10 1,29 0,98 0,95 0,89 0,62
171
Коэффициенты распределения ионов в ионообменной хроматографии
При разделении элементов методом ионообменной хроматографии желателен выбор таких условий, чтобы каждый элемент мог быть вымыт из хроматографической колонки отдельно от других и в минимальном объеме вымывающего раствора. Оптимальные условия находят по коэффициенту распределения каждого из разделяемых ионов и его зависимости от концентрации раствора.
Коэффициентом распределения в ионообменной хроматографии называют отношение концентраций распределяемого вещества в жидкой и твердой фазах. Коэффициент распределения может быть отнесен как к единице веса нонита (коэффициент весового распределения К^),так и к единице объема ионита (коэффициент объемного распределения Z)^).
количество вещества в ионите , количество вещества в растворе ^d ~ вес ионита, г * объем раствора, мл
где Q — плотность слоя смолы, г {мл.
В случае, если распределяемое вещество насыщает не более 1% емкости ионита, можно на основании изотермы обмена считать, что коэффициент распределения не зависит от концентрации этого вещества в растворе.
Число п свободных обьемов хроматографической колонки (за свободный объем колонки принимают объем раствора между зернами ионита в колонке), необходимое для вымывания вещества с получением максимальной концентрации его («пик»), связано с коэффициентом распределения уравнением:
Разделение двух элементов, находящихся в смеси, с помощью определенного ионита и элюента возможно при некотором различии в величинах п (или, следовательно, в величинах коэффициентов распределения).
Практическое применение коэффициентов распределения иллюстрируется рис. I, где представлено разделение сложной смеси элементов с помощью соляной кислоты на анионите дауэкс'1. Соответствующие коэффициенты распределения помещены на рис. 2.
Свойства различных ионитов см. стр. 148 и сл. Теоретические и практические вопросы ионообменной хроматографии и се применение в аналитической химии подробно рассмотрены в монографиях; 1. Ф. Г е л ь ф е.р и х. Пойнты. Основы ионного обмена, персв с нем., ИЛ, 1962. — 2. Р. Гриссбах, Теория и практика ионного обмена, перев. с нем., ПЛ. 1963.—3. О. Samuelson, Ion Exchange Separations in Analytical Chemistry, Нью-Йорк — Лондон, 1963,
172
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЕ! ХРОМАТОГРАФИИ
жении концентрации кислоты.
ви.нэлдй'е юдшаэьпи’ы алнчиэшпзотио
173
lJuc. 2. Поглощение элементов анионитом дауэкс-1 из солянокислых растворов.
— означает, что поглощение отсутствует (0,1 < А1 НС1 < 12); + означает слабое поглощение в 12 Л! НС1 (0,3 1); Н—I- означают
сильное поглощение (D IV
Рис. 3. Поглощение элементов анионитом АВ-17 из растворов уксусной кислоты.
4- означает, что Kd < 1; ++ означают, что A'd > 100; в случае ванадия приводятся коэффициен-ты распределения для различных его форм.
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ Я КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
К Со Sc Ti L Cr1" Mu Fe"1 Co" Ni Cu Zn Ca Ce As Se^
< . >
Rb Sr Y Zr Nb Movi + + Tcv" Ru" Rh Pd11 + + Ag Cd 1 . . . In Sn" i Sb _____ Te,v
Cs Ba La Hf Ta WVI | Re'" Os Ir Pt Al?" Hg TI AiPb" J Po
Рис. 4. Поглощение элементов анионитом АВ-17 из растворов муравьиной кислоты. + означает, что Кд < 1; 4- т означают, что Кд > 100.
12 Зак. 7S3
Рис. 5. Поглощение элементов анионитом дауэкс-1 из растворов азотной кислоты. СгШ не поглощается.
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
Концентрация NH^SCN, моль/л
Рис. 6. Поглощение элементов анионитом амберлит IRA-400 из водных растворов роданистого аммония (в присутствии 0,1 Л1 НС1).
Cu, Ag, Os, Ir, Pt, Au осаждаются с ионами SCN ; Nb, Та дают нерастворимые хлориды; хлориды вольфрама разлагаются в воде; СеШ не поглощается.
zr’v
LHf
. vIV Cr111
I _Nb MoVI
1 1.... 1 1 1
1 .Ta _w
.Се»1 _uv'
-Мп11 -Feln
ТС _Rui"
j д I [ 1 1 1 1
_Re —।—।—।—।— -Os
Cd11
ZnH
ThIV
igKd
4
2
О 0,4 1,2 2,0
Концентрация ЪМлЗСК1,иоль1л
Рис. 7. Поглощение элементов анионитом амберлит IRA-400 из водно-ацетоновых (1: 1) растворов роданистого аммония (в присутствии 0,1 М НС1).
Cu, Ag, Os, Ir, Pt, Au осаждаются с ионами SCN' ; Nb, Та дают нерастворимые хлориды; хлориды вольфрама разлагаются в воде; СеШ не поглощается; гидролизуется.
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ J КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
0 L ' 1 ' ' 0.4 1,2 2,0 Концентрация М\{л$>СЫ,моль]Г:
Pre. 8. Поглощение элементов анионитом амберлит IRA-400 из водно-спиртовых (1 :1) растворов роданистого аммония (в присутствии 0,1 М НС1).
Cu, Ag, Os, Ir, Pt, Au осаждаются с ионами SCN”; Nb, Та дают нерастворимые хлориды; хлориды вольфрама разлагаются в воде; Ce^I не адсорбируется; TpV гидролизуется.
Рис. 9. Поглощение элементов анионитом АВ-17 из растворов фтористоводородной кислоты,
означает, что поглощение отсутствует; + означает, что > 100,
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ I КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
Рис. 10. Поглощение элементов анионитом дауэкс-1 из растворов HCI 4~ HF (0,1 < Л4 НС1 12).
Обычно использовалась 1 М HF, для Zr^, Hf^, Nb^, Га^ и Ра^ применялась 0,5 М HF; + означает, что < i.
Рис. 11. Поглощение элементов анионитом дауэкс-1 из растворов HNO3-|~HF.
— означает, что элемент не поглошается; -}- означает сильное поглощение. 1 — 0,2 н. HF; 2—1,0 н. HF; 3 — 5,0 н. HF.
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ I КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
Рис. 12. Поглощение элементов катионитом дауэкс-50 из растворов соляной кислоты. +означает, что D < I.
184
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ.
185.
Li Be
- ‘ + + •
Na Mg
igKa|
4-
з-
2-
1 -
О 5101520
Концентрация НСООН, моль/л
AI + +
К Са Sc Ti Vv Mn - Fe"1 Ni Cu ^Zn Ca Ce As Se*
Rb Sr Y Zr Nb Mov Tcvu Ru" Rh 1. , , Pd + Ag Cd In -Sn" Sb Te,v
Ba ,La Hf Ta WVI —1—I—1— Rev,i Os Ir Pt Hg Tl >b^ Po
(JVI
Рис. 14. Поглощение элементов катионитом КУ-2 из растворов муравьиной кислоты. + означает, что Кд < 1; ++ означают, что Кд > iOO.
Be
Na
Mg
tgKd
5 4
2
1-
0 5 10 15
Концентрация СН3СООН, моль /л
К
Ca
Ti
t Fe
Mn
Co"
b+ +H
Ni
- Zn
Ca
As
Selv
-IT"
Рис. 15.
+означает, что К. а
Поглощение
1; ++ означают, что Кд
элементов катионитом КУ-2 из растворов уксусной кислоты.
100; в случае ванадия приводятся коэффициенты распределения для различных его форм.
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ I КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИЙ
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
pn Bi
Рис. 16. Поглощение элементов катионитом КУ-2 из растворов фтористоводородной кислоты. — означает, что поглощение отсутствует.
188
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
Рис. 17. Поглощение некоторых элементов катионитом дауэкс-50\У из растворов бромистоводородной кислоты.
Концентрация KSCN,mo/7o//z
Рис. 18. Поглощение некоторых элементов анионитом дауэкс-1 из растворов роданистого калия.
О'----------,____________________ь_
0.25 0,5 0.75 1,0
Концентрация HNO3, моль/л
Рис. 19. Поглощение некоторых элементов анионитом дауэкс-1 из смешанного растворителя тетрагидрофуран (90?б) — HNO3 (водный раствор) в зависимости от концентрации HNO3 в водном растворе.
189
КОЭФФИЦИЕНТЫ РАСПРЕДЕЛЕНИЯ ИОНОВ В ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
Концентрация NaNOa, моль/л
Рис. 20. Поглощение тиосульфата, сульфата, сульфида и сульфита натрия сильиоосновным анионитом диаион SA 100 из растворов азотнокислого натрия:
Т-S..O2"; 2-SO2-; 3-S2-; 4 -SO2
Рис. 21. Поглощение сульфита, селенита и теллурита натрия анионитом дауэкс-1 из растворов азотнокислого натрия:
Г —SOg-; 2 —SeOg-; 3 —ТеО2-.
Коэффициенты распределения щелочных металлов
Поглощение осуществляется с помощью фосфоромолибдата аммония в 0,1 М растворе NH4NO3.
Элемент Kd . Элемент Kd
Na 0 Rb 230
К 3,4 Cs 6000
Поглощение осуществляется с помощью катионита КУ-i из растворов соляной кислоты.
Концентрация НС1, молъ(л Kd
LI Na К Rb Cs
0,25 6 7—8
0,5 4 7 16—12 35
0,8 6—7 25-30
Коэффициенты распределения щелочноземельных элементов
Поглощение осуществляется с помощью катионита КУ-2 (илн дауэкс-50) из растворов
уксуснокислого аммоиня.
Концентрация CH3COONH4, молъ[л Kd
Mr С'а Sr Ва Ra
1,5 2,0 4,0 4 .8 18 8 33 8 18
190
Индивидуальные реакции ионов
В таблице приведены некоторые реактивы (специфичные или селективные), с помощью которых можно обнаруживать или определять отдельные ионы.
В первой графе указаны определяемые ионы, которые размещены в соответствии с положением элементов в периодической системе.
Во второй графе приведены реактивы, с помощью которых обнаруживаются данные ноны (в# этой графе указаны лишь реактивы, непосредственно участвующие в образовании обнаруживаемого соединения). Приготовление растворов реактивов см. в специальной таблице (стр. 17).
В третьей графе — «Метод определения» — приводится последовательность прибавления реактивов и получаемый результат (образование осадка, окрашенного соединения, окрашивание пламени, люминесценция под действием ультрафиолетового света). В некоторых случаях указывается, что реакция проводится на фильтровальной бумаге (капельные реакции) или выполняется микрокрнсталлоскопическим методом (на предметном стекле). Сведения о мнкрокристаллоскопнческнх реакциях см. также в таблице «Микрохимический анализ» (стр. 235). В случае проб на пламя указывается окраска пламени и длина волны наиболее характерных спектральных линий (более слабые линии даны в скобках). В таблице приведены лишь наиболее характерные люминесцентные (флуорометрические) определения. Более подробные сведения можно найти на стр. 461.
В четвертой графе дается чувствительность реакции, выраженная в миллиграммах на 1 мл раствора. В случае микрокристаллоскопических определений чувствительность реакции приведена для 75-кратного увеличения.
В пятой графе перечисляются ионы, мешающие определению данного иона (ионы, мешающие в малой степени, даны в скобках). Во многих случаях указаны ионы, не мешающие' определению данного иона; иногда указан реактив, маскирующий действие мешающего иона. Заряд иона не указывается для катионов обычной (устойчивой) валентности, а также в тех случаях, когда подразумевается любая валентность данного катиона.
Более подробные сведения см.: I. Реакции и реактивы для качественного анализа неорганических соединений, .перев. с франц, под ред. А. С. Комаровского, Госхим-издат. 1950. — 2. Н. А. Т а н а н а е в, Капельный анализ. Качественный анализ неорганических соединений капельным методом. 6-е изд., Госхимиздат, 1954.—3. Ф. Ф а й г л ь, Капельный анализ, Химтеорет, 1937 (4-е изд. на англ. яз. — «Spot Tests», 1954). — 4. Химические реактивы и препараты, ред. В. И. Кузнецов, Госхимиздат. 1953.— 5. F. J. W е I с h е г, Organic Analytical Reagents, т. 1—4, Нью-Йорк — Торонто — Лондон. 1953—1955.
Принятые сокращения
+ — добавляют окраш. — окрашивание, окрашенный
-> — получается, образуется сплавл. — сплавляют, сплавление
дифенилам. — дифениламин орг. — органический
крахм. — крахмал ф. б. — фильтровальная бумага (капель
л юм ин. — люминесценция ный метод)
микр — микрокристаллоскопическое Щ. 3. — щелочноземельные элементы
определение
Остальные сокращения см. стр. 16.
191
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг',мл Мешают определению
Н2О2 TiCI4 K3[Fe(CN)6](I) и FeCI3 (II) Анал. р-р + р-в -> желт, окраш. Анал. р-р + р-вы 1 и 11->син. ос. 0,00001 Восстановители
Опр. также с МпС12, или с СоС12 в шел. среде
I группа периодической системы
Li+ (проба Анал. р-р (НС1). Кр. окраш. (670,8 Л1Л1К) 10“5 % Na, Sr, С а (отд. LiCl экстр, аце-
на пламя) тоном или смесью сп. -|-+ эф.)
Na2CO3 (тв.) или (NH„)2 СО3 (тв.) Анал. р-р (копц.) + + р-в->крист. (микр.) 0,1 Са, Sr, Ва (не меш. Rb, Cs)
Na2HPO4, 0,2 н. Анал. р-р + р-в+сп. (нагр.) -> ос. 0,005 (не меш. Na, К, Rb, Cs)
К2 [FeJO6] * Анал. р-р хлоридов (нейтр. или шел.)+ + р-в (нагр.) ->ос. 0,005 NH4*', двухвалентные катионы (не меш. Na, К, Rb, Cs)
Na+ (проба на пламя) Анал. р-р (НО). Желт, окраш. (589,9 ммк) PO’“,AsOf- Li+. Sr2+ (в больших количествах Ag, К, Rb, Cs). He меш. NH + To же
Цинк-уранил-ацетат а) Анал. р-р (нейтр. пли слабокисл.) + + р-в -> желт. ос. б) Анал. р-р выпар. Раств. в р-ве, через несколько минут выпадают крист, (микр.) 0,3 0,01
К [Sb (ОН)6] Анал. р-р (нейтр., упар., охл.)Ч-р-в-> -> желт. ос. (микр.) 0,03 NH+, Mg, Li
Опр. также с Bi (NO3)3 -|- KNO2 CsNO3
K+, Na3 [Co (NO2)c[, Анал. p-p (pH~3) + 0,007 Li, Т1+, nh+
Rb+. Cs+ свежеприготовленный, Р-в - > желт. ос. (для K+) (N°r)
16% p-p
* Раствор 2 г KJO4 в 40 мл 2 н. КОН разбавляют Н2О до 50 мл, добавляют 3 мл 10% р-ра FeCls и разбавляют 2 и. КОН до 100 млл
192
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ НОНОВ
Продолжение
Определяемый нои (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
к+, Rb+, Cs+ H2PtCI6, Р-р + р-в->желт.-ор. ос. 0,5 (для К+) Т1+, J-, so2~.
10% р-р (микр.) < 0,5 (для Rb+, Cs+) NO“ (не меш. Li)
нею,, 70% р-р Анал. р-р (упар.) + бутил. СП. или СП. -> ->крист. ОС. 0,2 (для К+) < 0,2 (для Rb+, Cs+) (не меш. NH^, Na+)
Н2С4Н4О6, 2 и. (1) и CH3COONa, 2 н. (11) Анал. р-р (рН=5-т--=-7) -f-р в 1+р-в II—> -> крист. ОС. Кислоты, щелочи
Дипикриламин (гексанитродифениламин), а) Анал. р-р (ф. б.) + +р-в-[-пС1 (разб.)-> ->ор. пятно 1.0 Hg2+, Pb, Zr, Be, T1+, NH+ (не меш. Mg, Li, Na)
1% р-р б) Авал, р-р (выпар.) + + р-в->крист. (микр.) 0,002 To же
Cd2 [Fe (CN)6] (нас. в 10% р-ре NaJ или NaCl, или NaBr) Анал. р-р + р-в->ос.. 0,0005 (для Cs+) 0,002 (для Rb+) 0,1 (для NH+) 1,0 (для К+) NH +
Na (В (С6Н5)4), 3% р-р Анал. р-р (слабокисл.) + + р-в->ос. Ag+, TI*, NH+, Cu+, Th4+, Ce4+, Hg’+
(проба на пламя) Анал. р-р (НС1).Фиол,-син. окраш.: К+ — — 766.5 и 769,9 лоик; Rb* — 794,8 (780) лоик; Cs*— 852,1 (894,4) Л1Л1К кг4%
Опр. также с Na2Pb [Cu (NO2)6], пикриновой к-той, HJO4
К +
Na3[Co(NO2)6], свежеприготовленный, 16% р-р Pb (NO3)2, тв. (1), Со (NO3)2, тв. (11) и NaNO2, нас.
Р-Р (Ш)
Анал. р-р+сп.+р-в -> ' -> желт, крист, ос.
Анал. р-р выпар., раств. в HCI (0,1 н), добавл. р-в I, р-в II и р-в (III); выпадает черн. крист. ос. (микр.)
0,1 (визуально) 0,001 (микр.) 0,01
(не меш. Na, Rb, Cs, NH+)
Щ. 3., NH+ (не меш. Li, Na, Rb, Cs)
13 Зак. 783
193
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
Rb+, Cs+ <NH4)8(S1(Mo207)61 (нас.) AuBr3 (4,5% р-р в 40 %-ной HBr) (I) и AgBr (0,8% р-р в 40%-иой МВт) (II) Анал. р-р выпар., раств. в р-ве. Выпадают желт, крист, (микр.) Анал. р-р выпар., добавл. p-в I и p-в II. Через несколько минут выпадает кр. крист, ос. (микр.) 0,001 0,01 NH^ (не меш. Li, Na, К, Ва, Са, Mg, Hg2+) Sb, Sn, Ru, Rh, Pt (Na, K)
Опр. также с Н2 [SnCle], Н2 [SbCl6], Na2Ag [Bi (NO2)6]
Cs+
К [BiJ4] *
K3[Fe (CN)6] (нас. р-р) и (CH3COO)2Pb (нас. p-p)
а) Анал. р-р (хлориды) выпар., раств. в р-ве. Выпадают ор.-кр. крист, (микр.)
б) Анал. р-р (ф. б.) + + р-в-> ор.-кр. пятно
Анал. р-р + смесь р-вов (1 : 1) -> крист. ор.
ос. (микр.)
0.01
0,05
0,004
(не меш. Na+ Rb+, К+)
То же
(не меш. К, Rb, Na)
Опр. также с Н8 [Si (W2O7)6], (СН3СОО)2 Pb-[-KJ, AgJ-|-NaJ
Сиг + NH4OH)' 6 h. Анал. р-р + р-в (до 0,007
K4 [Fe (CN)e] раств. ос.)'->син. окраш. Анал. р-р (нейтр. или 0,0001 UO|+, Fe3+
ZnSO4, уксуснокисл.) + р-в -> -» кр.-кор. ОС. Р-в I + анал. р-р (разб.)—|- 0,005 Со, Fe3+ (Ni)
10% р-р (I) и (NH4)JHg(SCN),l** (П) Fe (SCN)3 + H2SO4 (2н.)+р-в II-> фиол. ос. Анал. р-р + р-в 1 + р-в 0,001 W, Se
(I) *** И Na2S2O3, 1% Р-Р (П) II -> моментально бц. (холостой опыт -> бц. через 1,5—2 мин)
* 1 г Bi2O3 растворяют в 10 мл 50% р-ра KJ н 25 мл лед. СНзСООН.
•* Раствор 30 г HgCl2 н 33 г NH,SCN в 100 мл Н2О.
*** Раствор 1,5 г FeCl3 н 2 г KSCN в 100 мл Н2О.
194
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
Си2 + NH2OH • НС1 (тв.) и купроин (2,2'-бихинолин, нас. сп. р-р) Анал. р-р + р-вы —> кр,-пурп. окраш. (если меш. окраш. ионы, экстр, образующееся соединение изоамил. СП.) 0,001 JO-
Рубеановодо-родная кислота (дитиооксамид, свежеприготовленный р-р) Анал. р-р (нейтр.) + + р-в (помещают на ф. б. рядом с анал. р-ром), действ, парами NH3. На месте соприкосновения пятен -> тм.-син. окраш. 0,001 Ag, Hg, Ni, Со, Au
Бензидинацетат, 0,1 % р-р в 2%-ной СН3СООН (I), салицилат натрия, 3% р-р (II) и KCN, 1% р-р (Ш) Анал. р-р+р-в 11 + +NH4OH (8 н.) + + р-в I и р-в III -> -> кр. до син.-фиол. окраш. 0,01 Hg', UO22+, Fe3+, Mn, Co, Ce~, окислители
(проба на пламя) Анал. р-р (HCI). З.-гол. окраш.
Опр. также с KJ. CdS, металлич. А1, дитизоном, а-бензоиноксимом, (NH4)2 [Сг (NH3)2 (SCN)4] • 2Н2О, пиридином + NH4SCN, о-оксифенилфлуороном, этилксантогенатом, N2H4-H2SO4, салицилальдоксимом, купфероном
Ag+ HCI Анал. р-р + р-в-> ос. 0,01
(раств. в NH4OH) < 0,01
KJ Анал. р-р (HNO3) + + р-в->желт. ос. (не-раств. в NH4OH) Hg+, Sn2+, Аиш,
Метол (л-ами- Анал. р-р + р-в + КВг 0,001
нофенолсуль-фат) * (0,02 н.) черн. ос. Pd2 ,SeIV, Fe3+ (Hg, Bi, V, Ce, Mo, W)
(NH4)2 СОз (1) и K2CrO4 (II) Анал. р-р + р-в I. Фильтр. К ф-ту добавл. СНзСООН и р-в 11 -> кирп.-кр. ос. (на ф. б. окр. пятно)
* 10 г метола и 50 г лимонной к-ты растворяют в 500 мл Н2О. к 50 мл р-ра добавляют 2 мл 0,1 н. AgNO3 н 1% гуммиарабика.
Перед употреблением
13*
195
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, MZfMJl Мешают определению
Ag + MnSO4, 0,1 % Р-Р (•). КМпО4, 0,1 н. (II) и НС1, 10 н. (111) Анал. р-р (слабокисл.) 4-4- смесь р-вов (1:1: : 1). Бур. окраш. р-р->бц. (быстрее чем в холостом опыте) 0,02 Восстановители, Hg’+, Cu+, As'11, Sb"’, Sn2+, Fe2+, Те, Rh, Pd, Ir
(NH4)2 [Се (NO3)d, 0,25 % р-р в 1%-ной HNO3 (I), HCI, Юн. (11) Р-в 4- анал. р-р (подкисл. НС1). Желт, окраш. р-р -> бц. (быстрее, чем в холостом опыте) 0,001 Восстановители, Mn2+ (маек. Fe2+ и Sn2+)
Формазилкарб-окснловая кислота (уксуснокисл, р-р) Анал. р-р 4-р-в ->кр.-бордов. окраш. (реакция специфична)
л-Диметил-аминобензпли-денроданин, 0,03% сп. р-р Р-в (ф. б.) 4- анал. р-р (подкисл. HNO,f)-> -> кр.-фиол. окраш. 0,002 Hg, Cu, Pb, Bi, Au, Rh, Pd2+. Os, Pt
Опр. также с NH4SCN, FeSO4, SnCl2, MnSO4 + KOH, RbCl
Aulll Восстанови- Анал. р-р 4- р-в-> кр. (Pt не меш. при
тели (Fe2-, Sn2+, H2PO3, H2O2, гидрохинон, C2O.|-, SO2, KJ и др.) Сульфат ани- ос. коллоидного Au Анал. р-р (слабокисл.) 0,01 действии Fe2+, NO~, SO2 или с2ог) V, Cr, Fe, NO“
лина (нас. р-р анилина в 1 н. H2SO4) л-Тетраметнл- нагр., добавл. р-в. Образуется фиол. окраш. и з. ос. Анал. р-р (слабо- 0,001 Окислители,
диаминодифг-нилметан, 0,5% р-р в сп. с 5%-ной СНзСООН КИСЛ.) + р-В “> СИН. окраш. окраш. ионы
Опр. также с пиридином —НВг, л-диметиламинобензилиденроданином (см. опр. Ag+)
II группа периодической системы
Ве2+ Хинализарин
Р-в 4- анал. р-р (слабо-кисл. или нейтр.) -> снн. ос.
0,01
Cu, Vv, Се3+, Р. 3.. V, Tl, Zr, Th, Mg
* К 100 мл 1% р-ра хинализарина добавляют 6 мл этилендиамина.
196
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг}мл Мешают определению
Ве2+ Берилон II ИРЕА, 0,01 % Р-Р Na-ЭДТА (нас. в NH4OH 1 : 10) (1) и морин (0,02% в ацетоне) (II) Анал. р-р (NaOH 0,12 и.) + р-в->фи-ол.-син. окраш. Анал. р-р + р-в I + р-в II -> желт, люмин. 0,0001 0,001 (не меш. Са, Со, Fe) Zr AI, Mg, Ni, Cu,
Ацетилацетон Анал. р-р (упар.) + + р-в-> бц. крист, (микр.) 0,1 (реакция финна) специ-
Na-ЭДТА (I), Na2HPO4 (II) или Na2HAsO4 (Па) Анал. р-р + р-в I + р-в II или Ila + NH4OH (до рН=5,2)->ос. ТЦмакс. Н2О2)
Na-ЭДТА (1) и NH4OH (II) Анал. р-р + р-в I 4- р-в II -> ос. (реакция фична) специ-
Опр. также с n-нитробензолазорезорцином, 8-оксихинальдином + Na-ЭДТА, (NH4)2 СО3-ф- [Со (NH3)c] CI3 -f Na-ЭДТА, арсеназо 111
Mg2+ J2 1,5?о в р-р | К р-ву I + р-в 11 (до 0,07 Hg2+, Bi, Fe3 + :
3% р-ре KJ (I) св.-желт. окраш.) + Мп, Со, Ni
и КОН, 0,1 н. (11) + анал. р-р -> тм.-бур. ос. (Hg2+,AI,NHf, Pb, Cd, Vv,
UO2 ' ,Ce3+,La)
Титановый Анал. р р + р-в I + р в 0,001 (не меш. Ba, Sr, Ca)
желт. 0,05% 11 -> кр. ос.
р-р сп. р-р (I) и КОН, 0,1 н.
(“) Магнезон 1 Айал, р-р (нейтр. или 0,01 Al, Cr, Fe (все
(и-нитробензол- слабокисл.) + р-в + осаждаются тв.
резорцин, 0,1 % + КОН (0,1 н.) -> NaNO2); Cu,
в 50% сп.) -> син. окраш. или ос. Cd, Co, Ni (все маек. CN-); Mn,
NH4+ (не меш. Ba, Ca, Sr)
Na2HPO4, Анал. р-р + NH4CI 0,001
ТВ. (2 н.) + ИН4ОН (6 н.) + р-в->крист. ос. (микр.)
8-Оксихино- Анал. р-р 4- NH4OH 0,005
лин, 5% сп. (до сл. запаха) 4-
Р-Р + р-в 4- изоамил. сп, -> з.-желт. окраш.
197
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый нон (вещество) Реактив Метод определения Чувствительность, мг[мл Мешают определению
Mg2+ Дифенилкарба-зид, 5% сп. р-р Анал. р-р (без NH4+) добавл. NaOH (2н.), р-в, нагр., фильтр., промыв, гор. Н2О -> -> кр.-фиол. ос. (не меш. Ba, Sr, Са, Sn2+, Сг3+, Al, Мп, Fe)
Опр. также с К4 [Fe(CN)6], хромоген, черн.
Са2+ (проба на пламя) H2SO4, 2 н. Анал. р-р (HCI). Кир-пично-кр. окраш. (443 и 593 мк) Анал. р-р упар., до- 0,003 Се3+, La, Th, Sc (Fe3+, Сг3+, Sr, Ba, Mg, Pb)
(NH4)2C2O4 (I) и Na-ЭДТА (II) Глиоксаль- бавл. р-в, нагр., выпадает крист, ос. (микр.) 0,005
Анал. р-р (СНзСООН до рН=4)+р-в 1 + 4-р-в П->ос. Анал. р-р.+ р-в + 10% Ba, Sr (не меш. лантаниды, Th)
бис-(2-окси-анил), нас. СП. р-р* р-р NaCN (содержащий 10% NaOH) + + СНС13->кр. окраш. СНС1з 0,005 Ba, Sr (маек. Na2CO3)
Опр. также с К4 [Fe (CN)6], пикролоновой к-той. лоретином (7-иод-8-оксихинолин-5-сульфоновая к-та)
Sr2+ (проба на пламя) Родизонат Анал. р-р (НС1). Тм.-кр. окраш. (461, 660, 683 ммк) Анал. р-р (нейтр. на 0,1 Ва (маек. К2СгО4),
натрия, 0,1 % Р-Р ф. б.) + р-в-> бур. пятно (при действии HCI -> бц., при действии AgNO3 -> син.) 0,02 Pb, Ag
H2SO4 Анал. р-р + сп. (1 объем) + р-в-> крист. ос. (микр.)
KJO3 Анал. р-р + р-в-> крист, ос. (микр.) 0,01
K2CrO4 Анал. р-р + р-в-> крист, ос. (микр.) 0,08
* Для приготовления р:ва растворяют 4,4 г свежесублимироваиного о-аминофенола в 1 л Н2О при 80° С, добавляют 3 г 40% р-ра глиоксаля в Н2О. Оставляют на 30 мин при 80° С н на 12 ч при охлаждении. Фильтруют и перекристаллизовывают из мет. сп.
198
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый нон вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
Sr2+ HNO3, 6 н. Анал. р-р выпар., раств. в р-ве, выпар., добавл. р-в, нагр.; выпадает крист, ос. (микр.) 0,1 Pb, Ba, Mo, W, Nb (не меш. Са)
CaSO4, нас. Р-Р Анал. р-р + р-в-> помутнение Ва
Опр. также с 2'-окси-4'-нитрохалконом-[- СНС13, пикриновой к-той, цинк-уранилацетатом, К4 [Fe (CN)6], Cu (NO3)2-[-KNO2 (микр.)
Ва2+ (проба на пламя) Родизонат натрия, 0,1% Р-Р
КМпО4, 5% р-р (I) и H2SO4, 1 н. (II)
H2SO4
К2СгО4, 5% р-р
Na-ЭДТА (1) и (NH4)2 SO4, 10% р-р (II)
CaSO4, нас. р-р
Анал. р-р (НС1).Желт.-з. окраш. (620, 530, 500 ммк) Анал. р-р (нейтр. или слабокисл, иа ф. б.) + 0,01 Pb (Sr)
+ р-в ->кр.-ор. пятно (ос.); с 2 н. НС1 пятно не становится бц., с H2SO4 -» бц. Анал. р-р (нейтр.) + 0,2 Pb (не меш. Са
+ р-в I + р-в II; р-р Mg, Sr)
SO2 (нас.). Фильтр, или центрифугируют->кр. ос. Анал. р-р+р-в ->крист. 0,01 Sr, Са, Pb
ОС. Анал. р-р (уксусно- 0,002 Pb, Bi, Hg, Tl+,
кисл.) + р-в + Ag
+ CH3COONa (10% р-р до pH=4,5) -> -> желт. ос. (микр.) Анал. р-р + р-в I + 0,01 (не меш. Sr)
+ ацетатн. буф. (рН = 5)+р-в II-> -> крист. ОС. Анал. р-р + р-в —> ос. Sr
Опр. также с SrSO4, KJO3, (NH4)2 [SiF6], K4 [Fe (CN)6p
Zn2+ CoCl2, 0,02% ‘ P-P (I) и (NH4)2 [Hg (SCN),]* Анал. p-p (подкисл. H2SO,) + р-в I + р-в . II -> син. ос. (микр.); 0,003 Со, Си
(**) Метиловый фиолетовый, 1,5% p-p (I), NH4SCN (II) и H3PO4 (III) Анал. р-р + р-в I + р-в II + р-в III -> фиол. ос. Be, В, Sb (Hg, Ag, Аи, металлы группы Pt), окраш. ионы)
♦ Для приготовления р-ва растворяют 2,7 г HgCI2 н 3 г NH,SCN в 100 мл Н2О.
199
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжен ие
Определяемый ЙОН (вещество) Реактив Метод определения Чувствительность, мг(мл Мешают определению
Zn»+ ч- Нитробензол-резорцин, нас. в 96% сп. Анал. р-р (слабопод-кисл. на ф. б.) + р-в + + NaOH (2 н.) -> кр.-ор. пятно 0,3 (Ni, Мп, Ag, Hg, Cu, Со, Be, Mg)
Бензоин (I), Mg (ОН)2 (II) и Na2SiO3 (III) Анал. р-р + р-в I + р-в II + р-в III -> люмин. Be
H2S Анал. р-р + формиатн. буф. (рН=2,2) + + р-в -> бел. ос. Элементы V и IV аналитических групп AsHi, Cd, Pb, Sn
Дитизон 0,01 % р-р в хлороформе Анал. р-р + ацетатн. буф. (pH=5) 4-Na2S2O3 (1 h.)+NH4C1 (2 М) + +р-в. Встрях. 1 мин-,-> -> кр. окраш. СНС1.з 0.001
Co(NO3)2, 0,3 н. Опр. так Анал. р-р + р-в. Вы-пар. и прокал. сухой остаток -> з. же с п-фенитидином -f- Кз [Fe(CN)6l Al
Cd2+ H2S Анал. р-р (кисл.) + + р-в ->желт. ос. 0,01 Элементы V и IV аналитических групп
Кадион (п-ни-трофенилдиазо-амино-и-азо-бензол), 0,02% р-р Анал. р-р (нейтр. или слабоуксуснокисл.) + + р-в + КОН (2 н.). Фиол. р-р ->роз. 0,01 Ag, Hg (Cu, Cr3+, Co, Ni, Mg, Fe3+)
силл/-Динитро-фенилкарбазид, 0,1% сп. р-р Анал. р-р (нейтр. или слабокисл.) + NaOH (5 н.) + KCN (5% Р Р) + Р в + НСОН (40% р-р)->з. окраш. и син. ос. 0,1 Co, Pt (Те, Fe)
Дифенилкарба-зид, нас. сп. р-р Анал. p-p+CH3COONa + + р-в -> кр.-фиол. ос. 0,1 Cu, Pb, Hg2+ (все маек. SCN и J )
Бруцин ацетат + NaBr * Анал. р-р (нейтр.) + + р-в -> ос. (микр.) 0,1 Hg, Bi, W, V (Au, Pt, Mo)
Na2C2O4, тв. Айал, р-р в тугоплавкой трубке выпар., добавл. р-в, натр, до кр. каления, образуется зеркало. Добавл. серу и натр.-> -> ор.-желт. налет с бур. каймой 0,1 Hg, As, Zn
• Раствор 6,5 г бруцина и 10 г NaBr в 50 мл 4 н. СНзСООН и 150 мл НгО.
200
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг(мл Мешают определению
Cd2+ К [BiJ,] (см. опр. Cs+) Р-в + анал. р-р (ф. б.) -> -»черн. ос.; добавл. KJ + Na2S2O3 ->бц.
Опр. также с динафтилкарбазидом, NH4C1O„ NH, [Сг (NH3)2 (SCN),]
Hg2/, Hg2+
Cu, металлич.
KJ
NH,OH
SnCl2 (I) и анилин (или AgNO3) (II)
Метиленовая синяя Ч- J2 *
Дифенилкарба-зид, 1% р-р в 96% сп.
Дифенилкарба-зон, 1% сп. р-р
(NHt)|Cr(NH3)J(SCN}<|
На медную пластинку (очищенную HNO3) наносят анал. р-р; через несколько минут смывают Н2О, протирают ф. б. -> -> серебрист, пятно
Анал. р-р + р-в: Hg2+->
-> з.-желт. ос.; при изб. р-ва -> черн.;
Hg2+ -> кр. ос.; при изб. р-ва -> бц.
Hg2+->4epH. ос.; Hg2+-> бел. ос.
Анал. р-р (ф. б.) + р-в
I + р-в II бур. или черн. пятно
Суспензия р-ва
(ф. б.) + анал. р-р (слабокисл.) -> бур,-син. (Hg/ ) или син.
(Hg2+) пятно
Анал. р-р + HNO3 (0,2 и.) + р-в -» син. или фиол. окраш.
Анал. р-р + HNO.3 (0,2 и.) + р-в -> фиол.-син. ос.
Анал. р-р + р-в + НС1 (0,1 н.)-> роз. ос. (К ос. добавл. р-р тиомочевины в ме-тилэтилкетоне -» окр. орг. слой)'
0,2
< 0,005 ..................
0,2 ..................
0,5 Cu, Au, Mo (Fe,
Pt, Pd)
0,1 Ag, As, Au, вос-
становители
0,01
0,01
0,0005
Au, Vv, Movl, CrVl, Cu. Fe3+, Co
СГ, Br", J~.
CN~
Au, Ag, Tl+
• Для приготовления р-ва к 0,1% р-ру метиленовой синей добавляют изб. 0,1 н. р-ра в KJ. Взбалтывают и через 24 ч фильтруют. Осадок промывают очень разб. р-ром KJ в 0.01 н. H2SO4. Образуется суспензия полииодида метиленовой синей.
201
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
Hg (в воздухе) CuSO4, KJ (реактивная бумажка) * Реактивная бумажка через 15—30 мин -» -» желт.-роз. 5 -10-’
Опр. также с HCI, NaNO2-|-AgNO3, Sn2+-|-H2PO2 (каталитическая реакция), алюминием, дитизоном, KJO3, H2S-f-HNOs
III группа периодической системы
В4°Г (Н3ВО3)
Сп. (I) и H2SO4, конц.
(II) Куркумовая бумажка **
А13+
Бромтимоловый синий, 0,04% р-р в 96% сп. (I), маннит, 10% р-р (нейтр. по р-ву (I) (II)
Хинализарин
Ализариновый красный S, 0,1% р-р
Анал. р-р выпар. + р-в 1 + р-в II; проба на пламя —»з. окраш.
Анал. р-р (НО) наносят на реактивную бумажку, высуш., появляется кр.-бур. окраш.; смачивают NaOH (1%)-»син. или тм.-син. окраш.
Анал. р-р (нейтр. по р-ву I) + равный объем р-ва II -» -> желт.-ор. окраш.
Анал. р-р (H2SO4) + + р-в-» син. окраш.
а) Анал. р-р + р-в + + NH4OH (до фиол. окраш.) + СНзСООН (разб. до исчезновения фиол.) ~» кр. окраш. В холостом опыте -» желт, окраш.
б) Анал. р-р (на ф. б.) + + K4lFe(CN)6]+p-B (на периферию пятна), обрабатывают парами NH3; высуш. -»роз. кольцо (в холостом опыте -» желт.)
0,02
0,0001 мг
0,01
Fe, Mo, TI и Zr окр. бумажку, но окраска не изменяется от NaOH
JO4~, Gelv
Bi, Tl, Се, Ga, Fe, V, Be, Mo, Zr (Ti и Zr маек. F-)
(не меш. большинство катионов)
• Смешивают по 200 мл 10% р-ра CuSO4 • 5НгО и 10% р-ра KJ. Осадок фильтруют, промывают (Н2О, 1% р-ром KJ. 1% р-ром- Na2S2O3). Смесь осадка со спиртом наносят на ф. б., высушивают.
•* Растворяют 20 г куркумы в 50 мл сп„ фильтруют. К ф-ту добавляют 50 мл Н2О. Пропитывают р-ром ф. б., высушивают.
202
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый иои (вещество) Реактив Метод определения Чувствительность, мг}мл Мешают определению
А13+ 8-Оксихииолин, 5°/0 Р-Р в 2н. СНзСООН Ализариновый красный RS 0,1% р-р Алюминон (NH4‘ соль ауринтрикарбоновой к-ты), 0,1 % р-р Хинализарин Морин, нас. р-р (~1%) Кислотный хром синечерный Р (2-оксинафта-лин-(1-азо-1)-2'-оксинафта-лин-4'-сульфо-кислота) CsSO4 (или CsCl + K2SO4) Анал. р-р + НС1 (2 н.) + + р-в. Натр, до 70° С, добавл. метил, ор. и CH3COONa до желт, окраш. -> ос. Хлороформ экстр, желт, соединение Анал. p-p+p-e + NHiOH (0,1 н.)‘. Harp, до кип., добавл. СНзСООН (0,1 н.); образуется кр. окраш. или кр,-ор. люмин. Анал. р-р (рН=5,5) + + р-в. Harp, до 7(Г С, охл., добавл. сп., образуется роз. окраш. Анал. р-р (на ф. б.) + + р-в; обрабатывают парами МНз и парами СНзСООН -> кр.-фиол. пятно Анал. р-р + НС1 (2н.) + + р-в -> з. люмин. Анал. р-р (рН=4,8) + + р-в -> кр.-фиол. окраш. Анал. р-р (нейтр.) + 4- р-в; высуш. без натр. -> бц. крист, (микр.) 0,01 0,0001 0,0005 0,001 0,00001 0,01 Zr, Th. Be, Sc, Ga, Bi, Aulil, Fe3+ (не меш. Ti) Cr3+, In, Ga, Ti, Fe (маек, экстр, роданида) Be2+ Zr, Th, Sc, Ga Fe3+ Fe, Cr, Ga, Hg, Те, Bi (W, Sr, Ba)
Опр. также с Со (NO3)3 (ср. опр. Zn2+), стильбазо,' арсеназо, эриохромцианином
Лантаниды
Н2С2О4, нас.
Р-Р
HF
Анал. р-р (0,3 н. НС1) + + р-в -> бел. крист, ос. (микр.)
Анал. р-р (нейтр. или слабокисл.) + р-в -> -> студенист, ос.
0,01
Th (Y, Ca, Sr, Ва)
Th, Y, Sc
203
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ИОИ (вещество) Реактив Метод определения Чувствительность, мг[мл Мешают определению
Элементы подгруппы Се* Элементы подгрупп ы у ** La3+ Се3+ Янтарнокислый аммоний, тв. Молочная кислота CH3COONa, 1% р-р (I) и J2 0,02 н. р-р в р-ре KJ (II) Антраниловая кислота, 5% сп. р-р (NH4)2S2O8 о-Толидин (нас. в СНзСООН) или бензидин AgNO3 + NH4OH Н7|Р(Мо3О10)4|, нас. р-р Н2О2, 3% р-р (1) и NH4OH, разб. (11) Лимонная кислота, 10% р-р (1), Н2О2, 30% р-р (11) NaCl (I), SrCl2-6H2O (II) Анал. р-р на стекле выпар., раств. в капле Н2О, добавл. р-в, выпадают крнст. . (микр.) Анал. р-р (на стекле) выпар., смачивают каплей Н2О, добавл. р-в, выпадают бц. крист, (микр.) Анал. р-р (нейтр.) + + р-в I (изб.) + р-в II + NH4OH -» син. ос. Анал. р-р (подкисл. HNO3) + РЬОг, нагр , фильтр., добавл. р-в -» тм.-син. ос.-» -» бур. окраш. Анал. р-р + р-в -> желт, окраш. Анал. р-р + Na2O2 (несколько крупинок) + +р-в (нейтр.)-» син. окраш. Анал. р-р (нейтр.), смесь р-вов. Слабо нагр., образуется черн. ос. или кор. окраш. р-ра Анал. р-р + р-в + NaOH (40% Р Р) -> син. ос. или снн. окраш. р-ра Айал, р-р + р-в I + + р-в 11 (нагр.) -> -» желт. ос. Анал. р-р + р-вы + 4- NH4OH (до рН = =6) -» тм.-кор. до з.-желт. окраш. Получение перла-»ор.-кр. люмин. (ср. опр. Еи3+) 3 1 0,7 0,1 0,01 0,02 0,01 0,01 0,0025 Fe3+ (не меш. Th, Sc, Nb, Са, элементы подгруппы Y) Sc (не меш. Nb, Та, Th, Zr, UO2+ Fe3~, Са, элементы подгруппы Се) Окраш. соединения (не меш. др. Р. 3.) Fe3+ (маек. Н3РО„), Au, V, CrVi,Sn2+,Seiv Ag, Sb, Au, Ir, V, Cr, TI, Mn, Co, Hg, Cu, F" Mn2+, Fe2+, восстановители (не меш. Zr, Th) Fe3+, Ga3+ (оба маек, тартратной ам и) (не меш. Р. 3.)
Опр. также с л-фенитидином, хинолином, 8-оксихннолином, ферроином, бруцином, пирогаллолом
* La. Се. Рг. Nd. Pm, Sm.
•• Eu. Gd, Tb, Dy, Ho, Er. Tu. Yb, Lu и Y.
204
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг]м.г Мешают определению
Ей3 г Sc3+ Оа3»- Какотелин, 0,25% р-р NaCl (I), SrCl2-6H2O (II) Кошениль (настойка) Салициловый альдегид, 10 % р-р + о-амино-феннларсоновая кислота, 1% р-р (проба на пламя) Ализариновый красный S МпС12 4- КВгО3 -|-+к4 [Fe(CN)6]* CsCI, тв. (I) и KHSO4, тв. (II) Родамин С, 0,2% р-р в 6 н. НС1 8-Оксихинолин Морин Г аллион ПРЕД ** Анал. p-p + HCl (5н.) + +крупинку Zn + p-B-> —> фиол. окраш. Получение перла -> гол. люмнн. (ср. опр. Се34) Анал. р-р + р-в + NaOH (2 н.)->фиол. окраш. Затем нагр., добавл. лед. СНзСООН, выпадает тм.-син. ос. Айал, р-р (нейтр. или слабоуксуснокисл.) + + смесь р-вов -> ярко-желт. окраш. и ос. Анал. р-р (НС1). Фиол. окраш. (417 ммк) Анал. р-р (кисл.) + + р-в-»кр. окраш. Смесь р-вов + анал. р-р -> бур.-кр. ос. Анал. р-р+р-в 1 + р-в II (слегка нагр.) -> -> бц. крист, (микр.) Анал. р-р (НС1 6 и.) + + р-в + бензол -> кр.-фиол. окраш. или ор.-кр. люмин. Анал. р-р (рН = 3) + + р-в+СНС13 -» -> жел.-з. люмин. Анал. р-р + р-в + НС1 + + СНС1з (экстр.) -» -» желт.-з. люмин. Анал. р-р + р-в ->гол. окраш. 0,003 0,02 0,0005 0,1 0,5 0,01 Movi, WVI, Vv, Nbv, Ti, UO2+, Re, Sn Элементы, осаждаемые H2S, Zr, Ti, UO|+, F- (Fe3+) Ga, Th, Ti (не меш. др. элементы III гр.) К. Rb ь Zr, Ti (Th) Cu, Mo, V. Ci'"’vi, UO2+. Ce44-, Ti, Sc, Co, Seiv, TI, Fe Al, Cr3+, In Sb, Au, Fe3+, TI, W, BrO-, CrVI, Hg, JO^, Mnvn, SCN-, Teiv In, Sc (др. элементы не меш.) Al, In, Fe34, Cu
* Реактив готовят смешиванием 120 мл 5% р-ра МпСЬ (в 7 н. НС1), 30 мл 1 и. Р-ра KJFe(CN)6] и 1 мл 0,1 н. р-ра КВгО3.
** 2-Окси-3-хлор-5-нитробензол-( 1-330-2')-1'-окси-8-аминонафталнн-3, 6-дисульфокислота.
205
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
Ga3+ Салицилиден--о-а.минофенол Основной ярко-зеленый или бриллиантовый зеленый, 0,5% р-р в 6 н. НС1 Анал. р-р (рН~5) + -ф- р-в -> желт, люмин. Анал. р-р + р-в+бен- зол-*ярко-з. окраш. 0,0001 0,001 In, Tl (Sbv, Hg, Au3+, Sn2+, W, Fe3+, окислители)
Опр. также с 5,7-дихлор-5,7-дииод-5-нитрозо-8-оксихинолином, хинализарином, кристаллическим фиолетовым, купфероном
1п3+
(проба на пламя) Анал. р-р (НС1). Син. Pb, Bi, Pd11, Ptlv.
окраш. 0,002 UO|+, Ga, Cr
Ализарин (нас. в 96% сп.) Р-в (на ф. б.)+анал. р-р (слабокисл.) обрабатывают парами NH3-*Kp. пятно (холостой опыт-* фиол.). При действии на пятно Н3ВО3 (нас.) кр. пятно становится яснее (в холостом опыте фиол.-» желт.) Zr, Ti, Be, Sc, Al, Fe, P. 3., Y, Ca, Sr, Ba_ (все маек. F ); Ag, Hg, Cu, Cd, Mn, Co, Ni (все маек. KCN)
Г ексаметилен-тетрамин, тв. (I) и NH4SCN, Анал. р-р (слабокисл.)+ + р-в I + p-в II ->роз. крист, (микр.) 0,3 Co (Pb, Sn, Fe3+, Sc)
тв. (Л) Al, Ga, Tl3+, Sn, Bi, Cu, Fe, Vv, MoVI, Ni (Co)
8-Оксихинолин, 0,15% р-р в хлороформе Анал. р-р (рН = 4) взбалт. с р-вом -> -» желт, люмин. СНС1з 0,0001
(проба на Анал. р-р (НС1). Син. окраш.
пламя) 0,01
KJ, 10% р-р (I) и Na2S2O3, Анал. р-р + р-в 1 + о-в II -> желт. ос.
2% р-р (II) Se, Те (не меш. Tl3+)
Bi (No3)3 0,4% р-р в20% HNO3 (I), KJ, 10% р-р (II) и Na,S2O, Анал. р-р (слабокисл.)+р-в 1 + р-в П + р-в 111 -> кр. ос. 0,02
(нас.) (Ill) (В, Pb, Mn, Th, Ti, Ce3+, Ga, восстановители)
Na2CrO4, 0,5 М (или Na2Cr2O7) Анал. р-р (H2SO4 или HNO3) +р-в -> желт. . ос.
206
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ионов
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
Т1 + Н7 [Р (Мо2О7)6], нас. р-р (I) и НВг, 50% р-р (II) Анал. р-р (слабокисл., на ф. б.)+р-в 1 + + р-в П->син. окраш. 0,01 Hg, Sb, Fe2+ (не меш. Т13+)
0 пр. также с К3 [Fe (CN)6J + КОН, Na, [( NH4 [Сг (SCN)4 (NH Зо (NO2)6], N 3)2] а [В (С6Н5)4],
Т13+ о-Толидин (нас. в лед. СНзСООН) Анал. р-р (слабокисл.) + -Ьр-в + NaOH (2н.)-> -» син. окраш. 0,01 Ag, Hg, Cu, Sb, Au, Ir, Pt, V, Fe3+, Ce4+, Co, окислители (не меш. Tl+)
Бензидин (I), НС1, 14 н. (II) и эф. (III) Анал. р-р + р-в И. Экстр, р-вом III, добавл. р-в I; получается син. окраш. эф. 0,03 Со (Hg, Pb, Sb, Fe, TI, Cr, U; не меш. Tl+)
2,4-Динитро-1-нафтол (нас. р-р в пиридине -)-Н2О 1:3) Анал. р-р (слабокисл.) + +р-в->ор. крист, (микр.) 0,03
(проба на пламя) Анал. р-р (НС1). Син. окраш. 0,001 См. опр. Ga3+
Бриллиантовый зеленый (I) и бензол (II) Анал. р-р+р-в 1+р-в II -> ярко-з. окраш. бензола
Опп. также с 8-оксихинолином, и-фенитидииом, 4-диметиламиноантипирин л-аминофенолсульфоиатом, метиловым фиолетовым+толуол
IV группа периодической системы
СО2" H2SO4,1 М (I), смесь Na2CO3, 0,05 М + фенолфталеин, 0,5% сп. р-р -4-Н2О (1:2:10) (II). Анал. р-р + К2Сг2О?+ + р-в I; выделяющийся газ проп.через р-в II. Р-р-»бц. 0,04 CN (маек. Ag+), F (маек. ZrCl4), NO" (маск. солянокисл. анилином), S2-, SO2" и
СН3СООН (I) и Ba (ОН)2 (II) Анал. р-р + р-в I; выде-ляющийся газ пропускают через р-в П, образуется помутнение S2O2- (все маек. Н2О2), СН3СОО~
Опр. также с (СНзСОО)2Бг (мнкр.), СО опр. с J2O3, кровью, Pd2+ или фосфорномолибденовой к-той
207
индивидуальные реакции ионов
П родолжение
Определяемый ио и (вещество) Реактив Метод определения Чувствительность, мг}мл Мешают определению
Sior SiO2 (силикаты) ТР+ НС1 (или HNO3, или NH4C1) (NHJ2 МоО4, Ю?6 р-р (1) и SnCI2> 5% р-р в 2,5 н. HCI (II) (NH4)2 МоО4 (I) и бензидин (11) NaF, тв. (I) и NaCI, 1 % р-р (П) NaF (1), (NH4), МоО, (II) и SnCl2 (или бензидин) (1П) Н2О2,3°о р-р(1), H2SO4, 4 и. (II) H3AsO4, 20% р-р (I), ZrOCl2, 1% р-р (II) и Н2О2, 3% р-р (III) Хромотроповая кислота (ф. б., пропитанная 5% р-ром) Аскорбиновая кислота Анал. р-р + р-в -» гель кремневой к-ты Анал. р-р + р-в 1 + + СН3СООН (до слабокисл.)+р-в 11 + + NaOH (до раств. ос.)-»син. окраш Анал. р-р+р-в 1 + р-в H+CH3COONa -> син. ос. Анал. р-р (в Pt тигле) + р-в I+H2SO4 (конц.); газ улавливают р-вом II на целлофане, получаются крист, (микр.) Анал. р-р (в Pt тигле) + р-в I+H2SO4 (конц.); газ улавливают каплей р-ра NaOH на целлофане. Опр. SiOj- (см. выше) Анал. р-р + р-в 11+р-в I -» желт.-ор.; добавл. NH4F -» бц. Анал. p-p+HCl (1 н.) + + р-в I+p-в II. Harp, до кип., центрифуг. Oc.+H2SO4 (4 н.) + + р-в III-» желт, окраш. Анал. р-р наносят на реактивную бумажку, добавл. H2SO4-> роз.-фиол. пятно Анал. р-р + р-в -» желт, окраш. 0,1 0,005 0,02 Ci 0,01 0,01 0,02 PO3”, AsO3-(отд. при дистилляции sif4), ВО3 (отд. дистилляцией с СН3ОН + + ITSOJ (не меш. РО3 ) ВО” (удал, ди--стилляцией с СН3ОН + + H2SO4) «. выше MoVI, Vv (NH,F не обесцвечивается) (реакция специфична) (реакция специфична) (не меш. Fe3+)
Опр. также с метиленовой синью или с Fe(SCN)3 (после восст. до Ti3+), ализариновым красным S, H3AsO4, 8-оксихннолином, купфероном, Na2HPO4+H2O2
• См. опр SiO2.
208
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, MZjMA Мешают определению
Zr4 + , Hf4+ Ализариновый красный S п-Диметил-аминоазофенил-арсоновая кислота, 2% р-р в 10 н. НС1 Арсеназо III (1,8-диоксинафталин-3,6- ди-сульфокислота-2,7-бис- (азо-2)-фениларсоновая кислота) Метилтимоловый синий а-Нитрозо-f- -нафтол, 2% р-р Куркумовая бумажка (стр. 202) Na2HPO4 (или Na2HAsO4) KJO3, нас. р-р Флавиановая кислота (1-ок-си-2,4-динитро-7-нафталин-сульфокислота) Анал. р-р + р-в + НС1 (конц.) -» кр. ос. Анал. р-р (на ф. б.) + + р-в. Погружают на несколько секунд в НС1 (2 н.), нагр. (— 50° С) -> бур.-ор. пятно Анал. р р (на ф. б.) + р-в » кр.-фиол. пятно Анал. p-p+HCl (0,2 — — 1 н.)+р-в-»син -фнол. окраш. Анал. р-р + НС1 + р-в -> -» кр. окраш. Анал. p-p + HCl наносят на реактивную бумажку, высуш. -» кр.-бур. пятно Анал. p-p + H2SO4 (до 20%) + Н2О2 + р-в -> -» бел. ос. Анал. p-p + HNOa (конц.) + р-в-> бел. ос. Анал. р-р + НС1 + р-в -» -> желт. ос. 0,03 0,01 0,00001 0,0002 0,005 0,004 (реакция специфична) (мешающие ионы маек. Н2О2) Th, UO3+, F~, C2OJ", РО3-(не меш. Ti, лантаниды, Sn, Be, Fe3 + , Cr3+, Ni, Cu) Bi, Sniv, Ti, Fe3+ (все маек, аскорбиновой к-той) F~, SO4“ (маек. Ba) Ti (маек, цинком HCI) Th, Ce4 \ Ti. Sn4 + Hg, Ag [не меш. P.3. (III)J (реакция специфична)
Опр. также с Н2О2, RbCl + NH4F (микр.), пирокатехиновым фиол., таннином, фталевой к-той, хлораниловой к-той, карминовой к-той, купфероном, миндальной к-той, C6H5SeO2NH4, CioH7Se02NH4
Th4+
Ализариновый красный S
Анал. р-р (нейтр. или слабокисл, на ф. б.) + + р-в -» фиол. окраш.
0,01
Cu, Fe3 + , Snlv, лантаниды, Y, Zr, Ti (Pb, U, Tl, Zn, Mn. Co, Ni)
14 Зак. 7ЯЗ
209
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг[мл Мешают определению
Th4 + Торон (бензол-2'-арсоновая к-та-(1-азо-1)-2-оксинафта-лин-3-6-дисульфокислота, тринатриевая соль, 0,1 % р-р Арсеназо III KJO3, нас. р-р Н2С2О4 (NH4)2 СО3, 10% р-р (1), T1NO3, тв. (И) Анал. р-р (НС1 или HNO3<l%) + p-B -> -> малиново-кр. ос. или роз. окраш. Анал. р-р (на ф. б.) + + р-в-»фиол. пятно (ср. опр. Zr4+) Анал. p-p + HNO3 (конц.) +р-в -> бел. ос. Анал. р-р + НС1 (0,3 н.) + + р-в->бел. ос. Анал. р-р (нейтр. или слабокисл.) + р-в 1 + + р-в 11->бц. крнст. (микр.) 0,001 0,00001 0,004 0,1 (Zr, Hf, Ti, лантаниды, Fe3+, ио21) (не меш. SO2-и РО3-; в прис. С2О2- не меш. Zr и Т1) Ti, Zr, Hf, Sn4+, Ag, Hg [не меш. P.3. (Ill)] Лантаниды (Y, Са, Sr, Ba) UO2+ (Cu, Pb, Ca, Sr, Ba, лантаниды)
Опр. также с K2SO4, Na4P2O?, (NH4)2MoO<, n-диметиламиноазофениларсоновой к-той. 8-оксихинолином, Н2О2
GeO2", (NH4)2MoO4, Ge4 + 5% водн. р-р
(NH4)2MoO4, 5% Р-Р* (I) и бензидин (0,1% в лед.
СН3СООН) (II) (NH4)2 МоО4, 5% р-р (I) и Na2SnO2 ** (11) Хинализарин (0,1% в 35%-ной H2SO4)
Анал. p-p + p-B + HNO3-» -»желт. окраш. (через 5 Л1нн)
Анал. р-р + р-в 1 + р-в II+CHsCOONa (нас. р-р) -»син. окраш.
Анал. р р + р-в 1+р-в II -> син. окраш.
Айал, р-р (свободный от С1“ и В г-) выпар., охл., добавл. р-в -> -> син. окраш. (при от-рипат. реакции слабо нагр.)
0,005
0,002
0,001
0,1
Asv, Pv, Si
Восстановители
Asv, Pv, Si, восстановители
B4O2- (др. ионы не меш.)
* К р-РУ 1 г (NH4)2Mo04 в 10 мл Н2О добавляют 10 мл HNOa (конц.),
•* 5%-иый р р SnCl2 в 5 н. р-ре NaOH.
210
индивидуальные реакции ионов
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг[мл Мешают определению
GeO2~, Ge«+ Маннит, тв. (I) и фенолфталеин, 1% СП. Р-Р (И) Фенилфлуорон Анал. р-р (подкисл.) + + р-в II + NaOH (0,01 и.) до появления кр. окраш. + р-в1 -» бц. Р-в наносят на ф. б., высуш. на воздухе; на желт, пятно помещают анал. р-р (3—6 н. по НС1) + + HNO3 (6н.)-»роз. окраш. усил. в течение нескольких минут 0,01 0,003 ВО- Окислнтели
(9-фенил-2,3,7-триокси-6-флу-орон), 0,05% сп. р-р,подкисл. 6 н. НС1
Опр. также с MgSO4, оксидифениламинами, гематином, гематоксилином,
морином, оксиантрахинонами, гидроксинафталенхинонсульфоновой к-той
Sn2+ Zn, металлич. Анал. р-р + р-в 1+р-в 0,01 Nbv, Asv'111
(1) и НС1, 10 и. (11) (проба на пламя) * 11. Син. окраш. 0,001
(NH4)2 МоО4 (I) и Na2HPO4 (II) Р-в 1 + р-в 11 нагр. 2— 3 мин, охл. Добавл. Н2О и анал. р-р -> -> син. окраш. V, UO2+, Ti, Co, Ni, Fe2+, Cr3+, Mn2+, АцШ, Pd, Ptlv, SeIV, TelV, Cu, MoVi, WVI, восстало-вители
FeCl3, 0,1 н. (I) и диметилглиоксим, I % СП. Р-Р (И) Анал. р-р + р-в 1+вин-ная к-та (2 н.)+р-в II + NH4OH (6 и.) -» -> кр. окраш. 0,001
В1С13 (1) и NaOH (II) Анал. р-р + р-в II (до раств. ос.)+р-в I-> -> черн. ос. Bi, Cu, Ag, Hg2 + , Mo, V, As, Те, Sb, Ge (Cr3+, Ni, Co)
Дитиол (1-ме-тил-3,4-димер-каптобензол) Анал. р-р (нейтр.) + + HCI (конц.) + р-в; нагр. (на водяной ба не), охл., образуется кр. ос. 0,01
HgCl2 Анал. р-р + р-в -> тм.- бур. ос.
Опр. также с K3[Fe(CN)6]+FeC13, KJ, какотелином, H2S, метиленовым синим+J2+KJ
* Стеклянную палочку (или пробирку с холодной водой) погружают в р-р и сразу вносят в пламя.
14*
211
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
П родолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг(мл Мешают определению
Sniv Ализариновый красный S Сильные восстановители Анал. р-р + НС1 + р-в -> -» кр. ос. Анал. р-р + р-в (Н3Р02 или металлы: Pb, Ni, Al, Fe, Zn). В ф-те опр. Sn2+ (см. выше) См. опр. Тй4+ и др. (см. опр. Тй4+) Sn2'-
Pb2+ KJ Анал. р-р+р-в -» желт, ос. Йагр. до раств., быстро охл., выпадают желт, крист, (микр.) 0,2
Бензидин ацетат, 0,25% р-р в 10% СН3СООН (I) и Н2О?, 3% Р-Р (П) Анал. р-р (на ф. б.) + + NaOH (3 н.)+р-в II + NH4OH. Высуш., слабо нагр., через 3—5 мин добавл. р-в I -»син. окраш. 0,1 Fe3 h, окислители
К2Сг2О7 H2SO4 (I) и К2СгО4 (11) Анал. р-р + р-в->желт. ос. Анал. р-р + р-в 1->ос. Фильтр., ос. раств. в СНзСООН, добавл. р-в II -» желт. ос. 0,02 Bi, Ag, Hg2+, Ba, Sb
Тиомочевина, ТВ. Анал. р-р высуш., раств. в HNO3 (2н.), добавл. р-в, выпадают бц. крист, (микр.) 0,1 Mo, W, Tl (Ag, Hg2+, Se, Cu)
Родизонат натрия Анал. р-р+тартратн. буф. (рН = 2,8)+р-в-» -> ярко-кр. окраш. 0,001 Ag+, Hg2+, Cu, Ba, Sr
Опр. также с H2S, дитизоном, НС1, анилином, антраниловой к-той,
(NH4)2MoO4, антрахинон-1-азо-4-диметил-п-диметилдиаминодиметнлметаном
V группа периодической системы
NH+ P-вы на NH3: Анал. р-р (в газовой
I. Кр. лакмусовая бумажка камере) нагр. при 40—60° С с NaOH (2 и.). Выделяющийся газ опр. с р вами на NH3
II. Hg2Cl2 (суспензия) Р-в I —>син. окраш. 0,001 Амины
III. MnSO4 + 4-AgNO3* Р-в II-> черн. окраш. 0,1 »
* К р-ру 2.87 г MnSO4 • 7Н2О в 40 мл Н2О добавляют р-р 3,55 г AgNO3 в 40 мл Н2О; разб. до 100 мл, нейтрализуют 0,1 н. р-ром NaOH до появления черн. ос., который отфильтровывают.
212
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ионов
Продолжение'
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг)мл Мешают определению
NH + 4 IV. Бензидин * V. Р-в Несслера и-Нитрофенил-диазоний, хлорид ** Бумажка, пропитанная р-вом III-» черн. окраш., затем при смачивании р-вом IV ~» син. окраш. -» син. окраш. Р-в V (в пробирке) -» -»кр.-ор. окраш. Анал. р-р + р-в+СаО (кусочек) -» кр. окраш. 0,0001 0,002 0,01 А ми ны Амины, Hg, Са, Mg, SO’-, S2-(ие меш. щелочные металлы)
Опр. также с Na3[Co(NO2)6], Н2[Р1С1б] (микр.), NaHC4H4O6, KJ + NaC10; по образованию возгона; NH3 опр. также со смесью AgNO3+HCH0
NH2OH и N2H4 опр. с р-вом Феллинга
NO" FeSO4 • 7Н2О, ТВ. Анал. р-р + р-в+осто-рожно, не перемет.. 0,04 NO2 t (удаляют
с NaN3), Cl-,,
Zn, металлич. H2SO4 (конц.)-» тм.-бур. кольцо Анал. р-р (в газовой 0,002 Вг-, СгО2-.. |Fe(CN)6]3-,. SCN', SO|-,. S о2~ NH+, NO-, CN“
Zn, металлич. камере) +КОН + + р-в -» NH3 (см. опр. NH+) Анал. p-p + Zn н 0,001 NO“ (удаляют
и СН3СООН; p-вы на NO£" Си, металлич. СН3СООН-»NO2 (см. опр. NO^“) Анал. р-р + р-в 1+р-в c NaN3 или CH3OH)
(1) и H,SO4 (II) Дифениламин, 11 -»бур. газ Р-в 1 + р-в И. Добавл. 0,01 NO-, окислители
тв. (1) и I+SO4, конц. (II) КМпО4, (!)• анал. р-р (осторожно) -» син. окраш. Анал. р-р+рв 1 + р-в
NO- и Zn, металлич. (II) СН3СООН, 2 и. 11 + H2SO4 -» быстрое . обесцвечивание (ср. холостой опыт) P-вы I, II и Ш+анал. 0,0001 Окислители
2 (I), КJ, 0,1 п. (II) и крахмал (III) р-р-> син. окраш. ।
* Раствор 0,05 г бензидина в 10 мл лед. СНзСООН разбавляют Н2О до 100 мл.
** К р-ру I г n-нитроанилина в 20 мл Н2О добавляют 2 мл разб. HCI и при энергичном перемешивании 160 мл Н2О. Затем добавляют 20 мл 2,5% р-ра NaNO2. При взбалтывании осадок растворяется. Реактив постепенно мутнеет, но им можно пользоваться, отфильтровав осадок.
213
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг{мл Мешают определению
NO" Сульфаниловая кислота (1% в 30%-ной СН3СООН) (I) и а-нафтиламин (0,3% в 30%-ной СН3СООН) Анал. р-р + р-вы -> роз. окраш. 0,0002 Fe3+ (маек, винной к-той) (не меш. NO~)
Индол, 0,015% в 96% сп. Анал. P P+P-B + H2SO4 (15 н.) —> кр.-фиол. окраш. 0,001 Окислители (не меш. NO~)
Опп также с p-вами на NH3 после восст. (в шел. ср.) с помощью цинка,
магния или алюминия; опр. также с бензидином + СНзСООН, резорцином
Na" FeCl3, 1% р-р Анал. р-р + р-в —> кр. окраш. 0,01 [Fe (СМ)6]4~. [Fe(CN)6]3-, SCN-, S2~, 52ОГ (F-, РО3-, С2О2-, С«Н4О2-)
CN~ FeSO4 (1) и FeCl3 (II) Анал. р-р + КОН + р-в I+HCl+p-в П > -> син. окраш.
(NH4)2 S„ (I) и FeCl3, 1% Р-Р (И) Анал. р-р + р-в I; выпар., добавл. НС1 + + р-в II —> кр. окраш.
Иодокрахмаль-ная бумажка (J2 + крахмал) Анал. p-p + H2SO4; HCN (газ)+р-вная бумажка -> бц. 0,02
(СНзСОО)г Си 3% р-р (I) и бензидин 1% в 10%-ной СН3СООН (II) Анал. p-p + NaHCO3 (тв.), слабо нагр. -» ->HCN (газ)+ф. б., пропитанную р-ва-ми -> син. окраш. 0,05 С12, Вг2, СЮ , BrO-
CuS (реактивная бумажка) * Анал. р-р наносят на реактивную бумажку -> бц. 0,05 (не меш. Вг , С1~, J", SCN-, [Fe (CN)6J3-, [Fe(CN)6]4-)
Аллоксан, тв. (I) и NH4OH, 2 н. (11) Анал. р-р + р-в 1 + р в II-> крист, ос. (микр.) 0,2 во|-, РО3“ (CNO-, SCN-, [Fe (CN)6[3-, [Fe (CN)6J4-)
Опр. также с HgfNOah, AgNOs, диметилглиоксиматом палладия (или никеля), пикриновой к-той
* Растворяют 0,1 г CuSO4 • 5Н2О в 100 мл Н2О. прибавляют несколько капель NH4OH и в р-р пропускают H2S. Суспензию наносят на фильтровальную бумагу или капельную пластинку.
214
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
SCN- FeCl3, 1% р-р Анал. р-р+НС14-р-в -> -> кр. окраш. 0,01 [Fe (CN)6]4-(маек. CdSO4), J". N- [Fe (CN)6]3“
CoSO4 и амиловый сп. (или ацетон) AgNO3 Анал. р-р выпар., добавл. р-вы -» син. окраш. Анал. р-р + р-в -> бел. ос. нераств. в HNO3 0,02 СГ, Br-, J" CN~
H2S (после восст. цинком)
Опр. также с HgCb, CuSO4, NaN3+J2‘, с p-вами на
po3- (NH4)2 MoO4 (I) * и бензидин (II) ** Анал. р-р (на ф. б.) + -f-р-вы I и II, затем NH3 (газ) -»син. окраш. 0,02 Окислители, восстановители, Si (маек, винной к-той), AsV, F , С2О42-, GeO|-
(NH4)2 MoO4 * Анал. р-р (HNO3, 1 н.) + +р-в -» желт, крист. 0,01
(NH4)2 MoO4 + сульфат хинина *** MgCl2-4-NH4Cl-[-+ NH4OH (стр. 22) Анал. р-р + р-в -» желт, ос. (через несколько минут или при натр.) Анал. р-р+р-вы -» -» крист, ос. (микр.) 0,002 Asv, Si, Ge, S2- , s2or. [Fe (CN)6J3- (мешающие катионы маек, ци-тратионами)
Опр. также c ZrOCI2 или Bi (ЬГО3)з
p2o<- p°r Th (NO3)4 KMnO4 AgNO3 Анал. р-р+НС! (10%) + +р-в-> ос. Анал. p-p + H2SO4+ +р-в -»бц. Анал. р-р+р-в (нагр.)-> -» черн. ос. ..... (не меш. РО3~) (не меш. POJ-)
po; p2or Р-р белка CdSO4 Анал. р-р, р-в-»ос. (коагуляция белка) Анал. р-р+СН3СООН-> -»ос. (не меш. РО3~) (не меш. РО3~ и роГ)
* 5 г (NH4)2MoO4, растворяют в 100 мл Н2О, добавляют 35 мл 5 М HNO3.
** 50 мг бензидина растворяют в Ю мл лед. СНзСООН разб. Н2О до 100 мл.
••* 4 г (NH4)2MgO4 и 0,1 г сульфата хинина растворяют в 100 мл HNO3 (65%).
215
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг]мл Мешают определению
As (общий) Zn, металлич. (I) и ф. б., пропитанная HgCl2, 3% р-р (II) Анал. р-р (в пробир ке) + р-в I + НС1 (5 н.); пробирку закрывают тампоном ваты, пропитанной р-ром CuCl (15% в 10 н. НС1); над отверстием пробирки помещают ф. б. с HgCh, появляется желт, или бур. пятно о,1 (Hg1», те)
NaH2PO2 Анал, р-р+ р-в ->ос.
SnCI2, нас. в конц. НС1 Анал. р-р + НС1 (конц.) + р-в. Нагр.— —бур. окраш., затем черн. ос. 0,02 Hg
H2S (газ) Анал. р-р+HCI (конц.), нагр., пропускают р-в. образуется желт. ос. 0,00001 —
-AsO3 J2 Анал. p-p + NaHCOg + + р-в-> бц. 0,1 Восстановители, щелочи(не меш. AsV)
AI, металлич. (I) и HgCl2 (II) Анал. р-р + КОН + р-в I -> AsH3, опр. с р-вом II (см. выше) 0,05 (не меш. Sb, AsV)
AgNO3 Анал. р-р+р-в -> желт. 0,1 РО® , J
AsO’~ FeMoO4 * (1) и NaF, нас. р-р (И) Р-в 1 + р-в П+анал. р-р. Через несколько минут ->тм.-син. окраш. (сравнивают с холостым опытом) 0,01 РО®-, Au111, W (В, Be, TI, Sc, Pd, Pt, V; не меш. Si)
(NH4)2 МоО4 Анал. p-p + HNO3 (2 и.) + р-в (изб.) -> желт, ос. (микр.). Ос. растворим в NH4OH 0,01 РО®" 4
AgNO3 Анал. р-р 4-р-в-Жор. ос. 0,002
Опр. также с KJ+крахмал, MgCk+NHiCl+NHiOl I
Sb (общая)
H2S (газ)
Анал. p-p + HCl (3 н.) + +р-в-»ор. ос. Ос. р-рим В (NH4>2S
0,0002
• К р-ру 0.484 г Na2MdOt 2HZO в 90 мл Н2О добавляют 4 мл р-ра 2.78 г FeSO4 • 7НаО в 100 мл 1 и. HaSO<. Когда р р обесцветится, разбавляют его НаО до 100 мл.
216
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжен не -
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
Sb (общая) Zn, металлич. Анал. р-р + р-в + конц. НС1 (нагр.) -» черн. хлопья 0,4 Hg, Au, Mo, W,_
Родамин С, а) Анал. р-р + НС1 (до 0,01
0,05% р-р в 15% р-ре КС1, 2 н. по НС1 15%)+KNO2 (тв., немного), погружают раскаленную Pt проволоку. Затем р-р прибавл. к р-ву -> -» фиол.-син. окраш. н люмин. б) Анал. p-p+H2SO4 (1: 3)+KJ (10%) + +бензол. Отделяют орг. слой, добавл. р-в (0,2%)фиол. 0,005 V (Fe3+) NO“, окислители
Г аллоцианин (ди метилам и но-оксиоксазон-карбоновая кислота), 0,05% в 1 н. НС1 окраш. Анал. р-р (содержащий минимальное количество к-ты для удержания в р-ре Sb) +р-в -» син. р-р или син. ос. 0,1 Mo, W, Те, Zr,. Th, Sc, Ga
Кристаллический фиолетовый или метиловый фиолетовый Анал. р-р + НС1 (конц.) +NaNO2+ + мочевина+ р в -> ->фиол. окраш. (ср. с холостым опытом) 0,0001 Сильные восстановители (а также Cu, V, Au, Se,. Те, Mo, W, TI)
Sb3+ Н7[Р(Мо2О7)6] (5% свежеприготовленный) * Анал. р-р+р-в (слабо нагр.) ->син. окраш. (экстр, амил, сп.) 0,01
KJ, 1% р-р (I] и пиридин (II) Анал. р-р+желатина + + р-вы I и II+H2SO( (6 н.) -> желт, окраш. Bi, Ni, Co
KJ, 11% р-р (I) и аскорби-новая кислота 2% р-р (П) Анал. p-p + H2SO4 (1:5) +р-вы I и 11 -5 -» желт, окраш.
(чувств. 0,004; не меш. Sbv)
0,05
Опр. также с. метилфлуороном
Bi3+ SnCl2 5% p-p в Анал. р-р + р-вы I 11
2,5 н. HCI (I) и KOH, 2 h. (II) II -> черн. ос.
Си (маек. KCN). (Pt, Ag, Hg, Au,.
TI)
* Растворяют фосфоромолибдат аммония в царской водке, выпаривают, растворяют в Н2О и дважды перекристаллизовывают. Сохраняют в темной банке.
217:
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг}мл Мешают определению
ВР+ SnCl2, 5% р-р в 3 н. HCI (I), КОН, 2 н. (II) и РЬ (СН3СОО)2, 1% Р-р (И!) Р-в III + анал. р-р (слабокисл.) +р-в II + р-в 1-»черн. ос. 0,002 Ag, Hg, Au, Pt, Те
Цинхонин -|-KJ* Анал. р-р (слабокисл, на ф. б.)+р-в-»ор. пятно 0,05 Au (Hg|+, Se)
KSCN, тв. Анал. р-р (слабокисл.) -р р-в -» желт, окраш. 0,02 Pt, Mo, UO^+, Cu, Au, Fe (Os, V> Cr, Co, Ni, Hg)
Тиомочевина, ТВ. Анал. р-р (слабокисл.) + р-в -» желт, окраш. 0,03 Sb, Se (Hg, Fe, Os, Pt, V, CrVt; не меш. Au)
8-Оксихинолин, 2% р-р в 0,2 н. H2SO4 и KJ (П) Анал. р-р (H2SO4 или HNO3, разб.)+р-в II (изб.)+р-в 1-»кр. ос. или желт, взвесь. Добавл. смесь ацетона и амил. сп.-> -» кр. орг. слой Cu2+, Fe3+, окислители (все маек. SO2)
(NH4)2 нро4 Анал. p-p + HNOg (разб.) + р-в-» ос. Ti, Zr, Sniv (Th)
Опр. также с Кз[Сг(5СН)в], пирогаллолом, хинальдином+ KJ
VO3+, vor НС1 или H2SO4 Анал. р-р (щел., бц.) + -|-р-в-»желт, окраш. 0,005
Н2О2, 1% р-р (I) и H2SO4, 3 н. (II) Анал. р-р + р-в 11 +через несколько минут р-в 1->кр. окраш. MoVI, CrVi, ci , Br“, J~, F~, окраш. ионы
Н3РО4, конц. (I), Na2WO4, 5% (или Na2MoO4) (И) Анал. р-р + р-вы I и II-» -»желт.-кор. окраш. (экстр. изобутил СП.) < 0,005 (Ti, Zr, Bi, Sb, Sn, восстановители, К, NH+)
НС1, конц. (I), FeCl3, 1% р-р (11) и диметил-глиокснм, I % сп. р-р (III) Анал. р-р+р-в I; упар. до половины объема, добавл. р-в П + р-в III+NH4OH (до щел. реакции)-»кр. окраш. 0,007 Окислители
Бензидин, нас. р-р в 10 %-ной СНдСООН Анал. р-р (на ф. б.) + + р-в-»син. или 3. пятно 0,005 CrVi (MoVI)
• Растворяют 1 г цинхонина в 100 мл горячей НгО, капель HNO3 (конц.). После охлаждения прибавляют 2 г
к которой прибавлено KJ. Раствор нестоек.
несколько
218
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг]мл Мешают определению
VO3-vo3+ 8-Оксихинолин, 2,5% р-р в 60% СН3СООН (I), изоамиловый сп. (или хлороформ) (II) Анал. р-р (щел.) + +СН3СООН (2 н.) + + р-вы 1 и II; смесь взбалт. -» тм.-кр. орг. слой (в хлороформе-» тм.-кр. до буро-фиол. окраш.) 0,0002 (Mo, W, Ti, Fe3+]
Опр. также с (NH4)2S, лимонной к-той, K4Fe(CN)6], K3[Fe(CN)6], таннином, 5,7-дибром-8-оксихинолином, дифенилкарбазидом, NH4C1 (тв.), (CH3COO)2UO2
Nbv> Фениларсоно- Анал. р-р+НС1 (0,3— 0,001 Zr, Hf, Ti, Sn
Tav * вая кислота, 3% р-р 3 н.) + р-в -»бел. ос.
ж-Дигалловая Анал. р-р (щел.) + W, Ti (не меш.
кислота или + NH4CI (тв.) + Fe)
таннин, тв. +CH3COONH4 (тв.);
нагр. до кип., добавл. р-в:
Nb -» ор. ос. 0,01
Та -» желт. ос. 0,04
CH3COONa, Анал. р-р+р-вы I и 0,4 (не меш. W, Fe>
нас. р-р (I), NaOH, 2 н. (II) II-» крист, ос. (микр.)
Пирокатехин Анал. p-p + CH3COONa 0,01 Ti, Fe3+ (не
нагр. + р-в-> желт, окраш. меш. W)
Опр. также с H2SeO3, арсеназо
Nbv KSCN, (тв.) (I) Р-в I+анал. р-р + р-в 0,05 (не меш. Та, Ti,
и Zn, метал- II + НС1 (конц.)-» W)
лич. (П) -> желт.-бур.-кр. окраш.
Пирогаллол, Анал. р-р (слабо- 0,01 li (не меш. Та)
7% р-р в нас. щел.) +р-в-» тм.-
р-ре Na2SO3 желт, окраш.
Н2О2 (I) и Анал. р-р+р-вы I и
H2SO4 (II) 11 -> желт, окраш.
Опр. также с К5СН+5пС12+эф.; H3PO4+H2O2+H2SO4
Tav Метиленовый Анал. р-р + р-в -» син. 0,1 (Sb, Sn, Mo, V,
синий, нас. р-р . ос. (ср. с холостым W, Al; не меш.
опытом) Nb, Ti, Zr, Hf)
KF, нас. р-р Анал. р-р (на целлофане или стекле, покрытом коллодием)+ 0,1 (Nb, Ti)
Ч-р-в -> крист. ос. (микр.)
* Раствор, полученный после сплавления минерала с К2СО3, КОН или K2S2O7 и последующего растворения в винной к-те или р-р минерала в плавиковой к-те.
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион • (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
Tav Родамин С, тв. Анал. р-р (ТаРз) + + р-в->фиол. р-р и хлопьевидный ос. 0,025 Hg, Sb, Au, Mov<, WVI, Fe3+ (не меш. Nb и Ti)
Диметил-флурон VI г р Анал. р-р + Н2С2О4 + + жел атина+ р-в-> ->кр. окраш. (или кр. ос.) уппа периодическ ой систем Ti (маек. H2O2) Ы
.S2 Na2|Fe(NO) (CN)5J, 1% р-р Анал. -> р-р + NH4OH 2 н.) + р-в-жр.-фиол. окраш. 0,02 (не меш. SO2-, s2or и so2;)
CdCO3, тв. Анал. р-р + р-в->желт. ОС. (не меш. S2O2 )
Реактивная бумажка, пропитанная (СН,СОО)2 РЬ коос— —(СНОН)2— —COOSbO (антимонил калий тартрат, 5% р-р) Анал. р-р + НС1; реак-тивная бумажка (над р-ром) черн. Р-в (на ф. б.) + анал. р-р->желт.-ор. пятно 0,1 (реакция специфична)
Опр. также с NaNa, метиленовым синим +J2
so2- Zn (NO3)2 На ф. б. р-вы I, II и 0,05 S2~ (не меш.
(нас. р-р) (I), K4[Fe(CN)6], 0,25 M (11), Na2|Fe(NO)(CN)5|, I % p-p (HI) III4-анал. р-р тр.)->бел. ->кр. ос. (некое.-* SO2' и S2O23-)
Zn. металлнч. (I), HCI (11) и (CH3COO)2 Pb или Na2[Fe(NOXCN)sl) Анал. р-р + р-в 11->газ. Опр. р-вом III 1+р-В H2S
(III) Малахитовый зеленый, 0,0025% р-р (или фуксин) Анал. р-р + р-в->бц. 0,05 S2-, С1О“, С№, CNO-, С2О2-, сю- юг, 4 о JO4~, SCN-, муравьиная и винная к-ты (не меш. HSO-, S2O2“, политн-онаты)
:220
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг)мл Мешают определению
SO2" Н2О2 (I) и ВаС12 (II) Анал. р-р + НС1 + р-вы I и П-*бел. ос. SO2-4
Опр. также с Ni(OH)2 + бензидин, иодной водой, КМпО4
so2- KMnO4, 1% р-р (0- Анал. р-р + р-вы I, 11 и III-» тм.-фиол. ос. 0,05 CIO", CN", CNO", SCN-
BaCI2, 1% р-р (II) и Н2О2, 3% р-р (111) (центрифугируют) [Fe (CN)6J3' [Fe(CN)6]’~
ВаС12 (I) н Анал. р-р + р-вы I и 11—> SeO2"
HCI (II) -» бел. крист, ос.
Бензидин, Анал. р-р + р-в ->бел. . . .
солянокислый ОС.
Родизонат ба- Анал. р-р (на ф. б.) +
рия + р-в -» бц.
Опр. также с реактивами на S2- (после восст. натрием или сплавлением с углем и содой)
s o2- AgNO3 Анал. р-р + р-в (изб.) -> S2 , восстанови-
-> черн. ос. тел и
CuSO, Анал. р-р + р-в (нагр •-> » черн. ос. S2-
FeCl3 Анал. р-р + р-в-> -> фиол. -» бц.
FeCl3 (I) и KCN (II) Анал. р-р + р-в 11 + + NaOH (кип.) + + НС1 (конц.) + р-в 1 —» кр. окраш. (не меш. SO2-)
Опр. также с иодокрахмалом, Na2[Fe(NO) (СМ)з] + Кз[Ре(СМ)б’, NaNs + иод, Ni(0H)2 + бензидин, HgCk + КС1, р вами на SO2 (после действия HCI)
5гО2" МпС12 (I) и КОН (11) Бензидин Анал. р-р + р-вы II -> з. окраш. Анал. р-р + р-в - I и >син. 0,02 СгО2-,
.окраш. [Fe(CN)6]3", МпО" СЮ" 4 (не меш. ВгО~, сю;, сю;, н2о2, JO”, NO3~)
221
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ НОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чуветвитель ность, мг/мл Мешают определению
s2or Seiv, SeVi SeO2~ SeO2~ 4 TelV, TeVl CH3COONa, нас. p-p (I), метиленовый синий, 0,5% p-p P-P (П) Na2S2O5, tb. (или SO2 газ) HJ, 46% p-p (или KJ, TB.) Пирокатехин, TB. Пиррол, 1% p-p в 96% сп. (I), FeCl3, 5% p-p (II) и H3PO4, 82% p-p (III) NH4SCN, нас. p-p (I) и HCI, 1 H. (II) 1,1-Дифенил-гидразин (1 г в 90 мл лед. СНзСООН све- жеприготов.) NaF, 5% р-р (I), дифенил-бензидин, 2,5% р-р (II) и НС1, разб. (III) ВаС12 (I) и HCI (II) SnCl2, 5% р-р в 0,5 н. НС1 (I) и NaOH 6 н. (II) Анал. р-р + р-в I; выпар., раств. в р-ве II (нагр.) -> крист. ос. (микр.) Опр. также с TiC Анал. p-p+p-e+H2SO4 (конц.). Кип. 1 мин, охл., образуется кр. окраш. или кр. ос. Р-в (или р-р KJ в конц. НС1) (на ф. б.) + аиал. р-р+ + НС1 -> бур.-черн. пятио (не исчезает при действии 5% р-ра NasSsOs) P-b+H2SO4 (конп.) + + анал. р-р->з.-син. окраш. Анал. р-р+р-в 11 + + р-в П1 + р-в I -» -> син.-з. окраш. Анал. р-р+р-в- 1+р-в П + Н2О (кип. 30 сек} -> кр. окраш. (ср. с холостым опытом) Р-в+НС! (2 н.)+анал. р-р -ж р.-фиол. окраш. Анал. р-р + р-вы I, II и III ->желт. ос. или желт, р-р Анал. р-р + р-вы I и II -> ос. Р-вы 1 и 11 +анал. р-р (шел.) -> черн. ос. 0,01 3 о,1 0,04 0,1 0,007 0,01 0,02 0,05 0,02 См. опр. С1О~ Sn2+ (не. меш. АзШ, Ое, Sniv и Те) Окислители, Мо (при 1 н. НС1 и 0,01 н. KJ TelV не меш., так как не восст.) Sn2+ (не меш. As'11, Sb"1, Sniv, Oeiv, Movi) TeO2~ (не меш. ТеОГ) As111, Sb1", Sn2+, Fe2+, MoVl Окислители (TelV) Au, Ce4+, Ptlv, Ruin, окислители so2-4 As111, Cu, Bi, Au, Sb1", SnIV, MoVI (не меш. Se,v- VI)
222
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжен ие
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
TelV, TeVl (NH4)2sn (I) и Na2SO3, нас. р-р (II) Н3РО2 (10 г NaH2PO2 в 15 мл конц. H2SO4 + 20 мл Н2О) Анал. p-p+NH4OH; натр, до кип., добавл. р-в I (до раств. ос.), затем р в II; натр. 15 мин, выпадает черн. ос. Анал. р-р+р-в (упар.)-> ->черн. ос. 0,015 0,005 As111, Sb111, Snn-lv, Movl (не меш. SeIV-VI, Oe,v) Selv> Vl, Sb111, Sniv
Опр. также с SO2+N2H4.HC1, Zn (металлич.), диэтилдитиокарбаматом
натрия + СС14, тиомочевиной, антрахинон-1-азо-4-диметиланилииом солянокислым (для Te,v)
TeO*~ CuSO4, 0,002% Анал. p-p (щел.)+р-вы 0,03 Asin, Sn2+, Oeiv,
p-p (I), NaOH, 2 н. (11) и K2S2O3, tb. (Ill) MnSO4-4~CuSO4 1, 11 и III; иагр. до кип.-> желт. окраш. Анал. р-р+р-вы I и II; 0,05 MoVI, JOT As, Sb, Sn, Mo
Cr3+ (I) * и NaBrO (II) ** H2O2, 3% p-p нагр. до кип.->бц. (в холостом опыте -> -> фиол.) Анал. р-р+КОН (2 н.) 0,01 (не меш. SeO2-)
(NH4)2 S2O3, + р-в (кип.)-> желт, окраш. Анал. р-р (HNO3, 2 н.) +
50% p-p (I) и AgNO3, 0,1 h. (П) Cs2SO4 или + р-вы I и II; кип. ->желт. окраш. Анал. р-р (слабо- 0,06 Al (Fe, UO*+, Co.
CsCl, тв. (1) и KHSO4, тв. (II) кисл.)+р-вы I и II; слегка упар,—>бл,-фиол. крист, (микр.) Sb, Au, Be, Ag, лантаниды, Y)
Опр. также с Вг2 + фенол, KNO3 (сплавляют), p-вами на СгО* (после окисления)
CrO*-4 AgNO3 . (CH3COO)2Pb H2O2, 3% p-p Анал. p-p (нейтр. или уксуснокисл.) + р-в -> -> кирпично-кр. ос. Анал. р-р (нейтр. или уксуснокисл.) + р-в -> -> желт. ос. Р-в I + HC1 (2 н.)+р в 0,2 (реакция специ-
(1) H ДИЭТИЛО- Н + анал. р р (слабо- фична)
вый эфир (II) кисл.)->син. окраш. (быстро исчезает)
* К раствору Ain SO, • 7НгО (0,05%) лооаиляют CuSO, • 5Н2О (0,01 лг/лог).
** Свежий рр брома в 2 н. р-ре NaOH.
223
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
П родолжение
Определяемы Й ИОН (вещество) Реактив Метод определения Чувствительность, мг[мл Мешают определению
СгО2~ 4 МоО2- Дифенилкар-базид, 1% сп. Р-Р Бензидин, уксуснокисл. р-р Хромотроповая кислота KSCN, 10% р-р (I) и SnCI2, 5% р-р в 3 н. HCI (II) Метиленовый синий, 0,0012% Р-Р (О и nsh4 • H2SO4, тв. (II) Этилксанто-генат калия, ТВ. Диэтилдитио-фосфорная кислота Na2HPO4 Н2О2 Zn или AI, металлич. Феиилгидразин (33% в лед. СН3СООН) Этилацетат (I) и Na2S2O3, 25% р-р (И) Р b + H2SO4 (2 н.) + + амил. сп. + анал. р-р -» фиол. орг. слой Анал. р-р + р-в-> син. окраш. Анал. p-p+HNOs (7,5 н.)+р-в->кр. окраш. Анал. р-р + р-вы 1 и 11->кр. окраш. Анал. р-р + р-вы 1 и II; нагр. 10 мин—> -> бц. (ср. холостой опыт) Анал. р-р (нейтр. или слабокисл.) +р-в + +НС1 (2 н.) -> роз,-фиол. окраш. Анал. р-р + р-в-> малинов. окраш. Анал. р-р + HNO3(2 н.) + + р-в (немного) -> -> желт. ос. Анал. р-р (выпар.) + + NH4OH (конц.) + + р-в + эф.-жр. или роз. окраш. эф. Анал. р-р + НС1 + р-в-> ->син. окраш. Анал. р-р+р-в-жр. окраш. (ср. с холостым опытом) Анал. р-р (НС1) + р-вы I и 11-> бур.-кр. окраш. р-ва I (ср. с холостым опытом) 0,01 0,005 0,02 0,002 0,0001 0,0007 0,002 0,001 Vv, Au111. Hg, Мп2+, MnVH (не меш. НО|+) Окислители (реакция специфична) SeIV, TeIV’VI, F", РО’-, орг. к-ты Окраш. ионы, NO-, S2-, S2O2-, Se, Sn2+, W (F-) Cu, Те, Fe, U, Co, Ni (W) (не меш. W, V, U, Zr, Ti) SeIV, Telv,vl, Sb111, SnIV, Wvl, Vv, JO", c2o2-, so2-w
224
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
МоО2' а, а'-Дипиридил, 3% р-р в 96% сп. (1) и SnCI2, 50% р-р в 10 н. HCI (II) о-Оксифенил-флуорон, 0,1% в 96 % сп., слабоподкисл. НС1 Анал. р р + р-вы 1 .и 11 -> кр. окраш. Р-в (на ф. б.) высуш. на воздухе, добавл. анал. р-р (I н. НС1), KF (20%), HCI (0,5н.) ->карминово-кр. окраш. 0,01 0,03 WVI (маек, винной к-той), Fe, SnIV, SeIV, Teiv-vl (не меш. As 41 и GeiV) Окислители
Опр. также с TINO3 (микр.), дифенилкарбазоном + дифенилкарбазидом, дитиолом, метиленовым синим, пирокатехином, TP + H2O2+NH4OH
WO2 SnCl2,25% р-р в К) н. HCI (1) и KSCN, 10% Р-Р (•)
HNO3, конц.
НС1 (10 н. на ф. б.) +
+ анал. р-р -> ->желт. + р-вы I и 11->спн. окраш.
f-Нафтохипо-лин, 2% р-р
Zn, металлич.
UO2+ К4 [Fe (CN)6], 2 5% р-р
KSCN, 50% р-р (I) и диэтиловый эфир (II).
HNO3, 1 II. (I) и диэтиловый эфир (II) Смесь крист.
KNaCO3 с крист. NaF (100:9)
Айал. р-р (щел.) + + р-в -> бел. ос., раств. в NH^OH
Анал. р-р (НС1, рН = = 3-е-4)+р-в-> бел. ос.
Анал. p-p + HCl (6 н.) + + р-в -> спи. окраш.
Анал. р-р (слабокисл.)+р-в -> кр.-бур. ос.
Анал. р-р (НС1 0,1— 2н.) + р-вы I и II-> -> желт, окраш. эф.
Анал. р-р + р-в I. Экстр, р-вом II, высуш. -> желт, люмин. Р-в сплавл. в Pt петле, смачивают анал. р-ром и вновь сплавл. —> желт, лю-
мин.
0,01 (не меш. Mo, Nb, Та) (кр. окр. Мо -> бц. при добавл. конц. HCI)
0,01 (не меш. Ni, Zn, Mn, Al, Ti, Pb, Be, Zr, V, Cr)
0,03 Fe2+, Cu2+ (оба маек. KJ, F1C1, Na2S2O3), MoVI, Ti4+, F-.PO2-, CN~, окси- кислоты
0,02 Cr2O2-
(F-, Fe, РОЗ*)
0,01 (Mn, Co, Cr, Cu, Fe, Ni, Pb, Pt, Au, Ca, Tli, Zn — отд. экстрагированием урана)
15 Зак. /83
225
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОИОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, м?!мл Мешают определению
ио|+ Опр. к-той, F" Антраниловая кислота, тв. Арсеназо (бен-зол-2'-арсоно-вая кислота-(Г-азо-2)-1,8-диоксинафта-лин-3,6-дисульфокислота, ди-натриевая соль) Флуоресцеин, 0,04% р-р (1) и хлороформ (И) также с салицил CH3COONa (м красным VII гр Ализариновый красный S и Zr(NO3): Анал. р-р выпар., раств. в НгО, добавл. р-в, слабо нагр., выпадают бц. крист, (микр.) Анал. р-р (нейтр. уротропином до pH=4,7 по конго красному) + + р-в -> син. окраш. Анал. р-р + р-вы I и П->св.-кр. окраш. 1атом натрия, (NH4)2COa-икр.), кверцетином, какст S, хинальдиновой к-той, уппа периодическ Р-в (на ф. б.) + + СНзСООН (50%) + + анал. р-р. Кр. р-в становится желт. 0,001 0,0001 0,002 4-TINO3 (мик елином, мор 8-оксихиноли ой с и с т е 0,002 Sb111’ v, F ", РО3’, Ag. Hg, Pb, анионы жирных оксикислот (As, Та) Fe3+, Al, Th, Zr, Ti, Nb, Ta, Cu, Be, POJ-, Asv , Vv, F-, H2O2 (sor) p.), аскорбиновой ином, ализарином ном л ы СЮ", ВгО", [Fe (CN)e]3~, pod c2od NO"
Опр. также с измельченным кварцем+ H2SO4, с LaCh, CaCls, T1CI4+H2O2, Fe(SCN)3
cr K2Cr2O7, tb. (I). H2SO4, КОИЦ. (II) и Анал. р-р (выпар.) + + р-в 1 + р-в II; пары улавливают каплей 0,1 F-, NO”, NO”
ВгО- (Вг-
BrOD
дифенил карбазид, 1% СП. Р-Р (41) Н2О + р-в III + H2SO4 (2 н.) ->кр. окраш.
AgNO3 (I) и HNO3 (II) Анал. р-р + р-вы II и 1 -> бел. ос., растворимый В NH4OH и (NH4)2COa (10%) 0,01 (не меш. СЮ”)
TINO3, ТВ. Анал. р-р + р-в—>бц. крист, (микр.) 0,01 . Вг , J , JO s2or
МпО2, тв. Айал. р-р + р-в + НзБОл, нагр. -> С12
Cl2 Анилин, нас. Анал. р-р + NaOH 0,03 S2 . S2O2 ,
ИЛИ р-р (I) и фе- (1 н.) + p-вы I и II; SCN-, S О2-,
CIO нол, 5% р-р (II) нагр.-> син. окраш. [Fe (CN)6D
* К 0,1% р-ру ZrOCh в 5 н. HCI добавляют небольшой изб. 0.2% сп. р-ра ализаринового красного S, нагревают 10 мин при 100° С. Пропитывают ф. б. и высушивают.
226
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион < вещество) Реактив Метод определения Чувствительность, мг/м.г Мешают определению
С12 или СЮ' С12 или С1О- С1О" сю4- Вг2, ВгО' KJ (1) и крахмал (11) Анилин и о-то-луидин * MnSO„ (нас.) + + Н3РО4 (конц.) (смесь 1:1) H2SO4, конц. On, /Метиленовый синий, 0,5% р-р /Метиленовый синий, 0,03% р-р (I), ZnSO4, 50% р-р (11) и NaNO3, 20% Р-Р (Ш) Флуоресцеин, 0,1% р-р в 50% сп., слабощел. Р-Р Фуксин 4-+ NaHSO3 ** Иодокрахмаль-иая бумага л-Фенилендиа-мин, 5% р-р, слабоподкисл. H2SO4 Анал. р-р (или газ) + +р-вы I и 11->син. окраш. Р-в (на ф. б.) + пары С1г -> син.-фиол. окраш. Анал. р-р + р-в; нагр. -> фиол. окраш. Анал. р-р + р-в-> -> желт.-з. газ . также р-вамн на СР (п Анал. p-p+CH3COONa (нас.). Выпар., раств. в р-ве (нагр.), выпадают фиол. крист, (микр.) Анал. р-р+р-вы II, 111 и I -> кр.-фнол. окраш. Ф. б. пропитывают р-вом, действуют парами, нагр. анал. р-ра -> роз. окраш. Пары анал. р-ра + р-в (на ф. б.) -> син. окраш. Анал. р-р (или пары) + + р-в->син. окраш. Анал. пары + р-в -> -> бц. крист, (микр.) Опр. также с СС14 или 0,01 0,1 осле восст.) 0,01 0,01 0,01 0,1 СНС13 Вг~ и J- (удаляют выпар, с РЬО2 + + СН3СООН) СЮ", ВгО~, JQ-, JO4-, s2oe2-, no-, [Fe (CN)6j4-, [Fe (CN)6]3- CIO-, CIO", Br-, J", S2- , S2O2-, N“, NO~, NO- S2O2-, окислители (не меш. сю3-) S2 . S2O2-, CN-. SCN' (не меш. NO") CN~
* Смесь 100 мл нас. р-ра анилина+20 мл СН?СООН. Сохраняется в коричневой бутыли
** Раствор фуксина, обесцвеченный NaHSOs-
нас. р-ра о-толуидина и 30 мл лед.
15*
227
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг(мл Мешают определению
Вг- КМпО4, 0,1 н. AgNO3 (I) и (NH4)2 со3, 10% р-р (11) а) Анал. р-р + р-в + +H2SO4 (2 и.); нагр. В выделяемых парах опр. Вгг б) Анал. р-р+СС14 + + HgSO4 (2 н.) + 4-р-в -> желт, окраш. Анал. p-p+HNO3+p-B I -> желт. ос., не-раств. в р-ве 11 (отличие от С1") 0.005 J- (маек. изб. Р-ва)
Опр. также с Hg(NO3)2 + дифенилкарбазид
Вг°- KBr (I) и флуоресцеин (II) MnSO4, 2% р-р (I) и бензидин, 0,05% в 10%-ной СН3СООН (II) Анал. р-р+р-в 1 + + НС1->Вг2. Опр. с р-вом II Анал. р-р+р-в 1 + + H3SO4. Нагр. 2 мин, охл., добавл. р-в II и CH3COONa (тв.)-> ->син. окраш. 0,3 (не меш. СЮ, и JO’)
J2 Крахмал. I % Р-Р Анал. р-р + р-в —> син. окраш. 0,05 С12, Вг2, CN ‘ (CN удаляют нагр. с NaHCO3)
Na2S2O3, 0,1 н. Анал. р-р + р-в —> бц.
СС14 или СНС13 Анал. р-р + р-в-> фиол. орг. слой
J NaNO2, 10% р-р (I) и крахмал (11) Анал. р-р+СН3СООН + +р-вы I и 11->син. окраш. 0,005 CN (удаляют нагр. с NaHCO3)
Хлорная вода (1), бензол или крахмал (II) Анал. р-р + р-вы I и II -> фиол. (или сии.) окраш. р-ва II; при пзб. С1г->бц. 0,0005
AgNO3 (I) и NH4OH (II) Анал. р-р + р-вы I и II-> желт. ос. (не меш. С1 и Вг-)
NHg2NO3 * Анал. р-р + р-в -» желт, до бур. ос. 0,1 C1O-.S2-, SiO2-, CN-, НСО2“, СН3СОО-, BrO-, N-SCN-, [Fe(CN)6]3-, [Fe (CN)6J4-
• Растворяют 10 г Hg(NO3)2 в смеси 5 мл конц. HNO3 и 50 мл Н2О, затем добавляют 60 мл 7,5 н. NH.OH.
228
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, м г/мл Мешают определению
J- JO- JO4- Мп2+ PdCI2, 1% р-р (NH4)2 [Се (5О4)з], 0,5 М в 2 н. H2SO4 (I) и NaAsO2, 0,5 Л4, нейтр. или слабокисл. (И) NH4SCN (I) и крахмал (II) AgNO3 Th (NO3)4 MnCI2, 10% р-р (1), n-те-траметилдиа-минодифенил-метан, нас. р-р в 2 н. СН3СООН (II) K2S2Og, ТВ. (I) И AgNOg, 1% р-р (11) KJO4, нас. р-р (I), п-тетраме-тилдиаминоди-фенилметан, нас. р-р в лед. СН3СООН (II) NaBiO3, тв. Br2(I), NH4OH (II) NaOH (I) и бензидинацетат (II) (NH4)2 S Анал. р-р (на ф. б.) + + р-в->тм.-бур. ос. Анал. р-р + р-вы 1 и П->бц. (быстрее, чем в холостом опыте) Анал. р-р (НС1)+р-вы I и П->син. окраш. Анал. p-p+HNO3+ +р-в->бел. ос. (микр.) Анал. p-p + HNO3+ +р-в.-» белый ос. Анал. р-р+р-вы I и П->син. окраш. Анал. p-p + HNO3 (1 н.) + + р-вы I и II (нагр.)-> -> фиол. окраш. Анал. р-р (слабокисл, на ф. б.)+р-вы I и 11->син. пятно Анал. p-p + HNO3 - (нагр.)+р-в->фиол. окраш. Анал. р-р + р-вы-> бур. ос. Анал. р-р + р-в I, через несколько минут добавл. р-в 11->син. окраш. Анал. р-р+р-в ->роз. ос. 0,02 0,0001 0,01 0,002 0,00003 0,003 0,003 CN’, SCN". S2" F", S2O2-, N", NO", SCN-, Os (C2O2-, [Fe (CN)3]3~, [Fe (CN)6]<-, JO", JO7, Cu, Fe3+, UO2+, Co, Ni) (не меш. C1O“, BrO;, JO-) (реакция специфична) (Cl“, СгО2-) Au, Rh, Ir, V, Cr, Ce4+
Опр. также с ацетилсалициловой к-той+Н2О2, с KNO3-l-Na2CO3 (сплавление), РЬО2, KJO4, дитизоном, Ks[Fe(CN)6], (NH4)2C2O4 (микр.)', AgNOs+NH4OH (на ф. б.)
229
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
МпОГ 4 о-Толидпн, нас. в лед. СНзСООН Анал. р-р (на ф. б.) + + р в—>син. пятно 0,0015 Ag, Bi, Аиш, Iriv, PtIV, Ce4+, Vv, CrVi
ReO~ 4 * SnCI2, 50% р-р в 10 н. HCI (I) и Na2TeO4, 1% р-р 00 Анал. р-р + р-вы II и I -> черн. ос. (быстрее, чем в холостом опыте) 0,0005 Hg, Ag, Au, Rh, Pd, MoVI, Ti
Диметилглиок-сим, нас. сп. р-р (I) и SnCI2, ТВ. (II) Р-в I + р-в II + HCI (10 н.) + анал. р-р (слабокисл.) -> кр,-бур. ос. 0,02 Hg, Au, Rh, Pd, Ir, Pt, TI, Mo
NH4SCN, 20% р-р (I) и SnCI2, 35% р-р (II) Анал. р-р + НС! (кони.) + р-вы I и 11-> желт.-кор. окраш. (экстр, бутил. СП.) 0,001 MoVI, Pt
CsCI (или TINO3, или AgNO3) Анал. р-р выпар., раств. в р-ве, выпадает крист. ос. (микр.) 0,001 CIO-, SnCI2-, Ptci*-b
(проба иа пламя) Анал. р-р (НС1). 3. окраш.
УЧИ группа периодической системы
Fe3 + nh4scn а) Анал. р-р + НС1 0,005 Окраш. в-ва, F~
(6 н.) +р-в ->крова-во-кр. окраш. б) при малом к-ве Fe^ анал. р-р+НЫОз (1:1) +р-в + смесь изоамил. сп. и эф. -> -> кр. орг. слой POJ", тартратной
K4 [Fe (CN)6], 10% p-p Анал. р-р + р-в ->син. ос. 0,03 Cu, 1Ю|+, MoVI. F-, РО4~ (Hg, Sbv, W, V, Ti, Zr, TI, Co н др.)
Сульфосалициловая кислота, 5% р-р Анал. рр (рН«2) + + р-в-> фиол.-кр. окраш. 0,003 F~, PO®-, анионы жирных к-т, Ti (не меш. Fe2+)
Феррои (7-ио-до-8-окси-хи-иолин-5-суль-фоновая кислота) Анал. р-р (рН~5) + + р-в-> син.-з. окраш.
Опр. также с 4-диметиламиноантипирином (микр.), салицнлальдоксимом, а также p-вами на Fe2+ (после восст. гидроксилам ином пли др. восст.)
230
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион • вещество) Реактив Метод определения Чувствительность, мг}мл Мешают определению
Fe2+ K3[Fe(CN)6] Анал. р-р (кисл.) + + р-в -> тм.-син. ос. 0,0001
Диметилглиок-сим, 1% сп. р-р Анал. р-р + р-в + + NH4OH (11 н.) -> -> кр. окраш. 0,002 Ni (Со, Rh, Ir, Pt, W) (не меш. Fe3+, F", РО3“, анионы жирных к-т)
а, а'-Дипири-дил, 0,02% р-р в 3 н. НС1 Анал. р-р + р-в+ +NH4OH до слабо-щел.->кр. окраш. 0,0005 (Со; не меш. Fe3+, F", РО43“)
о-Фенантролин, 0,025 Л! Анал. р-р (рН=2) + + р-в -> кр. окраш. 0,0002 к (Си, Sb111, Со; не меш. Fe3+, F-, РО3-)
Опр. также с нитрозо-Р-солью, а-нитрозо-Р-нафтолом, тиогликолевой к-той, сульфосалициловой к-той, а также с р-ва ми на Fe3+ (после окисления
ТВ. КгЗгОв или др. окислителями)
|Fe(CN'6p- НС1, 2 н. и Анал. р-р+р-в 1 + р-в 0,02 [Fe(CN)6]3-,
FeCl3, 1% р-р П->сии. окраш. или SCN-, С2О2-,
СИН. ОС. CN-,C1O",J-,
s2-, JO”
CuSO, Анал. р-р+р-в-> бур.
ОС.
|Fe (CN)6|3- FeSO4, 5% р-р Анал. p-p+HCl (2 н.) + 0,02 [Fe (CN)6]4-,
в 1 М Н25О4 +р-в->син. окраш. окислители,
ИЛИ син. ОС. восстановители
Бензидин, нас. Анал. р-р + р-в -> син. 0,02 Окислители,
в 2AI СН3СООН окраш. [Fe (CN)e]4“, маек. Pb2+
Опр. также с [Co(NH3)6](NO3)s, бруцином
Со2+ (NH4)2[Hg(SCN)4], Анал. р-р (слабо- 0,002 Cu (Fe3+ маек.
~3% р-р* (I) кисл.) + р-в II; упар. F )
и ZnSO4, 0,5% добавл. р-в I, обра-
Р-Р (П)- зуются син. крист, (иногда через 10 мин) (микр.) Fe3+ (маек. F~)
KSCN, тв. или' Анал. р-р (слабокисл. 0,001
NH4SCN, нас. или нейтр.) + р-в -> (Си, Bi, Sbv,
р-р в ацетоне ->син. окраш. (экстр. OsIV, PtIV,
амил, сп.) Мош, Wni, Vv, Cr"1, Uvl, Ce4+)
• .Раствор 2,7 г HgCh и 3 г NH4SCN в 100 мл НгО<
231
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый нон (вещество) Реактив Метод определения Чувствительность, мг[мл Мешают определению
Со2+ а-Нитрозо-(3-нафтол, 0,5% сп. или уксуснокислый р-р Анал. р-р (рН~2) + + р-в (без изб.) —> -> кр. ос. 0,001 Cu, Fe(Fe3+ маек. F ), СЮ|+, Се4+, Hg, Vv, Ti, Ni
Рубеановодо-родная кислота, нас. р-р в 96% СП. Анал. р-р (на ф. б.), нейтр. NH4OH, вы-суш., добавл. р-в, получается кр.-бур. окраш. 0,001 Fe3+ (маек. F"), Ni, Cu (Ag)
Na2O2, тв. (I) и NaHCO3, конц. (II) Анал. р-р + р-в 11 + + р-в 1->з. окраш. (глицерин или маннит стабилизирует окраш.) 0,0004 Vv (CrVI, Mnvn) (не меш. Ni)
Опр. также с KNO2, Р-нитрозо-а-нафтолом, нитрозо-Р-солью, дитизоном, 2-нитрозо-1-нафтол-4-сульфокнслотой, KCNO + амил. сп.
Ni2+ Диметилглнок- Анал. p-p+NH4OH (до 0,003 Fe2+ (маек. Н2О2),
сим, нас. р-р в 96% сп. шел. реакции). Фильтр. Ф-т-Ьр-в-> -> кр. окраш. и кр. ос. Си (Со маек. Н2О2 -|-N а2СО3; Pd)
Рубеановодо-родная кислота, нас. сп. р-р Анал. р-р (слабокисл, на ф. 6.)+CH3COONa (10°/о) + р-в->тм.-син. окраш. 0,001 Fe3+ (маек. F"), Си, Ag, Hg+
КОН (I) и бромная вода (П) Анал. р-р + р-вы I и II -> бур. ос.
Опр. также с дифенилглиоксимом и другими оксимами, с (NH4)2MoO4 (микр.)
Ионы НСООН (или Анал. р-р +
металлов группы Pt другие восст.) 4- CH3COON а + р-в—> —>черн. ос.
RuIV Тиомочевина, ТВ. НС1 (конц.)+анал. р-р + р-в ' (нагр.) -> -> син. окраш. 0,01 Не опр. Os
232
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжен ие
Определяемый иои (вещество) Реактив Метод определения Чувствительность, мг!мл Мешают определению
Ru3 + Рубеановодо-родная кислота, 0,2% р-р в лед. СНзСООН Анал. р-р + НС1 (2н.) + р-в (нагр.) -»син. окраш. 0,01 Cu, Со, Ni, Аи, Pd, Pt (не меш. ионы металлов группы Pt)
Rhlll n-Нитрозо дифениламин, 0,05% р-р в 50% СП. Анал. р-р + р-в (нагр. 5 мин при 100°С)-> -»ор.-кр. окраш. 0,01 CeiVt Fe34*, Os34*, NO~, Ptlv, SCN~, Zr
SnCl2, 40% р-р в 8 н. НС1 Анал. р-р + р-в (нагр.)-» ->бур. окраш. При охл.-»кр. окраш. 0,01 Au, Pd, Pt, Ru, Os, Ir
TiCl3 Анал. р-р + р-в -»ос. (Ir не меш.)
PdH Диметилглиоксим, ТВ. Анал. р-р (слабокисл.) + р-в -желт, крист, (микр.) 0,1 Au, Ni (не меш. ионы металлов группы Pt)
Диметилглиоксим, нас. сп. Р-Р (О» Nl (NO3)2, 5% р-р (II) и НС1 (HI) Анал. р-р (на ф. б.) + + р-в I; высуш., добавл. р-в II, промыв. Н2О, погружают в сп., высуш., добавл. р-в III, хол. Н2О, остается кр. пятно С,005 CN-,[Fe (CN)6]3-. Hg2+, S2O23- (не меш. Au, Ni, ионы металлов группы Pt)
Hg2CI2, тв. Анал. р-р взбалт. с р вом-»серый ос. 0,01 Au (не меш. ионы металлов группы Pt)
п-Диметилами-нобензилиден-роданин, нас. сп. р-р Анал. р-р (на ф. б., пропитанной р-вом) + + CH3COONa-» -»фиол. окраш. 0,001 Au, Pt (Ag, Hg+)
Антраниловая кислота, 5% Р-Р Анал. р-р (слабокисл.) + + CH3COONa + p-B. Через несколько минут-»бл.-желт. ос. 0,01 Аи (не меш. ионы металлов группы Pt)
OsVIn KSCN или NH4SCN, тв. Анал. р-р (слабопод-• кисл. HNO3)+p-e + +эф. или амил. сп. -» -» син. окраш. 0,001 (не меш. OslV и ионы металлов группы Pt)
KJ (I) и крахмал (II) Анал. р-р + р-вы 1 и II+H2SO4 -»син. окраш. (з. H2[HsJ4] экстр, эф.)
233
ИНДИВИДУАЛЬНЫЕ РЕАКЦИИ ИОНОВ
Продолжение
Определяемый ион (вещество) Реактив Метод определения Чувствительность, мг/мл Мешают определению
OsIV, Тиомочевина, Анал. р-p + HCl (5%) + 0,01 (реакция специ-
OsViu ТВ. + р-в (нагр.)->кр. окраш. фична)
а-Нафтиламин солянокислый, ТВ. Анал. р-р (слабокисл.) + р-в (нагр.) -> ->тм.-син. или черн. ос. 0,001 (Au, Ir, Pt)
Iriv H2SO4, 7,5 н. (I) HNO3, конц. (11) Анал. р-р (нагр.)-Ьр-в I (изб. до удаления НС1)+р-в II (нагр.)-* -*син. окраш. 0,15 (Ru, Rh, Pd)
Тетраметилди-аминотрифе-нилметан, I % р-р в 2 н. СН3СООН Анал. р-р+р-в ->з. окраш. 0,01 Au, окислители (Ru)
Бензидин, нас. р-р в лед. СНзСООН Анал. р-р (на ф. б.) + 4-р-в-> син. пятно 0,2 Au, Ru, OsViu
Ptiv KCI, тв. Анал. р-р + р-в (нагр.)-* -»крист, ос. (микр.) 0,1 Os, Ir
NaJ, тв. (1) и NH4OH, 1% р-р (11) Анал. р-р+р-в II (до щел. реакции)+р-в I-* крист. ос. (микр.) 0,1 (Ru, Pd)
Наркотин, 1% р-р в коиц. H2SO4 (I), SnCI2, 10% р-р (11) и FeSO4, 10% р-р (III) Анал. р-р (на ф. б.) + + смесь р-вов (1:1:1)-* желт, пятно (Au, Pd)
Рубеановодо-родная кислота, 0,02% р-р в лед. СНзСООН Айал, р-р + р-в-> фиол.-кр. ос. 0,1 Pd (Au, Ru)
л-Нитрозоди- Анал. р-р + 0,05 Aulll, Pd2+,
метиланилин, 0,05% р-р в 60% сп. + СН3СООН+р-в. Кип. 5 лшн-*кр. окраш. Ce4+, Rh3+, Ru3+, SCN", BrO-,[Fe(CN)6]3-. TeO3~
234
микрохимический анализ
235
Продолжение
СХ Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
Ag’ А13 + AsO3" 4 (NH4)2[Zn(SCN)4] Пиридин, КМпО4 Тиомочевина, соль Рей-неке Тиомочевина, пикрат калия Cs2SO4 или CsHSO4 KHSO4 nh4f (NH4)2MoO4, nh4ci AgNO3 Ag2[Zn(SCN)4] [Ag(CSN2H4)2]- • [Cr(NH3)2(SCN)4] [Ag(CSN2H4)2]- • CfiH2N3O7 CsA1(SO4)2- 12H2O KA1(SO4)2 12H2O (NH4)3[A1F6] 3(NH4)2O-ai2o3- • 12MoO3- 19H2O Ag3AsO4 Раздвоенные кристаллы, иглы Темно-фиолетовые иглы Пучки тонких игл Иглы, розетки Октаэдры » Мелкие октаэдры Ромбические пластинки Бурые звездочки и палочки 0,4 0,1 0,4 0,003 0,08 0,35 0,3 0,06 0,08 1 .-2 500 I: 10000 1:2 500 1:330 000 1: 12 500 1:3000 1:6500 1:50 000 1 : 12 500 Cd2+, Hg2+ Cu2+ Cd2+, Bi3+ Cd2+, Cu2+, Hg2+, Pb2 + In3+, Ga3+, Sc3+, Ca2+, Sr2+, Ba2+ In3+, Ga3+, Sc3+, Ca2+, Sr2+, Ba2+ L1+, Fe3+, In3+ Be2+, Fe3+, Cr3+ СГ, Br-, J-, PO3-
Ацетат кальция, NH4OH Hg2(NO3)2 NH4CaAsO4 6H2O Hg3AsO4 Прямоугольники Светло-желтые звезды и дендриты 0,04 0,3 1:25000 1:6 500 POJ- СГ, Br-, J-, PO3-
MgCl2, nh4ci, nh4oh (NH4)2MoO4, HNO3 NH4MgAsO4 • 6H2O (NH4)3AsO4 • 12MoO3 Трапеции, призмы, дендриты Желтые мелкие кристаллы 0,05 0,2 1:20 000 1:5000 PO3- 4 PO3-, SiO3-, Bi3+
(NH4)2MoO4, HNO3, моноэтанол а мин (H2NCH2CH2OH)5- • H7[As(Mo2O7)6-2HNO3. • 10H2O Желтые ромбы 0,015 1: 130 000 PO3-4
Хинолин, NaJ, HCI Желто-оранжевые иглы 0,0004 1:2500000 Сн2+, Cd2+, Bi3+
AsO3- Au3+ AgNO3 KJ, CsCl KJ, HCI AgCl, CsCl, HCI Кофеин Ag3AsO3 Cs2[AsJ5] или CsstAsJe] AsJ3 Cs2Ag[AuCl6] Желтые мелкие кристаллы Красные шестиугольники Желтые шестиугольники, треугольники Почти черные крестики, четырех- и шестилучевые звезды Светло-желтые иглы, призмы 0,01 0,02—0,2 0,01 1:100000 1:100000 PO3-, AsO3-, СГ, Br- Sb3+, Bi3+ Pb2+, Sn2+ Pt4 + Pd2+
Кофеин, NaBr NH4SCN NH4SCN, CsCl Пикриновая кислота, NH4OH Пиридин, НО Пиридин, НВг RbCl TINO3 C8Hi0O2N4 H[AuBr4] ’ 2H2O NH4[Au(SCN)4] Cs[Au(SCN)4] C5H5N • H[AuClJ CsH5N H[AuBr4] Rb[AuCl4] T1[AuC14] 5H2O Оранжево-желтые иг-лы Оранжево-желтые иглы, розетки Оранжево-желтые иглы Желтые иглы, розетки, Х-образные дендриты Желтые кристаллы Бурые призмы Желтые призмы Желтые длинные иглы 0,6 0,4 0,2 0,1 6 1:5000 1:2500 1:5000 1 : 10000 1 : 170 pt4 + Ag+, Hg2+ pt4+, pd2+, Sn’+ Co2 + , Ni2+, Cu2+, Ag+ pt4+ Zn2+, Co2+, Cu2+, Cd2+, Hg2+ Bi3+, Sb3+, Pt4+ Pt4+, MoO3-, WO2- 4
+ СЧ ca 237 Уротропин Н2С2О4 или (NH4)2C2O4 BaC2O4 • nH2O Светло-желтые иглы, дендриты Снопы и розетки из игл, дендриты 0,6 0,5 1:5000 1:2 000 Ag+, Hg2+, Sb3+, Bi3+, Pt4+ Ca2r. Sr?+, Pb2+, Z112T
МИКРОХИМИЧЕСКИЙ Н АНАЛИЗ
£3 Продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Иоиы, мешающие реакции и образующие аналогичные осадки
Ва2+ H2SO4 BaSO4 Мелкие крестики, четырехугольники 0,05 1:20 000 Са2', Sr2', Pb2'
К2С.Г2О7, СНзСООН ВаСгО4 Светло-желтые квадраты, прямоугольники 0,08 1: 12 500 РЬ2+
K4[Fe(CN)6] K2Ba[Fe(CN)6]- 5Н2О Бледно-желтые ромбы, параллелограммы, треугольники 0,2 1:5000 Са2', Cu2', Fe3'
KJO3 Ba(JO3)2 Ромбы, изогнутые иглы, дендриты 0,03 1: 100000 Са2', Sr2', Ag+
(NH4)2[SiF6J Ba[SiF6] Иглы, линзы, пучки игл 0,1 1:10000 Na+
Na[BF4] Ba[BF4]2 Призмы, палочки 0,06 1:50 000 К', Rb+, Cs+
Нафтоловый желтый Желтые мелкие иглы 2 1:500 K+, Rb', Cs', Ca2', Sr2'
Озазон диоксивинной кислоты (Na-соль) •Мелкие тонкие иглы 0,05 1:20 000 Ca2', Sr2'
Be2' Ацетилацетон (С5Н7О2)2Ве Шестиугольники, ромбы 0,008 1: 125000
Ацетаты натрия, уранила NaBe (UO2)3 (CH3COO)9-6H2O Бледно-желтые ромбоэдры 0,08 1 : 12 500 Mg2', Zn2', Co2', Ni2'
КНС2О4 BeCgCV К2С2О4 Призмы, двойники 0,08 1-12500 Ca2', Sr5', Ba2'
(NH4)2MoO4. nh4ci Иглы, пучки игл, ромбы 0,15 1:7000 Al3', T1+, Ni2'
Bi3i Бруцин, КВг, H2SO4 Зеленовато-желтые розетки из игл 0,4 1:2500 Cd2'. Hg2', Sb- -
К2С2О4 K[Bi(C2O4)2] Бипирамиды 0,3 1:6 500 Ca2', Sn2', Ce3 r
KJ, ацетат свинца Оранжевые иглы 0,1 1: 10000
K2SO4 3K2SO4-Bi2(SO4)3 Шестиугольники, звезды 0,3 1:6 500 Al3', Ca2', Sr2'. Ba2 + , Pb2'
Кофеин, НС1 Оранжевые призмы 0,5 I :2 000 Sb3'
N 3Na9SO4 • Bi2(SO4)3 Палочки, розетки 0,3 1 : 6 500 Ca2 , Sr2', Ba2'. Pb5', Ce3'
р-Нафтнламин, KJ Желтые, бурые параллелограммы, иглы, розетки из игл 1 1 ; 1 000 Sb3'
8-Оксихинолин, KJ C9H7NOH • H[BiJ4] Оранжевые или красные розетки из игл 0,008 1 : 125000 Cu5', Cd2', Sb3'
Пиперазин, NaJ Красные пластинки, призмы Sb3'
Пиридин, KJ C5H5N • H[BiJ4] Оранжевые и красные призмы и изогнутые иглы Sb3'
RbCl Rb2[BiCI5] • 2,5H2O Ромбы, шестиугольники 0,13 1 :7 500 Pb5'. Sb3', Cd2'
RbCl, KJ Rb[BiJ4] или Rb2[BiJs] Красные шестиуголь-ники .... Sb3', Au3', Pb2'
Сульфат ферро-а, а'-ди-пиридила, НС1 Черные шарики, друзы, красные розетки 0,1 1 : 10000 Hg2', Sb3', Sn4'
Тетраэтил аммоний иодид Оранжевые треугольники Sb3'
Тиомочевина, соль Рей-неке Bi(CSN2H4)6- • [Cr(NH3)2 • (SCN)4] Розетки из игл 0,17 1:6 000 Pb2', Cd2', Cu2'. Ag', Hg2'
Уротропин, НС1 (CeH,2N4 • HC1)3 • BiCl3 Ромбы, октаэдры 0,4 1:2 500 Ag ', Hg2', Sn2', Sb3', Au3'
Уротропин, KJ (C6Hi2N4-HJ)s- • 3H[BiJ4] • 4H2O Оранжево-желтые шестиугольники 0,05 1:20 000 Hg2', Sb3+,Sn2', Cd2'
Хинолин, KJ C9H7N • H[BiJ4] Оранжевые или бурые параллелограммы и прямоугольники 0,1—0,2 Cu2', Cd2', Sn2', Sb3'
Хинолии, NH4SCN Золотисто-желтые Х-образные кристаллы 0,3 1:6500 Co2', Cd2', Fe2', Ti4'. Zr4'
в°|- NH4F, КС1, НС1 K[BF4] Шестиугольники 0,1 1:10000
МИКРОХИМИЧЕСКИЙ
К) £ Продол мнение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции н образующие аналогичные осадки
Вг' AgNO3, NH4OH (C2H6Hg)3PO4 [Ag(NH3)2]Br C2HsHgBr Очень мелкие треугольники, шестиугольники, кубы Ромбы, прямоугольники 0,05 0,3 1 :20 000 1:6500 СГ, J", CN", SCN" СГ, J-, СгО2", JO3"
C2H5CH2HgOH C6HsCH2HgBr Квадраты, прямоугольники 0,1 I : 10 000 СГ, J", CN", SCN"
C.6H6HgOH C6HsHgBr Квадраты 0,05 1:20 000 СГ, J-, С№, SCN"
ВгО" Сд(МОз)2, пиридин K2SO4, Pt(SO4)2 TINO3, AuCl3 TINO3, Pt(SO4)2 AgNOa Hg2(NO3)2 [Cd (C5H5N)2]Br2 K2[PtBr6] Tl[AuBr4] Tl2[PtBr6] AgBrO3 Hg2(BrO3)2 Прямоугольники, Х-об-разные кристаллы, розетки из игл Бурые октаэдры Оранжево-красные призмы Желтые мелкие октаэдры Мелкие вытянутые шестиугольники, палочки, призмы Шестиугольники, иглы, пластинки 0,03 0,25 0,006 0,15 0,75 1 : 100 000 1:4 000 I : 160 000 1:7 000 1: 1 300 J", SCN" СГ, J", SCN" J", CN" СГ, J”, SCN ' СГ, Вг", J", CN", SCN" СГ, Br", J"
Ca2J H2C2O4 или (NH4)2C2O4 H2SO4 CaC2O4 • 3H2O CaSG4 • 2H2O Октаэдры, квадраты, крестики Длинные иглы, пучки игл, ромбы, параллелограммы 0,05 0,04 1:20 000 I : 25 000 Sr2+, Ba2+, Zn2-. Pb2r Sr2 + , Ba2+, Pb2 +
16 Зек. 783
Cd2+
1 KJO3 Na2SeOs Нафтоловый желтый Ca (JO3) 2 CaSeO3 Бипирамиды Ромбы Желтые иглы, пучки игл 0,1 1: 10000 St-U, Ва2 . Ag- Ва2- К+, Rb-, Cs-Sr2+, Ва2+
Пикролоновая кислота (C10H7N4Os)2Ca Мелкие призмы 0,1 1: 10 000 Pb2+
Тартрат калия-натрия Антипирин, КВг C4H4O6Ca • 4H2O (C„H12ON2)-H2|CdBr4]. 2CnH12ON, Ромбические призмы, шестиугольники, треугольники, трапеции Призмы, дендриты, Х-образные кристаллы 0,03 I : 100 000 К+, Rb+, Cs-, Sr2+, Ba2+ Zn2 +
Бруцин, КВг, H2SO4 RbCI (C23H26O4N2)2 • H2[CdBr4] Rb4[CdCl6] Розетки, ромбы,-параллелограммы Ромбоэдры 0,12 0,01 1:8000 1: 100 000 Hg2+, Bi3+, Sb3 + Bi3+, Sb3+, Sn4+, ln3+, PtIV
Н2С2О4 CdC2O4 • 3H2O Призмы, кресты, ромбы 0,35 Г. 3 000 Zn2+, Mn2+, Ca2+, Sr2+, Ba2+
K3[Co(CN)6] Морфолин, NH4SCN Cd3[Co(CN)6]2 Квадраты Бесцветные параллелограммы, ромбы 0,1 1:10000 Zn2+, Mn2+ Zn2 + , Pb2+, Hg2+, Cu2+, Ni2 +
(NH4)2[Hg(SCN)4] Cd[Hg(SCN)J Призмы I 1:1000 Zn2+, Co2+, Ni2+, Cu2+, Pb2+
(NH4)2[Zn(SCN)4] Р-Нафтиламин, NH4SCN Cd[Zn(SCN)4] Узкие длинные прямоугольники, иглы, розетки Пластинки 0,25 0,12 1:4000 1:8000 Ag+, Hg2 + Cu2+
Никотин, NH4SCN Дендриты,,, розетки 1 0,4 1:2 500 Mn2+, Zn2+, Fe2+. Co2+, Ni2+, Cu2+
МИКРОХИМИЧЕСКИЙ АНАЛИЗ
КЗ продолжение
4^
Откры- Пре дель- Ионы, мешающие
мая кон- реакции
Ион Реактив Состав осадка Характеристика осадка минимум, цеитрация, и образующие
мкг г/г аналогичные осадки
Cd2 + 8-Оксихинолин, KJ, Мелкокристаллический 1,2 1:800 Cu2+, Bi3+, Sb3+
HNO3 осадок
Пикрат калия, тиомо- [Cd (CSN2H4) 4] Х-образные кристаллы 0,03 1:100000 Cu2+,Hg2+,Pb2+,
чевина • (C6H2N3O7)2 Ag+
Пиридин, КВг [Cd(CsH5N)2]Br2 Мелкие призмы 0,05 1:20 000 Zn2+, Со24-, Cu2+,
Hg2-, Au3r
Пиридин, К2СГ2О7 [Cd(C5HsN)2]Cr2O7 Желтые мелкие шести- 0,3 1:6500 Zn2+, Co2+, Ni2+,
угольники, трапеции, Cu2 r, Hg2 h
параллелограммы,
палочки
Пиридин, NH4SCN [Cd(C5H5N)2](SCN)2 Мелкие призмы 0,05 1:20000 Zn2+, Co2 + ,
Cu2 ’, vo;
Тетрафенилфосфоний, Бесцветные Х-образ- 0,3 1:6500 Zn2+, Mno; 4
хлорид ные кристаллы
Тиомочевина, соль Рей- Мелкие иглы 0,02 1:50 000 Cu2-, Pb2C Ag-,
неке Hg2 —, Bi3-
Уротропин, KJ Шестиугольники 1 1: 1 000 Hg2-, Sn2+, Bi3+,
Sb3+
Се3- Н2С2О4 Ce2(C2O4)3- ЮН2О Призмы, двойники, Zr4+, Th4-, La3+,
тонкие иглы Sm3-
Na2SO4 Ce2(SO4)3 • Na2SO4 • Мелкие линзы, шести- La3+, ргз+, Nd3-,
2H2O угольники Sm3-, Bi3-
Сукцинат аммония [С2Н.,(СОО)2]зСе2- Бурые розетки, сферо- La3+, Pr3-, Nd3-,
•nH2O ЛИТЫ Sm3-
С1 AgNO3, NH4OH [Ag(NH3)2]Cl Мелкие треугольники, 0,05 1:20 000 Br , J , CN
шестиугольники, ку- SCN
бы
(C2HsHg)3PO4 C2H5HgCl Пластинки, прямо- 0,4 1 :2 500 Br , J , SCN
угольники, крестики CrO2-
C6H5CH2HgOH C6H5CH2HgCl Дендриты 0,15 1:7000 Br-, J-, SCN'. CN-
| С;Н3Н<тОН CJHHoC! ! Иглы, розетки, прямо 0.1 i : lillHhi I’.r . Г (Л-
угольники SCN
K2SO4, Pt(SO4)2 K2[PtClc] Желтые октаэдры 0,7 1 :1 400 Br', J-, SCN"
о Сульфат берберина CnpH.oOsN • HCI • Желтые розетки из игл 0,01 1 : 100001 ) Br , J , SCN',
•* • 2H2O no;
T1NO3 T1C1 Мелкие кубы, крестики 0.1 1 : 10000 J-, s2op
T1NO3, Pt(SO4)2 Tl2[PtCl6] Желтые мелкие окта- 0,004 1:250 001 Br', J-, SCN"
эдры
СЮ; Нитрон C20H16N4 • НСЮз Розетки из параллело- 3 1: 1 000 no;, no;,
граммов cio;, J'
Сульфат берберина C20H19O.5N ’ HCIO3 Пучки прямых игл 1 1: 1 000 СГ, Br-, J".
NO3-
сю; Метиленовая синяя Перхлорат метиле- Розетки из синих тон- 0,02 1:50 000 Mno;
новой синей ких игл
Р-Н афтохинолин C,3H9N • НСЮ4 Пучки игл
Нитрон C20HigN4-HC1O4 Розетки из игл 0,15 1:7 000 cio;, no;,
no;, J'
CN' AgNO3, HNO3 AgCN Палочки, иглы, мелкие 0,06 1:50 000 Cl', Br-, J-
звезды
Ацетат меди, бензидин, Синие иглы 0,02 1:50 000 J-, SC№,
СНзСООН Cr2°7“
SCN C6HsHgOH C6HsHgSCN Квадраты, пирамиды, 0,06 1:50 000 cr, Br', J~,
октаэдры CN
CuSO4, пиридин [Cu(C5HsN)2](SCN)2 Желтовато-зеленые ро- 0,3 1:6500 Br
зетки из палочек,
Х-образные изогну-
тые кристаллы
Нитрон C2oH16N4 • HSCN Иглы, пластинки 1 1:1 000 no;, no;, j~.
Cio;
Окисление до CN“, осаж- AgCN Иглы, палочки 0,1 1:10000 CN“
дение раствором
AgNO3
Сульфат берберина C20H19O5N • HSCN Иглы, дендриты 0,6 1:5000 cr, Br', J-,
ьо no;
МИКРОХИМИЧЕСКИЙ® ХНАЛИЗ
Продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
SCN- Сульфат ферро а,а’-дипиридила [Fe(C10H8N2)3](SCN)2 Оранжево-красные шестиугольники, приз- 0,2 1:5000 J-, МпО“, CrOp, NO~
Сб2+ Диметилглиоксим (спиртовый раствор) и KJ Желтые и красные ромбы 0,2 1:5000 Ni2+
2,4-Динитро-а нафтол Оранжевые кристаллы 0,5 1:2000 К+, Rb+, Cs+, T1 +
Cd(NO3)2, (NH4)2[Hg(SCN)4J (Cd, Co)[Hg(SCN)4] Голубые призмы 0,02 I : 50 000 Cu2+, Fe3 +
KNO2, СНзСООН K3[Co(NO2)6] Желтые небольшие кубы и друзы 0,1 1 :10000 Rh3 +
KNO2, CsNO3, СНзСООН Cs3[Co (NO2)gJ Желтые мелкие кубы 0,05 1:20 000 Rh3 +
KNO2, TINO3, СНзСООН Tl3[Co(NO2)6] То же 0,05 1:20000 Rh3+
K2[Hg(SeCN)4] Co[Hg(SeCN)4] Синевато-зеленые кристаллы 0,1 1:10000 Zn2+, Mn2+, Fe2+, Ni2-, Cd2-
(NH4)2[Hg(SCN)4] Co[Hg(SCN)4] Синие розетки, призмы, треугольники Желтые крупные звезды, октаэдры, кубы 0,2 1 :5000 Zn2', Cu2-, Cd2-, Fe2-
NaNO2, уротропин, СНзСООН 0,008 1:125 000 Mg2 + , Mn2-Ni2-, Fe2-
Na2HPO4, NH4C1, nh4oh NH4CoPO4 • 6H2O Трапеции, призмы, дендриты 0,4 1:2500
Пикриновая кислота, NHiOH Пучки тонких игл 0,3 1 :6500 Zn2 -, Ni2-, Cu2-, Ag-
Пиридин, K2Cr2O7 [Co(C5H5N)2]Cr2O7 Желтые мелкие прямоугольники 0,1 1: 10 000 Zn2-, Ni2 + , Cu2-
Пиридин, NH4SCN Синие призмы, розетки из палочек 0,01 1:100000 Zn2+, Cu2+, Cd2-, Fe3+, Ti4 + Cu2+, Fe3+
ZnSO4, . (NH4)z[Hg(SCN)41 (Zn, Co)[Hg(SCN)4] Голубые дендриты 0,02 1:50 000
co2- 1 Аиста г кальция СаСО.,
Ацетат свинца РЬСОз
Cr3+ KHSO4 KCr(SO4)2- 12Н2О
Cr2op Хинолин, H2C2O4 AgNO3 C9H7N • H[Cr(C2O4)2] Ag2Cr2O7
Ацетат свинца, КОН
Бензидин
(C2HsHg)3PO4 (C2H5Hg)2CrO4
C6HsHgOH (C6H5Hg)2CrO4
HgSO4, HNO3, пиридин Na2SO4, AgNOs [Hg(CsH5N)4]Cr2O7 Ag2SO4(CrO4)
Сульфат ферро-сс,а'-ди-пиридила ZnSO4, пиридин [Fe (C10HeN2) 3] (CrO4) [Zn (C5H5N)4]Cr2O7
Cs+ AuCl3, AgCl, НС1 Cs2Ag[AuCl6]
AgJ, KJ A11CI3 Cs[Ag2J3] Cs[AuCl4]
Ромбы, друзы SO2 , NO;,
с2о2-
Раздвоенные палочки. 0,3 1:6500 SO2-, J-, S2"
розетки Светло-фиолетовые
октаэдры Призмы Са2+, Sr2+, Ba2-
Оранжево-красные 0,025 1:80 000 so2-, VO"
ромбы, прямоугольники, шестиугольни-
ки, иглы
Желтые или оранже- 0,02 1:50 000 SO2-
во-красные друзы и крестики
Сине-фиолетовые иглы, 0,01 1:100000 Окислители,
пучки игл so2-, s2o|-
Желтые шестиугольни- 0,4 1:2500 cr, ВГ, J-
ки SCN
Желтые кристаллы не- 0,3 1:6500 СГ, вг, j-
правильной формы Желтые розетки, ден- 0,08 1: 12500 J-, SCN"
дриты Желтые или оранже- 0,0035 1:570 000 Ba2+, Pb2+, СГ
вые длинные шести-
угольники и ромбы J
Красные ромбы, ше- 0,08 1: 12500 MnO“, VO",
стиугольники ReO“, J-
Желтые прямоуголь- 0,03 1: 100000 Br~, SCN-
ные призмы, кубы Почти черные крести- 0,1 1:10 000 Rb+
ки, четырех- и шестилучевые звезды
Бледно-желтые иглы 0,15 1:7000 Rb+
Желтые призмы Rb-, T1+
МИКРОХИМИЧЕСКИЙ Ж ДИАЛИЗ
Продолжение
Ион Реактив । 1 Состав осадка Характеристика осадка Открываемый минимум, мкг Предела пая концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
Cs+ AuCl3, PdCl2 Bi2 (SO4) 3 Na2Pb[Cu(NO2)6] Cs2Au[PdC17] 3Cs2SO4- Bi2(SO4)3 Cs2Pb[Cu (NO2)s] Красные или краснооранжевые квадраты, прямоугольники Шестиугольники Черные мелкие кубы 0,03 0,03 0,003 1 : 100 000 1 : 100 000 1:330 000 Rb+ NH;, Li’, Rb+, Na* NH+, К . Rb+,
Г екса нитродифенил -амин K[BiJJ Кз[Ре(СМ)б], РЬ(СН3СОО)2 K2[PtCl6] KReO4. HJ NaClO4 Na2HPO4, Ni(NO3)2 Na3[Co(NO2)6] [(O2N)3C6H2]2NCs Cs[BiJ4] или Cs3[Bi2Js] CsPb2[Fe(CN)6] • (CH3COO)2 Cs2[PtCl6] Cs2[ReJ6] CsClO4 CsNiPO4 Cs3[Co(NO2)6] Оранжевые прямоугольники, ромбы, квадраты, часто с фигурами травления Оранжево-красные шестиугольники Желто-оранжевые пластинки Желтые мелкие октаэдры Почти черные мелкие звезды Ромбы, шестиугольни-ки, призмы Тетраэдры Желтые мелкие кубы 0,04 0,06 0,6 0,1 0,003 0,1 1 :25 000 1 :50 000 1:5000 1: 10000 1:330 000 1: 10000 ТВ K+, Rbr, Т1+ Rb+ г. soj- Rb+, T1 + Rb+ K+, Rb + Rb + NH+, K+, Rb’, 5 x
Na3[Bi(S2O3)3] Нафтоловый желтый Pr(NO3)3, NaNO2 SbCl3, NaJ Csa[Bi (520з)з] C10H4 (NO2)2 (OCs) (SO3H) Cs2Na[Pr(NO2)6] Cs[SbJ4] или Cs3[Sb2J9] Желто-зеленые иглы Желтые иглы, пучки игл Бледно-зеленые октаэдры Оранжево-красные шестиугольники 0,4 0,04 0,03 1:2500 1:25 000 1: 100000 Tl * K+, Rb* K!, Rb*, Ca2~, Sr2+, Ba2+ Rb + T5 О X X 3 X X m X X X
,,...айййими1
Си' 1 Анилин, NH4SCN. HCI Ацетат кадмия, анилин, NH4SCN, HCI Ацетат кадмия, (NH4)2[Hg(SCN)4] Ацетат свинца, KNO2, TINO3, СН3СООН Ацетат свинца, KNO2, СНзСООН Ацетат свинца, KNO2, CsCl, СНзСООН Бензидин, KJ K4[Fe(CN)6], NH4OH (NH4)2[Hg(SCN)4] Никотин, NH4SCN 8-Оксихинолин, KJ, HNO3 Пикриновая кислота, NH4OH Пиридин, К2СГ2О7 Пиридин, КМпО4 Уротропин, NH4SCN [Cu(C6HSi\H2) • 5H2O](SCN)2 (Cd, Cu)[Hg(SCN)4] Tl2Pb[Cu(NO2)6] K2Pb[Cu(NO2)6] Cs2Pb[Cu(NO2)6] Cu(NH4)2[Fe(CN)6] Cu[Hg(SCN)4] (C6H2N3O7)2[Cu(NH3)4) [Cu(CsH5N)4]Cr2O7 [Cu(C6H12N4)2](SCN)2- •H2O 1 Зеленовато-желтые Х-образные дендриты Желтые параллело- граммы, трапеции Фиолетовые призмы Черные мелкие кубы Черные кубы Черные мелкие кубы Синие и фиолетовые иглы и дендриты Светло-желтые, красноватые дендриты и пластинки непра- вильной формы, реже квадраты, ромбы Желто-зеленые розетки, иглы, расширенные посредине Зеленые шестиугольники и ромбы Желто-зеленые розетки из тонких игл Зеленовато-желтые кристаллы Желтые мелкие прямоугольники Светло-фиолетовые шестиугольники, звезды Зеленовато-желтые прямоугольники и Х-образные кристаллы 0,05 0,01 0,005 0,01 0,03 0,01 0,02 0,1 0,1 0,4 0,06 0,0012— 0,05 0,1 0,1 0,2 1 :20 000 1: 100 000 1:200 000 1:100 000 1:100 000 1:100 000 1:50 000 1:10000 1:10000 1:2 500 1:50 000 1: 10 000 1: 10 000 1:5000 Cd2*- pe3 + Ni2*-, Co2+ Ni2+, Co2 + Ni2+, Co2 + Окислители Zn2*, Co2*, Fe2+, Cd2 + , Pb2+ Mn2t, Fe2+, Zn2*, Co2+, Ni2+, Cd2+ Cd2+, Bi3+, Sb3+ Co2+, Ni2 n Zn2*-, Ag*-, Au3 + Cd2+, Zn2*, Co2+, Ni2+, Hg2* Ag* Zn2+, Co2*-,Cd2+ АНАЛИЗ
to 4^
продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
Cu2+ Антраниловая кислота Хинолин, KJ, HCI ZnSO4, (NH4)2[Hg(SCN)4] [C6H4(NH2)COO]2Cu (Zn, Cu)[HgSCN)4] Светло-зеленые шестиугольники, призмы, розетки Темно-бурые ромбы и восьмиугольники Фиолетовые дендриты 0,015 0,2 0,015 1 : 130 000 1 :5000 1 :130 000 Zn2+. UO3+, Ag+, Pd2+ Cd2+, Pb2 \ Bi3+, Sb3+, AsO3- Fe3+
Cu3+ Антраниловая кислота Светло-зеленые призмы, шестиугольники Почти бесцветные звезды Зеленые длинные призмы 0,015 1: 130000 Hg2 +
Изатин, NH4OH Янтарная кислота, NH4OH (CeH 4N О2) 2С U2 Сукцинат меди и аммония .... Ag+ La3+, Ce34-, Pr3+, Nd34-, Sm3 +
F” HCI, SiO2, ВаС12 HCI, SiO2, NaCI Ba[SiF6] Na2[SiF6] Палочки, линзы Шестиугольники, ро- зетки 0,15 0,4 1:7000 1 :2500 SO?-
Fe3+ K4[Fe(CN)6] NH4F ZnSO4, (NH4)2[Hg(SCN)4] Fe4[Fe(CN)6]3 (NH4)3[FeF6] Синий аморфный осадок Октаэдры Фиолетовые дендриты 0,07 0,2 0,02 1 :14 000 1:5000 1:50 000 Cu3+, UO3+, Co2+, Ni2 + Al3+, In3 + Cu2+, Co2 +
Fe2+ K3[Co(CN)6] Fe3[Co(CN)6]2 • 12H2O Розовые кристаллы .... Zn2+, Ni2 +, Mn2[ Bi3 + s
о-Нитрофениларсонат натрия, СНзСООН (O2NCeH4AsO3H)2Fe Кристаллы неправильной формы 0,1 1: 10000 Mn2+, Pb2+ X X T
Пикролоновая кислота (Cl0H7N4O5)2Fe Коричневые иглы 0,02 1 :50 000 Ca2+, Pb2+ 0
Пиридин, NH4SCN [Fe(CsHsN)2](SCN)2 Красные призмы 0,05 1:20 000 Zn2+, Cu2+, Co2+, Cd2 + X S
Хинолин, NH4SCN [Fe(C9H7N)2](SCN)2 Красные кристаллы 0,3 1:6500 Zn2*-, Cu2+, Co2-*-, Zr4+, Ti4+ X m X X
’6Г
|Fe(CN)6J4- Z11SO4, (NH4)2iHg(SCN)4] Бензидин, СНзСООН (Zn,Fej[Hg(SCN)4] Желтые или зеленовато-желтые дендриты Многолучевые звезды, 0,1 1 : 10000 Си2 », Со2 • , Fe3 т >
[Fe (CN)6]3“, X Sa
иглы, ромбы SO3', CrO2' X w
(C2H5Hg)3PO4 C6HsHgOH Сульфат берберина Почти бесцветные иглы. шестиугольники Овальные кристаллы Желтые розетки, палочки, сферолиты 1,5 0,1 0,5 1 :2000 1:10000 1 :2000 [Fe (CN)6]3-, СГ, Br-, J~ СГ, Br~, J-, CN~ cr, Br“, J-, NO3-
Сульфат ферра-а,а'-дипиридила Красные пластинки 0,2 1:5 000 J-, MnO“, CrO3-, VO-
IFe (CN)613- Хинолин, НС1 Уротропин, LiCl Уротропин, MgCl2 AgNO3, NH4OH Li4[Fe(CN)6]-2C6H12N4-• 2,5Н2О Ag3[Fe(CN)6] • 5NH3 Бледно-желтые прямоугольники, квадраты Розетки, сферолиты Бледно-желтые округленные кубы, октаэдры, пластинки, двойники Оранжево-красные призмы, октаэдры, палочки 0,25 0,07 0,2 0,7 1:4000 1: 14000 1:5000 1: 1 400 ReCl~ [Fe(CN)6]3- [Fe (CN)6]3~ СГ, Br", J’ CN-
Бензидин, СН3СООН Темно-фиолетовые звезды, палочки, шестиугольники 0,8 1:1 200 [Fe (CN)6]’-, so3-, s2o3-, CrO3"
(C2H5Hg)3PO4 Cu(CH3COO)2, NH4OH Сульфат ферро-а.а'-ди-пиридила [Cu(NH3)4]3[Fe(CN)6]2 Светло-коричневые, оранжевые иглы, Х-образные кристаллы Игольчатые изогнутые кристаллы Красные пластинки неправильной формы 0,3 0,008 0,03 1:6500 1: 125 000 1: 100 000 [Fe (CN)6]4~, СГ, Br-, J" Pt2+ J“, MnO“, CrO3-, vor
К5 g Продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/ г Ионы, мешающие реакции и образующие аналогичные осадки
|Fe(CN)6|3-OeIV Уротропин, LiCl NH4F, NaCl (NH4)2MoO4, RbCl Li3[Fe(CN)6] • • 2CeH|2N4 • 4Н2О Na2[GeF6] (NH4)8[Ge(Mo2O7)6]- • 28Н2О Желтые октаэдры и дендриты Шестиугольники Бледно-желтые мелкие октаэдры 0,05 0,1 0,02 1:20 000 1: 10000 1:50 000 [Fe (CN)6]4- SiO2" РО3", AsO3~, S1°r
НёГ Hg2- Антраниловая кислота FeCl3, (NH4)2[Zn(SCN)4] K2CrO4 (NH4)2[Co(SCN)4] Пиридин, K2Cr2O7 Сульфанилат натрия Бруцин, KBr, H2SO4 FeCl3, (NH4)2[Zn(SCN)4] Г ексанитродифенил-амин KJ (NH4)2[Co(SCN)4] а-Нафтиламин Пикриновая кислота, NH4OH [C6H4(NH2)COO]2Hgs Hg2CrO4 [СбНДИНг) SOg]2Hg2 [C6H2N3O6) 2N]2Hg HgJ2 Co[Hg(SCN)4] Пучки тонких игл Кирпично-красные иглы Красные или оранжевые мелкие кристаллы Синие кристаллы Желтые длинные иглы Мелкие Х-образные прямоугольники Розетки, ромбы, параллелограммы Кирпично-красные иглы Темно-красные октаэдры или бипирамиды, розетки Желтые и красные кристаллы Синие призмы, розетки из игл, треугольники Розетки Желтые изогнутые длинные иглы 0,06 0,025 0,5 0,6 0,08 0,7 0,4 0,012 0,5—1 0,08 0,04— 0,01 0,08 0,15 1:50 000 1 :80 000 1:2 000 1:5 000 1 : 12500 1:1 400 1:2500 1:80 000 1 : 12 500 1: 12 500 1:7000 Cu2+ Ag+, Cd2- Ba2 + , Pb2+, Ag+ Ag + Cu2 + , Co2 + ,Ni2+, Cd2+, Zn2 + Ag+, Hg2+ Cd2 + , Bi3-, Sb3 + Cd2-, Ag- К+, Rb+, Cs+ Ag- Pb2-, Bl3 + , Pd2- Fe3- Bi3- Cu2 + , Cd2+, Ag - Au3 +
1
Пиридин. К2Сг2О7 [Hg(C3H3N)4]Cr2O7 Желтые Х-образные 0,08 1 ; 12 500 • 7 Си- , Zn- ,
кристаллы Cd2', Со"-.
SnCl2 Hg2Cl2 Крестики, палочки 0,05 1 : 20 000 Ni- r Au3 г
Сульфанилат натрия [C6H4(NH2)SO3]2Hg Линзы, иглы 0,5 1:2 000 Ag+, Hg21
Сульфат ферро-сс,а'-ди- Красные палочки, чер- 0,02 1:50 000 Sn4 —, Sb3-, Bi3-
пиридила, НС1 ные кубы, призмы
Хлорид акридина, (CI3H9N)2- Желтые иглы 0,5 1:2000 Zn2-, Co2-,
NH4SCN • H2[Hg(SCN)4] UO24, Bi3+
[HgJ4]2 о-Фенилендиамин, [Cu(C6H8N2)2] • [HgJ4] Красные прямоуголь-
CuSO4, H2SO4 ники, ромбы, крести-
ln3+ CsCl Cs3[lnCl6] Мелкие октаэдры 0,02 1:50 000 Sn4-, Sb3-, Bi3-,
NH4F Au3-
(NH4)3[lnF6] Октаэдры Al3-, Fe3-
RbCl Rb3[lnCl6] » 0,25 1:4 000 Sn4-, Sb3+, Bi3-,
Au3-
lrCl6] CsCl Cs2[lrCl6] Темно-красные мелкие Pt4-, Ru4+, Rh3+,
KC1 октаэдры Sn4-
K2[IrCl6] Темно-красные окта- Pt4+, Ru4+, Rh3-,
Метиламин, хлоргид- эдры Sn4-
(CH3NH2)2 • H2[lrCl6] Красные октаэдры и Ru4-
рат шестиугольники
RbCl Rb2[lrCl6] Темно-красные окта- 0,1 1: 10 000 Pt4+, Ru4-, Rh3-,
Аминобензол, K2Cr2O7, эдры Sn4-
J 6C6H5NH2 • 3H2SO4 • Буро-красиые крн- 0,25 1:4 000
H2SO4 • HJ-J4 сталлы
Ацетат меди, бензидин. Пучки синих тонких 0,3 1:6 500 Br“, CN', SCN"
СНзСООН игл
HgCl2 HgJ2 Желтые и красные 0,2 1:5000
K2SO4, Pt(SO4)2 кристаллы
K2[PtJ6] Черные мелкие окта- 0,2 1:5 000 СГ, Br”, SCN"
PdCl2, NH4OH [Pd(NH3)2J2] эдры Бурые прямоугольные 0,1 1: 10000 СГ, Br”, SCN"
Jo3- AgNO3 дендриты
AgJO3 Иглы, мелкие звезды 0,03 1: 100 000 СГ, Br”, J”
МИКРОХИМИЧЕСКИЙ Я АНАЛИЗ
продолжение
•252 | 253
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
JO3- к+ Ацетат бария Ацетат стронция TINO3 Bi2(SO4)3 Г ексанитродифенил-амин H2[PtCl6] Na3[Bi(S2O3)3] NaClO4 Na3[Co(NO2)6] Na3[Co(NO2)6], AgNO3 Na3[Co(NO2)6], Pb(NO3)2 NaReO4, HJ Na[PbJ3] Na2Pb[Cu(NO2) 6] Ba(JO3)2-H2O Sr(JO3)2 - 6Н2О тио3 3K2SO4 • Bi2(SO4)3 [(O2N)3C6H2]2NK K2[PtCI6] Ks[Bi(S2O3)3] KC1O4 K2Na[Co(NO2)6] K2Ag[Co(NO2)6] KPb[Co(NO2)6] K2[ReJ6] K[PbJ3] • 2H2O K2Pb[Cu(NO2)6] Ромбы, изогнутые иглы, дендриты Иглы с расширением посередине, розетки Иглы Шестиугольники и мелкие звезды Желтые или оранжевые ромбы и квадраты Желтые октаэдры Желто-зеленые иглы Ромбы, шестиугольники, призмы Желтые мелкие кубы и друзы Желтые мелкие кубы Темно-желтые мелкие кубы Темно-бурые кристаллы Пучки длинных игл Черные блестящие кубы и прямоугольники 0,5 0,3 0,2 0,2 0,15 0,1—0,01 0,8 0,5 0,12 0,03 0,15 0,15 1:2000 1:6500 1:5000 1:5000 1:7000 1:1 200 1:2000 1:8000 1 :100000 1:7 000 1:7000 1 SO3-, СО3-, с2ог SO3-, СО|-, с2ог СГ, Br~, J- NH + , Na+, Li+, Rb + , Cs+ Rb+, Cs+, T1+ NH+,Rb+, Cs+, T1 + Rb+, Cs+ Rb+, Cs+ NH+, Rb+, Cs+, T1 + NH+, Rb + , Cs+, T1+ NH+, Rb*-, Cs+, T1 + Rb+, Cs+ NH+, Rb+, Cs+ NH+, Rb+, Cs+, T1+
La3+ Li+ Mg2+ Нафтоловый желтый 5-Нитробарбитуровая кислота Пикриновая кислота Тартрат натрия (однозамещенный) Н2С2О4 K4[Fe(CN)6] Сукцинат аммония Ацетаты уранила и цинка K3[Fe(CN)6], уротропин NH4F NaHCO3 Na2HPO4 n-Арсанилат натрия K4[Co(CN)sS2O3], уро-тропин К2СгО4, уротропин K4[Fe(CN)e], уротропин K3[Fe(CN)6], уротропин C10H4(NO2).(OK)(SO3H) c4h2n3o5k C6H2(NO2) 3ok c4h4o6hk La2(C2O4)3- 10H2O LaK[Fe(CN)6] [C2H4 (COO)2], La2-«H2O LIZn (UO2)3 (CH3COO),- 6H2O Li3[Fe(CN)6] • • 2C3Hi2N4 • 4H2O LiF Li2CO3 Li3PO4 (H2NC6H4AsO3H)2Mg 2MgCrO4 • 3C6Hi2N4 • • 15H2O MgK[Fe(CN)6]- 2C6Hi2N4 • 12H2O Желтые иглы, пучки игл Ромбы и параллелограммы Желтые длинные иглы Крупные призмы и пластинки Шестиугольники, параллелограммы Ромбы Параллелограммы, иглы, розетки Желтые тетраэдры Желтые блестящие октаэдры Розетки из прямоугольников, кубы Шарики, покрытые мелкими иглами, и розетки из игл Сферолиты Квадратные призмы, прямоугольники Желтые иглы Желтоватые ромбы, шестиугольники Бледно-желтые октаэдры, кресто- и эллипсообразные кристаллы Бледно-желтые прямоугольники 0,07 0,04 0,8 0,25 0,15 0,06 0,25 0,25 0,4 0,02 0,008 0,5 _ 0,002 0,0005 1 :14 000 1 :25 000 1 : 1200 1 : 4 0Э0 1:7 000 1:50000 1 :4000 1:4000 1:2500 1:50 000 1:125 000 1:2000 1:500 000 :2000000 Rb1 , Cs’* , NH', Ca2-, Sr2-, Ba2 + Rb+, Cs+, NH+, Mg24-, Ca2 + NH+, Rb+, Cs+, Tl1 NH+, Rb+, Cs+, Ca2+, Sr2+, Ba2+ Th4+, Zr4+, Sc3+, Ce3 + Fe3+, Cu2+, Ba2 + Ce3+, Pr3+, Nd3+, Sm3T Na+ Mg2+, Ca2+ Ca2+, Sr2+, Ba2+, Fe3\ Al3 + Mg2+, Ca2J-,Sr2+, Ba2+, Pb2+ Mg2+, Ca2+ Li+, Ca2+, Ba2+ Li+, Ca2+, Ba2+ Li+
МИКРОХИМИЧЕСКИЙ» ^нДЛиз
{S’ Продолжение
Иои Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
Mg2+ K[Sb(OH)6] Mg[Sb(OH)6]2 Шестиугольные приз- 0,8 1: 1200 Na+, Са2+, Ва2 +
Na2HPO4, CsCl Na2HPO4. NH4C1, nh4oh CsMgPO4 • 6Н2О NH4MgPO4 • 6Н2О МЫ Мелкие тетраэдры Трапеции, прямоугольные призмы, звезды, 0,012 1:80 000 Мп2- Li + , Мп2-, Со2-, Ni2+, Zn2*
Mn2+ 8-Оксихинолин, NH4OH H2C2O4 Mg(C9H6NO)2 • 2Н2О МпС2О4 • ЗН2О дендриты Линзы Звезды, шестиугольники, розетки 0,04 1 1 :25 000 1: 1 000 Са2+, Sr2+, Ва2+ Zn2>, Со2’, Ni2+, Са2-, Sr2+, Ва2 +
K2[Hg(SeCN)4] Mn[Hg(SeCN)4] Иглы ... Fe2+, Zn2+, Со2+, Ni2+, Cd2+
МпОГ 4 Na2HPO4, NH4C1 о-Нитрофениларсонат натрия, СНзСООН NH4MnPO4 - 6Н2О (ОгМСбЬЦАзОзН^Мп Трапеции, призмы, дендриты Кубы, призмы 0,3—0,02 0,25 I : 4 000 Mg2*, Fe2 *, Co21, Ni2-Fe2+, Pb2+
Метиленовая синяя Синие, сине-фиолето- 0,15 1:7 000 cio~
вые пучки игл Pb21, Cl
Na2SO4, AgNO3 Почти черные, фиолетово-бурые, фиолето- 0,01 1: 100 000
вые или розовые
кристаллы
RbCl, NaClO4 Rb(ClO4, МпО4) Розово-фиолетовые 0,12 1:8000 CrO2" 4
или розовые кри-
сталлы
Сульфат ферро- [Fe(Cl0H8N2)3](MnO4)2 Темно-фиолетовые па- 0,08 1: 12500 CrO2-, ReO'
а, а'-дипиридила лочки, мелкие звезды VO3-
Тетрафенилфосфоний, хлорид [(С6Н5)4Р]С1 [(C6Hs)4P]MnO4 Красно-фиолетовые 0,2 1:5000 Zn2 + , Cd2+
тонкие иглы
MoO*-4 Дибромоксихинолин Темно-зеленые мелкие 0,02 1:50000 ln3+, WO2~
МИКРОХИМИЧЕСКИ
Na-* Nbv Nd3’ nh; Ni2-* to СЛ Cn Na>HPO4, NH4C1, HNO3 T1NO3 Ацетаты уранила и кобальта Ацетаты уранила и магния Ацетаты уранила и никеля Ацетаты уранила и цинка Ацетат уранила Bi2(SO4)3 K[Sb(OH)6] (NH4)2[SiF6] Ацетат натрия, NaOH H2[PtCl6] Na3[Co(NO2)6] Na2HPO4, MgCl2, NaOH Na2Pb[Cu(NO2)6] Пикриновая кислота Ацетат свинца, KNO2, СНзСООН Диметилглиоксим (NH4)3PO4- I2MoO3 Т12МоО4 NaCo(UO2)3(CH3COO)9- 6Н2О N aMg (UO2) 3 (СН3СОО) <>• •6Н2О NaNi(UO2)3(CH3COO)9- •6Н2О NaZn(UO2)3(CH3COO)9-- 6Н2О NaUO2(CH3COO)3 3Na2SO4 • Bi2(SO4)3 Na[Sb(OH)6] Na2[SiF6] Na8Nb6O19- 16H2O Такие же peat (NH4)2[PtCl6] (NH4)3[Co(NO2)6] NH4MgPO4 • 6H2O (NH4)2Pb[Cu(NO2)6] C6H2(NO2)3ONH4 K2Pb[Ni(NO2)6] Ni (C4H,N2O2) 2 Желтые мелкие кристаллы Шестиугольники, звезды Желтые тетраэдры и октаэдры Зеленые тетраэдры и октаэдры Желтые тетраэдры и октаэдры Желтые тетраэдры и октаэдры Палочки, розетки из палочек Призмы, линзы Шестиугольники, шестилучевые мелкие розетки Иглы, палочки, шестиугольники щии, как и для празеоди Желтые октаэдры Желтые мелкие кубы, друзы Трапеции, прямоугольные призмы, звезды, дендриты Черные кубы и прямоугольники Желтые длинные иглы Желтые или буроватые мелкие кубы Красные иглы 0,01 0,03 0,6 0,4 0,4 0,01 0,8 0,04 0,3 0,1 0,6 ма 0,1 0,1 0,15 0,3 0,008 0,002 1 1:1000001 W О' „ I 1:100 000 WO2-, Аи3 + , | 1:5000 Li + 1:2500 Li+ 1:2500 Li+ 1: 100000 Li+ 1:1 200 Li+ 1:25 000 NH + , K+, Rb+, Cs + , Li + 1:6500 Li+, Mg2+, Ba2+ 1:10000 Ba2+ 1:5000 TaV 1:10 000 K+, Rb+, Cs+, T1 + .... K+, Rb+, Cs+ 1:10000 Rb+, Cs+ 1:7000 K+, Rb+, Cs+, T1 + 1:6500 K+, Rb+, Cs+, T1+ 1:125 000 Cu2+ 1:500 000 Pd2+
Продолжение
Ср Иои Реактив Состав осадка Характеристика осадкй Откры-ва емый минимум, мкг Предельная концентрация, г/г Иоиы, мешающие реакции и образующие аналогичные осадки
Ni2+ NO- NO~ ,OsO.l2- KMnO4, NH4OH Na2HPO4, NH4C1, nh4oh Никотин, NH4SCN Нитрозогуанидин Пикриновая кислота, NH4OH Пиридин, К2СГ2О7 Sr(NO3)2, KNO2, СНзСООН ZnSO4, (NH4)2[Hg(SCN)4] Ацетаты калия, свинца, меди, СНзСООН Нитрон л-Аминофенилмеркур-аиетат Нитрон Сульфат берберина CsCl, НС1 NH4NiPO4 • 6Н2О Ni(CH3N4O)2 [Ni(C5H5N)2]Cr2O7 K2Sr[Ni(NO2)6] (Zn, Ni)[Hg(SCN)4] K2Pb[Cu (NO2)6] C2oH16N4-HN02 C6H4(NH2)HgNO3 C20H16N4 • HNO3 CsoHisOsN • HNO3 Темно-фиолетовые кубы Трапеции, призмы Голубые друзы Кирпично-красные иглы Желтые мелкие шестиугольники, прямоугольники, параллелограммы Желтые мелкие прямоугольники Квадраты, кубы Зеленые кристаллы Черные кубы Иглы, розетки Розетки, призмы, Х-об-разные кристаллы Пучки тонких игл Желтые розетки из игл Зеленовато-желтые октаэдры 0,2 0,01 0,4 0,02 0,1 0,4 0,01 0,1 0,75 0,4 0,3 0,012— 0,025 0,005 0,1 1:5000 1 :100000 1:2500 1 :50 000 1: 10000 1 :2 500 I : 100000 1: 10 000 I : 1300 1:2500 1:6 500 1 :200 000 1 : 10Т)00 “и о z z ’ non о 3 2 ^+2’5-'z- о-1 • -+ + -+ с»-+ -+сХ+«/ + •+2? 'св । го" 1 Q : 2 Р +? 3 ' О । । w । • 4 + + О. + Q. ю л - ы । ' 1 м * - ыз * -f- + > > ~ -п I > +р + г ГО £ 4- 1 1 • 4. 4. ИИМЭПhHWHXOdMMW
17 Зак
К< HI, С,НзОН K2OsO4 • 2Н2О Красновато-фиолето- 0,1 1: 10 000
КОН, NH.,OH, С2Н5ОН вые октаэдры Ж
[Os(NH3)4]C12 Светло желтые палоч- 0,05 1 :20 000 Pt2’ 5a
РЬ2+ Ацетат меди. KNO2, K2Pb[Cu(NO2)6] ки и дендриты Черные кубы и пря- 0,01— Ca2r, Sr2*-, Ва2* X w
СНзСООН Гексанитродифенил- [ (СбНгЫзОб) sNfePb моугольники Буро-красные октаэд- 0,03 0,2—0,5 K+,Rb + ,Cs+,Tl+
амин ры, звездочки
Н2С2О4 PbC2O4 Иглы, шестиугольники, 0,2 1:5000 Ca2 r, Sr2+, Ва2+, Zn2 + , Мп2 +
НС1 дендриты
РЬС12 Призмы, шестиуголь- 0,2 1:5 000 Ag 1, Hg2+, Tl+
H2SO4 ники, дендриты
PbSO4 Дендриты, Х-образиые 0.04 1 :25 000 Са2+, Sr2+, Ва2 +
К2СгО4 кристаллы, ромбы, шестиугольники
PbCrO4 Желтые мелкие ромбы 0,15 1 : 7 000 Ва2 + , Ag+
KJ (конц. р-р) и призмы
K[PbJ3] Длинные тонкие иглы.
KJ пучки игл
PbJ2 Желтые шестиугольники, треугольники Иглы 0,07 1 : 14 000 Hg2*-, Ag+
KJ, CsCl (NH4)2[Hg(SCN)4]
CsfPbJJ 0,01 1 : 100 000 Bi3*-, Sb3’-, Au3+
Pb[Hg(SCN)4] Ромбы, шестиуголыш- Zn2-, Co2*-,
NaHCO3 ки, реже иглы Cu2 + , Cd2*-
РЬСОз Раздвоенные по краям 0,06 1 :50 000 Ca2 r, Sr2*-, Ba2*-
палочки
NaN3 Pb(N3)2 Пластинки, палочки 0,5 1 :2000 Ag+
о-Нитрофениларсонат (O2NC6H4AsO3H)2Pb Пучки игл 0,25 1:4000 Mn2+, Fe2 +
натрия, СНзСООН
Пикролоновая кислота (СщНЛШЬРЬ Пучки игл 0,008 1:125 000 Ca2*-
Pd2 * Диметилглиоксим Pd (C4H7N2O2) 2 Желтые иглы 0,005 1 :200 000 Ni2*-
KU, С2Н5ОН K2[PdCl4] Бледно-желтые длин- Pt4*-, Ru4+, Pb2+
ные иглы и пластин-
КС1, TINO3 Tl2[PdCl4] КИ Бурые палочки, иглы 0,2 1 :5 000 Pt4*-, Ru4+, Au3 +
KJ, NH4OH [Pd(NH3)2J2] Бурые, желтые прямо- 0,1 1: 10000 Pb2+, Hg2*-, Bi3 +
угольные дендриты
Продолженш
О1
о
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Пре де ль-ti а я концентрация, г. г Ионы, мешающие реакции и образующие аналогичные осадки
Pd2 + NHiSCN, T1NO3 Tl2[Pd(SCN)4] Буро-желтые прямоугольники, крестики, розетки 0,07 1 : 14 000 Ац3 + , Pb2’, Pt• т, МоО2"
NaBr, CsCl Cs2[PdBr4] Буро-красные иглы и призмы .... Au3», Bi3’, sb3+, Pb2 +
Нитрозогуанидин Pd(CH3N4O)2 Желтые иглы 0,1 1: 10 000 Ni2-, Ag4
RbCl Rb2[PdCl4] Желтые иглы, пластинки, призмы Темно-красные иглы .... Pt”-. RU4+, Pb2 +
Рубеаповодородная кислота .... Ni-’т, Co2+, Cu2 +
РОД Hg2(NO3)2 Hg3PO4 Пучки игл, розетки 0,35 1 :3 000 AsO3", BrO", cr
MgCl2, NH4C1, nh4oh NH4MgPO4 • 6H2O Трапеции, призмы, дендриты 0,01 1: 100000 AsO3" 4
(NH4)2MoO4, hno3 (NH4)3PO4- 12MoO3 Желтые мелкие кристаллы 0,6 1 :5 000 AsO3", SiO2", Bi34
(NH4)2MoO4, hno3, моноэтаноламин (H2NCH2CH2OH)s- • H7[P(Mo2O7)6]- • 2HNO3 • 10H2O Желтые ромбы 0,015 1: 130 000 AsO3"
р2оГ [Co(NH3)c]Cl3 Желтые, красноватые ромбы, прямоугольники PO3"
Рг’-» (NH4)2CrO4 Pr2(CrO4)3 Оранжевые призмы .... Y3» , Nd3 + , Ce34 Er3+, Pb2+
Na2SO4 Рг2 (SO4)3* Na2SO4- •nH2O Мелкие линзы Ce34, Nd3+, Sin3», Bi3+ La3», Ce3+, Nd34, Sm3 +
Сукцинат аммония ГС2Н4(СОО)2]3Рг2 • • nH2O Бурые розетки из тонких игл
Pt2 4 Ацетат меди, NH4C1. NH4OH [Cu(NH3)4].[PtCl4] Фиолетовые иглы 0,06 1 :50 000 Rhs +
КС1 K2[PtO4] Фиолетовые квадратные призмы .... Pt4+, Pd2 + , Ru4 + , Pb2 +
, Г1 1 K2[PtCI6l к. В С Т.10 - Ж €.1Т Ы С Gk T ft 1. '> (КМ1 bn ' h
Пиридин, NaBi (C3H5N)2 • H2[PtBr6] эдры Желтые, желто оранжевые прямоугольники, параллело- граммы, призмы Au3», Cd3»
RbCl Rb2[PtCl6] Желтые мелкие октаэдры 0,2 1 :5 000 Sn4 +, Au3», Bi3’-, Sb3’
Сульфат ферро-а,а'-ди-пирилила [Fe(CioH8N2)3]-[PtCl6] Красные звезды, дендриты 0,01 1 : 100 000 ReO", CrO2", SCN"
T1NO3 Tl2 [PtO6] Желтые мелкие октаэдры 0,004 1 : 250 000 Au3', MoO2", WO2"
м-Толуидин, НО [C6H4(NH2)CH3]2- • H2[PtCl6] Пучки желтых длинных кристаллов .... Br2
Уротропин C6H12N4 • H2[PtO6] Желтые октаэдры 0,5 1:2000 Ag + , Hg2+, Sb3~, Sn2 + , Au3 +
Rb4 AuCh, AgCl, НО 2AgCl-3AuCl3-6RbCl Темно-красные прямоугольники, призмы, иглы, крестики 0,1 1 :10 000 Cs+
AuCl3, PdCl2 Rb2Au[PdC17] Черные и красные квадраты, прямоугольники, восьмиугольники 0,15 1: 7000 Cs +
AuJ3, AgJ, H.I AgJ • 3AuJ • AuJ3 • • 4RbJ Черные шестиугольники 0,01 1: 100 000 Cs+
Bi2(SO4)3 3Rb2SO4 • Bi2(SO4)„ Шестиугольники 0,03 1: 100 000 Li», Na4, K4, Cs+, NH+
Гексанитродифениламин [ (O2N) зСбН2]2Н Rb Оранжевые прямоугольники, ромбы, квадраты 0,04 1 : 25 000 K + , Cs’-, T1 +
K2[PtCl6] Rb2[PtCl6] Желтые октаэдры 0,5 1 :2 000 Cs + , T1 +
KReO4, HJ Rb2[ReJg] Темно-бурые крестики, сростки из трех шестиугольников 0,01 1 : 100 000 Cs-
(NH4)4SiO4- 12MoO3 Rb4SiO4 • 12MoO3 • •nH2O Желтые почти круглые кристаллы, октаэдры 0,7 1:1400 Cs+, T1 +
МИКРОХИМИЧЕСКИЙ АНЛ.ПИЗ
Продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
Rb4 Na[BF4] Rb[BF,] Ромбоэдры, призмы 0,65 1:3 000 К+, Cs+, Ва2+
Na3[Co(NO2)6] Rb3[Co(NO2)6] Желтые мелкие кубы .... NH+, К+, Cs+, Т1 +
Na2Pb[Cu(NO2)6] Rb2Pb[Cu(NO2)6] Черные кубы 0,02 1 :50 000 NH+, К+, Cs+, Т1+
Na[PbJ3] Rb[PbJ3] Желтые иглы К+, Cs+, NH+
[ReCi,]" Акридин, HCI C13H9N • H[ReCl,] Оранжево-красные звезды, крестики 0,5 I : 2000 ReCi2"
CsCl Cs[ReCl,] Темно-красные ромбы, бипирамиды 0,2 I :5000 Pt4+, lr4+, Ru4+, Rh3 +
!ReCl6]2" CsCl Cs2[ReCi6] Зелено-желтые мелкие октаэдры 0,5 I :2000 Pt4+, Ir4+, Pd2+, Sn4 +
KC1 K2[ReCIe] Зелено-желтые октаэдры ♦ • • • Pt4+, Ir4+, Pd2+, Ru4+, Sn4+ Pt4+, lr4+, Pd2+, Sn4+
RbCl Rb2[ReCl6] Зелено-желтые мелкие октаэдры 0,5 1:2000
ReO," AgNO3 AgReO, Мелкие иглы Ci", Br", J"
CsCl CsReO, Бипирамиды 0,13 7 500 Pt4+, Ir4+, Sn4+, CIO"
Метиленовая синяя Синие иглы 0,25 1 :4 000 CIO" MnO;
Нитрон C20H16N4 • HReCh Желтые иглы, пучки игл 0,4 1 :2500 NO", no;, сю;
RbCl RbReO, Бипирамиды 0,25 1 : 4 000 Pt4+, Ir4+, Sn4+, CIO"
Сульфат ферро-а.а'-дипиридила [Fe(Ci0H6N2)3](ReO,)2 Красные палочки, шестиугольники, кубы 0,5 I :2 000 MnO", CrO2", 4 4 ’ no;
Rh34 kno2 K3[Rh(NO2)c] Желтые кубы 0,1 I : 10000 Co2+
KNO2, CsCl Cs3[Rh(NO2)6] То же 0,1 1 : 10 000 Co2+
(NH4)2[Hg(SCN)4| Желтые кристаллы Zn2 h, Со2 + , Си2 + . Cd2i
Ru3+ CsCl Cs3[RuC)6] Розово-красные иглы. .... .... Pt4 + , Pd2 + . Au3-. Sn4 +
палочки
kno2 Кз[Г?и (NO2) с] Желтые мелкие кубы од 1 : 10 000 Co2+, Pd2+ Zn2+,Co2+,Cu2+, Cd2+ Pt4+, Pd2+, Pb2+,
IRuCl6]2" (NH4)2[Hg(SCN)4], HNO3 CsCl Cs2[RuC16] Желтые кристаллы Красно-бурые мелкие 0,8 1 : 1 200
кристаллы Au3+
N(C2HE)4Br ' Красные трехлучевые Sb3 + , Bl3 +
розетки
S2" Br2, CaCl2 CaSO4 • 2H2O Длинные иглы, звезды, 0,2 1 :5000 SO2", SO2"
ромбы, пучки игл
SO|- AgNO3 Ag2SO3 Мелкие прямоугольники, ромбы 3 1 : 1000 Ci", Br , J , CN", SCN",
JO;
J2, CaCl2 CaSO4 • 2H2O Длинные иглы, звезды, SO2", S2"
ромбы, пучки игл
SO2" Ацетат кальция CaSO4 • 2H2O Длинные иглы, звезды, 0,04 1 :25 000 CO2", jo;,
ромбы, пучки игл c2op
Ацетат свинца PbSO4 Ромбы, шестиугольни- 0,02 1 :50 000 co2-, c2o2", J-
ки, Х-образные кри-
сталлы
Бензидин Ci2H,2N2 • H2SO4 Шестиугольники, тра- 0,5 1 : 2 000 S2o23", CrO2"
пеции 0,05 1 :20 000
Р-Нафтиламин (Ci0H7NH2)2-H2SO4 Ромбы, пластинки
s2or Ацетат свинца PbS2O3 Розетки из игл 0,08 1 : 12 500 SO2", CO2". J- 4 0
ВаС12 BaSsOg Прямоугольники, ро- 0,04 1:25 000 SO2", CO2",
зетки [Fe (CN)6]3"
Бензидин C12H12N2 • H2S2O3 Шестиугольники, вось- 0.008 1 : 125000 SO2", CrO2",
миугольники, прямоугольники 0,015 1 :130000 [Fe(CN)6]4-
TINO3 TI2S2O3 Призмы, палочки, иг- Cl , Br , J , SCN"
лы, крестики
to C>
МИКРОХИМИЧЕСКИЙ АНАЛИЗ
Продолжение
Ион Реактив Состав осадка Характеристика осадка Откры-ваемып минимум, мкг Предельная концентрация, г/г Ионы, мешающие реакции и образующие аналогичные осадки
Sb’1 Бруцин. KBr, H2SO4 Розетки из игл и палочек 0,3 1 :6500 Cd2\ Hg2 + , Bi3 +
CsCl CsstSbCk] • nH2O Шестиугольники 0,16 1 : 6 200 Cd2+, Bi3 + , Sn4 +
CsCl, NaJ Cs[SbJ4] или Cs2[SbJ5] Красные шестиугольники 0,1 1 :10000 Bi3+, Au3+, Pt4 +
NaCl, царская водка Na[Sb(OH)6] Призмы 0,05—0,5
Хинолин, KJ Оранжевые параллелограммы и прямоугольники 0,3 1 :6500 Cu2+, Cd2+, Bi3+
Уротропин, HCI • Крупные прямоугольники, октаэдры Оранжевые шести- угольники 0,4 I :2500 Hg2+, Sn2 + , Bi3 +
Sc3’ Уротропин, KJ Sc2(C2O4)3 nH2O 0,05 1 : 20 000 Cd2-, Hg2+, Sn2+, Bi3 +
H2C2O4 Мелкие призмы и Х-образные кристаллы Ce3’, La3 + , Th4+ Zr4 +
KHSO4 Sc2(SO4)3 • Na2SO4 • • 2H2O Мелкие линзы Al31-, In3 +
|SIF6 2- BaC)2 Ba[SiF6] Палочки, линзы so*-, s2o2-, CO2-
NaCl Na2[SiF6] Шестиугольники, розетки ....
51ОГ HF, BaCI2 Ba[SiF6] Палочки, линзы SO?-
HF, NaCl' Na2[SiF6] Шестиугольники, ро- зетки 0,05 1 : 20 000
(NH4)2MoO4, HNO3 (NH4)4SiO4- 12MoO3 Желтые мелкие кристаллы 0,1 1 : 10 000 PO3“, AsO3', Bi3 +
Sm3+ (NH4)2MoO4, RbCl, HNCh Rb4SiO4 • 12MoO3 То же 0,004 1 : 250 000 РО3", AsO3’, Bi3 +
K4Fe(CN)6] Шестиугольники Ba2+, Fe3 + , Cu24
Na2SO4 Sm2(SO4)3 • Na2SO4 • • 2H2O Мелкие линзы nJ Ce3+, La3+, Nd34. Pr3+, Bi3+
МИКРОХИМИЧЕСКИЙ
со
F (лнцнпат аммония [C2H4(COO)2LSm2-• nH2O Линзы, розетки Се3~, La3', Nd3 ‘ , Рг3 -
Sn24 Дибромоксихинолин Светло-зеленые прямоугольники 0,05 1 : 20 000 In3’, МоОГ, WO2-
H2C2O4 SnC2O4 Х-образные кристаллы, ромбы 0,1 1 : 10000
8-Оксихинолин Желтые прямоугольники 0,2 1 :5000 Т1-, Ti’4, In3+, Sb3-
Сульфат ферро-а,а'-дипиридила, НС1 Темпо-красные звезды, крестики 0,5 1 :2000 Hg2’, Bi3’, Sb3 +
Sn44 CsCl Cs2[SnC16] Очень мелкие октаэдры 0,2 1:5000 Bi34, Sb3’, Au3 +
RbCl Rb2[SnCl6] Мелкие октаэдры 0,2 1 :5000 Bi33-, Sb3’, Au34-
Сульфат ферро-а,а'-дипиридила, НС1 Темно-красные шести-и четырехлучевые звезды 0,001 1 : 1 000 000 Hg2 + , Bi34-, Zn2-, Cd2+
Sr2+ Н2С2О4 или (IN SrC2O4 Октаэдры, четырехлучевые розетки 0,8 1 : 1 200 Ca2 + , Ba2 + , Pb2+, Zn24, Mn24
H2SO4 SrSO4 Крестики 0,2 1 :5 000 Ca24, Ba24. Pb2+
КгСгО4 SrCrO4 Пучки желтых тонких игл 0,8 1 :1 200 Ba2 + , Pb2’
KJO3 Sr(JO3)2 • 6H2O Иглы с расширением посредине, Собраны в розетки 0.1 1 :10000 Ca2’, Ba24, Ag+
Нафтоловый желтый Желтые мелкие иглы 0,1 1: 10 000 K+, Rb4, Cs+, Ca2+, Ba2 +
Озазон диоксивинной кислоты (Na-соль) Мелкие тонкие иглы t 0,04 1 :25 000 Ca2+, Ba24
Тартрат калия-натрия C4H4O6Sr Призмы, шестиугольники, треугольники 0,4 1:2 500 K4, Rb+, Cs+, Ca24
Tav Ацетат натрия, NaOH NasTa6Oi9 • 25H2O Шестиугольники, розетки, палочки 1,2 1 :800 Nbv
NH4F, сульфат ферро-а, а'-дипиридила Темно-красные мелкие призмы 0,1 1 : 10 000 CrO2-, ReO~, VO", MnO~
ГеО2- CsCl, НС1 Cs2[TeCl6] Светло-желтые октаэдры 0,3 1 :6 500 Sn4+, Au3 + . Sb3 +
Hg2(NO3)2 Hg2TeO3 Желтые пластинки SeO|-, СГ, Br“, J-
f’O^
Продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г( г Ионы, мешающие реакции и образующие аналогичные осадки
ТеОГ KJ, НС1 TeJ4 Бурые ромбы, шестиугольники 0,6 1 :5 000 SeO2“, Pt4+, Pb2 +
KJ, NH4C1 (NH4)2TeO6 Желтые и темно-бурые призмы .... Pt4+, If4 +
W+ Н-,С2О4 Th(C2O4)2 Мелкие квадраты, палочки 0,1 1:10 000 Zr4+, Ce3+, La3+, Sc3+
(NH4)2CO3, NH4OH, T1NO3 Tl6[Th(CO3)5] Мелкие призмы, ромбы 0,05 1 : 20 000 UO2+
Т14+ Дибромоксихинолин, КВг Зеленые квадраты, прямоугольники 0,02 1 :50 000 Sn2+, MoO2-, wo2-
NH4F, RbCl Rb2[TiF6] • Н2О Тонкие шестиугольники 1 1 : 1 000 Zr4+, In3+, Sn4+
8-Оксихинолин (C9H6NO)TiO Желтые кубы, трапеции 0,02 1 :50 000 In34, VO", MoO2-, WO2", Sn2+, Sb3+, T1+
Пиридин, NH4SCN Оранжево-красные октаэдры 0,03 1 : 100 000 Co24, Zn2+, Cu2+, Cd2+
Хинолин, NH4SCN (C9H7N)2 • H2[TiO(SCN)J-• 4H2O Оранжево-желтые призмы 0,03 1 : 100 000 Co24, Zn2+, Cu24, Cd24
Т1 + 2,4-Динитро-сс-нафтол Оранжево-желтые призмы и иглы 0.04 I : 25 000 K+, Rb+, Cs+, Ca2-
Г ексаиитродифенил-амин (C6H2N3O6)2NT1 Желто-оранжевые квадраты, ромбы, прямоугольники 0,05 1 :20 000 K+, Rb+, Cs+
НС1 T1C1 Крестики, кубы 0,15 1 :7000 Ag+, Pb2+, Hg24
МИКРОХИМИЧЕСКИЙ
H2[P1CI6] Tl£[PtClc] Желтые мелкие окта- 1 0,008 : 125000 1 Nil,1, К', Rb4 , X
K2[HgJ4] Tl2[HgJ4] эдры Оранжево-желтые 0,1 1:10 000 Cs ; Ag4, Hg24, Bi3* X QJ
Tl34 KJ Na2Pb[Cu(NO2)6] Тиомочевина, HC1O4 NaJ, CsCl T1J TI2Pb[Cu(NO2)6] [T1(CSN2H4)4]C1O4 Cs[T1J4] призмы Желтые мелкие кубы Черные мелкие кубы Длинные тонкие иглы Оранжево-красные ше- 0,03 0,001 0,008 0,06 1 : 100 000 1:1 000 000 1:125 000 1:50 000 Ag+, Pb2+, Hg24, Hg24 NH+, K+, Rbt, Cs4 Ag4, Hg2+ Bi3+, Sb34, Pt4+
UO24 Антраниловая кис- [C6H4(NH2)COO]2UO2 стиугольники, прямоугольники, кубы Мелкие тонкие иглы и 0,012 1 :80 000 Zn24, Cu24, Ag4,
vor лота Ацетат натрия Ацетаты натрия и кадмия Ацетаты натрия и магния, СНзСООН Ацетаты натрия и никеля Ацетаты натрия и цинка (NH4)2CO3, TINO3 AgNO3 NaUO2(CH3COO)3 NaCd(UO2)3(CH3COO)9-6H2O NaMg(UO2)3(CH3CO0)9-6H2O NaNl(UO2)3(CH3COO)9-6H2O NaZn(UO2)3(CH3COO)9-6H2O T14[UO2(CO3)3] Ag4V2O7 розетки Желтые тетраэдры Бледно-желтые тетраэдры, октаэдры То же Зеленые тетраэдры Бледно-желтые тетраэдры, октаэдры Бледно-желтые ромбы Оранжевые палочки, 0,6 0,06 0,06 0,5 0,1 0,07 1:5 000 1 :50 000 1:50000 1 12000 1 : 10 000 1 1 14 000 Hg24, Pd2+ Th44 CrO2“, СГ, Br~,
NH4C1 NH4CI, T1NO3 NH4VO3 T1[VOC14] шестиугольники, звезды Мелкие линзы Овальные кристаллы 0,3 0,07 1 16 500 1 1 14 000 J , SCN Pt44, Au34 Au3+, Pt44, MoO2-, WO2" 4 ’ 4
Продолжение
Ион Реактив Состав осадка Характеристика осадка Открываемый минимум, мкг Предельная концентрация, г/ г Ионы, мешающие реакции и образующие аналогичные осадки
VO3- 8-Оксихинолин Оранжевые прямо- угольники, призмы 0,03 1 :100 000 1п3т, Ti4-, МоО2-, ТГ, Sn2 +
wof Дибромоксихинолин WO2(C9H4Br2ON')2 Темно-зеленые иглы и розетки 0,75 1 : 1 300 In34, МоО2-
КОН, T1NO3 T12WO4 Шестиугольники, звезды 0,08 1:12500 МоО2”, Au3'
NH4CI (NH4) 6^ ?О24 * 6Н2О (пара) Ромбы, палочки 0,15 1 :7 000 Au3+, Pt4+
Na2HPO4, NH4C1 (NH4)3PO4- I2WO.4-• ЗН2О Бесцветные мелкие кристаллы 0,12 1 :8 000 МоО2-4
8-Оксихинолин Темно-зеленые призмы и розетки 0,05 1 : 20 000 Т1-, In3+, Sn2+, МоО2-
Хинолин, KBr Зеленые длинные иглы 0,08 1 : 12 500 Си-’4-, Cd2 +
уз+ Н2С2О4 Y2(C2O4)3 9Н2О Мелкие палочки, ромбы, шестиугольники 0,03 1 : 100 000 Се3т, La3+, Sc3+, Zr4 +
ДАолочная кислота (C3H5O3)3Y Иглы Sc3-
Zn2+ Антраниловая кислота [C6H4(NH2)COO]2Zn Ромбы, шестиугольники, розетки 0,05 1 :20 000 L'O21, Cu24’, Ag', Hg2+, Pd2-
Н2С2О4 ZnC2O4 • 2H2O Октаэдры, реже ромбы 0,1 1 : 10 000 Mn2 + ,Pb2-, Ca2-, Sr2+, Ba2+
K3[Co(CN)6] Zn3[Co(CN)6]2- 12Н2О Квадраты 0,08 1 : 12 500 Ni2 r, Mn2+, Fe3 + , Bi3-
K2[Hg(SeCN)4] Zn[Hg(SeCN)J Белые кристаллы 0,01 1 : 100 000 Cd2 + , Co2-, Ni2 Mn2 +
МИКРОХИМИЧЕСКИЙ
lO'.iiU.. NHjOH Черные тетраэдры и 0,15 1 :7 000 МГ’- 3
кубы
(NiWHglSCNhl Zn[Hg(SCN)4] Кресты, дендриты, тре- 0,1 1 : 10000 Cd2-, Со2-, Си2 г, Fe2+ X
угольники
Na2CO3 3Na2COv 8ZnCO3 • - 8H2O Тетраэдры, треугольные призмы 0,01 1 : 100 000 Са2+, Sr2-, Ва2-, РЬ2-
Na2[Fe(CN)5NO] ZnlFe(CN)5NO] Округленные кубы 0,01 I : 100 000 Мп2 +
Пикриновая кислота. Желтые шлы 0,03 1 :100 000 Си2+,Со2Л Ni2+,
nh4oh
Пиридин, К2Сг2О7 [Zn(C5H5N)2]Cr2O7 Желтые мелкие пря- Со2-, Ni2-,Cu2+, Cd2-
моугольные призмы, кубы
Пиридин, NH4SCN [Zn(C5H5N)2](SCN)2 Тонкие иглы, призмы, 0,05 1 :20 000 Со2-, Си2-, Cd2-
розетки
Сульфат ферро-а,а'-ди- Красные иглы, трапе- 0,3 I : 6 500 Cd24-, Sn4-
пиридила нии, звезды Cd2 + , MnO~
Тетрафенилфосфоннй, [(CcH5)4P]ZnCl3-H2O Бесцветные бипирами- 0,6 1 :5000
хлорид ды Cd2-, Pb2-, Au3-
Хинолин, NaBr Ромбы, параллело- 0,5 1 :2 000
граммы
Хлорид акридина, (CnH9N)2- Желтые иглы, парал- 0,01 1 : 100000 Co2+, UO2+,
NH4SCN • H2[Zn(SCN)4] лелограммы Hg2 + , Bi3-
Zr- К 2С2О4 K4[Zr(C2O4)4 4H2O Октаэдры 0,06 1 : 50 000 Ti4 + , Ce3+, Ca24-Sr2+, Ba2-,
Th4+
NH4F, RbC) Rb3[ZrF7] Октаэдры, шестиуголь- 0,5 1 :2000 Ti4+, In3+, Sn4+,
ники
Хинолин, NH4SCN Дендриты .... Ti4+, Co2-, Zn24-Cu2+, Cd2 +
Абсорбциометрия
Ион Реагент Химическое соединение, в виде которого открывается элемент Открываемый минимум, мкг Предельная концентрация, г/г Предельное отношение к сопутствующим элементам Область измерения светопогло-щения, ммк
Ag+ (NH4)2MoO4 Ag2MoO4 0,2 1 :150000 313—280
Na3[Co(NO2)e] Ag3[Co(NO2)6] 4,0 1 :7500 313—280
А13 + Na3[Co(NO2)G] Al[Co(NO2)fi] 0,3 1 : 100000 365
Ва? т К2СГ2О7 BaCrO4 0,15 1 :33 000 Fe3 + (1:5000); Bi3 + (1:900); Ag+ (1 : 7000); Hg2 + (1 : 1500); Ca2+, Sr2+ (1 : 7500) 365
(NH4)2Mo04 BaMoO4 0,3 1 : 170000 Тяжелые металлы следует отделить 365
Bi3 + KJ K[BiJ4] 0,09 1:550 000 365—280
Са2- K4[Fe(CN)6] K2Ca[Fe(CN)6] 0,5 1:60 000 313—280
Cd2+ Na2[Fe(CN)5NO] Cd[Fe(CN)5NO] 0,01 1:3000000 365—280
Na2HPO4 Cd3(PO4)2 0,2 1 : 150000 365—280
Na2S CdS 0,02 1 : 1 500 000 Zn2+ (1 :20) 365—280
Со2' (NH4)2C2O4 COC2O4 0,15 1:20 000 Hg2 + , Cd2+ (1 : 3); Bi3+ (I :5); Pb2+ (1:7); N12+ (j ; 10) 313—280
nh4oh [Co(NH3)6](OH)2 0,2 1 : 150 000 Cu2+ (1 : 20); Ag+ (1 :30); Zn2- (1 : 35); Ni2+ (1 :40); Ca2 + (1 :50) 313—280
nh4oh, H2O2 [Co(NH8)6](OH)3 0,05 1 : 150000 Cu2+ (1 : 10); Ni2+ (1 :20); Pb2+ (1 :35); Ca2+ (1:60) 313—280
Сг3+ Си2- Fe3+ Hg|+ К + Мп2- NaOH, H2O2 Na2SO3 H2O2 N a2S2O3 nh4oh HCI K3AsO4 (NH4)CH3COO NaOH KC1 KBr Na3[Bi(S2O3)3] NaOH Co(OH)3 CoSO3 H2CrO4 Cr(OH)S2O3 [Cu(NH3)4](OH)2 FeCh FeAsO4 FeOH(CH3COO)2 Fe(OH)3 Hg2Cl2 Hg2Br2 K3[Bi(S2O3)3] Mn(OH)2 0,1 0,55 0,02 0,1 0,15 0,006 0,005 0,04 0,04 0,006 0,005 0,7 0,04 1 :500 000 1 :5 500 1 :2 500 000 1 :500 000 1 :20 000 1 :5000000 1:6 000 000 1:750 000 1 : 750 000 1; 167000 1 :200 000 1 : 70 060 1 : 750 000 Ni2 + (1:20); Cu2+ (1:50) Hg2— (1 :580); Bi3+ (1: I); Co2+ (1:95); Ni2+ (1 :60); Cr3+ (1 :40) Ba2+ (1:75); Sr2+ (1 : 45); Ca2+, Hg2+ (1:40); Mn2+, Co2-, Cu2- (1 :30); Cd2+ (1 :10) Mg2+, Mn2+ (1 : 120); Ba2+ (1:750); Ni2+, Co2+(1:125); Cr3 + (1 :100); Al3 + (1:50); Zn2+(1 :10) Sn4 + (1 : 125 000) Sn2+ (1: 1700); Bi3+ (1 : 1600); Cu2+ (1:1500); Sb3+ (1:400); Pb2+ (1 :300); Ag+ (1:40) Pb2+ (1:900); Bi3 + (1 :300); Ag+ (1:90) 313—280 313—280 365 313—280 313—280 365—280 365 365—280 365 365—280 365—280 365 313—280
ю СЭ CD 1
МИКРОХИМИЧЕСКИЙ Я АНАЛИЗ
_ Продолжение
Ион Химическое соетинение, °T‘^I«ae’ Предельная Предельное отношение измерения еаг т в вияе которого минимум концентрация, к сопутствующим светопогло- иткрывается элемент элементам щения,
ММК
Мп2* Na2S MnS 0,15 1:330000 313 280
nh; И2[Р1С1с] (NH4)2[PtCle] 0,04 1:25000 . . 355
Na3[Co(NO2)6] (NH4)3[Co(NO2)6J 0,3 1:3000 335
Ni2* Диметилглиоксим Ni(HC4H3N2O2)2 0,003 1:10 000000 Co2* (1:700); 355—980
Fe3*, Cr3* (1 : 900); S
Mn2* (1:950)
Pb2 + KBr PbBr2 0,16 1:190000 Bi3* (1:80); 313—280 g
Hg22* (1 : 140); |
Ag* (1:300) x
KJ PbJ2 0,05 1:600000 Hg2* (1 : 150); 313—280 £
Sn2* (1:230); 5
Ag* (1:300) s
Sb3 + HCI, H2O SbOCl 0,02 1:1500000 313—280 >
KJ KSbJ4 0,02 1:2500000 .... 313—280 ?
Sn2* K2CrO4 SnCrO4 0,6 1 :50 000 365 x
NaOH, NH4OH, HCI Sn(OH)2 0,08 1:625000 355—280
Ti4’ NH4OH, NH4C1 H2TiO3 0,5 1:100000 Al3*, V5*, Cr3*, Cu2* 335—280
Pb2*, Cd2* (1 : 50000);
Fe3*, Mn2*, Bi3*
Ag* (1: 10000)
V5* Pb(CH3COO)2 Pb(VO3)2 0,03 1:30000 Sn2* 11 Sb3* (1 : 1) 365—280
Zn2* K3[Fe(CN)c] Zn3[Fe(CN)6]2 0,4 1:75000 355—280
NaaS 0,015 1:3300000 Al3* (1:360) 365
Люминесцентные методы
открытия элементов
В таблицах приведены сведения о методах открытия элементов ио образованию люминеспирующих продуктов реакции и по гашению люминесценции реактива, а также цвета люминесценции некоторых индивидуальных неорганических химических соединений.
Приведенные реакции выполняются на предметном стекле. фарфоровой плас .инке, бумаге или в пробирке. Цвет люминесценции указан яри условии облучения продуктов реакции хльтрафиолетовыми лучами с длиной волны 365.7 ммк. Минимальный рабочий объем раствора (в мл), требующийся для выполнения одной реакции,, может быть рассчитан, исходя из данных об открываемом минимуме и предельной концентрации
по формуле: V= уде"» где С предельная концентрация, т — открываемый минимум.
Предельная концентрация выражена отношением наименьшей открываемой массы элемента (иона) к массе раствора.
Более подробные сведения см.: 1. К- П. Столяров Методы люминесцентного открытия и определения неорганических ионов, изд. ЛДНТП, 1961. — 2. Р. W. Danckwortt. J. Eisenbrand, Lumineszenz-Analyse im filtrierten ultra-violetten Licht. Лейпциг, 1956. — 3. Z. H о 1 z b ec h er, Lumi-niscencni analysa, Прага, 1957.
РЕАКЦИИ ОТКРЫТИЯ ИОНОВ (ЭЛЕМЕНТОВ) ПО ОБРАЗОВАНИЮ ЛЮМИНЕСЦИРУЮЩИХ ОСАДКОВ И РАСТВОРОВ
Редкоземельные элементы приведены в конце таблицы.
Принятые сокращения см. стр. 16.
Ион ИЛ I! элемент Реактив Ивет люминесценции Открываемый минимум, мкг Предельная концентрацня Мешающие элементы
Ag’ Фенилцинхониновая кислота, нас. сп. р-р Красный, оранжевый 0,5 I : 2 103 ZrIV, ThIV, Be2*, Sc3* , Ga3*
АГ- Ализариновый красный RS. 0,1% водн. р-р Красновато-желтый > 1: Ю3
Койсвая к-та+8-оксихино-лин, 0,5% р-р в СНС13 Желто-зеленый 0,03
Морин (или кверцетин) 2% сп. р-р » 0,005 1:5107 Ga3*, Cr3*, Be2*, Sc3*
2.З-Оксинафтойная кислота Голубой (рН=^2-<-3) зеленый (рН>3) 0,01 1 : 10*
8-Оксихипс.лин, 0,4—2% р-р в СНОз (СС14) или 1 н. СНзСООН Желто-зеленый In3-, Zn2*, Cd2*, Ga3*. Tl', ZrIV, Li*. Be2* , Mg2*, Ca2*, Ba2*
Салицилпден-о-аминофенол, 0,1% сп. р-р » 0,00001 1 : 108 Be2*, Zrlv, F"
4-Сульфо-2, 2'-диоксиазонаф-талин, аммиачный р-р Красный 0,1 1 : 5 - 10е Ga3*, Cr3*, Fe3*
Поодолжение
to
се
IS Зак. 783
Ион или элемент Реактив Цвет люминесценции Открываемый минимум, мкг Предельная концентрация Мешающие элементы
As3+ HgCl2 (высушивание) Синий 1,0
К4[Тё(С1\|)б] (высушивание) Желтый 0,1 1 : 8 -104 Sb3 +
AulH Родамин С, 0,05% р-р в Оранжево-красный . . . . Hg11, Sbv, TI111
конц. НС1
.во- Бензоин, 0,5% сп. р-р Желто-зеленый 0,02 1:5 -106
Резацетофенон, 0,5% сп. р-р Сине-белый 0,04 1 :2,5 • 10’
Ва2 * NasSiFs+KypKyMa, сп. р-р Коричневый 25,0 1 : 2 • 103 Mg2t"
8-Оксихинолин, 0,5—1% р-р Желто-зеленый Cd24-, Al34-, ln3 + , Оа3т,
с СНС13 или 1 н. СН3СООН TI1, Zriv, Li+, Be2+ ,
Mg2+, Ca2<-, Zn2’
Ве2 + Ализариновый красный RS, Красный Zrlv, ThIV, Al3 + ,
0,1% води, р-р Sc3+, Ga31-
1 -Амино-4-оксиантрахинон, Оранжевый 1,0 1:4- 106 CrVI
0,1% сп. р-р
1,4-Диоксиантрахинон, 0,1% Желтый
СП. р-р
Кверцетин, нас. р-р » 0,001 1 : 2 - 106 Zn2+, Ca2+, Li +
Морин, 0,02% сп. р-р » 0,001 1:5-10’ ln3+, Zrlv, Geiv, Sn2 + ,
Sb3+, Li + ,Ca2+, Sr2+,
Zn2”, Al3+, Ga3+
Na2B4O7 (высушивание) Зеленый 0,2 1 : Ю5 Au1", Cu", SnI1Hlv,
Vv, Mn", P. 3.
Na2HPO4 (высушивание) Желтый 2,5 1 :2 • 104
8-Оксихинальдин, 0,1 % сп. р-р » 0,00003 1: 3,3 - 106 Bi3+, Cd2+, Cr3+, Co2+
Cull, Fe3 +
8-Оксихинолин, 5% сп. р-р Желто-зеленый 0,025 1:2 - 106 Cd24-, Al3+, ln3+, Ga3+,
TI1, ZrIV, Li+, Mg24 ,
Ca2+, Ba2+, Zn2-,
Sb3+
Bi3” СаО (высушивание) Фиолетово-белый 0,02 1 : 106 TI1, Pb2+, Hg2+, Sb34 ,
Movl, WVI
Са2 + Мории + С2Н3ОН, 0,1 —0,02% Желто-зеленый In34’, Zriv, SrJ”, Ge'v,
сп. р-р Sn2 + , Sb3”, Be2”
Li + , Zn2”
8-Оксихинолин, 0,5—1% р-р » 0,1 1 :5 -10= Cd2+, Al3+, Zriv, In3”.
в СНС13 или 1н. СНзСООН Ga3 + , TI1, Li", Be2"
Mg2+, Ba2+, Zn2"
Cd2- Na2S; H2S Красноватый 0,02 1:5-10’
2 (о-Оксифен илбензоксазол) Синий 0,1 1 :5 -108
8-Оксихинолин, 0,5—1% р-р Желто-зеленый 0,1 1:5 - Ю3 In3", Ga3+, TI1, Be2" ,
в СНС13 или 1 и. СНзСООН Mg2", Ca2-, Zn2 + ,
Ai3+, ZrV, Ba2+, Li-
Пиридин + KJ Сине-белый Pb2 +
Си2’ Кошениль + NaOH » 0,1 1 : 5 • 10= Pb2+, Ptlv, Auln,Movl
WV1
Пропилтиоурацил Темно-красный
Оазт Ализариновый красный RS, Красновато-желтый ZrIV, Thlv, Be2+, Sc3+ ,
0,1% водн. р-р Al3 +
Морин, 0,1—0,02% сп. р-р Желто-зеленый Al3+, Zriv, In3", Geiv,
Sniv, Sbv
8-Оксихинолин, 0,5—1% р-р » Zn2+, Al34-, ln3+, Cd2 + ,
в СНС1з или 1н. СНзСООН TI1, ZrIV, Li", Be2* .
Mg24-, Ca2+, Ba2+
Салицилиден-о-а минофенол, »
0,1 % сп. р-р
4-Сульфо-2, 2'-диоксиазонаф- Красный Al3+
талин, аммиачный р-р
Oeiv Бензоин, 0,5% сп. р-р Зелено-желтый 0,01 1 :Ю5 Be2+, Sbv, Zn2+
Монооксинафтаценхинон- Желтый 0,25 1 : 4 104
сульфокислота
Морин, 0,1—0,02% сп. р-р Зеленый 1,5 1 :6,6 • 103 SnIV, Sbv
Gg’ 0,1н. НС1 Оранжево-красный 0,005 1:2 • IO3
КВг (высушивание) Красно-оранжевый 0,004 1 : 2,5 - 105
Hg- Родамин С, 0,05% р-р в Оранжево-красный TI111, Au111, Sbv
конц. НС1
СаО (высушивание) От белого до голу- 0,002 1:5 106 T1+, Pb2”, Sb3”, Bi3",
бого Movl, WVI
РЕАКЦИИ ОТКРЫТИЯ ИОНОВ (ЭЛЕМЕНТОВ) ПО ОБРАЗОВАНИЮ fl дЮМИНЕСЦИРУЮЩИХ ОСАДКОВ И РАСТВОРОВ
Продол vcch up
Ион или элемент Реактив Цвет люминесценции Открываемый минвмум, мкг Предельная концентрация Метающие элементы
Hg2* Na2B.,()7 (высушивание) Зеленый 0,4 1: 7,5-10*
In3* Морин, 0,1—0,02% сп. р-р 8-Оксихинолин, 0,5—1% р-р в СНС1з или 1н. СНзСООН » Желто-зеленый АР+, Zriv, Ga3*, OeIV, Snlv, Sbv Zn1”, Al”,Ga3+,Cd2 -. Tl1, Zrlv, Li+, Be2’. Mg2*, Ca2*, Ba2 +
Li* Морин (или кверцетин). 2% или нас. сп. р-р 8-Оксихпнолин, 0,5— 1 % р-р в СНС1з или 1 н. СНзСООН Цинк-уранилацетат Желтый Зеленый 1,0 1 :5 -104 In3', Zriv, QelV, Sniv, Sbv, Be2*, Ca2 + , Sr2*, Zn2*, Al3*, Ga3* Cd2*, Al3*, In3', Ga3*, Tl+,Zriv, Be2'.Mg2-, Ca2*. Ba2*, Zn2* Na*
Mg2* Na2SiF6 + куркума, сп. р-р 8-Оксихинолин, 0,5—1% р-р в СНС13 или 1 н. СНзСООН Коричневый Желто-зеленый 25,0 0,025 1 : 2 103 1:2-10® Ba2* Li *, Be2*, Cd2*, Al3’. In3*, Ga3*, T1-, Zr'V. Ba2*, Zn-’*
Mn2* СаСОз (высушивание) Na2HPO4 (высушивание) Желтый Рубиново-красный 0,0001 5,0 1 :4 • 1С3 Sb3*, Bi3*
MoVI СаО (высушивание) Кошениль, нас. сп. р-р Морин, 0,1—1% сп. р-р’ Церулейн, цинковая соль, 0,1% р-р в НС1 Бирюзовый Светло-красный Желтый » 67,0 0,025 1 : 1,5- 102 1 : 2 • 1и® Tl*, Pb2-, Hg2-*, Sb3 + , Bi3 *, WV! Cu", WVI Snlv, Vv, WVI
Na-1 Цинк-уранилацетат Желто-зеленый 0,03 1 : 3,3 • 105
Ni2* СаСОз (высушивание) Зелено-желтый
Pb2'* СаО (высушивание) Морин, 0,1% сп. р-р От белого до сиреневого Желто-зеленый 0,001 0,25 1 : 10® 1:2 10= T1 + , Hg2*, Sb3*, Bi3*, Movl, WV1
! KJ Желти коричпевый I Г j CJ'
Sb* Родамин C, 0,05% р-р в конц. HCI Оранжево-красный ТГ”. Au”1, Ну"
Sb1" Морин, 1% сп. р-р I<4[Fe(CN)6] (высушивание) Зеленый Желтый (',05 0,001 1 : 10® 1 : 10® Asm
СаО (высушивание) CaCOj (высушивание) 6-Нитро-2-нафтиламин-8 сульфокислота, аммонийная соль Желто-белый Зеленый 0.0001 0,0001 1 : 10 1 : 10' Т1 + , Pb-’+, Hg2 + , Bi3* MoVI, WV1 Bi3*. Mull
Sniv Голубой 1,0 1:2- 10’
Морин, 1 %, сп. р-р Зеленый 1,0 1 : 10®
Snii HCI + Zn Синий 0,03 1 : 1,60-к;6
KJ (высушивание) Желтый 0,0002 1:5- 10® Hg2*, Sb3*, Bi3’, As3-, Ag *, Pb2*, Fe3*. Cu2*
Sr2* Морин J-uso-CsHijOH Желто-зеленый 2,5 1:2-10’ Ca2*
8-Оксихкнолин, 0.1% р-р в 1 н. СНзСООН »
Родизонат натрия Зеленовато-желтый Au"1, Hg", Sbv, SCN-
TilH Родамин С, 0,05% р-р в конц HCI Желто-оранжевый 0,03 1 :6,6 - 10®
Tl1 KJ (высушивание) От желтого до фиолетового 0,001 1:2-10’ Sn2 *, Hg2*, Fe3*, Cu2 *, Pb2 *
КО (высушивание) Красный 1,0 1 : 10’
СаО (высушивание) От белого до желто-зеленого 0,02 1 : 5 - 10’ Hg2*, Pb2*, Sb3*, Bi3*, Movi, WVI
8 Оксихинолин. 0.5—1 % р-р в СНС13 или 1п. СНзСООН Желто-зеленый Zn2*, Al3*, Ga3 *,Cd2*, In3’, Zriv, Ы *, Be2*, Mg2*, Ca2 *, Ba2*
Vv ИазВК)? (высушивание) Слабо-желтый 1,0 1:2-10’ Audi, Ba2*, Cu2*, SiiH, MnVll
uvl Na2HPO4 (высушивание) Желто-зеленый 0,0005 1:2-10’
\yVi СаО (высушивание) Кошениль, нас. сп. р-р Рубиново-красный Светло-красный 100,0 1 : 102 Tl*, Pb2*, Hg2*, Sbv, Bi”, MoVI Cu'l, MoVI
Мории, 0,5% сп. р-р Желтый
РЕАКЦИИ ОТКРЫТИЯ ИОНОВ (ЭЛЕМЕНТОВ) ПО ОБРАЗОВАНИЮ и Н ЕСЦИРУЮЩИХ ОСАДКОВ И РАСТВОРОВ
РЕАКЦИИ ОТКРЫТИЯ ИОНОВ (ЭЛЕМЕНТОВ) ПО ОБРАЗОВАНИЮ ЛЮМИНЕСЦИРУЮЩИХ ОСАДКОВ И РАСТВОРОВ
Мешающие элементы >' +" 1-‘+ >' i > +'+*i 3 mi й -Л -О о UU < . >U+‘ +“ + 'С0 +“ > вга+‘> - +* р • щ ”. 5 - . "u <uujc > ьл+ • -СМ * *“я _ к. 1 и- —2 CJ и. , — CQN С < СМ N . - И N+"+ (=+ < . I 5./ - . -"ха =1, к’ +" "га ‘и. + +' -'га i СЛСЛ га га О? га О i 'J^'-Л « И 1 1-00—. = Й < < = О < _>
Предельная концентрация ’ о • о о * 2 ’ • о г”" • т'_| г”4 . г”" • ,, LQ • СЧ СЧ . Ю • •
Открываемый минимум, мкг • • Ч О) о — ‘ 1л ю ’ - С • -.’о 'о? с4 ’о L" i о н о° 4 О =<
Цвет люминесценции jS sS ’Z3 ’S 3 з 3 3 H t . X . X ч as 5 a g ф i—, 0; • Н» • H я i ¥ . s . s 0 £ .0.0 5 =s m S =ы ’= s 5 И А Й £ ТЧ CO • И 0 c ►у1 ХЬ* X p- X • Сац , l. aJ o> 14 *5 14 et 4QJ 4 »QJ . QJ 1 $ * S * $ . £ . S
Реактив Морин, 0,02—1% сп. р-р Na2S iO3+N агБгОз+бензоин+ -bMgCis 8-Оксихинолин, 0,5% р-р в CHCh или 1н. СНзСООН Ализариновый красный RS, 0,1 % волн, р-р Морин (NH4OH), 0,02% сп. р-р Морин (СНзСООН, НС1), 0,02% сп. р-р З-Оксифлавон, 0,01 % р-р в 1 Н. H2SO4 8-Оксихинолин, 0,5—1% р-р в СНС1з или 1 н. СНзСООН CaWO< (высушивание) На2В4О7+НзРО4 (высушива- ние)
Ион или элемент n n а
276
РЕАКЦИИ ОТКРЫТИЯ ИОНОВ (ЭЛЕМЕНТОВ) ПО ГАШЕНИЮ ЛЮМИНЕСЦЕНЦИИ РЕАКТИВА
РЕАКЦИИ ОТКРЫТИЯ ИОНОВ (ЭЛЕМЕНТОВ) ПО ГАШЕНИЮ ЛЮМИНЕСЦЕНЦИИ РЕАКТИВА
Мешающие элементы • « (•«••••••• * • ” ••••••»••« • • *«»»•»•»••• • • 5 • а »•«•••»«• • S о. < • • • ••••••••> 1 03 СЧ 00 "7* . Ц) . . ,Д . . ... fl QU (У • н . ft. . . а. < Ь
Предельная I концентрация | 2 2 2 ® ’ 2 '' ' « - 2 2 2 ю «• ио *"* •’’’’""'jL • ’ио • О О , «г, ’ О О ’ О ‘ О' с О г-н —< ’ Ю —1 Zh Ю г-н ю СЧ « »—CN г-1 . . rZ ..... LOC4 СЧ г-н 1—1 г-н гН < * г—< г-н —' ’ * г-Н * н-н
Открываемый минимум О Ю Ю О Ю —< СЧ о ю О * Ю Ю 1О О О ЛО н-Г Q О О О О О' ' U0 СЧ 10 • ’О О О ~ о СЧ
Цвет люминесценции 1 | реактива j • • 9Х • ’X »s • X ’ ’S X i • • 5 • S3 “ • • 6 • • 4 О б) Ш 0J со й • ’X 9S ‘ sS ’ О ’X • >Х 9S • sS 9Х m О ’= °’хЗ‘в’^л=’х='хх 2 х 5 га9 га о га гач аЗ 2 S Л- . Q- qj . Q. . —< Q. . Ct ф • ф Q. кх X. со . « , G . X м , со 'Z. z
О
о
□
о
□
о 5
S га *'Z. SO So SO Р» оо SI =0 S + о
S E-
S ф
- S og S и
cj
- > >
IP £
277
Л1ОМИНЕСЦЕНЦИЯ
НЕКОТОРЫХ ИНДИВИДУАЛЬНЫХ
ХИМИЧЕСКИХ СОЕДИНЕНИИ
1МИНЕСЦЕНЦИЯ НЕКОТОРЫХ ИНДИВИДУАЛЬНЫХ ХИМИЧЕСКИХ СОЕДИНЕНИИ
2
яствах карбона'
'.278
МЕТОДЫ ВЕСОВОГО И ОБЪЕМНОГО ОПРЕДЕЛЕНИЯ ЭЛЕМЕНТОВ
Весовой анализ
В таблице приведены методы весового определения важнейших неорганических веществ (ионон). В первой графе указаны определяемые вещества (ионы); во второй — реактивы, применяемые для определения данного вещества; в третьей - методика определения; в четвертой — формулы взвешиваемых веществ («весовая форма осадка»),
Третья графа построена в соответствии с ходом определения, Вначале приводятся < ведения о составе анализируемого раствора, указывается необходимая для определения среда; далее — прибавляемые реактивы, температура раствора и время выдерживания его •пред фильтрованием. Затем указан тип фильтра (ф, б. — фильтр бумажный илн ф. с.— фильтр стеклянный), после чего в скобках — раствор, применяемый для промывания осад-jа. В конце приводится температура прокаливания или высушивания осадка. В некоторых случаях в четвертой графе приведены две весовые формы осадка, соответствующие двум | омигратурам прокаливания.
Для некоторых методов весового определения веществ приведены только весовые формы осадка (иногда при этом в скобках указан осаждающий реактив)
Содержание определяемого компонента в анализируемом веществе рассчитывается по следующим формулам:
n af-100 . лМ]
Здесь Р — содержание определяемого компонента в анализируемом веществе (в %). а — весовое количество осадка (в г или мг). т — навеска анализируемого вещества (в тех же единицах, что и a}, f - стехиометрический множитель (фактор), Mi — молекулярный или атомный вес определяемого вещества, М2 — молекулярный или атомный вес взвешенно! о вещества, п — число молекул или атомов определяемого вещества, соответствующее одной молекуле, или одному атому вещества осадка.
Пример: стехиометрический множитель при вычислении весового количества алюминия, соответствующего данному количеству осадка А120з f— "j"=0,5292, где 26,98 — атомный вес А1; 101,96 — молекулярный вес AL2O3.
В случаях, когда формула осадка не вполне точно выражает его состав, эмпирическое значение стехиометрического множителя f (для пересчета на вес элемента) приводится ’• скобках в четвертой графе.
Таблица построена в порядке, отвечающем положению элементов в периодической сис геме.
Судить о веществах, мешающих определению данного вещества, и о методах удаления мешающих веществ можно на основании данных, приводимых в таблицах «Групповые реактивы», «Индивидуальные реакции ионов». «Некоторые частные методы разделения, ионов».
Принятые сокращения
бромкрезол. — бромкрезоловый
в ы д е рж. —вы д е рж ив а ют
мет. —метиловым
с бум. массой — с бумажной мацерированной) массой сплавл. —сплавляют
ф. б. — ф и л ьтру ют ч ере з б ума ж пни ф t л ьто
ф, с, —фильтруют через стеклянный фильтр
Ш. М. — щелочные .металлы
Остальные сокращения см стр. 16.
ВЕСОВОЙ АНАЛИЗ
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
I группа периодической системы
L1+ H2SO4 Анал. р-р. р-в. Выпар., вы-суш. при 200° С Li2SO4
НС1 Анал. р-р (хлориды Щ. М.) выпар.» смачивают конц. р-вом. Экстр, сухим ацетоном, выпар., прокал. до плавления LiCl
Na2HPO4 Анал. р-р (щел.), р-в. Выпар., раств. в NH4OH. Ф. б. Прокал. при 800° С Li3PO4
Опр. также в виде 21лз[Ре(СМ)6] • Кз[Ре(СН)6] • 5[(СН2)бМ, • 6Н2О] или в виде LiF
Na+ H2SO4 Анал. р-р выпар. 2 раза с Na2SO4
Цинк-уранил-ацетат р-вом, прокал. < 875° С с добавкой (NH4)2CO3 (тв.) Анал. р-р (1 мл, содержащий < 8 мг Na), р в (10 мл). Ф. с. (промыв, р-вом, сп., нас. натрий-цннк-уранилацетатом, эф.) Высуш при 118—125° С NaZn(UO2)3- ' (С2Н3О2)д
Прокал. при 360—670° С Na2U2O7-2ZnU2O7
Опр. также в виде NaMg(UO2)3(CH3COO)g• 6Н2О
K+ (NH4)2 so4 Анал. р-р, р-в. Выпар, прокал. при 400—800° С с (NH4)2CO3 (тв.) K2SO4
H2[PtCl6] а) Анал р-р, р-в. Выпар., добавл. сп. (80%-ный). Ф. б. (промыв, сп.). Высуш. при 130—200° С б) Осажд. K2[PtCl6] (см. п. «а»). Ос. раств. в гор. Н2О, добавл. HCOONa, выпар., добавл. НС1 (разб.). Ф. б. (промыв. Н2О). Прокал. при 1000°С К2(PtClJ Pt
НС1О4 Анал. р-р (хлориды Щ. М.), р-в. Выпар., добавл. Н2О (2—3 л(л), бутил, сп. (кипящий, 33 мл на 1 мл Н2О). Ф. с. (промыв, бутил. сп.). Высуш. при 350° С ксю4
Na [В (C6HS)4], 3% р-р (0,003% А1С13) Анал. р-р (НС1, 0,1 н,), р-в. Harp. 15 мин. Ф. с. (промыв. нас. р-ром К[В(С6Н5)4]). Высуш. при 110—130° С К [В (C6HS)4]
280
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
к+ Дипикриламин Анал. р-р нагр., добавл. гор. р-в. Выдерж. 1 сутки. Ф. с. (промыв, нас. р-ром р-ва). Высуш. при 100—105° С KN[C6H2(NO2)3]2
Опр. также в виде K2Na[Co(NO2)6] • Н2О (эмпир. фактор), КС1
Rb+ SnCl4, пас. р-р Анал. р-р (хлориды Щ. М. после отделения К+) нагр., добавл. кнп. р-в. Выдерж. 4 ч. Ф. с. Высуш. при 110° С Rb2 [SnCl6]
Опр. также в виде RbSO4, RbsfPtCle] и RbN[CsH2(NO2)3]2 (см. методы опр. К+) Cs+ опр. в виде CsSO4, Cs2[PtCle], Cs^SnCU] (см. методы опр. К+ и Rb+), а также в виде CsNa[La(NO2)6], Cs3[Bi2J9], Cs3[Co(NO2)6] • Н2О
Cuz + NH4SCN Анал. р-р (слабокисл.), нас. SO2, разб. Н2О. Нагр. до CuSCN
NH4SCN (I) и 100° С, добавл. р-в. Ф.с. (промыв. NH4SCN, р-ром SO2, 20%-ным сп.). Высуш. при 105—120° С Анал. р р, р-в I и р-в II [Си (СБНБМ)2] •
пиридин (II) (до син.). Ф.с. Высуш. при (SCN)2
Салицил аль- 20° С под вакуумом Анал. р-р (кисл.), р-в. Ф.с. Си (C7H6O2N)2
доксим Высуш. при 105—110° С Анал. р-р, H2SO4 (1 h.)i Си
(электролиз) Реактив Рейнеке HNO3 (0,25 н), добавл. :* а- ЭДТА (для маек. Fe3*). Электролиз (0,5—2 а/дм2) Анал. р-р (H2SO4<3 н.). Си [Cr (NH3)2.
N2H4 • H2SO4, нас. SnCl2, р-в. Ф.с. Высуш. при 110” С Анал. р-р (>0,2 мг Си; (SCN)J (/ = 0,1636) CuSO4 (N2H J -
Р-Р H2SO4), р-в. Ф.с. Высуш. H2SO4
при 100—НОРС
Опр. также в виде Cu(Ci2Hi0ONS)2 • Н2О (тионалидат), Cu(Ck>H6ON)2 • Н2О (хинальдинат), Си(С7НбО2\)2 (антранилат)
Ag+
НС1
Анал. р-р, HNO3 (1%), р-в. Harp, до 70° С. Оставляют на несколько часов в темноте. Ф. с. (промыв. 0,06% HNO3). Высуш. при ISO-l^C
AgCl
Опр. также в виде AgJ, AgCN, AgBr, Ag2S и Ag (электролизом)
AuHi
Гидрохинон
Анал. р-р (HCI, 1 н.), р-в. Harp, до 100° С. Ф. б. (промыв. гор. Н2О). Прокал. при 900° С
Au
281
ВЬСОВОЙ АНАЛИЗ
П родолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
АиШ so2 Анал. р-р (НС1, ~ 1,5%), р-в. Фильтр, с бум. массой. Ф. б. (промыв, гор. 0,3% НС1). Прокал. при 900° С Аи
Опр. также с помощью NaNO2, меркаптобепзтиазола, Н2СгО4, FeSO4
11 группа периодической систем ы
Ве2 + NH4OH Авал, р-р, Na-ЭДТА до 15% в р-ре). Нагр. до 100° С, добавл. NH(C1, р-в (без изб.). Ф. б (промыв, гор. 2% р-ром NH4NOj). Прокал. при 1000°С ВеО
(NH4)2 НРО4, 2А1 Анал. р-р, р-в, Na-ЭДТА (15% р-р), NH4OH (10%-ный до помутнения), CH3COONH4 (до pH ~5). Кип. 3 мин. Первое. Ф. б. (промыв. 1 % р-ром NH4NO3). Прокал. при 750—800° С Ве2Р2О7
(NH4)2 СОз (I) и Анал. р-р (3—4 мг Be), р-в I, [Ве2 (СО3)2(ОН)3«
(Со (NH3)6] CI3 р-в II (до ор.-желт.), до- • (Н2О)з1 •
(И) бавл. сп. Выдерж. 1,5 ч. Ф. с. (промыв, сп. г р-в II; сп., эф.) Высуш. в вакуум-эксикаторе •[Co(NH3)6. •ЗН2О] (/ = 0.041)
2,2-Диметил-гександион-3, 5, нас. водн. р-р Анал. р-р Na-ЭДТА, NH4OH (до pH = 7 4-8), р-в. Выдерж. 4 ч. ф. с. (промыв. Н2О). Высуш. при 50—55° С Be (С8Н13О2)2
‘Опр. также в виде BaBeF4, BeSO4, С22Н|4О4Ве (осажд. Р-окси-а-иафтойным альдегидом, /=0,02565)
Mg2-1’
(NH4)2 нро4
8-Оксихинолин (2% с добавл.
2 М СН3СООН)
а) Анал. р-р (слабокисл.), р-в, NH4OH. Ф. б. (промыв, хол. 10% р-ром NH4NO3). Прокал. при 1050—1100° С
б) Осажд. как в п. «а». Ф. с. (промыв. NH4OH, сп.). Высуш. при 20° С
Анал. р-р, р-в. Нагр. до 100° С, добавл. CH3COONH4, разб. NH4OH (небольшой изб.). Ф. с. (промыв, гор. Н2О). Высуш. при 250°С или при 150—160°С
Прокал при 1000° С
Mg2P2O7
MgNH4PO4-6Н2О
Mg (C9H6ON)2
Mg (C9HcON)2.2H2O
MgO
Опр. также в виде MgSO4 или MgO (после осажд. NaOH пли Na2COa)
282
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реакт ив Методика определения Весовая фо^мо осадка
Са2 ’’ (NH4)2C2O4, 4% Р-Р а) Анал. р р, р-в. Нагр. до 70—80° С, медленно нейтр. NH4OH. Нагр. еще 30 мин. Через 2 ч. Ф. с. (промыв разб. (NH-ihCsCh, сп.). Высуш. при 100е С. Прокал. при 475—525° С б) Осажд. CaQO-i (см. выше). Ф. б. (промыв, разб. (NH4)2C2O.j). Прокал. при 1000е С в) Осажд. СаС2О4 (см. выше). Прокал. при 800е С, добавл. H2SO4 (1 : 1), осторожно выпар. Прокал. при 500— 600° С СаС204-Н,О СаСО3 СаО CaSO4
H2SO4 (1 :1) Анал. р-р. (нейтр. или слабо кисл.), р-в (10-кратный изб.), сп. (4 объема). Вы-держ. 12 ч. Ф. б. (промыв. 75% сп.). Прокал. при 500— 600° С CaSO4
Опр. также в виде СаСО3, CaF2, CaWOi, СаМоО4
Sr2+ H2SO4 Анал. р-р (HCI), р-в (10-крат-иый изб.), СП. Ф. с. или ф. б. (промыв. 75% сп.; разб. H2SO4; сп). Высуш. при 100—300° С SrSO4
Опр. также в виде SrCO3 ЗгСгОф • НгО, ЗггРгО?, Sr(CjoH7N405)9 • 8Н2О (пиколинат)
Ва2+ H2SO4 Анал. р-р (кип.), р-в (гор.) Ф. с. или ф. б. (промыв. Н2О). Прокал. при >780° С BaSO4
(NH4)2 CrO4 Анал. р-р (уксуснокислый). Нагр. до 100° С, добавл. р-в. Ф. с. (промыв. 0,5% р-ром CH3COONH4). Высуш. при <60° С BaCrO4
Опр. также в виде ВаСОз, ВаС2О4, BaSiFo
Zn2+ H2S (газ) а) Анал. р-р (pH = 2,6-? 2,7), р-в. Ф. б. (промыв. Н2О). Прокал. при 950—1000° С б) Осажд. как в п «а». К ос. добавл. HNO3. Выпар. Прокал. при 500° С ZnO ZnSO4
H2S (газ) и ВаС12 Осажд. ZnS (см. выше), окисл. Опр. SO4~ BaSO4
283
ВЕСОВОЙ АНАЛИЗ
П родолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
Zn2+ (NH4)2 нро4 Анал. р-р (слабокисл.) натр., добавл. р-в (10—15-кратный изб.). Через 3 ч ф. б. [промыв, гор. 1% р-ром (NH4)2HPO4 50%-ным сп.]. Прокал. при 900° С Zn2P2O7
NH4SCN (I) и Анал. р-р, р-в I, р-в II. Ф. с. [Zn (C5H5N)2] •
пиридин (II) Высуш. при 20° С (под вакуумом) • (SCN)2
8-Оксихинолин Анал. р-р (в ацетатн. или тартратн. буф.), р-в. Ф. с. Высуш. при 130—140° С Zn (C9H6ON)2 • • 1,5H2O**
ЫагСОз Анал. р-р нагр. до 100° С, добавл. р-в (до роз. окраски фенолфт.). Ф. б. (промыв. Н2О). Прокал. при 950—1000° С ZnO
К2 [Hg (SCN)4J* Анал. р-р (р-р ZnS в H2SO4), винная к-та, KSCN, CHsCOONa, р-в. Через 10—12 ч ф. с (промыв, р-вом 1 : 400, Н2О). Высуш. при 110° С Zn [Hg (SCN)4]
(электролиз) Анал. р-р, лимон, к-та (рН= = 4-;-5). Электролиз на Pt-катоде (покрытом Си) при 1 а] дм2 Zn
Опр. также в виде Zn(C7H6ON)2 (антранилат), Zn(CioH602N)2• НгО (хиналь-
динат) и ZnNH4Pd4
Cd2+ H2S (газ) Анал. р-р (H2SO4, 1:20), р-в. К ос. добавл. H2SO4. Выпар. Высуш. при 140— 150° С CdSO,
2-о-Оксифенил-бензаксозол (1% сп. р-р) Анал. р-р (тартратн. буф. рН = 9), нагр. до 60°С, добавл. р-в (до рН=11). Ф. с. (промыв, сп. 1:1, Н2О). Высуш. при 130— 140° С C.d (C13HbO2N)2
(NH4)2 МоО4 Анал. р-р (кип.), р-в, NH4OH. Ф. с. (промыв, гор. Н2О). Высуш. при 120° С CdMoO4
р-Нафтохинолин, Анал. р-р (H2SO4, 6%), SO2 [C13H9N]2 •
2,5% свежепри- (нас. р-р), р-в II, р-в I. • H2CdJ4
готовленныйр-р в 0,5 н. H2SO4 (1) и KJ, 10% р-р(П) Ф. с. (промыв, р-вом + + SO2+KJ). Высуш. при 70—80° С (/ = 0,1147)
* Для приготовления' р-ра смешивают равные объемы водных р-ров HgCI2 (27 г/л) и
KSCN (39 г/л).
** Иногда приводят формулу Zn(CsH6ON)2.
284
ВЕСОВОЙ АНАЛИЗ
П родолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
Cd2+ (электролиз) Анал. р-р выпар., добавл. H2SO4, нейтр. по фенолфт., добавл. KCN (10% р-р) (до раств. ос.). Электролиз при 0,6 а/сЬи2, затем при 1 а!дм2. Электрод промыв, сп., эф. Высуш. при 100° С Cd
(NH4)2 нро, См. опр. Mg2+ CdNH4PO4 • Н2О или Cd2P 2O7
NH4SCN и пиридин См. опр. Zn2+ Cd (C5H5N)2. .(SCN)2
Опр. также в виде Cd(C9H6ON)2 или Cd(C9H6ON)2 • 2НгО (оксихинолинаты), Cd(CioH602N)2 (хинальдинат), Cd(C7H6O2N)2 (антранилат), Cd(C7H4NS2)2 (мер-каптобензтиазолат), CdS
Hg2+
H2S
(NH,)2 s
HCI (I) и H3PO3 (П)
SnCl2
KJO4, 4% p-p
Соль Рейнеке, нас. водн. р-р
Анал. р-р (кисл.), р-в. Ф. с. (промыв, р-ром H2S, сп., CS2). Высуш. при 105— 109° С
Анал. р-р (нейтр. Na2CO3), добавл. р-в, NaOH (10% р-р до осветления). Ф. б. или ф. с. Ф-т добавл. NH4NO3 (изб. 25% р-ра), кип. Ф. с. (промыв, р-ром H2S, Н2О, сп., CS2, сп., эф.). Высуш. при 105—109° С
Анал. р-р, p-вы. Ф. с. (промыв. Н2О). Высуш. при 100—105° С
Анал. р-р (НС1), р-в. Через 1 ч ф. с. (промыв. НС1, 1 : 1, Н2О, ацетоном). Высуш. при 20° С (в токе воздуха)
Анал. р-р (<0,5 г Hg), HNO3 (0,15 н.), H2SO4 (0,1 н.). Нагр. до 100° С, добавл. р-в. Ф. с. (промыв, гор. Н2О). Высуш. при 100° С
Анал. р-р (HNO3) нагр. до 60—70° С, добавл. р-в. Через 30 мин ф. б. (промыв. HNO3, 1:3). Прокал. при 1000° С
HgS
HgS
Hg2Cl2
Hg
Hg3 (JO3)2
Cr2O3 (/=1,319)
Опр. также в виде [Hg(C5H5N)2]Cr2O7
285
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (нон) Реактив Методика определения Весилая форма осадка
III группа периодической системы
ВОГ. СН3ОН Анал. р-р (нейтр.) упар., до- В2О3;
бавл. р-в(Юлл), отгоняют вычитаю! вес
В4О; Оп (при 80—90° С) (СН3О)3В в р-р (NH4)2CO3. добавл. (CH3COO)2Alg или (СН3СОО)2Са, выпар. Прокал. при 800—900° С р также в виде K[BF4] MgO или СаО *
АР nh4oh Анал. р-р, NH4C1, мет. кр. Нагр. до 100е С, добавл. р-в до желт. Ф. б. (промыв. 2% р-ром NH4C1). Прокал. при 1200° С А1„О3
NH3 (газ) Анал. р-р (рН = 3). Нагр. до 15° С, пропускают смесь р-ва с воздухом, ф. б. Прокал. при 1200° С А1,О3
(NH4)2HPO4 8-Окснхинолин Анал. р-р (НС1, 0,05%). Нагр. до 100" С, добавл. р-в, ацетатн. буф. (рН = = 5 ч-5,4). Фильтр, с бум. массой. Ф. б. (промыв. 5% р-ром NH4NO3), переос. Прокал. при 800—1100° С Анал. р-р (НС1). Нагр. до 70—80° С, добавл. ацетатн. буф. (рН = 7), р-в. Нагр. при 70—80° С I мин. Ф. с. (промыв. Н2О), высуш. при 110° С. Или ф. б., прокал. при 1200° С (под слоем Н9С2О4) А1РО4 Al (C9H6NO)3 A12O3
Опр. также осажд. А1С13-6Н2О (взвеш. А12О3)
Ga3+ NH4OH (пли пиридин) Анал. р-р (H2SO4). Нагр. до 100° С, добавл. р-в. Фильтр, с бум. массой. Ф. б. (промыв. 2% р-ром NH4NO3). Прокал. при 1000° С Оа2О3
Купферон, 6% р-р Айал, р-р (H2SO4, 14%) охл.' до 0° С, добавл. р-в. Фильтр, с бум. массой. Ф. б. (промыв. H2SO4+ + р-в). Прокал. при 1000° С Ga2O3
* Из веса остатка после прокаливания вычитают вес MgO или СаО, отвечающий количеству добавленного ацетата магния или кальция.
280
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
Ga3 + In3 r 8-Оксихинолип (или5,7-дибром-оксихинолин) NH4OH 8-Оксихинолин Анал. р-р (рН = 3,1), р-в. Ф. с. (промыв, гор. Н2О). Высуш. при 120° С Анал. р-р (HNO3; без С1“). Нагр. до 100° С, добавл. р-в. Фильтр, с бум. массой, ф. б. (промыв. 5% р-ром NH4NO3). Прокал. при 1200°С Анал. р-р (СН3СООН, рН = = Зч-4) нагр. до 70—80° С. Ф. с. (промыв. Н2О). Высуш. при 110—150° С Ga (C9HeON)3 1п2О3 In (C9HeON)3
Опр. также в виде 1п20з (осажд. ln2S3) пли In (осажд. при электролизе)
Т1+ К2СгО4 К3 [Fe (CN)6], 8% р-р KJ HJPtCl.l NaB (C6H5)4 Анал. р-р, NH4OH. Нагр. до 80° С, добавл. р-в. Ф. с. (промыв. 1% р-ром КгСгО4, 50% сп.). Прокал. при <745° С Анал. р-р, КОН (изб. 5% р-ра), р-в. Через 18 ч ф. с. (промыв, гор. Н2О). Высуш. при 200° С (в атм. СО2) Анал. р-р *, СНзСООН. Нагр. до 100° С, добавл. р-в. Через 12 ч ф. с. (промыв. KJ, СНзСООН, ацетоном). Высуш. при 120—130° С См. опр. К* См. опр. К+ Т12СгО4 Т12О3 T1J Tl2 [PtCle] Tl [(С6Н5)4 В]
Опр. также в виде TlJSnSJ, TI, T1HSO4 или T12SO4, Tl[Cr(SCN)4(NH3)2], NaTl2[Co(NO2)e] (/=0,5331), [Co(NH3)6]T1C15, T1(C7H4NS2) (меркаптобензтиазолат), T1SCH2CONHCioH? (тионалидат, /=0,4860)
Sc3 + Опр. в виде Sc(C9H6NO)3 ЯсгОз (осажд. NH4OH или орг. р-вами), CgHjNO (оксихинолииата). [Co(NH3)6][ScF6]
Y»+ La3 + и ланта- ниды NH4OH Н,С,О4 См. опр. La3+ Анал. р-р (НС1, 0,3 н.) ** нагр. до 60—80° С, добавл р-в (1 объем нас. р-ра). Ф. б. (промыв. 1% р-ром Н2С2О4). Прокал. при 700— 800° С У2О3 ЬагОз
“ При наличии Т13+ его восстанавливают ло Т1 "° действием 8О2.
*’ Дли маскировки Tl4 + , Та\ NtA добавляют Н2О2.
287
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
La3+ И лантаниды nh4oh Анал. р-р (содержащий NH4C1) нагр. до 100° С, добавл. р-в. Ф. б. (промыв. NH4NO3, NH4OH). Прокал. при 700—800° С Ьа2О3
Опр. также в виде La2(CO3)3 (осажд. щавелевой к-той)
Се3+ KJO3 + KBrO3 Н С,О4 NH4OH а) Анал. р-р (HNO3, 25%), КВгОз (0,5 a), KJO3 (10% в 36%-иой HNO3, 10—15-кратный изб.). Первое. Ф. с. (промыв. K'JO3, СП., эф.). Высуш. 10—15 мин при 40—50° С б) Осажд. как в п. «а». К ос. добавл. Н2С2О4, нагр., добавл. Н2О. Через 1—2 ч ф. б. (промыв. 1% р-ром Н2С2О4). Прокал. при 800° С См. опр. La3* См. опр. La3* 2Ce(JO3)4- KJO3- 8Н,О СеО2 СеО2
Опр. также в виде Ce(C9H6ON)3 (оксихинолинат)
IV группа периодической системы
CN- AgNO3 Анал. р-р (HNO3 очень разб.), р-в. Ф. с. Высуш. при 100° С AgCN
OCN" AgNO3 Анал. р-р (нейтр.), р в. Ф.с. Высуш. при 110е С AgOCN
SCN" AgNO3 Анал. р-р (HNO3 разб.), р-в. Ф. с. Высуш. при 115° С AgSCN
SiO|- HCI Анал. р-р, р-в, выпар, при 110—120° С, добавл. НС1 (разб.). Ф. б. (промыв. 1.5% р-ром НС1). Прокал. при 1000° С SiO2
OelV H2S (газ) (NH4)2MoO4 (I) и 8-оксихино-ЛИН (II) Анал. р-р (H2SO4, 6 н.), р-в (до нас.). Через 48 ч ф. б. (промыв, разб. H2SO4, нас. р-ром H2S), К ос. добавл.-NH4OH, Н2О2. Выпар. Прокал. при 900° С Анал. р-р (50 мл, ~0,03 мг GeO2), р-в I, H2SO4 (0,15 н.), р-в 11. Через 3— 12 ч ф. с. (промыв, разб. HCI+p-в). Высуш. при 110° С GeO2 (C9H7ON)4- H4GeMol2O40 (/ = 0,0311)
288
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (нон) Реактив Методика определения Весовая форма осадка
Geiv Mgso, Анал. р-р (слабокисл.), (NH4)2SO4 (2 н.), р-в, NH4OH (изб.). Нагр. до 100° С, охл. Через 12 ч ф. б. (промыв. 3% р-ром NH3). Прокал. при 1000— (100°С Mg2GeO4
Таннин Анал. р-р (300 мл 0,07 н. Н2С2О4), р-в (5%, 1 ил на 1 мг GeO2). Ф. б. (промыв. 5% р-ром NH4NO3). Прокал. при 900° С GeO2
Опр. также в виде (CioH22ON2)4 • GeMoi204o (осажд. цинхонином и молибдатом).
BajGeCeHeOu • 2И2О (осажд. винной к-той и (СН3СОО)2Ва)
Sniv NH4OH Анал. р р (HCI, NH4CI), р-в (по мет. кр.). Фильтр, с бум. массой. Ф. б. (промыв, гор. 2% р-ром NH4NO3). Прокал. при 900° С SnO2
Купферон, 6% р-р Анал. р-р (H2SO4 или НС1), Н3ВО3 (для маек. F~). Охл. до 0° С, добавл. р-в. Ф. б. (промыв. 1 % р-ром НС1). Прокал. при 900° С SnO2
Фениларсоновая кислота Анал. р-р (НС1, 1,5%), р-в. Нагр. Ф. б. (промыв. 4% р-ром NH4NO3). Прокал. при 900° С SnO2
(электролиз) Анал. р-р (25—200 мг Sn), Н2С2О4. Zn-анод, покрытый коллодием, Pt-катод. 1—3 ч (внутренний электролиз) Sn
Pb2+ H2SO4 (1:1) Анал. р р, р-в. Выпар, до появл. дыма (SO3), добавл. Н2О (до 8% H2SO4) Через 3—4 ч ф. с. (промыв. 6% H2SO4, нас. PbSO4), высуш. при 120—130° С. Или ф. б., прокал. при 300—600° С PbSO4
(NH4)2 МоО4 Анал. р-р (разб. HNO3). Нагр. до 100° С, добавл. р-в, нейтр. NH4OH, добавл. СНзСООН. Ф. с. (промыв. 2% р-ром NH4NO3). Прокал. при 600° С PbMoO4
(электролиз) Анал. р-р (HNO3, 10 объемн. %). Pt-чашка — анод (~ 3 а/дм2) при 70° С (электрод промыв. Н2О, сп.). Высуш. при 180° С PbO2
19 Зак. 7S3
289
ВЕСОВОЙ АНАЛИЗ
П родолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
РЬ2+ К2СгО4 или К2Сг2О7 K2SO4 Анал. р-р (HNO3, 0,3 н.) нагр. до 100° С, добавл. р-в (4-кратиый изб.). Ф. с., высуш. при 140° С. Или ф. б., прокал. при 550—600° С Анал. р-р, р-в (не <0,5 а/100 мл). Выдерж. 2—3 ч. Ф. с. (промыв. 0,03 М K2SO4). Высуш. при 130° С РЬСгО4 (/ = 0,637) K2SO4 • PbSO4 (/ = 0,4340)
Опр. также в виде PbS, РЬС12> PbOHSCN, Pb(C9H6ON)2 (оксихинолинат), Pb(C7H6O2N)2 (салицилальдоксимат), Pb(C7H4NS2)OH (меркаптобеизтиазолат), Pb(C7HcO2N)2 (антранилат), Pb(CioH7N405) • 1,5Н2О (пикринат)
TUV Купферон, 6% p-p Анал. р р (НС1 или H2SO4). Т1О2
Таннин, 10% p-p Охл. до 10° С, добавл. р-в. Ф. б. (промыв, хол. 1 % НС1 + р-в). Прокал. при 800—1000° С (осторожно) Анал. р-р (H2SO4, 6%), р-в тю2
(1) и антипирин * 20% р-р (II) 8-Оксихинолин, I, р-в II. Нагр. до 100° С, добавл. (NH4)2SO4. Ф. б. (промыв. H2SO4+p-B IK (NH4)2SO4). Прокал. при >650° С Анал. р-р (150 мл), винная ТЮ (C9H6ON)2
2% сп. р-р н-Оксифениларсо- к-та (1 a), CH3COONa (0,5 г), СНзСООН (лед.) (1,5 мл), р-в, нагр. до 60° С, затем при 100° С. Ф. с. (промыв, гор. Н2О). Высуш. при 110° С Анал. р-р, р-в (4% водн. Т1О2
новая кислота NH4OH или пи- р-р). Нагр. до 100° С. Ф. б. (промыв, р-вом, 0,5% в 0,25 н. к-те). Прокал. при 800—1000° С Анал. р-р, р-в (до рН=5-=-6). TiO2
Zr<+ ридин Опр. Купферон, 6% р-р Ф. б. Прокал. при 800— 1000°С также в виде Ti3(PO4)4 Анал. р-р (H2SO4, 20%); охл. ZrO2
до 10° С, добавл. р-в, фильтр, с бум. массой. Ф. б. (промыв. 3,5% р-ром HCI, охл. до 10° С). Прокал. при 1200°С
* 1-Феннл-2, З-диметилпиразолон-5-
290
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (нон) Реактив Методика определения Весовая форма осадка
Zr4+ H,SeO3,12,5% р-р Анал. р-р (НО, 1,5%) нагр. до 100° С, добавл. р-в, фильтр, с бум. массой. Ф. б. (промыв. НС1, 1% р-ром р-ва). Прокал. при 1200° С ZrO2
C6H5AsO (ОН)2, 10% р-р Анал. р-р (НС1 10%), Н2О2 (3% р-р), р-в (10—30 мл). Нагр. до 100°С (2 мин). Ф, б. (промыв. 1 % р-ром НС1, 0,1% р-ром р-ва). Прокал. при 1000° С ZrO2
(NH4)2 HAsO4 Анал. р-р (НС1), р-в (1%). Нагр. до 100° С, добавл. р-в. Ф. б. (промыв. 1 н. НС1, гор. Н2О). Прокал. при 1000°С ZrO2
(NH4)2 нро4, Анал. р-р (H2SO4, 10 обьемн. ZrP2O7
10% р-р %), Н2О2, р-в (10—100-кратный изб.). Нагр. до 50° С. Через 2—24 ч ф. б. (промыв. 5% р-ром NH4NOs). Переос. (из плава с Na2CO3). Прокал. при 1000° С (/ = 0,518)
Миндальная ки- Анал. р-р (НС1, 20%), р-в. vCcH,CHOHCOO),Zr
слота, 16% р-р Нагр. 25 мин при 85° С. Охл. Ф. с. (промыв. 2% НС1 + р-в; сп.). Высуш. при ПО—120° С (/ = 0,1772)
Опр. также в виде Zr(CgHeON)4 (оксихинолинат), Zr2PcO|9 (фитинат).
HF+ 2Zr(JO3)4- КЮз-8Н2О, Zr(SeO3)2 или 4ZrO • 3SeO2 18НгО См. опр. Zr4+
Th4+ Н2С2О4 Анал. р-р (НС1, 1,4%) нагр. до 100° С, добавл. кип. р-в (10% р-р). Выдерж. 10— 12 ч. Ф. б. (промыв. 2,5% р-ром р-ва, 1,2% р-ром НС1). Прокал. при 750° С ThO2
Уротропин 100 мл анал. р-ра (слабокисл.), NH4C1 (5 г). Нагр. до 30° С, добавл. р-в (рН= = 5,8). Ф. б. (промыв, тепл. 2% р-ром NH4NO3), переос. Прокал. при 750° С ThO2
Себациновая кислота Анал. р-р нейтр. при 100° С, добавл. р-в. Ф. б. (промыв, гор. Н2О). Прокал. при 750° С ThO2
Опр. также в виде ThO2 (после осажд. NH4OH, купфероном или H2O2), в виде
4Th(JO3)4- КЮз-18Н2О, Th(CioH7N4Os)4 • Н2О (пиколинат), Th(C6H5SO2)4 (бен-золсульфинат), Th(PO3)4 (осажд. фитином)
19»
291
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
V группа периодической системы
NH+ H2PtCl6
См. опр. К*
NO" Нитрон
Анал. р-р (H2SO4 или СН3СООН) нагр. до 100° С, добавл. р-в. Через 30 мин охл до 0° С. Ф. с. (промыв. хол. Н2О). Высуш. при 105е С
(NH4)2 PtCl6 (4< = °-08094 или Pt (4н-=0-1839) C20H16N4 • HNO3 (f = 0,1679\ I No3- )
Опр. также в виде (CioH7CH2)2NH • HNO3 после осажд.
(^о-=°’1721)
динафтодиметиламином
РО®“ 4 Магнезиальная смесь (стр. 22) Айал, р-р (для маек. Fes* добавл. лимоннокислый ам- Mg2P2O7
О (NH4)2 МоО4 ip. также в виде моний), р-в, NH4OH (25% NH3). Выдерж. несколько часов. Ф. б. (промыв, хол. 1,5% р-ром NH4OH). Прокал. при 900—1000° С а) Анал. р-р (>0,05 мг Р), NH4NO3 (5—10% ppi, HNO3 (5—10 объемн. %). Harp, до 40—50° С, добавл. р в (20-кратный изб.). Через 30 мин ф. с. (промыв. 5% р-ром NH4NO3). Прокал при 500—550° С Высуш. при 105° С Высуш. при 180° С б) Ос., полученный как в п. «а», раств. в NH4OH (10% NH3), добавл. НС1 и опр. по методу с магнезиальной смесью (см. выше) РЬМоО4, H7[P(Mo207)6]-(С9Н7С НРО3 • 12МоО3 (NH4)3PO4. • 12МоО3 (/ = 0,01637) (NH4)3 РО4 12МоО3 (/ = 0,01654) Mg2P2O7 IN) • 2Н3О
292
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (нон) Реактив Методика определения Весовая форма осадка
НРО|-Н3РО2 Р2О- Опр. в виде Hg2CI2, Mg2P2O7 Опр. в виде Mg2P2O7 Опр. в виде Ag4P20e
Asin H2S (газ) Айал, р-р (НС1, 30%) нагр. до 15—20° С, пропускают р-в. Ф. с. (промыв. 24% НС1, нас. H2S, сп., CS2 сп.). Высуш. при 105—110° С As2S3
AsO3" Магнезиальная смесь (стр. 22) Анал. р-р охл., добавл. р-в. Ф. с. (промыв. 1 % р-ром NH3). Высуш. при 40° С (под вакуумом) Прокал. при 850° С MgNH.AsO, 6Н2О Mg2As2O7
H2S (газ) Анал. р-р (НС1, 10 н.) охл. до 0° С, р-в (пропускают 60 мин). Через 1—2 ч ф.с. (промыв. 4 н. НС1, Н2О, сп.) Высуш. при 105—110°С As2S3
Опр. также в виде Ag3AsO4, Ag2T!AsO4, BaSO4 (после осажд. As2Ss)
Sb3+
H2S (газ)
Bi3+
Пирогаллол
(NH4)2 CO,
HCI (1:9)
а) Анал. р-р (HCI, 9%, гор.), р-в (до черн.), H2O (1 объем), р-в. Ф. с. (промыв. НгО, сп.). Высуш. при 170—290° С (в атм. СОг)
б) Осажд. Sb2S3 (см. выше) как в методе «а». Высуш. при 100° С, раств. в (NH4)2S. Ф. б. Ф-т упар., добавл. осторожно конц. HNO3, затем нагр.; разб. НгО, добавл. NH4OH. Упар. до удаления SO3. Прокал. при 800—850° С
Анал. р-р, винная к-та, р-в. Ф. с. (промыв. НгО). Высуш. при 100—105° С
Анал. р-р нагр. до 100° С, добавл. р-в, NH4OH. Ф. б. (промыв, гор. Ч2О). Прокал. при 1000°С
Анал. р-р (<5 мг Bi), NH4OH (до помутнения), р-в, Н2О (гор ). Нагр. 2 ч при 100° С. Ф. б. (промыв, гор. НгО, сп.). Высуш. при 100° С
Sb2S3
Sb2O4
SbO (СбН6О3)
Bi2O3
ВЮС1
293
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
В13+ (NH4)2HPO4, 10 % р-р в HNO3(1 :9) Анал. р-р (<250 мг Bi), NH4OH (до помутнения), р-в, нагр. до 80° С. Через 30 мин ф. б. или ф. с. (промыв. 2% р-ром NH4NO3). Прокал. при 800° С BiPO4
КВгО3 + КВг Анал. р-р нагр. до 100° С, добавл. р-в, переос. Ф. с. Высуш. при 110—120° С BiOBr (/ = 0,6894)
(электролиз) Айал, р-р, Fe-анод, коллоидная диафрагма, Pt-катод, 40—50 мин (внутренний электролиз) Bi
Опр. также в виде Bi2O3 (после осажд. купфероном, меркаптобензтназолом, Bi2S3, BiOBr, BiOJ, (BiO)2Cr2O?, Bi (осажд. восстановителями), BiC6H3O3 (осажд. пирогаллолом), Bi(C9H6ON)3 или Bi(C9H6ON)3 • Н2О (оксихинолинат), HB1J4 • C9H7ON, Bi (C12H10ONS)3 • Н2О (тионалидат), Bi[Cr(SCN)6], Со(С2Н4) (NH2)2 • BiJ4(SCN)2
VO-, Купферон, 6% р-р Анал. р-р (H2SO4, 20%) охл. до 10° С, добавл. р-в. Ф. б. (промыв. 1% р-ром H2SO4, р-вом). Прокал. при <658° С v2o5
VO3+ Hg2 (NO3)2
Анал. р-р, р-в. Ф. б. Прокал. при <658° С V2o6
NH4C1, нас. р-р Анал. р7р (конц.), р-в. Ф. б. Прокал. при <658° С V2O5
Опр. также в виде V2O5 (после осажд. таннином), Ag3VO4, V2O3(C9H6ON)4 (оксихинолинат), PbSO4 (через ванадат), 4СоО 9V20s, Ba2V2O?
Nbv, Tav
Таннин, 10% р-р
Окислы Nb или Та (0,25 г), KHSO4 (10 г) сплавл., раств. при нагр. в смеси Н2С2О4 (нас. р-р)+НС1 (конц.)+Н20 (3:1:10).
Ф-т, NH4C1, тартрат-ион, Na-ЭДТА, нейтр. нас. NH4CI до рН=5-т-6, добавл. р-в. Кип. 2 мин. Через 30 мин' ф. б. (промыв. NH4Cl, Na-ЭДТА). Прокал. при 900° С
Та2О5, Nb2O5
294
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
Nbv, Tav NaH2P2O2 (I) и таннин, 10% Р-Р (П) Окислы Nb и Та, K2S2C>7, сплавл., раств. в (NH4)2C2O4, добавл. NH4C1, р-в I. Нагр. до 100° С, добавл. HCI (25% р-р). Фильтр, с бум. массой. Ос. промыв, гор. Н2О, раств. в Н2С2О4 (6% р-р), добавл. р-в п, nh4oh, nh4ci, нагр. несколько минут. Ф. б. (промыв. NH4C1). Пересе. Прокал. при 900° С Та2О5
NaH2P2O2 (I) и таннин, 10% р-р (П) Фениларсоновая кислота, 3% р-р Ф-т от Та2О5, добавл. р-в II, NH4OH, нагр. несколько минут. Ф. б. (промыв. NH4C1). Прокал. при 900° С Анал. р-р (после сплавл. с K2S2O7 и раств. в винной к-те), НС1, нагр., добавл. р-в. Фильтр, с бум. массой. Ф. б. (промыв. NH4NO3). Прокал. при 1000° С Nb2O6 Ta2Os, Nb2O5
Опр. также в виде Ta>Os, Nb2Os (после осажд. купфероном), Nbv опр. в виде Nb2O5 (после осажд. 8-оксихинолином или H2SeOs)
VI группа периодической системы
so|~, s2ol-,s2-
Опр. в виде BaSO4 или PbSO4
SO24- BaCl2 См. опр. Ba2+. Прокал. при BaSO4
SeOl~ (CH3COO)2 Pb N2H4.HCI, 25% 780° C См. onp. Pb2+ Анал. р-р (HCI, 5 h.), Р-В, PbSO4 Se
P-P SO2 (I) и HCI (конц.) (II) нагр. до 90°C. Через 4 ч ф. с. (промыв. Н2О, сп.). Высуш. при 110° С Анал. р-р, р-в II. Нагр. при 15—20° С. Нас. р-вом I. Ф. с. (промыв, конц. НС1. Н2О, сп., ацетоном). Высуш. при 120—130° С Se
Опр. также в виде Se (осажд. тетраэтилтиоурамиддисульфидом; Те не осажд.)
295
ВЕСОВОЙ АНАЛИЗ
П родолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
ТеО3~, SO2 (нас. р-р) (I) Ф-т от Se (см. выше), до- Те
ТеО2- и N2H4-2HC1, бавл. HCI (3 н.). Нагр. до
15% р-р (11) 100°С, добавл. p-вы 1 и II, кип. Ф. с. (промыв. Н2О, сп.). Высуш. при 105° С [(С6Н5)4 As]2 •
(СВН5)4 AsCl или Анал. р-р (HCI. 4—5 н. и
(С6Н5)4 РС1 H2SO4, 3 и.), р-в. Ф. с. (не мешает Se) • ТеС16 (/ = 0,1158) или [(С6Н5)4 Р]2 ТеС16
Сг3+ nh4oh См. опр. А13+. Прокал. при 1200° С (в атм. Н2) СГ2ОЗ
CrO2” ВаС12 См. опр. Ва2+. Высуш. при 60° С ВаСгО4
Hg2 (NO3)2 Анал. р-р, р-в. Ф. б. Прокал. при 1200° С (в атм. Н2) СГ2О3
Опр. также в виде РЬСгО4, Ag2CrO4, Hg2CrO4
МоО2- (СН3СОО)2 РЬ Анал. р-р (200 мл уксуснокислого р-ра, содержащего — 0,1 мг Mo), CH3COONH4. Нагр. до 100° С, добавл. р-в. Ф. б. (промыв. 2% р-ром NH4NO3). Прокал. при 600° С РЬМоО, (/ = 0,2615)
а-Бензоиноксим, 2% сп. р-р Анал. р-р (5—10% H2SO4), р-в. Охл. до 5—10° С. Ф. б. (промыв. 0,1% р-ром р-ва). Прокал. при 500—550° С МоО3
Опр. также в виде MoS3, MoS2, М0О3 (после осажд. 8-оксихинолином или
р-нафтохинолином), Hg2Mo04, Ag2MoO4, Mo02(C<)Hc,ON)2 ВаМоО4, CaMo04, [Cr(NH3)5Cl]MoS4 (оксихинолинат),
wo2- HNO3 (конц.) Анал. р-р (шел.), р-в упар., добавл. NH4NO3. Оставляют на ночь, добавл. Н2О. Ф. б. (промыв. 5% р-ром HNO3, 0,5% р-ром NH4NO3). К ос. добавл. NH4OH. Ф-т выпар. Прокал. при 800°'С wo3
Цинхонин, 5% р-р или ₽-нафто-хинолин, 3% Р-Р Анал. р-р (щел.), HNO3, р-в, нагр. Ф. б. (промыв, разб. р-ром HNO3). Ос. раств. в NH4OH, переос. Прокал. при 800° С WO3
296
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (иои) Реактив Методика определения Весовая форма осадка
WO|~ Таннин (I) и цинхонин, 5% р-р (II) или Р-нафтохино-лин, 3% р-р (II) 8-Оксихинолин, 4% сп. р-р Анал. р-р (щел.), NH4C1, натр, до 50° С, добавл. свежеприготовленный р в I, НС1, р-в И. Фильтр, с бум. массой. Ф. б. (промыв. NH4C1). Прокал. при 800° С Анал. р-р, СНзСООН, р в. Ф. с. (промыв, гор. НгО). Высуш. при 120° С wos WO2 (C9H6ON)2
Опр. также в виде WO3 поел золон-5 е осажд. Hg2(NO3)2 или 1-фени (антипирином), бензидином л-2, 3-диметилпира-
1Ю2 + NH4OH или пиридин 8-Оксихинолин, 3% в 4 М СНзСООН Анал. р-р (кисл.) нагр. до 100" С. добавл. р-в (помет, кр.). Фильтр, с бум. массой. Ф. с. (промыв 2% р-ром NH4NO3, гор. Н2О). Прокал. при 750—900° С Анал. р-р, ацетатн. буф. (рН=5<-9), Na-ЭДТА. Harp, до 100° С, добавл. р-в. Ф. с. (промыв, гор. Н2О). Высуш. при 105— 110° С и3ов UO2 (C9H6ON)2. •(C9H7ON)
Опр. также в виде (UO2)2P2O7, Na2U2O7, V2O5-2UO3 или в виде UsOe (после осажд. действием Н2О2, смесью Н2С2О4 и восстановителя, таннином, хинальдиновой к-той, оксихинолином)
VII г р у п п а периодической системы
F- Pb (NO3)2 Анал. p-p (нейтр. или шел.), PbCIF
бромфеноловый син., NaCl (10% р-р), Н2О (до 250 мл). нейтр., добавл. р-в, CH3COONa. Нагр. 30 мин, оставляют на 10—15 ч. Ф. с. (промыв, нас. PbCIF, Н2О). Высуш при 130— 140° С
CaCl2, 5% p-p Анал. р р ((рН>3, без NH4+, SiO’-, РО’"), р-в (15 м.г на 1 г F-), желатина. К ос. добавл. СНзСООН, выпар., добавл. Н2О (15—20 мл). Ф. б. (промыв. 1—2% р-ром NH4OH). Прокал. при 800° С СаР 2
Опр. также в виде CaSO4 (после осажд. CaF2), LaF3, (CeHshSnF, StF4 (по потере веса), TiF4
297
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
СГ AgNO3, 5% р-р Анал. р-р (HNOs, разб.), р-в. AgCl
сю3- Опр. также в Опр. в виде AgCl, Нагр. до 100° С. Ф. с. (промыв. 0,5% р-ром HNOs). Высуш. при 130—150° С виде Ag (восстановлением Ag C20H16N4-HClOg /осажд. нитрон Cl) ом; f =0,2103\
С1О4- ' с1из ) (С10Н7СН;,)2МН-НС1Оз/осажд. динафтодиметиламином; f _=0,2186'\ \ С1оз ) Опр. в виде AgCl, C20H|6N4-HClO4 /осажд. нитроном;/ =0,2409\
Вг" (C10H7CH2)2NH-H( AgNO3, 5% р-р >Ю4 (осажд. динафтодиметилами Анал. р-р, HNO3 (разб.), р-в. С1°4 J ном; /сю_=0,2510\ AgBr
Г AgNO3) 5% р-р Кип. Оставляют в темноте. Ф.с. (промыв, разб. HNO3). Высуш. при 130—150е С Анал. р-р, NH4OH, р-в, HNO3 AgJ
JO<T, JO4- PdCl2 Опр. (до 1%). Ф. с. (промыв. 1% р-ром HNO3). Высуш. при 130—150°С Анал. р-р (НС1, 1%), р-в. Выдерж. 1—2 суток при 20—30е С. Ф. с. (промыв. Н2О, сп.), высуш. при 90— 95° С Или ф. б., прокал. при 1000° С (в атм. Н2) также в виде T1J3, Ag Опр. в виде AgJ PdJ2 Pd
Mn2+ (NH4)2 hpo4 Айал, р-р (слабокисл.), р-в, нагр. до 90—95° С, добавл. NH4OH. Ф. б. (промыв.
хол. 10% р-ром NH4NO3). Прокал. при 1000° С. Ф. с. (промыв NH4OH, сп. эф.). Высуш. при 20° С Мп2Р2О7 MnNH4PO4 • Н,О
(NH4)2s Анал. р-р, р-в. К ос. добавл. H2SO4, выпар. Прокал. при 450-500° С MnSO4
Опр. также в виде MnS, Мп3О4 (осажд. NH4OH пли КСЮ3), 2Mn(C5H5N4) (SCN)g, MnSO4 (осажд. (NH4)2CO3 или C5HsN и NH4SCN)
298
весовой анализ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
ИеО4- Нитрон ацетат, 5% р-р в 3% СНзСООН Анал. р-р (СНзСООН, 0,03 н.), р-в, H2SO4 (разб.). Нагр. до 80° С, затем охл. до 0° С. Через 2 ч ф. с. (промыв. Н2О, нас. C2oHi6N4 • HReO4). Высуш. при 110° С C2oH16N4 • HReO4
(C6H6)4AsC1, 1% водн. р-р Анал. р-р (гор. 0,5 А1 по NaCI), р-в. Ф. с. (промыв, лед. Н2О). Высуш. при 110° С (C6Hs)4AsReO4
Опр. также в виде Re (осажд. электролизом или H2S с последующим восстановлением осадка водородом), TlReO4
VIII группа периодической системы
Fe2+
Fe3+
Опр. как Fe3* после окисл. Н2О2, Вг2, С12 или HNO3
NH4OH Анал. р-р нагр. до кип., добавл. р-в. Ф. б. (промыв. 1% р-ром NH4NO3, декантацией). Прокал. при 1000—1100° С Fe,O3
Уротропин, 1096 Р-Р Анал. р-р (слабокисл.), NH4C1, р-в. Нагр. до 100° С. Ф. б. (промыв гор. Н2О). Прокал. при 1000—1100° С Fe2O3
n2h4• Н2О Анал. р-р, NH4CI, р-в. Нагр. до 100° С. Ф. б. (промыв. 1 % р-ром NH4C1, 1 % р-ром р-ва, гор. Н2О). Прокал. при 1000—1100° С Fe2O3
Купферон, 6% р-р Анал. р-р (H2SO4) охл. до 10° С, добавл. р-в. Фильтр, (с бум. массой). Ф. б. (промыв. 3,5% р-ром НС1, 0,15% р-ром р-ва, NH4OH, Н2О). Прокал. при 1000— 1100°С Fe2O3
Опр. также в виде Fe2Os после осажд. 8-окспхинолином
299
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (нов) Реактив Методика определения Весовая форма осадка
[Fe (CN)e]4 — Опр. в виде AgCN
[Fe (CN),]S- Co2 + а-Нитрозо-f-нафтол Анал. р-р (уксуснокислый), р-в (7% в лед. СНзСООН). Нагр. до 100е С. Ф. с. (промыв. гор. 33% р-ром СНзСООН, гор. Н2О). Высуш. при 130°С Со (CioHgOjNls • •2Н2О
Пиридин 4-NH4SCN Анал. р-р (нейтр.), р-в. Ос. нагр. до 100° С. Ф. с. Высуш. при 20еС (под вакуумом) Со (С5Н5)4 • • N (SCN)2
KNOj Анал. р-р, СНзСООН и CHaCOONa (8—10% р-р), р-в (50% р-р, нейтр. СНзСООН). Через 24 ч ф. б. (промыв. Н2О, СНзСООН), переос. Высуш. при 105—110° С 2К3Со (NO2)6- ЗН2О (/ = 0,1657)
Опр. также в виде Со (осажд. электролизом, см. опр. Ni2+), CONH4PO4 • Н2О или С02Р2О7 (см. опр. Mg2+), COSO4 или СО3О4 (осажд. CoS), CoHg(SCN)4, Со(С9НбОН)2 • 2Н2О (оксихинолинат), Со (CiqH6ONO)3 (а-нитро-р-нафтолат)
Ni2+ Диметилгли-оксим, 1% СП. Р-Р Анал. р-р нагр. до 60—80° С, добавл. р-в, NH4OH. Ф. с. (промыв, хол. НгО). Высуш. при НО—120° С Ni (C4H7O2N2)2
Салицилальд-оксим Анал. р-р (нейтр.), р-в. Ф. с. (промыв, хол. Н2О). Высуш. при ПО—120е С Ni (C7H6O2N)2 (/ = 0,2031)
NH4SCN и пиридин Анал. р-р (нейтр.), р-вы. Нагр. до 100° С. Ф. с. Высуш. при 20° С (под вакуумом) [Ni (C6H6N)41 • • (SCN)2
(электролиз) Анал. р-р (H2SO4), (NH4)2SO4, NH4OH. Электролиз при 3—3,5 а!дм? (промыв. Н2О, сп.). Высуш. при 100— 105° С. Совместно опр. Си2+ и Со2+ Ni
Опр. также в виде Ni2P2O7, N1SO4 (осажд. NiS), Ni(Ci4HiiN2O2)2 (бензоинокси-мат), Ni(CsHeON)s• 2НаО (хинолинат), Ni(C2HsN4O2)a-2H20 (дициандиаминат)
300
ВЕСОВОЙ АНАЛИЗ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
Ru111- ,v NaHCO3> 5% р-р Тиогликоль- Р-аминонафта-лид H2S (газ) Анал. р-р (кисл.), р-в (нейтр. до pH=5 4-7 по бромкрезолпурпур.). Кип. 5 мин. Ф. б. (промыв. 2% р-ром (NH4)2SO4). Прокал. при 800° С (в атм. Н2) Анал. р-р (0,2—0,5 М Ru), р-в. Нагр. до 100° С. Ф. б. (промыв, гор. Н2О). Прокал. при 800° С (в атм. Н2) Анал. р-р (кисл.), р-в. Ф. б. Прокал. при 800° С (в атм. Н2) Ru Ru Ru
Rh»1 H2S (газ) Т иобарбитуровая кислота, 1,4% сп. р-р TiCl3, 20% р-р Анал. р-р (НС1), р-в. Ф. б. (промыв. 2,5% р-ром H2SO4, 1% р-ром НС1). Прокал. при 800° С (в атм. Н2) Анал. р-р (НС1), р-в. Ф. б. (промыв, гор. Н2О). Прокал. при 800° С (в атм. Н2) Анал. р-р (H2SO4), р-в. Ф. б. (промыв. 2% р-ром H2SO4). Прокал. при 800° С (в атм. Н2) Rh Rh Rh
Опр. также в виде Rh (осажд. 2-меркаптобензоксазолом)
Pd"
KJ
Диметилглиоксйм, 1% сп. р-р
Анал. р-р (нейтр. или HNO3), р-в, кип. (или выдерж.
24 ч без нагр.). Ф. с. (промыв. гор. Н2О). Прокал. при <365° С
Анал. р-р (НСГ) нагр., добавл. р-в. Через 1 ч ф. с. (промыв, гор. Н2О). Высуш. при <171°С
PdJ2
Pd (C4H7O2N2)2
Опр. также в виде Pd, Pd(CioHeON02)2 (а-нитро-Р-нафтолат), Pd(CioH6ONO)i (а-нитрозо-р-пафтолат)
301
весовой анализ
Продолжение
Определяемое вещество (ион) Реактив Методика определения Весовая форма осадка
Osiv NaHCO3, 5% р-р Тионалид, 0,5% СП. р-р Опр. так Анал. р-р (кисл.) нагр. до 100° С, добавл. р-в (до рН= l,5-j-6,3). Ф. с. (промыв. 1% р-ром NH4C1, сп.). Прокал. при 800е С (в атм. Н2) Анал. р-р (кисл.) нагр. до 100° С, добавл. р-в (медленно в течение 1 ч). Ф. с. (промыв. 0,6% р-ром НС1). Прокал. при 800° С (в атм. Н2) же в виде Os (осажд. H2S) Os Os
VI КВгОз, 1О°/о р-р Меркаптобенз-тиазол, 1 % сп. Р-Р NH4C1, 10% р-р Анал. р-р (слабокисл.), р-в. Нагр. до 100° С, добавл. NaHCO3 (до рН=6 по бромкрезолпурп.). Ф. б. (промыв. 1 % р-ром (NH4)2SO4). Прокал. при 600° С (в атм. Н2) Анал. р-р (СН3СООН и CH3COONH4), р-в. Нагр. до 100° С. Ф. б. (промыв. 2% р-ром СНзСООН, 2% р-ром CH3COONH4). Прокал. при 600° С (в атм. Н2) Анал. р-р (нагр.), р-в, КС1О3. Ф. б. (промыв. NH4C1). Прокал. при 600° С (в атм. Н2) Ir Ir Ir
ptIV H2S (газ) Тиофенол, 10% сп. р-р НСООН Анал. р-р (НС1, 0,3%). р-в. Ф. б. (промыв. 1% р-ром NH4C1), Прокал. при 900° С Анал. р-р, р-в. Нагр. до 100° С. Ф. б. /промыв. Н2О). Прокал. при 900° С Анал. р-р, CH3COONa, р-в. Нагр. до 100° С. Ф. б. (промыв. 1% р-ром NH4C1). Прокал. при 900° С Pt Pt Pt
Опр. также в виде PtSg, (NH^IPtCleJ (/=0,4402), I\2[PtCle] или Pt (после осажд. в виде (NH4)2[PIC16])
302
Объемный анализ
Раздел состоит из двух таблиц: «Рабочие (титрованные) растворы» и «Методы определения неорганических веществ». Таблицы охватывают важнейшие неорганические вещества (ионы), определяемые методами объемного анализа, и рабочие растворы, имеющие наибольшее применение.
Сведения о приготовлении растворов, применяемых в объемном анализе, см. стр. 17.
Количества в концентрации реактивов, приводимые при описании методики определения, относятся к количеству 0,1 н. рабочего раствора, равному 20—30 мл. В случае работы с другими количествами или концентрациями рабочего раствора (например, при пользовании микробюреткой) количества веществ соответственно изменяются.
Количества и концентрации индикаторов в большинстве случаев не указаны: характеристики индикаторов приведены в таблицах на стр. 352 и сл. Если титрование проводится с крахмалом, то последний добавляют в конце титрования в количестве 2 мл 0,5% раствора.
Количество определяемого вещества вычисляется в случае прямого титрования по формуле
Q = VN9
а в случае обратного титрования по формуле
KVY^nV2}3
где О — количество определяемого титруемого вещества, мг;
N — нормальность рабочего раствора, мг-экв]мл;
V — объем рабочего раствора при прямом титровании, мл;
Г1 — объем первого рабочего раствора, приливаемого в избытке, при методе обратного титрования, мл;
V2 — объем второго рабочего раствора при оттитровывании остатка первого, мл;
jVi— нормальность первого рабочего рвствора;
Л;2 — » второго » »
п — отношение объема первого раствора к объему второго при титровании (определяемое предварительно);
Э — эквивалентный вес определяемого вещества, равный молекулярному весу вещества, деленному на приведенное в таблицах значение М/Э.
Концентрация анализируемого раствора при прямом титровании его рабочим раствором вычисляется по формуле
V
где /Vх — нормальность анализируемого раствора;
V' — объем анализируемого раствора.
Приведенными формулами (после преобразования) пользуются также для вычисления концентрации рабочего раствора (N илн М) по данным титрования навески стандартного вещества (Q мг) или измеренного объема другого рабочего раствора и его концентрации (!' и N'}.
Часто вместо нормальности раствора вычисляют коэффициент поправки К, равный отношению ' действительной нормальности данного раствора к точно округленной концентра-TV
ции, например, для 0,1 н. раствора К = ~q'|Qqq •
Иногда концентрацию рабочего раствора обозначают не через нормальность, а через титр ТЛ (весовое количество растворенного вещества а в 1 мл раствора) илн через титр по определяемому веществу Т а]д (весовое количество определяемого вещества q, эквивалентное 1 лы раствора а}. В этих случаях в приведенные выше формулы вместо произ-ведения N9 следует подставить, соответственно, ? или ? a!q (где ?a!q выражены
в .и г/мл).
Более подробные сведения см.: 1. И. М. Кольт го ф. В. А. Стенгер, Объемный анализ, перев. с англ., Госхимиздат, т. I, 1950; т. II, 1952. — 2. И. М. К о л ь т г о ф, Р. Белчер. В. А. Стенгер, Дж. Матс у ом а. Объемный анализ, перев. с англ., т. Ill, Госхимиздат, 1960. — 3. Р. Пршибил, Комплексоны в химическом анализе, перев. с чешек.. 2-е нзд., ИЛ, 1960. — 4. A. Berka, I. V u 1 t е г i п, J. Z у k a, Massanalytische Oxydations- und Reduktionsmeloden, перев. с I-го чешек, изд., Лейпциг, 1954.
Принятые сокращения
антр. — антраниловая б в. — безводным
Сромкрезол. — бромкрезоловый в-во — вещество ьариамин. — вариамнновый Дифенилам. — дифениламин а«’кр — закрывают, закрытый
Остальные сокращения см. стр. 16.
крахм. — крахмал.
метилен. — метиленовый
проп. — пропускают
рассч. — рассчитывают ст. — стандартный
фенилантр. — фенилантраниловая
303
РАБОЧИЕ (ТИТРОБАННЫЕ) РАСТВОРЫ
В первой графе таблицы приводится формула вещества, а также отношение его молекулярного веса (Л4) к эквивалентному весу (Э). Во второй графе указано стандартное вещество, с помощью которого точно устанавливается концентрация рабочего раствора. При этом, если стандартное вещество применяется в виде навески, то указан его эквивалентный вес. а если оно применяется в виде раствора, то указана концентрация этого раствора. Если вещество перед взвешиванием должно быть подвергнуто высушиванию, то приведена температура высушивания. В третьей графе описана методика определения концентрации рабочего раствора. Вначале указаны реактивы, последовательно добавляемые к пробе; между их названиями поставлены запятые; если же добавляется смесь, то стоит союз «н». Количество реактива и его концентрация указаны в скобках после названия реактива. Навески стандартных веществ и объемы рабочих растворов должны измеряться с от-
носительной погрешностью, не превышающей 0.1 0.2%. В четвертой графе указаны вещества (ионы), определяемые с помощью данного рабочего раствора. Вещества, определяемые при этом косвенным методом (с предварительным осаждением и др.) приведены в скобках. Па основании данных четвертой графы можно также судить о веществах, мешающих открытию данного вещества.
Таблица состоит нз четырех частей в соответствии с основными методами объемного анализа: нейтрализации, осаждения, комплексообразования, окисления-восстановления. В каждой части рабочие растворы расположены в алфавитном порядке.
Методы приготовления рабочих (титрованных) растворов приведены на стр. 17. Рабочие растворы могут быть также приготовлены из фиксаналов. В этом случае не требуется определения концентрации рабочего раствора.
Рабочий раствор
Определение концентрации рабочего раствора
стандартное вещество
методика определения
Вещества, определяемые рабочим раствором
I. Растворы для метода нейтрализации
НС1 (Л1/Э= 1) Na2B4O?* 10Н2О (3=190,7)
Na2CO3 (150° С, 3 = 53,00) N a2S2O3, 0,1 н.
Na2C2O4 (3=67,00)
NaOH, 0,1 н.
H„SO4 (М/Э —2) NaOH (М/Э = 1) Аналогично НС1 НС1, 0,1 н.
(СН2СООН)2 (100° С, 3=59,04)
Ст. в-во (0,4 г) раств. при нагр. в НгО (55 мл), охл. Титр, с мет. ор. до ор.
Ст. в-во (~(), 1 г) раств. в Н2О (25 мл). Титр, с мет. ор. до ор.
Рабочий р-р (10 мл), КЛОз (-0,1 г), KJ (2 г). Титр, с крахи, до бц.
Ст. в-во (0,12 г) прокал., раств. Титр, с мет. ор. до ор.
Р-р ст. в-ва (20 мл). Титр, с мет. ор. до ор. или с фенолфт. до бц.
Сильные и слабые основания, СО| > POJ-, НРО*-, В4О2- (Mg24 • Al3+, La3+, SiO2~, К+. Na+, NH + , NO3~, Bi3+, Nbv, Tav, F")
20 Зак. 783
(NH2SO3H (100° C, 3 = 97,00)
Аналогично NaOH
AgNO3 (М/Э = 1)
[1. Рас
NaCI (120е С, 3 = 58,44)
Hg2 (NO3)2 (М/Э = 2)
К4 [Fe (CN)6], 0,05 М (М/Э = 3)
NH4SCN
(М/Э = 1)
NaCI (120° С, 3=58.44)
Zn * (3 = 32,69)
КМпО4, 0,1 н.
AgNO3, 0,1 н.
Р-р ст. в-ва (20 мл). Титр, с мет. ор. до желт, или с фенолфт. до роз.
Ст. в-во (0,12 г) раств. р Н2О (30 мл). Титр, с фенолфт. до роз.
Ст. b-bo (~0,l г) раств. в H2O (30 мл). Титр, с мет. ор. до желт.
творы для метода осажден
1. Ст. в-во (~0,1 г) раств. в Н2О (25 мл). Титр, с К2СгО4 (1 мл 5% р-ра) до кр. ос.
2. Ст. в во (~0,1 г) раств. в Н2О (60 мл), добавл. HNO3 (8 мл 25% р-ра), FeNH4(SO4)2 (6 мл 1% ppa в 2,5% р-ре HNO3), рабочий р-р (25 мл). Титр 0,1 н. NH4SCN до роз.
3. Ст. в-во (0,1 г) раств. в Н2О (25 мл). Титр, с флюоресцеином (4 капли 0,2% сп. р-ра) до роз.
Ст. в-во (0,1 г) раств. в Н2О (20 -ял), добавл. HNO3 (10 мл р-ра 1 : 10). Тнтр. с дифенилкар-базоном (5 капель 1 % сп. р-ра) до темно-гол. (инд. добавл. в конце титр.)
Ст. в-во (0,12 г), H2SO4 (10 мл р-ра 1 : 1), Н2О (до 25 мл), (NH4)2SO4 (2 г), K3[Fe(CN)6] (2 капли 1% р-ра). Титр, при 60° С с дифенилам. (1 каплю 1 % в конц. H2SO4) до з.-желт. окраски, сохраняющейся 20 сек.
Рабочий р-р (40 мл), Н2О (150лл), H2SO4 (20 мл р-ра 1:4). Титр, р-ром ст. в-ва до кор.
Р-р ст. в-ва (20 лы), HNO3 (8 мл 25% р ра). Титр, с Fe3+ до роз.
Сильные и слабые кислоты, Ве2+, Mg2+, Gelv, NH+, Pb2+(Na+, K+, HPO2-,SO2 , MoO2-, wo2-, S>O|-)
и я
CN~, SCN-, СГ, Br-, J • HPOf (К + , Rb+, Cs+, Zn’\ Cd2+, Pb2+,S2~, F-.C1O-, Co2+)
СГ,Вг-,ВгО-,ВгО-, J2,Fe3+,Cu2+, Ce4+, MnO;, [Fe (CN)6]3“ (s2o2-, vv, сю-, cio-, h2o2, Hg2’, N2H4, Asin, Crin, CrVi)
Zn2+, Cd2+, Ga3+, ln3+, Fe3+ (Pb2+)
Ag+, Hg2+(Cu2+, НРС2", AsO®-. Se)
* Вместо Zn и H;SO( можно брать соответствующее количество рабочего раствора ZnSO4.
ОБЪЕМНЫЙ АНАЛИЗ/ (И РАБОЧИЕ РАСТВОРЫ
G5 О Г Продолжение
Рабочий раствор Определение концентрации рабочего раствора Вещества, определяемые рабочим раствором
стандартное вещество методика определения
NaBr (М/Э=1) — Рассч. по навеске и по объему р-ра Ag+
NaCl (Л4/Э=1) — То же Ag + , Hg2+
III. Растворы для метода комплексообразования
Hg (NO3)2 (М/Э = 2) NaCl (120° С, 3 = 58.44) NH4SCN, 0,1 н. Ст. в-во (0,1 г) раств. в Н2О (20 лл). Титр, с Na2[Fe(NO) (CN)s] (0,3 мл 10% р-ра) до появления мути или с дифенилкарбазоном (5 капель 2% сп. р-ра) до син. Рабочий р-р (20 мл). Титр, р-ром ст. в-ва с Fe3+ до кр. CN", SCN", Cl", Br", J"
KCN (М/Э = 1/2) AgNO3, 0,1 н. Рабочий р-р (20 мл), NH4OH (1 мл 6 н.), KJ (~50 мг). Титр, р-ром ст. в-ва до помутнения Cu2+, Co2 + , Ni2+
Na-ЭДТА (М/Э = 2) ZnCl2, 0,1 н. (стр. 25) СаС12, 0,1 н. (стр. 21) Р-р ст. в-ва (20 мл), мет. кр. Нейтр. до желт. Добавл. аммиаки. буф. (2 мл р-ра, рН = = 9,7*), Н2О (до 100 мл). Титр, с хромоген, черн. до син. а) Р-р ст. в-ва (20 мл), Н2О (до 100 мл), NaOH (3 мл 2% р-ра) мурексид до роз. Титр, до фиол. б) Р-р ст. в-ва (20 мл) нейтр. NH4OH по мет. кр. Добавл. аммиачн. буф. (2 мл р-ра рН = = 9,7*), хромоген, черн., Mg-ЭДТА (1 мл 0,1 н.), Н2О (до 100 мл). Титр, до син. Cu2+, Mg2+, Ca2+, Sr2+, Ba2+, Zn2+, Cd2+, Al3+, Sc3+, La3+, Ce3+, Ga3+, ln3+, Tl3+, Ti4+, Zr4+, Hf4+, Th4+, Sn4+, Pb2+, Bi3+, Cr3+, UO2+, Mn2+, Fe2+, Fe3+, Co2+, Ni2+, Pdlv(Na+, K+, Rb+. Cs+, T1+,CN",HPO2", Vv,Movl)
KJ 0 * ZnSO4 (М/Э=2) FeNH4(SO4)2, 0,1 н. Na-ЭДТА, 0.1 н. Р-р ст. в-ва (20 мл), конго кр., CH4COONH4 до бур. окраски, Н2О (25 мл), (NH4)2S2O4 (0,1 а). Нагр. до 60е С. Титр, с сульфосалициловой к-той до исчезновения роз. Рабочий р-р (25 мл) нейтр. NH4OH (25% NH3) по мет. кр. Добавл. аммначн. буф. (2 мл р-ра рН = = 9,7*), Н2О (до 100 мл). Титр, с хромоген, черн. до син. [Fe (CN)e]‘-
IV. Растворы д ля метода окисления-восстановления
Аскорбиновая кислота 0,1 н. (М/Э = 2) FeNH4(SO4)2, 0,1 н. J2, 0,1 н. Р-р ст. в-ва (20 мл), Н2О (25 мл). Нейтр. NH4OH (1:1) до мути, которую раств. в НС1 (несколько капель). Нагр. (45° С). Добавл. NH4SCN (10 мл 10% р-ра). Титр, до бц. Р-р ст. в-ва (20 мл) титр, с крахи, до бц. Ag+, Au3+, Cu2+, Hg2+, CIO", BrO", JO", Cr2O2", VO3 , BrO", H2O2, S2O2", MnO", Fe3+, PtIV, Iriv, SeIV, [Fe (CN)6]3~ (Zn2+, Pb2+, Sn2 b, [Fe (CN)6]4", Cl", Br", J")
Вг2, р-р в лед. СН3СООН или в 20% р-ре НС1 (М/Э = 2) Na2S2O3, 0,1 н. NaAsO2, 0,05 М Рабочий р-р (20 мл), KJ (1—2 г). Титр, р-ром ст. в-ва с крахи, до бц. Р-р ст. в-ва (20 мл). Титр, с инди- См. вещества, определяемые р-ром Са(С1О)2
гокармином до бц.
Са(С1О)2 (М/Э = 4) или NaClO (М/Э =2) Na2S2O3, 0,1 н. NaAsO2, 0,1 н. Рабочий р-р (20 мл), KJ (1 г), H2SO4 (5 мл 6 н.). Титр, с крахм. до бц. Р-р ст. в-ва (20 мл), КВг (1 г), NaHCO3 (0,5 г). Титр, с мет. ор. до бц. (бл.-желт.-з.^ Hg2+, Tl + , NH+, NO", (CH2)6N4, SCN", Sn2+, HPO|", AsO",Sb3+, H2O2, S2", SO2", S2O?", SeO2" J", Br", Fe2+, N2H4
* 54 г NH4CI и 350 жл 25% р-ра NH3 разбавить до 1 л.
рабочие растворы
Продолжение
оо Рабочий раствор Определение концентрации рабочего раствора Вещества, определяемые рабочим
стандартное вещество методика определения раствором
Се (SO4)2 или Ce(NO3)4 (М/Э=1) Na2C2O4 (240° С, 3 = 67,00) Na2S2O3, 0,1 н. As/)a (3= 49,46) Ст. в-во (0,13 г) раств. в Н2О (30 лл), добавл. НС1 (10 мл конц. к-ты), JC1 (5 мл 0,1 и.), Н2О (до 100 мл). Нагр. до 50°С. Титр, с ферроином (2 капли 2% р-ра) до гол. Рабочий р-р (20 мл), H2SO4 (10.ил р-ра 1:9), Na2CO3 (0,5 г), KJ (3 г). Через 10 мин титр, с крахм. до бц. Ст. в-во (0,1 г) раств. в NaOH (7 мл 1 н.), добавл. H2SO4 (30 мл 1 н.), OsO4 (3 капли 0,25% р-ра в 0,1 н. H5SO4). Титр, с ферроином до исчезновения кр. « + ’ 4. " к - / |? Z-. те те сч у, •* Й ь О SU," а> н х - <» О 1 . 1 „ < 4> + к СЧ СЧ z - +-и^о -о" - "о =.<> сч О- Ч- J) W . . 1 ы х О 1 + %,’ со 1 <£> tuo Q + х" Z "г- “с О Еч . О - " о Т о + i ж X, 01 «г г, W -С + 'z х d н н
FeNH, (SO4)2 (Л*/Э=1) Na2S2O3, 0,1 и. Рабочий р-р (20 мл), KJ (5 г), H2SO4 (5 мл р-ра 1 :3). Выдерж. 5 мин в темноте; титр, с крахм. до бц. ТР+, Sn2+, U4+, Cu+, Molli, MoV, WIn, Nb111, V11 (TI44, Movl, WVI. Nbv)
Соль Мора (или FeSO4) (М/Э = 1) КМпО<, 0,1 и. К2Сг2О7, 0,1 и. Рабочий р-р (20 лл), Н3РО4 (Змл). Титр, до роз. (не исчезающей 30 сек ) Рабочий р-р (20 мл), Н2О (до 200 мл), H2SO4 (10 мл конц. р-ра). Титр. ст. в-вом с фенил-антр. к-той (3 капли 0,33% р-ра) до кр.-фиол. Ce44, NO", VO", S2O82-, Cr2O*-, C1O-, BrO", CIO", MnO2, MnO", Rh44, PdIV (Zn24, Cd24, Hg2’. Ce34, SO2-, Cr34, Mn24, Co2’, Rha+, Ptlv) О 01 СГ* ги X s: S
Фишера реактив Н2О К обезвоженному СН3ОН* (10 мл) добавл. рабочий р р (по каплям) до бур., ст. в-во (0,1 г). Титр. H2O, органические вещества, реагирующие с выделением Н2О; SO3 в олеуме X Li X w
Гидрохинон, 0,1 н. (М/Э =2) К2Сг2О7, 0,1 н. в 20%-ной H2SO4 Рабочий р-р (20 мл). Титр, р-ром ст. в-ва с дифенилам, до син. Au34, J2, Br2, С12, СЮ-, Irlv, Cr2O2". Се44, Cu24, Ag4, Мп111, w 0
Н2О2 (44/3=2) (3 = 49,03) КМпО4, 0,1 н. Рабочий р-р (20 мл), Н2О (100мл), 52ОГ (NaN3) Се44, Sn24, [Fe(CN)e]3-, AsO|", X s ГВ 0 n
Hg2 (NO3)2, 0,1 и. Na2S2O3, 0,1 н. FeNH4(SO4)2, 0,1 н. H2SO4 (20 мл 2 н.). Титр, р-ром КМпО4 до роз. Рабочий р-р (20 мл), H2SO4 (10мл 4н.), KJ (6мл 1 н.), (NH4)2MoO4 (3 капли 1 н.). Титр, р-ром ст. в-ва с крахм. до бц. Р-р ст. в-ва (20 мл), Н2О (200 мл). СЮ", BrO", JO" Аи34, SCN", Fe34, Ce4+,Br2, BrO", 03 0 0 E
(44/3 = 2) J2 (М/Э =2) Na2S2O3, 0,1 н. HNO3 (10 мл р-ра 1 : 1), NH4SCN (10 мл 50% р-ра). Титр, до бц. Рабочий р-р (20 мл). Титр, р-ром BrO", [Fe(CN)6]4", Mn24 J , MoO2", Cu24, MnO4", S2O2", VO2+, Cr2O2", CIO", H2O2 (N2H4, AsO3", Cr34) Hg24, Hg24, Eu24, Sn24, CS2, тио-
As2O3 (3 = 49,46) ст. в-ва с крахм. до бц. Ст. в-во (0,2 г) раств. в 1 н. р-ре NaOH (10 мл), H2SO4 (15 мл 1 н.), NaHCO3 (1 г в 50 мл Н2О). Титр, с крахм. до бц. налид, неон, N2H4, nh3, HPO|~, H3PO2, AsO|~, общий As-Sb34, VO|", H2O2, S2", so|-, S2O|", TeO|", Fe24, [Fe (CN),]4", Rh111 (Cu24, Ag4, Zn24, Cd24, Eu34, TI4, Sn44, Pb24, SCN", Bi34, SO2", Fe34)
8
* Обезвоживание
или окисью кальции
проводят метилатом натрия
Продолжение
oir
Рабочий раствор Определение концентрации рабочего раствора • Вещества, определяемые рабочим
стандартное вещество методика определения раствором
JC1 (М/Э = 2)
NaAsO2, 0,05 M
K4[Fe(CN)6] • ЗН2О (3 = 422,4) N2H4-H2SO4 (110° С, 3 = 32,53)
КВгО3 (44/3 = 6) Na2S2O3, 0,1 н.
КВгОз + КВг
K2Cr2O7 (M/Э = 6)
K3[Fe (CN)6], 0,0.54-1 (М/Э = I)
KJO3 (М/Э = 4)
KMnO4(44/3 = 5)
Na2S2O3, 0,1 н.
Na2S2O3, 0,1 h.
Na2S2O3, 0,1 h.
N2H4-H2SO4 (110°C,
3 = 32,53)
Na2C2O4 (105—120° C, Э = 67,00) *
H2C2O4 - 2H2O (3 = 63,03)
Na2S2O3, 0,1 h.
As2O3 (3 = 49,46)
* После кристаллизации и высушивания
а) Ст. в-во, NaHCO3. Титр, с крахи, до син.
б) Ст. в-во, CH3COONa (до рН = = 6,5 = 7,5). Титр, с СНС13 до фиол.
в) Ст. в-во, HCI (1—2,5 н.), HgCl2 (изб.). Титр, с СНС13 до фиол.
Ст. в-во, ацетатн. буф. (pH = 6,5 — 7,5). Нагр. до 40° С. Титр, с СНС1з до фиол.
Ст. в-во, ацетатн. буф. (pH=7). Титр, с крахи, до син. или с СНС13 до фнол.
Рассч. по навеске и объему р-ра Рабочий р-р (20 мл), KJ (2 а), НС1 (5 мл конц. р-ра), (NH4)2MoO4 (2 капли 3% р-ра). Титр. 4 р-ром ст. в-ва с крахм. до бц.
Рабочий р-р (20 мл), KJ (2 г), H2SO4 (10 мл р-ра 1:2). Через 10 мин титр, с крахм. до бц. Вычитают поправку на холостой опыт.
AsO|~, Sb3+, CN-, [Fe (CN)6]4-, N2H4(NH2OH, S2o23~, Fe2+)
Рассч. no навеске и объему р-ра
См. опр. конц. рабочего р-ра Na2S2O3 (стр. 313)
Рабочий р-р (30 мл), ZnSO4 (30 мл 10% р-ра), KJ (3 г). Через 10 мин титр, с крахм. до бц. (вносят поправку на холостое титр.; конц. проверяют каждую неделю)'.
Рассч. по навеске и объему р-ра Ст. в-во (0,065 г) раств. в Н2О (30 мл), добавл. НС1 (30 мл конц. к-ты). Выдерж. 10 мин в темноте, добавл. 5 мл СС14 (или СНС13). Титр, до бц. СС14 (или СНС13)
Ст. в-во (0,13 г) раств. в Н2О (50 мл), добавл. H2SO4 (10 мл р-ра ^1 : 1). Harp, до 80° С. Титр, до роз.
То же
KJ (1 г) раств. в Н2О (1 мл), добавл. H2SO4 (10 мл р-ра ~1:5), рабочий р-р (20 мл), Н2О (до 200 мл). Титр, с крахм. до бц.
Ст. в-во (0,1 г) раств. в NaOH (7 мл 4 н.), добавл. НС1 (15 мл 6 н.), Н2О (до 120 мл), KJO3 (1 каплю 0,0025 Af), NaCl (1 г). Титр, с ферроином до гол.
применяют без повторного высущиванрц.
T1+, Sn2+, С2О2-, NO“, SCN“, N2H4, NH2OH, HPO2-, AsO7, H PO Sb3 + ,H О SeO2-, Se, J-, Fe2+ (Hg2+, Sn4+, Bi3+, Cl-,
Ni2+)
(Через оксихинолинаты: Сц2+, Be2 ~ Mg2+, Ca2+,Zn2+,Cd2+, Al3+,La3~ Ce3+, Ga3+, Ti4+, 2г4л Th44\ GeIV, Pb2+, Bi3+, VO-, MoO2-’ WO2- UO2+, Mn2+, Fe3+, Co2+, Ni2+ (Na+); через антранилаты: Cu2+, Zn2+, Cd2+, Pb2+, Mn2 + Co2+, Ni2+)
Сц+, Sn2+, Pb2+, AsO|", SO|-, SeO|~, ТеО|-, U4+, Re3+, Re4+, Fe2+, [Fe (CN)6]4~ (Na+, Cu2+, Ba2+, Tl4+, UO2+, Rev", Fe3+, Co2+)
S2-, AsO|-, Sn2+, VO2+, N2H4, NH2OH (MoVi)
Tl + , Sn2+, SCN-, N2H4, AsO|+, Sb3+, S2-, SO2-,S2O|-, J2, BrO-, Fe2+ (Cu2+, Zn2+, Cd2+, Hg2+, Bi3+, MoO2-, Br-, J-, Fe3+)
Hg2+, Ce3+, Eu2+j T1+i Sn2+, Pb2+. c2o2-,no-, CN-, SCN-,NH2OH. N2H4, HN3, HPO2-, As1", Sb3+, VO2+, H2O2, S2-, SO|-, S2O2-, SeO|-, SeO2-, Se, TeO|-, Cr3+, U4+, Br-, J-, JO-, Mn2+, Ru11, Ru111, ReO-, Fe2+, [Fe(CN)6]4-(K+, Rb+, Cs+, Eu3+, Ti4+, PO3-, Bi3+, Vv, Nbv, MoVI, UVI, Fe3+, Co2+, Ni2+, Rein, Reiv, RuV, RuVI", Ir1", Pt", Ptlv; при титровании оксалатов: Ca24-, Sr2+, Zn2+, Cd2+, Hg2+, La3+, Ce3+, Th4+, Pb2+, Bi3+, Ni2+)
ОБЪЕМНЫЙ АНАЛИЗ. РАБОЧИЕ РАСТВОРЫ
со ГЗ _ ‘ _ _ продолжение
Рабочий раствор Определение концентрации рабочего раствора Вещества, определяемые рабочим раствором
стандартное вещество методика определения
КМпО4 (М/Э = 5) NaAsO2, 0,1 н. KJ (3=83,0) K4[Fe(CN)6]-3H2O (3 = 422,4) К 50 мл р-ра, содержащего 6 мл 11 н. НС1 и 1 г NaCI, добавл. р-р ст. в-ва (50 мл), JC1 (1 мл 0,0025 М). Титр, с ферроииом до гол. Ст. в-во (0,35 г) раств. (в атм. СО2) в Н2О (100 мл). Добавл. НС1 (70 мл конц. к-ты). Охл. Добавл. СС14 (5 мл). Титр, до бц. Ст. в-во (~ 1,0 г) раств. в H2SO4 (40 мл 0,4 н.). Титр, с ферроином до гол. См. стр. 311
NH4VO3 (М/Э = 1) Соль Мора (или FeSO4), 0,1 и. N2H4-H2SO4 (110° С, 3 = 32,53) Р-р ст. в-ва (20 мл), 50 мл смеси кислот (300 мл Н2О, 100 мл конц. H2SO4, 100 мл конц. НзРО4). Титр, с фенилантр. к-той до син,-фиол. или с дифенилам, до кр.-фиол. Ст. в-во (0,065 г) раств. в Н2О (20 лл), добавл. рабочий р-р (25 мл). Нагр. до 70°С. Титр. 0,1 н. р-ром Fe(NH4)2SO4 с фенилантр. к-той до исчезновения кр. (отдельно опр. объемное соотношение р-ров Fe(NH4)2SO4 и рабочего р-ра) Hg2+, Т1+, Tis+, n2h4, н3ро2, vs+, AsO|-, SCN~, S2-, S2O2-, SO2’, U4+, J-, Fe2+ (Na+, Cu2+ , Zn2+, Pb2+, MoO2-, WO2-, UO2+, Mn2+, Co2+, Ni2-1-, Fe3+) 2
N2H4 • Н 2SO4, 0,1 н.(Л4/3 = 4) — Рассч. по навеске и объему р-ра J2, BrO”, Br2, СЮ", BrO"
NaJO4 в щел. среде (А1/Э = 2) NaAsO2, 0,1 н. (I) и J2, 0,1 н. (II) а) Рабочий р-р (20 мл), Na2B4O7 (20 мл нас. р-ра, содержащего Hg2+, Sn2+, N2H4, SCN~, AsOj", Sb3+, S2-, TeO|_, J',. Fe2+
313;
NaJO4 в кисл. среде (44/3=8) Na2S2Oa, 0,1 н. 0,5 г НзВОз), KJ (2 г). Титр. ' р-ром 1 до бц. б) Рабочий р-р (20 мл, нейтр. по фенолфт.), NaHCO3 (5 мл нас. р-ра), р-р 1 (15 мл 0,1 н.), KJ (1 мл 20% р-ра). Через 15 мин титр, р-ром II с крахи, до син. Рабочий р-р, KJ (2 г), НС1. Титр, р-ром ст. в-ва с крахм. до бц. (Cu2+, Zn2 + , Hg2 + Fe3+, Со2+) MnO;, PbO2,
Na2S2O3 (М/Э = 1) K2Cr2O7 (3 = 49,03) J2 (возогнанный) (3 = = 126,9) KJO3 (3=35,67) или КН (JO3) 2 (3 = 32,50) K3[Fe(CN)6]-3H2O (100° С, 3 = 329,3) КМпО4, 0,1 н. Ст. в-во (0,1 г) раств. в Н2О (50 мл), добавл. KJ (2 г), НС1 (5 мл 6 н.), оставляют на 10 мин в темноте, добавл. Н2О (до 200 мл). Титр, с крахм. до з. Ст. в-во (0,25 г) раств. в р-ре KJ (2 г в 0,5 мл Н2О). Титр, с крахм. до бц. Ст. в-во (0,07 г) раств. в Н2О (25 мл), добавл. KJ (2 г), НС1 (10 мл 1 н.). Титр, с крахм. до бц. Ст. в-во (0,65 г) раств. в Н2О (20 мл), добавл. KJ (10 мл 1 н.), НС1 (20 мл 4 н.), через 1 мин ZnSO4 (10 мл 30% р-ра). Титр, с крахм. до бц. Р-р ст. в-ва (20 мл), HCI (до 1 н.), KJ (до 6%). Титр, с крахм. до бц. Cu2+, Tl3+, Се4+, NO-, AsO3-, Sbv, vo-, о,, н2о2, s2o|-, SeO2~, Сг2О2", активный Cl, СЮ-, СЮ', СЮ", Br2, BrO-, BrO", J2, Ю-, JO”, MnO2, MnO", ReO-, Fe3+, [Fe(CN)6]3-(H+, Li+, NaT, Be2+, Mg2+, Ba2+, Zn2+, Hg2+, Hg2+, Al3+, Ce3+, Tl+, CN", Zr4+, Th4+, Ge,v, Pb2+, Bi3+, VO-, SeO|-, Br-, J", Mn2+, Co2+)
SnCl2, 0,1 н. (М/Э = 2) КЮз, 0,1 н. или КВгОз (0.1 н.) в присутствии KJ Р-р ст. в-ва (20 мл), НС1 (2 мл конц. к-ты). Титр, с крахм. до ГОЛ. Cu2+, VO", Cr2O2-, Cl2, CIO-, CIO-, C1O4-, J2, Br2, BrO3-, JO", [Fe(CN)6]3-, MnO2, Fe3+(NO“, SiO?-, Co2+, СГ, Br", J", SO2",
Zn2 + , Ag+, ln3+)
*
ОБЪЕМНЫЙ АНАЛИЗ. РАБОЧИЕ РАСТВОРЫ
ti
Рабочий раствор ——- — ‘ . д. —— Определение концентрации рабочего раствора продолжение Вещества, определяемые рабочим раствором
стандартное вещество методика определения
Т1С13 (М/Э = 1) FeNH4(SO4)2, 0,1 н. Н2О (50 мл свежепрокипяченной), сегнетова соль (20 мл 20% р-ра), H2SO4 (4 мл р-ра 1:1), NaHCO3 (0,25 г). Пропускают СО2, добавл. рабочий р-р (20 мл), НС1 (20 мл конц. р-ра), NHiSCN (10 мл 10% р-ра). Титр, р-ром ст. в-ва до кр. Cu2+, NO", Sbv, Сг2О2-, МоО2”, Fe3+, [Fe(CN)6]4- 4
К2Сг2О7, 0,1 н. Р-р ст. в-ва (20 мл), Н2О (30 мл), H2SO4 (10 мл р-ра 1 : I). Титр, с дифенилам, или фенилантр. к-той до слабо-з.
Хлорамин Т* (М/Э = 2) Na2S2Oa, 0,1 н. NaAsO2, 0,05 М Рассч. по навеске и объему р-ра Рабочий р-р (20 мл), KJ (20 мл 0,5 н.), НС1 (20 мл р-ра 1:4). Титр, с крахм. р-ром ст. в-ва до син. Р р ст. в-ва (содержащий NaHCOa), KJ (0,5 г). Титр, с крахм. до син. Hg2+, Т1+, cs2, Sn2+, NO-, CN-, SCN”, N2H4, H3PO2, AsO’-, Sb3+, s2-, so|~, s2o2-, j-, Fe2+, [Fe(CN)6]4- (Ti4+, Vv, MnO“, JO7, Cr2O72-, Fe3+)
* CH3CeH4SO2NCINa.3H2O.
ОБЪЕМНЫЙ АНАЛИЗ. РАБОЧИЕ РАСТВОРЫ
§
сл| — II о
ГС 8
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения Лич
к+ Се (SO4)2 (I) и FeSO, (II) Осажд. Кз[Со(НО2)б]. К ос. добавл. р-р I (изб.). Титр, с ферроином р-ром 11 до кр. Эмпир.
AgNO3 (I) и NH4SCN (II) Осажд. К[В(СвН5)4] при рН=5^-6 и при 70° С. Фильтр, (промыв, нас. р-ром К[В(СбН3)4] и Н2О). Ос. раств в ацетоне. Опр. как СГ (стр. 342) I
NaAsO2 Анал. р-р, HJO4. С2Н5ОН, СН3СООС2Н5. К ос. добавл. боратн. буф. (рН=7,5). В р-ре опр. JO~ (стр. 346) 8
NaOH См. опр. Na+ 1
Си’+ Na2S2O3 Анал. р-р, H2SO4 (5 мл 4 н.), KJ (2 г). I
« Н2О (до 100 мл). Титр, с крахм. до син.
KJO3 Анал. р-р (20 мг Си), H2SO4 (несколько капель 1 н.), р-р SO2 (нас.). Нагр. до 100° С, добавл. NH4SCN (10% р-р до прекращения изменения окраски, и еще 3—4 мл). Через 15 мин фильтр., промыв. (NH4)2SO4 (1% р-р). В ос. опр. SCN" (стр. 323) 7
K2Cr2O7 Осажд. CuSCN (NH4SCN и SO2) (стр. 281) или Си2О (глюкоза и NaOH). Фильтр. К ос. добавл. Fe2(SO4)3. Титр, с дифенилам. до фиол. 1
nh4vo3 Анал. р-р, НС1 (25 мл конц. к-ты) в атм. СО2, пропускают через Bi-амальгаму в р-р Fe3*. Титр, образовавшийся Fe2* с фенилантр. к-той до роз. 1
KBrO3 Осажд. CuSO4(N2H4)2 • H2SO4. Ос. раств. в НС1 (1 : 1). Титр, с фуксином до желт, или с тропеолином 00 до ор. Анал. р-р (Нг5О4<0,5 и.), тионалид (20 мл 1% сп. р-ра). Ос. раств. в смеси СН3СООН (50 мл лед.) и H2SO4 (4—5 мл 5 и.), добавл. KJ (0,1 г), NH4SCN (10 мл 1 н.). Опр. тионалид (стр. 324). 8
J, (I) и Na2S2O3 (II) 1
KCN Добавл. NH4OH (изб). Титр, до бц. Эмпир.
KBrO3+KBr (I) и Na,S,O3 (II) Осажд. антр. к-той (см. опр. Zn2*). В ос. опр. антр. к-ту (стр. 322). 12
Na-ЭДТА Анал. р-р (до 20 мг Си в 100 мл) нейтр. NH3 де рН=8. Титр, с мурексидом до фиол. 2
Na-ЭДТА (I) и MgSO4 (II) Анал. р-р, аммиачн. буф. (рН=9,7)„ р-р I (изб,). Титр, р-ром II с хромоген, черн. до кр. 2
316
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения /М/Э
Си«+ SnCl2 Анал. р р (в атм. СО2), HCI (0,2—0,7 н.), KSCN (10% Р р), (NH4)2MoO4 (2% Р-Р). Титр, до кр.-бур. 1
Гидрохинон Анал. р-р, CH3COONa. NH4SCN, NH4CL Титр, с дифенилам. 1
Ag* NH,SCN Анал. р-р (25 мг Ag). HNO3 (2 мл 4 н ). Титр, с Fe3* до роз. 1
NaCl Анал. р р, HNOs (0,8 М). Титр, (без инд.) до прекращения осажд. 1
NaCl (I) и AgNO3 (П) Анал. рр (нейтр.), р-р 1 (изб.). Титр, р-ром II с К2СгО4 до роз. 1
J2 (I) И Na2S2O3 (II) См. опр. Си2* (без добавл. NH4SCN) 1
Аскорбиновая кислота Анал. р-р, CH3COONa. Нагр. до 60° С. Титр, с вариамин. син. до бц. 1
Ан3+ NaAsO2, 0,01 н. Анал. р-р (~40 мг Au), НС1 (15мл. конц. к-ты), HNO3 (5 мл конц. р-ра). Нагр., добавл. NaClO (25 мл 5% р-ра), Н2О (35 мл). Кип. 10 мин. Охл., нейтр. (по лакмусу) NaHCO3 (нас. р-р), добавл. KJ (2 г). Титр, с крахм. до исчезновения син. 2
Аскорбиновая кислота Титр, с вариамин. син. при 60° С до бц. 3
Гидрохинон Титр, с о-дианизидином или с метилбен-зидином или с бензидином до исчезновения син. 3
II группа периодической системы
Ве2+ NaOH Анал. р р (нейтр. по мет. ор.); Са2* (для маек. F"). Титр, с фенолфт. до роз. (в конце титр. нагр. до- кип.) 2
Na2S2O3 Анал. р-р. HCI (10 мл р-ра 1:1), Н2О2 (1 мл 30% р-ра), Na-ЭДТА (7 мл 15% р-ра), NH4NO3 (10 г), Na2HAsO4 (5 г). Нейтр. NH4OH, (1:1) до помутнения, добавл. CH3COONH4 (20 мл 5% р-ра). Кип. 2 мин. Harp, до перехода ос. в крист. Фильтр., промыв. Ос. раств. в НС1 (1:3). Опр. AsO’~ (стр. 331) 2
КВгОз4-КВг (I) и Na2S2O3 . (») См опр. Mg2* (стр. 318). 8
317
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (•ИОВ) Рабочий раствор Методика определения М/Э
Mg2 + КВгО3 + КВг (I) и Na2S2O3 (П) Анал. р-р (100 мл-, 60—30 мг Mg), NH4C1 (2 г), NH4OH (6 н. до pH=9,5 и еще 2 мл). Нагр. до 70е С, добавл. 8-окси-хинолин (5%-ный; медленно до небольшого изб.). Через 10 мин фильтр., промыв. гор. Н2О. В ос. опр. 8-оксихинолин. (стр. 324). 8
Ce(NO3)4 (I) Осажд. 8-оксихинолином (см. выше). Ос. 59,5
и (NH4)2C2O4 раств. в НС1О4 (2 н.), добавл. р-р I. (эм-
(П) Нагр. при 95° С 15 мин. Титр, р-ром 11 с сетополином Ж до желт.-з. пир.)
• NaOH (I) и HCI (II) Анал. р-р (в мерной колбе), р-р I (изб.). После отстаивания часть р-ра титр, р-ром II с фенолфт. до бц. 2
Na2S2O3 Осажд. MgNH4AsO4 (аналогично осажд. MgNH4PO4). В ос. опр. AsO(стр. 331) 2
HCI (I) н NaOH (II) Осажд. MgNH4PO4 (стр. 282). К ос. добавл. р-р I. Титр, р-ром II с мет. ор. до желт. 2
Na-ЭДТА Анал. р-р (-<25 мг Mg в 100 мл) нейтр. NH4OH, добавл. аммиачи. буф. (2 мл; pH = 9,7) (стр. 307). Титр, с хромоген, черн. до син. илн с пнрокатехиновым фиол. до кр.-фиол. 2
Са2+ KMnO4 Осажд. СаС2О4 (при pH = 4) (стр. 283). Ос. р-ряют в H2SO4 (2 М), титр, до роз. или ф-т титр, до роз. 2
Ce (NO3)4 Осажд. СаС2О4 (стр. 283). В ос. опр. С2О4- как при опр. титра рабочего р-ра по Na2C2O4 (стр. 308) 2
Na-ЭДТА Анал. р-р (до 5 мг Са в 100 .мл), NaOH (5—6 мл 2 н.). Титр с мурексидом до фиол. 2
KBrO3 + KBr (I) и Na2S2O3 (II) См. опр. Mg2+ 8
Ca2+nMg2+ Na-ЭДТА (I) и СаС12 (II) Анал. р-р, 2 пробы: а) титр, р-ром 1 с хромоген, черн. (опр. Mg2++Ca2+); б) добавл. р-р I (изб.). Титр, р-ром II с мурексидом до ор. (опр. Са2+) 2
Sr2+ KMnO4 См. опр. Са2+ 2
Na-ЭДТА Анал. р-р нейтр. NaOH, добавл. Mg-ЭДТА (изб.). Титр, с хромоген, черн. до син. 2
Ва2+ Na2S2O3 Анал. р-р, нейтр., добавл. 0,1 н. К2СгО4 (изб.). Через 2 ч фильтр., промыв. CH3COONH4 (6 г/л). Ос. раств. в HCI (70 мл р-ра 1 : 10), добавл. KJ (2 г). Титр, с крахм. до бц. 2
318
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М/Э
Ва2 + К2СгО4 (1) и Na2S2O3 (П) К анал. р-ру (рН«5) в мерной колбе добавл. р-р I (изб.). Разб. до метки, через 2 ч фильтр, через сухой фильтр. В части ф-та опр. СгО4~ . 3
(NH4)2SO4 Анал. р-р (нейтр.), NH4C1 (2 г), ацетон (или сп. 35 мл), Н2О (до 100 мл), родизонат натрия (1 мл нас. свежеприготовленного р-ра). Через 2 мин титр, до желт. 2
Zn2+ К4 [Fe (CN)6] (Л4/Э = 3) 1. См. опр. конц. р-ра K4[Fe(CN)6] (стр. 305) 2. Анал. р-р (нейтр.), NH4C1. Титр, с (JO2+ (внешний инд.) до бур. 2 2
Na-ЭДТА а) См. опр. конц. ZnSO4 (стр. 307) б) Титр, при рН = 8ч-9 с мурексидом 2 2
KJO3 (или KJO4) Осажд. Zn[Hg(SCN)4] как при опр. Hg2*. В ос. опр. SCN” (стр. 323, 324) 24
KJO3 Осажд. ZnS (стр. 283). К ос. добавл. рабочий р-р (небольшой недостаток), НС1 (до 8,5—10 М), дотитр. с СС14 или с красителем (например, амарантовый) 4
KBrO3 -f- KBr (I) и Na2S2O3 (П) а) Анал. р-р, СН3СООН (5 мл 4 н.), CH3COONa (5 мл 2 н.), 8-оксихинолин до желт. Кип. 2 мин. Фильтр., промыв. В ос. опр. 8-оксихинолин (стр. 324) б) Анал. р-р (~0,1 г Zn), Н2О (150 мл), антр. к-та (3 г в 25 мл 1 н. NaOH). Через 20 мин фильтр, промыв, антр. к-той (0,2% р-р), сп. Ос, раств. в НС1 (4 н.). Опр. антр. к-ту (стр. 322) 8 8
J2 Осажд. ZnS (стр. 283). Ос. титр, с крахм. до сии. 2
AgNO3 (I) и NH4SCN (II) Осажд. ZnS (стр. 283). К ос. добавл. р-р I (изб.), фильтр. Ф-т титр, р-ром II (с Fe3+) до роз. 2
KMnO4 Осажд. ZnC2O4 и опр. как Са2+ 2
Na2S Анал. р-р титр, с PbSO4 (внешний инд.) до черн. 2
Аскорбиновая кислота Анал. р-р (рН<4), Ks[Fe(CN)6]. Титр, с вариамин. син. до бц. 2/3*
Cd2+ Na-ЭДТА См. опр. Mg2* 2
KBrO3 (I) и Na2S2O3 (II) См. опр. Mg2+ 8
KJO3 См. опр. Zn2+ 4
KBrO3 или KJO3 Осажд. в присутствии KJ нафтохинолином. В ос. опр. J* 8
KMnO4 Осажд. CdC2O4 и опр. как Са2+ (стр. 318), 2
♦ При титровании образуется осадок KtZn3[Fe(CN)6j2«
319
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения Л'ИЭ
Cd2 + KJFe (CN)eJ См. опр. Zn2+ (стр. 319) 2.4 *
(M/э = 3) KBrO3 + См. опр. Zn2+ (стр. 319) 8 или
+ KBr (I) и 12
Na,S,O3 (II) AgNO3 (I) и Осажд. CdS (стр. 284), добавл. р-р I. 2
NH4SCN (II) Фильтр., промыв. Ф-т титр, р-ром II (стр. 317).
Hg2 + KSCN Анал. р-р (без О-, 100—300 г Hg в 2
100 мл 0,6 н. HNO3). Титр, с Fe5*
J, (I) и NagSjOs (II) до кр. а) Анал. р-р (~0,2 г HgO2), KJ (2 г), NaOH (10 мл 4 н.), НСНО (10 мл 10% р-ра), СНзСООН (10 мл), р-р I (25 мл), взбалт. до раств. Hg. Титр, р-ром 11 с крахм. 1
б) См. опр. Си2+ (стр. 316) 1
Na2S2O3 Анал. р-р (HNOs<0,15 М или H2SO4< 16/5
<0,1 М). Кип., добавл. KJO4 (0,2 Л1),
смесь сп.-Ь этилацетат (1 : 1), охл., фильтр., промыв, этилацетатом. В ос.
опр. JO~ (стр. 346)
Na2S2O3 Анал. р-р ( ~ 150 мг Hg в 140 мл Н2О), 6
(NH4)2Cr2O7 (10 мл 20% р-ра), C5H5N (1 мл). Через 10 мин фильтр., промыв, ацетоном. Ос., НС1 (50 мл 1,2 н.), KJ.
Титр, с крахм. до бц.
KJO3 См. опр. Zn2+ (стр. 319) 4
KMnO4 Осажд. HgC2O4. Опр. как Са2+ (стр. 318) 2
KJO3 Анал. р-р (НО), 25 мл р-ра, содержаще- 24
(или KJO4) го NH4SCN (39 г/л) и ZnSO4 (29 г/л). Через 1 ч фильтр В ос. опр. SCN-(стр. 323, 324)
Аскорбиновая Анал. р-р (разб. HNO3, без О) нагр. 2
кислота до 60° С. Титр, с вариамин. син. (син.-> бц -> син.; в конце титр, добавл. CH3COONa)
Hg“+ J2 (I) и Hg2O2 (-0,2 г), KJ (1 г), р-р I (25 мл). 2
Na2S2O3 (II) Встрях. в закр. сосуде. Титр, р-ром II с крахм. до бц.
KJO3 Анал. р-р (50 мл), НС1 (2 мл 2 н.). Че- 2
рез 12 ч фильтр. К ос. добавл. Н2О (20 мл), НО (30 мл конц. р-ра). Титр, с СНОз до бц.
Хлорамин T См. опр. Sn2+ (стр. 325) 2
NH4VO3 См. опр. J* (стр. 345). 2
* При титровании образуется
осадок Cd5Ke[Fe(CN)e]4.
320
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М-Э
III группа периодической системы
н3во3 NaOH Анал. p-p, глицерин (равный объем) или маннит (1г, или глюкоза, или инвертированный сахар нейтр.). Титр, с фе-нолфт. до роз. 1
В4ОГ НС1 Титр, с мет. ор. до ор. См. опр. конц. НС1 (стр. 304) 2
АР+ КВгОдЦ-КВг (I) и Na2S2O3 (II) Анал. р-р (HCI), Н2С4Н4О6 (5-кратный изб.), CH3COONH4 (15 m/!~40% р-ра), NH4OH (по бромкрезол. до пурп.), 8-оксихинолин (2,5% р-р в СНдСООН; изб. ~20%). Кип. 1 мин, охл. до 60°С, фильтр, (промыв. ХОЛ. НгО). В ос. опр. 8-оксихинолин (стр. 324) 12
NaF Анал. р-р (нейтр.), изобутиловый сп. Титр, с Fe(SCN)3 до бц. 3
Na2S2Og Осажд. AIAsO4. Фильтр., промыв. К ос. добавл. НС1 (конц.), бензол (20 мл), KJ (3 мл 2 н.). Титр, до бц. 2
Na-ЭДТА (I) и ZnSO4 (II) или CuSO4 (Па) Анал. р-р, р-р I (изб.), Н2О (до 100 мл), C5H5N (5 мл). Титр, р-ром II с хромоген. черн. или р-ром Па с пирокатехин.-фиол. 2
(Ja3+ K4[Fe (CN)6] См. опр. Zn2+ (стр. 319) Эмпир.
KBrO3 (I) и Na2S2O3 (II) Анал. р-р (НС1), НгО (200 мл), 8-оксихинолин (5% сп. р-р; небольшой изб.). Нагр. до 70°С, добавл. NH4OH (изб.). Нагр. (30 мин). Охл. Через 1 ч фильтр., промыв. Н2О. Опр. в ос. 8-оксихинолин (стр. 324) 12
Na-ЭДТА Анал. р-р, ацетатн. буф. (pH=4,5-=-6). Титр, с пирокатехин.-фиол. до желт. 2
In3+ Na-ЭДТА, 0,02/4 Анал. р-р, этилендиамин (10 мл 0,2 М). Титр, с хромоген, черн. до син. 2
K4 [Fe (CN)6] Анал. р-р (без С1~), СН3СООН (до 40%). Титр, с дифенилбензидином до з. Эмпир.
содержащий 0,2 % K3 [Fe (CN)6], (~3)
Т1 + KMnO4 (M/Э = 4) Анал. р-р, НС1 (до 1,2 М). Титр, до роз. 2
KBfOg Титр, с мет. ор. до бц. 2
Ce (SO4)2 Титр, при 50° С с ферроином (0,025 М) до бл.-гол. 2
KJOg Анал. р-р титр, с СС14 (см. опр. AsO|~) 2
NH4VOg См. опр. J- (стр. 345) 2
Na2S2O3 Анал. р-р (слабокисл.). Кип. с бромной водой, добавл. фенол (5 мл 5% р-ра), KJ. Титр, до бц. 2
J2 (I) И Na2S2C>3 (П) Анал. р-р, Ь1а2С4Н40б (10 мл 20% р-ра), и KCN (до 5% р-ра), тионалид (5% р-р в ацетоне). См. опр. Си2+ (стр. 316) 1
21 Зак. 783
321
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения м/э
Sc3+ Na-ЭДТА Анал. р-р, яблочная (или малоновая) к-та, аммиачн. буф. (рН=8). Нагр. до 70—100° С. Титр, с хромоген, черн. до син. 2
La3 + и лантаниды КМпО4 Анал. р-р, Н2С2О4 (50 мл нас.). Через 10—20 ч фильтр., промыв. Н2О до нейтр. по мет. ор. Ос. раств. в гор. разб. H2SO4. Титр, до роз. 3
Na-ЭДТА Анал. р-р нейтр. до pH=4,5, Титр, со смесью ализарина с метил, син. 2
КВгОзД-КВг (I) и Na2S2O3 (П) См. опр. Mg2+ (стр. 318) 12
Се3+ КМпО. См. опр. La3+ 3
КВгОз+КВг (I) и Na2S2O3 (П) См. опр. Mg2+ (стр. 318) 12
FeSO4 Анал. р-р (200 мл р-ра 0,5 н. по H2SO4), AgNO3 (1 мл 0,1 н.), (NH4)2S2O3 (водн. р-р 2 г). Кип. 25 мин. Охл. Титр, с дифенилам. до бл.-з. 1
Na2S2O3 Опр. как Th (стр. 327) с добавл. КВгОз после KJO3 28
Na-ЭДТА См. опр. La3+ 2
Се4+ Na2S2O3 См. опр. конц. Ce(SO4)2 (стр. 308) 1
Н2О2 Анал. р-р (50—350 мг Се), H2SO4 (20 мл 20% р-ра). Нагр. до 50° С. Титр, до бц. 1
FeSO4 Титр, с дифенилам, до бл.-з. 1
Аскорбиновая кислота Анал. р-р (рН=2) титр, с вариамин. син. ДО бц. I
Г ндрохинон Анал. р-р (H2SO4, 10%) титр, с ферроином до кр. 1
VSO4 Анал. р-р (H2SO4) титр, с дифенилам, до бл.-желт. I
Еи3+ КМпО4 Восст. цинком до Еи2+, добавл. Fe3+ (изб.). Опр. Fe2+ (стр. 347). 1
J2 (I) и Na2S2O3 (II) Восст. до Еи2+, добавл. р-р I. Титр, р-ром 11 с крахм. до бц. 1
IV группа периодической системы
Антраниловая кислота
СО
КВгОз+КВг (I) и Na2S2O3 (II) Na2S2O3
Анал. р-р (НС1>1,6 н.), р-р .1. Через 30 мин добавл. KJ (2 г). Титр, р-ром II с крахм. до бц.
Газ пропускают над J2O6 (на силикагеле). Собирают выделенный иод в р-р NaOH (5 Al), окисляют J2 до JO^ (см. ’J-, стр. 345). Опр. JO3” (стр. 346)
6
2,4
322
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения Л1,Э
со AgNOg (I) и NH4SCN (II) P-p I (50 мл в толстостенной колбе), NaOH (50 мл 0,15 н.), пиридин (разб. р-р до раств. ос.) и анал. газ нагр. при 65е С 30 мин, добавл. СНзСООН. Фильтр. (Ag). Ф-т, HNO.3 (2 мл 4 н.). Титр, р-ром 11 с Fe3i до роз. 2
с2ог KMnO4 См. опр. конц. р-ра КМпО4 (стр. 311) 2
KBrOg Анал. р-р, Н2О (до 30 мл), MnSO, (0,5а), HgO (0,5 г), H2SO4 (20 мл конц. р-ра), Н3РО4 (5 мл). Гор. р-р титр, до кр. 2
со*- HCI а) Титр, с фенолфт. до НСО^ б) Титр, с мет. ор. до СО2 1 2
cs2 J2 Анал. в-во раств. в сп. р-ре КОН (1 Л1). Через 30 мин добавл. СНзСООН (до бц. по фенолфт.), СаСОз (1 г). Титр, с крахм. до син. 1
CN- AgNOg а) Анал. р-р (25 мл), NH4OH (1 мл 6 н.), KJ (~0,1 мг). Титр, до помутнения б) Анал. р-р (рН = 94- 12) титр, с дифе-нилкарбозоном (5 капель 0,3% сп. р-ра) до фиол. 1/2
[Cu (NH3)4]h Титр, до син. ~1/2
Hg (NO3)2 (I) и NH4SCN (II) Анал. р-р, р-р I, HNOg. Титр, р-ром II с Fe3+ до роз. I
KMnO4 (I) (М/Э = 1) и HCOONa (II) См. опр. J (стр. 345) 2
JC1 (M/3=l) Анал. р-р, NaHCOa. Титр, с крахм. до син. 1
N32SgOg Анал. р-р, Н3РО4 (5 мл 20% р-ра), бромная вода. Через несколько минут добавл. фенол (2 мл 5% р-ра), KJ (0,5г). Через несколько минут титр, с крахм. до бц. 2
NiSQ4 (I) (М/Э = 2) н Na-ЭДТА (II) Р-р I (изб.), NH4OH (10 мл конц. р-ра на 100 мл), анал. р-р. Титр, р-ром 11 с мурексидом до фиол. 2
SCN" AgNOg а) См. опр. конц. NH4SCN (стр. 305) б) Анал. р-р титр, с флюоресцеином 1 1
Hg (NO3)2 (I), и NH4SCN (II) Анал. р-р, р-р I (изб.). Титр, р-ром II с Fe3+ до кр. 1
KJOg См. опр. AsO|— (титр, быстро) (стр. 331 п. «а» или «б») 6
21*
323
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
П родолжение
Определяемое вещество (иои) Рабочий раствор Методика определения М/Э
SCN~ KJOg (I) и NaAsO2 (II) К анал. р-ру (нейтр.) в колбе с узким горлом, добавл. равный объем НС1 (1,5 н.), KCN (6 мл 0,5 н.), р-р I (изб.). Титр, р-ром II с крахм. до бц. 6
NaJO4(Af/3=6) Анал. р-р, НС1 (до 4—7 н.). Титр, с СНС13 до желт. 8
Na2S2O3 См. опр. CN- (стр. 323) 6
J2 (I) н Na2S2O3 (II) Р-р I (изб.), анал. р-р, (NH4)2B4Or (10 мл 1 н.), *. Через 1 мин добавл. НС1 (10 мл 2 н.). Титр, р-ром II 6
Ca (OC1)2 Анал. р-р, КВг (1 a), NaHCO3 (1 г). Титр, с мет. ор. (в конце титр.) до бц., вычитают поправку на инд. 8
KMnO4 (I) и HCOONa (II) См. опр. J’ (стр. 345) 8
Хлорамин T (M/Э = 2) См. опр. Sn2+ (стр. 325) 8
NH4VO3 См. опр. J~ (стр. 345) 6
8-Оксихи- KBrO34-KBr Анал. в-во (20—40 мг 8-оксихннолина или 4
НО ЛИН (I) и Na2S2O3 (II) р-р оксихинолината в 2 н. НС1), мет. кр. (несколько капель 0,2%), р-р I (до желт, и изб. 2 мл). Закр. колбу. Через 1 мин добавл. KJ (15 мл 20% р-ра). Титр, р-ром II с крахм. до бц.
Органиче- ские NaOH (без CO2) Титр, с фенолфт. до роз. . . .
кислоты Na2S2O3 (I) и J2 (II) Анал. р-р (20 мл), KJ (1 г), KJO3 (5 ли 3% р ра), Р Р I (изб.). Через 5 мин титр, р-ром II с крахм. до син. . . .
Тионалид J2, 0,02 h. (I) и Na2S2O3, 0,02 н. (II) Анал. р-р (в СН3ОН или СНзСООН), H2SO4 (5 мл 5 н.). Титр, р-ром I с крахм. до син. или добавл. р-р 1 (изб.) и титр, р-ром II с крахм. до бц. I
SiO2~ HCI (I) и NaOH (II) Анал. р-р (нейтр. по мет. ор.), нейтр. р-р KF. Добавл. р-р I (разб.). Титр, р-ром II до желт. 6
8-Оксихино-лин (I), KBrO34-KBr (II) и Na2S2O3 (III) Осажд. силикомолибдат-8-оксихинолина. В ф-те опр. 8-оксихинолин (см. выше) Эмпир.
ОеО2" (Ое4+) NaOH Анал. р-р нейтр. до pH = 6,2, добавл. изб. маннита (или фруктозу, или инвертир. сахар). Титр, (с бромкрезол. пурп. или с мет. кр., или с фенолфт.) I
KBrO3 4- KBr (I) и Na2S2O3 (II) Осажд. молибдатом аммония, добавл. 8-оксихинолин, далее см. опр. Mg2+ (стр. 318) 16
* Для приготовления р-ра в 170 мл 10% р-ра NH3 растворяют 20 г Н3ВО3 и разбавляют до 1 л.
324
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения /И/Э
Sn2+ J2 Анал. р-р, НС1. Титр, в атм. СОг с крахм. до син. 2
FeCl3 Анал. р-р, HCI. Титр, в атм. СО2 с индигокармином (или с SCN', или с метилен. син.) 2
KJO3 а) См. опр. AsO®- (стр. 331, п. «а») б) Анал. р-р нейтр. в колбе с узким горлом, добавл. равный объем НС 1 (2,5 н.), KCN (6 мл 0,5 н.). Титр, с крахм. до бц. 2
H2O2 Анал. р-р, НС1 (конц.). Титр, с KJ+ -Ькрахм. или с FeCl2 + NH4SCN или с Ti4* 2
Хлорамин Т Айал, р-р, НС1 (50 мл р-ра 1:1), JC1 (5 мл 0,02 М), СНС1з (5 мл). Титр, при сильном взбалт. до бл.-желт. 2
К2Сг2О7 или Се (SO4)2 Анал. р-р титр, в атм. СО2 с дифенилам, до фиол. 2
КВгО3 См. опр. AsO з~ (стр. 331) 2
Sniv Восст. до Sn2+ См. опр. Sn2* 2
J2 Анал. р-р, HCI, Н2С2О4, H2S. Ос. [SnS (С2О4) 2]2* титр с крахм. 2
Na-ЭДТА (I) и MgSO4 (II) или ZnSO4 (Па) См. опр. РЬ2* (стр. 326) 2
Pb2+ Na2S2O3 а) Анал. р-р (50 мл), CH3COONa (10 мл 2 н.), СНзСООН (10 мл 2 н.), Н2О (до 100 мл), К2СгО4 или КзСггО? (изб.). Нагр. 2 ч. Фильтр., промыв. Н2О. К ос. добавл. НС1 (25 мл 2 н.), Н2О (25 мл), KJ (1 г). Титр, с крахм.. до бц. б) Осажд. PbSO4 (стр. 289). Ос. раств. в CH3COONa. Далее опр. как в п. «а» 3 3
(NH4)2MoO4 Анал. р-р (0,1—0,9 г Pb), HNO3 (1 мл 0,1 М). Титр, с таннином (внешний инд.) 2
K4[Fe(CN)6] Анал. р-р титр, с UO^+ (внешний инд.) до бур. 2
KBrO3 + KBr (I) и • Na2S2O3 (II) Анал. р-р (нейтр.,~0,1 г РЬ), Н2О (до 100 мл), антр. к-та (30 мл 3% р-ра). Через 1 ч фильтр., промыв, антр. к-той (0,5% р-ром). Ос. раств. в гор. 10% р-ре CH3COONH4, добавл. НС1. Охл. См. опр. антр. к-ты (стр. 322) 12
KJO3 См. опр. Zn2* (стр. 319) 4
KMnO4 См. опр. Са2* (стр. 318) 2
J2 (I) и Na2S2O3 (11) См. опр. Си2* (стр. 316) 1
325
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (нои) Рабочий раствор Методика определения М/Э
РЬ2+ Na-ЭДТА (I) и MgSO4 (II) или ZnSO4 (Па) Анал. р-р, р-р I, аммиачн. буф. (рН=9). Титр, р-ром 11 или Па с хромоген, черн. до кр. 2
К? [Cu (JO6)2] или К9 [Си (ТеОв)2] Титр, в щел. р-ре до бур. 2
Аскорбиновая кислота Анал. р-р (рН<4), Кз[Ре(СН)6]. Титр, с вариамин. син. до бц. 1*
Ti<+ КМпО4 или Се (SO4)2, или К2Сг2О7 Анал. р-р (HCI), (NH«)2SO4 (15 мл нас. р-ра). Восст. Ti в атм. СО2 цинком или кадмием (в редукторе) или амальгамами Zn, Cd, Pb или Bi (при 60° С). Ф-т из редуктора собирают в р-р Fe34. Опр. Fe2+ 1
КВгОз+КВг (I) и Na2S2O3 (II) Анал. р-р, винная к-та (la), CH3COONa (0,5 г). Разб. до 150 мл, нейтр. по фенолфт., добавл. СНзСООН (1,5 мл). Harp, до 60° С, добавл. 8-оксихинолин (3% сп. р-р). Кип. (10 мин). Фильтр., промыв, гор. НгО. В ос. опр. 8-оксихи-нолин (стр. 324) 8
Na-ЭДТА (I) и ZnSO4 (II) или CuSO4 (Па) См. опр. А13+ (стр. 321) 2
Zr4+ Na-ЭДТА Анал. р-р (НС1, 0,5—2 Л1) при 100° С титр с хромоген, черн. до син. 2
Hf<+ КВгО3 + КВг (I) и NagSgOg (II) Na2S2O3 а) Анал. р-р (<12 мг Zr), HNO3 (Южл 33% р-ра). Выпар., добавл. еще HNO3 (5 мл). Выпар, до небольшого объема, добавл. Н2О (до 50 мл), 8-оксихинолин (7 мл 3% р-ра), CH3COONa (50 мл 2 н.). Кип. несколько минут. Фильтр., промыв, гор. Н2О. Ос. раств. в H2SOi (50 мл 50% р-ра). См. опр. 8-оксихи-нолина (стр. 324) б) Осажд. Zr(HPO4)2 (в среде HNO3). Фильтр., промыв. HNO3. Ос. раств. в Н2С2О4. Осажд. 8-окснхинолином и далее опр. как в п. «а» См. опр. Th4+ См. опр. Zr4+ 16 16 (эм-пир.) 27
Th4+ КМпО4 Анал. р-р (10 мл-, 1 и. по HNO3) нагр., добавл. Н2С2О4 (изб. нас. р-ра). Нагр. 1 ч. Через несколько часов фильтр, (промыв, разб. HNO3). Ос. раств. в 2 н; H2SO4. Титр, при 90° С до роз. 4
* При титровании образуется осадок Pt>2 1^е’Л+бЬ
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М1Э
Th4+ Na2S2O3 Анал. р-р (5 мл, 1—10 мг Th4+), HNO3 (2,5 мл конц. р-ра), KJO3 (5 мл 15% р-ра в 5О7о HNO3). Ос. центрифугируют (промыв. НгО 4 раза по 8 мл), добавл. KJ (1—2 г), НС1 (до раств. ос.). Титр с крахм. до бц. 25,5
Na-ЭДТА Анал. р-р (рН= 1,6-=-3,4) титр, с ализариновым кр. (4 капли 0,5%) или с пирокатехин.-фиол. (см. опр. Bi3+) 2
Се (SO4)2 Анал. р-р, лед. СНзСООН. Осажд. ди-фенилкарбазидом и молибдатом аммония. Фильтр, и промыв. В ос. опр. МоО4~ 2
КВгО3 4- КВг (I) и Na2S2O3 (11) Осажд. 8-оксихинолином при рН = 5. См. опр. Mg2+ (стр. 318) 20
V группа периодической системы
Азот в органических соединениях
Вг2 4- КВг, 0,05 н. (I) * и Na2SgO3 (II)
H2SO4 (I) и NaOH (II)
nh+
HC1 (I) и NaOH (II) .
NaOH (I) и НО (II)
Анал. в-во (в колбе Кьельдаля), H2SO4 (10 мл конц. к-ты). Кип. до прозрачного р-ра. Разб. до 0,05 н. по NH^. 10 мл этого р-ра нейтр. фосфата, буф. **, добавл. еще 15 мл и затем р-р I. Через 10 мин добавл. KJ (20 мл 0,2 н.), НзРО4 (15 мл 20% р-ра). Через 3 мин титр. Na2SgOa. Проводят холостой опыт
Анал. в-во (0,1 г; в колбе Кьельдаля), K2SO4 (10 г), Hg (0,6 г), H2SO4 (20 ли конц.). Кип. (до бц. и еще 15 мин). Harp. 1 ч (при слабом кип.). Охл., добавл. Н2О (200 мл), Na2S2O3 (80 г). Соединяют колбу с насадкой для перегонки, добавл. NaOH (изб.). Отгоняют NH3 в р-р I (перегоняют 200 мл жидкости). Титр, с мет. ор. р-ром II до желт.
Анал. р-р (~50 мг NH4h), КОН (50 мл 50% р-ра). Упар., улавливая NH3 р-ром I (50 мл). Титр, р-ром II с мет. ор. до желт.
Анал. р-р, р-р I (изб.). Упар на 1/3 до удаления NH3. Охл. Титр, с мет. ор. р-ром II до ор.
3 (эм-пир.)
1
1
1
* Для приготовления р-ра берут 60 г КВг. прибавляют 3 мл Вг2 и разбавляют водой до 1 л.
** Для приготовления р-ра берут 95 г Na2HPO4-2H2O, добавляют 5 г NaH2PO4-2H2O и растворяют в воде до 1 л.
327
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М/Э
NH+ NaOH Анал. p-p, HCHO (5 мл 40% р-ра нейтр. 1
NaOH, сп. p-p по фенолфт.). Титр, с фенолфт. до роз. Через 1 мин добавл. еще 5 мл НСНО и титр, до роз. Анал. р-р (в 50—97% сп.) Титр, с тимол- 1
NaBrO (I) и фтал, до син. Анал. р-р (25 мл в колбе с притертой 3
пробкой), Н2О (25 мл), КНСОз (10 мл (эм-
N2H4 KBrO3 1 н.), р р I. Перемеш. Через 30 мин добавл. KJ (10 мл 1 н.) и НС1 (15 мл 1 н.). Титр, с крахм. до бц. Анал. р-р (НС1, 20%). Титр, с индиго до бп пнр.) 4
KJOg См. опр. Т1* и опр. Sn2+, см. также опр. 4
J2 конц. КЛОз (стр. 311) Анал. р-р, NaHCOa (1 г на 25 мл). Титр. 4
JC1 до желт., сохраняющейся 2 мин окр. См. опр. конц. рабочего р-ра (стр. 310) 4
NaJO, (44/3=6) Анал. р-р (НС1 5 н.), СНС13. Титр, до 4
KMnO4 (I) желт. Р-р I (25 мл), NaOH (5 мл 4 в.), анал. 4
(M/Э = 5) и Na2S,O3 (II) Хлорамин T р-р (10 лгл-~0,1 и.). Через 0,5 ч добавл. КЛ, подкисл, и титр, р-ром II до бц. а) Анал. р-р, NaHCO3 (0,5 г), КЛ (кри- 4
(М'/Э = 2) NaClO сталлик). Титр, с крахм. до син. б) См. опр. Sn2+ (стр. 325) См. опр. конц. рабочего р-ра (стр. 307) 4 4
nh2oh KBrO3 (I) и Анал. р-р, НС1 (50 мл 6 н.), р-р I (изб.). 4
NaAsO2 (II) KMnO4 Через 15 мин добавл. р-р II (изб.). Титр, р-ром I с мет. ор. до бц. Анал. р-р, Fe2(SO4)3 • 9Н2О (50 мл 2
HN3 J2 (I) и 40 г/л), H2SO4 (15 мл 1:2). Кип. 5 мин. Охл., добавл. Н2О (до 100. мл). Титр, до роз. CS2 (0,5 мл), ацетон (7 мл), анал. р-р. Через 5—10 мин добавл. Н2О (250 лгл). Титр, р-ром II с крахм. 5 мл смеси (1 М H2SO4, 1 44 НзРО4 и I
Na2S2O3 (И) KMnO4 (I) и 1
№252б3 (II) NaNO2 1 41 MnSO4), H2SO4 (10 мл), р-р I (25 мл), анал. р-р (20 мл). Через 10 мин иодометрически опр. МпО“ Анал. р-р (0,5 мл 5% р-ра), FeCl3 (2 мл 1
NO2" KMnO4 10% р ра), H2SO4 (1 мл 4 н.). Титр, из микробюретки до бц. Рабочий р-р (25 мл), H2SO4 (20 мл 4 н.), 2
NaClO Н2О (200 лм). Нагр. до 40е С. Титр, анал. р-ром Рабочий р-р титр. анал. р-ром с иодо-крахм. бумагой до син. 2
328
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М!Э
NO" Хлорамин Т (I) и Na2S2O3 (II) Анал. p-p, p-p I (изб.), СНзСООН (2 мл разб.). Через 2 мин добавл. KJ (изб. 10% р-р). Титр, р-ром II с крахм. до бц. 2
Се (SO4)2 (I) и Na2C2O4 (II) НС1О< (5 мл 72% р-ра), Н2О (100 мл), р-р I (изб.), анал. р-р (10 .ил). Через 2 мин титр, р-ром II с нитроферроином до кр. 2
КВгО3 (I) и Na2S2O3 (II) Анал. р-р (~ 100 мг NaNO2), р-р I (изб.) HCI (5 мл конц. к-ты). Закр. Через ’3 мин добавл. KJ (2 г.) Титр, р-ром II с крахм. до бц. 2
Na2S2O3 ИаНСОз (12 г), KJ (3 г), амиловый сп. (1 мл), Н2О (25 мл), анал. р-р, СНзСООН (разб., 4 мл без взбалт.), H2SO4 (6 мл 20 н.). Титр, скрахм. до бц. 2
NO" HCI (I) и NaOH (II) Анал. р-р, Zn или сплав Деварда (А1 + + Zn+Cu), NaOH. Газ улавливают р-ром I. Титр, р-ром II с мет. ор. до желт. 1
FeSO4 (I) и Анал. р-р, р-р I (изб.), НО (70 мл 3
К2Сг2О7 (II) 12 н.). Натр, в атм. СО2. Кип. 3 мин, добавл. (NH4)2MoO4 (2 мл 1% р-ра). Кип. 10 мин. Охл., добавл. CH3COONH4 (6 н., 35 мл на 50 мл анал. р-ра), Н3РО4 4 мл 85% р-ра). Титр, р-ром II с дифенилам. до фиол. (эмпир.)
Н2С2О4 (I) и KMnO4 (II) Анал. р-р, MnSO4 (5 г), H2SO4 (12 мл конц. на 100 мл р-ра), р-р I (изб.). Натр, при 94° С с обратным холодильником. Титр, р-ром II до роз. 3
TiCl3 Анал. р-р нейтр. Натр, до кип. Титр, в атм. СО2 с ализарином (3 мл 0.1% сп. р-ра) до прекращения появления кр. 3
Н3РО2 KMnO4 (I) (M/Э = 1) и HCOONa (II) См. опр. J~ (стр. 345) 4
Ce (SO4)2 (I) и FeSQ4 (II) Анал. в-во, H2SO4 (25 мл р-ра 1:4), р-р 1 (изб.). Через 2 ч (или 30 мин при 60° С, затем охл.) титр, р-ром II с ферроином. НРО3~ не мешает (при 80— 100° С опр. НдРО2 и НРО|) 4
KBrO3 (I) и Na2S2O3 (II) Анал. р-р (~ 0,025 М), H2SO4 (5 мл 4 н.), р-р I (изб.). Натр, до появления паров брома. Через 30 мин кип. до его удаления. Охл., титр, иодометрически. Опр. совместно с НРО^-. 2,4’
* 5 моль Н3РО2 эквивалентны 2 моль, т. е. 12 г-экв ВгО
329
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М!Э
ПРО2 J2 (I) и Na2S2O3 (II) KMnO4 (I) (М/Э = 1) и HCOONa (II) KBrOg (I) и Na2S2O3 (II) NaBrO (I) и Na2S2O3 (II) Анал. р-р, р-р I (изб.), NH4BO2 (5 мл) *. Через 15 мин добавл. НС1 (2 н.).Титр. р-ром II (Н3РО2 не мешает) См. опр. J~ (стр. 345) Анал. р-р, смесь р-ра I (100 мл) и КВг (2 г); продолжают как при опр. Н3РО2 (опр. совместно с Н3РО2) Анал. р-р (10 мл ~0,05 Л1), р-р I, NaHCO3 (1 г). Через 30 мин опр. ВгО“ Йодометрически 2 2 2,4* 2
НРО42- NaOH (I) и HCI (II) HCI UO2 (NO3)2 AgNO3 (I) и NH4SCN (II) Pb (NO3)2 KOH, сп. p-p Осажд молибдатом аммония (стр. 292). К ос. добавл. р-р I (изб.). Титр, р-ром II с фенолфт. до бц. Титр, с мет. ор. до ор. Титр, с [Fe(CN)6]4- (внешний инд.) до кр.-бур. Анал. р-р, р-р I (изб.). Нейтр. р-ром NaOH (по феноловому кр.). Фильтр., промыв., ф-т титр, р-ром II (стр. 317) Анал. р-р нейтр. по фенолфт. Титр, с ди-бромфлюореспеином (3 капли 0,1 % р-ра) до роз. Осажд. молибдатом аммония (стр. 292). К ос. добавл. NH4OH, ацетон. Титр, с тимолфт. до син. 23 1 2 (эм-пир.) 3 3 28 (эм-пир.)
Na-ЭДТА (I) и Mg2+ (4) Анал. р-р, Na-ЭДТА, CeHsO?-. Осажд. MgNH4PO4 (стр 292). Ос. раств. в НС1, добавл. р-р I. NH4OH (по мет. ор.), аммиачн. буф. (рН = 9,7) (стр. 307). Титр, р-ром II с хромоген, черн. до кр. 2
н3ро4 NaOH а) Анал. р-р титр, с мет. ор. до желт, или с бромкрезол. з. до син. б) Анал. р-р титр, с фенолфт. (в присутствии NaCI) до роз. или с тимолфт. до син. в) Анал. р-р, СаС12 (30 мл 40% р-ра). Нагр. до кип. Охл. Титр, с' фенолфт. до роз. 1 2 3
Н4Р2О7 NaOH Анал. р-р титр, с мет. ор. до желт. 2
* Для приготовления р-ра в 170 мл 10 ?0' р-ра NH3 растворяют 20 г Н3ВО3 и разбавляют до I л.
* 5 моль НРО^- эквивалентны 2 моль, т. е. 12 г-экв ВгО^”.
330
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяе мое вещество (ион) Рабочий раствор Методика определения А1/Э
As (общий) J2 (I) и NaAsO2 (И) Анал. p-p, NaH2PO2 (5 г) *. Harp. <50°С, добавл. NaH2PO2 (10 г), кип. с обратным холодильником (15 мин). Фильтр промыв. НС1 (1:3) с NaH2PO2 (2% р-р), затем NH4C1 (5% р-р). К ос. добавл. NaHCO3 (2 г), р-р I (изб.). Через 5 мин добавл. Н2О (до 300 мл), NaHCOs (2 г). Титр р-ром II до бц. 5
AsO’" (AsO-) J2 Айал, р-р, As2O3 (~0,2 г) в NaOH (10 мл 1 н.), H2SO4 (15 мл 1 н.), КНСОз (I г в 50 мл Н2О). Титр, с крахм. до син. или с СС14, или с СНС13 до фиол. 2
KJO3 а) Анал. р-р (в колбе с притертой пробкой) разб. Н2О (до 50 мл), НС1 (50мл конц. р-ра), СС14 или СНС13 (5 мл). Охл., добавл. рабочий р-р до бледнокор. Колбу закр., взбалт. Титр, до бц. б) Поступают как в п «а», но без органического р-рителя. Титр, почти до конца, добавл инд. (краситель амарантовый) и титр, до разрушения красителя в) См. опр. Sn2+ (стр. 325, п. «б») 2 2 2
КВгО3 Анал. р-р (~50 мг As, 50 мл), НС1 (15 мл конц. к-ты), КВг (0,5 г). Титр, с мет. ор. до бц. 2
NaBrO Анал. р-р, КВг (1 г), NaHCO3 (0,5 г). Титр, с мет. ор. до бц. 2
NaClO Анал. р-р (5 мл ~ 0,005 н.), НС1 (5 мл конц. р-ра), Н2О (до 40 мл). Титр, с мет. ор. до бц. 2
Хлорамин Т См. опр. конц р-ра хлорамина Т (стр. 314) или опр. как Sn2+ (стр. 325) 2
Nay [Cu(JO6)2] Анал. р-р (0,5 мл), КОН (5 мл 10% р-ра). Титр, из микробюретки до з. 2 (эм-пир.)
NaJO4, 0,02 н. (М/Э - 2) Анал. р-р (1 н. H2SO4), соль Мора (2 капли 0,02 н.). Титр, с дифенилам, до фиол. 2
Се (SO4)2 См. опр. конц. р-ра Ce(SO4)2 (стр. 308) 2
KMnO4 • См. опр. конц. р-ра КМпО4 (стр. 312) 2
JC1 См. опр. конц. р-ра JC1 (стр. 310) 2
NH4VO3 См. опр. J (стр. 345) 2
AsO’" Na2S2O3 а) Анал. р-р, НС1 (20 мл 25% р-ра), NaHCO3 (немного), KJ (1 г)'. Закр. колбу. Через 5 мин титр, с крахм. до бц. 2
* Вместо МаНгРОг можно брать SnC12 с Hg2Cl2 ^катализатор).
331
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М',Э
AsOj-4 Na2S2O3 б) Анал. р-р (10 мл), НС1 (10 мл конц.), СбН6 или СНС1з (20 мл), KJ (3 мл 2 н.). Взбалт. несколько секунд, добавл. Н2О (~40 мл). Титр., сильно взбалт., до бц. 2
nh4scn Анал. р-р (pH = 7-е-9), AgNO3. Фильтр, и промыв. К ос. добавл. HNO3 (8 М). Титр, с Fe3+ до роз. 3
Sb3+ KMnO4 Анал. р-р (в конц. HCI), Н2О (до 150мл). Титр, при 20° С до роз. (сохраняющейся 20 сек) 2
J2 или KBrO3 См. опр. AsO|~ (стр. 331 п. «а» или «б») 2
Ce (SO4)2 KJO3 Анал. р-р (3 Л1 НС1). Титр, с мет. ор. до бц. См. опр. AsC>3~ (стр. 331 п. «а» или «б») или опр. Sn2+ (стр. 325) 2
NaJO4, 0,02 h. (M/Э = 2) Анал. р-р (H2SO4 1 н.), соль Мора (2 капли 0,02 и.). Титр, с дифенилам, до фиол. 2
NaClO См. опр. AsO|~ (стр. 331) 2
Хлорамин T См. опр. Sn2+ (стр. 325) 2
SbV, Na2S2O3 См. опр. AsO4- (стр. 331 и 332) 2
[SbCl6] TiCl3 Анал. р-р, НС1 (50 мл конц. р-ра), НгО (100 мл), Вг2 (5 капель). Кип. до удаления брома, проп. СОг. Титр, при 60° С с индигокармином (5 капель 0,1% р-ра) до бц. 2
Bi3+ KMnO4 (I) и HCOONa (И) Анал. р-р (~5 мг Bi на 25 мл; 0,3—1 н. по НЬЮз без С1-), K3[Cr(SCN)6] (изб. 10% р-ра). Через 10 мин фильтр., промыв. Н2О, NaOH (10 мл 1% р-ра), а затем H2SO4 до полного извлечения SCN-. Опр. SCN- (стр. 324) 48
KMnO4 а) Анал. р-р (не >0,25 г Bi), AI (порошок, 0,1 г). Через 15 мин охл., добавл. КОН (40 мл 15% р-ра). Нагр. до полного раств. А1, фильтр, и промыв. Ос. раств. в 15 мл р-ра FeCl3 (200 г и 250 мл НС1 на 1 л), добавл. реактив Циммермана-Реингарда (стр. 25), Н2О. Титр, до роз. б) Осажд. оксалат. Опр. С?О^_ в ос. или ф-те. См. опр. Са2+ (стр. 318) 3 2
332
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М/Э
Bi3+ J2, 0,02 н. (I) И Na2S2O3, 0,02 н. (II) Анал. р-р (0.1 н. H2SO4), тионалид (20 мл 1% сп. р-ра). Нагр. 20 мин. Фильтр, и промыв. Ос. раств. в Нг8О4, добавл. NH4C1 (до нас.). Опр. тионалид (стр. 324) 3
КВгО3 Анал. р-р (НО), СОг, Си. Титр. Си" с мет. ор. до гол. 3
KJO3 Анал. р-р (ИО^или SO4~), 8-оксихинолин (изб. 5% р-ра в 0,2 н. H2SO4), KJ (0,1 н. до появления хлопьев). Фильтр., промыв, р-ром KJ + 8-оксихинолин *. Ос. раств. в НС1 (1,2 н.). Опр. J- (стр. 345) 8
KBrOg (I) H Na2S2O3 (II) Na-ЭДТА См. опр. А13+ (стр. 321) а) Анал. р-р (рН=1,5<-2) титр, с KJ (1 мл 0,5% р-ра) до бц. б) Анал. р-р (до 50 мг В1 в 100 л!л), пирокатехин.-фиол., NH3 до син. (рН = =2 4-3). Титр, до желт. 12 2
VO2+ KMnO4 Анал. р-р, H2SO4, титр, при 75° С до роз. 1
Na-ЭДТА (I) и MnSO4 (II) Анал. р-р, р-р I (изб.). Титр, с хромоген, черн. р-ром II до кр. 2
vo-(VO+; FeSO4 Анал. р-р, H3SO4 (100 мл 10 Л1), Н2О (до 200 мл). Охл. до 20°С. Титр, с ферроином до кр. 1
vo3+) KMnO4 а) Анал. р-р (для маек. Fe3+ добавл. Н3РО4 и КМпО4 до роз.), H2SO4 (до 10%), FeSO4 (0,1 н.) (изб., проба с Кз[Ре(СН)6] и еще 3—5 мл). Перемеш. 1 мин, добавл. (NH4)3S2O3 (8 мл свежеприготовленного 15% р-ра). Титр, до роз. (остающейся 30 сек) или с дифенилам, до фиол. б) Восст. до VIV упариванием с HCI или действием восстановителей (Hg, Bi-амальгама, SO2, H2S, НгО2, Н2С2О4). Титр, до роз. 1 1
3nCl2 Анал. р-р (НС1 3 н. в атм. СОг) титр, с дифенилам, до фиол. или с молибдатом аммония (внешний инд.) до син. 1
КВгО3 (I). и Na2S2O3 (II) Анал. р-р, Н3РО4 (до 0,01 Л1). Нагр. до кип., добавл. 8-оксихинолин (4% в сп.; изб. 70%), CH3COONa (до рН=5,3). Кип. несколько минут. Фильтр., пром, гор. НгО. Раств. ос. в Н3РО4 (разб.) или НС1. Опр. 8-оксихинолии (стр. 324) 8
* 50 мл 2 н. H2SO4, 25 мл 0,1 н. KJ, 1,8 г 8-окснхинолина, несколько кристаллов Na2H4-H2SO4, разбавляют до 1л.
333
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ I
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М1Э
VO-, KJ (1) (Л1/Э=2) Анал. р-р (атм. СО2) охл., добавл. HCI (до 7 н.), р-р I (изб.) Через 2 мин титр, р-ром II с СНС1з до бц. (во время титр, добавл. HCI до 7 н.) Анал. р-р (H2SO4) быстро (!) титр, с вариамин. син. до бц. Анал. р-р (HCI), р-р 1 (изб.). Титр, р-ром II с SCN* до бц. Анал. р-р (10% H2SO4) титр, с дифенилам. до бц. Анал. в-во сплавляют с K2S2O7, добавл. 1
(VO+; VO3+) Nbv и KJO3 (И) Аскорбиновая кислота FeSO4 (I) и аскорбиновая кислота (II) Г идрохинон К Мп О., 1 1 1 1,86
NbV^-TaV FeNH4 (SO4)2 (I) и K2Cr2O7 (II) HCI (I) и H2SO4 (20 мл). Нагр. до раств. сплава, охл., добавл. Н2О2 (1 мл 30% р-ра), Н2О (100 лм), H2SO4 (20 мл), янтарную к-ту (2 г). Восст. действием Zn-амальгамы (в колонке), собирая ф-т в р-р Fe3* (изб.). Ф-т охлажд. лед. Н2О, добавл. Н3РО4 (10 мл 85% р-ра). Титр, до роз. Восст. (см. выше), добавл. р-р I (изб.). Титр, р-ром 11 или р-ром Ce(SO4)2 с дифенилам, до фиол. К щел. плаву добавл. NaCl. Фильтр. (эмпир.) Эмпир. 1,33
NaOH (II) К ос. добавл. р-р I (изб.). Титр, р-ром II с мет. ор. до желт. (TaV) 1,16 (NbV)
VI группа периодической системы
Н2о Реактив Фишера (стр. 25) Анал. в-во, содержащее 5—10 ммоль Н2О раств. (или суспендируют) в безводн. СНзОН в колбе с притертой пробкой. Титр, до кр.-кор. (для суспензии окр. должна сохраняться 15 мин). Вносят поправку на холостой опыт 1
Н2О2 Na2S2O3 Анал. р-р, H2SO4 (10 мл 4 н.), KJ (6 мл 1 и.), (NH4)2MoO4 (3 капли 1 и.). Титр, до бц. 2
J2 (I) и Na2S2O3 (II) Анал. р-р (в колбе с притертой пробкой), NaOH (10 мл 1 и.), р-р I (изб.). Через 5 мин добавл. НС1 и титр, р-ром II с крахм. до бц. 2
KMnO4 Анал. р-р (100 мл, —60 мг Н2О2), H2SO4 (10 мл р-ра 1:1). Титр, до роз. 2
FeSO4 (I) и KMnO4 (II) См. опр. S2O3- (стр. 337) 2
KBrO3 Анал. р-р, МпС12 (la), НС1 (25 мл 1 н.). Титр, до бл.-желт. Нагр. до 40° С. Титр, медленно до желт. 2
331
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определив-мое вещество (иои) Рабочий раствор Методика определения М/Э
Н2О2 Ce(SO4)2 Анал. p-p (~0,03% H2O2), H2SO4 (10 мл 9 н.). Титр, с ферроином до бл.-гол. 2
Аскорбиновая кислота Анал. р-р, Fe2+ (изб.). Далее см. опр. Fe3+ (стр. 349) 2
Кислород — Н2С2О4, 0,05 н. (I) и Анал. в-во (~0,3 г РЬО2), р-р 1 (изб.), 2
активный НСЮ4 (8 мл 60% р-ра), Н2О (42 мл).
(например, в КМпО4, 0,07 н. (И) Кип. в колбе, закр. воронкой, до раств.
РЬО2, МпО2, РЬ3О4) пробы, добавл. Н2О до 100 мл, нагр. до 80° С. Титр, р-ром 11 до роз. Проводят холостой опыт
Na2$2^3 Анал. в-во (~50 мг МпО2), KJ (0,5 г), Na-ЭДТА (10 мл 0,1 М), CH3COONa (0,5 г), СНзСООН (10 мл 5% р-ра). Перемеш. до раств. пробы. Титр, с крахм. до бц. 2
KJ(I) (М/Э=2) и KJO3 (11) Анал. в-во, р-р I (изб.), НС1 (25 мл конц). Взбалт. Титр р-ром II с СНС1з до бц. 2
(О2, растворенный в воде) Na2S2O3, 0,01 н. В толстостенном сосуде. Анал. р-р, MnSO4-4H2O (1 мл р-ра 480 г в 1 л), NaJ (1 мл р ра 900 г в 1 л, содержа щем 400 г NaOH). Закр. колбу и тщательно перемеш. После отстаивания добавл. H2SO4 (2 мл 1:1). Закр. и перемеш. Титр, часть р-ра с крахм. до бц. 2
Оз Na2S2O3 В поглотительный сосуд наливают KJ (100 мл 2% р-ра), пропускают анал. газ, добавл. H2SO4 (10 мл 1 М). Титр, с крахм. до бц. 2
S2- KJO3 (I) и (/4/3 = 6) Na2S2O3 (II) Анал. р-р, р-р I, NaOH (10 мл 10 и.). Кип. 10 мин, охл., добавл. KJ (5 мл 5% р-ра), H2SO4 (20 мл 8 н.). Титр, р-ром 11 с крахм. до бц. 8
J2 (I) и Na2S2O3 (II) Р-р 1 (изб.), НС1, анал. р-р. Титр, р-ром II с крахм. до бц. 2
KJO3 Анал. в-во (ос. сульфида), рабочий р-р (недостаток), НС1 (до 8,5—10,5 н.). Титр, с СС14 до бц. или с красителем амарантовым до бц. 4*
NaClO или NaBrO (I) и Na2S2O3 (II) Анал. р-р (4 и. NaOH), р-р I (изб.). Через 5 мин добавл. KJ (2 г), Н2О (4 объема), НС1 (конц. р-р до бур., затем небольшой изб.). Титр, р-ром II с крахм. до бц. 8
* 3S2 -г 4Н2О = 2Ь ; SO2 -г Ыр т 12е—.
335
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяе мое вещество (ион) Рабочий раствор Методика определения м/.э
S2- КМпО„ (I) P-p I (25 мл 0,1 н.), NaOH (5 мл 4 п.), 8 или
(Л1/Э = 5) и анал. р-р (10 лиг~0,1 н.). Через 5 мин 7*
Na2S2O3 (II) NH4VO3 подкисл., добавл. KJ, титр, р-ром II См. опр. J- (стр. 345) 8
К3 [Fe (CN)6] Анал. р-р, аммиачн. буф. (pH = 9). Титр. 2
К7 [Cu (JO6)2]_ с диацетилглиоксиматом Fe2* до бц. а) Анал. р-р (р-Н = 9,4-=-12) титр, до з. 2
б) Анал. р-р, NaOH (4—5 н.), OsO4 (ка- 8
HCI тал.), титр, до з. Титр, с мет. ор. до ор. 2
AgNO3 (I) и Анал. в-во (ос. сульфида) взбалт. с 2
S2°r NH4SCN (II) J2 р-ром I (изб.). Титр, р-ром II с Fe3* до роз. Анал. р-р (слабокисл.: при 0,1 н. рабочем 1
J2 (I) и р-ре рН<7,6, при 0,001 н. р-ре рН<5) титр, с крахм. до син. (SO|~ маек. НСОН) Анал. р-р (~0,01 Л1), NaOH (Юлл I н.), р-р I (изб.). Через 5 мин добавл. H2SO4. Титр, р-ром II с крахм. до бц. Рабочий р-р, KJ (1 а). Титр. анал. р-ром 8
Na2S2O3 (II) JC1 (М/Э = 2) 1
NH4VO3 с крахм. до бц. См. опр. J" (стр. 345) 8
so2- J2 (I) и Р-р I (изб.), анал. р-р. Титр, р-ром II с крахм. до бц. Р-р I (изб.), СНзСООН (до 2 н.), анал. р-р. Через 1 мин титр, р-ром II с фе-нилантр. к-той до з. См. опр. AsO®- (стр. 331 п. «а» или «б»; 2
N32S2O3 (II) K2Cr2O7 (I) и 2
соль Мора (II) KJO3 2
NH4VO3 (I) и перед добавл. НС1 ее охл. до 18° С) Р-р 1 (изб.), НО (до 5 н.), анал. .р-р, 2
(NH4)2Fe(SO4)2 (II) NaClO (I) и JC1 (1 мл) **. Через 5 мин титр, р-ром II с фенилантр. к-той до з. Анал. р-р (щел.), р-р I (изб.)', Н2О (до 2
Na2S2O3 (II) NaClO2 150 л(л). Далее см. опр. С1О“ (стр. 342, 343) Н2О (100 им), KJ (15 мл 10% р-ра), 2
(M/Э = 4) Хлорамин T (I) крахм., анал. р-р. Титр, до син. Анал. р-р, р-р I (изб.), KJ (I г). Титр, р-ром II с крахм. до бц. См. опр. S2' (см. выше) 2
и Na2S2O3 (II) KMnO4 (I) и 2
Na2S2O3 (II) NH4VO3 См. опр. J- (стр. 345) 2
* При титровании S2 окисляется до SO2 , а в присутствии Н6ТеО6 до S2O2 .
** KJ (25 мл 0,04 М), НС1 (40 мл 12 Af), KJO3 (20 мл 0,025 Л1), СС14 (3 мл), KJ или KJO3 до почти бц. СС14.
336
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения Л1/Э
52ОГ Na2S2O3 Анал. р-р (30 лиг), KJ (4 г). Через 15 мин добавл. СНзСООН (1 мл 6 и.). Титр, с крахм. до бц. 2
FeSO4 (I) и KMnO4 (II) Анал. р-р, Н3РО4 (5 мл 40% р-ра), H2SO4 (10 мл 5 н.), р-р I (изб.). Через 5 мин титр, р-ром И до роз. 2
H2SO4 NaOH Анал. р-р титр, с мет. ор. до желт, или с фенолфт. до роз. 2
Анал. р-р, KJO3 (5 мл 3% р-ра), KJ (2 г). Титр, с крахм. до бц. 2
SO*- BaCi2 Анал. р-р (рН=8), сп. (25 мл). Титр, с тетраоксихиноном (0,5 мг) до роз. 2
ВаС12 (I) и (NH4)2 so4 (р-р в 50% сп.) (П) Анал. р-р (~10 мг SOj" и 2 мг-экв HCI). Harp, до 90°С, добавл. р-р I (изб.), продолжают нагр. (10 мин)', охл., добавл. сп. (I объем). Титр, р-ром II с родизонатом натрия до бц. 2
BaCL (I) (Л4/Э = 3), K2CrO4 (II) и Na2S2O3 или FeSO4 (III) Анал. р-р, НС1 (до 0,2 н.). Нагр. до кип., добавл. медленно р-р I (~ полуторакратный изб.), нагр. (2 ч), добавл. NH4OH (до щел. реакции по лакмусу). Охл., добавл. р-р II (изб.). Фильтр, н промыв. Н2О. В ф-те опр. Сг2О*~ (стр. 340) 3
Na2S2O3 Анал. р-р (нейтр.), ВаСгО4 (изб.)'. Взбалт., фильтр, и промыв. Н2О. В ф-те опр. Сг2О*- 3
NaOH Анал. р-р (НС1 не >0,5 и.), бензидин* (60 мл 0,67% р-ра). Через 15 мин фильтр., промыв. Н2О (5 раз по 3 мл). Ос. раств. в НгО (60°С). Титр, с фенолфт. до роз. 2
Pb (NO3)2 Анап. р-р титр, с эозином до кр. 2
J2 Анал. р-р, HJ, NaH2PO2, HCI. Титр, с крахм. до син. 2
BaCI2, 0,02 и. (I) и Na-ЭДТА (II) Анал. р-р, HCI (1 мл 2 н.), добавл. р-р I (изб.). Кип. 5 мин. Охл., добавл. Mg-ЭДТА (5 мл)'. ** Титр, р-ром II с хромоген, черн. до сии. 2
Se Na2S2O3, 0,02 и. (I) и J2, 0,02 и. (II) Анал. в во (ос. Se; стр. 295), НС1 (10 мл конц. р-ра), Вг2 (4 капли), Н2О (20 лгл)\ фенол (5%> до бц), Н2О (до 100 мл), р-р I (изб.). Титр, р-ром II 4
* 6,7 г бензидина основания растворяют в 20 мл 6 н. НС1, разбавляют до 1 л.
** NH4CI (8,28 г) растворяют в конц. NH4OH (ИЗ мл), добавляют р-р Mg-ЭДТА (10 мл 10% р-ра MgC12. титруют в присутствии указанного буферного р-ра 10% р-ром Na-ЭДТА) и разбавляют до 1 л
22 Зак. 783
337
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяе-мое вещество (ион) Рабочий раствор Методика определения м/э
Se KBrOg (М/Э = 4) или КЛО3(Л4/Э = 4) Анал. в-во (ос. Se. стр. 295), KCN (р-р трехкратный изб.); выпар., добавл. Н2О (10 .мл), гуммиарабик (2 мл 1% р-ра), НО (10 мл конц. р-ра); продувают воздух (15 мин). Титр, до бц. 4
KMnO4 (I) и (NH4)2 Fe (SO4)2 (Н) Se раств. в смеси HNO3, H2SO4 и Н2О (1:1:1). Далее см. опр. SeO*- 2
H2SeO3 NaOH Анал. р-р титр, с мет. ор. до ор. или с фенолфт. до роз. 1 2
SeO*’ Na2S2O3 Анал. р-р, Н2О (150 мл), крахм. (15 мл 2%), KJ (10 мл 1 н.), НО (10 мл 5 н.). Через 5 мин титр, с крахм. до бц. 4
КгСг2О7 Анал. р-р, НО (8 н.), JC1 (катал.). Титр, с фенилантр. к-той до фиол. 2
KMnO4 (I) и (NH4)2 Fe (SO4)2 (II) Анал. р-р, H2SO4 (20 мл 18 н.), Н2О (100 мл), Na2HPO4 (12 г), р-р I (изб.). Титр, р-ром 11 с о-фенантролином до 2
KBrO3 (I) и NaAsO2 (II) кр. Навеска анал. в-ва (~0,2 г SeO2), р-р 1 (изб.). Кип. до удаления Вг2, добавл. р-р 11, НО (10 мл конц. р-ра). Титр, р-ром I с прочным кр. В (2 капли 0,5%) до бц. 2,4*
NaBrO (I) и Na2S2O3 (II) Анал. р-р, КНСО.-, (10 мл 1 н.), р-р I (нзб.), Н2О (50 мл), KJ (10 мл 1 н.), НО (5 мл 5 н.), (NH4)2MoO4 (5 капель р-ра). Титр р-ром II с крахм. до бц. 2
SeO*-4 Na2S2O3 Анал. р-р, НО или HBi (изб. конц. р-ра). Кип., улавливая О2 или Вг2 р-ром KJ. Титр, этот р-р с крахм. до бц. 2
TeO|- KMnO4 (I) н (NH4)2Fe(SO4)2 (П) Анал. р-р (18 н. H2SO4), NH2OH • НО (1г). Кип. Фильтр., промыв. В ос. опр. Se 2
J2 Анал. р-р (нейтр.), гуммиарабик (5 мл 1% р-ра), Н3РО4 (5 мл конц. р-ра), разб. Н2О (до 60 мл), добавл. NaH2PO2 (2—3 г). Нагр. до кип., охл. Разб. (до 150 мл). Титр, (в конце титр, добавл. СС14) до роз. 4
K2Cr2O7 (I) и FeSO4 (II) Анал. р-р (200 мл), НО (10 мл конц. р-ра), р-р I (изб.). Через 10 мин добавл. р-р 11 (изб.). Титр, р-ром I с Ks[Fe(CN)6] (внешний инд.) до син. 2
Ce (SO4)2 (I) и FeSO4 (II) Анал. р-р, H2SO4 (Юлм 1 : 1),Сг3+ (20.мг), разб. (до 200 мл), добавл. р-р I (изб.). Кип. (10 мин). Титр р-ром (11) с ферроином до кр 2
9_ __
*5 моль SeQg эквивалентны 2 моль, г. е 12 г~экв. БгО^
338
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ПОН) Рабочий раствор Методика определения м/э
ТеО|- NaJO4 (I) (А1/Э=2) и FeSO4 (II) Анал. р-р, р-р I (изб.), НзРОь H2SO4 (1 н.). Титр, р-ром II с дифенилам, до бц. 2
ТеО4~ Na2S2O3 J2 Анал. р-р, НО или НВг (изб. конц. р-ра). Кип., улавливая газ р-ром KJ. Титр, с крахм. до бц. См. опр. ТеО|~ 2
Сг3+ KMnO4 (М/Э= 1) Рабочий р-р (изб.), NaOH (до0,8—1,5 н.). ВаС12 (изб.). Титр. анал. р-ром до желт. 3
FeSO„ (I) и KMnO4 (II) или K2Cr2O7 (Па) Анал. р-р (содержащий H2SO4 1 Л1, HNO3 0,15 Л1), AgNO3 (1 мг/мг Сг), (NH4)2S2O8 (до 0,5 М). Кип. (10 мин). Опр. Сц>О7~ (стр. 340) 3
FeSO4 (I) и KMnO4 (II) Анал. р-р, HCIO4 (изб. конц. р-ра). Кип., охл., добавл. р-р 1 (изб.). Титр, р-ром II с ферроином до гол 3
KMnO4 (а) или K2Cr2O7 (6) или J2 (в) Анал. р-р проп. через Zn-редуктор в р р NH4Fe(SO4)2 (изб. в атм. СО2). Титр, р-ром (а) или (б) с дифенилам, до сии. или р-ром (в) с крахм. до син. 1
Na2S2O3 а) Айал, р-р, МпС12, H2SO4 (до 1 н.), Н3РО4 (5—10 мл 85% р-ра), КВгО3 (2 г). Кип. (5—10 мин), добавл. (NH4)2SO4 (5 г), кип. до удаления Вг2 (перед окончанием добавл. НС1 10 мл 1 н.). Опр. СггО7~ (стр. 340) б) Анал. р-р (0,02—0,03 г Сг в присутствии Mn2+), NaOH (20 мл 2 и.). Н2О2 (30 мл 3% р-ра). Кип., добавл. медленно Ni(NO3)2 (5 мл 5% р-ра), кип. (3 мин). Охл., добавл. KJ (2 мл 1 и.), НС1 (10 мл конц. р-ра). Титр, с крахм. до бц. 3 3
Ce (SO4)2 (I) и Na2C .O4 (II) Анал. р-р, р-р I (изб.), H2SO4 (до 1 Л1). Нагр. Титр, р-ром II 3
K7 [Cu (JO6)2[ ИЛИ K9 (Cu (TeO6)2J Анал. р-р (шел.). Титр, до бур. 3
NaBrO (I) и H2O, (II) Анал. р-р (нейтр.), NaOH (10 мл I н.), р-р I (изб.). Через 5 мин титр, р-ром II с люцигенином (люминесценция) 3
Na-ЭДТА (I) и MnSO4 (II) или ZnSO4 (Ila) Анал. р-р, аммиачн. б\ф. (рН=9,7) (в присутствии Мп2+ добавл., аскорбиновую к-ту), р-р I (изб.). Титр, р-ром II или Па с хромоген, черн. до кр. 2
22*
339
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ИОН) Рабочий раствор Методика определения М/Э
Сг2ОГ FeSO4 (I) и КМпО4 (11) или К2Сг2О7 (Па) Анал. p-p (кисл.), p-p I (изб.). Титр, р-ром II без ннд. до роз. или р-ром Па с дифениламинсульфонатом бария до фиол. 6
Na2S2O3 См. опр. конц. р-ра Na2S2O3 (стр. 313) 6
TiCl3 Анал. р-р, Н3РО4 (5 мл конц. перед концом титр.). Титр, с дифенилам, до бл.-з. 6
SnCl2 Анал. р-р, HCI (до 3—3,5 н.). В атм. СО2 титр, с дифенилам, до з. 6
vso4 Анал. р-р (кисл.) титр, с Fe(SCN)3 до з. 6
Аскорбиновая кислота Анал. р-р титр, с вариамин. син. до з. 6
Г идрохиион Анал. р-р (10—20% H2SO4 или 5% HNO3) титр, с дифенилам, до бл.-з. 6
МоОГ 4 КМпО4 Анал. р-р (120 мл, ~50 мг Мо, 6% H2SO4). Нагр., пропускают через Zn-pe-дуктор в р-р (20 мл), содержащий NH4Fe(SO4)2- 12Н2О (49 г/л), Н3РО4 (40 мл 85% на 1 л) и H2SO4 (50 мл конц. к-ты на 1 л). Титр, при сильном перемеш. до роз. 3
NH4VO3 Анал. р-р (1—2 н. НС1) пропускают через Bi- или Ag-редуктор или добавл. Hg или N2H4. Титр, с фенилантр. к-той до кр.-фиол. или с дифенилам, до фиол. 1
KJO3 Анал. р-р пропускают через Zn-редуктор, в р-р JCI (изб.) и НС1 (0,05 н.). Титр, с ССЦ до бц. 3
Се (SO4)2 Анал. р-р (3 н. HCI), Hg, взбалт., фильтр., промыв. НС1 (1:5). Ф-т, добавл. H2SO4 (20 мл р-ра 1:1), НС1 (до 300 мл р-ра 1:5). Титр, с феррон-ном до гол. 1
Pb (NO3)2 Анал. р-р (5*10'4 н. HNO3) титр, с эозином до кр. или с таннином 2
KBrO3 (I) и Na2S2O3 (II) Осажд. 8-оксихинолином. См. опр. VO^“ (ос. раств. в 2 н. NaOH) 8
wor 4 Na-ЭДТА Анал. р-р, СаС12. Фильтр., промыв. В ос. опр. Са2+ (стр. 318) 2
Pb (NO3)2 Анал. р-р (рН=9). Титр, с диаминовым прочным ярко-кр. или с бромтимоловым син. 2 S
nh4vo3 (или KMnO4) Осажд. WO3 действием HNO3 (стр. 296), фильтр., промыв. НС] (2% р-р). Ос. раств. в NaOH (5% р-р) или NH4OH. добавл. Н3РО4 (8 мл конц. р-ра) и H2SO4 (30 мл р-ра 1:3), Cd (3—5 г). Нагр. в колбе с клапаном на водяной бане до светло-з. (30—40 мин). Фильтр, (в атм. СО2), титр, с фенилантр. к-той до фиол.
340
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М/Э
WO*- КВгОз (I) и Na2S2O3 (П) Осажд. 8-оксихинолином (см. опр. VO~ (стр. 333). Ос. раств. в нагретом р-ре NaOH (4 н.), добавл. Н2С2О4 (10—20 мл 15% р-ра), НС1 (4 н., изб. по метил, кр.), добавл. р-р I (изб.). Опр. 8-оксихинолин (стр. 324) 8
NaOH (1) и НС1 (11) Осажд. WO3 действием HNO3 (стр. 296), фильтр., промыв. HCI (2% р-р), Н2О. К ос. добавл. р-р I (изб.). Титр, р-ром II с фенолфт. до бц. или в присутствии глицерина с мет. кр. до кр. 2
ио*+ NH4VO3 Анал. р-р (кисл.) пропускают через редуктор (Zn или Ag, Pb, Ni, Sn, Fe), или добавл. амальгаму (Cd, Bi, Pb, Zn) (при применении Zn или Sn окисл. воздухом U34), H3PO4 (5 мл). Титр, с фенилантр. к-той до фиол. 2
КМпО4 Опр. как с NH4VO3 титр, до роз. 2
Се (SO4)2 То же; титр, при 50° С (в конце титр.) с ферроином до бц. (св.-гол.) 2
К2Сг2О7 Восст. до U4+ (см. выше), добавл. FeCl3 (20 мл 2% р-ра), Н3РО4 (15 мл 85% р-ра). Титр, с дифениламинсульфонатом до кр.-фиол. 2
КВгОд И Na2S2O3 Анал. р-р нейтр. (до помутнения), добавл. CHsCOONa (25 мл 20% р-ра), разб. (до 100 мл). Нагр. до кип. осажд. 8-оксихинолином (4% в 1,5 н. СНзСООН), добавл. NH4OH (1 н. до нейтр. большей части СНзСООН), кип. I мин, охл. до 40° С. Фильтр., промыв. (0,04% гор. р-ром 8-оксихинолина). Ос. раств. в HCI. Опр. 8-оксихинолин (стр. 324). 12
Na-ЭДТА VII групп Анал. р-р, НС1 (до 0,1—0,2 М). Нагр. Титр, с хромоген, черн. до син. а периодической системы 2
F" Th (NO3)4 * Анал. р-р (100 мл, ~20 мг F"), добавл. ализариновый кр. S (8 капель 0,1% р-ра). Нейтр. (NaOH и НС]) до желт., добавл. 2,5 мл буф рН = 3**. Титр, до роз. 1
А1С13, 0,16 Л4 (М/Э = 3) Анал. р-р нейтр. по фенолфт., добавл. 1/2
NaCl (до нас.). Титр, при 70°С с мет. кр. до роз. (эмпир.)
* Концентрацию р-ра определяют по навеске NaF.
** 50 мл 1 н. р-ра CHgClCOOH нейтрализуют по фенолфталеину 1 н. р-ром NaOH, добавляют 50 мл 1 н. CH2CICOOH н разбавляют до 250 мл.
341
объемные методы определения неорганических веществ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М!Э
F" НС1, 0,25 н. (1) Анал. р-р (нейтр.), Na2SiO3 (нейтр. по 2/3
и NaOH (11) смеси мет. желт, с метилен, син. 0,1% сп. р-р 1 : 1), добавл. р-р 1 (изб.), КС1 (2 г/25 мл). Титр, р-ром II до з. (эмпир.)
СаС12 (1) и Na-ЭДТА (11) Анал. р-р (50 мл, 5—65 мг F"), НС1 (по мет. кр.), р-р I, изб. нейтр. NH4OH и НС1 (до роз). Кип. (15 сек). Через несколько часов добавл. 1 мл буф. * Титр, р-ром 11 с хромоген, черн. до син. 1
HF NaOH Анал. р-р титр, с фенолфт. до роз. 1
СГ AgNO3 а) Анал. р-р (pH=6,5-j-10,5) **. Титр, с К2СгО4 до кр. б) Анал. р-р (нейтр.). Титр, с флюорес-цеином до кр. ос. *** в) Анал. р-р (нейтр. или слабокисл.). Титр, с днхлорфлюоресцеином до кр. ос. 1 1 1
AgNO3 (I) и NH„SCN (11) Анал. р-р (30 мл. ~ 130 мг С1~, 3 мл 6 н. р-ра HNO3), нитробензол (3 мл), р-р 1 (изб.) 4*. Титр, р-ром II с Fe3+ до кр. 1
Hg2 (NO3)2 См. опр. конц. рабочего р-ра (стр. 305) 1
Hg (NO3)2 См. опр. конц. рабочего р-ра (стр. 306) 1
НС1 NaOH См. опр. H2SO4 (стр. 337) 1
Na2S2O3 См. опр. H2SO4 (стр. 337) 1
Активный С1, Na2S2O3 а) См. опр. конц. Са(СЮ)2 (стр. 307) I (активный С1)
СЮ . <Са (СЮ)2 б) Хлорную известь (5 г) растирают с Н2О (5 мл), Разб. (до 500 мл). К 50 мл полученного р-ра, добавл. KJ (10 мл 1 н.), H2SO4 (15 мл 4 н.) Титр, с крахм. до бц 2 (СЮ-) 4 [Са (С1О)2|
KJ, 0,02 M Анал. р-р хлорной извести (50 мл, см. выше), NaHCO3 (3 г). Титр, с крахм. до син. То же
NaAsO2, 0,05 н. (I), J2, 0,05 h. (11) Рабочий р-р (изб.), NaHCO3 (75 мл 5% р-ра), анал. р-р. Через 5 мин добавл. СНзСООН (2 н., до появления СО2). Титр, р-ром II с крахм. до син. » »
Мет. op., 0,02% p-p Анал. р-р (0,01 н. НС1) титр, до кр. (Метод позволяет опр. примесь СЮ“ в хлорамине Т) » »
H2O2 Анал. р-р, NaOH (до 0,1 п.). Титр, при 80° С с люцигенином (люминесценция) » »
* 67 г NH4CI, добавляют 570 мл конц. NH4OH, HgO до 950 мл, 50 мл р-ра 0,507 г MgCl2-6H2O и 0,93 г Na-ЭДТА.
** В присутствии NH4 иН-6,5ч- 7,2. 4 ‘
*** В присутствии 5 мл декстрина (2?б) окрашивание во всем объеме.
4* Рекомендуется осадок AgCl отфильтровать.
342
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М/Э
Актив- FeSO, (I) и Анал. р-р, р-р 1 (изб.) Титр, при 60е С 1 (актив-
ный С], аскорбиновая р-ром II с SCN" до бц. ный С1)
СЮ , Са (С1О)2 кислота (II) 2(СЮ“> 4[Са(С1О)Я
Г идрохинон Анал. р-р (1—15% НС1). Титр, с дифенилам. или с о-дианизидином до бц. То же
N2H4 H2SO4 Анал. р-р (HCI или СНзСООН). Титр, с люцигенином (люминесценция) » »
СЮ- в NaAsO2 (I) Анал. р-р, смесь фенола (10 мл 0,5% р-ра) и NaOH (10 мл 2 н.), NaHCO3 (75 мл 5% р-ра), СНзСООН (2 н. до появления СО2). Титр, р-ром 11 с крахм. до син. 2
присутствии ВгО и JO" и J2 (11)
СЮ- Соль Мора (1) и КМпО4 (11) Р-р I (1 н. H2SO4), H2SO4 (25 мл 1 н.), анал. р-р, осмиевая к-та (3 капли 0,1% р-ра). Нагр. при 80—90°С несколько минут, охл. Титр, р-ром II до роз. 6
SnCl2 (1) и КМпО„ (II) Анал. р-р (6 М H2SO4), Na2MoO4 (10 мл 0,1 М), р-р I (двойной изб.) Титр, р-ром II до роз. 6
Соль Мора (I) и K2Cr2O7 (11) Анал. р-р (нейтр. по фенолфт.), р р I (изб.), (NH4)2MoO4 (3 капли 10% р-ра), HCI (40 мл конц. р-ра). Через 1 мин добавл. буф. * (20 мл), Н2О (до 200 мл). Титр, с дифениламинсульфо-натом до кр. 6
NaAsO2 (1) и КВгО3 (11) Р-р 1 (изб.), НС1 (10 мл 1 н.), КВг (0,2 г), анал. р-р, осмиевая к-та (3 капли 0,05% р-ра). Нагр. при 80—90°С несколько минут. Титр, р-ром II с мет. ор. до бц. 6
NasSjOg Анал. р-р, КВг (1 г), HCI (конц. до 8 н.). Через 5 мин добавл. KJ (100 мл 1% р-ра). Титр, до бц. 6
Аскорбиновая кислота Анал. р-р (4 н. H2SO4 при 60е С), H2SeO3, MnSO4 (катал.). Титр, до выделения Se (перед окончанием энергично встрях.) 6
AgNO3 (I) и NH„SCN (11) Анал. р-р (H2SO4), Zn- или Bi-амальгама. В ф-те опр. С1“ 1
СЮ4" SnCI2 (I) и КМпО„ (11) См. опр. С1О^. Перед титр, р-ром И кип. в атм. N2 30 мин 8
Вг" AgNO3 а) См. опр. С1‘ (стр. 342) б) Анал. р-р (0.1 и. СНзСООН) титр, с эозином до кр. 1 1
* 250 мл конц. Н3РО4 смешивают с 1 л 4 7И р-ра CHaCOONa.
34Х
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М1Э
Вг“ AgNOg (I) и NH4SCN (II) См. опр. CI* (стр. 342) 1
Hg2 (NO3)2 Опр. как С1*; см. опр. конц. р-ра Hg2(NO3)s по NaCl (стр. 305) 1
Hg (NO3)2 См. опр. CI* (стр. 342) 1
KMnO4 Анал. р-р (100 мл), Нг5О4 (10 мл конц. р-ра). Титр. кнп. р-р до роз. 1
JNa2S2O3 Анал. р-р окисл. NaClO или хлорной водой (в щел. среде). Опр. ВгО^" (см. ниже) 6
KBrOg (I) и Na2S2O3 (II) Анал. р-р, KCN (10 мл 1 н.), НС1 (до 10% р-ра), р-р I (медленно до желт.), солянокнсл. анилин (20 мл 10% р-ра), КВг (10 мл 0,1 н.). Через 1 мин добавл. KJ (1 г). Тнтр. с крахм. до бц. 3
Вг2 <ВгО~) Na2S2O3 Анал. р-р, НС1 (до 0,1—2 М), KJ (1—2 г) Тнтр. с крахм. до бц. (СЮ* маек. KCN) 2
H2O2 Анал. р-р, NaOH (до 0,1 н.). Титр, с люцигенином (люминесценция) 2
N2H4 См. опр. СЮ* (стр. 343) 2
Г идрохинон Анал. р-р (1—3% HCI) тнтр. с о-днани-зидином до бц. или с дифенилам, до бц. 2
ВгО8~ Na2S2O3 Анал. р-р (нейтр.), KJ (1 мл 1 н.), НС1 (1 мл 4 и.), (NH4)2MoO4 (3 капли 1 н.). Титр, с крахм. до бц. 6
SnCl2 Анал. р-р (HCI), KJ (немного). Тнтр. с крахм. до бц. 6
n2h4 Анал. р-р (HCI), KJ. Титр, с крахм. до бц. 6
Аскорбиновая кислота См. опр. С1О“ (стр. 343) 6
J- AgNO3 а) Анал. р-р (нейтр. или уксуснокисл.). Титр, с эозином (или с днхлорфлуо-ресцеином) до кр. или без инд. до просветления. В присутствии С1* и Вг* тнтр. с диметилдниодфлуоресцеином до син.-кр. б) Анал. р-р (нейтр. или слабокислый), крахм., J2 (или KJO3) до снн. Титр, до желт. I 1
AgNOg (I) и NH4SCN (II) См. опр. С1* (стр. 342) 1
Hg (NO3)2, 0,02 h. Анал. р-р (50 мл, <130 мг J*), HNO3 (2 мл 0,5 н.), пиридин (5,7 мл I :9). Тнтр. с дифенилкарбазидом до син. 1
344
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М/Э
J' Na2S2O3 а) Анал. р-р, Н3РО4 (5 мл 4 н.), хлор- 6
ная известь (5% или хлорная вода) до бц., фенол (5 мл 10% р-ра). Через
5 мин добавл. KJ (5 мл 1 н.). Титр, с крахм. до бц.
б) Анал. р-р (100 мл, не <10 мг J2), 6
СНзСООН (5 мл лед. к-ты), CH3COONa (10 мл 20% р-ра), бромная вода (изб.). Через 10 мин добавл. НСООН (80% р-ра до бц.), KJ (2 г) и H2SO4 (разб.). Титр, до бц.
KJO3 а) Опр. как AsO|- или как Sn2+ 2
б) Анал. р-р, ацетон (20—30 мл), H2SO4 2
(до 2 н. в конце титр.). Титр, с крахм. до бц.
KBrO3 Анал. р-р, KCN (7 мл 1 н.), Н3РО4 (до 2
30% или НС1 до 10% р-ра). Титр, с крахм. до бц.
NaClO Анал. р-р, NaHCO3 (I г). Титр, с крахм. 6
ДО син.
Хлорамин Т Се (SO4)2 См. опр. Sn2+ (при 4 н. НС1) Анал. р-р, ацетон (25 мл), H2SO4 (10 мл 2 2
1:1). Титр, с ферроином до гол.
КМпО4 NaOH (1,5 г), Н3О (5 мл). Охл., добавл. 8
0,1 М (I) (М/Э — 1) и р-р I (изб.), анал. р-р. Через 1 мин добавл. BaCIs (6 мл пас. р-ра). Тнтр.
HCOONa (II) NH4VO3 р-ром II до бц. Анал. р-р, HCI (до 7 н.). Тнтр. с JC1 2
(5 мл 0,02 М) и СНС13 (или CCI4 5 мл) до св.-желт.
NaJO4 Анал. р-р (HCI 4—7 н.) тнтр. с СНС13 2
(М/Э = 6) до св.-желт.
J2 Na2S2O3 Анал. р-р (KJ 2 г; pH <7,6 при 0,1 н. и <5 при 0,001 н. J2). Титр, с крахм. до бц. 2
(JO )
или с СНОз до бц. или с варнамнн. син. до бц. (Вг2 связывают HCOONa)
NaAsO2 Анал. р-р (pH = 5,54-9,5) титр, с крахм. 2
Н2О2 до бц. Анал. р-р, NaOH (до 0,1 н.), Ni(OH)2. 2
Титр, с люцнгеннном (люминесценция)
SnCl2 Анал. р-р (HCI 2 н.) титр, (в атм. СО2) 2
Hg2 (NO3)2 с крахм. до бц. Анал. р-р (кисл.), NH4SCN (изб.). Тнтр. 2
с крахм. до бц. или без него до помутнения
Г идрохинон Анал. р-р (1—10 мкг J2; рН=6-^8), 2
NaHCO3. Титр, с крахм. до бц.
KJO3 См. опр J" 2
N2H4 Анал. р-р, NaHCO3 (до рН = 6-=8). Титр. 2
345 >
объемные методы определения неорганических веществ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения М!Э
,Ю- Na2S2O3 Анал. р-р (кисл.), НС1 (10 мл 1 н.). KJ 6
SnCl2 (2 г). Титр, с крахм. до бц. Анал. р-р, НО (конц.). Титр, с крахм. 6
до бц.
Аскорбиновая См. опр. С1О~ (стр. 343) 6
кислота
Na^SpOa Анал. р р, НО (50 Л1Л 2 н.). Через I ч 6
(в присут- добавл. фенол (10 мл 5% р-ра). Титр, с крахм. до би.
ствни ВгО“)
JO; NaAsO2 Анал. р-р, Na2B4O? (20 мл нас. р-ра, со- 2
держащего 0,5 г Н3ВО3), KJ (2 г). Титр, до бц.
Na2S2O3 Анал. р-р (кнсл.), KJ (~2 г). Титр, с 8
крахм. до бц.
Мп2+ KMnO4 а) Анал. р-р (500 мл слабокисл.), ZnO 2
(М/Э = 3) (1 г), ZnSO4 (1 г). Harp, до кип. Титр. (в конце титр, добавл. 1 мл СНзСООН' до роз.
KMnO4 б) Анал. р-р (<30 мг Мп), NH4C1 (2— 1
(М/Э = 4) 3 г). Нейтр. NH4OH, добавл. НС1 (15 мл 4 н.). Охл. ниже 10° С, добавл. NH4F (6 г). Титр, до роз.
H2C2O4 (I) и Анал. р-р (0,1 н. H2SO4; 3—55 мг Мп), 2
KMnO4 (И) Н2ТеО4 (80 мг/5 мг Мп), NaOH (до 2,5 н.), Н2О2 (20 объемн. %, 0,2 мл/5мг Мп). Harp, при 60°С (10 мин)-, нагр. до кип., добавл. р-р 1 (изб.), H2SO4 (2 н., изб.). Титр, при 70° С р-ром II
до роз.
FeSO4 Анал. р-р (200 мл 0,5 н. H2SO4), НРО3 (10 г), AgNO3, (4 тил 0,1 и.), (NH4)2S2O3 2 г в 10 мл Н2О). Кип. (25 мин), охл. 5
Титр, с дифенилам, до св.-з.
Na2S2O3 Н3РО4 (20 мл 20% р-ра), AgNO3 (10 мл 5
0,1 н.), HNO3 (1 мл 65% р-ра), HF (2,5 мл 40% р-ра), (NH4)2S2O8 (2,5 г), Н2О (30 мл). Harp, (при 60° С), добавл. анал. р-р, нагр. Кип. 5 мин после по-
явления фиол. окраски. Охл., добавл. Н2О (100 мл), KJ (10 мл 1 н.). Титр.
KBrO3 + КВг до бц. а) Анал. р-р, CH3COONa (1 <?/50 мг Мп), 8
(О и N2H4OH • НС1 (0,1 г) илн нас. р-р SO2
. Na2S2O3 (И) (несколько капель). Нейтр. (NaOH и НС1 по фенолфт.). Нагр. (до 60°С), добавл. 8-оксихинолин (изб. сп. р-ра). Нагр. до кнп. Через 15 мин фильтр., промыв. В ос. опр. 8-оксихииолин (стр. 324)
346
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
П родолжение
Определяемое вещество (ИОН) Рабочий раствор Методика определения ,м/.ч
Мп2> КВгОз + КВг (1) и Na2S2O3 (II) б) Анал. р-р, Н2О (80 мл на 0,1 г Мп), антранилат натрия (60 мл 3% р-ра на 0,1 г Мн). Через 1 ч фильтр., промыв. Ос. раств. в 4 н. НС1. Опр. антр. к-ту (стр. 322) 2
Na-ЭДТА Анал. р-р (100 мл, <25 мг Мп), NH2OH • • НС1 (несколько кристаллов), аммиачн. буф. (10 мл) *. Титр, с пирокатехин.-фиол. до кр.-фиол. 2
МпО2 NaAsO2 (I) и KMnO4 (11) Анал. в-во (~0,5 г), р-р I (изб.), H2SO4 (20 мл конц.). Кип., охл., добавл. Н2О (400 мл), KJ илн KJO3 (следы). Титр, р-ром II до роз. 2
Na2S2O3 Анал. в-во (~50 мг), KJ (0,5 г в Н2О), Na-ЭДТА (10 мл 0,1 М), CH3COONa (0,5 г), СНзСООН (10 мл 5% р-ра). Перемеш. до раств. Титр, до бц. 2
H2C2O4 (I) или FeSO4 (la) и KMnO4 (11) Анал. в-во, р-р I (или р-р 1а) (изб.), НСЮ4 (8 мл 60% р-ра) или H2SO4 (не >20% в конце кипячения), Н2О (42 мл). Кип. до раств., добавл. НгО (до 100 мл). При 80° С титр, р-ром II до роз. 2
МпОГ 4 FeSO4 (I) и KMnO4 (II) Анал. р-р (H2SO4 I М), р-р I (нзб.). Титр, р-ром 11 роз. 5
NaAsO2, или H2C2O4 или Na2S2O3 См. опр. конц. КМпО4 (стр. 311) 5
Hg2 (NO3)2 Анал. р-р, р-р соли Мора (изб.). Титр, с NHiSCN до бц. 5
Res+ и Re,+ Ce (SO4)2 (1) Анал. р-р, р-р I (изб.). Титр, р-ром II с 4 или.
и FeSO4 (II) ферроином до кр. 3
HReO4 KMnO4 Анал. р-р пропускают через редуктор (Zn илн др.) в р р Fe3+. Титр, до роз. 8
VIII группа периодической системы
Fe2+ КМпО4 а) Анал. р-р (без СП; H2SO4 5% и Н3РО4 1%). Титр, до роз., сохраняющейся 30 сек б) Анал. р-р НС1, реактив Циммермана-Рейнгарта (25 мл) (стр. 25), Н2О (400 мл). Титр, до роз. (сохраняющейся 30 сек); вносят поправку на холостой опыт. 1 1
* Смесь равных объемов NH4CI (1 н.) и NH4OH (1 н.).
347
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (мои) Рабочий раствор Методика определения м/э
Fe2+ К2СГ2О7 Анал. р-р, H2SO4 или НС1 (10 мл 4 н.), Н3РО4 (5 мл конц. р-ра). Титр. с дифе-ннламинсульфонатом натрия до фнол.-снн. 1
nh4vo3 См. опр. конц. р-ра NH4VO3 (стр. 312) (HCI до 4 н. не мешает) 1
Се (SO4)2 Анал. р-р (1 М H2SO4) тнтр. с ферроином до бц. 1
KJO3 Анал. р-р, JC1 (6 мл р-ра *), Н2О (до 50 мл), НС1 (50 мл конц. р-ра), СС14 (5 мл). Титр, с СС14 (или с красителем амарантовым) до бц. 1
NaJO4 (М/Э = 2) Анал. р-р (H2SO4 1 н.), Н3РО4. Титр, с дифенилам, до син. 1
NaJO4 (М/Э = 6) Анал. р-р (HCI 4—7 н.) тнтр с СС14 или с иодокрахм. до бц. 1
Хлорамин T См. опр. Sn2"* (стр. 325) 1
Рабочие р-ры для опр. Fe3+ (см. ниже) Анал. р-р, окислитель (КМпО4, С12, Вг2, Н2О2 или КС1О3), добавл. НС1, разрушают изб. окислителя кип. (КМпО4 в присутствии С2Н5ОН). Опр. Fe3+ 1
IFe (CN)6p- ZnSO4 (М/Э = 2) Анал. р-р, дифенилам., Кз[Ре(СМ)б] (3 капли 1% р-ра), H2SO4 (10 мл 4 н.). Тнтр. до син.-фиол. 3
КМпО4 См. опр. конц. К4[Ре(СМ)е] (стр. 305) 1
J2 (I) и Na2S2O3 (II) Анал. р-р (нейтр., содержащий не >1,5 мг-экв опр. в-ва), Na2HPO4-•12Н2О (25 мл 10% р ра), СНзСООН (25 мл 20% р-ра), р-р I (изб.). Выдерж. в темноте через 20 мин, добавл. Н2О (100 мл). Титр, р-ром П с крахм. до бц. 1
Се (SO4)2 Анал. р-р (100 мл), НС1 (5 мл). Титр, с ферроином до гол. I
Хлорамин Т (I) и NaAsO2 (II) Анал. р-р, НС1 (5 мл 0,5 н.), р-р 1 (изб.). Нагр. до 40° С, добавл. NaHCO3 (1 г), р-р II (изб.), KJ (несколько крист.)'. Титр, с крахм. р-ром I до бц. 1
JC1 (М/Э = 2) Анал. р-р, CH3COONa (до pH = 6,5ч-7,5). Нагр. до 40° С. Титр с СНС13 до фиол. 1
Со2 (SO4)3 Титр, в среде H2SO4 1
К2СГ2О7 (0,02 н.) Анал. р-р (~0,025 М), HCI (0,3 н.). Тнтр. с бензидинацетатом 1
Fe3+ КМпО4 Анал. р-р (2,5 н. НО) нагр. до 90° С, добавл. SnCl2 (5% в 2 н. НО) до бц. и еще 2 капли, охл., добавл. HgCl2 (10 мл нас. в 0,01 н. НС1) при перемеш. Через 2—5 мин добавл. Н2О (400 мл). Далее см. опр. Fe2+ 1
* См. стр. 21.
.343
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (иои) Рабочий раствор Методика определения м/э
Fe3+ Рабочие р-ры для опр. Fe2+ (см. выше) а) Анал. р-р (2 н. HCI) восст. металлами: Zn, Ag, Pb, Bi, Cd, Sb, Ni, Sn (пропускают через редуктор или взбалт. с амальгамой; см. стр. 28 и 52). Опр. Fe2* б) Анал. р-р (200 мл\ H2SO4 1 н.). Нас. SO2 (или вводят 50 мл нас. р-ра SO2). Медленно нагр. до кип., пропускают СО2 до удаления SO2. Опр. Fe2+ 1 1
NH4VO3 или К2СГ2О7, 0,005 н. Анал. р-р (0,1—10 мг Fe), CrSO4 (изб.). Окисляют воздухом. Опр. Fe2* 1
Na2S2O3 Анал. р-р (HCI 0,1 н.), KJ (1—2 а). Через 3 мин титр, с крахм.; в конец титр, быстро нагр. до 50° С и титр, до бц. 1
КВгО3 + + КВг (I) и Na2S2O3 (II) Анал. р-р, СНзСООН (до 25% р-ра), CH3COONa (3 г). Нагр. до 50°С, добавл. 8-оксихинолин. Фильтр., промыв. Н2О. Ос. раств. в НС1, добавл. Н3РО4 (10 мл 50% р-ра). Опр. 8-оксихинолин (стр. 324) 12
Аскорбиновая кислота или TiCl3, или SnCl2 Анал. р-р (нейтр.), НС1 (5 мл 2 н.), Н2О (до 50—100 мл в конце титр.). Нагр. до 60°С, добавл. KSCN (1 мл 0,5 н.). Титр, до бц. 1
Hg2 (NO3)2 Анал. р-р (HNO3 0,5 н.), NH4SCN (Юлы 40% р-ра), HNO3 (до 100 мл в конце титр.). Титр, до бц. (в конце титр, перед добавл. каждой капли р-ра выжидают по 15 сек) I
Na-ЭДТА (I) и ZnSO4 (II) Анал. р-р (слабо кисл.; не >25 мг Fe), р-р I (изб.), Н2О (до 100—200 мл, CsHsN (3—10 мл). Титр, р-ром II с хромоген, черн. до кр. 2
[Fe(CN)e]s Ыа252Оз Анал. р-р, KJ (10 мл 1 н.), НС1 (5—20 лм 25% р-ра). Через 30 сек титр, с крахм. до бц. 1
TiCl3 Анал. р-р, Н3РО4 (5 мл конц. р-ра), НС1 (100 мл конц. на 130 мл анал. р-ра). Титр, с дифенилам, до фиол. 1
Аскорбиновая кислота Анал. р-р, CHsCOONa. Титр, без инд. до желт, или с 2,6-дихлорфенолнндофено-лом до бц. (св.-желт.) 1
Г идрохинон Анал. р-р (H2SO4, 50% р-р) титр, с ферроином до кр. I
н2о2 Анал. р-р (NaOH, 0,1 н.) титр, при 80° С с люцигенином (люминесценция) 1
SnCl2 (СО2) Анал. р-р (HCI, 7% р-р) титр, (без инд.) до син. 1
Со2+ КМпО4 Анал. р-р (без NO~ и NH+; 100 мл), НСООН (35 мл). Нагр. до 70° С. Осажд. ' СоС2О4. В ос. опр. С2О4“ (стр. 323) 2
349
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (мои) Рабочим раствор Методика определения Л1/.-7
Со2* КМпО4 (1) и Na2S2O3 (И) Анал. р р (СНзСООН), KNO2 (изб.). Через 12 ч фильтр., промыв. (2% р-р NH4NO3). К ос. добавл. р-р I (изб.), H2SO4 (1:4). Нагр. до 50° С, охл. Опр. MnOf (стр. 347) 11
Na2S2O3 Анал. р-р (нейтр.), NaBO3-4H2O (1 г), NaOH (3 г). Кип. (10 мин), охл., пропускают СО2, добавл. KJ (2 г), H2SO4 (100 мл 20% р-ра). Закр. колбу, оставляют до раств. ос. Титр, с крахм. до бц. 1
K2Cr2O7 (I) и FeSO„ (II) Осажд. Кз[Со(ИО2)б]. К ос. добавл. р-р I (изб.), H2SO4 (10 мл 1 : I). Harp, до 60° С. К р-ру добавл. 15 мл смеси H2SO4 и Н3РО4 *, разб. до 200 мл. Тнтр. р-ром 11 с ферроином до кр. И
КВгОз + КВг (О и а) Опр. через 8-оксихинолинат. См. опр. АР 8
Na2S2O3 (II) б) Айал, р-р ( ~0.1 г Со в 300 мл) нагр. до кип., добавл. антр. к-ту (35 мл 3% р-ра на 100 мг Со), кип. 5 мин. Через 10 мин фильтр, промыв, антр. к-той (0,2% р-р) и сп. Ос. раств. в 4 н. HCI. Опр. антр. к-ту (стр. 322) 12
NaJO4 или NH4VO, Осажд. Co[Hg(SCN)4]. В ос. опр. SCN" (стр. 324) 24
Na-ЭДТА Анал. р-р (не >25 мг Со/100 мл), нейтр. NH4OH (до рН = 6), добавл. мурексиддо ор.-желт., NH4OH до желт., титр, до фиол. 2
КС№* (I) и AgNOg (11) Анал. р-р (нейтр. 100 мл), Na2B4O7 (20мл нас.), р-р I (изб.), Na2CO3 (10 мл 10% р-ра). Пропускают воздух 6 мин, добавл. NH4OH (10 мл р-ра 1:1), NH4CI (25 мл 20% р-ра). Титр, р-ром 11 до помутнения, а затем р-ром 1 до просветления. Для опр. конц. р-'ра I в оттитрованный р-р добавл. еще р-р I. Титр, р-ром 11 до помутнения Эмпир.
Ni2+ КВгОз+КВг (1) и а) Опр. через 8-оксихинолинат. См. опр. АР 8
Na2S2O3 (11) б) Опр. через антранилат. См. опр. Со2+ (ос. лучше раств. в конц. HCI и затем разб.) 12
КВгО3 (I) Na2S2O3 (I) пли Осажд. диметилглиокснмом (стр. 300). К ос. добавл. НС1 (50 мл 6 н.), р-р I (изб ). Через 15 мин добавл. KJ и титр. 24
NaAsO2 (Па) с крахм. р-ром II до бц. или добавл. р-р На (изб.) и титр, с мет. ор. р-ром I до бц.
* 150 мл конц. H2SO4 и 150 мл конц. Н3РО4 разбавляют до 1 л.
** Для приготовления р ра смешивают равные объемы р-ров KCN (4,8 г{л} и NaOH ( 3 г/л)
350
ОБЪЕМНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Продолжение
Определяемое вещество (ион) Рабочий раствор Методика определения м/э
Ni2+ KMnO4 Ссажд. NiC2O4. См. опр. Со2+ (стр. 349) 2
Na-ЭДТА (1) и MgSO4 (II) См. опр. Си2+ 2
Na-ЭДТА Анал. р-р (100 мл, не >15 мг Ni), му-рексид, NH4OH до желт. Титр, до изменения окр., добавл. NH4OH (10 мл конц. р-ра). Титр, до син.-фиол. 2
Диметилглио- Анал. р-р, NH4OH до запаха. Титр, до Эм пир.
ксим * (М/Э= 1) отрицательной пробы с диметилглиок-симом на бумажке (2)
KCN Анал. р-р, NH4OH (5 мл 6 н.), (NH4)2SC>4 (1 г), KJ (1 мл 25% р ра). Титр, до ослабления окраски, добавл. AgNO3 (3—4 капли 0,1 н.). Титр, до исчезновения мути; вносят поправку на Ag+
Rh111 FeSO4 Анал. р-р, NaBiO3 (изб.). Титр, до роз. 2
Pd11 Диэтилдитио- Анал. р-р (10 мл р-ра HCI 1: 1; 0,01— 2
карбамат натрия, 0,5% р-р (М/Э = 1) 1,0 мг Pd), р-р SnCl2 (500 г в 200мл конц. НС1) до бц., 5 мл бензола. Титр, с HgCl2 (5 капель 0,01% р-ра) при взбалт. до бц.
Na-ЭДТА, 0,01 М Анал. р-р (слабокисл.), K2[Ni(CN)4] (конц. свежеприготовленный; изб.), NH4OH, Н2О (до ~0,001 М Pd). Титр, с мурек- сидом до фиол. 2
Pdiv FeSO4 (I) и К2Сг2О7 (И) Анал. р-р, р-р I (изб.). Титр, р-ром II с фенилантр. к-той до бур. 2
kill КМпО4 или K3[Fe (CN)6J, или Се (SO4)2 Анал. р-р титр, с окисл.-восст. инд. или без него 1
Iriv Аскорбиновая кислота Анал. р-р (HCI 1 н.). Титр, с дифенилам, до бц. 1
Г идрохинон Анал. р-р (5% р-р H2SO4 или 10% р-р НС1) титр, с дихлорбензидином или с о-дианизндином, или с дифенилам, до бц.; Pt, Pd и Rh не мешают 1
Ptiv Диэтилдитиокарбамат натрия, 0,5% р-р См. опр. Pd11 2
КМпО4 Анал. р-р, CuCl (р-р в конц. НС1, изб.). Через 4 ч добавл. H2SO4 (5 мл конц. р-ра) MnSO4 (10 мл 1 и.; 7 н. по H2SO4), разб. до 600 мл. Титр, до ор. 2
Аскорбиновая кислота Анал. р-р титр, с вариамин. син; при 60° С до бц. 4
* К 11,6 г диметилглиоксима добавляют 100 мл NaOH (2 н.) и разбавляют до 1 л.
** 1 г-ион NP+ эквивалентен 4 г-ион CN-.
351
Кислотно-основные индикаторы
Таблица состоит из трех разделов: индивидуальные, смешанные н универсальные кислотно-основные индикаторы.
Индикаторы расположены в порядке возрастания значений pH в интервале перехода окраски.
Интервалы pH перехода окраски индикаторов даны для ионной силы раствора 0,1. В некоторых случаях приведен только показатель титрования (рТ), т. е. значение pH, при котором отчетливо заметно изменение окраски индикатора. При выборе индикатора нужно принимать во внимание реакцию среды в момент наступления точки эквивалентности. Индикаторы применяются в виде 0,1% водных или спиртовых растворов.
В конце таблицы «Индивидуальные кислотио-основные индикаторы» приведены индикаторы помутнения, позволяющие устанавливать точку эквивалентности при титровании очень слабых кислот (например, борная кислота, фенол и т. и.).
У казатель
Индикатор Рациональное название или синоним Раздел и № в таблице
Азоаиилин-л-бензолсульфо-кислота I, 53
Азодифеииламин-о-беизой-иая кислота 1, 75
Азометиланилии-л-бензол-сульфокислота • I, 82
Азолитмин I, 127; II. 12
Азосииий о-Толидиндисазоби-1 -иафтол-4-сульфо-кислота I. 198
Азо jw-хлордизтиланнлии-л-беизолсульфокислота I, 62
Али-зарии 1, 2-Диоксиаитрахинон I, 130, 194
Ализариновый желтый 2Г л/Нитробензолазосалнциловая кислота, натриевая соль; 4-окси-З-нитроазобеи-зол-3-карбоновая кислота, натриевая соль; протравный желтый; салицил желтый 1, 189
Ализариновый желтый Р n-Питробензолазосалициловокислый натрий I. 193; 11, 25, 26; 111, 4, 5
Ализариновый зеленый Б Диэксинафтоксазиисульфокислота I. 26, 218
Ализариновый красный S Ализарин S; ализаринсульфонат натрия; ализаринрот; 1,2-диоксиаитрахинон-З-сульфокислый натрий I, 96, 188; П, 8
Ализариновый синий Ализарииблау СА 1, 205
Ализариновый синий АБ 1, 2-Диоксиантрахинон-Р-хинолин Натрийбисульфитное соединение ализа-ринсинего 1, 9, 138
Ализариновый синий БС 1, 139, 207
Алканин 1, 174
л-Аминоазобсизол 1, 52
Аинлииовая синь 1-1, 4
Аурин 1, 152
Бензазурин 1, 199
Бензоил аура мии Ж 1, 121
Беизолазобеизилаиилин I, 59
Бемзолазодифениламин 1, 37
Бензол азо-а-иафтиламнн 1, 94
Беизолазофеиил-а-нафтил-амин 1, 44
Бензопурпурин 4Б о-Толидиндисазоби-1-иафтиламин-4-суль-фокислый натрий 1, 27, 42, 220
4. 4'-Бие-(2-амино-1-иафтил-азо)-2, 2'-стильбендисуль-фокислота, натриевая соль 1, 77
4, 4'-Бис-(о-толилтриазеио)- 2, 2' стильбендисульфо-кислота, натриевая соль 1, 101
Бразилеии 1, 140
Бриллиантовый желтый Бриллиантгельб; стильбен-2, 2'-днсульфо-кнслота-4, 4'-бис (I-азо)-4-оксибензол дмнатриевая соль; яркий желтый I, 151
352
Кислотно-основные индикаторы
Продолжение
Индикатор
Рациональное название или синоним
Раздел и № в таблице
Бриллиантовый зеленый
З-Бромбензолсульфокислота 1-(4-азо-4')-дифениламин 2-Бром-4'-диметиламиноазо-бе изоле ул ьфокисл ота-4
Бромкрезоловый пурпурный
Бромкрезоловый синий
Бромксилеиоловый синий Бромтимоловый синий
л-Бромфенолмалеин Бромфеноловый красный
Бром феноловый синий
Бриллиантгрюи; н, л'-бне-диэтиламино-трифенилкарбинол; яркая зеленая
Бромкрезол пурпур; дибром-о-крезолсуль-фофталеин
Бромкрезолгрюн; бромкрезолблау; бром-крезолзелеиый; тетрабром-ти-крезол-сульфофталеин
Бромтимолблау; дибромтимолсульфофта-леии
1, 15
I, 7
I, 48
I, 128; II, И; III, 9
I, 97: II, 5, 6, 8, 10
Бромхлорфеиол синий Водяной голубой
Галлеин
Гваяколовая настойка Гекса метоксикрасный
Гематоксилин Геитаметоксикрасный
Диазофиолетовый
Дииодфенолсульфофталеин и-Диметил аминоазобензолсульфамид
лг-Динитробензоиленмочеви-иа
о-Динитрофенол п-Динитрофенол ж-Дииитрофеиол Е-Динитрофенол а-Динитрофеиол р-Динитрофенол у-Динитрофеиол о-Дииитрофенол
3, 6-Дихлорбензолсульфо-кислота-1-(4-азо-4')-дифе-ннламии
2, 5-Дихлор-4'-диметилами-ноазобензолсульфокисло-та-4
Дихлорфлуоресцеин Желтый Марциуса
Изонитрозоацетил-о-амиио-азобеизол
Изонитрозоацетил-п-амино- бензол
Изопикрамииовая кислота Индигокармин Индооксин
Иидулии спирторастворимый
Иодный зеленый
Иодэозин
т-Карбокси азоднметил анилин
Бромфенолрот; дибромфеиолсульфофга -леин
Бромфеиолблау; тетрабромфеиолблау; тетрабромфеноловый синий; тетра-бромфенолсульфофталеии
Дихлордибромфеиолсульфофталеии
Ди- и трисульфокислота трифеинл-п-розанилина и дифеиилрозанилина
4, 5-Диоксифлуоресцеии
2, 4, 2', 4', 2", 4"-гексаметокситрифенил-карбииол
2, 4, 2', 4', 2", 4", 6"-гептаметокситрифенил-карбинол
Диазовиолет
1, 2-Динитрофеиол
1, 4-Дииитрофеиол
1, З-Дииитрофеиол
2, З-Дииитрофеиол; Е-Михаэлиса
2, 4-Динитрофеиол; а-Михаэлиса
2, 6-Дииитрофенол; р-Михаэлиса
2, 5-Динитрофеиол: у-Михаэлиса
3, 4-Динитрофеиол; (Т-Михаэлиса
1, 137
I, 136; II, 11, 12, 14 16; III, I, 2, 3, 4, 5, 6, 7, 8
1, 131
1, 129
1, 73; III, 9
1, 84
I, 120, 202
I, 13, 93, 187
I, 153
I, 64; И, 2
1, 122
I, 126
I, 192
I, 3, 85. 135
I, 72
I, 149
I, 67
1. 60
I, 102
I, 111
I, 6
1, 46
............................................1, 105
2,4-Динитро-1-иафтол; манчестерский 1, 55 желтый
............................................1, 224
........................................... I, 227
2, 6-Динитро-4-амннофенол И н д игодисул ьфокислота 5. 8-Хинолиихинол-8-окси-5-хинолил-5-имид 1, 109 1, 214; 11, 3 I, 141
Смесь хлористоводородных солей ди-, три- 1, 132
и тетрафениламинофеиилфеназония Гептаметилрозаиилии I. и
Тетраиодфлуоресцеин I, 115 I, 56
23 Зак. 783
353
Кислотно-основные индикаторы
Продолжение
Индикатор Рациональное название или синоним Раздел н № в таблице
о-Карбоксибензол азодифе-ииламии
о-Карбоксибензолазометил-аиилин
о-Карбоксибензолазо-а-на-фтиламин
о-Карбоксибензолазопропил-аиилии
о-Карбоксибензол азо-л<-фе-иилендиамин
Карвакролсульфофталеин
Карминовая кислота
Конго красный
Красио-фнолетовый 5РС
Красно-фиолетовый 5Р экстра
Крезоловый красный
Крезоловый пурпурный
о- Крезолтетра хлорфталеин о-Крезолфталеии
Кристаллический фиолето-
вый
Ксиленоловый синий л-Кси ленолфталеи и Куркума Куркумеин Куркумнн
Лакмозол
Лакмоид
Лигозии
Магдала красный
Малахитовая зелень, сернокислая илн щавелевокислая соль
Малахитовый зеленый
Метаниловый желтый
Метиленовый синий
Метиленовый фиолетовый
БН
Метиловый желтый
Метиловый зеленый
Метиловый красный
Метиловый оранжевый
Метиловый пурпуровый
Метиловый фиолетовый
I, 10, 71
I, 103
• • • - I, 69
I, 110
1, 20
I, 165 I. 119, 209
Бензидиидисазо-1-иафтиламии-4-сульфо- I, 78
кислый натрий; дифенил-4,4'-бис[(-азо-2)-1-амиионафталин-4-сульфокислота], динатриевая соль; днфенилдисазобн-1-иафтиламии-4-сульфокислый натрий;
конго рот Трисульфокислота этилрозаиилина 1, 92
Смесь моно-, дн- и триметил (этил)- I, и
роза иил и нов
Крезолрот; о-крезолсульфофталеин 1, 51, 156; II, 17, 18
Крезоловый пурпурный; л-крезолсульфо- I, 32, 164
фталеин I, 176 I, 172; III, 4
Гексаметнл-л-розанилин, хлористоводо- I, 31
родный; кристаллвиолет Ксилеиолблау; л-ксиленолсульфофталеии I, 33, 167 I, 181
I, 170 I, 2, 221
Ди-(4-окси-З-метоксициинамоил)-метан; I, 162, 195
диферуланметаи I, 112
Резорциновый синий I, 104
Ди-о-гидроксистирилкетон I, 159
Смесь хлористых амино- и диамино- I, 70
иафтнлдинафтазоиия I, 208
4, 4-'Бнс-диметиламинотрифеиилметан; I, 12, 211
малахитгрюн; тетра метилди-л-а миио-трифенилкарбииол
Виктория желтый; дифенил аминазо-л<- 1, 38
бен зол сульфокислота; мета ни л тел ьб; л -с у л ьфо бе и зол а зо д и фе и и л а м и н; тро-пеолнн Ж П, 1, 7, 13
Хлористоводородная соль З-амнио-7-дн- I, 4
метила минофенилфеназония л-Диметиламиноазобензол; диметилгельб; I, 68; II, 1; III, 2, 3
диметиловый желтый; масляио-желтый
индикатор Телфера Бромэтилгексамстил- и пентаметнлмоно- I, 23; II, 2, 20
этил-л-розаннлнн, двойная соль с хлористым цинком; метилгрюи I, 113; 11, 6, 7; III,
Диметила мипоазобензол-о-карбоновая
кислота; метилрот 1, 2, 3, 4, 5, 6, 7, 8
Гелиантик; л-диметиламиноазобензол- 1, 74; II, 3, 4 5;
сульфокислый натрий; метилоранж; 111, 3, 4, 5
оранж III 1, 83
Метил виолет; пентаметилбензол-л-розанн- I, 21, 35, 54
лин, хлористоводородная соль
354
Кислотно-основные индикаторы
Продолжение
Индикатор Рациональное название или синоним Раздел и № в таблице
2- (2'-Метокси-4'-нитрофеиил-азо)-1-нафтол-4, 8-дисульфокислота, натриевая соль Мышьяковый аналог конго красного Мышьяковый аналог мети-левого оранжевого Мышьяковый аналог этилового оранжевого Нафтиловый коричневый а- Н афтолбензеи и а- Нафтолкрасиый а Нафтолсульфофталеин а-Нафтолфталеин Нейтральный красный Нейтральный синий Нильская голубая А Нильская голубая 2Б Ннтразиновый желтый Нитрамин 4-Нитро-6-амииогваякол Нитротимолсульфофталеии 2-(4'-Нитрофеиилазо)-1-нафтол-3, 8-дисульфокислота, натриевая соль 2-(4'-Нитрофеиилазо)-1-иафтол-4, 8-дисульфокислота, натриевая соль Нитрофеиолсульфофталеии 1-Оксииафтохинометан Оксин синий Оранжевый III Оранжевый Ж Орсинсульфофталеин Параметиловый красный Пента метоксикрасный Пикриновая кислота Пинахром Пирокатехинсульфофталеин Пропиловый красный Прочный красный В Пуаррье-сииий Пурпурин Резазурин Резор циималеии Родамин С (В) Розоловая кислота Салицнлсульфофталеин Сафранин Сок красной капусты Спиртовый желтый Р «-Сул ьфобензол азо-а-и аф-тиламин 4-Сульфонафталииазо-а-иафтол Беизол-(азо-1)-4-амиионафталин; а-иа-фтирот Хлористоводородная соль 2-метил-З-амиио-6-диметиламииофеназина; иейтральрот Хлористый диметиламннофеиилнафто-феиазоний Сернокислый 3-амиио-7-диэтиламиио-1, 2-беизофеноксазин; иильблау 2, 4-Нитробензолазо-1-нафтол-3, 6-дисульфокислота Пикрилметилнитрамин; тетралит; тетрил; 2, 4, 6-тринитрофеинлметилнитрамии At-Ннтробензолазо-р-иафтол-3. 6-дисульфокислота Бензол азо-р-иафтол-4, 6-дисульфокислота п-Карбоксибензолазодиметил анилин; параметилрот 2, 4, 2', 4', 2"-пентаметокситрифеиилкар-бинол; пентаметоксирот 2, 4, 6-Трииитрофеиол о-Карбоксибензолазоднпропиланилии; пропил рот Нафталиназо-₽-нафтол-3, 6-днсульфокнс-лота 1, 2, 4-Триоксиантрахинон 3, 6-Бис-диэтиламинофлуорон Желтый кораллин; кораллинфталеин: ме-тилаурин о-Тол уи назо-о-тол уидин I, 182 I, 25 I. 50 I, 57 I, 142 •, 1. 177 I, 95 I, 163 1, 160; II, 18, 19, 22; 1П, 4, 7 I, 147; II, 13, 14 I, 185 I, 191; 11, 24, 26 I, 155 I, 144 I, 203 I, 117 1, 158, 184 1, 204 I, 169 1, 145 I, 65 I, 99 I, 63 1. 213 I, 180 I, 34 I. 41 I. 5 I, 134 I, 24, 106, 178, 196 I, 118 1, 200 I, 210 I, 19, 108, 217 I, 98 1, 123 I, 22 I, 143 I, 157 I, 28. 222 I, 61 I, 45 I, 88
23*
855
Кислотно-основные индикаторы
П родолжение
Индикатор Рациональное название или синоним Раздел и № в таблице
гг-Сульфобеизолазофенил-а-нафтнламин л-Сульфо-о-метоксибензо-азодиметил-а-иафтил-амии Тетрабромфенолфталеии Тетранодфенолсульфофта-леии Тетраиодфеиолфталеин, натриевая соль Тетраннтрофенолсульфо-фталеии Тетрахлорфенолсульфофта-леин Тимоловый синий Тимолфталеин л<-Толуолазоизонитрозоаце-тил-л-толуидин Л4-Толуолазоизоиитрозоаце-тил-о-тол у идии «-Толуолазоизоиитрозоаце-тил-ле-толуидин о-Толуолазоизонитрозоаце-тил-о-толуидии «-Толуолазонзоиитрозоаце-тил-/1-толуидии I,3, 5-Тринитробензойиая кислота 2, 4, 6-Тринитробензойиая кислота 1, 3, 5-Триинтробензол 2, 4, 6-Тринитротолуол Тропеолин 0 Тропеолин 00 Тропеолин ООО Ураиин Фенацетолин Фенолмалеин Феноловый красный Фенолфталеин Флоксин красный Фосфорный аналог конго красного Фосфорный аналог метило-вого оранжевого Фосфорный аналог этилово-го оранжевого Фуксин основание Фуксин С Хинальдиновый красный Хинолиновый синий З-Хлорбеизолсульфокислота 1-(4-азо-4') -дифенил амии Тимолблау; тимолсульфофталени 2. 2'-Диметил-5, 5'-диизопропилфенол-фталеин Золотисто-желтый; п-сульфобензолазо-резорции; N-.хризоии Анилингельб; дифеииламиназо-п-бензол-сульфокислый натрий; дифеиилоранж; ораиж IV; п-сульфобеизолазодифеиил-амии а-Нафтолазо-п-беизолсульфокислота: а-иафтолораиж Диоксифлуораи; резорцинфталеии Фенолрот; феиолсульфофталеии Цианозин Анилиновый красный; смесь розанилина и п-розанилииа Смесь дн- и трисульфокислот розанилина и п-розаиилина л-(я-Диметнламинофеиилэтилеи)-хииолин-иодэтилат; хннальдннрот 1, !'-Диизоамил-4. 4'-хиноцианиииодид; хииолииблау; цианин I, 90 I, 86 I, 166 I, 79 I, 175 I, 66 I, 76 I, 39. 168; II, 17, 21; Ill, 2, 3 I, 186; II, 23, 25; 14, 1. 7 I, 228 I, 226 I, 229 I, 225 I, 230 I, 215 I, 171 I, 219 I, 212 I, 206 I, 43; III, 4, 5 I, 161, 197 I, 91 I, 81, 190 I, 179 I, 148; 11, 15, 16; III, 6, 8, 9 I, 173; II, 19. 20, 21, 22, 23, 24; III, 1, 2. 4, 5, 7 I, 47 1, 58 I, 80 I, 89 I, 40 1, 216 I, 36 I, 154; II, 15 1, 8
356
Кислотно-основные индикаторы
Продолжение
Индикатор
Рациональное название или синоним
Раздел и № в таблице
2-Хлор-4'-диметиламиноазо-бензолсульфокислота-4 Хлорфеноловый красный
Хризоидин
Цианин
Щелочной голубой 2Б
Эмодин
Эозин БН
Эозин Ж
Эозииметилеиовый синий Эритрозин
Этиловый зеленый
Этиловый красный
Этиловый оранжевый
Этиловый фиолетовый
Дихлорфеиолсульфофталеин; хлорфенол-рот
Бензолазо-л<-фенилендиамнн
Смесь моиосульфокислот дифенилроз-аиилииа и трифеинлл-розанилина
1, 6, 8-Триокси-З-метилаитрахиион; реоэмо-дин; франулаэмодии
Дибромдинитрофлуоресцеии
Тетрабромфлуоресцеин
Тетраиодфлуоресцеии, натриевая или калиевая соль
Этилгексаметил-л-розаиилнн
о-Карбоксибензолазодиэтнлаиилии; этил-рот
Диэтиламиноазобеизолрульфокислый натрий; л-сульфобензолазоднэтилаиилин
Г ексаэтил-п-розаннлин
I, 87
I, 18, 116
I. ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
№ по пор. Индикатор Интервал pH перехода окраски индикатора
1 2 3 4 5 6 7 8 9 10 11 12 13 а-Нафтолбензеин (1-й переход; см. № 177) Куркумеин (1-й переход; см. № 221) Дииодфенолсульфофталеин (1-й переход; см. № 85, 135) Метиленовый фиолетовый БН Пикриновая кислота 3, 6-Дихлорбензолсульфокислота-1 - (4-азо-4') -дифениламин 3-БрОмбензолсульфокислота-1-(4-азо-4')-дифениламин 3-Хлорбензолсульфокислота-1 - (4-азо-4') -дифениламин Ализариновый синий АБ (1-й переход; см. № 138) о-Карбоксибензолазодифениламин (1-й переход; см. № 71) Красно-фиолетовый 5Р экстра Малахитовый зеленый (I-й переход; см. № 211) Галлеии (1-й переход; см. № 93, 187) 0,0 — 0,8 зеленая желтая 0,0 — 1,0 оранжевая желтая 0,0 — 1,2 оранжевая желтая 0,0 — 1,2 пурпурная фиолетовая бесцветная желтая рТ = 0,26 красная желтая рТ = 0,68 красная желтая рТ = 0,76 красная желтая 0,0 — 1,6 розовая желтая 0,0 — 1,6 п^пурная розовая зеленая синяя 0,0 — 2,0 желтая голубовато-зеленая 0,0 — 2,6 желтая коричневая
357
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор. Индикатор Интервал pH перехода окраски индикатора
14 Иодный зеленый 0,0 — 2,6 желтая синяя
15 Бриллиантовый зеленый 0,0 — 2,6 желтая зеленая
16 Эозин Ж 0,0 — 3,0 оранжевая розовая
17 Эритрозин 0,0 — 3,6 оранжевая розовая
18 Этиловый фиолетовый (1-й переход; см. № 116) 0,0 — 3,6 желтая синяя
19 Пурпурин (1-й переход; см. 108, 217) 0,0 — 4,0 желтая оранжевая
20 о-Карбоксибензолазо-л-феиилендиамин 0,0 — 4,6 желтая оранжевая
21 Метиловый фиолетовый (1-й переход; см. Хе 35, 54) 0,1 — 0,5 желтая зеленая
22 Родамин С (Б) 0,1 — 1,2 оранжевая розовая
23 Метиловый зеленый 0,1 — 5,0 зеленая голубая
24 Пирокатехинсульфофталеин (1-й переход; см. Хе 106, 178, 196) 0.2 — 0,8 розовая оранжевая
25 Мышьяковый аналог конго красного 0,2. — 5,8 пурпурно- желтокоричневая оранжевая
26 Ализариновый зеленый Б (1-й переход; см. Хе 218) 0,3 — 1,0 лиловая красная
27 Бензопурпурин 4Б (1-й переход; см. Хе 42, 220) 0,3 — 1,0 синяя фиолетовая
28 Сафранин (1-й переход; см. Хе 222) 0,3 — 1,0 синяя красная
29 Эозинметиленовый синий (1-й переход; см. Хе 223) 0,3 — 1,0 зеленая синяя
30 Этиловый зеленый 0,3 — 2,0 желтая синяя
31 Кристаллический фиолетовый 0,5 — 2,0 зеленая синяя
32 Крезоловый пурпурный (1-й переход; см. Хе 164) 0.5 — 2,5 красная желтая
33 Ксиленоловый синий (1-й переход; см. Хе 167) 0,6 — 2,8 пурпурная янтарно-желтая
34 Параметиловый красный 0,9 — 2,9 красная желтая
35 Метиловый фиолетовый (2-й переход; см. Хе 21, 54) 1,0 -- 1,5 зеленая синяя
36 Хинальдиновый красный 1,0 — 2,0 бесцветная красная
37 Бензолазодифениламин 1,1 — 2,8 пурпурная желтая
38 Метаниловый желтый 1,2 — 2,3 красная желтая
858
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор. Индикатор Интервал pH перехода окраски индикатора
39 Тимоловый синий (1-й переход; см. № 168) 1,2 — 2,8 красная желтая
40 Фуксии основание 1,2 — 3,0 пурпурная бледио-пурпур-ная
41 Пентаметоксикрасиый 1,2 — 3,2 красно-фиолетовая бесцветная
42 Бензопурпурии 4Б (2-й переход; см. Ks 27, 220) 1,3 — 4,0 фиолетовая оранжевая 1,4 — 2,6 розовая желтая
43 Тропеолин 00
44 Бензолазофеиил-а-нафтиламин 1,4 — 2,6 фиолетовая оранжевая
45 Спиртовый желтый Р 1,4 —2,8 оранжевая желтая
46 2, 5-Дихлор-4'-диметиламиноазобензол-сульфокислота-4 1,4 — 3,2 красная желтая
47 Флоксии красный (цианозин) 1,4 — 3,6 розовая красная
48 2-Бром-4'-диметиламиноазобензолсульфо-кислота-4 1,6 — 3,6 красная желтая
49 2-Хлор-4'-диметиламиноазобеизолсульфо-кнслота-4 1,6 — 3,7 красная желтая
50 Мышьяковый аналог метилового оранжевого 1,6 — 5,5 красно- желтая оранжевая (рТ=4,7)
51 Крезоловый красный (1 -й переход; см. Xs 156) 1,9 — 3,1 оранжевая желтая
52 п-Аминоазобензол 1,9 — 3,3 светло-желтая желтая
53 Азоанилин-п-бензолсульфокислота 1,9 — 3,3 красная желтая
54 Метиловый фиолетовый (3-й переход; см. № 21, 35) 2,0 — 2,5 синяя фиолетовая
55 Желтый Марциуса 2,0 — 4,0 светло-желтая желтая
56 л-Карбоксибензолазодиметиланилин 2,0 — 4,0 красная желтая
57 Мышьяковый аналог этилового оранжевого 2,1 — 5,5 оранжево- оранжево- красная (рТ=4,9) желтая 2,2 6,4 синяя (рТ=5,3) коричневооранжевая
58 Фосфорный аналог конго красного
59 Бензолазобензиланилин 2,3 — 3,3 розовая желтая
60 р-Динитрофенол 2,4 — 4,0 бесцветная желтая
61 Сок красной капусты 2,4 — 4,5 красная зеленая
359
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
П ро додже ниц
№ Интервал pH перехода окраски
пор. Индикатор индикатора
62 Азо-м-хлордиэтиланилин-н-бензолсульфо- 2,6 - 4,0
кислота красная желтая
63 Оранжевый III 2,6 — 4,6
красная желтая
64 Гексаметоксикрасный 2,6 — 4,6
красно-розовая бесцветная
65 1 -Оксинафтохинометан 2,7 — 3,7
бесцветная пурпурная
66 Тетранитрофенолсульфофталеин 2,8 - - 3,8
желтая красная
67 а-Дннитрофенол 2,8 — 4,4
бесцветная желтая
68 Метиловый желтый 2,9 — 4,0
красная желтая
69 о-Карбоксибензолазо-а-нафтиламин 2,9 — 5,8
красная желтая
70 Магдала красный 3.0 — 4,0
розовая желтая
флуоресценция
71 о-Карбоксибензолазодифениламин (2-й не- 3,0 — 4,0
реход; см. № 10) розовая желтая
72 n-Диметил аминоазобензолсульфамид 3,0 — 4,5
красная желтая
73 Бромфеноловый синий 3,0 4,6
желтая сине-фиолетовая
74 Метиловый оранжевый 3,0 4,4
красная оранжево-красная
75 Азодифениламин-о-бензойпая кислота 3,0 - 4,6
розовая желтая
76 Тетрахлорфенолсульфофталеин 3,0 - 4,6
желтая синяя
77 4, 4'-5ыс-(2-амино-1-нафтилазо)-2, 2'- 3,0 — 5,0
стильбендисульфокислота, натриевая синевато -пурпурная красная
СОЛЬ
78 Конго красный 3,0 - 5,2
сине-фиолетовая красная
79 Тетраиодфенолсульфофталеин 3,0 - 5,2
желтая пурпурная
80 Фосфорный аналог метилового оранжевого 3,0 — 5,9
красная оранжевая
(рТ —4,7)
81 Фенацетолин (1-й переход; см. № 190) 3,0 - 6,0
желтая . красная
82 Азометиланилин-п-бензолсульфокислота 3,1 — 4,2
красная желтая
83 Метиловый пурпуровый 3,1 — 4,4
красная оранжево-красная
84 Бромхлорфенолсиний 3,2 — 4,8
желтая СИНЯЯ
85 Дииодфенолсульфофталеин (2-й переход; 3,2 — 7,0
см. № 3, 135) желтая пурпурная
360
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор- Индикатор Интервал pH перехода окраски индикатора
86 п-Сульфо-о-метоксибензоазодиметил-а- 3,4 — 4,4
нафтиламин синяя оранжевая
87 Этиловый оранжевый 3,5 — 4,5 розовая желтая
88 n-Сульфобензолазо-а нафтиламин 3,5 — 5,7 красная оранжевая
89 Фосфорный аналог этилового оранжевого 3,5 — 5,8 красная оранжево-красная
90 п-Сульфобензолазофенил-а-нафтиламин 3,5 — 6,5 фиолетовая оранжевая
91 Уранин 3,6 — 5,6 бледно- желтая желтая флуоресценция
92 Красно-фиолетовый 5РС 3,6 — 6,0 розовая фиолетовая
93 Галлеин (2-й переход; см. № 13, 187) 3,6 — 7,0 коричневая розовая
94 Бензол азо-а-нафтиламин 3,7 — 5,0 красная желтая
95 а Нафтолкрасный 3,7 — 5,0 красная желтая
96 Ализариновый красный S (1-й переход; 3,7 — 5,2
см. № 188) желтая буро-розовая
97 Бромкрезоловый синий 3,8 — 5,4 желтая синяя
98 Резазурин 3,8 — 6,5 оранжевая темно-синяя
99 Оксин синий 3,9 — 5,5 синяя оранжевая
100 е-Динитрофенол 3,9 — 5,9 бесцветная желтая
101 4,4'-Быс-(о-толилтриазено)-2, 2'-стиль- 4,0 — 5,0
бендисульфокислота, натриевая соль желтая розовая
102 у-Динитрофенол 4,0 — 5,4 бесцветная желтая
103 о-Карбоксибензолазометиланилин 4,0 — 6,0 красная желтая
104 Лакмоид 4,0 — 6,4 красная синяя
105 Дихлорфлуоресцеин 4,0 — 6,6 желтая желтая флуоресценция
106 Пирокатехинсульфофталеин (2-й переход; 4,0 — 7,0
см. № 24, 178, 196) желтая зеленая
107 Хризоидин 4,0 — 7,0 оранжевая желтая
108 Пурпурин (2-й переход; см. № 19, 217) 4,0 — 8,0 оранжевая ^розовая розовая желтая
109 Изопикраминовая кислота
361
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор. Индикатор Интервал pH перехода окраски индикатора
но о- Карбоксибензол азопропиланилин 4,2 — 6,2 красная желтая
111 о-Динитрофенол 4,3 — 6,3 бесцветная желтая
112 Лакмозол 4,4 — 5,5 красная синяя
ИЗ Метиловый красный 4,4 — 6,2 красная желтая
114 о-Этиловый красный 4,4 — 6,2 красная желтая
115 Иодэозин 4,5 — 6,5 бесцветная розовая
116 Этиловый фиолетовый (2-й переход; см. № 18) 4,5 — 6,5 розовая темно-красная
117 4-Нитро-6-аминогваякол 4,5 — 8,0 желтая красная
118 Пропиловый красный 4,6 — 6,6 красная желтая
119 Карминовая кислота (1-й переход; см. № 209) 4,6 — 7,8 оранжевая розовая
120 Водяной голубой (1-й переход; см. Ns 202) 4,7 — 7,0 синяя бесцветная
121 Бензоилаурамин Ж 5,0 — 5,6 фиолетовая желтая
122 Гематоксилин 5,0 — 6,0 желтая фиолетовая
123 Резорцинмалеин 5,0 — 6,0 желтая оранжевая
124 Хлорфеноловый красный 5,0 — 6,6 желтая красная
125 о Динитрофенол 5,0 — 7,0 бесцветная желтая
126 Гептаметоксикрасный 5,0 — 7,0 красная бесцветная
127 Азолитмин 5,0 — 8,0 красная синяя
128 Бромкрезоловый пурпурный 5,2 — 6,8 желтая пурпурная
129 Бромфеноловый красный 5,4 — 7,0 желтая красная
130 Ализарин (1-й переход; см. Ns 194) 5,5 — 6,8 желтая красная
131 п-Бромфенолмалеин 5,5 — 7,2 желтая красная
132 Индулин спирторастворимый 5,6 — 7,0 синяя фиолетовая
133 п-Диннтрофенол 5,6 — 7,6 бесцветная желтая
134 Пинахром 5,6 — 8,0 слабо-красно- фиолетовая розовая
362
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор. Индикатор Интервал pH перехода окраски индикатора
135 136 137 138 139 140 141 142 143 144 145 146 147 148 149 150 151 152 153 154 155 156 157 158 Дииодфенолсульфофталеин (3-й переход; см. № 3, 85) Бромтимоловый синий Бромксиленоловый синий Ализариновый синий АБ (2-й переход; см. № 9) Ализариновый синий БС (1-й переход; см. № 207) Бразилеин Индооксин Нафтиловый коричневый Розоловая кислота Нитразиновый желтый Нитрофенолсульфофталеин Эмодин Нейтральный красный Феноловый красный л-Динитробензоиленмочевина м-Динитрофенол Бриллиантовый желтый Аурин Гваяколовая настойка Хинолиновый синий Нильская голубая 2Б Крезоловый красный (2-й переход; см. № 51) Салицилсульфофталеин Нитротимолсульфофталеин (1-й переход; см. № 184) 5,7 — 7,3 желтая пурпурная желтая синяя 6,0 — 7,6 желтая синяя 6,0 — 7,6 желтая зеленая 6,0 — 8, 0 желтая зеленая 6,0 — 8,0 бесцветная розовая 6,0 — 8,0 красная синяя 6,0 — 8,4 оранжевая розовая 6,2 — 8,0 красная желтая 6,4 — 6,8 желтая синяя 6,6 — 8,4 желтая пурпурная 6,8 — 7,6 желтая красная 6,8 — 8,0 красная оранжевая 6,8 — 8,0 желтая красная 6,8 — 8,0 бесцветная желтая 6,8 — 8,4 бесцветная желтая 6,8 — 8,5 желтая оранжевая 6,9 — 8,0 желтая красная 7,0 — 8,0 бесцветная зеленая 7,0 — 8,0 бесцветная фиолетовая 7,2 — 8,6 синяя розовая 7,2 — 8,8 янтарно- пурпурно- желтая красная 7,2 — 9,2 желтая розовая 7,2 — 9,4 желтая синяя
363
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение'
№ по пор. Индикатор Интервал pH перехода окраски индикатора
159 160 161 162 163 164 165 166 167 168 169 170 171 172 173 174 175 176 177 178 179 180 181 182 Лигозин а-Нафтолфталеин Тропеолин ООО (1-й переход; см. № 197) Куркумин (1-й переход; см. № 195) а-Нафтолсульфофталеин Крезоловый пурпурный (2-й переход; см. № 32) Карвакролсульфофталеин Тетрабромфенолфталеин Ксиленоловый синий (2-й переход; см. № 33) Тимоловый синий (2-й переход; см. №39) 2-(4'-Нитрофенилазо)-1 -нафтол-4, 8-дисульфокислота, натриевая соль Куркума 2, 4, 6-Трннитробензойная кислота о-Крезолфталеин Фенолфталеин Алканин Тетраиодфенолфталеин, натриевая соль о-Крезолтетрахлорфталеин а-Нафтолбензеин (2-й переход; см. № 1) Пирокатехинсульфофталеин (3-й переход; см. № 24, 106, 196) Фенолмалеин Орсинсульфофталеин п-Ксиленолфталеин 2-(2,-Метокси-4'’-нитрофенилазо)-1-наф-тол-4,8-дисульфокнслота, . натриевая соль 7,3 — 8,7 желтая зеленая 7,4 — 8,6 бесцветная сине-зеленая 7,4 — 8,6 оранжевая желтая 7,4 — 9,2 желтая буро-красная 7,5 — 9,0 желтая синяя 7,6 — 9,2 желтая пурпурная 7,8 — 9,6 желтая синяя 8,0 — 9,0 бесцветная фиолетовая 8,0 — 9,6 желтая фиолетово-синяя 8,0 — 9,6 желтая синяя 8,0 — 10,0 розовая пурпурная желтая оранжевая рТ = 8 бесцветная красная 8,2 — 9,8 бесцветная красная 8,2 — 10,0 бесцветная красная 8,3 — 10,0 красная синяя 8,4 — 10,2 бесцветная пурпурная 8,5 — 9,0 бесцветная пурпурная 8,5 — 9,8 желтая зеленая 8,5 — 10,2 фиолетовая синяя 8,5 — 10,5 бесцветная желтая 8,6 — • 10,0 желтая розовая флуоресценция 8,9 — 10,2 бесцветная синяя 9,0 — 11,0 розовая пурпурная
364
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
ПО пор. Индикатор Интервал pH перехода окраски индикатора
183 Щелочной голубой 2Б 9,0 - 14,0
лиловая розовая
184 Нитротимолсульфофталеин (2-й переход; 9,2 — 11,5
см. № 158) фиолетовая желтая
185 Нейтральный синий 9,3 — 10.2
186 Тимолфталеин 9,4 — 10,3
бесцветная синяя
187 Галлеин (3-й переход; см. № 13, 93) 9,4 - 14,0
розовая пурпурная
188 Ализариновый красный S (2-й переход; 10,0 — 12,0
см. № 96) фиолетовая бледно-желтая
189 Ализариновый желтый 2Г 10,0 — 12.1
бледно- красно-
желтая коричневая
190 Фенацетолин (2-й переход; см. № 81) 10,0 — 13,0
красная бесцветная
191 Нильская голубая А 10,1 — 11.1
синяя красная
192 Диазофиолетовый 10,1 — 12,0
желтая фиолетовая
193 Ализариновый желтый Р 10,1 — 12,1
бледно- красно-
желтая оранжевая
194 Ализарин (2-й переход; см. № 130) 10,1 — 12,1
фиолетовая пурпурная
195 Куркумин (2-й переход; см. Ns 162) 10,2 11,8
буро- оранжево-
красная желтая
196 Пирокатехинсульфофталеин (4-й переход; 10,2 — 12,5
см. Ns 24, 106, 196) синяя зеленая
197 Тропеолин 000 (2-й переход; см. Ns 161) 10,3 — 12,0
желтая красная
198 Азосиний 10,5 — 11,5
фиолетовая розовая
199 Бензазурин 10,5 — 12,0
200 Прочный красный В пурпурная розовая 12,5
розовая оранжевая
201 Эозин БН 10,5 — 14,0
розовая желтая
202 Водяной голубой (2-й переход; см. Ns 120) 10,5 — 14,0
203 Нитрамин пурпурная розовая — 12,5
бесцветная красно-
коричневая
204 2-(4'-Нитрофенилазо) -1-нафтол-3, 8-ди- 11,0 — 13,0
сульфокислота, натриевая соль розовая пурпурная
205 Ализариновый синий 11,0 — 13,0
оранжево- зелено-
желтая синяя
365
ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор. Индикатор Интервал pH перехода окраски индикатора
206 207 Тропеолин 0 11,0 — 13,0 желтая оранжевая
Ализариновый синий БС (2-й переход; 11,0 — 13,0
см. № 139) зеленая синяя
208 Малахитовая зелень 11,0 — 13,5 зеленая бесцветная
209 Карминовая кислота (2-й переход; см. 11,0 — 14,0
№ 119) фиолетовая розовая 11,2 — 12,7
210 Пуаррье-синий
211 синяя фиолетовая
Малахитовый зеленый (2-й переход; см. 11,5 — 13,2
212 № 12) зеленая бесцветная
2, 4, 6-Тринитротолуол 11,5 — 13,2 бесцветная оранжевая
213
Оранжевый Ж 11,5 — 14,0 желтая розовая
214
Индигокармин 11,6 — 14,0
синяя желтая
215 1.3, 5-Трнпитробензойная кислота 12,0 — 13,4 бесцветная оранжево-
216 красная
Фуксин С 12,0 — 14,0
217 Пурпурин (3-й переход; см. № 19, 108) Ализариновый зеленый Б (2-й переход; красная бледно-красная 12,0 — 14,0 лиловая фиолетовая
218
12,0 — 14,0
см. № 26) коричнево- коричневая желтая
219 220 1, 3, 5-Трипитробензол 12,2 — 14,0 бесцветная оранжевая
Бензопурпурин 4Б (3-й переход; см. № 27, 13,0 — 14,0
221 42) оранжевая красная
Куркумеин (2-й переход; см. № 2) 13,0 — 15,0
желтая зеленая
222 Сафранин (2-й переход; см. № 28) 14,0 — 15,0 красная фиолетовая
223 Эозпнметиленовый синий (2-й переход; 14,0 — 15,0
см. № 29) фиолетовая лиловая
Индикаторы помутнения (для титрования очень Интервал pH перехода
слабых кислот)
224 Изонитрозоацетил-о-аминоазобензол 9,0 — 9,2
225 п-Толуолазоизонитрозоацетил-о-толуидин 9,25— 9,35
226 .м-Толуолазоизонитрозоацетил-о-толуидин 9,3 — 9,4
227 Изонитрозоацетил-п-аминобензол 10,7 —11,0
228 л-Толуолазоизонитрозоацетнл-.и-толуидин 11,1 —11,5
229 п-Толуолазоизонитрозоацетил-.н-толуидин 11,5 —11,6
230 п-Толуолазоизонитрозоацетил-п-толуидин 11,55 — 11,56
366
II. СМЕШАННЫЕ ИНДИКАТОРЫ
Принятые сокращения см. стр. 16.
о" Цвет индикатора
№ по т Состав раствора индикатора рТ в кислой среде в щелочной среде Примечание
1 2 3 4 5 6 7 8 9 0,1% р-р метилового желтого (1 вес. ч.) в сп.; 0,01 % р-р метилового синего (1 вес. ч.) В СП. 0,1% Р Р гексаметоксикрасного (1 вес. ч.) в сп.; 0,1% р-р метилового зеленого (1 вес. ч.) в сп. 0,1% р-р метилового оранжевого (1 вес. ч.) в Н2О; 0,25% р-р индигокармина (1 вес. ч.) в Н2О 0,1% рр метилового оранжевого (1 вес. ч.) в Н2О; 0,1% р-р анилинового синего (1 вес ч.) в Н2О 0,1% р-р натриевой соли бромкрезолового синего (1 вес. ч.) в Н2О; 0,02% р-р метилового оранжевого (1 вес. ч.) в Н2О 0,1% р-р бромкрезолового синего (3 вес. ч.) в сп., 0,2% р-р метилового красного (1 вес. ч.) в сп. 0,2% р-р метилового красного (1 вес. ч.) в сП.; 0,1% р-р метиленового синего (1 вес. ч.) в сп. 0,1% р-р натриевой соли бромкрезолового синего (1 вес. ч.) в Н2О; 0,1% р-р ализаринового красного S (1 вес. ч.) в Н2О 0,1% р-р натриевой соли хлорфенолового красного (1 вес. ч.) в Н2О; 0,1% р-р анилинового синего (1 вес. ч. )в Н2О 3,25 4,0 4,1 4,3 4,3 5,1 5,4 5,6 5,8 Сине-фиолетовый Фиолетовый » » Оранжевый Виннокрасный Красно-фиолетовый Фиолетовый Зеленый Зеленый » » » Сине-зеленый Зеленый » Желто-зеленый Фиолетовый Зеленый при рН=3,4; сине-фиолетовый при pH=3,2; сохранять в темной склянке При pH = 4,0 цвет синефиолетовый; сохранять в темной склянке Особенно удобен для титрования при искусственном свете; сохранять в темной склянке Желтый при рН=3,5; зеленовато-желтый при pH = 4,05; слабозеленый при pH = 4,3 Очень резкое изменение окраски Красно-фиолетовый при рН = 5,2; грязно-синий при рН = 5,4 и грязнозеленый при pH = 5,6; сохранять в темной склянке Красно-коричневый при pH = 5,6 Бледно-фиолетовый при pH = 5,8
367
СМЕШАННЫЕ ИНДИКАТОРЫ
Продолжение
о
с с
£
10
11
12
13
14
15
16
17
Состав раствора индикатора рТ Цвет индикатора Примечание
в кислой среде в щелочной среде
0,1% р-р натриевой соли бромкрезолового синего (1 вес. ч.) в НгО; 0,1% р-р натриевой соли хлорфенолового красного (1 вес. ч.) в НгО 6,1 Желто-зеленый Сине-фиолетовый Сине-зеленый при рН = = 5,4; синий при рН = = 5,8; синий с фио летовым оттенком при рН=6,0; сине-фиолетовый при pH = 6,2.
0,1% р-р натриевой соли бромкрезолового пурпурного (1 вес. ч.) в Н2О; 0,1% р-р натриевой соли бромтимолового синего (1 вес. ч.) в Н2О 6,7 Желтый » Желто-фиолетовый при pH = 6,2; фиолетовый при рН = 6,6; синефиолетовый при рН = = 6,8
0,1% р-р натриевой соли бромтимолового синего (2 вес. ч.) в НгО; 0,1% р-р азо-литмина (1 вес. ч.) в НгО 6,9 Фиолетовый Синий Желто-фиолетовый прн рН=6,2; фиолетовый при pH = 6,6; синефиолетовый при pH = 6,8
0,01% р-р нейтрального красного (1 вес. ч.) в сп.; 0,1% р-р метиленового синего (1 вес. ч.) в сп. 7,0 Фиолетово-синий Зеленый Фиолетовый прн рН= = 7,0; сохранять в темной склянке
0,1 % р-р нейтрального красного (1 вес. ч.) в сп.: 0,1% р-р бром тимолового синего (I вес. ч.) в сп. 7,2 Розовый Грязно-зеленый при pH = 7.4; бледно-розовый при рН=7,2; отчетливо розовый прн pH = 7,0
0,1% р-р цианина (2 вес. ч.) в 50%-ном сп.; 0,1% р-р фенолового красного (1 вес. ч.) в 50%-ном сп. 7,3 Желтый Фиолетовый Оранжевый при рН = 7,2; фиолетовый при рН = = 7,4
0,1% р-р натриевой соли бромтимолового синего (1 вес. ч.) в НгО; 0,1% р-р натриевой соли фенолового красного (1 вес. ч.) в НгО 7,5 » » Грязно-зеленый при рН = 7,2; бледно-фиолетовый при pH = 7,4; ярко-фиолетовый при рН=7,6
0,1% р-р натриевой соли крезолового красного (1 вес. ч.) в НгО; 0,1% р-р натриевой соли тимолового синего (3 вес. ч.) в НгО 8,3 » » Розовый при рН=8,2; отчетливо фиолетовый при рН=8,4
368
СМЕШАННЫЕ ИНДИКАТОРЫ
Продолжение
№ по пор. 1 Состав раствора индикатора рТ Цвет индикатора Примечание
в кислой среде в щелочной среде
18 0,1% р-р а-нафтолфта-леина (2 вес. ч.) в сп.; 0,1% р-р крезолового красного (1 вес. ч.) в сп. 8,3 Бледно-розовый Фиолетовый Бледно-фиолетовый при pH = 8,2; ярко-фиолетовый при рН = 8,4
19 0,1 % р-р а-нафтолфта-леина (1 вес. ч.) в сп.; 0,1% р-р фенолфталеина (3 вес. ч.) в СП. 8,9 » » Бледно-зеленый прн pH = 8,6; фиолетовый при рН=9,0
20 0,1% р-р фенолфталеина (1 вес. ч.) в сп.; 0,1% р-р метилового зеленого (2 вес. 4.1 в СП. 8,9 Зеленый » Бледно-синий при рН = = 8,8; фиолетовый при pH = 9,0
21 0,1% р-р тимолового синего (1 вес. ч.) в 50%-ном сп.; 0,1% р-р фенолфталеина (3 вес. ч.) в 50%-ном СП. 9,0 Желтый » От желтого через зеленый к фиолетовому
22 0,1% р-р фенолфталеина (2 вес. ч.) в 50%-ном сп.; 0,1% рр а-нафтолфталеипа (1 вес. ч.) в 50%-ном СП. 9,6 Слаборозовый » Зеленый при pH = 9,6
23 0,1% р-р фенолфталеина (1 вес. ч.) в сп.; 0,1% р-р тимолфталеина (1 вес. ч.) в СП. 9,9 Бесцветный » Розовый при рН = 9,6; фиолетовый при рН = = 10
24 0,1% р-р фенолфталеина (1 вес. ч.) в сп.; 0,2% р-р нильской голубой А (2 вес. ч.) В СП. 10,0 Синий Красный Фиолетовый при рН=10
25 0,1% р-р тимолфталеина (2 вес. ч.) в сп.; 0,1% р-р ализаринового желтого Р (1 вес. ч.) в СП. 10,2 Желтый Фиолетовый То же
26 0,2% р-р нильской голубой А (2 вес. ч.) в НгО; 0,1% р-р ализаринового желтого Р (1 вес. ч.) в сп. 10,8 Зеленый Красно-коричневый » »
24 Зак. 783
369
Ml. УНИВЕРСАЛЬНЫЕ ИНДИКАТОРЫ
Принятые сокращения: абс. — абсолютный; инд. — индикатор. Остальные сокращения см. стр. 16.
№ по пор. I Способ приготовления индикатора pH раствора Окраска индикатора Примечание
1 2 3 4 б Смешивают 15 мл 0,1 % р-ра диметилового желтого, 20 мл 0,1% р-ра бромтимолового синего, 5 мл 0,1% р-ра метилового красного, 20 мл 0,1% р-ра фенолфталеина и 20 мл 0,1% р-ра тимолфталеина В 500 мл 96%-ного сп. раств. 0,1 г фенолфталеина, 0,2 г метилового красного, 0,3 г метилового желтого, 0,4 г бромтимолового синего, 0,5 г тимолового синего. К полученному р-ру добавл. 0,1 н. р-р NaOH до появления желтой окраски (pH = 6) В 500 мл абс. сп. раств. 0,1 г метилового оранжевого, 0,2 г метилового красного, 0,3 г метилового желтого, 0,4 г бромтимолового синего и 0,5 г тимолового синего. К полученному р-ру добавл. 0,1 н. NaOH до перехода красного цвета в желтый В 100 мл 70%-кого сп. раств. 0,07 г тропеолина 00, 0,1 г метилового оранжевого, 0,8 г метилового красного, 0,4 г бромтимолового синего, 0,5 г а-нафтолфталеина, 0,4 г о-крезолфталеина, 0,5 г фенолфталеина и 0.15 г ализаринового желтого Р В 100 мл 50%-ного сп. раств. 0,07 г тропеолина 00, 0,1 г метилового оранжевого, 0,08 г метилового красного, 0,4 г бромтимолового синего, 0,5 г фенолфталеина и 0,1 г ализаринового желтого Р 1,0 2,0 3,0 4,0 5,0 6,0 7,0 8,0 9,0 10,0 2,0 4,0 6,0 8,0 10,0 2,0 4,0 6,0 8,0 10,0 3,0 4,0 5,0 6,0 7,0 8,0 9,0 10,0 11,0 12,0 2,0 3,0 4,0 5,0 6,0 6,5 7,0 8,0 Розовая Светло-красная Красно-оранжевая Оранжевая Желто-оранжевая Лимонно-желтая Желто-зеленая Зеленая Сине-зеленая Фиолетовая Красная Оранжевая Желтая Зеленая Синяя Красная Оранжевая Желтая Зеленая Синяя Красно-оранжевая Оранжевая Желто-оранжевая Оранжево-желтая Зелено-желтая Зеленая Зелено-синяя Фиолетовая Красно-фиолетовая Фиолетово-красная Оранжево-красная ' Красно-оранжевая Оранжевая Желто-ораижевая Оранжево-желтая Желтая Зелено-желтая Зеленая К 10 мл анал. р-ра добавл. 0,1 мл спиртового р-ра смешанного инд. К 1 мл анал. р-ра добавл. 1 каплю инд. К 10 мл анал. р-ра добавл. 1 каплю инд.
370
УНИВЕРСАЛЬНЫЕ ИНДИКАТОРЫ
Продолжение
О к о 1= 2 Способ приготовления индикатора pH раствора Окраска индикатора Примечание
5 В 100 мл 50%-ного сп. раств. 0,07 г тропеолина 00, 0,1 г метилового оранжевого, 0,08 г метилового красного, 0,4 г бромтимолового синего, 0,5 г фенолфталеина и 0,1 г ализаринового желтого Р 9,0 9,5 10,0 12,0 Зелено-голубая Сине-фиолетовая Фиолетовая Красно-фиолетовая
6 Смешивают 1 объем 0,02% р-ра фенолового красного, 2 объема 0,02% р-ра метилового красного, 4 объема бромтимолового синего в 15—30 %-ном сп. 4,0—8,0 Переходы охватывают весь спектр от красного до синего
7 В 500 мл 96%-ного сп. раств. 0,1 г метилового красного, 0,1 г бромтимолового синего, 0,1 г а-нафтолфталеина, 0,1 г фенолфталеина и 0,1 г тимолфталеина 4,0 5,0 6,0 7,0 8,0 9,0 10,0 11,0 Красная Оранжевая Желтая Зелено-желтая Зеленая Сине-зеленая Сине-фиолетовая Красно-фиолетовая
8 Смешивают 2 объема 0,02% спиртового р-ра метилового красного, 2 объема 0,04% водного р-ра бромтимолового синего (мононатрие-вая соль), 1 объем 0,02% водного р-ра фенолового красного (мононатриевая соль) 4,3 4,8 5,3 6,3 6,8 7,2 7,3 7,8 Ярко-красная Красная Оранжево-желтая Желтая Зеленовато-желтая Зеленая Голубовато-зеленая Голубовато-фиолетовая
9 Смешивают 0,5 объема 0,04% р-ра бромфенолового синего, 6,5 объема 0,04% р-ра бромкрезолового пурпурного. 2 объема 0,02% р-ра фенолового красного (индикаторы берут в виде монокалиевых солей) 5,2—7,0 7,0 7,0—7,8 Желтая Красно-коричневая Малиновая Р-ры инд. приготовляются на 10 %-ном СП.
24*
371
Окислительно-восстановительные индикаторы
Таблица состоит из двух разделов: I — индикаторы, окраска которых мало зависит от pH н ноиной силы раствора: II — индикаторы, чувствительные к изменению pH и иоиной силы раствора.
Все индикаторы расположены в порядке понижения численного значения нормального окислительного потенциала (£с). измеренного по отношению к стандартному водородному электроду. В раздел I включен необратимый индикатор метиловый красный (№ 30), позволяющий с большой чувствительностью устанавливать избыток реагента. Для некоторых ин» дикаторов в этой таблице указаны изменения Ео.
У казатель
Индикатор Раздел и № в таблице Индикатор Раздел и № в таблице
Акронол бриллиантовый синий Метиленовый синий II, 24
БДЦ 1, 17 Метиловый Капри синий . . . II, 25
п-Аминоднфениламин .... I, 6 Метиловый красный 1, 30
Бензидин I, 26 Мускарин II, 28
Биндшельдера зеленый II, 8 1-Нафтол-2-натрийсульфонат-
Бриллиантовый ализариновый индо-2,6-дихлорфенол . . . II, 20
синий 11, 31 1-Нафтол-2-натрийсульфоиат-
Бриллиантовый крезоловый индофенол II, 19
синий П, 21 Нейтральный красный .... II, 42
.м-Бромбензолиндофенол . . . н, 3 Нейтральный синий . II, 48
о-Бромфенолиндофенол . . . II, 5 Нильский синий И, 26
Виологен ... 11, 50 п-Нитродифениламин .... I, 12
Галлофенин . ... И, 30 Нитро-о-фенантролнн + Ре504 I, 3
Галлоцнанин 11, 29 Патентный синий А I, 22
2,4-Диамннодифениламин . . . 1, 10 Патентный синий В 1, 33
о-Днанизидин I. 28 Пиоцианин 11,43,44
2, 6-Дибромбензолиндогваякол П, 17 Порфирексид I, 6
2, 6-Дибромбензолиидофенол II, 11 Порфирексин . I, 8
Днметилглиоксим (комплекс с Порфириндин I, 25
Fe2+) Прочный хлопковый синий 11, 27
Диметилфеиосафраиин .... li; 39 Розиндулин 2Ж II, 49
2,2'-Дипиридил (комплекс с Сафранин Т II, 41
Гр21) Сетоглюцин Ж I, 14
2.2'-Дипиридил (комплекс с Сетополин Ж I, 13
Ru) I. 1 Синий Вурстера II, 53
Дифениламин сернокислый . . I, 32 Тетраметнлфеносафранин иоди-
о, л'-Дифенила минодикарбоно- стый и. за
вая кислота I, 5 Тетраэтилфеносафранин хло-
о, о'-Дифениламинднкарбоновая р истый II, 36
кислота I, 2 Тимол индофенол п, 16
Дифениламиносульфонат Na о-Толидин I, 27
или Ва I, 29 .м-Толуилендиамининдофенол II, 18
Дифен ил бензидин сернокислый I, 31 Фенилантраниловая кислота I. 9
2.6-Дихлорфенолиндокрезол . . II, 15 о-Фенантролин4-Ре504 (фер-
2,6-Днхлорфенолиндофеиол . . II, 12 роин) .... .... I, Н
2, 6-Дихлорфенолиндо-о-хлор-фенол П, 10 Фенолиндофенол ...... Феноловый синий П, 7 П, 9
Изо розин дулип № 1 . Д 47 Фенол-ти-сульфонатиндо-2, 6-
Изорозиндулин № 2 II, 46 дибромфеиол П. 1
Изорозиндулин № 3 II, 45 Фенол-о-сульфон атиндо-2, 6-ди-
Индигодисульфоновая кислота II, 34 бром фенол И, 4
Индигомоносульфоновая кислота II, 35 Феносафранин II, 40
Индиготетрасульфоиовая кислота и; 32 Фиолетовый Лаута . . . . II, 22
Индиготрисульфоновая кисло- Хлорорафин II, 37
та II, 33 л<-Хлорфенолиндо-2, 6-дихлор-
Красный Вурстера II, 52 фенол ". 2
jw-Крезолиндофенол II, 13 о-Хлорфенолиндофенол .... 11, 6
о-Крезолиндофенол II, 14 Цианин Б I, 18
Ксилеиовый синий АС .... I, 16 Цианол прочный зеленый 2Ж I, 15
Ксиленовый синий ВС .... I, 7 Цибаскарлетсульфонат .... II, 54
Ксиленцианол 2Ф I, 21 Эриоглюцнн А . . . I, 23
2-Метил-3-гидроксн-1, 4-нафто- Эриозеленый Б 1, 19
хинон ......... . II, 55 Этиловый Капри синий ...» II, 23
372
. ИНДИКАТОРЫ, ОКРАСКА КОТОРЫХ МАЛО ЗАВИСИТ ОТ pH И ИОННОЙ СИЛЫ РАСТВОРА
ИНДИКАТОРЫ, ОКРАСКА КОТОРЫХ МАЛО ЗАВИСИТ ОТ pH И ИОННОЙ СИЛЫ РАСТВОРА
373
Продолжение
№ по пор. Индикатор Ео, в Цвет Примечание
окисленной формы | восстановленной формы
19 Эриозеленый Б (эрио-грюн В) 4-1,01 Бледно-розовый Желто-зеленый (в нейтральной среде — темно-сине-зеленый) S
20 п-Этоксихризоидин +1,0 Бледно-желтый Красный При рН = 0 §
21 Ксиленцианол 2Ф +0,99 Оранжевый Желтый (в нейтральной среде — синий) я к
22 Патентный синий А +0,99 » Желто-зеленый (в нейтральной среде — зеленовато-синий) о Е
23 Эриоглюцин А +0,99 » Желто-зеленый (в нейтральной среде — синий) ОКРАС И ИОН
24 5,6-Диметил-1, 10-фенан-тролин (комплекс с Fe2+) +0,97 Желто-зеленый Красный :ка ко НОЙ с
25 Порфириндин +0,94 Бесцветный Интенсивно-синий £о=О,67 в при pH = 5,U; sg £0=0,57 в при рН=7,0
26 Бензидин +0,92 Желтый (в нейтральной среде — темно-зелено-синий) Бесцветный £'о = О,86 в при рН=1,0; “S £о = О,8О в при рН = 2,0; >г £о=0,74 в при pH=3,0
27 о-Толидин +0,87 Желтый (в нейтральной среде — зеленосиний) » £о=О,81 в при рН=1,0; £о=О,75впри рН = 2,0; S £о=О,69впри рН = 3,0>>
28 о-Дианизидин +0,85 Красный » СО
29 Дифениламиносульфо-• нат Na или Ва +0,84 Красно-фиолетовый » . о Я
30 Метиловый красный (метилрот) +0,8 Бесцветный Красный Необратимый индика о тор н
31 Дифенилбензидин сернокислый +0,76 Фиолетовый Бесцветный о Я
32 Дифениламин сернокислый +0,76 Фиолетовый »
33 Патентный синий В +0,7 Оранжево-красный Желтый (в нейтраль ных и слабокислых р-рах — синий)
II. ИНДИКАТОРЫ, ЧУВСТВИТЕЛЬНЫЕ К ИЗМЕНЕНИЮ pH И ИОННОЙ СИЛЫ РАСТВОРА
Принятые сокращения: ок.—окисленная форма; восст. —восстановленная форма.
№ Eq в вольтах при pH равном
по Индикатор । j I I । t Примечание пор. 0|5|6 7 8 910 F
Я Индофенолы = 1 Фенол-л-сульфонатин- Д-0,69 Д-0,39 Д-0,33 —|—0,283 Д4),21 —J—0,15 . . . Индикаторы группы ии- ® до-2,6-дибромфенол дофенолов в восста- > 2 .м-Хлорфено л индо-2,6- Д-0,67 -{-0,37 —|—0,31 Д-0,254 -1-0,19 Д-0,13 . . . новленном состоянии о дихлорфенол бесцветны или очень я? 3 Jw-Бромбензолиндофе- Д-0,67 Д-0,37 Д-0,31 Д-0,248 Д-0,19 Д-0,13 . . . слабо окрашены, а в Л нол окисленном состоянии о5 4 , Феиол-о-сульфонатин- -}-0,66 Д-0,36 Д-0,30 Д-0,242 Д-0,18 Д-0,12 . - . окрашены в синий
5 о-Бромфенолиндофенол +0,659 +0,36 +0,30 +0,240 +0,18 6 о-Хлорфенолиидофенол -[-0,653 4-0,36 --0,30 +0,233 +0,18 7 Фенолиндофенол +0,649 -|-0,35 +0,29 +0,227 +0,17 8 Биндшельдера зеленый +0,64 +,34 +0,28 +0,224 +0,16 9 Феноловый синий +0,64 +0,34 --0,28 --0,224 +0,16 10 2,6-Дихлорфенолиндо- +0,64 +0,34 +0,28 +0,219 +0,16 о-хлорфенол 11 2, 6-Дибромбензолиндо- +0,64 +0,34 4-0,28 -[-0,218 +0,16 фенол (натриевая соль) 12 2,6-Дихлорфенолиндо- +0,64 +0,34 +0,28 +0,217 +0,16 фенол 13 .и-Крезол индофенол 4-0,63 +0,33 +0,27 +0,208 +0,15 14 о-Крезолиндофенол +0,616 +0,31 --0,25 --0,191 --0,13 15 2,6-Дихлорфенолиндо- +0,60 -(-0,30 --0,24 +0 181 +0 12 - 0,12 . . атома галогена) или s® - 0,12 . . . красный цвет n-j - 0,11 ... sg - 0,10 ... +.Ю . . ;Е - 0,10 . . ><* +.10 . . gs >3 +.Ю . . Е S +,09 ... 2 +,07 ... ° нООб г
крезол (натриевая соль) 16 Тимолиндофенол +0,592 +0,29 +0,23 -[-0,174 [-0,11 17 2,6-Дибромбензолиндо- 4-0,58 +0,28 +0,22 +0,159 [-0,10 гваякол Со Сл -0,05 . . . -0,04 . . .
Продолжение
№ по пор. Индикатор Eq в вольтах при pH равном Примечание
0 | 5 6 7 1 8 9 10
18 .и-Толуилендиаминин-дофенол +0,55 +0,25 +0,19
19 1-Нафтол-2-натрий-сульфонат индофенол +0,54. +0,24 +0,18
20 1-Нафтол-2-натрийсуль-фонат индо-2,6-ди-хлорфенол Оксазины и тиазины +0,54 +0,24 +0,18
21 Бриллиантовый крезоловый синий (брилли-антблау С; 3-амино-9-диметиламино-10-метилфеноксазинхло-рид) +0,583 +0,149 +0,089
22 Фиолетовый Лаута (тионин; диаминофенотиазин). +0,563 +0,101 +0,047
23 Этиловый Капри синий (3,9-бис-диметиламинофеноксазин азотнокислый) +0,540 +0,089 +0,001
24 Метиленовый синий (ме-тиленблау; тетраме-тилдиаминофеноти-азин) +0,532 +0,135 +0,093
+0,125 +0,07 +0,01
+0,123 +0,06 +0,00
+0,119 +0,06 +0,00
+0,047 +0,015 +0,016 Ок. при рН= 1-5-10— синяя; при рН>10 — красная; восст.— бесцветная
+0,011 —0,020 —0,050 Ок. — фиолетовая; восст. — бесцветная
—0,072 —0,115 —0,143 Ок. — зелено-синяя; восст. •— бесцветная
+0,060 +0,030 0,000 Ок. — синяя; восст. — бесцветная
ИНДИКАТОРЫ, ЧУВСТВИТЕЛЬНЫЕ К ИЗМЕНЕНИЮ;
25 Метиловый Капри си- +0,477 +0,038 —0,021 —0,061 —0,013 —0,123 Ок. — темно-синяя; в
ний (3,9-бис-диметил- восст. — бесцветная S
аминофеноксазин. S
7пС1г-соль) о
26 Нильский синий +0,406 —0,011 —0,071 —0,122 —0,159 —0,192 . . - Ок. при рН= 1-т-Ю— 2 о
синяя; при рН>10 — S
красная; восст. — бес- о
цветная
27 Прочный хлопковый си- +0,145 +0,105 +0,080 +0,050 . . . . Ок. — синяя; восст. — Е
НИЙ бесцветная о
28 Мускарин . . . . +0,130 +0,080 +0,050 +0,020 Ок. — синяя; восст. — Ci
бесцветная оэ о
29 Г аллоцианин +0,080 +0,021 —0,037 —0,095 -0,140 Ок. при рН=5ч-8
синяя; при рН<4 и>
>8 — красно-фиоле-
товая; восст. — бес-
цветная
30 Галлофенин .... —0,003 —0,077 —0,142 —0,202 —0,262 Ок. в кислотах — зеле-
ная; в воде — синяя;
в щелочах — пурпур-
ная; восст. — бесцвет-
ная
31 Бриллиантовый ализа- . . . . —0,040 —0,112 —0,173 —0,226 —0,337 Ок. в кислотах — синяя;
риновый синий в воде — фиолетовая
Индигосульфо-
новые кислоты
32 Индиготетрасульфоно- +0,365 +0,065 +0,06 —0,046 —0,083 —0,11 В восст. состоянии все
вая кислота индикаторы этой труп-
33 Индиготрисульфоновая +0,332 +0,032 —0,02 —0,081 —0,11 —0,14 пы почти бесцветны.
кислота в окисл. — синие. Чем
больше сульфогрупп,
тем интенсивнее от-
й тенок синего цвета
Продолжение
№ по пор. Индикатор Eq в вольтах при pH равном Примечание
° 5 6 7 8 9 10
34 Индигодисульфоновая кислота (индигокармин) +0,291 —0,010 —0,07 —0,125 —0,16 —0,20
35 Индигомоносульфоно-вая кислота +0,262 —0,04 —0,10 —0,16 —0,19 -0,22
Азины
36 Тетраэтилфеносафра- нин-хлористый (ирис-виолет; аметиствио-лет) +0,355 —0,080 —0,167 —0,254 —0,34 —0,43 Ок. — фиолетовая; восст. — бесцветная
37 Хлорорафин +0,305 +0,005 —0,055 —0,115 —0,175 —0,235 -0,295 Ок. — желтая; восст. — зеленая
38 Тетраметил феносафранин иодистый +0,288 —0,113 —0,193 —0,273 —0,35 —0,43 . . . Ок. — фиолетовая; восст. — бесцветная
39 Диметилфеносафранпн (фуксин; метилен -виолет) +0,286 —0,104 —0,182 —0,260 —0,34 —0,42 . . . Ок. — фиолетовая; восст. — бесцветная
40 Феносафранин +0,280 —0,100 —0,176 —0,252 —0,33 —0,40 • • • Ок. — красная; восст. — бесцветная
41 Сафранин Т +0,235 —0,139 —0,214 —0,289 —0,36 —0,44 . . . Ок. — красная; восст. — бесцветная
42 Нейтральный красный (нейтральрот; толу-иленрот) +0,237 —0,17 —0,26 —0,33 —0,39 —0,45 Ок. — красная; восст. — бесцветная
43 44 Пиоцианин (1-я ступень) Пиоцианин (2-я ступень) +0,207 (рН=3) +0,097 (рН=3) +0,082 +0,078 +0,026 —0,034 —0,093 —0,15 —0,20 В кислой среде ок.: 1-я ступень — красная; 2-я ступень—зеленая; восст. — бесцветная; в щелочной среде: ок. — синяя; восст. —• бесцветная
45 Изорозиидулин № 3 +0,202 —0,10 —0,16 —0,22 —0,28 —0,34 Ок. — синяя; восст. — бесцветная
46 Изорозиндулин № 2 +0,195 —0,10 —0,16 —0,22 —0,28 —0,34 Ок. — синяя; восст. — бесцветная
47 Изорозиидулин К» 1 +0,190 —0,11 —0,17 —0,23 —0,29 —0,35 Ок. — синяя; восст. — бесцветная
48 Нейтральный синий +0,170 —0,13 —0,19 —0,25 —0,31 —0,37 Ок. — синяя; восст. — бесцветная
49 Рознндулин 2Ж (натриевая соль моно-сульфорозиндона) .... —0,161 —0,221 —0,281 —0,340 —0,395 -0,438 Ок. — багряно-красная; восст. — бесцветная
50 Виологен . . . . —0,400 .... Ок. — синяя; восст. — желтая
51 Днметилглиоксим (комплекс с Fe2+) +0,25 Ок. — бесцветная; восст. — красная (только в щелочной среде)
52 Красный Вурстера (диметил-п-фенилен-диамин) +0,447 (рН=4,6) . . . Ок. — красная; восст. — бесцветная
53 Синий Вурстера (те-траметил-п-фенилен-диамин) .... +0,420 (рН=3,6) +0,365 (рН=4,05) . . . Ок. — синяя; восст. — бесцветная
54 Цибаскарлетсульфонат .... —0,036
55 2-Метил-3-гидрокси-1,4-нафтохинон —0,180
ИОННОЙ СИЛЫ РАСТВОРА
Адсорбционные индикаторы
Индикатор Определяемый ион Ион, которым производят титрование Изменение цвета индикатора (начальный — конечный)
Ализариновый красный S (0,4—1% водн. р-р) Бенгальский розовый А (1% водн. р-р) Бромкрезоловый зеленый (1% р-р в 20% сп.) Бромфеноловый синий (0,1—1% р-р в 20% СП.) Диаминовый голубой Диаминовый коричневый Диаминовый прочный красный Ф Дибромфлуоресцеин Дииодфлуоресцеин, двунатриевая соль Диметилдииодфлуорес-цеин, двунатриевая соль (1% водн. р-р) Дифениламиновый синий (1% водн. р-р) Дифениламин (1% р-р в 96 %-ной H2SO4) Дифенилбензидин (2% р-р в 96%-ной H2SO4) . Дифенилкарбазид (0,1% сп. р-р) Дифенилкарбазон (0,2— 0,3% сп. р-р) , Дихлорфлуоресцеин (0,1% водн. р-р или в 60% сп., или 0,025 н. NaOH) Индооксин (0,05% сп. Р-Р) Кармоазин Конго красный (0,1—1% водн. р-р) Родамин С Родамин 6Ж (0,1% водн Р Р) [Fe (CN)6]4- cr J- (в присутствии ci ) СГ СГ; Г РЬ2+ РЬ2+ РЬ2+ ВГ J (в присутствии С1 ) Вг-; J" СГ; ВГ Zn2+ In3+ CN~ СГ; Г; CN~ Вг~; Г SCN- СГ; Br-; J" СГ; SCN- ВГ; Г СГ; Br-; J- Ag+ Ag+ РЬ2+ Ag+ Ag+ Ag+ Ag+ MoO2- MoO2- 4 МоО2- Ag+ Ag+ Ag+ Ag+ [Fe (CN)6]4- [Fe (CN)6]4- Ag+ Hg22+; Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ ВГ ВГ Желтый — розово-красный Желтый — лилово-розовый Карминово-красный — сине-красный Фиолетовый — зеленоголубой Желто-зеленый — зеленовато-синий Бесцветный — фиолетовый (осадок) Бесцветный — желтый (осадок) Бесцветный — розовый (осадок) Оранжево-красный — фиолетовый Зеленый — фиолетовый Синий — зеленовато-желтый Синий — зеленый Красный — фиолетовый Фиолетовый — голубой Желтый — зеленый Розовый — синий Желто-зеленый — красный Красный — синий Розовый — серый Розовый — зеленый Красный — синий Желто-красный — красно-фиолетовый
;380
Адсорбционные индикаторы
Продолжение
Индикатор Определяемый нон Ион, которым производят титрование Изменение цвета индикатора (начальный — конечный)
Тартразин (тартрацин) •Г (в присутствии С1 ) Ag+ Ag+ Вг-; СГ; J-; SCN- Бесцветный — зеленый Желтый — зеленый
Тропеолин 00 (1 % водн. РР) СГ Ag+ Желтый — розовый
•Феносафранин (сафранин Т) (0,1—0,5% водн. р-р) С1 ; Вг Ag+ Красный — синий
Флуоресцеин, натриевая соль (0,1—0,2% водн. или сп. р-р) Cl ; Вг ; J ; SCN-; SeCN~; С2°Г Ag+ Желто-зеленый — розовый
Эозин (0,5% водн. или 0,1% в 60—70% сп.) J ; Вг-; SCN-; РЬ2+ Ag-*-; MoO2-4 Оранжевый — интенсивно-красный Красно-фиолетовый — оранжевый
Эритрозин (0,5% водн. Р-Р) MoO2-; J" 4 Pb2+; Ag+ Оранжевый — темнокрасный Красный — краснофиолетовый
Люминесцентные индикаторы
Люминесцентные индикаторы позволяют производить объемное определение в мутных и окрашенных растворах, так как при титровании наблюдают не изменение окраски раствора, •а изменение цвета люминесценции, который не зависит от окраски и прозрачности раствора, В графе «Изменение цвета люминесценции» знак обозначает отсутствие люминесцентного свечения; первый цвет относится к более кислой среде, второй — к более щелочной.
Более подробные сведения см. Люминесцентный анализ, сб. под ред. М. А. Ко н-•стаитииовой-Ш лезингер, Физматгиз, 1961.
№ по пор. Индикатор Интервал pH изменения цвета люминесценции Изменение цвета люминесценции
1 Эозин 0,0-3,0 — зел ен ы й
2 5-Метил-З-карбэтоксиумбел- 0,1—1,0 Фиолетовый — синий
лиферон
3 5,7-Диметокси-4-метилкума- 0,1-1,1
4 Этиловый эфир 5,7-димет- 0,1—3,1 То же
окси-4-диметилкумарин-
3-уксусной кислоты
5 Дикумарин 0,1—3,1 Желтый — синий
6 4, 8-Диметилумбеллиферон 0,1—3,1 То же
7 Бензофлавнн 0,3—1,7 Желтый — зеленый
381
Люминесцентные индикаторы
Продолжение
№ по пор. Индикатор Интервал pH изменения цвета люминесценции Изменение цвета люминесценции
8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 5-Метокси-4, 7-диметилкума-рин Родамин 6Ж 5, 7-Диметокси-4-метилкума-рин-3-уксусная кислота 4-Этоксиакридон Эскулин Антраниловая кислота (1-й переход; см. Ns 47,124) 3-Амино-(1)-нафтойная кислота (1-й переход; см. Ns 46,119) 1 -Нафтиламин-6-сульфамид (1-й переход; см. № 111) 2-Нафтиламин-6-сульфамид (1-й переход; см. Ns 114) 2-Нафтиламин-8-сульфамид (1-й переход; см. № 113) 1 -Нафтиламин-7-сульфамид (1-й переход; см. № 112) 1 -Нафтиламин-5-сульфамид (1-й переход; см. № ПО) Тимоловый синий Ксиленоловый синий АШ-кислота (1,8-аминонаф-тол-3, 6-дисульфокислота) а-Нафтойная кислота Салициловая кислота Флоксин ВА Р-Нафтиламин 3, 6,8-Трихлор-7-окси-4-метил-кумарин Нафтионовая кислота З-Окси-2-нафтойная кислота Морин (1-й переход; см. №95) 5-Аминосалициловая кислота о-Метоксибенз альдегид о-Фенилендиамин п-Фенилендиамин 8-Аллнл-4-метилумбеллифе-рон 0,5—3,1 1,0-1,3 1,1—3,1 1,4—3,2 1,5-2,0 1,5—3,0 1,5-3,0 1,9—3,9 1,9—3,9 1,9—3,9 1,9—3,9 2,0—4,0 >2 >2 2,2—3,6 2,5—3,5 2,5-3,5 2,5—4,0 2,8—4,4 3,0—5,0 3,0-6,0 3,0—6,8 3,1—4,4 3,1—4,4 3,1—4,4 3,1—4,4 3,1—4,4 3,1—8,1 Желтый — синий Оранжевый — розовый гмиий
Зеленый — » ГП П vfin Й
синий
зеленый ____уу
гммий
- у»
-- ЧРЛРНЫЙ
. У/РПТМИ
ппйнжрныЙ
— W р птый
синий ...»
- »
у,
- (ЬиПЛРТПИЫЙ
синий
Зеленый ГЙИОЛРТПКЫЙ
зеленый оранжевый Зеленый — синий
382
Люминесцентные индикаторы
Продолжение
№ по пор. Индикатор Интервал pH изменения цвета люминесценции Изменение цвета люминесценции
36 Диметилнафтейродин 3,2—3,8 Лиловый — оранжевый
37 Диэтилнафтейродин 3,2—4,7 » — сиреневый
38 Дибутилнафтейродин 3,2—5,3 Синий — »
39 Флуоресцеин 3,4—4,1 зеленый
40 2-Метокси-6, 9-дихлоракридин 3,4—4,3 Желто-зеленый — голубой
41 2-Метокси-7, 9-дихлоракридин 3,4—4,3 Желто-зеленый — синий
42 а-Нафтиламин 3,4—4,8 — »
43 Хинин сернокислый (1-й переход; см. № 107) 3,8—6,1 Голубой — фиолетовый
44 Эритрозин 4,0—4,5 зеленый
45 Хинная кислота 4,0—5,0 Желтый — синий
46 3-Амино-(1)-нафтойная кислота (2-й переход; см. № 14,119) 4,0—6,0 Зеленый —- »
47 Антраниловая кислота (2-й переход; см. № 13,124) 4,0—6,0 Синий — темно-синий
48 Р-Метилэскулетин 4,0—6,2 синий
49 2, 7-Дихлорфлуоресцеин 4,0—6,6 зеленый
50 Р-Нафтохинолин 4,4—6,3 Синий
51 Резоруфин 4,4—6,4 Желтый — оранжевый
52 9-Этнл-1,2-бензакридин 4,7—6,0 Зеленый — синий
53 Акридин 4,8—6,6 Зеленый — фиолетовый
54 8-Бром-7-окси-4-метилку марин 5,0—7,0
55 8-Хлор-7-окси-4-метилкума-рин 5,0—7,0
56 5-Метил-З-ацетилумбеллифе-рон 5,1—7,1
57 9-Метил-1, 2-бензакридин 5,4—6,1 Зеленый — фиолетовый
58 9-Метил-З, 4-бензакридин 5,7—7,0 То же
59 Лакмоид 5,8—7,0 синий
60 р-Метилумбел лифер он 5,8—7,6
61 Кислота Шеффера (2,6-нафтолсульфокислота) 5,8—8,0 ' — »
62 Дициангидрохинон 5,8—8,2 Синий — зеленый
63 Г идрохинондисульфокислота 6,0-7,0 Желтый — синий
64 Хромотроповая кислота 6,0—7,0
65 3, 6-Диоксифталимид 6,0—8,0 Зеленый — желтый
66 Хинин 6,0—10,0 Синий — фиолетовый
67 5,7-Диокси-4-метилкумарин- 6,1—7,1 » — зеленый
3-уксусная кислота
383
Люминесцентные индикаторы
Продолжение
№ по пор. Индикатор Интервал pH изменения цвета люминесценции 1! Изменение цвета люминесценции
68 5-Фенилумбеллиферон 6,1—7,1 Синий — зеленый 21
69 Хинолин 6,2—7,2
1 илуиим -'у
70 4-Кетимид-6-гексил-7-оксику- 6,2—7,6
марин 6,2—7,6 U.
71 6-Гексил-4, 7-диоксикумарин
72 4, 7-Диоксикумарин 6,2—7,6
73 1-Хлор-9-(р-диэтиламино-а- 6,4—7,8 Г олубой — зеленый
метилбутил) -аминоакридин-
дихлоргидрат 6,4—7,8
74 2-Хлор-9- (р-диэтиламино-а- То же
метилбутил)-аминоакридин-
дихлоргидрат 6,5—7,6
75 Умбеллиферрн
76 Орнинаурин 6,5—8,0
77 7-Аминоакридин 6,7—7,3 Оранжевый — зеленый
78 Феноловый красный 6,8—8,4 Зеленый — фиолетовый
79 Нейтральный красный 6,8 Фиолетовый — оранже-
вый
80 Розоловая кислота 7,0—8,2
товый
81 Тиофлавин > 7 желтый
82 Кислота Невиль-Винтера 7,0—9,0
И 'Я ipilUJlU”
(1,4-нафтолсульфокислота) 7,1—8,1 7,2—8,9 товый
83 8-Аллилумбеллиферон , синий
84 Кармин Синий — желтый
85 З-Окси-1-нафтойная кислота > 7 синий
86 Кумаровая кислота 7,2—9,0 зеленый
87 Г-соль 7,4—9,0 синий
88 Ж-кислота 7,5—9,1
89 4-Бутил-7-оксику марин > 7
90 4-(2-Фурил)-7-оксикумарин > 7
7,6—8,0
91 Ацетамидо-2-метилхинолин-5-
карбоновая кислота 7,8
92 Азолитмин синий
93 Куркума 8,0—9,3
94 Умбеллиферон+ацетат нат- 8,0—9,8 синий
рия 8,0—9,8
95 Морин (2-й переход; см. № зеленый
30) >8,0
96 Ализаринсульфонат натрия • — красный
97 R-соль 8,0—10,6 Зеленый — синий
384
Люминесцентные индикаторы
Продолжение
№ по пор- Индикатор Интервал pH изменения цвета люминесценции Изменение цвета люминесценции
98 R-кислота (2-нафтол-3,6-дисульфокислота) 8,1—10,6 Зеленый — синий
99 Нафтол АС 8,2—10,0 Желтый — зеленый
100 З-Окси-1-нафтойная кислота 8,2—10,0 синий
101 Акридиновый оранжевый (эухризин 3R) 8,4—10,4 Оранжевый — зеленый
102 а-Нафтолсульфокислота 8,2
103 104 а-Нафтол Р-Нафтол 8,6 8,5—9,5 синий голубой
105 Кумарин 8,9—12,0 зеленый
106 9-Аминоакрндин 9,0-11,0 Синий — »
107 Хинин сернокислый (2-й переход; см. № 43) 9,5—10,5 Фиолетовый —
108 6, 7-Диметилизохннолин-1-карбоновая кислота 9,5-11,0 Желтый — синий
109 1-Нафтилампн-4-сульфамид 9,5—13,0 Синий — голубой
110 1-Нафтиламин-5-сульфамид (2-й переход; см. № 19) 9,5-13,0 Желтый
111 1-Нафтиламин-6-сульфамид (2-й переход; см. № 15) 9,6—13,0 Зеленый
112 113 114 1-Нафтиламин-7-сульфамид (2-й переход; см. № 18) 2-Нафтиламин-8-сульфамид (2-й переход; см. № 17) 2-Нафтиламин-6-сульфамид (2-й переход; см. № 16) 9,6—13,0 9,6—13,0 9,6—13,0 » .— Синий » .—
115 Чикаго СС кислота 10,0—12,0 Фиолетовый — зеленый
116 9-Хлоракридин 10,0-12,0 Синий — »
117 7-Метокси-З-фенилкумарин 10,1—14,0 Синий
118 3-Ацетил-7-метокси-8-метил-кумарин 10,1—14,0 То же
119 3-Амино-(1)-нафтойная кислота (3-й переход; см. Ns 14, 46) 11,6—13,0 » >
120 1-Нафтиламинсульфокислота-5 12,0-13,0 Синий — зеленый
121 2-Нафтиламинсульфокислота-5 12,0-13,0 Синий — фиолетовый
122 2-Нафталин-6, 8-дисульфокислота 12,0-14,0 » — желтый
123 124 Риванол Антраниловая кислота (3-й переход; см. Ns 13, 47) 12,0-14,0 12,5—14,0 Желто-зеленый Синий —
125 Котарнин > 12,5 желтый
385
25 Зак. 783
Индикаторные и реактивные бумаги Г
Универсальные индикаторные бумаги позволяют определять как ориентировочное зна- ? чение величины pH раствора (0,5—2,0 единицы pH), так и более точное (0,2—0,3 едини- » цы pH). Для этого используют сначала индикаторные бумаги с интервалом pH перехода окраски 1,0—11,0 или 0—12, а затем применяют бумаги с более узким интервалом pH. Окраска индикатора в таблицах указана для начального и конечного значений pH (например, для индикаторной бумаги с интервалом pH перехода 1,0—11.0 красно-желтая окраска соответствует pH = 1,0, а фиолетовая 11,0). Количество промежуточных тоиов окраски устанавливается при помощи величин pH стандартной или сравнительной шкалы.
Определение значений pH при помощи индикаторной бумаги возможно только в водных буферных растворах с не очень высокой концентрацией солей, а также при отсутствии сильных окисляющих веществ. Определение pH производят путем сравнения окраски полоски индикаторной бумаги, смоченной испытуемым раствором, с цветной (сравнительной) шкалой, смоченной тем же раствором.
УНИВЕРСАЛЬНЫЕ ИНДИКАТОРНЫЕ БУМАГИ
Интервал pH перехода окраски Окраска индикатора в среде Величины pH стандартной шкалы
кислой щелочной
1,0—11,0 Красно-желтая Фиолетовая 1,0—3,0—5,0—7,0—9,0— 11,0
0—12 » » 0,1 —2—3—4—4.5—5— 5,5—6—6,5—7—7,5— 8—8.5—9—10—11—12
3,9—5,4 Желтая Синяя 3,9—4,1—4,3—4,5— 4,8— 5,0—5,2—5,4
4,5—6,3 » Пурпуровая 4,5—4,7—4,9—5,1—5,4— 5,7—6,0—6,3
5,0—6,8 » Фиолетовая 5,0—5,3—5,5—5,8—6,1 — 6,3—6,5—6,8
6,5—8,4 » Синяя 6,5—6,8—7,0—7,2—7,5— 7,8—8,1—8,4
РЕАКТИВНЫЕ БУМАГИ
Реактивная бумага Окраска реактивной бумаги в среде Чувств ительность
кислой щелочной
Гропеолип 00 Фиолетовая Желтая 9-10“® н. НС1
Метиловая фиолетовая Желтая Фиолетовая 5-10 3 н. НС1
Метиловая оранжевая Красная Желтая 7-10 4 н. НС1
Конго красная Синяя Красная 4-10 н. НС1
Метиловая красная Красная Желтая 4-10 5 н. НС1
Лакмусовая синяя » Синяя 9 -10 4 н. НС1
Лакмусовая красная » » 9-10 н. NaOH
Бриллиант желтая Желтая Красная 8 - 10 3 н. NaOH
Куркумовая » Красно-коричне- 8 -10 5 н. NaOH
вая
Крезолфталеиновая Белая Фиолетово-крас- 1-10 4 н. NaOH
пая
Фенолфталеиновая » Красная 9-10 4 н. NaOH
Тимолфталеиновая » Синяя 4-10 3 н. NaOH
386
ИНДИКАТОРНЫЕ БУМАГИ РИФАН
Интервал pH перехода окраски Окраска индикатора в среде Величины pH сравнительной шкалы
кислой щелочной
0,3—2,2 Пурпурно-фиолетовая Желтая 0,3—1,0—1,4—1,8—2,2
0,4—1,4 Желто-зеленая Фиолетовая 0,4—0,5—0,7—0,9—1,1 — 1.4
1,0—2,3 Красно-фиолетовая Желтая 1,0— 1,2—1,5—1,8— 2,0— 2,3
1,8—3,8 Синяя Красная 1,8—2,2—2,6—3,0— 3,4— 3,8
1,9—3,2 Красно-фиолетовая Желтая 1,9—2,2—2,5—2,8— 3,1 — 3,4
3,9—5,4 Желто-зеленая Синяя 3,9—4,2—4,5—4,8— 5,1 — 5,4
4,0—5,4 Желтая Зеленая 4,0—4,4—4,7—0.5—5,4
5,2—6,7 » Пурпуровая 5,2—5,5—5,8—6,1—6,4— 6,7
5,8—7,4 » Сине-фиолетовая 5,8—6,2—6,6—7,0-7,4
6,0—7,5 Желто-зеленая Синяя 6,0—6,3—6,6—6,9— 7,2 —- 7,5
6,6—8,1 » » 6.6—6,9—7,2—7,5— 7,8— 8,1
7,2—8,8 Желтая Красно-оранжевая 7,2—7,5—7,8—8,1—8,4— 8,8
7,3—8,8 Желто-коричневая Пурпуровая 7,3—7,6—7,9—8,2— 8,5— 8,8
7,8—9,0 Желтая Зеленая 7,8—8,1—8,4—8,7—9,0
8,7—10,0 Зеленая Сине-голубая 8,7—9,0—9,3—9,6—10,0
9,2—11,0 Желтая Фиолетовая 9,2 — 9,5 — 9,8 — 10,1 -
9,5—14,0 Синяя Желтая 10,4—10,7—11,0 9,5—10,5—11,5—12,5—
10,0—11,6 Желтая Фиолетовая 13.5—14,0 10,0—10,4—10,8—11,2—
11,0—13,1 Синяя • Розовая 11,6 11,0—11,3—11.6—11,9— 12,2—12,5—12,8—13,1
11,5—13,2 Желтая Фиолетовая 11,5—12,0—12,4 —12,8—• 13,2
12,0—14,0 Синяя Желтая 12,0—12.4—12.8—13,2— 14,0
12,4—13,6 Желтая Оранжевая 12,4—12.7—13.0—13,6
25*
387
Комплексометрические9 методы анализа
Таблица состоит из двух разделов: комплексометрическое титрование неорганических ионов раствором Na-ЭДТА и титрОвайиС растворами других комплексонов. Приведены основные характеристики, позволяющие выбрать методику титрования и маскирующий агент. Характеристика индикаторов приведена на стр. 400.
Более подробно см.; I. В. Д. Конкин, В. И. Жихарева, Комплексометрический анализ, 2-е изд.. Изд. «Техника», Киев, 1964.—2. Р. Лршибил, Комплексоны в химическом анализе, пере в. с чешек., 2-е изд., ИЛ, 1963.
Принятые
Комплексоны:
Na-ЭДТА — двунатриевая соль этилендиаминотетрауксусной кислоты (трилон Б, комплексон III)
БАК — И,И-бнс(карбоксиметил)антраниловая кислота
ОДК— оксиэтилэтилеидиаминтетрауксусная кислота
ДАК — диэтилеитриаминпентауксусная кислота
ДЦТК— ^З-диаминоциклогексан-М.Ы.П'.М'-тетрауксусная кислота
МТК— 2-метилэтилеидиамиитетрауксусиая кислота
НТА— иитрилтриуксусная кислота
ТЭА— тетраэтиленпентамии
ЭАК — этиленгликоль-бнс(р-аминэтилен)-М,М,№,М'-тетра-уксусная кислота
ЭПК — этилеидиамино-И.П.П'.И'-тетрапропионовая кислота
Тип титрования:
3—титрование заместителя, вытесненного определяемым ионом (в скобках), стандартным раствором комплексона
Н — непрямое титрование, прочие методы
О — обратное титрование остатка непрореагировавшего комплексона стандартным раствором иона (указанного в скобках)
П — прямое титрование определяемого ионз стандартным раствором комплексона
С — титрование стандартного раствора комплексона определяемым ионом
обозначения
Инд.икаторэ1:
А — арсеназо
АС —ализарин S
БПК — бромпнрогаллоловый красныЛ
ВС — вариаминовый синий В
Г — гематоксилин
Д— дитизон
КО — ксиленоловый оранжевый
М — мурексид
МТС — метилтимоловый синий ПАН— 1-(2'-пиридилазо)-2-нафтол
ПК — пирогаллоловый красный ПФ— пирокатехиновый фиолетовый ТМ — тиомочевииа
Т — тирои
ТФ — тимолфталексон
X— хромазурол S
Ц— цинкон
ХЧ— хромогеновый черный
Прочие обозначения:
Ас“— CH3COONa или СНзСООК или CH3COONH4 ДМП— 2. 3-димеркапто 1-пропанол
ТЭТА — триэтаноламин
Кроме того, см. сокращения на стр. 16.
КОМПЛЕКСОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ НЕОРГАНИЧЕСКИХ ИОНОВ РАСТВОРОМ Ка-ЭДТА
Определяемый ион Тип титрования Индикатор Условия титрования Маскируемые ионы Маскирующий агент
А13+ О (РЬ2+) О(РЬ2+) КО » Уротропин (pH = 5,5), гор. Р-Р Уротропин (до желт, окраски) Cu2+, Hg2-*, Т13+ Cd2+, Со2+, Мп2+, Ni2+, Zn2+ Цистин о-Фенантролин
AsHi Au3+ Ва2+ В13+ Са2+ Со со СО 1 п 1 О (£п2+) Н 3[Ni (CN)"] П О (Са2+) П • » » О (В13+) П » » » » О (Zn2+) О (Са2+) П О (Са2+) X д ХЧ ТФ ТМ ко ПФ ПК » ТМ г ПФ ТМ МТС д ТФ ХЧ ТФ СНзСООН, pH = 4,0; 80° С Ацетатн. буф. (рН=4ч-5,1), 50% сп.; 90е С Осажд. AS2S3 сероводородом, переводят в тиосоль, осажд. CdS и оттитровы-вают изб. Cd2+ р-ром Na-ЭДТА Аммиачн. буф. (рН=9-=-10), аскорбиновая к-та и обратное титр. изб. Na-ЭДТА р-ром Мп2+ рН=8-=- 10 NaOH, рН=12 НС1О4 или HNO3, pH=2 4-5 HNO3, РН=1-е-2 HNO3, pH=2-= 2,5 HNO3, рН=24-3 HNO3, pH=2 4-3 НС1О4 ИЛИ HNO3, pH =1,5-4-4-2,0 HNO3, рН=14-2 рН=24-2,5 НС1О4 или HNO3,,pH =1,54-2 рН=0,74-1,2 Ацетатн. буф. (pH=4,5), 50% сп. рН=104-И, добавл. аскорбиновую к-ту, охл., добавл. изб. Na-ЭДТА и NH3 рН = 10; см. опр. Mg2+ К кислому р-ру добавл. ТЭТА, NaOH до pH =12,5, добавл. KSCN и затем СНзСООН до рН=11 Fe3+ и CN- Fe3+ (предвар. восст. до Fe2+) Fe2+, Hg2+ Fe3+, Hg2+ Fe3+, Hg2+ Fe3+, Hg2+ Nbv, Tav Sb3+ Hg2+ (или Fe3+) Sb3+, Sn4+, Zr4+ Hg2+ Cr3+ As3+, Bi3+, Cd2+, Co2+, Hg2+, Ni2+, Pb2+, Sb3+, Sn4+, Zn2+, Fe3+ Mn2+ (предвар. окисляют в [Mn (CN)6]3—) Аскорбиновая к-та Аскорбиновая к-та Аскорбиновая к-та, тиосемикарбазид Аскорбиновая к-та То же » » F- F- НСООН или N2H4 Тартрат-ион CN- Аскорбиновая к-та ДМП С№
КОМПЛЕКСОМЕТРИЧЕСКОЕ ТИТРОВАНИЙ ЛЕ0РГАНИЧЕСКИХ ИОНОВ РАСТВОРОМ Ne-ЭДТА
Продолжение
CD О Определяемый ион Тип титрования Индикатор Условия титрования Маскируемые ионы Маскирующий агент
Ca*++Mg2+ Са2+ Cd2+ Со2+ CfS+4-Ni2+ Сг3+ Cs+ Cu2+ п О (Са2+) П О (Си2+) П О (Са2+) П В (РЬ2+) О (Си2+) П О (Си2+) П О (Са2+) О (Си2+) О(Th4+) п хч ТФ или Си-ПАН М ПАН ПАН или Си-ПАН МТС ПАН или Си-ПАН КО ПАН SCN- ПАН ПФ ТФ м ко X ПФ ПАН м рН=10,0 К кислому р-ру добавл. ТЭТА, затем NH3, нагр., охл., вводят изб. Na-ЭДТА и разб.; рН=10-=- 11 Добавл. к кислому р-ру ТЭТА, нейтр. до рН=12 и добавл. KCN Аммиачн. буф. (рН = 10,0) Ас-, нагр.; рН=5-4-6 Аммиак, рН=Г2 pH=5 ч-6;- см. опр. Cd2+ рН=5,5; см. опр. РЬ2+ pH=4 ч-5; см. опр. Си2* Добавл. Na4P2O?, доводят NH3 до pH = 8,0, добавл. NH4SCN, 50% ацетона pH = 4; аскорбиновая к-та, мет. сп.; 70° С Аммиачн. буф. (pH=9,3) Добавл. ТЭТА к кислому р-ру (рН=1,0), подщелачивают Аммиачн. буф. (рН=10); гор. р-р HCOONH4 (pH=4 4-4,5) См. опр. К+ CH3COONa или NH3; рН = = 64-6,5 pH = 6,0 рН=54-7 Fe3+ Al3+, Cr3+, Fe3+ Al3+. Mg2+, Мп2+, Pb2+, Sn2+, Sn4+ Sn2+, Th4+, Zr4+ Sn2+, Th4+, Zr4+ Cu2+, Hg2+, Tl3+ WVi Fe3+, Cr3+ Nbv, Tav> Ti4+, WVI, Fe3+ Fe3+ Al3+, Fe3+ Al3+. Ti4+ Fe3+ Fp3+ Диэтилдитиокарбамат натрия ТЭТА CN". ОН", ТЭТА Цитрат-ион Цитрат-ион Цистин F" р2о<- F-, тартрат-иои ТЭТА F- F-F-F-
О (Си2+) ПАН pH = 3,5 —3,8; добавл. мет. Fe3+ F-
Fe2+ Fe3+ Оа3+ Hg2+ п » » » О (РЬ2+, Т13+) П О (РЬ2+) п О (Си2+) п п О (BF+) П » » » » » tu-ПАН ПАН или Си-ПАН ХЧ ко Си-ПАН КО ПФ » КО ко ПК ПФ Си-ПАН КО сп.; 80° С pH = 6 4-6,4 рН=34-4, гор. р-р рН=7; 70° С рН=54-6 рН = 54-6 Аммиачн. буф. (рН=10); 80°С Уротропин или CH3COONH4 (pH = 4 4-4,5; 5 4-6) рН = 34-6, гор. р-р рН=5,5; см. опр. РЬ2+ Пиридин и Ас-, pH = 6 Пиридин и Ас-, рН = 6 Добавл. NH4F, продувают N2, добавл. FeSO4, pH=34-5 рН= 14-1,5; удаляют воздух продуванием N2, добавл. FeSO4 pH=24-3; см. опр. Bi3+ рН = 3,8; ацетатн. буф. рН=1,б4-2 Уротропин (рН=5-=6) Nbv, Tav, Ti4+ WVI Hg2+ Sb3+, uo2+ Sn2+, Th4+, Zr4+, WVI WV! Cu2+, Tl3+, Hg2+ Al3+, Ti4+ Al3+, Tl4+ Al3+, Zr4+ Th4+ Fe3+, Hg2+ Al3+ Al3+ F- H2O2 Тартрат-ион Цитрат-ион, тартрат-ион F- или PO3- Цистин F- F- F- so2~ Аскорбиновая к-та bf4-F-
In3* Со <о О (Ni3+, Си2+) О (В13+) П » О (Zn2+) м ПК хч ПФ ПАН ХЧ или ПФ Аммиачн. буф. (рН=9) рН=24-3; см. опр. Bi3+ Аммиачн. буф. (рН = 84-10) рН = 10, тартраты, этилендиамин; 100° С рН=74-8; CH3COONH4, тартраты Аммиачн. буф. (pH =10) Fe3+, Hg2+ Ag+, Cd2+, Co2+, Cu2+, Fe2+ (в присутствии Fe3+ добавл. аскорбиновую к-ту) Hg2+, Pd2+ Pt-металлы, Zn2+ Al3+ Аскорбиновая к-та, CN- F- или ТЭТА
Л НЕОРГАНИЧЕСКИХ ИОНОВ РАСТВОРОМ Na-ЭДТА
Продолжение
Определяемый ион
Тип титрования
Индикатор
Условия титрования
Маскируемые ионы
Маскирующий агент
1п3+ п » ко » pH = 3,0; 50—60° С pH = 3,0; 50—60° С Т13+ (восст. в Т1+) Cd2+, Со2+, Си2+, Mn2+, Ni2+, UO2+, HCOOH о-Фенантролин
К+ н Осажд. КВ(СбН5)4, изб. реа- Zn2+
La3+ и п Си-ПАН гейта связывают р-ром Н£2*-комплексоната и от-титровывают освобожденную Na-ЭДТА рН = б4-6 Sb3+, UO2' Тартрат-ион
лантаниды » ХЧ рН=10; см. опр. Мп2+ (до- Al3+, Fe3+, Sn4+, Ti4+ ТЭТА
Mg2+ » КО ХЧ бавл. NH2OH) Пиридин, Ас', pH = 5 4-6 Добавл. ДМП к кислому As3+, Bi3+, Cd2 1, Co2+, ДМП
Мп2+ П или О (Mg2+) п » О (Са2+) ХЧ ХЧ » ПФ ТФ р-ру, подщелачивают до рН=10,0 (аммиачн. буф.), подогревают pH =10,0 рН=10; добавл. Н2О2 к кислому р-ру, подщелачивают pH =10,0 Аммиачн. буф. (pH = 10,0) рН=10— 11; см. опр. Са2+ Hg2+, Ni2+, Pb2+, Sb3+, Sn4+, Zn2+ Fe3 + Ag+, Co2+, Cd2+,Cu2’, Fe2+, Hg2+, Ni2+, Pd2+, Pt-металлы, Zn2+ Ti4+ Cd2+, Cu2+, Hg2+, Zn2+ Cr3+ ДМП, ТЭТА CN- Н2О2 ТЭА Аскорбиновая к-та
п » ХЧ » pH = 10; см. опр. Mg2+ рН=10; добавл. аскорбиновую к-ту или NH2OH и нагр. до 65° С As3+, Bi3+, Cd2+, Co21-, Hg2+, Ni2+. Pb2+, Sb3+, Sn4+, Zn2 + ,Fe31 Ag+,Co2+, Cd2+, Cu2+, Fe2+, Hg2+, Ni2+, Pd2+, ' Pt-'металлы, . Zn2+ ДМП CN-
О(Са? ) ТФ 1 рН= 10; 54-12; см. опр. Са24; Ag , Cd-’ , Cu2' , Pb2 , Zn2+ Меркаптоуксусная к-та
II добавл. аскорбиновую к-ту
ХЧ рН=10; аскорбиновая к-та Al3+ Сульфосалициловая
» ТФ рН=104-11; к кислому р-ру Al3+, Fe3 + к-та ТЭТА
ХЧ добавл. ТЭТА, затем NH2OH, подщелачивают
» рН=104-11; к кислому р-ру Al3+, Fe3+, Sn4+, Ti4+ ТЭТА
О (Мп2+) добавл. ТЭТА, затем NHsOH, подщелачивают
» pH =10; аскорбиновая к-та Al3+, Ti4+ Bi3+, Cd2+, Pb2+, Sn2+, Тирон
п » рН=10; добавл. NH2OH. и Унитиол
ТЭТА * Zn2+
п pH =10; 50—60° С Al3+, Cu2+, Fe3+ и эле- Аскорбиновая к-та
менты комплексую- CN", F~, J", S,O2~
щиеся с CN
О (Си2+) ПАН Ацетатн. буф. (рН=4,5);
60° С
MoVI О (Си2+) » рН=4ч-5; см. опр. Си2+ wvi F~, тартрат-ион
п Си-ПАН рН=4,5-д-5; восст. MoVI Al3+, Се3+, Nbv, Tav, Р.З. (Ill), Th4+, Ti4+, Тартрат-ион
. р-ром N2H4, мет. сп.
О (Znz+) u4+ WVI
КО рН=5-г-5,5; CH3COONH4;
0°С
Na+ Н Осажд. NaZn(UO2)3{Ac)9-
• 6Н2О, разрушают и опр.
Na-ЭДТА Zn(Co, Mg, Ni)
Nb » рН=5—6; HCI—H2SO4 —
раствор Nb, (СНз)гСО,
H2O2, H2O, ZnCI2. Нейтр. NH3 до pH = 6 4-6,5 и осажд. Nb и Zn, фильтр., ос. раств. в НС1 (1:3),
добавл. Na-ЭДТА,
CH3COONH4 и NH3 (до pH = 5 4-6) и оттитровыва-
СО ют изб. Na-ЭДТА р-ром Си2+ с индикатором ПАН
&
КОМПЛЕКСОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ * НЕОРГАНИЧЕСКИХ ИОНОВ РАСТВОРОМ Na-ЭДТА
Продолжение
Определяемый иои Тип титрования Индикатор Условия титрования Маскируемые ионы Маскирующий агент
Nbv Ni2+ Pb2+ О (РЬ2+) п О (Zn2+) О (Са2+) П О (РЬ2+) О (Мп2+) П » » О (ВР+) п О (ВР+) п ко ХЧ МТС ВС ТФ ПАН или Си-ПАН КО ХЧ ПАН М ПАН или М ПФ М ПФ или КО ХЧ рН=5,5; уротропин, гор. р-р рН=5 4-6; добавл. Н2О2 и уротропин рН=54-6 pH =10; к кислому р-ру добавл. ТЭА, а затем подщелачивают до рН=10, вводят буф. рН=12, аммиак, тартраты Ацетатн. буф. (рН=5) рН=104-И; см. опр. Са2+ pH=5 4-6; см. опр. Cd2+ рН=5,5; см. опр. РЬ2+ рН=10, аскорбиновая к-та рН=34-4, гор. р-р рН= 104-11,5 (8,5-=-9,5); к кислому р-ру добавл. NH2OH рН=4 при 70° С или рН= =8,54-9; добавл. Na2S2Os к нейтр. р-ру и добавл. CH3COONH4 и CH3COONa Добавл. изб. Na-ЭДТА и до- водят pH до 2 pH=8,5 4-9,5; аммиак HNO3 при 0° С или ацетатн. буф. (рН=44-5) Добавл. ДМП к кислому р-ру, подщелачивают до рН=10,0 (аммиачн. буф.), подогревают, добавл. тартраты Cu2+, Tl3+, Hgz+ Fe3+, UO2' Cd2+, Zn2+ AP+, Fe3+, Sn4+, Tl4+ Hg2+, Ni2+, Zn2+ Cr3+ Sn2+, Th4+, Zr4+ Cuz+, Hg2+, Tl3+ AP+, Ca2+, Mg2+ wvi Fe3+ (восст. до Fe2+) Cu2+ Cd2+, Co2+, Cr3+, Hg2+, Mn2+, Pb2+, Tl3+, Zn2+ Ag+, Cd2+, Cu2+, Co2 ।, Niz+, Fez+, Hg2+, Pd2+, Pt-металлы, Zn2+ Цистин 2,4-Пентендиол и нитробензол о-Феиантролин ТЭТА ТЭА Аскорбиновая к-та Цитрат-ион Цистин F- Н2О2 э NH2OH 2 ь га S О2- 5 1,2 3 S з 0 X ГВ С5 X о ГВ CN- О 0 -- Я CN“ s
Со <О Сл
Pd2+ О (BF+) О (Th4+, Ti3+) О(Th4+) ПК или ВПК ко рН = 24-3; см. опр. Bi3+ Ацетатн. буф. (рН=3) Fe3+, Hg2 + Аскорбиновая к-та
Pu2+ AC рН = 2,54-3; НС1
Sb3+ О (Ti3+) КО рН = 4; CH3COONH4
Sc3+ П ХЧ Малеиново-аммиачн. буф. (рН=8); 70° С Cd2+, Со2+, Cu2 Ni2+, Zn2+, Fe2+, Pb2+ \Hg2+, Bi3+, ДМП, CN"
м pH=2,6; НС1 и CH3COONa
» ко Ацетатн. буф. (рН=2,2-=-5)
Sn21 О(Zn2+) ц Аммиачн. буф. (рН=94-10) Sn4+
П МТС рН = 5,54-6; пиридин и Ас- F"
Sn4+ O(Th4+) ко pH = 2,0 Cu2+ Тиокарбоксидазид
О(Th4+) » рН=2,0 Cuz+ Тиомочевина
Sn2+ 0 (Pb2+) рН=6,0; уротропин Cu2+ »
П МТС рН = 5,5>4-5,6; пиридин и Ас" Sb3+, Sn4+ F", окислитель Аскорбиновая к-та
Th4+ ПФ рН=2,5-4-3,5; 0,04 М HCI, Fe3+ (восст. до Fe2+)
33%-ный сп., HNO3; 40° С
ко pH=2,5—3 или 1,74-3,5; Fe3+ Аскорбиновая к-та или
HNO3 или ацетатн. буф. Bi3+, Pb2+ NH2OH
» рН = 2,5-4-3; HNO3 или ацетатн. буф. ДМП
ПФ р! 1 = 2-4- 2,5 Hg21’ (восст. до Hg) НСООН или НСНО
Ti4+ » А рН=Цб4-3; HNO3 или НС1
О (Zn2+) ХЧ рН=7, пиридин Fe3+ F-
О (Bi3+) ко Добавл. Н2О2 и изб. Na-
ЭДТА,. нейтр. NH3, подкисляют СНзСООН и титр.
изб. Na-ЭДТА р-ром Bi3+ при 20°*С
Tl3+ П ко Ацетатн. буф. (рН=44-5)
О (Pb2+, Bi3+) ПФ рН=2-е-3, ацетатн. буф. или
HNO3
U4+ 0(Th4+) ко рН=24-3,. «СНзСООН
UO|+ П ПАН рН=4,4, уротропин, 67%-ный пропил, ст; 80—90° С рН=34-6,ггсф. р-р ....
Vv » Си-ПАН WV! F~ или (РО3“),
- тартрат-ион
НЕОРГАНИЧЕСКИХ ИОНОВ РАСТВОРОМ Na-ЭДТА
Продолжение
Определяемый ион Тип титрования Индикатор Условия титрования Маскируемые ионы Маскирующий агент X
VO2+ п X pH = 4,0; Ас* О л ы гв X
VO+ » ко pH =1,8; 0,03 М НС1О4 Г) О
Zn2+ м рН = 8-4-9; к аммиачн. р-ру Си2+ Аскорбиновая к-та S W
добавл. аскорбиновую к-ту -i о
до обесцвечивания р-ра и S л
титр. п
рН=8-=-8,5 ио2+ со|- X о
ХЧ pH=8,5 4-9,5; 30° С АР+ Цитрат-ион *0 СИ
» ПАН или pH=5 4-6; см. опр. Cd2+ Sn2+, Th4+, Zr4+ » HS В5Н
Си-ПАН 05
О (РЬ2+) КО pH = 5,5; см. опр. РЬ2+ Cu2+, Tl3+, Hg2+ Цистин О В5
п ХЧ pH =10; 60° С Cd2+ Диэтилдитиокарбамат я ZS
натрия * ГВ
» ПАН рН = б4-6,4 Nbv, Tav, Ti4+ F-
» Си-ПАН рН=34-6; см. опр. Fe2+ WVI F- >о *0
ПАН рН = 54-6 Cu2+ S О2“ “1
» ХЧ pH =10,0 AF+ ТЭТА я я
» ПФ Аммиачн. буф. (рН= 1.0,0) ГВ
'» КО Ацетата, буф. (рН=54-6) О X
O(Bi3+, Th4+) Ацетатн. буф. (pH = 4,5) я X
Zr4+ (и О(В1ЗХ) Тиомоче- pH=2,0, H2SO4 Ti4+, Th’+ so2 4 я
Hf4+) вина о я
О (ВР+) То же pH=2 4-2,2, НС1 Nbv, Tav Тартрат-ион о 05
П КО 1 М HNO3 или 0,05—3 М
H2SO4; 90° С
— -• . ' •г*'*’-'-
КОМПЛЕКСОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ НЕОРГАНИЧЕСКИХ ИОНОВ РАЗЛИЧНЫМИ КОМПЛЕКСОНАМИ Принятые обозначения см. стр. 16 и 38ft-
Определяемый ион Комплексон Тип титрования Индикатор Условия титрования Переход индикатора в конечной точке q S я
AF+ Ва (Sr)2+ В13+ Са2+ Cd2+ Со2+ Си2* дцтк » » НТА ДАК ЭАК мтк дцтк » ЭАК НТА ЭТА ДЦТК » ЭАК НТА БАК ДЦТК » » ДАК ОД’С п О (Zn2+) О (РЬ2+) О(Си2+) 3 (Mg-ДАК) П » 3 (Mg-ДЦТК) п » » О (Mg2+) О (Си2+) п » » » » О (Mg2+) п с Си-ПАН ХЧ ПФ КО ВС ХЧ Zn-ХЧ КО МТС ХЧ Zn-Ц ПФ ХЧ Zn-Ц ХЧ ПАН М > » ПАН ПФ ХЧ Си-ПАН м Ас ; pH = 2 4-2,2 Пиридин; рН = 6,5-;-7 Пиридин и Ас-; pH = 5,5 4-6 Уротропин; pH = 54-6 pH=5,5 4-5,8 Аммиачн. буф. (рН=10,0) То же 0,1 М HNO3 NaOH (рН= 11 4-11,5) Аммиачн. буф. (pH = 84-10); 60— 70° С Боратн. буф. (рН=9,54-Ю) Аммиачн. буф. (иН=10,2) Аммиачн. буф. (рН=9-4-9,5) То же Аммиачн. буф. (рН=84-10) Ацетатн. буф. (рН=5,0), N2H4; 80—90° С рН=94-Ю рН=9,2 рН=74-7,5 Аммиачн. буф. (рН=94-10) Ацетатн. буф. (рН=54-5,5); 80— 90° С Пиридин; РН = б4-7 Аммиачн. буф. (оН=84-10) Ас~ или NH3; РН = 54-9,2; 60°С pH = о,0 ь m Красный — желтый п Синий — красный Синий — фиолетовый m Желтый — красно-фиолетовый m Фиолетовый — бесцветный Красный — синий gm То же я£ Красный — желтый ^о Синий — зеленовато-желтый Красный — синий Ss Я,п Синий — желтый go Зеленовато-синий — красно-фиоле товый я® Красный — синий дв Синий — желтый g я Синий — красный og Желтый — красный 3> Желтый — пурпурный ® ® То же г Желтый — фиолетовый " Желтый — пурпурный * Красный — желтый ® X Синий — желто-зеленый о Синий — красный о Красный — желтый w Фиолетовый — желтый
397
Продолжений
Определяемый ион Комплексон Тип титрования Индикатор Условия титрования Переход индикатора в конечной точке
Си2+ НТА п X Уротропин (pH = 5,56) Синий — зеленый
» » м Уротропин (рН = 54-6) Желтый — фиолетовый
» » » Аммиачн. буф. (рН = 8<-9) Фиолетовый — синий
» ВС Уротропин То же
ЭТА п (pH =54-5,5) М Аммиачн. буф. (pH =9,3 4-9,5) Желтый — розовый
Fe2+ дцтк » МТС Уротропин (рН = б4-6,5), аскорби- Синий — желтый
Fe3+ » » » новая к-та Уротропин (рН = 4,5-е-6,0) То же
» » ПФ Пиридин и Ас', рН = 5,54-6 Зеленовато-синий — красный
» с т pH = 2 4-4; 50—60е С Бесцветный — красный
» о (Mg2+, ХЧ Аммиачн. буф. (рН=6,54-7) Синий — красный
» Zn2+) О (Cu2+) ПАН Ацетатн. буф. (рН=54-5,5); 80— Желтый — красный
» О (Zn2+) ПФ 90° С Пиридин и Ас”, рН = 5,54-6. Желто-зеленый — синий
» О (Pb2+) КО Уротропин (рН = 54-5,5) Желтый — красно-фиолетовый
НТА П X С1СН2СООН, рН = 2,0; 50—60° С Синий — оранжевый
Hg2+ ЭТА » Zn-Ц Триэтаноламин, pH = 7,54-8 Синий — желтый
La3+ ДАК п Си-ПАН Ацетатн. буф. (pH=3-i-5); 60° С Красный — желтый
(лантаниды) и Y3 + » О (Си2+) ПАН Ас” или NHs, рН = 44-Ю Желтый — красно-коричневый
Mg2’ дцтк » ХЧ Аммиачн. буф. (рН=10,0) Красный — синий
» » МТС NHs, рН=11,0 Синий — серый
дцтк 3 (Zn-ДЦТК) ХЧ Аммиачн. буф. (pH =84-10); 60— Красный — синий
ДАК п » 70° С 1 Аммиачн. буф. (рН=10,0); 40° С I То же
Мп2’ ДЦТК » » Аммиачн. буф. (рН=94-10), три- » »
» » МТС этаноламин, NH2OH Уротропин, pH = 64-6,5 Синий — желтый
ЭАК п ХЧ Аммиачн. буф. (рН= 10,0) Красный — синий
Ni2’ БАК » м NHs, pH = 7 4-7,5 Желтый — сине-фиолетовый
ДЦТК О (Mg2+) ХЧ Аммиачн. буф. (рН=8-=-10) Синий — красный
БАК О (Си2+) м Аммиачн. буф. (pH = 7-=-8) Фи< летовый — желтый
ДЦТК О (Си2+) ПАН Ацетатн. буф. (pH = 54-5,5); 80— Желтый — красный
ЭАК п м 90° С Аммиачн. буф. (pH = 10,0) Фиолетовый — красный
- НТА » » Аммиачн. буф. (рН=8,24-10,0) » — красно-фиолетовь
РЬ2- ДЦТК » ХЧ Аммиачн. буф. (рН=10,0) » — зеленовато-синий
МТК » То же То же
НТА » » Аммиачн. буф. (рН=10,2) Красно-фиолетовый — синий
РЬ2’ » 3 (Zn-HTA) ХЧ Аммиачн. буф. (рН=10,2) Красный — синий
» О (Cd2+) » То же Синий — красный
Sc3’ НТА П м рН=7 Желтый — красный
Th4’ БАК » ПФ HNO3, pH = 2 4-3; 60—70° С Красный — желтый
Ti4’ ДЦТК О (Zn2+) ХЧ Пиридин, рН = 6,54-7 Синий — красный
» О (Си2+) ПАН pH = 5 4-5,5, Н2О2; 70—90° С Желтый — красно-фиолетовый
» О (Zn2+) ПФ Пиридин и Ас” (рН=5,54-6), Н2О2 Синий — фиолетовый
Zn2’ МТК П ХЧ Аммиачн. буф. (рН= 10,0) Красный — синий
НТА » м Аммиачн. буф. (рН = 9,1) Желтый — красно-фиолетовый
ТЭА » ХЧ Триэтаноламин, рН = 7,8 Синий — красный
» » ц NH3—NH4NO3 буф. (pH = 9,5) » — оранжево-желтый
ЭТА » » Триэтаноламин, рН = 7,8; аммиачн. » — желтый
Zn’ + дцтк О (Си2+) ПАН буф. (рН = 9,5) Ацетатн. буф. (рН = 54-5,5); з0— Желтый — красный
90° С
КОМПЛЕКСОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ НЕОРГАНИЧЕСКИ^ Я ИОНОВ РАЗЛИЧНЫМИ КОМПЛЕКСОНАМИ
399
Комплексометрические индикаторы
Индикаторы расположены в таблице в алфавитном порядке. В графе «Определяемые элементы» указаны только важнейшие элементы, содержание которых в растворах можно устанавливать титрованием в присутствии соответствующего
индикатора при данном значении pH.
Подробнее см : Р. П рш и б и л, Комплексоны в химическом анализе, перев. с чешек., 2-е нзд.. ИЛ, I960.
Индикатор Формула 1 pH среды Определяемые элементы
Ализариновый красный S (ализариирот; 3-ализариисульфокисло-та, Na-соль) О ОН II 1 он 1 II II J '^/X|j/\^\sO3Na- Н2О О 1.5—4,3 2 2,2—3,4 3,5—3,6 Th4 + Sc3+ P. 3. Al3 + P. 3.
Ализариикомплексон {[(3, 4-диокси-2-аитра-хииоиил) метил]-ими-нодиуксусная кислота} О СН2СООН)2 1 II II 1 VY । он 4 4,3 11,5 > 12 In3+ Co2+, Cu2+, Pb2 + Ba2+, Sr2+ Ca2+, Cd2 +
о он
Алюминон (ауриитри-карбоновая кислота) соон соон °\\А А/он II 1 II z'VZ 1 1—2 4,4 >9 Fe3+ Al3 + Ca2+, Mg2+
if li 'у'^СООН
он
Арссназо I (уранон) zAsO(OH)2 °Н °Н \=/ 1 II 1 HO3S/'^/^<?\o3H 0,1—0,2 A! HCI 1,6—3 1,7 10 Puiv Th4 + UIV Ca2+. Mg2+
Бензидин Al3+, Bi3+, Fe3+, Oa3+, Sn2+, Ti4+
Бриллиантовый конго синий 1 он _ _ 1 NaO3S-^^-N=NZ-N= N~f'X|fZ^l C S №O3s/V/\ANhC6H5 1 5—7,5 Pb2+
SO3Na
Бромпирогаллоловый красный (5', 5" — ди-бромпирогаллолсуль-фофталеии) он OH °\\/у°ууон ВгА/\/ЧАвг J\/s°3H 2—3 4—6 6—7 7—8 9—13 10 Bi3 + Pb2+ P. 3. Ni2+, Co2+ Cd2 + , Co2+, Ni2+ Mg2T, Mn2+
V
Вариамииовый синий Б [N- (л-метоксифеиил) -п-феиилеидиамии] СН3О-^2/-ХН y^-NHs 1,7—3 4—5 5 5,5 Fe3+ Al3+, Co2+, Pb2+, Zriv Cd2+, Zn2 i- Cu2+
Г аллоциани:: COOH 2,8 Ga3+
(CH3i2 X/'^/'4O/Y'^°
OH
Гематоксилин 5—6 Al3+
Глициитимоловый синий HOOC-CH2NH NHCH2—COOH 1 1 Cu2+
сн2 .. „ CH2 нохА /СНзНзС\ In у\-СН HC-^XY H3c/^\^CH3 H3C^^^\CH3 \cz
A/SOsH 1 II
КОМПЛЕКСОМЕТРИЧЕСКИЕ ИНДИКАТОРЫ
П родолжение
£
Ю ------------------
Индикатор
Формула
pH среды
Определяемые элементы
3, З'-Диметилнафтидин s~y H»N-O-O NH2 н3с/ \сн3 5 Zn2-, Cd2-, Cu2-, Ni2—, Pb2-
Дитизон (дифенилтио-карбазои) ,NH—NH—С6Н5 S q/ 4-n=n-c6h5 2,5—5 3 3,5 4,5 4,7—5,4 > 5 6 6—7 12 Bi3+ Th4+ Vv Al3+, Cd2-. Fe3+, In3—, P. 3. Pb2 + Ni2+ Mg2+. Mn2+ Zn2 + Ca2+
Дифеиилкарбазон ,NH — NH-C6H6 o=c< \n=N-C6H5 1 4,5—6,5 Hg2- Ni2+, Cd2+, Pbz+. Vlv
Кислотный хром синий К Кислотный хром. синий РРА или 2Р (хром синий 2Р; эриохромфио-летовый СБ) Кислотный хром темно-сииий 3 1 co j Z и m j О Z X g_^-w x X x . 5 x X S"O 1 \ z ° V-#* z “ 1 1 II О X Z z X z S a I || : V) A W % U 1 II % ° /Ч/\ о Z о u . z 9—10 10 10—11 12 8,35 8,5 9—10 10 10—11 Cd2+, Zn2+ Mn2+, Pb2- Mg2- Ca2 + Cd2+, Mn2+, Ni2+, Pb2+, Zn2 + Ca2+, Mg2 + Cd2-, Zn2- Mn2 + Mg2 + Ж о 2 я ь ГС ж Г) о 3 ГС 0 X X ГС Г) ж
Крезол фталексон Та же, что у ксиленолового оранжевого (см. ниже), только вместо —SO3H группа —СООН 10—11 Ba2+, Ca2 + , Cd2-, Mg2+, Sr2 + X
Ксиленоловый оранже-* вый {3, 3'-бис-[ди(карбоксиметил) -аминоме-тил]-о-крезолсульфо-фталеии} НОСС-СН2, ,СН2-СООН \n~CHj сн2—n< НООС-СН2/ \СН2-СООН но\^ ^^хсн3 АхХ» и 1—1,5 1—2 1—3 1,2—5 1,7—3,5 2—3 2,5—3,5 3—4,5 3—5 4—5 5—6 Fe3+ Zriv BF- Sc3+ Th4+ Fe2+, Vv Tb3 + ln3 + Sb3+ И3- Cd2+,Co2-,Cu2+,Hg2+ P. 3., Zn2 + X ж о Е
Магнезон ИРЕА NaO3S^ /ОН НО^ O-N=N-\Z/ С1/ / \ 4 11,5 12,5 Ni2 + Ca2+, Cd2+ Ba2+, Sr2 +
Метилтимоловый синий Морин (2', 3,4', 5, 7-пен-таоксифлавон) НООС-СН2. ,СН2 - СООН >nch2 ch2n< НООС—СН2/ I сн Н С 1 ХСН2- СООН НО\^\-СН Hb-j^^0 Н3с/^\^СНз НзСА^СН3 \<Z A/S°3H и он о АД/°н \ J l/~xoh «АХ \_/ онх 0—6,5 1—3 2,2 3 3—4 4,5—6,5 5—6 6—6,5 10—11,5 4,5—6,0 T1 + , Ti4+, Vv, Al3+, Ga3+, Zn3+ Bi3-, Zriv Sc3- Th4+ In3— Fe2+ Cd2+. Co2- Hg2+, Mn2-, Pb2+, P. 3, Sn2-, Ni2+, Ba2-, Ca2-, Cu2-, Mg2-, Sr2 + Oa3+, In3-
£
Продолжение
Индикатор
Определяемые элементы
Мурексид (NHj -соль пурпуровой кислоты)
Нафтилазоксии [8-окси-7- (1 -нафтилазо) -5-хи-нолиисульфокислота]
Нафтилазоксии С [8-ок-си-7- (6-сульфо-2-иаф-тилазо) -5-хииолии-сульфокислота]
8-Оксихинолии
Формула pH среды
z°— %
XNH —< NHX
O=< V- N=< >=O
\nh _nhZ
1—N=N—
NH
OH I
SO3H
I II |-n=n-HO3s/'4/z\^
SO3H
ПАН [1-(2-пиридилазо)-2-иафтол]
ПАР [4-(2-пиридилазо)-' резорцин]
Пирогаллоловый красный (пирогаллолсуль-фофталеин)
Пирокатехииовый фиолетовый (пирокате-хинсульфофталеии)
но/
но.
^nV-n=n-0-oh
OH
ii
SO3H
2,6 Sc3 +
4; 7—8 Cu2+
7; 8 Co2+
8 Mn2+
8—9 Zn2+
8,5—9,5 Ni2+
> 12 Ca2+, Ag+, Pb2+
3—3,5 Fe3+, Th4 +
4 Cu2!"
5—6,5 Cd2!-, Nl2+, P. 3., Zn2+
6—6,5 Pb2+
6,5 Co2+
6,7—7,0 Mn2+
4—5 Sc3+
5—9 Cu2+
5,5—6,5 Co2 +
6 Zn2+
6—6,5 Cd2!-, NP+
6—8 P. 3. x
8,5 Mn2+ 0
10 Ca2+, Mg2+ |
ь
га
2,2—2 Fe3+ n
2,5—3,5 Ga34- 0
5—6,5 Cu2+ w
5,5—6,5 Ni2+ т
5,5—9,5 Zn2+ ®
8—10 Mn2+ w
8,5—10 Cd2+ £
9—10 "
1—3
1,8
2—3,5
9—10
1—2
3—6
6—11,5
11,5
2—3
7—9,3
Bi3 +
Tl3h
Al3+, Cu2+, Ga3+, Hg2+, In3+, Sc3-, Th4 +
Cd2i-, Co2+, Fe3+, Ni2+, Pb2+, Vv, Zn2+
Ca2+, Mg2+, Mn2+
Bi3+, Т13+
Al3+, Hg2+, Cu2+, Ni2+, Р. 3.
Cd2+,Mn2+, Pb2+, Zn2+
Ba2+, Sr2 +
В13+
РЬ2+
Ni2+, Со2+
2; 8—9,3 Ni2+
2—3 Bi3+
2,5—3,5 Th4+
3—3,8 Ga3+
5—6,5 Cu2+, Fe34-, In3!-, Pb2+,
A13+, Ti4+
9,3 Co2+, Mn2+
10 Cd2+, Mg2-, Ca2+,Zn2+
Я
о
Е
§
£
Продолжение
Индикатор Формула pH среды Определяемые элементы
Солохром черный ПВ /ОН он 4 Fe2+, Fe3+
<^>-N=N fy\\ 10 Cd2+, Mg2+, Mn2+, Pb2+, Zn2+
NaOgS^ ОН 11,5 Ca2 +
Сульфофенилазохромо- он он 1,5—2,5 Zriv
троповая кислота №03s-0-N=N-f¥4 NaO3S/'^/X^XSO3Na 2,5—3,5 Th4+
ТАН [1-(2-тиазолилазо)- но^ 4—7 Co2+, Cu2+, Ni2+
2-нафтол] rN>-N=N-O ~ S/ /=< 7 Pb2+, Zn2+
ТАО [5- метил-4- (2-ти- НО/ 4 7 Co2+, Cu2+, Ni2+
азолилазо) -резорцин] ^-ОН — s' >=/ н3с' 7 Pb2+, Zn2 +
10 Ca2+, Cd2+, Mg2+
ТАР [4-(2-тиазолил)-ре- НО/ 4—7 Co2+, Cu2+, Ni2+
зорцин] Г nVn=n-6~V-oh — Sz 7 Pb2+, Zn2+
10 Ca2+, Cd2+, Mg2+, Mn2+
Тимолфталексои Та же, что у метилтимолового синего (см. выше), то- 10—11 Ba2+, Mn2+, Sr2 +
лько вместо —SO3H группа —СООН 10,5—12 11—13 Ca2 + Mg2 +
Тиомочевина ,nh2 s=c< xnh2 5—6 Bi3 +
Тирон он AzOH f 1 HOss/^^SOsH 2—3 Fe3+
1 а И X Э 3 h И d
Флуорексои (кальцеин, флуоресцеинкомплек-сои)
НООС-СН2ч ,СН2—СООН
yN М<
HOOC-CH/l | хсн2-соон
сн2 сн2
Н°ХА fY° с^\И\сн3
А/Соон
13 Са2+, Sr2+, Ва2+
Фталеиикомплексон (ме-таллфталеии; фталеии пурпурный; крезол- -фталексон)
10 10—11
Mg2+
Ва2+, Са2+, Sr2+
Хромазурол С (альбе-рои); бриллиаитблау; эриохромазурол S)
сн3 °у\\ N а ООС OON а
ск J, ,ci
СН3
I ,он
2 1—4 4—5 6—6,5 8—10
10
Zriv
Fe3 +
Al3+
| Cu2 +
Mg2+, Ca2+, Sr2+, Ba2+
^\so 3Na
Хромоген ЕТ-00 (эрио-хром черный Т; хром черный специальный ЕТ-00; кислотный хром черный специальный)
6,8; 10
6,5—9,5
7—8
7,5—8 7—9 8—10
9—10
10—10,5
Zn2 +
Ga3 + Al3 + Sc3 + P. 3. ln3+ Bi3+, Hg2+, Mn2+ Cd2+, Mg2+, Pb2+, Ba2+, Sr2+, Ca2+, Tl3+, CeIV, Fe3+, Nj2 + , Tj4+ ylV Co3+, Cr3+
КОМПЛЕКСОМЕТРИЧЕСКИЕ ИНДИКАТОРЫ
Продолжение
Объемный анализ с применением неводных растворителей
Методы титрования в неводных растворах находят широкое применение в аналитической практике. Их используют для анализа разнообразных неорганических и органических веществ и для дифференцированного титрования многокомпонентных смесей солей, кислот и оснований. Одно из важнейших преимуществ методов неводного титроваиия — возможность определять нерастворимые в воде соединения, а также вещества, разлагаемые водой или образующие в водиых растворах стойкие иерасслаивающиеся эмульсии. Титрование иеводных растворов может выполняться визуальным методом с применением индикаторов, потенциометрическим, кондуктометрическим, амперометрическим и другими физикохимическими методами.
Единая схема диссоциации электролитов (см., например, монографию Н. А. И з м а й-л о в а. Электрохимия растворов, Изд. ХГУ, Харьков, 1959) позволяет рассматривать химические реакции, происходящие в различных растворителях, с общей точки зрения. Ниже приводится сопоставление некоторых реакций, протекающих в водиых растворах, с аналогичными реакциями в неводных средах.
В водных растворах:
2Н2О Н3О + 4ОН"
2Na-~2H3O+ —> 2Na’1"+1Н24-2Н2О
Н3О+СГ + КОН —> КС1+2Н2О
Zn (NO3)2 + 2КОН —> 4-Zn(OH)2 + 2KNO3
BaC!2+2AgNO3 —> 4,2AgCl4 Ba (NO3)2
В среде жидкого аммиака:
2NH3 7* NH+ + NH"
2Na4 2NH4+ —> 2Na+ + ф H2 + 2NH3
NH4+C1“ + KNH2 KC1+ 2NH3
Zn(NO3)2 + 2KNH2 —> 4.Zn(NH2)24 2KNO3
Ba(NO3)2+ 2AgCI —> 4.BaCl2 + 2AgNO3
В среде этилового спирта:
2С н он 7* С Н ОН+ф-С Н О~ Л О — ЛОЛ Ли
2Na + 2С2Н5ОН2+ —> 2Na+ + фН2 + 2С2Н..ОН
с2н5он+сг + с2н5ок —> 2С2Н5ОН+КС1
Zn(NO3)2 Ь2С2Н5ОК —> Zn(C2H5O)2-;-2KNO3
В среде безводной уксусной кислоты:
2СН3СООН 7» CH3COOH2h4-CH3COO-
2Na +-2СН3СООН+ —> 2Na+ + фН2 + 2СН3СООН
СН3СООН2+С1~ + СН3СООК —> 2СН3СООН + KCI
Zn(NO3)j |-2СН3СООК —> Zn(CH3COO)2 + 2KNO3
Аналогия между реакциями нейтрализации, протекающими в водиых и иеводиых растворах, может быть показана на следующих примерах.
В водных растворах: .
Н3ОС1 -1 кислота г NaOH —5 основание ► NaCl соль 4- 2Н2О растворитель
в среде жидкого аммиака: NH4C1 4 кислота NaNH2 —3 основание ► NaCl соль + 2NH3 растворитель
в среде этилового спирта:
НС! 4 кислота С2Н5ОК — основание > КС1 соль 4- С2Н5ОН растворитель
409.
Объемный анализ с применением неводных растворителей
В среде безводной уксусной кислоты:
HCIO4 4-CH3COONa —> NaClO4 + СН3СООН кислота основание соль растворитель Приводим некоторые примеры реакций, протекающих в неводных растворах при кислотно-основном титровании.
Титрование амина RNH2 в среде уксусной кислоты раствором хлорной кислоты: RNH2 + CH3COOH rnh+ + ch3coo~
НСЮ4 + СН3СООН СН3СООн+-|-С1О~
СН3СООН+ + СН3СОО~ 2СНдСООН
RNH* + CIO" —> RNH2-HC1O4
RNH2-|-HC1O4 —> RNHj.HCIO,
Титрование амина RNH2 в среде этилового спирта дноксаиовым раствором хлорной кислоты:
2C2hsoh с2н5он+ + с2н5о-
RNH +с Н ОН* RNH++C Н ОН X X D Л О л, и
ZCH2CH2. zCH2CHj, А
НС1О4 + О< )OZ*O( >О+-Н+С1О~
'<СН2СН2/ X-CH2CH2Z 4
zCH2CH2x ,СН2СН2ч
С!Н.О- + О<СН1С„1>*-Н С.„.ОН+О<СН1СН1>
RNH* 4-С1О" —> RNH2- НС1О4
RNH2-|-HC1O4 —> RNH2-HC1O4
Титрование амина RNH2 в среде метнлэтнлкетона раствором хлориой кислоты:
ОН
СН3СОСН2СН3 СН2==С-СН2СНз
он о-
RNH„4-CH,=(J-CH9CH, RNH* + СН,=(1-СН,СН, XX Хм о X X о
он
НС1О4 + СН3СОСН2СН3 CH3^CHSCH3 + Cio7
о~ он
сн2=с—сн2сн3 + сн3<!!сн2сн3 2СН3СОСН2СН3
RNH+ + C1O- —>RNH2-HC1O4
i r
RNH2 + HC1O4 —> RNH2-HCIO4
Титрование кислоты НАп в среде пиридина бензольно-метаноловь;м раствором гидроокиси тетраэтиламмоння:
HAn4-C5H5N СбН5КН-ЬАп“
(С2Н5)4 NOH (C2H5)4N + + OH_
c5h5nh+oh~ C5H5N + H2o
(С2Н5)4N 4-An 4C2H5)4NAn
(C2H6)4NOH + HAn —> (C2HS)4NAn + H2O
410
Объемный анализ с применением неводных растворителей
Титрование кислоты НАп в среде этилового спирта бензольно-метаиоловым раствором гидроокиси тетраэтил аммония:
НАп + С2Н6ОН С2Н5ОН2 + Ап“
(С2НВ)4 NOH (С2Нб)4 N + + ОН-
С2Н5ОН2 + ОН- С2Н6ОН4-Н2О
(С2Н5)4 N + + An- —> (C2H5)4NAn
(С2Н6)4 NOH + НАп —> (С2Н5)4 NAn-r Н2О
Титрование кислоты НАп в среде метилэтилкетоиа бензольно-метаноловым раствором гидроокиси тетраэтиламмоиня:
ОН
НАп+СН3СОСН2СН3 СН3^СН2СН3 + Ап~
(C2Hb)4NOH 5±(C2H5)4N + + OH-
он
сн3Лсн2сн3+он- СН3СОСН2СН3+Н2О
(С2Н5)4 N + + Ап- —> (C2H5)4NAn
(C2H5)4NOH+HAn —> (C2HB)4NAn + H2O
Типичные кривые потенциометрического титрования в неводных растворах представлены на рис. 1—6. Во всех случаях индикаторным электродом служил стеклянный, а электродом сравнения — каломельный электрод. Титрование проводилось при концентрации титруемых растворов 0,01—0.02 н.
Чмл НСЮ4
Рис. 1. Типичные кривые потенциометрического титрования органических оснований в среде метилэтилкетоиа 0,1 н. раствором хлорной кислоты в метилэтилкетоне:
/ —лс-толуидин; 2— о-толундин; 3 — л-толуиднн; 4—анилин; 5 —днфеннлгуанидин; б —тнрамин; 7—акридин (1, 2, 3, 4—очень слабые основания; 5, 6, 7 —основания, не растворимые в воде).
Кривые титрования, приведенные на рнс. 2, показывают, что каждый компонент смесн оттнтровывается отдельно. Так, на кривой /, полученной прн титровании смесн едкого калн и о-феиантролина, первый скачок соответствует нейтрализации едкого кали, второй — о-фенантролина. Прн титроваинн двухкомпонентной смеси, содержащей гидроокись аммоиня и jw-толун лен диамин, получена кривая 2, на которой первый скачок соответствует нейтрализации гидроокиси аммония, а второй и третий скачки — раздельной нейтрализации двух аминогрупп молекулы диамина. Кривая 3 получена прн титровании трехкомпонентной смеси, состоящей нз пиперидина, п-фениленднамина и N, N-диметилаиилина; первый скачок соответствует нейтрализации пиперидина, второй — п-фенилеиднамнна, третий — N, N-днметнланилина,
411
Объемный анализ с применением неводных растворителей
масштаб
412
Объемный анализ с применением иеводных растворителей
Рис. 4. Типичные кривые потенциометрического титрования двух-, четырех-и шестикомпонентиых смесей сильных, слабых и очень слабых кислот в среде метилэтилкетона 0,1 и. бензольно-метаноловым раствором гидро-• окиси тетраэтиламмония:
1 — о-оксибензойная кнслота4 -w-оксибензойная кислота; 2—бензойная кислота4-фенол; 3— серная кислота 4 янтарная кислота; 4— пикриновая кислота42,4-динитрофенол 4 4- 0-нитрофенол 4 фенол; 5 —хлорная кислота 4 пикриновая кислота 4трнхлоруксусная кислота 4 салициловая кислота 4 валериановая кислота 4а-нафтол.
413
ВАЖНЕЙШИЕ НЕВОДНЫЕ РАСТВОРИТЕЛИ, ПРИМЕНЯЕМЫЕ В АНАЛИТИЧЕСКОЙ ХИМИИ
Растворители, в зависимости от своей химической природы. могут быть разделены на следующие группы.
Протогенные, или кислотные, растворители — вещества кислотного характера, молекулы которых отличаются выраженной склонностью отдавать свои протоны. Молекулы протогенного растворителя могут присоединять чужие протоны лишь от сильных кислот. Например, уксусная кислота присоединяет протоны от H2SCh, HCI, HCIO4.
Протофильные, или основные, растворители — вещества основного характера, молекулы которых обладают ясно выраженным сродством к протону. Только очень сильиые основания способны оторвать протоны от молекулы протофильного растворителя.
Амфипротные, или амфотерные, растворители — вещества амфотерного характера, проявляющие себя как основания по
отношению к кислотам и как кислоты по отношению к основаниям. Молекулы амфипротных растворителей отличаются способностью отдавать свои и присоединять чужие протоны. Так, вода отдает свои протоны NH3. N2H4. CH3NH2 и присоединяет протоны от HCI. H2SO4, СНзСООН.
Апротонные, или апротные, растворители — вещества нейтрального характера, молекулы которых не способны ни отдавать, ии присоединять протоны. Молекулы апротонных растворителей не ионизированы, кислоты и основания, растворенные в них, не диссоциируют на ионы.
Деление растворителей на протогенные, протофильные, амфипротные и апротонные является в известной степени условным.
Тип и название растворителя Формула Молекулярный вес Плотность при 15—20° с. г!см3 Т. плавл., °C Т. кип. прн 760 мм pm. cm., °C Показатель преломления и 20 nD
Протогенные растворители Муравьиная кислота нсоон 46,03 1,220 8,4 100,7 1,37137
Уксусная кислота СНзСООН 60,05 1,049 16,6 118,1 1,3715 (22,9°)
Пропионовая кислота . С2Н5СООН 74,08 0,9985 —20,83 141,1 1,38736
Масляная кислота . . . с3н7соон 88,10 0,9587 —5,3 163,5 1,39906
Хлоруксусная кислота . СН2С1СООН 94,49 1,370 (65°) 63 (а) 189 1,4297 (65°)
Трихлоруксусная кисло- та СС13СООН 163,38 1,6237 (70°) 55—56 (₽) 50 (у) 57,5 197,5
Трифторуксусная кисло- та CF3COOH 114,03 1,4890 —15,25 72,4 1,2850
Уксусный ангидрид . . (СН3СО)2О 102,09 1,0871 —73,1 140,0 1,39006
Серная кислота .... H2SO4 98,08 1,834 10,37 338 (ча- 1,4290
стично разлагается)
I ВАЖНЕЙШИЕ НЕВОДНЫЕ РАСТВОРИТЕЛИ, ПРИМЕНЯЕМЫЕ
В АНАЛИТИЧЕСКОЙ ХИМИИ
Продолжение
Тип и название растворителя Формула Молекулярный вес Плотность при 15—20 °C, г!см* т. плавл., °C Т. кип. при 760 мм рт. ст,, бС Показатель преломления „20 nD
Фтористый водсрод . . HF 20,01 0,9885 (13°) —87,2 19,5
Нитрометан .... CH3NO2 61,04 1,130 —28,5 101 1,38189
Нитробензол C6HsNO2 123,12 1,2082 5,7 210,9 1,5524
Протофильные
растворители
Аммиак ... NH3 17,03 0,817 (т. кип.) —77,8 —33,4 1,325
Г идразин N2H4 32,05 1,012 1,45 113,5 1,470(22°)
Этиламин c2h6nh2 45,09 0,7059 (О') —80,6 16,6
Бутиламии c4h9nh2 73,14 0,7401 —50,5 76,2 (752 мм 1,401
рт. ст.)
Диэтиламин ... (C2H5)2 NH 73,14 0,7056 —50 55,5 1,38730(18°) и
Триэтиламин (C2H5)3 N 101,20 0,7325 — П4,8 89,5 1,40032 >
Этилендиамин NH2CH2CH2NH2 60,10 0,8977 11,0 117,0 1,45677 *
Пиридин . . c5h6n 79,11 0,9878 —41,8 115,3 1,509 S
Пиперидин ..... CH2(CH2)4NH 1 1 85,16 0,8622 —13 106,3 1,4530 | м
2-Аминоэтанол .... NH2CH2CH2OH 61,09 1,0117(25°) 10,5 172,2 1,4539 х
1,4-Диоксан ZCH2—CH24 O< >0 88,10 1,0337 11,7 101,3 1,42241 S О
\сн2—CH2/ X
Формамид hconh2 45,04 1,1334 2,55 210,7 1,4472 S
Диметилформамид HCON(CH3)2 73,09 0,9445 (25°) —61 153,0 1,4269(25°) -о
Диэтилформамид . . HCON (C2H5)2 101,15 0,908 177,8 Q
Амфипротные О
растворители X
Ацетои CH3COCH3 58,08 0,7908 —95,35 56,24 1,3591 5
Метилат пикетов\ . . . ’’2^'
Метилпрлпилкетои . . CH3COC3H7 86,14 0,8089 —77,8 101,7 1,38946 з
Метилбутилкстон . . . CH3CO (CH,), CH, 100,16 0 8158 59 5 127 ? 1 40273 (15°) -
Метилизобутилкетон . - CH3COCH2CH (CH3)2 100,16 0,8017 —83,5 116,9 1,396
Ацетофенон ... CH3COC6H5 120,15 1,026 19,6 202,3 1,53631 (15°) g
Циклогексанон . . . . CH2(CH2)4CO 98,12 0,9478 —45 155,65 1,4507 з
1 1 Е
Метиловый спирт . . . CH3OH 32,04 0,7928 —97,49 64,6 1,3288 ”
Этиловый спирт .... CH3CH2OH 46,07 0,7893 —114,6 78,37 1,35954(25°) ’
Пропиловый спирт . . , CH3CH2CH2OH 60,09 0,8075 —127 97,8 1,3854 J
Изопропиловый спирт . (CH3)2CHOH 60,09 0,7851 —89,5 82,40 1,3747 (25°) |
Бутиловый спирт . . . CH3(CH2)2CH2OH 74,12 0,8098 79,9 117,5 1,40118(15°) £
Изобутиловый спирт . . (CH3)2CHCH2OH 74,12 0,8058 —108 107,89 1,39768 (15°) £
Амиловый спирт ... CH3(CH2)3CH2OH 88,15 0,8144 —78,5 138 1,4101 ”
Изоамиловый спирт (CH3)2 CHCH2CH2OH 88,15 0,8129 —117,2 132,00 1,40853(15°) §
Бензиловый спирт . . . C6H6CH2OH 108,14 1,0427 —15,3 205,2 1,53955 *
Ацетонитрил . . . . CHgCN 41,05 0,7828 —45,72 81,60 1,34423 s
Диэтиловый эфир . . . (C2H5)2 о 74,12 0,7135 —117.6(a) 35,6 1,3497(24,8°) s
—123,3 (₽)
Этилацетат CH3COOC2H5 88,10 0,901 —83,6 77,15 1,3728 (19,2°)
Пропилацетат CH3COOC3H7 102,14 0,887 —92,5 101,6 1,38438
Бутилацетат CH3COOC4H9 116,16 0,882 —76,8 126,114 1,3951
Амилацетат CH3COOC6Hn 130,19 0,8753 148 1,4012
Апротонные
растворители
Четыреххлористый угле-
род CC14 153,81 1,595 —22,6 76,8 1,4630
Циклогексан CH2 (CH2)4 CH2 1 1 84,16 0,7785 6,554 81,4 1,42623
Гептан CH3 (CH2)6CH3 100,20 0,68376 —90,610 98,43 1,38764
Беизсл c6H6 78,12 0,8737 (25°) 5,533 80,099 1,50165
Хлорбензол C6H6C1 112,56 1,1066 —45,58 132 1,52479
Хлороформ CHC13 119,37 1,4984 —63,5 61,152 1,44858 (15°)
ДИЭЛЕКТРИЧЕСКАЯ ПРОНИЦАЕМОСТЬ НЕКОТОРЫХ РАСТВОРИТЕЛЕЙ (в порядке возрастания)
Более подробно см. «Справочник химика», 2-е изд., т. 1, стр. 948.
Растворитель Диэлектрическая проницаемость Температура, Растворитель Диэлектрическая проницаемость Температура,
Пентан ... ... 1,843 25 Бензиловый эфир уксус-
Гексан . . ... 1,90 25 НОЙ кислоты 5,1 21
Гептан ... 1,927 25 Изобутиловый эфир ук-
Октан .... 1,946 25 сусной кислоты . . . 5,29 20
Декан ... ... 1,956 20 Бутиламин 5,3 21
Циклопентан ... 1,965 20 Хлорбензол . . 5,61 25
Нонан 1,974 25 Этиловый эфир пропио-
Метилциклопентан . . 1,985 20 новой кислоты .... 5,65 19
Метилциклогексан . . . 2,02 20 Прениловый эфир ук-
Циклогексан .... 2,02 20 сусной кислоты . . . 5,69 19
1,4-Диоксан . . . . 2,21 25 трет-Амиловый спирт . 5,69 25
Циклогексен 2,220 25 .и-Толуидин 5,95 18
Четыреххлористый угле- Этиловый эфир уксус-
род ....... 2,238 20 ной кислоты .... 6,02 25
л-Цимол ... 2,243 20 Этиловый эфир бензой-
п-Ксилол 2,265 25 ной кислоты .... 6,02 20
Бензол . . 2,275 25 Уксусная кислота . . . 6,19 25
Тетрахлорэтилен , . 2,30 25 о-Толуидии 6,34 18
л-Ксилол . . . 2,368 25 Изобутиловый эфир му-
Толуол 2,378 25 равниной кислоты . . 6,41 19
Изопропилбензол . . . 2,380 20 Метиловый эфир бен-
Этилбензол 2,403 20 зойной кислоты . . . 6,59 20
и-Ди хлорбензол .... 2,41 50 Метиловый эфир уксус-
Триэтиламин 2,42 25 ной кислоты .... 6.68 25
о-Ксилол 2,51 25 Анилин 6,99 25
Валериановая кислота 2,67 20 Этиловый эфир му-
Диамиловый эфир . . . 2,77 25 равьиной кислоты . . 7,16 25
Диизоамиловый эфир . 2,82 20 Пропиловый эфир му-
Диэтиловый эфир уголь- равьиной кислоты . . 7,72 19
ней кислоты 2,82 20 Диэтиловый эфир мало-
Масляная кислота . . 2,90 25 новой кислоты . . . 7,87 25
Бутиловый эфир . . . 3,06 25 1, 1, 2, 2-Тетрахлорэтан 8,08 20
Пропионовая кислота . 3,15 17 Диэтиловый эфир щаве-.
Пропиловый эфир . . . 3,39 26 левой кислоты . . . 8,1 21
Трихлорэтилен .... 3,409 20 Метиловый эфир му-
Диэтиламин ... 3,78 25 равьиной кислоты . . 8,50 20
Пентахлорэтан .... 3,83 20 Дихлорметан 9,08 20
Бензилэтиловый эфир 3,9 20 о-Дихлорбензол . . . 9,82 20
Диизопропиловый эфир 4,04 25 Октиловый спирт . . . 9,85 25
Диэтиловый эфир . . . 4,22 25 л-Крезол 9,91 58
Изобутиламин . . . . 4,4 21 1, 1-Дихлорэтан .... 10,0 18
Изоамиловый эфир ук- Фенол ...... 10,28 50
сусной кислоты . . . 4,63 30 1,2-Дихлорэтан . . . . 10,36 25
Хлороформ 4,724 25 .и-Крезол 11,75 25
Циклогексилам ин . . . 4,73 20 трет-Бутиловый спирт . 12,3 26
Амиловый эфир уксус- 3-Мети4циклогексанол 12,3 20
ной кислоты . . 4,75 20 Пиридин ... 12,3 25
п-Толуидии . . 4,88 58 Масляный ангидрид . . 12,9 20
Бутиловый эфир уксус- 2-Метилциклогекса нол 13,3 20
ной кислоты . . . . 5,01 20 Масляный альдегид . . 13,40 26
41b
ДИЭЛЕКТРИЧЕСКАЯ ПРОНИЦАЕМОСТЬ НЕКОТОРЫХ РАСТВОРИТЕЛЕЙ
Продолжение
Диэлек- Тем- Диэлек-
Растворитель ская проницаемость пера-ту^а, Растворитель триче-ская прони- цаемость пера-ту^а.
Этилендиамин . . . 14,2 20 Ацетон ... 20,74 25
Амиловый спирт . . . 14,4 25 Этиловый спирт .... 25,2 25
Пзоам иловый спирт . . 14,7 25 Бензонитрил 25,20 25
нтор-Бутиловый спирт . 16,35 25 Пропионитрил 27,7 20
Циклогексаиол .... 16,8 25 Нитроэтан 28,06 30
Пентанон-3 17,00 20 Пропилеигликоль 29,5 20
Ацетофенси 17,39 25 Метиловый спирт . . 32,65 25
Бензальдегид 17,6 18 Нитробензол ..... 34,75 25
Бутиловый спирт . . . 17,7 25 Триметиленглпколь 35,0 20
Изобутиловый спирт . . 17,70 25 Ацетонитрил 37,4 20
Пропионовый ангидрид Изопропиловый спирт . 18,3 18,3 16 25 Этиленгликоль Трифторуксусиая кисло- 37,7 25
Циклогексанон .... 18,3 20 та ... ... 39,5 20
Пропионовый альдегид . 1р,'> 17 Глицерин 42,4 25
Метилэтилкетои . . . 18,50 20 Муравьиная кислота 57,9 20
Пропиловый спирт . . 19,7 25 Вода ... 78,3 25
Уксусный ангидрид . . Аллиловый спирт . . . 20,5 20,6 20 21 Формамид 109,5 25
КОНСТАНТЫ АУТОПРОТОЛИЗА НЕКОТОРЫХ РАСТВОРИТЕЛЕЙ
Константой аутопротолиза называется ионное произведение растворителя, диссоциирующего с образованием нона Н + .
Растворитель К1 j Растворитель К1
Аммиак (—50е С) ... 3- КГ33 Вода (25° С) 1 -10-14
Г идразин 2-10 25 wi-Крезол 3-10 14
Этиловый спирт .... 8-10 20 Уксусная кислота . . . 2,5-10 13
Формамид 1-10 17 'Муравьиная кислота . . 5-10 7
Метиловый спирт . . . 2-10 17 :|Серная кислота .... 1-10 5
ПРОТОННОЕ СРОДСТВО АНИОНОВ
Протонным сродством аниона называется изменение энтальпии при диссоциации данной молекулы (или иона) на протон и соответствующий аннон.
Исходная молекула или ион Уравнение диссоциации Протонное сродство
по данным Яцимирского по данным других авторов
о а Ч se кдж/г-ион яоп-г/гояя кдж/г-ион
нею. НС1О4 5± н+ + С1О4- 285 1193 — —
h2so4 H2SO, 5± н+ + HSO4- 296 1239 — —
HJ HJ н+ 4-J- 307 1285 307; 315 1285; 1319
27*
419
Продолжение
ПРОТОННОЕ СРОДСТВО АНИОНОВ
Исходная молекула или пои Уравнение диссоциации Протонное сродство
по данным Яцимирского по данным других авторов
а: с а а * кдж'г-ион ккал!г-ион X о а * *
НВг НВг ЧЛ н+4-Вг- 315 1319 314; 322 1315; 1348
HNO3 HNO3 H+4-NO3- 320 1340 — —
HCI HCI н+4-cr 325 1361 326; 327 1365; 1369
H2S H2S h+4-hs- 343 1436 338; 351 1415; 1470
СНзСООН СН3СООН н+4-сн3соо- 343 1436 382 1599
С6Н5СООН С6Н5СООН н+ч-с6н5соо- 345 1444 — —
НСООН НСООН т* н+ 4-нсоо- 347 1453 382 1599
HCN HCN H+4-CN- 348 1457 338 1415
С2Н5СООН С2Н6СООН Н4 +С2Н5СОО- 352 1474 — —
HF HF H+4-F- 363 1520 361; 366 1511; 1532
Н2О Н2О н+ 4-он- 383 1604 370; 386; 392 1549; 1616; 1641
NH3 NH3 H+4-NH- 419 1754 380 1591
HSO4" hso- 4 H4+so=- 433 1803 — —
HCO3- НСО- Н+Ц-СО2' 498 2085 — —
HS~ HS- H+-4-S2- 541 2265 533 2232
ОН- ОН- н+4-02- 615 . 2575 612 2562
ВАЖНЕЙШИЕ СТАНДАРТНЫЕ ВЕЩЕСТВА, ПРИМЕНЯЕМЫЕ ПРИ КИСЛОТНООСНОВНОМ ТИТРОВАНИИ В НЕВОДНЫХ РАСТВОРАХ
Титрант Стандартное вещество Формула Молекулярный вес Растворитель
Кислоты (хлорная, хлористоводородная, п-то-луолсульфоки-слота и др.) Бифталат калия НООСС6Н4СООК 204,23 Уксусная, муравьиная, пропионовая кислоты, спирты и кетоны
Карбонат натрия Na2CO3 105,99 То же
Дифенил-гуанидин (C6H5NH)2 cnh 211,27 Спирты, кетоны, четыреххлористый углерод, хлороформ
420
ВАЖНЕЙШИЕ СТАНДАРТНЫЕ ВЕЩЕСТВА, ПРИМЕНЯЕМЫЕ ПРИ КИСЛОТНО-
ОСНОВНОМ ТИТРОВАНИИ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Титрант Стандартное вещество Формула Молекулярный вес Растворитель
Основания (четвертичные аммониевые основания, гидроокиси щелочных металлов, алкоголяты щелочных металлов, амины и др.) Бензойная кислота С6Н5СООН 112,13 Спирты, кетоны ацетонитрил, диметилформа-мид
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ ОСНОВНОГО ХАРАКТЕРА В НЕВОДНЫХ РАСТВОРАХ
В качестве индикаторного электрода при потенциометрическом титровании соединений основного характера обычно применяют стеклянный электрод.
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Алифатические п ароматические первичные, вторичные и третичные амины Хлорная кислота в уксусной кислоте Хлорная кислота в диоксане Хлорная кислота в метилэтилке-тоне Уксусная, муравьиная, пропионовая кислоты, уксусный ангидрид, уксусная кислота + уксусный ангидрид, уксусная кислота + хлороформ Ацетонитрил, нитрометан, этиленгликоль + изопропиловый спирт (1:1)*, метиловый, этиловый, бутиловый, пропиловый спирты, ацетон, метилэтнлке-тон, метвлбутнлке-тон Ацетонитрил, нитрометан, этиленгликоль+ изопропиловый спирт (1 : 1), метиловый, этиловый, бутиловый, пропиловый спирты, ацетон, метилэтилке-тон, метилбутилке-тон Визуальный, потенциометрический, высокочастотный Визуальный, потенциометрический То же
* Здесь и ниже указаны объемные соотношения.
421
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ ОСНОВНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения
титрант растворитель точки эквивалентности
Алифатические и ароматические первичные, вторичные и третичные амины Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1: 1) Хлорная кислота в пропионовой кислоте Этиленгликоль + изопропиловый спирт (1 : 1), диэтиленгликоль + изопропиловый спирт (1:1) Пропионовая кислота Потенциометрический То же
Гетероциклические азотсодержащие основания Хлорная кислота в уксусной кислоте Хлорная кислота в диоксане Хлорная кислота в метилэтилкето не Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1:1) Хлорная кислота в пропионовой кислоте Хлорная кислота в смеси муравьиная кислота — диоксан (1:1) Хлорная кислота в уксусной кислоте Уксусная кислота, уксусная кислота + бензол (1 : 1), уксусная кислота + уксусный ангидрид Уксусная кислота, ацетонитрил, нитрометан, этилацетат Ацетонитрил, этилацетат, бутилацетат, метиловый, этиловый, бутиловый, пропиловый спирты, этиленгликоль + изопропиловый спирт (1 : 1), бензол+метиловый спирт (1 : 1), ацетон, метилэтилкетои Этиленгликоль + изопропиловый спирт (1:1) Визуальный, потенциометрический, высокочастотный Визуальный, потенциометрический То же » »
Алкалоиды Пропионовая кислота . Муравьиная кислота, муравьиная кислота+ диоксан (1:1) Уксусная кислота, уксусный ангидрид, уксусная кислота + уксусный ангидрид, уксусная кислота + ацетонитрил (1 : 1), уксусная кислота+ хлороформ Потенциометрический То же Визуальный, потенциометрический, высокочастотный
422
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИИ ОСНОВНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения
титрант растворитель точки эквивалентности
Алкалоиды л-Толуолсульфо-кислота в смесях этиленгликоля с изопропиловым спиртом или диоксаном л/-Толуолсульфо-кислота в хлороформе Хлорная кислота в диоксане Хлорная кислота в смеси уксусная кислота — уксусный ангидрид Хлористый водород в спирте Хлорная кислота в нитрометане Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1 : 1) Хлористый водород в уксусной кислоте Различные комбинации этиленгликоля с изопропиловым спиртом Хлороформ Ацетон, нитробензол, ацетонитрил, хлороформ, этилацетат, фенол 4- хлороформ + ацетонитрил Уксусная кислота+ук-сусный ангидрид Вода 4- спирт Нитрометан, нитрометан 4- уксусный ангидрид (1:1) Этиленгликоль + изопропиловый спирт (1:1) Уксусная кислота Потенциометрический Визуальный, потенциометрический Потенциометрический Визуальный Высокочастотный Потенциометрический То же » »
Смеси первичных, вторичных и третичных алифатических аминов (о раздельном определении аминов см. примечание в конце таблицы) Хлорная кислота в уксусной кислоте Хлорная кислота в диоксане Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1:1) Уксусная кислота, уксусная кислота + уксусный ангидрид, бензол 4- изопропиловый спирт, диоксан Хлороформ, ацетонитрил, диоксан, ацетон Этиленгликоль 4- изопропиловый спирт (1:1) » » Визуальный
423
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ ОСНОВНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Смеси первичных, вторичных и третичных ароматических аминов (о раздельном определении аминов см. примечание в конце таблицы) Хлорная кислота в уксусной кислоте Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1:1) Хлорная кислота в диоксане Уксусная кислота, уксусная кислота+уксусный ангидрид Этиленгликоль + изопропиловый спирт (1:1) Ацетонитрил, хлороформ Потенциометрический Визуальный, потенциометрический Потенциометрический
Смеси алифатических, ароматических ^гетероциклических четвертичных аммониевых оснований, алкалоидов и др. Хлорная кислота в диоксане Хлорная кислота в смеси этиленгликоль — фенол (1 :1) Ацетонитрил, нитрометан, уксусная кислота-]- диоксан, ацетон, метилизобутилкетон Этиленгликоль-]-фенол Потенциометрический, кондуктометрический, высокочастотный Потенциометрический
Хлорная кислота в метилэтилке-тоне Ацетонитрил, метиловый, этиловый, бутиловый, пропиловый спирты, этиленгликоль 4- изопропиловый спирт, ацетон, метилэтилкетон, ме-тилбутилкетон, этилацетат, бутилацетат То же
Аминогруппы в аминокислотах Хлорная кислота в уксусной кислоте Уксусная кислота, трифторуксусная кислота, муравьиная кислота + уксусная кислота Визуальный, потенциометрический, кондуктометрический
Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1:1) Этиленгликоль 4- изопропиловый спирт (1 : 1) То же
424
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ ОСНОВНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Аминогруппы в высокомолекулярных соединениях Хлорная кислота в уксусной кислоте Нитрометан + муравьиная кислота (1 : 1), уксусная кислота, этиленгликоль + изопропиловый спирт, бензол, хлорбензол, бромбензол + ацетон Визуальный, потенциометрический, кондуктометрический
Примечание. При раздельном анализе смесей первичных, вторичных и третичных аминов в части анализируемой пробы определяют суммарное содержание аминов, а часть обрабатывают уксусным ангидридом, связывающим первичные н вторичные амины, после чего оттитровывают третичные амины.
Дальнейший ход анализа может осуществляться одним из следующих методов: I) обрабатывают смесь салициловым альдегидом, который переводит первичные амины в основания Шнффа, после чего определяют сумму вторичных и третичных аминов; 2) обрабатывают смесь избытком салицилового альдегида, после чего, оттитровывая избыток салицилового альдегида метилатом натрия, определяют содержание первичных аминов; 3) обрабатывают смесь фталевым ангидридом, который связывает первичные амины, и определяют сумму вторичных и третичных аминов; 4) обрабатывают смесь избытком 2.4-пентандиона, который количественно реагирует с первичными аминами; содержание первичных аминов определяют обратным титрованием избыточного количества 2.4-пеитан-диона метилатом натрия в среде пиридина.
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ КИСЛОТНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
В качестве индикаторного электрода при потенциометрическом титровании соединений кислотного характера обычно применяют стеклянный электрод.
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Минеральные Гидроокись натрия в Этиленгликоль Потенциометри-
кислоты (хлорная, хлористоводород- смеси этиленгли- коль — изопропиловый спирт (1:1)* изопропиловый спирт (1:1) ческий
пая. серная, азотная и др.) Гидроокись калия в этиловом спирте Четвертичные аммониевые основания в смеси бензол — метиловый спирт (10 : 1) Дифенилгуанидин в этиловом спирте Пиридин в бензоле Циклогексиламин в метиловом спирте Бензол метиловый спирт(10: 1), диметилформа-мид хлороформ (1:1) Пиридин, диме-тилформамид, метилэтилке-тон, ацетон Ацетонитрил, ацетон Муравьиная кислота -ф- бензол (1:1) Метиловый спирт Визуальный Потенциометрический То же » » » »
* Здесь и ниже указаны объемные соотношения.
425
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ КИСЛОТНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Карбоновые Г идроокись натрия в Пиридин 11отенциометри-
кислоты, их этиловом спирте ческий
окси-, гало- Гидроокись натрия в Этиленгликоль-)- То же
ген- и нитро- смеси этиленгли- изопропиловый
производные коль — изопропиловый спирт (1:1) спирт (1:1)
Гидроокись калия в этиловом спирте Ацетонитрил, кетоны, диметил-формамид, этилендиамин,
Метилат натрия в метиловом спирте спирты Ди мети л формамид Высокочастотный
Метилат, этилат, бути- Четыреххлорис- Визуальный, по-
лат, амилат натрия в тый углерод, тенциометриче-
соответствующем спирте толуол, хлороформ, бензол, диметилформа- с кий
Ацетат натрия в смеси бензол — метиловый спирт (3:1) мид, спирты Бензол+метило- вый спирт (3:1) Высокочастотный
Амииоэтилат натрия в этилендиамине Этилендиамин Визуальный, потенциометрический
Четвертичные аммоиие- Ацетонитрил, ке- Потенциометри-
вые основания в смеси бензол — метиловый спирт (10 : 1) тоны, пиридин, пиперидин, ди-метилформамид, этилендиамин ческий
Гидроокись тетрабутил-аммония в смеси бензол — метиловый спирт (10 : 1) Бензол-[-метило-вый спирт (2 : 1; 4:1), пиридин Высокочастотный
Триэтил а мин или пиридин в этиловом спирте Ацетон Кондуктометрический
Фенолы и их Г идроокись калия в Этилендиамин, Потенциометри-
производные этиловом спирте диметилформа-мид, бензол ческий
Метилат натрия или калия в смеси бензол — метиловый спирт (10 : 1) Этилендиамин, диметилформа-мид, бутиламин Визуальный
Метилат калия в смеси бензол — метиловый спирт (10: 1) Бензол-|-метило-вый спирт (2:1) Высокочастотный
426
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЙ КИСЛОТНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Фенолы и их производные Производные барбитуровой КИСЛОТЫ Енолы, имиды, амиды и другие слабые КИСЛОТЫ Эфиры Спирты Смеси кислот: смеси сильных кислот Амииоэтилат натрия в этилендиамине Четвертичные аммониевые основания в смеси бензол — метиловый спирт (10:1) Метилат лития или натрия в смеси бензол — метиловый спирт (10 : 1) Гидроокись тетрабу-тиламмония в смеси бензол — метиловый спирт (10:1) Метилат натрия в смеси бензол — метиловый спирт (10: 1) Аминоэтилат натрия в этилендиамине Четвертичные аммониевые основания в смеси бензол — метиловый спирт (10 : 1) Метилат натрия или калия в смеси бензол— метиловый спирт Четвертичные аммониевые основания в смеси бензол — метиловый спирт (10: 1) Литийалюмииийгидрид или • литийалюминий-амйд в тетрагидрофуране Гидроокись натрия в смеси этиленгли- коль — изопропиловый спирт (1:1) Ацетат лития или натрия в уксусной кислоте Этилендиамин Пиридин, ацетонитрил, ацетон, этилендиамин, диметилформа-мид, бензол-f-изопропиловый спирт Диметилформа-мид Бензол-|-изопро-пиловый спирт (10:1).бензол-|-хлороформ (10:1) Этилендиамин, диметилформа-мид Этилендиамин Пиридин, ацетон Этилендиамин, диметилформа-мид Пиридин, ацетон Бензол Этиленгликоль-|-изопропи левый спирт (1:1) Уксусная кислота Потенциометрический То же Визуальный Визуальный, потенциометрический Визуальный Потенциометрический То же Визуальный, потенциометрический Потенциометрический То же » » Потенциометрический, кондуктометрический
427
МЕТОДЫ ТИТРОВАНИЯ СОЕДИНЕНИЯ КИСЛОТНОГО ХАРАКТЕРА
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Смеси кислот: смеси силь- Четвертичные аммоине- Кетоны, пиридин Потенциометри-
ных кис- вые основания в сме- ческий
лот си бензол — метиловый спирт (10: 1) Циклогексиламин в ме- Метиловый спирт То же
смеси ела- тиловом спирте Гидроокись калия в Диметилформ- х> »
бых кис- этиловом спирте амид, этиленди-
лот Метилат калия в сме- амин, бензол Метиловый спирт, Кондуктометри-
си пиридин — бензол пиридин, диме- ческий
(1 : Ю) Метилат калия в сме- тилформамид и их смеси с бензолом и ксилолом Ацетон-|-пиридин Визуальный, по-
си бензол — метило- (10:1) тенциометриче-
вый спирт (10:1) Бутилат натрия в бу- Бутиловый спирт ский Потенциометри-
тиловом спирте Четвертичные аммоние- Диметилформа- ческий Потенциометри-
вые основания в сме- мид, эти лен ди- ческий, кондук-
си бензол — метило- амин, бензол, тометрический
смеси силь- вый спирт (10 : 1; 5:1) Четвертичные аммоние- пиридин, кетоны, ацетонитрил Пиридин, диме- Потенциометри-
ных и ела- вые основания в сме- тилформамид, ческий
бых кис- си бензол — метило- кетоны, ацето-
лот вый спирт (10:1; нитрил
5:1) Ацетат калия в ацето- Ацетонитрил Кондуктометри-
ангидриды нитриле Метилат натрия в сме- Бензол-|-метило- ческий Потенциометри-
и хлор- си бензол — метило- вый спирт (1: 2), ческий
ангидри- вый спирт (10: 1) диоксан, бутил-
ды кислот надкислоты Г идроокись натрия в амин, диэтиловый эфир, этилацетат, диме-тилфор.мамид, хлороформ Бензол То же
(надбензойная -J-бензой-ная) смесн бензол — метиловый спирт (10: 1)
428
МЕТОДЫ ТИТРОВАНИЯ СОЛЕЙ В НЕВОДНЫХ РАСТВОРАХ
В качестве индикаторного электрода при потенциометрическом титровании солей обычно применяют стеклянный электрод.
Определяемые Системы для титрования Метод определения
вещества титрант растворитель точки эквивалентности
Неорганические соли Соли, титруемые как основания (бромиды, хлориды, нитриты, бораты и др.)* Хлорная кислота в уксусной кислоте Хлорная кислота в смеси уксусная кислота — уксусный ангидрид (1:1) Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1:1) Хлорная кислота в диоксане Уксусная кислота, уксусный ангидрид То же Этиленгликоль-)-изопропиловый спирт (1:1) Уксусная кисло-та-|-хлороформ, уксусная кис-лота-|-метилизо-бутилкетон Визуальный, потенциометрический, косвенный потенциометрический Визуальный, потенциометрический То же Потенциометрический
Соли, титруемые как кислоты (хлориды олова и алюминия, бромид алюминия и др.) Метилат натрия в смеси бензол — метиловый спирт (5 : 1) Пиридин в хлористом тиониле Этилендиамин, диметилформа-мид Хлористый тиснил Визуальный То же
Соли, титруемые методом осаждения (бромиды, сульфаты) Нитрат серебра в ацетоне или ацетонитриле Ацетон, ацетонитрил Потенциометрический
Соли, титруемые как ацетаты ** Хлорная кислота в диоксане Уксусная кислота Косвенный визу-» альный, потенциометрический
* Сульфаты осаждаются избыточным количеством ацетата бария, после чего не-нрореагнровавший ацетат бария титруется стандартным уксуснокислым раствором хлорной кислоты. Метод применим только в том случае, когда основность ацетата барня выражена сильнее, чем ацетата определяемого металла.
** Соли, не титруемые как основания в среде уксусной кислоты, переводятся в ацетаты, проявляющие себя в этой среде основаниями, с помощью ацетата ртути;
2NaCl -|- HgAc2 —> HgCl2 + 2NaAc
429
МЕТОДЫ ТИТРОВАНИЯ СОЛЕЙ В НЕВОДНЫХ РАСТВОРАХ
П родолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Фосфаты, хлориды и нитриты натрия; бихромат калия и др. Соли одноосновных органических кислот с неорганическими катионами (ацетаты, бензоаты, лактаты и др.) Гидроокись тетрабутнл-аммония в смеси бензол — метиловый спирт (10:1) Ацетон, пиридин Косвенный потенциометрический *
Соли, титруемые как основания Хлорная кислота в уксусной кислоте Хлорная кислота в пропионовой кислоте Хлорная кислота в смеси уксусная кислота — уксусный ангидрид (1:1) Хлориая кислота в диоксане Хлорная кислота в ме-тилэтилкетоне Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1 : 1) Соляная кислота в спиртах Ацетат натрия в уксусной кислоте Уксусная кислота Пропионовая кислота Уксусный ангидрид Уксусная кислота, уксусная кисло-таф-хлороформ (1 :10). метиловый спирт Метилэтилкетон Этиленгликоль ф-изопропиловый спирт (1:1) Ацетонф-вода Уксусная кислота Визуальный, потенциометрический, фотометрический Визуальный, потенциометрический Потенциометрический Визуальный, потенциометрический Потенциометрический Визуальный, потенциометрический То же Косвенный потенциометрический **
* Метод остнован на подкислении анализируемой соли избытком стандартного водного раствора серной кислоты с последующим потенциометрическим титрованием кислоты, выделившейся из соли, н непрореагировавшего избытка серной кислоты в среде органического растворителя, в котором выпадают в осадок образовавшиеся сульфаты.
** Метод основан на предварительном растворении соли в избытке стандартного раствора хлоркой кислоты с последующим титрованием иепрореагировавшей кислоты стандартным уксуснокислым раствором ацетата натрия.
430
МЕТОДЫ ТИТРОВАНИЯ СОЛЕЙ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Соли, титруемые как кислоты Метилат лития в смеси бензол — метило-спирт (5:1) Гидроокись тетрабу-тиламмония в смеси бензол — метиловый спирт (10 : 1) Диметилформа-мид, гликоль-|-хлороформ, бутилам ин, пиридин Ацетон, пиридин Визуальный Косвенный потенциометрический *
Соли многоосновных органических кис- Хлорная кислота в уксусной кислоте Уксусная кислота Визуальный, потенциометрический
лот с неорганическими ка- Соляная кислота в спиртах Ацетон-|-вода То же
тио нами (цитраты, сукцинаты, тартраты и др.) Соли четвертичных аммониевых оснований с неорганическими и органическими анионами Ацетат натрия в уксусной кислоте Гидроокись тетрабу-тиламмония в смеси бензол — метиловый спирт (10 : 1) Уксусная кислота Ацетон, пиридин Косвенный потенциометрический ** Косвенный потенциометрический *
Соли, титруемые как основания Хлорная кислота в уксусной кислоте Хлорная кислота в сме- Уксусная кислота Уксусный ангнд- Визуальный, потенциометрический Потенциометри-
си уксусная кислота — уксусный ангидрид (1 : 1) рид ческий
Соли, титруемые методом осаждения Нитрат серебра в ацетоне или ацетонитриле Ацетон, ацетонитрил То же
* Метод основан на подкислении анализируемой соли избытком стандартного вод* него раствора серной кислоты с последующим потенциометрическим титрованием кислоты, выделившейся из соли, и непрореагировавшего избытка серной кислоты в среде органического растворителя, в котором выпадают в осадок образовавшиеся сульфаты.
♦♦ Метод основан на предварительном растворении соли в избытке стандартного раствора хлорной кислоты с последующим титрованием непрореагировавшей кислоты стаи* Дартным уксуснокислым раствором ацетата натрия.
431
МЕТОДЫ ТИТРОВАНИЯ СОЛЕЙ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Соли, титруе- Хлорная кислота в ди- Уксусная кисло- Косвенный визу-
мые как аце- оксане та, уксусная альный, потен-
таты * Соли органических оснований с неорганическими и органическими анионами кислота-|-ди-оксан циометриче-ский
Соли, титруе- Хлорная кислота в ук- Уксусная кислота, Визуальный, по-
мые как ос- сусной кислоте уксусный ан- тенциометриче-
иования гидрид, диоксан, ацетон, нитробензол, ацетонитрил ский
Хлорная кислота в сме- Уксусный ангид- Потенциометри-
си уксусная кислота — уксусный ангидрид (1:1) рид ческии
Хлорная кислота в ди- Уксусная кислота, Визуальный, по-
оксане диоксан тенциометриче-ский
То же Смесь этилового спирта, хлороформа и ацетонитрила Визуальный
Соли, титруе- Гидроокись тетрабутил- Метилизобутилке- Потенциометри-
мые как кислоты аммония в смеси бензол—метиловый спирт (Ю: 1) ТОН ческий
Гидроокись калия в этиловом спирте Спирты, кетоны Визуальный, потенциометрический
Этилат натрия в смеси спирт — ацетон То же То же
Соли, титруе- Хлорная кислота в ди- Уксусная кислота. Косвенный визу-
мые как аце- оксане уксусная кисло- альиый, по-
тэты * таЦ-диоксан тенциометриче-ский
* Соли, не титруемые как основания в среде уксусной кислоты, переводятся в ацетаты, проявляющие себя в этой среде основаниями, с помощью ацетата ртути:
2RNH3X4- HgAc2 —> 2RNH3Ac 1 HgXa
432
МЕТОДЫ ТИТРОВАНИЯ СОЛЕЙ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Системы для титрования Метод определения
титрант растворитель точки эквивалентности
фармацевтические препараты (сахарин-иатрпй, теобро-мпи-патрий и др.) Хлорная кислота в уксусной кислоте Хлорная кислота в диоксане Хлорная кислота в смеси этиленгликоль — изопропиловый спирт (1:1) Уксусная кислота, уксусная кислота Ц- бензол (1 :1), уксусная кислота дио-ксаи Уксусная кислота, уксусная кисло-та-|-бензол (1:1) Этиленгликоль 4-изопропиловый спирт (1 : 1) Визуальный, потенциометрический То же » »
МЕТОДЫ ТИТРОВАНИЯ СМЕСЕЙ ЭЛЕКТРОЛИТОВ В НЕВОДНЫХ РАСТВОРАХ
Определение бинарных смесей солей с кислотами основано иа взаимодействии аиа лизируемой смеси с серной кислотой в среде бензола или метилэтилкетона (МЭК). Полученную смесь кислот (кислота, содержащаяся в анализируемой смеси, кислота, выделившаяся из соли в результате взаимодействия ее с серией кислотой, и иепрореагировавший избыток серной кислоты) дифференцированно титруют гидроокисью тетраэтиламмоиия (ГТЭА); при потенциометрическом титровании в качестве индикаторного применяют стеклянный электрод.
Процесс этого определения может быть представлен рядом уравнений:
для смесей солей с одноосновными кислотами
2KtAn4 HAn4-rcH2SO4 —> Kt2SO4 Ч-ЗНАп-|-(щ — 1) H2SO4
для смесей солей с двухосновными кислотами
Kt2An 4-Н2Ап Ч- mH2SO4 —> Kt2SO44 2H2An (т — 1) H2SO4
для смесей солей с трехосновными кислотами
2КЛзАп-г HgAn + mH2SO4 —> 3Kt2SO4 4-ЗНзАп 4(w—3) H2SO4
Здесь KtAn, Kt2An, KtsAn—соли, содержащиеся в анализируемой смеси;
НАп, Н2Ап, НзАп — кислоты, содержащиеся в анализируемой смеси.
Содержание (в г) соли и кислоты в анализируемой смеси определяют по следующим Формулам:
содержание соли
Эс / ГгЛ'гЭНг5О4
° 3H2SO4 v'HjSO, 1000 /
общее количество кислоты (кислота, содержащаяся в анализируемой смеси и кнс-лота, выделившаяся из соли в результате взаимодействия с серной кислотой)
количество кислоты, выделившееся из соли в результате взаимодействия с серной кислотой
Эк “5— ^с содержание кислоты в анализируемой смеси
°3 —— °2
28 Зак. 783
433
МЕТОДЫ ТИТРОВАНИЯ СМЕСЕЙ ЭЛЕКТРОЛИТОВ В НЕВОДНЫХ РАСТВОРАХ
В этих формулах:
кислоты, взятой для анализа, серной кислоты;
определяемой соли; определяемой кислоты;
количество сеРн0Й эквивалентный вес <ЭС—эквивалентный вес эквивалентный вес
V—объем раствора ГТЭА, пошедший на титрование пример, 3HAn + (m — IJHaSOJ. мл\
Уг—-объем раствора ГТЭА, пошедший на титрование А’г — нормальность раствора ГТЭА.
Продолжение
общего количества кислоты [на-
избытка серной кислоты, мл\
Определение многокомпонентных смесей солей с другими солями, кислотами и основаниями отличается тем, что на анализируемую смесь действуют избыточным количеством хлориой кислоты. Полученную смесь кислот (избыточное количество хлорной кислоты, кислота, выделившаяся из соли в результате взаимодействия ее с хлорной кислотой, и в некоторых случаях кислота, содержащаяся в анализируемой смеси) дифференцированно титруют гидроокисью тетраэтиламмоиия (ГТЭА) в среде метилэтилкетона (МЭК); при потенциометрическом титровании в качестве индикаторного применяют стеклянный электрод.
Процесс этого определения может быть представлен рядом уравнений.
Для определения смесей солей:
KtAn + KtiAnj -Ь тНС1О4 —> KtClO4 -4- KtiClO4 + НАп -I- HAnj -4-(Щ— 2) НС1О4 Содержание (в г) солей в анализируемой смеси определяют по следующим формулам! содержание первой соли
(К - И Л Л'Э
\ г г/ г с а~ юоо
содержание второй соли
(V - к") A' V
\ г г/ г с
° = НЙО
Для определения многокомпонентных смесей солей с кислотами: Kt Ап 4- НАп 4- mHCIO4 —> KtClO4-T2HAn + (m — 1)НС1О4
KtAn +НАп 4-НАп| 4-тНС1О4 —> KtClO4-4-2НАп + HAnj — 1) НС1О4
Содержание (в г) соли и кислоты в анализируемой смеси определяют по следующим формулам:
содержание соли
( ИЛЭНС1О4 Эс
°\“нС1О4 1000 / ЭИС1О4
общее количество кислоты, сходной по аниону с солью, в анализируемой смеси (кислота, содержащаяся в анализируемой смеси, и кислота, выделившаяся из-соли в результате взаимодействия с хлорной кислотой)
количество кислоты, сходной по аниону с солью, выделившееся из соли в результате взаимодействия с хлорной кислотой
эк
^С
содержание кислоты, сходной по аниону с солью, в анализируемой смеси
«8 = Л1 — а%
содержание кислоты, не сходной по аннону с солью, в анализируемой смеси
434
МЕТОДЫ ТИТРОВАНИЯ СМЕСЕЙ ЭЛЕКТРОЛИТОВ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Для определения многокомпонентных смесей солей с основаниям и:
KtAn + KtOH+mHClO4 —> 2KtClO4 + HAn+(m-2) НС1О4 + H2O
Kt А п +Kt i An И-Kt ОН 4- гиНС1О4 —> 2KtC104 + KtjClO4 + HAn + НАщ +(m —3)ИСЮ4
Содержание (в г) солей и основания в анализируемой смеси определяют ио следующим формулам:
содержание первой соли
й ——-------------
содержание второй соли
общее количество основания и солей в пересчете на первую соль
Эс / КгЛ'гЭНС1О4 ’
<’НС1О4 ГНС1О4 1000
количество второй соли в пересчете на первую соль
°'Эс (^г-<)Л'гЭс
° 6 = ~ =---------------
Эс 1000
количество основания в пересчете на первую соль
а7 = аь-(ач л6)
содержание основания в анализируемой смеси
°75ОСН fl8=-3T~
В этих формулах:
UCio4 — количество хлорной кислоты, взятой для анализа, г;
’^ПС1О4 — эквивалентный Эс— эквивалентный Эс — эквивалентный
вес хлорной кислоты;
вес первой соли;
вес второй соли;
— эквивалентный вес кислоты, сходной по аниону с солью;
3R — эквивалентный вес кислоты, не сходной по аниону с солью;
^осн— эквивалентный вес основания;
Kj.—объем раствора ГТЭА, пошедший на
Иг— объем раствора ГТЭА, пошедший на
V — объем раствора ГТЭА, пошедший иа лоты, сходной по аниону с солью. мл;
титрование общего количества кислоты, мл;
титрование избытка хлорной кислоты, мл;
титрование избытка хлорной кислоты и кис-
TVj,—нормальность раствора ГТЭА.
28*
435
МЕТОДЫ ТИТРОВАНИЯ СМЕСЕЙ ЭЛЕКТРОЛИТОВ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые Системы для титрования Метод определения
вещества титрант растворитель точки эквивалентности
Смеси солей с основаниями Смеси солей с неорганическими основаниями (олеат натрия -(-гидроокись натрия и др.) Хлорная кислота в смеси этиленгликоль— изопропиловый спирт (1:1)* Гидроокись тетра-этиламмония в смеси бензол — —метиловый спирт (3:1) Этиленгликоль 4~ изопропиловый спирт (1: 1) Метилэтилкетон Визуальный, потенциометрический Косвенный потенциометрический
Смеси солей с органическими основаниями (ацетат калия-|-бу-тиламин и др.) Хлорная кислота в уксусной кислоте Хлорная кислота в смеси уксусная кислота—уксусный ангидрид (1:1) Хлорная кислота в диоксане Уксусная кислота--|- бензол (1:1) Уксусный ангидрид Уксусная кислота -f- хлороформ (1 = Ю) П от ен ци о м е тр и-ческий Визуальный, потенциометрический То же
Смеси солей с кислотами (бромид натрия-|-4- бромистый водород и др.) Нитрат серебра в ацетоне Гидроокись тетра-этиламмония в смеси бензол— метиловый спирт (3:1) Ацетон Бензол, метилэтилкетон » » Косвенный потенциометрический
Смеси солей (салицилат натрия бензоат калия и др.) Хлорная кислота в уксусной кислоте Хлорная кислота в смеси уксусная кислота — уксусный ангидрид (1 : 1) Уксусная кислота 4-бензол (1:1) Уксусный ангидрид Потенциометрический То же
* Здесь и ниже указаны объемные соотношения.
436
МЕТОДЫ ТИТРОВАНИЯ СМЕСЕЙ ЭЛЕКТРОНОВ В НЕВОДНЫХ РАСТВОРАХ
Продолженив-
Определяемые вешества Системы для титрования Метод определения точки эквивалентности
титрант растворитель
Смеси солей Хлорная кислота Уксусная кислота Потенциометри-
(салицилат натрия -|- бензоат в диоксане + хлороформ (1:Ю) ческий
калия и др.) Хлорная кислота в метнлэтилкетоне Соляная кислота в спиртах Нитрат серебра в ацетоне Бромид калия в ацетонитриле Г идроокись тетраэтилам мония в смеси бензол-метиловый спирт (3:1) Метилэтилкетон Ацетон вода Ацетон Ацетонитрил Метилэтилкетон То же Визуальный, потенциометрический Потенциометрический То же Косвенный потенциометрический
МЕТОДЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ В НЕВОДНЫХ РАСТВОРАХ
Определяемые вещества Система для титоования Метод определения точки эквивалентности
титрант растворитель
Хлориды, бромиды Тетраацетат Уксусная кис- Потенциометри-
свинца в уксусной кислоте лота ческий (электроды: платиновый — каломельный)
Йодиды в присутствии хлоридов и бромидов Двуокись хлора в уксусной кислоте То же То же
Бром, соли золота (III) и ртути (II), хлористый иод, перманга- Аскорбиновая кислота в уксусной кислоте » » » »
нат-, ванадат- и бихром ат-ионы
Бром, хромовый ангидрид, перманганат-, бромат- и иодат-ионы, Г идросульфнт натрия в уксусной кислоте » » » »
хлорамин Т
Железо (II), двухатомные фенолы Перманганат натрия в уксусной кислоте » » » »
437
МЕТОДЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Система для титрования Метод определения точки эквивалентности
титрант растворитель
Железо (Ill) Хлорид титана (III) в уксусной кислоте Уксусная кислота Потенциометрический (электроды: платиновый — каломельный)
Соли мышьяка (111), сурьмы (III), ртути (II) и железа (II); двухатомные фенолы, лимонен, фенол, масляная кислота, тимол, холестерин Бром в уксусной кислоте 1 То же То же
Соли сурьмы (111) в присутствии солей мышьяка, перекись водорода, дифениламин, двухатомные фенолы Хромовый ангидрид в уксусной кислоте » » » »
Щавелевая кислота Соль церия (IV) в уксусной кислоте » » Визуальный (индикаторы: ферроин, дифениламин, метиловый красный, янус зеленый)
Гидрохинон Нитрат церия (IV) в ацетонитриле Ацетонитрил или уксусная кислота То же
Аскорбиновая кислота, Бром в уксус- Уксусная кис- Визуальный (ин-
гидрохинон, Р-нафтсл ной кислоте лота в присутствии ацетата натрия дикатор: вари-аминовый синий Б)
Непредельные органические вещества: циклогексен, дициклопентадиен, рицинолевая кислота, эруковая кислота, лимонен, стирол, камфен, пинен, сабинен, сабинол, непредельные спирты; эфирные масла (определение иодных чисел) То же Уксусная кислота Один или несколько компонентов определяют полярографически, остальные — потенциометрическим методом
а- и р-Ненасыщенные альдегиды: кротоновый альдегид, этил-пропилакролеин У» » Метиловый спирт, насыщенный бромидом натрия и хлористым водородом Потенциометрический (электроды: серебряный — платиновый)
438
МЕТОДЫ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ
В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Система для титрования Метод определения точки эквивалентности
титрант растворитель
Натуральный каучук Перманганат калия в уксусной кислоте У ксусная кислота Потенциометрический (электроды: платиновый — каломельный)
Сульфаниламид, суль-фацетамид, сульфапиридин, сульфогуанидин, сульфанилмоче-вина Бром в уксусной кислоте Уксусная кислота с добавлением ацетата натрия То же
МЕТОДЫ СПЕКТРОФОТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ В НЕВОДНЫХ РАСТВОРАХ
Определяемые вещества Система для титрования Область измерен и» светопог лощения, ммк
титрант растворитель
Ацетат цинка, хлорид кобальта (11), хлорид железа (III), хлорид хрома (III), сульфат никеля (II), хлорид ртути (II) Дитизон в бензоле Метиловый спирт 550—640
Хлорид лития Перхлорат меди в ацетоне Ацетон, циклогексанон 366
Вода Уксусный ангидрид Уксусная кислота 256
Энзимы Хлорная кислота в диоксане Нитробензол 450—700
Ароматические углево- Тетрацианоэти- Хлористый ме- 460—560
породы лен в хлористом метилене тилен
Ароматические амины Уксусный ангидрид в пиридине Пиридин 310—370
Хлорная кислота в уксусной кислоте Уксусная кислота 312—555
Ароматические кислоты Г идроокись натрия в метиловом спирте Бутиламин 341—482
Г идроокись те-трабутиламмо-пия в смеси изопропиловый спирт—ацетон (9:1) Изопропиловый спирт 333—570
439
МЕТОДЫ СПЕКТРОФОТОМЕТРИЧЕСКОГО ТИТРОВАНИЯ В НЕВОДНЫХ РАСТВОРАХ
Продолжение
Определяемые вещества Система для титрования Область измерения светопоглощен ия. ммк
титрант растворитель
Смеси ароматических и алифатических аминов. смесь /г-хлордиэтил-анилина, о-хлор-анилина и 2,5-ди-хлоранилина смесь дибутилами-на, диэтиланили-на, анилина и о-хлоранилина Алкалоиды Мочевина, антипирин, N-метилпирролидон ТрифенилГуанидин Мочевина Ацетамид, антипирин, кофеин, 2,6-диметил-пирон, тиомсчевина, трифенилгуанидин, мочевина Натриевые соли ароматических и непредельных кислот Фталат калия, ацетат натрия, о-хлоранилин, мочевина Карбоциклические кислоты, сульфамиды, имиды, меркаптаны, фенолы, енолы Смеси соляной и серной, азотиой и серной кислот Хлорная кислота в уксусной кислоте Хлорная кислота в ацетонитриле Хлорная кислота в уксусной кислоте То же » » » » » » » » » » Гидроокись три-бутилметилам-монця в смеси бензол—метиловый спирт То же Уксусная кислота Ацетонитрил Уксусная кислота, уксусный ангидрид Уксусная кислота То же » » » » » » Ацетон » » 312—555
Индикатор К'
Метиловый ® фиолетовый ft Судан III ft Хинальдин I' Малахитовый ' зеленый, jf ’
нильский го- № лубои V Нильский голу- № бой, Судан III,
малахитовый ВЯ зеленый Метиловый фиолетовый С- А Ч Трифенилмета- * новые крас и- Н тели Z ) Азофиолето- & вый, тимол-фталеин, ти-моловый СИ- g ний, ней- I. тральный 1? красный ft. Нейтральный В, красный, ти- ? молфталеин
440
ВАЖНЕЙШИЕ ИНДИКАТОРЫ, ПРИМЕНЯЕМЫЕ ДЛЯ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ В НЕВОДНЫХ РАСТВОРАХ
Индикатор Концентрация, ?0 Растворитель Изменение окраски Определяемые вещества
Азофиолетовый [4- (п-нн-трофенил) -азорезор-цин] Диметилфор-мамид, пиридин Оранжевая — голубая Фенолы, енолы, имиды
п-Аминоазс бензол о,1 Хлороформ Желтая — красная Резорцин
Бензоилаурамин 0,1 Уксусная кислота Желтая — серо-фиолетовая Аминокислоты
Бриллиантовый крезоловый синий 0,1 То же Красная — синяя »
Бромкрезоловый зеленый 0,5 Хлороформ Зеленая — бесцветная Первичные и вторичные амины
Бромтимоловый синий 0,1 Пиридин, акрилонитрил, уксусная кислота Желтая — голубая Органические кислоты
Бромфеноловый синий 0,1 Хлорбензол, хлороформ, этиловый спирт, уксусная кислота Фиолетовая — желтая Амины, алкалоиды, сульфамидные препараты
Бромфталеин (этиловый эфир 3', 3", 5', 5"-те-трабромфенолфталеи-ва) 0,1 Бензол Желтая — краснофиолетовая Амины
Конго красный 0,1 Диоксан Красная — синяя »
Кристаллический фиолетовый 0,1 Уксусная кислота Г олубая — зеленая Алкалоиды, аминокислоты
Малахитовый зеленый о,1 То же Бесцветная — голубовато-зеленая Алкалоиды
Метиловый желтый 0,1 Хлороформ Желтая — красная Амины, никотин
Метиловый красный 0,1 » То же Кофеин, кофеинфосфат
Метиловый оранжевый 0,1 Г ликоль, углеводороды Желтая — малиновая Наркотики группы морфина
Метиловый фиолетовый 0,1 Уксусная кислота Зеленая — желтая Производные антипирина
а-Нафтолбензенн 0,1 То же Желтая — зеленая Аминокислоты, хинин
Нильский голубой 0,1 Бензол, метиловый спирт Красная — синяя Дифенилфосфат
441
КОЛОРИМЕТРИЧЕСКИЕ И СПЕКТРОФОТОМЕТРИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ КОЛОРИМЕТРИЧЕСКОЕ И СПЕКТРОФОТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ В ВИДИМОЙ (И БЛИЖНЕЙ ИНФРАКРАСНОЙ) ОБЛАСТИ СПЕКТРА
В таблице приведены основные условия колориметрического (спектрофотометрического) определения элементов. В графе сУсловия образования колориметрируемого соединения» обозначения типа 0,05 н. (к-та), 0,5—1 н. (к-та) показывают, что испытуемый раствор, содержащий определяемый ион, должеи быть 0,05 или 0,5—[ н. по подходящей для удержания в растворе определяемого иона минеральной кислоте (азотной, серной или соляной).
Более подробные сведения см.: 1. А. К. Б а б к о, А. Т. П и-липенко. Колориметрический анализ, Госхимиздат, 1951. — 2. Е. Б Сен дэл, Колориметрические методы определения следов металлов, перев. с англ.. Изд. <Мир», 1964. —
3. Д. Н. Финкельштейн, В. А. Борецкая, Методы
анализа минерального сырья, Госгеолтехиздат. 1958. — 4, Колориметрические (фотометрические) методы определения неметаллов, ред. Д. Больц, перев. с англ., ИЛ, 1963.
Принятые сокращения
ац. — ацетон бзл. — беизол колор. — колориметрическое комплексон Ш — этилеидиаминтетраацетат натрия, трилон Б проп. эф. — пропиловый эфир тол. — толуол
Остальные сокращения см. стр. 16.
Определяемый ион или элемент Реактив Область X измерения светопогло-щения, ммк Интервал концентраций, в котором выполняется закон Бера, мкг!мл Условия образования колориметрируемого соединения Главные мешаюшие компоненты
Ag + п-Диэтиламинсбензили-денродании 470 или 530 0,004—0,04 или 0,1—2,0 0,05 н. (к-та) Pd2 + , Aulll, Hg2-, Cu2 +
Дитизон 460 0,2—2,0 0,5—1 н. (к-та); экстр. СС1, или СНС1з Pd2-, Aulll, Hg2 +
А13 + Ализарин S 485 0,1-1,2 pH =4,5 Be2 + , Bl3*, Cu2 + , Fe3 + , MoVI, Vv, WVI
Алюминон 525 0,04—0,4 pH = 4,7; 5,5 Ag+, Be2 + , Cr3 + , Cu2 + , Pb2 + , Sc3 + , Sn2+, Th4+, Ti4 + , Vv. ZrIV Be2+, Vv, Zrlv
Эриохромиианин 535 0,04—0,4 рН = 4-г6
As3 + (NH4)2MoO4 + SnCl2 660—725 840 0—0.8 0,3—3 0,1—0,5 н. H2SO4 PO’". SiO2", Ba21 , GeIV, Pb2+, Sb3+, Sn2+
Zn, Al, Na(Hg) Метод ст. серий > 0,0002 Sb3+
КОЛОРИМЕТРИЧЕСКОЕ И СПЕКТРОФОТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ
Продолжение
444
Определяемый ион или элемент Реактив Область X измерения светопоглощения, ммк Интервал концентраций, в котором выполняется закон Бера, мкг! мл Условия образования колориметрируемого соединения Главные мешающие компоненты
АиШ во- Ва2+ Ве2+ В13+ п-Диэтиламинобензили-денроданин Родамин С о-Толидин SnCl2 . Ацетилхинализарин KJ + JO +маннит Кармин Куркумин Хинализарин KsCrOi Алюминон Бериллон II Куркумин 4- (п-Нитрофенилазо-) -орцин Хинализарин Эриохромцианин R KJ+1% аскорбиновая кислота 500 545 437 400—530 620 410 610 540 620 410 506 535 600 Метод ст. серий 515 650 512 465 0,1—1,5 0,3—3 0,04—0,4 0,4—4,0 0,15—10,0 >0,2 0,2—3,2 0,01—0,1 0,1—0,8 >0,1 0,02—4,0 0,04—0,45 1—8 0,1—10,0 0,04—0,4 2—25 0,1 и. НС1 Экстр, изопроп. эф. 0,5 М H2SO4 . - . 0,1—0,5 н. (к-та) 10—12 и. H2SO4 рН>7 Конц. H2SO4 96% H2SO4 pH=5,0 pH = 5,0 pH=7,6 рН=124- 13,2 рН>10 0,1 М NaOH, ЭДТА рН>10,0 рН=9,8 0,75—1,25 М H2SO4 Pd2+, PtIV, Ag+, Hg2+, Fe3+’ Cu2+, Pb2 + OsO4, Rulv, Vv, галогены PtIV, Pd2+, RuIV, Telv, SeIV, x Ag+, Hg2\ WV1 g NH+, R2O3, CO2" 1 Многие элементы m X Pb2+, Sr2+, Hg2+, Ag+, Bi3 + , T T1+ x Al3+, Ca2+, Cu2+, Fe2+, Mn2+, g Pb2+ я Ca2+. Mg2+, Al3+, Fe3+, _ Cu2+, Ni2+, Co2+. Mn2+, я Cr3+ 5 Многие элементы 0 Ca2+. Cu2+, Fe2+, Mg2+, g Ni2+, Zn2+ £ Co2+, Fe2+, Mg2+. Ni2+, Sc3+, 3 Ti4+, Zrlv н Sb3+, Fe3+, As3+, Cu2+, PtIV, £ Pd2+. Sn2+, Pb2+, T1+, O2. J
- . . %' - . «и» "
/ KSCN + SnCb 450—470 >0,1 1—3,5 и. (к-та) Fe3+, Wvl, Cu2+, MoVI, СГ, 0
J Дитизон 505 >1.0 pH = 8,5 4-9,0 Br , J Pb2 + 3 Q ГП
1 Тиомочевина 450—470 5—25,0 0,4—1.2 н. HNO-. OsVHl, RulV, Fe3+, Sb3 + , m
Ca2+ (NFL^sCsO^ Ce(SO4)2, 400—410 >2,0 pH >4,5 Ag + , Hg2+, Pb2+, Cu2 + , Cd2+, Sn2+ Na+, Mg2" , SO2- ia rt a X
KJ (NH4)2C2O4, Na3PO4, 680—700 >20,0 pH <4,0 <x>
(NH4)2MoO4 Мурексид 506 0,1—1,2 рН= 11.3 Ba2+> Fe3+, HfIV, Hg2T, Li+ , 3 X
Cd2+ Дитизон 518 0,1—1,3 рН=4-=-12; экстр. СС14 Mg2+, Sr2+, Zrlv, SOJ- Hg2+, Tl3+ О co
Ce4+ Кадион (NH4)2S2O8 + AgNO3 560 400 0,05—0,5 >0,5 1—2 н. H2SO4 Ag+, Co2+, Cu2+, Fe3+, Hg2+, Mg2+, Ni2+, Sn2+, CN” Cr3+, Mn2+, СГ, F“, PO3-
Co2+ Бруцин Лимонная кислота, Н2О2 8-Оксихинолин NH4SCN 400—430 Метод ст. серий 505 620 > 10,0 >2,5 2—20 5—50 1 и. H2SO4 pH = 5,5 4-7,5 рН=9,9 +10,5 рН=1; экстр, амил. Mn2+, CrVI, Fe3+, S2O2~ Многие элементы Vv, F- Fe3+, Vv
Corn Диметилглиоксим KSCN (ацетон) K3[Fe(CN)6]+NH4OH Комплексон III Комплексон 111 + -РКзСггО? 2-Нитрозо-1-нафтол 2, 2', 2"-Трипиридил Комплексон III Метод ст. серий 600—620 Колор. титр. 510 558 530 482; 505 540 >0,15 250—3750 10—80 0,2—4 0,5—25 1,0—11,0 сп. 4-эф. (3:1) pH = 7,0 pH=6,5+ 7,0 pH >8,0 рН=4,9 + 5,7 рН = 1,2 + 2,0 рН = 3 + 4; экстр. СНС13 pH=2,0-= 10,0 pH = 7,0 4-8,0 Fe3+, Cu2+, Cr3+. Ni2+, Bi3+ so2- Sn2+, Mn?r, Fe3" Fe2+, Pd2+, Sn2+ Cr3+, Fe3+, Vv Cu2+, Fe3+, Cr3 +
£ Нитрозо-К-соль 425 0,1—5,0 pH=5,0 4-6,5 N12t, Fe3 + , Cu2", Vv, WVI, MoVI
Продолжение
О — Опреде-ляемый ион или эле- мент Реактив Область X, измерения светопогло-щения, ммк Интервал концентраций, в котором выполняется Закон Бера, мкг]мл Условия образования колориметрируемого соединения Главные мешающие компоненты
Сг3+ CrVi Cu2+ F" Комплексон III (NH4)2S2O8-FAgNO3; H2O2 Дифеиилкарбазид Комплексон III + CoSO4 NH4OH Дибензилдитиокарбамат цинка 2,9-Диметил-1, 10-фе-нантролин (неокуп-роин) 2,9-Диметил-4,7-дифе-нил-1, 10-фенантро-лин (батокупроин) Дитизон 2,2'-Дихинолин (ку-проин) Диэтилдитиокарбамат натрия Нитрилтриуксусная кислота (комплексон I) Комплексон III Пиридин+ NH4SCN Th-ализариновый лак Zr-ализариновый лак 550 400—410 540 558 400—470; 580 670—680 435 454 479 545 545 440 690—710 700—750 700—750 650 525 525 «<>;*' 0 «WsnWW 1—80 1,0—10,0 0,01—2,6 5—30 <26; 8—40 >4,0 0,5—4 1—10 0,3—5,0 0,01—1,0 0,5—4 0,1—5,0 40—7000 35—3600 80—8000 >1,0 0,05—1 0,05—1,2 pH = 3,0 4-5,0 рН>12 0,2—2,0 н. H2SO4 рН = 1,2 4-2,0 рН>8 3,5 и. р-р NH3 I М HC1 рН = 34-9; экстр, пропил. или изоамил. сп. pH = 5-4-7; экстр, пропил. СП. рН = 2-е-3; экстр. СС14 pH = 4,4 4-7,5; экстр, амил. сп. pH = 9,0 4- 9,2; экстр. СС14 pH=4,0 4-5,0 pH =4,75-=-6,50 pH —10,0 Экстр. СС14, СНС1з 0,6—1 М H2SO4 Vv, UV1, Mn2+, CeIV, Cu2+ MoVI, Hg2+. Fe3+, Vv Sniv, Mn2+, Fe3+ Ni2+, Co2-, Fe2+, Al3+, Mn2-, Pb2+, Sn2+, Bi3+, Hg2+ Ag+, Bi3+, Co2-, Fe3+, Hg2-Ni2+, Sb3+ Ag+, AuHi, Bi3+, Fe3+, Hg2T, Pd2 + Fe3+, Ni2+, Co2+. Bi3+, UVI. Mn2+ Fe3+, Ni2+, Co2-, Zn2- Fe3+, Al3+, PO3" SQ.2 ~ .1 1
Fe2+ Fe3+ Ga3+ Oeiv Hg2- £ 1 Диметилглиокснм 2, Я'-Дипиркдил 1, 10-Фенантролин 2,2', 2"-Трипиридил 4, 7-Дифенил-1, 10-фе-нантролин (батофе-нантролин) Комплексон III + H2O2 KSCN KSCN + ацетон Салицилальдсксим Салициловая кислота Сульфосалициловая кислота 2,4, 6-Трипиридил-5-триазии Феррои Родамин С Хинализарин (NH4)2MoO4 Фенилфлуорон Дитизон Дифенилкарбазон 500—600 552 510 552 535 530 480—530 480—530 480 520 450—500 424 595 610 530; 565 Метод ст. серий 650—700 490—510 490; 625 Метод ст. серий >2,0 0,01—1,5 0,5—5 0,5—5 0,2—2,5 0—70 0,05—10,0 0.05—0,3 >0,01 >0,03 >0,04 0—5,4 0,2—2,5 > 0,015 0,1—1,0 >0,02 0,02—1,0 0,1—3,0 >0,1 pH = 3,0 4-9,0 pH = 2,0 4-9,0 pH = 3,0 4-10.0 pH = 4 4-5; экстр, изо-амил. сп. pH =9,0 4- 10,0 0,05—1 н. HNO3 0,05—1 и. HNO3 рН=6,24-6,6 рН = 2,54-2,7 pH = 4,5 4-7,0 рН = 8,54-Н,5 pH = 3,5 4-5,8 pH = 2,74-3,1 6М НС1; экстр, бзл.+ + эф. pH=5,0 pH <1,0; отгонка 0,6—1,8 и. НС1 рН= 1Д4-1,5; экстр. СНС13 или СС14 pH = 5 4-7; экстр, сп. Al3+, Mg2-, Zn2+ Ag-, Bi3’ , Cd-T, Zn2-, Be2’ MoVI, WVI, Cu2-, Sn2+ Ag-, Bi3-, Hg2+, MoVI, Ni2-WVI Co2t, Cu2t, Ni2T. WVI CN~ Ag+, Bi3+, Cu2+, Sn2+, Hg24 MoVI, TiIV, UVI, cr, r PO3' Ag+, Bi3-, Hg+, Ti4+, UV1, MoVI, Cu3-, Sn2+, СГ, F~, PO43~ Многие элементы To же Cu2-, Ni2-, Co2-, Cr3+, Cu2—, Ni2-, Co2- Ag+, Bi3-, Co2-, Cr3+, Cu2+. Hg'-, MoVI, Ni2+, CN' Sb3 + , Au3+, Fe3+, Tl3+, WVI Многие элементы Sb3+, Sn4+, As3+, POJ-, Ce4+, MoVI, Nbv Ag+, Cu2'*’, Pd2+, PtIV, Au111, Bi3+, CF , Br' Многие элементы
КОЛОРИМЕТРИЧЕСКОЕ И СПЕКТРОФОТОМЕТРИЧЕСКИМИ ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ
со Продолжение
Определяемый ион или элемент Реактив Область X измерения светопоглощен ия, ммк Интервал концентраций, в котором выполняется закон Бера, мкг] мл Условия образования колориметрируемого соединения Главные мешающие компоненты
1п3 + К4 Li4 Mg24 Mg2+ Mniii Mnvn Movi 5, 7-Дибром-8-оксихи-нолин 8-Оксихинолин Родамин 6Ж Дипикриламин + LisCOs Дипикриламинат магния HJPtClJ Торон FeCh+NaJO, 8-Оксихинолин + FeCh Титановый желтый Хинализарин Хромоген черный ЕТ-00 Комплексон III KJO4 (NH4)2S2O8+AgNO3 4-Метил-1, 2-димеркап-тобензол (дитиол) Морин 415 400 530 450 400—410 410 460—500 480—530 650 535 600 520 500 525 500—550 670 Метод 0,2—20 0,1—20,0 >0,03 0,2—1 0,2—1,0 >0,8 < 10,0 0,2—2,5 > 1,0 0,1—1,5 0,2—1,4 1—10 0,04—31 0,16—150 0,05—1 >0,05 pH = 3,5 4-4,5 pH=3.2 4-4,5; экстр. СНС1з 12—13 и. H2SO4; экстр, бзл. рН>8,0; экстр, ац. pH <5,0 1 % по КОН 0,05 и. НС1 рН = 9,54-12,7; экстр, дихлорэтаном или СС14 рН>12; (крахмал или желатина) pH >10,0 рН=84- Ю H2SO4+H3PO4 2—3,5 н. H2SO4+H3PO4 I,5MH2SO4 0,1—0,5 и. НС1; экстп. Al3+, Ga3+, Fe3+, Sn]v, Bi3+, Cu2+, Tl3+, Vv, MoVI, Ni2+ Fe3+, Cu2+, Sn24, Sb34, Tl3+, AulU, Hg24 Ba2 4 g Rb4, Cs4, T1+, NH4, Ba24 , § po2- S Na4, NH4 m Ca24, Mg2+ J Ca24, Mg24, Na+ x Fe3+, Ti4+, F" " X о m Al34, Cd24, Co24, Ni24, Zn24, s Sn24, Cu2+, As34, Hg24, „ NH4, Ca24, Ba2+, Sr2+ Й Be2+> P. 3., ZrIV, Th4+, Oa3 + , -J Bln ° Al34, Ca24, Co24, Fe24, c Mn2+, Ni24 о Sn2+, Mn24, Fe24, Cr34 3 Cu24, Ni24, Co24, Cr34, Ce44 " Fe31', CrVi, восстановители 5 X m vv R
-I- > 1 сч 1 эт " + 4- 1 » е х о о « о - 2 Z Z Z X Z О с- S О, £ 29 Зак. 783 449 KSCN + SnCI2 Na,HPOa + (NH4)2Fe(SO4)2 Zn(UO2) (СН3СОО)4 Пирогаллол KSCN + SnCIa K2HgJ4+KOH Диметилглиоксим + + (NH4)2S2O8(J2) Комплексон III а-Нафтиламин, сульфаниловая кислота Сульфаниловая кислота, фенол Дисульфофеноловая кислота Т иомочевина Дитизон Тетраметилдиаминодн-фенилметан Рубеановодородная кислота НВг (40%-ный р-р) п-Нитрозодифениламин п-Нитрозодиметилани- лин (NH4)2MoO4+Na2SO3 (NH4)2AAoO4 + SnCI2 (NH4) 2МоО4 + метол (NH4)2MoO4 + NH4VO3 KJ 465 670 450—525 Метод ст. серий 413 Метод ст. серий 520—540 580—720 Метод ст. серий То же » » 450—530 510—530 570—600 Метод ст. серий 505 525 525 640—680 650—770 650—700 400—470 485 0,1—5,0 <500 >1,0 >0,3 >0,1 >0,01 0,1—1,2 0,4—50 >0,02 >0,01 >0,1 0—3,0; 8—40 0,05—0,4 >0,2 0,06—10,0 40—200 0,01—0,1 0,2—1,0 >0,2 >0,2 1—50 0,05—20 >0,5 1—1,5 н. НС1 pH = 5,2 pH «7,0 pH = 6,0 4-8,0 2—3 и. НС1 рН> 3,0 pH = 5,55 4-6,82 4 н. HCI; 0,6 и. H2SO4 pH = 8 4- 10; экстр. СС14; рН = 8,5-~ 11; экстр.СНС13 рН>8 pH = 1,2 0,5—1,0 н. (к-та) 0,85 и. HNO3 pH «5,0 0,5-1,3 и. HNO3 pH <5,0 CrVI, Vv. Rcvn,Ti4+, UVI, WVI о K4, Li4, PO4. C2O2~ g Ti44 5 Mov, WVI, Fe3+, PO43", F“, ” SO2-, AsO3", C2O2~ S Многие элементы 3 Fe3+, Al3+, Mg2+, Co2+, о Cu2+, Mn2+ “ J-, Br-, Fe3+, Pb2+ cr Ruiv, Pd2+ Sn2+, Bi3+, PtIV, Pd2+, Au111, Ag+, Hg2+, Zn2+, Cd2+ cr, РОГ 4 Fe3+, Cu2+, Zn2+, Ni2+, Co2+, Mn2+, Cd2+, Cr3+ Ptlv, Au111, Ag+, CN-, J- Wvl, Vv, SiIV и др. WVI, Vv, Silv и др. WV1, Vv, Siiv и др. Cu2+, Cr3+, СГ, SO2- Pd2+, Аиш, Fe3+, Cu2+, Bi3+, Rhlv
Продолжение
Определяемый ион или элемент Реактив Область X измерения светопогло-щения, ммк Интервал концентраций, в котором выполняется закон Бера, мкг]мл Условия образования колориметриру емого соединения Главные мешающие компоненты
PtIV SnCls 410—420 0,1—2,0 1 и. НС1 Pd2+, Ruiv, Cu2+
Revu 2,4-Дифенилтиосеми- 510 0,2—2 Экстр. СНС13
карбазид KSCN + SnCl2 430—480 1,0—4,0 2% НС1; экстр, бутил. Movl, Cr3+, PtIV, RhIV, WVI
Метиловый фиолетовый 530 0,001—0,1 СП- pH = 3,5 4-5,0; экстр. MoVI, Wvl, Tav, Nbv, NO“,
ТОЛ. C1O4-, CIO7, HCOO“, SCN-, J", Br“
N a2T eO4 + SnCls 410 0,001—0,1 Солянокислый р-р MoVI
Тиомочевина 400 >0,8 2,5 н. НС1
RhIV SnCI2 420—500 0,1—1,5 2 н. НС1 lrIV, RhIV, PtIV, OsIV, Pd2+
Ruiv Дитиооксамид Тиомочевина 650 620 2—15 0,1—4 н. НС1 Ir”, OsIV, RhIV Co2+, Cr3+, Osiv, Pd2+
660—700 0,08—2,0 Osiv, Fe2+
Sb111 1, 10-Фенантролин KJ+пиридин 448 Метод 0,3—1,6 >1,0 7 и. H2SO4 Hg2+, Ag+, Sn2+, As3+, Fe3+.
ст. серий Bi3+, pb2+, C1
KJ + NaH2PO2 400—470 0,02—5,0 1 и. H2SO4 Bi3+, окислители
Н3РО4 • Н2МоО4 + H2SO3 Метиловый фиолетовый 650—700 >1,0 0,3—0,4 н. (к-та) Sn2+, Cu+, Fe2+
Sbv 530; 615 0,1—2,0; НС1 (1:8), экстр, тол. Tl, Cu2 +
2,5—15 или бзл.
Родамин С 565 0,1—0,6 2—5 н. (к-та) AuHI, CrVl, Fe3+, Ga3+,
Hg2+, T13+ wvi
SeVi 3, 3'-Диаминобензидин 420 1—10 рН = 6-=-7 Cu2+, Fe2+, Vv
Seiv СОЛЯНОКИСЛЫЙ SnCl2+ желатина 410 0,02—0,2 Солянокислый р-р As3+, Pb2+, Cu2+, Zn2+, Fe3+, Hg2+, MoVI
Sc3+ Ализариновый красный 520 0.3—4
SUV 8-Оксихинолип (NH4)2Mo04 378—400 595 1—4 0,5—50 рН= 104-10,4; экстр, бзл. 1.6—3,2 и. H2SO4 F~, PO3-, AsO3-, Vv
to CD * Snll Дитиол 2, 3,7-Тригидрокси-9-и-нитрофенил-6-флуо-рон (нитрофенилфлу-орон) Н3РО4 Н2МоО4 ' 530 510 640—680 2—16 0,4—1,6 >0,5 pH <4.0 pH =1,8 Экстр, амил. сп. Bi3 + , Cu2+, Ni2+, Co2+, Ag+, Hg2+, Cd2+, As3+, F~. PO2-, NO" Fe3+, Ga3+, Geiv, TaV, Zrlv Ti4+, Cu2+, SiO2“
Sr2+ Мурексид о-Крезолфталеинкомп-лексоп 525 575 0—10 0—2,8
Tav Диметилфлуорон Арсеназо I Метиловый фиолетовый Пирогаллол 530 570 570 Метод ст. серий 0,4—2,5 0,5—10 >0,05 40,0 рН<7 1—2 н. НС1 0,3 и. HF; экстр, бзл. рН=0,54-2,0 Nbv
TeVi SnCl2+ желатина 410 0.04—0,08 Солянокислый р-р
ThIV Арсеназо III Кверцетин Морин Торон, натриевая соль 665 422 410 545 0,06—0,7 0,6—6 0,1—1 2—15 4—10 н. НС1 pH = 2,7 4-3,5 рН = 2 рН = 0,3-4-1 ZrIV, UIV Al3+, Cr3+, Fe3+, Ni2+, UVI UVI, ZrIV, F~, PO3-
TilV Н2О2 Сульфосалициловая кислота Тирон Хромотроповая кислота 400—470 445 410 410 0,3—48 0,2—20 0,3—3 0,03—0,3 1,5—3,5 н. H2SO4 рН=3-=-5 pH=4,3 4-9,6 рН=2.54-3,0 Vv, Celv, MoVI, Fes+, WVI, Cu2+, Ni2+, Co2+, Cr3+, F~, PO2- Cr3+, Cu2+, Movl, Vv, WV1 Cr3+, Fe3+, Vv, Co2+, Cu2+, ni2+, f-
$ »—» Tl1 Тионалид Метод ст. серий >0,5 pH = 7,0
КОЛОРИМЕТРИЧЕСКОЕ И СПЕКТРОФОТОМЕТРИЧЕСКОЕ» ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ
Продолжение
Определяемый ион или элемент Реактив Область X измерения светопогло-щения, ммк Интервал концентраций, в котором выполняется закон Бера, мкг!мл Условия образования колориметрируемого соединения Главные мешающие компоненты
Tjin Бриллиантовый зеленый 630 0,05—4,0 0,08—0,16 н. НС1 Sb3+, Hg2+, An'»Sn2\ WVI, CrVI, C1O4~
KJ Кристаллический фиолетовый Метиловый фиолетовый Родамин С 600 530 530 565 >0,5 >0,2 0,03—1,3 Экстр, дитизоном 0,15—0,29 н. НС1; экстр. ТОЛ. 0,2—0,3 н. (к-та); экстр, тол. 2 н. НС1; экстр, бзл. Sb111, Hg2+, Au111 Aulll, Fe3+
uVI Арсеназо Дибензоилметан Диэтилдитиокарбамат натрия 2,2'-Дипиридил+Реш Н2О2 8-Оксихинолин 1- (2-Пиридилазо) -2-нафтол Сульфосалицилат натрия 650 405—416 496 570 400; 450 425—500 560 465 0—200 2—9 0,4—20 20—200; >0,5 <80 0,1—110 <10 pH=4,5 -4-5,0 pH = 7,0 pH = 7,0 рН = 34-9 pH «7,0 pH = 4,59,0 рН = 0-4-1,0; экстр. 9% р-ром трибутилфосфата в СНС13 рН = 4,4 Fe3+, Al3+, Cu2+, Ti4+, ZrIV, Th4+ AP+, Cd2+, Ca2+, Co2+, Cr34, Cu2+, Fe3+, Mg2+, Mn2+, Ni2+, wVI, Pb2 \ ZrIV, Th4+. SnIV, Ti4+, Vv, Zn2+ Fe3+, Cu2+, Mn2h, Ti4+, Vv CrVI, MoVI, Vv, CeIV, PO3~, F~ Fe34, Cu-’4
vIV Пирокатехин 2, 2'-Дипиридил + Ре1П 600 530 0,4—8 0—1,5 pH «5,0 pH = 3,0 ч-5,0 Fe2+, Ti4+, Mn2+, UVI, WVI
Vv Н2О2 530 460 >0,4 20—150 0,5—6 и. H2SO4 0,3—3 Al H2SO4 Ti4+, Fe3+, Cr3+, F> Br" MoVI, Ti4+, WVI
КОЛОРИМЕТРИЧЕСКОЕ И СПЕКТРОФОТОМЕТРИЧЕСКОЕ
Wvi Zn24 Zriv 1 ThPo7+Na2WO4 Гидрохинон Дитиол+5пС12 KSCN + SnCl2 Дитизон Цинкои Ализаринсульфонат на- 400—470 478 600 410—420 520—540; 620 620 530—560 2,5—20 1—25 1—4 0,2—4,0 0,1—1,0 0,1—2,4 0,1—4,0 0.03 и НС1. 0,1 AI Н;)РО4, 0,006 М Na2WO4 Конц. H2SO4 4,5 и. H2SO4 или 3,2 и. НС1 pH=6Д 4-10,0 рН=8,5ч-9,5 2 и. НС1 CrVi Cr3;, Fe3’, Movl. Rulv,Ti4' , Vv Mo vi MoVI, Asv, Sbv Sn2+, Bi3+, PtIV, Pd2+, Au111, Ag+, Hg2+, Iriv, Pb24, Cd24 Al34, Be24, Bi34, Cd24, Co24, Cu24, Fe34, Mn2+, Movi, Ni2+, Tl4+ Многие элементы 3 m m □: s m Q) ^3 m 5 n a о
трия Арсеназо I Арсеназо III Гематоксилин Кверцетин 550—572 650 580 440 0,2—5,0 0,1—6,0 0,2—2 рН=1,54- 1,8 2 и. НС1 0,12 М НС1 0,5 М НС1 Fe3+> HfIV, MoVI, SnIV, Th4+ , Ti4+, uVI UVI, Th4+, Cr34, PO3~, F- Fe3+, Ti4+, F-, POf- Cr3+, Fe3+, Oa3+, HfIV, MoVI, Nbv, Sc3+, Sb3+, Sn2+, Tav, ThIV, Ti4+, WVI, F“, PO3“
Метилтимоловый синий Морин п- Диметиламиноазофениларсоновая к-та Пирокатехиновый фиолетовый Фенилфлуорон 580 436 410—430 625 535 >0,2 0—5 >0,1 0,1—1,4 >0,3 0,2—1 и. НС1 0,4—0,7 и. НС1 pH=8,0 pH=5,6; ЭДТА 0,4—0,5 и. НС1 Bl3+, Sn2+, Ti4+, Fe3+ Fe34, Cr34, Ni2+, Co2+ WVI, MoVI, Ti4+, Tav, Nbv Th4 h, UVI, F“, POJ- Tav, Nbv, SnIV, Sb3+, Ti4+, F", po;-
5 Хлораниловая кислота Торон 525 555 2-10-б—5-10“5Л1 2А1 НС1О4 1,5—2% р-р НС1 Hfiv, uVI, Th4+, SnIV Fe3+, SnIV, Cr3+, SO2~ 4
ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ МЕТОДОМ УЛЬТРАФИОЛЕТОВОЙ СПЕКТРОФОТОМЕТРИИ
Приведенные характеристики позволяют выбрать метод определения элемента, наиболее подходящий для конкретных условий выполнения анализа.
Отсутствие в графе «Реагент» реактива означает, что в данном случае производят измерение собственного поглощения соответствующего растворимого соединения определяемого элемента. Часто в графе «Главные мешающие элементы» при-
ведена валентность элемента. Это означает, что мешающее влияние элемент оказывает при одной определенной валентности: Cr^I, V^, Се V* и т. д.
Более подробные сведения см.: К. П. Столяров, Спектрофотометрическое определение неорганических ионов в ультрафиолетовой области спектра, изд. ЛДНТП. 1963.
Принятые сокращения см. стр. 16.
Определяемый Область Интервал концентраций, Условия образования
ион или Реагент светопогло- в котором выполняется (выделения) спектрофотометрируемого Главные мешающие элементы
эле- закон Бера, соединения
мент мкг[мл
А13+ 8-Оксихинолин 390 2—120 pH=5,0 ч-9,5; экстр. СНС13
Феррон 370 0—1,6 pH=5,0 CrVi, Cu2+, Movi, Ni2+,
Th4+, Zn2+
AsV Na2MoO4 370 0—600 2 М НС1; экстр, бутил. CrVI, Fe3+, PO3", JO;
Аиш НВг 380—390 0,25—40 2А1 НВг; экстр, диизо- Pd2+, PtIV
пропиловым эфиром
НС1 311,5 4—30 0,1 и. НС1
во; Хромотроповая кисло- 361,5 0,1—2,4 рН=6,5-е-7 SiIV
Ва2+ ЮСгО, 250 0—1,6 HCI (1 : 10)
Ве2 + Ацетилацетон 295 >0,25
8-Оксихинолин 320—370 0—60 pH = 9,2; экстр, метил-
изобутилкетоном
Bi3 + НС1 327 3—12 6М НС1 Cu2+, Fe3+
НВг 365 0,2—6 1 —1.5А4 НВг Fe3+, Sb3+
КВг 365 0,2—6 <0,2 и. HCI Fe3+, Sb3+
КВг 375 0—12 6 М НВг + аскорбиио- Fe3+, Pb2+, Sn2+. Sb34
вая к-та
КВг 256 0—5 6М НВг Fe3+, Pb2+, Sn2+, Sb3+ Cu2t. Fe3+. Нг2+. Sb3+.
П иэтил питипкяпбамат ЗбО-^ЗТО- пНедЯ.5 J.II: кт>мгтлёк-Ч
1 Комплексон Ш 263,5 2—25 pH = 0,8 -у 1,2 Fe3+, Cu2+
1 нею. 222 2,5—12,5 1 и. НСЮ4
KJ 337 3—30 0,2—0,4 и. H2SO4
Тиомочевина 322 3—30 0,2—0,4 и. H2SO4
Са2+ Нафта лги дроксамат 339 0—7 0,1 М комплексон III Sr2+
натрия Fe3+, Zn2+
Cd2+ 1, 10-фенантролин 241 <9 pH=5,5 4-6,9
Се3+ NagCOs 304 0—30 рН= 10,1 4-10,5 UVI, Cr3+, Vv, [Fe (CN)]’-
Na4P2O7 305 13—275 рН=8 Gd3+, Fe3+
H2SO4 253,6 0—400 1 и. H2SO4 CeIV, UVI, HfIV, ZrIV, Th44 ,
Cu2+, no;
CeIV Бензидин 315 0,4—5 НС1 Vv, CrVI
H2SO4 365 0,7—10 1—2 и. H2SO4 cr, PO3-. no; ’ 4 0
H2SO4 315 6—19 1 н. H2SO4; предварительное осаждение в виде соли йодноватой к-ты Fe’+, P. 3., Vv, CrVI
Фермальдоксим 400 0—25 0,1 и. NaOH Gd3+, Fe34
Na4P2O7 278 2,7—22 рН=8
Ма2СОз 305 2—25 рН=11-=- 12 UVI, Cu2+, Fe3+, Vv, Mnvi
Na2MoO4 380 1—16 0,2 и. H2SO4
Со2+ N, '-Этиленди- (4-мет- 381 0,02—20 pH =14-7; экстр. CHCI3
окси-1,2-бензохино- I-okchm-2-имин) 0,02—25
Нитрозокрезол 360 Экстр. петролейным
260 эфиром
Na2CO3 ....... рН=10; Н2О2
1 -Нитрозо-2-нафтол 365 >0,05 рН = 8 Cu2+, Fe2+
317 0,2—10 pH = 4,0 4-5,5
KSCN (или NH4SCN) 312 0,2—10 pH = 3,0 4-5,3; экстр. Fe3+, UV1, Cr3+, Snlv, цит-
изоамил. сп. рат-ион
Пиридин + KSCN 335 4—15 рН=б4-7; экстр. CHClg
Диэтилдитиокарбамат 367 2—25 Экстр. СС14 Bi3+, CN
СоШ Диэтилдитиокарбамат 365 0—6 Экстр. СС14
натрия
IVтЬТРАФИОЛ ЕТОВОИ СПЕКТРОФОТОМЕТРИИ
УЛЬИ"
Д-Сп СП Продолжение
Определяемый ион или элемент Реагент Область измерения светопогло щеиия, ммк Интервал концентраций, в котором выполняется закон Бера, мкг! мл Условия образования (выделения) спектрофотометрируемого соединения Главные мешающие элементы
Crvi Cu+ Cu2+ Fe2+ Fe3+ Ga3+ Hg2+ NH3 Пиридин + KSCN 1, 3-Диметил-4-имино-5-оксииминоаллоксан 3-Ацетил-4-оксикумарин СНзСООН НС1 НС1 НС1 H2SO4 H2SO4 Аскорбиновая кислота НС1О4 Винная кислота НС1О4 Адипиновая кислота НС1 Комплексон III Пиридин + KSCN KSCN Родамин С KSCN 365—380 365 270 405 382 400 337,5 357 365 342,5 320 313 365 270 250—400 255 360 340 260 375 365 365 281 0—20 0,5—20 1,3—38 3—10 1—13 1,3—5,5 4—10 0,1—0,5 0,6—20 0,5—30 0,006—0,2 0,12—15 <28 50—70 0—40 2,5—12,5 0,02—1,5 0—40 0,006—17 6—20 0,2—7 0,05—1,0 0—15 1 н. НС1; экстр, метил-изобутилкетоном NH4OH (1 : 1) pH =13,5 рН = 5ч-7; экстр. СНС13 pH = 7 4-9,5 50%-ный сп. 50 %-ная СНзСООН 6М HCI рН=0-=-1 6М НС1 10 мл конц. H2SO4 на 100 мл р-ра > 0,2 и. H2SO4 6 н. НС1; экстр, эф. pH = 2,53,5 рН = 2,54-4,8; 8,04-10.9 1 н. НС1О4 2 н. НС1 ЗМ HCI 0,1 М HCI рН=5-=-7; экстр. СНС13 HNO3 (до 2 и.) 6 М НС1; экстр, эф. Со2+, Pd2+, Ni2+, Fe2+ Cu2+, MoVI, WVI, цитрат-ион Cu2+, Sb, Vv, Ti4+ Bi3+, Cu2+, Vv, NO“ NO" Cr3+ Cu2+, Ti4+,Cr, NO", SO2" PO3- Vv, Cu2+, Ti4+, Bi3+ Cu2+, Hg2+, Ti4’, NO3- Cu2+ qVI yV Cu2+ Q,2 + . F,.3 + ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ MET J
35 •ж
ir'v к' Mg-'1 Mn2 + MoV MoVI NO" no2~ Nbv Ni2" 1 Комплексон III i Na[B(C6H5)4| j 8 Okciixhiio.tiiii 8-Оксихинолин Пиридин-)-KSCN Тиогликолевая кислота Тиояблочная кислота Н2О2 KSCN Унитиол Тиогликолевая кислота Тиояблочная кислота Сульфаниловая кислота и-Хлорфенилендиамин Н2О2 KSCN Аскорбиновая кислота НС1 а-Бензилдиоксим Диэтилдитиокарбамат натрия НСЮ4 Н3РО4 313 274 388 357 300 352,5 352,5 ,330 320 335 365 365 302,5 302 210—220 270 355 320—400 342 385 345 281 275 328 395 395 5—60 50—750 < 1,0 0—60 20—60 1—40 1—40 0—150 1—6 1—40 1—40 0—120 000 0—15 000 1—10 0,06—1 0—4000 0—125 0,04—2,6 0,5—40 0—10 0—1,0 2—25 рН=11,4-{- 12.6 Н2О + ацетонитрил pH 11.0-^-11,5; экс гр. СНС13 рН=10,2; экстр, мегил-изобутилкетоном рН = 5н-7; экстр. СНС13 рН = 0,7ч-7 0,5 н. HCI 5—10 мл НС1О4 2 н. H2SO4; экстр, бутил. СП. pH =1,54-2,7 рН = 34-6 рН = 34-6 рН>5 НС1О4 (разб.) рН=1,4 pH <5 рН=54-7 H2SO4+H3PO4 НС1; экстр, эф. НС1 (разб.) 0,01 М HF, 0,12 н. HCI Экстр. СНС13 Экстр. СС14 Конц, р-р Ni(ClO4)2 в НС1О4 HNO3 (1 : 1)+Н3РО4 Металлы Pt-группы, NO3 СГ -н е X о ь о W WVI, Vv, Fe3+, Ti4+ » Fe3+, Ti4+, Vv, Cl" S m X О e CN~, CO2", OH- g - 3 n “O • • • X X Fe3+, MoVI, Ti4+, Vv, WVI, СЮ", СГ, NO", NO“, F~ PtIV, Cu2+, Hg2+, UVI, MoVI, WVI, Vv, Ti4+, Fe3+ TiIV, ’uv,’ UVI,’ MoVI, WVI, Ni2+, Co2+, PO’", F~ Vv, Cr3+, Pb2+, Fe3-t, Cu2+, MoVI, Ti4+
& со Продолжение
Определяемый ион или элемент Реагент Область измерения светопогло-щения, ммк Интервал концентраций, в котором выполняется закон Бера, мкг/мл Условия образования (выделения) спектрофотометрируемого соединения Главные мешающие элементы
Nis+' OsVin РО3" 4 рЬ2 + Pd2+ Р-Меркаптопрспионовая кислота KCN Пир идин + KSCN Na2MoO4 Na2MoO4 Na2MoO4, NH4VO3 Na2MoO4, NH4VO3 Na2MoO4 HCIO4 HBr HCI Феи ил-а- пиридилкето-ксим Нитрилотриуксусная кислота 1 -Нитрозо-2-нафтол SnBr2 330 268 360 282; 289; 297; 304; 312 310 380 400 315 230 208 290—303 270 340 330 370 385 0,5—10 0,2—2,5 40—1500 16—72; 16—76; 20—80; 20—96; 28—132 0—25 0—25 3—20 0,2—3,0 0,05—0,6 0,5—20 1—15 1,5—8 20—220 5—25 pH = 8,5 4-9,5 В токе N2 рН=5-=-7; экстр. CHClg OsO4; экстр. CHCI3 из азотнокислого р-ра Экстр. 20% р-ром бу-ТИЛ. СП. В CHCI3 HNO3 НС1О4 НС1 0,9—1,6 н. НС1О4 1,0 н. НС1О4 4,3 н. НВг 6 и. НС1 pH=6,5-=-7,5 рН= 1,0-=-2,0; экстр, то-луолом 3 н. НВг; экстр, изо-амил, сп. Fe3+ RuVHI, СГ Fe3*, Sitv As3+, OeIV, SiIV, NO" Fe3+, Bi3+, Sb3+, Sn2+ Aulll, CN" Большие количества элементов Pt-группы
KuViri S S2" | C2H5OH 1 Гексан 1 -Нитрозо-2-нафтол 274 276 366 0—40 5—40 0,1—2 40% С2Н5ОН рН=9,2-=-12,5 H2S, SO3”, SCN” Fe3+
so2 H2SO4 220; 278; 290 20—100 Конц. H2SO4 Fe3+
SO3" FeCl3 340 2—200
BaCl2 330 2,5—10 СаС12
Sbin HJ 330 0—4 2,4 н. H2SO4 Bi3+, Pb2+, Hg2+
Тиомочевина 365 0,2—12 3 н. H2SO4
SeVi о-Фенилендиамин 335 <30 рН= 1,5-л-2,5; экстр, толуолом Fe3+, SnIV, J”
1, 2, З-Бензоселенди-азол 330 20—100 рН = 2,4-^2,6; экстр. СНС13
Siiv N а2МоО4 390 0,2—2,8 Экстр. СНСЬ
Sniv Флаванол 390—406 0,5—3 рН=3
НС1 215 0—10 6 М НС1 Asv, GeIV, Fe3+, Vv, Sbv Ti4+, SeVI
Tav Пирокатехин 385—395 <200 (NH4)2C2O4 Ti4+, F”, РО3', тартрат-ион
Пирогаллол 325 <40 4 и. НС1 PtIV, UVI, MoVI, WVI, Sbv
TeVi KJ 335 260 0,2—2 < 1560 0,4 н. HCI 0,6—1 М NH„OH Bl3+, Fe3+, Cu2+, SeVi
Th iv 2,4-Дихлорфеноксиук-сусная кислота 230 2—20 pH=2,4 Fe2+, Ceiv, Zrlv
Tiiv Аскорбиновая кислота 355—360 0,1—25 pH=3,5 ~ 6 Vv, MoVI, РОГ, F"
Салицилгидроксамовая кислота 400 0,2—2,8 7 н. H2SO4 U1V, Vv
Н2О2 330 НСЮ4
TI111 1,2-Диаминоциклогексантетр ауксусная кислота 370 2—40 рН=5-=-7
НС1 240—260 <4 6 М НС1 T1 +
ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ МЕгЛЖлЬТРАФИОЛЕТОВОЙ СПЕКТРОФОТОМЕТРИИ
Продолжение Главные мешающие элементы ОПР ЕДЕЛЕНИЕ ЭЛЕМЕНТОВ МЕТОДОМ УЛЬТРАФИОЛЕТОВОЙ Ж СПЕКТРОФОТОМЕТРИИ К + ч- * • • • »* сч Д . С • ‘и. • • ... • . j" • • > +* • +* м . . -г. "я • > м • • •> я и ;> • И • • + “+ ’ • j. ' +' • ' - 31 • • Тс“о • . . Н Си • шй ® • • • • • £ С . . — . + . * /х. • • • • • I -J- J- CN г . . J s и. - Sv- • •• -с: < : : и >: й’Ш-: :§§ : : X 1 .. < н > , tb N а. о. , . О < . . . X
Условия образования (выделения) спектрофотометрируемого соединения pH = 6,67,0 рН=8-=-11 pH = 6,0 4-7,0; экстр, бутилацетатом Р - • > с» 3 1 pi I—jnvip. илuvn ia-НОМ pH = 4,5 рН~7 рН = 2 НС1, НС1О4 pH = 2,4; экстр. СНС1з 1 н. H2SO4 1 н. NaOH С7ксгр. зтилацегитом pH = 2,4; экстр. СНС13 nU о Л. pi 1—ЭЛСЦ,1. IVICIFIJI-изобутилкетоном HNO3 2M HC1O4
Интервал концентраций, в котором выполняется закон Бера, мкг[мл О* с С о с ® « V J с С с 5 О <5,0 <40 0—125 0—95 0,2—8 0—120 >0,05 0—100 П АП •
Область измерения светопогло- щения, ммк LC С" с а с 3 360—365 .365—375 5 о 300—360 360 290 365 со О О Ю 1Г - N С5 65 а со сч со со с* co c c* O' Ж 1 I
Реагент j i 2 Е плди 1 пипа pviaivi a i натрия Тиогликолевая кислота Ацетилацетон KSCN Трибутилфосфат НоО, Дибензоилметан Na2WO4 Н2О2 8-Оксихииолин KSCN АНИЛИН 8-Оксихинолин 8-Оксихинолин 1 N;>2MoO4. Na3PO4 I ж a - (V-J
Оппеде- И1ГИ нои И1ЧНЭН1Г i х к; х ® S ТИП uVI и > — + > "i Zriv
460
461
Продолжение
Концентра-
Определяемый Реактив Цвет Условия выполнения ционные пределы Главные мешающие
ион или люминесценции реакции применения элементы н ионы
элемент реакции, * мкг/мл
Ве2+ 1, 4-Диоксиантрахинон Желтый рН=11,0 0,1—1,0 Cr3+, Al3+, Mn2+, SiIV, Sn2+
Морин » рН=11,0 0,02—1,6 Li+, Sc3+, CN"
2- (о-Оксифенил) -бен- Голубой Эт. спирт; pH=4,5 0,1—2,0 Al3+, Sb3+, Zn2+ и др.
зотиазол
8-Оксихннальдин Желтый рН=8 0,03—0,3 Bi3+, Cd2+, Cr3+, Co2+, Cu2+, In3+, Fe3+, Ni2+,
Sn2+, Ti4+, Zn2+
Са2-*- Флуоресцеин-комплек- сон Желто-зеленый 0,1 н. NaOH 0,08—0,8 Cd2+, Co24', Fe3+, Mn2+, Ni2+
Cd24 2- (о-Оксифенил) -бензо- Синий pH = 11,0+уксусна я 0,00?—0,05 Al3+, Fe3+, Cu2+, Co2+, Ni2+
ксазол к-та
F А13++морин Гашение 50% эт. спирт; рН=4,9 0,002—0,15 Многие ионы
А13++8-оксихинолин » Экстр. СНС1з из р-ра с 0,01—1,5 To же
pH = 4,7
А13+4-суперхромгранат » pH=4,8 0,02—1,0 Be2+, Co2+, Cr3+, Cu2+, Fe3+, Ni2+, Th4+, ZrIV, Ti4+
А13++эриохромкрас- рН=4,8 0,02—1,0 Be2+, Co2+, Cr3+, Cu2+, Fe3+, Ni2+,Th4+,ZrIV
ный В
Ga3+ 5, 7-Дибромоксихинолнн Желтый Экстр. СНС1з из р-ра с 0,02—0,17 Al3+, Co2+, Cu2+, Fe3+,
pH=2,6 ч- 3,0 GeIV, MoVI, Pb2+ , Ti4+, Vv
Люмогаллион ИРЕА Желто-зеленый Изоамиловый спирт; 0,01—0,1 Al3+, Sn2+, ZrIV, Pd2+,
рН= 1,7 ч-4,0 Cu2+, Fe3+, Vv, MoVI при содержании >
> 0,1—1 мгк
Морин + купферон Зеленый
8-Оксихииальдин 8-Оксихинолин Понтахром синий Родамин 6Ж Родамин С Солохром красный Солохром черный Сульфонафтолазорезорцин Эриохромкрасный В » Желто-зеленый Оранжево-красный Оранжево-желтый Желто-оранжевый Красный » » Желтый
In3+ 8-Оксихинальдин 8-Оксихииолин Родамин ЗВ » Желто-зеленый Желто-оранжевый
Li+ 8-Оксихннолин Желто-зеленый
Sc3+ Морин Зеленый
Sniv Морин 6-Ннтро-2-нафтил-а мин- 8-сульфокислота, аммонийная соль » Г олубой
Snii *- 8-Оксихинолин Желто-зеленый
Экстр. СНСЛз из р-ра 0,17—1,0 Многие ионы
1,25 и. НСЛ
Экстр. СНСЛз из р-ра с 0,02—0,6 Cu2+, 1п3+, Т1+ (а так-
pH = 3,9 же лимонная к-та)
Экстр. СНС13 из р-ра с 0,03—2,0 Cu2+, Fe3+, MoVI, Sb34 ,
pH=2,6 Ti4+, Vv
pH=4,5 0,1—1,0 Co2+, Cu2+, Fe3+, MoVI, Ni2+, Ti4+, Vv
Экстр. СбНз из 6 М НС1 0,02—1,6 Многие ионы
Экстр. СзНб из 6 М НС1 0,02—0,2 Fe3+, Pb2+, IrlV
pH=4,7 0,1—0,4 Многие ионы
Амиловый спирт; рН = 0,3—0,8 To же
=4,7
50% эт. спирт; рН = 0,013—0,13
=3,0 ч-3,5
pH = 3,2; H2SO4 0,02—0,6 Fe3+, T1+, VO", Cr3+, Mn2+
Экстр. СбН6 из р-ра с 0,2—2,0 Co2+, Cu2+, Fe3+, Ni2+
pH=7,5
Экстр. СНС13 из р-ра с 0,1—6,0 Cu2+, Fe3+, MoVI, Sb3+
pH=3,5 ч- 3,7
Экстр. СеН6 из р-ра 0,04—0,4 Многие ионы
2,5 н. НВг
25% эт. спирт; слабо 0,02—0,6 Ca2+, Mg2+, Zn2+, Na+
щелочная
Экстр, этилацетатом из 0,02—0,5 Многие ионы
р-ра с рН~7
0,05 н. НС1 0,05—1,0 Fe3+, MoVI, WV1, F~
рН= 10,5 ч-10,8 0,4—3,0 Многие ионы
Экстр. СНСЛ3 из р-ра с 0,3—5,0 Al3+, Cu2+, Fe3+, GeIV,
рН=2,7ч-5,6 In3+, Zns+
ФЛУОРОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ВЖ ЭЛЕМЕНТОВ (ИОНОВ)
ФЛУОРОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ЭЛЕМЕНТОВ (ИОНОВ)
Продолжение
>
N
464
ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
В таблице приведены рабочие растворы, применяемые для определения кондуктометрическим методом важнейших неорганических веществ (нонов), и указаны условия титрования. В первой графе таблицы приведены определяемые вещества (ноны), во второй — границы значений — lg М (М — концентрация, моль/л), прн которых данное вещество можно определять кондуктометрическим титрованием. В третьей графе указаны рабочие растворы, применяемые для титрования, в четвертой — условия титрования. В последней графе приводится приблизительное значение погрешности данного определения в процентах.
Таблица построена в порядке, отвечающем положению элементов в периодической системе.
Более подробные сведения см.: 1. И. М. Кольтгоф. Г. А. Лайтннен. Определение концентрации водородных нонов и электротитрование, перев. с англ.. ИЛ. 1947. -2. Ю. С. Л я л и к о в, Физико-хнмнческне методы анализа, 3-е изд.. Изд. «Химия», 1964,— 3. К. S ande га, Konduktometrie. Прага, 1957.
Принятые сокращения см. стр. 16.
Определяемое вещество (ион) - 1g -И Рабочий раствор Условия тптрова: Погрешность, отн. %
н+ (кислоты: сильные рК< 2 1—5 NaOH Отсутствие СОг 0,1—1
слабые рК = 1—4 nh4oh То же 0,1—1
= 2ч-6 очень слабые 1—4 LiOH Отсутствие СОг; водо- . 0,5—5
рК<7) он- (основания: сильные 1-5 HCI нераств. к-ты в 75% сп. Отсутствие СОг тигр 0,1-1
слабые 1—4 СНзСООН То же 0,1-1
очень слабые) <3 HCI Отсутствие СОг; водо- >0,5
Н2О2 1—3 KMnO4 нераств. основания титр, в 75% сп. 0,05 М H2SO4 1
I г р у п п а периодической системы
к+ -2,3 Na [В (С0Н5)4] рН=5ч-10 0,5
Си-ч 1-2 Ы2С2О4 Нейтр, р-р 0,1
1—3 Na-ЭДТА рН = 5 (разб. ацетатн. буф.) 0,2
3—5 H,S, водны!! р-р (0,001 Л1) Нейтр. р-р; отсутствие СО2 1—5
30 Зак. 7S3
465
КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемое вещество (ион) — IgAI Рабочий раствор Условия титрования Погрешность, отн. %
Ag+ 1—4 NaCI или LiCl Нейтр. или слабокислый р-р 0,2
1—3 Na2CrO4 или Ы2С2О4 Нейтр. р-р 0,5
II г ру H2S, водный р-р (0,001 М) ппа периодичес Нейтр. р-р; отсутствие СО2 кой системы
Ве2+ 2—4 NaOH Хлориды или нитраты; отсутствие СО2; 80° С. В кислом р-ре два перегиба: 1-й — нейтрализация к-ты; 2-й—осажд. Ве(ОН)2 2—3
Mg2+ 1—2 NaOH рН= 10 (аммиачн. буф.) 1
1—2 Na-ЭДТА То же 0,2
Са2+ 1—2 Na-ЭДТА » » . . • Л
Sr2+ 2 Na-ЭДТА » » 0,2
1—2 Li2C2O4 Нейтр. р-р 1
Ва2+ 1—3 Li2SO4 или Li2CrO4 30% сп.; ожидать несколько минут после каждой порции рабочего р-ра до установления постоянной электропроводности 0,1—1
Zn2+ 2—3 NaOH В кислом р-ре два перегиба: 1-й — нейтрализация к-ты; 2-й — осажд. Zn(OH)2 0,5
2 Na-ЭДТА рН=5 (ацетатн. буф.) 0,2
Cd2+ 1 Li4[Fe(CN)6] (Не меш. РЬ2+) 0,5
1 Na-ЭДТА pH=5 (разб. ацетатн. буф.) 0,2
4-6 H2S, водный p-p (0,001 M) Нейтр. р-р; отсутствие СО2 1—5
Hg2+ 1—2 NaOH Рабочий р-р титр. анал. р-ром (HgCI2) 1
4—6 Ill гр H2S, водный p-p (0,002 M) у п п а периодиче рН=3; отсутствие СО2 с к о й системы 0,5—5
Al3+ 2—3 NaOH В кислом р-ре три перегиба; 1-й нейтрализация к-ты; 2-й — осажд. А1(ОН)3; 3-й — образование А1О“ 1
Т1+ ~2,3 Na2CrO4 Нейтр. р-р 0,2
2 Na [B (C6H6)4] То же 0,5
1—2 KSCN 0,5
466
КОНДУКТОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
. — Определяемое вещество (ион) — 1g Л1 Рабочий раствор Условия титрования Погрешность, ОТН. ?о'
IV группа периодической системы
CN" 1—3 AgNO3 В нейтр. р-ре два перегиба; 1-й — образование [Ag(CN)2]“ 2-й — осажд. AgCN. Положение 1 -го перегиба опр. с большей точностью 0,2
2 Hg (CIO4)2 В нейтр. р-ре два перегиба: 1-й образование [Hg(CN)4)F- (можно в присутствии СВ); 2-й — осажд. Hg(CN)2 0,1
CNO- 1—2 AgNO3 Нейтр. р-р 0,5
СО|- 2—4 HCI При титр, три скачка нейтрализации: 1-й—-ОН-, 2-й — СО|~, 3-й — НСО^~. Положение 3-го перегиба опр. более точно 0,5—1
2—3 BaCl2 Медленное титр. 0,1
SCN- 1—5 AgNO3 Нейтр. или слабокисл, р-р (при титр, очень разб. р-ров добавл. сп. до 90%) 0,2—10
РЬ2+ 1—4 L12C2O4 или K4 [Fe (CN)6[, или Na2CrO4 Нейтр. р-р 0,2
4—6 H2S, водный p-p (0,001 M) Нейтр. р-р; отсутствие СО2 1—5
2 Na-ЭДТА рН = 5 (разб. ацетатн. буф) 0,2
V группа периодической системы
NO- 0,3 Нитрон в СН3СООН Слабокисл, р-р 0,5
РО?“ 4 1—3 ВЮСЮ4 НС1О4 (0,3 М); отсутствие Asv . . .
2—3 Уранилацетат CH3COONa (0,01 М) 0,3
AsO|~ 4—5 Иод, сп. р-р НСО“; гладкий Pt-электрод 3—12
В13+ 4—6 H2S, водный р-р (0,001 М) Нейтр. р-р; отсутствие СО2 1—5
V111 2—3 КМпО4 H2SO4 (разб. р-р) 1
Vv 2 AgNO3 Нейтр. р-р 1
2—2,3 [Со (NH3)6]C13 Нейтр. р-р 1
30*
467
ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ В ВОДНОЙ СРЕДЕ
Данные, приведенные в таблице, дают общую характеристику условий выполнения титрования отдельных соединений. Значительное влияние на вид кривой высокочастотного титрования, его чувствительность и точность, а также на область концентраций определяемого вещества, в которой титрование является возможным, оказывает частота, при которой производят титрование, и электрическая характеристика используемой ячейки.
Более подробные сведения см.: 1. В. И. Ермаков, П. А. Загорец, Вести.-техн, и эконом, информ. НИИТЭХнм, № 2, 36 (1961). -2. В. А. Заринский. Д. И. К о ш к н л,
Д е л а х е й. Новые прн-англ,. ИЛ, 1957. —
G а с i m а п п.
6. К. Crus е, Т i m m 1 с к, . _ _____ ________ 12. № 3. 83
Conductimetric Analysis of Radio Sherrick, Dawe, Karr.
Ж. анал. хим., 13, 289 (1958).- 3. П. боры н методы в электрохимии, перев.
4, К- Crus е, Chimia, 14, 97 (1960). — 5. Т.
I. Н о i g п ё, Helv. chim. acta, 42, 426 (1959).
Chem. " ............
L. L. (1960). Frequency, Лондон, ------- .. ---------. . —
Ewin, Manuel of Chemical Oscillometry. Чикаго, 1954.
Принятые сокращения см. стр. 16.
Rundsehau.
8. G.
11, 441 ' (1958). - 7. Ап.
R. Hooser, Chem. Canada, Blake," 1950. — 9.
fe «Р
Определяемый ион (соединение) Рабочий раствор Область концентраций (количеств) определяемого соединения Относительная ошибка определения, ?ь Примечание
соединение концентрация
Н+ (сильные к-ты) NaOH 0,001—1,0 м 0,0002—0,02 М 0,01—0,5
Н+ (слабые к-ты) NaOH 0,02—1,0 М 0,002—1,0 М 0,1—1,0 У многоосновных к-т конец титр, слабо выражен
Н4 (смесь сильных и слабых к-т) Метилглюкамин (1-дезокси-1-ме-тил-аминосорбит) 0,01 м ~ 5—10 мг ~ 1,0
ОН- (основания) НС1 0,002—1,000 М 0,002—1,0 М 0,2—1
Ag+ NH4SCN или KSCN 5% < 2,5 10 4 М Титр, проводят в 1/300 М HNO3
АР+ NaOH или NaF 0,2 44 0,01—0,1 М См. также Ионы металлов и Mg2 +
(NH4)2HPO4 или 8-оксихинолин 2,7—7,0 мг В водно-спиртовом р-ре при рН = 4,1: см. также Cd2+ и Mg’*
Ва2+ KjCTjO; 0,1 М 0,01—1 М .... См. также Поны металлов
Ве2+ Вг (см. C1 ) CN" (см. СГ) СО2" (см. ОН") NaOH 0,5 М 10—40 мг ~ 1
с2ог СаС12 или (NH4)j нро4 >2- 10-3 М — 1,8
ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ В ВОДНОЙ СРЕДЕ
Продолжение
Определяемый ион (соединение) Рабочий раствор Область концентраций (количеств) определяемого соединения Относительная ошибка определения, % Примечание
соединение концентрация
Са2+ (NH4)2 С2О4 0,25 Al — 100 мг — 1 Титр, проводят в 50%-ном мет. сп. См. также Ионы металлов
С<Р+ (NH4)2 нро4 22,5—35,7 мг 0,5 Титр, проводят в водноспиртовом р-ре при pH = 6,0. При других значениях pH можно опр. ионы: Mg2* (рН= = 10,3). Мп2* (рН = 6,5), Zn2* (pH = 7,2), Al3* (pH=4,1); см. также Ионы металлов
СГ AgNO3 или Hg (NO3)2 0,001—0,1 A! 0,0002—0,02 АГ . . . . Так же можно титр. CN-, SCN-, Br, J’
Со2+ Си2+ (см. Ионы металлов) Диметилглиоксим 8-Оксихинолин 1,5% в 50% сп. ~0,1 мг .... См. также Ионы металлов и Mg2*
NiSO4 или CoSO4 0,005 Al ~ 0,0001 А1 . . . . Титр, проводят в амми-
F~ (СН3СООН)3 La или Al (NO3)3 0,03 M 0,01—0,03 Af — 1 ачной среде
Th (NO3)4 0,02 M 4—6 мг — 0,2
(CH3COO)2 Ca 0,025 Al — 1 Опр. во фторполимерах после сожжения в кислороде и поглощения окиси фтора 0,5% р-ром CH3COONa
Fes+ Купферон 0,15 Al Изменяя пределы pH осажд. (даны в скобках) можно опр.: Fe3* (2,3—3,4), Sn2* (2,75— 3,16), Sn4* (2,74—3,00), V3* (1,78—1,92), VO2*
ВЫСОКОЧАСТОТНОЕ ТИТРО
Fe»+ Hg2+ Ионы металлов J- (см. СГ) •»o3- K+ Лантаниды (см. Ионы металлов) Mg21 Мп2+ (см. Ионы металлов и Cd2+) MoVi Ni2+ Нитрилтриуксусная к-та Окситетр ацнклин КМпО4 NaCl или KSCN Na-ЭДТА НС1 Na [В (С6Н6)4] 0,002—0,02 Al 0,005—0,1 Al 0,02—0,1 Al 0,04 Af 0,1 Al 0,0001—0,02 M 0,001—0,1 Al 0,0002—0,005 Af • 0,04 ммоль — 8 мг 0,1—0,5 0,5 (4,2—4,45), Ti4* (2,45— 2,65) и ZrO2* (3.0— 3,4 при 5—10°С). Титр, в кислом р-ре. См. также Ионы металлов См. тнтр. Ag* Тнтр. А13*, Ва2*, Са2*, Cd2*, Со2*, Fe2*, лантаниды, Mg2*, Мп2*, Ni2*, Pb2*, Sr2*, Th4*, UVI, Zn2* Титр, в присутствии изб. KJ и Na2S2O3 сэ X X ГЛ 05 Е8 О X о X о ГН )а ГН
8-Оксихинолин (NH4)2 нро4 8-Оксихинолин Диметилглиоксим CuCl2 t Na-ЭДТА 1,5% в 50% сп. 0,05 Af 0,01 M ~ 0,1 мг — 0,1 мг — 0,1 г — 0,1 г 0,75 Изменяя пределы pH осаждения (даиы в скобках), можно опр.: Mg2* (8,2—9,2), Со2* (4,2—5,6), А13* (5,5— 6,2), TF* (3,7—4,6), Th4* (4,8—7,7), Vv (4,6—6,2), Mov (3,3— 7,6), Uvr (4,6—8,2). См. также Ионы металлов рН= 10,3. См. также Cd2* См. также Mg2* При pH = 2 добавл. изб. 0,01 Al FeCl3 и обратно титр, непрореагировавший Fe3* р-ром Na-ЭДТА
ВЫСОКОЧАСТОТНОЕ ТИТРОВАНИЕ В ВОДНОЙ СРЕДЕ
а I 4 о с 0J X X СЧ ф S С С 1 с С U i nip. в ov /о p-pc лиип-сана См. также Fe34 Добавл. изб. С2О4~ и проводят обратное титр. Прямое титр, можно производить с NaF pH=4,8 ч-7,7. См. также Mg2+ pH = 2,45 4-2,65. См. также Fe34 пир. пс ivicu-iaivi , Cu2+, СНзСООН, H2SO4, Na4, Zn2* См. также Mg24 nH = 46_i_62 См. тяк- же Mg24 См. также Fe34 D 5
Относительная ошибка определения, % . . . . . — . . .
Область концентраций (количеств) определяемого соединения ( 5 а с с ~ 0,5 ммоль 50 мг с • * • о • If . с с * M * • . ° < >
о-о ю СЧ концентрация 0,01 м 0,15 М 0,025 М 0,15 М 0,2 М 0,15 М
Рабочий f соединение (СН3СОО)2 Ва Купферон Th (NO3)4 8-Оксихинолин Купферон Na [В (С6Н5)4] 8-Оксихинолин 8-Оксихинолин Купферон a >»
Определяемый ион /огч a ITuuautiPl j [ Pb2+ (см. Ионы металлов) SCN (см. С1 ) so2~ Sr2+ (см. Ионы металлов) Sn2+ и Sn4+ Th4 + . тр- Т1’ UOj+ (см. Ионы металлов и Mg2+) Vv Zn2+ (см. Ионы металлов и Cd2+) ZrO2+
472
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
В таблице приведены сведения о методах амперометрического (полярометрического)-титрования неорганических веществ (ионов).
В первой графе таблицы указаны определяемые вещества (ионы); во второй — рабочие-растворы, которые можно применять для определения данного вещества (иона). Если рабочий раствор генерируется током (кулонометрическое титрование), рядом с ионом (веществом) стоит слово эл.-ген. В третьей графе приведены индикаторные электроды, применяемые прн данном титровании. В четвертой графе указаны эначеиня потенциала индикаторного электрода в вольтах по отношению к потенциалу насыщенного каломельного электрода (и. к. э.). Прн применении вместо насыщенного каломельного электрода меркур-иодидного электрода следует учитывать, что его потенциал на 0,25 в положительнее потенциала н.к. э. Для кулонометрического титрования приведены потенциалы, приложенные к индикаторной паре электродов (Pt - Pt). В пятой графе приводится состав фонового электролита, в шестой — форма кривой данного титрования. Прн этом римским цифрам отвечают следующие формы кривых:
I II III IV V
Прн проведении амперометрического титрования следует учитывать возможность протекания на электродах катодного восстановления Н+ нлн анодного окнслеиня ОН”, а-также катодного восстановления растворенного кислорода. Восстановление Н+на вращающемся платиновом электроде начинается при потенциале (по отношению к н. к. э.) — 0,65 в в нейтральной, —0.95 в в щелочной и —0,25 в в кислой среде. Эти потенциалы ограничивают катодную область определений ионов. Окисление ОН“ на том же электроде начинается прн потенциалах (по отношению к н. к. э.) —0,95 в в нейтральной, —0,55 в в щелочной и —1.25 в в кислой среде. Эти потенциалы ограничивают анодную область амперометрического титрования. Начало восстановления кислорода в нейтральной среде ^—0,2 в.
Таблица построена в порядке, отвечающем положению элементов в периодической системе.
Более подробные сведения см.: I. О. А. Сон гн на, Амперометрическое титрование-в анализе минерального сырья, Госгеолтехиздат, 1957. — 2. И. М. К о л ь т г о ф, Дж. Дж. Лингейн, Полярография. Полярографический анализ и вольтамперометрия. Амперометрические титрования, перев. с англ., Госхимиздат, 1948. — 3. Т. А. Крюкова, С. И. Синякова, Т. В. Арефьева, Полярографический анализ, Госхимиздат, 1959. — 4. А. П. Зозуля, Кулонометрический анализ, изд. «Химия», 1965.
Принятые сокращения
ан. — анодное окисление
Au-Hg — золотой. амальгамированный электрод
Hg — ртутный капельный электрод
Pt - вращающийся платиновый электрод Остальные сокращения см. стр. 16.
Определяемое вещество (нон) Рабочий pacTBQp Электрод E, в Условия определения Форма кривой
1 группа периодической системы
Н2О2 КМпО, Pt 0,35-4-0,75 H2SO4 «8 H.) 1
К+ Дипикрил-аминат натрия Hg —1,00-=--4—1,40 pH=H,5-=-12 (фосфатн. или боратн. буф.) 1
Ca2[Fe(CN)6] Pt (ан.) 0,55-4-0,75 Нейтр. р-р; сп. 60 объемы. % (отсутствие NH+) 1
Си2+ Na-ЭДТА Au-Hg —0,18 0,01—0,1 М KNO3 11
Салицилаль-доксим Hg —0,52 Присутствие NaF (для маек. Fe3+) 11
Салицилальдо кс им Pt —0,25 То же 11
Купрон Hg —0,25 Na2SO3, NH4OH (1:1) II
К, [Fe (CN)6J Pt (аи.) 0,55-e- -=-0,85 Без фона или 1 М р-р CH3COONa пли Na2SO4 1
473;
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжение
Определяемое вещество (ион) Рабочий раствор Электрод Et в Условия определения Форма кривой
Си2+ Na2S2O3 Pt 0,15 H2SO4 (1 и.), KJ (0,5 г), NaF (для маек. Fe3*) 11
Си+ KSCN Hg —0,50 Cu2+ предварительно восст. гидроксиламином 1
Agh KJ (0,005 Af) Pt 0,154-0,20 Кисл. р-р -С 0,01 и. (не меш. Cu2*, Sb3*, Bi3+) 11
KJ (0,005 Af) Pt (ан.) 0,75 NH4NO3, рН=6,5-5-8 1
FeSO4 Pt 0,0 Na-ЭДТА 11
Au3+ Меркапто-бензтиазол (сп. p-p) ОдофОДб 0,01—2,0 мг. Аи3* на 15 мл р-ра (меш. Си2*) 11
Na2S2O3 » 0,2 < 0,08 мг Аи3* (не меш. Си2*) 11
II группа периодической системы
Ве2+ NaF Pt 0,0 Инд. Fe3*; сп. (до 70%) pH=2,1 4-2,3 V
Mg2+ Na-ЭДТА Hg (ан.) 0,2 pH = 6,4 (фосфатн. буф.); рабочий p-p титр. анал. р-ром II
Са2+ Na-ЭДТА HgJ —1,50 ZnCl2 (0,001 Af), NH4OH (4—5 н.) V
» » —1,70 KOH (0,1 Al), KC1 (0,05 Al), Na2ZnO2 (0,001 Af) V
К4 [Fe (CN)6J Pt (ан.) 0,55 4-0,85 60% cn„ NH4C1 1
Ва2+ К2СгО4 Hg —1,00 СНзСООН+CH3COONa, pH=4.6; ацетон 1
Zn2+ K4 [Fe (CN)6[ » 0,10 pH=2,1, Na-ЭДТА, Ks [Fe(CN)6] II
K4 [Fe (CN)6) Pt (ан.) 0,45 CH3COONa (0,5 h.), NH4OH (0,1 h.) I
K4 [Fe (CN)6] » 0,75 NH4CI или H2SO4 (0,001—0,5 h.) I
K4 [Fe (CN)6] » 1,05 H2SO4 (0,6—8 h.) I
Na-ЭДТА Hg —1,20-s-4—1,5 СНзСООН (0.5Af) + +CH3COONa (0,5 Af) (1:1), Na-ЭДТА титр. анал. р-ром HI
8-Оксихино-лин » —1,55 pH = 8 4-11 (смесь СНзСООН с NH4OH или с NaOH) III
•Cd2+ K4 [Fe (CN)e] Pt (ан.) Z^(\85 NH4OH I
474
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжение
Определяемое Форма кривой
вещество (ион) Рабочий раствор Электрод Et в Условия определения
Cd2+ Na-ЭДТА Hg См. опр. Zn2+ и Mg2+ Il III
8-Оксихино-лин Cm. опр. Zn2+ III
Hgl+ К2СГ2О7 Cm. опр. Fe2+ I или 11
Hg2+ KJ Pt (ан.) 0,75 См. опр. Ag+ I
KJ III группа Pt п е р и 0 0,0-- —-0,15 д и ч e с к KNO3, H2SO4 или NH4NO3 ой системы II или III
Al3+ NaF Pt 0,0 Инд. Fe3+, сп. (до 50%) V
8-Оксихино-лин Hg —1,45 pH = 3,5 (СНзСООН) I
ln3+ К4 [Fe(CN)6] —0,75 NH4C1 (0,1 Al) II
Na-ЭДТА —0,6* рН=2; 4° С 11
Т1+ Вг2 эл.-ген. Hg —0,20 См. опр. J- I
KJO3 Pt 0,15 H2SO4 (2 и.), присутствие С1_ I
КВгО3 » 0,15 То же 1
KJ Pt (ан.) 0,75 NH4NO3 или KNO3 (0,1 М) I
KJ Pt —0,85 11
KJ Hg —0,60-=- - 0,70 KNO3 (0,3 и.), ацетон (10% р-р), атм. N2 11
Tl3+ КВг Pt (ан.) 1,05 H2SO4 (2 и.) 1
Се3+ Ag2+ эл.-ген. Pt 0,08 HNO3 (5 Al), AgNO3 (0,1 Al); 0°C; генерирующий анод из Au I
Се4+ FeSO4 Hg 0,10 H2SO4 (3A1) 11
Ti111 эл.-ген. IV групп Pt п e p и 0 0.15 дическ H2SO4 (7 Al), Ti(SO4)2 (0,6Al), соль Мора (10 мг) ой системы
CN- AgNO3 Pt 0,0 HNO3 или H2SO4, или KNO3 и СНзСООИа 1
SCN- AgNO3 » 0,0 HNO3 (или H2SO4), KNO3, CHsCOONa 1
С2°Г Ag2+ эл.-ген. » 0,20 См. опр. Се3* 1
КМпО4 » 0,35-0,75 H2SO4 (<8 и.) 1
* Титрование с получением серии полярограмм (полярометрнческое или осциллографическое титрование); для Cd h=0,70 в (не меш. опр.).
475
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжение
Определяемое вещество (ион) Рабочий раствор Электрод E, в Условия определения Форма кривой
Г идрохинон или метол Купферон Аскорбиновая кислота •8-Оксихи-нолин С„Н2„ Sn2+ ,РЬ2+ Ti4+ Ti3+ .Zr4+ Ce(SO4)2 Вг2 эл.-ген. Се4+ J2 K2Cr2O7 КМпО4 К2Сг2О7 К2Сг2О7 К2Сг2О7 KJFe (CN)e] Na-ЭДТА Na-ЭДТА Купферон » К2Сг2О7 NH4VO3 FeCl3 NaF Купферон Na-ЭДТА (I) и Bl (NO3)3 (П) Pt См. опр. См. опр. См. о Pt » » » » » » Pt (ан.) Pt Hg » » Pt Hg (ан.) » Hg Pt Hg » 0,80 Zr4+ и T Vv, SeIV- np. Al3+, 0,20 0,20 0,20 0,0 —1,00 1,05 0,55 —0,60 —0,72 —0,70 —0,80 0,50 0,50 —0,40 0,0 —0,84 —0,1ч- —0,3 H2SO4; см. также опр. Ru, Ir i4+ VI, Fe3+, IrIV Zn2 !-, Cd2+ СНзСООН (лед.), СНзОН, КВг, (CH3COO)2Hg HCI HCI (1 н.) См, onp. Fe2+ Cm. onp. C2O2“ KNO3, или СНзСОО-, или HNO3 (<0,ЗЛ1) То же HNO3, CHjCOONa; рН=3 pH >4 (ацетатн., тартратн. или цитратн. буф.) pH ~ 8 (аммиачн.-тар-тратн. буф.) H2SO4 (1,7 н.) (NH4)2SO4, H2SO4 . (0,1 н.) H2SO4 (2 н.) H2SO4 (2 и.) H2SO4 (1,7 н.), (NH4)2SO4 Инд. Fe34; pH = 2,2 (в начале титр.) H2SO4 (2 М)\ CH3COONH4, винная к-та; рН = 2; изб. р-ра I титр, р-ром II Ш; анодный, потом катодный ток IV I 1 I 1 I III 11 II Ill III I I II II I V I III
•476
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжение
.— Определяемое вещество (вон) Рабочий раствор Электрод Е, в Условия определения Форма кривой
Т1>4- (NH4)2 МоО4 Hg —0,95 NaCl (2,5 Л1), СНзСООН (7% Р-р); рН = 1,9 I
Nab Hg или Pt 0,0 Fe(ClO4)3, NaClOi (0,2 М). 50% сп. V
V группа периодической системы
nh; BrO эл.-ген. Pt 0,15—0,20 pH = 8,5 (боратн. буф.), NaBr (0,1 Al) I
РО3- AgNO3 » Он-0,15 NH4OH + NH4C1 I
Bi (NO3)3 » —0,05 HClOi (pH=l,2) или 1
HNO3 (pH = 1,5)
Ce (NO3)3 Pt (ан.) 1,35 CH3COONa, cn. 1
UO2 (NO3)2 Hg —0,80-- pH = 3,5; KC1, cn. 1
—0,55
AsO3- Br2 эл.-ген. Pt 0,20 H2SO4 (0,1 M), NaBr I
(0,2 Af)
Ag2* эл.-ген. » 0,20 Cm. onp. Ce3* -
KBrO3 » 0,0 HCl+KBr 1
KBrO3 » 0,30-0,45 H2SO4 + NaCl (не I
меш. Fe3*, Hg2*, Cu2*,
Bi3*, Ag*)
KBrO3 Pt (ан.) 1,05 HCI (1 h.) II
J2 Pt 0,15-0,25 CH3COO- или HCO- I
NaCIO или » 0,20 N аНСОз, KBr 1
NaBrO
K2Cr2O7 » Cm. onp. Fe2* I
AsO3- Na2S2O3 » 0,00 KJ, CH3COONa 11
KJ —0,05 HCI (10 h.) IV
Sbni Br2 эл.-ген. —0,20 Cm. onp. AsO|- 111
J2 0,20 Cm. onp. AsO|- I
KBrO3 или » 0,15-0,30 HCI (2 н.) + KBr (не I
KJO3 меш. Cu2*, Bi3*, Pb2*,
Fe3*)
KMnO4 » 0,35—0,75 H2SO4 (<8 н.) I или
III
Bi3+ Na-ЭДТА Hg -0,18 ±0,02 Тартрат- или цитрат- III
ион (0,3—0,5н.), или
HNO3 (pH = 1-2) II
KJ » —0,9 8-Оксихинолнн (изб.)
KJ 0,1 То же i
V<V Ag2+ эл.-ген. Pt 0,20 См. опр. Се3*
Ce4+ » 0,50 H2SO4 i
KMnO4 » 0,50 H2SO4 (2 н.) i
477
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжений
Определяемое вещество (ион) Рабочий раствор Электрод Е, в Условия определения Форма кривой
Vv FeSO4 Ti3+ эл.-ген. Cu+ эл.-геи. FeSO4 FeSO4 Аскорбиновая кислота Hg Pt Pt (ан.) 0,050 0,350 0,050 0,75 1,00 0,85 -=-1,0 H2SO4 (3 Af) См. опр. CeIV См. опр. JO3" H2SO4 (18—24 и.) H2SO4 (0,1 н.), H2SO4 (0,1—1,0 н.) II II III II I I
VI группа периодической системы
SO2- Pb (NO3)2 Pt (ан.) 1,45-7-1,55 NH4NO3 (0,5 Af)', I
CH3COONa
Pb (NO3)2 Hg 1,20 Cn. I
SO|- K2Cr2O7 Pt Cm. onp. Fe2+ I
KMnO4 » —0,35-=- -4-0,75 H2SO4 (8 h.) I
JCI » . ... Ацетатн. буф. (pH = 7); I
KJ
s2or J2 эл.-ген. Hg 0,135 HCI (0,1 Af), KJ I
SeIVliVI Hg2 (NO3)2 Pt 0,054-0,20 (0,1 M) H2SO4 (< 0,01 H.); 11
Аскорбиновая Hg —0,05 H2SO4 или HCI; pH= 11
кислота = 14-2; 60°C
TeO2- К2Сг2О7 (I) Pt 1,15 H2SO4; изб. р-ра I II
и FeSO„ (II) титр, р-ром II
cr2or FeSO4 Pt (ан.) 1,0 H2SO4 (0,1 н.) I
Cu+ эл.-ген. Pt 0,05 HCI (3,2 Al), CuSO4 III
(0,02 Al)
MoO2- Pb (NO3)2 (I) и —0,8 pH = 5; СНзСОО-; изб. 11
(NH4)2 MoO4 /II\ р-ра 1 титр, р-ром II
vv Pb (NO3)2 Pt (ан.) 1,454-1,55 NH4NO3 (0,5 Af), 1
CH3COONa
Pb (NO3)2 Hg —0,80 HNO3, CH3COONa, cn. I
Hg2 (NO3)2 Pt 0,05 4-0,15 KNO3, NH4NO3 I
wo2- Pb (NO3)2 Pt (ан.) См. onp. MoO2 I
4 Pb (NO3)2 Hg 0,6 KNO3 (0,1 H.), cn. 50%, I
>•20 мг W в 1 л
8-Оксихино- Hg 1,4 Щел. p-p, нейтр. I
ЛИН CH3COOH по лакмусу, CH3COONa
Hg2 (NO3)2 Pt 0,054-0,15 KNO3, NH4NO3 I
uo2+ Ti3+ эл.-ген. » 0,25 См. опр. Се4+ III
Ca (OC1)2 » 0,0 Выдел. (NH4)2U2O7; 1
титр. NH*
478
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжение
Определяемое вещество (ион) Рабочий раствор Электрод E, в Условия определения Форма кривой
и4+ nh4vo3 Pt 0,25 H2SO4 (12—16 н.) 1
К2СГ2О7 » См. onp. Fe2+ 1
КМпО4 VII групп » а перис Cm. onp. C2Oj” >дической системы I
F" СаС12 (I) и K4[Fe (CN)6J пп Pt (ан.) 0,75 H2SO4 (0,6—8 н.); изб. р-ра I титр, р-ром 11 1
vv Th (NO3)4 Hg —1,70 (ката-литич. восст. NO") КС1 (0,1 н.) 1
Pb (NO3)2 —1,00 КС1, pH = 4 4-5; сп. I
СГ AgNO3 Pt 0,0 HNO3, или H2SO4, или KNO3, или CH3COONa I
AgNO3 » 0,15 То же (ие меш. Си24) I
Вг- Hg2 (NO3)2 AgNO3 » 0,0-i-0,15 KNO3, или H2SO4, или NHtNO3 См. опр. С1_ I
СГ, Br~,J“ AgNO3 » 0,0 См. опр. С1“ (последовательные ступени) 1 1
J Ag+ эл.-ген. Pt-Ag 0,23 CH3COONa (0,32 М), + + СНзСООН (0,027 М) 1
Вг2 эл.-ген. Pt 0,13 НС1 . (2 Ж)', NaBr (0,1 М) III
Ce4+ эл.-ген. » 0,10 H2SO4 (1 Mj, Се34 (0,025 М)
KJO3 0,65 KCN или ацетон (при титр. образуется JCN или CH2JCOCH3) I
J2 Sn2+ эл.-ген. » 0,15 NaBr (4 М]', KJ (0,008 М), НС1 (0,02Af), SnCl4 (0,2 М) * 11
Na2S2O3 » 0,15 HCI (1h.J 11
Jo3- Cu+ эл.-ген. » 0,05 HCI (3,2 Af), C11SO4 (0,02 Af) II
KJ » 0,65 H2SO4 (1 Af) II
Мп2+ KMnO4 » 0,15 ZnO; pH = 5,5 I
* Данное амперометрическое титрование может быть применено для иодометрическнХ определений.
479
АМПЕРОМЕТРИЧЕСКОЕ (ПОЛЯРОМЕТРИЧЕСКОЕ) ТИТРОВАНИЕ
Продолжение
Определяемое вещество (ион) Рабочий раствор Электрод E, e Условия определения Форма Кривой
Мп2+ К4 [Fe (CN)eJ Pt (ан.) 0,55-0,85 K2SO4 (0,2 Al) 1
Na-ЭДТА Hg Cm. onp. Mg2+ 11
Мпо4- FeSO4 Pt (ан.) 1,00 HZSC>4 (1,4 h.), HNO3 (0,25 h.) 1
FeSO, VT11 групп » а перис 1,15 ) д и ч e с и H2SO4 (15 мл 9h.) + + HNO3 (5 мл 5h.) 0 й системы 1
Fe2+ K2Cr2O7 Pt 0,15 H2SO4 (4—6h.) 1
K2Cr2O7 » 0,45 H2SO4 (8—12 h.) I
K2Cr2O7 » 0,65 H2SO4 (12 h.) I
K2Cr2O7 Pt (ан.) 1,00 HCI 11
К2СГ2О7 » 0,90 H2SO4 (0,1 h.) 11
KMnO4 Pt 0,35-0,75 H2SO4 ( < 8 h.) I
NH.VOg 0,25 H2SOt (12—16 h.) I
NH«VO3 (1) 11 FeSO4 (11) Pt (ан.) 0,80 H2SO4, H3PO4; изб. р-ра I титр, р-ром 11 I
Ce (SO4)2 » 0,5 H2SO4 I
Fes+ Ti1" эл.-ген. Pt 0,250 См. onp. Се4+ III
KJ (1) и Na,S,O3 (II) » 0,0 CH3COONa, изб. р-ра I титр, р-ром II II
Аскорбиновая кислота » 0,0 НС1 (рН = 1,2 - 1,3) II
Na-ЭДТА » 0,02-0,10 pH=3 — 4,5 II
Со2+ K3 [Fe (CN)e[ (1) и CoSO4 (11) Na-ЭДТА —0,20 Cm. 01 NH4OH, изб. р-ра I титр, р-ром 11 ip. Mg2+ I I
K4 [Fe (CN)e] Pt (ан.) Cm. onp. Zn2+ I
Со111 Na2S2O3 (II) Pt —0,20 СН3СОО-, KJ II
Nl2+ Na-ЭДТА Hg -1,22 Ч--1.30 pH=2—10; любой фон, кроме тартрат-иона и СНзСОО” II
Na-ЭДТА Pt (ан.) —0,2 ме pH = 6,4 рабочий р-р титр. анал. р-ром II
Диметилглиоксим Hg —1,85 nh4oh II
KCN » —0,80 nh4oh 11
K4 [Fe(CN)e] Pt (ан.) ... * См. onp. Zn2+ 1
RulV Гидрохинон Pt . . . . НС1 (6 н.) II
IrIV Аскорбиновая кислота » 0,40—0,50 НС1 (0,001—10 и.) не меш. Rh, Pt, Pd, Ru, Cu, Ni, Pb, Se, Те II
Гидрохинон » . . • • Fe3+( + H3POt) 11
Pd" Диметилглиоксим Hg 0.0 NH4CI (0,5 h), HNO3 (0,05 hJ, KNO3 (0,1 h.) II
Меркаптобенз-тиазол 2> 0,5 Буф. pH=5 II
480
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Раздел состоит из двух таблиц: в первой таблице указаны рабочие (титрованные) растворы, с помощью которых возможно определять методом потенциометрического титрования различные неорганические вещества (ионы); во второй — даны условия потенциометрического определения важнейших неорганических веществ. В основном выбраны методы прямого титрования.
Более подробные сведения см.: 1. И. М. К о л ь т г о ф, Н. Фурмаи, Потенциометрическое титрование, перев. с англ.. ОНТИ, 1935. — 2. Ю.С. Л я л и к о в, Физико-химические методы анализа, 4-е нзд., Изд. «Химия», 1964.—3. Г. В. Юинг, Инструментальные методы химического анализа, перев. с англ., Госхимнздат, 1963. — 4. А. В е г k a, J. V 1Г1 1 е-г in, J. Z у к a, Vybrand oxydacne redukcni odmerne Metody, Prag, 1961 (перев. на нем. яз, Massanalytische Oxydation und Reduktionsmethoden, Лейпциг, 1964).
Принятые обозначения и сокращения
Для реакций нейтрализации-.
Н2 (Pt) — водородный электрод стекл. — стеклянный »
Sb — сурьмяный »
Pt | хинг. — хингидронный »
Для реакций осаждения:
Ag I Ag2C2O4 — серебряный электрод, покрытый слоем Ag2C2O4
Ag I AgCl — хлорсеребряный электрод Hg — ртутный электрод
Для комплексометрии:
Hg | Hg-ЭДТА — ртутный электрод в присутствии 10"6Af раствора комплекса ртути с этилен-диамиитетраацетатом натрия
Для реакций окисления-восстановления:
Pt — платиновый электрод
Для всех реакций:
^экв “ потенииал индикаторного электрода (по нормальному водородному электроду) в точке эквивалентности
Д £*макС — точка максимального изменения потенциала при титровании (максимальное значение АЕ/ДЙ, где V — объем стандартного раствора)
экв. — эквивалент
иодометр. — йодометрическое определение
катал. — катализатор к-во — количество ст. — стандартный
Остальные сокращения см. стр. 16.
Рабочие (титрованные) растворы
Таблица состоит из четырех частей (в соответствии с основными методами титрова-имя): нейтрализация, осаждение, комплексообразование и окисление-восстановление. Внутри каждой части рабочие растворы расположены в алфавитном порядке.
В первой графе таблицы приведены вещества рабочих растворов. В некоторых более сложных случаях здесь же указано отношение молекулярного веса вещества рабочего раствора к его эквивалентному весу (Af/Э). Во второй графе указан электрод, применяемый при титровании данным рабочим раствором, в третьей — стандартное вещество, используемое для установления концентрации данного рабочего раствора. Методика определения концентрации этого раствора может быть найдена при соответствующем ионе в следующей таблице или в таблице «Объемный анализ» (стр. 303).
В четвертой графе приводятся ионы (вещества), определяемые данным рабочим раствором; это позволяет судить о возможном использовании рабочего раствора, а также об ионах, мешающих определению данного вещества. Приготовление рабочих растворов см. стр. 17.
Рабочий раствор f Индикаторный электрод Стандартное вещество Определяемые вещества (ноны)
НС1 или H2SO4, или НС1О4 Метод н Стекл. или H2(Pt), или Sb е и т р а л и з а ц и 1 Na2B4O7 ЮН2О или Na2CO3 Сильные и слабые основания, их смеси, СО|~, НСО-, РО3"*, НРО42-, В4О2- н дру-гие анионы слабых к-т
31 Зак. 783
481
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Рабочий раствор Индикаторный электрод Стандартное вещество Определяемые вещества (ионы)
NaOH Стекл. или Sb, или Pt | хинг., или Н2 (Pt) Метод НС1 или H2SO4, или НС1О4, или янтарная к-та, или щавелевая к-та осаждения Слабые и сильные к-ты, их смеси
AgNOs Ag NaCl Br-, С1-, [Fe (CN)6p-, J-, рог. s2~, SCN"
Hg2 (NO3)2 или Hg2 (СЮ4)2 Hg КВг или КС1 Au"1, Br2, BrO“, BrO“ , C2O2-. Ce4+, СГ, CIO-, Cu2+, Fe3+, [Fe(CN)e]3-, J", MnO~ MoO2-. S2~ . 4 4 SCN-, Vv
K2CrO4 Pt ВаС12 или РЬ (СН3СОО)2 Ba2*, Pb2*
K4 [Fe (CN)e] (М/Э = 3) » ZnCl2 (р-р Zn в НС1) Zn2*
KJ Ag AgNO3 Ag*
NaF Pt KA1(SO4)2 • 12Н2О Al3*
(NH4)2C2O4 Ag 1 Ag2^2^4 1 CaC2( (электрод III рода) Метод комп >4 лексообразов Ca2+, Sr2+, Cd2+ а н и я
Na-ЭДТА (M/Э = 2) Hg | Hg-ЭДТА СаС12 (р-р СаСО3 в НС1) a) pH = 2; прямое титр.: Bi3*, Hg2+, Th4* 6) pH=4,5 ч-5,5; прямое титр.: Bi3*, Cd2*, Cu2*, Hg|+. Hg2*, La3* (и другие трехвалентные ионы Р. 3.), Мп2*, Pb2*, Sc3*, VIV, Y3*, Zn2* в) рН=4,5-ч-5,5; обратное титр, (р-ром, содержащим ионы Cd2*, Cu2*, Hg2*, Pb2* или Zn2*): Al34, Bi3*, Cd2*, Cr3*, Cu2*, Fe3*, Ga3*, Hf4*, Hg2*, In3*, La3* (и другие трехвалентные ионы Р. 3.), Мп2*, Ni2*, Pb2*, Sc3*, Th4*, Vv, Y3*, UO|+, Zn2*, Zr4*
482
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Рабочий раствор Индикаторный электрод Стандартное вещество Определяемые вещества (ионы)
Na-ЭДТА (М/Э = 2) Na-ЭДТА М Аскорбиновая кислота (М/Э = 2) Вг2 Се (SO4)2 Со2 (SO4)3 СгС12 CrSO4 CuCl* Hg I Hg-ЭДТА Pt етод ок и еле Pt » » » » » » СаС12 (р-р CaCOs в НС1) FeNH4 (SO4)2 • -12Н2О н и я-в осстанов FeNH4 (SO4)2 • • 12Н2О или J2 As2O3 As2O3 или Fe (NH4)2 (SO4)2- • 6H2O Fe (NH4)2(SO4)2. • 6H2O K2Cr2O7 CuSO4 •5H2O или K2Cr2O7 K2Cr2O7 Ce (SO4)2 r) pH = 8-е- 10; прямое титр.: Ва2*, Be2*, Sr2*, Са2*, Cd2*, Со2*, Си2*, In3*, Mg2*, Мп2*, Ni2*, Pb2*, Zn2* д) рН=8->10; обратное титр, (р-ром, содержащим ионы Са2+, Cd2*, Cu2+, Mg2+ или Zn2*): Bi3*, Ca2*, Cd2*, Co2*, Cr3*, Cu2*, Hg2*, La3+ (и другие трехвалентные ионы Р. 3.), Mg2*, Ni2*, Pb2*, Sc3*, TI3*, Y3*, Zn2* Прямое тнтр.: Fe3*, Cu2* Обратное титр, (р-ром, содержащим ионы Fe3*): Al3*, Cd2*, Zn2*, Ni2*, Pb2* ления Ag*, Au111, Cu2*, Fe3*, [Fe(CN)6]3-, Hg2*, IrIV, Pt’v As111, Fe2+, Hg2+, Sb111, Tl+ Asln, Fe2* Ce3*, Fe2*, [Fe(CN)e]«- Ag*, Au111, Bi3*, Co2*, Cr2O2-, Cu2+, Fe3+ , Hg2+> Hg2+, MoVI , NO", Sbv, SnIV, TiIV , UO|+, Vv, WVI Те же Au111, Ce4+, Cr2O2-, [Fe(CN)6]3-, Iriv JO-, MnO,;, PtIV, Vv
* CuCl получается пропусканием раствора СиС12 через серебряный-хлорсеребряный редуктор; раствор используется для титрования сразу после редуктора.
31*
483
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Рабочий раствор Индикаторный электрод Стандартное вешество Определяемые вещества (ионы)
FeCl3 или FeNH4 (SO4)2- •12Н2О Pt или Hg Cu*. Mo111, Sn2*, Ti3*, UIV (а также Al3+, Ni2+, PtIV, Zn2+)
FeSO4 или Fe (NH4)2 (SO4)2 Pt KMnO4 Ce4+,Cr2O“-,MnO4-,VIV (Cr3* и Мп2* после предварительного окисления)
Г идрохинон (М/Э —2) » K2Cr2O7 Ag+, Au111, Br*, Ce4*, СГ, Cr2O2-, Cu2+, [Fe(CN)0]3*, Ir'v, J-Mn2*, Pb4*, Tl3*, Vv
Н2О2 » Sn2*, Ce4*
Hg2(NO3)2 или (С1О4)2 » K3 [Fe (CN)e] Au"’, Br~, BrO-,BrO", Cl+4 CIO-, Cu2+, Fe3+, MnO", Movl 4
Hg C2O2-, СГ, Br~,a также Ca2+ и Cd2+ (no C2O2-)
JC1 Pt KJ или As2O3, или K4 [Fe CN)e], или N2H4-H2SO4 Au111, CN*, Fe2*, [Fe(CN)c]4*, J*, SCN*, SO2', S2O32-, Sn2+, Ti3*
КВгО8 » Sbv, SbnI
К2Сг2О7 3» Co2*, Fe2*, [Fe(CN)6J4*, Te°|-
К? [Cu (JO6)2] или Кв [Си (ТеО0)2] > K4 [Fe (CN)e] Asin, Au111,[Fe(CN)c]4*, CN", J~, JO", Sb111, Tl+
К3 [Fe (CN)J » Na2S2O3 (иодометр.) Аскорбиновая к-та, Asln, Ce3*, Co3*,Cr3*, Fe2*, H2O2, Mn2*, N2H4, NH2OH, S2*, Sb111, SeO|", Sn2+, SO2-. Ti3+, T1+,U1V, VO2*
К4 [Fe (CN)e] » KMnO4 MnO“
NaJO4 или HJO4 X- As2O3 или N2H4 • H2SO4 As111, Ce3+, Fe2+, Hg2+, J-,N2H4,Sbni, SCN~, Sn2+, TeO|-
484
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Рабочий раствор Индикаторный электрод 1 1 Стандартное вещество Определяемые вещества (ионы)
КМпО4 Pt Na2C2O4 или К4 [Fe (CN)0J, или As2O3 As111, Br-, Ce3*, CN-, C2O2~, Cr3+, Fe2+, J-, Mn2+, Pb2+, PtU, Sb"1, SeO|", Sn2+. SO|-, TeO2-, UIV, yll. III, IV
К3 [Мп (РО4)2] (М/Э = I) » Fe (NH4)2 (SO4)2 • • 6H2O, или гидрохинон As”1, C2OJ-, Fe2+, Sb1", Sn2+
(NH4)2MoO4, восстановленный » Ce (SO4)2 BrO", Cr2O2-. Ce4+, Fe3+, JO~ VO-
(стр. 22) NH4VO3 (М/Э = 1) As111, Fe2+, Hg2+, J-, N2H4, S2-, SCN-, SO2', S2O2-, Ti1". Ti+, U4+, V3+ Ag+, Auin, Br~, Cl~, Cr2O2-, Cu2+. [Fe (CN)e[3-, J-, JO-, JO' Hg2 +, Т[з+
N2H4 • H2SO4 »
Na3AsO3 » K2Cr2O7 Au111, CIO". Cr2O2
NaClO или NaBrO ч » As2O3 или n2h4 • H2SO4 Br-, Ce3+, CN-, J-. NH3, NH+, N2H4. S2-. SCN’-, SO2", S2O|-,SeO2-,TeO2-, T1+
Na2WO4, восстановленный (стр. 20) » K2Cr2O7 Cr2O2~, Cu2+, Fe3+, [Fe(CN)0]3-, VO"
Pb (СН3СОО)4 » n2h4.h2so4 или Na2S2O3 As111, Cr2+, Fe2+. N2H4, NO“, Rulv, Sb111, Sn2+, Ti111, Tl* Ag+, Au111, BrO”, Cr2O2-, Cu2+, Fe3+, J2, JO", Hg2+, MnO4~ , MoO2", NO~ PtIV, Sbv, Vv
SnCl2 » KBrO3 или KJO3
TiCl3 » K2Cr2O7 Auin, Cr2O2-, Fe3+ , MoO2", V,v 4
485
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Рабочий раствор Индикаторный электрод Стандартное вещество Определяемые вещества (ионы)
и (SO4)2 Pt К2Сг2О7 BrO-, Cr2O2-, Fe3+ [Fe(CN)e]3-, MnO-ТеО2-
VOSO4 или VO (СН3СОО)2 (М/Э=1) 3» КМпО4 или Се (SO4)2 Ag+, Au111, Bi3+ Cr2O2-, Cu2+, [Fe (CN)ep- Hg2+ TF+
VSO4 (М/Э = 2) » Fe2 (SO4)3 Ag+, Bi3+, Ce4+ Cr2O2-, Cu2+, Fe3+ Pd, Sbv, Tiiv, Tl+ Tl3+, UIV, vIV
Хлорамин Т (CHgCnlbSOjNClNa ЗН2О) К4 [Fe (CN)e] или Na2S2O3 As111, CN-, C2O2- CS2, Fe2+, [Fe(CN)6]4-, H2S Hg2+, J-, n2h4 NO-, SCN-, SOf-S2o2-, Sb111, Sn2+ Tl4+, Tl+, vo2+
Методы определения неорганических ионов
В первой графе таблицы приведены определяемые ионы (вещества), во второй и третьей — рабочие растворы н индикаторные электроды, которые можно применять для определения данного вещества. Для сложных реакций дано отношение молекулярного веса вещества рабочего раствора к его молекулярному весу (7И/Э). В четвертой графе указаны условия определения данного иона. В отдельных случаях приведен потенциал индикаторного электрода в точке эквивалентности по отношению к насыщенному каломе-левому электроду в милливольтах. В пятой графе дано отношение М/Э для определяемого вещества. Если это отношение устанавливается эмпирически, в таблице стоит сокращенное обозначение «эмпир.»
Поны расположены в таблице в порядке, отвечающем периодической системе эле-ментов.
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения М/Э
I группа периодической системы
H+ (кислоты) NaOH, Стекл. или Sb, или Н2 (Pt), или Pt | хинг. Титр, до А£макс 1
ОН (щелочи) HCI Стекл. или Sb, или Н2 (Pt) Титр, до Аймаке 1
К+ Na [В (С0Н5)4] (М/Э=1) (1) и AgNO3 (11) Pt Осажд. р-вом 1 (изб.), фильтр., промыв, ацетоном (50%-ным). Ф-т тнтр. р-вом II I
486
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения М/Э
Си2+ CrSO4 или СгС12 Pt HCI (5 Al), NaCl или I
SnCl2 Hg NH4C1; атм. СОг-Титр, при 80° С до £=Ю0 мв (не меш. Pb2*, Ag*, Al3*, Со2*, Ni2*, Sb3*, Asv, Hg2*, Fe3*) Титр, до £=100 мв I
Na-ЭДТА Hg 1 Hg-ЭДТА а) рН=4ч-5,5 (аце- 2
Na-ЭДТА (I) и To же » татн. буф.) б). pH=8 4-10 (ам- миачн. буф.) или рН=8,5 (0,5Af эта-ноламин. буф.)} pH = 4 4-5,5 (ацетатн. 2
ZnCl2 (11)* Na-ЭДТА Pt буф. или уротропин). Добавл. р-р 1 (изб.), тнтр. р-ром 11 CH3COONH4 (1 мл 2
Hg2 (NO3)2 или » 10% р-ра), NH4OH (0,1 мл 10% р-ра), NH4SCN (1 мл 5% р-ра); 40—50°С Ацетатн. буф., NH4F, 1
(СЮ4)2 VSO4 (Л4/Э = 1) » KSCN HCI; 95° С 1
voso4 » Лимонная к-та (3 мл 1 и 2
ч Аскорбиновая » 30% р-ра), КОН (5 мл нас. р-ра + 4- 100 мл 1 н. К2СО3); 50—85° С; атм. СО2 (Н2СО3) NH4C1, CHsCOONa 1
кислота N2.H4 • H2SO4 » СН3СОО-, СР, SCN- I
Ag+ KJ Ag HNO3 (0,01 Af) (Na- 1
Аскорбиновая Pl ** ЭДТА для маек. Bi3*, Cd2*, Cu2*, Fe3*, Pb2* и Zn2*) 60° C; CH3COONa (до- 1
кислота CrSO4 Pt бавл. вблизи точки эквивалентности) H2SO4 (2-20%); 60— 1
VSO4 (М/Э = 1) » 70° С СНзСООН; 90—95° С 1
voso4 » NH4OH или NaOH; 1
Г идрохинон 50° С; атм. N2 NaOH, NH4NO3, 1
CH3COONH4 (изб.)
* Вместо ZnCh для обратного титрования можно взять растворы солей Cd2+ Cu2+. Hg2+ и Pb2+.
** Стеклянный электрод сравнения.
487
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Опре- о деляемый иои Рабочий раствор Индикаторный электрод Условия определения М/Э
Ag+ N2H4 • H2SO4 Pt KOH (6—35% p-p), NH4NO3 (изб.) 1
Au111 Аскорбино&ая кислота Au Pt HCI (0,02—0,13 н.); 60—70° С рН=1,6-4-3; 50°С; [С1“]<0,1 и. (не меш. Hg2+, Cu2+, Fe3+) 3 3
Г идрохинон Au pH ~6; 20—60° С (не меш. NO^". небольшие количества PtIV; Rhni, lriv; меш. Pd") 3
CrSO4 Pt HCI, Cu2+ (известное количество); 60° С (не меш. Pb2+, Cd2+, Bi3+, Fe3+) 3
SnCl2 или Hg2 (NO3)t, или Hg2 (<?Ю4)2 » HCI (2 н.), атм. N2 H2SO4 (1 н.) (немеш. Pb2+, Cu2+, Fe3+, HNO3<0,5 h.; HC1< 0,1 h.) 3
К7 [Cu (JOe)2l или К9 [Си (ТеО6)21 » Кислая среда 3
VOSO4 NaOH (7,5—30% p-p); атм. N2 пли CO2; 50—70° C 3
n2h4.h2so4 II группа п » ериодическ Слабокисл. анал. p-p (содержащий 5» >5- IO-5M Au1"), 60° C (IrIV и Pd" меш. при высокой конц.) ой системы 3
Ве2+ Na-ЭДТА Hg I Hg-ЭДТА См. опр. Са2* 2
Mg2+ Na-ЭДТА To же См. опр. Са2+ 2
Са2+ Na-ЭДТА » рН=8-4-10 (аммиачн. буф.) или pH=8,5 (0,5 М триэтаноламин. буф.) 2
(NH4)2 С2О4 Ag | Ag2C2O41 CaC2O4 (электрод 111 рода) - - . 2
(NH4)2 С2О4 (I) и Hg2 (NO3)2 или Hg2 (C1O4)2 (II) (М/Э —2) Hg Добавл. р-в I (изб.). Титр, р-вом II 2
458
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения М/Э
Sr2+ Ва2+ Zn2+ Cd2+ Hg2+ Na-ЭДТА (NH4)2 С2О4 К2СгО4 Na-ЭДТА К4 [Fe (CN)e] (М/Э -- 3) Аскорбиновая кислота (М/Э—2) Na-ЭДТА (I) и FeCl3 (II) Na-ЭДТА (I) и FeCl3 (II) Na-ЭДТА Na-ЭДТА Na-ЭДТА (I) и FeCl3 (II) (NH4)2C2O4 (NH4)2C2O4 (I) и Hg2(NO3)2 (II) (М/Э = 2) Аскорбиновая кислота Na-ЭДТА Na-ЭДТА (I) и ZnCl2 (II) CrSO4 или СгС12 SnCl2 VOSO4 или VO (СН3СОО)2 n2h4- H2SO4 N2H4- H2SO4 Hg 1 Hg-ЭДТА Ag I Ag2C2O41 CaC2O4 (электрод III рода) Pt Hg | Hg-ЭДТА Pt » x> Pt* Hg 1 Hg-ЭДТА To же » Ag | Ag2C2O41 CaC2O4 Hg Pt Hg [ Hg-ЭДТА To же Pt » » » » См, опр, Са2+ См. опр. Са2+ 30% сп.; 70е С рН=9,6-=-10 (аммиачн. буф-). рН=2—3; K3[Fe(CN)6] (3—4 капли 1 % р-ра)', Na-ЭДТА для маек. Ми3+ K3[Fe(CN)e] (изб.); pH <4 CH3COONH4 (рН= =5ч-6), р-р I (изб.)', тнтр. р-ром 11 NHtOH, винная к-та, р-р I (изб.) титр, р-ром II См. опр. Си2+ См onp. Си2+ (тартрат. Na для маек. Al3+, La3+ и Mg2+) рН=4,6 (ацетатн. буф.) Добавл. р-в I (изб.)'. Титр, р-вом II HNO3 (меш. С1~); 60° С рН=2 (HNO3 и хлоруксусная к-та) или pH=4 5,5 (ацетатн. буф.)' См. опр. Сц2+ H2SO4 (3% р-р) или НС1 (3-5% р-р) H2SO4 (1Л1); 75° С; атм. N2 или СО2 KJ, NaOH (11—28% р-р); 80—90° С; атм. N3 KJ, КОН (23—33% Р-Р) КВг, кон (0,75—5% Р-Р) 2 2 2 2 2 2/3 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2
Электрод сравнения — вольфрам»
489
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения м/э
111 группа п ериоди ческой системы
в4°Г НС1 Стекл. или Sb, или Н2 (Pt) Титр. ДО Аймаке 2
А13+ Na-ЭДТА (1) и ZnCl2 (II) Hg | Hg-ЭДТА pH = 1->2; добавл. р-р I (изб.), кип. (1 мин), охл., добавл. ацетатн. буф. (pH=4,6). Титр. р-ром II 2
Na-ЭДТА (1) и FeCl3 (II) Pt См. опр. Zn2* 2
NaF Pt pH > 3 Fe2* (Fe3+ следы), NaCl (нас.), сп. (1 объем) 3
Оа3+ Na-ЭДТА (1) и ZnCl2 (11) Hg | Hg-ЭДТА рН=4,6 (ацетатн. буф. 0,2 Л1); нагр., добавл. р-р I (изб.) и титр, р-ром II 2
lns+ Na-ЭДТА (I) и ZnCl2 (II) To же См. опр. Ga3* и Си2* (при рН=4,0) 2
Т1+ Кз [Fe (CN)e] NaClO Pt » NaOH; Osvin (катал, следы); атм. N2 или СО2; 60° С NaOH (1,5—2 н. добавл. в конце титр.); атм. N2 2
Хлорамин T » HCI, КВг 2
NaJO4 или HJO4 » НС1 (6—9 н.) 2
Pb(CH3COO)4 » НС1 (8—10 н.) 2
К? [Cu (JO6)2] или K9 [Cu (TeO6)2] » 2
Т13+ vso„ » НС1 (6—10 н.) (не меш. Zn2*, Cd2*, Pb2*) 2
Г идрохинон » H2SO4 (5—20% р-р) 2
N2H4 H2SO4 » H2SO4 (разб.) 2
Sc3+ Na-ЭДТА (I) и ZnCl2 (11) Hg 1 Hg-ЭДТА См. опр. La3* 2
Y3 + Na-ЭДТА (I) и ZnCl2(Il) To же См. опр. La3* 2
La3+ Na-ЭДТА, 0,005 Al (I) и ZnCl2, 0,005 M Hg | Hg-ЭДТА Р-р 1 (изб.), NH4OH до рН=9,54-10, титр, р-ром II 2
Се3+ (B) Кз [Fe (CN)e] (М/Э = 1) Pt К2СО3 (4Л1); атм. N2 или СО2 1
KMnO4 (Al/3=3) » рН=8 (ацетатн. буф.) 1
Na-ЭДТА (1) и ZnCl2 (11) Hg | Hg-ЭДТА См. опр. La3* и Си2* 2
NaJO4 или HJO4 Pt рН=9,8 (карбонатн. буф. 2 М\ 1
490
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения М/Э
Се8+ K3[Fe(CN)6] ' Pt K2CO3 (20-50% р-р); 1
Се4+ (М/Э=1) Н2О2 » атм. СО2 или N2 (не меш. Th4+, Fe3+) H2SOt (10% р-р) 1
Hg2 (С1О4)2 » H2SO4 (0,5—6 н-j; ка- 1
сог IV группа п НС1 ериодичесе Sb или стекл., тал. AuCl3 ой системы Титр. ДО (Л£/ДУ)макс 2
с,о?" КМпО4 или Н2 (Pt) Pt H2SO4 (0,2—1М); 2
Hg2 (NO3)2 Hg 70° С HNO3 (очень разб.) 2
Хлорамин Т Pt Нагр. р-р 2
К3 [Мп (РО4)2] » То же 2
CN" КМпО4 (1) и » КОН (10% р-р), Си2+ 2
Н2С2О4 (И) или FeSO4 (Па) NaBrO (М/Э = 2) » (катал.), р-р 1 (изб.). Титр, р-ром 11 или Па Слабощелочн. р-р 2
Хлорамин Т » КНСОз, KJ 2
JC1 (М/Э = 1) » (0,3 г/100 мл). Титр, быстро NaHCOs 1
SCN AgNO3 Ag HNO3 (0,01 М), 1
Hg (NO3)2 Hg Ba(NO3)2 (5% р-р)' 1
(М/Э = 2) NaClO или Pt Слабощелочн. р-р 8
NaBrO (М/Э = 2) Хлорамин Т » КВг, Н3ВО3; 70° С 8
JC1 (М/Э = 6/7) » Слабокисл, р-р 6
JC1 (М/Э = 3/2) » Слабощелочн. р-р 6
Sn2+ КМпО4 (М/Э = » (NaHCOs) КОН; атм. N2 2
= 4*/з) К3 [Мп (РО4)2] » Кислый р-р 2
(М/Э=1) K3[Fe (CN)e] » NaOH; Osvni (катал. 2
(М/Э=1) Хлорамин Т » следы); 50—70° С HCI (1 н.); 55—65° С; 2
JC1 (М/Э = 2 » атм. СО2 Слабокисл, р-р (2 скач- 2
или 1) РЬ (СН3СОО)4 » ка титр.) H2SO4 (0,25—4 и.) 2
Н2О2 » или НС1 (0,25—2 н.) НС1 (конц.) 2
491
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения м/э
Sn,v Pb2+ TjlV Tini Zr4+, Hf«+ Th4+ CrSO4 или CrCl2 K2CrO4 Na-ЭДТА Na-ЭДТА (I) и FeCl3 (II) KMnO4 (M/3=3) CrSO4 или CrCl2 VSO4 FeNH„ (SO„)2 VOSO4 или VO (CH3COO)2 K3 [Fe (CN)e] Pb (CH3COO)4 NH4VO3 Na-ЭДТА (I) и Cu2+ (II) (NH4)2MoO4 Na-ЭДТА Pt Hg | Hg-ЭДТА Pt » Hg Pt » » » » Hg 1 Hg-ЭДТА Pt Hg 1 Hg-ЭДТА BiCl3 (экв. к-во), HCI (2,5 и.), СаС12 (30% p-p); кип. (5 мин); титр, в атм. СО2 См. опр. Ва2+ См. опр. Си2+ См. опр. Zn2* КОН (2.5 и.) катал, смесь Sn2+ и Hg2+ H2SO4 (4 и.); атм. СО2. Титр. до £=300 мв* H2SO4; 80° С Кислая среда; атм. СО2 HCI (1 н.), Н2С2О4; атм. СО2 pH=9,8 H2SO4 (0,5—4 и.)' НС1, Н2С2О4 рН=4 (ацетатн. буф.), изб. р-ра I титр, р-ром 11 СНзСООН (немного); pH=3,2 4 2 2 2 2/3 1 1 1 1 1 1 1 2 4 2
V группа периодической системы
NO" CrSO4 или CrCl2 Pt Ti(SO4)2 (0,1 M), H2SO4 (0,5M); 50± 8
±3°C; удаляют воздух (CO2 или N2); добавл. Fe3+. Титр, до £=106 мв
SnCl2 » Fe(NH4)2(SO4)2 (20% p-p), HCI; атм. CO2. Титр, образовавшееся Fe3+ 3
SnCl2 (1) и FeCl3 (II) 5» Рабочий p-p 1 (изб.)', HCI (конц.); атм. CO2; 100° С. Титр, р-ром 11 6
no; Хлорамин T » СНзСООН; рабочий р-р титр. анал. р-ром 2
n2h4 K3 [Fe (CN)e) » КОН (10-25% Р-Р) 6
JC1 » Ацетатн. буф. (pH р-ра мало влияет) 4
34-
* В присутствии Fe его предварительно тнтруют с Pi индикаторным электродом до £=200
492
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения ЫЦЭ
n2h4 AsOg Sb111 Sbv Bi3+ Pb (CH3COO)4 KJO4 или HJO4 Ce (SO4)2 KMnO4 (Af/3=3) K7 [Cu (JOg)2[ или K9 [Cu (TeOe)2J K3[Fe(CN)e[ Хлорамин T Pb (CH3COO)4 NH4VO3 KMnO4 (M/3=3) Kj [Cu (JOe)2] или Kg [Cu (TeO0)2] K3 [Fe (CN)e] Хлорамин T Pb(CH3COO)4 KBrO3 CrSO4 или CrCl2 SnCl2 VSO4 Na-ЭДТА Na-ЭДТА (l) и ZnCl2 (11) CrSO4 или CrCl2 VSO„ VOSO4 или VO (CH3COO)2 Pt » » » » » » » » » » » » » Hg 1 Hg-ЭДТА To же Pt » » Без добавл. к-ты HCI (4—7 н.) HCI (4 Al), JC1 NaOH (0,25 H.J, катал. TeVI КОН (10 Al) NaOH (конц.); катал. Osvnl; 50—70° С а) РН=4-ь9; KJ ' (0,005 Л4) б) НС1 (0,35—1,75 н.); 55 550 q H2SO4 (0,05—8 н.) или НС1 (0,005—8 и.) Н3РО4 NaOH (0,2 н.); катал. TeVI КОН (10 М) NaOH (конц.); катал. Osvni; 50—70° С а) рН = 6,5-г-7,5; тартрат-ион, KJ (~10~4 М) б); на (ЗЛ1), jci (0,01 Л!) H2SO4 (0,25—4 н.) или НС1 (0,35—6 H.J TiCh (изб.)\ НС1 (5% р-р); титр. до АДмакс = 400 мв. Два скачка: первый — изб. TiCls, второй — Sb111 (не меш. As) НО (20% Р-Р), СаС12; 80—85° С; атм. СО2 или N2 НС1 (конц.). НС1 (10—12 н.); См. опр. Hg2+ См. опр. А13+ НО (6 н.); атм. СО2 или N2 НС1 или H2SO4 (6— 10 н.) КОН (нас.); 60— 80° С; атм. Н2 4 4 2 2 Эмпир. 2 2 2 2 2 Эмпнр. 2 2 2 2 2 5 2 2 2 2 3 3 3
493
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения М1Э
VO2+ КМпО4 (Л1/Э=3) KMnO4 (Af/3=5) Pt a) NaOH (10 н.) или Na2CO3 (2 и.) б) Zn-Hg (амальгама или редуктор), H2SO4 (1 Л1); 70° С (в конец титр.); три скачка титр. при £экв =50; 440 и 1160 мв 1 1,2 и 3
VSO4 (Af/3=1) » НС1 или СНзСООН, NaCl; 100° С 1
VO2+, VOg Na-ЭДТА Hg 1 Hg-ЭДТА См. опр. Си2+ п. «а» 2
FeSO4 Pt H2SO4 (HF для маек. W), КМпО4, затем NaNOa (или мочевина) 1
VO + CrSO4 или CrCl2 » НС1 или H2SO4 (3— 5% р-р); катал. JC1. Два скачка титр. 1 и 2
VI группа периодической системы
SO|“ КМпО4 Pt H2SO4 (0,5 h.) 2
К3 [Fe (CN)6] » NaOH (4—5 и.); катал. Osvin; 50— 60° C 2
JC1 (I) и Na3AsO3 (II) P-p I (изб.)'. Титр, р-ром II 2
JC1 Ацетатн. буф. рН= = 6,5 = 7,5; KJ 2
s2- AgNO3 Ag Только в конц. р-рах 2
K3[Fe(CN)6] Pt NaOH (4—5 н.); катал. Osvnl; 50— 60° С 8
Se°|- KMnO4 а) М/Э = 1 » a) NaOH (2,5 н.), NaCl (10% р-р) 2
б) М/Э = 3 » б) NaOH (0.1 н.), NaCl (10% Р-Р); катал. АиС13; 90° С 2
K3 [Fe (CN)e] » КОН (3,5—5 н.); катал. Osvin; 60° С 2
ТеО|- KMnO4 (Л1/3=3) » NaOH (0,4—0,08 н.); катал. TeVI 2
K2Cr2O7 (I) и FeSO4 (II) » НС1 (0,6 М); изб. p-pa I титр, р-ром II 2
NaJO4 » Кислотность почти не влияет 2
Сг3+ Na-ЭДТА (I) и ZnCl2 (II) Hg I Hg-ЭДТА pH=3,5 (ацетатн. буф.), p-p I (изб.); нагр. 10 мин, охл., доводят до рН = = 4 = 8. Титр, р-ром II 2
494
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения М/Э
Сг34 FeSO4 Pt См. опр. Mn2+ 3
КМпО4 (М/Э=3) » Рабочий р-р, NaOH (0,8—1,5 и.). Титр, анал. р-ром 3
K3[Fe (CN)6] » NaOH (кони.); катал. T12SO4 или Osvnl 3
Сг2ОГ FeSO4 » H2SO4 или НС1 (2 н.) 6
Nag AsO з » H2SO4 (20% р-р) 6
TiCl3 » H2SO4 (10% Р-р) 6
CrSO4 или CrCl2 » H2SO4 (3-5% р-р); атм. СО2 или N2 6
VOSO4 или VO (CH3COO)2 » NaOH (15% р-р); атм. N2; 20—70° С 6
VSO4 (M/3 = 3 или 2) * » Два скачка титр.: первый -> Сг3+, второй _>VO3t; атм. СО2 или N2 6
Г идрохинон » H2SO4 (10—20% Р-Р) или HNO3 (5% р-р) (не меш. Fe3+) 6
МоО3-4 TiCl3 » Атм. N2 или СО2 1 (эмпир.)
CrSO4 или CrCl2 » НС1 или H2SO4; 80— 100° С; атм. СО2 или N2; два скачка титр. ** 1 и 3
SnCl2 » НС1 (8 н-1 1 (эмпир.)
Hg2 (СЮ4)2 или Hg (NO3)2 H2SO4 (1—1,5 и.) SCN- и J- Эмпир.
wo-r 4 CrSO4 или CrCl2 НС1 (10 н.); 70—90° С 1 (эмпир.)
ио22+ TiCl3 » НС1 (1-10% р-р), тартрат-ион; атм. N2 или СО2; 50° С 2
Na-ЭДТА (I) и ZnCl2 (II) Hg I Hg-ЭДТА См. опр. А13+ 2
KMnO4 Pt H2SO4 (2% р-р); атм. СО2; 90° С; Zn-Hg-амальгама; титр. UIV 2
K3 [Fe (CN)6] » NaHCO3; Zn-Hg-амаль-гама; титр. UIV 2
CrSO4 или CrCl2 НС1 (2—6 н.)' или H2SO4 (1—6 н.); нагр., добавл. Fe2+; атм. СО2 или N2 2
* М/Э=3 прн первом скачке титрования, Л4/3=2 — при втором.
** Добавление KSCN улучшает титрование.
495
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый ион Рабочий раствор Индикаторный электрод Условия определения луэ
UIV KMnO„ Pt H2SO4; 90= С; атм. co2 2
К3 [Fe (CNk] Fe (NH4)2 (SO4)2 VII группа n » N aHCO3 2
» ериодическ Harp, p-p о й системы 2
СГ AgNO3 Ag HNOs (0,01 M), Ba(NO3)2 (5% p-p) 1
Hg2 (NO3)2 или Hg? (CIO4)2 Hg HNO3 (0,2—5 h.). Еэк в—320 мв 1
Вг~ AgNO3 Ag HNO3 (0,01 H.|. £"экв=Ю5 Мв 1
NaClO Pt pH=9 4-10; 50—60° C 2
Hg2(NO3)2 (А1/Э = 2) или Hg (C1O4)2 Hg (Au-Hg) Кислый p-p. Титр, до Аймаке (-*'290 мв) 1
ВгО“ N2H4 • H2SO4 Pt Кислый p-p 6
J- AgNO3 Ag HNO3 (0,01 н.). Титр, до £=102 мв 1
HgCl? (Л4/Э = 2) Hg Титр, до £=110 мв 1
Na BrO или NaCIO Pt NaHCO3 6
Хлорамин T (М/Э = 2) » а) НС1 (3 4 н.) б) H2SO4 или СНзСООН (1Л1) 2 1
KMnO4 (AI/3=5) » H2SO4 (0,1— 0,25 М). Титр, до £=1000лв 1
JC1 » Нейтр. или слабокисл, р-р (0,05 н. НС1) 1
J2 SnCl2 » HCI (1 н.) 2
JO3~ N2H4 • H2SO4 » НС1 (в зависимости от кислотности образ. J- пли J2) 6 или 5
jo; N2H4 • H2SO4 » а) НС1 б) Боратн. или бикарбоната. буф. 8 или 7 2
Mn2+ K3[Fe(CN)6] » a) NeOH (1,5— 2 н.), глицерин или маннит, или этиленгликоль; атм. СО-.; 10—20= С б) NaOH (1,5— 2 и.) с винной к-той в) KCN, NH4C1, (NH4)2COs 2 1 1
KMnO4 (Af/3 = 4) » Na4P2Oz (свежеприготовленный нас. р-р); рН = = 5 =-7. Титр, до £ — 530 мв 1
496
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый мои Рабочий раствор Индикаторный электрод Условия определения м/э
Мп2+ FeSO4 или Fe(NH4)2(SO4)2 Pt H2SO4 (2—5 M), Ago (малыми порциями до черн. окраш.)', разб. до 150 мл I М H2SO4, (Д£/ДУ)ма.<с« «700 мв 5
Na-ЭДТА Hgl Hg-ЭДТА См. опр. Си2* 2
MnOf К4 [Fe (CN)6] Pt КОН, Ba(NO3)2 (не меш. MnOj“) 1
SnSO4 » 18" С; H2SO4 (IM) 5
FeSO4 или Fe(NH4)2(SO4)2 VIII группа » nep подичее H2SO4 (0,2— 1 Af), Н3РО4. Титр. до £=1090 мв кой системы 5
Fe2+ K3 [Fe (CN)6] Pt а) НС1 (12-20% Р-Р) б) Na2HPO4; рН= =4,3=-10 1
Хлорамин T НС1 (2—3 и.) 1
JC1 (Af/5 = 2) » рН = 0,5=1 (Na-ЭДТА) (2-й скачок J* -> J2 менее характерен)' 1
Pb(CH3COO)4 (М/Э = 2) » НС1 (1—4 н.): 1
KMnO4 » H2SO4 (0,2—1 М), Н3РО4. Титр. до £3кб=1090 Мв 1
» H2SO4 (0,5 М) 1
Ce (SO4)2 » H2SO4 (1Л1). Титр, до £=950 мв 1
Fe3+ T1C13 » H2SO4 (10% р-р)) 1
CrSO4 или CrCl2 » H2SO4. Титр, до £= =200 мв (см. опр. Ti4+); (не меш. MoVi, asvj 1
VSO4 (M/3 = 2 или I) » HCI. H2SO4 или СНзСООН (2-й скачок Viv->Vm) 1 и 2
KMnO4 K2Cr2O7 » » Восст. Zn-Hg (амальгама или редуктор) до Fe2+. Опр. Fe2+ SnCl2 (2-й скачок — окисл. Sn2+) 1
Na-ЭДТА » CH3COONH4 (1 мл 50% р-ра); не меш. F” и тартрат-ионы; меш. цнтрат-ионы 2
Na-ЭДТА (I) и ZnCl2 (II) Hg 1 Hg-ЭДТА См. опр. А13+ 2
32 Зак. 783
497
ПОТЕНЦИОМЕТРИЧЕСКОЕ ТИТРОВАНИЕ
Продолжение
Определяемый нон Рабочий раствор Индикаторный электрод Условия определения м/э
[Fe (CN)e]«- К2Сг2О7 Pt HCI (7% p-p); 50° C I
K7 [Cu (JO6)2] » KHCO3 или Na2B4O7, Эмпир.
или или СНзСООК
K9 [Cu (TeO0)2] Хлорамин T » HCI (1 н.) 1
JC1. 0,001 — » Слабокисл, или слабо 1
— 0,005 h. щел. р-р (NaHCOs)
VOSO4 или » NaHCOs; 20° С I
[Fe (CN)6p- VO (CH,COO)2 N2H4-H2SO4 » NaOH, ZnCl2; катал. OsO4; 20—50° С I
Co2+ Na-ЭДТА Hg 1 Hg-ЭДТА См. опр. Cu2* (рН = 2
=8-=- 10)
K3 [Fe (CN)„] Pt NH4OH (3 н.)', атм. 1
СО2- (не меш. Ni2*)
CrSO4 или CrCl2 » Na-ЭДТА, Ce(SO4)2, HCI, 60° С; охл. Титр. I
Со3+
Nl2+ FeSO4 (I) и K2C12O7 (II) » NaBiO3; NaOH, изб. р-ра I, H2SO4, р-р II, Н3РО4. Титр, р-ром I 1
Na-ЭДТА Hg 1 Hg-ЭДТА См. опр. Си2+ (рН= 2
=8-И0У
Na-ЭДТА (I) и Pt См. опр. Zn2’ 2
Ruiv FeCl3 (II) Pb (CH3COO)4 » НС1О4 (0.03—0,1 н.) 4
Pd vso4 » НС1 (0,2—2 н.) или H2SO4 (не меш. Ni2*, Со2*, Fe3*, Au111, Ag*; меш. Си2* и PtIV) Кислая среда 2
Ir,v CuCl » 1
Аскорбиновая » НС1 или H2SO4 (1 н.) 1
кислота
Г идрохинон » H2SO4 (5% р-р) или 1
НС1 (10% р-р)' (не меш. PtIV, Pd11,
Ptlv CuCl » Rh111) Кислая среда 2
SnCl2 » НС1 (4% р-р), NaBr 4
(4 Al); атм. CQ2 или N?; 75° С (меш. hno3), £ЭВ1!=200лв
Аскорбиновая » на (0.02 н.у. р-р 1 4
кислота (I) и (изб.). Титр, р-ром
Pt11 FeCl3 (II) II
KMnO4 » H2SO4>; кип. (для уда- 2
ления [IrClc]3")
498
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
В таблицах приведены потенциалы полуволн Ei/ полярографического восстановления или окисления неорганических и органических веществ на ртутном капельном электроде (в специально оговоренных случаях — на платиновом электроде) при 25° С. Величины Еу, выражены (в вольтах) по отношению к насыщенному каломельному электроду.
Более подробные сведения см.: 1. И. М. Кол ьтгоф, Д ж. Дж. Л и н г е й н, Полярография, перев. с англ., Госхимнздат, 1948. — 2. Т. А. Крюкова, М. И. Синякова, Т. А. Арефьева, Полярографический анализ, Госхимнздат, 1959. — 3. А. П. Терентьев, Л. А. Яновская, Полярографический метод в органической химии, Госхимнздат, 1957. - 4. Е. Н. Виноградова, 3. А. Галлай, 3. М. Финогенова, Методы полярографического и амперометрического анализа, Изд. МГУ, 1960. — 5. Я- Гейров-с к и й, Я- Кута. Основы полярографии, перев. с чешек., Изд. «Мир*, 1965.
Потенциалы полярографических полуволн неорганических веществ
Определяемые вещества (ионы) сгруппированы в таблице по фоновым электролитам; это позволяет установить, какие ионы мешают определению данного иона. Внутри каждой группы определяемые ионы расположены в алфавитном порядке.
Во второй графе приводится число электронов, участвующих в электродном процессе (Ле-). Положительное значение Ае~ указывает на катодный процесс, отрицательное — на анодный (ан.). Сокращенное обозначение «не восст.» означает, что в данном растворе определяемый нон восстанавливается позже вещества фона.
Значения Еу2 для небольших полярографических волн (с малой константой диффузионного тока) помещены в скобках.
Указатель фоновых электролитов
Ns табл. Фоновый электролит № табл. Фоновый электролит
К 2 НС1 13 CH3COOH+ ch3coonh4
3 НС1О4 или NaClO4 14 NaF
4 H3PO4 НС14 NaH2PO2 NaOH 15 H2C2O4 и NasCgO^, или (ЬШДэСэОд
5 6 16 17 Н2С4Н4О6 (винная к-та) Каг^ЩОб
7 КС1 или L1C1, NH4CI, 18 Н3С6Й5О7 (лимонная к-та)
[(CH3^Nj Cl 19 N азСфН^О, + N ЭОН Na-ЭДТА + СН3СООН Na-ЭДТА+ CH3COONH4
8 CaCI2 20
9 K2CO3 21
10 NH4OH + NH4CI 22 KSCN
11 N2H4 +NH4OH4 NH4C1 23 KCN
12 C5H5N+C5H6N.HCI
Указатель определяемых
ионов (веществ)
Ион № табл. Ион № табл.
ае+ 2,. 3, 5, 10, 12-14, 19 BrO Г 6—8, 10
А13 + 1, 4—7, 13, 16
AsIIl 1, 2, 4, 6, 10, 12, 13, 15. 16, Са2+ 7
18, 19, 21 Cd2 + 1-23
AsV 1, 2, 4, 6, 12, 13, 16. 19 Се3+ 4, 7, 9
Au+ 23 Се4 + 1—4, 7, 9, 12, 19, 22
AuI4 6, 10, 13, 14, 22, 23 СЮ 7
Ba2 + 7 сюг 6
Be2 + 7
Bi3 + 1, 2, 4—6, 9, 11—14, 16—21
32*
499
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Ион № табл. Ион № табл.
СЮ" 6, 7 NO- 1, 7
с юг 6, 7 Na + 7
Со2+ 4—14, 16, 18—23 NbHI 2
Со3 + Сг2+ 10, 17, 23 6, 7, 22, 23 Nbv Nd3 + Nl2 + Npl" O2 OsVI 1,2, 7, 14—16, 20 7 2—5, 7—14, 16, 18, 19-22
Ст3 + CrVi 1-4, 7-11, 13, 15, 16, 19, 22, 23 1, 2, 4, 6, 7, 9, 10, 12, 14, 19, 22 3 1, 2, 4, 6, 7 6, 23
Cs+ 7 OsVIl 12
Cu+ 5, 10 OsVIH 2, 3, 4, 6
Cu2 + 1—4, 6—10, 12—23 Pb2+' 1-9, 11-23
Dy3 + 7 Pd" 6, 10, 12, 13, 23
Er3 + 7 Pr3 + 7, 9
Eu2+ 3, 7, 8, 12, 14, 18 ptII 7, 10, 13, 23
Eu3 + 3, 7, 9, 13, 14, 16, 18, 21 ptIV 13
[Fe(CN)6|4 7 Ra2+ 7
Fe2+ 2, 4—7, 10—20. 22, 23 Rb + 7
Fe3+ 1, 2, 4, 6, 8, 9, 11—23 Re- Re3 + 14
Ga3 + 1, 5—7, 9, 10, 13, 14, 16, 23 3
Gd3 + 7, 9 Re>V 1
Ge2+ 1, 5 ReVI1 1, 3, 6, 7, 22
Gelv 1, 9, 10, 14—16, 21 RhHl 10, 12—14, 17, 22, 23
H+ 7, 8 Ru111 13
H2O2 6, 7, 18 RuIV 2, 3, 23
Hg 7 SO2- 1. 4, 13
Hg2+ 1, 7, 9, 13, 14 3
Hg^ 1, 7, 14 |SbS4]3- 7, 9
Sb111 1, 2, 4—6, 9, 11—21, 23
Ho3 + 7 SbV 1—6, 11, 12, 19
In3 + 1, 2, 5-7, 9, 11—13, 16, 22 Sc3 + 7, 9
Irlll 10, 23 Se2- 10
IrIV 10, 13, 14, 22, 23 SelV 1, 6, 7, 10, 14
JO- 14 SeVi 1, 6, 7, 10
jor 3, 6—8, 13, 18 Sm3+ 11-22
JO4- 3 Sn2+ SnIV 2 1-6, 9—19, 22
K+ 7 Sr2 + 7
La3+ 7 Tav 1, 6, 14—16
Ll+ 7 Tb3 + 7
Lu3+ 7 Те2- 10
Mg2+ 7 Te2 + 6
Mn2+ 2, 4—14, 17—23 TelV 6, 10, 13, 14
MnlV 17 TeVI 2, 4, 6, 7, 9—13, 15, 19, 22, 23
MnVH 7, 8 Th41- 5, 7, 9, 16
Mo VI 1—3, 6, 7, 9—11, 13, 15, 17, 20, T|U1 8
22 T1>V 1, 3, 5—9, 13, 15, 16, 18, 20, 22
nh+ 4 7 T1 + 1—7, 9—16, 18—23
|N(C2Hs)4]+ 7
500
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение'
Пон № табл. Ион № табл.
Т,з+ 1, 3, 7 VV 1, 4, 6, 9—13, 19, 21, 22
Tii3+ 7 WVI 1, 2, 4, 6, 7, 9-13. 16, 19, 20, 23
UIV 2, 3, 7, 13, 18 7
uVI 1-4, 7, 9-15, 19, 21, 22 Yb3+ 7, 16
VII1 6, 23 Zn2 + 2—7, 9—23
V1V 6, 9, 10, 15, 19 ZrIV 7, 13
Таблица 1
Фоновый электролит HCI (1 Af)
Определяемое вещество (ион) E42 Определяемое вещество (ион) he ЕЧ2
Al3+ Asiii Asv Bi3+ Cd2+ Ce4+ Cr3+ CrVi Cu2+ Fe3+ Ga3+ Oe2+ Oeiv Hg2/ Hg2+ In3+ Mo vi Nbv (NO3-) O2 He восст. 3 6 He восст. 3 2 1 1 3 3 1 2 1 3 2 He восст. 2 2 3 1 3 Восст.' NO~ 2 4 0,43 —0,6 (макс.) —0,09 —0,64 +0,1 —0,99 —1,26 —0,78 +0,04 —0,22 >0 —1,2* —0,35 >0 >0 —0,56 ** 0 14 —0^53 —0,76 —0,05 —0,94 Pb2+ Pu Reiv Revn SO2~ Sbin Sbv Seiv SeVi Sn2+ Sniv Tav Tiiv T1+ Tl3+ (jVI Vv WVI 2 1 1 —2 (ан.) 2 - 3 2 5 4 He восст. —2 (ан.) 2 2 4 1 1 1 2 3 2 3 1 3 He восст. —0,44 0,40 —0,53 4* —ОДО4* —0,6 —0,37 —0,15 > 0 —0,35 —0,55 (-0.1) —0,47 —0,1 —0,47 —1,165* —0,81 ** —0,48 > 0,3 «* —0,45 —0,20 7* —0,9 7* > 0 ** —0,80
* 0,001 М HCI.
*• 0,1 м но.
0,3 м но.
*• 2,4 Л! НС1.
« 0,9 Л1 НС1.
»• 0.6 М НС1.
’• 2 М НО.
501
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Таблица 2
Фоновый электролит HCI (12М)
Определяемое вещество (ион) Af Определяемое вещество (ион) Af
Ag+ 1 > 0 Ruiv 1 > 0
AsllI 3 —0,55 2 —0,51
AsV 5 >0 3 —0,62
8 —0,52 4 —0,75
ВР+ 1 —0,45 Sbin 1 —0,52
3 —0,57 3 —0,66
Cd2+ He восст. — Sbv 2 > 0
Ce4+ 1 —0,68 —0,48
Cr3+ He восст. — —0,57
CrVi 3 —0,61 Sn2+ 2 —0,83
Cu2+ 2 —0,71 Sniv 2 —0,50
Fe2+ He восст. — 4 —0,83
Fe3+ 1 >0 Те VI 1 >0
3 —0,65 —0,43
In3+ 3 —0,77 6(?) —0,79
Mn2+ He восст. —. T1+ He восст.
MoVl 2 —0,56 UIV 1
Nbin —2 (ан.) —0,32 2 —0,62 —0,75
Nbv 1 —0,40
Ni2+ —0,67 (jVI 2 > 0
2 —0,80 3 —0,63
O2 2 0 WVI 1 > 0
OsViu Pb2+ 4 5 2 —0,7 >0,11 —0,90 Zn2+ 3 He восст. —0,54
Таблица 3
Фоновый электролит HCIO4 (0,1 М) или NaClO4
Определяемый ио и Af Определяемый ион Ae £I/2
Ag+ 1 >0 JO4- 2 >0
Bi3+ Cd2+ 3 2- 0,22 —0,64 6 —0,04
Ce4+ 1 >0* Mo vi 1 —0,03
Cr3+ 1 —1,46** —0,24
Cu2+ 1 0,01 * Ni2+ —0,77
Eu2+ —1 (ан.) —0,47 2 —1,01
Eu3+ 1 —0,66
* 0.1 м нею,.
•* 0,5 М NaClO,.
502
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемый ион Ae f>/2 Определяемый ион Ae“
NplV 1 —0,10 *** Sniv He восст.
OsViu 5 > 0,10*** Tiiv 1 —0,81
Pb2+ 2 —0,38 *** T1 + —0,46 > Q *=?*
Re3+ 1 —0,28 ЦЗ+ 2
Revn Ruiv 3 3 1 —0,46 —0,40 >0 (jIV 3 1 Q *** —0*93
2 —0,21 r rVI 1 —0,18 4*
Sbv He восст. 3 —0,84
Sn2+ —2 (ан.) -|-0,i3*** 2 —1,00 ***
2 —0,43
*** 1 М НС1О4 или NaClO4.
« 0,5 М NaCIO4+0,01 М НС1О4.
Таблица 4
Фоновый электролит НдРО4 (7*3 Af)
Определяемое Определяемое
вещество (иои) Ae £>/2 вещество (ион) Ae Ё1/2
AP+ He восст. OsVin >0,6
Asm 3 —0,46 Pb2+ 2 —0,53
AsV 6 —0,71 sor 1 —0,67 *
He восст. — 3 2 —1,23*
Bi3+ Cd2+ 3 2 —0,15 —0,77 Sb1" 3 —0,29
Ce3+ He восст. Sbv He восст. —
Ce4+ 1 > 0 Sn2+ 2 —0,58
Co2+ 2 —1,20 Sniv (—0,65)
Cr3+ 1 —1,02 TeVi —0,87
CrVi 3 > 0 T1+ 1 —0,63
Cu2+ 2 —0,09 (jVI 1 —0,12
Fe2+ He восст. — —0,58
Fe3+ 1 4-0,06 Vv 1 >0
Mn2+ He восст. -— —0,54
Ni2+ 2 —1,18 5 —0,91
O2 2 —0,2 WVI 1 —0,59
4 —0,6 Zn2+ 2 —1,13
• Na2HPO4+KH2PO4; рН=6; l as волна отвечает восстановлению SO^ до S2O2 , 2-ая
до S2O|~ .
503
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Таблица 5
Фоновый электролит НС1 (2 Af) +NaH2PO2 (0,1 АГ)
Определяемый ион Де Е'к Определяемый ион Se £'/2
Ag+ 1 > 0 Мп2 + He восст.
А13 + Не восст. — Nj2+ —0,67
Bi3*- 3 —0,11 Pb“+ 2 —0,48
Cd 2+ 2 —0,72 Sb"1 —2 (ан.) —0,57
Со2+ Не восст. — 3 —1,25 —0,5 —0,3
Си + Си2+ * Fe2+ Fe3+ Оа3+ 1 1 Не восст. Не восст. Не восст. —0,20 —0,20 Sbv Sn2+ Sniv Th4+ He восст. 2 He восст.
Ое2+ —2 (ан.) —0,18 ** Tilv 1 > 0
2 —0,57 ** T1+ 1 -0,52
1п3 + 3 —0,65 Zn2*- He восст. —
* Иоиы Си2-*" в присутствии NaH2PO2 восстанавливаются ло Сц+.
** 4 М Н3РО2.
Таблица 6
Фоновый электролит NaOH (1 АТ)
Определяемое вещество (ион) Se Определяемое вещество (ион) Se E'h
Al3+ He восст. Crvi 3 —0,85
Asin —2 (ан.) —0,26 * Cu2+ 2 —0,41
3 —1,8 Fe2+ —1 (ан.) —0,94 *
AsV He восст. Fe3+ 1 —0,95*
Аиш 1 —0,2 ** 3 —1,5
2 —0 4 ** Oa3+ На восст. —
3 j 1 ** H2O2 —2 (ан.) —0,18
Bi3+ 3 —0,6 2 —1,0
BrOr 6 —1,78 In3+ 3 —1,09
Cd2+ 2 —0,78 jo- 6 —1,20
С1ОГ 4 —1,02 Mn2+ 2 —1,70
MoVI He восст. —
C1O3 He восст. — O2 2 0,17
C1O~ He восст. 4 —1,2
Co2+ 2 1 46 *** OsVi 2 —0,61
Cr2+ —L9 3 —1,54
• 0,5 М КОН.
•* 2 М КОН.
*“ I м кон.
4* Добавляют маннит, ” 0.1 М NaOH.
504
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение-
Определяемое вещество (ион) At? E'l, Определяемое вещество (ион) Ae fi/ /2
OsVin 4 —0,63 Sniv He восст.
5 —1,54 TaV To же —
Pb2+ 2 —0,76 Те2+ ... (ан.) —0,42
—2 (ан.) —0,50 ... (ан.) —1,02
Pdn 2 —1,41 6* Te'V 6 —1,19
ReVH ...... —1,5 TeVI 8 —1,57
Sb111 —2 (ан.) —0,45 Ti,v He восст. —
3 —1,15 T1+ 1 —0,48 7*
Sbv He восст. — vin —2 (ан.) —0,38
SeJV SeVi Sn2+ To же —2 (ан.) —0,73 vIV Vv —1 (ан.) 3 —0,43 —1,7
2 —1,22 WVI Не восст. —
Zn2+ 2 —1,53
« 2 Л1 NaOH.
’* С Pt-электродом.
Таблица 7
Фоновый электролит КС1 (0,1 Л1) илн LiCl, NH4CI, |(CH3)4N]CI
Определяемое вещество (ион) А^ ЕЧ, Определяемое вещество (ион) Де E'h
А13+ 3 —1,75 Dya+ 3 —1,85
Ва2+ 2 —1,92 Ег3+ 3 —1,85
Ве2+ 2 —1,8* Еи2+ —1 (ан.) —0,54
ВгОГ 6 —1,78 Еи3+ 1 —0,69
Са2+ Cd2+ Се3+ Се4+ сю- 2 2 3 1 2 —2,20 —0,60 —2,0 >0 >0 Fe2+ [Fe (CN)6]4~ Оа3+ Od3+ Н+ 3 2 —1 (ан.) 3 3 1 —2,47 * —1,3 > 0 1,1 1,75 —1 58 ***
СЮ3 He восст. — Н2О2 2 —0,94
\ сю; To же — Hg —1 (ан.) —0,2
Со2+ 2 —1,20 н«Г 2 >0
Сг2+ —1 (ан.) —0,5 Hg2+ 2 >0
Сг3+ 1 —0,60 Ho3+ 3 —1,85
3 —0,80 In3+ 3 —0,56 **
—3 (ан.) —1,50 JO,- 6 —1,2 —2,13
CrVl 3 —0,3 —1,0 —1 55 3 K+ 1
4 La3+ 3 —1,9
6 —1.8 Li + 1 —2,35
Cs+ 1 —2,1 ** Lu3+ —1,8
Cu2+ 1 +0,04
2 —0,22
• Без фонового электролита.
•• 0.1 М [(CHsbNJCl.
0,007 М LiCl, pH-3.
505
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемое вещество (ион) Определяемое вещество (иои) Ae E'h
Mg2+ 2 —2,30 Rb+ 1 —2,03
Мп2+ 2 —1,51 Revn 3 —1,7
Mnvn 5 > 0 [SbS4p- 5 —1,34
Movi He восст. —. Sc3+ 3 —1,80
NH+ 1 —2,21 Seiv 1 g ***
IN (С2Н5)4]+ —2,67 * SeVi Sm3+ He восст. 1 —1,8
NO3 (см. 3 —1,97 ***
также Th4+ Sr2+ 2 —2,10
и UVI) —2,10 TeVi (-1,1)
Na+ 1 —2,12 ** Tb3+ 2 —1,5
Nbv 1 —1,28 3 —1,85
—0,80 *** Th4+ Восст. NO^~ —1,0
Nd3+ 3 —1,83 T1+ 1 —0,46
Ni2+ 2 —1,1 Tl3+ 3 > 0
O2 2 —0,06 Tu3+ 3 —1,85
4 —0,94 UIV 1 —0,93
OH Pb2+ —1 (ан.) 2 —0,08 —0,40 UIV Восст. NO3~ —1,0
Pr3+ 3 —1,8 WV1 He восст.
Pt11 2 > 0 уз + 3 —1,8
Ptiv 1 —0,1 Yb3+ 1 —1,17
2 —1,0 —1,84 Zn2+ 3 —2,0
Ra2+ 2 2 —1,00
Zr4+ 4 —1,65
* Без фонового электролита.
*• 0,1 М [(CH3)4N]CL
*** LiCl или [(CH3)4N]J; H2SO4 (0,001 и.).
Таблица 8
Фоновый электролит СаС12 (5 Af)
Определяемый ион Atf E'h Определяемый ион Az? EV.
ВгОГ 6 —1,52 J03~ 6 —0,9
Cd2+ 2 —0,80 Mn2+ 2 —1,45
Co2+ 2 —0,82 Mnvn 7 —1,5
Cr3+ 1 —0,51 * Ni2+ 2 —0,56
Cu2+ Eu2+ 1 2 > 0 —0,33 —0,54 > 0 NO“ —1,74
Fe3+ —1 (ан.) 1 Pb2+ T1ni 2 —1 (ан.) —0,53 —0,12 *
H+ 3 1 —1,20 1,608 ** TiIV 1 —0,12 *
* Насыщенный раствор СаС12.
*• 0,5 М СаС12; рН=3.
506
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Таблица 9
Фоновый электролит К2СО3 (2 Af); рН = 11
Определяемый ион Ae E'h Определяемый ион Ae E'k
Asin He восст. Ni2+ 2 —1,2
Bi3+ 3 —0,64 Pb2+ 2 —0,66
Cd2+ 2 —0,74 Pr3+ He восст.
Ce3+ —1 (ан.) —0,16 Sb111 3 —1,1 —1,30
Ce4+ 1 —0,16 [SbS„]3- 5
Co2+ He восст. '—• Sc3- He восст.
Cr3+ To же — Sm3+ To же
CrVi 3 —0,47 Sniv —1,15 —1,37 *
Cu2+ 2 —0,24 TeVi 8
Eu3+ —1 (ан.) —0,53 Th4+ He восст.
Fe3+ 1 —0,86 TjiV 1 —1,5 —0,47 —1,01
Oa3+ He восст. •—- T1+ 1
Gd3+ OeVi To же —1,44 (jVI
Hg2+ 2 >*0 Vv 1 —1,08
In3+ 3 —1,24 vIV —1 (ан.) —0,16 **
Mn2+ MoVl —1 (ан.) He восст. —0,1 Wlv Zn2+ He восст. 2 —1,20
Nd3+ To же —.
» рН=8.5.
♦•0,1 Al NaHCO3.
Таблица 10
Фоновый электролит NH4OH (1 AI) NH4CI (1 Af) + желатина <0,005?,;)
Определяемый ион Ae E'h Определяемый ион Atf E'k
Ag+ 1 > 0 Fe2+ —1 (ан.) —0,34
As!» ...... —1,41 2 —1,49
—1,63 Oa3+ 3 —1,6
Aulll 3 >0 Geiv 2 —1,45**
BrO7 6 —1,72 1Г1П и IV He восст. —
Cd2+ Co2+ 2 2 —0,81 —1,29 Mn2+ Mo vi 2 1 —1,66 —1,71
Co3+ 1 —0,54 * Ni + 2 —1,10
3 ' —1,36 Pd11 2 —0,75
Cr3+ 1 —1,43 Ptn He восст.
CrVi 3 3 —1,71 —0,2 Rh111 2 —0,93
g —1,6 —0,22 —0,50 —0,24 Ru He восст. —
Cu+ Cu2+ —1 (ан.) 1 1 Se2“ Seiv SeVi —2 (ан.) 6 He восст. —0,84 —1,53
2 —0,51
* 2,5 М NH.OH+0,1 М NH4C1.
•» 0,5 М NH(OH + I Al NHjCI.
507
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемый ион Де ЕЧ» Определяемый ион Ae E'h
Sniv 2 4 > 0,3 —0,52 I vIV -1 (ан.) 2 —0,32 —1,28
Те2-Teiv —2 (ан.) 4 —1,1 —0,67 Vv 1 —0,96
TeVi 8 —1,21 3 —1,26
T1 + 1 —0,48 WV1 He восст. —
UVI 1 —0,8 Zn2+ 2 —1,35
3 —1,4
Таблица 11
Фоновый электролит N2H4 (1 Af) + NH4OH (1 Af) + NH4C1 (1 Af)
Определяемый ион Ae E4> Определяемый ион Де E'h
Bi3+ 3 —1,54 Sbv He восст.
Cd2+ 2 —0,84 Sn2+ —2 (ан.) —0,851
Co2+ 2 —1,29 2 —1,219
Cr3+ 1 —1,40 —1,57
Fe2+ 2 —1,47 Sniv He восст.
Fea+ 1 —1,09 Tevt 1 —1,21
3 —1,49 T1+ 1 >0
In’+ Mn!+ He восст. —1,15 uvl —0,98
MoVi To же — vv He восст. —
Ni2+ » — WVI To же —
Pb2+ 2 —0,77 Zn2+ 2 —1,52
Sb111 3 —1,21 .
Таблица 12
Фоновый электролит C5H5N (0,1 AfJ + CjHsN-HCl (0,1 Af)
Определяемый ион A₽ £1, /2 Определяемый ион A<? 4
Ag+ 1 >0 Eu2+ -1 (ан.) —0,49
As'11 — 0,90 Fe2+ He восст. —
AsV He восст. — Fe3+ To же
Bi3+ 3 —1,00 In3+ —
j 2 + Cd Ce4+ Co2+ Crvi 2 He восст. 2 3 —0,62 —1,06 > 0 Mn2+ Ni2+ OsVH Pb2+ » 2 2 2 —0,75 >0,3 —0,40
4 —1,20 Pd11 2 —0,31 *
Cu2+ 1 > 0 Rh111 2 —0,80
2 —0,22 Sb111 —0,47
• 1 A! CsHsN + 1 Af KCI.
.508
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемый ион Де~* E'h Определяемый ион Де 4
Sbv He восст. Vv 1 —0,11
Sn2+ 2 —1,12 —0,43
Sniv He восст. — 3 —0,77
TeVi To же — WVI He восст.
Ti+ 1 —0,451 Zn2+ 2 —1,03
UVI 1 —0,23
2 —0,45
3 —0,98
Таблица 13
Фоновый электролит СН3СООН (2 Af)-f-CH3COONH4 (2 Af)4-желатина (0,01%')
Определяемый ион Ac E'l2 Определяемый ион Де ЕЧ,
Ag+ 1 >0,1 Pt11 2 >0,4*
Al3+ He восст. — ptIV >0*
Asli i 3 —0,92 Rhin 3 >0*
AsV He восст. — Ruin 1 > 0*
Anin Bi3+ 3 >0,5 —0,25 so|- —0,54
Cd2+ 2 —0,65 Sb111 —0,40
Co2+ 2 —1,19* 3 —0,59
Cr3+ 1 —1,2 Sn2+ —2 (ан.) —0,16
Cu2+ 2 —0,07 2 —0,62
Eu3+ 1 —0,81 * Sniv 2 —1,1
Fe2+ He восст. — TeiV 4 —0,48 **
Fe3+ 1 > 0 TeVi 8 —1,18
Oa3+ He восст. — TUV 1 —0,85 ***
Hg2+ 2 >0 —1,50
In3+ 3 —0,71 T1+ 1 —0,47
Iriv 3 >0* UIV —1 (ан.) —0,12 ***
ю3 6 —0,5 (jIV 1 —0,45
Mn2+ He восст. — —1,2
MoVl • —0,6 Vv 1 >0
Ni2+ 2 —1,1 —1,2 —1,1 WV1 Zn2+ 2 (—0,70) —1,1
Pb2+ 2 —0,50 Zriv He восст. —
Pd11 2 —0,6
* 0.1 Al CHsCOONa; pH=5.
** pH=4.4.
♦** 0,2 М СНзСООН; рН=5,1.
509
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Таблица 14
Фоновый электролит NaF (1 Al) + желаткка (0,01%)
Определяемый ион Ле Определяемый ион E'k
Ag+ 1 >0 NbV 1 —1,908*
Аиш 3 >0 Ni2+ 2 —1,12
Bi3+ 3 —0,11 * Pb2+ 2 —0,41 9*
Cd2+ 2 —0,64 Re- ...(ан.) +0,03
Co2+ 2 —1,38 ** ...(ан.) —0,26
Crvi 1 —0,26 *** ...(ан.) —0,42
3 —1,1 ...(ан.) —0,54
Cu2+ 2 ±0,004* Rhni 2 —1,0
Eu2+ —1 (ан.) —0,10 Sb3+ 3 (—0,68)
Eu3+ 1 —1,15* Seiv —0,80
Fe2+ —1 (ан.) +0,116* Sn2+ —2 (ан.) —0,20 |0*
Fe3+ 1 —0,74 7* 2 —0,73
3 —1,44 Sniv Не восст. .—
Oa3+ 3 —1,38 TaV —0,95 5*
Oeiv He восст. — Teiv 4 —0,89
Hg22+ Hg2+ JO" 2 2 2 >0 >0 —0,6 T1+ (jvi 1 1 2 3 —0,50 —0,37 —0,94 0 2] ”*
Iriv Mn2+ 2 —1,4 —1,55 ** Zn2+ 2 1’14 ю*
* рН=0,7.
•• рН = 3-:-6.
*** pH = 9,3.
«* pH =5.
ь* Насыщенный раствор NaF.
« 0,1 Af KF.
7* рН = 7.
»• 3 М NH(F.
9* pH = 13.
ю* рН=4-:-6.
”• 0,01 Af HF.
Таблица 15
Фоновый Электролит Н2С2О4 (0,25 А1) и Na2C2O4 или
(NH4)2C2O4; рН=3-5-4
Определяемый ион Af E'h Определяемый ион
Asm 6 —0,79 Fe2+ —1 (ан.) —0,23
Cd2+ 2 —0,63 Fe3+ 1 —0,23
Cr3+ 1 1,0* GeIV He восст. —
2 —1,15* MoVI —0,35
Cu2+ 2 —0,15 Nbv —1,53 **
Pb2+ 2 -0,50
* 0,1 А1 К2С2О(; рН=5',1.
** рН=7.
510
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
П родолжение
Определяемый мои Ae E'k Определяемый ион A<f? E'h
Sblli -0,51 (jvi 2 —0,13 s*
Sn2+ —0,7 —0,44
Sniv 4 (?) —1.51 W 1 >0, 6*
TaV 1 । 4q *** 3 —1,33
TeVI 8 —1,234* Viv —1 (ан.) —0,1
THV 1 —0,37 Zn2+ 2 —1,3
T1+ 1 —0,46
0,5 Л1 К2С2О4; pH-0.5 +3.
4* Насыщенный раствор (МН4)2С2О4.
ы 0.5 М Н2С2О4.
'♦ 1 Л1 К2С2О4; pH-4,6.
Таблица 16
Фоновый электролит H2C4H4O6 (винная кислота) (0,25 М) или KNaC4H4Oe; pH=3-s-4
Определяемый ион Atf E'h Определяемый ион Ae ЕЧг
Al3+ 3 —1,79 Ni2+ 2 —1,13
Asm —0,62 Pb2+ 2 —0,42
6 —1,0 Sbin 3 —0,56
AsV He восст. — Sn2+ —2 (ан.) —0,18
Bi3+ 3 —0,14 2 —0,49
Cd2+ 2 —0,59 Sniv He восст. —
Co2+ —1,58 Tav 1 —1,57 **
Cr3+ 1 —1,00 Th4+ He восст. —
Cu2+ 2 —0,03 TiiV 1 —0,61
Eu3+ 1 —1,08 T1 + 1 —0,45
Fe2+ —1 (ан.) —0,12 wvi Каталнти- —1,63
Fe3+ 1 —0,12 ческая
3 —1,50 волна
Oa3+ He восст. водорода
OeIV To же — Yb3+ Не восст. —.
In3+ 3 —0,58 Zn2+ 2 —1,20
NbV —1,96 *
* 1 М К2С4Н4О6; pH=6,5.
* • 0.1 Л1 КгС^Ое; pH=3-4-5.
Таблица 17
Фоновый электролит Na2C4H4O6 (0,5 М); желатина (0,01%), рН=9
Определяемый ион Де Определяемый ион А^ ЕЧ.
Asin, v Не восст. — Со3+ 1 —0,31 *
Bi3+ 3 —0,70 3 —1,32
Cd2+ 2 —0,64 Си2+ Fe2+ 2 —1 (ан.) 2 —0,30 ** -0,6 —1,6
* [Co(NH3)£]3+ в 1 Л1 К2С4Н4О6. »*рН-10.
511
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемый ион Д<? Б>/2 Определяемый ион A/? £>/2
Fe3+ 1 —1,20 РЬ2+ 2 —0,7
3 —1,73 R11IU He восст. —
Мп2+ -1 (ан.) —0,4 Sbin 1 —1,0
2 —1,7 3 —1,2
AlniV 1 —1,1 Sn2+ —2 (ан.) —0,33
2 —1,3 2 —0,92
4 —1,7 Sniv He восст. -—-
MoVi Не восст. — Zn2+ 2 -1,15
Таблица 18
Фоновый электролит Н3С6Н5О7 (лимонная кислота) или К3СБН5О7, или
(1ЧН4)зС6Н5О7) рН=3 -т- 4
Определяемое вещество (ион) д<? £-Z2 1 Определяемое вещество (ион) Д/? E'h
Asin —0,75 Мп2+ He восст.
Bi3 + 3 —0,19 №2+ To же ~—
Cd2+ 2 —0,59 РЬ2+ 2 —0,43
Co2+ He восст. — Sbin 3 —0,64
Cu2+ 2 —0,03 Sn2+ —r2 (ан.) —0,21
Eu2+ —1 (ан.) —0,9 2 —0,54
Eu3+ 1 —1,16 Sniv He восст. **
Fe2+ —1 (ан.) —0,05 TilV 1 —0,73
Fe3+ 1 0,05 T1+ 1 —0,45
H£O2 —2 (ан.) —0,18 —1,0 (JIV Двойная волна —0,38 ***
JO“ 6 —0,65 * Zn2+ 2 —1,04
• рН = 5ч-6.
• • 0,25 М HsCjHsO,; рН=5.
’•* 0,1 М КзСеНсО, 4-0,1 М НзС6Н5О,.
Таблица 19
Фоновый электролит Na3CgHgO7 (1 Af) + NaOH (O,lAf)
Определяемый ион Д<? £'/2 Определяемый ион be E4i
Ag+ 1 > 0 CrVi —0,23
AsUl —2 (ан.) —0,31 3 —0,83
AsV He восст. — 4 —1,49
Bi3+ 1 —0,8 Cu2+ 2 —0,50
3 —0,9 Fe2+ —1 (ан.) —0,30
Cd2+ 2 —1,46 2 —0,49
Ce4+ 1 —0,3 Fe3+ 1 —0,93
4 —0,8 3 —1,70
Co2+ 2 —1,45 Mn2+ He восст. —
Cr3+ 1 —1,45
512
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемый ион Де Определяемый ион Де £-/2
Ni2+ Pb2 + Sbin SbV Sn21 Sniv * В цитрат Не восст. 2 -2 (ан.) 3 Не восст. —2 (ан.) 2 <о-аммиачн. буф * —0,78 —0,44 —1,24 —0,91 —1,12 —1,22 Е i(-2 =—1,09 i TeVi TI + (jVI Vlv Vv WVI Zn2+ -1,39 (Де--2) 1 —1 (ан.) 2 3 He восст. 2 —1,54 —0,56 —0,98 —0,47 —1,76 —1,70 —1,43
Таблица 20
Фоновый электролит Na-ЭДТА (0,05 Af)4-CH3COOH (0,8 Af); pHS2
Определяемый ион Де £-/2 Определяемый ион Де £|/2
Bi3+ 3 —0,5 Ni2+ He восст.
Cd2+ 2 —0,65 Pb2+ 2 —0,75
Co2 + He восст. — Sb111 3 —0,62
Cu2+ 2 —0,17 Sn2+ ~0J
Fe2+ Fe3+ Mn2+ MoVi — 1 (ан.) 1 He восст. —0,12 * —0,12 —0,63 ** Tiiv T1+ WVI 1 1 He восст. —O,224* —0,50
NbV 1 0 01 *** Zn2+ To же —
—1,05
' рН=4.
’» 0,1 н. Na-ЭДТА+0.1 н. СН3СООН+0.1 н. CH3COONH<.
•*’ рН=3.
« рН=1.0 + 2,5.
Таблица 21
Фоновый электролит Na-ЭДТА (0,05 AT) -I CH3COONH4 (0,8 Af); рН=^7
Определяемый йен Де £l/2 Определяемый ион Де £V2
As"l 1,0 Pb2+ 2 —1,37
Bi3+ 3 ’ —0,66 Sbin 3 —0,79
Cd2+ 2 —1,27 Sn2+ 2 —1,26
Co2+ He восст. — —2 (an.) —0,20
Cn2+ 2 —0,31 T1 + 1 —0,50
Eu3 + 1 —1,17* (jVI 1 —0,37
Fe3+ Oeiv Mn2+ 1 4 He восст. —0,15 -1,30* vv Zn21- 3 He восст. —1,22 **
Ni2+ To же —
• Na-ЭДТА (0.1 и ): рН=6-+8.
•• Na-ЭДТА (0.05 Al) +CH3COONa; рН=9,5.
33 Зак. 783
513
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Таблица 22
Фоновый электролит KSCN (1 М}
Определяемый нон Af Определяемый ноя Af E4,
АиШ 1 — 1,16* Mn2+ 9 —1,54
Cd2+ 2 —0,65 Mo vi He восст. —
Ce'V —0,53 Ni2 + 9 —0,69
Co2+ 2 — 1,08 Pb2+ 2 —0,45
Cr2+ —0,80 Pd" >0*
Cr3+ 1 —1,05** Rh111 —0,46
CrVi (>0) ReVH —1,2
4 (одна (—0,46) Sn2+ 2 —0,46
—0,94 Sniv TeVi THV T1 + 4 0 504*
Cu2+ ступень) 1 2 >0 —0,54 1 1 —1Д> —1,46 * —0,52 —0,26
Fe2+ Fe3+ 1 1,52 *** q *** (JVI 1
In3+ —0,72 2 —1,32
—1,73 Vv 3 —1,26
Iriv —1.6 Zn2+ 2 —1,05
• 0,1 М KSCN+0.1 Af NH<OH (Au111-> Au1).
* * Двойная волна.
•»» 1 A! KSCN+0.001 Af H,SO,.
« 1 Af KSCN+0,02 Af HCI.
Таблица 23
Фоновый электролит KCN (1 Al)
Определяемый ион Af £l/2 Определяемый нон Ae f-/2
Ag+ 1 —0,3* Mn2+ 1 —1,35
Au+ 1 —1,46 NI 2 —1,36 **
Аиш 2 >0 OsVl 3 >0,5
3 —1,46 4 —0,81
Cd2+ 2 —1,18 Pb2+ 2 —0,72
Co2+ 1 —1,3 Pd" 2 —1,77
Co3+ Cr2+ 2 —1 (an.) —1,45 —1,38 Pt" He восст.
Cr3+ 1 —1,38 Rh111 1 —1,47
3 —1,45 Ruiv He восст. —
Cu2+ He восст. SbiH 3 —1,13
Fe2+ To же ,,, T1+ 1 > 0
Fe3+ 1 —0,7 Те vi —1,36
Ga3+ 3 —1,29 V"1 1 —1.2
Irin He восст. —- WVI He восст. —
Iriv To же — Zn!+ To же —
• 1 Al KCN и 0,001 Al H2SO«.
•’ 0,1 Af KCN и 0.1 Al KC1.
514
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Потенциалы полярографических полуволн органических веществ
Принятые обозначения: к-Hg — ртутиыЙ катод; a-Pt — платиновый анод| a-!ig -- ртутный анод.
Остальные сокращения см. стр. 16.
Определяемое вещество Фоновый электролит Электрод ЕЧ1
состав pH
Азобензол Буф. в 48%-ном сп. 4,0 к-Hg —0,20
9,0 » —0,57
0,1 н. LiCl в 79%-ном сп. — » —0,91
Антраниловая кислота 0,05 н. [(CH3)4N]J — » от —1,52 до —1,60
Антрахинон Ацетатн. буф. в 40%- 7,4 » —0,54
ном диоксане
0,1 н. H2SO4 в 80%- — » —0,36
ном мет. сп.
Антрацен 0,175 М [(C4H9)4N]J в — » -1,94
75%-ном дноксане 0,1 М [(C4H9)4N|J в — » —2,09
D/.-Арабиноза 75%-ном дноксане Фосфатн. буф. 6,5 •» —1,54
7,0 » —1,57
7,5 » —1,57
Аскорбиновая кислота Фосфатн. буф., 1,5% 3,41 a-Hg 0,17
р-.р НРО3 Бифталатн. буф., 3% 2,71 » 0,24
р-р НРО3 0.1 М CdSO4 a-Pt —0,8*
Аурин Фосфатн. буф. в 7 к-Hg —0,76
30%-ном сп. (60° С) —1,20
Ацетальдегид 0,1 н. LiOH — » —1,73
Фосфатн. буф. 6,8 » —1,89
0,1 н. NH4C1 — » —1,60
Ацетилацетон 0,1 н. LiCl — » —1,07**
0,01 и. НС1, 0,1 н. КС1 — » —1,20 **
0.1 н. NH4C1 .— » —1,69 **
Ацетон 0,025М [(CH3)4N]J — » —2,20
0,05 М [(CH3)4N]Br в — » —2,46
75%-ном дноксане; 2,5 н. NH4OH, 2,5 н. 9,3 » —1,52
(NH4)2SO4
Ацетофенон Буф. (цптратно-фос-фатн.) 1,3 —1,14
4,9 » —1,33
8,4 » —1,58
11,3 » —1,60
Бензальдегид Цитратно-фосфатн. буф. 2,2 » —0,96 —1,32
8,0 » —1,33 —1,41
11,0 » —1,44
* £1'2 измерен относительно Cd-катода.
** Потенциал начала полярографической волны.
33*
515
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемое вещество Фоновый электролит Электрод E,-2
состав pH
Бензил (дибензоил) Цитратно-фосфатн. 1,2 к-Hg —0,27
буф- 7,2 » —0,64
11,3 » —0,75
Бензойная кислота 0,05 М [(CH3)4N]Br в — » —1,90
75%-ном диоксане —2,42
5 » 0,046
Бензофенон Цитратно-фосфатн. 1,5 » —0,93
буф-
—1,28
4,8 » —1,10
—1,29
7,9 » —1,33
11,0 » —1,43
Бензохинон-1,4 Цитратно-фосфатн. 5,3 » 0,04
буф- 7,0 » —0,11
11,0 » —0,35
Бромбензол 0,05М [(CH3)4N]Br в —т » —2,22
80%-ном сп.
Бромоформ 0,05М [(CH3)4N]Br в — » —0,60
75%-ном диоксане —1,47
Бутадиен 0,05 М [(C2H5)4N]Br в —. » —2,59
75%-ном диоксане
Винилацетилен 0,05 М [(C2H5)4N]Br в — » —2,40
75%-ном диоксине —2,58
Витамин Bi (тиамин) 0,1 н. КС1 — » —1,25
7,2 » —1,30
Бората. буф. И » —0,38
Витамин В2 (рибофла- Фосфата, буф. 7,2 » —0,40
вин, лактофлавин)
Витамин Вс (фолиевая Буф- 7,6 » —0,73
кислота) 9 » —0,87
D-Галактоза Фосфата, буф. 7 » —1,56
Галловая кислота Цитратно-фосфатн. 2,9 a-Hg 0,49
буф- 0,41
6,0 » 0,34
0,28
11,2 » 0,04
0,1 М КС1 — к-Hg —1,60
0,1 н. H2SO4 — a-Hg —0,57
а-Гексахлорцикло- 0,1 М [(C2H5)4N]J в — к-Hg —2,02
гексан 80%-ном сп.
рТ ексахлорцикло- То же — » —2,15
гексан
у-Гексахлорцикло- » » — » —1,61
гексан —2,58
6-Гексахлорцикло- » » -— » —2,08
гексан
Гексахлорэтан 0 05М [(.CH3)4N]Br в — » -1,84
75%-ном дноксане
516
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
П родолжение
Определяемое вещество Фоновый электролит Электрод M,2
состав ₽н
Гидроксиламин Буф, (ацетатн.-фос- фатн.-боратн.) 4,6 9,2 к-Hg » —1,42 —1,65
Гидрохинон Ацетатн. буф. Фосфатн. буф. 5,4 8,0 a-Hg » —0,136 —0,024
Гликолевая кислота 0.1 н. LJOH ——. к-Hg —1,40
Глиоксаль 0,1 н. NHiCI — » —1,50
D-Глюкоза Фосфатн. буф. 7 » —1,55
Диацетил То же 6,9 » —0,70 —1,75
Диацетилен 0,05/И [(C2H5)4N]Br в 75%-ном диоксане — » —2,27
Дибромуксусная кисло- Фосфатно-цитратн. 3,8 —0,24; —0,77
та буф. NH4OH+NH4C1 5,8 8,6 » —0,32; —1,10 —0,37; —1,21
Дивинилацетилен 0,05М ((C2H5)4N]Br в 75%-ном диоксане — » —2,07 —2,55
о-Динитробензол Буф. в 80%-ном сп. 7,4 » —0,41; —0,75
л-Дннитробензол То же 7,4 » —0,46; —0,71
/i-Динитробензол » » 7,4 » —0,35; —0,83
Дифенил 1, 2 Дихлорэтан 0.175Л4 [(C4H9)4N]J в 75%-ном диоксане 0,1 н. KCI — » —2,70 —1,32
Инден 0,175 М [(C4H9)4N]J в 75%-ном диоксане — » —2,77
Индигокармин Буф- 2,6 » —0,20
I (одбензол 0,05 М [(CH3)4N]Br в 80%-ном сп. » —1,58
Йодоформ 0,05 М [(CH3)4N]Br в 75%-ном диоксане — » —0,45 —1,05 —1,46
Карбазол 0,1 М [(C4H9)4N]J в 75%-ном диоксане — » —2,77
Коричная кислота 0,1 М [(C4H9)4N]J в 50%-ном диоксане i н. HCI KCI, LiCl в 50%-ном диоксане — » » » —1.89 —2,02 —1,13 —1,5 —2,0
Коричный альдегид Буф. 4.9 7.2 » » —0,82 —1,26 —0,94 —1,26
Кротоновая кислота 0,1 М LiOH 13 » —1,90
Кротоновый альдегид Ацетатн. буф. в 50%-ном диоксане 5 » —1,09
Малеиновая кислота Ацетатн. буф. 7,8 » —1,15 —1,34
D-Манноза Фосфатн. буф. 7 » —1,53
Масляный альдегид Водный раствор [(CH5)4N]J — » —1,88
Меркаптобензтиазол Фосфатно-боратн. буф. 7 a-Hg —0,25
517
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжен не
Определяемое вещество Фоновый электролит Электрод
состав pH
Метиленовый синий Фосфатно-боратн. буф. 6,7 к-Hg —0,22
9.2 » —0,41
Метилсалицнлат [(CtHg)tN]OH в 30%- — » —2,15
ном монометиловом
эфире этиленгликоля
fl-Метилстирол 0,175 М [(CtHe)tN]J в — » —2,54
75%-ном диоксане —2,25
Метнлэтилкетон 0,025 М [(CH3)4N]J — »
Монобром уксусная кис- Буф- 7,2 » —1,30
лота П,1 » —1,32
Муравьиная кислота 0,1 и. КС1 — » —1,38
Нафталин 0,175М [(GHshNJJ в — » —2,50
75%-ном диоксине
Нафтионовая кислота 0,05М [(CH3)iN]J — » от —1,42 до —1,52
Нейтральный красный Фосфатно-боратн. 7 » —0,57
буф- 10 » —0,72
Никотиновая кислота 0,1 н. HCI — » —0,83
Нитробензол Фосфатно-боратн. буф. 7 » —0,47
10 » —0,60
Нитрометан Фосфатно-боратн. буф. 4,6 » —0,85
в 30%-ном мет. сп. 11,6 » —0,90
а-Нитронафталин 0,1 н. НС1 в 50%-ном — » —0,22
СП.
о-Нитрофенол Фосфатно-боратн. буф. 7,0 » —0,73
в 80%-ном сп. 11,0 » —0,97
8-Оксихинолин Фосфатн. буф. 8 » —1,18 —1,71
Бератн. буф. 10 » —1,46 —1,81
Пикриновая кислота Буф. (СН3СООН + 4,2 » —0,34
+ L1OH) 11,7 » —0,36 —0,54
—0,96 —1,0
Пирен 0.175М [(C4H9)tN]J в — » —2,10
75%-пом диоксане —2,46
—2,68
Пиридин Ацетатн. буф. 5,4 —1,35
6,3 » —1,76
7,2 » —1,77
Пировиноградная кис- Цнтратно-фосфатн. 2,8 » —0,64 —0.91
лота буф.
4,0 —0,72 —1,07
5,8 —0,80 —1,18
Пирогаллол Фосфатно-боратн. буф. 4 a-Hg —0,18
7 » —0,36
9 > —0,47
618
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемое вещество Фоновый электролит Элек-
состав ₽н трод £1/2
Пропионовый альдегид Рибоза Салициловая кислота Стильбен Стирол Стрептомицин Стрихнин Сульфазол Тпомочевина 1, 3, 5-Трпннтробензол Тринитротолуол Трихлоруксусная кислота Фенантрен Фенол Фенолфталеин Флуорен Флуоресцеин Формальдегид 0.1 и. LiOH 0,1 н. NH4C1 Фосфатн. буф. 0,1 н. КС1 [(C4H9)4N]OH 0,175 41 [(C4H9)4N]J в 75%-ном диоксане 0,1 М [(CzHs)4N]J в 75%-ном диоксане 0.175М [(C4H9)4N]J в 75 % -ном диоксане 3%-ный р-р [(CHs)4N]OH Буф. 0,1 н. [(CH3)4N]J 40%-ный сп. р-р 6 н. НС1 Буф. Фталатн. буф. nh4oh, nh4ci 0,175М [(C4H9)4N]J в 75%-ном диоксане Фосфатн. буф. Бифталатно-фосфатн. буф. в 25%-ном сп. 0,175М [(C4H9)4N]J в 75%-ном диоксане Буф. 0,2 н. LiOH 0,05 н. LiOH 0,05 М [(CH3)tN]Br в 75%-ном диоксане 7,0 13,8 6,0 8,0 6,4 12 7,4 6,8— —8,8 9.0 2,5 6,9 10,1 7,1 9,0 10,8 к-Hg » » » » » » » » » » » » » » » » a-Pt к-Hg » » » » » » » » —1,76 —1,60 —1.77 —1,29 —2,39 —2,14 —2,17 —2,35 —1,41 —1,64* —1,55* —1,67 —0,3 —0,58 —0.26 —0,36 —0,48 —0,31 —0,44 —0,60 —0,31 —0,48 —0,62 —0,84 —1,56 —2,45 —2,69 —0,515 —0,67 —0,86 —1,01 —1,37 —2,65 —0,80 —1,07 —1.38 —1,20 —1,59 —1,56 —0,45 —1.05 —1,46
* Потенциал начала полярографической волны.
519
ПОЛЯРОГРАФИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ
Продолжение
Определяемое вещество Фоновый электролит Электрод ЕЧ2
состав pH
Фруктоза 0,1 н. LiCl — к-Hg —1,76
Фталевая кислота Буф. 2,9 » —1,24
4,1 » —1.35
0,03 М ВаС12 — » —1,50
Фтальимид Буф. 1,9 » —0,86
4,2 » —1,05 —1,45
Фумаровая кислота Ацетатн. буф. 5,9 —1,19
Фурфурол 4,0 —1,24
0,5 » —1,52 —1,72
Хинальдин 0,2 н. НС1 — —0,70
0,1 М NH4OH+0,1A1 9,9 » —1.51
NH4CI в 50%-ном сп.
Хинальдиновая кислота Фосфатн. буф. 8 X- —1,00 —1,16
Хинидин Цитратно-фосфатно- 12 » —1,55
боратн. буф. 12 —1,56
Хинин »
Хинолин Ацетатн. буф. в 50%- 3 » —1,25
НОМ СП. 4 X —1,25 —1,71
5,4 » —1,0 —1,30 —1,73
7,2 X —1,32 —1,71
Хлоральгидрат 0,1 н. КС1 в 50%-ном — X —1,51
СП.
Хлороформ [(CH3)4N]Br в смеси — X —1,68
СН3ОН + Н2О (1:1)
Хлоруксусная кислота 0,1 н. NaOH — X —1,56
а-Хлорэтилметилкетон 0,01 н. HCl+0,01 н. 3,3 » —1,26
КС1 в 80%-ном сп.
Циклогексанон 0,05 М [(CH3)4N]Br в — X —2,42
75%-ном дноксане 2,5 н. NHiOH+2,5 11. 9,3 » —1,50
(NH4)2SO4
Цинхонин Буф. 12 » —1,61
Четыреххлористый 0.1 М [(CHshNJBr в — » —0,75
углерод смеси СН3ОН + Н2О (2: 1) —1,70
Щавелевая кислота 0,1 в. КС1 — » —1,31
MgCl2 (или 8,25 » —1,9
Этнлмеркаптан (CH3COO)2Mg) 0,025 н. H2SO4 в a-Hg 0,02
Этилнитрат 85%-ном. сп.
LiOH - к-Hg —0,94
Этилнитрит LiOH — х> —0,65
520
МАГНИТНЫЕ И ЯДЕРНЫЕ МЕТОДЫ АНАЛИЗА
Масс-спектрометрия
Масс-спектрометрический метод рекомендуется для анализа газовых смесей, особенно смесей углеводородов. Анализ углеводородов можно проводить, используя пары жидкостей с весьма низким уровнем давления пара.
Эмпирические закономерности, связывающие определенные молекулярные структуры с масс-спектрами, служат основой для расшифровки строения молекул, идентификации органических веществ, качественного и количественного анализа их смесей. При использовании масс-спектрометров с большой разрешающей способностью (10 000—20 000) анализ смесей углеводородов облегчается, так как имеет место разрешение дублетов (например СО и N2); точные значения масс для расчета дублетов даны на стр. 522—525.
Для анализа состава твердых веществ и сплавов необходимо использовать масс-спектрометры с двойной фокусировкой и универсальным источником ионов (например искровым).
Более подробные сведения см.: 1. Дж. Б е й н о н, Масс-спектрометрия и ее применение в органической химии, Изд. «Мир», 1964. —2. Д ж. Бернард, Современная масс-спектрометрия, ИЛ, 1957.
Характер информации, получаемой с помощью масс-спектрометра
Область применения Характер информации
Неорганическая химия Качественный и количественный анализ газовых смесей. Анализ микропримесей в газах и твердых телах
Органическая химия Качественный и количественный анализ смесей углеводородов. Идентификация продуктов реакции. Определение структуры молекул отдельных веществ
Физическая Определение давления пара, теплот испарения и сублимации.
ХИМИЯ Определение энергии связи и потенциалов ионизации атомов и молекул
Г еохпмия Определение абсолютного возраста пород и минералов. Определение изотопного состава минералов
Биохимия Исследования с применением соединений, меченных стабильными изотопами
521
ОТНОСИТЕЛЬНЫЕ АТОМНЫЕ МАССЫ ИЗОТОПОВ
Относительные атомные массы изотопов по углеродной шкале
Таблица составлена по данным Международной комиссии по атомным весам на 1963 г. За стандарт принята масса С|2»=12. Погрешность приводимых величин составляет ±1 в последнем десятичном знаке.
Химический символ Атомный .номер Массовое число Относительная атомная масса Химический символ Атомный номер Массовое число Относительная атомная масса
н 1 1 1,007825 РЬ 82 204 203,9731
D 1 2 2,014102 206 205,9745
Т 1 3 3,016049 207 206,9759
Li 3 6 6,015126 208 207,9767
3 7 7,016005 Ra 88 226 226,0254
В 5 10 10,012939 и 92 233 233,0395
5 11 11,009305 234 234,0409
С 6 12 12 (стандарт) 235 235,0439
6 13 13,003354 236 236,0457
N 7 14 14,003074 238 238,0507
7 15 15,000108 Np 93 237 237,0480
О 8 16 15,994915 Pu 94 239 239,0521
8 17 16,999133 240 240,0540
8 18 17,999160 241 241,0567
Тс 43 99 98,906 242 242,0587
Pm 61 143 142,911
145 144,912
147 146,915
Относительные атомные массы изотопов по кислородной (физической) шкале
В таблице приводятся относительные атомные массы стабильных и некоторых радиоактивных изотопов, встречающихся в природе. За стандарт принята масса О10 = 16. Погрешность указана в единицах последнего десятичного знака.
Химический символ Атомный помер Массовое число Относительная атомная масса Химический символ Атомный номер Массовое число Относительная атомная масса
н 1 1 1,0081451 ±2 F 9 19 19,0044429 ±20
2 2,0147406 +6 Ne 10 20 19,9987953 ±15
Не 2 3 3,0169860 ±50 21 21,0005209+ 12
4 4,0038739 ±26 22 21,9983777±7
Li 3 6 6,017034 ±5 Na 11 23 22,9970913 ±21
7 7,018232 ±6 Mg 12 24 23,9926713± 16
Be 4 9 9,015046 ±6 25 24,9937832 ± 15
В 5 10 10,016127 ±4 26 25,9908541 ±14
11 11,012810±7 Al 13 27 26,9901111 + 25
С 6 12 12,0038156 ±4 Si 14 28 27,985821 ±8
13 13,0074929 + 9 29 28,985701 ±10
N 7 14 74,0075263 ±8 30 29,983288 ±7
15 15,0048793 ±4 P 15 31 30,9836126 ±6
О 8 16 16 (стандарт) S 16 32 31,9822388 ±9
17 17,0045364 ±5 33 32,981947Э±22
18 18,0048843 ±8 34 33,9786635 ±22
36 35,9785253 ±40
522
ОТНОСИТЕЛЬНЫЕ АТОМНЫЕ МАССЫ ИЗОТОПОВ
Продолжение
Химический символ Атомный номер Массовое число Относительная атомная масса Химический символ Атомный иомер Массовое число Относительная .атомная масса
С1 17 35 34,9799720 ±22 Ое 32 73 72,94645 ±10
37 36,9776573 ± 17 74 73,94459 ±10
Аг 18 36 35,9789825 ±24 76 75,94533±15
38 37,9748023 ±20 As 33 75 74,94540±10
40 39,9750926 ± 19 Se 34 74 73,94589± 10
К 19 39 38,9761002±20 76 75,94334 ±10
40 39,9767094 ±26 77 76,94436 ± 10
41 40,9748556 ±25 78 77,94209± 10
Са 20 40 39,9752931 ±21 80 79,94198 ±20
42 41,9719674 ±28 82 81,94261 ± 15
43 42,9724439 ±32 Br 35 79 78,94341 ± 15
44 43,9694714 ±24 81 80,94208 ±20
46 45,9682984 ±40 Кг 36 78 77,94489 ±20
48 47,9677660 ±57 80 79,94186 ±20
Sc 21 45 44,9702122 ±22 82 81,93940 ±20
Ti 22 45 45,9672420 ± 19 83 82,94034 ±20
47 46,9666862 ±33 84 83,93806 ±20
48 47,9331912± 16 86 85,93821 ±20
49 48,9634294 ±22 Rb 37 85 84,93888 ±20
50 49,9606687 ±24 87 86,93687 ± 15
V 23 50 49,9630450 ±22 Sr 38 84 83,93986 ±25
51 50,9601754 ±25 86 85,93662 ±20
Cr 24 50 49,9619308 ±24 87 86,93658 ±15
52 51,9570263 ±25 88 87,93375 ±20
53 52,9574817 ±28 Y 39 89 88,93408 ±20
54 53,9560231 ±30 Zr 40 90 89,93284 ±20
Мп 25 55 54,9555234+ 31 91 90,93414 ±20
Fe 26 54 53,956758 ±5 92 91,93382 ±21
56 55,952722 ±4 94 93,93580 ±35
57 56,953509 ±7 96 95,93853 ±50
58 57,951731 ±4 Nb 41 93 92,93526±24
Со 27 59 58,951919 ±3 Mo 42 92 91,9352.1 ±29
Ni 28 58 57,953767 ±7 94 93,93433 ±27
60 59,949823 ±6 95 94,93570 ±40
61 60,950460 ±5 96 95,93490 + 41
62 61,948033 + 7 97 96,93647 ±50
64 63,948285 ±4 98 97,93656 ±50
Cu 29 63 62,949607 ±8 100 99,93828 ±50
65 64,948427 ±5 Ru 44 96 95,93792 ±50
Zn 30 64 63,949472 ±3 98 97,93713 ± 65
* 66 65,947013 ±7 99 98,93820 ±90
67 66,9-18418 ±7 100
68 67,946456 ±5 101
70 69,947572 +6 102 101,93641 ±50
Ga 31 69 68,94757 ±20 104 103,93780 + 70
71 70,94737 ±20 Rh 45 103 102,93790’.; 50
Ge 32 70 69,94637 ±20 Pd 46 102 101,93753 ±50
72 71,94460 ±25 104 103,93687 ±50
523
ОТНОСИТЕЛЬНЫЕ АТОМНЫЕ МАССЫ ИЗОТОПОВ
Продолжение
Химический символ Атомный номер Массовое число Относительная атомная масса Химический символ Атомный номер Массовое число Относительная атомная масса
Pd 46 105 104,93808 ±50 Хе 54 129 128,94555 ±50
106 105,93640+ 50 130 129,94481 ±3
108 107,93780 ±40 131 130,94670+4
ПО 109,93960±50 132 131,94611 ±3
Ag 47 107 106,93891 ±40 134 133,94799 ±5
109 108,93934 ±40 136 135,950419±25
Cd 48 106 105,93952 ±50 Cs 55 133 132,94738 ±7
108 107,93820 ±40 Ва 56 130 129,94810 ±20
110 109,93830 ±40 132
111 110,93945 ±50 134 133,94683 ±8
112 И 1,93823 ±50 135 134,94845+10
ИЗ 112,94028 ±50 136 135,94758 ±9
114 113,93955 ±50 137 136,94906±6
116 115,94185 ±50 138 137,94873 ±8
In 49 ИЗ 112,94012 ±50 La 57 138 137,95059 + 20
115 И4,94050 ±50 139 138,95020 ±6
Sn 50 112 111,94026 ±51 Се 58 136 135,95028 ±20
114 113,93947 ±60 138 137,94987-г 20
115 И4,93996 ±50 140 139,94976 ±6
116 115,93897 ±50 142 141,95441 ±7
117 116,94020 + 50 Рг 59 141 140,95228 ±3
118 117,93930 ±50 Nd 60 142 141,95260+3
119 118,94100±50 143 142,95502+10
120 119,94006 + 50 144 143,95556 ±7
122 121,94210+50 145 144,95814 rt 19
124 123,94454 + 50 146 145,95908 ±6
Sb 51 121 120,94200 ±50 148 147,96349 + 6
123 122,94310 ±50 150 149,96849 ±7
Те 52 120 119,9425 + 2 Sm 62 144 143,95741 ±9
122 121,94156 ±50 147 146,96120 ±3
123 122,94330 ±90 148 147,96145 + 20
124 123,94211 ±50 149 148,96415±20
125 124,94408 + 50 150 149,96457 ±7
126 125,94360 ±50 152 151,96767 ±13
128 127,94610±50 154 153,97087 ±15
130 129,94780±50 Eu 63 151 150,96753 ±13
J 53 127 126,94480 + 50 153 152,96920 + 40
Xe 54 124 123,94539 + 50 . Od 64 152
126 125,94450±50 154 153,9697+ 10
128 127,94450 ±50
524
ОТНОСИТЕЛЬНЫЕ АТОМНЫЕ МАССЫ ИЗОТОПОВ
Продолжение
Химический символ Атомный номер Массовое число Относительная атомная масса Химический символ Атомный номер Массовое число Относительная атомная масса
Gd 64 155 154,9709±11 W 74 183 183,0053 + 20
156 155,9715±10 184 184,0063 + 20
157 156,9712± 10 186 186,0104 + 20
158 157,9734+ 10 Re 75 185
160 159,9777 ±10 187 187,0111+22
Tb 65 159 Os 76 184
Dy 66 156 186 186,0096 ±23
158 187 187,0110± 22
160 159,9758 ±20 188 188,0141+20
161 189 189,0181+20
162 161,9770 ±20 190 190,0174 + 20
163 192 192,0225+ 30
164 163,9804 + 20 Ir 77 191 191,0212+21
Но 67 165 164,9811 ±20 193 193,0252 + 20
Er 68 162 Pt 78 190
164 163,9817 + 10 192 192,0231 ±21
166 194 194,0240+15
167 195 195,0264±15
168 167,9839+10 196 196,0269 + 15
170 169,9894 ±20 198 198,0290 ±20
Tu 69 169 Ац 79 197 197,0285 ±30
Yb 70 168 Hg 80 196 196,028136±8
170 198 198,029692 ±7
171 199 199,031487±10
172 171,9838 ±30 200 200,031911 ±6
173 201 201,034192 ±9
174 173,9807 ±30 202 202,034845+9
176 204 204,038328 ±9
Lu 71 175 TI 81 203 203,0360 ±4
176 175,9974 ±20 205 205,0385± 1
Hf 72 174 Pb 82 204 204,037935+14
176 175,9963+20 206 206,039928 ±7
177 207 207,041695±11
178 177,9998 + 20 208 208,042779 ±6
179 ....... Bi 83 209 209,04579 ±5
180 179,9980±20 Th 90 232 232,11080±6
Ta 73 180 и 92 234 234,11408± 10
181 181,0029 ±20 235 235,11750± 14
W 74 180 180,0015 ±20 238 238,12522+11
182 182,0035±20
525
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИХ И НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
В таблицу включены соединения с числом углеродных атомов <7 и небольшое количество других соединений. Приведены массовые числа н интенсивность (в скобках) пяти важнейших пиков соединений: материнский пик (т. е. пик. соответствующий молекулярному весу соединения, а для молекул, содержащих многоизотопные элементы, — весу, который отвечает наиболее распространенным изотонам элементов, составляющих молекулу), основной (наиболее интенсивный) пик н три следующие пика в порядке уменьшения их интенсивности. Интенсивность во всех случаях нормирована по отношению к принятой за 100 интенсивности основного пика бутана с массовым числом г? =43.
При пользовании таблицей нужно учитывать следующее: а) возможно колебание относительной интенсивности в
пределах в зависимости от применяемого при-
бора;
б) отношение интенсивности двух пиков в спектре одного соединения при измерении на различных приборам варьирует меньше, чем отношение интенсивности любого пика соединения к основному пику бутана с массовым числом т=43_
Соединения расположены по суммарным формулам в порядке возрастания числа атомов углерода, а прн одинаковом числе атомов углерода — в порядке возрастания числа атомов водорода; остальные элементы расположены по алфавиту их символов. Неорганические соединения помещены в конце таблицы.
Все спектры получены прн энергии ионизирующих электронов 70 эв.
Формула Название Массовое число и интенсивность
материнский пик основной пнк трн следующие по интенсивности инка
CBrGlF2 CBr2F2
CC12F, CC13F СС1„ CF J CF.
CHBrCIF CHBiF, СНС13‘ CHF3 CHN CH2C1F CH2C1, ch2f,‘ CH2O‘ сн„о2 СН3С1 CH3F CI I. J
CH3NO2 CH4
Дифторхлорбромметан 164 (0,23) 85 (86) 87 (27) 129(17) 131 (16)
Дифтордибромметан 208 (1,7) 129 (70) 131 (68) 79 (18) 31(18)
Дифтордихлорметан . 120 (0,07) 85 (33) 87(11) 50 (3,9) 101 (2,8)
Трихлорфторметан 136 (0,04) 101(54) 103 (35) 66 (7,0) 35 (5,8)
Четырёххлористый углерод 152 (0,0) 117(39) 119(37) 35 (16) 47 (16)
Трифториодметан 196 (51) 196 (51) 127 (49) 69 (40) 177 (16)
Четырехфтористый углерод 88 (0,0) 69 (57) 50 (6,8) 19 (3,9) 31 (2,8)
Фторхлорбромметан 148 (5,5) 67 (120) 69 (38) 31(13) 111(11)
Дифторбромметан 130 (13) 51 (83) 31 (18) 132 (13) 79 (13)
Хлороформ 118(1,3) 83 (69) 85(44) 47 (24) 35 (13)
Фтороформ ... 70 (0,25) 69 (20) 51 (18) 31 (9,9) 50(2,9)
Водород цианистый 27 (92) 27 (92) 26 (15) 12 (3,8) 28 (1,6)
Фторхлорметан 68 (48) 68 (48) 33 (25) 70 (15) 49(11)
Дихлорметан - 84 (41) 49 (71) 86 (26) 51 (21) 47 (13)
Дифторметан 52 (2,7) 33 (26) 51 (25) 31 (7,3) 32 (2,9)
Муравьиный альдегид 30 (19) 29 (21) 28 (6,6) 14 (0,94) 13 (0,92)
Муравьиная кислота 46 (72) 29(118) 45 (56) 28 (20) 17(20)
Хлористый метил 50 (66) 50(66) 15 (54) 52 (21) 49 (6,6)
Фтористый метил .... 34 (29) 15 (31) 33 (28) 14 (5,3) 31 (3,2)
Йодистый метил ... . . 142 (78) 142 (78) 127 (29) 141 (11) 15(10)
Нитрометан . 61 (35) 30 (65) 15 (34) 46 (23) 29 (5,3)
Метан . . . 16 (67) 16 (67) 15 (58) 14(11) 13 (5,5)
CH,о CH4S CH3N c2f4 CT6 C2F6Hg CHI, CoH2CIN c;h2ci, C,H,C1, c;h2ci4 C‘H2Fo c2H3ci3 C2H3C13 C2H3F3 C,H3N C2H4 C2H4BrCl C2H4Br2 C2H4C12 C2H4C12 c2h4n2 c2h4o C2H4O C2H4O2 c2h4o2 C2H5Br C2H5C1 c2h5f c2h5n c2h5no2 c,h5no3 C2H6 C2H6O C2H6O C2H6O2 c2H6s
C,H6S2
Метиловый сттирт . . . . 1 32 (26) 31 (38) 29 (25) 28 (2,4) 18 (0,7)
Метилмеркаптан ... .... Мрти.пямим . . 48 (49) 31 (30) 47 (65) 30 (53) 45 (40) 28 (47) 46 (9,5) 29 (8,7) 15 (8,9) 27 (8,6)
Тетрас Г ексас игорэтилен ..... ггорэтан 100 (20) 138 (0,14) 31 (47) 69 (95) 81 (34) 119(39) 50(14) 31 (17) 12(3,6) 50 (9,6)
Гексас А нети. ггордиметилртуть . - • пен 340 (0,83) 26 (102) 69(111) 26 (102) 202 (26) 25 (20) 271 (22) 24 (5,7) 200(21) 13 (5,7)
Хлорацетонитрил иис-1.2-Дихлооэтилен 75 (51) 96(53) 75 (51) 61 (72) 48 (46) 98 (34) 40 (23) 63 (23) 77 (16) 26 (22)
тпанс- 1.2-Дихловэтилен ..... 96 (49) 61(73) 98 (32) 2b (25) 63 (23)
1, 1, 2, 2-Тетрахлорэтан 166 (5,9) 83 (95) 85(60) 95 (11) 87 (9,7)
1, 1 -Дифторэтилен . 64(32) 64 (32) 45(21) 31 (16) 33 (13)
1, 1, 1-Трихлорэтан 132 (0,0) 99(37) 99 (24) 61 (19) 117(7,1)
1, 1, 2-Трихлорэтан 132 (3,9) 97 (43) 83 (41) 99 (27) 85 (26)
1,1,1-Трифторэтан . 84 (0,94) 69 (81) 65(31) 15 (13) 45 (10)
Ацетонитрил 41 (89) 41 (89) 40 (46) 39 (17) 38 (10)
Этилен 28 (66) 28 (66) 27 (43) 25(41) 25 (7,8)
1-Хлор-2-бромэтан 142 (7,9) 63(93) 27 (82) 65 (30) 26 (24)
1,2-Дибромэтан 186(1,6) 27 (93) 107 (72) 109 (67) 26 (23)
1, 1-Дихлорэтан 98 (5,7) 63(89) 27 (64) 65 (28) 26 (21)
1, 2-Дихлорэтан 98 (1,7) 62 (12) 27(11) 49 (4,9) 64 (3,9)
Диазоэтан 56 (16) 28 (27) 27 (25) 26 (21) 41 (5,2)
Уксусный альдегид ..... 44 (30) 29 (66) 43 (18) 42 (6,1) 26 (6,1)
Окись этилена - 44 (30) 29 (46) 15 (30) 14(12) 43 (7,1)
Уксусная кислота 60 (19) 43 (37) 45 (33) 15(21) 14 (8,0)
Метилформиат 60(27) 31 (96) 29 (60) 32 (33) 28 (6,8)
Бромистый этил 108 (35) 29(54) 27 (48) 110(33) 26 (16)
Хлористый этил 64 (36) 64 (36) 28 (32) 29 (30) 27 (27)
Фтористый этил 48 (2,4) 47 (24) 27 (8,9) 33 (8,2) 26 (3,0)
Этиленимин 43 (31) 42(56) 28 (44) 15 (20) 41 (11)
Нитроэтан . 75 (0,0) 29 (85) 27 (74) 30 (19) 26(11)
Этилнитрат 91 (0,01) 46(95) 29 (42) 30 (29) 76 (23)
Этан 30 (26) 28 (99) 27 (33) 26 (23) 29 (21)
Этиловый спирт 46 (9,7) 31 (63) 45 (22) 29(14) 27 (14)
Диметиловый эфир 46(32) 45(71) 29 (56) 15 (41) 14 (8,9)
Перекись метила 62 (28) 29 (47) 31 (45) 15 (16) 30 (12)
Диметилсульфид(2-тиапропан) . . 62(56) 47 (69) 45 (42) 46(29) 35 (24)
Этилмеркаптан 62(44) 62 (44) 29 (43) 47 (36) 27(35)
Диметилдисульфид (2, 3-дитиабу-тан), 94 (95) 94 (95) 45(59) 79(56) 46(34)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИХ {И И НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Формула Название Массовое число и интенсивность
материнский пик основной пик трн следующие по интенсивности пика
C2H6S, 2, 3, 4-Трптиапентан .... 126 (54) 126 (54) 45 (32) 79 (27) 47 (19)
c2h7n Этиламин 45(18) 30 (96) 28 (28) 44(19) 27 (13)
c2h7n Диметиламин 45 (36) 44 (71) 28 (48) 15(14) 42(13)
Этилендиамин . 60 (2,7) 30(111) 18(14) 42 (6,9) 43 (5,9)
C3F6 Гексафторпропилен 150(16) 31 (56) 69 (44) 131 (41) 100(20)
c3f8 Октафторпропан 188 (0,0) 69(171) 31 (49) 169 (42) 50(16)
C3H3N Акрилонитрил .... 53 (55) 26 (55) 52 (41) 51 (18) 27 (10)
C3H4 Аллен(пропадиен) 40 (72) 40 (72) 39 (69) 38 (29) 37 (23)
C3H4 Аллилен(метилацетилен) .... 40(79) 40 (79) 39 (73) 38 (29) 37 (22)
C3H4C1N [З-Хлорпропионитрил 89 (12) 49 (68) 54 (54) 51 (29) 26 (20)
c3h4o Акролеин 56(16) 27 (25) 26(15) 28 (13) 55(11)
C3H5C1 1-Хлорпропен-1 76 (30) 41 (70) 39 (43) 40(10) 78 (9,6)
С3н5сю Эпихлоргидрин 92(0,19) 57 (55) 27 (53) 29 (40) 31 (21)
c3H5cio2 Метилхлорацетат 109 (0,23) 59 (56) 49 (44) 15 (43) 29(37)
СзН5С13 1,2,3-Трихлорпропан ....... 146(0,71) 75 (61) 110(22) 77(19) 61 (18)
c3h5n Пропионитрил .... 55 (8,3) 28 (83) 54 (51) 26 (17) 27(15)
е3н6 Циклопропан 42 (64) 42 (64) 41 (58) 39 (44) 27 (23)
c3h6 Пропилен 42 (39) 41 (58) 39 (41) 27 (22) 40(17)
C3H6C12 1, 1-Дихлорпропан ..... 112(0,0) 63 (27) 41 (25) 77 (22) 62 (19)
СзН6С1з 1,2-Дихлорпропан 112(2,6) 63 (51) 62 (36) 27 (29) 41 (25)
C3HcO Аллиловый спирт 58 (12) 57 (43) 29 (34) 31 (26) 27(19)
C3HcO Пропионовый альдегид 58 (25) 29 (66) 28 (46) 27 (38) 26 (14)
c3H6o Ацетон 58 (24) 43 (85) 15 (26) 27 (5,9) 42 (5,9)
C3H6O Окись пропилена 58 (19) 28 (44) 29 (30) 27 (28) 26(18)
H3HG(J2 1, 3-Диоксолан 74 (3,1) 73 (52) 43 (36) 44(30) 29(30)
C3H6O2 Пропионовая кислота 74 (27) 28 (34) 29 (28) 27 (21) 45 (19)
C3HSO2 Этилформиат 74 (5,8) 31 (82) 28 (60) 29(54) 27(36)
Метилацетат 74 (22) 43 (148) 29 (16) 42 (15) 59 (8,4)
c3H6o3 Метилкарбонат 90 (3,3) 15 (93) 45 (54) 29 (43) 31 (34)
C3H7Br 1 Бромпропан ... 122(14) 43 (94) 27 (55) 41 (47) 39 (22)
C3H7Br 2-Бромпропан 122(11) 43 (100) 27 (50) 41(47) 39 (24)
C3H7C1 1-Хлорпропан 78 (3,6) 42 (60) 29 (27) 27 (22) 41 (14)
C3H7C1 2-Хлорпропан 78 (14) 43 (58) 27 (20) 63 (15) 41 (13)
C3H7F i 2-Фторпропан 62(1,0) 47 (84) 46 (24) 61 (12) 27 (7,6)
c3ii7n j 1-Метилэтиленимин 57 (31) 42 (94) 15 (46) 28 (25) 27 (17)
c3h7n 2-Метилэтиленимин 57 (22) 28 (76) 56 (34) 30 (24) 29 (19)
c3h7no N, N-Диметилформамид 73 (54) 44 (63) 42 (29) 28 (25) 15 (24)
c3h7no2 1-Нитропропан 89 (0,0) 43 (68) 27 (67) 41 (58) 39 (24)
c3h7no2 2-Нитропропан 89 (0,0) 43 (75) 41 (55) 27 (53) 39 (23)
C3H8 Пропан . 44 (25) 29(85) 28 (50) 27 (33) 43 (19)
C3HgO Пропиловый спирт 60 (7,2) 31 (115) 27 (18) 29(17) 59 (10)
C3H8O втор-Пропиловый спирт 60 (0,45) 45(112) 43(19) 27 (18) 29 (11)
C3H8O Метилэтиловый эфир 60 (24) 45 (94) 29 (46) 15 (23) 27 (19)
Метилаль (диметокепметан) . - . 76 (1,6) 45(117) 29 (51) 75 (51) 15 (48)
C3H8O, 2-Метоксиэтанол (метилцеллозольв) 76 (7,3) 45 (122) 29 (44) 15 (38) 31 (32)
C3HES Метилэтилсульфид (2-тпабутан) 76 (47) 61 (73) 48 (40) 47 (30) 27 (27)
C3H8S Пропилмеркаптан (пропантиол-1) 76 (30) 47 (43) 43 (34) 27 (34) 41 (32)
c3H8s Изопропилмеркаптан
(пропантиол-2) 76 (41) 43(65) 41 (44) 27 (41) 61 (26)
c3H9N Пропиламин . 59(1,5) 30 (20) 28 (2,5) 27 (1,3) 41 (1,0)
c3h9n Трпметиламин 59 (37) 58 (95) 42 (44) 15 (32) 30(17)
c3h12b3n3 В, В', В" Триметилборазол . 123 (30) 108 (102) 107 (77) 67 (38) 66 (34)
c4f6 Гексафторциклобутен 162 (21) 93 (80) 31 (51) 143 (15) 74 (6,9)
c4fg Гексафторбутадиен-1, 3 162 (27) 93 (90) 31 (45) 74 (10) 112(10)
c,f6 Гексафторбутин-2 .... 162 (18) 93 (47) 143 (38) 31 (25) 69 (20)
C4F8 Октафторциклобутан 200(0,12) 100 (97) 131 (84) 31 (53) 69 (24)
C4r 8 Октафторизобутплен ... 200 (14) 69 (74) 181(54) 31 (44) 93 (22)
c4f8 Октафторбутен-1 . . . 200(11) 131 (122) 31 (86) 69 (44) 93(16)
C4F i0 Декафторбутан 238 (0,0) 69(178) 119(33) 31(22) 100 (15)
c4hf7o2 Гептафтормасляная кислота 214 (0,0) 45 (26) 69 (24) 119 (17) 100(14)
C4H2 Бутадиин-1,3 ... 50(133) 50 (133) 49 (57) 48 (14) 25 (12)
C4H4 Винилацетилен ... 52 (55) 52 (55) 51 (28) 50 (23) 49(7,2)
C4H4O Фуран 68 (36) 39 (58) 38 (9,7) 29 (9,3) 40 (6,7)
C4H4S Тиофен ..... 84 (93) 84 (93) 58 (56) 45 (49) 39(24)
C4H4S2 2-Тиофеитиол 116 (68) 116 (68) 71 (64) 45 (31) 39(11)
c4h5n З-Бутеннитрил 67 (27) 41 (80) 39 (36) 27 (30) 40 (20)
c4h5n Пиррол .... 67 (67) 67 (67) 39 (46) 41 (42) 40 (36)
C4H6 Бутадиен-1,2 54 (65) 54(65) 27 (35) 53 (29) 39(28)
C4H6 Бутадиен-1,3 54 (46) 39 (53) 27 (36) 53 (31) 28 (24)
C4H6 Бутин-1 54 (64) 54(64) 39 (49) 53 (27) 27 (26)
C4H6 Бутин-2 54 (93) 84 (93) 27(42) 53(41) 39 (24)
C4HGC12O2 Этилдихлорацетат 156 (0,12) 29 (192) 27 (58) 83 (23) 28 (19)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИХ и НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Формула Название -Массовое число и интенсивность
материнский пик ОСНОВНОЙ пик три следующие по интенсивности пика
С4Н6О2 Диацетил 86(13) 43(118) 15 (40) 14(12) 42 (8,6)
С4Н6О2 Метилакрилат • 86 (2,0) 55 (98) 27 (66) 15(27) 26 (22)
С4Н7ВгО2 2-Бромэтилацетат 166 (0,03) 43 (158) 27 (35) 106 (31) 108 (30)
С4Н7С1 2-Хлорбутен-2 . 90 (27) 55(68) 27 (21) 39 (21) 29(18)
С4Н7С1О2 2-Хлорэтилацетат 122 (0,0) 43(162) 73 (43) 15 (36) 27 (29)
С4Н7С1О2 Этилхлорацетат 122 (0,96) 29 (130) 27 (41) 77 (37) 49 (29)
c4h7n Бутиронитрил (бутаннитрил) . • 69 (0,15) 41 (112) 29 (70) 27 (38) 28(11)
c4h7n Изобутпронитрил (2-метилпропан-нитрил) 69 (1,7) 42 (79) 68 (38) 28 (26) 54(19)
с4н8. Циклобутан • 56(41) 28 (65) , 41 (58) 27 (27) 26 (15)
С4НВ Изобутилен 56 (36) 41 (85) 39 (37) 28 (18) 27 (17)
С4Н8 Бутен-1 • 56 (32) 41 (87) 39 (30) 27 (26) 28 (26)
С4Н8 1{ис-Бутен-2 56 (36) 41 (76) 39(27) 27 (25) 28 (24)
С4Н8 трс«с-Бутен-2 56(37) 41 (80) 27 (27) 39 (26) 28 (26)
С4Н8С1, 1, 2-Дихлорбутан 126 (0,30) 41 (39) 77 (35) 27 (20) 76(16)
С,Н8С1, 1,4-Дихлорбутан 126 (0,03) 55(87) 41 (29) 27 (24) 90 (23)
С4Н8С12 dl-2, З-Дихлорбхтан 126 (0,95) 63 (63) 62 (58) 27 (57) 55(29)
С4Н8С12 мсзо-2,З-Дихлорбутан 126 (0,95) 63 (64) 27 (57) 62(54) 55(31)
c4h8n2 Ацетальдазин 84(23) 42 (92) 15 (47) 28 (46) 69 (38)
С4Н8О Масляный альдегид 72 (19) 27 (41) 29 (38) 44 (34) 43 (32)
С4Н8О Метилэтилкетон . - 72 (17) 43(97) 29 (24) 27 (15) 57 (6,0)
С„Н8О Вииилэтиловый эфир ..... 72 (27) 44 (64) 43 (56) 29 (49) 27(43)
С4Н8О цис-2,3-Эноксибутан ...... 72 (3,6) 43 (67) 44 (39) 27(35) 29 (33)
С4Н8О транс-2,З-Эпоксибутан 72 (3,5) 43 (69) 44(35) 29 (32) 27 (31)
с4н8о Тетрагидрофуран . 72 (22) 42 (76) 41 (39) 27 (25) 71 (20)
2-Метил-1, 3-диоксолаи 88 (0,33) 73 (67) 43 (48) 45(44) 29(34)
С4Н8О2 1,4-Диоксан 88 (42) 28 (138) 29 (51) 58 (33) 31 (24)
Масляная кислота . ... 88 (1,0) 60 (40) 73 (12) 27 (9,6) 41 (9,1)
Изомасляная кислота .... 88 (8,1) 43 (77) 41 (33) 27(26) 73 (19)
Пронилформиат 88 (0,41) 31 (123) 42 (89) 29 (38) 27 (36)
Этилацетат .... 88 (7,1) 43 (181) 29 (46) 45 (24) 27 (24)
£4!i8?2 __ Метилпропиоиат . . . . 88 (23) 29(110) 57 (83) 27 (40) 1 59 (27)
•
C4HsS l ианиклопентан (тетрагидрогио- * —
фен) 88 (44) 60(82) 45 (29) 46 (29) 47 (22)
С4НэВг 1-Бромбутаи - - 136 (7,0) 57 (86) 41 (63) 29 (50) 27 (46)
Со С4Н9Вг 2-Бромбутан .... 136 (0,72) 57 (108) 41 (65) 29 (61) 27 (36)
* C,H9NO2 Пирролидин 71 (24) 43 (102) 28 (38) 70(33) 42 (20)
c4h9no2 Бутилнитрат 103 (0,0) 27 (55) 43(54) 41 (50) 30 (47)
C4H,0Hg Диэтплртуть 260(12) 29 (188) 27 (54) 28 (21) 231 (15)
с4н,0 Бутан - ... - 58 (12) 43(100) 29 (44) 27 (37) 28 (33)
C4H10 Изобутан ... 58 (3,2) 43(117) 41 (45) 42 (39) 27 (33)
с4н10о Бутиловый спирт 74 (0,37) 31 (52) 56(44) 41(31) 43 (30)
c4H,0o нтор-Бутиловый спирт 74 (0,30) 45(116) 31 (23) 59 (22) 27 (20)
c4HI0o трет-Бутиловый спирт ... 74 (0,0) 59 (92) 31 (31) 41 (19) 43(14)
c4H,0o Изобутиловый спирт .... 74 (7,5) 43(84) 31 (56) 42 (48) 41(47)
c4H10o Диэтиловый эфир 74 (22) 31 (73) 59 (34) 29 (29) 45 (28)
C4H10O Метнлизопропиловый эфир .... 74 (8,3) 59 (126) 29 (42) 43 (37) 15 (32)
C4H10O2 1, 1-Дпметоксиэтан (диметплаце-таль)' 90 (0,06) 59 (93) 29 (52) 15 (37) 31 (37)
C4H10O2 1, 2-Диметоксиэтан 90 (12) 45 (177) 29 (53) 15 (50) 60(16)
C4H10O2 2-Этоксиэтанол (этилцеллозольв) 90 (0,49) 31(112) 29 (57) 59 (56) 27 (31)
C4H10O2 Перекись этила 90 (20) 29(116) 15 (42) 45 (34) 62 (30)
C4H,OS Метилизопропилсульфид 75 (47)
(З-метил-2-тиабутан) . . . 90(41) 41(49) 43 (41) 48 (38)
C4HI0S Метилпропилсульфид (2-тиапентан) 90 (58) 61 (126) , 48(50) 41(43) 27 (43)
c4H10s Диэтилсульфид (3-тиапеитаи) 90 (41) 75 (59) 47 (51) 27 (39) 61 (33)
c4HIos Бутилыеркаптан (бутантиол-1) 90 (40) 56 (74) 41 (65) 27 (42) 47 (31)
c4HI0s втор-Бутилмеркаптан (бутан-
тиол-2) 90(34) 41 (56) 57 (50) 61 (46) 29 (46)
C4H10S трет-Бутилыеркаптан (2-метилпро-
пантиол-2) 90(34) 41 (68) 57 (61) 29(44) 39(21)
C4H10S Изобутилмеркаптан (2-метилпро-
пантиол-Г) 90 (35) 41 (60) 43 (46) 56(34) 47(29)
C4H10S2 Метилпропилдисульфид (2, 3-днтиа-
гексан) 122 (37) 80 (53) 43 (36) 41 (27) 27 (25)
C4H1052 Диэтилдисульфид (3, 4-дитиа-
гексан) ... 122 (73) 29(82) 66 (81) 27 (57) 94(53)
C4H]0SU3 Этилсульфит ..... 138 (3,3) 29(131) 31 (59) 45 (42) 27 (39)
c4h„n Диэтил амин 73 (17) 58 (83) 30 (81) 28 (30) 27 (24)
C4HnN Бутнламин - 73 (12) 30(200) 28 (23) 27(16) 18(12)
Й c4h„n «гор-Бутилам ин 73 (1,2) 44 (170) 18(25) 41(18) 58(18)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИМИ и НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Формула Название -Массовое число и интенсивность
материнский инк ОСНОВНОЙ инк три следующие по интенсивности пика
C4HnN c4h„n C4H12Pb c5F10 C5F12 c4f,, трет-Бутиламин Изобутиламин Тетраметилсвинец Декафторциклопентан . • - Додекафтор-2-метилбутан ... Додекафторпентан 73 (0,25) 73(1,0) 268 (0,14) 250 (0,62) 288 (0,0) 288 (0,08) 58 (127) 30 (22) 253 (69) 131 (173) 69 (277) 69 (259) 41 (26) 28 (2,0) 223 (59) 100(41) 119(45) 119(76) 42 (20) 41 (1,2) 208 (46) 31 (40) 131 (23) 169 (25) 15 (18) 27(1,1) 251 (36) 69 (28) 31 (18) 31 (24)
QHF, C5H5N сдп Нонафторциклопентан Пиридин . - • Циклопентадиен 232 (0,07) 79 (135) 66 (95) 131 (61) 79 (135) 66(95) 113(49) 52 (95) 65(40) 69 (34) 51 (48) 39 (35) 31 (19) 50(35) 40 (30)
СчН„ транс-Пентен-2-пн-4 - - • 66(77) 66(77) 39 (54) 65 (38) 40 (35)
C.H.N, 2-Метилпиразин . ... 94 (81) 94 (81) 67 (48) 26 (33) 39 (30)
C5H6O, фурфуриловый спирт • • 98 (3,4) 98 (3,4) 41 (3,3) 39 (3,3) 42 (2,6)
2-Метилтиофен 98 (68) 97(125) 45 (26) 39 (17) 53 (11)
C5H6S 3-Метилтиофен - 98 (74) 97 (138) 45 (35) 39 (14) 2 7 (11)
C8H8 .Метиленциклобутан 68 (38) 40 (67) 67 (48) 39 (47) 53 (21)
c;h; Сппропентан ... 68 (8,9) 67 (58) 40 (56) 39 (52) 53 (23)
C5H8 Циклопентен 68 (41) 67 (99) 39 (36) 53 (23) 41 (19)
C5H8 З-Метилбутадиен-1, 2 68 (53) 68 (53) 53 (40) 39 (28) 41 (26)
C8H8 2-Метилбутадиен-1,3 (изопрен)' 68 (40) 67 (48) 53(41) 39 (34) z7 (23)
СД Пеитадиен-1,2 ... 68 (39) 68 (39) 53 (38) 39 (37) 27 (31)
C5H8 ((нс-Пентадиен-1.3 68 (40) 67 (53) 39 (43) 53 (38) 41 (25)
C5H8 транс-Пента диен-1, 3 - . . . 68 (41) 67 (52) 39 (43) 53 ('Д 41(26)
CsHa Пентадиен-1,4 .......... 68 (40) 39 (47) 67 (35) 53 (33) 41 (30)
C5H8 Пентадиен-2,3 68 (62) 68 (62) 53 (42) 39 (36) 41 (<11)
C5H8 З-Метилбутин-1 ........ 68 (8,5) 53 (74) 67 (45) 27 (35) 39(21)
CsH8 Пентин-1 68 (8,7) 67 (50) 40 (44) 39 (42) 27(34)
C5H8 Пентин-2 68 (67) 68 (67) 53 (61) 39 (32) 27 (27)
c8h8n2 3,5-Диметилпиразол 96 (47) 96 (47) 95 (37) 39 (16) 54 (12)
CJLO-. Ацетилацетон (2,4-пентандион)' . 100(22) 100 (0,16) 43 (120) 85 (33) 15 (23) 27 (11)
C5H8O2 2-Пропенилацетат 43 (177) 41 (30) 39(29) 15 (28)
C5H8O2 Метилметакрилат 100 (26) 41 (78) 69 (52) 39 (31) 15 (16)
C5H9C1O2 Этил-₽-хлорпропионат 136 (0,70) 27 (65) 29 (62) 91 (42) 63 (37)
Q5H10 транс-1, 2 Диметилциклопропан 70 (42) 55 (79) 42 (34) 41 (33) 39 (30)
c5H,„ Этилциклопропан 70 (26) 42 (93) 55 (47) 41 (39) 39 (35)
CSHI0 Циклопентан 70 (44) 42(148) 55 (43) 41 (43) 39 (31)
C5U,o 2-Метплбутен-1 . 70 (30) 55 (97) 42 (36) 39 (34) 41 (28)
C5H,o З-Метилбутен-1 70 (26) 55 (102) 27(31) 42 (28) 29 (27)
c5H10 2-Метилбутен-2 70(31) 55 (88) 41 (31) 39 (28) 42 (27)
C5H10 Пентен-1 70 (27) 42 (89) 55 (53) 41 (39) 39(31)
CSH1O /(ис-Пентен-2 70 (30) 55 (89) 42(41) 39 (30) 29 (26)
CgHio транс-Пентен-2 70(31) 55 (93) 42 (41) 39 (30) 41 (28)
c5H10o Изовалериановый альдегид 86 (3,0) 41 (30) 43 (26) 58 (20) 29 (20)
C5H10O Метилпропнлкетон 86(16) 43(106) 29(23) 27 (23) 57 (20)
CsH10O Диэтилкетон 86(15) 57 (87) 29 (87) 27 (32) 28 (9,4)
C5H10O Аллилэтиловый эфир 86 (6,2) 41 (52) 29 (48) 58 (44) 57 (42)
C5H10O Винилизопропиловый эфир ... 86(21) 43 (87) 44 (69) 41 (46) 27 (45)
C5H10O 2-Метилтетрагидрофуран .... 86 (8,9) 71 (57) 43 (55) 41 (40) 27 (27)
c5H,0o, Тетрагидрофурфуриловый спирт 102 (0,02) 71 (8,9) 43 (6,8) 41 (4,8) 27 (3,8)
CsHi0O2 Винил-2-метоксиэтиловый эфир 102 (3,0) 29 (69) 45 (58) 15 (48) 58 (45)
csHI0o2 Ппв^левая (триметилуксусная)
кислота 102 (2,0) 57 (83) 41 (38) 29(27) 39 (12)
n I 0 0 а-Метилмасляная кислота . . . 102 (0,32) 74(54) 57 (34) 29 (33) 41 (28)
C5H10O2 Бутилформиат 102 (0,27) 56 (80) 41 (48) 31 (47) 29(42)
CsHl0O2 нтор-Бутилформиат 102(0,17) 45(99) 29 (49) 27 (32) 41 (31)
C5H|0O2 Изобутилформиат 102 (0,27) 43(8) 56(48) 41 (46) 31 (38)
C6H10O2 Пропилацетат 102 (0,07) 43(176) 61 (34) 31 (31) 27 (26)
C5H|0O2 Изопропилацетат ... 102 (0,17) 43 (155) 45 (50) 27 (22) 61 (18)
c5h10o2 Этилпропионат 102 (10) 29 (151) 57 (97) 27 (52) 28 (24)
C5H10O2 Метилбутират 102 (1,0) 43(53) 74 (37) 71 (29) 27 (23)
^5^10^2 Метилизобутират 102 (8,9) 43 (69) 71 (23) 41 (19) 59 (17)
CgHioOg Диэтилкарбонат 118(0,30) 29(114) 45 (80) 31 (60) 27 (46)
c5H10s 2-Метилтиациклопентан .... 102 (37) 87 (88) 41 (30) 45(29) 59 (18)
C5HI0S З-Метилтиациклопентан ..... 102 (40) 60(45) 41 (31) 45 (25) 74 (23)
C5H10S Тиациклогексан 102 (43) 87 (44) 68 (33) 61 (32) 41 (28)
C5H,„S Циклопентантиол 102 (19) 41 (48) 69 (47) 39 (26) 67 (18)
c5h„n Пиперидин 85 (22) 84 (43) 57 (22) 56(22) 44 (17)
C6HnNO N-Метилморфолин 101 (4,4) 43 (18) 42 (8,6) 15 (3,4) 71 (2,9)
C6H„NO, Изоамилнитрит 117(0,0) 29 (75) 41 (68) 57 (43) 30 (42)
C5H,2 2, 2-Диметилпропан (неопентан) 72 (0,01) 57 (126) 41 (52) 29 (49) 27 (20)
C5H,2 2-Метилбутан (изопентан) .... 72 (4,7) 43 (74) 42(64) 41 (49) 57 (40)
C5H12 Пентан 72 (10) 43(114) 42(66) 41 (45) 27 (39)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАН И Ч ECKl^Bf НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
52 Продолжений
Н* Массовое число и интенсивность
Формула Название материнский ОСНОВИОй
пик пик три следующие по интенсивности пика
сЕн12о 2-Метилбутаиол-1 . . 88 (0,18) 57 (57) 29 (55) 41 (53) 56(50)
С5Н12О З-Метилбутанол-1 88 (0,02) 55 (47) 42 (42) 43 (39) 41 (38)
С5Н12О 2-Метилбутанол-2 88 (0,0) 59 (43) 55 (37) 45 (25) 73 (22)
сЕн12о Пентанол-1 88 (0,0) 42 (41) 55(30) 41 (25) 70 (23)
С5Н12О Бутилметиловый эфир . . . . . 88 (3,1) 45(211) 56 (36) 29 (36) 27 (28)
СЕН12О гггор-Бутилметиловый эфир . . 88 (2,0) 59 (142) 29(50) 27 (27) 41 (25)
С5Н12О трет-Бутилметиловый эфир .... 88 (0,02) 73(119) 41 (33) 43 (32) 57 (32)
СЕН|2О Изобутилметиловый эфир .... 88(12) 45(186) 41 (30) 29 (30) 15(27)
С5Н12О Изопропилэтиловый эфир .... 88 (2,6) 45(143) 43(46) 73 (40) 27 (24)
СЕН|2О2 Диэтоксиметан (этилаль) . . - 104(2,1) 31(104) 59 (99) 29(62) 103 (39)
С5Н12О2 1, 1-Диметоксипропан 104(0,05) 75 (84) 73 (62) 29,(43) 45 (37)
CEH12S Бутилметилсульфид (2-тиагексаи) 104 (38) 61 (77) 56(50) 41 (39) 27(33)
c5H12s трет-Бутилметилсульфид
(3,З-диметил-2-тиабутан) . . - 104 (30) 57(83) 41 (62) 29 (42) 39 (16)
CEri12S Изобутилметилсульфид
(4-метил-2-тиапентан) 104 (37) 41 (46) 56(38) 27 (29) 39 (23)
CEH|2S 1 Тропилэтилсульфид (3-тиагексан) 104 (30) 75 (72) 27 (53) 47 (50) 62(33)
c5h12s Изопропилэтилсульфид
(2-метил-З-тиапеитаи) ... 104 (82) 89(119) 62 (79) 43 (63) 61 (58)
CEHI2S 2,2-Диметилпропаитиол-1 . . . . 104(31) 57 (100) 41 (55) 55 (48) 29(42)
C5H12S 2-Метилбутантиол-1 104(28) 41 (65) 29 (44) 57 (40) 70 (40)
CEH12S 2 Метилбутантиол-2 • 104(18) 43 (88) 71 (54) 41 (46) 55(34)
C5HI2S З-Метилбутантиол-2 ..... 104 (23) 61 (73) 43(55) 27 (33) 55 (28)
C5H12S Пентантиол-1 104(35) 42 (91) 55 (44) 41 (39) 70 (39)
CEHI2S Пентаитиол-2 .... ... 104 (28) 43 (72) 61 (52) 27 (39) 55(38)
CEH12S Пентантиол-3 ......... 104 (23) 43 (56) 41 (48) 75(29) 47 (23)
CEH12S2 трет-Бутил мети л д ис у льф ид
(4, 4-диметил-2. 3-дитпапентан) 136(12) 57 (74) 41 (38) 29(36) 80 (13)
CEHrS2 Изопропилэтилдисульфид
(2-метпл-З, 4-дитиагексан} . . 136 (20) 94 (49) 27 (46) 43 (39) 66 (37)
cEH14Pb Триметнлэтилсвииец . . . . . 282 (0,64) 223 (61) 253 (52) 208 (51) 221 (33)
C6Fe Гексафторбензол 186 (95) 186 (95) 117(59) । 31(58) 93(23)
C6F„ Тетралекафтор-2-метилпентан 338 (0,0) 69 (317) 131 (41) 119(36) 169 (29)
CeFH Тетра декафторгексан 338 (0,13) 69 (268) 119(74) 169(51) 131 (3/)
C6H5Br Бромбензол 156 (75) 77 (98) 158 (74) о! (41) 50 (36)
C6H5C1 Хлорбензол ... 112(102) 112(102) 77 (49) 114(33) 51 (17)
c6h5no2 Нитробензол 123(39) 77 (93) 51 (55) 50 (23) 30(15)
C6H6 Бензол 78(113) 78(113) 52(22) 77 (20) 51 (18)
C6H6 Гексадиин-1,5 . . 78 (58) 39 (65) 52 (38) 51 (32) 50 (26)
C6H6 Гекса диин-2, 4 78 (108) 78 (108) 51 (55) 52 (38) 50 (31)
C6H6S Тиофеиол 110(68) 110(68) 66 (26) 109(17) 51 (15)
c6h7n Анилин 93 (19) 93 (19) 66 (6,5) 65 (3,6) 39 (3,5)
c6h7n 2-Метилпиридин . - - • 93 (86) 93 (86) 66 (36) 39 (28) 51 (16)
c6h7no 1-Метил-2-пиридон 109(1) 109(1) 81 (49) 39 (34) 80 (29)
C6H8 Циклогексадиен-1,3 80 (53) 79 (92) 77 (35) 39(21) 27 (18)
C6H8O 2,5-Диметилфураи .... 96 (57) 43 (65) 95(48) 53 (37) 81 (24)
C6H6S 2,3-Диметплтиофен 112(44) 97(53) 111(44) 45 (16) 27 (9,4)
C6H8S 2, 4-Диметилтиофен 112(27) 111 (36) 97 (18) 45 (9,4) 39 (7,0)
C6H8S 2,5-Диметилтиофен 112(67) 111(95) 97 (59) 59 (23) 45 (19)
C6H8S 2-Этилтиофен ... . ... 112 (27) 97 (68) 45 (16) 39 (8,9) 27 (5,4)
C6H8S 3-Этилтиофен . . 112(54) 97 (147) 45 (38) 39 (20) 27 (12)
c6h9n 2,5-Диметилпиррол . 95 (73) 94 (127) 26 (52) 80 (22) 42(19)
c6h10 Изопропенилциклопропаи . . 82 (20) 67 (92) 41 (47) 39 (46) 27 (22)
C6H10 1 -Метилциклопентен 82 (26) 67 (98) 39 (21) 81 (16) 41 (16)
C6H,0 Циклогексен 82 (33) 67(83) 54(64) 41(31) 39(30)
C6HI0 2, З-Диметилбутадиен-1, 3 . . . . 82 (41) 67 (60) 39 (55) 41 (44) 54(22)
CeHl0 2-Метилпентадиен-1, 3 82 (23) 67 (48) 39 (30) 41 (26) 27 (13)
C6H,o Г ексадиен-1,5 82(1,3) 41 (98) 67 (80) 39 (60) 54 (52)
c6H10 3. З-Диметилбутпн-1 82 (0,57) 67 (101) 41 (57) 39(31) 27(11)
C6H10 4-Метилпентин-1 . ... 82 (2,3) 67 (82) 41 (74) 43(64) 39(55)
CeH,o Г ексии-1 .... 82(1,0) 67 (131) 41 (88) 27 (85) 43 (67)
C6H10 Г ексин-2 82 (56) 67 (58) 53(50) 27 (39) 41 (36)
C6HIO Гексин-3 82 (55) 67 (59) 41 (55) 39 (37) 53 (20)
C6H10O Циклогексанон 98 (32) 55 (102) 42 (86) 41 (35) 27(64)
C6H10O 4-Метилпентен-3-он-2 98 (40) 55 (82) 83 (82) 43 (64) 29 (38)
C6H10O2 Гександион-2,5 (ацетони.тацетои) . 114 (4,0) 43 (148) 15 (25) 99 (22) 14(14)
C6H10O3 Пропионовый ангидрид 130 (0,0) 57 (190) 29(119) 27 (62) 28 (26)
C6H10O3 Этилацетоацетат 130 (8,3) 43 (150) 29(52) 27 (32) 15 (27)
C6H„N Капронитрил . - 97 (0,54) 41 (73) 54 (49) 27 (43) 55 (40)
C6HnN Изокапронитрил 97 (0,13) 55 (98) 41 (51) 43(45) 27 (39)
CeH12 a СЛ 1, 1,2-Триметилциклопропан • . 84 (38) 41(132) 69 (81) 39 (34) 27 (24)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИМИ и НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Формула Название Массовое число и интенсивность
•материнский пик основной пик три следующие по интенсивности пика
СбН12 1-Метил-1-этилциклопропан . . 84 (25) 41 (78) 55 (58) 69(53) 27 (33)
СбН12 Изолропилциклопропан 84 (2,0) 56(114) 41 (84) 39 (30) 43 (28)
С6Н,2 Этилциклобутан 84 (3,8) 56 (138) 41 (89) 27 (35) 55 (34)
^еН12 Метилциклопентан 84(18) 56(116) 41 (74) 69 (37) 42(33)
С6Н12 Циклогексан 84 (58) 56 (75) 41 (44) 55 (25) 42 (21)
С6н12 2, З-Диметилбутен-1 84 (27) 41 (117) 69 (96) 39 (36) 27 (24)
СеН12 3, З-Диметилбутеи-1 84(23) 41 (112) 69 (107) 39 (28) 27 (26)
С6н12 2-Этилбутен-1 84 (30) 41 (74) 69(66) 55(56) 27 (38)
С6н12 2,3-Диметилбутен-2 84 (32) 41 (108) 69 (88) 39 (35) 27 (20)
С6н12 2-Метилпентен-1 84 (29) 56 (91) 41 (73) 55 (39) 39 (36)
С6Н12 З-Метилпентен-1 84 (25) 55(85) 41 (67) 69(60) 27 (43)
С6Н12 4-Метилпеитен-2 84(12) 43(110) 41 (80) 56 (47) 27 (37)
С6Н|2 2-Метилпентен-2 . 84 (36) 41 (120) 69(111) 39 (35) 27 (28)
С6Н12 З-Метил-цис-пентен-2 84(37) 41 (104) 69(82) 55 (46) 27 (36)
С6Н,2 З-Метил-транс-пентен-2 84 (38) 41 (102) 69 (81) 55 (47) 27 (35)
СсН12 4-Метил-г<«с-пентен-2 84 (35) 41(122) 69(114) 39 (35) 27 (26)
СбН|2 4-Метил-транс-пентен-2 84 (34) 41 (123) 69(112) 39 (34) 27 (26)
С6Н12 Гексен-1 84 (20) 41 (70) 56 (60) 42 (52) 27 (48)
^6^12 /(ис-Гексен-2 . 84 (27) 55(91) 42 (51) 41 (45) 27 (45)
^6^12 транс-Гексен-2 84 (32) 55(112) 42 (54) 41 (46) 27 (41)
С6Н12 Чис-Гексен-3 - 84 (28) 55 (81) 41 (62) 42 (54) 27 (32)
СсН12 гр«нс-Гексен-3 .......... 84 (32) 55 (89) 41 (72) 42 (62) 27 (35)
CcH,2N2 Ацетоназин (кетазин) 112(31) 56 (99) 15(31) 97 (31) 39 (26)
с6н12О Циклопентллметанол 100(0,02) 41 (35) 68 (32) 69 (31) 67 (24)
СеН12О Изобутилметилкетон 100(12) 43(115) 58 (37) 41 (22) 57(22)
С6Н12О Бутилвинпловый эфир 100 (5,7) 29 (80) 41 (59) 56 (45) 57 (35)
сен12о Винилизобутиловый эфир .... 100 (5,8) 29(73) 41 (65) 57 (58) 56 (40)
С6Н12О2 Диацетоновый спирт 116(0,0) 43(149) 15(45) 58(32) 27 (14)
С6н|2о2 Бутилацетат 116(0,03) 43(172) 56 (58) 41 (30) 27 (27)
С6Н|2О2 Пропилпропионат 116(0,03) 57 (147) 29 (84) 27 (57) 75 (47)
С6Н,2О2 С6Н12О2 Изопропилпропиоиат Метилпивалат (метиловый эфир 116(0,26) 1/ I 57(116) 43 (88) 29 (54) 27 (46)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИ
С,Н,,О Этилбутпрат . И6(2,2) 43 (50) 71 (45) 29 (43) J 27 (31) S
С(,1112О3 2, 4, 6-Триметил-1, 3, 5-триокси- X
циклогексан 132 (0,12) 45 (196) 43 (107) 29 (35) 89 (23) m
C6H12S Метилциклопентилсульфид . . . 116(31) 68 (72) 41 (64) 39 (37) 67 (37) С
C6H,2S zfuc-2, 5-Диметилтиациклопентан 116(32) 101 (85) 59 (34) 41 (26) 74 (24) с
C6H12S тронс-2, 5-Диметилтиацпклопентан 116(32) 101(85) 59 (34) 74 (25) 41 (25)
C6H12S 2-Метилтиациклогексан 116 (42) 101 (81) 41 (37) 27 (32) 67 (30) Е X
C6HI2S З-Метилтиациклогексан 116(41) 101(55) 41 (47) 39 (33) 45(28)
C6H12S 4-Метилтиациклогексан 116 (46) 116(46) 101 (44) 41 (40) 27 (39)
C6H12S Тиацпклогептан ... 116 (60) 87 (75) 41 (66) 67 (48) 47(46) о
CeHI2S 1-Метилциклопентаитиол 116(20) 83 (76) 55 (58) 41 (39) 67 (33) -1
C6H12S z^zzc-2-Метилциклопентаптпол . . . 116(32) 55 (55) 83 (54) 60(48) 41 (47) 3
c6H12s транс-2-Метилциклопентантиол . . 116(28) 67 (48) 55 (46) 41 (42) 83 (40) X
CcH12S Циклогекс антиол ... .... 116(21) 55(56) 41 (45) 67 (35) 83 (32) tfl
C6H13N Циклогексиламин 99 (8,9) 56(92) 43 (25) 28 (13) 30 (13) О Ж
C6H,3N З-Метилпиперидин 99 (23) 44 (49) 30 (34) 28 (27) 57 (26) .s
C6H13NO N-Этилморфолин 115(2,0) 42 (9,8) 57 (7,0) 100 (5,2) 28 (4,3)
C6H,4 2,2-Дпметилбутан 86 (0,04) 43 (85) 57 (82) 71 (61) 41 (51) с
C6H14 2,3-Диметилбутан - 86(5,3) 43 (157) 42 (136) 41 (49) 27 (40) п
C6HI4 2-Метилпентан 86(4,4) 43 (147) 42 (78) 41 (47) 27(40) S
C6H14 З-Метилпентан 86 (3,2) 57 (105) 56(80) 41 (67) 29 (64) X го
C6H14 Гексан 86 (12) 57 (87) 43 (71) 41 (64) 29 (55) X
c6h14n2 z{Zzc-2, 5-Диметилпиперазпп . . . 114(0,38) 58 (10) 28 (7,7) 30 (4,7) 44 (4,2) X
C6H14O 2-Этилбутанол-1 102 (0,0) 43(114) 70 (40) 29(39) 27 (38)
C6H14O 2-Метилпентанол-1 102 (0,0) 43(110) 41 (40) 29 (34) 27 (33)
C6H14O З-Метилпентанол-1 102 (0,0) 56(26) 41 (20) 29 (19) 55 (18)
C6H14O 4-Метил пентанол-2 102 (0,08) 45(111) 43 (34) 41 (17) 27 (14)
c6H14o Гексанол-1 102 (0,0) 56(63) 43 (52) 41 (37) 55(36)
c6H,4o Бутилэтиловый эфир 102 (3,8) 59 (108) 31 (87) 29 (61) 27 (42)
C6H,4O втор-Бутилэтиловый эфир ... 102(1,5) 45 (150) 73 (76) 29 (51) 27 (39)
C6H14O Изобутилэтиловый эфир . . 102 (8,7) 59 (124) 31 (95) 29 (53) 27 (38)
C6HI4O Диизопропиловый эфир . . . 102(1,4) 45 (125) 43 (66) 87 (23) 27(19)
C6H14O2 1, 1-Диэтоксиэтан (ацеталь) . . . 118(0,0) 45 (132) 73 (69) 29 (36) 27 (27)
C6H14O2 1, 2-Диэтоксиэтан 118(1,2) 31 (124) 59 (88) 29 (72) 45(53)
C6H14O3 биб>2-Метоксиэтиловый эфир . . 134 (0,0) 59 (140) 29(74) 58 (57) 15(56)
c6Hl4s Бутилэтилсульфид (3-тиагептан) 118(35) 75 (55) 29 (33) 27 (33) 62 (28)
C6H14S втор-Бутилэтилсульфид
(4-метил-З-тиагексан) 118(195) 89 (585) 29 (343) 27 (296) 41 (279)
a
Продолжение
Формула Название Массовое число и интенсивность
материнский пик основной пн к три следующие по интенсивности пика
C6H14S трет-Бутилэтилсульфид (2,2-диметил-З-тиапентан) . . . 118(33) 57(147) 41 (70) 29 (54) 27 (40)
C6H14S Изобутилэтилсульфпд (5-метил-З-тиагексан) 118(171) 75 (520) 41(230) 47 (224) 56(217)
C6H14S Дипропилсульф ид (4-тиагептан) 118(47) 43 (86) 89 (74) 41 (57) 27 (55)
Изопропилпропилсульфид (2-метил-Зтиагексан) 118(206) 43 (540) 41 (317) 42 (301) 27(287)
C6H14S Диизопропплсульфид (2, 4-диметил-З-тиапентан) - 118(33) 43 (94) 61 (85) 41 (48) 103(44)
c6H14s 2-Метилпентантиол-1 118(19) 43 (96) 41 (51) 56 (32) 27 (31)
C6H,-4S 4-Метилпеитантиол-1 118(30) 56 (142) 41 (57) 43(57) 27 (32)
C6H14S 4-Метилпентантиол-2 118(6,3) 43 (68) 69(61) 41 (56) 84 (42)
C6H14S 2-Метилпеитантиол-З ....... 118(20) 41 (64) 43(63) 75 (50) 27 (28)
CeH14S Гексантиол-1 118(16) 56 (66) 41 (41) 27 (40) 43 (38)
^-бН]4Ь'2 втор-Бутилэтилдисульфид (5-метил-3,4-дитиагептан) . . . 150 (14) 29 (86) 94 (66) 66 (57) 27(41)
СеН14Ьо Изобутилэтилдисульфид (6-метил-3,4-дитиагептан) • . 150 (4,9) 29 (42) 66(40) 122 (30) 94 (29)
^бЧ14^2 Дипропилдпсульфид (4, 5-дитиа- октан) 150 (44) г 43 (167) 27 (65) 41 (64) 108 (35)
СеНи52 Диизопропилдисульфид (2, 5-диметил-З, 4-дитиагексан) 150 (31) 43 (152) 108 (41) 41 (36) 27 (30)
Триэтиламин 101 (21) 86(134) 30 (46) 27 (36) 58 (35)
C6H15N Дипропиламин 101 (7,1) 30 (89) 72 (70) 44 (36) 43(28)
C6H15N Диизопропиламин - . 101 (5,0) 44(171) 86 (52) 58 (24) 42 (22)
C6H16Pb Днметилдиэтилсвииец 296 (0,98) 267 (89) 223 (83) 208 (79) 221(44)
C7F14 Тетрадекафторметилциклогексан 350 (0,0) 69 (244) 131 (107) 181 (48) 100(38)
16 Г ексадекафторгептан 388 (0,0) 69 (330) 119 (89) 169 (68) 131 (44)
c7h6n Бензонитрил 103 (246) 103 (246) 76 (80) 50 (42) 51 (24)
C7H7Br о-Бромтолуол 170(48) 91 (97) 172 (46) 39 (21) 63 (20)
C7H7Br п-Бромтолуол 170(46) 91 (97) 172 (45) 39 (20) 65 (19)
C7H7C1 о-Хлортолуол 126 (44) 91 (121) 63(20) 39(19) 89 (18) 1 QO zI
C7H7C1 м-Хлортолуол . 126 '5В , 91^2ф»1
С7Н7С1 л-Хлортолуол 126(44) 91 (120) 125 (19) 1 63 (18) 39 (17)
c7h7f л!-Фтортолуол • 110 (79) 109 (129) 83(17) 57 (12) 39 (12)
c7h7f n-Фтортолуол . .... 110(73) 109(122) 83 (16) 57 (12) । 39 (9,3)
С7Н8 Толуол 92 (82) 91 (108) 39 (20) 65 (14) 51 (10)
C7HBS Метилфенилсульфид 124(76) 124 (76) 109 (34) 78 (25) 91 (19)
c7h9n 2,4-Диметилпиридин . - . 107 (76) 107(76) 106 (29) 79(16) 92 (13)
c7h10s 2, 3, 4-Триметилтиофен 126 (50) 111 (81) 125(47) 45 (22) 39 (18)
C7H,a Винилциклопентан 96 (13) 67(118) 39(44) 68 (38) 54 (35)
с7н“ Этилиденциклопентан 96(40) 67 (180) 39 (44) 41 (30) 27 (30)
C7H,2 Бицикло [2.2.1] гептан . . 96(12) 67 (64) 68 (50) 81 (44) 54 (30)
CH З-Этилциклопентен 96 (29) 67 (193) 39 (36) 41 (35) 27 (26)
C7h“ 1 -Метилцнклогексен 96 (32) 81 (83) 68 (38) 67 (37) 39(33)
C7H12 4-Метилциклогексен 96(28) 81 (84) 54 (50) 39 (44) 55 (34)
c7H 4-Метилгексин-2 .... ... 96 (13) 81 (71) 67 (52) 41 (48) 39 (35)
C7H12 5-Метилгексин-2 96 (42) 43 (49) 81 (43) 27 (39) 39 (38)
C7H12 Г ептин-1 96 (0,44) 41 (75) 81 (70) 29 (65) 27 (47)
c7h14 1, 1, 2, 2-Тетраметилциклопропан 98 (21) 55 (92) 83 (90) 41 (69) 39 (41)
c7h14 цис-l, 2-Диметилциклопентаи 98 (19) 56 (85) 70 (77) 41 (65) 55 (65)
c7h14 транс-1,2-Диметилциклопентан 98 (25) 56 (93) 41 (63) 55 (61) 70 (54)
c7h14 цис-1,3 Диметилциклопеитан 98(12) 56 (81) 70 (78) 41 (64) 55 (59)
c7h14 транс-1, 3-Диметилциклопентан 98 (13) 56(81) 70 (68) 41 (63) 55 (58)
C7H14 1, 1-Диметилциклопеитан 98 (6,7) 56(81) 55 (63) 69 (56) 41 (55)
C7H,4 Этилциклопентан 98 (14) 69 (83) 41 (78) 68(60) 55 (46)
C7h“ Метилциклогексан 98 (41) 83 (94) 55(78) 41(55) 42(34)
C7HI4 Циклогептан .... . . 98 (37) 41 (57) 55 (54) 56 (50) 42 (49)
C7HI4 2, 3, З-Триметилбутен-1 98 (20) 83(101) 55 (83) 41 (61) 39 (33)
C7h“ З-Метил-2-этплбутен-1 98 (22) 41 (71) 69(71) 55 (62) 27 (38)
C7H14 2, З-Диметилпентен-1 98 (13) 41 (92) 69 (86) 55 (40) 39 (35)
C7H,4 2,4-Диметилпентен-1 . . . 98 (9,1) 56(117) 43 (68) 41 (61) 39 (39)
C7H,4 3, З-Диметилпентен-1 98 (9,4) 69 (104) 41 (85) 55 (42) 27 (36)
C7HI4 3, 4-Диметилпентен-1 . 98 (0,61) 56 (75) 55 (62) 43 (55) 41 (54)
C7H,4 4, 4-Диметилпентен-1 . . . . . 98 (2,6) 57(161) 41 (86) 29(52) 55 (49)
C7H14 З-Этилпентен-1 ... 98 (19) 41 (116) 69 (91) 27 (43) 39 (37)
C7H14 2, З-Диметилпентен-2 98 (31) 83 (80) 55 (75) 41 (63) 39(34)
C7H14 2,4-Диметилпентен-2 98 (26) 83 (97) 55(71) 41 (52) 39 (34)
C7HI4 3,4-Диметил-1{ис-пентен-2 ..... 98 (30) 83(87) 55 (82) 41 (52) 27 (32)
C7H14 3,4-Диметил-транс-пентен-2 .... 98 (31) 83 (89) 55(83) 41 (52) 27 (34)
C7HI4 4,4-Диметил-1<и<7-пентен-2 98(27) 83 (96) 55(92) 41 (62) 39 (35)
C7Hl4 4,4-Диметил-трснс-пентен-2 .... 98 (28) 83 (105) 55 (89) ' 41(58) 39 (31)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСКИМИ И НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Массовое число и интенсивность
материнский основной
пик пик трн следующие по интенсивности пика
Формула
Название
— —« CN CN CJ ЭТ CCCOOz.Z ос ' Z- 3- — — Zh ~ ’т 'г . 'г 'г 'г * in coocaoocootoxo со uuuuuuuuuuouuuuu uuuJuuuuuuuuuuoo!. З-Этилпентен-2 2-Метилгексен-1 З-Метилгексен-1 4-Метилгексен-1 5-Метилгексен-1 2-Метилгексен-2 З-Метилгексен-2 4-Метилгексен-2 5-Метилгексен-2 2-Метил-гронс-гексен-З ...... З-Метил-^нс-гексен-З З-Метил-гранс-гексен-З ...... Г ептен-1 тронс-Гептен-2 транс-Гептен-3 2,4-Диметилпентанон-З ...... Бутилпропионат Изобутилпропионат Пропилбутират Дипропилкарбонат 1{пс-2-Метилциклогексантиол . . . 2,6-Диметилпиперидин 2, 2, З-Триметилбутан 2,2- Диметилпентаи ..... 2,3- Диметилпентан 2,4- Диметилпентан 3,3-Диметилпентан З-Этилпентан 2-Метилгексан З-Метилгексан Г ептан i Гептанол-2 98 (33) 98 (4,6) 98 (7,7) 98 (4,9) 98 (1,6) 98 (28) 98 (30) 98 (23) 98 (13) 98 (24) 98 (28) 98 (28) 98 (15) 98 (27) 98 (27) 114(13) 130 (0,03) 130 (0,07) 130 (0,05) 146 (0,02) 130 (28) 113(5,3) 100 (0.03) 100 (0,06) 100 (2,1) 100(1,6) 100 (0,03) 100(3,1) 100 (5,9) 100 (4,0) 100(17) 116(0,01) 41 (86) 56 (105) 55 (76) 41 (98) 56 (91) 69(113) 41 (95) 69(118) 56 (90) 69 (86) 69 (98) 69 (97) 41 (91) 55 (64) 41 (98) 43 (226) 57 (152) 57 (187) 43 (96) 43(171) 55 (138) 98 (73) 57(110) 57 (130) 43 (94) 43(139) 43 (166) 43 (175) 43 (154) 43(110) 43(126) 45(131;. „ 69 (80) 41 (54) 41 (60) 57 (94) 41 (75) 41 (99) 69 (90) 41 (106) 55 (74) 41 (74) 41 (82) 41 (86) 56 (79) 56 (59) 56 (65) 71 (62) 29 (98) 29 (87) 71 (90) 27 (61) 97 (70) 44 (43) 43 (84) 43(95) 56 (93) 57 (93) 71 (103) 70 (77) 42 (59) 57 (52) 41 (65) 55 (74) 27 (30) 69 (57) 56 (80) 55 (47) 27 (36) 55 (42) 55 (40) 43(71) 55 (62) 39 (33) 55 (63) 29 (64) 41 (50) 69 (55) 27 (49) 56 (54) 56 (52) 27(54) 63 (55) 81 (44) 42 (34) 56 (67) 41 (59) 57 (67) 41 (59) 27 (38) 71 (77) 41 (57) 71 (52) 57 (60) 27 (33) 39 (27) 56 (48) 29 (70) 27 (42) 39 (33) 27 (36) 39 (35) 41(57) 56 (37) 27 (33) 39 (35) 55 (54) 27 (35) 55 (47) 41 (42) 27 (52) 27 (47) 89 (48) 41(49) 41(44) 28 (26) 41 (64) 56 (52) 41 (64) 56 (50) 41 (36) 29 (45) 85 (49) 41 (50) 29 (58) 9Q /9^
с7н1Со с7н16о с7н,6о2
С7н16о2
С7Н16О2 c7H16s
c7H16s
C7H16S C7H|6S C7H18Pb C7H,8Pb C7Hl8Pb c7Hl8Pb C8H10 CgHio CgH10 CsHio B2H6 B5H9 co cos co2 cs2 HCI H2S n2 NF3 NH3 n2h4 NO no2 n2o o2 PH3 so2
Г сптанол-4............
Бутилпропиловый эфир • . Дипропоксиметан (дипропил-форм аль), .....................
Диизопропоксиметан (диизопро-пилформаль)' ...................
1. 1-Диэтоксипропан ............
втор-Бутилизопропилсульфид
(2, 4-диметил-З-тиагексан) трет-Бутилизопропилсульфид
(2, 2, 4-триметил-З-тиапентан) - • Гексилметилсульфид (2-тиаоктан) Гептаитиол-1 . .................
Метилтриэтилсвинеп ............
Бутилтриметилсвинец ............
вгор-Бутилтриметилсвинец трет-Бутилтриметилсвинец о-Ксилол.....................
л-Ксилол ............
п-Ксилол ...........
Этилбензол - - Диборан.............
Пеитаборан . - Окись углерода . . Сероокись углерода Двуокись углерода Сероуглерод .... Хлористый водород Сероводород .........
Азот.....................
Трехфтористый азот . . . Аммиак ..............
Гидразин ....................
Окись азота................
Двуокись азота ..... Закись азота ....
Кислород ...........
Фосфин ................. •
Сернистый ангидрид.............
116(0,02) 116(3,7) 55 (102) 43 (120) 73(72) 57 (102) 43 (45) 41 (51) 27 (32) 29 (49)
132 (0,58) 43 (194) 73(114) 27 (45) 41 (34)
132 (0,16) 43 (133) 45 (84) 73(71) 27 (28)
132 (0,0) 59 (138) 47 (88) 87 (84) 29 (74)
132 (30) 57 (149) 41 (74) 29 (35) 43 (32)
132 (30) 61 (94) 103 (60) 41 (51) 43(46)
132 (34) 61 (73) 56 (53) 27 (46) 41 (44)
132 (14) 41 (48) 27 (40) 56 (39) 70 (38)
310 (0,84) 281 (86) 208 (76) 223 (66) 237 (60)
310(0,14) 253 (76) 223 (75) 208 (68) 295 (52)
310(1,8) 253 (94) 223 (85) 208 (74) 251 (45)
310 (0,09) 252 (95) 223 (82) 208 (65) 250 (46)
106 (52) 91 (91) 105 (22) 39 (15) 51 (14)
106 (58) 91 (93) 105 (26) 39 (17) 51 (14)
106 (52) 91 (85) 105(25) 51 (13) 39 (13)
106 (45) 91 (146) 51 (19) 39 (14) 65 (12)
28 (0,13) 26 (54) 27 (52) 24 (48) 25 (30)
64 (15) 59 (30) 60 (30) 62 (24) 61(21)
28 (78) 28 (78) 12(3,7) 16(1,3) 29 (0,9)
60 (83) 60 (83) 32 (48) 28 (6,9) 12 (5,0)
44 (76) 44 (76) 28 (5,0) 16 (4,7) 12(1.9)
76(184) 76(184) 32 (40) 44 (33) 78 (16)
36 (54) 36 (54) 38 (17) 35 (9,2) 37 (2,9)
34 (75) 34 (75) 32 (33) 33 (32) 1 (4.1)
28 (65) 28 (65) 14 (3,3) 29 (0,47)
71 (10) 52 (33) 33 (13) 14(3,0) 19 (2,7)
17 (32) 17(32) 16 (26) 15 (2,4) 14 (0,7)
32 (48) 32 (48) 31 (23) 29 (19) 30(15)
30(76) 30 (76) 14 (5,7) 15(1,8) 16(1,1)
46 (6,6) 30 (18) 16 (4,0) 14(1,7) 47 (0,02)
44 (60) 44 (60) 30 (19) 14 (7,8) 28 (6,5)
32 (54) 32 (54) 16 (2,7) 28 (1,7) 34 (0,22)
34 (59) 34 (59) 33 (20) 31 (19) 32 (7,5)
64 (47) 64(47) 48(23) 32 (4,9) 16(2,4)
СВОДНАЯ ТАБЛИЦА СПЕКТРОВ МАСС ОРГАНИЧЕСн^В и НЕКОТОРЫХ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Радиоактивационный анализ
Радиоактивационный анализ основан на образовании в определяемом веществе искусственных радиоактивных изотопов и последующем измерении их радиоактивности. Искусственные радиоактивные изотопы получаются в результате ядерной реакции при облучении исследуемого образца в реакторе, на ускорителе или с помощью другого источника ядер-ных частиц (нейтронов, протонов, Не3 и др.).
Радиоактивационный анализ обладает крайне высокой чувствительностью (до 10” 17г)« Для измерения радиоактивности изотопов, используемых ври анализе, рекомендуются следующие приборы:
Излучение Типы измерений Прибор
Альфа (a) Калибровочные СОГ, С С (4л)
Практические ЖС, ТС, ПД, ПС (2л) или с тонким окном
Бета (p и Калибровочные С С (4 л)
₽+) Практические ЖС, ПС (2л) или торцевые; в случае измерения по вто-|)ичном^ у-нзлучению ТС,
Гамма (у) Практические ИК, ТС, ПД
Рентгеновское Калибровочные С С (для рентгеновского излу-
(и б'-захват) Практические чения), ПС (с рассчитанной эффективностью)
ПС, ИК, тс
Примечание. СОГ —-счетчик с определенной (известной) геометрией, в частности, с 50% геометрией прн внешне?.! источнике излучения (2л-счетчик) и 100% геометрией (4л-счетчик); ИК —ионизационная камера; СС —счетчики в схеме совпадений; ЖС—счетчик с жидкий сцинтиллятором; ТС —счетчик с твердым сцинтиллятором; ПС — пропорциональный счетчик; ПД —полупроводниковый детектор.
Для случая наиболее распространенной активации иа медленных или котловых нейтро-нал активность, создаваемая нейтронным потоком в исследуемом образце, определяется по формуле:
. 6,02 1023o®W I ,
3,7.W-« .М
0,693/ Т
(1а)
где А — активность в момент времени t, кюри*; о — сечение активации, см2; Ф — поток нейтронов, нейтрЦсм2 • сек}; W — вес облучаемой мишени (в пересчете на исследуемый элемент), г; J — относительное содержание активируемого изотопа в исследуемом элементе; М — атомный вес элемента: Г—период полураспада образовавшегося радиоактивного изотопа, сек; t — время облучения, сек.
Обозначая группу множителей перед скобками через As, получим:
/ 0,693/ \
АЛ\'~е Т I <1б>
где A g— так называемая активность насыщения.
При времени облучения < 0,15 периода полураспада образующегося радиоактивного изотопа формулу (16) можно упростить (с погрешностью^ 5%):
Д^Д// (2)
где Х==0»693/Т — постоянная распада радиоактивного изотопа.
Из формулы (1а) непосредственно следует, что количество вещества W, необходимое чтобы создать активность А определяется следующим образом:
А<М ~----------
0,602оФ/
где А* выражено в распадах в секунду, а о—в барнах**.
Приведенные выше формулы справедливы в том случае, если можно пренебречь уменьшением числа атомов мншени, происходящим в результате ядерной реакции, по сравиеиию с первоначальным числом атомов (практически это всегда выполняется) и если можно считать постоянными величину потока частиц и их среднюю энергию вовсе время облучения.
Более подробные сведения см.: 1. Материалы Международной конференции в Женеве по мирному использованию атомной энергии, 1955 г., т. 15, Гостехиздат, 1957, стр. 93. — 2. G. В. С о о к, Риге a. Appl. Chem., 1, 241 (1960). - 3. Н. F. Atkins, A. A. Smells, Adv. in Inorg.' Chem. a. Radiochem., 1, 315 (1959). — 4. F. Baumgartner. Z. Elektro-chem., 64, 1077 (1960).
* 1 кюри ==3.7- 10’° распаек.
** 1 барн» 10“ 24 см\
542
Радиоактивационный анализ
Пояснения к таблице
В 1-й графе приведены химические символы элементов (по алфавиту) и их порядковые номера. Здесь же указаны ядерные реакции для тех случаев, когда радиоактивный изотоп получается не по реакции (п, у). Символ (£) относится к радиоактивным изотопам, которые получаются в результате Р —-распада изотопа, образующегося по реакции (n, у). Символы, применяющиеся при записи ядерной реакции, см. «Справочник химика», 2-е изд. т. 1, стр. 180.
Во 2-й графе указаны сечения поглощения нейтронов в естествениой смеси изотопов данного элемента; эти сведения нужны для учета уменьшения нейтронного потока внутри исследуемой мишени.
Если сечение поглощения значительно больше, чем сечение активации (графа 10), то большая часть нейтронов поглощается с образованием стабильного, а ие интересующего нас радиоактивного изотопа. При этом имеет место экранирование внутреннего объема мишени ее наружными слоями, что приводит к уменьшению величины полезного потока нейтронов. В подобных случаях необходимо применять мишень в виде’" тонкой фольги.
В 3-й графе приведены массовые числа радиоактивных изотопов, образующихся в результате ядерной реакции. Метастабильное состояние ядер показано буквой т.
Если изотоп, получающийся в результате ядерной реакции, имеет другой, но сравнению с исходным элементом, порядковый номер, то приводится химический символ образующегося элемента с указанием его массового Числа.
В 4-й графе приведены периоды полураспада радиоактивных изотопов.
В графах 5—8 содержатся величины AsKlg (g — навеска в г).
Величина A^/g представляет собой активность соответствующего радиоактивного изотопа в кюри, если 1 г элемента с естественным содержанием активируемого изотопа подвергается облучению потоком тепловых нейтронов 10’3 нейтрЦсм* • сек) в течение единицы времени. Эта величина применяется для определения активности, когда время облучения 0.15 периода полураспада. В этом случае активность мишени вычисляется умножением величины Лд hfg на массу мишени в граммах (в пересчете иа исследуемый элемент) и иа время облучения.
При времени облучения >0.15 периода полураспада в таблице стоит звездочка. В таком случае расчет активности должен производиться с использованием данных графы 9.
Если в графах 6—8 стоит символ А5 , то это означает, что в указанное время практически достигается насыщение активности.
В 9-й графе приведена удельная активность насыщения облучаемого элемента при потоке тепловых нейтронов 1013 нейтр/(см2 • сек). Эта величина (Aslg) служит для определения активности при времени облучения >0,15 периода полураспада. Активность мишени определяется в этом случае по формуле (16), причем выражение в скобках может быть вычислено по отношению времени облучения к времени полураспада или же взято из таблицы («Справочник химика», 2-е изд., т. 1, стр. 315).
В 10-й графе указаны сечения активации тепловыми нейтронами (по данным на конец 1969 г.), которые были использованы при вычислении величин, приведенных в графах 5—9. С помощью графы 10 можно исправить значения этих величин, если в дальнейшем соответствующие сечения активации будут уточнены. В подобных случаях исправленные величины As'g и A^lg могут быть вычислены умножением их табличных значений на отношение Ог/Оь где O2 — уточненные данные для сечения активации, а О| - данные таблицы.
В случае реакций на нейтронах деления для аналогичных расчетов используются величины. приведенные в графе 12.
В 11-й графе приводится интеграл резонансного сечения активации. Сопоставление сечения активации тепловыми нейтронами (графа 10) с резонансным сечением показывает без особых вычислений, какая дополнительная активность может ожидаться в результате резонансной активации.
В 12-й графе даны эффективные сечения взаимодействия для суммарного потока нейтронов деления. * Эти величины были использованы при расчете активности для реакций (n, Р), (п. а) и (п, 2п). При дальнейшем уточнении сечений взаимодействия значения могут быть легко исправлены (см. выше).
13-я графа содержит данные о типе радиоактивного распада и энергии излучения образующихся радиоактивных изотопов
Здесь приняты следующие условные обозначения: и. п. — изомерный переход (если после и. п. стоит цифра в скобках, она означает энергию сопутствующего у-излучеиия), э. з. — электронный захват, е~ — испускание электрона внутренней конверсии.
Для случая, когда образовавшийся в результате ядерной реакции радиоактивный изотоп имеет большое сечение захвата нейтронов, вследствие чего необходимо учитывать возможность уменьшения числа его атомов за счет вторичной реакции (п, у), приводится значение сечения поглощения о. Для случая делящихся изотопов приводится сечение деления Оу.
В скобках указаны значения энергий соответствующего излучения (в Мае). относящиеся к линиям, наиболее удобным для измерения.
* Для общего потока нейтронов деления во всех расчетах использована величина Ю13 нейтр /( см2 • сек), причем принято, что поток эпитермических нейтронов составляет около Ю'- нейтрКем1 • сек).
543
Радиоактиваци!
Химический Символ и ядерная реакция Поперечное сечеиие поглощения нейтронов, барн Массовое число Период полураспада
кюрицг-сек) кюриЦг- мин) кюри/(г-ч) 4
<7Ag 62 108 2,3 мин 0,17 * As ।
110m 253 дня 74,5-10"9 4,47-10" 6 0,268 • lO'i
ПО 24 сек 2,3 * i
13AI 0,23 28 2,3 мин 6,4-10-3 *
(л, Р) Mg27 9,5 мин 25,2- 10"6 1,5-10"3 * a
(л, а) Na24 15,0 ч 47•10"9 2,8- 10"6 0.17-IO"3!
1в-Аг 0,62 37 35 дней 19-Ю"9 1,1 • 10"6 68-10"®]
39 260 лет 0,17-10"'2 10- IO"12 0,63 • 10'4
41 1,85 ч 0,22-10" 3 13,4 10~3 * 1
33-^S 4,3 76 26,7 ч 84,7-10"6 5,1 • 10~3 0,3 !
79А11 98 198 2,7 дня 0,24- 10”3 14,2 • 10~3 0,85
(2л, v) 199 3,15 дня
5в 755 12 0,018 сек * А, Л3 I
(л, а) Li» 0,84 сек * As As I
(л, Р) Be10 2,7 -10» лет 4,6-10"16 0,276-10"12 16,6-10 ‘1
1,17 131 12 дней 9,8 -10"8 0,59-10" 6 35,2- 10" e|
133m 39 ч
133 72 года 48,3- 10'12 2,9-10"9 0,17- 10"®l
135 m 29 ч
\31m 2,6 мин 0,2 -10’3 * I
139 85 мин 56,6-10" 6 3,4-10~3 * 1
(л, Р) Cs132 6,2 дня 15,5-10'12 0,93 -10"9 55,8 • 10" j
(п, р) Cs136 13 дней 86,3-10"16 5,2-10"12 0,31 • 10" s|
(₽) Cs131 9,7 дня
4Ве 0,010 10 2,7 • 10» лет 1,47- 10'16 88-10"15 5,3-IO"1!
(л, а) fie6 0,83 сек Л As 1
«зВ1 0,032 210 (RaE) 5 дней 23,7 - 10'9 1,4-10"® 85,5 • 10"J
.210 2,6 • 10е лет 92,2- 10~18 5,5- 10"16 0,33- 10"’1
(₽) Po210 (RaF) 138,5 дня
544
ный анализ
Сечение Интеграл резонанс- Эффективное сечение взаимодействия для нейтронов деления, мбарн
кюри; (г-день} Aslg' кюри i г тепловыми нейтронами, барн него сечеиия активации, барн Тип и энергия излучения
As 6,4 • Ю"8 As 34,2 2,35 80,8 44 3,2 НО 74 1160 .... р-(1,77); р+(0,8); э. з,; у(©,64; 0,41; 0,60) И. п. (0,12); р-(0,09; 0,54); у(0,66; 0,88) р-(2,87; 2,16); у (0,66; 0,94)
As As * 1,27 20,7 -IO"3 3,6-10"3 0,21 0,16 3,43 0,6 р-(2,87); у (1,78) р-(1,75; 1,57); у(0,84; 1,02; 0,18) р-(1,39); у(2,75; 1,37)
1,6- ю"3 15-Ю"8 As 82,5 -IO"3 2,06 - Ю"3 2,15 6 0,8 0,53 • • ’ Э. з.; нет у Р'(0,57); нет у р-(1,2; 2,48); у(1,29]
* 11,75 5,4 36,8 .... р-(2,96; 2,41); у (0,56; 1,19)
* 79,4 96 26 000 1490 ... р-(0,96; 0,28); у (0,42; 0,68; 1,09); о=26000 р-(0,3; 0,25); у (0,16; 0,21)
As As -e 0,4-10 8 < 0,61 1 - IO"3 <57 <0,05 0,085 < 200 р-(13,4; 9,0); у(4,4); а (0,20) р-(13,2); а (3,2; 7—9) Р"(0,56); нет у
0.84-10"8 4,17-IO"6 As As * 7,45 • IO"8 14,6- Ю"3 15,8 • 10"3 48-IO"3 0,417 11,95-Ю"6-0,14-Ю"6 14,6-IO"3 9,5 7 0,5 0,5 5,3 0,0015 Э. з.; у (0,50; 0,12; 0,22) И. п. (0,28) Э. з.; у (0,36; 0,28) И. п. (0,27); е- И. п. (0,66); е-р-(2,22; 0,8; 2,38); у (0,17; 1,43); (Г Э, з.; у (0,67; 1,08—1,3) Р“(0,34; 0,66); у (1,04; 0,82) Э. з.
126,7 -10" 6 0,18 0,18 0,01 16 Р~ (0,56); нет у р-(3,5)
* 8,0- 10"12 14,8-IO"3 п-ю;3 14,8-10 3 0,019 0,014 .... Р~(1,17); нет у; а а (4,9) у (0,8); а (5,3)
35 Зак. 783
545
Радиоактивацион
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада
кюриЦг-сек) кюрицг-мин} кюриЦг-ч)
6,6 80,п 4,4 ч 0,13- ю-3 7,86- 10-3 *
80 17,6 мин 5,8 • 10-3 0,35 *
82 35,9 ч 18,9-10' 6 1,13- ю~з 68 • 10-3 j
вС 0,003 14 5570 лет 0,53-10“15 31,8 Ю-15 1,9-10"12
20^3 0,43 41 1,1 • 105 лет 0,17-10~12 10,4- 10“12 0,62 -10“9 1
45 153 дня 2,9 • 10~9 0,17 - 1Св 10,4-10-6 :
47 4,7 дня 52-10-12 3,12 -10-8 0,187 10 ® .
49 8,8 мин 9,4 -10~6 0,56- 10“ 3 As
(Р) Sc47 3,4 дня
(Р) Sc49 57 мин
2450 107 6,7 ч 0,51 • 10’6 30,5- 10 6 1,83-ю-3 ;
109 1,3 года
Him 49 мин 8,5-10“6 0,51 • 10-3 * '
113m 5,1 года 45 - 10—12 2,7-10*’ 0,16- ю-6
115m 43 дня 1,1 -10-8 0,65 • 10~6 39•10-3
115 54 ч 1,64.10-6 98,3 -10—° 5,9-10-3
117m 3,0 ч 10,6-10" 6 0,63 • 10-3 *
117 50 мин *
(Р) Agi07m 44 сек
(Р) Agiosm 40 сек
(Р) In"7m 1,9 ч
(р) In117 1,1 ч
(Р) Jnii5m 4,5 ч
(Р) In115 6 • 1014 лет
(«. р) Agiiom 253 года 0,57-10"12 34,2-10"12 2•10~9
(«. р-, Ag110 24 сек
и. п.)
snCe 0,7 137m 34 ч 7,5 • 10-9 0,45-10" 6 27-10-6
137 9 ч 0,3-10"6 17,9-10” 6 1,1 • 10-3
139,n 55 сек 0,267 -IO"6 * Л
139 140 дней 0,1 - 10~9 6,19 • 10-9 0,37 • 10-6
141 32 дня 77,45 10"9 4,65 • 10“‘ 0,28 -10”3
546
ный анализ
Продолжение
AJg, KtOpUft Сечение активации тепловыми нейтронами, барн Интеграл резонансного сечеиия активации, барн Эффективное сечение взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
кюриЦг*день)
3 2,9 И. п. (0,05); у (0,04); е~
Л 8,86 8,5 ₽-(2,0; 1,4); Р+(0,86); э. з.; у (0,62)
* 3,53 3,5 Р-(О,46); у (0,78; 0,55)
45,8- 10’12 0,136 - 10’3 0,0009 р~ (0,158); нет у
15-Ю’9 0,867 0,22 Э. з.
0,25 10“3 54,8-10’3 0,67 Р~(0,25); нет у
* 30,5-10’6 0,25 р-(0,66; 1,94); у(1,31; 0,48; 0,83)
Л 7,16-10’3 1,1 р-(1,95; 0,9); у (3,09; 4,05; 4,7)
. . . . * • 30,5 10’® Р (0,44; 0,60); у (0,16)
7,16-10 .... Р(2,05); нет у
* 17,7-10’3 1 Р* (0,32); э. з.; у (0,85)
Э. з.
36- 10’3 0,2 И. п. (0,15; 0,25); е~
3,9 -10 10,4 -10"3 0,03 И. п. (0,27); р-(0,58)'
0,94 10~3 58,5-10’3 0,14 р-(1.63); у(0,95; 0,45— 1,3)
* 0,46 1,1 ₽-(1,11; 0,58); у (0,52; 0,49)
Л 0,165 1,5 И. п.
As ₽ (1,6; 3,0); у (1,3; 0,27-2,0)
17,7-10’3 И. п. (0,09); е~
И. п. (0,088); Г
И. п. (0,31); ₽-(1,77; 1,61); у(0,16)
0,165 Р-(О,74); у(0,56; 0,16)
< 0,46 ...... И. п. (0,34); (Г (0,83); е~
Р-(О,6)
49,2-10’ 8 17,9 -10’® о,1 И. п. (0,12); р-(0,09; 0.54); у(0,66)
0,9-10’® р-(2,87; 2,16); у (0,66; 0,94)
* 1,3- 10”3 0,6 И. п. (0,26); э. з. (?)
* 13,9 • 10’3 6,3 .... Э. з.; у(0,44; 0,01)
Л 21,2-10’’ 0,007 . . . . И. п. (0,74)
8,9-10’ 1,8-10’3 0,6 .... Э. з.; у(0,17)
6,7- 10’3 0,31 0,3 .... р-(0,45; 0,59); у (0,15)
35*
547
Радиоактивацион
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада AsKls
кюри/(г>сек) кюриЦг- мин) кюри^г-ч)
seCe 0,7 143 33 ч 0,75- 10”6 45-10“6 2,7- 10”3
(₽) La137 6•104 лет
(₽) Рг143 13,8 дня
пС1 33,6 36 2,5- 105 лет 9,2-10"12 0,-55- 10”9 33-10”9
38m 1 сек -X- As
38 37,3 мин 0,195- 10“3 11,7- 10“3 -X
(л, Р) S36 87 дней 61 10"9 3,7 • 10“6 0,22-10”3
(п, Р) S37 5 мин 0,6- 10“6 У-
(П, а) Р32 14,2 дня 8-10~9 0,48 10”6 28,9 10 6
27С0 37,0 60m 10,5 мин 48,7 10”3 2,92 -X
60 5,2 года 0,234- 10“ 6 14,0-10”6 0,84-10“3
(л, Р) Fe59 45 дней 2,8- 10”9 0,17 -10“6 10,1 • 10”®
(п, а) Мп56 2,58 ч 28,8- 10“9 1,7- 10”6 *
24 Сг 2,9 51 27,8 дня 0,54 - 10“6 32,2-10”® 1,9- 10”3
55 3,6 мин 96,6- 10” 6 -X А
ssCs 29 134m 3,1 ч 1,2 - 10"6 73,1 -10”® X
134 2,1 года 0,39- 10”6 23,1 - 10“® 1,4- 10”3
(л, а) J130 12,6 ч 9,3-10”12 0,56 -10”9 33,6- 10“’
28^11 3,77 64 12,8 ч 0,114- 10”3 6,9-10”3 0,41
66 5,1 мин 3,24-10”3 * Аз
(л, а) Co60 5,2 года 5,4- 10”12 0,32-10”° 19,3- 10”9
66Dy 950 157 8,2 ч
159 1,34 дня
165/лг 1,3 мин 1,28 * А
165 2,3 ч 49,5- 10”3 2,97 *
(2л, V) 166 82 ч
(2л, y; Р) Но166 27,2 ч
евЕг 173 163 75 мин X-
165 10 ч л
167 m 2,5 сек * Л
648
ный анализ
П родолжение
As'S’ кюри/г Сечение активации тепловыми нейтронами, барн Интеграл резонансного сечения активации, барн Эффективное сечение взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
кюриЦгденъ}
* 0,129 15,2- 10“3 0,129 1 р-(1.13; 1,40); у (0,29) Э. з.; нет у Р“(0,93); нет у
0,79- 10“ 6 Л As 4,2-10'3 Л 0,695 • 10 3 104,2 5,6 10“3 0,63 0,66 0,27 10“3 14,24 -10“3 30 0,005 0,56 0,19 0,24 4,1 £“(0,71); э. з.; нет у И. п. (0,66) Р“(4,8; 1,1; 2,7); у(2,1; 1,6) Р“(0,167); нет у Р (1,6; 4,3); у (3,09) Р (1,71); нет у
As 20,2- 10“3 0,24 • 10“3 Л 44,25 55,3 15,76-10“3 0,39- 10~3 16 20 75 5.7 0,14 И. п. (0,069); £“(1,5); у (1,33); о =100 Р“(0,31); у(1,33; 1,17) Р“(0,46; 0,27); у(1,1: 1,3) Р“(2,8; 1,0); у(0,85; 1,8)
46,4 • 10"3 As 1,86 30,1 • 10“3 13,5 0,4 .... Э. з., у(0,32); е~ р“(2,8); нет у
As 33,5 • 10“3 * 19,6 • 10"3 36,8 0,61 • Ю“в 0,016 30 5- 10“4 И. п. (0,14); Р“(0,55); У (0,01) р-(0,65); у(0,61; 0,8) Р(0,6; 1,02); у (0,53; 0,66; 0,74)
<о 1 О * < 4 СО 7,6 1,43 1,27. 10“3 4,3 1,8 4,4 2,2 0,72 £“(0,57); £‘(0,66); э. з.; у(1,34) Р“(2,63, 1,59); у (1,04; 0,83) р-(0.31); у(1,33; 1,17)
• As As 143,8 592 510 2100 5000 .... .... Э. з.; у (0,06; 0,33) Э. з.; у (0,058) И. п. (0,11); р“(~1); У (0,36) р-(0,88; 1.25); у (0,1; 0,28); о=5000 Р’(0,3); у р-(1,85; 1,77); у(0,08; 1,38; 0,97—1,62)
As * Л . 14,7 45 . -- .... Э. з.; у(0,43; 1,1) И. п. (0,21)
649
Радиоактивацион
Химический символ и ядериая реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада As'!e
кюриЦг'Сек) кюри](г*мин) кюрицг-ч)
б»Ег 173 169 9,0 дней 0,47-10“6 28,3- 10“’ 1,7 - 10“3
171 7,8 ч 32,3-10“’ 1,9 - 10“3 0,128
(₽) Tu171 1,9 года
езЕи 4300 152 9,3 ч 14,8 - 10“3 0,89 53,4
152 12,5 года 6,5- 10' ’ 0,39-10“3 23,4 • 10“3
154 16 лет 0,3-10“’ 19,4- 10“’ 1,16- 10“3
(2п, Y) 155 1,7 года
(З/i, т) 156 14 дней
»F 0,001 20 И сек 4,86- 10“3 * As
(/>, Р) О18 29 сек 0,2-10“3 *
(п, а) N'6 7,4 сек 3,6- 10“3 As
2eFe 2,53 55 2,6 года 3,6-10“’ 0,22-10“’ 13,1-10“’
59 45 дней 0,17-10“’ 0,1 - 10“’ 6,1 -10“’
(и, Р) Мп64 278 дней 0,11-10“’ 6,86-10“’ 0,41-10“’
(ft, Р) Мп56 2,58 ч 87,7 • 10“’ 5,26-10“’ * :
(п, а) Сг61 27,8 дня 18,4-10“12 1,1 • 10“’ 66,2-10“’ :
aiGa 2,77 70 21 мин 1,1 • 10“3 65-10“3 *
72 14,1 ч 51-10“’ 3- 10“ 3 0,18
640d 46 0С0 153 236 дней <9-10“’ <0,54-10“’ <32,5-10“’ i
159 18 ч 11 -10“’ 0,65-10“3 39,2- 10“3
161 3,73 мин 0,56 • 10“3 * As
(₽) ТЬ161 7,1 дня
820е 2,45 71 11 дней 1,3-10“’ 78,7- 10“’ 4,7 - 10“3
73т 0,53 сек * As As
75т 49 сек 0,46-10“3 * As
75 82 мин 24,2 • 10“’ 1,45- Ю“3 *
77т 53 сек 0,18- 10“3 *
77 12,3 ч 0,22-10“’ 13,5-10“’ 0,79- 10“3
550
ный анализ
/7родолжение
Сеченнс Интеграл резонанс- Эффективное сечение
кюриЦг-день} Aslg. кюри! г активации тепловыми нейтронами, барн кого сечения активации, барн взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
40,8- 10"3 * * 0,56 27,9- 10"3 А А 0,314- 10"3 0,146-10"3 9,86-10" 6 е 1,58-10 А * <0,78-10" 3 * А 0,113 А As As As * 0,53 1,31 1,31 717,0 3 690 235 77,2 • Ю"3 8,5- 10"3 38,6- 10"3 0,43 9,44 • 10"3 3,96-10"3 1,18-10"3 63,7 - 10" 6 1,97 3,73 < 0,266 1,02 0,18. 0,18 1,8 0,615 32,8- 10"3 0,172 14,0 -10”3 14,0-10"3 2 9 1400 7 200 420 1500 14 000 0,009 2,5 0,98 1,4 4,0 < 125 4 0,8 3,9 1,0 0,04 0,21 0,08 0,08 850 950 9,2 15 0,99 4,5 23 0,44 0,37 р-(0,34); у (0,008), ₽-(1,11; 1,52); у(0,31; 0,30) Р“ (0,097); у (0,067); е~ ₽-(1,88); Р* (0,8); э. з.; у (0,96; 0,84) р-(1,46); э. з.; у(0,12); (3 (0,55; 0,25); у (0,12; 0,25); 0=1500 [>-(0,15; 0,25); у (0,087; 0,11); о=14000 р-(2,45; 0,45); у (0,089; 0,2—2,18); е-р-(5,42); у (1,63) р-(3,0; 4,5); у(0,2; 1,37)' р-(4,3; 10.3; 3,3); у (6,13; 7,1) Э. з.; нет у р-(0,46; 0,27; 1,6); у(1,1; 1,3) Э. з.; у(0,84) р-(2,8; 1,0); у(0,85; 1,8), Э. з.; у(0,32); е~ P-(1,65); у(1,04; 0,17; 1,22) Р“(0,64; 0,96); у (0,84; 2,2) Э. з.; у (0,097; 0,1) р-(0.95; 0,58); у (0,36); р-(1,6); у (0,057). Р-(О,52; 0,50); у (0,026; 0,11) Э. з.; нет у И. п. (0,05); у(0,01); fill. п. (0,14); е~ р-(1,18; 0,72); у(0,26) И. п. (0,16); р-(2,9); у(0,21) р-(2,2); у(0,2Ц
551
Радиоактивацион
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада
кюриЦг-сек} KK>pUl(2-MUH) кюрицг-ч)
32Ор- (Р) 2(₽) (/1, 2л) (л, Р1 (л, а) (л, а; и. п.) >н 2Не (л, Р) ;2Hf ao^g (h) б/Чо <sln 7/lr 552 2,45 0,33 0,007 105 380 64 190 430 ь As77 Se77m 69 Ga72 Zn69m Zn6B 3 Н3 175 178m 179 т 180 т 181 197 т 197 199 лг 203 205 Au197m 166 166 114т 114 116m 116m 116 192 m 192 194 39 ч 17 сек 40,4 ч 14,1 ч 13,9 ч 59 мин 12,26 года 12,26 года 70 дней 4,8 сек 19 сек 5,5 ч 45 дней 25 ч 65 ч 43 мин 47 дней 5,1 мин 7,4 сек >30 лет 27,2 ч 50 дней 72 сек 2,5 сек 54 ми н 15,9 сек 1,4 мин 74 дня 19 ч 3,29 • 10"9 <83,9- 10“12 <2,9- 10“8 24,7- 10"16 0,51 • 10"9 0,25. 10" 6 * 0,67 0,29-10"3 0,57- 10" 6 0,16- 10"6 50- 10"6 <5- 10"12 0,42 - 10"3 0,55 - 10" 6 1,18- 10"3 * 45- 10"3 3 0,7 24.6- 10" 6 0,68-10" 3 0,20- 10" 6 <50- 10"s <0,18.10“ 6 1,49- 10"12 30,8. 10"9 15,3- 10"6 л, * 17,1 • 10"3 34,4. 10" 6 9,9- 10"6 * <0,3. 10"9 25,2 - 10"3 33,1 • 10"6 * А, 2,7 * * 1,5-10"3 41,0. 10"3 11,8-Ю"6 <0,3. 10" 6 <10,6- 10" 6 89,1 • 10"12 1,85- 10"6 0,92- 10"3 Л Л X- 2,1.1(Г3 X- 0,59 • 10"3 As <18,2.10"8 1.5 1,98.10" 3 л, As Л 88,8- 10"3 2,5 ' 1 в ^д
ный анализ
Продолжение
Сечение Интеграл резонанс- е Эффективное сечение
к/ориЦг-дснь) кюри} г активации тепловыми нейтронами, барн него сечения активации, барн действия для нейтронов деления, мбарн Тип и энергия излучения
* * * 28,0 - 10"3 <0,28 - IO"3 0,69- 10"3 <6.15- 10"6 <0,615-10"3 <0,615-10"3 .... 1.5 < 0,01 < 1,0 р-(0,69); v(0,24; 0,52); И. п. (0,16) Зь(1,22); э. з.; у(1,12; 0,58); Р“(0,64; 0,96); у (0,84; 2,2) И. п. (0,44) Р'(0,92); нет у
2,14-10"6 13,8- 10"6 0,00057 Р~(0,018); нет у
44,3-10"6 0,286 5400 . . . . р (0,018); нет у
22,0-10"3 As -3 49,3-10 3 2,23 64,4 18,5 8,16 3,2 1500 380 75 65 10 .... Э. з.; у(0,34) И. п. (0,09); у (0,09) И. п. (0,16); у(0,22);е- И. п. (0,06); у(0,44) р-(0,41); у (0,48; 0,13))
* As -3 14,3-10 3 As 0.968 22,1 • 10"3 4 0,4 .... .... И. п. (0,17); э. з.; у (0,13); е~ Э. з.; у (0,078; 0,19); е' И. п. (0,37); у(0,16); е~ Р (0.21); у (0,28); е~ 0(1.8); у(0,2) И. п. (0,13); у(0,28)
<0,44-10" 6 * 6,9-10" 3 59,3 0,007 60 .... р-(0,18; 0,28); у(0,08; 0,84) р-(1,85; 1,77); у (0,08; 1,38)
47,8- Ю"3 A A £ 3,44 • 0,123 As 210,6 67,9 56 2 155 50 | 1050 | 2640 .... И. п. (0,19); э. з.; у (0,56; 0,72) р (1,98; 0,68); Р‘(0,40); Э. з.; у(1,3) И. п. (0,15) р-(1,0); у(1,27; 1,1) Р~(3,3); нет у
2,13 * 84,5 227,5 67,5 260 700 130 | 3500 1370 .... И. п. (0,057); р-; Р”(0,67); э. з.; у(0,31; 0,47) 0(2.24; 1,9); у (0,33; 0,64)'
553
Радиоактивацион
Химический СИМВОЛ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада AJ-lg
кюриКг-сек) кюри Ki' мин) кюриЦг-ч)
53-1 18К 36Кг B?La jLi («. а) jiLu is№ (n, p) (n, a) 2SMn (n, 2n) 4SMo (P) (P) (P) («. P) 554. 7,0 2,07 31 9,3 71 112 0,063 13,2 2,7 128 42 79т 79 81m 81 83/п 85m 85 87 140 8 Н3 176 177 27 Na25 Na24 56 54 93m 93 99 101 Гс9вт Тс’® Тс101 Nb®2 25 мин 12,46 ч 55 сек 34 ч 13 сек 2- 10s лет 1,86 ч 4,4 ч 10,4 года 78 мин 40,2 ч 0,84 сек 12,26 года 3.7 ч 6,8 дня 9,5 мин 60 сек 15,0 ч 2,58 ч 278 дней 6,9 ч ~ 2 лет 67 ч 14,6 мин 6,0 ч 2 • 10s лет 14,0 мин 10 дней 3,3-10" 3 4,3-10"6 77,0- 10" 8 0,223 1,1-10"3 4,81 • 10" 6 0,14- 10"8 3- 10"6 47,7-10" 6 2,97- 10" 6 1,65- 10"3 0,114 - 10"3 23,4 - 10" 6 15,7.10"6 87,4 • 10"в 2,9 • 10"3 4,3-10"12 <44,6- 10" 8 <0,88 • 10"в 0,52 • 10"6 25,6-10" 6 0,28- 10 8 0,2 0,26- 10"3 * 4,6- 10" 6 * 63- 10"3 0,29 • 10"3 8,4-10"8 0,18- 10"3 2,86- 10"3 А* 0,178- 10"3 99,1 • 10"3 6,85- 10"3 1,4. Ю"3 * 5,24-10" 6 0,18 0,26- 10" 8 <2,67- 10" 6 <53-10"8 31,4 -10"6 1,53. 10"3 16,7- 10”“ * 15,6-10"3 Л 0,28 • Ю"3 А * * 0,5-10" 6 * 0,17 As 10,6-10"3 * 0,41 л. л. 0,31 • 10"3 * 15,4.10~® * <3,2-10"6 1,88 • 10"3 * 1,0- 10"6 1
ный анализ
Продолжение
As'^' кюри!г Сечение активации тепловыми нейтронами, барн Интеграл резонансного сечейия активации, барн Эффективное сечение взаимо действия для нейтронов деления, мбарн Тип и энергия излучения
кюриЦг-день)
As 7,19 5,6 140 .... ₽-(2,1; 1,6); э. з.; у(0,45; 0,53; 0,98; 0,74)
* 0,28 1,0 р-(3,5; 2,0); у (1,5; 0,32)
. . • И. п. (0,13)’
* 13,6-10 3 2 ₽+(0,6; 0,34); э. з.; у(0,04; 0,26)
Л 4,2 95 И. п. (0,19)
Э. з.; у(0,012)
As 10,15 45 И, п. (0,03); Y (0,009); е~
As 0,11 0,1 И. п. (0,31); р-(0,83); у(0,15)
12,2 • Ю"6 66,6 -10 3 0,06 Р“ (0,67); у (0,52)'
Л 20,2 • 10~3 0,06 Р (3,8; 1,3); у(0,4; 2,57))
* 9.96 8,5 р-(1,34; 0,4); у(1,6;0,3))
А 0,72 0.033 р-(13); 2а(3,2; 7—9))
0,254 1656 950 Р“(0,018); нет у
As 31,75 35 р-(1,1; 1,2); у(0,09)
* 96,87 4000 р~(0,50; 0,18); у (0,21; 0,11)
Л 19,3- 10"3 0,03 .... р-(1,75; 1,57); у(0,84; 1,02)
А 1.36- 10 3 2,0 р-(4,0; 3,0); у (0,98; 0,58)
* 6,81-10 3 1,29 р-(1,39); у(2,75; 1,37)
Л 39,5 13,3 11,8 . . . . р (2,8; 1,0); у (0,85; 1,8))
0,37-10" 0,15-10"3 0,05 Э. з.; у (0,84)
As < 1,6-10-3 <0,006 И. п. (0,26); у(1,48; 0,69); е~
<76- 10~6 <80 -10 3 <0,3 • . . . Э. з.
* 0,182 0,45 .... Р~(1,23; 0,45); у(0,18; 0,74)
As 32,3 -10 3 0,2 3,73 р-(2,23; 0,6); у(0,19) И. п. (0,14); е‘
0.182 . . ...
0,182 Р~(0,29); нет у; а=22
32,3-10-3 .... р-(1,1; 1,3); у(0,31; 0,13)
24-10 6 0,347-10 3 1,3 Э. з.; у(0,93; 1,83)
555
Радиоактивацион
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада
кюри}(2'Сек) кюри/(г-мин) кюриКг-ч}
42Мо 2,7
(«. Р) Nb95 35 дней <6,1-10 12 < 0,37 - 10 9 < 22,0-10"®
{п, а) Zr89 79 ч 11 • 10“12 0,66- 10“9 39,6- 10“ 6
1,88 16 7,4 сек 80,5- 10“9 А
(п, р) С'4 5570 лет 80 - 10~12 4,8-10“9 0,29 -106
„Na 0,515 24 15,0 ч 51-10-6 3,1 10“6 0,18
(л, 2л) 22 2,6 года 0,36 • 10“ 12 21,6- 10“12 1,3-10“9
(п, р) Ne23 38 сек 0,13- ю“3 * As
(п, а) р20 И сек 0,18-10“3 * А
41Nb 1,15 94m 6,6 мин 3,06-10“3 0,18 А
(И. п.) 94 1,8 • 104 лет
(и, а) Y90 64,8 ч 0;125 • 10“9 7,5-10“9 0,45 10“6
soNd 46 147 11,1 дня 0,25-10“6 15,0 -10“6 0,9 • 10“3
149 1,8 ч 25,3- 10“ 6 1,5- 10“3 *
151 15 мин 0,136- 10“3 8,13 - 10“3 *
(₽) Pm147 2,65 года
(5) Pm149 50 ч .
(’) Pm161 27 ч
2 (Р) Sm147 1,2.10" лет
2(0) Sm161 80 лет
10Ne 1 23 38 сек 0,47 -10“3 -У- А
28Ni 4,8 59 7,5- 104 лет 2,4-10“12 0,15 -10“9 8,8 • 10“®
63 125 лет 0,27- 10“9 16,3-10“9 0,97-10“ 6
65 2,6 ч 3,3 -10“ 6 0,2 • 10“3 *
(л, 2л) 57 36 ч 12-10“12 0,73 -10“° 43,6-10“9
(«. Р) Co58m 9 ч 0,52- 10е 31,4 -10“6 1,9-10“3
(п, Р) Co58 71 день 48-10“9 2,9-10“6 0,17-10“3
(п, р) Co60 5,2 года 15-10“12 0,9-10“9 55- 10“9
(п, а) Fe55 2,6 года 2,7-10“12 0,16-10“9 9,7-10“ 9
(л, а) Fe59 45 дней 2,6-10“12 0,15- 10“ 9 9,2 - 10“в
556
ный анализ
Продолжение
л^/g, кюри! г Сечение активации тепловыми нейтронами, барн Интеграл резонансного сечения активации, барн Эффективное сечение взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
кюрицг-день)
< 0,53- 10'6 < 26,7-10'6 <0,1 р-(0,16; 0,93); у(0,76))
4,53- 10” 6 0,017 р* (0,9); э. з.
Л 0,86-10~ 6 2-10'6 .... ₽-(4,3; 10,3; 3,3); Y(6,13; 7,1)
6,9 10 6 20,3 1,75 . . . . Р (0,158); нет у
3,97 0,56 0,24 .... Р(1,39); у (2,75; 1,37)
31,0- 10'8 42,5- 10' 6 0,006 ₽+(0,54); э. з.; у (1,28)
As 7,1 10'3 .... 1,0 р-(4,4; 4.0); у (0,44; 1,65)
Л 2,8 • 10“3 0,4 р-(5,42); у(1,63)
1,75 1,0 3,87 .... И. п. (0,04); р-(1,3); у(0,9); е~
1,75 .... Р (0,5); у (0,87; 0,7; 1,57); о=15
* 42,1 • 10'6 0,024 р-(2,27); у(1,73)
21,6- 10"3 0,347 1,8 .... р-(0,81; 0,38); у(0,092; 0,53)
и, 0,237 3,7 . . . . р-(1,5); у (0,11)
0,176 2,8 .... р-(1,24; 1,79); у (0,8; 0,11)
0,347 Р'(0,22); у (1,2); о=60
0,237 р-(1,05); у(0,29; 1,3)
0,176 Р~(1,1); у(0,34; 0,17)
0,347 а(2,18)
0,176 .... р-(0,076); у(0,022); о=10 000
Л 25,9-10~3 0,036 .... .... р-(4,4; 4,0); у (0,44; 1,65)
0,21 • 10'6 8,31 4,4 Э. 3i; нет у
23,4 - 10'6 1,54 15 . . . . Р~ (0,067); нет у
As 44,4 • 1О'а 1,6 .... р-(2,1; 0,6); у (1,45; 1,09)
* 2,27-10-6 0,0012 ₽4(0,85; 0,72); э. з.; у(1,36; 0,13)
* 24,5-10'3 13 И. п. (0,025); е-
4,15- 10'3 0,425 .... 225 Р*(0,48); э. з.; у (0,8;
1,3- 10'6 3,6- 10'3 5 Р-(Ь,31); у (1,33; 1,17)
0,23- 10" 6 0,32-10'3 0,17 Э. з.; нет у
0,22- 10" 6 14,4 - 10'" 0,14 р-(0,46; 0,27); у (1,1; 1,3)
557
Радиоактивацион
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада As^!g
кюриЦг-сек) кюриЦг-мин) кюри^г’Ч)
8О («. р) («, р) («, а) 780s (₽) (Р; п, v) (Р; п, у) (Р; п, у) 16р (п, Р) (п, а) 82РЬ 46Pd (Р) (Р) (Р) 0,0002 15,3 0,20 0,17 8 19 N16 N17 С14 185 187m 188m 189 т 190m 191m 191 193 Ifisim Jfi9”m If182 If184 32 SF' A 1=8 205 207m 209 103 107m 107 109m 109 Him 111 Rh103"' Agiosm Agium Ag'" 29 сек 7,4 сек 4,14 сек 5570 лет 94 дня 39 ч 26 дней (?) 5,7 ч 10 мин 14 ч 14,6 дня 31,5 ч 4,53 сек 1.4 мин 74 дня 19 ч 14,2 дня 2,62 ч 2,3 мин 0,005 сек 0,85 сек 3,3 ч 17 дней 21 сек 7 • 106 лет 4,8 мин 13,6 ч 5,5 ч 22 мин 54 мин 40 сек 75 сек 7,5 .дня 4 14 4 4 4 4-41 • • ’ 4 4 А о о >- со о Л „ $2 • • • • со —* Р о • • со -Г"1 •—4 ' 5° ’ ’ ‘ ' nd - . ...ooco^©..oa> СО too . . . . — Ъ** • • • • • • * > • • • • • L * ' ’ 4 1 * • • И-1—4 С»5 ' 1 4 4 4 4 4 4 4 4 _ , ~ © Ф © © © о © о о О О Ф ОФ • • 4 • | | | | • • | | 1 1 I * • • II | 1 II о га го ci «5 «о а о сп <га> — ст> «з 4 4 4 4 4 4 4 4 4 4 41444 СО СЛ К> -М ’ Ю р о ’ ’ Л р • ' ’ ND СП * £-00 СО ' - О ' * ’ © фь МФ© OXd >—Ф>. , ND О f •—4 СЛ : ::: : :: . ООО © р со оо — о • ••III- I °. I 1 • • • • II- • • О 1 W ся со СТ> ’ Ы СП С*>О I - 1,11 4 0J 4 4. 4 • 4441 ^2 ЗДС044444 4444 4 4444 — । « т т <п | Q > • 4 4 4 | | > 4 4 « | | 4 4 14 4 о X © © о ф Л О} со Сп 7—1 .... .,—(1—t • '• ’ I CotQCQ ^-(Co'CoLQ. 4. 4 'ч ю . . . . .•• .. . • +• ^ ^ ^ * • s . д. + ь. —г N- тН ф_ со ° - • • • • ‘ • СМ ’“1 • ... (М V СО —1 © 1114 4 4.1»
558
ный анализ
Продолжение
Сечение Интеграл резонанс- Эффективное сечение
кюри/( г'день) л^/g, кюри! г активации тепловыми нейтронами, барн кого сечения активации, барн взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
• 00 Л о 1 • • • • со Р® • • • * Р^ * о "о и- 00 .СО , “to 4* о о e> и- о . . . . • | 1 . . . . 1 • О 1 ы w ы 1 <а • • • • • • * • м 4,16-10-6 0,19-КГ3 19,6-10-9 1,88-10-3 <31-10-3 1,81 0,562 1,81 1 0,16 7,5-10"3 8,6-10~3 4,9 10~3 0,25-10“3 76,5-10“3 28,7-КГ 3 4,9 3,6- 103 72,1 • 10~3 76,5- К)’3 4,85 75,7- 10~3 0,0002 <200 8 1,6 260 700 130 1,19 0,8 0,025 0,0006 5 0,07 12 0,02 0,4 0,092 0,019 0,0052 500 31,2 1,43 Р"(3,0; 4,5); у(0,2; 1,37); р-(4,3; 10,3); ’,’(6,13; 7,1) ₽~(3,7); л(1.0) Р”(0,158); нет у Э. з.; у (0,65; 0,88; 0,87) И. п. (?) И. п. (?) И. п. (0,03) И. п. (0,04); у(0,19; 0,36) И. п. (0,07) р-(0,14); у(0,042; 0,13)1 р-(1,13; 1,05); у(0,07; 0,14; 0,46) И. п. (0,042); э. з.; у(0.13); е* И. п. (0,057); р“; е~ Р*(0,67); э. з.; у(О,315 0.47; 0.14) р-(2,24; 1,9); у (0,33; 0,64; 0,29) Р*(1,71); нет у р-(1,48); у(1,26)' р-(2,87); у(1,78); И. п. (0,99) И. п. (1,06); у (0,57); е-р-(0,62); нет у Э. з.; у(0,05; 0,36); е~ И. п. (0,22); е-р-(0,04) И. п. (0,19) р-(1,0); у(0,31) И. п. (0,17) Р(2,13) И. п. (0,04); е- ~И. п. (0,088) И. п. (0,087); е-р-(1,04; 0,7); у (0,34; 0,25)
559
Радиоакт ивацион
Химический символ и ядериая реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада A^Ir
кюри!(г*сек) кюриЦг-мин) кюриЦг* ч)
sePr 11,2 142 19,1 ч 0,117-10~3 7,0- 10“3 0,42
?ePt 8,8 191 3 дня 25,5 10~9 1,5- 10"' 92- 10"'
193 4,4 дня 95-10"9 5,7- 10" 6 0,34 • 10~3
195m 3,5 дня 0,75- 10" 6 45,3-10"' 2,7-10"3
197m 1,4 ч -X
197 19 ч 1,7-10"' 0,1 -10"3 6.1-10"3
199 30 мин 92,4- 10"' 55,4 -10" 3 *
(Р) Au199 3,15 дня
(Р; «. y) Au198 2,7 дня
(P; 2л, у) Au199 3,15 дня
88^3 20 227 41 .мин 4,06-10"3 0,244 *
syRb 0,7 86m 1,0 .мин 0,8- 10~3 * Л,
86 18,6 дня 0,41 - 10"' 24,8-10"' 1,49-10"3 <
88 18 .мин 34-10“' 2,0-10"3 -х-
7sRe 84 186 89 ч 70- 10“' 4,22 • 10"3 0,253
188m 20 мин *
188 17 ч 0,5-10“3 28-10"3 1.68
45RIi 156 104m 4,4 мин 0,05 х- As
104 42 сек 3,66 * As
44R11 2,56 97 2,9 дня 51,7-10“9 3,1-10"' 0,186-10"3
103 40 дней 0,146-10“' 8,8-10"' 0,527 • 10"3
105 4,5 ч 8,9-10“' 0,53 10"3 *
(P) Rhl03m 54 мин
<P) Rhl05m 45 сек
(P) Rh195 36 ч
(P) Tc97m 91 день
(P) Tc97 2,6- 10е лет
560
ный анализ
Продолжение
Сечение Интеграл резонанс- Эффективное сечение
кюриКг-денъ) As/e’ кюри/г тепловыми нейтронами, барн ного сечения активации, барн действия для нейтронов деления, мбарн Тип и энергия излучения
Л СО СО со III ... 1 I ..... о о о о о — « «— 1—< “3 v «0 • • <0 со ' «о . со. со со . . | •• * . . . ^ * ч; . . . * ч; * * . 4 СМ СМ ГО оо о см го g ... « см • • • • • 11,6 9,55 10"3 52 • 10~3 0,33 0,168 0,24 0,24 14,4 68,8 • 10-3 0,96 53•10-3 32,5 41,3 19,0 222 18,7 -10-3 0,73 < 0,207 0.73 0.207 0,207 7,5- 10-е 18,7 -10-3 10 90 8 1,2 0,8 4 96 26000 20 0,05 0,7 0,1 100 75 12 . 140 0,21 1,44 0,7 11,3 1160 305 656 .... 3~(2,16; 0,6); у (1,57)); <з= 18 Э. з.; у (0,53; 0,36); fill. п. (0,14) И. п. (0,13); у (0,03; 0,099) И. п. (0,34); е-£-(0,67; 0,48); у (0,08; 0,19) ₽-(1,7; 1,3; 1,1); у(0,07; 0,96); а=15 Р-(О,ЗО; 0,25); у (0,16; 0,21) р-(0,96; 0,28; 1,37; 1,09); у (0,42; 0,68); о=26 000 £-(0,3; 0,25; 0,46); у (0,16; 0,21; 0,05)'; а=30 £-(1,30); у (0,29; 0,50) И. п. (0,56) £(1,77; 0,7); у(1,08) £-(5.3; 3.3); у (1,85; 0,91) £-(1,07; 0,93); э. з.; у(0,14; 0,12) И. п. (0,10); у(0,06); £-(2,12); у (0,16; 0,63), И. п. (0,08); ₽-; у (0,56)) £(2,4); у (0,56; 1,24) Э. з.; у(0,22; 0,33; 0,11; 0,57); е- £-(0,20; 0,13); у (0,50; 0,60) £(1,15); у (0,73)) И. п. (0,04); е- И. п. (0,13); е-р-(0,56; 0,27); у (0,31; 0,22)
36 Зак. 783
561
Радиоактивацио
Химический символ и ядериая реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада
кюриКг-сек) кюриЦг'Мин) кюриКг-ч}
16s 0,50 35 87 дней 5,14-10~9 0.31 • 10“ 6 18,5 • 10“8
37 5,0 мин 0,23 - 10-6 * и,
(«. р) рз2 14,2 дня 0,16- 10“8 9,83 10“9 0,59-10“*j
(п, р) рзз 25 дней 28,5-10“12 1,71 10“9 0,1 • 10"* 1
(п, а) Si31 2,62 ч 1,06- 10“8 63,8- 10“8 * i
5,Sb 5,5 122 т 3,5 мин * И. j
122 2,8 дня 14,6-10“8 0,89 • 10“3 53,6-10“3 •
124m 21 мин 9,5 • 10“8 0,58 • 10"3 * 1
124m 1,3 мин 0,15-10“3 * А 1
124 60 дней 0,19-Ю-8 11,5 - 10“6 0,69 • 10“ 3|
21Sc 23,5 46m 20 сек 1,25 * и, 1
46 84,0 дня 4,1 10“8 0,248 -10“3 1,5 • 10"3|
(п, а) К42 12,46 ч < 0,28 - 10“ 8 16,8-10“ 8 1,о-ю"3а
s4Se 12,3 75 120 дней 33,4 • 10“9 2-10"8 0,12 • 10"3|
77m 17 сек 53,4 • 10“3 * А 1
79m 3,9 мин 0,578 • 10"3 X л, 1
81m 57 мин 6,28 • 10"8 0,38 • 10"3 * 1
81 18 мин 0,33 10“3 20- 10“3 * 1
83 69 сек 93-10“ 8 * А 1
83 25 мин 0,34 • 10"8 20,6- 10“8 * 1
(Э. з.) Br83 2,3 ч
2 (Р) Kr83m 1,86 ч
14Si 0,13 31 2,62 ч 1,47- 10“ 8 88-10"8
(«> А) Al28 2,3 мин 0,1 • 10“3 А 1
(«. Р) Al29 6,6 мин 1,3-10“8 77,8-10“8 и, I
e2Sm 5600 145 340 дней 23-10“12 1,4-10“9 83,4 • 10“9|
151 80 лет
153 47 ч 0,166- 10"3 10•10“3 0,6 I
155 23 мин 0,68 • 10“3' 41 • 10“3 * 1
(Э. з.) Pm146 18 лет
562
ный анализ
Продолжение
Сечение Интеграл резонанс- Эффективное сечение взаимодействия для нейтронов деления, мбарн
кюриЦгдень) As,e' Ktopujz тепловыми нейтронами, барн него сечения активации, барн Тип и энергия излучения
0,44 10~3 As 14,15-10 6 2,46- 10“в и, 55,8 10“3 99,6 • 1О'в 0,29 89- 10~в 14,5 • 10-3 0,26 0,14 60 2,3 3 р-(0,167); нет у ₽-(1,6; 4,3); у (3,09) Р"(1,71); нет у Р"(0,25); нет у P-(1,48); у(1,26)
и, * As 5,2 17,3 -10-3 6,8 } 0,03 | 162 И. п. (0,08); е~ 3(1,4; 1,99); 6" (0,57); э. з.; у(0,56) И. п. (0,018) ; Р~(— 2,5) ;
и, 17.3 • 10~3 0,03 । 138 И. п. (0,012); 3 (3,2);
16,6- 10-3 1,44 2,5 j р-(0,61; 2,31): у(0,6; 1.7)
И, 0.36 36,1 43,4 < 18,1 -10~8 10 1 12 1 10,7 <5,0 II. п. (0,14) р-(0,36; 1,48); у (1,12; 0.89) Р (3,5;2,0); у (1,5; 0,32))
2.89 • 10~3 л, As Л As As As 0,5 1,3 0,195 31•10“3 0,52 9,3 • 10~3 0,74 -10-3 10-10~3 10 - 10-3 26 7 0,4 0,03 0,5 0,05 0,004 .... Э. з.; у(0,27; 0,14) И. п. (0,16) II. п. (0,096); е~ II. п. (0,10); е~ Р“(1,38); нет у р-(3,4); у(1,01; 2,02) 3 (1,5); у (0,4; 0,18) Р"(0,94); у(0,05) И. п. (0,03); у(0,009); е~
л, As л. 20-10-3 21,4-10-3 0,74 • 10-3 0,11 4 2,7 р-(1,48); у (1.26)) р-(2,87); у(1,78) р-(2,5; 1,4); у(1,28; 2,43)
2 - 10-e Л 0,982 - 10-3 40,7 1.36 0,96-10“3 0,03 140 5,5 > 1750 .... Э з.; у(0,061; 0,49) ₽-(0,076); у (0,022); <т=10 000 3(0.65; 0,72)'; у(0,1; 0.07) ₽ (1.8); у(0,25; 0,11) Э. з.; у(0,071; 0,067)
36*
563
Радиоактиват
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада
кюриЦг-сек) кюриЦг- мин) кюриЦг- ч)
eiSm ([>>) 5600 Ей155 1,7 года
(₽; п, у) Ен186 14 дней
(₽; п, у) Ей154 16 лет
(₽; «, v) Ен152”’ 9,3 ч
(Р; «. у) Ей152 12,5 года
6oSn 0,63 113 119 дней 1,23- 10'9 73,6- 10'9 4,4 • 10“*
117m 14 дней 0,67- 10'6 40,2- 10'9 2,4 • 10“'
119m 245 дней 0,108- 10'9 6,48- 10~9 0,39 • 10':
121 > 5 лет < 2-10'12 <0,12- 10'9 < 7,1 • 10'!
121 27 ч 0,45-10-6 26,7-10“® 1,6 - 10'1
123 130 дней 4- 10'12 0,24 - 10'9 14,6- 10^
123 40 мин , 3-10'е 0,18- 10'3 * 1
125 9,5 мин 20- 1О'е 1,2 - 10'3 As J
125 10 дней 0,27- 10'9 16,1-10'9 0,97 • IO]
(₽) Jnii3m 1,73 ч
(₽) Sb126 2,0 года
2 (₽) 58 дней
8sSr 1,16 85m 70 мин < 1,8-10“® < 0,1 • 10 3 * 1
85 65 дней 1,33- 10'9 79,9 • 10'9 4,8 10'!
87m 2,9 ч 15,9-10“® 0,96-10'3 * !
89 51 день 1,2-10'9 72-10'9 4,3 • 10“
(₽) y89W 16 сек
73Та 21,3 182m 16 мин 19,5- 10'6 1,17- 10'3 *
182 115 дней 1,2-10'® 71,6- 10'® 4,3 • 10'
(п, а) Lu178 19 мин 46,6-10'12 2,8- 10'9 * 1
(2л, у) 183 5 дней
esTb 44 160 72 дня > 2,5- 10'6 >0,15- 10'3 > 9,0 • 10'!
егТе 4,5 121m 150 дней
121 17 дней
564
ный анализ
Продолжение
кюриЦг^день) AJE. кюри, {г Сечение активации тепловыми нейтронами, барн Интеграл резонансного сечеиия активации, барн Эффективное сечеиие взаимодействия для нейтронов деления, мбарн Тип н энергия излучения
0,106- 10~3 57,9- 10“ 6 9,4 - 10“6 <0,17 • 10~6 * 0,35- 10“6 И, А 23,2- 10“6 и., 0,115- 10-3 и, 0,1 - ю“3 А 0,10 As >0,22 1,36 18,2-10“3 1,17- 10“3 3,3 - 10“3 <0,45- 10“3 62,5- 10“3 66- 10“ 6 10,5 - 10“3 16,8 • 10“3 0,335 • 10“3 18,2- 10“3 17-10“3 <10,8-10“3 10,8 • 10“3 0,24 7,65 - 10“3 0,765- 10“6 27,0-10“3 17,1 76,6- 10“ 9 > 22,5 14 000 420 1400 7200 1,3 0,006 0,01 0,001 0,14 0,001 0,16 0,2 0,004 < 1 1,0 1,3 0,005 0,03 19 17 000 > 22 | 590 8,5- 10“5 ₽-(0,15; 0,25); у (0,087; 0,11); а=14 000 ₽-(2,45; 0,5); у (0,089; 0,2); е- ₽-(0,55; 0,25; 0,15); Т(0,12; 0,25); а= 1500 ₽-(1,88); ₽+(0,8); э. з.; у(0,96; 9,84) р-(1,46); э, з.; у(0,12); а=5500 Э. з.; у(0,26)' И- п. (0,16); у(0,162; 0,3); е~ И. п. (0,065); у(0,02)'; е~ ₽-(0,42); у (0,026) (0,38); нет у ₽-(1,42); у(1,08) 3 (1,26); у(0,15) ₽-(2,1); у (0,33) ₽-(2,4); у(1,07) И. п, (0,39); е-Р"(0,30; 0,13); у(0,43; 0,60) И. п. (0,11); у(0,04);е~ И. п. (0,007); э. з.; у(0,15) Э. з.; у(0,51) И. п. (0,39) Р“(1,46); нет у II. п. (0,91) II. п. (0,18); ₽-(0,6)'; е~ ₽-(0,51); у(1,12; 1,19); 0=17 000 ₽-; у (0,34; 0,45) р-(0,62); у (0,25; 0,35) ₽-(0,57; 0,86); у (0,97; 0,88) у(1,13); е-
565
Радиоактивацио,
Поперечное сечение
символ и ядерная реакция поглощения нейтро- нов, барн Массовое число Период полураспада кюриЦг-сек) кюри[(г- мин) кюри1(г-ч^\
«Те 4,5 123m 125т 127т 104 дня 58 дней 105 дней 2,7-10“ 9 40- 10“9 1.6-10“9 0,16- 10“в 2,4 -10“ 6 98,5-10“9 9,73 • 10“’ 0,14- 10“3 5,9 • 10“’
127 129m 129 131m 9,4 ч 41 день 74 мин 1.2 дня 3,9-10“’ 1,19- 10“9 8,2-10“6 <23-10“9 0,23 • 10“3 71,6 - 10-9 0,49-10“3 < 1,4-10“’ 14,1 -10“’ 4,3-10“’ <84 10 •:
(₽) 131 J13I 25 мин 8,05 дня 44,7 • 10“’ 2,7- 10“3 * 1
(₽) J129 1,7 -107 лет
2(₽) эоТЬ 7,5 Xe,3,m 233 12 дней 22,4 мин 2,7-10“3 0,16 * 1
(₽) Ра233 27 дней
2(₽) (J233 1,6- 10е лет
(л, 2л) 231 (UY) 25,6 ч 65,4 -10“9 3,9- 10“в 0,235-10"’
(2л, у) 234 (UX.) 24,1 дня
(2л, у; ₽) Pa234 (UX2) 1,2 мин
(2л, у; р) Pa234 (UZ) 6.66 ч
(2л, у); 2(₽) («. 0) •22^1 5,8 U234 (UI1) Продукты деления 51 2,5 • 10е лет 5,8 мин 51 • 10“’ * и.
(«. Р) Sc4e 84 дня 0,11-10“9 6,4- 10“9 0,38 • 10“*
(«. Р) (п, р) Sc47 Sc48 3,4 дня 1.83 дня 0,12-10“9 0,85 • 10“9 7,37 • 10“9 51 • 10“9 0,44-10"" 3,1 • 10“’
(п, а) («. а) Ca45 Ca47 1,53 дня 4,7 дня 0,73- 10“12 62- 10“15 43.6- 10“12 3,7.10“12 о> о> 1 1 О О Ч 1-Н О СЧ СЧ о
.566
1
ный анализ
Продолжение
Сечение Интеграл резонанс- Эффективное сечеиие
кюри’(2‘денъ) A/g, кюри 1г активации тепловыми нейтронами, барн него сечения активации, барн взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
0,23- 10“3 3,46- 10“3 0,14 - 10-3 ч 0,10-10“3 И. * 35,1 -10"3 0,29 21,5-10"3 0,19 6,1 • 10"3 52,8 • 10"3 <3,5- 10“3 96,7 - 10“3 — 0,1 52,8 - 10“3 ~ 0,7 • 10“3 1,1 5 0,09 0,8 0,015 0,13 < 0,008 0,22 II. п. (0,09); у(0,16); <г II. п. (0,11); у(0,04); fill. п. (0,09); Р~; Y (0,059; 0,66) ₽-(0,70); y(0,42) II. п. (0,11); р-(1,53)? р-(1,45; 0,99); Y(0,03) II. п. (0,18); Р“(0,42); Y(0,77) ₽-(2,1); y(0,15I ₽-(0,61; 0,25); y(0,36; 0,08) ₽-(0,15); y(0,038); е-, 0=11 II. п. (0,16); е-
* 5,27 5,27 5,27 8,7'- 10“3 7.5 1400 <0,2 69,8 12,4 р-(1,23); y(0,03); о= = 1400 ₽-(0,26; 0,14); Y (0,086; 0,31) Y(0,044; 0,05); а(4,82); о=530 ₽-(0,30; 0,22); Y(0,03; 0,085) р-(0,19; 0,10); y(0,09; 0,064; 0,029) II. п.; Р (2,3); Y(0,04; 1,8) р-(0,32; 0,16; 0,53); Y(0,04; 1,7) Y(0,05; 0,12); а (4,77; 4,72); е-; о=90
S 5° о о 1 1 «э о> 25,5-10"3 1,12-10~3 52,1 -10~6 0,194-10~3 13,9 • 10"в 36,4 - 10“s 0,14 4,1 0,21 0,077 0,0055 0,0002 р-(2,1; 1,5); Y (0,32; 0,93) р-(0,36; 1,48); y(M2; 0,89) Р~(0,44; 0,60); y(0,16) р-(0,65); y(0,99; 1,04;. 1,31) Р~(0,25); нет y р-(0,66; 1,94); v(I>31; 0,48)
567
Радиоактивацион. ’ ный анализ Продолжение
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада V'? As/gt кюри/г Сечение активации тепловыми нейтронами, барн Интеграл резонансного сечения активации, барн Эффективное сечение взаимодействия ^для нейтронов деления, мбарн Тип н энергия излучения
кюриЦг-сек) кюри/(г- мин) кюри\г-ч) кюриЦ г'день)
в|Т1 («• р) egTu (2л, Y) ,92и (п. 2п) (2п, у) (Р) <Р; п, у) {2п. у; Р) (Р; п, у) (л, 2л; р) (2л, у); 2(Р) 2(Р) («, 0) 23^ 74W 54 Хе Б68 3,3 127 7,68 5,1 19,2 35 204 206 (RaE") Hg203 170 171 236 239 237 240 Np239 Np2«o Np2«o Np240 Np237 PU24O PU24O Продукты деления 52 Sc48 181 183 m 185 m 185 187 125m 125 127m 127 3,56 года 4,2 мин VI дней 127 дней 1.9 года 2,39 • 107 лет 23,5 мин 6.75 дня 14 ч 2,33 дня 7.3 мин 7,3 мин 1 ч 2,2 - 10е лет 6 600 лет 24 300 лет 3,77 мин 1,83 дня 145 дней 5,5 сек 1.7 мин 70 дней 24,0 ч 55 сек 18 ч 75 сек 36.4 дня 11,6 -10-9 0,15 10~3 80-10"15 7,9 10“в 0,48 • 10"15 0,98 • 10"3 3,8 • 10"9 0,044 11,2- 10"12 0,68 10"9 * 65,3 10"9 69,4- 10-в 0,92 • 10"в -х- 0,697- 10~6 4,8 - 10"12 0,47 • 10"3 28,9-10"15 59 • 10"3 0,23 • 10"в * 0.67- 10“ 9 41 • 10"9 As * 3,9-10~8 4,2 • 10"3 * 55,3 • 10"в * 41,8-Ю-6 A J 0,29-10"8 28 • 10"3 1,73 • 10"'2 ’ * 13,6 ю-3 ; -j Г А 1 А 40,2 10"8j ' 2,47 • 10"в> и, 1 -Л 0,235-10 Ж 0,25 К As .1 3,3-10 3 В А I 1 » А S * & 45» * Сп * * * • • * ••• Сд} • 05 05 СО w 05 _ о о ’bib, * • tb. tb. • * tb. • • • • • • -° • tb. . fe *й * Н- fe fe — * fe . . . — fe — . £ — й — О О о о СО о о • 1 1 » • • । । • II Ы о» ci: — to 00 • ю • 1.88 56,2-10"3 0,47 • 10~в 125,1 0,523 2,0 3,19-10~3 2,0 2,0 14,4 2,55-Ю-3 12,4-10"3 0,116 0,57 8,65 86,2- 10"3 8 0,1 130 150 107 3 22 35 25 4,2 4,5 10 0,5 2,1 } 34 74 129 0,5 297 355 0,002 4,7 0,08 ₽' (0,76); э. з. Р~(1,51); нет у р-(0,21); у (0,28); е' р-(0,95; 0,87); э. з.; Y (0,084); а =150 р-(0,097; 0,03); у (0,067); е~ у(0,05); а (4,50); е~\ 0 = 6 р-(1,21); у (0,074); а=22 р-(0,24; 0,08); у (0,06; 0,21); е- Р~(0,36); нет у Р-(О,33); у(0,11; 0,28), р-(2,2); у (0,56; 0,91; •,4) р-(2,2); у(0,56; 0,91; L4) р-(0,90); у (0,09; 1,16) Э. з.; у (0,03; 0,087); а(4,79; 4,77); о=170;. О; = 20 у(0,045); «.(5,16; 5,12); 0=250 у(0,052); а(5,15); о= =315; О/=750 р-(2,6); у (1,4) р-(0,65); у(0,99; 1,04) Э. з.; у (1,37; 0,15) И. п.; у(0,11; 0,16) И. п.; у (0,13; 0,16) Р“(0,43); нет у Р'(0,63; 1,33); у (0,69; 0,48) И. п. (0,075); у(0,11) Э. з.; у (0,19; 0,24) II. п. (0,18); у(0,13) Э. з.; у (0,20) 56'Л
Радиоактивация
Химический символ и ядерная реакция Поперечное сечение поглощения нейтронов, барн Массовое число Период полураспада
кюриКг-сек) кюриЦг-мин) кюриАг- ч)
54 Хе 35 129m 8 дней <0,12- 10'6 < 7,2 - 10“6 <0,43 - 10~
131m 12 дней 0,17-10'6 <10,2- 1О'в <о,б- ю7
133m 2,3 дня < 5,8-10 ® <0,35 • 10”3 < 21 • 10'
133 5,65 дня 95 - 10'9 5,7 - 10'6 0,34- 10'
135m 15 мин 50- 10“ 6 3-10“3 *
135 9,2 ч 0,54- 1О'в 32,4-10“ 6 1,94- 10'
137 3,8 мин 50.4 -10“ 6 * Я.
(Р) J125 60 дней
(Р) Cs135 2•10е лет
(Р) Cs137 30 лет
2 (Р) Ba137m 2,6 мин
39 ¥ 1.3 90 64.8 ч 6,53-10“ 6 0,4 - 10'3 23,5 • 10'
70Yb 36 169 31 день 3,6- 10“в 0,22- 10“3 13,0 • 10'
175 4,2 дня 34,2-10“ 6 2-10'3 0,12
177 1,9 ч 65,8-10“6 3,95 10“3 *
(Р) Lu'77 6,8 дня
30Zn 1,06 65 245 дней 17,5-10“9 1•10“в 63 • 10'
69m 13,9 ч 0,64 • 10“в 38,5-10“ 6 2,3 • 10',
69 59 мин 90,8 • 10"6 5,45- 10'3 *
71m 3 ч *
71 2,2 мин 7,0- 10“в * Л
<«> Р) Cu67 12,8 ч 0,64 • 1О'в 38,5 -10'6 2,3 • 10'
<п. Р) Cu67 61,6 ч 86-10“12 5,2- 10“9 0,31 • 10'
'(«. а) Ni63 125 лет <2,44- 10“16 <0,146-10'12 <8,78 • 10'
(п, а) Ni65 2,6 ч 0,7 -10“9 41 • 10"9 *
4<)Zr 0,18 93 9•10е лет 1,9- 10“15 0,114- 10~12 6,8 • 10'
95 65 дней 3,87-10“9 0,23 - 10'6 14-10'
97 17 ч 56,4 -10“9 3,4- 10'6 0,2 • 10'
(р) Nb93 12 лет
(Р) Nb957" 90 ч
(р) Nb95 35 дней
(р) Nb97m 1 мин
(р) Nb97 74 мин
370
ный анализ
Продолжение
Сечение Интеграл резонанс- Эффективное сечеиие
кюриКг-дешг) AslB, кюри! г активации тепловыми нейтронами, барн него сечения активации, барн взаимодействия для нейтронов деления, мбарн Тип и энергия излучения
10- ю-3 <14,7-10“3 К Z Л * 0,312 * As 1,5 - 10“3 * и. И. * -к <0,21 -10“9 и, 0,16-10“9 0,33-10“3 * < 0,12 < 0,25 < 1,67 66,8 • 10“3 <64,5-10“3 25,8-10“3 16,6-10“3 86,2 <0,09 16,6-10“3 15,3- 10“3 2,2 14 17,9 0,65 0,65 0,54 46,4 -10“3 0,464 1,34 -10“3 42,7-10“3 27,6-10“ 6 13,86- 10“в 9,27-10“ 6 77,7 -10“3 31,4-10“3 4,98 • 10“3 3,1 - 10“3 0,63 • 10“3 31,4 - 10“3 4,98 • 10“3 4,98-10“3 <5 <5 <5 < 0,2 < 0,5 0,2 0,15 1,2 11000 60 5,5 0,44 0,1 1,0 0.09 0,25 0,1 0,1 0,91 .... 35 0,27 <0,02 0,02 И. п. (0,2); у (0,04); er И. п. (0,16); е- II. п. (0,23); в” ₽-(0,35); у (0,08) И. п. (0,52); е~ р-(0,91; 0,55); у (0,25; 0,62); о=2 700 000 ₽-(3,5); у Э. з.; у (0,035) Р~(0,21); нет у; о= 15 ₽-(0,52; 1,18) И. п. (0,66); е~ р-(2,27); у(1,37) Э. з.; у(0,064; 0,20) р-(0,47); у (0,40; 0,28) р-(1,40); у(0,15; 1,09) Р~(О,БО; 0,18); у(0,21;. 0,11) Р+(0,32); э. з.; у(1,11), И. п. (0,44) Р (0,92); нет у Р (1,5); у(0,4; 0,5) р-(2,4); у (0,5) р-(0,57); Р+(0,66); э. з.;. у(1,34) Р"(0,40; 0,48); у (0,18) Р" (0,067); нет у р-(2,1; 0,6); у(1,45; 1,09): р-(0.06) Р(0,40; 0,36); у (0,76; 0,73) р-(1,91; 0,45); у(~0,7), И. п. (0,029); е- И. п. (0,23) Р~(0,16; 0,93); у (0,76) II. п. (0,75); е~ ₽“(1,27); у(0,67)
5711
ГАЗОВЫЙ АНАЛИЗ
В настоящем разделе приводятся основные сведения, необходимые для выбора метода газового анализа, для его осуществления и расчета результатов.
Более подробные сведения см.: 1. Автоматические газоанализаторы, сб. статей. ЦИНТИ-Электропром. 1961. —2. Д. И. Агейкин. Магнитные газоанализаторы. Госэнергоиздат, 1963.—3. А. Н. Блажеииова, А. А. Ильинская. Ф. М. Рапопорт. Анализ газов в химической промышленности. Госхимиздат, 1954. — 4. О. П. Б о ч к о в а. Е. Я. Ш р е й-дер. Спектральный анализ газовых смесей. 2-е изд., Физматгиз, 1963. — 5. Б. Г. Ер е-» мина. Газовый анализ, Госхимиздат. 1955.— 6. В. А. Павленко, Газоанализаторы, Изд «Машиностроение», 1965.—7. Приборы и средства автоматизации (каталог), т. 5 и 8. ОНТИПрибор, I960—1965. — 8. Ф. М. Рапопорт, А. А. Ильинская, Лабораторные ме-* тоды получения чистых газов, Госхимиздат 1963. — 9. В. А. Соколов, Методы анализа газов, Гостоптехиздат, 1958. — 10. Справочник по методам определения вредных веществ в воздухе, Институт гигиены труда и профзаболеваний АМН СССР, i960. — 11. F. Bayer, G. W a g п е г, Gasanalyse. Methoden der Arbeitspraxis, 3-е изд.. Штуттгарт, i960. — 12. Chemische Gasanalyse, Bearb. von К. Kessels. Дюссельдорф, 1960. — 13. H. Guerin. Traite de manipulation et d’analyse des gaz,Париж, 1952. — 14. Messen und Regeln in der chemischen Technik, Hrsg. von J. H e n g s t e n b e r g, B. Sturm, O. Winkler. 2-е изд.. Берлин — Геттингеи — Гейдельберг, 1964. — 15. Methods for the Sampling and Analysis of Fuel Gases, British Standard 3156:1959, Лондон. 1959. — 16. Process Instruments and Controls Handbook, D. M. Considine (Ed.), Нью-Йорк — Торонто — Лондон, 1957. — 17. G. Tine, Gas Sampling and Chemical Analysis in Combustion Processes, Оксфорд, 1961. — 18 F. T 6 d t, Elektrochemische Sauerstoffmessungen. Konzentrationsmessungen oxydierender 41 nd reduzierender Stoffe durch galvanische Modellelemente, Берлин, 1958.
Единицы измерения концентраций газов и паров и их взаимный пересчет
ТАБЛИЦА ДЛЯ ПЕРЕСЧЕТА КОНЦЕНТРАЦИИ ГАЗОВ И ПАРОВ
В таблице приняты следующие условные обозначения:
а — числовое зиачеиие концентрации в заданных единицах;
х _ числовое значение концентрации в искомых единицах;
— молекулярный вес газа;
р — общее давление газовой смеси в мм рт. ст.;
Т — температура в °К;
z — коэффициент разбавления (отношение общего объема газа к объему соответствующего компонента).
При пользовании таблицей следует иметь в виду следующие соотношения:
1 г/л<3=1 мг/дм3—1 мг/л
1 л<г/л<3=1 мкг/дм3~1 мкг/л.
1 моль/дм3^ I моль (л
1 СМ31м3^ 1 мл/м3
1 ММ3/М3^1 МЮЦМ*
672
ТАБЛИЦА ДЛЯ ПЕРЕСЧЕТА КОНЦЕНТРАЦИИ ГАЗОВ И ПАРОВ
573
ТАБЛИЦА ДЛЯ ПЕРЕСЧЕТА КОНЦЕНТРАЦИЙ ГАЗОВ И ПАРОВ
Продолжение
Пример пользования таблицей
Дапо: а=1С объеми. %, Г=293° К, Р=770 мм рт. ст. Требуется найти х — значение кон* центрации, выраженное в моль/дм3.
В первой графе находим горизонтальную строку, соответствующую заданным единицам концентрации (строка 4), а в этой строке — вертикальный столбец, соответствующий требуемым единицам концентрации (моль/дм3). На пересечении строки 4 и вертикального столбца иаходнм формулу, по которой определяем значение концентрации в требуемых единицах:
16,04-10”6 аР 16,04-10~6-10-770 ,
¥ = —!--~------— —1-------------— 0,0042 моль/дм3
НОМОГРАММА ДЛЯ ПЕРЕСЧЕТА КОНЦЕНТРАЦИЙ ГАЗОВ И ПАРОВ
Номограмма (стр. 575) предназначена для пересчета концентраций газов и паров (при температуре Г=293°К и общем давлении газовой смеси Р=760 мм рт. ст.) из объемн. % (V) в г/м3 (С), и обратно; при этом следует иметь в виду, что 1 г/м3=1 мг/дм3^\ мг/л.
Для пересчета находят на графике отрезок радиальной прямой, соответствующий данному газу (или радиальную прямую, соответствующую молекулярному весу газа М), н при1 помощи линейкн соединяют его с нулевой точкой. Ордината каждой точки полученной' прямой выражает концентрацию газа в объемн. %, а абсцисса — соответствующую вели-, чину в г/м3.
При отсутствии на графике радиальной линии молекулярного веса искомого газа, находят любую точку этой линии по одной из следующих формул:
V’=6,236 - - объеми. %
МР
Соединив найденную течку с нулевой точкой графика, получают прямую, которая и служит для пересчета.
На графике значения V даны только до 1,1, а значения С—до 16. Если заданная концентрация выше этих величии или ее абсолютное значение очень мало, то по графику, находят значение меньшее (большее) в X • ЮЛ раз (где К=1, 2, 3..........9, а л=0 или
±1, 2, 3...), а затем найденную величину увеличивают (уменьшают) в К • 1(7* раз.
574
НОМОГРАММА ДЛЯ ПЕРЕСЧЕТА КОНЦЕНТРАЦИИ ГАЗОВ И ПАРОВ
575
Некоторые физичесю
КОЭФФИЦИЕНТЫ ТЕПЛОПРОВОДНОСТИ НЕКОТОРЫХ
Приводимые ниже данные дополняют материалы, помещенные в первом томе «Справок# ника химика» (2-е изд., стр. 927—929). %
Для некоторых веществ данные имеются как в первом томе, так и в настоящей таблице» более достоверными следует считать последние: их предельная погрешность для темперах)» до''-200° С составляет ±1’%, для более высоких температур она может достигать ±3—4%- Я
Значения коэффициентов теплопроводности Л приведены в двух системах единиц: ндж чертой (в «числителе») — в единицах системы СГС, т. е. в калЦсм • сек • град), увеличенные в 10® раз (АсГС * Ю5)« а под чертой (в «знаменателе») — в единицах СИ, т. е. в втЦм • гра&$ увеличенные в 103 раз Р-СИ’ 10?)- Точное соотношение между этими двумя единицам^ 1 калЦсм • сек • град) = 4.1868-102 бтЦм • град).
Газ или пар Коэффициент теплопровод 'К
название формула о 25 50 1°°
Акрилонитрил ch2=chcn .... 2,31 9,67 д
Аммиак NH3 5,18 21,7 5,90 24,7 6,68 28,0 8,41 35,2
Аргон Ar 3,91 16,4 4,21 ' 17,6 4,50 18,8 5,09 . 21.3 1j
Ацетилен CHesCH 4,51 18,9 5,20 su 5,91 24,7 7,36 ‘ 30,8 У
Бутадиен * сн2=снсн=сн2 2,90 12,1 3,57 14,9 4,29 17,9 5,83 Ч 24,4
Бутан CH3 (СН2)2СН3 3,05 12,8 3,68 15,4 4,36 18,2 5,88 1 24Д t
Бутен-1 СН3СН2СН=СН2 3,02 12,6 3,60 15,1 4,24 17,7 5,70 23,8
Воздух 5,77 24,2 6,20 26,0 6,64 27,8 7,50 ... 31,4 Д
Двуокись углерода со2 3,48 14,6 3,92 16,4 4,37 18,3 5,33 22,3;
1, 1-Дихлорэтилен СН2=СС12 1,65 6,91 1,92 8,04 2,20 9,21 2,79 - 11,7 ;
Изобутан (СН3)3СН 3,16 14,5 3,79 15,9 4,47 18,7 5,98 : 25,0
* Вероятно, бутадиен- 3 (дивинил).
576
свойства газов и паров
ГАЗОВ И ПАРОВ ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ
Величины А, В и С, значения которых приведены иад чертой, — постоянные уравнения Я • Ю5 = Д 4- + Ci2 при пользовании единицами системы СГС, а под чертой — постоянные
уравнения X • 103=Д ±Bt+Ct2 при пользовании единицами СИ. С помощью этих уравнений можно интерполировать (в соответствующих единицах) значения коэффициентов теплопроводности при промежуточных температурах.
Сводка литературных данных о значениях коэффициентов теплопроводности чистых газов и паров при различных температурах и бинарных газовых смесей различных концентраций содержится в книге: Н. Б. В а р г а ф т и к, Справочник по теплофизическим свойствам газов и жидкостей, Физматгиз, 1963.
ности при температуре, °C Постоянные уравнения температурной зависимости коэффициента теплопроводности
150 200 300 400 А В с
10,36 12,54 17,6 23,5 5,18 0,0279 448 КГ7
43,38 52,50 73,7 98,4 21,7 0,117 188- 10-6
5,69 6,28 7,46 8,65 3,91 0,0119
23,8 26,3 31,2 36,2 16,4 0,0498
8,88 10,45 13,8 17,35 4,51 0,0273 12 - 10~в
37,2 43,75 57,8 72,64 18,9 0,114 50- 10~6
7,53 9,39 13,6 18,4 2,90 0,0262 311.10-7
31,5 39,3 56,9 77,0 12,1 0,110 130- 10-в
7,60 9,50 14,0 19,2 3,05 0,0243 403- 10~7
31,8 39,8 58,6 60,4 12,8 0,102 169- 10-в
7,39 9,31 13,9 19,3 3,02 0,0222 463-10-7
30,9 39,0 58,2 80,8 12,6 0,0929 194- 10" 6
8,37 9,23 10,96 12,70 5,77 0,0173
35,0 38,6 45,89 53,17 24,2 0,0724
6,34 7,41 9,67 12,04 3,48 0,0174 11 - 10-в
26,5 31,0 • 40,5 50,41 14,6 0,0728 46-10“в
3,41 4,07 5,49 7,04 1,65 0,0107 686 - 10~в
14,3 17,0 23,0 29,5 6,91 0,0448 287 10-7
7,69 9,60 14,02 19,23 3,16 0,0242 400-10-7
32,2 40,2 58,70 80,51 14,5 0,101 167- 10-в
37 Зак. 783
577
1' КОЭФФИЦИЕНТЫ ТЕПЛОПРОВОДНОСТИ НЕКОТОРЫХ ;1
Газ или пар Коэффициент теплопровод ?
название формула 0 25 50 100 J
Изопентан (СН3)2 СНС2Н5 2,80 11,7 3,35 14,0 3,95 16,5 5,32 F 22,3 у
Криптон Кг 1,95 8,16 2,07 8,67 2,20 9,21 2,44 10,2
Метан сн4 7,11 29,8 8,09 33,9 9,07 38,0 11,15 46,68 г.
2-Метилпропен (СН3)2 C—CHg 3,04 12,7 3,67 15,3 4,34 18,2 5,78 j 24,2 1
Окись этилена (СН2)2 О 2,47 10,3 2,97 12,4 3,53 14,8 4,82 j 20,2
Пропан СН3СН2СН3 3,56 14,9 4,26 17,8 5,01 21,0 6,64 ; 27,8 !
Пропилен СН3СН=СН2 3,48 14,6 4,14 17,3 4,85 20,3 6,44 , 27,0 j
Трихлорэтилен СНС1=СС12 .... 0,185 0,775 . . . . 1
Хлористый винил СН2=СНС1 2,21 9,25 2,60 10,9 3,03 12,7 3,95 16,5
Хлористый метил СН3С1 2,17 9,09 2,52 10,6 2,90 12,1 3,76 15,7
Хлористый метилен СН2С12 1,58 6,62 1,77 7,41 1,98 8,29 2,46 10,3
Хлористый этил СН3СН2С1 2,17 9,09 2,58 10,8 3,01 12,6 3,99 16,7 ;
Цианистый водород HCN 2,35 9,84 2,83 11,8 3,30 13,8 4,27 17,9
Этан СН3СН3 4,23 17,7 5,07 21,2 5,94 24,9 7,82 32,7
Этилен сн2=сн2 4,18 17,5 4,93 W 5,73 24,0 7,46 31,2
578
ГАЗОВ И ПАРОВ ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ
Продолжение
нести при температуре, °C Постоянные уравнения температурной зависимости коэффициента теплопроводности
150 200 300 400 А В С
6,90 28,9 8,70 12,9 18,0 2,80 0,0209 430 • 10“7
36,4 54,0 75,4 Н.7 0,0875 180- 10“6
2,68 2,90 3,36 3,83 1,95 0,00469
11,2 12,1 14,1 16,0 8,16 0,0196
13,3 15,5 20,25 25,3 7,11 0,0387 171-10“7
55,7 64,9 84,78 106 29,8 0,162 716-10’7
7,37 9,11 13,0 17,5 3,04 0,0244 295- 10“7
30,9 38,1 54,4 73,3 12,7 0,102 124- 10" 6
6,34 8,10 12,3 17,4 2,47 0,0189 464-10”7
26,5 33,9 51,5 72,9 10,3 0,0791 194-10 6
8,46 10,47 15,05 20,4 3,56 0,0271 374-10"7
35,4 43,84 63,01 85,4 14,9 0,113 157 • 10“6
8,24 10,3 14,9 20,4 3,48 0,0253 43- 10" 6
34,5 43,1 62,4 85,4 14,6 0,106 18- 10“5
4,99 6,14 8,78 11,9 2,21 0,0152 223- 10“7
20,9 25,7 36,8 46,4 9,25 0,0637 934 - 10“7
4,75 5,87 8,50 11,65 2,17 0,0132 261 10“7
19,9 24,6 35,6 48,78 9,09 0,0553 109- 10“6
3,03 3,68 5,24 7,15 1,58 0,00706 171 • 10“7
12,7 15,4 21,9 29,9 6,62 0,0296 716- 10“7
5,09 6,33 9,20 12,6 2,17 9,09 0,0155 263 10~7
21,3 26,5 ' 38,5 52,6 0,0649 ПО- 10“6
5,22 6,18 8,09 10,00 2,35 0,0191
21,9 25,9 33,9 41,9 9,84 0.0800
9,84 12,0 16,80 22,2 4,23 0,0329 298- 10“7
41,2 50,2 70,34 92,9 17,7 0,138 125- 10“6
9,87 11,45 16,1 21,6 4,18 0,0293 353 - 10 “7
41,3 47,94 67,4 90,4 17,5 0,123 148-10“6
37*
579
МАГНИТНАЯ ВОСПРИИМЧИВОСТЬ ГАЗОВ И ПАРОВ
В таблице приводятся значения удельной % н объемной (относительной) Лдо магнитной восприимчивости.
Под объемной магнитной восприимчивостью Лдо подразумевается коэффициент пропорциональности между намагниченностью (плотностью магнитного момента *) / единицы объема газа или пара н напряженностью Н магнитного поля в этом объеме, т. е. коэффициент в выражении Поскольку размерности величин J н Н одинаковы,
величина k м безразмерна и выражается в отвлеченных единицах.
Удельная магнитная восприимчивость связана с объемной соотношением:
где р — плотность газа или пара.
Величина X характеризует магнитную восприимчивость единицы массы вещества, fe единицах системы СГС X выражается в а в единицах СИ — в м3]кг.
Значения k м и X- выраженные в системе СГС (нерационализованной), могут быть пересчитаны в единицы СИ (рационализованная система) с помощью соотношений:
4Я*МСГС = *МСИ и 4л-103ХсГСетХСИ
Над чертой (в «числителе») приводятся значения X * 10е и ^М’Ю10 в единицах системы СГС, под чертой (в «знаменателе»)—значения % ИО3 и йду • 109 в единицах СИ.
Газ или пар X прн 20° С kft при 20° С и 760 мм рт. ст. Газ или пар х при 20° С /ем при 20° С н 760 мм рт. ст.
название фор- мула название фор- мула
Азот n2 —0,43 —5,01 Неон Ne —0,38 —3,19
—5,4 —6,30 —4,8 —4,01
Аммиак NH3 —1.1 —7,90 Окись азота . . NO +49 +611
—14 —9,93 +620 +768
Аргон Ar —0,48 —7,97 Окись углерода СО —0,42 —4,88
—6,0 —10,0 —5,3 —6,13
Ацетплен .... С2Н2 —0,48 —5,24 Сероводород . . H2S —0,75 —10,8
—6,0 —6,57 —9,4 —13,6
Водород .... н —2,0 —1,68 Хлор Cl2 —0,59 —17,7
Г12 —25 —2,11 —7,4 —22,2
Гелий Не —0,48 —0,80 Хлористый водород НС1 —0,60 —9,19
—6,0 —1,0 —7,5 —11,5
Двуокись углерода СО2 —0,48 —8,77 Хлористый метил СН3С1 —0,64 —14,2
—6,0 —11,0 —8,0 —17,8
Закись азота . . n2o —0,43 —7,93 Этан с2н6 —0,73 —9,24
—5,4 —9,97 —9,2 —11,6
Кислород .... о2 +106,2 +1414 С2Н4 —0,43 —5,05
+1335 +1777 —5,4 —6,35
Метан сн4 —0,76 —5,08
—9,6 —6,38
* Магнитный момент, обусловливающий намагниченность, выражается в единицах, которые определяются через напряженность магнитного поля, создаваемого этим моментом, но не через магнитную индукцию.
580
СКОРОСТЬ ЗВУКА В ГАЗАХ И ПАРАХ
Газ нлн пар Температура, Скорость звука С, м[сек Температурный коэффициент скорости звука (м(сек)1 град
название формула
Газы
Азот n2 0 334 0,6
Аммиак NH3 0 415 ........
Аргон Аг 0 319 0,56
Бромистый водород .... НВг 0 200
Водород н2 0 1284 2,2
Воздух 0 331 0,59
Гелий Не 0 965 0,8
Двуокись серы so2 0 213 0,47
Двуокись углерода .... со2 0 259 0,4
Дейтерий d2 0 890 1,6
Закись азота n2o 0 263 0,5
Йодистый водород .... HJ 0 157
Кислород О2 0 316 0,56
Метан сн4 0 430
Неон Ne 0 435 0,8
Ркись азота NO 10 324
_ Окись углерода СО 0 338 0,6
Сероводород H2S 0 289
Хлор Cl2 0 206 ••••а
Хлористый водород .... HCI 0 296
Четырехфтористый кремний SiF4 0 167 • ••••••а
Этан C2He 10 308
Этилен C2H4 0 317
Пары
Ацетон СН3СОСН3 97,1 239 0,32
134 251 . .......
Бензол . CeHe 97,1 202 0,3
134 213
Бутанон-2 СН3СОС2Н5 134 223
етор-Бутиловый спирт . . . С2Н5СНОНСН3 134 215
трет-Бутиловый спирт . . (СНз)зСОН 134 180
Винилацетат СН3СООСН=СН2 134 203
Вода Н2О 134 494
Гексан СН3 (СН2)4 СН3 134 199
Диметиловый эфир .... (СН3)2 о 25 246 0,39
97,1 274
Дипропиловый эфир . . . (С3Н7)2 о 97,1 194
Дихлорэтан С2Н4С12 97,1 181 6,24
134 190
Диэтиловый эфир (С2Н6)2 о 97,1 206 0,3
134 217 а . •
Изопропиловый спирт . . CH3CHOHCH3 97,1 255 0,4
134 270
Метиловый спирт СН3ОН 97,1 335 0,46
134 352
Метилциклогексан .... С6НПСН3 134 185 • ••••••*
Пентан СН3 (СН2)3 сн3 134 220
Пропиловый спирт .... СН3СН2СН2ОН 134 244
Сероуглерод cs2 97,1 220
Хлористый метилен .... СН2С12 97,1 204 0,24
134 213
681
СКОРОСТЬ ЗВУКА В ГАЗАХ И ПАРАХ
Продолжение
Газ или пар Температура, °C Скорость звука С, м/сек Температурный коэффициент скорости звука AC/At, (м/сек)/град
название формула
Хлороформ . . . Циклогексан Четыреххлористый углерод Этилацетат . Этиловый спирт СНС13 СвН12 СС14 СН3СООС2Н5 СН3СН2ОН 97,1 134 97,1 134 97,1 134 97,1 134 97,1 134 171 180 191 202 145 153 189 199 269 284 0,24 0,3 0,27 0,4
Расчет результатов газовых и газометрических анализов
Газовый анализ
Объем сухого газа Уо при 0° С н 760 мм рт. ст. находят по формуле:
V0 = VF (1)
где V — объем газа, измеренный прн данных температуре и давлении; F — коэффициент пересчета, значения которого приведены на стр. 583—587.
Значение F можно также вычислить по формуле:
/------------- (2)
(1 +Ct/) 760 ' ’
где Ро~~ атмосферное давление, приведенное к 0° С, мм рт. ст.; Ct — коэффициент объемного расширения газа, град / — температура газа, °C.
Для приведения атмосферного давления к 0° С с достаточной точностью можно воспользоваться формулой:
PQ^Pt-0,125/'
где Pt — давление при температуре /°C, мм рт. ст.; t'— температура ртути в барометре, °C.
Объем газа, собранный над водой или водными растворами солей, приводится к нормальным условиям по формуле (1)- В этих случаях величина Pq, входящая в формулу расчета коэффициента F, составляет:
Po==Pz_ 0,125/'-Рв (3;
где Рв—давление паров воды при соответствующей температуре, мм рт. ст.
При особо точных расчетах к установленному давлению добавляют поправку на капиллярную депрессию ртути («Справочник химика», 2-е изд., т. I, стр. 69). Коэффициент F в этих случаях следует вычислять по формуле (2), пользуясь значением а для данного газа.
Ниже приводятся значения а для некоторых газов в интервале температур 0—100° С при давлении 760 мм рт. ст.:
Двуокись углерода............... 0,00371
Кислород......................... 0,00367
Окись углерода................... 0,00367
Хлор............................. 0,00383
Азот ................................. 0,00367
Водород............................. 0,00366
Воздух . . ... 0,00367
Гелий................................. 0,00366
В соответствии с требованием ГОСТ 2939—63 при расчете объема газа следует исходить из объема, приведенного к 20° С и 760 мм рт. ст.
Объем газа при этих условиях устанавливают по формуле:
V2o=1,0733I/F
Газометрический анализ
Содержание газа в твердых и жидких веществах рассчитывают по формуле:
где Го— обьем газа при 0° С и 760 мм рт. ст., дм3; d — плотность газа при 0° С н 760 мм рт. ст., кг/м3; а — навеска анализируемого вещества, г.
Содержание определяемого вещества по количеству образовавшегося газа может быть вычислено следующим образом:
,z VGf-100
------ вес. %
а
где f — коэффициент пересчета (масса определяемого вещества в граммах, соответствующая 1 сЫ3 образовавшегося газа, .приведенного к 0° С и 760 мм рт. ст.), значения которого приведены на стр. 589.
582
ЗНАЧЕНИЯ КОЭФФИЦИЕНТА F ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИЯХ
Температура газа, °C Давление Р, мм рт. ст.
690 692 694 696 698 700 702
5 0,8915 0,8941 0,8967 0,8993 0,9019 0,9045 0,9070
6 0,8883 0,8909 0,8935 0,8961 0,8986 0,9012 0,9038
7 0,8852 0,8877 0,8903 0,8929 0,8954 0,8980 0,9006
8 0,8820 0,8846 0,8871 0,8897 0,8922 0,8947 0,8973
9 0,8789 0,8814 0,8840 0,8865 0,8891 0,8916 0,8942
10 0,8757 0,8783 0,8808 0,8834 0,8859 0,8884 0,8910
11 0,8727 0,8752 0,8777 0,8803 0,8828 0,8853 0,8878
12 0,8696 0,8721 0,8746 0,8772 0,8797 0,8822 0,8847
13 0,8665 0,8691 0,8716 0,8741 0,8766 0,8791 0,8816
14 0,8635 0,8660 0,8685 0,8710 0,8735 0,8760 0,8785
15 0,8605 0,8630 0,8655 0,8680 0,8705 0,8730 0,8755
16 0,8575 0,8600 0,8625 0,8650 0,8675 0,8700 0,8724
17 0,8546 0,8571 0,8595 0,8620 0,8645 0,8670 0,8694
18 0,8516 0,8541 0,8566 0,8590 0,8615 0,8640 0,8664
19 0,8487 0,8512 0,8536 0,8561 0,8586 0,8610 0,8635
20 0,8458 0,8483 0,8507 0,8532 0,8556 0,8581 0,8605
21 0,8429 0,8454 0,8478 0,8503 0,8527 0,8551 0,8576
22 0,8401 0,8425 0,8449 0,8474 0,8498 0,8522 0,8547
23 0,8372 0,8397 0,8421 0,8445 0,8469 0,8494 0,8518
24 0,8344 0,8368 0,8392 0,8416 0,8441 0,8465 0,8489
25 0,8316 0,8340 0,8364 0,8388 0,8412 0,8436 0,8461
26 0,8288 0,8312 0,8336 0,8360 0,8384 0,8408 0,8432
27 0,8260 0,8284 0,8308 0,8332 0,8356 0,8380 0,8404
28 0,8233 0,8257 0,8281 0,8304 0,8328 0,8352 0,8376
29 0,8206 0,8229 0,8253 0,8277 0,8301 0,8325 0,8348
30 0,8179 0,8202 0,8226 0,8250 0,8274 0,8297 0,8321
31 0,8152 0,8175 0,8199 0,8223 0,8246 0,8270 0,8294
32 0,8125 0,8149 0,8172 0,8196 0,8219 0,8243 0,8266
33 0,8098 0,8122 0,8145 0,8169 0,8192 0,8216 0,8239
34 0,8072 0,8095 0,8119 0,8142 0,8166 0,8189 0,821?
35 0,8046 0,8069 0,8092 0,8116 0,8139 0,8162 0,8185
36 0,8020 0,8043 0,8066 0,8089 0,8112 0,8136 0,8159
37 0,7994 0,8017 0,8040 0,8063 0,8086 0,8109 0,8132
38 0,7968 0,7991 0,8014 0,8037 0,8060 0,8083 0,8106
39 0,7942 0,7965 0,7988 0,8011 0,8034 0,8057 0,8080
40 0,7917 0,7940 0,7963 0,7986 0,8009 0,8031 0,8054
Темпера- Давление Р, мм рг г. ст.
"г °с 704 706 । 708 710 712 714 716
5 0,9096 0,9122 0,9148 0,9174 0,9200 0,9226 0,9251
6 0,9064 0,9091 0,9115 0,9141 0,9167 0,9192 0,9218
7 0,9031 0,9057 0,9082 0,9108 0,9134 0,9159 0,9185
8 0,8999 0,9025 0,9050 0,9076 0,9101 0,9127 0,9152
9 0,8967 0,8993 0,9018 0,9043 0,9069 0,9094 0,9120
10 0,8935 0,8931 0,8986 0,9011 0,9037 0,9062 0,9088
588
ЗНАЧЕНИЯ КОЭФФИЦИЕНТА F ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИЯХ
Продолжение
Температура газа, °C Давление Р, мм рт. ст.
704 706 708 710 712 714 716
11 0,8904 0.8929 0,8954 0,8980 0,9005 0,9030 0,9055
12 0,8872 0,8898 0,8923 0,8948 0,8973 0,8999 0,9024
13 0,8841 0,8866 0,8892 0,8917 0,8942 0,8967 0,8992
14 0,8810 0,8835 0,8861 0,8885 0,8911 0,8936 0,8961
15 0,8780 0,8805 0,8830 0,8855 0,8880 0,8905 0,8930
16 0,8749 0,8774 0,8799 0,8824 0,8849 0,8874 0,8899
17 0,8719 0,8744 0,8769 0,8793 0,8818 0,8843 0,8868
18 0,8689 0,8714 0,8739 0,8763 0,8788 0,8813 0,8837
19 0,8659 0,8684 0,8709 0,8733 0,8758 0,8782 0,8807
20 0.8630 0,8654 0,8679 0,8703 0,8728 0,8752 0,8777
21 0,8600 0,8625 0,8649 0,8674 0,8698 0,8722 0,8747
22 0,8571 0,8595 0,8620 0,8644 0,8669 0,8693 0,8717
23 0,8542 0,8566 0,8591 0,8615 0,8639 0,8663 0,8688
24 0,8513 0,8537 0,8562 0,8586 0,8610 0,8634 0,8658
25 0,8485 0,8509 0,8533 0,8557 0,8581 0,8605 0,8629
26 0,8456 0,8480 0,8504 0,8528 0,8552 0,8576 0,8600
27 0,8428 0,8452 0,8476 0,8500 0,8524 0,8548 0,8572
28 0,8400 0,8424 0,8448 0,8472 0,8496 0,8519 0,8543
29 0,8372 0,8396 0,8420 0,8443 0,8467 0,8491 0,8515
30 0,8345 0,8368 0,8392 0,8416 0,8439 0,8463 0,8487
31 0,8317 0,8341 0,8364 0,8388 0,8412 0,8435 0,8459
32 0,8290 0,8313 0,8337 0,8360 0,8384 0,8408 0,8431
33 0,8263 0,8286 0,8310 0,8333 0,8357 0,8380 0,8404
34 0,8236 0,8259 0,8282 0,8306 0,8329 0,8353 0,8376
35 0,8209 0,8232 0,8255 0,8279 0,8302 0,8325 0,8349
36 0,8182 0,8205 0,8229 0,8252 0,8275 0,8298 0,8322
37 0,8156 0,8179 0,8202 0,8225 0,8248 0,8271 0,8295
38 0,8129 0,8153 0,8176 0,8199 0,8222 0,8245 0,8268
39 0,8103 0.8126 0,8149 . 0,8176 0,8195 0,8218 0,8241
40 0,8077 0,8100 0,8123 0,8146 0,8169 0,8192 0,8215
Темпера- Давление Р, мм рт. ст.
тура газа, °C 718 720 722 724 726 728 730
5 0,9277 0,9303 0,9329 0,9355 0,9381 0.9406 0,9432
6 0,9244 0,9270 0,9295 0,9321 0,9347 0,9373 0,9398
7 0,9211 0,9236 0,9262 0,9288 0,9313 0,9339 0,9365
8 0,9178 0,9203 0,9229 0,9255 0,9280 0,9306 0,9331
9 0,9145 0,9171 0,9196 0,9222 0,9247 0,9273 0,9298
10 0,9113 0,9138 0,9164 0,9189 0,9214 0,9240 0,9265
11 0,9081 0,9106 0,9131 0,9157 0,9182 0,9207 0,9233
12 0,9049 0,9074 0,9099 0,9125 0,9150 0,9175 0,9200
13 0,9017 0,9042 0,9067 0,9092 0,9118 0,9143 0,9168
14 0,8986 0,9011 0,9036 0,9061 0,9086 0,9111 0,9136
15 0,8954 0,8979 0,9004 0,9029 0,9054 0,9079 0,9104
16 0,8923 0,8948 0,8973 0,8998 0,9023 0,9048 0,9073
17 0,8893 0,8917 0,8942 0,8967 0,8992 0,9017 0,9041
18 0,8862 0,8887 0,8911 0,8936 0,8961 0,8985 0,9010
19 0,8832 0,8856 0,8881 0,8905 0,8930 0,8955 0,8979
20 0,8801 0,8826 0,8850 0,8875 0,8899 0,8924 0,8948
584
ЗНАЧЕНИЯ КОЭФФИЦИЕНТА Л ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИЯХ
Продолжение
Температура газа, °C Давление Р, мм рт. ст.
718 720 722 724 726 728 730
21 0,8771 0,8796 0.8820 0,8845 0,8869 0,8894 0,8918
22 0,8742 0,8766 0,8790 0,8815 0,8839 0,8863 0,8888
23 0,8712 0,8736 0,8761 0,8785 0,8809 0,8833 0,8858
24 0,8683 0,8707 0,8731 0,8755 0,8779 0,8804 0,8828
25 0,8653 0,8678 0,8702 0,8726 0,8750 0,8774 0,8798
26 0,8624 0,8648 0,8672 0,8696 0,8720 0,8745 0,8769
27 0,8596 0,8620 0,8644 0,8667 0,8691 0,8715 0,8739
28 0,8567 0,8591 0,8615 0,8639 0,8662 0,8687 0,8710
29 0,8539 0,8562 0,8586 0,8610 0,8634 0,8658 0,8681
30 0,8510 0,8534 0,8558 0,8583 0,8605 0,8629 0,8653
31 0,8482 0,8506 0,8530 0,8553 0,8577 0,8601 0,8624
32 0,8455 0,8478 0,8502 0,8525 0,8549 0,8572 0,8596
33 0,8427 0,8450 0,8474 0,8497 0,8521 0,8544 0,8568
34 0,8399 0,8423 0.8446 0,8470 0,8493 0,8516 0,8540
35 0,8373 0,8395 0,8419 0,8442 0,8465 0,8489 0,8512
36 0,8345 0,8368 0,8391 0,8415 0,8438 0,8461 0,8484
37 0,8318 0,8341 0,8364 0,8387 0,8410 0,8434 0,8457
38 0,8291 0,8314 0,8337 0,8360 0,8383 0,8407 0,8430
39 0,8264 0,8287 0,8310 0,8333 0,8356 0,8380 0,8403
40 0,8238 0,8261 0,8284 0,8307 0,8330 0,8353 0,8376
Темпера- Давление Р, мм рт. ст.
°C 732 734 736 738 740 742 744
5 0,9458 0,9484 0,9510 0,9536 0,9561 0,9587 0,9613
6 0,9424 0,9450 0,9476 0,9501 0,9527 0,9553 0,9579
7 0,9390 0,9416 0,9442 0,9467 0,9493 0,9518 0,9544
8 0,9357 0,9383 0,9408 0,9434 0,9459 0,9485 0,9510
9 0,9324 0,9349 0,9375 0,9400 0,9426 0,9451 0,9477
10 0,9291 0,9316 0,9341 0,9367 0,9392 0,9418 0,9443
11 0,9258 0,9283 0,9308 0,9334 0,9359 0,9384 0,9410
12 0,9225 0,9251 0,9276 0,9301 0,9326 0,9351 0,9376
13 0,9193 0,9218 0,9243 0,9269 0,9294 0,9319 0,9344
14 0,9161 0,9186 0,9211 0,9236 0,9261 0,9286 0,9311
15 0,9129 0,9154 0,9179 0,9204 0,9229 0,9254 0,9279
16 0,9097 0,9122 0,9147 0,9172 0,9197 0,9222 0,9247
17 0,9066 0,9092 0,9116 0,9140 0,9165 0,9190 0,9215
18 0,9035 0,9059 0,9084 0,9109 0,9134 0,9158 0,9183
19 0,9004 0,9028 0,9053 0,9078 0,9102 0,9127 0,9151
20 0,8973 0,8997 0,9022 0,9046 0,9071 0,9096 0,9120
21 0,8942 0,8967 0,8991 0,9016 0,9040 0,9065 0,9089
22 0,8912 0,8936 0,8961 0,8985 0,9010 0,9034 0,9058
23 0,8882 0,8906 0,8930 0,8955 0,8979 0,9003 0,9028
24 0,8852 0,8876 0,8900 0,8924 0,8949 0,8973 0,8997
25 0,8822 0,8846 0,8870 0,8894 0,8919 0,8943 0,8967
26 0,8793 0,8817 0,8841 0,8865 0,8889 0,8913 0,8937
27 0,8763 0,8787 0,8811 0,8835 0,8859 0,8883 0,8907
28 0,8734 0,8758 0,8782 0,8806 0,8830 0,8853 0,8877
29 0,8705 0,8729 0,8753 0,8776 0,8800 0,8824 0,8848
30 0,8676 0,8700 0,8724 0,8748 0,8771 0,8795 0,8819
585
ЗНАЧЕНИЯ КОЭФФИЦИЕНТА Г ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИЯХ
Продолжение
Температура газа, °C Давление Р, мм рт. ст.
732 734 736 | 738 | 740 742 744
31 0,8648 0,8672 0,8695 0,8719 0,8742 0,8766 0,8790
32 0,8619 0,8643 0,8667 0,8691 0,8714 0,8736 0,8761
33 0,8591 0,8615 0,8638 0,8662 0,8685 0,8709 0,8732
34 0,8563 0,8587 0,8610 0,8634 0,8658 0,8680 0,8704
35 0,8535 0,8559 0,8582 0,8605 0,8629 0,8652 0,8675
36 0,8508 0,8531 0,8554 0,8577 0,8601 0,8624 0,8647
37 0,8480 0,8503 0,8526 0,8549 0,8573 0,8596 0,8619
38 0,8453 0,8476 0,8499 0,8522 0,8545 0,8568 0,8591
39 0,8426 0,8449 0,8472 0,8495 0,8518 0,8541 0,8564
40 0,8399 0,8422 0,8444 0,8467 0,8490 0,8513 0,8536
Темпера- Давление Р, мм рт. ст.
°C 746 748 | 750 752 754 756 | 758 | 760 762
5 0,9639 0,9665 0,9691 0,9717 0,9742 0,9768 0,9794 0,9820 0,9846
6 0,9604 0,9630 0,9656 0,9682 0,9707 0,9733 0,9759 0,9785 0,9810
7 0,9570 0,9596 0,9621 0,9647 0,9673 0,9698 0,9724 0,9750 0,9775
8 0,9536 0,9561 0,9587 0,9613 0,9638 0,9664 0,9689 0,9715 0,9741
9 0,9502 0,9528 0,9553 0,9578 0,9604 0,9629 0,9655 0,9680 0,9706
10 0,9468 0,9494 0,9519 0,9544 0,9570 0,9595 0,9621 0,9646 0,9671
11 0,9435 0,9460 0,9486 0,9511 0,9536 0,9562 0,9587 0,9612 0,9637
12 0,9402 0,9427 0,9452 0,9477 0,9503 0,9528 0,9553 0,9578 0,9603
13 0,9369 0,9394 0,9419 0,9444 0,9469 0,9495 0,9520 0,9545 0,9570
14 0,9336 0,9363 0,9386 0,9411 0,9436 0,9461 0,9486 0,9511 0,9536
15 0,9304 0,9329 0,9354 0,9378 0,9404 0,9428 0,9453 0,9478 0,9503
16 0,9271 0,9296 0,9321 0,9346 0,9371 0,9396 0,9420 0,9445 0,9470
17 0,9239 0,9264 0,9289 0,9314 0,9339 0,9363 0,9388 0,9413 0,9438
18 0,9207 0,9232 0,9257 0,9282 0,9306 0,9331 0,9356 0,9380 0,9405
19 0,9176 0,9200 0,9225 0,9250 0,9275 0,9299 0,9324 0,9348 0,9373
20 0,9145 0,9169 0,9194 0,9218 0,9243 0,9267 0,9292 0,9316 0,9341
21 0,9113 0,9138 0,9162 0,9187 0,9211 0,9236 0,9260 0,9285 0,9309
22 0,9083 0,9107 0,9131 0,9155 0,9180 0,9204 0,9229 0,9253 0,9277
23 0,9052 0,9076 0,9100 0,9125 0,9149 0,9173 0,9197 0,9222 0,9246
24 0,9021 0,9045 0,9070 0,9094 0,9118 0,9142 0,9165 0,9191 0,9215
25 0,8991 0,9015 0,9039 0,9063 0,9087 0,9112 0,9135 0,9160 0,9184
2g 0,8961 0,8985 0,9009 0,9033 0,9057 0,9081 0,9105 0,9129 0,9153
27 0,8931 0,8955 0,8979 0,9003 0,9027 0,9051 0,9074 0,9099 0,9122
28 0,8901 0,8925 0,8949 0,8973 0,8997 0,9021 0,9044 0,9068 0,9092
29 0,8872 0,8895 0,8919 0,8943 0,8967 0,8990 0,9014 0,9038 0,9062
30 0,8842 0,8866 0,8890 0,8914 0,8937 0,8961 0,8985 0,9008 0,9032
31 0,8813 0,8837 0,8861 0.8884 0,8908 0,8931 0,8955 0,8979 0,9002
32 0,8784 0,8808 0,8831 0,8855 0,8878 0,8902 0,8926 0,8949 0,8973
33 0,8756 0,8779 0,8803 0,8826 0,8850 0,8873 0,8897 0,8920 0,8943
34 0,8727 0,8750 0,8774 0,8797 0,8821 0,8844 0,8867 0,8891 0,8914
35 0,8699 0,8722 0,8745 0,8768 0,8792 0,8815 0,8839 0,8862 0,8885
36 0,8670 0,8694 0,8717 0,8740 0,8763 0,8787 0,8810 0,8833 0,8856
37 0,8642 0,8665 0,8689 0,8712 0,8735 0,8758 0,8781 0,8804 0,8828
38 0,8615 0,8638 0,8661 .0,8684 0,8707 0,8730 0,8753 0,8776 0,8799
39 0,8587 0,8610 0,8633 0,8656 0,8679 0,8702 0,8725 0,8748 0,8771
40 0,8559 0,8582 0,8605 0,8628 0,8651 0,8674 0,8697 0,8720 0,8743
686
ЗНАЧЕНИЯ КОЭФФИЦИЕНТА F ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ И ДАВЛЕНИЯХ
Продолжении
Температура газа, °C Давление Р, мм рт. ст.
764 766 । 768 770 772 774 776 778 780
5 0,9871 0,9897 0,9923 0,9949 0,9975 1,0001 1,0026 1,0051 1,0078
6 0,9836 0,9862 0,9888 0,9913 0,9939 0,9965 0,9990 1,0016 1,0042
7 0,9801 0,9827 0,9852 0,9878 0,9904 0,9929 0,9955 0,9980 1,0006
8 0,9766 0,9792 0,9817 0,9843 0,9868 0,9894 0,9919 0,9945 0,9970
9 0,9731 0,9757 0,9782 0,9807 0,9833 0,9859 0,9884 0,9910 0,9935
10 0,9697 0,9722 0,9747 0,9773 0,9798 0,9824 0,9849 0,9874 0,9900
11 0,9663 0,9688 0,9713 0,9739 0,9764 0,9789 0,9814 0,9839 0,9865
12 0,9629 0,9654 0,9679 0,9704 0,9730 0,9754 0,9780 0,9805 0,9830
13 0,9595 0,9620 0,9645 0,9670 0,9695 0,9720 0,9745 0,9771 0,9796
14 0,9561 0,9586 0,9612 0,9637 0,9661 0,9686 0,9711 0,9736 0,9762
15 0,9528 0,9553 0,9578 0,9603 0,9628 0,9653 0,9678 0,9703 0,9728
16 0,9495 0,9520 0,9545 0,9570 0,9595 0,9619 0,9644 0,9669 0,9694
17 0,9462 0,9487 0,9512 0,9537 0,9561 0,9586 0,9611 0,9636 0,9661
18 0,9430 0,9454 0,9479 0,9504 0,9528 0,9553 0,9578 0,9602 0,9627
19 0,9397 0,9422 0,9447 0,9471 0,9496 0,9520 0,9545 0,9569 0,9594
20 0,9365 0,9390 0,9414 0,9439 0,9463 0,9488 0,9512 0,9537 0,9561
. 21 0,9333 0,9359 0,9382 0,9407 0,9431 0,9455 0,9480 0,9504 0,9529
22 0,9302 0,9326 0,9350 0,9375 0,9399 0,9423 0,9448 0,9472 0,9496
23 0,9270 0,9294 0,9319 0,9343 0,9367 0,9391 0,9416 0,9440 0,9464
24 0,9239 0,9263 0,9287 0,9311 0,9336 0,9360 0,9384 0,9408 0,9432
25 0,9208 0,9232 0,9256 0,9280 0,9304 0,9328 0,9352 0,9377 0,9401
26 0,9177 0,9201 0,9225 0,9249 0,9273 0,9297 0,9321 0,9345 0,9369
27 0,9146 0,9170 0,9194 0,9218 0,9242 0,9266 0,9290 0,9314 0,9338
28 0,9116 0,9140 0,9164 0,9187 0,9211 0,9235 0,9259 0,9283 0,9307
29 0,9086 0,9109 0,9133 0,9157 0,9181 0,9205 0,9228 0,9252 0,9276
30 0,9056 0,9079 0,9109 0,9127 0,9151 0,9174 0,9198 0,9222 0,9245
31 0,9026 0,9050 0,9073 0,9097 0,9121 0,9144 0,9168 0,9191 0,9215
32 0,8996 0,9020 0,9043 0,9067 0,9091 0,9114 0,9138 0,9161 0,9185
33 0,8967 0,«990 0,9014 0,9037 0,9061 0,9084 0,9108 0,9131 0,9154
34 0,8938 0,8961 0,8984 0,9008 0,9031 0,9055 0,9078 0,9101 0,9125
35 0,8908 0,8932 0,8955 0,8978 0,9002 0,9025 0,9048 0,9072 0,9092
36 0,8880 0,8903 0,8926 0,8949 0,8972 0,8996 0,9019 0,9042 0,9065
37 0,8851 0,8874 0,8897 0,8920 0,8943 0,8967 0,8990 0,9013 0,9036
38 0,8822 0,8845 0,8869 0,8892 0,8915 0,8938 0,8961 0,8984 0,9007
39 0,8794 0,8817 0,8840 0,8863 0,8886 0,8909 0,8932 0,8955 0,8978
40 0,8766 0,8789 0,8812 0,8835 0,8857 0,8881 0,8903 0,8926 0,8949
587
НОМОГРАММА ДЛЯ ПРИВЕДЕНИЯ ОБЪЕМА ГАЗА К 0° С И 780 мм рт. ст.
Атмосферное давление, мм рт. ст,
780
770
760
750
740
730
•720
710
700
1емперотура,°С
АО-,
30-
г 40
20„-
-30
W--
'-10
0,800
10
20
30
100
150
1,9000
050
40
60
70
-Не
" 80-- —
§
ДО-L'
0,900- L
ян1
30 -i
50-\
60 ’
70 \
200
250
300
350
400
450
& е-
£
8-
1,9500
550
600
650
700
750
800
850
900
950
90 -
1,000 -^-0,0000
О
g
20 -i
Этой номограммой удобно пользоваться для ускорения вычислений при массовых ана-лизах.
Для расчета по номограмме соединяют линейкой точки, соответствующие давлению и температуре, прн которых измерен объем газа. В точке пересечения линейки со шкалой, находящейся в правой части номограммы, отыскивают коэффициент пересчета F (или его логарифм), на который умножают измеренный объем.
Пример (указан на номограмме пунктиром). При ^давлении 730 ммрт. ст. и температуре 20°_С получают для сухого газа F«0,895 и Ig F** 1,9517; для влажного газа F=0,873 и Ig F= 1,9410.
588
СООТНОШЕНИЯ МЕЖДУ ЗНАЧЕНИЯМИ ДАВЛЕНИЯ, ВЫРАЖЕННЫМИ В РАЗЛИЧНЫХ ЕДИНИЦАХ
См. также «Справочник химика». 2-е изд., т. I, стр. 48.
мм вод. ст. мм рт.\ ст. | мм вод. ст. мм рт. ст. мм вод. ммрт. ст. мм eod.l ст. | ммрт.Цммвод.\мм рт.Лмм вод. 1мм рт.
ст. || ст. | ст. || ст. | ст.
1 0,07 18 1,32 | 35 2,57 52 3,82 1 69 5,08 85 6,25
2 0,15 19 1,40 36 2,65 53 3,90 70 5,15 86 6,33
3 0,22 20 1,47 37 2,72 54 3,97 71 5,22 87 6,40
4 0,29 21 1,54 38 2,79 55 4,05 72 5,30 88 6,47
5 0,37 22 1,62 39 2,87 56 4,12 73 5,37 89 6,55
6 0,44 23 1,69 40 2,94 57 4,19 74 5,44 90 6,62
7 0,52 24 1,77 41 3,02 58 4,27 75 5,52 91 6,69
8 0,59 25 1,84 42 3,09 59 4,34 76 5,59 92 6,77
9 0,66 26 1.91 43 3,16 60 4,41 77 5,66 93 6,84
10 0,74 27 1,99 44 3,24 61 4,49 78 5,74 94 6,91
11 28 2,05 45 3,31 62 4,56 79 5,81 95 6,99
12 0,88 29 2,13 46 3,38 63 4,63 80 5,88 96 7,05
13 0,96 30 2,21 47 3,46 64 4,71 81 5,96 97 7,13
14 1,03 31 2,28 48 3,53 65 4,78 82 6,03 98 7,21
15 1Д0 32 2,35 49 3,60 66 4,85 83 6,10 99 7,28
16 1Д8 33 2,43 50 3,68 67 4,93 84 6,18 100 7,36
17 1,25 34 2,50 51 3,75 68 5,00
54 х.ои ’ о,/и W o.w
ЗНАЧЕНИЯ КОЭФФИЦИЕНТА f ПРИ 0° С И 760 мм рт. ст.
В основу приведенных данных положены экспериментально найденные плотности соответствующих газов. ___________________________________________________
Анализируемый газ Определяемое вещество f 1g/ Анализируемый газ Определяемое вещество f 1 1g /
со, со. С 0,5391 Г,73169 NO n2o3 1,6974 0,22979
СОГ 2,6955 0,43064 NO NO n205 NO3 2,4120 2,7690 2,8143 0,38239 0,44238
со2 3,7879 0,57840 NO HNO3 0,44937
со2 4,4968 0,65290 NO NaNO3 3,7963 0,57936
с,н, с,н. СаС2 Н2О 2,8850 0,8109 0,46018 T,90897 NO NO NO KNO3 NaNO2 KNO2 4,5152 3,0818 3,8008 0,65468 0,48880 0,57987
и. А1 0,8015 1,90391 NO nh4no3 ** 3,5748 0,55325
н. Fe 2,4899 0,39614 O2 1,4289 0,15500
Н, H,S . n2 Zn H,S n2 2,9145 1,5393 1,2505 0,46456 0,18732 0,09709 o2 O2 o2*** H2O2 4* 0,7145 3,0379 1,85397 0,48257
n2 n2* 1,2818 0,10782 02 H2O2 5* 1,5189 0,18154
n2 n2 NH3 NH3 * 1,5200 1,5582 0,18184 0,19263 02 Na2O2 MnO2 *** 6,9650 3,8817 0,84294 0,58902
Na CO(NH2)2 2,6806 0,42824 o2 S1F4 KMnO4 •** 2,8230 0,45065
NO NO n2 NO 0,6256 1,79633 Fs 3,4280 0,53498
1,3402 0,12717 sif4 CaF2 7,0430 0,84774
• При азотометрическнх методах При реакции с Н2О2. с бромощелочными растворами. *’ Каталитическое разложение. • • При нитрометрическом методе. Обработка КМпО4. РАСЧЕТ РЕЗУЛЬТАТОВ ГАЗОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ УГЛЕРОДА Процентное содержание углерода в анализируемом веществе определяется по формуле: «с = Х£ где V- измеренный объем СО2 при указанном давлении, см3; f — пересчетный коэффициент (см выше)- а —навеска анализируемого вещества, г. ’при измерении объема СО2 не иад ртутью вносят соответствующую поправку иа давление пара затворной жидкости (стр. 594). Формулу для приведения атмосферного Д Б ^таблице приведены'значення коэффициента / прн различных температурах и давлениях.
Температура, Давление, мм рт. ст.
730 735 740 | 745 | 750 1 755 | 769 765 | 770 | 775
10 12 14 16 18 20 22 24 26 28 0,0500 0,0496 0,0493 0,0489 0,0486 0,0483 0,0479 0,0476 0,0473 0,0470 0,0503 0,0500 0,0496 0,0493 0,0489 0,0486 0,0482 0,0479 0,0476 0,0473 0,0507 0,0503 0,0499 0,0496 0,0493 0,0489 0,0486 0,0483 0,0479 0,0476 0,0510 0,0506 0,0503 0,0499 0,0496 0,0492 0,0489 0,0486 0,0483 0,0479 0,0513 0,0510 0,0506 0,0503 0,0499 0,0496 0,0493 0,0489 0,0486 0,0483 0,0517 0,0513 0,0510 0,0506 0,0503 0,0499 0,0496 0,0492 0,0489 0,0486 0,0521 0,0517 0,0513 0,0509 0,0506 0,0502 0,0499 0,0496 0,0492 0,0489 0,0524 0,0520 0,0516 0,0513 0,0509 0,0506 0,0502 0,0499 0,0496 0,0492 0,0527 0,0523 0.0520 0,0516 0,0513 0,0509 0,0506 0,0503 0,0499 0,0496 0,0530 0,0527 0,0523 0,0519 0,0516 0,0512 0,0509 0,0505 0,0502 0,0499
589
Избирательная осушка Осушка и очистка сложных газовых смесей, в которых определяются один или несколько компонентов, требует избирательных сорбентов. Так, для очистки от сероводорода газовой смеси, содержащей даже небольшие примеси двуокиси углерода или других кислых газов, не могут быть применены щелочные сорбенты (аскарит, ХПИ, щелочи). Фосфорный ангидрид неприменим для осушки галогеноводородов, с которыми в присутствии влаги взаимодействует
Сор
Анализируемый компонент Среда Удаляемый компонент наименование состав
Азот, водород, кислород, инертные газы Азот, воздух Пары воды Силикагель кем •
ОС Силикагель 1 ШСК, пропи- | тайный СаС12 j (25 вес. %) J
Хлорид кальция СаС12 плавленый
Ангидрон Mg (С1О4)2 безводный
Фосфорный ангидрид Р2О5
Аммиак Азот, воздух, нейтральные газы, предельные углеводороды То же Гидроокись калия кон
Г идроокись натрия NaOH
Двуокись и окись углерода, предельные и ароматические углеводороды Воздух, углеводороды » » ос Силикагель ШСК, пропитанный СаС12 (25 вес. %)
Хлорид кальция СаС12 плавленый
Ангидрон Mg(ClO4)2 безводный
590
и очистка газовых смесей
с образованием галогенокислородных соединений фосфора. Применение силикагеля ограничивается его высокой сорбционной способностью по отношению ко многим газам. Ангидрон частично поглощает непредельные углеводороды, вследствие чего не может быть использован в качестве осушителя в их присутствии. Кроме того, выбор сорбента в каждом отдельном случае зависит от требуемой степени осушки или очистки газовой смеси.
бе нт Максимальная Остаточное содержание удаляемого компонента, мг!л Сорбционная емкость, вес. % от массы сорбента
зернение, мм Температура очистки, °C объемная скорость, отнесенная к объему сорбента, ч1 Условия регенерации сорбента
1 2—5 20—30 40 60 43—59 Сл О) ООО 1 1 1 и- м W 17—19 6 Многократно регенерируется продувкой воздухом, осушенным ангидроном и Р2О5 при 180—200° С
2—3 20 10 1.10“‘ 49 То же
2—6 20—60 75—240 2-10~‘ .... Не регенерируется
2—3 20—30 65—160 5-10~4 20—60 То же
Порошок 20—35 2-10-s .... » »
Таблетки диаметром 5—7 мл .... 55—65 2-10~3 .... » »
То же .... 75—170 2 - 10-1 » »
2—3 20 10 1.10-' 49 Многократно регенерируется продувкой воздухом, осушенным ангидроном и Р2О5 при 180—200° С
2—6 20—60 75—240 2-10~‘ Не регенерируется
2—3 20—30 65—160 5- 10—4 20—60 То же
591
ИЗБИРАТЕЛЬНАЯ ОСУШКА
Анализируемый компонент Среда Удаляемый компонент Сор. 5
наименование состав '1
Непредельные углеводороды Воздух, нейтральные газы Пары воды ос Силикагель ШСК, про- i питанный Cad, (25 вес. %)
Хлорид кальция СаС12 плавленый
Нейтральные газы, двуокись углерода, углеводороды Воздух или любой из определяемых газов Аммиак Купрамит Глииа, пемза или активи- . рованный уголь, пропитанные CuSO4.
Азот, водород, предельные углеводороды Воздух Сероводород То же То же ‘
Воздух, водород, предельные углеводороды, окись углерода Любой из определяемых газов Двуокись углерода ХПИ Смесь СаО (96%) и NaOH(4%)i
Аскарит NaOH на асбесте
Водород, воздух, предельные и ароматические углеводороды, двуокись и окись углерода Азот, воздух Окислы азота (NO, NO2) И-ХПИ ХПИ, пропитанный КМпО4 (4 вес. %)
Двуокись углерода и другие кислые газы Азот, воздух, углеводороды Сернистый газ 1—2 % раствор бертолетовой соли КСЮ»
Водород, воздух, предельные и ароматические углеводороды, окись углерода Азот, воздух То же Окись кальция СаО гранулированный
592
и ОЧИСТКА ГАЗОВЫХ СМЕСЕЙ
Продолжения
бент Температура очистки, °C Максимальная объемная скорость, отнесенная к объему сорбента, ч~1 Остаточное содержание удаляемого компонента, мг[л Сорбционная емкость, вес. % от массы сорбента Условия регенерации сорбента
зернение, мм
2—3 20 10 1 • ю-1 49 Многократно регенерируется продувкой воздухом, осушен- ным ангидроном и Р2О5 при 180—200° С
2—6 20—60 75—240 2-10“' .... Не регенерируется
2—3 20—30 13—15 То же
2—3 20—30 • Обычными методами не улавливается 7,0 » »
Гранулы диаметром 1,5—5 мм 20—25 1,1 25—30 » >
До 20
20—40 120 4-Ю”6 ....
» »
4-8
38 Зак. 783
593
Затворные жидкости, применяемые в газовом анализе
В качестве затворных жидкостей в газовом анализе чаще всего применяют концентрированные растворы солей (NaCl, Na2SO< и др.). При работе с такими растворами следует учитывать давление паров воды над ними (см. ниже, а также «Справочник хи^ мика», 2-е изд., т. 111, стр. 345).
Погрешности анализа за счет растворимости газов в затворной жидкости н давления паров растворителя над ней могут быть исключены, если в качестве такой жидкости применять очищенную и перегнанную ртуть; давление паров ртути очень мало и некоторые газы (например, Н2, N2, О2) в ней нерастворимы (давление насыщенных паров ртути см. «Справочник химика», 2-е изд., т. 1, стр. 725).
В случае анализа сероводорода и других газов, реагирующих с ртутью, в качестве затворной жидкости применяют смазочные масла, предварительно насыщенные анализируемым газом (давление паров смазочных масел см. стр. 595).
ЗАТВОРНЫЕ ЖИДКОСТИ
Затворная жидкость Примечание
Вода Применяется при не очень точных анализах в отсутствие щелочных и кислых газов
Глицерин, 50% водный раствор Заметно растворяет СОг
Ртуть Неприменима в присутствии F2, CIZ, НВг, HCI и H2S
Серная кислота, 10% водный рас- Применяется в отсутствие NH3 и дру-
твор гих щелочных газов
Смазочные масла Применяются в качестве затворных жидкостей для H2S и SO2
Сульфат натрия, 20% водный рас- Применяется при температурах выше
твор с добавкой серной кислоты 16° С, так как при более низкой тем-
(4—5 объемн. %) пературе из раствора выкристаллизовывается Na2SO4- IOH2O
Тиосульфат натрия, 4% водный Применяется в отсутствие газов-окис-
раствор лителей
Хлорид натрия. 22% водный раствор Очень слабо растворяет СО2
ДАВЛЕНИЕ ПАРОВ ВОДЫ НАД НАСЫЩЕННЫМИ РАСТВОРАМИ ХЛОРИДА И СУЛЬФАТА НАТРИЯ
Раствор Температура, °C Давление паров, мм рт. ст. Температура, °C Давление паров, мм рт. ст. Температура, °C Давление паров, мм рт. ст.
NaCl 5 4,9 14 9,1 23 15,9
6 5,3 15 9,7 24 16,9
7 5,7 16 10,3 25 17,9
8 6,1 17 11,0 26 19,0
9 6,5 18 11,7 27 20,2
10 6,9 19 12,4 28 21,4
11 7,4 20 13,2 29 22,7
12 7,9 21 14,1 30 24,0
13 8,5 22 15,0
Na2SO4 16 11,6 24 18,9 32,4 30,8
18 12,9 26 21,4 35 36,0
20 14,7 28 23,8 39 44,6
22 16,7. 30 27,2
594
ДАВЛЕНИЕ ПАРОВ НЕКОТОРЫХ СМАЗОЧНЫХ МАСЕЛ
Наименование масла Состав Давление пара при 20° С, мм рт. ст.
Д-1А Смесь углеводородов 2 10-9—4 • 10~8
Д-1Б То же 2-10 9—4-10 8
Г » » 1 • 10~6—5- 1(Г5
ВМ-4 » » 1 -10-6—4 • 10-5
Бутилфталат С6Н4(СООС4Н9)2 — 1 -10-5
ВКЖ-94А Смесь этилполисилоксанов Не более 5-10 8
ВКЖ-94Б То же 5 -10~8—1 • 10-6
ПФМС-2 Смесь метилфенилполи-силоксанов 5.Ю'9—7- 10“7
РАСТВОРИМОСТЬ ГАЗОВ В КОНЦЕНТРИРОВАННЫХ РАСТВОРАХ ХЛОРИДА НАТРИЯ
а — коэффициент абсорбции Бунзена, т. е. объем газа (приведенный к 0° С й 760 мм рт. ст.), поглощаемый единицей объема жидкости при парциальном давлении газа, равном 760 мм рт. ст.
Газ Концентрация NaCl, вес. % Значения а при температуре
5° С 10° с 15° с 20° С 25° С 30° С
Азот . 11,90 0,010 0,0092 0,0081 0,0066 0,0048
Ацетилен 26,42 0,320
Водород 6,10 0,0184 6,0175 0,0164 0,0153 0,0138
15,80 0,00699
23,84 0,00595
Двуокись серы .... 15,80 28,79
Двуокись углерода . . 15,70 1,399 1,205 1,043 0,915 0,816 6,727
18,70 0,577 0,503 0,442 0,393 0,352 0,319
Закись азота 25,25 0,172
Кислород 26,4 0,0059 0,0056 0,0054 0,0052 0,0050 0,0048
Сероводород 15,8 1,753 1,354 1,138
Хлор . 26,4 6,44 0,40 0,36 0,34 6,30 0,28
РАСТВОРИМОСТЬ ГАЗОВ В ВОДНОМ РАСТВОРЕ СУЛЬФАТА НАТРИЯ ПРИ 25°С
Состав раствора: 200 г безводного Na2SO4 + 800 г дистиллированной воды 4- 40 мл 96% H2SO4.
а — коэффициент абсорбции Бунзена (см. выше); а2з — объем газа (приведенный к 25° С и 760 мм рт. ст.), поглощаемый единицей объема жидкости при парциальном давлении газа, равном 760 мм рт. ст.
Г аз а «25 Газ а «25
Азот . 0,0045 0,0049 Кислород 0,0081 0,0089
Ацетилен 0,324 0,343 Метан 0,0085 0,0093
Водород 0,0067 0,0073 Окись углерода .... 0,0036 0,0039
Двуокись серы .... 12,5 13,6 Этан 0,0099 0,0108
Двуокись углерода . . 0,247 0,270 Этилен 0,022 0,024
Закись азота 0,146 0,159
38*
595
РАСТВОРИМОСТЬ ДВУОКИСИ УГЛЕРОДА В НЕКОТОРЫХ ЗАТВОРНЫХ ЖИДКОСТЯХ ПРИ 25° С
025—объем газа (приведенный к 25° С и 760 мм рт. ст.), поглощаемый единицей объема жидкости прн парциальном давлении газа, равном 760 мм рт. ст.
Затворная жидкость
Вода ..........................................................
Глицерин, 50% водный раствор...................................
Сульфат натрия, 20% водный раствор с добавкой серной кислоты
(4—5 объемн. %).............................................
Тиосульфат натрия, 4% водный раствор...........................
Хлорид натрия, 18,7% водный раствор............................
°25
0,759 0,540
0,270 0,125 0,352
Поглотительные растворы ПОГЛОТИТЕЛИ для АБСОРБЦИОННОГО АНАЛИЗА ГАЗОВ
Абсорбционная способность поглотителей по отношению к газам указана на стр. 597.
Определяемый газ Поглотитель Приготовление поглотительного раствора
Ацетилен и углеводороды ряда ацетилена Двуокись углерода, хлористый водород, хлор, сероводород, двуокись серы и другие кислые газы Кислород Тетраиодомеркуроат калия Хлорид меди в аммиачной среде Гидроокись калия Гидроокись калия или натрия Пирогаллол Триацетилоксигидрохинон Гидросульфит натрия Аммиакат меди Белый фосфор 25 г HgJ2 и 30 г KJ растворяют в 100 мл воды; перед применением реактив подщелачивают КОН 32 г Си2С12 растворяют в НО мл 25% водного раствора NH4C1 и добавляют 80— 100 ж л 25 % раствора NH3 30—35% водный раствор КОН Сухой поглотитель в палочках или гранулах 56 г пирогаллола растворяют в 100 мл воды и добавляют 260 мл 33% водного раствора КОН 40 г триацетилоксигидрохинона растворяют в 200 мл 38% водного раствора КОН Смешивают свежеприготовленные растворы: 1) 50 г Na2S2O4 в 250 мл воды и 2) 30 г NaOH в 40 мл воды Медиую проволоку погружают в смесь равных объемов конц. раствора NH3 и насыщенного водного раствора NH4C1 Сухой поглотитель в палочках
596
ПОГЛОТИТЕЛИ ДЛЯ АБСОРБЦИОННОГО АНАЛИЗА ГАЗОВ
Продолжение-
Определяемый газ Поглотитель Приготовление поглотительного раствора
Мышьяковистый водород Ацетат кадмия 80 г ацетата кадмия растворяют в 100 мл воды и добавляют несколько капель ледяной уксусной кислоты
Окись углерода Сульфат меди (I) с Р-нафтолом Хлорид меди в аммиачной среде К взвеси 20 г Си2О в 200 мл коиц. H2SO4 и 25 мл воды прибавляют 25 г Р-нафтола 32 г CU2CI2 растворяют в 110 мл 25% водного раствора NH4CI и добавляют 80—100 мл 25% раствора NH3
Сероводород Гидроокись калия Ацетат кадмия 30—35% водный раствор КОН 80 г ацетата кадмия растворяют в 100 мл воды и добавляют несколько капель ледяной уксусной кислоты
Фосфористый водород Селенистая кислота 80 г H2SeOs растворяют в 100 мл воды
Этилен Бромная вода Сульфоваиадиевый реактив 20% водный раствор КВг, насыщенный Вг2 1 г V2Os растворяют при нагревании в 100 г коиц. H2SO4
Этиленовые углеводо- Серная кислота 84% раствор H2SO4
роды ОТ Сз Бромная вода 20% водный раствор КВг, насыщенный Вг2
АБСОРБЦИОННАЯ СПОСОБНОСТЬ НЕКОТОРЫХ ПОГЛОТИТЕЛЬНЫХ РАСТВОРОВ ПО ОТНОШЕНИЮ К ГАЗАМ
В таблице указано число миллилитров газа, абсорбируемого 1 мл раствора. Состав поглотительных растворов см. выше.
Поглотитель
Ацетат кадмия . . . . Гидроокись калия . . Гидросульфит натрия . Пирогаллол ...........
Селенистая кислота . . Сульфат меди (I) с
0-иафтолом..........
Сульфоваиадиевый реактив ..............
Тетраиодомеркуроат калия ..................
Триацетилоксигидрохинон .....
Хлорид меди (I)' в аммиачной среде
597
Методы анализа газов и паров
лабораторные методы анализа
66S
Для спектральных методов анализа вместо воспроизводимости приводятся значения средней квадратичной погрешности.
Газ или пар Макроконцентрации Мнкроконцентрации
название формула метод интервал определяемых концентраций объемн. % воспроизводимость отн. % метод интервал определяемых концентраций, мг[л воспроизводимость, отн. %
Азот n2 Адсорбционный 0,01—1,3 2—10 Спектральный 0,12—3
Спектральный 0,Ь—25 4,5 Объемный 0,2—6 3—6
Аммиак NH3 Манометрический 0,5—100 0,5—8
То же 0,6—10 <6 Кондуктометрический 0,02—0,2 <2
Анилин c6h5nh2 Кондуктометрический Титрометрический Линейно-колористический * Колориметрический 0,002—0,2 0,002—0,02 10 >5
То же 0,001—0,02 <10
Линейно-колористиче- 0,003—0,01 <3
Аргон ский *
Ar Объемный 0,2—7 3—10 Спектральный 0,08—1,7
Спектральный 1,5—10 6
Ацетилен сн=сн Объемный 1—2 . . . . Колориметрический 0,005—0,05 2—3
Ацетон Cl IgCOC I Ig То же 0,005—0,5 . . .
Бензин Адсорбционно-весовой 0,5—1 Нефелометрический 0,001—0,01
. . . . . . < 1 Линейно-колористи- 0,5—30 - - .
0,5—1 ческий *
Бензол СбН6 Титрометрический . . . . Колориметрический 0,1—2,0
Адсорбционно-весовой 0,5—1,5 2—3 Адсорбционно-весовой 2—20 <2
Интерферометриче- . - . . Линейно-колористи- 0,2—2 >10
ский ческий *
Объемный 1—100 Колориметрический 0,002—0,04
Водород H2 2—3 Спектральный 0,0008—0,08 30
Абсорбционный 0,1—10 < 1
Г ел ин He Спектральный 0,05—2 7,5
То же 0.1—12 10 То же 0,07—0,9 7—10
Адсорбционно-мано- . . . .
Гидразин NH2—NHg метрический
V— -> . -4. —— aw— - Колориметрический 0,0002—0,002 *TWW.
Двуокись серы SO2 Титрометрический <0,2 То же 0,002—0,02 0,02—0,2 1,2—6
Абсорбционный .... Линейно-колористический *
Двуокись угле- co2 Йодометрический .... Кондуктометрический 0,001—7,0 5
рода Титром етр ический 0,7—5 1,0
Спектральный 0,5—30 6,0
Объемный 1—100 2—3 Абсорбционно-объемный Колориметрический 10
Дивинил СН2= =CH—CH=CH2 Абсорбционно-объемный .... 0,01—1 0,05—0,5
Диметиламин Закись азота (CH3)2NH n2o Объемный 1—5 1,4—3,2 То же » » 0,002—0,01 0,05—5,5 20
Иод J2 Адсорбционный 0,05—0,5 3—7 » » 0,001—0,01 >10
Керосин Кислород O2 Титрометрический Объемный 0,1—1 1—100 ’ 1—2 ’ Эмульсионный Колориметрический 0,05—0,5 0,001—0,15 10 3—10
Абсорбционно-объем- 10—35 < 1 Полярографический 0,05—5,0 1
Ксилидины CeH3(CH3)2NH, ный Спектральный 0,05—3 .... Колориметрический 0,0003—0,003 >10
Метан CH4 Объемный 0,1—16 < i Спектральный 0,015—1,5 12
То же 1—100 <з Кондуктометрический 0,005—3,0 5
Мышьякови- AsH3 Колориметрический 0,0005—0,02 5—10
стый водород Нафталин Озон CI0H8 O3 То же » » » » 0,001—0,01 0,0003—0,003 0,00005—0,0005 >10 >10 <4
Титрометрический 0,001—0,01 . . .
Окислы азота NO, NO2, n2o4, n2o5 Колориметрический 0—30 Колориметрический 0,01—0,08 < 10
Манометрический 0,1—4 0,5—3 Линейно-колористиче- 0,01—0,2 >12
NO Титрометрический 1—100 Титрометрический 0,005—0,05
Окись углерода CO Объемный 1—100 2—3 Кондуктометрический 0,061—7,0 -% о
Титрометрический 0,5—2 < 1 Титрометрический 0,003
Окись этилена (CH2)2 0 Спектральный Титрометрический 0,01—1 0—100 .... Колориметрический То же 0,006—0,04 0,02—0,2 ЛА
Титрометрический 0,05—0,5 . . 1
лабораторные методы ж анализа газов и паров
ЛАБОРАТОРНЫЕ МЕТОДЫ
АНАЛИЗА ГАЗОВ И ПАРОВ
-чз * воспроизводимость, отн. % 1 2—9 о тГ АА« • • L—S Ю-О —’ — пэо V/AAA 00 ю ю ДА А • QO А 2—10
•<о с <2 а « о. 0) интервал определяемых концен- гЗ* * X** X X X I 0,0025—0,1 0,005—3 0.00005—0.001 0,0001—0,01 0,001—0,01 • 0,01—0,36 с с 1 1 с 0,001—0,01 0,01—0,15 0,01—0,1 0,002—0,02 0,02—0,28 0,00035—0,0042 0,0003—0,005 0,003—0,05 0,01—0,15 0,01—0,06 0,0001—0,05 (Г ё с с г •
X о х о л X S метод | »Я 2 Я a я & 2 я у ктом етр ически й лометрический риметрический :е рбционный йно-колористи-кий * »х 3 * 4 5 S £ S S А лометрический риметрический йно-колористиче- й * риметрический се лометрический » 4» X1 Я S а 3 Я э Е Я й * лометрический йно-колористиче- й * уктометрический
о о я о X £ с X . о я о о о < о я Я о я с Е с * S о Н" Л % О <1) о> о Я ски Коло, То и Нефе Лине ски Нефе Лине! ски Конд:
воспроизводимость, £ с 3 7 СЧ СМ • 1 0,5—1 । ю сч W
X 9 о- интервал определяемых кон- В £ h - cu tfl S’g 0,5—25 1—10 0—10 со 4 о" 0,5—10 >3 о о
5 а X о х о л х »я Я я »я =я я • • КИЙ объем- »я я я >-объем- »я я я
S метод Объемный CU я Я & 2 о о. н я н Абсорбционны & Я & 2 О Я Н • • . О О я я . я х Q, О • S ф) у О CMS • о. о з н о Я • а Ю 1 Ь< 4> 3" Я 6 2 О Q. Н я Н I I с я я с с \с < иый 4> а я а S 1
Газ или пар формула и . ~ Z „ о Е( от О от— - U й . ао X г, 'иОч- «j* - и нх х £ У- го£ ьи £ J z ои
название 5 и as 4 г о 3 5 х 5= °я§- § So = 2 2 ч g" л a Sg5o3“ о * не- сс сх о q ^=нее ех
О X
Z о
Метод индикаторных трубок.
600
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ (КРАТКАЯ ХАРАКТЕРИСТИКА НЕКОТОРЫХ МЕТОДОВ И АППАРАТУРЫ)
Анализ по поглощению инфракрасной радиации (ИК-газоаиализаторы)
Принципиальные основы
Анализ основан на индивидуальном характере инфракрасных спектров по* глстения газов с гетероатомными молекулами (например, СО, HCN и т. п.). Мерой концентрации контролируемого компонента газовой смеси служит поглощаемая им мощность вспомогательного потока инфракрасной радиации надлежащего спектрального состава. Поглощенная (или оставшаяся после поглощения) мощность радиации преобразуется в лучеприемиике в теплоту замкнутого объема газа. При этом повышается температура газа. Последняя прямо (например, с помощью термоэлектрического приемника) или косвенно (например, с помощью оптико-акустического приемника, в котором повышение, давления газа, пропорциональное повышению температуры, воспринимается конденсаторным микрофоном) преобразуется в пропорциональный поглощенной мощности электрический сигнал. Этот сигнал измеряется прибором, градуированным в единицах концентрации контролируемого компонента газовой смеси.
Применение
ИК-газоаиализатор применяется для анализа сложных смесей. Метод в принципе избирательный, однако на практике возникают трудности при наличии существенного перекрытия спектров поглощения контролируемого и неконтролируемых компонентов смеси. Таким газоанализатором нельзя контролировать газы с одноатомными (например, Не) и гомеоатомными (например, На) молекулами. Повышение чувствительности может быть достигнуто увеличением толщины слоя газа, поглощающего радиацию, и сжатием газовой смеси (до 100—150 ат).
ИК-газоаиализаторы различных типов серийно выпускаются в СССР. Малая инерционность делает их пригодными для применения в системах автоматического управления технологическими процессами. При эксплуатации необходимо не реже одного раза в неделю проверять нулевое показание. ИК-газоана-лизаторы, в лучеприемниках которых используется оптико-акустический эффект Тиндаля—Рентгена, именуются нередко оптико-акустическими.
Технические характеристики
Пределы измеряемых концентраций. Минимальные значения пределов измерений составляют для СОа от 0 до 5 • 10-3 объемн. % (в специальных случаях до 1 • 10-4 объемн.%), для СО — от 0 до 1 • 10*2 объемн.% (и менее)', для паров жидких углеводородов — от 0 до 1 г/м3. Максимальные значения пределов измерений для газов—от 0 до 100% н для паров—от нуля до насыщения.
Погрешности. Основная приведенная погрешность от ±2 до ±3отн.% для пределов измерения не менее 0—1 объемн.% и от ±5 до ±10 отн.% для меньших пределов. Изменение температуры газа на ±10 град вызывает дополнительную приведенную погрешность от ±1 до ±5 отн.%, а изменение давления газа на ±10 мм рт.ст. — погрешность от ±0,5 до ±1,5 отн.%. Колебания напряжения и частоты питающей электросети также влияют на показания,
Порог чувствительности составляет 1—3% от диапазона шкалы, Постоянная времени: 30—40 сек и менее (до нескольких секунд).
Ионизационные методы анализа (ИН-газоанализаторы)
Принципиальные основы
Методы основаны на индивидуальном характере степени ионизации различ» ных газов и паров, возникающей под воздействием какого-либо ионизатора (при всех прочих равных условиях). Поэтому сила ионизационного тока, возникающего в ионизованной газовой смеси при наложении на нее электрического поля, зависит от концентрации компонентов, составляющих смесь. Зависимость эта
601
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
•определяется многими факторами, из числа которых для ИН-газоанализато-ров используются, в основном, следующие три *:
I. Неодинаковое поперечное сечение ионизации различных по своей химической природе молекул и атомов. Этот фактор лежит в основе метода анализа газов по образованию ионных пар (метод поперечных сечений ионизации).
II, Различное сродство к свободным электронам молекул некоторых газов (например, Ог, СО и др.) и некоторых твердых аэрозолей, образуемых посредством вспомогательных химических реакций из газов, не обладающих в заметной степени таким сродством. На этом свойстве основан анализ газов по способу захвата электронов (метод удаления электронов и ионов из газа введением в него примеси).
III. Неодинаковая интенсивность термической ионизации различных продуктов горения, используемая в пламенно-ионизационном методе анализа (ионизация по методам I и II осуществляется с помощью альфа- и бета-излучателей).
В любом случае измерение концентрации контролируемого компонента осуществляется измерением ионизационного тока (от 10~и до Ю-8 а перед усилением) приборами, градуированными в единицах концентрации соответствующего газа или пара или суммы нескольких компонентов (последнее — при измерении по методу III).
Применение
Метод неизбирательный, поэтому применим для контроля концентраций отдельных компонентов только бинарных или квазибинарных ** смесей. Применяется также (по варианту III) для определения концентраций суммы нескольких компонентов смеси, сходных по химической природе и физическим свойствам, например паров углеводородов. Метод пригоден для очень многих неорганических паров и газов, особенно в диапазонах субмикро-, микро- и малых концентраций.
ПН-газоанализаторы в СССР серийно не выпускаются. В зарубежной практике они находят применение для автоматической сигнализации о достижении заданной концентрации и в системах автоматического управления.
Технические характеристики
Пределы измеряемых концентраций. Минимальные пределы измерения в зависимости от вида пара или газа составляют от 0 до 5 • 10“6— 5-Ю"4 объемн.%, максимальные — от 0 до 1 объемн.%, в редких случаях — до десятков объемных процентов.
Воспроизводимость показаний равна примерно ±1,0 отн.%.
Порог чувствительности составляет ~ 1 • 10~7 объемн.%.
Время срабатывания — менее 15 сек.
Магнитные методы анализа (МН-газоанализаторы)
Принципиальные основы
Методы основаны на индивидуальных различиях в магнитных свойствах отдельных газов и паров. Большинство газов и паров диамагнитно. Парамагнитными свойствами обладает кислород, а также (но в гораздо меньшей степени) окислы азота и еще некоторые газы. При построении приборов для определения содержания существенно парамагнитных компонентов газовой смеси (практически это всегда кислород) используется по преимуществу одно из трех явлений:
I. Зависимость интенсивности конвекционных потоков («магнитного ветра» или термомагнитной конвекции), возникающих в газовой смеси при наложении
* Для ионизационных детекторов газовой хроматографии, помимо указанных факторов, используется ряд других явлений, связанных с ионизацией газов.
** Квазибинарными называются смеси с числом компонентов три и более, при условии, что используемое для анализа свойство контролируемого компонента резко отличается от свойств всех остальных компонентов.
•602
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
на ее объем определенным образом взаимно ориентированных магнитного и температурного полей, от содержания парамагнитного компонента в смеси (термомагнитный метод).
II. Зависимость скорости истечения газовой смеси из отверстия, помещенного в неравномерное магнитное поле, от содержания в этой смеси парамагнитного компонента (магнитомеханический эффузионный метод).
111. Зависимость механических усилий, действующих иа подвижное тело (ротор) в неоднородном магнитном поле, от концентрации парамагнитного компонента в газовой смеси, окружающей это тело (магнитомеханический роторный метод).
Измеряемый сигнал преобразуется перед измерением в электрическую форму в приборах I и II типа — всегда, а в приборах III типа — большей частью.
Применение
Значительный парамагнетизм кислорода, резко выделяющий его среди других газов и паров, делает магнитный метод селективным для кислорода, для определения которого он практически только и применяется.
MH-газоанализаторы различных типов, работающие на основе методов I и II, серийно выпускаются в СССР. Для сложных смесей переменного состава наиболее пригодны приборы, основанные на методах II и III, менее зависимые от переменного состава неизмеряемых компонентов. Для систем автоматического управления применяются наименее инерционные приборы 1 типа.
Технические характеристики
Пределы измеряемых концентраций для кислорода по методу I составляют минимально 0—0,5, чаще 0—1,0 объемн.%. При безнулевых шкалах минимальный диапазон равен 1,0 объемн.% (например, 20—21 объ-емв.%); при концентрациях свыше 60—70 объемн.% он равен 2,0 объемн.% (например, 98—100 объемн.%). Минимальный предел концентрации при измерениях по методу II составляет 0—5 объемн.%, по методу III — от 0 до 0,1 объемн.%. Максимальные пределы измерения концентраций для всех методов — от 0 до 100 объемн.%.
Погрешности. Основная приведенная погрешность измерения по методу I составляет ±10 отн.% для концентраций кислорода 0—0,5 и 0—1,0 объемн.%, ±5 отн.% для концентраций 0—2 и 98—100 объемн.% и от ±2,5 до ±2,0 отн.% для больших диапазонов измерения. При измерениях по методу II погрешность равна ±5 отн.%, по методу III — от 0,5 до 1,0 отн.%. Колебания напряжения, частоты питания, давления газа, температуры и состава неизме-рясмых компонентов вызывают дополнительные погрешности. Поэтому названные факторы стабилизируют или их влияние искусственно корректируют.
Запаздывание показаний для метода I равно 30—50 сек, для методов II и III — от 1,0 до 1,5 мин.
Масс-спектральные методы анализа (МС-газоанализаторы)
Принципиальные основы
Анализ основан на' строго определенном значении массы атома, молекулы или иона данного вещества определенного изотопного состава. Масс-спектраль-ный анализ веществ, в частности газов и паров, сводится, во-первых, к временному и пространственному разделению на группы различных по массе ионов, содержащихся в пробе вещества (электрически нейтральные атомы и молекулы предварительно подвергаются ионизации), посредством воздействия электромагнитного поля в высоком вакууме (до 10 7 мм рт. ст.), где взаимовлияние частиц сводится к минимуму, и, во-вторых, к измерению ионного тока, образуемого суммарным зарядом частиц одинаковой массы и характеризующего их относительное содержание (концентрацию) в пробе. В результате последовательного изменения значения электромагншных сил измерению подвергаются поочередно ионные токи (10'14—10 s а), соо|ветствующие группам
603
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
частиц с различными дискретными значениями массы (точнее — значениями отношения массы к заряду). Запись усиленных токов с разверткой по времени образует спектр масс анализируемой пробы. Последующая графическая и аналитическая обработка спектра масс позволяет провести полный качественный и количественный анализ молекулярного (химического) состава пробы, а также анализ ее изотопного состава.
Масс-спектрометры по своему устройству могут быть разделены на статические и динамические. В статических приборах используются медленно изменяемые (для осуществления развертки по массам) постоянные магнитные и электрические поля, образующие ионно-оптическую систему, управляющую движением в приборе пучков ионизированных частиц. В динамических приборах используются высокочастотные электрические и, иногда, вспомогательные постоянные магнитные поля. Статические масс-спектрометры более универсальны, они обладают большой разрешающей способностью и чувствительностью. Динамические приборы меньше по весу и габаритам и обладают высоким быстродействием; они удобны для анализа сред быстро изменяющегося состава, лапример, при процессах горения.
Применение
Масс-спектрометры, предназначенные в основном для анализа газов, представляют собой специализированные конструкции, обеспечивающие стабильность газового потока через прибор во время измерений, стабильность температуры системы напуска газа и источников ионов, минимальное остаточное давление в приборе и др. МС-газоанализаторы пригодны для анализа любых газовых смесей, вплоть до самых сложных, содержащих как легкие, так и -тяжелые газы, для анализа ионных атмосфер, состава сильно разреженных газовых смесей и т. д. В ряде случаев масс-спектрометры целесообразно сочетаются с газовыми хроматографами, в которых происходит предварительное разделение компонентов, с инфракрасными спектрометрами и т. п.
В СССР выпускается около 10 различных типов масс-спектрометров для газового анализа, в том числе одни автоматический для непрерывной работы в производственном потоке (остальные предназначены для анализов в лабораториях) .
Технические характеристики
Приводим основные характеристики лабораторного МС-газоанализатора с ручным управлением МХ1304, предназначенного для снятия масс-спектров при исследовательских работах, и автоматического регулирующего прибора MX 1201, предназначенного для управления производственным процессом по отношению суммы содержания двух компонентов к содержанию третьего (всего контролируется 8 компонентов):
Тип масс-спектрометра
МХ1304 МХ1201
Диапазон измерения по массовым числам 1—150 12—100
Разрешающая способность .............. 150 45
Чувствительность по аргону, объемы. % . . 1-10 4 1-10 2
Относительная погрешность определения компонентов, отн. %................... ±2 ±2*
* Прн измерении компонентов, сорбирующихся стенками приборов, погрешность возрастает до ±8 отн. %.
Объемные и манометрические методы анализа (ОМ-газоанализаторы)
Принципиальные основы
Анализ основан на изменении объема (или давления) пробы газовой смеси при постоянном давлении (или объеме) и постоянной температуре, происходящем в результате химического (реже — физического) воздействия на пробу. Это воздействие избирательно по отношению к контролируемому компоненту пробы (или к сумме нескольких компонентов) и приводит к удалению его (или их) из пробы или к переводу в другое соединение с иным молярным
€04
автоматический анализ газов
объемом. Удаление (перевод) осуществляется: 1) поглощением жидким (реже— твердым) реагентом, 2) сжиганием (иногда с последующей конденсацией продуктов горения), 3) комбинированным поглощением и сжиганием. Отношение уменьшенного объема пробы (в случае более распространенных объемных приборов) к первоначальному равно концентрации в газовой смеси соответствующего компонента. Анализ ведется циклически. При наличии в приборе нескольких устройств для раздельной избирательной обработки нескольких компонентов смеси возможно определение концентраций нескольких компонентов. Объемные приборы выпускаются в ручном и автоматическом исполнении, манометрические приборы бывают главным образом ручного действия и служат для периодических измерений.
Вариантом объемного метода газового анализа, особенно пригодным для инертных газов, является метод «остаточного газа», при котором контролируемый компонент поглощается реагентом, а неопределяемые компоненты образуют остаточную газовую фазу. Объем или расход последней является мерой определяемой концентрации. Расход остаточной газовой фазы измеряется в случае стабилизации всех влияющих факторов, при этом метод анализа из циклического превращается в непрерывный.
Применение
ОМ-газоанализаторы применимы для любых газов в любых смесях, если только может быть найден достаточно избирательный в условиях этой смеси способ удаления (либо конверсии) контролируемого компонента или, напротив, всех неопределяемых компонентов. При использовании автоматических объемных приборов метод ограничивается: 1) цикличностью анализов, что при частоте от 6 до 40 анализов в час исключает применение этих приборов для анализа быстро меняющихся по составу сред и для автоматического управления технологическими процессами, 2) невозможностью при обычных способах измерения объемов газа в автоматических приборах иметь шкалу с диапазоном менее 0—1 объемн.% (к лабораторным объемным приборам это не относится)', 3) наличием в приборе жидкостей, что исключает эксплуатацию его при наклонах, тряске и вибрации.
Возможно взрывобезопасное исполнение ОМ-газоанализаторов.
ОМ-газоанализаторы автоматического действия являются старейшими приборами подобного назначения. До недавнего времени они выпускались в СССР серийно под названием «химических автоматических газоанализаторов». Сейчас они вытеснены газоанализаторами других систем. За рубежом, в основном в ФРГ, их выпуск продолжается и в настоящее время. Манометрические приборы эпизодического действия изготовляются в Советском Союзе.
Технические характеристики
Пределы измеряемых концентраций у объемных автоматических приборов составляют от 0—5 объемн.% (в отдельных случаях 0—1 объ-емн. %) и до 0—100 объемн. %; диапазон безнулевых шкал не менее 5—10 объемн. %. Манометрические приборы эпизодического действия выполняются и для микроконцентраций (с накоплением пробы), например для определения от 10~3 до 10~7 объемн.% суммы N2+O2 в Н2.
Погрешность составляет ±2—3 отн.% для приборов, работающих в широких пределах концентраций, и до ±10 отн.%—для приборов, работающих в узких пределах концентраций.
Спектрофотометрический метод анализа (СФ-газоанализаторы)
Принципиальные основы
Метод основан на индивидуальном характере спектров излучения (линейчатых и полосатых) различных газов и паров. Интенсивность линий или полос спектра является мерой концентрации соответствующего газа или пара в смеси. В анализируемой смеси, находящейся при пониженном давлении, возбуждается высокочастотный электрический разряд, обусловливающий свечение
605
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
газа. Нужный участок спектра свечения выделяется с помощью светофильтра и воспринимается фотоэлектрической схемой, измеряющей интенсивность свечения. Выходной электроизмерительный прибор схемы градуируется эмпирически в единицах концентрации контролируемого газа.
Применение
Взаимное перекрытие спектров излучения многих газов и паров и затруднительность технического осуществления СФ-газоанализаторов, работающих иа единичной спектральной линии или полосе, является причиной того, что практически спектрофотометрический метод анализа газов является неизбирательным или малоизбирательным. Поэтому его применение целесообразно только в случаях бинарных газовых смесей, и притом таких, для которых другие методы использовать затруднительно или невозможно. К подобным случаям относится определение малого содержания (но не микросодержания) одних инертных газов в других (например, примеси азота в аргоне, гелии и др.).
Автоматические СФ-газоанализаторы серийно выпускаются в Советском Союзе для контроля в потоке чистоты аргона и гелия (от примеси азота) под давлением 150 ат.
Технические характеристики
Пределы измеряемых концентраций составляют 0—0,1; 0—0,5; 0—1 объемн.% и больше (до 0—15 объемн.%).
Погрешности. Основная приведенная погрешность составляет ±10 отн.%; воспроизводимость показаний равна ±5 отн.%.
Запаздывание показаний (время установления показаний в пределах основной погрешности) составляет 1—2 мин.
Анализ по теплопроводности (термокондуктометрические, ТП-газоанализаторы)
Принцшшальные основы
Анализ основан на индивидуальных значениях теплопроводности различных газов и паров. Теплопроводность смеси газов и паров является функцией теплопроводности и концентрации каждого из компонентов смеси. Поэтому термокондуктометрический метод газового анализа неизбирателен. Как правило, функция, связывающая теплопроводность и состав смеси, нелинейна даже для бинарных смесей и не подчиняется правилу аддитивности; в ряде случаев она еще и неоднозначна. Поэтому ТП-газоанализаторы градуируются эмпирически. Измерение теплопроводности осуществляется путем определения теплоотдачи проволоки, нагреваемой электрическим током и помещенной в контролируемую смесь газов и паров. О перепаде температуры проволоки судят по изменению электрического сопротивления последней. Выходной электроизмерительный прибор схемы измерения сопротивления градуируется в единицах концентрации соответствующего компонента газовой смеси.
Применение
Неизбирательность метода обусловливает его пригодность только для бинарных или квазибинарных смесей (т. е. смесей с практически постоянным соотношением концентраций неизмеряемых компонентов). В последнем случае, чтобы уменьшить влияние колебания состава неизмеряемых компонентов, применяют дифференциальный метод измерения, при котором теплопроводность анализируемой смеси сравнивают с теплопроводностью этой же смеси, но после удаления из нее контролируемого компонента. Метод пригоден для любой пары илн квазипары газов и паров с существенно различными значениями теплопроводности в диапазоне измеряемых концентраций. Чувствительность ТП-га-зоанализаторов в обычном исполнении позволяет применять их для диапазонов концентраций не менее 0,5 объемн.%; для меньших диапазонов необходимы специальные приборы с повышенной чувствительностью. Для контроля концентраций газовых смесей быстро изменяющегося состава обычные ТП-газоанализаторы непригодны, так как запаздывание их показаний (с точностью до основной погрешности) может достигать 2 мин. Достоинством ТП-газоанализаторов
606
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
является их высокая надежность, относительная простота и дешевизна при удовлетворительной точности.
ТП-газоанализаторы принадлежат к старейшим и наиболее распространенным в практике автоматическим газоанализаторам. В Советском Союзе они выпускаются серийно, в различном конструктивном исполнении.
Технические характеристики
Пределы измеряемых концентраций. Минимальные пределы измерения составляют от 0—0,5 объемн.% До 0—5 объемн.% в зависимости от вида газа (специальные конструкции приборов позволяют уменьшить минимальные пределы), максимальные — от 0 до 100 объемн.%; безнулевые шкалы возможны при минимальном диапазоне 1—3 объемн.% в зависимости от вида газа.
Погрешности. Основная приведенная погрешность составляет от ±1,5 до ±5,0 отн.% в зависимости от пределов измерений и вида газа; дополнительная температурная приведенная погрешность может достигать ±2—3 отн.% иа каждые 10 град изменения температуры газоанализатора (за пределами рабочего температурного интервала). Эта погрешность сводится к минимуму схемами температурной коррекции или термостатированием. Остальные влияюшие факторы (ток, давление и расход газа и т. д.) искусственно стабилизируются.
Порог чувствительности составляет не менее 1—2 отн.% от диапазона измерений.
Запаздывание показаний в пределах основной погрешности составляет от 10—15 сек до 2 мин.
Термохимические методы анализа (ТХ-газоанализаторы)
Принципиальные основы
Методы основаны на индивидуальных значениях теплового эффекта любой определенной химической реакции. При постоянных условиях реакции некоторому значению ее теплового эффекта отвечает соответствующее изменение температуры (термодинамический эффект). Если одним из взаимодействующих веществ является компонент газовой или паровой смеси, то термометрический эффект выбранной реакции может служить мерой концентрации контролируемого компонента.
По типу реакции ТХ-газоанализаторы разделяются на две группы: каталитические газовые, в которых реакция (чаще всего реакция горения) проводится в газовой фазе, обычно на твердом катализаторе, и термос ор б ц и о н-ные жидкостные, в которых анализируемая газовая смесь реагирует с известным жидким реагентом (в этом случае суммарные тепловой и термометрический эффекты определяются не только теплотой реакции в жидкой фазе, но и теплотой растворения в реагенте соответствующих компонентов газовой смеси). В обоих случаях с помощью термоэлектрических батарей или электрических термометров сопротивления измеряется происходящее в результате реакции повышение температуры газовой смеси (в каталитических ТХ-газоана-лизаторах) или жидкого реагента (в термосорбционных ТХ-газоанализаторах).
Существуют также фотометрические ТХ-газоанализаторы и газосигнализаторы, в которых повышение температуры газовой смеси, возникающее вследствие реакции горения контролируемого компонента (например, СН4 или С6Нб), определяется оптически по повышению интегральной яркости (свечения) пламени, измеряемой фотоэлектрически.
Избирательность термохимического метода ограничена из-за возможного присутствия в газовой смеси компонентов, вступающих, наряду с контролируемым компонентом, в химическую реакцию. При использовании каталитического варианта метода это ограничение удается иногда значительно ослабить подбором температуры катализатора.
П рименение
Метод пригоден для всех газов, легко вступающих в реакции, которые протекают количественно и со значительным тепловым эффектом. Сюда относятся
607
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
Н2, СО, H2S, углеводороды и другие газы, легко окисляющиеся (сгорающие) в избытке кислорода; О2, поддерживающий сгорание эквивалентного количества водорода при избытке последнего; СО2 и SO2, реагирующие с избытком водного раствора едкого натра или иного основания и т. д. Метод широко используется в газосигнализаторах, служащих индикаторами появления гремучих или приближающихся к ним по составу смесей, а также токсически опасных концентраций таких газов, как, например, H2S. Термохимический метод анализа газов применим в диапазоне от микроконцентраций до 100 объемн.%.
ТХ-газосигиализаторы горючих и взрывоопасных газов и ТХ-газоанализа-торы выпускаются в Советском Союзе в промышленном масштабе. Имеются приборы во взрывобезопасном исполнении.
Технические характеристики
Пределы измеряемых концентраций составляют от 0—0,001 до 0—100 объеми.%. ТХ-газосигнализаторы горючих и взрывоопасных газов часто градуируют в относительных процентах концентрации, соответствующей нижнему пределу диапазона воспламенения (взрыва).
Погрешности. Основная приведенная погрешность для газоанализаторов составляет от ±2 до ±10 отн.% в зависимости от пределов измерений и вида газа.
Запаздывание показаний. Для газосигнализаторов оно равно 0,5—1,0 мин, для газоанализаторов-автоматов — от 2 до 5 мин, а в некоторых случаях и более (до 15 мин).
Анализ по поглощению ультрафиолетовой (и видимой) радиации ( У Ф-газоаиализаторы)
Принципиальные основы
Анализ основан на индивидуальном характере спектров поглощения различных газов и паров в ближней ультрафиолетовой области (от 200 до 400 ммк) и в видимом свете (от 400 до 700 ммк). Мерой концентрации определяемого компонента смеси является светопоглощение в соответствующих областях спектра. При этом может использоваться либо интегральное поглощение (при отсутствии в смеси газов и паров неопределяемых компонентов, спектры которых существенно перекрывают спектр контролируемого компонента), либо частичное поглощение, избирательно выделенное с помощью светофильтров или диспергирующих оптических устройств (при наличии в смеси мешающих неопределяемых компонентов).
Газоанализаторы этого типа разделяются на следующие группы:
1. Собственно УФ-газоанализаторы—-по поглощению ультрафиолетовой, а в некоторых случаях и видимой радиации (или части последней).
II. Мерку р о метрически е УФ - газоанализаторы — по поглощению ультрафиолетовой радиации парами ртути — веществом, наиболее интенсивно поглощающим ультрафиолетовые лучи. Пары ртути выделяются из окиси ртути (вспомогательного реагента) в итоге воздействия на нее определяемого газо- или парообразного компонента смеси, который не поглощает этих лучей, но обладает способностью восстанавливать окись ртути до ртути.
III. Фотометрические — визуальные — газоанализаторы — по поглощению видимой радиации, обусловленному естественной окраской оптически прозрачного газа или пара.
Измерение поглощения производится фотометрически по ослаблению потока радиации, прошедшей через смесь газов и паров. Выходной прибор измерительной схемы градуируется эмпирически в единицах концентрации определяемого компонента.
Применение
Значительное взаимное наложение спектров поглощения в ультрафиолетовых лучах многих газов и паров ограничивает применение метода I относительно небольшим числом их (пары Hg, CI2, СеН6 и других ароматических углеводородов, H2S, SO2, CS2, Оз, NO2, галогензамещенные углеводороды, карбо-
608
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
иглы). Чувствительность метода наиболее высока при микрокоицентрациях и падает с увеличением концентраций. Метод II применим для определения суб-микро- и микроконцентраций восстановительных паров и газов (СО, Нг, С2Н4, H2S, НгО, формальдегида и других низших альдегидов, акролеина и т. п., а также горючих паров и газов). Метод III пригоден только для определения малых и средних значений концентраций газов, обладающих интенсивной естественной окраской в воздухе или в смесях с другими бесцветными газами и парами.
Автоматические УФ-газоанализаторы, основанные на методе 1 и предна-впаченпые для определения CI2, Ni(CO4), паров Hg и др., выпускаются в Советском Союзе небольшими партиями.
Технические характеристики
Пределы измеряемых концентраций по методу 1 составляют минимально 0—1 - 10~* объемн.% ( в зависимости от вида газа или пара), максимально 0—50 объемн.% (при концентрациях > 50% чувствительность метода становится очень малой). При измерениях по методу II минимальный предел концентраций составляет 0—5-J0-7 объемн.% в зависимости от вида газа или лара, максимальный — от 0 до 2 • 10-2 объемн.%.
Погрешности. Основная приведенная погрешность составляет от ±2 до ±10 отн. %. Погрешность резко возрастает с уменьшением пределов измерений.
Запаздывание показаний составляет от нескольких секунд до 1 мин.
Фотоколориметрические и фотометрические ленточные методы анализа (ФК- и ФЛ-газоанализаторы)
Принципиальные основы
Анализ основан на образовании специфически окрашенных продуктов некоторых химических реакций, протекающих в определенных условиях. Интенсивность окраски продуктов (измеряемая фотоэлектрически) при так называемой цветной или колориметрической реакции служит мерой концентрации реагирующего компонента. Выходной прибор соответствующей электроизмерительной схемы градуируется непосредственно в единицах концентрации контролируемого компонента.
Колориметрическая реакция проводится 1) в жидкой фазе, образуемой вспомогательным реагентом, сквозь который циклически или непрерывно пропускается контролируемый компонент (фотоколор и метрический, ФК-метод, характеризуемый применимостью закона Буге-—Ламберта — Бера), Или 2) в пропитанном вспомогательным реагентом слое бумажной или текстильной ленты, поверхность которой с одной стороны омывается смесью газов и паров, содержащей контролируемый компонент (фотометрический ленточный, ФЛ-метод, к которому неприложим вышеупомянутый закон).
Применение
ФК- и ФЛ-методы анализа газов применимы только для определения суб-микро- п микроконцентраций, поскольку чувствительность методов резко падает с переходом к концентрациям порядка нескольких объемных процентов и выше. Метод практически избирательный, поскольку для значительного числа определяемых газов и паров при известном составе неопределяемых компонентов смеси могут быть подобраны специфические цветные реакции. Номенклатура газов и паров, определяемых этими методами, исключительно широка и в этом смысле ФК- и ФЛ-методы принадлежат к наиболее универсальным; они применимы также и для контроля весьма малых концентраций многих аэрозолей. Для очень малых концентраций приходится накапливать сигналы. Вследствие своей инерционности фотоколориметрические и фотометрические методы непригодны для контроля быстро изменяющихся концентраций.
В СССР серийно выпускаются ФЛ-газоанализаторы универсального типа — для любых видов паров и газов,— используемые при условии подбора цветной реакции.
39 Зак. 783
6Э9
автоматический анализ газов
Технические характеристики
Пределы измеряемых концентраций. Минимальные пределы измерения составляют от 0 до 10 5—10-3 объемн.%, максимальные — от нуля до нескольких объемных процентов.
Порог чувствительности для Ф Л-газоанализаторов составляет 3-10-3—1 • 10“2 отн. %, а для ФКтазоанализаторов он равен ~ 1010 отн. % от верхнего предела измерений.
Погрешности. Основная приведенная погрешность составляет от ±5 до ±10 отн.%, в особо неблагоприятных случаях — до ±20 отп.%.
Запаздывание показаний составляет 3—10 мин в зависимости от выбранной реакции, а для ФК-метода также от способа подачи реагента и газа — циклического пли непрерывного.
Газохромагографические методы анализа (ХГ-газоанализаторы)
Принципиальные основы
Методы основаны на индивидуальной степени сорбции каждого газа и пара, т. е различной способности сорбироваться данным твердым или жидким сорбентом при всех прочих (температура, давление, скорость газа и т. д.) равных условиях. Дискретная (при обычной хроматографической методике) проба анализируемой газовой смеси вводится в непрерывно протекающий вдоль слоя сорбента поток газа-носителя, инертного в отношении пробы и сорбента. В результате многократных сорбции и десорбции каждый компонент пробы перемещается вдоль слоя сорбента с определенной свойственной ему скоростью, отличной от скоростей других компонентов. Поэтому' со слоя сорбента компоненты сходят раздельно (поочередно). Последовательность выхода отдельных компонентов смеси из хроматографической колонки, содержащей сорбент, характеризует их состав и способствует их качественной идентификации. На выходе колонки устанавливается газоанализатор (так называемый детектор), позволяющий получить развертку во времени (спектр) концентраций (количества) отдельных компонентов в пробе газовой смеси. Мерой этих количеств является интенсивность соответствующих сигналов детектора, записываемых на диаграмме выходного прибора в виде отдельных пиков. Применяются главным образом детекторы по теплопроводности и различные типы ионизационных детекторов.
Автоматический газовый хроматограф представляет собой, таким образом, спектрометр концентраций, работающий повторно-циклически.
Применение
ХГ-газоанализаторы пригодны для определения состава и концентрации компонентов практически любых смесей газов и паров, при условии, что речь идет о парах жидкостей с температурами кипения, не превышающими ~600 'С. ХГ-газоанализаторы допускают настройку, ограничивающую просматриваемый спектр заданными компонентами смеси. Уменьшение числа последних ускоряет цикл работы прибора, что в сочетании с другими методическими и конструктивными мерами позволяет настолько уменьшить время одного цикла (до I — 3 мин), что оказывается возможным применение ХГ-газоанализатора в системах автоматического управления производственными процессами.
Газовые хроматографы, которые могут служить ХГ-газоаналнзаторами, выпускаются в СССР в промышленных масштабах, как с ручным, так и с автоматическим управлением. Последние могут быть использованы не только для контроля производственных процессов, но и для их автоматического регулирования..
Технические характеристики
Методы хроматографирования и конструкции ХГ-газоаналпзаторов весьма разнообразны, поэтому привести для них средние значения показателей затруднительно. Приводимые здесь технические данные по автоматическим .газовым хроматографам являются только примером.
Пределы измеряемых концентраций составляют от ~ 10 4 до 100 объемн.%.
Воспроизводимость показаний составляет ~0,5% от веохнего предела измерений.
610
автоматический анализ газов
Порог чувствительности равен ~ 1010 объеми.% (у лабораторных газовых хроматографов для эпизодических анализов он равен объ-
емн.%).
Длительность одного цикла анализа смеси (до 6 компонентов) составляет от. 1 до 12 мин.
Анализ по электропроводности (электрокондуктометрические,ЭП-газоанализаторы)
Принципиальные основы
Анализ основан на зависимости удельной электропроводности раствора смеси электролитов от концентрации в нем соединений, образующихся в результате взаимодействия (при всех прочих равных условиях) определяемого компонента смеси газов и паров с находящимся в избытке раствором известного электролита. Взаимодействие заключается в растворении газа в жидком реагенте и сопровождается переходом газа или пара из молекулярной (редко атомарной) формы в ионную и образованием новых соединении, остающихся в растворе или выделяющихся из него. Характер взаимодействия определяется внешними условиями н химической природой раствора электролита и определяемого компонента (а также и неопределяемых компонентов). Изменение удельной электропроводности раствора электролита в результате взаимодействия со смесью газов (паров) является мерой концентрации в ней определяемого компонента. Хотя принципиально метод может быть избирательным, практически он таковым не является, поскольку лишь в очень редких случаях можно подобрать такой раствор электролита, который, взаимодействуя с определяемым компонентом, не взаимодействовал бы ни с одним из неопределяемых компонентов контролируемой смеси газов и паров. Поэтому ЭП-метод применяется по преимуществу при анализе бинарных или квазибинарных смесей.
Применение
ЭП-газоаналпзаторы чаще всего применяются для определения микроконцентраций и малых концентраций, так как чувствительность метода при этом наибольшая. В отдельных случаях метод применим и для средних и высоких концентраций, но лишь при условии, что диапазон измерений не соответствует участку двузначности удельной электропроводности раствора электролита как функции концентрации определяемого компонента газовой смеси. Метод пригоден для определения SO2, СО2, H2S, CS2, Cl2, СС14, СОС12, РН3, AsH.,, HCN, NH3. N2O, органических газов и паров, содержащих серу, гидролизующихся газообразных хлоридов, Н2О и любых газов и паров, которые могут быть переведены в перечисленные или им подобные соединения. ЭП-газоанализаторы обязательно либо тщательно термостатируются, либо снабжаются схемами автоматической коррекции влияния температуры, так как электропроводность растворов электролитов сильно зависит от температуры (от —1,5 до —7,0 отн.% на 1 град). Полуавтоматические ЭП-газоанализаторы находят применение для экспресс-анализа углерода, серы и кислорода в твердых веществах путем перевода определяемого элемента в газовую фазу (например, сжиганием) с после-дхюшим кондуктометрическим определением соответствующего компонента смеси газов.
Автоматические-ЭП-газоанализаторы в Советском Союзе серийно не выпускаются, изготовляются лишь неавтоматические лабораторные приборы.
Технические характеристики
Пределы измеряемых концентраций составляют минимально 0—4-10“s обьемн.% для SO2 и 0—0,1 объемн.% для CCU, максимально — от нуля до десятых долей процента или нескольких процентов в зависимости от вида газа.
Погрешности. Основная приведенная погрешность равна от ±5 до ±10 отн.% в зависимости от вида газа и пределов измерения.
Порог чувствительности для H2S и SO2 составляет 2—5 • 10-6 объемн.%.
Запаздывание показаний равно от 30 сек до нескольких минут.
39* 611
АВТОМАТИЧЕСКИЙ АНАЛИЗ ГАЗОВ
Электрохимические методы анализа (ЭХ-газоанализаторы)
П ринцшгиальные основы
Анализ основан на зависимости вольт-амперной характеристики гальванического элемента (электрохимической ячейки) от концентрации определяемого компонента в газовой смеси, находящейся в динамическом равновесии с электрохимической системой ячейки и определяющей значение окислительно-восстановительного потенциала раствора электролита и течение электродных процессов. На этой зависимости базируются две группы методов определения концентрации компонентов смесей газов и паров: 1) с приложением внешнего поляризующего напряжения к электродам ячейки и 2) без него (с внутренним электролизом).
К первой группе относятся потенциометрический метод (изменение окислительно-восстановительного потенциала раствора электролита, омывающего один из электродов ячейки, обусловленное реакцией с участием определяемого компонента газовой смеси и зависящее от его концентрации; мерой концентрации является изменение э. д. с. ячейки), амперометрический метод (в деполяризационном его варианте используется зависимость силы диффузионного тока, возникающего в поляризованной ячейке под деполяризующим действием определяемого компонента, от концентрации этого компонента газовой смеси) и кулонометрический метод (тот же амперометрический метод, но осуществляемый в условиях количественного проведения электрохимической реакции перевода определяемого вещества газовой смеси в другую форму или другое соединение; мерой концентрации является количество израсходованного на реакцию электричества или, при непрерывном стабилизированном подводе контролируемой газовой смеси, ток во внешней цепи ячейки). Кулонометрические ЭХ-газоанализаторы обычно выпускаются как автоматические титрометры непрерывного действия с так называемой электрохимической компенсацией. Мерой концентрации определяемого компонента газовой смеси служит в этих приборах ток электролиза, выделяющий из раствора электролита (в котором растворяется определяемый таз) титрант в стехиометрических количествах, что обеспечивается электрометрическим измерением точки эквивалентности и автоматическим управлением током электролиза.
Ко второй группе ЭХ-методов газового анализа относится гальванический метод; в нем используется зависимость — при определенных постоянных условиях — диффузионного тока ячейки от концентрации определяемого компонента газовой смеси; мерой концентрации является ток во внешней цепи ячейки.
П рименение
ЭХ-методы широко применяются прежде всего для определения кислорода в различных, часто сложных газовых смесях, причем гальванический и частично кулонометрический методы используются для измерения субмикро- и микроконцентраций. Этими методами определяется и кислород, растворенный в воде. Остальные методы применяются для измерения малых, средних и больших (до 100 объемн.%) концентраций. Для определения микро- и малых концентраций сернистых и сероорганических соединений применяются кулонометрические автоматические титрометры. ЭХ-методы применяют также для определения микроконцентраций паров воды. Их используют и для определения других газов и паров, в частности горючих, по остатку кислорода после сжигания. ЭХ-методы, особенно гальванический и деполяризационный, являются ограниченно избирательными.
В СССР серийно выпускаются гальванические, титрометрические и деполяризационные ЭХ-газоанализаторы.
Технические характеристики
Пределы измеряемыхконцентраций (в объемн. %) — от 0—1 • 10-4 до 0—100 для кислорода; от 0—1 • 10-2 до 0—5 для сернистых соединений.
Погрешности. Основная приведенная погрешность равна от ±2 до ±10 отн.% в зависимости от вида газа, пределов измерений и метода.
-Порог чувствительности составляет от 1 - 10-6 до 1 • 10*5 объемн.%.
Запаздывание показаний составляет от 10 сек до 5 мин в зависимости от вида газа, пределов измерений и метода.
612
ТИПИЧНЫЕ СЛУЧАИ ПРИМЕНЕНИЯ ПРОМЫШЛЕННЫХ АВТОМАТИЧЕСКИХ
ГАЗОАНАЛИЗАТОРОВ
В таблице приводятся сведения, позволяющие выбрать тип автоматического газо-» анализатора, пригодный для измерения различных концентраций некоторых газов, содержание которых в газовых смесях определяется наиболее часто. Минимальные и максимальные значения верхних пределов измеряемых концентраций указаны в головке таблицы; иижний предел измерения — нуль.
Табличные значения верхних пределов измерения соответствуют обычным средним условиям определения. Прн особо благоприятных обстоятельствах (постоянство внешних условий, отсутствие в газовой смеси мешающих компонентов н т. п.) чувствительность метода увеличивается, что равносильно снижению минимального значения верхнего предела измерения. При неблагоприятных условиях определения чувствительность метода снижается, т. е. минимальное значение верхнего предела измерения повышается.
Порог чувствительности составляет в среднем 3 оти. % от верхнего предела измерения.
В таблице приняты следующие сокращенные обозначения видов газоанализаторов, основанных на различных методах газового анализа:
ПК— по поглощению инфракрасной радиации;
ИН — ионизационные;
МН— по теплопроводности (термокондуктометрические);
ОМ—объемные и манометрические;
СФ— спектрофотометрические;
ТП-по теплопроводности (термокондуктометрические);
ТХ— термохимические (каталитические газовые н термосорбциоиные жидкостные);
УФ — по поглощению ультрафиолетовой (и видимой) радиации;
ФК—фотоколориметрические (по искусственной окраске жидкого реагента);
ФЛ—фотометрические ленточные;
ЭП— по электропроводности (электрокондуктометрические);
ЭХ— электрохимические (гальванические, деполяризационные и кулонометрические с «электрохимической компенсацией»).
Масс-спектральные и газохроматографические газоанализаторы, отличающиеся от перечисленных тем, что они показывают не концентрации определяемого компонента, а спектр состава газовой смеси, требующий расшифровки, здесь ие рассматриваются.
Газоанализаторы определенного вида, пригодные лишь в верхней области соответствующего предела измерений, отмечены звездочкой.
Газ или пар Значения верхних пределов измерения концентрации, объеми. %
0,0001-0,01 0,01—0,5 0,5-5 5—100
Аг ТП, СФ ИН, ТП, СФ ТП
СН4 ЭП* (от 0,0005 объемн. %), УФ* ИК, ТХ, ТП* ИК, тх, ТП, ом* ИК, ТП, ом
СО ЭП,ИК*,ТХ*,ФК*, ФЛ*, УФ* ЭП, ИК, ТХ, ФК*. ФЛ* ИК, тх, ом* ИК, ТХ, ом
СО2 ЭП, ИК ЭП, ИК, ТХ ИК, ТХ, ТП*, ом* ИК, ТП, ом
С12 ЭП, ФК, ИН ИН, ЭП, УФ, ФЛ УФ, ФЛ, ОМ*, ТП* УФ, ОМ, ТП
cs2 ЭП, ФК,ФЛ*, УФ* ЭХ, ФК, ФЛ
Н2 ТХ* (от 0,001 объемн. %), УФ* ТХ ТП, ом* ТП, ом
Не ТП*, СФ* ТП, СФ ТП
Hg УФ (от 1 • 10 6 объемн. %) УФ, ФК, ФЛ
Н2О ЭХ* (от 0,001 объемн. %), ЭП ЭХ, ЭП, ТХ ИК. ТП*
H2S ЭП, ФК,’ ФЛ, УФ ЭП, ФК, ФЛ, эх эх
n2 СФ* СФ
NH3 ИН, ЭП, ФК, ФЛ* ИН, ЭП, ФК, ФЛ, ИК* ЭП, ИК, ин, ОМ*, ТП* ИК, ОМ, ТП
NO ЭП, ФК, ФЛ* ФК, ФЛ, УФ УФ УФ
no2 ИН, ЭП, ФК, ФЛ* ИН, ФК, ФЛ, УФ УФ УФ
o2 ЭХ, ФК.ТХ* (от 0,001 объемн. %) ЭХ, ФК, ТХ тх, мн, ом* мн, ом
so2 ИН, ЭХ, ЭП, ФК, ФЛ* ИН, ЭХ, ЭП, ФК, ФЛ, Тх ТХ, ТП*, ом* ТХ, ТП, ом
Углеводороды , ФК ФК, ФЛ, ИК* ИК, УФ ИК, УФ
613
Приготовление контрольных газовых смесей для градуировки и поверки газоаналитических приборов
Для приготовления газовых смесей применяют технические Окись углерода 4- хлор * Углеводороды (алифатиче- и чистые газы, поставляемые промышленностью в сжиженном Сероводород + кислород ** ские)4-хлор* или сжатом состоянии в баллонах под давлением, а также Сероводород+двуокись угле- Этилен 4- хлор газы, получаемые лабораторным способом и используемые в рода ** момент получения или хранимые в газометрах. Контрольные газовые смеси обычно состоят из одного или двух опреде- После приготовления газовых смесей в статических усло- ляемых компонентов в среде газа-разбавителя, например, СО внях их следует выдержать до анализа в течение определен- о и Н2 в азоте, СН4 и другие углеводороды в воздухе или ного периода, необходимого для естественного перемешивания О азоте и т. п. газов. Осушка и очистка технических газов производятся, как Продолжительность перемешивания, т. е. выравнивания > правило, под давлением, но в тех случаях, когда это по концентраций по всему объему, зависит от плотности компо- сэ каким-либо причинам невозможно, примеси удаляют при атмо- центов, составляющих смесь. Газовые смеси, содержащие ком- сферном давлении, пропуская газ через систему жидких нли поненты с близкими значениями плотности (например, Ns и О2), ® твердых поглотителей. можно анализировать через сутки после приготовления. Га- х При составлении газовых смесей следует учитывать не- зовые смеси, содержащие компоненты, плотность которых за- О совместимость некоторых газов, т. е. возможность взаимодей- метно отличается друг от друга (например, СО2 и СО2 и ствия между ними в обычных условиях нли в присутствии N2), подлежат анализу не ранее, чем через двое суток после ® третьего компонента, что приводит к ошибочным результатам приготовления. Е анализа. К несовместимым газам можно отнести следующие: Газовые смеси, не содержащие агрессивных газов, можно * хранить в течение полугода без проведения повторных анали- -i Аммиак 4- галогены Водород + окислы хлора * зов. Газовые смеси с микроконцентрациями агрессивных газов > Аммиак 4- галогеноводороды Водород 4- хлор * (NO, NO2, SO2, NH3) могут храниться в баллонах, при coot- g Аммиак 4-окислы хлора Окись азота 4-.кислород ветствующей подготовке последних (отмывка, специальные Ацетилен 4- хлор Окись азота 4- хлор ** покрытия и др.), в течение длительного времени. Подобные .. . смеси необходимо, однако, периодически анализировать, так д # как содержание агрессивного компонента постепенно снижается, "и * леагиРУют ПРН освещении. Смеси с макро- и микрокоицентрациями сероводорода хране- S 1 еагируют в присутствии паров воды. нию в баллонах не подлежат. 3» гл 3 СОСТАВ ИСХОДНЫХ ГАЗОВ, ПРИМЕНЯЕМЫХ ДЛЯ ПРИГОТОВЛЕНИЯ КОНТРОЛЬНЫХ СМЕСЕЙ m
Газ Содержание примесей в газе, объемн. % л- Е Содержание паров воды (прн 760 мм рт. cm.), g мг/л ~
n2 Аг н2 Не со2 СО углеводороды в пересчете на СН4 о2
Азот, 2-й сорт Аргон чистый Водород технический, марка А Не менее 99,0 0,01—0,1 Те более 0,3 Те менее 99,9 Не менее 99,7 0,001-0,004 Менее 0,01 0,001-0,003 Менее 0,01 Менее 0,01 0,5—1,0 0,003—0,01 0,05—0,3 1РИГОТОВЛЕНИЯ * о" со I О LQ 1 о СЧ СЧ ° о о"
Воздух ком- 70,8 0,9 .... 0,005 Не более прессорный 0,04 Гелийтехниче- Не более ... Не более Не менее ский 0,4 0,05 99,1 Метай (из при- 2—3 0,1—0,5 родного газа) Углерода дву- ... ... Не менее окись пище- 98,5 вая Углерода окись 0,5—2 .... 0,3—1,5 .... 1—2 ОЧИСТКА И ОСУШКА ИСХОДНЫХ ГАЗОВ ПРИ 0,001-0,003 0,001—0,02 20,9 Не более * 0,2 S 0,001—0,01 Не более .... 0,01 ® 0,2—0,5 Не меиее 0,2—0,5 ... г 96,0 = <0,001 0,1 й о 3 90—96 0,1—1 . К W X о ПОВЫШЕННОМ ДАВЛЕНИИ ®
Назначение очистки 1 Режим работы Остаточное содержание примесей в очищенном газе, объемн. % S о г Условия регенерации поглотителя Е X X р
рекомендуемые поглотитель и температурный режим объемная скорость очищаемого газа, отнесенная к объему поглотителя, ч-1
Очистка от кислорода Очистка от водорода Очистка от окиси углерода Очистка от двуокиси углерода 2 Металлическая медь, восстановленная водородом из окиси, в гранулах диаметром 3—5 мм; 300—350° С Гранулированная окись меди; 300—320° С Гранулированная окись меди; 300—350° С Натронная известь, диаметр зерен 2—3 мм; комнатная температура 30—60 30—60 30—50 15—30 Не более 0,001 Не более 0,01 Не более 0,001 Не более 0,001 о Восстанавливают окись меди водородом при сг 300—350° С. При х очистке водорода ре- j генерации не тре- ы буется § Регенерацию производят воздухом при 300—350° С То же Не регенерируется
g Продолжение
Назначение очистки Режим работы рекомендуемые поглотитель и температурный режим объемная скорость очищаемого газа, отне- сенная к объему поглотителя, ч~1 Остаточное содержание примесей в очищенном газе, объемн. % Условия регенерации поглотителя
Осушка и одновременная очистка газов с температурой кипения ниже —180° С от примесей кислорода, азота, двуокиси и окиси углерода, углеводородов Очистка от углеводородов, масел и других органических веществ Очистка гелия или аргона от азота 04 Силикагель марки КСМ, охлаждаемый жидким азотом, диаметр зерен 1—5 мм; предварительно газ подвергают осушке силикагелем при комнатной температуре Активированный уголь марки АГ-2, диаметр зерен ‘ 2—4 мм; комнатная температура Металлический кальций; 650° С ИСТКА И ОСУШКА ИСХОДНЫХ 60—80 60—80 30—50 ГАЗОВ ПР1 Не более: О2 — 0,0005; СО, СО2 —0,001; влаги — 0,05 мг/л Не более 0,001 Не более 0,005 АТМОСФЕРНОМ ДАВЛЕН! т-> С Вакуумирование при л 200—230° С = п > S о п ч Вакуумирование при § 100° С. При очистке > от масел регенера- s цию рекомендуется * проводить отгонкой с о водяным паром с по-следующей сушкой Е Не регенерируется х U о 1И я
Газ Удаляемые примеси Поглотитель Газ Удаляемые примеси Поглотитель
Аммиак Ацетилен Влага СО2 РН3 H2S ] Влага ... СаО NaOH плавленный 10% раствор СгОз в разб. (1:1) H2SO4 Окись углерода со2 Fe (СО)5 NI (СО)4 Натронная известь или аскарит I Активная медь при [ 180—200° С
Двуокись азота NO 1 Окисление кислородом Непредельные углево- Влага Последовательно СаСТ2
N2O J с последующей кон- дороды и Р2О5
Влага денсацией при —80° С Предельные углеводо- О2 Медные стружки, смо-
р2о5 роды ченные аммиачным
Двуокись серы Влага Последовательно Непредель- раствором NH4C1
H2SO4 И Р2Оа Бромная вода или пем-
Двуокись углерода СО Гопкалит при 100° С ные угле- за, смоченная конц. H2SO4
Влага Последовательно СаС12 водороды
И Р2О5 Влага Последовательно СаС12
Закись азота NO Насыщенный раствор И Р2О5
FeSO4 Хлор НС1 | Последовательно Н2О,
со2 no2' | КОН плавленный Влага f конц. H2SO4, СаО и Р2О5 Я
Влага Р2О5 X
nPHPOTOBJ 1ЕНИЕ ГАЗОВЫХ СМЕСЕЙ о о оэ ь
Общепринятые методы приготовления газовых смесей основаны на законе Дальтона, согласно которому общее давление газовой д смеси равно сумме парциальных давлений ее компонентов; отсюда следует, что объем газовой смеси равен сумме объемов газов, соста- х вляющих смесь. m
Краткая характеристика метода >
Метод приготовления газовой смеси достоинства недостатки точность приготовления смеси, объемн. % о оэ Примечания Е и
В газометрах над затворной жидкостью (рис. 1, стр. 620) СГ. Быстрота приготовления смеси Малое количество смеси; нестабильность смеси из-за растворимости отдельных компонентов в затворной жидкости; увлажнение смеси; трудность обеспечения постоянного расхода смеси ±1 п гя При составлении смеси необходимо еле- s дить по манометру, чтобы давление в газометре не превышало атмосферного
Продолжение
>—1 со Метод приготовления газовой смеси Краткая характеристика метода Примечания
достоинства недостатки точность приготовления смеси, объемн.
В сухих бутылях * (рис. 2, стр. 620)
В баллонах под давлением (рис.
3, стр. 621)
Возможность получения микроконцентраций газов, нестабильных в баллонах или в присутствии затворных жидкостей
Возможность получения значительных количеств газа (до 4 м3); возможность получения стабильных смесей с микроконцентрациями агрессивных газов (Cl2, NO2, NH3, пары аминов и др.); удобство транспортировки смесей
Малое количество смеси; опасность разрушения бутылей при вакуумирова НИИ
Непригодность для получения смесей, содержащих макроконцентрации агрессивных газов и паров (H2S, HCI, H2SO4); необходимость отдельного помещения и специальной аппа-ра гуры; трудность приготовления смесей с одними и теми же номинальными значениями концентраций газов
В газосме- Возможность получе Необходимость по- ±2—3
сительной ния больших коли- стоянного наблюде-
уста- честв смесей с лю- ния за установкой
новке — быми газами; воз- в процессе эксплуа-
смешение можность больших тации; сложность
в динамя- расходов газа (до приготовления мно-
ческих 0,2 л/сек); возмож- гокомпонентных сме-
условиях (рис. 4, стр. 621) ность плавного изменения концентрации газов в широких пределах сей
Для приготовления смеси необходимое количество определяемого газа набирают в газовую пипетку соответствующей емкости, из которой засасывают газ в предварительно вакуумированную бутыль емкостью ~20 л, после чего набирают в нее газ-разбавитель до атмосферного давления. Аналогичным образом готовят смесь во второй бутыли. Обе бутыли соединяют последовательно таким образом, что при отборе пробы из первой бутыли объем газа, равный объему пробы, переходит из второй бутыли в первую, а во вторую засасывается такое же количество воздуха. При отборе проб общим объемом 5—6 л концентрация газа в первой бутыли изменяется незначительно.
В случае отсутствия пипетки требуемой емкости подбирают другую (близкую по емкости к расчетной) и после приготовления смеси уточняют концентрацию определяемого газа по формуле:
где Vi — объем пробы определяемого газа, мл; К—поправочный коэффициент на чистоту определяемого газа (К< 1); М— молекулярный вес определяемого газа; V — объем бутыли, л;
ПРИГОТОВЛЕНИЕ
V2 — объем 1 моль определяемого газа J при рабочих условиях, мл ш
Баллон, в котором приготовляется смесь, я промывают газом-разбавителем путем -многократного вакуумирования и после- * дующего заполнения этим газом. Затем § баллон, заполненный газом-разбавите- m лем до атмосферного давления, поме- й щают во взрывобезопасную кабину. s присоединяют к газовому коллектору и по соответствующей линии (промытой вначале газом-разбавителем) подают определяемый газ, а затем газ-разбавитель до заданных парциальных давлений. Подача исходных газов производится через коллектор непосредственно из баллонов или через дожимной компрессор. Воздух подается из компрессора также через коллектор; подача кислорода производится по специальной линии из баллона, установленного в отдельном помещении
При заданных концентрации С,- t-го компонента смеси (в объемн.%) и общем расходе смеси F (в л/сек) расход х,- этого компонента определяется по формуле:
Если содержание компонента смеси задано в мг/л, то его концентрацию в объемн. % находят по табл, на стр. 572 (или по графику на стр. 575) и устанавливают соответствующий расход на газосмесительной установке
2 * Подробнее см. Е. Д. Филянская, Т. Н. Козляева. И Г В,- пптлб ..
ных газов и паров в воздухе промышленных предприятий, Профнздат,' 1958, * ’ о-колористическии метод анализа ввел-
ПРИГОТОВЛЕНИЕ ГАЗОВЫХ СМЕСЕЙ
Рис. 1. Схема устройства для приготовления газовых смесей в газометрах:
/ — напорная склянка; 2—манометр.
Рис. 2. Схема устройства для приготовления газовых смесей в сухих бутылях:
/ — пипетка; 2—шлиф; 3— ловушка для ртути; 4— мятая фольга для улучшения перемешивания газовой смеси; 5 — манометр.
620
ПРИГОТОВЛЕНИЕ ГАЗОВЫХ СМЕСЕЙ
Рис. 3. Схема установки для приготовления газовых смесей в баллонах под давлением:
А — взрывобезопасная кабина; Б — помещение для приготовления смесей;
В — помещение для баллонов с исходными газами; Г—помещение для баллона с кислородом. /—дожимный компрессор; 2— гребенки; 3—веитилн.
Газовая
Рис. 4. Схема устройства для смешения газов в динамических условиях:
1 — реометры; 2 — смеситель; 3—капилляры.
621
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ПО ТЕМПЕРАТУРАМ ПЛАВЛЕНИЯ ИХ ПРОИЗВОДНЫХ
Ниже приводятся температуры плавления (в °C) производных некоторых органических соединений различных классов. В первой графе даны исходные соединения, в последующих — температуры плавления продуктов взаимодействия с соответствующими реагентами.
Более подробные сведения см.: 1. Г. е й е р, Анализ и определение органических соединений, т. 1—2, перев. с нем., ГОНТИ, 1937. — 2. Р. Шрайнер. Р. Ф ь ю с о и. Систематический качественный анализ органических соединений, перев. с англ., ИЛ, 1950. — 3. К. Г- Бауэр, Анализ органических соединений, ИЛ, 1953. — 4. В. С. Джонсон, Р. Д. Ше н н ан, Р. А. Р и д, Органические реактивы для органического анализа, перев. с англ.. ИЛ, 1946. — 5. Organic Reagents for Organic Analysis, 2-е изд., Лондон. 1950. — 6. S. V e i b e 1, Analytik organischer Verbindungen, Берлин, 1960.
Перечень таблиц
Алкалоиды
Альдегиды
Аминокислоты
Амииы первичные алифатические
Амины первичные ароматические
Амииы вторичные
Амииы третичные
Галогеналкилы
Диены
Карбоновые кислоты
Кетоны н хиноны
Спирты
Тиолы
Углеводороды ароматйческис
Углеводы
Фенолы
Эфиры (простые)
Алкалоиды
Алкалоид Пикриновая кислота Стиф-нивовая кислота Алкалоид Пикриновая кислота Стгф-ниновая кислота
Аконитин 166 120 Наркотин 141
Атропин 176 180 Нарцеин 195 • • .
Бруцин 280 266 Никотин . . ... 218 190
Героин 205 222 Папаверин . . . 220
Гиосциамин ... 165 - . . Пилокарпин 147 183
Г иосцин 188 « . . Скополамин 174
Дионин 155 Спартеин ... 206 . . .
Кодеин . • 197 115 Стрихнин . . . . 286 266
Кокаин 155 187 Хинидин . 149
Кониин . ... 75 . « . Хинин .... 132 154
Кофеин ....... 145 199. Цинхониднн 209
Морфин 228 189 Цинхонин 194 106
622
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Альдегиды
Предел жение
Альдегид Димедон Димедон (продукт дегидратации) 2, 4-Дини-трофенил-гидразин п-Нитро-фенилгид-разин Фенил-гидра-зин Г идро-ксмл-амнн солянокислый Семикарбазид солянокислый
Акролеин . . . . . . 192 163 165 151 171
Альдоль 147 ПО 194
о-Амииобеизойный 219 221 135
л-Аминобензойный 226 162 88 >280
гг-Аминобензойный . . 175 124 173
Бензойный . - . . 195 200 237 192 158 35 — 227
Валериановый . . 105 113 98 . . . . 52 . . . •
Ванилин 197 228 271 229 105 117 240
Глиоксаль 186 224 327 302 170 178 > 270
п-Диметиламинобен-
зойный 193 222 325 182 148 144 . . . •
Изовалериановый . . . 155 173 123 110 48 132
Изомасляный . . . 154 155 182 130 125
Капроновый . . 109 104 80 51 106
Коричный 213 175 255 195 168 138 216
Кротоновый 183 167 189 185 56 119 201
Куминовый 171 173 243 190 129 58 210
Масляный 136 136 126 91 104
о-Метоксибензойный 253 205 92 215
и-Метоксибензойный
(анисовый) .... 145 243 253 161 121 210
Муравьиный . . . 189 171 168 182 169
а-Нафтойный .... 237 80 98 222
f-Нафтойный 270 230 206 156 245
о-Нитробензойный 250 153 103 256
.м-Нитробензойный 198 172 293 120 118 246
гг-Нитробеизойный . 190 222 320 249 155 129 220
о-Окспбеизойный . . . 208 252 233 142 57 232
.и-Оксибензойный 260 222 130 88 199
п-Оксибеизойный 189 246 280 266 177 72 224
Пиперональ 178 220 266 200 103 ПО 234
Пропионовый ..... 155 143 155 124 40 89
о-Толуиловый .... 167 215 194 222 161 49 224
л-Толуиловый . . 172 206 194 157 91 60 216
п-Толуиловый 234 200 113 80 234
2, 4, 6-Трииитробепзои-
НЫЙ 208 247 202 214
Уксусный 140 174 168 128 63 47 163
Фенилуксусный . . 165 126 121 58 100 155
Фурфурол 162 165 229 127 97 89 203
Хлораль 131 56 . . . .
Цитраль 116 164
Энантовый 103 112 108 73 58 109
623
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
/ Аминокислоты Продолжение £ К
Аминокислота а-Нафтил-изоциа- нат л-Толуол-сульфо-хлорид Уксусный ангидрид Фенилизоцианат Хлористый бензоил Хлораце- । тилхлорид £
Р-Аланин 174
£)£-Аланин 139 . ... 190 166 г
D- или £-Аланин . . . 198 133 168 151 125 ?
о-Аминобензойная . . 185 181 182 С.
л-Аминобензойная . . . 250 270 248
л-Аминобензойная . . 252 300 278 .... ?-
£)£-а-Аминомасляная 194 170 147 &
£)-а-Аминомасляная 195 121
л-Аминофенилуксусная 170 198
5-Аминосалициловая 218 .... 252
£>£-Аргинин D- или £-Аспарагино- 115 .... 315
. вая ... 140 162 185
D- или £-Валин . . . . 147 147
£>£-Валин ...... 163 132 132
Глицин 190 147 206 163 187 100
£>£-Глутаминовая . . . 236 157
D- или £-Глутаминовая 117 138
£>£-Изолейцин .... 140 118 iii 0
D.- или £-Лейцин . . . 163 122 115 107 130 1
£)£-Лизин 196 249
£-Оксипролин 153 175 .... < J
£>£-Орнитин 192 267 ч*
£>.- или £-Орнитин 190 240 . . . .
£-Пролин 133 170
О£-Серин 213 169 171 ....
Саркозин 135 102 • • • •
£-Тирознн 205 114 104 166
£>£-Тирозин £-Триптофан ..... 158 176 166 197 i58
£>.£-Фенилаланин . . . 135 182 188 114
N-Фенилглицин .... 195 63
£-Цистин 203 117 181 • • • • !
Амины пе| >вичные алифатические
Амин Бензол- 2,4-Ди- а-Нафтил- Пикри- л-Толуол- Фенил-
сульфо- хлорбен- изотио- новая сульфо- изотио-
хлорид зол циаиат кислота хлорид цианат
Аллиламин 40 76 140 64 100
Амиламин . 81 io3 139 69
Бензиламин 88 116 172 199 116 147
Бутиламин 90 109 151 .... 65
втор-Бутиламин .... 71 . . . . 140 55 101
Гексиламин 96 39 79 127 .... 77
624
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Амии Беизол-сульфо-хлорид 2, 4-Ди-иитро-хлорбен-зол а-Нафтил-изотио-циаиат Пикриновая кислота л-Толуол-сульфо-хлсрид Феиил-изотио-цианат
Гептиламин 121 168
Г ексаметилендиамин 154 220 . ... 124
I, 3-Диаминопропан 96 148 ....
Изоамиламин 91 97 138 65 102
Пзобутиламин .... 53 80 137 151 78 82
Изогексиламин .... 79 125 112
Изопропиламин .... 26 95 143 150 .... 101
Метиламин 30 178 .... 215 77 113
Пентаметилендиамин 148
Пропиламин 36 97 103 135 52 63
Тетраметилендиамин 250 .... 168
6-Фенилэтиламин . . . 69 167 .... 135
Циклогексиламин . . . 89 156 142 158 87 150
Этаноламин 160 138
Этпламин 58 113 121 168 62 106
Этилендиамин .... 168 306 .... 233 160 102
Амины первичные ароматические
Амин Бензальдегид Бензол-сульФохлооид л-Нитробенз-альдегид Пикриновая кислота л-Толуолсуль-фохлорид Уксусный ангидрид Феиилизотио-цианат Хлористый бензоил
п-Аминоазобензол . . . 130 182 145 211
п-Аминодиметилаиилин 98 . 219 186 131 228
п-Амннодиэтиланилии . 142 104 172
п-Аминодифениламин 108 172 158 203
2-Аминопиридин . . . 223 71 165
о-Аминофенол .... 89 141 160 . . 139 142 146 184
л-Аминофенол .... 157 101 156 150
и-Аминофенол .... 182 154 168 ... 143 150 150 234
Анилин 54 ПО 93 165 103 114 154 163
Бензидин 238 235 242 243 317 ... 352
о-Дианизидин .... 225 243 ... 236
о-Метоксианилин . . . 81 ) 111 127 85 136 60
л-Метоксианилин . '. . 169 68 80
п-Метокснанилин . . 62 91 135 114 127 171 153
а-Нафтиламин .... 73 171 158 161 157 160 157 161
Р-Нафтиламин .... 102 98 121 195 133 134 157 162
1, 2-Нафтилендиамин 234 • . . 291
1, 4-Нафтилендиамин 188 303 ... 280
о-Нитроанилин .... 104 . . . 73 115 93 98
л-Нитроанилин .... 73 136 152 143 138 154 155 155
и-Нитроанилин .... 115 139 198 100 191 216 197
о-Толуидин 124 89 200 110 109 136 144
л-Толуидин 83 100 195 114 66 91 125
п-Толуидин 120 122 169 118 145 141 158
40 Зак. 783
625
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Амин Бензальдегид Бензолсульфохлорид И X Пикриновая кислота л-Толуолсуль-фохлорид Уксусный ангидрид Фенилизотно-цианат Хлористый бензоил
< 5 альдегид
о-Фенилендиамнн . . 106 185 280 208 202 186 301
л-Фенилендиамин . . . 105 194 184 172 190 ... 240
п-Фенилендиамин . . 140 247 266 303 ... >300
о-Хлоранилин 34 130 126 134 105 88 155 99
л-Хлораннлин 121 177 138 73 116 122
и-Хлоранилин 62 121 135 178 95 178 152 193
о-Этоксианилин . . 102 81 . . . 164 79 137 104
л-Этоксианилин .... 158 157 96 138 103
и-Этокснанилин . . 76 142 126 . . . 106 134 136 173
Амины вторичные
Амии Беизол-сульфо-хлорид Пикриновая кислота л-Толуол-сульфо-хлорид Уксусный ангидрид Фенилизо-тиоцнаиат Хлористый бензоил
Бензиланилин ... 119 140 58 103 107
Дибензиламин 68 81 112
Дибутиламин . . 60
Днизобутиламин 55 119 86 113
Диметиламин 47 155 79 135 42
Дипропиламин 51 75 69 . . . .
Дифениламин . . 122 182 142 101 152 180
Диэтаноламин . . 130 101 99
Диэтиламин ..... 42 74 60 34 42
Индол .... 187 68
Карбазол .... 182 69 98
Метиланилии 78 147 95 101 87 63
Метнл-а-нафтилампн 164 98 - 121
Метил-Р-нафтилампн 107 145 78 51* . . . 84
Метил-о-толуидпн . 90 120 56 66
Метил-л-толуидин . . 77
Мети л-п-толу идин 64 131 60 83 89 53
Морфолин 118 146 147 136 75
Пиперазин 282 280 134 191
Пиперидин ... 93 152 96 ioi 48
Пиррол 69
Скатол 171 68
Фенил-а-нафтиламип 115 152
Фенил-Р-нафтиламин 93 111
Этиланилин . . 38 132 88 54 89 60
Этил-а-нафтилампн 68
Этил-Р-нафтиламин . . 49
Этил-о-толуидин . . . 62 75 72
Этил-л-толуидин . . 72
Этил и-толуидин . . 66 .... 71 .... 40
626
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжение
Амины третичные
Амии Йодистый метил Пикриновая кислота j Амии Йодистый метил Пикриновая кислота
Акридин 224 208 Р-Нафтохино.тин .... 205 259
Антипирин 188 а-Пиколин . . . 230 169
Бензилметиланилпн 164 127 р Пиколин ... 92 150
Бензилэтиланилпн . . . 161 111 у-Пиколин 152 167
Дибензиланилин 135 131 Пиридин 117 167
Дибутиланилин .... 228 125 Триизоамиламин . . . 184 125
Диметиланилин . . . 162 Трибензиламин .... 190
Диметилбензпламин 179 Трибутиламин .... 180 105
Диметил-а-нафтиламин 145 Триметиламин . . . 230 216
Диметил-Р-нафтиламин "156* 200 Трипропиламин .... 208 117
Дипропиланилин . . - • . > Триэтиламип 195 173
Диэтиланилин ... 102 142 Хинальдин 191
Метилэтиланнлин 125 134 Хинолин . . . . 72 203
а-Нафтохинолии 179 192
Галогеналкилы
В таблице приведены производные, образуемые галогепал килами независимо от входящих в их состав галогенов.
В 4-й графе приведены температуры плавления продуктов присоединения галогенал-килов. полученных при последовательной обработке тиомочевиной и пикриновой кислотой.,
Алкил Фенилизоцианат а-Нафтил-изоцианат Тномочевина -j. пикриновая кислота
Аллил 114 155
Амил 92 112 154
втор-Амил (1-метнлбутил) .... 87 103
трет-Амил 91 138
Бензил 117 166 187
Бутил 63 109 177
втор-Бутил ... ... 107 129 166
трет-Бутил . . .... 130 147
Винил . . . 104
Г ексил . 65 ioe 157
Гептил 55 95 142
Изоамил (3-метплбутил) . - НО 111 173
Изобутил НО 126 167
Изопропил . . .... 104 196
Метил . 113 160 224
2-Метилбутп.т 88
Октил . . . . 57 91 134
Пропил 96 121 177
Фенил ... 161
Циклогексил 146 188
п-Хлорбензил 166 194
Этил . . 104 126 188
1-Этилпроппл 125 117
40*
627
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Диены
Диен Температура плавления продукта присоединения к малеиновому ангидриду Температура кипения продукта присоединения
к акролеину к кротоновому альдегиду
Аллоцимен .........................
2-Бромбутадиен-1,3 (бромопрен)
Бутадиен-1,3 (дивинил)' ...........
Гексадиен-1, 3 ..................
Гексадиен-2, 4.....................
трснс-Гексатриен-1,3, 5 ..........
2, 3-Диметилбутадиен-1,3 ........
2-Метилбутадиен-1, 3 (изопрен) . .
2-Метилпентадиен-1,3 ..............
З-Метилпентадиен-1, 3 .............
4-Метилпентадиен-1, 3 .............
Мирцен................. ...........
трснс-Пиперилен ...................
1 - Фени лбутадиен-1,3.............
2-Хлорбутадиен-1, 3 (хлоропрен)
84
187
101 51—52 (13) 75 (22)
95
51,5
79 79 (10) 89 (12)
64 63 (10) 93(25)
154 87 73 (10) 82 (12)
134 75 (12) 79—81 (12}
34 61 136(17) 144 (12)
120 144(12)
173
Примечание. В скобках указано давление в мм рт. ст.
Карбоновые кислоты
Кислота Анилин Бромистый л-нитро-бензил Бромистый л-бромфе-нацил л-Толуидин
Адипиновая 238 106 155 241
Азелаиновая 187 44 131 200
Акриловая 104 141
Анисовая 169 132 152 186
Бензиловая 175 100 152
о-Бензоилбензойная 195 100
Бензойная 164 89 119 119
Бромуксусная 131 89 91
Валериановая 63 75 74
Ванилиновая 141
Вератровая 154
D- или £-Винная 180 163 216 *
Галловая ... 207
Гидрокоричная 96 36 104 135
Гликолевая 96 107 138 143
Глутаровая 224 69 137 218
Дифеновая 230 183
Изовалериановая ПО 68 107
Изокротоновая 102 82
Изомасляная 105 77 107
Изофталевая — 264 179
Итаконовая 190 91 117
628
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продояжение
Кислота Анилин Бромистый w-нитро* бензил Бромистый п-бром-фенацил /1-Толуидин
Камфарная 226 67 67
Каприловая (октановая) 55 66 70
Каприновая (декановая) 70 66 78
Капроновая (гексановая) 92 72 73
Коричная 151 117 145 168
Кротоновая 118 67 96 132
Лауриновая 78 76 87
Левулиновая 102 61 84 109
Лимонная 192 102 148 189
Малеиновая 187 89 168 142
Малоновая 225 88 252
49 78
Масляная 96 35 63 75
DZ--Миндальная 151 124
Миристиновая 84 . . . . . 81 93
РТ-Молочная 89 113 107
Муравьиная 50 31 140 53
о-Нитробензойная 155 112 101 . . . .
льНитробензойная 154 142 137 162
/г-Питробензойная 211 169 134 203
а-Нафтойная 163 135 . . . • .
Р Нафтойная 173
л-Оксибензойная 156 106 168 163
и-Оксибензойная 197 198 184 204
З-Окси-Р-нафтойная 249 222
Олеиновая 41 . . . • . 46 43
Пальмитиновая 89 43 84 98
Пеларгоновая 57 69 84
Пирослизевая 124 134 139 108
Пробковая 187 85 144 219
Пропионовая 106 31 59 126
Салициловая . . - 135 96 140 . . . . »-
Себациновая 200 73 147 201
Слизевая (муциновая) 310 225 . . . . »
Стеариновая . . 94 90 102
Терефталевая 337 164 225 . . .
о-Толуиловая 125 91 57 144 •
л-Толуиловая 126 87 108 118
п-Толуиловая 144 104 153 160
Уксусная 112 78 85 153
Ундекановая 71 68 80
Фенилуксусная 118 65 89 136
Феноксиуксусная 99 • • • - . 148
Фталевая 169 156 153 . . . . •
Фумаровая 314 151 198 . . . . -
о-Хлорбензойная 118 106 106 131
л-Хлорбензойная 124 107 117 . . . . •
п-Хлорбензойная 194 130 126 . . . . »
Хлоруксусная 137 . . . * « 105 162
Щавелевая 246 204 242 268
Янтарная 228 88 211 255
629
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Кетоны и хиноны
Кетон 2, 4-Д ин «трофеи илг ид разни л-Нитро-фенил-гидразин Фенилгид-разин Г пдроксил-амин солянокислый Семикарбазид солянокислый
Ацетилацетон .... 209 100 149
Ацетон 126 148 42 60 188
Ацетоннлацетон 257 115 120 137 220
Ацетофенон . . 249 184 105 59 198
Бензальацетон .... 227 166 156 115 186
Бензальацетофенон . . 244 118 73 168
Бензил 189 290 225 237 244
Бензилметилкетон . . . 156 145 87 70 190
Бензилэтилкетон . . . 135
Бензоин ... 246 106 151 206
Бензофенон 238 154 138 141 164
Бензохинон 231 152 240 243
л-Бром ацетофенон . - . 230 126 128
Бутилметилкетон 106 88 . . . . 49 122
Диацетил 315 >310 239 238 278
Дибензилкетон ... 100 120 124 146
Дибутнлкетон .... 90
Ди-втор-бутилкетон . . 84
Дипзобутилкетон . . 66 210 121
Дипзопропилкетон . . 88 34 160
Днпропилкетон .... 75 133
Диэтилкетон 156 144 69 139
Изофорон 130 68 76 191
£>-Камфора 177 217 233 118 237
Ксантон 152 161
Метилпропилкетон . . 143 117 . . . . 58 108
Метилэтилкетон . . . 111 128 146
Окись мезитила . . 203 133 142 49 156
«-Нафтохинон 138 169 184
Р Нафтохинон 278 - 206 207 247
Пинаколин 125 79 158
Пропилэтилкетон 130 ПО
Пропиофенон . . 191 147 53 176
Пулегон 147 • . . . . 119 174
Форон ....... 112 ..... 48 186
Флуоренон 284 269 151 196 . . . . в
Циклогексанон .... 162 146 77 91 166
Циклопентанон ... 146 154 55 56 205
Хлорацетон ...... 161
Хлоранил 220
<530
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Спирты
Спирт n-Би фенил изоцианат «-Нафтил изоцианат rt-Нитро-фепил-изоци-аиат 3-Н нтр©-фтале-вый ангидрид Фенилизоцианат Хлористый 3, 5-ди-нитро-бензоил Хлористый п-нитро-бензоил
Аллиловый 109 108 . 124 67 50 28
Амиловый ... 99 68 86 136 46 46
втор-Амиловый (метил-
пропилкарбинол) 76 103 62
трет-Амиловый .... 72 42 118 85
Бензгидрол 197 136 150 140 141 131
Бензоин 140 183 163 123
Бензиловый .... 156 135 157 176 78 113 85
d-Борнеол 131 138 154 153
втор-Бутилкарбинол . . 82 • . . 158 70
Бутиловый 109 72 96 147 60 62 35
втор-Бутиловый . . • 106 98 75 131 65 76 26
трет-Бутиловый . . • 101 • . - 140 142 116
Г ексиловый 98 59 103 124 41 61
Гептиловый 105 60 105 127 59 48
Гераниол 47 117 63 35
Глицерин . . 192 216 180 188
Дециловый . . 111 71 117 123 61 57 30
Диэтилкарбипол 95 48 100 . . <.
Додециловый . . 113 80 117 124 74 60 45
Нзоамиловый .... . . . 68 98 166 55 62 . . •
Изоборнеол . 130 138 129
Изобутиловый .... 100 80 183 86 88 35
Изопропилметилкарби-
НОЛ 112 69 76 . • •
Изопропиловый . . . 138 106 П6 153 88 122 по
Коричный 114 91 121 78
Миристиновый 113 51 123 71 51
Метиловый 127 124 180 153 47 109 96
Метилфенилкарбинол 106 94 95 . . .
Монометпловый эфир .
этиленгликоля . , . 113 Ill 129 51
Моноэтиловый эфир
этиленгликоля . . . 67 80 121 75
Нониловый 115 65 104 125 62 52 . •
Октадециловый .... 114 89 115 119 76 . - . 64
Октиловый НО 66 111 128 74 62 . . о
нтор-Октиловый . . 63 - 114 32 28
Нропиленгликоль . . 153 127
Пропиловый .... 129 79 115 142 51 75 35
Терпинеол 147 112 79 139
Триметиленгликоль 164 137 178 119
а-Фенилэтиловый 106 94 94 43
Р-Фенилэтиловый 99 119 135 123 79 108 62
Фурфуриловый ... 130 45 81 76
Этиленгликоль . . 176 136 156 169 140
Этпленхлоргидрин 101 51 . . .
Этиловый 119 85 129 157 52 94 56
631
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Тиолы
2, 4-Динитро- 2, 4-Динитро-
хлорб ензол хлорбензол
Бутантиол-1 ( >6 Пентантиол-1 ..... 80
Гексадекантиол-1 . . . 91 Пропантиол-1 81
Гексантиол-1 ч Пропантиол-2 95
Гептантиол-1 82 Пропен-2-тиол-1 .... 72
Декантиол-1 85 1-Тионафтол 176
Додекантиол-1 .... 89 2-Тионафтол 145
Метантиол 128 Тиофенол 121
З-Метилбутантиол-1 . . 5 9 Ундекантиол 90
2-Метилпропантиол-1 7 6 Фенилметантиол . . - 130
Нонантиол-1 86 Этантиол 115
Октантиол-1 7 8
Углеводороды ароматические
Пикри- Фтале- Пикри- Фтале-
Углеводород новая ангид- Углеводород новая ангид-
кислота рид кислота рид
Антрацен 138 а-Метилнафталин . . . 141 169
Аценафтен 161 199 Р-Метилнафталин . . . 115
а-Бензилнафталин . . 101 • • . Нафталин 150 173
Р-Бензилнафталин . . 93 Пентаметилбензол . . 131
Бензол 84 127 Пирен 227 . • •
Бутилбензол 99 Пропилбензол .... 103 126
Гексаметилбензол . . . 170 . . • Псевдокумол 97 . • •
а, а'-Динафтил .... 145 ... Тетралин 154
Р, Р'-Динафтил .... 184 1, 2, 3, 4-Тетраметил-
Дифенил 225 бензол (пренитол)' 90 • « •
Дифенилацетилен . . . 111 . . . Толуол 88 138
Дурол 95 264 Фенантрен 143 . • •
Инден 96 . . . Флуорен 84 228
о-Ксилол 88 129 Хризен 273 214
-«-Ксилол 91 126 Цимол 124
л-Ксилол 90 132 Этилбензол 96 128
Кумол (изопропилбен- а-Этилнафталин . . . 98
зол) 133 Р-Этилнафталин . . . 71
Мезитилен 97 212
632
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжена
Углеводы
Углевод Фенилгидразни Углевод Феиилгидразин
L-Арабиноза 166 £)-Ликсоза ' 163
£>А-Арабиноза .... 169 Мальтоза 206
£>-Галактоза 201 В-Манноза 205
£>А-Глицериновый аль- /.-Рамноза 182
дегид 132 Р-Рибоза 166
Глюкоза 205 Сахароза ...... 205*
D-Ксилоза 163 D-Фруктоза 205
Лактоза 200 Целлобиоза 198
* Температуре плавления
фенилгидразоиов продуктов гидролиза сахарозы.
Фенолы
фенол а-Нафтил-изоцианат Фенилизоцианат Хлористый бензоил Хлористый 3, 5-динитро-бензоил Хлоруксусная кислота
78 . .... 189
Г ваякол 118 136 57 141 116
Гидрохинон 224 205 250
Карвакрол 116 135 138 151
о-Крезол 142 144 55 152
л-Крезол 128 125 165 103
п- Крезол 146 115 70 188 136
л-Метоксифенол . . 129 87 116
п-Метоксифенол . . 217 111
а-Нафтол 152 178 56 192
f-Нафтол 157 155 107 210 154
Орцин 160 154 88 190 217
Пирогаллол 160 173 90 205 198
Пирокатехин Псевдокуменол (2, 4, 5- 169 84 152 132 195
триметилфенол) . . . Резорцин 111 164 63 117 201
81
C33-
ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ соединений
Продолжение
Фенолы а-Нафтил-изоцианат Фенилизо-циаиат Хлористый бензоил Хлористый 3, 5-дин итро-бензоил Хлоруксусная кислота
Тимол ... 160 108 33 103 148
Фенол . . 133 126 69 146 99
Флороглюцин ... 191 174 162
о-Хлорфенол 120 120 144
м-Хлорфенол 158 71 109
л-Хлорфенол 166 149 86 156
Эфиры (простые)
Эфир Пикриновая кислота Эфир Пикриновая кислота
Аннзол 81 Изоамил-р-нафтило-
Бутил-а-нафтиловый 85 ВЫЙ 94
Бутил-Р-нафтиловый 67 Изобутил-сх-нафгило-
«гор-Бутил-а-иафтило- ВЫЙ 105
ВЫЙ .... 101 Изобутил-0-нафтило-
втор-Бутил-Р-нафтило- вый • . .... 84
ВЫЙ . - 86 Изопропил-а-нафтило-
Бутилфениловый . . 112 вый . . ..... 105
Гваякол . 89 Изопропил-р-нафтило-
Дибензиловый 78 ВЫЙ . .... 95
Метил-а-нафтнловый . 130
Диметиловый резорци
на 58 Метпл-р-нафтиловый 117
.Диметпловый гицро- а-Нафтилэтиловыи 119
хинона ... 119 р-Нафтилэтиловый 101
Дифениловый . . НО Пропил-а-нафтиловый 99
Диэтиловый резорцина 58 Пропил-р-нафтнловый 81
Диэтиловый пирокате- Фенетол ....... 92
хнна ... . . . 71
Изоамил-а-иафтнло-
вый 90
£34
^WVVXXWW WXXXXXX
XXXXXXXXXXXX XXXXX XXX XX
СПЕКТРАЛЬНЫЙ АНАЛИЗ
АТОМНЫЙ ЭМИССИОННЫЙ И АБСОРБЦИОННЫЙ СПЕКТРАЛЬНЫЙ АНАЛИЗ
АНАЛИТИЧЕСКИЕ ЛИНИИ ЭЛЕМЕНТОВ, ИСПОЛЬЗУЕМЫЕ ПРИ ЭМИССИОННОМ СПЕКТРАЛЬНОМ АНАЛИЗЕ
В таблице приведены основные чувствительные линии элементов, используемые для аналитических определений. Элементы расположены в алфавитном порядке их русских названий. Изотопы водорода (дейтерий и тритий), в связи с большой величиной изотопического смещения аналитических линий, выделены как отдельные элементы и включены в общий алфавит. Рядом с названием и символом элемента указана (в скобках) величина первого ионизационного потенциала.
В первой графе даны длины волн линий в воздухе в порядке убывания с точностью до 0,01 А. Длины волн меньше 2000 А приведены для вакуума. Рядом с длиной волны указана принадлежность линии атому или иону (I — линия, испускаемая нейтральным атомом, П — линия, испускаемая однократно ионизованным атомом, III—линия, испускаемая двукратно ионизованным атомом, и т. д:). ’
Во второй графе приведена последовательность исчезновения линий в дуговом спектре (если линия испускается нейтральным атомом) или в искровом спектре (если линия испускается ионом) по мере уменьшения содержания вещества (1 — линия, исчезающая последней, 2 — предпоследней и т. д.).
В третьей графе приведена энергия возбуждения линий (с точностью до 0,1 эв), отсчитываемая от основного уровня атома нли иона.
Последние три графы содержат данные об интенсивности линий. Интенсивность в угольной дуге, искре и разряде дана в условной шкале, принятой в таблицах Гаррисона н таблицах
Зайделя, Прокофьева, Райского и Шрейдер. В этой шкале (в ряде случаев действительной для линий только данного элемента) интенсивность самых сильных линий обозначена числом 9000, самых слабых — единицей; остальным линиям условно приписано 25 промежуточных значений. Числа, вырвжающие интенсивность в разряде, заключены в скобки.
В последней графе приведены значения относительной интенсивности линий в единой энергетической шкале (по данным Меггерса, Корлнса и Скрибнера). Эти данные получены при возбуждении в дуге постоянного тока спектра прессованных медных электродов, содержащих 0,1 ат. % исследуемого элемента. Каждая исследуемая линия сравнивается с выбранной линией меди, истинная интенсивность которой определяется при помощи стандартного источника света с известным распределением энергии в спектре. Установленные таким образом значения интенсивностей пропорционвльны относительным энергиям излучения соответствующих линий.
R — самообращающаяся линия.
Более подробные сведения см.: I. А. Н. Зайдель. В. К- Прокофьев, С. М. Райский, Е. Я- Шрейдер, Таблицы спектральных линий, Физматгиз. 1962.--2. W.F.Meg-g е г s. С. Н. Corliss, В. F. Scribner, Tables of Spectral Line intensities, pt. I, II, NBS, Monograph 32. Вашингтон, 1961. — 3. G. H. Harrison. Wavelength Tables. Massachusetts Institute of Technology, Нью-Йорк, 1939.
Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий
угольная дуга искра (разряд) медная дуга угольная дуга искра (разряд) медная дуга
Азот N (14,53 эв) Азот (продолжение)
5679,56 II 2 20,7 (500) 1238,80 V 10,0 (8)
5676,02 II 4 20,6 (100) 1200,71 1 10,3 (30)
5666,64 11 3 20,6 (300) 1200,23 1 10,3 (40)
4109,98 I 2 13,7 (1000) 1199,55 1 10,3 (50)
4103,37 III 30,5 (70) 953,66 I 13,0 (15)
4099,94 I 3 13,7 (150) 953,42 I 13,0 (15)
4097,31 III 30,5 (100) ..... 952,30 1 13,0 (8)
АНАЛИТИЧЕСКИЕ ЛИНИИ ЭЛЕМЕНТОВ
8
Продолжение
СО Длина волны, А Последо ватель-ность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий Длина волны, А Последо ватель-ность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий
угольная дуга искра (разряд) медная дуга угольная дуга искра (разряд) медная дуга
Актиний Ас (6,9 эв) Водород Н (ЬЗ,60 эв)
4507,20 И 2,8 2000 2000 6562,85 I 2 12,1 (2000)
4413,09 III . . . . . 2,9 40 3090 6562,73 I 2 12,1 (1000)
4179,98 I 3,0 1000 50 4861,33 1 3 12,7 '(500)
4168,40 П 3,6 1500 2000 1215,67 I 1 10,2 (ЮО R)
4088,44 II 4,0 2000 3000
3487,59 III 2626,44 HI 3,6 4,7 40 20 4000 5000 4302,11 t I Вольфрам 3,2 IV (7.98 эв) 60 60 240
6243,36 II Алюминий А1 (5,98 эв) 4294,61 I 4074,36 I 2 3,2 3,4 50 50 50 45 450 550
3 15,1 80 490875 I 3 3,4 45 45 959
6231,76 И 15,1 35 3613,79 II 5,2 10 30 10
3961,53 I 1 3,1 3003 2000 900 3215,56 I 4,6 10 9 130
3944,03 I 2 3,1 2000 1000 450 2946,98 I 4,6 20 18 300
3092,71 I 3 4,0 1000 /? 1000/? 650 2944,40 I 4,6 30 20 300
3082,16 I 4 4,0 800 R 800 /? 320 2734,35 I 4,9 20 10 320
2816,18 II 2 4,6 10 100 2589,17 II 5,6 15 25 40
2669,17 11 1 4,6 3 100 2551,35 I 4,9 12 289
2631,55 П 15.3 60 2397,09 11 5,6 18 30 34
6054,64 1 Америций Am (6.0 эв) Гадолиний Gd (6,16 эв)
..... 2,0 9000 4341,27 11 3,3 200 125 42
3510,13 I - .... 3,5 5000 4225,86 I 3,1 150 50 450
2969,29 II 2 4,5 1000 3768,39 II 3,4 20 20 850
2832,26 II 1 4,4 5000 3646,19 II 3,6 200 150 600
15,76 Эв) 3481,35 II 4,2 150 150 220
< Аргои Аг 3422,46 II 3,9 80 100 700
8115,31 I 2 13,0 (5000) I--... 3358,61 II 3,7 100 109 440
7503,87 1 4 13.4 (/00) 3350,48 II 3,8 150 180 550
7067,22 1 3 13,3 (400) 3032,84 II 4,2 100 100 180
69.65,43 I 3 13,3 (400)
1066.66 I 2 11,6 (15) Галлий Ga (6,00 эв)
1048,22 I 1 11,8 (25) 4172,05 1 1 3,1 3,1 2000 Р 1000 /? 2000
4032,98 I 2 1000 R 500 /? 1000
Ьарий Ва (5,21 эв) 2943,64 I 3 4.3 10 20 R 950
6496,90 II . . . . с 2,5 800 R 300 1200 2874,24 I 4 4,3 10 15 R 500
6141,72 II 2,7 2000 2000 2000
5777,62 I 2 3,8 500 R 100 /? 50 Гафний Hi (6,8 эв)
5535,48 I 1 2,2 1000 R 200 R 650 4093,16 II 3,5 25 20 48
5519,05 I 3 3,8 200 60 32 3399,78 II 3,6 69 100 260
5424,55 I 4 3,8 100 J? 30 V г Z -4/3 - 80 125 95
ЦМГ' I'K" W» - — МЕЙ**?' 4.0 80 18 240
3. — — 11 - 1 - у -—-V ч-
4554 04 II 1 ,7 1000 /? 200 6500 2940,76 1 4,2 60 12 I 220
- -• 50 /? 60 150 2916,48 I 4,8 50 15
3891 79 II 4 5,7 18 25 149 2904,41 1 4,8 ь 140
3071 58 I 4,0 100 R 50 /? 18 2898,26 I 4,6 50 12 200
2335^27 It 6.0 60 R 100 R 55 2866,37 I 4,3 50 12 240
2304*24 II 6,0 60/? 80 /? 28 2820,22 II 4,8 40 100 140
2773,36 II 5,3 25 60 ПО
Бериллий Be (9,32 эв) 2641,41 II 2516,88 II 5,7 5,3 40 35 125 10U 120 100
3321,34 I 2 6,4 1000 R 300 100 2513,03 II 5,7 25 70 65
3321,09 1 3 6,4 100 15
3321.01 I 4 6,4 50 . . . . . • 60 Гелий Не (24.58 эв)
3131,07 II 3130,42 II 2 1 3,9 200 150 320
3,9 200 480 5875,62 1 3 23,1 (1000)
265078 I 2348,61 1 7,4 25 4685,75 II 51,0 (300)
1 5,3 2000/? 50 300 3888,65 1 2 23,0 (1000)
584,33 I I 21,2 (10)
3451,41 II з Бор В (8,30 Эв) 12.7 1 100 Германий Ge (7,88 эв)
2497*73 I I 5,0 500 400 480 4226,57 I 5,0 2000 50 70
2496,78 I 2 5,0 300 300 240 3269,49 I 3 4,7 300 300 ПО
3039,06 I 2 5,0 1000 1000 750
4816,71 II Бром Вг (11,84 эв) 14,2 I (300) 2754,59 I 2709,63 1 2651,58 I 2651,18 I 2592,54 I 4,7 4,7 4,7 30 30 30 20 20 20 650 850 550
4785,50 II 14,2 (400) ..... 4,9 40 20 1200
4704,86 II 14,3 (250) 4Л) 20 15 500
Ванадий V (674 эв) 1649,19 II 7,7 (120)
4408,51 I 3,1 30 20 /? 360 Гольмий Но
4389,97 I 4384,72 I 4379,24 I 4111,79 I 3185,40 I 3183,98 I 3183,41 I 3125,28 II 1 2 3,1 3,0 3,1 3,3 4,0 3,9 3,9 4,3 80 R 125 R 200 R 100 R 500 R 500 R 200 R 80 60/? 125/? 200/? 100/? 400/? 400/? 100 /? 200/? 380 550 950 700 500 700 420 200 4103,84 1 4045,44 II 3891,02 11 3810,73 I 3796,75 I 3748,17 И 3456,00 11 3,о 400 200 200 20 20 60 60 400 80 40 40 40 40 60 1000 600 1500 1000 1000 360 1800
3118,38 II 4 4,3 70 200 Р 260
3110,71 II 3102.30 II 3 2 4,3 4,4 70 70 300 Р 300/? 340 400 Дейтерий D (3900)
3093,11 II 1 4,4 100 R 400/? 500 6561,06 I 2 1 1£1
4859,99 I з 12,7 (500)
4722,37 1 Висмут Bi 4,0 (7,29 эв) 1000 100 Диспрозий Dy (~ 6,2 эв) 1300
3067 ',72 I I 4,0 - 3000 /? 2000 360» 4211,75 I 200
2989,03 I 5,6 250 100 280 4186,78 I 100 950
2938,30 I 6,1 300 300 320 4167,99 I 50 460
2897,98 1 2 5,6 500 R 500 /? 400 4103,34 II 3,1 50 320
2809*63 I 6,3 200 100 14 4077,98 II 3,1 150 600
2780*52 I 5,9 2а) 100 36 4045,99 1 150 1000
2276,58 I 5,4 100 /? 40 5 4000,48 II 3,2 400 650
сэ ю 206170 I 6,0 300 R 100 55 3531,70 11 3,5 100 '2'ЮО
АНАЛИТИЧЕСКИЕ ЛИНИИ ЭЛЕМЕНТОВ, 1| ИСПОЛЬЗУЕМЫЕ ПРИ ЭМИССИОННОМ СПЕКТРАЛЬНОМ АНАЛИЗЕ
Продолжение
41 Зак. 783
<55
Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, ЭВ Интенсивность линий Длина волны, А Последовательность исчезновения ЛИНИЙ Энергия возбуждения линий, эв Интенсивность линий
угольная дуга искра (разряд) медная дуга угольная дуга искра (разряд) медная дуга
4205,05 II
4129,73 11
3971,99 11
3930,51 И
3907,11 И
3819,65 и
2727,77 II
3820,43 I
3748,26 I
3745,90 I
3745,56 I
3737,13 I
3734.87 1
3719,94 I
3581,20 I
3440,61 I
3020,64 I
2719,02 I
2599,40 П
2483,27 I
2404,88 II
2395,62 II
2382,04 II
2802,06 II
2675,95 I
2427,95 I
4511,32 I
4101,77 I
3258,56 I
3256,09 I
3039,36 I
5464,62 II
5161,20 II
2062,38
1830,38 I
3800,12 I
3513,65 I
3437,02 I
3220,78 I
3133,32 I
2924,79 I
2849,73 I
2824,45 I
2694,23 I
2664,79 I
2639,71 I
2543,97 I
3987,99 I
3694,20 II
3289,37 II
2891,39 II
4674,85 I
4643,70 I
4374,94 II
4174,13 I
4102,38 I
3982,60 II
3774,33 II
3710,29 II
3600,73 II
3242,28 II
6438,47 I
4799,91 I
3610,51 I
3466,20 I
3403,65 I
3261,05 I
2748,58 II
2572,93 II
2312,77 II
2288,02 1
2265,02 II
2144.41 II
Европий Ей (5,64 эв)
3,0 200 7? 50 4000
3,0 100 R 50 7? 2200
3,3 1000 7? 2000
3,4 1000 7? 400/? 2800
3,4 1000 7? 500 /? 2400
3,2 500 500 3400
4,5 300 500 420
Железо Fe (7,87 эв)
4,1 800 600 500
4 3,4 500 200 140
5 3.4 150 100 60
3 3,4 500 500 240
2 3,4 1000 7? 600 340
4,2 1000 7? 600 700
1 3,3 1000 7? 700 600
4,3 1000 R 600/? 600
3,6 500 300 400
4,1 1000 7? 600/? 280
4,6 500 R 300 7? 260
4,8 1000 1000 200
5,0 500 R 5 280
3 5,2 50 100 60
2 5,2 50 100 60
1 5,2 40 7? 100 7? 60
Золото Au (9,22 эв)
1 13,4 200
2 4,6 250 7? 100 340
1 5,1 400 7? 100 200
ИидиЙ In (5,78 эв)
1 3,0 5000 7? 4000/? 1800
2 3,0 2000/? 1000 7? 1709
5 4,1 500/? 300 /? 300
3 4,1 1500/? 600 /? 1300
4 4,1 1000 7? 500/? 800
Иод J (10,45 эв)
12,3 (900)
1 12.4. . Л • * « • • , (300) • • . ' •
р - L I
*
1 (900) 1
1 1 6,8 (1000)
Иридий 1г (9 эв)
3,3 150 100 320
2 3,5 100 100 320
4,4 20 15 65
1 4,2 100 30 500
4,7 40 2 340
4,2 25 15 320
4,3 40 20 280
4,7 20 15 90
5,0 150 50 220
4,6 200 50 200
4,7 100 15 170
5,2 200 100 380
Иттербий Y1 э (6,22 эв)
3,1 1000/? 500/? 1900
3,4 500 7? 1000/? 3200
3,8 500 7? 1000 7? 2600
4,3 50 100 500
Иттрий Y (6,51 эв)
1 2,7 80 100 170
2 2,7 50 100 170
3,2 150 150 1200
3,0 100 8 200
3,1 150 30 1000
3,2 60 100 360
3,4 12 100 1200
1 3,5 80 150 1500
3,6 100 300 1300
4,0 60 100 800
Кадмий Cd (8,99 эв)
7,3 2000 1000 26
6,4 300 300 140
7,4 1000 500 360
7,4 1000 500 250
7,4 800 500 80
3,8 300 300 32
10,3 5 200
10,3 3 150 5
11,1 1 200
1 5,4 1500 /? 300/? 1500
2 5,5 25 300 ПО
1 5,8 50 200 7? 60
Калий К (4.34 эв)
7698,98 I 7664,91 I 4047,20 I 4044,14 I 2 1 4 3 1,6 1,6 3,1 3,1 5000 7? 9000 7? 400 800 200 400 200 400 900 1800 16 32
Кальций С а (6,11 эв)
4454,78 I 2 4,7 200 5 140
4434,96 I 3 4,7 150 25 65
4425,44 I 4 4,7 100 20 30
4226,73 I 1 2,9 500 7? 50/? 1100
3968,47 II 2 3,1 500 7? 500 7? 2200
3933,67 II 1 3,2 600 7? 600 /? 4200
3179,33 II 3 7,1 100 400 50
3158,87 II 4 7,1 100 300 20
Кислород О (13,61 эв) >
7775,43 I 4 10,7 ...... (100) .... Я
7774,14 I 3 10,7 (300) Sa
7771,93 I 2 10,7 (1000) S
1217,62 I 1 14,4 12,0 (100)
1031,91 VI (20) .... S х
Кобальт Со (7,86 эв) гл о
4121,32 I 3,9 1000/? 25 190 S
4118,77 I 4,1 1000 7? 120 ГВ
3995,31 I 4,0 1000 7? 20 260 Sa
3529,81 I 3 4,0 1000 7? 30 460 S
3502,28 I 4,0 2000/? 20 600 Я
3465,80 I 2 3,6 2000 7? 25 320 S
3453,50 I 1 4,0 3000 7? 200 1300 S
3443,64 I 4Д 500 7? 100 550
3412,34 I 4,2 1000 7? 100 420 Sa
3405,12 I 4,1 2000 7? 150 700 ГВ
2519,82 II 6,2 40 200 12 3
2388,92 II 5,6 10 35 70 ГВ
2378,62 II 5,6 25 50 38 я
2363,79 II 5,7 25 50 30 о
2307,86 II 5,9 25 50 24 Е0
2286,16 II 1 5,8 * 300
Кремний S1 (8,15 эв) X
3905,53 I 5,1 20 15 11 3
2881,58 I i 5,1 500 400 260 о
2528'52 I 2 4,9 400 500 200 Sa
2524,12 I 4,9 400 400 240
2516,12 I 3 4,9 500 500 360 ч-
2514,33 I 4,9 300 200 160 гв
2506,90 1393,73 I IV 4 4,9 8,9 300 200 (100) 170 ЗЕ Z
Криптон Кг (14,00 эв) я
5870,92 I 2 12,1 (3000) ..... X
5570,29 I 3 12,1 (2000) . ....
1235,82 I 1 10,0 (30) ..... S
1164,87 I 1 10,7 (20) S
Ксенон Хе (12,13 эв) г X
4671,23 I 2 11,0 (2000) о я
4624,28 I 3 11,0 . . . . . . (1000) ..... X
4500,98 I 4 11,1 ...... (500) ..... о
1469,62 I 1 8,4 ...... (25) ..... S
1295,56 I 1 9,6 (25) ..... п
3
Кюрий Ст св X
4207,66 !00° н
3903,89 800 ь
Лантан La (5,61 эв) ег я
6249.93 I 1 2,5 100 55 о
5930,68 I 2 2,1 100 24 3:
5455,15 4333,74 I 11 3 2,4 3,0 200 800 1 500 38 460 я
4204,04 II 3,6 200 25 24
4196,55 II 3,3 200 150 150 Sa
4123',23 II 4 3,3 500 500 440 X
4086,72 II 3,0 500 500 550 п
4077,35 II 3 3,3 600 400 280
3988,52 II 1 3,5 1000 800 440
3949,10 II 2 3,5 1000 800 900
3794,78 II 3,5 400 200 460
3337,49 II 4,1 800 300 200
Литий Li (5,39 эв)
6707,84 I 1 1,9 3000 7? 200 3600
6103,64 I 3 3,9 2000 7? 300 320
4602,86 I 4 4,5 800 13
3232,61 I 2 3,8 1000 7? 500 17
2 .................................................................. Продолжение
ю Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий
угольная дуга искра (разряд) медная дуга угольная дуга искра (разряд) медная дуга
Лютеций Lu (6,15 эв)
4518,57 I 2,7 300 40
3554,44 II 5,6 50 100
3507,39 II 3,5 100 100
3472,49 II 5,1 50 150
3397,05 II 5,1 50 20 7?
3359,-58 I 3,9 150 15
3281,75 I 4,0 60 5
3077,61 II 5,6 100 200
2969,82 II 5,6 30 100
2911,39 II 6,0 100 300
2894,84 II 6,0 60 200
2615,42 II 4,7 100 250
Магний Mg (7,64 эв)
5183,62 5172,70 5167,34 3838,26 2 5,1 5,1 5,1 5,9 500 200 100 ЗОЭ 300 100 50 200
3832,31 3 5,9 250 200
3829,35 4 5,9 100 150
2852,13 1 4,3 300*/? 100 R
2802,70 I 2 4,4 150 300
2795,53 II 1 4,4 150 300
Марганец Мп (7,43 эв)
4034,49 I 3 3,1 250 20
4033,07 I 2 3,1 400 R 20
4030,76 I 1 3,1 500/? 20
2801,08 I 4,4 600/? 60
2798,27 I 4,4 800 R 80
2794,82 I 4,4 1000/? 5
2605,69 II 3 4,8 100 R •500/?
2593,73 II 2 4,8 200 7? 1000 R
2576,10 II 1 4,8 300/? 2000/?
Медь Си (7,72 эв)
5218,20 1 3 6,2 700
5153,24 I 4 6,2 600
5105,54 I 5 3,8 500
3273,96 I 2 3,8 3000/? 1500 7?
3247,54 I 1 3,8 5000 7? 2000 7?
Неон Ne (21,56 эв)
340 6402,25 I 18,6 (1000)
280 5852,49 I 19,0 (2000)
480 5400,56 I 19,0 (2000)
280 743,70 I 2 16,7 (12)
240 440 735,89 I 1 16,7 (30) ....
440 500 Нептуний Np
160 4290,9 1 | 50
600 3829,3 | .... 50
420 2957,9 1 1 50
1200 Никель Ni (7,63 эв)
3619,39 I 3,8 2000 7? 150 600
400 3524,54 I 3,5 1000 7? 100 750
220 3515,05 I 3,6 1000/? 50 600
75 3492,96 I 2 3,6 1000 7? 100 500
500 3461,65 I 3,6 800 7? 50 460 j»
300 3458,47 I 3.8 800/? 50 460 Я
140 3414,77 I 1 3,6 1000 7? 50
6000 3050,82 I 4,1 1000 7? 280 Sa
600 3002,49 I 4,2 1000/? 100 320
1000 2287,08 11 1 7,3 100 500 S
2270,21 II 2 6,6 100 400 -2
2264,46 II 3 6,7 150 400 re
800 2253,86 II 4 6,8 100 300 .... О Ж
1400 2000 Ниобий Nb (6,88 эв) ге
480 4163,66 I 3,0 60 40 460 sa
650 4137,10 I 5 3,0 100 60 240 S
800 4123,81 I 4 3,0 200 125 550 Я
550 4100,92 I 3 3,1 300 200 700 S
800 4079,73 I 2 3,1 1000 400 1200 S
1200 4058,93 I 1 3,2 1000 400 1700 W
3791,21 I 3,4 80 80 360 Sa
3580,28 II 3,6 100 300 600 ге
100 3225,48 II 4,1 150 800/? 95 3
20 3194,98 II 4,2 30 300 120 гв
40 3163,40 II 4,3 15 8 140
2500 3130,78 II 4,4 100 100 180 о
5000 3094,17 II i 1000 g*.
2824,37 I 5,8 1000 300 60
2247,00 I 3 8,2 30 500 4
2192,26 I 2 8,5 25 500 2
2135,98 I 1 8,5 25 500 6
фь
* Молибден Мо (7,10 эв)
3902,96 I 3 3,2 1000/? 500/? 1800
3864* 11 I 2 3,2 lOflOT? 500/? 2800
3798’25 I 1 3,3 1000 7? 1000/? 3200
3193* 97 I 3,9 1000/? 50/? 950
3170^35 3,9 1000/? 25 7? 1100
3158 17 I 3,9 300/? 30/? 750
3132*59 4,0 1000 R 300 R 1800
2909*11 II 5 5,7 25 40 75
2890'99 I 4 5,8 30 50 160
2871,51 I 3 5,9 100 100 220
2848*24 I 2 6,0 125 200 220
2816; 15 I 1 6,1 200 300 220
Мышьяк As (9,81 Эв)
2898,71 6,6 25 R 40 20
2860,44 6,6 -50 R 50 90
2780,22 6,8 75 R 75 140
2456,53 6,4 100/? 8 36
2370,77 7,5 50 R 3 16
2369,67 7,5 40 7? 20 20
2349;84 6,6 250/? 18 85
2288,12 6,8 250 7? 5 44
2003'34 7,6 300 R 10 28
1972,62 6,3 500
1937,59 6,4 500
1890,42 6,6 500
984,92 I 12,7 100
Натрий Na (5,14 эв)
5895 92 2,1 5000/? 500/? 1000
5889’ 95 2,1 9000/? 1000 7? 2000
5688,22 4,3 300 ...... 14
5682.66 [ 4,3 80 7
3302,99 I 3,7 300/? 150 R 15
3302)32 1 3,7 600/? 300/? 30
Неодим Nd (~5,45 эв)
4303,57 II 2,9 100 40 320
4177,32 II 3,0 15 25 140
4061,09 II 3,5 40 30 280
II 3,7 80 40 220
3951Д5 II 3,3 40 15 120
3863,41 £ II 3,2 20 20 220
Олово Sn 7,34 эв)
4524,74 I 4,9 500 50 40 Я
3262',34 I 3 4,9 400 300 550 о
3175^05 I 3034,12 I 4,3 4,3 500 200 400/? 150 550 850 ег W
3009Д4 I 2 4,3 300 200 700
2863,32 I 2839,99 I 4,3 300/? 300/? 1300 гв
1 4.8 300/? 300/? 1400 S Е
Осмий Os (8,73 эв) гв
4420,47 2,8 400 7? 100 440 3 *0
4260.85 1 2,9; 4,9 200 200 440 S
3301,56 3,8 500 R 50 800
3267,95 3,8 400/? 30 320 з»
3262;29 1 4,3 500 R 50 320 S
3058,66 4,0 500 R 500 900 о
3018,04 4,1 300 R 50 460 п
2909;06 i 4,3 500 R 400 900 S
2838,63 5,0 100/? 100 480 о я
Палладий Pd (8,33 эв) я о
3634,70 3 4,2 2000/? 1000/? 2200 3
3609,55 4,4 1000/? 700/? 2200
3516,94 4,-5 1000/? 500/? 1300
342^24 2 4,6 2000/? 1000/? 1400 гв
3404,58 3242,70 1 4,5 2000/? 1000/? 2600 X
4,6 2000 600/? 1200
2854,58 I 8,3 4 500 2
2658,72 I 8,7 20 300 Sa
I 9,2 3 30 er
2498,78 2488,92 11 II 9,0 8,1 4 10 150 30 4 8 я о 3
Платина Pt (9,0 эв) >
3064,71 2997,97 1 4,0 2000 7? 300/? 320 я
4,2 1000/? 200 7? 180 Sa
2929^ 79 4,2 800 R 200 170 S
2830,30 I 4,4 1000 R 600/? 140 W
2733,96 I 4,6 1000 200 180 гв
2702; 40 I 4,7 1000 300 200
2659,’45 I 2 4,7 2000 7? 500/? 280
Плутоний Ри
3989,7 II ; loo
3907,2 II 100
Полоний Ро (8,43 Эв)
3003,21 1 5,6 2500
2558,01 1 4,9 1500
2450,11 I 5,1 1500
ср Продолжение
Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий
угольная дуга искра (разряд) медная дуга угольная дуга искра (разряд) медная дуга
Празеодим Рг (~&,57 эв) Самарий Sm (5,6 эв)
4408,84 II 2,8 125 100 1-50 4434,34 II 2 3,2 200 200 120
4225,33 11 2,9 50 40 340 4424,35 11 1 3,3 300 300 200
4222,98 II з,о 125 40 340 4390,87 II 3,0 150 150 ПО
4189,52 11 3,3 100 50 220 4236,74 11 3,6 60 50 80
4179,42 и 3.2 200 40 460 3885,29 II 3,7 400 280
4164,19 II 3,2 200 50 150 3854,20 11 200 25 200
4143,14 и 3,4 200 50 240 3634,27 11 3,6 100 ‘Ж 280
4100,75 II 3,6 200 50 260 3609,48 11 3,7 60 100 280
4062,82 и 3,5 150 50 300 3592,62 11 3,8 40 50 350
3908,43 II 3,7 100 60 320 3568,28 II 4,0 40 50 350
Прометий Рт Свинец РЬ (7,42 эв)
3998,96 1000 5608,8 и 9,6 (40)
1000 4057,82 I 1 4,4 2000 7? 300 7? 3400
3919,09 1000 3683,47 I 2 4,3 300 50 1400
3910,26 1000 3639,58 I . . . . . 4,4 300 50 550
3892 16 1000 2833,07 I 4,4 500 7? 80 950
2802,00 I 5,7 250 7? 100 1000
Протактиний Ра 2614,18 2203,51 I 11 1 7Д 200 И 50 80 5000 7? 700 9
4248,1 100 2169,99 I 5.7 1000 И 1000 7? 22
4217,2 100
3957,8 100 Селен Se (9,75 эв)
3054,6 100 4742,25 I 6 8,6 (500)
3053,5 100 4739,03 I 5 8,6 (800)
3042,0 50 4730,78 I 4 8,6 (1000)
3025,3 юо . .... 2413,52 I 6,3 (100)
3004,6 100 2062,79 I 3 6,3 (800) 15
2987,9 100 . . . . . 2039,85 I 2 6,3 (1000) 40
2980,5 100 1960,90 I 6,3 100 (100 7?) 34
2959,7 100 . . ... 844,15 VI 14.7 (W)
2940,2 100
2909',6 100 Сера S (10,36 эв)
2893,0 100 9237,49 I 6 7,9 (200)
2796,2 100 9228,11 I □ 7,9 (200)
2743,9 200 9212,91 I 4 7,9 (200) . . . . .
2743,2 100 4815,52 II 16,3 (800)
2640,3 100 4696,25 I 9 9,2 (15)
I 8 9,2 (30)
Радий ка (о,28 эв) 4694,13 I 7 9,2 (50)
4825,91 I 1 2,6 (800) 4162,70 11 20,4; 18,9 (600)
4682,28 II 9 2,7 (800) 1820,37 I 1 6,9 (50)
3814,42 11 1 3,3 (2000) 933,38 VI 13,3 (50)
Радон Rn (10,75 эв) Серебро Ag (7,57 эв)
7450,00 I 2 8,4 (600) ..... 5465,49 I 4 6,0 1000 7? 500 7? 100
7055,42 I 3 8,5 (400) 5209,07 I 3 6,0 1500 7? 1000 7? 100
(7,87 эв) 3382,89 I 2 3,7 1000 7? 700 7? 2800
Реинй Re 3280,68 I 1 3,9 2000/? 1000 7? 5500
4889,14 I 2 2,5 2000 220 2437,79 II 1 9,9 60 500 8
3464,73 I 3,6 100 4000 2246,41 II 2 10,5 25 300 . . . .
3460,47 I 3451,88 I 1 3,6 3,6 1000 100 5500 1600 Скандий Sc (6,54 эв)
3424,62 I 5,1 300 800 4314.08 II 3,5 50 150 380
Родий Rh (7,45 эв) 4246,83 4023,69 11 I 3 3,2 3,1 80 100 500 25 1400 1800
4374,80 I 3,5 1000 500 360 4020,40 I 4 3,1 50 20 1800
3700,91 I 3,5 150 150 650 3911'81 I 1 3,2 150 30 2100
3692,36 I 3,4 500 150 800 3907,48 I 2 3,2 125 25 1800
3657,99 I 3,6 500 200 700 3642,79 II 3 3,4 60 50 1200
3528,02 I ‘ 3,7 1000 150 750 3630,74 II 2 3,4 50 70 1800
3502,52 I 3,5 1000 150 500 3613,84 II 1 3,5 40 70 2500
3462,04 I . • • • • 3,9 1000 150 500 37 2,52 II 3J5 30 50 1200
3434,89 1 3396,85 I 1 3,6 3,6 1000 7? 1000 7? 200 7? 500 7? 700 480 Стронций Sr (5,69 Эв)
3323.09 I 3.9 1000 И 200 7? 360 4962,26 1 4 4,3 40 80
Ртуть Hg (10,43 эв) (2000) 4872,49 4832,08 1 I 3 2 4,3 4,3 25 200 8 30 36
5460,73 I ..... 7,7 320 4607,33 I 1 2,7 1000 7? 50 7? 650
4358,33 I . . * . . 7,7 3000 500 400 4305,45 II 2 5,9 40 34
4046,56 I ..... 7,7 200 300 180 4215*52 II 2,9 300 7? 400 3200
3663,28 I 5 8,9 500 400 24 4077,71 11 1 3,0 400 7? 500 4600
3654,83 I 4 8,8 -— (200) 30 3474,89 II 6,6 80 50 12
3650,15 I 3 8,9 200 500 280 3464*46 11 6,6 200 200 95
2536,52 1 2 4,9 2000 7? 1000 7? 1500 3.380,71 II 6.6 150 200 65
1849,50 I 1 6,7 50 7? CvobMa Sb (8,64 эв)
Рубидий Rb (4,18 ЭВ) 3267,51 I 5,8 150 150 85
7947,60 I 2 1,6 5000 7? 1500 3232*52 I 6,1 150 250 100
7800,23 I 1 1,6 9000 7? 300 3000 2877,92 I 5,4 250 150 140
4215,56 I 4 2,9 1000 7? 16 2598,06 I 6,0 200 100 603
4201,85 I 3 2,9 2000 7? 500 32 2528,52 I 6,1 300 7? 200 320
Рутений Ru (7,36 эв) 2311,47 I 5,4 150 R 50 45
4199,89 1 3,8 3000 300 700 2175,88 I 2 5,7 300 40 38
3799*35 I 3,3 3000/? 150 700 2068,33 I 1 6,0 300 R 3 55
3798,90 I 3,4 3000 7? 150 700 Таллий Tl 6,11 эв)
3728,03 I 3,3 9000 7? 300 1000 5350,46 I 1 3,3 5000 7? 2000 7? 1800
3726,93 I 3,5 5000 300 800 3775,72 I 2 3,3 3000 1000 7? 1200
3596,18 I 3 3,7 2000 7? 200 650 3529*43 I 4,5 1000 800 500
3593,03 I . . . . . 3,8 3000 7? 200 /00 3519^24 I 3 4,5 2000 7? 1000 7? 2000
3498,94 I 1 3,5 60001? 600 850 3229*75 I 4,8 2000 800 120
3436,74 I 2 3,8 3000 7? 150 650 2918,32 I 5,2 400 7? 200 7? 280
2976,58 II ..... 6,6 50 200 15 2767,87 I 4,5 400 7? 300 7? 440
2965,55 II 6,7 75 200 18
2945,66 II 6,6 100 500 20 Тантал Та (7,88 Эв)
2712,41 И 5,9 100 300 22 3406,66 I 3,6 70 18 22
О 2692,12 II 5,9 250 400 3318,84 I 4,0 125 35 90
►Р* СП 2678,76 II 5,8 300 800 75 3311,16 I i 4,4 300 70 140
АНАЛИТИЧЕСКИЕ ЛИНИИ ЭЛЕМЕНТОВ. W ИСПОЛЬЗУЕМЫЕ ПРИ ЭМИССИОННОМ СПЕКТРАЛЬНОМ АНАЛИЗЕ
Продолжение
Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий Длина волны, А Последовательность исчезновения линий Энергия возбуждения линий, эв Интенсивность линий
угольная дуга искра (разряд) медная дуга угольная дуга искра (разряд) медная дуга
3012,54 II 2850,99 I 2714,67 I 2685,11 II 2675,90 II 2656,61 I 2653,27 I 2647,47 I 2635,58 I 2769,67 1 2530,70 I 2385.76 I 2383,25 I 2142,75 I 4278,52 II 4005,57 II 3874,19 II 3848,76 II 3702,85 II 3676,35 II 3568,51 II 3561,74 11 3509,17 II 3324,40 II 4297,06 I 2647,02 II 2610,00 II 2543,24 II 5007,21 I 4999,51 I 4991,07 I 4981,73 I 4536,05 I 4535,92 I 4535,58 I 2 3 1 Гантал (про 4,8 6,2 4,6 5,1 5,2 4,7 4,9 4,7 5,0 Теллур Тс 5,8 5,5 5,8 5,8 5,8 Терби Технеций 2,9 4,7 4,8 4,9 Титан Ti 3,3 3,3 3,3 3,3 3,5 3,6 3,6 должение) 125 400 200 15 150 200 R 200 200 (9,01 эв) 120 100 120 й ТЬ 200 100 200 100 50 100 50 200 200 70 Гс (7,28 эв) 500 300 400 500 (6,82 эв) 200 200 200 300 40 40 80 100 150 8 25 200 2 15 10 30 30 60 60 100 125 200 200 200 200 50 200 200 50 300 600 800 1000 40 80 100 125 20 20 50 240 220 300 180 90 220 300 280 140 12 70 55 55 70 180 320 340 460 380 440 340 600 400 340 380 440 550 100 100 200 3859,58 II 3854,66 II 3672,58 3670,07 II 3552,17 2554,90 I 2553,25 I 2535,61 I 2533,99 I 2136,18 I 1782,87 I 1118,02 V 6902,46 I 6856,02 I 958,59 I 955,54 I 954,82 I 951,87 I 4819,46 11 4810,06 II 4794,54 II 800,70 VII ’ 5208,42 I 5206,02 I 5204,51 I 4289,73 I 4274,81 I 4254,33 I 3605,32 I 3593,48 I 3578,68 I 3017,59 I 2860,92 II 2855,67 11 2849,83 II 2843,24 II 2835,63 II 8943,50 I 8521,10 I 4593,18 I 4555,36 I 4186,60 II 4165,61 II 4137,65 II 4133,80 II 4040,76 II 4012,39 11 3952,54 II 3801,53 II 3560,80 II 6362,35 I 4810,53 I 4722,16 I 4680,14 I 3345,02 I 3302,59 I 3282,33 I 2557,96 II 2502,00 II 2138,56 I 2061,91 II 2025,51 II 4772,31 1 4739,48 I 4710,08 I 4687,80 I 3601,19 I 3572,47 II 3556,60 II 3547,68 I 3519,61 I 3496,21 II 3438,23 II 3391,98 II 3279,27 II 4007,97 I 3906,34 Н 3692,64 II 3499,11 II 3 2 1 4 3 2 4 5 6 3 2 1 5 4 3 2 I 2 1 4 3 2 3 4 3 4 1 2 1 Ц» 4 1 4 2 3 3 2 1 Урай (продс 3,2 3,5 Фосфор Р ( 7,2 7,2 7,2 7,2 7,2 7,0 11,1 Фтор F (17 14,5 14,5 13,0 13,0 13,0 13,0 Хлор Cl (1 15,9 15,9 15,9 15,5 Хром Сг ( 3,3 3,3 3,3 2,9 2,9 2,5 3,4 3,4 3,5 5,1 5,8 5,8 5,9 5,9 [езиЙ Cs (3, 1,4 1,5 2,7 2,7 Цернй Се (5 3,8 3,9 3,5 3,9 3,5 3,7 3,5 4,2 4,2 Цинк Zn (9 7,7 6,7 6,7 6,7 7,8 7,8 7,8 11 11 5,8 6,0 6,1 {рконий Zr 3,2 3,3 3,3 3,4 3,6 3,5 4,0 3,6 3,5 3,6 3,7 3,8 3,9 Эрбий Ег (( 3,4 3,6 ыжение) 20 20 8 15 8 10,48 эв) 80 ,42 эв) 3,01 эв) 5,76 Эв) 500 7? 500 7? 400 7? 3000 7? 4000 7? 5000 7? 500 7? 500 500 7? 300 7? 60 60 80 125 30 30 15 18 12 (500) (600) (700) (500) (200) (200) (100) (500) (1000) (50) (60) (70) (50) (200) (200) (250) (30) 100 200 100 800 7? 800 7? 1000 7? 400 7? 400 7? 400 7? 200 100 200 150 7? 400 7? 400 7? 360 180 11 160 13 15 38 60 10 я ь X X m п X 900 5 700 ” 440 Ь 850 « 1300 X 1700 ® 1600 ® 2100 <в 2400 Ь 360 " SO ? 100 □ 140 н 190 О 280 « X 800 S 1500 о 20 Ь 40 S << W 250 3 90 Е 140 п 190 □ 150 "О 190 X 220 200 S по S о о 12 § 140 Я loo х 40 О 140 = 90 о 20 □ W X 1000 13 > 2 Ь Г X о 75 S 120 s. 160 £ 200 > 550 Ь 340 X 340 “ 280 и 320 650 750 900 360 1100 850 700 650
4534,78 I 4533,24 I 4305,92 I 3998,64 I 3653,50 I 3642,68 I 3635,46 I 3383,76 11 3372,80 II 3361,26 I 3349,41 II 3349,04 II 3234,52 II 4391,11 II 4381,86 II 4019,14 11 3741,19 II 3601,04 II 3538,75 III 3469,93 II 3392,04 II 3180,20 II 2837,30 11 6560,41 I I 4859,56 I | 4242,15 11 4105,84 1 4094,18 I 3848,02 II 3761,92 II 3761,33 II 3462,21 II 3131,26 II 2869,23 II 6582,85 II 6578,03 II 4267,27 II 4267,02 II 2837,60 II 2836,71 II 2478,57 I 2296,89 III 1657,00 I 1548,21 IV 4241,67 II CJ 4090,14 II 2$ 3890,36 11 2 3 2 1 1 2 1 з 1 2 3 5 4 2 1 3,6 3,6 3,7 3,1 3,4 3,4 3,4 3,7 3,7 3,7 3,7 4,3 3,9 Торий Th 3,4 3,7 3,1 3,5 4,9 4,1 3,8 4,1 Трмти! 12,1 I 12,7 | Тулий Tu 3,0 3,0 3,0 3,2 3,3 3,3 3,6 4,0 Углерод С 16,3 16,3 20,9 20,9 16,3 16,3 7,7 18,2 7,5 8,0 Уран U (- 3,5 3,2 3,2 100 150 300 150 500 300 200 70 80 80 7? 100 125 100 (6,2 эв) 50 30 8 80 8 12 10 15 15 Т । (6,2 эв) 500 300 300 400 200 250 250 400 100 (11,26 эв) 400 -6,2 эв) 40 25 35 | 40 40 150 100 200 125 100 300 7? 400 7? 50 7? 600 7? 800 7? 500 7? 40 30 8 80 10 50 15 15 15 10 100 30 30 250 120 150 200 500 300 200 500 500 350 40 200 (400) 200 (3) 30 50 1 40 30 1 300 500 500 650 600 550 400 480 480 600 1000 360 550 80 90 300 90 28 95 90 75 ПО 220 700 750 750 400 500 800 700 160 10 75 160 160 89 эв) 2000 7? 5000 7? 1000 7? 50 7? 2000 7? 100 ,57 эв) 80 25 40 6 25 12 35 8 70 5 60 20 60 30 25 3 300 2 39 эв) 1000 500 400 300 400 300 300 200 800 300 800 300 500 7? 300 10 300 20 400 800 500 100 100 200 200 (6,84 эв) 100 100 60 125 400 15 60 80 15 50 200 12 100 10 100 100 250 200 300 400 50 50 5,2 эв) 35 25 20 18
совпадения спектральных линий элементов
Совпадения спектральных линий даны для наиболее употребительных аналитических линий каждого элемента. Элементы (в том числе дейтерий н тритий) расположены в алфавитном порядке их русских названий. Приводятся все известные спектральные линии, которые могут вызвать ошибку в идентификации соответствующей аналитической линии.
В первой графе приведены аналитические и мешающие линии, расположенные в порядке убывания длин воли (аналитические линии выделены жирным шрифтом) во второй — элементы, атомы и ионы которых испускают этн линии.
В третьей и четвертой графах даиа интенсивность линий в условной шкале, принятой в таблицах Гаррисона (стр. 637). Для линий, едва заметных на спектрограмме, интенсивность не указывается.
k — кант полосы: остальные обозначения те же, что и в предыдущей таблице.
Области совпадений, выбранные с учетом падения дисперсии призменных спектрографов в длинноволновой области спектра, приводятся ниже:
Длина волны аналитической линии, А Область совпадений, А
для слабых мешающих линий (интенсивность < 100) для сильных мешающих линий
(интенсивность > 100)
10 000—4 500 ±1,5 ±3,0
4 500—3 500 ± 1,0 ±2,0
3 500—3 000 ±0,5 ±1,5
3 000—2 500 ±0,3 ±1,0
2 500—2 000 . ±0,2 ±0,5
Совпадения приводятся для следующих аналитических линий.
Азот - . . Актиний . Алюминий Америций Аргон . . Барий . . Бериллий Бор . . -Бром - -Ванадий . Висмут Водород . Вольфрам Г адолиний Г аллий Г афний Гелий . - -Германий Гольмий -Дейтерий Диспрозий Европий Железо
. 4109,98
. 4413,09; 4088,44
. 3961,53; 3944,03; 3092,71
. 3510,13
. 8115,31
6141,72; 5535,48; 4934,09; 4554,04
. 3131,07; 3130,42; 2348,61
. 2497,73; 2496,78
. 4704,86
. 4379,24; 3185,40; 3183,98; 3183,41; 3093,11
. 3067,72; 2897,98
. 6562,85; 4861,33
. 4302,11; 4008,75; 2944,40
. 3768,39; 3646,19
. 4172,05; 4032,98; 2943,64
. 3399,78; 3134,72; 2866,37
. 3888,65
. 3269,49; 3039,06; 2651,18
. 3891,02; 3456,00
. 6561,06; 4859,99
. 4211,75; 4000,48; 3531,70
. 4205,05; 3819-,65
. 3737,13; 3734,87; 3719,94; 3020,64; 2599,40
Неон ....................
Нептуний ... ............
Никель .............. .
Ниобий ..................
Олово ...................
Осмий ...................
Палладий ................
Платина .................
Плутоний ................
Полоний .................
Празеодим ...............
Прометий ................
Протактиний .............
Радий ...................
Радой ...................
Рений ...................
Родий ...................
Ртуть ...................
Рубидий .................
Рутений .................
Самарий .................
Свинец ..................
Селен ...................
5400,56
4290,9; 2957,9
3524,54; 3492,96; 3414,77; 3050,82
4058,93; 3094,17
3175,05; 3034,12; 2839,99
3058,66; 2909,06
3421,24; 3404,58
3064,71; 2659,45
3907,2
2558,01
4222,98; 4179,42
3998,96
2743,9
4825,91; 3814,42
7450,00
3464,73; 3460,47
3692,36; 3434,89; 3396,85
4358,33; 2536,52
7800,23; 4201,85
3728,03; 3498,94
4424,35; 3568,28
4057,82; 2833,07
4730,78; 2039,85
Золото ......................... 2675,95; 2427,95
Индий ........................ 4511,32; 3256,09
Иод ............................ 5464,62
Иридий ......................... 3220,78; 2664,79; 2543,97
Иттербий ....................... 3694,20; 3289,37
Иттрий ......................... 4674,85; 3710,29; 3600,73
Кадмий ......................... 6438,47; 2288,02
Калий .......................... 7698,98; 7664,91; 4047,20; 4044,14
Кальций ........................ 4226,73; 3968,47; 3933,67
Кислород ....................... 7771,93
Кобальт ........................ 3453,50; 3405,12
Кремний ........................ 2881,58; 2516,12
Криптон ........................ 5870,92
Ксенон .................... 4671,23
Кюрий .......................... 4207,66
Лантан ........................ 3949,10; 3337,49
Литий .......................... 6707,84; 6103,64; 3232,61
Лютеций ........................ 2911,39; 2615,42
Магний .........................2852,13; 2802,70; 2795,53
Марганец ........................4030,76; 2794,82; 2576,10
Медь .......................... 3273,96; 3247,54
Молибден ....................... 3798,25; 3170,35
Мышьяк ........................ 2860,44; 2780,22; 2349,84; 2288,12
Натрий ......................... 5895,92; 5889,95; 3302,99; 3302,32
Неодим ......................... 4303,57; 4061,09
Сера ....................
Серебро ................
Скандий .................
Стронций ................
Сурьма ..................
Таллий ..................
Тантал ..................
Теллур ..................
Тербий ..................
Техиеций ................
Титаи ...................
Торий ...................
Тулий ...................
Углерод .................
Уран ....................
Фосфор ..................
Фтор ....................
Хлор ........'...........
Хром ....................
Цезий ...................
Церий . .................
Циик ....................
Цирконий ................
Эрбий ...................
4815,52
3382,89; 3280,68
3911,81; 3907,48; 3613,84
4607,33; 4215,52; 4077,71
2877,92; 2598,06; 2528,52
5350,46; 3519,24
3311,16; 2714,67; 2653,27
2385,76; 2383,25
3874,19; 3509,17; 3324,40
2543,24
4981,73; 3653,50; 3349,04; 3234,52
4019,14; 3538,75; 2837,30
3761,33; 3462,21
2478,57
4241,67; 3859,58; 3854,66
2553,25; 2535,61
6856,02
4794,54
4289,73: 4274,81; 4254,33; 3593,48;
3578.68; 2843,24
8943,50; 8521,10; 4555,36
4186,60; 3952,54; 3801,53
4722,16; 3345,02; 3302,59; 2138,56
3601,19; 3438,23; 3391,98
4007,97; 3906,34
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ |< ЛИНИЙ ЭЛЕМЕНТОВ
Данные о совпадениях для других аналитических линий можно найти в литературе, приведенной на стр. 637, а также в следующих книгах: 1. И. Куба, Л. К у ч е р а, Ф. П л з а к, М. Дворжак, Я- М р а з, Таблицы совпадений по атомной спектроскопии, Чехословацкая Академия наук, Прага, 1964.—2. J. Кгоопеп, D. Vader, Line Interference In Emission Spectrographic Analysis, Амстердам, I9o3.
2
<£>
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Азот N Азот N (продолжение) Азот N (продолжение)
4110,92 Рг 10 2 4110,64 Th 5 5 4110,16 Кг 11 (5)
91 Cr I 20 61 Се 2 . . . . . 11 Рг 3 1
90 Мп 80 40 60 Gd 10 15 07 Со I 5
90 Ке 1 40 57 W 7 6 07 ть 3
87 Th 8 8 54 Со I 600 05 Zr II 3 1
85 То 4 51 Sn 11 (2) 03 Се 3
84 Се II 20 47 Nd 16 10 00 Вг (10)
83 83 Nb и 8 5 8 47 44 Рг и 5 6 1 1 4109,98 N I (1000)
80 Y 1 7 2 43 Gd 5 98 Са 2 3
79 О II (40) 41 Хе II (15) 90 Се . ..... 3
77 РЬ II (5) 38 Се 35 10 90 Ег 7
76 V 1 2 2 30 Nb 1 10 89 Ец 2
70 Мо 6 5 29 Мо 3 о 88 Ва 2
66 Zr I 4 18 Sm 11 5 5 81 Fe I 120 100
1
Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) Дуга искра (разряд)
Алюминий AI (продолжение)
Азот N (продолжение) Актиний Ас (продолжение)
4109,80 La I 15 10 4089,43 Re 2
79 V I 40 20 40 Nb 5
76 W 20 20 38 W 6 5
71 Хе I (60) 37 u 4
65 Ru I 20 6 33 Tb 20 1
61 Yb 3 27 О II (60)
58 Cr 1 40 10 25 p (30)
56 Се 12 22 Fe I 10 2
54 Mg II 2 20 Br (5)
53 и 6 16 Ce 4
51 Tb 5 13 Th 3
48 La I 15 5 06 W 2 1
46 Nd 30 30 01 Ce II 6
41 Pr 15 2 01 Re 2
41 Sm II 10 10 4088,88 SI 3
34 In II (5) 87 Pr 4 2
23 Кг II _ _ . . (100) 85 Ce 15 2
20 Dy 2 (70) 85 U 6 6
19 P II a 82 Ca 2 3
17 F II . • . (100) 80 Gd 6
09 Pr 5 1 79 Eu 3
09 Er 5 79 Nd 10 2
08 Tb 2 77 W 7 7
07 Nd 15 15 75 Sm 5 1
07 Fe I .12 2 66 Mo 5 5
04 V I 3 2 64 Tb 4
4108,83 Se II (800) 58 Ce 8 1
63 Ho 100 40 58 Fe 7 2
55 Nd 5 1
Актииий Ac 50 Rh I 5 4
4415,12 Fe I 600 400 44 Os 100 3
4414,88 74 Mn Gd 150 100 60 50 4088,44 Ac II 2000 3000
63 Cd 200 36 Ru 10 1
28 p (100) 35 Pr 3 1
16 Gd 100 60 33 W 12 10
14 Zr I 5 33 Kr II (500)
11 Tl 10 30 Co I 60 ......
4413,87 Cr 25 15 25 u 25 18
86 W 5 1 20 Zr 4 . .....
80 Ce 20 1 15 Cl . ..... (6)
78 Nd 5 1 12 Ce 3
76 Pr 90 40 03 Re 1 3
5961,62 62 59 55 54 CI II Nb Zr S I Yb 500 30 (12) 10 8 (10)
1961,53 AI 1 3000 2000
52 Ru 6 4
52 u 8 1
50 Mo 5 500
39 Ce 2
3 Ag 15 5
28 Pr 10 5
21 Er 6
18 w 9
14 Fe I 25 7
14 Eu 50
06 U 6
03 Re I 30
02 Os 125 20
00 Co I 60 10
3960,98 Nb 8 5
95 Th 2 1
91 Ce II 40 8
90 Fe 3 3
87 w 10
80 и 5 8
76 Cr 40 8
73 Eu 3 . ....
70 Tb 5
60 Pr 50 25
58 Re 15
56 Ir 1 4
55 Sb II 18
3945,57 Ru 50 100
54 Gd 200 150
33 Co I 200 15
09 Hg (100)
3944,95 Co 1 5 2
92 Ce 6
90 Pr 30 12
90 Fe I 15 8
СОВПАДЕНИЯ СПЕКТРАЛЬНЫЕ
68 Ba 10 3 4087,96 Hf 6 1 80 W 7 b
68 V I 15 10 86 Eu 8 78 Ru 4 X
67 Mo 6 6 79 Rh 3 4 75 Fe I 4 1 X
64 As II 50 74 Mo 3 4 74 Sm 5 5 X
63 Tb 4 71 Gd 80 100 73 Re 30 X
56 Ne I (15) 70 Tb 8 I 69 Dy 300 150 w
51 Eu 10 69 Zr I 12 1 69 Y 3 ь
51 Re 2 65 Ho 4 2 62 U 8 2 rn
47 Gd 5 2 64 Er 20 1 62 Pr 8 3 5
44 La I 3 61 Eu 2 59 Eu 5
38 Th 6 3 57 Ce 8 2 58 Sb II 8
33 Nd 10 2 52 Rh I 3 42 Er 12 о
29 Ru 12 47 Nd 10 2 42 Nd 20 05
25 Pr 5 46 Mo 3 3 38 Ir I 20 4
24 W 5 34 Pd I 500 100 35 Re 15
20 Ne II (50) 4086,72 La II 500 500 33 F II (20)
19 Ce 35 2 29 2
16 Se (20) Алюминий Al 27 Ar (50)
14 U 15 4 3963,11 Fe I 125 50 25 Th 3 1
3962,48 Re I 100 20 Tb 6
4413,09 Ac III 40 3000 47 U 1 4 19 Ru I 10 4
04 Cd I 3 2 44 Pr 60 50 15 La II 2
04 Zr I 12 44 Ir 6 14 Pr 9 5
02 w 10 2 42 In II (5) 13 и 8 15
4412,99 Cr 5 35 Fe I 7 1 13 NI I 5
90 Th 8 5 35 Th 8 8 09 Ce II 8
87 u 4 2 34 Kr II (10) 07 Se (20)
84 Tb 2 33 W 9 9 06 Ir 2
80 77 Dy Mo 3 30 20 28 28 Ca In II 3 2 (25) 3944,03 Al 1 2000 1000
77 Pr 3 27 u 4 2 02 Rh 5 4
74 Th 12 8 24 Sm II 10 5 02 Re 15
74 Ce 3 22 Nd 30 20 01 Er 2
62 Sr I 4 19 Cr 8 1 01 Eu 8
54 Ne II (15) 19 Pr 9 3 3943,89 Ce II 40 15
53 Th io' 6 17 Zr 2 82 u 35 5
52 Tb 3 16 Nb 10 80 Pb 5
51 u 3 2 16 u 5 75 Pr 10 8
43 Ti I 15 1 16 In II (18) 69 Th 10 10
39 Kr I (6) 15 Nb 3 67 Nb 20 50
37 J II (25) 14 Sm 5 3 66 V I 50 18
33 Ce 3 12 NI I 10 66 Tb 8
31 Cd II 10 10 Gd 25 25 63 Gd 20 20
30 Ca I 5 09 Ce 15 4 62 Sm 8 3
28 Ne I (20) 04 In II (25) 61 Cr I 18 4
26 Nd 40 15 03 La 2 3 60 Eu 3
25 As 10 3961,99 Eu 10 59 Fe 2
25 Cr I 35 10 99 Mo 3 57 Хе II (10)
22 Mo 25 98 u 6 2 51 Mo 5 4
21 La II 2 2 97 Tb 3 50 u 6 10
20 W 20 10 81 Sm 25 10 50 Ce 6 1
4411,88 Mn 100 20 76 w 5 5 47 As II 3
66 Ce 6 2 37 Pr 5 3
Cn »—* 4090,42 Cd I IO0 20 66 U 1 3 35 Fe I 40 8
Продолжение
ГО Длина волны, А Элемент Интенсивность Длина волны, A Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Алюминий А1 n po должение) Америций Am (продолжение) Барий Ва (продолжение)
3943,25 Gd 40 40 3509,72 Ru I 50 2 5534,55 Gd 8
24 Sm 11 40 25 68 V . ..... 6 54 Mo 5 4
20 Ir 6 . . . . . . 67 w 8 6 45 Ar 1 . ..... (60)
19 Er 10 . ..... 67 и 10 15 29 Gd 8 . .....
14 Ce II 12 3 20 Ru 10 100 2 k La 8
09 Mo 10 10 17 Tb 200 200 5533,05 Mo 200 100
08 Eu 50 15 04 V 2 150 5532,66 Re 100 ......
06 04 Hf Mo 3 10 6 Аргон Ar 4936,42 33 Ta 100
3942,59 Hg ...... (100) 8117,16 Sm II 150 ...... Cr 200 5
44 Ее I 100 70 8116,80 V I 150 ...... 4935,83 Nl 1 150 1
24 Hg (100) 41 Co I 80 ...... 55 p . . .... 15
20 Sm 12 . . . . . . 50 Yb 200 10
3094,20 V 20 125 8115,94 Xe ...... (30) 50 Er 35 . .....
1'8 3093,99 Nb II Cu I 100 150 1000 50 8115,31 Ar 1 (5000) 46 38 Sm Pr 20 2 .....
90 Ku 30 100 8114,28 Zr I 2 . ..... 3 * Mg 4 . .....
59 Os 125 15 10 Sn I 200 ...... 22 Co I 2 ......
49 Cr 1 100 04 Co I 10 (5000) 14 Pr 2 . .....
12 Tu 30 60 8112,90 Kr I ...... 03 N I 150 (250)
11 V II 100/? 400 /? 4934,82 La II 100
11 Dv 15 5 парии ва 61 Ru 4 . . ....
06 Th 12 6 6143,20 Zr I 300 ...... 48 Kr I ...... (4)
01 U 20 20 09 Sm 30 ...... 45 Hf II 40 •50
0 Rn (18) 06 Ne I ...... (1000) 24 Sc I ...... 8
00 Cl (4) 6142,98 La I 50 ..... 15 Mn 25 s
3092,99 Ta 18 1 91 Ce 6 ...... 09 Th 4 2
99 92 Mg I Mo 125 20 10 70 53 Si I SI I 6 5 4934,09 Ba II 400 400 3
92 Nd 8 6 51 Ne I (100) 07 Er 18 tl
91 Ne II (4) 51 Nb Ю 5 07 Pr 3 . . ....
89 Nb 1 44 Nd 2 ...... 06 Co 25 ..... X
84 AI 50 R 18 38 Pr 2 ...... 02 Fe 1 40 ...... s
82 Ce 4 1 24 Те (30) 00 Nl 1 3
78 Fe 50 30 13 Хе I (2) 4933,85 Th 8 1 n
73 Na II 50 (200) 6141,89 Nd 2 84 Dy 2 3
72 Ce 4 80 U 2 82 w 12 X
72 V 100 50 76 Fe I 10 ...... 74 Re 15 ......
72 u 3 3 72 Co 2 ...... 73 Mo 12 4 "O
3092,71 Al 1 1000 7? 1000 7? 6141,72 Ba II 2000 2000 66 64 U Zr I 8 4 8 Sa er
71 Y 8 . ..... 66 Pt 3 ...... 63 Fe 2 70 X
70 Mo 20 2 51 Pr 6 • ..... 53 Ta 5 1 0“
56 Yb 30 25 In J I.. . (И. so 1 2
52 Sc II 3 4 20 Ta 3 46 Mo 4 о ta
44 Ta 50 15 08 In II (20) 38 Tb 2 3
42 Sc 3 6140,97 w 2 35 Fe 50 30 X
41 Хе II (10) 71 Lu 10 (15) 33 Mo 15 3 s
40 Ir 5 66 Br 30 Sm II 25 (30)
40 Fe 4 5 66 In II (30) 25 F II Ф
39 Cd II 10 15 58 Sm 10 24 Ar (30) Sa
32 Те (15) 46 Zr I 40 22 Nb 5 6
28 W 7 3 39 Ba 10 10 Mo 30 15
24 Hf 11 20 20 37 U 2 (20) 06 U 6 3
24 Zr 3 36 In II 4932,88 Co I d —J
22 Cl II (50) 33 Er 4 82 Eu 8 О
07 Mo 30 100 3 k Sc 10 81 Pr 2
3091,58 Fe I 300 200 28 Те (15) 79 W 12 I
Америций Am 25 Cl I (30) 4556,61 Kr II (200)
3511,04 Ta 100 35 5537,03 In II (50) 35 Ta 200 5
3510,85 Bl I 200 30 5536,83 Eu 3 12 Fe 1 150 35
60 Sm 2 74 Ta 2 4555,94 Хе II .30 (100)
54 Tb 5 4 73 Те (25) 52 Zr I 2
54 Cr 40 8 68 Zr 2 49 Ti I 125 60
52 Y I 8 1 55 In II (70) 42 Ce □ (30)
51 U 10 44 Nd 2 39 Ne 1
46 Zr II 12 5 40 Br I (20) 38 Eu 4 4
45 Fe I 15 8 4 k La 10 36 Cs 1 2000 R 100
43 Ce 3 30 Br 25 (50) 33 w 7 1
40 Pr 5 2 27 Tb 30 Y I 2 2
35 Zr I 2 26 Er 8 30 Cr 15
34 u 6 20 Sm 2 27 Те 25 (30)
34 NI I 900/? 50 13 Eu 30 26 Tu 50
31 Ru 6 01 к II (Ю) 24 Dv 4
29 Ce 5 0 с II 5 14 Nd 15
27 V 10 5535,94 In II (70) 13 Zr I 15
26 Nb 15 200 80 U 6 2 10 U 20 40
22 Ce 8 1 67 La II 50 100 09 Cr 15 50
13 Sm 2 1 50 Sm 3 08 Tl I 12 2
3510,13 Am I 5000 5535,48 Ba 1 1000 7? 200 7? 07 03 Th Cr 11 3 40
10 Tb 50 8 48 Nd 3 4554,99 Gd 6 2
09 Dy 2 1 41 Fe 50 97 Nd •_> 1
07 Eu 4 39 N II (70) 83 Cr 25 2
03 w 10 10 38 V I 2 2 82 Ne I (40)
3509,99 La II 10 10 38 Tb 15 80 P II (ЮО)
99 Mo 1 3 27 Nd 2 ...... 79 Pr 4 1
93 Ce 8 24 Cc 15 78 Ir 4
87 Fe I 15 4 18 Pr 10 2 68 W 4
86 U 2 16 Gd 8 65 Tu 5
84 Tl II 8 20 04 Rh 80 1 59 Pt 10 5
84 Co I 400/? 40 5534,98 Cu II 3 59 Ca 2
80 Sm 3 1 86 Fe II 10 56 Ne I (-’)
8 Rn (5) 81 Sr 20 15 56 Ce 6 200
78 Ar (IS) 66 Fe I 20 51 Ru 1 1000 R
О Си 76 73 Tb Cc 8 12 58 Tb 10 50 Pr 2
Продолжение
Длниа волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Барий Ва (продолжение) Бериллий Be [продолжение) Бром Вг (продолжение)
4554,46 44 Y I Sm П 3 60 6 3130,57 57 56 56 Ba I Fe II Cr U 2 4 1 3 4 12 15 4706,23 22 20 Pr Th Mo 6 5 4 4 4
42 33 32 23 Ne I Се Аг I Dy 2 2 (10) (15) 52 48 46 3130,42 Ce SI W Be II 5 10 200 5 8 200 17 16 14 10 09 w V I Nb Cr Ta 15 15 50 30 200 i 12 50 1 2
4554,04 Ba II 1000/? 200 40 Хе II (2) 06 Mo 25 25
04 Се 35 38 p II (30) 4705,98 Eu 4
03 Мо 1 4 38 Ho 4 94 Os 15 1
4553,97 Zr II 4 12 38 TI 2 1 81 Er 6
95 Сг 20 3 37 и 3 77 Gd 25
86 и 4 1 33 Ce 30 1 76 Th 10 6
85 Th 3 2 29 Ta 15 1 73 Dy 3
84 Nb 5 8 28 Ir 4 58 Ce 3
80 Mo 20 20 28 Fe 5 4 57 Pr 5
78 Hf 10 27 V II 50 200 50 Nl I 2
76 Ce 2 25 La II 3 4 48 Tb 2
7 k Pb 6 24 Sm 5 46 Fe 2
€9 Ta 200 2 20 Ce 15 44 Tu 3 (2)
66 W 6 1 18 TI I 2 44 Кг II
56 Yb 20 60 16 Dy 4 2 35 BI II 50
50 Mo 25 16 w 5 4 32 О II (300)
50 Pr 4 12 Se (8) 30 Er 4 n
42 Ce 2 06 Zr I 3 16 Ru I 5 о co
42 TI I 6 06 Mo 20 09 V I 15 12 3
33 Co I 25 01 AS 25 15 03 Re 40
32 Mo 12 4 00 Os 30 8 00 Sm II 3 fa
31 Mn 12 3129,96 Gd 2 1 4704,96 Fe 10 1 m
з 3 95 Sm 5 90 Tb 2 ce
27 Ca 4 95 Ta 50 8 87 Yb 4 s
26 24 Pr Hf 5 5 93 91 Y II Th 8 10 50 8 4704,86 Br II (250) О
22 Mo 12 6 33 Fe I 100 60 67 Хе II (8) □
18 NI I 15 31 Nl I 125 63 Hg II 30 200 (200) ГП X
16 13 Ne II 5 (50) 3128,95 Re I 100 60 60 Eu Cu I 50
1 k C 2348,80 Re 9 58 Tb 2 • ••••• §
06 Ce 8 75 Nb 3 49 Er 2 ib er
05 V I 20 15 74 Те (5) 48 Sb 11 z
04 01 Th Zr I 3 3 74 Nl 1 ib 1 48 u 3 200 3 г
4552,89 Pd I 2
89 Hgll (30)
83 Pr 5
80 Mo 5 5
77 Кг II (3)
66 Sm II 80 40
64 Ca 3
64 Se II (2)
60 Ne I (30)
55 Fe 10 1
46 Ti 150 50
38 S II (200)
4551,95 Ta 400 8
30 Os 150 8
Бериллий Be
3132,59 Mo 1000 7? 300/?
06 Cr II 25 125
3131,83 Hg I 200 100
55 Hg I 400 300
53 и 4 2
50 Ce 2
48 Os 20 10
46 Fc 2
35 Tb 8 3
33 и 8 6
26 Tu 400 500
22 Ta 5 25
21 Cr 20 6
20 Mo 5
16 Os 125 30
11 Zr I 7
3131,07 Be II 200 150
07 Er 3
07 Th 12 10
3130,99 Ho 6 6
92 Ce 5
•87 Ce 30 2
81 Gd 3 1
80 Ar I (20)
80 TI II 25 100
79 Rh I 60 2
79 Nb 100 100
74 Eu 100 100
73 u 10 6
71 S (15)
7 Cs 0)
58 Ir 3
58 Ta 100 3-5
CD
СЛ
Ch
61 Os 3 ......
2348,61 Be I 2000 7? 50
60 Lu 2
59 Ta 12
59 Zr 15 1
58 Mo 9
56 J (12)
56 w 2
55 Pt II 3 20
46 Nd 20
46 Cc 2
Бор В •
2497,92 Pt 3
86 Mo 20 15
85 Al II (8)
82 Fe II 15 50
82 Ni II 5
78 Mn 3
77 Hg 3
2497,73 В 1 500 400
72 Sn 8
72 Fe II 1 3
68 Ru 50 1
66 Ca 5
66 V I 4
59 Th 3 12
58 Mo 30
33 p II (100)
2496,97 Nb 1 3
96 Ta 2
91 Ce 2
9 Cs (2)
88 N II (25)
85 Ru 9
78 Hg 3
2496,78 В 1 3C0 300
77 Sn 10
70 Re 20
69 Pd II 100
64 W II 10 20
64 Ta 29
Бром Br
4707,82 As II 200
28 Ее I 100 12
26 Mo 125 125
4706,31 Кг II (3)
3 k Y 4
27 Tb 3
40 39 Ne I Co I 3 (1500) ь s
29 Gd 4 a
15 Tb 2 s
08 Rh I 10 4 X
05 Ir 12 Q)
01 Ce 8 Ь
00 Pr 4 m
4703,99 Th 3 1 S
98 Sr I 2 m
93 Nb 3 5
89 Eu 8 о
86 Nd 15 co
81 Ni I 200
78 Ce 2
77 Er 3
77 Re 2
61 Hf II 4 12
58 Nd 20
47 Dy 5 2
36 Ar II (10)
28 La II 200 300
4702,53 Ne I (150)
32 Gd 50 100
32 Ar I (1200)
Ванадий V
4380,64 Gd 100 125
23 Dy 5 2
17 Eu 3
12 w 8 2
11 Kr (2)
07 Co I 5 3
06 Ce 30 2
4379,92 Rh I 60 25
91 Cl I (15)
88 Nd 4
84 Ce 2
81 Ец 5 2
78 Cr I 15 2
78 Br (6)
78 Zr II 10 8
74 Ar (80)
7 ft La 20
64 U 2 2
6 feLa 10
60 Tb 3
56 Pd I 6 2
55 О (-15)
52 Nb 2 3
52 Gd 2
50 Ne II (100)
44 Хе II (5)
41 Dy 2
Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент 1 Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Ванадий V (продолжение) Ванадий V (продолжение) Висмут Bi (продолжение)
4379,4 Bill 25 20 3183,57 Fe 5 3 3067,30 Хе 11 (20)
34 Рг 100 2 55 Th 8 6 25 и
32 Y 1 4 52 Се 40 24 Fe I 300 300
26 ТЬ 4 51 W 9 6 3066,38 V I 400 7? 125/?
25 Ag 5 1 41 Er 15 4
4379,24 V I 200/? 200/? 3183,41 V 1 200 100 7? 2898,36 27 Fe Be 1 100 20 30
17 Hf 10 4 32 Cr 6 150 27 Th 4 3
15 Но 3 ...... 32 Мо 6 26 Hf I so 12
11 Nd 2 1 30 4 2 26 Zr 4
08 Се 3 ...... 29 ть 15 3 25 w 8 3
4373,97 Br . ..... W 25 Nl 1 25 22 Ru 60
84 Pr 3 ...... 20 Dy 7 3 20 Tb 10
82 Та 40 2 16 Ba I 5 19 Be 1 15
«2 Се 4 И Ее II 7 50 09 W 11 3
/0 Tb 9 09 Ce 5 06 Fe 2
64 Pr 3 04 Ni I 5 01 U 6 6
58 Се а . . . ... 03 Mo 10 2897,99 Mn 15
57 53 Gd и 40 6 2 3182,98 87 Fe Re 1 125 100 70 2897,93 Bl I 5OO7? 500 7?
44 W 25 12 57 Os 100 15 90 V 25
43 Cu II 2 87 Pt 1 400 15
41 41 34 32 26 о п Се Ег Сг Рг 3 9 5 15 (10) 1 3 3094,18 3093,99 90 59 No 11 Сц I Ru Os 100 150 30 125 юоо 50 100 15 85 83 81 80 76 Fe J Nb Mn La 11 2 15 15 2 (20) 150 5 8
23 Sm 11 100 100 49 Cr 1 100 72 Ru 60 СЙ
20 Cu I 200 30 48 Ca Ru Yb 2 3 70 3 25 3
4377,76 3185,89 Мо 1г I 5 2 200 46 45 44 2 4 • 3 2 67 26 Y II Fe II 3 12 200 )= гс>
84 Sm 3 1 41 Ar 11 (50) Водород H S
71 Мо 8 3 37 u 4 3 6564,26 Ta 20 •S2
71 и 12 10 36 Fe 70 40 05 Sb 6
59 Rh I 100 20 34 Ce II 12 6563,95 Те (50) 3
56 Re 1 200 32 Zr I 3 93 Nd 4 СП
56 Ей 10 10 3 Au 11 5 70 Ta 2 Ж
55 Cd II (15) 28 SI 6 66 Gd 6
51 Tl II (6) 24 Ce 6 -52 Sm 20
51 Се 2 12 Tu 30 60 42 Co I 200 5 ь
5 48 Rn Ти 20 (10) 40 3093,11 V II 100 7? 400/? 24 22 Sn W 2 50 1 сг 3
44 Ru I 12 11 Dy _ 15 5, J Д9 Ul|- XeJ l £
41 40 Ce U 4 4
3185,40 V I 500/? 400/?
зз Os 150 12
32 Fe II 25
28 SI 3
25 Er 15 2
20 w 6 5
14 и 4 3
10 Mo 20 8
09 Ag 4
08 Zr I 2
05 W 11 1 10
3184,90 Th 10 10
90 Ru I 4
90 Fe 1 200 150
75 Re I 150
42 W 10 9
41 Ba 3
41 LI 6 2
40 Mo 3 1
37 Nl 1 150 3
34 Cr 30
34 Os 10 5
33 Ce 2
22 Nb 5 150
22 Eu 10
21 Ce II 20
20 Dy 9 1
19 Sm 3
15 AgU 20
13 Ho 4
11 Fe 2
09 Tl 11 3 10
04 w 10 7
02 Tl 5 1U
3183,99 Ce 4
3183,93 V 1 500/? 400/?
98 W II 1 6
97 Til 12 5
97 Tl 12 2
95 Ba 1 2
92 Sm 60 40
88 Tb 15 3
85 Ho 6 6
84 Ce 2
81 Eu 2 8
79 Th 8 8
73 Lu 3 6
64 Tb 15 3
58 J (10)
06 Th 12 6 6562,94 Sm 50
01 и 20 20 86 Hi 11 i 10
0 00 Rn Cl (IS) 0) 6562,85 H 1 (2000)
3092,99 Та 18 1 73 H I (1000)
99 Mg I 125 20 64 Sm 2
92 Мо 10 6561,60 Ta 40
92 Nd 8 6 06 D I (3000)
91 Ne II (4) 6560,84 Rb 150
89 Nb 1 -5 13 He II (1001
84 Al 50/? 18 6559,81 Br 1 (150)
82 Ce 4 1
78 Fe 50 30 4864,10 Те (800)
73 Na II 50 (200) 4863,08 Ne I (100)
72 Ce 4 4862,73 Pr 4
72 V 100 50 61 V 1 15 12
72 и 5 3 61 Gd 100 2
71 Al I 1000 1000 54 Хе II (400)
71 Y 8 53 Ta 15
70 Mo 20 2 39 Pt 3 . ...
07 Mo 30 100 31 Pr 3
3091,58 Fe I 300 200 31 J I (700)
27 Ra 1 (4)
Висмут Bi 13 J (25)
3068,9 Rn (100) 1 Kr (2)
18 Fe I 150 ISO 08 Sm 3
06 Nb 10 05 Mn 40 5
05 . J (5) 00 Dy 2
02 Zr II 2 2 4861,96 Pr 5 . . ...»
00 Mo 30 1 87 Ru 15 . . . . . .
3067,94 Fe 15 10 84 Cr 125 8
94 Ir 2 84 Kr I (2)
90 Ce 6 80 Gd 100
87 W 3 12 77 Nd 2
83 Lu 3 73 Ce 10
8 Cs (4) 59 Er 1
(8 Eu 7 49 Hf 3 2
76 U 8 6 38 Rh 4
76 73 Sn Th 10 12 15 20 4881,33 H 1 (500)
73 In 3 22 Th 8
21 Tb 2
3067,72 Bi 1 3000 R 2000 20 Cr 1 80
67 Sm 15 15 05 Sm 4
67 Eu. 8 04 Ta 3 1
64 Mo 10 50 02 U 10 10
57 w и 3 12 4860,93 о 11 (20)
53 Nb 15 91 La II 100 100
44 Ce 4 89 W 10
41 Hf 30 10 86 Eu 12
41 W II 2 5 76 Mo 10 8
39 Re I 60 70 Sm 2 .... •
37 Yb 3 67 Dy 3 . . .
30 Rb 80 1 56 Mo 5 4
Продолжение
Длина волны, А Элемент Иитенсгвность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Водород Н (продолжение) Вольфрам W (продолжение) Гадолиний Gd (продолжение)
4860,44 Ru 6 Вг (20) 3768,81 Sm 3
35 N П . . . . . . (5) 75 Nd 12 10 80 и 15 12
16 05 Ru Dy 4 2 4008,75 WI 45 45 79 76 Ег Се 5 8 2
05 Mo 25 20 150 50 74 4 5
04 Br ...... (12) 71 Рг 73 Cr I 35 25
4859,99 95 D I Pr 10 (500) 70 67 Мо 1 20 70 68 р II 1г I 60 (50) 10
88 Tb 2 66 Се 8 66 Се 2 1
85 Sm 5 49 Dy 5 (10) 62 4 4
85 Y I 50 5 48 Kr II 53 и 2 5
75 Fe I 150 40 46 HI II 5 8 51 8
41 4303,59 Ra II Вольф Pr рам W 100 (100) 60 45 42 33 33 28 Се * Nd Gd I Sm Nb 6 5 15 8 5 3 10 10 10 46 45 44 41 Gd W Th и 10 20 8 1 18 8 2
57 Nd 100 40 27 Ru I 20 20 3768,39 Gd II 20 20
03 Dy 8 22 Th 10 8
4302,98 TI I 10 18 Er 8 1 39 Pt II 10
98 Ta 125 40 17 V II 2 10 39 Pr 2 2
94 Tb 10 09 Sm II 10 3 35 Tb 8 8
91 Nb 2 10 08 Kr II (25) 31 10
89 Zr I 100 1 06 Tl I 50 7 30 Ce 4 8
77 Cr 40 2 05 Mo 4 5 25 Hf 4 1
72 Dy 10 05 Ir I 12 2 25 10
7 к Sr 4 02 Mn 15 5 25 Re 6
65 Ce 10 4007,98 Eu 6 24 Cr I 60 60
57 Dy 2 97 Er 35 7 23 Eu 18
53 u 2 96 Ho 4 3 22 Er 10
53 Ca I 50 25 94 Co I 3 16 Mn 10 10
45 Kr (10) 93 U 8 3 14 Os 80 15
43 Pt 2 90 Se II (150) 13 CI II (18)
29 Y I 30 8 78 S II (5) 10 Cd II 2
26 As 5 78 Pr 8 3 03 Fe I 15 8
19 Fe I 50 10 77 Dy 12 2 00 Ce 3
15 V I 8 7 3767,93 3 2
14 Bl II 2 50 2945,10 He I (100) 92 s (4)
4302,11 WI 60 60 06 2944,87 Fe Tb 100 5 30 90 90 Th Ce 20 3 15
10 Pr 60 5 82 Mo 2 50 88 Zr II 3 4
09 U 5 4 77 Ce 4 85 w 10 8
4301,93 Ti II 25 50 76 V I 2 84 и 2
93 Mo 10 10 75 Pt 1 15 2 76 Er n-— 2
СОВПАДЕНИЯ СПЕКТРАЛЬНЫЕ
1 2 8 (2) 300 1 20 1
72 62 60 60 59 58 56 54 54 и Но Ег Ir Zr I Pr Eu Ca Tb 6 3 25 200 4 20 5 2 2 1 2 10 30 1 5 72 71 64 64 61 57 56 51 50 Eu Hf Nb U Xe V II Dy Fe Ho 3 20 4 2 50 2 2 10 76 76 73 73 72 70 64 60 57 Nd Sm Mo S V Mn Dy Eu CI II Ce 15 । 15 4 2 12 15 15 2 20 10 25 (8) 10 12 5 5 (30) 4 S a s s Q) Ь m S 3
53 63 Ce Kr 11 10 (40) 46 40 Fe II 70 600 50 43 Tb Cr 75 20 8 10 о
47 28 26 u Sm Mo 15 7 20 15 1 20 2944,40 35 W 1 Ce 30 18 20 43 43 42 19 Ca I Nb 2 3 7 4 10 S3
26 25 Er Nd 4 15 8 32 29 Re Bl 5 4 Fe 1 500 400
21 18 18 17 15 09 4300,56 51 49 Nb Tb Cr V II Ru Tl I Tl I Cr Kr 1 ‘ 5 100 5 150 125 100 2 25 10 50 20 20 (200) 21 20 20 19 18 18 1 07 2943,99 99 Mo Zr II CI U Ru Ga Cs Er Mo Ce 25 2 8 12 10 12 6 2 3 (4) 12 15 (2) 3 3647,84 77 66 15 10 09 06 03 3646,96 Fe I Lu Co I W Ir I Co I Tb Eu Ce 500 100 100 4 3 30 30 2 15 400 5 8 3 4 8 5
4009,75 72 71 66 58 Sr Fe I Nb Tl I Al II 120 5 60 2 100 10 25 (4) 96 92 91 91 90 w Ru Nl I Mn U 5 50 50 2 10 4’ 5 20 2 25 89 89 88 87 85 Zr Th Pr Mo Dy u 5 4 3 4 4 4 2 5 10
55 Ce 2 1 85 V 20
55 64 Th Tb 3 10 1 Гадолиний Gd 78 75 Er 5 20 5
41 39 39 37 37 27 и S II Zr Nd Mo Tb 4 3 8 20 2 8 (3) 5 25 3770,37 3769,64 36 34 32 Ar I Nd Ce Nd Eu 100 2 12 12 (400) 20 6 5 66 65 63 60 52 49 Eu Ce Re $H 10 10 10 5 10 2 3 2 35 6
27 He I (10) 31 Re 6 Tb 8 3
24 21 19 17 16 Pr Gd Tb U Er 5 50 5 8 15 2 2 15 1 25 21 15 13 07 Ce W Nb Cl II V I Ce II 12 10 30 id 15 (20) 10 32 30 22 20 Rb II Pr U TI I 50* 10 70 (10) 15 25
07 Th 10 8 04 6 3646,19 Gd II 200 ISO
06 4008,97 93 92 92 87 87 Ce Ir I Tl I Gd U Fe Eu 12 5 80 20 8 5 8 35 3 1 2 0 00 3768,99 98 98 93 81 Eu Ir Cr La II W Pr He I 4 2 so 2 2 7 30 2 16 11 05 03 01 0 Cr Ru Ca U Sm k Sr 18 2 2 4 8 8 2 4
О Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент И нтенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) луга искра (разряд)
Гад 3645,97 олиний Gd Pd I (продолже 15 ние) Галлий Ga (продолжение) Галлий Ga (продолжение)
94 93 90 90 89 Er Nb V Ho Sm И 15 1 4 2 5 20 4 2 4034,49 4033.91 91 90 88 Мп I W Ti I Nd Hf II 250 R 40 10 5 20 10 3 4 8 2943.49 48 48 41 40 Sm Со I Ru I Хс и 8 30 30 6 3 (2)
86 Dy 6* 4 86 Pr 50 35 38 Мо 1 25
82 79 78 Fe Sm Nd 80 5 8 60 1 83 79 76 Ar Cc Ir 6 100 (30) 25 38 36 15 Re I Tu Со II 15 6 15 100
71 66 Ce Pr 2 30 20 73 69 U Eu 12 8 12 2942,90 Ar II (100)
63 Gd 20 20 68 P 11 (15)
63 60 Nd Tb 15 8 6 67 64 Dy N 15 4 (2) Гафний Hf
60 W II 4 20 63 Mo 6 6 3402,51 Os I 200
60 V 1 63 Mn 5 5 26 Fc 150 150
59 Re 6 58 Zr 3 3401,86 Os I 200 20
59 Mo 3 3 54 Sb 70 60 3400,25 Ce 8
58 Cr 4 3 50 Nd 10 21 Hf 15 2
54 Pr 20 8 49 Gd 10 18 Rb (5)
49 Ее I 15 7 43 U 12 10 16 Tl I 10 1
46 u 1 2 37 Ce 2 12 Os 20 10
45 43 Ce II Eu 10 2 31 26. Re I Cr I 40 30 8 11 10 Na II Mo 1 (5) 10
42 Dy 300 100 24 Pr 3 2 07 Xc I (2)
41 La II 100 60 20 Nb 5 5 00 Cs I 30
41 Ho 8 8 19 Sr I 6 3399,99 Gd 15 15
40 Y 4 4 07 Mn 1 400 7? 20 97 Ru I 4
40 Er 25 12 07 Cr 15 2 97 Tb 15 3
39 Sm 11 8 6 07 Ta 100 10 96 Nb 10 2
38 Tb 50 15 07 In 4 96 u 6 3
36 Nb 5 5 04 Tb 125 5 95 Tu 50 40
31 Sc II 50 50 4032,98 93 Sb и 1 2
30 Ir 25 2 Ga I 1000 R 500/? 84 Sm 10 3
29 Sm II 9 7 98 Sm 20 8 81 U 5 2
23 Cu 1 20 5 97 Pr 15 10
23 Co II 5 1 97 Ar I (20) 3399,78 Hf II 60 100
22 Fe 9 89 Se (Ю) 71 Nb 15 15
20 Co I 60 3 86 V I 2 1 70 Rn I 500 60
3644,41 Ca I 200 15 85 Br (20) 69 Sm 5 1
4173,23 j Галлий Ga 85 81 Dy S II 8 (125) 67 60 Cd II Er 5 5
Os 1 100 j 6 75 Ce 2 JJ 60
4172,97 89 и 10 2 15 2 70 63 Tb Tl I 35 1 41 U Nd 10 I 4
83 Kr I (3) 63 Fe I 80 15 40 Nb 20 30
82 ТЬ 10 63 Tb 4 38 Ru 60 3
80 Ей 12 3 55 Ce 3 35 Zr II 100 40
79 Р II (5) 54 Th 10 8 34 Dy , 3
77 35 15 52 Nb 30 50 34 Fe I 200 200
75 Мо 3 2 52 Ru 10 5 30 Re I 200
75 Fe I 60 10 51 Nd 2
65 Fe I 3 1 50 Mo 8 8 3135,89 Ta 35 100
62 Со 2 49 Pr 20 12 37 Dy 100 50
61 Ti I 5 48 Dy 20 12 36 Fc II 1 100
59 Tb 12 2 48 Er 9 19 V I 8
57 Os 60 3 47 Zr 5 18 Ce 15
56 Ir I 150 12 47 Fe 1 4 1 17 Y II 10 18
51 Kr II (20) 38 W 6 7 10 Kr II (8)
32 La I 8 38 Sr I 20 07 TI 1 2
27 Pr 75 40 29 u 2 2 07 Re I 15
23 Ho 2 28 Tb 30 04 Gd 5 2
23 Yb 2 2 27 Hf 5 2 02 8
18 U 3 3 22 Sc 11 (8) 0 Mg 4 2
16 Cc II 18 1 21 Ir 10 3134,93 V 30 150
13 Fe 80 50 20 Ru 1 20 20 92 10
4172,05 Ga 1 2000/? 1000/? 19 15 CI Re 10 (4) 90 90 Rb Nd 40 (10) 30
4171,99 Dy 15 09 J (10) 80 Ru I 10 100
96 Cc о 09 Th 3 8 (4)
92 Dy 4 2 4031,69 La II 400 300 79 О II (100)
90 TI II 15 70 63 Tc 300 200
90 Mo 25 3134,72 Hf If 80 125
85 Cu II 5 2944,57 V II 50 300/? Eu
82 Pr 75 40 40 Fe II 70 600 r-
80 Tb 8 2943,92 Ru 50 5
77 Cc 2 3 91 Ni I 50 R 20 65 Cc * • • • •
71 Gd ’i 1 91 Mn 2 2
71 70 68 63 59 57 56 55 48 45 39 35 30 Dr Fe Cr N U Sc I J I Sm II Zr I Mo Ce II Th V I 15 8 70 30 3 7 20 10 18 10 15 2 8 (5) 30 (8) 12 3 12 7 90 89 87 83 79 77 72 67 2943,64 64 63 62 u Cd II Ir V I Sm Ta Ir Cc Ga I V Ir Sn II 10 4 7 8 10 3 8 10 3 25 (5) 5 2 5 20/? 4 2 43 42 40 40 34 32 31 26 11 11 3133,89 33 Ca Th Se II Fe Ho Nb 0 II Cr Tb Fc I N[ I Tu V II 10 3 6 2 3 8 200 1000 /? 200 50 12 (70) 1 4 15 (10) 50 8 125 150 200 200/?
18 W 25 12 57 Fe 12 6
13 La I 8 55 La II 2 6 2866,74 Cr II 80 125
07 Mo 15 10 5 Pa 100 67 Nb 3 3
4170,45 Po I 1200 50 Nd 3 5 66 Ta 3 1
О
о ♦—
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ |( ЛИНИЙ ЭЛЕМЕНТОВ
8 - to ..-mrnr, т.п, .т - — - „ , ~ . .. .. Продолжение
Длина волны, A Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд* дуга искра (разряд)
Г 2866,64 63 62 59 57 46 45 44 44 42 42 2866,37 37 36 32 28 27 26 25 18 16 14 14 08 08 08 3890,32 18 3889,78 58 55 51 48 47 46 45 45 42 42 37 афний Hf (/ Ru 1 Fe I W II V I Ca In II LI Tb Th u V I Hf f W II Er Cs SI Dv Mb Ru Yb U Ta P Mo Ru Pt Гели Zr I V I In II Ir Ce Eu Ce II Au I Ta Mn Zr Pr U w гродолжени 60 125 3 25 3 6 3 35 50 .10 3 2 2 6 5 1 й Не 150 100 2 3 10 4 3 25 2 10 1 е) 25 80 9 6 7 (18) 2 10 3 4 12 10 (8) (7) 4 30 3 6 (20) 3 30 3 6 30 (100) 3 5 8 40 50 6 5 5 3887,67 67 3886,79 3269,96 90 89 86 82 78 77 76 66 66 63 53 3269,49 47 46 41 41 39 24 23 21 14 13 12 12 10 05 04 01 00 3268,24 3040,90 85 67 43 Гелий Не (л 1 Мо ТЬ 1 Cr I Герма! Fe Sc I Os Ne II Ag II Fe II Cr Eu Zr I W Dy Ge I Th U Eu Er Sm Fe U Os Ta Ce Dy Nb Ca I Ar II Re U Tu Fe I Os Cr I Sb II Fe I родолжени 1 * 125 кий Ge 5 30 8 10 4 12 10 2 300 10 2 2 18 20 2 200 70 10 20 2 10 30 3 40 125 200 500/? 400 ?) 1 3 3 125 3 12 2 (7) 10 6 4 35 1 12 1 300 10 2 1 4 15 6 1 20 7 3 10 2 (5) 2 150 100 100 200 (400) Ге1 2650,99 86 47 4 3892,03 3891,98 97 94 93 93 88 85 82 78 77 76 76 70 68 68 63 55 51 48 41 40 40 38 34 30 25 22 18 12 09 08 06 3891,02 3890,99 эмашй Ое Мп Pt I Be I Pb Голы Zr I Dy Ar Sm Cr I Fe Mo Dy U Ba II Ce Th Tb Pr U Co I Br II Si Nd Eu Ru Ar Re Zr I Eu Nb W V I Sm II V U Y Th Но II Ce II (продолжен 700 100 100 гиЙ Но 10 12 4 40 100 2 6 18 18 6 5 2 10 12 5 20 3 20 15 100 4 50 9 8 50 5 10 2 10 200 12 5. ие) 150 100 15 80 (25) 25 70 20 4 1 25 3 4 2 (25) 3 15 з (15) 5 100 5 2 8 10 3 10 40 3
Рг 150 70 3039,82 Nb 5 300 l Nd 20 1 20
33 Hf 5 1 55 Mn II 1 6 88 Gd 15 15
32 Ба 10 2 51 Ce 8 86 Y 4 4
30 Се 6 1 50 u 10 3 84 Fe 60 30
28 и 12 50 Se (20) 76 Ce 8 2
28 2 3 41 Nb 3 5 75 Nb 2 3
24 V I 12 2 36 Sm 6 2 74 w 7 6
23 Hf 4 1 36 tn I 1000 R 500/? 71 Ta 2 2
22 Nd 10 15 32 Fe 20 15 71 Mo 5 8
22 5 7 31 W 10 12 62 Er 10 2
15 4 4 31 Cs (4) 58 Ba I 3
14 Са I 8 26 u 15 12 58 Nd 30 25
06 02 Н I Ег 9 (60) 26 25 Ir I Ce 25 4 2 53 52 Ce 11 Tu 4 40 ' 10 ’
00 Zr 2 2 21 Ca I 1 4 50 Ta 2 10
00 . 12 3 19 Nb 2 3 46 As II 5
3888,99 95 Dy Но 20 40 20 14 13 U Sm 5 15 5 9 46 44 Mo Ce 2 2 3
93 89 88 Gd W 6 3 8 4 8 12 3039,06 Bl Ge I 1000 2 1000 42 42 42 Gd Ho W 5 5 10 8
82 Fe 40 15 06 Mo 25 39 Fe I 4 2
68 Eu 8 5 3038,99 Ce 4 36 U 35 30
65 Cs I 150 10 96 Nd 4 2 32 Zr I 150 6
79 Mo 3 24 Mg I 3 8
3888,65 He I (1000) 78 Ru 3 6 24 Fe 15
61 u 4 3 78 Fe II 3 22 Nd 12 8
52 52 Br Fe 1 4 (10) 3 71 71 Ti 11 V 2 20 40 1 20 18 Ru I V I 30 100 8 30
40 39 Dy Ce II 6 15 4 69 67 Ho In 4 6 3 17 07 Pr Sm 11 8 10 2 10
34 Rh ! 5 2 66 Sc II (60) 07 Cu II 3
33 29 V I 10 1 66 Tb 8 3 3889,78 In II 150 (100)
Pr 5 4 60 Mn 3 33 Pr 70
23 21 Bl I Tb 40 30 2 60 60 Th Zr 12 12 2 3457,15 V 2 150
21 18 и и Mo 12 10 2 6 8 3037,94 2652,04 Ni I He I 800/? 100 100 69 07 3456,44 44 Rh I Tn Co I 100 5 4 4
09 Er 18 1 2651,48 Ta SO 39 Tl II 25 125
08 V I 15 4 48 Se (10) 39 Mo 15 10
02 Tl 1 15 44 W 9 4 34 Ce II 10
3887,96 95 Mo Re 3 20 4 42 29 Ce Ru 1 2 60 5 30 2 U Ra II 3 2 (5)
94 W 10 29 Fe II 2 17 Hg ...... (10)
94 88 87 Bl I Tb Nd 5 10 25 2 20 22 2651,18 Ta Ge I 40 80 20 15 14 11 Mo Os Sm 5 20 4 6 10
81 Fu -U6 Hf II 15 49 03 Ce 2
78 Y 3 3 IS Nb 3 200 01 Dy 40 ......
77 74 Ru ! Gd 15 5 8 09 02 Pd II W 1 10 10 00 90 Nd Er 4 25 10
ст> 8 70 U 20 10 01 01 Ne Ge 25 (50) 2 3456,09 Ho I! 60 69
СОВПАДЕНИЯ СПЕКТРАЛЬНЫМИ ЛИНИЙ ЭЛЕМЕНТОВ
Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга < искра (разряд) дуга искра (разряд)
Гольмий Но (продолжение) Диспрозий Dy Диспрозий Dy (продолжение)
3455,99 ТЬ 8 4213,72 Хе H (200) 60 4000,48 Pr 8 4
97 Рг 30 3 65 Fe 100
95 Th 4 4 4212.95 Pd 1 500 300 4000,48 Dy II 400
93 и 3 2 70 Pr 5 2 46 Tb 15 2
91 Zr I 12 1 68 Ag 1 150 20 45 10
90 Sc I 3 2 66 Si 2 45 Er 35 6
86 Мо 10 66 Cr t 80 8 45 Ho 5
4 1 Nd 2 . ..... 62 Zr 1 15 39 Mo 6 5
7б Ti 1 6 ...... 58 Se И (200) 29 Tn 8 3
74 и 4 54 Tb 3 27 Fe I 8 1
73 Ru 12 ...... 53 Nd 2 3 19 Pr 50 25
70 Но 6 6 53 Hg 11 (50) 16 Gd 10
60 Сг 50 35 49 Sc I 3 09 VV
28 Bi 11 100 48 U □ 3 08 V I 8 2
- 23 Со I 2000 R 10 4 Na I 3 01 Tb
22 Rh 1 300 12 39 Ce 1 2 3999,98 N (15)
Дейтерий D 36 34 C Sc I 3 (5) 95 94 u Cr 6 3 8
6563,42 6562,85 73 6561,60 Co I H I H 1 Ta 200 40 5 (2000) (1000) 26 23 22 16 06 u Tb Hg, Zr I Ru 1 12 3 3 125 10 (30) 80 86 82 71 68 62 Mo Dv No Cr Br 3 1 40 5 2 5 10 (8)
6561,06 D ! (3000) 04 Nb 4 3 56 Ho 6 2
6560,87 84 75 68 65 45 29 J Rb Pr SI 1 Хе I Ru Nd 4 2 9 (30) 150 14) 02 4211,91 88 86 86 86 83 Gd Ce Zr 11 Cu 11 Pr Os Se II 150 1 18 1 50 150 50 2 15 6 25 50 (200) 3998,96 73 64 3533,36 01 3532,80 Pm V 1 Tl I Co I Na II Os I 100 150 200 5J 100 1000 25 100 (200) 20
13 He II (100) 75 Mn 30 20 70 Tb 30 8
6559,97 81 Хе 1 Br 1 (25) (ISO) 4211,75 Dy 1 200 65 63 N Hg , (15) (200)
58 Ti II 8 73 Ho 5 3 61 Ce 11 6 1
4862,61 73 Tl I 30 6 58 Fe 0 2
Gd 100 2 72 Tb 25 2 55 Mo 10
54 Хе II (400) 72 Er 30 5 54 Sm 20 4
31 J I Cr (700) 68 u 10 10 53 Nb 3 5
4861,84 125 8 64 Ca 2 46 Zr 8
80 Gd 100 62 U 18 44 Dy 6 2
49 Hf 3 2 58 Ce 3 39 Ce 4 1
38 Rh 4 52 Th 8 8 3 Г j Rn (10)
—— H I (500) 35 Cr 100 30 28 V 1 «5-
22 8 34 Zr I 12 27 Ir 12 3
21 Tb 2 32 To (15) 23 Eu D 1
20 Сг I 80 31 u 10 6 21 Ta 15 2
05 4 29 Nd 30 15 12 Mn 50 30
04 Ta 3 1 25 Dy 4 2 06 Ir 2
02 U 10 10 24 Ho 3 1 06 Ru 5
4860,93 О II (20) 24 Pr 5 2 05 U 1 2
91 La II 100 100 2 k Sr 3 01 Sm 5
89 W 10 16 Tb 2 1 00 Mn 50 8
86 12 14 Rh I 15 200 3531,94 Th 4 3
76 10 8 02 Mo 15 12 90 S (5)
70 2 4210,98 Nd 25 5 85 Mn 40/? 30 R
67 Dy 3 94 Ag 1 200 30 83 Eu 12 2
56 Mo 5 4 92 Th 8 3 80 Ir I 2
44 Ru 6 87 U 12 12 79 Ru 8 1
35 N II (5) 77 Th 3 1 74 Ho 10 20
16 Ru 4 75 Cr 12 71 Er 40 25
05 Dy 2 35 Fe I 300 200 71 Nd 6 4
05 25 20 71 Rn I (5)
04 Br (12) 4001,45 Br (4) 71 Y 7
44 Cr 200 80 3531,70 100
4859,99 D 1 (500) 38 La I 3 Dy II
95 Pr 10 37 W 9 9 70 ть i5 50
88 Tb 2 31 Eu 6 2 64 u 15 1
5 28 ть 5 62 Pr 4 2
&5 Y I 50 5 25 u 10 3 60 Rb II (100)
75 u 8 8 24 Gd 80 3 59 Ce 18 2
75 Fe I 150 40 23 Zr Л 9 58 Ta 35 3
60 Ne I (15) 20 К 11 (40) 45 Th 4 1
59 Nd 10 19 Re 1 5 45 Fe I 3 1
57 Sm II 80 18 Mn 12 5 44 w 9
52 Eu 2 18 V 9 39 Nd 4 1
48 Ce 15 13 Nb 10 15 38 Cs (4)
47 Os 3 09 Zr 1 10 30 Mo 3 3
44 Ar (5) 06 Th 10 5 26 Er 12 I
41 Ra II (100) 06 Ce II 20 2 25 Yb 2 о
37 F II (50) 4000,91 Pr 20 8 23 Hf 5 3
34 He II (7) 91 u 5 6 22 Ar II (3)
31 Ca 3 89 Yb 6 14 Eu 10 10
24 Hf 30 5 81 Eu 3 ...... 13 Os 15 12
23 Gd 50 80 Co 4 1 11 u 8 20
18 La II 5 73 u 6 1 09 Ca 2
12 V 7 6 72 Kr 1 (2) 08 Cr 15
06 Dy 2 70 Eu 3 02 W 7 7
04 Pr 40 69 W 12 10 3530,95 Ce 10 1
03 Nd 60 60 68 Ce 5 1 88 Dy 4
4858,89 Tb 4 63 Cr 5 87 Hf 5 1
75 Lu 2 8 62 Ho 4 87 V I 1 20
72 Ce 6 60 Nb 2 50 85 Zr II э 5
61 VV 15 56 Nd 8 3 84 Pr 9 2
58 Pr 9 55 Xe (3) 82 Nb 3 15
g- 4857,38 Nl 1 100 50 Mo 8 8 81 Mo 1 3
Си 20 Kr II (150) 49 Nd 10 5 77 V II 40 100
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ | лИНИЙ ЭЛЕМЕИТОВ
в
Продолжений
.666
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Диспрозий Dy (продолжение) Европий Eu (продолжение) Железо Fe (продолжение)
3530,76 W 8 7 3819,71 Ta 5 3 3736,33 Nb 3 5
74 1г 10 2 70 Nd 2 2 28 Be 1 10
71 К II (40) 68 Sm 10 20 26 Eu 4
06 3529,82 Os 100 125 20 80 3819,65 Eu II 500 500 22 20 w Tu 5 3 10 8
81 Co I 1000 R 30 61 Cs (4) 17 Mo 4 1
61 Нс I (50) 3735,93 Co I 200 R
Европий Eu 56 Cr I 60 40 85 La 11 20 10
4206,70 02 Fe I 125 25 53 Ce 2 3 83 Br (6)
Ru I 100 40 50 Fe 2 1 78 Kr II (40)
00 Tu 20 5 38 Hf 15 20 77 Ce 2
4205,92 92 Er 6 28 Th 2 5 76 Pr 2 2
Zr II 10 3 27 Er 12 2 75 Ba II 1 2
89 Ce 4 1 22 Mo 5 67 Tl 15 4
88 Ta 100 30 20 Co 3 3 62 Mo 5 5
81 2 1 15 Nb 12 10 60 Nd 10 50
79 Ce 4 07 Eu 2 1 60 Ce 3 4
77 4 2 07 Pr 3 3 54 Nd 10
72 Pr 5 05 и 5 4 54 Os 20 10
65 N (5) 05 Th 2 53 Th 8 I
64 Tb 3 04 Ar II (5) 50 Ir 8
64 Dy 5 2 03 Ru I 50 30 49 Ar (5)
63 u 3 02 Ce 11 18 6 4 Rn (5)
60 Nd 20 15 3818,86 Nb 8 300 33 Fe 1 30 20
56 W 7 12 84 Nd 4 6 33 Re 1 40
55 50 6 81 Ce 2 28 Rh I /0 2
40 Хе I (10) 76 Dy 5 22 Nd 2 25
4 TI (2) 76 Gd 10 15 17 V 3
36 8 4 76 U 8 3 02 Ru 4
31 Nb 15 15 75 Se II (5) 02 Sn 5
26 Nd 5 4 71 Pr 2 2 00 Re I 30
23 Tb 2 70 Er 10 1 3734,94 Ne II (40)
22 Os 9 1 69 Pt 40 10 94 Tb 8
22 In II (15) 69 Ho 6 91 Ca 3
19 Sc I 10 1 69 Ce II 5 2 87 Ca II (4)
16 15 Ce In II 6 2 (30) 67 66 Th Mo 8 8 5 15 3734,87 Fe I 1000 R 600
1 6 28 Pr 125 100 87 Co I 60
09 08 07 V II In 11 CI II 5 20 (50) 10 3738,76 I Железо Fe VI I 100 7 86 86 8 Nd Ce Pb II 6 2 4 2 (10)
31 Fe | 100 100 80 Tb 8
4205,05 Eu 11 200 Я .. ,100 30
_ - -..---л- , ‘’Л
«ь
03 Dy 7 •) 11 W 6 • 7 74 Nb 2 5
4204.91 Eu 5 07 Eu 10 10 72 Al II 12)
84 Gd 25 06 Nd 25 70 Yb 25 5
81 Sm II 8 10 05 U 8 20 68 U 6 1
81 Mo 25 20 00 Al II (10) 66 Eu 2
74 Ce 15 3737,99 V I 50 5 60 Th 8 10
70 Y II 15 15 96 Ce 4 59 Er 4
62 Ca 2 91 Mo 20 20 57 Al II (2)
61 Mo 15 10 89 Ar 11 (15) 50 Se 1 (8)
58 Pr 5 1 88 Hf II 15 25 46 Er 4
56 Os 12 87 Sm 2 43 V I 10 5
54 CI П (18) 84 W 4 5 41 Pr 40 30
54 Sc I 4 2 74 Ru 6 5 37 H I (8)
53 Re 25 74 Ce 10 2 37 Mo 15 5
47 Cr 80 30 67 Pr 10 7 35 J I (18)
41 W 20 10 65 Ho 6 10 34 Cs (10)
4 TI (2) 55 Cr 18 33 Ir 5
37 U 15 10 52 Ce II 5 28 V 1 3
35 Nd 10 3 51 Th 5 1 23 Eu 5
32 Nb 4 3 47 Sm II 2 2 21 Ce 2
31 Kr (3) 44 V I 2 2 21 Dy 4 2
30 Ce 1 3 40 Ru I 12 12 14 Co I 70
20 V II 2 6 39 Zr I 3 2 13 Tu 150 50
20 Cr I so 6 37 Eu 2 06 Ce 2
04 La 11 200 25 > 27 Rh 50 10 03 Pr 4 2
4203,99 Fe I 200 120 25 и 8 10 3733,92 Ca 2
73 Tu 250 25 20 Xe (3) 91 Al II (5)
59 Cr I 100 20 13 Sm 10 3 84 Mo 25
23 Rn (200) 3737,13 Fe I 1000 R 600 49 32 Co I Fe I 150 400 300
3821,18 Fe 100 100 12 Rh I 50 1
3820,54 Co 3 2 02 Ce 3 3721,84 Sm 100 50
43 Nd 40 3736,95 Th 5 5 64 Tl II 60 125
43 Fe I 800 600 91 Ce 2 1 35 Kr II (ISO)
’ 42 Ce 3 4 90 Ca II 12 50 3720,85 Ba I 2
41 Pr 2 2 90 Mn'- 25 25 83 Pr 10 8
30 V I 25 20 83 Re 15 82 Ir I 6
25 Cl II (100) 81 Nl 300 15 80 Хе II (20)
13 № (2) 80 Ru 3 78 Th 5
11 8 10 79 Tl 10 2 77 Cu I 10 1
09 Ir 4 76 Ta 35 3 75 La II 3
00 Ce 4 3 75 Ir 2 74 Ho 6 4
3819,98 Cr I 12 10 65 Ir I 2 74 Pt 5
96 Nd 15 4 60 U 2 70 Eu 4
96 V I 60 35 51 Zr 2 2 64 Sm 2
92 Hf 12 10 50 Pr 20 20 60 Ce 2
91 Co I 20 3 48 Ir 2 57 Sm 4 4
88 Pt 3 48 U 2 54 Nd 8 8
87 Mo 6 6 47 Ce 3 51 W 8 10
78 Mo 6 6 44 Nd 4 46 Nb 5 100
77 Ru I 12 6 42 La II 6 43 Ar (10)
76 He I (4) 40 Ce 3 3 40 Ca 3
40 Mo 20 39 U 6 10
35 Ho 6 ? 38 Tl I V) w
ь х X X 3
гп X
О W
СОВПАДЕНИЯ СПЕКТРАЛЬНЫ
Продолжение
Я ОФ
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Железо Fe (продолжение) Золото Ая Индий In (продолжение)
3720,38 Се 2 2676,95 Cl II ...... (150) 4511,09 Nb 5 15
36 Tb 8 25 Rh 1 100 4510,98 Ta 200 50
31 As II 15 i9 Ru 8 1U0 92 Ce 6
31 Th 15 10 13 Yb 2 92 Er 2
25 Mo 10 40 12 Nb 10 84 Al 6
22 Pr 15 6 12 Ce 81 Ho 9 1
13 Os I 80 40 11 Fe 15 7 76 Ce 3
3719,97 Th 2 1 11 Rh I 10 о 73 Ar I (1000)
Ce 2 08 Ti I 6 54 Th 30 20
WOO R 700 05 Eu 5 39 Gd 10 10
3719,94 Fe I 04 V 15 32 U 20 30
93 Ba I 9 03 Tl II (30) 21 Mn И 16)
. 80 Ce II 15 5 01 Co И 10 2 Rn (10)
74 Mo 30 2675,98 Co I 10 5 17 Ne I (15)
72 Tu 10 4 97 V I 6 17 Cc 4
70 Sb II 8 2675,95 Au f 250 R 100 16 Pr 200 125
69 69 Mo u 3 1 8 94 Nb 10 100 10 10 Ru I Os 25 2
64 Mb 50 90 la 150 200 08 Ce 2
60 Nd 10 8 88 15 10 00 Cr 15 1
Mo 3 87 W V I 12 6 4509,97 Dy 2
52 Os I 40 12 76 12 2 97 Er 2
46 Gd 40 40 76 TI и (30) 88 U 4
45 Sm 50 10 73 2 87 Ar (2)
45 Tb 30 8 12 82 Nd 6
44 TH 30 10 68 Cr 1 15 39 Cu I 150 30
44 43 Pr 15 8 10 67 66 La II 8 2 4 5 4508,48 Rn I (250)
42 Ta 3 64 Ne I (150) 3257,59 Fe 1 100 100
40 W 12 10 24 (150) 58 Ar I (100)
33 Ru 20 2-5 2428,20 Pt I 100 20 0 k В 100
30 Sin 3 10 Sr I 10 3256,77 Ta 100 1
30 Er 4 04 Pt I 100 10 46 J (18)
29 U 12 02 Cl II (10) 46 V 8 1
28 Hf II 15 30 2427,99 Th 3 25 46 и 2 1
17 Eu 30 ’98 Mn 50 43 Pt 2
08 Ce 11 3 96 Ir 5 35 Er 10 2
05 3718,93 Mo Mn 75 20 100 2427,95 Au 1 400/? 100 33 29 Ru Re 50 8 3
91 Pd I 300 200 90 Os 8 40 27 Th 10 15
88 Sm II 100 5 81 W II 1 7 27 Ho 4
63 Kr II (200) 79 CI II (20) 25 Ce 12
02 Kr II [300] 74 Mn . _ y>rt Dy 25 5
t • •.
3021,56 Cr I 300/? 200/? Индий In 23 Ce 6
0/ Fe I 700 /? 300 R 23 W 8 >-
04 Ce 15 . - .... 4513,44 Br 1 (100) 21 Mo 40 25
3020,92 U 8 12 30 Re 300 14 Mn 75 50
9 Cs (4) 1512,74 Tl I 100 60 13 Nb 2
88 88 Ce Ru I 15 60 40 73 71 V p 1 40 (15) 3256,09 In I 1500 R 600 R
70 Yb 5 63 J (30) 3255,96 VV 9 8
69 Mo *5 10 67 Eu 2 92 Pt I 3 30
67 Cr I 200 R ioo 61 Cr 8 89 Fc 11 20 100
67 Nb o 8 57 J (30) 84 Sm 6 2
65 Dy 10 56 Er 4 81 Ca 1 3
1000 /? 54 Ho 2 1 80 Re 4
3020,64 Fe I 600 R 49 Th 4 4 79 Er 10 1
64 Co 60 39 U 2 3 69 Ta 18 2
58 Tb 3 30 Sm 2 68 Sc I 15 8
57 и 6 6 29 Nd 3 65 V I 25 о
54 Lu 100 28 Ca I 10 63 U 3
53 Hi 15 2 27 Pr 8 62 Nd 8 4
50 Os 3 20 Er 3 62 Sm II 8 3
49 Fe I 3iX) R 300/? 18 u 2 4 34 Ge ...... 100
47 Zr 11 50 30 15 Mq 25 9^
3 Cs (4) 14 Eu 2 Иод J
29 Tb 8 15 13 Nb 2 3
24 и 8 6 03 Ir 5466,47 Y I 150 20
21 w 6 4511,90 Cr 80 100 23 Br 1 . ..... (ISO)
1-5 Ca I 9 2 83 Sm II 100 100 0 k Zr 8 ......
3019.37 Os 100 20 82 Nd 50 10 5465,9 Cs I 5
14 Ni 1 200 R 30 82 Pr 3 69 u 12 8
75 и 8 57 Mo 20 з
2600,27 Cu II I 200 72 Er 4 1 53 Tu 10
2-599,87 Mn 10 1 64 Ce 10 50 Lu 3
86 Re 80 53 Eu 3 3 49 Ag I 1000 R 500/?
SO u 4 2 52 Tb 40 4 k Zr 20
76 vv 9 12 51 Ne I (20) 34 Ce 20
66 Fe 6 50 Ta 300 40 17 Те II (15)
66 64 Ru Mo 10 20 25 1 46 43 Pr V I 2 2 5464,62 J II (900)
64 W II 1 5 37 Ne II (50) 46 W 4
57 Fe I 1000 35 Pr 4 39 Tb 10
52 Nb 5 34 Cd d 38 La II 25 30
40 40 Ir Ta 40 100 300 4511,32 In I 5000 R 4000 7? 28 24 Fe U 6
2599,40 Fe II 1000 1000 31 30 Sm Sn 40 200 20' 08 Ce Sb II (100)
22 Hf II 10 10 29 Ne II (15) 06 Zr I 2
21 Co I ь 29 Nd 2-5 5463,97 Cr 15
18 Mo 1 15 26 Pt I jr. 1 80 Sm 2
15 Yb 2 50 24 Mn 2 6 Sn 2 2
13 Fe 1 20 Ru I 25 38 Hf II 10 10
13 Os 5 1 17 Ti 40 10 28 Fe I 100
2598,90 Mn 5 100 17 Zr I b 28 Gd 8
О 88 Nb 150 16 u 4 8 17 Sm 2
81 Cu 11 200 09 Pr 3
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ' ЛИНИЙ ЭЛЕМЕНТОВ
Продолжение
О . —
о Интенсивность Интенсивность Интенс HBHOCTb
Длина волны, А Элемент дуга искра (разряд) Длина волны, A Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
— Иридий Ir Иридий Ir (продолжение) Иттербий Yb (продолжение}
3222,07 3221,28 Fe I Ir 200 10 100 1 2543,45 25 50 100 150 3289,39 39 38 Ar 1 V II Ей 10 2 (3) 70
27 Nl 1 35 38 Но 10 20
22 Yb 2 3 Иттербий Yb 1000 R 8
21 19 W Ru 12 4 10 3 3695,90 86 Nb V I 4 150 200 100 R 3289,37 36 Yb II Er 500/? 25
17 Co II 50 34 V I 125 70 35 Fe 11 40
15 Ti I 4 • ••••• 2 2 34 Dy 2 2
12 Nb 4 16 v 3 31 и 4 4
08 06 3220,93 87 86 82 Tu Ce Nb Ce Mo Cm 7 2 10 30 8 800 10 8 600 09 05 3694,97 95 95 94 Er Fe Cr Rh I W Mo 2 200 3 2 40 150 6 2 30 28 24 17 14 13 02 Ce Ru Ag Rh I Cs I Mo 10 5 150 2 40 5 50 30
78 Rh 4 91 Ce 15 2 3288,98 V 10 15
3220,78 Ir I too 30 89 Th 5 1 97 Fe 30 15
78 75 Pt Ca 2 3 82 82 Sm U 15 3 3 94 90 Ce Ti I 2 2
73 Er 25 5 81 Er 15 6
61 Hf II 25 35 81 Ho 4 Иттрий Y
60 54 53 49 К II Pb Nd Nb 50 2 3 (15) 4 80 79 76 75 Nb-Nd Tu Dy 30 20 20 5 20 20 30 4676,91 46 34 Sm II Xe Cc 100 2 50 (100) О о OS
47 Tl II 25 75 Tb 50 8 3 k Y X
47 45 40 30 28 25 3219,81 58 30 Pd 11 Dy Ce Th TI I Kr Fe I Fe I P 10 12 12 3 100 200 2 2 10 (6) 80 125 (100) 70 67 62 62 52 51 45 45 42 36 Pr Nb V 1 Ag Ta W Ir Tl I Mo Dy 40 10 60 2 7 10 2 80 ' ' * б’ ' 4 10 5 1 18 20 20 20 4 30 26 25 18 05 05 4675,81 78 74 70 Nd О II Pr Th J II Dy P Sb Mo 2 10 2 7 2 2 (125) 8 (5) 2 (70) (15) 4 ё m X s iO n X rn
2665,26 25 07 07 05 Nb Nl II Mn Ir I Ga 1 3 10 8 300 125 (40) 36 32 32 31 27 Th U Pr Sm La 11 5 6 3 15 4 1 1 1 8 10 64 64 63 62 55 Br NI I Ho Er Se 8 3 15 ; 15 (4) 1 4 (10) 2 § c X £ - SM*--.-
’л~ 03 Yb 10 60 3694,20 Yb II 600 7? г 100071? Г 53 J II lilWfiwWWl (50) Sr
00 Cc 2 20 Y 4 52 Nd X
2664,96 W 12 6 20 Ne II (250) 15 48 Eu 20 X
93 Sn II ...... (5) 19 25 47 Pr 3 s
81 Re 25 • ••••• 17 4 46 Hf II 10 10 X
12 Tb 8 39 Re 2
2664,79 Ir 1 200 50 12 Mn 5 5 37 Nb 50 30 b
76 75 74 66 64 49 24 Ru 1 La II Ce Fe 11 Pt I Rh Ta 60 1 2 20 30 1 10 5 3 300 30 100 03 01 01 00 3693,94 93 90 84 In II Gd Fe I Sm II Th Nl I In II Dy 25 400 100 2 50 4 (40) 25 300 150 3 (35) 1 31 31 29 18 12 09 08 04 Ce Tu Lu Tb TI I w Tu Pr 2 35 4 2 50 8 25 5 1 5 1 3= m X о os
82 Eu 25 1 03 Rh I 100 50
2544,83 Pd II 200 79 In 11 (25) 2 4674,98 N II (5)
80 Nb 5 300 76 Nb 1 89 Cs (10)
80 Cu II 700 7? 71 8 88 Ce 2
71 Fe 100 5 70 u И 18 85 Er 50 15
27 27 Ce Ta 3 2 70 67 Th Mn 50 4 60 4674,85 Y I 80 100
25 Co I 50 7? 100 59 Ru 20 5 80 Pr 25
25 Au II 10 ;6 Tb 30 76 Cu II 200 30
22 Rh 8 4 49 Pr 2 1 65 Ru I 20
22 Ru 60 6 48 Co I 35 10 62 Ho 4 3
21 Re 25 42 Ce 10 1 61 Dy 3
19 Au I 30 8 38 Mo 5 3 60 Nd 50 10
17 w 8 2 37 Nb 8 10 59 Sm II 80 40
04 и 4 2 36 Co I 18 56 Хе II (25),
00 w 5 36 Pr 30 8 52 Ru 7
2543,98 Nb 4 1 32 и 4 6 49 Ce 3
98 CI II (10) 23 Mo 3 30 Re 15
97 Mn 3 3692,36 Rh I 500 150 24 Pr 3
22 V 1 200 7? 150 7? 23 U 8 8
2543,87 Ir I 200 100 21 Tu 10
94 92 Rh Cs 15 100 7? (20) 3290,82 26 22 Mo Os Pt I 40 200 150 100 20 10 18 04 01 Nd Tb Os 5 2 3
92 88 84 Fe Na I Sb 40 127? 20 25 3289,85 85 84 Yb Y 1000 15 10 10 10 4673,99 98 80 W Nd Kr II 2 1 (3)
83 82 Re Dy 20 10 84 79 Ta Co 25 1 77 74 In II U (5) 3
82 Na I 67? 75 u 2 71 О (30)
80 Os 10 1 74 Hf II 5 з 66 Th 6 2
73 72 V I Те 12 9 (10) 72 64 CI Rh 50 (12) 5 62 62 Ba Dy 40 10 5 8
71 Gd 2 55 Nb 10 61 Tb 4
68 Ru 20 52 Ce 59 ! Nb 2 5
67 Re 20 R 45 Nb 2 56 । Cu II e
О1 65 Fe 700 44 Fe 10 4 46 Be II (W0)
38 Br И)
Продолжение
Зак. 783
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Иттрий Y {продолжение)
4672,2 09 08 Be Nb Pr 150 100 100 100 25 3600,81 80 77
3711,74 Tb 200 30 76
30 Ио 6 4 75
28 Cr 12 75
22 Fe I 80 30 74
22 Pr 3 2 74
15 1Г I 7 3600,73
15 Ta 0
12 V 80 73
. 10 Pr 8 3 73
07 Na II 8 (60) 70
00 Ce 2 68
3710,95 Lu 3 58
91 U 3 8 49
88 Eu 35 30 44
87 Sm И 100 7? 7 43
79 Ta 7 39
78 U 4 2 34
77 Cs (4) 29
75 Ca 3 29
75 Ho 8 8 28
73 Dy 4 2 22
60 Cr 2 2 21
59 La II 3 2 20
53 U 3 4 17
52 Sb и 2 5 12
45 p и (30) 08
45 Nb 15 20 06
36 F (10) 04
32 Ru 4 03
31 Yb 4 6 3599,97
31 U 8 1 97
30 Sm 25 15 94
29 Er 15 8 90
3710,29 Y II 80 150 88
29 Eu 20 1 87
29 w 4 5 84
25 Ce 2 1 83
19 Tl I 83
Av Si
14 Mo 20 15 —— -Мй 76
09 Cr 4 2 73
08 Dy 20 5
01 01 3709,96 Pr Eu Tl I 6 5 80 2 25 6440,22 6439,97 80
94 Re I 40
93 Ce 25 10 83
90 Ar (5) 83 72
88 U 2 2
74 Nb 2 2 32
67 Th 5 3
66 Pr 3
66 Fe 4 4
64 Ne II (40) 07
59 53 Ce Fc 5 6 6 6438,96
53 Sm 10 6 9
51 J II (3) 6438,47
46 U 3
42 Nb 5 10 08
33 30 V Tb 15 25 03 6437,69
25 Fe I 600 400 63
3708,82 Co I 100 60 63
72 V I 100 36
3602,08 Co I 200 35 16
3601,73 Eu 2
70 Sm II 5 5 01
67 Cr I 50 30 2288,19
6 Rn (5) 16
58 W 6 15
51 Ar II (5) 14
50 Tb 8 12
48 Ru 2 5 10
42 u 3 09
40 Ir 1 30 8
40 F (30) 2288,02
39 Dy 3 1 2287,93
38 Tl 15 89
32 Nd 10 2 88
27 Mil 15 15 85
25 Sm 4 1 84
19 Tl I 7 3 84
19 Zr I 400 15
05 La II 5 15
04 Tu 8 10 7700,20
02 Pr 10 2 7699,49
3600,97 Gd 30 30 14
96 95 W Ho 6 9 10 7698,98
о Nd 20 10 94
83 Th 3 1 00
1 1ттрий Y (n Co I Tb J Yb Rh I Pr Er Mo Y II Cs Ho Ta Rb Ce U Tb Th Yb Dy U w Mo Ar II J Mo Ne I Nd S Hf II Tb V I Ce Fe BI Zr II Kr II S Hf U Mo Er 1 родолжени 4 8 10 8 25 30 2 100 6 2 15 1 8 4 2 20 10 4 5 3 15 2 15 50 10 5 2 5 10 6 3 30 ir'i e) (5) 20 2 5 20 4 300 (10) 1 (20) 2 2 50 1 2 30 3 (3) (10) 3 (75) 10 (3) 8 3 40 1 5 (40) (5) 8 18 5 20 7697,73 7696,73 7695,78 7666,4 7665,72 7664,91 74 70 56 34 30 02 7663,75 52 4048,14 06 06 05 4047,96 94 88 87 85 85 79 77 74 74 70 63 62 61 56 51 50 4 40 39 39 (алий К (nj Sc I S I Sm k Tt Sc I К I Cd Cu II Хе I La I Fc 1 Хе I Kr Nd Pr U Th Os Hf w Ce Cl Er Gd Sc I Sc II Eu Dy Ce Y I Ce U Mo Ar II Ho Rb Mo Ce Yb bm II. , ^одолжение 20 100 6 9000/? 5 8 15 2 8 8 8 20 8 9 5 5 150 25 2 4 3 50 3 18 4 3 4 4 • <»' ) (200) 100 3 70 (30) 3 (10) (2) 4 2 8 2 25 8 (6) 50 10 (8) 2 10 3 4 (2) 3 0) 4 4 V Л
r - . Ru Th Кадм» J Eu Nd Rn I Co W Sin 11 Sm Nd Co Ca I Zr I In Ra I Cd I Br w Eu I Ar II Sm In II Ta Y I Те N I Pt II CI Pr Sb As I V Ir Cd I V J Ir Ce Ta Те Кал J I Yb Ta К I Nd Y 12 3 гй Cd 40 3 2 6 10 3 20 80 150 8 2000 3 700 10 2 4 15 5 250/? 3 1500 7? 20 5 ий К 2000 5 5000/? 2 4 100' • 1 (100) (2) 1 5o 5 (30) 1000 (2) 1 (4) (12) (1000) (30) 30 (4) 7 5 15 5 300/? 15 (12) 5 10 (5) (8) 200 35 33 31 28 20 4047,20 18 18 16 16 10 09 05 4046,96 89 85 84 76 76 73 70 70 64 56 54 52 49 45 40 34 27 26 4045,98 97 82 44 39 14 13 12 05 01 4044,95 90 89 82 82 7*> 71 67 64 61 58 Ca Ir Fe I Ce Mo К 1 Cs II Те Tb Nd Pr Gd U Er Mo Ce Gd NI I Сг I Ce Nd W Pr Hg I Ir U Sc I Pt II u Ce Nb V Dy Ar I Fc I Ho Co I U Mn Mo Sm 11 Gd I Sm Xc it U Pr N 11 Nb Kr II Xe Fe I Cl 2 4 3 18 4 400 9 12 20 6 6 8 3 3 10 2 30 2 8 10 8 200 8 5 10 3 30 3 1 150 400 200 400 4 15 2 10 20 10 2 10 50 70 3 2 3 200 (20) (15) 10 12 5 8 20 10 3 2 12 3 300 5 20 5 10 1 15 12 (150) 300 80 4 *3* ’ 6 5 • 10 2 35 (2) 3 (80) (3) 35 (10)
СОВПАДЕНИЯ СПЕКТРАЛЬНЫЙ ^ИНИИ ЭЛЕМЕНТОВ
Продолжение
Длина волны, А Интенсивность Интенсивность Интенсивность
Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Калий К (продолжение) Кальций Са (продолжение) Кальций Са (продолжение)
4044,56 Zr 1 25 2 4226,06 и 6 8 3934,23 Rb I 100 2
49 р II (150) 06 Rn I (50) 17 Dy 12
47 Tu 15 ...... 4225,96 Fe I 80 30 14 Nb 5 15
42 Са 5 3 87 As II 10 12 Ln II л 01
42 Аг 1 (1200) 86 Gd 150 50 12 Zr II 20 12
42 и 18 25 75 U 1 3 11 Br 1 (2)
39 Hf 10 4 75 Cc 6 8 И Nd 5
35 Nd 3 09 Nd 20
33 Се 4 1 3970,10 Ta 100 40 08 Ce 6
29 W 15 12 3969,75 Cr 1 200 90 01 V I 100 30
4044,14 К I 800 400 67 43 Os Er 100 6 100 1 3933,98 91 и Co I 6 60
11 Sm 4 42 U 5 90 Tb 4
- 10 Nb о 10 34 Th 3 2 90 Ir 20 8
10 Hg н 5 10 26 Sr I 30 73 60 60
09 Cl II (4) 26 Fc I 600 400 68 Ru 5 200
06 Ce 3 ...... 26 Gd 200 68 Eu 10
04 U 1 4 23 Dy 6
03 Gd 3 23 Eu 20 3933,67 Ca II 600 /? 600/?
4043,97 Eu 20 ...... 20 W 12 10 66 Hf II 20 15
96 Cc 3 • . г • . . 18 Те (10) 66 Ir 20
90 Fe I 25 7 17 Ir 30 10 66 u 2 10
88 J ...... (20) 16 Ce 2 65 80
80 Sc I 12 4 14 Nb 20 62 80 80
78 Tl 1 20 ...... 13 In 15 60 Fe I 200 200
75 Cu II 10 12 Co I 100 6 59 Sm II 200 200
75 Cc 3 ...... 06 Сг I 80 50 47 Tb 6
74 Mo 8 8 02 U 5 8 39 Nb 3 3
71 Gd 5 5 02 Mo 3 3 38 Sc I 60 60
70 Cr 30 2 00 Gd I 40 37 p (50) 2
66 Tb 8 1 00 Th 10 5 30 Pr 9
60 Nd 15 5 3968,88 Nd 20 4 29 S II (80)
58 Zr I 25 87 Eu 3 18 Zr I 9
54 N (10) 75 Mo 8 50 03 U 5 10
50 Cu II 25 73 Tb 2 01 Nb 3 з
47 Ce 4 (20) 72 Zr 3 3932,98 Dy 10
42 Cs 66 Br (8) 98 Ce 6 1
41 Ce 2 59 w 6 6 98 Pr 25 8
40 Th 8 1 48 Ir 25 97 Ir I 6
37 Sm II 5 3 47 Nb 3 10 97 Gd 10 10
27 Mo 3 2 47 Ce 35 35 97 Sm II 6 3
16 15 Nb Th 3 10 10 3 3968,47 Ca II 500 7? 500 7? 92 92 Fe 8 10 4
4042,91 La II 400 300 46 Lu 50 Th 10 3
Кальиий Ca 46 43 Ru Y 12 10 200 30 79 | 3931,82 1 Ce 1 Rn I 3 j (250)
4227,76 72 66 65 58 50 ' 46 43 41 41 33 3 29 Zr I Nd Th Tl I Eu Al II Re 1 Fe 1 Cc Al II U Rn I Hg 150 20 3 18 8 200 300 10 6 8 8 1 2 (30) 250 (8) 8 (15) (100) 40 37 37 36 35 26 22 17 16 16 16 15 09 Dy U Fe Ar Gd Zr I Rh I Ta Pr Tb V II 300 1 2 20 100 100 8 2 4 25 2 25 2 (200) 4 60 8 10 40 7774,14 14 7773,03 7772,90 83 40 4 12 11 0 7771,93 Кислор Ru О I Nd Rh I Sm II Kr I Sm Xe Nb Sb II Fe од О 100 3 100 30 2 5 3 (300) (5) (20) 15
16 In II (50) 03 Hg (50) 7771,93 O 1 (1000)
14 10 08 02 4226,99 92 Gd Cs II Mo Ar II Nd W 50 3 *6* 15 20 (50) 25 (Ю) 5 3 03 01 01 3967,97 92 78 Yb HI u Fe I Cc Sm 5 6 60 3 6 1 4 15 2 88 65 6 13 06 Ru Cr Sm CI I Sc I 100 12 2 5 ’ ’ <2)’ '
81 Al II (35) 70 Nd 20 Кобальт Co
76 74 73 Cr Ir Ce 125 30 50 30 30 69 68 66 65 Y II Sm II Pr Tb 3 8 10 6 6 3 3455,28 23 22 Bl II Co 1 Rh I 2000 /? 300 100 10 12
4226,73 73 73 66 65 63 62 60 57 Ca 1 Y Mo Ru I Ar II Ir V I u Ge 1 5001? 5 15 15 5 8 1 200 50/? 15 2 (2) 3 2 50 64 64 54 54 53 52 51 48 42 Ce U Xe 1 P Ce Dy Ir I U Fe 3 5 8 3 10 125 2 (200) (15) 1 100 3454,99 48 47 39 33 32 26 23 Cr Bl II Ce Pr Nd Dy Er Ce U 10 6 6 100 20 2 2 100 (5) 40 1 2 10 8 2
55 53 Mo Os Tb 10 12 50 5 6 3966,57 3934,84 Pr Ir I 100 200 70 50 22 21 20 Th Ne I 8 8 (75)
43 43 CI I Fe I 80 (Ю) 25 80 60 Gd 1 W 100 5 50 5 18 16 Y I Ti I 5 15
37 34 34 29 25 21 20 20 18 15 Sc II W Ce Mo Nb Nb Ir Ce Sm Tb 10 2 20 4 3 2 3 5 3 (20) 3 20 3 5 2 51 47 46 43 41 40 39 30 26 26 Ce U К In II Nb Tb Eu Yb Mo Pr 2 2 5 10 5 2 5 12 1 (20) (5) 5 4 5 2 16 15 15 13 10 07 06 05 02 3453,97 Eu Gd Pt 1 Ar Yb Tb Se Ce Nb 3 15 2 40 80 3 1 15 2 (Ю) 250 30 (8) *100 ’ •
15 15 1 Br В Rb 4 (4) 2 (8) 24 23 Tl I Fe 30 2 2 92 88 88 Th W Eu 4 2 10
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ huH„n апгмгнтов Ж. ЛИНИИ ЭЛ LMtnl и в
.-Oi Й Продолжение
Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент дуга искра . (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Кобальт Со (продолжение) Кремний SI (продолжение) Ксенон Хе (продолжение)
3453,86 Pt 1 8 2881,94 Мо 3 4671, да Ти 15 20
83 Tl И ...... (10) 93 Сг 1 30 90 Мо 30 30
78 Рг 6 ...... 92 Yb 3 85 Sm II 2
78 и 4 3 91 и 4 2 83 La II 100 150
76 Сс 3 80 Са 4 8 LI II (4)
74 Сг I 30 25 77 Со 2 71 Се 2
66 Ти 150 80 74 1г 3 69 Си II 10
65 Т1 I 3 70 О (10) 69 Мп 100 5
64 Се 2 ...... 64 Ir I 7 65 W 12 1
57 и 5 8 61 In 2 61 Kr I (Ю) I
55 Sm 15 4 59 Dy 2 58 Ег 3
53 Tl I 5 58 Со 4 1 41 и 20 30
3453,50 Со 1 3000 7? 200 2881,58 Si I 500 400 38 37 Ей Ru 10 5
50 Re I 40 58 Ce 40- 2 30 W 3 1
47 Ей 3 2 58 Gd 40 4671,23
46 Kr (3) 46 AI II (30) Хе I (2000)
46 Tb 15 3 42 Ce 4 18 Ей 30 1
35 Ta 10 37 Mo 10 10 Dy 4 4
33 Сг I 35 35 36 Ir 4 09 Nd 20
28 Re 20 33 Gd 2 3 09 Er 2
24 Ce 8 31 ть 10 4670,91 Се 4
23 Sm 4 4 91 Hf 5 2
17 La II 50 40 2516,40 In 3 91 Мо 2
13 Ho 30 20 36 Yb 2 5 88 Ne I (70) 2
12 Dy 5 2 34 Cd II 25 85 Gd 3 о
10 Er 12 1 25 Fe I 2 83 Sin 30 О
10 08 Ne II V (7) 60 2516,12 SI I 500 500 83 82 Y Tb 3 2 W 3
05 Os 20 10 12 Xe (6) 77 Sm 30 Ьэ
04 Er 12 1 12 V 25 100 74 Ce 4
02 Fe 30 15 12 Re 125 69 Os 6 X
0 Pb II (2) 11 Ta 6 2 58 Yb 12 15 S
3452,97 Ta 5 2 И Dy 5 56 Nd 20
96 u 2 И Mo 25 25 54 Pr 10
93 Pr 6 1 1 Воздух 7 49 V I 60 7? 40 X
90 Ru I 60 6 05 Br (3) 44 Ce 2 ги
89 Nl I 600 7? 50 01 Ru 20 5 40 Sc I! 100 300 X
81 Ce 5 2515,81 Zn 1 150 20 28 Cs II (20) 5
80 Mo 20 69 Bl I 100 25 24 Mo 5
77 Sm II 4 1 23 Tb ь
73 68 u Th 10 3 10 5872,98 Криптон Kr Eu II I 300 I 11 10 Те Nb 1 (30) 4 С" X
65 Nb 15 5 34 Er । 20 j 10 Ce 2
62 62 Се II W 5 7 4 15 03 Nc I Ta 7 ... .. , (75) ’ 16 03
Er Th 2 3 1 X
60 10 8 03 Hg I ...... (10) 00 Mo 2 X
54 Се 5 5871,80 Y I 2 4669,98 Ru I 40 s
51 W II 4 12 80 Те (15) 87 Nb 3 2
47 TI 11 12 100 77 Rh 1 3 77 N (10) w
35 Nb*" 5 200 73 Hg II (40) 14 Ta 300 15 ь
28 Fe I 150 8 65 w 7 4668,91 La II 200 /? 300 7? rn
3451,92 88 Fe I 100 60 61 Br (15) 60 Na I 200 100 3
Re I 100 60 Co 20 48 Ag I 200 70 X
69 Hg II (200) 52 29 Tb Fe 5 3 Кюрий Cm о
3405,89 58 Re I 150 06 Sm 25 4209,47 Xe 11 (100) w
Fe 1 04 Nd 5 4208,78 Mo 5 5
56 Th 3 4 04 Fe 4 70 Tb 15 1
44 '6 5870,97 Ne I (3) 70 Ce 2 50
41 Nb 80 50 95 и 15 62 Fe 100
33 28 Bi W 40 7 10 6 5870,92 Кг I (3000) 48 44 Xe II Ta 2 (200) 30
28 Ru 3 85 Ho 20 44 Ce 6
22 Cr 12 1 73 Re 4 38 Nd 8 5
20 Mo 8 5 62 Tb 25 36 Cr 100 25
16 Kr II (80) 60 Gd 4 30 Pr 18 12
16 V I 30 15 6 k Tl 2 24 Cc 4
57 Th 10 16 Eu 10 1
3405,12 Co I 2000 7? 150 32 3 16 Nb 4 4
09 Tl I 20 2 26 Ar I (2) 09 Zr I 5
03 Ag 3 2 01 W 7 06 Gd 5
3404,99 by 4 4 5869,97 La I 3 03 CI 11 ...... (30)
97 TI II 2 78 Mo 5 00 As 11 30
96 V I 8 1 76 Fe 10 4207,87 F II (3)
93 и 3 2 61 Nd 2 81 Pr 12 5
92 Au 3 5 k La 50 68 Dy 5
91 86 83 Ce Mo Zr II 18 6 40 2 4 35 50 Zr I Ксено 8 н Xe 4207,66 64 Cm Ru 1000 20
80 W 8 6 4673,46 Вс II (100) 62 La II 5 3
77 Ne II (12) 4672,70 As II 50 62 Co I 2
77 Sm 2 2 7 Hg I (5) 58 Ce 2
76 Nd 4 6 69 Nd 5 2 56 Mo 10 5
75 Fe I 2 6 k Sr 4 56 Tb 8
72 Re I 100 6 k Sc 10 44 F II (30)
71 Tb 3 8 60 Pr 3 40 Mo 10 5
65 Th 4 4 56 Br (12) 40 Hf II 4
58 Pd I 2000 7? 1000 7? 54 w 3 28 Ca ...... 10
36 Fe I 100 50 48 Dy 5 25 Mo 10 10
3403,65 Cd I 800 500 46 Nd 2 23 U 4 1
20 Хе II (50) 16 F II (50)
Кремний SI 2 Be 100 13 Fe I 80 40
2882,04 Mo 3 11 Br (4) 05 W 25 12
01 Th 10 12 09 Nb 150 100 4206,90 Cr 80 25
01 J (20) 09 Kr II (2) 83 Ce 8 25
2881,95 Tl I 2 08 Pr 100 25 70 Fe I 125
06 Tb 2 ......
сп Продолжение
СЮ Интенсивность Иитенвивность Интенсивность
Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Кюрий Ст {продолжение) 1 Лантан La (продолжение) Литий LI (продолжение)
4206,02 I Ru I I 100 | 40 3337,50 Та 35 1 3232,50 Rh I 6
4205,88 | Та 1 100 1 30 49 Th 3 1 50 Sm 4
Лантан La 3337,49 La II 800 300 49 38 W Ne II 9 8 (7)
3950,92 Хе I Y II 60 (125) 100 39 25 и Re 3 5 3 36 35 Cd II Pb 30 2
СЮ 3949,96 96 Ru CI II Fe I Nb 10 150 8 (10) 100 25 22 20 17 Er Cr I Ho Co 1 15 10 12 60 3 12 2 32 31 31 29 Pd I Eu Th Ce 2 4 8 15 1
17 Yb 25 30 28 TI II 30 100
90 87 84 84 82 78 C a J (20) 16 16 Zn Th 6 (5) 5 28 27 Ta Se 25 1 (8)
Sm Eu Ce Os 2 5 10 50 2 10 15 U 12’ 04 Sb Os Dy U 2 2 2 10 10 3 2 23 16 15 13 w и Kr W 3 12 6 (2) 12 (2) 9
62 59 58 57 Cr Eu Сг I Ca 6 50 1 01 00 3336,68 Nl 1 Tl II Mg 1 6 125 6' 60 12 06 3231,95 Th Os I V 3 500 7? 8 25 20 100
2 15 Os I 200 7? 50 42 Os 150 12
52 и 2 8 Литий Li Лютеций Lu
51 Ba II (20) 150 2912,26
51 Tb 10 3 6709,50 La I Pt I ;юо 25
45 Nd 2 33 Sm 2 16 Fc I 150 150
46 Nb 1 50 6708,81 N (50) 2911,74 Nb 8 100
44 Ag 3 8 34 Те (30) 68 Cr 40
44 Pr 150 100 33 Hf 3 66 V 1 10
42 Ru 1 100 . 5 28 F I (40) 65 Ca 2
39 Tb 4 18 W 20 64 Cd II (15)
38 Ce II 20 3 17 V I 2 55 и 12 6
33 Nb . 3 2 6707,86 Co 200 52 Yb 5 40
31 u 2 6 85 Mo 300 51 Ce 8
27 21 Tu w 50 5 3 6707,84 Li I 3000 77 200 46 45 Ne I In (25) 3
21 Gd 10 20 52 Ru 5 42 Er 30 15
15 12 Fe Eu 4 25 1 1 45 1 Sm II Sm 50 2 2911,39 Lu II 100 300
12 Co 6 6706,85 Sm 5 35 Те (10)
3949,10 La II 1000 800 79 46 Tb Ta 4 5 34 32 Os Th 5 8 5 6
3948,99 U 8 . .. А. . . . 29 u 3 2
98 Ar I (2000) 6104,82 Sm II 30. 27 Sm 15. 1
97 Th 30 30 60 Ar 1 (б) 23 Re I 8
95 Ce 4 1 57 Th 12 2 22 Cu I о (5)
90 Ca I 40 15 39 Sm 6 20 О II
85 Cr 25 2 27 ть 6 . . .... 14 Cr I 40 8
80 Se II (25) 2 Sm 3 12 Ce 2 ......
78 Fe 150 100 11 Nd 3 . . .... 10 U 6 4
78 Eu 4 6103,95 Sm 2 . • • . • • 06 V II 30 200
78 Nd 8 88 Хе I (3) 2910,59 Nb 10 100
74 As II 50 72 Sm 4 ...... 2615,70
72 Хе I (10) 67 Dy 2 ...... w 1 8
67 65 Tl I Mo 80 6 40 10 6103,64 Li I 2000 7? 300 68 66 Re Ta 10 50 1
62 Pr 9 2 56 Ar II (8) 59 Sr II ...... 4
61 Eu 3 49 Nb 6 1 46 Ta 50 1
51 Ir 4 37 Srn 30 ...... 45 Ce 5 ......
45 Ce 2 37 Dy 2 ...... 44 W II 6 20
40 Pt I 60 5 33 Fe ...... 40 42 Fc 25 10
35 32 Tb Nd 20 20 1э 10 18 6102,75 Fe I Ce 8 3 2615,42 Lu II 100 250
32 Ir 1 10 3 74 Co 10 . ..... 42 Er 15 10
29 № (100) 72 Ca I 80 50 40 V 50
20 5 72 Rh 100 39 Mo 25 3
16 Хе 1 (60) 71 Cr 10 . ..... 34 Co I 10 2
15 C II 2 59 Th 4 . . .... 26 Yb 3 12
И 50 50 54 Zn II 6 (20) 25 Ta 40
11 Fe I 125 50 26 S (50) 19 Nl II 900
3947,63 Pr 125 60 18 Fe I 15 20 13 Cl II (Ю)
50 Ar I (1000) 6101,96 Se II (200) 12 w 10 3
33 O I (300) 58 Ta 150 12 Pd (25)
43 Хе II (200) 12 u 2 2
3338,54 Rh I 200 50 09 Ru 60 100
17 Re I 150 3233,97 Fe I 300 150 2614,59 Ag II 300
3337,93 92 U Zr II 4 2 4 2 11 05 Zr I Fc 6 100 60 Магний Mg
87 Ce 10 02 Ca ...... 4 2852,83 Na I 100 7? 20
87 Th 12 15 3232,96 Nl I 300 7? 35 42 Hg (8)
85 Ti 11 12 60 88 Ce 3 42 Cs 11 (2)
85 Y I 2 2 87 Co I 60 25 40 Re 10
85 V 2 150 80 Kr I (2) 39 Xe (2)
84 Cu I 70 50 79 Nb 2 36 Ta 5 100
82 Ru I 60 8 79 Tl 1 8 35 Fe 2
82 Tu 5 15 79 Fe II 50 24 Ce 3
80 Ta 100 18 78 J (5) 13 Mo 10 10
79 20 3 75 Ru 1 50 4 13 ir 20
79 u 12 10 66 Ce 3 13 Fe 150 80
68 67 w К H 10 8 (2) 65 65 w gy 9 я 15 8 4 2852,13 Mg I 300 R 100 R
67 ть 15 63 Те (10) 13 Dy 5
67 Fe 125 100 62 Sm 10 3 12 Ce 50 1
58 Eu 2 2 3232,61 LI I 1000 7? 500 10 w 1 18
5 CI II (2) 01 Hf и 20 50
5 fe Sr 8 58 CI (4) 2851,98 Nb 4 5
©i 50 W 5 3 54 Os 150 10 97 Zr II 12 20
2 50 Ce 20 50 Sb I 150’ 250 80 Fe I 200 150
п о W л б гп X S ьо
° Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент И нте нс ивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд).
Магний Mg (продолжение) Марганец Мп (продолжение) Медь Си (продолжение)
2803,24 Pt I 400 5 4030,76 Zr I 20 3273,97 Sb 4
2802,95 W 12 10 76 и 5 6 96 Се 5
87 86 Ег Ей 6 150 1 4030,76 Mn I 500 7? 20 3273,96 Си I 3000 7? 1500 7?
86 Те (15) 68 Сг 40 30 96 Мо 20 • • • а
84 Re 5 67 Та 10 1 96 Са 2 4
81 Ru 50 150 66 Ей 5 93 Со 10
ВО Mn 12 66 Sc I 10 2 93 <е 5
во V 15 25 51 Ti 1 80 18 89 Nb 20 100
76 Hg 5 15 49 Fe I 120 60 88 Th 10 15
72 Nb 2 5 47 Nd 20 15 68 Аи 11 2
71 Bi II 10 42 Sm П 10 3 66 Hi II 20 10
71 Co 100 200 38 Sr I 40 62 Ru 2 5
70 Ta 10 4 34 Ce 11 18 4 62 Sc I 35 12
70 Dy 2 3 Ca 10 2 60 U 5
70 Ce 18 5 29 Th 8 5 58 Mo 25
2802,70 Mg II 150 300 29 20 Br Eu 10 (12) 54 52 О II Ce 4 (35)
68 Cu I 10 2 19 Fe 1 20 4 51 Nb 1 20
65 Mu 2 16 Ce 5 50 Fe II 6
66 u 15 30 14 Ru 7 48 Sm 30 8
55 Bl (I 3 07 Se 11 (150) 38 Os 15 5
53 Те (10) 04 Zr 1 35 2 36 Ar (5)
53 Er 12 1 00 Eu 5
50 Ti I 100 15 4029,97 Tb 3 3248,60 Ti 25 200
49 Ta 15 2 95 w 6 7 52 Ta 100 3
47 Pd II 10 94 Mo 1 30 52 Mn 100 100
44 Bl II 2 94 Ta 50 5 46 Ni I 150 2
41 Mn 12 92 u 6 4 21 Fe I 200 150
19 Au 200 91 Nd 10 3 03 Kr II (6)
07 Ta 300 80 84 Y 1 5 00 Os I 5
00 Pb 250 7? 100 80 U 1 2 3247,91 V 5
4028,79 S II (200) 90 Ce 3
2796,34 Ta 400 80 8 К n (Ю)
2795,82 Co 1 15 2795,53 Mg II 150 300 79 ть 8
82 Cr 35 3 21 Ra 11 (125) 74 Xe (4)
81 Kr (80) 10 Ne I (35) 71 U 4 5
77 Fe II 3 07 Yb 3 67 Ir I 3 1
70 Rh 1 15 01 Fe I 50 35 62 Mo 30 20
63 60 Yb Co 8 10 2794,82 Mn I 1000 7? 5 61 55 In Ce 15 15
55 w 1 10 82 Co 100 7? 15 55 Ar (3)
54 Fe I ' - - - . " 4 ч 55 i , f
53 Ag 10 10 70 Fe I 50 30 • ’ ’str' ‘
150 300 60 Tu 60 20 54 Mn 125
2795,53 Mg II 59 Ne I (5) 2000 7?
53 Au II 15 59 Tl II (2) 3247,54 Си I 5000 7?
52 Се 30 8 57 Mo 3 3 53 Eu 50 5
45 Аг (2) 55 Ir I 3 52 Er 18 2
38 Се 2 21 Pt II 10 100 5 Cs (4)
35 Ru 30 8 2793,89 Fe II 8 150 47 Nb 50 100
33 Си 11 2 39 Fe II 2
33 Аг (2) 2577,10 Pd il 3 150 37 Sm 4
23 и 18 12 2576,55 Pb II (100) so Eu 4 1
21 Ra II (125) 40 Pd II 100 28 Fe I 20 10
2794,82 Мп 1000 я 5 36 W 11 2 15 27 Cr 1 20 1
82 Со 100 7? 15 34 Th 6 3 25 Ce 3
32 Re 15 21 10 10
Марганец Мп 30 Hg I 20 15 21 U 2 1
4031,76 Рг 50 30 23 RU 2 2 18 Tb 15 3
75 TI I 35 1 17 Br (15) 18 Co I 80
75 Но 4 1 16 w 2 20 17 Fe II 10
69 La II 400 300 10 Zr I 8 17 Sm I 10
69 68 Ег W 6 8 7 2576,10 Mn II 300 7? 2000 7? 12 04 Ce La I 3 8 2
67 Се 10 10 Co 30 3246,96 Fe I 100 70
64 ТЬ 50 3 08 Ru 50
64 Re 2 2575,96 Nb 1 10 Молибден Mo
63 Al II (2) 93 Ce 6 3800,12 Ir 150 100
63 Тс 300 200 90 W 9 1 3799,55 Fe I 400 300
56 1г 1 3 80 Cr 4 35 Ru 1 3000 7? 150
54 Nd 10 3 75 Rh I 2 4 31 Rh I 25 100
41 Аг (2) 74 Ag 10 3 24 Nd 10 10
40 Sc I 10 2 74 Fe 80 10 22 Th 10 5
38 Ей 7 3 74 Ir I 10 2 21 s (8)
36 Zr II 3 1 70 Те (10) 20 In II (18)
34 Се II 40 8 51 Mn 150 1 20 U 6 12
33 РЬ I 5 49 Pd II 100 19 Pd I 200 150
33 Th 5 5 30 О II (100) 15 Tb 8
31 Nb 5 10 AI 200 7? 80 4? 12 In II (10)
31 и 8 8 10 Ce 3
24 22 Fe I V I 2 10 3 Медь Си 06 06 Ho In II 4 (Ю)
14 Al II (2) 3275,20 Os 200 15 04 Ce II 4
13 Cr 30 6 3274,95 Ta 200 35 01 Eu 1! 100
10 Cs (10) 46 Ta 35 1 00 Zn I 5
10 Th 5 5 45 Fe 80 60 3798.95 Tb 8 8
09 Pr 12 8 41 Ag 5 92 w 7 10
08 Dy 7 40 Th 6 3 90 Ru I 3000 я 150
00 Ru I 15 12 29 Eu 3 1 84 u 15 1
4330,92 Mo 3 5 24 ть 70 80 CI II (50)
88 Gd 8 22 Na 11 15 (40) 76 Tu 20 10
87 AI II (8) 20 Mo 5 71 Eu 2
86 Lu 5 11 Ce 8 67 Ir I 5
86 Th 10 8 06 Ce 10 66 Hf 5 3
о 85 Ce 2 05 Tl I 7 1 66 V I 7 5
СО »—» 83 Y 2 2 02 In II 15 65 Dy 2
СОВПАДЕНИЯ СПЕКТРАЛЬНЫЙ®., ^цний ЭЛЕМЕНТОВ
Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Молибден Мо {продолжение) Мышьяк As {продолжение) Натрий Na (продолжение)
3798,65 Ег 4 2860,52 In 5 Fe 4
62 Се 3 3 47 и 35 30 29 Eu 25
59 ть 15 20 Та 2
55 Tu 15 2860,44 As 1 50 7? 50 15 6
51 Fe I 400 300 40 Yb 1 8 09 Sb п (150)
51 Се 3 3 37 Ru з 5894,99 Хе I (100)
46 F II (6) 31 Hf II 15 30 85 La I 25
44 Yb 4 31 Lu 72 Sm 15
31 Tl I 10 6 28 Tl I 7 63 Sc I 5
28 Br (6) 26 Er 4 6 BI 11 6
27 Ir 8 21 Fe 2 56 Kr 11 (8)
26 Er 5 17 Dy 2 47 Dy 2
26 U 2 8 16 W 5 9 5893,46 Ge II 100
3798,25 Mo I 1000 77 1000 7? 29 Хе II (150)
25 24 19 Ho Ce La II 2 4 2' 2780,70 52 56 Cr I Bl I Ti П Ir I Cr 600/? 200 15 100 60 5891,43 42 30 Те Sm Ru 15 4 (15)
17 12 Yb Nb 4 50 80 41 30 3 100 29 27 Se Eu (8)
10 Th 5 1 28 W II 10 20 12 Tb
08 06 Ce Ir 2 6 2 28 28 J Cd (20) (25) 5890,98 63 S (8)
05 Ru I 30 40 25 TI II (20) 50 Nd
3797,95 Fe I 4 2 24 Nb 30 200 7?
93 Tb 15 23 La П 20 10 45 Hf 8
92 92 Ir Hf II 2 25 25 2780,22 As I 75 7? 75 33 26 W In 7
91 91 Th H I 2 5 (20) 21 15 Ta Ga П 4 (40) 16 5889,99 12 (40)
91 Cs (4) 1 К (2) 98 Mo 50
89 Nd 20 10 10 V 10 97 C II
83 Cu 11 2 06 Ne II (5) 5889,95
77 U 10 1 04 Fe II 20 Na I 9000 7? 1000 7?
76 Dy 4 04 Yb 2 75 S I
73 72 Sm Cr I 25 100 5 20 04 04 U Mo 8 60 8 100 74 70 Se II 20 (15)
59 Re 1 40 00 Ce 15 12 Хе I (20)
52 U 3 00 Mn 25 06 Tb 10
52 Fe 300 200 2779,91 Fe II 40 5888,94 Hg II (20) (8)
52 Th 8 10 82 Sn 80 100 89 Те
42 Sn 3 54 Rh I 100 6 78 Cr 31
40 Ta 6 3 30 Fe П 25 300 68 ti 15
32 Ce 2 26 В •_ 100 6 59 Вл, Ar 1
30 Mo 5 5 2350,04 Os 12 (300)
28 15 03 Nb 2 12. 49 Ta 5 100
28 Rb II (2) 2349,94 Ti 3 33 Mo 150
3796,39 Gd 150 150 89 Mo 25
1000 86 Cd 2 3303,49 Th 5 10
3171,67 La 2 35 Sb 8 I 47 Fe II 5 5
35 Fe 1 100 80 85 и 2 8 37 u 4 3
3170,75 Dy 10 3 85 Cu 5 34 Mo 25 5
72 Ni I 4 250 7? 34 W 7 3
63 Kr II 12) 2349,84 As 1 18 32 Nb 1 30
58 Ag *5 3 82 W 6 10 28 Mn 40
54 V 3 3 81 Os 40 6 22 Ce II 10
53 Ce 2 81 V 3 150 21 Re 30
43 Th 10 4 80 Rb (80) 11 Mo 4 2
38 Eu 15 1 78 Mo 10 11 La 11 400 150
3170,35 Mo 1 1000 R 25 7? 70 Y 8 09 Ir I 3 (25)
35 Fe II 10 50 68 66 Rh Ir 3 5 125 08 J II
29 26 23 Ta Pd II CI II 250 35 50 (15) 2288,30 25 U - Rh 2 3302,99 94 Na I Zn 300 7? 7(10 7? 150 7? 300/?
20 20 20 V Sm П W 15 15 3 5 9 25 19 16 Au II Pt II CI 15 2 30 (4) 94 91 88 Ca Ce Cr 4 10 30 6 2
16 Nb 2 3 86 Fe 11 1 5
12 J II . . „ a . (5) Sb 82 u 6 4
09 Ru 30 77 Ta 50 1
09 u 2 2 2288,12 As I 250/? 5 72 Mo 25
07 Ce 12 10 67 Zr II ib 6
02 Nd 10 66 Pr 15 2
3169,99 98 и Dy 6 100 3 50 02 2287,93 Cd I v 1500/? 300/? 15 64 62 Tb Nb 8 1 10
96 Mo 20 (12) 59 Zn I 800 300
93 w 10 15 88 56 J II (10)
89 Tu 15 40 Ce 10 55 Bl 150 ......
87 Sm II 25 8 84 Ta 54 Kr I (10)
85 Ca 1 10 2 84 Те (5) 51 В ...... 10
77 Co too 49 и 3 1
Мышьяк As Натрий Na 49 J II (5)
2861,09 Nb 10 100 5897,38 Sm 100 45 Dy Tu 125 80
2860,96 Os 100 25 22 Yb 7 100 44 7 5
93 Cr II 60 100 5896,87 Sm 3 43 J II (2) 1
73 Ar (5) 7 к La 80 33 Ta 3
71 Cl II (5) 65 Те (25)
70 68 w7 2 6 9 61 61 Hf Yb 2 3302,32 Na 1 600 7? 300 7?
68 Pt 11 30 150 28 5 28 Kr (4)
68 Rh I 30 02 5 26 u 1 2
67 64 Ir I Ce 12 2 2 5895,92 Na I 5000/? 500 7? 23 19 Re Cr 30 50 I
64 Pb 2 70 Pb 20 2 18 Nb 5 10
56 Hf 20 2 63 Tu 80 20 17 Y 5 2
56 Ce 3 62 Хе I (2) 13 Pd I 1000 200
55 Tu 10 58 Nd 2 12 Pt 2
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ® ! ЛИНИИ ЭЛЕМЕНТОВ
Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Натрий Na (продолжение) Неодим Nd (продолжение) Нептуний Np (продолжение)
3302,10 TI п 8 20 4061,16 Gd 3 4291,45 S II _ - _ _ . . (5)
09 Sm 8 4 11 Fe 3 1 40 ть 3
02 3301,95 . Dv Ей 2 25 2 4061,09 Nd II 40 30 40 36 Hr Ти 5 (150) 5
93 Er 15 2 08 Er 5 35 Zr I 6
91 Ru 30 8 06 Sr 1 8 6 30 V I 15 10
90 Се 10 06 Xe II (2) 21 Ti I 3 1
90 Pr 10 05 Dy 3 2 20 Zr 1 6
90 Та 25 3 05 Sm II 8 8 20 Mo 15 15
87 Ar (Ю) 00 О II (1) 19 Nb 10 15
86 Pt I 300 250 4060,99 Au It 3 4 19 О II (15)
86 AI 2 91 u 4 5 18 Re 100
85 W II I 10 89 Hg (10) 16 Ba 10 3
73 Sr I 100 1U 86 Tb 25 3 14 Tl 10 4
’56 Os I 500 R 50 85 V I 2 2 03 Y I 4 2
79 Nb 10 10 02 La I 4
неодим no 77 U 6 4290,99 Pr 5 1
4305,46 Fe I 100 50 76 Cr 12 6 96 Nd 15 8
45 Cr 1 150 20 72 Ce 8 1 94 11 I 70 30
4304,94 Sm II 100 100 71 w 8 4290,9
90 Gd 100 100 60 о 11 (30) Np ...... 50
55 Mo 4 5 58 Dy 8 ’ 2 89 Pt 2 1
47 U 8 6 58 Zr I 10 88 и 15 15
44 Nd 20 12 56 Nd 10 5 87 Fe I 20 2 п
41 Re I 5 47 Ce 10 2 78 Kr (4) о
41 Hf C 2 38 Tb 20 1 6 Na I 3 со
28 ть 4 32 La I 80 5 59 Ce 4 Я
28 15 Ce SI 15 2 2 31 30 Nb Eu 5 2 5 57 53 Se II Ru I 6 (20) ё
14 u 15 1 30 Ho 3 2 51 Pr 4 X
13 Se II (10) 26 Tl I 60 25 44 Dy 5 X
12 La II 3 2 23 w 4 9 43 Ce II 2 X
07 Cl II (40) 23 и 3 1 40 Ne II (100) о
02 Tb 12 20 Hf 10 4 38 Fe 35 5 я
02 Mo 12 10 18 J II (5) 35 Nb 2 m
0 c (10) 17 Ce 6 1 30 Ce 2 X
4303,96 Tl 8 10 u 4 8 23 T| II 35 60
96 Ne 1 (5) 4059,27 p (100) 21 Zr I 40 20
89 Mo 10 18 Mo 30 25
88 Nb 3 10 Неон Ne 17 Ho 2 2 сг
81 Er 12 5402,79 Eu 1000 14 W 8 3 X
78 О II (60) 72 Am 1000 12 Ca 5 £
60 Dy 3 57 Lu 150 10 11 Mn 8
60 Hf 10 6 06 ть 25 07 Gd • 6 — «а
59 Pr 100 60 01 Sm 2 4289,94 Ce 50 25 X
4303,57 Nd II 100 40 5401,98 Co I 100 92 ti i 15 2 X
93 V I 100 100 90 Gd 40 100 X
54 Ta I 15 55 Tb 10 72 Cr I 3000 7? 800 7? S
53 w 4 43 Sm 2 СЙ
53 V 15 39 Ru 1 20 2958,92 Po I (250) Sa
46 Gd 6 6 21 Ce 6 14 Th 8 6 ГС
33 w 15 05 Mg II 2 5 12 Ta 2
32 и 6 6 04 Ru 125 10 u Ji. 4 2
>*,» Ne 1 (30) 01 Se II (75) 04 Ce t. з
24 Co I 15 2 5400,95 u 10 6 02 Ht 30 5 О
17 Ее II 12 15 95 Pr 4 00 Ru I 60 5 со
14 Pr 20 о 94 w 7 2957,92 TH 8 8
03 Dv 8 86 Sm 3 <)2 w 7 7
4302,98 Tl I 10 77 8 2957,9 Np
98 Ta 125 40 61 Cr 30 1 50
94 Tb 10 5400,56 (2000) 88 Re 2
91 Nb 2 10 Ne 1 84 U 4 2
89 Zr I 100 1 50 Fe I 125 84 Ce 2
77 Cr 40 2 5 k F 10 83 s (8)
72 Dy 10 49 Tu 8 79 Ce 3
7 к Sr 4 47 Mo 20 15 76 Dy 3
65 Ce 10 45 Xe I (4) 75 Mo 3 1
57 Dy 2 30 W 6 74 u 4 2
4301,60 Ir 200 10 23 Ra I (500) 68 Co 50 1
20 Nd 5 66 J II (10)
4062,82 Pr 150 50 5399,93 Dy 3 63 Fe 2 2
70 Cu I 500 20 88 Se (8) 63 Yb 3
44 Fe I 120 100 80 Ra I (250) 50 Ta 100 30
08 p II 15 76 Co I 10 52 V I 20 125
08 Mo 80 <80 74 Yb 1 15 36 Fe I 300 300
06 Se II (70) 69 Eu 4
05 4061,98 Sm Nb 2 6 10 68 58 Sm W 2 5 Никель Ni
96 Fe 3 1 57 Ce 12 3525,50 Sm II 15 2
86 Re I 20 53 Gd 8 49 Pr 4 2
86 Gd 3 5 к F 5 4 к Sr 8
81 Ce 5 49 Mn 40 34 Br (3)
74 74 U Mn 2 80 5 30 Нептуний Np 29 2-3 Os Nb 4 15 5 30
72 Nd 5 3 4292,18 Sm II 100 60 16 Tl I 10 1
70 Ce 2 4291,86 Ti I 5 14 Th 2 1
66 Pt II 10 82 V I 40 30 14 u 5 8
57 Dy 3 80 Re 3 13 Tb 8 8
57 Tb 40 2 76 CI II (50) 09 Co I 2
55 Eu 12 2 72 TI II (2) 06 Sm 2
53 Zr I 25 1 67 Mo 3 2 3524,98 Ba I 20 5
42 Ce II 6 65 u 5 I 98 Mo 5 5
40 Ta 50 30 55 Re I 25 94 Nb 2 5
35 u 12 1 63 Pr 18 2 92 Dv 6
34 Pr 4 2 61 Sm 8 8 92 Er 20 8
30 Gd 8 12 47 Nd Г) 90 Ru I 12 2
26 Nb 4 3 47 Fe I 125 20 87 Tl 11 5
О со 05 Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Никель NI (продолжение) Никель Ni (продолжение) Ниобий Nb (продолжение)
3524,72 V II 10 60 3415,08 Рг 4 3 4059,23 1г 30 4
68 W 7 5 07 Се 8 04 Ей 4
Мо 5 50 3414,95 Sm II 10 2 02 и 1 2
61 Dy 6 4 95 Zr I 2 4058,98 Zr I 8
92 Но 30 30 96 Mg 2
3524,54 Ni I 1000 R 100 88 83 V Dy 35 4 5 4058,93 Nb I 1000 400
54 Mn 15 82 Ne II (4)
54 Sm 10 80 Kr II (Ю) 93 Mn 80 60
54 Zr J 9 2 79 Er 8 I 93 Ca I 3
47 Pr 3 2 77 Eu 40 ...... 92 Tu 20 6
45 37 Ru Ir 2 6 77 77 Pr Ce 7 5 88 87 Ru Sm II 10 30 20
34 28 27 Eu J Hg I 3 1 (3) (15) 3414,77 74 Ni I Co I 1000 R 200 50 78 77 Pr Cr Ее I 25 80 15 50
25 W 9 8 66 F II (15) 76 40 10
24 Zr 12 66 Zr 11 20 13 62 Zr I 9 1
24 60 50 64 Ru 1 50 5 61 Mo 10
24 Ti 2 63 u 3 1 60 Co I 100
24 Cu I 40 10 60 Ce 5 49 si 3
23 Mo 8 3 60 Ca 2 46 Ta 10 5
20 Gd 25 15 55 Ag 1 4 45 Eu 2
19 Hg II (100) 52 Sm 4 44 Tb 5 1
15 Ru 6 51 Th 6 8 25 Dy 2
07 Ce 8 49 Y 3 2 24 Ce II 18
07 Cd 11 8 46 Ar II (5) 23 Gd I 100 60
07 Fe 50 40 42 Mo 20 23 Fe 80 25
03 Dy 15 20 36 u 8 1 20 Se II . ...... (20)
01 Ce 8 31 Ce 8 19 Pr 6 8
3523,98 Er 25 8 30 Cr 8 19 Co 1 100
97 Ho 4 30 Dy 2 2 16 U 10 4
89 Mo 10 30 Nd 10 2 14 Tl I 50 6
74 Ce 5 28 Ru 12 14 Ta У 2 1
70 3 14 Ta 18 100 08 La II 4
67 Eu 2 1 3413,94 Ni I 300 10 02 Tb 2
66 ть 30 50 48 Ni I 500 15 0 k Sr 3
64 Os 150 30 4057,96 и 1 6
64 Zr I 5 1 3052,15 Pd 1! 150 95 Mn 80 20
62 Nd 15 8 3051,30 u 4 6 82 Pb I 2000 R 300 7?
61 Ce 2 2 29 W II 10 30 46 Xe II (100)
59 Cr 10 1 29 Ce 2 20 Co 1 100
56 u 4 15 25 In I (15) 07 In II (100)
56 Til 17 n«
- -- 1
55 44 w Ni I 100 5 16 1о Ce II Ir I 6 1 4056,94 In II ) (500)
43 Co 1 300 R 25 14 U 15 10 3094,69 Sn II <6)
12 ть 15 8 66 Mo 150 25
3493,85 Hg II (100) 11 Nd 6 2 63 Eu 3 1
41 Sm II 2 1 09 Ir I 5 62 Sc 4 i
41 Eu 7 00 Sm 6 2 62 Fe 3 4
41 U 2 5 3050,99 Th 10 10 62 Ir 3
34 Mo 6 10 98 Xe II (2) 56 Ru 6 50
33 u 6 15 93 Co I 60 53 Xe II (12)
29 Fe I 1 89 V I 30 46 и 3 4
28 Tl I 15 1 83 Er 5 1 39 Ru 50 3
27 26 Tb Dy 8 3 3050,82 Ni 1 1000/? 37 36 Ir I Nb 5 2
25 Ar I (20) 82 Sm 5 8 33 Fe 2 2
22 Ru 20 1 82 Rh 2 20 V 20 125
22 F 11 (3) 8 Cs (6) 18 Eu 10
20 17 w V II 6 15 3 100 76 73 Hf Tu 50 50 10 150 3094,17 Nb II 100 1000
16 Pr 10 2 73 V 1 50 08 Ne II (12)
11 Ce 12 1 73 Ho 4 07 Os 30 8
10 Ho 10 10 59 Ce 12 03 W 8 10
04 Kr 11 (8) 58 J (7) 01 Ir 1 20 10
04 w 5 4 50 и 4 6 3093,99 Cu i 150 50
3492,99 ть 15 50 Co I 60 95 Ce 4
98 Ce 3 46 Hg 1 2 95 Cr 25
97 Eu 2 40 V I 30 1 90 Ru 30 100
96 Tb 15 39 Os 100 50 88 Nd 6
96 Mn 10 35 Pr 2 4 88 Fe 40 30
3492,95 Nl I 1000/? 100 32 08 Zr I Pd II 3 100 88 87 Yb Ta 3 50 15 15
95 Au II 4 3049,56 Ta 150 30 87 U 3 4
90 Sm 3 52 Nb 150 82 Dy 10 1
82 Mo 3 4 81 Tl I 5
80 U 2 10 Ниобий Nb 81 Fe I 50 40
78 Sm 3 3 4059,88 Th 8 8 79 V I 30
77 Hg (50) 88 Gd 50 20 77 Y II 9 15
76 Rb (300) 88 Ca 2 3 75 Er 6 1
73 Pr 4 1 78 Er 18 2 74 Cd II 3 2
68 Th 2 2 72 Fe 15 8 68 Mo 10
62 Sm II 8 1 61 Mo 10 10 49 Cr 1 100
59 Tu 20 10 51 Er 7 И V II 100 7? 400 7?
56 ть 15 8 51 Nb 5 2 3092,99 Mg I 125 20
56 Ce 3 43 Ru 7 73 Na II 50 (200)
54 Er 25 2 40 Tb 3 1 72 V 100 50
52 Dy 2 1 39 Mn 20 15 71 Al I 1000 1000
5 Tl II 35 38 Eu 25
49 Ce 5 37 Pr 4 3
37 Ce 3 1 3175,52 Er 10 2
3415,78 Co II 100 7? 20 35 Gd 10 3 45 Tb 8 3
24 Ir 10 2 32 Ce 11 8 45 Fe I 200 200
22 Os 5 8 27 p (100) 36 U 8
Ci 13 Th 2 1 26 Th 8 5 30 Cl 11 (6)
со 12 Tb 8 25 W 5 4 30 Ru 30 40
СОВПАДЕНИЯ СПЕКТРАЛЬНЫЙ- лИНИЙ ЭЛЕМЕНТОВ
О GO Продолжение
ЦО Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент искра Длина волны, А Элемент искра Длина волны, A Элемент искра
дуга (разряд) дуга (разряд) (разряд)
Олово Sn {продолжение) Осмий Os {продолжение) Палладий Pd {продолжение)
3175,25 15 Хе Ки 20 (3) 100 3059,09 07 Fe I S 600 R 400 (8) 3419,24 p II 150 (100)
14 Р П (70) 00 Eu 20 3405,89 Re I
11 Те I 30 (15) 3058,99 Tu 10 30 12 Co I 2000 7? 150
09 Na II (15) 98 и 8 5 03 Ag 3 2
08 Fe II 2 97 Pr 5 3405,99 Dy 4 4
06 Се 10 79 Ru I 30 3 97 Tl II 2
3175,05 Sn I 500 400/; 79 Re I 50 96 93 V I и 8 3 1 2
05 Мо 2 60 3058,66 Os I 500/; 500 92 Au 3
05 J II (10) 66 Ru I 30 3 91 Ce 18 2
04 Fe 1 65 Ir 5 86 Mo 6 4
03 In 3 64 Ta 50 3 83 Zr II 40 35
3174.96 Fe 5 4 6 Cs (6) 80 W 8 (12)
90 Co I 80 60 Mo 20 77 Ne II 6
88 Dy 12 4 55 Ce 12 77 Sm 2 2
88 La 11 3 10 49 Fe 3 3 76 Nd 4 6
86 Ho 6 6 43 Th 10 10 75 Fe I 2 ..... а
84 u 6 34 Cr II 30 72 Re I 100
82 Pt I 2 3057,90 Lu 3 130 71 Tb 3 8
80 Ti II 100 64 Nl I 400 R 125 65 Til 4 4
78 76 Re Yb 20 2 4* 45 39 Fe I Ne I 400 400 (250) 3404,58 Pd I 2000/? 1000 R
67 Mo 4 1 52 La 1 9 2
66 Tb 15 15 2910,02 V II 35 150 45 In II 12 (10)
65 Mn 15 2909,74 Ru 150 43 Ce
62 Re I 30 6 Pa 100 42 V . ..... 50
54 V 1 80 36 Hg 11 (25) 36 Fe I 100 50
53 Pt 2 32 Dy .2 34 Mo 20 25
31 Fe 4 2 33 P II . . • • • . (50)
3034,95 Nb I 100 25 U 6 15 30 Fe I 2 т 25
62 Те (10) 22 Ru 12 2 30 III II (18)
56 Ir 1 20 19 Yb 2 7 24 к II (30)
54 Cr 30 12 W 8 8 24 Tb 15 3
54 Fe I 70 40 11 ( Mo II 25 40 22 w 8 7
54 54 Re I Ca I 30 2 2909,06 Os I 500 R 400 16 14 Ta W 5 I 4
49 Sm 5 2 05 Cr I 60 12 13 In II (18)
48 Ne II (18) 01 Eu 40 13 Er 8
43 Co I 80 2 2908,98 Nd <3 13 Ce 18
38 u 3 1 98 Nb 1 5 10 Yb 9 30
20 Pr 3 91 Ta 150 10 3403,65 Cd I 800 500
20 w WMW L-Ьч 200
44 Зак. 783
19 17 16 12 Сг 1 Sm Кг II In 200/? 5 8 60 (2) 1 88 88 88 86 86 Mn u Ru Fe Hf II 10 2 80 3 2 8 40 5 3066,10 3065,31 26
Платина Pt 2 100 200
Pd I Pd I Nb 150 10 10
3034,12 Sn I 200 150 82 V II 70 7? 400/? 21 Zr II 5 2
12 Fe 2 24 Nb 20 200 21 Sm 3 2
11 4 I 20 U 6 4
07 Th 15 15 Палладий Pd 14 Dy 4 1
06 Ru 1 60 5 3422,74 Cr II 35 125 11 Sc II 12 25
06 Gd 100 60 65 Fe 1 100 50 07 Cr 20 50
05 U 6 5 45 Gd 80 100 05 Yb 4 30
04 Ir I 4 3421,72 Pt 2 04 Mo 30 10
3033,89 Ru 6 72 Cr 12 01 Sm 4 2
86 Yb I 3 71 Ce 3 3064,97 Er 3 I
82 V II 20 90 69 u 8 8 96 Cd 15
77 u 4 4 69 Os 30 10 94 w 10 7
71 Хе II (8) 67 Eu 5 5 91 Yb 2 2
62 Ir 1 25 1 64 Ar (10) 91 u 1 2
44 Ra II (150) 64 Cr 2 6 84 Er 7
3032,84 Gd 100 100 64 Ho 20 20 84 Ru 70 50
84 As I 125 70 63 Co I 20 2 79 Ir I о
ч Nb 3 300 58 54 Re Ce II 15 5 3064,71 Pt I 2000 R 300 7?
2840,42 Fe I 125 20 48 Ba I 2 2 68 Hf II 10 30
24 Gd 50 60 45 Hf II 3 4 63 Zr II 5 3
22 W 9 4 43 W 7 62 Nl I 200 /? 50
22 Ir I 15 10 42 Zr I 3 6 Rn (40)
16 Ce 3 38 u 8 2 60 Re 20
16 Tn 8 6 35 Co 1 3 59 u 4 3
11 V 2 25 34 Nl I 30 8 56 Mo 15
10 w 9 2 32 Dv 7 5 53 Nb 5 200
05 AI (15) 30 Sm 2 51 Ir 1 20 1
02 Cr 25 125 25 Mo 6 6 45 Ga 2
00 Mn 20 3421,24 Pd I 2000/? 1000 7? 38 37 Hf 11 Na II 2 2 (20)
2839,99 Sn I 300 R 300 7? 21 Cr II 50 200 37 Co I 100
98 In 2 21 Ta 1 3 30 AI 20 20
92 W 10 20 NI I 4 28 Mo 80 10
89 Pd It 100 19 Th 10 10 22 Fe 4 4
89 U 18 20 16 Nb 10 50 3063,70 Ne I (150)
85 Tu 5 10 16 Rb (20) 42 Cu I 300 50
82 Fe II 10 13 w 3 20
81 W II 1 10 11 Pr 10 1 2660,39 AI I 150 R 60
80 , Tl II 100 07 Ce 6 2659,75 Cr 2
80 Nb 2 5 06 Er 9 1 72 Ce 2
78 Ta 8 2 01 Ba I 3 2 70 w 12
69 Nd 5 3420,96 Ce 5 69 Hf 3
82 Ca 2 66 Ta 15
Осмий Os 81 Dy 5 2 62 Ru I 80 12
3060,05 Co I 150 1 80 Mn 8 61 V 9 40
3059,43 Pd II 150 79 Co I 80 2 6 *c 20
16 Ne II (7) 76 Re I 40 60 Kr II (2)
11 J (5) 74 NI I 30 3 47 Rh I 3 3
СОВПАДЕНИЯ СПЕКТРАЛЬНЫЕ ' ? ЛИНИЙ ЭЛЕМЕНТОВ
О 8 Продолжение
Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент искра Длина волны, А Элемент дуга искра Длина волны, А Элемент дуга искра
дуга (разряд) (разряд) (разряд)
Платина Pt (продолжение} Празеодим Рг (продолжение) Празеодим Рг (продолжение)
2659,45 Pt I 2000 500 R 4223,92 Мо г» 4 4179,40 Ег 5
88 Се II 20 1 40 Ей 2 1
43 Au 88 Вг (80) 37 Ва 6
42 41 Ец Та 4 20 10 82 72 ТЬ Ег 3 9 2 31 29 Аг Се II 10 (20) 1
29 Cd П (5) 71 Sm II 50 20 26 Сг 100 40
28 Yb 2 (20) 69 Pt и 3 24 Те (70)
27 J и 6 1 23 Со I 15 2
24 21 Ре Мп 8 2 10 64 57 Но 2 5 08 06 Се V 8 2
19 11 2658,91 W Rh ТЬ 10 100 500 51 47 47 Рг Но Cr I 12 4 15 3 04 00 4178,97 Ge и ТЬ 15 50 25 12 2
74 72 CI II Pd II 20 (100) 300 38 34 ру Sb и 2 4 87 64 Fe 11 Рг 10 18 10 10
3907,96 94 Плутоний Ри 33 32 J То 10 (15) 1 64 60 Nd Ег iu 8 6
се Fe 2 100 60 30 21 и Nd 1 15 3 3 60 59 Re Е>У 3 8 2
91 91 Tb Хе II 10 20 3 (50) 16 15 Ir Се 15 3 2 56 54 Ть Мо 2 5 2
90 84 79 Ir I Nd Tb 2 12 3 09 06 05 Lu Sm TI 1 3 4 2 (25) 53 52 44 Nd и Nd 8 8
78 75 74 68 Cr 30 10 04 N I (25) 36 р (300)
Sb Fe 2 (8) I 00 4222,98 Xe II Gd ib (200) 4177,60 Fe I Промет IOO иЙ Pm 25
65 Tb 3 4222,98 Pr II 125 40 4000,45 Dy 400 300
65 64 Au Ce 5 2 3 1 98 96 К II Mo 15 (40) 10 3999,95 94 и Сг 6 3 8
59 Ag 3 2 94 u 1 2 86 Мо 5
56 и 6 8 91 Tb 6 82 Dy 3 2
52 V 125 2 88 Ce 3 71 Nb I Q
48 Sc I 25 8 Na I 3 68 Cr 40 10
47 44 Fe Ce 15 6 6 2 78 74 О U 6 (50) 62 56 Br Но 6 (8) 2
44 О II (18) 73 Cr I 100 15 41 ть 12 15
34 Th 8 3 71 Tb 9 39 Ru 3
30 29 Pr Ce 8 35 3 6 67 67 Ar Tu 10 (20) 4 39 38 Pr Nd 2 20 6
20 VV 6 5 60 Ce 80 18 36 Tl I 30 5
3907,2 Pu II too 41 Mo 20 15 28 Ta 30 20
— L-! —— -— “—.
19 17 15 12 J II V Sn Gd 2 100 (18) 2 4 100 40 38 31 26 Br U Eu Ho 18 3 (4) 8 1 24 19 19 18 Ce II V Pr U 80 50 10 20 40 40 3
£ 12 10 15 22 Dy 10 18 Nb □ 10
II Eu 1000 R 500 R 22 Fe I 200 200 18 VV 4 5
02 u 5 1 20 Kr II (20) 17 Er 5 2
3906,98 Mo 5 5 15 P 300 (150) 13 Ca 2 2
93 Cs II (20) 15 U 1 3 10 Br I ...... (3)
92 Ce 8 3 06 Nd 5 2 3998,97 Zr II 30 30
92 91 Mo Nb 5 5 5 06 02 w Tb 15 3 8 3998,98 Pm 1000
89 Hf 3 3 4221,08 Re I 100 94 Dy 5
80 6 5 93 Os 80 12
80 Th 8 4180,95 Hg (100) 89 Tb 5
75 Fe w 10 94 Se II (800) 86 Cr 25 2
75 V 1 50 20 87 Tl I 100 20 83 Ir 2
53 Tb 4 83 Yb 10 100 82 u 3 5
48 Fe I 300 200 40 Pr 5 2 82 Eu 3 (60)
48 Mo 5 10 40 Tb 20 I 79 S II
45 Ce 8 2 38 10 2 76 W 8 8
41 Hg I 25 15 33 Dy 2 2 75 Ce 2
32 Er 25 12 31 U 12 1 73 V I 100 25
29 Co I 150 28 Er 6 2 70 u 6 4
29 Pt I 2 1 24 W 10 5 69 Pr 4 2
26 Ho 3 3 2 Na 1 3 69 Nd 40 15
25 Kr II Полон иЙ Po (150) 10 02 4179,98 Xe II Tu Ac I 5 1000 (bob) 2 50 64 63 51 Tl 1 Mo Hf II 150 100 25 4
2558,29 Mn — 12 96 Th 8 8 44 Nb 2 5
09 Os 12 2 96 Cr 25 1 44 Pr 9 3
05 Re 60 — 94 Mo 8 5 40 Tb 7
05 Sn 30 6 88 Tl I 4 35 Sm 10 2
02 w 6 81 Zr II 15 8 29 Mo 8 5
02 Ru 4 10 81 Ce 1 2 28 Ho 40 6
2558,01 Po 1 1500 80 76 Tb Nb 6 10 1 20 24 24 U Ce 5 2 18
2557,96 U 4 2 75 Re 2 16 VV 7 6
96 Zn 11 10 300 74 Ca 2 16 Nd 20 12
94 Nb 100 72 Th 8 8 12 J (5)
94 Dy 8 68 N II (2) 10 Dy 3
92 Rh 1 50 64 Br (40) 06 Fe I 150 100
87 NI II 80 63 u 2 1' 3997,97 s (8)
82 Br (4) 58 Nd 10 10 96 Pr 20 9
77 Os 10 1 58 Кг II (20) 95 Kr II (100)
75 Hg (5) 53 HI II 5 ’ 8' 91 Co I 200 20
71 Al П (40) 51 Cu II I 6 40 Fe I 300 150
71 Ta 50 100 46 Dy 3 05 Pr 100 40
70 Yb 4 46 8 3996,70 Dy 200 80
20 Rh 1 100 43 и ib 1 Протактиний Pa
Празеодим Pr 2C0 2744,19 Mo 2 25
о 4224,18 Fe 1 200 80 4179,42 Pr II 40 13 Er 2 ! 2
co 4223,96 Ba 5 3 42 V I 20 10 09 Tu 20 50
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ Ж / ЛИНИЙ ЭЛЕМЕНТОВ
g Продолжение
Интенсивность Интенсивность Интенсивность
Длина Длина Длина
волны, А Элемент искра ВОЛНЫ. А Элемент искра волны, А Элемент искра
(разряд) дув a (разряд) дуга (разряд)
Протактиний Ра {продолжение) Радий Ra (продолжение) Рений Re (продолжение)
2744,07 Fe I 150 8 3814,62 Сг 35 30 3461,65 Ni 1 800/? •50
00 Ir I 12 2 62 Се 2 2 57 Rb II (200)
2743,93 Ru 50 100 59 Th 15 15 50 Tl 11 80 125
2743,9 Pa 200 58 58 Tl и ть 12 15 35 18 08 Со I Ar I 100 3 (300)
90 Ag II - . . . , . 50 57 Dy 4 3 3460,97 Dy 100 3
87 Re 25 52 Ее I 80 40 95 Ho 6 4
77 / V 7 30 52 Ce 4 3 90 Kr (2)
71 Mo 30 1 49 Mo 4 4 78 w 3 3
67 Ir I 3 46 Co I 35 78 Mo •25 25
66 и 4 8 43 w 2 6 78 Ce 2
64 Cr II 30 125 78 u 2
64 Hf 15 1 3814,42 Ra II ...... (2000) 77 Pd I 300/? 600 ’
20 Fe Ц 80 150 26 Os 30 10 72 18
2742,99 Ni II ...... 500 23 Yb 3 10 70 Sc 1 6 2
Радий Ra 10 07 Mo u 4 25 3 15 66 64 Pr Dy 3 4 I
4827,59 Ne I (300) 02 La II 2 2 63 Sm 3 1
34 Ne I (1000) 02 Lu 2 ...... 58 Ce 2
28 у 02 Cr 2 4 58 Nd 25 6
25 Pr 20 3813,98 Gd 100 60 54 Ir 3
24 Er 3 97 Tb 3 3 52 Ne I (75)
14 Те (50) 92 Co I 30 48 Tl II (20)
12 Dv 2 90 Mo 2 20
1 Hg I (15) 89 Fe 50 25 3460,47 Re I 1000
4826,99 Tu 10 25 85 Se (2) 43 Cr I 40 30 о
90 Mn 10 5 82 Sm 5 42 w 15 и
89 La II 15 30 79 U 20 15 40 Dy 20 2' □
82 Th 3 79 Ir I 5 38 Tb 15 8 >
80 ть 2 68 Dy 20 35 u 3 5 5
77 S II (3) 63 Fe 35 15 33 Mn Ц 60 500 5
75 Ir 15 63 Sm 10 4 31 La 11 2 3 X
66 Os 18 58 Ce 5 29 Eu 15 1 X
65 Pr 40 54 Cu I 8 27 Yb 30 5 Л
58 15 49 V I 50 23 Mo 5 5 а
56 Dy 4 2 47 Nb 3 5 16 Ce 6
55 Ru 4 3812,96 Fe I 400 300 13 Kr I (2) Ж
31 Pr 9 47 Co I 100 13 Nd 6 2 ±
22 19 Tb Ru 2 4 Радон Rn 09 08 Kr II Xe II (50) > (5) Ь
4825,97 Ar 1 (2) 7451,40 W 3 06 1) 5 сг
93 U 6 11 Nd 5 05 Dy 5 1 1
08 Dy 2 02 Mn II 5 5 Е
4825,91 Ra I • ••••• (800) 00 Xe I (25) 3459,02 Os 100 10 *
. ' J *
82 Pr 10 7450,65 Ru 4 Родий Rb ь
74 Ru о 4 Yb 2 X
65 Eu 5 2 36 Eu 6 3694,20 Yb 500/? 1000 7? *
62 Hg (70) 33 S I (15) 20 Ne II (250) =
59 Mn 20 5 30 Y II 15 10 01 Fe I 400 ЗОЭ s
53 Ne I (50) 00 Sm II ИХ) 150 ф
48 Nd 100 8 7450,00 Rn I (600) 3693,36 Co I 18 ь
47 Pr 5 7449,42 AI II (18) 36 Pr 30 8 W
46 Tl I 10 1 34 Fe II 6 32 и 4 6 m
43 Ta 150 28 Sm I 8 23 Mo 3
42 Cs (10) 09 S 1 (5) 13 Nd 20 8 q
39 Eu 2 7448,76 Nd 3 11 Co I 80 15 О
38 Sm 9 09 Cr 10 5 «
21 Er 5 05 Ta 35 3
18 Kr 11 (300) Рений Re 03 Fe 15 7
4824,97 Dy •5 2 3692,95 Tb 30 8
67 u .3 1 3466,20 Cd I 1000 500 91 и 5 10
66 Sin 10 3465,86 Fe 1 500 400 91 w 7
66 Pr 80 Co I 2000 R 25 90 Sm 10 2
59 Tb 2 22 Ir I 12 1 81 Mn 50 50
56 Er 3 20 Cs (4) 77 Nd 12 8
07 La II 150 150 20 Mn 2 76 Sm 20 6
4823,52 Mn 400 80 12 Er 8 75 U 10
41 Xe II (150) 09 W 10 72 w 7 3
17 Ne I (100) 04 Mn II (18) 69 Ir I 15 4
4822,98 Pr 125 10 02 Th 5 5 66 Eu 5
3464,99 Ce 12 65 Fe *5 1
3815,84 Fe I 700 700 95 u 4 4 65 Ho 10 15
8 BI II (300) 93 Nd 10 2 64 Er 20 12
39 V 1 150 92 Fe I 2 64 Mo 3 150
38 V 2 88 Os 15 5 64 Zr II 2 1
37 Ce 2 87 и 2 57 Th 10 2
36 Mo 8 86 Ce 12 55 Ce 2
34 Nd 6 4 84 Cr 30 3 53 Y I 7 7
16 w 5 44 О I (50)
15 и 1 6 3464,73 Re I 100 37 Ru 6
07 Th 8 8 72 Ce 2
06 Mo 5 4 67 U 2 3692,36 Rh I 500 150
01 Rh 20 20 66 s (8) 31 La II 2
01 Ce 3 63 Tb 8 3 29 Pr 4 1
3814,96 Zr II 5 5 54 Er 10 3 26 J II (5)
96 Tb 8 49 Fe II 1 1 22 V I 200/? 150 7?
93 Ce II 2 3 47 LJ 4 22 Ce 3
89 Nd 10 6 46 Dy 2 1 22 Sm II 90 40
88 Th 10 5 46 Sr II 200 200 22 Eu 4
87 Eu 5 5 45 w 12 20 Ir 2 5
86 Tl I 30 4 43 Sm II 3 1 18 Nb 5
86 Ru I 20 35 42 Th 2 2 13 Ti 12 1
78 Fe 10 5 37 Yb 200 7? 50 7? 13 Re 15
76 Gd 8 10 37 Cd II 10 08 Mo 5 3
72 Nd 6 8 36 Eu 15 08 Th 8 4
70 Rn I (12) 34 Ne I (75) 05 u 4 4
<Л 65 F II (Ю) 23 Ba 5 02 Tb 15 8 1
£2 63 Sm 11 5 3463,98 Gd 100 125 3691,98 Eu 3 1
fe • Продолжение
•F* Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Родий Rh (продолжение Ртуть Hg (продолжение) Рубидий Rb (продолжение)
3691,92 88 и Th 6 8 ) 8 2 4359,58 34 Nl I ТЬ 100 2 10 7800,74 44 Zr I Sc I 2 40
88 88 69 W Та Yb 4 10 20 15 31 24 16 Re Nd Gd 12 15 20 3 7800,23 22 Rb I F I 9000 R (50)
62 57 6 1 11 Pr 70 25 0 si 4
25 3 09 Ac 30 7799,58 Re 3
55 W П 5 9 08 Sc 12 51 Zr I 2
55 55 Eu II I 20 (2) 07 05 Ce Tb 15 2 2 51 36 Ta Zn I 3 10
50 Re I Pr 100 9 3 02 4358,83 Cs Th 3 (Ю) 2 . 4203,73 Tu 250 25
u 3 3 82 TI II (5) 59 Cr I 100 20
45 Ho 6 4 82 Ne I (2) 23 Rn (200)
42 Th 5 1 77 ть 2 4202,76 Fe 10 4
38 Re 12 74 Zr I 10 71 Ce 2
3690,90 Ar I Rh I 125 (ЗСЮ) 50 74 73 Ho Y II 3 60 50 70 68 Pr Eu 8 15 3
70 Nd 15 8 68 U 6 2
3435,37 V 20 69 Re I 80 52 Sr I 6
Dy 4 2 65 u 2 3 52 Ir 8
26 3 65 Ta 10 51 Gd 15
26 Os 20 10 64 Sc I 10 50 Br (25)
24 21 w Ce 6 20 35 5 2 60 56 55 Pd I Th Mo 25 4 20 4 10 43 41 4 Ir Pr Al Ц 8 3 2 (8) n © cs
20 u 10 50 Fe I 70 20 34 V II 6 15
19 Ru I 60 20 50 In II (2) 25 Dy 20 4 fe
08 06 J II 12 (7) 3 46 43 Dy Tb 25 3 4 24 22 P Mo 5 30 5 m x
3434,92 ть 30 200 R 42 34 Ca Pt I 2 5 15 06 Ni i Os 5 100 *4
3434,89 89 80 Rh I 1000 R 4358,33 33 3000 3 500 03 Fe I 400 300 о
Hf Qs 5 20 3 Hg 1 Th 03 4201,99 Eu Ar 5 (20) □ m
80 79 u 2 1 32 Mo 40 97 Ta 5 10
Mo 50 12 28 Ir 8 (250) 85 Th 8 u
76 76 Th Ir I 8 10 8 27 17. N Er 4 4201,85 Rb I 2000 R 500 2a cr
76 75 74 Pr 20 2 17 Nd 50 20 77 Ca 2 X
Ho 3 4 14 03 Os Ta 9 3 1 10 /6 72 Mn Nl I 40 30 20 г X
73 Hg 15 4357,98 Os 12 63 U 1 2
7 ...
Л ли- A
72 Rb (40) 97 Re 15 60 Er 8
65 Ag I 2 92 In II (2) 58 Ar II (2) s
63 Er 12 2 92 Ne 1 (5) 53 Pr 30 12 X
61 U 12 1 92 La 1 5 2 52 Nb 10 10 X
61 Yb 5 20 91 Ce 12 1 50 La Q 12 s
54 Tb 15 3 89 Sm 3 2 46 Zr I 50 3
50 Ta 35 18 87 Mo 6 2 45 Os 30 3 w
50 Mo 5 4 80 Gd 2 42 Kr II (30) rn
49 Pr 3 76 Eu 7 2 42 u 8 8 3
3433,56 Nl I 800/? 50 73 V 1 10 37 Dy 8 4 m
45 Pd I 1000 500 63 и 3 3 35 Br (5) X
59 Th 8 4 32 Dy 30 ©
3397,50 Tu 100 50 57 Fe 2 3 32 Mo 5 5 es
34 Ho 4 57 Nd 3 30 Ce 4 20
32 Nb 50 52 Cr 12 4 25 Хе II (8)
26 Hf 20 3 50 Pr 25 5 24 Ce 8 3
25 Ni 2 49 Tu 6 2 22 Pt I 2 2
21 Bl 1 100 50 47 Tb 5 18 Pr 15 10
21 Fe 1 45 V I 7 6 18 Mo 4 3
21 ть 15 39 Er 2 14 Tu 4 5
21 Re 15 13 u 4 4
20 u 12 2536,82 Ее II 10 4 01 Dy 5
19 Cs (61 80 Co 2 4200,99 Tb 40 4
11 Th 2 3 79 u 4 2 93 Fe I 80 20
08 Cc 12 76 La II 3 68 Ar I (1200)
07 Lu 50 20 75 Tb 3 10 4199,89 Ru I 3000 300
05 Y I 7 5 71 Pr 8
3396,98 Fe 1 125 25 71 Rh 15 5 Рутений Ru
3396,85 Rh I 1000 R 500/? 67 67 Fe II Ta 1 2 5 3729,82 29 Tl I Ar 500 150 (200)
83 Er 12 2 67 In II (10) 00 Ce 5
82 Mo 4 3 66 Ir 3 3728,98 La II 2
82 Ru I 20 60 W 1 12 96 Tb 8 3
82 Lu 30 1 60 u 3 2 93 Ni I 2
78 Pd I 10 56 Bi 5 2 93 Sm 10 4
73 Th 5 I 56 Th 5 10 89 Mn 75 100
72 66 Ce Zr 11 15 8 5 2536,52 Hg I 2000 R 1000 R 86 86 u Ir I 6 3 6
58 Pr 4 4 49 Co I 1 2 84 Co I 18
58 Eu 100 10 49 Pt I 100 10 83 Pb I 20
52 V I 15 12 24 LI 4 2 82 Ta 8
46 Co I 3 23 Ta 100 75 u 4
40 Th 2 2 22 Fe 3 74 Dy 4 2
38 Fe I 1 22 Ru 12 6 68 Tl I 15
37 Nb 2 150 2535,61 P I 700 67 Fe I 18 10
3395,61 Cr 2 100 60 Fe I 1000 67 Rb (20)
38 Co I 400 R 50 59 Ru 100 66 P II (50)
Ртуть Hg Рубидий Rb 65 65 Eu Tb 2 8 3
4360,93 Gd 200 7802,65 Хе I (100) 50 Mo 10 10
71 Sm II 100 60 7801,54 §m I 150 47 Sm II 100 100
4359,93 Tu 300 30 53 HI II 2 6 46 Ca 2 3
80 Pr 100 40 30 SI 3 46 Ir I 4
63 Cr I 200 150 05 Re 4 44 U §
Продолжение
8 Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга нскрз (разряд) дуга искра (разряд) дуга искра (разряд)
Рутений Ru (продолжение) Самарий Sm (продолжение) Самарий Sm (продолжение)
3728,42 50 10 4425,44 Са I 100 20 3568,51 N Ь 10 50
'41 Os 20 40 Ne I (150) 44 Ag . 2 1
34 V 20 150 25 То 2 43 Со I 2
30 Мо 10 5 22 Hg II (30) 42 Fe I 20 4
28 W 7 8 22 Рг 2 42 Сг 6
23 Ей 20 и 2 5 42 W 4 4
23 Se (20) 19 Kr I (100) 33 Dy 4 2
21 Hg (2) 14 Br I (12) 29 Рг 5 4
18 Се 5 1 13 Сг 15 1
16 15 2 12 Се 2 3568,28 Sm II 40 50
13 Nd 6 8 01 Gd 8 4
11 Та 7 4424,99 Sm 3 2 23 Re 40
04 Kr II (7) 96 Та 10 3 18 Мо 3 4
03 Ir 60 10 91 W 8 2 14 Zr II 4 2
80 Ne I (300) 13 Се 10 1
8728,03 Ru I 9000/? 300 78 . Ru 25 07 Мо 3 3
02 Се 8 5 75 Ir 3 04 W 10 10
00 Ег 5 66 Nb з 00 So И 1 6
3727.99 Dy 15 3 60 Pr 90 35 00 (г 15 5
90 Th 15 5 57 Er 10 00 Nb 2 50
86 W 6 7 56 V I 20 15 3567,98 С| (6)
84 Ir I 8 54 Ce 3 98 Тп 5 5
82 U 3 2 46 Tb 3 86 ТЬ 8
82 Fe I 5 3 39 Tl I 15 2 84 Lu 100 7 n
72 69 Zr II Mo 2 25 4 25 4424,35 Sm II 300 300 74 73 Мо Ba II 2 2 3 3 о D9
63 Ce 3 34 Nd 50 50 72 Ей 3 Z3
62 Fe I 200 150 31 Ce 6 72 Fe 2
49 Re 8 28 Cr I 25 35 71 Th 3 3 ГП
45 U 5 20 Mo 5 3 70 Sc II 15 40 3C
39 Ir 2 14 Ce 3 68 w 6 7 s
37 4 2 10 Gd 25 10 66 Ar I (300)
36 Cr з 08 Cr 10 2 58 Er 8 о
35 Xe (2) 05 Rh I 5 2 56 TI II (10) Z3
34 V II 40 200 05 Cs II (10) 49 u 3 1 m
33 Ce 3 0 4423,99 Ar I (80) 46 Mo 1 3 X
30 О II (50) 94 Th 8 4 38 Fe I 10 2 *0
27 Th 5 8 93 Pr 5 1 36 Hf 20 10
23 Nb 5 10 91 V I 7 6 36 Tu 10 ba
16 Th 3 9 P II (30) 35 Ta 4 cr
10 Fe I 30 10 90 La I 5 5 35 Tb 15 15
09 Y II 3 8 87 Nb 1 5 30 Dy 4 X
08 Ne II (125) 86 Tb 2 3566,37 Ni 1 2000 R 100
05 Tl I 2 82 Re 2 Свинец Pb ba
3726,93 Ru I 100 150 78 w 12 5 (100) s
92 Fe I 100 70 76 J II (80) 4059,27 P a:
80 Sm II 100 3 74 и 6 8 4058,94 Nb I 1000 400 s
24 Nb 30 100 72 к II (10) 81 Tb 3 s
68 Pr 2 78 Pr 25 15 Cp
3499,39 Ce 4 68 Ce 25 3 77 Cr 80 50 ba
37 Ir I 2 62 Mo 40 40 76 Fe I 40 10 rn
34 ть 15 55 P (30) 62 Zr 1 9 1
33 u 6 15 44 Ce 12 61 Mo 10
30 Ce 4 38 Sm 9 2 60 Co I 100
27 Os 3 2 35 Eu 4 49 SI 3 О
20 Mo 3 4422,70 Kr II (100) 46 Ta 10 5 co
11 Ir I 5 57 Fe I 300 125 46 Eu 2
10 Er 18 15 52 Ne I (300) 44 Tb 5 I
10 Ti I 25 10 41 Gd 100 40 25 Dv 2
09 Pr 40 3 24 Ce II 18
08 Ho 10 10 3570,18 Rh I 400 7? 150 23 Gd 100 60
07 u 6 8 10 Fe I 300 300 23 Fe 80 25
07 Mo 20 3569,78 Os 100 30 20 Se II (20)
3498,99 Th 8 8 38 Co I 400 7? 100 19 Pr 6 8
98 Hf 6 28 Cs (4) 19 Co I 100
95 Ir 25 25 Er 8 16 u 10 4
600 25 Dy 2 14 Tl I 50 6
3498,94 Ru I 6000/? 24 W 8 7 14 Ta 2 1
94 Y I 8 6 23 Nd 20 4 08 La II 4
94 Dy 15 19 Ta 2 02 Tb 2
92 Ce 2 17 Eu 4 1 0 k Sr 3
92 Mo 3 1 15 Cr 4 4 4057,96 U 1 6
92 Kr II (2) 08 V I 7 1 95 Mn 80 20
91 Sc I 8 2 06 и 12 20 87 In 80 10
87 Ho 8 10 04 Hf II 20 50 82 V I 10 2
83 Ce 2 3568,99 Dy 100 82 Th 2 3
76 74 Fe Ir 1 15 99 98 w Tb 9 15 9 15 4057,82 Pb I 2COO7? 300/?
73 Tb 8 98 Fe I 50 35 82 Er 30
73 Rh I 500 60 94 V I 20 15 71 Zn II 80
71 Er 10 3 91 Ca I 2 68 Tb 2
68 Ce 15 89 Sm II 4 1 65 Sm 10 3
* 67 Dy 50 50 88 Mo ’4J 2 63 Mg I 10
64 He I (3) 88 Nd 6 12 62 Ti I 40 6
63 Nb 30 50 88 Zr I 12 58 Mo 10 4
63 Th 6 3 82 Fe 15 7 56 Ce 2
60 u 2 4 82 U 6 3 oo Ho 2 2
56 Ce 8 72 Nb 5 5 46 Xe П (100)
54 Os 80 15 69 U 3 45 w 6 7
50 Kr 11 (4) 68 Tu 5 5 44 Mo 4 4
46 Sb II 300 65 Dy 4 43 Hf 3 2
3497,84 Fe I 200 200 57 Os 2 5 40 Dy 4 4
54 Mn II 15 150 53 Ne II (25) 39 p (50)
52 u 2 2 35 Nl I 2
Сак арий Sm 51 Ce 2 35 Fe I 20 3
4426,27 Ir 400 10 51 Tb 50 50 34 Th 10 8
co 01 Ar (300) 30 Ce 2
e> <£> Продолжение
Интенсивность Интенсивность Интенсивность
Длина Элемент Длина Элемент Длина
волны, A дуга искра волны, А дуга искра волны, А Элемент дуга искра
(разряд) (разряд) (разряд)
Свинец Pb (продолжение) Селен Se (продолжение) Серебро Ag (продолжение)
4057,20 Co I 100 4730,52 ть 3 3383,28 Се 8
19 In П (Ю) 48 Rb И . _ _ - - - 10 14 Sb 40 50
10 Ca 2 3 38 V I 9 8 12 W 18
08 CI (10) 38 J _ ~~ (25) 12 Th 5 10
07 V I 20 10 36 Мп 15 5 05 Y 3 3
07 In II (100) 31 Nb 5 5 3382,90 Zr 3
06 Tb 4 1 3 Bl II (25) 89 Er 18 1
01 Kr II (300) 16 Mg 1 2 3382,89 Ag I
4056,98 Co I 20 2 14 Gd 30 1000 7? 700/?
94 Nb 3 5 12 Та 100 5 89 Ce 8
94 In 11 (500) 4729,88 Th 6 5 83 Y 3 3
90 Ce 15 2 83 Те (50) 81 Nd 200 10
84 Nd 8 8 82 BI 2 80 Tb 15 g
54 Pr 100 60 72 Sm 2 70 Ce 8
72 Cr 30 6 68 Сг II 35 200
2834,06 Re 100 R 70 Fe I 25 25 68 O I (12)
2833,64 Ta 300 40 65 W 30 15 68 и 4 4
34 Th 8 8 53 V I 15 12 66 Pr 10 2
31 Tl II (25) 47 Sr I 4 61 w 10 12
31 Ce 50 45 S II (8) 57 Pd II 2
30 Nd 1 10 29 Nl I 10 53 V 125
28 Hr 25 4 23 Sc 1 100 50 51 Ce 8
25 Eu 10 5 4728,47 Gd 150 100 48 Mo 15 15
24 и 8 4 44 Sm 150 41 Eu 9
24 Ir 7 20 42 La II 400 R 300 41 Fe I 50 10 О Q
14 к 2 (2) 4727,94 Co I 300 41 Sm II 100 40 сэ
10 Fe II 5 Rh Zn II 41 Nb 40 □
2833,07 Pb I 500 R 80 2040,19 00 2 100 (250) 3381,50 Co I 100 la
06 Er 25 2039,93 Al II (15) 3281,17 Ho 4 re
06 Zr 2 1 91 Re 3 9 12 V 3 50 Z
06 In 3 2039,85 Se I (1000) 12 U 2 1 за
06 Eu 3 83 4 10 Ce 18
04 Ce 3 80 w 10 07 Mo 25 3 о
03 CI (4) 79 Те 300 03 Th 2 5
00 Kr II (ЮО) 79 Ir 8 3280,92 Os з ж
2832,95 w 10 3 70 Pt 12 20 91 Y II 8 12
95 93 Zn Ce 2 (25) 67 5 Rh 2“» 200 88 87 Mo Ta 3 25 2 й
92 Ne I (8) 84 Sm 20 6 cr
92 J (20) 76 Mn 60 30 z
79 Nb 5 4818,02 Xe II (100) 75 Zr II 3 2 E
77 Ir 5 4817,64 Ne I (300) 74 Th 2 2 X
1ЙЙ111Ж..1, ww............. _„
77 66 Rh I Mo 5 5 15 01 Rn Pd 4 (100) 2 69 68 In Cu 10 3 2 b s
64 U 2 2 4816,96 Mo 3 3 3280,68 Ag I 2000 R 1000 7? z
62 Ru 20 9 k Pb 6 — s
57 Ce 2 84 Gd 50 20 68 Co 2 s
46 Cr 2 . 125 82 w 5 68 Pd 2
44 Fe I 300 200 71 Br II (300) 67 Mo 3 Sa
26 Am II 5000 62 Er 2 67 Ce 6 re
16 Tl II 25 100 48 Sm II 8 61 u 1 2 3
Селен Se 40 38 Yb Nb 20 50 1 50 60 55 CI Rh I 30 R (8) 10 re z
4732,61 Gd 300 300 14 Cr 30 50 Lu 10 о
46 Ni 1 100 .<***. 13 Pr 7 48 Ce II 15 1 св
19 Pr 3 11 W 10 1 48 Xe (4)
08 Ar II (5) 03 Sm II 20 40 u 5 1
06 Co I 40 4815,96 Os 60 39 Tl I 3
02 Yb 1 15 89 Co I 4 1 37 Th 10 12
4731,86 Ir 8 5 81 Sm II 125 80 32 Mo 5 5
85 Dy 30 10 70 U 5 28 Tb 30 15
85 Tb 4 67 Pr 7 26 Fe 150 150
82 Eu 4 63 Zr I 40 22 Er 12 3
81 Nl I 100 2 52 Ru I 20 22 Sm 4
78 60 Nd U 40 40 ’ 50 ’ 4815,52 S II (800) 20 20 Nd P 2 4 (30)
59 49 Er Fe II 8 5 1 1 50 39 Os Ir 18 2 Скандий Sc
44 Mo 100 100 12 Ta 5 15 3913,64 Fe I 100 25
37 Hf II 15 20 11 Mn 15 3912,90 Pr 150 80
36 Sm 5 10 Ir 2 81 In 15
33 Ru I 60 05 Lu 20 2 78 ть 5 8
3 Rb (8) 04 Zr I 15 75 Mn 5 5
27 Те (70) 4814,84 U 2 74 и 2 4
25 V I 3 3 80 Ge 11 200 74 Gd 5
19 Xe П (50) 73 Tb 3 61 Pr 10 5
18 Rh .. . 2 72 Ru I 4 59 Kr II (70)
17 Tl I 50 6 62 Nl I 5 59 Tl I 15
15 s (15) 52 Eu 2 2 54 Dy 5
14 Zr I 5 49 ть 2 48 J (25)
10 Th 4 47 Mo 10 8 45 Fe 2 1
00 U 6 4 34 Pr 30 3 44 Ho 4 2
4730,98 J II (10) 34 Ne I (50) 44 Ce 50 5
96 Sm 2 33 Sm 3 44 Ta 15 10
92 As II 125 26 Cr 100 43 Eu 5 1
80 Tb 2 2 • P II (30) 43 Er 12
80 Er 2 10 Mo 2 5 41 Ir 2
4730,78 (1009) 4813,98 100 2 41 U 6 8
Se I 48 Co I 1000 6 31 NI 2
77 La II 2 2 4812,75 Ta 150 5 28 Th 15 15
74 4 27 Pr 10 3
71 Cr 100 50 Серебро Ag 25 ть 5
71 w 5 3383.98 Ее I 200 100 23 u 2 1
69 Pr 60 1 76 Ti II 70 300 7? 23 Nd 20 20
о 68 и 5 70 Fe I 100 70 21 V I 50 20
$ 06 Ar (5) 38 Pr 15 3 19 Ce Ц 25 3
Продолжение
© © Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность" Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Скандий Sc {продолжение) Скандий Sc (продолжение) Скандий Sc (продолжение)
3912,13 Та Ru 10 10 3 8 3907,12 12 Gd Sm 100 10 100 15 3613,03 01 S II Nb 2 (12) 2
09 05 00 О II Fe Сг 5 40 (5) 5 11 02 3906,98 Eu И и Мо 1000/? 5 500/? 1 5 3612,94 90 88 Fe I Те Cd I 20 800 4 (5) 500
3911,99 97 95 94 Рг Ей О II Мо 20 4 5 6 (150) 5 93 92 92 91 Cs II Се Мо Nb 8 5 5 (20) 3 5 5 87 87 86 86 Er Th CI In 10 5 2 . 1 (Ю) 15
91 91 91 Th Ег 8 5 3 89 80 HI Sm II 3 6 3 5 84 74 Ce Ni I 3 400 50
Nd 12 6 80 Th 8 10 20 47 Rh I 200 50
82 81 Cr I Os 10 30 5 75 75 53 Fe V I Tb 10 50 4 4609,91 Стро Ne I нций Sr (150)
3911,81 Sc I 150 30 48 Fe I 300 200 60 Ar II (300)
Но 3 48 Mo 5 10 38 Rn I (250)
80 Рг 8 2 29 Co I 150 4608,81 u 3 5
78 77 73 Re Lu Се 3 3 3 25 3614,80 Kr II W 6 (150) 2 81 78 78 Re Er Tb 3 2 3
70 68 Fe Dy и 1 5 1 8 78 k La Rh I 5 15 10 75 71 Ce Mo 2 10 10
67 18 18 77 Zr II 40 80 68 Ru 6
66 61 Gd Eu 5 5 74 72 Sm Fe 4 6 1 1 67 59 Ho Gd 3 6 1
58 56 Ar Er 8* (10) 71 70 Dy Eu 15 3 5 58 54 Nb Ca 2 3 ’ 2
42 Mn 15 15 69 Mo 1 20 49 Ce 6
36 Tl I 7 64 Er 12 1 46 Cu II 2
31 Th 5 3 63 Tb 30 8 44 Tb 8
31 Pr 5 3 56 Fe 15 6 42 К II (40)
30 Ce 15 1 51 Rh 4 2 34 и 2
29 W 6 5 45 Ir 2 2 28 Os 12
28 Yb 8 45 Cd I 60 100 15 Eu 2
23 u 3 3 41 Gd 3 12 Rh I 15 5
19 Ti I 40 5 4 k La 4 12 Mo 5 5
17 Nd 25 25 36 Ce 3 09 Hf 2j 4
14 Ru 6 2 26 w 5 2 02 Gd 8 3
12 Mn 20 25 Mo 50 30 00 Pr 5
09 Mo 20 20 23 Ce 3 0 Ho 2
09 Se II (2) 22 Cu I 50 6 4607,97 Y II 2
00 _ .Th - 2
00 Fe 6 2 2 к La ШМММММММ *3 . ...... адл- J 89 Tu 2 1
3910,98 U 10 3 12 Fe 10 3 81 Tb 4
92 Sm II 1 2 08 Eu 2 2 65 Fe I 50 5
91 Pt 5 2 08 Dy 30 10 62 Mn 50
85 Tb 5 * . . , « . 03 Ce 5 I 50 Au 15 /?
84 Fe I 30 10 01 Th 6 8 46 200
26 Pm 1000 00 Au 20 38 Nd 25
3909,93 Co I 200 00 u 2 34 Au 1 30 15
3908,76 Cr I 200 150 3613,94 90 Rh I Sm 2 2 4607,33 Sr I 1000 77 50 7?
47 u 8 10 3613,84 33 Co 2
43 Pr 100 GO Sc 11 40 70 3 k La 3
42 Er 10 82 Bl 30 29 Ce 3
41 Ce 30 6 81 J (10) 23 V 4 3
33 U 10 1 80 Mg II 4 17 N II (50)
32 V 50 2 8 к La 3 09 Ce 2
26 Sm 6 79 W II 10 30 08 Mo 8 io
25 Mo 5 3 78 Th 5 3 4606,92 Pr 3
20 Re 25 76 Cu I 60 7 83 Ru 4
16 Mn 3 3 76 Eu 2 1 8 ftSc 10
15 Gd 5 3 76 TI 12 77 w 2
09 Ce II 8 1 75 и 4 77 Nd 50 50
08 Tb 20 70 Zr I 9 72 Tl 4
03 Pr 100 50 70 Ce 18 5 65 Gd 3 3
3907,96 Ce 2 70 Pr 6 2 61 Er 20 1
94 Fe 100 60 68 Tb 15 3 60 Hg (5)
91 ть 5 67 Cr 10 8 52 Sin II 40
91 Хе II (50) 64 Mo 3 4 51 Mo 4 3
90 Ir I 10 2 €4 He I (30) 51 Th 4 2
84 Nd 20 12 61 Fe *3 45 Pr 30 3
79 Tb 3 3 61 Hg (40) 40 Ce 12 15
78 Cr 30 10 60 Sm 3 2 38 Cr 15 3
75 Ir I 4 55 W 6 23 Nl I 100
74 Sb (8) 52 Sm 2 2 2 *Sr 2
68 Fe 2 1 45 Nb 5 3 15 V 1 30 25
65 Tb 3 45 Fe 10 2 1 к C
65 Au 5 3 45 Zr II 7 1 06 Gd 5 2
64 Ce 2 1 44 Tl I 8 05 Dy 4
59 Ag 3 2 40 u 4 *3 4605.84 Eu 8
56 U 6 8 40 Gd 8 6 78 La II 100 100
52 V 2 37 Mo 5 5 36 Mn 150 15
3907,48 125 25 33 Ho 6 4604,99 Nl I 300 10
Sc I 33 Os 30 12 85 Ta 200
47 Fe 15 6 24 Nd 10 4 40 Rn (200)
44 Ce 6 2 24 Nb 2 5 34 Se II (300)
44 О II (18) 18 Cr 5 8 4217,27 Ru I 100 20
34 Th 8 3 15 u 3 2 20 Gd 100 100
30 Pr 8 3 15 Fe I 6 2 4216,36 Cr I 60 25
29 Ce 35 6 10 Zr II 40 40 23 Nb 1 10
20 w 6 5 10 Er 7 19 Fe I 200 100
20 Pu II 100 08 La I 12 3 10 Sc I 3
19 J II (18) 06 Dy 6 4 06 W 1 5
о 17 V 2 2 06 Хе I (8) 04 Ba II (25)
►—О 15 Sn 4 06 Tb 15 3 0 к C
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ ЛИНИИ ЭЛЕМЕНТОВ
Продолжение
С ЬЭ Инте нснвность И нтенсивность Интенсивность
Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
С тронций Sr (продолжение) Стронций Sr (продолжение) Таллий TI {продолжение)
4215,99 98 97 96 95 92 90 75 64 60 и Рг Fe I Ег ТЬ N I In Zr II Ci Хе II 4 2 9 3 3 3 1 (5) 3 (6) (100) 4076,96 95 85 81 80 73 72 4075,87 Аг Ей Sm II Ir Fe Ru 1 и О И Суры» 10 10 2 8 60 8 la Sb (10) 5 1 25 10 (800) (400) 20 15 5351,32 21 13 08 04 5350,90 74 62 58 5350,46 Yb N II Th Ti I Nb Zr I Nb Sm Ar I Tl 1 50 8 50 3 2 150 15 50001? 3 (30) 60 2 ’ 50 ' ’ (20) 20001?
56 53 Rb 1 Tu 1000 R 10 300 2878,64 21 20 .1 II Tu Та 3 4 44 44 W Er 18 12
4215,52 Sr 1! 300 7? 400 16 Nb W 2 4 8 41 41 Те Gd 25 (8)
51 51 42 4 38 U Re Fe I Na I W Zr I Dy Os Pr Tb Gd Se U W Co Nb Nb N I Ce Xe II Nb Nd Ru Th 3 20 60 3 12 2 15 5 04 02 02 2877,98 2877,92 Ru V Се Cr II Sb I 2 2 30 250 15 10 100 150 40 39 38 35 30 09 Eu Re V Zr II Sc I Zr II 60 2 4 3 4 3 5
31 17 16 14 13 02 02 01 4214,96 87 82 73 73 70 69 67 60 56 55 50 8 8 30 200 4 2 5 40 *4 10 8 1 3 1 150 (150) 4 1 1 10 (25) (3) 100 10 91 89 88 87 85 84 83 76 69 69 69 68 66 62 52 44 30 Са Ей Dy Pd И Nb Ru I и Eu Cu II V Ta Ir I N Nb Pt II TI II Fe 1 1 2 2 2 3 2 5 15 15 20 40 30 200 4 1 1 15 4 1 2 20 100/? 80 10 (8) 5 200 100 125 03 5349,92 88 86 79 74 70 65 62 62 58 58 47 47 31 31 29 Xe U Mn W Mo Fe I Sc I J Ba Gd Nd Ta Eu Ca I Cs Rh Sc I 20 6 6 4 6 7 8 4 30 2 12 20 30 (2) 3 4 (15) 12 (15)
3 2876,95 Nb 40 500 26 25 Nd Re 2 3
52 44 4213,72 65 Ir Ru Xe II Fe 100 40 (200) ^60 2598,90 88 81 Mn Nb Cu II 5 100 150 200 21 16 14 Ne I Cs II Sm 25 (150) (25)
4078,82 Xc I — (100) 37 Fe 11 700 1000 12 Lu 2”) 1
71 V 1 2 28 Ir I 8 09 Ta 80
71 Gd 1 20 10 25 Ce a 09 Co 1 80
61 Ce а 21 Ta 2 50 5348,32 Сг I „ 150 /? 15
58 Sc i 10 10 17 Mn 12
52 Ce а 1 11 W 6 3521.26 Fe I 300 200
47 Tl I 125 50 07 Rh 4 3 3520,47 Sb II (125)
47 46 Tb Gd 5 15 1 10 2598,06 Sb i 200 100 47 20 Ne I Mo 1 (1000) 20
38 Sb 4 04 Nb 2 10 16 Ho 8 10
38 Mo 5 3 03 Fe II 4 4 14 Eu 4 4
36 Fe 1 80 40 00 Ir I 2 13 Ru 60 40
35 Nb 4 3 2597,96 Re 20 10 Ce 2 1
32 Ce 15 4 95 w 12 08 Co I 100
31 Zr 1 10 94 Fe II 3 07 Sb 4 2
26 Ть 3 89 J (4) 06 Nb 20 20
23 Eu 3 86 Ir 3 03 Er 12 4
16 Pr ч I 83 Fe 6 03 Cu I 30 10
14 Zn II (5) 79 Ru 20 02 V II 5 50
12 W 7 6 /а Nb 15 00 Ar (15)
12 Re 10 07 Rh 3 150 00 Os 30 20
07 Mo 4 4 3519,96 u 6 12
00 Ho 3 3 2529,30 Cu II 600 94 Tl I 5
4077,98 Pr 10 2 2528,84 V 25 150 7? 93 Ce 3
98 V I 2 8 Cs (8) 92 Ho 10 10
98 Dy 150 100 77 U к 2 82 Co 2 25
97 Tb 25 2 72 Ru 30 77 Nd 10 2
97 Er 20 18 71 Ar II (5) 77 Dy 2 1
81 Hg I 150 150 70 Mn 12 2 77 Ni I 500 30
79 u 15 6 62 Co II 4 200 76 ть 50 15
72 Ta 4 2 59 Lu 5 74 Ce 18
72 Sn 2 3 □9 Ta 4 1 69 Th 3 6
72 Cu 5 2528,52 Sb 1 65 4
4077,71 500 300 7? 200 Nb Ru 5
Sr li 4001? 52 SI I 400 500 64 70 30
69 Pr 4 2 51 Ba II 50 60 Zr I 100 10
68 Mo 8 10 49 Dy 4 54 Rh I 40 2
68 Cr 30 10 49 Xe II (3) 45 Cr 6
62 Nd 8 3 47 V 50 150 7? 33 Nb 2 3
61 Pb 2 39 Ir 10 3519,24
57 Rh 1 5 4 36 Th Ti I 2000/? 1000 R
47 Ce II 18 4 33 Ar (10) 22 p II (15)
41 Co I 100 2 33 Yb 3 18 BI 10
37 Y I 50 40 29 Ce 15 1 18 Os 15 8
35 Dy 4 1 24 Cr I 30 17 V 1 10
35 La II 600 400 2527,90 V 35 300/? 13 Pr 10 2
27 Yb 30 100 09 Er 20 2
15 Tl I 18 2 Таллий Tl 08 Ce 25 4
15 Nd 10 4 5352,96 Yb 100 250 3518,98 Ru 30 3
09 Cr 35 10 05 Co I 500 96 ть 15
09 Nb 3 5 5351,92 Zr 3, 95 u 3
08 As 10 90 W 20 94 Os 20
06 W 6 5 67 Eu 150 91 Ir I 2
со 05 Zr II 3 1 56 Sm 13 3 90 Eu 5
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ И ЛИНИИ ЭЛЕМЕНТОВ
Продолжение
45 Зак. 783
Интенсивность 1 Интенсивность Интенсивность
Длина волны, А Элемент дуга искра 1 (разряд) Длина волны, A Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Таллий Т1 (продолжение} Тантал Та (продолжение) Тербий ТЬ (продолжение)
3518,89 88 87 75 73 73 71 Th Fe 1 Zr Hf II Ср 3 10 4 5 3 3 2 1 15 2653,56 50 48 43 38 Мп La I Nb W Nb 2 3 5 15 2 8 3 3874,14 13 12 11 07 TI Се Ег Но О II 12 4 18 2 4 4 1 8 (5)
Os Dy 200 4 30 2 2 35 32 32 Mo w Ca *6 150 2 05 04 00 Fe I и Dy 1 15 100 15
71 3873,96 Со I 400/? 80
68 68 68 63 60 Th Sm N! 1 3 5 90 8 2653,27 15 08 Та 1 Ru Ru 200 12 15 5 10 95 82 78 Fe Th Tb 1 10 8 5 3
P II Mo 1 ’ (50) 3 03 01 Ir W 8 2 5 9 76 75 Fe I к и 125 80 (20)
55 w u 5 2652,98 Os 10 2 72 Os 20 20
Pr 4 66 Rh I 100 25 72 Sm 12 3
50 48 Ce Eu W 3 20 10 10 7 49 Al I Телл 150/? yp Те 60 64 56 54 V I Pd I Eu 35 6 8 12 5
u 2 2385,95 Fe I 4 53 Er 5 I
Th 6 2 86 Ir 20 3 52 Ru I 30 45
40 Cr 8 1 82 V 100 47 Sin 10 3
38 Tb Hf II 8 3 82 79 Co w 9 5 28 26 Nb Mo 2 3 10
37 Ce 12 1 78 Hf II 3 26 Ce 4
35 30 3517,67 Co I Sm Nb 200 1 2 100 2 200 2385,76 74 73 Те 1 Cr I Ta 120 25 8 60 21 20 20 15 Ti I Sm II Mn Ir I 40 20 12 25 7 3 12 10
Тантал Ta 62 V 10 12 Co I 500/? 80
3312,18 11 Cr II 5 125 6 Rb ...... (2) 3872,50 Fe I 300 300
Lu 100 10 60 Rh 10 3511,04 Ta 100 35
3311,93 52 Cr II 6 125 58 Fe 2 3510,8» Bl I 200 30
Cs (4) 55 U 3 2 84 Tl II 40 125
51 Dy 5 50 Re 12 34 Nl I 900/? 50
50 Ce 15 1 49 VV 11 3 9 15 Sm 2 1
46 Ca 6 49 Os 15 2 13 Am 5000
45 Fe I 1 1 w 10 ть 50 8
39 Ce 3 2383,54 2 4 09 Dy 2 1
38 Wj 15 12 52 Mo 12 (40) 07 Eu 4
35 u 4 1 60 Ar II 03 W 10 10
34 Zr 11 8 3 48 Re 25 5 3509,99 La II 10 10
34 Nb 5 10 J 46 Co II 15 30 99 Mo 1 3
30 Ne II (') 45 Ir 93 Ce 8
30 Cr I 8 44 Ru 12 87 Fe I Ь 4
26 Ar (5) 44 u 3 86 и 2
3311,16 Ta I 300 70 44 40 V Pd II 2 4 50 84 84 Ti II Co I 8 400/? 20 40
11 W 5 4 40 Rh 50 10 80 Sm 3 1
09 Er 3 36 Mo 10 8 Rn (5)
02 Pd 4 2 33 Cr I 20 78 Ar (15)
02 Ir I 2 2383,25 76 Tb 8
00 Cu I 3 .Те 1 100 60 73 Ce 12
3310,96 Dy 5 3 24 Fe II 8 12 72 Ru 1 50 2
96 Ru I 30 5 24 Pd II 2 68 V 6
91 Os 200 30 21 Os 15 67 W 8 6
90 Nd 25 2 21 Ag II 25 67 U 10 15
88 Ce 10 20 w 3 53 Ce 3
87 U 2 2 17 Ir 10 45 Sm 4 4
86 Hf II . 15 8 06 Fe II 6 2 41 Dy 6 2
80 Eu 3 i 05 Mo 4 39 Cl ii (40)
80 Tb 8 3 00 V 8 80 38 vv 12
77 Mo 20 20 2382,99 w 15 3 35 Ho 'б 2
66 Nb 15 93 и 2 35 u 3 6
65 Cr 2 200 32 Zr I 40
34 Fe 100 80 Тербий Tb 31 Ce 3 2
3875,44 Kr II (150) 25 Ce II 10 2
2715,47 Re I 100 17 Sm 50 10 24 Ir I 8 2
34 Nb 2 100 16 U 8 24 Nd 10
31 Rh 50 500 15 Dv 3 23 Mo 3
2714,94 w . . .... 3 08 V I 70 50 20 Ru 10 100
90 Pd II . . .... 200 07 Au 3 20 Th 2
87 Fe I 40 15 04 Ce II 6
82 W 4 3 3874,98 Hg (30) 3 3509.17 Tb II 200 200
73 Mn 5 87 Th 5
72 Cc 5 76 Pr 2 5 13 Fe I 2
2714,67 Ta 1 200 8 73 70 Tb Ho 6 6 12 12 L) Sm 1 8 2 Ю
64 Os 50 10 69 Fe 3 11 Th 4 I
62 Th 9 4 68 Ce 6 2 06 Ce 2
58 u 10 8 67 Au 5 15 04 V 2 150
55 Ir I 4 65 Pb 2 02 w 9 7
54 La I 6 61 Lu 4 00 Dy 6 4
49 Kr II 12 (3) 53 Cr 1 70 12 3508,94 Ci II (12)
42 Co II 200 47 Gd 3 94 Er 5
41 Fe II 200 400 46 u 10 2 88 Хе II (10)
41 Rh 1 130 5 45 Pr 20 4 86 Ce 2
4 Rn (3) 41 w 12 12 86 Eu 10 1
40 Yb 4 37 Sm 5 4 85 Os 8 10
38 Cl II (8) 36 U 10 85 и 8 10 i
32 Pd 60 150 34 V I 10 2 84 Cr 12
20 V 100 33 Ce 4 81 Er 8
2713,94 In I 200/? 125 28 Mo 1 6 74 Eu 8
8 fe в 200 2 k Ca 4 74 w 9
2653,73 Yb 50 200 3874,19 Tb 11 200 200 72 71 Ir I Ce 2 12 9
vv u 10 15 15 Mo 5 6 71 Sm 3 2
О О вз 3
гв Z
S iS
Г а св X
О
Li СГ Z Е х
S Z S 3
QJ Sa tB 2 rn z
о СЭ
8
Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Тербий ТЬ {продолжение} Титан Ti {продолжение) Титан Ti {продолжение)
3508,60 Rh I 3 ...... 4982,83 Kr II ...... (50) 3653,11 Се 15 5
60 ТЬ '8 ...... 78 То 2 . ..... 05 Se II ...... (25)
58 1г 1 6 1 60 W 40 5 3652.97 Tb 15 8
54 Nb 5 э 51 Fe 200 . ..... 95 Tl I 150 50
54 Fe I 20 10 14 Y II 8 50 88 Er 20 4
48 Fe 40 20 13 Се 8 ..... 76 w 3 4
48 Mo 2 5 03 Ra (10) 73 Fe 6
47 Ce II 10 00 Рг 2 65 Eu 5 4
42 Lu 30 3 4981,96 Dy 2 ...... 59 Cr 3
42 Xe I ...... (2) 88 Ir 3 . ..... 58 Er 20 3
40 Er 15 С 83 Мо 10 3 56 Ca 3 2
35 Ho 4 56 Gd 20 25
34 Ce 4 . ..... 4981,73 Ti I 300 125 54 Co I 200
31 ' 22 21 21 2 3507,69 39 36 32 3325,50 46 3324,87 85 79 76 75 75 75 69 66 61 60 u Rn I Fe II Pr k Zr Nl I Lu P II Rh I Ar I Fe I Srn Ta Fe Ce Ti I Th Os W Nb Tl I U 1 12 20 100 100 500 100 3 5 2 12 10 10 15 8 4 2 3 (Ю) I 3 12 150 (ЮО) 125 (ЮО) 80 1 1 10 8 7 50 1 71 54 . 35 28 4980,95 89 82 71 69 69 57 54 52 38 37 35 26 16 4979,76 12 4978,89 84 Sm II Re I TI II Nd Th Nd Hg I Er Re I Tu he Tb Pr Pt Sc I Ru I Sm NI I Br I Mo Kr 11 Rn 50 15 10 8 2 2 4 5 4 3 4 6 60 4 500 ЮО (15) (6) 3 (70) 8 1 (125) 30 (100) (300) 54 3350,48 21 3349,53 52 46 44 43 42 41 40 40 35 34 34 33 29 22 22 19 17 07 Th Gd Ca I Co Nb Cu II Cs U Tb TI II Ce Au Nd W Th Cr Cu I Co I Sc I Mo Hf II Cr 10 150 100 7 30 4 30 100 4 15 5 2 5 35 70 3 4 6 5 125 10 180 10 5 2 (Ю) 3 50 400/? 5 5 100 10 10 50 40 5 4 40
59 58 Ce N II 3 (5) 10 3655,00 Al II (100) 06 04 Nb U 80 100
56 Nb 2 3654,83 Hg I (200)
55 54 Pr Fe I 10 100 1 80 64 59 Gd Ti I 200 100 200 40 3349,04 Ti 1! 125 800/?
5 Cs (4) 49 Os 100 15 3348,96 Th 4 0
47 Th 4 1 94 Mo 1 30
3324,40 Tb If 70 50 45 Ho 6 6 88 Dy 2
-t
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ
39 39 V I Са 7 1 6 6 1 45 42 Co I Pd I 35 4 87 1 84 8 m Ti II 12 1 12 s
37 Fe 5 3 42 Nb 10 10 78 Nb 1 30 a
35 Сг 10 60 40 Ru 3 40 78 Ce 6 s
33 Os 50 15 38 BI II 7 5 77 Tn 5 4 3
s; го Dy 3 36 Er 4 74 Er 10 1 CD
18 Hf II 8 6 36 Re I 8 72 Rb I 100 ь
17 Yb 6 20 34 Pr 8 2 72 Cs I 15 гя
14 Pr 10 1 .'30 Cu I 10 2 70 Ru I 50 2 2
Об Cr II 20 20 30 Tb 8 69 u 4 1
06 w 8 7 29 и 3 4 68 Sm 10 10
03 и 3 2-3 Nb 5 66 Os 30 15 О
3323,98 Ce 2 20 w 12 10 59 Nd 2 09
95 Dy 2 17 Dy 4 1 58 Ho 4
95 Mo 40 25 16 Nd 10 10 54 Tb 15
94 Ru * 5 13 U 5 1 54 TI I 7
93 Ca 5 09 Ce 2
90 TI I 3 3653,99 Pt I 2 1 3235,02 Mo 25
80 Pt I 150 10 98 Fe 4 2 01 Ce 10 1
74 Fe 150 150 97 Kr II (250) 00 Mn 30
09 Rh I 1000 200 93 Au 5 2 00 Th 5 1
3322,94 Tl II 80 300/? 93 Sr I 15 3 3234,99 Ca 2
91 Cr I 100 25 98 w 9 7
Технеций Tc 90 Mo 3 2 96 Ba 3
2543,97 Ir I 200 100 87 ть 15 8 93 Na II 6 (20)
94 Rh 15 100 83 Ta 3 1 89 Ce 18 5
65 Fe 700 76 Fe I 25 10 89 Zr I 2
54 Ce 4 76 Ir I 2 80 Er 4
47 Ru 8 72 Os 30 10 80 Ru I 10 1
45 Mn 4 100 67 Ce 18 8 73 Os 100 10
44 w 12 2 65 Pr 4 1 73 J (3)
43 Fe 11 5 62 Re I 15 73 V 1 8
38 Ее II 5 50 62 Nb 10 5 69 Ta 70 10
37 Hg II (3) 61 Tu 30 20 65 NI I 300 15
35 Pd II (2) 61 Y 5 2 64 Rb (5)
35 Mo 25 2 59 Th 3 2 61 Fe I 200 125
32 W 12 55 Mo 4 4 52 Ho 2 6
25 Ru 50 150 52 w 5 1 3234,52 Ti II 100 500/?
2543,24 Тс 11 500 1000 3653,50 TI 1 500 200 52 V 20
20 U 2 2 50 Ca 3 51 Ar I (100)
14 Cr 10 49 Au II 3 5 51 Ir I 3
13 Hf II 2 48 Sm 15 2 50 Tb 15 15
09 Ce 12 2 39 Ta 3 1 50 Ce 10 3
06 Br (2) 38 p (100) 43 Ru 3 50
2542,92 Mn 1 100 34 w 1 12 42 Sm 10 4
32 Ir I 3 30 Eu 3
Титан Ti 27 Sr I 30 8 27 Ce 5
4984,13 Ni I 500 1 21 U 10 1 22 Pr 12 2
4983,86 Fe I 200 - - - . • 20 Os 10 20 Os 150 12
26 Fe I 100 - _ . . . 19 Ir 15 50 18 Mo 8 5
4982,90 Nd 2 16 Re 4 16 Ce 40 8
S 90 Os 6 15 Nd 10 4 16 Cs (6)
84 Na I 200 100 11 Sm 10 2 12 Zr I 8 3
Продолжение
Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Гитан Ti (продолжение) Торий Th (продолжение) Тулий Tu (продолжение)
3234,12 Со I 2 3538,98 и 1 3 3762,05 Хе (3)
06 Сг 10 150 97 Но 4 00 Sr 1 3
05 SI 7 96 Се 3 3761,96 и 2 8
3233,97 05 Fe I Fe 300 100 150 60 92 90 Мо ТЬ 3 15 4 3 9> 94 Се 1г 2 2 4
86 Srn Н 10 1 92 Tu II 200 120
1ОрйИ in 86 ЙЧ " 8 89 Tl II 12 15
4020,90 Со I 500 86 20 6 87 Cr п 10
1 к Sr 2 • • , а . . 85 Рг 9 2 87 Pr 150 100
10 Th 3 3 84 Th 4 ...... 81 P II (30) 6
09 Mn 10 5 80 Fe 1 . ..... 76 Mo 6
06 Nd 6 3 79 Се 3 2 72 Ca I 2 4
06 Cl II (15) 76 Се 5 2 70 Cr 4 8
•03 02 Ir Ne I 80 100 (2) 3538,75 Th III 50 62 61 W Pr 7 10 8 6
4019,98 Sm II 30 15 68 и 6 60 u 2 6
90 Ce 8 3 63 W 8 9 58 Nd 20 10
84 Pr 15 8 ао Fe I 1 56 Ir 1 5
83 Sm II 8 8 53 Y 10 3 51 Ru 12 45
81 Nd 10 8 52 Dy 150 40 48 Th 10 1
80 VV 5 52 Ho 6 45 Ce 2
79 Mo 10 52 Er 18 9 44 V I 40 7
73 Gd 1.3 10 50 Dy 5 2 41 Fe I 20 8
72 Se 1 (20) 50 Tb 3 3 40 Dy 2
71 Eu 3 47 F II (6) 38 Pr 8 2
66 64 55 ть Pb Ru 1 2 6 12 6 8 46 44 42 Ce Th U 2 3 2 1 8 35 3761,33 Ta Tu II 8 250 150
50 Se II (10) 42 Ce 2 1 32 Tl II 100 300
48 Dy 5 2 31 Pr 3 2 18 Ce 3
48 Ce 6 1 30 Ce 2 14 Sm 6 2
45 p II (50) 29 Fe 2 1 13 Ец 11 10 10
44 Pr 10 3 27 AB 10 2 13 Nb 15 20
35 Yb 7 26 Rh I 50 4 12 Tb 15
30 Co I 80 24 V II 10 100 10 Th 15 8
28 Ce II 4 22 Th 8 3 04 и 4 8
23 VV 18 15 22 u 8 6 02 Re 2
20 и 6 8 15 Ir 18 1 00 Yb 3 6
19 Ce 2 14 Rh I loo 10 3760,96 Pr 5 3
14 Co I □ 09 Eu 20 10 94 Nd 10 4
4019,14 Th 11 8 8 08 3537,99 Xe II Ne II (2) (7> 93 88 Gd Mo 10 6 10 10
13 Re I 15 99 Os 1 4 88 U 10 15
ggaggsgl
12 Th 40
05 . V 6
05 Nl I 5
05 Мо 2 4
С4 Се 15 4
4018,99 и 25 15
92 Се 2
88 ' Са 4
83 Nd 15 10
6 Bl II 2
84 Sm II 4 5
52 Se II ...«•• (70)
51 Ce 2
44 ть 2
41 Re 25
46 Eu ' 10 4
40 Ce r
38 Zr II 8 5
S3 Br 1 (4)
31 VV 2 3
л и 8 3 1
28 Fe 1 50 7
2Ь Os 60 4
23 Ce II 2
20 Cr 1 35 8
4017,75 Rn (150)
3540,12 Fe I 100 60
3539,65 u 12 2
65 Nb 15 15
63 Pi 5 2
62 Dv 6 4
60 Er 9
59 Th 8 8
54 Kr 1 (15)
46 Mo 3 3
46 W II 3 7
88 Dv 18 2
37 Nd 4 4
37 Ru I 60 15
33 W 6 3
83 Re 25
32 Th 5 5
29 Er 3
26 Ru 30 5
26 Sm II 8 1
24 Eu 2
21 U 4 4
20 Fe 1 1
18 Nd 10 4
15 AI 8
12 Nb 1 15
69 Ce II 100 10
01 Zr II 4 3
95 Ru I 70 25
94 Tb 15 15
91 Tu 15 2
90 Fe 1 50 25
90 Mn 12
85 Ce 3
83 и 2
75 Eu 10 10
2838,24 Ta 2 150
12 Fe 1 150 150
2837,60 C II 40
60 Ce 8
55 Re 40
55 Cu II 250
51 Nd 5
42 Os 25 10
34 VV 12 10
33 и 10 . 8
33 Ir I 20 10
32 Mo 5 1
31 Sb 3
30 Fe II 25
2837,30 Th fl 15 10
29 Sc 4 7
29 Ce 50
27 Ru 20
23 Zr I 100
23 Pt I 2
21 Se (35)
19 U 10 8
Co 1 75
12 Pd II (40)
11 Er 5
10 Nd 5
03 Fe 1 2
02 Re 2
2836,91 Cd 1 200 80
71 C II 200
64 Ti II 100
Тулий Tu
3762,33 Eu 9
30 TI 10 1
28 Dy 3 1
28 Ce 4 5
26 Xe (5)
22 Ce 3
21 Gd 10 3
21 Fe I 7 3
21 II 2
11 и 10 6
09 Mo 10 30
84 Ir 2
82 Ce 2 . . . . .
8 Rn (10)
79 V I 30 5
76 Eu 10
76 Nb 2 8
72 Gd 25 25
70 Sm И 25 40
69 Ce 6
64 Nb 5 4
64 W 7 6
53 Fe 100 70
40 Rh I 6 2
40 Ce H 5 3
39 Co 30
38 VV 9
36 Er 15 1
36 Nd 10 6
34 u 1 2
34 10 10
05 Fe 1 150 loo
3462,80 Co I 1000 7? 80
69 Sm II 5 2
65 Nb 5 3
64 Ht II 15 12
62 Ca 2 4
58 Er 10
51 Tb 8 3
49 Na II 2 (15)
43 Ce 8
36 Fe I 10 3
36 Pr 3
32 La 2 2
23 Ce 3
21 Eu 5 1
3462,21 Tu 11 250 200
19 Os 20 10
18 Sc 1 4 2
10 Pr 6 . . • •
06 Mo 25
04 Ru 5
04 Rh I 1000 150
3461,96 Ho 20 20
96 Gd 5 5
92 Ru 30
87 Pr 6 2
81 W 9 5
79 Ce 10
71 Yb 1 3
Nl 1 800/? 50
57 Rb II (200)
18 Co I 100 3
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ М ЛИНИЙ ЭЛЕМЕНТОВ
S Продолжение
Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Тулий Ти (продолжение) Уран U (продолжение) Уран U (продолжение)
3461,08 I Ar I I (300) 4240,34 г, j 100 1 3854,-56 5 5
3460,97 Dy 100 3 4239,72 Мп 100 50 55 Th 20 20
77 I Pd 1 1 300/? 1 600 Со 1 54 Mg I 2 5
3861,16 300/? 15 32 Се II 6
2479,05 Углерод с 3860,99 CI II (100) 23 и 20
V 15 150 83 CI II - • - * . (150) 22 Cr 1 40 15
2478,99 Re 5 46 Cu I 30 7 20 200 25
93 Ru 80 60 40 Се 6 3 19 Ce 6 1
87 W II 8 31 La II 2 12 Nb 2 3
Ъо Kr 11 (3) 28 Sm II 4 п 12 Mg I 2 8
82 Xe (2) 15 18 Се 2 -1 1 4
80 Pd II 15 S II (8) 05 Pb I 100
66 Hr I 15 15 14 Sm о 1 05 Ho 10 20
. 65 Tl II 50 3859,98 VV 15 30 04 Tt> 2
62 V 2 20 94 Се 3 5 3853,90 Eu 3
59 Pb 2 91 Fe I 1000 /? 600 82 Fe
59 Cr 3 83 Th о 10 78 W 6 6
2478,57 C 1 400 (400) 80 79 Ta Cc 10 3 2 73 T] I u 12 g 3
57 Tu 15 15 71 Ru 6 15 44 Os 100 15
57 Fe II 4 40 68 Ca 6 5 04 Dy 100
57 56 56 Nb Pd Hf II 100 4 25 300 67 3859,58 Nd V II 25 20 25 30 3852,80 Pr Фосф 100 op P 50
45 Fe II 5 52 Eu 4 . > . . . . 2553,59 Ce 9
40 Ru 8 5 42 Nd 10 12 59 Na 121
31 Sb 75 100 42 Pr 3 3 56 In II (40) 2
37 Au II 3- 56 Cd I 25
4243.26 34 V I 20 8 56 Re
As 100 33 Al II (10) 50 Fe
06 Rn I 100 40 29 w 10 12 49 Nb I 30
4242,63 Nb 10 20 22 Eu 2 46 Ce 2
62 Ba 10 5 22 Fe I 100 100 41 Ag II 2 10
62 Zr I 3 21 Mg 1 2 40 l.a II 3
6 Rb (150) 14 Pr 4 4 38 NI 1 20
59 Fe I 3 01 u 8 4 37 Co I 10
57 U 3 3 38а8,95 Nb 20 оО 34 Ce 3
55 ть 12 2 89 Cr 1 35 20 33 In II (5)
47 Eu 6 1 85 w 5 6 31 Ru 6
47 Pb II 10 84 Mo 15 26 >6
47 МЯ II 4 81 Ca 2
38 29 Cr II U 4 6 50 3 78 7. Kr II Sm 20 (5) 2553,25 18 p 1 Fe 80 10 (W 20
J I
1 1
26 1 20 69 Ru 4 18 Ta 10 10
Ce 68 V I 50 15 16 VV 12 15
25 Tb 4 68 и 3 6 06 Cr 1 20 1
20 Ne II (5) 61 Ta 10 2 05 Zr II 2 2
20 Pb П 2 30 Ni I 800/? 70 02 V 7 15
15 Tu II 500 100 00 Co I 40 (10)
01 Zr I 4 3856,37 Fe I 500 300 2552,99 Cd H
01 Ce 10 3855,84 V 1 200 200 99 Mn 3
4241,97 93 Cs (10) 63 u 3 12 1 98 Tl I 10/?
Hf II 2 10 62 Sc 15 15 Hg I 1000/?
89 Co I 3 60 Au 4 4 2536,52 2000/?
83 Dy 2 60 Dy 8 2 49 Pt I 100 10
82 Re I N II 2 60 Ho 4 23 Ta 100
80 (100) 58 Gd 15 6 2535,94 Pd (3)
77 Au I 40 30 58 Tu 10 90 U 5 2
74 Ce . 3 58 Ru 4 15 87 Tl II 20 60
7 Pd I 2 57 Cr 1 30 30 87 Th a 2
69 Zr I 100 2 54 vv 10 9 64 Mn 8U
4241,67 64 U It Ce 40 50 50 45 Nb Nb ' 10 ' 50 2535,61 P I 100 (TOO)
6 Na I 3 44 U 8 1 60 Fe I woo
52 Os 9 43 Zr II 8 3 60 Ta 50 100
51 Co I 3 38 Tb 10 59 Ru
45 Nb 3 л 37 V I 50 R 50/? 58 U 8
W 30 10 33 Fe 2 1 58 w 10
40 Ce II •3 32 VV 6 57 J (30)
39 Re I 30 30 Ce 8 3 48 Fe II 20
38 CI II (60) 29 Cr 1 35 35 36 Fe 1 3
32 V I 15 8 24 Se (S) 2534,80 Re 100
30 Pr 10 2 19 Ce 2
28 Gd 10 16 u 2 2 Фтор F
24 21 20 20 19 16 11 11 08 Ce Nd Zr I La II Cr Re I U Fe I Tb 3 12 100 ’ ’ ' ib ’ ’ 20 10 1 4 4 2 15 4 15 08 3854,96 94 91 90 90 90 86 Nb N II Ce Sm II La II Mo Pr 5 3 5 4 80 5 2 5 (5) 3 5 40 5 30 2 6 6857,25 12 03 00 6856,82 53 50 03 Fe Gd Hf II Nd J Ce Dy Sm II 5 200 5 8 4 3 300 5 10 (15)
06 Ru I 100 20 86 Au 5 5 «856,02 F I (1000)
02 4240.9 83 81 8 75 Pr Eu Mo Dy k Ca Dy AI II Ca 50 2 30 2 3 3 12 1 25 82 79 76 75 73 70 Eu Cr Ba II CI II Ru 1 Os 6 20 10 30 15 (2) (30) 5 12 6855,73 29 18 6854,7 63 Tl Hf II Fe I Те 1 Zr I 20 7 60 6 50 80 (50)
75 74 (15) 8 70 68 Nb Rh 3 4 4 4 Хлор C! (300)
70 200 30 3854,66 30 4797,01 Hg
69 Gd 4 U I! 20 4796,37 Co I 100 ar....
66 Ce 2 64 Eu 3 17 Cr 125 1
59 u 10 10 57 Pr 2 4 4795,96 Hf 3 2
58 Ce 5 56 Er 4 1 90 Sm 2
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ ЛИНИЙ ЭЛЕМЕНТОВ
Продолжение
Длина волны. А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Инте нсивность
дуга искра (разряд) дуга искра (разряд) дуга искра (разряд)
Хлор С1 (продолжение) Хром Сг (продолжение) Хром С г (продолжение)
4795,89 Ей 2 4275,75 Кг (2) 4253,70 и 8 2
85 Со 1 100 73 и 12 8 70 Nb 25 40
83 Рг 68 Мо 12 12 65 Dy 3
67 1г 2 2 64 La II 40 500 62 Gd 50 50
62 Ne II (15) 56 Се 25 4 58 Er 9 2
57 Ru I 20 56 Ne I (70) 58 Mo 8 5
50 Ег 9 1 49 W 15 10 57 Zr I 20
40 Хе II (2) 47 О 11 (50) 54 Th 8 3
37 Мо 4 3 45 Dy 5 - ..... 51 Cl II (75)
25 Рг 20 37 ТЬ 3 5 Sr 2
25 1г 2 32 Рг 5 1 37 Gd 50 4
23 Вг (5) 21 ТЬ 15 1
10 V 5 4 21 F II (100) 3595,05 Dy 200 100
4794,96 Zr I 3 19 Аг (10) 3594,87 Co I 200
90 Рг 7 17 Рг 12 2 64 Fe I 125 100
85 Dy 3 1а W 6 2 46 S II (35)
60 Мо 12 10 13 Cu I 80 30 43 Hf II 2
56 10 08 Nd 20 10 39 Ir 15 30
07 Со I 3 31 Cr 4
4794,54 С1 11 (250) 02 00 и Dy 2 5 1 25 18 Tb Ne II 15 8 (12)
48 Са 2 4274,98 TI II (100) 15 Au 25 6
38 Ru I 25 96 Рг 3 ...... 14 Ir I 10 4
32 Рг 4 94 W 10 5 13 Er 9 ...... О
31 9 90 Os 9 1 12 Ca I 3 2 о
4793,99 Os 300 6 89 Nb 5 5 12 Th jy 2 Ев Я
82 82 Мо Tb 15 2 lo 4274,81 Сг 1 4000 7J 800/? 11 10 U Ce 1 5 4 2 ё
80 Си 2 77 Zr I 9 03 Ce 5 гв
66 N II (5) 69 Nb 5 3 02 Cu I 15 2 X
57 Re 2 66 Ne I (50) 01 Pt 3 S
45 Gd 5 58 TI I 100 40 00 Sm 2
41 Мо 30 30 w 20 12 3593,97 W 9 8 о
28 Zr I 3 41 Mo 30 97 Nb 80 50 =1
24 ть 2 40 Tl I 5 95 Er 8 ГН
18 Ir 2 36 Tb 2 89 Rh 3
06 3 34 Re 20 88 Th 5
4792,86 Co I 600 5 33 Th 8 4 75 Tb 30 8
62 Хе I (150) 27 Pr 8 1 73 Sm H 4 2 СГ*
50 Au I 200 60 24 Tl 11 (8) 68 U 8 1 S
51 Cr 200 40 18 Y 2 68 Pr 4 2 е
4791,60 Gd 150 17 Gd 100 64 Ne I (250) X
'58 Sm II 150 16 Sm 5 1 61 Ti ii (10)
Хоом Сг 05 Mo 6 6 6u N 11 (1U) b
04 Dy □ 2 56 w 4 3 s
4291,18 Re 100 04 Sm 3 1 55 Nb 15 3 3
4290,6 Na I 3 03 Th 10 8 53 Rh 1 10 2 s
'59 Се 4 4273,98 U 12 15 53 Ne I (500) 3
57 Se II (20) 97 Kr I 2 (1000) 3593,48 Cr I 500 7? 400 7? Q)
53 Ru I 6 91 Pt 48 Hg (10) b
51 Pr 4 91 Ca 2 43 Gd 15 15 rn
44 Dy 5 87 Fe T 10 2 40 Sm II 2 3 3
43 Ce II 2 28 Ll I 200 /? 100 40 Re 15 ZE
40 Ne II (100) Re 34 Те (5) -1
38 Fe 35 5 4255,34 2 33 V II 30 300 P О
35 Nb 2 27 Eu 15 33 Fe I 7 2 Ев
30 Ce 2 24 ть 25 1 29 La 2
23 Tl II 35 60 18 Ce 2 28 Ba I 3
21 Zr I 40 20 11 Re 2 22 К II (5)
18 Mo 30 25 00 Pr 4 1 21 Sr II 3 2
17 Ho 2 2 4254,96 Mo 25 2. 20 U 10 1
14 VV 8 3 95 Ar (10) 15 Dy 6 4
12 Ca 5 94 Fe 2 1 13 Ce II 8
11 Mn 8 so Ce 8 ...... 13 2
07 Gd 6 85 Kr II (100) 13 Ho 6 6
4289,94 Ce 50 25 77 Yb 4 4 13 Zr I 7 1
92 Tl I 15 2 75 N I 15 . . .... 12 Pb 30
90 Gd 40 100 70 Ce 20 ...... 1 k Zr 2
89 Pr 15 4 69 Nb 10 10 10 Tb 15 8
88 и 12 12 46 Th 8 6 09 Tl II 5 30
80 Ne I (2) 43 Ho 100 20 04 Pr 5 2
73 Tb 30 43 Mo 10 5 02 Ru 1 60 150
4289,73 Cr 1 3000/? 800 7? 42 42 V II Pr 3 &5 5 18 3592,98 97 W Hg I Ho 5 3 2
65 Se (10) 39 Nb 10 b 95 6
56 u 4 3 37 Ce 8 93 Eu 7 1
. 4-5 44 Cc II Nb 25 10 4 20 4254,33 Cr 1 5000 /? 1000/? 92 91 Pb Y I 80 3 25
42 Pr 12 3 32 Er 7 1 90 4
42 Mo 20 15 29 w 4 3 89 Fe I 3
36 Sm 15 2 15 Bj I 10 10 85 VV 6 3
36 Ca I 35 20 13 Ga 9 80 u 1 6
36 Nd 15 3 12 Be I (5) 80 Хе I (2)
35 Dy 2 06 W 8 2 78 Th 2 6
30 Sb II (6) оз Gd 3 70 Gd 50 70
29 w 1 5 00 Ce 3 69 Fe I 12 2
09 Ar (5) 00 Tb 5 Mo 20
07 Tl I 125 50 4253,98 О II (100) 62 Sm II 40 50
01 La I 4 93 Fe 2 1 60 Nd 20 30
4288,96 Fe I 5 1 88 Th 6 4 53 v 40
84 u 20 2 87 Nd 12 3 50 Ta 2 1
81 V II 3 2 85 и 12 3 49 Fe 3 1
71 Rh I 400 100 83 Ce 3 02 V II 50 300/?
64 Mo 80 100 81 Eu 15 3
00 Ni I 150 76 Be I (IS) 3580,28 Nb 100 300
74 о II (50) 3579,67 Ba I 10 8
сЗ 4275,76 Nd 15 3 72 Sm II 5 2 67 Sm 4 3
Продолжение
»£* Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент дуга искра (разряд) Длина волны, A Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Хром Сг (продолжение) Цезий Cs (продолжение) Церий Се (продолжение)
3579,66 56 55 Мп Fe Gd 3 2 1 5 8518,32 4558,03 TI I P II 100 (100) 4187,25 16 04 Со I Tb Fe I 50 15 250 3 200
50 4 2 4557,84 Те (300) 4186,98 и 10 4
45 Са 2 4556,84 Nb 3 5 90 Yb 10
45 Та 35 81 Th 4 86 Се 2
44 Ег 74 V 1 5 84 Но 3 3
42 36 8У 2 6 1 10 74 70 Nd Ne I 15 (2) 79 78 и Dy I 6 100 5
36 Ей 4 1 67 Tu 35 70 78 Zr I 3
Th 4 8 66 Pr 2 71 Er 8 2
ть 50 50 63 Sm 10 69 Zr II 3 3
13 Re I 50 61 Kr II (200) 60 ть 2
12 Dy Но 3 1 4 55 50 Br Sm 5 (4) 4186,60 Cc 11 80 25
V 1 7 1 46 Dy 3 4 48 u 6 5
Eu 6 1 45 Tb 20 42 Eu 6
Та 15 1 35 Ta 200 5 40 Pr 12 3
07 Мо 25 33 u 1 2 36 Cr 50 10
Со I 5 26 Pr 4 34 Sb и 25 5
3578,95 90 Се Со I 3 8 2 22 22 Ce W 3 6 1 31 31 Nd Tu 3 8
89 La II 2 3 17 Cr 40 12 28 Mo 15 12
Се 3 14 Nd 20 1 28 Ir 2
80 Dy 2 1 12 Fe I 150 35 24 Tb 10 1
76 Та 2 1 03 Mo 2 4 23 К II - • • • (60)
75 Рг 8 02 Re 2 12 Ti i 100. . 40
75 (40) 01 u 4 10 Nb 5 8
70 ТЬ 8 4555,98 Pr 3 04 U
69 Tj II 25 5 94 Xe II (100) 03 Nd 8 4
92 Cu II 2 /0 02 W 12 2
3578,68 Cr I 500 К 400 J? 90 Ее II 12 12 4185,95 S (15)
64 V 35 80 82 Th 3 89 ть 8 40
58 Nb 15 1 71 Eu 12 82 Mo 40
58 8 69 Er 3 82 Pr 15 5
57 Рг 2 1 62 Ce 2 78 и 6
49 2 1 61 Th 10 77 Nd 15 8
47 ОУ 4 2 56 Nb 3 2 72 Er 15
42 Рг 9 3 52 Zr I 30 2 72 Re 2
40 Ть 8 49 Tl I 125 60 67 Nb 2
38 Fe I 40 5 42 Ce 5 ...... 66 Ir 25
34 Gd 5 5 39 Ne I (30) 61 CI II (20) (150)
33 Er 3 38 Eu 4 4 45 О II
33 27 23 23 С Tl I Nb Zr II 8 8 1 5 1 1 5 6 | 4555,36 33 30 30 Cs I W Y I 2000/? 7 100 1 2 4184,90 3954,38 3953.52 Fe I О Nd 100 60 30 (100) 60
11 08 03 00 3577,99 96 92 88 87 85 80 Eu Pr Co I Co II ть Dy Rb II U Mn V I Pr Ce 6 10 18 8 150 10 50 50 6 2 1 5 30 50 (15) 25 40 2 27 26 24 14 13 10 09 08 07 03 4554,99 97 Те Tu Dy Nd Zr I U' Cr TI I Th Cr II Gd Nd 25 4 15 15 20 15 12 3 6 5 (30) 50 40 50 2 40 2 1 52 52 51 47 40 38 37 36 25 20 16 16 Pr Dy Nb Eu Nd Snr Gd I La Re Pr Cr I W 150 5 1 6 20 2 100 2 3 15 60 10 100 5 1 8 2 50 2 5 12 12
77 75 72 69 . 46 3576,87 Srn II Fe Nb Co I Ce Dy 20 2 10 2 300 200 3 15 12 50 83 82 80 79 78 68 65 Cr Ne I P II Pr Ir W Tu 25 4 4 4 5 2 (40) (100) 1 16 15 12 08 07 06 02 Fe I Eu Dy Nb Rh I О I Nb 80 4 3 3 3 4 40 1 (5)
2843,98 Fe I 300 300 59 Pt 10 с 02 Tb 3
63 Fe I 125 100 59 Ca 2 3952,99 Mo 1 5
52 Zr II 8 8 56 Ne I (5) 95 u 15
51 Ta 3 80 56 Ce 6 92 Co I 100 75
48 Fe il 3 51 Ru I 1000/? 200 90 w 8 8
39 Ho 10 50 Pr 2 89 Zr I 5
32 Fe II 3 46 Y I 3 6 87 Nd 25 20
27 Tl I 5 44 Sm II 60 84 Mn 60 75
2843,24 Cr 11 125 400 R 42 33 Ne I Ce 2 (10) 77 74 Os Ar 40 15 (15)
24 Fe 6 2 32 Ar I (15) 70 Fe I 8 1
17 Ru I 30 3 23 Dy 2 68 Ru 20 30
00 00 Re I Yb 30 5 04 04 Ba II 1000/? 35 200 62 62 Tb Ir I 2 20 3
2842.82 Ta 200 50 03 Mo 1 4 61 Fe I 80 50
65 Nb 10 100 4553,97 Zr II 4 12 60 Se II (5)
42 Ni II Цези Я Cs 150 95 86 Cr u 20 4 3 1 3952,54 Ce 11 60 30
8944,56 Re 2 69 4552,46 Ta TI 200 150 2 50 52 45 W Th 8 3 7 1
8943,50 Cs 1 2000/? 38 S II (200) 46 и 4 2
00 Fe I 3 4188,32 Церий Ce 40 37 Cr I Nb 60 3 18 50
8522,55 Xe 1 (30) Mo 100 80 36 (25)
8521,96 Ba I 2 4187,80 Fe I 200 150 36 Pr 8 з
57 Mn I 10 62 Tu 300 30 33 Co I 40 4
44 Ar I (2000) 59 Fe 3 1 29 Ru 4 1
4 Те I (12) 56 Zr I 9 3 28 Sc 3
Сп 8521,10 8520,95 Cs I Rn I 5000 R (20) 47 32 32 Zr Ce II La 1 4 35 50 15 40 27 26 26 Mo u w 4 3 5 । 2 6 4
СОВПАДЕНИЯ СПЕКТРАЛЬНЫХ ЛИНИЯ ЭЛЕМЕНТОВ
Продолжение
Интенсивность Интенсивность Интенсивность
Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд) Длина волны, А Элемент дуга искра (разряд)
Церий Се (продолжение) Церий Се {продолжение} Цинк Zn (продолжение)
3952,26 25 F 11 3 (3) 3800,67 67 Lu Но 5 4 3344,97 93 Хе II Т1 I 8 (2)
21 N (Ю) 62 Nd 20 6 90 W II 3 12
20 Nd 30 20 60 Th 2 2 88 Th 8 8
16 Та 8 3 55 Mn 60 60 87 и 6 6
п Се 10 1 55 Eu 10 10 80 Ru 5
08 С II 6 54 Kr I (30) 79 Аг (3)
05 02 ТЬ 2 30 Pr 100 50 79 Zr II 15 15
Рг 5 4 12 Ir 150 100 76 Се II 50 8
01 3951,99 97 Gd О I V II 100 35 60 (10) 50 3799,56 Fe I Цин 400 к Zn 300 76 75 75 Рг Ег Мо 2 8 50 I ' * 40
96 40 50 4724,42 Cr 125 10 73 Rb (Ь)
95 1г I 20 8 4723,74 Gd 100 200 66 Ag. 2
94 Pb I 50 45 Th 5 4 63 Т1 I 2
89 Nd 8 45 Mo 4 4 56 Рг 8 1
88 10 3 32 Mo 4 4 56 и 4
88 W 7 8 24 Er 3 56 La II 300 200
88 Tb 6 22 Ru 6 55 Се 4
Я6 и 1 4 17 Tl 1 40 7 55 Y 3 2
84 Рг 12 5 17 Dy 2 2 53 Ru I 60 6
84 (25) 15 Nb 1 3 51 Са I 100 7
83 Hf 15 4 10 Cr 125 8 35 Re I 150
76 Cr I 40 5 09 w 4 20 Rh I 100 20 Г
72 Co I 4 2 06 Mo 10 20 3343,90 Pt I 100 80 о
70 Tb 4 4722,95 Sm 3 La II 150 се
62 Ce 8 1 88 Ta 200 3303,11 400
61 Xe II (3) 86 V I 20 15 08 J II зоб r (25)
60 Y II 6 8 83 Bl I 10 5 3302,99 Na I 150 R (П
55 u 1 8 8 Hg I (5) 94 Zn 700 7? 300/? X
17 Fe 150 125 73 u 40 50 94 Ca 4 6 S
71 Ne I (15) 91 Ce 10 io
3802,52 Pd 3 70 Er 12 88 Cr 30 2 о
42 10 67 Pr 5 86 Fe II 1 о =3
34 Ce 3 63 Sm 3 82 U 6 4 tn
30 Pr 10 2 62 Tl 1 80 8 77 Ta 50 1 Ж
28 Fe 25 10 55 Bl I 1000 100 72 Mo 25 о -
23 4 3 28 Sr I 30 67 Zr II 10 6 3»
17 Tb 30 3 19 Bl I 10 5 66 Pr 15 2 ь
17 Mo 5 5 16 Kr (3) 64 Tb 8 10 ЗОЭ 3
15 07 02 Th P Ta 8 2 8 flOO) 4722,16 15 Zn 1 Ne I 400 300 (5) 62 3302,59 Nb Zn I 1 800 Е X
3801,98 98 Ли 1 Fe 1 25 5 (4 11 La II Th 2 2 56 55 ’ П BI 150 llG) s
96 и 15 02 Er 4 54 Kr I (10) X
93 Th 5 5 4721,91 Pr 3 51 В 10 X
92 Rb II (20) 88 Ir 2 49 и 3 1 s
92 Се 4 76 Rn I (ISO) 49 J II (5)
92 W 9 10 71 Hl 10 4 47 Dy 4 2 b
91 Мп 20 20 68 Pr 3 45 Tu 125 80 rrt
90 Хе I (3) 62 Ac (10) 44 Yb 7 s
88 Dy 8 2 54 Ne I (70) 43 J II (2) tn
84 Мо 20 25 51 V I 15 12 33 Ta 3 1 3
81 Fe 7 3 47 Pr 2 32 Na I 600/? 300/? о
80 Та 3 47 Gd 20 20 28 Kr 0) СП
80 ТЬ 15 43 CI II (25) 26 U 1 2
68 Fe 50 25 41 Co 8 100 23 Re 30
66 Hg I 15 2 40 Sm II 20 19 Cr 50 1
63 Мп II (6) 32 U 2 18 Nb 5 10
61 Ей 7 10 28 Os 12 17 Y 0 9
60 Os 20 5 28 CI I (6) 13 Pd I ЮЭ0 200
•56 Tl 7 3 25 V I 3 2 12 Pt 2
3801,53 Се II 25 3 23 06 Dy Er 12 5 5 10 09 TI II Sm 8 8 20 4
52 W 9 7 00 Xe (2) 3301,86 Pt I 300 250
5 In II (50) 00 Rh I 8 5 73 Sr I 100 10
45 J (5) 4720,93 Ir 2 56 Os I 500 50
39 Xe I (30) 92 Ru 15 49 Nb 1 100
37 Nd 60 40 91 Nd 4
37 U 3 5 83 Sc I 4 5 2138,75 Os 3 1
37 Tn 10 8 78 Yb 7 1 66 Rh 25
36 Eu 9 10 4719,95 La II 200 300 61 Os 8
35 Pr 30 9 84 Sm II 125 59 Fe I 8
33 Gd 15 58 Nl II 10
33 Fe 1 3346,20 Re I 100 57 Ir 15
30 Ho 6 4 3345,93 Zn I 150 50
30 Nb 5 8 90 V ...... 125 2138,56 Zn f 800 7? 500
20 Cr 35 3 57 Zn I 500 100 Nb 2
16 V I 3 1 5 Rn (2) 53 2
15 Nb 3 20 49 Ne II (7) 51 Си I 25
15 U 20 46 Er 6 1 40 Os 3 4
15 Ta 1 10 45 Be I 0
12 Nd 15 15 44 Ce 20 Цирконий Zr
09 F II (6) 37 Dy 3 2 3603,21 Fe 1 150 80
08 TI I 15 5 37 Cr 18 1 79 Eu IO0 50
05 Pt 4 35 Mn 15 3602,. 8 NI I 150 15
00 Sn 200 150 32 К (30) 12 Kr II (2)
3800,9'1 Xe (10) 32 Ru 6) 10 C! (12)
95 Re 3 31 Eu 3 2 09 i e I 20 5
94 Mo j 4 23 Ce 3 08 C > I 200 35
94 Nb 10 8 15 Cr 15 2 08 Ca 3
89 Sm II 20 25 11 Ta 3 3 06 Ir I 3
88 Y II 2 5 09 W 9 8 03 Cu 5;) 25
78 Sm 5 2 09 Nd 12 2 3601,98 Th 2 2
77 U 2 02 Sm 1 3 98 Sm 2 1
70 Zr II 5 1 3345,02 Zn I 800 300 92 Y II 18 60
Продолжение
со Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность Длина волны, А Элемент Интенсивность
дуга искра (разряд) луга искра (разряд) дуга искра (разряд)
Цирконий Zr {продолжение) Цирконий Zr (продолжение) Эрбий Ег (продолжение)
3601.92 87 Рг Но 3 6 3437,37 28 Та NI I 7 600# 300 40 4007,60 59 Zr I Се 25 15 1 4
84 Мо 1 3 3436,74 Ru I 3000/? 150 54 In II (15)
83 Os 60 20 54 Ru 20 10
8 Pb II (20) 3392,99 NI I 600# 100 49 Sm Н 50 25
80 w к 4 99 Cr II 10 47 Pd I 5
75 Tb 15 3 81 Ar 1 (100) 47 и 2 2
74 AI 71 Tl I 20 8 45 Ce 4
73 2 66 Fe I 300 200 45 Mo 4 5
70 Sm II 5 54 Ru 100 40 44 Nd 20 20
67 Сг I 50 30 48 Ir 2 4 36 Yb 5
6 Rn (5) 38 Re 3 35 Hf II 5 4
58 w 6 34 Nb 20 7? 30 33 Br 80 (10)
51 Аг II (5) 31 Fe I 125 8U 27 Fe I 50
50 Tb 8 31 Ar I (3) 23 Ta 4 2
48 Ru 9 5 26 Ce 3 ...... 19 Tl I 15 1
42 U 3 2 Rn (2) 14 Dy 6
40 Ir I 30 8 20 Tl 2 1 04 Mn 10 5
40 F (30) 17 Mo 15 2 03 Th 20 20
39 ft 3 1 05 Ho 6 8 02 Ce 2 ......
38 15 04 Th II 10 15 00 W 6
32 Nd 10 2 02 Cu I 7 00 Nb 5
27 15 15 01 Fe 20 6 4006,98 Sm 3
25 4 1 01 Tb 15 8 97 Gd I 3 (100) Г)
19 TI I 7 3 3391,99 Eu 40 5 50 Те ...... о
99 Dy 4 и
3601,19 Zr 1 400 15 99 Er 30 12 3908,03 Pr II 100 50 =1
* 05 04 La II Th 5 8 15 10 3391,98 Zr 11 300 400 3907,94 48 Fe Sc I 100 125 60 25 m
02 Pr 10 2 95 Nd 6 30 Pr 8 3 Я
3600,97 Gd 30 30 89 Ru 50 6 29 Ce 35 6 S
96 w 9 88 Ce 3 20 W 6 5
95 Ho 6 10 85 Mo 1 30 2 Pu II 100 о
92 Nd 20 10 84 Sm 2 3 19 J II ...... (18) =1
83 Th 3 1 73 Rh I 3 1 17 V 2 2 га
81 Co I 4 72 Tb 15 3 15 Sn ...... 4 X
80 Tb 8 72 Th 1 3 12 Gd 100 100 и
77 J (5) 59 Ce 10 12 Sm 10 15
76 Yb 10 20 59 Nb 1 5 И Eu II 1000# 500# ь
75 Rh I 8 2 55 Lu 10 2 1 Pu 100 СП
Pr 25 5 54 Mo 4 02 и 5 1
74 Er 30 20 53 W 10 10 3906,98 Mo 5 5 £
74 Mo 2 4 43 Cr II 4 150 93 Cs II (20)
73 1 II 100 300 40 u I 6 n 92 Ce 8 3 Ja
73 Cs (10) 37 Cr 12 92 Mo 5 5 s
73 Ho 6 33 Nb 5 3 91 Nb 5 5 я
70 Ta 2 1 29 Os 2 5 89 Hf 3 3 s
68 Rb (20) 05 Nl 1 400 40 80 Sm II 6 5 s
58 Ce 15 2 80 Th 8
49 u 1 2 эрбий h.r 75 Fe 10 10 s
44 Tb 8 50 4009,72 Fe I 120 100 75 V 1 50 20 гв
43 Th 4 1 4008,97 Ir I 5 53 To 4 s
39 Yb 2 2 93 TI I 80 35 48 Fe I 300 200 rn
34 Dy 20 30 92 Gd 20 3 48 Mo 5 10
29 U 10 92 и 8 45 Ce 8 2 о
29 w 4 3 87 Fe 5 1 41 Hg 1 25 15 СЯ
28 5 5 87 Eu 8 2
22 Аг II (3) 76 Br (20) 3906,34 Er 11 25
21 J (10) 75 Nd 12 10 29 Co I 150
20 Mo • 3 3 75 W I 45 45 29 Pt 1 2 1
3599,76 Ru 12 100 71 Pr 150 50 26 Ho 3 3
70 и 2 1 25 Kr II (150)
3438,84 Yb 20 100 67 Mo 20 15 Zr 3
73 Те (10) 66 Ce 8 10 Ce 2
72 Yb 4 80 49 Dy 5 10 Nd 15 10
71 Co I 80 48 Kr II (10) 09 Pr 6 8
70 u 2 3 46 Hf II 5 8 04 Fe II 2 2
61 Os 4 10 45 Ce 6 ...... 01 Ba I 4 2
57 ть 15 8 42 Nd 5 3 3905,99 Ru 6 3
52 In II (Ю) 33 Gd I 15 10 97 w 8 7
47 Nd 6 1 33 Sm 8 10 95 Dy 6 1
47 Er 9 1 28 Nb 5 10 92 Ce 3
43 Hf 12 3 27 Ru I 20 20 90 U 8
42 Nb 1 50 22 Th 10 8 89 Nd 40 30
41 U 3 3 18 Er 8 1 88 Yb 2 10
37 Ru 1 70 35 17 V II 2 10 85 Xe II (5)
34 In II (50) 09 Sm II 10 3 85 Ce 3
32 Er ’12 1 08 Kr II (25) 83 Tb 2
31 Eu 5 ...... 06 Tl I 50 7 78 Ho 30 6
31 Pr 25 1 05 Mo 4 5 72 J I (10)
31 Fe 10 3 05 Ir I 12 2 66 Cr 2 4
24 Hf II 25 25 02 Mn 15 5 66 Eu 3
24 Ce 3 4007,98 Eu 6 65 Gd 50 50
3438,23 Zr 11 250 200 4007,97 Er I 35 ...... 61 6 Tb Rn 10 (3)
21 W 7 3 96 Ho 4 3 56 Dy 6
09 Ir 1 6 94 Co I 3 56 Nd 10 10
07 Ce 15 93 u 8 3 55 Ho 15 8
05 Sm II 9 3 90 Se II (150) 53 SI 1 20 15
3437,95 Y 3 78 S II (5) 45 Ir I 8
95 Fe 15 7 78 Pr 8 3 42 Er 18 I
93 U 6 10 77 Dy 12 2 37 SI 4
87 V I 2 1 75 To 3 3904,83 Yb 12 150
81 Ce 10 69 u 2 4 78 P (100)
77 V 1 4 2 69 Eu 5
«о 72 Re 1 100 66 La 3 2
S 6Q Co I 150 61 In II (10)
АБСОЛЮТНАЯ ЧУВСТВИТЕЛЬНОСТЬ ЭМИССИОННОГО СПЕКТРАЛЬНОГО АНАЛИЗА
В таблице приведены ориентировочные данные о наименьших весовых количествах элементов, которые могут быть обнаружены с помощью эмиссионного спектрального анализа в электрических источниках света (дуге, искре, разрядной трубке). Приведенные значения получены для разных элементов различными техническими приемами, обеспечивающими достижение максимальной чувствительности. Данные для металлов относятся, как правило, к анализу микрообразцов, содержащих только определяемые элементы, данные для газов — к анализу газовых смесей.
Более подробные сведения см.: 1. А. Н. Зайдель. Н. И. К а л и т е е в с к и й, Л. В- Л и п и с, М. И. Ч а й к а. Эмиссионный спектральный анализ атомных материалов, Физматгиз. 1960. — 2. А. Н. Зайдель. Основы спектрального анализа. Изд. «Наука», 1965. —3. О. П. Бочкова. Е. Я. Шрейдер. Спектральный анализ газовых смесей, 2-е изд., Физматгиз, 1963.—4. J. Р. Cali, Trace Analysis of Semiconductor Materials, Лондой. 1964.
Элементы Наименьшее обнаруживаемое количество, г Элементы Наименьшее обнаруживаемое количество, г
и Ag, Ar «, Be, Не *, Кг * LI, Mg, Mn, N, Ne **, Sc, Хе* Y Al, В, Ba, Bl, Ca, Cd; Со, Сг, Си, Ей, Ее, Ga, Gd, Hg, К, La, Lu, Mo, Na, Nl, Pb, Pd, Pt, Ra, Rb. SI, Sn, TI, Tu, V, Yb, Zr IO-13 10“ 10 - I0~9 2-Ю-9 — 1-10—8 Au, Ce. Cs. Dy. Er, F, Hf. Ho, In. Nb, Nd, Pr, Sb. Sm, Sr, Ta, Tb. Те, Th. Tl, U. W As. Cl. Ir, Np, P, Pa, Pu. Re, S. Zn 2-Ю-8 - 1-Ю-7 2-Ю-7 — 10~8
* Чувствительность обнаружения в инертных газах 10 ~ 2 г.
** Чувствительность обнаружения в инертных газах 10 ~~ 3 г.
ТЕМПЕРАТУРЫ НЕКОТОРЫХ ПЛАМЕН, ИСПОЛЬЗУЕМЫХ В КАЧЕСТВЕ ИСТОЧНИКОВ ВОЗБУЖДЕНИЯ
Горючая смесь Температура, °C Горючая смесь Температура, °C
Ацетилен — воздух . , . . Ацетилен — кислород . . . Бутаи — воздух Водород — воздух .... Водород — кислород . f . 2100-2400 3100-3200 1300—1900 2000-2100 2500-2700 Карбюрированный газ — воздух , , Пропан — воздух Светильный газ — воздух Светильный газ — кислород 1700-1800 1900-2000 1700-1800 2700-2800
НАИБОЛЕЕ ИНТЕНСИВНЫЕ АНАЛИТИЧЕСКИЕ ЛИНИИ, ВОЗБУЖДАЕМЫЕ В ВОЗДУШНО-АЦЕТИЛЕНОВОМ ПЛАМЕНИ
Таблица содержит наиболее распространенные в аналитической практике линии. В первой графе приведены элементы или свободные радикалы, испускающие эти линии .(или полосы), во второй — длины волн линий в ммк, в третьей — интенсивности линий при содержании определяемого элемента 1 у/лсл; интенсивность аналитической линии калия при указанной концентрации принята за 100.
Элемент или радикал Длина волны, ммк Интен- Элемент Длина Интен- Элемент Длина Иитен-
снвность радикал сивность радикал ммк сивность
во2 547,6 0,5 In 451,1 3 Na 589.0 } 1000
ВаОН Са 873 422,7 1,5 20 к 766,5 769,9 } 100 Rb 589,6 780,0 794,8 460,7 378 535,1
СаОН Сг Cs Ее Ga 622,0 425,4 852.1 386,0 417,2 15 0,5 10 0,1 0,5 670,8 384,0 .403,1 403,4 100 2 | 20 Sr . Tl } 10 10 70
720
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС,
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
Таблица содержит важнейшие аналитические линии и полосы, возбуждаемые в воздушно-водородном, кислородно-водородном н кислородно-ацетиленовом пламенах прн использовании различных растворителей. Приводятся условные интенсивности линий в соответствующем пламени, отнесенные к одинаковой концентрации определяемого элемента. Данные для воздушно-водородного пламени относятся, за исключением особо оговоренных случаев, к водным растворам.
Недостаточно надежные данные заключены в скобки.
Более подробные сведения см.: 1. Н. С. Полуэктов, Методы анализа по фотометрии пламени, Госхимиздат. 1959. — 2. Ф. Бурр и ель-Март и, X. Рамирес-Му и ь о с, Фотометрия пламени, перев. с англ. ЙЛ, 1962. — 3. R. Mavrodineauu. J. Bolte их, L’analyse spectrale quantitative par la flamme, Париж, 1954. — 4. I. Dean, Flame Photometry, Нью-Йорк, 1960.
Условные обозначения
ац. — ацетон МБК — метил изобутнлкетои
аац. — ацетилацетон МГК — метилгексилкетои
бзл. — бензол мет. сп. — метиловый спирт
б. сп. — 4% раствор бутилового спирта в воде пр. сп. — изопропиловый спирт Г. — газолин э.с.в. —диэтиловый эфир — этиловый спирт —
к. — керосин вода (1:2:1)
л. — лигроин
В случае смесей органических растворителей с водой указывается процентное содержание растворителя в смеси по объему (например, 60% ац. обозначает, что смесь содержит 60 объемн. % ацетона и 40 объемн. % воды).
Элемент, молекула или радикал Дл::на волны, ммк Интенсивность в различных пламенах
воз душ ио-водородное кислородно-водородное к нс л о род но-a цетиле новое
вода неводный или смешанный растворитель вода неводный или смешанный растворитель
Ag 328.07 100 100 100 (э. с. в.) 50 30 (э. с. в.)
338,29 250 170 170 50 40 »
А1 394,4 0,3 0.8 20 (МБК) 1 100 (МБК)
396,15 0,35 1,0 30 2 200
А1О 464,8 1,7 10 » 0,13 17 »
467,2 | 0,8 2 10 0,15 17 »
469,5 1,7 7 0,14 11
471,6 1,7 5 » 0,13 6 »
484,2 3 50 » 0,13 70 »
486.6 J 115 3 30 » 0,25 50 н
507,9 2 7 0,15 11
510,2 2 10 » 0,18 17 »
512,3 2 10 » 0,18 17 »
514,3 2 5 » 0,17 7
Au 267.6 0.3 2 1,7
ВО2 453 1 7 15 (б. сп.) 1.2 2,5 (50% мет. сп.
471,5 2,5 20 30 2,5 5 »
494 5 30 <50 » •э 8 >
518,0 8 50 80 * 6 15
547,6 11 60 90 15 17
579 •7 30 70 10 10 *
603 2 10 70 » 7 5 »
620 1.5 7 50 » 3 3 »
Ва 553,56 170 40 100 » 10 50 (л.)
Ва+ 455,40 8 8 20 5 100 »
493,41 80 25 40 5 100 »
ВаО 496,5 80 25 35 » 1.7 3 »
521,4 80 25 35 2 3 »
534,9 80 20 30 » 2 2,5 *
549,2 80 20 25 1.7 2,5 »
564,4 80 20 22 1,5 2,5 »
570,1 80 20 2> 1,7 2/» »
586,4 70 20 25 1,7
604,0 70 20 25 » 1,7 • • •
46 Зак. 783
721
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ П»Л0С,
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
Продолжение
Элемент, молекула или радикал Длина волны, ммк Интенсивность в различных пламенах
воздушно-водородное кислородио-водородное кислородио-ацетилеиовое
вода неводный или смешанный растворитель вода неводный или смешанный растворитель
ВаОН 488 100 30 40 (б. сп.) 2 5 (л.)
502 80 25 35 » 1,7 3 »
513 150 30 50 3 5 »
524 80 25 35 » 3 3 »
745 50 10 10 (бзл.) 7 (100) »
830 200 30 25 15 (300) »
873 80 30 25 м 15 (300) »
ВеО 470,9 0.7 0,25
473,3 } 0,2 0,5 0.2
475,5 J 0,4 ...... о,п
505,5 1 0,25 0,10
507,6 } 0,1 0,25 0.10
509,5 1 0,25 . . .... 0,10
В1 306,77 0,2 0,017
472,26 0,5 0,25 0.005 (по. сп.) 0,05 1000 (э. с. в.)
Са 422,67 250 1000 1700 (б. СП.) 250
Са+ 393,37 25 30
СаО 396,85 815,3 20 1,5 17 5
СаОН 865,2 554 500 2 1709 2500 (б. СП.) 7 170 700 (э. с. в.) Rd
572 25 100 200 » 20
602 100 700 1000 250 OW » 1000 120 2,5 (МБК)
622 500 2500 5000 500
Cd 644 228,80 70 0,2 300 ] 700 17 (50% пп. сп.) 70 0,25
30 (пр. сп.} 5 (ап.)
326.11 20 2 5 (ац.) 0.25
Се СеО 6 (пр. СП.)
550—600 468,4 70 25 10 10 » 2.5 » 0,7 0,5
481 30 5 5 0,5
Со 494 40 7 5 » 0,7 5
340,51 40 20 30 (б. сп.)
341,25 40 25 30 к 3
343,2 10 4,5 7 » 1,5
344,32 20 10 20 » 2,5
344,93 25 12 25 N 3
345,4 45 25 50 » 7
346,5 20 12 25 ц 3
347,40 17 7 12 » 2
350,23 | 30 17 30 » 3
350,63 9 20 » 2
351,3 20 15 25 » 3
352,8 35 35 юс (сем 7 • •••••••••
356,94 8 15 (б. СП.) 1,7
357,52 15 25 » 2,5
359,49 17 10 17 2
384,55 22 11 17 2
387,35 30 20 30 » 4
389,44 22 10 17 » 2
399,53 25 9 15 » 2
412,0 25 И 20 2 1009 (л.)
Сг 357,87 40 80 80 (л.) 20
359,35 35 70 70 17 800 »
360,53 30 55 55 15 500 »
425,43 120 100 150 (60% ац.) 20 900 »
427,48 110 80 ПО 17 550 »
428,97 100 70 80 12 300 »
520,6 170 70 70 (6. СП.) 10 100 »
т
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС.
ВОЗБУЖДАЕМЫЕ в пламени
Продолжение
Элемент, молекула или радикал Длина волны, ммк Интенсивность в различных пламенах
воздушио-водородное кислород но-во до ро дно е кислородно-ацетиленовое
вода неводный или смешанный растворитель вода неводный или смешанный растворитель
СгО 535,6 200 20 70 (б. СП.) 10
541,7 200 20 80 я 10
556,4 200 20 90 я 10
562,3 200 20 90 я 10
579,4 250 20 120 я 15
585,2 250 25 100 я 17
605,2 250 25 100 я 20
639,4 10 50 я 17
683,0 10 50 и 15
Cs 455,54 20 25 30 я 0,3
459,32 5 7 15 я 0,1
852, И 1000 1000 2000 я 1000
894,35 300 500 700 я 500
Си 324,75 60 100 500 (мет. сп.) 100 300 (к.)
327,40 40 100 500 100 300 Я
510,5а 8 11 (б. СП.) 7
Cull 428,0 3 2,5 я 0,7
СиО 606,0 5 5 я 3
СиОН 505 50 7 9 и 2,5
524 70 12 15 я 5
DyO 537 100 17 20 я 6
457,2 8 10 МБК)
515 20 30 Я
520 25 30 я
526,3 70 80 я
540,4 60 70 я
549,3 60 70 я
572,9 120 150 х
583,4 120 150 я
586 по 140 я
600,6 15 70 я
605 15 70 я
608 15 55 я
ЕгО 504 30 55 и
515 17 30 я
546 40 60 я
553 50 80 »
559,6 561,3 1 1 35 70 *
567 25 50 »
Ей 459,40 25 35 я 10
462,72 20 30 я 10
466,19 17 25 » 10
ЕиОН 601,82 100 120 » (10)
598 100 120 я (10)
623 70 100 я (10)
647 25 150 я (10)
684 20 100 я (10)
702 50 100 я (10)
Ее 302,06 4 2,5 50 я 1,5
344,06 35 6 10 (б. сп.) 2 10 (аац.)
358,12 50 6 10 я 1,2 10 я
371,99 80 40 100 (СС1Д 15 100 Я
373,71 80 30 50 (б. сп.) 8 70 я
374,7 70 25 50 я 6 50 я
382,04 382,5 | 50 11 20 я 1.7 2 10 я 12 я
385,99 70 35 50 я 11 70
387,86 } 60 7 12 я 1,2 8 я
388,63 12 20 я 2,5 20 я
46*
723
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС,
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
Продолжение
Элемент, молекула или радикал Длина волны, ммк Интенсивность в различных пламенах
в оз д у ш некие лоро Д-ное квелородио-водородное кислородно-ацетилеиовое
вода неводный или смешанный растворитель вода неводный или смешанный растворитель
Ее 389,97 50 5 10 (6. СП.) 0,9 5 (аац.)
392,2 392,9 | 50 8 17 » 1,о 1,5 7 » 10 »
438,35 50 5 15 » 0,9 1,7 (ац.)
526,95 70 17 60 3,5
532,81 70 15 60 » 3,5
ЕеО 553,2 100 20 80 » 6
561,4 150 35 110 » 9
564,7 170 40 120 » 10
579,0 40 ПО » 10
581,9 | 170 40 120 » 11
586,8 40 100 » 10
609,5 100 20 50 » 12
618,1 100 20 50 » 10
621,9 100 20 50 » 10
Оа 403,30 10 100 150 » 10
417,21 20 200 300 » 20
О<1 591,14 (10) 80 250 (МБК) (20)
О<1О 461,7 17 30 »
463,4 15 15 »
489,3 12 15 »
491,0 12 20 »
492,8 7 15 »
540,5 j / 20 »
545 15 25 »
569 (3) 35 70 »
581 (5) 50 120 » (io)
592,7 (W) 80 250 (20)
599 (Ю) 80 250 (20)
608,1 (Ю) 70 200 Ж (20)
613 (Ю) 70 200 » (20)
621 (10) 70 250 » (20)
бе 259,25 0,7 (г.р. сп.' • . . • • • 0.025 (50% пр. сп.) 0,015 0,025 (50% пр. сп.)
265,14 2 » 0,03 » 0,04 0,05 »
270,96 0,4 0,01 0,02 »
275,46 0,7 » 0,008
Hg 253,65 2,5 » 0,3 1.7 (ац.) 1,2 4 (МБК)
НоО 5,10,5 Зо 40 (МБК)
515,7 50 50
527 50 50 »
532,0 50 50 »
566,0 120 170 »
569,6 ПО 150 »
584,9 35 50 »
In 303,94 5 3 3 (б. сп.) 3
325,61 10 10 10 2,5 30 (ац.)
410,18 150 200 300 Я 50 ПО »
451,13 250 350 500 » 70 140 »
то 428,3 1
К 404,5 30 70 100 (б. СП.) 10 6 (ац.)
766,49 769,90 1 10 000 30 000 50 000 » 30 000 20 000
LaO 438,4 5 25 25 (МБК) 17 80 (МБК)
442,3 5 25 30 » 17 80
538,1 I 15 25 5 15 »
540,7 1 3 20 30 м 7 20 »
543,2 20 30 7 25
545,8 J 17 30 » 6 20 »
560,1 70 100 » 17 170
562,7 50 100 » 17 170 »
586,8 10 25 » 12 100 *
589,5 у 3 10 25 » 12 100
592,2 1 10 25 » 12 100
724
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАИТЫ МОЛЕКУЛЯРНЫХ полос,
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
П родолжение
Элемент, молекула или радикал Длин a волны, MMK Интенсивность в различных пламенах
воздушно-водородное кислородно-водородное кислородио-ацетиленовое
вода неводный или смешанный растворитель вода иеводный или смешанный растворитель
LaO 743 30 20 1 000 (МБК) 100 120 (МБК)
792 25 20 1000 » 100 150
LI 460,29 2,5 3 (б, сп.) 0,5
610,36 30 20 30 » 10
670,78 10 000 50 000 70000 » ю ооо
LuO 466,2 30 80 (МБК)
517,0 50 ПО »
599 20 40 »
675 10 30 »
Mr 285,21 100 100 250 (ац.) 170 100 (э.с.в.)
517,1 518,36 } 5 20 (б. сп.) 0,6 0,5
MgO 500,7 10 25 » 1,7
MgO’i 362,4 100 25 25 (э.с.в.) 1
370,2 500 100 100 » 5
381—383 500 80 80 » 3,5
387,7 200 50 50 » 1,7
391,2 200 50 1,7
Mn 279,48 15 17 (г.) 1,8
279,83 11 1,7
280,11 8 11 » 1,5
403,2 500 1000 1 500 (л.) 500
MnO 515,9 20 30 (б. сп.) 3
519,2 | 50 25 40 » 4
522,9 25 35 3,5
536,0 45 70 » 8
539,0 | 100 50 80 » 8
542,4 35 70 • 7
558,6 80 120 » 17
561,0 120 60 100 > 17
586,0 40 50 8
588,1 70 50 70 » 8
591,0 40 • 50 » 8
617,6 30 25 30 . 5
MnOH 363-410 70 10 8 »
Mo 379,83 2,5 0,8 Ю (л.) (0,5) 2«.i 4
82я,41 3 0,8 10 > (0,3) 20 ’
:х),зо 3 0.8 5 » (0,25) 20 *
MoO2 550—600 25 10 (3)
Na 330,3 2,5 20 10 (б. СП.) 10
568,6 30 40 » 10
589,2 30 000 50 000 70000 » 25 000
819 5 10 » 20
Nb 450 5 1 0,17
650 5 1 0,3
NdO 461.9 3 6 (МБК)
531,3 5
599 10 25 « 1
622 2,5 20 0,7
637 2,5 30 » 2
643 2,5 40 » 3
650,0 5 60 » 5
661 10 100 » 10
691 10 500 5
702 10 500 . 10
712 10 500 10
Nl 300,3 4 3 5 (б. сп.» 1,1
336,96 17 9 17 3
338,06 12 7 10 » 2,5
* Растворитель; МБК 4 ац. 4 пр. сп. + вола (5 : 2: 2 :1).
725.
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС,
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
Продолжение
Элемент, молекула или радикал Длина волны, ммк Интенсивность в различных пламенах
воздушно-водород-иое кислород но-во дородное кнслородно-ацетиленовое
вода неводный или смешанный растворитель вода неводный или смешанный растворитель
NI ОНО Р РЬ Pd РгО 339,3 341,48 343,36 344,63 346,0 347,25 349,30 351,03 351,51 352,45 356,64 361,05 361,94 385,83 520-600 502,4 517,5 520 280,20 283,31 363,96 368,35 405,78 340,46 342,12 346,08 351,69 360,95 363,47 515,7 535,2 537 561 569,1 576,3 601.9 628 636,3 648,0 695 709,5 732,0 737,6 766,3 805 848,9 265,95 306,47 482,59 381,44 468,23 602 627 665 420,19 421,56 780,02 794,76 346,05 346,47 332,31 339,68 25 80 15 20 45 7 25 ) 45 80 20 15 40 10 30 4 1 1,5 3 3 45 И 6 8 30 55 17 50 10 12 20 4 17 7 22 50 10 7 22 4 17 12 15 0,4 5 10 10 70 10 10 20 45 80 7 10 10 11 12 15 10 5 5 5 (Ю) (Ю) 25 (б. сп.) 60 * 12 и 20 я 30 я 6 я 25 я 10 н 30 я 80 * 15 я 10 я 30 » 10 35 я 30 Я 35 я 9 „ (г.) 2,о я 7 я 15 я 15 я 200 (МБК) 50 я 20 я 40 я 90 я 150 я 3 я 6 6 Я 8 Я 10 Я 11 Я 20 11 я 15 я 17 » 50 50 > 5 10 3 5 7 2,5 7 5 9 15 3 2,5 5,0 1J 0,1 0,2 0,3 10 2 2 2 7 10 40 (МБК) 10 » 15 > 25 » 5 » 20 » 8 30 • 60 » 10 » 5 я 20 я 4 (г.) 5 » 10 » 10 »
Pt Ra Ra+ RaOH Rb Re Rh 0,11 0,25 20 10 3500 2500 0,00 0,00 2 4 (Ю) (Ю) (5) (2) 0,8 1 (5) (3) (1) (1) (5) (5) 35 15 3500 2500 0,00 0,00 2,5 . 8 30 » 20 я 10 Я 5 » 5 » 50 (б. сп.) 20 я 5000 » 3000 » 3,5 (пр. сп.) 12 » 0,5 0,7 2 1 2000 1700 0,035 0,018 1,7 5 0,7 (МБК) 0,08 (50% мет. сп.) 0,045 » 3 (90% пр. сп.) 8 я
726
i ~
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС.
ВОЗБУЖДАЕМЫЕ в ПЛАМЕНИ
Продолжение
Интенсивность в различных пламенах
Элемент, 1 ' молекула Длина кислородно-волородиое кис лоро дио-а цетиле новое
волны, воздушно- ‘
ммк водород- неводный неводный
ное вода или смешанный вода или смешанный
растворитель растворитель
Rh 343,49 2,5 15 25 (пр. сп.) 9 17 (90% пр. сп.)
350,25 3,5 8 10 » 5 8 »
352,80 3 7 9 » 4 7»
358,31 4,5 4 4 • 1,7 3
359,66 5 5 5 » 2,2 4 5 »
365,80 6 П 15 » 6 9 »
369,24 7 35 40 » 15 22 •
370,09 6 11 11 » 4,5 8 »
385,65 7 4 3,5 > 1,5 3 »
421,11 И 5 3 » 1,1 18 »
437.48 и 8 4 » 1,7 2 2 »
RhO 542,5 40 15 1
Ru 342,83 2 15 (50% мет. сп.) 1,5
343,67 1 10 » 1
349,89 ‘ * 5 30 » 3
359,3 ’ 1 ‘ ‘ 1 10 » 1
366,14 2 20 » 2
372,75 20 150 » 30
379,9 10 100 » 25
569,90 0,5 5 » 1
ScO 467,3 ’ ’ ’ 10 25 (МБК)
470,7 ’ 12 35 » .
474,2 8 25 »
485,8 ’ ‘ 20 60 •
489,4 ’ ’ 15 45 »
509,7 ’ ’ 8 30 »
513,4 9 35
517,1 ' 8 25 »
г>73,7 17 60 » 2
' 577,3 ‘ ’ 35 120 3
581,1 40 150 » 5
584,9 40 150 5
588,8 35 120 » 3
592,8 30 100 » 3
601,7 < ‘ '
60* 170 800 » 20
607,3 250 1700 • 30
611,0 200 1200 • 25
615 . 110 700 » 10
619,1 50 400 5
I 623 30 250 » 3
649 ю 70 » 1
Sm 471,66 10 10 »
k 586,81 30 50 • 0,3
t SmO 582,0 20 30 0,2
595 35 60 » 0,4
598.8 35 60 » 0,4
603,5 35 70 » 0,5
614 ' 40 80 » 2
624,3 . . 30 80 » 2,5
633,9 20 80 » 2
638 20 100 • . 2
642 20 100 » 2
651,0 ... 20 110 » 3
667 5 60 » 0,5
681 3 40 » 0,3
j Sn 284,00 0.08 (0,015) 0,2
12 (мет. сп.)
286,33 0 11 0,017 0,17
10 (мет. сп.)
300,91 0,2 0,04 0,3
8 (мет. сп.)
727
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
Продолжение
Элемент, молекула или радикал Длина волны, ммк Интенсивность в различных пламенах
воздушно-во дородное кислород но-во дородное кислородно-ацетиленовое
вода неводный или смешанный растворитель вода неводный илн смешанный растворитель
Sn 303,41 0.4 0,05 10 (л,- 0,4
16 (мет. сп.)
317,50 0,12 7 (пр. сп.) 0,12
326,23 0,4 10 (пр. сп.) 0,4
333,06 0.4
1,7 (пр. сп.)
SnO 380,10 2,5 3 (пр. сп.) 0,3
326,2 0,4 0,09 0,08 (60% ац.) 0,17
332,3 1,5 0,35 0,2 » 0,2
338,8 2,5 0,7 0,18 » 0,2
341,6 3 0,7 0,18 » 0,12
348,5 1,5 0,25 0,17 0,2
358,5 3,5 0,9 0,22 * 0.2
369,1 2,5 0,7 0,15 » 0,17
372,1 2,5 0,7 0 15 » 0,15
383,3 2,5 о,6 0.11 » 0,08
386,5 3,5 0,7 0,11 0,08
398,4 3 0.5 0,08 » 0,07
485 5 0,22
Sr 460,73 500 1000 2000 (60% ац.) 200
Sr-1- 407,77 30 50 (б. сп.) 17
SraOa 421,55 20 30 » 12
594,3 500 90 100 » 10
SrOH 597,0 500 80 100 » 10
605,9 5000 1000 1500 » 100
646,5 250 100 150 » 10
659 500 200 300 » 20
666 500 700 1000 » 40
682 250 1000 1000 30
TbO 704 461 70 8 100 » 10 (МБК)
535 40 60 »
544 30 40 »
гбз.э 40 70 ж
573 50 100 »
592,1 80 170 (10)
597,9 70 150 » (10)
607,8 40 100 (10)
TeO 634,9 2,5’ 17 30 » (5)
356,1 0,15 0,015
360,7 3 0,2 0,015
366,2 3,5 0,2 0,015
371,4 3,5 0,3 0,015
377,2 3,5 0,2 0,015
382,7 3,5 0,25 0,017
388,4 3,5 0,25 0,017
394,7 3,5 0,25 0,017
400,7 3,5 0,22 0.017
407,5 3,5 0,22 0,017
413,2 3,5 0,25 0,017
420,5 3,5 0,22 0.017
426,8 3 0,22 0,017
434,3 3,5 0.22 0,017
448,7 3 0,22 0,017
T1O 464,0 2,5 0,17 • 0,017
480.6 30 0,7
484.9 • • .... 30 0,8 1.1
495,6 35
500,0 35 1 1
.728
АНАЛИТИЧЕСКИЕ ЛИНИИ АТОМОВ И КАНТЫ МОЛЕКУЛЯРНЫХ ПОЛОС
ВОЗБУЖДАЕМЫЕ В ПЛАМЕНИ
Продолжение
Элемент, молекула или радикал Длина волны, ммк Интенсивность в различных пламенах
воздушио-водород-иое кислородно-водородное кислород но-a не т кленовое
вода неводный или смешанный растворитель вода неводный или смешанный растворитель
Т1О 516,8 40 1,5
545,0 45 1,5
576,1 45 1,5
673 20 10
713 20 10
Т| 276,79 0,5 1,5
351,92 4 3 25 (б. сп.) 0,7 2 (МГК)
377,57 50 100 170 10 30 »
535,05 30 70 100 5 20 »
ТцО 481,4 22 35 (МБК)
490 30 50 »
495 25 45 »
523 17 35 »
532,9 30 55 »
537 35 60
542 35 60 »
553 35 60
ио2 550 15 5 (1)
V 318,4 0,25 0,4 (50% мет. сп.)
VO 505,7 70 25 70 (б. сп.) 1,2
522,9 89 30 80 » 3
527,6 80 30 80 » 3
547,0 100 40 100 » 4
573,7 ПО 40 ПО 6
608,7 50 20 50 » 3
701,1
7O7’o | ..... 10 10
747 7 7
800 10 10
YO '465,0 8 17 (МБК)
467,7 10 20
470,7 9 18
481,8 30 50 »
484,2 22 40
505,0 7 20
507,8 6 20 »
574 8 50 » 1
587 10 50 » 1
599 300 1000 » 30 70 (МБК)
615 300 800 » 30 50 »
Yb 346,44 2 (1)
398,80 70 25 120 (МБК) (10)
555,65 250 70 60 » (10)
Yb + 369,42 1,5 (0,5)
YbOH 477,8 100 22 35 (МБК) (2)
485,0 100 25 35 » (2)
498,1 200 50 50 » (5)
517,4 150 40 40 » (3)
532,5 2э0 80 80 » (5)
544,3 120 35 45 » (3)
572.5 300 по 100 ПО)
587 80 25 35 (2)
602 30 10 25 (1)
Zn 213,86 0,04 0,06 1 (ац.) 0,017 0,13 (МБК)
0,15
(50% пр. сп.)
307,59 0,1 0,02
481,05 0,3 0,06 0,6 (л.) 1,7 (ац.)
520-600 0,5 0,12 12 (ац.) 4 »
ZrO 564 1,2 (0,1)
574 1,2 (0,1)
729а
ДЛИНЫ ВОЛН СПЕКТРАЛЬНЫХ ЛИНИИ И КАНТОВ МОЛЕКУЛЯРНЫХ полос,
ВОЗБУЖДАЕМЫХ В ПЛАМЕНИ (В ПОРЯДКЕ ВОЗРАСТАНИЯ)
Настоящая таблица предназначена для идентификации спектральных линий, возбу ждаемых в пламени, и для установления возможного совпадения этих линий.
Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал
213,86 Zn 285.21 Mg 351,04 1 Со 382.3 } Mg Sn
214,9 217,00 N Pb 286,33 294,4 Sn Ga 351,3 351,51 ’ NI 383,4 383,3
21?;58 Sb 300,3 Ni 351,69 Pd 384,55 Со
222,83 ) Bl 300,91 Sn 351,92 Т1 385,1 I N
223,06 302,06 Fe 352,45 N1 385,5 Rh
224,61 Sn 303,41 Sn 352,68 1 Со 385,65
226,3 N 303,94 In 352,95 J Rh 385,83 Nl
227,66 Bl 306,47 Pt 352,80 385,99 Fe
228,80 Cd 306,77 Bl 356,1 Те 386,2 N
228,81 As 307,59 Zn 356,64 NI 385,41 Mo
231,10 Nl 317,50 Sn 356,94 Со 386,5 Sn
231,15 Sb 318,4 V 357,52 Со 387,1 N
232,00 Nl 324i 75 Cu 357,87 Сг 387,2 CH
234,4 Si 325;61 In 358,12 Fe 387,35 Co
234,86 Be 326,11 Cd 358,31 Rh 387,7 Mg
234,98 As 326,2 Sn 358,5 Sn 387,86 Fe
235,48 Sn 326,23 Sn 358,92 | Ru 388,3 N
236,3 N 327,40 Cu 359,30 387,9 ) Te
237,5 P 328,07 Ag 359,62 389,1 Fe
238,3 P 330,3 Na 359,35 Cr 388,63
238,32 238,58 1 'Г 332,3 Sn 359,49 Co 388,9 CH
} Te 332,31 Rh 359,66 Rh 389,44 Co
239,6 p ззз;об Sn 360,53 Cr 389,97 Fe
241,4 SI 336,96 Nl 360,7 Te 390,30 Mo
242,80 Au 338,06 Nl 360,95 Pd 391,2 Mg
242,95 Sn 338,29 Ag 361,05 Nl 392,03
246,4 p 338,8 Sn 361,94 Nl 392,29 | Fe
247,1 N 339,11 362,4 Mg 392,79
247,64 Pb 339,30 363,47 Pd 393,03
247,8 P 339,68 Rh 363,96 Pb 393,37 Ca
247,86 C 340,46 Pd 365,80 Rh 394,40 Al
248,33 Fe 340,51 Co 366,14 Ru 394,1 } Te
248,7 SI 341,25 Co 366,2 Te 395,2
249,29 As 341,48 Nl 368,35 Pb 396,15 Al
250.4 As 341,6 Sn ' 369,1 Sn 396,85 Ca
250,69 SI 342,12 Pd 369,24 Rh 398,4 Sn
251,61 SI 342,83 Ru 369,42 Yb 398,80 Yb
252,41 SI 343,2 Co 370,09 Rh 399,53 Co
252,85 Sb 343,36 Nl 370,2 Mg 400,3 ) Te
252,85 SI 343,49 Rh 371,1 1 'Г 401,0
252,9 p 343,67 Ru 371,8 ) Ie 403,08 1 Mn
253,65 Hg 344,06 Fe 371,99 Fe 403,4
254,0 p 344,32 Co 372,1 Sn 403,30 Ga
257,4 Sb 344,63 Nl 372,75 Ru 404,41
257,6 s 344.93 Co 373,49 404,72 } К
259,0 s 345,4 Co 373,71 405,78 Pb
259,25 Ge 345,85 1 Nl 374,55 407,5 Te
259,81 Sb 346,17 374,9 j Fe 407,77 Sr
261,42 Po 346,05 Re 410,18 In
265,14 Ge 346,08 Pd j Te 411,88
265,95 266,32 267,60 270,65 270,96 275,46 276,79 279,48 279,83 280,11 Pt Pb Au Sn Ge Ge TI Mu Mn Mil 346,28 346,58 346,44 346,47 347,25 347,40 348,5 349,30 349,89 350,23 I Co Yb Re NI Co Sn Nl Ru Co 377,57 379,83 379,9 380,10 380,7 381,4 381,44 • 382,04 382,5 TI Mo Ru Sn I Mg Ra j Fe 412,13 412,5 413,6 417,21 420,19 420,5 421,11 421,55 421,56 422,67 425,43 426,8 | Co ) Iе Rb Te Rh Sr Rb Ca
280,20 Pb 350,25 Rh 382,0 } Te Cr
283,31 Pb 350,63 Co 383,5 Te
284,U0 Sn 351,03 NI
730
ДЛИНЫ ВОЛН СПЕКТРАЛЬНЫХ ЛИНИЙ И КАНТОВ МОЛЕКУЛЯРНЫХ полос,
ВОЗБУЖДАЕМЫХ в ПЛАМЕНИ (В ПОРЯДКЕ ВОЗРАСТАНИЯ)
Продолмение
Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал Длина ВОЛНЫ, ммк Элемент илн радикал
427,48 Сг 482,59 Ra 518,0 В 555 } Yb
428,0 Си 484,2 Al 519,2 Мп 555,65
428,3 In 484,2 Y 520 Dy 556,4 Bl
428,97 Сг 484,5 J 520,6 Сг 556,4 Cr
481,5 СН 484,9 TI 520,9 .1 558,5 С2
432,4 сн 485 Sn 521,4 Ва 558,6 Мп
434,3 Те 485,0 Yb 522,9 Мп 560,1 La
436,5 С2 485,8 Sc 522,9 V 559,6
437,1 с2 486,6 Al 523 Tu 561,3 J Er
437,48 Rh 488 Ba 524 Ва 561,0 Mn
438,2 С2 489,3 Gd 524 Си 559,7
438,35 Fe 489,4 Sc 526,3 Dy 561,2 } РГ
438,4 La 490 Tu 525,1 562,8
439,4 Bl 491,0 Gd 526,1 | Но 561,4 Fe
442,3 La 492,8 Gd 527,3 562,3 Cr
442,4 Bl 493,41 Ba 528,6 562,7 La
448,7 Те 493 1 R 526,95 Fe 563,5 C2
451,13 In 495 J ® 527,6 V 563,5 Co
453 В 494 Ce 530,8 .! 563,9 Tb
455,40 Ba 495 Tu 531,3 Nd 563,1 } Zr
455,54 Cs 495,6 Ti 532,0 Но 566,0
457,2 Dy 496,4 J 532,5 Yb 564,4 Ba
459,32 Cs 496,5 Ba 532,81 Fe 564,7 Fe
4-59,40 Eu 498,1 Yb 532,9 Tu 566,0 Ho-
460,29 LI 500,0 TI 534,9 Ba 567 Er
460,73 Sr 49V } Mg 535,05 Ti 568,26
461 Tb 500,7 535,2 Pr 568,82 568,1 569,9 569,6 569,1 570,5 569,90 570,1 572 572,5 572,9 573 573,0 573,7 573,7 572,1 575,1 573,1 574,7 576,4 576,1 576,3 577,3 579 579,0 579,4
461,7 Gd 502 Ba 534,0 ) Gd Ho } Pr
461,9 462,72 463,4 464,0 Nd Eu Gd Te 502,4 504 505 505,0 Nl Er Cu Y 535,1 536,9 535,6 536,0 | Tb Cr Mn
464,8 465,0 466,19 466,2 467,2 468,4 467,2 467,3 467,6 467,9 468,23 468,4 468,5 469,4 469,5 469,8 470,5 470,7 470,9 471,5 471,5 , Al Y Eu I Lu Al Sc Y c2 Ra Ce c2 J Al c2 Y Sc Be В C2 505,5 505,7 506,7 507,6 507,8 507,9 509,5 509,7 509,8 510,2 510,5 510,55 512,3 512,9 513 513,1 513,4 514,3 515 515 515,7 Be V Er Be Y Al Be Sc c2 Al Ho Cu Al C2 Ba .1 Sc Al Dy Er Ho 537 534,7 537.4 539,5 536,7 537,8 538,1 539,0 540,4 540,5 540,7 541,7 542 542,4 542,5 543,2 544 544,3 545 545,0 545,8 Cu } j Pr La Mn Dy Gd La Cr Tu Mn Rh La Tb Yb Gd TI La Ru Ba Ca Yb Dy Tb .1 Sc V } Zr } V TI Pr Sc В Fe Cr
471,6 Al 515,7 Pr 580,7 j Gd
471,66 472,26 Sm Bi 515,9 516,5 Mn C2 547,0 547,6 549,2 549,3 553 V 581,9 581,1 Sc
473,3 473,7 474,2 475,5 Be C2 Sc Be 516,8 516,1 517,0 518,6 TI | Lu Ba Dv Er 581,9 582,0 583,4 584,9 Fe Sm Dy Ho
477,8 480,6 Yb Tl 517,1 517,4 Sc Yb 553,2 553,3 553,56 554 554,1 Fe 584,9 585,2 Sc Cr
481 481,05 481,4 481,8 Ce Zn Tu Y 517,5 517,1 518,36 Ni ) Mg Ba Ca c2 585,6 586,8 586,0 586,4 } Dy Mn Ba
73L
ДЛИНЫ ВОЛН СПЕКТРАЛЬНЫХ ЛИНИИ И КАНТОВ МОЛЕКУЛЯРНЫХ полос,
ВОЗБУЖДАЕМЫХ В ПЛАМЕНИ (В ПОРЯДКЕ ВОЗРАСТАНИЯ)
Продолжение
Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал Длина волны, ммк Элемент или радикал
586,8 Ее 604,0 Ва 633,9 Sm 683,0 Сг
586,8 La 605 Dy 634,9 Tb 684 Ец
586,81 Sm 605,2 Сг 636,3 Рг 691 Nd
585,9 605,9 Sr 635,1 692,7 1 Рг
587,6 | V 606,0 Си 637,0 | Nd 695,0 i Рг
589,4 Yb 606,4 638,6 701,1 V
587 607,3 | Sc 637,7 | Sm 702 Ец
588,1 Mn 607,9 639,2 702 Nd
588,8 Sc 607,8 Tb 639,4 Cr 704 Sr
589,00 } Na 608 Dy 640,6 | Sm 707,0 V
589,59 608,1 Od 642,3 709,5 Pr
589,5 La 608,7 V 645,4 705,7
591,0 Mn 609,5 Fe 641,0 | Nd 709,0 Tl
591,14 Gd 610,36 LI 642,5 712,7
592,1 Tb 610,2 644,5 715,9
592,2 La 611,0 | Sc 644 Ca 709,2
592,7 Gd 611,6 646,5 Sr 711,5 | Nd
592,8 Sc 613,2 } Od 647 Eu 713
594,3 Sr 615,5 647,4 1 ₽r 732,0 ) Pr
595 Sm 613,5 | Sm 649,4 737,6
597 Sr 614,9 648,5 740,4
597,9 Tb 613,2 649,6 1 743,4 | La
598 Eu 614,8 650,0 Nd 746,5
598,8 Sm 616,5 648,5 745 Ba
599 Nd 618,2 651,0 747 V
597,1 614,0 653,2 Sm 766,3 Pr
599,3 | Lu 615,2 J Sc 655,7 766,49 1 К
601,4 617,6 Mn 658,0 769,9 J 14
598,8 Od 618,1 Fe 659 Sr 780,02 Rb
600,1 619,1 Sc 658,6 791,1
597,2 620 В 660,4 Nd 794,5 | La
593,8 620,4 Мц 663 798,0
600.4 Y 621,9 Fe 665,2 794,76 Rb
502,0 618,3 665 Ra 800 V
603,7 620,1 666 Sr 798,6
600,6 Dy 621,2 Od 667 Sm 804,8 | Pr
601,7 Sc 622,1 670,78 LI 811,0
601,82 Eu 622 668,1 815,3 Ca
602,0 Ca 622 Nd 671,7 Tl 818,33 } Na
602,0 Ra 622,0 674,7 819,48
602,0 Yb 623,1 } bc 678,1 830 Ba
091,9 623 Eu 668,8 848,9 Pr
Ы)з,б | Pr 624,3 674,9 । Lu 852,11 Cs
605,5 627 Ka 681,U 865,2 Ca
603 •603,5 В 627,5 629,8 } Fr 681 682 Sni Sr 873 894,35 Ba Cs
и03,6 Sc
732
В ЧУВСТВИТЕЛЬНОСТЬ ОБНАРУЖЕНИЯ ЭЛЕМЕНТОВ МЕТОДОМ АТОМНО-АБСОРБЦИОННОГО АНАЛИЗА В ПЛАМЕНИ таблице приняты следующие условные обозначения для различных типо пламеииг
BA — воздух-ацетилен КА — кислород-ацетилен В В — воздух-водород КВ — кисло род-водород ВП — воздух-пропан КЦ — кислород-циан ВС — воздух-светильный газ Случаи применения органических растворителей отмечены индексом «орг»; остальные данные относятся к водным растворам. Звездочка указывает на избыток ацетилена против стехиометрического соотношения (восстановительное пламя). Более подробные сведения см.: I. Б. В. Львов, Атомно-абсорбционный спектральный анализ, Изд. «Наука», (965. — 2. W. Т. Elwell, J. A. G i d I а у, Atomic-Absorbtion Spect-* roscopy, Лондон. 1961.
Эле- мент Длина волны аналитической линии, А Тип пламени Толщина поглощающего слоя, см Наименьшая обнаруживаемая концентрация, % Элемент Длина волны аналитической линии, А Тип пламени Толщина поглощающего слоя, см Наименьшая обнаруживаемая концентрация, %
Ag Al As Ац Ba Be Bl Ca Cd Co Cr Cs Cu Eu Fe Ga Hg In К LI Mg Mn Mo Na АБСО 4yt (однопр 3280.68 3961,53 1890,42 2427,95 5535,48 2348,61 3067,72 4226,73 2288,02 2407,25 3578,68 8521,10 3247,54 4594,04 2488,14 2874,24 2536,52 3039,36 7664,91 6707,84 2852,13 2794,82 3132,59 5895,92 5889,95 ЛЮТНАЯ ч ктвительнос оцеитное п вс * КА„ орг ВА ВС ВА КА* орг ВА ВА ВА ВА ВА* ВС КВ КАорг КВ ВА ВА ВА ВП ВС ВП ВА В А* } ВП УВСТВИ ть уста оглощеиг 10 12 10 10 12 12 12 12 12 10 12 12 12 12 10 12 12 10 12 ГЕЛЬНС ПРИ иовлена (е сиги! 5-Ю-6 8Л0—5 Ы0-4 ЗЛО-5 8Л0-4 1Л0-5 7Л0-5 8Л0“ 6 2Л0~ 6 2ЛО-5 5Л0-6 2Л0—5 ЫО-6 2Л0-3 ЗЛО-6 2Л0-4 5Л0-4 2Л0-5 2Л0—6 ЗЛО-6 ЗЛО-7 5Л0-6 5Л0—5 8Л0-7 СТЬ МЕТО ПРИМЕНЕН для иаиь ла) при и Nb Nl Pb Pd Pt Rb Re Rti Ru Sb Sc Se Sn Sr Те Tl Tl Tu V Y Yb Zn ДА ATOI 1ИИ ГР7 геиьших спользов 4058,93 2320,03 2833,07 2476,42 2659,45 7800,23 3460,47 3434,89 3728,03 2311,47 3907,48 1960,90 2863,32 4607,33 2142,75 3653,50 2767,87 4094,18 3183,98 4077,37 3987,99 2138,56 ИНО-АБСО .ОПТОВОЙ измеряемь ании кюве7 КА* КВ ВА ВА ВА ВС КАорг ВА ВА* ВА * КА орг ВА В А* ВА ВА * КА орг ВА КА* орг КА* _ орг * КА орг * КАорг ВАорг РБЦИОН КЮВЕТ IX опти гы диам 12 12 12 10 10 12 12 12 12 10 12 12 12 НОГО А ы леских етром 6Л0-3 1Л0-6 зло-3 5Л0—5 6Л0-5 1Л0-5 610-4 зло-5 210“ 5 5Л0—5 1Л0-5 5Л0-5 5Л0-4 5Л0-е 5Л0-5 1ЛО-3 зло-6 6Л0-3 6Л0-4 ЫО-3 2Л0-3 5Л0-7 НАЛИЗА плотностей мм.
Элемент Длина волны, А Наименьшее обнаруживаемое количество, г Элемент Длина волны. А Наименьшее обнаруживаемое количество, г
Al Ba Bl Cd Cr Cs Cu Fe Hg In 3092,71 5535,48 3067,72 2288,02 4254,33 4555,36 3247,54 3719,94 2536,52 4101,77 2-Ю-13 1 • 10-12 6-10“13 1,5 10“14 1Л0-12 8Л0-11 2-10-12 1,5Л0 —12 4Л0-12 4-10-12 к LI Mn Pb Rb Sb Sr Те Tl Zn 4044,14 6707,84 4030,76 2833,07 4201,85 2311,47 4607,33 2259,02 4981,73 2138,56 2.10" 5.10" 5-10" 4-10" 3-10" 4-10" 210" 7-10" 5-10" 6-10" П 13 и 13 и 13 13 12 II 15
733
СПЕКТРЫ ПОГЛОЩЕНИЯ
В настоящем разделе приводятся спектры поглощения неорганических, комплексных и органических соединений в ультрафиолетовой и видимой области.
Оптическая плотность D, пропускание Т (в %), поглощение А (в %) или молярный коэффициент экстинкции 8 представлены в зависимости от длины волны Л (в ммк) или волнового числа v (в см~~1). Эти величины связаны между собой следующими соотношениями:
D^ls—^eed- Т^4~ 100; Л = 100= 100-Т-, v =
* I ’ lo /о 'К
где /0 и / — интенсивность падающего и проходящего монохроматического излучения; с -- концентрация поглощающего вещества, моль/л; d — толщина поглощающего слоя, см.
Ниже приводятся таблицы для взаимного пересчета величин К, v, D и Т.
Таблица для пересчета X в v
Длина волны X, ммк
Де- Единицы
сяткн 0 1 2 3 4 5 6 8 9
Водно вое ч 1 С Л О V, см 1
200 50 000 49 751 49 505 49 261 49 020 48 780 48 544 48 309 48 077 47 847
210 47 619 47 393 47 170 46 948 46 729 46 512 46 296 46 083 45 872 45 662
220 45 455 45 249 45 045 44 843 44 648 44 444 44 248 44 053 43 860 43 668
230 43 478 43 290 43 103 42 918 42 735 42 553 42 373 42 194 42 016 41 841
240 41 667 41 494 41 322 41 152 40 984 40 816 40 650 40 486 40 323 40 161
250 40 000 39 841 39 683 39 526 39 370 39 216 39 063 38 911 38 760 38 610
260 38 462 38 314 38 168 38 023 37 879 37 736 37 594 37 453 37 313 37175
270 37 037 36 900 36 765 36 630 36 496 36 364 36 232 36 101 35 971 35 842
280 35 714 35 587 35 461 35 336 35 211 35 088 34 965 34 843 34 722 34 602
290 34 483 34 364 34 247 34 130 34 014 33 898 33 784 33 670 33 557 33 445
300 33 333 33 223 33 113 33 003 32 895 32 787 32 680 32 573 32 468 32 362
310 32 258 32 154 32 051 31 949 31 847 31 746 31 646 31546 31 447 31 348
320 31 250 31 153 31 056 30 960 30 864 30 769 30 675 30 581 30 488 30 395
330 30 303 30 211 30 120 30 030 29 940 29 851 29 762 29 674 29 586 29 499
340 29 412 29 326 29 240 29 155 29 070 28 986 28 902 28 818 28 736 28 653
350 28 571 28 490 28 409 28 329 28 249 28 169 28 090 28 011 27 933 27 855
360 27 778 27 701 27 624 27 548 27 473 27 397 27 322 27 248 27 174 27 100
370 27 027 26 954 26 882 26 810 26 738 26 667 26 596 26 525 26 455 26 385
380 26 316 26 247 26 178 26 ПО 26 042 25 974 25 907 25 840 25 773 25 707
390 - 25 641 25 575 25 510 25 445 25 381 25 316 25 253 25 189 25 126 25 063
400 25 000 24 938 24 876 24 814 24 752 24 691 24 630 24 570 24 510 24 450
410 24 390 24 331 24 272 24 213 24 155 24 096 24 038 23 981 23 923 23 866
420 23 810 23 753 23 697 23 641 23 585 23 529 23 474 23 419 23 364 23 310
430 23 256 23 202 23 148 23 095 23 041 22 989 22 936 22 883 22 831 22 779
440 22 727 22 676 22 624 22 573 22 523 22 472 22 422 22 371 22 321 22 272
450 22 222 22 173 22 124 22 075 22 026 21 978 21 930 21 882 21 834 21 786
734
Продолжение
Таблица для пересчета X в v
Длина волны X, ммк
Единицы
сятки 9 1 2 3 1 4 5 1 6 7 1 8 9
460 21 739 21 692 21 645 21 598 21 552 21 505 21 459 21 413 21 368 21 322
470 21 277 21 231 21 186 21 142 21 097 21053 21 008 20 964 20 921 20 877
480 20 833 20 790 20 747 20 704 20 661 20 619 20 576 20 534 20 492 20 450
490 20 408 20 367 20 325 20 284 20 243 20 202 20 161 20 121 20 080 20 040
500 20 000 19 960 19 920 19 881 19 841 19 802 19 763 19 724 19 685 19 646
510 19 608 19 569 19 531 19 493 19 455 19 417 19 380 19 342 19 305 19 268
520 19 231 19 194 19 157 19120 19 084 19 048 19 010 18 975 18 939 18 904
539 18 868 18 832 18 797 18 762 18 727 18 692 18 657 18 622 18 587 18 553
540 18 519 18 484 18 450 18 416 18 382 18 349 18 315 18 282 18 248 18 215
550 18 182 18 149 18 116. 18 083 18 051 18 018 17 986 17 953 17 921 17 889
560 17 857 17 825 17 794 17 762 17 731 17 699 17 668 17 637 17 606 17 575
570 17 544 17 513 17 483 17 452 17 422 17 391 17 361 17 331 17 301 17 271
580 17 241 17 212 17 182 17 153 17 123 17 094 17 065 17 035 17 007 16 978
590 16 949 16 920 16 892 16 863 16 835 16 807 16 779 16 750 16 722 16 694
600 16 667 16 639 16 611 16 584 16 556 16 529 16 502 16 474 16 447 16 420
610 16 393 16 367 16 340 16 313 16 287 16 260 16 234 16 207 16 181 16 155
620 16 129 16 103 16 077 16 051 16 026 16 000 15 974 15 949 15 924 15 898
630 15 873, 15 848 15 823 15 798 15 773 15 748 15 723 15 699 15 674 15 649
640 15 625 15 601 15 576 15 552 15 528 15 504 15 480 15 456 15 432 15 408
650 15 385 15 361 15 331 15 314 15 291 15 267 15 244 15 221 15 198 15 175
669 15 152 15 129 15 106 15 083 15 060 15 038 15 015 14 993 14 970 14 948
670 14 925 14 903 14 881 14 859 14 837 14 815 14 793 14 771 14 749 14 728
680 14 706 14 684 14 663 14 641 14 620 14 599 14 577 14 556 14 535 14 514
690 14 493 14 472 14 451 14 430 14 409 14 388 14 368 14 347 14 327 14 306
700 14 285 14 265 14 245 14 225 14 205 14 184 14 164 14 144 14 124 14 104
710 14 085 14 065 14 045 14 025 14 006 13 986 13 966 13 947 13 928 13 908
720 13 889 13 870 13 850 13 831 13 812 13 793 13 774 13 755 13 736 13 717
730 13 69» 13 680 13 661 13 643 13 624 13605 13 587 13 569 13 550 13 532
740 13 514 13 495 13 477 13 459 13 441 13 423 13 405 13 387 13 369 13 351
750 13 333 13 316 18 298 13 28'5 13 263 13 245 13 228 13 210 13 193 13 175
760 13 158 13 141 13 123 13 106 13 089 13 072 ' 13 055 13 038 13 021 13 004
770 12 987 12 970 12 953 12 937 12 920 12 903 12 887 12 870 12 853 12 837
780 12 821 12 804 12 788 12 771 12 755 12 739 12 722 12 706 12 690 12 674
790 12 658 12 642 12 626 12 610 12 594 12579 12 563 12 547 12 531 12 516
800 12 500 12 484 12 469 12 453 12 438 12 422 12 407 12 392 12 376 12 361
810 12 346 12 330 12 315 12 300 12 285 12 270 12 255 12 240 12 225 12 210
820 12 195 12 180 12 165 12 151 12 136 12 121 12 107 12 092 12 077 12 063
830 12 048 12 034 12 019 12 005 11 990 11 976 11 962 11 947 11 933 11 919
840 11 905 11 891 И 876 11 862 11 848 11 834 11 820 11 806 11 792 11 779
850 11 765 11 751 11 737 11 723 11 710 И 696 И 682 11 669 11 655 11 641
860 11 628 И 614 11 601 11 587 11 574 11 561 11 547 И 534 11 520 11 507
870 11494 11 481 11 468 11 455 11 442 11 429 11 416 11 403 11 390 11 376
880 11 364 11 351 11 338 11 325 11 312 11 299 11 287 11 274 11 261 11 249
890 11 236 11 223 • 11 211 11 198 11 186 11 173 11161 11 148 И 136 И 124
900 11111 11 099 11 086 11 074 11 062 11 0.50 И 038 11 025 11013 11 002
910 10 989 10 977 10 965 10 953 10 941 10 929 10 917 10 905 10 893 10 881
920 10 870 10 858 10 846 10 834 10 823 10 811 10 799 10 787 10 776 10 764
930 10 753 10 741 10 730 10 718 10 707 10 695 10 684 10 672 10 661 10 650
940 10 638 10 627 10 616 10 604 10 593 10 582 10 571 10 560 10 549 10 537
950 10 526 10 515 10 504 10 493 10 482 10 471 10 460 10 449 10 438 10 428
960 10 417 10 406 10 395 10 384 10 373 10 363 10 352 10 341 10 331 10 320
970 10 309 10 299 10 288 10 277 10 267 10 256 10 246 10 235 10 225 10 215
980 10 204 10 194 10 183 10 173 10 163 10 152 10 142 10 132 10 121 10 111
990 10 101 10 091 10 081 10 070 10 060 10 050 10 040 10 030 10 020 10 010
1000 10 000
735
Таблица для пересчета Т в D
Пропускание Т, %
Единицы Десятые доли
0 1 2 3 4 5 6 7 8 9
с п т и ч е с к а я п Л О Т Н о с т ь D
0 3,000 2,699 2,523 2,398 2,301 2,222 2,155 2,097 2,046
1 2,000 1,959 1,922 1,886 1,854 1,824 1,796 1,770 1,745 1,721
2 1,699 1,677 1,657 1,638 1,620 1,602 1,585 1,669 1,553 1,537
3 1,523 1,509 1,495 1,481 1,469 1,456 1,444 1,432 1,420 1,409
4 1,398 1,387 1,377 1,366 1,357 1,347 1,337 1,328 1,319 1,310
5 1,301 1,292 1,284 1,276 1,268 1,260 1,252 1,244 1,237 1,229
6 1,221 1,215 1,208 1,201 1,194 1,187 1,180 1,174 1,165 1,161
7 1,155 1,149 1,143 1,137 1,131 1,125 1,119 1,114 1,108 1,102
8 1,097 1,091 1,086 1,081 1,076 1,071 1,065 1,060 1,055 1,051
9 1,046 1,041 1,036 1,031 1,027 1,022 1,018 1^013 1,009 1,004
10 1,000 0,996 0,991 0,987 0,983 0,979 0,975 0,971 0,967 0,963
11 0,959 0,955 0,951 0,947 0,943 0,939 0,935 0*932 0,928 0,924
12 0,921 0,917 0,914 0,910 0,907 0,903 0,900 0^896 0,893 в,889
13 0,886 0,883 0,879 0,876 0,873 0,870 0,866 0,863 0,860 0,857
14 0,854 0,851 0,848 0,845 0,842 0,839 0,836 о;взз 0,830 0.827
15 0,823 0,821 0,818 0,815 0,812 0,810 0,807 0,804 0,801 0,799
16 0,796 0,793 0,790 0,788 0,785 0,782 0,780 0*777 0,775 0,772
17 0,770 0,767 0,764 0,762 0,759 0,757 0,754 0,752 0,750 0,747 :
18 0,745 0,742 0.719 0,740 0,737 0,735 0,733 0,730 0,728 0,726 0,723
19 0,721 0,717 0,714 0,712 0,710 0,708 0,705 0,703 0,701
20 0,699 0,697 0,695 0,692 0,690 0,688 0,686 0,684 0,682 0,680
21 0,678 0,676 0,674 0,672 0,670 0,668 0,665 0,663 0,644 0,661 0,660
22 0,658 0,656 0,654 0,652 0,650 0,643 0,646 0,642 0,640
23 0,638 0,636 0,618 0,634 0,632 0,631 0,629 0,627 0*625 0,623 0,622
24 0,620 0,616 0,614 0,613 0,611 0,609 0,607 0,605 0,604 :?
25 0,602 0,600 0,599 0,597 0,595 0,593 0,592 0,590 0,588 0,587
26 0,585 0,583 0,582 0,580 0,578 0,577 0,575 0,573 0,572 0,570
27 0,569 0,667 0,565 0,664 . 0,562 0,561 0,559 0,557 0,556 0,554
28 0,553 0,551 0;550 0,548 0,647 0,545 0,544 0,542 0,541 0,539
29 0,638 0,536 0,535 0,533 0,532 0,530 0,529 0,527 0,526 0,524
30 0,523 0,521 0,520 0,519 0,617 0,516 0,514 0,513 0,511 0,510
31 0,509 0,507 0,506 0,504 0,503 0,502 0,500 О; 499 0,498 0,496
32 0,495 0,493 0,492 0,491 0,489 0,488 0,487 0*485 0,484 0,483
33 0,481 0,480 0,479 0,478 0,476 0,475 0,474 О; 472 0,471 0,470
34 0,468 0,467 0,466 0,465 0,463 0,462 0,461 о; 4бо 0,458 0,457
35 0,456 0,455 0,453 0,452 0,451 0,450 0,448 0,447 0,446 0,445
36 0,444 0,442 0,441 0,440 0,439 0,438 0,436 0^35 0,434 0,433
37 0,432 o;43i 0,429 0,428 0,427 0,426 0,425 0Л24 0,422 0,421
38 0,420 0,419 0,418 0,417 0,416 0,414 0,413 0,412 0,411 0,410
39 0,409 0,408 0,407 0,406 0,404 0,403 0,402 0,401 0,400 0,399
40 0,398 0,397 0,396 0,395 0,394 0,392 0,391 0,390 0,389 0,388 1
41 0,387 0,386 0,385 0,384 0,383 0,382 0,381 0,380 0,379 0,378
42 0,377 0,376 0,376 0,374 0,373 0,372 0,371 0,370 0,369 0,367
43 0,366 0,365 0,364 0,363 0,362 0,361 0,360 0,359 0,358 0,357
44 0,356 0,356 0,355 0,354 0,353 0,352 0,351 0,350 0,349 0,348
45 0,347 0,346 0,345 0,344 0,343 0,342 0,341 0,340 0,339 0,338
46 0,337 0,336 0,335 0,334 0,333 0,332 0,332 0,331 0,330 0,329
47 0,328 0,327 0,326 0,325 0,324 0,323 0,322 0,321 0,321 0,320
48 0,319 0,318 0,317 0,316 0,315 0,314 0,313 0,312 0,312 0,311
49 0,310 0,309 0,308 0.3Q7 0,306 0,305 0,304 0,304 0,303 0,302 j
736
Таблица для пересчета Т в D
П родолжение
Пропускание Г, %
Еди- Десятые доли
ницы 0 1 2 3 4 5 6 7 8 9
50 0,301 0,300 0,299 0,298 0,298 0,297 0,296 0,295 0,294 0,293
51 0,292 0,292 0,291 0,290 0,289 0,288 0,287 0,286 О; 286 0,285
52 0,284 0,283 0,282 0,281 0,280 0,280 0,279 0,278 0,277 0,276
53 0,276 0,275 0,274 0,273 0,272 0,272 0,271 0,270 0'269 0'268
54 0,268 0,267 0,266 0,265 0,264 0,264 0,263 0,262 0,261 0,260
55 0,260 0,259 0,258 0,257 0.256 0,256 0,25-5 0,254 0,253 0,253
56 0,252 0,251 0,250 0,249 0,249 0,248 0,247 0,246 0'246 0 245
57 0,244 0,243 0,243 0,242 0,241 0,240 0,240 0,239 0 238 0/237
58 0,237 0,236 0,235 0,234 0,234 0,233 О',232 О',231 0,231 0 230
59 0,229 0,228 0,228 0,227 0,226 0,225 0,225 0,224 0,223 0,223
60 0,222 0,221 0,221 0,220 0,219 0,218 0,218 0,217 0,216 0 215
61 0,215 0,214 0,213 0,213 0,212 0,211 0,210 0,210 0,209 0’208
62 0,208 0,207 0,206 0,205 0,205 0,204 0,203 0,203 0,202 0’201
63 0,201 0,200 0,199 0,199 0,198 0,197 0,196 0,196 О; 195 ОД 94
64 0,194 0,193 0,192 0,192 0,191 0,190 0,190 0,189 0,188 0,188
65 0,187 0,186 0,186 0,185 0,184 0,184 0,183 0,182 0,182 0,181
66 0,180 0,180 0,179 0,178 0,178 0,177 0,176 0,176 0,175 ОД 75-
67 0,174 0,173 0,173 0,172 0.172 0,171 0,170 0,169 0’169 0'168
68 0,167 0,167 0,166 0,166 0,165 0,164 0,164 0,163 0,162 0,162
69 0,161 0,160 0,160 0,159 0,159 0,158 0,157 0,157 о; 156 о; 155
70 0,155 0,154 0,154 0,153 0,152 0,152 0,151 0,151 0,150 0,149
71 0,149 0,148 0,147 0,147 0,146 0,146 0,145 0,144 0,144 0,143
72 0,143 0,142 0,141 0,141 0,140 0,140 0,139 0,138 0,138 О; 137
73 0,137 0,136 0,135 0,135 0,134 0,134 0,133 0,132 0,132 О; 131
74 0,131 0,130 0,130 0,129 0,128 0,128 0.127 0,127 0,126 0,125
75 0,125 0,124 0,124 0,123 0,123 0,122 0,121 0,121 0,120 0,120
76 0,119 0,119 0,118 0,117 0,117 0,116 0,116 0,115 0,115 0,114
77 0,113 0,113 0,112 0,112 0,111 0,111 0,110 0,110 0,109 0,108
78 0,108 0.107 0,107 0,106 0,106 0,105 0,105 0,104 0,103 0,103
79 0,102 0,102 0,101 0,101 0,109 0,1<Ю 0,099 0,098 0,098 0,097
80 0,097 0,096 0,096 0,095 0,095 0,094 0,094 0,093 0,093 . 0,092
81 0,091 0,091 0,090 0,090 0,089 0,089 0,088 0,088 0,087 0,087
82 0,086 0,086 0,085 0,085 0,084 0,083 0,083 0,082 0,082 0,081
83 0,081 0,080 0,080 0,079 0,079 0,078 0,078 0,077 0,077 0,076
84 0,076 0,075 0,075 0,074 0,074 0,073 0,073 0,072 0,072 0,071
85 0,071 0,070 0,070 0,069 0,069 0,068 0,067 0,067 0,066 0,066
86 0,065 0,065 0,064 0,064 0.063 0,063 0,062 0,062 0,061 0,061
87 о.обо 0,060 0.059 0,059 0,058 0,058 0,057 0,0.57 0,056 0,056
8» 0,055 0,055 0,054 0,054 0,053 0,053 0,053 0,052 0,052 0,051
89 0,051 0,050 0,050 0,049 0,049 0,048 0,048 0,047 0,047 0,046
90 0,045 0,045 . 0,045 0,044 0,044 0,043 0,043 0,042 0,042 0,041
91 0,041 0,04) 0,040 0,039 0,039 0,039 0,038 0,038 0,037 0,037
92 0,036 0,036 0,035 0,035 0,034 0,034 0,033 0,033 0,032 0,032
93 0,031 0,031 0,031 0,030 0,030 0,029 0,029 0,028 0,028 0,027
94 0,027 0,026 0,026 0,025 0,025 0,025 0,024 0,024 0,023 0,023
95 0,022 0,022 0,021 0,021 0,020 0,020 0,019 0,0)9 0,019 0,018
96 0,018 0,017 0,017 0,016 0,016 0,015 0,015 0,015 0,014 0,014
97 0,013 0,013 0,012 0 012 0,011 0,011 0,010 0,010 0,010 0,009
98 0,009 0,008 0,008 0,007 0,007 0,007 0,006 о,ооб 0,005 0,005
99 0,004 0,004 0,003 0.003 0.003 0,002 0,092 0,001 0,001 0,000
100 0,000
47 Зак. 7*3
737
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ И КОМПЛЕКСНЫХ СОЕДИНЕНИЙ В УЛЬТРАФИОЛЕТОВОЙ И ВИДИМОЙ ОБЛАСТИ
Спектры поглощения приведены в той форме, в какой они даны в оригинальных работах. Всюду, где это специально не оговорено, спектры измерены по отношению к растворителю (р.).
Спектры редкоземельных элементов и таблица величин е для нонов редкоземельных элементов помещены в конце раздела.
Указатель
№ рисунка
H рисунка
Ас ..... 1
Ag............2.3
Al ...........4-6
Am............7-10
As............П, 12
Au............13
В.............14—16
Be............17
Bl............11, 18-23, 28
Br............24—27
C ............29, 31
Cd............ 2, 30, 32, 35
Ce............ 33, 34, 36, 37
Cl............ 24—26, 29, 38—40
Co............ 32, 41-47, 68, 114
Cr............ 43, 45. 48-53, 176
Cu............ 22, 32, 48, 54-64, 68
Dy............194
Er............195
Eu............1'06
F.............65
Fe............ 22, 32, 41, 43, 45, 57, 66—74
Ga............75
Gd............197
Ge............76
H2O«..........77, 107
Hg............ 18—20, 55, 78, 80-82
Ho............198
In............85-87
Ir............88—90
J............. 24—27. 79, 83, 84
К.............91
Mg............92, 93
Mu............ 52, 53, 94-97, 144, 176
Mo............ 16, 54, 98-101
N............. 29, 31, 39, 102-105
Nb............106-111, 163
Nd..............199
Nl.............. 32, 45, 52, 56, 57, 112-117
Np..............118-120
Os..............121, 122
P ..............16, 29, 123
Pa..............124
Pb.............. 2, 18-20, 28, 56, 82, 12.5,126, 131
Pd.............. 121, 127-130, 132-134
Pr..............200
Pt.............. 88, 135-138
Pu..............139-142
Re..............101, 143-145
Rh..............146, 147
Ru..............121, 148-150
S............... 24, 31, 103. 151, 152
Sb.............. 11, 82, 153, 154, 158
Sc .............156
Se..............155, 157
SI .............159
Sm..............201
Sn.............. 5, 54, 69, 160
Ta.............. 106, 107, 110, 163
Tb..............202
Tc..............173
Те..............155,1157, 161
Th.............. 65, 71, 162, 164, 165, 168
Tl ............. 54, 101, 166, 167, 172
Tl.............. 2, 18—20, 169—171
Tu..............203
U............... 22, 174-180
V............... 48. 52, 71, 106, 181-188
W............... 29, 101, 189, 190
V...............5
Yb..............204
Zn..............2, 191, 192
Zr..............101, 193
738
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 1. АсШ (0,0016 А1); р. 1 Л1 HCI, d = 1 см.
Рис. 2. / — AgClO,; 2—РЬ (С1О4)2;
3—Т1С1О4; 4 — Zn (С1О4)2;
5— Cd (С1О4); р. вода.
Рис. 3. Ag> (2,697 мг/л), комплекс с дитизоИом; р. CCI4, d = 1 см.
А., ммк
Рис. 4. А1|Г1 (0,47 мг[л), комплекс с алюминоном; р. вода, d = 1 см, в кювете сравнения раствор реагента.
Рис. 5. 1 — А1(С1О4)3; 2 — Y (С1О4)3; 3— Sn(CIO4)2; 4—Sn(ClO4)4;p. вода.
47*
739
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 6. AI111 (/—2,45 мг/л,
2 — 0,245 мг/л), комплекс с 8-оксихинолином; р. СНС13, d = 1 см.
Рис. «. АщШ; р. 0,1 М НС1О4.
Рис. 9. AniV; р. 0,1 М НС1О4.
Рис. 10. AmVi; р. О,2А1НСЮ4.
740
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 11. / —As(C104)3; 2—- As (С1О4)5; 3— Sb (С1О4)а;
4— Bi (С1О4)а; р. вода.
Рис. 13/ Au"1 (AuBr.f) . (2,5 • 10~4 М); р. вода, pH < 1, rf =1 см.
Рис. 12. Asv (2 мг/л); р. вода-f-Na2MoO4 - 2Н2О. d — 1 см.
Рис. 14. 1 — В1" (30 мг:л), комплекс с куркумином; 2—курку-мпн; р. вода, rf = 1 см.
741
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 15. 1 — В111 (80 мг!л), комплекс с хинализарином; 2—хинализарин; р. вода, d = l см.
Рис. 17. Be” (5 • КГ5 М): 1 — р. СС14; 2—р. СНС13; d= 1 см, в кювете сравнения раствор реагента.
W2
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рнс. 19. 1 — В1’Ч (10 мг/л); 2—Hg11 (10 мг/л); 3—РЬП (10 мг/л); 4 — Т11 (10 мг/л); р. 4 М NaBr, d — 1 см.
Рис. 22. Комплексы с диэтилдитиокарбаматом: 1 — В1,п (16 мг/л);
2 — СиЧ (4 мг/л); 3 — Fell (20 мг/л);
4 — UVI (20 мг/л); р. СНС13, d = 1 см.
А, ммк
Рис. 20. 1 — В1,п (10 мг/л); 2— Hg11
(10 мг/л); 3—РЬП (10 мг/л); 4 — Т1*
(10 мг/л); р. 4 М NaJ, d — 1 см.
Рис. 23. В!’» (20 мг/л), комплекс с 8-оксихннолнном; р. СНС13, d = 1 см.
А. ммк
Рис. 21. Bi111 (1 мг/л). комплекс с дитизоном; р. СС14, d = 1 см.
743
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Л, ммм
Рис. 24. 1 — КВгО3; 2 — КСЮ3;
3— КЮ3; 4 — K2SO3; 5—Na2SO4; р. вода.
Рис. 25. / — Вг2; 2— С12; 3— J2; р. СС14.
Рис. 26. / — NaBr; 2—NaCl; Рис. 27. / — CsBrJ2; 2 — CsBr,J; 3— CsBr3;
3—NaJ; p. вода. 4 — CsJ3; p. C2H5OH.
744
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Л, ммк
Рнс. 28. 1 — Bi1" (2 • 10’5 М); 2—Pb"(2-IO-5 Af);3—Bi"I(2-10~5Af). комплекс с ЭДТА; 4—Pb"(2-10~5 А1), комплекс с ЭДТА; р. 0,01 М НС1О4, d = 1 см.
W~j,cm''
Рис. 30. 1 — Cd (С1О4)2, р. вода; 2—CdBr2 (2,8 • IO-2 Af), р. вода; 3—CdBr2 (2,7 Af) ,р. вода; 4 — CdJ2 (l-10~2Af), р. вода; 5— CdJ2, р. С2Н5ОН.
Рис. 29. / —NaClO,; 2— КаРО3; 3—NaH2PO2; 4— KCN; 5— KCNO; 6— NaCH3COO; 7—Na2WO4;
p. вода.
Л, ммк
Pyc.31./—Na.,C3H,O6;2—K3C6H5O7;
3—NaSCN; 4—K2C2O4; p. вода.
745
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 32.
1 — Cd (С1О4)2 (1,05 -10~3 Af);
2—CoSO4 (1,015 10 5 Л1);
3— Си (С1О4)2 (1,12- 10~4 Л1).
4 — Кз [Fe(CN)6] (1,43-10~4 М);
5—NiSO4 (9,3-10-5 /И); р. 2 -10'2 М KCN, rf = 1 см.
Рис. 33. СеС13 (8,13 г/л);
р. вода, rf == 5 см.
Рис. 35. Cd11 (1,405 мг/л), комплекс с дитизоном; р. СС14, rf = 1 см.
Рис. 36.
Се,[| (53 мг)л}, комплекс с 8-окснхинолином; р. СНС13, rf => 1 см.
?46
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 37. Ce,v (1,92- IO '5 Af); р. 1 М H2SO4, rf = 10 см.
Л, ммк
Рис. 38. С12 (1 мг/л), продукт окисления о-толи-дина жлором; р. вода, pH = 1,6, d — 1 см.
Рнс. 39. I — НОС1;
2—ОСГ;3—С1О2 ;
4— ЫО2’; р. вода.
Л,, ммм
Рис. 40. С1О4 (0,2 мг/л), комплекс с метиленовым синим; р. СНС13.
Рис. 41.
1—Со2 (SO4)3(l,0 • 10~2 Л1), р. 9 М H2SO4;
2—CoS04 (5 • 10-2 Al). р. IM H2SO4;
3— Fe2SO4(l,2- 10-4Л1), р 1 М H2SO4;
4—K3[Fe(CN)6](4,4- 10-6М),р. 1 М H2SO4; rf = 1 см.
747
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рнс. 42. СоЧ (0,737 .иг/л), комплекс с дитизоном; р. CCI4, d — I см.
Рис. 43. Комплексы с роданидом: /—Со11 (4,0-10“1 М)', 2—Fe,[l (5,4 • 10~5 44); 3—Сг|П(6,б- 10~3А1); р. (СН3)2СО, d = 1 см.
Рис. 44. СоЧ (6 мг/л), комплекс с роданидом; р. изоамиловый спирт, насыщенный NH4SCN, d = 1 см.
Рис. 45. Комплексы с диэтилдитиокарбаматом: 1 — FeHi (16 мг/л)', 2—Со» (20 мг/л); 3— Сг2О*“ (100 мг/л); 4 —Niu(4 мг/л); р. СНС13, d = 1 см.
300
500
748
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 46. СоЧ (20 мг/л), комплекс с 8-оксихинолином;
р. СНС13, d = 1 см.
Рис. 48.
1 — СиЧ (10 мг/л)', 2—СгЧ1 (Южг/Л);
3 —Vv (10 мг/л); р. 6,7 Al НС1, d = 1 см.
Рис. 47. I — СоЧ1, комплекс с и-нитрозо-р-мафтолом; 2— а-нитрозо-Р-нафтол; 3—Со111, комплекс с р-нитрозо-а-пафтолом; 4 — р-нн-трозо-«-нафтол; р. СНС13.
Рис. 49. CrHi, комплекс с 8-оксихинолином; р. СНС13.
749“
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 51. 1 — К2СгО4, р. 5 • 10~2 М NaOH;
2 — К2Сг2О7, р. 2,5-10 H2SO4.
Л, мм л
Рис. 54. 1 — Си> (10 мг!л)\
2— Tilv (10 мг!л\, 3— MoVI (10 мг/л);
4 — 5пи(10 мг/л); 5 — Ti111 (10 мг/л);
р. 6 М HCI, d = 1 см.
2—Cr2O*-(10-3 Л1);3-УО+(10~3Л1);
4 — Niu (0,1 Л1); р. 1 М H2SO4 + -4- 0.7 М Н3РО4, d = 1 см.
750
СПЕКТРЫ ПОГЛОЩЕНИЯ
НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 55. / —HgC104(5,26 10~5M), р. 0,2 М Н3РО4;
2 — СиСЮ4(],12 • 10~4 Л1), р. 0,1 М К4Р2О7;
3— CuC1O4(1,12- I0"4 А1), р. 0,01 М Na3C6HsO7; d = 1 см.
Рис. 57. 1 — Cui (200 мг/л), комплекс с NH3; 2—Ni11 (4,8 мг/л), комплекс с диметилглкоксимом; 3—геШ (1 г/л), комплекс с СвН6О’“; р. вода, 1 см.
Рис. 56. Комплексы с роданидом:
7 — Св1 (1,12- 10-2ЛО;
2—N1’1 (4,28- 10“'АП;
3— РЬ11 (5,75 • 10-4 А1);
р. (СН3)2 СО, d = 1 см.
Рис. 58. Cui (7,7 мг/л), комплекс с батокупроином; р. гексиловый спирт, d= 1 см.
751
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОН
в кювете сравнения реагента.
Рис. 60. / — Си (СЮ4)2; 2 — CnSO4; 3 — СиВг2; р. вода.
62. с
Рис. 59.
Си* (10,609 мг/л), комплекс с нео-купроином; р. изоамиловый спирт, d = I см, раствор
Рис. плекс
том; р.
Си*1 (2 мг/л), ком-диэтнлдитиокарбама-СНС13, d = 1 см.
А, ммк
Л.,ммк
Рис. 63. Си**, комплекс с 8-оксихинолнном; р. СНС13.
Рис. 61.
Си** (1 жг/л), комплекс с дитизоном; р. СС14, d = 1 см.
752
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 64. Cull (20 мг/л), комплекс с роданидом; р. (СН3)2 СО + вода (1 : 1), d ~ 1 см.
Л, ммк
Рис. 65. 1 — торийализариновый лак (80 мг иатрийализаринсульфоната Ц-+ 40 мг Th,v на 1л); 2 — F- (10 мг/л), комплекс с торийализариновым лаком;
р. вода.
Рис. 66. Fell (1 мг/л), комплекс с меркаптоуксуспой кислотой; р. вода, рН = 7-~ 12, d — 1 см. в кювете сравнения раствор реагента.
Рис. 67. Fell (4,2 мг/л), комплекс с 1,10-фенантролином; р. СНС134-С2Н5ОН (4:1), d = 1 см, в кювете сравнения раствор реагента.
48 Зак. 783
753
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 68. / — Fe (С1О4)2; 2—Fe (СЮ4)3; 3—Со(С1О4)2; 4 — Си(С1О4)2;
р. вода.
Рис. 69. / — Fe111 (10 мг/л)\ 2— Sniv (Ю лг/л); р. 6,7 М HCI, cl = 1 см.
Рис. 70. Fe (С1О4)3 (1,21 10“ М): 1 — р. 2 М Н3РО4; 2 — р. 1 МНС1О,;
3 — р. 0,01 М К4Р2О7; d = 1 см.
Рис. 71. .
/ —Fe2 (SO4)3 (1 • 10~4 Л1);
2 — Tli(NO3)4(l •Ю"3Л0;
3— NH4VO3 (5 • 10“3 М);
р. 0,5 H2SO4, d = 10 см.
Рис. 72. FeHi (4,8 мг]л), комплекс с 8-оксихинолином; р. СНС13, d = 1сл«.
754
СПЕКТРЫ ПОГЛОЩЕНИЯ
НЕОРГАНИЧЕСКИХ ИОИОВ
Рис. 73. Feiil (5,0 мг/л), комплекс с салицилатом; р. вода, pH = 2,6-=-2,8, d = 1,96 см.
Рис. 76. Oe>V, комплекс с фе-нилфлуороном: I —6 мг^л, в кювете сравнения вода;
2 — 0,347 мг/л, в кювете сравнения раствор реагента;
р. вода, d = 1 см.
Рис. 74. Feiil (5,0 мг/л), комплекс с салицилальдоксимом; р. вода, pH = 6,2 -г-6,6, d = 1,96 см', в кювете сравнения раствор реагента.
В
Л, ммк
Рис. 77. /—Н2О2,р. разб. NaOH;
2— Н2О2, р. вода.
Рис. 75.
Оа>ч (1,0 мг!л), комплекс с 8-оксихи-нолнном; р. СНС134-0,75% С2Н5ОН, d = 5 см.
755
48*
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 78. / — Hg2 (С1О4)2; 2— Hg (С1О4)2; р. вода.
Рис. 80. HgH (0,247 мг/л), комплекс с дитизоном; р. CHCI3, d = l см.
Рис. 81. Hgi 1 (40 мг/л), комплекс с диэтилдитиокарбаматом; р. СС14, (1—1см, в кювете сравнения раствор реагента.
Рис. 82. 1 — Hg11 (10 мг/л);
2— РЬ11 (10 мг/л);
3—Sb111 (10мг/л); р.6,7 М HCI, 3=1 см.
756
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 83. J2: 1 — р. 5% KJ; 2 — р. С6Не;
3—р. С6Н5СН3.
Рис. 85. Inin (1 мг/л), комплекс с дитизоном; р. СС14, <1 = 1 см.
Рис. 86. 1пШ (4,32 мг)л), комплекс с 5,7-дихлор-8-оксихинолином;
р. СНС1з + 0,75% С2Н5ОН,
3 = 5 см.
1пШ (2,0.«г/л), комплекс с 8-оксихи- jC0 полином; р. CHCia0,75% С2Н6ОН, d — 5 см.
Рис.
350 400 450
Л, мм и
757
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 90. Iriv (51 комплекс с р. вода, pH—11,4н-12,6, d — 1 см.
мг/лу, ЭДТА;
Рис. 88. 1 — Кз [1г (CN)6J; 2 — IrCI,; 3 — K2[Pt(CN)J; р. вода.
Рис. 89. IriV (100 мг!л); р. НС1О4 4" 4- Н3РО4, <7=1 см.
Рис. 91. К1 (50 мг/л), комплекс с дипикрнламином; р. вода4-(СН3)2СО, pH = = 10ч-11, d = 1 см, в кювете сравнения раствор реагента.
Рис.
/—MgH (2 мг-л), комплекс с титановым желтым; 2— титановый желтый; р. вода, pH > 12. <7 = 1 см.
92.
758
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 93. / — MgH (100 мг/л), комплекс с эриохром черным; 2—эриохром черный (4 мг/л)', р. вода, pH =10,1, d = 1 см.
Л, ммк
Рис. 94. Mnll; р. разб. НС1.
Рис. 95. Мп"1 (2,94- 10-3 Л4) ; р. 10,0 А4 НС1.
Рис. 96. Mniii, комплекс с диэтилдитиокарбаматом: 1 — 4 мг!л\ 2—0,4 мг!л\ р. CCI4, d = 5 см.
Рис. 97.
MnVi (К2 (Мп (С2О4)2 (ОН)2] . 2Н2О}; р. 0,1 М Н2С2О4.
Л.ММИ
759
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
1,ммк
мг/л), комплекс с роданидом; р. изо-ый спирт -|- 40г/л NH4SCN, d = 1 см.
Рис. 100. MoVI (6,95 • 10~5 Ж), комплекс с роданидом; р. (СН3)2СО -|-+ вода (3:2)+ 0,6 Ж NH4SCN, d — 1 см.
Рис. ;99. MoVI (МоО=+), комплекс с 8-оксихинолином:
1 — 4,78 мг/л-, 2 — 1,19 мг/л;
р. СНС13, d = 1 см.
500 600
Рис. 101.1 — Мо (96 мг/л), р. 96% H2SO4-|-4-9 • 10-2 М Н2О2; 2— Re (100,6 мг/л), р. 96% H2SO4 + 9-10-2 Ж Н2О2;
3 — Т1 (100,6 мг)л), р. 96% H2SO4 -f--(-9 • 10~2 Ж Н2О2; 4 — W (99,3 мг/л), р. 96% H2SO4 + 9 10~2 Ж Н2О2;
5—Zr (91,2 мг/л), р. 96% H2SO4; d — 1 см.
800 900 W00 Рис- 102.
Л ммл (5 мг'л “Ь K2HgJ4; р. вода, d = 1 см.
760
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 103. 1 — NaNO2; 2 — NaNO3;
3— Na2S2O3j 4 — Na2S2O8; p. вода.
Рис. 104. NO- (0,5 л/г/л); p. сульфаниловая кислота -|--4- а-нафтиламин в воде, d — 2 см.
Рис. 105. NO3 (~ 4,6 .иг/л); р. 1,2,4-фенолдисульфоновая кислота в воде, d — 1 см.
Рис. 106. 1 — Nb (50 мг/л), р. 96 % H2SO4 + 4-9-10241 Н2О2; 2—Та (100 мг 'л),
р. 96% H2SO4 + 9- 10-2 44 Н2О2;
3— V (107 .иг/л), р. 10% H.-SO4 + 4-9- 10"2 41 Н2О2; d = 1 см.
761
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 107./ —Nb (53 лг/л); 2— Та (102 мг/л)-, 3—Н2О2(9- 10-2Л1);
р. 96% H,SO4, d = 1 см.
А, ммл
Рис. 109. Nbv (5,6 мг/л), комплекс с 8-оксихинолином: р. СНС13, 3=1 см.
Рис. 108. Nbv (5 лгг/л); р. НС1, d = 1 см.
Рис. 110. / — Nbv (5,6 мг/л), комплекс с пирогаллолом; 2—ТаV (6,55 мг/л), комплекс с пирогаллолом; 3 — пирогаллол; р. вода, d = 1 см.
325 375 425 475
А, ммк
— s
М), комплекс с роданидом;
р. (СН3), СО 4- вода (1:1) + 1,8 М NH4SCN, 3 = 1 см.
762
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 115. N111, комплекс с 8-оксихинолином; р. СНС18.
Рис. 112. ЫР’О.Об г/Л)-,
А, ммк
Рис. 113. Ni11 (0,733 мг!л), комплекс с дитизоном; р. СС14, <7=1 см.
Рис. 116. N1”, комплекс с диметилглиоксимом;
p.CHCls
Рис. 114.
Комплексы с диэтилдитиокарбаматом; 7 — N111 (2 мг/л)-, 2— Со11 (2.кг/л);
р. СНС18, <7=1 см.
763
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 117.
Ni111, комплекс с днметилглиоксимом: / -р. С2Н5ОН 4- вода (1: 1) + NH3; 2—р. С2Н5ОН-f-вода (1: 1)-j— NaOH; 3 — реагент.
Рис. 119. / —NpIH; 2— NpIV;
3 — NpV; 4 — NpVI; p. 1 M HC1O«.
Pnc. 121. Комплексы с тиомочевиной: I — OsUl (20 г/л\, 2— Ru (20 г/л); 3— Ru (20 г/л) (после нагревания раствора до температуры кипения); 4 — Pd (20 г/лу, р. вода, d — 1 см.
Рис. 118. / — NpHI; 2 — NplV;
р. 1 М НСЮ4.
А. ммк
Рис. 120. / — NpV; 2—NpVI;
р. 1 М НСЮ4.
764
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 122. / — OsCl4;
2— К4 [Os (CN)6]; р. вода.
Рис. 123. Pv (РО4-) (0,6 згг. л). комплекс с молибдатом; р. 95% изобутиловый спирт, d = 1 см.
Л., ммк
Рис. 124. 1 — Ра1'' (в условиях, исключающих окисление); 2—PaV; р. 1 М НС(.
Л. ммк
Рис. 125. РЬ“ (10 мг/л)-. / —р. 6 М HCI; 2 — р. 4 М NaBr; 3—р. 4Af NaJ; d = 1 см
Рис. 126. РЬ11 (1,06 мг/л), комплекс с дитизоном;
р. СС14, d = 1 см.
СПЕКТРЫ ПОГЛОЩЕНИЯ
НЕОРГАНИЧЕСКИХ ИОИОВ
v 10 3, см'1 Рис. 127.1 —PdCl..; 2— К? [PdCl4], 3 — К? [PdCl6]; р. вода.
Рис. 129. Pd11 (100 мг/л), комплекс с бромидом; р. 0,1—0.8 Л4 НС1О4,3=1 см, в кювете сравнения раствор реагента.
А., ммк
Рис. 128. Pd11 (5 мг/л), комплекс с иодилом; р. НС1 « 2Л4) или H2SO4 -f- KJ, d = 1 см, в кювете сравнения раствор реагента.
Рис. 130. Pd11, комплекс с дн-метилглиоксимом; р. СНС1з-
Рис. 131.
РЬ11, комплекс
1 — 4 мг/л, 2 — 0,4 мг/л, р. СС14,3 = 5 см.
с диэтилдитиокарбаматом:
766
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Л.лшк >
Рис. 132. Pd11 (1 мг/л), комплекс с дитизоном; р. СС14, d = 1 см.
Рис. 133. Pd11, комплекс с диэтилдитиокарбаматом: 1 — 4 мг/л; 2— 0,4 мг/л-, р. СС14, d = 5 см.
Рис. 135. / — Pt11 (Ю .«г/л); 2—Ptlv (10 .«г/л); р. 0,5 М HCI, d — 1 см.
Л., ммк
Рис. 134. Pd11 (0,5 мг/л), комплекс с л-нитрозоднфениланнлином;
р. вода, pH = 4,4 -т- 5,2, d = 1 см, в кювете сравнения раствор реагента.
Рис. 137.
Ptlv(PtJ®-) (10 мг[л)\ р. вода, pH = 1,6, d = 1 см.
767
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 138. Pt11 (2,19 мг/л), комплекс с дитизоном; р. СС14, d = 1 см.
Рис. 141. Puv; р. 1 М NH4CI + + 0,03 44 СЮ~.
л, имк Л, ммк
Рис. 139. РцШ; р. 1 М НС1О4. р„с. 142. puvl; р. 1 м НС1О4.
е
400 500 000 700 800 900
Л, ммк
Рис. 140. PulV; р. 1 м НС1О4.
Рнс. 143.
1 — HReO4, р. вода; 2— Rev, р. 441 HCI + SnCL; 3 - К2 [ReClJ;
р. 4 44 НС1.
768
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 144. 7 — К2 [ReCI6]; 2— КМпО4;
р. вода.
5— Nas [RhClJ; 3— К3 [Rh (CN)6]; р. вода.
Рис. 148-Ruin, р. 1 М НС1О4: 1 — свежеприготовленный раствор; 2—тот же раствор после стояния в течение 10 ч при 0° С.
Рис. 145. ReVH (30 мг/л), комплекс с роданидом; р. вода-|-5пС12, pH < 0, d = 1 см.
Рис. 147. Rh111 (20 мг/л); р. > 2 М НС! --j- SnCl2, d — 1 см.
49 Зак. 783
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Л, ммк
Рис. 149. / —RuVl, р. 1 A! NaOH;
2— RuVII, р. 0,0114 М НС1О4;
3 — RuVIII, р. 0.0114 М НС1О4.
Л, ммк
Рис. 150. Ruin (3,5 мг/л), комплекс с рубеановой кислотой; р. 4 М НС1 в С2Н5ОН -4- года (1:1), 3 = 1 см.
Рис. 151. 1 — H2S; 2—Na2S;
3— H2SO3; 4 — Na2SO4; p. вода.
Рис. 152. гексан;
3— Na2SO;
1 — S2C12, р. 2— Na2S2O3, •з. Р-
гептан или р. вода; вода; 4 — Na2S2O6, р. вода.
Рис.
Sb111, комплекс с диэтилдитиокарбаматом: I —4 мг/л', 2— 0,4 мг/л', р. СCl4, d = 5 см.
153.
T70
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Л, ммк
Рис. 154. Sb111, комплекс с нодидом: 1 — 3 мг/л', 2—24 мг/л\ р. H2SO4 1,5 Л!) -|- KJ (70 г/л)-(-аскорбиновая кислота (5 г/Л), <7=1 см, в кювете сравнения раствор реагента.
Л, ммк
Рис. 156. ScHl (4,41 мг/л), комплекс с 8-оксихинолином;
Рис. 155. 1 — SeO2, р. вода; 2— Na2SeO3, р. вода; 3— Н6ТеО6, р. вода;
4 — Н6ТеО6, р. водаNaOH.
Рис. 158. Sbv(24,4 мг/л): 1 — р. 4,09 М HCI; 2 — р. 6,10 Л4 НС1; 3 — р. 8,11 М HC1J 4 — р. 9,97 М HCI; <7 = 1 см.
49’
771
СПЕКТРЫ ПОГЛОЩЕНИЯ
НЕОРГАНИЧЕСКИХ ионов
Рис. 159. Si,v (1 лгг/л), комплекс с молибдатом аммония (желтая форма); р. вода, d = 1 см.
Рис. 161. TelV, комплекс с ди-этилдитиокарба матом:
1 — 4 мг/л', 2—Q,4 мг/л-, р. СС14, d = 5 см.
Рис. 160. Sniv (4 мг/л), комплекс с диэтилдитиокарбаматом; р. СС14, d — 5 см.
Рис. 162. 1 — Thlv (14,8 мг/л), комплекс с ализариновым красным S (19,5 мг/л)\ 2—ализариновый красный S (19,5 мг/л)', р. вода, pH = 2.0, d — 1 см.
Рис. 163.
Комплексы с пирогаллолом: 1—Tav (26,2 мг/л)', 2 — Nbv (700.иг/л); р. вода, d = 1 см.
772
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 164.
1—ThIV (4,4 мг/л), комплекс с морииом (12 мг/л)-, 2—морин (12 мг/л); р. вода, pH = 1,96, d=\ см.
Рис. 165. Th,v (6,7 мг/л), ком-вода,
плекс с тороном; р. rf = 1 см.
Л, ммк
Рис. 166.
TiIV (1,94 • 10~5 Л4), комплекс с роданидом; р. (СН3)2СО -4- вода (4:1)4-2,4 44 NH4SCN, rf = 1 см.
А, ммк
Рис. 167. Titv (1 мг/л), комплекс с
pH = 4.3=9,6, rf =1 см, в кювете сравнения раствор реагента.
тороном; р. вода,
Рис. 168.
Thlv (5мг/л), комплекс с 8-оксихинолином: 1 — р. абс. С2Н5ОН; 2—р.
С2Н5ОН 4- вода (4:1): rf = 5 см.
773
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 169.
Т1'« (4 мг/л), комплекс с 8-оксихииолином; р. СНС1з4-0,75% С2Н5ОН, d = 5c3f.
Na-солью хромотроповой кислоты; р. вода, pH = 2,7-«-4,6, <7=1 см, в кювете сравнения раствор реагента.
Л, ммк
дити-
Рис. 170. TI1 (1 мг/л), комплекс с зоиом; р. CHCI3, d =Н
см.
Рис. 171. Т11Н (4 мг/л), комплекс с диэтилдитио-карбаматом; р. СС14, d = 5 см.
Рис. 173. ТсО“ (5 • 10~4 м); р. 0,1 Л4 НС1, d = 1 см.
174.
Рис.
1 — и111; 2— UIV; 3— Uvi;
р. 1 Л4 НС1.
Т74
СПЕКТРЫ ПОГЛОЩЕНИЯ неорганических ионов
Рис. 175. UVI (6,5 г/л); р. разб. H2SO4, d — 2 см.
Рис. 176. 1 — UO2SO4 (5 • 10“5 М);
2— UO2SO4(1 • 10-3 Af);
3— К2Сг2О7 (6,7 10~6 А1);
4 — KMnO4 (1 • 10~4 М\, р. 0,5 М H2SO4, rf = 10 см.
Рис. 177. UVI (5 мг/л). комплекс с дибензоилметаном; р. вода, pH = 6,5-ь8,5, d = 1 см, в кювете сравнения раствор реагента.
Рис. 178. UV1 (40 мг/л), комплекс с диэтилдитиокарбаматом; р. вода. pH — 6,5-г-7,2, rf = 1 см.
Рис. 179.
UVI (100 мг/л), комплекс с Na2O2; р. разб. NaOH, rf — 1 см, в кювете срав-пения раствор реагента.
775
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 180. Uvl (68,0 мг/л), комплекс с роданидом;
р. (СН3)2СО + 2 М nh4scn, d = 1 см-
Л,/ими
Рис. 181. V1”; р. 1 М НСЮ4.
Рис. 182. V111, комплекс с 8-оксихинолином; р. СН3ОН.
Л.мми
Рис. 184. V111 (7,54 10-5 А1), комплекс с роданидом;
р. (СН3)2СО-|-вода (3:2) -4-+ 1,8 М NH4SCN, d = 1 см.
Рис. 183. VO2+; р. 1 М НС1О4.
Рис. 185. VIV(VO2+), комплекс с 8-оксихинолином; р. СН3ОН.
776
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 186.
Vv, комплекс с диэтилдитиокарбаматом:
Л, ммк
Рис. 187. Vv, комплекс с 8-оксихинолином; р. СНС13. Закон Бера соблюдается в интервале концентраций 1—5 мг/л.
Л, ммк
Рис. 189. Wv (11,32 мг)л), комплекс с роданидом; р. (СН3)2 СО -|-вода (3:2) —0,6 Л1 NH4SCN, d = 1 см.
Рис. 190.
WVI, комплекс с 8-оксихинолнном:
1 — 1,71 мг/л', 2—17.1 мг/л; р.СНС13, d — 1 см.
777
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ионов
Рис. 191.
Znli, комплекс с диэтилдитиокарбаматом: 1 — 4 мг/л', 2— 0,4 мг/л', р. СС14, d — 5 см.
0,4
0.2
о
0,8
0,6
250 300 350
450
Л, мм и
Рис. 192. Znli, комплекс с 8-окси-хинолином: 1 — 0,745 мг[л', 2 — 9,33 мг/л-, р. СНС13, d = 1 см.
Рис. 193. Zriv (2 мг/л), комплекс с ализариновым красным S; р. вода, pH = 0,б-г-1,5, d — 4 см.
Рис. 194. Dyiii (17,15 г/д); р. 1 М НСЮ4, d=\ см.
778
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 195. ЕгП1 (8,3 г/л); р. 1 М НС1О4, d = 1 см.
Рис. 196. ЕиШ (17,27 г/л); р. 1 М рис. 197. Gdni (17 34 г/л);
НС1О4, d = 1 см. р. 1 м НСЮ4, d = 1 см.
Л, ммк.
Рис. 198. НоП1 (17,46 г/л); р. 1 Л4 НСЮ4, d = 1 см.
779
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Рис. 200.
РгШ (1б,55 г/л);
р. 1 Л1 НС1О4, d = 1 см.
Рис. 202. ТЬП1 (17,23 г/л); р. 1 Л1 НС1О4, d = 5 см.
Рис. 203. ТцШ (17,52 г/л); р. 1 Af НС1О4, d = 1 см.
780
СПЕКТРЫ ПОГЛОЩЕНИЯ НЕОРГАНИЧЕСКИХ ИОНОВ
Продолжение
Важнейшие характеристики спектров поглощения ионов редкоземельных элементов в водных растворах НС1О4
Элемент Длина волны, ммк Ширина щели, мм Молярный коэффициент экстинкции е Эле- мент Длина волны, ммк Ширина щели, мм Молярный коэффициент экстинкции е
Nd 354,0 0,020 5,05 Dy 908,0 0,020 2,38
521,6 0,020 4,29 Но 287,0 0,020 3,31
575,5 0,020 6,93 361,1 0,020 2,18
739,5 0,020 7,03 450,8 0,020 4,00
794,0 0,020 9,96 537,0 0,020 4,58
Рг 444,2 0,020 10,31 690,4 0,020 3,05
Sm 401,5 0,035 3,23 Ег 379,6 0,055 6,57
би 394,2 0,045 2,91 523,5 0,020 3,20
Gd 272,8 0,020 3,35 Tu 683,0 0,030 2,56
Dy 350,4 0,020 2,52 Yb 908.0 0,020 1,97
365,0 0,020 2,05
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В УЛЬТРАФИОЛЕТОВОЙ ОБЛАСТИ
Спектры поглощения органических соединений приводятся в следующей системе координат: по осн абсцисс отложены длины волн X в ммк (или волновые числа v в а по оси ординат — значения 1g е (е — молярный коэффициент экстинкции); на рнс. 28 по оси ординат отложены значения е.
В подписях к рисункам буква р. означает растворитель.
Указатель
№ рисунка
№ рисунка
транс-Азобензол , -. . ^ыс-Азобензол . . . . Акридин .............
Акриловая кйслота . . Акролеин ..........
Аллилбензол . . . . Аллилгорчичное масло Аллиловый спирт. . . 2-Аминопиридин . . . о-Аминофенол . ж » . лс-Аминофенол . . . . п-Аминофенол . . . . 2-Амииохинолин . . . Анизол ..............
Анилин ..............
Антрахинон ..........
Антрацен ....
Ацетамид.............
Ацетат натрия . . . . З-Ацетилпиридни . . Ацетилхлорид . . . . Ацетофенон...........
1,2-Бензантрацен , , , 2,3-Бензантрацен . . . Бензаитреи ..........
Бензиламин...........
Бензилиденацетон . . Бензилидинацстон . . Бензойная кислота .
Бензол ..............
Бензофенон...........
n-Бензохинон . . . .
1,2-Бензпирен . » . . 4,5-Бенз пирен . . . . З-Винилпиридин .
Гексаметнлбензол . . Гептен-3 ............
Глицин, хлоргидрат ,
106
106
134
2
3
17
13
2
117
101
102
103
129
22, 80
94
88
51
9
5
119
9
7
52
51
97
82 8-1
89
15, 30,
7, 81
86
57
58
118
22
1
II
51
Глицинат натрия . . * 1,2,5,6-Дибензантрацен Днбензнлдисульфнд Дибензилсульфид . . 1,2-Днгидронафталин 1,4-Дигидронафталин . Диметнланилин . . . 1,2-Диметилнафталин . 1,3-Диметилнафталин . 1,4-Диметилнафталин . 1,5-Диметил нафта л ин . 1,6-Диметилнафталин . 1,7-Диметилнафталин . 1,8-Диметилнафталин . 2,3-Днметилнафталин . 2,6-Диметилнафталин . 2,7-Диметилнафталин . Диметилокса лат . . . 2,4-Днметилпнридин 2,6-Диметилпиридин а, а'-Дипиридил . . . Y, у'-Ди пиридил . . . Дифенил...............
Дифенилацетилен . . транс, транс-1,4-Дифенил-бутадиен-1,3 ....
Дифенилметан .... Дифенилполиены . . . 2. 2'-Дихлордифенил 4,4'-Дихлорднфенил . . Диэтиламин............
Диэтиламин, хлоргидрат Диэтилдисульфид . . Додека гидротрифенилен лс-Додецифенил . . . Изохинолин ...........
Индан ................
Ий дол................
11
54
ПО
109
36
37
98
41
42
43
44
45
46
47
48
49
50
8
120
121
125
126
30, 31, 32
21
27
23
28
104
105
10
10
14
56
32
128
59
140
781
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
№ рисунка
№ рисунка
Калийдинитрометан . . КфЛйЙнитроформ . . . К$мфора...............
Карбазол .............
Кватерфен ил ....
л-Квиндецифенил . . Квмнквефенил .... Коронен ............
о-Крезол ...... ж-Крезол .............
л-Крезбл..............
Кротоновый альдегид .
2.3-Ксиленол » - • .
6,4-Ксиленол « > . .
3.8-Ксиленол « . .
2,6-Ксиленол « ► . .
3,4-Ксиленол «... 3,5-Ксиленол .... Лепидин ...... а, а'-Л ути дин .... а, у-Л утидин .... З-Метилинден .... 1-Метилнафталин . . .
2-Метилнафталин . » . й-Метилстнрол .... р-Метилстирол .... d-Метилстнрол ....
I-Метил-5.6,7,6-тетр а гидронафталин ...........
2-Метил-5,6,7,8-тетрагидро нафталин ..............
а-Метилтетралин . « . 0-Метилтетр ал ин . . . 2-Метилхинолин . . . 4-Метилхииолнн . • . 6-Метилхинолин . » . 7-Метилхинолнн . . . 3-Метилхолантрен . . Мочевая кислота . . . Муравьиная кислота . -Натрийннтрометаи . . Нафталин ..... Нафтацен .............
1-Нафтнламии .... 2-Нафтиламин .... 1-Нафтилфенилметан . I-Нафтойная кислота .
2-Нафтойная кислота . I-Нафтол..............
2-Нафтол..............
1,4-Нафтохннон » т . Нитрометан . . . ж . ж-Новифенил . « . . Окись мезитила в . . Оксалат натрия « . . 1-Оксиакрнднн .... 2-Оксн акридин . . . . З-Окснакрндин . . . . 4-Окснакридин .... 0-Окснакридин .... Пентацен ...... а-Пиколин ..... Э-Пнколин ..... у-Пнколнн s « . . .
12
12
7 141
31
32 31
56 66
67
68
3 72 73 74 75 %
131 121 120
60 34 35
19 18
20
39
40
39
40
130
131
53
142
6
12
33, 51
51
99
100
53
90
91
78
79
87
12
32
4
8
135
136
137
138
139
51
114
115
116
Пикриновая кислота . Пирен ....... Пиридин ...... Пирокатехин .... Пиррол................
ж-Полифеиилы .... п-Полифенилы .... Пропилен .............
Резорцин..............
цис-Стильбен .... гра«с-Стильбен . . . о-Терфенил............
ж-Терфен ил ..... п-Терфенил............
1,2.3.4-Тетрагндро-2-на-фтойная кислота
Б,6,7,8-Тетрагидро-2-иа-фтойная кислота .
Тетралин ............
1-Тетралон . . . . . Тетраметилэтилен » . Тетранитрометан , . . Тетрафен ...... Тетрацен ...... Тиофен ....... Тиофенол ...... о-Толуидин ...........
ж-Толуидин » . . . . Толуол .....
Триметилэтилен . . . Трифенилен ...........
Трифенилметан . . . Уксусная кислота . . Уксусный ангндрнд . . Фенантрен ............
Феннлацетилен ,. . . а-Фенилпириднн » . . Р-Фенилпнридин . « . у-Феннлпнридин . . . 1-Феинлпропен . . . . 2-Феннлпропен . . . . Феиилэтилсульфнд . . Фенол ................
Флорол ...... Флуорен ...... Формиат натрия . . . Форон ....... Фуран ....... Хинальдин ............
Хинолин .............
Хлористый ацетил . . Хризен ...............
Циклогексанон . . . . Циклопентанон . . . . Циклопропан . . . . Цнн нам ил идеи ацетон . Цнстинат натрия . . . Щавелевая кислота . . Этнлацетат ...........
Этилмеркаптан . . . Этнлмеркаптнд натрия о-Этнлфенол...........
ж-Этнлфенол . « . . п-Этнлфенол , • . <
63
55
112, 113
64
111
32
31
65
24
25
30
30, 32
30, 31
92
93
12
52
51 112 107
95
96
16
56 29
5
9
52 26
122 123
124
18
19 108
62 69
61
6
4 Ш 130 127
9 54
7
7
83
14
8
5
13
13
69
70
71
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
3
783
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 4. 1 — окись мезитила, р. гексан;
2— форон, р. гексан.
а, ммк
Рис. 6. 1 — муравьиная кислота, р. вода; 2— формиат натрия, р. вода.
Л, ммк
Рис. 5. 1 — уксусная кислота, р. вода; 2— ацетат натрия, р. вода; 3 — этилацетат, р. вода.
р. гептан; 2 — циклопентанон, р. гептан; 3— камфора, р. гептан; 4 — ацетофенон, р. гексан;
5 — бензофенон, р. гексан.
784
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ ^.ммк
Рис. 8. 1 — щавелевая кислота, р. вода; 2—оксалат натрия, р. вода; 3— диметилоксалат, р. гексан.
Рис. 10. / — диэтиламин, хлор-гидрат, р. вода; 2—диэтиламин, р. гексан.
А, ммк
Рис. 9. / — хлористый ацетил (ацетилхлорид), без р.; 2—уксусный ангидрид, без р.; 3 — ацетамид, р. вода.
v 10 см ’’
Рис. 11./ — глицин, хлоргидрат, р. вода; 2—глицинат натрия, р. вода.
785
50 Зак. 783
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
метан, р. 0,01 н. NaOH; 3 — калийдинитрометан, р. 0,005 н. NaOH; 4 — калийнитроформ, р. 0,005 н. NaOH; 5—тетранитрометан, р. вода.
Рис. 13. 1 — этилмеркаптан, р. этанол; 2—этилмеркаитид натрия, р. этанол; 3 — аллилгорчичное масло, без р.
Рис. 14. 1 — диэтилдисульфид, р. этанол; 2 — цистинат натрия, р. вода.
786
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
т)ИГ3,см~1
Рис. 16. Толуол, р. циклогексан.
Рис. 18. 1-Фенилпропен (₽-метил-стирол).
50*
787
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 19. 2-Фенилпропен («-метилстирол).
Рис. 20. о-Метилстирол р. этанол.
Рис. 21. Дифенилацетилен, р. циклогексан.
зол, р. гексан-
788
СПЕКТРЫ ПОГЛОЩЕНИЯ
ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 27. транс, транс- 1,4-Дифенилбута-диен-1,3, р. циклогексан.
А,ннк
Рис. 26. Фенилацетилен, р. гексан.
789
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
К,ммк
Рис. 28. Дифенилполиены, р. диэтиловый эфир — этанол (1:1) (при —196° С).
790
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
A, ММК
300 350 МО 500 600
791
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
У)-Ю'3,СМ'1
Рис. 33. Нафталин, р. этанол.
Л,нмк
Рис. 34. 1-Метилнафталин, р. этанол.
792
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 37. 1,4-Дигидронафталин, р. гексан.
Рис. 39. 1-Метил-5,6,7,8-тетра-гидронафталин (а-метилтетра-лин), р. изооктан.
Рис. 38. Тетралин, р. изооктан.
Рис. 40. 2-Метил-5,6,7,8-тетрагидронафта-лин (Р-метилтетралин), р. изооктан.
793
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 44. 1,5-Диметилнафталин, р. изооктан.
5.0 V
9,5
9.0
3.0
2,5
20'
200 220 290 260 280 300 320 390
Л ммк
Рис. 42. 1,3-Диметилнафталин, р. изооктан.
Л, мм к
Рис. 43.
1,4-Диметилнафталин, р.
Рис. 45.
1,6-Диметилнафталин, р. изооктан.
изооктан.
794
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
?1,ммк
Рис. 46. 1,7-Диметилнафталин, р. изооктан.
Рис. 47. 1,8-Диметилнафталии, р. изооктан.
Рис. 49. 2,6-Диметилнафталин, р. изооктан.
Рис. 50. 2,7-Диметилнафталии, р. изооктан
Рис. 48.
2,3-Диметилнафталин, р. изооктан.
795
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 51. 1 — бензол, р. этанол; 2— нафталин, р. этанол; 3 — антрацен, р. этанол, 4 — нафтацен (тетрацен; 2,3-бензантрацен), р. бензол; 5—-нентацен, р. бензол.
Л, ммк
Рис. 52. 1 — фенантрен, р. этанол; 2— тетрафен (1,2-бензантрацен), р. этанол.
Л, ммк
796
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 54.
/ — хризен, р. этанол; 2—1,2,5,6-дибензантрацен, р. метанол.
А, ммк
45 35 30 25 20
V tO'3, см
V-10~3,cm
-1
Рис. 55. 1 — пирен, р. этанол; 2— 3-метилхолантрен, р. этанол.
Рис. 56.
/ — доденагидротрифенилен, р. этанол; 2 — трифенилен, р. этанол; 3 — коронен, растворители: ---- бензол,-----этанол.
797
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 57. 1,2-Бензпирен, р. этанол.
Л, мм к
Рис. 60. З-Метилинден, р. этанол
Aw
Рис. 58. 4,5-Бензпирен, р. этанол.
тМО'3,™1
г, р. гексан.
798
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 65. Резорцин, р. этанол.
Л.ЖГ
Рис. 63. Пикриновая кислота, р. этанол.
Рис. 66. о-Крезол, р. циклогексан.
рис. 64. Пирокатехин, р. циклогексан.
799
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 70. л/-Этилфенол, р. циклогексан.
Рис. 71. л-Этилфенол, р. цикло-
Рис. 69. о-Этилфенол (флорол), р. циклогексан.
гексан.
800
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 73. 2,4-Ксиленол, р. циклогексан.
Рис. 75. 2,6-Кспленол, р. циклогексан.
сан.
Рис. 76. 3,4-Ксилеиол, р. циклогексан.
51 Зак. 763
801
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
тН0'3,см~1
Рис. 78. 1-Нафтол, р. циклогексан.
802
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
i)-10'3, см"
200 220 240 260 280 300 320 340 360 380
з £з
61*
803
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Л, ими
Рис. 83. Циннамилиденацетон, р. этанол.
804
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 85.
1-Тетралон, р. этанол.
Л, мми
Рис. 86. л-Бензохинон. р. гексан.
Рис. 87.
1,4-Нафтохинон, р. 1,4-диоксаи.
805
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 89. Бензойная кислота, р. циклогексан.
Л. ммк
Рис. 88. Антрахинон, р. 1,4-диоксан.
Рис 90. 1-Нафтойная кислота, р. этанол.
Рис. 91. 2-Нафтойная кислота, р. этанол.
806
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 92. 1,2,3,4-Тетрагидро-2-нафтойная кислота, р. циклогексан.
Рис. 93. 5,6,7,8-Тетрагидро-2-нафтойиая кислота, р. циклогексан.
Рис. 95. о-Толуидин, р. изооктан.
807
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 96. лг-Толуидин, р. изооктан.
Рис. 98. Диметиланилин, р. гептан
Рис. 99. 1-Нафтиламин, р. этанол.
/I, мм к
Рис. 97. Бензиламин, р. изооктан.
Рис. 100. 2-Нафтиламин, р. этанол.
808
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЯ
Рис. 102. лт-Амииофенол, р. этанол.
•д-10'3,см'1
Рис. 103. л-Аминофенол, р. этанол.
Рис. 104. 2,2'-Дихлордифеиил, р. циклогексан.
809
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
^-МГ^См"'
Ь,МГ1К
Рис. 105. 4,4'-Дихлордифенил, р. циклогексан.
Рис. 107. Тиофенол, р. изооктан.
Л. ими
Рис. 106. 1 — транс-азобензол. р. этанол; 2 — цис-азобензол, р. этанол.
Рис. 108. Фенилэтилсульфид, р. изооктан.
810
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Рис. 109. Дибензилсульфид, р. изооктан.
Рис. 110. Дибензилдисульфид, р. изооктан.
Рис. 112. 1 — тиофен, р. гексан; 2—пиридин, р. гексан.
811
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 113.
Пиридин, растворители: ------ этанол,
--- 0,045 н. НС1 в этаноле.
А, мм к
•$10, СМ
р. изооктан.
Рис. 114. а-Пиколин, р. изооктан.
Рис. 116. у-Пиколин, р. изооктан.
Рис. 117;
2-Аминопиридин, р. изооктан.
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЯ
VAT? см
Рис. 118. З-Винилпиридин, растворители: ----этанол, ... 0,045 и. НС1 в этаноле.
Рис. 119.3-Ацетилпиридин, растворители: ---- этанол,----- 6,045 н.
НС1 в этаноле.
Рис. 120.
а, у-Лутидин (2,4-диметилпири-дии), р. изооктан.
Рис. 121. а,а'-Лутидин (2,6-ди-метилпиридин), р. изооктан.
Рис.
а-Фенилпириднн, р. этанол.
122.
813
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
i-Ю З.см
Л, ммк
Рис. 123. Р-Фенилпиридин, р. этанол.
Л, ММК
124. у-Фенилпиридин, р. этанол.
Рис.
Л, мм к
Рис. 125. а, а'-Дипиридил, р. гексан.
\ммк
Рис. 126. у, у'-Дипиридил, р- гексан.
Рис. 127. Хинолин, р. цикло* гексан.
Рис. 128. Изохинолин, р. циклогексан.
814
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
О-ИГ^См"1
Рис. 130. Хинальдин (2-ме-тилхинолин), р. изооктан.
Рис. 132. 6-Метилхинолин, р. изооктан.
v- 10~ъ, см~1
Рис. 131. Лепидин (4-метилхи-нолин), р. изооктаи.
И.нмк
Рис. 133. 7-Метнлхинолин, р. изооктан.
815
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЯ
Рис. 135. l-Оксиакридин, р. этанол.
816
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
ЛЮ 220 ZW 260 280 300 320340 360 380 000 420 440 480 480 500
Л. ммк
Рис. 137. З-Оксиакридип, р. этанол.
20(1 220 240 260 280 300 320 340 360 380 400 420 440 4S0
Л, ммк Рис. 138. 4-Окспакриди11, р. этанол.
52 Зак. 783
817
СПЕКТРЫ ПОГЛОЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Рис. 139. 9-Оксиакридин, р. этанол.
у)-10~3,см~'
Р;.с. 140. Индол, р. циклогексан.
растворители: ----- вода,
----1 н. NaOH.
818
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
ХХ\Х<ХХХХХХХХХХХХХХХХХХХЛ.хл.л.^^^^
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
В этой таблице приведены показатели преломления уПр) различных, главным образом органических, соединений, расположенных в порядке возрастания (от 1,254 до 1,885) показателей преломления. Для каждого соединения, кроме того, приведены плотность (^4) и температура (/, ° С), при которой определены показатель преломления и плотность. В последней графе дается номер соответствующего соединения по таблице «Свойства органических соединений» (т. II стр. 398). В конце таблицы дан формульный указатель помещенных в ней соединений.
№ по пор. Название Формула 1,CC "o № по табл. «Свойства органических соединений»
1 Цианистый водород HCN 19 0,698 1,254 8877
2 Этиловый эфир трифтор-уксусной к-ты FjCCOOCJis 20 1,19 1,306 —-
3 1. 1, 2, 2-Тетрафтор-h 2-дихлорэтан CCIF.CC1F, 0 1,5312 1,3092 9201
4 Метиловый спирт стон 20 0,791 1,3288 5048
j) Пентен-2 CHCH-CHC1I СНз 20 0,651 1,3308 6081
б Вода но 20 0,9982 1,3330 —
7 Уксусный альдегид сн.сно 18 0,7834 1,3392 8077
8 Дифторуксусная к-та FoCHCOOH 20 1,526 1,3419 8020
9 Метиловый эфир муравьиной к-ты НСООСНз 20 0,975 1,344 5290
10 Ацетонитрил CH3CN 20 0,7828 1,34423 900
п Этиловый эфир C.H5OC2Hs 24,8 0,708 1,3497 9498
12 Метилаль СН2(ОСН3)2 20 0,8560 1,3534 4949
13 2-Метилбутаи СН3СН2СН(СН3)2 20 0,62007 1,3549 3779
14 1, 2, 2-Трифтор-1, 1, 2-трихлорэтан CFCLCF.C1 25 1,56354 1,35572 9229
15 Фтористый амил CH3(CH2)aCH2F 20 0,7880 1,3574 255
16 Метилизопропнловый эфир СН.,ОСН(СН3)2 20 0,735 1,35756 —-
17 Пентан СН3(СН2):,СН3 20 0,62632 1,35769 5979
18 Ацетон ClhCOCHj 20 0,792 1,3591 856
19 Тетра метил моносил ан (CHs).Si 18,7 0,648 1,3591 1,3593 7069
20 Метиловый эфир уксусной к-ты CH3COOCHS 20 0,9280 7984
21 Этиловый спирт CHiCFLOH 25 0,78513 1,35954 9497
22 Окись этилена (CHahO 7 0,887 1,35965 9451
23 Этиловый эфир муравьиной к-ты НСООСНоСНз 20 0,91678 1,35975 5295
24 Изоцианистый этил CJ1:,NC 25 0,74421 1,36 9342
25 Метил пропиловый эфир CH,OCH2CH2CH3 14,3 0,74 1,36019 5111
26 Пропилнитрит CH.,CH CH.ONO 20 0,935 1,3613 6681
27 Пропионовый альдегид CHjCHjCHO 20 807 1,3636 6784
28 Этиленфторгидрин CH2FCH2OII 20 1,114 1,3639 9313
29 Пропиоиитрил CHjCH-CN 25 0,7770 1,3659 6732
30 1, 1-Диметил циклопропан (CHO2CCH2CH2 1 1 20 0,6604 1,366 8989
31 Ди мети л а деталь CH„CH (OCHih 20 0,85015 1,3668 9185
32 З-Метнл бутен -1 (CH,)..CHCH = CH2 15 0,63197 1,3675 2084
33 2, 2-Ди мети л бутан CFLCH.CICHjh 20 0,64916 1.3675 1969
34 Изопропиловый эфир l(CHj)2CH].O 23 0,72 1,3678 379>
821
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
Продолжение
О. № по табл.
Е «Свойства . ;
О Название Формула t, °C 4 по оргаииче-
С ских соеди*
g нений»
35 Диметиловый эфир уголь- СО(ОСНз)г 20 1,0694 1,3687 7959
36 37 ной к-ты Этилпропиловый эфир Муравьиная к-та СН3СН2О(СН2)2СН3 НСООН 20 20 0,7386 1,220 1,36948 1,37137 6695 $ 5277
38 Пентен-1 СН3(СН2)2СН=СН2 20 0,64050 1,37148 6073
39 Уксусная к-та СНзСООН 22,9 1,046 1,3715 7969
40 Изобутилиитрит (CH3)2CHCH2ONO 22 0,8699 1,3715 3654 '
41 Этиловый эфир уксусной CH3COOC2Hs 19,2 0,901 1,3728 7992
42 к-ты Изомасляиый альдегид (CHshCHCHO 20 0,7938 1,37302 3763
43 2-Метилпеитан (СН3)2СН(СН2)2СНз 20 0,6599 1,3735 5993
44 Этил изобутилов ый эфир СНзСН2ОСН2СН(СНз)2 25 0,7323 1,3739 3664
45 2, З-Д и метил бутан (СНз)2СНСН(СНз)2 20 0,6612 1,3750 1970 !
46 Гексаи СН3(СН2)4СН3 20 0,65937 1,37а06 2404
47 Циклобутаи СН2СН2СН2СН2 1 1 0 0,703 1,3/52 8893
48 Этил-втор-бутиловыЙ эфир СНзСН2ОСН(СН;|)СН2СНз 25 0,7377 1,3753 —
49 3, З-Диметилбутси-1 (СНз)зССН=СН2 20 0,65310 1,37620 2082
-50 З-Метилпента н СН3СН(СН2СН3)2 20 0,66431 1,37652 5994 ?
51 Этиловый эфир фторуксус- FCH2COOC2Hs 20 1,093 1,3767 —
иой к-ты 0,917 1,37697 6745 J
52 Метиловый эфир пропио- СНзСН2СООСНз 18,9
новой к-ты 0,694 1,37698 3790
-53 Изовропиламин (CH3)2CHNH2 15,4
-54 Изопропиловый эфир ук- СН3СО0СН(СН3)2 20 0,872 1,3770 7981
сусиой к-ты 0,901 1,3771 5292 .
55 Пропиловый эфир му- НСООСН2СН2СНз 20
равьииой к-ты 0,7855 1,37757 3798 *
-56 Изопропиловый спирт СН3СН(ОН)СН3 20
Ъ1 2-Метилбутен-! СН3СН2С(СН3)=СН2 16 0,66 1,378 2083 1
58 Триметиловый эфир орто- НС(ОСНз)з 20 0,9676 1,3793 5885
муравьиной к-ты 0,7519 1,3794 2198
59 Этил-трет-бутиловый эфир (СНз)зСОСН2СНз 20
•60 грет-Бутил амии (CH3)3CNH2 18 0,698 1,37940 2143
•61 Этилбутиловый эфир СНз(СН2)зОСН2СНз 25 0,7447 1,3798 2197
•62 Метилбутиловый эфир CH3CH7CH2CH2OCH3 20 0,74433 1,38 2165
•63 Триэтиловый эфир борной В(ОС2Н5)3 20 0,88 1,3808 9369
64 Метилэтилкетон СН3СОС2Н5 15 0,81005 1,38140 2062
-65 Нитрил масляной к-ты СНз(СН2)2СЫ 24 0,78 1,3816 2219 J
•66 Ацеталь СН3СН(ОС2Н3)2 20 0,8254 1,38193 717 j
67 Гексен-1 СНг=СН(СН2)зСНз 20 0,67317 1,3821 2467 ;
•68 Этиловый эфир цианому- cncooch2ch3 20 1,0034 1,3821 5309 !
равьииой к-ты 0,67385
69 2, 2-Диметилпеитаи (СН3)зС(СН2)2СНз 20 1,38233 5987
70 4 -Мети л пеитеи -1 СН2=СНСН2СН(СНз)2 20 0,66370 1,3825 6079
71 2, 4-Диметилпеитан [(СНз)2СН]2СН2 20 0,67270 1,38256 5989
72 Глиоксаль оснсно 20 1,14 1,3826 2907
/3 Пропиловый эфир (СН3СН2СН2)2О 14,5 0,75 1,3832 6683
74 З-Метилпеитеи-1 СН2=СНСН (СНз)СН2СН3 20 0,6700 1,3835 6078
75 Метилциклобутан СН3СН(СН2)2СН2 1 | 20 0,6931 1,3836 8895 ।
76 Этиловый эфир пропионо- СН3СН2СООСН2СН3 20 0,891 1,38385 6752
77 вой к-ты 3750
Метиловый эфир изомасля- (СНз)2СНСООСНз 20 0,8906 1,3840
ной к-ты
/8 Масляный альдегид СН3(СН2)2СНО 20 0,817 1,38433 4819
79 Пропиловый эфир уксус- СН3СОО(СН2)2СН3 20 0,887 1,38438 7986
.80 ной к-ты & 7962
Диэтиловый эфир уголь- СО(ОС2Н5)2 20 0,9751 1,38456
ной к-ты
81 Этилнитрат C2H5ONO2 21,5 1,104 1,38484 9495
Метиламиловый эфир СНзОСН,(СН2)зСНз 20 0,754 1,3849 6000
S3 Амилнитрпт CH3(CH»),ONO 20 0,8528 1,38506 277
2-Мел илгексаи (СНз)2СН(СН2)зСНз 20 0,67859 1,3851 2415
-85 Пропиловый спирт . СН3СН2СН?ОН 20 0,8044 1,3854 6682
86 Пзобутпловый эфир му- НСООСН2СН(СНз)2 20 0,875 1,3857 5287
равьииой к-ты
822
№ по пор. Название Формула t, °C 4 nD № по табл. «Свойства органических соединений»
87 Триметиловый эфир орто-уксусиой к-ты СН3С(ОСН3)3 25 0,94375 1,38585 -
88 Фтористый гептил CH3(CH2)sCH2F 20 0,804 1,3861 —
89 Трихлорфторметаи CC13F 18,5 1,494 1,3865 5030
90 dl-втор- Бутиловый эфир уксусной к-ты СНзСООСН (С Н3) С2Н5 25 0,8648 1,3866 7975
91 Метиловый эфир хлормуравьиной к-ты асооснз 20 1,2231 1,38675 5305
92 грет-Хлористый бутил (СН3)3СС1 17,8 0,843 1,3869 2131
93 Нитрил пропиоловой к-ты HC^CCN 17 0,816 1,3870 —
94 Изоамилнитрит (CH3)2CHCH2CH2ONO 20,7 0,871 1,38708 3614
95 Диэтиламин (CH3CH2)2NH 18 0,7108 1,38730 3501
96 Пропионовая к-та СН3СН2СООН 19,9 0,992 1,38736 6737
97 Диметилсульфат (CH3)2SO. 20 1,3322 1,3874 5115
98 Гептан СН3(СН2)3СН3 20 0,68376 1,38764 2572
99 трет Бутиловый спирт (CH3)SCOH 20 0,7887 1,38779 2173
100 2-Метилбутен-2 (СН3)2С=СНСН3 20 0,6623 1,3878 2089
101 Метилизопропилкетон СН3СОСН(СН3)2 16 0,8046 1,38788 2066
102 Метиловый эфир масляной СН3(СН2)2СООСН3 20 0,8982 1,3879 4786
103 к-ты ццс-2-Метилпеитен-З СН3СН=СНСН(СН3)2 20 0,66918 1,38793 6088
104 Этилаллиловый эфир С2Н6ОСН2СН = СН2 20 0,7651 1,38810 213
105 Пента диен-1, 3 СНз—сн = сн-сн - сн2 20 0,6594 1,3883 5967
106 Хлористый пропил СН3(СН2)2С1 20 0,890 1,38956 6650
107 cfZ-3-Метилгексан СН3СН2СН2СН (СН3) СН2СНз 20 0,6868 1,38864 2416
108 транс-4-Метилпентеи-2 СНзСН = СНСН(СНз)2 20 0,66862 1,38878 6088
109 Бутиловый эфир муравьиной к-ты НСООСН2(СН2)2СН3 20 0,89 1,3891 5281
по 2, 2, З-Триметилбутан СНзС (СН3) 2СН (СНз) СНз 20 0,69011 1,38944 1997
111 Метилпропилкетой СН3СО(СН2)2СН3 20,2 0,8089 1,38946 6058
112 Хлораигидрид уксусной снзсоа 20 1,1051 1,38976 791
113 2, 2-ДифтсТр-1-бромэтан CHF2CH2Br 20 1,8 1,39 —
114 Этиловый эфир валериановой к-ты СН3(СН2)3СООС2НВ 20 0,8739 1,39 2246
115 Пропиламин CH3(CH2)2NH2 16,6 0,72 1,39006 6652
116 Уксусный ангидрид (СН3СО)2О 20 1,0820 1,39006 8095
117 Нитроэтан CH3CH2NO2 24,3 1,0472 1,39007 9208
118 Диэтил сул ьф ат (C2H5O)2SO2 20 1,178 1,3902 9509
119 Йзовалериановый альде- (CHS)2CHCH2CHO 20 0,802 1,39023 3685
120 гид Этиловый эфир изомасля-ной к-ты (СН3)2СНСООСН2СН3 20 0,86930 1,3903 3755
121 Изобутиловый эфир уксусной к-ты СНзСООСН2СН(СН3)2 18,8 0,870 1,3907 7980
122 3, З-Диметилпеитан (CH3)2C(C2HS)2 20 0,69327 1,39092 5990
123 Диметиловый эфир щавелевой к-ты (СООСН3)2 66,6 1,14 1,3915 9062
124 2, 2, 4-Триметилпеитан (СНз)3ССН2СН(СНз)2 20 0,6919 1,3916 3778
125 Бутии-2 dl-Ч, З-Диметилпентаи СН3С^=ССН3 20 0,6906 1,3918 2202
126 снзстсн^сщснзхун» 20 0,69514 1,39201 5988
127 2-Метилпеитен-! СН2=С(СН3)(СН2)2СН3 20 0,6817 1,3921 6077
128 Триэтиловый эфир ортому-равьииой к-ты НС(ОС2НЕ)3 18,8 0,8971 1,3922 5888
129 втор- Бутиловый спирт CH3CH(OH)C2Hs 22 0,806 1,3924 2172
130 2, 5-Днметилгексаи 1(СНз)2СНСН2]2 20 0,69354 1,39246 2411
131 dl-втор - Б ути ла мин CH3CH.2CH(NH2)CH3 20 0,7225 1,3928 2141
132 Нитрил акриловой к-ты ch2=chcn 20 0,797 1,393 128
133 Изомасляиая к-та (CH3)2CHCOOH 20 0,949 1,3930 3742
134 Пивалевая к-та (СНз)зССООН 36,5 0,91 1,3931 6113
135 Пропиловый эфир пропионовой к-ты СН3СН2СОО(СН2)2СН3 20 0,883 1,3933 6747
136 Диацетил СНзСОСОСНз 18,5 0,981 1,3933 2030
137 Нитрометан CH3NO2 20 1,130 1,3935 4990
138 Тетраэтиловый эфир орто-угольиой к-ты CfOGHs), 18,5 0,9197 1,39354
823
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
| № по nop. 1 Название Формула t, °C 4 nD № по табл. «Свойства органических соединений»
139 транс-1 ексен-2 СН3СН-СН(СН2)2СН3 20 0,67795 1,39363 2473
но З-Этил пентан (СН3СН2).,СН 20 0,6984 1,39366 6009
141 Диэтилкетон (СН3СН,)2СО 16,6 0,82 1,3930 6063
142 транс-1 ексен-З СН3СН2СН = СНСН СИ, 20 0,6771 1,3943 2480
143 Валериановый альдегид СН3(СН-,)3СНО 20 0,80952 1,39436 2225
144 Фтористый октил CH,(CH2)„CH»F 20 0,803 1,3947
145 трег-Бутиловый эфир ук- СН3СООС(СН3)3 20 0,896 1,3947
146 с ус ной к-ты Триэтиловый эфир орто- СН3С(ОС-Н3)3 25 0,8847 1,39485 5891
147 уксусной к-ты Чис-Гексен-З СН3СН2СН-СНСН2СН3 20 0,6799 1,3950 2480
148 Бутиловый эфир уксусной СН:,СОО(СИ,).СН3 20 0,882 1,3951 7974
149 втор-Бутиловый эфир про- СН;<СН3СООСИ (СН3)С2Н5 20 0,866 1,3952
150 пионовой к-ты Виниловый эфир уксусной СН3СООСН-СН. 20 0,9317 1,3953 7976
151 втор-Хлор истый бутил СН,СН2СНС1СН, СН3СН2СН(ОН)СН3 25,2 1,138 1,3953 2130
152 J-вгор-Бутиловый спирт 20 0,8080 1,3954 2172
153 5-Метилгексен-1 СНо-СН(СН,),СН(СН3).. 20 0,6936 1,3954 2472
154 Этиловый эфир хлор му- С1СООСН.СН, 20 1,138 1,39548 5308
155 равьипой к-ты Пропиловый эфир изомас- (CHS)2CHCOOCH2C,HS 20 0,87 1,3959 3753
156 ляиой к-ты
Метил из об ути л кетон СН3СОСН2СН(СН3), 20 0,8017 1,396 6061
157 Изобутиловый спирт (СН3)2СНСН2ОН 17,5 0,805 1,3968 3655
158 2-Этилбутен 1 СН3СН2С(С,Н6)=-СН. 20 0,68958 1,3969 2086
159 Хлористый изобутил (СН3)2СНСН2С) 17,8 0,879 1,3970 3638
160 2. 4-Диметилпентен-1 СН2 = С(СН3)СН,СН(СН3)2 20 0,6937- 1,3970 6075
161 З-Метилгексен 1 СН3(СН2)2СН(СН3)СН=-СН2 20 0,6958 1,3970 2470
162 втор-Изоамиловый спирт (СН3)2СНСНОНСН3 20 0,819 1,3973 3617
163 Хлорметил метиловый С1СН2ОСН3 20 1,070 1,39737 5139
164 эфир Этиловый эфир изовале- (СН3)2СНСН2СООСН2СН., 18,4 0,87 1,3974 3679
165 риановой к-ты Изобутиловый эфир про- C.-HsCOOCHjCH (СН.,), 20 0,869 1,3975 6743
166 пионовой к-ты Октаи СП,(СН.),.СИ. 20 0,70252 1,39750 5791
167 цис- Гексен-2 СН3СН = СН(СН2)2СН, 20 0,68720 1,39761 2473
168 Изоамиловый эфир му- НСиО(СН2)СВ(СН,). 20 0,871 1,3977 5286
169 равьипой к-ты 4-Метил гептан СП3С11(СН2СН2СН3)2 25 0,70463 1,3978 2580
170 Пропилнитрат CH3CH2CH2ONO2 20 1,0548 1,3979 6680
171 4-Метилгексен-2 (а-форма) СН,СН = СНСН(СН3)С,Н3 20 0,7007 1,3980 2476
172 2-Метил гептан (СН3)2СН(СН2),СН3 20 0,69792 1,3981 2578
173 Метиловый эфир акрило* СН=СНСООСН3 20 0,953 1,3984 104
вой к-ты
174 З-Метил гептан СНаСНгСН (СНа) (СН2)3С113 20 0,70584 1,39848 2579
1?5 4-Метилгексен-1 СН,=СНСН2СН(СН3)СН>СН3 20 0,6969 1,3985 2471
1?6 2. 2-Диметилпентсн-З СНчСН=СНС(СН3)з (С Нз)2СНСН2СН (СН3)С,Н5 20 0,6881 1,3986 6085
177 dl-2, 4-Диметилгексан 25 0,7 1,3986 2410
178 Изобутила ми и (CH3)2CHCH2NH2 17 0,74 1,3988 3640
179 Этилпропилкетон С2Н5СОС31,7 22 0,81491 1,39899 2462
180 2-Метилгексен-4 (а-форма) (СН3)2СНСН2СН = СНСН3 20 0,6990 1,3990 2477
18! Гексин-1 HCsC-C,H» 20 0,7156 1,3990 2508
182 Масляная к-та СН3СН СНгСООН 20 0,9587 1,39906 4775
183 2-Метил гексе н -3 СН3СН2СН = СНС11 (СН3)2 20 0,6942 1,3991 2482
184 3, 3-Ди метил пентен-1 СН2 = СНС (СН3) 2С НС н3 20 0,6961 1,3991 6076
185 Нитрил валериановой к-ты CH3(CH,)3CN 15 0,80348 1,39913 2270
186 Бутиловый эфир (С2Н5СН.,СН2)2О 20 0,769 1,3992 2175
187 З-Этилгексан (СН.СН2)2СНСН2СН2С113 25 0,71 1,3993 2421
188 Бутиловый спирт СН3СН2СН2СН2ОН 20 0,8098 1,39931 2171
189 2, З-Диметилбутеп-1 (СН3)2СНС(СН3)-СН, 20 0,6803 1,3995 2081
190 2-Метилгексен-4 (3 форма) 2-Метил-3-этил пентан СН3СН-СНСН2СН(СН,); 20 0,7020 1,3995 2477
191 (СН3).СНСН(СН2СН.)2 25 0,7 1,3996 5998
824
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О Г" е Название Формула t,C nD № по табл. «Свойства органических соединений'»
192 Нитрил а-оксиизомасляной (CH„);C(OH)CN 20 0,9300 1,3396 3761
193 Акролеин СН2-СНСНО 20 0,841 1,39975 131
194 Гептеи-1 СН2 = СН(СН2).СН3 20 0,69698 1,39980 2610
195 Изобутиловый эфир изо- (СН.,) СНСООСНгСЩСНзИ 20 0,87 1,3999 3748
масляной к-ты
196 Окись этилеиэтилидеиа СН3СН-(ОСН2)2 20 0,981 1,40
197 3, 4-Диметилпентен-2 СН3СН=С(СН3)СН(СН3)2 20 0,7126 1,40 6084
198 Тетраэтилгерманий Ge(C2H5)4 20 1,198 1,400
199 4-Метилгексен-2 (₽-форма> СН3СН = СНСН(СН3)С2115 20 0,6981 1,4000 2476
200 Триизопропиловый эфир СН[ОСН(СНа)2)а 20 0,8621 1,4000 5884
201 ортомуравьиной к-ты
Этиловый эфир масляной СН3(СН2).СООС2Н5 20 0,879 1,40002 4793
202 З-Метилпентен-2 (форма I) СН3СН = С(СН3)С2Нс 20 0,6976 1,4002 6387
203 Нитрил метакриловой к-ты CH2=C(CH3)CN 20 0,805 1,4002 4911
204 Метил -втор-бутил кетой СН3СОСН(СН,)С2Н5 18 0,8145 1,4002 6060
205 1-Нитропропан CH3(CH2)2NO2 24,3 1,0081 1,40027 6478
206 Триэтиламин (C2Hs),N 20 0,728 1,40032 7920
207 Пентии-2 СН3С=СС2Нь 20 0,687 1,40044 6103
208 2-Метилпеитеи-2 (СН3)2С=СНС2Н5 20 0,6904 1,4005 6086
209 Пропиловый эфир масля- СНзСН2СН2СООС3Н; 20 0,879 1,4005 4789
ной к-ты
210 2, 6-Ди метил гептан (СН3)2СН(СН2),СН(СН3)2 20 0,70891 1,40373 2576
211 3. 3-Пи метил гексаи СН3СН-.СН2С(СН3)2СН2СН1 20 0,7107 1,4008
212 (1, 3-Диметил) бутиловый СНзСООСН (СН3) СН2СН(СН3) 20 0,8580 1,4008 6044
эфир уксусной к-ты
213 d-Изобутиламиловый эфир (СН.,)2СНСН2ОС5Нц 20,2 0,77 1,4008
214 Бутиламии CH3(CH2),CH,NH2 20 0,7401 1,401 2135
215 Амиловый эфир уксусной к-ты (2-Метил) бутиловый эфир СН3СОО(СН2)4СН3 20 0,879 1,4012 7971
216 СН,СООСН2СН(СН3)С2Н6 20 0,88 1,4012
уксусной к-ты
217 Пейта идион-2, 3 СН,СОСОСН2СН3 19 0,9565 1.40135 6027
218 2, 4-Диметилгептан СН3(СН2)2СН (СН3)СН2СН (СН3)2 25 0,71 1,4014
219 Изоамиловый эфир уксус- СН3СОО(СН2)2СН(СН3)2 18,1 0,87 1,4014 7979
иой к-ты
220 Хлористый бутил СН,,(СН2)2СН2С1 20 0,884 1,4015 2129
221 Метил бутил амии c,h9nhch, 18,1 0,7363 1,40180 2136
222 Гексилнитрит CH3(CH2)4CH2ONO 20 0,8851 1,4018 2499
223 2. 4-Диметилпеитеи-2 (СНз)2С=СНСН(СН,)2 20 0,6947 1,4020 6083
224 гП-2, 5-Ди метилгепта н СН3СН2СН(СН1) (СН2)2СН (СН3)2 25 0,71 1,4020
225 2, З-Диметилпентеи-1 СН2=С(СН3)СН(СНз)С2Н5 20 0,7054 1,4022 6074
226 Метил целлозольв (2-мето- СН3ОСН2СН2ОН 20 0,9660 1,40238 9302
ксиэтанол)
227 4-Метилоктан СН3(СН2)2СН(СН3)(СН2)3СН3 25 0,72 1,4027
228 Изобутилнитрат (CH,),CHCH2ONO2 20 1,0152 1,4028 3653
229 Б-Этоксиэтиловый эфир С.Н5ОСН2СН,ООССН3 20 0,973 1,4030 9318
уксусной к-ты CH3(CHJ,COOCH2CH(CH3)2
230 Изобутиловый эфир масля- 18,4 0,862 1,4030 4784
ной к-ты
231 2, 2-Диметилгептан СН,(СН2)4С(СН3)з 20 0,7105 1,4035
232 Пропиловый эфир хлор- С1СОО(СН2)2СН3 20 1,0901 1,40350 5306
муравьиной к ты
233 Этиловый эфир имидоук- HN=C(CH3)OC2Hs 18,8 0,873 1,4035
234 сусной к-ты
Пропионовый ангидрид (С2Н:.СО)2О 20 1,010 1,4038 6787
235 Циклопеитаи СНДСН2)3СН2 1 1 20 0,74358 1,4039 8969
236 3-Этокси пропин-1 СНг=ССН2ОСН»СН, 20 0,8326 1,40390 6704
237 2-Метил гексен -1 CH2 = C(CH3)C,HS 20 0,7000 1,4040 2469
238 Пропиловый эфир изова- (CHshCHCH2COOCH2CH2CH3 17,8 0,8643 1,40413 3676
л ери а новой к-ты
239 Гептеи-3 СН,СН2СН-СН(СН2)2СН3 20 0,7043 1,40419 2612
240 Изовалериановая к-та (СНа).СНСЦ,СООН 20 0,93 1,4043 3669
825
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
Продолжение
1 № по пор. I Название Формула Г, °C 4 "о № по табл* «Свойства ;• оргаииче- : ск их соединений»
241 Гексадиен-1,5 СН2-СН(СН2)2СН=СН2 20 0,6912 1,4044 2389
242 Аллиловый эфир уксусной СН3СООСН2СН = СНг 20 0,928 1,40448 7970
243 Дипропиламин (CH3CH2CH2)2NH 20 0,7384 1,40445 3327
244 Паральдегид ОСН (CHs)OCH (СНз) ОСНСНз 20 0,9943 1,40486 5929
245 Бутиловый эфир масляной СН3(СН2)2СООСН2(СН2)2СН3 20 0,872 1,4049 4780
246 Этиловый эфир акриловой СН2=СНСООСгНЕ 20 0,924 1,405 106
847 Хлорангидрид пропионовой СН3СН2СОС1 20 1,0646 1,40507 6730
248 Q-Метилмасляиая к-та СН3СН2СН(СН3)СООН 20 0,941 1,4051 4810
249 грет-Амиловый спирт СНзСН2С(СНз)2ОН 20 0,809 1,4052 2057
250 d-Пента нол-2 СНз(СН2)2СН(ОН)СНз 20 0,8103 1,4053 6047 f
251 а-Хлорэтилэтиловый эфир СН3СНС1ОС2НЕ 20 0,9655 1,4053 8796
252 Ноиаи СНз(СН2)7СНз 20 1,7176 1,40542 5670 J
253 Изобутиловый эфир изова-лериаиовой к-ты (СН3)2СНСН2СООС4Н„ 20 0,8534 1,4057 3673
254 3, 4-Диметилгексан СН3СН2СН(СН3)СН (СНз) CsHs 20 0,71923 1,4058 2412
255 Нитрил молочной к-ты CH3CH(OH)CN 18,4 0,992 1,4058 5179
256 Нитрил нзокапроновой (CH3)2CH(CH2)2CN 20 0,806 1,406 3720 }
257 2-Хлорпентан СНзСНС1(СН2)2СНз 20 0,870 1,4060 6007 1
258 Цианистый аллил ch2=chch2cn 20 0,8318 1,40602 186
259 Изоамиловый эфир пропионовой к-ты СНзСНгСОО (СН2)2СН(СНз)г 20 0,870 1,4065 6742 ?
260 Т риэтил фосфат (С2Н5)3РО4 17,1 1,0686 1,40674 9517 I
261 трет-ХлористыЙ амил СНзСН2ССЦСНз)2 18 0,869 1,407 1989
262 втор-Бутиловый эфир валериановой к-ты С,Н8СООСН (СНз) (С2ИЕ) 20 0,860 1,4070 2237 ,
263 ДиизобутиловыЙ эфир угольной к-ты СО[ОСН2СН (СН3)2]2 20 0,9138 1,4072 7958
264 Этиловый эфир капроновой к-ты СНз(СН2)1СООСН2СНз 20 0,8710 1,40727 4045
265 Дипропилкетон (СНзСН2СН2)2СО 20 0,8174 1,40732 2606
266 Трипропиловый эфир ортом уравьииоЙ к-ты НС(ОСзН,)з 20 0,8805 1,4074 5886 1
267 dl-2, З-Диметилгексан (СНз)2СНСН(СНз)СН2СН2СНз 25 0,7 1,4075 2409 :
268 2-Метилгексеи-2 (СНз)2С=СН(СН2)2СНз 20 0,7089 1,4075 2474 ’
269 несплои-Диметилгидразин (CH3)2NNH2 22,3 0,791 1,4075
270 Амиловый эфир изомасля-иой к-ты (СНз)2СНСОО(СНг).СНз 20 0,859 1,4076 3745
271 Тетра гидрофуран ОСН2СН2СН2СН2 1 1 21 0,888 1,40762 8569
272 Пейта нол-3 (С2Н5)2СНОН 25 0,8154 1,4077 6050
273 Пеитин-1 СН^ССН2СН2СНз 18 0,70 1,4079 6102 •
274 Хлорангидрид изомасля-ной к-ты (СН3)2СНСОС1 20 1,0174 1,4079 3754 ;
275 Этилцеллозольв (2-этокси-этаиол) С2НЕОСН2СН2ОН 20 0,9311 1,40797 9317
276 2-Метилнонан (СНз)2СН(СН2)еСНз 20 0,72 1,408
277 278 Изоамиловый эфир Этиловый эфир пировиноградной к-ты [(СНз)2СНСН2СН2]2О СНзСОСООСНгСНз 20 15,6 0,78 1,0596 1,408 1,408 3618 6316
279 З-Метилгексеи-2 СНз(С112)2С (СНз) = СНСНз 20 0,7120 1,4080 2475
280 Диэтнлфосфит (С2Н5О)2РОН 22 1,074 1,4082 — Й
281 N, N-Диметиламиламин СНз(СН2)4М(СНз)2 20 0,743 1,4083 263
282 Метиламилкетои СНзСО(СН2)4СНз 20 0,817 1,4083 2603
283 2, З-Диметилгептаи СНз(СН2)зСН(СНз)СН (СН,)2 20 0,7235 1,4085
284 Изоамиловый спирт (СН3)2СНСН2СН2ОН 15 0,8129 1,4085 3616
285 Триизобутилбор ат В[ОСН2СН(СНз)2]з 20 0,858 1,4086 3644
286 3. З-Д и метил гептан СНз(СН2)зС(СНз)2СН2СНз 20 0,72560 1,40878 8971
287 826 Метил циклопентан СНзСН(СН2)зСН2 1 1 21 0,7474 1,4088
№ по пор. Название Формула (,°С 4 "о № по табл. «Свойства органических соединений»
288 Октен-1 СН3(СН2)ЕСН = СН2 20 0,7155 1,40880 5821
289 Валериановая к-та СНз(СН2)аСООН 19,1 0,94 1,409 2232
290 Трибутиловый эфир лимонной к-ты НОС3Н4(СООС4Н9)3 20 1,04 1,4091 —
291 2, 7-Диметилоктаи 1(СН,)2СНСН2СН2]2 18,1 0,72 1,4092 5796
292 2, 2-Дихлорпропаи СН3СС12СН3 |(CH3)2CHCH2]2NH 20 1,093 1,4093 6453
293 Диизобутиламин 20 0,7450 1,40934 3235
294 Изоамиламии (CH3)2CHCH2CH2NH2 18 0,751 1,4096 3601
295 Амиловый эфир пропионовой к-ты СН3СН2СОО(СН2)4СН3 15 0,8761 1,4096 6739
296 Дибутиламии (CH3CH2CH2CH2)2NH 20 0,767 1,4097 3192
297 Сернистый ангидрид SO2 20 1,078 1,4100 —
298 Бутиловый эфир хлормуравьиной к-ты С1СОО(СН2)3СН3 20 1,41 5302
299 Амиловый спирт СН3(СН2)3СН2ОН 20 0,8144 1,4101 6038
300 0-Амииоэтилэтиловый эфир C2HeOCH2CH2NH2 20 0,8512 1,4101 9365
301 Диэтиловый эфир щавелевой к-ты (СООС2НЕ)2 20 1,0785 1,41011 9065
302 Этиловый эфир имидопропионовой к-ты HN=C(C2HE)OC2HE 16,9 0,871 1,4103 —
303 (2-Этил)-бутиловый эфир уксусной к-ты (С2НЕ)2СНСН2ОСОСН3 20 0,879 1,4103 2053
304 ДиэтиловыЙ эфир диметилмалоновой к-ты (СН3)2С(СООС2НЕ)2 24,1 0,995 1,4105 4742
305 Этиловый эфир вииил-уксусной к-ты СН2=СНСН2СООС2НЕ 20 0,91224 1,41054 —
306 dZ-4-Метил пентанол-2 (СН3)2СНСН2СН(ОН)СН3 20 0,813 1,411 6049
307 Амиловый эфир масляной jk-ты СН3 (СН2)2СООСН2 (СН2) 3СН3 20 0,87 1,4110 4778
308 Метил-2-хлорэтиловыЙ эфир Гексин-3 СН3ОСН2СН2С1 20 1,046 1,4111 —
309 CjHsCssCCjHs 25 0,7263 1,4112 2510
310 Хлористый изоамил (СН3)2СНСН2СН2С1 18 0,800 1,4112 3599
311 d-a-Метилвалериа новая СН3(СН2)2СН(СН3)СООН 25 0,908 1,4112 2257
312 0-ХлорэтилэтиловыЙ эфир СН,С1СН2ОС2НЕ 20 0,98945 1,41134 8797
313 Нитрил капроновой к-ты CH3(CH2)4CN 20 0,809 1,41154 4036
314 трпяс-Октен-4 С3Н,СН = СНС3Н, 20 0,7147 1,4116 5825
315 5-Метилнонаи (С4Н9)2СНСН3 20 0,732 1,4116 —
316 Z-a-Метнлвалериаиовая CH3(CH2)2CH(CHs)COOH 25 0,920 1,4117 2257
317 Ди бутиловый эфир угольной к-ты СО(ОС4Н9)2 20 0,9244 1,4117 7954
318 Нитрил гликолевой к-ты hoch2cn 19 1,104 1,4117 —
319 a-ХлорэтиловыЙ эфир уксусной к-ты СН3СООСНС1СН3 20 1,112 1,4118 —
320 Хлористый амил СН3(СН2)4С1 20 0,883 1,4119 256
321 Диизобутилкетон [(СНз)2СНСН2]2СО 21 0,805 1,412 2607
322 Декан СН3(СН2)8СН3 20 0,73005 1,41203 3066
323 Хлорангидрид масляной СНз(СН2)2СОС1 20 1,028 1,41209 2213
324 2, З-Диметилбутеи-2 (СН3)2С=С(СНз)2 20 0,7081 1,4121 2088
325 Изоамил нитрат (CH3)2CHCH2CH2ONO2 22 0,9961 1,4122 3613
326 Метиловый эфир а, а-ди-метоксипропионовой СН3С(ОСНз)2СООСНз 17,6 1,068 1,4122 —
327 гранс-Октеи-З СН3СН2СН = СН (СН2) 3СН3 20 0,7163 1,4124 5823
328 цнс-Октен-3 С113СН2СН = СН(СН2)3СН3 20 0,7189 1,4125 5822
329 2-Метилпентаиол-2 (СН3)2С(ОН)(СН2)2СН3 15,5 0,8350 1,4125 6043
330 Этиловый эфир молочной СН3СНО11СООС2НЕ 20 1,031 1,4125 5181
331 Метиловый эфир карбаминовой к-ты NH2COOCH3 55,6 1,136 1,4125 4069
азг 333 З-Метилноиаи С2НЕ(СН,)СНСЕН13 20 0,735 1.4126 —
Диэтилцианамид NCN(C2He)2 48 0,85: 1,4126 8874
827
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
П родолжение
Продолжение
№ по пор 1 Название Формула /, °C 4 "D № по табл. «Свойства органических соединений»
334 Пропилиропилидепамин СНзСН.СН- NC3H? 17,5 0,760 1,4127
335 dl Пентанол-2 СН3(СН2).СН(ОН)СН3 20 0,8303 1,4127 6048
336 Триизоамилборат В(ОС5Н„)з 22 0,845 1,4128 3602
337 Триамиламии (C,,Hn)3N 22 0,845 1,4128 —
338 Этиловый эфир энаптовой СНз(СН-)6СООС.Н5 20 0,8685 1,41296 9120
339 к-ты 1, 2-Дифтор-1, 1, 2. 2-тетра- CC12FCCI2F 25 1,64470 1,41297 9194
340 хлорэтан Изоамиловый эфир изо- (CF з)2СНСН2СО,СН2СН2СН(СНз)2 18,7 0,8583 1.41300 3672
валериановой к-ты 0,936 1,413 4907
341 Метиловый эфир ct-мет- СН,-С(СН.)СООСНз 20
акриловой к-ты 0,97 1,4131 9518
342 Триэтилфосфит (С2Н5О)3Р 10
343 Диэтиловый эфир метил- CH3CH(COOC,HS)2 20 1,018 1,4131 4753
малоиовой к-ты 24,2 1,056 1,4131^
344 Диметиловый эфир диме- (СНз)-,С(СООСНз)2 —-
тилмалоновой к-ты 0,8186 1,41326
345 Гексиловый спирт СН,(СН»)4СН2ОН 20 2443
346 Аллиловый спирт СН2=СНСН2ОН 20 0,855 1,41345 200
347 г7-Гексаиол-2 СНзСН(ОН)(СН2)зСНз 20 0,814 1,4135 2449
348 2, 6-Диметилоктан (СНз)2СН(СН21зСН(СНз)С2Н6 15 0,74 1,4135 —
349 2-Мети.тпентанол-З (СНз)2СНСН(ОН)С2Н5 20 0,8243 1,4135 6054
350 /'мс-Октен-4 [СНз(СН2)2СН-]2 20 0,7212 1,4136 5824
351 Ди эти л кетен (С2Н5)2С-СО 14,9 0,834 1,4136 —
352 Метиловый эфир энанто- СНз(СН2)г,СООСНа 15 0,8806 1,41366 9117
вой к-ты 0,7172
353 З-Этилпентен-2 СНзСН = С(СН,СНз)2 20 1,4139 6089
354 Перекись водорода Н2О2 • 2Н2О 22 0,73 ’ 1,414 •—
355 3-Пропил гептан (СзН;)зСН 20 1,414 —
356 Октиловый эфир муравьи- НСООСН2(СН,)(.СН, 20 0,87 1,414 5291
ной к-ты 0,907
357 Этиловый эфир метакри- СН2=С(СНз)СООСН2СНз 20 1,414 4909
ловой к-ты 0,82]
358 2, З-Диметилбутанол-2 (СНз),СОНСН(СНз)2 20 1.4140 2055
359 Диметиловый эфир метил- СН3СН(СООСНз)2 20 1,095 1,4140 4752
малоновой к-ты 1,1544 1,4140
360 Диметиловый эфир мало- СНДСООСНА 20 4720
новой к-ты 0,8188
361 Г ексанол-3 с2н5снонсн2с2н5 20 1,4141 2452
362 2-Хлоргексан СНз(СН2)зСНС1СНз 21 0,869 1,4142 2420
333 Диэтиловый эфир малоно- СН2(СООС2Н5)2 20 1,055 1,41428 4723
вой к-ты
364 Уретан nh,cooc2h5 52 0,9 1,4144 4071
365 Изокапроновая к-та (СНз)2СН(СН2)2СООН 20 0,9225 1,4144 3721
366 Амиловый эфир валерна- СНз(СН2)зСОО(СН2)1СН, 20 0,87 1,4145 2234
новой к-ты
367 Рицинолевая CHsCCHJsCE (OH)CH?CH-CH(CII2)7COOII 15 0,9496 1,4145 6908
368 к-та 1, I, 2-Трифтор-1, 2-дибром- CF_>BrCHFBr 14 2,254 1,4145
этан 6141
369 Пинаколиновый спирт (СН:),ССНОНСНз 20 0,82 1,4146
370 Аллилкарбииол СН-СНСН2СНоОН 17,5 0,8379 1,4146 2109
371 a. f}-Ди метил масляная СНзСН(СН.,)СН(СН3)СООН 20 0,9275 1,4146 4806
372 к-та Нитрил малоиовой к-ты CFMCNh 34,2 1,049 1,41463 4765
373 B-Метила мииоэтилэтило- СНчПНСН\СН2ОС=Н5 20 0,8363 1,4147 9361
вый эфир 0,93 1,4147
374 Изовалериановый ангид- [(СН,)2СНСН2СО]2О 26 —
375 рид Г ептин-3 С2Н.зС^С(СН).СН3 25 0,7337 1,415 2635
376 Ацетоксиацетон СНзСООСН.СОСНз 20 1,075 1,4150 854
377 Этиловый эфир а. а-ди- СН,С(ОС2Н5)2СООС2Н5 17,1 0,979 1,4151 -—
этоксипропионовой к-ты 0,8202 1.41512 5818
378 .Метил гексилкетон СНзСО(СН2)5СПз 20
37!) N-Этил гидроксилами» СНзСН NHOH 20 0,9079 1,41519 2766
380 Гептиловый эфир уксус- - СН,СОО(СН )„СН3 20 0,87 1,4153 7978
ной к-ты
О. О Е О Я Название Формула t, °C nD № по табл. «Свойства органических соединений»
381 Цикло 11 ент а нол СН.(СН »5СНОН 1 | 20 0,9488 1,41530 8980
382 Хлористый аллил CH'CHCIbCI 20 0,9379 1,41538 184
383 Этилам ил кетон СН,СН,СО(СН2)4СН3 20 0,82 1,4156 5819
384 Нитрил кротоновой к-ты CH3CH = CHCN 20 0,822 1,4156 4459
385 Хлорангидрид нзовалериа-новой к-ты (СН3);СНСН2СОС1 20 0,989 1,4156 3678
386 Метиловый эфир с//-молоч-Пой к-ты СН3СН(ОН)СООСНз 16 1,0898 1,4156 5189
387 4-Этилгептан СН3(СН2)2СН(С2Н3)(СН,)2СН3 20 0,7407 1,41564 2584
388 а-Моноацетин СН,(ОН)СН(ОП)СН2ОСОСН3 20 1,2060 1,4157 2924
389 Пойен-1 CH3(CH2)f,CH = CH2 20 0,72922 1,41572 5689
390 rfZ-P-Метил валериановая к-та СН3СН2СН(СН3)СН2СООН 20 0,9262 1,4159 2258
391 а-Этилк а ироновый альдегид СН3(СН,),СН(С2Н5)СНО 20 0,823 1,4160 4030
392 Диизобутилен (CH-,)2C = CHC4HS 20 0,72177 1,41611 3236
393 З-Хлорпеитап (CHSCH2)2CHC1 15 0,8967 1,4163 6008
394 Метиловый эфир а-метил-ацетоуксусной к-ты CH,COCH(CU3)COOCH3 23,8 1,031 1,4163 —
395 Капроновая к-та СНз(СН.)4СООН 20 0,929 1,41635 4037
396 N-Метил гидроксил амин СНз N НОН 20 1,0003 1,41638 2760
397 2, 2, З-Триметилпептан (СНз)зССН(СНз)С2Н5 25 0,712 1,4164
398 Нитрил янтарной к-ты cnch2ch2cn 63,1 0,985 1,41645 7227
399 ж-Дноксан ОСН?ОСН2СН2СН2 1 1 20 1,03422 1,41652 3300
400 1, 1-Дихлорэтан СН3СНС12 20 1,174 1,41655 9196
401 несимм-Диметил аллен СН2=С=С(СН,)2 20 0,683 1,41658 1944
402 Метиловый эфир гликолевой к-ты НОСН2СООСНз 20 1,1768 1,41677 2840
403 Метокси уксусная к-та СН3ОСН2СООН (СООС3Н7)2 20 1,1768 1,41677 2839
404 Дипропиловый эфир щавелевой к-ты 20 1,01693 1,4168 9063
405 2-Метил гептен-2 (СИз)2С = СН(СН2)зСНз 20 0,725 1,4169
406 Днметилундецилкарбииол (СНзЬСОНСцНгз 81,8 .... 1,417
407 Диизопропилкетон [(СНз)2СН]2СО 20 0,8062 1,417 6064
408 Диэтиловый эфир имидо-угольиой к-ты (C2H5O)2C = NH 18,2 0,964 1,4170 —
409 Ct - Три фтортол уол CeHsCFs 14 1,196 1,41707 7744
410 4 -Метил ге пте н -3 С2Н5СН = С(СНз)СзН7 25 0,741 1,4171
411 2, 4-Диметилпентанол-2 (СНз) 2С (ОН) СН2СН (СНз)2 20 0,8103 1,4172 6042
412 Ундекан СНз(СН2)8СНз 20 0,74024 1,41725 8100
413 Метил гептилкетои СНзСО(СН2)6СНз 22 0,8188 1,4175 5685
414 2-Метил гексанол-2 (СН3)2С(ОН)(СН2)зСНз 20 0,8119 1,4175 2450
415 Нзоамиловый эфир карбаминовой к-ты NH2COOC5Hn 70,6 0,944 1,4175 4067
416 Трипропиламии (CH3CH2CH2)3N 19,4 0,757 1,41756 7887
417 Этиловый эфир каприловой к-ты CH3(CH2)eCOOC2Hs 20 0,8667 1,41775 4009
418 Диэтилуксусная к-.та (С2Н5)2СНСООН 10 0,9331 1,41788 4818
419 Этиловый эфир циапуксус-ной к-ты CNCH2COOC2H5 20,5 1,062 1,41793 8071
420 Диизобутиловый эфир щавелевой к-ты [СООСН2СН(СН3)2]2 20 0,97373 1,4180 9061
421 Диэтиловый эфир этил малоновой к-ты C2HSCH(COOC2H5)2 14,8 1,01 1,41802 4760
422 4 - Нитро-2- метил бута н (CH3)2CHCH2CH2NO2 20,6 0,960 1,4181
423 2-Метилпентаиол-1 СНз(СН2)2СН(СНз)СН2ОН 20 0,8263 1,4182 6039
424 З-Метил пентанол-1 СНзСН2СН(СНз)СН,СН2ОН 25 0,8205 1,4182 6040
425 Этиловый эфир а, а-ди метилацетоуксусной к-ты СНзСОС(СНз)2СООС2Н5 18,8 0,98 1,4183 —
426 Гл и кол ьд и а цета т (СН2ОСОСН3), 15 1,108 1,4183 2853
427 Бутиловый эфир акриловой к-ты СН2=СНСООС4Н9 20 0,898 1,4183 103
428 Этиловый эфир а-хлор-пропиоиовой к-ты CH3CHCICOOC2HS 20 1,0864 1,41850 6779
828
829
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C 4 "о № по табл. «Свойства органических соединений»
429 Глутаровая к-та СООН(СН2)3СООН 106,4 1,192 1,4188 2979
430 7-а-Метилкапроиовая к-та СН3(СН2)3СН (СНз) соон 25 0,909 1,4189 4049
431 Диэтиловый эфир мезокса-левоЙ к-ты COfCOOGHsh 15,6 1,1419 1,419 4848
432 Диэтиловый эфир метил-этилмалоновой к-ты С2Н5С(СНз) (СООСзНзЪ 18,2 0,99 0,4190
433 а-Метилакролеин СН2-С(СН3)СНО 20 0,830 1,4191 133
434 Бутил целл озол ь в С4Н9ОСН2СН2ОН 20 0,9027 1,4191 9291
435 Изопрен СН2=СНС(СНз) = СН2 20 0,6806 1,4194 3780
436 Аллиламин ch2=chch2nh2 21,8 0,761 1,4194 187
437 Ацетоии СНзСОСНОНСНз 15 1,002 1,4194 850
438 1-Хлоргекса н СН3(СН2)4СН2С1 20 0,8759 1,4194 2419
439 Нитрил эиантовой к-ты CH3(CH2)3CN 20 0,8107 1,4195 9124
440 З-Метил пентанол-3 (С2Нз)2С(ОН)СНз 20 0,824 1,4196 6055
441 Метилэтиловый эфир пи-ровинной к-ты С5НвО4(СНз) (С2Н6) 21,9 1,029 1,4196 —
442 Метиловый эфир ацетоуксусной к-ты СНзСОСН2СООСНз 20 1,076 1,4196 928
443 Этиловый эфир этаисуль-фокислоты CiHsSOiOGHt 20 1,145 1,4196 —
444 а-Моиоацетат пропилен-гликоля СНзСООС Н2СНОНСНз 20 1,055 1,4197 —
445 Диметиловый эфир янтарной к-ты СНзООС(СН2)2СООСНз 18 1,1202 1,41976 9552
446 Диэтил ОБ ый эфир пировииной к-ты :н3сн(соос2н5)сн2соос2н5 19,1 1,012 1,4198 —
447 Ацетоуксусный эфир СНзСОСН2СООСгН5 20 1,025 1,4198 929
448 Диэтилсульф ИТ (C2HEO)2SO 11 1,08 1,4198 9511
449 2-Амииогептаи CH3(CH2)4CH(NH2)CH3 19 0,7665 1,41997 2494
450 Этиловый эфир пропиоло-вой к-ты CHsCCOOC2Hs 15 0,968 1,42 6711
451 Диизоамиловый эфир щавелевой к-ты (COOCsH„)2 11 0,968 1,42 9060
452 Хлораигидрид валериановой к-ты СНз(СН2)зСОС1 20 1,01 1,42 2265
453 Этиловый эфир имидоизо-капроновой к-ты CsHnC( = NH)OC2Hs 17,9 0,858 1,4200 —
454 Метил уретан СНзЫНСООСзНз 18,9 1,009 1,4200 4087
455 Диэтиловый эфир янтарной к-ты (СН2СООС2Н3)2 20 1,0402 1,42007 9553
456 2-Метилгептаиол-5 (СНз)2СН(СН2)2СНОНС2Нз 20 0,808 1,4201 —
457 2-Метилгептанол-4 (СН3)2СНСН2СНОНС3Н7 20 0,821 1,4203 —
458 2-Метилгептаиол-З (СНз)2СНСНОНС4Нв 20 0,825 1,4204 —
459 (2-Этил) гексиловый С эфир уксусной к-ты Нз(СН2)зСН(С2Нз) СН2ОСОСН3 20 0,872 1,4204 2448
460 Октиловый эфир уксусной СНзСООСзНн 20 0,88 1,4204 —
461 к-ты Диметиловый эфир пиро-ВИИИОЙ к-ты СН3СН(СООСН3)СН2СООСН3 19,6 1,069 1,4202 —
462 Пропаргиловый эфир уксусной к-ты СНзСООСН2С=СН 20 1,0052 1,42047 6708
463 Гепта нол-4 [СНз(СН2)2]2СНОН 20 0,8183 1,4205 2598
464 З-Метилпеитаиол-2 СНзСНОНСН (СНз) С2Н5 18 0,831 1,4205 —
465 2, З-Диметилпентеи-2 (СН3)2С=С(СН3)СН2СНз 20 0,7280 1,4206 6082
466 d-Гептанол-З СНз(СН2)3СН(ОН)СН2СНз 20 0,8227 1,4206 —
467 а-Мети л ацетоуксусный СНзСОС Н (СНз) СООС2Н5 17,8 1,02 1,42066 932
468 эфир Геитии-2 снас—с (СН2)3СН3 21 0,748 1,4208 2634
469 Октин-1 СН=С(СН2)5СНз 12,5 0,753 1,4208 5841
470 2-Этилбутаиол-1 (С2Н5)2СНСНЙОН 20 0,831 1,4208 2052
471 Додекан СНз(СН2)19СНз 20 0,7511 1,4209 3544
472 гГГептаиол-2 СНз(СН2)4СН(ОН)СНз 20 0,8190 1,4209 2595
473 2, 5-Ди метил гекса нол -2 (СНзЪСН (СН2),С(СНз)2ОН 20 0,823 1,4209 —
474 б-Метилкапроиовая к-та (СНз)2СН(СН2)зСООН 19 0,912 1,4209 4050
475 транс-1, 4-Диметилцикло-гексан CfiHio(CHa)a 20 0,76254 1,42090 8919
Продолжение
1 № по пор. 1 Название Формула t, °C пО № по табл. «Свойства органических соединений»
476 Этилаллен сн2=с=снсн2сн3 20 0,69257 1,42091 5966
477 dZ-Гепта нол-2 СН3(СН2)4СН(ОН)СН3 20 0,8167 1,4210 2595
478 Оксим энаитового альдегида CH3(CH2)sCH=NOH 83,9 0,833 1,421 9122
479 (1-Этил) гептиловый эфир муравьиной к-ты HCOOCeH js 20 0,869 1,421 —
480 Диэтиловый эфир а, а-ди-метнлянтарной к-ты (СН3)2С (СО2С2Н3) СН2СО2С2НБ 20 0,993 1,421 —
481 Ди этиловый эфир а, 0-ди-метилянтариой к-ты (фумароидиая форма) [СН(СН3)СООС2НБ]2 20 0,995 1,421 —
482 Аллилацетон СН2=СН(СН2)2СОСН3 15,4 0,848 1,42126 2488
483 Децеи-1 СН2-СН(СН2)7СН3 20 0,74081 1,42146 3091
484 2-Метилгексанол-З (СН3)2СНСНОНСН2С2Н5 20 0,82 1,4215 —
485 Фураи осн=снсн-сн 1 1 20 0Д366 1,42157 8554
486 Энаитовая к-та СН3(СН2)3СООН 19,8 0,918 1,4216 9114
487 Каприловый альдегид СН3(СН2)БСНО 20 0^821 1,4217 4012
488 Метиловый эфир а. а-ди-мети л ацетоуксусной к-ты СН3СОС(СН3)2СООСН3 16,8 1'012 1,4217
489 Метилдециловый эфир СЮН2,ОСН3 20 0,797 1,4218
490 1-Нитропентан CH3(CH2)3CH2NO2 20 0,948 1,4218
491 Этилуретан C2H3NHCOOC2Hs 20 0'981 1,42192 4095
492 транс-2, 5-Диметилгексен-3-диол-2, 5 [(СН3)2СОНСН=]2 99,2 0^863 1,422 —
493 Метиловый эфир а, а-ди-метилглутаровой к-ты СН2[СН(СН3)СООС2Н5]2 20 0,977 1,422 —
* * 494 5-Диметиламинопентеи-1 СН2=CHCH2CH2CH,N (СН3)2 19,2 0,759 1,4220
495 2-Хлоргептан СН3(СН2)4СНС1СН3 20 0,8672 1,4221 __
496 Метиловый эфир хлоруксусной к-ты С1СН2СООСН3 20 L236 1,4221 8065
497 Этилдециловый эфир С10Н21ОС2Н5 20 0,794 1,4223
498 Пропантиол-2 CH3CH(SH)CH3 25 0,8055 1,4223 6584
499 Акриловая к-та сн2=снсоон 20 1,051 1,4224 100
500 л-Диоксаи ОСН2СН2ОСН2СН2 1 1 20 1Д3375 1,42241 3301
501 Циклопеитеи СН=СН(СН2)2СН2 20 0,77199 1,42246 8982
502 2, 4-Ди метил пеита иол-3 [(СН3)2СН]2СНОН 20 0,8288 1,42259 6052
503 Ш-2-Метилгексапол-1 СН3(СН-)3СН (СН,)СН2ОН 20 0,8270 1,4226 2445
504 а-Этилацетоуксусиый эфир СН3СОСН (С2Н5) СООС2Н3 18,7 0,99 1,4226
505 Этиловый эфир хлор-уксусиой к-ты СН,С1СООС2Н3 20 1,159 1,42274 8068
506 5-Пропил иоиан (С4Н9)2СНС3Н7 20 0,756 1,4228 __
507 Ш-З-Хлоргептан СН3(СН2)3СНС1СН2СН3 20 0^69 1,4228 .
508 Этиловый эфир левулиновой к-ты СН3СО(СН2)2СООС2Н5 20 1,01114 1,42288 4639
509 510 Диизоамиламин цис-1, 3-Ди метил циклогек- [(CH3)2CH(CH2)2]2NH СбНю(СН3)2 21 20 0,7672 1,76603 1,42289 1,42294 3228 8918
511 Диизобутилкарбинол [(СН3)2СНСН2]2СНОН 21 0,809 1,423 2599
512 Нитрил 3-пентеиовой к-ты CH3CH = CHCH.CN 20 0*841 1,423
513 цис-2, 5-Диметилгексен-З-диол-2, 5 [(СН3)2С(ОН)СН=]2 98,9 0,869 1,423 —
514 Диэтиловый эфир а, а'-диметилглутаровой к-ты (малеииоидиая форма) СН2[СН(СН3)СООС2Н3]2 20 0,980 1,423 —
515 Диэтиловый эфир а, 0-ди-метиляитарной к-ты (малеииоидиая форма) [СН(СН3)СООС:Н3]2 20 0,996 1,423 —
516 З-Метил гекса нол -3 СН3(СН2)2С(ОН) (СН3)СН2СН3 20 0,8234 1,4231 2453
517 4-Хлоргептаи СН3(СН2),СНС1(СН2)2СН3 20 0,8710 1,4231
518 Метилциклогексан СН3СН(СН,)4СН2 1—! 1 20 0,76936 1,42312 8922
830
831
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула 7, С "о № по табл. «Свойства органических соединений»
519 2-Аминооктан CH3(CH2)5CH(NH2)CH3 24,5 0,771 1,4232 2619
520 (2-Этил)гексиловый эфир муравьиной к-ты НСООСН2СН(С2НЕ)С4Н8 20 0,88 1,4232 —
521 Диэтиловый эфир метил-циапмалоновой к-ты NCC(CH3)(COOC2Hs)2 20 1,070 1,4232 —
522 Гептиловый i спирт CH3(CH2)SCH2OH 22,4 0,817 1,4233 2594
523 Метиловый эфир левулиновой к-ты CHSCOCH2CH2COOCH3 20 1,04745 1,42333 -
524 Каприновый ангидрид [СН3(СН2)8СО]2О 70 0,8596 1,4234 4026
525 Дибутиловый эфир щавелевой к-ты (COOC,HS)2 20 0,98732 1,4234 9059
526 2-11итро-2, 4 -диметнлпентаи (СН3)2С (NO2) СН2СН (СН3)2 30 0,94 1,4235 .—
527 Трикозан СН3(СН2)2,СН3 80,8 0,7 1,4236 7849
528 у-Ацетокси-Т-валерол актом СН3СООС(СН3)СН2СН2СОО 1 1 78,6 1,123 1,4236
529 Хлористый метилен СН2С12 20 1,336 1,4237 5088
530 2-Метил гептанол-6 (СН3)2СН(СН2)3СНОНСН3 20 0,813 1,4238 —
531 (2-Этил)гексиловый эфир пропионовой к-ты С2Н5СООСН2СН(С2Н5)С,Н8 20 0,87 1,4238 —
532 Ди-втор-бутиловый эфир янтарной к-ты (СН2СООС4Н<))2 25,3 0,97 1,4238 —
533 Бромистый этил CHiCHj.Br 20 1,4555 1,42386 9341
534 ГеиэЙкозаи СН3(СН2),8СН3 70 0,7587 1,4240 2551
535 Гептиламии CH3(CH2)6NH2 20 0,777 1,424 2618
536 d-Окта иол-2 СН3СН(О11)(СН2)5СН3 20 0,8221 1,424 —
537 Пентеи-1-ол-З СН2=СНСН(ОН)СН2СН3 20 0,840 1,4240 6095
538 Кротиловый спирт СН3СН = СНСН2О11 20 0,854 1,4240 2107
539 Диэтиловый эфир глутаровой к-ты С2Н5ОСО(СН2)3СООС2Н5 20 1,025 1,4241 2980
540 Пеларгоновый альдегид СН3(СН2)еСН2СНО 18,6 0,827 1,4242 5952
541 Этилбутиловый эфир малоновой к-ты СН2 (СООС2Не) соос,н8 20 0,98 1,4242 —
542 О-Метиловый эфир эиан-тальдоксима CH3(CH2)eCH=NOCH3 19,4 0,838 1,4243 —
543 Г ексагидроксилол (СНз)гСбНю 20 0,769 1,4244 —
544 Октанол-2 (смесь 1 и dl) СН3СН(ОН)(СН2)5СН3 20 0,8193 1,42444 5816
545 Трибутилфосфат (С«НвО)3РО 20 0,977 1,4245 2192
546 Тетраэтилсилаи (C2H5hSi 25,1 0,7620 1,4246 7072
547 Этиловый эфир а-кротоио-вой к-ты СН3СН = СНСООС2Н3 20 0,919 1,4246 —
548 Этиловый эфир нзокрото-иовой к-ты CH3CH = CHCOOC2HS 20 0,925 1,4246 3733
549 Этиловый эфир Р-хлормас-ляиой к-ты CH3CHCICH2COOC2HS 20 1,052 1,4246
550 0-Хлорэтиловый эфир уксусной к-ты СН3СООСН2СН2С1 20 1,17 1,4247 9315
551 Окти и-4 [CH3(CH2)2Cas]2 20 0,7509 1,4248 5844
552 Этилизобутиловый эфир малоновой к-ты СН2(СООС2Н5)СООС,Н8 20 0,97 1,4248 —
553 Пропилдециловый эфир СН3СН2СН2ОС,оН2! 20 0,797 1,4249 —
554 Пеитеи-1-ол-4 СН2=СНСН2СН (OH)CHs 20 0,834 1,425 —
555 Окти и-3 С2Н3С—C(CH2)3CI13 сн3 20 0,7522 1,4250 5843
556 1-Метил-З-изопропилцикло-пеитап (СН3)2СНСН(СН2)2СНСН2 1 1 19 0,773 1,4250 —
557 2-Б ром пропан СНзСНВгСНэ 20 1,310 1,4251 3784
558 Триизобутиламнн [(CH3)2CHCH2]3N 17,3 0,7711 1,42519 7838
559 Диэтиловый эфир диэтил-малоновой к-ты (C2HS)2C(COOC2HS)2 16,6 0,99 1,4252 4744
560 Диметиловый эфир диэтил-малоиовой к-ты (С2Н5)2С(СООСН3)2 24,5 1,031 1,4253
561 Этиловый эфир р-хлорпро-пионовой к-ты СН2С1СН2СООСН2СН3 20 1,1086 1,42537 6781
562 З-Метил фуран сн=сносн=ссн3 1 1 18 0,923 1,4255 8567
832
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О Е О Е £ Название Формула t,°C "d № по табл. «Свойства органических соединений»
563 Оксим уксусного альдегида CH3CH = NOH 20,-1 0,965 1,42567 8081
564 Левулиновый альдегид СН3СОСН2СН2СНО 21/ 1,02 1,4257 4640
565 Эиантовый альдегид СН3(СН2)ЕСНО 20 0,8495 1,42571 9121
566 Вииилуксусиая к-та СН2=СНСН2СООН 15 1,013 1,42572 2104
567 Изоамнл-изоамилидеи-амин C5H„N= СНСН2СН (СНз)2 18,£ 0,772 1,4258 —
568 «еспл<л-Метилбутил-гидразин NH2N(C4Hs)CH3 21,3 0,804 1,4259 —
569 Изопропилпропиловый эфир малоновой к-ты СН2(СООС3Н7), сн3 20 0,98 1,4259
570 а. а-Метилэтилацетоуксусный эфир СН3СОС( CiHE) COsCsHs 17,7 0,973 1,426 —
571 Янтарный альдегид СНО(СН2)2СНО 18 1,069 1,42617 9580
572 Пентакозан 80 0,8 1,4262 —-
573 Ди метил ацетил ацетон CH3COC(CH3)2COCHs 27,8 0,950 1,4262 —
574 Циклогексан CH2(CH2j4CH2 1 I 20 0,77855 1,42623 8907
575 Мет и л ок тил кетон CH3CO(CH2)7CH3 22 0,8230 1,4263 3082
576 Метиловый эфир втор-бу-тилкарбаминовой к-ты C2H5CH (CH3) NHCOOCH, 24,9 0,965 1,4263 —
577 Диэтиловый эфир циано-малоиовой к-ты NCCH(COOC2HE)2 20 1,093 1,4263 —
578 Монометиловый эфир диэтиленгликоля СН3ОСН2СН2ОСН2СН2ОН 27 1,03 1,4264 3523
579 2-Этилгексиловый эфир масляной к-ты С3Н7СООСН2СН (С2Н6) с,н» 20 0,87 1,4266 —
580 Лауриновая к-та CH3(CH2)wCOOH 60 0,864 1,4267 4624
581 втор-Бутилуретаи C2H5CH(CH3)NHCOOC2He 26 0,940 1,4267 —
582 Диэтиловый эфир этил-цианомалоиовой к-ты NCC(C2H5)(COOC2Hs)2 20 1,052 1,4267 —
583 Диэтиловый эфир (СН трнметиляитарной к-ты )2С (СО2С2Н6) CH (CH3£O2C2H5 20 0,993 1,427 —
584 Этиловый эфир а-оксиме-тиленпропионовой к-ты HOCH - С (CH3) СООСгН3 20 1,024 1,4270 —
585 Дециловый эфир муравьиной к-ты HCOOCH2(CH2)8CH3 20 0,873 1,4271 —
586 Диметилфуразан CH3C=NON=CCH3 I 1 18,9 1,050 1,4271 —
587 Этиловый эфир гндракри-ловой к-ты HOCH2CH2COOC2HS 23 1,07 1,4271 -
588 Моноэтиловый эфир малоновой к-ты CH2(COOH)COOC2H5 20 1,176 1,4271 —
589 Дециловый альдегид CH3(CH2)6CHO 22 0,82 1,4273 4025
590 Изоамилэтиловый эфир малоновой к-ты CH2(COOC2HS)COOC6H„ 20 0,95 1,4275 —
591 Метиловый эфир изобутилкарбаминовой' к-ты (CH3)2CHCH2NHCOOCH3 21,6 0,965 1,4275 —
592 ТриэтиловыЙ эфир метаи-трикарбоновой к-ты HC(COOC2H5)s 16,2 1,108 1,4275 —
593 Диметилаллилкарбииол CH2=CHCH2C(OH)(CH3)2 17 0,8326 1,4277 6099
594 Октин-2 CH3C=C(CH2)4CH, 20 0,7596 1,4278 5842
595 Бутилдециловый эфир С4Н9ОС10Н21 20 0,801 1,4278 . -
596 Бутнлуретаи C4H..NHCOOC2H5 25,6 0,943 1,4278
597 З-Метилгептаиол-З CH3(CH2)3C(CH3) (OH)CH2CH, 20 0,8282 1,4279 2597
598 Капроновый альдегид CH3(CH2)4CHO 20 0,8335 1,4279 4027
599 Этиловый эфир а-этилкро-тоновой к-ты СН3СН = С(С2Н5)СООС2Н5 20 0,899 1,428
600 трет-Бромистый бутил (CH,)3CBr 20 1,222 1,428 2121
601 Изоксазол OCH=CH-CH=N 1 | 20 1,g78 1,428
602 Диметилгексадецилэтилеи (CH3|.C-CHCieH33 79,] 1,428
53 Зах 783
833
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула 1, °C nD № по табл. «Свойства органических соединений»
603 ДиэтиловыЙ эфир адипиновой к-ты (CH2CH2COOC2Hs)2 20 1,009 1,4281 11
604 Метилпропеиилкарбинол СН3СН = СНСНОНСН3 18 0,839 1,4282 —
605 Цетиловый спирт СНз(СНз)иСН2ОН 79 0,798 1,4283 8862
606 Трикозаиои-12 [СН3(СН2),0]2СО 79,5 0,8 1,4283 7850
607 Уидецен-1 СН3(СН2)3СН = СН2 20 0,763 1,4284 —
608 Этил-втор-бутиловыЙ эфир малоиовой к-ты СН2(СООС2Н5) COOC4Hs 20 0,99 1,4284 —
609 Пеитадиеи-2, 3 СН3СН-С = СНСН3 20 0,69502 1,42842 5969
610 Хлористый гептил СН3(СН2)ЬСН2С1 20 0,8725 1,42844 2583
611 Каприловая к-та СН3(СН2)6СООН 20 0,910 1,4285 4005
612 Каприновая к-та CH3(CH2)SCOOH 40 0,8858 1,42855 4020
613 2, 4-Диметилгексаиол-4 (СНз)2СНСН2СОН(СНз)С2Н6 18 0,83 1,4286 —
614 Диметиловый эфир адипиновой к-ты (СН2СН2СООСНз)2 20 1,063 1,4286 —
615 2, З-Диметилпентаиол-З (СН3)2СНС(О11)(СН3)СН2СН3 20 0,8402 1,4287 6051
616 Оксим пропионового аль- CH3CH2CH = NOH 20 0,9258 1,4287 6785
617 дегида Изобутилуретаи (CH3)2CHCH2NHCOOC2He 20 0,9432 1,4288 4086
618 , Метиловый эфир бутил-карбаминовой к-ты c4h9nhcooch3 23,3 0,969 i,4289 —
619 Серная к-та H2SO4 20 1,834 1,4290 ——
620 Трибутиламин (C4H8)8N 20 0,778 1,4291 7819
621 Дециловый эфир пропионовой к-ты C2H5COOC10H21 20 0,864 1,4291 —
622 Диэтиловый эфир пропил-цианмалоновой к-ты NCC(C3H;) (COOC2H5)2 20 1,033 1,4291 —
623 Октиловый спирт CH3(CH2)(,CH2OH 20 0,8246 1,42920 5813
624 Лауриновый ангидрид (СцНгзСОЪО 70 0,8533 1,4292 4634
625 Изопропилизоамиловый эфир малоиовой к-ты СН2(СООС3Н7)СООС3Нц 20 0,96 1,4293 —
626 Проп ил ей гл иколь CH3CHOHCH2OH 27 1,03 1,4293 6516
627 Ди метил форм а мид HCON(CH3)2 22,4 0,948 1,4294 —
628 Ацетол СН3СОСН2ОН 20 ’°82 2-0 1,4295 853
629 цисА, 4-Диметилциклогек- C6H,0(CH3)2 20 0,78285 1,42967 8919-
630 Гентриаконтаион-16 (C1,H3,)2CO 93,5 0,79 1,4297 2549
63] Хлоруксусиая к-та CH2C1COOH 65 1,370 1,4297 8063
632 Дипропилцианамид (C3H7)2NCN 24,4 0,857 1,4298 —
633 d-2-Нониловый спирт CH3CH(OH) (CH,)eCH3 20 0,8230 1,4299 5680
634 Этиловый эфир тр'иметил-акриловой к-ты (CH3)2C-C(CH3)COOC2HS 19,3 0,907 1,4299 —
635 Дотриаконтан CH3(CH2)»CH3 79,4 0,775 1,43 3568
636 2-Диметиламииоэтанол (CH3)2NCH2CH2OH 20 0,8866 1,43 9294
637 а-Кротоновая к-та (твердая) CH3CH = CHCOOH 72 0,96 1,43 4447
638 Аллил уксусная к-та CH2=CHCH2CH2COOH 17,7 0,984 1,43 1,43 6094
639 Азелаиновая к-та HOOC(CH2)7COOH 107,3 1,0 21
640 Пропионамид CH3CH2CONH2 20 1,042 1,43 6722
641 Октиламин CH3(CH2);NH2 26,8 0,777 1,430 5827
642 5-Ноииловый спирт (C4H9)2CHOH 20 0,823 1,430 5683
643 Нитрил Р-изобутнлакрило-вой к-ты (CH3)2CHCH2CH = CHCN 20 0,826 1,430 —
644 Моиоэтиловый эфир ди- этил ейгликоля C2H5O(CH2)2OCH2CH2OH 20 0,9902 1,4300 3524
645 Додецеи-1 CH3(CH2)9CH=CH2 20 0,75836 1,43002 355-5
646 Уидеканои-2 CH3CO(CH2)fCH3 17,3 0,8295 1,43002 8104
647 1, 2-Диметилциклогексаи (CH3)7CeHi9 17,9 0,78 1,4392 —г-
648 2-Метил пеитен-3-ол-2 CH3CH = CHC(OH)(CH3)2 20 0,8343 1,4302 6096
649 Оксим изомасляиого аль- (CH3),CHCH = NOH 20,5 0,902 1,43022 3764
650 дегида Пировиноградная к-та CHjCOCOOH 15,3 1,2668 1,43025 6313
651 Тетракозан CH3(CH2)22CH3 65 0,65077 1,43026 7326
834
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C 4 "о № по табл. «Свойства органических соединений»
сн3
652 2,6-Диметилоктеи-2 (CH3)2C=CH(CH2)2CHC2H5 20 0,75 1,4303
653 2,7-Диметилоктеи-2 (СН3)2СН(СН2)3СН= С(СН,)2 20 0,75 1,4304
654 Пальмитиновая к-та СНз(СН2)цСООН 70 0,8487 1,4304 5901
655 Диэтиловый эфир пиме-лииовой к-ты СН2(СН2СН2СООС2Н5)2 20 0,99 1,4395 6138
656 Триацетат глицерина (СН3СОО)3С3Н5 20 1,16 1,4306 2934
657 Пропаргиловый спирт СН^ССН2ОН 20 0,9715 1,43064 6707
658 dZ-3-Ноинловый спирт СН3С112СН(ОН) (СН2)5СН3 20 0,825 1,4308 5681
659 Миристиновая к-та СН3(СН2),2СООН 70 0,8533 1,4268 5158
660 Дециловый эфир масляной к-ты C2HsCH2COOCH2(CH2)sCHs 20 0,862 1,4308 —
661 транс-1, 3-Диметил циклогексан С«Н10(СН3)2 20 1,78472 1,43085 8918
662 2, 5-Диметилгексадиеи-1,5 [СН2=С(СН3)СН2]2 20 0,75 1,4309 —-
663 1, 2, 4-Триметил циклогексан Этиловый эфир Р-этил-акриловой к-ты (CHshCsHs 16,9 0,780 1,431 —
664 СН3СН2СН = CHCOOC2HS 20 0,909 1,431 —
665 Этиловый эфир ангеликовой к-ты С,Н,СООС2Н5 CH, 19,5 0,918 1,431 —
666 2, 5-Диметилгептанол-5 (СН3)2СН (СН2)2СОНС2Н, 20 0,829 1,4310 —
667 Нониловый спирт СНз(СН2),СН2ОН 20 0,8279 1,43П 1,4311 5678
668 Изопропилбутиловый эфир малоиовой к-ты СН2 (COOC.Hs) СООСзНу 20 0,97 —
669 Гексеи-2-ол-4 СН3СН=-СНСНОНС2Н, 25 0,841 1,4312 —
670 Трихлорпропилсилан CsH/SiCh 20,3 1,196 1,4312 —
671 Моноэтиловый эфир ме-тиляитариой к-ты СН,СН (COOC2HS) СН2СООН 20,2 1,098 1,4312 —
672 Циклопропилкарбинол СН2СН2СНСН2ОН 1 1 15,1 0,90 1,4313 —
673 Триэтилкарбииол (СН3СН2)3СОН 20 0,83892 1,4314 6057
674 а-Метилакриловая к-та СН2=С(СН3)СООН 20 1,0153 1,43143 4903
675 Метиловый эфир а-меток-сиакриловой к-ты СН2=С(ОСН3)СООСН, 20 1,068 1,4316 —
676 2-Нитро-2, 5-диметилгексаи (CH3)2C(NO2) (СН2)2СН(СН,), 20 0,921 1,4316
677 со, со-Диметилацетонилаце- (СН3)2СНСОСН2СН2 сосн3 23 0,934 1,4317 —
678 тон З-Метилоктанол-4 С2Н5(СН2)2СНОНСН(СН3)С2Н3 20 0,834 1,4317 —
679 Этиленгликоль СН2ОНСН2ОН 20 1,1088 1,43178 2852
680 I, 3, 5-Триметилциклогексан (СН,),С6Н9 13,1 0,778 1,4318 8923
681 2, 4-Диметилгепта иол-4 (СН3)2СНСН2СОН(СНз)СН2С2Н5 18 0,827 1,4318 —
682 Гептиловый эфир эн антовой к-ты СН3(СН2)5СООС7Н,5 18,8 0,865 1,4318 9116
683 Нитрил гексеи-З-овой-1 c2h5ch=chch2cn 20 0,841 1,432 —
684 к ты Этиловый эфир 2-метил-пентен-З-овой-5 к-ты (СН3)гСНСН = СНСООС2Н6 20 0,896 1,432 —
685 Метиловый эфир гидрак-риловой к-ты НОСН2СН2СООСН, 20 1,12 1,432 —
686 Метиловый эфир Р, Р-ди-метилакриловой к-ты (СН3)2С=СНСООСН3 19,8 0,934 1,4321
687 Монобутиловый эфир диэтиленгликоля (бутил-карбитол) Этиловый эфир лауриновой к-ты СНз(СН2)зО(СН2)2ОСН2СН2ОН 20 0,9553 1,4321 3520
688 СН,(СН2)10СООС2Н5 20 0,8615 1,4321 4632
689 Диэтилпропилкарбинол (CH.,CH,bC(OH)(CHo)2CH3 13 0,84 1,43216 2457
690 Ундециловый альдегид СИ3(СН2)»СНО 23 0,8251 1,4322 8115
691 3, 5-Днметилгептанол-4 [С2Н5(СН3)СН],СНО11 20 0,836 1,4322 —
692 Нитрозоэтилvpстаи C2HsN(NO)COOC2H£ 20 1,071 1,4322 —
693 Моиометиловый эфир метилянтарной к-ты СН3СН (СООСНз) СН2СООН 20,7 1,144 1,4323
53*
835
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула f, сс 4 "D № по табл» «Свойства органических соединений»
694 Этиловый эфир а-этокси- СН2 = С (ОС2Н5) СООС2Н5 17,2 0,996 1,4324
акриловой к-ты 18,.8 1,08 1,4326
695 Этилметилфуразан C2HsC=NON=CCH3 1 1
696 Этиловый эфир а, а-ди- СНзСОС (C2Hs)2COOC2Hs 17 0,971 1,4326 930
этилацетоуксусной к-ты 0,9822 1,43278 6412
697 Диэтиловый эфир пробко- [(СН2)2СН2СООС2Н6]2 20
вой к-ты 0,8328
698 2-Этил гексаиол-1 СН3(СН2)3СН (С2Н5) СН2ОН 20 1,4328 2447
699 бпс-Диэтил ацеталь [(С2Н5О)2СНСН2 26 0,953 1,4328 —-
700 Нитрил Р-этилакриловой C2HsCH = CHCN 20 0,828 1,433 —
к-ты 1,976 1,433
701 а, а-Диметил ангелика лак- СН3С = СНС(СН3)2СОО 20 —
той 1 1
702 у-Вал еролактон СН3СНСН2СН2СОО 1 1 22,4 1,050 1,4331 2260
703 Ундецен-2 СН3СН = СН(СН2)7СН3 15 0,774 1,4333 8107
704 Гексакозан СН3(СН2)24СН3 65 0,8 1,4333 —
705 Диметилдиэтиловый эфир С(СООСН3)2(СООС2Н3)2 17,2 1,183 1,4333 —-
метаитетракарбоновой
706 К-ТЫ Стеариновая к-та СНз(СН2)нСООН 70 0,847 1,4335 7122
707 Миристиновый ангидрид (С13Н27СО)2О 70 0,8502 1,433о 5168
708 Циклобутанол СН2СН2СН2СНОН 1 1 20 0,92 1,4335
709 Энантовый ангидрид [СН3(СН2)ЕСО]2О 15 0,94 1,4335 9115
710 Диэтиловый эфир ацетил- СН3СОС(С2Н3) (СООС2Н5)2 19,3 1,054 1,4338 —
этил малоновой к-ты 25,3 1,4339
711 1, 1, З-Триметилциклогек- (СН3)3С6Н9 0,787 —
712 сан Эйкозан СНэ(СН2)18СНз 42,9 0,77 1,434 9086
713 Этиловый эфир гексен-2- СН3(СН2)2СН = СНСООС2Н5 20 0,901 1,434 —-
овой-1 к-ты 20,5 0,999 1,434
714 Диэтиловый эфир гидразо- [HNC(CH3)2COOC2Hs]2 —
изомасляной к-ты 1,055 1,434
715 Амиловый эфир хлор- С1СН2СООС5НП 20 —
716 уксусной к-ты rfZ-Диэтилкетол СН3СН2СОСН (ОН)СНоСН3 21 0,9.56 1,4340 —
717 Дихлорангидрид щавеле- (СОС1)2 12,9 1,489 1,4340 9064
вой к-ты 26,8 0,923 1,4341
718 Гексилурстаи CcH13NHCOOC2H5 —
719 Бромистый пропил СН3(СН2)2Вг 20 1,3529 1,43414 6646
720 Тетраиитрометан C(NO2)4 21,2 1,6377 1,43416 5003
721 Маргариновая к-та СН3(СН,)15СООН 60 0,8578 1,4342 4773
722 2-Метилфуран (а-форма) осн-снсн=ссн3 1 1 20 0,913 1,4344 8566
723 втор-Бромистый бутил СН3СН2СНВгСН3 25,3 1,251 1,4344 2120
724 Гептакозан СН3(СН2)23СН3 65 0,77 1,4345 2566
725 3, 3, 4-Триметилгексанол-4 C2HsC(CH3)2COH(CH3)C2Hs 20 0,832 1,4345 •—
726 2-Мети л гексеи -5-ол-2 СН2 = СН(СН2)2СОН(СН3)2 16,2 0,838 1,4345 —
727 Диэтилизобутилкарбииол (С2Н5),С(ОН)СН,СН(СН3Ь 13 0,8 1,43457 ’ 2455
728 Бутироин CZH5CH2CH(OH)OCH2C2H5 16,7 0,911 1,4346 —
729 Октадекан СН3(СН2),еСН3 35,2 0,77 1,4349 5755
730 Пентаидиол-2, 4 СН3СН(ОН)СН2СН(ОН)СНз 20 0,9635 1,4349 —
731 Этиловый эфир триазо- N3CH2COOC2H5 24,9 1,13 1,4349 —-
732 уксусной к-ты Этиловый эфир а-этил- СНСН = С (С2Н5)СООС2Н5 20 0,908 1,435 —
кротоновой к-ты 0,913 1,435
733 Этиловый эфир Р, Р-ДНМ€- (СНзЪС - СНСООС2Н5 20 —
тилакриловой к-ты СН3СН = СНСОСН3 0,8624 1,4350 6100
734 Этилидеиацетон 20
735 Цикло-у-оксивалериановый СНоСНС1<СН2СН(ОН)О 20 1,019 1,4350 —
альдегид 1 1
Г Продолжение
о. о Е Название № по табл.
О С g Формула t, °C nD органических соединений»
736 Этилмеркаптан C2Hr,SH 25 0,83147 1,4351 9330
737 Пропилмеркаптан CH3(CH2)2SH 25 0,83572 1,4351 6582
738 Диэтиловый эфир хлор-малоиовой к-ты CICH(COOC2HS)2 19,3 1,205 1,4353
739 Октакозан 65 0,77 1,4354
740 Трипропилкарбииол (С3Н7)3СОН 21 0,834 1'4356 2601
741 Пеитеи-2-овая-5 к-та СН3СН=СНСН2СООН 18,8 0,99 1,4357
742 2-Нитро-2,7-диметилоктан (CH3)2C(NO2) (СН2)4СН (СН3)2 20 0,909 1,4357
743 Цетиловый эфир уксусной СН3СОО(СН2),ЕСН3 33,9 0,85 1,4358 7990
744 Трибутират глицерина C3HS(OCOC3H7)3 20 1,0350 1,43587 2937
745 Диэтиловый эфир себаци-иовой к-ты [(СН2)4СООСН2СН3]2 20 0,96461 1,43585 7013
746 Нонадекаи СН3(СН2),7СН3 34,6 0,775 1,436 5664
747 Этиловый эфир 2-метил-гексен-4 -овой-6 к-ты (СН3)2СНСН2СН = СНСООС2НЕ 20 0,889 1,436
748 Этиловый эфир тиглиио-вой к-ты СН3СН - С (СН3) СООС2Н5 19,5 0,924 1,436 -
749 Диэтнловый эфир тетра-метилянтариой к-ты [(СН3)2ССООС2Н5]2 20 0,995 1,436 —
750 Тетраэтиловый эфир метантетракарбоновой к-ты С(СООС2Нз)4 17 1,136 1,436 -
751 Бромистый изобутил (СНз)2СНСН2Вг 20 1,264 1,436 3634
752 Кротоновый альдегид СН3СН-СНСНО 20,5 0,852 1'4362 4457
753 Этиловый эфир миристиновой к-ты С13Н27СООС2Н5 20 0,8589 1,4362 5166
754 2-Хлорпропиловый спирт СНзСНС1СН2ОН 20 1,103 1,4362
755 Диэтнловый эфир С /-яблочной к-ты ,2НЕОСОСН(ОН)С Н2СООС2НЕ 20 1,1280 1,4362 9547
756 2, 5-Диметилфураи С4Н2О(СНз)2 20 0,888 1,4363 8560
757 Метилиитрозоуретан CH3N(NO)COOC2H5 20 1,122 1,4363
758 Нонакозан 65 0,77 1,4364
759 Этиловый эфир диаллил-уксусиой к-ты (СН2=CHCH2)2CHCOOC2HS 19,1 0,897 1Л364 —
760 Нитрил глутаровой к-ты CN(CH2)3CN 23,2 0,99 1,4365 2981
761 Тетрагидрофурфурол С4Н7ОСНО 20 1,0727 1,43658 8634
762 Брассидииовый ангидрид (QjHj.COhO 100 0,8 1,4366 1920
763 Цикловеитанои СН2(СН2)3СО I 1 20 0,9480 1,4366 8981
764 Триэтиловый эфир аце-тилметантрикарбоновой к-ты СНзСОС (СООС2Н6)з 13,5 1,128 1,4366 —
765 Оксим изовалерианового альдегида (CH3)2CHCH2CH = NOH 20 0,8934 1,4367 3686
766 rf-2-Уидециловый спирт CH3(CH2)sCH(OH)CH3 20 0,8270 1,4369 8103
767 Г Бром-2, 2-диметилпропаи (СН3)зССН2Вг 20 1,260 1,4369 6433
768 Амиловый эфир а-крото-новой к-ты СНзСН = СНСООС5Нц 20 0,896 1Л371
769 N. КГДиметилацет^мнд CH,CON(CH3)2 22,5 0,94 1,4371
770 Циклогексил амин CH2(CH2)4CHNH2 1 j 20 0,8191 1,43716 8956
771 Дециловый спирт СН3(СН2)8СН,ОН 20 0,8297 1,43719 3076
772 I, 2, 4, 5-Тетраметилцикло-гексан (СНз)4С6Нв 13,1 0,791 1,4372
773 Гевтен-2-ол-4 СН3СН = СНСНОНСН2С,НЕ 20 0,845 1,4373
774 Нитрил 2-метилпентен-З-овой-5 к-ты (CH3)2CHCH-CHCN 20 0,855 1'4374 —
775 Диэтиловый эфир ацетилмалоновой к-ты СН3СОСН (СООС2Н3)2 26 1,083 1,4374 4732
776 Диметил нитроза мин <ch3)2nno 18 1,0049 1,43743 3270
777 п-Дифторбензол CeH4F2 20 1,164 1'4375
778 1 уйан 20 0,814 1'4376
779 4-Метилгептеп-1-ол-4 СН2=СНСН2СОН (СН3)СН2С2Н5 21,3 0,834 1,4376 2613
836
837
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. 1 Название Формула t, °C nD № по табл. «Свойства органических соединений»
780 1, З-Диметил-5-циклогекси-ловый эфир уксусной CH3COOCeHs(CH3)2 20,2 0,928 1,4376 -
781 к-ты 1, 1, 1-Трихлорэтан CH3CC13 21 1,32 1,4377 9231
782 2, З-Диметилбутадиен-1, 3 СН2=С (СН 3) С (СН 3) = СН2 20 0,7264 1,437717 1947
783 4-Метилпиперидин ch2ch2nhch2ch2chch3 1 1 21,6 0,845 1,4378 6152
784 Диэтиловый эфир ацетон-дикарбоиовой к-ты СО(СН2СООСгНс)2 23,6 1,107 1,4378 —
785 Хлористый децил СН3(СН2)оС1 20 0,8696 1,43799 —
786 Пулеген с»н,6 22 0,791 1,4380 —
787 Ш-3,7-Ди метилоктанол-1 (СН3 )2СН (СН2)зСН (СН3)СН2СН2ОН 18 0,828 1,438 5814
788 Эпихлоргидрин ОСН2СНСН2С1 1 1 20 1,1801 1,438 9132
789 Диэтиловый эфир СГ ацетилянтариой к-ты эСОСН (СООС2Н5) СН2СО2С2Н5 16 1,109 1,438 9561
790 несылои-Метил ацетил ацетон СНЭСОСII (СНз) СОСНз 13,5 0,978 1,4380 —
791 п-Меитаи СНзС(,Н,оСН(СНз)2 20 0,793 1,4380 4876
792 Дипропиловый эфир /-яблочной к-ты С3НгОСОСН(ОН)СН2СООС3Н 20 1,0736 1,4380 9546
793 Диизоамилкарбинол f(CH3)2CH(CH2)2]2CHOH 12,6 0,8305 1,43801 5684
794 Трипальмитат глицерина (С15Нз1СОО)зСзНв 80 0,866 1,43807 2943
795 Изопропнлсульфид [(CH3)2CH]2S 20 0,8135 1,4381 3 801
796 Гексадиеи-2, 4 СНзСН = СНСН = СНСНз 20 0,7108 1,4384 2390
797 2-Метил а м и ноэтаиол CH3NHCH2CH2OH 20 0,937 1,4385 9300
798 Тристеарат глицерина (с,7НззСод)3СзН6 80 0,862 1,4385 2944
799 Изобутил меркаптан (CH3)2CHCH2SH 20 0,8357 1,4386 6583
800 Этиловый эфир днхлор-уксусиой к-ты СНС12СООС2Н5 20 1,2821 1,43860 8022
801 Диэтилиитрозамии (CH3CH2)2NNO 20 0,9422 1,43864 3509
802 1, 2-Дихлорпропаи СН2С1СНС1СН3 20 1,157 1,438 / 6451
803 2, 6-Диметилоктаиол-6 СНз)2СН(С112)зС(СНз)ОНС2Н5 15 0,836 1,4388 —
804 Этиловый эфир Ch аллил ацетоуксусной к-ты 13СОСН (СН2СН = СН2) СО2С2Н5 17,6 0,992 1,4388 —
805 Этиловый эфир итаконовой к-ты С2Н3ОСОС (= СН2) СН2СО2С2Нь 20,2 1,045 1,4388
806 2, 4-Диметилпеитадиен-1, 3 (СНз)2С=СНС(СНз) = СН2 23 0,734 1,4390 —
807 Циклопропанкарбоиовая к-та СН2СН2СНСООН 1 1 20 1,0885 1,43901 8992
808 Ундециловый спирт СН3(СН2)9СН2ОН 23 0,8334 1,4392 8102
809 Диизоамилцианамид [(CHa)2CHCH2CH2]2NCN 23,7 0,846 ],4392 —
810 1-Хлорп роп аиол-2 СН?С!СНОНСНз 20 1,114 0,792 1,43924 6567
811 тран с-п-М сита и СН3СсН,сСН(СНз)2 20 1,4393 4876
812 2-Метилгексеи-З-овая-I к-та C2H5CH=CHCH(CHjCOOH 20 0,942 1,4395 —
813 несимм-Этил ацетил ацетон СН3СОСН(С2Н5)СОСН3 16,9 0,956 1,4397 —
814 втор-Бутилнитроурегаи C4H9N(NO2)COOC2Hu 21,4 1,086 1,4397 —
815 Бромистый бутил СН3С1 |2СН2СН2Вг 20 1,299 1,4398 2119
816 Этиловый эфир а-мети л-0-оксикарбэтоксикрото-новой к-ты СН3С(ОСО2С2Н6) = ССО2С2Н3 1 сн. 20 1,078 1,4398
817 Триметилеигликоль НОСН2СН2СН2ОН 20 1,0597 1,43983 6521
818 Церотиновая к-та СН3(СН2)2)СООН 79 0,836 1,44 8853
819 Элаидиновая к-та СНз(СН2ЪСН = СН(СН2)7СООН 79,4 0,851 1,44 9100
820 Этиловый эфир 3-изопро-п нл -1 - метил циклопеи-танкарбоиовой-2 к-ты СН3С6Н7(СзН7) СООС2Н6 11,8 0,918 1,44
821 Тиглииовая к-та СНзСН = С(СНз) соон 76 0,964 1,44 7349
822 Гексеи-З-овая-1 к-та С.НзСН = СНСН2СООН 23 0,964 1,44 —-
823 у-Метилизоксазол CH3C==NOCH=CH | | 20 1,022 1,44
824 а-Метилизоксазол CH3C=CHCH = NO 1 L 20 1,023 1,44 —
838
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
I № по пор. 1 Название Формула t, °C 4 № по табл, «Свойства органических соединений»
825 dZ-Молочиая к-та СНзСНОНСООН 20 1,24 1,44 5185
«26 Изопропил циклогексан СзН.СеНи 20 0,80221 1,440087 8920
827 1,1 - Дихлорциклопроп аи С Н2С Н2СС1г 1 1 17,7 1,211 1,4402 —
828 2- И зобу тил амин оэта иол (tH3)2CHCH2NHCH2CH,OH 20 0,8818 1,4402 9299
829 ДиэтнловыЙ эфир изобути-рилмалоиовоЙ к-ты (СН3)2СНСОСН(СОбС2Н5)2 20 1,050 1,4403 —
830 Тетраэтиловый эфир оксалил метантрикарбоновоЙ к-ты С2НЕООССОС (СООСгНз), 15,5 1,167 1,4403 —
831 Трилаурат глицерина С3Н5 (OCOCj j Н23)з 60 0,8944 1,44039 2938
832 Гептадекаи СН3(СН2),5СН3 20 0,778 1,44052 2552
833 ДиэтиловыЙ эфир этили-деималоиовой к-ты СНзСН=С(СООСгН5)2 16,1 1,043 1,4408
834 <5 -Этокси- у-валеролактои с2нБосн,снсн2сн2сор 24,9 1,072 1,4408 —
835 Моиоэтиловый эфир фумаровой к-ты НООССН = СНСООС2Н5 83 1,115 1,4409 8547
836 1, 2, 3, 4-Тетрагидро-л«-кси- (СН3)2СбНя 20 0,798 1,441 —
837 €?/-Пентаидиол-1, 2 СН3(СН2)2СН(ОН)СН2ОН 20 0,980 1,441 6020
838 Аллилдиэтилкарбинол СН2 = СНСН2СОН(С2Н5)2 21,7 0,847 1,4410 2487
839 Диэтиловый эфир фумаровой к-ты (=СНСООС2Н5)2 20,4 1,052 1,4410 8546
840 Изоамилмеркаптан (CH3)2CHCH2CH2SH 20 0,83475 1,44118 2075
841 Гептии-1 СН=С(СН2)4СН3 20 0,7369 1,4412 2633
842 Дидециловый эфир [СН3(СН2)в]2О 20 0,819 1,4412
843 Бромистый изоамил (СН3)2СНСН2СН2Вг 20 1,215 1,4412 3596
844 Триформиат глицерина С3Н6(ОСОН)3 18 1,320 1,4412
845 Гексадиии-1, 5 СН^С(СН2)2С^СН 20 0,8049 1,4414 2395
846 Этиловый эфир диметил-оксамииовой к-ты (CH3)2NCOCOOC2Hs 22,5 1,074 1,4414
847 Диметнловый эфир малеиновой к-ты ( = СНСООСН3)2 19,9 1,151 1,441556 4706
848 ДиэтиловыЙ эфир малеиновой к-ты (=СНСООС2Н5)2 20,1 1,067 1,4416 4707
849 Метилдиаллилкарбииол (СН2=СНСН2)2СОНСН3 26 0,844 1,4417
850 Метиловый эфир втор-бу-тилнитрокарбамииовой C4H„N(NO2)COOCH3 23,3 1,125 1,4417 —
851 At-Дифторбеизол c6h4f2 22 1,172 1,4417
852 Гексаидиол-2.4 СН3СН2СН(ОН)СН2СН(ОН)СНз 21 0,9516 1,4418 ——
853 Цианамид CNNHi 48 1,073 1,4418 8870
854 dZ-Изокамфаи СЮН|8 67 0,82757 1,44186 3714
855 2-Хлорэтаиол С1СН2СН2ОН 20 1,1988 1,44189 9314
856 Тридекан СН3(СН2)„СН3 16,8 0,76 1,4419 7823
857 Гексадецен-1 CH3(CH2),SCH = CH2 20 0,7825 1,4419 —
858 Этиловый эфир Коненковой-! к-ты СН3(СН2)5СН = СНСООС2Н5 20 0,889 1,442 —
859 а, у-Диметилизоксазол CH3C=CHC(CH3)=NO 1 1 20 0,983 1,442 —
860 л«-Ментаи CH3C6Hl0CH(CHs)2 20 0,79 1,4420
861 2-Этилгексен-3-овая-1 к-та СН3СН2СН=СНСН(С2Нб) СООН 20 0,928 1,4421 ___
862 трет-Бромистый амил C2UsCBr(CH3)2 20 1,216 1,4421 —
863 p-Хлормасляиая к-та CH3CHC1CI |2СООН 19,9 1,186 1,4421 —.
864 Дециловый эфир каприновой к-ты CaHjgCOOCioHsi 20 0,859 1,4423 —
865 Этил сульф ид (C2H5)2S 20 0,8368 1,44233 9510
866 Диэтиладеталь гексилпро-пполового альдегида CH3(CH2)sC2=CCH(OC2He)2 12,1 0,881 1,4424
867 Диметиловый эфир /-яблочной к-ты CH3OCOCH(OH)CH2COOCH3 20 1,2334 1,4425 9545
868 1-Нитро-2, 7-диметил- (СН3)2СН(СН2)4СН(СН3) CH2NO2 октан | 21 0,925 1,4426 —
839
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула 6 °C 4 nD Ле по табл. «Свойства органических соединений»
869 а-Этилкротоновая к-та С Н3С Н - С (С2Н6) соон 56,1 0,948 1,4426 4455
870 Трикапронат глицерина (C„H1,COO)3C3HS 20 0,988 1,4427 —
871 Метил этил кетоксим CH3C(C2Hs)=NOII 20 0,9232 1,4428 2063
872 Тримиристат глицерина СзНб(ОСОС1зН27)з 60 0,8848 1,44285 2939
873 несимм - П роп ил а цетил а це -тон СН3СОСН(С3Н;)СОСН3 20 0,935 1,4429 —
874 Левулиновая к-та СН3СОСН2СН2СООН 17 1,143 1,4429 4638
875 1, 2, 4, 6-Тетраметилпипери-дин (CH3)4C5H7N 19,7 0,823 1,4430 —
876 Ш-1-Метил циклогексанон-3 СН3СН(СН2)3СОСН2 1 1 20 0,9136 1,4430 8942
877 Этиловый эфир а-этил-Р-оксикарбэтоксикрото-новой к-ты СН3С(ОСО2С2Н6) =ССО2С2Нь 1 С2Н5 20 1,056 1,4431 —
878 1, 3-Диметилциклогексанон-5 (СН3)2С6Н3О 1.8,2 0,896 1,4433 —
879 Изобутилнитроуретан C4H.,N(NO2)COOC2IIs 20,5 1,094 1,4433 —
880 p-Бромэтиловый эфир уксусной к-ты СН3СООСН2СН2Вг 20 1,462 1,4433 9289
881 Аигелнковая к-та СН3СН-С(СН3)СООН 47 0,983 1,4434 317
882 Циклобутанкарбоновая к-та СН2(СН2)2СНСООН 1 1 19 1,053 1,4434 —
883 2, 4, 6-Триметилпиперидин (CH:,)3C6H3N 19 0,830 1,4435 —
884 Дипропиловый эфир фумаровой к-ты (-СНСООС3Н7)2 20 1,022 1,4435 —
885 Этилментиловый эфир С2Н5ОС10Н19 17,1 0,86 1,4435 —
886 Этиловый эфир Р-ОКСИ- С карбэтоксикротоновой Н3С (ОСООС2Н5> - С НСО2С2Н5 20 1,093 1,4435 —
887 Диэтиловый эфир пропионилмалоновой к-ты C2HsCOCH(COOC2Hs)2 16,4 1,079 1,4436
888 Амил меркапта н CH3(CH2)4SH 20 0,857 1,44366 6068
889 2-Бутил аминоэтанол CH3(CH2)3NHCH2CH2OH 20 0,8907 1,4437 9290
890 Дипропиловый эфир малеиновой к-ты (=-СНСООС3Н7>2 20 1,029 1,4437 —
891 Лауролен СН2СН2СН(СН3)С(СН3)-С(СН3) 20 0,797 1,4438 —
892 Изоамилдихлорамин (CH3)2CHCH2CH2NC12 25,7 1,027 1,4438 —
893 Циклогексен СН2СН-СН(СН2)2СН2 1 1 25 0,80609 1,4438 8948
894 Ш-Пентандиол-1, 4 СН3СН(ОН)(СН2)2СН2ОН 16,8 0,996 1,44388 6021
895 1 -Метилциклогексанон-4 СН3СН(СН2)2СОСН2СН2 1 1 20 0,9138 1,4439 8943
896 Диизобутилнитрозамин [(CH3)2CHCH2]2NNO 21,2 0,892 1,4439
897 Пулен ен С9Н,« 23 0,803 1,444 —
898 Окись мезитила (СН3)2С-СНСОСН3 20 0,8539 1,444 4842
899 2-Этиламиноэтанол C2H6NHCH2CH2OH 20 0,914 1,444 9316
900 Бутилмеркаптан CH3CH2CH2CH2SH 20 0,8337 1,44402 2073
901 Камфолен С9Н|„ 20 0,803 1,4441 —
902 Диметиловый эфир итаконовой к-ты СН3ОСОС(-СН2)СН2СО2СН3 20 1,122 1,4441 —-
903 1, 1, 4-Триметилциклогек-сен-3 (СН3)3СбН, 23,2 0,802 1,4442 —
904 Ш-2-Бромоктан СН3СНВг(СН2)3СН3 25 1,0878 1,4442 —
905 1-Метил цикл огексен-3 СН3С6Н2 16 0,8 1,4443 8949
906 Ацетоксиметиленпинаколин (СН3)3ССОСН = СНООССН3 53,3 0,965 1,4443 ——
907 1, 2-Дихлорэтан СН2С1СН2С1 20 1,257 1,44432 9455
908 Бромистый амил СН3(СН2)4Вг 20 1,218 1,4444 249
909 1 -Этилпиперидин C2H5NCsHio 18,9 0,826 1,4445 6189
910 2-Метил гептен-2-он-б (СН3)2С-СН(СН2)2СОСН3 20 0,860 1,4445 2614
840
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
/7родолжение
№ по пор. Название Формула t, °C nD № по табл. «Свойства органических соединений»
911 Аллилдипропилкарбинол (С3Н7)2СОНСН2СН = СН2 19 0,845 1,4445 1,4446
912 Циклопентадиен-1, 3 сн=снсн-снсн2 1 1 19 0,80475 8968
913 Дипропнлнитрозамии (C3H7)2NNO 20 0,916 1,4446 3328
914 Трикапринат глицерина С3Н5(ОСОСдН19)з 40 0,921 1,4446 —
915 Днэтиловый эфир (а-хлор- C1CH2COCI1 (СООС2Н5)2 12,3 1,195 1,4446 —
ацетил)малоновой к-ты 0,797
916 Тетрагидромезитилен 1, 3, 5-(СН3)3С6Н, 21 1,4447 —
917 Дизтиловый эфир ИЗО- 1 СН3)2СНСН2СОСН(СООС2Н5)2 20 1,034 1,4447 —
вал ер ил малоновой к-ты
918 Этиловый эфир Р-ацет- СН3СООС(СН3)=СНСООС2Н5 20 1,060 1,4447 —
оксикротоновой к-ты
919 Циклогептан СН2(СН2)6СН2 1 1 20 0,8109 1,4449 8964
920 Нитрил нонен-2-овой-1 c£hI3ch=chcn 20 0,833 1,445 —
к-ты
921 2, З-Дихлор-2-метилбутан (CH3)2CCICHCICH, 18 1,06 1,445 —
922 Метилпропилкетоксим CH3CH2CH2(CH3)C = NOH 20 0,9095 1,4450 6059
923 Диэтиловый эфир н-бути- С2Н5СН2СОСН (СООС2НЕ)2 20 1,055 1,4451 —
рил малоновой к-ты
924 1,1-Диметилциклогексен-З (СН3)2ССН2СН -сн—СН2СН2 16,2 0,806 1,4452 —
925 Гераниолен С9Н,е 21,5 0,768 1,4453
926 1, 2. 3, 4-Тетрагидро-лч-кси- (СН3)2С6Н8 22,4 0,800 1,4453 —
лол
927 Этиловый эфир амилпро- СбНцС—ССООС2Н5 25 0,910 1,4453 —_
пиоловой к-ты
928 6-Метокси-у-валеролактон СН3ОСН2СНСН2СН2СОО 1 1 23,2 1,120 1,4453 —
929 1, 2, 3, 4-Тетрагидротолуол СН3С6Н9 20 0,805 1,4454
930 Дипропилкарбнмид (C3H7N = )2C 23 0,838 1,4454
931 Диэтилкетоксим (C2H6)2C = NOH 20 0,914 1,4454
932 а- М ети л - В -этил акроле и н С2Н5СН = С(СН3)СНО 20 0,856 1,4454
933 а- и (//-Диэтнловый С2Н5О2ССН(ОН)СН(ОН)СО2С2Н5 25 1,20 1,4454 2319, 2327
эфир винной к-ты
934 Этиловый эфир бутилнит- C4HsN(NO2)COOC2H5 20,7 1,099 1,4455
рокарбаминовой к-ты
935 Триэтиловый эфир лимон- С3Н4ОН(СООС2Н5)3 20 1,137 1,4455 —
иой к-ты
936 Цитронелл иловый эфир ук- CH3COOCwH,9 17,5 0,893 1,4456 __
сусной к-ты
937 d-3- Метил цикл огекса н он СН3СНСН2СО(СН2)2СН2 1 1 21 0,915 1,4456 8942
938 Тетрадекан СН3(СН2),2СН3 20 0,7645 1,4459 7303
939 1 ,2, 3, 6-Тетрагидро-п-кси- (СН3)2С6Н8 20 0,802 1,4459 —
лол
940 Триэтил фосфин (С2Н5)3Р 20 0,801 1,446 —
941 Метиловый эфир элаиди- С,7Н33СООСН3 25 0,8702 1,446 9102
новой к-ты
942 Ангидро-д-ацетобутиловый СН3С=СНСН2СН2СН2О 20 0,906 1,446 ——
спирт 1 1
943 Изокротоновая к-та СН3СН = СНСООН 19,6 1,026 1,446 3732
944 /-Линалиловый эфир ук- СН3СООС,оН17 20 0,8951 1,4460 7982
сусной к-ты
945 Метиловый эфир изобу- (CH3)2CHCH2N (NO2) СООСНз 21,9 1,135 1,4461 —
тилнитрокарбаминовой
к-ты 20,9 0,859 1,4462
946 несылш-Диаллилацетон (СН2=СНСН2)2СНСОСН3 —
947 Диметилнитрамин (CH3),NNO2 72 1,109 1,44622 3269
948 3. 5-Диметил-1-метилен- (СН3)2(СН2=)С6Н» 14,6 0,792 1,4463 —
949 циклогексан Изобутилсульф ид [(CH3)2CHCH2]2S 20 0,8262 1,4463 3660
841
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
Q. С Е о Е й Название Формула t, °C 4 „t nD Ns по табл. «Свойства органических соединений»
950 dZ-3-Пипеколин CH3CH(CH2)3NHCH2 24,3 0,8446 1,4463 6151
951 Дибутиловый эфир винной к-ты (CHOHCOOC.Hsh 20 1,090 1,4463 2315
952 1-Метилпиперидин C5H10NCH3 20 0,8207 1,4464 6176
953 <Д-2-Пипеколин СН2(СН2)зЫНСНСНз 1 1 23,6 0,8436 1,4464 6150
954 Этиловый эфир гексилпро-п иол о ВОЙ К-ТЫ CeHjsCsCCOOCaHs 25 0,903 1,4464 —
955 Гексеи-2-овая-1 к-та СНз(СН2)2СН=СНСООН 40 0,95 1,4466 2486
956 Диэтиловый эфир глута-коновой к-ты С3Н((СООС2НЕ)2 19 1,05 1,4466 —
957 2-Бромпропен СН3СВг=СН2 15,75 1,3965 1,44665 6599
958 Ментиловый эфир уксусной к-ты СН3СООСюН,9 20 0,919 1,4467 —
959 Тетроловый альдегид CHsC=sCCHO 17 0,927 1,4467
960 2, 4-Диметилпентадиен-2,4 (СНз)2С-СНС(СНз)-СН2 СНэС(ОС2Н5) = СНСООС2Н, 12 0,749 1,4468
961 Этиловый эфир 0-ЭТОКСИ-кротоиовой к-ты 37,6 0,966 1,4468 —
962 Диэтнловый эфир цитраконовой к-ты С НзС (COOC2Hs) = с НСООС2Н 20,3 1,062 1,4468 —
963 1, 2-Динитроэтан 5-Циано-2-метилгексен-4-овая-6 к-та 20 1,4597 1,4468
964 (CH3)2CHCH2CH=C(CN)CO2H 99,6 0,972 1,4469 —
965 Этиловый эфир а-бром-пропиоиовой к-ты СН3СНВгСООСН2СН, 20 1,394 1,4469 6763
966 З-Хлорпропиловый спирт С1СН2СН2СН2ОН 20 1,1309 1,44693 6556
967 О-Ментаи СИзС6Н|0СН(СНз)2 21 0,814 1,447 —
968 Хлорангидрид гексеи-3-овой-1 к-ты С2НзСН = СНСН2СОС1 20 1,014 1,447 —
969 0-Туйен 20 0,821 1,4471 —
970 Дипропнлкетоксим (C3H,)2C-NOH 24,1 0,888 1,4472 ——
971 Формамид hconh2 20 1,1334 1,4472 8444
972 Этиловый эфир 0-ацет-оксиакриловой к-ты СНзСООСН = CHCOOC2Hs 18,1 1,090 1,4474
973 Тиглиновый альдегид СНзСН = С(СНз)СНО 20 0,8710 1,4475 7350
974 Диэтиловый эфир диаллилмалоновой к-ты (CH2=.CHCH2)2C(COOC2Hs)2 17,2 0,996 1,4475 —
975 d-2-Бромоктаи СН3СНВг(СН2)зСНз 25 1,0982 1,4475 —
976 Диметиловый эфир цитраконовой к-ты СНзС(СООСНз)-СНСООСНз 20,1 1,12 1,4475 —
977 1, 1-Диметил циклогекса-иои-3 (СНз)2С(СН2)зСОСН2 1 1 18,6 0,907 1,4476 —
978 Бромистый гексил СНз(СН2)4СН2Вг 20 1,1763 1,44778 2407
979 Этиловый эфир 0-этокси-акриловой к-ты С2Н5ОСН-СНСООС2Нз 18,1 0,995 1,448 —
980 а-Цианоэиантовая к-та C2Hs(CH2)sCH(CN)COOH 20 1,022 1,448
981 Хлорангидрид пеитеи-3-овой-1 к-ты СНзСН-СНСН2СОС1 20 1,064 1,448 —
982 а-Ангеликалактон СН3С = СНСН2СОО 1 1 20 1,084 1,448 —
983 2,4-Диметилгексеи- (Cf 4-овая-6 к-та з)2СНСН2С(СНз) = СНСООН 15,8 0,936 1,4480 -
984 d-1, 4-Диметилцнклогекса-нон-2 (СНз)2С6НзСО 20 0,8985 1,44807 8940
985 Пропилсульфид (C3H,)2S 20 0,8358 1,4481 6685
986 Трикаприлат глицерина (С7Н,5СОО)зСзНз 20 0,954 1,4482 —
987 Пиновая к-та С9Н,(О4 109,4 1,093 1,4482
988 Этиловый эфир а, 0-дн-хлорпропионовой к-ты СН2С1СНС1СООС2Н5 20 1,246 1,4482 —
989 1, 1-Ди фтор-1, 2-дибром-этан CF2BrCH2Br 17,5 2,24 1,4482
842
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О с о к Название Формула Л °C 4 "d № по табл. «Свойства органических соединений»
99Э Этиловый эфир питроме-тилкарбамииовой к-ты CH3N(NO2)COOC2HS 23 1,229 1,4483 -
991 Метнл циклогекса нон-2 СН3СН(СН2)4СО 1 1 20 0,9250 1,4483 8941
992 Изобутилдихлорамин (CH3)2CHCH2NC12 24 1,090 1,4484
993 Триэтиловый эфир лимонной к-ты СзН<ОН(СООС2Н5)з 20 1,102 1,4484 —
994 Диэтнловый эфир О-карб-С этокси -р -оксиэтилиден -малоновой к-ты Н3С(ОСООС2Н3) = С (СО2С2Н3)2 20 1,127 1,4484 —
995 1, 1, 4, 4-Тетраметилцикло-гексанон-2 (CHshCsHeCO 14,3 0,893 1,4485 —
996 Ментиловый эфир изова-лериановой к-ты CisH2bO2 20 0,906 1,4485 —
997 Хлороформ СНС13 15 1,49845 1,44858 8789
998 Гептадиен-2, 4 CI-l3CH = CHCH-CHCH2CHs 21,5 0,7341 1,4486 2563
999 1, 1-Диметилциклогексанон-2 (СН3)2С6НВО 20 0,913 1,4486
1000 Диэтиловый эфир изопро-пилиденмалоновой к-ты (CHS),C=C(COOC2H5)2 17 1,028 1,4486 —
1001 Метиловый эфир бутил-нитрокарбаминовой к-ты C.HSN(NO.)COOCH3 22 1,139 1,4486 —
1002 Диэтиле н гл и кол ь (HOCH2CH2)2O 15 1,1197 1,4488 3516
1003 1, 1-Динитроэтан CH3CH(NO2)2 20 1,35 1,4488 9186
1004 Ацетонил ацетон (CH3COCH2)2 20 0,97370 1,449 2436
1005 Изогексиловый спирт (CH3)2CH(CH2)2CH,OH 20 0,8156 1,4490 6041
1006 Бромистый изогексил (CH3),CH(CH2)2CH2Br 20 1,168 1,4490 —
1007 транс-\, 2-Днхлорэтилен CHC1 = CHC1 15 1,265 1,4490 —
1008 Диэтиловый эфир мезаконовой к-ты CH3C (CO2C2H5) - CHCO2C2H5 20 1,047 1,4494 —
1009 2, 3, 4, 5-Тетр а гидротолуол CH3ctHs 20 0,810 1,4496
1010 Трнэтиловый эфир оксалил малоновой к-ты C2H5OOCCOCH (COOC2H3)2 16,1 1,160 1,4496 —
1011 2,6-Диметил- СН3СН = октадиен-2, 6 = С(СНз)(СН2)2СН = С(СНз)СНз 19 0,78 1,4497 5783
1012 Аллилтетрагидрофурфуриловый эфир C3H5OCH2C.H2O 20 0,975 1,4498 —
1013 Тетр а гидропсевдокумол (CH3)3CtH7 16,2 0,838 1,4499 —
1014 Пентанднол-1, 5 CH2(OH)(CH2),CH2OH 20 0,994 1,4499 6022
1015 Этилендиамин (гидрат) H2NCH2CH2NH2 • H2O 20,5 0,9634 1,44997 9460
1016 2, 6-Днметил-Зметилал-(СН3)1СНСН2СН = С(СНО)СН(СН3)2 гептен-3 17,4 0,854 1,45 —
1017 цис-Эруковая к-та СН3(СН2)2СН = СН(СН2)„СООН 55 0,860 1,45 9150
1018 2-Циано-1-метил- CH2CH2CH(CH3)CH(CN)CHCH(CH3)2 3-изопропил- J | циклопентан 16,2 0,881 1,45 —
1019 Брассидиновая к-та СН3(СН2)7СН==СН(СН2)П СООН 57 0,8585 1,45 1919
1020 Фенхоламид CioHigON 108,2 0,907 1,45 —-
1021 9-Ундеценовая к-та CH3CH=CH(CH2)ICOOH 24 0,907 1,45
1022 Циклопентилуксусная к-та ch2(Ch2)3chch-.cooh 1 1 18 1,022 1,45 —
1023 Гексанол-б-он-2 CH3COCH2(CH2)2CH2OH 20 0,990 1,450
1024 Диэтиловый эфир транс-гексагидрофталевой к-ты C6H10(COOC2H5)2 20 1,040 1,450 —
1025 1, 2, 4-Три метил циклогексанон-5 (CH3)3C6H7O 17,4 0,899 1,4501 —
1026 Этиловый эфир а-метил-p-этоксиакриловой к-ты C2H5OCH=C(CH3) COOC2I is 21,6 0,979 1,4501 —“
1027 Фенхилен (б-фенхен) C10H16 20 0,838 1,4502 ——
1028 Диэтиловый эфир днаце-тилмалоновой к-ты (CH3CO)2C(COOC2Hs)2 20 1,115 1,4502 —
1029 З-Метилгексен-З-овая-6 к-та CH3CH2C(CH3) = CHCH2COOH 20 0,966 1,4503 —
843
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула /, °C 4 "D № по табл. «Свойства органических соединений»
1030 Этиловый эфир тиоуксус-ной к-ты CH3COSCH2CH3 28 0,9755 1,4503 7425
1031 Бромистый ОКТИЛ СН3(СН2)еСН2Вг 25 1,10788 1,4503 5794
1032 симм-Диаллилацетон (СН2 = СНСН2СН2)2СО 14 0,868 1,4504 —
1033 Тетрагидрофурфуриловый спирт С4Н7О • СН2ОН 25 1,1326 1,4505 8623
1034 2-Метилгептен-2-ол-6 (СН3)2С = СН (СН2)2 СНОНСНз 20 0,854 1,4505 —
1035 /-Ментон (СН3)2СНСН (СН2)2СН (СН3) СН2СО 20 0,8954 1,4505 4894
1036 2, 6-Диметилгептен-2-ол-6 (СНз)2С-СН(СН2)2СОН(СНз)2 20 0,855 1,4506
1037 p-Изопропилакриловая к-та (СНз)2СНСН = СНСООН 16 0,96 1,4506 6093
1038 Метиловый эфир а-бром-пропионовой к-ты СНзСНВгСООСНз 20 1,492 1,4506 —
1039 Этиловый эфир трихлоруксусной к-ты СС1зСООС2Нз 20 1,383 1,45068 8056
1040 Циклогексанон СО(СН2)4СН2 1 1 20 0,9478 1,4507 8939
1041 Диаллил уксусная к-та (СН2=СНСН2)2СНСООН 21,6 0,947 1,4508
1042 1,2-Диметилциклогекса-нон-4 (СНз)2С5НзСО 12,6 0,912 1,4509
1043 Метиловый эфир амилпро-пиоловой к-ты СзНцС=ССООСНз 12,3 0,934 1,4509 5845
1044 Диэтиловый эфир метил-(ацетокси) метиленмалоновой к-ты ЗНзСООС(СНз) = С(СООС2Нз)2 17,7 1,117 1,451 —
1045 Ацетоназии (CH3)2C-NN=C(CH3)2 25 0,8381 1,45102 885
1046 Метилгексилкетоксим CH3C( = NOH)CcNi3 20 0,886 1,4511
1047 а-Этилкротоновая к-та CH:,CH = C(C2Hs)COOH 20 0,976 1,4511 4455
1048 Хлорангидрид р-хлормас-ляной к-ты CH3CHC1CH2COCI 20 1,217 1,4511
1049 d-Кониии CsHzCoHicN 21,9 0,84 1,4512 4304
1050 Апоциклеи 40 0,871 1,4514
1051 цц<?-п-Ментан CH3C6HioCH(CH3)2 20 0,816 Ц4515 1,4515 4876
1052 а-Туйен CioH]6 20 0,830 —
1053 Метилэтилкетазии [CH3(C2H5)C = N]2 26,6 0,834 1,4516 —
1054 Гександион-2, 4 C2H5COCH2COCHs 20 0,959 1,4516 —-
1055 Этиловый эфир циклопентанол-1-карбоновой-1 к-ты CH2(CH2)3COHCOOC2H5 ! 1 16 1,060 L4516 —
1056 2-Бром-2, 3-диметилбутан (CH3)2CHCBr(CH,)2 20 1,177 1,4517 —
1057 Метиловый эфир гексил-пропиоловой к-ты СсН13С—CCOOCH3 12,5 0,924 1,4518
1058 Этиловый эфир Р-амнл- -p-этоксиакриловой к-ты C!H,1C(OC2H5) = CHCOOC2H5 23,2 0,931 1,4518 —’
1059 1, 1, 3, З-Тетраэтилцикло-бутаидион-2, 4 (C2HshC2(CO)2 17,8 0,946 1,4518 —
1060 Ацетилацетон СНзСОСН2СОСНз 18,5 0,977 1,4518 6029
1061 цис-1, 2-Дихлорэтилен 1, З-Диметилциклогекса-нон-2 CHC1=CHC1 15 1,2913 1,45189 —
1062 (CH3)2CeHBO 11,9 0,92 1,4519 —
1063 Этиловый эфир циклогек-сапкарбоновой к-ты СсНцСООСгНй 16 0,962 1,452
1064 Триметил изоксазол N-C(CH3)C(CH.,)-C(CH,)O 1 1 CH3 20 0,981 1,452
1065 ДиэтиловыЙ эфир цис- Р-метилглутаконовой к-ты C2HSO2CCH = CCH2CO2C2H5 20 1,034 1,452 —
1066 Диэтиловый эфир транс-Р-метилглутаконовой к-ты C2H5O2CCH = CCH2CO2 C2Hs 1 CH3 20 1,034 1,452
844
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C 4 "o № по табл. «Свойства органических соединений»
1067 Диэтиловый эфир цис-\, 3-цнклогександикарбоно-ВОЙ К-ТЫ 1, 3-С6Н10(СООС2Н5)2 20 1,045 1,452 —
1068 Диэтиловый эфир цис-1, 4-циклогександйкарбоно-вой к-ты 1,4 Сг,Н,0(СООС2Н5)г 20,6 1,052 1,452 —
1069 Циклогексанкарбоновая к-та СН2(СН2)4СНСООН 38 1,0251 1,4520 8931
1070 Диметиламид хлормуравьиной к-ты ClCONfCHsh 22,1 1,166 1,4520 —
1071 Циклофен хеп C10H16 20,4 0,859 1,4521
1072 dZ-Ментон CioHisO 20 0,898 1,4521 ——
1073 Бутиловый эфир СНз олеиновой к-ты (СН2)7СН-СН(СН2)7СО2С1Н9 20 0,864 1,4522 5849
1074 р-Туйон CjoHicO 17,6 0,92 1,4522 — ™
1075 Пропилфурфуриловый эфир Этиловый эфир а-нзопро-пилиденацетоуксусной к-ты С2Н5СН2ОСН2С<Н3О 20 0,966 1,4523 —
1076 СН3СОС(СООС2Н5) = С (CH3)2 19,9 1,001 1,4523 —
1077 11зоамилсульфид [(CH3)2CH(CH2)2]2S 20 0,84314 1,45238 3621
1078 d-n-Ментен-З A3-«-CH,CfHBCH(CHs)2 20 0,8122 1,4524 4883
1079 2-Метилгексен-4-овая-6 (CH3)2CHCH2CH = CHCOOH 20 0,942 1,4524 3696
1080. к-та Этиловый эфир а-цианокротоновой к-ты CH3CH = C(CN)COOC2H6 20 1,024 1,4525 —
1081 Пропилдихлорамин C;H:CII,NCI2 23 1,145 1,4525 ——
1082 2-Нитро-2, 6-диметилгеп-тан (CH3)2C(NO,)(CH2)3CH(CHs)2 18 0,915 1,4526 —
1083 Оксиметилеипинаколин (С Нз)зССОСН=С нон 20 0,935 1,4527 —
1084 Метнленциклогексан С„2=С(СИ2)1СН2 1 1 20 0,803 1,4528 —
1085 Этиловый эфир а-этили-денацетоуксусной к-ты CH3COC(COOC2Hi.) =СНСНз 18 1,023 1,4528 —
1086 Этиловый эфир 2-циано-пентеи-2-овой-1 к-ты C2HsCH = C(CN)COOC2Hs 20 1,000 1,4529 —
1087 Дизтиловый эфир транс-гекса гидрогомофтал е-вой к-ты C6H,o(COOC2H5)CH2COOC2Hs 20 1,038 1,453
1088 Этиловый эфир р-ацетил-акрлловой к-ты CH3COCH = CHCOOC2H5 20 1,037 1,453 —
1089 ДиэтиловыЙ эфир цис-гск-сагидрофталевой к-ты CeH,o(COOC2H5)2 20 1,054 1,453 —
1090 Этиловый эфир транс-$-метил -а- этилглутаконовой к-ты C2H5C(COOC2II5) = C(CH3) CH2 C2H5OOC 20 1,014 1,453
1091 Этиловый эфир «-хлоризо-крото И О вой к-ты CH3CH=CC1COOC2HB 20 1,100 1,453 —
1092 Этиловый эфир’ а-хлор-кротоновой к-ты CH3CH = CClCOOQHs 20,1 1,108 1,453 —
1093 Пиперидин CH2(CH2)4NH 1 1 20 0,8606 1,4530 6166
1094 а-TviioH CioHieO 20 0,913 1,4530 7944
1095 Эти юзый эфир (этилокс-имияо)-циануксусной к-ты NCC(=-NOC2H5)COOC2H6 20 1,082 1,4530 —
1096 транс-1-Метил циклогскса-нол-4 СНзСбНюОН 20,7 0,9118 1,45307 8938
1097 dZ-3-Этнл пиперидин c-h5c5h9nh 23,2 0,857 1,4531 6191
1098 2 - Мстил -а- пи р а н CH3CHCH = C1ICH=CHO 1 1 20 0,917 1,4532
1099 Циклопеитанкарбоновая к-та CH2(C11.)3CHCOOH 1 1 20 1,053 1,4532 —
845
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула /, °C ”d № по табл. «Свойства органических соединений»
псо Петрозелиновая к-та СИ 3(СН2)19СН = СН(СН2)4СООН 40 0,870 1,4533
1101 1. 1-Диметилциклогекса- (СН3)2С6Н3О 24,2 0,928 1,4533 —
1102 нон-4 2-Бромнонан СН3(СН2)6СНВгСН3 20 1,081 1,4536
1103 1, 3, 5-Триметилциклогекса- (CHS)3C6HSOH 16,3 0,888 1,4537 —
1104 нол-1 1-Хлор-1, 4-ди метил цикло- (СН3)2С6Н9С1 18,5 0,944 1,4537 —
1105 гексан Бромангидрид уксусной СНзСОВг 15,8 1,663 1,4537 786
1106 к-ты Изобутиловый эфир рици- НОС|;Н32СО2С4Н9 22 0,9028 1,4538 6911
1107 нолевой к-ты Недокись углерода ос=с=со 0 1,114 1,4538 5620
1108 Этаноламин NH2CH2CH2OH 20 1,022 1,4539 9285
1109 Гептадиен-1.5-ол-4 СН2=СНСН2СНОНСН = СНСНз 20 0,861 1,454 —
1110 Нонен-2-овая-1 к-та СН3(СН2)6СН=СНСООН 20 0,930 1,454 —
1111 Р-Этилакриловая к-та С2Н5СН = СНСООН 14,7 0,992 1,454 —•
1112 Диэтиловый эфир цис- СН3С(СООС2Н3)-С(СН3) сн2 20 1,024 1,454 —
1113 а, Р-диметилглутакоио-вой к-ты Диэтиловый эфир СНзС(С( С2Н5ООС )ОС2Н5) = С(СН3)СН2СООС2Н5 20 1,031 1,454
1114 транс-а, р-диметилглу-таконовой к-ш Диэтиловый эфир цис- С6Ню(СООС2Н6)С H2COOCjH5 20 1,040 1,454
1115 гекса гидрогомофталевой к-ты цис-1, 3-Диметилциклогек- (СН3)2СеН9ОН 20 0,911 1,4540
1116 санол-5 Этилендиамин (безводн.) h2nch2ch2nh2 26,1 0,8919 1,45400 9459
1117 ^пс-Метилциклогексанол-3 CH3CSH19OH 21,8 0,9173 1,45403 8937
1118 1, 3-Ди метил циклогексанол (СН3)2С6Н9ОН 22,9 0,903 1,4541 —
1119 Этиловый эфир Р-хлор- CH3CCI-CHCOOC2Hs 18,7 1,092 1,4542 —
1120 изокротоновой к-ты Этиловый эфир бромуксус- BrCH2COOC2H5 13 1,514 1,45420 8006
1121 ной к-ты 7-Метилоктадиен-2, 4 С9Н16 18 0,7521 1,4543 5784
1122 ццс-1-Метилциклогекса- СН3С6Н10ОН 21,5 0,9129 1,4543 8938
1123 нол-4 Этиловый эфир СН (СН2),СН = С Н (СН2) 11СО2С2Н5 20 0,865 1,4543 —
1124 эруковой к-ты Линалиловый эфир уксус- СН3СООС]оН17 21 0,895 1,4544 7982
1125 ной к-ты 1, 1, З-Триметилциклогек- (СН3).С6Н,О 19 0,902 1,4545 —
1126 санон-4 Диэтиловый эфир транс- С8Н|4(СООС2Н5)2 21,6 1,029 1,4545 —
1127 /-камфорной к-ты Р-Метил-а-ангеликалактон СН3С = С(СН3)СН2СОО 1 1 20 1,056 1,4545 -
1128 1-Бромпропен-1 (р-форма) СН3СН = СНВг 15,8 1,417 1,4549 6598
1129 Метиловый эфир [3-амил-р- С6Н„С (ОСН3) =снсоосн3 23,1 0,961 1,4549 —
изо метоксиакриловой к-ты Этиловый эфир (СЕ 3)2СНСН2СН= C(CN)COOC2Hj 20 0,966 1,4549 —
1131 2-циано-5-метилгексен-2-овой-1 к-ты транс-1 -Метил циклогекса- CHjCsHwOH 21,8 0,9145 1,45497 8937
1132 нол-3 2, 6-Диметилокта- (СН3)2< 3 = СН(СН2)2СН(СН3)СН = СН2 20 0,788 1,455 —
1133 диен-2,7 1 d-Цитронеллаль СН2=С(СНз) (СН2)3СН (СНз)СН2СНО 1 .или 1 (CH3)2C = CH(CH2hCH(CH3)CH2CHO 1 14 0,86 1,455 9047
846
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О
j № по пор. Название Формула t, °C "D № no nop. «Свойства органических соединений»
1134 1, 4-Диметилцикло-гексанол-3 (СН3)2С„Н9ОН 16 0,907 1,455 -
1135 Диэтиловый эфир цис* -р-метил-а-этилглута коновой к-ты С2Н5С(СООС2Н5) -С(СН3)СН2 С2Н5ООС 20 1,019 1,455 —
1136 1-Хлор-1, 3, 5-триметилциклогексан (СНз)3СбНвС1 20 0,929 1,4550 —
1137 Р-Бромэтиловый эфир уксусной к-ты СН3СООС2Н4Вг 20 1,514 1,4550 —
1138 Бромистый децил СН3(СН2)9Вг 20 1,0683 1,45504 —
1139 Циклогептен СН-СН(СН2)4СН2 1 1 20 0,8228 1,4552 8967
1140 2-Изобутилпиперидин C4H9CH(CH2)4NH 1 1 21,7 0,851 1,4553 -
1141 Нитрил амилпропиоловой к-ты C5Hn№CCN 13 0,851 1,4553 —
1142 Карвоментои (СН3) (CsH,)CeH,O 20 0,9 0,906 1,4553 1,4553 —
1143 1, 4-Диметилциклогексанол (СН3)2СВН9ОН 23,9 —
1144 1-Бромпропен-1 (а-форма) СН3СН = СНВг 20 1,428 1,4554 6598
1145 2, 6-Диметилоктен-2-ол-6 (СН3)2С = СН(СН2)?СОН (СНз)С2Нк 15,9 0,858 1,4555 —
1146 Этил-^-борннловый эфир C2HSOC10H17 24,7 0,9 1,4555 —•
1147 Цитронеллиловый эфир муравьиной к-ты HCOOC.oHis 20 0,884 1,4556 —
1148 Триэтиловый эфир аконитовой к-ты С3Нз(СООС2Н5)з 20 1,106 1,4556 —
1149 Олеиновый альдегид СпНззСНО 20 0,85 1,4557 —
1150 Диметиловый эфир мезаконовой к-ты СНзС(СООСНз) = СНСООСНз 19,9 1,121 1,4557 —
1151 Хлораль СС1зСНО 20 1,512 1,45572 8772
1152 Метиловый эфир СБ эруковой к-ты з(СН2)7СН -СН (СН2) И СО2СНз 20 0,870 1,4558 —-
1153 Диэтиловый эфир d-камфорной к-ты С8Н14(СООС2Н6)2 19,1 1,032 1,456 —
1154 1, 1, 2-Триметилциклогек-сен-2 (СН3)3СВН7 20,4 0,822 1,4560 —
1155 1, З-Диметилциклогексанол-5 (СН3)2СВН9ОН 18,6 0,900 1,4560 —
1156 2- (Хлорметил)тетра гидрофур а и С4Н7ОСН2С1 20 1,110 1,4560 8570
1157 Триолеат глицерина (СпНззСОО)зСзНб 60 0,9 1,4561 2942
1158 N-Нитрометилизобутил- (CH3)2CHCH2N(NO2)CH3 22,5 1,021 1,4561 —
1159 Диэтил овый эфир оксиметиленмалоновой к-ты НОСН = С(СООС2Н3)2 14,3 1,128 1,4561 —
1160 2, З-Дибромбутен-2 CH3CBr = CBrCH3 25,5 1,318 1,4562 —
1161 Бромметилметиловый эфир BrCH2OCH3 20 1,598 1,4562 —
1162 d-Карвоментен СН2СН2С(СН3)-СНСН2СНСН(СНз)2 18 0,8246 1,4563 4246
1163 N-Нитрометилбутиламин CH3N(NO2)C4H9 23,6 1,023 1,4563 —
1164 V-Окснкротоиолактои CH2CH=CHCOO 1 1 99,3 1,262 1,4563 —
1165 Метиловый эфир а-хлор-кротоновой к-ты CH3CH = CC1COOCH3 22,6 1,159 1,4563 —
1166 Нитрил гексилпропиоловой к-ты CeHi3CsCCN 14,4 0,849 1,4564
1167 б-Ацетил-р. р-диметилва-лериановая к-та CH3CO(CH2)2C(CH3)2CH2CO2H 20 1,032 1,4564 —
1168 Бутиловый эфир рициио-левой к-ты CH3(CH2)5CH(OH)CH2CH II C4H9OOC(CH2);HC 22 0,9058 1,4566 6909
847
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
с£ о О Е £ Название Формула t, °C "о № по табл. «Свойства органических соединений»
1169 Этиловый эфир 5-окси-1,3* диметилциклогексил-5-ук- (СН3)2С6Н,(ОН) СИ2СООС2И5 14,9 0,990 1,4566 -
СУСНОЙ к-ты
1170 Дифосген С1СООСС1, 22 1,65 1,4566 3473
1171 1 -Этил циклогексен-1 С2Н5С = СН(СН2)3СН2 19,1 0,824 1,4567 —
1172 Каран СюН18 20 0,838 1,4567 —
1173 Метиловый эфир цикло- СН2(СН2)3С(ОН)СООСН3 17 1,105 1,4567 —-
пентанол-1-карбоновой-1 1 1
1174 к-ты Тетраэтиловый эфир ди- (С1Н5ООССО)2С(СООС2И5)2 14,9 1,193 1,4567 —
оксалил малоновой к-ты 1,4568
1175 4-Пропилгепта- СН2=СНСН2)2С(ОН)СН2С2Н5 21,1 0,865
1176 днен-1, 6-ол-4 2-Хлорфуран С«Н3ОС1 20 1,1923 1,45687 1,457 8573
1177 транс-1, З-Диметилцнкло- (СН3)2С„НвОН 16 0,902
1178 гексанол-5 2-Метилфуран (форма 11) С4Н3ОСН, 18 0,9406 1,457 1,457 8566 1868
1179 р, Р-Дихлор диэтиловый (С1С2Н4)2О 20 1,222
1180 эфир Метил фурфуриловый эфир С4Н3ОСН2ОСН3 20 1,0163 1,4570 1,4570 5137
1181 Метиловый эфир р-бром- ВгСН2СН2СООСН3 20 1,519
пропионовой к-ты 1,4571
1182 2, 2. 5, 5-Тетраметилцикло- (СН3)4С6Н7ОН 30,2 0,894
гексанол 1,4571
1183 N - Нитрометилэтнл амин CH3N(NO2)C2Hs 19,2 1,097
1134 Этиловый эфир а, а- (СН 2-СНСН2)2С(СОСН3)СО2С2Н5 17,4 0,982 1,4572
1185 диаллил ацетоуксусной
к-ты Изокамфан (форма I, CjqHis 20 0,8524 1,45733 3714
1186 жидк.) Этиловый эфир 1,3-диме- (СН3)2С6Н8=СНСООС2Н3 20,3 0,937 1,4575 —
т ил циклогексил и дену к-сусной-5 к-ты 1,4576
1187 /-Цитронеллол CtoH?oO 18 0,859 7930
1188 Т риэтиленгликоль (СН2ОСН2СН2ОН)2 15 1,1274 1,4578
1189 Диэтиловый эфир хлор- С1С(СООС2НГ.) -СНСООС2Н5 18,3 1,19
1190 фумаровой к-ты Бромангндрид пропиоио- СН3СН2СОВг 16,4 1,5210 1,45783 6726
вой к-ты 1,4579
1191 а-Окси мети лен диэтилкетон С2Н5СОС(СН3) -снон 48,9 0,965 4892
1192 /-Ментол СН3С6Н0(ОН)СН(СН3)2 25 0,88 1,458
1193 1, 2-Диметилциклогекса- (СН3)2С6Н8ОН 16 0,907 1,458
1194 нол-4 1, З-Диметилциклогекса-иол-4 (СН3)2С6Н8ОН 16 0,912 1,458 1,458 —
1195 Этиловый эфир 1,3-диме- (CH3)2CcH7CH2COOC2Hs 20,3 0,938
тилциклогексеи-4-ил-
1196 5-уксуспой к-ты /-З-Метилциклогексанол СНзСбН.оОН 20 0,914 1,4581 8937
1197 N-нитро-втор-бутиламин C2HeCH(CH3)NHNO2 21,9 1,057 1,4581 8786
1198 Хлоропрен СН2=СНСС1=СН2 20 0,958 1,4583
1199 2-Бромбутен-2 СН3СН=СВгСН3 25,4 1,322 1,4583
1209 Цинеол CioHjgO 20 0,927 1,4584
1201 1202 1, 2, 4-Триметилциклогекса-нол-5 (СН3)3С6Н,ОН 19,2 0,899 1,4585
Циклооктан СН2(СН2)6СН2 1 1 20 0,839 1,4586
1203 3, 4, 5, 6-Тетрагидро-о-кси- (СНз)2СсНз 20 0,823 1,4587 —
1204 Этиловый эфнр брассиди- СаН|7СН = СНСпН72СООС2Н5 35 .... 1,4587 —
1205 новой к-ты 1. 2, 4. 5-Тетраметилцикло- (СП3)4С6Н6 16,5 0,820 1,4588 —
1206 гексен-1
Метиловый эфир рицино- НОСнНззСООСНз 22 0,924 1,4388 —
левой к-ты
848
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула /, °C "d № по табл. «Свойства органических соединений»
1207 Р-Амил-Р-метоксиакрило-вая к-та С6НпС(ОСНз) =снсоон СНз 60,8 0,969 1,4588 —
1208 Метиловый эфир 1,4-диме-тилциклогексен-3-карбо-новой-1 к-ты ЗН2СН-С(СН2)2С(СН3)СО;СН, 1 20 0,970 1,4588 —
1209 Этиловый эфир диазо-уксусной к-ты И2СНСООС2Н5 17,6 1,0852 1,4588 8011
1210 1. 1-Диметилциклогекса-нол-3 (СН3)2СеН9ОН 19,7 0,909 1,4589 —
1211 3. З-Дихлорпентандиои-2, 4 СН3СОСС12СОСН3 16,8 1,307 1,4589 —
1212 Этиловый эфир р-хлоркро-тоновой к-ты CH3CC1 = C1ICOOC2HS 19,6 1,106 1,459 —
1213 Метиловый эфир метил-оксиминоциануксусной к-ты NCC(=NOCH3) СООСНз 20 1,177 1,4591
1214 N-Нитрогексиламин C2Hs(CH2)3CH2NHNO2 25,2 1,004 1,4593 —
1215 1. 1-Дииодгептан CH:,(CH2)SCHJ2 20 1,4 1,4594
1216 1» 2, 4, 5-Тетраметилциклогекса иол-1 (CH3)4CeH7OH 18,1 0,898 1,4595 —
1217 Гексилпропиоловая к-та C6H,3C=CCOOH 25 0,944 1,4596
1218 Триформальпропиламин (H2C = NC3H7)s 18,8 0,880 1,4597 ——
1219 Дииитрил адипиновой к-ты (CH2CH2CN)2 20 0,950 1,4597 —
1220 V, у-Дихлоркротоновая к-та C12CHCH=CHCOOH 99,4 1,333 1,4597
1221 Кадаверин H2N(CH2)5NH2 16 0,88 1,46 3941
1222 Циклогексилуксусиая к-та CH2(CH2)3CH2CHCH2COOH 1 1 33,5 1,001 1,46 —
1223 Р-Ангеликалактон CH3CHCH=CHCOO 1 1 20 0,967 1,460 —
1224 Метиловый эфир акриловой к-ты (жидкий полимер) (CH2 = CHCOOCH3)n 20 0,950 1,4600 104
1225 Борниловый эфир изовалериан овой к-ты (CH3)2CHCH2COOC10H„ 22,2 0,95 1,4600 —
1226 Хлорангидрид сс-кротоио-вой к-ты CH3CH=CHCOCI 17,9 1,09 1,4600
1227 Днэтиловый эфир тио-угольной К-тЫ CS(OC2Hs)2 17,5 1,027 1,4601 —
1228 Диэтиловый эфир (а-бромацетил) -малоновой к-ты BrCH2COCH (COOC2H5)2 18,1 1,391 1,4602
1229 /-Неоментол слон 20 0,900 1,4603 —
1230 Этиловый эфир а-пропио-а-циануксусной к-ты C2HSCOCH (CN )COOC2H5 20 1,076 1,4603 —
1231 Триформальэтнламин (НСН-ЭД1;)., 20,2 0,894 1,4604 —
1232 N-Нитробутиламин CH3(CH2)2CH2NHNO2 23 1,058 1,4604 —
1233 /-Линалоол C.oHhOH 20 0,8622 1,4604 4673
1234 Этоксиметил енпн на кол ни (CH3)3CCOCH = CHOC2HS 14,2 0,916 1,4605 ——
1235 Z-Ментил а мин C10H19NH2 20 0,860 1,4606 —
1236 Этиловый эфир а-изобути-ро-а-циануксусной к-ты (CH3)2CHCOCH(CN)COOC2H5 20 1,054 1,4606 —
1237 т-Фенхен 20 0,8539 1,46063 —
1238 у-Коиицеин CH3(CH2)2C^CHCH2CH2CH2NH 18,4 0,875 1,46068 4314
1239 Ч«с-Октадецен-9-ол-1 CHS(CH2),CH-=CH(CH2)7 СН2ОН 20 0,8489 1,4607 5770
1240 Циклогептанон CH2(CH2)5CO 1 1 20 0,9508 1,4608 8966
1241 Хлорпикрин CCI no2 22,8 1,651 1,4608 8793
1242 Пииокамфан CjoHis 20 0,855 1,4609
54 Зак. 783
849
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула /,°с 4 nD № по табл. «Свойства органических соединений»
1243 Циклогексанол СН2(СН2)4СНОН 1 1 37 0,9 1,461 8933
1244 Хлор ангидрид 2-метилгек-сен-4-овой-6 к-ты (СН3)2СНСН2СН-СНСОС1 20 0,991 1,461 -
1245 Нитрил 1-метилциклогек- санон-2-карбоновой к-ты CH3(CN)C6H8O 20 1,015 1,461 —
1246 Хлорангидрид 2-метилпеи-тен-З-овой-5 к-ты (С Н3) 2С НСН = С НСОС1 20 1,018 1,461 —
1247 гракс-1-Метилциклогекса-нол-2 СНзСвНюОН 20 0,9238 1,4611 8936
1248 1. I Диметилциклогексанол-4 (СН3)2СбН»ОН 24,7 0,922 1,4613 —
1249 Этиловый эфир а-бутиро-а-циануксусной к-ты C2HsCH2COCH(CN)COOC2Hs 20 1,056 1,4614 —
1250 3, 4, 5. 6-Тетрагидрокумол (СН3)2СНС = СН(СН2)3СН2 1 1 15,2 0,83 1,4615 —
1251 N-Нитрометиламин CH3NHNO2 49 1,243 1,4616
1252 Дихлорангидрид малоиовой к-ты Н2С(СОС1)2 22,1 1,449 1,4617 —
1253 Этиловый эфир рицинолевой к-ты НОСПН32СООС2Н5 22 0,915 1,4618 —
1254 Кар во мен тол 20 0,908 1,4619 4247
1255 Этиловый эфир у, у-ди-хлоркротоиовой к-ты CHCl2CH = CHCOOC2Hs 20 1,229 1,4619 —
1256 Амиловый эфир тиоциановой к-ты CH3(CH2).SCN 25 0,9412 1,462 7492
1257 2, 6-Ди метилгепта- СН2 диен-1, 3 = С(СН3)СН= СНСН2СН(СН3)2 10 0,765 1,4620 2562
1258 1-Метил циклогекса нол СН3СОН(СН2)4СН2 1 1 20 0,930 1,4620 —
1259 Тропинон 99,6 0,987 1,4621
1260 1-Бромбутен-З СН2ВгСН2СН-СН2 20 1,3230 1,46215 2080
1261 Озонид олеиновой к-ты 20,5 1,028 1,4622
1262 2, 2-Дифтор-1, 1-дибром-этан Br2CHCHF2 20 2,312 1,4622 —
1263 с//-Линалоол 20 0,868 1,4623 4674
1264 5-Этилнонадиен-1. 8-ол-5 (СН2-СНСН2СН2)2С(ОН)С2Н6 20,7 0,866 1,4623 —
1265 d-Фенхои С]0Н1еО 20 0,9465 1,4623 8383
1266 d- Борниловый эфир уксусной к-ты СюНпОСОСНз 22,6 0,99 1,4623 1906
1267 d-Пинан 20 0,839 1,4624
1268 Метил-d-борниловый эфир СНзОСюНп 23,4 0,914 1,4624 —-
1269 1-Хлор-1, 2, 4, 5-тетраметил-циклогексаи (СН3)4С6Н7С1 20 0,936 1,4624 —
1270 1, 2-Диметилциклогекса-иол-1 СН3С(ОН)СН(СН3)(СН2)3СН2 13,7 0,925 1,4625 —
1271 Этил идеи циклогексан СН3СН=С(СН2).СН2 20 0,822 1,4626 —
1272 Хлор циклогексан С1СН(СН2)4СН2 1 1 20 1,000 1,46264 —
1273 Гераниловый эфир уксусной к-ты С,оН17ОСОСН3 15 0,9174 1,4628 2639
1274 d- Борниловый эфир валериановой к-ты C2Hs(CH2)2COOCtoH,7 15 0,956 1,4628 —
1275 Олеиновая к-та С8Н17СН=СН(СН2)7СООН 17,7 0,895 1,463 5846
1276 1, 2, З-Три метил циклогексен-1 (СНзЪСеН, 11,8 0,835 1,4630 —
1277 dl-Бори иловый эфир уксусной к-ты СюНпОСОСНз 20 0,985 1,4630 1910
1278 Четыреххлористый углерод CCh 20 1,595 1,4630 7953
1279 1, 1-Диметил-4, 4-ди этил-циклогексанон-2 (СН3)2(С2Н5)2С6Н6О 15,2 0,911 1,4631
850
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t,°c 4 "d № по табл.; «Свойства органических соединений»
1280 Диэтиловый эфир (этоксиметилен)-малоновой к-ты С2Н5ОСН=С (СООС2Н5)2 сн3 15,3 1,081 1,4631 —
1281 /-Неокарвоментол СН2С Н2СНСН(ОН)СН2СНСН(СНа)2 1 20 0,9012 1,4632 —
1282 rfZ-Пуленол CsHMO 16,5 0,91 1,4632 —
1283 Триформ ал ьметил а мин (H2C = NCH3)3 19 0,918 1,4632 —-
1284 Диметиловый эфир камфорной к-ты С8Ни(СООСН3)2 16,9 1,077 1,4633
1285 2-Октиновая к-та с5н„с=ссоон 12,6 0,962 1,4634 —
1286 Этиловый эфир а-бром-ацетоуксусной к-ты С НзСОСН В гСООС2Н5 14,1 1,429 1,4634 —
1287 Туйиловый спирт CjoHnOH 20 0,921 1,4635 —
1288 Фитол СгоНзэОН 20 0,852 1,4638 8394
1289 rf-Борниловый эфир масляной к-ты C2HsCH2COOCroHn 15 0,966 1,4638 —
1290 Ч«с-2-Метилциклогексанол СН2С6НюОН 20 0,9337 1,4640 8936
1291 Нопинан С9Н16 20 0,86 1,4641 —
1292 1-Изопропилциклогекса-нол (СН3)2СНСОН(СН2).СН2 1 . .1 15,5 0,914 1,4642 —
1293 втор-Хлористый меитил С10Н19С1 20 0,941 1,4642 —
1294 Саитен С9Н14 20 0,87 1,4644 —
1295 rf-Борниловый эфир пропионовой к-ты СгНйСООСюН и 15 0,979 1,4644 —
1296 Диэтиловый эфир dl-RG-гидрокамфорной к-ты (СН3)3С5Н3(СООС2Н6)2 сн3 20 1,039 1,4644
1297 Этиловый эфир «-(циклогексен-!-ил) -пропионовой к-ты СН2(СН2)3СН = ССНСООС2Н5 1 1 17,5 0,968 1,4646 —
1298 Этиловый эфир р-ацет-окси-у, у, v-трихлормас-ляной к-ты СН3СООСН(СС13)СН2СООС2Н3 14,1 1,340 1,4646
1299 2, 6-Диметилнонандиен-2,8-ол-6 (СН3)2С9Н13ОН 16,6 0,866 1,4647 —
1300 Дицианацетилеи NCC=CCN 25 0,970 1,4647 —
1301 1, 1-Диметилциклогекса-нол-2 (СН3)2ССН(ОН)(СН2)3СН2 1 1 20 0,923 1,4648 —
1302 Гексагидробензиловый спирт СН2(СН2)4СНСН2ОН 1 1 20 0,928 1,4649 —
1303 Изоборниловый эфир уксусной к-ты СНзСООСюН,, 20 0,984 1,4649 —
1304 Ацетоксиметил ен ди этил-кетон С2Н5СОС(СН3) = снооссн3 18,3 1,034 1,4649 —
1305 Хлорангидрид пентен-2-овой-1 к-ты С2Н5СН = СНСОС1 20 1,063 1,465 —
1306 Этиловый зфир изо- CH2CH2C(CH3)2C(CH3)=CCO2C2HS лауроленрвой к-ты 1 1 20 0,953 1,4650 —•
1307 rf-p-Феихен СгоН]б 20 0,8599 1,46511 —
1308 rf-Лииалоол СюНиОН 20 0,8679 1,4652 4672
1309 Этиловый эфир тиоциановой к-ты c2h5scn 22,9 1,00715 1,4653 7504
1310 Бромистый аллил СН2-СНСН2Вг 20 1,398 1,46545 177
1311 трет-Хлористый ментил C10H19CI 18,8 0,948 1,4655 —
1312 3, 4-Диметилпиразол (CHs)2C3H2N2 99,3 0,933 1,4657 —
1313 rfZ-d-Пинен 20 0,8582 1,4658 6145
1314 Гераниловый эфир муравьиной к-ты СюН,7ОСНО 20 0,927 1,4659 2641
1315 Дихлоруксусная к-та снсьсоон 20 1,5634 1,4659 8021
1316 Йодистый водород HJ 12 1,466
54*
851
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t,°c < nD № по табл. «Свойства органических соединений»
1317 1318 1319 1320 1321 1322 1323 1324 1325 1326 1327 1328 1329 1330 1331 1332 1333 1336 1337 1338 1339 1340 1341 1342 1343 1344 1345 1346 1347 1348 1349 1350 1351 852 Нитрил 1-этнлциклогекса-нон-2-карбоновой-1 к-ты 1, 2-Дигидротолуол Бензиловый эфир стеариновой к-ты Пиррол ин О-Этиловый эфир ацетил-ацетона Метиловый эфир а-(циклогексен-1-ил) пропионовой к-ты 1, 2, 2-Трифтор-1, 1, 2-трн-бромэтан Нитрил 1-пропилцикло- гексанон-2-карбоновой-1 к-ты Триэтиларсин 1-Хлор-1, 2-диметилцнкло-гексан Дигидрокарвон 3, 4-Дигидро-о-ксилол Триаллил овый эфир три-карбаллиловой к-ты Этиловый эфир линоленовой к-ты (смесь а- и р-форм) Шоамиловый эфир а-ацетоциануксусной к-ты втор -И зобу тил овый эфир 2-фураикарбоновой к-ты Фторбензол d-Сабинец N-МетиЛдиэтаноламин Диметиловый эфир изоде-гидрокамфорной к-ты 1, 2, 2-Триметилциклогекса-нол Диэтиловый эфир муконовой к-ты Метиловый эфир тноциа-иовой к-ты 2, 2-Дифтор-1-нодэтан Изопропиловый эфир пи-рослизевой к-ты Днхлорангидрид себаци-новой к-ты Днхлорангидрид субериновой к-ты Метиловый эфир циклогексен-1-ил-уксусной-1 к-ты О-Метиловый эфир а цетил-ацетона Бензиловый эфир пальмитиновой к-ты Метиловый эфир изол ауроновой к-ты Этиловый зфнр 3, 4, 5, 6-тетрагидробензойиой к-ты г/-Изопулегон Этиловый эфир циклогексен-1-ил-1-уксусной к-ты .и-Фтор толуол C2H5(CN)CCO(CH,)3CH2 ! । CcHzCIIt С„НзьСООСН2СбН5 nhch2ch-chch2 1 1 СН3С(ОС2НЕ) = СНСОСН3 С5Н!,СН(СН3)СООСН3 CFBr2CBrF2 C3H7(CN)CCO(CH2)3CH2 l_ 1 (C2Hs)3As CH3C (Cl) CH (CHS) (CH2)3CH2 1 1 CioHieO (CH4)2C6H6 (CH2COOC3H;,)2CHCOOC3HS с17нксоос2н3 CH3C0CH (CN) COOCsHn C«H3OCOOCsHs CeHsF CioHie CH3N(CH2CH2OH)2 (СНа)3С5Н5(СООСНз)2 (CH3)3C£HBOH (CH=CHCOOC2H5)2 CH3SCN chf2ch2j C4H3OCOOCH(CH3)2 I(CH2)4COC1]2 I(CH2)3COC1]> CH2(CH2) ,CH-CCH.COOCHa 1 1 CH3C(OCH3) -СНСОСНз C)6H3,COOCH2C£H5 (CH3)3C£H4COOCH3 C£HSCOOC2H5 CipHmO C6H»CH2COOC.H5 ch3c6h4f 20 22,5 50 20 16,3 18,3 20 20 20 13,3 18,9 20 15,9 20 20 27,5 20 20 20 17,5 19,9 99,1 23,8 12,2 23,7 18,3 20,6 18,2 20 50 20 20 20 16,2 20 1,008 0,8252 0,908 0,9097 0,948 0,986 2,6 0,997 1,150 0,971 0,923 0,823 1,097 0,8919 1,033 1,0383 1,0236 0,842 1,0377 1,085 0,926 0,983 1,069 2.243 1,0655 1,172 1,003 0,971 0,9 0,970 0,998 0,919 0,989 0,999 1,466 1,4662 1,4663 1,4664 1,4665 1,4665 1,4666 1,467 1,467 1,4672 1,4674 1,4675 1,4675 1,46753 1,4676 1,4676 1,46773 1,4678 1,4678 1,4678 1,4679 1,468 1,46801 1,4681 1,4682 1,4684 1,4685 1,4687 1,4688 1,4689 1,469 1,469 1,4690 1,4691 1,4691 1 7692 7126 6399 673 4679 6360 1625 6946 7499 5903 7749
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
П родолжение'
1 № по пор. Название Формула t, °C "о № по табл. «Свойства органических соединений»
1352 Метиловый эфир у, у-ди-хлоркротоновой к-ты С12СНСН = СНСООСНз 20 1,302 1,4694 —
1353 Этиловый эфир диацетилуксусной к-ты (СН3СО)2СНСООСН2СН3 18,3 1,08 1,4695 3155
1354 транс-Декагидронафталин СюН18 18 0,8703 1,46968 534S
1355 Y-Терпинеол СюНщО 80 0,895 1,47 —.
1356 а-Фен холен амид CH3C5HeC(CH3)2CONH2 117,9 0,933 1,47 —
1357 Гидразин H2NNH2 22 1,470
1358 Этиловый, эфир р-винил-акриловой к-ты СН2-СНСН=СНСООС2НЕ 20 6,938 1,470 —
1359 Этиловый эфир 3-метил-циклогексен-1-карбоновой-1 к-ты СНзСеНвСОоСгНб 20 0,975 1,470 —
1360 н-Фтортолуол CHsCsHJF 20 0,99 1,470 7750
1361 Этилкакодил (С2Н5) 2AS2 (CgHgla 23 1,1388 1,470 3144
1362 Пиразол NHN=CHCH-CH 1 I 99,8 1,001 1,47027 6210
1363 о-Фтортолуол CH3CEH4F 20 1,001 1,4704 7748
1364 Мирцен (CH3)2C-CH(CH2)2C( = CH2)CH = CH2 20 0,802 1,4707 5173
1365 d- Борниловый эфир муравьиной к-ты НСООСюНп 15 1,017 1,4708 —
1366 Нитрил 2-метилгексанол-1-овой-6 к-ты CH3(CN)C6H6O 20 1,040 1,471 —
1367 Этиловый эфир а-циан-ацетоуксусной к-ты СНзСОСН (CN) COOC2H6 20 1,111 1,4710 —
1368 Линолевая к-та Ci7H3lCOOH 20 0,9031 1,4711 4675'
1369 /-Дигидрокарвон СюН ic,O 20 0,9253 1,4711 4249
1370 Этиловый эфир 5-окси-1. 3-диметилциклогек-сен-З-нл-5-уксусной к-ты (СНз)2СЕНс(ОН)СН2 COOCsHs 17,6 1,012 1.4713 —
1370а 1, а-Фенхен C10H16 20 0,8670 1,47133 8382'
1371 Метиловый эфир гераниевой к-ты C9H1SCOOCH3 19,1 0,923 1,4714 —
1372 Триаллиловый эфир лимонной к-ты C3H4(OH)(COOC3H3)3 17,4 1,136 1,4714 —
1373 снаш-Дихлор ацетон CH2C1COCH2C1 46 1,3826 1,47144 6576
1374 dZ-Пинол СюН|бО 20 0,942 1,4715 6147
1375 а-Этоксиметилендиэтилке-тон С2Н5СОС(СНз)=СНОС2Нз 18,2 0,945 1,4717 —
1376 Цитраконовый ангидрид ОСОС(СНа) = СНСО 1 1 20 1,245 1,4717 9041
1377 а-Этилкамфора С12Н20О 20 0,937 1,4719
1378 1, 1, 2-Трихлорэтан СН2С1СНС12 22 1,446 1,4719 9232
1379 1 -Этил -3- м етил пир азол CH = CHC(CHs)=-NNC2Hs 1 1 20 0,945 1,472 —
1380 Тетраамилолово (C3H„)4Sn 20 1,0206 1,4720
1381 1,2-Дигидро-А£-ксилол С Н,СНСН2С(СН3) = СНСН = сн 1 1 19,7 0,823 1,4721 —
1382 Изопропнлиденциклогексан (СНз)2С=С(СН2)4СН2 1 1 20 0,836 1,4723 —
1383 Z-Изо пуле гол С,0Н,7ОН 20 0,911 1,4723
1384 Тетраэтилолово (C2Hs)4Sn 19,7 1,1988 1,4724 5868
1385 Диэтиловый эфир сукци-номалоновой к-ты СОСН2СН2СОС(СООС2Нз)2 73 1,167 1,4725 —
1386 Гераниламин c10h17nh2 20 0,83 1.4727
1387 а-Камфил амин CwH,7NH2 17,8 0,874 1,4728
1388 Хлорангидрнд глутаровой к-ты СН2(СН2СОС1)2 20,2 1,324 1,4728 —
1389 Циклогексадиен-1. 4 СН = СНСН2СН=СНСН2 1 1 20 0,8471 1,4729 8903
1390 Изопулегол с10н„он 20 0,914 1,4729
1391 Глицерин сн2онснонсн2он 20 1,260 1,4729 2915
853
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C "о № по табл. «Свойства органических соединений»
1392 1, З-Диметилпиразол СН = СНС(СН3) = NNCHg | 1 20 0,966 1,473 -
1393 Этиловый эфир 5-амиио-1, 1, 3-триметилциклогек-саикарбоновой-2 к-ты (СНз) 3СвН, (N Н2) СООС2Н5 20 0,98 1,473 —
1394 Тетра-акт-амилолово [CH3CH2CH(CH3)CH2]4Sn 20 1,0222 1,4730 ——
1395 Тетрабутилолово (C4Hs)4Sn 20 1,0572 1,4730 —
1396 1397 /-а-Фелландрен /-а-Фенхен CioHie См. 20 1370s 0,8425 1,4732 —
1398 Хлористый сукцинил (СН2СОС1)2 15,2 1,3948 1,4735 7223
1399 1, 3, 5-Триметилциклогек-сеи-1-ол-З (СНз)зСеНвОН 19,3 0,913 1,4735 —
1400 Диметиловый эфир rf-де-гидрокамфорной к-ты (СНз)зС5Нз(СООСН3)2 18,1 1,088 1,4736 —
1401 Моиоэтиловый эфир a-d-камфориой к-ты СзНн(СООН) (СООС2Н5) 16.8 1,102 1,4737 —
1402 Пропиловый эфир пиро-слизе вой к-ты С.НзОСООСзНз 25,9 1,0745 1,4737 6363
1403 Этиловый эфир 1-метил-циклогексилиден-4-уксус-ной к-ты СНгС5Н9С = СНСООС2Н5 17 0,994 1,4738 —
1404 Этиловый эфир а-оксиме-тиленацетоуксусной к-ты СНзСОС(=СНОН)СООС2Н5 16,9 1,134 1,4738 —
1405 Геранилуксусная к-та С12Н20О2 21 0,938 1,4739 —
1406 р, v-Пулененол (СН3 )2ССН = СНСН(СНз)СН2СНОН 1 1 18,5 0,921 1,4740 —
1407 Хлористый геранил CioHnCl 20 0,92 1,4741
1408 Тетраизобутилолово [(CH3)2CHCH2]4Sn 23 1,0540 1,4742 ——
1409 Пропионилтропеин CuH19O2N 19,6 1,040 1,4743 —
1410 Кротоновый ангидрид (СНзСН = СНСО)2О 20 1,0397 1,47446 4458
1411 P-Терпинеол С,0Н,зО 20 0,919 1,4747 —
1412 Этиловый эфир цис-Ъ-амино-1, 1, 3-триметил-циклогексанкарбоиовой-2 к-ты (СНз)зСбН2(МН2)СООС2Н6 20 0,990 1,475 —
1413 Этиловый эфир ацетонилщавелевой к-ты СНзСОСН2СОСООС2Н6 17,6 1,128 1,4750 —
1414 3, 4, 5, 6-Тетрагидротропо-вая к-та С6Н9СН(СН3)СООН 20,3 1,010 1,4753 —
1415 сИ-а-Бромпропионовая к-та СНзСНВгСООН 20 1,700 1,4753 6762
1416 Р-Терпинеи СН2=С6Н,СН(СН3)2 22 0,838 1,4754 7293
1417 Метиловый эфир 1, 4-ди-метилциклогексадиеи-1, 3 карбоновой-2 к-ты (СНз)2С6НзСООСНз 18,2 0,977 1,4755 —
1418 а, а, р-Трихлормасляный альдегид СН2СНС1СС12СНО 20 1,3956 1,47554 —
1419 Этиловый эфир 2-тропа и-карбоиовой к-ты C11H19O2N 20,5 1,041 1,4756 —
1420 Пропилселеномеркаптан C2H5CH2SeH 20 1,302 1,4756 —
1421 d-Сильвестрен CioHjg 20 0,863 1,4757 7 097
1422 Цикл огексадиен-1,3 СН = СНСН=СНСН2СН2 1 1 20 0,8404 1,4758 8901
1423 Метиловый эфир 1-метил-циклогексилиден-4-ук-сусной к-ты СНзС6Н5=СНСООСНа 16,9 0,970 1,4758 —
1424 2, 2-Диметил-5, 5-диэтил-циклогексаиол (СН3)2С6Н,(С2Нз)2ОН 13,6 0,922 1,4759 -г
1425 1, 3, 4-Триметнлпиразол CII-C(CIIS)C(CII,)'NNCH, 1 1 20 0.951 1,476 —
1426 3, 4, 5, 6-Тетрагидро-Асто-лунловая к-та СНзСгНсСООН 69 1,013 1,476 -
1427 Этиловый эфир борннлеи-карбоновой к-ты С10Н,аСООС2Н5 19,8 0,983 1,4760 —
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Назваине Формула f,°C 4 "D № по табл. «Свойства органических соединений»
1428 Псевдопельтьерии 99,5 1,001 1,4760 6828
1429 Изоамиловый эфир 3-камфоркарбоновой К-ТЫ С1бН2бОз 17,2 1,014 1,4760 —
1430 г/(7)-а-Терпинеол С,0Н,7ОН 16 0,93 1,4762 —•
1431 Этиловый эфир «-(этоксиметилен) -ацетоуксусной к-ты :насос(-снос2н6) соос2н6 16,9 1,071 1,4762
1432 2, 3-Дигидротолуол СНзСсН? 20 0,835 1,4763 —
1433 N-Метилкамфидии CioHjsNCHa 19 0,901 1,4763 —
1434 Метиловый эфир 1, 3-диме-тилциклогексилидеи-5-уксусной к-ты (СН3)2С6Н8 = СНСООСНз 15 0,957 1,4763
1435 Метиловый эфир а-бутиро-циануксусной к-ты C2HECH2COCH(CN)COOCH8 20 1,093 1,4763 —
1436 Этиловый эфир О-изовале-рил-еиол-3-камфоркар-боновой к-ты CisHssO^ 22,7 1,022 1,4764
1437 Тропан CrHisN 21,6 0.93 1,4766
1438 Диэтилселеи (C2HEj2Se 20 1,2300 1,4768 9506
1439 Аскаридол СюН1бО2 20 0,999 1,4769 —
1440 Тропеииовый эфир уксусной к-ты c8h14nococh3 15,4 1,063 1,4769 —
1441 Нитрил циклогексанон-1-карбоиовой-2 к-ты CH2(CH2)3COCHCN 1 I 20 1,070 1,477 —•
1442 1, 3-Диметил циклогексен-1-ол-3 (СНз)2СЕН;ОН 17,5 0,933 1,4771 —
1443 Амиловый эфир О-ацетил-енол-3-камфоркарбоио- CibHmO* 20,5 1,022 1,4772 —
1444 вой к-ты Гераниол CwHpOH 15 0,883 1,4773 2638
1445 1, З-Диметилциклогексеи-4-ил-5-уксусиая к-та (СН3)2СеН;СН2СООН 20,3 0,955 1,4773 —
1446 Этиловый эфир 1-метил-циклогексилиден-3-уксусной к-ты Диэтаноламин CH3C6H9=CHCOOC2H6 15 0,957 1,4773 —
1447 (HOCH2CH2)2NH 20 1,0966 1,4776 3500
1448 d-a-Фелландреи 20 0,8463 1,4777 8132
1449 Трихлорэтилен CHC1=CC12 19,8 1,463 1,4777 9438
1450 2, 5-Диметилгексадиен-2, 4 (CH3)2C = CHCH=C(CH3)2 20 0,7615 1,4781 2391
1451 а-Терпинен CioHifi 19,4 0,836 1,4781 7292
1452 d-Дигидрокарвеол C10H17OH 16 0,9223 1,4784 —
1453 d-4-Терпинеол СиНиОН 19 0,93 1,4785 —
1454 d-Этнловый эфир камфорокси м а CioHieNOCsHe 17 0,947 1,4785 —-
1455 1-Метил пир а зол CH=CHCH=NNCH3 1 1 13,7 0,993 1,4786 —
1456 симм-Диацетилацетон (CH3COCH2)2CO 60 1,06 1,4787 —
1457 d-fJ-Феллапдрен 20 0,8520 1,4788 —•
1458 d Карон 18,8 0,958 1,4788 —
1459 Этиловый эфир изофорои-карбоновой к-ты OC«Ht3COOC2HE 20,4 1,029 1,4788 —
1460 5, 6-Дигидро-о-ксилол (CH3)2C6He 19,5 0,830 1,4789 —
1461 Хлорангидрид ft. 0-диме-тилакриловой к-ты (CH3)2C-CHCOC1 12,4 1,065 1,479 —
1462 Этиловый эфир 1-метилциклогексил иден-2-уксусной к-ты Метиловый эфир 1-метил-циклогексилиден-3-ук-сусной к-ты CHaCeHs-CHCOOC2HE 14,8 0,959 1,4791 —
1463 C H3CcHe - CH COOC H3 15,5 0,975 1,4793 —
1464 1, 1, З-Триметилциклогек-сен-2-ои-4 (CH3)3CEHECO 16,3 0,933 1,4795 —
1465 d-Метиловый эфир кам-фороксима CioH.eNOCHg 22,5 0,958 1,4795
;>5
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О. о с о с 2. Название Формула t, °C 4 nD № по табл. «Свойства органических соединений»
1466 а, Р-Пулсненон (СН3)2ССОСН = С(СН3)СН2СН, 1 1 16,5 0,932 1,4796 -
1467 2, З-Дигидро-л-ксилол (СН3)2СеН6 19 0,83 1,4797
1468 Этиловый эфир пирослизевой к-ты С4Н3ОСООСН,СН3 20,8 1,1174 1.4797 6365
1469 Нитрил пнрослизевой к-ты c4h3ocn 20 1,0822 1,4798 —
1470 З-Хлорацетилацетон CH3COCHC1COCH3 16,7 1,169 1,4798 —
1471 1, 2-Диазидоэтан (CH2N3)2 24,9 1,170 1,4798 —
1472 Дициклогексил СбНцСбНц 20 0,886 1,48 3495
1473 Триметилсурьм а (CHshSb 15 1,52 1,48 7162
1474 Гексаэтилбензол C6(C2H5)s 130 0,831 1,480 1470
1475 Терпинолен CioHje 19 0,855 1,480 7297
1476 1, 3, 4, 5-Тетраметилпира-зол CH3C = (CCH3)2 = NNCH3 1 1 20 0,947 1,480 —
1477 4-Бром-1, 1, 4-триметил-циклогексан (CH3)3C6H8Br 17,4 1,170 1,4800 —
1478 /-Изофеихиловый спирт C.cHhOH 15 0,961 1,4801 3829
1479 1, З-Дихлорпропанол-2 (CH2C1)2CHOH 17 1,3506 1,480245 6562
1480 цыс-Декагидроиафталин C10H18 18 0,895 1,4804 5348
1481 Динитрил а-оксиглутаро-вой к-ты C3H6(OH)(CN)2 20 1,181 1,4805 —
1482 dZ-Карвотанацетон (CH3)2CHC7HSO 20 0,935 1,4806 —
1483 Йодистый цетил CH3(CH2),4CH,J 20 1,123 1,4806 8856
1484 Метиловый эфир 1-метилциклогексил иден-2-ук-сусной к-ты CH3C6Hs=CHCOOCH3 14,2 0,977 1,4807 —
1485 Этиловый эфир циклогексил идеи уксусной к-ты СбНю—CHCOOC2H5 16,9 0,983 1,4808 —
1486 Диэтиловый эфир кро-тонилидеималоновой к-ты СНзСН = CHCH =C (COOC2H3)2 20 1,045 1,481 —
1487 Гликолевый альдегид CH2(OH)CHO 11 1,4 1,4811 2893
1488 Тропин CsHisNO 99,8 1,016 1,48113 7936
1489 1, 1. 1, 2-Тетрахлорэтан 1-Метилциклогексен-2-ил-1-уксусная к-та CH2C1CCI3 23,2 1,58 1,48162 9222
1490 CH3C8HECH2COOH 15,8 1,028 1,4817 —
1491 Этиловый эфир О-метил-епол-изофоронкарбоно-вой к-ты (CH3) 3C6H3 (OCH3) COOC2H5 19 1,025 1,4818 ~
1492 1, З-Диметилциклогексен-З-он-5 (CH3)2C6H6CO 22 0,94 1,4819 —
1493 Бензиловый эфир миристиновой к-ты C,3H27COOCH2C8H6 20 0,93 1,482 —
1494 1, 1,2, 4-Тетраметилцикло-гексадиен-2, 5-ол-4 (CH3),C6H3OH 20 0,925 1,4824 —
1495 1-Метил-4-этил циклогексадиен-1, 3 СН3С6Н6С2Н5 19,4 0,837 1,4825 —
1496 cfZ-Карвенон СюН1бО 20 0,9263 1,4825 4242
1497 й/-а-Терпинеол CioIIl7OH 20 0,936 1,4827 7295
1498 1-Бром-1, 3, 5-триметилцик-логексан (CH3),C8HeBr 11,1 1,175 1,4828 —
1499 Этиловый эфир О-этил-енол-изофоронкарбоно-вой к-ты (CH3)3C6H3(OC2H3) COOC2H5 19 1,011 1,4829
1500 Бензиловый эфир лауриновой к-ты CnH23COOCH2C8H6 20 0,95 1,4830 4625
1501 Метиловый эфир цикло-гексилиденуксусной к-ты C8H,0-CHCOOCH3 19,7 0,999 1,4831 —
1502 Этиловый эфир у-бром-ацетоуксусной к-ты BrCH2COCH2COOC2H5 18,1 1,528 1,4831 —
1503 5-Бром-1, 3-диметнлцикло-гексан (CH3)2C6II9Br 18,2 1,207 1,4832 —
1504 Метиловый эфир 3-камфоркарбоновой к-ты C12HI8O3 18 1,085 1,4833
856
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О с о Е Название Формула t, °C d4 "d № по табл. «Свойства органических соединений»
1505 Метиловый эфир О-аце-тил-енол-3-камфоркар- СцНгоО* 19,8 1,082 1,4844 —
боковой к-ты
1506 Ацетилметилгептенон (СБ 13)2С-СН(СН2)2СОСН2 СОСН, 15 0,945 1,4849
1507 Этиловый эфир диосфенола СгНбОСюНиО 20 0,977 1,485
1-508 Метиловый эфир диосфе- СНзОС,оН150 20 0,988 1,485 —
1509 нол а Ундецилфенилкетон CH3(CH2)l0COCEHs 52,4 0,897 1,4850
1510 Фурфуриловый спирт С4113ОСН2ОН 23 1,1282 1,48515 8618
1511 Триэтаноламин N(CH2CH2OH)3 20 1,1242 1,4852 7919
1512 5-Метилфурфуриловый СН3С4Н2ОСН2ОН 20 1,0769 1,4853 8622
1513 спирт 1, 2, З-Триазол CH-NNHN-CH 1 1 25,3 1,186 1,4854 —
1514 1515 Йодистый децил Метиловый эфир пиросли- CH,(CH2)8J СЛлОСООСНз 20 20 1,2567 1,18 1,48589 1,4860 3068 6361
зевой к-ты 0,898
1516 Децилфеииловый эфир СН3(СН2)„ОСЕНБ 20 1,4862 —
1517 И зоб ути л бен зол СеН5СН2СН(СН3)2 20 0,85321 1,48646 1521
1518 Амиловый эфир 3-хлор- С,бН2ЬОзС1 19 1,091 1,4866 —
камфоркарбоновой-3
1519 Хлорангидрид капроновой СНз(СН2)4СОС1 20 .... 1,4867 —
1520 к-ты Изоамилбензол С6Н5(СН2)2СН(СНз)2 15,6 0,863 1,4867 1519
1521 Этилгексиловый эфир фта- С6Н4(СОО)2(С2НЕ)СбНц 20 0,98 1,4867 —
левой к-ты 14,2 1,338 1,4869
1522 Этиловый эфир V, у. v-трн- С13ССН-СНСООС2Н6 —
хлоркротоновой к-ты 0,909 1,487
1523 Ацетом ети л - трет- бутил о- СНэОС(СНз)2СН2СОСНз 20 —
1524 вый эфир 1, 3, 4-Триметил-5-хлорпи- CH3NCC1-C(CH3)C(CH3)-N 20 1,108 1,487 —
разол 1 1
1525 Гераниевая к-та (СГ з)2С = СН(СН2)2С = СНСО2Н 22,2 0,951 1,4870 2637
сн3
1526 2-Пропилимидазолин c3h,c=nch2ch2nh 1 1 17 0,964 1,4871 —
1527 З-Метилеи-1 -метил цикло- СНзСбН;-СН2 17 0,839 1,4872 —
гексен-1
1528 2-Феиилпеитан С6Н5С Н (С Н3) С Н2С Н2С Нз 21 0,8594 1,4875 —
1529 Бензиловый эфир олеино- С17Н33СООСН2С6Н5 25 0,933 1,4875 5848
вой к-ты 1,4875
1530 2-Ацетоксиметиленментон СН3СООС11Н17О 16 1,032 —
1531 Дналлилсульфид (CH2-CHCH2)2S 27 0,88765 1,4877 206
1532 Метиловый эфир 1-экго- СзНиОМСООСНз 20,5 1,147 1,4877 —
ииновой к-ты 18,5
1533 Этиловый эфир Р, 6-ди- (СН3)2С“СНС(СНз) = СНСО2С2Н5 0,934 1,488 —
метилсорбиновой к-ты
1534 Сабинол CjoHigOH 20 0,943 1,488 —
1535 Пулегон СюН1бО 19 0,937 1,4880 6835
1536 Триметилеибромгидрин ВгСН2СН2СН2ОН 20 1,571 1,4883 6544
1537 4-Этилендипиперидин Ci2H24N2 17,8 0,921 1,4887 —-
1538 1-Метил пиррол N(CH3)CH-CHCH-CH 1 1 16 0,91o 1,4888 6383
1539 Бутил- (2-этилгексиловый) СьН4(СООС4Н,.)СООСеН,, 20 1,01 1,4888 —
эфир фталевой к-ты сн,
1540 Этиловый эфир 1-аллил- C3H5NC(CO2C2H5)=CHC-N 20 1,046 1,489
3-метилпиразолкарбоно- 1 1
вой-5 к-ты
1541 I-Иодоктан CH3(CH..)f,CH2J 20 1,333 1,489 5797
1542 1-Иод-2-метилгекс ан CH3(CH2)3CH(CH3)CHJ 21 1,366 1,4891 —
857
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О с с с Название Формула Г, °C 4 "о № по табл. «Свойства органических соединений»
1543 Этиловый эфир а-(л-тол-окси)-нзомасляной к-ты (СНз)2С(ОС6Н4СН3)СО2С2Н5 20 1,027 1,4893 -
1544 Ct-Цитраль (гераниаль) С9Н|5СНО 17 0,890 1,4895 9043
1545 Этиловый эфир а-(3, 5-ди-метилцнклогексадиен-1, 5-ил)-изомасляной к-ты (СНз)2СеН5С (СНз)2СО2С2Н5 13,4 0,969 1,4895
1546 2-Этоксиметиленментон С2Н5ОС„Н„О 15,2 0,970 1,4895 .
1547 1 - Дихл орметнл -1- метил циклогексан (СНз)(СНС12)СеН10 23,7 1,127 1,4895 —
1548 Бутилбензол С6Нз(СН2)зСНз 20 0,86013 1,48979 1455
1549 Неролидол 20 0,87 1,4898
1550 Метиловый эфир у, у, v-трихлоркротоиовой к-ты С1зССН = СНСООСНз 21,2 1,397 1,4898 —
1551 Фарнезол С15Н25ОН 20 0,88 1,4899
1552 1, 3, 5-Гексатрисн Н2С-СНСН = СНСН-СН2 16,2 0,741 1,49
1553 Дурол (CHS)4C8H2 81,3 0,838 1,49 3575
1554 Изоамилфеии левый эфир СеН5ОСН2СН2СН(СНз)2 22,1 0,920 1,49 3624
1555 В-Цнтраль (нераль) С9Н18СНО 19 0,888 1,4900 9044
1556 р-Оксим окиси мезитила (стабильн.) (СНз)2С = СНС(=ЫОН)СНз 40 0,969 1,4900 —
1557 втор-Бутилбензол С6НьСН(СНз)С2Н5 20 0,86207 1,49020 1456
1558 Фелландраль CeHcsCHO 20 0,93 1,4903
1559 Циклогексен-1 -карбоновая-1 к-та СН2(СН2)зСН-ССООН 1 1 20 1,109 1,4903 8951
1560 Тропидии CsH.sN 18,4 0,95 1,4904
1561 З-Пропионилкамфора С13Н20О2 18,1 1,019 1,4905 —-
1562 а-Оксим окисн мезитила (СНз)2С = СНС( = МОН)СНз 21 0,942 1,49083 ——
1563 л-Цимол СНэС8Н4СН(СНа)2 20 0,8570 1,4909 8999
1564 о-Толиловый эфир изомас-ляной к-ты (СНз)2СНСООС6Н4СНз 20 1,001 1,491 —
1565 Бензиловый эфир изомас-ляиой к-ты (СНз)2СНСООСН2СвН5 18 1,016 1,4910 —
1566 Метиловый эфир 3-аллил-камфоркарбоновой-3 C15H22O3 20,2 1,067 1,4911 —
1567 п-Бутилтолуол СН3С£Н4(СН2)3СНз 14 0,86132 1,4912 7685
1568 Кумол С8Н8СН(СН3)2 20 0,86179 1,49145 4595
1569 трет-Амилбензол С6НзС(СНз)2С2Нз 23 0,8 1,49154 1429
1570 4-Хлор-1, 3-диметилпира-зол СНзМСН -СС1С(СН3) =N 1 1 20 1,153 1,492 —
1571 Пропилбензол С6Н5СН2СН2СНз 20 0,86204 1,49202 1572
1572 а-Сантален С15Н24 15 0,913 1,4921
1573 1, 1,2, 2-Тетрахлорэтан СНС12СНС12 18,5 1,6 1,4921 9223
1574 Бензиловый эфир d-a-ме-тилмасляиой к-ты СНзСН2СН(СНз) СООС112С8Н8 20,4 0,98 1,4922 —
1575 З-Бутирилкамфора С14Н22О2 17,4 1,016 1,4923 —
1576 Дибутиловый эфир фталевой к-ты С6Н4(СООС4Н9)2 25 1,045 1,4925 8498
1577 Йодистый гексил CH3(CH2)4CH2J 20 1,4414 1,4925 2490
1578 цис- Декагидрохинолин c8hI2n 20 0,9426 1,4926 8691
1579 Триметилизоамнлсвинец (СНз)зРЬС5Ни 20,3 1,525 1,4926 —
1580 трет-Бутилбензол СвН5С(СНз)з 20 0,86650 1,49266 1457
1581 Этиловый эфир иминопи- < рослизевой к-ты :2h6oc(-=nh)c=chch-cho 1 1 17,8 1,078 1,4930 —
1582 Бутиловый эфир бензойной к-ты СеН8СООС4Н9 20 1,000 1,4930 1228
1583 d-втор-Бутиловый эфир бензойной к-ты СбНзСООСН (СНз) С2Н5 20 1,0018 1,4930 —
1584 м-Бутилтолуол СНзС8Н4(СН2)зСНз 18 0,8624 1,49315 7684
1585 1-Изопроп илиденциклопен-таиои-2 (СНз)2С = ССО(СН2)2СН2 1 1 20 0,957 1,4932 —
1586 1 -Нитрозопиперидин CsHioNNO 18,5 1,063 1,4933 —
1587 Камфенамин CkHnN 20 0,940 1,4935 —
«5’.
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
П родолжение
о. о с о Е Название Формула «,°с 4 nD № по табл. «Свойства органических соединений»
1588 1, 4-Диметилциклогекса-диен-1, З-карбоновая-2 (СН3)2СеН5СООН 18,5 1,045 1,4938 —
1689 к та З-Ацетнлкамфора C12H18O2 19 1,031 1,4939 —
1590 Этиловый эфир СНзСН—СНСН=С(С2Нб)СО2С2Н5 20 0,931 1,494 —-
1591 а-этил сорбин свой к-ты Амиловый эфир бензойной СЬНЕСООС5Н11 20 0,989 1,494 —
1592 к-ты Этиловый эфир у-фенил- С6Н5(СН2)3СООС2Н5 20 1,001 1,494 —
масляной к-ты C2HsOC = C(CN)CH2(CH2)2CH2 1,019 1,494
1593 Нитрил 2-этоксициклогек- 20 —
сен-1-карбоиовой-1 к-ты 1 1
1594 Цннгиберен С1бН24 20 0,873 1,4940 —
1595 5-Метил пиразол N=C(CH3)CH-CHNH 1 1 13,7 1,023 1,4941
1596 2-Хлорм ети л фу рай С4Н,ОСН2С1 20 1,1783 1,4941 8574
1597 Амилбеизол С6НЕ(СН2)4СН3 20 0,86 1,4943 1427
1598 Б-Саиталеи С15Н24 20 0,894 1,4946 —
1599 Тетраизоамилсвинец [(СН3)2СНСН2СН2]4РЬ 20,5 1,233 1,4946 —
1600 гг-трет-Бутил толуол СН3СеН.С(СНя)3 13,3 0,867 1,4947 —
1601 Этиловый эфир тропиди- C«H!2NCOOC2Hb 21,3 1,063 1,4948 —
1602 иокарбоновой-2 к-ты 1, 4-Диэтилбензол СбННСгНй^ 20 0,86196 1,49483 1512
1603 п - Эти лтол уол СН,С6Н4С,Н5 20 0,86118 1,49500 7761
1604 л-Пропилтолуол СН8С6Н,(СН2)2СН3 20 0,862 1,4951 7785
1605 Пиразин N=CHCH=NCH-CH 1 1 60,9 1,0311 1,4953 6205
1606 Этиловый эфир тропинон- C»H,2ONCOOC2Hs 20,8 1,121 1,4954 —
1607 1608 карбоиовой-2 к-ты 1 - Н итро пи п ери ди н Этиловый эфир гидроко- CsH,0NNO2 CeH6CH2CH2COOC2Hs 26,4 20 1,152 1,015 1,4954 1,49542 2744
1609 ричиой к-ты 4-Пропил-о-ксилол (СН3)2СеН3С3Н, 20 0,866 1,4955 —
1610 З-Хлор-1, 1-диметилцикло- (СНз)2СвН5ОС1 19,7 1,084 1,4955 —
1611 гексеи-З-он-4 Этилбензиловый эфир C2H5OCH,C6H5 20 0,9490 1,4955 1194
1612 1 -Метил циклогексен - 1-он-З СНзС=СНСО(СН2)2СН2 1 1 18,7 0,971 1,4955
1613 Йодистый амил CHa(CH2)3CH2J 20 1,517 1,4955 252
1614 1, 3-Диэтил бензол C6H4(C2HS)2 20 0,86394 1,49552 1511
1615 1616 1617 Спинацен Бром циклогексан З-Бромфуран СгэНад CsHnBr OCH-CBrCH=CH 1 1 20 14,6 20 0,862 1,3 1,6606 1,4956 1,4956 1,49575 8954 8557
1618 1, 3, 5-Триэтилбензол С6Н3(С2Нг,)з 20 0,8633 1,4958 1618
1619 п-Ксилол C6H4(CH,)2 20 0,86105 1,49582 4548
1620 2-Пропил-п-цимол (CH3) (C3H7) CeH,CH (CH3)2 15 0,869 1,4959 —
1621 Этилбензол CeHEC2H5 20 0,86690 1,49594 1630
1622 Йодистый изобутил (CH3)2CHCH2J 20 1,606 1.49597 3636
1623 Мезитилэтиловый эфир (CH3)2C6HSCH2OC,H5 20 0,930 1,496 —
1624 Этиловый эфир а, Р-ДИ- C2H5CHBrCHBrCOOC2H5 20 1,613 1,496 —“
1625 бромвалериановой к-ты Изобутилтриизоамилсвинец (СН3)2СНСН2РЬ(С5Ни)3 19,5 1,252 1,4962 —
1626 Метилтриизоамилсвинец СН3РЫСН2СН2СН (СН3)2]3 22 1,313 1,4962 —
1627 а, С-Дихлор-у-валеролак- C1CH2CHCH2CHC1COO 24,6 1,436 1,4962
тон
1628 льЭтилтолуол CH3C6H4C2H5 20 0,86452 1,4966 7760
1629 о-Б ути л тол уол CH3CfH4(CH,).,CH3 18 0,87023 1,49662 7683
1630 Мезитилен (СН,)зС6Нз 20 0,86518 1,49684 4832
1631 2- Этокс и - м - КС и л ол (СН.,);СеН ОС2Н5 13,9 0,942 1,4969 —
1632 2-Бромэтанол CH BrCHjOH 20 1,7723 1,4969 9288
1633 Толуол СбНбСНз 20 0,86694 1,49693 7669
859
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор, Название Формула /,°с 4 "о № по табл. «Свойства органических соединений»
1634 п-П ропилтолуол СН3С6Н4(СН2)2СН3 15,4 0,8642 1,497 7736
1635 1, 5-Диметил-4-хлорпиразол N=СНСС1 = С (СНз) NCHj 1 1 20 1,166 1,497 —
1636 Пропилтриизоамилсвинец С2НьСН2РЬ(С5Нп)з 22 1,274 1,4970
1637 Р - Циклоц итр аль СюН1бО 13,3 0,96 1,4971
1638 З-Метилпиразол N = C(CH3)CH~CHNH 1 1 16,3 1,01 1,4971 —
1639 м-Ксилол С«Н.(СНз)2 20 0,86417 1,49722 4531
1640 Нитрил V, у-дихлоркрото- C12CHCH=CHCN 20 1,305 1,4974 —-
новой к-ты
1641 5-Оксиметилен- НОСН = 1,2-диметилцикло гексанон-4 ССОСН2СН(СНз)СН(СНз)СН2 20 1,022 1,4977 —
1642 1-Дихлорметил-1-метнлцик- С ,Н3С(СНС12)СН2СН2СОСН2 сн2 52,8 1,221 1,4978 —
логекса нон-4 1 _ 1
,1643 2-Изоамилтиофен (СН3)2СН(СН2)2С=СНСН =CHS 1 1 20 0,941 1,498 —
1644 Этиловый эфир СНзСН— СНСН=С(СНз) СООС2Н5 20 0,947 1,498 —
а-метилсорбиновой к-ты
1645 Этиловый эфир а-ацетил-СбНб(СН2)2СН(СОСН3)СООС2Н5 20 1,048 1,498 —
1646 у-феи ил масляной к-ты ₽, у-Тетрагидробензизокса- C,H0ON 20 1,095 1,498
1647 зол
1-Иод-2-метил бут ан CH3CH2CH(CH3)CH2J 15 1,523 1,4981 1975
1648 ц«с-2-Хлор-1-бромэтилен ВгСН = СНС1 15 1,797 1,4982 —
1649 1, 2, 4-Триэтилбензол С6Нз(С2Н5)з 17 0,8819 1,4983 1617
1650 Этилтриизоамил свинец С2Н6РЬ(С5Н„)з 19,6 1,292 1,4983 —
1651 а-Ионон СюН16=СНСОСНз 22,3 0,93 1,4984 3930
1652 Пачулей 20 0,930 1,4984 —
1653 Вербеной СюНи 20 0,882 1,4986 —
1654 2-Этил-п-цнмол (СНз)(С2Н5)(СзН7)С6Нз 15,6 0,871 1,4988 —
1655 Дихлорангидрид камфор- СеН„(СОС1)2 20,7 1,227 1,4988 —
1656 дикарбоновой к-ты
2-Бромбутадиен-1, 3 СН2=СВгСН-СН2 20 1,397 1,4988 1946
1657 1-Метил-4-этилциклогекса- (СНз) (С2Н3)С(,Н6СООН 14,8 1,028 1,4989 —.
диен-1, З-карбоновая-З
1658 к-та
Этиловый эфир СН3С1 4=С(СНз)СН- CHCO2C2HS 20 0,946 1,499 —
1659 у-метилсорбиновой к-ты «-Крезиловый эфир уксус- СНзСООСбН.СНз 23 1,050 1,4991
1660 ной к-ты
Хлорангидрид v, у-дихлор- С12СНСН = СНСОС1 20 1,442 1,4991 —
1661 кротоновой к-ты а-Санталол С,зН2,ОН 20 0,978 1,4992
166.: Кетии (2, 5-ди метил пира- CH3C=CHN-C(CH3)CH=N 23,6 0,986 1,4992 4270
зин) 1 1
1663 Этиловый эфир а-толуило- С6НБСН2СООСН2СНз 18,5 1,034 1,49921 7642
1664 ВОЙ К-ТЫ 2, 4-Диметилпиррол (CH3)2C4H2NH 13,7 0,927 1,4993 6381
166о d-Карвои СН2СОС(СН3) = СНСН2СНС( = СН2)СН3 1 1 18,7 0,96 1,4994 4248
1666 2-Ацетокснметиленцикло- СНзСООСН-СбНвО 15,6 1,115 1,4994
1667 гексанон
т’ранс-2-Хлор-1-бромэтилен ВгСН = СНС1 20 1,77 1,4998 —
1668 а-Кариофиллен С15Н24 20 0,903 1,4998 .—
1669 Форон СО[СН=С(СНз)2]2 20 0,8850 1,49982 8466
1670 3-Метоксиметилен-б!-кам- С12Н18О2 47,3 1,002 1,4999 —
1671 фора
Гидрокоричная к-та С6Н5СН.СН2СООН 80 1,06 1,50 2742
1672 о-Цимол СНзСг,Н,СН(СН3)2 20 0,876 1,500 8997
1673 5-Метил-2-этилтетрагидро- C10H16N2 20 0,987 1,500 —
индазол
.860
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула 7,°C nD № по табл. «Свойства органических соединений»
1674 Диэтнловый эфир изо- С Н5ОСОСН = С(СН3)СН = 20 1,056 1,500 —
прендикарбоновой к-ты = СНСО2С2Н5 15,5 0,874 1,5000
1675 2-Метил-я-ци мол С6Н3(СН3)2СН(СН3)2 —
1676 2-Формилментон СПН18О2 15,5 1,001 1,5000
1677 Пропиловый эфир бензой- C6HsCOOCH2C2Hs 20,3 1,027 1,5000 1237
ной к-ты
1678 I, 1, 1-Трихлорнонин-3-ол-2 С13ССНОНС=С(СН2)4СН3 9,9 1,234 1,5000 —
1679 Йодистый бутил CH3CH2CH2CH2J 20 1,6166 1,50006 2125
1680 Этиловый эфир 1-метил- (СН3) (С3Н7)С6Н5СООС2Н5 16,9 0,977 1,5001 —
4-изопропилциклогекса-диен-1, З-карбоновой-З
1681 2-Этоксиметиленцикло- С2Н6ОСН = С6Н8О 10,8 1,029 1,5002 —
гексанон 1,5004 8543
1682 Дихлорангндрид фумаро- (С1СОСН = )2 18,1 1,410
вой к-ты 1,5005 3820
1683 Изобутиловый эфир изо- (CHs)2CHCH2NCS 14 0,9638
тиоциановой к-ты 1,5005
1684 1, 4-Диметил-1-дихлорме-тил циклогексен-3 (СН3)2СВН7СНС12 20 1,125
1685 Д им етил диизоа м ил свинец (СН3)2РЬ(С5Н11)2 20 1,430 1,5005 —
1686 4-Пропионнл-о-ксилол (СН3)2С6Н3сОС2Н5 20 0,871 1,5007 —-
1687 Кловен С15Н24 18 0,930 1,5007
1688 Этиловый эфир р-амино- CH3C(NH2) =СНСООС2Н5 18,8 1,022 1,5007 •—-
кротоновой к-ты CH3CsHsCOCHC12
1689 1-Дихлорметил-1-метилцик- 17,5 1,235 1,5008 —
логекса нон-2 6118
1690 2-Пиколин ch3c5h4n 20 0,95 1,501
1691 гг-Фторфенол FCJUOH 56 1,189 1,5010 ——
1692 Триизобутилизоамилсвииец (С4Н&)3РЬС5Н11 20,6 1,298 1,5010 •—
1693 2-Метил-п-ментатриен C11H16 19 0,874 1,5012 --
1694 2-Фтор-1, 2-дибромэтан FBrCHCH2Br 19 2,26 1,5012 1—*
1695 d-Камфорилдихлорид C10H14O2CI2 19,9 1,245 1,5013 —
1696 о-П ропилтолуол CH3CBH4(CH2)2CH3 15,8 0,877 1,5014 7734
1697 2,5-Диметил-З-этил- N-C(CH3)C(C2H5) = NCH=C(CH3) 24 0,966 1,5014 —
пиразин 1 . - J
5698 1-Дихлорметил- (СН3)С(СИС12)СН = СНС(С3Н7)СН2СС 16,8 1,142 1,5014 —
4-изопропил-1-метил- 1 I
циклогексен-2-он-6
1699 Бензол CBHB 20 0,879 1,50165 1424
1700 Этиловый эфир дибромук- Br2CHCOOC2H5 12,5 1,91 1,5017 8013
1701 сусной к-ты р-Ирон CioHi6=CHCOCH3 18 0,939 1,502 3938
.1702 1, З-Диметил-2-метоксибен- CH3OCBH3(CH3)2 20 0,956 1,502 —*
зол
1703 5-Метнл-1-этилтетрагидро- CH3C6H,CH = NNC2Hs 20 0,985 1,502
индазол 1 1
1704 Этиловый эфир 1-алил- C3FL NC(CHj)=CHC(COOC,H5) = N 20 1,077 1,502 —
5-метилпиразолкарбо- 1 1
новой-3 к-ты
1705 Диметил пропилизоамил- (CH3)2(C3H7)PbC3H,i 22 1,503 1,5020 —1
свинец C17H21O4N 1,103
1706 d, Z-Псевдококаин 99,5 1,5021 —-
1707 2-Этилпиридин ch3ch2c5h4n 22,5 0,94 1,50214 6265
1708 d-Псевдококаин c,7h2,o4n 99,6 1,102 1,5022 —
1709 1-Фтор-1, 1, 2-трнбромэтан BrCH2CFBr2 17,5 2,605 1,5022 ——
1710 Этиловый 5>Фир сорбиновой CH3(CH = CH)2COOC2H5 20 0,956 1,5023 —
1711 к-ты Метилтимиловый эфир (CH,)(C3H;)CBH3OCH3 28 0,931 1,5024 —
1712 Днизобутилдиметилсвииец (CH3)2Pb(C4Hs)2 20 1,505 1,5024 —
1713 1, 2-Диэтилбензол CBH4(C2Hs)2 22 0,8662 1,5026 1о10
1714 Этил-л-ксилол (CH,)3CBH3C,H5 17 0,882 1,-5026 4562
Д715 Изобутилтриметилсвинец (СН3)3РЬС4НЭ 20 1,672 1,5026
£61
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C 4 nD № no табл. «Свойства органических соединений»
1716 Йодистый изопропил СНзСШСНз 20 1,7033 1,5026 3786
1717 4-Этил-о-ксилол (СН3)2С6Н3С2Н8 20 0,869 1,5027 4530
1718 2-Проп и л меитатриеи С13Н20 15 0,880 1,5027 —
1719 I-Дихлорметил- (CH3)C(CHCI2)CH= CHCH(C2HS)CH2CO 17,4 1,167 1,5029 —-
1-метил-4-этил- 1 1
циклогексен-2-он-6
1720 Фениловый эфир уксусной СИзСООС,! 15 20 1,077 1,503 8193
1721 1, 1-Диметил-4-метилеи- (С нз)2ССН = СНС(=СН2)СН=СН 15,8 0,836 1,5030 —
циклогексадиен-2, 5 1 1
1722 а-Элемол 20 0,941 1,5030 —
1723 Метил’триизобутилсвииец (С4Н9)3РЬСН3 19,6 1,398 1,5032 —
1724 4-Этил-л-ксилол (СНз)2СвН3С2Н5 16 0,87 1,5033 4546
1725 Пиррол NHCH=CHCH=CH 1 1 20 0,948 1,5035 6378
1726 2, 5-Диметилпиррол NHC(CH3)=CHCH = C(CH3) 20 0,935 1,5036 6382
1727 Пии ил амии 20 0,940 1,5036 —
1728 силл-Дивин ил ацетилен си2=снс^ссн>=сн2 20 0,7851 1,504 2394
1729 Этокси-л-ксилол (СН3)2С6Н3ОС2Н5 20 0,938 1,504 —
1730 2-Этил-л-меитатриеи 18 0,886 1,5041 —
1731 1, 2, 4, 5-Тетраэтилбензол С6Н2(С2Н6)4 16 0,883 1,5041 1591
1732 v-Санталеи 20 0,936 1,5042 —
1733 1, 1-Диметил-4-пропилиден-циклогексадиен-2, 5 (СН3)2СбН4-СНС2Н5 20 0,858 0,881 1,5042 1,5042 7759
1734 о-Этилтолуол СН3С6Н4С2Н5 20
1735 Тетраизобутилсвинец [(CH3)2CHCH2]4Pb 20,2 1,324 1,5042 —
1736 1737 З-Пиколин rf-Дегидрокамфорилдихло- ch3c6h4n (CH3)3C5H3(COCI)2 24 48 0,95 1,219 1,5043 1,5043 6119
1738 рид Этиловый эфир Р-метил- C6H6C(CH3)CHO (COOCjlIs) 1 1 20 1,091 1,5045 —
Р-феиилглицидиой к-ты
1739 5-Хлор-1, 3-диметил цикло- (CHshCoHsCl 15,4 1,007 1,5046 —
гексадиен-3, 5 1,678 1,5046
1740 Бутилтриметилсвинец (CH3)3PbC4H9 20 —
1741 Формилэтилкамфора C13H20O2 (C3H?)3PbC5Hi, 17,9 1,00 i 1,5047
1742 Трипропилизоамилсвинец 21 1,381 1,5047 —
1743 2-Иод-2, 3-диметилбутан (CH3)2CHJC(CH3)2 20 1,446 1,5047
1744 1, З-Дибромпентаи CH3CH2CHBrCH2CH2Br 20 1,6721 1,5048 —-
1745 Псевдокумол (CH3),CeH3 20 0,8758 1,50484 6821
1746 Пентаметил беизол CtH(CH3)s 72,8 0,9 1,50489 1563
1747 Диэтиловый эфир фтале- C6H4(COOC2H5)2 14 1,232 1,50490 8502
вой к-ты 1,505
1748 5-Этокси-л-ксилол (CH3)2C6H3OC2Hs 20 0,939 —
1749 Диметиловый эфир СН3ОСОСН = С(СН3)СН= СНСО2СН3 42,7 1,096 1,505 —
1750 нзопренднкарбоновой к-ты (CH=CHCH2CH»CH)2 35 0,976 1,5050 3497
Дициклопентадиен
1751 Этиловый эфир л-толуило- CHsCcH4COOCH2CH3 21,6 1.03 1,50502 7624
вой к-ты 1,5052
1752 Диметилэтилизоамилсви- (CH3)2(C2Hs)PbCsHn 21,7 1,558 —
1753 нец Пеитахлорэтаи CHC12CC13 15 1,6846 1,50542 9212
1754 о-Ксилол C6H4(CH3)2 20 0,8968 1,50545 4515
1755 Йодистый пропил CH3(CH2)2J 20 1,7471 1,50546 6648
1756 Метил мезитиловый эфир CH3OC6H2(CH3)3 14,4 0,953 1,5055 —
1757 Этилтриизобутилсвинец C2H3Pb(C4H9)3 22,1 1,376 1,5055 —
1758 Тетрахлорэтилен CC12-CC12 20 1,619 1,5055 9433
1759 1760 1761 П роп илтриизобутилсви нец Атрактилен 2, 3, 4-Трихлорфуран CsH7Pb(C4Hs)3 C16H,4 C4HC13O 19,6 20 20 1,351 0,927 1,547 l,i>056 1,5057 1,5057 8572
862
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолтение
№ по пор. Название Формула «,°С “4 "о № по табл. «Свойства органических соединений»
1762 Этил-п-толнловый эфир СН,С6Н<ОС!Н5 17,6 0,8 1,5058 7549
1763 Метиловый эфир карвак- (СН3)2СНС6На(СН3)ОСН3 20 0,944 1,506 —
1764 Нзоамиловый эфир салициловой к-ты НОСеН4СООС3Нц 20 1,05 1,506 6958
1765 1, 2-Дибромгексаи СН3(СН2)3СНВгСН2Вг 13,5 1,596 1,5060 —
1766 Этиловый эфир о-толокси-уксусной к-ты СН3С6Н4ОСН2СООС2Н5 12,9 1,085 1,5061 —
1767 Диэтилдисульфид (C2H5)2S2 20 0,99267 1,50633 9375
1768 Метилэтилпроп ил изоамил- (СНз) (С2Н5) (С3Н,)РЬС5Н,1 21 1,479 1,5064 —
1769 Этиловый эфир кумалино-вой к-ты СН=СНСООСН=ССООС2Н5 1 1 39,2 1,209 1,5066 —
1770 Днэтилпропнлнзоамилсви- (С2Н5)2(СзН,)РЬС5Нц 22,1 1,439 1,5066 —
1771 нец Метилпиразии CH3C-CHN=CHCH=N 1 1 18,7 1,030 1,5067 —
1772 Трипропилизобутилсвинец (С3Н7) .РЬС4Н9 22,6 1,403 1,5067 —
1773 Этиловый эфир бензойной к-ты СвН5СООС2Н5 17,3 1,0496 1,5068 1241
1774 4-Этокси-л/-ксилол (СН3)2С6НаОС2Н6 14 0,949 1,5069 —
1775 Этиловый эфир «-(!, 3-ди-метил циклогексилидеи -5) -пропионовой к-ты (СНг)2С6Нй.= С(СН3)СООС2П5 20 0,969 1,5069 —
1776 7-Метил-2-этилтетрагидро-иидазол C2H5NCH = C£H7(CH3)=N 20 0,990 1,507 —
1777 2» 2, 7-Триметилкумаранон (т. пл. 68°) СНзС6НзСОС(СН3)2О 1 1 100,6 1,001 1,507 —
1778 Изобутиловый эфир анисовой к-ты СН3ОСеН4СООС4Н9 20 1,052 1,507 —
1779 З-Оксиметилен- НОС 1 -метилциклогексаион-2 1 = ССОСН(СН3)СН£СН2СН2 1 1 15,4 1,056 1,507 —
1780 1, З-Дибромбутан CH.CHBrCH2CH2Br 20 1,806 1,507
1781 Этиловый эфир о-толуило-вой к-ты CH.,CeH.COOC2IU 21,6 1,033 1,5070 7610
1782 /-Кадииеи С15Н24 20 0,918 1,5073 —
1783 Метилдиэтилизоамнлсви-нец (СН3)(С2Н5)2РЬС5Ни 20,8 1,523 1,5078 —
1784 Диметилэтилизобутилсви- (CH3)2(C2Hs)PbC4H9 20,7 1,623 1,5078 —
1785 нец 2, З-Дибромпентан C2Ha(CHBr)aCH3 20 1,678 1,5078 —
1786 Этил-о-толиловый эфир СН3С£Н4ОС2Н5 13,3 0,959 1,5079 7547
178/ Этиловый эфир иодук-СУСНОЙ к-ты JCH2COOC2H6 12,7 1,817 1,5079 —
1788 1, 2-Дифтор-1, 1, 2-трибром-этан CBr2FCHBrF 17,5 2,6 1,5079 —
1789 З-Метил-1 -фенилбутаиол-1 C£HSCH(OH)CH2CH(CH3)2 18 0,9597 1,50798 2049
1790 Аллилтимиловый эфир (СНз) (С3Н7)С£Н3ОСН2СН = СН2 20 0,935 1,508 —
1791 Бутиловый эфир анисовой к-ты СН3ОС£Н4СООС4Н9 20 1,054 1,508 -
1792 Тропакокаин C15H19NO2 100 1,043 1,5080 7934
1793 З-Хлор-а-камфорилдихло- С,9Н13О2С13 31,3 1,322 1,5080 —
1794 рид Этиловый эфир бензоил-этилуксусной к-ты CcHr.COCH (С2Н5) СООСгНг 20 1,066 1,5082
1795 Диэтиловый эфир изофта-левой к-ты С£Н4(СООС2Н5)2 17,5 1,13 1,5082 3839
1796 Диизоамнлаиилии C£H6N(C9H„)2 24,9 0,889 1,5083 ——
1797 Амиловый эфир 2-фурилакриловой к-ты С4Н3ОСН=СНСОО(СН2)4СНз 20 1,032 1,5083 8577
f63
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C । nD № по табл. «Свойства органических соединений»
1798 Нитрил V, Y. Y-трихлоркро-тоновой к-ты CI3CCH=CHCN 20 1,420 1,5083 -
1799 Фенетол С6Н5ОС2Н5 18,8 0,97 1,5084 8183
1800 1, 2, 3, 4-Тетраэтилбензол С6Н2(С2Н5), 19,6 0,887 1,5085 1590
1801 Пропиловый эфир изотио-циановой к-ты C3H7NCS 16 0,9781 1,5085 3824
1802 Изоамиловый эфир анисовой к-ты СНгОС6Н«СООС5Н11 20 1,040 1,5085 —
1803 трет-Бутилфеинлкетоп С6Н5СОС(СН3)3 19,2 0,968 1,5086 •—-
1804 Д иэтилдиизоб утилсвинец (СаНвНРЬССдНоЬ 20 1,444 1,5086 —
1805 Диметилдипропилсвинец (СНз)2РЬ(СзН7)2 20 1,627 1,5086 —
1806 Эукарвон 21,2 0,948 1,5087
1807 3, З-Диэтилфталид СбН4СО—О—С(С2Н5)з 1 1 61,6 1,040 1,5087 —
1808 Фурфуриловый эфир (С4Н3О • СН2)2О 20 1,140 1,5088 8625
1809 Этиловый эфир п-толуило-вой к-ты СН3С6Н(СООС2Н5 18,2 1,03 1,50888 7634
1810 1 - Ф ен ил п ентен-2 CellsCH^H-CHCsHs 16,2 0,888 1,5089 —
1811 2, 3, 5-Триметилпиррол СН3С- СНС(СНз) = С(СНа) NI I 1 1 15,8 0,935 1,509 —
1812 Псевдокумилэтиловый эфир Пиридин (СН3)аС6Н2ОС2Н5 20 0,942 1,509 —
1813 N=CHCH=CHCH«=CH 1 1 20 0,982 1,509 6232
1814 Моноэтиловый эфир фталевой к-ты СеН, (СООС2Н5) соон 22 1,1877 1,509 8503
1815 Р-Санталол С15Н24О 20 0,972 1,5091 —
1816 Метиловый эфир а-толу^ иловой к-ты CtHsCH2COOCHa 16 1,044 1,5091 7640
1817 Метилтрипропилсвинец (С3Н7)3РЬСНз 22,3 1,522 1,5091 —
1818 Триметилпропилсвииец (СНз)зРЬСзНг 20 1,767 1,5095 —
1819 Триэтилизоамилсвииец (C2H5)3PbC5Hn 20 1,484 1,5099 —
1820 ж-Толуиловая к-та СН3С6Н4СООН 111,6 1,054 1,51 7620
1821 Фенилуксусная к-та СеН5СНгСООН 79,8 1,081 1,51 7637
1822 4-Этокси-о-ксилол (СНз)2С6НзОС2Н6 20 0,950 1,510 —•
1823 З-Этокси-о-ксилол (CHshCeHgOCsHs 20 0,952 1,510 ——
1824 о-Этилбензойная к-та СДЬСсП.СООП 99,6 1,042 1,51012 1409
1825 5-Этил псевдокумол (СНз)зС(.Н2С2Н5 15,8 0,887 1,5105 —
1826 Бензилацетон Сг,Н6СН2СН2СОСНз 22 0,9849 1,511 2071
1827 1, 6-Дибромгексан (СН2СН2СН2Вг)2 15 1,595 1,5111 —•
1828 Этилтрипропилсвинец С2Н5РЬ(С3Н7)3 21,3 1,485 1,5115 —
1829 1, 2-Дибром-2-метилпропаи (СНз)2СВгСН2Вг 20 1,7827 1,51186 6442
1830 2, 7-Днметилтетрагидро-индазол С H3NCH = С6Н; (СН3) = N 1 1 20 1,012 1,512
1831 О-Толуиловая к-та СНзС6Н4СООН 114,6 1,062 1,512 7606
1832 1» 1, 2, 3, З-Пентахлорпро- НСС12СНС1СНС12 20 1,6 1,512 —
1833 пан З-Метокси-о-ксилол (СНз)2С«Н.,ОСНз 39,7 0,960 1,5120 —
1834 Диэтилпропилизобутил- (С2Н6)2(С3Н7)РЬСН2СН(СНз)2 20 1,489 1,5120 —
1835 свинец Тетраметилсвинец РЬ(СНз), 20 1,9951 1,5120 7009
1836 1-Оксиметиленциклогекса-нон-2 СН2(СН2)зСОС=СНОН 20,5 1,08о 1,5122 —
1837 Метил-n-толиловый эфир СН3С,Н4ОСН3 19,3 0,9709 1,51237 5129
1838 4-Этилнден-1. 1,3, 6-тетра-метилциклогексадиен-2, 5 (СН3)4СеН2-СНСНа 20 0,880 1,5125 —
1839 Изокапрофенон (CH3bCH(CH2)2COCeHs 15 0,962 1,5125 3724
1840 Метиловый эфир О-мето-ксигидрокоричной к-ты СНзОС6Н4СН2СН2СООСНз 18,4 1,095 1,5126 —
1841 Этилмезнтилен (СНз).,С6Н2С2Н5 16,4 0,889 1,о127 ——
1842 Триэтилнзобутнлсвииец (С,Н5)зРЬС.Нв 20 1,531 1,5127
1843 1. 1-Дпбромэтан СН3СНВг2 20 2,089 1,512767 9181
864
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
П родолжение
С, № по табл,-
с «Свойства
о Название Формула (,rC ri4 nD органиче-
ских соеди-
нений»
1844 Изсамилэвгенилсвый СЬ эфнр 1-СНСН1С,В3(ОСВ..)ОС5Н1| 14,8 0,973 1,5128 -
1845 Бутиловый эфир 2-фура и- С,Н3ОСН=СНСООС<НЬ 20 1,0482 1,5129 8578
акриловой к-ты 0,949
1846 Эти л-л-толиловый эфир СНгС,.Н4ОС;Н., 20 1,513 7548
1847 5-Метокси -1, 3-диметвлбеи- (CHJiCtH.OCHs 20 0,958 1,513 —
1848 2-Этил тиофен C.H.C=CHCH-CHS 1 1 20 0,992 1,513 7437
1849 П-ТОЛИЛОБЫЙ эфир СН..СН=С(С Hc)CO2C,H.CHs 20 1,039 1,513 —
а-этилкротоновой и-ты 0,946
1850 З-Метокси-i, 5-диметил-2, 4-диэтилбензол (СНо)ЛС.Н£);СеНОСНг 20 1,513
0,915 1,5131
1851 2-Диметил амиио-1, 3-диме- (CH3)3CtH3N(CH3): 20 —
тилбензол 20 0,9753
1852 2, 3, 5-Триметилтнофен Йодистый этил (CH3)3C4HS 1,5131 7453
1853 CHsCHJ 20 1,933 1,5133 9343
1854 Изодурол (CH3)4Cr,H2 20 0,8906 1,5134 3706
1855 Гемимеллитол CeH3(CH3)3 19,6 0,894 1,5134 2524
1856 4-Этилидеи-1, 1-ди метил- (CHs)2CcH.=CHCH3 20 0,857 1,5135 —
циклогекса диен-2, 5 15,3 0,991 1,51385
1857 Изовалерофенон (CH.,)2CHCJi.COC,llt 3689
1858 4-Метилен-1, I, 2-триметил- (CH3)3CtH3-CH2 20 0,866 1,5139 —
циклогексадиен-2, 5 0,948
1859 5-Аллилокси-1, 3-диметил- (CH3)1CfHaOCH2CH-CH2 20 1,314 —
бензол 1,09
I860 Пролиловый эфир анисо- CHjOCtH.COOC.H, 20 1,514 —
вой к-ты 1,222
1861 м- Фторфенол FC.H.OH 20 1,514 —
1862 Этиловый эфир диэтил- CHsOC, 1 :.,coc (c. ns) co c2i h 20 1,086 1,5140 —
о- метоксибензоил) -уксус-
ной к-ты 22,1 19 1,643
1863 Метнлдиэтвлпропилсвинец (CH.HC!B!.)2PbC,H; 1,5141 —
1864 2, 5-Ди метилтиофен (Cb3)2c,h3s 0,9859 1,51418 7439
1865 ₽, fJ-Диметвл-а-этилстирол C(.H5C(C2H5)-C(CH3)2 17,5 0,889 1,5142 .—
1866 Этиловый эфир изотиоцва- ch2ch2ncs 18 1,5142 3828
новой к-ты 20 0,9i>9
1867 Аллилбензол C.HsCHjCH-CH- 1,5143 —
1868 Изопропиловый эфир 2- C.H.OC H = CHCOOCH (CH:,)2 20 l,05U 1 5146 —
1869 фурилакрнловой к-ты 1,70
1. 5-Дибромпеитан Br(CH,)fBr 15 20 1,3146 5986
1870 4-Метилен-1, 1, 3, 6-тетра- (CH3).CfH; = CH2 0,877 1,5147 —
1871 мстилциклогексаднсн-2. 5 0,879
4-Метилен-1, 1, 2, 6-тетра- (CHj)4CcHi = CH; 20 1,5149 —
1872 метилциклогсксадиеи-2, 5 1,533
Диэтилдипропилсвинец (C2B5)2Pb(C.,H,). 20 1,5149 —
1873 5-Метокси-1. 3-диметил- (CH,),(C-H:)C(H.OCH. 20 1,515 —
4 этилбензол 20 0,963
1874 М еток с и п - ксилол CB3OC,Hs(CH.b C( H„(COOCH.)2 1,515 —•
1875 Ди метиловый эфир фтале- 20,/ 1,1905 1,515 8499
вой к-ты 45,8 1,207
1876 4 Дихлорметил- • СН3С = CHCOC(CU,)(CHCls)CH.CH- 1,5151 —
1, 4-лиметилцикло- | 1
гекссн-1-он-З 1,113
1877 а-Ацетокси пропиофенон CtH.COCH(CH-.)OCOCH-, 19,7 2) 1,5153
1878 Т риметмлэтиловинем (CH.hPbC.H, 1,882 1,5154 —
1879 2, 7-Диамоксвнафталвн CtcHvtOCcHiilj 99, б’ 0,934 1,5155 —
1880 Треххлористый фосфор PCh 14 0,764 1,516 —
1881 Гептатриен-1. 3, 5 CHL=CHCH-CHCH- CHCHa 20 1.516 —
1882 Э ти л г е м и мел л мтени л с вы й (CH.bCelI.OC H.. (1. 2. 3, 5) 20 0,956 1,516 —
эфир 0,879
1883 1, 1, З-Трнметил-4-этилилен- (CH..).C,H. = CHCH 20 1,5160 —
циклогексадиен-2. 5 99,9 0,941
1884 1. 5-Диамок* ннафталвн C.cHtCOCtH.i): 1,5160 —
(Т пл 't')
;65
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t,°c 4 "о № по табл. «Свойства органических соединений»
1885 Диметил-л-толилкарбинол СН3СеН4С(СНэ)2ОН 20 0,977 1,5162
1886 а, р, Р-Триметилстирол С«Н5С(СН3) = С(СН3)2 20 0,892 1,5164
1887 Метил-л-толиловый эфир СНзС6Н,ОСНз 12,9 0,978 1,5164 5128
1888 а-Бромкротоновый альде- СНзСН=СВгСНО 23 1,566 1,5165 —
гид 18.7 0,892
1889 Р, Р-Диэтилстирол СвН5СН=С(С2Н5)2 1,5168
1890 Метилбензилкетон СНзСОСН2СеНб 20 1,0157 1,5168 6580
1891 Триэтилпропилсвинец (С2Н5)3РЬС3Н2 20 1,589 1,5168 —
1892 Этиловый эфир 3-метил- (СНз) (С2НзО) С6Н3СООС,Н5 20 1,057 1,5169
4-этоксибензойной к-ты 0,965
1893 Аллил-о-толиловый эфир СН3СеН4ОСН2СН=СН2 20 1,517 208
1894 7-Метокси-о-ксилол (СН3)2С6Н3ОСН3 20 0,969 1,517 —
1895 2-М ети л тет ра ги дрои нда зол CH3NCH=C6H8=N 1 1 20 1,030 1,517 —
1896 Этиловый эфир л-метокси- CHgOCfjI ЦСООСИ 1g 16,4 1,103 1,5170
бензойной к-ты 0,970 1
1897 4-Метокси-ле-ксилол (СНзНСзНзОСНз 12,9 1,5173 —-
1898 1-Фенилпропанол-2 СвН5С1 ЬСНОНСНз 20 0,991 1,5174
1899 Бензилтетрагидрофурфури- С4Н7ОСН2ОСН2С8Н8 20 1,048 1,5174 —
1900 ловый эфир 2, 4, 6-Три метил ацетофе- (СНз)зС6Н2СОСНз 20 0,975 1,5175 —
1901 2-Ацетокси-Р-метилстирол СН3СООСеН4СН=СНСН3 13,5 1,048 1,5175
1902 Хлорангидрид V, у, у-три- С13ССН=СНСОС1 20 1,528 1,5176 —
1903 хлоркротоиовой к-ты Пропиофеиои-о-карбоновая CJIsCOCJhCOOH 99,1 1,140 1,5177
1904 к-та (т. пл. 93° С)
1-Д ихлорметил-1-ме- СН3С (СНС12) СОСН •= С (С3Н7) СН2СН2 15,8 1,165 • 1,5177 —
ТИЛ-4-ИЗОПрОПИЛ- I 1
1905 циклогексен-З-он-2 Диметилдиэтилсвинец (CH3)2Pb(C2Hs)2 20 1,785 1,5177
1906 n-Этокси алл ил бензол С2Н5ОС8Н4СН2СН=СН2 12,2 0,961 1,5179
1907 Анизол СеНзОСНз 20 0,9954 1,51791 337
1908 Диэтилтеллур (С2Н5)2Те 15 1,599 1,5182 9516
1909 Метилтриэтилсвинец CH3Pb(C2Hs)3 20 1,713 1,5183 —
1910 п-Метнлизобутирофенон (СН3)2СНСОСвН4СН3 21,2 0,968 1,5187
1911 Метил-о-толиловый эфир СН3С8Н4ОСН3 15,3 0,985 1,5189 5127
1912 4-Бром-1, 3-диметил пиразол CH3NCH = CBrC(CH3) =N 20 1,490 1,519 —
1913 Метил псевдокумиловый (СНз)зС6Н2ОСНз (1,2,4, 5) 20 0,964 1,519
1914 эфир
ТподиглиКОЛЬ S(CH2CH2OH)2 20 1,1824 1,519 7379
1915 Этиловый эфир бензоил- CeHsCOCOOC^Hg 25,1 1,122 1,5190 ——
1916 муравьиной к-ты
1, 2-Дихлор-1-бромэтилен С1ВгС = СНС1 16 1,91 1,5190
1917 2, З-Д и метилтиофен (CH3)2C4H2S 20 1,0021 1,5192 7437
1918 Этиловый эфир СН3С Н4С (СНз) = С (СН3) СООСгНз 18,5 1,ооз 1,5192 —
п, а, Р-триметилкоричной
1919 к-ты 2-Ацетил-5-метилтетрагид- CHaCONCH = С8Н, (СН3) = N 20 1,079 1,5192 —
роиидазол 1 1
1920 п-Хлортолуол СН3С6Н,С1 24,4 1,06 1,5193 7754
1921 л-Фтораиилин fc6h4nh2 20 1,1725 1,51954 478
1922 Изобутирофеиои (СНз)2СНСОС6Нз 16 0,9871 1,5196 3667
1923 ₽-Ионон С10Н,Е=СНСОСН3 18,9 0,95 1,51977 3932
1924 Тетраэтилсвинец (С2Н5)4РЬ 20 1,6528 1,5198 7011
1925 З-Метокси-З-этилфталид СвН4С(СзН5) (ОСНз)ОСО 1 1 20,4 1,132 1,5199 —
1926 Пеитаэтилбензол СбН(СгН5)5 20,3 0,896 1,52 1565
1927 4-Бром-З-метилпиразол CH = CBrC(CH3)=NNH 1 1 99,6 1,564 1,52 —
1928 Этиловый эфир jw-хлорбен- ЙСоНЛООСгН, 20 1,181 1,520
зойной к-ты
866
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор, Название Формула f,°C 4 "D № по табл. «Свойства органических соединений»
1929 Нитрил - а, р-дибромвале- CH3CH2CHBrCHBrCN 20 1,756 1,520
риаиовой к-ты 0,996
1930 Этилфенилкарбинол С2Н6СНОНС6Н6 20 1,5200 6553
1931 4-Диметиламиио-о-ксилол (CH3)2CeH3N(CH3)2 20 0,916 1,5201 —
1932 Преиитол (СН3)4С„Н2 16 0,90 1,5203 6410
1933 1, 2-Дибромпропан СН2ВгСНВгСН3 20 1,9333 1,5203 6439
1934 Метиловый эфир беизой- С6Н5СООСН3 15 1,0937 1,5205 1234
иой к-ты
1935 Эвгениловый эфир уксус- C12H14O3 20 1,084 1,5207 —
иой к-ты
1936 а-Метил бензиловый спирт СвНбСНОНСНз 20 1,013 1,5211 1173
1937 Этиловый эфир а, Р-Ди- CeHsC(CH3) = C(CHJ CO2C2Hs 15,2 1,020 1,5212 —
1938 метилкоричиой к-ты О-Тетраэтилдиамииобензол CfiHjN (CsHgHL 12,6 0,927 1,5213 —
1939 Этиловый эфир Р, Р-ДИ- Cl2CHCH(CcH4CH3)COOC2Hs 18,7 1,202 1,5214 —•
хлор-а-(я-толил)-пропионовой к-ты
1940 Ди хлор а и гидрид хлорфу- C1COCC1=C1ICOC1 17,6 1,566 1,5217 —
маровой к-ты CH3CeH3(OCH3)COCH (CH,)2
1941 З-Изобутиро-4-метоксито- 13,7 1,024 1,5218 —
1942 луо л Диметилдисульфнд CHsSSCHs 16 1,057 1,52192 5084
1943 Р, р-Диметилтиофеи (CH3)2C,H2S 15 0,99 1,522 —-
1944 5-Хлор-2, 2-диметил-кума- C1C6H3COC(CH3)2O 99,6 1,148 1,522 —
раной (т. пл. 67° С) 1 1
1945 Ацеталь феиилпропиоло- CeHsC^CCHtOCjHs)! 13 0,994 1,5222 —
вого альдегида 1,5225
1946 л-Хлортолуол CH3C6H.CI 18,7 1,07 7753
1947 Ацетилсалициловый альде- CH3COOCBH4CHO 44,5 1,158 1,5225 —
1948 гид Этиловый эфир салицило- HOC6H.COOCH2CH3 20 1,131 1,5226 6963
вой к-ты
1949 Тимол (CH3) (C3H,)CBH3OH 20 0,969 1,5227 7356
19.50 Пропиловый эфир Р-2-фу- С.НдОСН=CHCOOC3H7 20 1,0744 1,5229 8580
1951 рилакриловой к-ты Карвакрол CH3(C3H7)CBH3OH 20 0,976 1,52295 4239
1952 Аллил-2, 5-диаллилфенило- (C3H5)2CBH3OC3H5 20 0,950 1,523 —
1953 вый эфир Этиловый эфир о-хлорбеи- C1CBH4COOC2H5 20 1,189 1,523 —
1954 ЗОИНОЙ к-ты Бензиловый эфир хлорук- C1CH2COOCH2CBH5 20 1,2 1,523 —
1955 сусной к-ты Эстрагол CH2=CHCH2CBH4OCH3 17,3 0,971 1,5230 9155
1956 Пиридазин n-nch=chch=ch 1 1 23,5 1,1035 1,5231 6228
1957 1 Дихлорметил-1-ме- СН3С( CHC12)COCH=C(C2HS)CH2CH2 17 1,196 1,5233 —
тил-4-этвлциклоге- 1 1
ксен-З-он-2
1958 Этиловый эфир Y, Т-ДИ- CI2CHCHBrCHBrCOOC2Hs 20 1,830 1,5235 —
1959 хлор-а, Р-диброммасляной к-ты
о-Хлортолуол CH3CBH4CI 20 1,0817 1,5238 7752
I960 Этиловый эфир о-метокси- CH3OCBH4COOC2HB 14,6 1,116 1,5238 —
1961 бензойной к-ты 1, 4-Пирои OCH=CHCOCH=CH 1 1 40,3 1,190 1,5238 6349
CHC12 CH,
1962 1-Дихлорметил-1, 4, 5-три- СНзССОСН=CCH (CH3) CH2 20 1,197 1,5238 —
метилциклогексен-З-он-2 1 1
1963 2-Метил-6-изопропилфеиол (СН3)(С3Н7)СеН3ОН 15,2 0,987 1,5239 —
1964 Диметилаллиланизол (1,3. (CH3)2(C3HS)C6H2OCH3 20 0,960 1,524 —
4. 5)
55*
867
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t. °C "о № по табл. «Свойства органических соединений»
1965 Аллил-2-аллилфенилоаый С эфир Метилгемеллитиловый эфир о-Аллиланизол Н2 = CHCH2CsH.OCH2CH=СН2 20 0,963 1,524 —
1966 (СН,)зСеН2ОСН, (1.2. 3.5) 20 0,976 1.524
1967 СН3ОС.Н.СН2СН=СН2 20 0,972 1,524 1,524 —
1968 Этиловый эфир п-хлорбензойной к-ты CICsHiCOOCzHs 20 1,181 —
1969 Метиловый эфир пропиофенон-о-карбоиовой СаН5СОС6Н.СООСН3 15,2 1,129 1.5240 —
1970 о-Метил ацетофенон СНзСОСсН.СНз 16,8 1,001 1,5242 —
1971 Нитрил фенилуксусной к-ты c6h6ch2cn 20 1,018 1,5242 7665 7973
1972 Бензиловый эфир уксусной к-ты СНзСООСН2С8Н5 21 1,06 1,5242'
1973 1 -Метил-З-оксиэтилбензол СН3СН(ОН)СбН4СНз 20 0,993 1,5243 7427
1974 Тиофен SCH-CHCH=CH 1 1 20 1,0617 1,5246
1975 Трифенилфосфнн (СЕН5)3Р 69 1,1 1,52475 8476
1976 Хлорбензол CeHsCl 20 1,1066 1,52479 1627
1977 Этиловый эфир анисовой СНзОСгН.СООСгН; 20 1,106 1,5249 500
1978 к-ты 1, З-Дибромпропан Вг(СНг)3Вг 15 1,987 1,5249 6440
1979 гс-Метилбутирофенон СгНьС! 1.СОС,.Н,СНз 20 0,97 1,5250 —
1980 Этиловый эфир гидроку-мариловой к-ты С6Н.СН2СН(СООС2Н6)О 1 .. 1 13,9 1,154 1,5250
1981 Бензиловый эфир молочной к-ты СН3СН(ОН)СООСН2СбН5 25 0,9286. 1,5252 —
1982 N, N-Диметил-о-толуидин CH.,C(,H.N(CH3)2 20 1,5255 7565
1983 Фенилуксусиый альдегид свньси2сно 19,6 1,0272 1,525а 7660
1984 Метилизотиоцианат CHsNCS 37,2 1,06912 1,52576 3823
1985 о-Аллилтимол (СН3)(С3Н№Н2(СзН5)ОН 20 0,966 1,526 —
1986 Этиловый эфир 2-тиофенкарбоновой к-ты SCH = CHCH = CCOOC2H5 1 1 20 1,159 1,526
1987 Бензиловый эфир дихлоруксусной к-ты С12СНСООСН2СсН5 20 1.3 1,526 —
1988 4, 7-Диметил-2. 2-диэтил-индандион-1. 3 (СН3)2С6Н2СОС(С2Н5)2СО 1 1 62,4 1.017 1,5260
1989 Фурфурол осн=снсн-ссно 1 1 20 1,1598 1,52608 8627
1990 Тропилидии СН2(СН = СН)2СН = СН 1 1 20 0,888 1,5261 —
1991 Этиловый эфир атроповой C6H5C(=CH2)COOC2HS 16,1 1,051 1,5261 —
1992 ж-Фториитробснзол FCeH,NO2 19 1,3254 1,52622 1551
1993 Аллиловый эфир изотио-циановой к-ты ch2=chch2ncs 20 1,013 1,5266 3813
1994 1, 4-Дихлорбензол С6Н4С12 69,9 1,4 1,5266 1508
1995 Фенэтиловый спирт С6Н6СН2СН2ОН 18 1,02 1,5267 8385
1996 Хлористый тиоиил SOCI2 10 0,990 1,527 —
1997 п-Метилпропиофенон C2HsCOC6H<CHj 20,7 1,5271 —
1998 о-Толунитрил CH.C.slb.CN 25 0,9941 0,899 1,52720 7662
1999 В. В-Диметилстирол C6H5CH = C(CH3)2 19,6 1,5273 —
2000 Этиловый эфир СНг—СНСНгСвНзСОСгНбЮСНз (1,3,4) хавибстола 11,5 1,013 1,5276 —
2001 Метиловый эфир алло-Р-метилкоричной к-ты CcHr,C(CH3) -СНСООСНз 38,1 1,037 1,5276 —
2002 2, 5-Диметилкумаран СНзСсНзСН2СН(СНз)О 1 1 13,7 1,015 1,5279 —
2003 /-Никотин C10H14N2 20 1,0097 1,5280 5633
2004 3-Ацетокси-5-метил-2-изо- СНзСбН^СЮСОСНз) =С(С3Н7) О пропилкумарон 1 [ 20 1,081 1,5281
868
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
О с о с Название Формула t, °C d4 nD № по табл. «Свойства органических соединений»
2005 3. 4-Дибром-!, !, 4-триме-тилциклогексан (СН3)3СсН,В» 18,7 1,532 1,5281 -
2006 1, 1-Дихлор-2-(п-толил)-бу-тан С2Н6СН(СсН,СН3)СНС12 19,8 1,112 1,5283 —
2007 Элем иц ин СН2=СНСН2С6Н2(ОСН3)3 20 • 1,063 1.5285 —
2008 Этиловый эфир 0-2-фур ил -акриловой к-ты С,Н,ОСН-СНСООС,НЬ 20 1,0891 1,5286 8581
2009 о-(а-Бромизобутирил)- СН3СООСбНл(СН3)СОСВг(СНзИ n-крезиловый эфир уксусной к-ты 25,7 1,317 1,5288 —
2010 Бензиловый эфир трихлор’ уксусной к-ты С1,ССООСН2С6Н5 18,8 1,38 1,5288 —
2011 Нитрил бензойной к-ты CcHsCN 20 1,005 1,52892 1731
2012 О-Фенил-0. у-ангеликалак-тон C6HSCH2C = CHCH,COO 1 1 20 1,113 1,529 —
2013 Йодистый метил CH3J 21 2,277 1,5293 5068
2014 2. 7-Диметилкумараи СН3СЬН.,СН2СН(СН3)О 1 1 13,8 1,015 1,5297 —
2015 Кумалии сн=снсн=сносо 1 1 20 1,198 1,5298 -
2016 2. 2, 2-Трихлор-1. 1-дибром-этан BtjCHCCl., 25,7 2,3 1,5299 -
2017 Этилэвгениловый эфир С2Н5ОС10Н,,О 18,3 1,014 1,53 —
2018 Вератрол СбНаоснзъ 21 1,08 1,53 2295
2019 Трихлорбромметан СВгСЬ 20 1,94 1,5300 4931
2020 n-Куминовый альдегид C3lI,Cf.H3CHO 20 0,978 1,5301 4598
2021 2, 4-Диметилацетофенон (СНзЬСсНзСОСНл 18,6 0,996 1,5301
2022 3-Ацетокси-4,6-диметил-2 (СНзЬСбНАДОСОСНз) =» С(С2Н5)О этилкумарон 1 1 20 1,078 1,5303 —
2023 а-Этоксистирол СбН5С(ОС2Н5)~СН2 17,5 0,977 1,5304 —
2024 (0-Мезитиламин (CHS)2CSH3CH2NH2 20,5 0,950 1,5305 ——
2025 З-Изопропенил-4-метокси-толуол СНзС( = СН2»СъН3(ОСН3)СН, 17,6 0,966 1,5308 —
2026 2-Нитро-п-цимол (CH.)2CHC6H3(CH:,)NO2 20 1,0744 1,53093 оа) 1
2027 5-Метил-2, 2-диэтилкума-раиои CH3CeH3COC(C2H5)2O 1 1 22,6 1,032 1,531 —
2028 2- Ацетнлтетрагидроинда -зол CH;CONCH=CeHe=N I 1 20 1,119 1,531 —
2029 Этиловый эфир бснзоилук-сусной к-ты CSH5COCH2COOC2H5 16 1.12 1,53115 8004
2030 Псевдо нонон 18,8 0,90 1,5312 —
2031 d-Спартеин 20 1,027 1,5312 7119
2032 Этиловый эфир бензоил-формилуксусной к-ты CJIsCOCH (CHO) COOC2H5 24,9 1,140 1,5313 —
2033 4-Метокси-З-пропиотолуол CH3C6H (OCH.)COC2H5 20 1,047 1,5313
2034 Ди -(а-хлорэтия) сульфид (CH3CHC1)2S 20 1,27 1,5313 —
2035 а. а-Ди метил бензиловый спирт C6H6C(OH) (CH3)2 19 0,9724 1,5314 6566
2036 2-Метокси-а-метилстирол CH<OCcH.C(CH )=CH2 19 0,99 1,5315 —
2037 л-Фторнитробензол fc0h<no2 20 1,3300 1,53156 1552
2038 Этиловый эфир 1-метилциклогексен- 1 -метилен-карбоновой-3 к-ты CH3CeH, = CHCOOC2H5 20 0,998 1,5319 —
2039 Бутирофенон CH3CH2CH2COC0H3 20 0,988 1,532 2223
2040 2-Изовалеро-л-крезол (CHsljCHCH^OCcH.fCHjjOH 20 1,028 1,5320 —
2041 2-Этокси-2. 5-диметилкума-ранон CH3C6H3COC(CH3) (OC,Hb)O 1 1 14,1 1,103 1,5322 —
2042 а-Нитротолуол CbH5CH2NO2 20 1,16 1,5323
2043 о-Фториитробеизол FCtHtNQ, "1 1.338 1,5323 1550
869
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
•№ по пор. Название Формула 1, °C 4 t nD № по табл. «Свойства оргвииче-ских соединений»
2044 З-Ацетокси-а-метилстирол СНзСООСб! 1.С (СНз) =сн2 14,1 15,3 1,061 1,5325
2045 ж-Метилацетофеиои СНзСОСбН.СНз 1,011 1,5327 —
2046 Диметил ртуть Не(СН3)2 22,2 2,95412 1,5327 6924
2047 1-Дихлорметил 1-метил- СН3С(СНС12)СОСН= СНСН = СН 33,5 1,270 1,5328 —
циклогексадиеи-3, 5-ои-2 1 1
2048 Феиилциклогексан СбНбСсНп 20 0,9502 1,5329 8924
2049 а-Бензилоксим окиси ме- (СН3)2С-=СНС(СН3) = 20 0,987 1,533 —
2050 зитила = NOCH2C6Hb -
Аллилгваяциловый эфир СНзОСвН.ОС! 12СН=СН2 20 1,054 1,533 —
2051 Гексагидронафталин CjoH|4 18,4 0,94 1,53311 5347
2052 л-(а-Оксиэтил-)-толуол СНзСеН.СН(ОН)СНз 20 1,003 1,5332 —
2053 Изоспартеин 17 1,028 1,5332 —
2054 л-Метилацетофенои (т. пл. СНзСОСбН.СНз 20 1,0051 1,5335 963
28е С)
2055 Этиловый эфир р-ЭТОКСИ- CeHsCfOQHs) =CI 1СООС2Н3 16 1,074 1,5336 —
коричной к-ты 1,225 1,5336
2056 1-Ди хлор мет ил-1,5 ди- СН3С(СНС12)СОСН = СНС(СН3) = СН 20 ——
метилциклогекса- [ I
2057 диеи-3,5-он 2 цис-\, 2-Дибромпропилеи CHsCBr=CHBr 17,4 2,02 1,5337 —
2058 2-Метилкумараи СеН.СН2СН(СН2)О 1 1 13,7 1,036 1,5338 —
2059 а. Р-Диметилстирол С6НзС(СНз) = СНСНз 19,7 0,910 1,5339 —
2050 Этилфенилкетои С2Н5СОС6Н5 20 1,012 1,534 8227
2061 1, З-Диметил-5-феиилцикло-гексен-3 (СНз)2(СбН6)С6Н7 20 0,942 1,5341 —
2062 а-Тр и азотолуол СбН6СН2Мз 24,9 1,066 1,5341 7739
2063 Ацетофенон СНзСОСбНб 20 1,026 1,53418 939
2064 Метиловый эфир о-мето- СНзОСбН.СООСНз 19,5 1,157 1,5342
2065 ксибензойной к-ты
1-Дихлорметил-1-метил- СН3С(СНС12)СН = СНСОСН = СН 56,2 1,26 1,5342 —
циклогексадиеи-2, 5-ои-4 1 1
2066 3-Ацетокси-5-метил-2-этил- СН3СбН3С(ООССН3)«= С(С2Н5)О 20 1,107 1,5343 —
кумарои 1 1
2067 4-Метил-а-метилстирол СН3СбН.С(СН,)=СН2 18,7 0,902 1,5345 —
2068 ж-Этилбензойная к-та С2Н5СбН.СООН 100 1,042 1,5345 1410
2069 л-Нитротолуол СНзС6Н4НО2 62,5 1,13 1,5346 7723
2070 2-Этил-5, 6, 7, 8-тетрагидро- СгНвСюНц 17,6 0,950 1,5347 —
2071 нафталин
о-(5-оксиизобутиро)- (СН3)2СОНСОС6Н3(ОН)(СН3) (2,1.4) 54 1,094 1,5347 —
2072 72-КреЗОЛ
Этиловый эфир 2, 3-дигид- С10Н9СООС2Н5 20 1,089 1,535 —
2073 ронафтойной-1 к-ты а-Этилбензальдоксим C6H5CH = NOC2Hs 21,7 0,992 1,5350 —
2074 Индан СеН.СН2СН2СН2 1 1 20,8 0,96 1,5351 3888
2075 З-Метоксифталид СбН.СООСН(ОСНз) 1 1 22,8 1,215 1,5352 —
2076 Креозол СНзОСбНз(СНз)ОН 25 1,0919 1,5353 4437
2077 2, 5-Диметокси-а-оксипро- (3, 1, 4) (СНзО)2СЕНзСОСН(ОН)СНз 13,4 1,149 1,5353 —
2078 пиофеиои 2-Метил-5-трет-бутилкума- (СНз)зСС6НзСН= С(СНз)О 20 0,988 1,5355
рон 1
2079 Изобутиро-л-крезол (СНз)2СНСОС6Нз(СНэ)ОН 21,3 1,043 1,5355 —
2080 а-Оксипропиофенон СзН5СОСН(ОН)СНз 22,8 1,104 1,5356 —
2081 Гидрокоричный спирт СеНйССНг^СНгОН 25 0,995 1,53565 :554
2082 5, 7-Диметилкумаран (СНз)2СбН2СН2СН2О L । 18,9 1,026 1,5358 —
870
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C 4 nD № no табл. «Свойства органических соединений»
2083 Этиловый эфир а-(л-то- С^3С6Н4С( = СНС1)СО2С2Н3 19,7 1,136 1,5358
лил)-р-хлоракриловой
к-ты
2084 2-Изовалеротиофен (СН3)2СНСН2СОС= CHCH=CHS 1 1 20 1,062 1,536 —
2085 Этиловый эфир 2.5-ди- СН3С6Н3СОС(СН3) (СООС2Н5)О 20 1,161 1,536
метил-З-кумаранон-2-кар- 1 1
боновой к-ты
2086 Фталид С6Н.СООСН2 1 1 99,1 1,1636 1,536 8523
2087 2, 5-Диметил-2-этилкума- СН3С6Н3СОС(СН3) (С2Н6) О 19,6 1,056 1,5360
район 1 1
2088 Октагидроантрацен 88,8 0,965 1,5363
2089 Этиловый эфир 2-метил- С2Н6ООСС6Н3СН2СН СН3)О 1 1 14,3 1,118 1,5363
кумаранкарбоиовой-5
к-ты 1
2090 п-Ксилиламин ch3c3h4ch2nh2 20 0,952 1,5364
2091 Метиловый эфир бензоил- С6Н3СОСН2СООСН3 24,7 1,15 1,53654 8003
2092 уксусной к-ты
Этиловый эфир 2-этил-З- C6H4COC(C2HS) (СО0С2Н3)О 18,6 1,115 1,5366
кумаронои-2-карбоно- 1 1
вой к-ты
2093 2094 N, N-Диметил-п-толуидии лс-Метоксиацетофенои CH3C6H4N(CH3)2 СН3СОС6Н4ОСН3 20 19 0,9287 1,094 1,53664 1,5367 7592 965
2095 Фениловый эфир изоциа- C6HSN=CO 19,6 1,0956 1,53684 3858
новой к-ты
2096 транс-1, 2-Дибромпропан СН3СНВгСН2Вг 17,4 2,02 1,5369
2097 2-Изобутиро-л-крезол (СН3)2СНСОС6Н3(СН3)ОН 20 1,047 1,537
2098 Диэтиловый эфир дитиол- CO(SC2H5)2 18,2 1,084 1,5370 7964
2099 угольной к-ты 15,1
2-Метил-5, 6, 7, 8-тетрагид- СНзСюНп 0,954 1,5372
2100 роиафталии Триэтилолово [(СгНбЬБпЬ 17,8 1,4 1,5374 5855
2101 N-Фенилуретаи C6HbNHCOOC2Hs 30,4 1,106 1,5376 4107
2102 З-Метил-6-метоксиацето- (СН3О) (СН3)С6Н3СОСН3 13,8 1,069 1,5377
2103 фенои Метиловый эфир салици- НОСеН4СООСН3 18,1 1,186 1,5377 6961
2104 ловой к-ты
Р-Эпидибромгидрин ВгСН2СН = СНВг 25 1,995 1,5378
2105 Бромистый этилен СН2ВгСН2Вг 20 2,1785 1,53789 9444
2106 О-Метоксиацетофенои СН3СОСеН4ОСН3 23,6 1,0849 1,5379 964
2107 6-Аллил-о-крезол СН2=СНСН2С6Н3(СН3)ОН 20 1,000 1,538
2108 (1.2, 3)
2-Инда нои СеН4СН2СОСН2 1 1 66,3 1,07 1,538 3890
2109 Аниол CI 42=СНСН2С6Н(О2СН2)(ОСН3)2 14 1,176 1,5380 636
2110 а-Ацетил- а- метил ацето- CcHsCOCH (СН3) сосн3 20 1,079 1,5382
2111 феиои
4-Аллилвератрол ’ СН2-СНСН2СЕН3(ОСН3)2 17 1,036 1,5383 2296
2112 Сафрол сн2=снсн2ссн,(О2сн2) 20 1,100 1,5383 7001
2113 2-Метокси-2, 5-диметилку- СНгС6Н3СОС(СН3) (ОСНз)О 22,6 1,130 1,5383
маранои 1 1
2114 а-Метил стирол СГ1Н5С(СНз) =С?12 17,4 0,9134 1,5384
2115 Р-Этил стирол С6НЬСН=СНС2Н3 20 0,910 1,5387
2116 Диэтиловый эфир бензаль- CellsCI 1-С(СООС2Н6)2 20,4 1,105 1,5389
2117 малоновой к-ты
а-Пири ди л альдегид C6H4NCHO 18,5 1,13 1,9389
2118 З-Ацетокси-2, о-диметилку- СН3С6Н3С(ООССН3) = С(СН3)О 20 1,132 1,5389
марон 1 !
2119 2. 6-Диметил-З-этилхрома- СН3СеН3СОСН(С2Н.) СН(СН3)О 21 1/VJ 1,539
НОН 1 1
871
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
Продолжение
показатели преломления жидкостей
О. о Е О Е g Название Формула t,cc d4 nD № по табл. «Свойства органических соединений» 1
2120 о-Аллнлгваякол CH^CIICHiC<H,(OCH,)O!l :н3ос„н4с(сн3) =сн€оосн3 20 1,066 1,539
2121 Метиловый эфир алло- С 17 1,098 1,5390 ——
Р-метил-о-метоксикорич-ной к-ты 16,7 1,192 1,5390 *
2122 Этиловый эфир 2-мстил- С6Н.СОС(СН.) (COOCJI-JO —
кумараиои-3-карбоно- 1 1
вой-2 к-ты 17,4 1,103 1,5391
2123 Хлористый бензил С„1 IsCHjCl 1136
2124 /г-Изобутироанизол (СН3)2СНСОС6Н4ОСН3 16,6 1,050 1,5393 —
2125 2, 2-Диэтилиндандион-1, 3 СсН4СОС(С2Н5)2СО 20 1,064 1,5393 —
2126 1, 4-Тетраэтилднамино-нафталин CioHcJNlCjHsJjJa 99,6 0,932 1,0347 1,5394 1,5395 4418
2127 «-Крезол CH,CtH4OH 20
2128 Бензиловый спирт CrfKCHjOII 20 1,043 1,065 1,53955 1169
2129 Хавибетол СН2-СНСН2С6НЭ(ОН) (ОСН3) 16 1,5397 8635
2130 Бензойная к-та С6Н5СООН 15 1,2659 1,53974 1223
2131 м-Крезол СН,С,.Н4ОН 20 1,0336 1,5398 4409
2132 Диэтилртуть (CH2CH3)2Hg 23,2 2,423 1,53990 6931
2133 Фенол C„H6OH 45 1,07 1,54 8235
2134 м - Ок си а цетоф е иои CHaCOC«H4OH 109 1,099 1,54 971
2135 2, 5-Диаллилфенол (CH2-CHCH2)2C3HaOH 20 0,998 1,540 —
2136 6-Изобутиро-л£-крезол (CH3)2CHCOCeHs(CH3) (OH) 20 1,042 1,540 —
2137 4, 6-Диметил-2-изопропил- (CH3)2C,H2COCH(C3H;)O 20 1,048 1,5400 —
кумаранон 1 1
2138 2.4-Диметил-7-изопрспил- ( CH,) (C<H,)CEH2CH =C(C1I3)O 20 0,994 1,5401 —
кумарон 1 1
2139 5-Метилкумараи . CI13C,H.,CH2CH.O 1 1 18,6 1,046 1,5404 -
2140 2, 2, 5-Триметилкумаранон CH3CeH3COC(CHj)2O ) 1 19,3 1,073 1,5404 -
2141 Этиловый эфир 5-метил- СН3( :6н3с(ос2н5) = c.(cooc2he)o 52,6 1,104 l,54u4 —
3-этокс ику ма р в л о 1 1
вой к-ты
2142 о-Фторанилии FC.H.NH, 20 1,151 1,5407 476
2143 3, 4-Диметилацетофеион (CH3)2CeHsCOCH3 15,5 1,007 1,5408 1,5408 —-
2144 Метиловый эфир р. «-ди- CH3C«H.C(CH,)- CHCOOCH, 60,2 1,014 —
метилкоричной к-ты 1,031 1,5408
2145 2, 2-Диметилиндавон-1 CtH4CH2C(CH3)2CO 1 1 13,9 —
2146 1, З-Диметил-5, 6, 7. 8-тет- (CH,)2C«1L€H..CH;CH2CH2 21 0,959 1,5409 —
рагидронафталнн 1 1
2147 2. 4, 6-Триаллилфенол (CH2-CHCH2),Ct;H2OH 20 0,974 1,541 —
2148 4-Метил-2-аллнлфеисл CBiCfiH3(OH)CH?CH=CH2 20 1,002 1,541 —
2149 л-Толуиловый альдегид CHaCelhCHO 21,4 1,0189 1,541 7658
2150 6-Окси-З-метилацетофенои CI1,C,.H3(OH)COCHS 53 1,080 1,5410 —
2151 N. N- Диэтил анилин C6H,N(C2H5)2 22,3 0,93 1,54105 41.5.
2152 2, 4, 5-Три метил ацетофено и (CH,)sC«H2COCH3 14,9 1,004 1,5411 1,5411 —•
2153 Диэтиловый эфир фтали- CeH4COOC=C (COOC2HS) J 84,4 1,189 —•
денмалоновой к-ты 1 1
2154 Эвгенол CH2-CHCH2Cf,H,(OCH.,)OH 19,4 1,07 1,5416 9076
2155 а-Метил-З-метокснстирол C113OCf H4C (С H,) - CH2 20 0,99 1,5417 ——
2156 Р-Хлор-4-метил а-эти лети- CII3CeH4C(C,Hs)=CHCl 19,9 1,036 1,5418 —
рол 1,068 1,542
2157 Тритиоацетон (CH3CSCH4)s 20 —-
2158 2-Бутиротиофен C,H,COC-CHCH-CHS 1 1 20 1,098 1,542 —
2159 3. 4-Ксиленол (CH3)2C,H3OH 14 1,0276 1,5420 4484
2160 Кумаран C6H4CH2CH2O 1 1 19 1,057 1,5420 —
к
№ по пор. Название Формула t, ’С d4 ”d № по табл. «Свойства органических соединений»
2161 6-Метил хромай СН3С6НаСН2СН,СН2О 1 1 14,3 1,037 1,5421 -
2162 а-Метоксистирол C6H5C(OCHS)=CH2 20 1,00 1,5422 341
2163 2-М.етокси-р, Р-5-три- СН3(СН,О)СсН3СН = С(СН,)2 17,1 0,968 1,5425 —
2164 Этиловый эфир а-этилко-ричной к-ты CeHsCH=С (С2Н5) СООС2Н5 13,8 1,025 1,5425 -
2165 Гомопирокатехин CHsCdl 1,(ОН), 73,6 1,1287 1,5425 3017
2166 о- Нит р оф ен ето л NO?C(11,ОС2Н5 20 1,19 1,067 1,5425 8185
2167 4, 6-Диметил-2-этилкумара-ион (СН3)2СсН2СОСН(С,Нй)О 1 1 20 1,5426 —
2168 3, З-Д и метили нда нон-1 С0Н4С(СН...);СН2СО 1 1 20 1.027 1,5427 —
2169 а-Метилстнроловый £фир уксусной к-ты С6Н3С(СН3) -СНООССНз 15,2 1,057 1,5428 —
2170 2, 2, 4. 6-Тетраметилкума-раной (СНз)2С6Н2СОС(СНз)2О 20 1,060 1,5428 —
2171 5-Метил -2-изопропилку мара нон СН.,С6Н3СОСН (СзН,) о 1 1 13,8 1,071 1,5429 —
2172 Изоамиловый эфир 2-индазолкарбоновой к-ты 1 1 C6H4CHN (СООСзН ,1) N 1 1 15,1 1,110 1,543 —
2173 Этиловый эфир л«-бромбен-зойиой к-ты ВгСвН4СООС2Н5 20 1,430 1,543 —
2174 Этиловый эфир о-бромбеи-зойной к-ты ВгСсН4СООС2Н5 20 1,439 1,543 —
2175 Карвакриламин CH3(C:,H,)C0HaNH2 19 0,995 1,543 4237
2176 цис-\. 2-Дибромэтилен СНВг=СНВг 17,5 2,2846 1,54312 9390
2177 2, 5-Диметил-З-этилкумарои СН 4С6НзС (С2Н5) = С (СНз) о 1 1 20 1,003 1,5433 —
2178 2, 6-Ди метилокта- (СНз)гС] триен-3. 5, 7 1СН-СНСН = С(СН3)СН=СН2 20 0,809 1,5436 -
2179 Этиловый эфир трнбром-уксусной к-ты Вг3ССООС2Нз 12,5 2,2 1,5438 —
2180 5-(Р, Р-Дихлорэтил)-I, 2, 3-триметилбензол (СНз)зС6Н2СН4СНС12 20 1,144 1,5439 —
2181 Хроман С6Н4СН2СН2СН2О 1 1 20 1,059 1,544 8826
2182 2, 5-Диметил-З-метоксику-марои СН3СсНзС(ОСНз) =С(СНз) О 1 I 19 1,081 1,5440 —
2183 5-Метил-З-этоксикумарон СНзС6Н3С(ОС2Н3) =сно 1 1 15,6 1,083 1,5440 —
2184 1 Диклорметил СН3(С1 1,3-диметилциклогекса-диен 2, б-он-4 4С12)ССН=С(СНз) сосн-сн 1 1 20 1,241 1,5440 —
2185 Бензиламин CeH6CH2NH2 19,5 0,98 1,5441 1113
2186 Хавикол СН2=СНСН2С«Н4ОН 18 1,033 1,5441 8636
2187 1-Беизилциклогексен-1 C6HSCH2C = СН (СН2) Зсн2 1 1 14,1 0,969 1,5443 —
2188 «-Метилстирол СН,С6Н4СН=СН2 16,4 0,900 1,5447
2189 З-Метилфталид С0Н4СООСН(СН3) 1 1 20 1,158 1,5447 —
2190 2, З-Диамоксинафталин СюНб (ОСзН и) 2 20 0,991 1,545
2191 о-Аллилфенол СН.-СНСН2СсН4ОН 20 1,021 1,545 —
2192 5-Ацетил-2-пропнлтиофен CaH,C=CHCH = C(COCHa)S 1 1 20 1,061 1,545
873
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула Л °с "о № по табл. «Свойства органических соединений»
2193 5-Метил-2-пропйлкумара-ион СНзСбНзСОСН (СзН7) о 1 1 20 1,064 1,545 —
2194 Этиловый эфир аллокорич-ной к-ты С6Н5СН=СНСООСзНз 20 1,048 1,5451 —
2195 ж-Фторанилин FCJI.NHi 18,5 1,1561 1,54528 477
2196 1. 2, 3, 4-Тетрагидроиафта-лии С,оН12 17 0,9738 1,54529 5399
2197 о-Крезол СН3С6Н4ОН 20 1,4065 1,5453 4397
2198 Этиловый эфир 0-метилко-ричной к-ты СбНзС (СНз) =СНСООС2Н6 16,6 1,039 1,5456 —
2199 Бензальдегид С6Н5СНО 19,5 1,049 1,5456 1020
2200 1 - И зо а м и л индазол CeH4CH=NN(CH2)2CH(CH3)s 1 1 20 1,001 1,546 —
2201 5-Мети л-2-феиил оксазол ин N = С (С6Н5) ОСН (СН3) сн2 1 1 22,9 1,070 1,5460 -
2202 Стирол с£н.сн=сн2 20 0,9090 1,5462 7179
2203 dl-( а-Бромэтил) бензол СвНзСНВгСНз 20 1,3478 1,5462 1454
2204 Этиловый эфир 3, 5-диме- СН3С6Н3С(СН3)= С(СООС2Н5)О тил кум ариловой к-ты | [ 59 1,093 1,5464 —
2205 п- Гомосалициловый альде- НОС6Нз(СНз)СНО 59,2 1,091 1,5466 —
2206 I ид п-Метоксиацетофенон СНзСОСеН.ОСНз 41,3 1,082 1,54684 966
2207 «-Толуиловый альдегид СНзСвН.СНО 16,6 1,019 1,5469 7659
2208 Метиловый эфир СН3(СН3О)С6Н3С(СН3) =СНСО2СН3 2-метокси-р, 5-диметил-коричной к-ты 12,7 1,087 1,5472 —•
2209 л-Дихлорбеизол С,НЧС12 17,3 1,28 ' 1,5472 1507
2210 Иодметиловый эфир ЗСНгОСНз 20 2,030 1,5472 —
2211 0-(Триметилацето)-стирол С6Н5СН-СНСОС(СН,)з 45,7 0,94 1,5473 —-
2212 о-Хлорфеиол С1СеН4ОН 40 1.2 1,5473 8359
2213 о-Нитротолуол СНзС6Н,МО2 20,4 1,163 1,54739 7721
2214 Этиловый эфир а-метил-коричной к-ты СвНзСН - С (СН.) СООС2Н5 20,6 1,032 1,5475 —
2215 м - Н нт ротол уол CH3CeH4NO2 20 1,157 1,5475 7722
2216 0-Бутиро-0-этил стирол С6НзСН=С(СгН5)СОС,Н, 23,9 0,972 1,5476 —
2217 о-Метилстирол СНэСвН(СН = СНз 14,1 0,916 1,5477
2218 З-Этоксику марой СбН4С(ОС2Н5)=СНО 1 1 17,9 1,106 1,5477 —
2219 О-Метиловый эфир бензальдоксима CeH5CH = NOCH3 20 1,020 1,548 —
2220 3, 4 Диметил-2-этил- (СН3) (ОН)СсН2СН(СН3)СН(С2НБ)СО инданол-7-он-1 | | 20 1,073 1,548 —
2221 4-Диметиламино-ж -ксилол (CH3)2C6H3N(CH3)2 20 0,939 1,5481 —
2222 Этиловый эфир индеикар-боновой-2 к-ты СсН.СН=С (СООС2Н5) сн2 1 1 73,9 1,054 1,5481 —
2223 Этиловый эфир 3-метил-кумариловой к-ты СбН,С (СНз) ="С(СООС2НЬ)О 1 1 56,6 1,116 1,5482 —
2224 Трихлорметилмеркаптан ClsCSH 17,5 1,695 1,5484 —
2225 3, 5-Диметилкумарои СНзС6НзС(СНз)-СНО 1 1 22,2 1,035 1,5485 —
2226 2-Пропио-п-крезол (НО) (СВДСзНзСОСгНз 13,8 1,084 1,5485 —
2227 5-Бром-2-этокситолуол СНзС6Нз(ОС2Н5)Вг 11,4 1,359 1,5486 —
2228 2-Хлортиофен SCC1=CHCH=CH 1 1 20 1,2863 1,5487 7456
2229 Метиловый эфир 0-метил- С о-метоксикоричиой к-ты )НзОС6Н4С(СНз) = СНСООСН, 16,7 1,104 1,5488 -
2230 3,5-Диметил-1-бензил- СН3С=СНС(СН3) «= NN(CH2C6H5) пиразол 1 ] 20 1,034 1,549
874
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t, °C 4 "о № по табл. «Свойства органических соединений»
2231 1. 3, 5-Три метнл пиразол CH3C = CHC(CH3) = NN(CH3) 20 1,034 1,549 —
2232 о-Толуиловый альдегид СН3С«Н.СНО 19 1,0386 1,549 7657
2233 а-Метил-о-оксистирол НОСсН4С(СН3) = СН2 18,5 1,030 1,5490 —
2234 п-Бромтолуол СНзСвН.Вг 20 1,3898 1,5490 7677
2235 Р-Метилстирол С6Н6СН=СНСН3 20 0,914 1,5492 1569
2236 N, М-Диметил-Л1-толуидин СН3С3Н4Ы(СН3)2 20 0,941 1,5492 7578
2237 р-Фенилвиииловый эфир уксусной к-ты СН3СООСН=СНС»Не 22,9 1,066 1,5494 —
2233 1, З-ДибромпропаноЛ'2 ВгСН2СНОНСН2Вг 25 2,120 1,5495 —
2239 Метиловый эфир Р-метоксикоричной к-ты СеНЕС (ОСН3) = СНСООСНз 24,7 1,118 1,5497 —
2240 Этиловый эфир 3-метокси-кумариловой к-ты СбН.С(ОСН3) = С(СООС2Н3)О 70 1,160 1,5499 —
2241 2-Фенил-1-этилгидразин ch3ch2nhnhc6h6 15 1,004 1,55 2706
2242 Фенилацетилеи CeHsC^CH 17,4 0,93 1,5501 1632
2243 2-Окси-р, р, 5-три мет ил ст и- (СН3) (ОН)СеН3СН-С(СН3)2 21,5 0,991 1,5501 —
2244 рол 3-Хлор-4-(Р, Р-дихлорэтил)-1-метил бензол (СН3)С1СВН3СН2СНС12 20,3 1,287 1,5501 —
2245 Стирилэтиловый эфир С6Н5СН-СНОС2Н5 21,2 0,971 1,5502 —
2246 Этиловый эфир фенилпро-пиоловой к-ты СбНьС^ССООС2Н5 25 1,0550 1,5502 6716
2247 5-Метил-З-метоксикумарон СН3С6Н3С (ОСН3) =сно 1 1 24,3 1,107 1,5504 —
2248 3, 6-Диметилкумарои СН3С3Н3С(СН3)-СНО 1 1 20 1,046 1,5505 —
2249 Метиловый эфир Р-метил-коричной к-ты С6Н3С(СН3) =снсоосн3 37,8 1,054 1,5505 —
2250 транс-1, 2-Дибромэтилеи СНВг=СНВг 17,5 2,2667 1,55054 9390
2251 2, 3, 5-Триметилкумарон СН3С«Н3С (СН3) = С (СН3) о 1 1 20 1,021 1,5506 —
2252 5-Ацетил-2-этилтиофеи CH3COC=CHCH = C(C2Ht)S 1 1 20 1,079 1,551 —
2253 Этиловый эфир 3, 4-дигид-ро-2-нафтойноЙ к-ты C,oHsCOOC2H6 20 1,085 1,551 —
2254 к-Бромтолуол CH3C«H4Br 20 1,4099 1,551 7676
2255 2, 2-Диметил-а-хромеи СеН.(СН)2С(СН3)2О 20 1,013 1,5512 —
2256 2, 4, 6-Триметил-а-хромен С НзС6Н3С(СН3) =СНСН (СНз) о 1 1 20 1,012 1,5513 —
2257 2-Окси-а, 5-диметилстирол (СНз) (НО)С6Н3С(СН3)=СН2 20 1,012 1,5514
2258 2-Бром-л-ксилол ВгС6Нз(СНз)2 18,5 1,36 1,5514 4550
2259 2-Метил-1, 2, 3, 4-тетрагид-ронафталииои-1 СвН.СОСН (СН3) СН2СН2 1 1 20,9 1,060 1,5515 —
2260 Хлористый бензилиден СВН6СНС12 19,4 1,3 1,5515 1157
2261 N-Нитрометилбеизиламин C6H3CH2N(NO2)CH3 25,7 1,171 1,5515 —
2262 Бутилстирилкетон СН3(СН2)2СН2СОСН= CHCcHs 44,7 0,960 1,5518 ——
2263 4-Хлор-2-изобутирофенол (НО)С1С6Н3СОСН(СН3)2 20 1,192 1,552 1,5522 —
2264 1-Метилиндазол c6h4ch==nnch3 1 1 99,2 1,032 —
2265 Изокумараион ОС6Н4СН2СО 1 1 20 1,217 1,5523 —
2266 Нитробензол cbhsno2 20 1,21 1,5524 1548
2267 1, 2-Дихлорбеизол 7-Метнлкумарон С6Н4С12 17 1,30 1,5524 1506
2268 СН3С6Н3СН = СНО J 1 17 1,05 1,5525
875
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
1 № по пор Название Формуле t, с с 4 "о № по табл. «Свойства органических соединений»
2269 З-Метилкум а рои СеН4С(СН3)=СНО 1 1 23,4 1,054 1,5526 —
2270 5-Хлор-1, 3-диметил-4-(0, 0-дихлорэтил)бензол (СН3)2(С1)С6Н2СН2СНС12 16,1 1,262 1,5528 -
2271 я-Этиланилин H2NCcH4C2Hs 22 0,975 1,5529 485
2272 1 - Бутилизоиндазол C6H4CH=NNC4H8 1 1 20 1,019 1,553 —
2273 Л£-Метоксибеизальдегид СН3ОС6Н4СНО 20 1,119 0,97 1,5530 —
2274 п-Толуидин ch3c„h4nh2 59,1 1,55324 7586
2275 2, 5-Диметилкумарои СН3С6Н3СН = С(СНЭ)О 1 1 20 1,031 1,5534 —
2276 2-М етокси-л-тол уи ловы й альдегид (СН,)(СН3О)С6Н3СНО 20 1,098 1,5534 -
2277 Хлорангидрид бензойной к-ты CtHsCOCl 20 1,212 1,55369 1208
2278 Тетраэтил-л-фенилеидиа-мин CeH4|N(C2H5)2b 11,8 0,952 1,5537 —
2279 2-Метил ииданон-1 С6Н4СН2СН(СН3)СО 1 1 20 1,066 1,5538 —
2280 З-Метнл-1-беизилпиразол СН-СНС(СН,)= NNCHjCtHf 1 1 20 1,049 1,554 —
2281 Метиловый эфир о-анис-альдоксима СНЯОСЕН4СН = NOCH3 20 1,092 1,5.54 —
2282 2, 7-Диметилкумарон СН,С6Н3СН = С(СН3)О 1 I 20 1,036 1,5546 —
2283 1, 4-Дигндроиафталии CioHw 32,7 0,9928 1,55489 5354
2284 2-Изовалерилиндазол (ста-бильн.) N - С£Н4-CHNCOC4Hs 1 1 16,3 1,088 1,555
2285 2-Хлор-2. 5-диметилкумара-нои СН,СеН,СОС(С1)СН3О 1 1 20 1,217 1,555 —
2286 о-Окси а цетофенон CH3COCcH4OH 21,3 1,131 1,5550 970
2287 Мета никотин 19,7 1,002 1,5551 —
2288 н-Хлорбензальдегид С1СеН4СНО 61 1,196 1,55525 1058
2289 6-Метилхромаион-4 СН3СеН3'СОСН2СНиО 1 1 57,1 1,125 1,5553
2290 Этиловый эфир о-метил-коричной к-ты СН,СеН4СН-СНСООС2Н5 16,3 1,043 1,5555 -
2291 N-Этнланилин c„h3nhc2h3 20 0,9631 1,55558 486
2292 2- Нитро-1 -хлорметилбензол NO2CtH4CH,Cl 61,5 1,5557 —
2293 4 -М етокс и -2- п ролей ил - (СН3) (СН3О)С«Н3СН = снсня 12,3 0,986 1,5557
2294 о-Оксигидрокоричный спирт HOCtH4CH2CH2CH2OH 15 1,126 1,5558 —
2295 Этиловый эфир 6-метил кума риловой к-ты СНаСеН3СН С(СООС2Н3)О 1 1 43,9 1,119 1,5558
2296 и-(а-Бутенил)-аиизол СН3ОС6Н4СН = СНС2Н5 19 0,980 1,5559 1,55592 —
2297 n-Анизи дин CHaOCeH4NH2 67 1,0605 329
2298 2- П роп ион и лтиоф ен C2H«COC-CHCH=CHS 1 1 20 1,131 1,556 —
2299 4-Хлор-3-метил-1 -беизил- СН = С(С1)С (СН.,) - NNCH2CeH. пиразол 1 1 20 1,156 1,556 -
2300 Три-о-толилфосфат (СН.,С<,Н4О)3РО 20 1,17 1,556 1,5562
2301 Хлорангидрид сорбиновой к-ты СН3(СН = СН)2СОС1 20 1,065 —
2302 2-Беизил-п-цимол (СН3) (С,Н,)С6Н3СН(СН„)2 20 0,963 1,5564 —
2303 л-Хлорфеиол С1С»Н4ОН 40 1,2 1,5565 8360
2304 а-Бромизобутирофеиои (СН3)2СВгСОСеН5 20 1,355 1,5567
876
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
। № по пор. Название Формула t. cc "d № по табл. «Свойства органических соединений»
2305 1-Кето-7-метил-1, 2, 3. 4-тетрагидроиафтзлии CH.C6HXOCH2CHaCHj 1 1 35 1,057 1,5567 —
2306 Двухлористая сера SCI, 14 1,557
2307 О-Виниланизол CH2=CHC6H4OCHS 17,4 1,003 1,5570 344
2308 4-Бром-о-ксилол BrCeH:,(CH3h 18,4 1,37 1,5571 4517
2309 о-Океистирол CHa=CliCEH4OH 17,4 1,06 1,5572 8274
2310 5- Метил кумарон СН3Сб*ЬСН=СНО 1 1 19 1,060 1,5573 —
2311 2, 4, 6-Триметилкумаранои (CH.),GH.COCH(CH)O 1 1 19,2 1,099 1,5574 -
2312 3, 4, 6-Триметил-а-хромев CHeCeH?C(CH3)C= (CH3)CH2O 1 1 20 1,029 1,5575 -
2313 Метиловый эфир аллско-ричной к-ты QII.CH = CHCOOCH3 20 1,078 1,5575 —
2314 2, 3-Д иб ром пропа нол-1 CH.BrCIIBrCH3OH 25 2,126 1,5577 6545
2315 Этиловый эфир N-беизил-Р-иминомасляной к-ты CH;.C( = NC;H-,)CHiCOOC,HI 26 1,060 1,5579 —
2316 п-Хлорфенол CICJI.OH 40 1,2 1,5579 83Я
2317 3. 5-Ксилидин (CHa)2CcHsNH2 20 0,972 1,558 4493
2318 2-Изоамилиидазол N=CfH4=CHNC5Hu | | 20 1,007 1,558 —
2319 Метиловый эфир л-метил-коричной к-ты CH3CtH4OH = CHCOOCH3 56,6 1,027 1,5581 —
2320 Диметвлаинлин CtHtN(CHs)2 20 0,9557 1,55819 398
2321 о-Этиланилин NH,C6H,C£H5 22 0,983 1,5584 483
2322 Беизотрихлорид CEH,CC13 19,2 1,37 1,5584 7745
2323 З-Иодпропанол-1 JCH,C1ICH,OH 20 1,98 1,5585 —
2324 ДиэтиловыЙ эфир нафта-левой к-ты CwHe(COOC2Ur,)2 70 1,140 1,5586 —
2325 2-Метил-6-метоксиин да-ион- 1 CIWQHbCH,CH(CHs)CO 1 1 16,9 1,119 1,5588
2326 2- Мет ил к у м а рои Cf.H4CH-C(CH.)O 1 1 20 1,054 1,5589 —
2327 3-Меток си к у м а рон CeH4C(OCH3)-CHO ) 1 19,3 1,144 1,5589 —
2328 Этиловый эфир 3, 4-дигид-ро-а-нафтойной к-ты CeH4CH;CH;CH-CCOOC;HE 1 1 20 1,102 1,559 —
2329 1, 2. З-Трибромпеитав CsHbCHBrCHBrCILBr 20 2,09 1.559 —
2330 1-Метилииден C6H4C(CHJ=CHCH2 I | 27 0,968 1,5591 —
2331 2, 5-Ксилидин (CH3)!CtH3NH2 21,3 0,979 1,55914 4490
2332 Этиловый эфир 3-этокси-кум ариловой к-ты CEH4C(OC.HE) = С(СООС:НЕЮ 1 1 14,3 1,168 1,5592 —
2333 О-Метиловый эфир бензоил ацетон а CeHEC(OCll3) = CHCOCH3 16 1,068 1,5598 —
2334 Этиловый эфир транс-ко-ричвой к-ты C,J i-CH = C HCOOCjHs 20 1,0490 1,55982 4334
2335 1-Кето-7-этил-1. 2, 3, 4-тетра гидрона фтал ин C2HECEH3COCH2CH:CH2 1 1 17,2 1,056 1,5599 —
2336 Чстырехскись осмия OsO4 45 1,56
2337 п - Ок си а цетофе н он HOCtH.COCH, 109 1,109 1,56
2338 Т риметилвисмут (CH3)3Bi 15 2,3 1,56 2331
2339 5-Анетил-2-метилтисфен CH,COC=CHCH = C(CH?)S 1 1 24,7 1,119 1,560 —
2340 о-Анисовый альдегид CHSOCEH4CHO 20 1,133 1,560 1044
2341 Этиловый эфир 3-м ет-окси-2-вафтойиой к-ты CH.oclcHEcdoc2Ht 20 1,159 1,560
877
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
о. о Е О Е £ Название Формула t, °C 4 "D № по табл. «Свойства органических соединений»
2342 4-Хлор-1-беизил-5-метил- Ь пиразол “CHC(C1)=C(CH3)NCH2C6H6 20 1,178 1,560 —
2343 Метиловый эфир фенил-пропиоловой к-ты CeHsC=CCOOCII3 30,5 1,077 1,5601 —
2344 а-Этилиденацетофеион СН3СН = СНСОСеН5 20 1,028 1,5601
2345 Этиловый эфир изохави-бетола СН3СН=СНСеН3(ОС2Н5)ОСН3 11 1,039 1,5602 —
2346 2, 2’-Диэтоксидифеиил СгН6ОСеН4С8Н4ОС2Н5 47,4 1,043 1,5602 —
2347 dl-\, 2, 3, 4-Тетрагидро-2-вминоиафталии CbH4C4HjNH2 22,2 1,0295 1,56039 —
2348 о-Пропениланизол СП3ОС6Н4СН = СНСН, NH2C6H3CH2CH2CH,CH2 1 1 20 0,993 1,5604 —
2349 5, 6, 7, 8-Тетрагидро-2-ами-иоиафталин 22,2 1,029 1,5604 5472
2350 Бром бе изол CsHsBr 20 1,495 1,5604 1442
2351 а-Изовалерилацетофенон C6H5COCH2COCH2CH(CH3)2 20 1,031 1,5605 —
2352 п-Бромаиизол BrCsH4OCH3 20 1,4569 1,56051 343
2353 2, 4-Ксилидин (ClI,)zCeII3NH, 19,6 0,9783 1,56066 4489
2354 Этилизоэвгениловый эфир СН3СН=СНС6Н3(ОСН,)ОС2Н> 11 1,044 1,5607 —
2355 Инданон-1 CeH4CH2CH2CO 1 1 45 1,101 1,5608 3889
2356 о-Бромтолуол ВгСбН4СНз 20 1,422 1,5608 7675
2357 Этиловый эфир 1-метил-2-инденкарбоновой к-ты СНзСэНвСООСгНз 39,1 1,074 1,5609 —
2358 2, 6-Ксилидин (CII,)2C«H3NH2 20 0,979 1,561 4491 ’’
2359 З-Метил-1 -этнлизоиидазол C6H4C(CH3)=NNC2H5 20 1,035 1,561
2360 1 -Изопропнлнзоиндазол C<,H4CH = NNCH(CH3)2 20 1,037 1,561 <4
2361 З-Иодфуран CH=CHCJ«=CHO 1 1 20 2,045 1,5610 8565
2362 Аиетол СНзСН-СНСвНдОСНз 21 0,990 1,5614 326
2363 4-Пропенилвератрол CH,CH=CHCeH3(OCH3)2 20 1,0521 1,5616 2297
2364 о-Нитроанизол О2МСвН4ОСН, 20 1,2527 1,56188 348 •и
2365 Этиловый эфир л-метокси-коричиой к-ты СН3ОСбН4СН = СНСООС2Н5 59,2 1,066 1,5619
2366 Этиловый эфир кумарило-вой к-ты СвН.СН = С (СООС2Н5) о 32,2 1,162 1,5619
2367 N-Метилацетанилид CH3CON(CH3)CcH6 120 0,977 1,562 765 а
2368 2-Бутил ии да зол N=C6H4 = CHNC4Hs 1 1 20 1,025 1,562
2369 2-Изобутирилиндазол (ста-бильн.) N-CeH4=CHNCOCH(CH3)2 1 1 20 1,112 1,562 - ! *
2370 а- Бромбутирофенон C2H5CHBrCOCcH3 20 1,364 1,562
2371 Р-Метокси стирол С6НЕСН = СНОСН3 24,3 1,0 1,5620 i
2372 а-Хлорстирол С6Н6СС1=СН2 16,6 1,10 1,5623 7193
2373 мезо- Дигидроизоамил антрацен СИ,Н22 44,4 0,994 1,5626 - '1
2374 2-Этил-1 -п ропил беизимида -зол c3h7nc6h4n»cc2h5 1 1 20,8 1,034 1,5626 ~ is
2375 1 - Бензил циклогексен -1 -он-6 С6Н5СН2С=СН(СН2)3СО 1 1 21.7 1,061 1,5628 — 7!
2376 1-Кетооктагидрофеиантрен СиН.вО 100 1,064 1,5628 — -4
2377 Этиловым эфир Змет- СН3С6Н3С(ОСН3) =С(СООС2Н5)О окси-о-метилкумари- | | ловой к-ты 23,8 1,170 1,5628
2378 1-Пропилизоиндазол c6h4ch=nnc3h7 1 1 20 1,039 1,563 1
2379 878 Лактон у-окси-у-бензил-кротоновой к-ты СеН6СН2СНСН=СНСОО 1 I 20 1,149 1,563 1
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
Ns по пор. Название Формула t, °C < nD № по табл. «Свойства органических соединений»
2380 Иидоксазол CeH<CH=N—О 1 1 20 1,170 1,563 -
2381 Этиловый эфир н-метилко- СН3С6Н4СН = СПСООС2Н5 15,9 1,034 1,5630 —
2382 ричной к-ты
2-Метилкумараион СвН4СОСН(СН3)О 19,7 1,153 1,5632 —•
2383 1-Фенил пентин-1-ол-З C6HSC^CCHOHCH2CH3 13 1,014 1,5633 —
2384 7-Метокси-2-метилкумарон CU3OCcH3CH=C(CH3)O 1 1 20 1,119 1,5636 —
2385 2-Фтор-1, 1. 2-трибромэтан FBrCHCHBr; 18 2,674 1,5638 —
2386 Метиловый эфир C!I..CcII<CII-C(CU,)CO2CHs 18,3 1,051 1,5640 —
а. n-диметилкоричной к-ты
2387 п-Метоксистирол сн.,осен(сн=сн2 20 1,0 1,5642 346
2388 Метиловый эфир (СНз) (СНзО)СбНзСН=С(СНз)С02СНз 14,6 1,099 1,5642 —
а, лг-диметил-о-метокси-коричной к-ты 1592
2389 Триазобензол C6H6N3 22,5 22,7 1,086 1,56421
2390 Кумарон C6H<OCH=CH 1 1 1,09 1,56450 1782
2391 Этиловый эфир антранило- NH2C6H4COOC2H6 20 1,117 1,5646 523
вой к-ты N=CoH3 = CHNCOCH2C2Hs 1,565
2392 2-Бутирил индазол (ста- 20 1,120 —
бильн.) 1 1
2393 1-Кето-5, 7-диметил-1, 2, 3,4-тетрагидрон афтал ин (CH3)2CeH2CH2CH2CH2CO 15,5 1,065 1,5650 —
2394 .м-Хлорбензальдегид С1С<И,.СНО 20 1,241 1,5650 1057
2395 5-Метилкумаранон CH3C6H3COCH2O 1 1 53,8 1,151 1,5652 —
2396 2-Фенилокса золин OCH2CH2N = CC6Hs 1 1 23,4 1,122 1,5655 —
2397 1 -Фенил -1 - (и-тол ил) -этаи СН3СРН,СН(С6Н6)СН3 17,2 1,985 1,56-59 —
2398 Этиловый эфир 1-этилизо- C2HsNC6H5C(COOC2H5) = N 17,3 1,143 1,566
индазолкарбоновой-3 1 1
2399 2400 к-ты 2-Иодфуран 2-Ацетилтиофен C.IIjJO SCH=CHCH-CCOCH3 1 . 1 20 21,8 2,024 1,168 1,5661 1,5663 8564 5124
2401 Октагидрофенантрен С14Н18 20 1,025 1,5668 —
2402 Изопропилстирилкетон (CH3)2CHCOCH -CHCeHs 24,6 1056
2403 о-Хлорбензальдегид C!C6H<CHO 20 1,252
2404 7-Окси-2, 5-диметилиида- (СН3) (НО)СбН2СН2СН(СНз)СО 20 1,567
нои-1 1 1
2405 1, 2, З-Трибромбутан CH3CHBrCHBrCH2Br 20 2,19 1,567 —
2406 dl-1, 2, 3, 4-Тетрагидро- СДСДОН 17 1,0896 1,5671 0oj4
2407 1-нафтол 1, 2, 4-Трихлорбеизол C6H3C13 20 1,45 1,5671 1615
2408 2-Фенил-п-ментатриеи 20 0,971 —
2409 Бензоил ацетон CH3COCH2COC„HS 77,8 1,08 1,56775 869
2410 3. 5-Дихлор-4(Р, Р-дихлор- (CU3)CI2CeH2CH2CHCI2 19,2 1,397 1,5678 —
этил) -1 -мети лбензол 1,043 1,568
2411 5-Метил-1 -этнлизоиндазол CH3C£H3CH = NNC2Hj 1 1 20
2412 1 -Фенилтетра гидроизоинда- C6H6CH=NNC6Hs 99,9 1,061 1,568 —
зол 1 1
2413 Этиловый эфир о-хлорко- ClCcHtCH=CHCOOC,H5 20 1,171 1,568 —
ричной к-ты 15 0,978 1,5680
2414 2-Фенилцимол (CH3) Cf.HsCJIjCH (CH3)2 •—
2415 Пропилстирилкетои CjHsClhCOCH-CHCeHs 24 0,992 1,5680
879
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
Q. О е о Название Формула t, °C nD № по табл. «Свойства органических соединений»
2416 Диэтилкадмнй (C-HsbCd 18,1 1,65 1,5689 —
2417 5-Хлор-1-днхлор метил-1. 3- СНС|2СН, Ct 1 1 1 1,73 1,269 1.5631 —
диметнл-4-метенцикло-
гексаднен-2, 5 СН,ССН=СС(=СН2)С = СН I 1
2418 Этилстирилкетон CoHsCOCH =CHCgHs 50,3 0,987 1,5684 —
2419 Бензиловый эфир бензой- C6H5COOCH2C0Hs 21.5 1,12 1,5685 1227
ной к-ты 7574
2420 л-Тол ундин CH,CbH,NH2 20 0,989 1,56859
2421 о-Толуидии СН&ВДН, 20 1,004 1,5688 7561
2422 Этиловый эфир индазол- N=CeH, = CHNCOOC2H5 1 f 13,2 1,206 1,569 —
2-карбоновой к-ты
2423 а-Метил бензил иденацетон CcHsCH - С(СНз) COCHj 45,3 1,002 1,5691 —
2424 Этиловый эфир 1-днхлор- CHCI2 CHCO2C2H5 22,1 1,215 1,5691 —
метил-1-метилциклогек- 1 II
саднен-2, 5-метенкарбо-новой-4 к-ты CH3CCH-CHCCH = CH 1 1
2425 транс-4-Пропенилвератрол СНзСН=СНС6Н,(ОСН,.)2 20 1,0528 1,5692 —
2426 Фталоилхлорид C6H4(COCI)2 20 1,4089 1,5692 8533
2427 2, 3-Кен л иди н (CH3)2C6H3NH, 20 0,99 1,570 4488
2428 Этиловый эфир «метил- CHJOCSH1CH = C(CH1)CO.C2HS 15,6 1,089 1,5701 —
л-метокенкоричной к-ты 432
2429 Метнланилнн CeHsNHCH, 21,5 0,986 1,5702
2430 Изоапиол 12 1,197 1,5703 ——
2431 Изоамил-1-нафтиловый эфир Октраценон C,oH,OCH,CH2CH(CH3)2 14,2 1,00689 1,5705 3611
2432 C6HSCH = C6HGO=CH 1 1 62,4 1,076 1,5707 —
2433 и-Ннтроаннзол O2NCGH4OCH3 60 1,2192 1,57072 350
2434 Фенил-л-толилметан CGH5CH2CGH4CH3 19,3 0,99 1,5710 1,571 5010
2435 1-Этил-1-фенилгндразнн C„H,N(C2HG)NH2 20,8 1,018 2705
2436 3, 4, 5-Триметнл-1-фенил- CH3C = C(CH3)C(CHt) = NNC6H5 20 1,044 1,571 —
пиразол 1 1
2437 2 - А л л и л а дети п н н да зол CeHnON, 22,6 1,117 1,571 —
(стабилы!.)
2438 Этиловый эфир 2-этил- N = C6H.=C(COOCH5)NC>Hs 22,8 1,129 1,571 —
3-индазолкарбоновой к-ты 1
2439 а-Бутирил ацетофенон CeH5COCH2COCH2C,H5 20 1,049 1,5712 —
2440 1-Кето-1, 2, 3, 4-тетр а гидро- C6H,COCH2CH2CH2 15,5 1,099 1,5712 ——
нафталин 1 1
2441 о-а-Бромнзобутиро- (CHj) (OH)CsH3COCBr(CH,)j 22,3 1,367 1,5714 —
«крезол
2442 1-Фенилциклогексен-1 C6H3C=CH(CH2)3CH2 I 1 20 0,993 1,5718 —
2443 а-Бромпропиофенон CsHsCOCHBrCH, 19,6 1,430 1,5718 —
2444 Азарон (CHjOhC,H2CH=CHCH, 11 1,091 1,5719 1570
2445 1 Метил-2-фенилгндразии CoHsNHNHCH, 23,1 1,03 1,572 —
2446 Этиловый эфир 1-метил- СбНХНгСНгСДСООСгНз) =ССН3 20 1,087 1,572 —
3, 4-дн гидро-2-нафтой- 1
нои к-ты
2447 Метиловый эфир а-метил- СН3ОСвН.СН=С(СН,)СО2СН3 15,2 1,126 1,5721 —
о-метокенкоричмой к-ты 342
2448 о-Броманизол BrC6H.OCH, 20 1,3018 1,57245
2449 2-Метнлтетр а гидрохинол ин C,0H„N 20 1,02 1,5727 —
24-50 5-Бром-2-метнлкумаран ВгС.5Н4СН2СН(СН4)О 1 1 14,4 1,458 1,5727 —
2451 6-Изобутиро-2, 4-ксиленол (CHjhCoH2(OH)COCII(CH,l. 2» [ ,028 1,573 —
880
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
п. о № по табл.
Название «Свойства
о Формула t, °c 4 nD органнче-
скнх со ед и-
•£, нений»
2452 1 - Бензнлтетра гидронндазол ‘ C,!I„CH = NNC,K, 1 1 20 1,089 1,573 -
2453 1 - Фен и л бути н -1 -ол -3 СбН5С^=ССН(ОН)СН3 12,6 1,036 1,5731
2454 З-Окси-а-метилстирол НОСсН4С(СН3) = СН2 13,0 1,048 1,5734 —
2455 2, 4-Днметил-1-фенилпира- CeHsNN = C(CH3)CH = CCH3 19,3 1,057 1,5738 —
зол 1 1
2456 Инден С6Н4СН2СН=СН 1 1 16,1 1,01 1,5739 3892
2457 Изоэвгепол СНзСН = СНСвН8 (ОСН.,) он 19 1,08 1,5739 3864
2458 3. 5-Диметнл-1-фенилпира- CH.,C = CHC(CH3) = NNCeHs 20 1,055 1,574 —
зол 1 1
2459 Салициловый альдегид НОСбЩСНО 20 1,669 1,574 6982
2460 I, 5-Тетраэтилдиамннонаф- C,0H6[N(C2H5)2|2 26,8 0,989 1,5742 —
талии
2461 1. 4-Днбромбензол 99,3 1,9 1,5743 1477
2462 Днбензиламнн (CeH6CH2)..NH 22 1,0256 1,57432 3164
2463 1-Этилизоиндазол C6H4CH-NNC2HS 1 1 15,7 1,07 1,5747 —
2464 1, З-Диметил-5-фе- (СН3)СНСН2С(СН3)= СНС(СеН3) = СН 17 0,972 1,5749 —
НИЛЦИКЛО- 1 1
2465 гексаднен-3, 5 Изоникотеин C10HI2N2 20 1,0984 1,5749 3768
2466 4. 5-Диметил-1-фенилпира- СН3С = С (СН3) CH = N NCcHb 20 1,065 1,575 —
зол 1 1
2467 о Аннзнднн CH3OC6H4NH2 20 1,0923 1,57536 327
2468 5-Метил-1 -аллилизонндазол CHSCSHSCH=NNCH-,CH =CH2 1 1 20 1,047 1,576 —
2469 1, З-Дифеннлпропан (C6H5CH2)2CH2 20 1,007 1,5760
2470 1, 1-Дифеннлэтан 2-Нитро-д-крезол (CeHshCHCHa 20 1,004 1,5761 9188
2471 (Сн3нно)ссн..мо2 38,6 1,240 1.5763 4423
2472 Анисовый альдегид CH3OC„H4CHO 12,6 1,13 1,57641 502
2473 Метиловый эфир корнч- CeH5CH-CHCOOCH3 21,4 1,05 1,57661 4330
2474 ной к-ты
Бензойный ангидрид (CsHsCOhO 15 1,1989 1,57665 1419
2475 Изоамнл-2-иафтнловый C,0H,OCH2CH2CH(CH3)2 12 1,01555 1,57679 3612
2476 эфир
М-Метнл-N-ннтрозоаннлнн C6H5N(CH3)NO 20 1,1240 1,57688 433
2477 З-Хлор-1 -бром бензол BrC6H4CI 20 1,6302 1,577 1452
Р-Хлорстнрол CeH5CH=CHCI 18 1,1095 1,5774 7194
2479 2-Пропеиил-д-крезол (CH3) (HO)C6H,CH = CHCH3 9 1,029 1,5777 —
2-Фенилтетрагндронндазол c6h5nn=c6h,=ch 1 1 99,6 1,054 1,578 —
2481 Этиловый эфир 3, 4-ди гид- CflH4CH2CHC(COOC,H..,) =CH 1 1 20 1,093 1.578 —
ро-2-иафтойной к-ты
2482 Метила нтраи ил ГП1 CeH4NOCCHj 1 1 20 1,133 1,5780 —
2483 2484 2485 rpawc-Изосафрол CH2(O2)CeH3CH=CHCH3 20 1,122 1,5782 3807
Днфеинлметан 2, З-Диэтилнндазол С3НбСН2СвНь C2H5NN-CeH4=CC2Hs 1 1 16,8 20 1,01 1,039 1,5788 1.579 4958
2486 2487 2-Окси-З-пропнлдифенил CH3CH2CH2(OH)C,H3C«H5 20 1,047 1,579
2- Бензилтетрагидронндазол C6H3CH2NN = C6H3=CH 1 1 20 1,086 1'579 —
2488 2489 1. 1-Дифеннлпропен 1, 2. 3. 4-Тетрагндроизохи- CH3CH=C(C6Hs)2 CgHnN 63,5 23,1 0.981 1,07 1,5791 1,5798 6602
нол ин
56 Зак. 783
£81
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ Продолжение
пор. № по табл. «Свойства
о Е £ Название Формула t, °C d4 nD органических соединений»
2490 2-Изопро пил индазол (CHJ2CHNN=CeH4=CH 1 1 20 1,051 1,580 -
2491 5-Хлор-З- метил -1 -феинл пиразол С1С=СНС(СН3) = NNCeHs I 1 20 1,193 1,580 —
2492 1, 2-Днхлор-1, 2-дибромэти-лен BrCIC = CCIBr С1 СН2С1 1 II 1 16 2,4 1,5800 —
2493 3, 5-Дихлор-Ьдихлорме- (СНС12) (СН3)ССН = С—С—С—СН тнл-4-метеи-1-метнл- | | циклогексадиен-2. 5 16,7 1,408 1,5801 —
2494 Кайролнн CH2CH2CH2N(CH3)C6H4 1 1 23,1 1,019 1,5802 3945
2495 2-Метнл-1-этнлбензимида-аол CtH4N = C(CH3)NC2H5 1 1 19,8 1,073 1,5802 — -
2496 5-М етил-2-этил индазол C2H5NN=СцНз (СПз) =сн 20 1,050 1,5810 —
2497 Иодпсевдокумол (CHshQHJ 65,3 1,511 1,644 1,5813 1
2498 2-Хлор-1-бромбензол ВгС6Н<С1 20 1,5814
2499 Коричный спирт СбНзСН-СНСНгОН 20 1,0440 1,58190 4365 i
2500 5-Д1етнл- 1-фенилпиразол СН3С-СНСН = NNCcHs 1 1 20 1,086 1,582 — 1
2501 1-Аллилиндазол ch2=chch2nc6h4chn 1 1 20 1,067 1,582 —
2502 Нафталин С,оН, 98,4 0,962 1,5823 5341
2503 1-Метил-1-фенилгидразин C6HbN(CHa)NH2 21,6 1,038 1,58235 2687
2504 Фениловый эфир (C,HS)2O 24 1,07 1,5826
2505 Изобутеннлфеннлацетилен (CH3hC = CHG=CC6H5 13 0,930 1,5828
2506 Бромпнкрин NO2CBr3 12,5 2,811 1,5831 1932
2507 1, 2-Дигидронафталнн CioHio 18,3 0.998 1,5832 —
2508 Метилфенйлсульфид CsHsSCHj 25 1,0533 1.021350 1,5832 5133
2509 Бензил идеи ацетон СбН5СН = СНСОСНз 45,9 1,5836 868 1
2510 о-Пропеннлфенол CH3CH = CHC6H4OH 14,3 1,044 1,5837 1
2511 Трифенилметан (CeHehCH 99 1,01405 1,5839 5023 1
2512 3-Хлор-5-метил-1-фенилпи-разол CH3C = CHC(C1) = NNC6H6 1 1 20 1,205 1,584
2513 Метиловый эфир о-амиио-беизойной к-ты NH2C6H4COOCH3 20 1,16 1,5844 522
2514 со-Пропионилацетофенон C6H5COCH2COC2Hs 20 1,078 1,5844 —
2515 Антранил CjHsNO 20 1,1827 1,5845 518
2516 5-Метил-2-метоксибензоил- ( ацетон СНз) (СНзО)С6НзСОСН2СОСНз 20 1,118 1,5847 —
2517 Диметилкадмий (СНз).;С<1 17,9 1,9846 1,5849 3942
2518 Нитрил фенилпропиоловой к-ты CdHiiC—CCN 41,5 1,005 1,5854 — i
2519 Метиловый эфир о-мет-оксикоричной к-ты СНзОСбН.СН = СНСООСНз 16,7 1,137 1,5854 —
2520 6-Метил-1 -фенил-гепта- C«HS(CH=CH)2CH2CH (СНз)2 20 0,951 1,5855 —
2521 днен-1, 3 Кумаральацетон CH3OCcH4CH=СНСОСНз 61,4 1,053 1,5859
2522 а- (о-Метилбензнл) тиофен SCH =СНСН=ССН2С6Н4СН3 20 1,083 1,586 —
2523 Тнофенол CeHgSH 23,2 1,074 1,58613 7477 4
2524 Анилин c6h6nh2 20 1,022 1,5863 354
2525 2-Ацетнл-6-метилиндазол (стабильн.) CH3CONN = C6HS(CH3)=CH 5 1,162 1,587 —
2526 З-Метил-2-этилиндазол C2HENN = C6H4-CCH3 1 1 20 1,058 1,587 — j
2527 Ц-Кротонилаиизол СНзСН-СНСОС6Н,ОСНз 11,7 1,091 1,587 —
882
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
1 № по пор. Название Формула t.’C A "D № по табл. «Свойства органических соединений»
2528 3, 4-Днметил-1-феиилпира- СИ - С (СНз) с (СНз) - N NCsHs 1 1 20 1,061 1,587 —
2529 Мс ^ловый эфир аци-фе-нилиитрометаиа CsH5CH = N(OCH3)-O 15 1,124 1,5871 —
2530 5-Метил-1-феиилгекса-диен-1, 3 CeH5(CH=СН)2СН(СН3)2 20 0,925 1,5873 —
2531 Форманнлид CeHiNHCH—О 25 1,14 1,5876 8455
2532 2-Ацетил индазол (ста- бильн.) CH3CONN-C6H4-CH 1 1 20 1,186 1,588 —
2533 Этиловый эфир 1-метокси-2-нафтойной к-ты СНзОС,оН6СООС2Н5 20 1,146 1,588 —
2534 а-Бромстирол С6Н6СВг=СН2 20 1,4057 1,588 7180
2535 1-Этнл-1, 4-дифенилбутен-З С2Н5СН(С6Н5)СН2СН=СНС6Нз 20 0,992 1,5880 —
2535 Дифенил СбНбСбНб 77,1 0,99 1,58822 3363
2537 Этиловый эфир а-беизил-коричной к-ты С.Н.СН-С (С Н2С6Н5) СООС2Н5 16,1 1,08 1,5885 —
2538 1, 1, 2-Трибромэтан СН2ВгСНВг2 20 2,57896 1,58902 9224
2539 о-Хлрранилин cicch4nh2 20 1,21253 1,58951 479
2540 5, 6, 7, 8-Тетрагидро-1-ами-ноиафтални NH2C6HsCH2CH2CH2CU2 1 1 23,1 1,054 1,58964 5457
2541 1, 6-Дннодгексан JCH2(CH2),CH2J 15 2,1 1,5899 2408
2542 2-Бромтнофен BrC=CHCH=CHS 1 1 20 1,684 1,59 7432
2543 2-Аллил-5-метилиндазол C3H3NN = CeH3(CH3)-CH 1 1 20 1,050 1,590 —
2544 траяс-Оксим бензальдегида CeHsCH=NOH 20 1,111 1,5908 1023
2545 2-Этилнидазол C2HsNN —CeHi—CH 1 | 20 1,073 1,591 —
2546 Метиловый эфир о-беи-зоилбензойной к-ты СбН5СОСвН4СООСНз 19,7 1,190 1,5913 -
2547 2-Метнл ди ф ен нл CcH6C6H4CH3 20 1,01134 1,5914 3394
2548 5-Бром-2-метилкумарои ВгСбН3СН-С(СНз)О 1 1 34,8 1 477 1,5915 —
2549 Тетрахлортиофен C4CI4S 30 1,7036 1,5915 7451
2550 З-Метнл д ифеи ил CtHsOH.CHj 22 1,010 1,5916 3395
2551 З-Окси-4, 4, 4-трихлор-1-фе-нилбутии-1 C6H5C^CCH(OH)CC13 9,5 1,354 1,5917 —
2552 Этиловый эфир 2-тиоиаф-теикарбоновой к-ты Cgb^SC (COOC2H5) = сн I 1 55,4 1,172 1,592 —
2553 Дифенил ацетальдегид (C6Hs)2CHCHO 20 1,100 1,5921
2554 1-Метил-2, 4-днэтилнафта-лии (CH3) (CzHsIjCioHs 13,3 0,987 1,5923 —
2555 Пропил-1-иафтиловый эфир CioH7OCH2CH2CHj 18,4 1,04471 1,59277 5509
2556 ж-Хлораннлии C1C6H4NH2 20 1,216 1,59305 480
2557 1, 2, 3, 4-Тетрагидрохинолии C6H4(CH2)3NH 1 1 23,9 1,0546 1,5933 8716
2558 N, М-Диэтил-1-нафтнламни CioHzN(C2H5)2 18,1 1,007 1,59331 5452
2559 1-Фторнафталнн C,0H,F 19,5 1,1332 1,59389 5410
2560 Этиловый эфир 1-нафтой-ной к-ты CioH/COOCaHs 20 1,122 1,594 —
2561 Этиловый эфир 1-метнл-2-нафтойной к-ты СНзСюНбСООСгНб 20 1,113 1,5950 —
2562 1, 8-Бис-(диэтнламино)-нафталин CwH6[N(C2H5)2]2 18 1,012 1,5951 —
2563 Этиловый эфир 2-нафтой-ной к-ты C10H7COOC2HS 22,7 1,114 1,5951 —
2564 1-Фенилпиразол CH-CHCH = NNC8Hs 1 | 20 1,111 1,596 —
2565 сажж-Иод-ж-кснлол (СНзЪСвНзЛ 20 1,607 1,596
2566 Бензгидриламин (CeHs)2CHNH2 21.5 1,064 1,59631 1097
56*
883
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
П р одолжение
№ по пор. Название Формула <, °C "o № по табл. «Свойства органических соединений»
2567 1. 4-Диэтил нафталин CwHe(C2Hs)2 13,1 0,998 1,5970
2568 Фтор-1, 1, 1, 2-тетрабром-этан Br3CCHBrF 16 1,939 1,5971 —
2569 Этиловый эфир а-феннлко-ричной к-ты CeH5CH = C(C6Hs) СООС2Н5 18,6 1,097 1,5972 —
2570 Этнл-2-нафтнловый эфир С2Н5ОС,«Н, 35,6 1,05 1,5975 5515
2571 1 - Б ро м - 3- ннтробе н зол BrCsHiNOj 20 1,7036 1,5979 1449
2572 2-Алл ил н н да зол C3H5NN=C«H,= CH 1 1 20 1,074 1,593
2573 Иод-л-ксилол (СНз)2СбНзЗ 20 1,613 1,598
2574 Бромоформ СН В rs 19 2,892 1,5980 1930
2575 1-Феинлгексадиен-1, 3 C«H,(CH-CH)2CsH6 20 0,919 1,5989
2576 1, 2-Днхлор-1, 1, 2-трибром-этан Вг2СС1СНВгС1 15,5 2,63 1,5989 —
2577 4-Иод -м-ксилол 20 1,623 1,599
2578 Р-Бромстнрол CeHsCH=CHBr 22,5 1,425 1,5990 7181
2579 Трибромэтнлен CHBr=CBr2 20 2,708 1,5992 9434
2580 1, 2, З-Трибромпропан Аллилтиомочсвнна CH2BrCHBrCH2Br 23 2,436 1,6 6486
2581 CH2=CHCH2NHCSNH2 78,1 1,2 0,933 1,60 7393
2582 1-Феннлпентадиен-1, 3 CeH5(CH = CH)2CH3 15,2 1,6000
2583 Пятихлорнстая сурьма SbCl6 14 1,601 __
2584 Этиловый эфир С6Ь V-метил цнниамил-идеиуксусиой к-ты sCH = C (CH3) CH= CHCOOC2H6 20 1,037 1,601 —
2585 З-Аллил-2-оксндифенил CeHEC6H3(OH) (CH2CH=CH2) 20 1,072 1,601 .
2586 1-Метил бен зим и да зол C6H,N(CH,)CH=N 1 I 17,1 1,128 1,6013 —
2587 1-Метил-2-этилнафталин CH3CraHcC2Hs 15,4 1,001 1,6014
2588 Этиловый эфир 0-метил- С«1-цнинамилиденуксусной к-ты sCH = CHC(CI I.) = CHCO2C2H5 20 1,043 1,602
2589 2, 8-Диметилхннолин (CH,)2C9HsN 20 1,0394 1,6022
2590 2-Метилнафталин CioHtCH, 39,9 0,994 1,6026 5386
2591 2-Этилнафталин C|«H7CH2CH3 15 0,9958 1,6028 5416
2592 1-Хлор-1, 2, 2-трнбромэтан ClBrCHCHBr2 20 2,65 1,603
2593 М-Ацетил-М-этил-2- нафтил-амин CioH7N(C2H6)COCH3 23,1 1,089 1,6031 —
2594 4- Иод-о-ксилол (CHsBCbHsJ 20 1,631 1,604
2595 1, 5-Дннодпентан Аценафтен JCH2(CH2)3CH2J 15 2,20 1,6046 —
2596 CwHe(CH2)2 99 1,024 1,6048 713
2597 З-Этокситионафтен C,H4C(OC2H6) = CHS 1 1 17,9 1,159 1,6050 __
25£8 Фенилдихлорфосфнп CeHsPCl2 7 1,32 1,6053 8472
2599 1 - Метнл-4-этилнафта лин сн3с,он6с2н5 13,1 1,009 1,6057 —
2600 Метиловый эфир 6-метнл-1-нафтойной к-ты CH3C10H6COOCH3 20 1,135 1,606 —
2601 Р-Бензофенон (лабильн.) (CflLhCO 23,4 1,108 1,6060 1747
2602 N, N-Днбензиланилии (CeHsCHz) aNCeHs 80 1,04436 1,60647 3166
2603 1, 6-Диметилнафталин (CH3)2CioHe 20 1,002 1,607
2604 З-Иод-о-кснлол (CH3)2C„H3J 20 1,639 1,091 1,6072 —
2605 а-Бензофенои (стабильн.) (CcH5)2CO 19 1,6077 1747
2606 1, 1,4, 4-Тетрабромбутан Br2CHCH2CH2CHBr2 20 2,529 1,6077 -—
2607 Фениллропиоловый альдегид CeH5C=CCHO 12,6 1,068 1,6079 —
2608 Окись дифенила CeH.CcH.O 1 I 99,3 1,089 1,6079 —
2609 2-Хлорнафталин C,3H,C1 70,7 1,138 1,6079 5413
2610 Феннлгндразии c6h5nhnh2 20,3 1,0978 1,60813 2703
2611 1, З-Дибромбензол СбНдВгг 17,4 1,962 1,6083 1476
2612 1-Этил нафталин C|0HjCH2CH3 14,2 1,0111 1,6089 5415
2613 о-Иодтолуол CHCcHJ 20 1,698 1,609 7715
884
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t,‘C 4 "d № по табл. «Свойства органических соединений»
2614 Р-Бромстирол (форма I) С6Н5СН=СНВг 16,6 1,42 1,6091 7181
2615 1, 7-Днхлорнафталнн 1 -Метилизох ннол и и 99,5 1,261 1,6092 5378
2616 C6H,CH = CHN = CCH3 1 1 20,5 1,076 1,6095 —
2617 Четыреххлорнстый титан TiCI, 10,5 1,61
2618 1. 1-Дифенн лэтилеи (С€Н5)2С = СН2 14 1,038 1,610 9400
2619 9-Метнлфлуорен С6Н.С6Н4СНСН3 1 1 66,2 1,026 1,6101 —
2620 1. 2-Днбромбензол СсНДЗгг 17,4 1,964 1,6117 1475
2621 N-Бензнланнлнн C6H5CH2NHCeH5 24,8 1,065 1,6118 1150
2622 2-Ацетил-1-метнл-4-этил-нафталин CioHs(CH3)(C2Hs) (COCHJ 15,1 1,074 1,6118
2623 Хинальдин CHsCsHsN 20 1,0585 1,6126 8649
2624 1-Фенилбутаднеи-!, 3 CeH5CH = CHCH=CH2 16 0,931 1,6128
2625 Этиловый эфир циннами-лиденуксусной к-ты CcHsCH = CHCH= CHCOOC2Hs 42,2 1,029 1,613 —
2626 Этиловый эфир 2, 7-ди-бром-9-флуоренуксусной к-ты С17Н14О2ВГ2 99,8 1,512 1,6130 —
2627 Метнл-1-иафтиловый эфир CwHfOCHs 34,5 1,07931 1,61341 5098
2628 Хлористый циннамоил C6HECH=CHCOC1 42,5 1,6136 4333
2629 Изохинолнн c6h4ch=nch-ch I 1 20 1,0986 1,6148 3849
2630 5-Метилтнонафтен CH3CEH3CH=CHS 1 1 21,7 1,111 1,6148 -
2631 7 - Мет нлхи но л и н CH3CsHeN 20,8 1,067 1,6149 8706
2632 Этиловый эфир а-ме- СсН тилцнниамнлнденуксус-ной к-ты 5CH = CHCH=C (CH3) COOC2H5 20 1,041 1,615
2633 Дифен илкетен (СбН5)2С=СО 14,1 1,11 1,615 5355
2634 1, 4-Днметилнафталнн 6-Мет ил хинолин C,oH6(CH3h 16 1,01803 1,61567 —
2635 CH3CsHc,N 20 1,0654 1,6157 7705
2636 1, 2-Днметилнафталин 8-Метил х ннол ин CwH6(CH3)2 20 1,019 1,616
2637 CHaCsHeN 20,8 1,0722 1,6162 8707
2638 З-Метнлхинолин chsCjH.n 20 1,0673 1,6171 8703
2639 1-Метнлнафталин C,0H7CH3 20 1,00 1,618 5385
2640 Этиловый эфир аллоцин-намилнденуксусной к-ты C,H,(CH=CH)2COOC:Hs 20 1,043 1,619 —
2641 N-Метилдифениламин (CeHs)2NCH3 20 1,0476 1,61928 3421
2642 Коричный альдегид CeH6CH=CHCHO 20 1,0497 1,61949 4363
2643 4-Ацетил- 1-этнлнафтали и C2HcC,oH6COCH3 15,7 1,092 1,6198
2644 4-Метилхннолин C«H4C(CH3)=CHCH=N 1 1 20 1,0862 1,6206 4654
2645 1-Нафтол C10H7OH 98,7 1,09539 1,62064 5534
2646 2-Нафтальдегнд C10H7CHO 99,4 1,078 1,6211 5442
2647 6-Метилхиноксалин CH.,C6H3N-CHCH = N 1 1 18,4 1,118 1,6211 —
2648 Иодбензол C„HEJ 17,8 1,835 1,6213 1531
2649 1, 4-Дихлорнафталин СюНбСБ 75,9 1,300 1,62282 5375
2650 Хиноксалин c6h4n=chch=n 1 1 48 1,1334 1,6231 8682
2651 1. 8-Днхлорнафталин CjoHcCK 99,8 1,292 1,62357 5379
2652 8-Ацетнл-2-метилнафталнн CH3Clt,H6COCH3 13,3 1,099 1,6244 —
2653 л-Броманилин BrCEH4NH2 20,4 1,5793 1,62604 384
2654 Метнл-о-аминофенилсуль-фид CHsSCeH4NH2 17 1,133 1,6263 —
2655 Хинолин c6h4n=chch=ch 1 1 20 1,095 1,6268 8686
2656 2-Ацетил-1-метил нафталин CH3C,oH„COCH3 16,1 1,105 1,6270
2657 Сероуглерод cs2 20 1,2628 1,6276 —
885
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
Продолжение
№ по пор. Название Формула t,°c 4 "d № по табл, «Свойства органических соединений»
2658 3-Меток ситионафтен С6Н4С(ОСНз) =CHS 1 1 13,6 1,209 1,6277 -
2659 1, 1, 1, 2-Тетрабромэтаи СН2ВгСВгз 20 2,87482 1,62772 9218
2660 1-Ацетилнафтални СНзСОС.оН, 21,5 1,117 1,6280 —
2661 Нитрил 1-нафтойной к-ты CioHtCN 17,8 1,11 1,6298 5598
2662 2, 5-Дибромтиофен BrC = CHCH-CBrS 1 1 20 2,141 1,63 7433
2663 Метнл-о-бромфеиилсуль- CH3SCeH4Br 20 1,522 1,6319 —
2664 фид N, №-Днэтил-2-нафтиламин CioH7N(C2H5)2 21,6 1,025 1,6321
2665 1-Хлорнафталнн CioHiCI 20 1,1938 1,63321 5412
2666 Тионафтеи C6H4SCH=CH 1 1 36,2 1,15 1,63324 7408
2667 1, 2-Дихлориафталнн CioHeClz 48,5 1,315 1,63375 5373
2668 л-Фениленднамнн C6H4(NH2)2 57,7 1,10696 1,63390 8202
2669 2-Хлорхинолин CeH4CH=CHC(Cl) = N 1 1 24,6 1,246 1,6342 8724
2670 Дифенилсульфнд (CeH6)2S 18,5 1,117 1,635 8219
2671 Л4-Д1етилстильбен CH3CeH4CH-CHC6H5 60,5 1,989 1,6363
2672 1, З-Дниодпропан JCH2CH2CH2J 15 2,576 1,6363
2673 мезо- И зоа мил а нтрацен Ci4H»CH2CH2CH(CH3)2 71,1 1,002 1,6364 —
2674 1, 1. 2, 2-Тетрабромэтан CHBr2CHBr2 20 2,96725 1,63795 9219
2675 N, Ы-Диметил-2-нафтнламии CioHzNfCHah 53,2 1,028 1,64432 5466
2676 4-Метил-1 -нафтальдегид СНзСюНбСНО 38,2 1,125 1,6457 —
2677 Бензальацетофенон C6H5CH=CHCOC6HS 62,3 1,071 1,6458 8638
2678 М-Этил-1-нафтиламнн CioHjNHCjH, 15,1 1,06 1,64773 5462
2679 Фениловый эфир изотио- CeHsNCS 23,4 1,126 1,64918 3827
циановой к-ты 1,0614 1,64927
2680 2-Нафтиламнн C,oH7NH2 98 5463
2681 4-Метокси-1 -нафтальдегид СНзОСюНбСНО 43,7 1,183 1,6530 —
2682 М-Этил-2-нафтнламин C,0H7NHC2Hs 21,3 1,06 1,65440 5476
2683 1-Нафтальдегид С10Н7СНО 19,3 1,15 1,65464 5440
2684 1-Бромнафталнн С10Н7ВГ 16,5 1,48875 1,66011 5345
2685 Азоксибензол (мономер) C6Hs(NON)C6Hs 26 1,24 1,6644 62
2686 Хлористая сера S2C12 14 1,632 1,666 —
2687 2-Иоднафталии C10H7J 99,4 1,6617 5384
2688 1-Нафтиламнн CwH?NH2 51 1,1 1,6703 5447
2689 мезо-Эти л антрацен C,4HsC2Hb 99,2 1,041 1,6762 617
2690 1-Метилантрацен C14H9CH3 99,4 1,047 1,6803 611
2691 1, 8-Нафтиленднамнн С,оНс(МН2)2 99,4 1,127 1,6828 5499
2692 Днфеинлтеллур (C6Hs)2Te 15,8 1,603 1,6930 —
2693 .мезо-Метил а нтрацен СнНэСНз 99,4 1,066 1,6959 613
2694 1-Хлорантрацен CI4H9C1 99,5 1,171 1,6959 —
2695 Трехбромистый фосфор РВгз 26,6 1,747 1,697
2696 1-Иоднафталнн C10H7J 14 1,70540 5383
2697 цис-1, 2-Дииодэтилен JCH=CHJ 11,2 3,1 1,706 —
2698 1, 6-Нафтнленднамнн CwHs(NH2)2 99,4 1,147 1,7083 5497
2699 Бромистая сера S2Br2 3,33 * 1,736 —
2700 Йодистый метнлен CH2J2 15 1,7425 5086
2701 Двусернистый водород H2S2 .... 1,885 —
ФОРМУЛЬНЫЙ УКАЗАТЕЛЬ
К ТАБЛИЦЕ «ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ»
В этом указателе суммарные формулы органических соединений расположены по группам (арабская цифра) в зависимости от числа атомов углерода н в каждой группе — по подгруппам (римская цифра) в зависимости от числа других элементов, входящих в формулу. Например, соединения с суммарными формулами C4H4O2CI2 (№ 1220) или C4H8N2S (№ 2581) следует искать под общим групповым знаком 4 III, так как в обеих формулах имеются 4 атома углерода и 3 других элемента. Элементы в суммарных формулах размещены в следующем порядке: С, Н, О, N, S, F, Cl, Вг, J, затем все другие — в алфавитном порядке символов. Суммарные формулы в подгруппах расположены одна за другой в той же последовательности элементов и, кроме того, в порядке возрастания числа атомов каждого элемента. Рядом с формулой приведен номер или несколько номеров соединений, помещенных в таблице и соответствующих данной суммарной формуле.
Названия неорганических соединений, показатели преломления которых приведены в этой таблице, помещены в конце указателя в алфавитном порядке.
11 C2H2J2 C2HSN 2697 10 C2H3OC1 C2H3OBr 112 1105
cs2 2657 c2h8n3 1513 C2H3O2C1 91, 631
СС14 1278 C2H3C13 781, 1378 c2h3ns 1339, 1984
C2H3Br3 2538 C2H,FBr2 1694
1 II C2H4O 7, 22 C2H3F2Br 113
C2H4O2 9, 39, 1487 C2H3F 2j 1340
CHN 1 c2h4n 6 1471 c2h4o4n2 963, 1003
СНС1. 997 C2H4C la 400, 907 c2h0on 563
СНВг. 2574 C2H4Br2 1843, 2105 c2h5of 28
СН2О2 37 С2Н5Вг 533 C2H3OC1 163, 855
ch2n2 853 C2H5J 1853 C2H5OBr 1161, 1632
СН2С12 529 C2H6O 21 C2H5OJ 2210
CH2J2 2700 СаНвОг 679 C2H5O2N 117, 331
CH3J 2013 C2H6S 736 C2H5OsN 81
СН4О4 4 C2H6S2 1942 C2H5O4S 118
COsN 720 C2H6Cd 2517 C2HeON2 776
CFCI, 89 C2HeHg 2046 c2h6o2n2 947
СС13Вг 2019 CjHgNa 269, 1015, 1116 c2h,o4s 97
C2O2C12 717 c2h7on 379, 1108
1 III C2O2C14 1170
CHSC1, 2224 C2F2C14 C2F3C1s 339 14 3 I
CH3ON 971 C2F3Br8 1323
CHsO2N 137 C2F4CI2 3 C3O2 1107
с H4O2N2 CH6ON 1251 396 C2Cl2Br2 2492
CO2NC13 1241 3 II
CO2NBr3 2506 2 III
C3HN 93
2 I C2HOC13 1151 c3h2n2 372
C2HFBr4 2568 C3H3N 132
C2C14 1758 C2HF2Br3 1788 C3H3CI5 1832
C2HF3Br2 368 c3H4o 193, 657
2 II C2HCl2Br 1У16 C3H4O2 499
C2HCl2Br3 2576 C3H4O3 650
C2HC13 1449 C2HCl3Br2 2016 c3h4n2 1362
C2HC16 1753 C2H2O2F2 8 C3H4C1. 827
C2HBr, 2579 C2H2O2C12 1315 C3H4Br2 2057, 2104
C2H2O2 72 C2H2FBrs 1709, 2385 C3HSN 24, 29
C2H2C12 1007, 1061 C2H2F2Br2 989, 1262 C3H3C1 382
C2H2CI4 1489, 1573 C2H2ClBr 1648, 1667 C3H5Br 957, 1128, 1144, 1310
C2H2Br2 2250, 2176 С2Н2С1Вг3 2592 C3H3Br3 2580
C2HaBr 4 2659, 2674 C2H3ON 318 CsHcO 18, 346
887
isssisi » . ядо „ »уцвд*да
i 5 ^S!»s I Ж « Й *? I " S> ‘ ? I h
g Ж I ?r,fe S»S*? 8S s kw
S h" fe S5 8ЙГ S 858
ООП
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ I ФОРМУЛЬНЫЙ УКАЗАТЕЛЬ
nnnp p x x x x x o^zp p
n nnprip x xxxzx p oz^p
pp pp
XX XX pp po
xxxx
<e os x oo
2^00
pppppppppppp
*x'xx^xx*xx"x"x'x"x
<r “J N 'J 7 s: cn ci ^1
о СТ О “0 zoo О 0712
“ (CT113 cT
X
§i=®6s%sgi.s»y8ipssHgagigigg8|sii5i|||8Ss a
JeWf 1 »S 4 g « 3
Bfe ®sl Sfel s is i Й I s
-йЖ1Я§Язр1га ё§ a§§gS |Sg
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
7 11 C,H18 124, 130, 166, c8h18n 1053
С,н12с>4 С7Н14О2 363 114, 149, 165, 209, 216, 219, 164, 215, 430, 169. 172, 177, 187, 211, 254, 397 174, 191, 267, c8h„n C8H17F C8H17Br C8Hl7J 883, 1049 144 904, 975, 1031 1541
474, 486, 1523 8 II С8НрО 186, 456, 457
c7hI4n2 632, 930 «8- 473, Бад;
c'h”i2 1215 C8H8O 2390 636, 597, 613.
c,h15n c7hI8f 494, 909, 1097 88 C3H6O2 C8H6N2 2086, 2265 2650 c8h„o, 623, 639, 698 146, 687 949 293, 296, 519, 641 1361 198
C,H15C1 495, 507, 610 517, C8H6C12 C8HeS 2493 2666 c8h18n
C7H16J c7H16o 1542 411, 414, 463, c8h,n C8H7C1 1971, 1998 2372. 2478 C8H20As2 Q8H2oGe G8H2gPb
466, 472, 477, C8H;Br 2534. 2578. 2614 1579, 1784, 1805.
484, 502, 503, C,H8O 1983, 2063, 2149, C8 H2OS1 G8H2oSn 1863, 1924
516, 522, 673 615, 2160, 2207, 2309 2232, 1384
C7H18O. 128 Gg ^8^2 1720, 1820. 1821,
c7h17n 281, 449, 535 1831, 1934, 2134, 8 HI
C7HlsPb 1715, 1740, 1909 2205, 2273, 2286,
7 III C8HSO8 2337, 2340, 2103 2472 C8H4ONle 1046
ceH8o, 1769 C8H4O2C12 2426
C,H5ON 2095, 2380, 2515 C$H8N2 2264, 2586 2203, 2258, 230 c8h7on C8H,OC12 2482 2047, 2065
C7H5OC1 227/, 22«8, 23У4, C,H8J 2565, 2573, 2577, c«h8on 2219
c,h5ns 2403 2594, 2604 c8h3o2n 2513, 2529
2679 C8H щО 1799, 1837, 1887, c8h„o3n 2166
c7h7on 2531, 2544 1911,1936, 1995 2159 C,HWOS 2158, 2252
C7H7OBr 2352, 2448 2213, 2018. 2076 C8Hl0O2N2 2261
C7H7O2N 2042, 2069, 1402. 1410. 1341 c8h„on 1245
C7H7OsN 2215 c8h„n 1141, 2090, 2271, C8HnOCl 1610
2364, 2433, 2471 2291, 2317, 2320, 964, 1086
C7H7SBr 2000 2321, 2331, 2353, 1230, 1435
С7Н8ОЫ2 2476 2358 , 2427 C8H„O4N 577
C7H8OS 2298, 2339 C8H„C1 1739 C8H„O4C1 1189
C7H8O2S 1986 2297, 1492. 1585 C8H„O4C13 1298
C;H9ON 1441, 1646, c8h‘12o2 1041; 1075. 1285. C8Hl2OCl2 1642, 1689
C7HsO2N 2467 1426, 1710 C8H,2O2C12 1343
1080, 1581 1085, 1304 c„h18on 1259
C7HgO8N 1367 839, 848, 918, c8h15on 1488
C7H8NS 2654 1353 c8h;7on 453, 542
C7Hio03N2 1095 1159 c8h„o2n 676
C7HnOCl C7HnO2CI 1244 738 c8hi2n2 1697, 1895. 2435 2241, C8Hl8ON2 896
СуНхзОгВГа C7H12O4 1624 363 C8H18N C8HI4O 1560 849, 878, 910, 9 I
C7H i^OgC 1 715 977. 984. 999.
C,H14O4N2 014, 879, 934 C,H,6ON 478, 970 C,H15O2N 526, 581, 596, 7 IV C7H6O2NC1 2292 8 I C8H8 2242 C«H8 2202 617 C8H14O2 G8HI4O8 C8H14O, c8Hl4o6 c8H14oe 1042, 1062, 1101, 1442 599, 634, 677, 684, 713, 732, 861, 873, 983, 1012, 1222, 1375 425, 504, 961, 1026. 1055 343, 404, 441, 455, 614 755 933 1547 GgH8 CgHl0 CgH12 CgHl4 C0HIfi 2456 1867, 2074 i. 2188. 2217 2235 114’ 158®. }®71. 1603, rJV721, 1°5°. J*®4- 1495 389’ даб 680,
C8Hio 1619, 1621, 1639, 1238, 1437
1754 C8H,5C1 1104, 1326 GgH2() g && 252.
C8H12 1328, 1381, 1460, 1503
1467, 1527 C„H16O 378. 383, 391, C.H20
C8HM 469, 551, 555, 487, 779, 838, 22'1
594, 662, 836, 1034. 1115, 1118,
891, 924, 926, 1134, 1143. 1155, 9 u
939, 1171, 1203, 1177, 1193, 1194,
1271, 1450 1210, 1248, 1270,
c,H16 288, 314, 327, 1301, CgH.N 251?
328, 350, 392, C8Ht6O2 195, 212, 230, 238, C.H.O 26& _ 26'4. -
405, 410, 475, 245, 259, 264, 352. C,H,N C,H8O
510, 543, 629, 295; 303. 21$1W*Sl 2269,
647, 661, 1202 492,513, 611, 728 231 2642
890
формульный указатель
9 11 C8H2tlO4 138 CioHgPa 2343
c8h21n 416 c10h8n 2616, 2623, 2631,
сэн8о, 2189, 2327, 2382, c8h21n8 1231 2635, 2637, 2638,
C8H22Pb 1752, 1891 2644, 2680, 268
CfiHgOs 2395 1947, 2075 Сх8Н24РЬ 1872 C joHjoO 2225, 2248, 2279, 2282, 2275, 2449,
CgHgNj 2564, 2647 2453, 2509
CeHgS 2630 9 III Cj8H|o02 2112, 2218, 2237,
С9Н9С14 2410 2247, 2289, 2313,
C8H9Cle CgHjoO CjHioOf 2244 1890, 1970, 2045, 2054, 2058, 2060, 2139, 2162, 2181, 2186, 2191, 2233, 2307, 2371, 2387, 2454, 2499, 2510 1659, 1671, 1773, 1816, 1824, 1972, 2068, 2080, 2094, 2106, 2150, 2206, CfiH6NCl C9H7OC1 C8H7OBr C9H7O2CI3 C8H8ON2 c8h8os C8HgO2C12 c9h8on C8HBOBr CBH8O2C1 2669 2628 2548 2010 2532 2658 1987 2396 2443, 2450 1928, 1953, 1954, 1968 CjoH10Os C ioHxo04 CioHjoNa C10HnCl3 c10H12o 2384, 2409, 2483 1808, 1903, 2091 1814, 1875 2500, 2501, 2691, 2698 2270, 2417 1826, 1893, 1955, 1967, 2002, 2014, 2473, 1915, 2572, 1922, 1997, 2020,
C9Hx8O3 C9Hl0N3 C.HnN 2276 1948, 2008, 2064 2463, 2545 2489, 2557 C8H9O2Br C9H|oOCl2 CfiHnON CgHjjOBf 2173, 2174 2056, 2184 2073, 2367 2227 2021, 2023, 2039, 2082, 2143, 2148, 2161, 2245, 2036, 2107, 2155, 2257,
CgHjjJ CfiHjjO 2497 1611, 1702, 1762, 1786, 1833, 1846, 1847, 1874, 1894, 1897, 1898, 1930, 1973, 2035, 2052, C8HnO2N CQH12ON2 C9Hl2OS C8H12OC12 c8h1son CBH13OC13 C9H13OgN C9H1SO4N C9HI3O5C1 С8НхзОйВг c8h15on C9H18O2N 2101, 2281, 2391 2028 2084, 2192 1876 1317, 1593 1678 СхоН1202 2348, 2362, 2406, 2479 1663, 1677, 1751, 1781, 1809, 2050, 2102, 2120, 2129, 2154, 2226, 2457
C8H12O2 2081 1588, 2294 1236, 1249 521 C|cHj2Os 1868, 1896, 1960, 1977, 1981 1950, ,2319
C9HI2O3 1332, 1666 915 C|oH12N2 2359, 2360, 2378,
C9H12O4 CBH13N 1749 1166, 1982, 2024, 1228 1428 2411, 2465, 2490, 2495. 2496, 2526
C8Hi4O 2093, 2236 946, 1032, 1464, 718, 1082 C10HlsN 2347, 2349, 2494, 2540 2449,
CBH14O2 1466, 1669 с|Сн14о 1631. 1665. 1729.
1043, 1217, 1344, 10 I 1748.1756.1774.1806.
1348, 1414, 1490, 1822, 1823, 1885,
1501, 1641, 1644, 1913, 1949, 1951,
CBH14O3 1658, 1681 c10hb 2502 1963, 1966
804, 906, 1076 CioHjo 2283, 2330, 2507, 2624 CxoH|402 1417, 1657
C9H14O4 805, 833, 956, 962, CjoHj2 1750, 1999, 2059, СщН|4О4 1338
C8H14O3 987, 1008, 1431 2067, 2115, 2196 CXoHx4N2 2003, 2287
775, 784, 886 1517, 1548, 1553, C1OH1SN 1851, 1931, 2151,
C9H14Oe 656 1557, 1563, 1580, 2175, 2221
CgH14N2 1830 1602, 1604, 1614, CioHjgO 1074, 1094, 1265,
C9H14S 1643 1634, 1653, 1672, 1327, 1349, 1369,
C8Hl4C12 1684 1696, 1713, 1714, 1374, 1458, 1482,
C8H|5N 920 1724, 1854, 1856, 1494, 1496, 1534,
C8Hi6O 1025, 1125, 1399, 1858, 1932, 2051 1535, 1544, 1555,
1406 ClcH16 969, 1027, 1052, 1558, 1637
747, 768, 1063, 1110, 1071, 1237, 1307, C10H16O2 759, 927, 1057, 1208,
C9H16O3 1234 1313, 1334, 1364, 1322. 1347.1350.1359,
570, 1167, 1207 1396, 1397, 1416, 1423,1439,1445 1463,
C8HjgO4 304, 421, 446, 539, 1421, 1448, 1451, 1484, 1485. 1506.
541, 552, 560, 569, 1457, 1475, 2178 1525. 1533, 1590
C8HjgBr2 608, 639 CiqH|8 778, 854, 1011, 1078, С10H ieO4 884, 890, 1000, 106.5,
2005 1132, 1162, 1172. 1066
C8H17N 1578 1185, 1205, 1242, CigHjgOg 816, 789, 887, 1280
CgHjyCl 1136 1267, 1354, 1480, C10HieO6 592
C8HX7Br 1477, 1498 CxqH2o 483, 652, 653, 772, CXBHjgN2 1673, 1703, 1776
C8HWO 321, 413, 540, 1036, 791, 811, 860, 967 cwh17n 1018. 1587, 1727
1103, 1201, 1282, Cl0H22 276, 291, 315, 322, CWH17C1 1407
C8H18O2 1292, 1337 253, 262, 270, 307, 338, 356, 380, 520 332, 348, 355 cwH1Bo 995, 1016, 1035 1133, 1142, 1200, 1233, 1072, 1175, 1263,
C8HJ8Og C8H18O4 263, 317 377 10 II 1287, 1308, 1383, 1390, 1355, 1411,
CgHi8S8N C0H19Br 2157 875, 1140 С1ВН6С12 2615, 2649, 2651, 2667 1430, 1444, 1453, 1478, 1452, 1497
CgHl8Br 1102 Cx8H7Cl 2609, 2665 C|8HXgO2 780
C9H20O 213, 511, 633, 642, C1BH7Br 2684 СщН. jgOg 374, 696, 1129
658, 666, 667, 678, C10H7J 2696 CwHjgCh 420, 480, 481 515,
681, 691, 725, 727 C10H8O 2645 525, 590, 603, 668
891
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
10 II CnHnN СцН12О 2589 2145, 2168, 2251, 12 I
СюН18О5 c10h18n 792 1386, 1387 2255, 2383, 2259, 2418, 2305, 2423 C12H10 C H 2536, 2596 2505, 2591, 2612, 2634, 2442, 2575
CwHi9Cl 1269, 1293, 1311 СцН(2О2 1777, 1901, 1991, ^I2rl12 2603,
С 10^20^ 575, 589, 911, 1145, 2001, 2044. 2110, C T-I 2636
1182, 1187, 1192, 2140, 2169, 2182, v>i2riI4 C T-I
1216, 1229, 1254, 2183, 2194, 2249, ^12n16 1865, 1889, 2070, 2146 1618, 1654, 1838 1472 645 2048,
с I0H20o2 1281 340, 366, 417, 459, 2311, 2334, 2325, 2404, 2333, 2514, CI2H18 1730,
460, 479, 612 2521, 2527 C H
Ci0H21N 567, 1235 СПН12О3 1877, 1925, 1969, v>i2n22 С
С1(1Н21С1 785 1980, 2029, 2113, '^12rl24 C.oH
С10Н21Вг 1138 2239, 2519 v>i2r*26 471, 506
C1CH21J 1514 ChHi2N2 2280, 2455, 2458,
СюН22О 277, 740, 771, 803 787, 2466, 2543 2468, 2528, 12 II
С48Н22О3 200, 266 СцН)3С1 2156
c10H22s 1077 спн14о 1686, 1803, 1857, C12H8O 2608
C10H23N 509 1783, 1859, 1900, 1906, Cl2H,0O 2504. 2663. 9676
CjoH24Pb 1705, 1712, 1910, 1979, 2025, Ci2HiqO2 2681
1817, 1842 2152, 2243, 2293, c12h10s 2670
2296 CI2H10Te 2692
10 III СцНнОа 1564, 1565, 1582, C12H12O 2570
1583, 1608, 2033, Cj2 Hj2O2 2222
2079, 2097, 2111, Cl2H,2O3 2118, 2223, 2295
2551 2124, 2136, 2363, C12H12O4 2032, 2122. 2240
Сц)НдО2С1 1944, 2285 2425 1840, 1845, C>2Hi2S 2522
C1()H9N2C1 2491, 2512 СцН14О3 1766, c12h13n 2675, 2678, 2682
Ci0H10ON2 2525 1860, 2071 CI2Hl4O 1965, 2135, 2177,
C10H10OS 2597 СПН14О4 2077 2256, 2312, 2335,
C10H10O2N2 2422 СцН14О0 1385 2368, 2485 2402, 2415
C10HnON 2201 СцН14М2 2272, C12H14N2 2230, 2436
С^НцОЕт 2304, 2370 СПН14С13 2006, 2180 CI2H14O2 1807, 2087, 2144,
Ci0HuO2C1 2263 СцН16О 1554, 1623, 1711, 2167, 2170, 2171,
CI0Hi2O2Cl 1737 1763, 1812, 1873, 2193, 2198, 2214,
CiqHi3O2N 2026 1882, 1884 2290, 2381, 2386,
CWH13O2C1 1793 СцН16О2 2038 2439
CioHjflONj 1919 СцН4бО4 705, 1486, 1674 C12H14O3 1738, 1935, 2041,
С1оН14ОС12 1719, 1957. 1962 СцН16О6 1028, 1044 2089, 2121, 2229,
C10H14O2N2 1540, 1704 CgiHieOj 1010 2365, 2447, 2516
CioH.l402Cl 1655, 1695 СцН|6Ов 705 1297, 1306, C12H14O4 1747, 1795, 2109,
C10H15ON 1324 СцН|зО2 954, 2430
CioHjgOjN ИЗО 1365, 1371, 1403, C12H1PO 1839, 1964. 2163
CiqHibOjN 1331 1434, 1446, 1462, C12HICO2 1574, 1591, 1592,
CioHib04N 582 1508, 1676 1899, 1941, 2300,
CioH1602C1 1342 С 11^18^4 1112, 1113 877, 2017, 2040, 2345,
Ck>H17ON 1356 СцН18Оя 710,. 829, 2354, 2451
CioHj702N 1440 923 1268, 1299 ^12^16^3 1764, 1778, 1791,
C10H17O3N 1532 С j|H2gO 1264, 1797, 1892, 2007,
C,0H18ON 1020 СпН20О2 858, 1021, 1147 2444
Ci0H21O2N 742, 868 С11Н20О4 493, 514, 559, Cl2H.|pN2 2200. 2318
11 I cuh21n CjiH22O 588, 625, 1433 646, 690 655 C)2Hi7N2 c12Htso2 C12HlsO3 2374 1589, 1670 1184. 1459. 1504
С11Н22О2 531, 585 12H4sO4 1336, 1400
СцН Ю 2590, 2639 СцЫ22^2 8U0 766, 793, Cj2H18Oe 1148
СцН|2 2582 С цН24О 489, Cj2H lgO7 764, 994
C„HI4 1810, 1886, 2099 808 1819, 1828, C i2H2oO 1377
СцН16 1-520, 1528, 1567, СцН26РЬ 1768, C12H2qO2 944, 1059, 1124,
1569, 1584, 1597, 1834 1166, 1195, 1273,
1600, 1609, 1629, 1277, 1303, 1405,
1675, 1693, 1733, 1507
1746, 1825, 1841, 11 111 С^НэдОз 1370
1870, 1871, 1883 С12Н2<)О4 1024, 1067, 1068,
син22 607, 703 CuHioOjS 2552 1089, 1090, 1135,
СцН24 412 СПНПО2С1 2413 1284, 1401
СиНцКгС! 2299, 2342 Cj2H2o05 917
CnH12ON2 2369, 2392
11 II CnH13O2Br 2441 12 II
СцН16ОС12 1608, 1904
cuh7n 2661 C11H17O2N 1601
cnH6o 2646, 2683 CnH17O3N 1606 Cl2H20O7 935
СцН4оО 2627 ChHI7O4N 622 C42H22O 1146, 1279
СцНцОг 2012, 2246, 2379, CjjHjoON 1465 C|2H22O2 820, 936, 958
СцН10О2 2366 CiiH19O2N 1409, 1419 Ci2H22O3 1058, 1169
892
ФОРМУЛЬНЫЙ указатель
431, 532, 697, 699, CigHjyON 2049 CisH22Os 1566
749 CiaH17O2N 2315 ClsH24O 1661, 1815
С12н22о6 951 С15Н26О 1549, 1551, 1722
С12Н24О 885. 1424 14 I с 15Н26О2 1225, 1274
С[2Н24О2 579, 580 2618, 2619 С ir,H2GO6 744
Ci2H24N2 1537 CisH26Nj 2031, 2053
С|2Н2бО 497 СцНм 2434, 2470 C|sH23O2 996
Ci2H27N 558, 620 2нж116 2464 2401, ClgUggN 337
Ci2H27Ns 1218 СцН18 2061 2088, Cl5H34Pb 1759
•СчгНэдРЬ 1685, 1770, 1804 2520
Cl2H30Sn2 2100 Ci4HS0 938 15 ill
12 HI 14 II CJ-H.AN 1792
CizHjoONg Ci2Hi2ON2 2685 2437 Cf4HgCl СцН10О С14Н10О? Cl4Hl2O СиНиО2 С14Н,4О Cl4HI4O2 Ci4H14O3 2694 2633 2474 cI5H33o3B 336 16 I
^izHj^OgCl £12Hi4ON2 C12HuO2N2 C12Hi4O2CI Ci2H21ON 2083 2284 2398, 2438 1939, 2424 1454 2553 2419 2643 2561 2341, 2533 C16Hl4 ClfiHie £ 1бН2б CieH32 2689 2408, 2414 1926 857
'C12H23O2N C12H24O4N2 1393, 1412 714 c14hI4n ^цН|6О 2462 2376, 2432 16 fl
Ci2H27O3B Ci2H27O4P 285 545 13 I С14Н1сОг C14HI6O4 2446, 25’84, 2632 2004 2116, 2141 2588, C16Hl6O4 C16Hi8O2 С 1бН2о04 CrH22O4 2324 2346 1521 1576, 1862
Ci4H|eN2 2452, 2487 1516
С1зН12 2484, 2547, 2550 c14h17n 2558, 2664 *“* 16* ,26v-’ 1429
С1аН,4 1717, 2587, 2599, СмНюо 2216 '“'16ll26M3 C,rH„N 1796
C1SH,6 ,'-*13r*20 2640 2187, 2530 1620, 1718 С]4Н18О2 cI4HI8o? £i4H20O4 1918 1645 1505 ^*16 27х’ С16Нз2О2 C16HS3J 654, 753 1483 605
^12Hj8 856 Ci4H20O8 830 ^16* х34'-х CI6H36Pb 1626, 1735
С14Н22О2 1545, 1575 C IgHggSn 1395, 1408
13 II Син22о4 1296
£цН22О3 1499 16 HI
^is^toO 2601, 2605 ^цН24О2 1289
£i3^l2O 2652, 2656 С14Н24О4 1126, 1153 Cl6H25O8Cl 1518
C 13^12^2 2560, 2563, 2600 C14H24N2 1938, 2278
C13H13N 2566, 2621, 2641 Ci4H26Os 709 17 I
CI3HI4O 2375, 2555 С14Н26О4 745
C12HHO2 2072, 2125, 2253, С и Н28О2 659, 660, 682 C|7H2Q 2302
2357, 2481, 2625, 2640 С14Н30О 406, 595 Cl7H36 832
С1зН14О2 2328 С14Н32РЬ 1742, 1757
£1зНцО3 2066, 2204 17 ||
CWHl4O4 2085, 2092, 2332, 2377 14 III C17H16O2 2569
€„HmN2 2412, 2480 Ci4H15ON 2593 C|7H34O2 721
CisHi6O 2078, 2138, 2211, 2262 15 I Cl7Hs8Pb 1650, 1692
Cis^igOz 1937, 1849, 1945, 2027, 2119, 2137, с15н12 2690, 2693 17 111
2164, 2351 £tsHl4 2488, 2671 C]7HHO2Br 2626
C13Hl8O3 1794, 2055, 2208, £tsH16 2397, 2469 C17H2lO4N 1706. 1708
2428 c16Hr 2554
c18H18o 1790, 1985 С 15^24 1572, 1594. 1598, 18 I
Ci3H18O3 1543, 1802 1652, 1668, 1687,
С|зН20О 1651, 1701, 1850, 1732, 1760, 1782 CieHgo 2535
1923, 2030 Ci8H3o 1474
'Си^гоОг 1427, 1680, 1741 ’ 15 П C18HS4 729
13^20^3 1491, 1530
^13^20^4 974 2677 18 II
С 13^20^8 750 С15н12о3 2546
£ 1зН2гОг 1295, 1546, 1775 £i5Hi4O 2585 CI8H15P 1975
С13Н22О4 1087. 1114 Ci5Hi4O6 2153 C18H,eO2 2537
£1зН24О2 866 Cl5HlfiO 2486, 2622 C1$H26^2 2126, 2460, 2562
С^НгвОг 621 £15^170- 2022 CJ8H23O 1509
С|3Н2вО 553 С15Н|8О 1952, 2147, 2431, C 18^28^4 1436, 1443
‘С 13Н30Р ь 1723, 1772 2475 C18HS.O2 1368
13 in Ci5Hi8O2 1988 C j8Hg2O7 290
Ci5H20O6 1329 c18H34o 1149
С15Н20О7 1372 C,SHMO2 819, 1100, 1275
?С13Н15О3Вг 2009 С15Н20О., 1174 C18H^4O} 367
2172 с15н22о. 1844 C18Hl4O. 1261
893
ПОКАЗАТЕЛИ ПРЕЛОМЛЕНИЯ ЖИДКОСТЕЙ
18 II 23 I
С1вН86О 1239 ^28^48 527
CuHjcOj 706, 743
СщНдеРЬ 1636 23 II
19 I C28.HsbO2 1346
C28H44O2 1152
CieHie 2511 C2aH4bO 606
С|9Н20 2673
C19H22 1373 24 I
CwH4o 746 C24H50 651
19 11
24 II
CjsHjoOa Ci aHocOo 1500 941 C24H46O2 1123, 1204
'“'18х *86v-'2 CigH32O3 1206 C24H46O3 624
CjeH^Pb 1625 25 I
20 I C2gHs2 572
C20H40 602
C20H42 712 25 II
c 25^ 40^2 1529
20 II C25H42O2 1319
C2oH19N 2602
C20H23O2 1879, 1884, 2190 26 I
C20H30O4 1539 СчгНг! 704
C20H34O2 1330 '“'26х 64
524, 1253 26 II
C20H40O 1288
C20H40O2 864 C2cHB2O2 818
C20H42O 842
C2oH4<Pb 1599 27 I
C20H 44$П 1380, 1394 С2?Н5е 724
21 I
27 11
C21H44 534 С27Н6оОс 986
21 11
28 I
C2jHS4O2 1493
Сг1Н38Ов 870 ^28^68 739
21 III 28 II
C21H2IO4P 2300 707.
22 II 29 1
C22H42O2 1017, 1019, 1073 С29Н48 1615
C22H42O3 1106, 1168 С29Н50 758
31 II
C8IH62O 630
32 I
C32He6 635
33 II
СззНе2Ос 914
39 II
C39H74O6 831
44 II
C44H82O3 762
45 11
C46H86Oe 872
51 II
C5iH8BOe 794
57 11
СоуНкмОб С57Нп0О6 1157 798
Неорганические соединения
Бромистая сера 2699
Вода 6
Гидразин 1357
Двусернистый водород 2702
Двуххлористая сера 2306
Иоднстый водород 1316
Перекись водорода 354
Пятнхлористая сурьма 2583
Сернистый ангидрид 297
Сериая к-та 619
Трехбромистый фосфор 2695
Треххлористый фосфор 1880
Хлористая сера 2686
Хлористый тионил 1996
Четырехокись осмня 2336
Четыреххлористый тнтан 2617
ОПТИЧЕСКАЯ AKittBtiUCTo ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Оптической активностью называется способность вещества вращать плпскпгт баиий (и плоскость поляризации) в проходящей поляризованной световой волне Ь КОле*
Оптически активные вещества, вращающие плоскость колебаний по часовой стпелк (если смотреть навстречу лучу света), называются правовращающими, а вещества, вращающие плоскость колебаний против часовой стрелки, — левовращающими. В таблице правое вращение обозначено знаком «+» перед величиной угла вращения и буквой d перед назввиием соединения; левое вращение обозначено знаком «—» и буквой I. Буквы D и L перед названием соединения указывают на его принадлежность к стерическим рядам D- или L-глицеринового альдегида.
Величина угла вращения для данного вещества зависит от его концентрации в растворе, от толщины слоя раствора, от длины волны проходящего света, от температуры и от растворителя. Поэтому оптическую активность различных веществ можно сопоставлять, если измерения углов вращения произведены для монохроматического света с определенной длиной волны (чаще всего для D-линин натрия — длина волны 5893 А), при одинаковой температуре (обычно при 20° С), в одном и том же оптически неактивном растворителе (или без растворителя), при одинаковой концентрации раствора и при одной и той же толщине его слоя.
Обычно для сравнения оптической активности различных веществ вычисляется удельное вращение — угол поворота плоскости колебаний линейно-полярнзованиого монохрома* тического света, проходящего через слой раствора (или чистой жидкости) толщиной 1 дм при температуре t и концентрации оптически активного вещества 1 г[см3. Для чистой активной жидкости:
Для растворов:
t 100а 100а
Здесь а — наблюдаемый угол вращения, град;
I — толщина слоя, дм;
р— плотность, г 1см3;
(/--концентрация оптически активного вещества в граммах иа 100 см3 раствора;
Р - концентрация оптически активного вещества в граммах на 100 г раствора.
Приведенные формулы для растворов предполагают линейную зависимость угла вращения от концентрации. Однако прямая пропорциональность часто не соблюдается, и в таких случаях удельное вращение характеризует не само вещество, а лишь данный его раствор.
В настоящей таблице приводятся значения [afp. т. е. удельные вращения, относящиеся ° t
к длине волны 5893 А. Для отдельных веществ даны значения Эти цифры выде*
.лены курсивом. Для мута ротирующих сахаров, как правило, приведены начальный н равновесный углы вращения; стрелка показывает направление мутаротацин.
Если удельное вращение определено для чистой активной жидкости, то в графе «Растворитель» поставлены буквы б. р. (без растворителя); в этом случае в графе «Концентрация» поставлено условно число 100 (100-процентная концентрация). Кроме того, в графе «Растворитель» встречаются следующие сокращения:
абс. — абсолютный; хлф. — хлороформ;
ац. — ацетон; сп. — этиловый спирт;
бзл. — бензол; этац. — этилацетат;
мет. сп. — метиловый спирт; зф. — днэтиловый (этиловый) эфир.
тол, — толуол;
Отсутствие данных в графе «Температура» указывает на то, что определение производилось при комнатной температуре.
Для исследования строения органических соединений, изучения явления таутомерии, а также для аналитических целей большое значение приобрело установление зависимости величины угла вращения от длины волны проходящего света. Эту зависимость называют дисперсией оптического вращения.
Более подробные сведения об оптической активности, а также о дисперсии оптического вращения органических соединений можно найти в следующих книгах: 1. Landolt-Bornsteins Zahlenwerte und Funktionen, 6-е изд., т. II, ч. 8, Берлин, 1962. — 2. L. М е i t е s, Handbook of Analytical Chemistry, Лондон — Нью-Йорк — Торонто, 1963. — 3. СТЭ, Справочник физических, химических и технологических величин. Изд. «Советская энциклопедия, т. 1П, 1929 — т. VIII, 1932.—4. К- Джерасси, Дисперсия оптического вращения. Применение в органической химии, перев. с англ., ИЛ, 1962.
895
ОС 8= Название Формула Растворитель Концентрация, г/100 см3 г, °C Но
Абиетиновая кислота С20Н30О2 абс. сп. 1 25 —116°
Аденозиптрифосфорная кислота C10H16O13N5P3 H2O 3,1 22 —26,7°
d-Адреналин (HO)2C6H3CH(OH)CH2NHCH3 0,3 и. HC1 4,1 19,8 +51,9°
/-Адреналин (HO)2C6H3CH(OH)CH2NHCH3 0,4 н. HC1 4,9 19,8 —51,4°
хлф. 9 —15,1°
/••Алании CH3CH(NH2)COOH H2O 4 22 +2°
1 н. НС1 4,8 25 +14,5°
D-Алаиин CH3CH(NH2)COOH 1 н. НС1 4,7 25 —14,4°
/-Аллантоин c4h6o3n4 20 —92,24°
p-D-Аллоза HOCH2CH(CHOH)4O Н2О 5 20 —0,2° ->
1 1 -> +14,4°
P-L-Аллоза HOCH2CH (CHOH)4O Н2О 4 20 —1,90°->
1 1 ->—13,9°
p-D-Альтроза HOCH2CH(CHOH)4O 1 1 Н2О 8 20 +32,6°
р-А-Альтроза HOCH2CH(CHOH)4O Н2О 4 20 —28,8°->
1 1 -> —32,3°
d-P-Аминогпдрокоричная кислота C6H5CH (NH2)CH2COOH Н2О 20 +7°
/-Р-Аминогидрокоричная кислота C6H5CH (NHo) CH2COOH Н2О . л ... . 25 -7,5°
А-а-Аминомасляиая кислота C2H5CH(NH2)COOH Н2О 5,4 20 +8°
6 н. НС1 4,8 19 +18,7°
D-a-Аминомасляиая кислота C2HsCH(NH2)COOH Н2О 5,3 20 —7,92°
d-p-Аминомасляная кислота CH3CH(NH2)CH2COOH Н2О 9,6% 20 --35,3°
1 н. HCI 9,4% 20 --29,7°
1 н. NaOH 9,0% 20 +14,7°
/-Р-Амииомасляиая кислота CH3CH(NH2)CH2COOH Н2О 10% 20 —35,2°
d-3-Амннопропандиол-!, 2 H2NCH2CH (OH)CH2OH 20% НС1 18 +17,7°
Н2О 18 +2,4°
/-З-Аминопропандиол-1, 2 H2NCH2CH(OH)CH2OH разб. НС1 18 —14,1°
d-a-Амино-у-фенилмасляная кислота C6H5 (CH2) 2CH (NH2) cooh 20% НС1 . ..... +33,0°
/-а-Амино-у-фенилмасляная кислота C6H6 (CH2) 2CH (NHz) COOH 20% НС1 —29,6°
Б-а-Аминофеннлуксусная кислота C6H5CH(NH2)COOH Н2О 20 +112,6°
5 н. HCI 1 26 +168,0°
D-a-Аминофенилуксусная кислота C6H5CH(NH2)COOH Н2О 1 26 —114,6°
• 5 н. HCI . 1 ,26 —169,9°
ОПТИЧЕСКАЯ АКТИВНОСТЬ
57 Зак. 7S3
Андростерон С]оН3о02 1 абс. сп. о..- ‘ +94 6°,. С
Р-£-Арабиноза ОСН2(СНОН)3СНОН 1 1 Н2О 3 20 + 190,Ь -» •V 1
—> +104,5° S
р-Р-Арабииоза ОСН2(СНОН)3СНОН 1 1 Н2О 20 —175°-> ->—105° S л га
80% сп 20 -173 -> О >4
—81,7° X
/.-Аргинин C6H14O2N4 Н2О 3,5 20 -12,5° X
1 н. НС1 2,0 28 -13,1° о о
/.-Аскорбиновая кислота ОСОС(ОН)=С(ОН)СНСН(ОН)СН2ОН Н2О 1 25 -21° га
1 1 мет. сп. 1 23 -48° S
D-Аскорбиновая кислота ОСОС(ОН)=С(ОН)СНСН(ОН)СН2ОН 1 1 мет. сп. 23 —48,3° S га я
О-р-Аспарагии H2NCOCH2CH (NH2) cooh Н2О 15 +5,41° X S
/.-р-Аспарагин H2NCOCH2CH(NH2)COOH Н2О 1,3 20
1 н. НС1 20 +Д),О’
/.-Аспарагиновая кислота H2NCH (COOH)CH2COOH Н2О 1,3 18 +4,7°
1 н. НС1 8 20 +25,5°
1 и. NaOH 1,6 27 -20,0°
D-Аспарагиновая кислота H2NCH (COOH)CH2COOH 0,97 н. НС1 4,3 20 -25,5°
d-Ацетоин CH3COCH(OH)CH3 б. р. 100 20
d-Бензилметилкарбинол C6H5CH2CH(OH)CH3 СП- 5,6 20 +16,13°
/-Бензилметнлкарбннол C6H5CH2CH(OH)CH3 б. р. 100 . . . . -26,6
d-Бензилфенилкарбинол C6H6CH(OH)CH2C6H5 СП. ...... 25 +52,8“
/-Бензилфенилкарбннол C6H5CH(OH)CH2C6H5 СП. . . . . . . 25
«-Бензил- (а-фенилэтил) -амин C6H5CH2NHCH(CH3)C6H5 СП. 20 +56,2°
/-Бензил- (а-фенилэтил) -амин C6H5CH2NHCH (CH3)C6H5 СП. 0,05 20 -56,1“
d-Бензоии C6H5CH (OH)COC6H5 бзл. 19 +125“
ац. ...... 12 +120,5°
/-Бензоин C6H5CH (OH)COC6H6 ац. 1,2 12 117,5°
d-Борнеол CioHieO 20% сп. тол. 0,9 11,5 20 4 -37,7° -37,9°
/-Борнеол CioHisO 20% сп. 0,9 20 -37,7°
ТОЛ. 11,5 - . —37,9°
d-Бориилен C10H16 тол. +30,5°
/-Борнилен CjoHie бзл. . ..... 20 -22,27°
d-a-Бромгидрокоричная кислота C6H5CH2CHBrCOOH б. р. 100 20 +7,9°
/-а-Бромгидрокоричная кислота C6H5CH2CHBrCOOH б. р. 100 20 -8,3°
d p-Бромгидрокоричная кислота С£Н5СНВгСН2СООН СП. 4 -96°
<о
Продолжение
Название Формула Растворитель Концентрация, г/100 см3 t, °C 1«1Ь
D-a-Бромизовалериановая кислота (СНз)2СНСНВгСООН Н2О 1 20 +9°
бзл. 10 20 +22,8°
d-2-Бромоктан СН3(СН2)5СНВгСН3 б. р. 100 17 4-27,5°
/-2-Бромоктан СНз(СН2)5СНВгСНз б. р. 100 17 —27,5°
rf-1 -Бромпропанол-2 ВгСН2СН (ОН) СНз б. р. 100 +1,15°
1- 1-Бромпропанол-2 ВгСН2СН (ОН) СНз б. р. 100 20 —2,87°
D-a-Бромпропиоиовая кислота СНзСНВгСООН б. р. 100 20 4-29,0°
Б-а-Бромпропионовая кислота СНзСНВгСООН б. р. 100 20 —29,0°
D-a-Бромфенилуксусиая кислота С6Н5СНВгСООН бзл. 20 —145°
D-Бромянтарная кислота ВгСН (СООН)СН2СООН Н2О 5,0 15 |-41,9°
бзл. 20 4-64,7°
Б-Бромянтарная кислота ВгСН (СООН)СН2СООН Н2О 6 —43,8°
этац. 20 —70,2°
d-Бутандиол-!, 3 СН3СН(ОН)СН2СН2ОН СП. 22 +7,5°
/-Бутандиол-1, 3 СНзСН (ОН)СН2СН2ОН СП. 25 —18,8°
d-втор-Бутил бромистый С2Н5СНВгСНз б. р. 100 25 +10,81°
/-втор-Бутил бромистый С2Н5СНВгСНз б. р. 100 25 —13,7°
d-втор-Бутил йодистый С2Н5СШСНз ац. 20 +29,2° —31,98°
/-втор-Бутил йодистый С2Н5СШСНз б. р. 100 17
d-втор- Бутила цетат СНзСООСН (СН3)С2Н5 б. р. 100 20 +25+ +13,87°
d-втор-Бутиловый спирт С2Н5СН(ОН)СНз б. р. 100 20
Б-Валин (СНз) 2СНСН (NH2) cooh Н2О 3,6 20 4-6,42°
D-Валин (СНз) 2СНСН (NH2) cooh 6 н. НС1 Н2О 3,4 6,2 20 20 +28,8° —6,06°
d-Вербенон 6 н. НС1 3,2 20 —99,04°
'СюНнО б. р. 100 18 +249.6°
/-Вербеной С10Н14О СП. б. р. 8,3 100 18 4-229,6° 144°
D-Винная кислота [СН(ОН)СООН]2 Н2О 20 % 20 +11,98°
Б-Винная кислота [СН(ОН)СООН]2 мет. сп. Н2О 10 20% 15 20 +2,6° 11 98°
a-D-Г алактоза НОСН2СН(СНОН)4О 1 1 Н2О 5 20 +150,7° -> -> +80,2° +52,8° ->
P-D-Г алактоза НОСН2СН (СНОН)4О 1 1 Н2О 4 20
->4-80,2°
Б-Галактоза НОСН2СН (СНОН)4О 1 1 H2O ... 1 —74°
D-Галактоновая кислота НОСН2(СНОН)4СООН H2O 1,1 —11, 2 -> ->—57,6°
d-Гекса нол-2 СНз(СН2)зСН(ОН)СН3 6. p. СП. 100 25 20 +11,6° +12,70°
/-Гексанол-2 [IT еициобиоза СНз(СН2)3СН (ОН)СНз Ci2H22On 6. p. H2O 100 3 25 22 —1,75° —5,9° -> ->+9,6°
d-Гептанол-2 СНз(СН2)4СН(ОН)СН3 СП. 100 100 20 +11,45° —10,48° 4-6,68° 9|°
/-Гептанол-2 d-Гептанол-З СН3(СН2)4СН(ОН)СНз СНз(СН2)3СН(ОН)С2Н5 6. p. 6. p. 1/ 20
/-Гиосциамин D-Г петидин C17H23O3N C3H3N2CH2CH (NH2)COOH СП. H2O 1 h. HCI 1 2,7 4,0 23 20 +39,8° —10,2°
Б-Г истидии C3H3N2CH2CH (NH2) cooh H2O 0,5 н. HCI 2,2 0,8 20 20 —39,74° +11,1°
1 h. NaOH 3,9 28 —10,3°
Гликоген D-Глицериновый альдегид Б-Глицериновый альдегид Б-Глутаминовая кислота (CeHioOs)* HOCH2CH(OH)CHO HOCH2CH(OH)CHO H2NCH (COOH) CH2CH2COOH H2O H2O H2O H2O 10% HCI 18 9 1,5 25 15 26 18 20 +197° , +21,2° —20,9° +11,5° 4-34,9°
1 h. NaOH 2,0 24 —7,0°
D-Глутамииовая кислота H2NCH (COOH)CH2CH2COOH H2O 0,4 н. HCI 5,7 26 20 —12,9° —30,0°
a-D-Глюкоза HOCH2CH (CHOH)4O H2O 3,9 20 +112,2°-> -> +52,7°
p-D-Глюкоза HOCH2CH(CHOH)4O 1 1 H2O 3,9 20 +18,7° -> ->4-52,7°
а-Б-Глюкоза HOCH2CH (CHOH)4O 1 1 H2O 4,3 20 —95,5° -> ->—51,4°
D-Глюкоиовая кислота HOCH2(CHOH)4COOH H2O 2,8 20 —6,7°-> ->+H,9°
P-D-Глюкуроновая кислота OCH(CHOH)4COOH H2O 5,6 24 4-11,73° -> -> +36,26°
Б-Гулоза HOCH2CH (CHOH)4O 1 1 H2O 1 20 4-61,6°
ОПТИЧЕСКАЯ АКТИВНОСТЬ I ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Продолжение
Название Формула Растворитель Концентрация, г/100 cjh3 t, °C [clp
Д-Гулоза d-cz, ₽-Дибромянтарная кислота l-а, РДпбромянтарная кислота Д-З,4-Диоксифенилаланин £-3,4-Диоксифенилаланин 1-Додека нол-3 Д-Идит £-Идит £-Идоза d-Изоборнео.т /-Изоборнеол £-Изолейцин Д-Изолейцнн /-cz-Изоморфин /-р-Изоморфин /-у-Изоморфин /-Изопротеренол /-Изофенхиловый спирт Д-Инозит £-Инозит d-ct-Иодпроппоновая кислота Z-ct-Иодпропионовая кислота d-Ирон d-Камфен Z-Камфен d-Камфора 1-К.амфрра . , « НОСН2СН(СНОН)4О 1 1 (СНВгСООН)2 (СНВгСООН)2 (ОН) 2С6Н3СН2СН (NH2) соон (ОН) 2С6Н3СН2СН (,NH2) соон СНз(СН2)8СН (ОН)С2Н5 НОСН2(СНОН)4СН2ОН НОСН2(СНОН)4СН2ОН НОСН2(СНОН)4СНО Ск>Н]зО CtoHisO C2HsCH (СНз)СН (NH2)COOH С2Н5СН (СНз) CH (NHz) СООН C17H19O3N c,7h19o3n Ci7Hi9O3N (HO)2C„H3CH(OH)CH2NHC Н(С Н3)2 с10н17он С6Н6(ОН)6 С6Н6(ОН)6 СНзСШСООН СНзСШСООН с14н22о СюН16 С]оН1б СюН16О СюНцО Н2О этац. этац. 4% НС1 4% HCI СП. Н2О Н2О Н2О СП. этац. СП. этац. Н2О 20% НС1 Н2О 20% НС1 мет. сп. мет. сп. мет. сп. 2 н. НС1 СП. Н2О Н2О эф. эф. б. р. эф. бзл. эф. тол. СП. хлф. СП. 5,8 3 3 10 10 6,2 5 5 ’ 2 12 1 100 4 4 20% 5,3% 20% 20 24 20 20 20 20 20 20 20 20 ’20 ’ 20 20 20 25 17 20 19 24 ’22 ' 17 17 17 ’ 20 19 25 20 20 20 —20,4° 4-126,3° —148,0° +11,5° —11,5° —6,10° +3,5° —3,53° +52,7° --33,89° --34,1° —34,6° —34,3° +10,7° 4-40,8° —10,7° —41,6° —164,3° —216,2“ —93,6° —45° —19,92° +65° —69° +50,7° —49,9° +47° +103,9° +107,7° —106,1° —117,5° +44,2° +41,0° —44,2°
d-Камфор-р-сульфокислота /-Ка мфор- р-сульфокислота Z-Карвоментон d-Карвон /-Карвон с/-Д3-Карен с/-Д4-Карен Кодеин /-Р-Кокаин d-Конинн /-Кониин Кортикостерон сх-Д-Ксилоза а-£-Ксилоза а-Лактоза (гидрат) Р-Лактоза Д-Лейцин £-Лейцин £-Лизин Д-Лизин а-£-Ликсоза сх-Д-Ликсоза CioH|604S CioHie04S CioHisO CioHi40 С10Н14О CioHie CioHie CisHziOaN • Н2О C17H21O4N NH(CH2)4CHC3H7 J 1 NH (СН2)4СНСзН7 1 1 С21Нзо04 ОСН2(СНОН)зСНОН I 1 ОСН2(СНОН)3СНОН 1 1 С12Н220ц • H2O С12Н220ц (СНз) 2СНСН2СН (NHz) СООН (СНз) 2СНСН2СН (NHz) соон HzN (CHz) 4СН (NHz) СООН H2N (СН2) 4СН (NHz) СООН ОСН2(СНОН)3СНОН I I ОСН2(СНОН)зСНОН 1 I Н2О Н2О б. р. мет. сп. б. р. бзл. б. р. б. р. б. р. СП. хлф. разб. НС1 б. р. б. р. СП. Н2О Н2О Н2О Н2О Н2О 6 н. НС1 Н2О 6 н. НС1 1 н. NaOH Н2О 6 н. НС1 3 и. NaOH 0,27 и. НС1 Н2О Н2О 1,7 3,7 100 100 10 100 100 100 2,8 0,4 100 100 1,1 4 8 4 2,1 4,0 2,2 2 3,2 6,5 2,0 2,2 2,0 4 20 20 16 19 20 20 ’2i 30 25 20 19 ’ 15 20 20 20 20 20 20 20 20 28 20 22,9 20 20 20 +22,6° —20,7° —13,41° —27,95° +62,9° +61,1° —62,46° +15,2° +62,2° —136° —16,15° —78,5° +15,7° —15,6° +223° +93,6°-> -> +18,8° —79,3“-> ->—18,6° +85,0°-> ->+52,6° +34,9° -> ->+55,4° +10,34° —15,6° —10,42° +15,1° +7,5° +14,6° +25,9° +7,6° —23,48° —5,8°ч> ->+13,5° ->5,6°-> ->—13,8°
ОПТИЧЕСКАЯ АКТИВНОСТЬ» ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
• S Продолжение
Название Формула Р астворитель Концентрация, г/100 см8 «, °с 1“1о
З-Р-Ликсоза ОСН2(СНОН)3СНОН 1 1 Н2О 4 20 —72,6° -> -> —13,8°
«/-Лимонен CjoHis б. р. 100 20 +126°
хлф. 0,1 20 +117о°
/-Лимонен C10H16 б. р. 100 20 —122°
d Линалоол CioHieO б. р. 100 20 4-19,18°
/-Линалоол CioHieO б. р. 100 .... —19,37°
P-Мальтоза (гидрат) C12H22O11 • Н2О Н2О 4 20 4-111,7° ->
Н2О ->4-130,4°
Л-Маннпт НОСН2 (СНОН) 4СН2ОН 25 —0,49°
a-jD-Манноза НОСН2СН(СНОН)4О 1 1 Н2О 4 20 4-29,3°->
->4-14,2°
Р-Д-Манноза НОСН2СН(СНОН)4О Н2О 4 20 —17,0° ->
1 1 ->4-14,2°
р-£-Манноза НОСН2СН (СНОН)4О 1 1 Н2О 4-14° -> ->—14°
р-Мелибиоза С12Н22ОП Н2О 4-124° ->
->4-142,5°
Р-Мелибиоза (дигидрат) С12Н22О11 • 2НгО Н2О 4 20 4-111,7°->
бзл. ->4-129,5°
d- Д3.8Р)-п-МеНТа диен C10H16 100 18 4-98,2°
d-л-Ментан С10Н20 б. р. 23 4-1,6°
/-лгМентан СюНго б. р. 100 —0,3°
З-Д^п-Ментен СюН]8 б. р. 100 . . . . 4-118°*
</-Д3-п-Ментен СюН|8 б. р. 100 12 4-113,8°
«/-Ментол СюН2оО СП. 5,2 4-48,3°
/-Ментол СюН2оО СП. 20 -49,5°
(/-Ментон CioHieO б. р. 100 18 4-24,85°
абс. сп. 20 20 4-28,1°
/Ментон CioHjgO б. р. 100 20 —29,6°
абс. сп. 20 20 —28,2°
</-2-Метилбутанол-1 С2Н5СН(СН3)СН2ОН б. р. 100 20 4-5,90°
/-2-Метилбутанол-1 С2Н5СН(СНз)СН2ОН б. р. 100 20 —5,90°
d-a-Метилвалериановая кислота СНз (CHshCH (СНз) соон эф. 25 4-5,58°
1-а-Метплвалериановая кислота СНз (СН2) 2СН (СНз) соон эф. 25 —7,08°
d-p-Метилвалериановая кислота СН3СН2СН (СН3) СН2СООН б. р. 100 26 -Н,01°
/-p-Метплвалериановая кислота СНзСН2СН (СНз) СН2СООН б. р. 100 26 —2,54°
гептан 25 —10,4°
«/-Метилфенилкарбинол С6Н5СН(ОН)СНз б. р. 100 19 -4-/3,02°
/-Метилфенилкарбинол С6Н5СН(ОН)СНз б. р. 100 18 —13,27°
L-a-Метилмасляная кислота С2Н5СН (СНз) соон б. р. 100 25 4-19,14°
О-а-Метилмасляная кислота С2НБСН (СНз) соон б. р. 100 25 —19,8°
«/-а-Метилмасляный альдегид С2Н5СН(СНз)СНО б. р. 100 . . . . 4-31,2°
//-Метионин CH3S (СН2)2СН (NH2) соон 1 н. НС1 3 27 —23,3°
/.-Метионин CH3S (СН2) 2СН (N Н2) соон Н2О 1,0 25 —8,2°
1 н. НО 3 25 4-23,4°
1 и. NaOH 3,2 28 4-2,з°
/.-Миндальная кислота С6Н5СН(ОН)СООН Н2О 2,9% 20 4-156,57°
//-Миндальная кислота С6Н5СН(ОН)СООН Н2О 1,6 20 —157°
СП. 20 —159,73°
/.-Молочная кислота СНЭСН(ОН)СООН Н2О 9,7 20 4-1,69°
/5-Молочная кислота СН3СН(ОН)СООН Н2О —2,26°
/Морфин C17H19O3N мет. сп. 2 23 —130,9°
/.-Мускарин (хлорид) СдНгоОгК^С!- 20 4-6,7°
d-a-l/аркотин хлф. 4-199,9°
/-а-Наркотин СггНгзОтЫ хлф. 1 25 —200°
0,1 н. НС1 2 32 4-57,5°
d-P-Наркотин C22H23O7N хлф. 18 -4-/03°
/р-Наркотнн хлф. 18 —101°
«/-Никотин CH3N (CH2)3CH-C6H4N 1 1 б. р. 100 20 4-163,17°
/-Никотин CH3N(CH2)3CH-C5H4N 1 1 б. р. 100 20 —169,3°
«/-Норадреналин (НО) 2С6Н3СН (ОН) ch2nh2 Н2О 25 4-37,4°
/Норадреналин (НО) 2С6Н3СН (ОН) СНгИНг Н2О 5 25 —37,3°
«/-Окись пропилена ОСН2СНСН3 1 1 б. р. 100 18 4-12,72°
/-Окись пропилена ОСН2СНСНз 1 1 б. р. 100 18 —8,26°
«/-Р-Оксигидрокоричная кислота С6Н5СН (ОН) СН2СООН СП. 18 4-19,2°
мет. сп. 5 18 4-20,6°
g -------------
оЗ * Для длины волны 5791 А.
ОПТИЧЕСКАЯ АКТИВНОСТЬ 1 ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Продолжен ие
Название Формула Растворитель Концентрация, г/100 смз t, °C 1«1р
1 (З-Оксигидрокоричная кислота С6Н5СН(ОН)СН2СООН СП. мет. сп. 0,5 18 —18,9° —21,3°
rf-P-Оксимасляная кислота СН.,СН (ОН) СН2СООН Н2О 6 15 +25,2°
/-р-Оксимасляная кислота СНзСН (ОН)СН2СООН Н2О 5 25 —24,5°
г/-Октанол-2 СНз(СН2)6СН(ОН)СНз б. р. 100 20 +9,8°
/-Октанол-2 СНз(СН2)6СН(ОН)СНз б. р. 100 17 —9,9°
rf-Октанол-З СН3(СН2)4СН(ОН)С2Н5 СП. 4,9 20 +11,13°
/Октанол-3 СНз(СН2)4СН(ОН)С2Н5 СП. 27 —7,40°
rf-Окта нол-4 СНз(СН2)зСН(ОН)СзН7 б. р. 100 22 +0,74°
/;Орнитин H2N(CH2)3CH(NH2)COOH Н2о 0,7 20 4-9,7°
5 н. НС1 1 25 +27,7°
й-Пентанол-2 CSH7CH(OH)CH3 б. р. 100 20 +13,70°
/-Пентанол-2 С3Н7СН(ОН)СНз б. р. 100 20 —13,4°
Персеит НОСН2(СНОН)5СН2ОН насыщ. р-р Na2B4O7 8,9 20 +1,53°
Пилокарпин CnHi6O2N2 20 +100,5°
rf-a-Пинен С10Н]б б. р. 100 20 +51°
/-«-Пинен CioHie б. р. 100 20 —51,3°
rf-p-Пинен CioHie б. р. 100 20 +16°
/ Р Пинен CioHie б. р. 100 25 —22,3°
Преднизолон С21Н2зО5 1,4-диоксан +102°
D-Пролин NH(CH2)3CHCOOH 1 1 Н2О 20 +81,9°
/Пролин NH(CH2)3CHCOOH 1 1 Н2О 20 —80,9°
1 н. НС1 1,7 30 —58,0°
1 н. NaOH 1,8 30 —99,1°
/-Пропапдиол-1,2 СНзСН (ОН) СН2ОН Н2О сп. 6,6 18 22 +13,71° +4,2°
£>-Пропандиол-1, 2 СНзСН (ОН )СН2ОН Н2О 100 20 —9,8°
d-Пропилендиамин СНзСН (NH2)CH2NH2 б. р. 25 +29,78°
/-Пропилендиамин СНзСН (NH2)CH2NH2 б. р. 100 25 —29,70°
rf-Пропилфенилкарбинол СНз(СН2)2СН(ОН)СвН5 бзл. +52,2°
/-Пропилфенилкарби нол СНз(СН2)2СН(ОН)С6Н5 бзл. —53,5°
ОПТИЧЕСКАЯ АКТИВНОСТЬ
58 Зак. 783
D-Пспкоза
/-Пспкоза
rf-Пулегон
ct-L-Рамноза (гидрат)
р-/-Рамиоза
Р-Рамноза (гидрат)
Рафиноза (безводная) Рафиноза (пентагидрат) Резерпин
Л-Рибоза
/)-Рибоза
D-Рибофлавин
rf-Рицинолевая кислота rf-Сабинен
/Сабинен rf-Сабинол «-Санталол Р-Санталол /-Сарколизин
D-Сахарная кислота
Сахароза D-Сер ин
/.-Серин
ОСН2 (СНОН) 3С (ОН) СН2ОН Н2О 1,6 20 +3,1° О т
ОСН2 (СНОН)зС (ОН)СН2ОН 1 1 Н2О 3 21 —3,3° > X S
СюН1бО б. р. 100 20 +23,75“ п
бзл. 10% 20 +25,58“ X
СН3СН(СНОН)4О-Н2О Н2О 4 20 —8,6° -> X
1 1 ->+8,2° о
СНзСН (СНОН)4О Н2о 4 20 +38,4° -> о м
1 1 ->+8,9°
СН3СН(СНОН)4О-Н2О Н2о 16,5 —8,25° X ГА
z
С18н32о1б Н2О +123° s s
С18Н32О16 • 5Н2О Н2о 4 20 +105,2°
Сзз! +O9N2 хлф. 1 23 —118°
пиридин 1 26 —164°
ОСН2(СНОН)зСНОН Н2О 4 20 +20,3° ->
1 1 -> +20,7°
ОСН2(СНОН)зСНОН Н2О 4 20 —23,1° ->
1 1 -> —23,7°
С17Н1ЮО6К4 Н2О —9,80°
0,05 н. —125°
NaOH
. С18Н34О3 б. р. 100 22 +7°
C10H16 б. р. 100 +80,17°
СюН1б б. р. 100 15 —42,5°
СюН]бО б. р. 100 15 +17,04°
с15н24о б. р. 100 .... +/0,3°
с15н24о б. р. 100 —87,1°
C1SHI8O2N2C12 1 н. НО 1,3 22 +7,5°
мет. сп. 0,7 —31,5°
НОСО (СНОН)4СООН Н2о 2,8 19 +6,8° ->
->+20,6°
С12Н22Оц н2о 26 20 +66,53°
HOCH2CH(NH2)COOH Н2О 10,4 20 +-6,87°
1 н. НС1 9,4 25 —14,32°
HOCH2CH(NH2)COOH Н2О 10,4 20 —6,83°
1 н. НО 9,3 25 +14,45°
Продолжение
8
Название Формула Растворитель Концентрация, 2/100 см% г. °с Мд
d-Сильвестрен CioHis б.р. 100 18 4-83,18°
хлф. 20 +66,3°
Z-Сильвестрен СюН1б этац. 5 18 —68,2°
Z-Скополамин (гиосцин) c17h21o4n Н2о 20 —28°
СП. 20 —18°
D-Сорбит НОСН2(СНОН)4СН2ОН Н2о 9 20 —2,01°
D-Сорбоза ОСН2 (СИОН) 3С (ОН) СН2ОН 1 1 Н2О 20 +42,9°
^.-Сорбоза ОСН2 (СНОН) зС (ОН) СН2ОН 1 1 Н2О 20 —42,9°
rf-Спартеин C15H26N2 20 +16,1°
Z-Спартеин C15H26N2' абс. сп. 10 21 —16,4°
Стрихнин C21H22O2N2 абс. сп. 0,5 20 —104°
хлф. 1 18 —139,3°
D-Тагатоза ОСН2(СНОН)зС(ОН)СН2ОН н2о 2 20 —2,3°
I I н2о 22 +1,0°
a-D-Талоза НОСН2СН(СНОН)4О н2о 4 20 +68,0° ->
1 1 ->+20,8°
P-D-Талоза НОСН2СН(СНОН)4О н2о 4 20 +13,2° ->
! 1 ->+21,0°
Тебаин C19H21O3N СП. 2 25 —215,5°
хлф. 5 23 —230°
Тестостерон с19н28о2 СП. 4 24 +109°
D-n-Тирозин НОС6Н4СН2СН (NH2) соон 6,3 н. НС1 5,15 20 +8,64°
Т-п-Тнрозин НОС6Н4СН2СН (NH2) соон 6,3 н. НС1 4,4 20 —8,64°
2 н. NaOH 3,8 25 —14,4°
а, а-Трегалоза (безводная) С12Н22Оц Н2О 6 20 +197,0°
а, а-Трегалоза (днгидрат) С12Н22Оц • 2Н2О Н2О 7 20 +178,3°
ОПТИЧЕСКАЯ АКТИВНОСТЬ
р, Р-Трегалоза С12Н22Оц H20 1 17 —41,5° О т
£-Треоза НОСН2(СНОН)2СНО H2O 4,5 20 -1-13,2° >
Сд D-Треоза НОСН2(СНОН)2СНО H2O 4 20 —12,3° S S
СО * D-Треонин СНзСН (ОН) CH (NH2) соон H2O 2 18 +29,3° m
£-Треоннн СНзСН (ОН) CH (NH2)COOH H2O 2 18 —29,2° Г) X
5 H. HC1 25 —14,5° S х
D-Триптофан ChHi2O2N2 H2O 0,5 20 +32,9 п
£-Триптофан C11H12O2N2 H2O 0,5 20 —32,1° о W
0,5 H. HC1 1 20 +2,4° Ё
0,5 h. NaOH 2,4 20 +6,17° 3 СП
а-Туйон CioHieO 6. p. 100 20 —11,58° з: S
Р-Туйон CioHieO 6. p. 100 20 +77,33° S
Тураноза С12Н220ц H2O 4 20 +27,3° ->
->+75,8°
/-Ундеканол-3 CH3(CH2)7CH (ОН)С2Н5 СП. 20 —6,22°
Z-a-Фелландрен CioHie 6. p. 100 20 —112,0°
d-P-Фелландрен С10Н16 6. p. 100 +18,54°
d-a-Фенилаланин С6Н5С(СН3) (NH2)COOH H2O 18 4-70°
Z-a-Фенила ланин C6HSC(CH3) (NH2)COOH H2O 20 -69,5°
О-Р-Фенилаланнн C6H5CH2CH(NH2)COOH H2O 1,7 20 +35,1°
20% HC1 3,5 20 +6,86°
£-Р-Фенилаланнн C6H5CH2CH(NH2)COOH H2o 1,9 20 —35,1°
1 h. HC1 3,3 25 —11,6°
1 h. NaOH 3,4 25 —1,2°
rf-a-Фенилэтиламин C6HeCH(NH2)CH3 6. p. 100 21 +39,64°
абс. сп. 2,1 20 +31,0°
Z-a-Фенилэтиламин C6H5CH(NH2)CH3 б. p. 100 21 —38,5°
абс. сп. 3,2 20 —31,5°
d-Фенилянтарная кислота C6H5CH (COOH) CH2COOH ац. 2,0 25 +171,1°
СП. 16,5 +148,3°
Z-Фенилянтарная кислота C6H5CH (COOH)CH2COOH ац. 2,0 25 —171,0°
о о мет. сп. 12,5 —147,1°
Продолжение
Название Формула Растворитель Концентрация, г/100 см$ t, °C 1“1д
Феноксиметилпеницнллин (К-соль) rf-a-Фенхиловый спирт /-a-Фенхиловый спирт Z-p-Фенхиловый спирт rf-Фенхон Z-Фенхон p-D-Фруктоза a-D-Фукоза a-L-Фукоза Хинин (безводный) Хинин (тригидрат) D-a-Хлормасляная кислота L-а,-Хлормасляная кислота rf-p-Хлормасляная кислота Z-P-Хлормасляная кислота d-2-Хлорпропанол-1 Z-2-Хлорпропа нол-1 L-a-Хлорпропионовая кислота rf a-Хлорфенилуксусная кислота Z-a-Хлорфенилуксусная кислота D-Хлорянтарная кислота ^4-Хлрр1Штарпая кислота - ’-vr'i, -.д..,uniiwi,,^. Холестерин р-Целлобиоза Цинхонин L-Цистеин D Цистин L-Цистин rf-Цитропеллаль /-Цитронеллаль rf-Цитронеллол Z-Цитронеллол Z-Шнкимовая кислота L-Эритрит D-Эритрит L-Эритроза D-Эритроза Р-Эстрадиол /-Эфедрин D-Яблочная кислота L-Яблочпая кислота C16H17O5N2SK С10Н17ОН СщНиОН СюНиОН CioHieO CioHieO ОСН2 (СНОН) 3С (ОН) СН2ОН 1 1 СН3СН(СНОН)4О 1 1 СН3СН(СНОН)4О 1 1 C2oH2402N2 c20h24o2n2 ЗН2О С2Н5СНС1СООН С2Н5СНС1СООН СНзСНС1СН2СООН СН3СНС1СН2СООН СН3СНС1СН2ОН СН3СНС1СН2ОН сн3снс1соон С6Н5СНС1СООН С6Н5СНС1СООН СЮН (СООН) СН2СООН С1СН(СООН) СН2СООН с27н45он Ci2H22On Ci2H22ON2 HSCH2CH(NH2)COOH [SCH2CH(NH2)COOH]2 [SCH2CH(NH2)COOH]2 CioHisO CioHieO CioH2oO СюН2оО C7H10O5 HOCH2(CHOH)2CH2OH HOCH2 (CHOH) 2CH2OH HOCH2(CHOH)2CHO HOCH2(CHOH)2CHO CisH24O2 C6H6CH (OH) CH (NHCH3) CH3 HOCH (COOH) CH2COOH HOCH(COOH)CH2COOH H2o cn. cn. СП. б. р. сп. б. р. Н2О Н2О Н2О Н2О 99% сп. 0,1 н. H2SO4 СП. б. р-б. р. Н2О ТОЛ. б. р. б. р. б. р. бзл. бзл. Н2О Н2О эф. хлф. Н2О СП. хлф. Н2О 1 н. НС1 1 н. НС1 1 н. НС1 2 н. NaOH б. р. б. р. б. р. б. р-Н2О Н2О СП. Н2О СП. Н2О Н2О 1,4-диоксан СП. Н2О мет. сп. Н2О мет. сп. 0,2 5 5 100 8,3 100 10 10 4 0,3—3 2 100 100 10 100 100 100 2 2 8 0,6 0,6 1,3 1 0,4 1 0,5 100 100 100 100 4 5% 11 0,9 3,6 7 8,7 10 25 20 18 16 20 19 20 20 15 15 15 25 20 18 18 17 20 18 19 19 20 20 20 20 17 30 20 25 20 31 20 20 17 18 18 20 20 20 19 20 15 4-223° 4-10,36° —15,0° —28,(Р 4-67° 4-72,0° —51,2° —133,5° -> ->—92,0° 4-127°-> ->4-76,0° —152,6° -> ->—75,9° —172° —158,2° —284,5° —145,2° +17,5° —8,6° § 4-49,8° х —33,4° я 4-9,26° 5 —2,92° й —2,36° > 4-191,9° 5 —191,3° “ +20,1° ° —19,67° J —31,5° о —39,5° +14,2° -> ® ->+34,6° х +225,2° £ +209,6° = +9,8° g +17,5° ° +221,2° s -223° “ —92° =5 +11,82° s —2,5° +4° —2,4° —184° +4,3° —11,1° —4,4° +11° +2,4° -> ->+21,5° +1°-> ->—14,5° 4-55° —6,3° +2,3° +2,92° —2,30° —5,9°
<о 5 со cj 5> ал I ОО К — 5 <0 00 & Cm 4=. Co РС го* № по пор. О го
Ш □ ь т 9-э Водород (НгО И Н2О2) Водород Висмут Ванадии Бром dog Бериллий Барий Астат Аргон Амернцнй Алюминий Актиний Актиниды s 0 я Z Д * + 1 дородом и Азот (соединения с во- Азот (окисли и ноны №“, NO", CN-, SCN", CNO") > о си го 2 го Я Ниже привод эпических соед
to № СЛ <3 р< 1 813 ‘ZI3 218, 219 227, 228 PC PC 196, 197 § 1 1 1 202, 203 1 1 212, 213 213, 214, 215 1 индивидуальные реакции 5 го Я S3 го го я » я
275, 277 1 272, 278 1 1 272, 278 PC PC 272, 278 1 1 271, 278 1 1 1 люминесцентный анализ о о ’Ч >5 О £ стран; й и и
1 КЗ сл СО PC 1 1 1 PC О co 1 1 1 8 CO PC ё абсорбциометрия ± л я s 2 $ г s h 5 ГО « q и цы, ( онов,
1 1 238, 239 265, 266 240, 241 1 PC w 00 237, 238 1 1 1 PC 8 PC Oil СЛ 243, 244, 256 микрокристаллоскопия кротче-:не соды ы я го содержащие в состав к<
1 1 W СО СО СО 1 1 CO w CO CO 1 1 co 1 1 1 1 абсорбционный спектральный
а 00 1 >£ь 477, 478 (О 1 1 1 СЛ § сл 1 амперометрический О Го гоз я 3“ го я ь
1 1 PC о PC to PC to ОС PC GO CT) PC GO PC PC ce 1 PC X 1 PC 0 PC 288, 292 весовой ;ения по оп < входит эт
1 1 СП to ас 1 1 1 1 1 1 1 СЛ co 1 1 on 8 599, 600 Сл 8 газовый и газометрический > QJ
453, 460, 745, 760, 777 439, 755, 762 1 £ 776, 777 444, 445, 454, 741— 452, 460, 749, 750, 754, 761, 744, 745 1 ' 444, 454, 741 742 444, 454 1 444, 454 1 1 § 443, 454, 739, 740 oo r-o 449, 457, 761 1 колориметрический и спектрофотометрический ределению . от элемент. > m ь го >
1 1 1 389, 397 395, 396 I 1 389, 397 1 1 1 388, 389, 397 1 1 1 1 комплексом етрический Мето цанно) Дани го о
1 $ ал 465, ' 469 о 467, 472 468, 469 I 466, 469 466, 469 1 1 466, 469 1 1 467, 469, 472 : 1 кондуктометрический анализ и высокочастотное титрование я с 2 6 го 0) я ь» о го )з о (Я
1 1 I 1 1 1 I 1 1 1 1 1 1 1 СЛ ап Он масс-спектрометрия го го о го Я Д ГО СО я
оо >£ь 334, 335 1 : 332, 333 333, 334 343, 344 Й 318, 319 1 1 PC 1 327, 328 323, 324 328, 329 | объемный ’венного или неделе нию ь я W >
05 5 о СП СО м О <£? 00 roj сл ап Ок се К го* № по пор. в> Я в> Ьэ и S о о t3 Я я
501—503, 505—509, 1511, 513, 514 504, 505, 512 505, 506 501—504, 506—513 501, 503, 505, 507—509, 513, 514 сл © т о 1 ал ал СП ал 1 1 1 501, 503—505, 509, 511 1 1 СЛ о О) сл о О) 1 полярографический * Я со со >в CN~, SCJ рубриками > W J3 го ь го
1 ОО ел ё со ё 8 8 О* 00 со оэ Ю 1 1 О 1 1 492, 493 ё 1 потенциометрический й Z Ь я к я К а
% оо 1 сл сп РО Сл сл СП сл ал ап ал 1 ал 1 ап 1 1 1 1 сл СЛ СЛ радиоактиванионный CNO" п ганиды» W й 2 т Я
1 1 1 1 1 сл ё РО S 1 1 ё 1 1 1 1 1 флуорометрический омею и «Ai
638, 658, 659, 720 1 638, 639, 647, 656— 658, 720 639, 656, 657, 720 ' 639, 655— 657, 720 639, 654, 655 639, 655, 720 639, 654, 655, 720 638, 639, 652— 654, 720 1 638, 652. 720 638, 652, 653 638, 651, 652, 720 638, 650, 651 1 1 1 637, 649, 650, 720 эмиссионный спектральный ,ены при СТИНИДЫ» о го
о сл (L О СО о ” СО сл СЛ СО 35, 53, 55 30- 32, 37, 43, 49, 52, 54—57, 67 30—34, 37, 43, 49, 52—56, 67 1 30, 31, 33—35, 44, 53, 54, 70 30, 31, 33—35, 40, 55, 56, 62 1 30—32, 34, 35, 39, 47, 55—57, 60 30-32, 37, 39, 47, 53, 54, 56, 60, 61 1 1 1 30—32, 34, 35, 37, 40, 47, 52—57, 62 1 30, 31 30, 31, 35, 42, 53, 55, 66 I 30, 31, 33—35, , 42, 52—55, 66 1 аналитические реакции азоте, гедкозе » (выделены тол
1 1 1 123-124, 126 132-134 РС 07 § 1 130, 132 123, 124, 127, 128, 132-134 1 1 123, 124, 126, 132-134 1 1 8 § 1 на бумаге хроматог Методы раз. мельные и трансуранивые ько Eu, Се, Am, Cm, Np и
1 174-188 1 1 174-177. 181—188, 189 174—188 174, 181, 184—186 184, 185 174—176, 181-188 174—177, 181, 184— 188, 190 174, 181, 184-186 1 184. 185 175, 176, 182—188 174, 177 5 1 184, 185 i 1 ионообменная рафия и ГО 1з ГО Я я я
ОО Г— 32, 69, 73, 75, 79, 80, 84, 1 88-97, 109 1 1 32, 76, 79—83, 85, 88-97, 101, 102 32, 73—75, 77, 79—84, 87—97, 109 84, 93-97, 102 84, 101 32, 60, 72, 76— 78, 82, 83, 85, 88—92, 101 со i 1 1 83, 85, 88—97 32, 62, 72, 76— 79, 82, 83, 88—97, 101 83, 88-97 83, 93—97 1 □0 1 экстракция Л • 2 го я р J3 м Я 2
УКАЗАТЕЛЬ МЕТОДОВ АНАЛИЗА ! i И РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ /7 родолжение
анализа Методы разделения
О с о Е Элемент Методы качественного анализа Методы количественного 1
о к о Е 2 полярографический потенциометрический радиоактивационный флуорометрический эмиссионный спектральный аналитические реакции хроматография экстракция
индивидуальные реакции люминесцентный анализ микрохимические методы абсорбционный спектральный амперометрический . весовой газовый и газометрический колориметрический и спектрофотометрический комплексометрический кондуктометрический анализ и высокочастот-ное титрование масс-спектрометрия объемный
на бумаге ионообменная
абсорбциометрия микрокристаллоскопия
19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 501. 504, 505 507, 509-511, 514 501, 504, 507. 510, 511, 513 502, 505—513 501—514 504, 507, 509, 510, 514 501, 502, 504, 505, 507—509, 511, 514 502, 504— 506, 509, 510, 512 507, 509, 510, 514 506 501-514 505 505 501—504, 506 503, 514 490 492 497, 498 488 490 496 498 490 489 486 488 498 550 552 552 550, 552 559 550 544 552 554 552 570 546 554 546 558 548 562 554 462, 463 463 464 462 462 638, 660, 661, 720 638, 639, 660-662, 720 639, 662, 663, 720 639, 662, 663 640, 666, 367, 720 640, 666— 669, 720 640, 668, 720 640, 668, 669, 720 640, 641, 669 641, 670, 671, 720 641, 670- 673, 720 641. 673, 720 640, 672— 674, 720 640, 674, 675, 720 640, 675 640, 675- 677, 720 641, 676 677, 720 641. 676 677, 720 30-32, 37, 40, 47, 55—57, 62, 63 30, 31, 41, 48, 52, 54, 56, 65 30-32, 41, 49, 53, 56, 64 30—35, 37, 45, 51, 52—56, 70, 71 30—32, 38, 46, 52-55 30-32, 40, 54—57, 63 30, 31, 33—35, 44, 53, 54, 70 30, 31, 45, 51, 54—56. 71 30, 31, 40 30—32, 37, 39, 47, 52-57, 61 30, 31, 38, 46, 52, 53, 59 30—32, 37, 39, 47, 55—57, 60, 61 55 30-33, 37 , 45, 51. 53-56, 71 30, 31, 33, 35, 41, 54, 64 130 129 130 123, 124, 126, 132—134 129 130 130 129 123—126, 132—134 123, 128. 132—134 123, 124, 127, 128, 132—134 123, 124, 127, 132—134 174, 177, 181, 182, 184-188 173—188 174-177, 181, 182, 184-188 173—182. 184—188 174-181, 184—188 173—177, 181, 182, 184-188 174, 181, 184—186 174, 181, 183—188 174—177 174—181, 184—189 174—177, 181, 184-188, 190 174-177, 181, 184- 188, 190 173—181, 184—189 32, 62, 63, 72, 74, 75 , 77, 78, 80—82, 85, 88—97, 103 65, 82, 83, 85. 88—97, 103 32, 64, 72, 74, 77, 85, 88-97, 103 32, 70, 72—83, 85 , 88 -97, 103 32, 73, 75, 76, 80, 81, 88-97, 101 32, 63, 72, 74, 75, 77—83, 86, 88 -97, 103, 104 84 , 93—97, 101 71, 77, 88-97 79, 82. 83, 88 100 61 72, 75, 76, 78-81, 85, 88-97, 102 88-97, 104 60, 61, 75, 78, 83, 88-97, 102 32, 72, 73, 75— 83 85, 88—97, 102 93-97, 107 I 913
19 20 21 22 23 "24 25 26 27 28 29 30 31 32 33 34 35 36 Г аллий Гафний Гелий Германий Европий Железо Золото Индий Иод Иридий Иттрий Кадмий Калий Кальций Кислород Кобальт Кремний Криптон 203, 206 209 210, 211 205 230, 231 196 206 228, 229 234 200, 201 192, 193 198 208 273 273 277 272, 277 274 275 273, 278 273 277 269 268 269 268 268, 269 250 248 — 250 237 251 251, 252 251 266 241, 242 252, 253 241 244 733 733 733 733 733 733 733 733 733 733 480 474 475 479 480 474, 475 473 474 480 286, 287 291 288, 289 299, 300 281, 282 287 298 302 287 284, 285 280, 281 283 300 288 598 599 599 447, 456, 755 447, 775 779 447, 456, 743, 746—748', 751,753—755 444, 453, 741 448, 757 744, 745, 756, 757 457, 758 739 445, 455, 739, 745, 746 448, 457 445, 455 445, 455, 746, 748, 749, 754, 763 451, 559, 772 391 396 391, 398 389 391, 392 397, 398 392 389, 391, 397 390, 397 468, 470, 471 468, 471 466, 470 465, 471 466, 470 468, 471 U 1 1 g 1 1 1 1 1 1 1 1 1 1 1 1 1 1 326 324 322 347—349 317 321 344—346 351 319, 320 315, 316 318 335 349, 350 324 4
912
УКАЗАТЕЛЬ МЕТОДОВ АНАЛИЗА
Методы качественного анализа Методы количественного
Элемент о дй анализ микрохимические методы [ спек- в X О Я ф S 5= X X Я Ф ф =х г X S ЬЙ «5 X id О ф X = S sS к X
по пор. аивидуальнь 1КЦИИ 33 я ф ЕГ О ф я я S о §•& га id S gs «s 3 я я о _ из ко я о ч X ф S О Ф »х о СП О ювый и газе ;кий х S я^о ь о |а О id ф S о о id ф ч я S О X CL.O В Г? 3 га 2 И и S о О S Q. X га s ч ч ь S о, X ф я о CJ 3 л S ф
ъ я ф X о. S «=: \0 ф га 5 я о S ч rt Н S га ф СЕ га ф и, X 6 я id о о X С X О id га я га S «о о
37 Ксенон — — — - — - — — - — - — —
38 Кюрий - - — - - — — — — - - —
39 Лантан 204 - 253 - - - - 392, 398 — - 322
40 Лантаниды 203 — 205 276 255, 258, 262 733 287, 288 778-780 392, 398 471 322
41 Литий 192 — — 253 , 733 — 280 — 448 — — — 315
42 Магний 197, 198 274 - 253, 254 733 474 282 448, 457, 758, 759 390, 392, 398 463, 471 - 318
43 Марганец 229, 230 274 269, 270 254 733 479, 480 298 — 448, 457, 750, 759, 762, 775 392, 393, 399 471 — 346, 347
44 Медь 194, 195 277, 278 269 247, 248 733 473, 474 281 — 446, 456. 743, 746, 749—754 390, 391, 397, 398 465, 470 — 316, 317
45 Молибден 224 274 — 733 478 296 — 448, 457, 742, 750. 760 393 471 — 340
46 Мышьяк 216 272 — 236, 237 733 477 293 — 443, 453, 741 389 467 — 330, 331
47 Натрий 192, 193 274 — 255 733 — 280 - 449, 745 393 - - 315
48 Неон — - — - — - — — - — — —
49 Нептуний 764 - — — —
50 Никель 231, 232 274, 277 270 255, 256 733 480 300 - 449, 457, 458, 746, 748, 750, 751, 763, 764 390, 394, 399 468, 471 - 350, 351
51 Ниобий 219 — — 255 733 — 294, 295 — 449, 457, 761, 762, 772 393, 394 — — 334
52 Олово 211, 212 275 270 263 733 476 289 — 451, 459, 464, 739, 750, 754, 772 395 472 — 325
914
Продолжение
И РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
анализа Методы разделения
| № по пор. полярографический потенциометрический радиоактивационный флуорометрический эмиссионный спектральный аналитические реакции хроматография экстракция
на бумаге ионообменная
37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 505 505-507, 511 505 506 502—504, 506-510, 512-514 501-514 501-504, 506—510, 512—514 501—504, 507—513 507 503 502—504, 506—514 501, 502, 506. 510, 511, 513 501—505, 507—514 490 488 496, 497 487 495 493 498 491, 492 568, 570 554 548, 550, 552, 554, 556, 560, 562, 564, 568, 570 554 554 554 548 554, 556 544 556 556 556 556 564 464 463 463 641, 676, 677, 720 641, 677, 678 641, 678, 679, 720 638. 639, 641, 643, 644, 647, 658—660, 662—666, 670, 671, 678, 679, 684, 685, 690, 691, 704-710, 718—720 641, 678, 679 642. 679—681, 720 642, 680, 681, 720 642, 643, 680, 681, 720 643, 681-683, 720 643, 682, 683, 720 643, 682—684, 720 642, 684, 685, 720 642, 684, 685, 720 642, 685-687, 720 642, 686, 687, 720 643, 687—689, 720 37, 40, 48, 56, 57, 83 30, 31, 40, 48, 56, 57, 64 30, 31, 38, 59 30—32, 37, 39, 47, 55—57, 60/, 30—33, 35, 37, 45, 50, 52—57, 70 30—32, 35, 37, 38, 46, 52—56, 59,60 30—33, 35, 37, 44, 50, 52-57, 68, 69 30—35, 42, 49, 52—55, 66, 70 30, 31, 38, 46, 59 30—32, 37, 45, 51, 53—57, 71 30, 31, 33, 43, 49, 52, 54—57, 67, 68 30—32, 35, 37, 42, 49, 53—57, 64 129 128, 132 123, 124, 127, 128, 132—134 123, 124, 127, 132—134 123-126, 132—134 127 123, 124, 126, 130, 133, 134 123, 128, 132—134 123, 124, 127, 132—134 129 123, 124, 126, 132—134 184, 185 175-177 174, 177—182, 184—188 174—176, 181, 184- 188, 190 174-177, 181, 184- 188, 190 173—181, 184—189 174-181, 184—188 174-188 174-177, 181, 182, 184-188 174—177, 181, 184- 188, 190 177, 184, 185 174—181, 183-188 174-188 174-177, 181-188 83 93-100, 104 64, 82, 83, 88—100 59, 88-92, 104 78, 88-97, 104 32, 72, 78, 79-84, 86, 88—97, 104 32, 72, 75, 76, 78, 83, 85, 88—97, 102, 103 32, 68, 72, 74-82, 84, 86, 88—97, 104, 10-5 32, 72, 73, 75, 76, 80, 81, 84, 85, 88—97, 101 59, 83, 88—97, 105 83. 86, 88—97, 105 32, 72, 74, 75, 78, 80, 81, 83, 88—97, 105 72, 74, 77, 78—80, 82. 86. 88 —97, 105 32, 72, 74, 75, 77-81, 86. 88-97. 107
91Б
53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 № по пор.
переори Скандий Стронций Сурьма 1 Рубидий Рутений Свинец Селен Сера гении Роднй П — ..п. 11ротактиннп Радий плутонии Полоний г ь S -и Осмнй Палладий Элемент
202* 192 — 194 233 212 222 220- 222 195, 196 205 198, 199 216, 217 i о ЬЭ 2 1 g 1 1 233, 234 233 232, 234 индивидуальные реакции Методы качествен- ] ного анализа
274, 275, 278 277 271, 277, 278 275, 278 275, 277 273, 274, 278 1111 люминесцентный анализ
270 268 _ I 270 1 gill 1111 абсорбциометрия микрохимические методы
260 260 250, 251 259, 260 261 257 262 261 235, 236 263 262 256, 257 257, 258 258, 259 микрокристаллоскопия
733 733 733 733 733 733 733 733 733 733 733 733 733 абсорбционный спектральный Методы количественного
475 480 476 478 470 474 477 1 1 амперометрический
299 301 285 281 301 289, 290 295 295 281 287 1 283 293 302 301 302 весовой
1 1 1 Сл . , g 1 1 1 8 । 1 1 1 1 1 газовый и газометрический
449, 458, 764, 765 449, 458, 765, 766, 767 449, 450, 758, 767, 768 768 765 450, 458, 760,' 768, 769 450, 769 447, 456, 742, 743, 751, 756 , 450, 459, 764, 770 449, 458, 739, 742—744, 751, 756, 765, 766 450, 459, 771 459, 745, I 761, 770 443, 739 450, 771 451 450, 459, 741, 756, 770, 771 колориметрический и спектрофотометрический
394, 399 395, 399 397 395 391, 398 i 1 1 1 1 «э 1 сл 1 комплексометрический
467, 472 468 468, 472 466, 469 466, 472 466, 471 1 1 1 1 кондуктометрический анализ и высокочастотное титрование
1 1 1 g 1 1 1 1 1 1 1 масс-спектрометрия
325, 326 335—337 317 322, 337, 338 318 332 347 351 320 351 351 1 объемный
УКАЗАТЕЛЬ МЕТОДОВ АНАЛИЗА
анализа । И РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ П родолжение
53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 № no nop.
509 502, 504, 507—510, 512 ; 506, 507 506 501—514 507, 510 501. 503. сл 2 g □1 1 501. 514 СЛ о О" JI □i Ю СЛ Л О в 501, 507, 509. 510 507—510, 512. 514 506, 507, 509, 514 506 501, 503, 505, 506. 510. 514 505, 507— 509. 514 502—505, , 50R. 514 полярографический
498 492 494 494 : 487 490 489 493 ос CO 1 498 498 потенциометрический
560 560 I 560 552 560 560 558 562 562 * 544 562 564 562 558 558 560 радиоактив анионный
463 464 1 1 1 1 флуорометрический
645, 698, 699, 720 ' 645, 699—701 645, 700— 703, 720 645, 702, 703, 720 699, 720 644, 698, 699, 720 644, 698, 699 720 3g g- . 644, 691, 692, 720 644, 692, 693, 720 645, 692, 693, 720 645, 693, 694 645, 694, 695, 720 645, 694, 695, 720 А4.Ч 605 643, 688, 689 643, 688, 689, 720 643, 689, 690, 720 643, 690, 691, 720 эмиссионный спектральный
43, 52—57 47, 53* 55* 56* 60, 61 ЯЛ Q9 ЯЧ Q7 30, 31, 40, 52, 55, 56, 63 ЯП—Я2 Я7 ЯО 68 30—32, 38, 46, 59 54—57 АЛ 30, 31, 3-3—35, 4Я 59—55 30—32, 37, 42, 49, 53—57, 64 30—33, 35, 42, 4Я 59—54 AR 30, 31, 38, 52, 53, 59 30, 31, 45, 5Я_5A 71 30—32, 39, 47, 59_5fi Al .4 J’-j ‘ZS ‘SI- ‘IS ‘0E 01 ‘SS ‘£S ‘SI ‘IE ‘0E £S ‘6E ‘IS ‘0E 1 £ 30, 31, 37, 45, ; 51, 52, 54 —56, 71 30, 31, 45, 51, KA K7 71 30, 31, 45, 5Я—АА 71 аналитические реакции I Методы разделения
123, 124, 126, 132—134 124, 125, 132, 133 129 123, 124, 127, 19R 1Я?_ 1Я4 128 129 123—126, 132, 133 129 123—126, 1Я9—134 1 129 129, 132 129, 132 на бумаге хроматография
1/у—1//, 181, 182, 1R1 IRQ 188, 190 2 174—177, 189 188, 190 190 174-181, 1R4 1RG » J » 181, 182,* 184—189 17A__177 4 I 181, 184— 188, 190 174—181, 1R4 1RR 184—186* 17Л. 177 181, 184— 188 174, 182, 184, 185 174, 177, 184, 185, 190 174-181, 183—188 174—181, 184—188 174_1R1 183—188* 177, 184, 185 17 A 177 —VLi 881—£81 J 1 0 - I 174—181, I 1R3—1RR I ионообменная
63, 77, 78, 83, 84, 88—97, 107 78, 83, 88—97 32, 72, 74, 75, 77, 79, 80, 81, 86, 88—97, 106 917 оч, уо—у* 72, 75, 80, 81, QA QQ О'? 1Л1 с “ j = tv а» ya j.» *08 ‘9Z *ZL ‘Z2 71, 82, 86, 88-97, 106 32, 76, 78, 80-RR RR 07 ins 71, 77, 88—97, 106 32, 72, 74-76, 78—82, 85—97, 103 5Q RQ П7 1ЛЛ 70, 72, 80, 84, RR 07 inc 0 0 4 c о 71, 80, 88—97 71, 76—78, 80, 81, 88—97, 105, 106 71, 74, 77, 80, 81, 86, 88—97, 106 82, 83, 86, 88—97, 106 83, 86, 88—97 106 74, 79, 83, 86, экстракция
а а 00 •ч х х оо х оо X со со tO 1— о 00 3 х х 3 х to № по пор.
Г о Я Я Цинк Церий Цезий Хром Хлор Франций Фтор Фосфор Уран Углерод Торий , Титан 1 Технеций Тантал Теллур Таллий Элемент
to о сс 199, 200 to 2 192 — 194 223, 224 226, 227 225, 226 213 О 209, 210 to X 222, 223 219, 220 206, 207 индивидуальные реакции Мет н
to х to X 1 to X to 1 1 1 to Cm 1 № X 1 1 1 275, 278 люминесцентный анализ о о Р0 □ (а я я
1 to о 1 1 s © 1 1 1 1 1 1 1 to 1 1 1 абсорбциометрия МИК хим» CKI мет< Я В5 Ь Я pj £ о
ГО X 266, 267 to 245 — 248 to 242, 243 to fe 1 to X X X to X 1 to X to to Ji. X to X 264, 265 микрокристаллоскопия 2 го 2^ Е ? Т го я
. 1 й 1 w w 1 1 1 1 1 1 1 x w s X X абсорбционный спектральный
476, 477 л 1 1 X 475, 479 to 1 $ 478, 479 X fe X 1 X 1 X амперометрический
290, 291 283, 284 X со 1 to X to Ю X to , 1 292, 293 to © 1 to tg to s . to 1 8 to Ю to X весовой
1 1 1 1 1 X X . § 1 1 1 fe 1 1 1 1 1 1 газовый и газометрический
453, 460, 760, 778 453, 460, 739, 778 445, 455, 746, 747 1 446, 456, 748—750, 775 fe 446, 753 449, 458, 742, 745, 765 452, 460, 743, 774- 776 X 451, 459, . 753, 754, 772. 773 451, 750, 760, 773, 774 451, 771, 772, 774 774 451, 459, 761, 762, 772 451, 452, 459, -460, 739, 742, 743, 774 колориметрический и спектрофотометрический
х 8 396, 399 1 о 8 1 1 1 1 X © X 1 395, 399 395, 399 1 1 1 bo X комплексометрический г С i-Р <Г
Л. to 466, 472 1 1 8 468, 470 468, 470 X 468, 472 467, 469 to to 1 1 1 466, 472 кондуктометрический анализ и высокочастот-иое титрование
||| 1 1 1 1 1 £• 1 1 1 1 । । । 1 масс-спектрометрия S >£ Л Г
X to X 5 ы to to 1 339, 340 fe fe 1 329, 330 (X 322, 323 326, 327 8 338, 339 X (X X to объемный с л л а с
1*1''
00 х со X X X •*да X о to X X X ja! to № мО nop.
§ 8 502—514 501—503, 505, 507,508. 512, 514 О 501—512, 514 EOS ‘tOS i i 1 1 501—503, 506—514 1 504, 507, 511 1 501, 503— 507, 509, 511—514 502, 503, 505-511, 513, 514 j 501, 505, 510, 511 501-514 полярографический W Р0
В х <£> 1 1 X S 490, 491, 496 I i 1 1 495, 496 fe fe fe 1 fe 1 8 потенциометрический
СП о X О 546, 548 X X СЛ X Cl X X [ о 1 X X X X X X X X 8 X X 1 564, 566 a X X X радиоактивационный
fe О: 1 1 . 1 1 fe 1 to 1 g 1 1 1 1 X fe флуорометрический
719, 720| 647, 717— >47, 716. 47, 720 05 D 646, 712— 715, 720 547, 714, 45, 720 646, 711— 713 79П 546, 711, 720 646, 647, 710, 711, 720 646, 710, 711, 720 647, 710 646, 647, 1 706— 708, 720 647, 708, 709, 720 X c 645— 647, 704, 705, 720 646, 704, 705, 720 645, 702— 704, 72C эмиссионный спектральный
54—57, 65* X -L £ л-г* 30-32, 37, 39, 47, 53—57. 61 35, 37, 40, 48, 52-57 30, 31, 38, 52, 53, 59 ,8 g Sg Xx x x л. 30, 31, 33—35, 44, 52, 55, 56, 70 30, 31, 33—35, 44, 52—55, 70 30—32, 37, 44, 50, 52—54, 56, 57, 69, 70 30, 31, 33—35, 42, 52—54, 56, 66 30—32, 37, 41, 48, 52, 54—57, 65 .30, 31, 34, 37, 41, 48, 52-57, 65, 66 30, 31, 33—35, 30, 31, 33, 43, 49, 52, 54-57, 67, 68 30—35, 43, 52—54, 68 30—32, 40, 47, 52—56, 63 аналитические реакции
to ГО о ы to Л>. to 1 to X 123, 124, 126, 132—134 § § 1 130, 131 126, 130, 132 1 129, 130 1 X 1 1 to to на бумаге хро.мато: Методы ра
S L х о со « 173—182, (ОЛ юл 174—177, 181, 184— 188, 190 174-181, 184—188 181, 184— 186 174, 177 184, 185 173-188, 189 184, 185, 189 174, 175, 177—180, 184—188 173-188 1 X 174-177, 181, 183— 188, 190 189 174—188 174—177, 181, 182, 184—188, ионообменная граф; я W го л S
82, 83, 87—97, 109 32, 73, 75—77, 79—82, 87—97, 109 32, 65, 73, 79, 78, 79. 82, 83, 93—100, 102 88—97, 102 59, 83, 88—97, 102 32, 72, 73, 76, 78, 80—85, 84, 93-97 88—97 84, 103 108, 109 84, 93-97, 105 32, 69, 73, 77—83, 87—97, 107, 108 108 78, 79, 82, 83, 86, 88—97. 32, 73, 77-79 82, 87, 88—97, 86. 88—97. 107 32, 73, 74, 75, 76, 80, 81, 84, 88—97, 107 68, 73, 77, 86, 88—97, 107 32, 63, 73- 75, 78, 80, 81, 83, 88—97, 108 экстракция Про до.>1 окон и е
УКАЗАТЕЛЬ МЕТОДОВ АНАЛИЗА
СПРАВОЧНИК ХИМИКА, токг IV
с. 920
УДК 54/083
Никол. 64
Издательство „Химия**, Ленинградское отделение Невский пр., 28
Редакторы: 3. И. Грива, В. А, Коц, С. Л. Томарченко Техн, редакторы: 3. Е. Маркова, Ф. Т. Черкасская Корректоры: Г. П. Батракова, Л. А. Любсвич
Подписано к печати 19/VI 1967 г. М-13701. Бумага тип. № 2 60x90l/ie. Уч.-изд. л. 82,64. Печ. л. 57,5. Тираж 25 000 экз. Цена 4 р. 33 к. Заказ № 783.
Ленинградская типография № 2 имени Евгении Соколовой Главполиграфпрома Комитета по печати при Совете Министров СССР. Измайловский проспект, 29.