Текст
химия
жизнь
Е ЗАГРЯЗНЯЙТЕ ВОДОЕМЫ!
is
В ЭТОМ НОМЕРЕ:
Нельзя травить рыбу!
Элемент № 22: титан
Рождение мезомолекулы
«Микроскоп» для атомов
Судьба лекарств
Клуб Юный химик
Полезно ли кислое?
Все о зубной пасте
■з
ho
>
С
О
с
I
о
X
у
>
аз
х
с:
> 1966
■3
2
х
а
ее
с;
>
с
о
с
I
о
X
у
СП
<^/Ч> fa ы\ КГГ i
//Uls l^sy Via A*~»
с j- J
СТАТЬЮ ПРОФЕССОРА П. М.
ЛУКЬЯНОВА О ПЕРВЫХ ХИМИЧЕСКИХ
ЛАБОРАТОРИЯХ В РОССИИ
ЧИТАЙТЕ НА СТР. 33
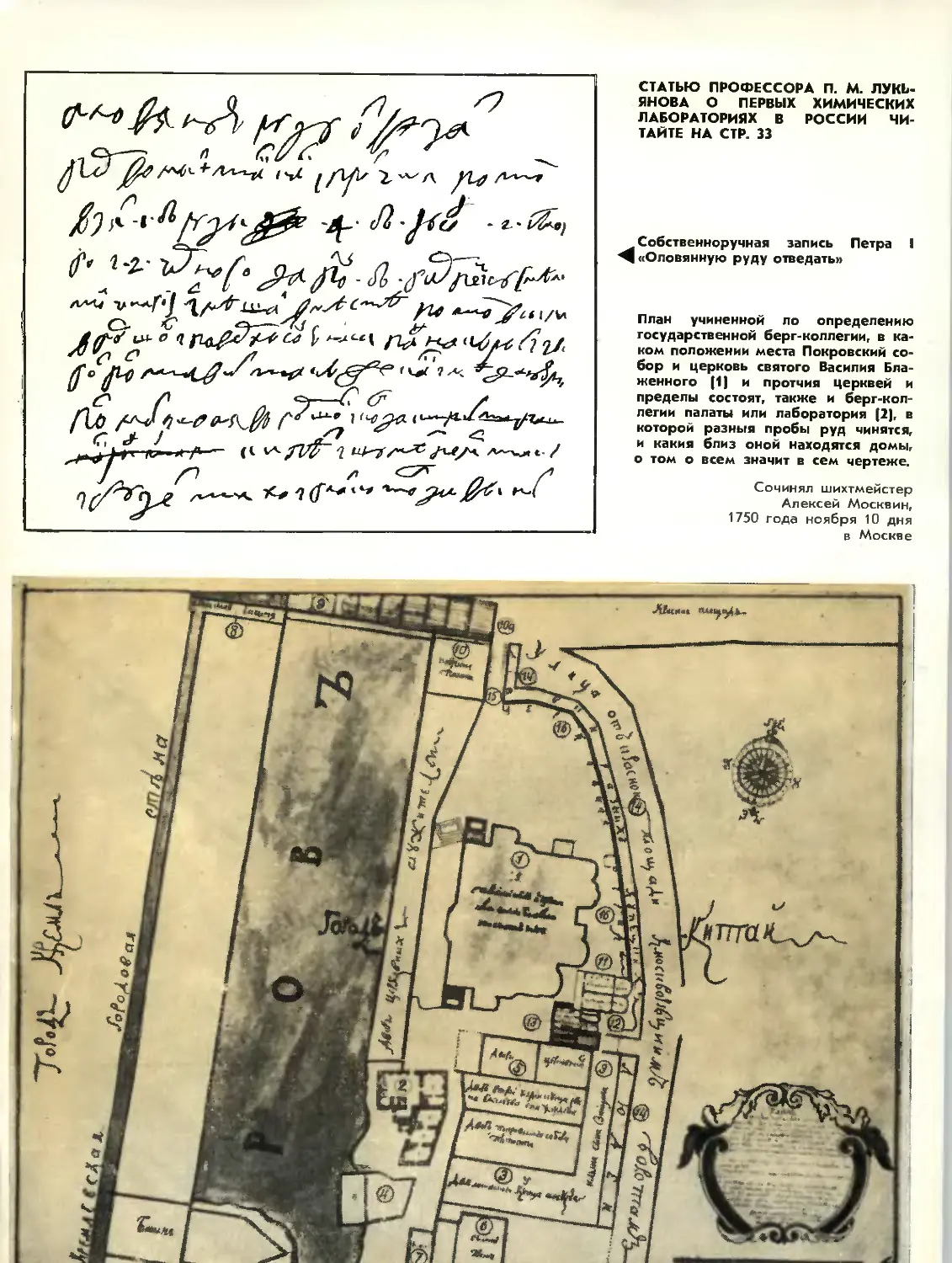
Собственноручная запись Петра
^«Оловянную руду отведать»
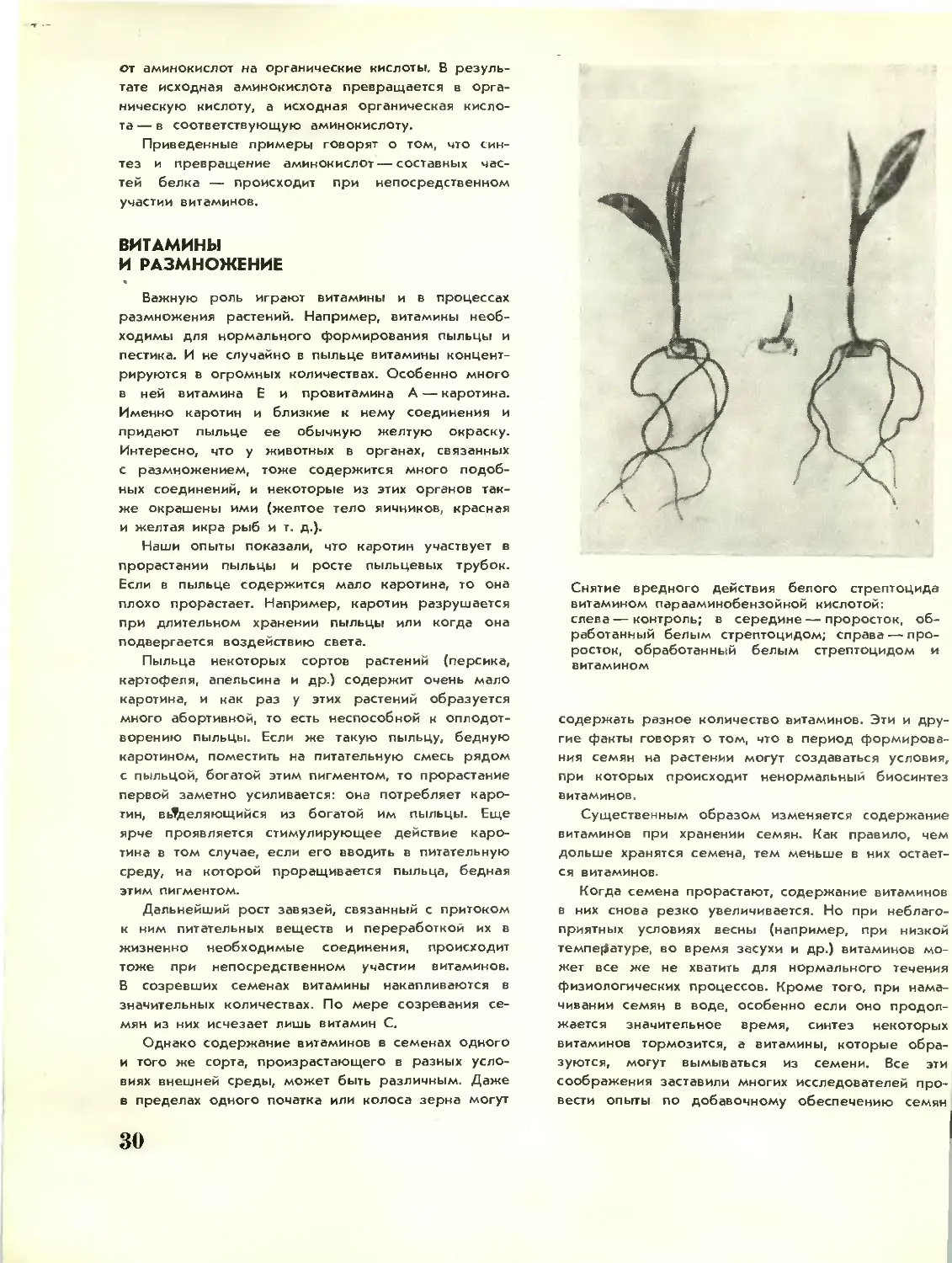
План учиненной ло определению
государственной берг-коллегииг в
каком положении места Покровский
собор и церковь святого Василия
Блаженного A) и протчия церквей и
пределы состоят, также и берг-кол-
легии палаты или лаборатория B], в
которой разныя пробы руд чинятся,
и какия близ оной находятся домы,
о том о всем значит в сем чертеже.
Сочинял шихтмейстер
Алексей Москвин,
1750 года ноября 10 дня
в Москве
химия
жизнь
В НОМЕРЕ:
Экономика и производство. БОЛЬШЕ ПЛАТИТЬ — ЧТОБЫ БОЛЬШЕ
ПРОИЗВОДИТЬ. БОЛЬШЕ ПРОИЗВОДИТЬ — ЧТОБЫ БОЛЬШЕ ПЛАТИТЬ. Очерк М.
Черненко 2
МЕЗОННАЯ ХИМИЯ — ВОЗМОЖНО ЛИ ЭТО! Рассказывает кандидат физико-
математических наук Л. И. Пономарев 6
ХИМИЯ АТОМНЫХ ЯДЕР И ЭЛЕМЕНТАРНЫХ ЧАСТИЦ. Статью Л. И. Пономарева
комментирует член-корреспондент АН СССР В. И. Гольданский 11
Страница интервью. ЛАУРЕАТ ЛЕНИНСКОЙ ПРЕМИИ. БЕСЕДА С АКАДЕМИКОМ
А. Н. НЕСМЕЯНОВЫМ 14
ЭЛЕМЕНТ № 22: ТИТАН. Рассказывают инженеры Я. Розенцвейг и
С. Венецкий . . 17
ХИМИЯ И РЫБА. Статья кандидата биологических наук А. Г. Гусева .... 24
ВИТАМИНЫ В ЖИЗНИ РАСТЕНИЯ. Рассказывают доктор биологических наук
К. Е. Овчаров и Н. Д. Мурашова 29
Страницы истории. ПЕРВЫЕ ХИМИЧЕСКИЕ ЛАБОРАТОРИИ В РОССИИ. Заметки
профессора П. М. Лукьянова 33
ЖЕЛЕЗНЫЕ НЕРВЫ. Статья инженеров М. А. ГуревичаиВ. А. Литвиненко 36
СКАЗКА: 1,98. Артур Порджесс 42
Как делают вещи и вещества. СВЕРХЧИСТЫЕ. Рассказывает кандидат химических
наук Г. М. К у р д ю м о в : 45
ИОННЫЙ МИКРОПРОЕКТОР — «МИКРОСКОП» ДЛЯ НАБЛЮДЕНИЯ
ОДИНОЧНЫХ АТОМОВ. Статья Д. Брендона 48
БУДЬ ЗДОРОВ, ДОМ. О полимерных строительных герметиках рассказывает
режиссер В. Цукерман 49
Страницы разных мнений. ПАМЯТЬ, ХИМИЯ И КИБЕРНЕТИКА. Статья доктора
химических наук В. А. Кухтина 51
КИСЛОТА В НАШЕЙ ПИЩЕ. Рассказывает И. Вольпер 56
ПОЛЕЗНО ЛИ КИСЛОЕ! На вопрос отвечает профессор М. С. Маршак . . . 59
СУДЬБА ЛЕКАРСТВ. Рассказывает кандидат медицинских наук В. М. А в а к у м о в 60
КОГДА, ОДНАЖДЫ, КАК-ТО РАЗ 65
ИЗ ПИСЕМ В РЕДАКЦИЮ 66
Учитесь переводить. АНГЛИЙСКИЙ — ДЛЯ ХИМИКОВ 68
ВСПЫШКА ГЕНИЯ. Перевод с английского 70
Химическая кухня. С = ! И = \ Об анализе углерода и водорода рассказывает
кандидат химических наук А. И. Артеменко 74
ДЕСЯТЬ ЗАПОВЕДЕЙ ХИМИКА-ОРГАНИКА 77
Клуб Юный химик - - 79
Наш практикум. СТЕКЛОДУВНАЯ МАСТЕРСКАЯ 86
Уголок фотолюбителя, СОЛЯРИЗАЦИЯ. Советы оператора Б. Плужникова 88
ЧТО ПОЛЕЗНО ЗНАТЬ О НОВЫХ ЧИСТЯЩИХ СРЕДСТВАХ! . 90
Страница садовода и огородника. ГИДРОПОНИКА ПРИ ИСКУССТВЕННОМ
ОСВЕЩЕНИИ. Советы агронома А. А. Новоселова 92
Книжная лолка. ВСТРЕЧА НА ПЕРЕКРЕСТКЕ. Лев Разгон 93
СПУТНИКИ ЗУБАСТЫХ. Четыре рассказа о зубной пасте 94
НАУЧНО-ПОПУЛЯРНЫЙ октябрь 1966
ЖУРНАЛ $gO Ю
АКАДЕМИИ НАУК СССР год издания 2-й
больше платить —
чтобы больше производить,
больше производить —
чтобы больше платить
заметки о переходе
рязанского комбината химического волокна
на новую хозяйственную систему
Из первой части этих заметок следовалог
что хозяйственная реформа изменяет не
столько служебные бумаги, сколько
экономические отношения. Приведем несколько
примеров, подтверждающих это.
ИСТОРИЯ О ХОРОШЕМ РАБОТНИКЕ
(гример из области экономических
отношений внутри предприятия)
Жил да был, работал в отделе капиталь-
ного строительства молодой специалист
товарищ Н. Техник по образованию,
продолжающий учиться в институте заочно.
Получал 130 рублей в месяц.
Товарищу Н. приходилось то и дело
бывать по делам строительства в самых
разных учреждениях. К нему пригляделись и
поняли, что он хороший работник. И в один
прекрасный день товарищ Н. получил
предложение перейти на другой завод — здесь
же в Рязани. На работу в такой же ОКС,
но с окладом 170 рублей. И товарищ Н.
подал заявление об уходе по собственному
желанию.
Директор комбината и его заместитель
по капитальному строительству
посоветовались и решили, что отпускать товарища Н.
жалко и что пора предложить ему
должность повыше. Но таковой должности не
оказалось — все они были заняты другими
людьми.
И тогда директор Рязанского комбината
химического волокна Василий Иванович
Воробьев взял — и повысил своей властью
должностной оклад товарищу Н. со 130
рублей в месяц до 170 рублей в месяц. И това-
Окончание. Начало — в предыдущем
номере.
рищ Н. остался на своем заводе, где
оценили его хорошую работу.
Это и есть права директора в действии.
На наш взгляд, товарищ Воробьев
пользуется ими совершенно правильно. И можно
пожелать, чтобы те хозяйственники и
инженеры, которые, несмотря на данные им
права, захотят по старой привычке
согласовывать и увязывать каждый свой
экономический шаг, поступали бы так же, как он.
ЧТО, КУДА, КОГДА И НА ЧЕМ ВОЗИТЬ
(пример из области экономических
отношений с вышестоящими организациями
и родственными предприятиями)
На складе Рязанского комбината
химического волокна хранится немало тонн
разных красителей. Склады здесь хорошие, а
красители приходится получать издалека
и за большие деньги, поэтому завозят их
сюда сразу для нескольких предприятий,
выпускающих штапельное волокно.
Но красители на складе— это
оборотные средства, это деньги. Большой запас
красителей — это на сегодня омертвленные,
сверхнормативные фонды.
И вот в мае месяце Рязанский комбинат
погрузил на автомашины 27 тонн
красителей и отправил их на Каменский комбинат —
тот самый, для которого эти красители были
закуплены. (Прибегнуть к более дорогому
автомобильному транспорту пришлось
потому, что перевозить сырье по железной
дороге дважды не разрешается — таково
правило, преследующее простую и ясную
цель, — побудить промышленные
организации не возить материалы с места на место,
а направлять их сразу туда, где они будут
использованы).
2
Но благодарности от Каменского
комбината не последовало. Вместо нее пришла
телеграмма, суть которой можно передать
так: доставлять нам сейчас красители мы не
просили, эти 27 тонн нужны нам будут
только в июле, на июль они у нас записаны в
плане, в июле мы за них и переведем вам
деньги... И еще — возить на автомобилях
очень дорого. Можем платить только по
тарифу железной дороги...
Мы не собираемся находить в этой
истории «правых» и «виноватых»! Но она
кажется нам заслуживающей внимания потому,
что в ней отражается внутренняя «работа»,
«механизм» реформы, заставившей считать
деньги.
Главк и сейчас настаивает, чтобы
Рязанский комбинат принимал красители «на
всех». Но счет деньгам сразу же выставил
напоказ простую истину: это невыгодно —
дважды возить, дважды разгружать и снова
грузить одну и ту же тонну. Это
невыгодно— завозить материал на три месяца
раньше, чем он потребуется. Это
невыгодно— цех в Казани, а склад в Рязани... А то,
что невыгодно, — при новой системе будет
изживаться.
РОМАН В ТЕЛЕГРАММАХ
(пример из области экономических
отношений с постоянными потребителями)
В первых числах мая Рязанский
комбинат искусственного волокна отгрузил
Тбилисской бумагопрядильной фабрике
штапельное волокно на 31 268 рублей и
47 копеек...
Телеграмма:
«...Прошу отавизовать телеграфом сумму
платежному требованию номер 1361
Директор комбината Воробьев
18 мая.»
Ответная телеграмма:
«За неимением средств оплата счетов по
бумагопрядильной фабрике задерживается
Управляющий отделением Госбанка Качарэва
19 мая.»
В Тбилиси снова летят телеграммы. Они
напоминают о постановлении, которое
требует оплачивать счета предприятий,
переведенных на новую систему планирования
и экономического стимулирования, в
первую очередь — как же им работать за
деньги, если им этих денег платить не будут?
И настаивают: «...Ускорить оплату
платежного требования нр 1361 копеек 3126847».
В переводе с банковско-телеграфного
языка на обыкновенный это и означает те
самые 31 тысячу с лишним рублей.
А 1 июня в 13 часов (теперь на
денежных документах отмечают и час
поступления) прибыло такое послание:
«На вашу телеграмму дирекция Тбилисской
бумагопрядильной фабрики сообщает, что ввиду
финансового затруднения счет 1361 оплачивается частично.
24 мая оплачено рублей 8268-47, оставшаяся сумма
будет погашена в ближайшие дни.
Директор фабрики Махатадзе,
Главный бухгалтер Атунян.»
Оставшаяся сумма — это, как можно
убедиться, вычтя 8268 из 31268, ни много
ни мало 23 тысячи рублей.
И вот тогда-то появилась последняя (на
день моего отъезда из Рязани) бумага в
этой истории. Это уже не телеграмма, а
простая служебная записка:
«Начальнику отдела сбыта комбината тов.
Шарапову Ф. Е. Ввиду длительного финансового
затруднения у Тбилисской бумагопрядильной фабрики
прошу производить отгрузку волокна последней
только против аккредитива, начиная с 1 июня
1966 года.
Начальник финотдела Понукалина
1 июня 1966 г.»
Что же будет дальше? На комбинате
отвечают: сократим выпуск тех сортов
волокна, которые потребляет только эта
фабрика. Получим аккредитивы — отгрузим им
волокно и снова подождем оплаты.
Можно возмутиться: что за
дезорганизация — ведь это же социалистические
предприятия! Верно — дезорганизация. Но
кто ее вносит? Разве не то предприятие,
которое не выполняет своих финансовых
обязательств? И если наши экономисты нашли
способ, который автоматически наказывает
дезорганизатора, не позволяя ему укрыться
за спиной хорошо работающего
предприятия, — то разве это плохо? Верно —
социалистические предприятия. Но разве именно
социализм не предполагает, впервые в
истории, объективную возможность научно
четкой организации производства? И если наши
экономисты нашли способ, который
автоматически сигнализирует о несоответствии
между этой возможностью и способностью
того или иного хозяйственника
использовать ее, — то разве это плохо?
з
!•
По традиции в конце подобных заметок
полагается сообщать о трудностях, которые
еще предстоит преодолевать. Правильная
традиция — последуем ей.
ТРУДНОСТИ, СВЯЗАННЫЕ
С ПЛАНИРОВАНИЕМ ПРОИЗВОДСТВА
Это планирование, по выражению
директора комбината В. И. Воробьева, еще
«далеко не синхронно». Цехи и комбинат в
целом увеличили по собственной
инициативе и годовой план, и свою пятилетку. Но
чтобы выпустить больше волокна, нужно
больше сырья — целлюлозы и химикатов.
А в плане материально-технического
снабжения (он сверстан и утвержден для
любого предприятия еще до экономической
реформы) это увеличение, естественно, не
могло быть предусмотрено...
Уже на третий квартал этого года
комбинату потребуется больше 12 тысяч тонн
едкого натра, выделено же ему пока менее
восьми с половиной тысяч. Не меньшие
сложности предстоят и со стоимостью
основного сырья — целлюлозы. Сейчас ее
возят в Рязань, самое дальнее, из
Архангельской области. И железной дороге
платят 18—20 рублей за вагон. Но на будущие
годы целлюлоза планируется из Сибири, и
тогда уже не 20, а 100 рублей станут
обычной ценой... А оборотные средства
запланированы, исходя из уровня 1965 года.
Значит, если ничего не изменить в этой
ситуации, то Рязанский комбинат превратится из
прибыльного предприятия в убыточное.
ТРУДНОСТИ, СВЯЗАННЫЕ
С РАЗВИТИЕМ ПРОИЗВОДСТВА —
С КАПИТАЛЬНЫМ СТРОИТЕЛЬСТВОМ
Когда завод строится «на пустом месте»,
у него есть дирекция строящегося
предприятия— организация, финансируемая
целиком и полностью из государственного
бюджета. Но сейчас на Рязанском
комбинате строится его вторая очередь, а это уже
совсем другое дело.
На ее строительство комбинату
отпущены из бюджета миллионы рублей.
Отчитаться в некоторой части этой суммы —
значит построить очередной объект, например
здание будущего цеха. Но как только этр
здание готово, оно немедленно переходит
на баланс действующего комбината. Оно
входит в его основные фонды, из чего
следует, что от него должна быть
фондоотдача. И что комбинат должен немедленно
начать вносить в банк амортизационные
отчисления, которые покроют в конце концов
расходы на строительство...
Но на самом-то деле такой цех еще не
дает и не может давать никакой продукции.
Она появится только тогда, когда будет
построена, оборудована и пущена в
эксплуатацию вся вторая очередь комбината, по
существу,—большой новый завод!
ТРУДНОСТИ, СВЯЗАННЫЕ
С ВЗАИМООТНОШЕНИЯМИ
МЕЖДУ ЦЕХАМИ
Инженерам и экономистам Рязанского
комбината стало ясно с самого начала
реформы, что оценивать работу цехов (то же
самое относится к участкам, сменам, к
каждому рабочему) нужно только по таким
показателям, которые зависят от работы
именно этого цеха (участка, смены,
рабочего). И не по каким-то умозрительным
величинам. Нужна вещественная продукция —
ведь речь идет о деньгах!
Но, поразмыслив, руководители
комбината убедились, что для самых важных
цехов завести такой учет они не могут,
потому что нельзя с необходимой точностью
зафиксировать предмет труда, который эти
цехи получают. Нет или не хватает
счетчиков энергии, счетчиков воды, измерителей
потоков химических полупродуктов и
реактивов. А значит, нет и достоверного учета
обращающихся в производстве ценностей.
Значит, не всегда можно правильно решить,
кто, сколько и чего израсходовал, что и
куда сбросил... Все это было привычным при
«котловом методе» планирования и учета,
который, естественно, никуда не годится в
хозяйстве, собирающемся считать деньги и
труд-
Сейчас комбинат интенсивно
раздобывает счетчики. Для замеров расхода
вискозного раствора в каждой смене, для
каустика и для умягченной воды. Но и с их
помощью полностью учесть обращение
всех материальных ценностей между
цехами не удастся.
И комбинат берется за решение «с дру-
4
гой стороны». Создается новое
подразделение— штапельное производство,
объединяющее три основных цеха с их
технологическими процессами, от подготовки и резки
целлюлозы до упаковки готового волокна.
Создается даже свой, комбинатский
межцеховой арбитраж: в новых условиях один
цех может предъявить материальные
претензии другому цеху... Потому что теперь
главный показатель их работы — это мера
труда—рубль и копейка.
Кстати, слово «показатель», так часто
встречающееся на этих страницах,
употребляется здесь, конечно, по старой памяти —
нового слова еще нет. Но возможно, оно
скоро появится. И вероятно, произведут его
уже не от глагола «показать», а от какого-
то другого. Может быть — «делать».
М. ЧЕРНЕНКО,
специальный корреспондент
«Химии и жизни»
ТЕХНОЛОГИ, ВНИМАНИЕ!
К ПРОБЛЕМЕ «ШПИЛЕК»
Тонкие каблуки женских туфель
испытывают огромные
раздавливающие нагрузки — до 300 кг/см2.
Кожаные набойки не могут
выдержать таких нагрузок и за два-
три дня выходят из строя. Метал-
Рис. В. ЗУЙКОВА
лические набойки, получившие
широкое распространение,
достаточно прочны, но они портят
деревянные лолы и слишком громко
стучат при ходьбе.
Есть еще один материал для
набоек — полуэбонит.
Изготовленный из высокостирольного
каучука, он обладает достаточной
износостойкостью и в то же время
твердостью. Важно правильно
подобрать степень вулканизации
материала, чтобы он был прочным и
в то же время не хрупким.
На калининском комбинате
«Искож» выпущена партия
полуэбонитовых набоек из каучука
БС-45К. Эксплуатационные
испытания прошли успешно — такие
набойки выдерживают по меньшей
мере 10—15 дней ежедневной
носки.
(«Кожевенно -обувная
промышленность», 1966, № 5)
ВСЕГО ТРИ МИНУТЫ
Стеклоткань, из которой делают
стеклопластик, приходится
расшлихтовывать — удалять с нее за-
масливатель. Без этой операции
прочность и водостойкость
пластика будут невелики, так как
синтетическая смола плохо смачивает
«жирное» волокно. Обычно зама-
сливатель удаляют либо нагревом,
либо химической обработкой.
Удачный химический состав
для расшлихтовки был предложен
недавно советскими
исследователями, которые порекомендовали
использовать хромовую смесь.
Уже за 3 минуты эта смесь
обезжиривает волокно. Правда, чтобы
уложиться в три минуты, реактив
нужно нагреть до 80°С. Но
операцию можно проводить и при
комнатной температуре,
разумеется, несколько увеличив время
обработки.
(«Пластические массы»,
1966, № 6)
СМАЗКИ ИЗ СИНТЕТИКИ
Ни для кого не секрет, что
естественные жиры дефицитны. В
производстве массовых смазок они
уже заменены синтетическим омы-
ляемым сырьем. Но для литиевых.
бариевых и прочих смазок
ответственного назначения все еще
используются природные жиры.
В Московском институте
нефтехимической и газовой
промышленности проведены работы по
изготовлению консистентных
литиевых смазок на синтетическом
сырье. Лучшие смазки получены
на мыловаренных фракциях тер-
мооблагороженных синтетических
жирных кислот, особенно тех. у
которых углеродная цепочка
содержит от 10 до 16 атомов
углерода.
На качестве смазки очень
вредно отражаются примеси, а
синтетическое сырье, к
сожалению, содержит их в достаточном
количестве. Отсюда — такие
недостатки смазок, как пониженная
водостойкость и склонность к же-
латинизации. Однако когда
промышленность наладит выпуск
более чистых синтетических жирных
кислот, они будут вполне
приемлемыми дпя производства
литиевых смазок.
(«Нефтепереработка
и пефтехимия», 1966, № 5)
ЦЕРИЙ В СМАЗКЕ
Силиконовые масла — важнейший
компонент высокотемпературных
смазок (например, применяемых
в турбинах реактивных
двигателей] и гидравлических жидкостей.
Небольшие добавки церия @,02% ]
повышают устойчивость такого
масла при температурах около
400°С.
(«Chemical and Engineering
News», 1966, № 14)
5
МЕЗОННАЯ ХИМИЯ-
ВОЗМОЖНО ЛИ ЭТО?
Кандидат физико-математических наук Л. И. ПОНОМАРЕВ,
Объединенный институт ядерных исследований, г. Дубка
МОЖНО ЛИ НАЙТИ ИГОЛКУ В СТОГЕ
СЕНА! Сравнительно просто это делается
только в сказках. А можно ли с помощью
этой самой иглы установить, как устроен
стог сена внутри! Даже если вы верите
сказкам, и то вряд ли согласитесь заняться
такой работой.
А между тем нечто похожее все-таки
возможно. Только изучать мы будем «стог»
величиной с молекулу, а вместо иглы
используем т?~-мезон — одну из
элементарных частиц. Наша задача от этого не станет
проще: ведь даже самая маленькая
молекула больше ir-мезона примерно в
100 000 раз, тогда как самый большой стог
сена больше обычной швейной иглы «всего
лишь» в 10 000 раз.
В этой статье речь пойдет о новой и
неожиданной области знаний, которая
возникает буквально на наших глазах: о
применении методов физики элементарных частиц
при исследовании химического строения
веществ и структуры молекул.
ЧТО ЖЕ МЫ ЗНАЕМ СЕЙЧАС О
МОЛЕКУЛЕ И ПОЧЕМУ ЕЕ ИНТЕРЕСНО ИЗУЧАТЬ!
Прежде всего то, что «молекула состоит из
атомов» — утверждение, в наши дни
знакомое каждому школьнику. Атомы построены
из ядра и нескольких электронов, которые
вокруг него «вращаются». Мы взяли слово
«вращаются» в кавычки, потому что на
самом деле все это гораздо сложнее.
Размеры атома 10 8 см, т. е. 0,00000001 см,
размеры ядра 10~13—10 |2 см, о
размерах же электрона никто пока не решается
говорить всерьез. Однако у электрона в
атоме есть характерная «область влияния»,
которая, в сущности, и определяет размеры
атома. Поэтому лучше говорить не об
отдельных электронах в атоме, а об
«электронном облаке», которое окружает ядро
и удерживается около него электрическими
силами. При сближении атомов их
электронные облака изменяются, смешиваются, и
между ними возникают обменные силы,
которые и связывают атомы в молекулу.
Связи в молекуле слабее, чем
электрические силы в атоме, и носят название
химических. Еще слабее силы
межмолекулярного притяжения. Слабость их, конечно,
относительна: ведь все знают, что испарить
ведро воды или забить гвоздь в кирпичную
стену не так легко. Чтобы разорвать связи
между молекулами в 1 грамме воды
(попросту говоря, для испарения 1 грамма
воды) необходимо затратить 539 калорий,
для разрыва химических связей в том же
грамме нужно 12 200 калорий. А для
полного разрушения оставшихся после этого
атомов водорода и кислорода потребуется
еще 3 390 000 калорий.
В этой своеобразной иерархии сил нам
интересны сейчас силы химические, т. е.
силы, связывающие различные атомы в
молекулы. Многообразие этих связей
огромно: ведь всего из нескольких десятков
элементов построены миллионы химических
соединений. И число их непрерывно растет:
каждый час во всем мире синтезируют
десятки новых веществ.
С помощью квантовой механики в
принципе можно вычислить энергию связи
любой молекулы. В действительности, однако,
это очень трудная математическая задача,
которую пока удалось решить лишь для
простейших молекул. Но даже решение
этой задачи — только половина дела: для
нас гораздо важнее знать не сами связи, а
то, как они меняются в процессе реакций,
при добавлении примесей, при растворении
веществ и т. д. И хотя стало уже традицией
изображать молекулу в виде гантели, где
перекладина — связь между
гирями-атомами, гораздо точнее сравнивать ее с живой
клеткой, в которой протоплазму заменяет
электронное облако. Причем эта живая
плазма все время движется, колеблется и
чутко реагирует на все изменения
окружающей среды.
6
Чтобы уловить эти движения, придумано
множество способов — так много, что
сразу становится ясно: задача решена далеко
не полностью. Но как бы далеко ни ушла
физика в своем развитии, она никогда не
оставит попыток решить эту задачу и
всегда — с новыми идеями и новыми
приборами — будет возвращаться к ней. Ведь
молекула — это последний кирпичик
вещества, который еще сохраняет его свойства,
и интерес к ее жизни не может угаснуть,
пока существует наука.
Мы уже говорили, что все эти сложные
превращения происходят в области,
размеры которой 10~8 см.
КАК МЫ НАМЕРЕНЫ ПРОНИКНУТЬ В
НЕЕ НА ЭТОТ РАЗ И ЧТО МЫ ЗНАЕМ
СЕЙЧАС О НАШЕЙ «ИГЛЕ»— - -МЕЗОНЕ!
Прежде всего, это частица, которая живет
очень мало — 10 8 сек. Заряд ее равен
заряду электрона, а масса в 270 раз больше
электронной. У - -мезона есть
«двойник» — тг+ -мезон, который отличается от
него только знаком заряда. Кроме того,
существует нейтральный -°-мезон,
который живет всего лишь 10 16 сек, так как
сразу же после образования распадается на
два очень энергичных фотона — '{-кванта.
Получают мезоны при торможении в
мишенях протонов от ускорителей.
Электромагнитные свойства электрона и тг-мезона
вполне аналогичны. Поэтому как электрон,
встречая протон, образует атом, так и
- -мезон с протоном может образовать
мезоатом водорода. Этот тг -мезоатом очень
похож на обычный атом водорода, но
меньше него в 270 раз.
Второе и более важное отличие
мезоатома от обычного атома — чрезвычайно
малое время жизни: всего 10 ~15 сек.
Причина этого явления — так называемое
сильное взаимодействие, которое существует
между 7и-мезонами и протонами наряду с
электромагнитным. Это совершенно новое
взаимодействие: оно примерно в 100 раз
сильнее электромагнитного, а радиус его
действия равен примерно 10 1( см.
Заметим, кстати, что именно благодаря этим
силам существуют атомные ядра; поэтому
такие силы названы ядерными.
При сильном взаимодействии
?t~-мезона и протона образуются нейтрон и
-"-мезон, который, в свою очередь, тут же
распадается на два у-кванта:
71**+ р — > 7С°-|- П
71° ^> 2?
Хотя эта цепочка ядерных реакций
возможна и «на лету», т. е. при столкновении
тг" -мезона и протона, однако вероятность
такого события чрезвычайно мала.
Значительно более вероятна эта реакция из
промежуточного состояния ти-мезоатома.
На опыте все это происходит так:
полученный от ускорителя пучок - -мезонов
фокусируется и со скоростью, близкой к
скорости света, падает на водородную мишень.
Сталкиваясь с частицами мишени, т: -мезон
отдает им часть своей энергии и
постепенно замедляется. Наконец наступает момент,
когда он становится «спутником» протона,
т. е. образует с ним тг-мезоатом. Но,
чтобы произошла ядерная реакция, --мезону
необходимо еще потерять энергию, или,
как говорят физики, перейти из
возбужденного состояния мезоатома в основное,
Теперь, однако, мезон может терять энергию
только строго определенными порциями-
квантами до тех пор, пока не перейдет в
наинизшее устойчивое состояние
мезоатома. Впрочем, для --мезоатома эта
устойчивость эфемерна: уже через 10 1) сек
произойдет ядерная реакция перезарядки
~~ + Р-> 7С° г п. Поскольку образующийся
при этом тг° -мезон практически покоится,
то образовавшиеся при его распаде у
-кванты летят почти строго в противоположные^
стороны. Этот характерный «почерк»
реакции позволяет надежно выделять ее на
фоне других, похожих процессов.
Наглядно атом и процесс его девозбуж-
дения можно представить в виде воронки с
полочками, по которым скатывается вниз
тг- -мезон, пока не достигнет дна воронки.
При этом, чем выше полочка, т. е. чем
сильнее возбужден атом, тем больше и
размеры атома, и радиус воронки.
7
А как представить себе все явление в
целом!
Наверное, каждому из нас приходилось
бросать плоские камешки-голыши в пруд.
Теперь представьте себег что пруд это
водородная мишень, вместо кувшинок в
пруду плавают наши воронки, а мы
по-прежнему бросаем в него камешки. И при этом,
следуя известному совету Козьмы
Пруткова, смотрим на круги, ими образуемые.
Что же мы увидим! Вот сильно брошенный
камень коснулся поверхности воды и,
словно ожегшись, отпрыгнул, затем еще и еще.
Прыжки становятся все короче, постепенно
они сливаются в сплошную черту и наконец
камень исчезает под водой. Этот момент
как раз и соответствует переходу мезона в
связанное состояние --мезоатома.
Заглянем теперь под воду и проследим
дальнейшую судьбу нашего камешка. Мы увидим
там воронку, на одну из верхних полочек
которой попал камешек. Самопроизвольно,
а также при столкновениях и колебаниях
воронки, камешек «стряхивается» с
верхних уровней на нижние и наконец достигает
дна воронки. Здесь он замыкает
своеобразный контакт и через 10 15 сек происходит
ядерный взрыв. Это не преувеличение: при
реакции гс~ р -+ тг° -, щ rJ ->2^
выделяется 0,5-10 ~и калорий. Много это или мало!
Вы помните, что для разрыва химических
связей в 1 грамме воды нам потребовалось
12 200 калорий. Если же «прореагирует» 1 г
тг" -мезонов, то выделится огромная
энергия 0,2 • 10 u калорий — всего лишь в 10 раз
меньше, чем при взрыве первой атомной
бомбы.
На самом деле, конечно, водород в
мишени существует не в виде отдельных
атомов, а в виде молекул Н>. Но это лишь
немного изменит нашу картинку: просто
вместо отдельных воронок под водой будут
плавать сдвоенные.
При этом часть уровней-полочек по-
прежнему принадлежит отдельным атомам.
но другая часть будет принадлежат теперь
всей молекуле в целом. При падении
камешек вначале попадет в общую часть
сдвоенной воронки и только потом — в одну из
них. Однако на окончательный результат
ядерной реакции это повлиять не может.
А ЧТО ПРОИЗОЙДЕТ, ЕСЛИ ВМЕСТО
МИШЕНИ ИЗ ЧИСТОГО ВОДОРОДА МЫ
ВОЗЬМЕМ СМЕСЬ АТОМОВ! Например,
водорода и азота! Тогда в нашем пруду будут
плавать уже два типа воронок: поменьше,
соответствующие атому водорода, и
побольше— атомы азота.
Теперь, если камешек попадает в
маленькую воронку, мы по-прежнему увидим
характерный автограф ядерной реакции —
распад т?"->-2у . Но если он попадет в
большую воронку, мы этот процесс увидеть не
сможем. Почему! Ведь каждое ядро
состоит из протонов и нейтронов, и реакция
перезарядки на них по-прежнему возможна!
Да, конечно, но взрыв, который при этом
происходит, разрушает сложное ядро азота,
и на фоне его обломков невозможно
выделить реакцию распада тс° -мезона.
И последнее: атомы никогда не остаются
в покое, поэтому наши воронки, плавающие
в пруду, также непрерывно движутся,
беспорядочно сталкиваются, опрокидываются
и вновь расходятся. Как повлияет это
движение на падение наших камешков,
попавших вначале в маленькие воронки! Часть их
по-прежнему достигает дна. Но другая их
часть при столкновениях «пересыпается» в
большие воронки атомов азота и оттуда
уже не возвращается. Поэтому, если к
водороду добавлять азот, то число событий
распада 7и°->2у должно уменьшаться.
Опыт подтверждает это заключение.
8
Итак, теперь понятие о нашей «игле»
расширилось — это ядерная реакция с
очень характерным почерком и уникальной
избирательностью.
ЧЕМ ОНА МОЖЕТ БЫТЬ ПОЛЕЗНА И
КАК ЕЮ ПОЛЬЗОВАТЬСЯ!
Все большие и малые открытия
рождаются, в сущности, из детского
любопытства: «А что находится внутри той красивой
игрушки?» И как ребенок, ломая игрушку,
не задумывается над тем, что он будет
делать потом с грудой ржавых пружин, так и
физик, изучающий какое-либо явление, не
всегда знает заранее, где пригодится знание
многих деталей явления, на первый взгляд
незначительных.
В 1952 г. американский ученый В. Па-
нофский изучал свойства^" -мезонов и их
поведение в веществе. И вдруг он
обнаружил странное явление: реакция
перезарядки, которая очень хорошо шла в чистом
водороде, исчезала, если тот же водород
входил в состав химического соединения.
Приборы в то время были плохие, узнать
ничего больше об этом не удалось, а
главное, неясно было, что с этим делать. В 1960 г.
физики из Дубны В. Петрухин и Ю. Про-
кошкин построили новые, более
чувствительные приборы и вновь возвратились к
этой реакции. Оказалось, что она все-таки
идет, только очень-очень слабо. Удалось
даже установить закон этого ослабления.
Опишем коротко полученные ими
результаты.
Пусть у нас есть мишень из чистого
водорода, в которой содержится N молекул
Н2 (например, если взять 2 г водорода, то
N = 6,02 -1023 — числу Авогадро). Если
мы направим на мишень пучок тс -мезонов,
то наши приборы зарегистрируют за одну
секунду 7V0 событий распада к- -> 2 у. Теперь
вместо водорода возьмем такое
количество химического соединения Zm H„ , чтобы
в нем остановилось то же число п~
-мезонов, что и прежде в водороде (с
небольшими поправками для этого нужно взять
примерно те же 2 г вещества, например,
этилена С2Н4 или обыкновенной воды Н20).
Тогда при том же пучке тс -мезонов мы
зарегистрируем только Nt событий, причем:
где Z означает заряд ядра атома,
образующего соединение с водородом. Это —
очень сильное подавление реакции
перезарядки, например, для гидразина N2Hi
отношение Ni/N0 ^1/200. Подчеркнем, что
истинная причина такого подавления
кроется именно в том, что N2H4 —
химическое соединение. Действительно, если
взять эквивалентную механическую смесь
N2 + 2Н2, то отношение Ni/N0^1/7.
Вдумаемся в эти факты. Мы уже знаем,
что химические силы слабее ядерных
примерно в 100 раз и, кроме того, по
сравнению с ними «размазаны» по громадной
области. Как же эти слабые силы смогли так
сильно изменить ход ядерной реакции!
Хотя, конечно, с такими «странными»
явлениями нам приходилось встречаться и раньше:
ведь даже самая большая ракета взлетает,
если нажимают маленькую красную кнопку.
ГДЕ ЖЕ НАХОДИТСЯ КНОПКА,
КОТОРАЯ УПРАВЛЯЕТ НАШИМ ЯДЕРНЫМ
ВЗРЫВОМ!
Возвратимся для этого к нашему тихому
пруду и вновь станем бросать в него
камешки. Только пусть под водой теперь
плавают не такие симметричные воронки, как
на рисунке на стр. 8, а несимметричные,
такие, как на рисунке на стр. 10. Это
довольно хорошая модель бинарной, т. е.
состоящей из двух атомов молекулы,
например гидрида лития LiH. Для более
сложных молекул, например, воды Н20 или
этилена С2Н4 картинки отличаются только
большим числом воронок, соединенных
вместе. Однако и в этих системах всегда
будут уровни, принадлежащие всем
воронкам сразу. Проследим судьбу камешков
теперь. Как и прежде, ударяясь о
поверхность пруда, камешки постепенно теряют
энергию, пока не исчезнут под водой.
Дальнейшее почти очевидно: попадая в
широкую общую воронку, они вначале
задержатся там на полочках уровней, общих дпя
всей молекулы, а затем упадут в одну из
воронок— большую или маленькую. И,
конечно же, гораздо чаще камешки будут
падать в большую воронку, а не в
маленькую.. Но мы можем заметить только
камешки, попавшие в маленькую воронку,
так как только они, как мы знаем,
вызывают цепочку реакций к~ р ->тг | п, тг ^2^;*
А поскольку теперь таких камешков мало,
то на опыте это выглядит как резкое
подавление реакции перезарядки в химических
соединениях по сравнению с чистым водо-
9
родом. Несмотря на очевидную простоту
схемы, описанной здесь, она довольно
точно передает суть явления.
Физиков, конечно, такие простые
модели удовлетворить не могут: они потребуют
формулы и числа, которые в данном
случае дает только квантовая механика. Такие
расчеты действительно можно выполнить и
оценить ту долю к~ -мезонов, которая в
присутствии других атомов в молекуле по-
прежнему попадает на ядро водорода,
вызывая тем самым цепочку реакций
перезарядки и распада тг -мезона. Результаты
расчетов согласуются с экспериментом.
СТРАННОЕ, СТАВ ПОНЯТНЫМ, ДОЛГО
КАЖЕТСЯ УДИВИТЕЛЬНЫМ И ПОТОМУ
ВЫЗЫВАЕТ НЕДОВЕРИЕ, ПОКА НЕ
СТАНЕТ ПРИВЫЧНЫМ. Сейчас мы поняли
явление. А что это нам может дать! (Конечно,
кроме чистого удовольствия созерцать
истину, что уже немало.) Можно ли его
избрать орудием исследования строения
молекул? Ведь если ход ядерной реакции
зависит от вида химических связей, то
ло характеру нарушений ядерной
реакции можно судить о деталях строения
молекул.
В частности, этот эффект позволяет
надежно отличать связанный водород от
свободного, а для некоторых веществ,
содержащих водород, этот вопрос до сих пор не
решен окончательно. Об одном из таких
опытов, иллюстрирующих это различие для
гидразина и смеси азота с водородом, мы
уже рассказали.
Далее, эта ядерная реакция чувствует и
более тонкие различия в химическом
строении веществ. Возьмем, например, ацетилен
С Н. и этилен С2Н4 в таких количествах,
чтобы в них останавливалось равное число
т.~ -мезонов. Тогда, по закону ослабления.
число событий распада тг' ->2-f во втором
случае должно быть вдвое больше, чем в
первом. В действительности же оно
больше в 2,5 раза и это объясняется, конечно,
различным строением внешних электронных
оболочек у молекул С2Н2 и С2Н4.
В некоторых случаях важно знать,
например, как меняется структура химической
связи под влиянием катализаторов. Опыты,
устанавливающие это изменение, еще не
поставлены, но, возможно, явление, о
котором мы рассказали, поможет решить и
эту задачу.
Не будем сейчас фантазировать о
будущем « тг-мезонной химии». Хочется,
однако, обратить внимание на своеобразие
периода, который переживает сейчас физика
элементарных частиц: после длительного
накопления фактов об их свойствах и
строении ученые впервые задумались над
тем, как можно использовать уже
известные свойства.
История повторяется. Еще не все
забыли, какая тайна и даже мистика окружала
открытие рентгеновских лучей. Была и
паника, были и курьезы: одна парижская
газета, например, призывала модниц шить
свинцовые туалеты, ибо по Елисейским
полям бродят молодчики с аппаратами для
х-лучей. Затем началась демократизация
тайны и ныне «таинственные лучи смерти»
стерилизуют консервы и даже укорачивают
сроки изготовления вин.
■ Элементарные частицы постигла сходная
"судьба. В самом деле, четверть века на-
I зад даже само слово нейтрон было почти
I что запрещено произносить вслух вне стен
I секретных лабораторий. А теперь термин
(«нейтронография» столь же обычен, как и
рентгенография. Те же нейтроны
позволили создать новые химические реакции, с
помощью ;а -мезонов узнают константы
скоростей химических реакций, над
определением которых раньше бились годами; а
т: -мезоны, для которых 30 лет назад не I
придумали еще даже названия, сейчас при- |
меняют при лечении рака.
Здесь мы рассказали еще об одном
интересном и красивом явлении из области
«ядерной химии». Имеет ли оно будущее!
Придет время, и будущее само непременно
даст ответ на этот вопрос.
10
АТОМЫ И МЕЗОАТОМЫ
Любые, даже самые сложные идеи, можно
пересказать простыми словами. Но физика — это не
только идеи: кроме идей ей нужны числа и
формулы — без них она навсегда осталась бы
натурфилософией.
И если вас заинтересовала напечатанная здесь
статья и вы хотите чуть поглубже проникнуть в суть
описанных явлений, то без расчетов, хотя бы и
несложных, обойтись не удастся.
Что такое мезоатом и в чем его отличие от
обычного атома!
Атом — это система из ядра и нескольких
электронов.
Мезоатом — это система из ядра с зарядом Z и
отрицательного мезона с массой гп, который вокруг
ядра «вращается». Если это ~. -мезон, то образуется
--мезоатом Z~ . Если же система состоит из ядра
Z и \х -мезона, то говорят о i^-мезоатоме. Как и в
обычном атоме, энергия мезона в такой системе
не может быть произвольной. Она строго
определена на каждой орбите и меняется только
скачками.
Пронумеруем все уровни системы Z;j- (или Zt)
в порядке возрастания их энергии. (В статье, в
примере с воронками это соответствует нумерации
попочек снизу вверх, причем «дну» воронки
соответствует первый уровень п- 1). Тогда, согласно
квантовой механике, энергия уровня с номером п равна:
_ rnZ*
En — ~~ п2 М),
а радиус орбиты, которая соответствует этому
уровню
п2
Гп= mZ Г('
где Е0=2,2-10 и эргов, г0 = 5,3-10 J см, a m—масса
мезона, выраженная в электронных массах m (m -
е' fi
Статью Л. Пономарева «Мезонная химия —
возможно ли это?» комментирует
член-корреспондент АН СССР В. И. Гольданский
Ни один этап развития физики не проходил для
химии бесследно. Молекулярная физика, учения о
теплоте и электричестве привели к возникновению фи-
= 207т е; тп= 273т е; те= 1J. При n = Z энергия
мезоатома (независимо от заряда его ядра ZJ
равна:
Е = - шЕо,
а его размеры:
Z
г= m Г"-
(Именно поэтому в статье в схеме процессов
мезоатому азота соответствует в Z раз большие воронки,
чем мезоатому водорода).
Почему интересно изучать мезоатомы! До сих
пор мы подчеркивали сходство в строении атомов
и мезоатомов. Но новое о строении вещества мы
узнаем как раз благодаря их различиям.
Во-первых, мезоатомы очень малы: например,
размеры а -мезоатома водорода в основном
состоянии (Z—1; n —1J равны:
1
тх = 2?у7 г° ^=2,5-10 u см.
Такая малая нейтральная система подобно
нейтрону свободно блуждает в «электронных облаках»
атомов, близко подходит к их ядрам и таким
образом помогает изучать взаимодействие \х -мезонов
и -~ -мезонов с нуклонами, из которых состоят ядра.
А это чрезвычайно важно — в наши дни физики
озабочены именно этим: как понять природу и законы
взаимодействия элементарных частиц.
Кроме того, для многих тяжелых ядер радиус
орбиты Г] основного состояния и -мезоатома еще
меньше. Например, для свинца (Z = 82)
1
гх ^- ~2щ . 32~ г° ^ 5,8хЮ~13 ем.
Если вспомнить, что радиус ядра свинца равен
8,5 • 10~'3 см, то (как это ни невероятно) орбита
р.-мезона проходит внутри ядра свинца. Изучая
свойства такого мезоатома, удалось гораздо точнее, чем
иными методами, найти размеры и свойства ядер.
зической химии. В дальнейшем атомная физика и
электроника, будучи «экстраполированы» в химию,
легли в основу химической физики, в частности,
современной химической кинетики.
Уже на заре существования ядерной физики она
оказалась тесно связанной с химией — появилась
радиохимия, оказавшая неоценимую помощь физи-
химия атомных ядер
и элементарных частиц
11
кам-ядерщикам. Но и ядерная физика не осталась в
долгу перед химиками — достаточно вспомнить ра-
диоактивационный анализ, применение меченых
атомов, радиационную химию. Тем не менее долгое
время и процессы, происходящие в недрах атомного
ядра, и превращения элементарных частиц казались
отгороженными от химических свойств вещества
«китайской стеной». Кому не знакомо со школьных лет
утверждение, что радиоактивный распад ядер никак
не зависит от таких внешних условий, как
температура, давление, химический состав радиоактивных
препаратов!
Однако последние годы ученые все чаще
наблюдают и изучают явления, в которых решающим
образом сказывается связь и взаимное влияние
превращений атомных ядер или элементарных частиц —
позитронов, мю- и пи-мезонов — и электронного
строения окружающей среды, ее химических свойств.
На наших глазах происходит становление новой
области науки — ядерной химии, изучающей эту
связь, это влияние. Круг интересов ядерной химии
очень широк.
С одной стороны, это — влияние ядерных
процессов на строение электронных оболочек,
окружающих ядро, так называемые «химические последствия
ядерных превращений». Это — встряска, глубокая
перестройка оболочек при мгновенном изменении
заряда ядра (например, вследствие бета-распада),
образование «горячих» атомов с большой
кинетической энергией и последующие, подчас совершенно
необычные, химические реакции с их участием,
локальный кратковременный разогрев вещества вдоль
треков сильно ионизирующих частиц.
С другой стороны, это — влияние структуры
электронных оболочек на различные характеристики
распада ядер или гибели элементарных частиц. В
некоторых видах радиоактивного распада время жизни
атомных ядер хотя и слабо, но вполне измеримо
зависит от химических связей.
В № 8 опубликована статья Е. Ф. Макарова и
Ю. Ш. Мошковского «Локация молекул» об эффекте
Мессбауэра, на основе которого развивается гамма-
резонансная спектроскопия, нашедшая сейчас
широчайшие применения в самых разнообразных областях
химии.
Ждет исследователей и еще один очень
перспективный метод — изучение «возмущенных угловых
корреляций». Дело в том, что когда возбужденное
ядро излучает «каскад» из двух гамма-квантов или
бета-частицы и гамма-квантов, углы между
направлениями их вылета тоже должны зависеть от
строения электронных оболочек. Теория этого явления
опередила эксперимент. Приглашаем желающих
заняться этой проблемой!
В современной ядерной физике выделилась как
самостоятельный важнейший раздел физика
элементарных частиц. Аналогично и ядерная химия
получает сейчас свое развитие в своеобразной химии
элементарных частиц.
Интересные и неожиданные явления были
обнаружены в последнее время советскими физиками в
Дубне, изучавшими замедление и захват в веществе
отрицательных пи- и мю-м^зонов. Многое в этих
явлениях удалось успешно объяснить молодому
теоретику Л. И. Пономареву — автору статьи, которую вы
только что прочли. Думается, что продолжение «ме-
зохимических» экспериментов и развитие теории,
объясняющей их, приведут к важным успехам
ядерной химии, в частности, к созданию нового
метода изучения свойств водородной связи, вскроют
особенности «прилипания» электронов к
молекулам не только в газах, но и в жидкостях и
твердых телах, к новым иллюстрациям периодичности
свойств атомов в соответствии с законом Д. И.
Менделеева.
Будем надеяться, что ядерная химия еще не раз
расскажет о себе со страниц нашего журнала.
Вы узнали из этих статей о физическом методе исследования
химического строения веществ, который сейчас только зарождается.
В следующем номере журнала мы расскажем о физическом методе,
который уже вошел в химическую практику, и несмотря на молодость,
принес разнообразные и глубокие результаты — об электронном
парамагнитном резонансе — ЭПР.
НАШИ
В школьном учебнике химии написано, что соли
азотной кислоты отличают от солей других кислот ло
выделению двуокиси азота при нагревании соли с
концентрированной серной кислотой и медью.
Школьницу из Чувашии Галину Охтерову интересует, как
протекает эта реакция.
Реакция солей азотной кислоты (нитратов) с
концентрированной серной кислотой и металлической
медью — характерная качественная реакция,
открывающая присутствие этих солей. Однако
непосредственный продукт этой реакции — не двуокись, а окись
азота. Под действием кислорода воздуха окись
азота NO окисляется в дальнейшем до двуокиси азота
NO2. Вот как можно записать эти реакции:
2HN03 -I- 3H2S04 -;- ЗС11 -> 3CuS04 ^ 4Н20 г 2N0;
2N0 ;-02->2N02.
Как отличить этиловый спирт от метилового! Этот
вопрос задает читательница нашего журнала А. В. Уголь-
нова из Ульяновска.
Метиловый и этиловый спирты — представители
одного гомологического ряда одноатомных
алифатических первичных спиртов. Качественные реакции,
позволяющие различить эти вещества, сложны. Их
можно провести только в хорошо оборудованной
химической лаборатории.
Однако различить эти спирты можно и
физическими способами. Проще всего отличить этиловый
спирт от метилового можно по запаху. Но так как
запахи запомнить трудно, то нужно иметь эталонное
вещество — скажем, пузырек с этиловым спиртом.
Сравнивая запах неизвестного спирта с запахом
эталонного вещества, можно определить, с каким
спиртом имеешь дело. Впрочем, это удается не всем.
Второй, более надежный способ — определение
температуры кипения. Чистый метиловый спирт кипит
при температуре около 65° С, а температура кипения
чистого этилового спирта примерно 78е С. При
проведении опыта будьте осторожны: спирты легко
воспламеняются.
И еще одно ПРЕДУПРЕЖДЕНИЕ — тем, кто
заинтересовался бы распознаванием спиртов для
решения вопроса — «пить или воздержаться». Метиловый
спирт смертельно ядовит, а при анализе можно и
ошибиться. Впрочем, если даже есть уверенность в
том, что спирт — винный, тоже лучше
воздержаться...
И. Г. Петраков из Норильска пишет нам: «Я живу за
полярным кругом. Может быть, вам, москвичам, и
КОНСУЛЬТАЦИИ
забавно смотреть, как мороз иногда выводит узоры
на окнах. А у нас зима длится девять месяцев.
Очень бы хотелось, чтобы в моем доме и зимой
и летом были чистые прозрачные стекла. Не может
ли здесь помочь химия!»
Для ответов предоставляем слово кандидату
технических наук В. Ф. Чурилкиной.
В настоящее время у нас выпускается
специальный препарат «Антиобледенитель», который быстро
снимает лед с оконных стекол. Действие препарата
основано на том, что температура замерзания его
значительно ниже температуры замерзания воды.
Смазывая замерзшее стекло составом, у
которого температура замерзания минус 70° или минус
80°С, мы как бы «нагреваем» лед и он начинает
«таять».
При повышенной влажности в помещении влага
обычно конденсируется на холодных стеклах, стекло
«запотевает». Чтобы стекло не «запотевало», его
следует смазать жидкостью «ПК-10», очень тонким
слоем. При конденсации влаги на стекле, покрытом
слоем «ПК-10», влага впитывается в казеиновую
пленку и стекло в течение некоторого времени
остается прозрачным.
«Химический» способ борьбы с замерзанием
окон хорош, но обладает одним большим
недостатком: недолго действует, смазывание стекла нужно
часто повторять. Да и достать «Антиобледенитель»
нелегко.
Но при помощи физической химии можно с
успехом заставить сам мороз удалять свои узоры с окон!
Упругость водяного пара в воздухе очень резко
уменьшается с понижением температуры. Морозный
воздух очень сух. Воздух теплой комнаты —
влажный. Замерзнут окна в вашей комнате или нет,
зависит от того, какой воздух будет в межрамном
пространстве. Если стекла и рамы будут плохо
загерметизированы со стороны теплого жилья, — окна
замерзнут. Если же очень тщательно изолировать
внутренние рамы и добиться очень малого,
ничтожного воздухообмена с наружным воздухом, — окна
замерзать не будут. Сам мороз высушит всю влагу
со стекол.
В Норильске морозы очень сильны. Быть может,
потери тепла через окна у вас так велики, что
температура внутренних стекол падает ниже нуля и
узоры на стеклах образуются прямо в комнате. Тогда
нужно проверить, нет ли больших щелей в
наружных рамах, и устранить их. Если это не поможет —
тогда надо добавить третье стекло для улучшения
теплоизоляции.
13
ш
Q_
О
DC
о
I
ш
I-
<
ш
>
<
В нынешнем году высокого звания лауреата Ленинской премии удостоен
академик А. Н. Несмеянов. Эта награда присуждена ему за цикл работ в
области химии элементоорганических соединений.
Недавно у Александра Николаевича Несмеянова побывал корреспондент
«Химии и жизни» В. Батраков. Ниже приведена запись его разговора с
лауреатом.
— Александр Николаевич, расскажите,
пожалуйста, читателям «Химии и жизни» о себе.
— Так неолредепенно... это довольно сложно...
вы уж лучше задавайте вопросы.
— Это тоже довольно сложно. Ведь о работах,
за которые вы получили Ленинскую премию, уже
много писали... Впрочем: что, если вы расскажете
на этот раз не о том, что сделали, а о том, что
хотели бы сделать, но почему-либо не сделали?
— О, куда вы загнули! Это уж совсем не
годится. Я расскажу, а потом все будут смеяться.
— Тогда вот конкретный вопрос. Работы, за
которые вы получили Ленинскую премию, связаны
между собой единой научной логикой. Но вот
работы по созданию синтетической пищи (ваш доклад
об этом на IX Менделеевском съезде был
опубликован в № 7—8 нашего журнала за прошлый год)
воспринимаются как совершенно неожиданный
поворот в вашей научной деятельности; переход к
новой тематике кажется ничем внутренне не
оправданным, или, во всяком случае, непонятным. Не
могли бы вы объяснить, в чем тут дело?
— Это извольте. Дело в том, что я еще десяти
лет от роду пришел к твердому убеждению, что
убиение животных с целью употребления их в пищу
есть ничем не оправданные зверство и жестокость.
После этого я перестал есть мясо и до сих пор
твердо придерживаюсь и этих убеждений, и
вегетарианской диеты.
Это определило и мой первый научный интерес.
Еще когда я был дипломником, я пошеп к моему
учителю Николаю Дмитриевичу Зелинскому — он
тогда, в частности, занимался белками — и попросил
у него тему. Оказалась эта тема не очень
интересной. На диплом-то ее хватило, а дальше заниматься
явно не стоило. Вот тогда я и начал работать в
области элементоорганических соединений. Это было
в 1921 году.
Но все время я таил мысль когда-нибудь
заняться пищей. Я считал, что это мой долг. И, как видите,
теперь я этот Долг исполняю.
Прежде чем заняться этой работой, я провел
простые экономические расчеты, и они меня убедили в
том, что все совершенно реально. Идею сделать
искусственную пищу с восторгом восприняли не
только такие исправные вегетарианцы, как я. Хотя
подобная тематика была совершенно чуждой
Институту элементоорганических соединений, нашлась
группа энтузиастов, которая с жаром принялась за
дело.
В качестве первого объекта мы выбрали черную
икру. Это — и по экономическим соображениям, и
по чисто демонстрационным. Ведь надо было и
самим убедиться, и других убедить, что все это
действительно возможно.
И, как вы знаете, с задачей этой мы справились
вполне успешно. Сейчас мы учимся делать
белковые крупу и макароны, искусственное мясо, молоко.
...Вот видите, я по сути дела ответил сразу на все
ваши вопросы: рассказал и о себе, и о том, что
хотел сделать, но почему-либо не делал. Л вот сейчас
все-таки делаю.
— Спасибо за подробный ответ. Но мне
приходится задать еще один вопрос. Судя по вашему
рассказу, искусственной пищей вы занялись только
потому, что, попросту говоря, нашли, наконец, время
ею заняться. Но «со стороны» это выглядело так,
будто химию элементоорганических соединений вы
сочли уже законченным этапом вашей деятельности.
Ведь если говорить о «чистой» органической химии,
то можно, наверное, сказать, что она себя в
значительной мере уже исчерпала: работы Нобелевского
лауреата Роберта Вудворда показали, что сейчас
химик-органик в принципе способен синтезировать
любую структуру. А в таких случаях (если
проводить параллель с другими областями знания)
исследователи обычно «оставляют» теорию, занимаясь,
в основном, практическим прилржением уже
накопленного материала.
— Во-первых, синтетической пищей я занялся не
потому, что сейчас мне нечего стало делать, а
потому, что только сейчас химическая наука и
химическая промышленность достигли такого уровня, что
этим стало целесообразно заниматься. А, во-вторых,
у вас слишком мрачный и, в общем-то, совершенно
неверный взгляд на будущее органической химии.
Вудворд действительно доказал, что
современному органику под силу синтезировать любую струк-
15
туру. Но это можно сказать только о тех структурах,
о которых знаешь, что они могут существовать. Тот
же Вудворд, например, расшифровал структуру
ферроцена, но не предвидел ее. Л сейчас что ни
день, то сообщения о новых, чертовски интересных
типах веществ, о совершенно неожиданных
структурах.
В органической химии начался тот же процесс,
который недавно происходил в биологии. Когда-то
биология была наукой чисто описательной. Но
потом в нее стали проникать химия, физика,
математика. В результате, хотя описательная биология и
осталась существовать, она ушла на второй план, а
«а первом месте оказалась молекулярная биология,
изучающая процессы, происходящие в глубине
клетки.
В органическую химию тоже все глубже и
глубже проникают и физика, и математика; все шире
используются квантовомеханические представления.
Да и внутри самой химии происходит интересный
процесс слияния ее различных областей: например,
процесс слияния органической и неорганической
химии. Последнее стало возможным именно
благодаря исследованиям эпементоорганических
соединений — этого моста между органикой и
неорганикой-
Так что все дело в том, что органическая химия
все время меняется — и это должны понимать все,
кто ею занимается, — но она остается
интереснейшей наукой.
— Спасибо за беседу, Александр Николаевич.
Редакция желает вам всего доброго, до свиданья!
ТЕХНОЛОГИ, ВНИМАНИЕ! -
ИНЕРТНЫЙ ГАЗ В ФОРМЕ
Пластики формуются достаточно
быстро, но даже незначительное
ускорение процесса сулит
немалую экономию. Если повысить
температуру материала, то
готовое изделие можно получить
быстрее, но, к сожалению,
перегревать пластики нельзя. Под
действием кислорода воздуха
начинается термоокислительная
деструкция, и материал разрушается.
Недавно была предложена
система нагрева формы для
пластиков инертным газом. В данном
случае инертность — это просто
отсутствие взаимодействия газа с
материалом. В этом смысле
инертными являются и углекислый газ,
и азот. Один из этих газов по
специальной системе накачивается в
форму, вытесняя из нее воздух.
Газ, разумеется, предварительно
нагревают. Когда форму нужно
охладить, газ выпускают, а в
форму накачивают холодный воздух.
Если нужно ускорить охлаждение,
то по тем же каналам можно
подать в форму холодную воду.
(«Plastics», 1966, № 343)
ИОД—ТОЖЕ СМАЗКА
Круг материалов, которые
используются как смазки, все время
расширяется. Иод теперь — тоже
смазка. Всего 0,6% иода нужно
добавить к углеводородному
маслу, чтобы подшипники из
нержавеющей стали и титана работали
без заедания.
Как же объясняется влияние
иода на трение! Иод реагирует с
железом и титаном, и при этом
образуются дииодиды. Их кри-
сталпическая структура —
слоистая, как у графита. Под
нагрузкой эти слои скользят друг
относительно друга. Интересно, что в
масло вводится не дииодид, а иод.
Соль же образуется в процессе
работы.
И все же добавлять в масло
иод не так просто. Иод очень
мало растворим в масле, и
растворы не обладают необходимым
комплексом свойств. Свойства
смазки намного улучшаются, если
использовать некоторые
органические соединения иода,
например, пара-иодбутилбензол.
Добавка таких соединений позволяет
увеличить нагрузку на трущиеся
детали больше чем в пятьдесят
раз по сравнению со смазкой без
иода.
{«Chemical Engineering»,
[966, JVs 2)
МЕТАЛЛ В ПЛАСТМАССЕ
Очень многие пластмассовые
изделия имеют металлические
детали. Металлическую арматуру
заранее устанавливают в форме,
которую заполняют пластмассой;
при съеме изделия они остаются
в пластмассе.
Этот традиционный и
испытанный способ — не единственный.
Недавно предложена технология,
по которой металл внедряется в
пластмассу с помощью
ультразвука. По новой технологии
ультразвуковые волны передаются
через пластик к поверхности
металла. В результате вибрации
поверхность пластмассовой детали в
месте контакта с металлом
расплавляется, и вкладыш легко
входит в соответствующее гнездо
детали. Время такой операции очень
невелико — одной секунды
достаточно, чтобы вставить в деталь
металлическую резьбовую втулку.
(<<Chemieal and Engineering
News», 1966, № 15)
СКОЛЬКО ЯДА В ГАЗАХ!
Вода — каталитический яд для
многих процессов. Синтез
аммиака из азота и водорода,
полимеризация этилена и некоторые
другие важные промышленные
процессы должны проходить
практически при полном
отсутствии воды. Реагирующие газы
необходимо анализировать —
определять их влажность.
Оригинальный и сравнительно
простой способ определения
воды в углеводородных газах
описан в журнале «Заводская
лаборатория». Анализ делается
электрометрическим способом с
применением реактива Фишера.
Разработана модель прибора, схема
которого помещена в журнале.
Чтобы избежать влияния
атмосферной влаги, прибор должен
быть полностью герметизирован.
Вода, содержащаяся в газах,
растворяется в метаноле, и затем I
определяется ее концентрация
в растворе.
(«Заводская лаборатория»,
1966, № 6)
16
Монумент в честь покорителей космоса,
фотографию которого вы увидите на
следующей странице, воздвигнут в Москве
два года назад. Почти семь лет
A958—1964 гг.) ушло на проектирование и
сооружение этого обелиска. Авторам
пришлось решать не только
архитектурно-художественные, но и технические задачи.
Первой из них был выбор материалов, в том
числе и облицовочных. После долгих
экспериментов остановились на отполированных
до блеска титановых листах.
Действительно, по многим
характеристикам, и прежде всего по коррозионной
стойкости, титан превосходит подавляющее
большинство металлов и сплавов. Иногда
(особенно в популярной литературе) титан
называют вечным металлом. Но расскажем
сначала об истории этого элемента.
ОКИСЕЛ ИЛИ НЕ ОКИСЕЛ!
До 1795 года элемент № 22 назывался
«менакином». Так назвал его в 1791 году
английский химик и минералог Вильям Гре-
гор, открывший новый элемент в минерале
менаканите. (Не ищите это название в
современных минералогических
справочниках— менаканит тоже переименован, сейчас
он называется ильменитом).
ТИТАН
Инженеры Я. РОЗЕНЦВЕИГ и С. ВЕНЕЦКИИ
Рисунок Д. ПЕТРОВА
Спустя четыре года после открытия Гре-
гора немецкий химик Мартин Клапрот
обнаружил новый химический элемент в другом
минерале — рутиле и в честь царицы
эльфов Титании (германская мифология)
назвал его титаном. По другой версии
название элемента происходит от титанов —
могучих сыновей богини земли — Геи
(греческая мифология).
В 1797 году выяснилось, что Грегор и
Клапрот открыли один и тот же элемент/
и хотя Грегор сделал это раньше, за новым
элементом утвердилось имя, данное ему
Клапротом.
Но ни Грегору, ни Клапроту не удалось
получить элементарный титан. Выделенный
ими белый кристаллический порошок был
двуокисью титана ТЮг- Восстановить этот
окисел, выделить из него чистый металл
долгое время не удавалось никому из
химиков.
В 1823 году английский ученый У. Вол-
ластон сообщил, что кристаллы,
обнаруженные им в металлургических шлаках завода
«Мертир-Тидвиль», — не что иное, как
чистый титан. А спустя 33 года известный
немецкий химик Ф. Велер доказал, что и эти
кристаллы были опять-таки соединением
титана, на этот раз — металлоподобным
карбонитридом.
2 Химия и Жизнь, № 10
17
Много лет считалось, что металлический
титан впервые был получен знаменитым
шведским ученым Пенсом Якобом Берце-
лиусом в 1825 году. Берцелиус
восстанавливал фтортитанат калия металлическим
натрием. Однако сегодня, сравнивая свойства
титана и продукта, полученного Берцелиу-
сом, можно утверждать, что президент
Шведской Академии наук ошибался, ибо
чистый титан быстро растворяется в
плавиковой кислоте (в отличие от многих других
кислот), а металлический титан Берцелиуса
успешно сопротивлялся ее действию.
В действительности, титан был впервые
получен в 1875 году русским ученым
Д. К. Кирилловым. Результаты этой работы
опубликованы в его брошюре
«Исследования над титаном». Но работа
малоизвестного русского ученого осталась
незамеченной. Еще через 12 лет довольно чистый
продукт — около 95 % титана — получили
соотечественники Берцелиуса, известные
химики Л. Нильсон и О. Петерсон,
восстанавливавшие четыреххлористый титан
металлическим натрием в стальной герметической
бомбе.
В 1895 г. французский химик А. Муассан,
восстанавливая двуокись титана углеродом
в дуговой печи и подвергая полученный
материал двукратному рафинированию,
получил титан, содержавший всего 2%
примесей, в основном углерода. Наконец, в
1910 году американский химик М. Хантер,
усовершенствовав способ Нильсона и Пе-
терсона, сумел получить несколько
граммов титана чистотой около 99%- Именно
поэтому в большинстве книг приоритет
получения металлического титана
приписывается Хантеру, а не Кириллову, Нильсону
или Муассану.
Однако ни Хантер, ни его современники
не предсказывали титану большого
будущего. Всего несколько десятых процента
примесей содержалось в металле, но эти
примеси делали титан хрупким, непрочным,
непригодным к механической обработке.
Поэтому некоторые соединения титана
нашли применение раньше, чем сам металл.
Четыреххлористый титан, например, широко
использовали в первую мировую войну для
создания дымовых завес.
М
Монумент в честь покорителей космоса,
облицованный листами титана
ПРОФЕССИИ ДВУОКИСИ
В 1908 году в США и Норвегии началось
изготовление белил не из соединений
свинца и цинка, как делалось прежде, а из
двуокиси титана. Такими белилами можно
окрасить в несколько раз большую поверхность,
чем тем же количеством свинцовых или
цинковых белил. К тому же, у титановых
белил больше отражательная способность,
они не ядовиты и не темнеют под действием
сероводорода. В медицинской литературе
описан случай, когда человек за один раз
«принял» 460 граммов двуокиси титана!
(Интересно, с чем он ее спутал?)
«Любитель» двуокиси титана не испытал при этом
никаких болезненных ощущений.
Двуокись титана входит в состав
некоторых медицинских препаратов, в частности,
мазей против кожных заболеваний.
Однако не медицина, а лакокрасочная
промышленность потребляет наибольшие
количества ТЮг- Мировое производство
этого соединения намного превысило
полмиллиона тонн в год. Эмали на основе
двуокиси титана широко используют в качестве
защитных и декоративных покрытий по
металлу и дереву в судостроении,
строительстве и машиностроении. Срок службы
сооружений и деталей при этом значительно
повышается. Титановыми белилами
окрашивают ткани, кожу и другие материалы.
Двуокись титана входит в состав
фарфоровых масс, тугоплавких стекол,
керамических материалов с высокой диэлектрической
проницаемостью. Как наполнитель,
повышающий прочность и термостойкость, ее
вводят в резиновые смеси. Однако все
достоинства соединений титана кажутся
несущественными на фоне уникальных свойств
чистого металлического титана.
ЭЛЕМЕНТАРНЫЙ ТИТАН
В 1925 году голландские ученые ван
Аркель и де Бур иодидным способом
(о нем — ниже) получили титан высокой
степени чистоты — 99,9%. В отличие от
титана, полученного Хантером, он обладал
пластичностью: его можно было ковать на
холоде, прокатывать в листы, ленту,
проволоку и даже тончайшую фольгу. Но даже
не это главное. Исследования
физико-химических свойств металлического титана
приводили к почти фантастическим результа-
2*
19
*r ^
<*&%$&&**r:
£
>£*
.*+$
Усть-Каменогорский титано-магниевый комбинат. Получена титановая губка
там. Оказалось, например, что титан,
будучи почти вдвое легче железа (плотность
титана 4,5 г/см3), по прочности превосходит
многие стали. Сравнение с алюминием
тоже оказалось в пользу титана: титан всего
в полтора раза тяжелее алюминия, но зато
в шесть раз прочнее, и что особенно
важно— он сохраняет свою прочность при
температурах до 500°С (а при добавке
легирующих элементов — до 650°С), в то
время как прочность алюминиевых и магниевых
сплавов резко падает уже при 300СС.
Титан обладает и значительной
твердостью: он в 12 раз тверже алюминия, в
4 раза — железа и меди. Еще одна важная
характеристика металла — предел
текучести. Чем он выше, тем лучше детали из
этого металла сопротивляются
эксплуатационным нагрузкам, тем дольше они
сохраняют свои формы и размеры. Предел
текучести у титана почти в 18 раз выше, чем у
алюминия, почти в 4 раза выше, чем у меди,
и в два с половиной раза выше, чем у
железа.
В отличие от большинства металлов,
титан обладает значительным
электросопротивлением: если электропроводность
серебра принять за 100, то
электропроводность меди равна 94, алюминия 55, железа
и ртути 2, а титана — всего 0,3. Вряд ли
нужно объяснять, что это свойство, как и
немагнитность титана, представляет
интерес для радиоэлектроники и
электротехники.
Замечательна устойчивость титана
против коррозии. На пластинке из этого
металла за 10 лет пребывания в морской воде не
появилось и следов коррозии. За такой
срок от железной пластинки остались бы
одни воспоминания. Поэтому не случаен
интерес к титану авиаконструкторов,
судостроителей и гидростроителей.
КАК ПОЛУЧАЮТ ТИТАН
Цена — вот что сегодня еще тормозит
производство и потребление титана.
Собственно, высокая стоимость— не
врожденный порок титана. В земной коре его
немало — 0,61%. Дорогая цена — следствие
20
Дробление титановой губки
чрезвычайной сложности извлечения
титана из руд- Если принять стоимость титана в
концентрате за единицу, то стоимость
готовой продукции — титанового листа —
выразится цифрами 500—600. Объясняется
это высоким сродством титана ко многим
элементам и прочностью химических
связей в его природных соединениях.
Отсюда — сложности технологии.
Электролитическое разложение
двуокиси титана — процесс еще не освоенный
промышленностью, а восстановить ее
углеродом можно только в вакууме при
температуре около 3000°С. Поэтому получение
металлического титана идет пока
«окольными путями». Вот как выглядит магниетер-
мический способ промышленного
производства титана, разработанный в 1940 году
американским ученым У. Кролем.
Двуокись титана с помощью хлора (в
присутствии углерода) переводят в четы-
реххлористый титан:
ТЮ2 + С -;- 2С1а - TiGl4 | С02.
Процесс идет в шахтных электропечах при
температуре 800—1250°С. Другой
вариант — хлорирование в расплаве солей
щелочных металлов: NaCl и КС1.
Следующая операция (в одинаковой
мере важная и трудоемкая) — очистка
ЛСЦ от примесей — проводится разными
способами и веществами. Четыреххлори-
стый титан в обычных условиях
представляет собой жидкость с температурой
кипения 136°С
Разорвать связь титана с хлором легче,
чем с кислородом. Это можно сделать с
помощью магния по реакции:
TiCl4 2Mg - Ti + 2MgCl2.
Эта реакция идет в стальных реакторах при
температуре 900°С В результате
образуется так называемая титановая губка,
пропитанная магнием и хлоридом магния. Их
испаряют в герметичном вакуумном аппарате
при 950СС, а титановую губку затем
спекают или переплавляют в компактный металл.
Натриетермический метод получения
металлического титана, в принципе, мало
чем отличается от магниетермического.
Эти два метода наиболее широко
применяются в промышленности.
Для получения более чистого титана и
поныне используется иодидный метод,
предложенный ван Аркелем и де Буром.
Металлотермический губчатый титан
превращают в иодид (TiJ/J, который затем
возгоняют в вакууме. На своем пути пары
иодида титана встречают раскаленную до
1400°С титановую проволоку. При этом
иодид разлагается и на проволоке
нарастает слой чистого титана. Этот метод
производства титана малопроизводителен и
дорог, поэтому в промышленности он
применяется крайне ограниченно.
Несмотря на трудоемкость и
энергоемкость производства титана, оно уже сейчас
становится одной из важнейших отраслей
металлургии. Если в 1947 году в США было
получено всего 2 тонны этого металла, то
через пятнадцать лет — более 350 000 тонн.
Двадцать лет назад титан называли редким
металлом — сейчас он важнейший
конструкционный материал. Объясняется это
только одним: редким сочетанием
полезных свойств элемента № 22. И, естественно,
потребностями техники.
ТИТАН РАБОТАЕТ
Два года назад в зарубежной печати
появилось сообщение о создании в США
21
сверхзвукового реактивного самолета,
способного развивать скорость свыше 3200
километров в час; дальность полета —
свыше шести тысяч километров, потолок —
23 км. Сообщалось, что корпус этой
машины изготовлен из титана.
Не только корпус, но и другие детали —
от двигателя до болтов и гаек — все чаще
изготовляют из титана. Кстати, о болтах.
По мнению зарубежных специалистов,
замена стальных болтов титановыми в
двигателях самолетов-истребителей, снизит вес
каждого двигателя примерно на сто
килограммов. Уменьшение веса двигателя
повлечет за собой значительное облегчение
фюзеляжа, и общий выигрыш в весе
самолета составит почти тонну. Это даст в
конечном счете, большую экономию:
известно, что уменьшение веса самолета
гражданской авиации всего на один килограмм
экономит до 400 рублей в год.
Несмотря на то, что титан еще очень
дорог, замена им более дешевых материалов
во многих случаях оказывается
экономически выгодной. Вот характерный пример.
Корпус химического аппарата,
изготовленный из нержавеющей стали, стоит 150
рублей, а из титанового сплава — 600 рублей.
Но при этом стальной реактор служит лишь
шесть месяцев, а титановый — 10 лет. Лри-
бавьте затраты на замену стальных
реакторов, вынужденные простои оборудования —
и станет очевидно, что применять
дорогостоящий титан бывает выгоднее, чем
сталь.
Значительные количества титана
использует металлургия. Существуют сотни марок
сталей и других сплавов, в состав которых
титан входит как легирующая добавка. Его
вводят для улучшения структуры металла,
увеличения прочности и антикоррозионной
стойкости.
Высокая коррозионная стойкость титана
объясняется не строением атома, а
образованием на его поверхности окисной
пленки TiC>2.
Титан часто называют металлом буду^
щего. Факты, которыми уже сейчас
располагают наука и техника, убеждают, что это
не просто слова.
ТОЛЬКО ФАКТЫ
ТИТАН —
НЕ РЕДКИЙ
МЕТАЛЛ
До последнего времени титан
совершенно необоснованно
относили к редким металлам. В
действительности же лишь три
металла — алюминий, железо и
магний — распространены в природе
больше, чем титан. Количество
титана в земной коре в несколько
раз превышает запасы медиг
цинка, свинца, золота, серебра,
платины, хрома, вольфрама, ртути,
молибдена, висмута, сурьмы,
никеля и олова, вместе взятых.
МИНЕРАЛЫ
ТИТАНА
Известно около 70 минералов
титана, в которых он находится в
виде двуокиси или солей титановой
кислоты. Наибольшее
практическое значение имеют ильменит,
рутил, перовскит и сфен.
Ильменит — метатитанат
железа FeTiOa — содержит 52,65%
Ti02. Название этого минерала
связано с тем, что он был найден
на Урале в Ильменских горах.
Крупнейшие россыпи ильменито-
вых песков имеются в Индии.
Другой важнейший минерал — рутил
представляет собой двуокись
титана ТЮ> Промышленное
значение имеют также титаномагнети-
ты — механическая смесь
ильменита с минералами железа.
Богатые месторождения титановых
руд есть в СССР, США, Индии,
Норвегии, Канаде, Австралии и
других странах.
Всего на земном шаре
известно более 150 значительных
рудных и россыпных
месторождений титана.
В ЖИВЫХ ОРГАНИЗМАХ
В человеческом организме
содержится до 20 миллиграммов
титана. Больше всего титана в
селезенке, надпочечниках и
щитовидной железе. В этих органах
содержание элемента № 22 с
возрастом не изменяется, но в
легких за 65 пет жизни оно
возрастает более чем в 100 раз.
Из представителей флоры
богата титаном водоросль
кладофора: содержание в ней этого
элемента превышает 0,03%.
...И НА СОЛНЦЕ
Спектральным анализом титан
обнаружен на Солнце и в составе
некоторых звездных атмосфер,
где он, кстати, преобладает над
большинством элементов. Но если
на земле титан существует глав-
99
ным образом в виде двуокиси
(TiO:), то в космосе, очевидно, в
виде моноокиси [TiO].
ПЬЕЗОЭЛЕКТРИК
Титанат бария, будучи
наэлектризован, проявляет высокие
пьезоэлектрические свойства, то есть
может превращать механическую
энергию сжатия или расширения
ИЗ ТИТАНА:
...АППАРАТ
кристалла в электрическую. Пье-
зокристаллы титаната бария по
многим характеристикам
превосходят такие распространенные
пьезоэлектрики, как кварц и сег-
нетова соль |С1НО( KNa ■ 4Н20].
ТИТАН И РАКЕТЫ
Титан используется для
производства баллонов, в которых газы
могут храниться длительное время
под большим давлением. В
американских ракетах типа «Атлас»
сферические резервуары для
хранения сжатого гелия сделаны из
титана.
Из титановых сплавов
изготовляют баки для жидкого
кислорода, применяемые в ракетных
двигателях
На снимке — хорошо знакомый каждому химику кожухо-труб-
«ый теплообменник. Он сделан из биметалла сталь — титан,
изготовленного методом прокатки в вакууме. Трубы такого
теплообменника выдерживают действие агрессивных жидкостей,
нагретых до 300°С даже под давлением до 50 атмосфер.
...АРМАТУРА
При электролитическом рафинировании никеля коррозия не
только разрушает арматуру, но и служит причиной загрязнения
готового продукта — получить чистый никель не удается. Нэ
одном из заводов вентили из нержавеющей стали были
заменены титановыми — и тогда удалось добиться необходимой
чистоты готового никеля.
...ДЕТАЛИ
А на этих трех снимках — детали, работавшие в соляной кислоте.
Справа -— кислотоупорный чугун после 200 часов работы. Не
лучше выглядит и нержавеющая сталь (левое фото]; через
300 часов она превратилась буквально в обломки. Между
ними — титановая деталь. Фото сделано после того, как она
проработала в кислоте 8 000 (восемь тысяч!) часов.
химия
Химия и рыба! Что может быть между
ними общего? В недалеком прошлом такое
сочетание могло показаться весьма
странным. Однако в наш век взаимосвязь
между химией и многими отдаленными от нее,
на первый взгляд, областями жизни и
народного хозяйства становится все более и
более близкой и разносторонней.
Химия оказывает большое влияние на
развитие рыбного хозяйства нашей
страны. Многие продукты, получаемые
химическим путем, — например, известь,
азотнокислый аммоний, суперфосфат —
применяют для удобрения рыбохозяйственных
водоемов. В обогащенных ими водах
создаются благоприятные условия для
жизнедеятельности низших организмов,
которые служат пищей для рыб, и
рыбопродуктивность водоемов возрастает.
Различные химические вещества, вплоть до
витаминов, используются в качестве добавок к
пищевому рациону рыб и для лечения их
болезней. Существуют даже химические
способы «прополки» водоемов,
предназначенных для разведения ценных видов рыб.
В Государственном
научно-исследовательском институте озерного и речного рыбного
И РЫБА
хозяйства (ГосНИОРХ) разработан и начал
применяться метод уничтожения
ненужных рыб (их так и называют — сорными:
это окунь, плотва и другая рыбная мелочь)
с помощью полихлорпирена. В озере,
обработанном этим сильным ядом, можно уже
через 2 года разводить ценные породы рыб,
не опасаясь конкуренции со стороны рыб
ненужных.
Но на химических предприятиях,
производящих важные, нужные химические
продукты, образуются также и вредные
отходы, отработанные сточные воды,
которые сбрасываются в реки и озера и
сильно их загрязняют.
В зависимости от характера
производства, совершенства его технологии и
степени очистки и обезвреживания сточных
вод, в их составе могут находиться
кислоты, щелочи, соли, металлы, фенолы и их
производные, аммиак, сероводород,
галогены, фосфорорганические соединения,
красители, смолы и многие другие
органические и неорганические, растворимые и
нерастворимые вещества.
Влияние этих загрязнителей на
водоемы и живущие в них организмы весьма
разнообразно. Нерастворимые и плохо
растворимые минеральные вещества (гипс,
известняк, некоторые окислы металлов и
др.) образуют донные отложения, которые
мешают развитию корневой системы
водных растений и уничтожают живущих на
дне животных (бентос), которые служат
пищей для рыб. Мелкие взвешенные
частицы этих веществ засоряют рыбам
жабры, что вызывает различные заболевания
дыхательных путей, а также наносят
механические повреждения рыбам и
кормовым беспозвоночным.
Нерастворимые органические вещества
также образуют донные отложения и столь
же отрицательно влияют на условия
жизни в водоемах. Кроме того, в результате
жизнедеятельности микроорганизмов они
разлагаются, образуя различные ядовитые
газы (сероводород, метан, аммиак и др.).
Это ухудшает качество воды, вредно
действует на водные организмы. Кроме того,
окисляясь, эти газы поглощают
растворенный в воде кислород, необходимый для
дыхания рыб.
Особенно большое количество
кислорода поглощают из воды легко окисляемые
органические загрязнители сточных вод.
Сток их в реки и озера нередко приводит
к возникновению в воде кислородного
дефицита и к замору — массовой гибели рыб
и других водных организмов.
Различные загрязнители, поступая со ^
сточными водами в водоем, могут изме-
нять кислотность воды, ее солевой состав,
жесткость, окисляемость, запах, вкус, цвет, ^
прозрачность. В итоге происходит корен- го
ное изменение гидрохимического режима 5
реки или озера. ж
Многие вещества, содержащиеся в зс
сточных водах предприятий химической [
промышленности, ядовиты и оказывают те
прямое токсическое воздействие на рыб и 5
другие водные организмы. Например, рас- ^
творенный в воде активный хлор смерте- Я
лен для рыб уже при концентрации, пре- ^
вышающей 0,1 мг на литр. Рыбы гибнут в
воде, содержащей более 0,3 мг/л смолис- ф
25
тых веществ, свыше 10—25 мг/л фенолов.
Ядовит для рыб и сероводород, а также
его соли. Кроме того, они оказывают еще
и косвенное отрицательное влияние:
окисляясь, они поглощают из воды кислород
и, таким образом, способствуют созданию
в водоеме кислородного дефицита.
Вообще говоря, понятие о токсичности
химических соединений весьма условно.
Например, сочетание различных веществ
может оказаться вреднее, чем каждое из
них в отдельности. Токсичность фенола
сильно возрастает в присутствии крезола.
Фенол и хлор по отдельности меньше
портят воду, чем при совместном присутствии,
так как в последнем случае образуются
хлорфенолы, обладающие сильным
неприятным запахом. Токсичность тех или иных
загрязнителей может также сильно
изменяться в зависимости от температуры.
Обычно при повышении температуры их
действие усиливается.
Вредное действие загрязнителей
иногда проявляется не прямо на живых
организмах, а на их потомстве. Например,
служащие хорошим кормом для рыб рачки
дафнии живут в слабых растворах солей
некоторых тяжелых металлов, но в
третьем поколении они становятся бесплодными.
Некоторые загрязнители сточных вод
предприятий химической промышленности
влияют на водные организмы постепенно,
при длительном воздействии, вызывая
различные нежелательные изменения в
живых тканях, которые в итоге приводят
к гибели организмов. Например,
содержание в воде фурфурола в количестве
5—10 мг/л в течение первых нескольких
месяцев как будто не вредит рыбам.
Наоборот, в таких растворах они очень
активны, хорошо поедают корм и прибавляют в
весе. Однако впоследствии рыбы
начинают гибнуть, и при вскрытии в их
жабрах и печени обнаруживаются
кровоизлияния.
Токсическое влияние на организм
могут оказывать и такие вещества, которые
принято считать неядовитыми, если они
действуют продолжительное время или в
больших количествах. Например, обычная
поваренная соль в малых концентрациях
не вредит рыбам, несколько повышенные
концентрации ее вызывают у рыб
депрессию, а высокие — гибель. Икра некоторых
рыб хорошо развивается в слабо
солоноватых водах, повышение же концентрации
поваренной соли ведет к гибели икры.
Некоторые вещества, содержащиеся в
сточных водах предприятий химической
промышленности, могут постепенно
накапливаться в теле рыо и других водных
организмов, что в конце концов приводит
к их гибели или к порче вкусовых качеств
рыбы. К таким веществам, в частности,
относятся различные ядохимикаты для
борьбы с вредными насекомыми,
сорняками и т. д. Попадают они в водоемы со
сточными водами заводов по производству
ядохимикатов. Кроме того, ядохимикаты,
которыми обрабатывали поля, леса и луга,
могут быть смыты в реки или озера. Все
подобные вещества в той или иной
степени токсичны для живых организмов,
способны в них накапливаться и оказывают
сильное отрицательное влияние на
физико-химические свойства воды. Многие
гербициды имеют стойкий неприятный
запах, который они придают воде и
водным организмам.
Загрязнение рек и озер сточными
водами химических предприятий часто
приводит к подрыву и даже к уничтожению
рыбных запасов.
Исследованиями ГосНИОРХ
установлено, например, что река Ока в нижнем
своем течении практически потеряла
всякое рыбохозяйственное значение. Причина
этого — сброс в нее большого количества
плохо очищенных сточных вод химических
предприятий. Ежесуточно в Оку с этими
стоками поступает около 490 т
минеральных и 60 т органических веществ. Верхние
участки Оки также сильно загрязнены
различными сточными водами, в том числе
и стоками предприятий химической
промышленности. В результате в Оке
ежегодно наблюдается гибель рыбы и порча
ее товарных качеств. По данным
Центрального управления по охране и
воспроизводству рыбных запасов, запасы
леща в реке к 1963 г. сократились по
сравнению с 1959 г. более чем вдвое, судака —
в 5 раз, щуки — в 22 раза, стерлядь и сом
почти исчезли из уловов...
До последнего времени очень сильно
загрязнялась стоками химических
предприятий река Кама на участке от
Соликамска до Перми. Рыба здесь
систематически болела и гибла. Практически рыбные
запасы в реке были почти уничтожены:
2G
максимальные уловы не превышали
800 центнеров в год.
После того, как было построено
Камское водохранилище и улучшена очистка
сточных вод предприятий Соликамска и
Березников, загрязнение значительно
снизилось, рыбные запасы стали
восстанавливаться. Летом, когда водохранилище
заполнено, влияние загрязнения заметно
только непосредственно там, где
происходит сброс сточных вод. Правда, зимой,
когда объем воды в водохранилище
сокращается в шесть раз, загрязнение все же
распространяется по всему основному
руслу реки Камы вплоть до плотины.
Поэтому рыба в водохранилище и сейчас болеет
и гибнет, а часть ее зимой скатывается
через плотину или уходит в боковые
притоки.
Рыбопродуктивность водохранилища в
последние годы не растет — ежегодные
уловы здесь не превышают 5—6 тысяч
центнеров, тогда как при нормальном
гидрохимическом режиме водохранилище
могло бы давать в год до 15—17 тысяч
центнеров рыбы.
Продолжается ежегодная гибель рыбы
и ниже по Каме, в районе Перми, где в
реку по-прежнему поступает большое
количество сточных вод химических
предприятий. На этом участке реки имеются
хорошие места для нереста и нагула таких
промысловых рыб, как лещ, язь и др.
И если бы не загрязнения, то рыбные
запасы здесь могли бы намного увеличиться.
Не лучше обстоит дело на одном из
главных притоков Камы — реке Белой.
Исследования ГосНИОРХ, проведенные
здесь в 1962—1963 гг., показали, что Белая
сильно загрязнена сточными водами
предприятий химической и нефтехимической
промышленности. Загрязнение воды и
грунтов обнаруживается летом на сотни
километров ниже Уфы, а зимой — даже и
в Каме вплоть до ее устья, то есть на
расстоянии до 900 км. Расположенный в Уфе
завод по производству гербицидов
сбрасывает в реку сточные воды с резким
неприятным запахом, который исчезает только
при разведении сточной воды в 12, 25, а то
л в 50 тысяч раз! Рыба, выловленная
зимой в устье Камы, всегда имеет
неприятный запах и привкус химикатов.
Загрязнение реки Белой привело к
почти полному уничтожению ее рыбных
запасов, В недалеком прошлом в этой реке и
ее притоках находились основные
нерестилища белорыбицы, где
воспроизводилось ежегодно около 10 тысяч центнеров
этой рыбы. Еще больше вылавливалось
в бассейне Белой других рыб, в основном
частиковых. Теперь же воспроизводство
белорыбицы прекратилось, и в реке почти
ежегодно рыба гибнет. Несмотря на
сильное повышение интенсивности промысла
ежегодные уловы в бассейне Белой
снизились вчетверо, да и вылавливают теперь в
основном мелкую частиковую рыбу,
нередко пахнущую химикатами.
Особенно сильное отрицательное
влияние на рыбное хозяйство оказывают
неочищенные сточные воды
коксохимических и нефтеперерабатывающих заводов,
содержащие фенолы. Из-за загрязнения
такими сточными водами еще 20 лет назад
полностью потеряла свое рыбохозяйствен-
ное значение сибирская река Томь (приток
Оби).
Раньше здесь были мощные
нерестилища, где воспроизводилось ежегодно
15—20 тысяч центнеров рыбы. В самой
реке вылавливалось около 5 тысяч
центнеров рыбы, из которых 20% составляли
ценные породы.
Стоки коксохимических заводов
полностью уничтожили эти рыбные богатства.
Нанесенный рыбному хозяйству
материальный ущерб, по данным ГосНИОРХ,
выражается здесь суммой около 8 млн.
рублей ежегодно.
Нужно сказать, что в последние годы
на этой реке были приняты меры по
очистке сточных вод, и в первую очередь, —
по удалению из них фенолов. В реке
стала появляться рыба, начали заходить сюда
даже рыбы ценных пород. Но рыбохозян-
ственное значение Томи еще не
восстановлено: годовые уловы пока составляют
только 400—500 центнеров...
Эти примеры показывают, какой вред
может быть нанесен промышленностью
рыбному хозяйству, если сточные воды
предприятий будут продолжать
сбрасывать в водоемы без надлежащей очистки
и обезвреживания. Ориентировочный
подсчет, произведенный ГосНИОРХ, показал,
что в результате загрязнения рыбохозяй-
ственных водоемов неочищенными и недо-
очищенными сточными водами ежегодно
погибает и портится больше полутора
2?
миллионов центнеров рыбы. Стоимость
этой рыбы — свыше 350 миллионов
рублей. И немалая доля этих потерь вызвана
сточными водами химической
промышленности!
Такова теневая сторона бурного
развития химии (в том числе нефтепереработки,
бумажного производства, металлургии и
др.), которую мы наблюдаем в последние
годы. Невольно возникает вопрос:
обязательна ли она или можно ее избежать?
Научный ответ на этот вопрос только
один: конечно, можно и должно!
Загрязнение водоемов сточными
водами — не столько следствие роста
промышленности, сколько результат
неорганизованности и плохой работы отдельных лиц.
Вопросы очистки сточных вод и охраны
водоемов от загрязнения нередко
рассматриваются как второстепенные, неважные.
За выполнением планов своих
предприятий некоторые руководители не видят
общегосударственных, общенародных
интересов. Они смотрят на воду лишь с точки
зрения своего производства и совершенно
не учитывают того, что она нужна и для
других отраслей хозяйства, для бытовых
нужд человека, что она, кроме того,
служит средой обитания рыб и других водных
организмов.
Там, где производством руководят
люди с широким кругозором, которые
учитывают общегосударственные и
общенародные интересы, выполнение плана и
расширение производства не влечет за собой
загрязнения водоемов. Примером этому
может служить Новогорьковский
нефтеперерабатывающий завод, где само
производство, а также сброс и очистка сточных
вод организованы так, что эти воды не
загрязняют Волгу.
В новом пятилетнем плане развития
народного хозяйства намечено дальнейшее
возрастание мощностей промышленности.
Это повлечет за собой рост потребления
воды предприятиями и сброса
отработанных сточных вод в водоемы.
В этих условиях вопрос о
предотвращении загрязнения рек и озер, об охране
их рыбных запасов приобретает особую
остроту.
Химики, нефтяники, металлурги,
бумажники, машиностроители, энергетики
должны сделать все возможное, чтобы
сохранить все богатства нашей природы!
Кандидат биологических наук
А- Г- ГУСЕВ,
Государственный научно-исследовательский
институт озерного и речного рыбного
хозяйства
Рисунок Л. КУЛАГИНА,
новости отовсюду
ДДТ ОТРАВЛЯЕТ
птиц
В течение нескольких пет в
штате Нью-Хэмпшир (США)
применяли ДДТ для борьбы с одним
видом жуков, который считается
переносчиком грибка,
поражающего вязы. Американские ученые
Д. и К. Вурстер и В. Стрикленд
решили выяснить, как этот
инсектицид влияет на птиц, Оказалось,
что после распыления ДДТ над
песом в течение трех дней из
расчета 2,15 кг на гектар было
отравлено около 70% малиновок
и значительное число других птиц,
особенно тех, которые питаются
насекомыми, живущими в коре
деревьев [в частности, дятлов).
Большая часть птиц,
подвергнутых действию ДДТ, впоследствии
погибла.
В то же время жуки, против
которых ДДТ был применен,
постепенно привыкли к нему, и у них
появился стойкий иммунитет.
ЧЕГО ТОЛЬКО НЕТ
В МОРЕ
Что в морской воде есть
множество солей, это известно каждому.
Но в ней есть немало и
органических веществ. Может быть, их
удастся извлекать и использовать!
Такой эксперимент ставится
сейчас американскими учеными.
Тысячи литров воды перекачиваются
через колонну, в которой все
органические вещества
экстрагируются растворителем метипизобу-
тилкетоном.
Если эксперимент закончится с
положительным результатом, то,
возможно, придется подумать о
промышленной добыче органики
из морской воды. Кроме того,
такая техника может пригодиться
и для научных исследований — с
ее помощью удается определить
степень загрязненности морской
воды.
28
ВИТАМИНЫ
в жизни растения
Доктор биологических наук К. Е. ОВЧАРОВ,
Н. Д. МУРАШОВА,
Институт физиологии растений АН СССР
Исследования последних лет показали, что
витамины не менее необходимы растениям, чем животным
и человеку. При недостатке витаминов нарушаются
многие стороны обмена веществ, тормозятся
ростовые процессы. Например, обработка растений
белым стрептоцидом — антагонистом витамина пара-
аминобензойной кислоты — вызывает недостаток
этого витамина и сильно тормозит рост проростка.
Если же добавить витамин, то растение развивается
нормально.
Усилия ученых сейчас направлены на то, чтобы
во всех деталях выяснить физиологическую роль
витаминов в жизни растений. Уже установлено, что
витамины принимают непосредственное участие в
наиболее важных жизненных процессах,
происходящих в растительных организмах, и прежде всего, —
в процессе фотосинтеза.
ВИТАМИНЫ И ФОТОСИНТЕЗ
Физиологам и биохимикам удалось шаг за шагом
проследить путь поглощения углекислоты листом
зеленого растения и превращения ее в конечном
счете в углеводы, аминокислоты и белки. Выяснена
роль многих ферментов, принимающих участие в
этих процессах. И оказалось, что в состав некоторых
ферментов входят витамины: В6, РР, биотин и др.
Например, в хлоропластах — органах клеток, где
происходит усвоение углекислоты, — всегда
содержится провитамин А — каротин, который участвует
в поглощении энергии света, а вместе с тем
предохраняет хлорофилл от разрушения коротковолновой
радиацией. Витамин С защищает хлорофилл от
окисления и вместе с витамином К участвует во многих
реакциях, происходящих при фотосинтезе.
Эксперименты показали, что под влиянием
витаминов резко повышается интенсивность
фотосинтеза. Это связано не только с непосредственным
участием витаминов в усвоении углекислоты, но и с
активацией всех физиологических процессов в листе,
с изменением содержания хлорофилла и других
пигментов, а также водного режима листа. Усиливая
превращение продуктов фотосинтеза, витамины РР,
Bi и другие ускоряют отток из листа Сахаров и тем
самым создают благоприятные условия для более
интенсивного усвоения углекислого газа зеленым
растением.
ВИТАМИНЫ И ПИТАНИЕ
Значительная роль принадлежит витаминам
также в усвоении и превращении питательных веществ
в растительном организме, в частности — в
усвоении атмосферного азота и поглощении растением
микроэлементов. Наши исследования показали,
например, что при обогащении растений витамином РР
или при внесении его в почву заметно
увеличивается поглощение фосфора.
Иную роль выполняет витамин Be: при его
участии происходит присоединение к некоторым
органическим кислотам аммиака, поступающего из
почвы; при этом образуются аминокислоты, которые из
корней поднимаются вверх по растению, поступают
в растущие побеги и используются для образования
белков. Так, в результате присоединения аммиака к
щавелевоуксусной кислоте образуется широко
распространенная в растениях аспарагиновая кислота:
НООССНоШШОН J NHa - 2Н —
щавелевоуксусная аммиак водород
кислота
- HOOCCHoCH(NH2)COOH -г Н20
аспарапшовая кислота вода
Если же аммиак присоединяется к другим
органическим кислотам — пировиноградной и кетоглу-
таровой, то образуются новые аминокислоты —
соответственно аланин и глутаминовая кислота.
Важное значение имеет витамин В6 и в
образовании аминокислот путем так называемого пере-
аминирования, то есть переноса аминогруппы (NH2)
О?
с;
О
С
<
ас
>»
<
29
от аминокислот на органические кислоты. В
результате исходная аминокислота превращается в
органическую кислоту, а исходная органическая
кислота — в соответствующую аминокислоту.
Приведенные примеры говорят о том, что
синтез и превращение аминокислот — составных
частей белка — происходит при непосредственном
участии витаминов.
ВИТАМИНЫ
И РАЗМНОЖЕНИЕ
Важную роль играют витамины и в процессах
размножения растений. Например, витамины
необходимы для нормального формирования пыльцы и
пестика. И не случайно в пыльце витамины
концентрируются в огромных количествах. Особенно много
в ней витамина Е и провитамина А — каротина.
Именно каротин и близкие к нему соединения и
придают пыльце ее обычную желтую окраску.
Интересно, что у животных в органах, связанных
с размножением, тоже содержится много
подобных соединений, и некоторые из этих органов
также окрашены ими (желтое тело яичников, красная
и желтая икра рыб и т. д.).
Наши опыты показали, что каротин участвует в
прорастании пыльцы и росте пыльцевых трубок.
Если в пыльце содержится мало каротина, то она
плохо прорастает. Например, каротин разрушается
при длительном хранении пыльцы или когда она
подвергается воздействию света.
Пыльца некоторых сортов растений (персика,
картофеля, апельсина и др.) содержит очень мало
каротина, и как раз у этих растений образуется
много абортивной, то есть неспособной к
оплодотворению пыльцы. Если же такую пыльцу, бедную
каротином, поместить на питательную смесь рядом
с пыльцой, богатой этим пигментом, то прорастание
первой заметно усиливается: она потребляет
каротин, выделяющийся из богатой им пыльцы. Еще
ярче проявляется стимулирующее действие
каротина в том случае, если его вводить в питательную
среду, на которой проращивается пыльца, бедная
этим пигментом.
Дальнейший рост завязей, связанный с притоком
к ним питательных веществ и переработкой их в
жизненно необходимые соединения, происходит
тоже при непосредственном участии витаминов.
В созревших семенах витамины накапливаются в
значительных количествах. По мере созревания
семян из них исчезает лишь витамин С.
Однако содержание витаминов в семенах одного
и того же сорта, произрастающего в разных
условиях внешней среды, может быть различным. Даже
в пределах одного початка или колоса зерна могут
30
Снятие вредного действия белого стрептоцида
витамином парааминобензойной кислотой:
слева—контроль; в середине — проросток,
обработанный белым стрептоцидом; справа —
проросток, обработанный белым стрептоцидом и
витамином
содержать разное количество витаминов. Эти и
другие факты говорят о том, что в период
формирования семян на растении могут создаваться условия,
при которых происходит ненормальный биосинтез
витаминов.
Существенным образом изменяется содержание
витаминов при хранении семян. Как правило, чем
дольше хранятся семена, тем меньше в них
остается витаминов.
Когда семена прорастают, содержание витаминов
в них снова резко увеличивается. Но при
неблагоприятных условиях весны (например, при низкой
температуре, во время засухи и др.) витаминов
может все же не хватить для нормального течения
физиологических процессов. Кроме того, при
намачивании семян в воде, особенно если оно
продолжается значительное время, синтез некоторых
витаминов тормозится, а витамины, которые
образуются, могут вымываться из семени. Все эти
соображения заставили многих исследователей
провести опыты по добавочному обеспечению семян
Влияние витаминов на рост корней люцерны:
слева — корень, выросший в среде, лишенной
витаминов, справа — в среде, богатой витаминами
витаминами. Результаты таких опытов показали, что
предпосевное обогащение семян некоторыми
витаминами стимулирует их прорастание, усиливает
ростовые процессы, приводит к повышению урожая.
Так, обработка семян витаминами В» и РР в
концентрации 5—10 мг/л привела к увеличению
урожая моркови на 10%, редиса — на 23%, сахарной
свеклы — на 10—20%, семян люпина — на 29%.
Предпосевное обеспечение семян витаминами
способствует появлению и других биологических
особенностей. Как известно, цитрусовым растениям
присуща полиэмбриония, то есть развитие из
одного семени нескольких проростков. Оказалось, что
это явление может быть усилено путем обработки
семян витаминами РР и Bi- При намачивании
зерновок пшеницы в растворе витамина РР такие семена
давали растения с заметно большим колосом,
содержавшим больше зерен, что в конечном счете
повышало урожай. Очень ценно то, что подобные
полезные отклонения от нормы сохранялись и в
последующих поколениях.
ОТКУДА РАСТЕНИЯ
БЕРУТ
ВИТАМИНЫ!
Большинство высших растений синтезирует почти
все необходимые им витамины. Но не все органы
растения обеспечены витаминами в равной степени.
Например, корни многих растений обладают
недостаточной способностью к синтезу витаминов, в том
числе В|, В2 и PP. Такие корни не растут в условиях
стерильной культуры на среде, не содержащей этих
витаминов. Но стоит их добавить в среду, как
авитаминоз исчезает, и рост корней возобновляется.
А почему же корни таких растений способны
расти в естественных условиях? Оказывается, они
получают витамины из надземных частей растения.
Из листьев, где витамины синтезируются, эти
жизненно необходимые вещества передвигаются по
всему растению.
Корни поглощают витамины и из почвы, где они
накапливаются иногда в больших количествах в
результате деятельности микроорганизмов. Например,
в черноземе, содержащем много почвенных
бактерий, витаминов В| и Вг во много раз больше, чем в
подзоле — почве с невысокой микробиологической
активностью. Существенно влияет на содержание
витаминов в почве и наличие остатков растений и
животных, при разложении которых образуются
витамины.
Корни растений также выделяют в почву
витамины; этот процесс идет по-разному в зависимости от
физиологического состояния растений. Так,
10-дневные проростки выделяют в почву в несколько раз
больше витаминов, чем 45-дневные.
Таким образом, в почве постоянно идут
процессы взаимного обмена витаминов. Выделяя в почву
одни витамины, которые используются
микроорганизмами, высшие растения получают из почвы
другие витамины, синтезированные микробами.
Такое поглощение витаминов из внешней среды —
важный дополнительный резерв этих веществ,
особенно для тех растений, корни которых слабо
синтезируют витамины.
Если внести в почву дополнительные количества
витаминов, они интенсивно поглощаются корневой
системой и передвигаются в листья, в точки роста,
в плоды. Такое обогащение растений витаминами
стимулирует образование и рост корней, усиливает
рост надземных частей растения. Так, вводя в
песчаную культуру витамин В», удалось заметно
увеличить рост мятлика и полевицы: растения,
подкормленные витамином, имели более высокие стебли,
большего размера листья и более развитую
корневую систему. Введение в питательную среду
витаминов В» и особенно РР стимулировало ростовые
31
процессы у орхидей: под влиянием витамина РР
сухой вес орхидей увеличился в 3 раза.
Особенно интенсивно поступают растворы
витаминов в черенки. Опыты показали, что
выдерживание черенков роз, яблони, шелковицы, сливы и
других растений в растворе, содержащем витамины и
стимуляторы роста, ускоряет образование и развитие
корневой системы. Значит, дополнительное введение
витаминов оказывает благотворное действие прежде
всего на корни растений.
Надземные части растения реже страдают от
недостатка витаминов: ведь именно здесь они в
основном и образуются. Однако иногда нормальное
образование витаминов в растении может
нарушаться. Например, при недостатке света или некоторых
элементов минерального питания биосинтез
витаминов в растении задерживается. Нередко усиленный
обмен веществ, в котором принимает участие тот
или иной витамин, ведет к повышенному его
расходу. Это также может быть одной из причин
необеспеченности растения витаминами.
В таких случаях хорошие результаты дает
опрыскивание растений витаминами. При этом витамины,
нанесенные на листья, быстро поступают в ткани
растения. Мы проделали такие опыты и с помощью
изотопного метода убедились, что витамин В,,
введенный в черешок среднего листа, быстро
передвигается как в верхние и нижние листья, так и в плоды
и корни.
Опрыскивание растений растворами витаминов
вызывает усиление обмена веществ и стимулирует
ростовые процессы. Так, при внекорневой
подкормке хлопчатника витамином РР увеличивается высота
стебля, число листьев и побегов. У обработанных
витамином растений раньше и в большем количестве
образуются бутоны, раньше созревают коробочки.
Опрыскивание витамином РР сахарной свеклы
усиливает рост листьев и корней. При обработке
витаминами подсолнечника увеличивается вес семян и
повышается содержание жира в ядре семени.
Изучение значения витаминов в жизни растений
не только позволяет вскрыть новые важные функции
этих веществ в жизнедеятельности организмов, но
и подсказывает новые возможности усиления
процессов роста и развития сельскохозяйственных
культур,
новости отовсюду
КРАСКИ-ХАМЕЛЕОНЫ
Общеизвестно, что при
увеличении скорости лолета температура
летящего тела увеличивается
[если, конечно, полет происходит
в воздухе, а не в космическом
вакууме). Изменение цвета
специальных красок под действием
температуры заложено в основу
нового метода исследования
форм сверхзвуковых самолетов.
Метод создан одной из
лабораторий фирмы «Локхид». Краски-«ха-
мелеоны» уже разработаны и
сейчас проходят испытания.
Экспериментальные модели из
керамики, окрашенные такими
красками, исследовали при
скоростях от 10 до 21 тысячи
километров в час. Резкое изменение
окраски образца
свидетельствовало о превышении определенного
для каждой краски температурно-
скоростного порога. Сейчас стоит
задача — увеличить
быстродействие красок-«хамелеонов».
Исследуется возможность создания
красок, срабатывающих за
несколько миллисекунд.
«ТРЯПИЧНЫЕ»
ГРАНУЛЫ
В Англии разработан метод
производства сверхчистой
целлюлозы нового типа. Она отличается
от прочих сортов не только
консистенцией и чистотой, но и тем,
что после специальной
обработки и грануляции приобретает
ярко выраженные ионообменные
свойства. Все это позволяет
применять новый тип целлюлозы
в биологии и медицине. С
помощью ионообменной целлюлозы
можно выделить из смеси многие
сложные компоненты,
содержание которых весьма мало.
Изготовляют эту целлюлозу из
хлопчатобумажного тряпья.
Производительность первой
опытно-промышленной установки — 30 тонн
в год.
И ГИБКОСТЬ
и жаростойкость
Журнал «Anti-Corrosion Methods
and Materials» сообщил, что в
космической технике США
широко применяется проволока из
молибдена высокой чистоты. Эта
проволока не теряет гибкости
при температурах до 1925 С.
ОРИГИНАЛЬНЫЙ
МЕТОД
Грулла зарубежных специалистов
занята сейчас изучением
процесса сварки титановых листов. Такое
исследование было начато после
того, как фирма «Норт америкен
авиэйшен» приступила к
разработке титановых баков для ракетного
топлива и окислителя.
Предполагается, что баки будут
двухслойными. Внутренний гофрированный
лист титана придется сваривать
с наружным листом.
Чтобы сохранить форму
гофрировки и избежать прогиба
листов, предложен оригинальный
способ. Между листами перед их
соединением помещают железные
прокладки, а затем прокладки не
извлекают, а химически
растворяют. Титан, обладающий
большей химической стойкостью, при
этом не повреждается.
32
ПЕРВЫЕ
ХИМИЧЕСКИЕ
ЛАБОРАТОРИИ
В РОССИИ
Профессор П. М. ЛУКЬЯНОВ
Рисунок В. СКОБЕЛЕВА
Историки долгое время считали, что
первая русская химическая лаборатория была
создана М. В. Ломоносовым в 1748 г. в
Петербурге. Но исследования профессора
П. М. Лукьянова, обнаружившего в
Архиве древних актов интереснейшие
документы и приходно-расходные книги XVII—
XVIII вв., показывают, что лабораторные
анализы проводились в России
значительно раньше. Они носили довольно
разнообразный характер.
АЛХИМИЧЕСКИЕ КАЗЕНКИ. В XVII в. при
аптеках, принадлежавших казне, существовали
так называемые «алхимические казенки» —
своеобразные мастерские, где помощники
аптекарей, «алхимисты» изготовляли лекарства и
химикалии, служившие сырьем для лекарств
(азотная кислота, квасцы, серная кислота,
очищенная селитра). Там же изготовлялись
некоторые краски, которые в то время применялись
в качестве лекарств. Например, приехавший в
1602 г. в Россию «оптекарь» Френшам имел
3 Химия и Жизнь, № 10
33
в своей мастерской желтый и красный сандал,
крокус, ляпис-лазурь и другие краски.
Некоторые лекари применяли и краску — ярь-медянку
(уксуснокислую медь), про которую современник
писал: «Ярь такову силу имеет, что сушит и огнь
из очей выводит, но слезное течение от того
родится... И язвы огные заживляет и от опухоли
охраняет».
Из свинцовых белил, красного сурика, воска
и сосновой серы в алхимических казенках
изготовляли особые пластыри. По утверждению в
рукописной книге 1672 г., такой пластырь «зело
сушит раны и живит».
Для «алхимистских работ» изготовлялась
специальная посуда. Она перечисляется в
«Приходно-расходной книге Оптекарьского приказа»
за 1701 г. Там названы «скляницы» (колбы,
реторты), «сулеи» (большие стеклянные бутыли).
В другой книге упомянуты «реципиенты»
(приемники), «кохвы» (видимо, колбы), «иготи»
(ступки), «бутыли разных рук» и прочее
лабораторное оборудование.
В аптекарских мастерских кроме «алхимис-
тов» работали и другие специалисты: «дистиля-
торы», «перепущики» и другие. Они занимались
перегонкой разных составов, применявшихся
при изготовлении лекарств. Перегонка
жидкостей на две фракции называлась «двоением».
ПРОБОВАЛЬНЫЕ ПАЛАТКИ. В 30-е годы
XVIII в. были организованы «пробовальные
палатки» (то, что теперь называется «пробирной
лабораторией»). Указ Правительствующего
сената 1738 г. предписывал всем клеймить
драгоценные украшения из золота и серебра в «пробо-
вальной палатке», где на драгоценные металлы
ставилась проба.
РУДОСЫСКНЫЕ РАБОТЫ ПЕТРА I. Царь
Петр придавал большое значение развитию
горнорудного дела в России. Во время своих
заграничных поездок он познакомился со многими
выдающимися учеными, которые советовали ему
организовать в России свои лаборатории и
заводы. Философ и математик Готфрид Вильгельм
Лейбниц даже предлагал ему свое участие. По-
видимому, первая лаборатория для испытаний
руд была основана около 1709 г. и находилась в
подчинении «Приказа рудных дел». В
«Приходно-расходной книге» приказа за 1709 г. записано:
«...да к опытам рудам и к рудокопным делам
куплено припасов...» Среди «припасов» названы
винный камень, горючая сера, ярь, нашатырь,
желтый мышьяк, селитра, смальчуг (так в то
время называли приготовленный особым
способом поташ), порох. Упомянуты и расходы на
покупку «двоих пробирных весков».
34
Видимо, Петр [ сам проводил испытания руд
в так называемой «пробирной печи». В архиве
Петра нами найден чертеж такой печи. Петр
писал в 1711 г. из Риги в Правительствующий
сенат: «Також прислать пробовальную печку,
которая у нас во дворе в Преображенском, и
велите такую же другую зделать, тол(ь)ко немного
побол(ь)ше оной». В Архиве древних актов есть
собственноручные записи Петра с анализами руд
на содержание в них золота, серебра, свинца,
меди, олова. Он же описал метод приготовления
азотной кислоты, перечислил составные части
пороха. Петр I пользовался химической
символикой, обозначая селитру кружком, серу —
полумесяцем и т. п.
Приведем собственноручную запись Петра I
об анализе руды (на содержание в ней олова):
«Оловяную руду отведать. Пер во мыть та ко же,
как и протчие, потом взять 1 л руды, 4 л флюсов,
2 л белого и 2 черного, да пол л гарпиесу
(канифоли. — П. Л.) и смешать вместе, потом всыпать
в горшок и, поверх солью посыпав, накрыть и в
огонь поставить так же, как и медную руду,
посматривая в горшок, и когда кипеть и шуметь
перестанет и будет тихо и глатко, тогда вынять».
Буквой «л» Петр I, вероятно, обозначает лот —
старую русскую весовую меру A лот
соответствует 3 золотникам или 13 граммам). Белый и
черный флюсы, как пояснил в книге «Первые
основания металлургии или рудных дел» в
1763 г. М. В. Ломоносов, изготовлялись из
селитры и винного камня.
ЛАБОРАТОРИЯ ПРИ БЕРГ-КОЛЛЕГИИ.
Сохранились точные сведения о химической
лаборатории при Берг-коллегии, построенной в
Петербурге за 5 лет до смерти Петра (то есть в
172G г.) «супротив литейного двора». Для ее
постройки было закуплено 50 тысяч кирпича и
150 бочек извести. Построена лаборатория
«против чертежа» наемными каменщиками под
руководством капитана Челищева. На постройку
ассигнована тысяча рублей. Лаборатория была
предназначена для проб разных руд. По записям
в архивах 1721 г., для «пробовальных печей»,
необходимых в лаборатории, из Берг-коллегии
были затребованы глина, проволока, а также
другие материалы, которые предписывалось
взять с Литейного двора. Для изготовления
«пробирной сковороды» выписывалось 5 пудов
(около 80 кг) свинца и 25 фунтов (около 10 кг)
железа.
Примерно в зто же время в Петербурге
работали и другие лаборатории. Там исследовалась
продукция первых русских химических заводов.
Сохранилась запись пробирного мастера Шлат-
тера о качестве химикалиев, изготовленных на
заводе Савельева и братьев Томилиных:
«Скипидар зело хорош... крепкая водка (азотная
кислота.— П. Л.) не очень хороша... калофониум
(канифоль. — П. Л.) из самых лучших». В другом
архивном документе перечисляются работники
другой лаборатории. Там названы «мастера
серного дела», «пробовалыцик». В одной из
лабораторий металлург Шлаттер исследовал разные
краски: празелень, доставленную из Копорского
уезда под Петербургом, черлень, мумию, «вохру».
ИСТОРИЯ «ПСКОВСКОГО ПОДВОРЬЯ».
Когда построенная в 1735 г. химическая лаборатория
на 5-й линии Васильевского острова пришла в
ветхость, Коммерц-коллегией было решено
построить новую лабораторию. От архитектора
Осипа Трефина была затребована смета и
разработана «кондиция о перестройке старой
лаборатории, находящейся на Васильевском острове,
5-й линии, на углу третьей Прешпективной (по-
видимому, Малого проспекта. — П. Л.).
Лаборатория должна была состоять из «двух светлиц». Но
строительство почему-то было прекращено, и в
1760 г. была построена новая лаборатория «в
Сант-Петербургской крепости, а оный
лабораторный на Васильевском острове дом остался и
ныне стоит празден». Берг-коллегия постановила
продать этот дом «охочим людям с аукционного
торгу».
В 1766 г. Правительствующий сенат сообщил
Берг-коллегии, что на Васильевском острове, в
доме, называемом «Псковское подворье»,
установлены «химические печи», туда же переведено
оборудование из старой лаборатории. Но и о
новом помещении Берг-коллегия в 1766 г. писала
Сенату: «На Васильевском острову в 24-й линии
Псковского подворья палаты, в коих та
лаборатория ныне состоит, так ветхи, что в оных
определенных при той лаборатории горным и обер и
ундер офицерам и ученикам не только жить, но
и работать яко то рудных проб и протчих
химических действ производить никаким образом не
можно, потому что те покои кои со сводами
весьма опасны и потолки с подмазкою
обваливаться начинают».
В 1772 г. обер-пробирер И. Клембкен (ученик
и помощник М. В. Ломоносова) приискал на
Васильевском острове принадлежавший раньше
М. JVI. Хераскову дом, нижний этаж которого
был арендован под лабораторию. Туда же было
передано оставшееся оборудование с Псковского
подворья.
ЛАБОРАТОРИЯ В МОСКВЕ. У нас нет
точных сведений, когда была создана первая
московская химическая лаборатория. По-видимому,
это относится к началу 30-х годов XVIII в
В архивных документах сохранилось дело о
выдаче заработной платы «обретающемуся в
Москве при лаборатории Увару Леонтьеву». Ему
предписано принять у обер-пробирера Шамше-
ва «всякие инструменты и материалы». Уварову
платили в день 3 копейки и, кроме того, 90
копеек в месяц «кормовых денег».
В Московскую лабораторию посылались
пробы рудных и нерудных ископаемых и другие
хи ми чески е продукты.
ДЕРЕВЯННОЕ СТРОЕНИЕ ЗАЙЦЕВА.
В 1745 г. на Красной площади, около собора
Василия Блаженного, в старом здании коллегии
была организована новая лаборатория. В одном
из доношений Сенату Берг-коллегия сообщала,
что купец Зайцев построил «анбар», вследствие
чего «удобного места для поклажи и топлению
во оной палате дров и в запас ко оной же
лаборатории для всегда случающихся проб и других
работ... не имеется». Берг-пробирер Леман
написал Сенату, что «деревянное строение» Зайцева
в пожарном отношении весьма опасно. Зайцеву,
по-видимому, было предписано его «деревянное
строение» сломать.
О размерах и местонахождении этой
лаборатории дает представление план, найденный нами
в архиве. Лаборатория состояла из пяти комнат.
Общая площадь, исходя из масштаба,
указанного в чертеже, составляла около 250 м2. Здание
стояло позади собора Василия Блаженного (если
смотреть на него со стороны Лобного места).
В 90-х годах XVIII в. эта лаборатория,
видимо, уже не существовала. Об этом
свидетельствуют записи в некоторых архивных документах.
ЗАВОДСКИЕ ЛАБОРАТОРИИ. Кроме
Петербурга и Москвы, существовали лаборатории и в
других городах. Например, в последней четверти
XVIII в. специально для пробы золота и серебра
была построена лаборатория в Екатеринбурге.
В середине XVIII в. работала лаборатория на
Барнаульском металлургическом заводе; там
были установлены пробирные и «самодувные»
печи, сделаны «каморы» для взвешивания проб.
Известна лаборатория и при казенном
квасцовом заводе в Тамбове.
Совершенно особое место среди первых
химических лабораторий и мастерских занимала
организованная в 1748 г. в Петербурге
лаборатория Михаила Васильевича Ломоносова.
Замечательный русский естествоиспытатель провел там
целый ряд крупнейших исследований,
прославивших русскую науку, и вырастил учеников,
ставших выдающимися исследователями.
Но это уже тема отдельной статьи.
3*
35
железные
нервы
Инженеры М. А. ГУРЕВИЧ
и В. Л. ЛИТВИНЕНКО
Заголовок статьи не надо принимать за
метафору.
Речь пойдет о нервах, сделанных из
обыкновенного железа, того самого
железа, из которого делают конторские скрепки
и дверные ручки.
необычные свойства
обычной проволоки
В начале нашего века химики обратили
внимание на странное поведение железа в
крепкой азотной кислоте. От
прикосновения цинковой палочки железная пластинка
(или проволочка) мгновенно меняла
окраску, уподобляясь хамелеону: становилась
то черной, то светло-серой.
В двадцатые годы физиолог Р. С. Лилли
поставил несколько довольно простых
опытов. Опустив в стакан с концентрированной
азотной кислотой кусок железной
проволоки, он наносил на один из ее концов
царапину. Мгновенно по черной проволочке
пробегала светло-серая волна и выделялись
пузырьки газа. Ученый повторил опыт на
железном колечке: волна делала
несколько кругов, а затем исчезала. Эксперимент
был еще усложнен: кроме исследуемой
проволочки в кислоту был опущен
дополнительный электрод. Схема (она показана
на рисунке) предельно проста — такой опыт
Схема опыта Лилли:
1 — железная проволочка; 2 — анод; 3 — ключ; 4 —
батарея; 5 — реостат; 6 — амперметр; 7 — прибор
для измерения потенциала (вольтметр или
осциллограф)
может поставить и читатель. (Единственное
предупреждение — в железе должно быть
как можно меньше углерода. Лучше всего
взять армко-железо).
36
Лилли обнаружил, что постоянный
электрический ток действует на железную
проволочку так же, как и механическое
повреждение ее поверхности. При включении
тока наблюдалась своеобразная цветовая
волна (условимся называть ее волной
активации).
Интересные зависимости обнаружились
и при измерении электрического потенциала
проволочки. Оказалось, что волна
активации сопровождается резким скачком
потенциала. Однако не всякий электрический
импульс вызывал загадочную волну. Если
сила тока в цепи недостаточно велика, то
осциллограф вычерчивает прямую. Но сто-
время
Изменение потенциала железной проволочки при
прохождении волны активации
ит току превысить определенный предел —
и на экране возникает характерный всплеск.
Если же с определенной частотой
подавать на проволочку электрические
импульсы, которые поодиночке не вызывают
активацию, то через некоторое время железо
все-таки «возбудится».
И еще одна интересная особенность.
Если постоянно питать ячейку
электрическим током определенной силы, то волна
активации будет равномерно пробегать по
1.
Изменение потенциала железной проволочки при
активировании длительным постоянным током
проволочке через строго определенные
промежутки времени, зависящие от
условий опыта.
Лилли не был химиком. Эти опыты он
ставил во время лекций для демонстрации
студентам свойств живого нерва.
НУЖНЫ ЛИ МОДЕЛИ!
В последние годы медики и физики,
химики и радисты, биологи и кибернетики
всерьез занялись нервной клеткой —
нейроном. Не зная тончайших процессов,
протекающих в отдельном «кирпичике», нельзя
понять деятельности нервной системы в
целом. Классический путь — проникновение
внутрь нейрона, изучение его строения и
свойств. Но есть и иной путь —
моделирование нейронов и нейронных сетей
средствами неживой материи.
Это новое направление преследует две
основные цели. Во-первых, упрощенная
модель — кратчайший путь к пониманию
сложного оригинала. Недаром конструктор
самолета начинает свою работу со
скромной настольной модели. А во-вторых...
О второй цели моделирования следует
рассказать подробнее.
Даже поверхностное сравнение самых
сложных кибернетических автоматов и
нашей переносной машины — мозга будет в
пользу последнего. Ни одна современная
электронная машина не способна ко всем
многочисленным логическим операциям,
которые легко проделывает человеческий
мозг; ни одна машина не обладает такой
памятью; ни одна машина,
запрограммированная человеком, не способна работать в
непредвиденных ситуациях, которыми так
богата повседневная жизнь. Подсчитано, что
в среднем в нашем мозгу что-то около 1014
нервных клеток, нейронов. Для построения
электронно-вычислительной машины с
таким количеством «кирпичиков» на земном,
шаре попросту не хватит элементов —
транзисторов, сопротивлений,
конденсаторов. Но это еще не все. Стоит хоть одному
элементу электронной машины выйти из
строя (скажем, сгорело сопротивление), как
машина серьезно «заболеет». Каждый час в
нашем мозгу отмирает около тысячи
нейронов, а новые нервные клетки не
образуются. Авторы подсчитали, что каждый из
них уже лишился примерно сотни
миллионов нейронов, однако это не помешало им
37
написать настоящую статью. Одним словом,
мозг, живая электронная машина,
построенная из ненадежных элементов, обладает
удивительно высокой надежностью.
Создавая модели нейронов, ученые
пытаются подражать лучшему из того, что
есть в их распоряжении. Это и есть вторая
цель моделирования нейронов.
НЕМНОГО ОБ ОРИГИНАЛЕ
Прежде чем говорить о моделях,
вспомним свойства оригинала — нейрона.
«Все или ничего», «да или нет» —
основной принцип деятельности нейрона.
«Кирпичик» клубка нервов признает только два
состояния: возбуждение и покой. Эти
состояния легко обнаруживаются
электрическими методами. Объясняется это тем, что
возбужденный участок нервов заряжается
отрицательно по отношению к
невозбужденному.
Нейрон приходит в состояние
возбуждения под действием внешнего
сигнала-раздражителя (например, от механического
или теплового импульса). Он может
возбудиться и от импульса соседней нервной
клетки.
| ПОКОЙ \ ВОЗБУЖДЕНИЕ
rv
* о» оо* с**
покой
ВРЕМЯ
Примерная осциллограмма возбуждения
биологического нейрона
Но нейрон «пробуждается» не от
всякого толчка. Для возбуждения каждой
нервной клетки нужна вполне определенная
минимальная сила импульса. Это — так
называемый порог возбудимости- Более слабые
импульсы не могут вывести нервную клетку
из состояния покоя, но и они не пропадают
даром, а «запоминаются». А когда сумма
этих слабых импульсов, действующих либо
в разное время, либо на разных участках
нейрона, превысит определенный предел,
нейрон возбудится. Это свойство нейрона
называется подпороговым
интегрированием.
И, наконец, еще одно очень важное
свойство нейрона. После прохождения
импульса клетка не может сразу возбудиться
вновь- Ей необходим отдых для
восполнения энергетических потерь. То время, когда
нейрон «отдыхает», называется периодом
невосприимчивости, или рефрактерности.
Сейчас существует много типов
искусственных нейронов («квази-нейронов») на
полупроводниковых элементах, ферритовых
сердечниках, механических устройствах.
Однако все эти модели достаточно сложны,
возбуждаются лишь от каких-то
специфических импульсов и не могут воспроизвести
все важнейшие свойства биологического
нейрона.
КАК РАБОТАЮТ ЖЕЛЕЗНЫЕ НЕРВЫ
А теперь снова вернемся к опытам Лил-
ли. Когда вы читали предыдущую главу, то,
наверное, заметили, что железная
проволочка, погруженная в азотную кислоту,
ведет себя чрезвычайно схоже с нервной
клеткой.
Сравните примерные осциллограммы
волны активации железа и возбуждения
биологического нейрона. Они похожи, как
две капли воды. У проволочки тоже налицо
порог возбудимости и подпороговое
интегрирование. А промежутки между
импульсами при постоянном возбуждении — это
не что иное, как периоды рефрактерности.
Более того — скорость распространения
цветовой волны по проволочке вполне
сопоставима со скоростью нервного импульса.
Железная проволочка в азотной
кислоте стала классической моделью нерва и
получила в научной литературе название
квазинейрона Лилли. Как же работает эта
модель?
Железо весьма энергично растворяется
в разбавленной азотной кислоте. Но в
концентрированной кислоте железо, частично
растворившись в первый момент после
погружения, покрывается тончайшей пленкой
окислов. Она предохраняет металл от
дальнейшего растворения. Такое состояние
металла называется пассивным.
Однако и в пассивном состоянии
железо все же частично растворяется через
38
пленку окислов. При этом образуются ионы
железа, а азотная кислота
восстанавливается до азотистой:
Fe — 2е -> Fe2+.
5+ 3^
HN03 + 2e->HN02.
При включении постоянного тока вторая
реакция — основная. Процесс превращения
азотной кислоты в азотистую потребляет
львиную долю энергии.
Увеличим силу тока. Реакция
образования азотистой кислоты пойдет еще
быстрее, и, наконец, наступит момент, когда из
глубины раствора к электроду (железной
проволочке) не будут успевать поступать
новые порции азотной кислоты. Начинается
другая электрохимическая реакция —
выделение водорода:
2W + 2е -» Н2.
Водород химически восстанавливает
пассивную пленку, превращая окисел в
металл. Обнаженный, активный участок
поверхности и пассивная пленка оказываются
рядом. Образуется короткозамкнутый
гальванический элемент (такой же, как при
коррозии луженого железа), анодом
которого является активное железо. При этом
АКТИВНАЯ
ЗОНА
При распространении волны активации цвет
проволочки изменяется — металл светлее окисной пленки
пассивная пленка окислов
электрохимически восстанавливается до металла, и
активная зона расширяется. Волна активации
побежала по проволочке!
Вспомните, отчего началась активация
пассивного металла: где-то не хватило
азотной кислоты. Через 1—2 секунды кислота
продиффундирует из раствора к активной
зоне и вновь покроет ее пассивной
пленкой. Значит постоянный электрический ток
или, как говорят, катодная поляризация
лишь стимулирует начало процесса.
В случае механического повреждения
пленки все обстоит еще проще — сразу же
образуется короткозамкнутый элемент
железо — пленка.
Чтобы началось восстановление окислов,
нужен вполне определенный ток — это и
есть порог возбудимости. Если же подавать
на проволочку слабые импульсы, то
электролит возле нее становится все беднее
азотной кислотой. Наконец наступает
момент, когда начинает выделяться водород
и образуется гальванический элемент —
идет волна активации. Так объясняется под-
пороговое интегрирование.
А период рефрактерности? После
каждого импульса у поверхности проволоки
собирается много азотистой кислоты, и
пока она не распределится равномерно по
всему объему раствора, активация
«железного нерва» не повторяется.
Отметим еще одно чрезвычайно важное
обстоятельство. Электрохимический
нейрон значительно ближе по своей природе к
биологическому оригиналу, чем другие
модели. По современным представлениям,
свойства биологического нейрона
объясняются сложными электрохимическими
процессами, протекающими в живой клетке.
Нельзя, конечно, утверждать
безапелляционно, но все же можно предположить, что
железный нерв окажется прообразом
искусственной живой нервной клетки.
ОТ БИОЛОГИИ
ДО КИБЕРНЕТИКИ
В начале статьи мы говорили о двух
аспектах моделирования нейронов:
биологическом и кибернетическом. Посмотрим, что
же успел дать железный нерв биологии и
кибернетике.
Японец Кадзума Ямагива провел на
модели Лилли обширный комплекс
исследований. Он изучил зависимость скорости
распространения импульса от его
интенсивности и размеров площади активации.
Опуская в азотную кислоту сразу несколько
железных проволочек и располагая их под
разными углами друг относительно друга,
Ямагива исследовал механизм передачи
волны возбуждения от одного нейрона к
другому. По результатам опытов он сумел
предсказать ряд свойств живого нерва,
которые в дальнейшем были подтверждены
экспериментально.
Пожалуй, подобные опыты на живых
нервных клетках очень затруднены, если во-
39
обще возможны. Это — один из примеров
биологического аспекта моделирования.
Теперь — о кибернетике. Помните
железное колечко, по которому несколько раз
пробегает волна активации? Недавно
появилось сообщение о том, что уже создан
кольцевой элемент, поддерживающий
волну возбуждения в течение нескольких
минут. Предполагают, что это время можно
довести до нескольких часов. Представьте,
что в колечко подали электрический сигнал.
Этот сигнал в виде волны возбуждения
длительное время хранится в устройстве; он
как бы запоминается. Это прекрасный
элемент памяти, который так нужен
современной электронно-вычислительной технике.
Еще более широкие возможности для
технической кибернетики открывают
различные многоэлектродные комбинации
модели Лилли. На рисунке показана одна из
возможных схем электрохимического эле-
ПОЛИЭТИЛЕНОвМ?
ЯЧЕЙКА
Схематическое изображение элемента аналоговой
машины, построенного на модели Лилли
мента аналоговой машины. В
полиэтиленовой ячейке, заполненной азотной кислотой,
две камеры. В одной из них две железные
проволочки, в другой — одна. Такой
элемент может выполнять одну из важнейших
логических операций — схему запрета. Если
на входе возбудить одну из проволочек, то
на выходе получим сигнал в виде волны
возбуждения. Если же возбудить сразу два
входных «нерва», сигнала на выходе не
будет.
Железные нервы могут найти
применение не только как самостоятельные
элементы, но и как надежные посредники,
связывающие между собой электронные схемы.
Современные радиотехнические детали
микроминиатюрны. Это ставит инженеров
перед необходимостью пользоваться
тончайшими, почти невидимыми монтажными
проводами. Сопротивление таких проводов
достигает нескольких сотен ом на
сантиметр длины. Естественно, что в схеме,
соединенной такими «волосками», сигнал будет
очень сильно ослабляться, а то и совсем
теряться. Устройства, в которых сигнал не
ослабляется, называются линиями с
распределенными параметрами, или нейристора-
ми. Простейшей иллюстрацией нейристора,
правда, одноразового действия, может
служить бикфордов шнур. Отросток нервной
клетки — аксон и, конечно, наша железная
проволочка — тоже нейристоры. Кстати, не
только железная — уже известны
никелевые и кобальтовые нервы с аналогичными
свойствами.
Электрохимическими средствами можно
моделировать не только отдельные
нервные клетки, но и создавать целые нервные
сети со всей присущей им сложностью
соединений и способностью в процессе работы
совершенствовать и изменять свою
структуру. Но об этом — в другой раз.
Письмо
в редакцию
Э нашей статье «Локация
молекул», напечатанной в восьмом
номере журнала, имеются
неточности, о которых мы просим
сообщить читателям журнала.
1. В примере, относящемся к
определению относительного
разброса частот гамма-квантов
(стр. 19, левая колонка), цифры
относятся к гамма-квантам с
энергией 24 кэв (Snn9*).
2. Из-за типографской
опечатки в статье упоминается о
«твердых телах с прозрачными связями
между атомами» (стр. 20, правая
колонка). В действительности же
речь должна идти о прочных
связях.
3. Последнюю фразу в левой
колонке на стр. 22 следует читать:
«Поэтому вид скоростного
спектра меняется в зависимости от
типа атомных групп и характера
химических связей мессбауэров-
ского атома с другими атомами в
источнике и поглотителе.»
4. В настоящее время эффект
Мессбауэра уже наблюдался не
только на всех элементах,
отмеченных в таблице на стр. 26, но
и на калии, германии, рутении,
десяти лантанидах (празеодим,
самарий, европий, гадолиний,
тербий, диспрозий, гольмий, эрбий,
тулий, иттербий), а также на
нептунии.
Кандидат физико-математических
наук Е. Ф. МАКАРОВ,
кандидат химических наук
Ю. Ш. МОШКОВСКИЙ
40
НАШИ
«Давно меня интересует вопрос о том, какой образ
жизни ведет рыба белый речной карась. Дело в
том, что никто из рыбаков никогда не видел, как
эта рыба размножается, как происходит
оплодотворение, какая рыба оплодотворяет икру самки
карася: самец карася не имеет молок».
Н. Н. Макей, пос. Заречный,
Кореновского р-на.
Краснодарского края
Рыба, о которой пишет Н. Н. Макей, широко
распространена в реках и озерах Европы и Азии, а
также служит важным объектом прудового
рыбоводства. Она принадлежит к семейству карповых и
известна в науке под названием «серебряный карась».
Между прочим, серебряный карась —
родоначальник известных пород аквариумных рыбок: золотой
рыбки, телескопа, вуалехвоста.
Размножение серебряного карася долгое время
представляло загадку для ученых. Самцы этой
рыбы, в самом деле, встречаются очень редко, а в
некоторых закрытых водоемах их вообще нет.
Например, в 1940 г. в одной из стариц Кубани,
неподалеку от Усть-Лабинской, ихтиологи поймали 600
карасей, и все они при вскрытии оказались самками!
Но тогда как же оплодотворяется икра карася?
Только сравнительно недавно, в 1948 г.,
советские исследователи К. А. Головинская и Д. Д.
Ромашов сумели доказать, что размножение серебряного
карася происходит... с помощью других рыб. Икру
карася оплодотворяют его «родственники» по
семейству карповых — например, карп, сазан, линь. При
этом «чужой» сперматозоид играет лишь роль
стимулятора деления ядра икринки, а обычно наблю-
Если Вы хотите узнать об увлекательных
открытиях астрономов, исследующих
Луну, планеты. Солнце, звезды и
далекие галактики;
Если Вас интересуют новейшие данные
о природе нашей планеты — Земли, ее
недрах, океанах и атмосфере;
Если Вы хотите изготовить самодельный
телескоп и с его помощью наблюдать
сокровища необозримого звездного
неба;
дающегося слияния ядер самца и самки в яйце не
происходит. И потомство, появляющееся на свет в
результате такого оплодотворения, состоит поэтому
не из гибридов, а из тех же серебряных карасей, и
при этом, естественно, только из самок. Подобное
явление известно и у некоторых других животных и
носит название гиногенеза.
Почему именно у карася появился такой
необычный способ размножения, — до сих пор еще
окончательно не выяснено. По всей вероятности, это
просто один из механизмов борьбы за существование
в неблагоприятных условиях: ведь при таком
способе размножения достаточно остаться в озере хоть
одной самке карася, — и через несколько лет все
карасиное стадо будет восстановлено...
Рис. В. ЗУЙКОВА
Наконец, если Вы просто любите читать
о путешествиях и экспедициях,
увлекаетесь научной фантастикой или
космической филателией, —
подписывайтесь на научно-популярный журнал
Академии наук СССР — «Земля и
Вселенная».
Индекс 70336. Стоимость годовой
подписки 1 руб. 80 коп.
41
1,98
АРТУР ПОРДЖЕСС
Рисунки Л. КУЛАГИНА
Уилл Говард почувствовал, что кто-то легонько дергает его за штанину. Он
посмотрел себе под ноги и увидел, что в манжету его брюк отчаянно вцепилась
крохотная полевая мышка. Разинув рот, Уилл уставился на дрожащего зверька,
пораженный столь странным поведением обычно пугливого грызуна. Но вдруг
на тропинке появилась ловкая, быстрая ласка, до того решительно настроенная,
что даже не побоялась человека.
Уилл поспешно подхватил перепуганную мышку на руки. Ласка остановилась,
отвратительно заурчала, на ее треугольной морде, похожей на свирепую
карнавальную маску, красным светом вспыхнули глаза. Вереща от ярости, она
метнулась в чащу.
— Ах ты, бедняга! — обратился Уилл к комочку меха, лежавшему у него на
ладони, и горько усмехнулся. — Неравные же у тебя были шансы — точь-в-точь
как у меня против Харли Томпсона!
Он наклонился и осторожно посадил мышку в кусты. И тут у него от
изумления отвисла челюсть. На месте полевой мыши он увидел толстощекого
человечка, смахивающего на Будду, но ростом не более двух дюймов.
Удивительно звучным, хотя и слабым голосом человечек произнес:
— Прими, о добрый смертный, горячую благодарность от бога Иипа. Как
я могу вознаградить тебя за то, что ты спас меня от кровожадного чудовища?
Уилл судорожно глотнул, но быстро пришел в себя.
— Так ты... ты бог? — пролепетал он.
— Воистину я бог, — благодушно подтвердило диковинное существо. — В
наказание за то, что я жульничал в шахматах, мне каждые сто лет приходится
ненадолго становиться мышью... Но ты, без сомнения, читал подобные истории,
и они тебе давно наскучили. Достаточно сказать, что ты вмешался как раз
вовремя. Теперь ближайшие сто лет мне ничего не грозит — если, конечно, я снова
не поддамся искушению и не подменю пешку слоном.
Уилл снова вспомнил о Харли Томпсоне. Кажется, ему наконец представился
случай обскакать соперника.
— Ты упомянул о... о награде, — робко начал Уилл.
— Безусловно, — заверил его бог. — Но, увы, награда будет невелика. Видишь
ли, я очень мелкое божество.
— Вот как... А можно у тебя попросить маленький-маленький капитал?
— Конечно. Но он будет чрезвычайно маленьким. Я не могу превысить сумму
в один доллар и девяносто восемь центов.
— Только и всего?
— Боюсь, что да. Нам, мелким божествам, вечно урезывают сметы.
— Послушай, — прервал Уилл. — А как насчет бриллианта? В конце концов,
бриллиант с грецкий орех величиной — это тоже мелкий предмет...
— Извини, — с сожалением сказал бог, — но он будет совсем малюсенький.
Это должен быть бриллиант стоимостью не больше доллара и девяноста восьми
центов.
— Проклятье! — простонал Уилл. — Есть же, наверное, что-нибудь
маленькое...
— Конечно, — добродушно согласился бог. — Все, что в моих силах, в пределах
доллара и девяноста восьми центов, — только слово скажи.
— Тогда я пас,— сказал Уилл. Иип явно расстроился, и он добавил более
ласковым тоном: •
— Да не смущайся. Я знаю, ты от души хотел мне помочь. Не твоя вина, что
ты так стеснен в средствах. Может быть, ты еще что-нибудь надумаешь? Я за- ^
нимаюсь торговым посредничеством,— во всяком случае, пытаюсь, хоть мак- ю
лер из меня и неважный. Но если ты мог бы организовать мне выгодную 2
сделку... U
— Она принесет тебе один доллар и девяносто восемь центов чистой
прибыли, ф
43
— Это не так-то просто, — криво усмехнулся Уилл. — В настоящее время я
занимаюсь дизельными локомотивами, нежилыми помещениями и заброшенными
рудниками. И еще я вице-президент компании по эксплуатации иссякших
нефтяных скважин.
— Ну, и как идут дела? — спросил божок и лягнул кузнечика, который тут же
с негодованием ускакал.
— Мне почти удалось продать одному богатому калифорнийцу заброшенный
медный рудник под бомбоубежище, но Харли Томпсон, как всегда, оставил меня
с носом. Он показал этому покупателю, как на другом руднике можно
переоборудовать штрек в самый длинный — и самый безопасный — бар в мире. Ох уж этот
Харли! Я не против, что он стал начальником вместо меня: все равно я плохой
руководитель. Или что он переманивает у меня самых выгодных клиентов.
Я даже прощаю ему вечные подлые розыгрыши. Но когда дошло до Риты... А она
только-только стала замечать мое существование, — горько прибавил он.
— Рита? — переспросил бог.
— Рита Генри... Она работает у нас в конторе. Изумительная девушка!
— Понятно, — вставил Иип и показал нос стрекозе, вертевшейся поблизости.
— Вот тут-то мне бы и нужна была помощь. Так что сделай, что можешь,
хотя толку будет немного — ведь твой предел...
— Один доллар и девяносто восемь центов, — подхватил бог. — Ладно. Я
проведу здесь, в этом лесу, весь день и весь вечер в созерцании места, где находился
бы мой пупок, если бы я появился на свет, как простой смертный. Доверься
великому (хоть и мелкому) богу Иип у. Прощай.
И он скрылся в траве.
Вернувшись с прогулки поздно вечером, Уилл безрадостно улегся в постель,
убежденный, что помощь ценой в один доллар и девяносто восемь центов
наверняка не разрешит волнующую его проблему, даже если будет исходить от бога.
Несмотря на мрачные мысли, он так устал и изнервничался, что сразу же
заснул, но через полчаса проснулся, разбуженный звонком. Ничего не видя
спросонья, он накинул поверх пижамы халат и открыл дверь.
На пороге стояла девушка.
— Рита! — прошептал Уилл. — Наконец-то!
Она взяла его за руку.
— Меня словно какая-то сила толкала... Я не могла не прийти... Мы созданы
друг для друга...
Наутро Уилл подобрал с полу клочок бумаги. Это была газетная вырезка; на
полях бисерным почерком было написано: «От благодарного (в пределах 1,98
доллара) бога Иипа».
А краткая рекламная заметка гласила: «При современных ценах все
химические соединения, из которых состоит организм человека, можно купить всего
лишь за 1 доллар 98 центов».
Сокращенный перевод с английского Н. М, ЕВДОКИМОВОЙ
свер х ч истые
Чтобы определить
физико-химические константы (скажем,
температуру плавления вещества),
необходимо, чтобы вещество было
идеально чистым. Идеал этот,
конечно, недостижим, но исследователи
старались приблизиться к нему.
На лабораторных установках они
получали ничтожные количества
сверхчистых веществ.
Но настало время, когда
техника тоже потребовала особо
чистых веществ. Без них не могло,
например, развиваться
производство люминофоров. Наиболее
распространенные
люминофоры — сульфиды цинка и кадмия.
На их светоотдачу пагубно
влияют примеси железа и меди.
Содержание этих примесей
необходимо было понизить до 0,0005%-
Атомной энергетике также
требуются химические элементы и
Кандидат химических наук
Г. М. КУРДЮМОВ
соединения в высокочистом
состоянии — многие примеси
нарушают характер поглощения
нейтронов. Глубокой очистке
подлежат ядерные горючие — уран и
торий, и вспомогательные
материалы — бериллий, цирконий,
висмут, кадмий и другие. Так,
содержание примеси бора в уране
не должно превышать
стотысячной доли процента.
Еще одна область
применения — монокристаллы для
квантовых генераторов -— лазеров.
Конечно, науке и технике
нужны и особо чистые органические
вещества. Классический пример
(классика, которой меньше
полувека) — мономеры.
Высококачественный полимер получается из
них лишь при условии, что
содержание отдельных примесей не
будет превышать 0,01—0,001%- Без
биологических препаратов
высокой чистоты (витаминов,
ферментов, гормонов, антибиотиков)
немыслим прогресс
научно-исследовательских работ в области
молекулярной биологии.
Пожалуй, наиболее яркой
страницей в истории применения
высокочистых веществ останется
разработка полупроводниковых
материалов. Здесь потребовалось
получить ряд веществ такой
степени чистоты, которая до этого
казалась фантастической. Чтобы
полупроводниковый германий
имел требуемые
электрофизические параметры, содержание
большого числа примесей
пришлось понизить до 1*10~7 %! Это
означает, что один атом примеси
приходится на миллиард атомов
германия.
Развитие полупроводниковой
<
CQ
Ш
CQ
X
^
Я
<
с;
<
45
техники повлекло за собой
организацию промышленного
производства особо чистых веществ.
Правда, по сравнению с
«обычными» химическими веществами,
сверхчистые изготовляют в очень
малых количествах. Иногда даже
трудно провести грань между
лабораторным и промышленным
производством высокочистого
материала.
ни одной пылинки
Прежде чем рассказывать о
методах глубокой очистки
веществ, скажем несколько слов о
«смежных» проблемах. Очевидно,
сверхчистое вещество нужно
получать в сверхчистой аппаратуре,
воздух в помещении тоже должен
быть сверхчистым. Тривиальные
химические операции —
подготовка и мойка аппаратуры!
фильтрование, сушка, выпаривание,
прокаливание — в производстве
высокочистых веществ выглядят
совершенно по-иному, нежели при
изготовлении реактивов, не
говоря уже о технических продуктах.
Если не учесть хотя бы один из
факторов, влияющих на чистоту
конечного продукта, то результат
может оказаться плачевным.
Итак, прежде всего нужно
создать стерильные условия
производства. Первая опасность -— это
загрязнения, которые попадают в
очищаемые объекты из
окружающего воздуха. В атмосфере более
чем достаточно пыли, копоти,
пыльцы растений. Поэтому воздух
обязательно проходит через
систему фильтров. Глухие окна с
двойными рамами изолируют
помещение от внешней среды. На
стены, потолки, рабочие
поверхности наносят пылеотталкивающие
полимерные покрытия. Открытые
металлические поверхности,
представляющие потенциальный
источник «заражения» воздуха
продуктами коррозии металла,
полностью отсутствуют. В помещении
создают небольшое избыточное
давление, которое препятствует
проникновению извне
неочищенного, запыленного воздуха.
При работе с агрессивными
веществами все операции
выполняют не в обычных вытяжных
шкафах, а в шкафах-боксах. В них
обрабатываемый объект защищен
невидимой стеной очищенного
воздуха, который непрерывно
подается из специальных дюз.
Оператор находится в тамбуре,
примыкающем к шкафу-боксу.
Для самых ответственных
работ строят герметические
защитные камеры из органического
стекла. В такие камеры вводят
только перчатки для выполнения
всех манипуляций. Внутри
камеры — тщательно очищенный
инертный газ. Камеры загружают
и разгружают через шлюзы.
Одежда работников — тоже
ультрачистая. Она сделана из
синтетических химически стойких
тканей (лавсана, капрона и т. п.)-
У таких тканей есть одно важное
достоинство — они «не ворсят».
В некоторых, особо ответственных
случаях недопустима даже
косметика. Так, американская фирма
«Ай-Би-Эм» требует, чтобы
сотрудницы, работающие с
материалами высокой чистоты, отказались
от пудры, помады и кремов.
ФТОРОПЛАСТ ВЫРУЧАЕТ
А из каких материалов
изготовляют аппаратуру для
получения сверхчистых? Главным
образом — из полимеров. Впрочем,
если требования к чистоте не
слишком высоки (содержание
отдельных микропримесей в
очищенном материале 1*10~4 —
— 1-10-5%), то пригодны стекло,
фарфор, титан, специальные сорта
стали. Когда содержание
отдельных микропримесей не превышает
1 .Ю -МО"9 %, круг
используемых материалов резко
сужается. Например, для
производства некоторых сверхчистых
веществ потребовалось наладить
промышленный выпуск особо
чистого кварцевого стекла и
графита, что само по себе было
нелегкой задачей.
Особенно мало материалов,
пригодных для процессов
получения сверхчистых кислот, галогени-
дов германия и кремния, бора,
фосфора и других химически
активных веществ. Например, для
очистки весьма агрессивного
соединения — трихлорсилана
(основного сырья для
полупроводникового кремния) аппаратура и тара
могут быть изготовлены только из
фторопласта. Различные марки
фторопластов — единственно
приемлемые конструкционные
материалы и при получении
плавиковой кислоты особой чистоты,
широко применяемой в
полупроводниковой технике.
Хранение и транспортировка
ухудшают качество агрессивных
высокочистых веществ. Поэтому
такие продукты удобнее делать не
на каком-то одном химическом
предприятии, а прямо на местах
потребления, используя
небольшие установки. Малогабаритная
полностью автоматизированная
установка по получению плавиковой
кислоты особой чистоты была
разработана во Всесоюзном научно-
исследовательском институте хи-
.мических реактивов и особо
чистых химических веществ; она
демонстрировалась на
Московской международной химической
выставке и отмечена почетным
дипломом.
ДОСТИЖИМА ЛИ
АБСОЛЮТНАЯ ЧИСТОТА!
Высокочистые вещества
получают и традиционными способами
(например, экстракцией), и
современными способами глубокой
очистки. Разумеется, такое
деление несколько условно; и те, и
другие способы часто применяют
в сочетании Друг с другом.
Как глубоко можно очистить
вещество? В основе многих
способов очистки лежит такой прием.
В аппарате «сосуществуют» две
фазы: жидкость и твердое
вещество, жидкость и газ, две несме-
шивающиеся жидкости. Примесь
охотнее переходит в одну из фаз,
а другая (в ней находится
очищаемое вещество) становится беднее
примесью. Повторив такой
процесс много раз, можно добиться
высокой степени очистки.
Теоретически, если примесь
растворяется в жидкой фазе
лучше, чем в твердой, то ее
концентрацию можно понизить
неограниченно. Однако реально
достижимая степень очистки
определяется, как уже говорилось выше,
чистотой материала аппаратуры и
его химической стойкостью.
Абсолютно чистых и абсолютно
инертных материалов не существует. Во
время очистки наступает такой
момент, когда устанавливается
равновесие: сколько примеси
удаляется из материала, столько же
поступает из аппаратуры или
очищающего агента.
Конечно, идеальный вариант
процесса ультраочистки — это
удаление примеси без
соприкосновения очищаемого материала со
стенками аппаратуры, когда сам
материал помещен в вакуум.
Такой вариант реален — можно, к
примеру, испарять легколетучие
примеси из металла,
подвешенного в магнитном поле. Весьма
заманчиво вести такие операции в
46
«даровом» вакууме — в
космическом пространстве. Но вернемся
на Землю.
ИЗ ЖИДКОСТИ И ПАРА
Самый простой и веками
испытанный способ очистки —
кристаллизация из растворов. Этот
способ особенно широко
применяется при глубокой очистке
солей, которые многократно
кристаллизуют из водной среды.
Часто в раствор вводят комплек-
сообразователи, которые
препятствуют попаданию примесей в
выпавшие кристаллы вещества.
Иногда поступают наоборот:
осаждают примеси с каким-либо
труднорастворимым соединением, так
называемым коллектором, очищая
при этом исходный раствор.
Кристаллизация довольно
трудоемка. Нужно растворить
загрязненные кристаллы, провести
кристаллизацию, отделить чистые
кристаллы от загрязненного
раствора — и вновь повторить эти
операции.
■ч$к: • •* • • •
При зонной плавке вещества-
примеси передвигаются к краю
образца
Гораздо совершеннее метод
зонной плавки (его иногда
называют зонной
перекристаллизацией). Примесь неодинаково
растворяется в твердой и жидкой фазах
очищаемого вещества. Если
вещество заключить в длинную
узкую трубку и расплавить его у
одного конца трубки, то примесь в
этом месте перейдет в раствор.
Теперь расплавленную зону
заставляют двигаться вдоль трубки.
Расплав подхватывает по дороге
примеси и переносит их в конец
образца. После большого числа
таких проходов начальная часть
образца становится очень чистой.
Зонная плавка обычно
применяется на финише
технологической схемы получения
сверхчистого вещества (например, полу-
_,
На*
Са++,
_
erf
SOA=
^ J
v J
ОСОБОЙ ЧИСТОТЫ
исходная H20
Иониты «вытаскивают» из воды растворенные примеси
проводниковых германия и
кремния). Раньше зонную плавку
использовали только для очистки
металлов и полупроводниковых
соединений. В последние годы
этим методом получают в
высокочистом состоянии различные
вещества — и неорганические, и
органические. Правда, зонная
плавка малопроизводительна. Но
так как масштабы производства
сверхчистых веществ невелики, с
этим недостатком можно
мириться.
Если вещество испаряется при
невысокой температуре, го
ультраочистку можно провести таким
испытанным способом, как
ректификация. Очищаемое вещество и
вещество-примесь имеют разную
летучесть паров, и поэтому их
можно разделить в газообразном
состоянии. Многие элементы
сначала переводят в летучие
соединения (например, в хлориды),
которые затем очищают
ректифицированием, после чего вновь
выделяют элемент.
Различная растворимость
примеси в очищаемом веществе и
специально подобранной
жидкости — экстрагенте лежит в
основе метода жидкостной экстракции.
Вещество растворяют в
каком-нибудь растворителе (чаще всего —
в воде), и раствор приводят в
соприкосновение с экстрагентом.
В результате примеси
«высасываются» экстрагентом из
очищаемого раствора. Применяя несколько
экстрагентов, можно добиться
высокой степени очистки. Впервые
экстракция как способ глубокой
очистки была применена для
разделения и очистки соединений
урана, тория, циркония, гафния,
используемых в атомной технике.
Примеси из растворов
электролитов можно удалять и в ионооб-
менниках. Типичный пример —
получение воды особой чистоты.
Вода последовательно проходит
через колонку с катионитом,
поглощающим ионы металлов, и
анионитом, поглощающим
кислотные остатки. Содержание
примесей в очищенной воде колеблется
от миллионной до стомиллионной
доли процента.
основное вещество
примесь 2
мшм
л
I »Ш//Ж\
J2
3£
Препаративная газовая
хроматография — один из методов
глубокой очистки веществ
ПОЛЕЗНОЕ РАВНОДУШИЕ
В последнее время завоевал
признание сорбционный метод
очистки. Суть его состоит в том,
что исходный препарат
обрабатывается сорбентом — веществом,
«равнодушно» относящимся к
молекулам очищаемого вещества, и
в то же время жадно
поглощающим молекулы примеси.
Сорбенты — это чаще всего
активированные угли, силикагели, цеолиты, —
разумеется тщательно очищенные.
(Окончание на стр. 55)
47
ИОННЫЙ МИКРОПРОЕКТОР-
„микросноп"
для наблюдения
одиночных атомов
Д. БРЕНДОН
Ионный микропроектор (рис. 1)
мало похож на микроскоп.
Строго говоря, это даже вовсе не
микроскоп, так как частицы,
которые создают изображение, не
фокусируются, а
непосредственно переносятся от поверхности
исследуемого образца прямо к
флуоресцирующему экрану.
Главный «рабочий элемент»
ионного микропроектора — тон-
Рис. 1. Ионный микропроектор
используется для исследования
поверхности острия тонкой
металлической проволочки,
полученного при помощи электрополировки.
Для улучшения качества
изображения ее охлаждают жидким
азотом или водородом. Камера мик-
кая заостренная проволочка,
изготовленная из исследуемого
металла при помощи
электрополировки. Эта проволочка находится
в камере, содержащей
разреженный газ — например гелий,
неон или водород.
Чтобы получить изображение
поверхности острия, проволочку
охлаждают как можно сильнее и
затем заряжают до высокого по-
роскопа содержит сильно
разреженный газ, — например,
гелий или неон. Металлическая
проволочка заряжена до очень
высокого потенциала, и атомы
собираются вокруг вершины -—
зоны ионизации. Здесь они
теряют электроны и превращаются
ложительного потенциала. Близ
острия атомы разреженного газа
теряют электроны, передают их
положительно заряженному
металлу и становятся ионами; эти
ионы перемещаются затем
электростатическим полем по прямым
пиниям и, попадая на
флуоресцирующий экран, создают сильно
увеличенное изображение
поверхности острия.
в положительные ионы, которые
под действием поля немедленно
направляются прямо к экрану.
Каждый ион при попадании на
экран дает световую вспышку;
сфотографировав экран, можно
получить изображение атомов на
поверхности острия (см. вклейку).
к насосу низкого вакуума
от-3 до-ЗОкв
внутренний сосуд
Дьюара
индиевое металлическое
уплотнение
к сосуду с гелием
внешний сосуд
Дьюара
медный цилиндр
флуоресцирующий
экран
индиевое
металлическое
уплотнение
га
от-З \
до-ЗОкв
1 зона
i ионизации
П**^
*
г
/
[L
^острие}
^ооразцг
TLVWyZ'ffl'
Щш
1
i
,-\
'
i
>
/ s
л*
атомы газа .
^р— м-*
\
радиальные
троектории
ионов
\
_Л
+
флуоресцирующий экран
4S
Вероятность того, что атом
газа потеряет электрон и станет
ионом в значительной степени
зависит от напряженности
электростатического поля близ
поверхности острия; ионы
образуются только в местах, где это
поле особенно сильно, например,
над атомами, выступающими из
поверхности. Таким образом
ионное изображение есть по сути
дела изображение атомной
структуры поверхности металла.
Увеличение, которое дает
ионный микропроектор, равно
отношению расстояния между
вершиной острия и экраном к диаметру
острия; его порядок — миллион.
Однако практически увеличение
ограничивается размером атомов
газа, находящегося в
микропроекторе, а также температурой острия
проволочки, Еспи острие
охлаждено до температуры кипения
жидкого азота, толщина его —
несколько сот атомных
диаметров, а в качестве
«изображающего» (то есть создающего
изображение] газа используются гелий,
неон или водород, то с помощью
микропроектора можно увидеть
отдельные атомы.
Поскольку в ионном микро-
1
2\
3
|4
5 1
6 |
БУДЬ ЗДОРОВ9 ДОМ!
полимерные строительные герметики
В. ЦУКЕРМАН, режиссер студии ссМоснаучфильм»
«Герметика, это хорошо сказано... Мне всегда
нравилось слово «герметический». Волшебное слово,
вызывающее неопределенные и далеко идущие
ассоциации»
Томас Манн. «Волшебная гора»
Я вспомнил слова Томаса Манна, когда мне
поручили поставить фильм о полимерных строительных
герме тиках.
Тема, действительно, вызывала «неопределенные
и далеко идущие ассоциации». Слова «герметик»,
«герметизация» родились в древней Греции.
Произошли они от имени бога Гермеса. Считается, что
этот греческий бог занимался герметизацией
бутылок с вином, обмакивая их горлышки в сургуч.
Но какое отношение имеют бутылки к
строительству! Разве дома можно и нужно герметизировать!
Если это так, то почему для этой цели
употребляются полимеры! И как строили, когда полимеров не
было! Сейчас фильм готов, и я почти без труда
могу ответить на эти вопросы.
Строительные герметики — это материалы,
предохраняющие дом от проникновения внутрь дождя,
ветра, холодного воздуха. С незапамятных времен
люди строят дома, но необходимость в полимерных
герметиках возникла только недавно, и возникла она
тогда, когда появилось крупнопанельное
строительство.
В кирпичном доме между кирпичами —
цементный раствор. Он кадежно защищает внутренность
дома от атмосферных воздействий. В деревянном
доме между бревнами лежит просмоленная пакпя —
и она защищает дом от дождя. Когда начали строить
панельные дома, попробовали между панелями
прокладывать цементный раствор или пакпю. Результат
получился плачевный: стены новых домов протекали
при каждом косом дожде.
Депо в том, что панели гораздо больше бревен
и, тем более, кирпичей. А чем больше предмет, тем,
естественно, сильнее он расширяется при
нагревании и сжимается при охлаждении. С изменением
погоды размеры панелей сильно меняются, меняется
и величина щели между ними. В такой
«пульсирующей» щепи пакля сминается, а цементный раствор
крошится. Нужны были герметики — эластичные,
повторяющие за панелью каждое ее движение и при
этом не теряющие герметизирующих свойств.
Способными на такую работу оказались только
полимеры. Полимерные герметики пришли на
стройки, и теперь можно не опасаться за «здоровье»
панельных домов.
На цветной вклейке вы видите кадры из нашего
фильма:
1. Геодезический купол, построенный в Москве
америквнцами. Он загерметизирован очень дорогим
герметиком — тиоколом. Гигантские масштабы
нашего массового строительства требуют более
дешевых герметиков.
2. Дешевый полимер — полиизобутилен
смешивается на вальцах с другими компонентами. Так
рождается полимерный герметик.
3. Новый герметик получает в лаборатории
порцию косого дождя. Тяжело в ученье — легко в бою.
4. Главное достоинство — эластичность. Мастика
УМС-50, полученная из попиизобутипена, проходит
испытание на разрывной машине.
5. Эти жгуты — тоже строительные герметики:
черные — пороизол, серые — гернит П.
6. Гернит П изготовляют из синтетического
каучука найрита. Пористая структура делает герметик
упругим и эластичным.
4 Химия и Жизнь, № 10
49
&ьб 4 4,5 6 О.Ь
о
Напряженность поля в/А
Рис. 3. Влияние
температуры на
электростатический
потенциал, необходимый
для возникновения
потока ионов между
образцом и экраном.
С понижением
температуры этот
потенциал уменьшается
проекторе напряженность
электростатического попя очекь
велика, выступающие из поверхности
вершины атомы металла могут
свми превратиться в ионы. Это
явление носит название
испарения попем и используется
для окончательной очистки
поверхности вершины от
загрязнений, а также для ее завершающей
полировки; иногда, удалив
таким способом с поверхности
образца несколько слоев атомов,
удается исследовать внутреннюю
структуру металла.
Стабильное ионное
изображение получается только тогда,
когда атомы «изображающего»
газа уже ионизируются, а
испарения полем еще не происходит;
в ином случае образец будет
испаряться во время
наблюдения.
Если образец — сплав, то это
приведет к искажению картины
|рис. 2J.
Рис. 2. Сплав вольфрама и рения
дает при испарении полем
«шероховатую» поверхность, так как
его компоненты улетучиваются с
различной скоростью
Напряженность
электростатического поля, необходимая для
того, чтобы возникло ионное
изображение, возрастает с
ионизационным потенциалом
используемого газа, а также с
температурой острия {рис. 3). Три газа, с
помощью которых можно
получить изображения единичных
атомов, — гелий, неон и водород —
имеют ионизационные
потенциалы 24,6; 21,6 и 13,6 эпектрон-вопьт
соответственно. Ионизационный
потенциал гепия так высок, что он
дает удовлетворительное
изображение только тех металлов, у
которых температура плавления
очень высока; для металлов,
температура ппавпения которых ниже
1500 С, испарение попем
начинается раньше, чем создается
изображение.
С другой стороны, если в на-
честве «изображающего» газа
используется неон, то яркость
изображения (особенно при больших
увеличениях] резко снижается.
Впрочем, сконструированные
недавно усилители изображения
сделали это препятствие
несущественным: теперь картины,
полученные с помощью ионкого
микропроектора, можно
фотографировать с выдержками меньше
секунды. Другой путь увеличения
яркости — это преобразование
ионного изображения в
электронное вне микроскопа. В этом
случае экран покрывается
веществом, испускающим электроны при
бомбардировке ионами;
электроны, в свою очередь, создают
изображение на флуоресцирующем
экране.
Информацию, полученную лри
помощи ионного микропроектора,
не так уж просто расшифровать.
До последнего времени
большинство исследователей
довольствовалось скорее записью единичных
изображений и их интерпретацией
на основе предварительных
данных об образце, не исследуя
влияние условий ионного испарения
и проецирования на характер
изображения. В результате
действительные возможности
прибора редко использовались
полностью даже тогда, когда
полученная информация была
уникальной.
Сокращенный перевод
Е. СЕНЧЕНКОВА
из журнала «Discovery»
50
ПАМЯТЬ, ХИМИЯ
И КИБЕРНЕТИКА
Доктор химических наук В. А. КУХТИН
Рисунок Д. АНИКЕЕВА
Память — одно из самых важных и самых
интересных свойств мозга. Память,
позволяющая нам помнить, что огонь жжет, а нож
режет. Память, позволяющая живому
существу быстро ориентироваться в сложнейших
ситуациях и находить правильное решение.
Память, позволяющая человеку мыслить,
творить, познавать неведомое.
Иногда она очень капризна — не может
отыскать нужное нам имя, мешает
повторить любимые стихи; а иногда видишь будто
бы незнакомое лицо, чужой пейзаж — и
вдруг все озаряется вспышкой: я видел это-
го человека, был здесь когда-то, давным-
давно...
«ЭЛЕКТРИЧЕСКАЯ» ПАМЯТЬ?
Первые научные гипотезы памяти
возникли на основе исследований
электрической активности мозга. Сейчас точно уста-
51
новлено, что передача нервного импульса
имеет электрохимическую природу. Мозг
состоит из 14 миллиардов нервных клеток —
нейронов, связанных между собой в
причудливую мозаику отростками — аксонами
и дендритами, причем один нейрон
может иметь десятки, сотни и даже тысячи
связей.
Во время работы мозга по сложным
цепям этой мозаики проносится неисчислимое
количество электрических импульсов.
Изучение электрофизиологической картины мозга
позволило разработать «электрическую»
теорию памяти — теорию реверберирую-
щих сетей (в акустике реверберацией
называют «запаздывание» звука, который
благодаря отражению и рассеянию звуковых волн
может быть слышен еще некоторое время
после выключения его источника).
Основные положения этой теории сводились к
тому, что память обусловливается
существованием в сложной системе нейронов
долговременных замкнутых токов, кодирующих
своим сочетанием тот или иной образ.
Количество нейронов в мозгу и возможных
связей между ними позволяет закодировать
такими сочетаниями большое количество
информации.
, Однако эта теория вскоре оказалась
недостаточной. Прежде всего, опыты
показали, что при действии на живой организм
глубокого охлаждения, наркоза или
электрошока электрическая активность мозга
исчезает почти полностью.
Но память при этом не исчезает и не
ослабляется.
Во-вторых, существование огромного
количества постоянно действующих
электрических цепей требовало бы от мозга
огромной затраты энергии (если не предположить,
что нейронные цепи являются
сверхпроводниками, что совершенно невероятно).
Все это приводило к мысли, что
недолговременная электрическая активность в ре-
верберирующих сетях может быть основой
лишь кратковременной памяти. Сеть
возбуждения, кодирующая условный образ,
быстро затухает, образ исчезает из памяти,
если... если за это время в нейроне не
успевают произойти определенные изменения
на молекулярном уровне, оставляющие
долговременный след.
Какова же природа этих молекулярных
изменений, или, как говорят многие ученые,
какова «энграмма памяти»?
В ПОИСКАХ ЭНГРАММЫ
В последние годы в разных странах
велись активные поиски молекулярных основ
памяти — тех нестираемых следов, которые
остаются в нервной клетке после
многократного прохождения определенной
системы импульсов. Если через многие годы на
одной из клеток кодирующей цепи
возникнет сходная ситуация, благодаря этим
«следам» во всей цепи должен произойти
разряд, аналогичный исходному, и таким
образом «вспоминается» образ.
Мне кажется, что из существующих
гипотез памяти наиболее интересны три:
гипотеза Хидена о роли РНК как энграммы
памяти, гипотеза Ландауэра о значении гли-
альных РНК в механизме запоминания и
гипотеза Рыжкова, полагающего, что следы
памяти хранятся в ДНК.
Мы не будем подробно описывать
эксперименты, позволившие X. Хидену
высказать свою гипотезу: этим работам
посвящена опубликованная в № 9 статья доктора
химических наук В. С. Тонгура. Сформулируем
лишь вкратце основные положения, которые
лежат в основе этой гипотезы.
Электрохимическая природа нервного
импульса состоит в том, что при его
прохождении через данный участок нервного
волокна (аксона) ионы натрия поступают
внутрь аксона через его мембрану, а ионы
калия почти в то же мгновение выходят
наружу. Таким образом, ионная среда
нервной клетки изменяется. По мнению Хидена,
эти изменения способны воздействовать на
устойчивость азотистых оснований,
входящих в состав молекулы РНК. Далее может
происходить замена того основания, связь
которого с молекулой ослаблена, каким
либо другим основанием, содержащимся в
клетке; новая молекула РНК, подвергшаяся
такой мутации, будет синтезировать белок,
отличающийся от синтезированного
исходной молекулой, Хиден предполагает, что
новый белок способен реагировать на те же
самые импульсы, под действием которых
возникла измененная РНК, Если через
некоторое время на клетку подействует такой
импульс, происходит замыкание нервной
цепи, определившей ранее изменения РНК
в образующих ее клетках, и мозг
вспоминает закодированный данной системой образ.
Что здесь можно считать более или
менее доказанным? Во-первых, то, что во вре-
52
мя стимуляции нервной клетки
увеличивается суммарное количество РНК в клетке и
изменяется ее суммарный нуклеотидный
состав. Во-вторых, то, что подавление или
стимулирование синтеза РНК подавляет или
стимулирует способность к обучению, не
влияя на ранее приобретенный опыт.
Что касается первого результата, то
противники гипотезы Хидена справедливо
заметили, что в нем нет ничего удивительного.
Наоборот, было бы странно и непонятно,
если бы количество и состав РНК в нервной
клетке не изменились в период ее активной
деятельности. РНК — это
приказы-инструкции, посылаемые ДНК в рибосомы — цехи
синтеза белка. ДНК все время посылает
тысячи таких приказов. И когда активность
клетки (любой клетки, будь то нервная,
мышечная, печеночная и т. д.) возрастает,
растет и количество приказов о синтезе
нужных клетке белков, а их содержание,
естественно, изменяется.
Второй результат более значителен. Он
может свидетельствовать о том, что в
общем потоке новых РНК имеются такие, без
которых не может произойти запоминание.
Другими словами, ясно, что какое-то
участие в процессах памяти РНК принимает. Но
это отнюдь не значит, что РНК и есть
субстрат памяти, носитель энграммы памяти.
Если клетке для запоминания необходим
синтез какого-то белка-фермента, то этот
синтез может совершиться только под
влиянием приказа-инструкции в виде новой
РНК.
И вероятнее всего, что молекулы РНК
в этом случае играют не какую-то особую,
специфическую роль, а выступают в
обычной для них роли передатчиков
информации. С точки зрения химика кажется
невероятным, чтобы такое грубое воздействие,
как изменение концентрации ионов, могло
приводить к тонким направленным
мутациям в какой-либо части какой-либо одной из
многих сотен РНК, как это предполагает Хи-
ден. С другой стороны, едва ли изменения
ионной силы в клетке настолько велики,
чтобы порвать связи в РНК. А если они
достаточны для этого, то должны были бы
изменить одновременно все аналогичные
участки РНК, а это привело бы к полной
дезорганизации работы клетки и ее гибели.
Кроме того, известно, что
информационные РНК в большинстве случаев,
очевидно, существуют очень недолго. Молекула
передала приказ-инструкцию на синтез
белка, белок получен, инструкция-матрица
больше не нужна и сразу же разрушается.
Следовательно, и по своей природе РНК
едва ли может быть долговременным
хранилищем какого-то отпечатка.
Вот почему гипотеза Хидена кажется
многим ученым маловероятной.
КЛАДОВАЯ ПАМЯТИ?
Вторая гипотеза о механизме памяти
была выдвинута американским ученым
Т. Ландауэром.
Известно, что поверхность каждого
нейрона покрыта так называемыми глиальными
клетками. Они заполняют и все
пространство между нейронами. Глиальных клеток в
мозгу человека около 140 миллиардов —
в 10 раз больше, чем нервных; на их долю
приходится более половины веса всего
мозга. Одна из основных функций глиальных
клеток точно установлена: это как бы
кладовая нейрона и в то же время его
защитный барьер. Все вещества поступают из
кровеносных сосудов сначала в глию, и только
из нее попадает в нейрон все, что
необходимо ему для жизнедеятельности.
При прохождении импульса по нервному
волокну внутренний потенциал клеточной
мембраны сильно изменяется за очень
короткое время. По мнению Ландауэра, в этот
момент нейрон может «вытаскивать» из
своей «кладовой» — из глии — путем
электрофореза большое количество РНК.
В остальном механизм, предлагаемый
Ландауером, сходен с механизмом,
рассматриваемым в гипотезе Хидена.
Появление новых РНК в клетке должно привести к
усиленному синтезу специфичного белка-
фермента, способного изменить
проницаемость синапса — места контакта нервных
клеток, придать ему специфичную
частотную настройку. В дальнейшем, при
воспоминании, нервная цепь, кодирующая данный
образ, будет легко воссоздаваться.
Гипотеза Ландауэра представляет
определенный интерес, хотя никаких
экспериментальных данных ни в ее защиту, ни для ее
опровержения, к сожалению, нет.
ПАМЯТЬ И ХРОМОСОМЫ
Третья упомянутая нами гипотеза
выдвинута совсем недавно советским
биологом, членом-корреспондентом АН СССР
53
В. Л. Рыжковым. Она основана на работах
автора по влиянию ионов натрия и калия на
функционирование хромосом слюнной
железы насекомых. Казалось бы, от слюнных
желез насекомого до мозга человека —
дистанция огромного размера. Но в природе
чрезвычайно много общих
закономерностей, объединяющих очень далекие друг от
друга живые организмы. Природа никогда
не «выдумывает» принципиально нового
механизма, если может использовать уже
имеющийся. Поэтому такой подход к проблеме
памяти весьма обоснован и логичен.
Хромосома в «спокойном» состоянии —
это как бы закрытая книга. Чтобы на
определенном участке ее ДНК начался синтез
информационной РНК, необходимо открыть
нужную страницу — отделить каким-то
образом друг от друга комплементарные цепи
ДНК. Недавние наблюдения на слюнных
железах насекомых показали, что при
изменении концентрации натрия и калия в ядре
клетки на хромосомах образуются
«пуфы»— участки, где одна из цепей ДНК как
бы «отлипает» от второй. На
освободившемся участке, вероятно, и начинается синтез
нужной РНК.
Почему же не предположить, что
аналогичный механизм может срабатывать и в
нервной клетке? Рыжков формулирует свою
гипотезу примерно следующим образом.
При нервном возбуждении в
хромосомном аппарате ядра нервной клетки под
влиянием изменений концентраций натрия и
калия может происходить раскручивание
двойной спирали ДНК и образование
активных центров синтеза РНК. Такие изменения
в хромосоме немедленно отразятся на
характере синтеза информационных РНК и
белков в клетке. В. Л. Рыжков считает, что
такая специфическая спирализация или де-
спирализация хромосом может быть весьма
устойчивой и может, таким образом,
надолго сохранять, запечатлевать пережитое
клеткой возбуждение.
Иными словами, гипотеза Рыжкова
предполагает, что энграммой памяти может
быть временная или постоянная активация
или дезактивация отдельных участков
хромосом нервных клеток.
Гипотеза Рыжкова, особенно в первой ее
части, заслуживает серьезного внимания.
Действительно, раз известно, что тончайшие
изменения концентраций натрия и калия
способны управлять хромосомами, то
почему бы природе не использовать этот
механизм, чтобы заставить ДНК под действием
нервного возбуждения дать приказ о
синтезе белка, необходимого клетке для
сохранения следов памяти?
Что же касается второй части этой
гипотезы— о сохранении следов возбуждения в
структуре ДНК,— то здесь уместно задать
вопрос: а действительно ли это
необходимо? Действительно ли необходима какая-то
специфичная «энграмма», способная при
помощи тонких изменений структуры
сохранять многообразные специфичные следы
старых возбуждений? И нужно ли говорить
вообще об «энграмме» памяти, искать
молекулу, способную закодировать память в
своей структуре? Мне кажется, что это
обусловлено могучим притягательным
действием грандиозных успехов молекулярной
генетики — раскрытия кода наследственной
генетической памяти организма. Но нужно
ли и должно ли подходить к памяти мозга
лишь с этих позиций?
НУЖНА ЛИ ЭНГРАММА?
Давайте попробуем подойти к этой
проблеме с другой стороны — с точки зрения
нейрофизиологии, кибернетики и теории
информации.
В одной клетке, возникшей после
слияния двух половых клеток, хранится
зашифрованная в ДНК информация о развитии
всего организма. В хромосомном аппарате
зашифрован весь механизм развития
организма, вся специфика биологического вида,
все механизмы внутренней регуляции, все
инстинкты и безусловные рефлексы,
характер и темперамент индивидуума. Я не знаю,
как это измерить в битах информации, но
думаю, что здесь содержится сведений
гораздо больше, чем может вместить вся
система памяти человека, состоящая из
14 миллиардов клеток мозга.
И если в одном случае природе удалось
втиснуть огромную информацию в одну
клетку, а в другом случае для хранения
памяти понадобились миллиарды клеток, то,
очевидно, основные механизмы, основные
принципы хранения информации здесь
совершенно различны.
Последние достижения нейрофизиологии
и нейрокибернетики, попытки
моделирования процессов опознавания образов говорят
о том, что мыслительные процессы в мозгу
54
основаны, вероятно, на тех же законах
теории информации, что и в электронных
машинах. Доказано, что нервный импульс тоже
подчиняется закону «да — нет». В любом
нейроне, независимо от силы раздражения,
импульс имеет постоянную амплитуду и
форму. Интенсивность ощущения изменяет
лишь количество импульсов и количество
возбужденных нейронов.
Конечно, нельзя сводить нейрон к
простой лампе или транзистору. По мнению
многих ученых, нейрон — это скорее целый
блок в механизме мышления и памяти. В
отличие от элемента кибернетической машины
он может участвовать в сотнях связей и
тысячах комбинаций.
Но принцип экономной передачи
информации гласит, что невыгодно все время
передавать образ целиком — можно его как-
то закодировать и передать лишь начало и
конец действия. Когда вы посылаете
поздравительную телеграмму, телеграф
передает не изображение художественного
бланка, а лишь его шифр.
И вот недавно нейрофизиологи
обнаружили, что отдельные нейроны, подобно
элементам электронной машины, реагируют
лишь на изменение раздражения —
фиксируют движение, начало и конец
действия.
Не пытаясь свести структуру мозга к
упрощенной схеме кибернетической
машины, мы все же вполне обоснованно можем
предполагать, что работой мозга управляют
законы передачи и хранения информации в
кибернетических устройствах, а не законы
передачи генетической информации —
законы совершенно другого, внутриклеточного
порядка.
А если подходить к нервной клетке с
этих позиций, то мы прежде всего должны
понять принципиальную разницу между
наследственной памятью и памятью
мышления. В любой клетке закодирована вся
история вида и специфические особенности
родителей. А нейрон, один отдельно взятый
нейрон, не несет никакого образа: он
должен «помнить» лишь количество и качество
прошедших через него импульсов. Это
позволяет ему в определенных условиях
включаться в нужную цепь, которая и служит эн-
граммой образа.
Как же нейрон суммирует количество и
направленность прошедших через него
импульсов? Каков механизм этой суммации,
как она происходит? Вот вопросы, которые,
как мне кажется, должны мы обсуждать и
решать вместе с биофизиками и нейроки-
бернетиками. Здесь, вероятно, основную
роль играет изменение проницаемости
мембран нейрона, их специфичная настройка,
изменение реакции синаптических связей на
импульс. Но для этого не надо ни
перестановки нуклеотидов в РНК, ни нестираемых
пуфов в ДНК. Всего лишь один
специфический и стандартный для всех нервных клеток
белок может в зависимости от его конфор-
мации и количества вступать в комплекс с
липидной мембраной и менять ее
проницаемость и, возможно, частотную настройку.
Картина может оказаться и более
сложной— мы еще очень мало знаем, впереди
огромная целина, которую должен
вспахать эксперимент. Но самое важное,
по-моему,— это не только искать с позиций
молекулярной генетики таинственную «энграмму
памяти», а изучать в совокупности весь
механизм памяти.
СВЕРХЧИСТЫЕ
Сорбционную очистку можно
вести и в жидкой, и в перовой фазе.
Изменяя в широких пределах
соотношение количеств сорбента и
очищаемого вещества, скорости
потоков, температуру и т. д.,
можно достичь исключительно
высокой чистоты. Сорбционным
методом пользуются, например, при
ультраочистке хлористого
водорода с последующим получением
Окончание. Начало на стр. 45.
соляной кислоты особой чистоты
и хлоридов полупроводниковых
элементов.
К сорбционным процессам
относится и препаративная газовая
хроматография — способ очень
перспективный для глубокой
очистки многих трудноочищаемых
веществ, прежде всего —
органических. Исходная смесь (в виде
пара) подхватывается потоком газа-
носителя и поступает в колонку —
длинную узкую трубку,
заполненную специальным веществом, так
называемой неподвижной фазой.
Это вещество поглощает
введенную в нее смесь, и затем
выделяет ее вновь под влиянием
«вымывающего» действия
газа-носителя. Но компоненты смеси
неодинаково поглощаются
неподвижной фазой, и она по-разному
тормозит их передвижение через
колонку. В результате на выходе
из колонки компоненты смеси
разделяются и выделяются в
чистом состоянии.
Описанные здесь способы
далеко не исчерпывают
многообразия приемов ультраочистки. Эти
способы уже перешагнули порог
лабораторий и поставлены на
службу производству.
55
КИСЛОТА
В НАШЕЙ ПИЩЕ
И. ВОЛЬПЕР
Стремление сдабривать пищу кислым, равно,
как и соленым, возникло еще во времена
глубокой древности. Во всяком случае, уксусом как
вкусовой приправой люди пользовались еще две-
три тысячи лет тому назад. Само слово «уксус»
происходит от греческого «оксос», что значит —
кислый. В старину уксус был единственной
пищевой кислотой, и неудивительно, что название
его отождествлялось с самим представлением
о кислом. Со временем в пищу стали добавлять
и другие кислые вещества: люди начали
употреблять лимонный еок, а потом научились
извлекать из него лимонную кислоту. Обратили
внимание на кислый вкус винного камня,
осаждающегося на внутренней поверхности винных
бочек, и разработали способ получения из него
винной кислоты.
Позже открыли еще молочную кислоту и
много других.
Почему же кислоты кислы, какова природа
ощущения кислого?
Общеизвестно, что в водных растворах любая
кислота диссоциирует на ионы водорода и ионы,
которые мы называем радикалами кислот. Так,
соляная кислота разлагается на положительно
заряженный ион водорода И ' и отрицательно
заряженный ион хлора С) '; серная кислота дает
в растворе два иона водорода и отрицательно
заряженный радикал S04 . To же самое
происходит и при диссоциации органических кислот.
Ионы водорода, действуя на окончания вкусовых
нерв»в, и вызывают ощущения кислого. Не
случайно кислотность любого раствора измеряется
количеством граммионов водорода на литр
раствора. Так как концентрация водородных
ионов в растворе — величина очень малая, то для
удобства пользуются не действительным
значением ее, а десятичным логарифмом этого числа,
взятым с обратным знаком. Этот водородный
показатель, по предложению датского химика
Серенсена, принято обозначать символом рН
(рН — первые буквы от латинских слов pundus
Hydrogenium, т. е. вес водорода). Обозначив
концентрацию ионов водорода [Н ], можно написать:
рН=—lg[H ].
Если рН = 7, то это значит, что в одном литре
раствора содержится 10 граммионов водорода,
и такой раствор принято считать совершенно
нейтральным. Если этот раствор попробовать на
вкус, никакой кислинки не почувствуешь. При
значениях рН меньше 7 мы имеем дело с
кислыми растворами; чем меньше рН, тем, стало быть,
больше водородных ионов в растворе, и тем он
кислее. Были времена, когда единственным
индикатором на кислотность раствора был его вкус.
Химик, титруя кислоту щелочью, время от
времени пробовал раствор и определял конец
титрования по исчезновению кислого вкуса.
Но величина рН (активная кислотность) не
всегда совпадает с ощущаемой на вкус. Дело
в том, что «кислотность» — субъективное
ощущение кислого — связана не только с кислотностью,
но и с некоторыми сопутствующими
ощущениями — е температурой вещества, его запахом и
неодинаковым побочным действием разных кислот
на наши вкусовые органы.
Так, достаточно чтобы в 100 мл раствора
содержалось 0,0036 г соляной кислоты, как мы уже
ясно ощущаем вкус кислого; а вот молочной
кислоты для этого потребуется почти в шесть
раз больше @,0207 г на 100 мл). Из органических
кислот самая «кислая» — винная, а наименее
кислая — молочная. Среднее положение между
ними занимают уксусная и яблочная кислоты.
А теперь поговорим об отдельных, самых
распространенных пищевых кислотах.
НАПИТОК
ЦАРИЦЫ
КЛЕОПАТРЫ
Самая древняя пищевая кислота — уксусная.
По свидетельству знаменитого историка
древности Плиния старшего, для египетской царицы
56
Клеопатры приготовили особый напиток,
растворив в уксусе... жемчуг. Вряд-ли кто-нибудь
сейчас отважится попробовать этот драгоценный
напиток!
Но и в наше время уксус незаменим, когда
надо заправить салат или сварить маринад.
Из чего же делают уксус? Если вино долго
хранить в открытом виде, оно скисает —
превращается в уксус. Это было известно еще в
старину, но тогда считалось, что вино скисает «само
по себе», без какого-либо постороннего
вмешательства. На самом деле скисание вина или
превращение любой жидкости, содержащей
этиловый спирт, в уксус — это химический или точнее
биохимический процесс, происходящий при
обязательном участии особых микроорганизмов —
уксуснокислых бактерий. Они окисляют
этиловый спирт и превращают его в уксусную
кислоту:
сн,сн2он ; о2 >сн3соон ; н2о.
спирт уксусная
кислота
Этот процесс — основа наиболее
распространенного способа получения так называемого
«столового» уксуса из вина, пива или других
жидкостей, содержащих спирт. Иногда полученный
таким образом уксус настаивают на душистых
травах или пряностях. Так получается
ароматический уксус, содержащий 5—6 процентов
уксусной кислоты.
Синтетическую уксусную кислоту получают из
ацетилена. В основе этого способа лежит
классическая реакция образования уксусного
альдегида, открытая в конце прошлого века русским
химиком М. Г. Кучеровым. По этой реакции (она
вошла в науку под названием реакции Кучеро-
ва) ацетилен присоединяет воду и превращается
в уксусный альдегид:
/Н
СН НС | Н20 > СН3С.
ацетилен О
уксусный
альдегид
Уксусный альдегид нужно окислить, и тогда
получится уксусная кислота:
/Н
СНдС^ + О -> СН3СООН.
о
уксусный уксусная
альдегид кислота
Эти две реакции — основа промышленного
синтеза уксусной кислоты из такого дешевого
и доступного сырья, как ацетилен. Уксусную
кислоту извлекают также при сухой перегонке
дерева.
/#*Щ332у ЛИМОННАЯ —
ЧШ§^т значит
-Ш^^ЩЛ из лимонов?
Еще лет сорок назад на зтот вопрос можно
было ответить только утвердительно. Лимонную
кислоту получали только из лимонов. Мякоть
лимонов содержит до 7% лимонной кислоты. Из
плодов отжимали сок. В отжатый сок добавляли
химически чистый мел, который вступал в
реакцию с кислотой, и образовывалась кальциевая
лимоннокислая соль — цитрат кальция. Эта соль
выпадала в осадок, ее отделяли от раствора и
обрабатывали серной кислотой. Затем
освобождались от гипса (CaS04), и после этого раствор
концентрировали и подвергали кристаллизации.
Технология была довольно хлопотной. Но
дело не только в этом. Лимонную кислоту могли
производить только те страны, жаркий климат
которых позволял выращивать лимоны в
больших количествах. Кислота стоила довольно
дорого: чтобы получить полтора-два килограмма
кристаллической кислоты приходилось
перерабатывать чуть ли не целую тонну плодов.
Но ведь лимонная кислота играет важную
роль в народном хозяйстве; она нужна не только
пищевикам, но и медикам, текстильщикам,
фотографам. Естественно, что найти другой, более
экономичный способ получения лимонной
кислоты стремились давно.
Решение задачи, на первый взгляд, кажется
несколько неожиданным. Выяснилось, что,
используя плесневые грибки из семейства «Аспер-
гиллус нигер», лимонную кислоту можно
получить из сахара, превращая сладкое в кислое.
Способ зтот был разработан еще в тридцатых
годах, и тогда монополии лимонов в
производстве лимонной кислоты наступил конец. Со
временем технологи сумели использовать для
производства лимонной кислоты даже отходы
сахарного производства — мелассу. Меласса содержит
до 50 процентов сахара, а также азотистые
вещества, которыми питаются плесневые грибки.
Они вызывают лимоннокислое брожение сахара.
Лимоннокислое брожение» с химической точки
зрения, — это процесс окисления простейшего
сахара — глюкозы в лимонную кислоту:
2ССН1206 | ■ 302 -> гС.ад 4НзО.
глюкоза лимонная
кислота
57
Все последующие операции выделения
лимонной кислоты из полученного маточного раствора
принципиально не отличаются от способа
получения кислоты из лимонов. С экономической
точки зрения, биохимическое производство
лимонной кислоты гораздо выгоднее, чем
производство ее из лимонов. Подсчитано, что урожай
лимонов с одного гектара плантации дает в среднем
400 килограммов кристаллической кислоты, а из
сахара, полученного с одного гектара
свекловичного поля, можно выработать 1600 килограммов
кислоты. Преимущества нового способа очевидны.
Вот почему на вопрос, поставленный в
заголовке, следует ответить отрицательно. Нет,
лимонная кислота — не из лимонов, а из сахара.
Это и доступнее и выгоднее.
ЯБЛОЧНАЯ КИСЛОТА
ИЗ УГЛЯ
Извлекать лимонную кислоту из лимонов
невыгодно. Но как бы то ни было, в мякоти лимо-
*i/нов — 7% лимонной кислоты. А яблочной
кислоты содержится в яблоках: всего лишь десятые
доли процента. Добывать яблочную кислоту из
яблок было делом явно неразумным.
Лет десять с лишним назад ученые
Украинского научно-исследовательского института
пищевой промышленности разработали синтез
яблочной кислоты из такого широко
распространенного химического сырья, как бензол. Этот
синтез протекает так. Сначала бензол окисляют
кислородом воздуха в малеиновый ангидрид —
исходный продукт многих органических
синтезов:
сн со\
С6Н6 5,50, -> || О -ч 2С02 + 2Н20.
СН СО
бензол малепноаый
ангидрид
Затем малеиновый ангидрид подвергают
гидратации (гидратация — реакция присоединения
воды):
СН—СО\ СН-СООН
|' О -^Н20 -> I'
сн—со/ сн—шин
малеиновый ангидрид малеиновая кислота
СН^СООН СН2—СООН
ФН20 ->
Самый трудный зтап н зтом синтезе —
окисление бензола. Оно происходит только при
высокой температуре (около 400—500°С) в
присутствии сложного катализатора, состоящего из трех
металлов: ванадия, молибдена и кобальта в
соотношении 7:4:1. Гидратацию малеиновой
кислоты осуществить легче. Катализатор в этой
реакции простой и общедоступный — серная
кислота.
Бензол — основное сырье для синтеза
яблочной кислоты — продукт переработки каменного
угля. Поэтому мы с полным основанием можем
сказать — кислота получается из угля.
и для нейлона;
И ДЛЯ МОНПАНСЬЕ
СН—СООН
ма леи новая кислота
НОСИ - СООН
яблочная кислота
Мы рассказали только о некоторых, наиболее
важных пищевых кислотах. Кроме них,
пищевики часто используют также молочную и
виннокаменную кислоты. В последнее время стали
вырабатывать также очень дешевую триоксиглу-
таровую кислоту. Еще в двадцатые годы
академик П. П. Шорыгин указывал на возможность
использования триоксиглутаровой кислоты в
пищевой промышленности. Сейчас безвредность ее
для человека полностью доказана, и Всесоюзная
государственная санитарная инспекция
разрешила употреблять ее как пищевкусовой продукт.
Триоксиглутаровую кислоту вырабатывают из
хлопковой шелухи. Производство ее было
впервые освоено на Ферганском гидролизном заводе.
Хлопковую шелуху обрабатывают серной
кислотой, происходит гидролиз, и полученный при
этом продукт нейтрализуют, уваривают и затем
окисляют азотной кислотой в триоксиглутаровую
кислоту.
Остановимся еще на одной кислоте. Пока зта
кислота (адипиновая) — только сырье для
производства широко известного синтетического
волокна — нейлона.
Адипиновая кислота — полностью
синтетический продукт. Установлено, что она совершенно
безвредна и обладает приятным кислым вкусом.
Ее начинают применять не только в
производстве нейлона, но и для подкисления
лимонадов, монпансье и других пищевых продуктов.
Рисунки А. КО Л МАНОК
58
Статью «Кислота в нашей
пище» комментирует руководитель
сектора по изучению и
внедрению лечебного питания
Института питания профессор
М. С. МАРШАК
Жизнедеятельность нашего
организма тесно связана с
кислотами. Дыхание, мышечная
работа, обмен углеводов, жиров,
белков сопровождается
окислительными процессами,
образованием кислот.
Первый источник этих
необходимых кислот — сам
организм, а второй, не менее
важный, — пища.
МОЛОЧНАЯ КИСЛОТА
занимает главное место среди
кислот, которые мы едим. Вкус
всех молочнокислых
продуктов: простокваши, творога,
сыра, сметаны — обусловлен
молочной кислотой. Ее главное
свойство — способность
свертывать белки молока.
Свернутые белки легче поддаются
воздействию пищеварительных
ферментов, легче
перевариваются и усваиваются. При
недостаточной желудочной
секреции сквашенное молоко лучше
переносится, чем свежее.
Молочная кислота придает
продукту особый вкус, возбуждает
аппетит. Как и другие кислоты,
молочная вызывает обильное
выделение слюны, и поэтому
хорошо утоляет жажду.
ЛИМОННАЯ КИСЛОТА
отличается невысокой степенью
так называемой вкусовой
кислотности, и ее кислый вкус
легко нейтрализуется сахаром.
Источник лимонной кислоты —
фрукты и ягоды. Кроме
лимонной, в плодах и ягодах обычно
содержатся еще яблочная,
винная и некоторые другие
кислоты. Только клюква и плоды
цитрусовых содержат почти
одну лимонную кислоту. Клюква
и цитрусовые вообще очень
хороши как источники кислоты,
потому что в них нет
дубильных веществ, придающих
другим ягодам и плодам терпкий
вкус. Поэтому эти плоды и
соки из них наиболее
целесообразны в питании здорового и
больного. Клюквенный морс
или кисель лучше всего
утоляет жажду при лихорадке.
полезно ли
Нужно знать, что те люди, у
которых больны почки,
лимонную кислоту переносят хуже,
чем уксусную. Это связано с
тем, что в процессе обмена
веществ из лимонной кислоты
образуются щавелевоуксусная
и янтарная кислоты, которые у
почечных больных не
полностью усваиваются и
раздражают почки.
УКСУСНАЯ КИСЛОТА
участвует во многих обменных
процессах в организме. Все
углеводистые продукты —
сахар, мед, сладости, хлеб, крупы,
макароны, картофель — в
процессе обмена веществ
превращаются в ацетоуксусную и
уксусную кислоты. За сутки
организм человека вырабатывает
примерно полкилограмма
уксусной кислоты. Часть ацето-
уксусной и уксусной кислот
используется организмом для
синтеза холестерина. Количество
холестерина, которое образуется
в организме, в несколько раз
больше, чем его содержание в
обычном пищевом рационе.
Некоторые заболевания такие,
например, как желчекаменная
болезнь, ксантоматоз
(отложение холестерина в подкожной
клетчатке) связаны в той или
иной степени с нарушением
холестеринового обмена.
Особенно опасно нарушение
холестеринового обмена при
атеросклерозе, потому что
часто оно сопровождается
гипертонией. При всех этих
заболеваниях играет, конечно, роль и
уксусная кислота, из которой
образуется холестерин.
Чрезмерное потребление
углеводистых продуктов, и особенно
легкоусвояемых Сахаров, ведет
к избыточному образованию
уксусной кислоты и,
следовательно, холестерина в
организме. Позтому при заболеваниях,
связанных с нарушением
холестеринового обмена,
рекомендуется резкое ограничение в
пищевом рационе сахара и
кондитерских изделий. И,
конечно, в этих случаях уксус
кислое?
можно употреблять в очень
незначительном количестве.
ЩАВЕЛЕВАЯ КИСЛОТА —
распространенная пищевая
кислота. Зеленые щи из
щавеля — излюбленное блюдо в
летнее время. Но употреблять ее
надо с осторожностью, так как
щавелевая кислота
отрицательно влияет на солевой обмен в
организме. Дело в том, что
щавелевая кислота легко
связывается в кишечнике с
кальцием, причем образуются
нерастворимые соли, и важный
для организма кальций не
всасывается. Щанелевокислые
соли образуются также в крови,
способствуя образованию
почечных камней. Кроме того,
щавелевая кислота
препятствует всасыванию железа.
Кроме кислот, о которых мы
рассказали, в различных
плодах и овощах содержатся и
другие органические кислоты.
В яблоках, грушах, айве,
персиках и абрикосах довольно
много яблочной кислоты,
придающей им в сочетании с
сахаром кисло-сладкий вкус.
В винограде преобладает
винная кислота, в кислых сортах
ее до 0,5—1,4 процентов. В
бруснике содержится до 0,14
процента бензойной кислоты,
обладающей противогнилостными
свойствами, есть бензойная
кислота и в клюкве.
Употребление всех этих кислот для
здорового человека полезно.
Особенно же необходимы
становятся кислоты в том случае,
когда в железах желудка
синтезируется недостаточное
количество соляной кислоты,
взаимодействующей с
белковыми веществами пищи и
способствующей желудочному
пищеварению. В этих случаях
потребность в кислом
повышается, и иногда по назначению
врача больной принимает даже
неорганическую соляную
кислоту.
59
СУДЬБА
ЛЕКАРСТВ
Кандидат медицинских наук
В. М. АБАКУМОВ,
Научно-исследовательский институт
фармакологии и химиотерапии
Лекарство! Миллионы человеческих жизней
были спасены правильным и
своевременным применением лекарственных веществ.
Их становится все больше и больше. Почти
все новые химические соединения проходят
фармакологическое испытание, которое
устанавливает их влияние на живой
организм. Однако международная статистика
показывает, что только одно из десяти
тысяч вновь синтезированных соединений,
оказывается пригодным для лечения болезней.
Огромный труд затрачивается, чтобы
выявить это новое эффективное средство.
В последние годы все чаще и чаще
возникает речь о теории, которая дала бы
возможность направленного синтеза
лекарственных веществ с заранее известными
терапевтическими свойствами. Пока это
желание еще граничит с фантастикой, но
первые вехи этой жизненно важной для
человечества теории можно увидеть уже сейчас.
Одна из таких вех — гениальное
предвидение русского академика Н. П. Кравкова о
связи между химической структурой
вещества и его физиологическим действием,
высказанное им еще в 1910 г.
Но иногда, может быть, немалая помощь
при создании новых лекарств приходит со
стороны самого организма. Именно живым
организмом и была решена
ЗАГАДКА КРАСНОГО СТРЕПТОЦИДА
В 1908 году во Франции Ж. Гельмо
впервые синтезировал амид сульфаниловой
кислоты. Он обратил внимание только на то,
что новое соединение — хорошая основа
для синтеза красителей. На следующий год
соотечественники Гельмо — В. Хорлейн,
Р. Дрессель и А. Котэ обнаружили, что
краситель, полученный из сульфаниламида,
особенно прочно окрашивает шерсть, т. е.
обладает сродством к веществам белковой
природы. Тогда ученые решили провести
биологические испытания.
В начале века воспаление легких,
ангины, раневые инфекции были настоящим
бичом человечества — от воспалительных
заболеваний, вызванных различными
кокковыми микроорганизмами, умирали сотни
тысяч человек. Во всех развитых странах
велись интенсивные поиски новых
противовоспалительных средств. Вот почему для
своих опытов Р. Дрессель и А. Котэ
выбрали мышей, зараженных гемолитическим
стрептококком, вызывающим сепсис.
Испытания дали небольшой положительный
эффект, и ученые... не придали никакого
значения своим наблюдениям. Их открытие
пролежало под спудом почти 30 лет!
Только в 1932 году англичане Д. Митч и
Р. Кларер получают патент на
малорастворимый в воде краситель — производное
сульфаниламида, известное под названием
пронтозил.
В декабре того же года Г. Домаг в
Германии обнаружил, что мыши, зараженные
смертельными дозами гемолитического
стрептококка, если им ввести пронтозил, не
гибнут. Эти результаты он опубликовал
только в феврале 1935 года. И с этого
времени почти во всех странах мира начались
интенсивные работы по синтезу и изучению
соединений такого типа. В апреле 1935 года
француз Л. Жирар получает рубиазол —
тот же пронтозил, к которому
присоединена карбоксильная группа. Но по активности
рубиазол уступает пронтозилу и
значительно токсичнее его. В июле 1935 года тот же
Догмаг сообщает о неопронтозиле. Нео-
пронтозил хорошо растворим, и врачи
рекомендуют применять его внутрь. В
Советском Союзе этот препарат синтезирует
О. Ю. Магидсон. Соединение называют
60
красным стрептоцидом. После клинических
испытаний красный стрептоцид начинают
широко применять для лечения многих
воспалительных заболеваний.
Но вскоре радость открытия сменилась
горечью разочарования — слишком велики
были побочные явления при применении
этого лекарства. Увеличение дозы,
необходимое для борьбы с такими тяжелыми
заболеваниями, как менингит, воспаление
легких, приводило к серьезным поражениям
печени и других органов и систем живого
организма.
Начались дальнейшие поиски новых
производных красного стрептоцида. Но
причина его токсичности оставалась
неразгаданной.
Решение этого вопроса пришло только
тогда, когда фармакологи стали изучать
превращение лекарства в самом организме
животного.
Французские исследователи супруги
Трефель, А. Нитти и Ж. Бове решили
проследить судьбу пронтозила и рубиазола в
организме животного. Они ввели
препараты кроликам с тем, чтобы через некоторое
время определить содержание этих
веществ в крови подопытных животных.
Однако выделить рубиазол и пронтозил из
крови им не удалось. В организме
подопытных животных они расщепились —
образовался сульфаниламид и 1,2,4-триаминобен-
зол:
1,2,4-три-
аминобензол
пронтозил сульфаниламид
Именно отщепившаяся группа, как
выяснилось позже, и была ответственной за
токсичность, а сульфаниламид
(зашифрованный авторами как соединение F-1162)
оказался активным ядром пронтозила и
рубиазола. Это соединение под названием белый
стрептоцид вскоре стали применять и в
Советском Союзе. Теперь можно было
увеличивать дозировки, и белый стрептоцид стали
широко применять при лечении тяжелых
инфекционных заболеваний.
Но белый стрептоцид не был панацеей
от всех зол. Так, хорошо излечивая
воспаление легких и раневые инфекции, он
почти не помогал больным, страдающим,
например, воспалительными заболеваниями
кишечника.
Фармакологи надеялись, что
возможности других сульфамидных препаратов будут
гораздо шире, и химики повсюду стали
синтезировать разнообразные производные
сульфаниламида.
Теперь полученные препараты
фармакологи исследовали так же, как ранее
рубиазол и пронтозил — биохимики
прослеживали превращение соединения в
организме животного. Судьба всех производных
сульфаниламида в организме оказалась
похожей: потеря активности препарата (как
говорят фармакологи, его инактивация),
вызывающая антимикробное действие
лекарства, происходила благодаря
присоединению к исследуемым веществам
ацетильной группы (СОСНз). Открытие механизма
биологического превращения
(биотрансформации) сульфаниламидов имело,
казалось, только теоретическое значение. Что
это не так — стало хорошо видно на
примере синтеза противодиабетического
средства — бутамида.
В 1955 году немецкий ученый Р. Ахелис,
изменяя структуру боковой серусодержа-
щей цепи сульфаниламидов, получил
препарат надизан. Этот препарат снижал
концентрацию сахара в крови больных
диабетом. Но кроме этого замечательного
свойства, надизан, как и все сульфамиды,
обладал противомикробным действием.
Однако больным диабетом это приносило
скорее вред, чем пользу. Надизан
уничтожал микрофлору кишечника, а это влекло
не только нарушение процесса
пищеварения, но и создавало благоприятные условия
для возникновения различных грибковых
заболеваний слизистой оболочки
кишечника.
Но ученые уже знали, что противоми-
кробные свойства лекарств исчезают после
ацетилирования аминогруппы. А если
заменить аминогруппу в молекуле надизана на
метильную? Так синтезировали бутамид —
вещество, обладающее антидиабетическим
действием, и в то же время лишенное
антибактериальных свойств.
Этот синтез еще раз убедительно
показал, что важно знать не только
химическое строение любого препарата. Важно
знать —
G1
КАКОВА ЖЕ СУДЬБА ЛЕКАРСТВА
В ОРГАНИЗМЕ!
В 1842 году в Германии в химической
лаборатории Велера был поставлен
необычный для того времени эксперимент:
животным ввели бензойную кислоту. Все
подопытные мыши погибли. Другой партии
мышей вместе с бензойной кислотой ввели
аминокислоту—глицин. Большая часть
мышей осталась жива. В моче оставшихся в
живых животных обнаружили гиппуровую
кислоту (бензоилглицин) — соединение
малотоксичное, быстро выводящееся из
организма.
Так был впервые установлен еще один
распространенный путь превращения
препарата в организме — образование парных
соединений с глицином:
соон
1 II
\/
Бензойная
кислота
(токсичное
соединение)
NH2
4. 1
+ сн,
/
соон
Глицин
(аминокислота)
CONHCHXOOH
Гиппуроваи кислота
(малотокси чное соедimeние)
Несколько позднее тот же Велер
обнаружил еще одно удивительное явление.
Сотрудники, занятые синтезом новых
селено- и теллуросодержащих соединений,
выдыхали воздух с резким чесночным
запахом. Такой же запах появлялся у воздуха,
который выдыхали кролики и собаки после
введения им соединений теллура. Так же
пахли внутренние органы животных,
вскрытых после опыта. Какого-нибудь
обоснованного толкования этому интересному факту
Велер сначала дать не мог.
Современник Велера — биохимик Франц
Гофмайстер высказал предположение, что в
организме животных и человека к
производным теллура присоединяется метильная
группа. Тогда Велер синтезировал диметил-
теллурид. У этого летучего вещества
оказался резкий чесночный запах. Догадка
Гофмейстера косвенно подтверждалась. Позже
Гофмайстер разработал качественную
реакцию на метилированный продукт теллура
и установил, что уже через 30 минут после
введения собакам, кошкам, кроликам,
лягушкам и рыбам теллуровой или теллу-
ристой кислот или их солей в выдыхаемом
воздухе и во внутренних органах вскрытых
животных содержится диметилтеллурид. Так
был открыт еще один путь превращения
химических веществ в организме — процесс
метилирования.
Исследования Велера и Гофмайстера
были стартом, с которого начались поиски
новых дорог в организме для
многочисленных лекарственных веществ. Они оказались
разнообразными. Фармакологам удалось
показать, что кроме различных процессов
присоединения, о которых мы рассказали —
ацетилирования, образования парных
соединений с глицином, метилирования,
лекарственные вещества в организме могут
терять карбоксильные, метильные и
ацетильные группы, могут окисляться и
восстанавливаться, отщеплять аминогруппу и
образовывать парные соединения с глюку-
роновой и серной кислотами. При этом
обнаруживались порой удивительные факты.
Фармакологи установили, что при
биотрансформации могут образовываться не
только менее активные соединения, но и
вещества, физиологические свойства
которых выражены сильнее, чем у исходных.
Причем, и то и другое может происходить
для различных соединений в одном и том
же процессе превращения.
Обилие данных о судьбе лекарственных
веществ настоятельно требовало создания
теории, в которой было бы отражено не
только многообразие таких процессов, но и
определено их значение для живого
организма. Была нужна теория, в которой была
бы сделана
ПОПЫТКА ОБОБЩЕНИЯ
Первым предпринял эту попытку в
1949 году английский ученый Р. Вильяме в
своей книге «Механизмы детоксикации».
Когда наука накапливает множество
разрозненных фактов, то первый шаг к теории,
первый метод
обобщения—классификация. Ее и создал Вильяме.
Подробно рассматривая
многочисленные процессы превращения различных
лекарств, он пришел к выводу, что все
реакции биотрансформации можно
подразделить на четыре основные группы: на реакции
окисления, восстановления, гидролиза и
62
синтеза. Это, так сказать,
химические разновидности
процессов превращения. (Неактивное
А физиологически, считает соединение)
Вильяме, превращение
любых чужеродных
соединений в организме, в том числе и
лекарственных веществ, происходит в два этапа.
Первый этап (реакции 1 фазы) —
окисление, восстановление, гидролиз или
различные сочетания этих процессов; в
организме образуются соединения, активность
которых больше или меньше активности
введенного лекарства. Иногда возникают и
совершенно неактивные соединения. К
реакциям 1 фазы относятся и те процессы,
при которых введенное в организм
неактивное соединение, превращается в
лекарство. На втором этапе (реакции 2 фазы)
всегда происходит синтез — связывание с
гиппуровой, серной, глюкуроновой
кислотой или другими веществами, постоянно
присутствующими в организме
млекопитающих. Все реакции второй фазы — это
только процессы детоксикации. При этих
процессах образуются неактивные
продукты, которые легко и быстро выводятся из
организма.
Концепцию Р. Вильямса можно
представить в виде такой схемы:
Улпрялг.трят ВосстановлениеТги„пгэтянпл Синтез
1 фаза
Итак, лекарственное вещество может
пройти один из четырех путей
биотрансформации. Хорошо известное в
медицинской практике наркотическое вещество —
хлоралгидрат, само по себе не оказывает
на организм никакого действия. Попадая в
организм, оно восстанавливается (реакция
1 фазы) и превращается в трихлорэтанол,
который и вызывает наркоз. Вещество из
неактивного превращается в активное. На
втором этапе биотрансформации
трихлорэтанол соединяется с глюкуроновой
кислотой и полностью теряет активность.
Классификация процессов биотрансфор-
(Активное
соединение)
2 фаза
Глюку ронид
трпхлорэтанола
(Неактивное
соединение)
мации, предложенная Вильямсом, далеко
не полна. Она не учитывает, например, что,
кроме изменения химического строения
лекарства при превращении в организме,
меняются и его физико-химические
свойства, играющие важную роль в активности
промежуточных продуктов. В эту
классификацию не укладывается и так называемый
смертельный — летальный, как говорят
врачи, синтез.
В 1952 году был раскрыт механизм
ядовитого действия фторуксусной кислоты.
Само по себе это соединение нетоксично, но,
попадая в организм, оно включается в
жизненно важный биохимический цикл
углеводного и жирового обмена. Происходит
это из-за структурного сходства между
фторуксусной кислотой и уксусной,
участвующей в этом обмене. В организме
синтезируется фторлимонная кислота, которая
подавляет необходимый для
жизнедеятельности организма фермент аконидазу, и,
таким образом, выключается углеводный и
жировой обмен. Сам организм синтезирует
яд, от которого и погибает. По теории
Вильямса «летальный синтез» — это
реакция 2 фазы, но ведь по Вильямсу на втором
этапе должно всегда получаться неактивное
вещество.
Поиски теории более совершенной, чем
теория Вильямса, продолжаются и сейчас,
но пока еще она наиболее полная и
удачная.
К началу 50-х годов накопилось
множество данных о превращениях лекарств; в
общем виде их охватывала классификация,
разработанная Вильямсом, но большей
частью сам механизм реакций
биотрансформации оставался неясным. Перед учеными
встала задача обнаружить и расшифровать
тончайшие биохимические структуры,
вызывающие эти процессы, установить — кто
же
ВЕРШИТЕЛИ СУДЕБ ЛЕКАРСТВ
«Одна из наиболее бросающихся в
глаза особенностей химических реакций,
протекающих в живом организме, есть та лег-
63
кость, с которой подчас весьма стойкие
вещества подвергаются расщеплению. Так
глюкоза окисляется до углекислоты и воды,
белок расщепляется на аминокислоты. При
обычных лабораторных условиях
требовались бы сильнейшие реактивы, вроде
хромовой и кипящей соляной кислот, чтобы
разложить эти вещества... Препарат лакта-
зы расщепляет в течение одного часа такое
количество молочного сахара, которое при
помощи двунормальной соляной кислоты
при той же температуре удается гидроли-
зовать только в течение пяти недель», —
так еще в 1927 году писал о колоссальных
возможностях организма как
своеобразного химического реактора английский
биохимик В. Бейлис в книге «Природа действия
ферментов».
В процессе эволюции в живом
организме возникают системы ферментов, которые
не только играют первостепенную
физиологическую роль в обмене веществ, но и
обезвреживают (осуществляют детоксика-
цию, говорят биохимики) чужеродные
химические соединения, попадающие в
организм вместе с продуктами питания. Эти
же системы играют главную роль в
превращении лекарственных средств —
определяют их судьбу.
Но присутствия одних ферментов часто
оказывается мало.
Рассмотрим механизм одного из
процессов биотрансформации —
метилирования — полностью, во всей его сложности.
В 1951 году Ж. Кантони предположил,
что для метилирования нужен не только
фермент, но и АТФ (аденозинтрифосфор-
ная кислота) — известный поставщик
энергии в живых организмах. Но в этом случае
АТФ выступает не в своей обычной роли.
Она принимает участие в превращении
аминокислоты метионина — поставщика ме-
тильных групп для реакции метилирования,
в так называемый S-аденозилметионин —
«активный метионин». Именно от этого
«активного метионина» метильные группы
переносятся к молекуле, принимающей
«метилы», например, к молекуле
лекарства никотинамида — витамина PP.
Метионин -| АТФ —> «Активный метионин» -£- ЗР04
Правильность своей гипотезы Ж.
Кантони подтвердил прямым опытом. Он
смешивал измельченную печень кролика,
содержащую необходимый для метилирования
фермент, витамин РР и метионин. Никакого
метилирования никотинамида не
наблюдалось. Прибавляли АТФ — метилирование
шло. Затем синтезировали «активный
метионин», заменяли им метионин в
предыдущем опыте — метилирование шло без АТФ.
Значит, для этого процесса
биотрансформации лекарства источник метильных
групп важен не меньше, чем фермент.
Значит, увеличивая или уменьшая
количество «подвижных метилов», можно
изменять интенсивность процессов
метилирования и деметилирования, т. е. регулировать
действие лекарства. Это подтвердил опыт.
Животным ввели малоэффективное
снотворное средство норгексенал. После этого
опыта они спали всего 20 минут. Во втором
опыте животным вводили ту же дозу
снотворного, но предварительно еще и дозу
метионина (сам метионин снотворным
действием не обладает). Животные спали после
второго опыта полтора часа.
Подобные опыты фармакологи
проводили и с другими препаратами, и постепенно
становилось ясно, что, влияя на
интенсивность процессов биотрансформации
лекарств, на их тонкий механизм, можно
изменять их действие на живой организм,
создавать процессы, которые в обычных
условиях не протекают. Это уже
УПРАВЛЕНИЕ СУДЬБОЙ ЛЕКАРСТВ
Одно из самых важных лекарств,
действие которого давно интересует ученых,—
адреналин — средство, влияющее на
деятельность сердечно-сосудистой и нервной
системы.
Еще в 1939 году русский биохимик
А. М. Утевский установил два пути
инактивации адреналина в организме: окисление
и дезаминирование. Контроль за процессом
дезаминирования осуществляет фермент
моноаминоксидаза (МАО). Влиять на
МАО — первый путь управления судьбой
адреналина. Была откры-
Метпльные группы та целая группа веществ,
f тормозящих действие
этого фермента,—
ингибиторов МАО. Ингибиторы
МАО защищали адрена-
\
S-Аденозплгомо-
цнстеин
С4
лин от разрушения, и эффективность
действия лекарства на нервную систему
несколько повышалась, но все же была
недостаточной. Кроме того, ингибиторы МАО не
меняли действия адреналина как средства,
регулирующего кровяное давление,
В 1959 г. американец Ю. Аксельрод
открывает еще один путь разрушения
адреналина в организме — О-метилирование,
контролируемое ферментом со сложным
названием катехол-О-метил-транс-фераза.
Аксельрод находит ингибитор для этой
реакции — пирогаллол. Пирогаллол в
безвредных дозах вводят подопытным
животным вместе с адреналином, и действие
лекарства становится сильнее. Но, как и в
первом случае, когда речь шла об
ингибиторах МАО, действие пирогаллола не
достаточно для такого повышения активности
адреналина, которое нужно врачам.
Объяснение этим явлениям прозвучало
с трибуны Международного
биохимического конгресса в Москве в 1961 году.
Применив метод меченых атомов,
биохимики Н. Киршнер и А. Шепдрайвер
показали, что, когда подавляется один процесс
дезаминирования, процесс метилирования
течет интенсивнее и наоборот. При
подавлении этих двух процессов усиливается еще
один путь инактивации, открытый
немецким ученым Д. Рихтером,—синтез с
серной и глюкуроновой кислотой. Необходим
такой ингибитор, который бы подавлял все
процессы разрушения адреналина. Его и
ищут сейчас фармакологи, правда, пока
безуспешно.
За последнее время фармакологи
вместе с биохимиками открыли множество
разнообразных веществ — стимуляторов и
ингибиторов различных процессов,
определяющих судьбу лекарств в организме. Уже
сейчас во многих случаях, регулируя
процессы превращения, можно изменять
активность лекарственных веществ в ту или иную
сторону. Но пока это только предпосылки
для направленного синтеза новых
эффективных лекарств, только подступы к теории,
руководствуясь которой химики будут
заранее точно знать, какую структуру должно
иметь новое соединение, чтобы победить
именно эту болезнь. Данные для этой
теории накапливаются.
| Каи-то раз один из учеников
известного немецкого химика
К. Винклера пришел в
лабораторию в фартуке. Винклер,
требовавший от учеников величайшей
аккуратности и считавший, что
химик должен быть настолько
ловким, чтобы работать даже во
фраке, встретил его словами:
— Уж не собираетесь ли вы
здесь гасить известь!
И заставил его снять фартук,
Когда...
однажды...
как-то раз...
Рисунки В. ЗУЙКОВА
■ Когда в 1850 году знаменитый
французский химик и физик
Ж. Л. Гей-Люссак тяжело заболел
и был уже при смерти, он жалел
только об одном: что должен
покинуть этот мир как раз в то
время, когда наука и техника начали
так стремительно развиваться, а
электричество начало менять весь
облик человеческой цивилизации.
— Жаль уходить, — сказал
он, —все это становится
интересным...
■ Когда Роберт Бунзен читал
лекции о своих открытиях, он
никогда не называл себя их
автором, а говорил: «открыто...»,
«обнаружено...», «показано...».
Стремясь избежать оваций, он строил
лекции так, чтобы о собственных
работах приходилось упоминать
лишь в самом конце. И едва
начинались аплодисменты, он быстро
уходил из аудитории.
В. ГОЛЕМБОВИЧ
Перевод с польского И. Д. ЛЕВИ
Ь Химия и Жизнь, № 10
С5
из писем
в редакцию
Все получаемые редакцией
письма читателей можно подразделить
на две категории: письма с
вопросами и письма без вопросов.
И среди тех и среди других
нередко встречаются такие, которые
представляют интерес не только
для их авторов и адресата. Но
если наиболее интересные письма
первого рода и ответы на них
лубликуются в журнале (в
разделе «Наши консультации»), то
письма второго рода до сих пор
оставались достоянием одних лишь
сотрудников редакции. Для того,
чтобы устранить эту
несправедливость, в журнале учреждается
новая рубрика «Из писем в
редакцию».
Опубликование здесь того или
иного лисьма (или выдержки из
него) не будет означать, что
редакция непременно разделяет
мнение его автора.
£ При изучении взаимосвязи
между зарядом (Z), атомным
весом (А), числом электронных
оболочек (S) и числом валентных
электронов (V) химических
элементов я обнаружил
функциональную зависимость Q=f(Z), где
В процессе построения
графика зависимости Q от Z
происходит самопроизвольная
классификация химических элементов,
которые группируются так, как они
сгруппированы в коротком,
классическом варианте периодической
системы элементов Д. И.
Менделеева.
Ю. СЫРЕЙЩИКОВ,
Свердловск
ф Недавно я зашел в магазин за
молоком, молока не оказалось.
Когда я обратился к директору
с вопросом, почему нет молока,
директор ответил, что накануне
была гроза, а во время грозы
молоко, которое возят в
цистернах, скисает. Я усомнился в отве->
те, директор посоветовал мне
позвонить на Останкинский
молочный комбинат. Когда я позвонил
туда, то они подтвердили
правильность ответа директора.
Комбинату неизвестна причина этого
явления...
А. И. ЛЕЕНСОН,
Москва
С просьбой разъяснить
загадочное явление редакция
обратилась во Всесоюзный
научно-исследовательский институт молочной
промышленности. Работники
института подтвердили, что такие
случаи, действительно, изредка
бывают (чаще всего с сырым
молоком, перевозимым из колхозов
и совхозов на заводы), но
причины этого неизвестны, и
исследованием этого вопроса никто
специально не занимается. — Ред.
Ф У нас в школе работает
химический кружок, правда, в нем
всего 12 участников (школа
сельская, 8-летняя, всего 162
учащихся). Но ребята очень
интересуются всем новым, которое
появляется на страницах журналов.
Многие опыты мы повторяем по
описаниям в журналах, иногда их
демонстрируем на вечерах перед
родителями... Решил я вам
прислать описание одного
занимательного опыта, который мы
разработали (если можно так
выразиться) сами. Опыт называется
«Химическая радуга».
Перед большим белым листом
бумаги поставьте в один ряд
шесть неграненых стаканов. В
первый стакан до '/з его объема
налейте слабый раствор хлорного
железа, во второй — столько же
«раствора» свежеполученного
гидрата окиси железа, в третий —
концентрированный раствор
хлорной меди, в четвертый и пятый —
голубого цвета слабый раствор
хлорной меди, в шестой —
фиолетовый раствор марганцевокислого
калия.
Как видно, это еще не радуга,
а скорее всего «изображение
цветов перед наступлением
грозы».
Теперь в первый стакан до
2/з его объема налейте раствор
роданистого аммония, во
второй — раствор лимонной кислоты,
в третий — концентрированный
раствор хлористого аммония,
в четвертый — раствор хлорной
меди, в пятый — раствор
аммиака, в шестой — раствор
марганцевокислого калия.
Получилась красивая радуга
цветов: красный, желтый,
зеленый, голубой, фиолетовый.
Но мы знаем, что радуга
исчезает так же быстро, как
появляется. Для демонстрации
исчезновения радуги в первый, третий,
четвертый стаканы налейте до
верха раствор тиосульфата нат-
рия, во второй — раствор серной4 i
кислоты, в пятый и шестой — '
раствор сернистокислого натрия.
66
подкисленного серной кислотой.
При этом во всех стаканах
получаются бесцветные прозрачные
растворы.
В. НИКОЛАЕВ,
Чувашская АССР,
дер. Анаткас Туруново
Ф Ю. В. Лермонтова... не
первая русская женщина-химик. За
ряд лет до нее, в 1869 —
1876 гг., Анна Федоровна
Волкова, работавшая у Энгельгардта,
Кочубея и Менделеева,
опубликовала большую серию (до
двадцати) замечательных работ по суль-
фокислотам и амидам кислот,
легших позднее в основу синтеза
сахарина и сульфаниламидных
препаратов. Синтезированные
Волковой новые соединения
в 1876 г. демонстрировались на
Лондонской всемирной выставке.
В 1871 г. она
председательствовала на заседании химической
секции III съезда Русских
естествоиспытателей и врачей и
сфотографировалась в группе, между
Менделеевым и Бутлеровым,
которые ее очень высоко ценили
и поддерживали подыскиванием
оплачиваемых работ, поскольку
она жила в большой бедности.
Еще в 1870 г. Волкова была
избрана в состав Русского
химического общества. Таким образом
неверно и утверждение
Сергеевой («Химия и жизнь», 1966, № 1. —
Р е д.), что кроме Лермонтовой в
течение долгого времени в
списках РХО «не появляется более ни
одного женского имени». До
Лермонтовой начала работать и
опубликовала свои исследования в
1871—1873 гг. в ЖРХО и в
«Бюллетене» Академии наук Аделаида
Луканина, ученица А. П.
Бородина-
Профессор
Ю. С. МУСАБЕКОВ,
Ярославль
Ф Предлагаю Вашему вниманию
так называемые «химические
сказочки». Перед тем, как это
сделать, я дал почитать эти сказочки.
Товарищи смеялись. Серьезный
доцент ободряюще похлопал
меня по плечу. «А вы знаете,
молодой человек, довольно забавно и
до некоторой степени
познавательно».
Единодушие было только в том,
что все посоветовали мне послать
эти сказочки в ваш журнал,
который уже второй год является
нашей настольной книгой, а
некоторые особо талантливые и
изобретательные товарищи
умудряются даже сдавать экзамены,
используя ваш журнал, как
шпаргалку.
Вот я и посылаю свое
«творение» вам.
С уважением — студент IV
курса химического факультета
Днепропетровского государственного
университета
СЕЛЕЗНЕВ Виктор Викторович.
1. ОБЫКНОВЕННАЯ
РЕАКЦИЯ
В темном, неосвещенном
переулке Перманганбт совместно с
какой-то Кислотой изловили
Тиосульфат. Общеизвестно, что Дру-
жинники-пассиваторы в темные
переулки почти никогда не
заглядывают, поэтому Перманганат со
своей подругой в мгновение ока
обобрали Тиосульфат до
ниточки.
И, представьте, никто не
наказал злоумышленников, просто
пожали плечами:
— Что же тут такого?
Произошла обыкновенная окислительно-
восстановительная реакция!
Перманганат восстановился,
Тиосульфат окислился, а Кислота
просто-напросто способствовала
реакции.
Да, хорошо, когда пожимают
плечами, если речь идет о
химической реакции. Но иногда
пожимают плечами, когда дело
совершенно не имеет к химии никакого
отношения...
2. МОЯ ХАТА С КРАЮ
— Я, что ни есть, самая
настоящая кислота, — кричала
Гидроокись Алюминия, попадая в
кислотное окружение.
— Вообще-то, кислоты слова
доброго не стоят. Другое дело
мы, основания, — кичилась она
в щелочной среде.
Простодушные Кислоты и
Основания считали ее своей. Только
одна лишь Вода знала, что
Гидроокись Алюминия — вещество не
настоящее, амфотерное.
Но Вода молчала, ревностно
охраняя свою нейтральность,
3. ГАДКИЙ УТЕНОК
— Вы только посмотрите на
этого чумазого, — указывали
Драгоценные Камни на кусочек
Графита, брезгливо обходя его,
чтобы не испачкаться. И кто
только создал такую погань!
Но тут откуда не возьмись,
нагрянули Высокое Давление и
Температура. Драгоценные Камни
моментально превратились в
ничто. А на том месте, где лежал
кусочек Графита, засверкал,
переливаясь всеми своими гранями,
великолепный Бриллиант, перед
которым самые аристократические
Самоцветы выглядели
обыкновенными булыжниками.
...Сказка — ложь, но в ней
намек.
Ф Меня очень заинтересовала
помещенная в Вашем журнале
рубрика «Учитесь переводить». По
специальности я химик-технолог.
В последние годы мне часто
приходится переводить химический
текст с немецкого языка на
русский. Думаю, что для многих
читателей журнала «Химия и Жизнь»
было бы весьма желательным
включение в упомянутую
рубрику раздела «Немецкий для
химиков».
С Н. САРАЕВА,
Харьков
5*
67
АНГЛИЙСКИЙ—
ДЛЯ ХИМИКОВ
АБСОЛЮТНЫЙ ПРИЧАСТНЫЙ ОБОРОТ
е£
О
ю
ш
а
ш
С
JQ
и
ш
X
т
Абсолютный причастный оборот представляет собой
своеобразное развернутое обстоятельство; поэтому
он может находиться как до, так и после «костяка»
предложения (см. № 2, 3). Этот оборот содержит
инговую форму (причастие), собственное
подлежащее, но не имеет личной формы глагола. Исходя
из таких соображений, можно вывести следующую
формулу абсолютного причастного оборота:
подлежащее (I) Н~ инговая форма глагола (II) +
+ отсутствие личной формы глагола (III) + главное
предложение, находящееся до или после оборота
(IV).
Например:
The experiment having been carried out
we went home.
The experiment (I) -f- having been carried
out (II) + (III) + we went home (IV).
«После того как был закончен опыт, мы пошли
домой».
Особенность абсолютного причастного оборота
состоит в том, что «обстоятельственность» в этом
случае выражается не словами (как в русском языке),
а особой грамматической формой. Как видно из
перевода, в русском языке этот оборот соответствует
целому обстоятельственному предложению со своим
подлежащим, сказуемым (личной формой глагола)
и обстоятельственным словом (союзом).
Англичанин, исходя из грамматической структуры
оборота, как бы «домысливает» одно из
обстоятельственных слов: причем, а, и; так как, потому что,
поскольку; хотя, если; когда, после того как, при этом;
где. Мы же, обнаружив абсолютный причастный
оборот, должны как бы «вытянуть» из него один из
вышеприведенных союзов и перевести причастие
личной формой глагола (сказуемым). Выбор союза
диктуется контекстом.
Например:
The temperature being 100° water boiled
quickly.
«Так как температура была 100°, вода быстро
закипела», но:
The temperature being 10° water boiled
quickly.
«Хотя температура была 10°, вода быстро
закипела» (например, в вакууме — А. П.).
Наиболее распространенная ошибка при переводе
английского оборота состоит в том, что его
смешивают с причастием в функции определения. Этой
ошибки легко избежать, запомнив следующее
правило: если данная инговая форма представляет
собой причастие в функции определения, то в
предложении должна быть личная форма глагола; если же
таковая отсутствует, то это значит, что перед нами —
абсолютный причастный оборот.
Сравните:
The reaction taking place was found to
be very strong.
«Нашли, что протекающая реакция — очень
энергичная».
Здесь taking place является причастием в
функции определения к существительному reaction. Но:
The reaction taking place we could not
leave the room.
«Когда шла реакция, мы не могли выйти из ком-*
наты».
Здесь taking place входит в состав абсолютного
причастного оборота, так как в предложении нет
личной формы глагола.
В заключение этой темы проанализируйте
несколько приведенных ниже предложений. Пользуясь
формулой, обратите внимание на то, что абсолютный
причастный оборот часто стоит после главного
предложения, и нередко отделяется от него запятой:
Polarisation effect being neglected, the
distance of the lines joining centers of the
attracting dipoles have the following values...
«Если пренебречь эффектом поляризации, то
расстояние между линиями, соединяющими центры
притягивающих диполей, будет выражаться в
следующих значениях...»
The diastereoisomers of these compounds
are designated by the prefixes L-allo and
D-allo, the letter denoting the configuration
of the ос-carbon atom.
«Диастереоизомеры этих соединений
обозначаются приставками L-алло, и D-алло, причем буква
указывает конфигурацию а -углеродного атома».
Обратите внимание и на то, что абсолютный
причастный оборот иногда заключается в скобки:
68
The good solvating medium provides
stabilisation of a transition slate similar to
«a» (charge being created).
«Хорошо сольватирующая среда обеспечивает
стабилизацию переходного состояния, аналогичного
состоянию «а» (при этом возникает заряд)».
Теперь рассмотрим специфику перевода
предложений № 40—45, приведенных в прошлом номере
журнала.
40. The equilibrium initial stress is seen to
be markedly affected.
Помимо оборота «подлежащее с инфинтивом»
(см. № 6), в этом предложении содержится глагол
to affect, который имеет значения «влиять на (что
либо)», «воздействовать на (что либо)». Если после
to be affected отсутствует указание на «действующее
лицо» (вводимое предлогом by), то можно рекомен-*
довать переводить эту конструкцию значением «из-*
меняться». Поэтому наше предложение переводится
следующим образом:
«Видно, что начальное равновесное напряжение
заметно изменилось».
41. The new procedure enabled us to overcome
the above difficulties. Again there took place
an unexpected drop in the demand for this
product.
Мы уже знаем, что определенный артикль the
часто выступает в лексическом значении «этот» (см.
№ 3, 8). Мы знаем также, что procedure в химической
литературе означает не «процедура», а «методика»,
«метод», «процесс», «пропись» (см. № 2 и № 3).
Наконец, мы познакомились со словами,
устанавливающими логические связи между отдельными
предложениями и целыми абзацами (см. № 5), причем в их
числе мы указали на вводное слово again.
Это слово хорошо известно в значении «снова».
Однако очень часто такой перевод совершенно не
подходит по контексту и поэтому надо использовать
другие значения — «с другой стороны», «и в этом
случае», «в свою очередь», «кроме того»;
конкретное значение зависит от характера логической связи
между двумя предложениями, В данном случае
переводим:
«Эта новая методика позволила нам преодолеть
указанные трудности. С другой стороны,
произошло неожиданное падение спроса на этот
продукт».
Приведем примеры с другими значениями слова
again:
The motion of a valency electron in its
orbital is again equivalent to the flow of
a current in the locus of its motion.
«И в этом случае движение валентного
электрона по его орбите эквивалентно току
электрических зарядов по траектории его движения».
Access is given to passage Q by two
horizontal channels K, each of which is again
connected to two passages U.
«Доступ в проход Q обеспечивается двумя
горизонтальными каналами К, каждый из которых, в
свою очередь, связан с двумя проходами U».
42. We obtained a complex product which
was to be expected.
Для правильного перевода этого предложения
надо знать следующее:
а) местоимение which, помимо хорошо
известного значения «который», нередко выступает в
значении «что»;
б) глагол to be с последующим инфинитивом
смыслового глагола имеет модальное значение.
Отсюда перевод этого предложения:
«Мы получили сложный продукт, что и следовало
ожидать».
43. Polyesters and polyamides are spinned
from melts. The latter are more polar.
Неправильный перевод:
«Полиэфиры и полиамиды прядутся из расплавов.
Последние более полярны».
Из такого перевода получается, что расплавы
более полярны. Но более полярны чем что?
Непонятно! Да и не может быть понятно, так как в
английском тексте указывается, что полиамиды (а не
расплавы) более полярны, чем полиэфиры. Дело в
том, что the former и the latter (вместе или по
отдельности) употребляются в английском тексте в тех
случаях, когда нужно заменить упомянутые ранее
существительные. При этом the former заменяет
первое, a the latter — второе из них. Отсюда
правильный перевод:
«Полиэфиры и полиамиды прядутся из расплавов.
Полиамиды более полярны».
44. The reaction started at a temperature
over 100—150 .
Неправильный перевод:
«Реакция началась при температуре выше 106—■
150°».
Если, пользуясь этим переводом, начать работать,
то можно и взорваться... Экспериментатор спокойно
ждет, пока температура превысит 150°, а реакция...
уже идет. Over — очень важное «псевдопростое»
слово. Помимо хорошо известных значений «над»,
«свыше», оно часто выступает в значениях «на
протяжении» «от ... до». Поэтому наше предложение
означает:
«Реакция началась в температурном интервале
100—150°».
45. These compounds were previously assigned
the following structure.
Хорошо известно значение слов previous,
previously (предварительный, предварительно). Однако
69
чаще всего их следует переводить как «прежний»,
«предшествующий», «ранее». Разница между «ранее»
и «предварительно» существенна! Наше предложение
почти всегда означает:
«Ранее этим соединениям приписывалась
следующая структура».
В следующем номере мы познакомимся с
причастными оборотами, начинающимися с предлога with
и рассмотрим перевод следующих предложений:
46. A new paper has also been published
this year.
47. Eecently the properties of many
compounds previously investigated by chemical
Как совершается открытие! Что приводит к вспышке
гения, к решающему моменту в научном
исследовании' Об этом рассказывается в сборнике А. Гаррета
«Вспышка гения», отрывки из которого мы начали
печатать в № 9 и продолжаем в этом номере.
ОТКРЫТИЕ ИНСУЛИНА —
ФРЕДЕРИК БАНТИНГ
Инсулин — лекарство, которое применяют
теперь для лечения сахарной болезни, не
был известен еще в начале века. Его открыл
в 1922 году канадский врач Фредерик Бан-
тинг. Вот как описывает это один из его
биографов.
Бантингу тогда шел 31-й год. Он
собирался стать хирургом, но, не сумев найти
практику, вынужден был преподавать
фармакологию в медицинской школе.
Однажды вечером, готовясь к лекции о диабете,
о котором он знал тогда очень немного,
Бантинг прочел в медицинском журнале
статью о поджелудочной железе.
Из этой статьи он узнал, что диабет
связан с какими-то нарушениями в работе
поджелудочной железы, из-за которых сахар
не усваивается в организме должным
образом, а накапливается в кровеносной
системе до тех пор, пока не наступает смерть.
Под впечатлением прочитанного Бантинг не
мог уснуть. Значит здоровая
поджелудочная железа выделяет что-то,
содействующее усвоению сахара? Он знал, что
поджелудочная железа, во-первых,
выделяет пищеварительные секреты и что, кроме
methods have, therefore, been studied
physically in this laboratory.
48. In many ways such a reduction resembles
the action of a Grignard reagent, hydrogen
entering into the reactant molecule.
49. Definite proof to that effect is lacking.
50. A number of derived and related
compounds were prepared and tested with few
results of any promise.
Кандидат филологических наук
А. Л. ПУМПЯНСКИЙ
того, у поджелудочной железы существуют
своеобразные включения, которые
называются «островками» Лангерганса, не
участвующие в выделении этих секретов. Он
вспомнил, что «островки» остаются
здоровыми даже тогда, когда закупоривается
выводной проток поджелудочной железы, и
происходит распад той ее части, которая
вырабатывает пищеварительные секреты *.
Было известно, что у больных диабетом
клетки этих «островков» сморщены. Может
быть лангергансовы островки выделяют
вещество, которое сжигает сахар? Бантинг
тут же вскочил с постели и записал:
«Перевязать протоки поджелудочной железы
собаки. Подождать шесть или восемь недель
до распада тканей железы. Удалить
здоровый остаток и экстрагировать из него
секрецию».
Он добился рабочего места в отделении
физиологии, которым руководил
профессор Дж. Маклеод, и приступил к
исследованиям. Ему помогал студент Чарльз Бест.
Они усыпляли собак, перевязывали им
протоки поджелудочной железы и определяли
содержание сахара в крови и моче до тех
пор, пока не наступало перерождение
поджелудочной железы. Из клеток лангерган-
совых островков они получали небольшое
количество экстракта.
Девяносто вторая собака, у которой
была удалена поджелудочная железа, умира-
* Это наблюдение, послужившее толчком к
открытию Бантинга, сделано впервые Л. В. Соболевым
и содержится в его диссертации, защищенной
в 1901 году в Петербурге. — Прим. пере в.
ВСПЫШКА ГЕНИЯ
70
ла от диабета. Ей ввели порцию секреции
лангергансовых островков — и она пришла
в себя. Это был первый успех. Они
продолжали следить за сахаром в крови у этой
собаки. Через некоторое время
содержание сахара снова увеличилось, и собака
умерла. Может быть, если бы собака
продолжала получать порции экстракта,
который Бантинг тогда называл «айлетином» (от
английского island — остров), она
продолжала бы жить? Опыт на другом животном
подтвердил это предположение.
Следующий важный шаг—Бантинг и
Бест выделили айлетин из поджелудочных
желез скота, убитого на бойнях.
Оставалось выяснить, будет ли этот
экстракт предотвращать диабет у людей так же,
как у животных. Первым пациентом был
14-летний мальчик, умиравший от тяжелой
формы диабета. Инъекция «айлетина»
спасла его. Вторым пациентом стал друг
детства и одноклассник Бантинга, Джо Джил-
крист, безнадежно больной диабетом. Он
добровольно разрешил делать на себе
необходимые опыты, стал
«человеком-кроликом». Вводя ему разные дозы препарата,
Бантинг определил дозу, необходимую для
лечения сахарной болезни.
В этих работах активно участвовал
профессор Маклеод. Он разработал наилучший
.метод экстракции и стандартизации
айлетина. Он же предложил название «инсулин»
от латинского insula — остров.
В январе 1922 года Бантинг, Бест и
Маклеод сообщили Американскому
физиологическому обществу о своем открытии, а в
1923 году Бантинг и Маклеод получили
Нобелевскую премию..
ОТКРЫТИЕ
ИЗОТОПОВ КИСЛОРОДА —
В. Ф. ЖСК И X. Л. ДЖОНСТОН
В 1905 году кислород был выбран как
эталон для определения атомных весов.
В то время такой выбор казался
идеальным. Но менее чем через 25 лет было
установлено, что чистого кислорода с
атомным весом 16 в природе нет.
Открытие изотопов кислорода
аспирантом X. Л. Джонстоном и его руководителем
профессором В. Ф. Жоком дало
возможность учесть эту сложность и создать
международную систему эталонов атомных
весов. Джонстон готовил диссертацию по
термодинамике кислорода. Он измерял
теплоемкость кислорода в большом
интервале температур: от температуры жидкого
гелия до комнатной температуры. Ему были
нужны данные спектров кислорода, для
того чтобы вычислить энтропию.
Как раз перед этим появилась в печати
статья «Спектры поглощения кислорода в
земной атмосфере». Авторы этой статьи
сообщали об успешной расшифровке
спектров, но в заключение писали: «В спектрах
есть небольшое количество слабых линий
атмосферной природы, которые не
поддаются классификации. Возможно, они
вызваны парами воды». Эти слова и были ключом
к открытию Жока и Джонстона. Мы
приводим выдержки из научной статьи,
описывающей успешный анализ нерасшифрованных
линий спектра:
«В связи с изучением энтропии газов мы
недавно рассмотрели имеющиеся для
кислорода спектроскопические данные.
Спектры поглощения атмосферного кислорода
содержат необходимую информацию о
вращательных уровнях молекулы кислорода,
но... мы не могли найти никакой схемы,
которая объясняла бы возникновение всех
полос поглощения, если существует
только простая молекулярная форма
кислорода».
«Нам пришло в голову, что часть полос
поглощения может быть вызвана изотопом
кислорода и их можно полностью
объяснить, приняв существование кислородной
молекулы, состоящей из атома с м&ссои
16 и атома с M&ccoyi 18. Существование
подобного изотопа ранее не наблюдалось,
хотя теоретически и не опровергалось. Так как
у этого атома практически та же масс&г что
и у молекулы воды —18, их могли путать
при масс-спектроскопическом
исследовании».
«Поэтому мы пришли к заключению, что
изотоп кислорода с массой 18 присутствует
в атмосфере Земли. Судя по относительной
интенсивности полос поглощения,
содержание его должно быть очень мало, и
поэтому, его трудно определить при помощи
масс-спектрографа. Кажется вероятным, что
молекула с атомными весами кислорода 16
и 18 может быть более эффективным
поглотителем излучения, чем молекула
16—16». ^
Перевод с английского Л. СОЛОДКИНА
;i
i
••»••••••
'I'M' НОВОСТИ ОТОВСЮДУ
АРГОН ПРОТИВ
КИСЛОРОДА
Аргон нашел еще одно
применение в промышленности — его
используют для продувки жидкой
стали. Содержание кислорода
в стали, обработанной аргоном,
в пять раз меньше, чем в
обычной стали. Это положительно
сказывается на механических
характеристиках металла.
Расход аргона не так уж
велик — не более 3,5 м3 на тонну
стали.
И БЕНЗИН
И АПЕЛЬСИНОВЫЙ СОК
В США проходит испытания
экспериментальная автоцистерна
емкостью в 25 м3, изготовленная
из особой нержавеющей стали. Ее
главное преимущество состоит в
том, что она легко промывается
изнутри щелочными моющими
средствами. Поэтому в ней можно
транспортировать поочередно
жидкости с совершенно
различными свойствами, например, в
одном направлении перевозить
бензин, а в обратном — апельсиновый
сок.
ПОРОФЕН ЗАМЕНЯЕТ КИРПИЧ
Новый строительный материал —
лорофен разработан в
Чехословацкой Социалистической
Республике. Порофен
представляет собой жесткую пеиу фе-
нольной смолы. Он пегок,
достаточно прочен, не воспламеняется
при температурах до 150°С,
обладает хорошими тепло- и
звукоизолирующими свойствами. Поро-
феном можно частично заменить
кирпич в строительстве.
СТЕКЛОВОЛОКНО
ВМЕСТО ЭЛЕКТРОФИЛЬТРОВ
В сернокислотном производстве
для отделения капель тумана
серной кислоты, образующихся
в абсорберах, применяют
дорогие электрофильтры.
На заводе «Электроцинк» эти
фильтры заменили фильтрами из
стекловолокна, которое
вырабатывается на Ивотском стеклозаводе.
Такая фильтрация намного
проще и дешевле.
ПРОТИВОПОЖАРНАЯ РАКЕТА
В Японии ведется разработка
ракет для борьбы с пожарами в
многоэтажных домах и на складах
горючего. Опытный образец
противопожарной ракеты
представляет собой пластмассовый корпус,
наполненный водой и
специальными химикатами, с прикрепленным
к нему капсюлем-детонатором. К
нижней части корпуса
присоединяется стартовый реактивный
двигатель, работающий на твердом
топливе. Когда срабатывает
капсюль-детонатор, корпус
разрывается — и вода и химикалии,
помещенные в нем, разбрызгиваются
на 70 метров вокруг.
В декабре прошлого года был
проведен испытательный запуск.
Ракета, пущенная с расстояния
300 м, упала в метре от цели.
ОДНОЙ ПРИМЕСЬЮ
МЕНЬШЕ
В техническом бензоле есть
немало примесей, но, пожалуй,
самая нежелательная — это тио-
фен.
Японские ученые
разработали эффективный метод очистки
бензола от тиофена.
Опыт был поставлен так.
Бензол, содержавший 0,0037%
тиофена, пропускали через
адсорбционную колонку, заполненную сили-
кагелем марки 02з- Силикагель
предварительно обработали 98%-
ной серной кислотой. В колонке
происходило сульфирование
тиофена и поглощение
образовавшихся продуктов реакции. Анализ
очищенного бензола показал,
что он совершенно свободен от
тиофена.
ЛИСТ
ЗА РЕШЕТКОЙ
Блестящий металлический лист
кажется совершенно гладким,
пока на него не нанесут покрытие.
И тут неожиданно выясняется, что
на поверхности есть и выпуклости,
и выбоины. Для многих изделий
такие дефекты поверхности
недопустимы, и лист приходится
выправлять. При этом, конечно,
портится покрытие.
Как же обнаружить неровности
листа до обработки! Фирма «Ай-
Си-Ай» предлагает покрывать
металл временной пленкой, хорошо
отражающей свет. Покрытый лист
кладут за решетку и освещают его
непрямым светом. Тень от
решетки ложится на лист, и если на
поверхности есть дефект, то линия
тени либо искривляется, либо
прерывается.
Временное покрытие очень
дешево. Можно использовать
минеральное масло с добавкой малого
количества краски для улучшения
контрастности. После контроля
такое покрытие смывается
растворителем (например, трихлорэтиле-
ном) или водяным паром. Б
некоторых же случаях его можно
оставить на листе.
АЛМАЗ ИЗМЕРЯЕТ
ТЕМПЕРАТУРУ
В сентябре этого года фирма
«Дженерал Электрик»
предполагает начать выпуск термисторов
(датчиков температуры), в
которых термочувствительным
элементом будет служить кристалл
искусственного алмаза. Новые
приборы смогут измерять
температуру в диапазоне от минус
200°С до плюс 650°С. Достоинство
алмазного термистора состоит,
прежде всего, в его малой
инерционности — он очень быстро
реагирует на изменение
температуры, так как имеет малые
размеры и свойственную алмазу
высокую теплопроводность.
Термистор очень стабилен в
работе; так как алмаз устойчив
к коррозии, он может быть
использован для измерения
температуры почти любой
жидкости.
Предполагается, что алмазный
термистор найдет широкое
применение в промышленности и
исследовательской работе.
АТОМНАЯ —
НЕ ДОРОЖЕ
ТЕПЛОВОЙ
Ни у кого не вызывает сомнений,
что у атомной энергетики большое
будущее. Но как приблизить это
будущее! Такая проблема стоит,
в первую очередь, перед теми
странами, которые бедны углем,
нефтью и водной энергией.
Среди этих стран — Япония.
Первая экспериментальная
атомная установка в Японии дала
ток в 1963 году. Два года спустя
была пущена атомная
электростанция в Токио мощностью
166 тысяч киловатт. К 1970 году
запланировано построить еще
несколько электростанций
мощностью до 320 тысяч киловатт.
А каковы более далекие
перспективы развития атомной
энергетики в Японии! По мнению
японских специалистов, атомные
электростанции страны к 2000
году будут вырабатывать две трети
всей электроэнергии. А
электроэнергия атомных станций уже
через десять лет будет стоить,
вероятно, не дороже энергии
тепловых станций.
ЧИСТЫЙ ВОДОРОД
Промышленный способ
получения чистого водорода,
основанный на способности элемента
палладия поглощать, а затем снова
возвращать значительные
количества этого газа, разработан в ФРГ.
Процесс поглощения водорода
идет под давлением 30 атмосфер
при температуре около 400°С.
Палладиевые фильтры
изготовлены в виде тонких лленок,
которые наносятся на поверхность
пористого металлического или
неметаллического материала. В
целях усиления сорбционных свойств
в палладий добавляется примерно
25% серебра.
Производительность установок,
работающих по этому методу, до
14 кубометров водорода в час.
Количество лримесей в
полученном водороде не превы шает
0,0001%.
ЖИДКИЙ АЗОТ ЛЕЧИТ
Акромегалия — болезнь,
которая возникает при нарушении
деятельности мозгового
придатка — гипофиза. При этой болезни
искажается форма лица,
возникают утолщения кистей рук и
стоп. Методы лечения, которые
сейчас применяются, — рентгено-
или радиотерапия и
хирургическое вмешательство — не всегда
приводят к положительным
результатам.
Ученые из Калифорнийского
университета установили, что
акромегалию можно лечить
охлаждая гипофиз. Гипофиз
замораживают, вводя охлаждаемый
жидким азотом зонд через нос.
Больные, которых лечили этим
способом, выздоровели. Болезнь
уже 20 месяцев не дает
рецидивов.
НОВЫЙ МЕТОД
ОЧИСТКИ ТАНТАЛА
В Японии разработан новый
метод очистки тантала, тяжелого
тугоплавкого металла, все шире
применяемого в электронике,
электротехнике, химическом
машиностроении, ядерной технике
и даже хирургии.
По этому методу тантал
осаждается на вольфрамовом или
угольном катоде в процессе
электролиза его соли из расплава
хлоридов натрия и калия.
Температура процесса 750—850°С.
Метод позволяет получать
высококачественный тантал при
сравнительно небольшом расходе
электроэнергии.
НЕ СОВСЕМ ПОЛИЭТИЛЕН
Японские специалисты
предприняли попытку улучшить свойства
одного из самых распространенных
пластиков — полиэтилена. Для
этого во время полимеризации
этилена в реактор ввели мономер
синтетического каучука —
бутадиен. Полученный сополиМер
дополнительно обработали
перекисью дикумила, что привело к
изменению его структуры — так
называемому сшиванию
сополимера. В результате получился
пластик, значительно превосходящий
полиэтилен по прочности и
эластичности.
НОВОСТИ ОТОВСЮДУ MM*>Mt
Ежедневно в химических лабораториях
мира синтезируется несметное число новых
органических соединений. Новых — это
значит соединений с неизвестной (в лучшем
случае—с предполагаемой) структурой.
Но прежде чем приступить к главной
задаче — установлению строения нового
вещества— химик должен иметь о нем
какую-то предварительную, саглую основную
информацию: он должен знать его
качественный и количественный состав.
КОГДА РЕЧЬ ИДЕТ об органических
соединениях, приходится думать, главным
образом, об установлении именно
количественного состава — ведь «ассортимент»
элементов, из которых строятся органические
молекулы, довольно скуден и, как правило,
заранее известен: углерод, водород,
кислород; реже — азот, еще реже — сера,
фосфор... Поэтому речь обычно идет об
определении углерода и водорода — уж эти-то
элементы обязательно (во всяком случае
углерод) должны содержаться в любом
органическом соединении.
Этой цели и служит элементный
количественный анализ.
^ Данные количественного анализа
позволяют вычислить процентный состав вещест-
^5 ва, а по процентному составу можно рас-
>< считать простейшую формулу соедине-
^ ния — соотношение между числом атомов,
составляющих его молекулу.
«< Классический микрометод определения
?? этих элементов заключается в том, что ана-
ш лизируемое вещество сжигают, а количест-
X во образующихся окислов углерода (угле-
X
Наверху — установка для микроанализа на углерод
ф и водород
74
С=?
Н=?
Кандидат химических наук
А. И. АРТЁМЕНКО
кислоты) и водорода (воды) определяют по
привесу специальных поглотительных
приборов.
Пусть, например, при сожжении 1,400
миллиграмма анализируемого вещества
образовалось 1,800 миллиграмма воды и 4,400
миллиграмма двуокиси углерода.
Поскольку 44 весовые части СО:; содержат 12
весовых частей С, то для вычисления
количества углерода необходимо полученный вес
СО2 умножить на 12!аащ1 точно также для
вычисления количества водорода полученный
вес воды надо умножить на 2Ав, поскольку
18 весовых частей НгО содержат 2 весовые
части водорода.
Итак, находим, что в 1,400 миллиграмма
вещества содержится 4,400 ■ *21и = 1,200
миллиграмма углерода и 1,800 • 2Лв = 0,200
миллиграмма водорода. Следовательно,
процентное содержание углерода и водорода
соответственно равно:
1,200-100
% углерода (% С) = ~Т~4<кГ~ ^ 85,71,
0,200-100
% водорода (% Н) = —{~Щ~ = 7
Таким образом, в исследуемом
веществе содержится 85,71 процента углерода и
14,28 процента водорода. Именно эти
цифры и даст химик-аналитик химику-органику,
сдавшему вещество на анализ.
Ну, а дальше? Чтобы установить теперь I
простейшую химическую формулу соеди- I
нения по его количественному составу,
процентное содержание каждого элемента
делят на его атомный вес; полученные числа
показывают, сколько грамм-атомов того или
иного элемента содержится в 100 граммах
вещества:
85,71 М.28
Т2Ж^7'14; ХОГ^14'13-
Теперь уже нетрудно найти соотношение
.между числом атомов углерода и
водорода:
Число грамм-атомов С число атомов С 7,14 1
Число грамм-атомов A ~~ число атомов Н ^ 14,13 ^ 2
Приближенное равенство получилось
вследствие погрешности самого анализа. Но,
несмотря на это, можно сказать, что на
каждый атом углерода приходится два атома
водорода: простейшая формула
анализируемого вещества будет СНз.
Впрочем, такому же соотношению
атомов отвечает целый ряд формул: С2Н4,
С3Н6, С4Н8 и т. д. Выбрать одну из них
можно только в том случае, если известен
молекулярный вес вещества; однако это
особый вопрос *.
ВПЕРВЫЕ ВЕСОВОЙ МЕТОД
определения углерода и водорода применил в
прошлом веке 5L Берцелиус. В качестве
окислителя он использовал бертолетову соль, а
для поглощения углекислого газа и воды,
образующихся при сгорании органического
вещества, — твердый едкий кали и безвод-
лый хлористый кальций (рис. 1).
Несколько позже в эту методи+су были
внесены существенные изменения. Ю. Ли-
бих, ученик Ж. Гей-Люссака, в качестве
окислителя решил использовать окись
меди. Для поглощения двуокиси углерода он
применил не твердый едкий кали, а его
раствор, помещенный в так называемый «кали-
аппарат» (рис. 2). Была сконструирована и
особая печь для сожжения, допускающая
постепенный разогрев трубки. На эти
изыскания у Либиха ушло шесть лет
напряженной работы.
Но, несмотря на все
усовершенствования, этот метод имел еще существенный
недостаток: для анализа на углерод и
водород было необходимо значительное
количество вещества (не менее 0,2 грамма).
В 1912 году австрийский врач и химик
Ф. Прегль занялся разработкой новой
методики определения углерода и водорода,
которая позволила бы выполнять анализ с
очень малой навеской. Спустя несколько
лет, после многочисленных экспериментов,
Прегль добился успеха: его метод можно
было действительно назвать микромето-
* В дальнейшем мы расскажем и о методах
определения молекулярного веса органических
веществ. — Ред.
Рис. 1. Прибор Берцелиуса для определения
углерода и водорода:
а — сожигательная трубка; б — трубка с безводным
хлористым кальцием; в — сосудик с твердым едким
кали; г — ртуть
дом, так как на один анализ шло всего
несколько миллиграммов вещества.
Для того чтобы при столь малой
навеске анализ был бы все же достаточно
точным, Прегль уменьшил размеры прибора,
а также использовал для наполнения сожи-
гательной трубки несколько
веществ-окислителей. Благодаря этому углерод
органического вещества полностью сгорал до
углекислого газа (при старом методе
анализа могла частично образоваться окись
углерода), а водород — до воды.
Благодаря работам Прегля (которые,
кстати сказать, были отмечены в 1923 году
Нобелевской премией), микроанализ стал
мощным оружием в руках химиков. Можно
без преувеличения сказать, что
подавляющее число больших открытий, сделанных в
химии за последние полвека, было бы
невозможно сделать без помощи
микроанализа. Так, в тридцатых годах, спустя не-
Рис. 2. Прибор Либиха для определения углерода и
водорода:
а — печь; б — сожигательная трубка; в — трубка с
безводным хлористым кальцием; г — кали-аппарат
7о
Рис. 3. Схема современной установки для
микроопределения углерода и водорода:
а— газометр с кислородом; б — осушительная
склянка; в — винтовой зажим; г — прибор для
очистки кислорода: д — электрическая печь; е —
осушители кислорода (U-образные трубки с ангидро-
сколько лет после работ Прегля, А. Буте-
нандт открыл половой гормон — андросте-
рон. Ученому пришлось тщательно
переработать 15 тонн мочи, чтобы получить
^миллиграммов этого гормона! И только
благодаря микроанализу Бутенандт не только
определил количественный состав
полученного им соединения, но и приготовил из
оставшегося вещества некоторые
производные и снова проанализировать их.
Предъявляя все более и более строгие
требования к элементарному анализу,
ученые постоянно добивались повышения
точности главного аналитического «оружия» —
весов. Если раньше химиков-аналитиков
устраивала точность в сотые доли грамма,
то сейчас, при микрометоде определения
элементов, это уже тысячные доли
миллиграмма! Не правда ли, очень похоже на то,
как увеличение мощности пушек всегда
приводило к увеличению толщины брони?
КАК ЖЕ ДЕЛАЮТ АНАЛИЗ? Точно
взвешенное количество вещества (при
микрометоде— до 8 мг) помещают в платиновую
(или кварцевую) «лодочку» и сжигают в
кварцевой трубке, нагретой до 800—900°С,
через которую с постоянной скоростью
пропускают ток кислорода. Образующиеся
двуокись углерода и вода переносятся
газом в предварительно взвешенные
поглотительные аппаратики (рис. 3),
расположенные сразу же за трубкой. Вода поглощается
в аппаратике, заполненном перхлоратом
магния («ангидроном»), двуокись углеро-
ном и аскаритом); ж — трубка для сожжения; з —
электрическая печь; и — поглотительный аппаратик с
ангидроном; к — поглотительный аппаратик с
аскаритом; л — заключительная трубка с ангидроном;
м — склянка Маргитта (регулятор скорости тока);
н — мерный цилиндр
да — в аппаратике с едким натром,
нанесенном на асбест («аскаритом»); после того, как
сожжение закончено, кислород пропускают
еще некоторое время, чтобы полностью
вытеснить из трубки продукты сгорания.
Наконец, поглотительные аппаратики
тщательно взвешивают и по привесу
рассчитывают содержание углерода и водорода.
Следует подчеркнуть, что
поглотительные аппаратики надо взвешивать со «сверх-
ювел ирной» точностью: от тщательности
выполнения этой операции и зависит
результат анализа (при условии, конечно, что
все остальные операции были сделаны
правильно).
Итак, углерод и водород определяют
одновременно, из одной навески. Но
органические вещества часто содержат и
другие элементы, и это может осложнить
анализ: для определения каждого нового
элемента придется делать дополнительное
сожжение.
Поэтому сейчас чаще всего пользуются
методом одновременного
микроопределения углерода и водорода с другими
элементами (например, хлором, бромом,
фтором, серой, фосфором и многими
другими — почти половиной таблицы
Менделеева), разработанным советскими учеными
М. О. Коршун и В. А. Климовой. Этот метод
заключается в том, что органическое
вещество подвергают пиролитическому
разложению в пустой трубке для сожжения
(вспомним, что при определении по Прег-
70
лю в трубке находились наполнители),
через которую с большой скоростью
пропускают ток кислорода. В результате этого
продукты разложения попадают в
накаленную до высокой температуры богатую
кислородом зону и полностью окисляются до
двуокиси углерода и воды.
Поскольку при этом методе анализа в
сожигательной трубке нет никаких
наполнителей, то для связывания сопутствующих
элементов можно применять
соответствующие избирательно действующие
поглотители.
За последние годы наметилась
тенденция к полной автоматизации процесса
сожжения. С этой целью применяют
автоматические печи различной конструкции.
Автоматическое сожжение предусматривает
точный контроль за температурным
режимом, допускает параллельное сожжение
двух навесок; одним словом, делается все
возможное, чтобы исключить влияние на
результаты анализа индивидуальных
особенностей аналитика.
Но нужно не только автоматизировать и
совершенствовать традиционные методы
анализа. Нужно непрестанно искать
принципиально новые решения: только это
позволит органическому анализу не отставать от
все более и более строгих требований,
которые предъявляет к нему современная
органическая химия.
СДЕЛАЙТЕ,
ПОЖАЛУЙСТА,
АНАЛИЗ.»
десять заповедей химина-органина
Настоящее практическое руководство
представляет собой попытку обобщить богатый жизненный
опыт научных сотрудников, проработавших немало
лет в области органической химии. Редакция
надеется, что оно принесет пользу начинающим
ученым и не будет воспринято читателями с излишней
в этом случае серьезностью.
Вещество, подготовленное для
анализа, обязательно нужно
зашифровать — снабдить каким-
нибудь таинственным набором
букв и цифр.
Шифр создается так. Сначала
вы берете первую букву своей
фамилии, затем пишете перед ней
первую букву фамилии своего
непосредственного руководителя и
потом — первую букву фамилии
заведующего лабораторией.
Теоретически этот процесс можно
было бы продолжать и далее,
перебрав последовательно все
начальство, вплоть до президента
Академии наук, но практически
принято ограничиваться тремя
буквами. Впрочем, этого вполне
достаточно, чтобы польстить
руководству.
Вторая часть шифра —
условный номер вещества, или же
номер опыта, из которого оно
получено. Счет не следует вести
с единицы. Начните хотя бы с
сотни — это сразу же возвысит вас
в глазах аналитиков.
В общении с аналитиками
будьте вежливы и скромны.
Приходите точно в назначенное
время (от... до...), не забудьте
постучаться и на всякий случай
спросить разрешения войти. Войдя,
тихо поздоровайтесь и тотчас же
закройте за собой дверь —
плотно, но без стука. (Помните:
аналитики терпеть не могут шума
и сквозняков!).
Не беда, если ваша вежливость
будет походить на заискивание —
за это вас никто не осудит; зато
ваши акции в лаборатории
микроанализа значительно повысятся.
У всех аналитиков сильно
развито эстетическое чувство.
Поэтому сдавайте анализы в
красивых, тщательно отмытых
снаружи (и внутри тоже) баночках,
аккуратно закрытых чистыми
пробками. Этикетки должны быть
наклеены ровно и подписаны
изящно.
Трудно! Потренируйтесь.
На одно определение
углерода и водорода теоретически
требуется 1—2 миллиграмма
вещества. Если сжечь две навески, то
надо всего пять, от силы десять
миллиграммов. Аналитики же ста-
77
раются взять как можно больше.
Так, на всякий случай. И еще
потому, что с большими навесками
легче работать.
Не попадайтесь на эту удочку.
Давайте миллиграммов двадцать
и жалобным голосом говорите,
что больше нет. Не скандальте.
Если в вашем веществе есть
сера или хлор (а также бромг
йод)г не забудьте написать об
этом в требовании на анализ;
иначе прибор для сожжения
окажется испорченным. Такая
забывчивость вам никогда не простится.
Чтобы анализ был готов
раньше чем через две недели, делайте
испуганные глаза и шепотом
говорите, что вещество крайне
неустойчиво, что вам надо срочно
кончить статью, что у вас очень
сильно заболела любимая
бабушка — но только просите, а не
требуйте!
Помогает также близкое
знакомство с младшим лаборантским
составом.
Прежде чем дать вам
результат, от вас обязательно потребуют
так называемую «теорию» —
теоретическое содержание в
вашем веществе углерода и
водорода.
Неопытный органик заводит
в таком случае нудный и
бесплодный разговор:
— Л сколько у вас
получилось!
— А вам скопько нужно!
— Нет, вы скажите сначала,
сколько у вас получилось...
Не делайте этого. Подумав
секунду-другую, назовите два
первых пришедших в голову
правдоподобных числа. Сразу же после
этого хватайте бланк анализа и
убегайте. Некоторое время
спустя зайдите еще раз и дайте
чуточку измененные результаты,
списанные с бланка.
После того как вы попучипи
анализ, можно приступить к
самой захватывающей части
работы: вы должны попытаться
рассчитать состав вещества.
Сначала посчитайте составы
всех веществ, которые могли
получиться из ваших исходных
продуктов в результате всех
мыслимых и немыслимых реакций. Не
отчаивайтесь, если ни один состав
не подойдет под данные анализа.
Пересчитайте анализ, допустив,
что в веществе был негорючий
остаток; если и это не поможет,
предположите, что ваше вещество
содержало воду, или же какой-
нибудь органический
растворитель.
Кстати, подбирая разные
растворители, можно гибко
регулировать процентное содержание
углерода и водорода.
Умелой комбинацией всех этих
методов вы почти наверняка
подгоните данные любого анализа к
составу любого вещества.
Может случиться и так, что
вам все-таки не удастся опознать
вещество. Не отчаивайтесь,
сдайте его на повторный анализ (под
новым шифром!) — наверняка
получатся совсем другие
результаты.
Не сдавайте на анализ
поваренную соль — после того как
в ней не удастся обнаружить ни
углерода, ни водорода, ваша
репутация будет безвозвратно
подмочена...
С 1967 ГОДА НАЧИНАЕТ ВЫХОДИТЬ ЖУРНАЛ
«ХИМИЯ ТВЕРДОГО ТОПЛИВА»
Новый журнал — единственное
периодическое издание в СССР,
систематизирующее научную информацию по всем
вопросам химии твердого топлива и его
практическому применению.
В нем будут публиковаться
результаты теоретических и экспериментальных
работ в области научных и прикладных
химических проблем, связанных с
добычей и хранением различных видов
твердого топлива, их переработкой и
использованием в народном хозяйстве.
В журнале будут печататься
оригинальные статьи, обзоры, краткие
сообщения, переводы, критика и
библиография, научная хроника и письма в
редакцию,
Журнал рассчитан на широкий круг
химиков, горняков, энергетиков,
металлургов, работников
научно-исследовательских институтов, преподавателей и
студентов высших учебных заведений,
аспирантов и инженеров, занимающихся
переработкой и использованием
различных видов твердого топлива.
Журнал выходит 6 раз в год. Объем
номера 10 печатных листов. Подписная
цена на год 7 р. 50 к.
Подписка на журнал принимается в
пунктах подписки «Союзпечать»,
почтамтах и отделениях связи, общественными
распространителями печати на
предприятиях, в учреждениях и учебных
заведениях.
78
КЛУБ
юный
химик
вниманию новичков!
Устав клуба состоит всего из двух пунктов.
Пункт первый. Членом клуба может быть каждый школьник.
Пункт второй. Ответы на вопросы викторины клуба Юный химик нужно
высылать в редакцию до выхода в свет следующего номера журнала (потому
что в этом следующем номере ответы будут уже опубликованы).
Десять школьников, которые пришлют лучшие ответы в течение учебного года,
будут премированы подпиской на наш журнал на следующий год.
стол справок
КАК ПРОВОДЯТСЯ
ОЛИМПИАДЫ
«Ждем вас в нашем институте. Считаем, что экзамен
по химии вы уже выдержали», — сказал ректор
Казанского химико-техноиогического института
профессор П. А. Кирпичников. Эти слова были, пожалуй,
лучшим подарком для участников Второй
всероссийской химической олимпиады, проходившей в этом
году в Казани. Ребята получили рекомендации,
дающие им преимущественное право
поступления в химические вузы (при прочих равных
условиях).
Только в областных химических олимпиадах
РСФСР участвовало свыше 20 000
старшеклассников. Однако не все школьники знают, как
принять участие в химической олимпиаде. Об этом
свидетельствуют письма, приходящие в кпуб Юный
химик.
Как проводятся олимпиады! Корреспондент
журнала Жанна Мельникова попросила ответить на этот
вопрос председателя Организационного
комитета школьных олимпиад по математике, физике и
химии академика Исаака Константиновича КИКОИНА.
— Олимпиады начинаются в школах.
Учитель химии, физики или математики
организует в школе олимпиаду по
соответствующему предмету. В ней может принять
участие каждый школьник. Конечно,
олимпиады проводятся отдельно для восьмых,
девятых и десятых классов.
Победители школьной олимпиады
допускаются на олимпиаду районную.
Следующий этап — областная олимпиада. Из
сел, поселков, районных центров
школьники, победившие в районных олимпиадах,
приезжают в областной город. Средства на
поездку дает областной отдел народного
образования.
79
Представители Оргкомитета школьных
олимпиад помогают областному отделу
народного образования организовать
олимпиаду. После подведения итогов
олимпиады, они вместе выявляют четверых
сильнейших от 8, 9, 10 классов и рекомендуют их
для участия в заключительном туре. В этом
году, как вы знаете, заключительный тур
Всероссийской химической олимпиады
проводился в Казани.
Мы придаем большое значение
школьным олимпиадам. Мы не только помогаем
ребятам найти свое призвание, но и готовим
себе смену в науке. Кроме того, подготовка
олимпиад повышает уровень преподавания
точных наук в школе.
Чтобы облегчить школьникам
подготовку к олимпиаде, организованы заочные
олимпиады и конкурсы. Читатели журнала
«Химия и Жизнь» могут познакомиться с
химическими задачами, решение которых даст
им необходимые навыки и улучшит знание
предмета.
По третьей программе телевидения
проводятся и телевизионные олимпиады.
Победителей третьего тура мы вызываем в
Москву и организуем их встречи с учеными.
опыты ■ и
Еспи вам доведется побывать в Виннице, обязательно
зайдите в среднюю школу № 4 имени Д. И.
Менделеева. Вам покажут прекрасно оборудованный
химический кабинет с десятками электрифицированных
схем и таблиц, поясняющих ход химических
процессов. Вы увидите хитроумные приборы, наглядно
демонстрирующие тонкости химических реакций.
Несомненно, вы обратите внимание на
машину-экзаменатор «Лакмус», которая опрашивает весь класс за
три минуты и никогда не ошибается при
выставлении отметки, и на машину-репетитор «ДИМ-1»,
сделанную из старого автомата для газированной воды.
Но разве мало у нас хорошо оборудованных
кабинетов химии! Однако кабинет в винницкой
школе — особенный. Все в нем сделано руками
школьников.
Задачи и вопросы каждой прошедшей
олимпиады рассылаются в областные
отделы народного образования. Работники
отделов передают эти материалы в школы,
чтобы учителя могли ознакомить с ними
школьников, интересующихся химией,
физикой и математикой.
Чтобы успешно выступить в олимпиаде,
нужно не только уметь решать задачи, но и
самостоятельно делать несложные
лабораторные работы. В будущем мы
предполагаем включить в программу олимпиады
демонстрацию нового прибора собственной
конструкции или доклада по современному
состоянию какой-либо научной проблемы.
Ведь очень важно, чтобы участники
олимпиады умели творчески мыслить и
обладали прикладными навыками.
Основная доля в подготовке
школьников к олимпиаде принадлежит учителям.
Нередко жюри премирует и учителя за
хорошую подготовку школьников.
Много хлопот с подготовкой олимпиад и
их проведением, но сколько радости
приносят нам, организаторам, ваши отличные
знания.
По-разному проходят занятия в химических
кружках. Некоторых вполне удовлетворяют
эффектные химические реакции и получение известных
веществ известными способами. Спору нет, и это тоже
полезно и интересно. Но у винницких школьников
иная цель. Они хотят не только глубже познать
химию, но и помочь в этом своим одноклассникам,
и тем, кто пока еще учится в младших классах.
Приборы, описания которых помещены в этом номере,
расшифровывают — и весьма наглядно — такое
теоретическое понятие, как степень диссоциации
электролита. Тот, кто будет работать с такими
приборами, наверняка лучше усвоит этот раздел
школьной программы.
Общество любителей химии существует в
винницкой школе не первый год. Чтобы стать действи-
своими руками
80
тельным членом общества мало ходить на
внеклассные занятия. Нужно еще и хорошо учиться, а по
химии иметь отметку не ниже четверки. И, конечно,
таких ребят немало. Если бы все приборы, таблицы
и коллекции оставались в школе, то, наверное,
ребятам не хватило бы места для занятий. Но члены
общества охотно отдают свои приборы в другие
школы, особенно в сельские. (Впрочем, экспонаты
школьного химического музея уже заполнили
и школьные коридоры.)
Многие члены общества носят медали Выставки
достижений народного хозяйства. Лучшие работы
винницких юных химиков ежегодно экспонируются
на выставке.
Конечно, ребята занимаются не только
изготовлением приборов. Многие увлекаются
препаративной химией, агрохимией, фотохимией. Сейчас в
обществе действуют 11 секций. Но, пожалуй, основная
цель каждой секции, каждого члена общества —
помочь учителю преподавать химию. Результат —
отличные знания химии у выпускников школы,
носящей имя Д. И. Менделеева.
В Столе слравок этого номера журнала
академик И. К. Кикоин пишет, что от участников олимпиад
будут требовать демонстрации оригинальных
приборов. Пожалуй, почти каждый прибор, сделанный
в винницкой школе № 4, удовлетворит жюри
олимпиады.
Клуб Юный хнмик предлагает вам на этот раз
описания и схемы трех приборов, сделанных
любителями химии из Винницы. Эти приборы нетрудно
воспроизвести. Конечно, конструкция и детали могут
быть несколько иными. Ведь авторы приборов
делают их из тех материалов и деталей, которые
есть под рукой. Тут-то как раз и нужна
изобретательность и выдумка.
В заключение назовем имена тех, кто руководит
работой Общества любителей химии четвертой вин-
Один из создателей машины-экзаменатора,
выпускник винницкой школы № 4 Александр Гирич
Фото ученика восьмого класса Яши Дегина
ницкой школы. Это прекрасный педагог, основатель
общества Л. Е. Сомин и его бывший ученик, а теперь
школьный лаборант Ф. И. Крылов.
как определить
степень диссоциации
электролита»»»
ЛАМПОЧКОЙ
Круглая полочка, вращающаяся вокруг
вертикальной осиг установлена на деревянной
подставке. Через деревянную ножку
прибора проходит электрошнур. В полочке (ее
диаметр около 36 см) просверлено 11
отверстий и в каждое вставлен стограммовый
стаканчик (конечно, можно поставить
больше или меньше стаканов). Все стаканы
закрыты плексигласовыми крышками, сквозь
которые проходят два медных или уголь-
6 химия и Жизнь, № 10
«1
ных электрода. На крышке обязательно
напишите химическую формулу электролита,
налитого в стакан.
В центре круглой полочки закреплен
электропатрон с 25-ваттной лампой. Тут же
на полке находится пульт управления —12
гильз от малокалиберных патронов. Одна
из этих гильз (ее удобнее поместить в
центре) связана со шнуром от лампы. Остальные
11 включены в цепь, как показано на рис. 1.
Около каждого стакана хорошо поместить
по индикаторной лампочке. Они покажут,
через какой стакан идет ток.
Теперь в две гильзы (центральную и
произвольную) нужно вставить контактную
вилку. Цепь замкнется, и электрический ток
будет проходить через центральную лампу,
через стакан с электролитом и
индикаторную лампочку. Чем ярче горит центральная
лампа, тем больше степень диссоциации
электролита (при одинаковой нормальной
концентрации различных электролитов).
ДИНАМИКОМ
Прибор — это небольшой ящичек,
изготовленный из листового пластика или
фанеры. В верхней панели ящика просверлены
четыре отверстия диаметром 5 см, в
которые вставлены стаканчики стограммовой
емкости. Каждый стакан накрыт
пластмассовой крышкой, а на ней написана формула
вещества, раствор которого находится в
стакане. Через крышки пропущены медные
или угольные электроды. Тут же в верхней
панели просверлены отверстия. За ними
закреплен маленький динамик
репродуктора. Рядом с каждым стаканом —
выключатель. Схема прибора показана на рис. 2.
Включите прибор в розетку радиотрансля-
X«,
ф*11
-в =
4=3
Рис. 1
Рис. 2
ЕМА^ £ Д7А Д7Ж
п.
Рис. 3
ей
ционной сети. Звук в динамике будет то
громче, то тише — в зависимости от
степени диссоциации электролита.
Если в помещение не проведено радио,
то можно заменить динамик самодельным
генератором высокой частоты. Тогда
достаточно будет батарейки от карманного
фонарика, чтобы прибор работал.
АМПЕРМЕТРОМ
Этот прибор — тоже коробка из
листового пластика или фанеры. В верхней
панели прибора просверлены три отверстия
диаметром 5 см, в которые вставлены
стаканчики. Рядом с ними — миллиамперметр,
который будет оценивать степень электро-
«ДВОЙКА ПО ХИМИИ»
1. О ЗОЛОТЕ (А. Н. ТОЛСТОЙ].
Вопреки распространенному мнению, золото
растворяется в ртути очень ограничено — примерно 0,2%.
Извлечение золотых крупинок и пылинок ртутью
основано не на растворимости золота, а на хорошей
смачиваемости золота ртутью. В «жидких
дробинках» не может быть 90% золота.
2. О ФОСФОРЕ (Р. А. ШТИЛЬМАРК).
Фосфор не воспламеняется от воды. Наоборот, во
избежание окисления, фосфор хранят под водой.
J. О СОСТАВЕ МОРСКОЙ ВОДЫ [ЖЮЛЬ БЕРН).
Серной кислоты в морской воде нет. Морская вода
имеет щелочную реакцию (рН около 7,4).
ЧТО ЭТО ТАКОЕ!
На ладони плавится галлий — элемент № 31. Его
температура плавления всего 29,8°С. Значит,
теплоты нашего тела достаточно, чтобы превратить
твердый кусочек галлия в блестящую, как ртуть,
жидкость. Только два металла имеют температуру
плавления меньшую, чем галлий. Это ртуть и цезий.
А вот точка кипения галлия очень высока — око-
литической диссоциации того или иного
электролита.
Питается прибор от батарейки
карманного фонарика или от сети. В последнем
случае нужен понижающий трансформатор
(например, выходной трансформатор от
любого радиоприемника второго класса),
выпрямитель на диоде типа Д7Ж и
электрический конденсатор 200 мкф X 8 вольт. Как
их соединить — показано на рис. 3.
Ток подается на миллиамперметр
(чувствительностью не более 5 ма) через
кнопочный выключатель и один из стаканчиков
с раствором электролита. В зависимости от
степени диссоциации этого электролита
стрелка прибора отклонится на
определенное количество делений.
по 2240 С. Это позволяет применять галлий в
высокотемпературных термометрах. Кроме того, он
используется в специальных оптических зеркалах и
в полупроводниковой электронике.
ПОРОШОК ПРАЙСА
Для опытного химика в этой истории нет ничего
загадочного. Джеймс Прайс действительно сделал
открытие. Но ничего общего с алхимией оно не
имело — Прайс никогда не изготовлял золото. Он
извлекал его из ртути.
В XVIII веке большая часть запасов ртути
доставлялась в Англию с континента, причем она
содержала незначительную примесь золота. Прайс просто-
напросто выделял небольшие количества этого
драгоценного металла. Его болезнь, по всей
вероятности, была вызвана мышьяком, который входил
в состав красного порошка, или парами ртути.
Что же заставило Прайса столь неожиданно
расстаться с жизнью! Очевидно, во время рокового
эксперимента Прайс обнаружил свою ошибку.
Попробуйте представить себе столь ужасное
прозрение: золото все время присутствовало в ртути! В
отчаянии он схватил бутылку с синильной кислотой...
ответы
на вопросы
прошлого
номера
S3
ВИКТОРИНА
НЕЗНАКОМЕЦ МУТИТ ВОДУ
В повести писатепя Брет Гарта «История
одного рудника» есть такой эпизод.
«..Незнакомец вынул из притороченного
к седлу мешка маленький кожаный футляр
с несколькими склянками. Одну склянку,
завернутую в синюю бумагу, он протянул
Кончо...
— Налей-ка воды в котелок.
Кончо опорожнил бутылку с водой в
котелок и подал его незнакомцу. Тот опустил
в одну из склянок сухую былинку и
стряхнул в воду две капли. Вода осталась такой
же прозрачной.
— Теперь брось туда щепотку соли,—
сказал незнакомец.
Кончо посолил воду. На поверхности
тотчас же выступила белая пленка, и
вскоре вода приняла молочный цвет.
Кончо быстро перекрестился.
— Матерь божия, да это колдовство!»
Какую химическую реакцию Кончо
принял за колдовство! Почему склянка была
завернута в синюю бумагу!
ВВЕРХ И ВНИЗ
Если опустить сырое яйцо в слабый раствор
соляной кислоты, то можно наблюдать
странную картину. Яйцо сначала опускается
на дно, но через некоторое время оно
всплывает. На поверхности яйцо держится
недолго, и вновь тонет — и так до тех пор,
пока не растворится скорлупа.
Что же заставляет яйцо то нырять, то
всплывать на поверхность!
ИЗ СТАКАНА В СТАКАН
В один стакан налили воду, в другой —
равное количество сиропа. Оба стакана
поставили на стекло и сверху плотно накрыли
прозрачным сосудом. Воздух извне к
стаканам не поступает. Через несколько часов
обнаружилось, что уровень жидкости в
одном стакане понизился, а в другом
повысился.
Почему это произошло! В каком
стакане — с водой или с сиропом — понизился
уровень!
что это такое?
84
ХОТИТЕ ПОДГОТОВИТЬСЯ
К ЭКЗАМЕНАМ ПОЛУЧШЕ?
«На чашках весов уравновешены два сосуда, в
которые налиты равные объемы одного и того же
раствора сопяной кислоты»... Так начинаются все три
задачи, помещенные в этом номере журнала. Вам
предстоит решить, нарушится ли равновесие, если
ввести в сосуды те ипи иные вещества.
ЗАДАЧА 1. В один из сосудов насыпали 1 г мела.
Сколько нужно прибавить карбоната бария в другой
сосуд, чтобы равновесие не нарушилось!
ЗАДАЧА 2. В один сосуд добавили некоторое
количество мела, в другой — такое же количество
карбоната магния. Как изменится положение чашек
весов после окончания реакции! Возможен пи такой
случай, когда равновесие сохранится!
ЗАДАЧА 3. Сосуды — это колбы емкостью 100 и
500 мл. Обе колбы закрыты пробками, в которые
вставлены газоотводные трубки. В каждую колбу
помещают по 3 г магниевых стружек. Будет ли
сохраняться равновесие во время реакции и после
полного растворения магния! (Реакция в обеих
колбах идет с одинаковой скоростью),
ОТВЕТЫ К ЗАДАЧАМ
К ЗАДАЧЕ 1. Сначала запишем уравнения
реакций:
Са(Ю3 -;- 2НС1 = СаС12 -'- Н20 -г С02 f ;
100 44
ВаСОз '- 2НС1 = ВаС12 Н20 -f CO- Т.
197 44
На первой чашке после добавления мела и
выделения углекислого газа вес увеличивается. 100 г
карбоната кальция увеличивают вес этой чашки на
100—44= 56 г, значит, 1 г карбоната даст
увеличение веса на 0,56 г.
Сколько же нужно карбоната бария, чтобы
равновесие сохранилось! Так как и в этом случае
выделяется углекислый газ, то 1 г-м ВаС03 увеличит вес
сосуда на 197 — 44 = 153 г.
Составим пропорцию:
197 г 153 г 197 0,56
х г - 0,56 г х = 153 = °-71 г-
Напоминаем школьникам, что с первого
номера 1967 года под рубрикой «Хотите
подготовиться к экзаменам получше?» клуб
Юный химик начнет публиковать ВОПРОСЫ
ДЛЯ САМОПОДГОТОВКИ. Эти вопросы
(разумеется с ответами) облегчат вам
повторение всех разделов школьной програм-
Обычная ошибка при решении этой задачи
заключается в том, что вместо расчета увеличения
веса после добавления твердых реагентов
подсчитывают только потерю веса от выделения СО .
К ЗАДАЧЕ 2. Уравнения реакций:
СаСО, 2НС1 СаС12 11,0 С02Т ;
100
MgCQs 2HC1 MgClo H ,0 С02 Т -
84 '
Равное число молей карбоната кальция и
карбоната магния, растворенных в двух сосудах, вызовет
равную потерю веса (выделяется одно и то же
количество С02). Но чиспо молей в одинаковых
навесках этих веществ не равно: молей MgCO больше,
так как его молекулярный вес меньше. Значит, из
сосуда с карбонатом магния выделится больше
углекислого газа. Сосуд с карбонатом кальция
перетянет. Вы заметили, что в этом рассуждении есть
небольшая погрешность! Ведь нам неизвестно,
достаточно ли кислоты для того, чтобы реакции
растворения карбонатов прошпи полностью! А количество
кислоты (если она была взята в недостатке]
определяет вес выделяющегося углекислого газа. Если
кислота была взята в недостатке, то в обоих
сосудах выделится одинаковое количество газа, и
равновесие не нарушится.
К ЗАДАЧЕ 3. При уравновешивании сосудов
взвешивается и находящийся в них воздух. Когда в
результате реакции выделяется водород, он
вытесняет воздух из колб и общий вес сосудов с газом
уменьшается. Ее пи бы колбы были одинаковой
емкости, то выделение водорода не изменило бы
положения весов. Но поскольку одна из колб намного
больше другой, то она потеряет больше воздуха, и
маленькая колба перетянет. Правда, после
окончания реакции чашки весов постепенно уравновесятся,
так как произойдет диффузия водорода.
А зачем в условиях задачи упоминались пробки
с трубками для отвода газа! Если бы колбы были
открытыми, то выделяющийся водород не смог бы
полностью вытеснить из них более тяжелый воздух.
мы и помогут успешно сдать экзамен по
химии. Образцы вопросов для
самоподготовки напечатаны в прошлом номере
журнала.
Конечно, наряду с вопросами по теории,
клуб Юный химик будет продолжать
публикацию задач.
85
СТЕКЛОДУВНАЯ
МАСТЕРСКАЯ
На предыдущих занятиях мы рассказывали об
«азах» стеклодувного мастерства: каждый
химик — начиная от участника школьного
химического кружка и кончая опытным научным
сотрудником — должен уметь резать трубки,
оттягивать капилляры, делать пробирки, стаканчики.
Ведь не беспокоить же по таким пустякам
опытного мастера-стеклодува! Химика, не владеющего
всеми этими приемами, можно сравнить разве
что с плотником, который для того, чтобы
разогнуть гвоздь, бежит в слесарную мастерскую...
Но иногда бывает полезно уметь делать и
более сложные вещи. Поэтому на последних
занятиях мы разберем еще несколько операций. К их
числу следует отнести способы изготовления
различных спаев.
КАК ДЕЛАТЬ
«ПРОСТОЙ» СПАЯ
Простым спаем соединяют трубки «торец в то^
рец»: этот спай действительно самый простой.
Для начала возьмите трубку диаметром 8—
10 миллиметров, сделайте на нее обычную
заготовку и один из оттянутых кончиков обломайте.
Когда заготовка остынет, разрежьте ее пополам,
стараясь сделать чистый срез, строго
перпендикулярный оси трубки. Полученные половинки
возьмите в руки за оттяжки (а) и начните
нагревать оба торца одновременно (б). Когда стекло
достаточно сильно размягчится, быстро (но не
сильно!) соедините их друг с другом (в). При
этом надо следить за тем, чтобы по окружности
образовавшегося шва не было щелей: этот
дефект практически неисправим, так как
поставить на стекло «заплату» — дело почти
безнадежное.
Но пока что настоящего спая еще не
получилось: после охлаждения шов или сам собой
лопнет, или же окажется настолько ненадежным,
что изделием нельзя будет пользоваться.
Поэтому его нужно еще, как говорят стеклодувы,
«пропаять», то есть разгладить, сделать
равномерным по толщине.
Пропаивать шов можно или сразу, или же
«по частям». Если трубка не очень широкая (как,
например, в нашем случае), шов можно пропаять
по всей окружности одновременно. Для этого
надо вынуть трубку из пламени и немного
поддуть через оттяжку — на месте шва при этом
получится небольшое вздутие. Это вздутие надо
снова разогреть (г), дать стеклу осесть, потом
снова выдуть небольшой шарик и т. д. до тех
пор, пока вы не увидите, что спай стал
совершенно прозрачным. Тогда надо еще раз раздуть
небольшой шарик и очень осторожно потянуть
концы трубки в разные стороны. При этом
шарик растянется и диаметр трубки на месте спая
станет равным диаметру самой трубки.
Но если вам надо спаять два отрезка широкой
трубки (или если вы еще не научились уверенно
обращаться со стеклом) шов можно пропаивать
приемом «по частям». Для этого его надо внести
в пламя, но только не вращать при этом трубку;
когда часть шва размягчится и осядет, надо
вынуть трубку из пламени и немного поддуть через
оттяжку. После этого надо пропаять соседний
участок и т. д. — пока весь шов совершенно не
разгладится.
Следует иметь в виду, что при пропаивании
«по частям» получается некрасивый волнистый
спай; поэтому в заключение рекомендуется
разогреть трубку по всей окружности и выровнять ее
поддуванием.
Лучше учится делать спай сразу, а прием «по
частям» использовать только при спаивании
очень широких трубок.
И еще одно замечание: приемом пропаивания
«по частям» нельзя пользоваться в том случае,
если диаметр трубки очень мал: просвет между
стенками может затянуться расплавленным
стеклом и на месте соединения получится
стеклянная «пробка». Торцы таких трубок перед
спаиванием следует немного развернуть.
Научившись делать простой спай, вы можете
попробовать ускорить его изготовление.
Опытные стеклодувы обычно поступают так: торцы
трубок слегка развертывают, затем быстро
и сильно разогревают, соединяют вместе и тут
же поддувают (пока стекло еще не затвердело),
одновременно немного растягивая спай — с
такой скоростью, чтобы диаметр трубки в месте
соединения оставался неизменным. В этом
случае спай получается особенно чистым и
красивым.
Если нужно спаять между собой трубки
разных диаметров, то поступают так: у широкой
трубки делают круглое дно, в центре дна
продувают отверстие (его диаметр должен быть
равен диаметру узкой трубки) и затем, как
обычно, делают простой спай.
8G
КАК ДЕЛАТЬ
«ТРОЙНИКОВЫЙ» СПАЙ
Очень часто возникает необходимость сделать
Т-образную трубку — «тройник». Сделать «трой-
н иконы и» спай — это и значит припаять одну
трубку к другой сбоку.
Технология изготовления такого спая
несложна: его делают в общем так же, как и простое
•соединение между трубками разных диаметров.
Но расскажем все по порядку. Сделайте две
заготовки и одну из них разрежьте пополам,
причем одну оттяжку целой заготовки
обломайте, а оттяжку половинки — оставьте запаянной.
После этого в стенке целой заготовки продуйте
отверстие, размягчите его края, а также торец
узкой трубки, соедините их вместе так же, как
Открыта подписка на 1967 год на
ежемесячный научно-технический журнал
[[ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ».
Орган Министерства химической
промышленности СССР.
Журнал выходит 12 раз в год. Объем
номера 10 печатных листов.
это делалось при изготовлении простого спая
(при этом надо особенно тщательно следить за
тем, чтобы образовавшийся шов был без щелей),
и одним из известных вам приемов пропаяйте
место соединения.
Имейте в виду: при пропаивании «по частям»
надо следить за тем, чтобы противоположная
спаю сторона трубки не размягчалась, но,
одновременно, и не слишком охлаждалась. Если вы
хотите пропаивать спай сразу по окружности, то
Т-образную трубку надо вращать приемом,
применяемым для вращения согнутых трубок.
После того, как спай готов, надо слегка
обогреть противоположную сторону трубки горячим
(не коптящим!) пламенем и затем отжечь как
обычно.
В. ЖВИРБЛИС
Подписная цена на год 9 р. 60 коп.
Подписка на журнал принимается в
пунктах подписки «Союзпечать»,
почтамтах, отделениях связи, общественными
распространителями печати на
предприятиях, в учреждениях и учебных
заведениях.
87
СОЛЯРИЗАЦИЯ
Оператор Б. ПЛУЖНИКОВ
Натюрморт, жанровая сцена и
городской пейзаж, которые вы
видите на фотографиях,
сняты с использованием
фотографического эффекта, известного
под названием соляризации.
Соляризация — это
получение обращенного изображения
при сильных передержках.
В сильно передержанных
местах негатива металлическое
серебро теряет способность к
восстановлению. Поэтому после
проявления возникает не
только обычное негативное
изображение, но и участки
позитивного. Отпечатав такой негатив,
получат, например, фотографию
На фотографиях (слева
направо):
Натюрморт — соляризация в
негативе; В одной упряжке —
соляризация в позитиве и
фотобарельеф; Город — соляризация
в позитиве
пейзажа, диск солнца на
котором будет черным.
Обычно экспозиции,
необходимые для соляризации,
настолько больше обычных, что
хорошая фотография с
элементами обращенного изображения
не получается. Кроме того, для
создания эффекта соляризации
пригодны не все
фотографические материалы.
Если в эмульсии есть
акцепторы галоида, например
гидразин, или в проявителе
содержится растворитель галоидного
серебра, то создать эффект
соляризации трудно. Способность
к соляризации исчезает и при
низких температурах.
На практике эффект
соляризации получается
по-другому. Частично проявленный
негатив равномерно освещают, а
затем проявляют вновь. Б этом
случае некоторые его участки,
на которых сохранилась
способность к восстановлению
металлического серебра, темвеют.
В этих местах происходит
обращение, соотношение тонов
частично или полностью
изменяется. Так же, как и в случае
мокрой маски, здесь действует
«эффект Сабатье», о котором
мы писали в статье «Как снять
привидение», напечатанной в
№ 7. Вокруг позитивного
изображения возникает черный
контур. Ширина черного
контура и характер перемены тонов
зависят от того, насколько
продолжительно было
засвечивание, и от степени
предварительного проявления перед ним.
Засвечивание прежде всего
увеличивает плотность на
неэкспонированных или
недодержанных участках негатива.
Этим иногда пользуются,
чтобы снизить контрастность и ис-
S8
■f'Zi*
править недодержки. Нужно,
однако, помнить, что в этих
случаях, несмотря на то, что
плотность недодержанных
участков увеличивается, фактуры
в них не возникает.
Чтобы получить в негативе
задуманный эффект
перестановки тонов, нужно иметь
несколько фотопленок, проэкспо-
нированных в одних и тех же
условиях. С этими дублями
проводят пробы, по которым
устанавливают время
предварительного проявления и
время засвечивания. Первую
пробу обычно делают так: пленку,
снятую с нормальной
экспозицией, проявляют две трети
положенного времени, затем
вынимают ее из проявителя,
промывают, равномерно освещают
с выдержкой в полсекунды и
опять опускают в проявитель.
Эффект соляризации
получают (как, впрочем, и все
другие фотографические эффекты)
не при обработке
оригинального негатива, а после того как
отпечатают заранее отобранные
и подготовленные фотографии
или диапозитивы.
После засвечивания и
вторичного проявления негатив
может оказаться слишком
плотным. В таких случаях его
ослабляют, обрабатывая,
например, в ослабителе Фармера,
содержащем красную кровяную
соль и тиосульфат натрия.
Эффект соляризации можно
получить и в позитивном
процессе. В этом случае
происходит обратная перестановка
тонов: передержанные или
слишком плотные, непропечатываю-
щиеся участки негатива
благодаря дополнительному
засвечиванию и последующему
проявлению дадут нужную
плотность в позитиве. Таким
способом также можно создать на
снимке черное солнце и небо.
Если при засвечивании
негатива тона сдвигаются в сторону
позитива, то в этом случае
происходит обратное: в позитиве
появляются негативные тона.
Сначала нужно установить
нормальное время проявления, а
уже затем после частичного
проявления отпечатка найти
время засвечивания.
Образование белого и
черного контура в негативном или
позитивном процессе позволяет
получить изображение без
каких-либо деталей.
Фотографические эффекты,.
в том числе и соляризацию,
часто сочетают с особыми
способами печатания. Например, на
фотографии «В одной
упряжке» эффект соляризации
дополнен специальным способом
печати, создающим впечатление
фотобарельефа. Для этого
фотографию печатают со
сложенных вместе — эмульсия к
эмульсии — негатива и
диапозитива. Чтобы отпечаток
производил впечатление
барельефа, негатив и диапозитив-
должны немного не совпадать.
На этой фотографии такая
печать дала контур вокруг
изображения. А благодаря
дополнительному засвечиванию
(отдельные участки снимка
были перекрыты) после первого
проявления получилось темное-
небо и, кроме того, не
выражена фактура одежды и катка,.
который волокут люди. Такое
обобщение придало
фотографии монументальность.
8Ь
4\
Г»А'
что полезно знать
о новых чистямцих
средствах?
Многие читатели — в основном читательницы —
спрашивают нас в письмах: какие новые чистящие
средства рекомендует бытовая химия! На чем
основан принцип действия отдельных препаратов!
На их вопросы отвечает сотрудник Министерства
торговли РСФСР Тамара Сергеевна Горяинова.
■ Все мы знаем, что кастрюли, чайники,
сковородки и прочая «аппаратура» кухни от длительного
употребления темнеет, покрывается липким налетом.
Отмыть такой налет просто мылом и водой
невозможно. И каждая хозяйка становится химиком.
Лабораторное исследование налетов на посуде
показало, что они состоят из непостоянного
комплекса углеродистых веществ, окисленных жиров,
остатков Сахаров и смолистых веществ. Многие из
этих соединений нерастворимы в воде.
Щ Ученые, специалисты по бытовой химии,
называют эти налеты и осадки «естественными
загрязнениями». Они утверждают, что естественные
загрязнения обладают большой клейкостью и
удерживаются на поверхности посуды силами
молекулярного и электростатического притяжения,
адсорбции (сгущения на поверхности без проникновения
в глубь твердого тела) и диффузии (проникновения
одного вещества в другое при их непосредственном
соприкосновении).
Загрязнения на металлических предметах,
применяемых в быту, но- не связанных с приготовлением
пищи, носят Другой характер. Это в основном
известковые и окисные пленки. Они менее клейки и
удаляются легче.
■ На раковинах, ваннах и в унитазах, а также на
кафельных стенах кухни, ванной, уборной оседают
частицы мыльных растворов, пото-жировые
вещества, различные соли и окисные соединения.
И Американские ученые Сэндерс и Лемберт
изучали состав уличной грязи и пыли. Они утверждают,
что городская пыль состоит из водо- и эфирораство-
римых масел, жиров, углеводов, окислов металлов
и золы. Эти же элементы входят в загрязнения,
покрывающие поверхность оконных стекол, стен,
ковровых и текстильных изделий.
■ Чистящие средства — это, конечно, не только
достижения химии середины XX века. С древних
времен хозяйки во всех странах мира чистят и
скребут свою посуду золой и песком, толченым
кирпичом и мелом. В основе их стихийных «физических
и химических опытов» лежит простой принцип: чтобы
облегчить свой труд, они используют так называемые
абразивные материалы (название происходит от
латинского «abrasio» — «соскабливание»).
■ Абразивы, абразивные материалы — основной
компонент (до 70—85%) большинства и
современных чистящих препаратов. Зерна абразива снимают
мельчайшую стружку загрязнений — сначала с
«выступов» поверхности изделия, а затем и со всей
очищаемой площади. Зерна абразивных материалов,
применяемых в распространенных чистящих
средствах — это молотая пемза, каолин, кварцевый песок,
наждачный порошок, отходы гончарного
производства. У них острые режущие края и, кроме того, они
обладают способностью самозатачиваться.
Происходит это потому, что абразивы не только
тверды, но и хрупки; их частицы легко
разламываются, образуя меньшие частички с острыми краями.
■ Введение в чистящий состав того или иного
абразива зависит от общего назначения препарата.
Например, если он предназначается для очистки
изделия из цветного металла или сплава,
берутся мягкие абразивные материалы тонкой
структуры: химически осажденный мел, каолин, диатомит.
Это исключает появление царапин и повреждение
полировки, так как твердость абразивов здесь
меньше, чем твердость поверхности очищаемых
материалов.
■ Наоборот, в чистящие препараты,
предназначенные для очистки предметов, изготовленных из
стали и чугуна, травленого алюминия, кафеля,
вводятся более твердые абразивные материалы,
имеющие крупнозернистую структуру (кварцевый песок,
молотая пемза, электрокорунд, наждачный
порошок).
В некоторые чистящие средства вводятся разные
виды абразивов — и твердые, и мягкие (с
твердостью по шкале Мооса от 4,5 до 7). Такое сочетание
смягчает действие слишком твердых материалов.
90
■ В чистящие препараты кроме абразивов входят
многие другие компоненты. Это — синтетические
поверхностно-активные вещества и моющие
соединения — сульфонол, прогресс, алкилсульфат, ДС-
РАС, хозяйственное мыло и другие,— либо
щелочные соли — кальцинированная сода, силикат натрия,
тринатрийфосфат, сульфат натрия *, а также
полезные добавки и ингибиторы (вещества, замедляющие
или прекращающие реакцию), глицерин, карбокси-
метилцеллюлоза, отдушки, красители.
■ Щелочные соли — до того, как они растворяются
в воде — действуют так же, как абразивы. Затем,
растворяясь, они расщепляют жиры и масла.
По другому ведут себя поверхностно-активные и
специальные моющие вещества. При нарушении
структуры загрязнений (от действия абразивов) они
«улавливают» отдельные «отчуждающиеся» частицы.
Некоторые из этих средств, например
пальмитиновая и олеиновая кислоты, вступают в химические
соединения с окислами металлов, смываемыми с
загрязненной поверхности; другие — понижают
поверхностное натяжение водной пленки, «усваивая»
загрязнения, не удерживаемые силами адсорбции.
■ Остальные компоненты чистящих средств
смягчают действие щелочей, защищая поверхность от
коррозии и ослабляя действие препарата на кожу
рук. Другие добавки придают ему
дезинфицирующие свойства, приятный цвет и запах и т. п.
■ Промышленностью бытовой химии выпускаются
и специализированные чистящие препараты: для
удаления накипи с посуды (антинакипин);
дезинфицирующие; предохраняющие окна от запотевания и
обледенения и другие. Состав этих препаратов более
сложен. В них входят парахлорбензолсульфокислота,
тиомочевина, олеиновая кислота, триэтаноламин,
сульфаминовая кислота и другие соединения.
■ Всего нашей промышленностью бытовой химии
выпускается около 60 наименований чистящих
средств. В хозяйственных магазинах в большом
выборе разные флаконы, коробки, пакеты с чистящими
препаратами. Перечислим некоторые из них.
* Обычно берется одна из этих солейз
■ Для очистки фарфора, хрусталя, стекла, мраморе,
оконных стекол, зеркал в продаже имеются
жидкости «Нитхинол», «Свет», «Кристалл», «Янтарь» а
также концентрированные жидкие препараты
«Быстрый», «Сподриба», «Нитхинолконцентрат» и другие.
■ Для чистки хозяйственной посуды, ванн, раковин,
кафеля, металлических вещей выпускаются порошки
«Пемоксоль», «Чистоль», «Блеск», «Слава»,
«Алюминии», «Гигиена», «Швара», «Спидола», «Эмалир»,
«Зеркальный» и другие. Пасты: «НЭДЭ»,
«Универсальная», «Ангарская», «Рефракс», «Юра», «Ару»,
специальная паста для чистки ванн и ряд других.
■ Для ухода за изделиями из меди, бронзы,
мельхиора, золота, серебра, никеля можно
использовать чистящие средства «Асидол», «Ниро», пасты
«Луч», «Идеал», вату «Металлин», эмульсию «Огонек».
■ Ковры и искусственный мех, декоративные ткани,
кожу и кожезаменители можно чистить жидкими
препаратами «Коврин», «Мехочистка», «Эфра», «Ка-
ро-мехочистка», «Пеночистка» и другие.
■ Эффективность действия чистящих средств
зависит от многих причин. Самая важная из них —
строгое соблюдение рекомендаций по употреблению,
которые обычно приложены к каждому изделию
бытовой химии. Эти рекомендации — не праздная
выдумка изготовителей, а необходимое условие
применения химических «помощников в быту».
Например, не случайно рекомендуется тщательно
ополаскивать вычищенную посуду холодной и
теплой водой и протирать ее полотенцем, так как в
трещинах, местах сколов эмали, в мельчайших
раковинках алюминиевой посуды могут оставаться
зерна абразивов или их обломки, а также
незначительные количества кислот, щелочей и .других веществ.
Чистящие средства, как и вообще все товары
бытовой химии, следует хранить отдельно от
пищевых продуктов, в местах, недоступных детям.
Яркие пакеты, банки, флаконы могут привлечь их
внимание, — а это совсем не безобидные игрушки!
Товары бытовой химии сейчас приобрели право
на жительство в каждом доме. Познакомьтесь же
с ними получше!
91
ГИДРОПОНИКА
ПРИ ИСКУССТВЕННОМ
ОСВЕЩЕНИИ
<
ас
X
ЕС
О
о.
О
<
ЕС
о
со
О
ЕС
<
и
<
<
О.
U
Если вы воспользовались
нашими советами, напечатанными в
предыдущих номерах журнала, и
начали выращивать у себя на окне
огурцы или земляникуж то теперь,
когда наступила осень, вам пора
подумать о подсвечивании.
Оконные стекла вообще плохо
пропускают свет — через двойные
рамы проходит всего около 60%
лучистой энергии. А необходимые
растению ультрафиолетовые лучи
стекло поглощает почти
полностью.
Особенно же плохо чувствуют
себя выращиваемые в комнате
растения в осенне-зимний период,
когда дни становятся короткими,
а небо большей частью покрыто
облаками. В это время без
подсвечивания комнатных растений
не обойтись.
Растения требуют довольно
сильного света. Если применять
лампы накаливания, то их
мощность должна быть не менее 300—
500 ватт. Такие мощные лампы
выделяют много тепла, поэтому
их нужно подвешивать не ближе
На снимке вверху справа —
разработанная автором установка
для подсвечивания комнатных
растений, которая, с успехом
применяется при выращивании
огурцов и помидоров на питательном
растворе
чем в 50—60 см от верхушек
растений, а по мере их роста лампы
нужно поднимать. Сильные лампы
заметно иссушают воздух,
поэтому растения при искусственном
освещении следует почаще
опрыскивать водой.
А лучше всего использовать
для подсвечивания растений в
осенне-зимнее время
люминесцентные лампы. Они значительно
экономичнее в эксплуатации, чем
лампы накаливания: при той же
мощности люминесцентные лампы
дают в 3—4 раза больше Света,
почти не отличающегося по
спектру от рассеянного света летнего
дня. Кроме того, такие лампы
слабо нагреваются и не обжигают
растений; их можно подвешивать
в 4—5 см от верхушек.
При прочих равных условиях
подсвечивание люминесцентными
лампами дает возможность
сократить сроки выращивания
огуречной и помидорной рассады
почти вдвое и получать
продукцию на 15—20 дней раньше.
Урожай при этом увеличивается на
30—35%. Это происходит потому,
что при свете люминесцентных
ламп усвоение растениями
углекислоты из воздуха идет
значительно энергичнее, чем при свете
ламп накаливания. Растения
полнее поглощают лучистую
энергию, интенсивнее идет фотосинтез
и накапливается больше
органического вещества.
Наша промышленность
изготовляет люминесцентные лампы
мощностью 30, 40 и 80 ватт. Лампы
различаются также и по
спектральной характеристике
излучаемого ими света: бывают лампы
белого света («ЛБ»), дневного
света («ЛД» и «ЛДЦ») и теплого
белого света («ЛТБ»). Наиболее
распространены 30-ваттные лампы
«ЛД», которые лучше всего
применять и для подсвечивания
комнатных растений.
Продолжительность
подсвечивания зависит от длины дня. В
общей сложности растение должно
быть освещено не менее 10—\2 и
не более 16 часов в сутки. Более
продолжительное действие света
неблагоприятно отражается на
растениях.
Люминесцентные лампы лучше
всего подвешивать над
растениями с помощью железной или
деревянной рамки, к которой
параллельно одна другой
прикрепляются лампы. Так как по мере роста
растений лампы приходится
поднимать, рамку подвешивают на
тросе или проволоке, которую
перекидывают через блоки,
прикрепленные к косякам окна.
А. А. НОВОСЕЛОВ,,
агроном
92
встреча
на
перекрестке
Эта книга * чуть-чуть
загадочна с первого взгляда —
незнакомый герб на обложке, название —
и своеобразный сллав биологии,
физики, химии, инженерных
догадок, истории, литературы.
Но эксцентричен не автор —
эксцентрична наука, о которой
написана книга. Она поражает
парадоксальностью увиденного и
неожиданностью выводов.
Бионика — наука новая. Еще совсем
недавно о ней писали только
молодежные научно-популярные
журналы, которым снисходительно
разрешали пропагандировать
самые «безумные» идеи
современного естествознания. Но,
применяя к ней слова Нильса Бора,
бионика оказалась достаточно
«безумной», чтобы стать настоящей
наукой — имеющей свои
институты, лаборатории, ставшей темой
не только полуфантастических
журнальных заметок, но и
солидных книг.
«Третий триумвират» Игоря
Миронова не принадлежит к
числу этих солидных монографий.
Книга написана не ученым, а ли-
тератором, написана для того,
чтобы рассказать юным
читателям о новой науке,
необыкновенной по тому, чем она занимается,
и фантастической по перспекти-
* И. Миронов. «Третий
триумвират». М., Изд-во «Детская
литература», 1965.
вам своего развития. Бионика
занимается конструктированием
механизмов, в основу которых
положены идеи, заимствованные
у живых приборов, созданных
природой и прошедших наладку
и испытания в течение
тысячелетий упорной и безжалостной
борьбы за существование. Эта
новая наука создана
сотрудничеством биологов и физиков,
математиков и инженеров. Поэтому-то
на обложке книги герб, главные
элементы которого — скальпель,
интеграл и паяльник. Поэтому
и названа она «Третий
триумвират».
Бионика — наука, которая не
имеет еще готовых и
сформулированных истин. И это касается
не только сложных инженерных
решений, но и самой проблемы.
И автор книжки рассказывает об
опытах, заброшенных и
возобновленных через полтора столетия.
Он приводит примеры гипотез,
которым не хватало
доказательств, чтобы превратиться в
убеждение, внезапных озарений,
гасших в противоречиях
наблюдений. Мы и поныне наблюдаем
явления, которым нет пока еще
обоснованных объяснений.
Почему слепые свободно ходят по
многолюдному городу и обходят
препятствия, даже не коснувшись
их палочкой? Каким образом
птицы и насекомые ориентируются
по солнцу и звездам? Существует
ли «кожное зрение»?... Автор
«Третьего триумвирата» отвечает
на эти вопросы, опираясь на
последние достижения физиологии,
химии, физики, отвечает с
абсолютным убеждением, что человек
не только способен разгадать
тайны природы, но и обогнать ее
в своем конструкторском
творчестве.
Можно и не соглашаться с
подобным оптимизмом. Но одно
несомненно: И. Миронов всегда
проводит точную границу между
желаемым и существующим.
Этот элемент научной
добросовестности мне представляется
очень важным в любой книге,
популяризирующей новые научные
идеи. Возможность сомнений,
право на любую критику — как
часто мы наблюдаем изгнание
этих необходимых нравственных
основ науки из многих
популярных книг! В «Третьем
триумвирате» первые выводы, первые
успехи новой науки не превращаются
в догму. И. Миронов ссылается на
остроумно-печальный плакат,
повешенный в одном из
авиационных конструкторских бюро:
«Конструктор, помни, что по законам
аэродинамики жук не должен
летать!»... Творческим духом
беспокойства, сомнений, проверки,
поисков наполнена книга И.
Миронова, как и та наука, о которой
она написана.
Лев РАЗГОН
Уважаемые читатели! Подписка на «Химию и жизнь» на 1967 год
принимается во всех почтовых отделениях, всеми общественными уполномоченными.
Индекс журнала по каталогу Союзпечати—71050.
Цена годовой подписки A2 номеров] 3 рубля 60 копеек.
Редакция
93
СПУТНИКИ ЗУБАСТЫХ
четыре рассказа
о зубной пасте
1. Рассказ пострадавшего.
Эту историю, немного
напоминающую гпаву из «Приключений
Мюнхгаузена», мне рассказал
журналист Н.
— Пресс-конференция,
посвященная открытию
международного научного конгресса, была
назначена на 10 часов утра. Я уже
кончил гимнастику, умылся, сел
перед зеркалом, включил бритву...
Искра, треск — и привычное
жужжание смолкло. До ближайшей
парикмахерской от нашего дома
ходьбы минут пятнадцать. Да там
проведешь в лучшем случае
столько же.
Я стал судорожно искать
старые, не электрифицированные
принадлежности для бритья.
Нашел лезвие и помозок, тощий, как
хвост вымокшего котенка. Взбить
им пену обычного мыла не
удавалось, хотя, кажется, никогда
ничего в жизни я не делал с большей
старательностью. А стрелки часов
на месте не стояли, положение
становилось угрожающим.
И тогда меня осенило: ведь
только что я чистил зубы
импортной пастой с явным мыльным
привкусом! Чистила она хорошо,
но рот обрастал хлопьями пены,
как у коня после трудной скачки.
Недолго думая, я выдавил из
тюбика на щеку белую колбаску,
смочил помазок: взмах, другой,
третий...
Ровно без пяти десять я сидел
в зале пресс-конференции.
Эта история не выдумана: она
просто оказалась той зацепкой,
которая побудила нас обратиться
с вопросами к специалистам по
зубной пасте.
2. Рассказ Е. Н. Кисповой,
зам. начальника
исследовательской лаборатории
парфюмерной фабрики
«Свобода»
Екатерина Николаевна Киспова,
узнав о цели моего визита,
начала с вопроса:
— Простите, а чем вы чистите
зубы?
— Дома обычно порошком, а
в командировку беру тюбик
«Мятной» или «Детской».
— Давно вы не были в
командировках. «Детская» уже год не
выпускается. И производство
«Мятной» мы будем постепенно
сворачивать.
А порошком чистите напрасно.
Много лет назад какой-то не очень
сведующий ученый объявил, что
зубные пасты вредны, и зубы
следует чистить только порошком.
Давно уже забылось имя этого
ученого, а предрассудок живет.
А ведь любой порошок — это, в
сущности, только мел, химически
осажденный, очень мелкий, с
развитой поверхностью. Отдушка *
из него улетучивается. Не будешь
же герметически упаковывать
зубной порошок — он станет
дорогим и потеряет свое
единственное преимущество перед пастой.
В порошок бессмысленно вводить
какие-либо специальные добавки
профилактического или лечебного
назначения. Улетят на ветер. К
тому же, как ни мелок порошок, его
твердые кристаллы все-таки
царапают зубную эмаль. А пасты,
естественно, нет. В них нет ни од-»
ного мало-мальски вредного
компонента. А полезные, даже
целебные, входят во многие сорта.
Вы никогда не пользовались
«Лесной»? Зеленоватого цвета,
невкусная, горчащая паста. С 1960
года в Одесском
стоматологическом институте исследуют
свойства десятков сортов зубных паст,
И отечественных и зарубежных,
Оказалась, что наша «Лесная»
(горчащая, невкусная, зеленая) —
самая полезная. Она не телько
хорошо «отмывает» зубы, не и
* Отдушкой парфюмеры
называют специальные добавки
душистых веществ, вводимые в
мыло, кремы, пасты. Количество
отдушки, как правило, не
превышает 1 %.
убивает всю вредную
микрофлору полости рта.
Антисептическим действием
обладают и зубные пасты
других марок, выпускаемые нашей
фабрикой, —«Бороглицериновая»,
«Жемчуг», «Ягодка»,
«Апельсиновая». Последние три сорта к
тому же очень ароматны и приятны
на вкус.
3. Рассказ И. С. Шехтман,
химика, ведущего специалиста
лаборатории
по зубным пастам
— В любой пасте
количественно преобладают мел и
связующее. Мел — тот же, что идет на
приготовление порошка. Он всегда
одинаков. А вот связующие
бывают разные. В старых рецептурах
связующим был глицероль —
крахмальный клейстер,
приготовленный на водном растворе
глицерина. С точки зрения химии,
это обычный коллоидный
раствор. Чтобы придать ему
определенную физическую
стабильность, в глицероль добавляют
немного мыльного порошка —
примерно полтора процента от веса
глицероля.
У такого связующего два явных
недостатка. Во-первых,
крахмальный клейстер — очень
«неплохая» питательная среда для
микробов; во-вторых, в это
связующее приходится вводить слишком
много глицерина — 36% от веса
пасты. Глицерин не вреден для
полости рта, но дефицитен и
дорог.
Лучшие зарубежные сорта
зубной пасты сделаны на
бескрахмальном связующем — растворе
тилозы с уменьшенным
содержанием глицерина. Тилоза — это
натриевая соль карбоксиметил-
целлюлозы (Na-КМЦ):
[CbH00,OCH2COONa]n.
Сейчас уже освоена очистка
Na-КМЦ от вредных примесей
(метод очистки предложен
Харьковским
химико-фармацевтическим институтом), и мы готовим
на ней несколько сортов пасты —
обычную «Мятную», с<Апельсино-
вую», «Жемчуг». Они теперь
содержат почти вдвое меньше
глицерина, чем раньше.
Чем отличается «Мятная» от
современных сортов и почему
мы считаем нецелесообразным
ее дальнейший выпуск? Зубная
паста «Мятная» не содержит
биологически-активных добавок.
Кроме мела и связующего, в ней
есть только ментол, мятное и
анисовое масла, придающие вкус
и запах. «Мятная» неплохо
очищает зубы, создает во рту
приятное ощущение прохлады, но на
бактерии практически не
действует. Главная же особенность
новых паст —
биологически-активные добавки. «Лесная» содержит
5% хлорофигло-каротиновой
пасты, извлекаемой из игл хвои. Это
сложный комплекс биологически-
активных веществ, главным
образом, хлорофилла, провитамина А
(каротина), жирных и смоляных
кислот.
Растворимые в воде
соединения хлорофилла способствуют
заживлению ран и ссадин на деснах
и других тканях рта,
препятствуют развитию бацилл,
вызывающих порчу зубов — кариес.
Интересно действие хлорофилла и его
соединений на запахи: они
уничтожают неприятные запахи
полости рта, но не заглушают
приятных запахов косметических
добавок отдушки. Другой компонент
этой пасть! — каротин
способствует защите и восстановлению
живых тканей полости рта.
Схема
комплексно-механизированной линии по
производству зубных паст
1. Просеиватель мела; 2.
циклоны с шлюзовыми затворами;
3. шнек; 4. бункер для мела;
5. мерник для воды; 6. мерник
для глицерина; 7. мерник для
Вот и решайте после этого, чем
лучше чистить зубы: порошком,
«Мятной» пастой или невкусной,
зеленой «Лесной».
Сорта . «Ягодка» (преемник
«Детской») и «Апельсиновая»
тоже обладают бактерицидным
действием.
В «Ягодку» в качестве
антисептика вводится бороглицерин.
А приятный вкус ей придают
добавки пищевых эссенций —
клубничной или ананасной.
В «Апельсиновой» пасте
работает другой антисептик — пара-
формальдегид, полимер
формальдегида: НО(СН20) Н, впервые
полученный и исследованный еще
в f859 году знаменитым химиком
А. М. Бутлеровым. Количество
этого вещества, введенное в пасту
@,1%), настолько ничтожно, что
человек его даже не замечает, но
эта доза достаточна для
обезвреживания микробов полости рта.
Тот же антисептик применен и
в «Жемчуге». В эту рецептуру
введены еще два компонента —
по 2,5% поваренной соли и
глицерофосфата кальция.
мыльной стружки; 8. мерник
для крахмальной суспензии;
9. насос для глицерина; 10.
варочный котел; 11. насос для
связующего; 12.
котел-холодильник; 13. мешальная
машина; 14. дозатор для полезных
добавок и отдушки; 15. насос
для зубной пасты; 16.
вальцовка; 17. расфасовочный автомат
93
Назначение этих веществ —
укрепление минеральной решетки
зуба. Глицерофосфат повышает
также сопротивляемость кариесу
и, как говорят медики, уменьшает
чувствительность шеек зубов к
внешним раздражителям.
— Не значит пи это, что
зубную пасту «Жемчуг» можно
особо рекомендовать драчунам и
боксерам!
— Драчунов она вряд ли
спасет, а спортсменам будет
безусловно полезна.
— В чем особенности
знаменитых импортных паст
«Хлородонт» и «Поморин»!
— «Хлородонт», выпускаемый
предприятиями ГДР, содержит
несколько процентов бертолетовой
соли: КСЮз. Это довольно
эффективное отбеливающее средство.
Поэтому паста «Хлородонт»
придает зубам белизну скорее, чем
другие. Однако многие медики не
убеждены в полной безвредности
столь значительной добавки
хлората калия и не рекомендуют
сводить этот компонент в наши
новые рецептуры.
Болгарский «Поморин» —
действительно целебная паста. В нее
вводится концентрат воды
морских лиманов, поэтому «Поморин»
богат многими элементами,
нужными человеческому организму,
он благотворно действует на
зубы и десны.
В нашей лаборатории
разработана рецептура новой пасты
подобного типа. Воду из лиманов в
ней заменит природный
концентратор элементов морской воды —
широко известная водоросль
морская капуста. Она богата калием,
-фосфором, йодом, бромом,
кальцием и многими другими
элементами.
Еще один интересный сорт
зубной пасты фабрика «Свобода»
начнет выпускать в ближайшее
время. Тех, кто будет ею
пользоваться, эта паста избавит от
зубного камня: один ее компонент
будет раствлрять органическую
часть зубных отложений,
другой — неорганическую.
Разумеется, паста не снимет старых, уже
обызвесткованных, как говорят
стоматологи, отложений. Их
придется удалять, как и раньше, у
зубного врача, но паста не даст
нарасти новому камню.
Самое важное назначение
зубных паст, — заканчивает Инна
Соломоновна, — сделать ваши зубы
здоровыми, помочь
врачам-стоматологам укоротить очереди
возле их кабинетов.
4. Рассказ И. С. Аратова,
директора фабрики «Свобода»
— Если несколько лет назад
нас больше всего волновали
вопросы расширения ассортимента,
то сейчас, как это ни странно, на
первый план вышел «вал».
У нас есть Очень хорошие
рецептуры зубных паст, однако они
пока не вытеснили ни порошка, ни
«Мятной». И в этом году мы
ввели в строй пять
комплексно-механизированных линий
непрерывного производства паст.
Иван Сергеевич подводит меня
к красочной схеме (в несколько
упрощенном виде она
воспроизведена на стр. 95), показывает и
объясняет.
— Здесь, внизу, узел
подготовки мела. На смешение со
связующим его уносит воздух,
засасываемый циклонами, а после
шлюзовых затворов—шнек. В
правом верхнем углу — узел
подготовки связующего: мерники,
насосы. На схеме показан процесс
приготовления пасты на глице-
рольном связующем, при работе
с тилозой схема будет проще.
Отдушка и биологически-активные
добавки вводятся прямо в
метальную машину (тоже через
мерник). Оттуда готовая паста
поступает на вальцы и еще раз
перетирается, гомогенизируется.
После этого идет на
расфасовочный автомат.
Пока нам не удалось
механизировать последние операции:
упаковку туб в футляры, а
футляров — в коробки. Если сумеем и
здесь поставить автоматы, то
каждая такая линия даст экономию
около семнадцати тысяч рублей в
год.
До последнего времени мы не
могли особенно рекламировать
наши новые пасты из-за
неизбежного вопроса: «А где их купить?»
Расширение производства
автоматически снимет этот вопрос.
В заключение я задал и тот
вопрос, с которого началось мое
знакомство с проблемами
зубной пасты: будут ли выпускаться
сильно пенящиеся зубные пасты!
Почему они пенятся!
Директор ответил:
— Пенятся из-за мыла.
Достаточно ввести его вместо одного
5—6 процентов, и паста даст
обильную пену. Только вряд ли
это нужно. Бриться зубной пастой
приходится не часто, а привкус
мыла во рту — не так уж приятен.
Рассказы записал
В. СТАНИЦЫ! 4
На обложке журнала воспроизведена этикетка спичечного коробка, которая могла
бы служить иллюстрацией к статье кандидата биологических наук А. Г. Гусева,
напечатанной под рубрикой «И химия — и жизнь!»
Редакционная коллегия:
Главный редактор И. В. Петрянов-Соколов
П. Ф. Баденков, В. И. Гольданский, Н. М. Жаворонков, С. В. Кафтанов, Л. И. Мазур,
Б. Д. Мельник, В. И. Рабинович (ответственный секретарь), П. А. Ребиндер,
М. И. Рохлин (зам. главного редактора), С. С. Скороходов, Б. И. Степанов, А. С. Хохлов,
М. Б. Черненко (зам. главного редактора), Н. М. Эмануэль
Рукописи не возвращаются. При перепечатке ссылка на журнал «Химия и Жизнь» обязательна
Оформление С. Верховского Технический редактор Э. Язловская
Адрес редакции: Москва, В-333, Ленинский проспект, 61/1. Телефоны АВ 7-72-64 и АВ 7-66-23
Подписано к печати 22/IX-1966 г. Т 13806. Бумага 84 X lOe'/ie- Бумага л. 3,0. Печ. л. 6.0. Усл. п. л. 10,08 + 1 вкл. Уч.-изд. л. 11.
Тираж 79 000. Зак. № 1308. Цена 30 коп. Набор и печать выполнены в Московской типографии № 2 Главполиграфпрома Комитета по
печати при Совете Министров СССР. Москва, Проспект Мира, 105.
Печать обложки и цветной вклейки и брошюровочные работы выполнены во 2-й типографии издательства «Наука». Москва,
Шубинский пер., 10.
В СЛЕДУЮЩЕМ
НОМЕРЕ:
Новая рубрика: обзоры,
классика науки. Магнето-
химия
Активные поверхности
и жизнь
Гипсолюбка ищет медь ^
Наш календарь:
300-летие этилена
Рассказы о лекарствах:
хинин
Внимание, ядохимикаты!
Элемент № 26: железо
Что такое антипузыри ^
Минералы,
изготовленные в цеху
Клуб Юный химик:
Опыты без взрывов.
Викторина, Вопросы
для самоподготовки.
Стол справок
и другие материалы
Схемы растут в растворе
Микроорганизмы —
источник энергии
Изразцы древние
и сегодняшние ^
Можно ли сделать самому
пасту для шариковой
ручки
Индекс 71050
Цена 30 коп.