Текст
Б. В. ЛИНЧЕВСКИЙ
ТЕХНИКА
МЕТАЛЛУРГИЧЕСКОГО
ЭКСПЕРИМЕНТА
Издание второе, переработанное
Допущено Министерством высшего и среднего
специального образования СССР в качестве учебного пособия для
студентов вузов, обучающихся по специальностям
«Физико-химические исследования металлургических процессов»
и «Физика металлов»
Москва «Металлургия» 1979
УДК 62.669.001.5
УДК 62.669.001.5
Техника металлургического эксперимента. Изд. 2-е. Л и н ч е в-
с к и й Б. В. М., «Металлургиям 1979. 256 с.
Основной задачей данного учебного пособия является
подготовка студентов к самостоятельной научной деятельности, ознакомление
их с основными направлениями работ в области исследований
теории металлургических процессов, изучения свойств жидких металла
и шлака. Отдельно рассматриваются анализ газов в металлах и
методы оценки загрязненности стали неметаллическими включениями.
Книга может быть полезна инженерам-исследователям,
аспирантам и работникам научно-исследовательских институтов. Ил. 112.
Табл. 3.
31002—118
л ^ГГ, 133—79 2601000000
040(01)—79
© Издательство «Металлургия», 1979
ПРЕДИСЛОВИЕ
Для современной металлургии характерно значительное
внимание к вопросам повышения качества сталей и
сплавов и эффективности производства, что стало
возможным благодаря значительно возросшему уровню
научных исследований. Сегодняшнее положение в теоре-ш
тичеокой металлургии показалось бы фантастическим
ученым XIX в. как по объему выполняемых
научно-исследовательских работ, так и по уровню их технической
оснащенности. Значительно усложнилась техника
экспериментальной работы, улучшилось обеспечение
лабораторий сложным отечественным и импортным научным
оборудованием, возросла роль математической обработки
результатов. В связи с этим стала более сложной работа
исследователя, которая требует широкой подготовки в
различных областях знаний и в первую очередь в области
теоретической металлургии.
В металлургических и политехнических институтах в
учебные планы введены курсы, освещающие вопросы
организации и проведения физико-химических
исследований металлургических процессов. Помимо
обязательных лекционных курсов, широкое развитие в последние
годы получила самостоятельная научная работа
студентов, проводимая на кафедрах, в отраслевых и
производственных лабораториях.
В данной книге систематизирован обширный
материал из 'периодической печати, научных монографий и
сборников трудов в применении к методической стороне
исследований. В одних случаях даны лишь общие
принципы постановки тех или иных исследований, в других
рассмотрены конкретные приборы и способы работы на
них. Показаны возможности различных методов
исследования, отмечены их преимущества и недостатки по
сравнению с другими.
Первые четыре главы посвящены общим вопросам
высокотемпературного эксперимента: способам получения
высоких температур, конструкциям нагревательных
устройств — печей, методам измерения высоких
температур, созданию защитных атмосфер в опытных установках.
Достаточно подробно рассмотрен материал по вакуумной
технике, столь необходимой для проведения многих
работ.
В главах V и VI освещены вопросы исследования
свойств жидкого металла и шлака, процесов межфазово-
=1* Зак. 664
3
го взаимодействия, диффузии элементов в расплавах,
кинетики процессов рафинирования металлов,
калориметрических исследований, восстановления и
диссоциации окислов. В главах VII и VIII рассмотрены способы
определения содержания газов и неметаллических
включений в стали и в сплавах.
По сравнению с первым изданием, вышедшим в
1967 г., настоящая книга значительно переработана. Она
не содержит многих данных сугубо справочного
характера; опущены методы математической обработки
результатов наблюдений, так как они читаются в специальных
курсах; исключены устаревшие методы анализа газов,
редко применяемые методики исследований. Значительно
обновлен материал по исследованию активности
компонентов в расплавах, отражены вопросы
калориметрических измерений, методы исследования восстановительных
процессов, определения неметаллических включений,
рассмотрены но-вые способы исследований в области
диффузии, электрохимического контроля окисленности металла.
Автор выражает благодарность коллективу
преподавателей кафедры теории металлургических процессов
МИСиСа за ценные замечания, сделанные при
рецензировании рукописи.
ГЛАВА I
МЕТОДЫ ПОЛУЧЕНИЯ ВЫСОКИХ ТЕМПЕРАТУР
Процессы получения и очистки большинства металлов
связаны с применением высоких температур.
Исследования выплавки металлов, взаимодействия жидких
металлических расплавов со шлаками, газовыми
атмосферами, огнеупорными материалами, наконец, изучение
свойств жидких металлов и шлаков требуют создания
источников высокотемпературного нагрева,
нагревательных устройств — печей.
Основная задача нагревательного устройства
сводится к созданию зоны равномерного нагрева в
определенном ограниченном объеме и обеспечению температурного
режима во времени. Любая печная установка должна
содержать: а) источник тепловой энергии; б) камеру
нагрева; в) средства управления и контроля теплового
режима.
Наибольшее распространение в лабораторной
практике получили электрические печи. В зависимости от
способа нагрева различают:
1. Печи сопротивления. Они хорошо поддаются
регулированию, удобны для создания заданного
распределения температуры в камере нагрева. Для этих печей
можно применять нагреватели различной формы. Для
получения температур в области 1200—1600°С ib качестве
нагревателей используют благородные металлы, а для
более высоких темоератур — молибден, вольфрам,
тантал, графит. Нагреватели из дисилицида молибдена
могут работать в окислительной атмосфере до 1600°С.
2. Дуговые печи. В основном это вакуумные печи для
плавления металла в вакууме или в атмосфере
нейтрального газа. Дуговые печи позволяют достигать высокой
температуры, но с трудом поддаются регулированию.
Зону равномерного нагрева в большом объеме в этих печах
создавать сложно.
3. Плазменно-дуговые печи. В этих установках можно
осуществлять весьма высокий нагрев в разнообразных
атмосферах, но поддерживать заданную температуру
расплавов и однородный нагрев во всей камере печи
сложно.
4. Высокочастотные печи. К их достоинствам
относятся: универсальность бесконтактного нагрева, хорошая
регулируемость теплового режима, возможность получе-
5
ния высоких температур и питания различных установок
от одного генератора.
Трудность нагрева неметаллических и немагнитных
материалов, ограничение размеров нагреваемого
пространства контуром индуктора являются недостатком печей
этого типа.
Расчеты печей
Расчеты лабораторных установок сложны и редко выполняются на
практике. Для проведения расчета необходимо знать величины
нагреваемых и теплопроводящих поверхностей, толщины стенок,
теплопроводность и другие характеристики материалов. Необходимая
мощность печи зависит от толщины теплоизоляции и
приблизительно пропорциональна температуре нагрева. Для оценки
необходимой мощности можно пользоваться приближенной 4юРмУл°й
Кинджери, Вт:
Q = 0,0015 Лmtll
где Ат — средняя поверхность, см2; t — температура в печи, °С;
/ — толщина теплоизоляции, см.
Расчетную мощность необходимо увеличить на 20—30% для
достижения заданной температуры в приемлемое время и на 20%
для учета потерь тепла через отверстия в концах трубчатой
камеры и т. п., или всего на 40—50% против расчетной.
1. ПЕЧИ СОПРОТИВЛЕНИЯ
Печи сопротивления используются для исследования
физико-химических свойств жидких и твердых металлов,
взаимодействия металла со шлаком и газом при высоких
температурах.
Эти печи представляют собой камерные или
трубчатые конструкции с заложенными в стенки, навитыми на
трубы или свободно расположенными нагревательными
элементами, через которые пропускается ток. В
некоторых случаях сам нагреватель образует камеру печи. В
зависимости от требуемой температуры нагрева и
атмосферы нагревательной установки для нагревателей
используются самые различные материалы в виде
проволоки, ленты, труб, стержней.
Металлические нагреватели
При использовании для нагревателей проволоки с
невысоким омическим сопротивлением рекомендуется
изготовить из нее спираль, которую помещают внутрь печных
стенок. Металлы с высоким сопротивлением (молибден,
вольфрам, платина и ее сплавы) применяют в виде
толстой проволоки, ленты, стержней. Такие нагреватели под-
вешивают на стенках камеры, собирают в виде различных
конструкций: «шпилечных», «беличья колеса» и т. д.
Большинство металлов и сплавов, кроме платины, в
окислительной атмосфере работать не может. Поэтому
пространство печи, где смонтирован нагреватель, заполняют
защитной нейтральной атмосферой или создают в нем
вакуум. Нагреватели из благородных металлов и сплавов
могут использоваться в окислительной атмосфере, но в
результате испарения уменьшаются в сечении. По этой
причине их обмазывают цементными покрытиями,
которые не должны содержать разрушающие нагреватель
кремнезем и железо. Лучшими считаются обмазки из
глинозема и огнеупорной глины.
Наибольшее распространение из лабораторных печей
сопротивления получила трубчатая печь, в .которой
нагревательная обмотка, навитая на внешнюю поверхность
трубы — муфеля, сверху обмазана цементом.
Фарфоровую, корундовую, силлиманитовую или цирконовую
трубу на керамических подставках вставляют в корпус и
засыпают пространство между корпусом и трубой тепло-
изолятором.
Следует учитывать, что при температуре выше 1700°С
двуокись циркония взаимодействует с глиноземом, а цир-
коновые трубы становятся электропроводными. В
вакуумных печах, работающих при температуре до 2000°С,
термическую изоляцию обычно заменяют радиационными
экранами из листового молибдена или тантала,
устанавливаемыми вокруг нагревателя внутри металлического
корпуса.
Чтобы проволока ровно ложилась на трубу,
поверхность ее перед обмоткой покрывают слоем незатвердёв-
шего цемента. Для компенсации тепловых потерь около
краев трубы намотку делают более плотной.
Максимально допустимая температура в печах
сопротивления зависит от устройства печи и от планируемого
ооока службы нагревателя. Платиновая спираль служит
достаточно долго при работе в области 1400—1500°С.
Сплавы платины с родием могут применяться при
нагреве до 1700°С, но срок их службы меньше, чем у платины.
Молибденовую проволоку или вольфрахмовые прутки
допускается применять в вакууме и при создании
восстановительной атмосферы, например водородной. Водород
подают в печь непрерывно, поддерживая в корпусе
установки положительное давление, что устраняет возмож-
7
ность подсоса воздуха и образования гремучей смеси. На
выходе из печи водород сжигают.
Вольфрам чаще применяют в виде толстых прутков,
из которых оплетают нагреватель в виде «беличьей
клетки». Из листового тантала и молибдена толщиной 0,25—
0,4 мм изготовляют нагреватели для установок с быстрым
нагревом. На концах металлических листовых
нагревателей нужно делать пропилы и прорези с целью
уменьшения сечения для повышения электросопротивления.
Для повышения рабочей температуры проволока из
молибдена, вольфрама или тантала не должна
соприкасаться с огнеупорными деталями печи. При нагреве выше
ШОО^С спирали подвешивают внутри печного
корпуса. Во избежание провисания спирали необходимо пра-^
вильное сочетание диаметра спирали и температуры
нагрева. Так, при температуре нагрева до 2100°С
применяют спираль из вольфрама диаметром 19—20 мм, а до
2500qC диаметр спирали должен быть 12—13 мм. Такие
подвесные бесконтактные опирали из тугоплавких
металлов могут обеспечить длительный нагрев печи до
2000°С.
В глубоком -вакууме (<0,01 Па) происходит сильное
испарение материала спирали при ее нагреве до
температуры, °С:>1800 для молибдена, >2400 для
вольфрама и>2200 для тантала. При внезапном отключении
тока металлические нагреватели коробятся.
Неметаллические нагреватели
Наибольшее распространение получили силитовые
нагреватели — готовые стержни, трубы из карбида
кремния и стержни из дисилицида молибдена, работающие
в окислительных условиях. В печи стержни могут
располагаться как вертикально, так и горизонтально.
Силитовые нагреватели при правильной
эксплуатации работают в условиях высоких температур в течение
нескольких сотен и даже тысяч часов.
Большое значение имеет закрепление стержней в
токоподводах, через которые проходят большие токи.
Для плотного закрепления конец нагревательного
стержня можно сделать на 0,25 мм больше по диаметру,
чем отверстие в токоподводе, и пропилить его вдоль на
2—3 диаметра, что обеспечит плотный и надежный
контакт. Существует конструкция высокотемпературной
8
Вход доды
печи, в которой 12 силитовых стержней длиной по
480 мм, расположенных по окружности, подвешены
только сверху. Это дает возможность свободно изменять их
длину. Утолщенные концы стержней проходят через
асбоцементные диски, теплоизоляционные подушки из
легковеса и алундовые кольца. На нижнем кольце
устанавливают керамическую
подставку и держатель тигля.
Пространство между двойным
кожухом печи и внутренними
керамическими деталями
заполняют ультралегковесом.
Сверху и снизу печь
закрывают экранами и защитными
кожухами.
Использование вместо
стержней нагревательных труб
позволяет увеличить отношение
поверхности излучения к
сопротивлению, использовать
меньший ток при более
высоком напряжении.
ДЛЯо,ллоТеНИЯ ТеМПеРаТУ- Рис. 1. Горизонтальная графи-
РЫ ДО 2400 С Сконструирована товая трубчатая печь:
печь с трубчатым нагревате- J = X™i™7Pt^lT™£-
ЛеМ ИЗ ДВуОКИСИ ТОрИЯ. Трубы ба; 4 — порошкообразная уголь-
отливали в гипсовые формы. ™ Ж^Ье;5^11»^
Концы труб насыщали иттрием ^иап^™е:эк7р^орпус; *~
для повышения
электропроводности, чтобы сопротивление трубы в месте, контакта
соответствовало сопротивлению цирконового блока.
Контактные блоки готовили из двуокиси циркония,
стабилизированной присадкой 5—6% СаО.
Большое распространение получили печи с
графитовыми нагревателями. Применение до 2000°С графитовых
нагревателей объясняется их доступностью,
удовлетворительными электрическими свойствами, хорошей
обрабатываемостью.
Печи с графитовыми нагревателями могут быть
вертикальными и горизонтальными. В горизонтальной печи
(рис. 1) графитовая труба, окруженная графитовой
засыпкой, укрепляется в двух контакгных углеродистых
блоках, которые соединены с медными шинами.
Соединение графитовых труб с держателями рекомендуется
9
производить на пасте, состоящей из 70% графитового
порошка, 15% декстрина и 15% воды. Конец трубы
можно запрессовывать в водоохлаждаемый медный
наконечник. Графитовый нагреватель может иметь фланец,
который {посредством медного кольца прижимается к
плите токоподвода.
Вертикальный графитовый нагреватель представляет
собой стакан с утолщением снизу и сверху, окруженный
четырьмя радиальными и двумя тарелочными
графитовыми экранами, которые расклиниваются корундовыми
пластинками. Внизу нагреватель заканчивается конусным
контактом, прижимаемым к нижнему токоподводу.
Верхняя утолщенная часть нагревателя имеет
скользящий контакт со втулкой, которая вмонтирована в
медный токоподвод. Такая конструкция обеспечивает контакт
при термическом расширении нагревателя.
Нагреватель обычно окружают системой
графитовых, молибденовых и стальных экранов из нержавеющей
стали.
Для различных физико-химических опытов,
проводимых в" огнеупорных лодочках, применяются
горизонтальные трубчатые печи. В одной из таких печей,
рассчитанной на работу при 1500—1800°С, графитовая труба
с толщиной стенки 6,3 мм и нарезными головками
помещается между двумя латунными водоохлаждаемыми
зажимами. На головки печи навинчивают латунные
наконечники. После засыпки снаружи термоизоляции трубу
помещают в металлический корпус. Изоляцией служат
ламповая сажа, древесный уголь, молотый кокс.
Внутри нагревателя располагается корундовая труба,
которая проходит через уплотнения в латунных
наконечниках. Между корундовой трубой и нагревателем
пропускают азот или аргон для защиты нагревателя от
разрушения изнутри. В центре печи в зоне длиной 2,5 см
температура постоянная (±ГС).
В металлургических лабораториях до сих пор
распространена графитовая печь сопротивления Таммана. На
клеммах трансформатора (шинах) укреплен
цилиндрический корпус печи диаметром 300—400 мм и высотой 300—
350 мм. Нагревателем служит графитовая труба
диаметром 50—70 мм, закрепленная сверху и снизу медными
контактами. Пространство между контактами и водоох-
лаждаемым корпусом печи засыпают термоизоляцией.
Печь может работать в горизонтальном и вертикальном
10
положениях. Для улучшения электрического контакта на
криитол, засыпанный между трубой и корпусом, ставят
асбестовое кольцо, сверху набивают слой графитового
порошка, затем помещают стальное кольцо, через отверстие
в котором свободно проходит графитовая труба.
Для предохранения внутренней поверхности
графитовой трубы от окисления ее можно обмазать пастой из
корунда и огнеупорной глины. Для высоких температур
пасту можно изготовлять из плавленого магнезита с
добавкой жидкого стекла. Массу либо наносят слоями, либо
заливают в трубу и после некоторой выдержки выливают
из трубы. Затем трубу сушат в термостате и далее
непосредственно до 1500—1600°С в печи Таммана.
Недостатком графитовых нагревателей и графитовой
термоизоляции является необходимость исключения
контакта 'их с окисляющей средой. Кожухи <печей, в которых
засыпана изоляция, должны быть герметичными,
исключающими возможность проникновения воздуха.
Желательно, чтобы графитовые печи работали в вакууме
или в нейтральной атмосфере.
Вместо трубчатых применяют точеные, спиральные
графитовые нагреватели. При замене трубы спиралью
повышается электросопротивление, что позволяет
понизить силу тока. Графитовую спираль выпиливали из
графитовой трубки диаметром 32/34 мм. На рабочей длине
(100 мм) спираль имеет три витка. При экранировании
нагревателя молибденовыми экранами и кварцевой
трубкой в зависимости от силы тока достигают температуры
от 1400до2200°С.
В одной из печей спираль внутренним диаметром 60 мм
подвешена к верхнему зажиму и свободно входит в
нижний. Конусные части верхнего зажима и спирали создают
надежный контакт, а в нижний зажим с этой целью
засыпан порошок криптола или графита.
Кожухи печей выполняются из металла с водяным
охлаждением. Небольшие установки могут иметь кварцевые
корпуса.
Неотъемлемой частью печей сопротивления являются
экраны.
Увеличением числа экранов до 20-^25 можно
существенно повысить температуру в печи. Близкие к
нагревателю экраны делают из вольфрамовой, а остальные—из
молибденовой жести. Экраны могут быть выполнены в
виде набора цилиндров или в виде опирали из ленты, на
11
которой делаются насечки двумя параллельными
линиями. При свертывании ленты в спираль эти насечки
позволяют получить довольно заметный промежуток между
отдельными витками спирали, поэтому общая толщина
стенки из 25 экранов равна примерно 12 мм.
Отечественная промышленность выпускает
высокотемпературные течи сопротивления для плавки металла,
например печь СШВЛ-
1.2,5/25М04. Она
имеет установленную
мощность 63 кВт и может
обеспечивать нагрев до
2500°С в рабочем
пространстве диаметром
100 и высотой 250 мм.
На рис. 2 представлен
общий вид
электропечи 1 со щитом
управления 2 и вакуумной
системой 3.
Нагревательная
цилиндрическая
вертикальная камера
открытие. 2. Печь сопротивления СШВЛ-1.2.5/ ВаеТСЯ СВеРХУ> 0На ИМе"
/25М04 ет сплошное водяное
охлаждение.
Нагреватель трехфазный изготовлен из прутков вольфрама.
Теплоизоляция осуществляется вольфрамовыми и
молибденовыми экранами. Напряжение высокой стороны
трансформатора регулируется тиристорным регулятором.
Крышка камеры имеет два отверстия для гляделок,
в одно из 'которых можно установить шлюз с затвором и
вакуумным уплотнением для ввода в камеру
необходимых для экспериментатора устройств.
Горизонтальная печь сопротивления СШВЛ-1,31/
/20МО1 имеет установленную мощность 70 и мощность
нагревателя 54 кВт. Эта .печь обеспечивает нагрев садки
массой 5 кг до 2000°С. Размеры рабочего пространства
печи 300 X ЮО X Ю0 мм. Нагреватель печи сделан из
прутков вольфрама зигзагообразной формы. Печь имеет
боковую крышку, откидывающуюся на петлях в сторону.
Вспомогательные устройства могут быть смонтированы
на крышке.
2. ВЫСОКОЧАСТОТНЫЕ ИНДУКЦИОННЫЕ ПЕЧИ
Благодаря своим преимуществам эти печи получили
широкое распространение в металлургических
лабораториях. Источником питания печей служат высокочастотные
ламповые и машинные генераторы, выпускаемые
промышленностью для лабораторных установок различной
мощности.
В лабораторной практике индуктор приходится
рассчитывать редко. Чаще его подбирают к имеющемуся
генератору и нагреваемому металлическому объекту, т. е. к
тиглю с металлом. При конструировании индуктора
необходимо учитывать, что электромагнитная связь между
индуктором и образцом пропорциональна отношению их
диаметров: о?обр/Фвн.инд. Это обстоятельство создает
определенные трудности при конструировании .аппаратуры,
так как заставляет уменьшать толщину теплоизоляции
между металлом (жидким или твердым) и индуктором.
Для лучшего использования мощности необходимо,
чтобы глубина проникновения тока была незначительной.
Чем выше частота v, тем глубина проникновения £
меньше:
Материал v, Гц б, см
Медь жидкая / 2G00 0,5
I ЮООО 0,00
Вольфрам, молибден (2000°С) . . 2 000 3,0
Платина (1500°С), железо жидкое . ЮООО 0,5
Графит (2О00°С) /2 000 10
I ЮООО 1,5
Для нагрева графита, платины, вольфрама,
молибдена, железа пригодны частоты до 10000 Гц. Для
материалов с более высоким электросопротивлением требуются
и более высокие частоты. Хорошие проводники, вроде
меди, с трудом поддаются высокочастотному нагреву.
Для плавки таких материалов приходится прибегать либо
к пониженной частоте, либо к косвенному индукционному
нагреву, используя в качестве нагревателя графит в
форме трубы или тигля. Графитовый нагреватель может быть
заменен металлическим, например молибденовым.
Индукционные печи для нагрева и плавки могут быть
открытыми или закрытыми. В открытых печах в
индукторе помещают слой изоляции, внутри которой
располагается тигель-контейнер для исследуемого вещества.
Для нагрева непроводников, например шлаков, можно
применять тигли из железа, платины, графита. Индуктор
1
изготовляют из медной трубки, по которой циркулирует
вода. Чтобы разместить большее число витков индуктору
на необходимой высоте, трубку делают «профилированной,
прямоугольной, квадратной или эллипсовидной.
Закрытые индукционные печи работают в защитной
атмосфере и в вакууме. В этих печах индуктор может
быть вынесен за пределы камеры натрева или плавильной
камеры. В таком случае корпусом печи служит кварцевая
труба.
Верхняя часть кварцевого корпуса обычно делается
герметичной. В узкий патрубок впаивается
плоскопараллельное стекло для наблюдения и оптического измерения
температуры, магазины для сбрасывания добавок в
тигель и трубопровод, подсоединяющий печь к системе
откачки или подачи газа. В некоторых конструкциях
верхняя часть печи имеет съемную пришлифованную
металлическую или стеклянную толовку, в которой могут
располагаться необходимые устройства для введения добавок,
термопары погружения, стопоры и т. п. В таких печах
после плавки металл замораживают в тигле и после
разборки печи извлекают тигель вместе с металлом. Однако
может быть произведена и разливка металла через дно
тигля в стоящую ниже изложницу с помощью стопора,
который плотно пришлифован к отверстию в дне тигля.
Кварцевые печи легко изготовляются. Но при работе в
вакууме ниже 13,3 Па внутри кварцевого корпуса
появляется блуждающий электрический разряд вследствие
испарения металла и возникновения ионизированной
атмосферы в печи. Это нарушает электрический режим,
затрудняет измерение температуры, наблюдение и может привести
к пробою корпуса.
Более удобными для исследования являются печи с
металлическими корпусами. В этих печах индуктор
помещен внутри вакуумной камеры с водяным охлаждением.
На рис. 3 показана схема лабораторной вакуумной
индукционной печи емкостью 10 кг, в которой можно
продувать металл через пористую пробку в дне тигля, брать
пробы металла, измерять температуру и активность
кислорода в металле.
Выпускаемые лабораторные вакуумные индукционные
печи имеют емкость 4 кг, мощность 52 кВт (ИСВ-
0,004пиМ1) и соответственно 10 кг и 100 кВт (ИСВ-
0,01 пиМ2).
Индукционные печи применяют также для зонной очи-
14
стки металла. При этом возможно либо движение
керамического тигля с нагреваемым объектом внутри индуктора,
либо перемещение последнего вдоль тигля. В зонной печи
важно сконцентрировать энергию в узкой зоне.
Рассмотрим устройство печи для зонной очистки железа. Печь
имеет вертикальное раслоложение. Рафинируемый пруток
железа помещают вертикально, расплавленная зона
удерживается силами поверхностного натяжения.
£=Д
Рис. 3. Лабораторная вакуумная индукционная печь емкостью 10 кг:
/ — корпус печи; 2 — тигель; 3 — пористая пробка; 4 — водоохлаждаемый
ломик; 5 — приспособление для отбора проб и измерения температуры
металла; 6 — гляделка; 7 —ротаметр; 8, 9 — газоочистка; 10 — баллон с газом
Внутри индуктора располагается наружная
'керамическая трубка длиной 600 и внутренним диаметром 25 мм
и реакционная керамическая трубка длиной 300 и
диаметром 12 мм, в которой помещают пруток железа 300 X 10
мм. Двухслойный индуктор (по 14 витков в каждом слое)
может равномерно перемещаться со скоростью 6—0,26
см/ч.
На рис. 4 приведена схема установки для очистки
кремния методом плавающей зоны. Расплавленная зона
создается индуктором, перемещающимся вверх или вниз
15
вдоль кварцевой трубки, внутри которой установлен в
цанговых вольфрамовых зажимах кремниевый слиток.
Индуктор перемещается вдоль стержня с постоянной
скоростью, создаваемой электромеханическим приводом,
Рис. 4. Установка для зонной
плавки с концентратором
высокочастотного поля:
/ — установочный винт; 2 — ввод
охлаждающей воды; 3 — вывод
воды; 4 — расплавленная зона; 5 —
монтажная стойка; 6 — водоохлаж-
даемый индуктор; 7 — гибкий
шланг; 8 — вывод воды,
охлаждающей концентратор; 9 — вывод
охлаждающей воды; 10 — к
вакуумной системе; // — резиновая
втулка; 12 — подача охлаждающей воды
к латунному фланцу; 13 —
изоляция; 14 — водоохлаждаемый
высокочастотный концентратор; 15 —
образец; 16 — вольфрамовый зажим
для крепления образца; 17 —
стержень диаметром 6 мм; 18 —
кварцевый корпус
Рис. 5. Схема двухвиткового
индуктора типа «лодочка»
при этом в слитке образуется расплавленная зона. После
каждого прохода индуктора ток выключают и вручную
или механическим способом переводят индуктор в
первоначальное положение для следующего прохода.
Основным недостатком индукционных печей является
контакт расплавляемого металла с окисной огнеупорной
футеровкой. В случае плавки металла в водоохлажда-
емом тигле без футеровки этот недостаток ликвидируется.
Для расплавления металла тигель делают из нескольких
секций таким образом, чтобы предотвратить образование
замкнутых линий магнитного поля.
16
Существует также способ расплавления слитка,
вводимого в индуктор сверху. Металл расплавляется в
индукторе и -собирается в медном водоохлаждаемом тигле,,
стоящем внизу.
Для плавки титана в индукционной печи тигель
изготовляли из меди. Для снижения электрических потерь в
тигле стенки его должны быть тоньше «глубины
проникновения тока и частота тока должна быть низкой. Для
предотвращения появления замкнутых линий тока в
стенках тигля прорезали тонкие продольные щели (для
больших тиглей четыре). На индуктор из семи витков
подавали ток силой до 150 А, напряжением 900 В, частотой
2000 Гц. Внутренний диаметр тигля равен 73, толщина
стенок 3,2, высота 173 мм, мощность печи 100 ikB • А.
Наилучшим конструктивным решением индукционных
печей без футеровки является плавка металла во
взвешенном состоянии (ПВС). Для поддержания металла во
взвешенном состоянии индуктору придается особая
форма. Вес капли металла во взвешенном состоянии зависит
от мощности электромагнитного поля и капиллярной
составляющей, определяемой поверхностным натяжением
и плотностью металла. Для плавки используют
высокочастотные ламповые генераторы. Конфигурация
индукторов самая разнообразная. На рис. 5 приведена схема
двухвиткового индуктора типа «лодочка». На его дно,
образуемое одним из витков, помещают шарик или
кусочек из переплавляемого металла, причем шарик не
должен замыкать витков с разным потенциалом. При
увеличении мощности на индукторе шихта поднимается вверх
и повисает в поле. Мощность, подводимая ж
расплавленному металлу, уменьшается. При этом, несмотря яа го что
мощность, подводимая к индуктору, увеличивается в 10
раз, мощность, передаваемая расплавленному металлу,
снижается в 2 раза. Это объясняется перемещением
шихты в зону с другой конфигурацией поля и с
соответствующим уменьшением к. п. д. передачи энергии от индуктора
к металлу. Электромагнитное поле, действующее на
металл, частично уравновешивает металл и частично
уравновешивается само благодаря симметричному
расположению капли металла в индукторе.
Вес металла, висящего в электромагнитном поле,
определяется по формуле
17
где F — электромагнитная сила, уравновешивающая
образец; Ps — мощность, передаваемая металлу,
отнесенная к единице поверхности; S — поверхность; р —
удельное электросопротивление металла; / — частота тюля;
jute — магнитная проницаемость в вакууме.
При заданной частоте поля, определяемой
генератором и электрическим сопротивлением металла, масса
металла, удерживаемого в висячем положении, зависит
только от мощности.
Большое распространение получили и ,многовитковые
индукторы. Индукторы состоят из двух секций, навитых
в противоположном направлении, что позволяет
возбуждать неоднородное высокочастотное поле, напряженность
которого убывает таким образом, что на металл,
помещенный внутри индуктора, действует сила,
уравновешивающая его силу тяжести. Индуктор навивают таким
образом, чтобы два нижних его витка оказались
компланарными, т. е. находились в одной плоскости, и были
эквивалентны витку меньшего диаметра. Эти витки
стабилизируют положение жидкого образца и препятствуют его
вытеканию из катушки. Следующие три витка образуют
вместе с внутренним из двух компланарных конус с углом
при вершине 45°. Над ними располагаются два верхних
компланарных витка, намотанных в обратном
направлении. Диаметр обоих внутренних (верхнего и нижнего)
витков одинаков. Расположение обратных витков
повышает устойчивость расплава в горизонтальной плоскости
и предохраняет катушку от соприкосновения с образцом.
Силовые линии электромагнитного поля такой катушки
почти параллельны в нижней ее части и очень сильно
расходятся в промежутке между прямым и обратными
витками, вследствие чего градиент напряженности по
высоте катушки изменяется значительно.
Индуктор иной конструкции состоит из восьми нижних
витков — четырех 'компланарных и четырех аналогичных
им обратных витков. Такая катушка обеспечивает плавку
небольших образцов во взвешенном состоянии,
помещенных в кварцевую трубку, проходящую внутри катушки.
Катушка, таким образом, выносится за пределы
изолированной камеры, внутри которой можно создавать вакуум
или необходимую тазовую атмосферу.
Температура нагреваемого металла зависит от
электросопротивления и плотности образца. Сплавы с
высоким электросопротивлением, как и тяжелые металлы,
18
нагреваются сильнее. Для перевода их в подвешенное
состояние требуется большая мощность, поэтому и
нагреваются они сильнее, чем легкие металлы. Температура
образцов массой 10 г и более быстро превышает
температуру «плавления, а маленькие образцы выдерживаются
достаточно долго при невысокой температуре. При
снижении подводимой мощности образец опускается в
нижнюю часть индуктора, где напряженность поля выше, а
силовые линии расходятся в меньшей степени. При той же
уравновешивающей силе достигаются более высокие
температуры.
Склонность расплава к вытеканию из катушки
значительно увеличивается при уменьшении.отношения
поверхностного натяжения к плотности металла.
Изготовление индукторов установок ПВС. Для двух-
вишовых индукторов применяют профилированную
медную трубку. Лучше всего профилирование производить
волочением в нескольких последовательных ручьях.
Профилирование небольших трубок производится вручную
молотком. Перед профилированием в трубку заливают
свинец, после профилирования трубку нагревают и
свинец выливают. Для изгиба трубки ее отжигают, набивя-
ют песком и на шаблоне получают нужную
'конфигурацию.
Для многовитковых индукторов пользуются круглыми
трубками без профилирования диаметром 3—5 мм. Мно-
говитковые индукторы паяют серебряными припоями,
двухвитковые индукторы сваривают аргоно-дуговой
сваркой.
Индукционные плавки металла во взвешенном
состоянии осуществляют в установках двух типов: с индуктором
внутри и вне реакционной системы.
В первом случае используются закалочные ламповые
генераторы и двух- или многовитковые индукторы,
которые могут работать в вакууме или в атмосфере
нейтрального газа. Вторая группа установок обслуживается
генераторами без закалочного контура и имеет
многовитковые индукторы.
На рис. 6 показана схема установки для исследования
термодинамического равновесия между металлом и
шлаком. Корпус печи сделан из нержавеющей стали, сверху и
сниву он закрыт крышками из органического стекла,
присоединенными через резиновые уплотнения к корпусу.
Индуктор и стабилизирующее кольцо введены в печь че-
19
рез уплотнения так, что можно производить
вращательные и поступательные движения деталей индуктора. Поле
индуктора возбуждает в кольце вихревые токи,
вследствие чего он действует как обратный виток и
стабилизирует положение металла в индукторе. Под индуктором на
вращающемся поддоне
расположена изложница
для замораживания
капли металла со шлаком. В
индуктор помещают
подготовленный образец,
подогревают его, создают в
камере печи нужную
атмосферу или вакуум. При
дальнейшем увеличении
мощности образец
начинает «парить» в
индукторе, а затем полностью
расплавляется. В
зависимости от природы
металла, его массы,
конструкции индуктора и
подводимой мощности
длительность процесса
составляет несколько секунд или
минут. Так, например,
медь и цирконий «висят»
в индукторе по 5 мин,
алюминий 15 мин,
кобальт и ниобий после
расплавления сразу же
стекают в изложницу.
Диаметр заготовок
для плавки, как правило,
не превышает 10—12 мм,
а масса от 0,1—0,5 до 25—30 г. Благодаря интенсивному
перемешиванию жидкого металла можно выплавлять
металлы с различной температурой плавления, получать
слитки высокореакционных металлов, рафинировать
металлы от испаряющихся примесей. В таких установках
получали литые образцы галлия и индия, которые при
плавке в огнеупорных тиглях обычно загрязняются
материалом тигля. Выравнивание состава сплава в установке
ПВС происходит очень быстро.
Рис. 6. Схема печи для плавки
металла во взвешенном состоянии:
/ — кольцо; 2 — коаксиальный
подвод воды; 3 — корпус печи; 4 —
верхняя крышка; 5, 9 — вакуумные
уплотнения; 6 — гляделка;
7—стекло гляделки; 8— токоподводы; 10 —
кристаллизатор; //— индуктор; 12—
керамическая палочка; 13 —
изложница; 14 — платформа для
изложниц; 15 — нижняя крышка; 16 —
вакуумный штуцер; 17 —
оптический пиромет.р; 18 — зеркало
20
При плавке в ПВС происходит значительное
испарение летучих составляющих, поэтому при изготовлении
сплавов необходимо шихтовать заготовку, с учетом
испарения.
В конце плавки выключают ток, металл сливают в
изложницу или замораживают в индукторе. Скорости
кристаллизации достигают нескольких тысяч градусов в
секунду, 'что позволяет получать исключительно тонкие и
равномерные структуры. Можно производить достаточно
длинные плоские, цилиндрические образцы путем
последовательной отливки нескольких плавок, при этом металл
хорошо сваривается. ПВС с успехом применяют для
исследований равновесия металла со шлаком,
растворимости газов в металлах.
Установки ПВС могут быть использованы для
исследования свойств жидкого металла, например плотности,
поверхностного натяжения. От других типов печей
установки ПВС отличаются отсутствием 'контакта металла с
огнеупорной футеровкой, хорошим перемешиванием,
высокой скоростью наплавления образца. Дальнейшее
усовершенствование данного способа позволит увеличить
массу металла и удлинить выдержку металла в жидком
состоянии. Требуют совершенствования методы
регулирования температуры жидкой капли.
3. ДУГОВЫЕ ПЕЧИ
Использование дуги в качестве источника нагрева в
лабораторной практике имеет довольно ограниченное
применение. Нагрев камеры печи дугой, горящей между двух
электродов, трудно осуществим, так как нелегко
добиться равномерного распределения и регулирования
температуры. Для"выплавки слитков сталей, сплавов или
чистых металлов в основном применяют дуговые
однофазные вакуумные печи, а для исследования
восстановительных процессов, связанных с ферросплавным
производством, — дуговые однофазные.
Плавку в дуговых печах производят в медный водоох-
лаждаемый кристаллизатор. Печи работают либо в
вакууме, либо в атмосфере нейтрального газа. Различают
печи с расходуемым или с нерасходуемым электродом.
Печи с нерасходуемым электродом предназначены для
получения сплавов в виде небольших слитков для
исследований. В качестве нерасходуемого электрода
применяют штангу из вольфрама.
21
Расплавляемый металл подается под электрод илиг
располагается на поддоне в лунке «ли изложнице под
электродом. При включении дуги материал
переплавляется, образуется слиточек металла. На одном поддоне
можно выплавить несколько композиций сплавов без
перезарядки печи.
Особенное значение дуговые печи с нерасходуемым
электродом имеют для ванной плавки в водоохлажда-
емом тигле. Они называются гарниссажными
вакуумными дуговыми печами. Принципиальной особенностью
таких печей является медный во-
доохлаждаемый или
графитовый тигель, в котором
расплавляют и выдерживают в
жидком состоянии
переплавляемый металл. Благодаря
высокой теплопроводности
материала тигля на его стенках
образуется корка из непроплавлен-
ного металла — гарниссаж.
При плавке в печах такого
типа удается получать металл
однородного химического
состава, производить
необходимые добавки, переплавлять
различную шихту — скрап,
стружку, брикеты и т. п.
Разливку металла осуществляют
либо через дно (путем про-
плавления пробки,
закрывающей отверстие в дне печи),
либо при наклоне чаши.
Подобные печи часто используют
для отливки различных
изделий из жаропрочных сплавов.
Дуговые печи с
расходуемым электродом
предназначены для выплавки слитков. На рис. 7 показана схема
дуговой печи с расходуемым электродом. Печь состоит из
герметичной камеры 5 с прикрепленным к ней медным
водоохлаждаемым кристаллизатором — тиглем 6. В
камеру печи через уплотнение входит электрододержатель 2,
который соединяется с электродом. Электрод 4 круглой
или квадратной формы может быть литым, кованым, ка-
К о ткач ной
Рис. 7. Схема дуговой
вакуумной печи с расходуемым
электродом:
/ — механизм подачи
электрода; 2— электрододержатель; 3—
уплотнение; 4 — электрод; 5 —
вакуумная камера; 5
—кристаллизатор; 7 — подвод тока к
кристаллизатору
22
таным, сварным «ли прессованным. Камера печи связана
с откачной системой. Для плавки электрод опускают,
чтобы он коснулся днища кристаллизатора, на которое
кладут шайбу-затравку из того же материала, что и
переплавляемый электрод. Когда между концом электрода и
затравкой возникает дуга, электрод поднимают и
устанавливают требуемые силу тока и напряжение. Под
влиянием энергии дуги происходит расплавление металла,
который каплями стекает в кристаллизатор и образует
слиток. По мере расплавления электрода его опускают вниз.
Дуговые вакуумные печи, как правило, работают на
постоянном токе (минус — на электроде, плюс — на
кристаллизаторе),
4. ПЛАЗМЕННО-ДУГОВЫЕ ПЕЧИ
В низкоинтенсивной дуге на угольных электродах
температура может достигать 3600 К. Если
увеличивать силу тока дуги при постоянном сечении
анода, то плотность насыщающего тока будет достигаться
тогда, когда температура конца анода будет равна
температуре кипения его материала. В этой точке
характеристика дуги изменяется и температура ее скачком
повышается до 7000—8000 К, с анода вырывается поток
раскаленного пара вследствие высокой концентрации энергии в
анодном кратере.
Высокотемпературная плазма создается и при
использовании водяного пара или инертного газа, вдуваемого в
дугу. Плазменный поток с помощью магнитного поля
концентрируется в кольцевом электроде, создавая
возможность (получения высоких температур.
Газ инжектируется в корпус дуговой горелки.
Возникает интенсивный вихревой поток, который вдоль оси
электрода имеет небольшую область низких давлений. В
этой области происходит интенсивная ионизация.
Охлаждение внешней области дуги газом делает ее менее
проводящей, поэтому дута «сжимается» в узкий столб вдоль
оси электрода. Так как газ непрерывно поступает в
камеру плазменной горелки, горячая плазма выбрасывается из
сопла. Под воздействием магнитных сил плазма еще
более «сжимается», возникает столб раскаленной плазмы,
имеющей температуру до 30000 К, который можно
использовать для нагрева и плавления других материалов.
Для работы плазменной горелки предпочтительно
использовать нейтральный газ. При этом плазменная
23
струя не так агрессивно воздействует на нагреваемый
материал.
Плазменные нагреватели в зависимости от режима
работы разделяются на две группы. В нагревателях,
работающих в режиме плазменной струи, последняя
представляет собой поток газа, сильно нагретого в плазматроне.
Нагреватели второй группы работают в режиме
плазменной дуги, образующейся между нагреваемым изделием и
внутренним электродом плазматрона. Дуга обдувается
потоком газа в продольном направлении и сжимается< в
поперечном направлении стенками сопла 'или магнитным
полем.
На рис. 8 представлена схема дугового плазматрона.
Он имеет внутренний электрод в виде стержня и
расположенный соосно с ним внешний электрод, имеющий фор>му
сопла. При постоянном токе внутренний электрод служит
катодом, а наружный — анодом. Поток газа выдувает
дугу из отверстия сопла. Дуга горит в ограниченном объеме
сопла. Газ нагревается внутри канала сопла и с большой
скоростью вырывается из сопла в виде факела. Стенки
сопла отделены от плазмы тонким слоем холодного неио-
низированного газа, который служит также
электрической изоляцией. Существует тип плазматрона, в котором
для плавки металла сжатой дугой плазменная струя,
подведенная к нагреваемому изделию, позволяет возбудить
дугу между внутренним электродом плазматрона и
изделием. Дуга проходит через отверстие сопла, которое и
ограничивает ее диаметр. В продольном направлении дугу
обдувают потоком газа, защищающим сопло.
В металлургических целях плазменный напрев может
быть использован для переплава подготовленных
заготовок на слиток в медном водоохлаждаемогм
кристаллизаторе или для плавки металла в ванных печах с огнеупорным
тиглем.
На рис. 9 представлена схема плазменно-дуговой печи
с огнеупорным тиглем. Корпус печи делается
герметичным с плотно закрывающимся загрузочным окном и
задвижкой на сливном носке. Через свод печи с помощью
уплотнения вводится плаз-матрон, работающий на
постоянном токе. В футеровку подины печи заделан медный во-
доохлаждаемый подовый электрод — анод, находящийся
в контакте с расплавленным металлом. Катод из
молибдена, тантала, ванадия или ниобия с эмиссионными
добавками закреплен в медном, водоохлаждаемом электро-
24
додержателе. От брызг металла катод защищен медным
водоохлаждаемым соплом. Торец сопла покрыт слоем
жаростойкого изоляционного материала для
предотвращения появления «паразитной» дуги металл — сопло. Конец
катода скрыт в сопле на 3—6 мм — это стабилизирует ду-
Рис. 8. Схема плазматрона Рис. 9. Схема плазменно-дуговой
с независимой дугой: печи с керамическим .тиглем:
/ — источник электролита- 1 — плазматрон; 2 — уплотнение
ния; 2 — плазмообразующий свода; 3 — подовый электрод; 4—
газ; 3 — охлаждающая во- разливочное отверстие
да; 4 — катод; 5 — сопло;
6 — нагреваемый металл
гу и уменьшает эрозию катода. Защитный газ поступает
по кольцевому зазору между корпусом и электрододержа-
телем вдоль катода и дополнительно через осевое
отверстие катода в отверстие сопла. Скорость газового потока
не менее 3 м/с при силе тока 3—5 кА. Расход газа
составляет 1,4—2,0 г/с.
Плазмен'но-дуговые печи с керамическим тиглем с
успехом используются в лабораторной практике. Они
проще вакуумных печей, позволяют вести процессы в
инертной атмосфере, исследовать процессы взаимодействия
металла с различными газами, в частности с азотом,
водородом, окислительными газовыми смесями. Отсутствие
углеродистых электродов исключает загрязнение металла
углеродом. Можно достичь высоких и достаточно
надежно регулируемых температур. Эти печи весьма удобны
для исследования литейных процессов.
Плазменно-дуговой переплав. Схема печи с двумя или
более плазматронами представлена на рис. 10. Переплав-
25
8
^f3
>^/~
ляемая заготовка 7, плазматроны 6, медный водоохлаж-
даемый кристаллизатор 4, в котором наплавляется
слиток 5, размещаются в герметичной камере 5. Источник
переменного или постоянного тока / подключается к плаз-
матронам и слитку. Плазменные струи каждого плазма-
трона направлены на ванну
жидкого металла в
кристаллизаторе и на торец заготовки.
Механизм 8 вращает и подает
заготовку вниз. Входя в
соприкосновение с плазменными
струями, заготовка плавится и
металл по каплям стекает в
ванну.
По мере наплавления
слитка механизм 2 вытягивает его
из кристаллизатора. Процесс
настлавления и вытягивания
слитка происходит
согласованно и непрерывно.
Плазматроны размещаются
на камере радиально вокруг
слитка. Это позволяет
направлять плазменную струю в
любой участок ванны.
Использование нескольких плазматро-
нов дает возможность
рассредоточить тепловую нагрузку и регулировать обогрев
различных участков ванны. При этом можно переплавлять
металл, не подключая ток к заготовке. Если же
заготовку подключить к полюсу источника, то до 15—20%
анодного тока можно отвести через заготовку. Слиток
металла получается плотным, без усадочной рыхлости в
головной части, без усадочной раковины. Металл
характеризуется повышенной чистотой по неметаллическим
включениям, однородностью химического состава.
5. ЭЛЕКТРОННОЛУЧЕВЫЕ ПЕЧИ
Способ плавки электронным лучом обладает
рядом преимуществ. Можно использовать шихту
любого вида.^Благодаря достижению высокой температуры,
длительной выдержке металла при низком давлении
обеспечиваются отличные условия для рафинирования.
Принцип электроннолучевого нагрева состоит в том,
Рис. 10. Схема плазменно-
дуговой печи для переплава
с несколькими плазматрона-
ми
26 j
что благодаря термоэлектронной эмиссии с поверхности
накаленного катода происходит испускание электронов,
устремляющихся к аноду. Анод заземляют, а катод
изолируют. Между катодом и анодом прикладывают
разгоняющее напряжение порядка 10—30 кВ. Вокруг катода
устанавливают фокусирующий электрод-прожектор,
находящийся под небольшим отрицательным потенциалом.
Это обеспечивает нужное направление электронного луча.
Поток электронов бомбардирует поверхность
нагреваемой металлической заготовки. Кинетическая энергия
электронов превращается в тепловую. Металл
нагревается и плавится. Расплавленный металл стекает в медный
водоохлаждаемый кристаллизатор.
Электроннолучевая печь для плавки металла состоит
из одной или нескольких электронных пушек, плавильной
камеры, водоохлаждаемого медного кристаллизатора,
вакуумной откачной системы и источника питания.
Различают трл типа электроннолучевых установок: с
кольцевым катодом, с радиальными и аксиальными
электроннолучевыми пушками.
Рис. 11. Схема электроннолучевой печи с одним (а) и двумя (б) кольцевыми
катодами:
/—•переплавляемая штанга; 2 —кольцевой катод; 3 — второй кольцевой
катод; 4 — кристаллизатор; 5 — механизм вытягивания слитка; 6 — шлюз для
подачи штанги; 7 — плавильная камера; 8 — слиток; 9 — камера слитка; 10 —
трансформаторы накала катодов; // — источники высокого напряжения
На рис. 11 представлена схема электроннолучевой
печи с одним (а) и двумя (б) кольцевыми катодами.
Кольцевой катод 2У являясь излучателем электронов,
нагревается при (пропускании по нему переменного тока высокого
напряжения. Переплавляемая заготовка /, являющаяся
27
анодом, подключена к заземленному положительному
полюсу выпрямителя.
Преимущество печей этого типа состоит в простоте
конструкции и меньшем расходе электроэнергии, что
объясняется отсутствием отражения электронов пучка,
бомбардирующих металл, так как электрическое поле
полностью тормозит электроны, отражаемые от металла.
К недостаткам таких установок относится
непосредственное расположение катода поблизости от
расплавляемого металла. Пары и брызги металла оседают на
катоде и вызывают его разрушение. Кроме того, -между като-
до'м и электродом возникает электрический разряд
вследствие ионизации газового промежутка.
Электроннолучевые печи с радиальными пушками
отличаются от других конструкций тем, что между катодом
и расплавляемым металлом устанавливается
разгоняющий электрод. Тем самым зоны нагрева и плавления не
находятся в электрическом поле. Разновидностью этих
установок являются электроннолучевые пушки с плоским
лучом.
Большое распространение в лабораторной и
производственной практике получили установки с аксиальными
электронными пушками. Электронная пушка имеет катод,
который разогревается благодаря электронной
бомбардировке от вспомогательного катода. С помощью
фокусирующего электрода электронный пучок направляется в
анодную диафрагму. Между катодом и анодом
прилагается разгоняющее напряжение до 30 кВ. Электронный
пучок, пройдя анод по лучеводу, попадает в камеру печи на
поверхность нагреваемого объекта. Вокруг лучевода
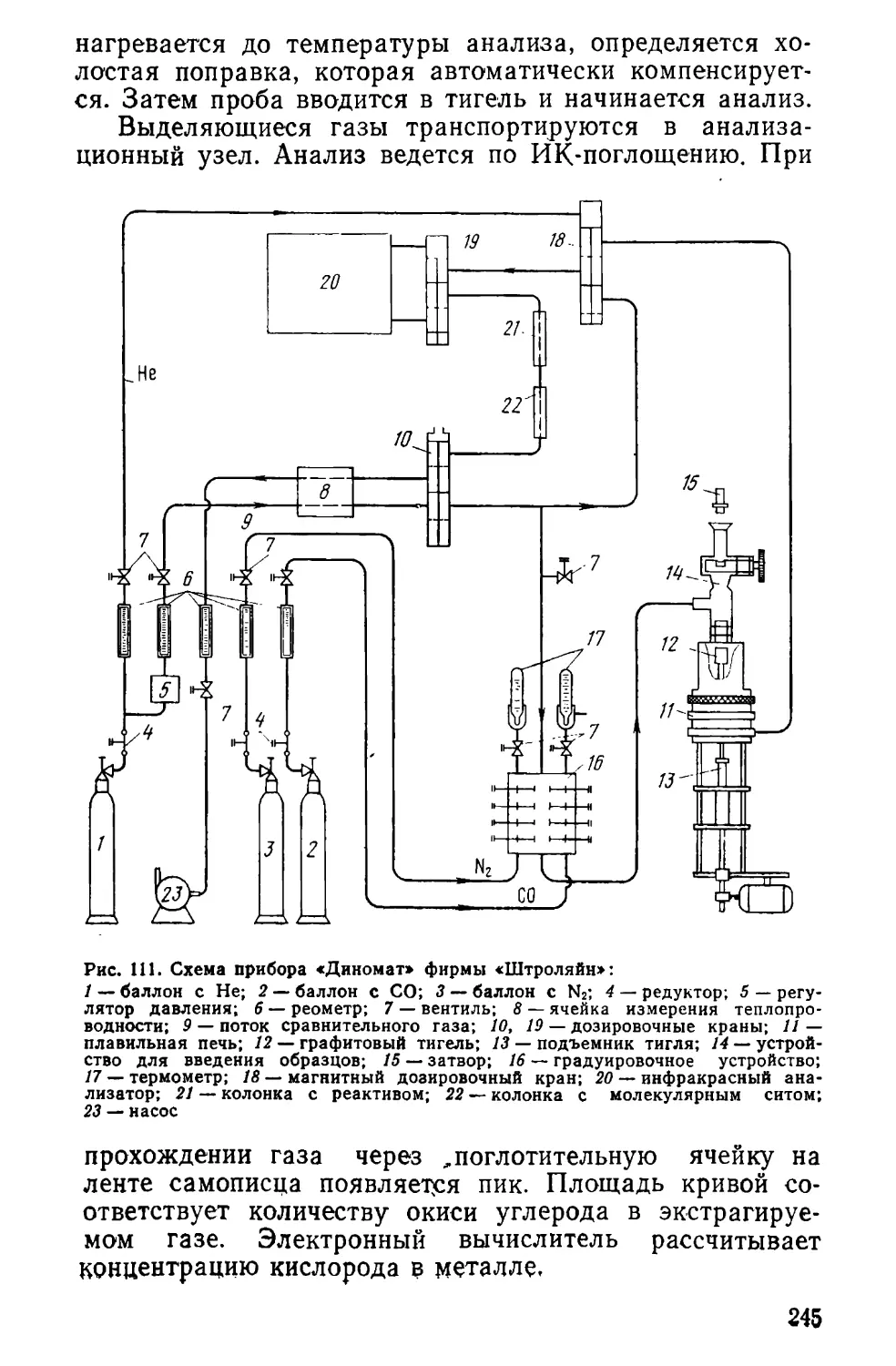
располагаются электромагнитные катушки отклонения и
развертки луча.
Одной из лучших конструкций электронных
.аксиальных^ пушек является пушка системы Арденна (ГДР). В
этой пушке (рис. 12) применена многокамерная
вакуумная откачка корпуса. Давление в зоне образования
электронного пучка не должно превышать 1,33 мПа, а
давление в плавильной камере печи из-за газовыделений
переплавляемого металла может быть выше указанной
величины. Поэтому в данной пушке имеются диафрагмы,
перегораживающие путь луча, и промежуточные
патрубки для вакуумной откачки. Это способствует устойчивой
работе печи при давлении в плавильном пространстве
133 мПа.
28
Фокусировка луча осуществляется линза-ми 6 и 7.
Непосредственно в плавильной камере располагается
электромагнитная катушка, развертывающая луч то
поверхности объекта. В зависимости от требований
технологии траектория луча может
меняться в широком
диапазоне.
Основным
преимуществом печей данного типа
является стабильная работа
электронных пушек, так как
они защищены от попадания
паров металла. Для
увеличения равномерности
нагрева используют установки,
имеющие несколько
электронных пушек.
Электроннолучевой нагрев применяют
для выплавки сложных
композиционных составов на
медном водоохлаждаемом
поду—луночная плавка.
Поворотный поддон имеет
несколько лунок, в которые
заранее помещают
переплавляемую шихту.
Для получения круглых
образцов в поддоне можно
выточить кольцевую
канавку для шихты.
Из отечественных
лабораторных установок ЭЛП-
1А/50 имеет мощность
50 кВт, ускоряющее
напряжение 30 кВ, анодный ток
1,7 А, диаметр
кристаллизатора 30—50 мм при длине
слитка 150 мм. Установка
ЭЛП-1А/125 имеет
мощность 125 кВт, анодный
ток 4 А, диаметр
кристаллизатора 60—100 мм при
длине слитка 300 мм.
Плавка
в электроннолу-
Рис. 12. Схема электронной пушки
системы Арденна от печи ЭМО-200:
/ — излучающая система; 2
—вспомогательный катод; 3 — основной
катод; 4 — фокусирующий
электрод; 5 — анод; 6, 7 — магнитные
линзы; 8 — электронный луч; 9 —
ванна металла; 10 — воздушное
охлаждение; И — водяное
охлаждение; 12 — система диафрагм; 13 —
к диффузионным насосам;
/4—промежуточная камера; 15 —
вакуумный затвор
29
чевых печах идет при низких давлениях и высокой
температуре, поэтому имеет место сильное испарение
металлической ванны. В результате смотровые окна
оказываются покрытыми слоем непрозрачного конденсата.
Наилучшими способами защиты стекол от напыления в
ЭЛП являются газовая завеса и вращающийся
обтюратор.
Способ газовой завесы состоит в том, что патрубок
смотрового устройства отделен от камеры печи
диафрагмой, достаточной для наблюдения, но создающей
значительный перепад давления атмосферы. Поэтому при
подаче в (пространство между стеклом и диафрагмой
нейтрального газа давление в этом объеме может быть
повышено настолько, что пары металла, попадающие в
него, не будут оседать на стекле.
Обтюраторное устройство состоит из двигателя,
вращающего диск, в котором имеется щель шириной
1 см. Другой стеклянный диск медленно вращается,
защищая непосредственно смотровое стекло от оседания
конденсата.
Для наблюдения за состоянием плавильной ванны
достаточно отверстия диаметром 5 мм. Непосредственно
к гляделке прилегает монокулярный телескоп. Скорость
вращения двигателя до 2500 об/мин.
Опыт работы показал, что если наблюдение через
обычную гляделку затруднено уже через 60 с
экспозиции, то с обтюратором стекло можно не менять (или не
чистить) ;в течение 150 ч работы.
Электроннолучевой нагрев с успехом применяется в
лабораторной практике для зонной очистки металла,
для выращивания монокристаллов.
ГЛАВА II
ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ
Ни одно современное исследование немыслимо без точного
измерения температуры опыта. Во многих случаях точность ее измерения
определяет погрешность всего исследования.
Методы измерения температуры можно разделить на прямые
(контактные, осуществляемые с помощью термометров, термоэлект-
ЗЮ
рических пирометров и термометров сопротивления1) и косвенные
(бесконтактные, оптические2) .
В СССР принята Международная практическая шкала
температур (МПТШ). Температуру, выраженную в МПТШ, сопровождают
знаком °С (градус Цельсия). Во многих физических и
физико-химических законах используют термодинамическую температуру,
численные значения которой, выраженные в абсолютной
термодинамической шкале, сопровождаются знаком К (градус Кельвина).
Температура таяния льда по абсолютной термодинамической шкале
равна 273,15 К. МПТШ является практическим осуществлением
термодинамической шкалы. МПТШ основана на шести реперных
температурных точках.
t равн- °с
Жидкий кислород —его пар — 182,97
Лед —вода, насыщенная воздухом 0в0О
Вода — ее пар (при кипении, р=1100 кПа) . . . 100,00
Жидкая сера—ее пар (при кипении, р=100кПа) 444t60
Жидкое серебро — твердое серебро ..... 960,80
Жидкое золото — твердое золото 1063,00
1. ТЕРМОЭЛЕКТРИЧЕСКИЕ ПИРОМЕТРЫ— ТЕРМОПАРЫ
При нагревании спая двух разнородных металлических проводников
появляется э. д. с.*, являющаяся суммой э. д. с. Лельтье,
возникающей в спае, и э. д. с. Томпсона, возникающей вследствие градиента
температур в каждой проволоке. Суммарная э. д. с. является
функцией температуры для данной пары металлов. Если один спай
термопары поддерживать при постоянной температуре tQ, то т. э. д. с.
термопары будет функцией температуры U, при которой находится
другой ее спай. Если отградуировать данную термопару, т. е.
найти зависимость ее т. э. д. с. от температуры одного из спаев при
сохранении постоянной температуры второго спая, то по измеряемой
затем величине т. э. д. с. можно находить значения температур.
Рабочий спай обычно называют горячим, а термостатируемый
спай — холодным. Для определения т. э. д. с. в цепь термопары
включают измерительный прибор, который с помощью медных
проводов соединяют со свободными концами термопары. Обычно
холодный спай поддерживают при температуре (fC в сосуде Дьюара
с водой и льдом. При отдаленном расположении холодного спая
используют компенсационные провода, которые экономят
термопарную проводку. В цепь термопары компенсационные провода
включают с соответствующим соблюдением полярности. Зависимость от
температуры для компенсационных проводов и термопары должна
1 Датчик измерительного инструмента помещается в
непосредственной близости к измеряемому и нагреваемому объекту.
2 В оптических методах измеряется либо интенсивность
монохроматического излучения, либо изменение общего количества
излучаемой энергии, либо изменение спектрального распределения излучения
в функции температуры. Оптические методы обладают тем
преимуществом, что нет необходимости делать вводы в реакционные
камеры, для измерения достаточна очень небольшая видимая площадь
поверхности нагреваемого тела.
М
быть одинаковой, как и сама температура в месте соединения
компенсационных проводов с термоэлектродами.
Если холодные спаи не термостатируются при 0°С, то нужно
знать их температуру во время опыта t0 и вводить соответствующую
поправку на температуру холодных опаев, которая будет равна
разности з. д. с. холодного спая при данной температуре и 0°С.
Для измерения малой разности температур применяют батарею
последовательно соединенных термопар (рис. 13). Одна группа
спаев приводится в контакт с объектом А, другая с объектам Б. При
этом измерения рекомендуется выполнять компенсационным
прибором. Приближенно точность измерения температуры батареей из п
термопар ib п раз выше, чем одной термопарой.
ити
Рис. 13. Схема термопарной
батареи
Рис. 14. Схема
дифференциальной термопары
Э. д. с. всех термопар суммируется. Применение термобатареи
позволяет снизить относительную погрешность отсчета т. э. д. с,
но не повышает точности измерения разности температур объектов,
так как термоэлектроды неоднородны, имеют разные
характеристики и градуировка термобатареи осуществляется с меньшей
точностью, чем градуировка отдельной термопары.
На рис. 14 приведена схема дифференциальной термопары для
измерения разности температур. Это двухспайная термопара.
Рабочие концы двух термопар направлены навстречу друг другу. Общий
электрод а соединен в двух спаях с электродом Ь, концы которого
выведены в зоны с температурами t, t\ и далее к измерительному
прибору. В интервале температур 16—20°С зависимость э. д. с.
линейная, Т. е. ЕаЬ (t, ti).= kab (t—ti).
Материалы для термопар
При выборе материала для термопар руководствуются следующими
требованиями: прямая зависимость между т. э. д. с. и температурой,
достаточно большая, устойчивая и воспроизводимая величина
т. э. д. с, материалы термопар должны быть коррозионностойкими,
механически прочными.
Термопары из благородных металлов
Платинородий-платиновая термопара (ПП) имеет положительный
электрод из сплаш 90% Pt и 10% Rh, а отрицательный из чистой
платины. Эти термопары наиболее изучены, их применяют при
эталонных работах до 1063°С и в качестве образцовых термопар для
проверки других термопар. Допустимые пределы использования ПП
32
термопар I разряда до ЛИХГС, II и III разряда — до 1300°С:
Длительное применение термопар возможно при 1300, а
кратковременное— до 1600°С. Выдержка при высокой температуре отрицательно
сказывается на свойствах термопары. В платиновом электроде
происходит рост зерна, т. э. д. с. снижается^ электрод охрупчивается.
При высоких температурах платина поглощает СО, СОг, >иары
металлов, окислы и карбиды. К техническим термопарам выпускаются
компенсационные провода: к платинородиевому электроду — медный
в оплетке красного цвета, к платиновому — провод из сплава 99,6%
Си и 0,4% Ni в зеленой оплетке.
Е,мВ
Е,мд
500 W00 1500 tf С
WOO 2000
t,*C
Рис. 15. Характеристики термопар группы:
а —платиновой (1 — ПП; 2 — ПР 13/1; 3 — ПР 30/6; 4 — ПР 100/20; .5 — ПР
30/13; 6 — ПР 40/20); б — вольфрам-рениевой {!' — ВР 5/20; Г — ВР 10/20)
Улучшенными свойствами обладают термопары, изготовленные
из оплавов платины с родием, которые можно объединить в ряд1:
ПР 13/1; 20/5; 30/6; 30/13; 40/20; 100/20. На рис. 15 приведены
характеристики термопар этой группы.
Наиболее распространенной является термопара ПР 30/6,
обладающая линейной характеристикой при температурах выше
1000°С. Ее чувствительность при измерениях около 1800°С
составляет 9>—'12 м!кВ/°С. При колебаниях температуры холодных (концов от
0 до 100°С погрешность не превышает 4°С, что дает возможность
отказаться от компенсационных проводов. Термопару можно
длительно использовать при температуре до 1600 и кратковременно
при нагреве до 1вОО°С.
Термопары ПП могут работать в окислительной среде и вакууме.
При измерениях температуры з-тими термопарами можно
пользоваться стандартными таблицами. Точность измерения составляет при
температуре до 1550°С ±2°С, а выше 1550°С гЬЗ°С.'
1 В числителе — содержание родия в сплаве с платиной в
положительном электроде, в знаменателе — то же, в отрицательном
электроде.
2 Зак. 664
33
Термопары из тугоплавких металлов
В вольфрам-молибденовой термопаре (ВМ) положительным
электродом является вольфрам. Особенностью термолары ВМ является
то, что в интервале температур О—1300°С ее э. д. с. отрицательная,
вблизи 1300°С она равна нулю, а выше 1300°С характеристика
термопары положительная. Термопару ВМ можно использовать в
вакууме, восстановительной среде. Чувствительность термопары
невелика (~7 мкВ/°С). Специальная термопарная проволока из вольфрама
и молибдена не выпускается, поэтому градуировочные
характеристики термопар ВМ, сделанных из проволок различных партий, /могут
значительно различаться. После первых же измерений при
повышенных температурах происходящие в вольфрамовом электроде
превращения изменяют характеристики спая. >В месте перехода
появляется участок термоэлектрической неоднородности. При измерениях
этот участок может явиться причиной образования дополнительной
э. д. с.
К лучшим высокотемпературным термопарам относится вольф-
рам-рениевая ВР 5/20, положительный электрод которой изготовлен
из сплава 95% W и 5% Re, а отрицательный—из сплава 80% W и
20% Re. Ее характеристика приведена на рис. 15,6. Применяется
также термопара ВР 10/20. До 2000°С термопары имеют плавное
изменение характеристики от 0 до 20—30 мВ. Достоинством этих
термопар является также их высокая механическая прочность до 1,47 Па
при удлинении 18—20%, широкий диапазон применения: в вакууме,
водороде, в присутствии угольной и керамической пыли, на воздухе.
Длительные измерения с их помощью можно проводить до 2300°С
в инертной атмосфере, а кратковременные — в окислительной. В
качестве компенсационных проводов для термопары ВР 5/10
попользуют медь и сплав меди с 2,215% Ni или железом а нганин, а
для термопары ВР 10/20 —медь и сплав меди с 1,25'% Ni или
железомедь.
Для уменьшения неоднородности и получения стабильности
показаний (рекомендуется подвергать проволоку предварительному
отжигу в водороде при 1'5(Ю—1600°С в течение 5—10 мин. Однако
отжиг не может полностью ликвидировать неоднородность проволоки
из разных партий, поэтому для каждой термопары приходится
строить индивидуальную характеристику. Погрешность показаний
электродов, сделанных из проволоки разных партий, достигает 5°С при
работе до 1500°С
Термопары из неметаллических материалов
Основными материалами для этих термопар служат керамические
или углеродистые материалы. Используются графит, карбид
кремния или бора. Одним из первых устройств является термопара Фит-
терера, в графитовом колпачке которой помещают стержень из
карбида кремния. Такая термопара обладает высоким значением э. д. с.
(до 500 imB при 1750°С), хорошей чувствительностью (30 мкВ/°С),
линейной характеристикой в области температур 100—2000°С и
хорошей воспроизводимостью.
(Конструктивное оформление термопар этого типа примерно
одинаково: внутренний электрод-стержень вставляется в наружный
электрод-чехол. Стержень соединяется с донышком чехла спеканием.
Свободные концы термоэлектродов выведены в водоохлаждаемый
34
корпус-головку. На задней стенке головки укреплена колодка с
клеммой для подсоединения к измерительным приборам.
Представляется перспективным использование следующих
термопар: карбид титана — графит, борид циркония — графит, борид
циркония — карбид циркония, дисилицид молибдена *— дисилицид
вольфрама. Термопара TMGB-340M (положительный электрод —
дисилицид молибдена, отрицательный — то же, вольфрама) применима
до 1650°С в восстановительной и окислительной атмосферах.
Термопара ТГБЦ-350М (положительный электрод — графит,
отрицательный— борид циркония) используется до 2000°С в инертной или
восстановительной атмосферах. Термопара ТГКТ-60М (графит
—карбид титана) применима до 2500°С. При температуре свыше 500°С
характеристика этой термопары почти линейна/я, температурная
чувствительность до 70 мкВ/°С; при 200СГС т. э. д. с. равна 125 imB.
Термопары из неметаллических материалов трудно приспосабливать
к опытным установкам, они обладают большой тепловой инерцией.
Градуировка термопар
Новые термопары, особенно те, характеристика которых зависит от
партии проволоки, должны быть отградуированы. Градуировка
осуществляется по постоянным релерным точкам, либо по
температурам кристаллизации чистых металлов, либо методом сличения с
помощью образцовых пирометров.
Градуировка по постоянным температурным
точкам
Этот метод основан на том, что при кристаллизации чистого
металла температура его от начала и до конца кристаллизации остается
постоянной. Рекомендуется пользоваться процессом
кристаллизации, а не плавления, так как в последнем случае трудно обеспечить
достаточно медленное изменение температуры металла.
Используется ряд вспомогательных точек МПТШ, а именно
температуры кристаллизации, °С: Си 1083, Ni 1453, Со 1492, Pt 1769,
Rh 1960, Ir 2443 и температура плавления вольфрама 3380°С.
Градуировку термопары осуществляют в печи сопротивления.
Навеску (металла плавят в графитовом тигле при глубине ванны не
менее 120 mim. Тигель устанавливают в зоне равномерного нагрева
печи. Термопару в защитном колпачке погружают в металл, не
доводя ее до дна тигля и избегая соприкосновения со стенками. Печь
с термопарой выдерживают 10—15 мин при температуре на 10—15°С
выше температуры кристаллизации металла. Затем температуру
понижают со скоростью 1—1,5°С/мин и отсчитывают э. д. с. термопары.
Строят график изменения э. д. с, отмечают площадку
кристаллизации, соответствующую табличной температуре. Тщательное
проведение такой градуировки обеспечивает среднюю квадратичную
ошибку не более ±0,3°С при температуре 1083°С.
Этот метод наиболее точный. Градуировка в индукционной печи
менее точна, но позволяет увеличить интервал температур от
300 до 180043. Тигель с навеской металла (200—300 г)
устанавливают в индукторе. Нагрев регулируют таким образом, чтобы
температура металла была несколько выше температуры затвердевания.
В этом методе рабочий участок термопары попадает в область
с большим градиентом температуры, в результате развиваются
«паразитные» э. д. с, которые и учитываются при градуировке. Уста-
2* Зак. 664
35
Новлено, что в. термопаре не возникает наводок от высокочастотного
поля, так как сдай экранирован слоем металла. Средняя
квадратична^ ошибка при градуировке термопар этим методом составляет
■±66С::ПРИ температуре 1770°С.
Мет о д : с л и ч.е н и я .. .„.
Этот метод применяют, для термопар II разряда и для технических
термопар.
Несколько градуируемых термопар вместе с образцовой
термопарой I разряда связывают в один пучок, помещая образцовую
термопару в центр. Рабочие концы обвязывают платиновой проволокой
для улучшения -контакта. Свободные «концы всех термопар термоста-
тируют при одной температуре, которую измеряют с точностью
±0,1°С,
Куст термопар помещают в печь сопротивления, нагретую до
температуры, близкой к постоянным точкам.
Печь термостатнруют, затем поочередно для каждой термопары
выполняют несколько циклов отсчета при одной температуре,
начиная и заканчивая каждый цикл с термопары I разряда. Затем
переходят на новую температуру. Т. э. д. с. измеряют с точностью до
0,001 мВ.
Высокотемпературные термопары .градуируют в вакуумной печи
сопротивления, в которую помещают молибденовый блок с тремя
отверстиями. В одно отверстие помещают образцовую термопару,
в другое — градуируемую. В третье отверстие фокусируют
оптический пирометр. Блок лодвешивают в печи в зоне максимального
нагрева. Платиновую образцовую термопару в печь помещают в
герметичном корундовом чехле (с учетом воздушной атмосферы),
градуируемую термопару вводят через вакуумное уплотнение и
нагревают ее в вакууме.
Измерение т. э. д. с.
Простейший метод измерения т. э. д. с. с помощью
.милливольтметра. При этом сопротивление линии, термопары и контактов влияет
на ток в цепи и отражается на ол*ределяемых величинах.
Измеряемая т. э. д. с. так относится к истинной т. э. д. с, как
сопротивление прибора относится к сопротивлению линии, термопары и
прибора: £'пр/£ист=#пр/(/?л+#т+#пр). Необходимо пользоваться
прибором -с большим внутренним сопротивлением.
Метод потенциометрического измерения исключает влияние
сопротивления цепи и дает точные показания. Шкала прибора может
быть использована для отсчета температуры. Точность регистрации
температуры 0,1—0,5%.
При определении ошибок измерения температуры необходимо
точное знание их источников. Первую группу составляют ошибки,
связанные с изменением состава термоэлектродов,
рекристаллизацией, появлением химической неоднородности в них под влиянием
нагрева и поглощения примесей. Во вторую группу входят ошибки
при измерениях т. э. д. с. и в третью группу — ошибки при
определении истинной температуры в связи с расположением термопары
относительно измеряемого объекта, градиента температур в спае
и т. п.
36
Относительные ошибки измерения термопары суммируют -с
относительной ошибкой -прибора, которым измеряют т. э. д. с. Например,
если термопара имеет относительную ошибку ±0,65%, а прибор
относится iK I классу, то суммарная ошибка равна ±1,65% от
верхнего предела измерения пирометра.
2. ОПТИЧЕСКИЕ МЕТОДЫ ИЗМЕРЕНИЯ ТЕМПЕРАТУР
Принципы оптической пирометрии
Оптичеокие -методы основаны на измерении излучательной
способности нагретого тела, соответствующей температуре тела. Если тело
при любой температуре полностью поглощает все падающее на него
электромагнитное излучение независимо от длины волны, то оно
является абсолютно черным телом (АЧТ). Коэффициент поглощения
АЧТ при любой температуре равен единице, а коэффициент
поглощения других тел меньше единицы.
Полная энергетическая яркость АЧТ определяется по закону
Стефана—Больцмана, Bt/im2:
где .а — постоянная Стефана—'Больцмана,
о = 5,6696-10~8 Вт/(м*К4).
Для каждой температуры существует своя зависимость
интенсивности излучения от длины волны, обычно имеющая вид кривой с
максимумом. Для области инфракрасного излучения при (малых
значениях произведения XT применим закон Вина. С помощью
этого закона можно приближенно представить ту часть кривой
излучательной способности тела, которая соответствует малым длинам
волн, Bt/im2:
!k = C1X-5e-c*'kT,
где d=2n/ic2=3,7413.10-16 Вт-м2; С2=пф= 1,438-10"2 м-К;
h—постоянная Планка; X — длина волны излучения; с — скорость
света в вакууме; k — постоянная Больцмана.
Этой формулой можно пользоваться до 4000 К для длин волн
до 0,6 мкм.
Оптические приборы для измерения температуры фиксируют не
истинную температуру тела, а псевдотемпературу, которая тем
больше отличается от истинной температуры, чем значительнее
различие характеров излучения исследуемого тела и АЧТ. В этом
заключается принципиальный недостаток бесконтактных методов
измерения температуры. Остановимся на некоторых основных
понятиях оптической пирометрии.
Яipкостная температура
Яркостная температура тела Тя равна такой температуре АЧТ, при
которой спектральная плотность его энергетической яркости для
определенной длины волны Я0 равна спектральной плотности
энергетической яркости (для Я=Хо) рассматриваемого тела. .По формуле
37
Вина—-Плавка можно определить реальную истинную температуру
тела:
J___J ^ _J
Тя ~~ Т " С2 П Ч. т *
где е т— коэффициент черноты излучения тела. Истинная темпера-
тура всегда больше яркостной температуры Тя, так как значения
е лежат в пределах от 0 до 1.
л, т
Если тело находится в условиях АЧТ, то измеряется его
истинная температура. Во всех остальных случаях определяют яркост-
ную, или кажущуюся температуру. Весьма близко к условиям АЧТ
находится жидкий металл в тигле индукционной печи или в печи
сопротивления. Если глубина цилиндра в б раз больше его
диаметра, то цилиндр является АЧТ даже в случае, когда стенки тигля
гладкие изнутри и состоят из вещества с низкой
лучеиспускательной способностью. Если стенки тигля шероховатые, а материал его
имеет лучеиспускательную 'способность, близкую к единице, то
глубина тигля может быть только в 2 раза больше его
диаметра..Если стенки 'цилиндра нагреты до той же температуры, что и объект,
то такая система будет весьма близка к АЧТ. Если же стенки
нагреты до более высокой температуры, чем тело, то оно отражает в
объектив пирометра излучение и от стенок, т. е. будет казаться
более горячим.
Цветовая температура
Цветовая температура Тц — это такая температура АЧТ, при
которой отношение его излучательной способности для двух
определенных значений длины волны \К{ и Я2 равно отношению тех же
величин для исследуемого тела.
Если Е ^ ги Е^ т—монохром атичеокие изл уча тельные
способности тела при его истинной температуре Т для длин волн %i и Х2,
то цветовой температурой Тц будет такая температура АЧТ, при
которой соблюдается равенство: Е^ т*/Еу т =Е^ т № \ т
При цветовой температуре цвет черного и нечерного тел
одинаков.
Взаимосвязь истинной и цветовой температур нечерного тела в
зависимости от величины отношения его монохроматических
коэффициентов черноты излучения ei и Ег Для двух длин волн К\ и 1г
выражается уравнением
_L_ J lnei/e2
Т Т*~ cJ— —i-) '
Для серых тел, у которых в данном участке опектра
коэффициент черноты излучения не меняется с длиной волны, цветовая
температура равна истинной: ТЦ = Т. Серые тела излучают постоянное
количество энергии для всех длин волн.
При измерении высоких температур пользуются ослабляющими
светофильтрами, которые пропускают определенную часть светового
потока без изменения длины волны. Так как, кроме ослабляющих
светофильтров, перед объективом пирометра могут находиться стек-
38
л а гляделок и иные прозрачные преграды, то необходимо строить
градуиров очную кривую для условий измерения температуры в
данном опыте с помощью термопары или по точкам плавления
чистых металлов. Большое значение имеет и лучеиспускательная
способность тела.
В печи сопротивления или в индукционной печи даже при низкой
эмиссионной способности объекта общее излучение,
представляющее собой сумму излучения от тигля и стенок печи, будет
приближаться к излучению АЧТ, что дает возможность измерять
истинную температуру тела.
Для многих металлов с убывающим по мере роста длины волны
значением коэффициента черноты излучения In (81/62) >0 цветовая
температура выше истинной Гц>7\ Для неметаллических веществ,
у которых по мере роста длины волны коэффициент черноты
излучения возрастает, цветовая температура ниже истинной.
Цветовые температуры тел можно связать с яркостными
температурами, измеренными для длин волн Х{ и Я2, по формуле
т (lAQ-OAa)
ц (1А1^я1)-(1/^гя2) *
(Радиационная температура — это температура АЧТ, при которой
полные энергетические яркости черного и нечерного тел (отнесенные
ко всему диапазону длин волн спектра теплового излучения) равны
между собой. Радиационная температура определяется с помощью
закона Стефана—Больцмана: ТР = 7,ЛЛ"^Г.
3. ОСНОВНЫЕ ТИПЫ ОПТИЧЕСКИХ ПИРОМЕТРОВ
Пирометры с исчезающей нитью
Оптический пирометр с исчезающей нитью измеряет энергию
монохроматического излучения тела, т. е. яркостную температуру при
определенной фиксированной длине волны 65 мкм, которая выделяется
из (Спектра излучения с помощью красного фильтра.
(Измерение температуры пирометрами с исчезающей нитью
производится путем сравнения яркости исследуемого тела и нити
фотометрической лампы, проградуированной по АЧТ при длине волны
65 мкм. С помощью оптической системы изображение нагретого
тела проектируется на плоскость нити лампы накаливания. Реостатом
сила тока накала нити регулируется таким образом, чтобы яркость
лампы сравнялась с яркостью измеряемого тела. Температура
определяется по силе тока накала нити в момент ее «исчезновения» на
фоне ,раскаленного тела. 'Принципиальная схема пирометра
показана на рис. 16.
Нить накала лампы питается от аккумулятора. Сила тока
накала отмечается на шкале стрелочного прибора. Для визирования и
фокусирования нити лампы и объекта служит оптическая система.
Имеются устройства для введения красного и ослабляющего
фильтров. Кажущаяся температура на шкале прибора с помощью граду-
ировочной кривой переводится в истинную температуру.
Для лабораторных измерений температуры применяют
стационарные оптические пирометры типа ЭОП и ОП, в которых
цилиндрическая нить лампы со стороны наблюдателя шлифованием
утончена до половины своего диаметра, что способствует улучшению ее
«исчезновения».
39
Для градуировки образцовых пирометров, по которым
проверяют технические пирометры, служат эталонные пирометры типа ЭОП.
Образцовые пирометры позволяют измерять температуру с точностью.
0,2—0,5% в пределах от 800 до 3000°С, эталонные пирометры имеют
точность измерения 0,05% при 1000°С.
Рис. 16. Схема оптического пирометра с исчезающей нитью:
/ — линза объектива; 2 — тубус объектива; 3 — поглощающие стекла; 4, 5 —
сопротивления; 6 — движок реостата; 7 — части показывающего прибора; Я —
тубус окуляра; 9 — красный светофильтр; 10— постоянный магнит
показывающего прибора; // — кольцевой реостат; /2 —батарея аккумуляторов; 13 —
шунтирующее сопротивление; 14 — зажимы для измерения силы тока
пирометрической лампы; 15 — пирометрическая лампа; 16 — накаленное тело
Приближенная калибровка оптических пирометров
осуществляется по точкам плавления чистых металлов; фиксируют силу тока
лампы в момент начала затвердевания. Используя закон .Вина,
можно обойтись одной реперной точкой, но для более тачной
«градуировки рекомендуется использовать несколько точек.
При (градуировке пирометров экстраполяцией температуры от
температур реперных точек возникают в среднем следующие ошиб-
■ки, °С: 1500±3; 1700±3,5; 2000±4,6. Однако ошибки измерений
значительно выше. Так, для пирометров типа ОП при работе в
пределах 1200—2000°С основная ошибка составляет ±13°С и до
±40°С при намерениях температур в пределах 1800—3200°С. В
технических пирометрах основная погрешность определений для
приведенных интервалов температур соответственно составляет ±20 и
±50°С.
Фотоэлектрические пирометры
Фотоэлектрический пирометр измеряет яркостную температуру тела
с помощью фотоэлемента. Принципиальная схема хода лучей в
фотоэлектрическом пирометре представлена на рис. 17.
40
Объектив / создает в плоскости диафрагмы 2 -перед
фотоэлементом 3 изображение объекта Л, Угол ф, ограниченный размером
отверстия диафрагмы 2, определяет ту часть светового потока,
которая создает освещенность катода фотоэлемента. Если размеры
объекта таковы, что он перекрывает основание конуса лучей, то все
отверстие диафрагмы оказывается -полностью перекрытым
изображением объекта аа. Тогда освещенность катода фотоэлемента
пропорциональна яркости изображения аа, т. е. яркости объекта Л.
Фотоэлектрические пирометры разделяют на две группы. К первой
относят приборы, в которых на фотоэлемент попадают лучи от
измеряемого источника и от источника сравнения. В этом случае
фотоэлемент работает в нулевом режиме. К таким приборам относятся
приборы типа ФЭЛ-3 (рис. 18) и ФЭП-4.
Рис. 17. Схема хода лучей в фотоэлектрическом пирометре
Рис. 18. Принципиальная схема пирометра ФЭП-3
С помощью объектива 2 (рис. \8) создается изображение
источника излучения ; в плоскости отверстия диафрагмы 4,
расположенной перед фотоэлементом 5. Через отверстие 7 на катод
фотоэлемента направлен овет, исходящий от вспомогательного источника
света 6. С помощью специальной заслонки отверстия 4 и 7
поочередно перекрываются. При неравенстве освещенностей в дели
фотоэлемента возникает переменная составляющая фототока которая
увеличивается усилителем 8, выпрямляется и подается на сетку
выходного каскада усилителя 9, в анодную деть которого включена
лампочка о.
Сила тока накала лампочки меняется до тех пор, пока на
катоде фотоэлемента не уравняются освещенности от визируемого
объекта и лампочки и переменная составляющая фототока не обратит-
41
ся в нуль. Тогда сила тока накала лампочки будет соответствовать
яркостной температуре объекта. В цепь лампы включено постоянное
сопротивление, падение напряжения на котором измеряется
электронным потенциометром. Скорость измерения равна 1 с, ошибка
определения составляет 1% от верхнего предела измерения 2000°С.
Фотоэлектрические пирометры позволяют производить непрерывную
запись температуры.
Радиационные пирометры
Эти пирометры измеряют радиационную температуру по
результатам измерения теплового излучения во всем спектре длин волн.
Радиационный пирометр состоит из двух блоков: телескопа, в который
входит оптическая система и приемник излучения, и
показывающего или регистрирующего измерительного прибора —
милливольтметра или автоматического потенциометра. Приемником излучения
служит тонкая металлическая пластина, покрытая сажей,
преобразующая лучистую энергию в тепловую. Температура пластины
измеряется термобатареей. Оптическая система пирометра фокусирует
поток лучистой энергии на теплоприемник.
На рис. 19 представлена схема пирометра с телескопом ТЭРА-
50. Для измерения т. э. д. с. используются электронные
потенциометры. Пирометр имеет неподвижный объектив, настроенный на
фокусировку объекта, расположенного на расстоянии 1О00 мм от
входной линзы. Прибор снабжен диафрагмой, которая, «подрезая» пучок
света, позволяет производить измерения в различных
температурных диапазонах. Для компенсации влияния температуры
окружающей среды термобатарею шунтируют компенсационным
сопротивлением.
Основными источниками ошибок при градуировке и
использовании радиационных пирометров являются иаменение количества
энергии, попадающей в прибор, и несоблюдение условий излучения
АЧТ. Ошибка измерения пирометра ТЭРА-50 в диапазоне
температур 1200-^2600°С составляет zb(20-f-30°C).
Рис. 19. Устройство пирометра с телескопом ТЭРА-50:
/ — линза; 2 — установочный фланец; 3 —- сменная втулка; 4 — термобатарея;
5 — компенсационная катушка; 6 — камера термобатареи; 7 — крышка; 8 —
отверстие для наблюдения; 9 — ввод проводов
42
Цветовые пирометры
В отечественных цветовых пирометрах использован метод красно-
синего отношения. Для измерения обоих монохроматических
яркостей используют один приемник излучения (фотоэлемент или
фотосопротивление) с общим каналам усиления измеряемых сигналов.
Преимущество метода цветовой пирометрии перед другими
бесконтактными оптическими способами измерения температуры
состоит в том, что в качестве объекта измерения не обязательно иметь
АЧТ. Кроме того, исключается влияние излучений, изменения
рельефов поверхности, расстояния от пирометра, неселективных
поглотителей лучистой энергии, расположенных между объектом измерения
и пирометром (сеток, стекол, диафрагм, призм и т. п.).
Типичными образцами цветовых пирометров являются приборы
ЦЭП-ЗМ (рис. 20) и ИЭП-4. Комплект прибора состоит из трех
блоков: датчика, блока электроники, включающего усилительную и
решающую схемы, показывающего или регистрирующего прибора.
Рис. 20. Принципиальная схема измерения температуры цветовым
пирометром:
/ — оптическая схема; 2 — диск со светофильтрами; 3 — фотоэлемент; 4 —
блок измерения; 5 — самописец
Принцип действия прибора основан на автоматическом
измерении логарифма отношения спектральных яркостей в красном и
синем участке спектра. Вычислительное устройство автоматически
осуществляет логарифмирование отношения яркостей. Логарифм
спектрального отношения яркостей пропорционален обратным
значениям цветовой температуры.
Измеряемое излучение попадает на фотоэлемент через
оптическую систему прибора и через обтюратор, вращаемый синхронным
двигателем. Обтюратор выполнен в виде диска с отверстиями,
закрытыми красными и синими светофильтрами таким образом, что при
вращении диска на фотоэлемент попеременно попадает то красная,
то оиняя энергетическая яркость. Импульсы фототока,
пропорциональные красной и синей спектральным энергетическим яркостям,
усиливаются и подаются на вход измерительной системы.
Фотоэлемент термостатирован. Все эти устройства вмонтированы в головке
прибора. Усиленный ток подается в измерительный блок, в
котором после соответствующих преобразований сигнал поступает в
электронную логарифмирующую систему, позволяющую получать
линейную шкалу.
В головке датчика находятся также устройства для ручной и
автоматической регулировки уровня энергетической яркости,
индикаторы и органы управления. Для удаления пыли и дыма из поля
зрения при измерении температуры открытых объектов в бленду,
43
надеваемую на тубус объектива, подается сжатый воздух.
Диапазон измерений температуры составляет 1400—2800°С. Прибор
имеет от 3 до 5 поддиапазонов с интервалом 200—400°С. Показания
прибора переводятся в градусы Цельсия с помощью градуировоч-
ного -графика для данного поддиапазона. Градуировку прибора
проводят по образцовым температурным лампам. Предельная ошибка
измерения цветовой температуры 2000°С равна ±30°С.
Метод дихроматической цветовой пирометрии для измерения
и регулирования температуры заключается в том, что на выходе
приемника излучения получают два сигнала, пропорциональные
спектральным энергетическим яркостям LQl и Ьъ2 со значениями
длин волн %i и Х2- Для нахождения требуемого значения
температуры имеется редуцирующее устройство, которым сигнал Ui}
пропорциональный одной из спектральных энергетических яркостей,
например £эь может быть уменьшен в п раз до величины сигнала
U2i пропорционального Ьъ2. При значении регулируемой температуры
объекта Т, равной установленной температуре 7уст, nUl=n(J2 и
ra=iy£/1 = const ZW^ai-
В качестве импульса для регулирования в данном методе
используют 'результирующий сигнал Uv, определяемый разностью
сигналов 1)\ и U2, а именно: £/р=л£/1—U2. При Т=Туст, (/Р = 0 и
температура, определяемая отношением п, является цветовой
температурой Гц. Когда температура объекта выше заданной температуры
регулирования (Г>7,Уст), /7Р>0.
В методе <бихроматичеокой цветовой пирометрии сигнал для
регулирования определяется разностью двух спектральных
энергетических яркостей. При достижении регулируемой температуры Т
установленного значения 7уСт величина результирующего сигнала
равна 0. При этом равенство nU\ = U2 и температура определяются
отношением спектральных энергетических яркостей.
Данный метод регулирования цветовой температуры исключает
необходимость применения какой-либо схемы или логометра,
измеряющего отношение яркостей. На этом принципе работает пирометр
РЭД-1, имеющий один фотоэлемент и разделяющий сигналы,
пропорциональные соответствующим спектральным энергетическим
яркостям во времени, с помощью вращающегося диска со
светофильтрами. В качестве редуцирующего элемента применен* цветовой клин,
принцип действия которого следующий. Пропускание клином двух
спектральных длин волн Х\ и >* зависит от его толщины. При
перемещении клина пропускание в длинноволновой красной области
спектра изменяется более -чем на 100%, в то время как для
коротковолновой синей области оно меньше 10%.
ГЛАВА III
КОНТРОЛИРУЕМЫЕ АТМОСФЕРЫ
В различных физико-химических исследованиях, при изучении
свойств жидких металлов и шлаков большое значение имеют
атмосферы, используемые в экспериментальных установках. Применение
тех или иных газов зависит от цели исследования, необходимой
среды, например защитной безокислительной (Аг, Не, N2),
окислительной (02, Н20, С02), восстановительной (Н2, СН4, СО), для иссле-
44
дования растворимости газов и определения различных
физико-химических величин.
В лабораторной практике газы используют как - в чистом виде,
так. и в виде различных смесей определенного состава. К наиболее
распространенным относятся смеси Н2—Н20—Аг (для исследования,
процессов восстановления руд, раскисления металла), СО — С02,
СН4—Н2, H2S—H2 (для, установления величин, связанных с
растворимостью углерода, серы в металлах.и шлаках).
1. СПОСОБЫ ПОЛУЧЕНИЯ ЧИСТЫХ ГАЗОВ
В настоящее время почти каждая металлургическая
исследовательская лаборатория снабжается баллонами готового элементарного и
сложного (СО2, CH4, NH3, CO, S02, H2S, ССЦ) газа. Иногда
некоторые газы приходится получать- в лаборатории.
Хлор получают при нагреве концентрированной соляной кислоты
с двуокисью марганца или на холоду перманганатом калия.
Выделяющийся хлор содержит примеси кислорода и хлористого
водорода. Для очистки от хлористого водорода его пропускают через
воду, а для высушивания через серную кислоту и поглотителън'ые
колонки с Р205 и СаО. Образующийся газ конденсируют при —78°С
смесью твердой двуокиси углерода и ацетона или бензина, с
жидким азотом. Для очистки от кислорода хлор многократно
перегоняют и откачивают несконденсировавшиеся газы. ■-. . ,
Электролитически хлор получают в электролизере из
концентрированного раствора соляной кислоты или раствора поваренной
соли, насыщенного хлористым водородом.
Сероводород. Наиболее просто H2S получают в аппарате Кип-
па разложением сульфидов натрия.или железа 20%-ной соляной
кислотой. Образующийся газ промывают 10—20%-ной соляной
кислотой, водой и растворами гидросульфата калия. Высушивание
производят с помощью СаС12 и P2Os.
Высокая степень очистки газа достигается фракционной
дистилляцией в вакууме или пропусканием паров серы и водорода через
печь, нагретую до 600°С и наполненную пористой керамикой.
Сернистый газ получают при нагреве концентрированной серной
кислоты и медных стружек. Для поглощения примеси серного
ангидрида и высушивания газ пропускают через серную кислбту и
пятиокись фосфора. Полученный сернистый газ сжижают при тем-,
пературе —70°С. Для высокой очистки газ дистиллируют.
Аммиак получают при нагревании смеси хлорида или сульфата
аммония либо с окисью кальция, количество которой должно быть;
вдвое, больше стехиометрического количества, либо с 50%-ным
раствором КОН или iNaOH. Для удаления влаги аммиак пропускают
через конденсационные сосуды, помещенные в бане, при 0°С. Далее
аммиак пропускают над едким натром и направляют в конденсатор
при —80°С. Для дальнейшей очистки производят 'фракционную
дистилляцию аммиака с откачкой неаконденсировавшихся газов'й
с отбором наиболее чистой средней его фракции.
Окись углерода чистотой до 99,'9% получают при действии
серной или фосфорной кислоты на муравьиную кислоту ripk нагреве.
При использовании фосфорной кислоты окись углерода 'более чис-:
тая. Особенное внимание при получении окиси углерода должно'
быть уделено технике безопасности, так как газ очень ядовит и
взрывоопасен. Окись углерода очищают с помощью
амальгамированного цинка, сульфата ванадия и воды. При прохождении над на-:
45
гретой медью окись углерода очищается от кислорода; сушку газа
производят пятиокисью фосфора. ■
Окись углерода можно получать при нагреве щавелевой кислоты
в присутствии концентрированной серной кислоты. При этом
выделяющаяся одновременно двуокись углерода поглощается раствором
едкого кали.
Двуокись углерода получают при взаимодействии бикарбоната
калия с серной кислотой либо нагреве бикарбоната натрия до 110—
1'20°С в стеклянной колбе. Отводную трубку для конденсации влаги
охлаждают льдом, а последующую осушку производят хлористым
кальцием и пятиокисью фосфора.
Метан можно получить нагревом смеси СО и Н2 (1:3) при
290—300°С в присутствии никелевого катализатора. Последний
готовят, расплавляя нитрат никеля и пропитывая им кусочки
обожженной глины, которую затем прокаливают при 550—600°С. Глину
помещают в реакционную трубку, и в атмосфере проточного
водорода при 280°С в течение 12 -ч реагент восстанавливают до
"металлического никеля.
Очищают метан с помощью СаС12, КОН, активированной окиси
меди. Метан можно получать также, воздействуя металлическим
магнием на метилиодид или метилбромид с последующим
разложением образующихся соединений бенз иловым спиртам.
2. ТЕХНИКА БЕЗОПАСНОСТИ ПРИ РАБОТЕ С ГАЗАМИ
При (работе с газами необходимо уделять серьезное внимание
правилам техники безопасности во избежание взрывов опытных
установок, отравления людей. Общими правилами при работе с
тазами являются: хорошая вентиляция всего помещения и
индивидуальная вентиляция опытной установки, прекращение ра!боты при
малейшем появлении токсичных газов, предотвращение возможности
попадания открытого огня или электрической искры в объем, где
могут накапливаться или выделяться взрывоопасные газы.
(Важным условием техники «безопасности является герметичность
прибора. Если в ходе опыта газ не должен оставаться в установке,
то необходимо предусмотреть его отвод из помещения, ядовитые
газы требуется поглощать, горючие сжигать.
Промышленные тазы поступают в лаборатории в баллонах
емкостью 12; 20 и 40 л с соответствующей окраской и маркировкой.
Сверху баллоны закрыты вентилями, к которым привинчиваются
понижающие редукторы. Баллоны с горючими газами имеют левую
резьбу, остальные — правую. Баллоны должны быть укреплены в
лаборатории хомутами в специальных стойках. Переноска баллонов
вручную не разрешается.
3. МЕТОДЫ ОЧИСТКИ ГАЗОВ,
ПРИМЕНЯЕМЫЕ В ЛАБОРАТОРИИ
Большинство газов, поставляемых в лаборатории промышленностью,
содержит примеси. При выборе метода очистки газа
предварительно необходимо оценить, какую степень погрешности вносит
загрязненность газа на получаемые результаты. Рассмотрим только
методы очистки готовых промышленных газов. Наиболее чистые газы
получают при фракционной дистилляции. Этот метод пригоден для
всех газов, но он весьма трудоемок, нуждается в специальном
оборудовании и вымораживающих средствах.
46
.Перспективно в технике работы с газами применение молекуляр- .
ных сит Для осушки, очистки и разделения газов для анализа.
Молекулярные сита -— это мел/кие пористые кристаллы
природных или синтетических минералов — цеолитов. Размер пор этих
кристаллов фиэмерим -с размером (молекул отдельных веществ.
Такие молекулы^ могут входить в поры и адсорбироваться цеолитами.
Более крупные молекулы проходят мимо пор, т. е. пропускаются
цеолитам.
Природные цеолиты—это различные алюмосиликаты,
представляющие собой сочетания ионов металлов с анионами кремниевых
кислот. Синтетические (цеолиты имеют марки NaA, CaA, NaX, CaX.
Цеолиты обладают необычайно развитой внутренней поверхностью
пор, порядка £00—1000 im2/i\ такой, как и активированный уголь.
Молекулярные сита —хорошие осушители. Например, при
одних и тех же условиях упругость водяного пара составляет, Па:
20 — над активной AI2O3, 20 — над силикагелем, 2 — над
перхлоратом магния и 0,01 — над цеолитом NaA. Сита применимы и при
повышенных температурах, когда поглотительная способность
обычных осушителей понижается. Кроме того, для цеолитов характерны
высокая поглотительная способность в области малых парциальных
давлений водяного пара, возможность осушки газов при
повышенных давлениях и температурах, стабильная степень осушки.
Цеолиты можно использовать для одновременной с парами
воды очистки газа от двуокиси углерода и сернистых соединений.
Для регенерации «цеолитов их нагревают до высокой
температуры либо с продувкой сухим газом, либо в вакууме.
Цеолиты можно эффективно использовать для разделения и
анализа таких газов, как: Н2, О^ Na, СО, СН4> С^Нг и др.
Рассмотрим очистку наиболее часто используемых в
экспериментах газов.
Кислород. Для осушки и очистки кислорода от двуокиси
углерода его промывают» (концентрированным раствором перманганата
калия, едкою кали и серной кислоты.
Водород. Баллонный водород имеет обычно степень чистоты
99,7-^9,8, содержит влагу и воздух. 'По одному из наиболее
эффективных методов очистки водорода (диффузионному) его
пропускают через трубчатую кварцевую печь, в которой находятся
опирали из никелевой или лалладиевой трубки, нагретые до 750—900°С.
Водород диффундирует сквозь металл и поступает в газгольдер или
реакционную систему. При давлении в трубке 2—4 кПа можно
получать 1—5 л/ч очень чистого водорода.
Кислород удаляют из водорода различными способами.
Например, пропусканием водорода над активной красной медью при
температуре 300—400°С или над катализатором, который
способствует образованию водяного пара. Пары воды, поглощают
осушителями. Пределы осушения составляют, im-г воды на 1 л воздуха:
Р2О5<2,5-10-5; Mg(ClO4h<5-10-4; H2S04 0,003; СаС12 0,14—0,25.
Кроме химических поглотителей, применяют вымораживающие
ловушки с жидким азотом или смесью сухой двуокиси углерода с
ацетоном. По ходу газа сначала располагают колонки с
относительно слабыми осушителями и в последнюю очередь колонки с
сильными поглотителями. Для достижения содержания кислорода в
водороде менее 0,001% применяют активную медь.
Азот главным образом очищают от влаги и кислорода.
Кислород удаляют с помощью меди при 650°С или жидкого поглотителя—
47
J
Вада_
'Ma
раствора сульфата ванадия в присутствии а1мальгамирован»6го
цинка. От кислорода азот очищают наиболее эффективтю
молекулярными ситами в 'зернах размером 0,2—0,5 мм в (колонках/длиной до
62 м. /
Аргон, гелий. Эти газы очищают от влаги или обычными
способами сушки или нагретыми до высокой температур^ магниевой
Газ стружкой, титановой гибкой,
древесным активированным < углем, охлаж-
^3 даемым с помощью жидкого азота.
Существует барботажная очистка
аргона и гелия от влаги и кислорода,
при этом используется жидкий сплав,
активно поглощающий влагу и
кислород. На рис. 21. показана схема
осушителя. В качестве поглотителя
можно использовать жидкий литий или
сплав магния (68%) с алюминием
(32%), имеющий температуру
плавления 435°С.
Для очистки инертных газов от
кислорода можно использовать также
низшие окислы переходных
металлов. Газ после осушительной колонки
с молекулярными ситами поступает
в колонку с вермикулитом,
покрытым оксалатом двухвалентного
марганца.
Хло,р сжиженный баллонный
содержит 02, N2, H20, HC1. Для
очистки хлор пропускают через серную
кислоту, окись кальция и пятиокись
фосфора. Хлор конденсируют при
температуре твердой двуокиси углерода,
несконденсировавшиеся газы
откачивают. Затем вновь испаряют хлор,
конденсируют его в другом
резервуаре и откачивают
несконденсировавшиеся газы. Так проделывают
несколько раз. Для окончательного
удаления кислорода через жидкий
хлор можно пропускать водород.
0*ись углерода. Баллонный газ СО содержит примеси С02, 02,
Н2, СН4, N2. Для удаления С02 используют -КОН, аакарит, MgC104.
Для удаления кислорода применяют медь, нагретую до 600°С, или
активную медь при 170—'200°С. Более глубокая очистка достигается
методами фракционной разгонки или газо-адсорбционно хроматогра-
фическим способом.
м q ДоК°ШгЬ УглеР°да содержит в виде примесей 02, N2, СО, Н20,
Н2Ь, Ь02. Сернистые -соединения удаляют шролуаканйем С02 через
насыщенный раствор CuS04 и раствор КНС03. Для удаления
органических примесей используют расгйор 100 объемн ч.
концентрированной серной кислоты и 3,3 объемн. ч. 40%-ного'водного раствора
формалина. Для удаления кислорода двуокись углерода
пропускают через раствор ацетата хрома или сульфата ванадия в лр.йсутст-
Рис. 21. Барботер для очистки
нейтральных газов:
/ — корпус; 2 — головка; 3 —
трубка; 4 — ртуть; 5 — выход
газа
48
вии амальгамированного цинка и далее через раствор бикарбоната
натрия. Для этой же щели применяют активную медь, закись меди
при 170—12О0°С, ангидрон.
Аммиак сушат с помощью СаО и NaOH с последующей
фракционной перепонкой.
\.
4. СОЗДАНИЕ ПРОТОЧНЫХ АТМОСФЕР
Проточная атмосфера создается для осуществления динамических
методов установления равновесия в системе. Для этого через
систему постоянно пропускают свежий газ из баллона или газгольдера.
При статических методах установления равновесия введенную
в систему порцию газа или образовавшуюся в ней атмосферу
неоднократно перекачивают, создавая замкнутый цикл газовой атмосферы.
Для этих целей используют .циркуляционные насосы различных
конструкций.
В качестве примера циркуляционного наооса с движущимися
частями /можно привести насос, представленный на рис. 22. Поршень
Рис. 22. Схема циркуляционного электромагнитного насоса
1 насоса представляет собой запаянную стеклянную трубку,
заполненную полосками трансформаторного железа. Удар поршня в
цилиндре 9 амортизируется молибденовой пружиной 2, залитой в
основании сплавом Вуда. Клапанами 3 насоса служат покровные
микроскопные стекла. Для приведения поршня в движение
использована феррорезонансная электрическая схема, обеспечивающая его
автоматическое поднятие и опускание. Электрическая цепь состоит
из последовательно включенных дросселя 4, соленоида 5 и батареи
конденсаторов 6. Сердечник 7 поршня весит 50 т. Насос включается
в сеть переменного тока через автотрансформатор 8. Ход поршня
49
s
к П
^^■.■■■■■.■■■■■.■■■■■■■■■,^^'i
5
Рис. 23. Схема приготовления смеси. Аг—Hj—НаО:
/ — осушитель с силикагелем; 2 — трехходовой кран; 3 — печь с катализатором; 4 —
осушитель; 5 — секторный кран; 6 — печь с медной стружкой; 7—печь с титановой
губкой; 8 — манометр; 9, 10 — реометры; И — спираль для подогрева влажной
смеси; 12 — насытительная система; 13 — термостат; 14 — печь для подогрева газовой
смеси
регулируется изменением напряжения, подаваемого в электрическую
цепь насоса. Производительность насоса составляет 250—300 мл/
/мин. При емкости циркуляционной системы 2,5—3,0 л газовая смесь
совершает одй,н цикл за 10 мин.
В большинстве случаев для создания атмосферы в
экспериментальной установке 'через систему пропускают газовую смесь
определенного состава. Широко употребляется смесь водорода,
водяного пара и аргона. Схема подготовки такой смеси показана на
рис. 23. Водород из (баллона проходит осушитель с силикагелем,
печь с платинированным асбестом и: осушитель с пятиокисью
фосфора. Аргон пропускают через печи с медной и титановой стружкой,
осушитель с пятиокисью фосфора и направляют для насыщения
водяным паром в насытитель с дистиллированной водой, помещенной
в водяной бане термостата. Далее тазовые потоки смешивают.
Скорости аргона и водорода регулируют по показаниям реометра.
5. ИЗМЕРЕНИЕ СКОРОСТИ И ДАВЛЕНИЯ
ГАЗОВЫХ ПОТОКОВ
Скорость тазовых потоков можно измерять с помощью
капиллярных или диафрагменных реометров, газовых часов, ротаметров
поплавкового типа. Действие реометра основано на переладе давления
на концах капилляра '(капиллярный реометр) или до и после
диафрагмы (диафрагменный). Разность давлений зависит от акорости
газа, температуры, диаметра капилляра или диафрагмы, вязкости
газа. Для каждого реометра и газа все параметры, за исключением
скорости, являются величинами постоянными, поэтому можно
отградуировать показания реометра, т. е. высоту столба жидкости,
находящейся в нем, в зависимости от скорости газа.
На рис. 24,а представлены распространенные модели реометров.
Для одной и той же.жидкости 2 в реометре можно попользовать
капилляры / различного диаметра и работать в широком
интервале скоростей газа. При небольших скоростях газа (0,1—1,0 л/мин)
следует применять в реометре легкие жидкости (бензин, дибутил-
фталат), при больших расходах газа — тяжелые.
Для точного измерения (~ 1 % независимо от вязкости)
скорости потока и расхода газа применяют пенный измеритель.
Пенный (измеритель (рис. 24,6) состоит из соединенных
тройником 2 градуированной бюретки / и небольшой резиновой груши 3
с мыльным раствором. Для измерения акорости потока и расхода
один конец тройника присоединяют к газовой магистрали и,
нажимая на грушу, вводят в бюретку пену. С помощью секундомера
определяют время, за которое мыльная пленка проходит расстояние
между двумя калибровочными метками на бюретке.
Большие расходы газа измеряют газовыми часами,
выпускаемыми промышленностью. Они непригодны для работы с агрессивными
газами и тазами, растворяющимися в воде.
Для приближенного намерения скоростей газа — от см3 до
м3 в минуту—удобно пользоваться промышленными ротаметрами.
Ротаметр представляет собой стеклянную коническую трубку, внутри
которой движется поплавок-волчок. При прохождении газа через
ротаметр волчок плавает в струе паза на высоте, соответствующей
скорости газового потока. Чем больше расход газа, тем выше
поднимается поплавок. Зазор между поплавком и стенками трубки
определяет проводимость ротаметра.
Г 5J
Для калибровки реометров используют ичэтовые,
отградуированные для данного газа 'реометры, газовые часы, газометрь^ О
скорости газа судят но количеству воды, вытекающей в единицу времени
из газометра при атмосферном давлении. Газометр по/соединяют к
реометру, а последний к источнику измеряемого газа: Градуировку
можно производить по воздуху, а для пересчета на требуемый газ
использовать формулу: ^2=^i'ni/rl2, где т^ и т]2 — соответственно
вязкость воздуха и газа.
Рис. 24. Схемы реометров (а) и пенного измерителя (б)
Давление газа измеряют с помощью различных жидкостных
манометров, заполненных жидкостями, не взаимодействующими с
газовыми атмосферами, -ртутью, дибутилфталатом,
характеризующимся низкой упругостью пара.
Для измерения давления газов в последнее время широко
применяют электромеханические датчики — механотроны,
предназначенные для преобразования механических величин в электрические.
Механотроны могут измерять перемещения чувствительных
элементов с точностью от 0,0-1 до 100 мкм и давление от 0,1 Па до 1 МПа.
Принцип работы (механотрона состоит в том, что один или
несколько электродов могут перемещаться относительно неподвижного
катода. При этом изменяется величина и конфигурация
электрического поля и соответственно анодный ток. Механотроны могут быть
диодами, триодами, тетродами. Весьма распространены диодные
механотроны; их вводят в мостовые измерительные схемы. Механотро*
ны отличаются высокой чувствительностью по току (до 7А/ам) и
напряжению (до 25 кВ/см), стабильностью и надежностью показаний
52
при MajiVx габаритах. Принцип действия im ex а нотрон а можно понять
из схемы, приведенной на рис. 25. Подача механического сигнала на
щуп датчика вызывает удаление от катода одного и приближение
другого анода. При этом ток первого анода .уменьшается, а второго
увеличивается. В результате в /мостовой схеме возникает разбаланс
напряжений, который и измеряется выходным прибором. Прибор
можно сконструировать таким образам, что будет иметь место
нелинейная зависимость между давлением (перемещением) и силой
тока. Чувствительность прибора можно повысить, применяя
.гальванометры с малым внутренним сопротивлением.
5 4 9 10 2
Рис. 25. Схема механотрона:
/ — подогреваемый оксидный катод; 2 — электровводы; 3, 9 — подвижные
аноды; 4 — изолятор; 5 —коваровая мембрана; 6 — молибденовый стержень; 7 —
фланец; 8 — колба; 10 — эластичная пружина; // —электроизмерительная
схема
Для регулирования давления в системах применяются
различные маностаты. Например можно регулировать давление от 2,6 до
100 кПа. Ртуть, налитая в резервуар, поддерживает поплавок,
соединенный со стержнем, на конце которого находится стеклянный
шарик, садящийся в седло. Шарик закрывает труб^ку, по которой в
систему поступает газ. Трубка соединяет маностат с регулируемой
системой. Установкой разности уровней ртути между резервуаром
и передвижной склянкой задают давление в системе.
Электрические регуляторы давления представляют собой
закрытые или открытые U-образные манометры, в которых при изменении
давления уровень ртути изменяется, замыкая или размыкая при
этом контакты.
ГЛАВА IV
ТЕХНИКА РАБОТЫ С ВАКУУМОМ
Многие металлургические измерения производятся *
герметичных или вакуумных установках. Для их
создания необходимо знать основные положения вакуумной
техники.
Перед конструированием установки определяют, при
каком давлении должна работать система, оценивают
53
возможное количество газовыделений, приближенные
конструктивные размеры камеры печи.
При создании установки задаются предельным
рабочим вакуумом. Подбирают насосы, которые могут
создать требуемое разрежение при достаточной скорости
откачки, чтобы поддерживать заданное давление по
ходу эксперимента.
Производительность вакуумной системы (л-Па/с) —
это количество газов, удаляемое из установки в единицу
времени. Скорость откачки (л/с) — это объем газов,
удаляемый насосом из камеры в единицу времени охри
данном давлении. Скорость откачки установки связана с
рабочим давлением и количеством удаляемых газов
s = Q/p. Приближенно скорость откачки камеры
объемом V для изменения давления от р\ до р2 за время т
равна:
s = X In _*Z1*L f (2)
* Р2 — Р0
Ро — предельный вакуум установки.
На практике при определении мощности вакуумной
системы главную роль играет газоотделение со стенок
установки и из нагреваемого объекта. Для поддержания
давления Ю-2—10~5 Па в системе с площадью
поверхности внутренних стенок 10 м2 можно -применять насос
со скоростью откачки 100 л/с при условии, что откачку
можно производить в течение нескольких часов. Если же
давление в системе требуется получ'ить за несколько
минут, то необходим насос со скоростью откачки
1000—100000 л/с.
В зависимости от объема металлической или
стеклянной системы можно рекомендовать Насосы со следующей
скоростью откачки, л/с: 100—при емкости до 10 л; до
500—при емкости 10—100 л и до 1500—при емкости
более 100 л.
1. ВАКУУМНЫЕ МАТЕРИАЛЫ
Материалы для создания вакуумных установок должны
удовлетворять следующим требованиям: а) быть ©аку-
умплотными, герметичными; б) характеризоваться
низкой^ упругостью пара; иметь высокую антикоррозионную
стойкость; г) хорошо свариваться, паяться,
полироваться и т. п.
54
Металлы черные. В литом виде используются серые
чугуны. Из прокатных материалов широко применяется
нержавеющая сталь марок 1Х18Н9Т—0Х18Н9. Эта сталь
хорошо поддается пластической обработке, полируется,
сваривается под слоем флюса аргоно-дуговым способом,
ее можно сваривать с медью. Если установка не
рассчитана на длительный срок работы, то можно применять
газовую сварку стали. Нержавеющие стали паяются
серебряными или оловянно-свинцовыми припоями с
обычной сталью, медью, никелем-
Медь находит применение для изготовления
электрических контактов, электровводов, индукторов, магаито-
проводов, водяных магистралей, .корпусов,
кристаллизаторов с водяным охлаждением и т. п. Медь можно
сваривать .постоянным током под слоем флюса. Для тонких
медных сечений применима аргоно-дуговая сварка.
Пайка меди производится многими видами оловянных и
серебряных припоев ic большинством применяемых
(металлов.
Бронзы и латуни. Бронзы БрБ2, БрА5 применяют для
изготовления конструктивных узлов, крепежа, токопод-
водов и т. п. Используемые латуни (Л21, ЛС59) не
должны подвергаться нагреву, так как произойдет
испарение цинка из них.
Алюминий. Высокими герметичными свойствами
обладают литейные алюминиевые (сплавы АЛ2, АЛ5, АЛ9.
Широко используется дюралюминий, отличающийся
хорошей обрабатываемостью, однако он не соединяется
пайкой. Если требуется создание переходников, то в
сложных паяных узлах применяют никель, который
хорошо паяется со сталью, медью, алюминием.
Стекло хорошо паяется, сваривается с рядом
металлов, оно коррозионностойко. Стеклянные установки легко
контролируются на герметичность, в них легко
устраняются повреждения. Отрицательным свойством стекла
является его хрупкость. При небольших напряжениях,
механических деформациях, неравномерном нагреве или
охлаждении в стеклянных деталях появляются трещины.
Поэтому рекомендуется, во-первых, жестко крепить
стеклянные детали к металлическому каркасу установки,
освобождая их от нагрузки, во-вторых, крупные детали
изготовлять из металла.
Марки стекол различаются главным образом
коэффициентом линейного расширения. В марке стекла пос-
55
ле индекса С указывается величина коэффициента
линейного (расширения а-107. В табл. 1 приведены свойства
наиболее распространенных марок стекол. Для
смотровых окон в зависимости от температуры нагрева
используются плоакопараллельные молибденовые или
кварцевые стекла.
ТАБЛИЦА 1. ХАРАКТЕРИСТИКА СТЕКЛА ОТДЕЛЬНЫХ МАРОК
Показатель
а-107 (20—100°С)
t °C:
отжига
Металл, с которым
возможна спайка
Марка стекла
С-90-1
87—92
400—500
540—560
Си, Pt,
сталь
1Х18ТФМ
С-88-4,
свинцовое
86—90
360^-450
480—500
Pt, сталь
1Х18ТФМ
С-47-1,
молибденовое
4в-48
420—455
68О-600
Ковар,
Мо, Та
Показатель
а-107 (20— 100°С) . .
/, °С:
отжига
размягчения . . .
Металл, с которым
возможна спайка . .
С-49-2,
калиевое
48—50
410—535
570—580
Ковар, Мо
Продолжение
Марка стекла
пирекс
33—34
550
590—610
Мо, W
С-39-1,
нонекс
38—40
410—540
630—650
Мо, W
кварц
прозрачный
5—5,6
—
1500
Мо, W (до
диам.
0,5 мм)
Пластмассы используются в качестве
электроизоляционных и уплотняющих материалов. Большое значение
имеет для вакуумной техники фторопласте с
термостойкостью до 200° С, морозостойкостью, химической
стойкостью, малым газоотделением, низкой упругостью пара,
малой теплопроводностью. Фторопласт сваривается при
375°С под давлением.
Технологичным материалом является органическое
стекло оно вакуумшлотно, является хорошим
электрическим изолятором, склеивается дихлорэтаном,
сваривается под давлением с нагревом до 200°С. Для
вакуумных конструкций можно использовать стеклотекстолит
56
АГ-4, стекловолокно, оропитанное форм альдегидной
смолой, полиэтилен и полистирол.
Резина, Вакуумная резина выпускается в виде
масло-стойкой черной резины марки 9024, ИРП 1015,
ИРП 2043 и белой немаслостойкой резины 7889,
ИРП 1368, термостойкость резины от 50 до 90°С.
2. КОНСТРУИРОВАНИЕ ВАКУУМНЫХ УСТАНОВОК
При создании вакуумных установок исследователь
использует различные готовые узлы и изготовленные в
лаборатории несерийные детали. Вакуумная арматура
объединяет конструктивные части установок, служит для
регулирования направления и скорости газовых потоков.
Важнейшим элементом конструкций является
соединение отдельных узлов.
Соединения, вводы, затворы, натекатели
Соединения. Наибольшее распространение при стыковке
отдельных частей (конструкции получили фланцевые
соединения. На рис. 26
показаны виды
фланцевых соединений с
резиновыми или
металлическими уплотнениями.
Резиновые прокладки
вырезаются из листовой
резины или склеиваются из
вакуумного шнура или
трубки. Разборные
соединения должны
конструироваться так, чтобы
резиновый уплотнитель
не воспринимал
механической нагрузки и не
влиял на точность
установки деталей. Следует
учитывать
«несжимаемость резины.
Фланцы разъемных соединений рекомендуется
затягивать до соприкосновения металлических поверхностей.
Объем канавки, в которой лежит уплотнение, должен
быть равен или несколько больше объема уплотнителя.
При нажатии резиновое уплотнение должно сжиматься
на 30—40% первоначальной толщины.
Рис. 26. Вакуумные соединения с
неподвижными (/) и подвижными (//)
фланцами:
а — V-образная канавка; б — U-образ-
ная канавка; в — плоский нажимной
зуб; г — фигурный нажимной зуб
57
Допустимо удельное давление на резиновые
прокладки 0,98—1,96 МПа. Для фторопластовых прокладок
допустимое давление увеличивается до 2,74—3,14 МПа.
При повышенных температурах и низких давлениях в
системах менее К)-5 Па июпользуют металлические
прокладки: свинец до 100°С, алюминий до 350°С, медь
до 500°С. При этом нажимное давление должно
составлять, МПа: на овинец 118—176, алюминий 196—264,
медь 294—343.
Рис. 27. Сальниковые уплотнительные элементы:
/ — полированный вал; 2 — корпус уплотнения; 3 — нажимная гайка; 4
—нажимной фланец; 5 — резиновые кольца; 6 — металлическая шайба; 7 —
пружина; 8 — фторопластовая втулка
Для уплотнений с небольшим нажимом можно
использовать индиевую проволоку.
Наилучшим способом соединения стеклянных трубок
в случае нежелательности их сварки является
соединение <на шлифе. С успехом используются переходники из
резиновых или поливиниловых шлангов.
Вводы. Для (введения в вакуумные камеры различных
трубок, вакуумметрических ламп, штоков, приводов для
вращения используют сальниковые и грибковые
уплотнения. На рис. 27 представлено сальниковое уплотнение с
резиновыми шайбами (а), кольцами земмеринга (б),
фторопластовой втулкой (в). Полированный вал плотно
обжимается уплотняющими шайбами из тонкой (1,5—
2,0 mim) маслостойкой резины. Внутренний диаметр
шайбы равен 7з диаметра вала. Шайбы уплотняются с
помощью металлических фигурных шайб и нажимной
гайки. Вся система смазывается маслом из масленки.
58
Резиновые шайбы можно заменить шайбами из
политетрафторэтилена или хлорвинила. В уплотнениях типа
колец земмеринга шайбы изготовляются методом литья
из черной резины; внутрь шайб помещается кольцевая
пружина для полного обжатия вала. Уплотнение
работает со смазкой и способно хорошо передавать
вращательное движение, обладая малым сопротивлением
проходу вала. Если нежелательно иметь смазку, то для
Рис. 28. Электритеский
вакуумный слаботочный (а) и
сильноточный (б) ввод:
/ — латунное кольцо; 2 — стенка
вакумяой камеры; 3 — пайка
медью; 4 — изолирующая
прокладка; 5 — прижимное кольцо;
6 — медный ввод; 7 — резиновое
кольцо; 8 — медный стержень;
9 — резиновый уплотнитель;
10 — изоляционные кольца; // —
нагреватель
лередачи поворота на угол до 180° надевают гибкую
трубку на штуцер, приваренный к камере, и на
наружную часть вала.
Схемы электрических вводов (приведены на рис. 28.
Ввод б диаметром 12,5 мм позволяет пропускать то«
силой 325 А при напряжении 360 В. Небольшие токо-
■вводы пропускают через стенку камеры с помощью колец
из полиэтилена, создающих вакуумное уплотнение и
электрическую изоляцию, и нажимной гайки. Холодные
электройводы (проволоки термопар и т. п.) в вакуумных
установках осуществляют путем их зажима в вакуумном
шланге, например хомутиком на болтах.
59
Вакуумные затворы. Для регулирования газовых
потоков, отсекания трубопроводов служат различные
запирающие устройства: стеклянные краны, металлические
вентили, шиберы, задвижки.
Шиберы — это плоские затворы с перемещающимся
внутри корпуса затвора в горизонтальной плоскости
дискам с уплотняющим кольцом. Диск надвигается на
отверстие затвора 'и уплотняет его.
Форточные затворы, как правило, угловые, в которых
тарелка, закрывающая проход, из горизонтального
положения откидывается подобно дверце в вертикальное.
Прижим тарелки к уплотнению осуществляется с
помощью эксцентрикового механизма.
В вентилях сильфонного типа затворный диск
перекрывает отверстие. Его поднимают и опускают
вращением винта, на 'котором он укреплен. Герметизация
между винтом и корпусом вентиля создается с помощью
сильфона. Сильфоиный вентиль позволяет постепенно
приоткрывать трубопровод. При конструировании
вакуумных установок необходимо, чтобы нажимные крышки
вакуумных затворов были обращены в сторону
емкостей, находящихся под разрежением, чтобы атмосферное
давление прижимало крышку к седлу.
Натекатели. Для напуска в системы порций газов с
определенной скоростью служат натекатели. Простейшие
натекатели — это сильфониые вентили или стеклянные
вакуумные .краны с капилляром.
Более точную регулировку дают металлические
натекатели, в которых стальная игла вводится в седло из
мягкого металла — меди или свинца. В натекателе
типа Б-23 шток иглы при вывинчивании голов»ки под
действием пружины закрывает проходное отверстие в седле.
Когда игла плотно войдет в отверстие, головка
освободится, т. е. натекатель закрыт. С помощью муфты
регулируют нажатие пружины так, чтобы игла не
раздавливала седло, сделанное из свинца или фторопласта.
При завинчивании головки игла поднимается вследствие
разности шага резьбы на штоке и втулке. Пропускная
способность такого натекателяот4- 10-4 до 4- КНл-Па/с.
3. ВАКУУМНЫЕ НАСОСЫ
Вакуумные насосы различных конструкций используют
для создания разрежения в установках.
60
Механические насосы
Насосы предварительного разрежения создают вакуум
до 0,5 Па. Их используют и в качестве вспомогательных
насосов для работы пароструйных насосов. Наиболее
распространены механические вакуумные юасосы
золотникового, или плунжерного типа.
На рис. 29 показана схема такого насоса. Обойма 2,
61
укрепленная на эксцентрике /, скользит по внутренней
поверхности корпуса и выталкивает газ, всасываемый
через отверстие 6. Газ выталкивается через клапан 8
в отверстие 7. Недостатками этих насосав являются:
быстрое снижение скорости откачки при падении
давления, опасность повреждения абразивными частицами
пыли, 'конденсация водяных паров в масле с образованием
водо-масляной эмульсии.
При откачивании запыленных объемов следует
устанавливать механические фильтры. Для предотвращения
конденсации влаги золотниковые насосы снабжают
газобалластным устройством, которое представляет собой
клапан, установленный в стенке камеры сжатия насоса.
При сжатие газа в камеру сжатия автоматически
подается порция воздуха, повышающая давление внутри
насоса выше предела, при котором происходит
конденсация паров воды. Однако при работе с газобалластом
происходит снижение 'предельного вакуума насоса.
Для небольших систем используются
пластинчато-роторные насосы. В корпусе насоса вращается ротор, в
пазах которого расположены две пластины,
разжимаемые в разные стороны пружиной. Ротор, расположенный
эксцентрично, при вращении всегда соприкасается с
верхней частью корпуса, а пластина создает с одной
стороны расширяющийся объем, в который поступает газ
из всасывающего патрубка. По другую сторону
пластины происходит сжатие газа и его выброс через
выхлопной клапан. Корпус насоса погружен в бак с маслом,
которое является уплотняющей жидкостью. Для
увеличения предельной глубины вакуума насосы делаются
двухступенчатыми.
Схема пластинчато-статорного насоса приведена на
рис. 30. В этом насосе ось вращения ротора совпадает
с геометрической осью камеры -насоса, но са-м ротор
расположен эксцентрично. Одной из своих образующих
ротор скользит по внутренней поверхности цилиндрической
камеры насоса и тем самым описывает в камере насоса
объемы, аналогичные образующимся в камере
пластинчато-статорного насоса. Всасывание и сжатие газа
осуществляется самим ротором. В прорези корпуса насоса
помещена пластина для разделения камеры разрежения
и камеры сжатия. В насосе ВН-461 пластина к
поверхности ротора прижимается пружиной. В насосе РВН-20
пластина выполнена в виде поршня, который скользит
62
в цилиндре, установленном над корпусом насоса.
Сжатый вращением ротора газ 1вьгбрасывается в цилиндр под
поршень. При движении ротора пластина опускается и
поршень сжимает газ, который через клапан
выбрасывается в верхнюю часть цилиндра над поршнем. При
Рис. 30. Схема пластинчато-статорного насоса с пластиной в виде поршня:
а — в — последовательные стадии работы; / — полость всасывания; // —
полость сжатия; / — корпус; 2 — ротор; 3 — вход газа; 4 — отверстие; 5 —
пластина; 6 — поршень; 7,8 — клапаны; 9 — ролик
дальнейшем движении поршня .газ из 'верхней части
цилиндра выбрасывается через «выхлопной клапан в
атмосферу, а в нижнее пространство под поршнем
попадает газ из роторного пространства. Таким образом,
поршень с цилиндром является по отношению к
роторному насосу второй ступенью.
Двухроторные насосы
Эти насосы обладают высокой производительностью.
Принцип действия такого насоса отражен на схеме
рис. 31. Двухроторные насосы обеспечивают высокую
Рис. 31. Принцип действия двухроторного насоса:
а, б, в — последовательные стадии всасывания и выхлопа газа
63
скорость откачки в диапазоне давлений от 100 до 1 Па.
Две восьмеркообразные лопасти насоса вращаются в
разные стороны. Лопасти не касаются друг друга
благодаря высокому качеству обработки поверхностей и
специальной (профилировке. Зазор между «ими не
превышает 0,1—0,15 мм. Скорость вращения лопастей до
3000 об/мин.
Основное достоинство насосов заключается в
отсутствии трения в роторном механизме .и в возможности
работать без уплотняющего масла. Хорошая
балансировка роторов позволяет достигать высоких скоростей
вращения при небольших размерах.
Двухроторные насосы нуждаются в предварительном
разрежении.
Молекулярные насосы
Вращательные механические молекулярные насосы
создают давление до -10~6 Па. Принцип действия этих
насосов заключается в том, что испарение молекул -газа,
адсорбирующегося на
вращающейся твердой поверхности, про-
„ исходит таким образом, что век-
Я 1] (] Д тор скорости испаряющейся мо-
^' ™ ™ ^ лекулы совпадает по
направлению и величине с вектором
скорости вращающегося твердого тела.
На рис. 32 представлена
схема действия молекулярного
насоса. Между статором / и ротором
2 имеется канал 3,
расширяющийся сверху вниз. В верхней
части, между ротором и
статором, имеется тонкий зазор. Так
как пропускная способность
канала больше, чем зазора, то
перемещение молекул откачиваемого газа в основном
происходит в канале, куда они увлекаются вращением
ротора. Молекулярный насос имеет заметную скорость
откачки, когда выходное давление невелико. Впускное
давление пропорционально выпускному. Зависимость
впускного давления от давления на выходе из насоса
проявляется с того момента, когда средняя длина
свободного пробега молекул в канале превысит его ширину.
Рис. 32. Схема действия
молекулярного насоса
64
При этом начинает играть роль молекулярная вязкость,
прямо пропорциональная давлению газа.
Преимущество молекулярных насосов заключается в
там, 'что их не нужно разогревать как диффузионные
насосы.
Для удовлетворительной работы достаточна скорость
вращения ротора до 16000 об/мин. Обычно
молекулярные насосы делают многоступенчатыми в виде турбины.
В камере насоса помещен ротор, состоящий из дисков с
прорезями. Каждый диск вращается в зазоре толщиной
1 мм между двумя диска-ми статора, которые также
имеют прорези. Для каждой 1пары роторных и статарных
дисков щрорези располагаются зеркально относительно
друг друга. Газ перемещается от статора к ротору, от
одной пары отверстий к другой. Каждая пара отверстий
является миниатюрным молекулярным насосом, который
создает небольшое сжатие газов. В каждой паре дисков
может быть до 40 отверстий, поэтому при параллельной
работе они создают значительную скорость откачки.
Если на оси ротора насажено 20 пар дисков слева и
20 пар дисков справа, то имеется 20 ступеней, которые
создают перепад давлений рВып/Рвп = 5-107. Скорость
откачки такого турбомолекулярного насоса 140 л/ч в
интервале давлений 1—Ю-6 Па. Турбомолекулярный
насос можно включать одновременно с насосом
предварительного разрежения.
Пароструйные насосы
Для создания глубокого вакуума применяют
пароструйные засосы. Рабочей жидкостью этих насосов служит
масло или ртуть. Жидкость кипит в кипятильнике насоса.
Пар по паропроводу поступает к соплу, из которого
истекает с большой скоростью. Откачиваемый газ попа^
дает в корпус насоса через всасывающий патрубок,
захватывается струей пара и вместе с ней передается
внутрь насоса. На охлаждаемых стенках насоса пар
конденсируется 'и жидкость поступает назад в
кипятильник насоса. Откачиваемый газ сгущается и подается к
следующей ступени откачки—к соплу ©торой ступени,
затем к третьей 'и далее достигает выхлопного патрубка.
От патрубка газ откачивается иасосом предварительного
разрежения, создающим давление 1—10 Па. Ступени
пароструйного насоса служат для последовательного
сгущения газа от давления 10~4—10~5 до 10—1 Па.
3 Зак. 664
65
В зависимости от режима истечения пара насосы
можно разделить на эжекторные, бустерные и
диффузионные.
Для масляных насосов используют масла ВМ-1,
ВМ-2, ВМ-3 или крамнийорганические масла ПФМС-1 и
ПФМС-2. Для предотвращения попадания паров масла в
откачиваемый объем «ад насосом устанавливают
вымораживающую ловушку.
В небольших насосах применяют ртуть.
Преимущество ртути состоит ib том, что насосы могут работать при
высоком предварительном давлении. Кроме того, ртуть
не взаимодействует с откачиваемым газом. Упругость
паров ртути высокая (~0,1 Па), поэтому для
достижения низкого давления порядка 10~4 Па необходимо
применять вымораживающие или охлаждающие ловушки.
Весьма удобны для конструирования вакуумные посты,
в состав которых входят форвакуумный и диффузионный
насосы, вакуумный затвор, вакуумметры. На базе такого
поста может быть создана экспериментальная
вакуумная установка.
Адсорбционные насосы
Это насосы безмасляной откачки. Их используют для
откачки объемов до давлений 1—Ю-2 Па. Насос
представляет собой емкость, в которую помещен цеолит
(молекулярное сито). При охлаждении до температуры
жидкого азота цеолит поглощает 02, N2, CO^ и другие газы.
Не поглощаются инертные газы, водород. Через
определенное время адсорбент насыщается откачиваемым
газом. Для регенерации насоса его подогревают до
комнатной температуры. Ранее поглощенные газы десор-
бируются и выделяются в атмосферу. При откачке
водяных паров регенерацию насоса следует производить при
550°С. Для получения низких давлений рекомендуется
предварительная откачка объема форвакуумным
насосом. Преимущество этих насосов состоит в том, что
загрязненность откачиваемого объема органическими
компонентами масла отсутствует.
Геттерные насосы
Принцип действия этих насосов основан на испарении
титана и его ионизации. На охлаждаемых стенках
насоса образуется пористая пленка с высокими сорбционны-
66
ми свойствами. Поглощение газа происходит на
обновляемой (Поверхности пленки благодаря физической
адсорбции, хемосорбции, химическим реакциям и
растворению в твердой фазе. Поглощаются все газы, за
исключением инертных и углеводородов.
Преимущество этих насосов состоит в том, что они
не загрязняют объема, не требуют ловушек. Насос
может быть присоединен к откачиваемому объекту без
вентиля. Быстрота действия насоса ГИН-05М1 мощностью
0,85 кВт составляет 400 л/с при давлениях от 5-10-5 до
5•10-а Па. Испарение титана происходит с поверхности
молибденового нагревателя, на который нанесен слой
иодидного титана толщиной 0,5 мм. Общий запас
титана на двух испарителях составляет 7 г. Более крупные
насосы ГИН-4 и ГИН-5 имеют скорости откачки
соответственно до 1800 и 5000 л/с при давлении Ю-7 Па
(начальное давление 0,1 Па). При 'использовании геттерных
насосов желательно обеспечивать безмасляную
предварительную откачку объема с помощью адсорбционных
или пароструйных насосов с эффективными ловушками.
Магнитные электроразрядные насосы
В этих насосах, являющихся геттерно-ионными, для
распыления и ионизации геттера используют газовый
разряд в магнитном поле. Схема простейшего диодного
машиторазрядно1го насоса показана на рис. 33. Анод /
Рис. 33. Схема диодного
магниторазрядного насоса
с источником питания:
/ — анод; 2 — катод; 3 —
балластное сопротивление;
4 — направление магнитного
поля
насоса образован набором ячеек из нержавеющей стали,
с открытых концов которых расположены общие катоды 2
из титана. Эта система помещается в магнитное поле,
перпендикулярное к плоскости катода. При подаче на
электроды разности потенциалов в несколько киловольт
в ячейках .возникает газовый разряд, поддерживающий-
-~\Ц
3* Зак. 664
67
ся в широком диапазоне давлений. Положительные ионы
газов, образующиеся в разряде, ускоряются полем
в направлении катодов и внедряются в них, вызывая
распыление материала катодов. Распыленный с катодов
титан осаждается на все внутренние поверхности
электродов. Непрерывно возобновляемая пленка титана
образуется на аноде. Откачиваемые газы поглощаются
пленкой на аноде. Сложные газы: пары воды, углекислый
газ, аммиак, углеводороды— диссоциируют в разряде.
Ионы осколков молекул бомбардируют катод. Ионы
легких газов могут внедряться ib материал катода. Чем
больше давление в насосе, тем сильнее бомбардируется
катод и больше распыляется титан, т. е. тем выше
скорость откачки. При понижении давления скорость
откачки уменьшается. Насос автоматически регулирует
скорость распыления катодов.
Скорость действия насосов НЭМ-30, НЭМ-100 и
НЭМ-300 составляет 30; 100 и 300 л/с при давлении
Ю-4 Па. При более низкцх давлениях скорость откачки
резко снижается. В насосах с водяным охлаждением ано-
вдв (диодные магниторазря'дные насосы типа НОРД)
высокое отрицательное напряжение подается на катоды,
изолированные от корпуса. Анод насоса заземляют.
Эти насосы имеют диапазон рабочих давлений от 6,5 до
10~7 Па и скорость откачки от 10 до 500 л/с.
4. ИЗМЕРЕНИЕ ВАКУУМА
Приборы для измерения низкого давления можно
разделить на механические, жидкостные и электрические.
Для приближенного измерения вакуума с точностью до
133—1330 Па служат трубчатые, мембранные или силь-
фонные манометры. Мерой давления в них служит
величина деформации чувствительного элемента под
действием приложенной к этому элементу разности давлений.
Одним из основных достоинств этих манометров
является независимость показаний от рода газа. Трубчатые
манометры измеряют разность атмосферного давления
и давления в системе: рИзм=ратм — Рман. Мембранные
(или сильфонные) манометры имеют откачанный до
0,1 Па замкнутый объем, закрытый чувствительной
мембраной (или сильфоном), (внешняя поверхность
которой воспринимает измеряемое давление. Показания
та>ких манометров не-зависят от атмосферного давления.
68
Жидкостные манометры
Эти приборы можно разделить на дифференциальные и
компрессионные. К дифференциальным относится U-об-
разный вакуумметр с открытым или запаянным
коленом. Рабочей жидкостью является ртуть или масло.
В этих вакуумметрах неизвестное
давление р> приложенное к
одному концу [/-образной трубки,
сравнивается с известным
давлением роу приложенным к другому
ее концу. Разность давлений р—
— ро уравновешивается весом
столба рабочей жидкости в одном
из колен вакуумметра,
представляющим разность уровней
жидкости в.левом и правом коленах.
Манометры могут иметь
запаянное «ли открытое колено,
откачиваемое вакуумным 'насосом до
давления 1 Па. Точность
измерения давления ртутными
вакуумметрами составляет 65 Па и
зависит от точности замера
разности урОБней ртути и влияния сил
поверхностного натяжения.
Применение вакуумного масла с
плотностью ~ 1 г/см3 позволяет измерять давления с
точностью до 6,5 Па, но при работе с маслом
необходимо учитывать смачивание стенок трубки маслом и перед
произведением отсчета делать необходимую выдержку
для установления равновесного мениска масла. Для
повышения точности отсчета следует применять
оптические катетометры. Для повышения чувствительности
прибора одно из его колен может быть наклонным.
Компрессионные вакуумметры Мак Леода являются
абсолютными/ так как их показания не зависят от
природы газа, за 'исключением конденсирующихся паров.
Вакуумметры Мак Леода (рис. 34) измеряют давления в
пределах 13Э0—1Q-3 Па. Их используют для градуировки
других типов вакуумметров.
Рис. 34. Схема простейшего
манометра Мак Леода:
1,2 — капилляры; 3 —
измерительный баллон
Теплоэлектрические вакуумметры
Вакуумметры этого типа 'позволяют записывать
измерения in автоматизировать контроль за работой установки.
Они работают на основе принципа зависимости
теплопроводности от давления газа.
Манометр сопротивления. Индикатором давления в
нем служит изменение сопротивления нити накала в
зависимости от ее температуры. По нити накала
пропускается стабилизированный ток. При изменении давления
теплоотвод в датчике вакуумметра увеличивается или
уменьшается, температура нити и ее сопротивление
соответственно изменяются. Так как последнее измеряют
с помощью мостиковой схемы, то происходит разбалан-
сировка моста, позволяющая судить о давлении в
датчике. Датчик представляет собой стальную трубку,
внутри которой на двух вводах натянута вольфрамовая
нить «акала. Измерение давления обычно проводят три
постоянной температуре нити. Уменьшением или
увеличением тока накала температуру нити манометра
возвращают к исходному значению. Диапазон действия
манометра ПМТ-6 с прибором ВСБ-1 от 4000 до 1 Па.
Термопарный вакуумметр. В датчике термопарного
вакуумметра ПМТ-2 находится платиновая нить накала,
к которой приварена хромель-копелевая термопара. На
нить накала лампы подают ток от выносного прибора
ВТ-3. При неизменном токе накала температура нити, а
следовательно, и т. э. д. с. термопары зависят от
теплопроводности разреженного газа, находящегося в лампе.
Теплопроводность зависит от давления газа: чем ниже
давление, тем выше температура и измеряемая э. д. с.
Диапазон работы прибора 65—650 Па с точностью 30%.
и 65—0,1 Па с точностью 10%- Датчики ПМТ-4 и
ПМТ-4М имеют металлический корпус.
Главным источником ошибок этих вакуумметров
является изменение состояния поверхности нити накала
и зависимость показаний от рода газа. Так, при
измерении давления водорода показания вакуумметра
необходимо умножать на 0,67, а для аргона — на 1,56.
Ионизационные вакуумметры
Принцип их действия основан на том, что электроны,
эмиттируемые с накаленного катода, ускоряются
электрическим полем между катодом и сеткой и при своем дви-
70
жении ионизируют газ, ионы которого 'направляются на
отрицательно заряженный коллектор ионов. Ионный ток
служит /мерой давления таза. Манометр ВИТ-3 с
датчиками ПМИ-10 и ПМИ-2 работает в диапазоне давлений
1СН—Ю-5 Па. Вакуумметр ВИЧ4 с датчиками ПМИ-12
измеряет давления до Ю-8 Па. Ионизационные датчики
в случае попадания в них во время работы воздуха
перегорают. Для учета влияния рода газа показания
вакуумметра с датчиком ПМИ-2 следует корректировать,
вводя коэффициент 2,18 для На, 0,65 для С02, 0,9 для СО
и 0,8 для СН4.
Ионизационные радиоактивные вакуумметры
В этом вакуум-метре мерой, давления также является
ионный ток, возникающий вследствие ионизации газа
«-частицами, образующимися при радиоактивном
распаде препарата, помещбнного в вакуумметр. Стабильность
работы радиоактивного вакуумметра обеспечивается
независимостью радиоактивного распада от температуры
окружающей среды, продолжительности работы и
взаимодействия с газом, наполняющим датчик. Большим
достоинством вакуумметра является линейная градуи-
ровочная характеристика в широком интервале
давлений. Ионный ток пропорционален интенсивности а-излу-
чения и плотности тока. Вакуумметр ВР-4 с датчиком
МР-8 измеряет давления в интервале от 100 кПа до
10-* Па.
Магнитные электроразрядные вакуумметры
В 'манометрах этого типа постоянный -магнит создает
поле, в котором располагается катод и внутри него анод.
Катодом может служить корпус вакуумметра. При
наложении разности потенциалов в магнитном поле
возникает электрический разряд. Ток разряда зависит от
давления.
Магнитное поле влияет на поток электронов,
искривляя их траекторию. Путь электронов удлиняется, и
возрастает вероятность их встречи с частицами газов.
Ионизированные молекулы дают возможность измерить
ионный ток и по его величине определить давление в
датчике. Положительные ионы ©следствие своей большой
массы слабо отклоняются магнитным полем и
прямолинейно движутся к катоду.
71
Более широкий диапазон измерений имеют
двухкамерные вакуумметры и вакуумметры с
секционированным катодом. Вакуумметр ВМБ-3 с датчиком ММ-13
измеряет давления от 2,5 до 10~5 Па, а вакуумметр ВМЭБ-1
с датчиком ПММ-28 — от 1,33 до 10"3 Па.
Датчики вакуумметров должны располагаться
таким образом, чтобы ib них не попадали пыль, пары
масла и испарения из исследуемого объема. Следует
защищать вакуумметры от действия тепловых,
электрических щ -магнитных полей.
5. ОТЫСКАНИЕ ТЕЧИ
Любая вакуумная установка перед введением в
-эксплуатацию должна быть испытана на герметичность. Оценку
герметичности проводят то натеканию в установку
атмосферного воздуха. Для этого ее откачивают до
возможно более низкого давления и отключают от насосов.
В определенные промежутки времени измеряют
изменения давления и рассчитывают натекание по формуле
E=VAp/x, где V — объем установки, л; Др— изменение
давления, Па; т — (время измерения, с.
Рекомендуется проводить измерения натекания после
длительной отка-чки установки с целью максимально
возможного удаления адсорбированных газов.
В любой установке будет происходить газоотделение
из уплотнений, смазки и других узлов. При проведении
опытов следует задаваться минимально возможным
натеканием газа в установку, оценивая допустимое
натекание с точки зрения заданной точности измерений.
При величине натекания, превышающей допустимую,
необходимо принять меры по устранению имеющихся
неплотностей.
Различают следующие способы обнаружения течей.
Опрессование. В испытуемом объеме создается
повышенное давление газа. Объем погружается в бак с водой
или подозреваемые места смачиваются жидким мыльным
раствором. Образование пузырьков служит индикатором
течи.
Вакуумметрический способ. Испытуемое место
обмазывают летучей индикаторной жидкостью (эфиром,
ацетоном, спиртом и т. п.). По изменению показания
вакуумметра судят о наличии течи.
Метод высокочастотного разряда применяют при
оценке натекания в стеклянные системы. При давлении
72
от нескольких сотен до 0,1 Па /в -системе можно возбудить
электрический светящийся разряд. С приближением >к
наружной поверхности стекла щупа высоковольтного
разрядника с него на стекло бьет беспорядочный поток
искр, который превращается в шнуровидный пучок,
концентрирующийся на неплотности.
Метод галоидного течеискателя. В этом методе в
испытуемом объеме создают повышенное давление газа,
содержащего галоид, например фреон, четьгреххлористый
углерод, хлороформ, йодоформ. К подозрительным
местам подносят щуп датчика течеискателя. При
обнаружении течи течеискатель дает электрический и
звуковой сигналы.
Принцип действия течеискателя состоит в том, что
при попадании галоидов на поверхность нагретой
до 800—900°С платины резко увеличивается эмиссия
положительных ионов с поверхности платины.
Галоидный течеискатель ГТИ-6 представляет собой
переносной прибор со щупом ъ виде пистолета, в кото-ром
находится небольшой вентилятор, засасывающий поток
воздуха. Внутри расположен чувствительный элемент
датчика — диод с платиновыми электродами.
Центральным электродом является платиновая спираль,
намотанная на керамическую трубку. Спираль
нагревается до 900°С. Коллектор ионов выполнен в виде
платинового цилиндрика, окружающего эмиттер. Цилиндр
по отношению к электроду находится под отрицательным
потенциалом. Ионный ток коллектора усиливается и
отмечается на приборе одновременно со звуковой
индикацией.
Недостаток галоидного течеискателя состоит в весьма
большой его чувствительности (к загрязнениям
окружающей атмосферы. Галоидный течеискатель позволяет
обследовать как вакуумные системы, так и системы,
находящиеся под положительным давлением. Вакуумные
системы, откачанные до давления 133—0,1 Па,
обдуваются снаружи 1гало1Идсодержащим газом.
Датчик течеискателя подсоединен к патрубку
вакуумной системы установки.
Метод гелиевого течеискателя. Масс-спектрометри-
чеокий метод обнаружения течей с помощью гелиевого
течеискателя наиболее -чувствительный. Он состоит в
том, что течеискатель подсоединяется к испытуемой
установке и с помощью собственной откачной системы
73
прокачивает через свой датчик—масс-спектрометр —
небольшой поток газа из установки. Подозрителыные
места установки обдуваются снаружи гелием. Масс-
спектрометр прибора настроен на гелий. При наличии
течи и попадании гелия в вакуумную установку
последний неизбежно оказывается в камере
маос-спектрометра. Это регистрируется выносным прибором, а звуковой
генератор дает сигнал о попадании гелия в установку.
Таким образом, течь отмечают в том месте, которое
обдувалось гелием.
Течеискатель рекомендуется подсоединять к
вакуумной системе на линии 'между «механическим и
диффузионным насосами. Течеискатель ПТИ-10 обнаруживает течи
порядка 6-1014 л -Па/с.
глава v
ИССЛЕДОВАНИЕ СВОЙСТВ ЖИДКИХ
МЕТАЛЛИЧЕСКИХ И ШЛАКОВЫХ РАСПЛАВОВ
1. АКТИВНОСТИ КОМПОНЕНТОВ В РАСТВОРАХ
Законы физической химии в применении к
металлургическим процессам следует рассматривать для веществ,
находящихся в растворенном состоянии в металлах или
шлаках. Взаимодействие атомов и 'молекул веществ в
реальных растворах приводит к отклонениям от законов,
действующих в идеальных растворах. Чтобы
использовать уравнения химической термодинамики для
реальных растворов, вместо концентрации введена
термодинамическая функция — активность а.
Активность является безразмерной величиной. Ее
физическую сущность можно определить как
эффективную концентрацию вещества в растворе, которую
учитывают при взаимодействии его с другими веществами,
в тех или иных физических или химических
превращениях. Активность данного компонента в растворе
а.г есть отношение упругости пара этого (компонента
над раствором к упругости пара его в стандартном
состоянии: т=р{/р*т. Стандартным считают такое
состояние раствора, когда активность равна концентрации.
Растворы, близкие к идеальным, можно разделить на
группы: бесконечно разбавленные и совершенные.
74
В совершенных растворах все компоненты,
образующие раствор, подчиняются закону Рауля pi=Po N\ во
всем интервале концентраций и в широком .диапазоне
температур и давлений.
Для растворов, близких к совершенным, за
стандартное принято состояние чистого -компонента (рс/ = Р/).
Активность компонента в совершенном растворе равна
мольной доле. При отклонении раствора от закона Рауля
активность ai=yi Nu где у*— коэффициент активности,
учитывающий степень отклонения раствора от
идеального.
Для растворов, близких к (разбавленным, в качестве
стандартного принимают: для растворителя — состояние
чистого компонента, для растворенного вещества —
такое состояние, при котором в растворе любой
концентрации соблюдался бы закон Генри. За стандартное
состояние часто выбирают 1%-ный или бесконечно
разбавленный раствор, для которого /:f=(l.
Для реальных растворов, близких к разбавленным, к
которым относят металлические сплавы, концентрации
элементов выражают -в процентах по массе, тогда
ai = U [i]% где fi — коэффициент активности.
Активности различных компонентов в растворе
взаимосвязаны уравнением Гиббса — Дюгема:
"*(тг) =м>(д-£г) ■ (3)
\ oNx }р,т \ dN2 ]р,т
Зная активность одного из компонентов раствора,
можно определить активность другого.
Рассмотрим некоторые экспериментальные методы
определения активностей компонентов в металлических и
шлаковых растворах.
2. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ПО РАВНОВЕСИЮ
РАСТВОРА С ГАЗОВОЙ ФАЗОЙ
По данному методу расплав выдерживается при
определенной температуре под газовой фазой заданного
состава до наступления равновесия. В составе газовой фазы
должен находиться элемент, активность которого
определяют. По химическому составу металла и по известной
активности элемента в газовой фазе определяют его
активность в металле или шлаке.
75
Метод универсален, имеет высокую точность
определения.
Этим «методом изучено поведение углерода, кислорода
■и серы в металлических и шлаковых расплавах.
Недостатки метода сводятся к следующему. Во-лер-
вых, состав газовой фазы трудно поддерживать
постоянным ib течение длительного времени. В печи, в системе
подачи и отвода .газа могут протекать побочные
реакции, развиваться термическая диффузия. Все -это влияет
на состав газа на.д расплавом. Истинный его состав
будет отличаться от среднего, учитываемого в расчетах. Во-
вторых, ib некоторых системах для наступления
равновесия требуется длительное время.
Определение активности углерода
В этом случае часто используют атмосферу из СО и
С02. Металлический расплав, в который может быть
добавлен углерод для ускорения достижения равновесия,
выдерживают иод атмосферой из СО и С02. При этом
фиксируют состав -газовой фазы >и анализируют металл.
Таким образом исследуется реакция
[С]+С02 = 2СО, (а)
константа равновесия которой К=Рс01(рсо2а[С]). Для
получения величины константы экспериментальные данные
на графике в координатах р со/Рсо2— [С]
экстраполируются к нулевой концентрации углерода, где Я[С1={С] (за
стандартное состояние принимается состояние
бесконечно разбавленного раствора углерода в металле). Для
всех остальных равновесных условий активность
получают из уравнения (pQ0/pco2) (l/К), а коэффициент
активности fc=a[C]/ [С].
Если обозначить для бинарного сплава константу
равновесия К'у активность углерода afCj, а для тройного
сплава Fe—С—х\ соответственно К" и а'^ , то
К' = Рсо/Рсо2 а[су К" = Рсо/Рсо2 alci
для одних и тех же отношения pQ0/pco2^ содержания
углерода, для которых взяты константы
ВДе / с— коэффициент активности углерода в зависимо-
76
сти от содержания третьего компонента -в тройном
сплаве:
ig /с=ig /с-—ig /с- = ig /; — ig /с,
где f*Q— суммарный .коэффициент активности углерода
в тройном сплаве Fe—С—хи a f'c —коэффициент
активности углерода в сплаве Fe—С.
Рис. 35. Схема установки для плавки металла под атмосферой СО и С02:
/ — баллон с Аг; 2 — баллон с С02; 3 — поглотители с ангидроном; 4 — печь
с магниевой стружкой, 590°С; 5 — реометр; 6 — поглотитель с аскаритом; 7 —
печь с медной стружкой, 450°С; 8 — выход в атмосферу; 9 — к
газоанализатору; 10 — печь для конверсии С02 в СО; // — сосуд с графитом; 12 —
ртутный клапан избыточного давления; 13 — смеситель; 14 — реакционная печь
А. Рист и Дж. Чипман изучали равновесие жидкого
металла с газовой атмосферой, состоявшей из СО и С02.
Схема установки приведена на рис. 35. Аргон и
углекислый газ из баллонов после соответствующей очистки
смешивали с окисью углерода, которую получали в
газогенераторной печи (Пропусканием сухого углекислого
газа через графит при 1100°С. Очистку окиси углерода
от С02 вели с помощью КОН. Расход аргона и окиси
углерода поддерживали постоянным, изменяли только
расход углекислоты. Отношение р2со[рсо2 увеличивали от
100 до 4300. Состав газа контролировали гравиметри-
77
чеоким методом по .количеству С02, поглощенной аска-
ритом. Определяли также содержание (20 в газе.
Газовую смесь подводили ;к поверхности металла с
помощью корундовой трубки, окруженной .графитовым
пустотелым .нагревателем, который должен
предотвращать выпадение свободного графита из газа. При
больших отношениях концентраций СО и С02 выпадение
свободного углерода все же происходило
2СО = Сгр+С02. (б)
Для ускорения наступления равновесия в расплав
железа присаживали графит. По достижении равновесия
металл закаливали и определяли содержание углерода.
Основной трудностью ттри проведении подобных
экспериментов является создание таких условий опыта,
которые «предотвращали бы (выпадение углерода на
стенках печи и в подводящих трубопроводах.
Это «приводит к отклонению отношения р^ //? от
расчетного значения, определяемому по данным анализа входящих или
выходящих газов или по установленному соотношению pCQ /Peot •
Хорошим катализаторам для разложения окиси /углерода является
конденсат железа, оседающий на стенках установки.
Источником ошибок является также термическая
диффузия в газовой смеои.
Окись углерода как легкий таз будет диффундировать к
нагретой "поверхности, т. е. отношение Рсо/Рсо над повеРХН(>стью
металла и в подводящем трубопроводе будет неодинаковым.
Кроме того, возможно недостижение термического
равновесия между газом и металлом.
Вследствие краткости контакта газовых молекул с металлом
они не успевают нагреваться, поэтому число активированных
молекул значительно меньше их общего числа и реакции протекают
медленно. Время до наступления равновесия обычно достигает
нескольких часов.
При концентрации углерода .в <металле>1 %
содержание С02 в тазовой смеси ничтожно мало и не
поддается точному измерению. Даже слабое окисление газа
начинает влиять на получаемые результаты.
При использовании углеродсодержащих смесей
метана с водородом опыты проводили в замкнутой системе
с постоянной циркуляцией таза над металлом.
Содержание -метана и газе определяли с помощью инфракрасного
газоанализатора. После промыеки системы аргоном в
нее после расплавления металла напускали водород и
78
выдерживали систему до наступления равновесия, о чем
судили по неизменному составу газовой фазы, т. е. по
концентрации ^тана в газе.
Исследованию подвергается реакция [С]+2Н2 = СН4,
для которой
К = РснЛРк <W- (4)
В качестве стандартного выбирали состояние
(^графита. Активность растворенного в металле углерода
определяли как отношение величины Рсн4/Рн§» равновесной
с данным -расплавом, к величине рсн4/рн.» Равновесной
с р-лрафитом при той же температуре. Поледнее
отношение вычисляли по литературным данным для реакции:
Ср4~2Н2=СН4.
Трудность этой методики заключается в том, что при
высоких температурах метан разлагается, поэтому
результаты необходимо корректировать.
Этим способом исследован интервал концентраций
углерода в железе от 1,52 до 4,95%.
Определение активности кислорода
Активность кислорода в жидких растворах определяют
в основном методом установления равновесия жидкого
металла с пароводородной атмосферой известного
состава. Содержание кислорода и легирующих
компонентов в металле определяют для равновесной системы.
Исследуется реакция ЯуОх+хНг=хН2Ог+у[Щ, для
которой К=(рн2о1р Ht-)*[R]y9 (R — раскислитель или
легирующий компонент; RyOx — твердый или жидкий
окисел, образующий конденсированную фазу, не
составляющую растворов с металлом, его концентрация не
входит в выражение константы равновесия).
Отношение рн2о/рн, либо задается исследователем, либо
точно фиксируется в ходе опыта. По зависимости
величины константы равновесия от температуры определяют
и температурную зависимость AG.
При определении растворимости или активности
кислорода в чистых металлах исследуют реакцию
1°]л*е + Н2 = Н20, (5)
для которой К=Рнло/(рнг а [0]). Комбинация реакции
79
(а) с реакцией диссоциации водяного гйра: Н20 = Н2 +
+ V2O2, позволяет получить необходимые
термодинамические данные для реакции /
V202 = [0]^. , (6)
Для реакции растворения кислорода в чистом
железе установлено отрицательное отклонение растворов
железа с кислородом от идеальных.
Сумма термодинамических функций реакций (а) и
(б) дает термодинамические функции для реакции
1/202=[0]м<н-я.
С помощью этого метода можно получать данные
по активности кислорода в жидких металлических
расплавах.
При равновесии чистого жидкого металла с окисной
фазой и с газовой атмосферой константу равновесия
можно записать следующим образом:
^ = Рн2о _J
РН2 а[0]
В состоянии равновесия аог=ЯоОКф =0[О]. Если за
стандартное состояние принять бесконечно
разбавленный раствор кислорода в жидком металле, то
константа равновесия примет вид:
С добавкой в жидкий металл раскислителя
активность кислорода изменяется, и константа равновесия
запишется в виде отношения
К' = рн2о __ _К_
Рн2$[0] " /§■ '
где f g — коэффициент активности кислорода в
жидком металле в присутствии раскислителя R. Тогда
/о =К/К'у где /('— эффективная константа
равновесия реакции Н2+Г01м^я=Н20г. Для данного
содержания элемента-раскислителя
*'=Рн,о/Рн.[°1-
Таким образом можно определять раскислительную
способность элементов и состав окисной фазы,
образующейся при раскислении.
80
' -1,5 -1,0 -0,5 О +0,5 +1,0 +1,5
IgECr]
Рис. 36. Взаимосвязь \g (pu л/ри ) и lg [Сг] при температуре, °С:
/ — 1525; 2— 1710
Покажем это на примере системы железо — хром —
кислород. Для реакции
СЮ, + х Н2 = х Н20 + [Сг] (7)
константа равновесия имеет вид
K = [Cv}{pHi0/pHiy,
где х — отношение числа атомов кислорода к числу
атомов хрома в молекуле окисла. На рис. 36 показана
зависимость \g(p н,о/Р н2) от lg[Cr].
Отношение р н,о/р н2 фиксировали в момент
появления окисной пленки на поверхности металла, т. е. при
наступлении трехфазного равновесия окисел —
металл—газ. Для этого состояния определяли
содержание хрома в металле. По экспериментальным точкам
концентрации хрома от 0 до 6% можно провести
прямую, угловой коэффициент ее наклона равен 2. Этот
коэффициент численно равен величине х. Тогда реакция
(7) для данного интервала концентраций примет вид:
Сг02+2Н2=2Н20+:[Сг].
Окисел Сг02. неизвестен, поэтому можно
предположить существование окисла FeO-Cr203 (шпинель окиси
хрома), в котором на один атом хрома приходятся два
атома кислорода. Для этого случая реакция (7) примет
вид: FeO.Cr203+4H2=4H20+2[Cr]+iFe. После
комбинирования ее с изученной реакцией [0]+Н2=Н20
получаем реакцию окисления хрома в железе: 2[Сг] +
+4[0]+Fe=FeO-Cr203. На участке прямой, соответ-
81
ствующем концентрации хрома от 6 до 46%, угловой
коэффициент равен 2/з, т. е. окисление хрома
происходит по реакции 2 [Сг] +3[О] = Сг203. /
Схема экспериментальной устаиовк^ для работы по
этому методу представлена на рис. .23. Температура
воды в термостате может поддерживаться с точностью
до 4=0,05° С. Наилучшее насыщение/ аргона водяным
паром достигается при скорости потока аргона
1000 мл/мин.
При определении раскислительной способности
сильных раскислителей, например алюминия, низкие
парциальные давления водяного пара в газе
получают пропусканием аргона через раствор хлористого
лития.
Определенное отношение парциальных давлений
водяных паров и водорода получают, подмешивая
водород к аргоно-пароводяной струе постоянного состава.
Трубки, по которым движется газовая фаза, несущая
водяной пар, от термостата-насытителя до реакционной
печи, подогревают, чтобы не было конденсации воды.
Непосредственно перед реакционной печью газовую
смесь нагревают до 1000° С с целью уменьшения
влияния термической диффузии на состав газа и создания
лучших условий для достижения равновесия. Плавки
ведут в кварцевой печи с индукционным, нагревом,
обеспечивающим хорошее перемешивание металла. Печь
снизу закрывают пришлифованной или прижимной
вставкой. В защитном тигле большего размера
помещают маленький плавильный тигель. Для плавки
используют готовые корундовые или цирконовые тигли.
Газовую смесь подают через трубку, нижний конец которой
подходит почти к самой поверхности жидкого металла.
Пробы металла отбирают кварцевой
трубочкой-пипеткой (диаметром 5—6 мм), которая проходит в
реакционную систему через водоохлаждаемый кран,
установленный на верху печи. Трубочка перемещается без
нарушения герметичности системы либо с помощью
резинового сильфона, либо с помощью сальникового
уплотнения. Через трехходовой кран трубка продувается
нейтральным газом. Верхний конец пипетки
присоединен резиновым шлангом к груше для отсоса проб
металла. Отвод газа из печи происходит снизу.
Методика проведения экспериментов состоит в
следующем. Расплавляют чистый металл; ванну выдержи-
82
вают под заданной атмосферой при определенной
температуре от 15у до 40 мин, после чего отбирают пробу
металла. Далее^изманяют или состав газовой фазы, или
температуру металла и отбирают новую пробу и т. д.
Если на поверхности жидкого металла появляется
окисная фаза, чтчр соответствует достижению предела
растворимости кислорода в данном металле, то
выдержка под пароводородной атмосферой должна быть
уменьшена для снижения взаимодействия окионой фазы
со стенками тигля.
При плавке металла с добавкой легирующего или
раскислителя момент установления равновесия
фиксируется по появлению на поверхности металла окисной
фазы, соответствующей данному содержанию элемента-
раскислителя в металле. Появление окислов на
поверхности металла определяют визуально. Состояние
равновесия может быть достигнуто постепенным изменением
состава газовой фазы, например увеличением ее
окислительного потенциала, т. е. повышением
парциального давления водяного пара. В момент появления
окисной фазы перестают изменять состав газовой фазы
и, таким образом, фиксируют равновесный
окислительный потенциал. После нескольких проверок, т. е.
понижения или повышения окислительного потенциала,
уточняют правильность установления равновесия.
Отбор пробы металла после достижения равновесия
позволяет определить содержание кислорода в металле,
соответствующее пределу растворимости кислорода в
металле при данных условиях.
При определении активности закиси железа в
шлаках путем установления равновесия с газовой
атмосферой, состоящей из водорода и водяного пара, одной из
труднейших проблем является подбор тигля, не
взаимодействующего с расплавом. Тигель может быть сделан
из того же материала, который входит в состав шлака.
При исследовании силикатных шлаков использовали
железные тигли. Исследовали равновесие реакции:
Fe + H20 = H2+ (FeO)sio2,cao,Fe203. За стандартное
принимали состояние чистой закиси железа в равновесии с
железом. Температуру измеряли термопарой,
подведенной к дну тигля. Шлак нагревали в атмосфере азота.
По достижении необходимой температуры опускали в
печь трубку, подводящую газ к поверхности жидкого
шлака. Изменение состава газа, выходившего из печи,
83
контролировали с помощью катарометра/ Затем,
подбирали температуру насытителя таким образом, чтобы
состав газа, выходящего из печи, оставался
постоянным. При этом любое изменение состава газа
объясняли (взаимодействием газа со шлаком.^ Газ продували
через шлак в течение 14 ч, затем намораживали пробу
шлака на железный штырек. Состав шлака заранее
подбирали таким образом, чтобы содержание FeO было
на 2—6% ниже ожидаемого для газовой атмосферы
данного состава. По достижении равновесия тигель
поднимали в холодную зону печи и закаливали там в
течение 1 мин. Шлак анализировали на содержание
двух- и трехвалентного железа.
Основные ошибки этого метода исследования
сводятся к следующему: 1. Возможно несоответствие
истинного содержания водяных паров в газе, подходящем
к поверхности расплава, тому содержанию паров,
которое принимают для расчета по температуре воды в
насытительной колбе и по скоростям газовых потоков.
2. Ошибки при измерении температуры. 3.
Неопределенность точного фиксирования состояния равновесия и
времени для осуществления равновесного состояния.
При работе с легко окисляющимися или
испаряющимися элементами, например марганцем!, состав ванны во
время равновесной выдержки изменяется. Приходится
по ходу плавки добавлять легирующие для
поддержания состава металла на постоянном уровне.
Достоинством рассматриваемого метода является
возможность точного фиксирования равновесия между
окисной, металлической и газовой фазами, а также
возможность в одном опыте исследовать различные
концентрации элементов в металле или производить
замеры при различных температурах.
Определение активности серы
Активность серы исследуют путем выдержки жидкого
металла под газовой атмосферой, состоящей из
сероводорода и водорода.
Изучают реакцию
[S]+H2 = H2S, (8)
для которой
^ = Phs 1
РН* a[S]
84
Величину \константы равновесия можно определить,
приняв за стандартное состояние 1%-ный раствор серы
в железе, когд^ ajs]=[S], или бесконечно
разбавленный раствор. Активность серы в расплавах, содержащих
третий элемент, вычисляется следующим образом:
где Ph2s/Ph2 — равновесное отношение для данного
раствора серы в железе с добавкой легирующего
компонента; К — константа равновесия реакции (8),
полученная путем экстраполяции на нулевую концентрацию
серы, при которой коэффициент активности серы в
железе равен единице. Коэффициент активности можно
рассчитать, как и отношение концентраций серы в
чистом железе и в данном растворе при одних и тех же
значениях Ph2s/Ph2. Для тройной системы коэффициент
активности серы равен: /| =/g /s, где fg
—коэффициент активности серы в системе Fe—S—х; fs — то же,
в зависимости только от серы; f's — то же, в
зависимости только от третьего компонента.
Исследование активности серы в расплаве можно
производить динамическим- и циркуляционным
методами. По методу динамического равновесия плавки вели
в индукционной печи с графитовым нагревателем,
помещенным внутри корпуса печи. Газовую смесь
сероводорода и водорода к поверхности металла подводили
после тщательной промывки печи аргоном с водородом.
Состав смеси газов регулировали скоростями потоков.
На выходе и входе смесь отбирали двумя бюретками и
анализировали на масс-спектрометре. Для быстрого
наступления равновесия смесь продували через металл.
Смешивание сероводорода и водорода может быть
также осуществлено в предварительно откачанном,
стальном баллоне. После анализа смеси исследователь
пользуется атмосферой постоянного состава. Точность
определения сероводорода в газе ±5%, а других газов,
присутствующих в виде примесей, ±1,0%. Оценка
влияния термической диффузии на состав газа
показала, что результаты не зависели от скорости подачи газа
к металлу. Поэтому можно считать, что термическая
диффузия не оказывает заметного влияния на
получаемые результаты.
85
Опытная установка для работы по одному из
вариантов циркуляционного метода представлена на рис. 37.
В установку перед началом опыта впускают
определенное количество очищенного водорода. В результате
взаимодействия водорода с жидким металлом,
содержащим серу, образуется сероводород. Смесь
сероводорода и водорода в системе перекачивается с помощью
1- Чк*
Рис. 37. Схема установки для определения активности серы в металлических
расплавах:
/—баллон с Н2; 2 — предохранительный клапан; 3 — поглотитель с КОН; 4 —
печь с катализатором; 5 — силикагель; 6 — алюмогель; 7— активированный
уголь, погруженный в сосуд Дьюара с жидким азотом; 8 — резиновая
камера; 9 — холодильник; 10 — реакционная кварцевая высокочастотная печь; 11—
циркуляционный насос; 12 — форвакуумный насос; 13 — ртутный термометр;
14 — оптический интерферометр; 15 — оптический пирометр
циркуляционного насоса до наступления равновесия, о
чем судят по постоянству отношения парциальных
давлений сероводорода и водорода. Для анализа
состава газовой фазы в циркуляционную часть системы
включен оптический интерферометр типа ИТР-1,
который позволяет определять состав газовой фазы
непрерывно. Перед поступлением в интерферометр газовая
смесь проходит холодильник для охлаждения до ком-
86
на^ной температуры. Точность определения
сероводорода и водорода равна ±0,004%. Принцип работы
интерферометра основан на измерении спектров преломления
эталонного газа (водорода) и исследуемого газа.
Предварительно прибор калибруют по газовой смеси
определенного состава, показатель преломления которой из
вестей.
В другом варианте циркуляционного метода
водород пропускали через вспомогательную печь, в которой
находился расплав серы с медью, нагретой до 1200° С.
В печи происходило насыщение водорода
сероводородом. Опыты продолжались в течение 14 ч. С помощью
радиоактивной серы определяли постоянство активно
сти серы в газе.
Для определения активности серы используют и
другие смеси. Например, аргон и сероуглерод. Для
получения такой смеси аргон пропускают через колбы с
дисульфидом углерода при известном давлении паров
CS2.
Для определения активности CaS в шлаках
равновесные плавки металла и шлака ведут под атмосферой
из СО, С02, «SO^, т. е. исследуются реакции:
СаО + S02 + 3 СО = (CaS) + 3 С02;
СаО + S02 + С02 = (CaS04) + СО.
Если S02 заменить серой, то имеем в
восстановительных условиях
CaO + VsS^CaSj + ViO,,
а в окислительных условиях
СаО + V. S2 + 3/2 02 = (CaS04).
Если Ро2<1 Па, то образуется только сульфид
■кальция. На рис. 38 дана схема опытной установки, в
которой С02 и S02 берут из баллонов, а СО получают,
пропуская С02 при 1100° С через порошок графита,
предварительно прокаленный при этой температуре в
атмосфере С02. Газ перед подачей в печь анализируют
гравиметрическим способом на СО и 02, определяют для
проб газа отношение /?co/(pco2 + Pso2)-
Внутри платиновой печи сопротивления на
подложке устанавливают два платиновых тигля, рассчитанных
на 0,25—0,40 г шлака. Внутреннее пространство печи
заполняют корундовыми изделиями так, что м.ежду ни-
87
ми и подложкой остается очень^маленькое
пространство. Так как плотности трех рабочих газов различаются
незначительно и содержание сернистого газа очень
мало, то при подогреве смеси перед введением в
реакционную 30iHy термодиффузия почти отсутствует. После
Графит, 1100°С
Рис. 38. Схема установки для изучения равновесия системы шлак — металл —
газ:
1 — манометр; 2 — уравнительные клапаны; 3 — смеситель; 4 — бюретки для
анализа газовой смеси; 5 — титрование NaOH; 6 — платиновая печь; 7 — мул-
литовая труба; 8 — платиновые тигли; 9 — термопара; 10 — корундовая
насадка; П — шлак; /2 — поглотитель с Mg(Cl04h
промывки печи азотом ее продувают реакционной
газовой смесью в течение 1 ч. Равновесное состояние
системы под газом постоянного состава достигается через
3 ч. Затем подложку опускают в холодную зону печи и
закаливают без доступа воздуха при выключенной
подаче газа.
3. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ПО УПРУГОСТИ ПАРА
Для совершенных растворов активность определяется
следующим отношением:
at = PjPi> (Ю)
где pi —давление пара данного компонента над
раствором; р ] —давление пара чистого компонента.
88
Для разбавленных растворов активность
растворителя будет равна а\ = р\1р\ , а активность
растворенного вещества а2=гр2у где г — постоянная, находится из
соотношения С* = гр*; С*2 и р*—соответственно
концентрация и упругость пара при весьма большом
разбавлении. Для измерения упругости пара применяют методы
Лангмюра и Кнудсена.
Метод Лангмюра
Упругость пара определяют по скорости сублимации
или испарения в вакууме с открытой поверхности, Па:
р = 2279,6 -£/£. (И)
где G — количество испарившегося металла, г; 5 —
площадь испарения, см2; т — время испарения, с; Т —
температура, К; М — атомная масса пара.
При этом предполагается, что все атомы пара,
ударяющиеся о поверхность стенок печи или мишени,
конденсируются. В качестве мишени используют инертную
пластину, на которой может происходить конденсация.
Для определения коэффициента активности в
бинарном растворе f I —dpi/dNj достаточно определить
характер зависимости парциальной упругости пара
компонентов от концентрации компонентов в растворе.
Тогда для массы металла G при постоянных значениях
S, т, Т, М имеем
f{=dGldNr
Для исследования необходимо, чтобы один из
компонентов обладал значительно меньшей летучестью по
сравнению с другим., чтобы изменение массы целиком
зависело от второго компонента.
Метод Лангмюра обладает большой
чувствительностью и позволяет измерять упругости пара до 10~4Па.
Однако он пригоден только для чистых металлов, так
как при испарении происходит обеднение поверхности
ванны легколетучим компонентом.
Рассмотрим исследование активности углерода з
железе и никеле по методу Лангмюра. За стандартное
89
Рис. 39. Схема установки для исследования активности углерода в жидком
металле:
/ — нагреватель; 2 — тигель; 3 — молибденовая обойма; 4 — экран из
нержавеющей стали; 5 — графитовый экран; 6 — токоподвод; 7 — термопара; 8 —
корпус; 9 — гляделка; 10 — вакуумное уплотнение; // — подвод аргона
90
состояние приняты чистые железо и никель. Активность
железа в растворе находили из соотношения
aFe = AG7AG°, (12)
где AG' — потеря м.ассы сплава данного состава; AG° —
потеря массы чистого железа при прочих постоянных
условиях опыта. Зная активность железа, определяли
активность углерода по уравнению Гиббса—Дюгема:
*¥-*Ps=- F-jr<"«ir- (13>
"о "<;_ "г, "с "г,
нас снас
где arci , Л/с > . N?e —соответственно активность
* LV^JHac' °яас' генас
углерода и мольные доли углерода и железа, отвечающие
насыщенным концентрациям углерода в растворах; а[с],
#Fe, Nc, N?e — соответственно активности и мольные
доли углерода и железа в растворах данного состава.
Экспериментальная установка представлена на
рис. 39. Тигель закрывали сверху крышкой с
отверстием диаметром 5,5 мм, что позволяло получать доста-
точно заметные потери железа. Чтобы создать
равномерный нагрев в окружающем пространстве и
предотвратить конденсацию железа на внутренней
поверхности крышки, тигель помещали в массивную обойму из
кованого молибдена. После изотермической выдержки
определяли потерю массы сплава.
Этим же методом определяли влияние кремния на
активность серы в расплаве Fe—Si—S. Скорость
улетучивания серы рассчитывали по изменению
концентрации серы до и после проведения опыта. Коэффициент
активности серы находили как соотношение скоростей
улетучивания серы для раствора с определенным
содержанием кремния и для раствора, не содержащего
кремния, при постоянной начальной концентрации серы.
Метод Кнудсена
В этом методе измеряют упругость пара по скорости
его истечения в высоком вакууме через калиброванное
отверстие. Пар должен истекать молекулярным
потоком при условии, что длина свободного пробега его
молекул во много раз больше диаметра отверстия.
Давление пара вычисляется по формуле, Па:
91
р= 2279,6^/^, (И)
где G — масса испарившегося вещества, г; К —
функция 1/г (I — толщина диафрагмы, закрывающей тигель,
см; г — радиус отверстия, см); 5 — площадь отверстия,
см2; т — время, с; Г —температура, К; М — атомная
масса пара, г.
Скорость эффузии измеряется по изменению массы
тигля с металлом до и после опыта или по увеличению
массы мишени (конденсатора), располагаемой над
отверстием, через которое истекает пар. Ошибка,
связанная с применением мишени, состоит в том-, что
аккомодация молекул пара жа мишени будет отличаться от
единицы, т. е. не все молекулы конденсируются при
ударе о. мишень.
Таким методом определяли активность никеля з
расплавах. При этом использовали уравнение Гиббса —
Дюгема:
//NI=Nir •
ln«Ni- 1 Т? dlnNm> (15)
где am — активность никеля в жидком железе; Л^. —
мольная доля никеля в паровой фазе; iV ре — мольная
доля железа в расплаве; N^e — мольная доля железа
в паровой фазе.
Тигель ставили в печь и закрывали корундовой
крышечкой с отверстием. Нагрев производили с помощью
экранов в индукционной пирексоовой печи с водоохлаж-
даемыми стенками. Конденсат, осевший на стенках
колбы, собирали и анализировали на железо и никель.
В данном методе применимы радиоактивные
изотопы. Для этого металл, содержащий изотоп, плавят в
вакуумной печи. Над тиглем, закрытым крышкой с
отверстием, помещают обойму с мишенями, на
которых оседают пары, выходящие из металла. Через
определенные промежутки времени мишени меняют и
счетчиком определяют активность конденсата и
рассчитывают скорость испарения.
Метод несущего газа
Метод состоит в том, что над поверхностью жидкого
сплава пропускают нейтральный газ, уносящий пары
92
компонентов. Далее пары конденсируются на стенках
камеры. После снятия конденсата со стенок определяют
содержание в нем того или иного компонента.
Давление пара компонента вычисляют по формуле
(G/V)V0 (16)
где робщ — общее давление, Па; G/V — количество
испарившегося вещества, приходящееся на 1 л газа, г;
Vo —объем 1 моля газа при нормальных условиях;
М — молекулярная масса вещества, г.
Подобным методом, измеряют активности в системе
Fe—Ni сравнением упругостеи пара над раствором и над
чистым компонентом.
К поверхности металлического расплава подводят
две трубки, через которые входит
и отводится гелий со скоростью
600 — 700 мл/мин. Гелий
насыщается парами металла. Опыты
показали, что при подобном
способе подвода газа происходит
равновесное насыщение его
парами металла. Затем газ
пропускают через корундовую трубку
большого диаметра, в которой
происходит конденсация.
Конденсат взвешивают и определяют
содержание в нем iNi и Fe, по
которым и рассчитывают упругость
пара.
В качестве несущего газа
можно использовать аргон. Схема
экспериментальной установки
представлена на рис. 40. Аргон к
поверхности металла подводят
через сопла в кварцевой трубке.
Конденсат, осевший на
поверхности трубки, смывают раствором
кислот и определяют содержание
железа в растворах. Равновесная
характеристика газовой фазы
находится экстраполяцией данных, полученных при
некоторых скоростях потока, на нулевую скорость.
Рис. 40. Схема установки
для определения активности
серы методом несущего
газа:
1 — жидкий металл; 2 —
кварцевый тигель; 3 —
кварцевая трубка с соплом; 4 —
кварцевый корпус; 6 —
резиновое уплотнение; 6 —
смотровое стекло; 7 — резиновая
пробка; 8 — огнеупорная
замазка; 9 — магнезитовая
засыпка
93
4. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ПО РАСТВОРИМОСТИ
ЭЛЕМЕНТА В РАСПЛАВЕ
Этим методом находят влияние третьего элемента на
растворимость и активность исследуемого вещества.
Метод пригоден для изучения насыщенных растворов.
Рассмотрим его применение на примере исследования
активности углерода. Расплавляют
железоуглеродистый сплав в графитовом тигле и присаживают третий
комлонент. Для увеличения контакта металла с тиглем
перемешивают металл графитовым стержнем или
вращают тигель. Плавку проводят в атмосфере аргона.
Принимают, что активность углерода в графите равна
единице. Так как при равновесии с графитом тигля
активность углерода в расплаве должна быть равна
единице, изменение коэффициента активности углерода
соответствует изменению растворимости углерода в
металле.
При постоянной активности компонента это
соотношение может быть выражено так: <31gfc=—dlgCc.
Добавление третьего компонента / в раствор влияет на
коэффициент активности углерода fc следующим
образом:
'с ~ /с/с •
Полный дифференциал от логарифма коэффициента
активности составит:
Считая, что логарифм коэффициента активности
углерода является функцией логарифмов концентрации
углерода и третьего компонента, разделим равенство
на dCy.
М (ai*fc\ (*ЪСс\ ■ /a Ч/с \
\ дс} )Сс [d\gcc)Cr0[ ас, )aJ{ дС/ )Сс
При постоянной активности углерода dlgfc=
= —dlgCc, поэтому, заменив в предыдущем уравнении
числитель во втором слагаемом правой части, получим
fd\gfc\ __г / aig/c ч 1 /aigcc\
dC* /CC L Ч-s^c /CroJ
94
Считая предел растворимости углерода в железе
при 1550° С Nc=0,2, получим:
f-Щ _Ш „ ItMi) __2,79 ВД .
Таким образом, установив изменение растворимости
углерода в сплаве, можно найти его коэффициент
активности. Практически определяют предел
растворимости углерода © зависимости от концентрации
добавляемого компонента, строят графики и рассчитывают
параметр взаимодействия углерода:
\ dNj ) ас тах
где А£ —растворимость углерода в разбавленном
растворе. Тогда lgf{, =e£ [/].
5. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ ПО РАСПРЕДЕЛЕНИЮ
ЭЛЕМЕНТА МЕЖДУ ДВУМЯ ФАЗАМИ
Если известна активность элемента в одной из двух
контактирующих равновесных фаз, то можно
определить его активность в другой фазе. Фазы должны быть
несмешивающимися, например при исследовании
активности марганца в железе это были железо и
серебро.
После выдержки железа и серебра до наступления
равновесия активность марганца в железе будет равна
активности (марганца в серебре: a[Mn]Fe =tf[Mn]Ag. Для
исследования углеродистые сплавы плавили в
графитовом тигле, а безуглеродистые — в корундовом. Плавки
вели в атмосфере аргона. Сначала устанавливали
равновесие между безуглеродистым железо-марганцевым
расплавом, коэффициент активности марганца в
котором принимали ра-вным единице, и серебром, тогда:
a[Mn]Ag=V[Mn]Ag[Mn]Ag=[Mn]Fe. ВЫЧИСЛЯЛИ КО-эффИЦИ-
ент активности марганца в серебре. В следующем
опыте устанавливали равновесие между серебром и
железоуглеродистым марганцевым расплавом с неизвестной
активностью марганца. По активности марганца в
серебре определяли его активность в расплавах железа с
углеродом.
95
Подобным образом устанавливали активность меди
в железе, изучая ее распределение между железом и
свинцом. Коэффициент активности меди в свинце
рассчитывали по теплотам смешивания меди и свинца, а
коэффициент активности меди в железе находили из
данных равновесия: 7[Си]Ре N [cu]Fe =T[CujPb N[cu]Pb •
Для определения активности серы использовали
радиоактивную серу. Расплав железа, содержащий
радиоактивную серу, выдерживали в контакте с
лепешкой двуокиси циркония до наступления равновесия.
Затем измеряли радиоактивность серы в обеих фазах
и рассчитывали термодинамическую активность серы в
металле.
Активность кислорода в железе можно установить,
исследуя равновесие железа со шлаком, в котором
известна активность FeO. Для реакции [0]+Fe= (FeO)
константа равновесия К=а(РеО)/й[0]. При a(FeO)=l
растворимость кислорода в железе в условиях 1600°С
равна 0,23%. Если считать раствор кислорода в железе
разбавленным, то а[О]=0,23 a(FeOi-
6. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ МЕТОДОМ Э.Д.С.
Этим методом определяют активности компонентов в
расплавах, создавая концентрационный гальванический
элемент. По уравнению Нернста э.д.с. гальванического,
элемента MeXi\электролит\MeXz равна
где п — число молей электронов, переносимых при по-
генциалопределяющем процессе; F — постоянная Фара-
дея; ахх и ах2 —активности компонентов Х\ и Хг.
Э.д.с. необходимо определять компенсационным
способом. В этом случае ток в цепи отсутствует и элемент
работает обратимо. При этом величина э.д.с. будет
максимальной, так как нет падения потенциала внутри
элемента.
Если один из электродов принят за стандартный
(активность измеряемого «компонента постоянна aXi =
=const), то по -величине э.д.с. можно рассчитать
активность компонента Хг во втором, электроде.
Метод э.д.с. позволяет получать точные значения
активности в металлах и шлаках, вести автоматическую
9в
регистрацию результатов наблюдений. Точность
измерения э.д.с. и других электрических характеристик
высокая. Успешное применение данного метода
возможно при учете некоторых его недостатков.
1. В реакционной ячейке возникает температурный
градиент, приводящий к появлению дополнительной
э.д.с, величина которой может значительно превышать
электрохимическую э.д.с.
2. Перед измерениями необходимо устанавливать
характер химической реакции, имеющей место на
электродах.
3. Необходимо знание активности в стандартном
электроде, т. е. используются данные, полученные в
других экспериментах.
4. Нежелательными являются взаимодействие
электролита и ячейки, конвекционные потоки в электролите.
Определение активностей элементов в металле
Данным» методом определяют активность С, Si, P, V з
расплавах железа. Например, для определения
активности ванадия в железоуглеродистых сплавах
использовали цепь:
(FeV)ICaO, Si02, Al2Os, B203, V203l [Fe, V(39,5<>/0)]
Сплав Шлак Стандартный
сплав
Так как концентрация ионов железа в шлаке весьма
мала, то потенциал определялся процессом обмена
между ионами ванадия. Если ванадий в шлаке находится в
виде двухвалентных ионов я=2, то э.д.с. элемента
равна:
где а у — активность ванадия в электроде сравнения (в
стандартном сплаве); a" v — то же, в исследуемом
металле.
При вычислении активности ванадия в железе
учитывали, что его активность в шлаке для всех сплавов
одинакова, а в стандартном, электроде постоянна.
Элемент состоял из графитового тигля с четырьмя
отверстиями, в которые вставляли алундовые тигли.
В одном тигле расплавляли сплав с постоянным
составом (39,5% V), в трех других — с переменным. Ячейку
4 Зак. 664
97
помещали в печь и покрывали сверху слоем
синтетического шлака из CaO, Si02, А1203, В203. После
расплавления шлака и металла в металл сквозь шлак опускали
два токоподвода из вольфрама, защищенные от
растворения корундовыми трубочками.
Таким образом устанавливают активность ванадия
в трех сплавах в одном, опыте, измеряя поочередно
э.д.с, возникающую между стандартным и
исследуемым сплавами.
Определение активности кислорода в металле
При определении активности кислорода в
металлическом расплаве электрохимическим методом
конструируют концентрационный гальванический элемент, в
котором электролитом служит огнеупорная окисная
керамика. При этом потенциалопределяющими процессами
являются: на аноде 1/202+2е=02_; на катоде О2-—
_2е=х1202. Величина э.д.с, определенная по
уравнению Нернста, равиа:
nF Ро.
Между э.д.с. элемента и логарифмом давления
кислорода существует линейная зависимость, которая
сохраняется в известном интервале температур и
парциальных давлений кислорода. Нижний предел по
температуре определяется высоким электросопротивлением
электролита и малой подвижностью ионов, а верхний —
разупорядочением решетки электролита и возможным
появлением направленного движения электродов.
Характерной особенностью электролитов из
двуокисей циркония и тория является наличие в их структуре
кислородных вакансий в узлах решетки, что определяет
возможность движения ионов кислорода и высокую
электропроводность этих материалов.
При постоянной температуре и весьма низком или
высоком парциальном давлении кислорода в
электролитах протекают реакции: 0* = V202+£+2e, V2O2+
+5 = 0*+2ф, где О* — анионный узел в решетке
окисла, занятый кислородом; В — вакантный узел; е —
электрон; © — дырка. Появление электронной (при
низких ро2) и дырочной (при высоких ро2) проводимо-
стей приводит к необходимости ввода в уравнение
Нернста значения доли ионной проводимости *и.
98
Величина п зависит от соотношения электронной и
ионной проводимостей в твердом электролите. При
смешанном типе проводимости в электролите фактическое
значение э.д.с. связано с расчетной или максимальной
э.д.с. по уравнению Вагнера: £ф=£тах(1— Лэ), где пэ —
число переноса электронов (доля проводимости). Чисто
ионная проводимость даже в специально приготовлен*
ных твердых электролитах соблюдается лишь в
определенной области температур и парциальных давлений
кислорода.
Доля ионной проводимости зависит также от пар*
циального давления кислорода в контактирующей с
электролитом фазе. В значительной мере ионная
проводимость зависит от пористости электролита, сопро*
тивления кислородной проницаемости, которая при
большом перепаде химических потенциалов и отсутсг*
вии интенсивного перемешивания приводит к
заниженным показаниям измерительных схем.
В настоящее время в качестве твердых электролитов
используют: двуокись циркония, окись магния,
трехокись алюминия, кварц, окись кальция, тория и др.
Ниже перечислены основные требования, которые
предъявляют к окисным электролитам: 1) чисто ионный
характер проводимости электролита или доля его
ионной проводимости должна быть стабильной и
известной; 2) минимальная кислородопроницаемость; 3)
высокая термостойкость, химическая стойкость по
отношению к расплавам.
Наиболее широко используют двуокись циркония и
трехокись алюминия (последнюю можно применять при
содержаниях кислорода в металле от 0,002 до 0,09%).
Трехокись алюминия имеет высокую термостойкость и
химическую стойкость. Доля ионной проводимости
этого окисла составляет 70—80% при низкой кислородо-
проницаемости.
Для измерения э.д.с. необходим электрод сравнения,
который должен обеспечивать стабильное
парциальное давление или активность кислорода, обладать
высокой обратимостью, способствовать хорошему контакту
стандартного электрода с электролитом. Кроме того,
электрод сравнения не должен взаимодействовать с
твердым электродом, так как в противном случае в
последнем будет увеличиваться электронная
проводимость. Парциальное давление кислорода над
электродом должно находиться в пределах, при которых в
4* Зак. 664
99
твердом электролите электронная проводимость «е
возникает или не изменяется в процессе измерения.
В качестве электрода сравнения применяют ряд
электродов.
I. Кислородно-платиновый газовый элемент
работает на воздухе, в 02, смесях 02—Аг, Н20—Н2, СО—С02
с переменной активностью кислорода. Применение
газовых смесей с различным парциальным давлением
кислорода дает дополнительные преимущества.
Можно проверять правильность работы ячейки
непосредственно по ходу измерения, использовать
твердый электролит со смешанным характером
проводимости и неизвестной долей ионной проводимости. При
этом активность кислорода измеряется с высокой
степенью точности.
Для обеспечения постоянства парциального
давления кислорода б электроде сравнения платиновую
проволоку необходимо омывать
потоком газа. В противном случае
на границе
кислородно-платинового электрода с твердым
электролитом может образоваться
диффузионный слой с пониженной
активностью кислорода, т. е. э.д.с.
измерительной ячейки может
уменьшиться. Для стабилизации
э.д.с. скорость подачи газа
должна быть не менее 0,2 л/мин.
II. Кислородно - платиновый
электрод, комбинированный со
смесью металл — окисел металла
(например Сг—Сг203),
характеризуется значительной
зависимостью парциального давления
кислорода от температуры,
незначительные колебания которой
приводят к заметным изменениям
э.д.с. Давление кислорода
определяется в соответствии с
реакцией окисления металла: Ме +
+ Ч202=МеО.
На рис. 41 представлен акти-
вометр, разработанный И.
Скалой (ЧССР). Электролитом явля-
Рис. 41. Схема активометра:
1 — железный колпачок; 2 —
таблетка Zr02; 3 —
кварцевый корпус; 4 —
молибденовый токоподвод; 5 -—
набивка из А1203; 6 — железный
токосъемник-электрод; I —
термоизоляция; 8 —
термопара BP 10/15; 9—
пластмассовая втулка; 10 —
картонная труба держателя; 11 —
картонная вставка
100
ется таблетка ZrCb, к которой подведен молибденовый
электрод. Таблетка вварена в кварцевую трубочку, внутрь
которой запрессована смесь из порошка хрома итрехоки-
си хрома. Противоположный конец трубочки
герметизирован огнеупорным высокоглиноземистым цементом. Ак-
тивометр скомбинирован с железным колпачком,
который является токосъемником во время замера
активности. В этой же измерительной головке находится спай
платина-платинородиевой термопары. Все
электрические выводы (их четыре) скомпонованы на штекере,
который вставляется в специальный разъем,
установленный на держателе. Измеренную величину э.д.с.
необходимо корректировать на т.э.д.с., возникающую между
железным колпачком и молибденовым электродом..
Рассчитывают также влияние температуры на
парциальное давление кислорода в реакции 2Сг+3/г02=
=Сг203.
III. Угольно-кислородный электрод. В этом
элементе парциальное давление кислорода определяют по
реакции Сгр+7202=СО. Графитовый стержень
омывается кислородом. Электрод имеет хорошую обратимость
и воспроизводимость, но он может восстанавливать
окисную керамику при высоких температурах.
IV. Электрод из сплава с постоянной концентрацией
кислорода, например из чугуна. Постоянство
концентрации кислорода обеспечивается насыщением металла
углеродом или другим металлом. Насыщение
углеродом осуществляется графитовым стержнем, опущенным
в расплав.
Рассмотрим подробнее метод работы с газовым
электродом. Принципиальная схема ячейки имеет вид:
Pt
pQ Ца1А или Zr02, или MgO ||Расплав ImomhW,
г°*|| * э " ь |[ металла, atoil
где ро2 — парциальное давление кислорода в электроде
сравнения; що] — активность кислорода в исследуемом
расплаве. В приведенной цепи происходит растворение
газообразного кислорода по реакции: 1/202(газ)=[0],
константа равновесия которой
К = а[0]/]//^7. (18)
101
Изменение свободной энергии выражается
уравнением
AG = AG° — RT\nK. (19)
Если гальваническая ячейка работает обратимо, то
AG = —nFE. Подставляя в уравнение (19) константу
равновесия (18), получим
nF nF y/p0t
ИЛИ
ДО0 RT [О]/п
*—ту-туь.^. от
где Е — э.д.с, В. Механизм электродного процесса в
ячейке представлен выше.
Если окисная керамика имеет смешанный характер
проводимости, то расчетная формула имеет вид:
\—t0 nF nF у/ p0i
где /, —доля электронной проводимости, для
определения которой окислительный потенциал в электроде
сравнения задается двумя газами или газовыми смеся*
ми с известным парциальным давлением кислорода;
/1=2. В этом случае:
Е, = AG0 RT [Ol/o
*«
= _ ^! _ — inl01 /о
1-U 2F 2F Yfl0t'
Если температура и произведение [0]fc> постоянны,
то
АЕ RT л V рог
= In
или
0. ч nF &E
- О = А—-. ^г • (22)
102
Для создания
данного парциального
давления кислорода в
электроде сравнения
используют смеси
кислорода, воздуха и
аргона.
Для исследований
активности кислорода
в металле в условиях
плавки в ва;кууме или
в атмосфере
инертного газа изготовлен
вакуумный актинометр
(рис, 42). Схема
опытной установки
представлена на рис. 43.
Корпус активомет*
ра представляет собой
трубу из меди или
нержавеющей стали с
двойными стенками
для водяного
охлаждения. Внизу а-ктиво-
метр .кончается
втулкой для зажима
корундового чехла.
Верхний конец
актинометра снабжен зажимным
устройством, через
которое пропускают
алундовую трубку
диаметром 2 jm-m. Внутри
алундовой трубки
проходит платиновая
проволока— токоподвод к
электроду сравнения. Для обеспечения плотного
контакта платины с поверхностью твердого электролита
нижний конец проволоки запрессовывают в порошок из
А120з или Zr02. Газ подают по корундовой трубке с
постоянной скоростью.
Из-за наличия двух разнородных токосъемников в
цепи возникает дополнительная т.э.д.с. пары Pt—Mo или
Pt—W, противоположная по полярности концентраци-
Рис. 42. Схема вакуумного газового акти-
вометра конструкции МВМИ:
/ — корпус; 2 — гиездо с резьбой; 3, 10 —
уплотнения Вильсона; 4 —
колпачок-электролит; 5 — газопроводящая трубка; 6 —
термопара ПР 30/6; 7 — платиновый
токосъемник; 8 — алундовая соломка; 9 —
контакт токосъемника с колпачком; // —
вакуумная-насадка; 12 — патрубок; 13 —
газовые вводы; 14 — вентиль; 15 —
патрубок для отвода газа; 16 — ко второму
токосъемнику
103
онной э.д.с. ячейки. Поэтому измеряемую прибором
величину э.д.с. корректируют:
Ем = Е +Е
ф изм ' •
(23)
W»S»M
Рис. 43. Схема экспериментальной установки для измерения активности
кислорода в жидком металле (МВМИ):
/ — активометр; 2 — пробник; 3 — токосъемник; 4— пробница; 5— термопара:
6 — нагреватель; 7 — корпус печи; 8 — тигель; 9 — жидкий металл; 10 —
реометр для подачи воздуха; 11 — высокоомный милливольтметр; 12 —
потенциометр
104
где Дф — э.д.с. концентрационного гальванического $ле^
мента; Еиш — измеряемая прибором величина э.д.с;
-Ет.э.д.с. — т.э.д.с. пары Pt—Mo или Pt—W.
Измерительная часть установки состоит из высоко-
омного потенциометра, нормального элемента,
вспомогательной батареи питания и микроамперметра с
чувствительностью 10-9 А/деление, используемого в качестве
нуль-прибора. Может быть также использован высоко-
омный цифровой вольтметр.
Э.д.с. измеряют компенсационным методом при
отсутствии тока в цепи, что исключает влияние
сопротивления самой цепи. Возникающая при этом в гальвани*
ческом элементе э.д.с. компенсируется равной по вели*
чине, но обратной по знаку э.д.с. источника тока
измерительного прибора.
Компенсационный метод измерения активности
кислорода
Большинство электролитов имеет смешанный характер
проводимости. Поэтому необходимо или непрерывно
контролировать долю ионной проводимости
электролита по ходу измерения, или полностью исключить ее
влияние. Это можно осуществить компенсационным
способом измерения.
В схему включается кислородный гальванический
элемент, который используется в качестве
нуль-индикатора. В электроде сравнения задается активность
кислорода, равная активности кислорода исследуемого
электрода. Равенство активностей регистрируется по
нулевому значению э.д.с. ячейки.
На рис. 44 представлена схема устройства,
разработанного Институтом металлургии АН СССР. При
различии активностей кислорода в металле-электроде 1 и
в электроде сравнения 2 развивается э.д.с, величина
которой определяется значением lgPo/ Pot и Долей
ионной проводимости в момент измерения. Знак
указывает на то, в каком электроде активность кислорода
больше. Под действием э.д.с. регулятор 6 изменяет
парциальное давление в электроде сравнения 2 до тех пор,
пока оно не будет соответствовать давлению 02, т. е.
активности кислорода в электроде 1. Э.д.с. будет равна
нулю. Это достигается изменением парциального
давления водяного пара в подаваемой на электрод сравнения
газовой смеси, состоящей из аргона,, водорода и водяно-
105
to пара, По парциальному давлению кислорода в
электроде сравнения, т. е. по активности . кислорода,
определяют активность кислорода в металле.
Г^"
ТУГТТ" 1
Г-
^_
'J Mil L
^ Y
'
prtLr~rLjr:
1 5
-3
-2
-7
Г'
|t[
1 r^-
!/J
i !t
7~]=| 7 ]
С
10
1
T]
/2 |
"T
Рис. 44. Схема устройства для измерения активности кислорода в расплаве,
работающего компенсационным способом:
/ — жидкий металл; 2 — электрод сравнения; 3 — твердый электролит; 4 —
термопара; б — прибор для измерения з. д. е.; £ — регулятор парциального
давления кислорода; 7 — источник водорода; 8 — стабилизатор расхода
водорода; 9 —источник аргона; 10 — стабилизатор расхода аргона; И — источник
водяного пара; /2 — прибор для регистрации активности кислорода; 13 —
регулятор расхода водяного пара; 14 — прибор для измерения температуры
Активности компонентов шлака
Определение активностей компонентов шлака
электрохимическим способом имеет значительные
преимущества перед другими способами. При конструировании
гальванических элементов для работы со шлаком
рекомендуется один из электродов делать газовым —
кислородным, В качестве такого электрода берут либо
графит, контактирующий со шлаком и омываемый
печными газами, содержащими кислород, либо твердую окись
магния или платану.
Другой электрод — это проводник, содержащий
элемент исследуемого окисла. Например, для кремнезема
берут ферросилиций, для глинозема — карборунд и т. д.
Для шлаков, состоящих из СаО, А1203 и Si02,
можно построить, например, следующие цепи:
Fe, Sij
Сплав
fe Ai
Сплав
СаО, А1А, Si02
Шлак
СаО, А1Д, SiOj
Шлак
С или MgO;
С или MgO.
106
В первой цепи электрическая энергия будет
эквивалентна тепловому эффекту реакции с кислородом
газового электрода О*:
[Si] + 20* = (SiO,);
во второй цепи — тепловому эффекту реакции
образования А1203:
2[А1]+3 0*=(А1А).
Т.э.д.с. первого элемента определяется по формуле
^sio, = £sio3 + — In aSi0a.
Fe,Si
CaO, MgO, A1203, SiOJ
CaO, MgO, A1203, Si02,
Fe, Si.
Так как возникают достаточно большие э.д.с,
электрические цепи можно осуществить без переноса.
Чтобы избежать искажающего влияния диффузионного
потенциала, объединяют две химические цепи с
одинаковым составом электродов, но с разными шлаками»
включая составляющие цепи навстречу друг другу.
Например:
С
или
MgO|
Содержание кремния в обоих электродах одинаково,
состав одного из шлаков постоянный, поэтому э.д.с.
цепи равняется разности потенциалов э.д.с. для двух
полуэлементов:
£ = £a_£1=B£L.ln-^2l.
Принимая одну из активностей за стандартную, т. е.
приравнивая ее к мольной доле (а^ю = Nsio2), можно
по э.д.с. рассчитать активность и коэффициент
активности кремнезем-а в любом шлаке, оценить парциальный
изобарный потенциал компонента при переходе его из
стандартного шлака в любой другой АОаьоз^—nFE*.
Для измерения э.д.с. и определения активности закиси
железа в расплавленных шлаках железные электроды
опускали в шлак сверху в специальные отверстия, а
выступающие концы электродов защищали обмазкой из
MgO. Всю ячейку помещали в печь и измеряли э.д.с.
компенсационным методом с применением лампового вольт-
107
метра. Параллельно с электрическими измерениями
брали пробы шлака для анализа. Измеряли э.д.с. цепи:
Fe|CaO, FeO, Si02, MgO, Fe203[MgO.
На железном электроде происходила реакция:
FeMeT—2e=iFe^+, а на кислородном (MgO) имела место
реакция Ом&о+2е=0 ^-. Суммарная реакция элемента
имеет вид: Ре+0Мео = Ре2ш+ +0^ .
Так же можно составить гальванический элемент с
цепью без переноса, т. е. с одинаковыми электродами:
Fe|CaO, MgO, SiOa, FeO, Fea081 MgO | CaO, MgO,
Si02, FeO, Fe203|Fe.
7. КАЛОРИМЕТРИЯ
Калориметрические измерения позволяют получать
данные, необходимые для термодинамических расчетов
высокотемпературных процессов. Применение
калориметрических методов; дае)т необходимые
термодинамические величины, которые трудно, а иногда и
невозможно получать другими способам-и. Наиболее
распространенным является определение теплоемкостей, теплот
реакций, теплот растворения или теплот смешивания.
При смешивании двух чистых компонентов
выделяется теплота, которую называют теплотой смешивания,
или теплотой образования сплава. Для сплава из Na и
NB молей компонентов изменение энтальпии составит:
bHM=HK-(NAH0A+NBH0B),
где Н °А и Н °в — энтальпии чистых компонентов А и
В при данной температуре; Ям — энтальпия сплава.
При растворении 1 моля чистого компонента в
жидкости А при постоянной температуре и определенном
объеме возможен случай, когда концентрация раствора
существенно не изменится и чистая жидкость А
перейдет в раствор АВ. При этом увеличение энтальпии, или
парциальная мольная теплота смешивания компонента
А, составит:
А #л = На — На,
где На — парциальная мольная энтальпия компонента
А в растворе, а Н°А —энтальпия чистого металла.
106
Интегральная теплота смешивания связана с парци«
альными теплотами следующим образом:
AHM = NAAHA + NBbHB,
где NA и NB — мольные концентрации А и В,
Теплоты смешивания и растворения можно
определять либо непосредственно при высоких температурах,
либо при низких температурах, а затем с помощью
закона Кирхгофа рассчитывать тепловой эффект
смешивания при высоких температурах.
Известны два метода калориметрических
измерений: изотермический и адиабатический. Калориметр —
это прибор, позволяющий определять количество тепла,
выделившегося в строго постоянных условиях, путем
измерения изменения температуры системы с известной
энтальпией.
Схема изотермического калориметра приведена на
рис. 45,а. Температура внешнего кожуха
поддерживается постоянной. Калориметрический блок
(внутренний сосуд) изготовляется из высокотеплопроводного
металла, обеспечивающего получение однородной
температуры во всем объеме сосуда. Между внутренним
сосудом и внешней стенкой устанавливают
металлический экран, который предотвращает конвективные
потоки. Кривая изменения температуры, характерная для
экзотермических реакций, показана на рис. 45, б.
В начальный и конечный периоды снижение
температуры подчиняется закону Ньютона: тепловой поток
Время
а б :..л
Рис. 45. Схема изотермического калориметра (а) и кривая изменения
температуры во времени (б):
/ — термометр; 2 — блок калориметра; 3 — экраны; 4 — кожух с постоянной
температурой; 5 — начальный период; 6 — период реакции; 7 — период охлаж»
дсния; 8 — температура кожуха
109
пропорционален разности температур. Изменение
температуры в результате протекания реакции можно
определить с различной степенью точности.
Неточный метод. Кривые начального и конечного
периодов экстраполируют до значения времени,
соответствующего половине второго периода подъема
температуры. При этом разность температур Д/
определяется количеством тепла, выделившегося при реакции.
Точный метод использует закон Ньютона. Если
обозначить через tn постоянную температуру среды, tCp
среднюю температуру в конечный период реакции и 1и
среднюю температуру начального периода, то скорость
снижения температуры составит, °С/с:
Ян = *('.- У. *ср = k (/ср - у, k = (*ср - *н)/(*ср - д,
где k — константа; Ru, #ср — начальная и средняя
скорости снижения температуры.
Снижение температуры вследствие теплопередачи
необходимо добавить к измеренному в опыте
повышению температуры калориметра для получения
откорректированной величины:
где tx — средняя температура в период реакции; 8 —
продолжительность реакционного периода.
Калибруя калориметр для определения постоянной
k, необходимо задать определенные скорости RK и Rc?>
поэтому начальный период в процессе измерения не
является обязательным. Величина tx—tcv обычно
невелика, поэтому изменение окружающей температуры
вносит небольшую ошибку в измерения. При точной
оаботе, когда величина tx—tcv существенна, необходимо
учитывать начальный и конечный участки кривой.
Тогда скорректированная температура выражается
следующим образом:
Тогда общее изменение температуры калориметра
составит:
А 'кал = (t2 — h) + A tKop .
В адиабатическом методе температура внешней
оболочки поддерживается такой же, как и температура
бомбы или блока, т. е. между «ими должен отсутство-
110
вать теплообмен (Д*кор=0), В этом случае увеличение
температуры калориметра прямо пропорционально
тепловому эффекту.
Для калибровки калориметров пользуются понятием
«водяного эквивалента», или «эффективной энтальпии»
калориметра: <7=Ц7дгкал.
При определении теплового эффекта
эндотермических реакций заранее определенное количество металла
известной энтальпии сбрасывают в калориметр.
Эффективная энтальпия калориметра определится
равенством:
где /0—начальная температура образца; сР
—теплоемкость образца. Измерение энтальпии методом
сбрасывания производят, как и'в случае, когда образец имеет
более высокую температуру, чем калориметр.
Для^ измерения теплового эффекта экзотермических
реакций по расположенному внутри калориметра
элементу с известным
электросопротивлением пропускают
ток, сила которого точно
измеряется в определенное
время т. Из соотношения
q = ИШкал = 0,2389^/4 (где | tk
R — сопротивление, Ом; /— c=L
сила тока, А; т —время, с) |
можно определить водяной ^
эквивалент калориметра.
Обычно калориметры
используют для определения
теплоты растворения,
энтальпии, теплот реакции.
Зная зависимость энтальпии
от температуры, легко
вычислить теплоемкость, теплоты фазовых превращений и
теплоту плавления. Теплоты образования и горения
определяют в калориметрической бомбе при постоянных
объемах и избыточном, давлении кислорода.
Для изучения фазовых равновесий и исследования
термодинамических свойств применяют методы
термического анализа, например для определения теплового
эффекта.
Термический анализ производят, нагревая или
охлаждая образец й печи, температура которой измбня-
Врепя
Рис. 46. Кривая охлаждения
образцов (1) при постоянной скорости
изменения температуры печи (2)
1П
ется с постоянной скоростью R (рис. 46). Через
некоторое время температура образца будет отставать от
температуры печи на величину Д/=/?Ср/&. В период
реакции температура образца tc остается постоянной
(линия ВС) у а градиент температуры между печью и
образцом (например, EG) определится из выражения
EG = R (тЕ-тв)+ Rcpfk.
Скорость теплопередачи равна
Интегрируя от хв до Тс, получим зависимость
теплового эффекта от общей величины теплопередачи:
AH=kR Kc 2 B) + Rcp {Tc-xJ.
Тепловой эффект реакции прямо пропорционален
площади BCHF, эквивалентной ДЯ/fe. Эта площадь не
зависит от скорости охлаждения и теплоемкости. Если
теплоемкости равны (c2=ci), то кривая охлаждения
CD' должна асимптотически приближаться к
продолжению BD', и в результате площадь BCD'=AH/k. Если
С2>С\, то кривая охлаждения будет приближаться к
линии ED, соответствующей более высокому значению
теплоемкости с2. В этом случае скрытая теплота
плавления пропорциональна сумме площадей: BEGF-\-
+ECD=AH/k.
По мере возрастания величины теплового эффекта
продолжительность остановки увеличивается. Для
определения теплового эффекта реакции по площади,
замкнутой между кривыми охлаждения, необходимо знать
температуру окружающей среды и величину
коэффициента теплопередачи между образцом и средой..
При высоких температурах, когда теплопередача
осуществляется благодаря радиации, закон Ньютона
справедлив для небольших градиентов температуры.
В целом при высоких температурах этот метод даег
весьма приближенные результаты, так как для
получения точных данных необходимо экспериментально
определить коэффициент теплопередачи при различных
температурах на веществах с известными тепловыми
эффектами, геометрия и свойства поверхности которых
были бы идентичны изучаемым объектам.
112
В дифференциальном термическом анализе два
образца нагреваются совместно в печи при идентичных
условиях нагрева. Затем определяют разность
температур обоих образцов. Преимущество дифференциального
метода в том, что он исключает значительное число
погрешностей.
Метод смешивания
Метод смешивания, или метод падающего тела, применяют
для определения энтальпии, теплот плавления и теплот
превращения. Нагретый образец сбрасывают в
калориметр. Тепло, поглощенное калориметром, эквивалентно
разности энтальпий при начальной и конечной
температурах образца. Из этих данных графическим или
аналитическим путем определяют теплоемкость. Теплоты
превращений и теплоты плавления определяют по
разности энтальпий при температурах выше и ниже точки
перехода путем экстраполяции
соответствующих кривых до
температуры перехода.
В изотермическом водяном
калориметре образец сбрасывают в
резервуар с водой. Блок
калориметра окружен рубашкой, в
которой поддерживается постоянная
температура. Калориметр имеет
хорошую теплоизоляцию.
Изменение температуры в блоке
калориметра измеряют с точностью
±0,0005°С с интервалом 1 мин в
течение периодов нагрева или
реакции до тех пор, пока не
установится постоянная скорость
изменения температуры.
Схема безжидкостного, или
анероидного, калориметра
приведена на рис. 47. Медный блок
погружают в масляную ванну,
находящуюся при .постоянной
температуре. Однородное
распределение тепла в калориметре этого
типа достигается благодаря
высокой теплопроводности металла,
использованного для изготовле-
Рис. 47. Схема анероидного
изотермического
калориметра:
/ — механизм сбрасывания;
2 — образец; 3 — печь; 4 —
заслонка; 5 — медный блок
калориметра; 6 —
изотермический затвор
113
ния блока. По сравнению с калориметром, в котором
водяная баня перемешивается мешалкой, в данном
случае требуется больше времени для установления
однородной температуры.
Калибровку калориметров производят пропусканием
тока известной силы. Зная сопротивление нагревателя,
легко определить водяной эквивалент калориметра.
При работе методом сбрасывания калибровку
производят по образцу с известной энтальпией (чаще всего по
платине).
Печи, используемые при определении энтальпии,
должны иметь длинную изотермическую зону и быть
надежно защищенными тепловой изоляцией от
калориметра. Наиболее важными источниками ошибок
являются операции измерения температуры печи и
получения однородного распределения температуры. В
калориметрах применяют печи сопротивления и
высокочастотные печи. Рекомендуется использовать
вакуумные печи и герметизированный калориметр. Весьма
ответственным является узел передачи образца в
калориметр. Узел имеет теплоизолирующую задвижку с
водяным охлаждением-. Механизм сбрасывания состоит из
подвески на платиновой нити. При пропускании тока нить
нагревается, расплавляется и образец падает в
калориметр.
Образец может быть подвешен также на платиновой
нити к стальному плунжеру. Плунжер связан с
пружиной спусковым крючком. При нажатии на крючок
образец падает вниз. Время падения должно быть
малым, а само сбрасывание во всех случаях идентичным.
Если применяется контейнер для образца, то
необходим холостой опыт для определения поправки на
контейнер.
Основным! недостатком метода падающего тела
является неточность при определении теплового эффекта
в точке перехода. Неточность возрастает, если тепловой
эффект имеет малую абсолютную величину, так как в
этом случае эффект определяется как разность двух
больших величин.
Если исследуемые превращения не воспроизводятся
при охлаждении, то определения энтальпии требуется
проводить в низкотемпературной области.
Обычно теплота реакций при высоких температурах
определяется разностью энтальпий, а теплота реакций
114
при комнатной температуре измеряется
непосредственно в калориметрической бомбе.
Основные ошибки высокотемпературных
определений в первую очередь связаны с точностью измерения
температуры, с получением однородного
температурного поля. Известно, что скорость теплопередачи
пропорциональна площади L2, а скорость изменения
температуры пропорциональна 1/L.
Общие тепловые потери прямо пропорциональны
времени или обратно пропорциональны скорости
теплопередачи и, или 1/uL. Ошибки, возникающие вследствие
неравномерного распределения температуры внутри
калориметра в случае отсутствия перемешивания, про-
порциональны величине uL2.
Прямые измерения энтальпии и теплоты плавления
при высоких температурах могут быть выполнены
двумя способами:
1. Постепенно увеличивают температуру печи, в
которой помещен калориметр, и определяют скорость
теплопередачи к калориметру.
2. Создают такие условия, чтобы температура печи
соответствовала температуре образца и отсутствовал
тепловой поток от калориметра к печи. При этом
измеряют величину повышения температуры и вычисляют
энтальпию образца.
Для адиабатических калориметров необходимо
иметь нагреватель с тонкой регулировкой температуры,
материал нагревателя должен обладать высокой
теплопроводностью. Чтобы уменьшить тепловой поток от
печи к образцу, вокруг образца создают изотермическую
зону с равномерным распределением температуры.
Рекомендуется применять образцы сферической
формы. В некоторых исследованиях используют
цилиндрические образцы, нагреваемые от источника тепла,
расположенного внутри образца. Температуру вокруг
образца поддерживают постоянной. -
Для исключения теплообм-ена между нагревателем
и образцом применяют металлические экраны из
молибдена или никеля. Градиент температуры между
образцом и печью контролируют с помощью
дифференциальных термопар.
Удельную теплоемкость определяют в калориметре,
приведенном на рис. 48. Образец в виде металлического
блока помещают в глиняный контейнер. Нагревание
115
осуществляют путем создания постоянного градиента
температур в стенке тигля. В этих условиях
температура металлического образца равномерная, и
теплоемкость можно вычислять по скорости подъема
температуры, т. е. q*=Smdtfdx, где q — поступление тепла. Эта
величина определяется калибровкой по веществу с
известной теплоемкостью. Такой калориметр может быть
использован и для термического анализа. Наличие
постоянного градиента температуры позволяет точнее
фиксировать остановки или фазовые превращения ре-
Рис. 48. Схема калориметра
для измерения удельной
теплоты:
/ — термическая изоляция;
2 — огнеупорный контейнер;
3 — образец; 4 — подставка;
5 — дифференциальная
контрольная термопара
Время
Рис. 49. Схематическая
кривая калориметрического
опыта
акций. После остановок отсутствуют переходные
участки, где наблюдается плавное изменение кривых, что
позволяет определить меньшие по абсолютной величине
тепловые эффекты.
Для определения теплоты образования сплава его
твердые компоненты помещают в калориметре в
керамический тигель (при комнатной температуре). Затем
116
заливают жидкий компонент. Разность теплоты,
выделившейся при этом, и теплоты, выделяющейся при
охлаждении одного расплавленного компонента,
определяет теплоту образования сплава.
Трудность этого метода состоит в том>, что
необходимо добиваться полного перемешивания компонентов.
Для прямых измерений теплот реакций при высоких
температурах применяют изотермические калориметры,
В этих приборах измерения осуществляют при высоких
скоростях теплопередачи, поддерживая равномерное
распределение температуры, используют ванну из
жидкого олова. Графитовый блок устанавливают в
перемешиваемой ванне. Средняя ошибка измерений
составляет 7—38%.
Адиабатический калориметр используют в сочетании
с индукционной печью, обеспечивающей достаточное
перемешивание компонентов. Тепловые потери на
радиацию и конвекцию компенсируют изменением
расхода энергии. В таком калориметре жидкое железо (29—
45 кг) служит ванной, нагревательным элементом и
растворителем. Потери тепла с поверхности
незначительны. Для калибровки в тигель помещают навеску
железа, энтальпия которого известна. Это позволяет по
изменению температуры определять энтальпию
калориметра. Затем добавляют в ванну исследуемый элемент,
например кремний, и по изменению температуры
рассчитывают энтальпию кремния и теплоту реакции. При
этом учитывают тепловой эффект реакции окисления
кремния кислородом, находившимся в ванне.
Подобным! методом определяли теплоты
растворения элементов в жидком металле. Типичный ход кривой
опыта представлен на рис. 49. На кривой
прослеживаются три периода: начальный (система находится в
стационарном состоянии), главный (происходит нагрев
добавки до температуры расплава и ее растворение) и
конечный (расплав охлаждается и температура
приближается к стационарной в соответствии с законом
Ньютона). Тепловой баланс калориметрической
установки можно выразить уравнением
w (тк-т„) = -(н1*-н1°)-анл-
хк
-k j (Т-Т„) dxf (24)
где W — тепловое значение калориметра, характеризуй
117
ющее количество тепла, которое вызывает изменение
температуры калориметрической системы на 1 К, Дж/К;
(Я дГк—Н т°) — увеличение энтальпии добавки при
нагреве ее от начальной температуры добавки Т0
до температуры расплава Ти, Дж; АЯД — теплота
растворения добавки, Дж; Гк — ^оо — изменение температуры
расплава при сбрасывании добавки, К; k — константа
теплообмена калориметра, характеризующая скорость
теплообмена калориметрической системы с
«изотермической оболочкой» при отклонении температуры от
конвергационной на 1 К, Дж/(К-с).
Левая часть уравнения представляет собой
наблюдаемое увеличение энтальпии калориметрической
системы за главный период опыта, а правая часть —сумму
тепловых эффектов трех процессов, одновременно
протекающих в калориметре и приводящих к изменению
его энтальпии. Имеются в виду нагрев добавки, ее
растворение, дополнительный теплообмен
калориметрической системе с изотермической оболочкой в результате
отклонения температуры от конвергационной.
Методика позволяет учесть вклад процессов,
сопутствующих растворению, и определить величину энталь-
пии растворения. Для вычисления интеграла J (T—
—Too)dx можно использовать графический-метод.
Величину k или отношение k/W определяют в каждом
эксперименте, анализируя конечный участок кривой
калориметрического опыта. В соответствии с законом Ньютона
w ч^[ ; • ^
где Тх и Т2 — температуры расплава в конечный
период, соответствующие'моментам времени %\ и t2-
Градуировку калориметра для определения
величины W проводили путем введения в исходный расплаз
пяти — восьми добавок железа, имевших комнатную
температуру.
Установка состояла из вакуумной печи
сопротивления, системы стабилизации температуры, нагревателя,
системы измерения и автоматической регистрации
температуры расплава и системы очистки и напуска газа.
Схема печи представлена на рис. 50. В тигле помещали
200—300 г металла. Сверху тигель накрывали крышкой
с двумя отверстиями — одно для трубки, по которой
118
сбрасывали добавки, другое для колпачка термопары.
Тигель стоял на подставке, которая вращалась со
скоростью 75 об/мин. Металл перемешивался колпачком
термопары, расположенным эксцентрично.
Рис. 60. Схема высокотемпературного калориметра:
I -»fокопоДводы; 2~ привод вращений тигля; 3 — корпус пе<!й; 4 — Экраны;
5 —• нагреватель; 6 -~ термопара измерительной системы; 7 — натекаТель; 6-±
Дбаатьр; 9 — вакуумные датчики; 10 — тигель с металлом; // — тёрмодатчйк
системы Стабилизации
119
Нагреватель был выполнен йЗ Листового молибдена.
Температуру нагревателя — основного элемента
изотермической оболочки калориметра — поддерживали
постоянной с помощью двухпозиционного
автоматического регулятора. Датчиками служили две последовательно
включенные термопары ВР 5/10. Термопара имела
тщательно термостатированные концы и была включена на
входе потенциометра КИ-59, который служил для
компенсации и измерения основной э.д.с.
Некомпенсированный сигнал, возникавший при
сбрасывании в расплав добавки, подавали на внешнюю
цепь из микровольтамперметра и электронного
потенциометра. Таким образом, отсчет температуры
производили по шкале потенциометра с точностью ±Ю°С, а
отсчет изменения температуры в ходе
калориметрического опыта — по шкале автоматического потенциометра
с точностью ±0,03°С. В случае применения
прецизионного изодромного регулятора температуры можно
поддерживать температуру нагревателя с точностью ±0,ГС.
В результате проведения опытов установлена
теплота растворения кремния, Дж/моль:
Д/Zsi = — 151200 ± 7140
и изменение свободной энергии, Дж/моль Si:
AGs, = — 151200 — 8,997.
Динамический метод
Для исследования динамики выделения тепла в
процессе затвердевания сталей, кристаллизующихся в
интервале температур, метод смешивания непригоден.
В этом случае можно использовать метод динамической
калориметрии. Этот метод исследования состоит в
следующем. Нагретый образец металла помещают в
калориметр и охлаждают с небольшой скоростью. При этом
измеряют понижение температуры образца синхронно с
температурой калориметра. Динамику выделения тепла
устанавливают для интервала температур
кристаллизации. Схема установки представлена на рис. 51.
Калориметрический сосуд изготовлен из латуни толщиной
0,3 мм и заполнен 10 л сухого трансформаторного
масла. Сосуд из листовой стали толщиной 0,5 мм также
заполнен 75 л сухого трансформаторного масла и
служит адиабатной оболочкой. Масло в калориметриче-
120
ском сосуде и оболочке интенсивно перемешивается
трехпропеллерным-и мешалками, вращающимися со
скоростью 1200 об/мин. Разность температур
калориметра и оболочки контролируется дифференциальной
термобатареей из 32 медь-константановых термопар.
В зависимости от э.дх. термобатареи
автоматический терморегулятор обеспечивает необходимую
скорость нагрева оболочки. Нихромовые нагреватели
оболочки изготовлены в виде спиралей и подвешены на
текстолитовых опорах без внешней изоляции, что позволило
свести их инерционность к минимуму. Автоматическая
Рис. oi. Схема динамического калориметра:
/ — калориметрический сосуд; 2 — эбонитовая подставка; 3 — латунный
сосуд; 4 — текстолитовая крышка; 5 — наружный сосуд; 6 — внешний кожух;
7 — асбестовая крышка; 8, 9 — мешалки; 10 — приемный стакан; 11 — пробка;
12, 13 — нагреватели; 14 — дифференциальная термобатарея; 15, 24 —
потенциометры; 16 — регулятор температуры оболочки; 17 — блок магнитных
пускателей; 18 — тигель с образцом; 19 — молибденовый подвес; 20 —
асбоцементный диск; 21 — молибденовый экран; 22 — термопара; 23 —
термобатарея; 25 — источник регулируемого напряжения; 26, 27 — термостаты
121
регулировка обеспечивает равенство температур
калориметра и оболочки с точностью ±0,1° С. Для
измерения температуры калориметрической жидкости
используется термобатарея из трех хромель-алюмелевых
термопар. Контроль температуры образца
осуществляется платина-платинородиевой термопарой.
Градуировку калориметра производят на образцах
железа и никеля. Тепловой эквивалент калориметра
рассчитывают по известным теплотам кристаллизации
и повышению температуры, соответствующему
затвердеванию образца при данной его массе.
Тепловой эквивалент калориметра составил 16250±
±340 Дж/г- Кривую энтальпии тигля, колпачка и
деталей крепления находили по разности
экспериментальных кривых общей энтальпии и энтальпии чистых
металлов, построенных по литературным данным. Во
всех опытах применяли тигли и детали крепления той
же массы, что и при градуировке. Для исследуемых
сплавов строили зависимости изменения температуры
калориметра от температуры образца, по которым
получали кривые изменения общей энтальпии. Вычитая
из полученных величин энтальпии тигля и деталей
крепления, получали энтальпию образцов исследуемых
сплавов.
Выделение теплоты затвердевания в интервале
температур кристаллизации неравномерно.
Кристаллизация замедляется от температур ликвидуса к
температурам солидуса. Теплота кристаллизации данного
сплава, содержащего 0,2% С, равна 15 200 Дж/моль.
8. ИЗМЕРЕНИЯ ДИФФУЗИОННЫХ ХАРАКТЕРИСТИК
В ЖИДКИХ МЕТАЛЛАХ И ШЛАКАХ
Процессы переноса компонента в теле называются
диффузией. Основным условием возникновения
диффузии является градиент концентрации вещества.
Самопроизвольное выравнивание концентрации, т. е.
диффузия, происходит в результате блуждания диффундиру*
ющих частиц.
Поток П компонента через единицу площади
определяется первым законом Фика:
П^~ DdC/dx,
где дС/дх — градиент концентрации компонента в
направлении диффузии; D — коэффициент диффузии, см2/с
122
При постоянном значении коэффициента диффузий
поток компонента и его градиент концентрации связаны
линейно. Одной из основных задач изучения массопере-
носа (вещества является определение коэффициента
диффузии.
Для экспериментального определения коэффициента
диффузии необходимо создать условия постоянного
градиента концентрации. Это условие достаточно трудно
выполнимо. Легче поддается измерению распределение
концентрации вещества вдоль направления диффузии по
истечении определенного интервала времени или
изменение концентрации в какой-либо точке объема с
течением времени.
В этом случае вычисление постоянного коэффициента
диффузии основано на втором законе Фика;
dCfdx = Dd*C/dx*.
Для решения этого уравнения необходимо
определить граничные условия его применения. В простейшем
случае можно представить себе цилиндр постоянного
сечения, разделенный посередине. В момент времени
т=0 в одной его половине (х<0) концентрация всюду
равна Сь а в другой половине (х>0) ^-С* За время
опыта в середине цилиндра должно произойти заметное
изменение концентрации, в то время как на обоих
внешних концах концентрация должна остаться неизменной.
Эти условия соответствуют диффузии в бесконечном
пространстве. Каждая половина цилиндра представляет
собой полубесконечное диффузионное пространство.
Окончательное решение уравнения имеет вид:
с _ d + Ct _ Ci-fr eff / х \ (2б
2 . 2 \2 YDx ] v '
где С — текущая концентрация диффундирующего
вещества; Сх и С2 —исходные его концентрации; х—
расстояние от границы раздела; т — время диффузии.
Пользуясь таблицами функции erf, можно определить
коэффициент диффузии вещества.
Способы определения коэффициентов диффузии
можно разделить на прямые и косвенные. Прямые методы
основаны' на применении уравнений диффузии, а
косвенные— на измерении электрических характеристик.
По сравнению с твердым телом измерение
коэффициентов диффузии в жидкости осложняется явлениями
конвекции, которые усиливаются градиентом температу-
123
ры. Следует учитывать также возможное возникновение
поверхностной диффузии вдоль стенок сосуда, в котором
находится расплав. Рассмотрим прямые методы
определения диффузионных характеристик.
Капиллярный метод с использованием
радиоактивных изотопов
Расплавляют металл или шлак в огнеупорном
капилляре. На поверхность расплава помещают тонкий
слой жидкого шлака или металла, обогащенного
радиоактивным изотопом элемента, диффузию
которого изучают. Капилляр помещают в печь с
равномерным температурным полем и выдерживают
определенное время. После выдержки капилляр с расплавом
закаливают. Из столбика металла или шлака нарезают
образцы длиной несколько миллиметров и подвергают
радиохимическому анализу. В этом методе
обеспечиваются условия диффузии из плоского постоянного
источника в полубесконечное пространство.
Распределение элемента подчиняется уравнению
с^х)--у^иТе ' (27)
где х — расстояние от верхнего мениска образца; Q —
начальное количество радиоактивного изотопа.
Коэффициент диффузии определяют по углу
наклона прямой в координатах In С — х2. Угловой
коэффициент прямой l/4Dt позволяет определить значение Z).
Разновидностью этого метода является применение
двух капилляров, например для определения
коэффициента диффузии в шлаке. В одном капилляре
помещают исследуемый расплав, не содержащий примеси, в
другом — расплав, «помеченный» радиоактивным
изотопом. Капилляры помещают в печь и выдерживают при
определенной температуре, приводя в соприкосновение
открытые концы капилляров. После некоторой
выдержки капилляры закаливают и анализируют распределение
элемента в них. Уравнение диффузии имеет вид:
С = С0/2 (\-ex!2V]rx),
где Со — начальная концентрация изотопа в одном капи-
ляре; С —концентрация изотопа на расстоянии х за
время отжига т.
124
Основными недостатками этого метода являю1*сй
конвективное перемешивание, искривление поверхности
раздела между активным и неактивным шлаком,
трудность установления точного времени отжига.
При использовании метода «стриженой» границы
концы капилляров закрепляют в двух вращающихся
пришлифованных друг к другу дисках. В капилляры
помещают навески шлака, одна из которых «помечена»
радиоактивным изотопом. Диски помещают в печь таким
образом,- чтобы оси (капилляров не сов/надали. i Послъ
расплавления смеси в капиллярах и установления
термического равновесия диск поворачивают до
совмещения отверстий капилляров. При этом срезаются
мениски расплавов у поверхности капилляров, т. е. границу
раздела образцов можно считать плоской и точно
фиксировать момент начала диффузии. Расчет ведут, как и
в предыдущем методе.
Метод капилляра с резервуаром
Схема метода приведена на рис. 52. В большом
резервуаре / находится расплав с определенной
концентрацией примеси. В капилляре 2 находится расплав без
Рис. 52. Схема метода
определения коэффициента
диффузии методом капилляр —
резервуар:
/ — тигель с металлом; 2 —
капилляры; 3 — держатель
капилляров; 4 — термопара;
5 — печь
примеси. По достижении системой заданной
температуры капилляр опускают в жидкость, находящуюся в
резервуаре. Так как объем жидкости в резервуаре
значительно больше, чем в капилляре, то концентрация
примеси Со (В резервуаре во время диффузионного опыта
будет оставаться практически постоянной.
125
Таким образом, диффузия в капилляре будет
проходить при граничном условии, когда je=0, C0=const.
Отметим, что в большом резервуаре влияние конвекции
на диффузию устраняется. Коэффициент диффузии
определяется из уравнения
где Сх — концентрация диффундирующей примеси на
расстоянии х от открытого конца капилляра; С\ и С0 —
начальная концентрация компонента в капилляре и его
концентрация в большом объеме.
Приведенные выше капиллярные методы имеют ряд
специфических погрешностей. Главная из них —
конвекция расплавов. Конвекция происходит вследствие не*
равномерности температурного поля печи,
неоднородности состава ванны, вибрации опытной установки и т. п.
Для устранения конвекции необходимо создавать
постоянное температурное поле с разностью температур
между верхней и нижней частями капилляра 3—б°С.
Температура верха должна быть выше температуры
низа. Диаметр капилляров допустим от 2 до б мм.
Смеси в 'капиллярах располагают так, чтобы тяжелый
компонент диффундировал снизу вверх, а легкий —
сверху вниз.
Для выявления картины распределения изучаемого
элемента в капилляре после диффузионного отжига с
успехом применяют радиоактивные изотопы. В этом
случае для подсчета распределения элемента в столбике
шлака или металла требуется значительно меньше
вещества, чем для химического анализа. Кроме того,
метод посекционного сканирования позволяет вообще
отказаться от проб из образцов. Для анализа
распределения радиоактивности в столбике применяют также
метод авторадиографии.
Для секционного определения распределения
активности столбик шлака или металла распиливают на
дольки, из которых приготовляют порошки, просчитываемые
на счетчике.
Наконец, капилляр с застывшим веществам можно
перемещать вдоль блока со щелью, за которой стоит
счетчик. Постепенно перемещая образец, измеряют
радиоактивность всех его слоев.
126
Метод вращающегося диска
Для устранения влияния явления конвекции был
предложен метод вращающегося диска. Этим методом
(рис. 53) можно исследовать диффузию вещества,
слабо растворимого в данной жидкости. Исследуемое
вещество наносится на торец вращающегося диска радиу-
Рис. 53. Схема определеяия коэффициента диффузии методом вращающегося
диска:
/ — цилиндрический образец; 2— огнеупорная обойма; 3 — алуидовый
стержень; 4 — центрирующая муфта; 5 — вал редуктора; б — импульсный счетчик;
7 — датчик; 8 — электродвигатель; 9 — печь сопротивления; 10 — тигель с
расплавом; 11 — алундовая подставка
са R. Диск вносят .в расплав и вращают в нем
некоторое время. Жидкость в резервуаре приходит в
движение. По мере приближения к поверхности диска
угловая скорость вращения жидкости возрастает до тех пор,
пока не сравняется с угловой скоростью вращения дис-
127
ка. Если имеет место обменная реакция вещества
диска с расплавом, то возникает тонкий диффузионный
слой между поверхностью диска и жидкостью, в
котором течение жидкости происходит ламинарно. Толщина
этого слоя зависит от молекулярных свойств расплава,
скорости потока и от природы диффундирующего
вещества. Скорость перехода данного компонента в расплав
из диска не должна лимитировать процесс;
определяющим звеном процесса насыщения жидкости является
диффузия элемента в жидкости. Коэффициент
диффузии находят из уравнения
/ = 0,62DVe v-v«(0,/2Co, (28)
где / — скорость растворения; v—кинематическая
вязкость жидкости; со— угловая скорость вращения диска;
Со — концентрация насыщения расплава. Отсюда
дУ, ^ 1,62 m vi;'
S х ©1/2 С0 '
где т — количество вещества (г), перешедшего в
раствор за время т; S — площадь диска. Для нахождения
коэффициента- диффузии строят график зависимости
скорости растворения от величины о)1/2. Коэффициент
диффузии D определяется наклоном прямой на этом
графике.
Для исследования диффузии железа в шлаках
наносят на поверхность диска слой радиоактивного
железа. Поток радиоактивного железа с поверхности
вращающегося цилиндра пропорционален равновесной
концентрации в шлаке, прилегающем к поверхности
твердого тела.
Для малого времени опыта поток вещества равен:
n = fiDxCx0Tt (29)
где Dx —коэффициент самодиффузии железа в
твердом образце; Я — количество вещества, перешедшего
из диска в шлак за время т через единицу поверхности
диска, И1мп/(мин-см2-с); h — постоянная; С\ —
концентрация насыщения шлака.
Для большого времени опыта поток вещества равен:
2 Vi>% — гх
128
или
л-(*'У!—r)«-
(30)
Если построить график в координатах /—|Ч, то
прямая линия отсекает на оси ординат отрезок, равный
С J/Л, а угловой коэффициент прямой равен 2CJYDT/
/УяГ
Косвенные методы определения коэффициентов
диффузии
Эти методы сводятся к поляризации электродов
переменным или постоянным током. Для шлаковых систем
при поляризации переменным током определяют
омическое и емкостное сопротивления электродов. В общее
омическое сопротивление г0бщ, помимо диффузионного
сопротивления гд, входят и другие составляющие, но
графически можно найти гд. Это делают с помощью
графика в координатах г0бщ и (о1'8 (со — частота
переменного тока), учитывая, что, только диффузионное
сопротивление зависит от частоты тока.
Диффузионное сопротивление следующим образом
связано с коэффициентом диффузии:
RT
гд — 2аЯС
где Z — заряд иона; С
—концентрация потенциалопределяющих
ионов в электролите; со — частота
переменного тока; F—аюстоянная
Фарадея. В этой методике
используют постоянный ток. Прибор
состоит из большого резервуара и
капилляра (рис. 54). Постоянный i
ток пропускают между электро- *Рис 54
дами I, a
II измеряют с ломощью компен
сационного метода.
После включения постоянного
тока в капилляре начинается
злектроперенос зарядов 'путем диффузии ионов
скольку концентрация в резервуаре
5 Зак. 664
Схема ячейки для
раЗ'НОСТЬ ПОТеНЦИаЛОВ определения коэффициентов
диффузии методом
поляризации постоянным током:
/ — графитовый тигель; 2 —
расплав; 3—-капилляр; 4 —
расплав в капилляре; 5 —
электровводы
По-
входе в
129
и при
капилляр остается постоянной, то средний состав
расплава в капилляре изменяется до некоторого
равновесного постоянного значения. Электросопротивление
расплава в капилляре R определяют, зная силу тока и
падение напряжения в капилляре. Если R0 и #Ст —
электросопротивление расплава в капилляре соответственно
до пропускания тока и в стационарном состоянии, то в
координатах R— т наклон линии определяется
равенством: a=dR/dx и a/(RcT — Ro):=2D/l2' (где ./ — длина
столбика в капилляре).
Разновидностью косвенного электрического метода
является метод поляризации электрода. Так как
поляризация в окисных шлаках носит концентрационный
характер, то по величине предельной силы тока можно
судить о коэффициенте диффузии иона,
разряжающегося на электроде. Величина предельной силы тока равна:
lnp = nFD4> uj* v~1/e лГ1/а Со, (31)
где п — число электронов для разрядки иона;
F—постоянная Фарадея; ы0 — скорость движения жидкости
относительно электрода; v — кинематическая вязкость
шлака; х — расстояние рассматриваемой точки
электрода от точки в электролите; С0 — исходная
концентрация диффундирующего иона.
При добавке исследуемой примеси не более 3%
величины u0, v, х можно считать постоянными. Исходные
атомные концентрации С0 потенциалопределяющих
ионов также одинаковы. В этих условиях величина
предельной силы тока определяется коэффициентом
диффузии:
где
K = Fy4^-4*x-xuC0.
По значению inp определяют величину,
пропорциональную коэффициенту диффузии. Достоинство метода
состоит в устранении влияния конвекции. Этим
методом исследовали диффузию Ti, Si, Nb, В, Zr, Fe, Mn,
Co, Ni в шлаке. Катодом служило расплавленное железо
или медь, анодом — платиновая проволока. Электрод
сравнения представлял собой платиновую проволоку,
130
проходившую внутри корундовой трубки, через которую
продували кислород. Потенциал такого электрода в
шлаковых расплавах устойчив. Токоподводами служили
вольфрамовые проволоки, нерастворимые в меди.
Площадь электрода вычисляли по диаметру проволоки.
Рис. 55. Схема электрохимической ячейки (а) и установки для определения
коэффициента диффузии кислорода потенциометрическим методом (б):
/ — чехол из корунда или двуокиси циркония — твердый электролит; 2 — ме-
таллокерамический токосъемник; 3 — жидкий металл; 4 — покрытие из
платины; 5 — платиновая проволока — токосъемник; 6 — печь сопротивления с
герметичной внутренней трубой нагрева; 7 — высокоомный милливольтметр; 8 —
потенциометр; 9 — потенциостат
При потенциостатическом определении
коэффициентов диффузии кислорода в жидких металлах
используется электрохимическая ячейка (рис. 55): PtPo I
|2г02эл-т+СаО|Л1е'р0 , где р'0 —парциальное
давление кислорода в электроде сравнения; р"0 — активность
кислорода на границе раздела твердый электролит —
исследуемый расплав. Для этой ячейки э.д.с. можно
выразить уравнением
Бели к электродам ячейки приложить напряжение
■Ег, то концентрация кислорода в исследуемом расплаве
5» Зак. 664
131
металла Me" на границе раздела металл — твердый
электролит изменится и станет равной p'Q :
Е2 = In —тг1- .
Таким образом, концентрация кислорода в жидком
металле Me" на границе раздела металл — твердый
электролит будет отличаться от концентрации
кислорода в объеме металла. Вследствие этого возникнет
перенос кислорода из исследуемого расплава в среду с
постоянным парциальным давлением кислорода (в
электрод сравнения) или наоборот, в зависимости от
знака и величины приложенного напряжения £2.
Диффузионный перенос кислорода будет происходить до тех
пор, пока перепад концентраций кислорода в жидком
металле Me" не станет равным нулю.
Во время диффузии кислорода в цели будет
протекать ионный ток, величина которого зависит от
коэффициента диффузии кислорода в металле и от разности
При использовании твердого электролита в виде
огнеупорного колпачка диффузия кислорода в жидком
металле подчиняется второму закону Фика для
цилиндрических координат:
i^L = JL -i_(rDo^O, (32)
дх г дг \ дг )
где С0 — концентрация кислорода в металле, %; Do —
коэффициент диффузии кислорода в металле, см2/с; г —
внутренний радиус капилляра см. После ряда
преобразований уравнение (32) при дится к виду:
,м. 2,4052/ . , о /ооч
In 1ион = '■ (- In p , (33)
т
где t=r?/Do; т — время; {$ — постоянная. Зависимость
1шИон от времени имеет прямолинейный характер.
Тангенс угла наклона прямой равен: tga=—5,76Do/r2. Из
этого соотношения можно вычислить Do.
Для исследования металлов с относительно низкой
температурой плавления наружный электрод сравнения
выполняют из платинового покрытия.
При работе с железом^ и никелем в качестве
электрода сравнения можно применить расплав с постоянной
активностью кислорода — никель или железо. Токопод-
13-2
водом к жидкому металлу служит металлокерамика из
АЬОз с молибденом.
Применяли капилляры внутренним диаметрам 5 и
длиной 250—300 мм. Высота столба жидкого металла
в капилляре составляла 80—100 мм. Тигель с
расплавом, имеющим постоянную активность кислорода,
помещали на огнеупорной подставке в реакционной зоне
печи сопротивления. Для устранения конвективных
потоков жидкого металла в капилляре градиент
температуры по высоте столба металла поддерживали в преде-
л ах 5°С. Опыты проводили в атмосфере аргона.
Были получены следующие значения коэффициен-
1600 1600
тов диффузии, 10"4 см2/с: DlQ]Fe =1,4; £[0]ж ^=0,95;
Д[О]Си=6,0.
Волюмометрический метод определения коэффициентов
диффузии водорода и азота в жидких металлах
Для определения диффузионной подвижности газов
в жидких металлах использовали капиллярный
волюмометрический метод. Диффузионная ячейка для
проведения опытов представлена на
рис. 56. В реакционной трубе 1,
проходящей внутри графитовой
печи сопротивления, расположен
цилиндрический тигель с
металлом 2. В расплав на
определенную глубину погружают
капилляр 3. Через верхний конец
капилляра к поверхности расплава
подают азот или водород. Снизу
тигель с металлом обдувается
потоком чистого аргона.
В момент времени т=0
концентрация газа в металле внутри
капилляра в сечении А—А
определяется его парциальным
давлением в атмосфере над расплавом.
При рн2, n2=100 кПа
содержание газа в металле соответствует Рис 56 Схема ячейки для
ТерМОДИНаМИЧеСКОИ раСТВОрИМО- определения коэффициента
сти газа при данной температуре. ^мФУме7ОДОмВОЛЮМОметриче*
м2,н.
133
В момент времени т = 0 и по прошествии
определенного времени т концентрация газа в металле в сечении
капилляра В—В равна нулю. Если считать, что столб
жидкого металла в капилляре является
полубесконечным диффузионным пространством для времени т, то
для указанных граничных условий решение второго
закона Фика дает выражение
Си-
- 1—erf
ЫЫ • <34>
где х — расстояние от поверхности раздела газ —
металл; т — время диффузии; С— концентрация газа в
точке х диффузионного пространства; С0—начальная
концентрация газа в металле; Сп—растворимость
газа при данной температуре и парциальном давлении
газа 100 кПа.
Интегральное решение этого уравнения приводит к
равенству
:р-Со = 2 /Dt
п — Со L т я
где Сср — средняя концентрация газа в столбике
расплава в (момент времени т; L — высота расплава.
Представим Сср в виде массы абсорбированного за
время т газа, отнесенной к массе жидкого расплава,
находящегося в капилляре:
Сср= „> 100,
~~4~~ L Рм
где V — объем абсорбированного газа, см ; рг, рм —
плотность газа и плотность металла, г/см3; d — диаметр
капилляра, см; L — высота столба металла, см.
Если принять, что С0=0, то в окончательном
решении уравнение примет вид:
v mjr • <35)
Из этого выражения можно получить величину
коэффициента диффузии. При этом отбрасывают
начальный момент термического расширения газа и
парциальное давление газа поддерживают равным 100 кПа.
134
Схема опытной установки представлена на рис. 57.
Тигель с расплавом помещают на огнеупорной
трубчатой подставке в реакционную зону печи сопротивления.
Реакционную зону формируют с помощью корундовой
трубы диаметром 40 и длиной 1000 мм. Через верхнюю
крышку печи вводят абсорбционный корундовый
капилляр диаметром 4—6 мм. Верхний его конец с помощью
резинового шланга соединяют с линией подачи газа.
Рис. 57. Схема установки для определения коэффициентов диффузии Н2 и
N2 волюмометрическим методом:
/ — баллон с Нг; 2 —ротаметр; 3 — колонка с ангидроном; 4 — колонка с
цеолитом; 5 —колонка с палладированным алюмогелем; 5 — барботеры ртутно-
амальгамной очистки; 7 — колонка со стекловатой и СаС12; 8 — масляный
манометр; 9 — вакуумные краны; 10 — реометры; // — ртутный манометр; 12 —
винтовой механизм; 13 — ртутная микробюретка; 14 — контрольный масляный
манометр; 15 — масляный барботер; 16 — датчик ЛТ-2; 17 — абсорбционная
трубка; 18 — верхняя крышка печи; 19 — реакционная трубка; 20 —
графитовый нагреватель; 21 — блок теплоизоляции; 22 — тигель с исследуемым
расплавом; 23 — термопара; 24 — корпус печи; 25 — нижняя крышка печи; 26 —
прибор для измерения температуры; 27 — вакуумный насос; 28 — печь q
титановой губкой; 29 — баллон с Аг
Газ поступает из баллона 1 через ротаметр 2,
отградуированный с точностью 0,01 мл/мин. Давление газа
контролируют с помощью U-образного манометра // и
масляного манометра 8. Измерение объема газа,
абсорбированного металлом, в течение опыта производят с
135
помощью ртутной микробюретки объемом 4 см3 с
ценой деления 0,005—0,002 см3. Открытый конец
микробюретки соединен с ртутным резервуаром, который
перемещается микровинтом вверх или вниз.
Опыт заключается в следующем. После загрузки
металла, откачки установки, нагрева и расплавления
металла в реакционное пространство подают аргон.
После выдержки и достижения заданной температуры
в абсорбционную трубку вводят исследуемый газ (расход
0,03—0,04 см8/мин при давлении 2,5—3,0 кПа).
Абсорбционная трубка находится на уровне 200 мм над
металлом. Затем ее медленно, в течение 1 мин, опускают в
тигель. В момент касания металла в тигле трубкой
фиксируют верхний уровень металла, и абсорбционную
трубку опускают в расплав на глубину 50—80 мм.
Сразу же .после этого закрывают подачу газа в
абсорбционное пространство и соединяют абсорбционную трубку
с масляным манометром и микробюреткой.
Перемещая уровень ртути в микробюретке,
устанавливают давление в замкнутой системе
абсорбционная трубка — масляный манометр — микробюретка,
равное 100 кПа. С момента погружения абсорбционной
трубки в металл начинают отсчет времени. Фиксируют
изменение объема газа в системе во времени, т. е.
измеряют скорость абсорбции газа расплавом,
находящимся в абсорбционной трубке, пр.и давлении 100 кПа.
Для вычисления коэффициента диффузии газа
строят график зависимости объема абсорбированного газа
V от времени т (рис. 58). Тангенс угла наклона прямой
представляет собой коэффициент диффузии газа. В
условиях эксперимента при
опускании абсорбционной
трубки в расплав
происходит первоначальное
термическое расширение газа.
Фактический процесс
представлен линией ОЕ'С. Участок
ОЕ' характеризует
суммарный процесс: абсорбцию и
термическое расширение
газа.
Чтобы исключить из
дальнейшего рассмотрения
данные, относящиеся к пе-
Рис. 58. Зависимость изменения
объема поглощенного газа от вре-
136
риоду расширения газа, проводят холостые опыты. В
качестве инертного газа используют гелий или аргон.
Расширение инертного газа, закончившееся через
некоторое время, показано линией OEF. Так как наклон
линии, характеризующей процесс абсорбции газа, не
зависит от выбора нулевой точки по оси ординат, за начало
процесса можно принять точку £, соответствующую
времени окончания термического расширения газа, и
провести линию Е"ВУ параллельную линии Е'С. Расчеты
производят для линии ОА, полученной переносом линии
Е"В в начало координат.
По мере распространения диффузионной волны от
поверхности .металла в капилляре к его нижнему концу
концентрация растворенного газа у нижнего конца
капилляра изменяется в соответствии с расчетным
уравнением. При его выводе принято, что концентрация
газа в капилляре в сечении В—В (см. рис. 56) после
протекания времени т равна нулю, поэтому следует
ожидать, что на графике V—У% будет наблюдаться
отклонение от линейности. Специальные опыты позволяют
установить время, когда концентрация газа в сечении
В—В начинает сказываться на результатах опыта.
Время достижения некоторой концентрации газа у
конца капилляра в сечении В—В пропорционально
квадрату высоты расплава в капилляре.
Этим методом получены следующие значения
коэффициентов диффузии водорода и азота в жидких
металлах при 1600°С, см2/с: Отоа=Л,\Ь-1(У-2\ D[H]C0 =
= 3,3-10-3; 0[H]Fe =1,68-1 (И; D[H]Ni =1,47-10-3;
£>[N]Fe =7,68-10"5; D[NlN. =10,6- Ю-4.
9. ПОВЕРХНОСТНЫЕ СВОЙСТВА ЖИДКИХ РАСПЛАВОВ
Поверхностные свойства жидких расплавов в
металлургических процессах имеют не меньшее значение, чем
объемные.
Поверхностное натяжение жидких металлов и
шлаков, смачивание металлом шлака, огнеупоров во
многом определяют взаимоотношение этих фаз. Адгезия
стали к продуктам раскисления характеризует
скорости выделения их из металла и,перехода в шлак.
Для образования новой поверхности раздела
необходима затрата определенного количества энергии, эк-
137
Бивалентной силе на единицу длины поверхности (10~5Н/
/см). Для жидкости поверхностная энергия равна
поверхностному натяжению. Чтобы увеличить поверхность
раздела одной фазы в объеме другой, необходимо
совершить работу
6A = ApdV = odS,
где Ар — градиент давления; V — объем; о —
поверхностное натяжение; S — поверхность.
Для капли жидкости сферической формы: dV=
= 4nR2dR; dS = 8nRdR и Ap-=o8nRdR/4nR2dR = 2o/R.
Если форма капли жидкости несферическая, то
Лр = а (1/7?! + 1//« , (36)
где /?! и /?2 — главные радиусы кривизны.
Большинство методов определения поверхностного
натяжения жидких расплавов основывается на
использовании последнего уравнения. Остановимся на
главных способах определения поверхностных
характеристик.
Метод висящей капли
Этот метод часто применяют для исследования
тугоплавких металлов с температурой плавления выше
2000°С. Существо метода заключается в том, что
проволоку известного диаметра нагревают электронным
лучом до образования на ее конце капли, которая
удерживается силами поверхностного натяжения. Как
только эти силы сравняются с весом капли, она отрывается
от конца проволоки. Существует вариант этого метода,
в котором жидкий' металл вытекает из конца
огнеупорной трубки. Вес капли G уравновешивается силой
поверхностного натяжения 2пга (где г — радиус
трубки; о — поверхностное натяжение).
Висящую жидкую каплю фотографируют в
момент, предшествующий отрыву, и определяют по
негативу или его проекции радиус на границе твердой и
жидкой частей образца. После затвердевания каплю
взвешивают. Точный расчет о производят с помощью
таблиц.
Недостаток метода заключается в том, что вес
оторвавшейся капли меньше веса висящей капли,
т. е. требуется соответствующая поправка. Точность
138
измерения можно повысить, если определять радиус
шейки капли в момент отрыва, когда силы
поверхностного натяжения уравновешивают вес капли.
Трудность метода состоит также в смачивании
металлом стенок трубки. Если жидкость смачивает стенки
трубки, то капля получается больше равновесной, и
наоборот. В том и другом случае трудно правильно
выбрать расчетный радиус.
Метод капиллярного подъема
Если опустить капилляр в смачивающую жидкость, то
жидкость в капилляре поднимается на некоторую
высоту, зависящую от поверхностного натяжения
кривизны мениска и плотности расплава. Высоту можно
рассчитывать по формуле
, 2 a cos 0
h= ,
gr (р2 —Pi)
где рь р2 — плотности газа и жидкости; в — краевой
угол смачивания жидкостью материала капилляра;
г —радиус капилляра; g — ускорение силы тяжести.
Основной недостаток этого метода состоит в том,
что необходимо знать краевой угол смачивания. Для
проведения опыта важно обеспечить правильную
геометрическую форму капилляра.
Метод отрыва кольца или пластины
Если на поверхности жидкости расположить пластину
или кольцо, то усилие отрыва Р этих предметов от
поверхности жидкости будет пропорционально
поверхностному натяжению и радиусу R кольца или
пластины: <ji=P/4nJR.
Для кольца большого радиуса и любой толщины с
прямоугольным поперечным сечением в случае, если
жидкость не смачивает кольцо, необходимо
пользоваться сложным уравнением Тихановского,
учитывающим краевые углы смачивания.
Недостаток метода заключается в трудности
доказательства того, что краевые углы смачивания,
полученные в других условиях, совпадают с углами
смачивания при использовании данного метода. Этот
метод трудно применить для высокотемпературного
139
эксперимента. С его помощью определяли величины
поверхностного натяжения таких легкоплавких
сплавов, как магний — алюминий, алюминий — медь.
Метод лежащей капли
При контакте двух жидких фаз межфазное натяжение
равно разности поверхностного натяжения для чистых
жидкостей. При контакте жидкости с твердым телом
жидкость растекается по его поверхности, образуя
каплю.
Для определения поверхностного натяжения
измеряют контуры капли жидкости на твердом
материале или профиль капли, лежащей на другой жидкости,
например шлака на металле.
Методика, исследования сводится к расплавлению
капли металла на горизонтальной огнеупорной
подложке. Для нагрева пользуются трубчатыми печами
сопротивления или индукционными печами. Плавку
проводят в вакууме или в атмосфере нейтрального
газа.
Каплю фотографируют или делают рентгеновский
снимок. С помощью диапроектора изображение капли
увеличивают на экране, измеряют ее геометрические
параметры и по ним рассчитывают: поверхностное
натяжение, краевой угол смачивания, межфазную
энергию, работу адгезии и т. п. По массе капли и по
вычисленному объему можно определить плотность
вещества.
Краевой угол смачивания по формуле Лапласа
равен
cos6= ат.г~ат.ж 9 (37)
аж.г
где 0Т.Г — поверхностное натяжение на границе твердое
тело — газ; <огт.ж — то же, твердое тело — жидкость;
<*ж.г — то же, жидкость — газ. Если ат.ж><*г.г, то
краевой угол более 90°. Если <тт.ж<<51г.г, то краевой угол
меньше 90°. Если ат.г=огт.ж + йк.г, то металл будет
смачивать поверхность подложки. Межфазная энергия
может быть определена из краевого угла и
поверхностного натяжения жидкости, если известна поверхностная
энергия твердого тела. Если она неизвестна, но остается
постоянной, то изменения межфазной энергии в
зависимо
мости от состава или температуры могут быть получены
расчетом переменных по уравнению: ат.ж=Ю'т.г—спж.гСОэО.
Поверхностное натяжение получают решением
уравнения поверхности капли:
о (l//?i + 1//?2) - (Pl - р2) g х + 2 а/Я0, (38)
где а — поверхностное или межфазное натяжение на
границе раздела фаз; Rx и R2 — главные радиусы
кривизны элемента поверхности в рассматриваемой точке;
/?о — радиус кривизны в вершине капли; р2 — плотность
среды, в которой находится капля; pi —плотность
вещества капли; g —ускорение силы тяжести; я
—координаты точки на поверхности капли по вертикальной
оси.
С. И. Попель предложил приближенное графическое
интегрирование этого уравнения. Если считать каплю
симметричным телом вращения относительно оси х
(рис. 59), то достаточно определить лишь координаты
точек контура капли. Если по координатам точек
составлено уравнение кривой ху то для любой ее точки
радиус кривизны выразится сложным
дифференциальным уравнением. Метод расчета состоит в
приближенном графическом интегрировании основного уравнения
поверхности капли.
6 т. ж бт.г
Рис. 59. Схема капли металла на твердой подложке (а) и геометрия
лежащей капли (б)
Поверхностное натяжение можно также
рассчитывать по формуле: o = a2pg, где а2— квадрат
капиллярной постоянной; р — плотность; g — ускорение силы
тяжести. Величину а2 определяют по координатам точек
контура капли.
Главными источниками ошибок являются
несимметричность капли, отклонение ее от тела вращения. Чем
141
ближе форма капли к телу вращения, тем она должна
быть меньше и тем труднее определять ее размеры.
Существует метод определения поверхностного
натяжения с применением таблиц для расчета по
уравнению
о (i^ + ^^^ + S (Рж-Рг) г, (39)
где /?i — радиус, проведенный в вершине капли; z —
вертикальная координата; х — горизонтальная
координата; ф — угол, образуемый радиусом кривизны в
данной точке и осью вращения.
Экспериментальной трудностью метода лежащей
капли является необходимость соблюдения строго
горизонтального расположения капли и совпадения
оптических осей фотоаппарата и объекта. Чаще всего печь
и фотокамеру устанавливают на одной оптической
скамье (рис. 60). Водоохлаждаемый корпус печи вместе
с нагревателем откатывают в сторону по рельсам,
открывая доступ к подложке. Подложка расположена
на молибденовой или ниобиевой подставке,
укрепленной в корундовой трубе, которая закреплена в стальной
трубе. Съемку капли можно вести как с помощью
пленочного фотоаппарата, так и на пластинку. Точность
съемки на пластинку выше. Увеличение на пластинке
или на пленке находят по съемке эталонного образца с
известными размерами.
Рис. 60. Схема установки для измерения плотности и пове'нлностного
натяжения металлических расплавов:
/ — печь сопротивления; 2 — фотокамера; 3 — оптическая скамья; 4 —
нагреватель; 5 — предохраняющая задвижка; 6 — уплотнение Вильсона; 7— опора;
8 — фланец; 9 — винтовой держатель; 10 — корундовая трубка; // — горячий
спай термопары; 12 — капля; 13 — экран; 14 — токоподвод
142
Большой точности можно добиться, применяя
рентгеновскую съемку контура капли. На опытной
установке производили съемку капли с экспозицией 20—40 с с
расстояния не более 35 мм в интервале 1000—1800° С.
Источник рентгеновского излучения (аппарат УРС-55)
позволяет получать рентгенограммы с резкоочерченным
контуром капли.
Применяли цилиндрические образцы .массой 1—3 г.
Расплавление и выдержку до установления
температурного равновесия производили в атмосфере гелия.
Параметры капли измеряли на микроскопе УИМ-21 с
точностью 0,00015 см.
При определении межфазного натяжения жидкого
шлака и металла каплю шлака помещают на каплю
жидкого металла или жидкий металл помещают в шлак
и производят рентгеносъемку. Капля жидкого шлака
формируется на металле в виде линзы (рис. 61),
нижняя часть которой погружена в металл. Для учета
этого С. И. Попель применил определенную систему
уравнений.
Рис. 61. Схема
капли шлака, лежащей
на металле
Принимая, что Z_a=0, <хш.г sin© — ам.ш sinp = 0 и
аш.г oos6 + aM.iii C<>SP— сПм=0. Решение этих уравнений
позволяет определить
ам.ш = (сгш sin6)/sin p;
ам.ш = {Ои-Ош cos 9) i/ 1 + ( °ш$1пЬ й)\
у \ <7М — °ш cos 6 /
Для измерения межфазного натяжения на границе
шлак — железо каплю шлака помещали на жидком
железе, для чего из графитовой трубки на поверхность
расплавленного железа выдавливали аргоном каплю
изучаемого шлака. Фотографирование капли осуществляли
пленочным фотоаппаратом. После проектирования кон-
143
Металл
тура капли на диапроекторе определяли краевой угол
контакта и объем капли.
Более сложным является метод рентгеносъемки.
В печи сопротивления с угольным нагревателем
располагали тигель, в который помещали 10 г металла и 30 г
шлака. Для просвечивания печь имела горизонтальный
канал, закрытый с торцов слюдой. Рентгеновская трубка
имела свинцовую диафрагму для ограничения пучка
лучей. На противоположном конце печи строго
вертикально устанавливали кассету с рентгеновской пленкой
и свинцовый экран. Калибровку производили с помощью
шарика определенного размера.
Достоинства метода лежащей капли обусловили
широкое применение этого способа. В расчетные
формулы определения поверхностного натяжения не входит
величина краевого угла смачивания, который может
быть определен в этом же опыте наряду с
поверхностным натяжением. Исследования можно проводить в
вакууме и в газовой атмосфере. Метод позволяет
получать весьма точные и надежные результаты для
большинства металлов и сплавов.
К его недостаткам относятся трудоемкость расчетов,
трудности при исследовании сплавов, содержащих
компоненты с высокой упругостью пара.
Для получения точных результатов следует
тщательно измерять профиль капли, добиваться строго
горизонтального ее положения для получения тела
вращения правильной формы. Необходимо принимать строгие
меры против загрязнения металла капли, так как
малейшие примеси влияют на результаты. Для
применения этого метода необходимо иметь каплю достаточно
больших размеров. В. Н. Еременко и В. И. Ниженко
предложили метод большой капли для точного
определения поверхностного натяжения жидкостей,
смачивающих и не смачивающих материал подложки.
На рис. 62 приведена схема профиля большой капли.
В отличие от рассмотренных выше способов, когда
капля жидкого металла покоилась на плоской подложке, в
этом методе капля жидкого металла находится в
огнеупорной чаше с ровными острыми краями,
образующими правильную окружность для гарантии точной
симметрии капли. Часть капли, выступающую из чаши,
легко сфотографировать и измерить ее геометрические
параметры. Краевой угол 9 зависит от степени смачива-
144
ния материала чаши жидкостью, а — угол среза кромки
чаши. Устойчивая капля образуется в широком
диапазоне значений угла q>, определяемого неравенством
а<чр<в. Угол а может быть легко доведен до 10—20°,
-ез
Е1чч\чччч\\\1?1
Рис. 62. Схема
большой капли
профиля
Рис. 63. Схема установки для
измерения плотности металлов
методом капли во взвешенном
состоянии:
/ — уплотнения; 2 — индуктор; 3 —
жидкий металл; 4 —
стабилизирующее кольцо; 5—9 — оптическая
система для съемки капли металла
кинокамерой; 10 — керамический
шток; И — основание
поэтому данный метод можно применять и для
жидкостей, значительно смачивающих материал чаши.
Точность измерений достигает 0,5%.
Метод капли во взвешенном состоянии
Расплавляемая капля «подвешивается» в
электромагнитном поле. Схема установки приведена на рис. 63.
Капля, принимает сферическую форму под влиянием сил
поверхностного натяжения, так как отсутствуют силы
гравитации. Капля находится в состоянии непрерывного
движения под влиянием энергии, связанной с
образованием поверхности, и кинетической энергии движения,
связанной с наличием электромагнитного поля.
Математически обоснована теория осцилляции формы капли,
основанной на малых вибрациях жидкой массы вокруг
сферической равновесной формы. Симметричные
вибрации капли могут быть подсчитаны, частота осцилляции
в отсутствие гравитации функционально связана с
поверхностным натяжением. С помощью скоростной кино-
145
съемки фиксируют движение кашш. Затем проектируют
полученные изображения на экран и, зная скорость
съемки, определяют частоту осцилляции, т. е. время,
за которое происходит полный цикл изменения ее
формы. Расчетное уравнение имеет вид:
0 = 4/з Я т <°2 ,
где а — поверхностное натяжение; т — масса капли;
со — частота осцилляции в секунду. Массу капли
определяли взвешиванием после опыта. Температуру
измеряли оптическим способом.
Метод максимального давления в пузырьке газа
Капилляр, изготовленный из материала, инертного по
отношению к расплаву, погружается в жидкий шлак
или металл. Через капилляр продувается инертный газ
Стружка Л / J
Аг
Рис. 64. Схема установки для определения поверхностного натяжения шлака:
/ — капилляр; 2 — крепление капилляра; 3 — микрометр; 4 — наклонный
манометр; 5 — печь Таммана; 6 — шлак; 7 — ввод термопары
146
и измеряется максимальное давление, необходимое для
отрыва пузырька с конца капилляра (рис. 64).
Общее давление, при котором образуется пузырь,
равно гидростатическому давлению и силе
поверхностного натяжения. Давление в пузырьке равно, Па:
p = (2o/r) + gh (рж —ft),
где h — глубина погружения капилляра; рж и рг —
плотность расплава и газа; г — радиус капилляра,
который определяет размеры пузыря, соответствующие
градиенту давления; <j, — поверхностное натяжение.
Давление р равно давлению в манометре p = g#pM
(здесь Н — высота столба жидкости в манометре; рм —
ее плотность; g — ускорение силы тяжести).
Пренебрегая величиной рг, получим:
(2ог/г) + £АРж = £#рм;
o = (rg/2) (Ярм-Лрж)- (40)
Конец керамического капилляра затачивают на
«нож», чтобы иметь известный радиус капилляра.
Так как форма пузырька отклоняется от
сферической, то в измеряемую величину радиуса капилляра
необходимо вносить поправку. Предложено пользоваться
методом последовательных приближений и с помощью
капиллярной постоянной находить правильный
расчетный радиус капилляра. Если а — капиллярная
постоянная, г — фактический радиус капилляра, х —
исправленный радиус капилляра и Л — максимальное давление
газа в пузырьке, то в первом приближении а\ —rh\y a
во втором а\х =x\h\. По первому равенству находят
отношение г/а и с помощью таблиц определяют xjr.
Полученное значение Х\ подставляют во второе
уравнение и находят значение ац и т. д. Обычно после второго
или третьего приближения значения х становятся
постоянными и х подставляют вместо г в формулу (40).
На рис. 65 показана схема установки для
определения поверхностного натяжения металлов методом
максимального давления в пузырьке. Опыты проводили
в вакуумной печи сопротивления.
На крышке печи смонтирован механизм для
перемещения капилляра, шлюз для отбора проб и введения
добавок, ввод термопары и смотровое стекло. Газ
продували через корундовый капилляр диаметром 6 мм.
Перемещение капилляра измеряли индикатором ^асово:
147
го типа с точностью 0,01 .мм. Момент касания капилляра
поверхности металла определяется по искажению его
отражения в зеркале металла вследствие изменения
кривизны отражающей поверхности. Точность фиксации
этого момента составляла 0,05 мм,
Рис. 65. Схема установки для измерения поверхностного натяжения жидких
металлов:
/ — печи с медной стружкой и с титановой губкой; 2 — поглотители с
жидким литием; 3 — емкость; 4 — резиновая камера; 5 — индикатор часового
типа; 6 — тензометрический датчик давления; 7 — механизм перемещения
капилляра; 8 — шток с пробницей; 9 — медная водоохлаждаемая фурма; /0 —кран;
//—крышка; 12 — нагреватель; 13 — капилляр; 14 — тигель; /5 — термопара;
16 — потенциометр регистрации давления в пузырьке; 17 — мановакуумметр;
18 — потенциометр регистрации температуры; 19 — потенциометр регистрации
температуры в печах газоочистки
Газ к трубке подавали через игольчатый натекатель.
Давление в газовом пузырьке измеряли датчиком,
состоявшим из четырех тензосопротивлений из фольги.
Два тензосопротивления наклеены на измерительную
пластинку, связанную с чувствительной «мембраной,
вторые два сопротивления образуют с первыми
электрический мост, сигнал от которого поступает на потен-
148
циометр. Точность измерения таким прибором
составила 1,5 Па.
К недостаткам метода следует отнести
необходимость подбора нейтральных по отношению к расплаву
капилляров (особенно при работе с агрессивными
шлаками при высокой температуре). Разрушение
капилляра не позволяет выбрать правильный расчетный радиус
и понижает точность измерения.
Достоинство метода заключается в хорошей
теоретической разработке и обосновании, в возможности
исследования различных расплавов, в высокой его
точности.
Метод продавливания
Этот метод применяют для исследования тугоплавких
металлов. Измерение поверхностного натяжения
основано на определении силы,
возникающей при
вдавливании графитового щупа
в поверхность жидкости.
Сила деформирует
упругий элемент, на котором
подвешен щуп и
соответствующие тензодатчики.
Возникающий при этом
сигнал усиливается,
подается на осциллограф и
измеряется. Схема
установки показана на рис. 66.
Внутри камеры печи
8 расположен медный во-
доохлаждаемый поддон У,
на котором в лунке 2
расплавляют
электронным пучком
.металлический образец.
Электроны испускаются кольцевым катодом 7. Графитовый щуп
3 подвешен на танталовом стержне 6, прикрепленном к
упругому элементу 5, на который наклеены
тензодатчики. Датчики подсоединены к обмотке выходного
трансформатора усилителя. Щуп перемещают механизмом 4.
При соприкосновении щупа с расплавом датчики под
воздействием деформации меняют сопротивление,
вследствие чего происходит разбаланс моста. Сигнал усили-
Рис. 66. Схема установки для
измерения поверхностного натяжения
методом продавливания
149
теля, пропорциональный измеряемой деформации,
подается на шлейфовый осциллограф. Перед опытом датчики
тарируют и строят градуировочный график.
Поверхностное натяжение рассчитывают по формуле
a=yyLcos6, (41)
где F0— сила смачивания; L — периметр смачивания;
9 — краевой угол смачивания.
10. ПЛОТНОСТЬ ЖИДКИХ РАСПЛАВОВ
Установление зависимости плотности расплава от его
состава и температуры позволяет сделать определенные
заключения о структуре жидкости. Все структурные
превращения сопровождаются изменениями плотности.
Исследование плотности позволяет уточнить строение
сложных растворов. Для измерения плотности
используют различные способы.
Метод гидростатического взвешивания ,
Метод основан на законе Архимеда. В жидкий расплав
опускают поплавок. Измеряя силу, выталкивающую
поплавок, можно вычислить плотность расплава. При
вычислениях необходимо
учитывать термическое
расширение поплавка,
поверхностные, силы между
поплавком, подвеской и
расплавом, искажающие
подъемную силу.
Поплавок не должен взаимодей-
Я ствовать с расплавом.
Рис. 67. Схема установки для
определения плотности расплавов методом
гидростатического взвешивания:
g 1 — жидкий металл; 2 — тигель; 3 —
колпачок термопары; 4 — ввод
термопары; 5 — поплавок; 6 — шток с
противовесом; 7 —термопара; 8 — силито-
вые стержни; 9 — пробка печи; 10 —
кварцевая трубка; 11 — микроскоп;
12 — шлюзы; 13 — огнеупорная
футеровка; 14 — динамометр; 15 —
терморегулятор
160
На рис. 67 показана схема установки, с помощью
которой определяли плотность расплавов жидкого
ферросилиция. Корундовый поплавок 5 объемом 10—20 см3
на штоке с противовесом 6 подсоединен к динамометру
14. Перемещение стрелки динамометра по шкале
отмечается с помощью оптического устройства.
Для измерения плотности шлака применяли шарик
из сплава платины с 20% Rh. В железном тигле
расплавляли шлак и погружали bi него шарик, 'имевший объем
1,86 ам3 и массу 35 г. Шарик на платиновой проволоке
был подвешен к коромыслу весов, расположенных над
печью. Вначале прогревали пустой тигель, доводя его до
заданной температуры, затем насыпали шлак и после
его расплавления надвигали на печь весы с шариком,
который опускали до уровня шлака. С помощью
зеркала центрировали шарик над шлаком. Затем с помощью
специальной передачи поднимали тигель со шлаком
таким образом, чтобы шарик опустился в шлак. При
этом измеряли новый вес шарика. Сразу же после
опыта шарик помещали в концентрированную соляную
кислоту и после высушивания взвешивали и измеряли
размеры.
Метод дилатометра
Этот метод основан на измерении высоты расплава,
помещенного в тигель известных размеров. Используют
уравнение для плотности расплава:
p = 4G/7tD2tf, (42)
где G — масса расплава; D — диаметр тигля; Я —
высота расплава в тигле.
Тигель с жидким металлом (рис. 68) подвешен на
двух молибденовых проволоках к корпусу установки.
Через верхнюю головку печи проходит шток, в котором
укреплены контактные молибденовые стержни,
измеряющие уровень расплава. Снаружи шток соединен с
микрометром. Один из стержней электрически
изолирован от штока и имеет вывод на омметр. Второй полюс
подсоединен к корпусу прибора. При достижении
стержнями уровня металла цепь замыкается. Чтобы
молибденовые стержни не растворялись в металле, они
замыкаются через дно корундовой лодочки, покрытое
графитом или листочком фольги; при всплывании поплавок
151
Рис. 68. Схема установки
для измерения плотносги
жидких металлов:
/ — жидкий металл; 2 —
средняя часть печи; 3 —
молибденовая подвеска; 4 —
молибденовые стержни,
измеряющие уровни расплава;
5 — графитовый нагреватель;
6 — экран; 7 — корпус печи;
8 — термопара; 9 — верхняя
съемная часть установки;
10 — уплотнения; 11 — виль-
соновское уплотнение; 12 —
подвижной шток; 13 —
микрометр; 14 —
ампервольтметр; 15 —
лодочка-поплавок
замыкает контакт. Объем тигля
измеряют три комнатной
температуре, строят график
зависимости емкости тигля от уровня
жидкости, наливаемой в тигель, и
после опыта по уровню расплава
определяют объем жидкого
металла.
Метод пикнометра
Этот метод состоит в том, что
взвешивают твердый металл,
заполнивший в жидком состоянии
известный объем сосуда,
называемого пикнометром. Объем
пикнометра определяют с помощью
ртути. Важнолодобрать материал
пикнометра, не
взаимодействующий с расплавом. В качестве
пикнометра можно исполызовать
либо закрытый сосуд, сделанный из
графита или корунда, либо
тигель.
Металл расплавляют в
корундовом тигле так, чтобы мениск
металла выступал над краем
тигля. По достижении определенной
температуры на тигель опускают
плоскопараллельный
магнезитовый диск, который выдавливает
избыток металла, оставляя в
титле количество металла,
соответствующее объему тигля. После
охлаждения и кристаллизации
металл взвешивают и
рассчитывают плотность.
Для расчета термического
расширения тигля применяют
известные коэффициенты расширения
или проводят специальные
измерения коэффициентов
расширения. Точность определения
плотности этим способом 0,5%.
152
Метод проникающего излучения
Этот метод относится к числу бесконтактных методов и
пригоден для работы с агрессивными расплавами. Он
дает возможность быстро получать результаты.
Сущность метода состоит в следующем.
Интенсивность у-излучения, прошедшего через слой металла
толщиной dy можно определить без учета рассеяния:
/ = /о*-*р-', (43)
где /0 — интенсивность падающего пучка, имп/с; / —
интенсивность потока излучения. перед прохождением
через металл, имп/с; \l — массовый коэффициент
поглощения, см2/г; ро — плотность металла, г/см3; d —
толщина образца, см.
Пусть плотность металла в результате изменения
температуры или действия легирующих получила
приращение, г/см3: р=р0+Ар, где ро — плотность чистого
металла при определенной температуре; Ар —
приращение плотности; р — плотность металла при другой
температуре или после введения присадки. Тогда, используя
формулу (43), получим:
/ = /0<ГМ(Ро + др) (44)
или /1 = /0е",1Р#£|, (45)
где / — интенсивность проходящего излучения при
начальной температуре или при работе без присадок;
1\ — интенсивность излучения при данной температуре с
присадкой легирующего.
Подставляя равенство (45) в уравнение (44),
получим
I = I1e-ll*pd (46)
или после логарифмирования:
In Д — In /0 = — ц ро d; (47)
In/ — In Л = — jiApd. (48)
Разделив уравнение (48) на (47), получим
Др==Ро Jn^L. (49)
V V In Л/Л, v ;
Формула (49) позволяет рассчитать изменение
плотности жидкого и кристаллизующегося металла, если
известна плотность металла при какой-то температуре.
Для твердого металла с учетом его сжатия или
расширения в направлении ^-излучения можно получить только
153
2/з величины изменения плотности. Чтобы получить
истинную ее величину, результат следует умножить на
3/г, т. е.
Дртв=А p'-HL/ZZL, (50)
V 2 К° In IJIo
где Pq —плотность твердого металла, рассчитанная
при какой-то температуре.
При использовании метода необходимо знать
коэффициенты линейного расширения тигля. Недостаток
метода состоит в том, что отсутствует строгое
соотношение числа импульсов и плотности. Кроме того, имеет
место эффект рассеивания.
Опытная установка Ю. Н.. Кармалина для работы по
этому методу состоит из плавильной печи, источника и
приемника излучения
(рис. 69). Источником
излучения служит
радиоактивный изотоп
137Cs, обладающий
интенсивностью 2 г-экв.
Для регистрации
потока излучения
использовали электронный
датчик УСД-1, усиленный
сигнал которого
поступал на пересчетное
устройство ПП-15.
Образец в алундовом тигле
помещали внутрь
графитового нагревателя.
Нагрев и расплавление
образца при -измерении
плотности осуществляли в атмосфере гелия.
Конструкция установки позволяет присаживать модификаторы без
разгерметизации печи. Присадки вводили на алундовой
соломке в пакете из фольги в количестве от 0,01 до 0,2%
при установившемся температурном режиме.
Измерение плотности до ввода добавок производили
в течение 8—10 мин после установления стабильной
температуры и в течение 10—15 мин после ввода
добавок (каждые 100 с). Время фиксировали высокоточным
кварцевым счетчиком времени пересчетного прибора.
Точность измерения плотности составляла 0,2%.
Рис. 69. Схема установки для
определения плотности металлов методом
проникающего излучения:
/ — источник излучения; 2 — регистратор
излучения УСД-1; 3 — пересчетное
устройство ПП-15; 4 — тигель; 5 — блок
питания; 6 — коллиматор; 7 — графитовый
нагреватель; 8 — подставка; 9 — кожух печи;
10 — контактные пластины
154
Метод лежащей капли
Особенности этого метода рассмотрены выше. Объем
капли металла определяют по ее геометрическому
контуру, а массу — взвешиванием твердой капли.
Используют также и метод большой капли, помещаемой в чаше.
Количество жидкости, помещенной в чаше,
должно превышать внутренний ее объем, чтобы избыток
металла образовывал каплю над чашей. В этом случае
в основании выступающей капли будет окружность, т. е.
в расчет можно принимать предварительно
калиброванный объем чаши.
Выступающий объем капли можно рассчитать
достаточно точно. Объем металла внутри чаши
определяют по объему собственно чаши, которая
калибруется, например, ртутью. В качестве материала для чаши
можно использовать графит, окись бериллия, корунд.
Общая масса капли достигает 40—60 г, что повышает
точность определения плотности до ±(0,2—0,5),%.
Так же как и в методе пикнометра, в данном случае
необходимо учитывать расширение чаши во время
нагрева.
Достоинство метода заключается в отсутствии
контакта металла с измерительным прибором.
Объем капли можно получить суммированием
элементарных объемов, на которые ее делят. Профиль
капли делят на сегменты и шаровые слои. Объем
каждого сегмента находят отдельно. Точность определения
равна ±(0,2—0,5),%.
Разновидностью метода лежащей капли является
метод капли во взвешенном состоянии. Схема
экспериментальной установки для определения плотности
металла приведена на рис. 63. Образцы жидкого металла,
«подвешенного» в индукторе, фотографируют с помощью
скоростной кинокамеры. Специальной оптической
системой фиксируют горизонтальный и вертикальный контуры
капли, используя только те снимки! капли, ось которых
совпадает с осью индуктора.
Расчет плотности производят по увеличенным
изображениям капли, которая имеет яйцевидную форму,
удобную для расчета. Таким методом могут быть сняты
характеристики высокореакционных металлов,
взаимодействующих с огнеупорной футеровкой.
155
Метод максимального давления газа в пузырьке
Методом максимального давления газа в пузырьке
можно определить плотность жидкости. Для этого
измерения производят на двух уровнях, фиксируя положение
капилляра микровинтом. Плотность рассчитывают по
формуле
р = РмД///ДЛ, (51)
где рм — плотность жидкости в манометре; Д# —
изменение столба жидкости в манометре при погружении
капилляра на глубину h. Так как при погружении
капилляра уровень расплава .в тигле изменяется, то <в
формулу (51) рекомендуется подставлять исправленное
значение Л:
* = *'(' + -«£г)- <52>
где Л7 —глубина погружения капилляра по
микровинту; /н — наружный радиус капилляра, см; R —
внутренний радиус тигля, см.
11. ВЯЗКОСТЬ РАСПЛАВОВ
Для выбора правильной технологии металлургического
процесса и для оценки способа удаления примесей из
расплавленных металлов большое значение имеет
знание вязкости металла и шлаков различного состава и
зависимости вязкости от температуры.
Вязкость металлических расплавов определяет
скорость диффузионных процессов, протекающих в жидком
металле. Процессы, происходящие при затвердевании
слитков и отливок, неразрывно связаны с вязкостью
жидкого металла. Вязкость, так же как и плотность,
является структурно чувствительным параметром
жидкого состояния. А. М. Бачинский установил зависимость
вязкости жидкости от свободного объема, т. е. от
строения жидкости.
Вязкость обратно пропорциональна свободному
объему. Чем больше свободный объем, т. е. чем разря-
женнее структура жидкости, тем жидкость более текуча,
ее вязкость меньше. Я. И. Френкель, основываясь на
теории о дырочном строении жидкости, разработал
теорию вязкого течения, согласно которой в жидкости
156
передвигаются только активированные атомы, для
течения которых необходимо образование «дырок» в
жидкости. Для жидкости в ламинарном режиме течения
применимо выражение Ньютона:
Р = Ч (dV/dy) S,
где Р — сила, необходимая для перемещения слоя
жидкости и направленная параллельно потоку; dV/dy —
градиент скорости в направлении у, перпендикулярном
движению; S — площадь; г\ — коэффициент
динамической вязкости, г/(см-с). Вязкость измеряют в пуазах
О П = 0,1 Н-с/м2). В отличие от динамической вязкости
коэффициент кинематической вязкости обозначают v,
см2/с (л? = г]/р, где р — плотность, г/см3). Кинематическая
вязкость измеряется в стоксах (м2/с). Коэффициент
вязкости связан с энергией активации Е вязкого течения:
ц = АеЕп/«г.
Величина вязкости, ее температурная зависимость,
энергия активации процесса перемещения в
значительной мере зависят от структуры жидкости. Вязкость
большинства шлаков подчиняется уравнению Ньютона.
Для определения вязкости при высоких температурах
используют стационарные и нестационарные методы.
Последние (метод крутильных колебаний Швидковско-
го, метод затухающих колебаний, метод параболоида
вращения) основаны на .измерении параметров системы,
находящейся в контакте с исследуемой жидкостью в
процессе крутильных колебаний. Рассмотрение начнем
со стационарных методов.
Метод падающего шарика
Если шарик не взаимодействует с жидкостью, то при
стационарном движении его в неограниченно вязкой
среде вязкость жидкости можно рассчитать по формуле
Стокса:
Ч - Ч^ <*&=** — . (53)
(l+2.3^)(l+3,lf) '
где рш— плотность шарика; рж — плотность жидкости;
г — радиус шарика; R — радиус сосуда, в котором
падает шарик; L — длина сосуда; v — скорость
равномерного движения шарика.
Этот метод характеризуется большими эксперимен-
157
тальными трудностями при высоких температурах:
большой размер прогреваемого резервуара; требование
точной сферичности шарика, инертного к жидкости;
способ наблюдения за движением шарика в непрозрачной
жидкости.
Метод капиллярного истечения
В этом методе измеряется объем жидкости,
протекающей по капилляру, соединяющему два широких
резервуара. Объем жидкости определяется по изменению ее
уровня в резервуарах. Вязкость рассчитывается по
формуле Пуазейля:
T] = 7r^Ap/8Q/,
Кдакуум-^
насосу
К хронографу
/с Оакуум-
j насосу
Рис. 70. Схема капиллярного
вискозиметра:
/ _ резервуар; 2 — тигель; 3 — пень
сопротивления; 4 — экран; 5 —
контакты хронографа; 6 — термопары;
7 — капилляр
(54)
где R — радиус
капилляра; Ар —разность
давления на концах капилляра
относительно одного
уровня; I — длина капилляра;
Q — объем жидкости,
протекающей в единицу
времени.
Необходимо пользо-
!ваться достаточно
длинными капиллярами, чтобы
свести к минимуму
поправки на кинетическую
энергию струи жидкости,
связанную с разностью
давлений в капилляре.
К недостаткам
данного метода относятся: не
полностью теоретически
обоснованное движение
жидкости при входе в
капилляр, характер
движения, краевой эффект,
связанный с 'переходом
жидкости от нулевой
скорости 'перед капилляром к
конечной скорости :в
капилляре.
На рис. 70
'представлена схема капиллярного
вискозиметра для работы
158
-в вакууме и в контролируемой атмосфере. Отсчет
времени наполнения калиброванного сосуда производил-и по
разрыву электрической цепи жидкий металл —
контакты. Основная трудность заключается в очистке металла
от нерастворимых шримесей и в изготовлении ва'куум-
плотното (высокоогнеупорного капилляра.
Метод концентрических вращающихся цилиндров
Исследуемую жидкость помещают между двумя
концентрическими цилиндрами. Внешний или внутренний
цилиндр вращается, жидкость увлекается силами
внутреннего трения или вязкости и замедляет вращение
цилиндра. Величину вязкости (Н-с/м2) рассчитывают
по уравнению
п = м R2~r* (55)
4яи(/ + с) £2 г2 '
где М — крутильный момент вращающегося цилиндра,
г-см2/с2; / — длина цилиндра, см; с — поправка на
влияние концов, см; со — угловая скорость вращения, с-1;
R — внутренний радиус тигля, см; г—внешний радиус
тела вращения, см.
Наиболее просто измерения осуществляются путем
относительного определения вязкости — калибровкой.
В качестве градуировочной жидкости используют
различные масла, растворы, вязкость которых хорошо
изучена. Тогда вязкость определяют по отношению
ц = КМ/(й, где К — постоянная прибора; М — момент
вращения.
Вискозиметры этого типа могут иметь гибкую и
жесткую подвески внутреннего цилиндра. В первом
случае во вращение приводится наружный цилиндр, т. е.
тигель, в котором находится расплав. Вращение
передается на внутренний цилиндр — шпиндель — благодаря
вязкости жидкости. По углу закручивания нити, на
которой подвешен внутренний цилиндр, и определяют
вязкость. Путем несложных преобразований получают:
Ti = /C6/(D, (56)
где К— константа прибора, включающая жесткость
подвески; о — угловая скорость вращения; 6—угол
закручивания.
159
Константу прибора рассчитывают
с помощью жидкости известной
вязкости. Угол закручивания
определяют оптическим способом.
На нити (подвеске) укрепляют
зеркальце, на 'которое падает
пучок света. Для повышения
чувствительности прибора шкалу для
светового зайчика значительно
удаляют от зеркальца. На рис.71
показана схема вискозиметра с
вращающимся наружным
цилиндром (тиглем) и
неподвижным внутренним (шпинделем).
Молибденовый тигель,
обмазанный глиноземистым цементом,
помещен в графитовый тигель.
Шлак плавят в молибденовом
тигле. Сверху в печь проходит
графитовый шпиндель, на конце
которого укреплен цилиндр из
молибдена. Шпиндель через
переходник подсоединен к корундо-.
вой подвеске с зеркальцем, на ко-
которой намотана проволочная
спираль. Спираль помещена в
поле постоянного магнита. Тигель
с расплавом вращается снизу
специальным приводом со
скоростью 50 об/мин. Крутильный
момент шпинделя
уравновешивается пропусканием тока через
спираль, помещенную в магнитном
поле. При равновесии
крутильный момент М пропорционален
силе тока /, проходящего через
нить:
(57)
пропорциональности; К —
константа вискозиметра. Тогда вязкость
л = /с7/е-//©.
Так как константа К является функцией глубины
погружения шпинделя, то строят зависимость отношения
Рис. 71. Схема
вискозиметра с вращающимся тиглем:
/ — опорные стойки; 2 —
корундовая труба; 3 —
подставка тигля; 4 — двигатель;
5 — редуктор; 6 — передача
вращения тиглю; 7 —корпус
печи; 5 —засыпка из
ламповой сажи; 9 — графитовый
шпиндель; 10 — спирали из
Mg—A1; // — магнит; 12 —
зеркало; 13 — крепление
нити; 14 — нить; 15 —
центровые подвески; 16 —
молибденовый нагреватель; 17 —
призма для измерения
температуры
где К! — коэффициент
160
//© от глубины погружения для градуировочной
жидкости и затем определяют вязкость любой жидкости:
Ч--7ТГ"^£' (58)
\ <0 /г.ж
где (//(о)г.ж—отношение, эквивалентное глубине
погружения для градуировочной жидкости, а (//о) —
отношение для изучаемой жидкости при той же глубине
погружения; Е — поправка на термическое (расширение
молибденового цилиндра.
Приборы с гибкой подвеской обладают высокой
чувствительностью, но весьма капризны, так как нить
теряет упругие свойства и требуется центровка
шпинделя.
Вискозиметры с жесткой подвеской шпинделя более
компактны, в них не требуется строгая центровка нити.
Шпиндель приводится во вращение электродвигателем.
Вязкое сопротивление жидкости вращению
шпинделя оказывает влияние на усилие двигателя.
Вязкость определяют по изменению электрических
характеристик электродвигателя. Момент трения на валу
двигателя пропорционален вязкости жидкости, если
отсутствует турбулентное течение. Для регистрации изменения
силы тока обмотку двигателя включают в
измерительную схему.
Общий недостаток вискозиметров данного типа
состоит в том, что биение шпинделя изменяет
воспроизводимость показаний. Трение в подшипниках и щетках
двигателя снижает чувствительность приборов в области
малых вязкостей, К преимуществам ротационных
вискозиметров относятся: широкий диапазон измерений
вязкостей (10~2—10~3 Н-с/м2), высокая точность
измерения, непрерывное перемешивание расплава в тигле.
Схема ротационного вискозиметра показана на
рис. 72. Электродвигатель приводит во вращение
молибденовый шпиндель, на конце которого насажена
цилиндрическая головка диаметром 7 и длиной 11 мм.
Электрическая схема вискозиметра представляет
собой измерительный мост. В одно плечо моста включен
электродвигатель постоянного тока без обмотки
возбуждения, в другое — сопротивление.
Перед тем как производится измерение вязкости при
вращении шпинделя на воздухе мост сопротивления
уравновешивают. Опускают шпиндель в расплав и вклю-
6 Зак. 664
161
чают показывающий прибор. Сопротивление шлака
вращению тормозит двигатель. Нагрузка на его валу
повышается, в нулевой цепи появляется ток, который
фиксируется указывающим гальванометром или
микроамперметром. Величина тока и
характеризует вязкость
среды.
Скорость вращения
двигателя должна быть
выше определенной
величины, иначе возникает
биение шпинделя. Число
оборотов на воздухе
составляет 400—500 в
минуту. Когда шпиндель
погружается в среду с
большой вязкостью (15—20
Н-с/м2), скорость
вращения уменьшается до 2—
3 об/мин.
Прибор градуируют по
■касторовому маслу или
по буре в зависимости от
диапазона измерений. В
промышленном
вискозиметре ЭВИ-57 измеряют
не силу тока в обмотках
двигателя, а угол между
вектором приложенного
напряжения и э.д.с,
индуктируемой в обмотке
статора синхронного двигателя под влиянием
приложенного к шпинделю момента, обусловленного вязкостью.
Скорость вращения шпинделя поддерживают постоянной
(250 об/мин).
Точность измерения вязкости этим вискозиметром
составляет ±1,5—2%. При измерении расплавов с
низкими значениями вязкости погрешности возрастают.
Рис. 72. Схема ротационного
вискозиметра:
/ — электродвигатель; 2 — эластичная
муфта; 3 — стальной валик; 4 —
подшипники; 5 — штатив; 6 —
молибденовый шпиндель; 7 — тигель со шлаком;
8 — головка шпинделя; 9 — енлитовые
нагреватели
Вибрационный метод
Принцип этого метода состоит в том, что амплитуда
вынужденных колебаний шпинделя, погруженного в
расплав, зависит от вязкости среды. Это весьма точный
162
метод, чувствительность которого повышается с
уменьшением вязкости.
Из теории колебаний известно, что если меняется
частота вынуждающей силы а) при сохранении
постоянной частоты собственных колебаний (о0, то амплитуда
колебаний будет меняться и достигнет максимального
значения при частоте вынуждающей силы ©рез,
удовлетворяющей соотношению (о*ез =<0q—2б2 (где б
—коэффициент затухания, характеризующий вязкость среды).
Резонансная амплитуда будет равна
а= / , , (59)
2 6/соо 1/1 _ (6V<og)
где L — смещение, вызываемое внешней возмущающей
силой.
Рассмотрим устройство электромагнитного
вибрационного вискозиметра (рис. 73). Напряжение от сети
через стабилизатор и звуковой генератор, который
регулирует частоту тока, подается на обмотку вибратора,
который состоит из пакета трансформаторного железа,
якоря и стоек.
При прохождении тока через обмотку вибратора в
Рис. 73. Схема электромагнитного вибрационного вискозиметра:
/ — стабилизатор напряжения; 2 — звуковой генератор; 3 — обмотка вибрато-
?а; 4 — пакет трансформаторного железа; 5—7 — измерительная аппаратура;
— крепление якоря; 9 — латунные стойки; 10 — понижающий
трансформатор; // — сопротивления; 12 — обмотки датчика; 13 — обмотки
дифференциального трансформатора; 14 — подвижный сердечник; 15 — колеблющийся
стержень; 16 — жидкий шлак; 17 — сердечник трансформатора; 18 —
выпрямитель; 19 — пружина
6* Зак. 664 163
пакете железа создается переменное магйитноё поле.
Взаимодействие поля с якорем, укрепленным на
пружинах, заставляет подвижную систему вискозиметра
совершать вертикальные колебания, которые передаются
стержню с лопаточкой, опускаемому в расплав.
Напряжение на датчик подается через стабилизатор,
понижающий трансформатор, потенциометр и обмотки
дифференциального .трансформатора. Внутри обмоток
датчика имеется подвижный сердечник, который связан
с якорем вибратора и со стержнем, погружаемым в
расплав. Амплитуда колебаний сердечника фиксируется с
помощью обмоток датчика. Когда сердечник вибрирует,
то амплитуды его колебаний ах и а2 изменяются так, что
при увеличении одной из них другая уменьшается.
Соответственно изменяются и индуктивные сопротивления
обмоток. Так как с этими обмотками соединены
последовательно обмотки дифференциального трансформатора,
то в них идут равные по силе токи, которые в железе
трансформатора создают два разных по величине
магнитных потока Fi и F2t направленных в
противоположные стороны. Разность этих потоков возбуждает в
обмотке дифференциального трансформатора переменную
э.д.с., которая после выпрямителя измеряется
милливольтметром.
По показаниям милливольтметра, с помощью граду-
ировочной кривой и определяют вязкость расплава. Для
измерения вязкости шлака вискозиметр настраивают на
резонанс с помощью звукового генератора так, что
амплитуды о,\ и а2 становятся максимальными и вольтметр
показывает максимальное отклонение. При погружении
в расплавленный шлак лопаточки из молибдена
резонанс нарушается.
Метод крутильных колебаний Швидковского
Во вращение приводится тигель с жидкостью. Тигель
подвешивают в печи на упругой нити. Подвеска тигля
связана с системой отсчета свободных колебаний. После
снятия вынуждающих колебаний затухает колебание,
связанное с наличием вязкого течения слоев жидкости,
и измеряются логарифмические декременты затухания
свободных колебаний. Метод в основном применим для
жидкостей с малой вязкостью, а именно для металлов.
Теоретический метод обоснован следующим образом.
164
Скольжение между жидкостью и внутренней стенкой
тигля отсутствует, слой жидкости непосредственно у
стенки движется со стенкой с одинаковой скоростью;
вращение тигля рассматривают в момент, когда режим
становится регулярным — начальные скорости не
оказывают влияния на режим вращения. Амплитуда
колебаний невелика.
Вязкость жидкости может быть вычислена по
формуле
V--1 МЦ' у^ *) , (60)
л \MRJ ax
где v — кинематическая вязкость, смЗ/с; К—момент
инерции подвесной системы без металла, г/см2; М —
масса жидкого металла, г; R — радиус столба жидкого
металла, см; б —логарифмический декремент затуханий
крутильных колебаний тигля с жидким металлом; бо —
логарифмический декремент затухания колебаний тигля
без металла; т—период колебаний подвесной системы
с жидким металлом, с; то — то же, без жидкого металла;
а — коэффициент, учитывающий влияние дна тигля.
Метод пригоден в случае, если имеется линейная
зависимость логарифмов амплитуд колебаний от их числа.
Расчет производят методом последовательных
приближений. Сначала рассчитывают vo, затем vi, v2 и т. д. до
тех пор, пока новое значение v не окажется достаточно
близким к предыдущему.
Положительной стороной данного метода расчета
является отсутствие необходимости учитывать свойства
нити, точно определять т0 и бо, так как член в уравнении
(60), в который они входят, бесконечно мал по
сравнению с б.
Момент инерции определяется по формуле
где то —период колебаний системы с пустым тиглем;
Ti — период колебаний системы с эталоном с известным
моментом инерции; К! — момент инерции эталона.
Эталон должен быть легким, но обладать большим
моментом инерции. Эталоном может служить металлический
диск. Декременты затухания рассчитывают по формуле
Л--Lin-*
п Ап
165
где п — число колебаний в данной серии; А0 и Ап —
начальная и конечная амплитуда колебаний.
При конструктивном осуществлении данного метода
большое внимание следует уделять креплению
вискозиметра, применять специальные антивибрационные опоры
для устранения внешних колебаний, которые могут
искажать собственные колебания тигля с металлом. Нить
подвески должна быть строго совмещена с центром
тигля.
На рис. 74 показана схема установки для
определения вязкости металла. Корундовый тигель установлен
на молибденовой подставке, которая центрируется в
двух тарелках. Тарелки, соединяющие внутренние части
с наружными деталями, опираются на мостик, сквозь
который пропущен подвес из стальной проволоки,
проходящей в защитной трубе. На конце проволоки подвешен
медный груз, так что центр тяжести лежит ниже точки
опоры, что обеспечивает устойчивое равновесие.
Колебательная система, включая тигель, весит до
1,5 кг. На конце проволоки на переходнике между
грузом и проволокой установлено зеркальце, которое
отбрасывает световой зайчик от осветителя на шкалу. Система
помещена в вакуумплотный корпус со стеклянными
наконечниками для зеркала. Закручивание нити и
сообщение системе колебаний происходит электромагнитным
способом, а для быстрого гашения колебания
применяется электромагнитный тормоз постоянного тока,
создающий вихревые токи в медном противовесе. Измерения
проводятся в атмосфере нейтрального газа. Печь имеет
бифилярную обмотку из молибденовой проволоки для
устранения магнитного поля. После закручивания нити
с помощью светового зайчика на шкале измеряют
амплитуды колебаний, следующих друг за другом, и
вычисляют логарифмический декремент б.
Движение зайчика на световой шкале может
отчитываться с помощью фотоэлемента и счетной установки.
Причем определяется не угол затухания колебаний, а
время прохождения зайчика через мерную длину — щель
фотодатчика. Например, при ширине щели 3 см время
прохождения зайчика в нулевом колебании равно 0,1874,
а в третьем 0,2130 с. Логарифмический декремент
колебаний определяют по формуле
б = J- In -£l ,
п Г0
166
где Т0 и Тп — время прохождения щели световым
зайчиком в нулевом и n-ном колебании. Точность измерения
составляет 6—7%.
Рис. 74. Схема установки для
измерения вязкости жидкого металла методом
крутильных колебаний:
1 — корундовый тигель; 2 —
молибденовая подставка; 3 — центрирующие
тарелки; 4 — промежуточный штуцер;
5 — штанга; 6 — противовес; 7 —
зеркало; 8 — стеклянный корпус; 9 — ввод
газа; 10 — окно; // —
электромагнитный тормоз; 12 — нагревательный
элемент; 13 — крышка печи; 14 — вывод
газа; 15 — термоизоляция; 16 —
термопара; 17 — кварцевое стекло; 18 —
корундовая трубка; 19 — опорный мост:
20 — опора; 21 — нить подвески; 22 —
источник света; 23 — шкала
167
Метод затухающих колебаний
Вязкость рассчитывают по разности логарифмов
декрементов затухания двух колебаний, следующих друг за
другом. Тело, подвешенное на упругой нити, помещают
в расплав и приводят во вращение, например,
электромагнитом. Нить закручивается, и после прекращения
внешнего воздействия измеряют затухание колебаний.
По затуханию колебаний судят о внутреннем трении
жидкости, т. е. о ее вязкости. Логарифмический
декремент затухания б равен
\gAp-\gAm
о = ,
р — m
где Ар — амплитуда р-колебаний; Аш— амплитуда т-
колебания из непрерывного ряда затухающих
колебаний. Соотношение между логарифмическим декрементом
и вязкостью имеет вид:
Ь-Ь0 = С1УрЧ + С2ч + Сз9г\у (61)
где бо — логарифмический декремент колебаний на
воздухе; б — логарифмический декремент
колебаний в измеряемой жидкости; т\ — вязкость
мН-с/м2; р — плотность, г/см3; Сь С2, С3 —
постоянные, зависящие от метода изменения и
определяемые при градуировке по жидкостям с
известной плотностью и вязкостью.
К недостаткам метода относятся невысокая точность,
ограниченный верхний предел измеряемой вязкости,
трудность соблюдения колебаний тела только вокруг
своей оси, совпадающей с осью подвески.
Поэтому логарифмический декремент затухания
зависит от амплитуды колебаний. Отсутствие перемещения
расплава может привести к возникновению
концентрационного и температурного градиентов в расплаве.
Метод параболоида вращения
По этому методу вязкость расплава определяют по
времени изменения интенсивности проникающего у-излуче-
ния при образовании параболоида вращения на
поверхности вращающегося металла.
При вращении тигля с расплавом вокруг
вертикальной оси с постоянной угловой скоростью поверхность
168
расплаба принимает форму параболоида вращения. Сш>
рость образования параболоида вращения при постоянной
угловой скорости есть функция вязкости. Измерив
время, необходимое для получения параболоида вращения,
получим значение коэффициента вязкости. Вращение
тигля происходит со скоростью 400—450 об/мин.
Система для определения времени образования
параболоида вращения состоит из источника -у~излУчения и
детектора излучения УСД-1, усиленный сигнал которого
поступает на самопишущий потенциометр со шкалой
0—10 мВ. Потенциометр производит запись графика
зависимости логарифма интенсивности проходящего
излучения от времени т. По графику замеряют время т0,5,
соответствующее половине амплитуды изменения
логарифма интенсивности излучения.
Из гидродинамического подобия движения жидкого
металла получается уравнение, не учитывающее силы
поверхностного натяжения и волны на поверхности
расплава, а именно:
1п /т - In 1±
„"-■.,, -Wfrvj. <62>
где 1\ — интенсивность в начальный момент %х\ /То5 —
интенсивность, соответствующая времени то,5-
Кинематическую вязкость v вычисляют по формуле
V=aC/T0.5'
где С — постоянная, не зависящая от рода металла; С =
=г*^5(здесь v* — известное значение кинематической
вязкости, определенное каким-либо другим способом;
г 05 —время, определенное из диаграммной записи для
данного металла, обладающего кинематической
вязкостью V*).
12. ЭЛЕКТРОПРОВОДНОСТЬ И МАГНИТНЫЕ СВОЙСТВА
ЖИДКИХ МЕТАЛЛОВ
Электрические свойства жидких металлов зависят от
строения жидкости. Сопоставляя изменение
электрических свойств жидкости с ее составом и другими
характеристиками, можно получить ценные выводы о
строении жидкости. Измерение электропроводности жидких
металлических расплавов можно производить бескон-
169
тактным способом Регеля. Измеряется момент сил,
действующих на проводящее тело во вращающемся
магнитном поле. Предпочтительнее, однако, определять
не электропроводность,
а
электросопротивление, которое находится
в прямой зависимости
от температуры в
отличие от гиперболической
зависимости
электропроводности.
Неточности измерения
температуры при
определении
электросопротивления будут менее
существенны, чем для
эл ектр о п рово дн-ости.
Измерения
осуществляются в
вискозиметре, схема которого
представлена на рис.
75. Прибор
градуируют по олову, свинцу,
меди в жидком и
твердом состоянии.
Удельное
электросопротивление определяют по
формуле
Р = К
/»
LIP, (63)
Рис. 75. Схема установки для. измерения
электропроводности и вязкости жидких
металлов:
/ — стеклянный шлиф со смотровым,
стеклом; 2, 5 — цанговые зажимы; 3— нить;
4 — труба; 6 ~ зеркало; 7 — штанга
крепления тигля; 8 — груз; 9 — водоохлаждае-
мый корпус; 10 — обмотки статора; 11 —
крышка тигля; 12 — нагреватель; 13 —
чехол термопары; 14 — текстолитовый
корпус; /5 — прижим токоподвода; М —
термопара; 17 — ввод термопары; 18 — токо-
подвод; 19 — шины
Д ф
где К — постоянная
прибора, которая
определяется калибровкой
по веществу с
известной
электропроводностью; / — сила тока,
создающего
вращающее поле; Аф — угол
поворота; L и R —
соответственно длина и
радиус образца.
Тигель из корунда
жестко соединен со
170
штангой, на верхнем конце которой укреплены
зеркальце, крыльчатка масляного демпфера и цанга,
зажимающая тонкую вольфрамовую нить. Второй
конец нити также крепится цанговым зажимом, что
обеспечивает полное затухание колебаний в течение 5—10 с.
Угол закручивания определяется соотношением
tgAq>==z/Z, где z — отклонение зайчика на шкале от
нулевой точки; / — расстояние от зеркальца до световой
шкалы. Так как угол закручивания не превышает 4—
5°, то можно принять, что «Дф пропорционально z.
Вариантом метода измерения электропроводности,
разработанным А. А. Вертманом, является применение
механотрона для фиксирования поворота образца во
вращающемся магнитном поле. Момент, возникающий
при наложении на образец вращающегося магнитного
поля, передается системой рычагов на мембрану
механотрона. Механотрон является весьма чувствительным
датчиком, поэтому можно измерять изменение угла
поворота до 0,5'. Поскольку в установке (рис. 76)
всегда открыт доступ к поверхности металла, то можно не-
Рис. 76. Схема установки для измерения электропроводности с механотрон-
ным датчиком:
/ — механотрон; 2 — система рычагов; 3 — нагреватель; 4 — сгатор; 5 — тигель
с расплавом; 6 — термопара
171
прерывно измерять изменение электропроводности при
легировании, модифицировании, растворении добавок в
широком диапазоне температур.
Магнитная восприимчивость жидких расплавов, как
и электропроводность, характеризует структуру
жидкости. Магнитную восприимчивость жидких сплавов
измеряли на приборе, схема которого представлена на
рис. 77.
Магнитную восприимчивость оценивают по
изменению массы образца в магнитном поле: х= {FjH)VdHldx,
Рис. 77. Схема установки для измерения магнитной восприимчивости жидких
металлов:
/ — ярмо электромагнита; 2 — нагреватель; 3 — микроаналитические весы;
4 — соленоид; 5 — призма; б — сердечник соленоида; / — арретир весов; 5 —
сильфон; 9 — экран; 10 — образец; 11 — кожух печи; 12 — водоохлаждаемые
контакты; 13 — термопара; 14 — подвеска; 15 — плата весов; 16 —
установочный винт; 17 — колпак весов; 18 — смотровое окно; 19 — полюсные
наконечники; 20 —катушка; 21 — прижимной винт сердечников магнита
172
где х — магнитная восприимчивость; dH/dx — градиент
магнитного поля по оси х; V — объем образца; F —
сила, с которой поле действует на образец. Магнитная
восприимчивость пропорциональна изменению массы
образца, фиксируемой весами, т. е. k=KF, где К —
постоянная прибора, определяемая по веществу с
известной магнитной восприимчивостью.
Прибор состоит из электромагнита, создающего
поле 12000 Э, весов и печи сопротивления с бифилярнои
графитовой спиралью. Взвешивание производится
весами с механотронным датчиком, с точностью
взвешивания ±0,5—1,0 мг в диапазоне 0—10 г.
Для уравновешивания образца служит контргруз.
Применение механотрона позволяет сделать жестким
крепление тигля с металлом, исключая «прилипание»
образца к одному из полюсов магнита.
Механотронные весы позволяют легко записать
изменение массы образца в зависимости от температуры.
Вся система герметизирована, а блок механотрона
термостатирован.
Важным моментом является исключение влияния
магнитного поля нагревателя, так как нагреватель
сконструирован таким образом, что его поле
перпендикулярно полю, создаваемому магнитом.
Электромагнит питается от селенового
выпрямителя. Все части весов и электромагнита сделаны из
немагнитных материалов. Навеску образца 2 г
помещают в корундовый тигель, подсоединяют его к механо-
трону. Длину подвеса регулируют так, чтобы тигель с
металлом всегда находился в одной точке. Изменения
массы составляли 200—500 мг. Зная магнитную
восприимчивость эталона xi и соответствующее изменение
его массы AGj в магнитном поле напряженностью Н,
получим искомую величину магнитной восприимчивости
жидкого металла:
*а -Xl ТоГдГ • (64)
где AG! и AG2 — изменение массы образца и эталона в
магнитном поле напряженностью Н; Gx и G2 — масса
образца и эталона. Общая ошибка измерений составлю
ет менее ^,5%,
173
13. ЭЛЕКТРИЧЕСКИЕ СВОЙСТВА ШЛАКОВ
Расплавленные шлаки представляют собой растворы
электролитов. Этим объясняется механизм
большинства химических реакций, идущих с участием шлаков.
Методы измерения электропроводности
жидких шлаков
Для определения электропроводности расплавов
широко применим метод Кольрауша, основанный на
измерении электросопротивления жидкости между двумя
электродами при помощи переменного тока. Сопротивление
цепи измеряется мостовой схемой.
Удельную электропроводность можно вычислить из
измеренного сопротивления, если знать «сопротивление
ячейки». Последнее определяется по раствору
электролита с известной электропроводностью х:
(7?-Z)x = tf (65)
где К—константа ячейки, см-1; х — удельная
электропроводность расплава, Ом-1-см-1; Z — сопротивление
проводов, Ом; R — активное сопротивление расплава,
Ом. Величину К можно измерить или рассчитать. Для
уничтожения э.д. с. поляризации применяют токи
высокой частоты порядка 1—2 кГц.
Установка для измерения электропроводности
шлаков состоит из электрической ячейки и измерительных
приборов. Наибольшее применение нашли два типа
датчиков: 1) тигель с двумя параллельными
электродами; 2) тигель с центральным электродом. Применяют
железные, молибденовые, платиновые и графитовые
тигли и электроды. Измерения осуществляют с
помощью мостика Уитстона или Томпсона.
Одинарный мост Уитстона дает высокую точность,
когда абсолютная величина измеряемого сопротивления
^1 Ом. В качестве нуль-индикатора используют
электронный осциллограф. Двойной мост Томпсона
позволяет измерять с высокой точностью сопротивления до
Ю-6 Ом. Погрешность измерения для одинарного и
двойного мостов зависит от чувствительности - нуль-
гальванометра как указателя равновесия моста.
Для компенсации емкости составляющей тока
применяют магазины емкостей, которые включают парал-
174
лельно магазину сопротивления. Источником тока
высокой частоты до 1,500 кГц служат ламповые
генераторы типа ЗГ-10 и ЗГ-17.
Для определения константы датчика К необходимо
найти оптимальную глубину погружения электродов,
при которой погрешность минимальна. Зависимость
сопротивления 0,1 н. раствора КС1 от глубины
погружения показывает, что, начиная с глубины 11—12 мм,
сопротивление электролита изменяется мало.
Влияние температуры на константу датчика
учитывается по формуле
Kt = Ktl [1-a ft-/i)], (66)
где Ki — константа датчика при температуре измерения,
см-1; Ktt'— константа датчика при температуре
градуировки, см-1; а — коэффициент линейного расширения
электродов; /А — температура, при которой производили
градуировку, °С; t2 — температура, при которой
производили измерение, °С.
Если в расплав погружают два электрода, то для
исключения сопротивления подводящих проводов и
электродов производят измерения при двух
погружениях электродов на разную глубину.
Удельную электропроводность вычисляют по
формуле
х = Mfr-Si) t (67)
где AR — разность сопротивлений; б — расстояние
между электродами; Si и S2 — площадь погружаемой части
электродов при первом и втором погружении.
Измерения с помощью моста переменного тока
прерывисты; большая длительность измерений приводит к
значительным ошибкам из-за изменения температуры
шлака. Непрерывность измерения сопротивления
обеспечивает схема вольтметр—амперметр.
Падение напряжения на ячейке измеряется
ламповым вольтметром. С его помощью контролируется
активная составляющая измеряемого напряжения.
Подбором частоты тока ее снижают до нуля. В
зависимости от состава шлака и его температуры частота тока
колеблется от 2 до 10 кГц, причем, как правило, с
понижением температуры шлака она повышается. Для
опытов использовали молибденовый тигель-электрод,
вторым электродом являлся вольфрамовый пруток.
175
Электролиз шлаков
Для электролиза расплавленных шлаков и расчета
выхода по току используют ячейки, изготовленные из
магнезита. Одно из таких устройств показано на рис. 78.
Рис. 78. Схема
электролизера:
/ — угольный анод; 2 —
анодное отделение; 3 —
промежуточное отделение; 4—
шлак; 5 — магнезитовый
тигель; 6 — обмазка; 7 —
крышка; 8 — катодное
отделение; 9 — углубление для
катода; 10 — углубление для
свидетеля; 11 — катод; /2 —
свидетель; 13 — токоподво-
ды из вольфрама или
молибдена; 14 — заделка токо-
подводов; 15 — соединение
железной трубки и
проволоки; 16 — кварцевая
трубка; 17 — изоляторы
В блоке из плавленого магнезита вытачивают три
отделения: анодное, катодное и промежуточное. В
анодное отделение вставляют угольный анод, в катодное
отделение в одно углубление в качестве катода
помещают серебро, которое через вольфрамовый или
молибденовый токоподвод соединено с внешним токоподво-
дом. В другое углубление катодного пространства
помещают серебро в качестве контрольного свидетеля,
ток через него не пропускают. Роль свидетеля сводится
к контролю металла, попадающего в катод в результате
оседания из расплава, независимо от электролиза.
Через ячейку пропускают постоянный ток плотностью 0,2—
0,5 А/см2. Количество электричества измеряется медным
кулонометром. По ходу электролиза отбирают пробы
шлака. По окончании электролиза тигель с содержимым
замораживают, анализируют катод и свидетель на
содержание в них железа. По полученным результатам
рассчитывают выход по току.
В железный тигель можно запрессовать навеску
шлака. В этом случае плавку вели в аргоне с
выдержкой и перемешиванием расплава в течение 16 ч. После
установления равновесия брали пробы шлака и вводи-
176
ли железный стержень (известной массы) на глубину
9,5 мм. Стержень подсоединяли к положительному
полюсу батареи, а тигель — к отрицательному.
После пропускания 1000 Кл электричества стержень
извлекают, очищают от остатков шлака и взвешивают.
Анодный выход по току рассчитывают по формуле
.= 100 AG
1 27,93F '
где AG — потеря массы, г; F — количество
электричества, пропущенного через ячейку, Ф.
Определение чисел переноса
Определение чисел переноса позволяет уточнить
строение жидких шлаков. Число переноса — это доля
электричества, переносимого данным ионом в расплаве.
Числа переноса равны соответственно f+—/+/(/++
+ /-) и tr=/"/(/++/~), где /+ и /- — подвижности
катионов и анионов. В электролите ток может
переноситься катионами, анионами, электронами. Если характер
тока полностью ионный, то эквиваленты электродных
реакций равны общему количеству электричества,
прошедшего через ячейку. Если имеет место электронная
проводимость, то закон Фарадея не выполняется.
Числа переноса ионов и электронов могут определяться
анализом анодных и катодных продуктов после
электролиза.
Определение чисел переноса основано на том, что
при электролизе из-за различной подвижности ионов
вблизи катода и анода изменяется концентрация
ионов, определяемых анализом. Для устранения ошибки
необходимо предотвратить перемешивание расплавов
около электродов. Для этого анод помещают в
корундовой трубочке с открытым нижним концом, которую
погружают в шлак. Анодную ячейку окружает трубка
большего диаметра, имеющая четыре отверстия для
сообщения с пространством, расположенным выше конца
анода на 25 мм. В других опытах в тигель со шлаком
вставляли кварцевую пробирку, в которой расплавляли
шлак с добавкой изотопа 59Fe. В пробирку опускают
железный стержень, служащий анодом. Шлак в
пробирке отделен от ванны в тигле твердым кремнеземом.
С помощью изотопа 59Fe определяют концентрационную
неоднородность и числа переноса.
177
Электрическая ячейка может состоять из
корундового тигля большого размера, в который помещают два
малых тигля. Один из малых тиглей имеет отверстие и
является анодной диафрагмой, в него помещают
электрод — анод. Другой электрод — катод — опускают в
расплав, находящийся в большом тигле. Шлак во
втором малом тигле является свидетелем. Измерения
проводят также с помощью изотопа 59Fe. По изменению
радиоактивности в тигле-свидетеле судят об улете
исследуемого элемента из шлака. При расчете активность
исходного шлака приравнивают -к активности шлака в
свидетеле. Для определения числа переноса Са2+
применяли изотоп 45Са.
Числа переноса для расплава FeO—CaO находили
следующим образом. Принимали, что fFe+-fca=l. Если
количество прошедшего электричества F, то при выходе
по анодному току / анодная ячейка теряет 0,2793/F^re
граммов железа и 0,2004//^са граммов кальция.
Допустим, х — неизвестное количество шлака в
анодной области. До электролиза доля железа и кальция
составляет fae и /са, а после электролиза т^е и тса.
Тогда потери железа и кальция выразятся следующим
образом:
т Fe — х /Fe = 0,2793 / F (1 — /Fe);
х /с — тса = 0,2004 / F tea.
Число переноса кальция окажется равным:
/С = fc."Fe-/Fe"4* щ
JF (0,2004/Fe+0,2793/Са) V '
14. РАСТВОРИМОСТЬ ГАЗОВ В МЕТАЛЛЕ И ШЛАКЕ
Содержание азота и водорода в металле в большинстве
случаев отрицательно влияет на свойства готовых
изделий. Знание процессов растворения газов в металле,
пределов растворимости и факторов, влияющих на
поведение газов в жидком металле, позволяет выработать
правильные технологические приемы выплавки стали и
сплавов с низким содержанием азота и водорода.
Для определения растворимости азота и водорода в
металле и шлаке используют либо метод Сивертса (в
частности, метод горячего объема), либо метод
закалки проб.
178
Метод Сивертса применим, если газы образуют в
металле раствор, подчиняющийся закону Генри. При
этом растворимость азота и водорода в металле
пропорциональна корню квадратному из парциального давле-
ния газа над металлом: [Щ=к{]/р^2, [Н]=^2УРн2-
Этим методом можно определять коэффициенты
активности водорода или азота в тройных сплавах.
Сначала определяют растворимость газа в чистом металле,
а затем в сплаве:
fMe [NlFe
Метод Сивертса
В герметичной плавильной системе помещают тигель с
металлом. Перед началом опыта систему вакуумируют.
Затем в систему напускают точно отмеренное
количество рабочего газа. Жидкий металл поглощает газ из
атмосферы. Систему при заданных условиях опыта
выдерживают до тех пор, пока не прекратится насыщение
металла, о чем судят по стабилизации давления или
объема газовой фазы.
Разновидностями метода Сивертса являются методы:
а) изохорный — когда поддерживается постоянный
объем системы и при этом регистрируется изменение
давления газовой атмосферы; б) изобарный, когда
постоянным поддерживается давление газовой
атмосферы, а регистрируется изменение объема. При этом
объемы изменяют перемещением уровня жидкости в
бюретке, связанной с реакционной камерой.
По изменению давления или объема вычисляют
количество газа, поглощенного металлом. Зная массу
металла, рассчитывают удельное поглощение газа.
В обоих вариантах метода Сивертса необходимо
знание «горячего объема системы», т. е. объема рабочего
газа (при нормальных условиях), создающего в
системе при заданной температуре давление 100 кПа.
Величина горячего объема зависит от конструкции
реакционной камеры, объема металлической ванны, ее
температуры и свойств газа. Для измерения горячего
объема систему заполняют инертным газом. При
работе с азотом применяют аргон, при работе с
водородом — гелий. При этом считают, что горячий объем
для гелия и водорода или для азота и аргона одинаков.
179
Горячий объем системы определяют для той же
.температуры, при которой исследуется растворимость по
количеству газа, напускаемого в печь:
уд У°Ш , (69)
Р
где Vo — нормальный объем газа, которым заполняется
печь, см3; р — измеренное давление, кПа.
Точность метода Сивертса зависит от величины
горячего объема. Чем он меньше, тем больше
относительное изменение объема или давления газа в системе, тем
точнее это изменение можно зарегистрировать. Объем
ячейки можно уменьшать, помещая внутрь нее
«инертные вставки». Однако это мероприятие удлиняет период
дегазации системы, увеличивает количество
конденсирующихся на стенках возгонов из металла, замедляет
достижение термического равновесия. Более
рациональным способом уменьшения объема ячейки считается
применение водяного охлаждения ее стенок. Объем
ячейки установок 30—40 см3. Чувствительность метода
может быть повышена путем увеличения объема
жидкого металла в системе (особенно это относится к
случаю малой растворимости газа в металле), применения
автоматической бюретки, поддерживающей постоянное
давление в системе, более точных манометров Мак Ле-
ода или механотронов для измерения давления,
микровизирования уровня ртути в бюретке с помощью
катетометров.
Объем поглощенного газа в изохорном методе
определения растворимости рассчитывают по формуле, см3:
Vm= <*-оу"г t (70)
где Vr — горячий объем системы, см3; рп — давление в
оистеме отри напуске газа, кПа; рк — давление при
установлении равновесия системы, кПа.
Для изобарного процесса объем поглощенного газа
в условиях равновесия VM равен разности VBIl—Vr (где
Увп — объем газа, впущенного в систему). Тогда
y-v--v'>Sr-ish-- <">
где Pi — давление в системе, кПа; t — температура
газа, °С.
180
Формула (71) определяет объем газа,
поглощенного металлом, приведенный к нормальным условиям.
Растворимость азота, например, составит, %:
N VM28 /-J0ri00>
22400G у pNe
где G — масса металла, г; Pn2 — парциальное давление
азота, кПа, при установлении равновесия, если считать,
что раствор азота подчиняется закону Генри.
Для точного определения растворимости газа в
металле к полученной на установке величине необходимо
добавить содержание азота или водорода в металле в
момент впуска в реакционную камеру азота или
водорода.
Основные ошибки определения растворимости газа
методом Сивертса представлены рядом величин.
Точность измерения температуры составляет ±10°С
(ошибка ±1,5%). Точность измерения объема газа зависит
от цены деления газовой бюретки, которая может иметь
градуировку 0,002—0,005 см3, и от возможных
колебаний температуры воды в термостате бюретки. При
колебании температуры на ±0,5°С и при полном
заполнении объема бюретки максимальная точность
измерения составляет ±0,2 см3 (ошибка ±5%). При большой
растворимости газа (например, >0,02,°/0( азота в
металле) общая ошибка измерения не превышает ±3%, а
при малой растворимости газа ошибка значительно
возрастает.
К достоинствам метода Сивертса относятся: 1)
возможность непосредственного измерения растворимости
в условиях опыта; 2) отсутствие необходимости в
газовом анализе образцов; 3) простота фиксирования
равновесия; 4) возможность исследования термодинамики
растворения газов, кинетических особенностей
процессов растворения или дегазации и 5) возможность
изучения воздействия различных факторов (температуры,
давления, состава металла).
Однако результаты опыта могут быть искажены
трудноучитываемой адсорбцией газа на конденсате,
оседающем на стенках реакционной камеры. Для
уменьшения влияния возгонов приходится значительно
повышать давление в реакционной камере или применять
181
смеси газов, например азота с аргоном, с известным
парциальным давлением одного из компонентов.
Рассмотрим устройство некоторых установок. Для
нагрева и расплавления металла применяют
индукционную печь, обеспечивающую хорошее перемешивание
металла.
Рис. 79. Схема установки для изучения растворимости водорода в жидких
сплавах железа:
/ — призма; 2 — трубка с экраном для сохранения присаживаемых металлов;
3 — термометр для контроля температуры отходящей воды; 4 — тигель; 5 —
подставка для тигля; 6 — крышка тигля; 7 — индуктор; 8 — металл; 9 —
наружный экранирующий тигель с засыпкой из АЬОз; 10 — водоохлаждаемая
кварцевая реакционная трубка; // — выводы и заземление термопары; 12 —
механотронный датчик давления; 13 — форвакуумный насос; 14 —
диффузионный насос; 15 — лампа вакуумметра; 16 — ртутный манометр; 17 —
измерительные бюретки
На рис. 79 приведена схема установки МИСиСа для
определения растворимости водорода. В установке
предусмотрено непрерывное определение температуры
металла и точное измерение давления в реакционной
камере с помощью микроманометра с мембранным механо-
тронным датчиком и автоматической записью резуль^
татов измерений. Давление в камере фиксируют также
манометром Мак Леода, точность измерений которого
можно довести до 6,65 Па.
Для ввода добавок по ходу опыта в центральной
отводной трубке устанавливают магазин для добавок
с магнитным толкателем или вакуумным краном, кото-
182
рый позволяет производить операцию без длительного
взаимодействия добавки с атмосферой печи. Чтобы не
увеличивать горячий объем системы, рекомендуется
использовать газопроводящие трубки диаметром не
более 1 мм. Газовая бюретка должна иметь
термостатированную водяную рубашку.
Опыт начинают с длительной дегазации системы без
нагрева, чтобы убедиться в ее герметичности. Затем
шихту нагревают и дегазируют в вакууме или в
атмосфере высокочистого аргона или гелия. Измеряют
горячий объем системы. Откачивают инертный газ и
напускают измеренное количество водорода или азота до
заданного давления. Выдерживают систему до
наступления равновесия. Измеряют давление газа в
равновесном состоянии. Приступают к следующему циклу,
изменяя температуру, или состав металла, или давление
в камере.
Для измерения поглощения газов с повышенной
скоростью абсорбции разработана установка, схема
которой представлена на рис. 80. Реакционная камера
соединена с газовой системой через быстродействующий
электромагнитный клапан, время срабатывания
которого 10 мс. Этот клапан поддерживает избыточное
давление в обоих направлениях, давая тем самым
возможность изучать процессы абсорбции и десорбции.
Давление в реакционной системе без изменения ее объема в
течение опыта измеряли дифференциальным датчиком
мембранного типа, расположенным в верхней части
газового резервуара. Электрический сигнал от датчика
поступал на вход регистрирующего потенциометра.
Измерение статических давлений в системе перед
каждым экспериментом и калибровку электрической цепи
датчика производили с помощью трех ртутных
манометров, которые отключали от реакционной системы на
время эксперимента.
На установках горячего объема удобно измерять
кинетические особенности процессов растворения газов.
Для изучения кинетики поглощения азота в
измерительную газовую бюретку помещают платиновую
спираль, являющуюся плечом моста сопротивления.
Изменение сопротивления спирали в зависимости от уровня
[ртути фиксируется потенциометром. Уровень ртути в
♦бюретке стремятся поддерживать постоянным, чтобы
обеспечить постоянное давление газа в системе до на-
183
ступлёнйя равновесия. Электрическую цепь калибруй^
с учетом температуры воды в термостате, окружающем
бюретку. Таким же образом исследуют кинетику
выделения газа из металла, для чего понижают уровень
ртути в бюретке. При этом давление в системе понижается.
Не нг
Рис. 80. Схема установки для определения растворимости газов с
повышенной скоростью абсорбции в металлах:
/ — от генератора высокой частоты; 2 — охлаждающая вода; 3 — датчик
давления; 4 — магнитный клапан; 5 — вакуум; 6 — манометр; 7 — манометрическая
бюретка; 8 — резервуар газа
Метод закалки
Этот метод состоит в насыщении металла исследуемого
состава водородом или азотом и отборе пробы
металла. После кристаллизации .пробы определяют
содержание газа в ней. К недостаткам метода относятся: 1)
количество газа, определяемое в металле пробы, включает
газ, растворенный в металле и скопившийся в микропо-
184
pax пробы; 2) несмотря на большую скорость
кристаллизации пробы, некоторое количество газа теряется и
при кристаллизации, и в период от момента отбора
пробы до начала анализа; 3) ошибки анализа
накладываются; 4) определение момента наступления равновесия
затруднено. В каждом конкретном случае (температура,
состав металла, давление газовой фазы) необходимы
предварительные плавки с отбором проб через
определенные промежутки времени, последующим анализом
для установления момента, когда наступает насыщение
металла газом.
Достоинство метода заключается в простоте
конструкции экспериментальной установки, возможности
проведения опытов при высоких парциальных
давлениях газа, предотвращающих испарение из металла, в
получении абсолютных значений растворимости газа.
Метод закалки проб можно рекомендовать для расплавов,
дающих большие возгоны, или в тех случаях, когда
невозможно путем предварительной дегазации получить в
металле ничтожно малую концентрацию газа.
Установки для определения растворимости газа
методом закалки проб состоят из: герметизированной
плавильной печи; системы подготовки и подачи газа в
плавильное пространство; устройств для отбора проб
металла, измерения температуры, давления в печи.
Для ускорения наступления равновесия можно
продувать металл газом через корундовую трубку,
погруженную на несколько миллиметров в металлическую
ванну, или обдувать зеркало металла. В процессе
исследований при повышенных давлениях рекомендуется
применять вакуумную печь с металлическим корпусом.
Для насыщения металла водородом, кроме чистого
водорода, можно использовать смесь бутана и пропана.
Большое влияние на результаты метода закалки
оказывает способ отбора и хранения проб. Способ
отбора должен гарантировать точное соответствие
концентрации газа в пробе и в жидкой металлической
ванне. Для отбора проб применяют отсос металла в
кварцевые трубки или заливку в медные кокили.
Не менее важным является способ сохранения газа
в пробе до момента анализа. Особенно это относится к
водороду, который, обладая большим коэффициентом
диффузии в твердом металле, при непрерывном
хранении пробы неизбежно теряется, приводя к заниженным
185
результатам анализа. Для сохранения водорода в
металле пробу погружают в сосуд с жидким твердым
хладагентом, помещают в запаиваемый сосуд, хранят
под слоем жидкости, например ртути, собирая
выделяющийся водород.
Например, применяют кварцевую пипетку длиной
90, диаметром 14 мм, оканчивающуюся капилляром
длиной 21 мм с сужением от 0,5 до 0,2 мм. Такой
капилляр не позволяет железу вытекать из пипетки.
Капилляр запаивают хлоридом серебра, хорошо
смачивающим кварц. Пипетку откачивают на вакуумной
установке и запаивают сверху. Для отбора пробы пипетку
укрепляют на держателе и погружают в металл,
пробка из хлорида серебра расплавляется и металл под
действием атмосферного давления заполняет пипетку.
После отбора пробы пипетку погружают в ртуть. Под
ртутью обламывают капилляр, собирают выделившийся
водород и определяют его количество. В последующем
анализируют самую пробу.
Опыты показали, что количество водорода,
выделяющееся под слоем ртути за время хранения, составляет
до 50% всего водорода, содержащегося в металле.
Проще хранить пробы в хладагенте. Это не связано с
применением токсичной ртути.
Большие преимущества для исследования
растворимости газов в жидких металлах представляет плавка
во взвешенном состоянии, так как отсутствует
взаимодействие металла с тиглем, возможна быстрая закалка
образцов путем сливания «висящей» капли в медную
изложницу. Так как капля металла имеет массу в
несколько граммов, что во много раз меньше массы
изложницы, то скорость закалки жидкого металла
составляет 104°С/с. Благодаря таким высоким скоростям
закалки удается наиболее полно зафиксировать
растворенные в жидком металле газы. С помощью особых
приспособлений, по своему действию похожих на
наковальню, осуществляют закалку жидкого металла со
скоростью до 108°С/с. Эти устройства, разработанные
в Институте физики твердого тела АН СССР,
действуют автоматически, синхронно с высокочастотным
генератором. После выключения генератора образец
металла мгновенно расплющивается между двумя медными
водоохлаждаемыми плитами. Подвижная плита
приводится в действие либо электромагнитом, либо с помо-
186
щью гидравлической или механической системы. Схема
подобного устройства приведена на рис. 81, Толщина
получаемой фольги составляет 20—70 мкм.
Большое внимание уделяется выяснению
закономерностей растворимости водорода в шлаках. Для
установления равновесия шлак заданного состава расплав-
Рис. 81. Схема установки для
плавки во взвешенном
состоянии с устройством для
сверхбыстрой кристаллизации:
/ — жидкий металл; 2 —
плавильный индуктор; 3 — медные
плиты для закалки образца;
4 — медный блок и основание
устройства для сверхбыстрой
закалки; 5 — ударные
приспособления
К пирометру
ляют в платиновом тигле и выдерживают в
зависимости от цели исследования в сухом воздухе или
атмосфере водяного "пара. Затем в печь дают смесь водорода,
аргона и водяного пара с заданным отношением
Рн2о/рн2. После выдержки в течение 5—7 ч шлак
закаливают (с тиглем) в потоке гелия или в ртутной или
водяной ванне. При этом не должно быть
соприкосновения шлака со ртутью или водой. В потоке гелия
закаливают высокоосновные шлаки, способные
поглощать воду.
Не меньшее значение в подобных исследованиях
имеет анализ шлака на содержание водорода.
Содержание водорода в шлаке можно определять в
горизонтальной трубчатой печи сопротивления с
угольным нагревателем. В нагревательную трубу помещают
широкую корундовую трубку, а в нее — реакционную
камеру. Низ корундовой трубки закрывают резиновой
пробкой с тепловым экраном. Навеску шлака сушат в
лодочке при 300—400°С, затем вносят в камеру. Над
лодочкой, помещенной в пробирке, помещают отводную
корундовую трубку. Через камеру пропускают азот,
который вместе с парами воды уходит в стеклянную
охлаждаемую ловушку. После 30—40 мин выдержки ло-
187
вушку отсоединяют от системы и вместе с
измерительным баллоном откачивают до давления 4 Па. Затем
вынимают ловушку из холодильной смеси и помещают в
воду. Сконденсированная в ловушке влага испаряется.
О количестве воды судят по давлению в
калиброванном объеме с помощью ртутного микроманометра.
Для определения растворимости азота в шлаке
опыты проводили в установке, схема которой
представлена на рис. 82. Для нагрева использовали индукцион-
Рис. 82. Схема установки для насыщения шлака азотом:
1 — сосуд Дьюара с жидким азотом; 2 — маностат; 3 — вентиль; 4 — реометр;
5 — электролизер (источник Н2); € — печь для дожигания водорода; 7, 8—
колонки с силикагелем и ангидроном; 9 — реакционная ячейка
ную печь. Нагревателем служил молибденовый
цилиндр, который вместе с тиглем был заключен в
герметичную кварцевую колбу. Термопару помещали между
тиглем и нагревателем. В тигле расплавляли 5 см3
металла и шлака. Пробы шлака и металла отбирали, не
нарушая герметичности установки, кварцевой
пипеткой. Через шлак пропускали азот с помощью
молибденового капилляра. Азот поступал в систему из сосуда
Дьюара. К нему подмешивали водород, получаемый в
электролизере, и дожигали следы кислорода в печи
сопротивления. Содержание азота в шлаке определяли
химическим путем. Для установления равновесия
достаточной была выдержка в течение 2 ч.
188
15. ОБМЕННЫЕ РЕАКЦИИ МЕЖДУ
ЖИДКИМ МЕТАЛЛОМ И ШЛАКОМ
Вопросы равновесия между металлом и шлаком
различного состава являются важнейшей составной
частью теории металлургических процессов. В работах по
исследованию равновесия между металлом и шлаком
выясняют природу шлака, распределение компонентов
металлической ванны между металлом и шлаком,
определяют окислительную способность шлака, его влияние
на десульфурацию, дефрсфорацию металла, очищение
от неметаллических включений и т. п.
В лабораторных условиях ванну металла
покрывают слоем шлака исследуемого состава, выдерживают в
неизменных условиях до наступления равновесия.
Затем отбирают пробы металла и шлака и подвергают их
химическому анализу. В этом методе имеют место
взаимодействие шлака с материалом тигля и окисление
металла атмосферой.
Для устранения взаимодействия шлака с тиглем
последний изготовляют из материала, компоненты
которого входят и в состав шлака. Например, для
определения активности закиси железа в шлаке из FeO, MnO,
Si02, MgO и определения равновесия между шлаком и
металлом плавки вели в тигле из окиси магния и
кремнезема. При исследовании равновесия между
доломитом, шлаком и железом тигель изготовляли из
доломита. При изучении равновесия железа с алюминатными
расплавами опыты проводили в корундовых тиглях.
Распределение фосфора между расплавленным
железом и известковым шлаком изучали в известковом
тигле, для изготовления которого применяли обожженную
известь, или в тигле из три- либо тетракальцийфосфата.
Для плавки углеродистых сплавов чаще всего
употребляют графитовые тигли.
Чтобы избежать контакта расплавленного шлака со
стенками тигля, применяют вращение тигля. При этом
более тяжелый, чем шлак, металл образует вогнутую
поверхность, и шлак собирается в центре, не
соприкасаясь со стенками тигля. Этот метод ускоряет
наступление равновесия благодаря активному перемешиванию
шлака с металлом.
В печи Таммана вращение графитового тигля с
металлом и шлаком производили со скоростью 80 об/мин.
189
Для создания большей контактной поверхности между
металлом и шлаком ось печи была наклонена. Кроме
того, в тигель через графитовую крышку вводили
мешалку. Внутри мешалки высверлено отверстие для из-,
мерения температуры с помощью термопары или
оптического пирометра. Более сложным является
устройство вращающейся индукционной печи. Внутри
неподвижного индуктора вращается корпус печи с
магнезитовым тиглем со скоростью от 3 до 10 об/мин.
Для предохранения металла и шлака от окисления
опыты обычно проводят под атмосферой Аг, N2, СО или
СОг. Для создания восстановительной атмосферы в
печи можно использовать графитовый цилиндр, внутри
которого на графитовой подставке-блоке помещают
тигель. Благодаря окислению графита при нагреве в
атмосфере печи содержится некоторое количество СО,
предотвращающее окисление металла. Для подобных
исследований пригодны печи сопротивления с
графитовыми трубчатыми нагревателями.
При исследовании взаимодействия металла со
шлаком в индукционной печи отрицательным моментом
является разность температур металла и шлака. Шлаки в
индукционной печи холоднее металла. Для подогрева
шлака в тигель сверху вставляют графитовый шаблон.
В шаблоне имеется отверстие для отбора проб,
измерения температуры, подачи нейтрального газа для
предотвращения окисления металла и шлака. С целью
ускорить взаимодействие металла со шлаком в
кварцевую индукционную печь помещают графитовый тигель
для расплавления 200 г шлака. В этот большой тигель
на графитовой подвеске опускают малый тигель с
пробой металла 6 г. Шлак и металл нагревают отдельно.
По достижении заданной температуры металл
опускают в шлак. В конце опыта тигель с металлом
поднимают и закаливают его в холодной зоне печи. Затем
металл и шлак анализируют.
Распределение компонентов между металлом и
шлаком изучали в ЦНИИчермете с помощью метода
последовательного насыщения. Сущность метода состоит в
том, что на поверхность металла, расплавленного в
магнезитовом тигле при заданной температуре,
подается малыми порциями шлак, содержащий, например,
изотоп серы. Шлак впитывается стенками
магнезитового тигля, установленного в магнезитовом стакане с маг-
19Q
незитовой засыпкой, а изотоп серы частично
поглощается металлом. Прореагировавший шлак уходит через
стенки тигля в магнезитовую засыпку и не
взаимодействует со стенками тигля. После введения
определенного количества шлака в металле достигается
концентрация серы, равновесная со шлаком данного
состава. В пробах металла, отобранных по ходу плавки,
измеряют активность радиоактивного излучения. Когда
активность в пробах становится
постоянной, считают, что
равновесие установилось.
Для изучения распределения
фосфора и серы радиоактивные
добавки того или иного
компонента можно вводить в шлак и
путем отбора проб и
последующего их просчета фиксировать
наступление равновесия.
Например, тигель печи был сделан из
магнезита с двумя
сообщающимися отверстиями для устранения
перемешивания металла и шлака.
В одном отделении плавили
металл и шлак, в другом — только
металл. Добавку изотопа производили в металл и шлак.
Пробы отбирали только в одном месте для устранения
перемешивания.
Для изучения кинетики перехода, распределения
элементов между металлом и шлаком, а также для
определения лимитирующего звена важно устранить
перемешивание шлака с металлом. Подобную задачу
можно осуществить в специальном магнезитовом тигле
(рис. 83) с двумя сообщающимися отделениями. Вниз
помещают металл. В одно из отделений выше уровня
сообщающегося канала вводят шлак. В другом
отделении на поверхность металла присаживают
радиоактивную серу. Это позволяет устранить попадание серы в
шлак и перемешивание металла со шлаком.
Специальная выемка сбоку тигля позволяет отбирать пробы
шлака с одной глубины без перемешивания металла со
шлаком.
Рис. 83. Тигель для
исследования скорости десульфу-
рации металла шлаком
16. ИССЛЕДОВАНИЯ РАСПЛАВОВ В ВАКУУМЕ
Испарение из металла примесей или компонентов
В вакуумной индукционной печи или печи
сопротивления плавят металл с известным содержанием примеси,
испарение которой изучается. Через определенные
промежутки времени отбирают пробы металла, фиксируя
температуру и давление. При проведении подобных
опытов важны хорошая стойкость тигля, точное
измерение температуры и поддержание заданного давления.
Пробы металла отбирают кварцевыми пробирками с
отверстиями сбоку, кварцевыми тиглями,
закрепленными на держателе, металлическими кокилями.
Изучать испарения можно и по конденсатам,
оседающим на конденсаторе. Последним может служить
медная водоохлаждаемая трубка, помещенная над тиглем
так, чтобы ее можно было менять по ходу опыта, или
металлическая пластинка.
Дегазация металла
Дегазацию металла можно исследовать методом
последовательного отбора и анализа проб металла из
вакуумной печи при заданных давлении и температуре.
Для ускорения дегазации поверхность металла
обдувают инертным или углеводородсодержащим газом.
Применяют также продувку металла через донную
пробку.
Для изучения дегазации проба металла может
весить всего несколько граммов. Каплю металла
помещают в печь на вогнутой пластинке из окиси магния и
расплавляют под атмосферой СО. Затем печь
откачивают до необходимого давления, причем малая масса
пробы позволяет достичь состояния равновесия за 20—
30 с. После выключения тока кристаллизация капли
происходит "в течение 1 с. Преимущество такой
методики заключается в быстроте достижения равновесия.
Недостаток ее объясняется трудностью анализа
небольшого количества металла.
Для исследований газа, выделяющегося при
вакуумной плавке, к плавильной печи подсоединяют масс-
спектрометр и непрерывно анализируют отдельные
порции газа, выделившегося из металла. При этом
основной методической трудностью является достижение
истинного соответствия составов газа, выделяющегося из
192
металла, и газа, анализируемого в камере
масс-спектрометра. Прибор должен быть как можно ближе
присоединен к установке. Более точные результаты
получают при работе масс-спектрометра с миниатюрными
вакуумными печами, которые можно располагать очень
близко к входу прибора. Малый объем установки
способствует тому, что состав газа, анализируемый в
приборе, точно соответствует в каждый момент времени
составу газа, выделяющегося из металла при плавке в
вакууме.
Рис. 84. Схема установки для изучения кинетики газовыделения из металла
в вакууме:
1 — реакционная камера; 2 — генератор ЛГЗ-)10А; 3—азотная ловушка; 4 —
вакуумные краны; 5 — диффузионный насос; 6 — форвакуумный насос; 7 —
вакуумметр; 8 — потенциометр ЭПП-09; 9 — обогреваемая трубка из нержа*
веющей стали; 10 — масс-спектрометр МХ1302
Пример использования масс-спектрометра для
исследования процесса дегазации приведен на схеме
рис. 84. Масс-спектрометр МХ1302 подсоединен к
установке плавки во взвешенном состоянии через
обогреваемую трубку из нержавеющей стали. Масса капли в
печи 4 г. Температуру капли измеряли автоматическим
цветовым пирометром ЦЕП-ЗМ. Фиксировали
изменение состава в газовой фазе СО, N2, C02, Н2.
Раскисление металла углеродом
Изучается равновесие реакции [С] + [0] =СОг.
Исследования ведут либо с помощью электрохимических ак-
тивометров с одновременным отбором проб металла
7 Зак. 664
193
для анализа .на углерод, либо методом плавки в
электроннолучевой печи на медном водоохлаждаемом
поддоне. Последний метод позволяет осуществить процесс
без взаимодействия с огнеупорным тиглем и при
высокой температуре. Плавки ведут при различных
давлениях газовой атмосферы, состоящей из окиси углерода.
Подобные исследования проводят в установках для
плавки металла во взвешенном состоянии (рис. 85) при
давлениях в камере печи 10~2—Ю-3 Па. Подсоединение
к установке циркуляционного насоса обеспечивает
хорошее перемешивание атмосферы из окиси углерода в
опытах с высоким (до 100 кПа) давлением.
Магнитные ловушки
собирали металлические
пары, что уменьшало
влияние конденсатов на
состав газовой
атмосферы.
При плавке в вакууме
необходимо изучать
взаимодействие, углерода с
оксидными
неметаллическими включениями и с окис-
ными материалами, из
которых изготовлены тигли
для плавки металла.
Оценку взаимодействия
ведут либо по
результатам анализа проб
металла, либо по составу
газовой атмосферы.
Для оценки
взаимодействия металла с
огнеупорными окислами в
вакууме огнеупорные
прессованные цилиндрические
образцы длиной до 100 и
диаметром 10 мм
погружали в металлическую
ванну в вакуумной лечи.
Скорость растворения
определяли по изменению
диаметра образцов после
выдержки.
Рис. 85. Схема реакционной камеры
для исследования процессов
взаимодействия углерода с кислородом в
жидком металле в вакууме:
1 — жидкий металл; 2 — индуктор; 3 —
стабилизирующее устройство; 4 —
корпус -реакционной камеры; 5 — трубка
для обдува образца; 6 — подвод воды
к стабилизирующему устройству; 7 —
верхний фланец и прокладка; 8 —
керамическая палочка для подачи
исходного образца; 9 — изложница; 10 —
пирометрическая трубка; 11 —
поворотный столик; 12 — напуск воздуха; 13 —
трубка для отбора газа на анализ;
14 — фланец для токоподводов
194
Для устранения погрешностей, связанных -с методом,
отбора проб, взаимодействие металла с корундом в
вакууме изучали методом изотопного уравновешивания.
Суть метода состоит в том, что регистрируют изменение
отношения С160/С180 в газовой фазе в результате
распределения изотопов кислорода между газом, жидким
металлом и огнеупорными материалами реакционной
системы по реакции А1'6 03+3[С] =2[А1] + ЗС160.
Преимущество данного метода состоит в том, что
изотопный состав смеси С160—С180 не зависит от
адсорбции газа на конденсате, а определяется лишь
временем достижения изотопного равновесия. При этом
регистрация отношения С160/С180 не зависит от
полноты экстракции кислорода из металла -в газовую фазу.
Кроме того, ввиду быстрого изотопного обмена
кислорода в газовой фазе есть возможность непрерывно
контролировать процесс.
Опытная установка (рис. 86) состоит из системы
получения и хранения изотопа 180, реакционной системы,
устройства для отбора проб газа и регистрации его
изотопного отношения. Кислород получали электролизом
тяжелой воды, очищали от влаги силикагелем и
цеолитом. Кислород адсорбировали на цеолите при —196°С.
Десорбированный, осушенный кислород собирали в
объеме 11, а затем перепускали в колбу. Состав
кислорода в холодном обменнике контролировали
масс-спектрометром. Графит предварительно дегазировали в
вакууме 1(Н Па в течение 4—б ч при 1950°С. В систему
напускали кислород 180 и нагревали графит при 1700°С.
За 15—20 мин в системе образовывалась смесь,
обогащенная С160. Полученную смесь С160—С180
перепускали в систему ампул с цеолитом 17, где она
адсорбировалась при —196°С. Каждая из шести ампул
снабжена вакуумным краном и печью сопротивления,
которую можно заменить сосудом Дьюара. Плавку
вели в кварцевой водоохлаждаемой печи /.
Систему откачивали диффузионным и форвакуум-
ным насосами. В процессе опыта пуск обогащенной
смеси в реакционную печь совмещали с замером
давления манометром Мак Леода 19 с чувствительностью
±0,1 Па. Ртутный манометр с микроскопной
приставкой 18 служил для замера конечного давления газа.
Отбор проб газа производили вакуумным краном 9
через обогреваемую трубку 8. Во время опыта
производили контроль отношения С160/С180 с интервалами
7* Зак. 664
195
1,5—2 мин. Изотопное отношение регистрировали
масс-спектрометром.
Ход опыта можно представить следующим образом:
в реакционную камеру впускают эталонный газ с
известным соотношением С160/С180 и расплавляют
металл; Происходит изотопный обмен с участием
кислорода атмосферы, металла и кислорода, который
Рис. 86. Установка для исследования взаимодействия металла с тиглем при
плавке в вакууме:
7 —кварцевая водоохлаждаемая печь; 5 —подставка; 3 — индуктор; 4 —
тигель; 5 — шлиф из нержавеющей стали; 6 — призма; 7 — пирометр; 8 —
обогреваемая металлическая трубка напуска (к масс-спектрометру); 9 — вакуумный
кран; 10 — датчики вакуумметра; // — баллон; 12 — цеолит при —196°С; 13 —
силикагель; 14 — электролизер; 15 — форвакуумный насос; 16 —
вымораживающие ловушки; 17 — система ампул с цеолитом; 1В — ртутный манометр с
микроскопной приставкой (чувствительностью ±0,1 Па); 19 — манометр Мак
Леода; 20 — диффузионный насос
поступает в металл из корундового тигля при
взаимодействии металла с тиглем. При этом эталонное
отношение С016/С018 изменяется. По этому изменению
можно вычислить количество кислорода, перешедшего
в металл из тигля. Рассмотренный метод дает
достаточно точные результаты, хотя и является сложным.
В более простых методах исследования после
определенной выдержки металла в тигле под вакуумом
196
определяли изменение содержания алюминия,
циркония в металле в результате его взаимодействия с
огнеупорными окислами футеровки.
Моделирование вакуумных процессов
Моделирование образования пузырей газа проводят на жидкостях,
вязкость (которых приближается к вязкости жидкой стали, например
диффузионное масло, глицерин .и т. п. (Процессы образования и
воплывания пузырей фиксируют скоростными кинокамерами,
позволяющими оценить скорость роста зародышей газовой фазы,
наиболее вероятные места образования пузырей газовой фазы.
.Рассмотрим методику, применявшуюся в одной из последних
работ. В качестве жидкости, моделирующей расплавленное железо,
выбран тетрадекан, обладающий вязкостью, |близкой к вязкости
жидкого железа, и низкой упругостью пара. Лентан имитировал
азот, растворенный в железе. Коэффициент диффузии пентана в
тетрадекане 'близок к коэффициенту диффузии азота в железе. Пен-
тан— легко возгоняемая жидкость с температурой кипения 36°С.
Ниже приведены основные физические параметры образца и
модели:
Образец
Среда '. Железо
t, °С 1600
р, г/см3 6,9
\Ь Н/(м-с) 0,05
Модель
Тетрадекан
20
0,772
0,023
'Исследования вели на плоской модели тигля вакуумной
индукционной печи, которая представляла собой стеклянный
параллелепипед размерами 250X 50X400 мм. Модель устанавливали под
вакуумный колпак. Воздух откачивали. Схема установки
представлена на рис. 67.
* S 6 7 8 9 10
17 16
15 т
Рис. 87. Схема опытной установки для моделирования процессов
газовыделения при вакуумной индукционной плавке:
/ — баллон с Не; 2 — редуктор; 3 — хроматограф; 4 — пробница; 5 —
манометр; б —двигатель; 7 —дозатор; 8 — термометр; 9 — тахометр; 10 —
термостат; 11 — натекатель; 12 — расходомер; 13 — подушка с Не; 14 —
мешалка; 15 — вакуумная камера; 16 — вакуумный насос; 17 — пористая пробка
197
К дну (модели можно было подводить с регламентированной
скоростью таз (аргон) через (калилляр или пористую пробку. Для
имитации электромагнитного ^перемешивания металла в тигле
индукционной печи в модели установлены по бокам емкости две че-
тырехлопастные мешалки, радиус которых подобран равным
глубине проникновения тока при работе 100-кг индукционной печи. В
профиль 1мешалки представляют собой две трапеции, соединенные
по широкому основанию. Это позволяет получать в металле
картину двушонтурного перемешивания. Мешалки приводили во
вращение от двигателя постоянного тока с регулируемой окоростью
вращения. Температуру жидкости в модели поддерживали постоянной.
Контроль расхода газа для продувки устанавливали с помощью
игольчатого натекателя. Количественный анализ удаления пентана
из тетрадекана проводили с помощью газовой хроматографии.
Аналитическая часть установки состояла из системы отбора и
возвращения жидкой пробы, пробницы, термостатированного газопровода
и хроматографа ЛХМ-ЗМД. На модели можно создавать
различные режимы продувки металла и с помощью фото- и киносъемки
фиксировать картину прохождения пузырей газа через ванну.
Гидродинамическое подобие движения металла и моделирующей
жидкости определяли из критериев Рейнольдса для образца и
модели. Из равенства критериев Рейнольдса находили скорость
движения жидкости в модели:
Рм о>м ^м Ро ю0 Iq
Им f*o
где ро и рм — плотность образца и жидкости модели; <о0 и <ом —
скорость движения жидкости образца и модели; /0 и
/м—характеристическая длина образца и модели (принимается равной глубине
проникновения тока в расплав и радиусу мешалки); ц0 и ,jxM —
динамическая вязкость образца и модели.
Скорость движения металла в тигле вакуумной индукционной
печи равна 0,3 м/с. Скорость движения жидкости в модели для
соблюдения равенства критериев Рейнольдса составит 1,24 м/с, а
-скорость вращения мешалок 1240 об/мин.
ГЛАВА VI
ИЗУЧЕНИЕ ПРОЦЕССОВ ВОССТАНОВЛЕНИЯ
И ДИССОЦИАЦИИ ОКИСЛОВ
Большинство металлов в природе находится в виде
окислов. Путем восстановления окислов получают
чистые металлы и сплавы. Восстановителями могут
быть твердые и газообразные вещества. В общем
случае реакция восстановления имеет вид: МеО + В =
=Ме-{-ВО, где В— восстановитель. В качестве
восстановителей применяют вещества, обладающие в
данных условиях большим сродством к кислороду, чем
восстанавливаемый элемент.
198
Для разработки эффективных методов
промышленного получения металлов из окисленных руд
необходимо знание физико-химических равновесных и
кинетических характеристик процессов восстановления.
1. МЕТОДЫ ИССЛЕДОВАНИЯ ПРОЦЕССОВ
ВОССТАНОВЛЕНИЯ
Для определения термодинамических характеристик
восстановительных реакций необходимо создание или
достижение равновесных состояний. В гетерогенных
системах: газ — твердая или жидкая фаза и в системах
из различных твердых фаз о достижении равновесного
состояния судят по изменению давления или объема
газовой фазы, по изменению массы реагирующих фаз,
по кривым нагрева и охлаждения и т. п.
Наибольшее распространение при изучении
восстановительных процессов получили методы с участием
газовой фазы, а именно статический и динамический.
Статический метод. В герметичной установке
выдерживают заданные количества вещества и газовой
фазы при заданных температуре и давлении. Через
определенные промежутки времени анализируют
пробы газа. Состояние равновесия считают достигнутым,
если результаты нескольких последовательных
анализов совпадают.
К достоинствам метода относится сравнительная
простота аппаратуры.
Недостатки связаны, во-первых, с малой скоростью
установления равновесия во всем объеме газовой
фазы. Газовая атмосфера неподвижна, поэтому, несмотря
на то что вблизи поверхности твердой фазы равновесие
устанавливается быстро, обновление атмосферы у
поверхности путем диффузионного переноса происходит
медленно. Это приводит к неравномерности газовой
атмосферы вблизи и вдали от реакционной поверхности
и к нерепрезентативному анализу газовых проб.
Более широкое применение получил статический
метод с исследованием равновесия по измерению не
состава, а давления газовой фазы. Таким методом
исследуют реакции: 2МеО = 2Ме + 02\ МеС03 = МеО +
+ С02; МеО + С=Ме+СО.
Динамический метод. В этом методе над
поверхностью твердого вещества создается поток газа с такой
скоростью, чтобы за время прохождения над твердой
199
или через твердую фазу успевало наступить состояние
равновесия. В этом случае последующий анализ
газообразной фазы дает непосредственные равновесные
величины.
Циркуляционный метод состоит в том, что над
поверхностью твердой или жидкой фазы пропускается
газовый поток. Вся установка герметизирована. Газ
неоднократно проходит над твердым веществом до
наступления постоянства состава, которое фиксируют
химическим, хроматографическим анализами проб газа,
по теплопроводности, интерференционной способности
и т. п.
Этот метод сложен в аппаратурном оформлении;
для его осуществления необходимы циркуляционные
насосы, сложное термостатирование и т. п.
Важное значение имеют исследования кинетики
процессов восстановления. В этом случае непрерывно при
данных условиях опыта регистрируют изменение таких
характеристик взаимодействующих фаз, как давление
газовой атмосферы, ее состав, масса и состав твердых
фаз или теплопроводность, электропроводность и др.
Ниже приведены некоторые экспериментальные методы
анализа.
Циркуляционный метод
Рассмотрим исследование процесса науглероживания
восстановленного железа восстановительными
газовыми смесями, состоящими из СО, С02, Н2, СН4. В
системе одновременно протекают следующие реакции:
H2Q+CO = H2+C02; [C]Fe+C02=2CO; [C]Fe+2H2=
= СН4.
Для определения науглероживающего потенциала
газовой фазы необходимо подобрать такие
концентрации углерода в железе, чтобы обеспечить постоянство
количественных отношений Н/С и О/С в исходной
и равновесной газовых фазах. Экспериментальная
установка (рис. 88) позволяет приводить систему к
равновесию последовательно, в две стадии. Первая стадия
включает перераспределение углерода между газовой
и твердой фазами, а вторая — контроль равновесного
состояния системы. Установка содержит узлы
подготовки, маностатирования, контроля расхода газа,
увлажнения, осушки, очистки, циркуляции и термостатиро>
вания газовой фазы сложного составу
200
я « 3
1* *
«835
H О) К H
Л К p.*
Я Я
U я g
Л - О
оо о я К.
оо е(Я 5
а> g *
Я о О Я
а, я и с*
5 з
о S 5 » £
г? о о. ч я
« I я о
з^ t-
Sens -
s«*'*
S 2|i
о •* Ю
о.я я >. i
57 о ч o. '
I о» >»
о<*э I I 5 ка i о ci"* o.~ ft я
о ад 5
о
< 4 v
5 ft-
5 ft *
я «и (_
2 s Й
S Й5
л n «
4 rt S
Я я
зе i
i ь.
S..B
о я °
lis
Я O^.
4 «-•
'*Sp3 5 5 Жид
iris 2.8а&&£«
is&ei^fSiSf is
|?t|gg gI § 1^ g
л I В I 1 йо I l Эе
^,q OJOOCN! CJ I
° ° « Н ...
и е р,& _
P s\o I о u I I I 2 .. I и
И н Н*^ OX<Nc^es 2U«b P, W
201
Система подготовки газовой смеси состоит из двух
сообщающихся герметичных сосудов: подвижного / и
неподвижного для газовой фазы 3, баллонов с газами
С02, Н2, СН4 и аппарата для получения СО. В сосуды
в качестве запорной жидкости налит насыщенный
водный раствор поваренной соли, подкисленный
соляной кислотой.
В сосуд 3 газы Н2, СО и СН4 подают через систему
очистки, наполненную активированным углем 6 и
пирогаллолом 7, для очистки от кислорода. Давление газа
в сосуде 3 поддерживают постоянным и контролируют
манометром 9. Объем газа фиксируют по уровню
жидкости в мерной трубке 4. Газовый сосуд термоста-
тирован водяным охлаждением. После заполнения
сосуда 3 газовой атмосферой приводом 2 перемещают
подвижный сосуд / вверх. Чтобы кислород не попадал
в газовую смесь при истечении раствора в сосуд 3,
в подвижный резервуар / подают аргон, избыточное
давление уменьшают регулятором 5, соединенным
с манометром 10, Таким образом, раствор жидкости
является оборотным, что способствует стабилизации
состава газовой фазы.
Применение мешалки с электроприводом 5
исключает расслоение жидкости по удельному весу. Расход
газа устанавливают регулятором входного давления 11
и контролируют реометром 12. На выходе из реометра
газ осушается системой поглотителей 13 или
увлажняется в термостате 16.
Ход опыта можно представить следующим образом.
Навеску железного порошка 30 помещают на конце
кварцевой трубочки в реакционную печь. Систему
продувают очищенным аргоном. Температуру в печи
контролируют и регулируют с помощью термопар 31 и 32.
В первой динамической части опыта происходит
перераспределение углерода между газовой и
конденсированной фазами. Отходящий газ выпускается в
атмосферу через кран 34 и склянку Тищенко. С помощью
пробоотборников 24 порции газа отбирают для
анализа на хроматографе.
По достижении постоянного состава газовой фазы
включают циркуляционный контур, состоящий из
компенсатора давления 20, мембранного насоса 21 и
ртутного манометра 23. Для предупреждения конденсации
водяного пара циркуляционный контур помещен
в термостатирующее устройство 19.
202
При циркуляции газовой среды состав ее несколько
изменяется, поэтому в циркуляционный контур время
от времени добавляют порции исходной газовой фазы.
Операции повторяют до установления постоянного
состава газовой атмосферы, который и является
равновесным для данного содержания углерода в железе.
Исследование восстановления окислов металлом
проводят на установке, схема которой приведена на
рис. 89. В печи сопротивления 10 помещена
реакционная трубка 11, внутри которой находится навеска
образца. Циркуляция газов в объеме осуществляется
мембранным насосом со скоростью 50 л/ч. Давление
в системе поддерживается постоянным с помощью
компенсатора давления 16. Датчик изменения давления
выполнен на базе манометра НМ-П1К-5. К стрелке ма-
Рис. 89. Схема установки для исследования процессов восстановления
циркуляционным способом:
/ — регулятор содержания паров воды в газовой фазе; 2 — электронный блок
управления влагомера; 3 — фотосопротивление; 4 — источник света; 6 —
термостат; 6 — рабочая камера датчика влажности; 7 — хромель-копелевая
термопара; 8 — краны переключателя газовой системы; 9 — датчик изменения
давления; 10 — печь сопротивления; // — реакционная трубка; 12 — образец;
13 — реверсивный двигатель; 14 — реохорд; 15 — регистратор изменения
объема системы; 16 — компенсатор давления; 17 — возбудитель циркуляции газя
203
нометра прикреплен легкий светонепроницаемый
флажок, закрывающий два фотосопротивления ФС-1,
входящих в электронную схему управления работой
реверсивного двигателя РД-09-6.
При постоянном давлении в системе флажок
закрывает оба фотосопротивления. С изменением давления
в ту или иную сторону флажок смещается и открывает
одно из фотосопротивлений. Срабатывает реле,
замыкающее цепь питания реверсивного двигателя. При
вращении реверсивного двигателя колокол
компенсатора давления отходит от первоначального положения,
что соответствует изменению объема системы, которое
вызывает отклонение давления ±50 Па. В качестве
запирающей жидкости в компенсаторе давления
использовали полиметилсилоксановую жидкость ПМЖ-5,
обладающую высокими гидрофобными свойствами.
Совместно с комплексом стабилизации давления
в системе смонтирован датчик регистрации изменения
объема газа. На валу реверсивного двигателя
закреплен движок реохорда, питаемого постоянным
напряжением. Регистрируемая потенциометром величина
сигнала, снимаемого с реохорда, прямо
пропорциональна изменению объема газа, что в свою очередь
характеризует степень превращения метана.
В системе автоматизирована запись определения
содержания водяного пара с помощью датчика
влажности, выполненного на базе влагомера ВИГ-ЗМ.
Для определения объема всей газовой системы ее
длительное время промывают двуокисью углерода,
которую затем вытесняют инертным газом в поглотитель
с аскаритом. Объем С02, соответствующий объему
системы, определяют методом взвешивания. По объему
системы и по конечному равновесному составу газа
рассчитывают минимально необходимое количество
окиси железа, достаточное для изучения равновесия,
на различных ступенях восстановления.
Опыты проводили в атмосфере метана, который
получали из природного газа методом препаративной
хроматографии на четырехметровой колонке диаметром
18 мм, заполненной активированным углем. Опыт
продолжался в течение 18 ч. Газовую систему
продували метаном. Исходный газ анализировали на
хроматографе, определяли в нем также содержание паров
воды.
204
Последовательное включение датчика влажности
в газовую схему установки позволяет определять
концентрацию паров воды по мере приближения системы
к равновесию, свидетельством которого является
стабилизация объема и содержания паров воды в газовой
фазе. Основой для заключения о достижении системой
равновесия является постоянство состава газовой фазы.
Гравиметрический метод
При изучении кинетики восстановления окислов газами
о скорости восстановления судят по изменению массы
образца или по составу отходящего газа. Такими
методами исследуют реакции: МеО-\-СО=Ме-{-С02\
МеО+Н2=Ме+Н20\ МеО+С=Ме+СО. В системе
Fe — 02 — С — Н2 кинетика восстановления значительно
осложняется науглероживанием образца, которое
.протекает одновременно с восстановлением.
Термогравиметрический метод
Наибольшее распространение среди гравиметрических
получили методы, в которых взвешивание производят
по ходу процесса восстановления. Причем
взвешивающее устройство может быть расположено как вне
реакционного пространства, так и внутри него. Сама
операция взвешивания может осуществляться дискретно
или непрерывно.
При создании экспериментальных установок такого
типа возникают существенные трудности, связанные
с герметизацией установки. Необходимо предотвращать
конденсацию паров или возгоны твердой фазы на
частях измерительного устройства, окисление
металлических подвесок и иных деталей устройства, влияние
тепловых излучений и газодинамических потоков на
работу весового устройства. Весовое устройство должно
быть компактным, чтобы реакционный объем установки
не был излишне большим.
Рассмотрим устройство термогравиметрической
установки с непрерывным анализом газа и взвешиванием
образца. Общая схема установки представлена на
рис. §0. Газ-восстановитель из баллонов через систему
очистки и реометр поступает в реакционное
пространство, которое представляет собой кварцевую трубку.
Из печи газ попадает в приемник газоанализатора
и затем выпускается в атмосферу.
205
Печь сопротивления снабжена системой
терморегулирования, которая поддерживает заданный
температурный режим с точностью до ±1°С. Печь может
перемещаться по вертикали, что позволяет быстро
охлаждать навеску по окончании опыта.
?
CSpoc
г П \
\ч\
У
\
со
С02
сщ
Ш]
Рис. 90. Схема установки для исследования процессов восстановления с
непрерывным автоматическим анализом газа:
1 — поглотители; 2, 3 — реометры; 4 — автоматические газоанализаторы; 5 —
печь; 6 — потенциометр КСП-4 для измерения температуры; 7 — термопара;
8 — устройства для вертикального перемещения печи
Для непрерывной автоматической записи массы
пробы применен индуктивный датчик ИМП-2,
связанный с потенциометром ЭПД-09. Чувствительность
датчика ±0,005 г при диапазоне взвешивания 0,1—
100 г.
Разновидностью весового устройства является ме-
ханоэлектрический преобразователь Э-2Д1, который
линейно преобразует изменение массы образца,
подвешенного, к чувствительному элементу, в сигнал
постоянного, тока. Этот сигнал делится постоянным
сопротивлением, и часть его направляется на потенциометр
ЭПП-09 и непрерывно записывается на диаграммной
ленте. С помощью сопротивления и балансировочного
206
устройства, вмонтированного в датчик, можно
регулировать величину выходного сигнала в зависимости от
нужного масштаба и градуировки потенциометра. При
общей массе подвесной системы до 20 г изменение
массы в 1 г фиксируется с ошибкой <0,5%.
К коромыслу датчика подвешена кварцевая трубка
со шлифом, к которому подсоединен стакан с пробкой.
В дне стакана имеются прорези для прохождения
реакционного газа. Газ проходит через стакан и затем
поступает в газоанализаторы.
Блок газоанализаторов состоит из трех оптико-
акустических газоанализаторов ОА-2109, ОА-2209,
ОА-2309, для определения метана, окиси углерода и
углекислоты и электрического газоанализатора на
водород ТП-1120.
Перед началом восстановления пробу нагревают до
заданной температуры в среде инертного газа.
Охлаждение пробы также производят в инертном газе. Затем
напускают природный газ и анализируют его состав во
времени на Н2, СО, СН4, С02 и Н20.
Для проведения опыта используют динамический
метод. В реакционный сосуд с пробой подают
восстановительный газ постоянного состава. Изменение
состава газа в результате протекания процесса
восстановления устанавливают методом анализа проб газа
после прохождения его через реакционный сосуд.
Этим методом изучали процесс восстановления
окислов металлов твердым углеродом с вымыванием
продуктов реакции инертным газом. В результате
протекания реакции: МеО-\-С=--Ме + СО (или С02)
происходит уменьшение массы образца. Скорость
уменьшения массы образца и0бр равна сумме скоростей
образования СО (усо) и С02 (<исо2) в газовой фазе,
которые определяются из выражения для скорости,
мг/мин:
V{=MLiJLJ™f (72)
где Mi — молекулярная масса i-того компонента
отходящего газа; и* —объем 1 моля газа при комнатной
температуре; i — содержание /-того компонента в
отходящем газе, %; Q — расход инертного газа,
подаваемого в систему, см3/мин; Висх и В0тх —концентрация
инертного газа в исходном и отходящем газах» %.
207
Отношение Висх/Вотх характеризует коэффициент
увеличения объема газа вследствие протекания всех
реакций в системе. Так как и£°= — Vco и ио°* =
28
32
= 44 Vc°21 то сУммаРная скорость восстановления Wo
в данный момент времени может быть определена из
выражения
% =
16Q£„
(*со + 2 /со2)
щ 100 Вотх
Скорость обезуглероживания образца vq
рассчитывается аналогичным образом:
12Q5„CX
^ =
(*со + *со2) •
щ 100 Яотх
Кроме химических методов анализа газовой фазы,
применяют хроматографический анализ.
Образующуюся в ходе опыта газо-
АДВ-200
вую атмосферу через
определенные
промежутки времени
отсасывают газовыми
пипетками, которые
располагают на выходе из
реакционного
пространства.
В некоторых опытах
на пути газа,
отсасываемого в пипетки,
для поглощения
водяного пара
устанавливают патрон с
карбидом кальция.
Образующийся в результате
взаимодействия
водяного пара с СаС2
ацетилен служит
показателем содержания
водяного пара в газовой
атмосфере. Пробу газа
направляют в
хроматограф.
Кроме электромеханических датчиков, используют
и обычные аналитические весы. На рис. 91
представлена схема установки, в которой взвешивающим
Рис. 91. Схема термовесовой установки
208
устройством являются стандартные аналитические весы
АДВ-200 с автоматической компенсацией изменения
массы образца. На одном из плеч коромысла весов /
подвешен магнит 2У находящийся внутри соленоида 5.
На другом плече коромысла закреплены чашки 4,
к одной из которых на платиновой отожженной нити
подвешена чашка 5 с исследуемым веществом. Весы
герметично закрыты колпаком из органического стекла.
Чашки 4 служат для уравновешивания исследуемого
образца в исходном положении. Это позволяет
уравновешивать с помощью соленоида лишь изменения массы
образца, возникающие при протекании процесса
восстановления.
Схема автоматической компенсации изменения
массы образца собрана на базе потенциометра 6 типа
ЭПП-09 с использованием его усилителя, реверсивного
двигателя и реохорда.
При изменении массы на 0,1 мг замыкается
соответствующая пара платиновых контактов <5,
укрепленных на стрелке и по обе ее стороны на шкале весов.
При этом сигнал постоянного тока от потенциометра 7
поступает на потенциометр 6. Усиленный сигнал
приводит во вращение двигатель, перемещающий контакт
реохорда, и тем самым изменяет силу тока в соленоиде
3, т. е. происходит компенсация изменения массы.
Одновременно этот параметр регистрируется.
Для оценки регистрируемого изменения массы
служит градуированная шкала прибора ЭПП-09.
Градуировка осуществляется с помощью стабилизированного
источника постоянного тока 9 и разновесов,
помещаемых на балластную чашку 4,
Метод регистрации фазового состава
Применяемые методы регистрации изменения массы
образца не позволяют непосредственно судить о
фазовом составе продуктов.
Существуют установки, в которых одновременно
производится и взвешивание образца, и регистрация
изменения фазового состава, например по магнитной
проницаемости.
На рис. 92 приведена схема установки, в
реакционной трубке которой подвешена кварцевая корзинка
с прорезями для омывания пробы газом. Реакционная
трубка через соответствующее переходное устройство
209
^ fi&ZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZZ
Аргон_ ^
bssssKl^l^ \
в
S
а—-7
Подвод газа
крепится к плите, на которой смонтировано весовое
устройство. Сверху весовой датчик закрыт герметичной
крышкой. Под крышку вводится аргон для создания
избыточного давления, затрудняющего проникновение
к весовому датчику газообразных продуктов реакции.
В качестве весового датчика использована
индуктивная катушка от прибора ЭПИД. Ее сердечник'
подвешен на двух плоских пружинах 12. Катушку 13 при
помощи варьерного устройства 14 можно перемещать
относительно сердечника.
Корзинка с восстанавливаемым образцом
подвешивается на нихромовой цепочке к сердечнику 11 таким
образом, чтобы центр ее совпадал с центром верхней
катушки датчика магнитной проницаемости 15. Датчик
предохраняется от нагрева водоохлаждаемой
кварцевой рубашкой 16.
Регистрирующая часть установки состоит из двух
схем, конечными элементами которых являются
электронные потенциометры, записывающие изменения
магнитной проницаемости и массы образца как
функции времени восстановления.
Запись изменения массы производится следующим
образом. На первичную обмотку индуктивной катушки
датчика подается напряжение при частоте 1000 Гц. Со
вторичной обмотки катушки э. д. с. снимается на
усилитель, выходной сигнал которого после выпрямителя
записывается на диаграмме самописца ЭПП-09. Перед
началом опыта перемещением катушки датчика
относительно сердечника измерительная система
балансируется на нуль (к сердечнику при этом подвешивается
груз, равный весу кюветы с восстанавливаемой пробой)
и калибруется с помощью гирь. Чувствительность
схемы в широких пределах можно регулировать
жесткостью пружин, поддерживающих сердечник, величиной
напряжения на первичной обмотке катушки и
изменением коэффициента усиления усилителя.
Компенсационные схемы, поставленные на входе приборов для
Рис. 92. Схема установки для исследования фазового состава:
/ — кварцевая корзинка; 2 — фарфоровая труба; 3 — нихромовый
нагреватель; 4 — металлический стакан; 5 — металлическая труба; 6, 10 — крышки;
7— гайка; 8 — фланец; 9 —плита; // — сердечник; 12 — плоские пружины;
/5 —катушка; 14 — варьерное устройство; 15 — датчик магнитной
проницаемости; 16 — водоохлаждаемая кварцевая рубашка; 17 — регулирующая
термопара; 18 — измерительная термопара
211
регистрации изменения массы и магнитной
проницаемости, позволяют менять уровень записи и тем самым
растягивать ординаты кривых.
Помимо гравиметрических методов исследования
восстановительных процессов, с успехом используются
и другие способы оценки изменения состава, количества
и структуры образующихся и изменяющихся фаз.
Например, исследование с применением рентгеновской
микроскопии. Этот способ дает возможность
«заглянуть» непосредственно в микрообъемы реагирующих
веществ.
Метод рентгеновской' спектроскопии заключается
в том, что рентгеновское излучение через навеску
образца, помещенного в реакционном объеме,
фиксируется пленкой. Изменения, происходящие в образце,
отражаются на рентгенограммах.
Рентгеновские лучи проходят через камеру
высокотемпературного рентгеновского микроскопа, сквозь
образец, помещенный на прозрачной для излучения
подставке. Образец из рудно-топливной смеси готовят
в виде таблетки. Нагреватель печи сопротивления
графитовый. Под установкой в кассете помещают
рентгеновскую пленку. Кассету перемещают по
направляющим пазам таким образом, чтобы в ходе опыта
получить до 30 снимков с экспозицией от 0,5 с до
5 мин. Рентгенограммы отражают физические
изменения, происходившие в образце, например рост
кристаллов восстановленного железа.
Для непосредственной фиксации объемных фазово-
структурных превращений, происходящих с материалом
в ходе восстановления, применяют дилатометрический
метод. Схема установки представлена на рис. 93.
Возможны два варианта работы установки. В первом
варианте образцы помещают в калиброванный
кварцевый тигель-и засыпают кварцевыми шариками
диаметром 0,3—0,4 мм. Шарики плотно укладываются поверх
образца и трансформируют объемные изменения,
происходящие с образцом, в линейные, которые
фиксируются с помощью штока, опирающегося на поверхность
шариков. По перемещению штока определяют
объемные превращения в образце.
Во втором варианте шток непосредственно
опирается на поверхность образца. Перемещение штока
определяется с помощью индикатора часового типа с ценой
212
деления 1 мкм либо индуктивным датчиком ИМП-2.
Шток проходит через резиновую диафрагму,
допускающую его перемещение в пределах нескольких
миллиметров.
Рис. 93. Схема дилатометрической установки:
1 — исследуемые образцы; 2 — кварцевый тигель; 3 — кварцевые шарики; 4 —
металлическая сетка; 5, 11 — кварцевые трубки; 6, 12 — фторопластовые
пробки; 7, 15 -— термопары; 8 — шток; 9 — индикатор перемещения; 10 — груз;
/3 —диафрагма; 14 — электропечь; 16 — водоохлаждаемый кожух; 17 — штанга
для монтажа
Большое распространение получили исследования
восстановления расплавленных окислов жидкими
металлами. Так как в основе взаимодействия металла со
шлаком лежат электрохимические процессы, то для
213
изучения их успешно могут быть применены
электрические методы. Суть их заключается в том, что на
металл, находящийся в равновесии со шлаком,
накладывается импульс постоянного тока и на осциллографе
записывается кривая изменения напряжения во
времени. Обработка осциллограмм позволяет определить
кинетические параметры процесса, а в ряде случаев
и характеристики массопереноса или процессов
адсорбции.
2. ИССЛЕДОВАНИЕ ДИССОЦИАЦИИ ОКИСЛОВ
Важное значение для теории процессов восстановления имеет
изучение закономерностей реакций диссоциации и образования окислов,
т. е, изучение систем: окисел—металл—(газообразный кислород.
Методы изучения этих равновесий можно разделить на две
группы. В первой группе исследуемая твердая фаза приводится в
равновесие с газовой фазой при данной температуре и определяется
состав всех трех фаз. Эксперименты могут проводиться в
статических или динамических условиях. Здесь возможны три варианта:
а) по составу конденсированных фаз находят состав газовой фазы;
б) задают в газовой фазе определенное парциальное давление
кислорода и после наступления равновесия определяют состав
конденсированных фаз; в) находят составы всех трех фаз.
Во второй .группе исследований определяют химический
потенциал кислорода в гальванических ячейках с участием окислов.
Статические условия опыта. Окисел нагревают до нужной
температуры в замкнутом откачанном объеме и измеряют давление
кислорода, (установившееся в системе над равновесными
конденсированными фазами. Использование этого метода ограничено
малыми давлениями кислорода, от 133 до 0,1 Па. Необходимо иметь в
виду, что при высоких температурах тазовая фаза может наряду
с кислородом содержать пары окисла и продуктов его
диссоциации — низших окислов, металла.
Динамические условия опыта. В этом методе газовую фазу
постоянного состава непрерывно пропускают над реагентами. По
достижении равновесия анализируют конденсированные фазы. iB
качестве газовых смесей с контролируемым парциальным давлением
кислорода могут быть использованы кислород при давлении
100 кПа, воздух (Рог—21 кПа), амеси кислорода с инертным газом,
смеси СО-^С02, Н2—Н20.
Успешно применяется метод измерения равновесного отношения
Рн2о IP н21!ЛИ PcoJPz°- Метод заключается в определении состава
газовой фазы, равновесной по отношению к конденсированным
фазам известного состава, при определенной температуре.
Если определить равновесное отношение рн 0 //? н или рсо /
/рсо для реакции Me«0y+H2(CO)^tAle»O»+H20(C02) и константу
равновесия реакции H2O^H2-f V2O2 (С02^СО+7202)
К = РН2 (СО) Ро2*/РнгО (СО,) .
214
то для реакции МехОум±МехОу-1+х1202 парциальное давление
кислорода составит
Ро22 = % Рн20 (СО )/Рн, (СО) •
Для окислов постоянного состава величины х и у обычно
известны, и задача сводится лишь к определению Рц2о /Рн2» Pcot I
/рсо. Если конденсированные фазы, находящиеся в состоянии
равновесия, представлены окислами переменного состава (твердые
растворы)
(Ме1^ • Ме1 • • ■ ■ • Ме*п) °у - (^i, • Ме\\. ■■■• *К) °у-т •
то необходим анализ их состава.
Описание метода. Навеоку окислов выдерживают при
определенной температуре в атмосфере Н2+Н20 (СО+С02) в условиях
непрерывной циркуляции «газовой фазы до установления
равновесия. По достижении равновесия анализируют газовую фазу.
Водяной пар или двуокись углерода вымораживают в ловушке жидким
азотом и измеряют давления рн (СО)- При необходимости
анализируют и твердую фазу химическим или рентгеновским методом. При
использовании смеси СО—С02 надо иметь в виду, что при 300—
700°С возможна реакция разложения окиси углерода.
Рис. 94. Установка для определения равновесного соотношения
/ — навеска; 2 — ловушка с водой; 3 — электропечь; 4 — кварцевая трубка;
5 — циркуляционные насосы
На рис. 94 представлена схема установки для исследования в
атмосфере Н2—Н20. Опыты проводят в замкнутом объеме
циркуляционным способом. Источником фиксированного давления
водяного пара ;служит сосуд с водой, помещенный в соответствующую
холодильную смесь. Задавая различное давление водорода, можно
215
создавать восстановительную или окислительную атмосферу и
таким образом приближаться к равновесию, а также регулировать
степень восстановления.
При термогравиметрическом методе исследования диссоциации
окислов в замкнутом объеме непрерывно взвешивается образец при
изменяющемся давлении кислорода и постоянной температуре или
при постоянном давлении кислорода и непрерывно меняющейся
температуре. Момент появления
новой фазы фиксируется по
изменению массы образца.
Методом э. д. с. определяют
химический потенциал
кислорода в гальванической ячейке с
твердым электролитом.
Измеряют э. д. с. ячейки, одним из
электродов которой является
иоследуемая система, другим —
система с известным
кислородным потенциалом. Рассмотрим
два варианта этого метода.
В камере с неразделенным
газовым пространством (рис.
95) ячейка состоит из твердого
электролита и электродов,
закрепленных между брусками
плавленого кварца. Ячейку
помещают в кварцевый реактор,
находящийся в электропечи. В
качестве электрода сравнения
используют металл с окислом,
например Fe—FeO, Ni—NiO,
Si—SiC>2. Этот метод пригоден
для бинарных систем, когда
состав фаз в результате
окислительно-восстановительных
процессов остается неизменным.
Если исследуемый электрод
включает фазы переменного
состава, например твердые
растворы, то состав их может
изменяться в ходе опыта,
приводя к неверным результатам.
Возможен также
неэлектрохимический перенос кислорода
между электродами. Это создает возможность протекания
дополнительных неучитываемых окислительно-восстановительных реакций.
В камере с разделенным газовым пространством в пробирку,
изготовленную из твердого электролита, например из двуокиси
■циркония, помещают образец. Электрод сравнения находится с
внешней стороны пробирки, омывая ее в случае газового электрода
или контактируя с ней, если электрод сравнения твердый. Такая
ячейка помещается в кварцевый кожух, который в свою очередь
вводится в печь для нагрева до заданной температуры.
Метод э. д. с. имеет недостатки. При исследовании окислов с
низким коэффициентом диффузии установление равновесия в объ-
Рис. 95. Прибор для измерения э. д. с.
гальванической ячейки с
неразделенным газовым пространством:
/ — таблетка А1203; 2 — платиновая
пластина; 3 — образец; 4 — таблетки
твердого электролита; 5 — электрод
сравнения; 6 — подложки для образца;
7 — термопара; 8 — токоотводы; 9 —
трубка из корунда; 10 — кварцевая
трубка; // — стеклянный шлиф
216
i
еме образца сильно затруднено. На поверхности образуется
пленка, отличающаяся по составу от образца. Кислород может
диффундировать сквозь электролит при значительной разности давлений
по обе стороны электролита. Может -иметь место взаимодействие
электролита с исследуемым объектом.
ГЛАВА VII
НЕМЕТАЛЛИЧЕСКИЕ ВКЛЮЧЕНИЯ В МЕТАЛЛАХ
Большое влияние на свойства сталей и сплавов оказывают
неметаллические включения, присутствующие в твердом готовом
металле. Состав, строение, размер этих частиц во многом определяют
качество металла. Количество неметаллических включений,
находящихся в металле, является мерой степени загрязненности металла, как и
содержание газов. Состав и природа включений, которые образуются
вследствие процессов взаимодействия элементов металла, могут
дать важный материал для понимания сущности процессов,
происходящих в твердом и жидком состоянии.
iB зависимости от способа образования включения делятся на
эндогенные -(образовавшиеся в результате протекания различных
процессов в самом металле) и экзогенные (занесенные в металл
извне). По химическому составу наиболее часто встречающиеся
неметаллические включения можно разбить на группы: а) оксидные;
б) -сульфидные; в) нитридные; г) карбидные; д) смешанные,
например оксисульфидные, карбонитридные.
1. МЕТАЛЛОГРАФИЧЕСКАЯ ОЦЕНКА ВКЛЮЧЕНИЙ
На практике для оценки загрязненности металла большое значение
имеет подсчет числа неметаллических включений, встречающихся на
металлографических шлифах. Для объективной оценки
загрязненности партии металла служат специальные методики отбора проб для
изготовления шлифов, методы подсчета и выведения оценки
загрязненности по определенным шкалам в баллах или процентах по массе.
Рассмотрение включений на шлифах дает возможность сделать
предварительные выводы о характере включений, о чистоте металла
без выделения включений и их химического анализа.
Металлографический метод (позволяет выявить распределение
включений в готовом металле, слитке или изделии, дать
качественную характеристику включений. (Полностью достоинства
металлографического метода раокрываются только в сочетании с другими
методами исследования включений.
Изготовление металлографических шлифов
Важнейшее значение для металлографического метода имеет
подготовка шлифов. Для изготовления металлографического шлифа
образцы вырезают из проб металла. Если размер образцов небольшой,
то один или несколько образцов заливают в оправку с помощью
серы, свинца, тритника, полистирола и других пластмасс. Перед
шлифовкой образец из мягкого металла рекомендуется закаливать, В за-
217
висимости от вида рассматриваемого металла выбирают тот или
иной метод «подготовки шлифов. Сначала -поверхность образца
выравнивают на наждачном «руге. Далее шлифуют на станках с
помощью шлифовальной бумаги. Шлифовка .последовательно
производится на бумагах № 180, 220, 240, 280, 320. Шлифовка -производится
таким образом, чтобы после поворота шлифа на 90° вывести риски
на шлифе от бумаги предыдущего номера. После шлифовки образец
предварительно полируют на полировальном диске, обтянутом
парусиной или сукнам, наждачным порошком с величиной зерна 7—
10 мкм с водной мыльной эмульсией или водно-спиртовым раствором.
Окончательную полировку производят на плотном сукне, фетре.
Из абразивов лучше всего применять отмученную трехокись
алюминия или окись хрома с величиной зерна 0,5—3 мкм.
Электромеханическая полировка позволяет быстро подготовить поверхность шлифа
без механических ее повреждений. Во время полировки шлиф
является анодам. Применяются различные электролиты и режимы
полирования в зависимости от состава сплава. В качестве электролита
служит концентрированная азотная кислота или смесь азотной (75%)
и уксусной (25%) кислот. Перед просмотром под микроскопом шлиф
протирают спиртам для удаления остатков полировочных
материалов.
Оценка загрязнения металла включениями
Вначале включения рассматривают под микроскопом при
увеличении в 100 раз в светлом поле зрения. Оценивают качественную
картину загрязненности металла, расположение включений, их внешние
признаки. Затем переходят к большим увеличениям (до 500 раз),
подробно рассматривая отдельные виды включений, в особенности
сложные.
Следующая ступень осмотра — наблюдение в темном поле зрения,
в котором определяют прозрачность включений, цвет включений,
строение прозрачных частиц. С помощью наблюдения в скрещенных
николях анализируют оптические включения в поляризованном свете,
что дает возможность разделить неметаллические включения на
изотропные и анизотропные. Изотропные включения всегда
остаются темными при любых положениях анализатора.
Обнаруженные включения сравнивают с табличными данными, с
фотографиями эталонов, определяя принадлежность включений к
тому «или иному типу.
Количественную оценку загрязненности металла производят по
двум основным методикам: 1) подсчет включений, встречающихся
на шлифе, в процентном отношении по массе и 2) подсчет по
эталонным шкалам.
'В первом случае делают следующие допущения: а) масса
включений так относится к массе металла, как площадь, занимаемая
включениями, к площади шлифа под микроскопом; б) пластичные
включения представляют собой тела вращения — эллипсоиды, а
непластичные— сферы. Для оценки по первой методике
просматривают 10 полей зрения при увеличении в 100 раз. На каждом поле
зрения определяют -размеры всех включений, подсчитывают их площадь
в единицах шкалы окулярмикрометра и распределяют их по восьми
труппам, имеющим пределы от 0,1—0,25 до 21,6—42,9 мкм в
единицах шкалы.
213
Каждая группа имеет свой определенный индекс значимости.
Путем умножения числа включений данной группы на ее индекс и
последующего сложения восьми произведений числа включений в
группах-на их индекс значимости определяют общую площадь
включений. Далее подсчитывают количество включений в процентах по
массе, используя формулу
Q=100//Sd ,
где i — индекс, представляющий площадь всех включений,
приходящихся на одно поле зрения (1 = общая площадь включений/число
полей зрения); S — площадь поля зрения, в тех же единицах (при
увеличении в 100 раз 5= 100* 100= 10000); d — отношение
плотности железа к средней плотности включений (можно принять его
равным 3).
Для повышения точности расчета необходимо число образцов
увеличить до 12, а число полей зрения — до 20.
Во втором случае при использовании эталонных шкал
загрязненность поля зрения шлифа сравнивают с эталоном стандартной
шкалы и выражают в баллах данной шкалы. В СССР для оценки
загрязненности стали используют шкалы ГОСТ 1778—70, в которые
входят основные типы оксидных, сульфидных и нитридных
включений.
Наиболее распространенным методом оценки является метод
максимального (балла. Отдельно оценивают загрязненность металла
оксидами, сульфидами, глобулями. В каждом образце выбирают
место, наиболее загрязненное включением данного типа, и
оценивают баллом шкалы. При этом методе оценивается только соответствие
или несоответствие металла условиям ГОСТа, так как не дается
общего загрязнения металла, а принимается во внимание наличие
хотя бы одного поля, но загрязненного включениями самого большого
размера. Для получения надежных, результатов по этому методу
требуется просмотр большого числа шлифов.
Метод оценки загрязненности стали по всей площади шлифа
состоит в том, что один шлиф просматривают целиком при увеличении
в 100 раз, постепенно перемещая его вдоль объектива по строчкам
слева направо и сверху вниз. Отыскивают наиболее загрязненное
поле, сравнивают с таблицей ГОСТа и оценивают баллом эталонной
шкалы. Такую оценку производят для многих шлифов, взятых для
металла одной плавки. Затем определяют количество образцов
(т. е. шлифов) в процентах с баллом 1,0; 1,5; 2,0; 2,5; 3,0; 3,5; 4,0 и
вычисляют среднеарифметический балл для каждого вида
включений (табл. 2).
Для оценки загрязненности применяют метод среднего балла,
для чего сравнивают наиболее загрязненное поле со шкалой. Для
каждого вида включений выбирают наиболее за-грязненное поле по
этому виду включений. Подсчитывают средний балл как
среднеарифметическое из оценок каждого образца для включений данного вида.
Приведенные методики металлографического определения
загрязненности металла, во-первых, «страдают субъективностью
оценки, во-вторых, исключительно трудоемки. В последнее время они
вытесняются способами автоматического подсчета включений на
микроскопах (рис. 96) с одновременной демонстрацией поля шлифа
на большом экране.
В приборе имеется микроскопная оптическая система для
наблюдения за полем шлифа и электронная система для подсчета
219
включений. Фиксация включений основана на различий
отражательной способности металла шлифа и неметаллического включения.
Электронная система развертывает оптический луч последовательно
по всей площади шлифа по методу .горизонтальной либо биллиардо-
шаровой развертки. Отраженный от поверхности образца луч
направляется через щель в фотоэлектронный умножитель. При
изменении интенсивности отраженного света возникает соответствующий
импульс, (который подается в вычислительную часть устройства.
Оно, во-первых, классифицирует включения на оксиды и сульфиды,
регистрирует их по величине, например по длине. Во-вторых,
отдельно подсчитывает долю оксидных и сульфидных включений в общей
массе включений.
.Прибор за 1—5 мин автоматически производит все операции по
просмотру шлифа и оценке включений. Результаты оценки
выдаются на экран или на самопишущую приставку. В некоторых
установках рассматриваемый шлиф проецируется на экране с помощью
телевизионной трубки.
ТАБЛИЦА 2. ОПРЕДЕЛЕНИЕ
ВКЛЮЧЕНИЙ МЕТОДОМ
СРЕДНЕГО БАЛЛА
Номер
образца
1
2
3
4
5
6
7
8
9
10
Средний
балл
Оксиды
хрупкие
2,0
2,5
1,5
1.5
2,0
2,0
3.0
3,5
2,5
1,0
2,15
Сульфиды
1,0
1,0
0,5
0,5
1,0
1,0
0,5
0,5
0,5
0,5
0,65
Силикаты
1,0
1,0
1,0
1,0
0
КО
2,0
1,0
1,5
0
0,95
(Весьма ценную информацию о составе включений дают
современные электронные, рентгеновские и лазерные методы
исследования неметаллических включений на металлографических шлифах.
По сравнению с анализом выделенных включений эти методы
исключают стадию электролитического или химического выделения
включений, которая может «быть сопряжена с разрушением некоторых
целых включений и требует длительного времени. Точность
определения составляющих неметаллических фаз может превышать
точность химического метода анализа выделенных включений.
2. МЕТОДЫ АНАЛИЗА ВКЛЮЧЕНИЙ НА ШЛИФАХ
Микрорентгеноспектральный анализ
На рис. 97 воспроизведена схема электронного микрозонда.
Электронный луч 2, генерируемый электронным устройством У,
фокусируется и развертывается с помощью генератора развертки 7
1Я\ЧЧЧЧ\Ч\ЧчЧЧЧЧЧЧУЧ^
Рис. 96. Принципиальная схема
микроскопа с автоматическим подсчетом
неметаллических включений:
/ — образец; 2 — объектив; 3 — лампа;
4 — окуляр; 5 — фотоэлектронный
умножитель; 6 — щель; 7 — столик; 8 —
переключатель положения столика
220
й си-стемы электромагнитных линз 3, 4. Луч направляется на
поверхность образца 6. Возникающее при столкновении электронов луча
с неметаллическим включением или с металлической основной
характеристическое рентгеновское излучение измеряется спектрометрами
5, а вторичные рассеянные электроны фиксируются детекторами 14.
Усиленные и преобразованные в
блоках 8 и 13 сигналы подаются на
телевизионные трубки 10 и 11 или на
регистрирующие устройства 9 и 12.
Электронный пучок имеет диаметр
~ 1 мкм и перемещается по двум
взаимно перпендикулярным
направлениям. Две электроннолучевые трубки
смещаются синхронно с
перемещением электронного пучка и дают
изображение зондируемой области. На
обеих трубках возникает
изображение поверхности шлифа, которое
снимают кинокамерой или
поляризационной камерой. Обычно электронный
луч сканирует изображение
линейно — это дает полуколичественную
оценку. Для количественной оценки
измерения необходимо проводить в
исследуемых точках образца. На
рис. 98 показано распределение А1
(a), Mg (б), S (в) и Сг (г) в
глобулярном неметаллическом включении в
стали ШХ'15 (белые точки — наличие
элемента).
В настоящее время
микроанализаторы с электронным зондом
способны определять все элементы, начиная
от бора и кончая ураном. Практический предел чувствительности
электронного зонда 0,01—0,001:%. Для анализа достаточно
исключительно малое количество вещества (Ю-14 г). Кроме
количественного анализа химического состава различных участков
микрошлифа, микроанализатор позволяет методом сканирования электронного
пучка по площади изучать картину распределения элементов на
площади от 40X40 до 300X300 мкм. В лабораториях используют
отечественные приборы типа MAP, французские MS-46 «Камека»,
английские «Геоскан» и др.
Метод 1МИ)Крорентгеновского спектрального анализа с
электронным зондом позволяет установить распределение элементов по
объему включения, выявить состав ядра включения, его оболочки.
Необходимо отметить, что по сравнению с методом выделения этот
способ дает объективную картину действительности, в то время как
при выделении «могут быть разрушены жак целые включения, так и
отдельные их части.
Метод эмиссионного лазерного микроспектрального анализа
Лазерный микрозонд для анализа неметаллических включений
успешно конкурирует «с электронным зондом. На рис. 99 представлена
схема прибора. (Квантовый генератор 2 обеспечивает работу лампы
3. Рубиновый стержень-резонатор 4 испускает световой луч с дли-
Рис. 97. Схема микрорентге-
носпектрального
анализатора
221
Рис. 98. Сканограммы неметаллических включений в стали ШХ15
ной волны 694 нм. Луч проходит через оптический мижроскоп и с
помощью линз 5 направляется на шлиф 6. Фокусировка луча
позволяет получать пятно диаметром 25—40 mikm. С помощью микроскопа
на шлифе выбирают включение для анализа и направляют на
него лазерный луч. Под воздействием луча происходит испарение
вещества включения. Пары проходят между электродами 7,
находящимися под напряжением. Генератор возбуждения 1 возбуждает
газ, образуется спектр свечения паров, фиксируемый спектрографом.
При этом производят спектральный анализ пара и соответственно
элементов на шлифе. Лазерный анализатор имеет пятно большого
размера, до 30 миш, а масса испаряемого вещества равна 10-11 г.
Метод ионного микроанализатора
Принцип работы этого прибора основан на ионной бомбардировке
исследуемой поверхности. Испаряющиеся с поверхности
положительные ионы вещества составляют ионный ток. Измерение
интенсивности тока дает сведения о химическом составе включений.
Схема прибора представлена на рис. 100. Ионный источник /
дает луч ионов, направленный на образец 2. В результате
бомбардировки поверхности образца образуются вторичные ионы, характе-
222
ризующие распределение химических элементов по поверхности.
Облучаемая точка имеет диаметр 1 imikm. Ионы ускоряются
эмиссионной линзой 3, электрод которой находится под высоким
напряжением и связан с электростатическим экраном 4. Ионы фокусируются в
плоскости разделительной диафрагмы 5. Образуется первичное
ионное изображение. Ионы элемента изображения, выделенные
отверстием в разделительной диафрагме, тормозятся в линзе 6 и
попадают в пространство между угловыми 8 и круглыми 7 электродами
монопольного iMacc-анализатора.
Рис. .99. Схема лазерного мик- Рис. 100. Схема ионного микро-
розонда зонда
Сочетание высокочастотного и постоянного полей в этом
пространстве приводит к тому, что на детектор ионов 10 попадают ионы
с определенным отношением заряда к массе. Усилитель 11 дает
сигнал на кинескоп 12. Развертывающее устройство 9, 13 перемещает
пятно на кинескопе 'синхронно с перемещением ионного
изображения относительно разделительной диафрагмы. .На экране получают
изображение поверхности с соответствующим распределением ионов
определенного сорта. С помощью этого метода можно получать ионы
лепких элементов, таких как .Н2, Be, 02.
3. ВЫДЕЛЕНИЕ ВКЛЮЧЕНИИ ИЗ ТВЕРДОГО МЕТАЛЛА
Неметаллические включения, выделенные в чистом виде из твердого
металла, представляют большой интерес. Можно рассмотреть
включения в их природном состоянии, но уже в твердом виде. Кроме
поверхностного анализа, выделенные включения могут быть
подвергнуты химическому анализу, петрографическому исследованию,
рентгеновскому или спектральному анализу. Полный комплекс ис-
223
следований для определения природы включений требует проведения
большой исследовательской работы, причем в зависимости от вида
включений иногда .приходится разрабатывать -совершенно новые
методики выделения включений и их анализа.
Электролитический метод выделения
Образец металла подвергают электролитическому растворению.
Собирают нерастворимый осадок неметаллических включений, который
подвергается дальнейшему изучению. Круглый стальной образец
диаметром 10—16 и длиной 100—150 мм подвешивают на медной
подвеске к шине, на которую подается положительный полюс
постоянного тока. Образец помещен в коллодиевый чехол с анолитам.
Чехол является диафрагмой и сборником осадка неметалличеоких
включений. Набор образцов подвешивают в медной электролизной
ванне, присоединенной к отрицательному полюсу выпрямителя. На
рис. 101 приведена схема электролизной установки.
Рис. 101. Электролизная ванна для выделения неметаллических включений:
/ — ванна из медного листа; 2 — электролит; 3 — металлические образцы;
4 — мешочки из коллодия; 5 — медные шины; 6 — выпрямитель
Выделение включений электролизом может быть проведено
методом Фиттерера — Лукашевич-Дувановой (растворение в одном
электролите). В качестве электролита используют водный раствор
З^/о-ного сульфата железа (FeS04-7H20), 1%-ного хлорида натрия
(NaCl) и 0,2%-ной сегнетовой соли (КАМаС^Об). Образцы в
количестве 8—10 шт. помещают в медной ванне емкостью 16—22 л
электролита. Коллодиевые чехлы подклеивают к стеклянным кольцам
с держателями, которые опираются на края ванны и дают
возможность подвешивать и вынимать образцы, не трогая самих чехлов.
Плотность тока на образце до 0,025 А/ем2 при напряжении 3—12 В.
Электролиз продолжается от 24 до 4в ч. За 1 ч растворяют около
1 it металла. По окончании электролиза образцы снимают и
стеклянной палочкой с резиновым наконечником с поверхности
образцов удаляют остатки осадка, Переносят осадок в стеклянный стакан
и отмывают их от сернокислотных солей. Образец высушивают
фильтровальной бумагой и взвешивают. Разность масс образца до и
после анализа равна количеству растворенного металла. По отношению
массы осадка включений к массе растворенного металла
рассчитывают процентное содержание включений в образце.
Подобный метод применяют для безуглеродистого железа,
углеродистых сталей, стали ШХ15, трансформаторной, конструкцион-
224
ной стали, малолегированных сталей. Он непригоден для
нержавеющих .сталей из-за выкрашивания металлических частиц. Осыпание
металла в коллодиевыи чехол делает невозможным количественный
анализ неметаллических включений. Этот недостаток устраним при
электролизе по методу Мчедлишвили. На рис. Ш представлена
схема установки, В стеклянном сосуде 1 вместимостью ^4л находится
№лС^чдайСХеМа уСТановки МчеДлишвили для электролитического выделения
пористая диафрагма 2 Внутри диафрагмы в анодном простран*
стве подвешен образец 3. Через резиновое уплотнение 4 сосуд сое^
диняется со штативом, через уплотнение проходит стеклянная
воронка 5 с пробкой 6, закрывающая снизу диафрагму. Снизу воронка
оканчивается фланцем со шлифом. К фланцу снизу крепится
воронка / с краном Я. Между-фланцами с помощью резиновых
прокладок закрепляется бумажный фильтр, уложенный на ситообразной
пластине из нержавеющей стали толщиной 2-8 мм, опирающейся
$ Зак. 664
2?5
на стеклянную дырчатую воронку 9. Катодное пространство
заливается католитом— 5%-ным растворам лимоннокислого натрия с
лимонной кислотой при рН =2,5-г-3,0. Лимонная кислота
добавляется в раствор каждый час для поддержания необходимого рН.
Катодом служит стальная спираль 10. Из сосуда 11 в анодное
пространство поступает анолит, состоящий из 5%-ного KCNS, 1%-ного
лимоннокислого натрия и 0,08%-ного AS2O3. Колба, или склянка,
12 служит затвором. Отработанный анолит каплями стекает в бутыль
13. Уровень анолита в диафрагме поддерживается автоматически.
Скорость потока анолита регулируется краном на воронке 7 в
пределах 80—100 капель в минуту. Кислотность анолита
поддерживается в пределах рН=6-г-4. Образец подсоединяется к выпрямителю.
При режиме электролиза (плотность тока 0,031—0,05 А/см2,
напряжение на полюсах 20—24 В) за 1 ч растворяется ~ 1 г металла.
Осадок включений оседает и удерживается на фильтре. Перед
растворением образцы стали для удаления пассивированной
поверхности травятся в той же установке в течение 0,5—1 ч в зависимости от
степени пассивации.
В методе Клингера и Коха ячейка состоит из двух резервуаров,
отделенных пористой перегородкой. Изнутри керамическая
фарфоровая диафрагма покрыта пленкой из пластика. Образец
изолируется от раствора нейлоновой рукавичкой. Уровень проточного
электролита в анодном пространстве поддерживается постоянным. Над
катодным пространством создается нейтральная атмосфера.
Электролиз образцов проводят также в ванне из
полихлорвинила в 'целлофановой ячейке. Во избежание выпадения осадка гидро-
ксида железа применен опоооб ионного удаления железа из
электролита. Электролит из анодного пространства откачивают насосом
и прогоняют через колонку с ионитом со скоростью б мл/мин, при
этом происходит очищение раствора от ионов железа.
Выделенный осадок неметаллических включений содержит
наряду с сульфидными и оксидными включениями большое
количество карбидов, затрудняющих изучение основных включений. Перед
началом исследования осадка проводят разрушение и удаление
карбидов, стараясь не повредить оксиды или сульфиды. Для
разрушения карбидов используют азотнокислотный метод. Часть
карбидов предварительно отделяют путем отмывания осадка на
часовом стекле. В углеродистых сталях частицы карбидов отделяют
с помощью магнита.
Для полного удаления карбидов нагревают стакан с раствором
и осадком включений до кипения, добавляют концентрированную
азотную кислоту до 10%-ной концентрации и приливают 4%-ный
раствор перманганата калия. Затем снова доливают азотной
кислоты до 110%-ной концентрации, нагревают до 90°С -и выдерживают.
-После этого по каплям приливают пероксид водорода для
разрушения двуокиси марганца. Если осадок перед электролизом
содержал аморфную кремнбкислоту, то его обрабатывают 3—|5%-ным
раствором соды в присутствии лимоннокислых солей, после чего
проводят азотнокислую обработку. После полного разрушения
карбидов осадок фильтруют и анализируют.
Существует метод разрушения карбидов путем медно-аммоний-
ной обра^ботки. Обработку карбидов медно-аммонийной хлористой
солью производят в присутствии закисного железа. В стакан с
осадком доливают ilOO мл 8%-ного раствора лимоннокислого аммония и
100 мл 20%-ного раствора медно-аммонийной хлористой соли. Смесь
нагревают. Через день жидкость сливают сифоном, а осадок отмы-
226
вают водой и аммиакам от меди. Для более полного разрушения
карбидов проводят повторную обработку, добавляя электролит и
вышеупомянутые растворы. После нагрева отмывают осадок на
центрифуге, обрабатывают 10%-ным раствором лимоннокислого
натрия для освобождения его от адсорбированного железа. Аморфный
углерод удаляют сжиганием. Медь из осадка определяют
аналитически, рассчитывая ее количество на СиО. Полученный результат
вычитают из массы осадка.
Для сохранения нестойких оксидных включений применяют
хлорвакуумный метод разложения карбидов. При обработке осадка
включений хлором карбиды, нитриды и сульфиды полностью
разлагаются, а оксиды, в там числе и малоустойчивые богатые закисями
марганца и железа, не взаимодействуют с хлором и остаются в
естественном виде, если температура не превышает 350°С.
(Все неметаллические включения из осадка, за исключением
оксидов, посредством хлора или другого галоида превращаются в
летучие галоиды, которые при нагреве сублимируют и таким образом
отделяются от окислов, например по реакции 2>Fe3C+9Cl2=
=6FeCl3+2C.
Преимущество хлорного или галоидного метода разрушения
карбидов состоит в том, что сохраняются все оксидные включения.
В кислотном методе происходит разрушение оксидных частиц,
особенно в результате растворения закиси марганца, железа, окиси
кремния. Опасность потери включений в кислотном методе
разрушения карбидов возрастает в связи с многократным повторением
циклов разрушения. Например, для нержавеющих сталей приходится
проводить до 10, а для шарикоподшипниковой — до 10—16 циклов.
При обработке карбидов медно-аммонийным опособом при
содержании в стали >0,1,% С полного разложения карбидов добиться
трудно.
Выделение сульфидов
Выделение сульфидов из стали производится также
электролитическим способом. Образец помещают в коллодиевый мешочек, который
опускают в шамотный стакан, служащий диафрагмой. Анолит
(раствор 0,1%-ного бромистого калия с добавкой 10%-ного
лимоннокислого натрия) наливают в мешочек и в стакан. Шамотный стакан
устанавливают в стеклянном сосуде, в который наливают католит.
Катод в виде спирали обвивает внешние стенки стакана в виде
медной ленты шириной 20 мм. В качестве католита применяют 10%-ный
раствор сульфата меди. Плотность тока устанавливают из расчета
0,1 А/см2, напряжение 6—7 В, время электролиза 20—24 ч.
Добавляемый в анолит лимоннокислый натрий, во-первых, .служит буфером,
препятствующим сильному повышению кислотности при электролизе,
во-вторых, образуя с железом комплексные соединения, он
препятствует выпадению основных солей железа. Кислотность анолита
меняется в пределах 5,2—7,0. Это позволяет выделить наиболее
легкорастворимые соединения, такие как свободные оксиды и сульфиды
марганца в высокодисперсном состоянии.
Полученный осадок включений отфильтровывают на центрифуге,
промывая его сначала 200 мл свежего анолита, разбавленного
дистиллированной водой, а затем только водой до полной отмывки
ионов железа. Затем осадок обрабатывают раствором сульфата
аммония для растворения оксидов и водой и пероксидом водорода.
Определяют в фильтрате марганец, железо, никель и пересчитывают
на соответствующие сульфиды.
8* Зак. 664
227
Выделение нитридов
Для выделения нитридов титана электролиз проводят в электролите,
•содержащем 15% хлорида натрия и 12,5% винной кислоты. Осадок
отмывают на центрифуге, вышаривают из него остаток воды,
добавляют 16 мг H2S04 (конц.), 2 г KHSO* и 6 мг 2%-ного раствора
К2СГ2О7. Нагревают колбу до полного растворения осадка, затем
переносят ее в прибор для определения содержания газообразного
азота, (Полученное содержание азота пересчитывают на нитриды
титана.
Ори определении нитридов алюминия электролитический осадок
переносится прямо в колбу азотной установки со щелочью. При этом
происходит растворение нитрида алюминия и отгонка
образовавшегося аммиака. При одновременном анализе нитридов алюминия и
титана в одной пробе определяют суммарное количество азота в
осадке, в другой пробе — нитрид алюминия без растворения осадка.
По разности рассчитывают количество каждого нитрида.
|Выделенный осадок неметаллических включений подвергают
затем химическому, рентгенослектральному, петрографическому
анализам. Цель анализа определить, к какому виду материалов
принадлежат те или иные виды включений.
Петрографический анализ проводят на поляризационном
микроокопе в проходящем свете при окрещенных николях. Определяют
форму, величину, прозрачность, цвет, анизотропность включений.
Только по совокупности всех данных можно точно
идентифицировать включения, указать источники их возникновения и наметить
меры для устранения неметаллических включений.
ГЛА'ВА VIII
АНАЛИЗ ГАЗОВ В МЕТАЛЛАХ
Современные методы исследований металлургического
производства служат цели получения чистых металлов
и сплавов, обладающих высокими эксплуатационными
свойствами. Большую роль в процессах получения
чистых металлов играет очищение металлов от
растворенных газов. При разработке способов удаления газов,
а также при исследовании факторов влияния
растворенного газа на свойства металла большое значение
имеет метод определения содержания газов. От
точности, воспроизводимости, надежности, скорости газового
анализа во многом зависит конечный результат
исследования, оценка данного способа производства металла.
Существующие способы определения содержания
газов в металле можно разделить в зависимости от их
производительности и точности на две группы. Первую
группу составляют методы для обслуживания
массового «потребителя; они отличаются высокой надежностью,
228
ТАБЛИЦА 3. СПОСОБЫ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ГАЗОВ
В МЕТАЛЛАХ
Способ
экстракции
Вакуум-плавление
В несущем
газе
Спектральный
Метод определения
Химическое поглощение
Вымораживание,
объемное определение
Газовая хроматография
ИК-поглощение
Кулонометрическое
титрование
Кондуктометрическое
титрование
Спектральный анализ
Изотопное разбавление
Масс-спектрометриче-
скяй
Продолжительность
анализа»
мин
10—30
10—30
30
1—5
3—130
5
0,5
в0—120
10-60
Навеска, г
б—Ю
1-ч5
1—20
1—2
1—2
1—2
0,001
<1
быстротой анализа, достаточной точностью и, главное,
высокой1 производительностью.
Вторую группу составляют «арбитражные» способы,
отличающиеся ультраточностью, высокой
чувствительностью, но небольшой производительностью.
Анализ металла на содержание кислорода, водорода
и азота может производиться как на одной установке,
так и на различных приборах. Способы определения
газов различаются как методом выделения газа из
металла, так и способом определения количества
выделившегося газа.
В табл. 3 приведены характеристики способов опре-,
деления газов в металле.
1. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ КИСЛОРОДА
Метод вакуум-плавления
Одним из самых распространенных методов
определения кислорода является метод вакуум-плавления или
вакуумной экстракции. Сущность метода заключается
в том, что анализируемый образец расплавляют в
графитовом тигле. Углерод растворяется в металле почти
до предела насыщения, восстанавливает окислы,
находящиеся в металле, и взаимодействует с растворенным
кислородом. Этому способствует также большая по-
229
верхность контакта металлической ванны со стенками
тигля. Образующаяся при взаимодействии углерода
с кислородом СО откачивается из плавильной печи
либо с помощью вакуумных насосов, либо уносится
потоком «нейтрального» несущего газа. Как при
вакуумной откачке, так и при использовании несущего газа
парциальное давление СО в газовой' атмосфере очень
низкое, и это способствует полному протеканию
реакции
[С] + 10] = СО, или [С] + МеО = [Me] + СО.
Выделившийся газ поступает в ту часть установки,
которая определяет содержание окиси углерода в
газовой фазе и соответственно содержание кислорода
в металле.
Принципиально прибор для анализа металла
состоит из трех узлов:
а) вакуумной печи с устройствами для введения
образцов, в которой нагревают и расплавляют образец;
б) узла откачки печи и перекачки газов из печи
в анализатор; в) вакуумного анализатора.
Загрузочные устройства действуют по принципу
шлюза и позволяют вводить образцы в печь без
попадания воздуха в систему.
В последнее время получили признание
автоматические установки для определения содержания
кислорода в металле фирм «Бальцерс» и «Леко».
Рассмотрим схему и принцип работы прибора
«Эксхалограф-202» фирмы «Бальцерс» (рис. 103).
Прибор производит автоматическое определение
кислорода в металлах с точностью до ±5-10-4% при
массе пробы 1 г со скоростью определения 0,5—1 мин.
Расплавление пробы производится в капсульной
печи (рис. 103,6) мощностью 3,5 кВ-А. В нижний
медный блок закладывают графитовую капсулу,
закрытую графитовой крышкой. Внутри капсулы
помещают образец. Применение закрытой капсулы
обеспечивает полную изоляцию металла, который не
может выплескиваться из тигля при анализе. При этом
исключается загрязнение газопроводящих путей.
Двуокись углерода, образующаяся в ходе анализа, при
диффундировании через раскаленную графитовую
стенку полностью превращается в окись углерода.
Капсула предохраняет от выхода паров металла, не
образуются металлические пленки на стенках вакуумной
230
части прибора, которые могли бы послужить геттерами.
Сверху печь закрывают крышкой с массивным медным
блоком. Медные блоки заполняют все пространство
Рис. 103. Прибор «Эксхало-
граф-202» фирмы «Баль-
церс»:
а — внешний вид; б — схема
капсульной печи; / — низ
печи; 2 — крышка печи; 3 —
тигель; 4 — вакуум-провод
/ J 4 5
печи, между ними остается только щель для откачки
газа. Они же служат и контактами для импульсного
нагрева,
231
При закрывании крышки печи колпак накрывает
печь, и медный блок прижимается к капсуле. Печь
откачивают, и крышка поджимается к корпусу
атмосферным давлением. Откачка печи происходит в
течение 30 с. Затем автоматически включается ток, и за
25 с импульс тока проходит через капсулу с образцом,
которая играет роль элемента сопротивления. Образец
нагревается и расплавляется, температура при анализе
достигает 2500°'С.
Выделяющиеся при расплавлении пробы газы
откачиваются собирающим насосом в камеру
газоанализатора. Затем газ перемещается в смесительную камеру.
Остаточный газ из трубопроводов вымывается в
смесительную камеру атмосферным воздухом, попадающим
в систему через напускной вентиль, который
автоматически открывается на 1 с. Из смесительной камеры
аликвотная часть газа отбирается в инфракрасный
анализатор, в котором по поглощению инфракрасного
излучения определяется содержание окиси углерода.
Результаты анализа показываются стрелочным
прибором. Перед началом расплавления производят
кратковременное включение тока для определения холостой
поправки, но так чтобы не происходило расплавления
образцов. Для калибровки прибора в него напускают
определенную порцию окиси углерода, которую и
анализируют.
Высокая температура, большая величина отношения
поверхности графита к массе металла обеспечивают
полное восстановление окислов и удаление
растворенного кислорода. Ошибка определения не превышает
±1О-5 г кислорода.
Большое значение для получения репрезентативных
результатов анализа имеют правильный отбор и
приготовление проб. Для получения плотной пробы и для
устранения потерь окиси углерода, выделяющейся из
металла вследствие понижения предела растворимости
кислорода при его затвердевании, пробы раскисляют
алюминием. Алюминий помещают в пробницу в виде
небольшого кусочка проволоки или фольги. При этом
кислород связывается в глинозем.
Из карандашей пробы или отливочки изготовляют
пробу нужного размера, свободную от окалины,
остатков шлака. Наиболее простым способом подготовки
проб является токарная обработка. Пробу обтачиэадет
233
ДО Дйамбтра на 6,5—i,6 мм больше требуемого, не
обращая внимания на ее разогрев, а затем доводят до
необходимого размера без нагрева пробы. Поверхность
пробы должна быть чистой.
После изготовления пробы необходимо свести к
минимуму возможные загрязнения поверхности в
результате процессов адсорбции, окисления и т. д. Следует
избегать использования стружки в качестве пробы.
Применение растворителей для очистки поверхности
образца перед анализом должно быть ограничено.
Остатки растворителя в микрораковинах и трещинах
удаляются с большим трудом. После промывки пробы
растворителем необходимо провести вакуумную сушку
проб.
Одной из распространенных отечественных
установок для определения содержания газов в металлах
является установка системы Гиредмет С911М,
основанная на принцице вакуум-плавления пробы металла
в графитовом тигле. Корпус печи кварцевый. Схема
установки представлена на рис. 104.
А ШЛТ-2
Рис. 104. Схема установки
для газового анализа
системы Гиредмет С911М:
1 — экстракционная печь;
2 — соединительный шлиф;
3 — загрузочное устройство;
4 — смотровое стекло; 5,
10 — диффузионный насос;
6, 11 — ловушка; 7 —
резервный баллон; 8 —
окислительная печь; 9 —
компрессионный манометр; 12 —
механический форвакуумный
насос
Пробу вводят в экстракционную печь с помощью
шлюза, затем откачивают газы парортутным насосом.
Окись углерода и водород, соединяясь в печи с закисью
меди, нагретой до 350°С, образуют С02 и Н20. Далее
производят фракционное их вымораживание. Газы раз-
233
МораЖйвают поочередно, сначала С02, потом Н20.
Измеряют давление газа в калиброванном объеме
в целом, затем вымораживают воду и узнают давление
водяного пара. По последней величине определяют
содержание водорода. Затем вымораживают С02 и по
количеству С02 находят содержание кислорода, а по
остаточному давлению вычисляют содержание азота.
Давление газов измеряют автоматическим
компрессионным манометром.
Метод газа-носителя
В отличие от метода вакуум-плавления этот метод
состоит в том, что в реакционную печь, в которой
расплавляют образец, напускают порцию нейтрального
газа-носителя или устанавливают поток нейтрального
газа через печь. Так как парциальное давление окиси
углерода, водорода или азота в газе-носителе равно
нулю, то физико-химические условия выделения
растворенных в металле газов такие, как и при плавке
в вакууме. В отличие от вакуум-плавления этот метод
обладает следующими преимуществами: 1) частично
устранены трудности работы с вакуумом; 2) более
простая в обслуживании аппаратура; 3) метод
поддается автоматизации.
К недостаткам способа относится необходимость
иметь особо чистый (99,99%) газ-носитель — гелий или
аргон.
Рис. 105. Блок-схема прибора для
восстановительного плавления в
токе газа-носителя:
1 — устройство для загрузки
образцов; 2 — источник газа-носителя;
3 — узел измерения и
регулирования расхода газа-носителя; 4 —
очистка газа-носителя; 5 —
плавильная печь; 6 — анализатор
На рис. 105 приведена блок-схема прибора для
восстановительного плавления в токе газа-носителя. Кроме
печи и газоанализатора, приборы для плавления
в инертной атмосфере содержат устройства для
поддержания расхода газа-носителя и для очистки его от
примесей.
[Т
4
i
г
!
5
Т1
[D^Z}^z}^ZJ^
234
Печи для установок газового анализа методом
восстановительного плавления
Наиболее -распространенными' являются
высокочастотный нагрев и нагрев в печи сопротивления.
Индукционные печи. В приборах газового анализа,
работающих с индукционным нагревом, корпус печи
выполняют из кварцевого стекла с водяным
охлаждением. Внутри корпуса располагаются на подвеске или
на подставке графитовый тигель и другие графитовые
детали — экраны, направляющие трубки, воронки,
крышечки тигля. Как правило, в одном тигле производится
серия анализов образцов примерно одинакового
химического состава. Температура нагрева в обычных печах
достигает 1600—3000°*С и лимитируется скоростью
испарения графита и расплава. Высокая температура
в печи достигается за длительный отрезок времени.
Печь работает в режиме непрерывного нагрева.
Преимуществом печей' индукционного нагрева
является малая величина холостой поправки на
газовыделение из деталей печи благодаря отсутствию
токовводов, равномерному прогреву всего тигля и
охлаждению стенок печи. На рис. 106 приведены схемы
индукционных печей для газового анализа.
Печи сопротивления. В настоящее время
наибольшее распространение получил прямой нагрев в
импульсном режиме. Принцип импульсной печи состоит
в том, что маленький графитовый тигель, рассчитанный
на один образец, закрытый крышкой, зажимают
с торцов между водоохлаждаемыми токоподводами
и пропускают через тигель ток большой силы. Схемы
таких печей приведены на рис. 107. При диаметре
тиглей 6—12 мм, толщине стенок 1 мм и силе тока
600 А за 3—30 с нагрева температура повышается до
2500—3000°С. При таких температурах графит
интенсивно испаряется, но так как время нагрева невелико,
то тигель не разрушается. Благодаря
высокоинтенсивному «агреву происходит быстрое выделение газов.
Весьма важным для установок газового анализа
является холостое выделение газов из внутренних частей
печи: От величины.холостой поправки зависят
чувствительность и точность анализа.
Источниками газов холостой поправки могут быть
стенки печи, тигель, газ-носитель, содержащий примеси.
Наибольший вклад в холостую поправку дает графи-
235
товый тигель. Для уменьшения газовыделения тигли
необходимо изготовлять из высокоплотного графита
высшей степени очистки, марок МПГ-6, МПГ-8. Тигли
должны быть предварительно дегазированы при
высокой температуре, в глубоком вакууме.
236
Уменьшению холостой поправки способствует
и уменьшение размеров тигля. Индивидуальные тигли
потребовали разработки конструкций печей с быстрой
заменой тиглей и загрузкой в них образцов после
дегазации тигля, чтобы воздух не попадал в печь. Для
замены тигля в печи сопротивления устраивают
подвижное дно, которое опускают при помощи рукоятки
(рис. 108). Тигель снимают, ставят новый тигель, а дно
переводят в верхнее положение, где оно уплотняется
с помощью резиновых прокладок.
Замену капсулы в печи, показанной на рис. 108,
производят пинцетом через загрузочный люк при оття-
Рис. 106. Схемы индукционных печей для плавления металла в токе газа-
носителя:
а —без теплоизоляции тигля (/ — кран для загрузки образцов; 2 — смотровое
стекло; 3 — разъемные соединения; 4 — водоохлаждаемый корпус из кварца;
5 —графитовый тигель); б — печь с теплоизоляцией тигля (/ — корпус печи;
2 — индуктор; 3 — кварцевый стакан; 4 — графитовый порошок; 5 —
графитовый тигель; 6 — направляющая воронка); 9 — печь с концентратором тока
237
нутом подвижном электроде. Воздух не попадает в печь
из-за повышенного давления газа-носителя в печи.
После дегазации пустого тигля в него с помощью
шлюза сбрасывают образец. После дегазации образцы
помещают в капсулы либо на воздухе, либо в сообща-
Рнс. 107. Схемдл печей сопротивления для
импульсного нагрева:
ющемся с печью перчаточном боксе с инертной
атмосферой.
При анализе тугоплавких металлов зарядку
капсулы производят на воздухе и нагревают .в печи
двумя импульсами тока. Первый короткий импульс
нагревает и дегазирует капсулу, образец расплавляет-
238
ся. Второй, более продолжительный' импульс
расплавляет образец и обеспечивает выделение газов. Печи
для импульсного нагрева должны иметь малый
свободный объем для минимального разбавления
выделенных газов газом-носителем.
• Рис. 108. Схема печи прибора
фирмы «Леко» с устройством
для быстрой смены тигля и
шлюзом для загрузки
образцов:
/ — шлюз для загрузки
образцов; 2 — отверстие для входа
образца; 3 — верхний электрод;
4 — кольцевые уплотнения; 5 —
графитовый тигель; б — нижний
электрод
Анализ газов, выделенных из образца
Основной составляющей газа, выделяющегося из
образца при его плавлении, является окись углерода.
Содержание окиси углерода в газе определяют прямым
методом ИК-поглощения. Газоанализатор такого типа
имеет два источника -непрерывного ИК-излучения,
которое направляется через две пары кювет (рис. 109) в
лучеприемник. Кюветы представляют собой полые
цилиндры, изнутри покрытые золотой пленкой для полного
239
(УграЖенйя. Лучеприемник 1 состоит из двух камер,
имеющих окна в верхней части и разделенных
мембраной 2 из металлической фольги. Параллельно мембране
укреплена пластина 3, которая вместе с мембраной
образует электрический конденсатор.
Рис. 109. Принципиальная схема ИК-газоанализатора:
/ — лучеприемник; 2 — мембрана; 3 — пластина; 4 — заслонка для установки
нуля; 5 —фильтровые кюветы; 6 — источник постоянного напряжения; 7—
измерительные кюветы; 8 — рабочая кювета; 9 — сравнительная кювета; 10 —
высокоомное сопротивление; 1J — источник радиации; 12 — двигатель
обтюратора; 13 — обтюратор; 14 — усилитель; 15 — стабилизатор
Обе камеры лучеприемника заполняют раствором
окиси углерода в газе, не поглощающем ИК-радиации.
Кювету 7 заполняют чистым газом-носителем. Через
кювету 8 пропускают анализируемую смесь. Если в
газе есть окись углерода, то она будет поглощать
соответствующую часть излучения. Тогда повышение
давления в камере лучеприемника, куда попадает излучение
через кювету 8, будет меньше, чем в камере,
находящейся напротив кюветы 9. Разность давлений в
камерах, возникающая вследствие разного их нагрева, тем
больше, чем больше концентрация СО в измерительной
кювете. Эта разность давлений вызывает изменение
240
емкости конденсатора, образуемого изгибающей
мембраной 2 и пластиной 3. Источник ИК-излучения
периодически закрывается вращающимся обтюратором
13. В результате мембрана 2 совершает колебания
с амплитудой, зависящей от концентрации СО.
Мембрана 2 имеет небольшое отверстие для
выравнивания давления в камерах лучеприемника, вызванное
неравномерным длительным нагревом газа. Кюветы 5
служат для устранения влияния компонентов
анализируемой газовой смеси, спектры поглощения которых
частично перекрываются спектром поглощения СО. Их
заполняют газом с нужной концентрацией мешающих
компонентов, благодаря чему излучение с длинами
волн, общими для СО и мешающих примесей,
«вырезается» из спектра источника излучения.
ИК-анализаторы должны быть термостатированы,
так как их показания зависят от температуры
окружающей среды. Эти приборы дают относительные
показания, поэтому их необходимо калибровать. Калибровку
осуществляют либо смесями с известным содержанием
СО, либо по данным анализа стандартных
металлических образцов.
Способом определения количества окиси углерода
является также косвенный метод, в котором СО
переводят в С02, а последнюю определяют аналитически.
Окисление СО до С02 чаще всего осуществляют при
450°'С с помощью окиси меди с добавками окислов
марганца, редкоземельных металлов или окиси железа
или с помощью специальных химических реактивов.
Образующуюся С02 определяют кондуктометричееким
или кулонометрическим способом. Кондуктометриче-
ский способ заключается в измерении сопротивления
слоя жидкости в абсорбционной ячейке, в которой газ-
носитель, содержащий С02, барботирует через водный
раствор Ва(ОН2) или NaOH. Все примеси, кроме С02,
способные взаимодействовать с поглощающим
раствором, должны быть удалены из тока газа-носителя.
Чувствительность таких приборов может быть доведена
до 0,2 мкг 02. Недостаток метода заключается в
необходимости частой замены поглотительного раствора
и калибровки системы.
Более удобным является метод кулонометрического
титрования. Углекислый газ поглощается водным
щелочным раствором, при этом происходит уменьшение
241
рН среды. Исходное значение рН может быть
восстановлено путем титрования ионами ОН, получаемыми
в результате электролиза. Количество электричества,
израсходованное на титрование, пропорционально
количеству- поглощенной С02 и соответствует содержанию
кислорода в образце. Схема ячейки для титрования
Рис. ПО. Схема ячейки для куло-
нометрического титрования
углекислого газа:
/ — катодная камера с раствором
перхлората бария; 2 — камера
серебряного электрода; 3, 8 —
пористая керамическая диафрагма; 4 —
стеклянный электрод; 5 —
электропривод мешалки; 6 — мешалка; 7 —
катод; 9 — анодная камера с
раствором перхлората бария; 10 — анод;
// — порошок карбоната бария
В ячейке анодное и катодное пространство
разделено пористой перегородкой. Электролитом чаще всего
служит раствор перхлората бария. В анодную камеру
добавляют также порошок карбоната бария для
нейтрализации кислоты, образующейся при электролизе, и в
катодное пространство вводят немного изопропанола
для пенообразования. Раствор в катодной ячейке
перемешивается мешалкой, газ подают в нижнюю часть
катодной ячейки. Благодаря дроблению пузырей газа
мешалкой и присутствию пенообразователя образуется
большая поверхность раздела фаз, способствующая
быстрому поглощению С02 из газа-носителя.
При помощи рН-метра в катодной ячейке
непрерывно измеряется рН раствора. Погружаемый электрод
рН-метра представляет собой комбинацию стеклянного
электрода и электрода сравнения. Свежий электролит
подвергают электролизу пока в катодной камере не
установится выбранное значение рН, после чего.начи-
приведена на рис. ПО.
242
нают анализ образца. Как только в результате,
поглощения С02 величина рН изменится, автоматически
включается ток электролиза, который отключится как
только будет достигнуто исходное значение рН. Сила
тока тем больше, чем больше отклонение рН.
Количество электричества, израсходованного на
титрование, измеряется при помощи безынерционного
мотора-интегратора тока, скорость вращения которого
строго пропорциональна силе тока электролиза. На
валу двигателя имеется диск с прорезями, который при
вращении периодически перекрывает луч света,
направленный на фотоэлемент. Частота возникновения
импульсов тока в фотоэлементе пропорциональна
скорости вращения двигателя. Импульс после усиления
подают на электронный счетчик, который показывает
результаты анализа в цифровой форме. Один импульс
на счетчике соответствует 0,2—0,5 кг кислорода в
образце. Автоматические приборы для титрования
выпускаются в СССР (АН-160 и АН-29), ФРГ («Ку-
ломат-7000» фирмы «Штроляйн») и т. д.
Содержание С02 в газе хорошо определяется также
методами ИК-логлощения, причем чувствительность
определения может быть доведена до 0,03 мкг
кислорода. Применяют и методы хроматографии для
определения содержания СОг-
При проведении анализов методом
вакуум-плавления возникает ряд методических осложнений.
Состав металлической ванны. При повышенных
концентрациях в металле летучих элементов, например
марганца или хрома, результаты анализа могут
получиться заниженными вследствие адсорбции газа
возгонами и конденсатами паров металла на стенках печи.
Для устранения этого применяют капсульные тигли,
закрытые крышками; плавку ведут в атмосфере газа-
носителя.
Неполное восстановление окислов. При повышенном
содержании алюминия и других элементов,
образующих трудновосстановимые окислы, анализ может дать
заниженный результат из-за неполного восстановления
окислов в металлической ванне. Поэтому желательно,
чтобы при проведении анализа в металлической ванне
было не более 0,1% S, 1,5% Мп, 0,2% А1, 1,1% Ti,
10—12% Сг. Для понижения концентрации этих
элементов в графитовом тигле создают ванну из чистых
243
железа, олова, меди. Железная ванна дает надежные
результаты для сплавов, легированных никелем,
молибденом, танталом, кремнием, хромом, теллуром,
марганцем, бериллием.
При анализе образцов с высоким содержанием
марганца подходящим материалом является медь.
Образующийся при этом конденсат менее способен к
адсорбции газа. Количество меди должно быть таким,
чтобы концентрация марганца не превышала 30%.
Анализ ведут при 1100°С.
При использовании оловянной ванны олово
испаряется и оседает на стенках тигля и печи. Возгон олова,
оседающий на возгонах других компонентов,
препятствует поглощению газов из атмосферы печи.
Нержавеющие стали анализируются с применением никелевых
ванн, при этом концентрация хрома не должна
превышать 10%. Особое внимание должно быть обращено на
анализ металла с повышенным содержанием
алюминия. Полнота анализа сталей, раскисленных
алюминием, зависит от температуры плавки. При повышении
температуры, как правило, содержание кислорода,
определяемое в металле, увеличивается. Так, при ШвбХ
за 230 мин восстанавливается 75% включений, а при
1750°С за 120 мин восстанавливается 71,2% включений
и при 1850°'С восстанавливается за 30 мин 95%
включений.
В качестве примера анализа с применением газа-
носителя рассмотрим работу установки «Диномат»
фирмы «Штроляйн» (ФРГ). Схема установки приведена
на рис. 111. Проба расплавляется в индивидуальном
графитовом тигле при температуре 1900°С. Плавку
осуществляют в печи сопротивления с графитовым
нагревателем. Печь имеет электромеханический
подъемник для графитовых тиглей. Пробы загружают
в тигель через головную часть печи. Нагрев печи
регулируют плавным изменением силы тока в зависимости
от показаний оптического пирометра.
В более совершенных конструкциях, например «Мо-
номат 300», имеется открытая импульсная печь с
автоматическим включением нагрева после закрывания
печи. Сначала прогревают тигель, а установку
промывают газом-носителем. В шлюзовое устройство
вставляется проба. Нажимом пусковой кнопки включается
автоматическая программа анализа. Сначала тигель
244
нагревается до температуры анализа, определяется
холостая поправка, которая автоматически
компенсируется. Затем проба вводится в тигель и начинается анализ.
Выделяющиеся газы транспортируются в анализа-
ционный узел. Анализ ведется по ИК-поглощению. При
Рис. Ш. Схема прибора «Диномат» фирмы «Штроляйн»:
/ — баллон с Не; 2 — баллон с СО; 3 — баллон с N2; 4 — редуктор; 5 —
регулятор давления; б — реометр; 7 — вентиль; 8 — ячейка измерения
теплопроводности; 9 — поток сравнительного газа; 10, 19 — дозировочные краны; // —
плавильная печь; 12 — графитовый тигель; 13 — подъемник тигля; 14 —
устройство для введения образцов; 15 — затвор; 16 — градуировочное устройство;
17 — термометр; 18 — магнитный дозировочный кран; 20 — инфракрасный
анализатор; 21 — колонка с реактивом; 22 — колонка с молекулярным ситом;
23 — насос
прохождении газа через „поглотительную ячейку на
ленте самописца появляется пик. Площадь кривой
соответствует количеству окиси углерода в
экстрагируемом газе. Электронный вычислитель рассчитывает
концентрацию кислорода в металле.
245
Большое распространение получили приборы фирмы
«Леко» (США) с хроматографическим газовым
анализатором. В качестве примера рассмотрим работу
прибора ТС-30.
В плавильную печь, представленную на рис. 108,
устанавливают пустой индивидуальный графитовый
тигель, в загрузочное устройство помещают образец.
Затем печь закрывают, но образец еще не попадает в
тигель. После нажима на кнопку «Промывка»
включается нагрев тигля на 30 с. Гелий, предназначенный
для промывки, проходит через печь и выпускается
в атмосферу. Поток гелия для анализа разветвляется
таким образом, чтобы одна часть проходила через
окислитель, осушитель, хроматографическую колонку,
рабочий канал катарометра и реометр, а другая —
через канал сравнения катарометра и второй реометр
в атмосферу.
Через 90 с промывка установки и дегазация тигля
заканчиваются. Поворотом плунжера загрузочного
устройства образец сбрасывают в печь.
При нажатии на кнопку «Анализ» переключаются
электромагнитные клапаны и путь газа-носителя
изменяется. Гелий поступает сначала в устройство для
дозирования калибровочных газов, затем в печь и далее
в анализатор. Включается нагрев тигля. Выделенные из
образца газы сначала окисляются закисью меди до
С02 и Н20, затем перхлоратом магния происходит
осушение газа, удаление паров воды, и далее газы
поступают в хроматографическую колонку. Хроматогра-
фический анализатор определяет содержание в газе
С02 и N2. С помощью ручек управления в
вычислитель прибора вводятся масса образца и значение
холостой поправки. Длительность анализа 2,5 мин,
чувствительность прибора 10~4 % 02 (или N2) при массе
образца 0,5 г. Величина холостой поправки 3-10^4%,
Принцип работы Хроматографа состоит в
следующем. Колонка хроматографа содержит силикагель или
молекулярное сито, которое сорбирует С02 при
комнатной температуре. Десорбция С02 происходит при
300°С. Другие газы, выделяющиеся при
восстановительном плавлении образца, не сорбируются при комнатной
температуре на молекулярном сите. Быстрым нагревом
до 300°С десорбируют сконцентрированную на
молекулярном сите С02 и с газом-носителем подают ее
непосредственно в детектор по теплопроводности,
246
Определение кислорода методом
изотопного разбавления
Этот метод заключается в том, что жидкий металл
выдерживается под газовой смесью, содержащей'
известный объем изотопа 180. По достижении равновесия
анализ газа производится на масс-спектрометре.
Метод изотопного обмена обладает тем
преимуществом перед другими методами, что изотоп кислорода,
введенный в систему, равномерно распределяется
между всеми фазами и нет необходимости полной
экстракции кислорода из металла; не важны потери
газа при анализе, так как изотопный состав газа не
изменяется.
Для введения в металл изотопа кислорода 180
применяют дозировочные образцы, содержащие известные
количества изотопа. Для этого порошок металла
насыщают кислородом с изотопом 180. Для анализа образец
смешивают с дозировочным образцом и помещают
в графитовый тигель. По расплавлении образца его
выдерживают 0,5—1 ч для протекания изотопного обмена.
Когда отношение 180/1вО во всех частях системы
металл — газ — металлический возгон станет одинаковым,
отбирают газ для проведения анализа. Так как газ
состоит в основном из окиси углерода, то, зная величину
отношения 180/160 в дозировочном образце и определяя
это отношение для пробы газа, по правилу простых
смесей рассчитывают содержание кислорода в металле.
В пробе газа благодаря наличию кислорода 160 в
металле отношение 180/160 уменьшится по сравнению с
дозировочным образцом.
2. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ВОДОРОДА
Различают следующие методы определения содержания
водорода в стали:
1) метод вакуумного нагрева; 2) плавление; 3)
плавление в атмосфере газа-носителя.
Многие установки и методы газового анализа
являются универсальными, пригодными для определения
всех трех газов в металле, например установка Ги-
редмета.
Однако в настоящее время определение водорода
осуществляют на установках, предназначенных для
анализа только на водород. Благодаря высокой ско-
247
рости диффузии водорода в твердом металле стали
возможными способы определения водорода в металле
без плавления, при нагреве до температуры,
обеспечивающей полное извлечение водорода из твердого
металлического образца. Ряд методик определения
водорода основан на анализе твердых образцов.
Метод вакуумного нагрева
Этот метод анализа отличается простым устройством
прибора и несложной' техникой определения.
Реакционная кварцевая трубка объемом 50—60 см3, диаметром
20 мм с помощью шлифа присоединяется к
трехходовому вакуумному крану. Поворотом мрана
калиброванный объем трубки можно соединить либо с
вакуумными насосами, либо с U-образным ртутным или
масляным манометром, В трубку помещают образец
и откачивают атмосферу. Поворотом крана соединяют
вакуумированный объем с манометром и измеряют
холостую поправку. Затем на трубку надвигают печь
сопротивления и нагревают образец до 600—700°'С.
Происходит выделение диффузионно подвижного
водорода в течение 20—30 мин.
Количество выделившегося водорода определяют по
изменению давления в системе. На одном штативе
может быть установлено несколько приборов для
определения водорода, которые подсоединяются поочередно
к вакуумной системе.
Количество выделившегося водорода рассчитывают
по формуле
У mvjp-pr) 100
101 G (273 + /)
где Vk2 — количество водорода, мл на 100 г металла;
V — объем прибора, мл; р — давление в приборе к
концу опыта, кПа; G — масса образца, г; t — температура
помещения, °С; р' — холостая поправка, кПа,
отнесенная ко времени дегазации.
Погрешность этого способа определения состоит
в выделении адсорбированной влаги с поверхности
образца, которое может привести к окислению
образца. Кроме того, часть водорода расходуется на вос-
248
становление окислов с поверхности образца.
Образующиеся водяные пары адсорбируются на стенках
прибора и не определяются при измерении количества
водорода. Прибор позволяет находить содержание
водорода с точностью до 0,15 мл на 100 г металла, т. е.
до ±0,00002%.
1 Л Ш Ш
Рис. 112. Схема прибора фирмы «Штроляйн» для анализа диффузионного
подвижного водорода:
/ — хроматограф; // — насос Тепплера; III, /V —печи; V — вакуумметр; 1 —
диффузионный насос; 2 — вентиль; 3 — манометр Мак Леода; 4 — магнитный
вентиль; 5 — кварцевая трубка; 6 — шлюз для загрузки образцов; 7 —
подъемник для образцов; 8 — экстракционная печь
В более сложных установках, например фирмы
«Штроляйн», выделяющийся из образца газ собирается
насосом Тепплера в калиброванном объеме. Давление
в объеме с помощью С02 доводится до атмосферного,
и газ вымывается в хроматограф, где все газы, кроме
водорода, поглощаются. Содержание водорода
определяется волюмометрическим способом. На рис. 112
приведена схема этого прибора.
Метод газа-носителя
Достоинства данного метода сводятся к следующему:
а) не нужен вакуумный шлюз для внесения образца
в печь; б) уменьшена конденсация паров и снижены
потери водорода; в) не требуется частая манипуляция
249
вакуумными кранами. Метод газа-носителя имеет
разновидности.
Определение водорода с помощью палладиевого
фильтра. Спектрально чистый аргон пропускают через
два последовательно соединенных дозировочных
редуктора со скоростью 5 л/ч. При открывании печи скорость
подачи аргона увеличивают до 30 л/ч во избежание
попадания наружного воздуха. Образцы нагревают
в печи при 1200°С. Смесь аргона с другими газами,
выделившимися из образца, пропускают через палла-
диевую спиральную трубку. Так как палладий
пропускает только водород, то последний проходит через
стенки спирали в стеклянную ампулу, окружающую
спираль и откачанную до давления 3-Ю-2 кПа, далее
откачивается из нее насосом и собирается в бюретке,
где измеряется его количество. Палладиевая спираль
изготовлена из фольги в виде трубки длиной 1 м
с внутренним диаметром 1 мм и толщиной стенки
0,2 мм. Стеклянную капсулу со спиралью помещают
в печь, нагретую до 300—400°С. Стеклянная капсула
закрыта пришлифованной серебряной пробкой,
охлаждаемой водой. Этот метод не требует калибровки.
Определение водорода по теплопроводности. Этот
метод основан на большой разности теплопроводности
анализируемых газов. Теплопроводность водорода
в 7 раз выше теплопроводности азота, окиси углерода
и аргона. Детектором теплопроводности служит ката-
рометр. Катарометр может служить индикатором
в хроматографической части установки анализатора,
однако часто хроматографическая колонка исключается
из прибора и включается колонка с молекулярным
ситом, которая задерживает СО и N2- Окись углерода
удаляется из потока газа с носителя химическим
поглощением.
Прибор фирмы «Леко» RH-1 имеет импульсную печь
для плавки образца в индивидуальных тиглях. Масса
образца 1 г. В качестве несущего газа используется
аргон. Выделяющаяся из образца окись углерода
специальным реагентом окисляется до двуокиси углерода,
которая поглощается аскаритом. Азот хроматографиче-
ски поглощается в колонке с молекулярным ситом.
Смесь водорода и аргона направляется в катарометр,
который дает сигнал на электронное пересчетное
устройство, выдающее цифровые значения содержания
250
водорода. Область работы прибора от 10~5 до 1(Н6/0 с
точностью до ±3%. Прибор калибруют с помощью
чистого водорода, определенную порцию которого
впускают в анализатор.
Одна из конструкций катарометра представляет
собой 8-мм трубку с двумя вольфрамовыми вводами,
к которым прикреплены никелевые подвески. На
подвесках висит тонкая платиновая проволочка длиной
16 мм. На одном, более длинном никелевом подвесе
находится вольфрамовая спираль, к которой
прикрепляют один конец платиновой проволочки; другой ее
конец подсоединяют к короткому вводу. К
вольфрамовым вводам присоединено плечо мостика Уитстона.
Ячейку термостатируют при 0°С.
Платиновую проволоку нагревают током до
постоянной температуры. Равновесие моста устанавливают
пропусканием чистого водорода. По разбалансировке
моста во время введения в измерительную ячейку
смеси газов и определяют содержание водорода в газе.
Расчеты производят по калибровочным кривым завиг
симостей теплопроводности чистых азота, водорода
и окиси углерода от давления и от наличия водорода
в смеси газов. При анализе учитывают холостую
поправку.
Другие методы определения водорода в
выделяющемся газе с помощью кулонометрии, гравиметрии
основаны на определении количества водяного пара,
получающегося при окислении водорода. Однако эти
способы не нашли широкого распространения.
3. ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЗОТА
Определение азота в металле осуществляют методами:
а) вакуум-плавления и плавления в токе
газа-носителя; б) химическими и в) спектральными.
Метод вакуум-плавления
Одновременное определение азота и кислорода
производят на автоматическом газоанализаторе фирмы
«Бальцерс» EAN-202. Принцип работы прибора
заключается в том, что все экстрагированные из образца
газы поглощают адсорбентами, представляющими
251
собой смбсь молекулярных сит и окислителя. После
каждого анализа адсорбент регенерируют путем
перемещения его в зону нагрева. Давление газов измеряют
с помощью манометра сопротивления. Количество
азота определяют по разности измеренных давлений. Весь
цикл анализа продолжается 3 мин и состоит из
десорбции реагента, т. е. его регенерации, расплавления
пробы и экстракции газов. Выделившаяся окись
углерода адсорбируется, а водород сначала окисляется до
Н20, а затем адсорбируется. Измеряют давление в
газосборнике до и после адсорбции и находят содержание
азота. Прибор может определять содержание азота с
точностью до ±0,1 мг при средней ошибке анализа
0,5%. Масса образца для определения ~0,5 г.
Прибором для определения содержания азота в токе
газа-носителя является установка Т-14 фирмы «Леко».
Экстракция азота совместно с другими газами в
атмосфере газа-носителя (гелия) происходит в
импульсной печи сопротивления. Плавки осуществляются в
индивидуальном графитовом тигле.
Для определения содержания азота газы
пропускают через колонку с окислителем (окисью меди), где СО
окисляется до С02, а Н2 до Н20. Азот с гелием
попадают в ячейку, где содержание азота
устанавливают по теплопроводности. Ячейка состоит из двух
кювет, в которых расположены по паре проволочек,
являющихся плечами электрического моста. Одна
кювета служит для прохождения смеси азота с гелием,
другая — для чистого гелия. При прохождении
анализируемого газа мост выводится из состояния
равновесия и по отклонению нуль-прибора судят о
количестве азота в несущем газе, т. е. о содержании азота
в образце. При попадании азота в кювету температура
термистера будет повышаться, так как
теплопроводность азота значительно меньше теплопроводности
гелия. Градуировку прибора проводят по чистым газам
(СО и N2). Время анализа 90 с после введения образца
массой до 0,5 г. Точность определения азота ±5-10~5%
в пределах его концентрации 0,1—0,0001%. Можно
проводить анализ всех видов сталей и тугоплавких
металлов, ферросплавов. В случае повышенных концентраций
азота в азотированных сталях или ферросплавах
анализу подвергают несколько образцов массой от 0,01 г,
предварительно тщательно измельчая материал.
252
Химический метод
Распространенным методом определения азота в сталях
и сплавах на основе железа является
усовершенствованный метод Кьельдаля. Принцип определения азота
состоит в растворении металлического образца в виде
стружки в кислоте с переводом всего азота в соли
аммония. Затем аммоний дистиллируют из кипящего
щелочного раствора и титруют. Обычные стали
растворяют в хлорной кислоте иногда с добавками фтористого
натрия. Легированные стали растворяют в серной
кислоте (1:4) с фтористым натрием. Растворение ведут
при медленном нагреве в колбочках, закрытых
пробками, со сборниками конденсата, соблюдая
предосторожности от окисления аммония.
По прекращении видимого растворения раствор
выливают в установку, а к нерастворившемуся осадку
добавляют новую порцию кислоты, фтористого натрия
и уже окончательно ведут растворение.
Параллельно работают два аппарата: в одном
определяют азот в образце, в другом ведут холостое
определение. При титровании дистиллята добавляют
индикаторный раствор до исчезновения интенсивной
окраски. По количеству израсходованной кислоты судят
о количестве азота в образце.
Основной ошибкой данного метода является
выщелачивание аммиака из стекла. Для уменьшения ошибки
рекомендуется снижать количество дистиллята.
Все методы химического определения азота в
металлах позволяют определить азот, находящийся
только в твердом растворе. Для определения азота,
связанного с различными нитридообразующими элементами,
растворяемую стружку обрабатывают эфирным
раствором галоидов, например раствором брома в мети-
лацетате или этилформитате. Нерастворившиеся
нитриды отделяют центрифугированием или
фильтрацией. Их состав определяют рентгеновским путем, а
содержание азота — обычным химическим путем.
Спектральный метод
При спектральном анализе для определения количества
и состава газов, содержащихся в металле, можно либо
анализировать состав газов, выделяющихся из метал-
253
ла, либо непосредственно определять газы в металле.
Для анализа требуется мощный источник света
способный обеспечить достаточную- экстракцию газа из
металла и интенсивное свечение спектра атомов
кислорода.
Применяли спектрограф ИСП-51, в котором
источником света служит искра высоковольтная импульсная
с разрядом в водороде или низковольтная.
Для анализа газа, выделенного из металла, в
экстракционной части установки использовали масс-
спектрометр. Прибор переделан таким образом, чтобы
напуск газа из ампул, подсоединяемых к нему,
происходил в молекулярном режиме. Кроме того, можно
быстро и автоматически изменять магнитное поле
анализатора в интервале от 2-й до 50-й массы и получать
автоматическую запись спектра масс. Для
количественных определений прибор градуируют по газовым
смесям известного состава. Строят график зависимости
интенсивности пика данной массы от давления смеси
в натекателе.
Весьма быстрым является способ анализа
экстрагированной из металла газовой смеси спектральным
фотометром. Свечение газовой смеси вызывается
высокочастотным полем при помощи катушки, надетой на
разрядную трубку. Спектральный аппарат снабжен
двумя монохроматорами, один из которых служит для
определения азота, а другой — для определения окиси
углерода. Содержание водорода определяется по
интенсивности неразложенного в спектр излучения
определенного участка плазмы, на котором интенсивность
зависит от содержания водорода. Величины
максимумов на кривых, вычерчиваемых самописцами, и служат
мерой количества газа в смеси. Градуировочные
графики для определения азота и окиси углерода получают
для эталонных смесей газа. Содержание окиси
углерода в газе не зависит от содержания азота и водорода,
в то время как содержание азота зависит от
содержания водорода. Поэтому определению азота должно
предшествовать определение водорода.
К преимуществам спектральных методов анализа
следует отнести быстроту анализа, возможность
автоматизации анализа, малый размер образцов.
Недостатки метода связаны с необходимостью иметь эталонные
образцы и сложностью оборудования.
ОГЛАВЛЕНИЕ
Предисловие 3
ГЛАВА I. МЕТОДЫ ПОЛУЧЕНИЯ ВЫСОКИХ ТЕМПЕРАТУР ... 5
1. Печи сопротивления 6
2. Высокочастотные индукционные печи 13
3. Дуговые печи 21
4. Плазменно-дуговые печи 23
5. Электроннолучевые печи 26
ГЛАВА II. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ 30
1. Термоэлектрические пирометры — термопары 31
2. Оптические методы измерения температур 37
3. Основные типы оптических пирометров 39
ГЛАВА III. КОНТРОЛИРУЕМЫЕ АТМОСФЕРЫ 44
1. Способы получения чистых газов 45
2. Техника безопасности при работе с газами 46
3. Методы очистки газов, применяемые в лафоратории ... 46
4. Создание проточных атмосфер 49
5. Измерение скорости и давления газовых потоков .... 51
ГЛАВА IV. ТЕХНИКА РАБОТЫ С ВАКУУМОМ 53
1. Вакуумные материалы 54
2. Конструирование вакуумных установок 57
3. Вакуумные насосы 60
4. Измерение вакуума 68
5. Отыскание течи 72
ГЛАВА V. ИССЛЕДОВАНИЕ СВОЙСТВ ЖИДКИХ
МЕТАЛЛИЧЕСКИХ И ШЛАКОВЫХ РАСПЛАВОВ 74
>1. Активности компонентов в растворах 74
2. Определение активности по равновесию раствора с газовой
фазой 75
3. Определение активности по упругости пара ...... 88
4. Определение активности по растворимости элемента в
расплаве 94
6. Определение активности по распределению элемента между
двумя фазами 95
6. Определение активности методом э.д.с 96
7. Калориметрия 108
8. Измерения диффузионных характеристик в жидких
металлах и шлаках . 122
9. .Поверхностные свойства жидких расплавов ...... 137
10. Плотность жидких расплавов 150
11. Вязкость расплавов 156
12. Электропроводность и магнитные свойства жидких
металлов 169
13. Электрические свойства шлаков ' 174
14.^ Растворимость газов в металле и шлаке ....... 178
15.'Обменные реакции между жидким металлом и шлаком . 189
16. Исследования расплавов в вакууме 192
255
ГЛАВА VI. ИЗУЧЕНИЕ ПРОЦЕССОВ ВОССТАНОВЛЕНИЯ И
ДИССОЦИАЦИИ окислов 198
1. Методы исследования процессов восстановления .... 199
2. Исследование диссоциации окислов 214
ГЛАВА VII. НЕМЕТАЛЛИЧЕСКИЕ ВКЛЮЧЕНИЯ В МЕТАЛЛАХ . 217
1. Металлографическая оценка включений 217
2. Методы анализа включений на шлифах 220
3. Выделение включений из твердого металла 223
ГЛАВА VIII. АНАЛИЗ ГАЗОВ В МЕТАЛЛАХ 228
1. Определение содержания кислорода 229
2. Определение содержания водорода 247
3. Определение содержания азота . 251
м ИБ Кг 1129
БОРИС ВАДИМОВИЧ ЛИНЧЕВСКИЙ
ТЕХНИКА МЕТАЛЛУРГИЧЕСКОГО ЭКСПЕРИМЕНТА
Редактор издательства Л. А. Левченкова
Художественный редактор Г. А. Ж е г и н
Технический редактор Н. В. Сидорова
Корректоры Ф. Б. Цалкина, О. В. Щербакова
Переплет художика Е. Н. Щегловой
Сдано в набор 25.10.78 Подписано в печать 18.04.79 Т-09208
Формат бумаги 84Х1087з2 Бумага типографская № 2
Гарнитура литературная Печать высокая Усл. печ. л. 13,44
Уч.-изд. л. 14,70 Тираж 6200 экз. Заказ 664 Цена 65 к. Изд. № 3467
Издательство «Металлургия», 119034, Москва, Г-34,
2-й Обыденский пер., д. 14
Подольский филиал ПО «Периодика» Союзполиграфпрома
при Государственном комитете СССР
по делам издательств, полиграфии и книжной торговли
г. Подольск, ул. Кироэа, 25