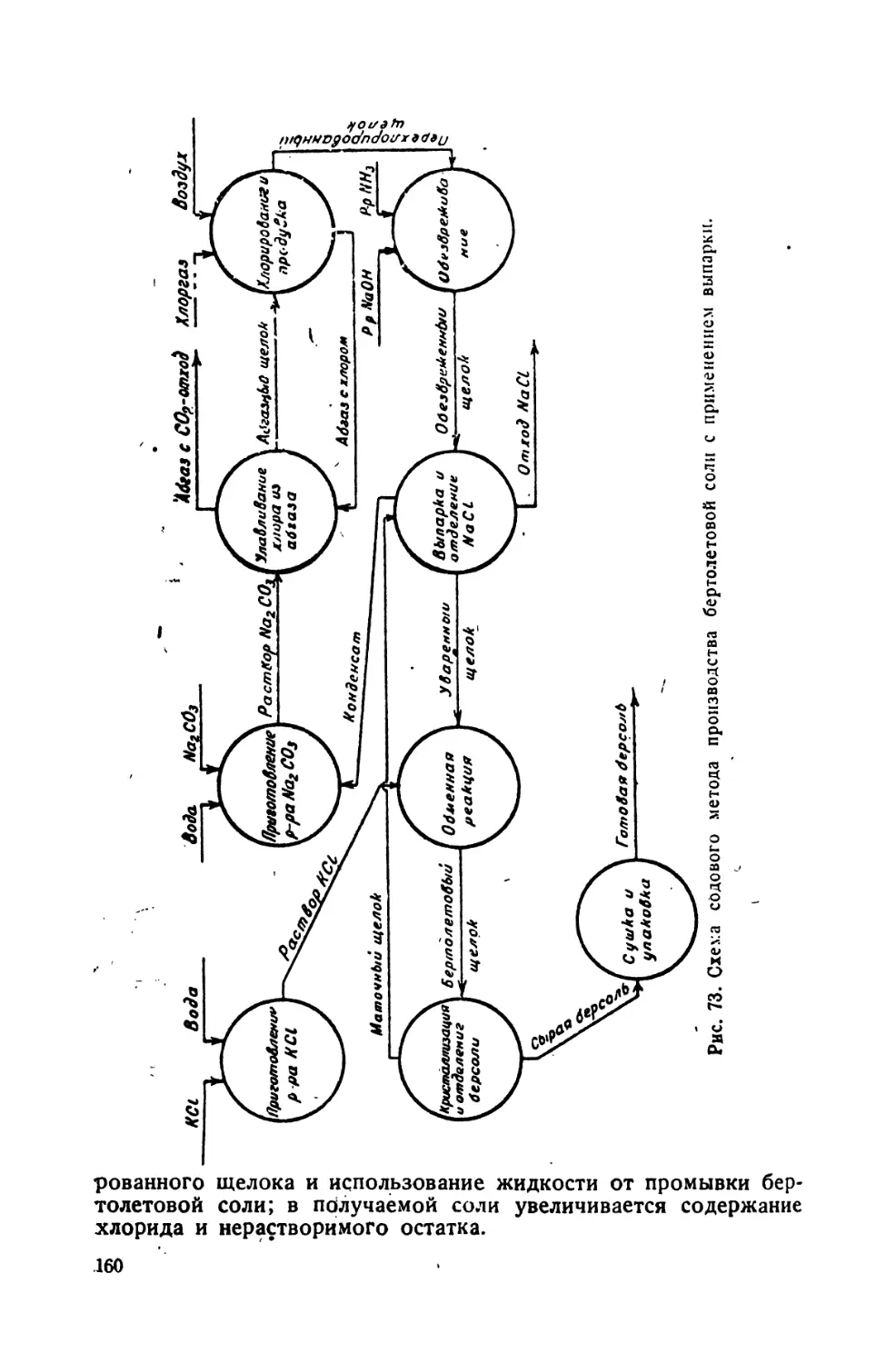
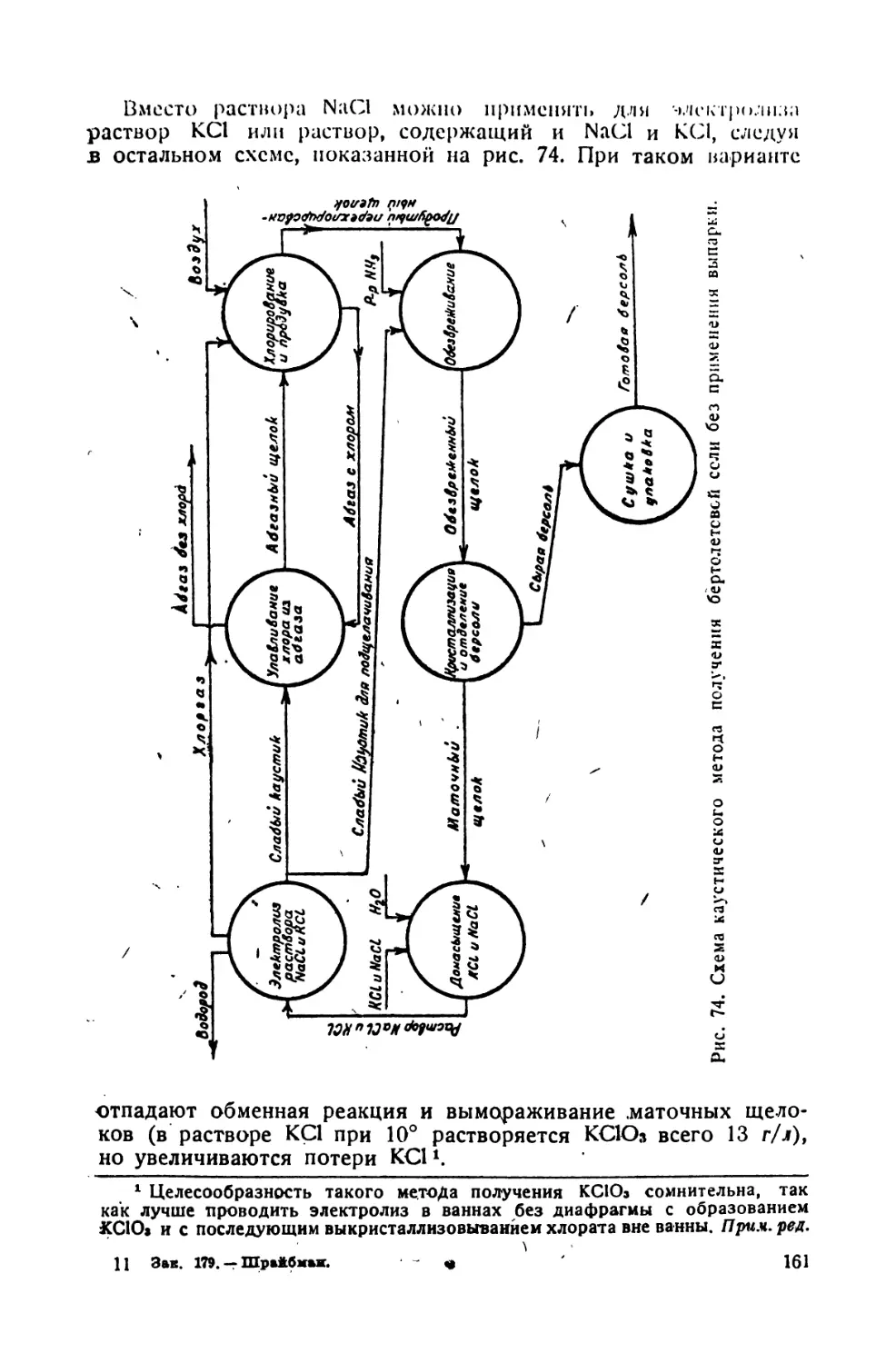
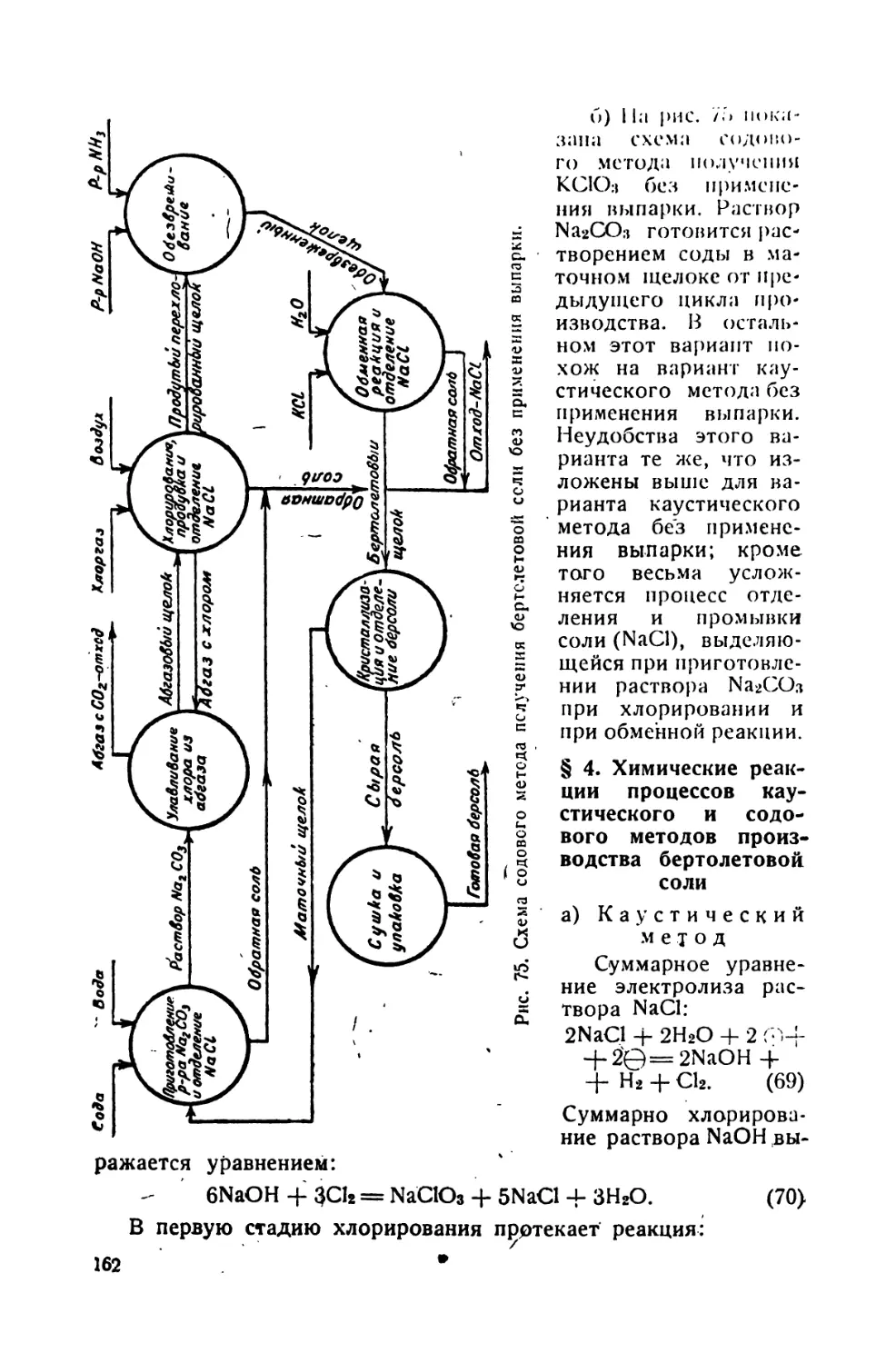
Автор: Шрайбман С.С.
Теги: химия химические производства химические вещества химическая технология
Год: 1938
Текст
Цена 8 р. 50 к., переп. 1 р.
С. С. ШРАЙБМАН
ПРОИЗВОДСТВО
БЕРТОЛЕТОВОЙ СОЛИ
И ДРУГИХ ХЛОРАТОВ
ПОД РЕДАКЦИЕЙ
Н. К ВОРОНИНА
РЕДАКЦИЯ ХИМИЧЕСКОЙ ЛИТЕРАТУРЫ ГОНТИ НКТП
' МОСКВА • 1938
ХМ-23-5-3
В книге описываются свойства и методы производства бертолетовой соли и
других хлоратов. Дается описание техно
логического процесса при различных методах производства и основной аппаратуры. Приведены данные ряда исследований в области производства хлоратов,
а также данные по контролю производства, 'технике безопасности, применению
хлоратов и т. д.
Книга предназначена для инженеров,
техников и мастеров и может быть полезна для студентов втузов.
К ЧИТАТЕЛЮ
Издательство просит присылать Ваши замечания и отзывы об этой книге
по адресу: Москва, Новая пл. 10, подъезд 11, Редакции химической литера-
туры.
Отв. редактор И. С. Митропольский Техредактор П. В. Погудкик
Сдано в набор 20/Н 1938 г. Подписано к печати 27/IX 1933 г.
Формат 62X94 ^/le- Бум. л. 11 у* Уполномоченный Главлита № Б-26059.
Тираж 1500 экз. Уч.-авт. л. 30,27. . Печ. л. 23/ Тип. зн. в 1 бум. л. 94400.
Дог. № 6264. # ( РХЛ 956. Бумага Окуловской ф-ки. Заказ X® 179.
В-я голография ГОНГИ азе. Евг. Соколовой. Ленинград, лр. Кр. Командиров, 29.
V
ОГЛАВЛЕНИЕ
Ctp.
Перечень таблиц . м 9
Предисловие .13
Введение. История развития производства бертолетовой соли . . .15
1. Метод Либиха —
2. Варианты метода Либиха —
3. Хлорирование MgO, ZnO, NaOH и Na»CO» 16
4. Электролитические способы 17
5. Развитие производства бертолетовой соли в СССР
Свойства бертолетовой соли • * 1&
1. Физические и химические свойства- —
2. Физиологические свойства 25
n 3. Качественные пробы на ион СЮз' -
4. Количественные методы определения иона СЮ»' 27
ЧАСТЬ ПЕРВАЯ. ИЗВЕСТКОВЫЙ МЕТОД ПРОИЗВОДСТВА
БЕРТОЛЕТОВОЙ СОЛИ
Глава 1. Способы производства бертолетовой соли известковым методом 29
1. Способ, основанный на хлорировании известкового молока невысокой концентрации —
2. Способ, основанный на получении при хлорировании щелока вы¬
сокой концентрации 32
3. Способ., основанный на выделении части СаСЬ из хлорированного
щелока *. . . 34
4. Некоторые замечания по сравнению разных способов производства бертолетовой соли известковым1 методом 35
Глава 2. Основное сырье для производства бертолетовой соли известковым методом ...... —
1. Известняк 36
а) Состав известняка —
б) Физические и химические свойства . . 37
2. Известь 38
а) Получение извести —
б) Состав извести 39
в) Физические и химические свойства ......... —
г) Гашение извести и пушонка 41
3. Хлор . . ‘ 42
а) Получение хлора .1 • . —
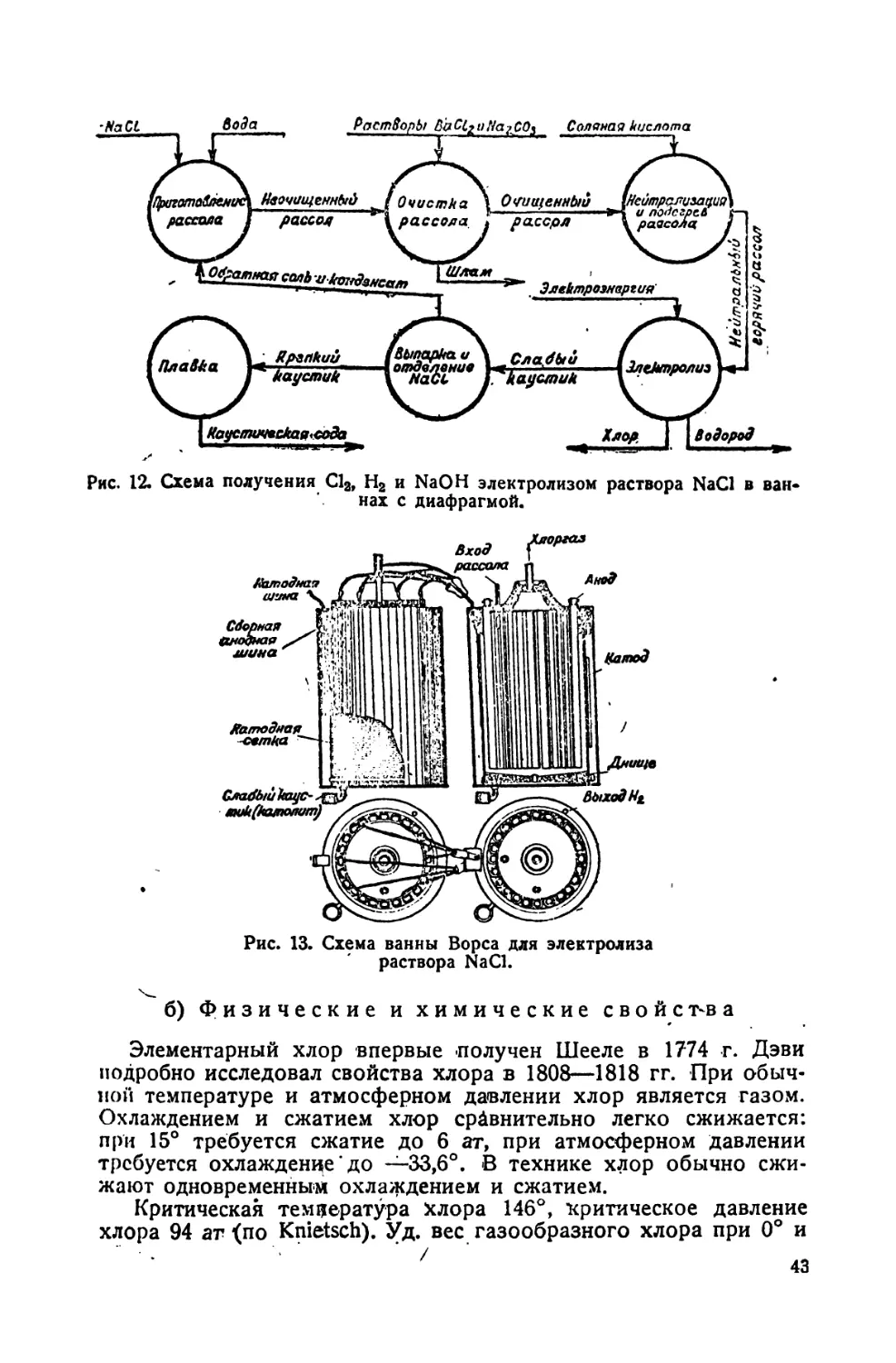
б) Физические и химические свойства 43
в) Состав хлоргаза 47
г) Перекачка хлоргаза 48
4. Хлористый калий
1*
Ст
* а) Получение хлористого калии 48
6) Физические <и химические свойства 4У
Глава 3. Получение известкового молока 50
1. Приготовление известкового молока —
2. .Очистка известкового ' молока ... 51
3. Хранение, охлаждение и перекачка молока 53
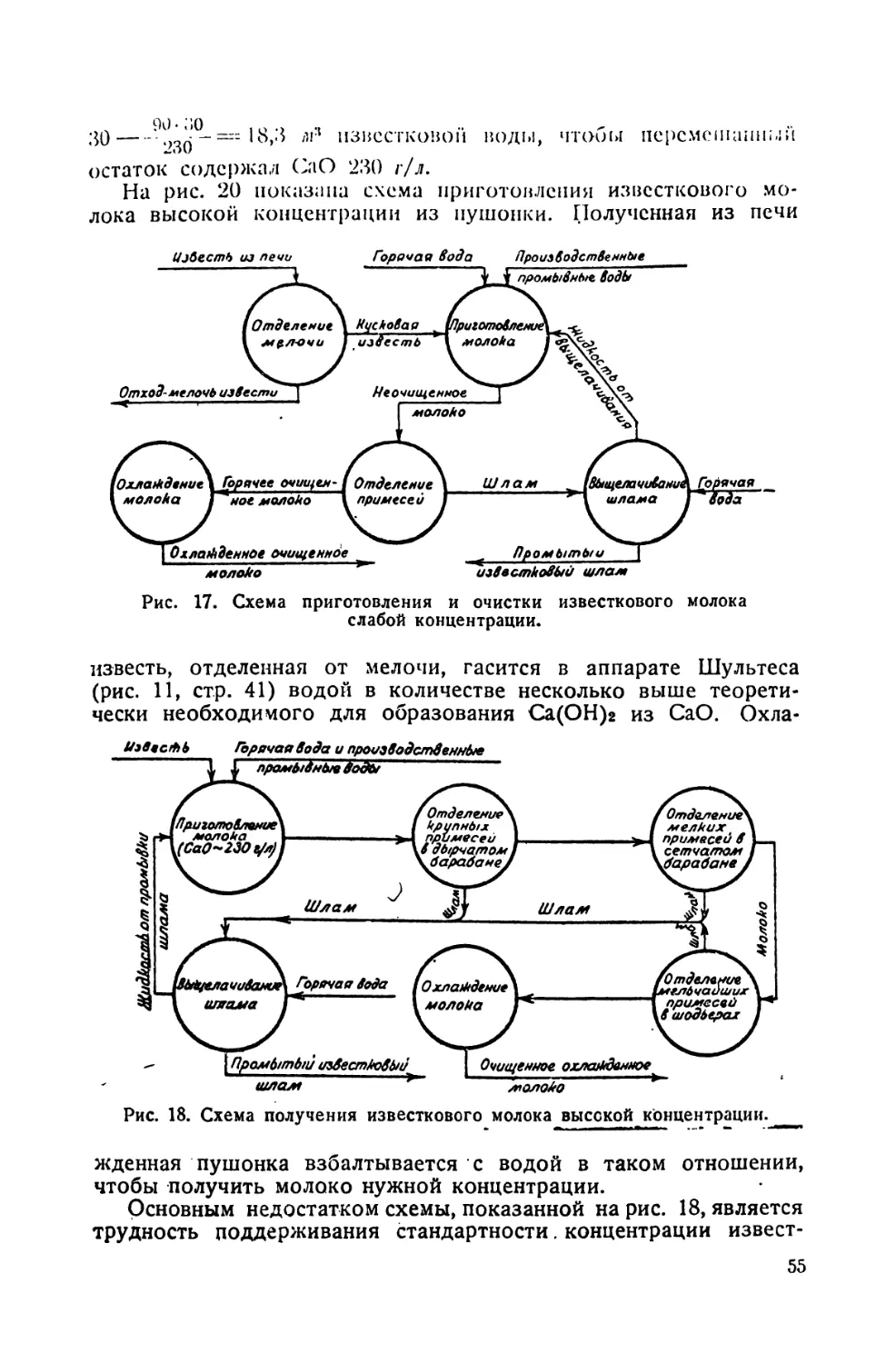
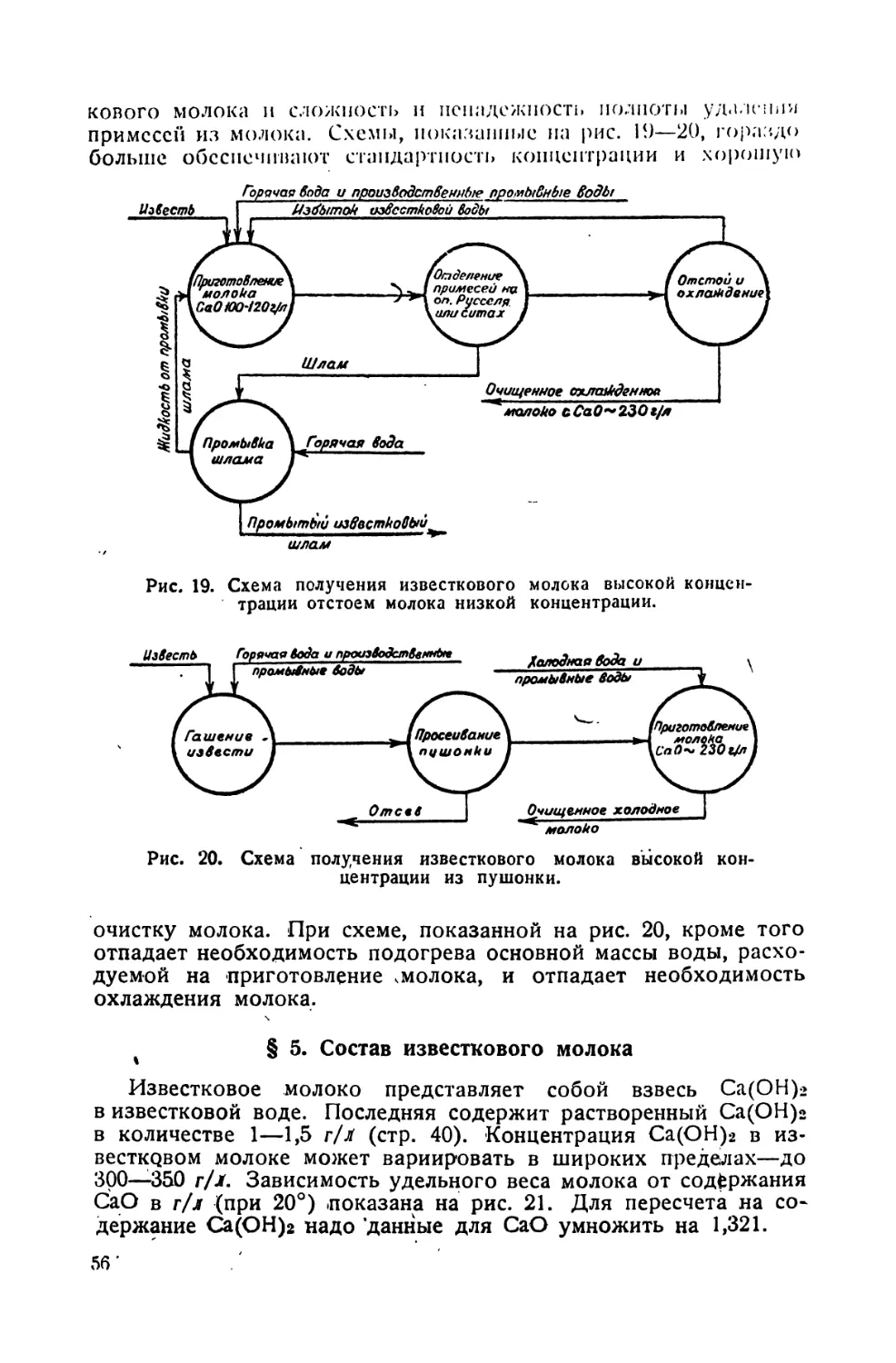
4. Схемы приготовления и очистки известкового молока .... 54
5. Состав известкового молока 56
Глава 4. Хлорирование известкового молока . . . •4 . > • • 58
1. Процессы хлорировании —
а) Химические реакции, происходящие при хлорировании . . . —
б) Факторы, влияющие на образование хлората и на выделение
кислорода при хлорировании 60
в) Тепловой эффект хлорирования 61
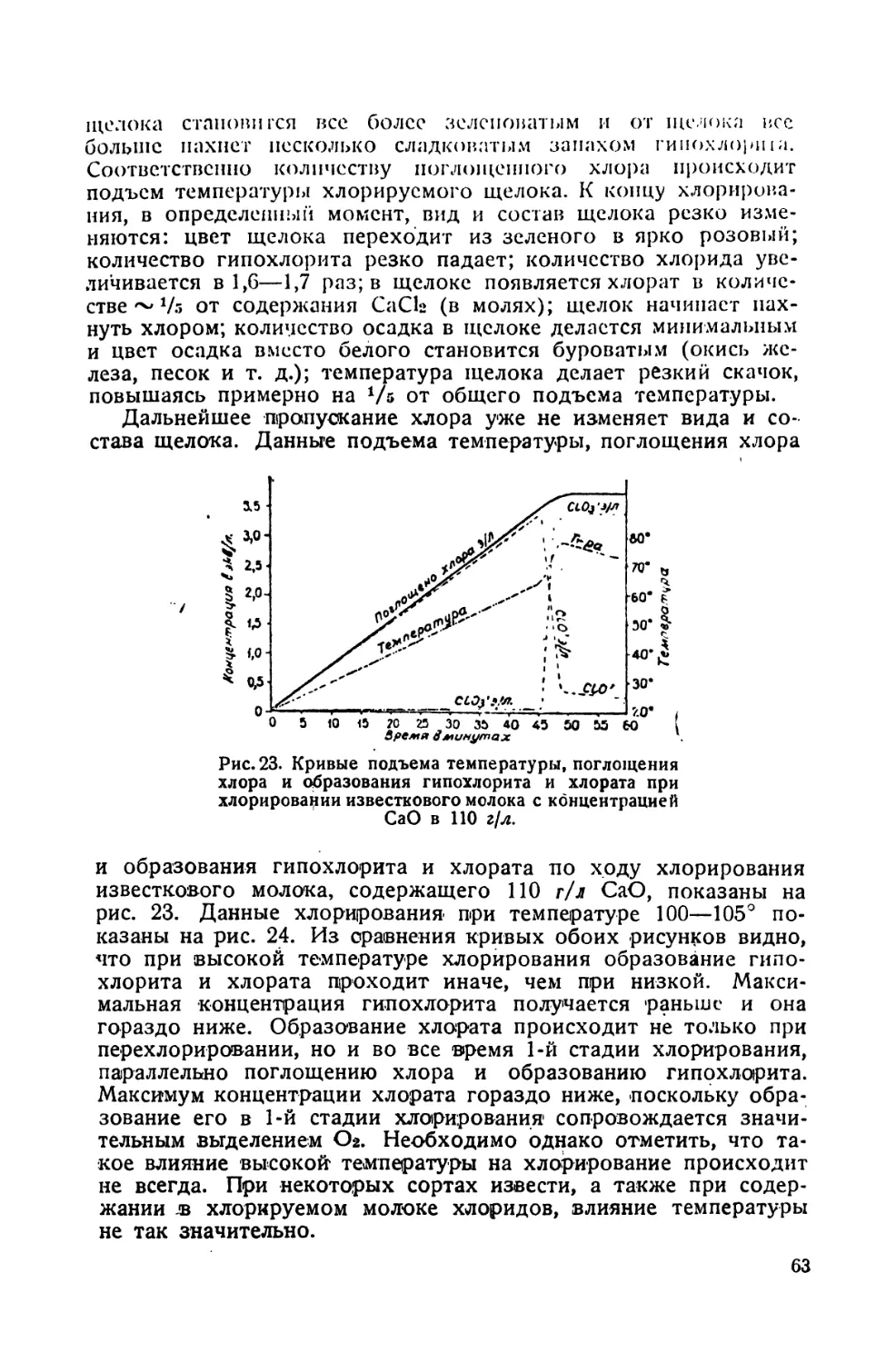
г) Некоторые опытные данные по изучению хлорирования . . 62
д) Внешний вид, состав и’свойства хлорированного щелока . . 66
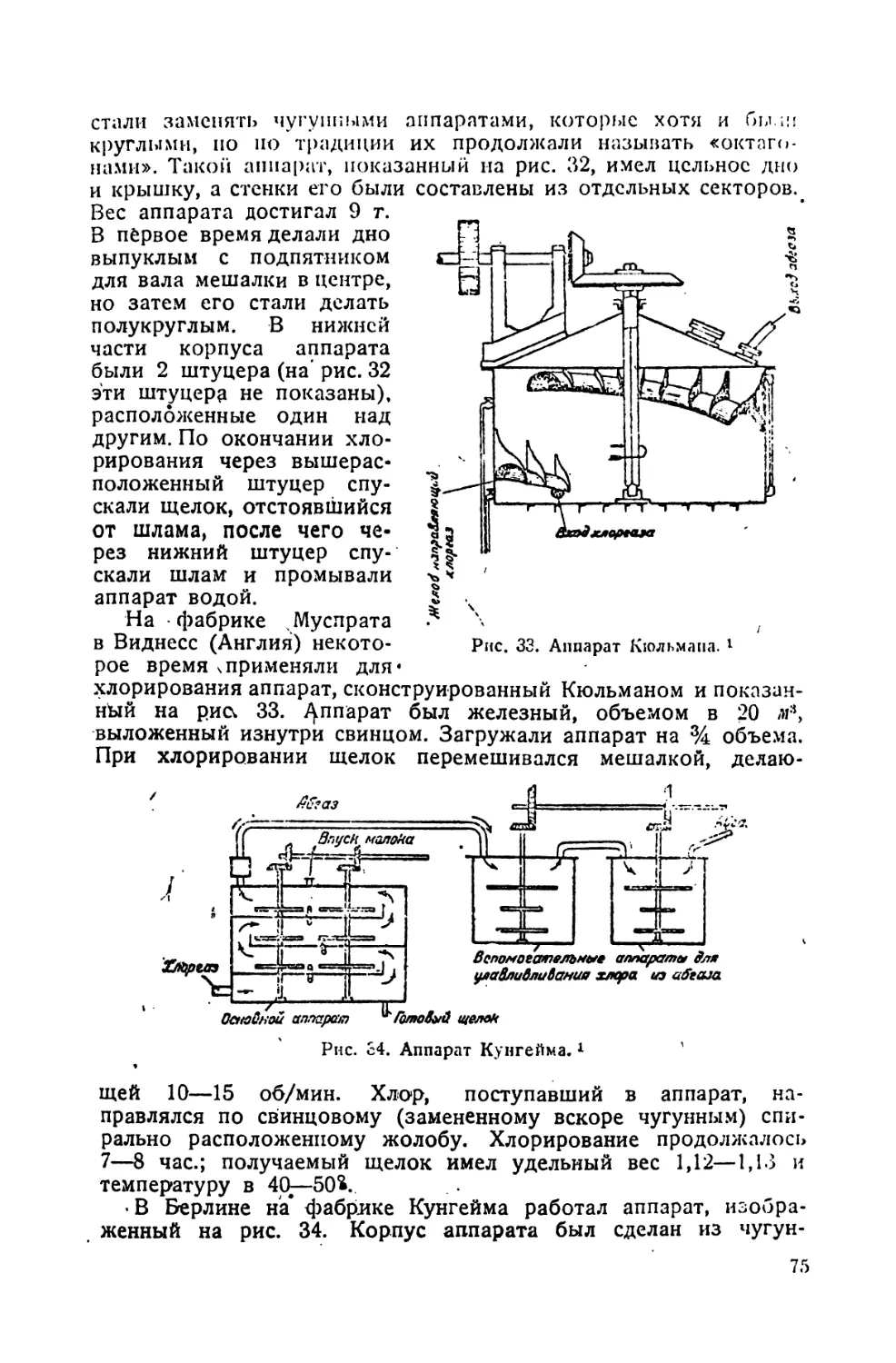
2. Аппаратура и техника хлорирования 70
а) Методы хлорирования & промышленном масштабе . . . .
б) Аппараты для хлорирования, имеющие исторический интерес 74
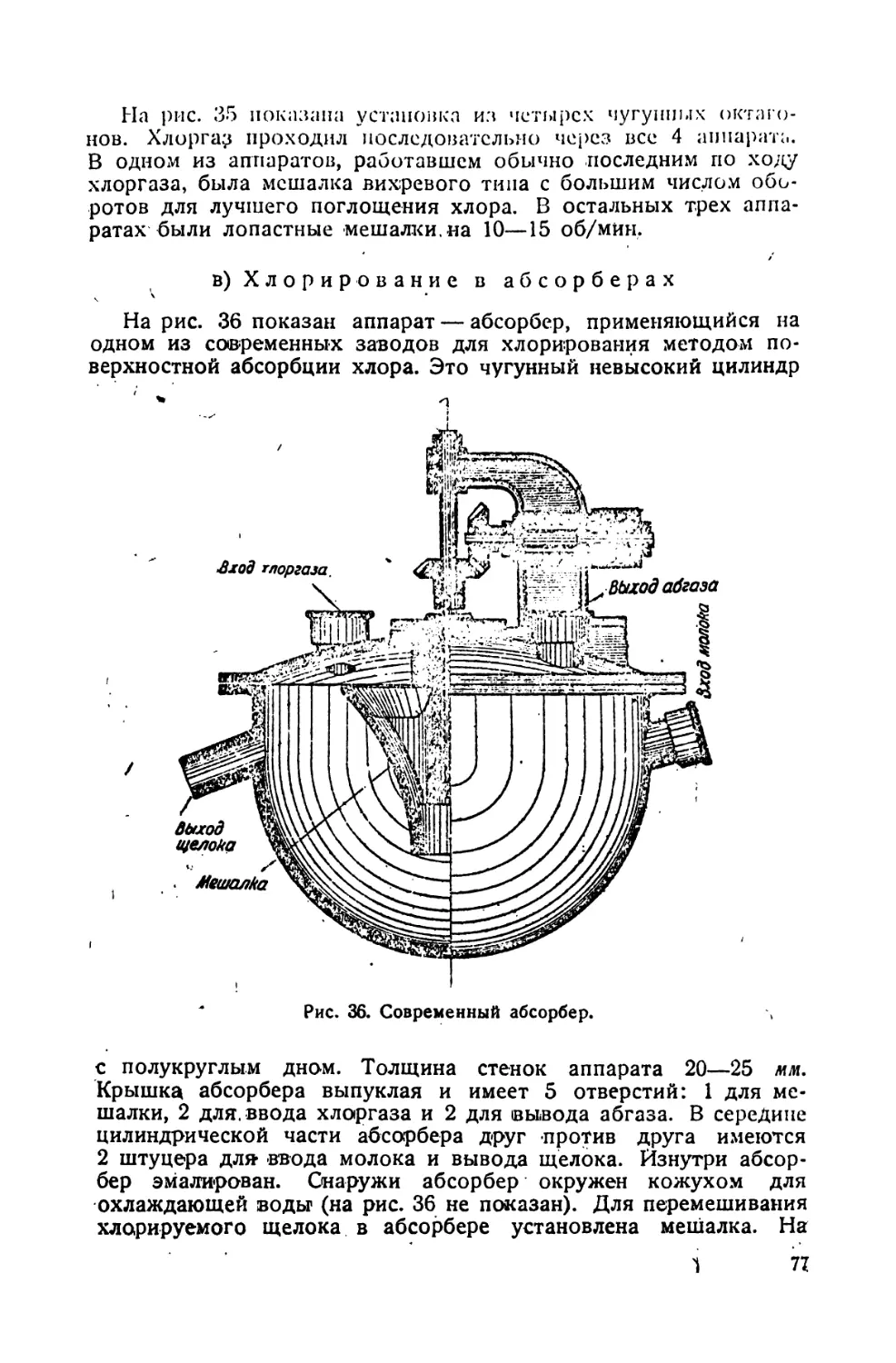
в) Хлорирование в абсорберах 77
г) Хлорирование барботажем в башнях 80
д) Сравнение хлорирования поверхностным поглощением в абсорберах и барботажем в башнях 82
е) Другие аппараты для хлорирования 84
ж) Состав абгаза при хлорировании абсорбцией и барбатажем . 89
3. Расчеты выходов и потерь при хлорировании 90
а) Расчет выхода хлората по анализу хлорированного щелока . —
б) Расчет ^выхода гипохлорита по анализу хлорирЪванного щелока 91
в) Расчет процента потери при хлорировании —
г) Расчет процента потери хлора с абгазом ....... 92
Глава 5. Обезвреживание хлорированных щелоков 94
L Сущность обезвреживания —
2. Обезвреживание неорганическими восстановителями .95
3. Обезвреживание органическими веществами 97
4. Аппаратура и техника обезвреживания —
Глава 6. Отделение шлама от хлорированных щелоков 99
1. Состав шлама —
2. Отделение шлама отстоем и выщелачиванием 100
3. Отделение шлама на фильтрпрессах —
4. Схема отделения шлама от щелока низкой и высокой концентрации 101
5. Потеря хлората со шламом ' . 102
Глава 7. Выпарка хлорированных щелоков 103
1. Цель' выпарки и место ее в схеме производства —
2. Пределы концентрации увариваемых щелоков . . . - . . . .104
. 3. Аппаратура- и техника выпарки 105
,4. Разложение хлората при -выпарке . . . . .106
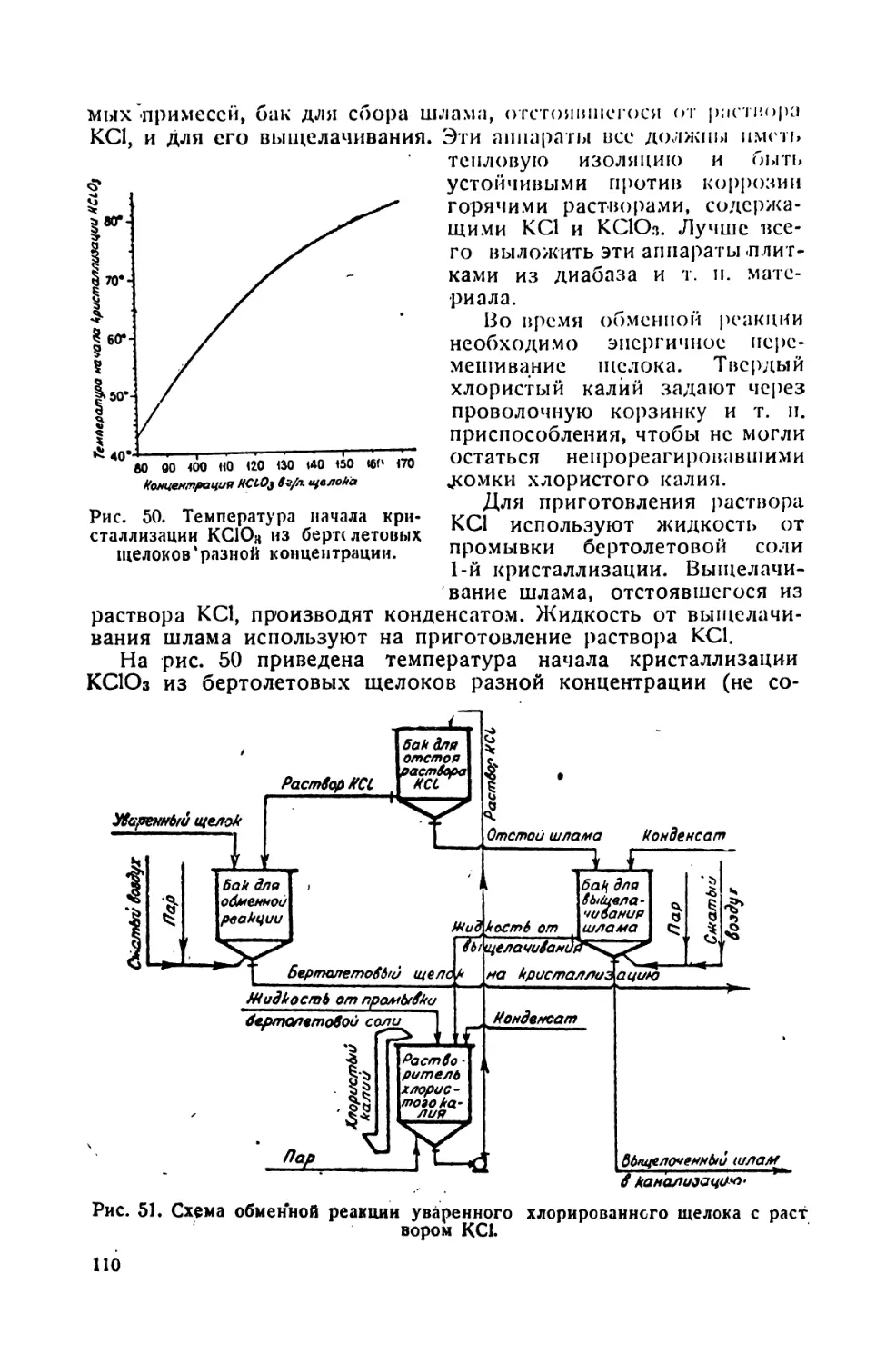
Глава 8. Обменная реакция 107
1. Сущность обменной реакции ....... —
2. Аппаратура и техника обменной реакции 109
3 Некоторые расчеты по анализам бертолетовых щелоков/. . .111
/
4
r.ri.
Глава 0. Кристаллизация КСЮ3 из бертолетовых щелоков . * • П2
1. Сущность кристаллизации —
2. Аппаратура для кристаллизации КСЮз ИЗ
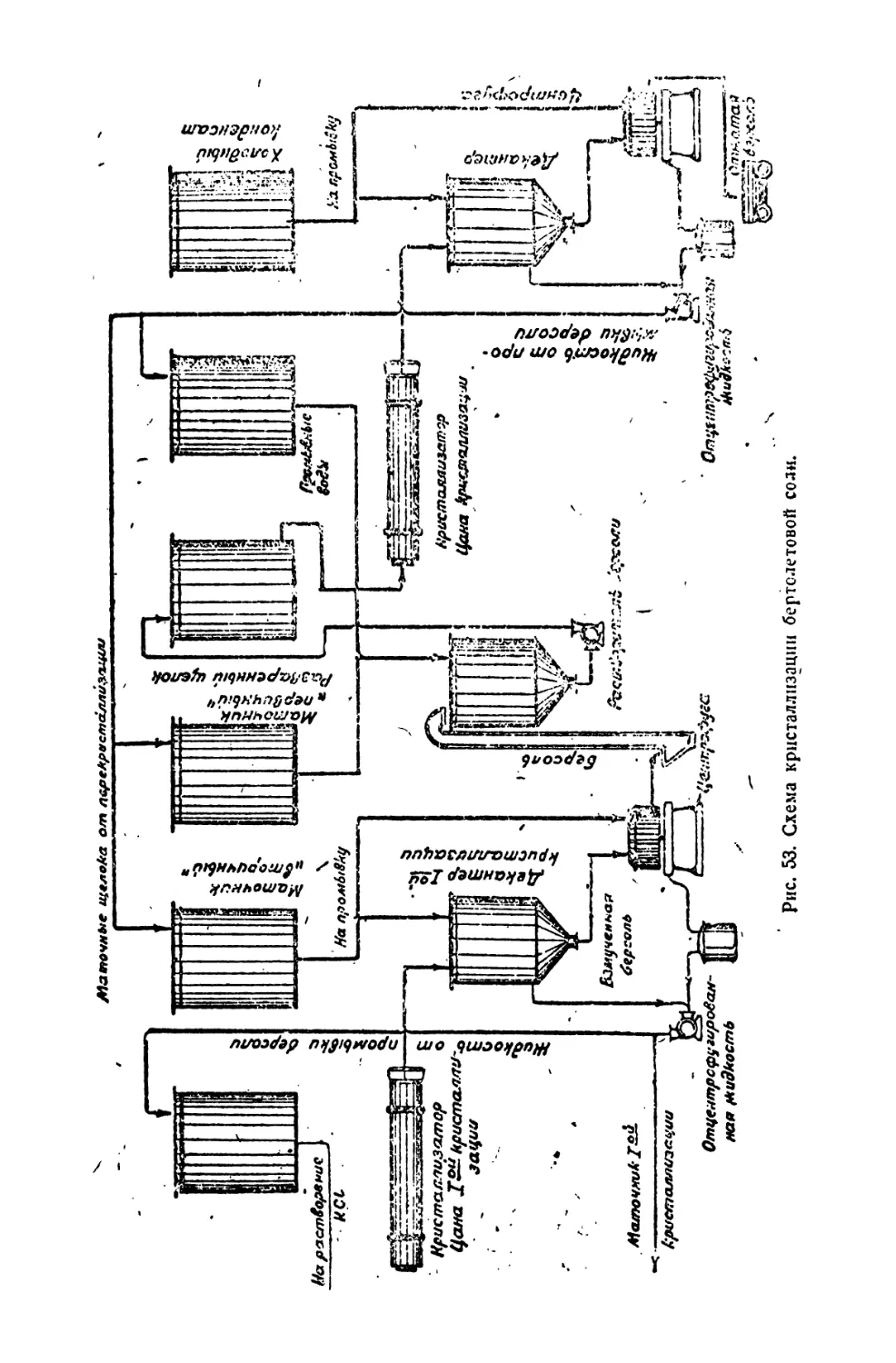
8, Рациональная схема кристаллизации 115
4* Состав бертолетовой соли первой и -второй кристаллизации . .ПН
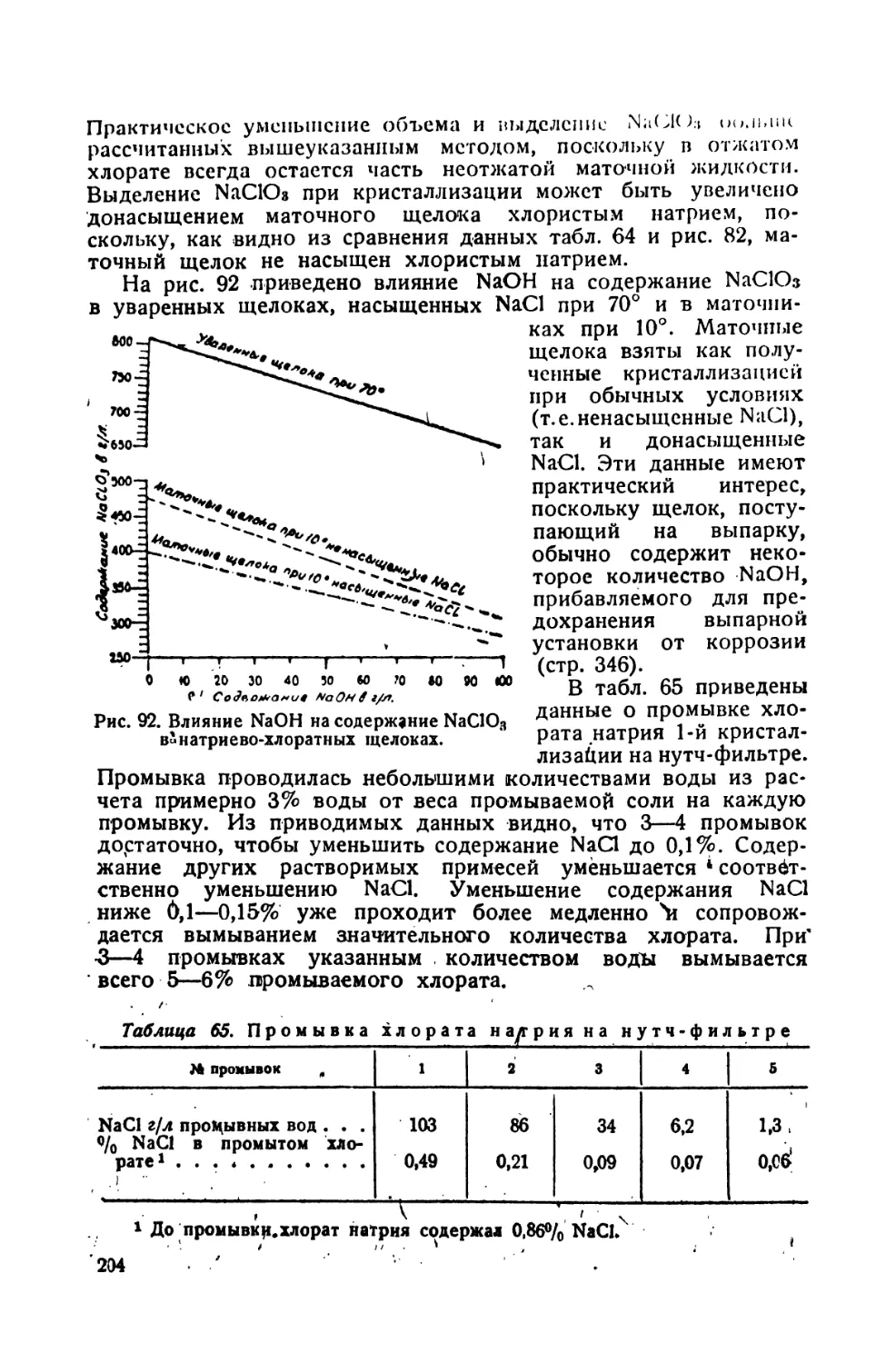
5. Промывка бертолетовой соли первой кристаллизации 121
6. Состав- -маточных щелоков первой и второй кристаллизации . . —
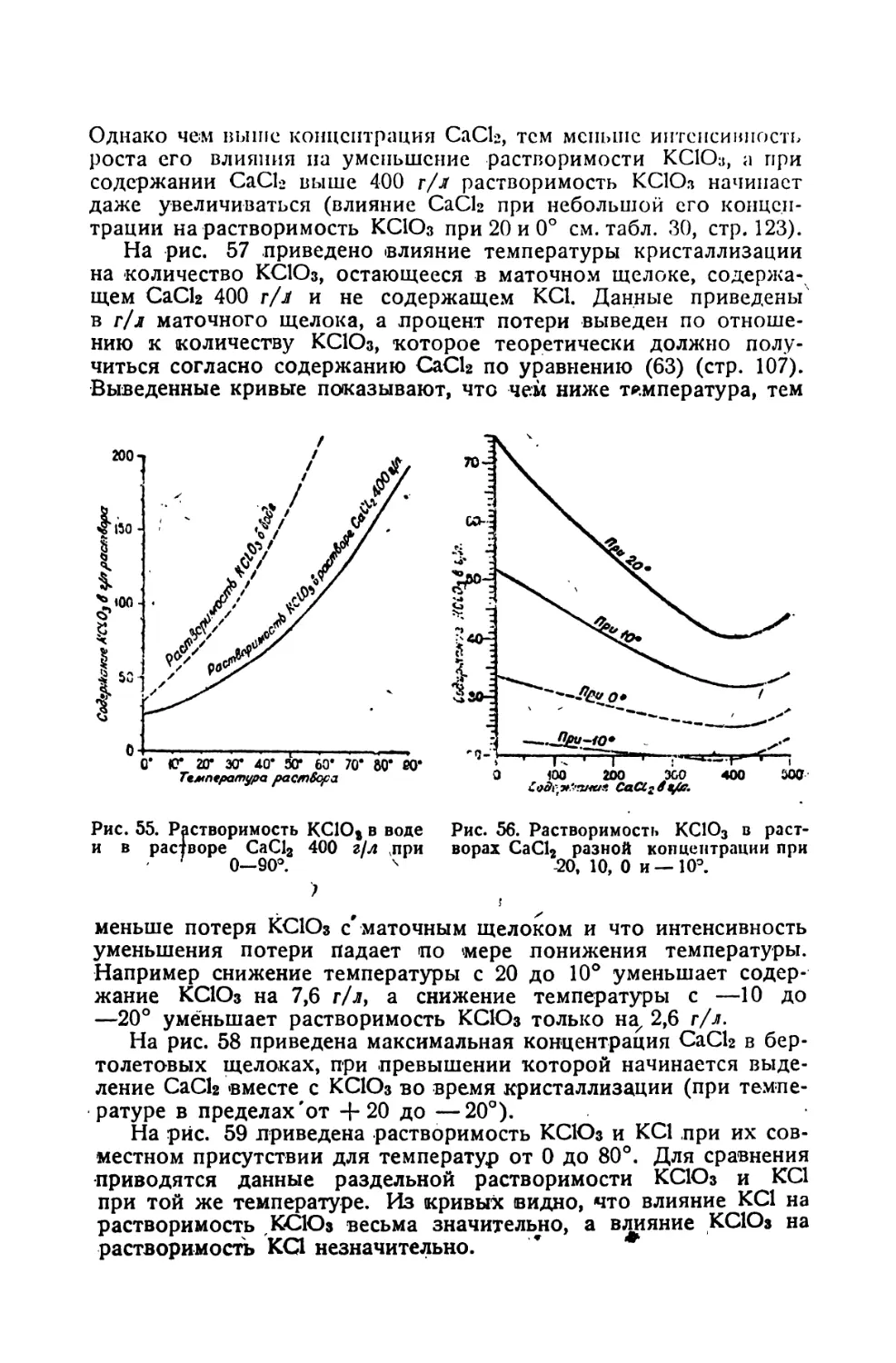
7. Влияние некоторых факторов на кристаллизацию КСЮз . . . 123
8. Некоторые расчеты -по процессам кристаллизации Ц‘2
Глава 10. Обработка сырой бертолетовой соли 133
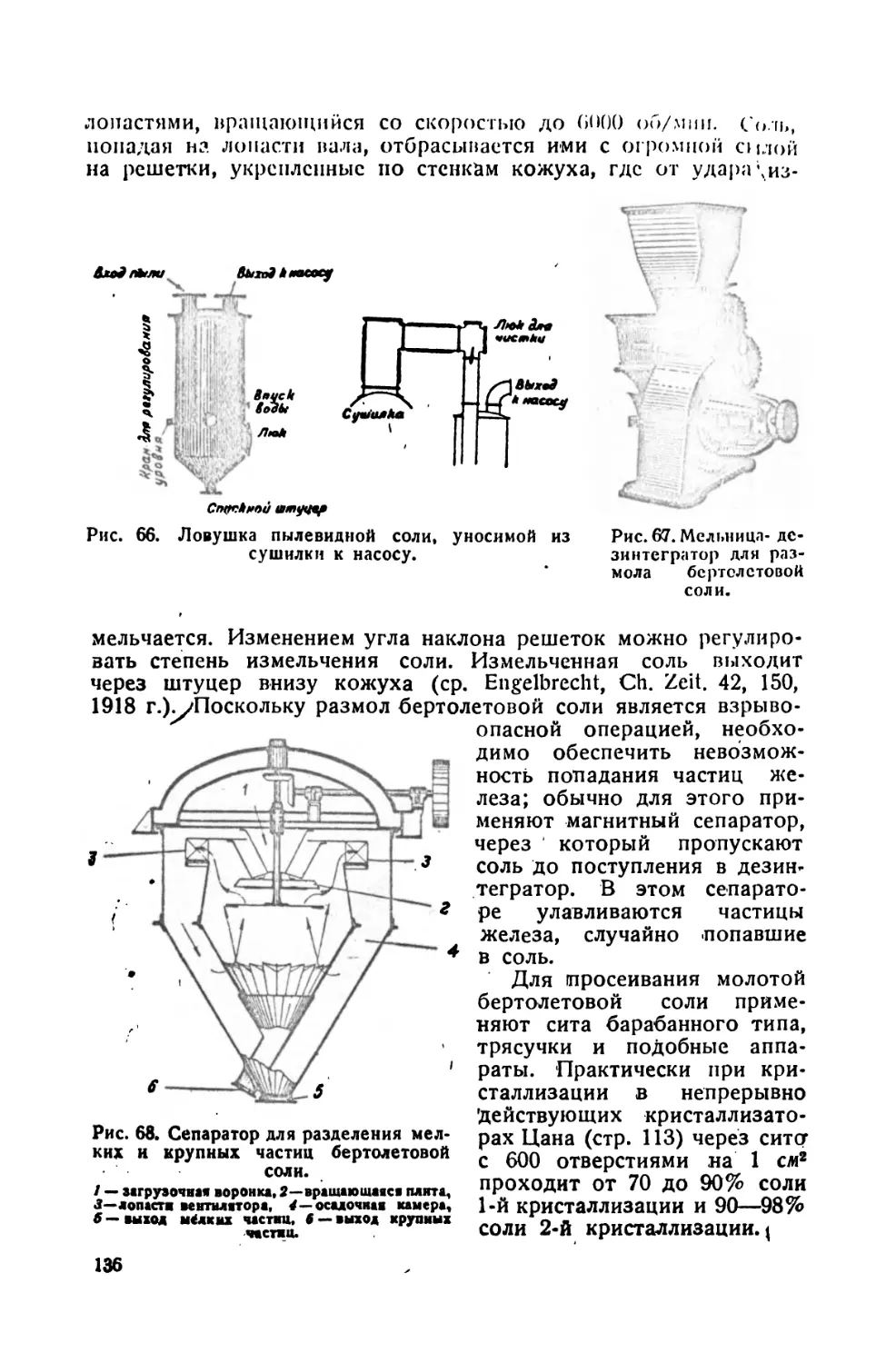
1. Аппаратура сушки, размола и просеивания 134
2. Схема и техника обработки сырой бертолетовой соли . . . .137
Глава 11. Использование маточных щелоков первой кристаллизации . . 138
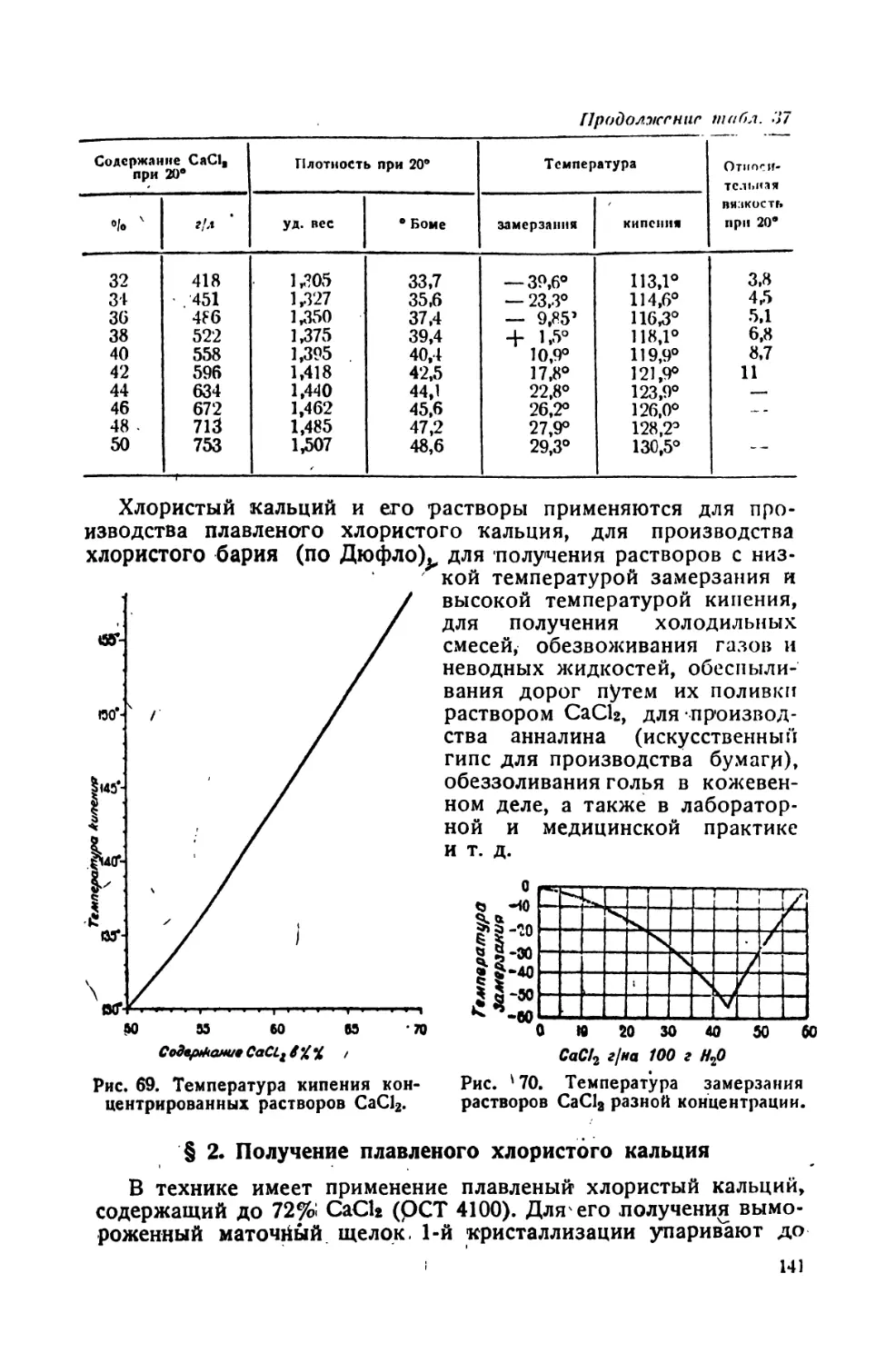
1. Свойства и применение СаСЬ и его растворов 139
2. Получение -плавленого хлористого кальция 141
3. Применение бертолетовых щелоков для получения хлористого бария (но Дюфло) 142
4. Использование хлората!, остающегося в маточном щелоке первой
кристаллизации . . 145
Глава 12. Основные коэфициенты получения бертолетовой соли известковым методом 146
к
1. Состав и количества производственных растворов и баланс потерь —
2. Расходные ковфициенты, количества получаемых отходов, расход
воды и пара * 150
3. Баланс воды для приготовления 'Известкового молока и раствора
КС1; распределение конденсата, получаемого при -выпарке хлорированных щелоков 152
4. Калькуляция готовой бертолетовой соли и штат завода производительностью 15 т КСЮз в сутки 153
ЧАСТЬ ВТОРАЯ. ДРУГИЕ МЕТОДЫ ПРОИЗВОДСТВА БЕРТОЛЕТОВОЙ
СОЛИ И МЕТОДЫ ПОЛУЧЕНИЯ ДРУГИХ ХЛОРАТОВ
Глава 13. Каустический и содовый! метод получения бертолетовой соли 156
1. Основная схема каустического метода
3. Варианты каустического и содового методов —
4. Химические реакции процессов каустического и содового методов^
производства бертолетовой соли 162
'5. Тепловой эффект хлорирования растворов NaOH и №2СОз . . .164
^4. Химические .реакции процессов каустического и Содового методов
по сравнению с известковым методом 165
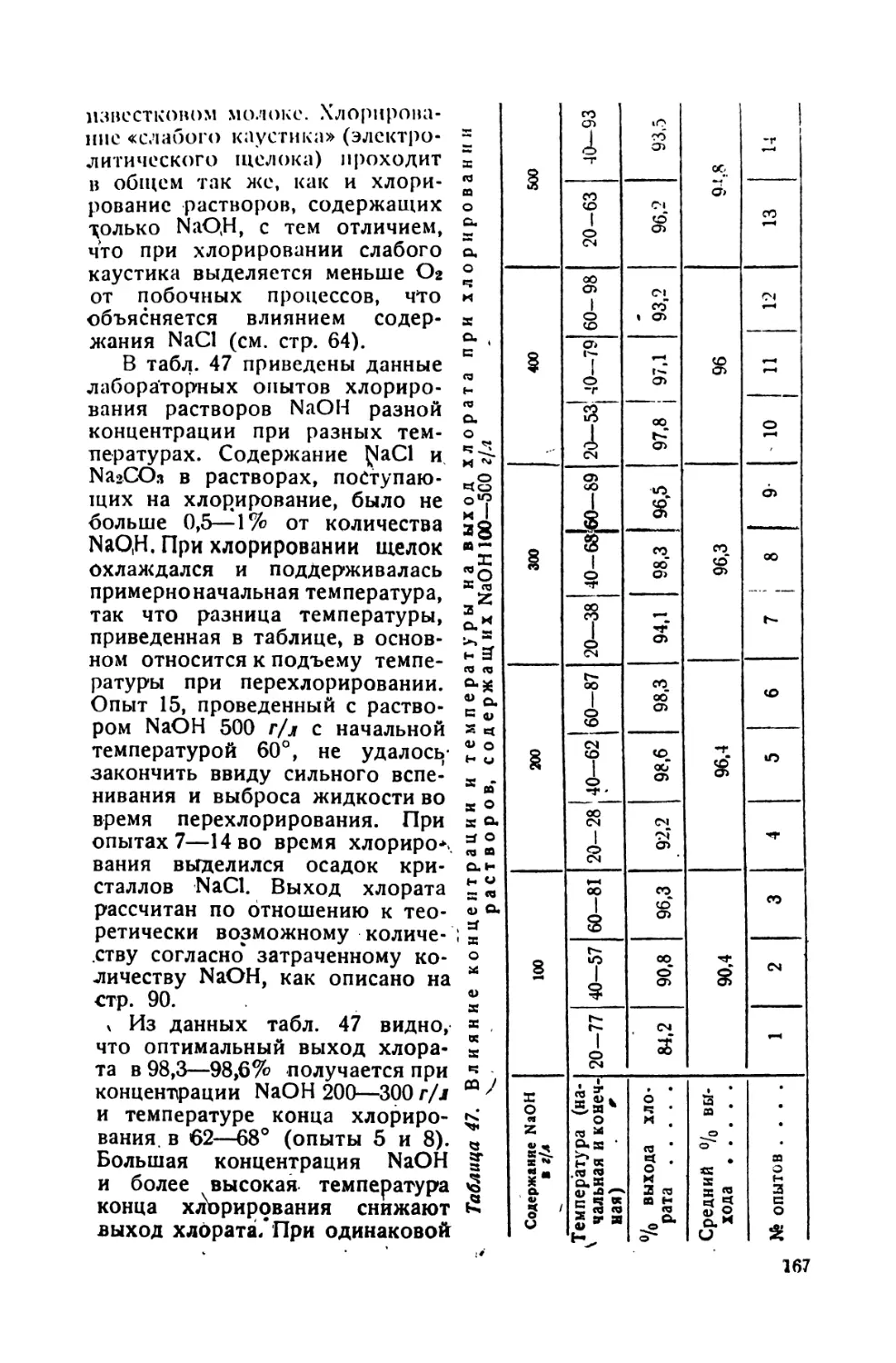
7. Некоторые данные по изучению хлорирования растворов NaOH . 166
8. Некоторые данные по изучению хлорирования растворов Na2COa 169
9. Количественные изменения при хлорировании растворов NaOH и
ИагСОз; состав и некоторые свойства щелоков 171
10. Некоторые данные по хлоратным щелокам 174
11. Некоторые данные по изучению кристаллизации КСЮз при каусти¬
ческом и содовом методах 175
12. Основные коэфициенты получения КСЮз каустическим и содовым
методами . . . . 178
Глава 14. Получение бертолетовой соли хлорированием MgO| ZnO, К2СОэ;
хлорирование С&СОз .180
1. Применение окиси магния для получения бертолетовой соли . • —
2. Применение окиси цинка для получения бертолетовой соли • .182
5
!
(,ф.
«3. Применение поташа для -получения бертолетовой соли . . .'’ . 182
4. Хлорирование СаСОп 183
Глава 15. Хлорат натрия 186
1. Физические и химические свойства 187
2. Получение хлората натрия из бертолетовой соли 190
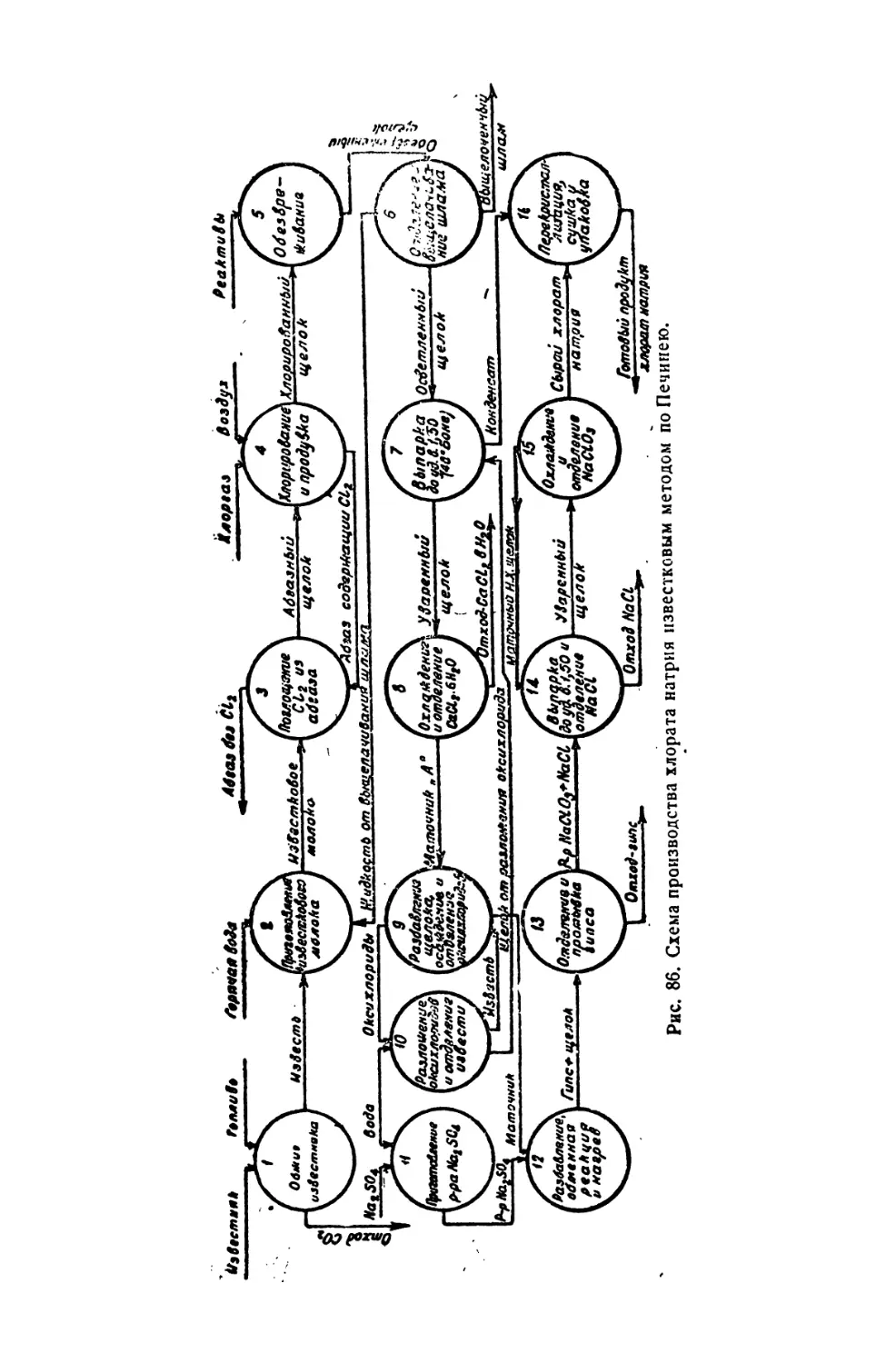
3. Известковый метод ГГсчннея * .НИ
4. Магнезиальный метод —
5. Метод с окисыо цинка 193
6. Методы с NaMnCH, Na2C*04 и бурой
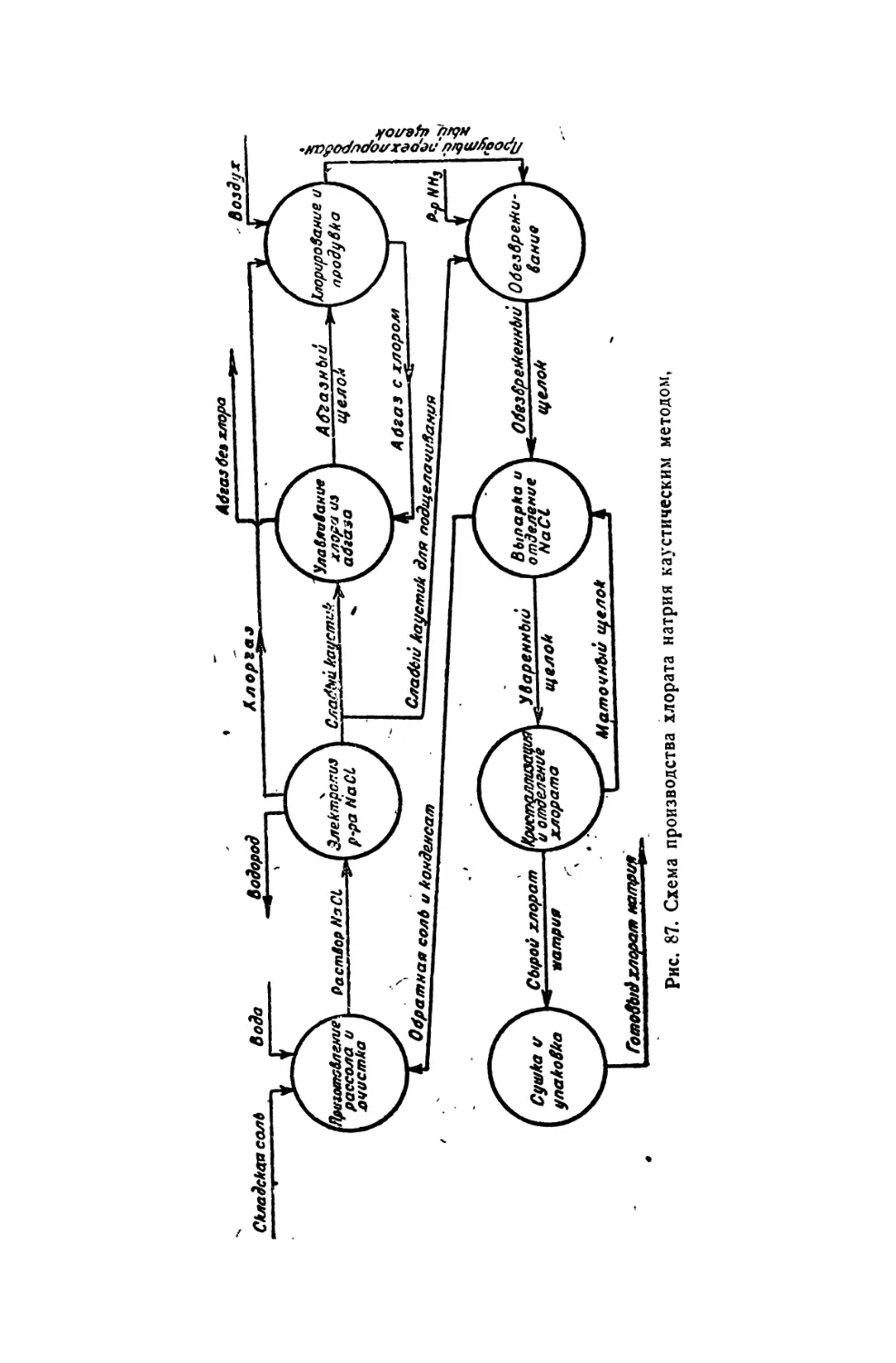
7. Каустический -метод 4 —
8. Способы с КагСОз 195
9. Электролитическое получение NaCICb 196
10. Переработка н атриев о - х ло р атн ых щелоков —
11. Изучение выделения хлорида по Печинею 197
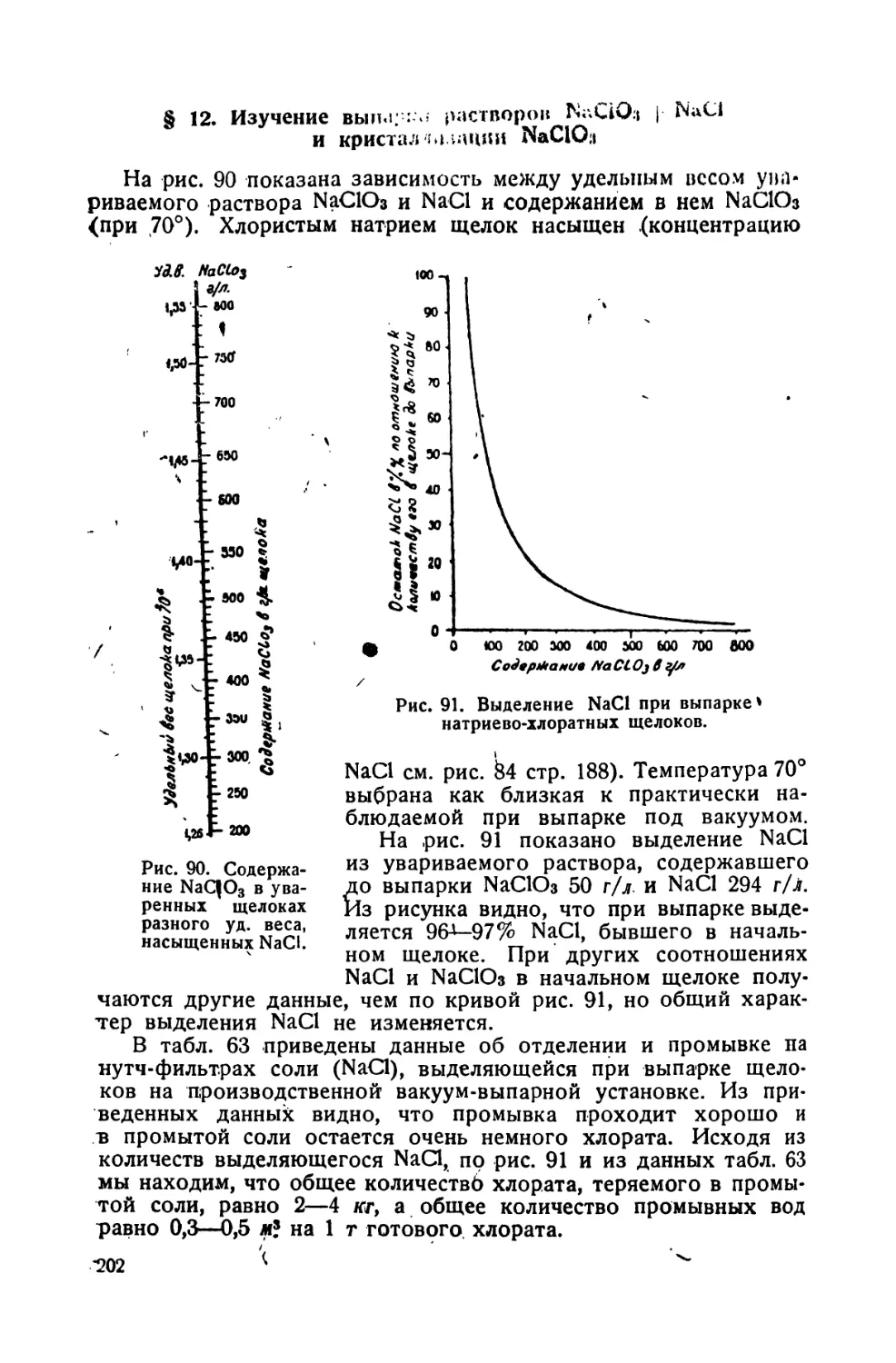
12. Изучение выпарки растворов NaClOa -f NaCl и кристаллизации NaClOs 202
13. Основные коэфициенты получения хлората натрия 207
Глава 16. Хлорат бария и хлорат кальция 210
Хлорат бария • . . . —
1. Физические и химические свойства 211
2. Получение хлората бария из бертолетовой соли 212
3. Получение хлората бария из хлората натрия • 213
4. Известковый метод получения хлората бария . . 1 216
. 5. Получение хлората бария, хлорированием баритового молока . . -
6. Основные коэфициенты получения хлората бария 216
Хлорат кальция 218
7. Физические и химические свойства хлората кальция —
8. Способы получения хлората кальция 219
9. Некоторые коэфициенты получения хлората кальция ... . . . 220
Глава 17. Хлораты других металлов; хлорноватая кислота 221
1. Хлораты лития, рубидия, цезия, меди, серебра, аммония .... —
2. Хлораты бериллия, магния, стронция, цинка, кадмия, ртути . . . 228
3. Хлораты алюминия, скандия, иттрия, эрбия, талия, циркония, олова,
свинца, висмута 234
4. Хлораты хрома, урана, марганца, железа, кобальта, никеля . . . 237
5. Хлорноватая кислота . . . : . . .241
6. Сводные таблицы свойств хлоратов 242
ЧАСТЬ ТРЕТЬЯ. ЭЛЕКТРОЛИТИЧЕСКИЕ МЕТОДЫ ПОЛУЧЕНИЯ
/ ХЛОРАТОВ
Глава 18. Электролиз с платиновыми анодами 248
1. Электролиз нейтрального раствора хлорида —
2. Электролиз щелочного раствора хлорида 254
3. Электролиз слабокислого раствора хлорида . 257
4. Материал катодов и защита от катодного восстановления . . • 264
5. Общие замечания по электролизу с платиновыми 'анодами . . . 269
Глава 19. Электролиз с магнетитовыми, угольными и графитовыми
анодами 270
1. Электролиз с магнетитовыми анодами —
2. Электролиз с угольными и графитовыми анодами 272
Глава 20. Схемы электролитического получения хлоратов» классификации
ванн, производственные коэфициенты 279
1. Общие данные режима работы • —
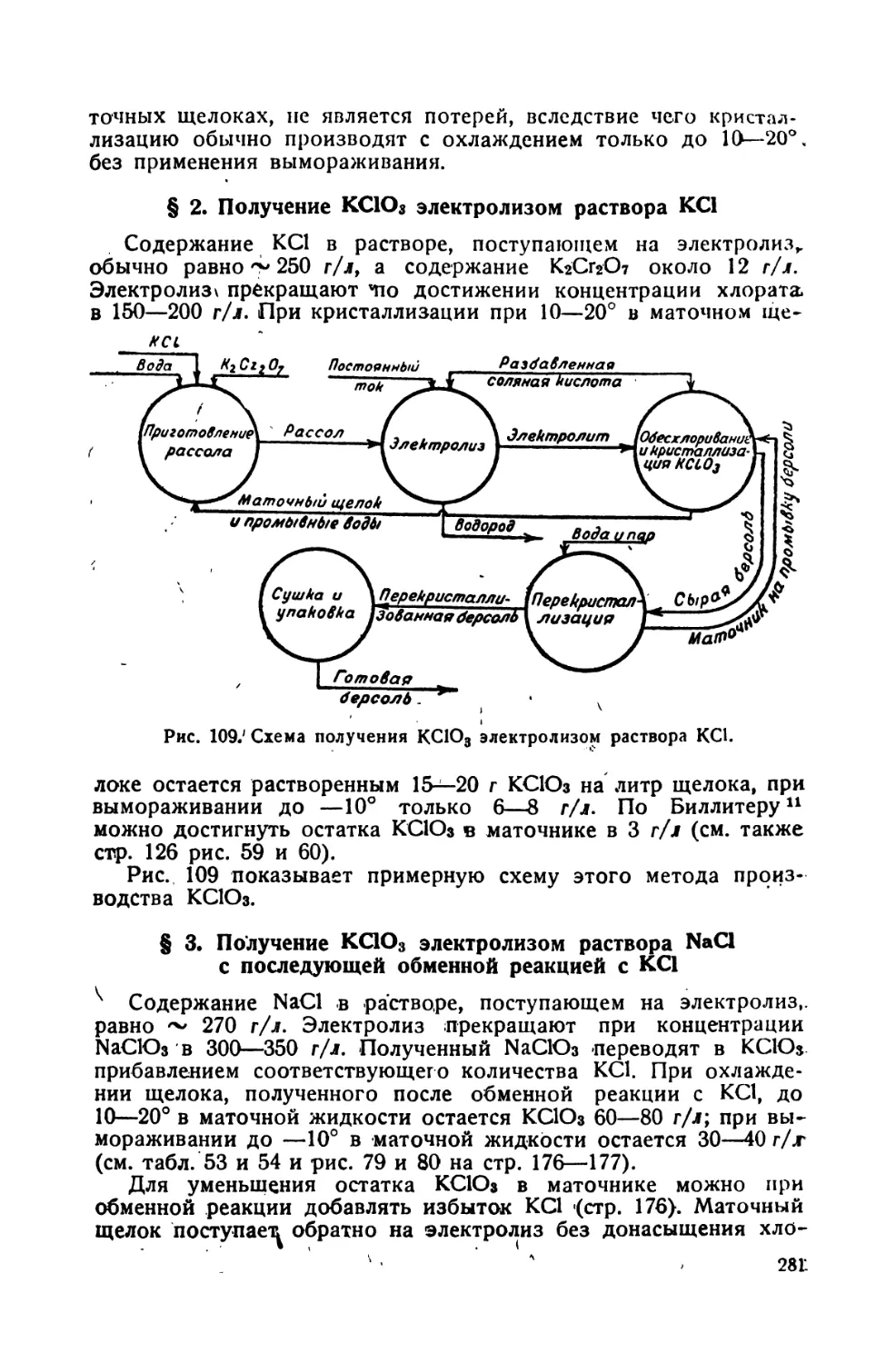
2. Получение КСЮз электролизом раствора КС1 ....... 281
6
Стр.
3. Получение KOI Од электролизом растпрра NaCl с последующей о 6-
мешюи реакцией с KOI 281
4. Получение NaCICh " 28l>
5. Получение NaCICh и КСЮз из бикарбонатов ‘-'КЗ
6. Получение хлоратов лития, бария и кальция —
7. Классификация «ванн, применяемых для получения хлоратов
• электролизом 284
8. Коэфициенты электролитического получения хлоратов .... 285
Глава 21. Описание отдел*-- -особое и ванн, применяемых для получения хлората. - '.’ ролнзом 286
1. Ванна Уатта —
2. Способ и ванны Галля и Монтлора 287
3. Способ Карлсона 288
4. Способ Блюменберга 289
5. Способ Nat. Electric. Со 290
6. Способы и ванны Гертера, Брука, Кельнера, Спилкера и Лове,
Гиббса, Зильбермана и Имгоффа 293
7. Способ и ванны Корбэна и* Ледерлзна 295
8. Способ Гаслиегера 300
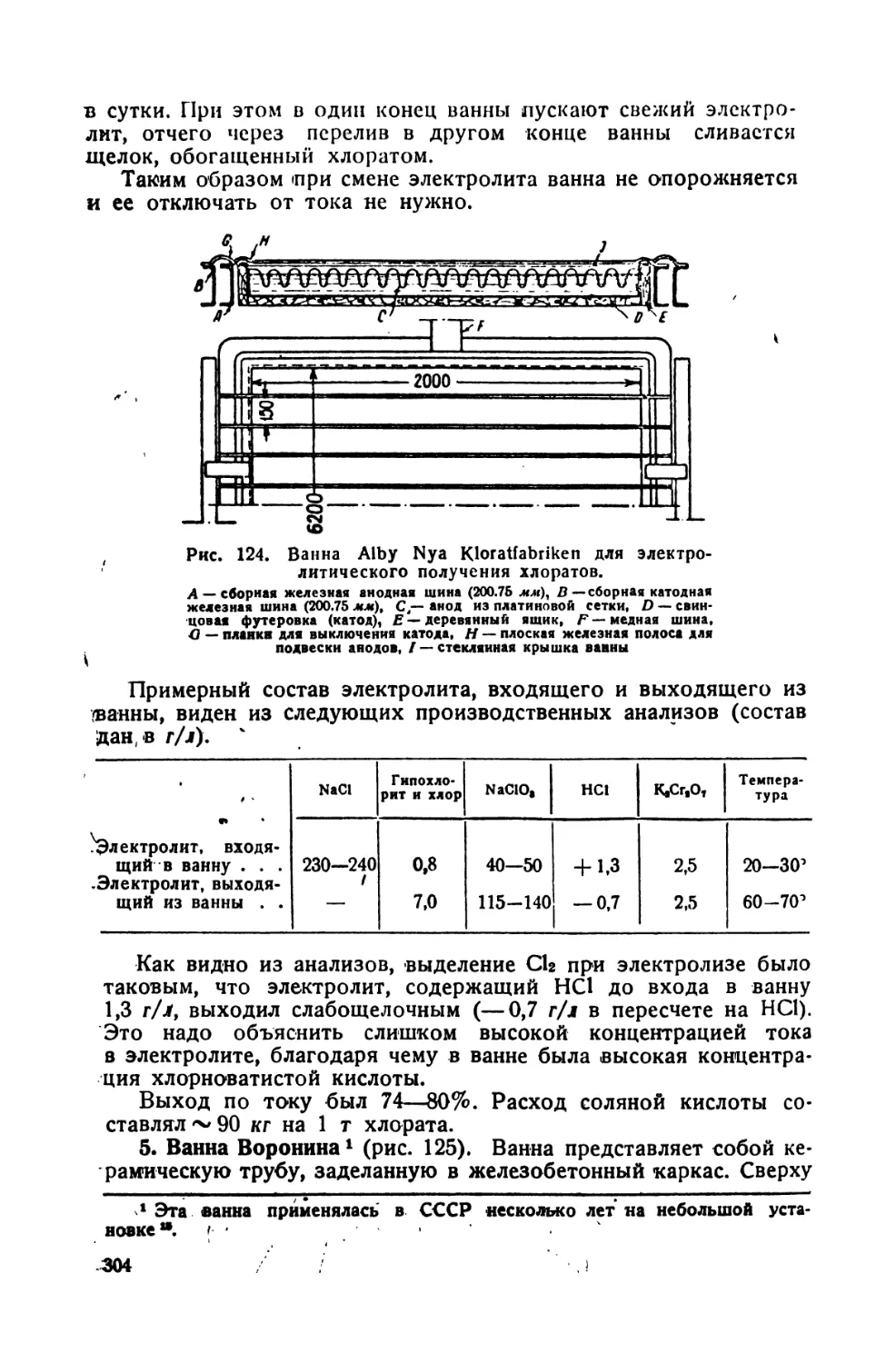
9. Современные ванны Баркера, Ангела, Аус^игского союза, Abby .
Nya Kloratfabriken, Воронина 301
ЧАСТЬ ЧЕТВЕРТАЯ. КОНТРОЛЬ ПРОИЗВОДСТВА, ТЕХНИКА БЕЗОПАСНОСТИ, ПОТРЕБИТЕЛИ ХЛОРАТОВ, ПРОИЗВОДСТВЕННЫЕ
ИНСТРУКЦИИ
Глава 22. Лабораторный контроль производства хлоратов 307
1. Наиболее частые аналитические определения, применяемые при
контроле производства хлоратов —
2. Анализы сырья, применяемого при производстве бертолетовой
соли известковым методом 313
3. Анализы производственных растворов^ получаемых при производстве бертолетовой соли известковым методом 314
4. Анализы отходов, получаемых при производстве бертолетовой
соли известковым методом * 318
5. Контроль готовой бертолетовой соли 319
6. Особенности контроля производства бертолетовой соли каустическим, содовым и электролитическим методами 322
7. Контроль получения хлората натрия и хлората бария .... 324
Глава 23. Техника безопасности, охрана труда и противопожарные
мероприятия ..... 325
1. Влияние хлора па организм и личные меры предосторожности 326
2. Влияние содержания хлора в атмосфере производственных помещений на ход производства 327
3. Наиболее частые причины содержания хлора в атмосфере про-
, иэводственных помещений —
4. Опасность образования взрывчатых смесей в абгазе 328
5. Пожаро- и взрывоопасность бертолетовой соли и ее растворов 329
6. Описание некоторых аварий в производстве бертолетовой соли 330
7. Меры предосторожности против взрывов и пожаров . . . . . 332
Глава 24. Основные потребители хлоратов 333
1. Применение бертолетовой соли в производстве спичек .... —
2. Применение- хлоратов для приготовления взрывчатых веществ,
воспламенительных составов, фейерверков и т. д 334
3. Применение хлоратов в качестве гербесидов 335
7
, Crp.
Глава 25. Некоторые данные по режиму работы основных стадий производства 337
1. Хлорирование на абсорберной установке —
2. Хлорирование барботажем в башнях 339
3. Улавливание хлора из абгаза 340
4. Перекристаллизация бертолетовой соли 341
5. Сушка бертолетовой соли —
ПРИЛОЖЕНИЯ
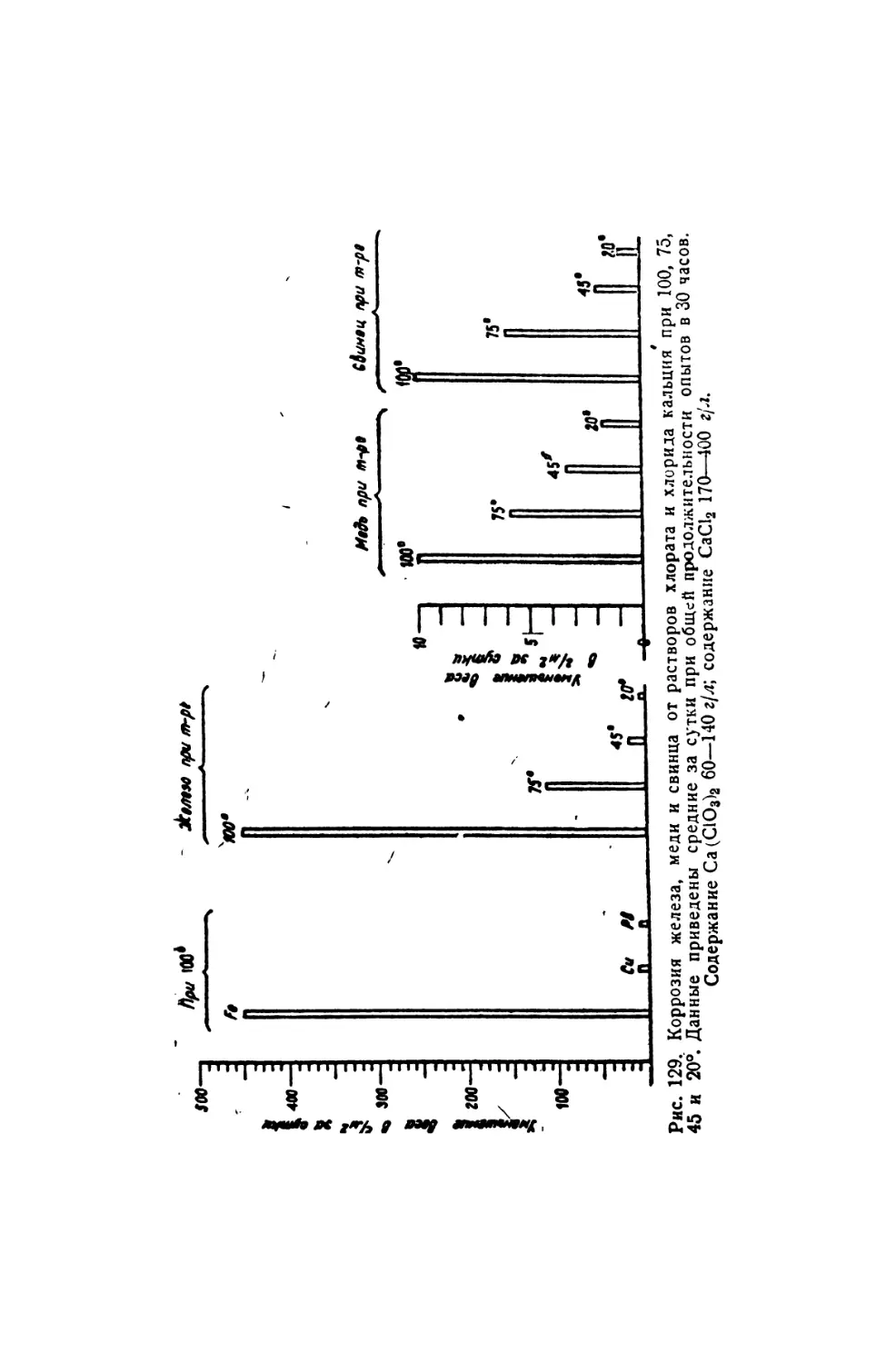
1. Замечания по коррозии аппаратуры при производстве хлоратов . .343
2. ОСГы .347
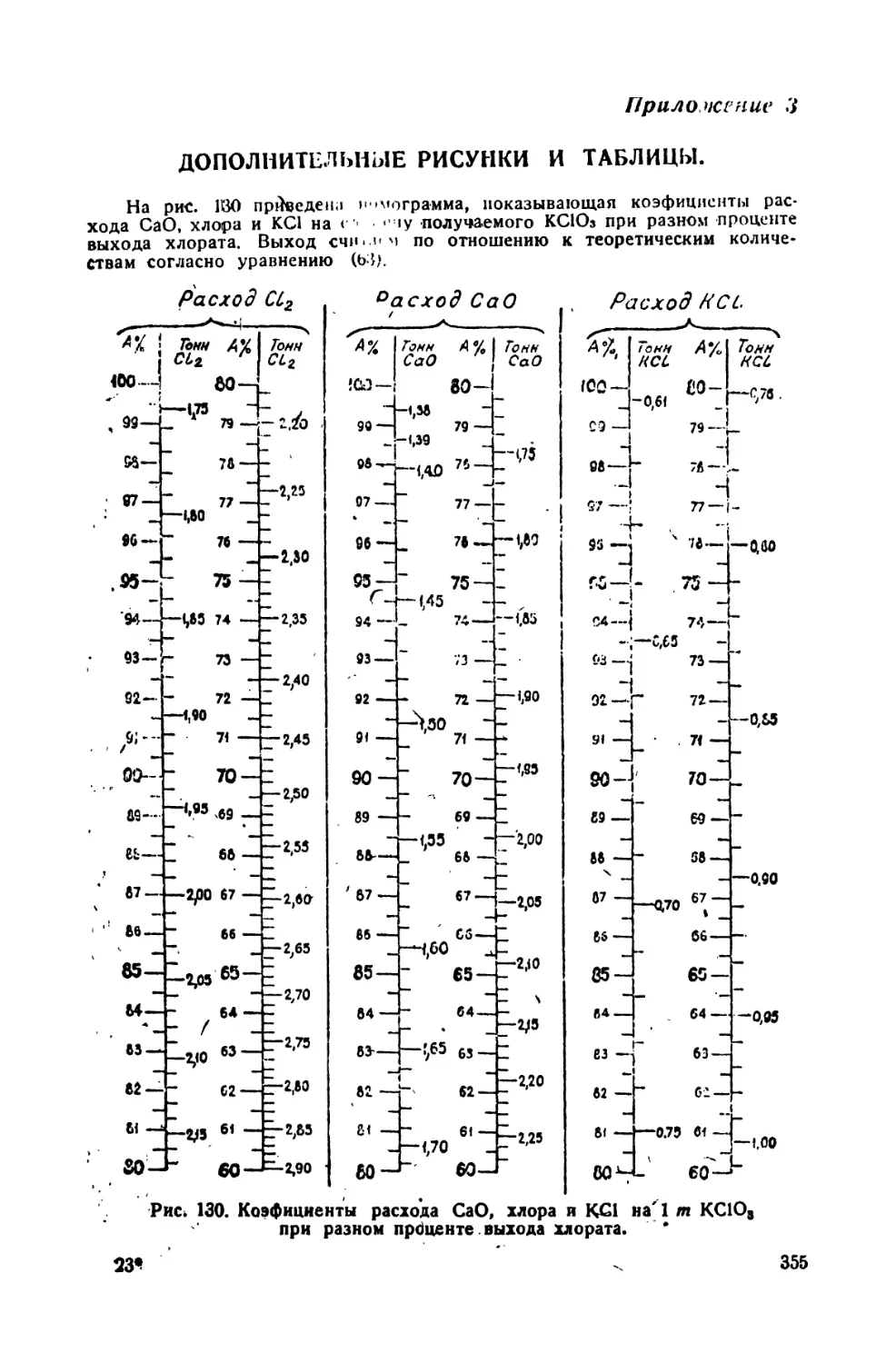
'3. Дополнительные рисунки и таблицы 355
Соисок литературы 359
Именной указатель 361
Предметный указатель . . " 363
ПЕРЕЧЕНЬ ТАБЛИЦ
Стр.
1. Электропроводность КСЮ3 при разной температуре 19
2. Плотность и концентрация растворов КСЮ3, насыщенных при температурах от 0 до 100° —
3. Плотность растворов КСЮ3 при 20° 21
За. Упругость паров растворов КС103 —
4. Понижение упругости паров растворов КС103 при 100° в зависимости от концентрации " —
4а. Понижение температуры замерзания растворов КС103 разной концентрации —
46. Удельная теплоемкость (в кал.) растворов КСЮ3 —
5. Вязкость растворов КСЮ3 —
5а. Степень диссоциации (а) КСЮ3 в водных растворах при 18э . . . . 22
6. Температура начала выделения кислорода при нагреве КС103 в смеси
с некоторыми веществами
7. Цветные реакции на ион СЮ3' • . . . • . .
8. Состав известняков некоторых месторождений в СССР
9. Зависимость между давлением С02 и температурой при термической
диссоциации СаС03
10. Растворимость СаО в воде при температуре от 0 до 100° . . * . . > 40
11. Растворимость СаО в водных растворах СаС12 при температуре J
20—100э —
11а. Растворимость Са(ОН)2 в водном растворе глицерина при 25э . . . 41
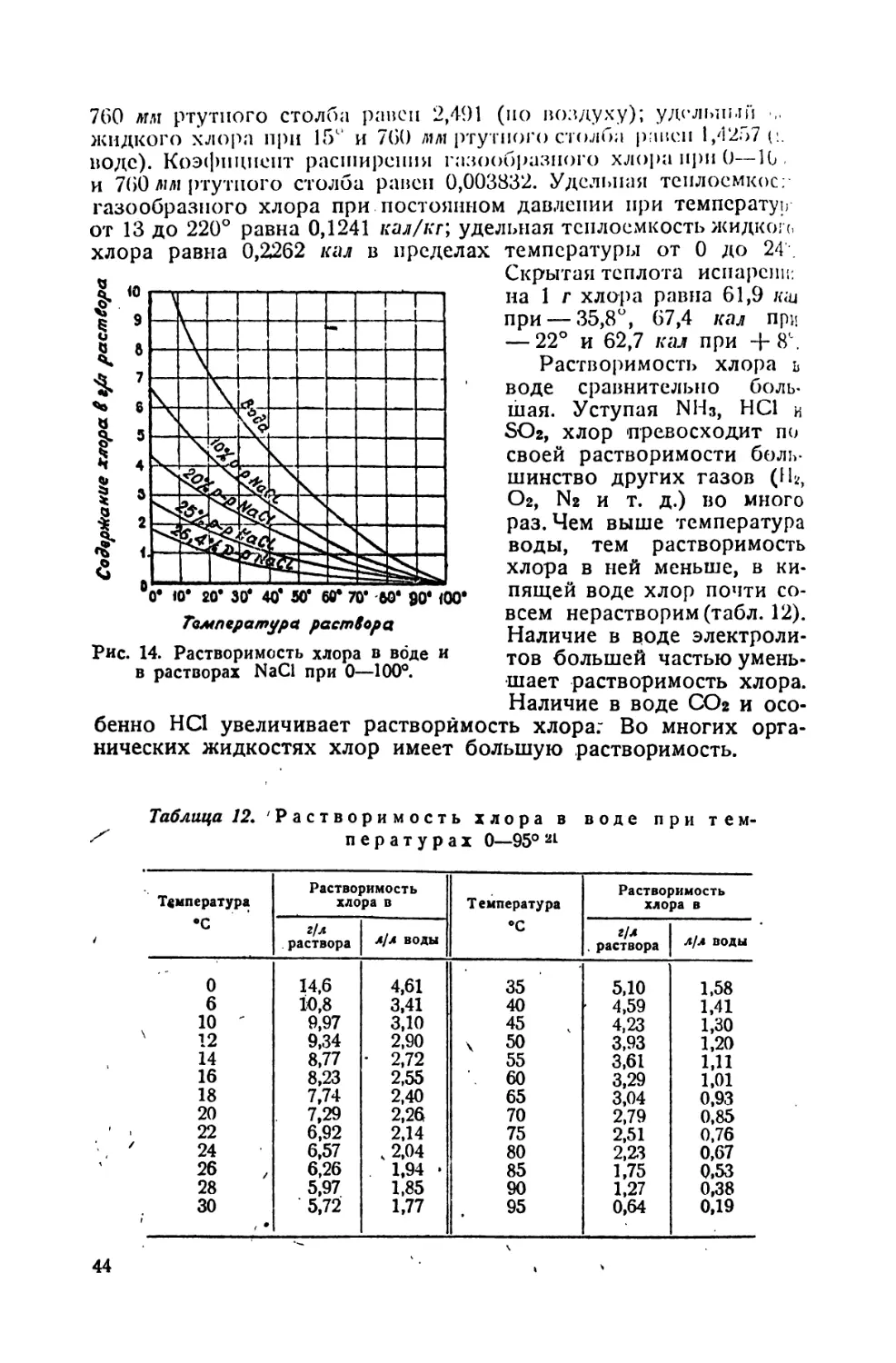
12. Растворимость хлора в воде при температуре от 0 до 95° 44
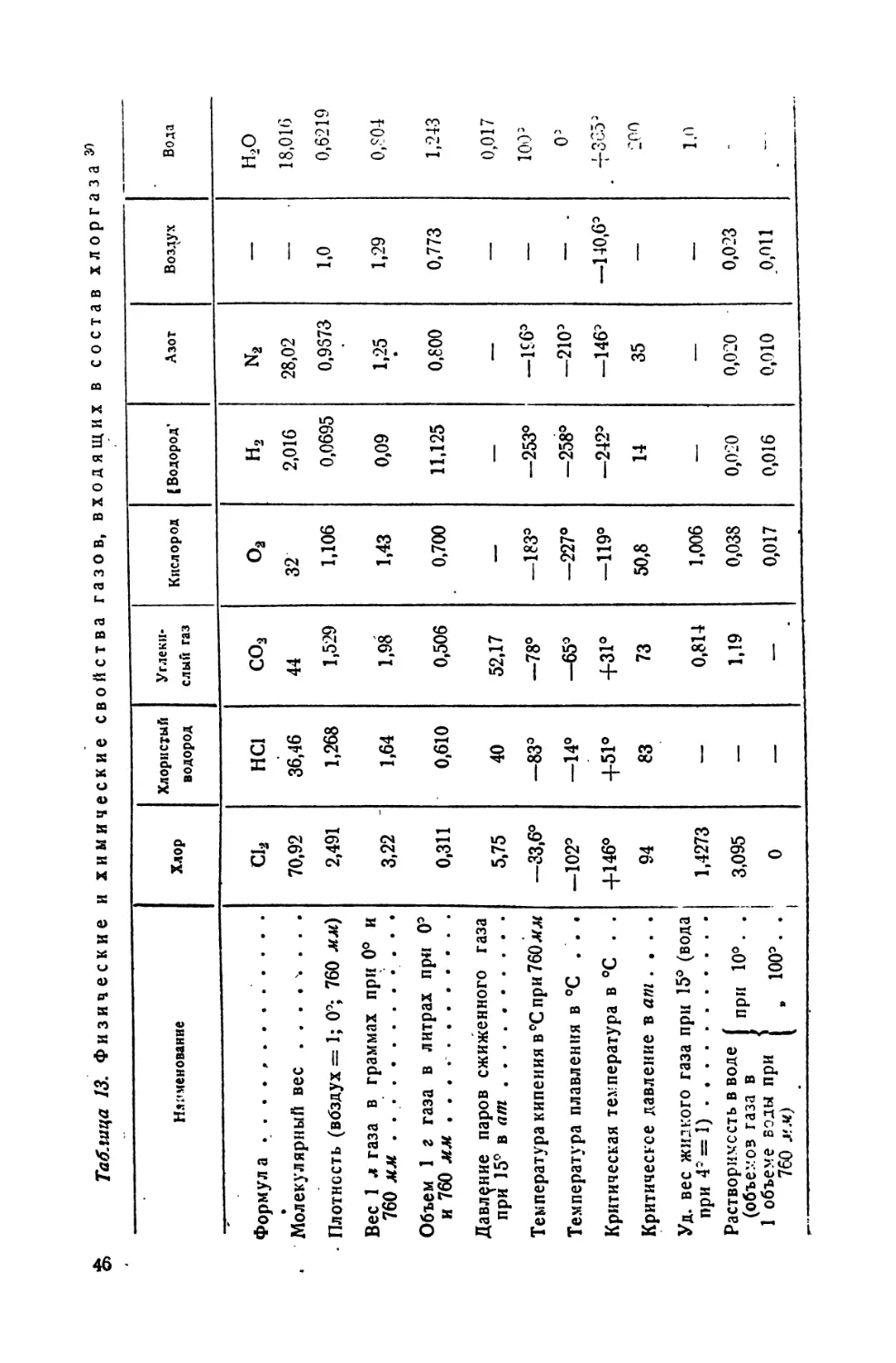
13. Физические и химические свойства газов, входящих в состав хлоргаза 46
14. Зависимость некоторых величин от процента С13 в хлоргазе 47
.15. Плотность и концентрация растворов КС1, насыщенных при температурах от 0 до 108° .* 49
16. Теплота реакции хлорирования известкового молока 62
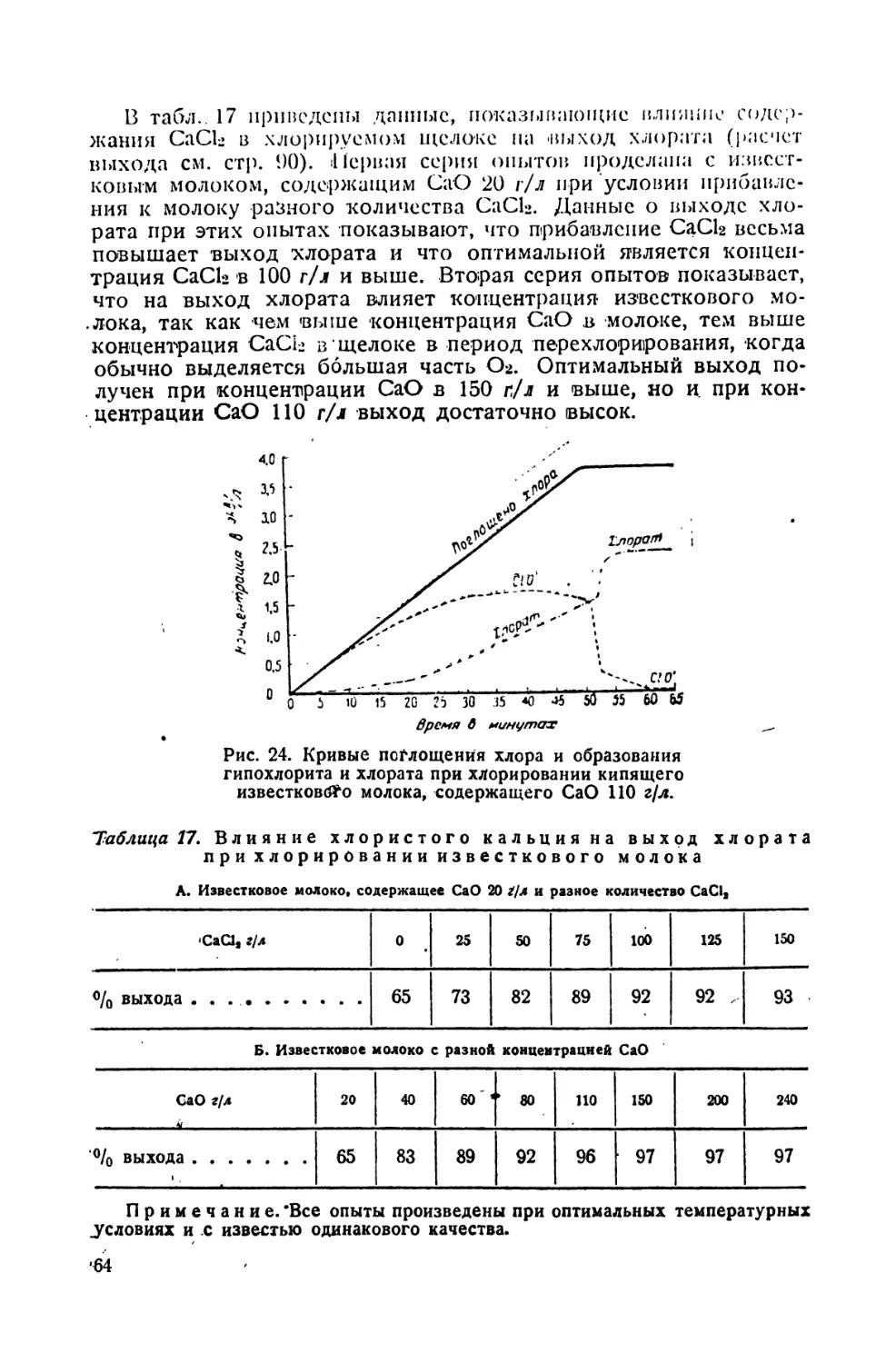
17. Влияние хлористого кальция па выход хлората при хлорировании
известкового молока 64
. 18. Выхода хлората при 100 заводских операциях хлорирования известкового молока высокой концентрации 65
19. Относительная вязкость, температура кипения и температура замерзания хлорированных щелоков разной концентрации 70
20. Средний состав щелоков по абсорберам при хлорировании и пюстко-
вого молока, содержащего СаО 100—110 г/л 79
21. Примеры расчета процента потери хлората при хлорировании по
анализам хлоргаза и абгаза 92
22. Содержание Са (С103)2 и СаС12 и температура замерзания жидкости,
получаемой при промывке и выщелачивании шлама, отделенного от
хлорированных щелоков 103
23. Примерный состав фильтрпрессного Шлама до и после промывки . —
24. Разложение хлората при выпарке хлорированных щелоков в присутствии железных пластинок при 110—115° 106
25. Содержание КС1 в растворах разного удельного веса при 20, 60, 80° 111
26. Формулы расчет* содержания СаОа» Са(СЮ3)и, КС1, КС103 в бертолетовых щелоках' " 112
24
26
36
37
9
Опр,
27. Состав примесей бертолетовой соли нерпой и второй кристаллизации
28. Длпимс нескольких опытов промывки бертолетовой соли па центрифуге
29. Данные нескольких опытов промывки бертолетовой соли па путч-
фильтре •
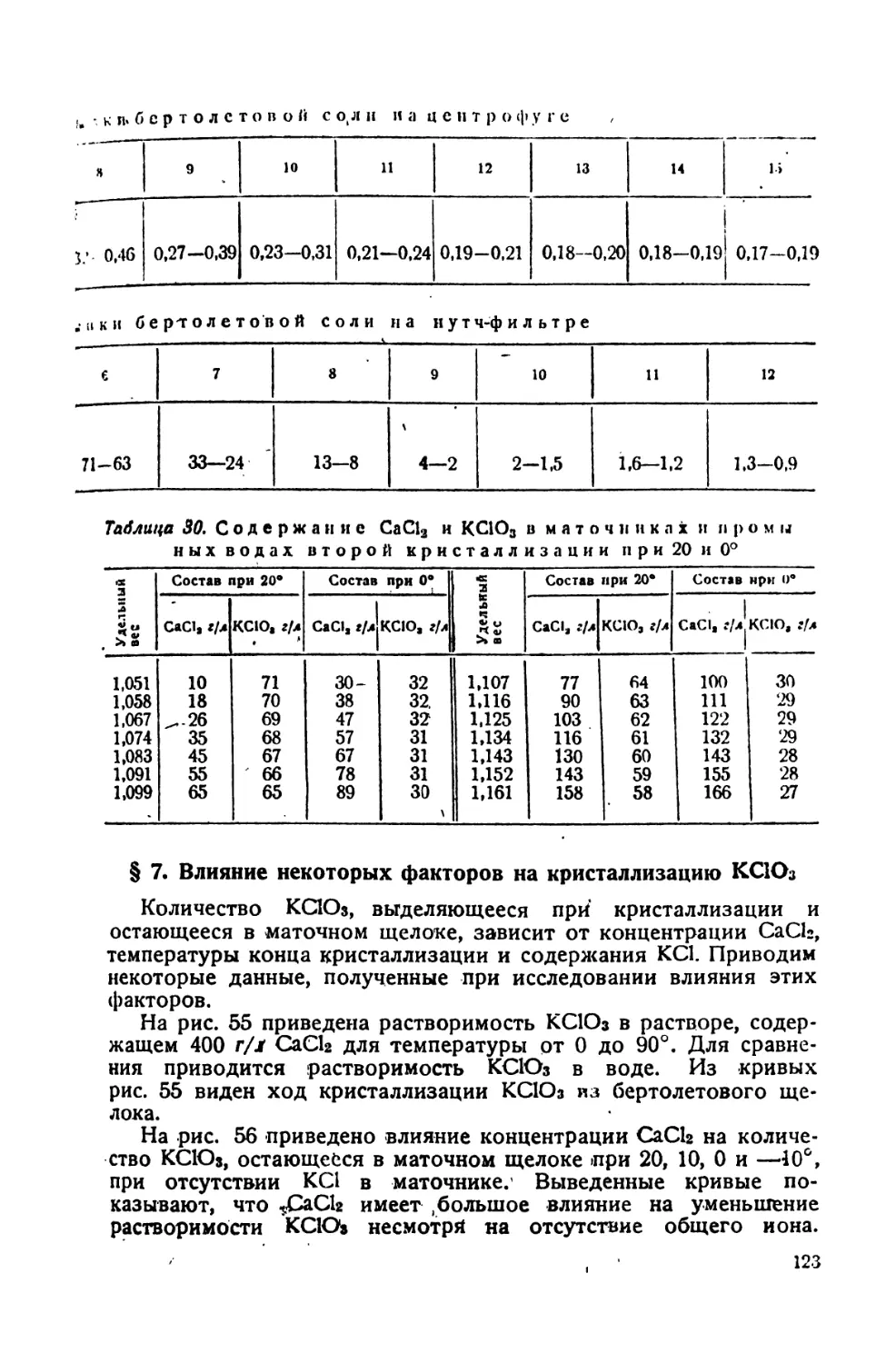
30. Содержание СаСЬ и КСЮ3 в маточниках и промывных водах второй
кристаллизации при 20 и 0' . . .'
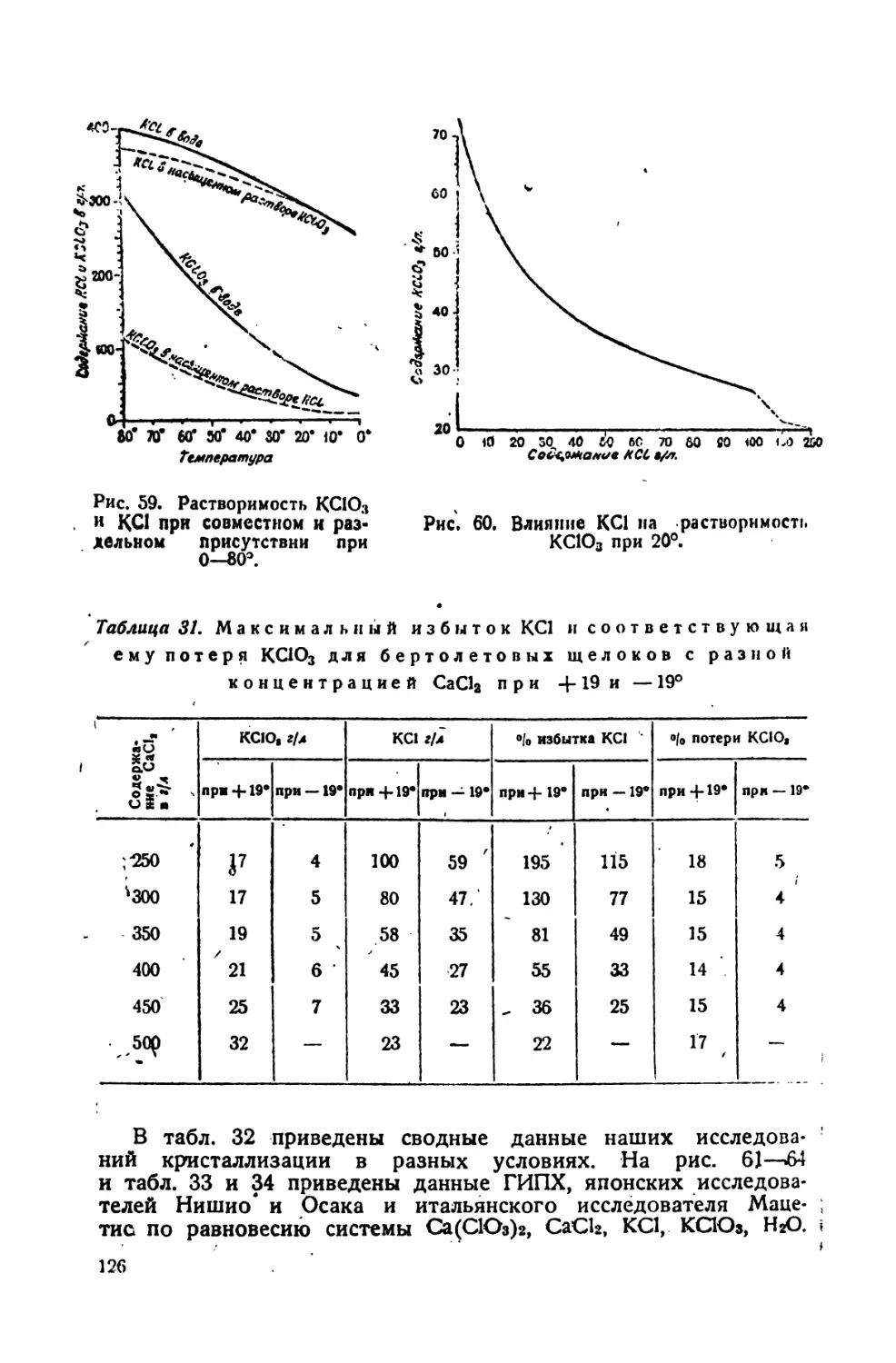
31. Максимальный избыток КО и соответствующая ему потеря КСЮ:<
для бертолетовых щелоков с разной концентрацией CaCU при -|-19°
и —19J
32. Сводные данные влияния процента избытка КО, концентрации СаС12
и температуры конца кристаллизации на потерю КС103 с маточниками v
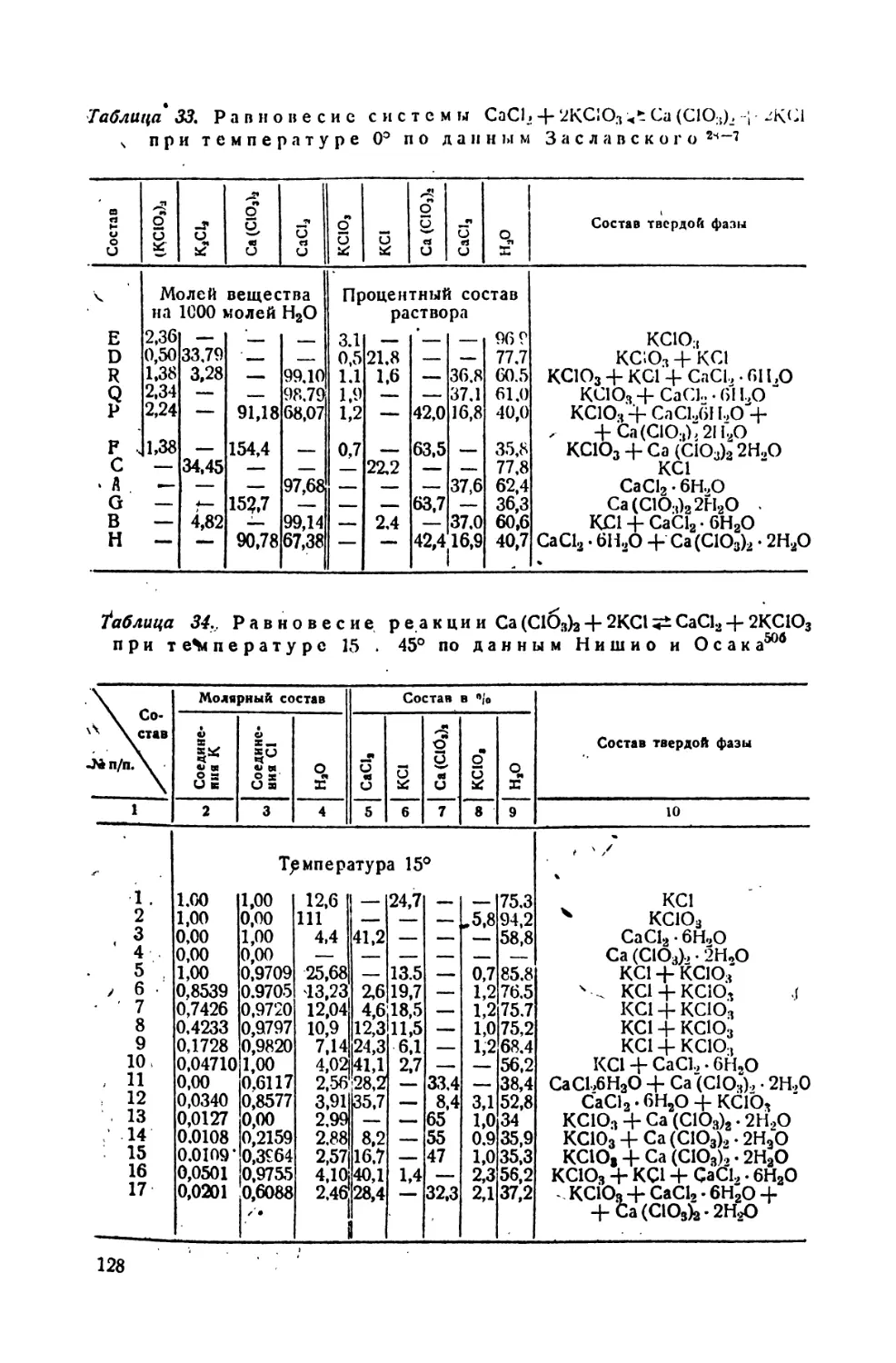
33. Равновесие системы Са(СЮ3)а + 2КС1 2КС103 + СаС12 при 0° по
данным Заславского (ГИПХ) . . . . • (
34. Равновесие системы Са (СЮ3)2 + 2КС1 CaCl2 + 2КС103 /при 15 и
45° по данным Нишио и Осака ”
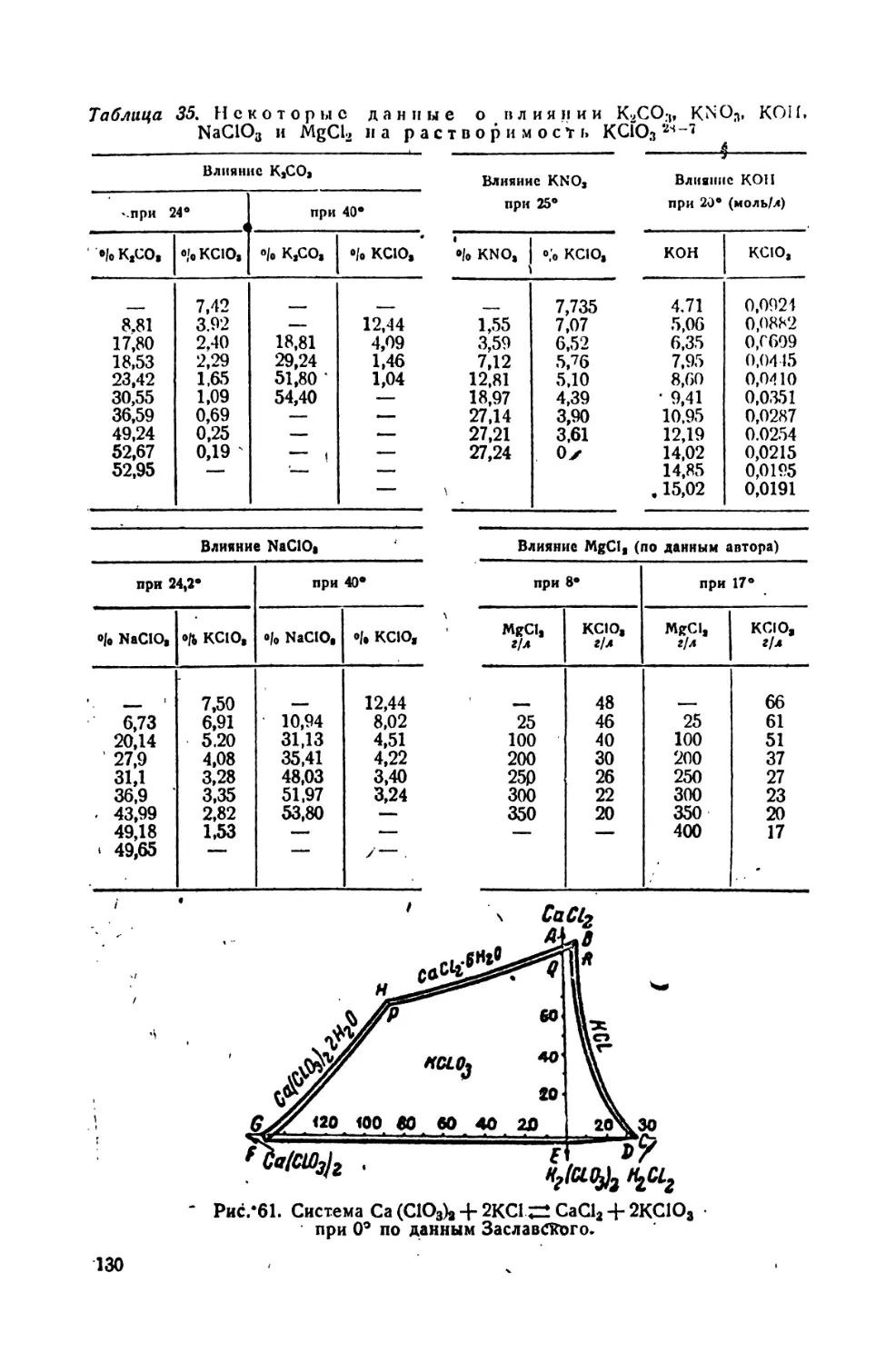
35. Некоторые данные о влиянии КгС03, KN03, КОН, NaC103 и MgCl2
на растворимость ~ •
36. Плотность и концентрация насыщенных водных растворов СаС13 при
температурах от—55 до 170° 140
37. Некоторые свойства водных растворов СаС12 разной концентрации . —
38. Плотность и концентрация насыщенных растворов ВаС12 при температурах от 0 до 100° 145
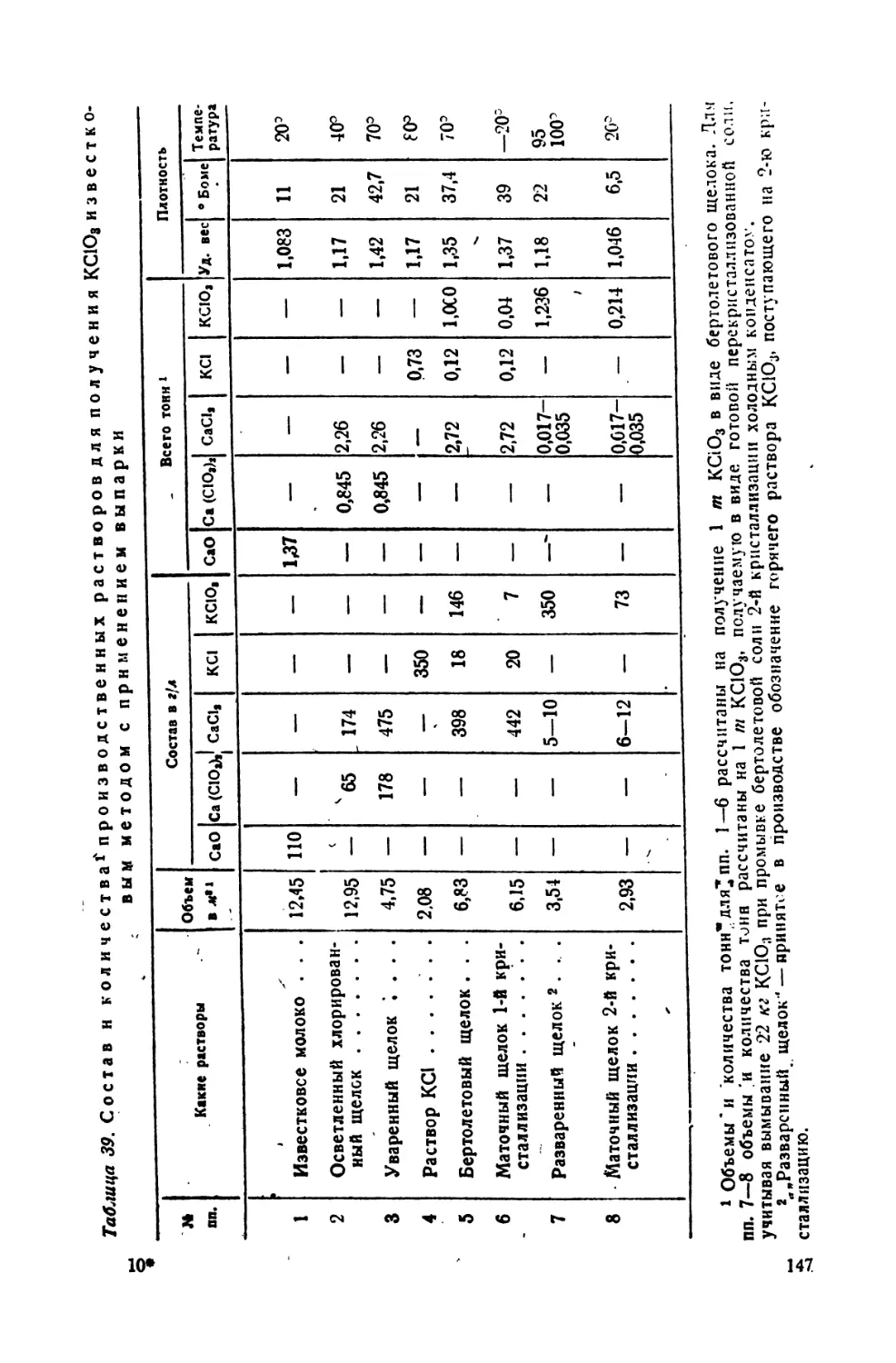
39. Состав и количества производственных растворов для получения
КСЮ3 известковым методом с применением выпарки 147
40. Состав и количества производственных растворов для получения
КСЮ3 известковым методом без применения выпарки 148
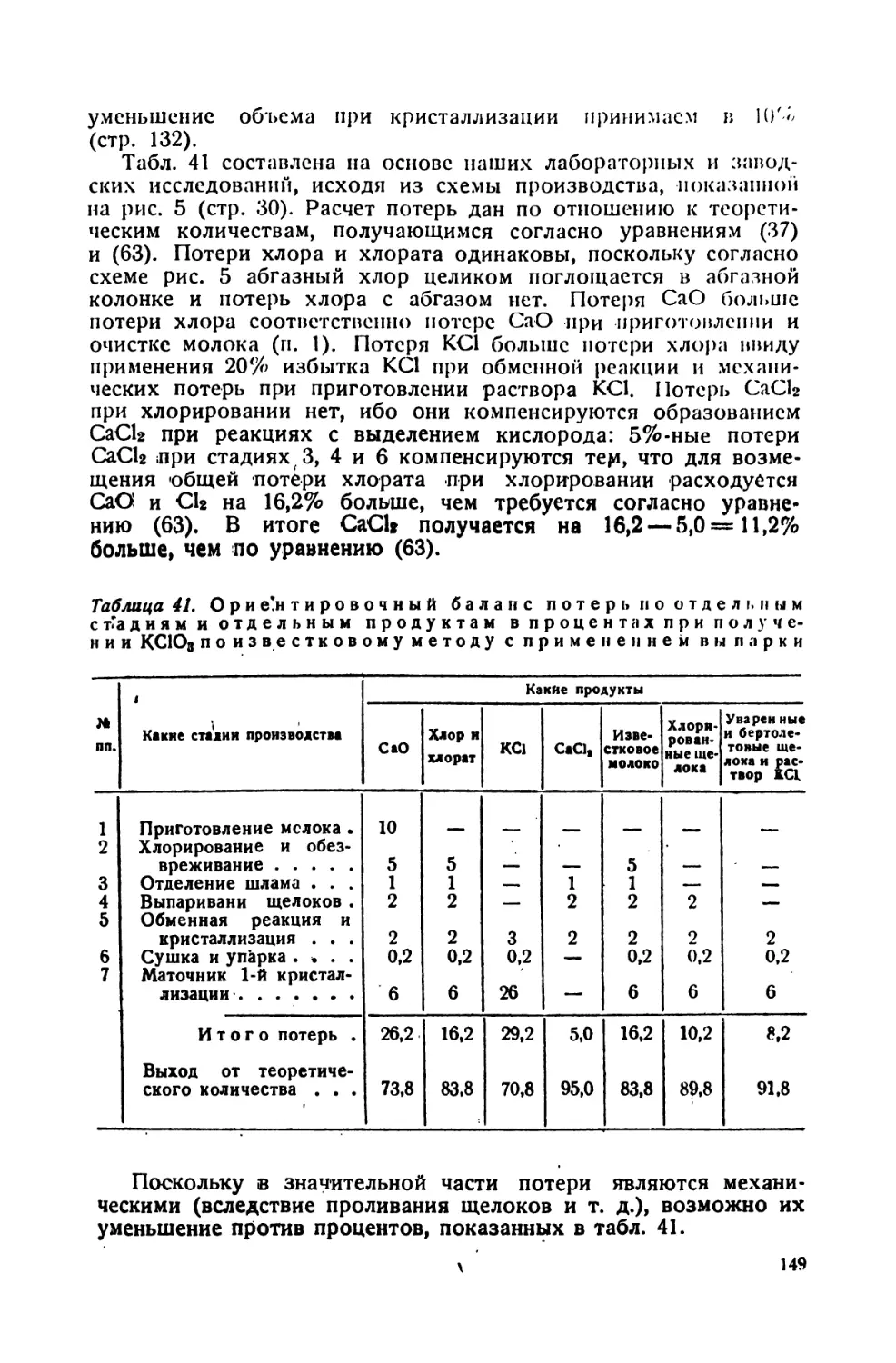
41. Ориентировочный баланс потерь по отдельным стадиям и отдельным
продуктам при получении К(Д03 по известковому методу с применением выпаркн 149
42. Количества основных продуктов и полупродуктов, необходимых для
получения 1 m готовой КСЮ3 по известковому методу с применением выпарки 150
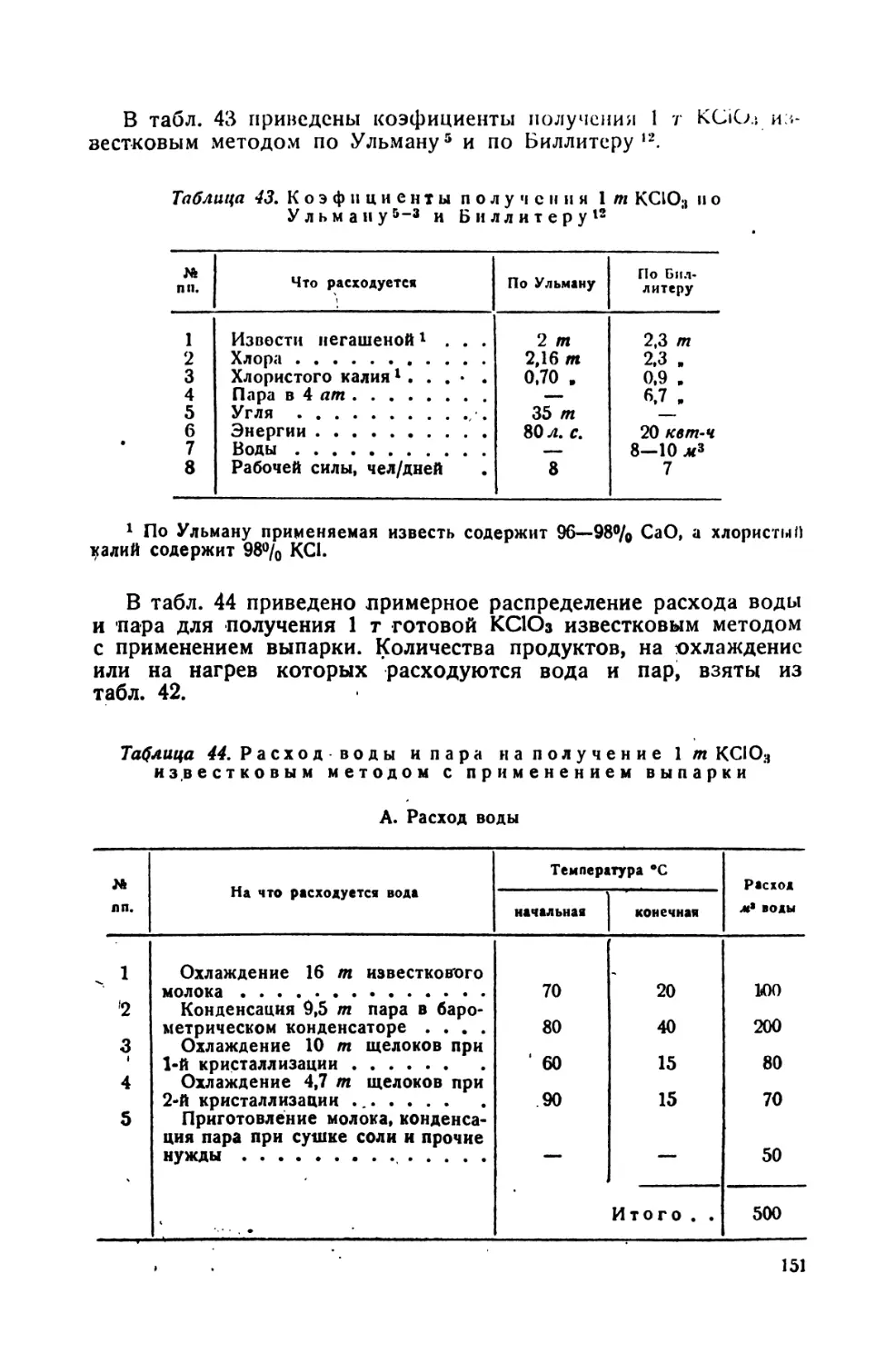
43. Коэфициенты получения 1 m бертолетовой соли по Ульману и Бил-
литеру 151
44. Расход воды и пара на получение 1 тп КСЮ3 известковым методом
с применением выпарки —
45. Примерная калькуляция заводской себестоимости 1 m бертолетовой
соли при известковом методе производства с применением выпарки 154
46. Ориентировочный штат завода производительностью в 15 m КСЮ3
в сутки при известковом методе производства (с применением
выпарки) 155
47. Влияние концентрации и температуры на выход хлората при хлорировании растворов, содержащих NaOH 100—500 г/л 167
48. Увеличение объема при хлорировании растворов NaOH или слабого
, каустика 168
49. Ход хлорирования раствора, содержащего Na3C03 200 г/л 169
50. Состав щелоков, выход хлората и увеличение объема при хлорировании растворов Na2C03 разной концентрации 170
31. Коэфициенты реакций при каустическом и содовом методах производства бертолетовой соли 173
52. Состав и количества уваренных и бертолетовых щелоков и количество КС103, выделяющейся при кристаллизации, при каустическом
и содовом методах производства ' . . • 174
53. Растворимость КСЮ3 в насыщенных растворах NaCl, содержащих
КС1 до 100 г/л при разной температуре • 176
54. Состав ]растворов, насыщенных по КСЮ3, КС1 и NaCl при 0—80° . —
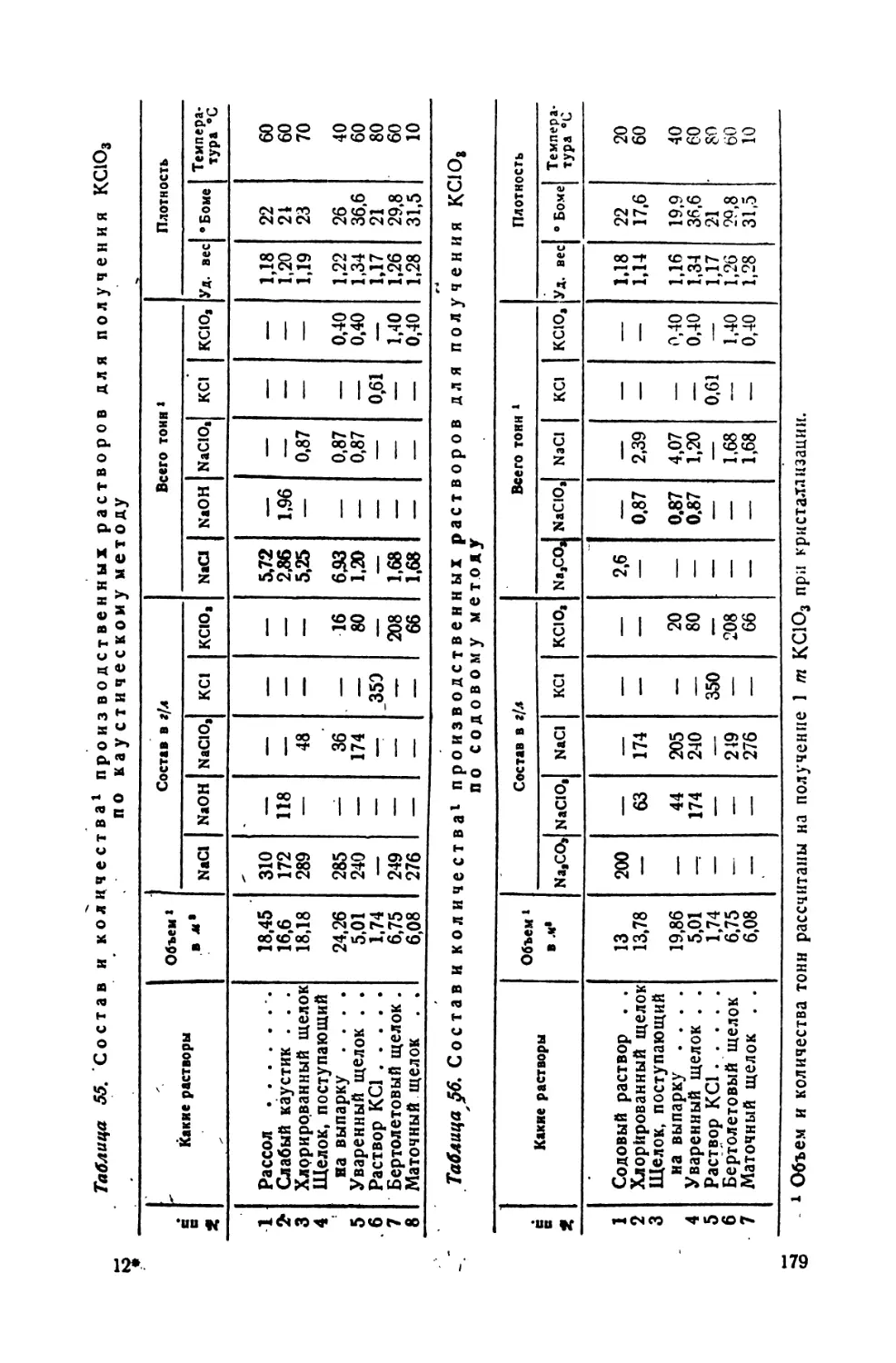
55. Состав «^количества производственных растворов при получении
КСЮ8 по "каустическому методу : 179
121
122
123
126
127
128
130
10
56. Состав и количества производственных растворов при получении
КСЮ;; по содовому методу ^
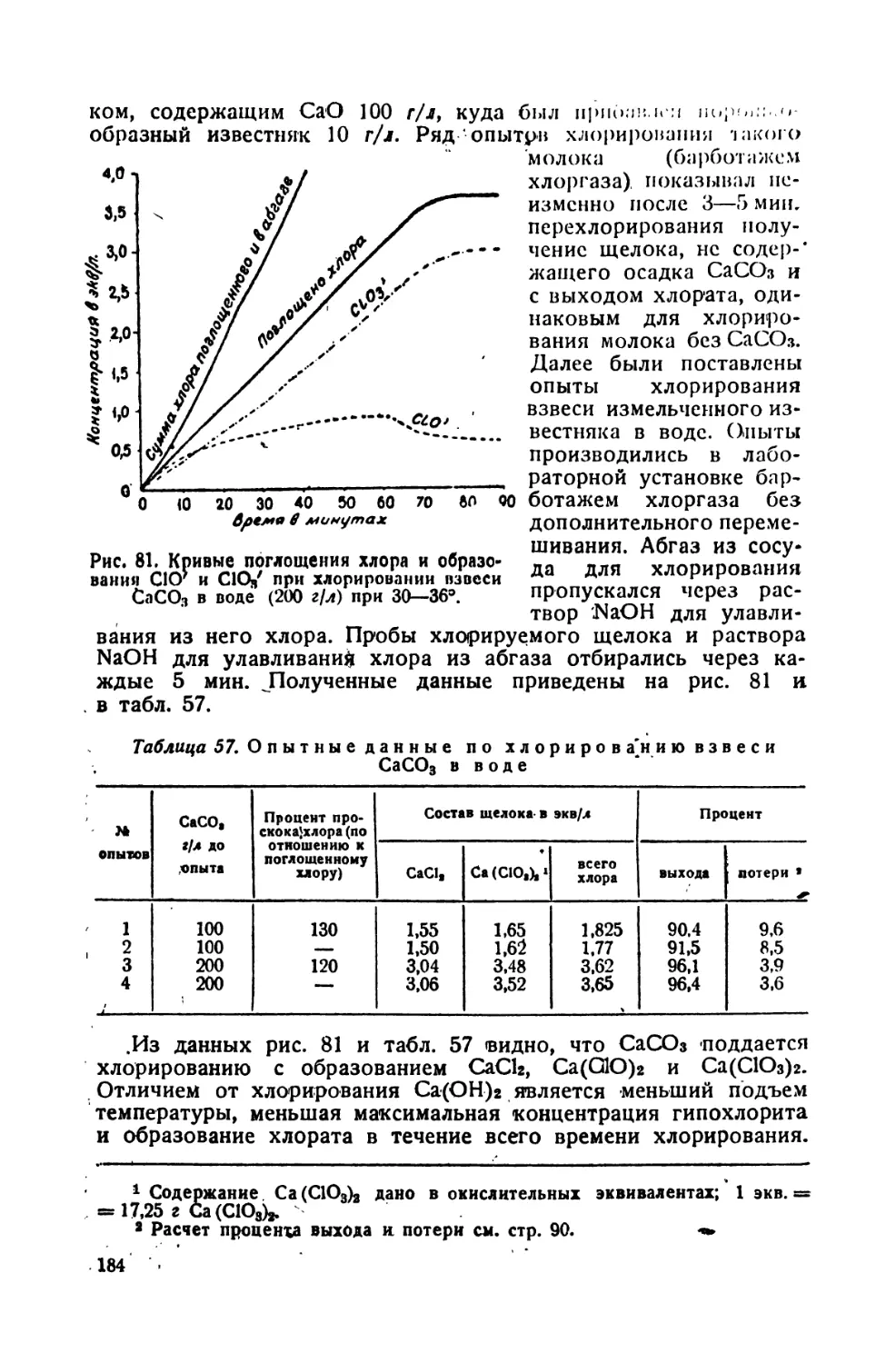
57. Опытные данные по хлорированию нанеси СаС03 н иоде
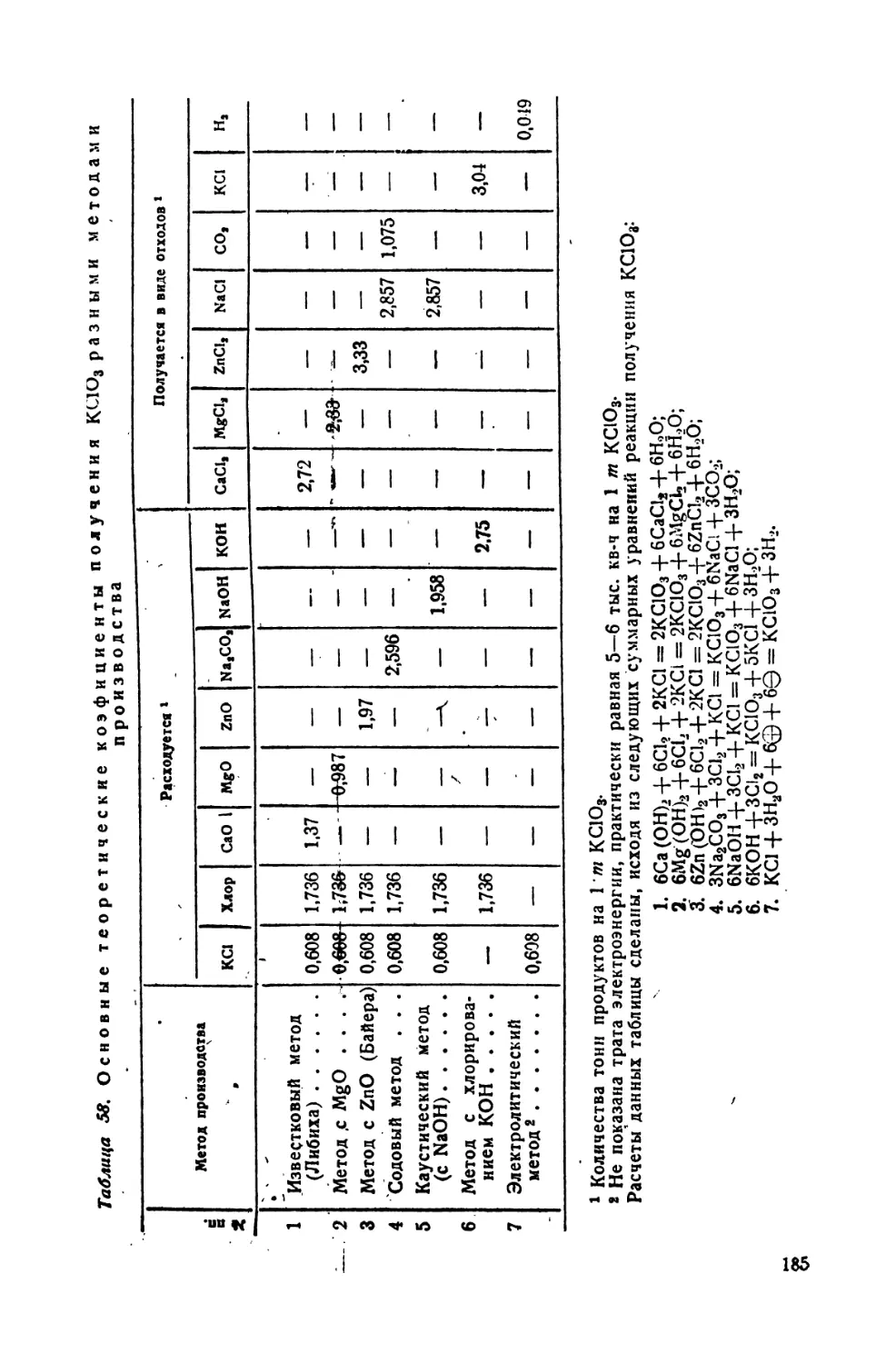
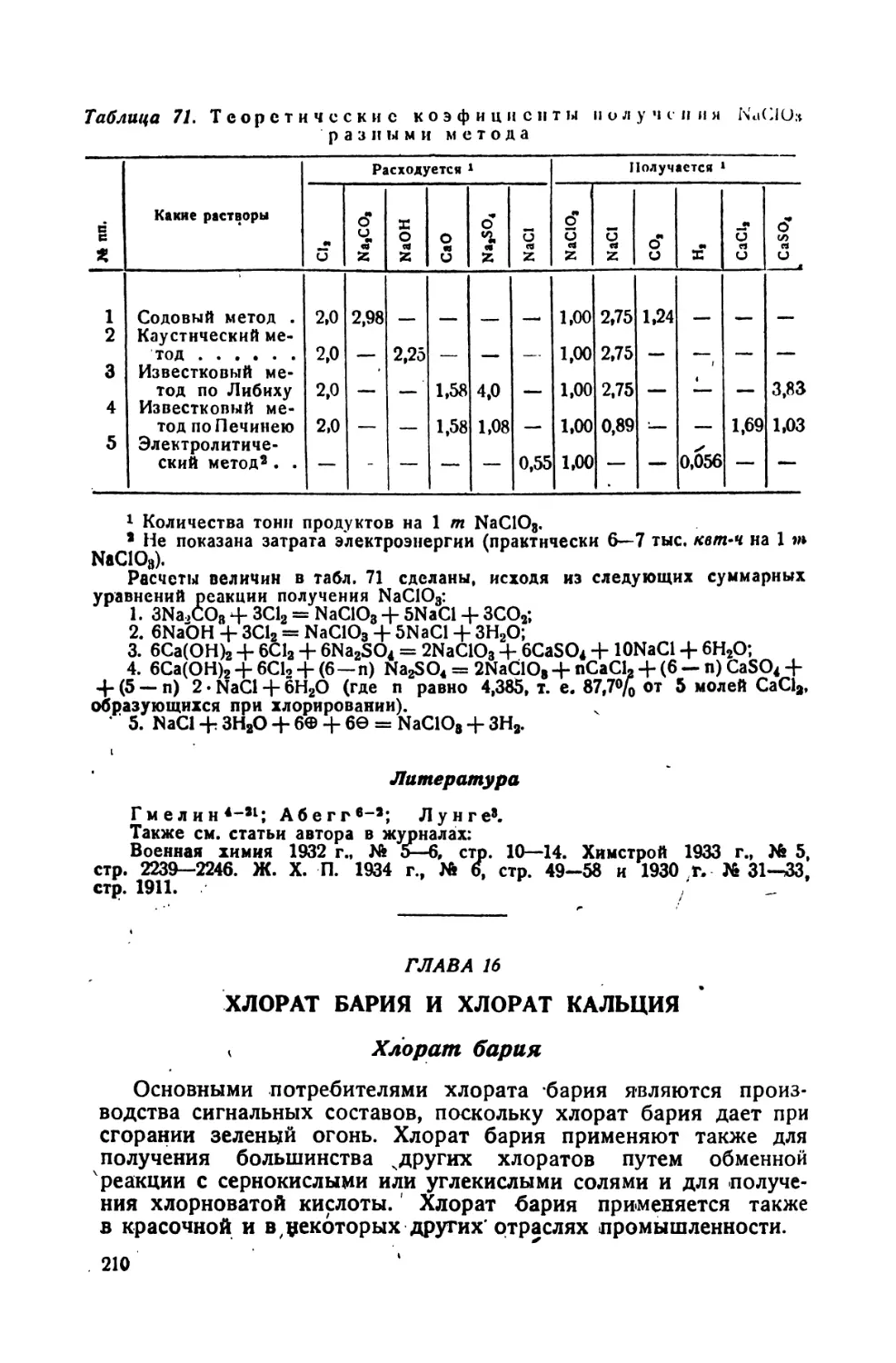
Ь$. Теоретические коэфициенты получения КСЮ3 разными методами
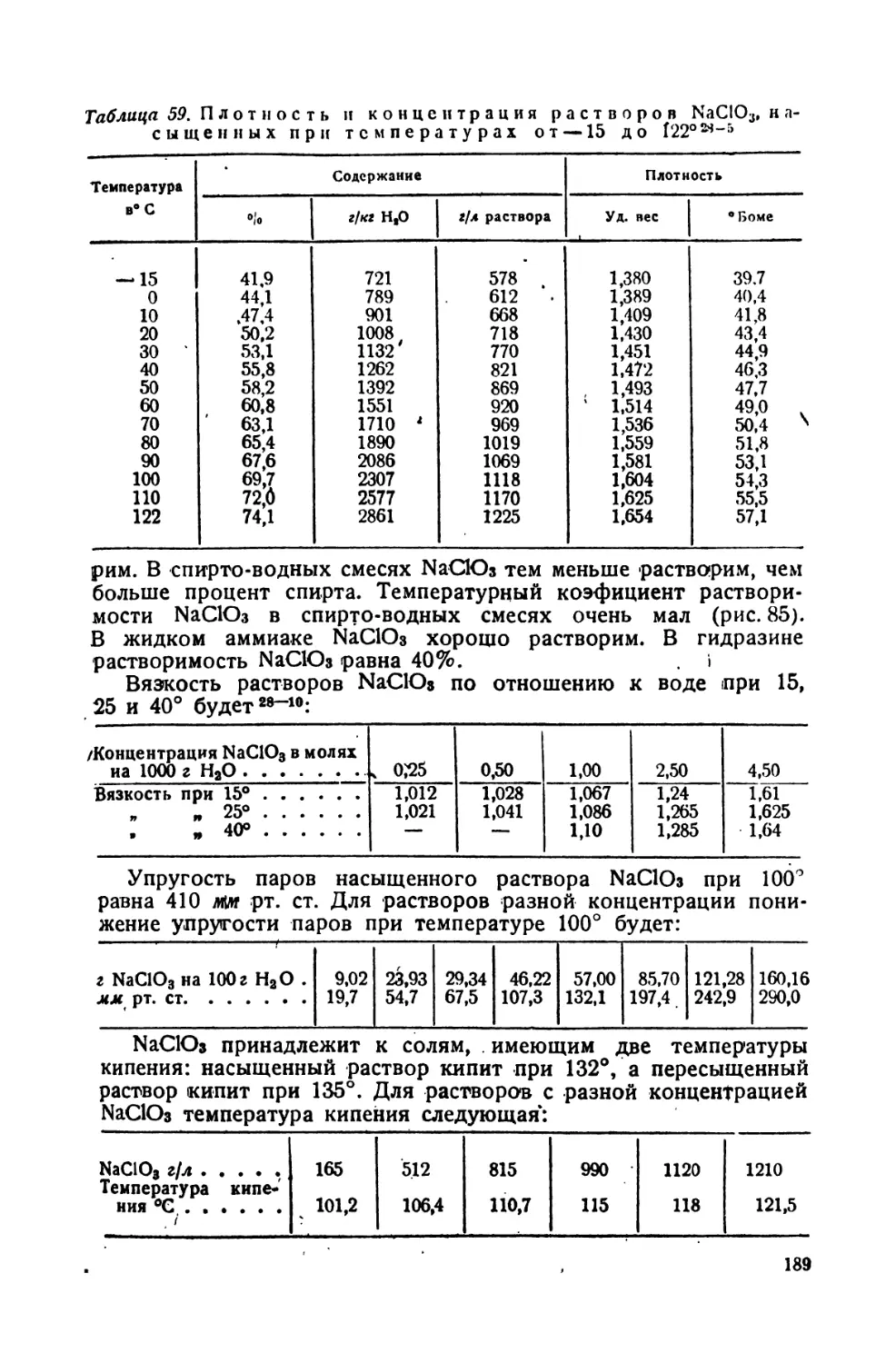
5М. Плотность и концентрация растворов NaC103, насыщенных при температурах от - -15 до 1225 . •
ГО. Выделение хлорида н виде СаС12*6Н20 из щелоков, уваренных до
удельного веса 1,44—1,60
61. Выделение хлорида из хлорированных щелоков в виде оксихлоридов
(V2. Выделепи хлорида в виде оксихлоридов из маточников, полученных
после выделения СаС12 • 611.20
63. Некоторые данные по отделению и промывке соли, выделяющейся
при выпарке натриево-хлоратных щелоков
64. Кристаллизация NaC103 из щелока, насыщенного NaC103 и NaCl
при 70° •
65. Промывка хлората натрия на нутч-фильтре .ч .*
66. Некоторые данные по перекристаллизации технического хлората
натрия
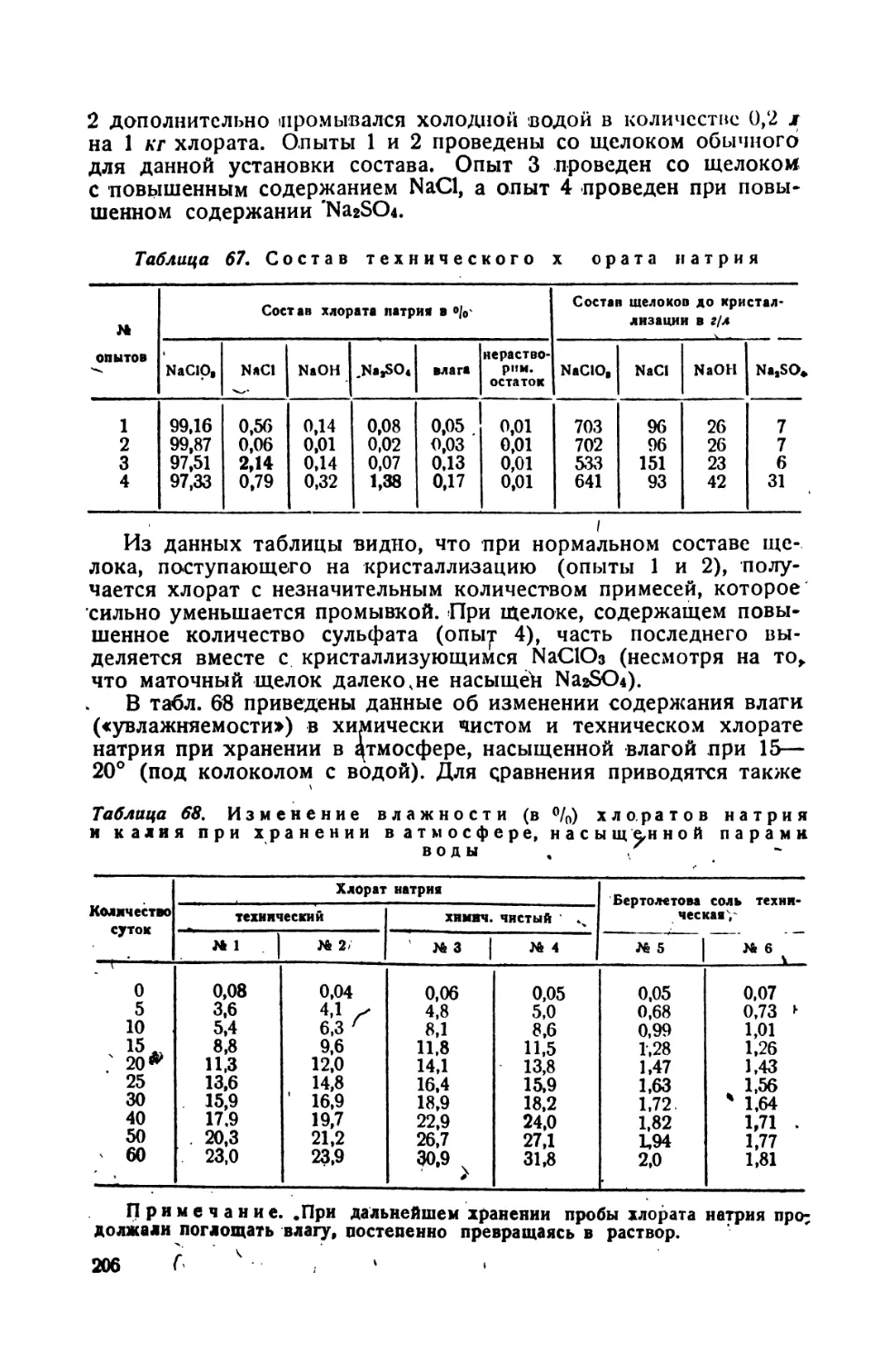
67. Состав технического хлората натрия
68. Изменение влажности хлоратов натрия и калии при хранении в атмо¬
сфере, насыщенной парами воды .
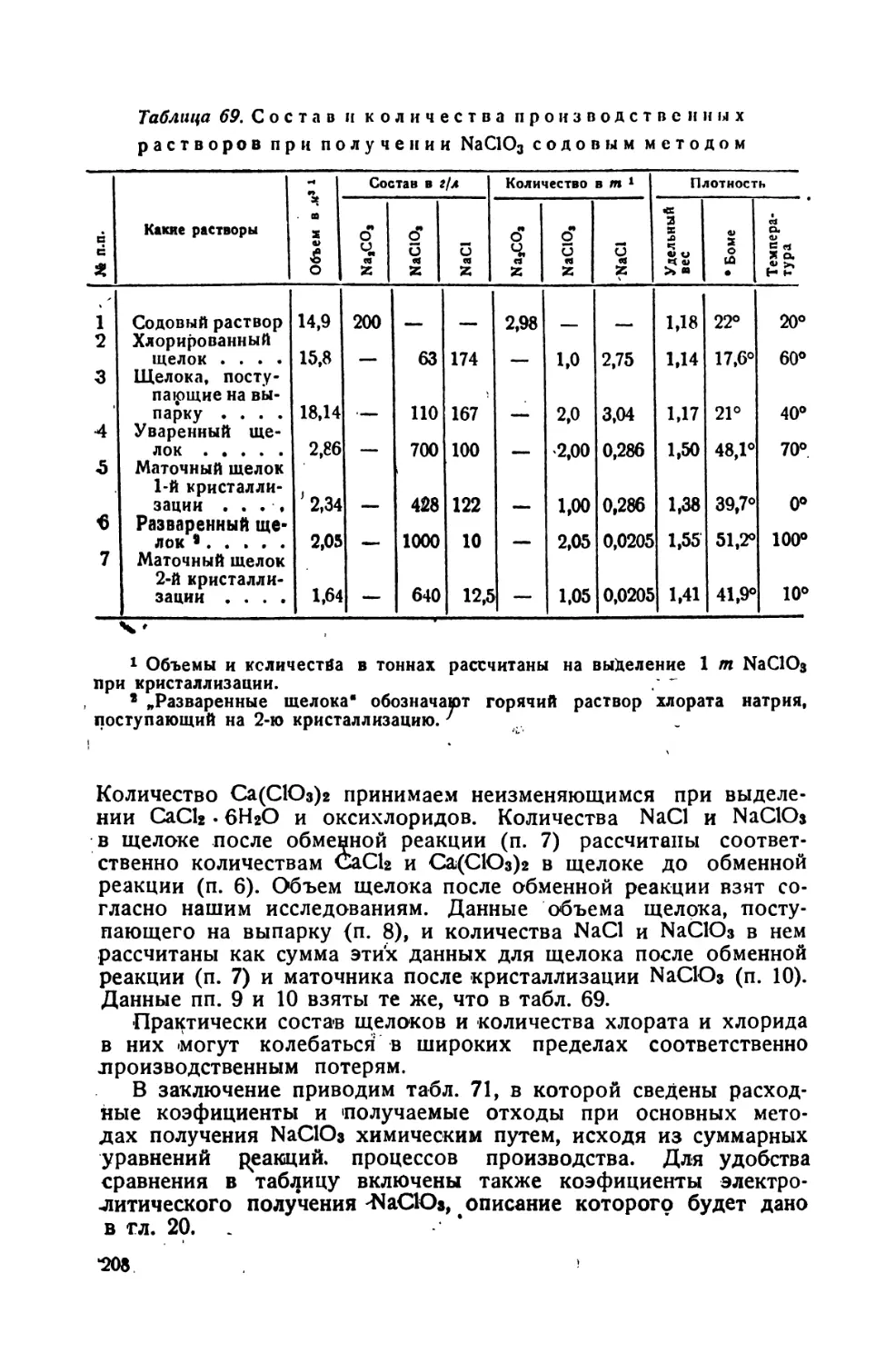
69. Состав и количества производственных растворов при получении
NaC103 содовым методом ' \ . . .
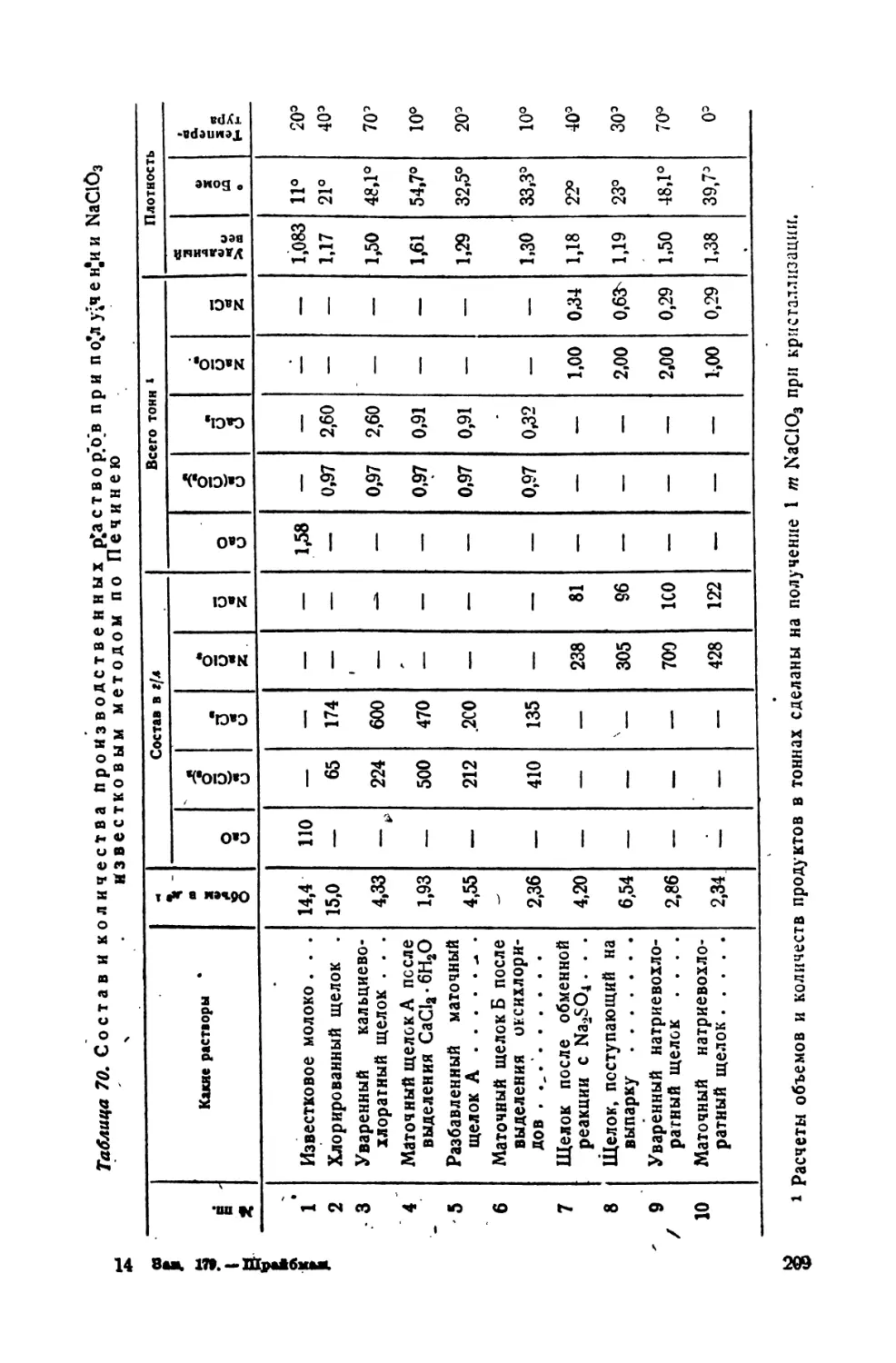
70. Состав и количества производственных растворов при получении
NaClOs известковым методом по Печинею
71. Теоретические коэфициенты получения NaC103 разными методами .
72. Плотность и концентрация растворов Ва (С103)2, насыщенных при
температурах от 0 до 105,6° .
73. Состав и количества производственных растворов при получении
Ва(С10з)г методом обменной реакции NaC103 с ВаС12
74. Теоретические коэфициенты получения хлората бария разными методами . . .
75. Плотность растворов Са(СЮ3)2 при 18°
76. Состав продукта, содержащего 25—27% Са(СЮ3)2
•77. Молекулярные и уд. веса, температура плавления, устойчивость при
хранении на воздухе и растворимость при 18° для некоторых хлоратов
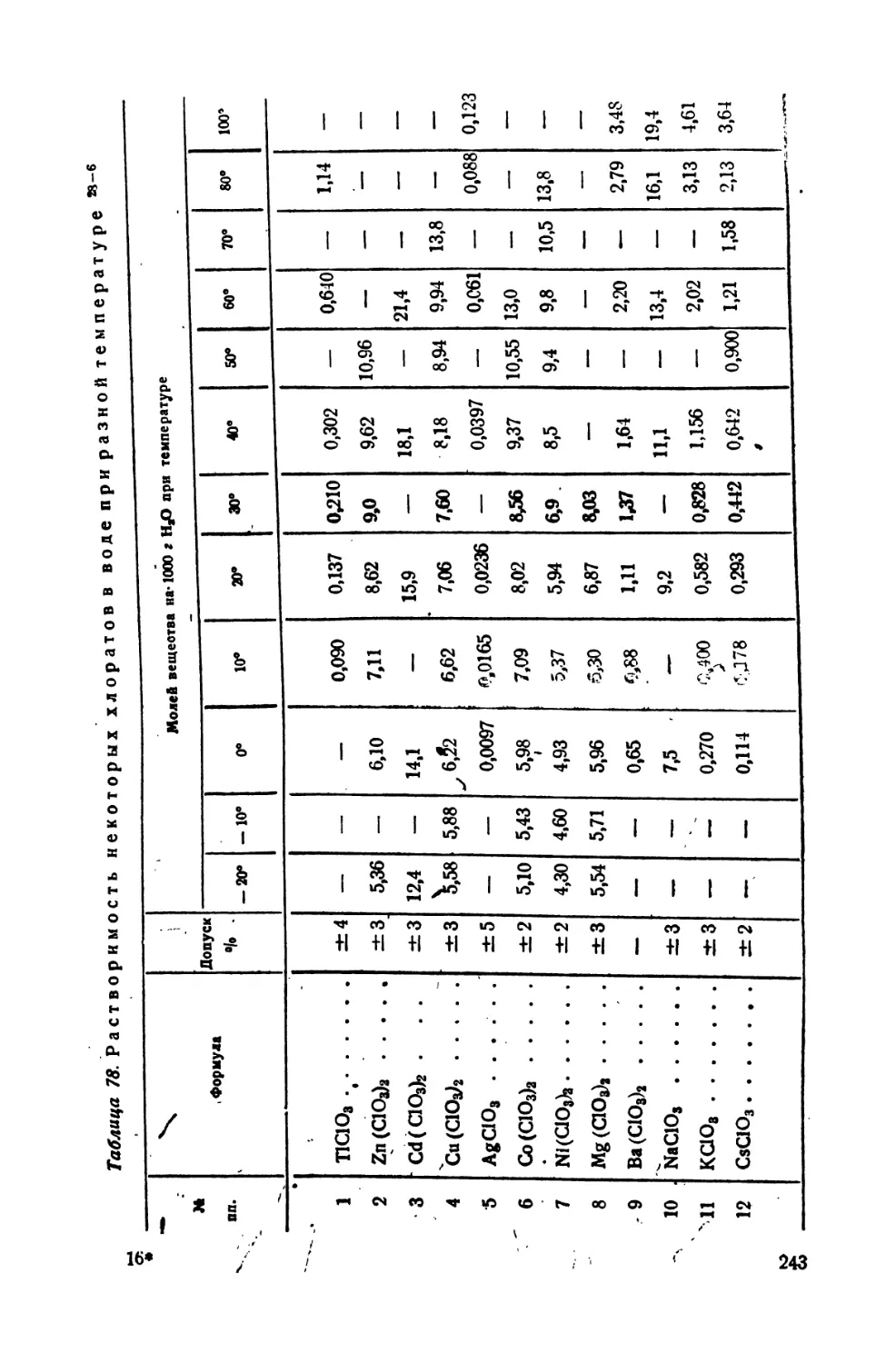
78. Растворимость некоторых хлоратов при разной температуре ....
79. Эквивалентная электропроводность (в обратных омах) растворов
' хлоратов
79а. Кристаллические формы некоторых хлоратов
80. Влияние перемешивания электролита, концентрации NaCl, темпера¬
туры и плотности тока на ход электролиза нейтрального раствора
NaCl при платиновых и платинированных анодах
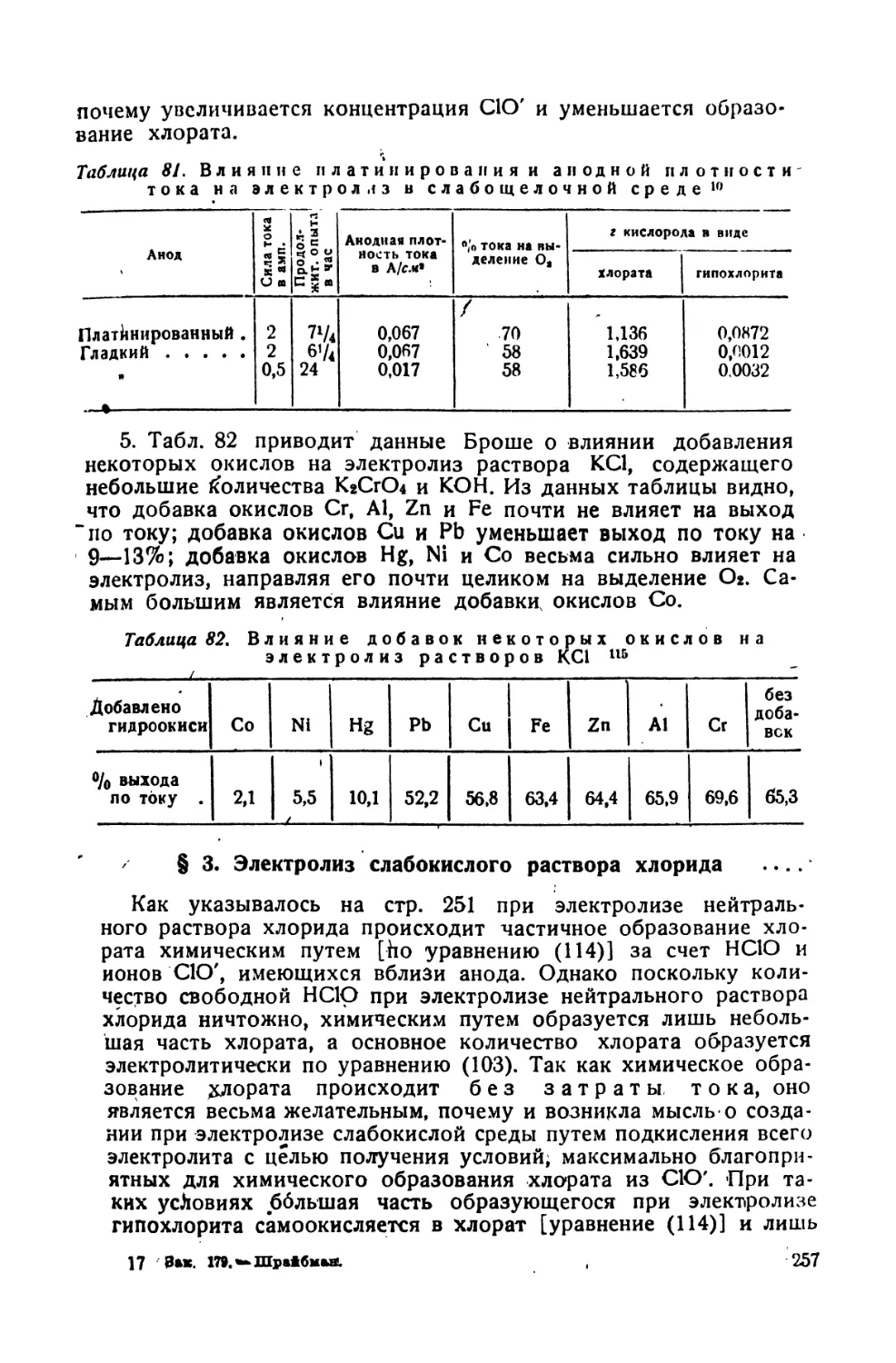
.81. Влияние платинирования и анодной плотности тока на электролиз
в слабо щелочной среде ' • . .
82. Влияние добавок некоторых окислов на электролиз растворов КС1
(содержащих КоСЮ* и КОН) ’
83. Электролиз растворов NaCl при разной кислотности и при разной
температуре .
84. Процент выхода по току и процент восстановления при электролизе
25%-ных растворов NaCl, содержащих 0,2, 3 и 5% К2Сг207 . . . .
85. Данные Эттеля об электролизе раствора NaCl, содержащего добавки
NaOH, Са (ОН)2, СаС12. и NaHC03 ’
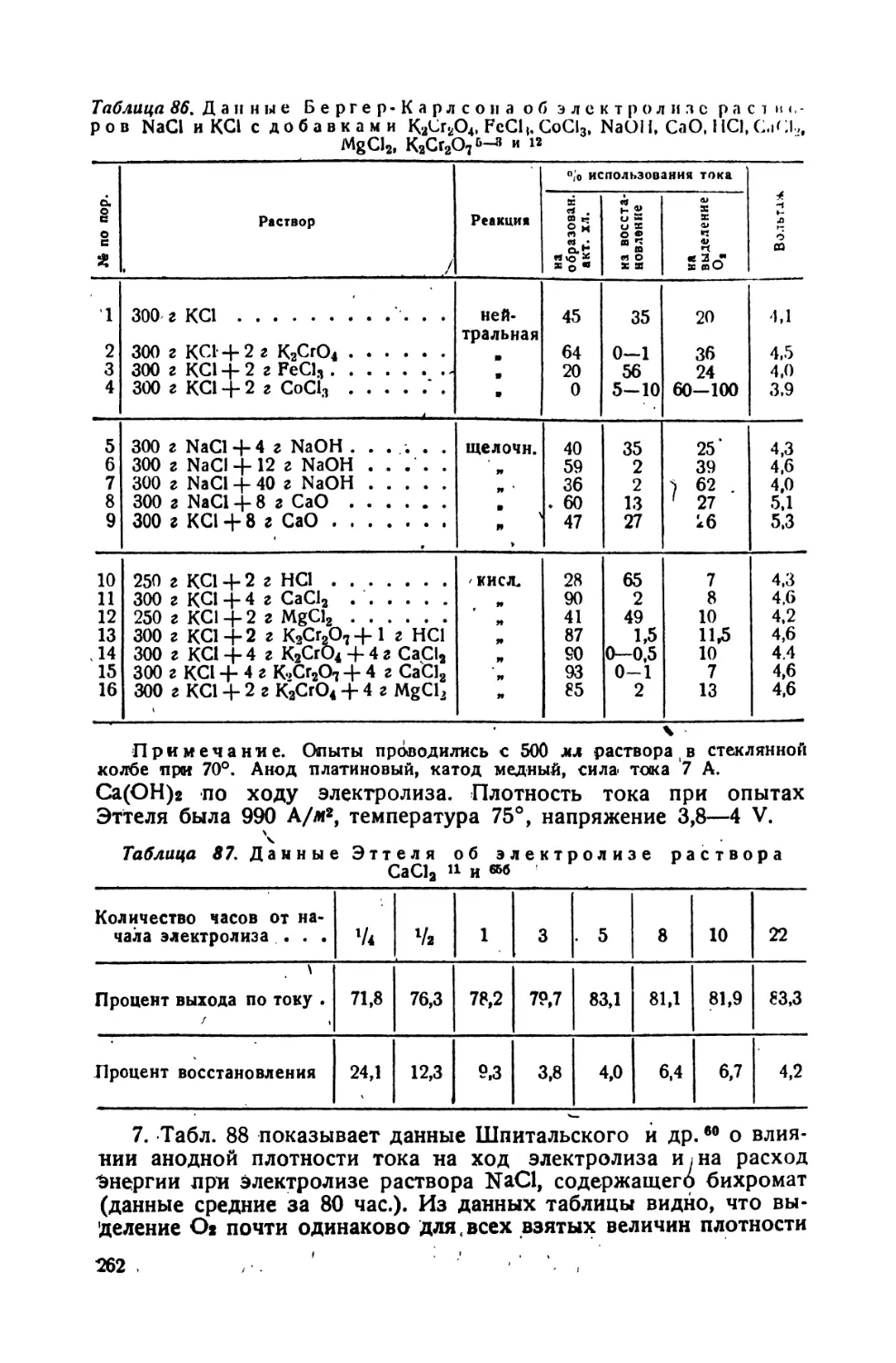
86. Данные Бергер-Карлсонл об электролизе растворов NaCl и КС1
с добавками КгСгО*, FeCia. СоС1э, NaOH, CaO, НС1, СаС12, MgCl2,
К2СГ2О7 •
• 87. Данные Эггелн об электролизе раствора СаС12., . .
88. Влияние анодной плотности тока на электролиз 25%-ного раствора
NaCl с платиновыми анодами
( >// /7.
179
т
185
189
198
200
201
208
204
205
206
208
209
210
211
217
219
220
242
243
244
246
253
257
259
260
261
262
262
263
11
('nip-
89. Влияние концентрации NaCl и NaC10;. ил выход по току 263
90. Влияние примеси некоторых солей ил электролиз растворов КС1 . 200
91. Влияние примеси солей ванадия па электролиз раствора КО . . —
92. Влияние материала катода, хромирования и добавки хромата на
восстановление при электролизе 5,1 N раствора NaCl при анодах
из гладкой платины 207
93. Электролиз 25%-ного раствора NaCl с матово-хромированным железным катодом при 50° —
94. Электролиз 25%-ного раствора NaCl с глянцево-хромированным
железным катодом при 50° 268
95. Электролиз 25%-ного раствора NaCl с матово-хромированным медным катодом при 50° . • —
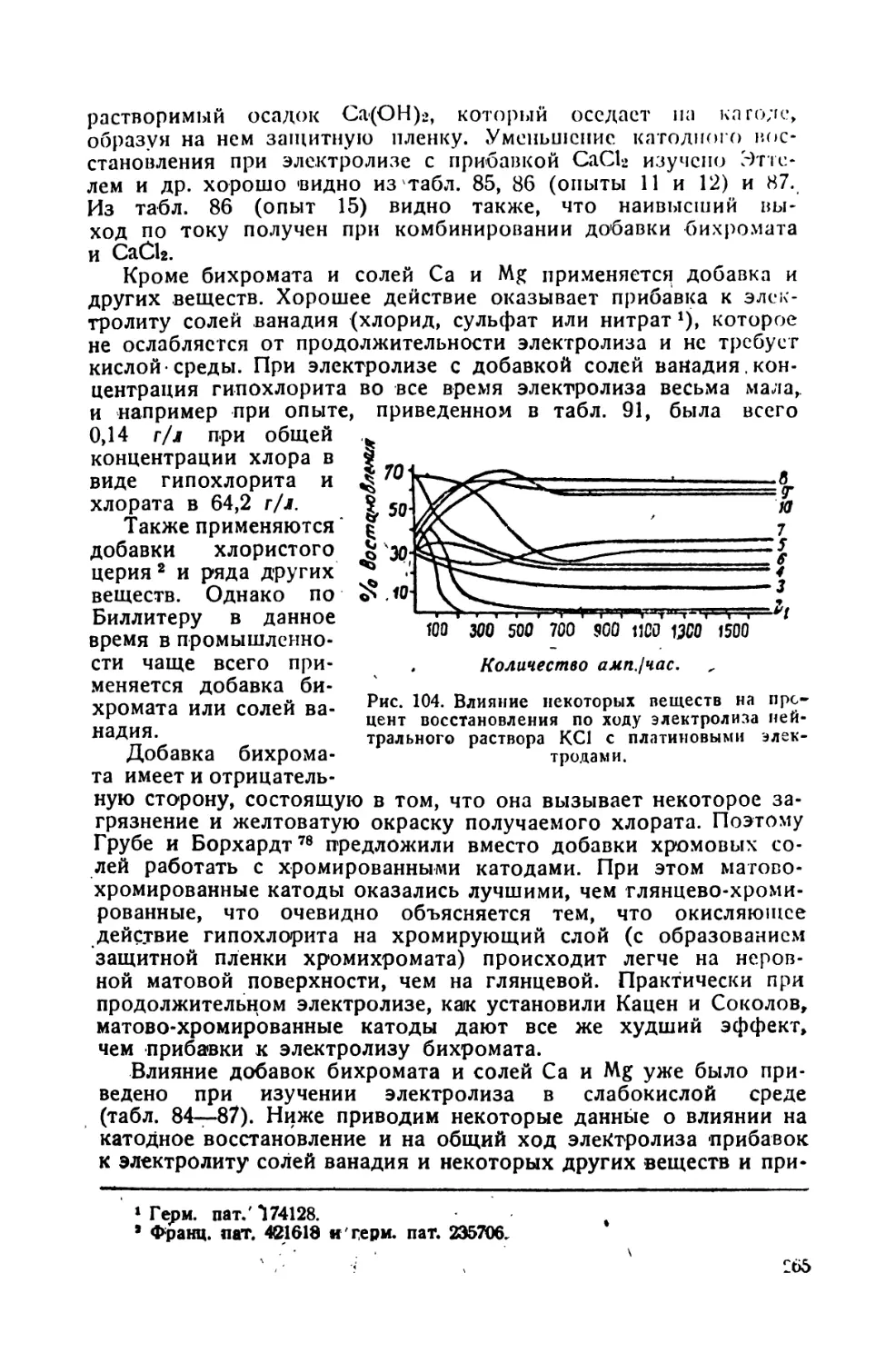
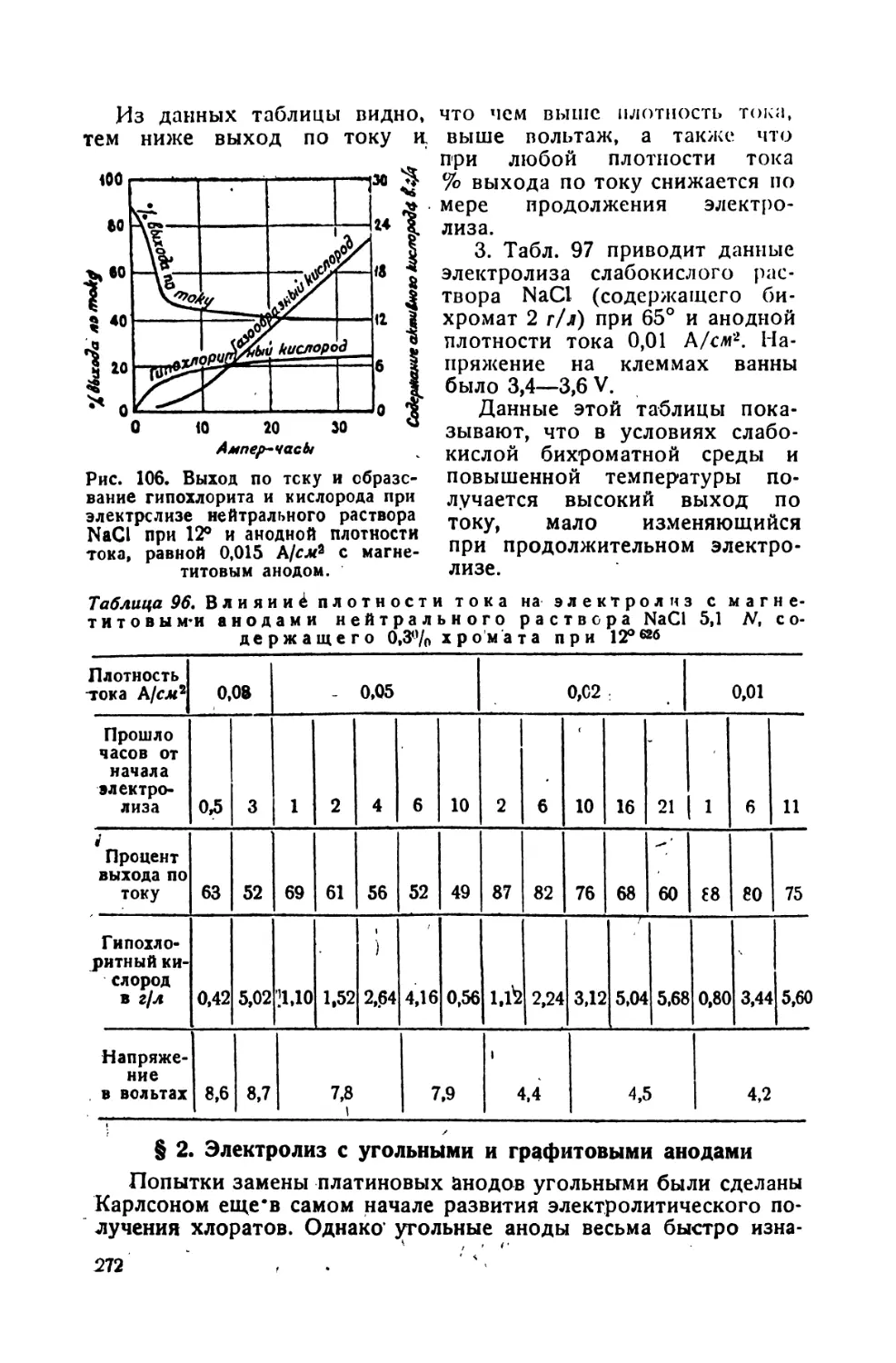
96. Влияние плотности тока на электролиз с магнетитовым анодом нейтрального раствора NaCl 5,1 N, содержащего 0,3% хромата при 12° 272
97. Электролиз слабокислого раствора NaCl 5,1 N с магнетитовым анодом при 65° и при анодной плотности тока 0,01 А/см2 273
98. Данные Ферстера по испытанию угольных и графитовых анодов при
электролизе нейтральною раствора NaCl при 60° 276
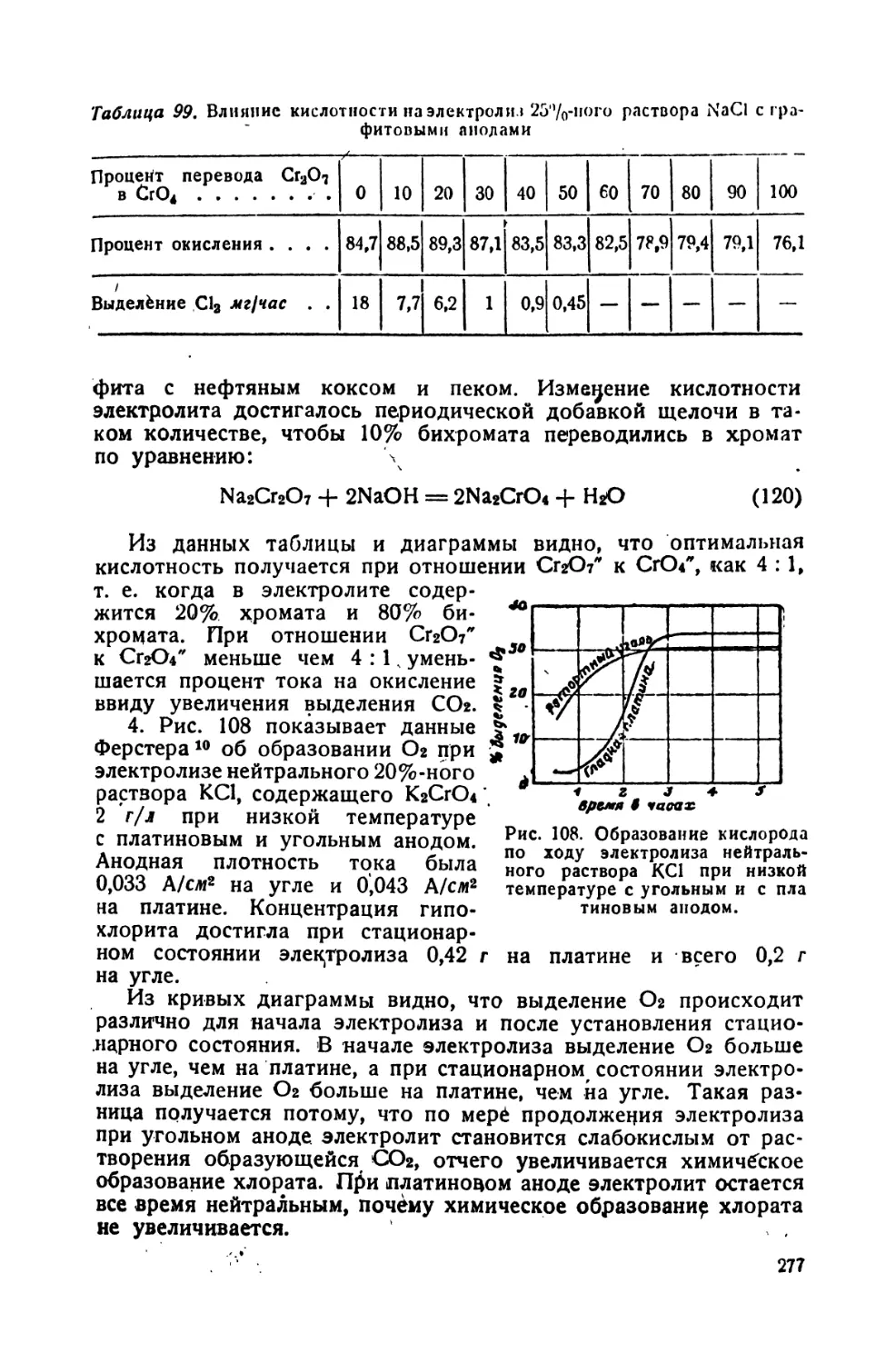
99. Влияние , кислотности на электролиз 25%-иого раствора-NaCl с графитовыми анодами 277
100. Влияние анодной плотности тока на разрушение графитовых анодов при электролизе 25%-ного раствора NaCl 278
101. Данные Арндта и Фезе о разрушении графитовых анодов при
электролизе 25%-ного раствора NaCl при 60° —
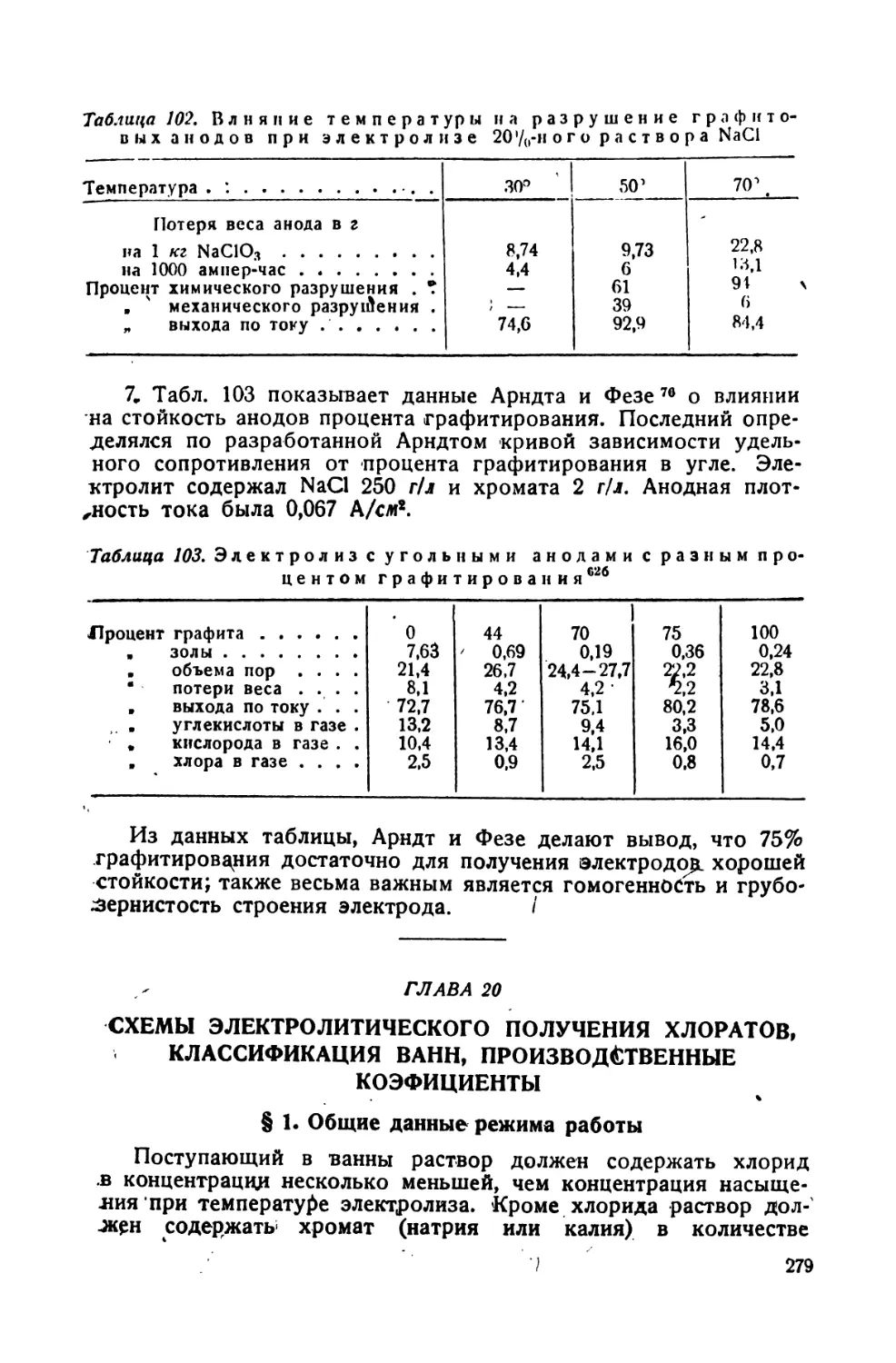
102. Влияние температуры на разрушение графитовых анодов при электролизе 25%-ного раствора NaCl 279
103. Электролиз на угольных анодах с разным процентом графитиро-
вания . . .' —
104. Указатель данных о свойствах хлоратов, приведенных в справочнике СТЭ 358
ПРЕДИСЛОВИЕ
Впервые производство бертолетовой соли было осуществлено
» промышленном млешглбе is. IS-1’ с, Однако iu4Moi|»t »ui почт
столетнюю историю, литература по производству хлоратов
весьма скудна. Известные работы Юриша, Луигс, Ксршау,
Гаммиля, Печииея опубликованы очень давно и содержат
весьма устарелые данные. Новейшие химико-технологические
справочники Гмелина, Ульмана, Даммсра и др. содержат в отношении производства хлоратов очень мало нового по сравнению
с данными Юриша и других старых авторов.
На русском языке до последнего времени имелись лишь
весьма краткие сведения о хлоратах в курсах химической технологии Любавина и др. Между тем народное хозяйство предъявляет огромный спрос на хлораты (спички, гербесиды, горные
работы и т. д.). За последние годы появился ряд исследовательских работ в области хлоратов и накопился также производственный опыт на крупных установках.
Автор, работая по вопросам хлоратов ряд лет, поставил
себе целью данной книгой по возможности восполнить пробел
в литературе по вопросам хлоратов, объединив в' ней производственные данные, результаты исследований и имеющийся литературный материал. Одновременно в книге собраны ряд таблиц,
диаграмм и тому подобный справочный материал по вопросам
хлоратов.
Книга состоит из четырех частей. Первая часть объединяет
главы по производству бертолетовой соли известковым методом,
так как другие методы производства бертолетовой соли b методы получения других хлоратов в большинстве стадий аналогичны- известковому методу получения КСЮз. Во вторую часть
книги выделены производство бертолетовой соли каустическим
и содовым методами, производство хлоратов натрия, кальция и
бария и данные по другим хлоратам. В третьей части описываются электролитические способы производства хлоратов.
В четвертой /части приведены контроль производства, техника
безопасности, производственные инструкции, данные о потребителях, хлоратов'и некоторые приложения. Кроме того дана
вводная глава по историческому обзору получения хлоратов.
I
13
_ ВВЕДЕНИЕ
ИСТОРИЯ РАЗВИТИЯ ПРОИЗВОДСТВА БЕРТОЛЕТОВОЙ СОЛИ
§ 1. Метод Либиха
Впервые КСЮз был получен в 1786 г. Бертолле при пропускании хлора в горячий раствор КОН. В 1808 г. Берцелиус обнаружил КСЮз в жидкости от электролиза раствора КС1. Более
детально изучил КСЮз Гей-Люссак. Способ получения КСЮз,
осуществленный впоследствии в промышленности, разработан
впервые Либихом, которого можно считать основоположником
производства хлоратов. Либих исходил из хлорирования взвеси
Са(ОН)г в растворе КС1. Щелок, получаемый после хлорирования, отделялся от шлама и уваривался до удельного веса
1,36—1,38 (38—40° Боме). При охлаждении уваренного щелока
из него выделялись кристаллы КСЮз. По этому методу в 1847 г.
начал работать завод в Англии в Сан-Эллён. В ближайшие годы
после начала работы первого завода производство бертолетовой
соли по методу Либиха было осуществлено и на других заводах
(в Виднесс в Англии, в Лилле, Салиндрей и Сан-Гобэйн во Франции, в Ауссиге в Австрии, в Берлине, Аахене и Людвигсгафене
в Германии). При этом большинство фабрик стало прибавлять
КС1 после хлорирования.
§ 2. Варианты метода Либиха
При вышеизложенном способе производства терялось много
КСЮз с маточным щелоком, остающимся после кристаллизации.
Для уменьшения этих потерь с маточниками Печиией, руководитель хлоратной фабрики в Салиндрей (Франция)*, разработал
способ выделения большей части СаСЬ, образующегося при
хлорировании, до (прибавления к щелоку КС1, благодаря чему
уменьшалось количество маточного щелока и потери КСЮз
с ним. Этот метод имеет большое значение для получения хлоратов натрия и бария, при которых исходят из хлорирования
известкового молоха.
1 О. Р. 16493 [1881]; Jber. ch. Technol., [1881], 296.
I
15
В 1888 г. Гаммил опубликовал способ вымораживания КОЮ:-,
из маточной жидкости, получающейся после кристаллизации
КСЮз, благодаря чему в маточной жидкости остается лишь
очень небольшое количество КСЮз (герм. пат. 15097, 1888 г.;
J. Soc. chem. Ind. 1889, 168—172).
. В 1929 г. в институте Карпова (Новаковская и др.!И) был разработан способ уменьшения потерь КСЮз путем высаливания
его большим избытком KCI, прибавляемым к щелокам после
хлорирования. После отделения выделившихся кристаллов КСЮз
маточный щелок упаривают для обратного получения КС1.
Нами в 1930 г. установлен оптимальный избыток КС1
в 20—30 г/л маточного щелока. При таком избытке КС1 и одновременном применении вымораживания маточных щелоков
в последних остается КСЮз .всего 5—гб г/л (см. стр. 126).
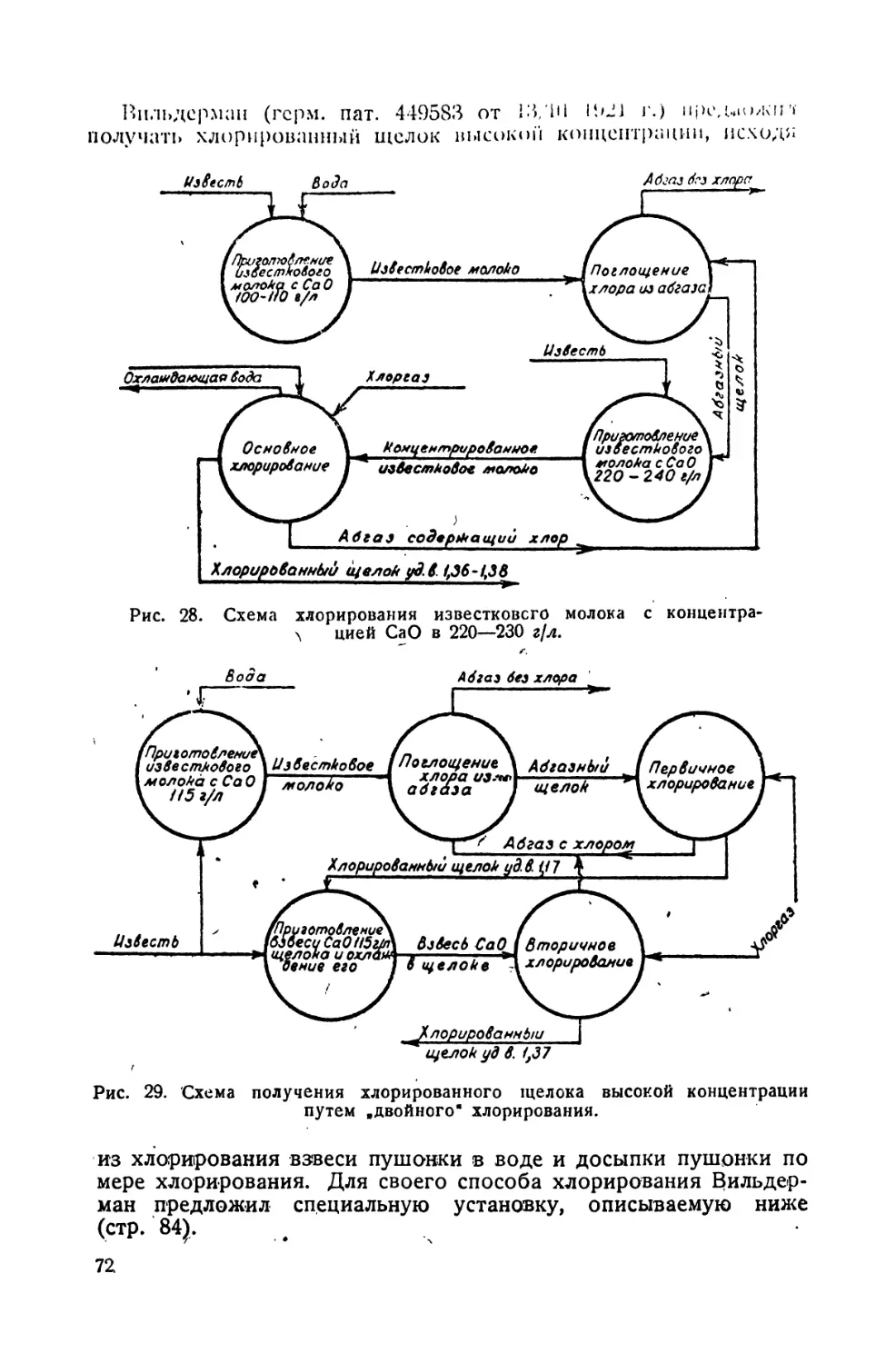
Основным изменением метода Либиха, осуществленным в настоящее время на некоторых хлоратных заводах, является получение щелока такой высокой концентрации, при которой выпарка щелока становится излишней. Такой способ производства
может быть осуществлен в разных вариантах, изложенных на
стр. 32.
При всех вышеизложенных способах на образование хлората
при хлорировании тратится теоретически лишь Ув поглощенного
хлора, а остальные 5/с хлора тратятся на образование хлорида.
Немецкий химик Шульц в своих патентах (герм. пат. 328211,1915 г.
и 330941,1919 г.) указывает на возможность каталитического воздействия на хлорирование с целью использования на образование хлората больше ‘/в затрачиваемого хлора. Для этого он
рекомендует хлорировать взвесь СаСОз в растворе КС1 хлор-
газом, разбавленным воздухом и НС1 с применением МпОг в качестве катализатора. Практического подтверждения осуществления этих патентов нам неизвестно.
§ 3. Хлорирование MgO, ZnO, Na'OH и Na^CO t
i
• а) Муспрат (герм. пат. 26698, 1883 г.) разработал метод получения КСЮз хлорированием взвеси MgO в воде. Остальные
стадии этого процесса идентичны соответствующим стадиям способов Либиха или Печинея (см. стр. 180).
б) Байер (герм. пат. 81804, 1894 г.), предложил хлорировать
вместо известкового молока взвесь ZnO в воде или в растворе
КС1. В качестве отхода при таком методе производства бертолетовой соли получается ценный хлористый цинк (стр. 182).
в) Вместо известкового молока хлорируют раствор NaOH
или 1ЧагСОз. Полученный хлорированный щелок, содержащий
ИаСЮз и NaCl, выпаривают до удельного веса 1,31—1,33
(34—36° Боме). Во время выпарки из щелоков выделяется большая часть NaGl, который используется как отход. К горячему
концентрированному щелоку прибавляют раствор хлористого
калия-и; охлаждают, отчего выделяется большая часть КСЮз
в виде кристаллов. Последние отделяются, а маточный щелок
if>
возврощасгсФТкмиУшфку. Гз'кой метод ир<.м.Уподства бортолото-
iioii соли, iiponcpoiitibiii па одном на современных заводов, дал
весьма хорошие результаты. Известны также друппе варианты
.метода ■производства бертолетовой соли, основанного на хлорировании NaOH или NaaCXDj (см. стр. 159).
§ 4. Электролитические способы
Совершенно отдельно стоят способы получения КООз, основанные на электролизе растворов хлоридов в ваннах без диафрагм. Однако несмотря на то что, как указано выше,
Берцелиус .впервые наблюдал КСЮ» в жидкости от электролиза
раствора КС1 еще в 1808 г., первый патент на этот метод был
взят только в 1851 г. (стр. 2SG), а .первая промышленная установка начала работать только в 1887 г.
В 1890—1910 годах получение хлоратов электролизом сильно
развилось и количество хлоратои, добытых электролитическим
путем, превысило количество хлоратов, добытых химическим
путем (хлорированием щелочей). В послевоенные годы из-за
избытка мощности производства- хлора и большого спроса на
каустик (NaOH) химические методы опять получили сильное
распространение (рм. стр. 286 примечание 4). В самые последние
годы замечается бпять поворот к электролитическим методам.
§ 5. Развитие производства бертолетовой соли в СССР
Спрос на хлораты в дореволюционной России почти целиком
•удовлетворялся импортом из-за границы. Только в 1913 г. были
пущены установки в Финляндии и в Польше, вскоре отошедшие
от нас. Инициатором производства бертолетовой соли в России
был П. П. Федотьев, под руководством которого были проведены исследования и опыты получения бертолетовой соли в Петербургском политехническом институте.
13 дальнейшем (Н. Н. Ворониным) была организована небольшая промышленная установка.
Опыты по получению бертолетовой соли электролизом ставились также проф. В. Г1. Ильинским в ГИПХ’е, проф. Памфиловым в Иваново-Вознесенском политехническом институте, проф.
Шпитальским с сотрудниками в институте Карпова в Москве и
в последние годы Каценом и Соколовым в Институте азота
в Москве и Н. Н. Ворониным с И. Б. Бормашенко в Киеве>.
В настоящее время потребность СССР в- хлоратах вполне
удовлетворяется собственным производством, несмотря на боль-
1 Получение бертолетовой соли по известковому-методу .в. небольшом
заводском масштабе было организовано в 1920 г, на одно^. из'.лффых заводов химиками Кулепетрвым и Поповым, а в 1924—
эти установки .вскоре были закрыты.
2 Зак. 179* — Шрайбман.
17
шоп рост спичечной промышленности н других потребителей
хлоратов.
СВОЙСТВА БЕРТОЛЕТОВОЙ СОЛИ
§ 1. Физические и химические свойства
Процентный состав КСЮ» следующий: калия — 31,92/',
хлора — 28,92% и ы: : юрода— 39,16'/".
Молекулярный веч КСЮ» равен 122,56. Окислительный эквивалент КСЮ» равен 20,43. Структурная формула КСЮ»:
/О
0 = Cl<f
Х> — К
Как видно из структурной формулы, хлор в КСЮ» имеет 5 положительных зарядов.
Кристаллы КСЮз относятся к моноклинической системе н
не содержат кристаллизационной воды. Величина и форма кристаллов зависят от условий кристаллизации-: при медленном
охлаждении горячего насыщенного раствора КСЮ» выделяются
чешуйчатые пластинки, величина которых варьирует обычно
в пределах 0,5—2 см2. При быстрой кристаллизации выделяются
мелкие игольчатые кристаллы. Юриш 1 (стр. 47) описывает кристаллы величиной в 200.200.2 мм, полученные при многодневной кристаллизации из концентрированных растворов КСЮ»
в СаО». Чистые кристаллы КСЮ» негигроскопичны. Гигроско
пичность технической бертолетовой соли зависит от содержания
в ней примесей *.
Уд. вес КСЮ» равен 2,33. Температура плавления КСЮ» равна
370—372° **. Теплоемкость КСЮ» в пределах 16—98° равна
0,194—0,210 кал. Теплота образования КСЮ» из элементов
равна 93,8—95,8 ккал/ыол. Теплота растворения 1 моля КСЮ»
в 200—400 молях воды равна 9,95—10,04- кал.
Вкус КСЮ» солено-прохлаждающий. Реакция раствора КСЮ»
нейтральная.
* Druezka (Glasnik chem. Drustva—Югославия 3, 1932, 106) шринодит
следующие данные влияния ■ примеси КС1 на гигроскопичность КСЮ» ври
комнатной т-ре:
Состав со tif
Ушгажнясмость после хранении в течение
24 час. |
| 51 Vs часа
75 */2 часа
Хим. чистый КСЮз
0,01%
0,27»/о
0,89%
0,04%
О ПН»,
КСЮ,+0,05% КС!
KClO,-HU% КС1
|0
0,57%
1,76%
** По дав к разных авторов.
\
18
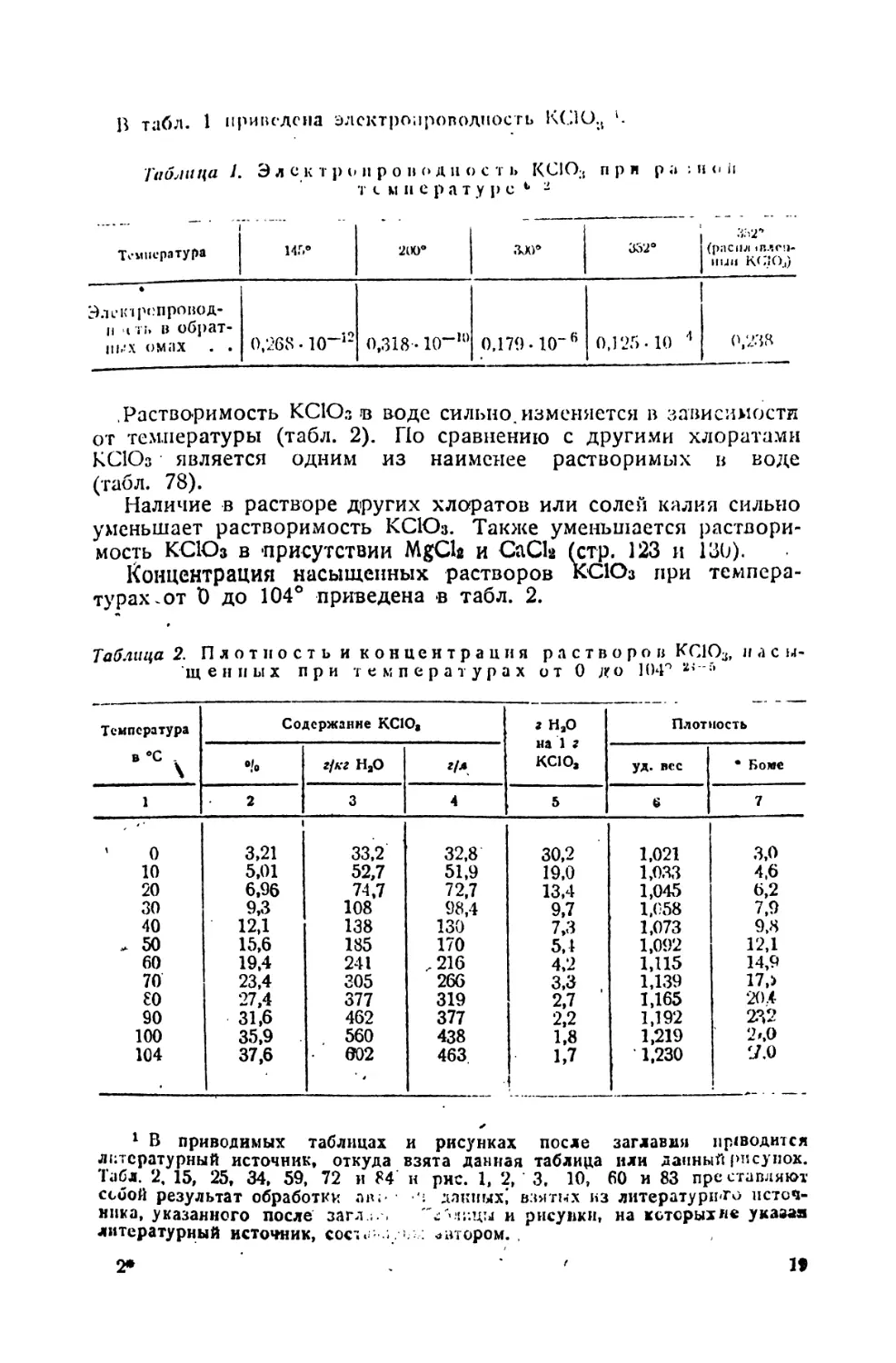
В табл. 1 приведена электропроводноеть КСЮ;1 1.
Таблица L Э л с к т р «про и о д и о с т ь КСЮ;, при ра : н <* ii
т с м п е р а т у р с ь -
(
Температура
14.V
21Ю°
I
, 352е j
к,г
I (pilCllJI iRJO'l-
| nun KCIO.,)
•
Элс1прспровод-
п i «т, в обратных омах . .
0,268 • 10_!2
0,318 • 10-,|)
0.179-10" в
0,12Г>-10 1
0,1*33
Растворимость КСЮз в воде сильно.изменяется в зависимости
от температуры (табл. 2). По сравнению с другими хлоратами
КСЮз является одним из наименее растворимых в воде
(табл. 78).
Наличие в растворе других хлоратов или солей калия сильно
уменьшает растворимость КСЮз. Также уменьшается растворимость КСЮз в •присутствии MgCla и СаСЬ (стр. 123 и 130).
Концентрация насыщенных растворов КСЮз при температурах.от Ъ до 104° приведена в табл. 2.
Таблица 2. Плотность и концентрация растворов КОО^, и л с и
щепных при температурах от 0 до 104° г*
Температура
в °C .
\
Содержание KC10a
г HaO
на 1 г
ксю.
Плотность
°!o
zjKt HaO
г/л
УД. вес
• Боме
1
2
3
4
5
6
7
' 0
•
3,21
33,2
32,8
30,2
1,021
3,0
10
5,01
52,7
51,9
19,0
1,033
4,6
20
6,96
74,7
72,7
13.4
1,045
6,2
30
9,3
108
98,4
9,7
1,058
7,9
40
12,1
138
130
7,3
1,073
9,8
. 50
15,6
185
170
5,1
1,092
12,1
60
19,4
241
.216
4,2
1,115
14,9
70
23,4
305
266
3,3 ,
1,139
17,>
£0
27,4
377
319
2,7
1,165
20.4
90
31,6
462
377
2,2
1,192
232
100
35,9
560
438
1.8
1,219
2*,0
104
37,6
602
463
1Д
1,230
'7.0
1 В приводимых таблицах и рисунках после заглавия пр<водится
литературный источник, откуда взята данная таблица или данный рисунок.
Табл. 2, 15, 25, 34, 59, 72 и 84 и рис. 1, 2, 3. 10, 60 и 83 проставляют
собой результат обработки ani- з данных,' взятых из литературного источника, указанного после загл и рисунки, на которых не укаэая
литературный источник, cocii ^ : ^втором. .
2*
19
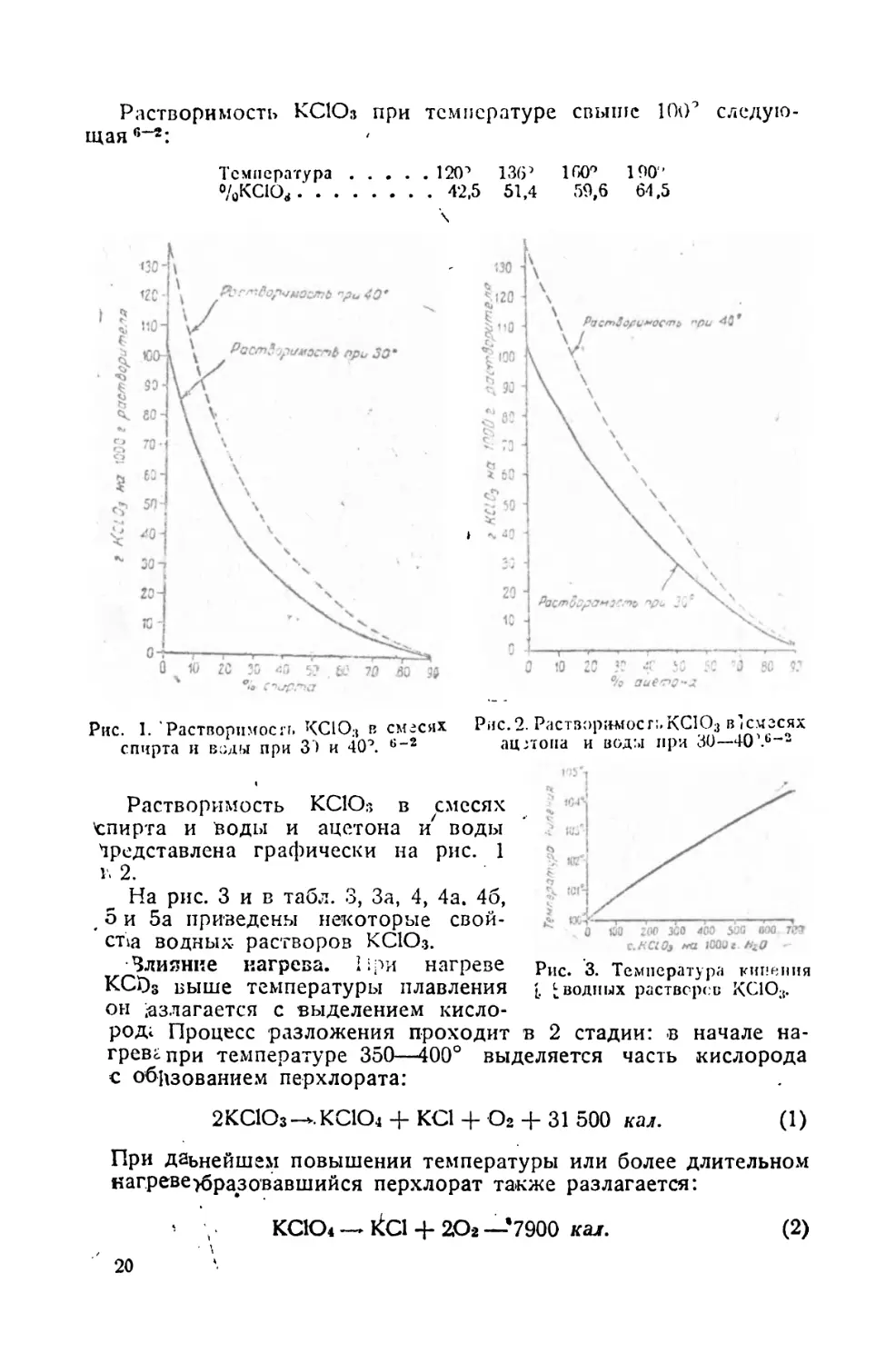
Растворимость КСЮз при температуре свыше 100’ следующая 8-4:
Температура l!^ 13(55 160° 100"
°ДКСЮ* 42,5 51,4 59,6 64,5
\
Рис. 1. Растворимое:!. КСЮ:, в смесях Рис. 2. РастворамосгаКСЮз в1снзсях
спирта и воды при 3 ) и 40°. G”2 ац :тоиа и веды при 30 40 . ~*1
Растворимость КСЮз в смесях
спирта и Воды и ацетона и воды
Представлена графически на рис. 1
V. 2.
На рис. 3 и в табл. 3, За, 4, 4а. 46,
, о и 5а приведены некоторые свойства водных- растворов КСЮз.
Влияние нагрева. При нагреве
KCDs выше температуры плавления
он Излагается с выделением кислород; Процесс разложения проходит в 2 стадии: в начале нагрева при температуре 350—400° выделяется часть кислорода
с обизованием перхлората:
Рис. 3. Температура кипения
^ водных растворов КСЮ;1.
2КСЮз—КСЮз -I- KU -(- О2 -)- 31 500 (1)
При даьнейшем повышении температуры или более длительном
нагревеубразовавшийся перхлорат также разлагается:
’ , КСЮз — кС14- 2,Ог —’7900 кал. (2)
20
Таблица 3. Плотность растворов КС103 и р и 18° *^ц -г>
као, | *
2
з
4
5
G
7
Удельный вес . .
°Ьсмо
],(К)5
0,7
i
1,011
1,5
1,018
2,5
1,024
3,4
1,031
4.2
1,038
5,3
1,045
6,1
Таблица За. Упругость» л ров растворов КСЮ3, н а с ы щ с иных
при разной температуре
Темпера¬
тура
40°
45°
53,3°
61,6°
69,9°
74,7°
80,2°
!
85,8° .
90,6°
90,4°
103,8°
ММ
рт. ст.
52,2
68,8
103.8
151,0
215,3
262,7
328,0
405,6
482,7
654,8
756,7
Таблица 4. Понижение упругости паров растворов КСЮ{
при 100° в зависимости от концентрации
KCIO, г/кг Н,0
39,2
103,3
158,4
196,7
306,5
376,7
i
Понижение упругости парсв
в мм рт. ст
7.0
18,1
28,0
35,1
51,6
**
63,1
«2,
Таблица 4а. Понижение температуры замерзания растворов
КСЮ3 разной концентрации
KCIO3 г/кг Н20
12,8
26,0
51,9
77,2
102,3
114,8
128,0
д
0,03734
0,07493
0,1462
0,2149
0,2799
0,3124
0,3477
Таблица 46. Удельная т е п л о е м.к о с f ь (в кал) растворов КС 103
°/g КСЮ3
'6,37
10,9
11,98
14,54
18,49
25,39
0,915
0,869
0,847
0,819
0,778
0,715
Таблица 5. Вязкость растворов КСЮ328-10
(по отношении^ к воде при той же температуре)
/ • ;
Концентрация КСЮ9
в молях на 1000 г НаО
0,1
0,2
0,3 1
0,5
Вязкость при 15°... .
. . . 25».
. . 35°
. . 45® .
0,994
0,999
0,999
1,002
0,990
0,998
0,999
1,004
-л
' 0,987
0,996
1,000
1,0С6
0,981
21
Таблица .5 а.Стспон и л и с " <> н " •'< и и и КОС:
Концентрация
ксю3
эк п./л ....
0,0
0,0001
0,0002
0,о.'
0,00 и
•/'*»
0,0
0,012
0,024
0.0G1
0,12;
Э*иипллсптпач элоктронронодность
при бесконечном ралблиленип . .
Степень лнссоцилцпп » °/оч • • • •
11Р,70
101)
11 км
99,1
118,35
98,9
117,08
Общее уравнение разложения КСЮз при нагреве будет:
2 КСЮз = 2КС1 + ЗОг + 23 600 (3)
Таким образом суммарный тепловой эффект разложении КСЮл
положителен.
Если остаток после прокаливания КСЮз растворить в воде,
то раствор будет иметь щелочную реакцию, ибо в нем кроме
КС1 содержатся также следы КОН. Одновременно если тщательно исследовать газ, выделяющийся при прокаливании КСЮ*,
то в нем можно обнаружить кроме кислорода также и следы
хлора. Это доказывает, что кроме вышеприведенного хода реакции разложения КСЮз происходит также, хотя бы частично,
реакция с выделением хлора:
2 КСЮз = К20 + 50 + СЬ. (4)
Разложение бертолетовой тсоли посредством нагрева часто
используется в лабораторий для получения кислорода. Из
грамма КСЮ* теоретически по уравнению (3) выделяется 0,3916 г
кислорода (273 см3).
По Г. и В. Бильцу при медленном, осторожном нагреве
КСЮз не выше температуры плавления реакция проходит с образованием КСЮ4 и КС1 без выделения кислорода по уравнению:
4КСЮз == ЗКСЮ4 + КС1. ' (5)
Примечание. Гофман и Морин (Zts. anorg. Ch. 71,1911,3861) приводят
следующий ход разложения КСЮз при нагреве до 490° в отсутствии катализаторов:
-—•—А
Выделилось
Образовалось
Осталось
кислорода
КС1
КСЮ4
/ КСЮ3
После 1 часа нагрева ...
1%
4,7%
17,9’/о
76,7%
После 6 часов нагрева . .
4%
19У»
72,4%
5,3%
22
водных растворах при 18° «-*
6,0020
0,2 Г»
0,<Хй0
0,01
0,02
0,05
0.1
0.2
0,613
1,226
2,451
6,128
12.2G
24,51
11.VI
<’6.8
113,84
95,1
111,64
93,3
108,81
<Ю,9
103,74
86,7
99,19
82,9
93,73
78,3
0.5
61,28 .
85,28
71,3
Блюм (диссертация Дрезден 1908 г.) привадит следующую зависимость
количества выделяющегося в 1 минуту кислорода от температуры нагрева
КСЮз (без катализаторов):
Температура нагрева
360
t
380
400
420
440 ,
450
Быделяется см* 02 п 1 мин
0,41
in
1/.
• 2,5 \ 5,0
1*
1
Каталитическое разложение КСЮз. В смеси с другими веществами выделение кислорода из КСЮз начинается большей
частью при бол^с низкой температуре и весь процесс разложения
КСЮз протекает равномернее и полнее, а стадии образования
перхлората часто вовсе не наблюдается. Такими свойствами
обладают соединения Fe, Mn, Си, А1, РЬ и многие другие (например обыкновенный песок). В лабораторной практике для получения кислорода из бертолетовой соли ее нагревают с перекисью
марганца (1 ч. КСЮз + 1 ч. МпОг). Если прибавлять примесь
Fe2Os, то ее достаточно взять 0,1% от количества бертолетовой
соли.
По Беллами (Юриш стр. 4) понижение температуры выделения кислорода происходит благодаря образованию промежуточных продуктов. Для перекиси марганца он дает следующую
схему:
2КСЮз + 2МпОг = 2КМп04 + 02 Ч- СЬ. . (6) .
2КМп04 = К2Мп04 + Мп02 + 02. (7)
КгМпО, + МпОг -К KClOj = 2КМп04.+ КС1 + j О, . (8)
Согласно этой схеме суммарное уравнение разложения КСЮз
при нагревании с МпО* будет:
ЗКСЮз + 2МпО, = 2КМпО<'+ КС1 + 50 + CU *. (9)
* После образования некоторого количества КМпО« дальнейший процесс
идет без выделения С1» по ур*«ияи (7, 8). Прим. ред.
V.
В табл. 6 приведено влияние некоторых примесей на температуру, выделения кислорода из бертолетовой соли.
Таблица 6. Температура начала выделении кислорода при
нагреве КС10з в смеси с некоторыми веществам иа
Какая примесь
Без при-
мссей
Платиновая чернь
РЬОя
Си О
Мп02
Fc(OH)s
Температура начала
выделения кислорода
350°
260 270°
280 -285°
230 235°
200 • 203°
ПО 120^
Химическая активность. КСЮз является сильным окислителем, отдавая свой кислород и превращаясь в КС1. При этом
хлор-ион получает один отрицательный заряд вместо пяти положительных зарядов, которые имеет хлор в КСЮз, т. е. в реакциях окисления КСЮз шестивалентен. Повышение температуры,
а также наличие кислой среды увеличивают химическую активность КСЮз.
Окись азота окисляется КСЮз уже при обыкновенной температуре до KNOs с одновременным образованием хлора и кислорода I
2NO + 2КСЮз = 2КЫОз +СМ-Оз. (10)
(частично при этой реакции образуется и КСЮ4).
Серная кислота реагирует с КСЮз уже на холоду, образуя
КСЮ4, KHSO4 и СЮ2:
ЗКСЮз + 2H2SO4 = 2KHSO4 + КСЮ4 + НгО + 2СЮг. (11)
При нагревании серная кислота с КСЮз образует K2SO4, хлор
и кислород:
2КСЮз -(- H2SO4 = K2SO4 -J- НгО + CI2 -f- 214O2. (12)
Соляная кислота также реагирует с КСЮз уже на холоду.
Обычно реакцию КСЮз с соляной кислотой выражают следующим уравнением:
КСЮз + 6НС1 = КС1 + ЗН2О + ЗС12. ' (13)
Практически при реакции КСЮз с соляной кислотой выделяется
кроме хлора еще и СЮг:
4КСЮ3 + 1-2НС1 = 4КС1 + ЗСЮг + 4^-С12 + 6НгО. (14)
Концентрированная ^азотная кислота реагирует с КСЮз, выделяя
хлор. Фосфорная, щавелевая, винная, лимонная, уксусная и
мышьяковистая кислоты реагируют с КСЮз только при нагре-
24 ' /
панни. Реакция с щавелевой кислотой проходит но следующему
уравнению:
КСЮз + ЗН2С2О4 = КС1 + ЗН2О + 6СО2. (15)
Борная, угольная и т. п. кислоты не реагируют с КСЮа.
Йодные растворы КСЮз не изменяются под влиянием света,
воздуха или нагрева. Реакции между водными растворами
КСЮа и кислотами происходят тем интенсивнее, чем выше концентрация КСЮз в растворе и чем выше концентрация самой
кислоты.
В смеси с серой, углем и многими другими веществами КСЮа,
дает взрыв от удара или от толчка. КСЮа также взрывает от
соприкосновения с каплей спиртового или эфирного раствора
SOs. На этом свойстве образовывать с легко окисляющимися
веществами взрывчатые смеси основано применение бертолетовой соли в горных работах, военном деле и т. д. (стр. 33-1).
КСЮа обладает также свойством детонации. По данным некоторых исследователей (Berthelot, С. п, том 129, стр. 920 и.
Dupre, Chem. Trad. Journ. 11 /XI 1899 г.) при внезапном нагреве
до высокой температуры (выше точки- плавления) может взрываться и чистый КСЮз без примесей.
. § 2. Физиологические свойства
Ион СЮ'з является протоплазматическим ядом, поэтому бертолетова соль, как и другие хлораты, ядовита. Прием внутрь
'2—3 г КСЮз может вызвать смертельное отравление. Известны
случаи отравления при длительном применении КСЮз для полоскания рта и горла — очевидно ввиду попадания КСЮз в желудок. Поэтому, поскольку ИаСЮз несколько менее ядовит, чем
КСЮз, надо предпочесть применение для медицинских целей
NaClOa. Некоторые врачи все же прописывают КСЮз даже
внутрь по 0,1—0,3 г на один прием. На свойстве СЮ'з отравлять
протоплазму клеток основано применение хлоратов для борьбы
с сорняками (см. стр. 336).
§ 3. Качественные пробы на ион СЮ'з
/
1. При прокаливании хлората выделяется кислород (уравнения 1—3).
2. Если на бертолетову соль капнуть серной кислотой, выделяется СЮз и СЬ (уравнения 11—12).
3. Если в пробирку с небольшим количеством КСЮз прилитй-
соляной кислоты, то выделяются СЬ и СЮг (уравнения 13—14).
4. От прибавления соляной кислоты к раствору KJ, содержащему хлорат, выделяется иод: ,
КСЮ* + 6KJ + 6НС1 = 7КС1 + ЗН2ОН- 6J. (16)
25
5. Растпор индиго, подкисленный соляной кислотой, желтеет
в присутствии хлората от образовании изатина:
Ct«HioN*0* + 2НСЮ= 2C3H5N02 + 2НС1. (17)
6. Восстановители, как FeSC>4, цинк, H2SO3, HNO2, H2S, AS2O3
и др.. окисляются хлоратами, которые превращаются в хлориды;
последние можно обнаружить раствором AgNOs и т. и.
В табл. 7 приводим некоторые цветные реакции па ион
CIO's (Woodruff, J. Am. Soc. 19, 1897, 156).
Таблица 7. Цветные pen к ц и и паи о н Г.КУ., < с
№
П11.
Рсактни
Окрашивание
1
Фенол* •
Красно-желтое
2
а-11лфтиллмин
Желто-красное
3
Гидрохинон
Желто-ь'оричнеиос
4
Креигл
Коричнево-желтое
5
а-Няфтол
»• »•
6
Пирогалол • ...
Темнокоричневое
7
Салициловая кислота .......
Темио-желто-горг.чиевое
8
Галловая кислота ...
Желтее
9
Ализарин
10
Метел 4
w
11
Амидол
Красное
12
Орцйиол .....
Зеленое
13
Ацетанилид . . .
Красно-коричневое
14
Ортотолуидин
Сильнс-сииее
15
Паратслуидин .
Интенсивно-коричневое
Для демонстрации свойств «хлоратов можно рекомендовать
•следующие опыты.
1. Смешать на керамиковой или стеклянной пластинке 14 г
размолотой в порошок бертолетовой соли с 5 г сахарной пудры
(бертолетова соль и сахар должны измельчаться обязательно
отдельно). К смеси прикоснуться стеклянной палочкой, смочен-
,ной крепкой серной кислотой: смесь сгорает моментально, наподобие взрыва.
2. Внести в фарфоровую ступку несколько кристалликов бертолетовой соли и щепотку серы (не больше чем по 0,1—0,2 г)
и осторожно растирать пестиком: происходит ряд небольших
взрывов. При растирании надо завернуть для предосторожности
руку полотенцем. ;
3. 2—3 г бертолетовой соли поместить в сухую пробирку и,
нагревая на спиртовке, показать сравнительную легкость плавления бертолетовой соли. Сделать то же со смесью бертолетовой
соли и сухого мелкого песку, поднося к пробирке тлеющую
спичку, показать выделение из пробирки кислорода, т. е. что
•от примеси леска понижается температура плавления и ускоряется разложение бертолетовой соли. Показать, что NaCl или
КС1 не плавятся при нагреве на спиртовой лампочке.
/ ' •
26
•1. Поместить 4- Г> г бертолетовой соли н широкий гигель и
расплавить нагреванием на песчаной баис. Бросить на плав маленький уголек: уголек загорается и искрится, прыгая но плаву.
5. Нагреть в сухой пробирке смесь 0,1 г порошка магния и
0,3 г порошка бертолетовой соли. При этом обязательно обернуть руку полотенцем: происходит взрыв, разбивающий пробирку. Магний при этом сгорает в окись магния:
ЗМк + КСЮ:{ = 3MgO + КС1. (18)
6. Лучинкой, на конце которой находится горящий кусочек
серы, зажечь щепотку (0,1—0,2 г) смеси порошка-магния и бертолетовой соли (! :2): смесь моментально сгорает с выделением
яркого света. Применяется в фотографии для моментальных снимков.
7. Нагревать в ’ сухой колбе
Вюрца смесь перекиси марганца
(МпОг) и бертолетовой соли
(в пропорции 2 : 3). Выделяющийся кислород собрать над водой
в цилиндры для собирания газов.
11оказать свойство собранного
газа зажигать тлеющую лучину.
На рис. 4 приведена схема получения кислорода нагревом смеси
бертолетовой соли и перекиси марганца.
8. Поместить в стаканчик 20—25 г бертолетовой соли и налить
сверху 20—30 мл воды. Положить над бертолетовой солью 2—
3 кусочка желтого фосфора и приливать осторожно по каплям
серную кислоту уд. веса 1,84: фосфор на месте соприкосновения с бертолетовой солью загорается под.водо^.
§ 4. Количественные методы определения иона СЮ'.;
1. К 1 г сухой бертолетовой соли, помещенной в фарфоровый
тигель, прибавить 5 мл соляной кислоты уд. в. 1,19 и выпарить
досуха (на водяной бане). К сухому остатку прилить еще 5 см3
соляной кислоты и снова выпарить досуха. Вторично полученный сухой остаток слегка прокалить и взвесить. Содержание
KClOs равно:
потеря в весе *100 07
0ДП6 'О'
2. Полученный по п. 1 сухой остаток растворить в воде и от-
титровать ибн СГ 0,1 N раствором AgNCh. Параллельно надо
в отдельной навеске непрокаленной бертолетовой соли определить ион СГ. 1 мл0,1 N раствора AgNOj соответствует 0,012256
КСЮг
3. К раствору 0,05—0,10 г бертолетовой соли в 5—10 мл воды
прибавить 1 гKJ и 10 mj соляной кислоты уд. в. 1,19 и оставить
на холоду на 10—15 мин. для полноты реакции выделения иода.
Рнс. . (олучеиие кислорода на-
грезом смеси КСЮ» и МиСУ,.
27
Выделившийся иод оттитровать 0,1 N раствором гниосульфита-
1 ям 0,1 N раствора N:i2S20:i соответствует 0,002042 г КОС)*:
КСЮз + 6KJ + 6НС1 7КС1 + ЗН*0 + 6J. (16)
2J + 2Na2S203 = 2NaJ + Na-AOo. (19)
4. К раствору 0,25—0,40 г бертолетовой соли прибавить 50 ям
0,5 N раствора FeSC>4 и вскипятить в колбе, закрытой пробкой
с клапаном Бунзена. Охладить и оттитровать избыток FeSO*
0,5 N раствором КМпО.»:
КСЮз + GFeSOi + 3H2S04 = КС1 + 3Fe2(SC>4)s + 3H20 (20>
10FeSO4 + 2KMn04 + 8H2SO., = 5Fc2(S04)s + K2S04 +
+ 2MnSO'4 + 8HsO. (21)
Вместо FeS04 можно брать раствор As2Oa, титруя избыток As2O.T
раствором КВЮз: ,
2 КСЮз + 3As208 = 2КС1 + 3As205. (22)
3As808 + 2КВЮз = 3As206 + 2KBr. (23)
1 ям связавшегося 0,1 iV раствора FeS04 или АзгОз соответствует-
0,002042 г КСЮз.
Примечание. По данным автора кипячение в открытой колбе практически не дает заметных отклонений от анализа с кипячением в колбе,,
закрытой пробкой с клапаном Бунзена. При условии же прибавления избытка H:SCb в. количестве 20—30% от общего объема жидкости перед титрованием реакция (20) проходит и на холоду в 2—3 мин. (журнал Заводская
"лаборатория № 4, 1936 г., стр. 425).
5. Раствор 0,2—0,3 г КСЮз кипятить с кислым раствором
FeS04 или с цинком в кислой или щелочной среде, с H2SOs
и т. п. Образовавшийся С1' титровать раствором AgNOe (по
Фольгардту).
Восстановить. СЮз' в СГ возможно и па холоду без кипячения, прибавляя к раствору хлората нитрит и азотную кислоту.
Реакции восстановления КСЮз в KCi выражаются следующими уравнениями:
КСЮз 4- ЗНз = КС1 + ЗН20. * (24)
КСЮз + 3H2S08 = KCI + 3H2SO4. (25)
, - КСЮз + 3KNO* = КС1 + ЗКЖЭз. (26)
6. К раствору 0,1 г КСЮз прибавить соляной кислоты и солянокислого алюминия. Полученное синее окрашивание сравнить
с окраской стандартных растворов (см. Джон Г. Йоу, Колориметрия, изд. 1935 г.,, стр. 375; J. Biol. Chem. 58, 675, 1923—
1934).
Литература
Гнелин*, № 6, 21, 22; Абегг*, т. 2, ч. 2; Бердь-Лунге* т. 2,
ч. 1; Юриш1; Мерияг*:
* Водород восстанавливает хлораты только in status niscendi. Прим. рея.
' ,
28 .
ЧАСТЬ ПЕРВАЯ
ИЗВЕСТКОВЫЙ МЕТОД ПРОИЗВОДСТВА БЕРТОЛЕТОВОЙ
СОЛИ
ГЛАВА I
СПОСОБЫ ПРОИЗВОДСТВА БЕРТОЛЕТОВОЙ СОЛИ
ИЗВЕСТКОВЫМ МЕТОДОМ
Метод производства бертолетовой соли, основанный на хлорировании известкового молока, с последующим обменным разложением с хлористым калием является старейшим и наиболее
распространенном. Отдельные варианты известкового метода
отличаются между собой по концентрации щелока, получаемого
при хлорировании, и схемой последующей обработки хлорированных щелоков. В данной главе приводим схемы трех наиболее часто применяемых вариантов известкового метода производства бертолетовой соли.
§ 1. Способ, основанный на хлорировании известкового молока
невысокой концентрации
В основном этот способ разработан еще Либихом. В дальнейшем в схему, осуществленную Либихом, было введено много
изменений, главными из которых являются обезвреживание щелоков после хлорирования, прибавление при обменной реакции
избытка КС1 и вьшораживание маточников. Также изменилась и
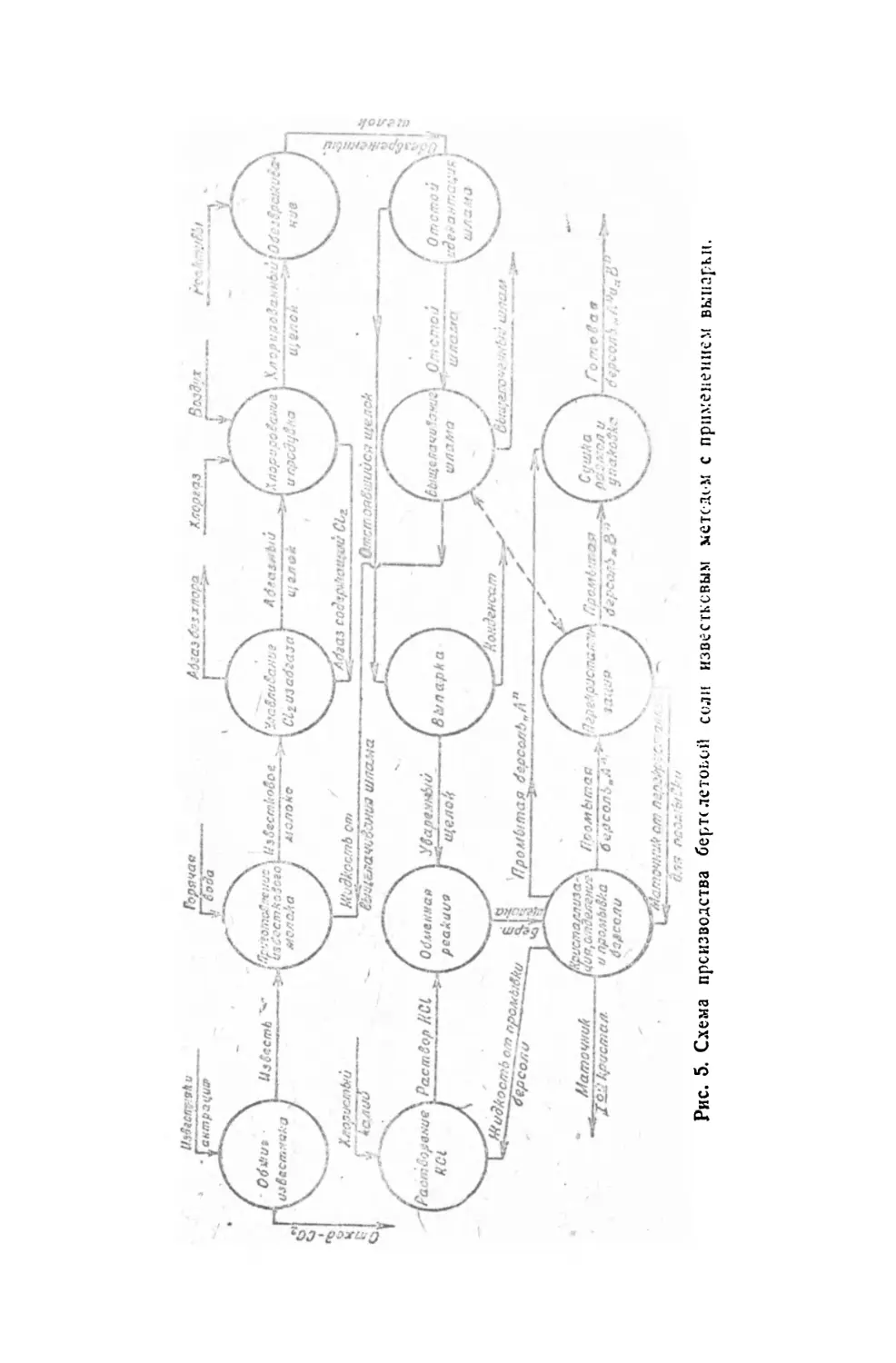
аппаратура производства, особенно аппаратура для хлорирования, выпарки и кристаллизации. На рис. 5 показана схема этого
способа производства бертолетовой соли, принятая на одном из
современных заводов.
1. Приготовление известкового молока. % Из обожженной
извести и воды приготовляется известковое молоко с кониентраг
иней СаО в 110 г/л. Вместо воды частично используются производственные промывные жидкости.
2. Очистка и охлаждение молока. Приготовленное молоко
отделяется от недопала и т. п. примесей. Обычно для очистки
молока применяются аппараты с ситами, либо аппараты, где для
отделения примесей используется различие в? уд. весе
Са(ОН)* и примесей. Очищенное молоко охлаждаете^ до температуры 20°.
3. Улавливание хлора из абгаза. Очищенное и охлажденное
молоко пропускается через колонку, в которой навстречу молоку
проходит абгаз' от хлорирований по п. 4. Абгаз, выходящий из
колонки, не содержйт хлора и выпускается * атмосферу.
Стхсд-CC*
Рис. 5. Схема производства берклетоьой соли известковым методом с применением выпарки.
лок
4. Основное хлорирование. Щелока, выходящие па пбгжм.
вон колонки, поступают в банши (млн абсорберы и т. н. ainia
рагы) для хлорирования. Последнее ведется до прореагироиа-
ппя ксего СаО н появления в щелоке избытка хлора.
Г». Обезвреживание. Хлорированным щелок содержит СЮ',
вредным для дальнейших стадии производства, почему его удаляют продувкой . аса воздухом и прибавлением особых
реагентов. ;
О. Отделение - Обезвреженный щелок содержит нерастворимый осадо хлам. Его удаляют отстоем щелока (или
фильтрацией щ . ■). Отделенный шлам выщелачивают или
промывают горячен водой. Промытый шлам является отбросом.
I (ромывпую жидкость используют для приготовления известкового молока и т. д.
7. Выпарка. Щелок, отделенный от шлама, упаривают до
уд. в. 1,42. Конденсат выпарки применяют для перекристаллизации бертолетовой соли, выщелачивания шлама и приготовления
известкового молока.
8. Обменная реакция. К уваренному щелоку прибавляют раствор КС1 (из расчета 20% избытка), не содержащий нсраство-
ренных веществ и соединений SO*' и СОз". Для растворения
КС1 может быть использована жидкость от промывки бертолетовой соли первой кристаллизации и от выщелачивания шлама.
9. Первая кристаллизация. Полученный после обменной
реакции берголетовый щелок охлаждают в кристаллизаторах до
температуры 10—20’ выше нуля. Выделяющиеся кристаллы
КСЮз отделяют на центрофугах от маточного щелока и промывают маточным щелоком второй кристаллизации.
10. Вымораживание. Маточный щелок, полученный по п. 9,
охлаждают до 10—20° ниже нуля. При этом выделяется дополнительное количество КСЮз, которое отделяют, как в п. 9.
11. Использование маточного щелока первой кристаллизации.
Маточный щелок .после вымораживания, содержащий СаС1?
400—450 г/л, КСЮз 5—15 г/л и КС1 до 25 г/л, является отходом
производства бертолетовой соли и используется для получения
плавленого хлористого кальция, а также применяется для производства хлористого бария ,и г. п.
12. Вторая кристаллизация. Бертолетова соль, полученная
по пп. 9 и 10, содержит ряд примесей. Для очистки от них
бертолетову соль растворяют при нагревании в жидкости от
промывки бертолетовой соли 2-й кристаллизации или в маточном щелоке от предыдущего цикла 2-й кристаллизации,
отстаивают от нерастворимого остатка, декантируют и охлаждают. Выпавшие кристаллы КСЮз отжимают на центрофугах
и промывают охлажденным конденсатом. Маточный щелок
используется для промывки бертолетовой соли первой кристаллизации.
13. Обработка бертолетовой соли. Промытая и отжатая бертолетова соль первой или второй кристаллизации подвергается
сушке. Суфка обычно производится в вакуум-сушилках. Вы-
' ‘31
сушсиппя соли просешкк'Тся п упакоиыппется. Для некоторых
потроОителои соль дополпнгелыю ие.ме^и.чагтся.
Примечания: а) па некоторых з.шодах и отличие от изложенной
схемы хлористый калий дли обменной реакции .приоаилнетсн и аиле гиер-
дой соли, а не п пиле растиора, и операцию обменной реакции промодят
до 'пьшарки щелок он;
б) многих потребителей удоплетпориет 'бертолетова соль нерпой кристаллизации, так что вторая кристаллизация •производится только по мере надобности.
uJLjfOSOQ
I I Росюйоритълй Ьор^м
Ofnqe/ium&Jis cojju
/
/JoSdU/b,
сопи
чзг
Рис. 6. Схема производства бертолетовой \:олн по Лупге.
А\ А" и Л'" — абсорберы, В — главная газовая труба, С —запасной сосуд, /Г, Е — отстойники,
О—-паровая машина, Н — насос, Г и /"—сосуды для шлама, /С—сосуд для концентрированного щелока, /. — сосуд для промывных вод, ММ —выпарные котлы, QQ — сосуды для растворения корок, // — кристаллизаторы, 00 — сосуды для стскания маточника от соли, РРР — ловушки
взвешенных кристаллов КСЮ3 из маточника.
На рис. 6 показана схема производства бертолетовой соли
хлорированием молока невысокой концентрации, которая приведена у Лунге3.
§ 2. Способ, основанный на получении при хлорировании
щелока высокой концентрации
Этот способ отличается 1от вышеизложенного тем, что при
хлорировании сразу получается щелок такой концентрации, что
выпарка становится излишней. Остальные стадии производства
подобны соответствующим стадиям способа, изложенного в § 1.
Только обменная реакция производится с твердым хлористым
калием, а не с раствором КС1. При таком способе производства
отпадает необходимость в выпарных аппаратах, уменьшается
расход пара и -устраняются потери щелока в стадии выпарки.
Приготовление хлорированного 'щелока высокой концентрации
32 /
дитоявдш — ‘и«е
Разрез по Ct
' Рлайно* $&сг*ий-
Отдйленив MpuCrfiTfr/lUsaiyjU//
Рис. 7. Схема производства бертслетовсП если по Биллитеру.
JW? —аппараты с мешалками дня хлорирования, V— керамиковый вентилятор, подающий хдоргаз, LK — аппараты для приготовления исходных растзороз,
FT — воронки для наполнения аппаратов для хлорирования» VK и НК — кристаллизаторы» $А — отделитель соли, RZ — центрофуги.
может быть произведено по-разному и будет описано па
стр. 70—73 (рис. 23”30).
Необходимо упомянуть, что в схемах производств;! бертолетовой соли известковым методом, приводимых Ульманом •* и
Биллитером 12, нет указаний на применение 'выпарки хлорированного щелока. Схема, приводимая Биллитером12, показана на
рис. 7.
На хлорирование поступает известковое молоко с концентрацией СаО ~130 r/j при одновременном добавлении хлористого
калия. Хлорирование ндится в грех аппаратах R, снаб¬
женных мешалками, iложные растворы готовятся в аппаратах
LK и поступают из RR, RM и RMM через воронки FT. Хлор
нагнетается керамиковым вентилятором V. Полученный после
хлорирования щелок, содержащий КСЮз ~ 130 r/л, охлаждают
в НК и VK и выделившиеся кристаллы отделяют на солеотдели-
телях Sa и центрофугах RZ. Выгодно подвергать щелок глубокому охлаждению, что производится в АК.
§ 3. Способ, основанный на выделении части СаСЬ из
хлорированного щелока (способ Печинея)
Способ основан на выделении части СаСЬ, содержащегося
в хлорированном щелоке, с целью уменьшения количества маточных щелоков и потерь КСЮз в этих щелоках. Для выделения СаСЬ Печинеем разработаны два варианта, которые могут
быть осуществлены каждый в отдельности или оба последовательно.
а) Выделение СаСЬ из концентрированных щелоков. Щелок,
полученный хлорированием известкового молока, упаривают до
уд. в. ~ 1,50 (~ 48° Боме). Концентрированный щелок охлаждают до 10°; при охлаждении из него выделяется часть хлорида в виде СаСЬ • 6НгО. Обладающий же большей растворимостью Са(С10з)г остается в маточном щелоке. Выделившийся
хлорид отделяется на центрофугах от маточного щелока и представляет собой отход. Маточный щелок подогревается- и поступает на обменную реакцию с КС1.
б) Выделение СаСЬ в виде оксихлоридов. К подогретому
хлорированному щелоку или к маточному щелоку после выделения СаСЬ • 6Н2О по варианту (а) прибавляют известь из расчета
3 моля СаО на 1 моль СаСЬ, содержащегося в щелоке. По охлаждении образуется оксихлорид примерного состава ЗСаО •
• СаСЬ • 15НгО, который отделяют от маточного щелока. Последний подогревают и передают на обменную реакцию с КС1.
Отделенный оксихлорид обрабатывают горячей водой, отчего из
него выделяется известь. Последняя отделяется и поступает на
хлорирование или на новое выделение оксихлорида. Жидкость
от разложения оксихлорида содержит СаСЬ и Са(С10з)г и может
быть обработана по варианту (а).
По варианту (а) удается выделить 60—70% СаСЬ, содержащегося в хлорированном щелоке. При последовательном приме-
34
неинн обоих вариантов можно .выделить 90—95% СаСЬ (некоторые данные, полученные нами три исследовании обоих вариантов способа Печннея, см. стр. 191 и 197).
§ 4. Некоторые замечания по сравнению разных способов
производства бертолетовой соли известковым методом
Способ Печинея не получил широкого распространения для
производства бертолетовой соли, так как схема этого способа
гораздо сложнее, чем схемы способов, изложенных в § 1 и 2.
Кроме того основное преимущество способа Печинея (уменьшение потерь КСЮз с маточником) потеряло свое значение, так
как благодаря применению избытка КС1 три обменной реакции
и благодаря вымораживанию маточника общая потеря КСЮз
с маточником значительно уменьшилась. В большей степени способ Печинея сохранил свое значение для производства хлората
натрия (стр. 191).
При сравнении способов, изложенных в § 1 и 2, сразу видно,
что основным преимуществом хлорирования щелока высокой
концентрации является ненужность выпарки хлорированного щелока (как отмечалось выше, не нужны выпарные аппараты, отпадают расход пара и потери щелоков при выпарке). Однако
этот способ обладает рядом недостатков по сравнению со способом, исходящим из хлорирования известкового молока невысокой концентрации. Основные недостатки следующие:
1) сложнее приготовление и очистка известкового молока;
2) сложнее хлорирование;
3) сложнее отделение шлама;
4) усложняется вопрос поглощения хлора из абгаза;
5) больше механические потери (при хлорировании и при отделении шлама).
Литература
Лунге*, Биллитер1*, Ульман5, Печиней*.
ГЛАВА 2
ОСНОВНОЕ СЫРЬЕ ДЛЯ ПРОИЗВОДСТВА БЕРТОЛЕТОВОЙ
СОЛИ ИЗВЕСТКОВЫМ МЕТОДОМ
Как видно из главы 1, при известковом методе производства
бертолетовой соли основным сырьем являются известь, хлор и
хлористый калий. Приводим основные данные для этих продуктов: химические и физические свойства, месторождения, применение и схемы получения и т. д.
При этом приводим также и данные для известняка, так как
получение извести из известняка производится часто на самом
заводе бертолетовой соли.
35
§ 1. Известняк
Известняк очень распространен в природе. Многие горные
цени целиком состоят из известняков: Пиренеи, Лннснипм, Но-
гезы и т. д. В СССР известняки встречаются почти всюду. Разработку известняков ведут карьерами, применяя взрывы породы
динамитом и т. д. Общее количество добываемого известняка
огромно, но учет его затруднен из-за разбросанности и многочисленности разработок. Главная масса добываемого известняка
расходуется как строп чча.ный камень, как плавень для шихты
в металлургии и дл. производства извести. Меньшие количества
известняка потребляются для производства СОг, для нейтрализации кислот, в медицине и т. д.
а) Состав известняка
Природный известняк состоит в основном из углекислого
кальция (СаСОз). Основными примесями, обычно содержащимися в известняке, являются соединения Mg, Al, Fe, SO4, Si и
органические вещества. Другие примеси встречаются реже и
обычно в меньших количествах (соединения Мп, К, Na, Li, Р, Cl).
Примесь соединений Mg в известняках может дойти до 19—20%
(доломиты), соединений Fe и А1 до 20—25% (мергеля), органических веществ до 3—5% (битуминозные известняки). Для производства извесТи, применяемой для получения бертолетовой
соли, годятся только известняки, содержащие мало примесей
(см. стр. 39', п. б). В табл. 8 приводится состав известняков некоторых месторождений СССР.
Таблица 8. Состав известняков некоторых месторождений СССР **
№
пп.
Месторождение
СаС08
MgCO,
CaS04
Окиси железа и
алюминия
Нераство¬
римый
остаток
Влага
1
Ширяево (Самарского
района)
98—99
0,6-1,2
0,3
0,11
0,1—0,5
—
2
Район Перми
86,8
1,13
1,5
1,6
9,5
—
3
Всеволодо-Вильва
(Урал)
93,9
1,83
следы
1,4
2,4
0,2
4
Елабуга (Татария) . .
92,1
0,84
0,11
0,44
1,9
4,7
5
Кривой Рог (Украина)
95
0,02
—
0,92
0,8
1,0
6
Мел Лисичанский (Ук¬
раина)
95—93
0,4—1,3
0,4—0,6
со
«н
1
о
4,8—12,7
0,5
б) Физические и химические свойства
Цвет и свойства известняков зависят от количества приме-
оей в них. Химически чистый СаСО» бесцветен. Природные известняки бывают разных цветов и оттенков, но чаще ветре-
36
чаются белые и серые. Пес кубического метра известняк;! рлыл:
1,8—2,2 т. Удельный пес чистого СаСОз 2,6--2,0. Твердость и t-
всстников по минералогической шкале Мооса варьирует от
1 до 3.
Кристаллы СаСОз бывают гексагональной системы (кальцит
или известковый шпат') и ромбической системы (арагонит).
СаСОз бывает также а ;:ым (в меле и в отложениях в организмах).
По Густаву Розе < 'апин 14, том И, стр. 367) искусственный
СаСОз, полученный осаждением из растворов, лолучается в виде
кристаллов гексагональной системы из холодных и ромбической
системы из подогретых растворов. Удельный вес, твердость и
другие свойства кальцита и аргонита несколько разнятся. Природные известняки большей частью состоят в основном из кристаллов кальцита. Для последнего теплоемкость при 20—100°
равна 0,20287 кал.
При нагреве до высокой температуры СаСОз диссоциирует
на СаО и СОг (с поглощением тепла) по уравнению:^
СаООз = СаО + СОг — 42,5 ккал. (27)
Однако эта реакция обратима и направление ее зависит от
температуры и от давления СОг над разлагаемым СаСОз.
Каждому давлению соответствует определенная температура,
ниже которой начинается «ассоциация» СаО и СОг в СаСОз
(обратное уравнение 27). Точно так же каждой температуре
соответствует давление, выше которого начинается «ассоциация».
Например при давлении в 1 ат диссоциация СаСОз начинается
лишь при 900°. При 700° для начала диссоциации СаСОз давление над СаСОз должно быть ниже 25 мм рт. ст. Эта зависимость
между температурой и давлением в процессе диссоциации СаСОз
показана в табл. 9.
•
Таблица 9. Зависимость между давлением С02 и температурой при термической диссоциации CaCOj 29
Температура
500
600
700
800
850
900
950
1000
Давление С02 в мм
рт. ст.1
од
2,4
25,3
168
373
773
1490
2710
1 Давление, виже которого начинается диссоциация.
Наличие в известняках примесей изменяет данные табл. ЭГ'На-
пример известняки С содержанием большого количества соединений магния разлагаются при температуре на 100—200° ниже,
чем более чистые известняки.
37
§ 2. Известь
а) Получение и з б е с т и
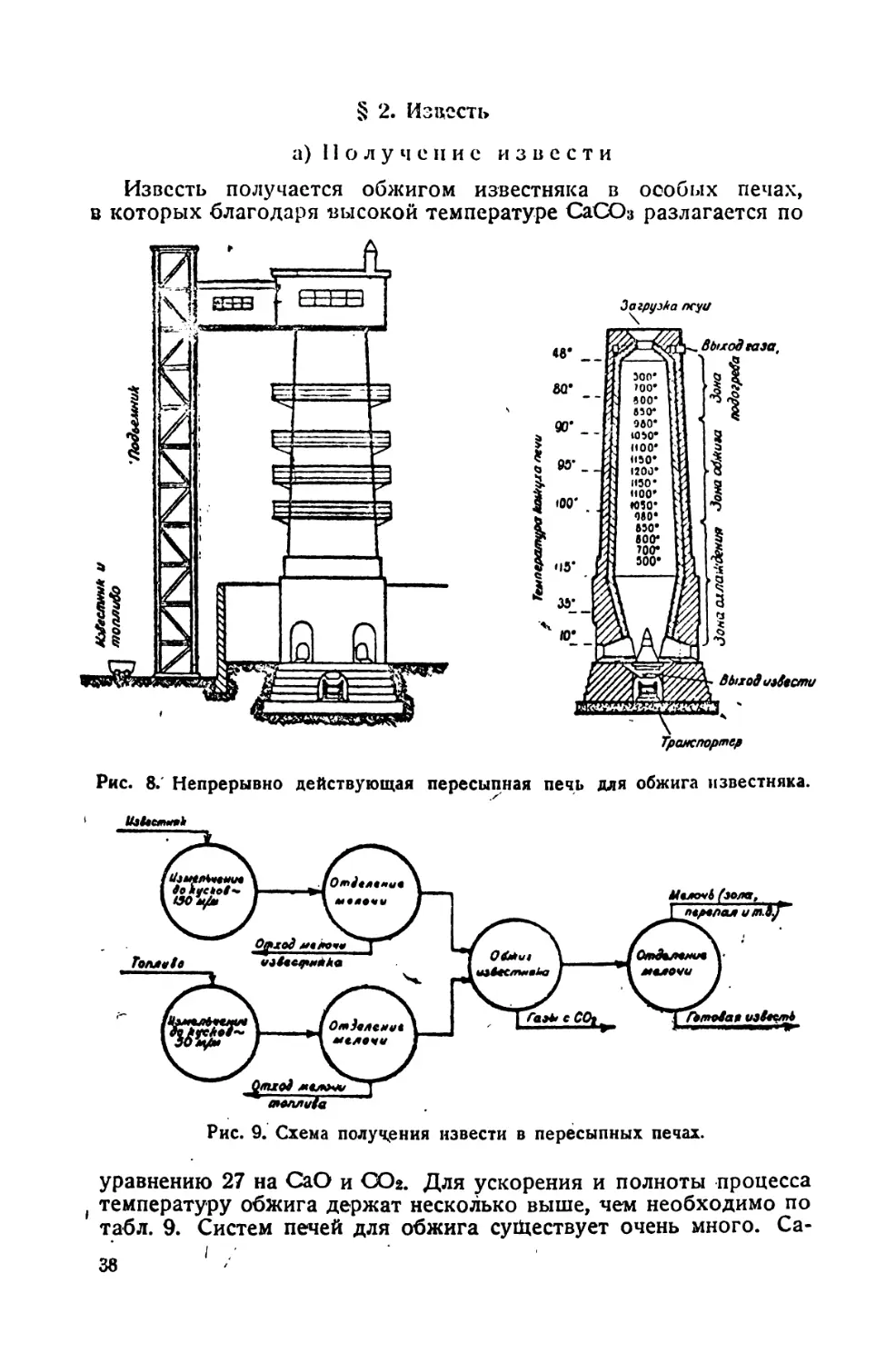
Известь получается обжигом известняка в особых печах,
в которых благодаря высокой температуре СаСОз разлагается по
Загрузка ncytf
Рис. 8. Непрерывно действующая пересыпная печь для обжига известняка.
UsUcmfh
уравнению 27 на СаО и СОг. Для ускорения и полноты процесса
, температуру обжига держат несколько выше, чем необходимо по
табл. 9. Систем печей для обжига существует очень много. Са-
38
мые старые типы печен—это «костры» или «кучи» и постинг -
«напольные» *нсчи, применившиеся уже тысячи лет тому на.;;:д.
В данное нреми эти печи применяются лини» при временной (сезонной) небольшой потребности в извести и в местах, где отсутствуют более совершенные лечи. На заводах применяются пересыпные шахтные печи, длиннопламенные шахтные печи, кольцевые печи и вращающиеся печи. Наиболее распространенными
являются пересыпные печи. На рис. 9 приведена схема получения
извести обжигом в шахтной пересыпной печи, принятая в одном
из современных проектов производства бертолетовой соли.
б) Состав извести
Техническая известь состоит в основном из СаО. В качестве
примесей в извести могут содержаться: примеси, бывшие в известняке, из которого она получена; необожженный СаООз
(недбпал); зола топлива (при пересыпных печах). Известь, получаемая при правильном обжиге из известняка хорошего качества, должна содержать не меньше 93—94% СаО. Только такая
известь и годна для производства хлоратов. Наличие в извести
недодала1 и соединений SO4 и Si, Fe и А1 усложняет очистку
известкового молока (стр. 51) и увеличивает количество шлама,
остающегося после хлорирования >(стр. 99). Наличие в извести
соединений тяжелых метал-1
лов может вызвать каталитическое разложение при хлорировании (стр. 106). Кроме
примесей на качество извести
влияет еще температура обжига: при слишком высокой
температуре обжига получается" мало активная известь — перепал.
в) ,Ф изи чески е и химические свойства
Удельный вес кристаллического СаО равен 3,1—3,2.
Насыпной или объемный вес
извести гораздо меньше, так
как при обжиге вес камней известняка уменьшается -
почти наполовину (СаО = 56,
СОг = 44), а объем уменьшается весьма мало (5—10%). Практический вес кубического
метра кусковой извести равен 0,8—1 г, а объем 1 т извести равен 1^—1,2 л8, Плавится СаО при 2572°.
СаО химически весьма активен, особенно по отношению
к воде и к СОг, Однако абсолютно сухой СаО совершенно не-
^,(Jpu2om
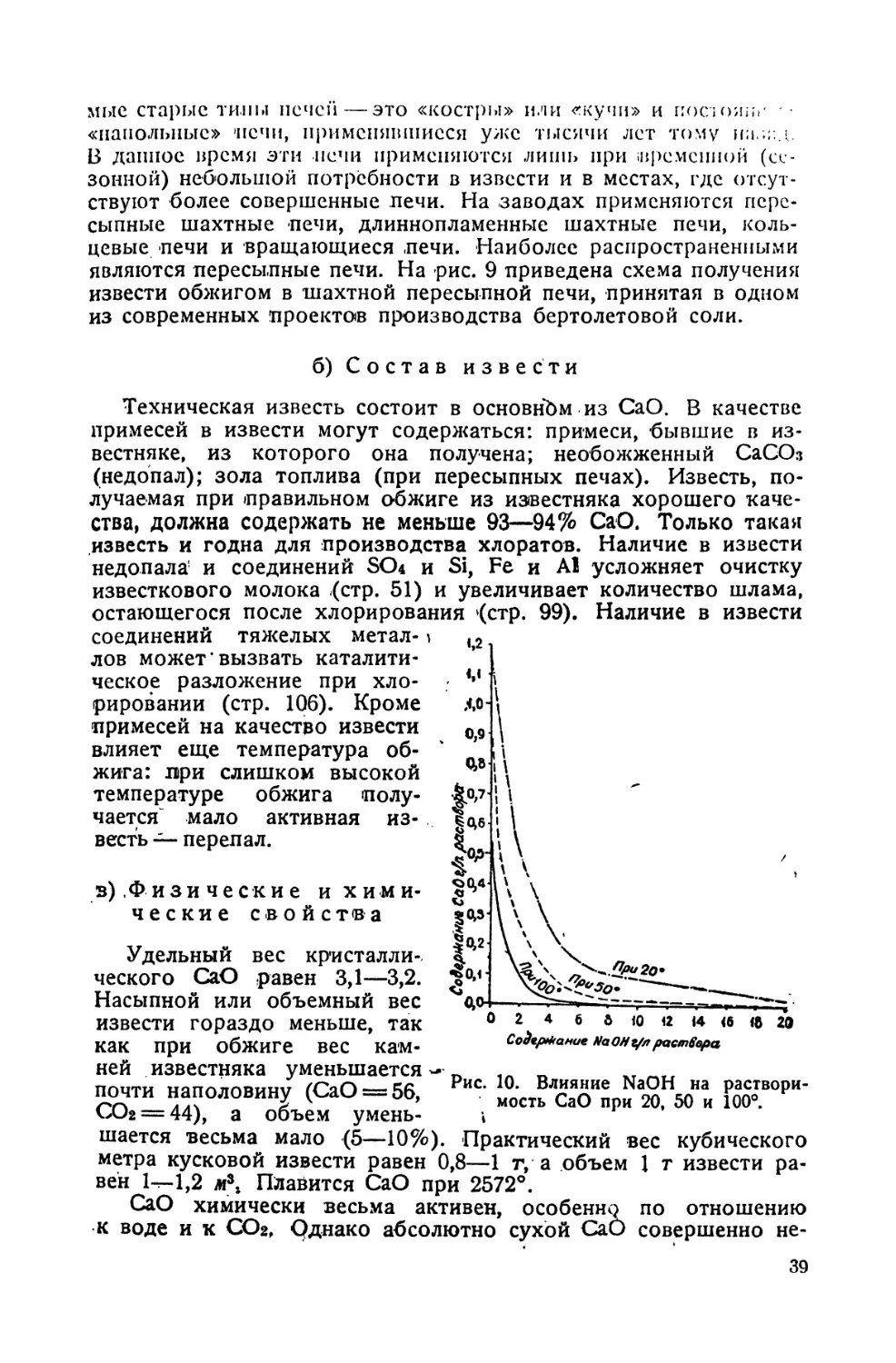
2 4 6 & i0 12 14 <6 ib 20
Содержание NaOHz/л раствора
Рис. 10. Влияние NaOH на растворимость СаО при 20, 50 и 100°.
39
активен. Кроме содержания влаги активность СаО зависит о г
температуры обжига, при котором получена данная нанести.
Например нанести, полученная обжигом при 1600°, не реагирует
ни с подои, ни с сол я и о и к и с л о т о й даже при длительном
хранении в них но взвешенном состоянии. Так же снижается
активность извести от наличия в ней примесей.
С водой СаО образует гидрат Са(ОН)2 и дигидрат СаО • 2НгО;
с хлористым кальцием СаО образует ЗСаО . СаС12* 15НгО (оксихлориды).
Растворимость извести в воде незначительна и тем меньше,
чем выше температура воды (табл. 10). Наличие в воде электролитов большей частью увеличивает растворимость СаО. Однако
наличие в воде NaOH или КОН уменьшает растворимость СаО
(что показано на рис. 106-2). Для производства бертолетовой
соли интересной является растворимость СаО <в растворах
Таблица 10. Растворимость СаО в воде при температуре 0—100° 6”2
Температура *С
10
20
30
40
60
60 70
80
90
100
Растворимость СаО
в г/л
1,34
1,29
1,22
1.12
0,98
0,88
0,78
0,74
\
—V—
0,70
^
0,60
Таблица 11. Растворимость СаО в водных растворах СаС12 при температурах 20—100°ш
Содержание
Растворимость СаО в г/д раствора при
CaCls
в г! л
20е
' 40е
60е
80е
100*
\
0
1,37
1,16
1,03
0,85
0,66
5
1,37
1,16
1,02
0,94
0,91
10
1.66,
1,42
1,31
1,33
1,39
15
\ /-
1,99
1,78
1.71
1.74
1,84
20
1,&
2,25
2,20
2,30
2,33
25
1,66
3,02
2,99
' 3,26
3,71
30
1,63
3,66
3,66
4,11
4,92
1 По системе СаО, СаС12, Н20 см. также J. Milikan, Zts. Physic, chem.
т. 92, 1917 г. и J. Апг. chem. $ос. 53, 3976, 1931 г.
40
СаСк, которую приводим в табл. 11. Весьма сильно повышается
растворимость СаО н поде при содержании в ней сахара.
В спирте растворяются лишь следы СаО. В глицерине растворимость СаО больше, чем в в<^де.
Таблица 11а. Растворимость Са(ОН)г в водном
растворе глицерина при 95°
% глицерина .
. . .
0
20,41
40,95
62,2
% Ca(OHXi
0,16
0,52
1,33
2,94
г) Гашение извести
Соединение СаО с водой называется гашением. Оно проходит с выделением тепла по следующему уравнению
СаО + НЮ = Са(ОН)2 + 15,5 ккал (28)
(на 1 г СаО выделяется 0,28 ккал). Подъем температуры при гашении извести тем больший, чем меньше избыток воды, взятой
для гашения.
При гашении теоретическим количеством воды (32,2% от
веса СаО) кусочки извести накаливаются так, что светятся в темноте. Поэтому, при неосторожном гашении
в присутствии горючих материалов часто
возникают пожары.
Активность извести
к гашению уменьшается с увеличением
количества примесей
в ней, а также при
слишком высокой температуре обжига. Наличие СаСк и некоторых других электролитов в воде, употребляемой для гашения, ускоряет процесс гашения.
Известь, соединяясь с количеством воды, близким к теоретическому, по уравнению 28 (оо 32% от веса СаО) образует Са(ОН)г,
распадаясь в порошок 4 «пушонку». Теоретически пушонка
должна состоять из 75,7% СаО и 24,3% НгО; практически в ней
всегда есть некоторый избыток СаО или НгО. Кроме того
в пушонке содержатся примеси, бывшие в извести до гашения.
Интересно отметить большое увеличение объема при получении
Загрузка
изоесаи
Выход пара и газов
Вода Выход пушонки.
зЩЩЩЩВц
у Ч\'
ж_х
Сшчатый цилиндр Вал
Рис. П. Схема аппарата Шультеса для получения
пушонки.
41
пушонки и тем большее, чем иыше была температура пниетш
(в 3—4 .раза больше объема взятой извести). е)то явление об.
ясипстся тем, что пары йоды, образующиеся внутри нор извес:
разрывают ее на очень мелкие частички.
Приготовление пушонки производится в аппарате Шультеса
(рис. 11). Полученная пушонка просеивается через сита для
отделения от более грубых частиц Са(ОН)г и примесей.
Хорошая пушонка должна на 80—90% пройти через сито
с 1500 отверстиями на 1 см-. Дисперсность пушонки особенно
важна также для р.о-номерности хлорирования при производстве
хлорной извести п т. п. Уд. вес кристаллического Са(ОН)г равен
2,1—2,2; насыпной вес 1 м3 составляет 0,5—0,8 т. Удаление воды
из Са(ОН)г происходит лишь при высокой температуре; например при атмосферном давлении разложение Са(ОН)г начинается
лишь при температуре выше 500°. На воздухе пушонка энергично поглощает СОг, превращаясь в СаСОз по уравнению
Са(ОН)2 + СОг = СаСОз + НгО. (29)
•При хранении пушонки часто смачивают ее верхний слой водой' для более быстрого превращения этого слоя в СаСОз, образующего корку, которая предохраняет остальную пушонку от
доступа воздуха.
Литература по известнякам и извести
А б е г г', Любавин1*, т. % ч. 1; Ост5* вып, 3, Гольштейн**,
-Лукьянов**, ч. I; ТЭ”, 8; Knibs Limeu Magnesia, London, 1924.
§ 3. Хлор
а) Получение хлора
Хлор в свободном состоянии в природе не встречается, но
весьма распространен в виде различных соединений (NaCl, КС1,
MgCb и др.), из которых его и получают химическим путем или
электролизом. Химические .методы получения хлора окислением
соляной кислоты по Вельдону или по Дикону в настоящее время
почти совсем оставлены и получение хлора производится почти
исключительно электролизом растворов хлоридов (чаще всего
растворов NaCl и в меньших количествах растворов КС1 и
MgCb). Из методов, применяемых для электролитического получения хлора, наиболее распространен диафрагменный метод,
схема которого показана на рис. 12. Реже применяется ртутный
метод, колокольный и другие методы электролитического получения хлора. Аппарат, в котором производится электролиз,
в заводской практике называется «ванной». При диафрагменном методе. применяются ванны Х-2, Ворса (рис. 13), Сименс-
Биллитера, Кребса и др.
42
*NaCl
Вода
PacmSopbt BaCjz о,Ча?С0$ Соляная кислота
Рис. 12. Схема получения С12> Н2 и NaOH электролизом раствора NaCl в ван*
нах с диафрагмой.
Вход
рассола л
}ргаз
Слабый
тик{кшпышт)
Рис. 13. Схема ванны Ворса для электролиза
раствора NaCl.
б) Физические и химические свойства
Элементарный хлор впервые получен Шееле в 1774 г. Дэви
подробно исследовал свойства хлора в 1808—1818 гг. При обычной температуре и атмосферном давлении хлор является газом.
Охлаждением и сжатием хлор сравнительно легко сжижается:
при 15° требуется сжатие до 6 ат, при атмосферном давлении
требуется охлаждение' до —33,6°. В технике хлор обычно сжижают одновременным охлаждением и сжатием.
Критическая температура хлора 146°, критическое давление
хлора 94 аг '(по Knietsch). Уд. вес газообразного хлора при 0° и
760 mi ртутного столба ранен 2,491 (по воздуху); удельный
жидкого хлора при 15° и 760 aim ртутного столба ранен 1/1267
воде). Коэфпцнент расширения газообразного хлора при 0—10
и 760 мм ртутного столба ранен 0,003832. Удельная теплоемкое:
газообразного хлора при постоянном давлении при температур
от 13 до 220° равна 0,1241 кал/кг, удельная теплоемкость жидком,
хлора равна 0,2262 кал в пределах температуры от 0 до 24
Скрытая теплота испарена:
на 1 г хлора равна 61,9 кт
при — 35,8°, 67,4 кал при
— 22° и 62,7 кал при +8' .
Растворимость хлора ь
воде сравнительно большая. Уступая NH3, НС1 и
БОг, хлор превосходит по
своей растворимости большинство других газов (1U,
Ог, N2 и т. д.) во много
раз. Чем выше температура
воды, тем растворимость
хлора в ней меньше, в кипящей воде хлор почти совсем нерастворим (табл. 12).
Наличие в воде электролитов большей частью уменьшает растворимость хлора.
Наличие в воде СОг и особенно НО увеличивает растворимость хлора: Во многих органических жидкостях хлор имеет большую растворимость.
Рис. 14. Растворимость хлора в воде и
в растворах NaCl при 0—100°.
Таблица 12. 'Растворимость хлора в воде при тем-
пературах 0—95°21
Температура
•С
Растворимость
хлора в
Температура
°С
Растворимость
хлора в
г/л
раствора
aJa воды
г/л
. раствора
AfA ВОДЫ
0
14,6
4,61
35
5,10
1,58
6
16,8
3,41
40
- 4,59
1,41
10 "
9,97
3,10
45
4,23
1,30
1 12
9,34
2,90
V 50
3,93
1,20
14
8,77
* 2,72
55
3,61
1,11
16
8,23
2,55
60
3,29
1,01
18
7,74
2,40
65
3,04
0,93
20
7,29
2,26
70
2,79
0,85
22
6,92
2,14
75
2,51
0,76
24
6,57
,2,04
80
2,23
0,67
26
6,26
1,94 *
85
1,75
0,53
28
5,97
1,85
90
1,27
0,38
30
t ф
5,72
1,77
95
0,64
0,19
44
В табл. 12 и на рис! 14 приведена растворимость хлора а ..о;;'’
и п растворах NaCl.
Растворенным в воде хлор гидролизуется по уравнению
(Яковкина)
С12 + Н20 НС1 + НСЮ. (30)
Реакция гидролиза хлора обратима и равновесие устанавливается медленно. Количество гидролизованного хлора зависит
от температуры и степени насыщения раствора хлором, хлоридом и соляной кислотой. Например в насыщенном водном растворе хлора при 0° гидролизуется 33% хлора, а при 33° гидролизуется уже 83% хлора. Таким образом в водных растворах
хлора обычно содержатся и хлор и продукты гидролиза (НС1
и НСЮ). При хранении растворов хлора на свету НСЮ разлагается, выделяя 02 по уравнению
2НСЮ — 2НС1 + Ог. (30а)
Через некоторое время в такой воде остается только НС1.
При хранении без доступа света, но в открытом сосуде, хлор
постепенно выделяется из раствора, отчего реакция (30) проходит справа налево, и через некоторое время в такой воде нельзя
уже обнаружить ни хлора, ни НСЮ, ни НС1. Однако последние
следы хлора удаляются весьма медленно (см. стр. 94, рис. 47).
Из воды, насыщенной хлором, выделяются при охлаждении
желтые игольчатые кристаллы хлоргидрата состава СЬ • 8Н20
уд. веса 1,22—1,24. При нагреве хлоргидрат разлагается на
хлор и воду. Высшей температурой существования кристаллов
хлоргидрата при атмосферном давлении является 9,6°. При давлении, большем чем в 1 ат, хлоргидрат может существовать и
при более высокой температуре, но не выше 28,7°.
Влажный хлор весьма активен и непосредственно соединяется
со всеми элементами кроме углерода. Металлический натрий,
тонкие листочки меди и порошок сурьмы загораются в атмосфере хлора, сгорая в NaCl, CuCl2 и SbCb. Так же горят в атмосфере хлора скипидар и некоторые другие органические вещества. Органические краски большей частью обесцвечиваются
хлором. После длительного действия хлора на материю она
расползается при малейшем натяжении. В смеси с водородом
хлор под действием солнечных лучей взрывается (см. стр. 328).
С кислородом хлор образует многочисленные соединения, которые можно классифицировать следующим образом: 1) хлорноватистая кисло'Га (НСЮ) и ее соли, 2) хлористая кислота
(НС102) — известны только некоторые ее соли (КСЮ2 и т. д.);
3) двуокись хлора (СЮ2 или С1204) — соединения ее неизвестны;
4) хлорноватая кислота (НСЮз) и ее соли; 5) хлорная кислота
(HCIO4) и ее соли. В противоположность некислородным соединениям хлора (NaCl^ К Cl, MgCl2 и т.. д.), в которых хлор
имеет один отрицательный заряд, в кислородных соединениях
хлор заряжен положительно и имеет от -одного заряда (НСЮ)
ДО семи зарядов (HCIQ4). .Чем выше валентность хлора в его
/
45
Таб.шца 13. Физические и химические свойства газов, входящих в состав хлоргаза 30
Хлористый
Углеки¬
На именование
Хлор
водород
слый газ
Кислород
[Водород’
Азот
Воздух
Вода
Формула ......
CI*
НС1
со3
02
н2
N*
—
Н,0
Молекулярный вес .
70,92
36,46
44
32
2,016
28,02
-
18,016
Плотность (воздух = 1
; 0°; 760 мм)
2,491
1,268
1,529
1,106
0,0695
0.9S73
1,0
0,6219
Вес 1 л газа в граммах при 0° и
1,29
0,804
760 мм ......
3,22 ‘
1,64
1,98
1,43
0,09
1,25
Объем 1 г газа в литрах при 0°
0,800
0,773
1,243
и 760 мм .....
0,311
0,610
0,506
0,700
11,125
Давление паров сжиженного газа
0,017
при 15° в am . . .
5,75
40
52,17
—
—
—
—
Температура кипения в
°С при760.*лм
—33,6°
—83°
О
ОО
Г>-
1
—183°
—253°
—i£6°
—
100°
Температура плавления в °С ...
—102°
—14°
—65°
—227°
-258°
—210°
О3
Критическая температура в °С . .
+146°
+51°
о
м
со
+
—119°
—242°
—146°
—140,6°
-f3co2
Критическое давление
в am ... .
94
83
73
50,8
14
35
—
200
Уд. вес жидкого газа при 15° (вода
1,0
при 4- = I) . . . .
1,4273
—
0,814
1,006
—
—
—
Растворимость в воде
(объемоз газа в
о
О
О.
с
3,095
—
1,19
0,03S
0,020
0,020
0,023
-
1 объеме боды при
760 мм)
. 100а . . !
1
0
—
—
0,017
0,016
0,010
0,011
.
кислородных соединениях, тем последние.являются более устойчивыми (исключая соединения хлористой кислоты и двуокиси
хлора).
в) Состав хлор га за
Для получения хлоратов обычно пользуются электролитическим хлором. Последний об:.:содержит кроме СЬ еще ряд
примесей и называется х ;< • ..ом. Состав и количества примесей зависят от метода и > с;й производства хлора. Обычно
наибольшей примесью, содержащейся в хлоргазе в широких
пределах, является примесь атмосферного воздуха, т. с. азот
и кислород (от 1—2 до 50—90%). В меньших количествах, но
также в широких пределах от десятых долей до целых процентов, содержатся СОг и Нг. В сотых долях процента содержится влага, количество которой зависит от способа сушки
хлоргаза. При отсутствии сушки количество влаги в хлоргазе
зависит от температуры, поскольку хлоргаз выделяется при
электролизе из водного раствора NaCl.
' В табл. 13 приведены физические и химические' свойства
газов, входящих в состав хлоргаза. В табл. 14 приведена зависимость некоторых величин от процента СЬ в хлоргазе.
Наличие СОг, Нг и Ог в хлоргазе, применяемом для получения хлоратов, является вредным. СОг, содержащийся в хлоргазе, реагирует при хлорировании с Са(ОН)г, образуя осадок
СаСОз, что увеличивает содержание шлама в хлорированном
щелоке (стр. 99). Водород и кислород, содержащиеся в хлоргазе, могут образовать взрывчатые смеси в абгазе, получающемся после хлорирования (стр. 328). При содержании в хлоргазе Нг, процент последнего в абгазе тем больше, чем выше
процент С1г в хлоргазе (стр. 89). При хлорировании методом
Таблица 14. 3 а в и с и м о с т ^некоторых величин о'т процента С i
в хлоргазе
Объемный
процент
С1я
Весовой
процент
С12
1 м* хлоргаза
весит
кг
На 1 т хлора получается
хлоргаза
абгаза
т
м»
т
м»
100
100
3,220
1,00
311
90
95,6
3,027
1,045
346
0,045
35
80
90,9
2,835
1,101
389
0,101
. 78
70
85,3
* 2,643
. 1,172
444
0,172
133
60
78,7
2,449
1,268
519
0,269
208
50
71,4
2,256
1,403
622
0,403
311
40
62,3
2,063
1,604
778
0,604
467
30
51,5
1,870
1,939
1037
0,94
725
20
38,4
1,677
* 2,610
1554
1,61
1243
10
21,7
1,485
4,620
3110
3,62
2799
Примеч а н не. При расчетах принято, что в основном хлоргаз содержит
хроме хлора только воздух.
47
поверхностного поглощении хлора (стр. 77—79) процесс проходит тем полнее и быстрее, чем выше процент СЬ и хлор-
газе. При хлорировании методом барботажа (стр. 80) полнота
поглощения хлора мало зависит от процента СЬ в хлоргазс.
Чем ниже процент СЬ в хлоргазе, тем больше загрузка компрессоров для перекачки хлоргаза и вентиляторов для отсасывания абгаза при любом методе хлорирования.
г) Перекачка хлоргаза
Влажный хлоргаз можно передавать по керамиковым или
свинцовым хлоропроводам. Керамика вполне устойчива против
влажного хлоргаза, но она хрупка и ее невозможно чинить при
поломках. Свинцовые хлоропроводы приходится обычно подвергать капитальному ремонту через б—9 мес. *
Применяя хлоргаз, освобожденный от влаги пропусканием
через башни, орошаемые серной кислотой, можно употреблять
железные хлоропроводы и чугунные вентиляторы и компрессоры. Количество влаги в высушенном хлоргазе не должно превышать 1—1,5 r/л®. При таком содержании влаги коррозия
хлоропроводов незначительна. Раз в несколько месяцев хлоропроводы приходится очищать от продуктов коррозии и загрязнений, оседающих хлоргаза.
- Литература по производству и свойствам хлора
Г и е л и н \ №. 6; А б е г г •, т. 4, ч. 2, Б и л л и т е р “, **, 1S; С а с с-Т и с-
с о в с к и й **; Генин и др. Г. Ангел**.
§ 4. Хлористый калий
а) Получение хлористого калия
В природе КС1 встречается в значительных количествах, но
меньше и реже, чем NaCl (например в морской воде содержится
2,8% NaCl и только 0,06% КС1). До мировой войны КС1 добывался почти исключительно в Германии (Стасфуртское и Эльзасское месторождения). Во время войны ряд стран начал изыскания собственных калийных месторождений. В данное время
кроме Германии КС1 добывается в значительных количествах
во Франции (Эльзас), Испании, Польше, США, а в меньших количествах еще в некоторых других странах. В СССР, в 1925 г.
были открыты Соликамские месторождения КС1/ оказавшиеся
богатейшими в мире и дающие уже в настоящее время весьма
значительное количество КС1.
Кроме Соликамска в СССР открыты еще месторождения
в Средней Азии, хотя и менее значительные.
Добыча калийных солей обычно производится шахтным способом. КС1 — в большинстве месторождений содержится в виде
разных минералов, чаще всего в виде сильвинита и карналита.
* В последнее время в практику стали входить трубопроводы из текстолита—вполне устойчивые против действия хлора. Прим. ред.
48 /
Получение KCI из этих минералов основано на разной pan коримое™ КС1 и других составных частей этих- минералов а иоде
■при разных температурах.
Больше 90% мировой добычи КС1 потребляется как удобрение в сельском хозяйстве. В промышленности КС1 применяется
для получения ряда калийных соединений, для получения хлора
электролизом и т. д.
Технический хлористый калий содержит обычно ряд примесей (соединенна Мд, SO.i, Na, Вг и др.). Хлористый калий, применяемый в производстве бертолетовой соли,, должен содержать
минимум примесей, так как последние загрязняют полупродукты
и даже готовую соль.
„ б) Физические и химические свойства
КС1 образует бесцветные, прозрачные кристаллы кубической
формы, не содержащие кристаллизационной воды и на воздухе
постоянные. Удельный вес КО 1,95—2,0. Насыпной вес технического хлористого калия зависит от величины кристаллов и
их уплотненности в таре и обычно колеблется в пределах 1,0—1,2.
Температура плавления КО 768°, температура кипения КО 1415°.
Теплота образования КО из элементов равна 105,6 ккая на 1 моль.
При растворении 1 моля КО в 200 молях НгО поглощается
4,4 ккая. Удельная теплоемкость хлористого калия равна
0,1616 кая. Теплоемкость 22,7%-ного раствора КО равна
0,753* кая. Температура замерзания раствора, содержащего
243,9 г КО в 1 кг НгО, равна —10,66°, а температура замерзания
раствора, содержащего 148,3 г КС1 в 1 кг НгО равна —6,46°.
Таблица 15. Плотность и концентрация растворов КС1, н а-
сыщенных при температурах отОдо 108°5
Темпера*
Содержание КС1
г Н,0 на 1 г
Плотность
т*рс‘
°/о
г/кг Н.О
г/л раствора
КС1
уд. вес
°Боме
1
2
3
4 1
! ■
6
7
0
21,9
280
252
i
3,6
1,153
\
19,1
10
23,9
313
278
3,2
1,165
20,3
20
25,7
345
301
2,9
1,174
21,4
30
27,3
375
322
2,7
1,182
22,2
40
28,8
404
342
2,5
1,188
22,8 *
50
30,1
431
360
2,3
1,194
23,4 -
60
31,4
458
376
2,2
1,198
23,8
70
32,6
484
392
2,1
1,202
24,2
80
.33,7
509
406
2,0
1,205
24,5 '
90
&4,8 ,,
534
420
1,9
1,207
24,7
100
35,9
560
434
1,8
1,210
25,0
108
36,8
581
446
1,7
1,212
25,2
4. Зав. 179. — Шрайбхак.
t
49
По растворимости КС1 можно отмести к срслпорастворнмым
солям. При 'повышении температуры растворимость 'Л увеличивается (табл. 15). Присутствие в растворе NaCl, GiCb, K-SO4
или других соединений калия значительно уменьшает растворимость КС1 (табл. 31, стр. 126). В спирту .растворяются лишь
следы КС1.
Литература по хлористому калию и его свойствам
А б б е г * т. 2, ч. I; Д а м м е р ч, т. 3; Любавин и, т. 2; ТЭ. г". т. 9;
Иольфкович34; Ульман6, т. 6
ГЛАВА 3
ПОЛУЧЕНИЕ ИЗВЕСТКОВОГО МОЛОКА
§ 1. Приготовление известкового молока
*
Приготовление известкового молока состоит в смешивании извести с водой, отчего происходит гашение СаО
в Са(ОН)г и образование
взвеси Са(ОН)г в воде.
Кустарное приготовлен
ние молока в различных
мешалках — баках в настоящее время оставлено и заменено непрерывно действующими аппаратами. Примером такого аппарата. является
аппарат Мика, применяющийся на многих
заводах для приготовления известкового молока. Такой аппарат изображен на рис. 15.
Аппарат представляет
собою клепаный или
сваренный железный цилиндр, расположенный горизонтально
с небольшим уклоном к выходу-известкового молока. Цилиндр
. установлен на роликах и вращается со скоростью 8—12 об/мин.
■В центре задней крышки цилиндра имеется отверстие /, куда
вставлена неподвижная воронка для ввода в аппарат воды и
извести. Внутри цилиндра по спирали насажены пластины, помогающие перемешиванию и передвижению молока-. В передней крышке аппарата имеется отверстие (£» — 0,5—0,7 м), через
которое выливается известковое молоко. Приемником молока
служит неглубокий неподвижный цилиндр 2 большего диаметра,
Рис. 15. Аппарат1 Мика для приготовления
известкового молока.
1 — отверстие для загрузки извести и воды, 2 — неподвижный цилиндр-приемник молока, 5 —штуцер (для
выхода молока, 4 — труба дла отвода пара.
чем основной цилиндр аппарата, окружающий переднюю часть
последнего. Из цилиндра-приемника молоко иытекаот но штуцеру 3 в жолоб или трубу и дальше поступает на очистку.
Образующиеся при гашении нары НаО отводятся через
отверстие 4, над которым делается вытяжка в атмосферу вне
здания.
Остающиеся в аппарате куски недопала вычерпываются ковшами, имеющимися в передней части основного цилиндра аппарата. Периодически в переднюю часть аппарата вставляется
лоток, на который при вращении аппарата падают куски нсдо-
пала из ковшей.
Размеры аппарата Мика зависят от желательной производительности и большей частью колеблются в следующих пределах:
длина 3—6 м, диаметр 0,9—1,2 дг. Производительность такого
аппарата равна от 10 до 30 лг> известкового молока в час.
Регулирование концентрации известкового молока производится особыми приспособлениями для подачи извести и воды.
Для этого перед приемной воронкой Мика располагают особый
прибор, при изменении величины эксцентрика и числа оборотов
которого изменяется количество задаваемой извести. Количество
воды лучше всего регулировать циферблатным краном и т. и.
Кроме того, необходимо как можно чаще проверять плотность
выходящего из аппарата известкового молока (см. рис. 21,
стр. 57).
Согласно уравнению (28) реакция гашения извести экзотср-
мична: на 1 моль СаО выделяется 15,5 ккад (на 1 г СаО выделяется — 0,28 ккад). Но все же приготовление молока производится на горячей воде, так как чем выше температура молока,
тем меньше его вязкость и тем легче протекает очистка.
Поскольку СаСЬ ускоряет гашение извести и использование перепала, а также улучшает последующее хлорирование известкового молока (стр. 64), то для приготовления молока используются
жидкости от выщелачивания шлама, остающегося после хлорирования (стр. 99); и др. производственные промывные воды.
6 описанном аппарате Мика может быть приготовлено известковое молоко с концентрацией СаО до 250—300 г/д. Однако
в целях лучшей очистки известкового .молока высокой концентрации его иногда готовят отстоем известкового молока слабой
концентрации в особых баках-отстойниках или взбалтыванием
в воде гашеной извести-пушонки (см. рис. 18, 19, 20- стр. 55).
§ 2. Очистка известкового молока
Известковое молоко, полученное в аппарате Мика (рис. 15),
обычно содержит ряд примесей (см. ниже § 5, стр. 56), которые
обусловливают образование шлама при последующей стадии
хлорирования известнякового молока; поэтому известковое молоко должно подвергаться «очистке» от нерастворимых примесей.
Очистку известкового молока производят, используя разный
удельный вес Са(ОН)г и большей части примесей, либо разную
51
4#
величину частиц Ca(OI l)j * и примесей. Чем ниже копнет рации
СаО в молоке и выше температура известкового молока, тем
меньше вязкость и легче очистка молока. Молоко, приготовленное из пушонки (рис. 20), нс требует очистки; так как большая
.часть примесей отделяется при приготовлении пушонки просеиванием последней (стр. 42). При очистке молока слабой концентрации часто применяется аппарат, изображенный на рис. 16
(аппарат Русселя). Аппарат представляет собой открытое корыто
длиной в 2—2,5 м, шириной ~ 1 м и глубиной 0,7—0,8 м, разделенное перегородками 2 на несколько секций. Вдоль аппарата проходит вал 3, делающий-1—1,5 об/мин. На валу насажены лопасти
двух родов, по две в каждой секции. Более короткие лопасти 4
перемешивают молоко, чтобы оно нс расслаивалось; более длинные лопасти 5, особой формы, доходят до дна каждой секции
и выгребают осевшие более тяжелые частицы примесей, перебрасывая их в следующую секцию в направлении, обратном ходу
молока. Из секции, где молоко входит в аппарат, лопасть выбрасывает примеси в пустое отделение аппарата б, откуда они
шнеком 7 подаются в вагонетку для вывоза в отвал. Молоко,
пройдя все секции, освобождается от примесей и проходит в последнюю секцию, где уже нет лопастей и где, пройдя еще особую решетку, выходит через штуцер 8 в приемный бак.
Для очистки известкового молока высокой концентрации
аппарат Русселя не подходит, так как благодаря значительной
вязкости концентрированного молока большая часть примесей
не оседает на дно секции аппарата Русселя. На содовых заводах очистка известкового молока высокой концентрации -производится пропусканием его через целую систему очистных
аппаратов, построенных на принципе отделения примесей на
ситах и оседания примесей.
Известковое молоко из аппаратов для приготовления — «диссольверов» -поступает в дырчатый барабан, имеющий отверстия
диаметром в 5—10 мм и заключенный в железный кожух. Барабан насажен на вал и вращается со скоростью 5—10 об/мин.
Кожух барабана неподвижен. Примеси молока в виде кусочков
больше 5—10 мм остаются в барабане, откуда выгребаются
особым устройством. Молоко и более мелкие примеси проходят
через отверстия барабана в кожух, откуда по жолобу или по
сливной трубе -переходят в следующий «сетчатый» барабан. Этот
барабан вращается со скоростью 20—30 об/мин. и тоже заключен в неподвижный кожух. Сетка этого барабана имеет отверстия диаметром в 1—2 мм; для большей прочности сетка заключена между двумя более толстыми сетками с большими отверстиями. В этом барабане удерживаются мелкие примеси. Известковое молоко, прошедшее через сетчатый барабан, содержит
уже лишь очень мелкие примеси. Для их отделения известковое
молоко пропускается последовательно через несколько шодье-
ров-цилиндров с конусным дном. Известковое молоко поступает
по трубе в нижнюю часть цилиндра шодьера и выходит через
* Размер частиц Са(ОН)а составляет б. ч. ~ 1 микрона.
52
штуцер нверху шодьера. Мелкие примеси изнесткомого молока,
имеющие удельный изес больше чем Са(ОП):», оседают и конусе
шодьера. Чтобы молоко в шодьерах не расслаивалось, чнодьеры
снабжены мешалками, делающими 5—10 об/мин.
Так как чем выше температура, тем легче очистка известкового молока, кожуха дырчатого и сетчатого барабанов и
шодьеры должны иметь тепловую изоляцию. Периодически
сетки барабанов промываются водой. Для отделения примесей
могут также применяться классификаторы Дорра или другие
Рис. 16. Аппарат Русселя для отделения примесей
известкового молока.
1 — корыто аппарата, 2 — перегородки, разделяющие корыто на
секции, 3 — вал, 4 — короткие лопасти для перемешивания молока,
5 —лопасти, выгребающие осевшие примеси, б—последняя секция
аппарата, 7 — шнек для выгребания шлама, 8 — выход чистого
молока, 9— привод.
подобные аппараты. Шлам из конусов шодьеров и примеси,
отделяемые в барабанах, собираются в особый бак-выщелачиватель, где промываются горячей водой от Са(ОН)г. Полученное
от промывки слабое известковое молоко перекачивается на приготовление обычного молока, а промытый шлам отвозится как
отброс.
§ 3. Хранение, охлаждение и перекачка известкового молока
Очищенное известковое' молоко перекачивается в баки-хранилища, служащие для расхода молока на хлорирование. Объем
этих баков должен быть достаточно большим, чтобы создать
резерв на случай остановки в приготовлении или перекачке
известкового молока. Эти же баки служат для охлаждения молока. Это охлаждение необходимо производить потому, что
известковое молоко после очистки имеет температуру в 50—60°,
а на хлорирование оно должно поступать с температурой
в 15—20°. Поэтому эти баки оборудуются кожухами
или змеевиками, для охлаждающей воды. Чтобы молоко не
расслаивалось яри хранении, баки должны иметь мешалки,
которые делают 5—1Q об/мцн. Баки могут служить также для
53
дополнительного отстоя известконого молока от примесей, д.:и
чего их делают подобными вышеописанным шодьерам. Молоко можно передавать непрерывно через последовательный ряд
баков.
Перекачка молока осуществляется обычно центробежными
насосами. Коррозия насосов и трубопроводов от известкового
молока почти совершенно нс наблюдается. В местностях с низкой зимней температурой трубопроводы для перекачки молока
надо ставить в утепленной эстакаде или галерее, так как температура замерзания известкового молока близка к 0°. На случай
засорения и т. п. необходимо подвести к трубопроводу известкового молока воду для промывки и воздух для продувки.
§ 4. Схемы приготовления и очистки известкового молока
На рис. 17 показана схема получения известкового молока
с концентрацией СаО в 100—120 г/л. Полученная в известковой
печи известь отделяется на грохоте от мелочи, содержащей
обычно много примесей (зола • топлива в пересыпных печах,
перепал и т. д.). Куски извести подаются в аппарат Мика, куда
поступают также горячая вода, производственные промывные
воды и жидкость от выщелачивания известкового шлама. Полученное известковое молоко отделяется на аппарате Русселя
или ситах от примесей, после чего поступает в баки для охлаждения. Отделенные примеси поступают в выщелачиватель, где
выщелачиваются горячей водой. Жидкость от выщелачивания
возвращается на приготовление молока, а выщелоченный шлам
отвозится как отброс.
На рис. 18 показана схема получения известкового молока
с концентрацией СаО. в 220—240 r/л. Приготовленное молоко
отделяется в дырчатом барабане от крупных примесей, затем
в сетчатом барабане от мелких примесей и наконец в шодьерах
от наиболее мелких примесей, после чего поступает на охлаждение. Примеси, отделенные в дырчатом и сетчатом барабане и
в шодьерах, поступают в выщелачиватель, где горячей водой
выщелачивается Са(ОН)г.
На рис. 19 показана схема получения известкового молока
высокой концентрации, исходя из отстоя молока низкой концентрации. Молоко низкой концентрации, полученное в аппарате
Мика, имеющее небольшую вязкость, очищается от примесей
в аппарате Русселя или ситах, после чего поступает в баки-
отстойники, служащие и для охлаждения .молока. При отстаивании молоко расслаивается на более концентрированное молоко
и известковую воду (содержащую СаО 1—1,5 г/л). В соответствии с анализом начального молока и объемом баков, из них
спускают часть известковой воды (используемую снова на приготовление молока слабой концентрации), а воду и концентри-
рованное молоко, оставшиеся в баках, перемешивают и расходуют
на хлорирование. Например если в начальном молоке содержалось СаО 90 г/л, а объем бака 30 я3, надо спустить
54
90 • * »0 t о • > •» ^
30 .,3(j-~l8,3 лг* известковом поды, чтооы перемешанный
остаток содержал СаО 230 г/л.
На рис. 20 показана схема приготовлении известкового молока высокой концентрации из пушонки. Полученная из печи
ПзбестЬ из печи
Горячая вода Производственные
\ Охлажденное очищенное
молоко
известкоВЫй шлам
Горячая
** вода
Рис. 17. Схема приготовления и очистки известкового молока
слабой концентрации.
известь, отделенная от мелочи, гасится в аппарате Шультеса
(рис. 11, стр. 41) водой в количестве несколько выше теоретически необходимого для образования Са(ОН)г из СаО. Охла-
UxBecthb Горячая Вода и производственные
шлал! молоко
Рис. 18. Схема получения известкового молока высокой концентрации.
жденная пушонка взбалтывается с водой в таком отношении,
чтобы получить молоко нужной концентрации.
Основным недостатком схемы, показанной на рис. 18, является
трудность поддерживания стандартности. концентрации извест-
55
кового молока и сложность и ненадежность полноты удалении
примсссн из молока. Схемы, показанные на рис. 19—20, гораздо
больше обеспечивают стандартность концентрации и хорошую
ЦэбестЬ
Горячая вода и проиоводствешФге промЫвнЬ/е 6одЫ
Избыток известковой воды
I ПромЫтЬш извасткоСЫи
шлам
Рис. 19. Схема получения известкового молока высокой концентрации отстоем молока низкой концентрации.
Рис. 20. Схема получения известкового молока высокой концентрации из пушонки.
очистку молока. При схеме, показанной на рис. 20, кроме того
отпадает необходимость подогрева основной массы воды, расходуемой на приготовление .молока, и отпадает необходимость
охлаждения молока.
\
% § 5. Состав известкового молока
Известковое молоко представляет собой взвесь Са(ОН)»
в известковой воде. Последняя содержит растворенный Са(ОН)«
в количестве 1—1,5 г/Л (стр. 40). Концентрация Са(ОН)* в известковом молоке может вариировать в широких пределах—до
300—350 г/л. Зависимость удельного веса молока от содержания
СаО в г/л (при 20°) показана на рис. 21. Для пересчета на содержание Са(ОН)г надо 'данные для СаО умножить на 1,321.
56 ’
10 —
1 — 1,010
го—:
— Ц020
30
40 ‘
I
§ “Г
50-
*§
§
<§
з
60 •
4 =:
о - -
5 "4
1
о
%
§*
•5 30-
<2
90-
100-
’V» ч
Оч
*
5.
•1,040 1,1
' с-
%
■ i
г
•1,050 £ „
5
I
WO
:Г^
г/л. i/3J
ido -j -
1 '
j}-
“1.030
HO
110 —
130 — .
-5 140
!'
Q
ty
I ^50
i
з £
•SJ60
ч»
<a
«2
s>
g 170
О
a
480-
190 ■
200-
-ifiM
ЧЮО
t
_ о»
*
rJ-<,»o 3»
s
5
-1Д0 §■
<\>
О
1 1
•1,130
■U40
г/л.
200-
210 —
220-i:
230 —
<3
о
§
240-
ч =:
iso—;
*2
$
о
«8
2
>$
> 230-
4>
Ъ
C>
* 270-
I
3- i:
ZBO-zГ
200-:
-
500-3^
i,d.s.
-1,150
•1,160
■1,170
&
*
c:.
S*
(a
S>
О
-1-1,190 5
*
§
о
S?
--*,20Q
-f,2<0 •
U20
Рис. 21. Содержание СаО в известковом молоке разного
уд. веса при 20°.
57
(Госта» приMccci't известкового молоки зависит иг спайка
извести (стр. 39) и воды или производственных .промывных вод,
применяемых для приготовления .молоки, и от тщателмтсти
очистки молока. Частично в известковом молоке может образоваться СаСОз под влиянием СО-» воздуха. По нашим наблюдениям при нормальном обжиге известняка Волжских месторождений в неочищенном известковом молоке невысокой концентрации содержание нерастворимых примесей (СаСОз, песок,
частично CaS04) составляло от 3 до 8% от количества
СаО, содержащегося в молоке. В этом же известковом молоке,
содержащем СаО 100—110 г/л, после очистки молока пропусканием через сито с 100 отверстиями на 1 см- оставалось примесей в количестве 0,5% от количества СаО.
Чем выше концентрация известкового молока, тем больше
его вязкость. Вязкость известкового молока зависит также
от температуры обжига извести, из которой приготовлено
молоко, и от температуры приготовления молока. Чем выше
температура обжига и ниже температура приготовления известкового молока, тем меньше вязкость молока; соответственно*
вязкости меняется и быстрота расслаивания молока. Молоко,
приготовленное из пушонки, имеет очень малую вязкость и
весьма быстро расслаивается на известковую воду и молоко,
содержащее СаО 300—350 г/л. Молоко, приготовленное из извести, полученной при обжиге при 1000—1100°, и горячей воды,
имеет сметанообразную консистенцию и расслаивается весьма
медленно.
ГЛАВА I4
ХЛОРИРОВАНИЕ ИЗВЕСТКОВОГО МОЛОКА
Получение хлорированного щелока является основной стадией производства бертолетовой соли; при хлорировании происходят основные химические процессы и образование хлората.
Поэтому мы останавливаемся более подробно на изложении
теории процесса, описании аппаратуры и режиме работы этой
стадии процесса.
§ 1. Процессы хлорирования
а) Химические реакции, происходящие при
хлорировании
Хлорирование известкового молока заключается в реагировании хлора с Са(ОН)г. Исходя из данных, полученных рядом
исследователей, занимавшихся изучением процессов хлорирования (Бертолле, Гей-Люссак, Либих, Муспрат, Лунге и особенно
Ферстер и его ученики), реакции, происходящие при хлорировании, можно представить следующим образом.
58
При поступлении хлора в известковое молоко прежде всею
происходит растворение хлора в воде и гидролиз его:
С\> + Н20 = НСЮ + НС1. (30)
Образующиеся НСЮ и НС1 сейчас же нейтрализуются растворенным Са(ОН)г:
2НСЮ + Са(ОН)2 = Са(СЮ)2 +2Н20. (31)
2НС1 + Са(ОН)2 = СаСЬ + 2Н»0. (32)
По мере реагирования растворенного Са(ОН)2 по уравнениям (31) и (32) новое количество взвешенного Са(ОН)2 переходит в раствор, и поглощается новое количество хлора. Так
продолжается до прореагирования всего Са(ОН)2> содержавшегося в известковом молоке. Продолжающий после этого поступать хлор образует новое количество НСЮ и НС1, которым уже
нечем нейтрализоваться, отчего в хлорируемом щелоке создается
слабокислая среда. В такой среде Са(СЮ)2 окисляется хлорноватистой кислотой в хлорат:
Са(СЮ)2 + 4 НСЮ = Са(СЮз)г + 4НС1 (33)
Образующиеся 4НС1 тоже реагируют с Са(СЮ)2, образуя
малодиссоциированные молекулы НСЮ:
2Са(СЮ)2 + 4НС1 = 2СаС1» + 4НСЮ. (34)
Образовавшаяся НСЮ окисляет новое количество Са(СЮ)2
по уравнению (33). Так продолжается до тех пор, пока весь
Са(СЮ)2 не перейдет в Са(СЮз)г и СаС1*. Таким образом сама
НСЮ не тратится на образование хлората и является как бы
переносчиком кислорода.
Из приведенных реакций видно, что хлорирование проходит
в 2 стадии. Пока в жидкости еще есть Са(ОН)2, происходит
образование гипохлорита и хлорида по следующему суммарному уравнению [реакции (30), (31) и (32)]:
2Са(ОН)2 + 2СЬ = Са(СЮ)2 + СаС12 -+- 2Н20. (35)
Вторая стадия начинается после того как весь Са(ОН)2 прореагировал и в жидкости получилась свободная НСЮ. Эта
стадия может быть выражена. следующим суммарным уравнением реакций (33) и (34):
ЗСа(СЮ)2 = Са(СЮз)2 -+- 2СаС12. . (36)
Общее уравнение образования хлората при хлорировании будет:
6Ca(OH)8 + 6С12=Са(СЮ8)2 + 5СаС12 + 6Н20. (37)
Практически кроме указанных реакций происходит еще образование кислорода вследствие разложения гипохлорита:
Са(СЮ)2 СаС12 -}- 02. (68)
59
Хлорат тоже может разлагаться с выделением кислорода, но
в условиях хлорирования этого почти незаметно. Суммарное
уравнение выделения 02 при хлорировании, исходя из реакций (35) и (38), будет:
2Ca(OH)s + 2CU = 2СаС1> + 2Н-0 + 02. (39)
•Примечание. П ' д гипохлорита в хлорат и хлорид по уравнению (36) может про не только при получении кислой среды от
введения избытка хлор. от подкисления щелока, содержащего гипо¬
хлорит, любой кислотой. . леи степень диссоциации больше 11СЮ (каковыми являются болып.i:i-v iI кислот). При демонстрации такого опыта
надо брать отстоявшийся щелок, слитый с осадка Са((>Н)г, и прибавлять
разбавленную кислоту (НС!, HsSO«, CHsCOOH и т. д.) по каплям при перемешивании щелока до появления слабого запаха хлора. При быстром при-
ливании кислоты гипохлорит разлагается с образованием хлора согласно
реакции
Са(СЮ)* -Ь 4НС1 = СаСЬ +> 2СЬ + 2НЮ. (40)
Подкисление щелока можно также производить пропусканием через щелок СОг.
б) Факторы, влияющие на образование хлората
и на выделение кислорода при хлорировании
Основным фактором образования хлората является перехло-
рирование, т. е. создание слабокислой среды введением в хлорируемый щелок избытка хлора. Вторым фактором образования хлората является температура, так как чем выше температура, тем быстрее проходят реакции
суммарного уравнения (36).
Скорость перехода гипохлорита в хлорат в щелоке, содержащем ,НСЮ, может
быть'' выражена уравнением
— = К- [СЮ'] • [НСЮ]2,
где К — константа скорости реакции,
[СЮ'] — концентрация аниона гипохлорита в экв/л,
[НСЮ] —молекулярная концентрация
хлорноватистой кислоты.
На рис. 22 приведена диаграмма Книббса,116 выражающая зависимость К от температуры.
Однако повышение температуры, ускоряя реакцию (36), увеличивает также выделение 02 по уравнению (38). Оптимальной
температурой стадии образования хлората является 75—80°.
При этой температуре выделение 02 минимально.
В присутствии щелочи образование хлората может иметь
место лишь как побочный процесс для незначительной части
гипохлорита, сопровождаясь разложением гипохлорита с выделением кислорода по уравнению (38). Чем выше температура,
тем в щелочной среде больше разложение гипохлорита по урав-
60 '
—у
А Ь-Нгт I I I I J
4в* 50* 60* 70* 80* ЯГ
Температура
Рис. 22. Диаграмма скорости перехода СЮ' в
СЮ3' по Книббсу.
пению (36) и (3S). При низкой температуре разложение гипохлорита в щелочной среде незначительно.
Разложение гипохлорита с выделением О» по уравнению (38)
усиливается от наличии некоторых примесей, могущих содержаться в хлорируемом щелоке. Такими свойствами обладает
большинство соединений тяжелых металлов. Особенно усиливает
выделение О» кобальт и его соединения. Влияние таких примесей также усиливается с повышением температуры.
Содержание в известковом молоке СаСЬ (или других хлоридов) уменьшает выделение О» при прочих равных условиях
хлорирования (табл. 17, стр. 64).
Примечание. Выделение Ог при хлорировании можно хорошо наблюдать при следующем опыте. Хлорирование производят барботажем
хлора через известковое молоко. Из сосуда, в котором производится хлорирование (колбочка и т. и.), абгаз отводится в цилиндр для сбора газов,
наполненный раствором NaOH. Для хлорирования применяется хлор из
баллона, почему абгаз состоит только из Ог. Могущие проскочить CI* и
СОг поглощаются раствором NaOH и в цилиндре собирается чистый кислород, в чем можно убедиться последующим анализом. По количеству и времени появления газа в цилиндре и судят об интенсивности выделения О»
лри хлорировании (методика данного опыта разработана И. Б. Фрайманбм).
в) Тепловой эффект хлорирования
Суммарные уравнения обеих стадий хлорирования (стр. 59)
показывают положительный тепловой эффект. Ниже приводим
расчет количества выделенного тепла при хлорировании, исходя
из теплоты образования исходных и .получающихся веществ
[величины, взяты согласно СТЭ28, т. VII, кроме данных для
Са(С10з)г, найденных автором].
Тепловой эффект 1-й стадии хлорирования:
6Са (ОН), Н- 6С12 = ЗСа (СЮ),+ЗСаС12+6Н20 (35»)
6-236,2 3-181,5 3-206,5 6-68,5
Теплота образования исходных веществ равна 6-236,2 =
= 1417,2 ккая. Теплота образования получающихся веществ
равна
3 • 181,5 + 3 - 206,5 + 6 • 68,5= 1575 ккая.
Тепловой эффект равен 1575 —1417,2=157,8 ккая.
Тепловой эффект второй стадии хлорирования:
ЗСа (СЮ)2 = Са (СЮД+2СаС1а (36)
3-181,5 168,2 2-206,5
Теплота образования исходных веществ равна 3-181,5 =
= 544,5. ккая.
Теплота образования получающихся веществ равна
168,2 + 2 - 206,5 = 581,2 ккая.
Тепловой эффект равен 581,2 — 544,5 = 36,7 ккая.
61
Тепловой эффект обеих стадий хлорирования равен
157,8 + 36,7 — 194,5 к кал
на 1 моль хлората.
В табл. 16 приведены данные теплоты реакции хлорирования
из расчета на 6 и 1 моль Са(ОН)г, на 1 / СаО, на 1 г Ca(ClO)», на
1 г Са(СЮз)г и на 1 г хлора.
Таблица 16. Теплота реакции хлорировании известкового
молок а
Выделяется калорий на
6 молей
Са (ОН).
1 моль
Са (ОН).
1 г СаО
1 г хлора
1 г
Са(СЮ),
1 г
Са(СЮ.).
1-я стадия хлорирования [уравне¬
26,3
0,763
ние (35)]
2-я стадия хлорирования [уравне¬
157,8
0,47
0,371
0,368
ние (36)]
Обе стадии хлорирования [уравне¬
36,7
6,1
0,11
0,086
0,085
ОД 77
ние (37)]
194,5
•32,4
0,58
0,457
0,453
0,94
Практически, при хлорировании в производственных аппаратах хлоргазом с высокой концентрацией СЬ, без искусственного охлаждения, подъем температуры составляет 0,55—0,57° на
1 г СаО в 1 л известкового молока (так как меньшая теплоемкость щелока компенсирует увеличение веса от поглощения
хлора). Уменьшение подъема температуры хлорируемого щелока вследствие содержания в хлоргазе воздуха и других примесей, не реагирующих при хлорировании, сравнительно незначительно. Например при хлоргазе, содержащем 50% СЬ, подъем
температуры на 1 г СаО в 1 л молока равен ~ 0,53°, а при хлоргазе, содержащем 10% СЬ, подъем температуры равен — 0,42°.
г) Некоторые опытные данные по изучению
хлорирования v
Если проследить практическое протекание процесса хлорирования при барботаже хлора через известковое молоко, отбирая
и анализируя пробы хлорируемой жидкости через небольшие
промежутки -времени, то можно заметить следующее. В начале
хлорирования отбираемые пробы содержат Са(ОН)«, СаСЬ и
Са(СЮ)г и не содержат хлората; цвет проб белый. По мере продолжения хлорирования уменьшается содержание Са(ОН)> и количество осадка в отстоявшемся щелоке и увеличивается содержание Са(С01)г и СаСЬ и плотность щелока. Цвет отстоявшегося
62
щелока стаиопигся все более зеленоватым и от щелока все
больше пахнет несколько сладковатым запахом гипохлорша.
Соответственно количеству поглощенного хлора происходит
подъем температуры хлорируемого щелока. К концу хлорирования, в определенный момент, вид и состав щелока резко изменяются: цвет щелока переходит из зеленого в ярко розовый;
количество гипохлорита резко падает; количество хлорида увеличивается в 1,6—1,7 раз; в щелоке появляется хлорат в количестве ~ 7з от содержания СаСЬ (в молях); щелок начинает пахнуть хлором; количество осадка в щелоке делается минимальным
и цвет осадка вместо белого становится буроватым (окись железа, песок и т. д.); температура щелока делает резкий скачок,
повышаясь примерно на Vs от общего подъема температуры.
Дальнейшее пропускание хлора уже не изменяет вида и состава щелока. Данные подъема температуры, поглощения хлора
Рис. 23. Кривые подъема температуры, поглощения
хлора и образования гипохлорита и хлората при
хлорировании известкового молока с концентрацией
СаО в 110 г/л.
и образования гипохлорита и хлората по ходу хлорирования
известкового молока, содержащего 110 г/л СаО, показаны на
рис. 23. Данные хлорирования при температуре 100—105° показаны на рис. 24. Из сравнения кривых обоих рисунков видно,
что при высокой температуре хлорирования образование гипохлорита и хлората проходит иначе, чем при низкой. Максимальная концентрация гипохлорита получается раньше и она
гораздо ниже. Образование хлората происходит не только при
перехлорировании, но и во все время 1-й стадии хлорирования,
параллельно поглощению хлора и образованию гипохлорита.
Максимум концентрации хлората гораздо ниже, поскольку образование его в 1-й стадии хлорирования1 сопровождается значительным выделением Ог. Необходимо однако отметить, что такое влияние высокой- температуры на хлорирование происходит
не всегда. При некоторых сортах извести, а также при содержании jb хлорируемом молоке хлоридов, влияние температуры
не так значительно.
63
В табл.. 17 приведены данные, показывающие влияние содержания СаСЬ в хлорируемом щелоке па выход хлората (расчет
выхода см. стр. 90). (Первая серия опытов, проделана с известковым молоком, содержащим СаО 20 r/л при условии прибавления к молоку разного количества СаСЬ. Данные о выходе хлората при этих опытах показывают, что прибавление СаСЬ весьма
повышает выход хлората и что оптимальной является концентрация СаСЬ в 100 г/л и выше. Вторая серия опытов показывает,
что на выход хлората влияет концентрация известкового мо-
.лока, так как чем выше концентрация СаО в молоке, тем выше
концентрация СаСЬ в щелоке в период перехлорирования, когда
обычно выделяется большая часть О*. Оптимальный выход получен при концентрации СаО в 150 r/л и выше, но и. при концентрации СаО 110 г/л выход достаточно высок.
Рис. 24. Кривые поглощения хлора и образования
гипохлорита и хлората при хлорировании кипящего
известковбГо молока, содержащего СаО 110 г/л.
Таблица 17. Влияние хлористого кальция на выход хлората
при хлорировании известкового молока
А. Известковое молоко, содержащее СаО 20 */д и разное количество СаС1,
<СаС1, г/д
0
25
50
75
100
125
150
% выхода ...
65
73
82
89
92
92 .
93
Б. Известковое молоко с разной концентрацией СаО
СаО г/д
20
40
60'1
* 80
110
150
200
240
'% выхода
65
83
89
92
96
97
97
97
Примечание."Все опыты произведены при оптимальных температурных
условиях и с известью одинакового качества.
'64
Необходимо ОТМСТИТЬ, ЧТО при хлориронпини И П|н>п Ж<щ-
ственных условиях (барботажем) известкового молока, содержащего СаО 110 г/л и СжСЬ 16—20 г/л, мы неизменно получали
выход хлората в 95—97%. Подобно хлористому кальцию влияет
и прибавка других хлоридов. С этой точки зрения имеет известный смысл применявшееся Либихом прибавление КС1 в из-
всстковое молоко. Одцако такая схема работы вызывает большие механические потери КС1 и КСЮа, чем обычно, и осложняет отделение шлама, выпарку и перекачку щелоков благодаря
легкому выделению КСЮ3 при случайном охлаждении щелоков.
В табл. 18 приведены данные 100 заводских операций хлорирования известкового молока высокой концентрации. Хлорирование производилось барботажем электролитического хлоргаза
через молоко в башне, показанной на рис. 38 (стр. 81) Каждая
операция проводилась с 3 л» молока. Во время хлорирования
производилось охлаждение щелока зюдой по свинцовым змеевикам, вставленным в башню. Данные систематизированы по аиа-
Таблица 18. Выходы хлората п р и 100 заводских операциях хлорирования известкового молока высокой концентрации
№
опер.
°/о
выхода
№
опер.
%
выхода
№
опер.
выхода
30
88
92
87
40
51
31
• 92
96
95
41
65
32
94
100
92
43 ‘
81
37
98
48
79
38
91
Средний выход
49
59
44
87
90 о/.
50
84
45
92
51
81
46
84
СаО 250—280
57
89
52
81
г/л
58
75
54
89
59
74
55
71
1
79
'65
86
60
94
2
83 ,
66
75
61
96
3
81
67
72
62
92
9
95
•72
71
63
83
10
71
73
83
68
87
16
84
79
76
69
89
17
83
80
77 <
70
93
ч 18
79
81
' 80
75
S6
19
55
87
68
76
95
26
86
88
64
77
87
27'
76
91
72
83
81 ,
28
• 83
93
74
85
88
34
/ 80
94
84
86
85
35
* 71
95
96
90
90
36
72
№
опер.
•/ О
выхода
опер.
выхода
СаО 200—220
г/л
14
25
39
56
71
84
98
90
89
96
92
98
93
91
Средний выход
93%
СаО 220—250
г/л
5
92
6
86
7
90
8
95
12
72
13
- 92
20
93
21
91
23
86
л 24
89
П р и м е ч
97
99
89
91
Средний выход
81%
СаО >280 Цл
4
11
15
22
29
33
42
47
53
64
74
78
82
89
49
57
83
69
32
78
56
52
85
55
69
76
42
76
Средний выход
бЗО/о
ству ющей СаО^Юг/^бмл^°^И^°вания* Щелока с концентрацией, соответ-
жал^ гипохлоп^т иKdK правил0» сильно недохлорированными (содер-
после Гбмботажя “'“'°:0ТРЯ «а проход большей’ части хлора в абгазе
после барботажа.
5 Зак. 179.*—Шра&бхдн^
65
лизам щелоков с пересчетом содержании Са и щелоке на
содержание СаО и известковом молоке (рис. 2G, стр. 09). 1>ыход
хлората рассчитан, как указано на стр. 90; хоти на выход
хлората влияли различные условии, которые нс были идентичны
при всех операциях (ненадежность режима охлаждении при
хлорировании, большие колебания концентрации хлоргаза, плохая. очистка молока и т. д.), все же видно, что наивысший процент выхода при хлорировании получался при концентрации СаО
в 200—220 г/л и что дальнейшее п о в ы ш е и и е к о н-
центрации СаО сильно с н и ж а с т в ы х о д х л орат а.
В проведенных нами лабораторных опытах хлорирования
известкового молока высокой концентрации • также получался
оптимальный выход при содержании СаО не свыше 220—240 г/л.
При большей концентрации СаО хлорирование часто не удавалось довести до конца, и несмотря на избыток пропускаемого
хлора (который больше не поглощался щелоком) в таком щёлоке оставались значительные количества Са(СЮ)2 и Са(ОН)2.
Это объясняется главным образом образованием соединений
Са(СЮг) и СаСЬ с Са(ОН)2, выделяющихся в осадок, отчего получалась густая трудно перемешиваемая масса. Кроме того по
нашим данным растворимость СаО и хлора в щелоке с большой
концентрацией СаСЬ, Са(СЮ)2 и Са(СЮз)г весьма мала, что
также замедляет процесс хлорирования. Таким образом при
условии тщательного регулирования температуры (искусственным охлаждением и т.-д.), чтобы хлорирование заканчивалось
при температуре не свыше 75—80°, оптимальной концентрацией
СаО в известковом молоке является 200—220 г/л. При хлорировании такого молока надо одновременно следить, чтобы тем^
пература хлорируемого, щелока была и не ниже 40—50°, так как
'при бояее низкой температуре обычно образуются оксихлориды,
отчего масса густеет и хлорирование не удается довести до
конца. ^
д) Внешний вид, состав и свойства хлорирован-
н ы х щелоков
Нормальный щелок, получаемый по окончании хлорирования,
должен быть «перехлорирован», т. е. содержать растворенный
хлор. Такой щелок пахнет хлором и имеет ярко розовый цвет.
Недохлорированный щелок не пахнет хлором, имеет зеленый
или слабо розовый цвет и содержит трудно оседающий осадок,
содержащий Са(ОН)2. Причиной розового цвета является феррат
кальция, образующийся .из хлора, примеси ^селеза и Са(ОН)2.
У ранение образования феррата будет следующее:
^ 5Са(ОН)2 + ЗСЬ + 2Fe(OH)j = 2CaFe04 + ЗСаСЬ + 8Н20.. (41)
Как и другие соединения шестивалентного железа, феррат
кальция малоустойчив и разрушается от прибавления восстановителей и даже без восстановителей при кипячении иди при длительном хранении на свету. Если к розовому перехлорирован-
ному чцелоку прибавить Са(ОН)2, то розовый цвет становится
более устойчивым при кипячении и при действии спета. При
разрушении феррата цвет щелока из розоного делается грязно-
желтым от образующегося нерастворимого F6(OH)3. Уравнение
этой реакции будет
4CaFeC>4 + 10Н2О = 4Са(ОН)2 + 4Fe(OH)3 + 302. (42)
Примечание. Имеющиеся у Ульмана6 (и др.) указания, что
причиной розового цвета являются примеси соединения марганца, неверны.
Хлорируя молоко из химически чистой извести, получают розовый щелок
только от прибавления примеси соединений железа, но не марганца. Кроме
того, розовый цвет исчезает от прибавления к щелоку восстановителей,
ис обесцвечивающих МпОЧ (раствор NIb.j| др.).
В основном, хлорированной щелок является раствором СаС12
и Са(СЮз)2. Кроме этих соединений в щелоке могут содержаться
растворенный хлор, гипохлорит, нсдоразложенный по уравнению (36) или (38), и примеси, бывшие в извести, из которой
приготовлен щелок (соединения Mg, SO4 и др.), обычно в небольшом количестве. Количество растворенного хлора и гипохлорите
зависит от степени перехлорирования щелока и температуры
конца хлорирования. Количество нерастворимых примесей в пе-
рехлорированном щелоке зависит от чистоты хлорируемого известкового молока и концентрации щелока. Эти примеси обычно
образуют в щелоке осадок (шлам), состоящий из СаСОз, песка,
окисей железа и алюминия и т. д. Горячий щелок уд. веса 1,17
и ниже осветляется от нерастворимых примесей "в несколько
минут. При более высокой .концентрации щелока оседание
шлама^ происходит медленнее и тем дольше, чем выше концентрация щелока. По нашим наблюдениям при хлорировании
в производственных условиях известкового молока, содержащего СаО 110 г/л (барботажем хлора в башне, рис. 38, стр. 81),
содержание шлама бкло равно 0,5—1 r/л щелока, а объем шлама
после 30—60 мин. отстоя был равен 2—4% от общего объема
щелока. При тех же условиях хлорирования известкового молока, содержащего СаО 220—240 г/л, содержание шлама было
5—10 г/л щелока, а объем шлама после нескольких ^часов отстоя
был равен 20—у30% от общего объема щелока.
. На рис. 25 приведены содержание Са(СЮз)2 и СаС12 в хлорированном щелоке разной концентрации и соответствующая составу щелока концентрация СаО в известковом молоке. Номограмма составлена без учета испарения воды при хлорировании,
которое обычно редко превышает 2—3%. Соотношения Са(СЮз)г
и СаСЬ даны1 без учета выделения Ог при хлорировании, которое при нормальной работе производства равно 4—6% от количества кислорода, получаемого в виде хлората. * f
На рис. 26 приведено определение содержания СаО в г/л известкового молока по содержанию Са или общего хлора (хлора
в виде хлората, гипохлорита и хлорида) в экв/л хлорированного
щелока. Увеличение объема при хлорировании не учтено при
составлении шкал, поскольку это увеличение незначительно и
обычно компенсируется испарением воды, уносимой абгазом. Во
5й ‘ 67
Рис. 25. Удельный вес, содержание Са(СЮ3)2 и. СаС12 н
увеличение объема при хлорировании известкового молока
„ разной концентрации.
Концентрация Са или общего хлора в экВ/л. хлорироСаннозо щелоке.
ЗМ/л< Г/л
ЗЬс/л.
(У
УС —-
3»0 —
.J40
40—г-
Т90
£
,.Л
v-=: s
Z <00&
v-=- "I
• =:■ !'/
3,7
*ej~ 8
з*® * - о*
=: Д
3.9- J»0 c
• u
Z" ?
^rt
4- I
v-Er* £*
4.9- 3;
4? -El
:Ii»t
V-:
4,5-^
^ 4JM
4.7-i
4,6
4,9 Tt
5fi
_ -i-
5.)
-J
?v-?-
§ qnao
^ i
о 5,4
<u ~
h-%- s
|wf f
H 5^7 JJjM |
sS -L.
^ 5,8 -T t>
V
3" S’
э#о—^
^ 4-
*.v|r t
s
9 :- S
%o.
§ -Г no
^•-T. I
J40
о
1‘Л-Т
v J—
«Mi
sf 6,4- Z 'lM
!«•’-£:
6,eif-
6,7
6,8-
6,9^-
7,0j
S'
4
~T ^
7в -4_ . *
4^> $
5 M-
Рис. 26. Определение содержания CaO в г/л известкового молока по концентрации Са или общего хлора
в эк в/л хлорированного щелока.
69
венком случае практические дачные редко :о ,, о, ,кк.., : ,
найденных по рис. 2G, больше чем на 2—?>’/<-. .'оно точность oi-
бора средней пробы щелока как легко перемешиваемого рае
твора на много выше, чем для известкового молока (особенно
при высокой концентрации СаО).
' В табл. 19 приведены относительная вязкость, температура
кипения и температура замерзания хлорированного щеЛока разного удельного веса.
Таблица 19. Относительная вязкость, температур а к и п е и и я
и температура замерзания хлорированных щелоков разной концентрации , «
Плотность
(
Вязкость при температуре
Температура ( f 0,
°Боме
Уд. пес
23е
У'
--5е
— 18е
кипения
замерзания
10
ч 1,074
1,39
лед
102°
— 7"
15
N 1.1J6
0,95
1,54
*
104°
— 11°
20
1,161
1,03
1,78
107°
— 17"'
25
1,210
1,20
2,15
2,72
109°
— 26"
.28
1,240
1,34
1 2,51
3,46
110°
— 30"
30
1,262
1,45
2,84
3,91
111°
34
32
1,285
1,69
3,19
4,58
113°
— 38е
34
1,308
1,84
3,70
5,76
115°
— 44"
36
1,332
' 2,13
4,59
6,13
117°
— 40"
38
1,357
2,50
5,82
6,68
119°
-36"
40
1,383
2,88
7,00
7,52
121°
•г- 15°
42
1,411
3,6
Л73
~
123°
— 5"
.Примечания: 1) Вязкость приводится по отношению к вязкости воды
при 20°. I
I 2) При охлаждении щелоков уд. веса выше 1,383 выделяется лед и
СаС1а-6НаО.
\
§ 2. Аппаратура и техника хлорирования
I а) Методы ХчЛ орирования в п р ом ышленном
масштабе
В промышленном масштабе хлорирование производится либо
абсорбцией хлора поверхностью сильно перемешиваемого молока, либо барботажем хлора через молоко. Реже применяется
'хлорирование^ посредством орошения молоком противоточной
струи хлора или посредством поглощения хлора распиливаемым
молоком и т. д. Отдельные методы хлорирования будут разобраны ниже при описаний отдельных аппаратов, применяемых
для хлорирования.
Концентрация известкового молока, применяемого для хлорирования, может вариировать в широких пределах. Ю,риш *, Пе-
чиней9 и Лунге» указывают концентрацию СаО в, 50—100 г/л
молока. * Биллитер12 * указывает концентрацию ОаО в при-
70
меняемом известковом молоке н 130 г/л. Ульман-1 ;ь- ; к;.-
зьжаст концентрацию молока, но приводит схему нроизводе-П!:
бертолетовой соли без 'применении выпарки, из чего можно
лать вывод, что в новых заграничных установках получают при
хлорировании щелок настолько высокой концентрации, что выпарка становится излишней. Такой щелок можно получить либо
хлорированием известкового молока с .концентрацией СаО
в 220—240 г/л, либо хлорированием взвеси извести в щелоке невысокой концентрации.
На рис. 27 показана схема хлорирования молока, содержащего СаО 100—110 г/л. На рис. 28 показана схема хлорирования
молока, содержащего СаО 220—230 г/л. Основное усложнение
в последнем случае заключается в обязательности искусственного
охлаждения щелока во время хлорирования и обязательности
IhSec/nb 8оба Абхаз без хлора
Рис. 27. Схема хлорирования известкового молока с концентрацией СаО 100—110 г/л.
стандартной концентрации и большой чистоты известкового
молока. Для охлаждения .вводят в'аппараты для хлорирования
змеевики и т. п. приспособления, требующие непрерывного наблюдения и регулирования. Последнее необходимо, так как при
температуре выше 75—80° увеличивается выделение Ог (ухудшается выход хлората), а* при температуре ниже 40—50° часто
образуются оксихлориды, вызывающие загустевание хлорируемой массы и необходимость останавливать хлорирование для
чистки башен от загустевшей массы и т. д. Так же образуются
оксихлориды и снижается выход хлората при слишком высокой
концентрации известкового молока. Для поглощения хлора из
абгаза, отходящего из аппаратов для хлорирования, приходится
приготовлять отдельно известковое молоко невысокой концентрации, так как молоко высокой концентрации благодаря своей
вязкости и способности к образованию оксихлоридов при низкой
температуре' неудобно для поглощения хлора из абгаза.
71
Впльдсрмаи (герм. пат. 449583 от 13/iH 19J] г.) 11|>o,>^kii?»
получать хлорированный щелок высокой концентрации, исходи
Рис. 28. Схема хлорирования известкового молока с концентра-
х* цией СаО в 220—230 г/л.
Рис. 29. Схема получения хлорированного щелока высокой концентрации
путем .двойного* хлорирования.
из хлорирования взвеси пушонки в воде и досыпки пушонки по
мере хлорирования. Для своего способа хлорирования Вильдер-
ман предложил специальную установку, описываемую ниже
(стр. 84). ..
72
11а рис. 29 пока.’.апа схема предложенного актором (:;.1я;’.оч-
мое свидетельство № 627II, XII, 1929 г.) способа .получения хлорированного щелока высоком концентрации бел наода искусственного охлаждения н аппараты для хлорирования. Для этого
хлорирование производится на двух параллельно работающих
установках. На одной хлорируется известковое молоко с концентрацией СаО в НО г/л. К полученному щелоку прибавляется
известь из расчета СаО 110 г/л. Полученная (взвесь охлаждается
и подвергается хлорированию, как Обычно. Хлор из абгаза от
обеих установок поглощается молоком с СаО ПО г/л, а абгаз-
ный щелок поступает на первичное хлорирование. ,
И. Б. Фрайманом предложено видоизменение метода «двойного» хлорирования, схематически показанное на рис. 30. Приготовляется известковое молоко концентрацией СаО в 230 г/л.
Рис. 30. Схема получения хлорированного щелока, предложенная И. Б. Фрайманом.'
Это молоко смешивается со щелоком уд. веса 1,37 (при 20’).
Смесь’щелока с молоком, содержащим СаО 110 г/л, хлорируется.
Полученный щелок частично поступает на приготовление нового
количества смеси щелока с молоком, а частично поступает на
обезвреживание и дальнейшие стадии производства.
Схемы, показанные на рис. 29 и рис. 30, удобны тем, что не
требуют искусственного охлаждения во время хлорирования и
обеспечивают хлорирование с очень малым выделением Оч (благодаря концентрации СаСЬ — см. табл. 17, стр.- 64). Проверка
этих методов в производственном масштабе , показала малое выделение кислорода даже при температуре конца хлорирования
в 90—95°. Недостатком «двойного» хлорирования является необходимость параллельной работы двух установок для первичного и вторичного хлорирования. Схема способа И. Б. Фрай-
мана требует работы лишь одной установки для хлорирования,
но вводится стадия приготовления смеси молока со щелоком
и усложняется поглощение хлора из абгаза. При всех трех схемах, показанных на рис. 28, 29 и 80, обслуживание процесса гораздо сложнее, чем при схеме, показанной на рис. 27.
б) Аппараты для хлорирования, имеющие'
исторический интерес
Первыми аппаратами для хлорирования в промышленном
масштабе были «октагоны»—восьмиугольные сосуды, соста-
Рис. 31. Каменный октагон.1
пленные из плит песчаника и т. п. материала, емкостью в 7—8 м3
•(рис. 31). В крышках октагонов были отверстия для загрузки
извести и воды, (молоко
готовилось в самих октагонах), для - вала мешалки, для входа хлор-
газа и для выхода абгаза. Мешалки делали
10—15 об/мин. Отверстие для загрузки извести и воды закрывалось воронкой, нижний
конец которой был погружен в жидкость, чем
создавался жидкостный
затвор для хлоргаза..
Через воронку можно
было отбирать пробы
щелока и вообще наблюдать за ходом процесса.
Каменные октагоны
были очень неудобны
ухчныо мок ввиду трудности их уплотнения, невозможности
передвижения и т. д.
Рис. 32. Чугунный -октагон. * • С семидесятых годов их
1 N
Вход
Хлоргахх
74
стали заменять чугунными аппаратами, которые хотя и были
круглыми, по по традиции их продолжали называть «октагонами». Такой аппарат, показанный на рис. 32, имел цельное дно
и крышку, а стенки его были составлены из отдельных секторов._
Вес аппарата достигал 9 г.
В первое время делали дно
выпуклым с подпятником
для вала мешалки в центре,
но затем его стали делать
полукруглым. В нижней
части корпуса аппарата
были 2 штуцера (на' рис. 32
эти штуцера не показаны),
расположенные один над
другим. По окончании хлорирования через вышерас*
положенный штуцер спускали щелок, отстоявшийся
от шлама, после чего через нижний штуцер спускали шлам и промывали
аппарат водой.
На фабрике Муспрата
в Виднесс (Англия) некоторое время чприменяли для*
хлорирования аппарат, сконструированный Кюльманом и показанный на рио. 33. Дппарат был железный, объемом в 20 Л13,
выложенный изнутри свинцом. Загружали аппарат на % объема.
При хлорировании щелок перемешивался мешалкой, делаю-
Хлэрип
Вспомогательные аппараты для
уяаОливлибания хлера из aSeaja
Основной аппарат
Готовый щелок
Рнс. £4. Аппарат Куигейма.1
щей 10—15 об/мин. Хлор, поступавший в аппарат, направлялся по свинцовому (замененному вскоре чугунным) спирально расположенному жолобу. Хлорирование продолжалось
7—8 час.; получаемый щелок имел удельный вес 1,12—1,13 и
температуру в 40^-504.
• В Берлине на* фабрике Кунгейма работал аппарат, изображенный на рис. 34. Корпус аппарата был сделан из чугун-
75
пых плит и раздолен горизонтальными 11 с | > t* городками на
4 отделения, расположенные одно над другим. Через г.сс
4 отделения проходили дне лопастные мешалки для перемешивания. Известковое молоко поступало вверху аппарата, протекая последовательно через все 4 отделения; готовый нрохло-
рированный щелок выходил внизу аппарата. Хлоргаз входил
снизу ;■ .рата, пройдя по принципу противотока над известковым м. ом через все 4 отделения аппарата. Абгаз выходил
вверху арата. Путь хлоргаза показан на рис. 34 стрелками.
Для о» , вождения от остатка хлора абгаз проходил еще через
2 аппарата меньшего размера.
Хлорирование во всех вышеописанных аппаратах (за исключением аппарата Кунгейма) проходило прерывно отдельными
операциям^. Кроме того часто прерывали хлорирование, не заканчивая всей операции при окончании рабочего дня. Температура щелока в конце хлорирования обычно не превышала
40—50°, ввиду невысокой концентрации молока, длительности
хлорирования и перерывов. Перед концом хлорирования в щелок часто пускали пар для повышения температуры и ускорения
перехода гипохлорита в хлорат и хлорид. Хлоргаз подавался
по свинцовым перекидным трубам и проходил ряд аппаратов для
хлорирования. Ход хлоргаза изменялся таким образом, чтобы
он проходил сначала через аппараты с наиболее прохлорирован-
ным щелоком и в самом конце — через аппарат со свежим известковым молоком.
76
На рис. 35 показана устанонка и.ч четырех чугунных октаго-
нов. Хлоргар проходил последовательно через все 4 аппарат;..
В одном из аппаратов, работавшем обычно последним по ходу
хлоргаза, была мешалка вихревого типа с большим числом оборотов для лучшего поглощения хлора. В остальных трех аппаратах были лопастные мешалки, на 10—15 об/мин,
в) Хлорирование в абсорберах
На рис. 36 показан аппарат — абсорбер, применяющийся на
одном из современных заводов для хлорирования методом поверхностной абсорбции хлора. Это чугунный невысокий цилиндр
* л
с полукруглым дном. Толщина стенок аппарата 20—25 «л.
Крышка абсорбера выпуклая и имеет 5 отверстий: 1 для мешалки, 2 для. ввода хлоргаза и 2 для вывода абгаза. В середине
цилиндрической части абсорбера друг против друга имеются
2 штуцера дл» ввода молока и вывода щелока. Изнутри абсорбер эмалирован. Снаружи абсорбер окружен кожухом для
охлаждающей воды (на рис. 36 не показан). Для перемешивания
хлорируемого щелока в абсорбере установлена мешалка. На
77
1
рис. 36 показана эмалированная мешалка вихревого тина, делающая 250—500 об/мин. Эта мешалка очень тяжела (—0,8 г),
почему приходится часто ремонтировать вал мешалки. Целесообразнее применять пропеллерные мешалки на 100—200 об/мин.
которые гораздо легче показанных на рис. 36 и создают достаточно хорошее перемешивание. По нашим наблюдениям такие
мешалки (нсэмалироюанные) приходится вынимать на ремонт раз
в 2—4 месяца. Мешалка абсорбера может работать от общей
трансмиссии, но удобнее иметь индивидуальный мотор к мешалке каждого абсорбера.
От 3 до 5 таких абсорберов располагаются террасообразио,
составляя непрерывно работающую серию или систему (рис. 37).
Между собой абсорберы соединяются свинцовыми трубами для
перетекания щелока и свинцовыми газопроводами для хлора.
Молоко поступает в самый верхний абсорбер, а хлоргаз — в самый нижний, так что создается противоток известкового молока
Рис. 37. Схема современной абсорбериой установки для хлорирования.
и хлора. Из нижнего абсорбера выходит уже прохлорированный
щелок. Из верхнего абсорбера удаляется абгаз. Вход молока
в верхний абсорбер и выход щелока из нижнего абсорбера производятся через U-образные трубы, чтобы создать гидравлические затворы во избежание попадания хлоргаза в атмосферу
помещения. Для контроля за работой установки на переходных
щелокопроводах устанавливаются термометры, а на переходных
газопроводах термометры и манометры.
Концентрация% СаО в хлорируемом молоке должна быть
100—110 г/л при хлорировании без охлаждения. Применяя охлаждение (проточной водой по кожухам абсорберов), можно хлорировать молоко с концентрацией СаО до 140—150 г/л. Молоко
большей концентрации трудно хлорировать в абсорберах, так
как благодаря большой вязкости затрудняется перемешивание
молока, ухудшается поглощение хлора и получаемый щелок часто содержит значительные количества Са(СЮ)г и Ca(OH)s.
Кроме того весьма увеличивается выделение Os и ухудшается
выход хлората . X. П. А1» 31—33, стр. 1909—1910, 1930 г.). При
концентрашь > молоке в 100—110 г/л на такой установке
легко наладить бесперебойное получение перехлорированного ще-
78
лока с выходом хлората н 94—96%
и с содержанием небольшого количества шлама. При большей концентрации СаО количество шлама и случаи получения недохлорированного
шелока резко возрастают.
В табл. 20 приведены средние'данные работы установки из четырех
абсорберов при хлорировании известкового молока с концентрацией
СаО в J 00—120 г/л хлоргазом, содержащим 90—95(% СЬ. Хлорирование
проводилось без искусственного охлаждения. Пробы щелока $ газа отбирались и анализировались после
каждого абсорбера.
Из данных табл. 20 видно, что в
основном хлор поглощается во 2-м
и 3-м абсорберах (по ходу молока).
1-й абсорбер поглощает лишь остатки хлора, 4-й абсорбер поглощает
тоже немного хлора, ибо в нем происходят дехлорирование остатка
Са(ОН)2 и перехлорирование щелока.
Хлррат в основном образуется в 4-м
абсорбере. Содержание хлората в
щелоке из 3-го абсорбера объясняется явлениями местного перегрева
и перехлорирования.
Так как в 1-м абсорбере поглощается мало хлора, а в абгазе, выходящем из 1-го абсорбера, обычно содержится хлор (хотя бы следы), что
недопустимо из-за коррозии вентиляторов и аппаратуры и отравления атмосферы, то по нашему мнению целесообразнее работать на установке
из трех абсорберов, отсасывая абгаз
через колонку, орошаемую известковым молоком. Одна колонка может
обслужить несколько серий абсорберов. Работа на сериях из пяти абсорберов без абгазной установки создает оптимальных условий получения
абгаза без хлора, так как холодное
молоко в 1-м абсорбере плохо поглощает хлор из поступающего в 1-й
абсорбер низкопроцентного хлор-
газа, обычно содержащего всего 3—
10% С12.
Л
rt г ч
1
1Г Ю 1Г. С.. !
С 1 о л 1
о
С
Mil
г-
£
р.
О Ю ш Ю
*
О
н
С 1 Г9Ю 1"
рг
—
—
о
О о
О
2 х я
Ю со go
U
W и
ез о
ММ
с
о-а 54
О я
О (4
ою©
Г-н О
о
в
а
_ _
Л
о ■
н
и
з а
'О о
о© ~
Г- СО Ю со
мм
<L>
О. г;
О И
1 1 1 1
со © с ю
сэ
и
С 4 Т
СО
ю
п
.
S
1
Ю
ОЮ сою
д
1
5 а*
Ю Г—1 t
III!
3 о
1 1 I i
*2 Г*
ю о о о
д
о И
*rcf
Г—* Г“И
СЗ
СО
с8«
о
*»
(fllTjHH
и
1 1 II
с w
Си**-!.
п
<3
W8SS
О **
кГ
с- О
4 (N
К V-H
1
ш
<4
X
О
ч
о
0
«83
1 1 II
= О
§
. О О ОС.
сио
а
во
и
—' ю
?.б
И
и
о
о
О
О О СМ _
N СЭ (J
и
О.
и
1 1 м
О °
<4
юоом
чэ 't-
си О
и
со GO
о
о S’
—1 О о
гн © -г
О СЗ
О
1 1 I 1
о х
«4
и
1 1 1
ОООО 1
* о.
OI-C4
|Н
О «
с *
Л
к
см г— ©
CQ
«К
О О с-1 «-ч
S w
<4
X
3 ы
3 о
* •> •> »
Т-Н Г—1 г—< г-<
и;
о
о
ч
в
* ^
о 3
н
М ' ■
*<Г см Г-
ОСНН
ч
-
и
о
<и
о
=г
<5
■S
rH*tCC-
са
3
з
. к • к
ч сз
J3
ег
X О
1 1 1 1
н
о
с* ч
II 1 1
о
■t
у а»
S я
СП
со
Ol см rt* Г"- ,
о 1
и
r""t
»—с Т—» Т-Ч У—*
JG5
S
я 3
о о ос
X
■ rt
2 и
СО
1 II 1
4)
41 О
о о см см
си
I® в
40 of- .
О в
Т*4 СО г-н
и
а
<N
. о
Й•>*«
С
•» и 5
»оо
2*х ч
1-нСМСОгй*
Я о
Г*
»©
«Os
'Sc
*2
2
ч
г) X л о р и р о и
Г) л р о и Т (1 Ж С М «II
О у in п и х
Хлорирование в бгл
вое молоко имеет ряд :
сорберах (см. ниже стр.
тажем следующая: изт
абгазной колонки для }
абгазный щелок пер'
поступает в башни,
вают в башню та:
барботажем хлора через изиестко-
:неств перед хлорированием в аб-
Общая схема хлорирования барбо-
е молоко поступает на орошение
звания хлора из абгаза. Полученный
•ается в сборники, откуда самотеком
сс в башнях ведется прерывно. Зали-
!ичество известкового молока, чтобы
оно занимало не ольше половины объема башни, после чего
пускают в эту башшо хлоргаз и начинают хлорирование. В аб-
газе появляется хлор только в концу хлорирования. Для поглощения хлора из абгаза последний из башни поступает в абгаз-
ную колонку, орошаемую известковым молоком. Абгаз, лишенный
хлора, выбрасывается в атмосферу. , В башню хлоргаз для бар-
ботажа-людается под давлением (обычно 0,4—0,5 ат) компрессором. Абгаз из башни отсасывается вентилятором через абгаз-
ную колонку. Когда температура в башне перестает подниматься
и в абгазе появляется много хлора, открывают вентиль на входе
хлоргаза в башню со свеженалитым известковым молоком и закрывают вентиль на входе хлоргаза в работавшую ранее башню,
пуская туда ток воздуха для выдувания растворенного хлора<-
Газы от продувки содержат хлор, почему их пропускают через
абгазную колонку. Окончание продувки узнается по прекращению уменьшения концентрации СЮ' ® пробах щелока из башни.
По окончании продувки щелок выпускается из башни, в нее наливают свежее молоко и начинают новый цикл хлорирования.
В такой башне получают хорошие результаты при хлорировании молока, содержащего СаО до 220—240 г/л. Однако при
хлорировании молока, содержащего СаО выше 110 г/л, надо
вставить в башню змеевики и во время хлорирования производить охлаждение водой, что усложняет обслуживание процесса.
Щелок, получаемый при хлорировании барботажем, всегда
перехлорирован и содержит гораздо меньше осадка, чем при
хлорировании в абсорберах, так как конец хлорирования в башнях легче поддается регулированию и контролю,
у На рис. 38 показана башня для хлорирования барботажем.
Корпус башни железобетонный или железный, изнутри футерован кислотоупорным кирпичом, на хлороустойчивой замазке
из молотого кварца и жидкого стекла и т. п. Футеровку можно
делать также из диабаза, андезита и т. д. В самой нижней части
башни имеется чугунный штуцер, соединенный с щелокопрово-
дом для вывода щелока из башни. Молоко поступает через
штуцер, вделанный в стенку башни. Несколько выше 1 я от низа
башни в стенку башни вделана чугунная втулка, через которую
вставлена труба, хлоропровода. Втулка сделана с выточкой для
набивки графитированного асбеста, подтягиваемого чугунной
буксой (см. рис. 39). Внутри башни труба хлоропровода оканчивается. литым флянцем, к которому присоединен на болтах, ли-
той флянец барботера. Последний опускается почти до дна
башни, оканчиваясь •крсстонп;'; ii п т. и. для лучшего раенреде-
iep и внутренняя часть хлоро-
уоогшя жидкости; это лучше
. лее в верхней части башни,
горячие пары воды. Труба,
.. ром, снаружи соединяете^
■ я и воздухопроводом (см.
Предо хранитолЬ
Ad га 'опробод
Ьлод*кхлЫ*а
т/ляалютр
ления газа. Таким образом б
провода находятся целиком с.: :
и отношении коррозии, котора/
где все ;>емя содержатся хлорг
соед лая внутри башни с б.
нос; вом тройника с хлоропр
рис ')• На соединительном
т лке устанавливаются
лый и воздушный вентили. Хорошо показал себя в
практической работе как хлорный вентиль обычный аммиачный вентиль с заточкой
гнезда на конус и свинцовой
наплавкой на клапане. Такие
вентили работают, не пропуская хлора, 20—30 суток,
после чего приходится менять
наплавку клапана. На случай
смены вентилей и других ре- •
монтов необходим обводный •,
хлоропровод, который, минуя башни, подводит хлоргаз ирарр^в
непосредственно к абгазной (
КОЛОНКе. ДЛЯ реМОНТОВ ВНУТРИ Bapdomtp
башни в корпус башни вму- >—
рована чугунная горловина
(0 = 0,6 м), закрытая чугунной крышкой на болтах с резиновым уплотнением. В
крышке люка имеется штуцер
с краном для отбора проб
щелока, патрон для термометра и если нужно, то еще
2 штуцера для ввода и вывода змеевика для охлаждающей
воды. Сверху башня закрыта массивной чугунной крышкой.
Крышка имеет шипы, заделанные в стенке башни на цементе.
В крышке имеется штуцер для вывода абгаза, в штуцере имеется
отверстие для соединения с манометром и для отбора проб абгаза. Кроме того в крышке имеется штуцер, соединенный с U-об-
разной трубой, залитой водой и служащей предохранителем на
случай образования большого давления. Конец этой трубы выводится над крышей здания. При ремонте внутри башен и т. п. на
штуцере, соединенном с абгазопроводом, ставится заглушка.
Башня, показанная на рис. 38, заполняется на у2 геометрического объема. При большем заполнении башни молоком, к концу
хлорирования часто случались/ выбросы жидкости из башни.
Целесообразнее вести хлорирование в башнях больших разме-
Впуск хлера
v доз духа
ббтуск
u+Qfioka
г-1д 4- U
Рис. 38. "Башня"для хлорирования бар
ботажем.
Зак, 179. — Шр&йбман.
81
ров, так как основное обслуживание (ваполиенпе, опорожнение.,
определение конца хлорирования, начало и прекращение доел у не,
хлора и воздуха и т. д.) нанимает почти одинаковое время как
при малощЧЗашнс, так и при большой. 'Кроме того чем больше
рабочий объем башни, тем меньше количество хлора, уходящего
в абгаз, и легче учет расхода молока и количества 'поглощенного
хлора и т. д. Проведснн >; » нами в 1936 г. опыты хлорирования
в башне с рабочим об\. -ом в 25 лт3 дали вполне удовлетворительные результаты
Хлор^ Воздут
7Ъло
Ьтулки
Стела башни
Шпилька
Набивка
(предложение о работе в больших башнях сделано автором
в 1935 г.).
В башню, показанную на рис. 38, подается компримированный сухой хлор-
газ. На одном из
заводов производства хлоратов осуществлен? подача электролитического хлоргаза без предварительной сушки посредством инжекции хлора воздухом (давлением
в 6—7 ат). По нашему мнению такой способ уступает способу
барботажа компримированным хлоргазом, так как большой
расход воздуха на,инжектирование стоит дороже, чем стоимость
сушки и компримирования хлоргаза, тем более, что транспорт
влажного хлоргаза сложнее, чем транспорт высушенного хлоргаза.
Phcj 39. Ввод хлора и воздуха в башню и трой
ник подачи хлора и воздуха в баднт.
д) Сравнение хлорирования поверхностным
поглощением в абсорберах и б арб от ало ем
в башнях
При хлорировании известкового молока высокой концентрации более выгоден способ хлорирования барботажем, так как
в абсорберах- хлорирование молока с СаО выше 150—160 т/з
вызывает большие затруднения (стр. 65). Хлорирование молока
с СаО 100—110 г/з можно вести обоими способами, имеющими
•каждый свои преимущества и недостатки, основные из которых
и приводим.
Преимущества хлорирования в абсорберах:
1. Непрерывность процесса хлорирования.
2. Ненужность компримирования хлора — лросасывание хлора
и абгаза производится вентилятором низкого давления, ибо в системе имеется разрежение в 10—20 мм вод. ст.
3. Необязательна сушка хлоргаза — можно применять влажный хлоргаз.
Недостатки хлорирования в абсорберах:
1. Даже небольшие изменения в количестве и концентрации
известкового1 молока и хлора расстраивают работу абсорберов.
82
Требуется тщательное и непрерывное регулирование процесса
хлорирования.
2. Трудно добиться постоянного получения перехлори-
рованиых щелоков, нередко получаются нсдохлорированиые
щелока.
3. Ввиду коррозии требуется довольно частая замена или ремонт мешалок, часто случаются аварии с приводами мешалок
и т. д. — приходится остапгг.лиюпь всю серию из-за остановки
мешалки отдельного абсорбера. .
4. Из-за коррозии часто получается пегерметнчность трубопроводов; при забивании соединительных труб осадками и т. п.
неполадках вместо разрежения получается давление и, как следствие, проникание хлора в помещение.
5. При равных прочих условиях количество шлама при работе на абсорберах больше, чем при барботаже хлора. Даже при
небольших расстройствах режима работы получаются недохло-
рированные щелока.
6. Площадь, занимаемая абсорберной установкой, обычно,
в 2—3 раза больше, чем площадь при методе барботажа.
7. Обслуживание абсорберной системы во много раз сложнее, чем башни для барботажа, ввиду наличия большего количества движущихся частей, приводных ремней, деталей подвергающихся коррозии, большого количества точек, требующих
надзора и контроля, и т. д.
8. Сложен пуск серии в работу — обязательно получается некоторое количество недохлорированного щелока и т. д.
Преимущества хлорирования барботажем следующие:
, 1. Стабильные условия перехлорирования и отсутствие случаев получения недохлорированных щелоков.
' Постоянство выходов хлората благодаря указанной стабильности условий хлорирования.
3. Значительно меньшее количество шлама, поскольку барботаж обеспечивает большое перехлорирование при лучшем взмучивании осадка.
4. Более простое обслуживание, которое сводится фактически только к открыванию и закрыванию вентилей от хлора, от
воздуха и от известкового молока и к выпуску щелока.
5. Площадь для башен в 2—3 раза меньше площади для
абсорберов.
6. Отсутствие движущихся частей и передаточных ремней,
малое количество корродирующих деталей.
Недостатки хлорирования барботажем:
v 1. Необходимость применения компримированного (0,4—
0,6 ати) и сухого хлоргаза.
2. Значительно большее количество хлора, попадающего
в Дбгаз. :
3. Прерывность процесса *.
1 В последнее время сделан ряд предложений о переводе хлорирования в башнях на непрерывный режим.
6*
83
е) Д р у г и о а п и араты д л я х л о р к р о в а п и я
1. Установка Вильдер
для хлорирования прел
пат. 449583, 1921 г.). Ус г
ного сосуда Ь и сосуд
неско :<о, с параллель:,
хло;: за. Материал 6ai
за
1
h -
К.
- ||
|
11
На рис. 40 показана установка,
мая Вильдерманом (согласно герм,
а состоит из башни а, промежуточ-
Таких комплектов может работать
ли (чаще) последовательным ходом
а промежуточного сосуда Ь — глазированная керамика и т. и.
Сосуды с железные или
железобетонные, выложенные керамическими плит-
. нами. Сверху башня имеет
крышку, а снизу от-
, крыта и погружена в ще¬
лок, содержащийся в со-
, суде b и образующий ги¬
дравлический затвор. Непосредственно под крышкой
в башне а устраивается при-
• .» способление для распреде¬
ления молока, например в
виде дырчатой тарелки с
•работающей над ней мешалкой. Для увеличения
реакционной поверхности
в башню подвешиваются
цепочки (покрытые хлороустойчивым эбонитом), на
которых располагаются
стеклянные шары. Форма шара выбрана как
форма наиболее обтекаемая, а стекло выбрано
как материал, не реагирующий ни с хлором, ни со щелоком и известью. При высоте башни 7 я и диаметре
0,85 я в нее подвешены
40 цепочек с шарами диаметром в 8 ся. Сосуды Ь и
с име^т мешалки J и т,
делающие 15—20 об/мин.,
чтобы не выпал Са(ОН)г.
Для пуска’ комплекта установки заливают в сосуд с воду и
засыпают охлажденную просеянную пушонку. Полученное
молоко перекачивают насосом р по трубопроводу g в башню а
.через штуцер в крышке башни d. Хлоргаз поступает внизу
башни .через штуцер е и выходит через штуцер f{ соединенный
с вентиляторов или с е другой башни. Получившийся от реакции
Рис. 40. Башня Вильдермана для хлорирования орошением (DRP 449583 1921 г.)
д и я' — башни для хлорирования, dud' — крышки
башен, b — промежуточный сосуд, сис'- сосуды
для приготовления молока, g и g* — трубопровод
для молока и щелока, орошающего башни, е и
е’ — хлоропроводы, / и / — абгазопроводы, i — стеклянные шары в башнях, К и К' — сифоны-щелоко-
проводы из b в С и С', г и г' —шибера щелокопро-
водов К и К', Р — насос, О и О' — трубопроводы
для щелоков к насосу Р, 5 и 5' — шибера щелоко-
проводов О и О, / —мешалка промежуточного сосуда Ь; т и т* — мешалки сосудов Си С*» /—мешалка сосуда Ь.
н
между хлором и Са(ОН)'> щелок стекает в сосуд h. Избыток щелока в сосуде h над уровнем, минимально необходимым для создания гидравлического затвора, стекает по сифонной трубе К
в сосуд С. Тут к щелоку добавляется пушонка и полученная
взвесь Са(ОН)» в щелоке перекачивается обратно для орошения
башни. Так продолжают, пока не получится хлорированный щелок, соответствующий содержанию в маточном щелоке (после
обменной реакции и кристаллизации) 40—50 г СаСЬ на 100 г НгО.
После этого полученный хлорированный щелок в сосуде С продолжительное время перемешивают и направляют для дальнейшей переработки (фильтрация от шлама, обменная реакция, кристаллизация и т. д.). t
При хлорировании температура не должна превышать 70°
во избежание большого разложения гипохлорита с выделением
кислорода. Поэтому в начале перехлорирования, когда происходит быстрый подъем температуры, рекомендуется добавлять
в башню холодную воду, чтобы снизить температуру. Так как от
этого щелок разбабляется, то надо готовить щелок из расчета
.большей концентрации, чем указано выше, с тем чтобы после
разбавления получить необходимую концентрацию.
К концу хлорирования, когда уже имеется щелок большой
концентрации, ухудшается поглощение хлора. Поэтому рекомендуется хлор пускать последовательно через 2 башни: свежий
хлоргаз поступает в башню, орошаемую щелоком с добавленной известью; абгаз из этой башни поступает в другую башню,
орошаемую известковым молоком. Когда операция в одном комплекте установки заканчивается (т. е. получается уже перехлори-
рованный щелок), цикл начинается сначала — орошают башню
известковым молоком и меняют последовательность поступления хлоргаза. Изменение же последовательности хода щелока
перекачиванием его из одного сосуда в.другой менее удобно.
2. Башня t распылением. Имеются указания, что за границей
применяются башни для хлорирования распыленного известкового молока. Взбрызгивание осуществляется либо давлением,
создаваемым насосом, либо сжатым воздухом. Благодаря образованию «пыли» или «туМана» мельчайшие частички Са(ОН)»
сразу реагируют с хлором; падающий вниз башни щело^
является полностью прохлорированным. Если щелок, выходящий снизу башни, недохлорирован, его направляют на вторичное разбрызгивание.
Абгаз из башни отсасывается вентилятором. Дл?Г большей
.обеспеченности полноты процесса можно работать на установке
из двух башен, из которых одна поглощает остатки хлора из
абгаза свежим известковым молоком, а образующийся в ней
недохлорированный щелок взбрызгивается во вторую башню,
где и перехлорируется свежим хлоргазом.
На рис. 41 показана башня для хлорированного распыленного
известкового молока, работавшая на фабрике Печинея для улавливания хлора из абгаза, получавшегося после абсорберной
установки. (. -
I
85
3. Башня с орошением. На рис. 42 показана башня, успешно
применяемая для улавливании хлора из абгаза.
' Чугунный цилиндр, имеющий чугунное коническое дно,
установлен на фундаменте. Уплотнение между цилиндром
и конусом достигается графитированной асбестовой прокладкой, выложенной в специальной выточке в теле конуса.
Высота конуса 0,4 м. В 'башне имеются 2 штуцера для подвода
хлора и для вывода из колонки хлорированного щелока. Хлоро-
провод вводится в нижнюю
■дер для вывода щелока установлен в самом низу конуса, чтобы
в башне не могло быть скопления шлама. Для создания гидравлического затвора, чтобы хлоргаз не мог попасть в щелокопро-
вод, последний по выходе из башни имеет U-образный изгиб.
Внутри башни находятся 13 чугунных секций, состоящих каждая из тарелки, колокола и стойки. Края колоколов выступают
на 5——10 мм за края тарелок. Самая нижняя тарелка опирается
на более длинных стойках на конус башни. Для осмотра башни
и ее. ремонта в нижней части цилиндра башни имеется люк.
Сверху башня закрывается чугунной крышкой. Крышка при-
£6
креплястся болтами к флянцу, которым оканчивается цилиндр
банши. В крышке имеются 2 штуцера — один для анода
орошающего раствора и один для вывода абгаза. Трубопровод для раствора, питающего башню, имеет U-образный
изгиб для создания гидравлического затвора против проскока
абгаза. Для ремонта секций их вынимают из башни. Для
этого снимается крышка башни и секции поочередно вытягиваются посредством кольца, имеющегося в центре колокола
каждой секции.
Мы наблюдали работу такой башни для поглощения хлора
из абгаза после аппаратов для хлорирования растворов NaOH.
Содержание хлора в абгазе до башни менялось от нуля до
80—90%; при этом хлор полностью поглощался.
Ремонт башни и секций требовался весьма редко. Практически приходилось 1 раз в год сменять 2—3 нижние секции ввиду
их сильного разъедания. Тело башни, как и верхние секции, совершенно не было разъедено и не требовало ремонта, так что
очевидно, что чугун является для данной башни подходящим
материалом.
Несомненно, что подавая вместо NaOH известковое молоко,
также можно обеспечить бесперебойную работу такой башни;
необходимо только применять известковое молоко с невысокой
концентрацией СаО и не содержащее грубых примесей.
4. Хлоринатор. При хлорировании в абсорберах (стр. 77) количество хлора, поглощаемого в единицу времени, при прочих
равных условиях определяется ловерхностью- соприкосновения
хлора с известковым молоком. Эта поверхность в свою очередь
определяется интенсивностью перемешивания. Чем больше число
оборотов мешалки и совершеннее .перемешивание, тем больше
общее количество хлора, могущего фыть поглощенным в единицу времени.
Для максимального увеличения производительности при методе хлорирования поверхностной абсорбцией хлора автором и
Д. И. Хренниковым был предложен аппарат, могущий заменить
серию из трех.-четырех абсорберов, показанный на рис. 43
(Л. С. Генин предложил применить в этом аппарате лопасти центробежного типа).
87
Аппарат представляет собой горизонтально расположенный
чугунный цилиндр. На 5—(> он шоке оси цилиндра проходит над
с насаженными на нем 20—30 лопастями пропеллерного тина. Нал
с лопастями вращается, делая 200—300 об/мин., благодаря чему
известковое молоко в аппарате находится в почти распыленном
состоянии. Внизу лопасти не доходят до стенок аппарата только
на 0,5 см, благодаря чему Са{ОН)г или шлам не может осесть
в нижней части аппарата. Наверху лопасти не доходят до стенок аппарата на 10—12 t Известковое молоко и хлоргаз движутся в противоположных направлениях. С обеих сторон цилиндр аппарата закрывается крышками, через которые проходит
вал и через одну выходит готовый щелок. Вход хлоргаза и
известкового молока и вывод абгаза осуществляется через штуцера в верхней части цилиндра, недалеко от крышек.
известковое нолоно
I*
Абеаз
а*г
верхний >
абсорбер L
Щелок
Общо я схема
вход щелока
оз верхнего
абсорбера л
г Иио/Снии
абсорбер
Дбгаэ
Хлоргаз
Внутри
освинцован
выход щелока
Ниэкний абсорбер
Рис. 44. Схема абсорберной установки для хлорирования барботажем по Ульману.
Один такой аппарат заменяет целую серию абсорберов, что
значительно сокращает площадь, необходимую для процесса
хлорирования, упрощает наблюдение и регулирование процесса
и т. д. При изресткрвом молоке, содержащем СаО 110 г/л, охлаждение аппарата не нужно. При более высокой концентрации молока можно осуществить охлаждение, пропуская воду
по змеевикам внутри аппарата, либо по кожуху кругом аппарата. При этом в основном надо охлаждать среднюю часть
аппарата, где происходит поглощение наибольшего количества
хлора.
5. Установка для барботажа по Ульману. На рис. 44 показана схема установки для хлорирования, приводимая Ульманом. 5 Хлорирование производится барботажем хлора последовательно через 2 чугунных изнутри освинцованных аппарата.
Несмотря на то что ^барботирующий хлор перемешивает молоко,
аппараты снабжены мешалками.
88
ж) Состав а б г а з а при х л о р и р о в а и и и а б с о р б ц и с i:
и б а р б о т а ж с м
Как указано на стр. 47, хлоргаз обычно содержит кроме
хлора ООз, Нг, Ог, N2. При хлорировании, СЬ и СОг реагируют с Са(ОН)г, а Нг, Ог и N2 уходят в виде абгаза. Также
уходит в абгЪз и СЬ, образующийся при хлорировании (стр. 59).
При хлорировании поверхностным поглощением хлора в абсорберах в абгазе обычно содержится также некоторое количество
СЬ и СОг — обычно в 'пределах десятых долей процента. При
хлорировании барботажем СЬ и СОг появляются в абгазе
только в конце операции, при перехлорировании. При этом содержание СОг в абгазе может быть больше, чем в хлоргазе, так
как частично выделяется СОг, получающаяся вследствие реакции
хлора с СаСОз [уравнение (82), стр. 186].
Содержание Нг и Ог в абгазе является опасным в отношении возможности образования взрывчатой смеси (см. стр. 328).
Чем выше процент СЬ в хлоргазе, тем больше концентрация На
И Оа в абгазе при их одинаковой концентрации в хлоргазе. Например при содержаний в хлоргазе 1% На и 96% СЬ в абгазе
, / ыоо
после поглощения всего хлора будет содержаться тщзГдб =
= 25% Нг (исходим из отсутствия засоса воздуха при хлорировании и не принимаем во внимание изменения объема газа
от выделения Ог при хлорировании). При тех же условиях, но при содержании в хлоргазе 1% Нг и 50% СЬ в абгазе будет содержаться '70о—°ао = Н*- Поэтому при содер¬
жании в хлоргазе больше 0,1—0,2% Нг и высокой концентрации
СЬ надо хлоргаз перед хлорированием разбавлять воздухом до
концентрации СЬ в 50—450%.
Содержание Ог в абгазе зависит еще от образования Ог при
хлорировании [уравнение (38)]. Абсолютное количество Os,
образующееся при хлорировании, равно 1,555 • А • я3 на 1 т
хлора, поглощенного при хлорировании, где А обозначает процент потери при хлорировании, рассчитанный, как указано на
стр. 91, и 1,555 показывает количество «3 кислорода, соответствующее 1% от объема 1 т хлора [поскольку, как видно из уравнения (39), 1 объем СЬ соответствует Уг объема кислорода].'
Высокое содержание Ог в абгазе, связанное с выделением Ог
при хлорировании, обычно сопутствует сильному вспениванию
щелока.
Содержание СЬ в абгазе вредно не только из-за потери
хлора, но главное из-за отравления окружающей атмосферы и
разъедания вентиляторов (отсасывающих абгаз), близко расположенных машин и арматуры. Особенно недопустимо не
улавливать хлор из абгаза при хлорировании барботажем,
поскольку, как указано выше, в период перехлорирова-
, ния почти ве'сь хлор, содержащийся в хлоргазе, уходит
в абгаз.
89
I la одном из хлоратпых за подо» улавливание хлора из абга;
осуществлялось в башне, показанной на рис. 42, орошасмссь
раствором NaOII. В абгазе после башни никогда нс содержало,
даже следов хлора. е
, ч
§ 3. Расчеты выходов и потерь при хлорировании
а) Расчет выхода хлората по анализу хлорированного щелока ^
\
• Выходом хлората мы называем процент фактически полученного хлората по отношению к количеству его, которое должно
получиться теоретически, при отсутствии побочных реакций
с выделением 02, т. е. но уравнению
6Са(ОН)« + 6С12 = Са(СЮз)2 + 5СаС12 + 6Н20. (37)
По уравнению (37) в щелоке, получаемом после хлорирования, должно быть столько же эквивалентов СЮз1, сколько
имеется и эквивалентов Са. Практически эквивалентов СЮз
всегда получается меньше, чем Са, поскольку- при хлорировании
происходят побочные реакции с выделением 02 и практическое
суммарное уравнение хлорирования 'будет:
6Ca(OH)2 + 6С12= (1 — л)Са(СЮз)2 + (5 + л)СаС12 +
+ 6Н20 + ЗпОг. (43)
Сравнивая уравнения (37)- и (43), видно, что от выделения Оа
(величины л) изменяется содержание СЮз и не изменяется содержание Са. Поэтому выход хлората можно рассчитать по
формуле
. СЮз-100о/
выход хлората = —^—%,
где СЮз и Са обозначают их содержание в экв/j щелока.
Эта формула расчета выхода хлората верна также для щелоков, содержащих кроме хлората и хлорида еще и гипохлорит,
но неприменима, если известковое молоко до хлорирования содержало хлорат, хлорид или гипохлорит. В этих случаях расчет
выхода хлората надо делать по формуле
выход хлората = ■ % или
I О)
(А-м — а) 100 0/
я /о
где а и А обозначают содержание хлората в экв/л щелока до
и после хлорирования, б и Б обозначают содержание кальция
(Са) или хлора в виде хлорида, гипохлорита и хлората в экв/л
щелока до и после хлорирования, в обозначает содержание
Са(ОН)2 в экв/л щелока до хлорирования и м обозначает отношение объема щелока после хлорирования к объему щелока до
хлорирования, рассчитываемое по изменении молярности щелока (сумма молей щелочи, хлорида, гипохлорита и хлората).
Расчет выхода хлората по последней формуле прйкодится часто
применять, поскольку для приготовления известкового молока
1 Как окислитель СЮ* имеет шесть окислительных эквивалентов.
')Л1>зуются 'производственные иромыштыс поды, спдгржпщис
>, it и хлорид, а также при обследовании отдельных периодов
х, ровапия (как в башнях, так и в абсорберах и т. д.). При
эт1 ак как в формулу расчета входит коэфициепт изменения
об в /и, необходимо строго следить, чтобы не произошло ни
ра: ения, ни испарения пробы с момента отбора до момента
ан . Если щелок до хлорирования содержал только хлорид
и »держал ни гипохлорита, ни хлората, то расчет выхода
мг производить без учета изменения объема яг.
А (в “f* б) 100 л.
выход хлората = jTy—%,
где обозначения те же, что и выше. При расчете по данной
формуле изменения объема от разбавления водой или от испарения воды из пробы, взятой для анализа, не влияют на правильность расчета. /
Впервые расчет выхода хлората по изложенному принципу
соотношения составных частей щелоков был разработан и применен автором совместно с Jf. С. Гениным в 1929 г. Расчет хлората в приведенных формулах, как и в дальнейшем, (производится в окислительных эквивалентах.
б) Рас чет выхода гипохлорита по анализу
хлорированного щелока
При недохлорированном щелоке содержащийся в нем
Са(СЮ)г может при дальнейшем хлорировании перейти либо
в хлорат и хлорид (36) либо в хлорид и Ог (38). Поэтому гипохлорит, содержащийся в недохлорированном щелоке, нельзя
считать определенной потерей, и в таком щелоке надо параллельно выходу хлората рассчитать и выход гипохлорита. Этот
расчет делается по тому же принципу, что и расчет выхода
хлората, по формуле
СЮ-Ю0п;
выход гипохлорита = —^—%,
где СЮ и .Са обозначают их содержание в экв/j щелока К Содержание в щелоке СЮз кроме СЮ не влияет на правильность
расчета.
в) Расчет .процента потери при хлорировании
Потерей при хлорировании мы обозначаем выраженное в процентах отношение количества кислорода, выделив'шегося в виде
Ог по уравнению (39), к количеству кислорода, которое должн5
получиться по уравнению (37) в виде хлората, согласно количеству Са, содержащемуся в щелоке. По анализу хлорированного щелока процент потери рассчитывается по формуле
потеря от выделения Ог = 1,00 — (т + пг)%,
1 СЮ, как и СЮ», надо считать в. окислительных эквивалентах.
91
где т и пч обознпч.'иот проценты выхода хлората и гипохлорита,
рассчитанные, как наложено в пп. а и б.
Потеря от выделения ()« при хлорировании может быть также
рассчитана по анализу хлоргаза и абгаза при условии отсутствия
разбавления их воздухом во время хлорирования. Такой метод
расчета возможен однако только при непрерывности процесса
хлорирования (в абсорберах и т. и.), когда состав абгаза сравнительно мало изменяется. При этом расчете исходим из того,
что абсолютное количество азота одинаково в хлоргазе и аб-
газе. Формула «расчета будет:
потеря от выделения кислорода = v-—~ %,
где к и а обозначают содержание кислорода (к) и азота (а)
в абгазе, а К, А и X обозначают содержание кислорода (К),
азота (А) и хлора (X) в хлоргазе. Примеры расчета процента,
потери по этой формуле приведены в табл. 21.
Таблица 21. Примеры р л счета процента потери хлората при
хлорировании по анализам хлоргаза и абгаза
№• примеров
Состав хлоргаза
в “/о
Состав абгаза
в °/о
Расчет процента потери хлората по формуле
( кА - Ко) 200 .
ал
значают содержание кислорода (к) и азота (а) о
абгазе, а Я, А и X обозначают содержание
кислорода (Я), азота (А) и хлора (X) в хлоргаз
хлор
кисло¬
род
а^от
хлор
кисло¬
род
азот
1
90
2,1
7,9
50
12,5
37,5
(12,5 • 7,9 — 2,1 • 37,5) • 200:37,5 • 90 = 1,19
•2
90
2,1
7,9
15
23
62
(23 • 7,9 — 2,1 • 62) • 200:62 • 90 = 1,85
3
94
13
4,7
1,0
40
59
(40.4,7 —1,3 • 59) • 200 : 59-94 = 4,0
4
40
17
43
0,5
30
69,5
(30• 43 —17- 693) • 200:69,5 • 40 = 17,9
5
40
17
43
0,5
33
66,5
(33-43 -17-663)-200:66,5-40 = 18,9
'
г) Расчет процента потери хлора с абгазом (при*
непрерывном методе хлорирования)
При содержании в абгазе примеси хлора, процент потери
хлора не равен проценту содержания хлора в абгазе, поскольку
объем абгаза не равен объему хлоргаза. Согласно содержанию
процента хлора и> процента азота в хлоргазе и абгазе формула
расчета потери хлора будет:
потеря хлора с абгазом
где х и а обозначают содержания хлора (х) и азота (а) в абгазе,
а X и'А обозначают [содержание хлора (X) и азота (А) в хлоргазе. Расчет верен .только при отсутствии подсоса воздуха во
время хлорирования.
92
Ecjjh пренебречь цзмг.челнем ооъемл аоглза от кислорода*
выделяющегося при хлорировании, можно рассчитать потерю
при хлорировании по формуле
М • (ЮО — М) 100
потеря при хлорировании —°/
/
в/ ' % абсорбции
j. .:азе хлора
АЦЩО —л)
%CLt6t
adzase
Рис. 45. Номограмма для расчета проценту абсорбции
хлора при хлорировании
0, х х (А — В)» 10000
% абсорбции = L_2__,
где А — % С12 в хлоргазе, а В — % С12 в абгазе.
где М обозначает процент хлора и СОг в хлоргазе, а л— процент хлора и СОг в абгазе. Эта формула проще для практического г применения, поскольку требуется только определение
суммы хлор + СО*, что весьма просто. Для расчета можно также
пользоваться но'мограммой рис. 45.
/> .. >
\
93
ГЛАВА 5
ОБЕЗВРЕЖИВАНИЕ ХЛОРИРОВАННЫХ ЩЕЛОКОВ '
§ 1. Сущность обезвреживания
Как указано на стр. 66, щелок, полученный в результате хлорирования, содержит растворенный хлор и часть неразложен-
ного гипохлорита, и тем больше, чем ниже была температура
конца хлорирования. Как растворенный хлор, так и гипохлорит,
содержащиеся в щелоке, являются вредными для дальнейших
Рис. 46. Содержание СЮ' в
экв/л щелока при разной ко- Рис. 47. Изменение содержания СЮ' в пененной температуре хлорирс- рехлорированных щелоках при их хра-
вания известкового молока, сс- нении при 20, 50 и 100°.
держащего СаО 100—110%.
стадий производства из-за сильно коррозийных свойств; поЗтому
щелок после хлорирования подвергают «обезвреживанию» —
обработке, имеющей целью перевести хлор и гипохлорит в безвредные соединения (в дальнейшем сумму хлора и гипохлорита
будем обозначать как СЮ').
Обезвреживание можно производить нагревом щелока и продувкой его воздухом или прибавлением неорганических или
органических восстановителей. При нагреве щелока уменьшается
растворимость хлора, почему избыток его выделяется из щелока,
94 ' ч
и происходит разложение гипохлорита но уравнениям (36) и (-•)■
Продувкой воздухом значительно ускоряется действие нагрева,
а частично выдувается хлор и без подогрева. Однако полное
удаление СЮ' нагревом и продувкой весьма длительно, так как
чем меньше концентрация СЮ', тем медленнее его уменьшение
(рис. 46, стр. 94). Прибавляя восстановители, переводят СЮ'
в СГ, так как хлор и гипохлорит являются весьма энергичными
окислителями. Схематически уравнение обезвреживания восстановителями будет:
СЮ' + М = С1' + МО, (44).
где М обозначает восстановитель.
В зависимости от характера восстановителя, эта реакция проходит с разной скоростью и при разной температуре.
Если щелок содержит щелочь, то в нем не может содержаться:
хлора, а гипохлорит становится более трудным обезвредить.
Нагрев такого щелока весьма медленно разрушает гипохлорит.
Большинство восстановителей в щелочной среде также реагируют гораздо медленнее.
На рис. 46 показана зависимость содержания СЮ' в щелоке,
полученном хлорированием известкового молока с концентрацией СаО в 110 г/х от температуры конца хлорирования.
На рис. 47 приведена диаграмма изменения содержания СЮ'
в перехлорированном щелоке, хранившемся при различной температуре. Опыты производились в колбах с обратными холодильниками, чтобы не изменялась концентрация щелока от
испарения при нагреве.
Необходимо отметить, что анализы щелоков после полного
исчезновения в них гипохлорита показали, что разложение
гипохлорита шло почти исключительно в сторону образования
хлората (36) при незначительном выделении Оа (38). При других проведенных нами опытах с нагревом щелока, содержавшего^
гипохлорит и Са(ОН)2, разложение гипохлорита шло почти
поровну по уравнению (36) и уравнению (38).
§ 2. Обезвреживание неорганическими восстановителями
В практике хлоратных производств для обезвреживания щелоков от СЮ' применяют аммиак, гипосульфит и другие восстановители. Аммиак прибавляют в виде разбавленного раствора к горячему щелоку. При взаимодействии с СЮ' аммиак
окисляется до азота, а СЮ' восстанавливается до СГ:
ЗСЮ' + 2NHS = ЗС1' + N2 + ЗНаО. (45)
Полностью реакция по уравнению (45) проходит лишь при
60—70°. При более низкой температуре частично от взаимодействия аммиака и СЮ' образуете^ монохлорамин:
: СЮ' + NHs = NHaCl + ОН'. (46>
95
Чем ниже температура щелока, тем большая часть С1' реагирует
по уравнению (46) и меньшая часть реагирует но уравнению (46).
При избытке аммиака расход его на обезвреживание растворенного хлора больше, чем по уравнению (45), так как часть
.аммиака уходит на нейтрализацию хлора и кислоты, содержащихся в щелоке:
ЗСЬ + 8NH3 = N2 + 6NH4CI (47)
ИДИ
ЗНСЮ + ЗНС1 + 8NH3 = N2 + 6NH4CI + ЗН2О. (48)
Хлор и аммиак могут образовать также хлористый азот,
-являющийся сильно взрывчатым веществом: ' '
NHj + 3CU = NCls + ЗНС1. ' (49)
Однако реакция (49) проходит только при большом избытке
аммиака или NH4CI, например при пропускании хлора в их насыщенный раствор.. При. обезвреживании хлорированных щелоков
таким образом нет условий для образования NCU.
В присутствии щелочи реакция (45) проходит несколько
медленнее и требует более высокой температуры, чем в нейтральной или слабокислой среде. В производственных условиях
обычно задают аммиак несколько меньше теоретически необходимого согласно содержанию СЮ' и остаток СЮ' дообезврежи-
вают раствором гипосульфита.
Схематически реакция СЮ' с гипосульфитом идет по следующему уравнению:
4СЮ' + S2O3" + НгО == 2С1' + 2НС1 + 2SO4". (50)
Реакции СЮ' с гипосульфитом в разной среде выражаются следующими уравнениями: -
2Са(СЮ)г + Na2S20s + Са(ОН)2 = 2CaS04 + 2NaCl +
-f- СаС1г НгО. (51)
2Са(СЮ)г + Na2S203 + Н»0= 2CaS04 + 2NaCl + 2НС1. (52)
4С1г + ИагЭгОз + 5НгО == 2H2SO4 +.6НС1 + 2NaCl. (53)
4НСЮ + 4НС1 + Na2S203 + НгО = 2H2SO4 + 6НС1 + 2NaCl. (54)
Реакция (51Упроходит в щелочной среде, реакция (52) в нейтральной среде, реакции (53) и (54) в кислой среде (щелок с растворенным хлором). Отрицательной стороной Обезвреживания
типосульфитом является образование в хлорированном щелоке
малорастворимого CaS04 (обменная реакция Na2S04 и H2SO4
■с СаСЬ).
Положительной стороной обезвреживания гипосульфитом
является то, что реакция с СЮ' происходит очень быстро, вне
зависимости от среды и температуры. ,
/Применение Na2SOs для обезвреживания менее выгодно ввиду
•большого расходного коэфициента. Реакция СЮ' с Na2S03 про-
тсбдит по следующему уравнению:
СЮ' + Na2SOs = Cl' + NasSol (55)
NaaS реагирует с гипохлоритом, частично окисляясь до Na^SOi,
а частично только до серы:
СЮ' -b Na2S + НоО = СГ + 2NaOH +S. (56)
4CIO' + Na»S = 4СГ + Na2S04. (57)
Нитриты окисляются СЮ' до нитратов:
СЮ' + NaN02 = Cl' + NaNO;». (58)
Перекись водорода (и другие перекиси) реагируют с СЮ'
с выделением кислорода, что может быть использовано для
газволюметрического определения СЮ':
СЮ' + Н2О2 = Q' + Н20 + 02. (59)
В промышленном масштабе последние реагенты не применяются
для обезвреживания вследствие их дороговизны по. сравнению
с аммиаком и гипосульфитом.
§ 3. Обезвреживание органическими веществами
Большинство органических веществ окисляется СЮ'. Схематически эту реакцию можно изобразить следующим уравнением:
2СЮ' + С = 2СГ + СОг. (60)
Практически, при реакции СЮ' с органическими веществами
большей частью образуется не С02, а различные промежуточные
продукты окисления. В заводской практике для обезвреживания СЮ' часто применяют мелассу {отход сахарного производства). Мы встречали также успешное (применение сахара,
спирта, муки, опилок, угля, экскрементов. Механизм реакции
всех этих веществ в основном одинаков и разница только в скорости реакции и удобстве применения. Растворимые вещества
(сахар, спирт) реагируют гораздо быстрее, чем нерастворимые
(опилки, мука и т. д.). Кроме того избыток последних образует шлам, загрязняющий щелок. Чем меньше концентрация
СЮ' и ниже температура щелока, тем длительнее идет
обезвреживание. Особенно замедляете^ обезвреживание от наличия щелочи. Практически, минимальной температурой. обезвреживания органическими веществами является 60—70°.
§ 4. Аппаратура и техника обезвреживания
При получении сильно недохлорированного щелока, содержащего много Са(СЮ)2 и Са(ОН)2, следует его возвратить на
дохлорирование. Если это невозможно, надо дать щелоку отстояться, отдекантировать прозрачный щелок от осадка и осветленный щелок обезвредить обычным путем. Такой щелок, слитый с осадка Са(ОН)2, целесообразно продуть углекислотой или
дымовыми газами, чтобы деревести , растворенный в щелоке
7 Зав. 179. - Шройбм&н.
97
Са(011)г и СаСОя, a Ca(Cl())j и I К'К), поело «кто обсзпрс/мпы-
иис обычными реагентами проходит очень быстро.
При получении нормального «перехлорировапиого» толока,
не содержащего Са(ОН)г, следует сразу после окончания хлори-
рокания продуть щелок сжатым воздухом. При хлорироиании
барботажем и башнях, продувка производится в самих башнях.
При непрерывном методе хлорирования (в абсорберах и т. и.)
продувку производят в баках-сборниках щелока. Чем выше
температура щелока, тем эффективнее продувка. При 70—76;
после продувки в течение 10—15 мин. в щелоке остается СЮ'
не больше 0,01—0,02 экв/л. Газы от продувки следует пускать
на абгазную установку для поглощения из них хлора.
После продувки к энергично перемешиваемому щелоку добавляют восстановитель (аммиак, гипосульфит, меласса и т. и.)
в виде раствора, разбавленного щелоком. Прибавление восстановителя производится согласно анализу щелока;1 обезвреживание считают оконченным, когда щелок показывает отрицательную реакцию на СЮ'. При обезвреживании аммиаком или
мелассой надо щелок предварительно подогреть до 60—70".
Обезвреживание производится в специальных баках — обез-
вреживателях, объемом в 15—20 м*. Если хлорирование производится в башнях (барботажем) с рабочим объемом, соответствующим 3—6-часовому поступлению хлора, то обезвреживание
можно производить в баи!нях для хлорирования, обеспечив невозможность попадания известкового молока, а особенно хлор-
газа в башни во время обезвреживания. Обезвреживаемый щелок обладает очень сильно коррозирующими свойствами (горячий раствор кальциевых солей, содержащий растворенный хлор),
почему обезвреживатели должны быть выложены диабазом, андезитом, кислотоупорным кирпичом и т. п. материалами. Снаружи баки-обезвреживатели должны иметь тепловую изоляцию.
К бакам должна быть подводка пара для подогрева щелока и
воздуха для перемешивания. При способе производства с применением выпарки щелоков подогрев можно вести открытым
.паром, так как змеевики и т. п. устройства сильно корродируются. 2 При способе производства без применения выпарки
разбавление щелоков от нагрева открытым паром нежелательно
и подогрев производят паром по чугунным змеевикам, расположенным в нижней части баков> Форма баков-обезвреживате-
лей обычно принимается цилиндрическая с конусным дном.
Сверху баки должны быть закрыты коническими крышками (или
1 Приводим пример расчета количества аммиачной воды, необходимой
для обезвреживания.
'Количество хлорированного щелока 12 л*.
Содержание СЮ' в щелоке равно 0,02 экв/л.•
Содержание NH* в аммиачной воде равно 126 г/л.
„ , . 5.67-0,02-12.1000 ,.и
^ Надо .прибавить аммиачной воды jjg = 10,8.*, где ко
эфициент 5,67 выведен из ур-ния (45).
* Разбавление щелока при нагреве открытым паром равно 2—3%.
зонтами) с отводном трубой для вывода пара и газон, выделяющихся при обезвреживании н атмосферу над крышей здания.
Над обезвреживатслнми располагают бачок для растворов реактивов, применяемых для обезвреживания (аммиак, гипосульфит и 1. д.). Этот реактивный бачок должен иметь мерное стекло
с делениями для замера прибавляемого раствора реактива; от
бачка должен быть трубопровод ко всем бакам-обсзвреживате-
лям (см. Ж. X. П. № 28—30, 1930 г., стр. 1747 -1748 и Ж. П. X.
1937, № I, стр. 36 и № 8, стр. 1380).
ГЛАВА 6
ОТДЕЛЕНИЕ ШЛАМА ОТ ХЛОРИРОВАННЫХ ЩЕЛОКОВ
§ I. Состав шлама
Как указано на стр. 67, щелок, получаемый после хлорирования, содержит некоторое количество нерастворимых примесей,
образующих осадок (шлам). Состав шлама зависит от состава
примесей в извести, применяемой для хлорирования (стр. 39).
Обычно шлам состоит в основном из СаСОз и соединений Не,
Al, Si. Если щелок недохлорирован, то шлама особенно много,
и в основном он тогда состоит из Са(ОН)». Чем выше концентрация щелока, получаемого при хлорировании, тем больше в нем
шлама, ибо тем больше трудно реагирующих с хлором примесей остается в осадке (СаОО*, соединения Mg'' и SOC и некоторые другие).
Содержащийся в щелоке шлам должен быть отделен до выпарки и до обменной реакции. При выпарке щелока, содержащего шлам, на стенках нагревательных тел выпарных аппаратов
образуется осадок, ухудшающий теплопередачу и т. д. При плохом отделении шлама последний может также попасть на кристаллизацию и загрязнить готовую продукцию. При отделении
шлама после обменной реакции потери хлората увеличиваются
вследствие более легкой кристаллизации КСЮз в отделяемом
шламе. Содержание СЮ' в щелоке при отделении шлама недопустимо ввиду возможности разъедания аппаратуры, в которой
производится отделение шлама.
Отделение шлама от щелока производится отстоем или
фильтрацией. Оба метода отделения шлама имеют свои преимущества и недостатки и будут подробно рассмотрены ниже.
Отделение шлама отстоем требует баков больших объемов, но
зато щелока получаются более чистые. Кроме того при отделении шлама отстоем меньше механические _ потери щелоков и
процесс требует меньше обслуживания. Однако отстоем легко
отделить шлам только от щелоков низкой концентрации. Щелок
высокой концентрации имеет большую вязкость и -отстой шлама
из него очень длителен.
7е
89
§ 2. Отделение шлама отстоем и выщелачиванием
Обезвреженный щелок перекачивается в баки-отстойники,
где отстаивается от шлама. Через несколько часов обычно осветляется большая часть щелока, который декантируется и пере-'
качивается для дальнейших стадий производства. Отстоявшийся
шлам спускается из отстойников в баки-выщелачиватели. По наполнении этих баков в них происходит дополнительный отстой,
при котором шлам уплотняется, а 60—70% щелока осветвлястся.
Щелок перекачивают в сборник осветленного щелока, а уплотненный шлам разбавляют горячей водой (конденсат с выпарки),
перемешивают воздухом и оставляют на несколько часов. Осветленная * жидкость декантируется и перекачивается на выпарку
или на приготовление известкового молока и т. д. (в зависимости от ее удельного веса). Осевший шлам еще 2—3 раза выщелачивают таким же образом, после чего шлам, в котором уже
содержится очень мало хлората, спускают в канализацию.
Отстойники и обезвреживатели обычно представляют собой
железные цилиндрические баки с коническим дном. Щелока и
жидкости от выщелачивания, находящиеся в этих баках, не содержат СЮ' и имеют температуру обычно не выше 40—50°;
поэтому коррозия от обезвреженных щелоков и от жидкостей,
получающихся при выщелачивании шлама, гораздо меньше, чем
например от перехлорированных щелоков, и баки для этих жидкостей можно не футеровать, а достаточно покрыть их внутреннюю поверхность антикоррозийным лаком и т. п. Снаружи эти
баки должны иметь тщательную тепловую изоляцию, поскольку
скорость отстоя шлама тем больше, чем выше температура
щелока. К бакам должны быть подведены воздух для перемешивания, пар для подогрева, а также конденсат и вода. Первичный отстой можно также производить о баках, служащих для
обезвреживания щелока от СЮ'. При такой схеме отделения
шладоа количество необходимых баков значительно сокращается.
§ 3. Отделение шлама на фильтрпрессах
При отделении шлама фильтрацией объем отделенного шлама
гораздо меньше, чем при отделении шлама отстоем. При щелоках высокой концентрации осветление щелоков отстоем кроме
того весьма длительно. Поэтому метод отделения шлама фильтрацией имеет много сторонников, особенно при щелоках высокой концентрации. Недостатком отделения шлама фильтрацией
является то, что практически отфильтрованные щелока часто
получаются мутные и имеются значительные механические потери щелоков.
Имеется много типов аппаратов для отделения шлама фильтрацией. В дарное время большей частью применяются рамочные фильтрпрессы, состоящие из 30—50 рам и плит. Щелок
с взвешенным в нем шламом подается под давлением в фильтрпресс, при прохождении щелока через фильтрпресс шлам удер-
100
живается полотнами, натянутыми на плиты. Давление, иод которым подастся щелок, должно повышаться постепенно, по мере
увеличения количества шлама, осевшего в плитах фильтрпресса.
Слишком большое давление может вызвать прорыв полотен
фильтрпресса. Малейшее содержание СЮ' в фильтруемом щелоке вызывает весьма быстрый износ полотен (даже через
30—60 мин. работы). При щелоке, не содержащем СЮ', полотна
выдерж :акУг 5—10 операций. По заполнении плит фильтрпресса ..1Мом (что замечается по сильному замедлению вытекания > лока из фильтрпресса) останавливают подачу щелока и
пускают в фильтрпресс горячую воду для промывки отжатого
шлама. Промывку горячей водой продолжают до получения
промывных вод с уд. вес. 1,005—1,010. После этого фильтрпресс
разбирают и очищают рамы от «хлебов» отжатого и промытого
шлама, являющегося отбросом производства. Промывные воды
используются для приготовления известкового молока и т. д.
Вместо промывки можно также производить выщелачивание
'отжатого шлама в специальном баке-выщелачиватслс.
Рамы и плиты фильтрпрессов могут быть чугунные или деревянные. И те и другие обычно быстро изнашиваются ввиду
разъедающего действия горячих щелоков. Износ в основном
выражается в том, что фильтрпресс пропускает мутные щелока
и что становится трудно создать значительное давление, вследствие чего ухудшается отжатие шлама, и т. д. Несколько длительнее и спокойнее работа с 'деревянными плитами и
рамами.
§ 4. Схемы отделения шлама от щелока низкой и высокой
концентрации
При производстве бертолетовой соли с применением выпарки
несомненно надо отдать предпочтение отделению шлама
Рис. 48. Схема [отделения шлама от хлорированных щелоков слабой концентрации.
отстоем. Осветление горячего щелока низкой концентрации происходит весьма быстро и обычно через 1—2 часа отстоя осветляется 90—95%-щелока. Схема отделения шлама от щелока низкой концентрации показана на рис. 48.
101
При способе производства бертолетовой соли, при ко’ю.юм
хлорированием получаются щелока высокой концентрации,
•можно рекомендовать комбинирование отделения шлама отстоем
и фильтрацией, что показано на рис. 49. Целесообразнее приме¬
рно. 49. Схема отделения шлама от щелоков высокой концентрации.
нение варианта а схемы, показанной на рис. 49, так как при этом
через фильтрпрессы проходит только часть щелока, вследствие
чего меньше и потеря щелока.
Хлорат, который остается в выщелоченном или промытом
шламе, является потерей. Поэтому чем больше общее количество
шлама и больше содержание хлората в шламе, тем больше и
потеря хлората со шламом. При отделении шлама отстоем и
выщелачиванием и при хлорированном щелоке низкой концентрации в выщелоченном шламе остается очень мало хлората,— практически меньше 1% от общего количества хлората
в щелоке, от котор.ого отделяется шлам. Однако потерей
является и часть хлората, попадающего в жидкость от выщелачивания, поскольку при использовании этой жидкости (на приготовление известкового молока и т. д.) имеются потери. Гораздо выше потери при отделении шлама на ^фильтрпрессах.
В основном эти потери являются механическими ввиду течи
фильтрпрессов и т. д. На одном известном нам заводе производства бертолетовой соли при отделений шлама на фильтрпрессах
потери (среднемесячные) доходили до 5—8% от общего количества хлората.
В заключение -приводим анализ выщелоченного шлама, содержание СаС1г и Са(СЮз)г и температуру замерзания жидкости от
Вариант вд
Хлорированный щелок
§ 5. Потеря хлората со шламом
102
лытолачиияппя разт
фильтрнрсссного шлам.
' -льного псса (табл. 22) и сошли
: после промиики (табл. 2:)).
Таблица 22. С о д е р ж а пне - н Са(СЮ3)« и темпер а т у р а :» а м е р-
з а н и я жидкости, п о л у ч • ‘I при п р о м ы в к е и н ы щ е л а ч ir-
п а и ни шлама, отделен И' от хлорированных щелок о и
г
Удельный вес
1,007
1,014
1,021
1,029
1,(М
1
i .-на
1,051
1,059
1,067
1,074
1,083
1,091
1
1,099 |
1
1,107
CaCIo г/л . . .
7
13
20
27
33
40
47
53
61
69
77
85
93
102
Са(СЮ3)2 z/л •
Температура
2
5
7
10
12
15
18
20
23
26
29
32
35
38
замерзания °С.
*
—1
—2
-3
—4
-4,5
-5
—5,5
-6
:блица 23. Примерный состав фильтрпрессного шлама до и.
п о с л е п р о м ы в к и .
Состав
°/о нерастворимого остатка
°!о влаги
®/о СаС1„
°1о Са(С10,),
После промывки . .
. . .
35—40
50—60
40—50
30—40
6—9
1—2
2-3
ОД—0.6
ГЛАВА 7
ВЫПАРКА ХЛОРИРОВАННЫХ ЩЕЛОКОВ
§ 1. Цель выпарки и место ее в схеме производства
При хлорировании известкового молока с концентрацией СаО
'110—120 г/л получается щелок с содержанием Са(СЮз)з 60—
70 г/л. После обменной реакции такого щелока с КС1 получаемый бертолетовый щелок содержит КСЮз 70—80 г/л. При
охлаждении такого щелока выпадает лишь небольшая часть
КСЮз в виде кристаллов, а остальное количество КСЮз остается
в растворенном состоянии. Для увеличения выхода хлората при
кристаллизации производят упаривание хлорированных щелоков.
Этим достигается повышение концентрации хлората, что увеличивает выход кристаллов бертолетовой соли при кристаллизации. Кроме того выход хлората еще увеличивается оттого, что
растворимость КСЮз понижается от повышения концентрации
СаСЬ (стр. 123).
Содержание в щелоке СЮ' весьма сильно увеличивает коррозию выпарных аппаратов. Содержание нерастворимого шлама
в щелоке, уменьшает теплопроводность нагревательных тел ввиду
образования накипи. Поэтому щелока до их выпарки надо обезвредить от СЮ' и отделить от шлама.
/
103
■Вопрос о проведении выпарки до пли после обменной реакции разрешается отдельными заводами по-разному. Мы сипаем
более целесообразным выпарку производить до обменной реакции, исходя из следующих соображении.
1. При перекачке щелоков, уваренных после обменной реакции, часто бывают случаи выделения КСЮз в трубопроводах
и т. д. Поэтому в производственных условиях из предосторожности не доваривают щелок, что увеличивает объем маточного
щелока и потери КООз с ним, либо снижают вакуум в аппаратах
(чтобы повысить температуру кипения), что снижает произиО-
дительность выпарной установки и увеличивает коррозию аппаратуры.
2. Щёлок, уваренный после обменной реакции, нельзя отстаивать от нерастворимых осадков, так как вследствие охлаждения
при отстое происходит выделение КСЮз. Поэтому соль, получаемая при кристаллизации из ;гаких щелоков, более загрязнена
нерастворимыми примесями.
3. Ввиду возможного выделения KClOis при перекачках, а
также при отборе проб, отобранная проба может быть частью
щелока, из которого частично выделился КСЮз или, наоборот,
» котором частично 'растворился КСЮз, ранее выпавший. Ilo-i
этому весьма затрудняется контроль выпарки и потерь хлората, что не дает возможности вести правильную борьбу
с нотерями.
Мы считаем, что трудность контроля выпарки при обменной
реакции до уваривания щелоков и является причиной разноречивых данных, приводимых в литературе о разложении хлората при выпарке (см. ниже § 4).
§ 2. Пределы концентрации увариваемых щелоков
Пределы концентрации увариваемых щелоков зависят or
того, производят ли обменную реакцию с раствором КС1 или
с твердым хлористым калием и от того, какой применяют избыток КС1 при обменной реакции и какая принята температура
конца кристаллизации. На основании наших исследований мы
считаем, что в случае выпарки до обменной реакции и в условиях избытка КС1 в 20% и вымораживания маточников 1-й кристаллизации до 10—20° ниже нуля оптимальным уд. весом
уваренного щелока при 70° является: 1,41 (42° Боме) при
обменной, реакции с раствором КС1 и 1,34—1,35 (36,6—37,4°
Боме) при обменной реакции с твердым хлористым калием.
При более низкой концентрации уваренного щелока увеличивается объем маточного щелока и потеря КСЮз с ним. При
более высокой концентрации уваренного щелока может выпасть
некоторое количество СаСЬ • 6НгО при вымораживании (см.
рис. 58, стр. 125).
При меньшем избытке КО или отсутствии избытка и при
более высокой температуре кристаллизации концентрация ува-
104
репного щелока может быть несколько больше иышспрннс/и п-
ной.
При выпарке щелока после обменной реакции концентрации
уваренного щелрка нрй избытке КС1 в 20% и применения вымораживания маточника должна быть уд. веса 1,34 (36,6° Боме
при 70°).
§ 3. Аппаратура и техника выпарки
Систем выпарных a jаратов много и их касаться мы тут не
будем. В производечве хлоратов применяются как однокорпусные, так и многокорпусные агрегаты. В отношении расхода пара
несомненно выгоднее работа на 2- даже 3-корпусной системе;
однако в многокорпусных системах температура кипения в первых корпусах высока, что вызывает увеличение коррозии их..
Последняя весьма значительна. Вообще надо стремиться к максимальному вакууму в выпарных аппаратах — к максимальному
снижению температуры. Многокорпусная система допустима
только в тех случаях, когда выпарные аппараты изготовлены из
антикоррозийного материала.
Железо, чугун, сталь весьма сильно разъедаются щелоком,
содержащим СаСЬ и Са(СЮз)г (или СаСЬ и КСЮз), и тем
больше, чем выше температура щелока. Свинец и особенно медь-
разъедаются во много раз меньше, ибо на них при выпарке образуется защитная пленка. Поэтому выпарные аппараты надо
делать медными или хотя бы с медными нагревательными телами. Еще лучше сделать аппараты футерованными диабазом
и т. п. Арматура аппаратов должна быть целиком медная. Перед,
поступлением в выпарные аппараты щелок должен пройти
теплообменник для подогрева. После выпарных аппаратов уваренный щелок поступает в баки для отстоя и оттуда в баки
обменной реакции. В случае уварки щелока после обменной
реакции уваренный щелок поступает из выпарных аппаратов непосредственно в напорные бачки над кристаллизаторами, по
щелокопроводам, которые должны иметь тепловую изоляцию или
даже паровую рубашку, чтобы в них не начался процесс кристаллизации. После выпарных аппаратов перед вакуум-насосами
должны быть 1 или 2 ловушки для улавливания брызг уваренного щелока. Одновременно должны часто производиться анализы проб барометрической, воды на содержание щелока (CIOs'
или СГ). Конденсат выпарки используется для промывки и перекристаллизации бертолетовой соли, для выщелачивания шлама
и для приготовления известкового молока (см. стр. 152).
При выпарке щелоков после обменной реакции весьма важно
расположить аппараты так, чтобы уваренный щелок поступал на
кристаллизацию самотеком. Перекачка уваренного щелока, содержащего КСЮз, неудобна ввиду возможности выпадения
КСЮз и засорения им насоса и трубопроводов от охлаждения
щелока при перекачке. При выпарке щелоков до обменной реакции располагают аппаратуру так, как удобнее в смысле обслу-
105
жи вании и уменьшения занимаемого здпшы (uuu--mu л один
этаж), так как перекачка не вызывает усложнении.
§ 4. Разложение хлората при выпарке
Литературные данные по этому вопросу разноречивы:
Юриш 1 указывает на большой процент разложения и даже приводит баланс одной операции выпарки в чугунных котлах,
обогреваемых голым огнем, где разложилось 40% хлората.
Лунге3 однако указывает на маловероятность этого факта
и считает, что в этом случае вероятно упаривали телок,
содержавший аюлыпос количество гипохлорита, который и
разложился. Вильдсрман (герм. пат. 449583, 1921 г.) считает
среднюю потерю от разложения хлората при выпарке в 15%,
указывая, что эго разложение имеет каталитический характер.
Лечцней9 указывает, что при многократном производственном
упаривании хлорированного щелока (до обменной реакции) до
удельного веса 1,50 (48° Боме) в чугунных котлах, обогреваемых
голым огнем, им ни разу не было замечено ни малейшего разложения хлората.
Нами вопрос о разложении хлоратов при выпарке изучался
в порядке производственных наблюдений и специальными лабораторными опытами. При обычной продолжительности выпарки
в 3—6 час. нами ни разу не было найдено заметного разложения
хлората. Если же упаривать щелок с железными пластинками
в течение многих суток непрерывно, то обнаруживается уменьшение содержания хлората при одновременном превращении
железа в Fe(OH)3 в - количествах, близких к эквивалентным.
Таким образом каталитического характера разложения нами не
обнаружено. Поскольку разложение хлората связано с величиной коррозии металла, величина разложения хлората при непродолжительной выпарке в 3—6 час. обычно измеряется сотыми, максимум десятыми долями процента, почему их и трудно обнаружить анализом.
В табл. 24 приведены полученные нами данные по изучению
разложения хлората при выпарке щелока в присутствии желез-
Таблица 24. Разложение хлората при выпарке хлорированных щелоков в присутствии железных пласт'инок прр
110—115°
/ Время нагрева
Содержание
в экв/л
Разложение
хлората
Уменьшение
веса железа;
К
СЮ/
сг
экв/л
гл
°/о
в г
1 сутки . .
2,77
2,48
0,09
0,39
3.1
0,3456
1,13
10 суток . . • ....
1.96
2,61
0,90
3,9
31,5
4,7131
0,83
20 ' *
0,93
2,78
1,93
8.3
67
11,1378
0,75
-30
0,43
2,87
2,43
10,5
85
133122
0,79
.306
)H,I\ ]|.l;iCTlll|OK. Опыт ПроВОДИЛСЯ П течение 30 суток при 1ГМ-
нературе 105—-III) и колос с обратным холодильником (чтобы
нс изменялась концентрация щелока). Начальный щелок содержал СГ 2,46 эк и/л и C1CV 2,86 эк в/я [СаСЪ 137 г/я и Са(СЮз)»
40,4 г/я |. Поверхность пластинок была 126 см2 на 250 пя щелока,
или 50,4 я2 на 1 м3. Графа К показывает уменьшение граммов
хлората на 1 г железа (см. также Ж. X. П. № 28—30, 1930 г.,
стр. 1748, журнал Химстрой № 11, 1932 г., стр. 1883 и журнал
Калий № 2, 1937 г., стр. 20).
ГЛАВА 8
ОБМЕННАЯ РЕАКЦИЯ
$ 1. Сущность обменной реакции
Целью обменной реакции является перевод Са(СЮз)2, содержавшегося в хлорированных щелоках, в КСЮз. Для этого к хлорированному щелоку прибавляют КС1 в количестве, эквивалентном содержанию Са(СЮз)2. Уравнение обменной реакции будет:
Са(СЮз)г + 2КС1 = СаС12 + 2КСЮз. (61)
Если исходить из общего состава хлорированных щелоков по
уравнению (37), то уравнение обменной реакции будет:
Са(СЮз)2 + 5СаСЬ + 2КС1 = 2КСЮ3 + 6СаС12. (62)
Складывая уравнения (37) и (62), получаем полное уравнение
получения КСЮз из извести, хлора и КС1:
6Са(ОН)2 + 6С12 + 2КС1 — 2КСЮ3 + бСаСЬ + 6Н20. (63)
Вместо КС1 для обменной реакции можно применять и другие
фли • калия, лишь бы КСЮз был наименее растворимым из четырех возможных компонентов системы, или чтобы образующееся соединение Са было нерастворимо (СаСОз, CaSC>4 и т. д.),
дабы возможна была дальнейшая кристаллизация КСЮз. Практически для обменной реакции кроме хлористого калия длительное время применяли поташ. Реакция с поташом проходит по
следующему уравнению
Са(СЮз)2 + К2СО3 = СаСОз + 2КСЮз. (64)
При этой реакции не образуется СаС12, что является ее преимуществом .в случае применения выпарки после обменной
реакции (объем маточника после кристаллизации получится на
Ve меньше, т. е. меньше будут и потери КСЮз с ним). Недостатком применения К2СОз является образование осадка СаСОз, при
отделении которого неизбежны потери щелока. Возможно применение для обменной реакции также K2SO<, KNOs, КОН. и т. д.
107
Коэфициенты обменном реакции с этими соединениями калия
рассчитываются из следующих уравнении:
1) Са(С10з)а Н- 2КС1 = 2КСЮз + СаСЬ;
2) Са(СЮ3)2 + К2СОз = 2КСЮз + СаСОз;
3) Са(СЮз)г + K2S04 = 2КСЮз + CaS04;
4) Са(СЮз)г + 2KNOs = 2КСЮз + Ca(NOj)2;
5) Са(СЮз)2 + 2КОН = 2КСЮз + Са(ОН)2.
При правильно проведенной обменной реакции в получаемом
бертолетовом щелоке содержатся только КСЮз и СаС12. Обычно
при обменной реакции дают избыток КС1 против теоретически
необходимого [соответственно • содержанию Са(СЮз)2], поскольку наличие КС1 в бертолетовом щелоке увеличивает процент выделения КСЮз при кристаллизации (стр.123). Избыток
КС1 разный для разных хлоратных заводов. По Ульману5
дают избыток КС1 в 3%, по Вильдерману (стр. 84) —в 2%; по
нашим исследованиям целесообразно давать избыток КС1
в 15—25% от теоретически необходимого. В начальном' периоде
производства бертолетовой соли, когда хлористый калий был дорог, его давали в недостатке против теоретически необходимого количества, с тем чтобы использование КС1 достигало
100% за счет меньшего использования хлора. Са(СЮз)2, остающийся в маточном щелоке при таком способе работы, разлагали
соляной кислотой для получения хлора (стр. 146).
Большинство заводов производит обменную реакцию с твердым хлористым калием. Большие преимущества имеет проведение обменной реакции с раствором КС1 особенно при хлористом
калии, загрязненном примесями (предложено И. Б. Фрайманом).
Основные преимущества такого способа работы следующие.
1. Проведение обменной реакции с раствором КС1 проще,
чем с твердым хлористым калием: не ^требуется элеватора, шнеков и т. п. устройств и уменьшается затрата труда.
2. Раствор КС1 легче дозировать, чем твердую соль — умень¬
шается возможность недодачи или передачи против рассчитанного Количества. '
3. Приготовленный раствор КС1 легко отстаивается от нерастворимых примесей и его можно очистить от соединения SO4"
и СОз", если таковые содержатся. Благодаря этому меньше
примесей попадает нй кристаллизацию, что улучшает качество
готового продукта.
4. В растворе КС1 легче определить примеси, чем в твердой
соли (однородность средней пробы), что облегчает контроль.
5. Обменную реакцию с раствором КС1 можно проводить при
более низкой температуре, благодаря чему уменьшается коррозия аппаратуры и увеличивается производительность кристаллизаторов.
6. 'Продолжительность обменной реакции с- раствором КС1
(прибавление раствора КС1 и перемешивание) равна 10—15 мин.
108
«место 2—3 час., обычно необходимых при твердой соли, благодаря чему уменьшается количество обменников и т. д.
При способе, исходящем из хлорирования известкового молока слабой концентрации и выпарки хлорированного щелока,
общий баланс выпариваемой воды не увеличивается заметно от
применения для обменной реакции раствора КС1, так как растворение КС1 производится на различных производственных промывных водах. При способе полученйя при хлорировании щелоков высокой концентрации без применения выпарки при обменной реакции с раствором КС1 увеличивается количество маточного щелока 1-й кристаллизации и потери с ним КСЮз. Однако
ввиду вышеизложенных преимуществ мы считаем целесообразным и при этом способе производить обменную реакцию
с раствором КС1, а не с твердой солью.
Обычно обменная реакция производится так, чтобы температура получающегося «бертолетового» щелока соответствовала
растворимости всей образовавшейся КСЮз. По нашим исследованиям обменная реакция проходит полностью через несколько
минут энергичного перемешивания, даже если прибавить твердый хлористый калий к холодному хлорированному щелоку (как
низкой, так и высокой концентрации). При таком способе
обменной реакции отпадает необходимость в кристаллизаторах,
и сразу после обменной реакции можно отжать полученную соль
от маточника. Недостатком такого способа обменной реакции
является очень мелкокристаллическая структура полученной
соли, вследствие чего ее труднее отжать от маточника и труднее промыть; содержание влаги в такой соли, отжатой на нуч-
фильтрах, равно 15—20%. /
§ 2. Аппаратура и техника обменной реакции
•Основными аппаратами обменной реакции являются баки-
обменники. Целесообразно придать обменникам форму цилиндра
с коническим дном. Изнутри обменники должны быть выложены
материалом, устойчивым против коррозии, поскольку продукты
коррозии попадают отсюда на кристаллизацию и в готовую продукцию. Довольно устойчивыми являются свинец и медь. Лучше
всего выложить обменники плитками из диабаза и т. п. Внизу
конуса обменника должен иметься штуцер для спуска щелока
после обменной реакции на кристаллизацию. К этому штуцеру
должны быть подведены воздух для продувки трубопровода и
Для перемешивания щелока и пар на случай необходимости
разогрева щелока. При обменной реакции с твердым хлористым калием обменники должны иметь тепловую изоляцию,
змеевики для подогрева и зонты для отвода паров.
При обменной реакции с твердым хлористым калием необходимы приспособления для взвешивании и для подачи хлористого калия в обменники (весы, элеватор, шнек и т. л-). При
обменной реакции с раствором КС1 необходимы растворитель
хлористого калия, бак для отстоя раствора КС1 от нераствори-
109
мых примесей, бак для сбора шлама, отстоявшегося от раствора
КС1, и для его выщелачивания. Эти аппараты все должны иметь
тепловую изоляцию и быть
устойчивыми против коррозии
горячими растворами, содержащими КС1 и КСЮз. Лучше всего выложить эти аппараты .плитками из диабаза и т. и. материала.
Во время обменной реакции
необходимо энергичное перемешивание щелока. Твердый
хлористый калий задают через
проволочную корзинку и т. и.
приспособления, чтобы нс могли
остаться непрореагировавшими
домки хлористого калия.
Для приготовления раствора
КС1 используют жидкость от
промывки бертолетовой соли
1-й кристаллизации. Выщелачивание шлама, отстоявшегося из
раствора КС1, производят конденсатом. Жидкость от выщелачивания шлама используют на приготовление раствора КС1.
На рис. 50 приведена температура начала кристаллизации
КСЮз из бертолетовых щелоков разной концентрации (не со-
Рис. 50. Температура начала кристаллизации КСЮа из берт( летовых
щелоков'разной концентрации.
Раствор ffCL
Уверенный щелок
-L
бак для
отстоя
раствора
r кСС
бак для
обменной
реакции
Шид
7б
Бертолетовой щелс к
МидкостЬ от прамЫвки
бертолетовой соли ^ |
1
Пар
VI
Раст во -
рителЬ
х/юри с -
то 90 калия
И
Отстой шлама
L
конденсат
костб от
\цела чабан
1
б а/f для
вьщела-
•w бания
шлама
на кристаллизацию
конденсат
БЬнцелоченнЫй шлам_
в камалиоацою
Рис. 51. Схема обменной реакции уваренного хлорированнсго щелока с pact
вором КС1.
110
держащих избытка КО). На рис. 51 приведена примерная* схема
расположении аппаратов и случае применения обменной реакции
с раствором КО. В табл. 25 приведено содержание КС1 в г/л
раствора разного удельного веса при 20, 60 и 8(Г.
Таблица 25. Содержание КС1 в растворах разного у дельно г (»
веса пр и 20, 60 и 80° »*•-»
Удельный вес раствора
1,00
1,07
1,08
1,09
1,10
1,11
1,12
1,13
1,14
1,15
1,1«
1,17
Содержание КС1 г/л
при 20°
100
117
135
153'
170
188
205
223
1
241
258
276
294
Содержание КС1 г/л
при 60°
129
146
163
180
198
215
233
251
269
288
307
327
Содержание КС1 г/л
при 80э
147
164
181
199
216
234
252
270
287
301
322
338
!
§ 3. Некоторые расчеты по анализам бертолетовых щелоков
1. Расчет выхода хлората. Выход хлората рассчитывается но
практическому количеству экв. СЮз, содержащемуся в бертолетовом щелоке, и теоретическому количеству эквивалентов СЮ#Г
которое равно найденному в щелоках количеству эквивалентов
Ра..Расчет выхода производится по формуле:
СЮ- • юо
* выход хлората = — Сд — °/0,
*
где СЮз и Са обозначают их содержание в экв/л бсртолеговОго
щелока. Формула расчета основана на том, что количество Са
не изменяется при разложении хлората и что при теоретическом
ходе процесса (уравнение 63, стр. 107) количество эквивалентов
СЮз и Са должно быть одинаково. Так как количество Са и
СЮз не изменяется при обменной реакции, то прибавление избытка КС1 или недодача КС1 не влияют на правильность расчета.
Если часть КСЮз уже выкристаллизовалась из щелока, то расчет
выхода по данной формуле уже нельзя делать.
2. Расчет состава бертолетовых щелоков. При правильно проведенной обменной реакции в бертолетовых щелоках должны
содержаться только СаСЬ и КСЮз. Практически, обычно содержатся еще или КС1 или Са(СЮз)г в зависимости от того, проведена ли обменная реакция с избытком КО или с недостатком
КС1. Поэтому при анализе бертолетовых щелоков для точного
расчета их состава необходимо определить кроме СЮз и С1 еще
калий. Формулы, расчета приведены в табл. 26.
3. Расчет процента недостатка или избытка КС1, заданного
при обменной реакции. Если в бертолетовом щелоке обнаружен
Ш
Таблица 26. Формулы расчёта содержал й я СаСЬ, Са (СЮ3)2, КСЮ3 и KCI
и:
О
*=:
о
U
tc
6
г*.
Са(СЮ»)а или КО, то правильность
проведения обменной реакции рассчитывают но следующим формулам:
недостаток KCI = -1-0
Са • М
о/
/о
х
3
е
о
о.
о
чо
о
Г?
о
б
8»&
о"£2
гь я г)
UU-
и 11
U
«1
и
и о.
IIII
б!
Но
OCJ (J "
ОО 3j?
II
О-,»
U
о
8 б
о"$
оу
о
КГ
й КСЬ6Ю0о,
избыток КС1 = ~~са~-~лГ~ ■0 ’
где Са(СЮа)а, КО и Са обозначают их содержание в ши/л щелока,
а УМ обозначает коэфициент выхода
хлората в щелоке до обменной реакции. Если М неизвестен, то принимают средний коэфициент выхода хлората для данных условий производства
(обычно в пределах 0,90 — 0,95).
Кристаллизация части КСЮз из
анализируемого щелока не влияет
на правильность данных формул
расчета.
Расчет формулы для процента недодачи КС1 основан на том, что до
обменной реакции количество окислительных эквивалентов Са(СЮя)г
равно количеству эквивалентов Са,
умноженному на коэфициент выхода
хлората. Расчет формулы для процента избытка КС1 основан на том,
что при обменной реакции прибавляется КС1 в количестве V» от количества Са (в эквивалентах), умноженного на коэфициент выхода хлората.
В
I
X
S2 22
ши (JCJ
ен о* Г573
[V.BA
*к kk
jto
2*
ГЛАВА 9
КРИСТАЛЛИЗАЦИЯ КСЮз ИЗ
БЕРТОЛЕТОВЫХ ЩЕЛОКОВ
§ 1. Сущность кристаллизации
Кристаллизация КСЮз основана на
разной растворимости его при высокой и низкой температуре как в чистой воде, так и в растворах СаСЬ.
Эта разница растворимости при высокой и низкой температуре весьма
значительна для КСЮз (выше чем
для большинства других солей), что
облегчает ее кристаллизацию.
/ •
112
В маточном щслокс после отделения выкристаллизовавшейся
КСЮз остается растворенной часть КСЮз, тем мепыиая,
чем ниже температура конца кристаллизации. Поэтому мри кристаллизации КСЮз из бертолетовых щелоков обычно применяют
вымораживание щелоков, охлаждая их до 10—20° ниже нуля.
Для этого кристаллизацию ведут в две стадии: сначала охлаждают щелок до температуры помещения, в котором производится кристаллизация, отделяют выделившиеся кристаллы
КСЮз и оставшийся маточный щелок охлаждают до низкой температуры. Такой способ кристаллизации в две стадии удобен
тем, что вести охлаждение до комнатной температуры можно,
используя атмосферный воздух или водопроводиую воду, и искусственный холод тратить только на вымораживание. Кроме
того кристаллы, выделяющиеся при низкой температуре, обычно
больше загрязнены примесями и при их отделении от холодного
маточника в них остается больше неотжатой Жидкости.
Основной примесью в бертолетовой соли, отделенной от
маточного щелока, является СаСЬ. Содержание СаСЬ и большинства других примесей значительно уменьшается промывкой
бертолетовой соли. При необходимости в особо чистом продукте соль, полученную при 1-й кристаллизации, перекристал-
лизовывают.
§ 2. Аппаратура для кристаллизации КСЮз
***
Основным аппаратом для кристаллизации КСЮз является
кристаллизатор. На современных хлоратных заводах распро-,
странено применение непрерывно-действующих кристаллизаторов Цана, охлаждаемых водой или воздухом. Кристаллизатор
Цана с водяным охлаждением показан на рис. 52.
Этот кристаллизатор представляет собой металлическую
трубу длиной в 10 лг и диаметром в 0,5 м, закрытую с обоих
концов крышками с отверстиями для входа щелока и для выхода маточйого щелока с кристаллами. Снаружи на трубу надет
кожух, По которому проходит охлаждающая вода. Кристалли-
8 За*. 179. — Шрайбжан. . 113
затор расноло ксн горизонтально (с уклоном н одну сторону на
5—10 см) на роликах н прощается со скоростью К)-- 15 об/мин.
Движение щелока и охлаждающей воды происходит но принципу противотока. Внутри трубы кристаллизатора помещается
брус сечением 30 X 40 лш и длиной, равной длине трубы.
При вращении кристаллизатора брус скользит по стенкам, благодаря чему выделяющиеся кристаллы не прилипают к аппарату.
Время пребывания щелока в кристаллизаторе очень незначительно (обычно 5—15 мин.), почему выделяющиеся кристаллы
весьма мелки. Производительность кристаллизатора зависит от
температуры и концентрации входящего щелока и температуры
и количества охлаждающей воды. Практически можно достигнуть суточной производительности в 3—4 т бертолетовой соли
на один аппарат. Труба кристаллизатора и брус должны быть из
материала, устойчивого против корродирующего действия бертолетовых щелоков и против механического износа. Хорошо
устойчива нержавеющая сталь. Если в цилиндре кристаллизатора получается течь, то ее легко обнаружить по разбавлению щелока, так как охлаждающая вода подается под давлением.
Гораздо меньшее распространение имеют кристаллизаторы
прерывного действия, так как их производительность во много
раз меньше, чем кристаллизаторов Цана и т. п. аппаратов.
Обычно это цилиндрический сосуд с коническим дном, окруженный кожухом для охлаждающей воды. Для ускорения кристаллизации и уменьшения прилипания кристаллов к стенкам такого
аппарата, щелок непрерывно перемешивается мешалкой со скреб-
• ками, делающей 10—15 об/мин. Устройство в таких кристаллизаторах змеевиков для охлаждающей воды нецелесообразно, так
как змеевики быстро обрастают кристаллами, отчего сильно
уменьшается их теплопроводность. Кристаллизация в таком
аппарате продолжается обычно 12—18 час. и больше. При отсутствии перемешивания происходит нарастание кристаллов на
стенки аппарата, снятие которых требует специальных приспособлений и ручного труда. Кристаллы, снятые со стенок, обычно
загрязнены продуктами коррозии аппарата. Ряд таких кристаллизаторов может работать последовательно, чем устанавливается
непрерывность в их работе. При этом устанавливают противоток, так что свежий холодильный рассол поступает в кожух
кристаллизатора с наиболее холодным маточным щелоком. Холод вымороженного маточника можно использовать для начального охлаждения нового количества неохлажденного маточника.
Для отделения выделившихся кристаллов от маточного и(е-
лока в практике хлоратных заводов применяются большей
частью центрофуги *. Кроме того применяются также «декан-
теры» — цилиндрические невысокие сосуды с коническим дном,
1 Удобными являются центрофуги с подвешенным барабаном на одной
оси с мотором, расположенным вверху.
- 114
и которые собирают кристаллы и маточную жидкость пч iieiipe-
рывнодсйствующпх кристаллизаторов. По заполнении дсканге-
ров после 10—15 мин. отйтоя спускают из них отстоявшийся
маточный щелок, после чего осевшие кристаллы передаются на
центрофуги для отжатия от остатка маточника. В декантерах
возможна также промывка осевшей соли энергичным перемешиванием ее водой.
Вместо центрофуг применяются иногда нутч-фильтры, которые имеют некоторые преимущества: отсутствие трущихся частей и моторов, что весьма важно в отношении техники безопасности (см. стр. 330) и возможность лучшей промывки соли, что
значительно улучшает качество продукции (см. табл. 29,
стр. 122). Недостатком нутч-фильтров является повышенная
влажность отжатой на них соли по сравнению с солью, отжатой
на центрофугах (на 1—2%).
Из других основных аппаратов, применяемых в фазе кристаллизации, необходимо отметить растворитель для перекристаллизации соли и отстойники «разваренного щелока» (под таким
названием фигурирует на хлоратных производствах горячий
раствор перекристаллиэуемой бертолетовой соли). В качестве
растворителя можно применять простой бак с мешалкой и с. подводом пара и воды. Требуемая производительность растворителя невелика — обычно не больше 10—15 т КСЮз в сутки.
Отстойники «разваренного щелока» применяются для отстоя
щелока от нерастворимых примесей, бывших в бертолетовой
соли первой кристаллизации.
Материалами, довольно, устойчивыми против корродирующего действия «разваренных щелоков», являются медь и свинец,
которыми целесообразно выложить растворитель и отстойники,
чтобы не загрязнить продуктами коррозии перекристаллизуе-
мую соль. Еще лучше футеровать эти аппараты плитками из
диабаза и т. п. материала. Снаружи растворитель и отстойники
должны иметь тщательную тепловую изоляцию.
Кроме этих аппаратов в фазе кристаллизации применяются
еще баки-сборники для маточных щелоков и промывных
жидкостей. Эти баки делаются обычно железные, так как корродирующее действие холодных маточных щелоков и Цромывных
Жидкостей невелико.
' ‘ ■> У
§ 3. Рациональная схема кристаллизации
• Бертолетовый щелок из обменников 'самотеком поступает
"в кристаллизаторы Цана. Мея^ду ними ставится промежуточный
'желоб — распределитель щелока. Выходящий из Цан’ов охлажденный щелок вместе с выделившимися кристаллами поступает
в декантеры, в которых кристаллы КСЮз оседают, а отстоявшийся маточник декантируется и .перекачивается в выморажива-
тели для дополнительного выделения КСЮз путем охлаждения
до низкой температуры. Вымораживание производится в вертикальных цилиндрических кристаллизаторах. * По достижении
-
115
достаточно низкой температуры прекращают псрсмсппшанис,
дают осесть выделившимся кристаллам КСЮз и отстоявшийся
«вымороженный» маточный щелок декантируют и перекачивают
к потребителю (гл. 12). Очень важно, чтобы с вымороженным
маточным щелоком не ушли взвешенные кристаллы КСЮз, для
чего по пути щелока ставится ловушка, в которой благодаря
потери скорости движения маточника взвешенные кристаллы
улавливаются посредством различных приспособлений. Отстоявшиеся в вымораживателях кристаллы взмучиваются с остатком
маточного щелока и перекачиваются в декаитсры.
Осевшая в декантерах соль после спуска маточной жидкости
1— 2 раза промывается посредством взмучивания с маточной
жидкостью от 2-й кристаллизации при тщательном перемешивании сжатым воздухом. При этом в жидкость переходит большая
часть растворимых примесей бертолетовой соли, осевшей при
кристаллизации. Также переходит в промывные воды часть нерастворимых примесей (CaSC>4, глина) более мелких и легких, чем
кристаллы КСЮз (если таков,ые примеси имеются). Жидкость от
промывки в зависимости от ее удельного веса перекачивают
в вымораживатели или в сборник жидкости для приготовления
раствора КС1 для обменной/реакции.
Соль, промытая в декантерах, отжимается на центрофугах от
избытка маточной жидкости и тут же дополнительно промывается
маточной жидкостью от 2-й кристаллизации. Передача соли из
декантеров в центрофуги осуществляется самотеком или взмученная, в небольшом количестве маточного щелока соль перекачивается насосом. Над ц€нтрофугами устанавливается бачок-
мерник для промывной жидкости (см. табл. 30,,стр.-123)1
Отжатая на центрофугах соль выгружается и передается в вагонетки для отвозки на сушку (если готовят соль 1-й кристаллизации) или в растворитель для приготовления «разваренного
щелока» горячего раствора удельного веса 1,18—1,2Г, содержащего КСЮз 300—350 г/л. Растворение соли производится
в жидкости от промывки соли 2-й кристаллизации и в маточной
жидкости от предыдущего цикла перекристаллизации, содержащей еще мало СаС1г. Растворение производится при подогреве
открытым, паром до 100—105°. Полученный «разваренный щелок» перекачивается в бак-отстойник, где оставляется для отстоя
от нерастворимых примесей. Хорошо прибавить к разваренному
щелоку ИагСОз (0,1—0,2 г/л) для осаждения соединений“Fe, Pb,
Си и др. Отстоявшийся щелок пускается на кристаллизацию.
Отстой шлама спускается в особый бачок, в котором произвол
дится выщелачивание КСЮз горячей водой.
Вторая кристаллизация производится аналогично первой
кристаллизации. Только маточный щелок 2-й кристаллизации не
вымораживается, а используется для промывки соли 1-й кристаллизации. Для промывки соли 2-й кристаллизации применяют
холодный кондецеат. Промывную жидкость используют для растворения соли 1-й кристаллизации. Промытая, отжатая соль
2- й кристаллизации- передается на сушку.
116
‘ •
Рис. 53. Схема кристаллизации бертолетовой соли.
tr
т>
*§
л и
^«1
гЛ
У.
</ мтро<рч г с.
X элодиЫй
конденсат
I
/
nntru£nVirpUJOB<fif9tf9V ШО VffOifltl з^ньотсм
Ыа рис. 53 показана схема расположении основной аппаратуры кристаллизации (за исключением вымораживателей).
Вместо декантеров и центрофуг возможно применение нутч-
фильтров, что имеет некоторые преимущества (см. стр. 115).
При кристаллизации и особенно при перекристаллизации
необходимо обращать особое внимание на чистоту, 'чтобы не
загрязнять готовую продукцию. Также необходимо строго
соблюдать правильную последовательность в использовании
промывных вод и маточных щелоков, чтобы при минимальном
расходе воды для промывки получать продукцию лучшего качества.
При способе производства бертолетовой соли без Применения
выпарки, когда применяют для обменной реакции твердый хлористый калий4 (а не раствор КС1), жидкость от промывки соли
1-й кристаллизации вымораживают для выделения КСЮз. При
этом охлаждение можно «вести до температуры^ тем более низкой,
чем выше концентрация СаСЬ в жидкости. Вымороженную жидкость, содержащую СаСЬ не больше 30—50 г/л, .можно использовать на приготовление известкового мблока. Количество КСЮз
в 'жидкости от промывки соли 1-й кристаллизации можно также
уменьшить прибавкой хлористого калия или выпаркой с последующей кристаллизацией и т. д.
Примечание. На одном из современных заводов бертолетовой
соли -по способу хлорирования известкового молока высокой концентрации, накопился шлам, содержащий 70—75% влаги и примерно
\по 10—15% кристаллов КСЮз и нерастворимых примесей. Последние состояли из глины, CaS04 и т. п. веществ и образовали устойчивую взвесь,
которую трудно было разрушить. Утилизацию кристаллов КСЮз из этого
-шлама удалось* провести путем разбавления в Э—4 раза холодной водой
при перемешивании. При этом'' нерастворимые примеси более легкие, чем
кристаллы КСЮз, взмучивались, а кристаллы оставались >на дне сосуда.
Сливая жидкость с взмученным шламом, получали более или менее чистую
соль, которая дальше уже могла фять перекристаллизована по-обычному
(предложение И. Б. Фраймана).
§ 4. Состав бертолетовой соли первой, и второй
^ ’ кристаллизаций
Кроме КСЮз соль, отжатая от маточного щелока, содержит
обычно примеси, состав и количество .которых зависят от
состава и концентрации маточника, от которого отжата соль, от
степени отжатия соли; от промывки соли. Отчасти количество
примесей зависит и от величины кристаллов, так как в крупных
кристаллах' (и групповых соединениях кристаллов), получающихся при медленной кристаллизации, удерживается часть маточной жидкости. Необходимо еще отметить замечаемое 'при
перекристаллизации ерли одновременное оседание некоторых
растворенных примесей вместе с кристаллами КСЮз, почему соотношение растврримых1 примесей и влаги в соли 2-й кристаллизации обычно больше соотношения их в маточной жидкости,
от которой отжата соль. При известковом 'методе в берто-
летовой соли кроме примеси СаС1* обычно содержатся
118 ' /
еше небольшие примеси КО, NaO, нерастворимых соединении,
соединений Mg, SCV', Hr и т. д.
1. Содержание влаги. При центрофугиропании непромытой
соли 1-й кристаллизации в отжатой соли остается 6—7% влаги,
а в промытой соли — 5—6%. При центрофугиропании соли 2-й
кристаллизации остается 4—б7г> влаги. При отжатии соли на
нутч-фильтрах количество ©лаги в соли обычно на 1—2%
больше, чем при отжатии на центрофугах. Чем меньше кристаллы
и чем ниже температура, тем труднее отжатис соли и тем больше
влаги остается в отжатой соли.
2. Содержание СаСЬ. Наибольшей примесыо в бертолетовой
соли, полученной известковым методом, является СаСЬ, поскольку маточный щелок, от которого отжимается соль, является
в основном раствором СаСЬ + КСЮз. В непромытой соли 1-й
кристаллизации содержание СаСЬ равно 3—3,5%. Однако если
бертолетовый щелок, который применялся для кристаллизации,
был слишком концентрирован по СаСЬ, то содержание последнего может быть гораздо, больше из-за одновременной кристаллизации СаСЬ с KClOs (рис. 58, стр. 125).
Промывкой на нутч-фильтрах удается уменьшить содержание
СаСЬ в соли 1-й кристаллизаций до 0,06—0,08%. Промывкой на
центрофугах обычно достигают уменьшения СаСЬ до 0,15—
0,20%. Содержание СаСЬ в соли 2-й кристаллизации зависит от
содержания СаСЬ в применяемой для перекристаллизации соли
1- й кристаллизации и- в жидкости для ее растворения. Обычно
при нормальном ходе процесса соль 2-й кристаллизации получается с содержанием СаСЬ 0,03—0,06%.
3. Содержание К.С1 и NaCl. Содержание КС1 зависит от процента избытка КС1, заданного при обменной реакции (гл. 9). При
избытке КС1 в 15—20% содержание КС1 в соли 1-й кристаллизации обычно в 20—40 раз меньше содержания СаСЬ, а в соли
2- й кристаллизации КС1 совсем не обнаруживается.
Содержание NaCl в соли 1-й кристаллизации зависит от количества примеси NaCl в хлористом калии, применяемом для
обменной реакции, так как растворимость NaCl в маточной жидкости 1-й кристаллизации незначительна. В соли 2-й кристаллизации примеси NaCl обычно не содержится.
4. Содержание нерастворимых примесей. Примеси взвешенного осадка или мути, содержавшиеся в щелоке, из которого
происходит кристаллизация, переходят в отжатую соль. Эта
муть является следствием неполного осветления щелока при. отделении шлама (гл. 7) или коррозии аппаратуры. Поэтому для
• уменьшения нерастворимых примесей в соли необходимо, чтобы
щелок и раствор КС1, поступафщие на обменную реакцию, были
хорошо отстоявшимися (прозрачными) и чтобы аппаратура обменной реакции и кристаллизации была, сделана из материалов
устойчивых против коррозии. Последнее особенно важно для
аппаратуры перекристаллизации. Промывка и степень отжатия
соли не влияют на процент содержания нерастворимых примесей
в соли. Состав нерастворимых примесей: СаОО$, SiOs, окислы
119
Fe и Al, соединения Fb и др. При нормальном ходе произнодстf;;.
содержание нерасгиоримых примесей в соли 1-й кристаллизация,
не превышает 0,05%, а в соли 2-й кристаллизации—0,01—0,02%.
При плохом состоянии оборудования, в соли 1-й кристаллизации
появляются СаСОз, CaSC>4 и даже Са(ОН)г и общее содержание
нерастворимых примесей сильно возрастает. При таких
условиях можно несколько уменьшить содержание примесей
в соли, взмучивая соль с маточной жидкостью и затем промывной жидкостью в декантерах и сливая жидкость, пока частицы
примесей (обычно весьма мелкие) не успели > осесть вместе
с солью.
5. Другие примеси. Из других примесей необходимо упомянуть соединения SO4", Mg и Вг. Сульфаты попадают в соль из
извести и воды, а также при обезвреживании CIO' гипосульфитом (стр. 96). Соли Mg образуются при хлорировании из соответствующих примесей извести. Соединения брома попадают
как примесь хлористого калия, применяемого для обменной-
реакции.
Большей частью в соли 1-й кристаллизации содержание сульфатов не превышает едтых долей процента, а солей магния и
брома — тысячных долей. В перекристаллизованной соли этих
примесей обычно нет 1.
В табл. 27 приведен • средний состав бертолетовой соли, получаемой на одном из современных заводов при известковом
методе производства. Бертолетовый щелок перед кристаллизацией содержал СаСЬ ~ 450 г/л и КС1 ~ 20 г/л. Выделившаяся
при кристаллизации соль отжималась и промывалась на центро-
фугах. «Разваренный щелбк» содержал СаСЬ ~ 5 г/л. Промывка
соли 1-й кристаллизации производилась маточным щелоком 2-й
кристаллизации, а соли 2-й кристаллизации — холодным конденсатом.
1 Приводим анализ (1930 г.) примесей бертолетовой соли 1-й кристаллизации при производстве известковым методом без применения выпарки
(хлорировалось известковое молоко высокой концентрации — см. стр. 72)/
Производство работало плохо.
1. Растворимого в воде CaS04 0,56\о
2. СаО 0,03®;„
3. Растворимых соединений магния следы
4. Растворимых соединений Ре и Pb нет
5. Веществ, нерастворимых в воде 0,56°/о
Остаток нерастворившихся в воде веществ был растворен в соляной кислоте, после чего был определен его состав:
I СаСО, 53,5°/о
2. CaS04 1,7°/®
3. FetO 12,5»/®
4. Других примесе^. . 5,5°/®
б. Примесей, нерастворимых в соляной
кислоте' 26,8»;о
0,30»/®
0,01о|о
0,07о/в
0,03»;®
0»1б*/о
А хз о/0 по отношению к количеству
остатка, нерастворимого в воде.
V
Б = о/о по отношению ко всей берто-
; лотовой соли.
120
/
Таблица 27. С о с т а к примесей б о |> т о л с т о и о п соли п с р и о й
и второй кристаллизаций (досушки)
{)1 о влаги
°/о CaClj,
e;0 Kci
°,0
сульфатов
нераство¬
римых
примесей
°,о
Сроматоп
Соль 1-й
кристаллизации
До '
промывки
6-8
3-3,5
до 0,2
0,05-0,10
0,03—0,20
до 0,10
После
промывки
5-6
0,15—0,25
до 0,02
0,02-0,03
0,03-0,20
—
Соль 2-й
кристаллизации
До
промывки
5—6
0,05-0,15
—
следы
0,01—0,02
!до 0,01-0,02
После
промывки
4-5
0,03-0,06
—
слабые
следы
0,01—0,02
1 _
§ 5. Промывка бертолетовой соли 1-й кристаллизации
В 'табл. 28 приведены данные нескольких опытов промывки
бертолетовой соли на центрофуге емкостью 200 кг отжатой
соли.
Промывка производилась последовательным обливанием поверхности отжатой соли порциями в 10 л холодного конденсата.
Всего было сделано 16 промывок. Новая порция воды прибавлялась лишь после всасывания и отжатия предыдущей порции
воды.
В таблице приведены анализы соли после каждой промывки.
В жидкость от каждой промывки переходило ~ 0,7 кг, т. е.
около 0,35% от веса промываемой соли.
В табл. 29 приведены данные нескольких опытов промывки
бертолетовой соли на нутч-фильтре емкостью в 300 кг отжатой
соли. Промывка производилась последовательно порциями
в 10 л холодного конденсата. Всего было проведено 12 промывок. В жидкость от каждой промывки переходило ~ 0,7 кг, т. е.
~0,25% от веса промываемой соли.
Из данных табл. 29 видно, что основная масса хлорида вымывается первыми порциями воды! Практически на одном из
заводов применяли промывку соли 50—60 литрами холодного
конденсата на нутч-фильтре емкостью в 300 кг, получая соль,
содержащую хлорида меньше 0,1%.
§ 6. Состав маточных щелоков первой и второй
кристаллизаций
Маточный щелок 1-й кристаллизации представляет собой
в основном раствор СаСЬ 400—500 г/л. Количество примеси
других солей обычно не превышает 5т—10% от количества СаСЬ.
Кроме СаСЬ в маточном щелоке 1-й кристаллизации содержится
' R 121
Таблица 28. Данные нисколь к и х о п ы г о и i,
№
иромыпок
1
2
1 3
1 3
4
5
Г>
7
% хлорида В
■
0,5-0,8
1
!
| °*4
отжатой соли
3—4
2—3
1,4-2,2
ы—1,6
0,7-1,1
Таблица 29. Данные нескольких опытов п
м
промывок
1
2
3
4
5
Содержание хлорида
в г/л промывных
вод
250—230
210—190
17q—140
130—110
90—81
т
<,37-
CaCLf
г/л.
460
*-*50
•-400
КСЮ* и почти всегда КС1. Кроме того могут содержаться нс-
большие количества MgCb, NaCl, а в виде следов еще соединения
SO*", брома и др. Содержание КСЮз зависит от концентрации СаСЬ, температуры щелока и содержания КС1. Последнее зависит от процента избытка КС1, заданного при обменной реакции, а также
от температуры щелока и концентрации
СаСЬ (табл. 31 стр. 126). Содержание других примесей зависит от их содержания
в употребляемых извести, воде и хлористом калии.
Маточный щелок 2-й кристаллизации
представляет собой в основном раствор
КСЮз с примесью СаСЬ. Концентрация
КСЮз зависит от температуры и содержания СаСЬ. Концентрация СаСЬ зависит
от содержания СаСЬ в перекристаллизуе-
мой соли и в жидкости, применяемой для
приготовления разваренного щелока.
Другие примеси в маточном щелоке 2-й
кристаллизации обычно содержатся
в очень небольших количествах или
совсем отсутствуют. ■
На рис. 54 приведено примерное содержание СаСЬ в маточниках 1-й
кристаллизации разного удельного веса
при 20°. В табл. 30 приведено содержание СаСЬ и КСЮз в маточном щелоке
2-й кристаллизации равного удельного
веса при 20 и 0°. г
I
£
$
о
«2
*
>о
*
>»
1
Ч
i
:-»о ,•?
Ч»
<2
{
X
<0 .
О
э* я
2 О.
а я
ю g/ '
-
и 5
s 2.
я ^
2 °
ж и
От О
о я
е* п
О
О О.
О
-300
я
6 §
я
|я
Si s
S' ч
я ч
о.
с— н
»— о
я
3 *
о
я >.
От
■230
}.*, кп» бертолетовой с о^л н ил цент р о ф у г е
9
10
и
12
13
и
1>
V 0.46
0,27-0,39
0,23—0,31
0,21—0,24
0,19—0,21
0,18-0,20
\
0,18-0,19
! '
0,17-0.19
.аки бертолетовой соли на и у т ч-ф и л ь т р е
€
7
8
9
10
11
12
71-63
33—24
13-8
4—2
2-1,5
1.6—1,2
1,3-0,9
Таблица 30. Содержание СаС12 и КС103 в маточниках и и ром и
ных водах второй кристаллизации при 20 и 0°
Удельный
^ вес
Состав при 20°
Состав
при 0® IJ
Удельный
вес
Состав при 20®
Состав нри 0е
СаС1, г/д
КСЮ, г/д
CaCI, г/д
КСЮ, г/д 1
СаС1, г/д
КСЮ, г/д
CaCI, г/д|ксю, г/д
1,051
10
71
30-
32
1,107
77
64
100
30
1,058
18
70
38
32.
1Л16
90
63
111
29
1,067
^-26
69
47
32
1,125
103
62
122
29
1,074
35
68
57
31
1,134
116
61
132
29
1,083
45
67
67
31
1,143
130
60
143
28
1,091
55
66
78
31
1,152
143
59
155
28
1,099
65
65
89
30
\ 1
1,161
158
58
166
27
§ 7. Влияние некоторых факторов на кристаллизацию КСЮз
Количество КСЮз, выделяющееся при кристаллизации и
остающееся в маточном щелоке, зависит от концентрации СаСЬ,
температуры конца кристаллизации и содержания КС1. Приводим
некоторые данные, полученные при исследовании влияния этих
факторов.
На рис. 55 приведена растворимость КСЮз в растворе, содержащем 400 г/л СаСЬ для температуры от 0 до 90°. Для сравнения приводится растворимость КСЮз в воде. Из кривых
рис. 55 виден ход кристаллизации КСЮз из бертолетового щелока.
На рис. 56 приведено влияние концентрации СаСЬ на количество КСЮз, остающееся в маточном щелоке при 20, 10, 0 и —10°,
при отсутствии КС1 в маточнике.' Выведенные кривые показывают, что ?СаСЬ имеет , большое влияние на уменьшение
растворимости КСЮз несмотря на отсутствие общего иона.
Однако чем нише концентрация СаСЬ, тем меньше интенсивность
роста его влияния на уменьшение растворимости КСЮз, а при
содержании СаСЬ выше 400 г/л растворимость КСЮз начинает
даже увеличиваться (влияние СаСЬ при небольшой его концентрации на растворимость КСЮз при 20 и 0° см. табл. 30, стр. 123).
На рис. 57 приведено влияние температуры кристаллизации
на количество КСЮз, остающееся в маточном щелоке, содержащем СаСЬ 400 т/л и не содержащем КС1. Данные приведены
в г/л маточного щелока, а процент потери выведен по отношению к количеству КСЮз, которое теоретически должно получиться согласно содержанию СаСЬ по уравнению (63) (стр. 107).
Выведенные кривые показывают, что чем ниже температура, тем
Рис. 55. Растворимость КСЮ» в воде Рис. 56. Растворимость КС103 в раст-
и в растворе СаС1а 400 г/л .при ворах СаС12 разной концентрации при
0—90°. 4 -20, 10, 0 и —10э.
>
S
меньше потеря КСЮз с маточным щелоком и что интенсивность
уменьшения потери падает по мере понижения температуры.
Например снижение температуры с 20 до 10° уменьшает содержание КСЮз на 7,6 г/л, а снижение температуры с —10 до
—20° уменьшает растворимость КСЮз только на, 2,6 г/л.
На рис. 58 приведена максимальная концентрация СаСЬ в бертолетовых щелоках, при превышении которой начинается выделение СаСЬ вместе с КСЮз во время кристаллизации (при температуре в пределах'от +20 до —20°).
На рис. 59 приведена растворимость КСЮз и КС1 при их совместном присутствии для температур от 0 до 80°. Для сравнения
приводятся данные раздельной растворимости КСЮз и КС1
при той же температуре. Из кривых видно, что влияние КС1 на
растворимость КСЮз весьма значительно, а влияние КСЮз на
растворимость КС1 незначительно.
Ка рис. 60 приведены данные Виптелера о растворимости
КСЮз в растворах КС1 разной концентрации при 20° (Zlsclir.
Elektroch. том 7, стр. 360. Из выведенной кривой видно, что
влияние КС1 весьма значительно, но что интенсивность влияния
КС1 падает по мере роста концентрации КС1. Например повышение концентрации КС1 с 0 до 30 г/л уменьшает растворимость
ГлСС*
ф
Т-ра
300—2Q4
<i90 •
Н5*
1
«470
--10е
Й
450
О
§4зэЧ
-5е
с5
+-|
^430
ч«0
«О
§
^4Ш
>400-
300
—5*
. с*
—15*
-20*
Co^V’2
Ф ^
350-
Т-ра
340
530
f 3Z0
ь0
I Я1
|500-
^ 490
i
>8°
<S«70 •
!«0
^450-
<о
440
430
-Ю* ^
S
-3*
1
•*
л
-0*
*
§
о
Л
§
-to-1
г
--13е $
t
—20- %
Рис. 57. Влияние температуры
конца кристаллизации на потерю
КСЮ8 с мато шиком, содержащим
СаС12 400 г/л.
Рис. 58. Температура начала
выделения кристаллов хлористого кальция из бертолетовых
щелоков разной концентрации.
КСЮз больше, чеТН дальнейшее повышение концентрации KCI до
250 г/л.
В табл. 31 приведено максимальное содержание КСЮз и КС1
в маточном щелоке с разной концентрацией СаСЬг при +19 и
—19°, пересчет их на процент избытка КС1 (стр. 112) и' процент потери КСЮз (стр. 111). Из .приведенных в таблице
данных видно, что повышение концентрации СаСЬ сильно уменьшает растворимость КС1, одновременно сильно уменьшая расход
KQ на избыточно выделенный КСЮз и что при обычной концентрации СаСЬ в. маточном щелоке 1-й кристаллизации в 400—
450 г/л и вымораживания до 10—20° ниже нуля, целесообразный
избыток КС1 при обменной реакции составляет 23—27 г/л.
125
Рис. 59. Растворимость KClO.i
и KCI при совместном и раз- Рис. 60. Влияние КС1 на растворимость
дельном присутствии при КСЮ3 при 20°.
О—80э.
Таблица 31. Максимальный избыток КС1 и соответствующая
ему потеря КСЮ3 для бертолетовых щелоков с разной
концентрацией СаС13 при +19 и —19°
Содержание СаО,
в г\л
КСЮ. г!А
KCI г!л
°/о избытка KCI '
°/о потери КСЮ*
при 4-19°
при —19*
при -f 19*
при —19*
при 4- 19е
при -19°
при 4-19*
при —19*
;-250
V
4
100
59 '
195
115
18
5
^300
17
5
80
47/
130
77
15
4 ’
350
19
5
58
35
81
49
15
4
400
" 21
6
45
27
55
33
14
4
450
25
7
33
23
^ 36
25
15
4
50ф
32
—
23
—
22
—
17
—
В табл. 32 приведены сводные данные наших исследова- ’
ний кристаллизации в разных условиях. На рис. 61—£4
и табл. 33 и 34 приведены данные ГИПХ, японских исследователей Нишио* и Осака и итальянского исследователя Маце- ;
тис по равновесию системы Са(С10з)г, СаСЬ, KCI, KCIOs, HjO. \
126
Таблица 32. Сводные дан п ые в л и я и и я и :t С и т к a KCI, к о и и с н-
т рации СаС13 и температуры конца кристаллизации на
потерю хлората с маточниками
—X
СаС1,
' КС1
КСЮ» г!л при
°;о
потери
КСЮ, при
*!*
'
г1л
1 о
избытка
15*
4е
— 4е
— 20°
15е
4е
— 4*
S
-20е
0
0
37
28
23
16
28
22
18
13
350
8
10
33
21
20
14
26
16
16
11
' 16
20
29
17
15
9
23
13
12
7
24
30
25
15
12
7
20
12
: 9
5.5
\
0
0
36
26
22
16
25
18
15
11
9
10
31
20
18
12
21
14
12
. 8
400
18
20
26
16
ц
7
/18
11
10
4,7
27
N
30
23
13
11
6
15
9
8
1
1
4
1
1
0
0
37
27
23
18
23
16
14
11
450
10
10
31
20
18
10
19
12
11
6
20
20
25
16
14
7
15
10
8
4.2
30
30
22
13
11
—
13
8
7
—
0
• 0
39
29
25
‘ 20
21
16
14
11
500
г
И
10
34
22
19
10
18
12
11
5Д
, 22
20
.30
18
—
—
16
11
—
'
33 .
, 30
—
_
—
"
—
—
- -
Примечание. Процент потери КСЮз рассчитан по формуле ,
где СЮ3 и Са обозначают их содержание в экв/л щелока. Содержание' КС1
Р* Са
в экв/л щелока рассчитывается по формуле KCI = —~~ экв/л, где Р обозна-
• OUU
чает процент избытка, а КС1 и Са обозначают содержание их в экв/л щелока.
127
Таблица 33. Равновесие системы СаСЬ + 2КСЮЛ «<* Са (С10;}), -j -'КС1
s при температуре 0° по данным Заславского 2s“?
Состав
о
б
-У
о
<п
6
б
5
б
CJ
и
ксю,
б
о
б
и
L)
«1
и
Ч
X
Состав твердой фазы
ч
Молей вещества
на 1С00 молей Н20
Процентный состав
раствора
Е
2,36
—
__
3.1
-
96 9
ксю,
D
0,50
33,79
■ —
—
0,5
21,8
—
—
77,7
ксю, + ко
R
1,38
3,28
—
99,10
1.1
1,6
—
36.8
60.5
КСЮ3 + КС1 + CaCl, • 611,0
Q
2,34
—
—
98,79
1,9
—
—
37.1
61,0
КСЮ, + CaCl.. • 611,0 "
Р
2,24
91,18
68,07
1,2
—
42,0
16,8
40,0
КСЮ,'4- CaCUil 1,0+
. + Са(СЮ(); 21 КО
F ч
1,38
—
154,4
—
0,7
—
63.5
—
35,8
КС10з + Са (С10з)з 2Н.Ю
С
—
34.45
—
—
—
22,2
—
—
77,8
КС1
• А
—
—
—
97,68
—
—
37,6
62,4
СаС12 • бН.,0
G
—
+—
15?,7
—
—
—
63,7
—
36,3
Са(СЮ,)22Н20 •
В
—
4,82
—
99,14
—
2,4
—
37,0
60,6
КС1 + СаС12.6Н20
Н
90,78
67,38
42,4
1
16,9
40,7
СаС12 • 6Н.,0 + Са (СЮ3), • 2НаО
ta6Aui^a 34., Равновесие реакции Са(Cl63)a + 2КС1 ^СаС12 + 2КСЮ3
при температуре 15 . 45° по данным Нишио и Осак а506
\ Со-
\ став
J*n/n\
Молярный состав
Состав
в •/*
а>
SE
5*
4» В
с>
Хм
§«
4* И.
о
т
и
£3
т
т
о
б
т
о
п
О,
Состав твердой фазы
\
и в
5 a
X
Л
о
5
ё
X
1
2
3
4
5
6
7
8
9
10
г-
Температура 15°
♦ ' /
%
1 .
1,00
1,00
12,6
24,7
__
75,3
КС1
2
1,00
0,00
111
—
—
—
.5,8
94,2
4 КСЮ3
3
0,00
1,00
4,4
41,2
—
—
—
58,8
СаС12 • 6Н..0
' 4
0,00
0,00
Са (СЮ3>, • 2Н.О
5
1,00
0,9709
25,68
—
13.5
—
0,7
85,8
КС1 + КСЮ,
> 6
0,8539
0.9705
13,23
2,6
19,7
—
1,2
76,5
КС1 + КСЮ, .(
7
0,7426
0,9720
12,04
4,6
18,5
—
1,2
75,7
КС1 + ксю,
8
0,4233
0,9797
10,9
12,3
11,5
—
1,0
75,2
КС1 + КСЮ3
9
0,1728
0,9820
7.14
24,3
6,1
—
1,2
68.4
КС1 + КСЮ,
10,
0,04710
1,00
4,02
41,1
2.7
—
56,2
КС1 + CaCl., • 6НгО
, И
0,00
0.6117
2,56
28,2
33,4
—
38,4
СаС1,6Н30 + Са (СЮ,), • 2Н,0
12
0,0340
0,8577
3,91
35,7
—
8,4
3,1
52,8
CaCl 2 • 6HsO + КСЮ,
13
0,0127
0,00
2.99
—
65
1,0
34
КСЮ, + Са (С103), • 2Н.,0
14
0,0108
0,2159
2.88
8.2
—
55
0.9
35,9
КС103 + Са (СЮ3), • 2Н.О
15
0,0109*
0,3964
2,57
16.7
—
47
1,0
35,3
КСЮ, + Са (СЮ,)', • 2Н30
16
0,0501
0,9755
4,10
40,1
1,4
—
2,3
56,2
КСЮ, + КС1 + CaCl, • 6НаО
17
0,0201
0,6088
/•
2.46^
28,4
32,3
2,1
37,2
- КСЮ. + СаС12 • 6Н20 4-
+ Са(СЮ3)2-2Н.Ю
128
flpOOd.l.'irtiri.'
\ Со-
\ став
№ пи. \
/ '
Молярный состав
Состав в “(о
Состав твердой фазы
Соединения К
Соединения С1
о
X
ев
О
«в
и
б
*
о
б
ев
и
о
о
*
9,
X
1
*
3
4
5
6
7
8
9
10
Температура 45°
1
1,00
1,00
9,9 I
29,5
—
—
70,5
ко
2
1,00
0,00
40 5
, —
*—
—
14,4
85,6
ксю.,
3
0,00
1,00
2,4
РАЗ
—
—
—
43,7
СаС1., • ШгО
4 -
0,00
0,00
-
Са (СЮ;1), • 211..0
5
1,00
0,9043
8,94
—
28
—
.4,9
67,1
ко + Коо",
6
0,2472
0,9481
4,85
27,8
9,75
—
4,2
58,15
КС! КСЮ,
7
0,1061
1,00
2,17
51,3
8,2
—
—
40,5
Ка + СаС1.-4П,0
8
0,0163
1,00
2 35
555
1.2
—
—
43,3
СаС12 • 2НаО + CnCl.i" 4 ИЮ
9
0,00
0,9857
2,36
55,5
—
1,5
—
43,3
СаС12 • 2Н30 + СаС12 • 4Н.“0
10
0,00
0.5422
1,56
28,8
—
44-/2
—
27
CaCJ? • 2Нг° + Са (СЮ;,),. 2МаО
11
0,0847
0,7307
1,69
40,4
—
18,9
10,3
30,4
КСЮ;, + СаС13. 211,0 +
Са (00»'* • 21 1гО
12
00453
0,00
2,28
—
67,9
3,8
28,3
КОО;, 4- Са (СЮ.,), • 211.,0
13
0,0427
0,1150
2,27
4.6
—
62,5
3,7
29,2
КОО., + Са (ОО4, • 21 Г,О
14
0,1170
0,9299
1,99
50 6
3,6
—
8.9
1 36,9
КООг, + КО + СаО, • 2П.О
15
0,0813
; 0,5238
1,42
27,6
38,6
1 9,5
.24,3
КСЮ., + СаО, • 2! 1,0 +"
+ Са (СЮ:|>, • 21 Г,О
Примечание. В оригинале приведены только данные о составе раствора в виде К, С1 и Н20 (графы 2, 3 и 4), обозначающие молярную концентрацию веды и соединений калия и хлора; остальные пересчеты сделаны нами,
исходя /из того, что молярные концентрации Са и СЮ3 рассчитываются из
содержания К и С1 следующими равенствами:
Са - -1-^— нСЮ, = 1 — С1.
Для примера приводим расчет состава раствора при 15° п. 17 этой таблицы.
По оригиналу в растворе содержатся К = 0,0201,’ С1 = 0,6088 и Н20 = 2,46.
Отсюда рассчитываем содержание соединений Са и С103: JLrT ==
= 0,48995 Са и 1—0,6088 = 0,3912 С103. Поскольку в твердой фазе содержится
Са(СЮ3)2, исключается возможнссть содержания в растворе KCJ, т. е. весь К
содержится в в^де КСЮ3 (0,0201) и весь С1 в виде СаС12 = 0,3044^ .
Содержание Са(СЮ3)2 рассчитываем по разнице СЮ3 — КС103 илиСа — СаС12
0,3912iff1. = 0,1855 или 0,48995 — 0,3044 = 0,1855.
Таким образом состав раствора будет:
Соединений
Молей
Граммов
Процентов
СаС1,
КСЮ.
Са<Я?»>*
н2о
0,3044
0,0201
ОД 855
.2,46
I
0,3044-111 =33,8
0,0201-122,56 = 2,5
0,1 £55 • 207 = 38,4
2,46 - 18 = 44,3-
33,8-100:119 = 28,4
2,5-100:119= 2,1
38,4-100:119 = 32,3
44,3-100:119 = 37,2
Итого .... 119,0
Итого .... 100
у
9 Зав. 179. — Шрайбмаи.
1 о«»
Таблица 35. Некоторые данные о влиянии КХО:„ KN03, КОП»
NaC103 и MgCl2 на растворимость КСЮ3
Влияние К,СО,
'~при 24е
4
при 40е
®/о К,СО,
о/оКСЮа
•/. к,со,
•/• ксю,
7,42
8.81
3.92
—
12,44
17,80
2.40
18,81
4,09
18,53
2,29
29,24
1,46
23,42
1,65
51,80 ‘
1,04
30,55
1,09
54,40
—
36,59
0,69
—
—
49,24
0,25
—
—
52,67
0,19 '
— (
—
52,95
—
—
Влияние KNO, Влияние КОП
при
25е
при 20°
(моль/л)
*/. KNO, j
•;. ксю,
1
КОН
КСЮа
7,735
4,71
0,0924
1,55
7,07
5,06
0,0882
3,59
6,52
6,35
0,С699
7,12
5,76
7,95
0,0415
12,81
5,10
8,60
0,0410
18,97
4,39
• 9,41
0,0351
27,14
3,90
10,95
0,0287
27,21
3,61
12,19
0.0254
27,24
0 у
14,02
0,0215
14,85
0,0195
. 15,02
0,0191
Влияние NaClOa Влияние MgCIt (по данным автора)
при 24,2°
при 40е
при
8е
при 17е
о/о NaCIO,
•ft ксю,
о/о NaCIO,
\
о/о КСЮ,
MgCI,
г/л
КСЮ,
г/л
MgCI,
г/л
ксю,
г/л
,
7,50
12,44
,
48
66
6,73
6,91
10,94
8,02
25
46
25
61
20,14
5.20
31,13
4,51
100
40
100
51
27,9
4,08
35,41
4,22
200
30
200
37
31,1
3,28
48,03
3,40
250
26
250
27
36,9 ’
3,35
51,97
3,24
300
22
300
23
■ 43,99
2,82
53,80
—
350
20
350
20
49,18
* 49,65
1,53
—
✓ — .
400
17
* Рис.*61. Система Са (С103)а + 2КС1 .;=2 СаС12 + 2КС103
при 0° по данным Заславского*
130
Ci/О^ема kCiOjtCafClOjfapNg0
Система HCLfCaCLg^HgO
При 15* При 45*
Рис. 64. Система Са(СЮ3)2 + 2KCI ;=! СаС1а + 2КСЮ3 при 15 и
45° по данным Нишио и Осака.
§ 8. Некоторые расчеты по процессам кристаллизации
1. Изменение объема щелока при кристаллизации. Объем
щелока уменьшается при кристаллизации вследствие выделения
КСЮз, понижения температуры и удержания части маточной,
жидкости в отжатой соли. На 1 г КСЮз, выделившегося при
кристаллизации, объем щелока уменьшается примерно на 0,4 пи.
На каждый 10° снижения температуры объем щелока уменьшается примерно на 0,4%. Общее уменьшение объема при
1-й кристаллизации равно 8—12%; а при 2-й кристаллизации
12—18%. Уменьшение объема от выделения КСЮз и снижения
температуры можно рассчитать по увеличению концентрации
хлорида в щелоке, исключая случаи, когда при кристаллизации
выделяется кроме КСЮз еще и хлорид. Уменьшение объема маточника вследствие удержания его в отжатой соли обычно равно
~1% для 1-й кристаллизации и~2% для 2-й кристаллизации
(соли 2-й кристаллизации выделяется на единицу объема примерно в 2 раза больше, чем соли 1-й кристаллизации).
'2. Определение процента потери хлората с маточным щелоком. Потеря хлората с маточным щелоком рассчитывается по
его отношению к количеству, которое должно было получиться соответственно содержанию Са по уравнению (63)
(стр. 107) по формуле:
СЮ:,-100 0/
потеря хлората = ——%,
где СЮз и Са обозначают их содержания в экв/j маточного-
щелока. Эта формула важна для правильного расчета баланса
производства. Однако этот расчет нельзя применять, если при.
кристаллизации выделяются кристаллы СаСЬ. '
132
3. Определение процента выхода при кристаллизации. Вы*
ход при ■кристаллизации показывает отношение (выраженное
в процентах) количества хлората, выделившегося и виде кристаллов, к количеству хлората, содержавшегося в щелоке до
начала кристаллизации. Формула расчета будет
(А — с)100о,
выход при кристаллизации = - —%,
•где А и а обозначают количество хлората на 1 г НгО в щелоке
до и после кристаллизации. Расчет ведется по отношению
к воде, а не в г/л, поскольку объем щелока при кристаллизации
значительно изменяется, а количество воды в щелоке почти не
изменяется.
4. Определение расхода КС1 на единицу КСЮд, полученной
благодаря избытку КС1, заданному при обменной реакции. Расчет производится для выявления эффективности прибавления
избытка КС1 при обменной реакции. Формула для расчета будет:
Л
расход КС1 = g—6,
где А и б обозначают содержание КС1 и КСЮз в г/л маточника,
Б обозначает растворимость КСЮз-в 'растворе, содержащем соответствующее количество СаСЬ (см. рис. 56, стр. 124)..
ГЛАВА 10
ОБРАБОТКА СЫРОЙ БЕРТОЛЕТОВОЙ СОЛИ
\
БертолеЪ'Ова соль, отделенная на центрофугах или нутч-филь-
трах от маточной жидкости, содержит 4—8% влаги (стр. 121).
Дальнейшая обработка соли заключается в сушке, размоле, просеивании и укупорке. Сушка бертолетовой соли необходима для
лучшего хранения и перевозки и для удобства дозировки соли
и правильного перемешивания с другими компонентами. При
хранении влажной соли она может затвердеть почти до монолитного состояния, что весьма неудобно для потребителей. Тара,
в которой хранится влажная соль, сильно портится: мешки расползаются, железо корродируется и т. д. Размол ерли
применяется только для некоторых потребителей. Производя кристаллизацию в аппаратах непрерывного действия (Цаца и т. п.),
получают настолько мелкие кристаллы соли, что они удовлетворяют большинство потребителей без дальнейшего размола.
Просеивание необходимо для разделения мелких и крупных
кристаллов, а также для отделения некоторых случайно попадающих механических примесей.
133
§ 1. Аппаратура сушки, размола и просеивании
Поскольку бертолетопа соль является взрывоопасным веществом, ее сушку надо производить при возможно более низкой
температуре, что достигается применением вакуум-сушилок с паровым обогревом. Для предотвращения возможности спекания
соли у стенок сушилки последняя должна иметь приспособления для непрерывного перемешивания высушиваемой соли. Для
предотвращения попадания в соль смазочного масла от подшипников вала сушилки (что может вызвать взрыв) сушилка также должна иметь специальные 'приспособления. На
Jrrtp а берсоли
Рис. 65. Вакуум-сушилка барабанного типа для сушки бертолетовой соли.
рис. 65 показана сушилка «Пасбург», применяющаяся на многих заводах для сушки бертолетовой соли. Сушилка представляет собой горизонтально расположенный барабан с паровой
рубашкой. . С обеих сторон барабан закрыт чугунными крышками. Через весь барабан и крышки проходит стальной вал, на
котором насажены лопасти, не доходящие на 1—2 до стенок
барабана. Для облегчения нагрузки подшипников и уменьшения
опасности прогиба вала (что неизбежно приводит к поломкам
лопастей и т. д.) часто делают вал полым. Вал с лопастями
делает 10—15 об/мин. Снаружи аппарата на один конец вала
•надевается шкив для привода. С внутренней стороны крышек
; аппарата устраиваются карманы, охватывающие вал и служащие ловушками для масла, могущего попасть от смазки подшипников. Эти карманы снабжены подводкой и отводом воды
'для их промывки, Сверху барабан имеет люк для загрузки соли,
состоящий из чугунного штуцера, проходящего через рубашку
к внутренней стенке барабана. Штуцер закрывается крышкой.
Флянцы, крышка и штуцер делаются плотно пригнанными и
уплотняются резиновой прокладкой. Благодаря вакууму в ап-
'134' '
парате нет надобности н прикреплении крышки болтами. Поскольку крышка держится собстпснным несом (бел болтои), она
служит и предохранителем на случай образования в аппарате давления. В штуцере люка имеются патрубки для соединения с линией вакуума, с вакуумметром и с воздухом (для прекращения
вакуума по окончании сушки). Для выгрузки соли в нижней
части аппарата имеются два люка в виде штуцеров с внутренними и наружными крышками. Внутренние крышки расположены
на уровне стенки аппарата и поворачиваются шарнирным приспособлением . извне. Снаружи штуцера закрыты крышками на
резиновых прокладках, прикрепленных откидными болтами. Паровая рубашка аппарата имеет штуцера для подводки пара,
спуска конденсата, спуска воздуха, для манометра и для предохранительного клапана. Через рубашку и внутреннюю стенку
аппарата проходит патрон для термометра, показываюшего температуру внутри аппарата. Термометрами также должны быть
снабжены оба подшипника вала. Внутренняя часть барабана,
а также вал и лопасти мешалки должны быть из коррозионно-
устойчивбго материала; достаточно устойчива медь. Сталь, железо и чугун сильно разъедаются, загрязняя высушиваемую соль
продуктами коррозии, что сильно увеличивает взрывоопасность
соли. '
Примечание. Необходимо отметить, что сырая бертолетова соль,
хранимая в открытом виде тонко насыпанным слоем 11а воздухе с относительной влажностью не евьцие 50-Чз0%, сравнительно быстро высыхает
при комнатной температуре до содержаиия влаги ~ 0,1%. См. прим. стр. 13.
Вамуум в сушильном аппарате создается удалением воздуха
и паров воды насосом. Между вакуум-насосом и сушильным
аппаратом ставится ловушка для пылевидной соли, уносимой
отсасываемыми газами к насосу. Такая ловушка показана на
рис. 66. Это — вертикально расположенный цилиндрический сосуд. Через верхнюю крышку цилиндра проходят две трубы, соединенные трубопроводами одна с сушилкой, а другая с вакуум-
насосом. Первая труба опущена почти до дна ловушки. "В ловушке всегда должна быть жидкость, так чтобы конец длинной
.трубы был несколько погружен в нее. Уносимый из сушилки
пар конденсируется в ловушке, а пыль растворяется в жидкости.
По мере накопления жидкости в ловушке ее спускают и иепбль-
зуют как раствор КСЮз.
Для наблюдения за уровнем жидкости в ловушке имеются
два смотровых стекла.
Для размола бертолетовой соли часто применяют дезинтегратор Матодор, показанный на рис. 67 (Каст 35). Дезинтегратор
состоит из массивного круглого кожуха диаметром в 40—50 см
и шириной в 20—25 см. Сверху кожуха имеется воронка для
входа соли с приспособлением для автоматического дозирования подачи соли.-На одной из боковых стенок кожуха
имеется люк * с герметбчно закрывающейся крышкой. Через другую боковую стенку кожуха проходит вал с четырьмя
135
лопастями, вращающийся со скоростью до (ИЮО об/мии. Сои.,
попадая на лопасти пала, отбрасынается ими с огромной силой
на решетки, укрепленные но стенкам кожуха, где от удара\из-
бжсЭгЪли
Bh/тод кюсосд
1
I
III!
В пуск
ёодЫ
Люк
JBL
Стгскмои штуцер
Рис. 66. Ловушка пылевидной соли, уносимой из
сушилки к насосу.
Рис. 67. Мельница- дезинтегратор для размола бертолетовой
соли.
мельчается. Изменением угла наклона решеток можно регулировать степень измельчения соли. Измельченная соль выходит
через штуцер внизу кожуха (ср. Engelbrecht, Ch. Zeit. 42, 150,
1918 r.V/Поскольку размол бертолетовой соли является взрывоопасной операцией, необходимо обеспечить невозможность попадания частиц железа; обычно для этого применяют магнитный сепаратор,
через который пропускают
соль до поступления в дезинтегратор. В этом сепараторе улавливаются частицы
железа, случайно попавшие
в соль.
Для просеивания молотой
бертолетовой соли применяют сита барабанного типа,
трясучки и подобные аппараты. Практически при кристаллизации в непрерывно
'действующих кристаллизаторах Цана (стр. 113) через ситсг
с 600 отверстиями на 1 с«*
проходит от 70 до 90% соли
1-й кристаллизации и 90—98%
соли 2-й кристаллизации.
Рис. 68. Сепаратор для разделения мелких и крупных частиц бертолетовой
соли.
/ — загрузочная воронка, 2—вращающаяся плита,
3—лопасти вентилятора, 4 — осадочная камера,
б — выход мелких частни, б — выход крупных
частно.
136
Вместо просепиании молотой бертолетовой соли иногда применяют воздушный сепаратор, показанный на рис. 68, работающий на принципе отделения струей воздуха более легких мелких
частиц от более тяжелых крупных частиц. Сухая соль подастся
элеватором в загрузочную воронку 7, откуда попадает на
плиту 2, укрепленную на быстро вращающемся валу. В направлении, обратном падающей соли, вентилятором 3 просасывается через плиту 2 струя воздуха, увлекающая с собой более
мелкие частицы соли — «пудру» в камеру 4, ® которой движение
воздуха настолько замедляется, что пудра оседает на дно камеры. Отсюда пудра удаляется через люк 5 на укупорку. Более
грубые частицы соли, не уносимые струей воздуха, падают
с плиты 2 на дно сепаратора, откуда удаляются через люк 6.
§ 2. Схема и техника обработки сырой бертолетовой соли
Ввиду взрыво- и пожароопасности процессов сушки и размола бертолетовой соли для этих стадий производства обычно
строится отдельное здание, расположенное вдали от остальных
производственных помещений (стр. 332,). Из помещения кристаллизации сырая соль подвозится в закрытых деревянных вагонетках (внутри оцинкованных). Для лучшего учета целесообразно емкость вагонеток делать равной или хотя бы кратной
рабочей емкости аппарата для сушки.
Поступившая вагонетка с солью взвешивается, после чего
соль выгружается в бункер сырой соли, проходя медную сетку
с отверстиями диаметром в 5—10 им2. Из бункера соль шнеком
и элеватором подается в загрузочный люк сушилки. По окончании сушки прекращают вакуум в сушилке и открывают нижние два люка сушилки, через которые соль выгружается в бункер
сухой соли. Из этого бункера сухая соль элеватором подается
на размол или на просеивание. Размол соли производится не
всегда, так как это опасная операция, а при современных методах кристаллизации в непрерывно действующих аппаратах получаются настолько мелкие кристаллы, что они удовлетворяют
;&1ьшинство потребителей. Просеивание целесообразно произ-
ве;ить и пр^отгсутствии размола.
На1з апп«**' во»Для просеивания соль поступает непосредственно
Л /чтллп г» Лпд*гтЮ ttl ттт.»тл
pow)v
-/
в
J
j\oрки, а отсев поступает в специальный сборник
r^ H для перекристаллизации, так как отсев содер-
АлцЪлыпе нерастворимых примесей.
B(ffT ко слеживания соли просеивание и укупорку надо
д солью, охладившейся после сушки. Сырую соль
^РоРать.
Ъельз' бертолетовой соли обычно служат деревянные
7» вянными обручами (без гвоздей) небольшого раз-
*>«, * кг и т. д.) *. * Реже применяют железные барабаны
^е/>а (змеров. Изнутри бочки обклеиваются плотной бу-
: : —-
1 вес технической бертолетовой соли колеблется от 1,2 до 1,6.
137
магой; часто бочки выкладываются еще матерчатыми мешками.
Такие* предохранительные меры необходимы потому, чго рассыпка соли из тары является нс только потерей, но и представляет опасность для мест нросынки и пожарном отношении.
При насыпке бочки должны стоять на хорошо заземленном
металлическом листе во избежание образования разрядов статического электричества, получающихся от трения соли об рукав, соединяющий бочку с просевальным аппаратом, и об стенки
бочки. Мы наблюдали случай, когда при насыпке соли через
матерчатый рукав в деревянную бочку, установленную на резиновом листе, получался разряд напряжением до 500 вольт. Во
избежание новообразования применяемые для укупорки соли
молотки и т. п. инструменты должны быть медными,
а И ПЙГПЩ1 WWM ИИ ПМММИН' IIIW ироовииннни н нрн уму-
соли выделяется пылевидная бертолетова соль, которую
необходимо улавливать как во избежание потерь и вредности
для обслуживающего персонала, так особенно из-за пожарной
опасности. Поэтому над местами выделения этой пыли ставятся
приспособления для ее отсоса и отвода к специальным пылеуловителям. На одном из заводов улавливание этой пыли производится в двух последовательно расположенных камерах
в виде железных четырехугольных ящиков с коническим дном.
В этих камерах расположен ряд сетчатых перегородок, при
ударе об которые пыль оседает. Вентилятор для отсоса воздуха
с пылью установлен до входа в камеры, в которых скорость
движения воздуха сильно уменьшается, и пыль падает на коническое дно. Пыль, осевшая на перегородках внутри камеры,
снимается путем периодического встряхивания их. Очистка камер от накопившейся пыли производится раз в 30—40 суток.
В этик камерах удерживается 0,3—0,6 кг пыли КСЮз на 1 г готовой соли (0,03—0,06%). Анализы воздуха, выходящего ,из последней камеры, показывали отсутствие КСЮз.
.п
. ГЛАВА 11
I '
У ИСПОЛЬЗОВАНИЕ МАТОЧНЫХ ЩЕЛОКОВ ПЕРВОЙ!
КРИСТАЛЛИЗАЦИИ ,
Маточный щелок, остающийся после выделения КСЮ *
1-й кристаллизации и вымораживании, представляет собоЬбоЛЬ.
твор, содержащий СаСЬ 400—500 г/л и сравнительно Н'»"" ги
шие количества КСЮз и КС1 (,по 10—20 г/j). Другие пР\ольку
содержатся реже и в меньших количествах (стр. 121). Пось^ по_
маточный щелок содержит больше 5/в от количества хло/Ji ’ его
глощенного при хлорировании, вопрос использован: gep.
является весьма вадшым для рентабельности производст v
■ \ ’
138
толстопоп соли. Полного разрешения этот попрос пе нашел и
но настоящее нремя.
Маточный щелок представляет собой в основном раствор
СаСЬ, почему приводим данные о свойствах СаСЬ и его растворов. Кроме того приводим способ использования хлората,
содержащегося в маточнике, а также способ использования маточника для получения плавленого хлористого кальция и для
производства хлористого бария по Дюфло.
§ 1. Свойства и применение СаСЬ и его растворов
Безводный хлористый кальций имеет удельный вес 2,22 и
температуру плавления 774°, весьма гигроскопичен и при хранений в открытом виде притягивает влагу, превращаясь в гидрат
с все увеличивающимся количеством молекул гидратной воды
вплоть до СаСЬ • бНгО. Последний имеет уд. вес 1,65 и температуру плавления 29°. При нагревании СаСЬ • 6Н2О из него
удаляется гидратная вода и он постепенно переходит в гидраты
с меньшим количеством воды; при 260° гидрат превращается
в безводный СаСЬ.
Молекулярная теплоемкость СаСЬ при 13—100° равна
18,2 ккал *. Теплота образования из элементов равна 196,6 ккал 1
для СаСЬ и 218,4 клал1 для СаСЬ - 6Н2О. Скрытая теплота плавления равна 6,1 ккал1 для СаСЬ и 8,9 ккал1 для СаСЬ • 6Н2О;
теплота гидратации СаСЬ • 6Н2О равна 21,75 ккал1. Теплота
растворения 1 моля СаСЬ в 300 молях воды равна 17,4 ккал1;
теплота растворения 1 моля СаСЬ • 6НгО в 400 молях воды равна
— 4,31 ккал.
Растворимость СаСЬ в воде весьма значительна. В спиртах
и в ацетоне СаСЬ также хорошо растворяется, образуя с ними
молекулярные соединения. С аммиаком СаСЬ образует соединения СаСЬ • 4NHs и СаСЬ • 8NH3.
В табл. 36 и 37 приведены концентрация и состав насыщенных
растворов СаСЬ при температуре от —55 до 175,5° и некоторые
свойства растворов СаСЬ разной концентрации. На рис. 69; приведена температура кипения концентрированных растворов СаСЬ.
На рис. 70 приведена кривая температуры замерзания растворов СаСЬ разной концентрации.
Растворимость СаСЬ в спирту (СаСЬ • ЗС«ШОН)33-1
, Температура
'0
20
40
60
80
90
97
14,9
19,7
L-5
25,2
31,8
37,2
39,4
42,9
t •
т , 1 На 1 г!моль.
139
Таблица 36. Плотность и концентрация к а с ы щ е н н ы х ь о ;i и ь< ..
растворов СаС12 при температурах от — 55 д о + 170J
Содержание СаС1,
Температура
°;о г/кг Н,0
— 55° I
— 25°‘
29,9 426
33,3 500
0°
37,5
+ 10°
39,4
20°
42,7
29,8° 8
50,1
40° 8
53,5
60°*
57,8
70°
58,6
80°
59,5
90°
60,4
100°
61,4
120°
63,4
140°
65,6
170’
71,5
175,5° 8
74,8
600
650
745
V 1001
1150
1370
1415
1470
1525
1590
1733
1907
2510
2968
* Лед + СаС1а.6Н,0.
5 6aq + 4aq.
8 4aq.
* 2а q.
5 2aq + laq.
Плотность
г/л
Уд. нес
• Ьоме
440
1,32
35
510
1,36
38,2
514
1,38
39,8
602
1,41
42.0
742
1,48
46,8
808
1,51
48,7
890
1,54
50,6
908
„ 1,55
51,2
928
1,56
51,8
954
1,58
53,0
—
—
—.
—
—
—
Таблица 37. Некоторые свойству водных растворов СаС12 разной концентрации
Содержание CaCI, '
при 20*
Плотность при 20°
Температура
Относительная
вязкость
при 20°
1ш
г/л
1
уд. вес
"Боме
эам ерзания
кипения
о
, 20
1,015
2.1
— 1°
100,1°
4
41
1,032
х 4,2
— 1,9°
100,4°
6
63
1,049
6,8
— 3,0°
100,7°
4 8
85
1,067
8,9
— 43°'
101,1°
10 ч
108
1,085
11,2 ,
— 5,9°
101,6°
12
132
1,103
133
— 7,7°
102,2°
. 14
157
1,121
15,5
— 9,8°
102,9°
16
182
1,140
17,6
— 12,2°
103,6°
18
209
1,159
19,7
— 15,2°
104,5°
1,7
20
.236
1,179
\ ' 21,8
— 18,6°
105,4°
1,9
22
264
1,199
23,9
— 22,6°
106,4°
2,1
24 '
293
1,219
25,9
— 27,9°
107,6°
2,4
26
322
1,239
27,9
— 32,8° •
108,9°
2,5
28
353
1,261
29,9
— 39,7°
110,1°
2,9
30
!
385
1,283
313
—,48°
1113°
3,4
140
Продолжение табл. 1П
Содержание СаС1а
при 20е
Плотность при 20®
Температура
Относи¬
тельная
Wo 4
г/л
уд. вес
® Боме
'
замерзания
кипения
ВИ.1КОСТГ,
при 20®
32
418
1,305
33,7
— 39,6°
113,1°
3,8
31
.451
1,327
35,6
— 23,3°
114,6°
4,5
36
486
1,350
37,4
— 9,85*
116,3°
5,1
38
522
1,375
39,4
+ 1 *5°
11ЙД°
6,8
40
558
1,395 .
40,4
10,9°
119,9°
8,7
42
596
1,418
42,5
17,8°
121,9°
11
44
634
1,440
44,1
22,8°
123,9°
—
46
672
1,462
45,6
26,2°
126,0°
48 -
713
1,485
47,2
27,9°
128,2°
50
753
1,507
48,6
29,3°
130,5°
- ~
Хлористый кальций и его растворы применяются для производства плавленого хлористого кальция, для производства
хлористого бария (по Дюфло)
Рис. 69. Температура кипения концентрированных растворов СаС12.
для получения растворов с низкой температурой замерзания и
высокой температурой кипения,
для получения холодильных
смесей, обезвоживания газов и
неводных жидкостей, обеспыливания дорог путем их поливки
раствором СаСЬ, для производства анналина (искусственный
гипс для производства бумаги),
обеззоливания голья в кожевенном деле, а также в лабораторной и медицинской практике
и т. д.
СаС12 г/на 100 г Н20
Рис. ' 70. Температура замерзания
растворов СаС1а разной концентрации.
§ 2. Получение плавленого хлористого кальция
В технике имеет применение плавленый хлористый кальций,
содержащий до 72%: СаСЬ (QCT 4100). Для его получения вымороженный маточйый щелок. 1-й кристаллизации упаривают до
| 141
температуры кипения, рапной <N0 160°. Упарю; прои ..юда1• .1
обычно в чугунных котлах, обогреваемых голым огнем. Для
лучшего использовании тепла каждые два котла располагают
терасообразно, так что вышерасположснный котел подогревается
за счет тепла газов, отходящих после обогрева нижсрасполо-
женного котла. Частично уваренная горячая жидкость из
вышерасположенного котла поступает /в нижерасположепныи
котел, в котором окончательно уваривается. Продолжительность
уварки обычно 2—3 суток. По достижении температуры кипения
жидкости в нижнем котле в 160° прекращают подогрев и, дав
жидкости несколько отстояться, сливают се из котла в железные барабаны. Слип жидкости осуществляется либо вычерпыванием вручную, либо опусканием в жидкость вертикального
центробежного насоса и выкачкой жидкости но жолобу в подставленные барабаны. По охлаждении барабанов в них получается* твердый плав с содержанием СаСЬ 66—70%. Плав представляет собой смесь гидратов СаСЬ • 2НгО и СаСЬ • 4ЬЬО.
На открытом воздухе полученный плав жадно притягивает влагу.
Приготовление продукта с содержанием СаСЬ выше 70% затруднительно в отношении слива продукта из котла в барабаны,
ибо чем меньше НгО в плаве, тем, выше его температура пла->
вления и тем чаще его застывание в период самого слива.
Полученный продукт содержит все .примеси, бывшие в маточном щелоке. По нашим наблюдениям несмотря на нагрев голым
огнем в чугунных котлах до столь высокой температуры, КСЮз,
содержавшийся в маточнике, почти целиком переходит в плавленый хлористый кальций, не разлагаясь. Кроме примесей,
бывших в маточниках, плавленый хлористый кальций содержит
также продукты коррозии выпарного котла.
Выпарные котлы с толщиной стенок в 40—50 мм выдерживают до 100 плавок.' Если упаривать маточный щелок, не содержащий КСЮз, то коррозия котла много меньше. Поэтому
имеются предложения разлагать КСЮз прибавлением в маточник соляной кислоты (используя выделяющийся хлор), после
чего уже производить упарку. По некоторым наблюдениям коррозия котлов значительно уменьшается от .прибавления щелочи
к упариваемому маточнику.
§ 3. Применение маточных щелоков для получения хлористого
бария (по Дюфло)44
По методу Дюфло хлористый барий производится, исходя из
BaSO« и СаСЬ, на чем и основано использование для этого бертолетовых маточных щелоков. Практически обычно применяют
минерал тяжелый шпат (барит). Содержание в барите BaSOi
равно 80—95%.. Кроме BaSCb барит содержит примеси железа,
марганца и др.; уд. вес барита равен 4—5. В СССР барит встречается на Кавказе близ Кутаиси, в Азербайджане близ Кировабада, в Туркмении в бассейне реки Сумбур, на Урале близ
г. Миаса и ст. Кыштым. Бертолетовый маточный щелок ула-
142 1
ривастся до Температуры кипения 100° и сливается в корытообразный сосуд для остывания. Остывший плав измельчается до
кусочков величиной нс больше 5—10 cm и загружается в тамбур
вместе со смесью тонко измельченного барита и угля. Тамбур
представляет собой железный цилиндрический барабан длиной
ооб лг й диаметром счэ 1,5 т, вращающийся со скоростью
1 об/мин. .Изнутри тамбур выложен огнеупорным кирпичом.
В тамбуре шихта прокаливается пламенем нефтяной форсунки в течение 5—7 час. Для загрузки шихты и выгрузки полученного после прокалки плава в тамбуре имеется герметически
закрывающийся* люк. Перед выгрузкой прекращают вращение
тамбура в положении, когда люк наверху. Отвинтив крышку
люка,7 Поворачивают тамбур так, чтобы открытый люк очутился
внизу — плав выльется из тамбура в подставленное железное
корыто, где он и застынет.
При прокалке, начиная с температуры счэ 800°, уголь восстанавливает сернокислый барий в сернистый: • ^
BaS04 + 2C = BaS + 2C02. ' ' (G5)
Поскольку С02 улетучивается с топорными газами, реакция (65) проходит полностью. Образующийся BaS реагирует
с расплавленным при данной температуре безводным хлористым
кальцием: 4
BaS'+ СаСЬ = CaS + ВаСЬ. (66)
Суммарное уравнение' реакций, происходящих в печи, может
быть выражено следующим уравнением:
BaSO* + 2С + СаСЬ = BaCU + CaS + 2СОг. (67)
Практический расход угля значительно выше, чем должен
быть по расчету согласно уравнению (67), ибо часть угля сгорает при высокой температуре. Кроме того часть угля реагирует
с BaS04 не до С02, а только до СО:
BaS04 + 4С = BaS + 4СО. (68)
Застывший плав состоит в основном из BaCU и CaS. Примесями
являются непрореагировавшие BaS04, уголь, СаС12, а также примеси, бывшие в исходных продуктах: КС1 и NaCl из хлористого
кальция, зола из угля и др. (КСЮз весь разлагается на КС1 и
кислород). Массу разламывают на куски, которые измельчают
на дробилке Блека. Измельченный плав выщелачивают горячей
водой в особых чанах-выщелачивателях по принципу противотока до тех пор, пока удельный вес отстоявшегося раствора достигнет 1,345 (37° Боме). Остающийся нерастворимый остаток,
состоящий из CaS с примесями BaS04, золы, угля и т. п., отжимают от раствора на центрофугах (или нутч-фильтрах) и тщательно промывают горячей водой. Промытый шлам является
отбросом и практически пока не используется. 1
148
Полученный раствор уд. веса 1,345 (37” 1>о\к ) и щ u ; i.i.;
воды отстаиваются, декантируются от осадка и упариваются
в башне Гаяра *. Последняя представляет собой вертикальную
печь, отапливаемую снизу нефтяной форсункой и орошаемую
сверху упариваемым щелоком. Примерные размеры башни: И
—15 м и D= 1,5 лг внизу и 0,9 м наверху. Изнутри башня выкладывается огнеупорным кирпичом. Падающий сверху печи распыленный раствор встречает горячие топочные газы и упаривается. Уваренный щелок, вытекающий из печи, перекачивается
в кристаллизаторы, где охлаждается, и из него выделяется часть
хлористого бария в виде кристаллов ВаСЬ • 2НгО. Их отделяют
на центрофутах и сушат горячим воздухом во вращающихся барабанных сушилках.
Маточный щелок, содержащий еще значительное количество
ВаСЬ и все растворимые примеси плава (СаСЬ, КС1, NaCl и т. д.),
поступает опять на выпарку вместе с раствором от выщелачивания нового количества плава. Таким образом с каждым циклом
производства щелока до и после кристаллизации хлористого,
бария все более обогащаются примесями. Поскольку обычно
70—90% от общего количества примесей составляет СаСЬ, маточный щелок по достижении в нем содержания СаСЬ
200—250 г/л упаривают для получения плавленого хлористого
кальция.
Высушенный хлористый барий содержит 95—97% ВаСЬ • 2ЬЬО
и годен как технический продукт. Для получения более чистого
продукта его перекристаллизовывают из воды, пользуясь различной растворимостью ВаСЬ в воде при разной температуре
(см. табл. 38 стр. 145).
На рис. 71 приведена схема получения хлористого бария по-
Дюфло.
1 Возможна конечно упаркащ в других аппаратах.
144
Теоретические коэфициенты производства хлористого Пария
этим методом выводятся из уравнении (07) на 1 г ВаСЬ • 2НгО:
расход СаСЬ:
расход BaSO«:
расход угля:
получается отхода CaS:
СаС12
liaCL • 211./):
BaSOj
ВаС12 • 2НаО
244,3
2С
24
ВаС12.‘2Н20
244,3
CaS
72
ВаСЬ.2Н20
244,3
=^г0'45 2
233,3 Л пс -
0,098 г
0,29 г
Практические коэфициенты рассчитываются, исходя из теоретических коэфициентов с учетом производственных потерь и
содержания 'примесей в исходных и получаемых продуктах.
На готовый продукт «хлористый барий» имеется стандарт
ОСТ 4894. Обычно содержание ВаСЬ • 2НгО равно 95—96'/.
Основные примеси: СаСЬ 0,5—1%, NaCl 1—3%, нерастворимый
остаток до 1%, гигроскопическая влага до 2%. Содержание
СаСЬ делает продукт гигроскопичным. Примеси железа окрашивают продукт в желтый цвет, а примеси угля в серый цвет.
Чистый хлористый барий образует бесцветные кристаллы
ВаСЬ • 2НгО ромбической формы, горько соленого вкуса;
весьма ядоьит; удельный вес 3,1; в спирту нерастворим; неги-
гроскапичен, кристаллическую влагу теряет при нагревании до
температуры 130°.
В табл. 38 приведены плотность и концентрация насыщенных
растворов ВаСЬ при температуре от 0 до 100°.
Таблица 38. Плотность и концентрация насыщенных растворов ВаСЬ при температурах
от 0 до 100°®
Темпе¬
ратура
Содержание ВаС1,
Плотность
°!о
t/кг HtO
г/л
уд. вес
• Боме
0°
24
' 316
300
1,25
28,8
10°
25
333
317
1,27
30,7
20°
26,3
357
337
1,28
31,5
30°
27,6
381
356
1,29
32,4
40°
. 29
408
377
1,30
33,3
50°
30,4
437
398
1,31
34,2
60°
31,7
464
422
1,33
35,9
80°
34,4
525
464
1,35
37,4
100°
37
587
503
1,36
38,2
§ 4. Использование хлората, остающегося в. маточном щелоке
первой кристаллизации
Хлорат, остающийся в маточном щелоке, является потерей.
Кроме того этот хлорат является баластом и даже вредным для
10 Зав, 179. — Щройбман.
145
потребителей, использующих маточный щелок как распюр (JaCb.
Наиболее важной рационализацией в этом вопросе явилось применение вымораживания маточных щелоков и .прибавление
15—25% избытка КС1 при обменной реакции, благодаря чему
содержание КСЮз в маточниках уменьшилось до 5—8 г/л.
Дальнейшая утилизация этого остатка КООз пока не нашла
удовлетворительного разрешения.
Юриш 1 и Лунге3 приводят нижеописываемые условия для
разложения хлората соляной кислотой с образованием хлора.
Маточный щелок прибавляли к разбавленной соляной кислоте
при энергичном перемешивании открытым паром и отсасывании
паров и выделяющегося хлора; последний использовался для
хлорирования. Маточный щелок прибавляют до полноты прореагирования всей кислоты. При отсутствии .перемешивания паром реакция между хлоратом и кислотой шла неравномерно и
получались взрывы с выбросом жидкости и крышки реакционного котла, чему вероятно было причиной образование СЮг
|по уравнению (14) стр. 24]. Для уменьшения опасности взрывов геометрический объем реакционного котла должен быть
в два раза больше рабочего объема, крышка котла должна
иметь предохранительный затвор, залитый водой, и хлороотвод
должен быть достаточно большого диаметра.
Согласно реакции КООз с соляной кислотой по уравнению
(13) на 1 г КСЮз тратится
6HCI _ 6-36-46
КСЮ;,— 122,56'
—1,79 г НС1
и следовательно получается
6С1 6-35-46 .
КСЮз- 122,56 1.74 г хлора.
В данное время имеются попытки возобновления и усовер*
шенствования этого способа с целью получения раствора СаС1г,
не содержащего хлората.
ГЛАВА 12
ОСНОВНЫЕ КОЭФИЦИЕНТЫ ПОЛУЧЕНИЯ БЕРТОЛЕТОВОЙ
СОЛИ ИЗВЕСТКОВЫМ МЕТОДОМ
В данной главе приводим расходные коэфициенты, состав и
количества производственных растворов, баланс потерь, основные точки расхода воды и пара, движение материального потока,
а также калькуляцию готовой продукции и примерный штат для
производства бертолетовой соли известковым методом.
; § 1. Состав и количества производственных растворов и
баланс потерь
Табл. 39 составлена соответственно схеме, показанной на
рис. 5 (стр. 30). Количества СаО, Са(СЮ»)*, Cad*, КС1 и
146
Таблица 39. С о с т а в н количества1'производственных растворов для получения КС103 известковым методом с применением выпарки
н
Какие растворы
Объем
Состав в г/л
Всего тонн i
Плотность
пп.
В
СаО
Са (ClOahj CaCI,
КС!
KClOg
СаО |са (СЮа),
СаС!*
КС!
KCIOj
Уд. вес
° Боме
Темпе¬
ратура
1
'
Известковое молоко . . .
12,45
110
137
_
_
_
1,083
11
20э
2
Осветленный хлорирован*
ный щелок
12,95
<
4 65
. 174
—
—
—
0,845
2,26
—
—
1.17
21
40°
3
Уваренный щелок .
4,75
—
178
475
—
—
—
0,845
2,26
—
—
1,42
42,7
70°
4
Раствор KCI .
2,08
—
—
—
350
—
—
—
—
Р,73
—
1.17
21
803
5
Бертолетовый щелок . . .
6,83
—
—
398
18
146
—
—
2,72
0,12
1.0С0
1,35
37,4
70э
6
Маточный щелок 1-й кристаллизации .
6,15
—
—
442
20
7
—
—
2,72
0,12
0,04
1,37
39
о
1
7
Разваренный щелок 2 . .
3,54
—
—
5—10
—
350
0,017-
0,035
—
1,236
1,18
22
95
100^
8
Маточный щелок 2-й кристаллизации
2,93
—
—
6-12
*
73
—
—
0,017—
0,035
. —
0,214
1,046
6,5
20"
1 Объемы*и количества тонн*для^пп. 1—6 рассчитаны на получение 1 m КСЮ3 в виде бертолетового щелока. Для
пп. 7—8 объемы [и количества тона рассчитаны на 1 m КСЮ3, получаемую в виде готовой перекристаллнзованной соли,
учитывая вымывание 22 кг КСЮЛ при промывке бертолетовой соли 2-й кристаллизации холодным конденсатом.
2„„Разваренный щелок-'— принятое в производстве обозначение горячего раствора КС103, поступающего на 2-ю кристаллизацию.
Таблица 40. Состав
KClOii и ни. 1—f> pacci и i ;i и м
согласно уравнениям (.47) и (03)
(стр. 59 и 107) с учетом применения 20% избытка КС1 при
обменной реакции. Принимаем
4,2%-ное увеличение объема при
хлорировании (стр. 69), 10%-нос
уменьшение объема при 1-й
кристаллизации и 17,4%-ное
уменьшение объема при 2-й
кристаллизации (стр. 132). Практически объем щелоков и количества СаО, Са(СЮа)2, СаСЬ и
КС1 будут несколько иные
' (соответственно производственным потерям — см. табл. 41).
Состав щелоков и их плотность
* не зависят от производственных
потерь, а только от налаженности режима работы.
Табл. 40 составлена соответственно схеме хлорирования, показанной на рис. 28 (стр. 72).
При схемах хлорирования, показанных на рис. 29 и 30 (стр. 73),
изменяются только состав и
объем известкового молока.
Состав и количества бертолетовых и маточных щелоков
приведены, исходя из обменной
реакции с раствором КС1. При
обменной реакции с твердым
хлористым калием состав и количества бертолетовых и маточных щелоков будут те же, что
в табл. 39, почему их не при-
■ водим. Состав и количества раз^
gf варенных и маточных щелоков'
«-• при 2-й кристаллизации такие
« же, как в щелочах, показанных
* в табл. 39, почему и не приве-
<и дены.
* Количества СаО, Са(СЮз)«,
?. СаС1г и КС1 в пп. 1—3 рас-
* считаны, как и в табл. 39, из
g- уравнений (37) и (63). Концен-
а- трацию СаО в известковом мо-
и локе принимаем в 230 r/j. Уве-
~ личение объема при хлориро¬
вании принимаем в 7,2% (стр. 69);
уменьшение объема при кристаллизации принимаем и
(стр. 132).
Табл. 41 составлена на основе наших лабораторных и заводских исследований, исходя из схемы производства, показанной
на рис. 5 (стр. 30). Расчет потерь дан по отношению к теоретическим количествам, получающимся согласно уравнениям (37)
и (63). Потери хлора и хлората одинаковы, поскольку согласно
схеме рис. 5 абгазный хлор целиком поглощается в абгазной
колонке и потерь хлора с абгазом нет. Потеря СаО больше
потери хлора соответственно потере СаО при приготовлении и
очистке молока (п. 1). Потеря КС1 больше потери хлора ввиду
применения 20% избытка КС1 при обменной реакции и механических потерь при приготовлении раствора КО. Потерь СаСЬ
при хлорировании нет, ибо они компенсируются образованием
СаСЬ при реакциях с выделением кислорода: 5%-ные потери
СаСЬ при стадиях,3, 4 и 6 компенсируются тем, что для возмещения общей потери хлората при хлорировании расходуется
СаО и СЬ на 16,2% больше, чем требуется согласно уравнению (63). В итоге СаСЬ получается на 16,2 — 5,0=11,2%
больше, чем по уравнению (63).
Таблица 41. Ориентировочный баланс потерь по отдельным
стГадиям и отдельным продуктам в процентах при получении КСЮ8 по известковому методу с применением выпарки
1
Какие продукты
и
пп.
Какие стадии производства
СаО
Хлор и
хлорат
КС1
СаС)а
Изве¬
стковое
молоко
Хлорированные щелока
Уварен ные
и бертоле-
товые щелока и раствор КС1
1
Приготовление мслока .
10
2
Хлорирование и обез-
вреживание
5
5
.._
5
. .
3
Отделение шлама . . .
1
1
—
1
1
—
—
4
Выпаривани щелоков .
2
2
—
2
2
2
—
5
Обменная реакция и
кристаллизация . . .
2
2
3
2
2
2
2
6
Сушка и упарка ....
0,2
0,2
0,2
—
0,2
0,2
0,2
7
Маточник 1-й кристаллизации
6
6
26
—
6
6
6
Итого потерь .
26,2
16,2
29,2
5.0
16,2
10,2
8.2
Выход от теоретического количества . . .
73,8
83.8
70,8
95,0
83,8
89,8
91,8
Поскольку в значительной части потери являются механическими (вследствие проливания щелоков и т. д.), возможно их
уменьшение против процентов, показанных в табл. 41.
У
149
§ 2. Расходные коэфициенты, количества получаемых о i холоп,
расход воды и пара
В табл. 42 приведены количества основных продуктов, полупродуктов и отходов из расчета получения 1 т готовой КСЮя
известковым • методом с применением выпарки. Данные пп. 1—4
рассчитаны, исходя из уравнения (63) и табл. 41. Данные
пп. 5—12 рассчитаны по соответствующим величинам из табл. 39
и 41. Данные пп. 13—15 и 20—22 взяты из практики. Данные
пп. 16—19 взяты из табл. 44.
Таблица Количества основных продуктов и полу продуктов, необходимых для получения 1 /п готовой КС103 по и з в е-
. с т к о в ом у м е т о д у с п р и м е не н и е м в ы п а р ки
Еди-
Количества
Процент
потерь
н
пп.
Какой продукт или полупродукт
ница
изме¬
рения
без учета
потерь
практи¬
ческие
1
Известь (при расчете на СаО 100%)
m
1,37
1,86
26,2
2
Хлоргаз (при расчете на С13 100%)
п
1,74
2,08
16,2
3
Хлористый калий (при расчете на
КС! 100%)
п
0,61
0,86
29,2
4
СаСЬ в маточных щелоках 1-й кри-
сталлизации
п
2,72
3,02
+ 11*
5
Известковое мслоко, очищенное от
примесей
мъ
12,45
14,8
16,2
6
Хлорированные щелока, обезвреженные и осветленные от шлама
п
12,95
14,5
10,2
7
Уваренные щелока
п
4,75
5,18
Ч
8
Раствор КС1
п
2,08
2,27
8,2
9
Бертолетовые щелока
п
6,83
7,45
8,2
10
Маточные щелока 1-й кристаллиза-
ции
ft
6,15
6,65
___
11
Разваренные щелока 2-й кристаллч-
зации
п
3,54
3,61
2
12
Маточные щелока 2-й кристаллизации
п
2,93
2,93
_.
13
Жидкость от промывки соли 1-й
кристаллизации
_____
0,30
' __
14
Выщелоченный шлам от хлорированных щелоков
п
0,47
1
15
Жидкость от выщелачивания шлама
п
—
4,2
—
16
Количество воды, выпариваемой из
хлорированных щелоков
m
9.5
—
17
Количество конденсата, получаемого
от выпарки
ft
11
—
18
Общий расход пара
Щ
—
15
—
19
Общий расход воды
М3
—
500
—
20
Расход электроэнергии
Ksm-ч
\
200
—
21
Аммиачная вода для обезврежива-
вания (в пересчете на 100% NH3)
кг
2-3
\ —
22
Гипосульфит для обезвреживания .
0,1—0,2
г -
i
* Получается больше теоретического
ходу СаО и С1а (см% стр. 149).
(на 11%) благодаря большему рас-
150
В табл. 43 приведены коэфициенты получения 1 г KCiO.i известковым методом по Ульману5 и по Биллитеру ,2.
Таблица ^.Коэфициенты получения 1 их КСЮ;1 н о
Ульману5-3 и Биллитеру12
№
П11.
Что расходуется
По Ульману
По Биллитеру
1
Извести негашеной1 . . .
2 т
2,3 т
2
Хлора
2,16 т
2.3 .
3
Хлористого калия1 . . . • .
0,70 .
0.9 „
4
Пара в 4 am
—
6,7 ,
5
Угля
35 т
6
Энергии
80 л. с.
20 квт-ч
7
Воды
—
8-10 л<3
8
Рабочей силы, чел/дней
8
7
1 По Ульману применяемая известь содержит 96—98% СаО, а хлористый
реалий содержит 98% КС1.
В табл. 44 приведено примерное распределение расхода воды
и пара для получения 1 т готовой КСЮз известковым методом
с применением выпарки. Количества продуктов, на охлаждение
или на нагрев которых расходуются вода и пар, взяты из
табл. 42.
Таблица Расход воды и пара на получение 1т КСЮ3
известковым методом с применением выпарки
А. Расход воды
м
На что расходуется вода
Температура вС
Расход
лп.
■
начальная
'
конечная
м■ воды
1
Охлаждение 16 т известкового
молока
70
20
ЮО
2
Конденсация 9,5 т пара в барометрическом конденсаторе ....
80
40
200
3
1
Охлаждение 10 т щелоков при
1-й кристаллизации
‘ 60
15
80
4
Охлаждение 4,7 т щелоков при
2-й кристаллизации
90
15
70
S
Приготовление молока, конденсация пара при сушке соли и прочие
нужды .
—
—
50
'
Итого . .
500
151
Б. Расход пара
Па что расходуется пар
Температура ®С
Расход
пп.
начальная
конечная
m пара
1
Подогрев 14,5 m поды для приготовления известкового молока . .
40
90
1
2
Выпарка 9,5 m воды из хлорированных щелоков
40
80
11
3
Приготовление 2,6 m раствора
KCI для обменной реакции ....
20
100
0,45
4
Растворение соли прн перекристаллизации (4,7 m раствора) . . .
20
% 100
0,75
5
Сушка 1,07 m бертолетовой соли
и прочие нужды
—
—
1,8
'
Итого. .
15
§ 3. Баланс воды для приготовления известкового молока и раствора КС1; распределение конденсата, получающегося при
выпарке хлорированных щелоков
Нижеприведенные данные относятся для производства КСЮ*
известковым методом с применением вьипарки.
1. Баланс воды в жидкости для приготовления известкового
молока
Вода в жидкости от выщелачивания шлама 4,2 т
Конденсат от вьгпарки (см. ниже п. *2) . . . . . • 5,1 »
i Вода из барометрического конденсатора 5,2 »
Итого 14,5 г
Примечание. Для полу*Иения 1 т готовой КСЮ» по табл^ 39 необходимо 12,45 м* известкового молока, что соответствует 13,6 г молока.
Практически с учетом производственных потерь необходимо 16 г молока,
содержащего (при СаО ПО г/д) 14,5 г НЮ.
2. Использование конденсата, шолучающегося при выпарке
хлорированных щелоков
На промывку соли 2-й кристаллизации . . . . . . . 0,3 г
На приготовление раствора КС1 .(см. ниже п. 3) . 1,4 »
На выщелачивание шлама ". .... 4,2 »
На приготовление известкового молока (см. выше л. 1) . . 5,1 >
Итого 11 г
Примечание. 11 т конденсата получаетсй rfa 1 г готовой КСЮ»
(см. табл. 42)л
152
/
3. Баланс воды для приготовления КС1
Воды в жидкости от промывки соли 1-й кристаллизации . • 0,3 т
Конденсат от выпарки (см. выше п. 2) 1,4 >
Итого. . . 1,7 г
Примечание. Для получения 1 т готовой КСЮз по табл. ЗЭ требуется 2,08 л3 раствора КО 360 г/л, что соответствует 2,43 т раствора. Практически с учетом потерь требуется 2,6 г раствора, содержащего 1,7 г 11=0.
§ 4. Калькуляция стоимости готовой бертолетовой соли и штат
завода производительностью в 15 т КС103 в сутки
Приведенные в табл. 45 и 46 данные относятся для производства бертолетовой соли известковым методом с применением выпарки.
Таблица 45, П р и м с р и а я к а л ь к у л я ц и и з а » с» л i ~ f < ч • < • *■ с
мости 1 т бертолетовой соли при известно и о м мп оде
производства с применением выпарки
Наименование статей
Расход
Процент
е
е
*
ед. измерения
количество
общей
стоимости
1
Основные материалы
Известь (содержание СаО 94%) . .
т
1,9
13
2
Хлоргаз
п
2,1
36
-3
Хлористый калий ^содержание
КС198<у0)
п
0,86
14
4
Итого ...
'Вспомогательные материалы
Реактивы для обезвреживания . .
кг
5
G3
\
5
Сода кальцинированная ......
9
5
0,1
б
Полотно для центрофугирования .
м
1
1
7
Итого . . .
Пар, вода, электроэнергия,
холод
Пар
т
15
0,1
4.5
8
Вода , . . . . .
м»
500
0,5
9
Электроэнергия . •
квт-ч
200
0.5
10
Холод для вымораживания ....
ккал
250000
5.0
11
Итого ...
Труд
Рабсила — основная зарплата . . .
чел-час
40
10,5
3,5
12
Дополнительная зарплата с начис-
лениями '
—
—
0,8
Итого . . .
/
4,3
13
Накладные расходы
Текущий ремонт
3,8
14
Амортизация
—
—
3,7
15
Административно-технический лер-
сонал
,
2,9
16
Подсобный персонал
—
—
3,4
17
Прочие цеховые расходы
/
—
2,0
18
Общезаводские расходы
—
—
6,3
Итого...
22,1
/
Примечание; При производстве бертолетовой соли получается от-
.ход — маточник 1-й кристаллизации, содержащий СаС1а~3 т на 1 т готовой
бертолетовой соли. Стоимость отхода 5—10% от стоимости бертолетовой
соли. ,
154
Таблица ^.Ориентировочный штат завод а п р о и з в о д и ч о л i»-
о тыо в 15 w КСЮ3 в сутки при известковом метоле
производства (с применением выпарки)
Стадия производства
Выполняемая работа
Колпчсс гео
1 смену
всего
Приготовление известно-
Аппаратчик
1
4
вого молока
Хлорирование, обезврежи-
Аппаратчик по хлорированию . . .
1
4
ванне, отделение шлама
Аппаратчик по обезвреживанию и
и выпарка
отделению ^шлама (он же старший
рабочий)
1
4
Аппаратчик по выпарке
1
4
Обменная реакция, 1-я кри-
Аппаратчик по приготовлению рас-
сталлизация и 2-я кристал-
твора КС1 и обменной реакции .
1
4
лизация
Аппаратчик и помаппаратчика по
1-й кристаллизации
2
К
Аппаратчик и помаппаратчика по
2-й кристаллизации
2
8
>
Старший рабочий отделения . . .
1
4
Сушка, размол, просеива¬
Аппаратчик * и помаппаратчика по
ние, укупорка
сушке и просеиванию
2
8
Рабочий по укупорке бертолетовой
соли
1
J
Мастер
—
1
Вспомогательные рабочие
Машинист компрессоров и вакуум-
насосов
1
4
Дежурный слесарь-электрик ....
1
4
Уборщица
1
4
✓
Рабочие по прдвозке материалов и
отвозке отходов и готовой про¬
1 '■
дукции
4
Обслуживающий персонал
Кладовщик-завхоз
1
Счетовод-табельщик
1
Лаборатория
Заведующий цеховой лабораторией
1
Дневные лаборанты
—
2
Сменные лаборанты
1
4
Административно-техниче¬
Зав. и пом зав. производством . .
2
ский персонал
. Дежурные инженеры
1
4
*
Механик производства ......
1
Итого . .ч .
18
85
155
ЧАСТЬ ВТОРАЯ ,
ДРУГИЕ МЕТОДЫ ПРОИЗВОДСТВА
БЕРТОЛЕТОВОЙ СОЛИ И МЕТОДЫ ПОЛУЧЕНИЯ ДРУГИХ
ХЛОРАТОВ
ГЛАВА 13
КАУСТИЧЕСКИЙ И СОДОВЫЙ МЕТОДЫ ПОЛУЧЕНИЯ
БЕРТОЛЕТОВОЙ СОЛИ
Каустический и содовый методы получения бертолетовой
соли исходят из применения для хлорирования NaOH и №гСОз
вместо извести, .применяемой при известковом методе. Хотя
NaOH и №гСОз являются более ценными продуктами, чем известь, схема и техника производства при каустическом и содовом методе имеют ряд преимуществ, вследствие чего при некоторых условиях эти способы могут стать конкурентноспособными по отношению к известковому методу. В литературе
имеются указания на применение содового способа Гаргривса
(Ульман ®~*, Гмелин 4-21 (ряд патентов). Выгода каустенического
и содового методов заключается -в простоте процесса, меньших
химических потерях, также в возможности получения при одной
и той же аппаратуре КСЮз, NaClOe и Ва(СЮз)г, что дает возможность более широкого маневрирования.
§ 1. Основная схема каустического метода
На рис. 72 показана схема каустического метода, проверенная на одном из современных заводов. Поскольку хлор и
NaOH являются при данном методе только полупродуктами,
получается замкнутый цикл, где тратится только КС1 и получается КСЮз. Трата NaCl происходит только на возмещение механических потерь в разных стадиях производства. Отдельные стадии этого способа .производства следующие.
1. Приготовляется «рассол» — раствор, содержащий NaCl
300—310 г/л. В основном рассол приготовляется из «обратной»
соли, выделяющейся 'При выпарке (п. 5) и конденсата. Соль со
склада и вода расходуются только в возмещение производственных потерь. Часть рассола, приготовляемая из складской соли,
должна очищаться! от соединений Са, Mg, SO4 и от нерастворимых примесей. Рассол из обратной соли обычно не содержит
этих примесей.
2. Рассол подогревается до 70—80° и подвергается электролизу. Получающийся при электролизе водород является отходом, а хлор и слабый каустик являются полупродуктами для
получения- КСЮ*.
/ •
166
Рис. 72. Схема каустического метода производства бертолетовой соли с применением выпарки.
ш персхлориробыь
3. Слабый каустик, .полученный при электролизе (ох.шжщм-
ный до 30—40°), содержащий NaOH 100—120 r/л, поступает на
орошение в колонку (рис. 42, стр. 8G), через которую вентилятором просасывается абгаз, содержащий хлор. Абгаз после колонки хлора не содержит и выбрасывается вентилятором
в атмосферу. Абгазиый щелок, вытекающий из колонки, поступает в аппараты для основного хлорирования (башни, рис. 38,
стр. 81). Для лучшего выхода хлората температура конца
хлорирования должна быть 70—80°. Искусственного охлаждения
при хлорировании слабого каустика нс нужно.
4. Щелок, полученный после хлорирования, содержит небольшие количества гипохлорита и растворенного хлора, которые
после продувки воздухом обезвреживаются раствором аммиака.
Температура обезвреживания должна быть нс ниже (>5—70°.
Избытка аммиака задавать не надо. Для уверенности в полноте
обезвреживания обычно задают еще гипосульфит в количестве
10—15 г на 1 /и3 щелока.
5. Обезвреженный щелок в смеси с маточным щелоком
(п. 7) упаривается до удельного веса 1,32—1,34 (35—37" Боме).
При выпарке выделяется большая часть NaCl, содержавшегося
в щелоке до выпарки (83%, см. табл. 55), и увеличивается концентрация хлората. Упариваемые щелока должны содержать
NaOH 3—5 r/л для предохранения железных частей выпарной
установки от коррозии. Выделяющаяся «обратная» соль отделяется от уваренного щелока на нутч-фильтрах и промывается
горячей водой, после чего используется для приготовления рассола (п. 1). Промывные воды возвращаются на выпарку. Конденсат выпарки используется для приготовления рассола и т. д.
6. К щелокам, уваренным до удельного веса 1,32—1,34, прибавляется раствор KQ из расчета соответственно содержанию
NaClOs в уваренном щелоке. Избыток КС1 вреден, ибо увеличивает отношение КСЮз: NaClOs в увариваемом щелоке, что может вызвать кристаллизацию КСЮз в выпарных аппаратах.
-V 7. Полученный после обменной реакции «бертолетовый»
щелок охлаждается, отчего выделяется большая часть КСЮз.
Выделившаяся соль отделяется на центрофугах или нутч-филь-
трах от маточника щелока, который возвращается на выпарку
в следующий цикл производства (п. 5). Так как КСЮз, остающийся в маточном щелоке, не теряется, а возвращается в цикл
производства, то вымораживание маточного щелока нецелесообразно. Промывка отжатой соли и дальнейшая ее обработка
такие же, как при известковом методе (см. гл. 10 п. И).*
Примечания, а) При отсутствии очистки от SO," рассола, получаемого из поваренной соли и водопроводной воды, и применения гипосульфита для обезвреживания может получиться значительное содержание
* Каустический метод связан с электролизом поваренной соли и потребляет как хлор, так и щелочь. Поэтому этот метод ие имеет преимуществ
по сравнению с получением хлоратов электролизом, а аппаратурно сложнее.
Он может иметь однако значение в отдельных местах при отсутствии потребности в едкой щелочи. Прим. рея.
158
NasSO* в уол репных п маточных ще. юках, что ухудшает yc. ioumi им парки
и вызыиает загрязнение готовой соли сульфатом. Поэтому при таких условиях надо периодически (раз в 1- 2 мес.) очищать маточные щелока от
сульфатов прибавлением раствора ВаС1г.
б) При концентрации NaCI в рассоле выше 300 г/л при хлорировании
часть образующейся NaCI выделяется в виде кристаллов, что может вызвать забивание щелокопроводов. Для слабого каустика суммарное содержание NaOH и NaCI не должно превышать 5,5—5,6 молей на 1 л; при
большей концентрации — при хлорировании выделяется часть NaCI в виде
кристаллов.
в) Хлорированный щелок окрашен от наличия феррата.
г) В упариваемой смеси маточных и обезвреженных щелоков (п. 5)
хлорат содержится в .виде КСЮз к NaClOs. Соотношение КСЮ» и NaCIO*
должно быть близко к 1:2. Чем больше КСЮз, тем ниже должма быть
концентрация щелока «в конце выпарки, иначе увеличивается содержание
хлората в обратной соли, часть КСЮз может выпасть во время перекачки
щелоков ит.д.
§ 2. Основная схема содового метода
На рис. 73 приведена схема содового метода, разработанного
нами и проверенного на заводской установке. В общем схема
этого метода идентична с вышеприведенной схемой каустического метода за исключением следующих моментов.
1. На хлорирование поступает раствор №гСОз 200 r/я, подогретый до 60—70°, так как при хлорировании выделяется
очень немного тепла (см. стр. 164), а оптимальные условия хлорирования создаются при 65—75° (стр. 170).
2. Абгаз после хлорирования содержит СОг в концентрации,,
примерно равной концентрации СЬ в хлоргазе; поэтому абгаз
является отходом и может быть использован.
. 3. «Обратная» соль, выделяющаяся при выпарке, является
отходом.
§ 3. Варианты каустического и содового методов
а) На рис. 74 показана схема каустического метода производства бертолетовой соли без применения выпарки (предложение
И. Б. Фраймана). Горячий щелок, полученный после хлорирования слабого каустика и обезвреживания от СЮ', поступает на
обменную реакцию с твердым хлористым калием (избыток
КС1 — 30 г/я) и дальше на кристаллизацию, которая проводится
с вымораживанием маточного щелока до 10—20° ниже нуля.
Вымороженный маточный щелок, содержащий кроме NaCI еще
КС1 30 г/я и КСЮз 10—20. г/я, поступает на электролиз — начинается новый цикл производства. Преимуществом данного варианта является отсутствие выпарки (расход пара, стоимость
выпарной установки, потери при выпарке и т. д.). Недостатками ■
данного варианта являются: 1) необходимость вымораживания
маточника (расход холода, стоимость холодильной установки);
2) малый выход КСЮз на единицу объема щелока при кристаллизации (30—40 г/я), почему требуется увеличенная мощность
аппаратуры кристаллизации; 3) потеря при электролизе ~ 50%
хлората, содержащегося в маточном щелоке вследствие катодного восстановления; 4) усложняется отделение мути от хлори-
■ '
та
С
3
CQ
а
<L>
<V
Q.
с
о
о
U
О
CD
О
н
V
г»
о
н
о,
<и
о
га
ш
н
о
г(
о
m
£2
о
Q,
с
та
*=С
о
н
а>
о
и
О
26
О
»=(
о
о
та
г»
И
О
со
о
Я
О*
рованного щелока и использование жидкости от промывки бертолетовой соли; в получаемой соли увеличивается содержание
хлорида и нерастворимого остатка.
160
Вместо раствора NaCl можно применить дли члектролила
раствор КС1 или раствор, содержащий и NaCl и КО, следуй
в остальном схеме, показанной на рис. 74. При таком варианте
гз
С
-а
со
ЗГ
О»
Си
с
СП
а>
ю
о
о
о
со
о
си
/ и
X
<и
о
е
г(
О
О
и
о
СО
2
И
и
''Г
о
S
Ди
отпадают обменная реакция и вымораживание .маточных щелоков (в растворе КС1 при 10° растворяется КС1СЪ всего 13 г/л),
но увеличиваются потери КС1
1 Целесообразность такого метода получения КСЮЭ сомнительна, так
как лучше проводить электролиз в ваннах без диафрагмы с образованием
КОЮ» и с последующим выкристаллизовьгванйем хлората вне ванны. Прим. ред.
\
11 Зав. 179. -г Шрайбмаж.
161
ражается уравнением:
6) 11л рис. /.г> показана схема содово-
го метода получения
КСЮа без применения выпарки. Раствор
Na2CC>3 готовится растворением соды в маточном щелоке от предыдущего цикла производства. В остальном этот вариант похож на вариант каустического метода без
применения выпарки.
Неудобства этого варианта те же, что изложены выше для варианта каустического
метода бе'з применения выпарки; кроме
того весьма усложняется процесс отделения и промывки
соли (NaCl), выделяющейся при приготовлении раствора Na^CCh
при хлорировании и
при обменной реакции.
§ 4. Химические реакции процессов каустического и содового методов производства бертолетовой
соли
а) Каустический
м е т о д
Суммарное уравнение электролиза рас-
Твора NaCl:
2NaCl + 2Н20 + 2 fO-f
-f-2©= 2NaOH +
—[- H2 -}- СЬ. (69)
Суммарно хлорирование раствора NaOH вы-
6NaOH + ЗС12 = NaClOa + 5NaCl + 3H20. (70)
В первую стадию хлорирования протекает реакция:
162
6NaOI I -f 3C12 — 3 NaCIO, + 3NaC1 +• 3H20 (71)
Введение избытка хлора вызывает образование хлорнова¬
тистой кислоты:
. С12 + Н20 ;=* НСЮ + НС1
NaCIO + НС1 = НСЮ +' NaCl
(30)
(71а)
или
Cl2 -f NaCIO + НгО = 2НСЮ + Nad. (71°)
Образовавшаяся хлорноватистая кислота окисляет гипохло¬
рит в хлорат:
2НСЮ + NaCIO = NaClOs + 2НС1
2НС1 + 2NaC10 = 2НСЮ -f 2NaCl
или
(71")
(710
(72)
3NaC10 = NaCIO» + 2NaC1.
Суммируя ур-ния 71 и 72, получаем уравнение 70.
Обезвреживание СЮ' проходит по тем же реакциям, что и
при известковом методе (стр. 95—97)/ Обменная реаюшя проходит по уравнению:
NaCIO, + КС1 = КСЮз -f NaCl. (73)
Суммарное уравнение получения КСЮз каустическим методом, исходя от стадии хлорирования, будет:
6NaO,H + ЗС1-2 -f КС1 = КСЮз 4- 6NaCl -f 3H20. (74)
Складывая уравнения (69) и (74), получаем суммарное уравнение:
ка 4- ЗН20 4- 6 0 4- 60= КСЮз 4- ЗН2, (75)
выражающее стехиометрическое отношение для всего процесса
в целом. (
' б) С о до вый метод
Хлорирование Na2C03 проходит в три стадии. Первая стадия
заключается в образовании гипохлорита и бикарбоната по
уравнениям: 4
3Na2COs 4- ЗС12 = 3NaC10 -f 3NaCl 4- 3C02. (76)
✓ 3Na2C0s + 3C024-3H20 = 6NaHC03. . (77)
-Или суммарно:
6Na2COs 4- ЗС12 4- ЗН20 = 3NaC10 4- 3NaCl 4- 6NaHC03. (78)
Вторая стадия хлорирования начинается после прореагирования всего Na2COs и заключается в реакции хлора с бикарбонатом:
6NaHCOa 4- ЗС12 = 3NaC10 + 3NaCl 4- 6С02 4- ЗН20. (79)
Третья стадия хлорирования заключается в переходе гипохлорита в хлорат и хлорид и благодаря растворенной С02' проходит параллельно второй стадии хлорирования.
И* 1€3
3NaCto — NaClOu + 2NaCl. (/2)
Суммарное уравнение хлорировании будет
3Na2C03 + 3CI* = NaClO.i + 5NaCl + 3C02. (80)
Обезвреживание CIO' проходит по тем же реакциям, что и
при известковом методе (стр. 96—97). Обменная реакция проходит по. тому же уравнению, что и при каустическом методе (73).
Полное уравнение получения" КСЮа содовым методом будет:
' ЗЫазСОя + ЗСЬ + КС1 = КСЮз + 6NaCl + ЗСОг. (81)
Кроме приведенных реакций при хлорировании растворов
NaOH и NasCOa происходит также образование 02 по уравнению (38).
$ 5. Тепловой эффект реакции хлорирования растворов NaOH
и NasCOj
а) Хлорирование NaOH
1- я стадия хлорирования:
, 6NaOH +- ЗС1„ — 3NaC10+3NaCl + 3H20 (71)
6 112,5 3-83,8 ' 3-97,7 3-68,5
Теплота образования исходных веществ равна 6 • 112,5 =
= 675 ккал.
Теплота образования получающихся веществ равна:
3 • 83,4 -J- 3 • 97,7 +• 3 - 68,5 = 748,8 ккал.
Тепловой эффект равен 748,8 — 675 = 73,8 ккал.
2- я стадия хлорирования:
' 3NaC10 = NaC103+2NaCl (72)
3-83,4 77,1 2-97,7
i >
, Теплота образования исходных веществ равна 3-83,4 =
= 250,2 ккал.
Теплота образования получающихся веществ рав^а:
> 77,1 + 2 • 97,7 = 272,5 ккал.
Тепловой эффект равен 272,5 — 250,2 = 22,3 ккал.
Тепловой эффект обеих стадий' хлорирования равен:
73,8 + 22,3 = 96,1 ккал 4 ‘
96 1
или Hfi 1 г NaOH выделяется-g-^-=0,40 ккал.
б) Хлорирование Na2COs
1-я стадия хлорирования:
6Na.?CO0 +- ЗС18 -+ ЗН20 = 3NaC10 -+ 3NaCl •+ 6NaHCOs. (78)
6-278 v ^ 3-69,5 3-83,4 3-97,7 6-223
Теплота образования исходных веществ равна:
' • * 6 • 278 + 3 - 68,5 = 1873,5 ккал.
S'
161
Теплота образования получающихся веществ равна:
3 • 83,4 + 3 • 97,7 + 6 • 223 = 1881,3 к кил.
Тепловой эффект равен 1881,3—1873,5 = 7,8 ккал.
2-я стадия хлорирования:
6NaHC08 + 3CL = 3NaC10 + 3NaCl + 6C09 + 3H.,0. (79)
6-233 ( 3-83,4 3-97,7 6-94,4 3-68,5
Теплота образования исходных веществ равна 6 • 223 =
=г 1338 шал.
Теплота образования получающихся веществ равна:
3 • 83,4 + 3 • 97,7 + 6 • 94,4 +' 3 • 68,5 =1315,2 ккал.
Тепловой эффект равен 1315,2 — 1338 = — 22,8 ккал.
3-я стадия хлорирования: ‘ j
6NaC10 = 2NaC10..+ 4NaCl. (72)
6-83,4 2-77,1 4-97,7
Теплота образования исходных веществ равна 6 • 83,4 =
= 500,4 тал.
Теплота образования получающихся веществ равна:
2 • 77,1 + 4 • 97,7 = 545 ккал.
Тепловой эффект равен 545 — 500,4 = 44,6 ккал.
Тепловой эффект всею процесса хлорирования равен:
7,8 + (—22,8) + 44,6 = 29,6 ккал.
или-«а 1 г ЫагСОа. выделится б7Щ5 = °,046 тел.
Примечание. Данные теплообразования веществ,
в реакциях хлорирования, взяты из СТЭ24"7
участвующих
§ 6. Преимущества и недостатки каустического и содового
методов по сравнению с известковым методом
а) П р еимущества каустического метода
1. Отпадают совершенно стадия приготовления и очистки, известкового молока, стадия отделения шлама и стадия вымораживания, вследствие чего уменьшается штат, оборудование, здание, амортизация.
2. Хлорирование и улавливание хлефа из абгаза проще, так
как приходится работать с раствором, а не со взвесью твердого
вещества в воде.
3. Нет потерь от КСЮз, остающегося в маточнике и при
отделении шлама. Расход КС1 меньше, так как не нужен избыток КС1 при обменной реакции.
4. Выше качество бертолетовой соли, так как в ней не содержится СаСЬ и гораздо меньше нерастворимого остатка.
5. Легко 'Осуществить переход с производства КСЮз на про¬
изводство NaClOs и Ва(СЮ>)з без особого переоборудования
(см. гл. 15 и 16). ' / •
165
6. Отсутствует потеря тока на образование ■'•■ч' i‘ б, и;>а >.и •
ктролнзе, так как NaClOa слабого каустика утилизируется. ■
7. Большая часть рассола, поступающего на электролиз, не
содержит Са и Mg, что уменьшает затраты на очистку рассола.
б) Недостатки каустического метода
1. Вместо дешевой и всегда доступной извести тратится
более ценный едкий натр. Правда, абсолютная цена NaOH в виде
слабого каустика обычно не на много выше цены извести, но
едкий натр более ценен с точки зрения общехозяйственного
баланса.
2. При известковом методе на 1 т КСЮз получается в виде
отхода СаО*. Стоимость этого отхода равна 5—10% от 1
общей стоимости бертолетовой соли (табл. 45, стр. 155) и кроме
того* он является в настоящее время продуктом, на который
имеется большой спрос. При каустическом методе этого отхода
нет.
3. При каустическом методе приходится выпаривать в
2—2,5 раза больше воды, чем .при известковом методе, т. е. значительно увеличивается расход пара, необходимая мощность
оборудования и т. д. Кроме того процесс выпарки при каустическом методе много сложнее, ибо приходится отделять непрерывно выделяющийся NaCl, а при известковом методе приходится только выпаривать воду.
в) Преимущества и недостатки содового
метода
Применение соды вместо извести в основном имеет те же
преимущества, что и применение NaOH. Уступает содовый метод
каустическому тем, что при последнем получается процесс
с характером замкнутого цикла и фактически тратится NaOH
в виде полупродукта (слабый каустик), а не готовый продукт,
каким является сода.
§ 7. Некоторые данные по изучению хлорирования растворов
NaOH
Хлорирование растворов NaOH протекает так же, как и хлорирование известкового молока; пока в растворе есть NaOH,
происходит образование гипохлорита, а когда уже больше NaOH
нет, наступает стадия «перехлорирования» — в щелоке появляется растворенный хлор и гипохлорит переходит в хлорат
и хлорид. Как и при хлорировании известкового молока, во
время 1-й стадии хлорирования' растворов NaOH происходит постепенный подъем температуры, а в момент перехлорирования
происходит скачок температуры (рис. 23, стр. 63). Отличием
хлорирования растворов NaOH является более простая техника
процесса, поскрльку хлорируется раствор, а не взвесь, как при
166
известковом молоке. Хлорирова-
ние «слабого каустика» (электро- =
литического щелока) проходит £
в общем так же, как и хлори- 2
рованис растворов, содержащих о
только NaO.H, с тем отличием,
что при хлорировании слабого о.
каустика выделяется меньше Ог £
от побочных процессов, что и
объясняется влиянием содер- *
жания NaCl (см. стр. 64). 2* '
В табл. 47 приведены данные
лабораторных опытов хлориро- Z
вания растворов NaOH разной
концентрации при разных тем- о ^
пературах. Содержание ^аС1 и JJ'S'
NasCO.1 в растворах, поступаю-
щих на хлорирование, было не <="?
больше 0,5—1% от количества 3g
NaO,H, При хлорировании щелок
охлаждался и поддерживалась «о
примерноначальная температура, *2?
так что разница температуры, 2.*
приведенная в таблице, в основ- >,*
ном относится к подъему темпе- 2 I
ратуры при перехлорировании.
Опыт 15, проведенный с раство- е £■
ром NaOH 500 r/j с начальной а ^
температурой 60°, не удалось- " °
закончить ввиду сильного вспе- s .
нивания и выброса жидкости во я £
время перехлорирования. При х о.
опытах 7—14 во время хлориро*.. 2 а
вания выделился осадок кри- о.*-
сталлов NaCl. Выход хлората % 2
рассчитан по отношению к тео- <° ®*
ретически возможному количе-; *
ству согласно' затраченному ко- °
личеству NaOH, как описано на *
стр. 90. 2
, Из данных табл. 47 видно, *
что оптимальный выход хлора- *
та в 98,3—98,6% получается при 4
концентрации NaOH 200—300 г/л ю '
и температуре конца хлориро- ^
вания. в 62—-68° (опыты 5 и 8). „
Большая концентрация NaOH 5f
и более высокая температура <§
конца хлорирования снижают £
выход хлората/ При одинаковой
го
СП
X
со
со
I
о
сч
»о
со
СП
о
О)
ос
а*
ОО
СП
о
со
со
о
я
X
ОО
с-/
о>
JL
$
ю
8
со
90
со
СО~
о>
S
сч
СО
СО
ОО
СП
ОО
О)
8
СЧ
04
а>
о
ю
I
я
ОО
о
о>
8
О
(М
сч
о£
о
ч
a
S3
Et .
о
и
3 со
со н
<2
* «
s§
о.и
U
3
а
о
%
167
концентрации NaOII слишком низкая и слишком нысокля пм-
нература снижают выход хлората (опыты 1 и .4, II и 12, 18 и I I).
Однако влияние температуры тем меньше, чем выше копнет рация NaOH (оньгг 1 и 4, 2 и 5, 2 и 10). При концентрации NaOII
в 100 г/л выход хлората ниже, чем при более высокой концентрации при примерно одинаковой температуре. Последнее объясняется влиянием хлорида, образующегося при хлорировании
(см. стр. 64). При хлорировании слабого -каустика, содержащего NaOH 100—120 г/л и NaCl 170—190 г/л при температуре
конца хлорирования в 60—80°, выход хлората равен 96—98%.
При этом понижение температуры не имело такого влияния, как
например при опыте табл. 47, что объясняется наличием хлорида.
В табл. 48 приведены данные увеличения объема при хлорировании растворов NaOH или слабого каустика, в зависимости
от концентрации NaOH. Опыты были проведены хлором из баллона (СЬ 99,7%) в сосуде с обратным холодильником для конденсирования паров воды. / (
Таблица 48. Увеличейие объема при хлорировании
растворов NaOH или слабого каустика
Содержание NaOH
в г! л
70
80
90
100
/
по
120
130
140
150
200
250
% увеличения
объема ....
5,8
6,6
7.4
8,1
8,9
9,6
. /
10,3
11,0
11,6
14,9
18,1
В заводских условиях хлорирования увеличение объема
обычно меньше, поскольку применяют хлоргаз с меньшим содержанием СЬ и абгаз уносит значительное количество паров НгО.
По Нашим наблюдениям при концентрации NaOH 90—ПО г/л и
концентрации СЬ в хлоргазе в 70—80% практическое увеличение
объема было в среднем 6—7%. При продувке щелока воздухом
для уменьшения содержания СЮ' объем щелока обычно уменьшается на 1—3%. Изменение объейа при хлорировании рассчитывается по изменению суммарной молярной концентрации
твердых веществ в щелоке, так как при постоянстве объема
молярная концентрация при процессах хлорирования остается
неизменной. Расчет правилен конечно только при отсутствии
выделения NaCl во время хлорирования и неизменении объема
проб щелока от времени отбора проб до их анализа.
Примечание. Принимая, что на хлорирование поступает сухой
хлоргаз, а отходящий абгаз имеет температуру 50° и степень насыщения
влагой в 80%, на 1 кг прореагировавшего хлора испарится А г воды:
- \ * % С1а в хлоргазе .... 90 70 50 30 10
'А ... . % . 2 9 20"-48 184
На 1 кг прореагировавшего NaOH испарится А • 0,8865 г воды.
' I
164,
/
§ 8. Некоторые данные по изучению хлорировании растворов
NaaCOn
В табл. 49 приведены данные хлорирования раствора NasCOs-
200 г/л. -До хлорирования раствор был подогрет до 53', так как
по другим нашим опытам температура в 50—60° является оптимальной для хлорирования раствора NaaCOa. Хлоргаз поступал
из баллона (СЬ = 99,7%) через барботср, опущенный вниз сосуда с раствором ИагСОз. Абгаз из сосуда для хлорирования
отводился во второй сосуд с раствором NaOH для улавливания
СЬ и СОг из абгаза. Через равные промежутки времени из
обоих сосудов отбирались пробы щелоков, по анализам которых узнавали- состав хлорируемого щелока и проскок хлора
в абгаз.
Таблица 49. 'Ход хлорирования раствора, содержащего
Ыа2СОв 200 г/л
проб
Темпера*
Состав щелока
в экв/л
Всего хлора в *кп/д
щелока
тура
•С
СО.”
\
НСО,'
СЮ'
сг
СЮ.'
f
поглощено
проскочило
1
53,0
3,77
0,01
V
2
53,6
2,60
0,59
0,56
0,29
—
0,56
—
3
54,3
1,58
1,07
1,11
0,57
—
1,12
4
55,7
0,44
1,58
1,70
0,87
—
1,71
—
5
56,9
нет
1.42
1,89
1,28
0,37
2,28
—
6
58,2
•
0,84
1,32
1,48
1,48
2,83
нет
7
59,9
г*
, 0.35
0,70
2,53
2,58
3,30
а 0,02
W 0,41
4 8
61,0
т
нет
0,49
2,61
2,96
3,55
9
60,7
»
1»
0,41
2,85
*
3,04
3,53
1
0,96
Из данных табл. 49 видно, что NaHCOs начинает образовываться сразу после начала хлорирования; максимум NaHCO»
содержится в пробах 4 и 5, где ЙагСОз уже мало или совсем
нет; дальнейшее хлорирование приводит к уменьшению количества NaHCC>3 до полного его исчезновения. Содержание
NaCIO сначала увеличивается соответственно увеличению
NaHCOs; после прореагирования всего NasCOs содержание
NaCIO начинает уменьшаться и по окончании хлорирования
остается в пределах, соответствующих температуре конца хлорирования (стр. 94). Иа'СЮз ^образуется, начиная с Жомента
прореагирования всего NasCOe. -Подъем температуры равен
всего 8°. Проскок хлора в абгаз начинается только после про-
реагирований всего №гСОз и почти всего NaHCOs.
В табл. 50 приведены данные хлорирования растворов Na»COs
разной концентрации. Температура хлорирования для всех пяти
опытов была 60—70°. При опыте 3 во время хлорирования выделился небольшой осадок (NaHCOs), который к концу хлорирования перешел‘обратно в раствор. При опытах 4 и 5 выделение-осадка было больше, а при попытках хлорировать- раствор
189
Na«COj 400 r/л выделилось столько осадка (NallOb и nni . .. ■ i),
что образовывалась трудно перемешиваемая масса, которую не
удавалось дохлорпронать. К концу хлорирования аамсчалось
сильное нспенивание из-за выделения СО», и тем большее, чем
выше была концентрация хлорируемого раствора NaaCO». Хлорирование производилось в сосуде с обратным холодильником
для конденсации испаряющейся воды. Увеличение объема рассчитано по изменению молярности щелока до и после хлорирования. Выход хлората рассчитан, как указало на стр. 90.
Таблица 50. Состав щелоков, выход хлората и увеличение
объема при хлорировании растворов Na2CO,' р а з и о й
концентрации
Содержание
Na,CO, в г/л
содового раствора
Состав хлорированного щелока в экв/д
Процент
выхода хлората
Процент
увеличения
объема
NaCIO.
NaCl
Общий хлор
20
0,22
0,33
0,37
59
0,5
50
0,81
0,83
0,97
84
1.2
100
1,67
1,59
1,87
89,3
2,7
200
3,47
2,99
3,57
97,2 '
6,0
300
5,03
4,37
5,21
96,7
9,2
Из данных таблицы видно, что оптимальный выход хлората
получается при концентрации NaaCOs в 200 г/л. При более низкой концентрации №гСОз выход хлората тем меньше, чем ниже
содержание №гСОз и при NaeCOa 20 г/л выход всего равен 59 л.
Это явление объясняется влиянием концентрации хлорида, образующегося при хлорировании, на Переход гипохлорита в хлорат
и хлорид с наименьшим выделением Ог (стр. 64). Хлорируя
раствор, содержащий NaCl, мы неизменно получали выход хлората в 95—97% вне зависимости от концентрации NaaCOj.
Отдельные опыты, поставленные для изучения влияния температуры хлорирования раствора NaCOs 200 г/л на выход хлората, показали, что лучшие выхода получаются в пределах
температуры в 40—80°, несколько меньше выход при 20—30°
(93—95%) и значительно уменьшается выход при хлорировании
при 90—100° (88—9?%). Оптимальной температурой является
предел в 60—70°, так как при этом не только получается лучший выход хлората, но и больше растворимость NaH(X>3 (чем
при более низкой температуре), что уменьшает выделение его
в осадок при хлорировании и облегчает технику хлорирования.
Вместе с тем более высокая температура уменьшает содержание
СЮ' в щелоке, что облегчает обезвреживание щелока и уменьшает потери от восстановления СЮ' в СГ при обезвреживании.
Также были поставлены опыты по изучению влияния
продолжительности хлорирования раствора Na*GOs 200 r/л на
^выход хлората. , Изменение продолжительности хлорирования
достигалось регулированием величины струи хлоргаза (из бал-
170
лона). Хлорироиапие производилось при ч им игра type Ь)ч ,
чтобы легче было определить влияние продолжительности хлорирования, так как чем выше температура, гем больше выделение Оа. Были проведены три опыта продолжительностью в 26,
45 и 162 мин. Выход хлората при всех трех опытах был примерно одинаков ~ 90%.
Проведенные опыты хлорирования раствора ИагСОп 200 г/я
электролитическим хлоргазом в заводских условиях (по 3 л*
раствора) не дали заметных отклонений от результатов выше
приведенных лабораторных опытов.
§ 9. Количественные изменения при хлорировании растворов
N&OH и Na2COa; состав и некоторые свойства щелоков
\
Вес. При хлорировании раствора NaOH на 1 г NaOH поглощается 0,887 г хлора. При хлорировании раствора ЫагСОз на
1 г Na*COj поглощается 0,67 г хлора и выделяется 0,415 г COs
т. е. вес должен увеличиться на 0,67 — 0,415 = 0,255 г.
Объем. При хлорировании растворов NaOH объем увеличивается (значительнее, чем при хлорировании известкового молока). При хлорировании растворов ЫагСОз объем увеличивается, но меньше (из-за выделения СО*), чем при растворах
NaOH.
Плотность. Щелока от хлорирования растворов NaOH и
NajCOj имеют меньший удельный вес, чем растворы до хлорирования, (обратно тому, что имеет место при хлорировании известкового молока, когда плотность сильно возрастает). Однако
171
Состаё и уВ. Все
ЛлорироВамнЫх щслоАоВ
AbCtOj
г/л
20 --
ЫаСЬ-
'/* V
УД
Вес
105
НаОН
•f*
HdC0j\
*/' I
со 1
| ИаЛСО}
*/*
— 60
\р%
• 50
i
;—«во
1 _
—70
107
—60
СО—
- .i
г
30 —
1 -и
—90
IJD8
— 70
go-;
«00 !
1—«•
«00
1W
—60
««0 —
44» —^
— НО
%
«ДО
—90
«20—
-
—«20
ЮО
«30—
—-ш
I
— «30
«А
— НО
МО—
1»
—«40
1»
—«20
460—
гч»
—260
—*00
1*4
—130
170—
60—=
...ML
—а&-
ICO—
.
—1ЕО
м*
—«о
160—
-200
—300
70 —I
—«90
~*°° «А.
220—
360
—2«0
V*
—по
230—
00 —^
—220
—«60
240—
. —г
—230
«л
—«00
400
ал “
— 240
1Л2
—^*200
260—
» —
:—250
Vм
—*2«0
270
_
- 260
^ 124
—220
2р0
460
«оо —
— 270
_Jb2L
600
Концентрация
исходных растВороВ
г Рис. 77. Зависимость состава и уд. весаГ
1Целоков, получающихся при хлорировании растворов NaOH, и Na2COa и
NaHCOa от концентрации последних.
р:пшщ;| уд. iu*im до и п.,' i1
хлорп|)< шпиня гораздо мгиь-
пю, чем при хлорнрошпши
известкового молока (ер.
рис. 25, сгр. 68).
Примечание. В производственных условиях изменения веса
и объема при хлорировании зависят
также от концентрации СЬ в хлор--
газе и температуры хлорирования,
так как чем ниже процент С1г и
чем выше температура, тем большее количество влаги уносится аб-
тазом.
В табл. 51 приведены расчетные коэфициенты реакций хлорирования растворов
NaOH и NazCOs.
Щелока, полученные после хлорирования растворов
NaOH, ИагСОя или NaHCOs,
одинаковы по составу, являясь
в основном раствором NaCIO*
и NaCl. Если исходные растворы содержали примеси
Na2S04, NaCl и т. .п., то они
переходят без изменения
в хлорированные щелока. До
обезвреживания щелока содержат также NaCIO и растворенный хлор в количествах
тем больших, чем ниже была
температура конца хлорирования. Цвет щелоков, полученных хлорированием в производственных условиях,, слабо розовый от образовавшегося Na2FeOs (см. стр. 66).
Недохлорированные щелока,
содержащие NaO.H, обычно
зеленоваты от наличия
Na2Fe04. При обезвреживании
эти соединения железа разрушаются, образуя Fe(OH)j.
На рис. 76 приведена растворимость NaHCOs в растворах NaCl при 15, 30 и 45°.
На рис. 77^приведено содержание NaCIO* и NaCl и
плотность для щелоков
от хлорирования растворов
172
Таблица 51. Коэфициенты реакций при каустическом и содовом методах производства
ч ^
• бертолетовой соли
; /
•
' * 0
V
4
Расходуется г
X
Образуется г
J
7
к -
NaOH
Na,CO,
-
КС1
Как промежуточный продукт
После хлорирования
После обменной
реакции
•
0
Хлор
NaCIO
NaHCO,
NaCIO,
. NaCl
н,о
СО,
КСЮ,
NaCl
Расчет на 1 г NaOH
1
.
0,8865
03106
0,93
0,444
1,218
0,225
0,511
1,461
Расчет на 1 г NajC03
—
1
0,669
0,234
0,351
0,792
0,335
0,919
—
0.415
0,с85
1,103
Расчет на
0
при каустическом
методе ....
1,958
1,736
0,608
0,869
2,385
0.41
1
2,859
1 г КС103
при содовом методе'
—
2,595
1,736
0,608
-Г"
0.869
2,385
—
1,075
1
2,859
*
-j
т>—
4 ✓
Примечание. Расчеты сделаны по гоэфициеитам следующих уравнений:
2NaOH.+ CIa = NaCIO + NaCl + Н,0;
6NaOH + ЗС1, = NaC103 + 5Nad + ЗИЛ);
6NaOH + ЗСЬ + КС! = КС103 + 6NaCl + ЗН.,0;
6NaaC03 + ЗС1а + ЗН30 = 6NaHCOa+ 3NaCIO + 3NaCl;
3NaX03 + ЗСЬ = NaC103 + 5NaCl + 3C02. »
3Na3C03+ ЗС13 + KC1 = KC103 + 6NaCI -f 3COa
NaOH или N.'i-.CO;, разной концентрации (без учета испарения
воды, выделения кислорода и увеличения объема при хлорировании, поскольку практически обычно эти величины невелики
и не вносят больших отклонений в приведенные данные).
§ 10. Некоторые данные по хлоратным щелокам
Щелока, поступающие на выпарку при каустическом и содовом методах, отличаются между собой только по концентрации
NaClOs, которая при содовом методе несколько выше, чем при
каустическом (см. табл. 55—56, стр. 179). При обоих методах
щелока, поступающие на выпарку, содержат кроме NaClCb и
Таблица 52. Состав и количества уваре иных-и бертолетовых
щелоков и количество КС10Я, выделяющееся при кристаллизации, при каустическом и содовом методах производства
Уваренные щелока 1
Бертолетовые щелока 1
Выделится КСЮ, при
кристаллизации »
Хлорат в г/д
(сумма КСЮ,
и NaClO, в
пересчете на
КСЮ,)
Объем в
м■ (из расчета на
1 т КСЮ,
Температура
начала кристаллизации
, КСЮ, .
Объем в м9
(из расчета
на 1 m
КСЮ,) .
КСЮ,
г/л
Г
кг из 1 мя
уваренных
щелоков
п1оп'п по отношению к- к-ву
КСЮ, в
бертолетовых
щелоках
Ч
150
6,67
15° с
7,89
128
62
49
160
6,25
—
7,47-
134
68 ’•
51
170
5,88
20°
7,10
^ 141
75
53
• 180
5,56
—
6,78
148
82
55
190
. 5,26
25°
6,48
154
88
57
• 200
5,00
—
6,22 ,
161
94
58
210
4,76
30°
5,98
167
101 ,
60
220
4,55 '
—
5,77
173
. 107
62
230
' 4,35
35°
5,57
180
114
63
240
4,17
• —
5,39
186
120
65 .
250
4,00
40°
5,22
192
126
66
260
3,85
• —
5,07
197
131
67
270
1 3,70
45°
4,92
203 ^
.137
68
280
3,57
—
, 4,79
209
143
68
1 Состав .и объем щелоков дан при 80°.
2 Исходим из охлаждения до 10° без учета уменьшения объема щелока
при кристаллизации.
NaCl еще часть КСЮз, поскольку выпаривается смесь хлорированных и маточных щелоков.
На рис. 78 приведена взаимная зависимость содержания хлората в уваренных щелоках1 при 70° и удельного веса этих щелоков при условии отсутствия в них значительных .количеств
174 * ■*
примесей (NasSOi, NaOIl н т. д.) и отношении содержащихся
NaClOa и КСЮз как 2 : 1 (щелока насыщены NaCl).
В табл. 52 приведена зависимость объема уваренных и бертолетовых щелоков, температуры начала кристаллизации КСЮа
и количества КСЮа, выделяющегося при кристаллизации, — от
концентрации уваренных щелоков. Данные выведены на 1 т хлората (в пересчете на КСЮа) в уваренных щелоках, содержащих
NaClOa и КСЮз в соотношении 2:1, и не
содержащих большого количества примесей Уу.1 хпаратф
NaaSQi и NaOH. Объем бертолетовых щелоков рассчитан как сумма объема уваренных щелоков и 1,22 л* раствора КС1, необходимого для получения 0,67 г КСЮа из
NaClOa. Количество КСЮз, получаемого при
кристаллизации, рассчитано, исходя из
остатка в маточных щелоках при 10° КСЮз
66 г/л (см. рис. 79).
1.S3
— 300
§11. Некоторые данные по изучению
кристаллизации КСЮз
£
!
-гм
ио-
I
«в
I
<3
' 5
*
А
ч
«I
£
*
I
5
ч»
Ь 200 §
*
а
*
0
1
При правильно проведенной обменной
реакции в получаемых 'бертолетовых щелоках должны содержаться только КСЮз
и NaCl. До обменной реакции в уваренных
щелоках содержится кроме NaClOa и NaCl
еще КСЮз. При варианте каустического
метода без выпарки (стр. 161) бертолетовые
и маточные щелока содержат кроме КСЮз
и NaCl еще КС1. Поэтому является интересным изучение кристаллизации КСЮз из
растворов, содержащих: 1) КСЮз и NaCl,
2) КСЮз, NaClOa и NaCl и 3) КСЮз,
NaCl и КС1. <
На рис. 79 приведена растворимость
КСЮз и NaCl при их совместном ‘присутствии, растворимость КСЮз в насыщенном
растворе NaCl в присутствии NaClOa 150 г/л
и растворимость КСЮз и NaCl в чистой воде
(последние данные приведены для сравнения) при температуре от 0 .до 100°. Из приведенных кривых видно, что растворимость
КСЮз в растворах NaCl при температуре
выше 40° ниже, чем в чистой воде, а при температуре нйже 40°
выше, чем в чистой воде. Растворимость NaCl в насыщенных
растворах КСЮз- тем ниже, чем выше температура. Однако
в общем обоюдное влияние NaCl и КСЮз незначительно.
В табл. 53 приведена растворимость КСЮз в насыщенных
растворах NaCl в присутствии КС1 до 100 г/л при разной тем-
175
12S-
I- 40
Рис. 78. Содержание
хлората в уваренных щелоках разного
удельного веса при
70э при каустическом и содовом методах производства
бертолетовой соли.
псратурс. В табл. 54 приведен состав раствора насыщенного
КС1, КСЮз и NaCl при 0—80°.
Таблица 53. Р а с т в о р и м о с т I. КСЮЯ в и а с ы щ е м и ы х раствор а х
NaCl, содержат их КС1 до 100 г/л при разной температуре
г/л
0
10
20
30
40
60
75
100
Гемперат. *с''\
ч КС103 г/л
16
78 -
61
54
48
43
39
36
27
10-
66
50
45
39
33
30
27
—
0
48
41
36
30
25
22
* 19
. —
—10 -
36
30
24
18,5
14
12
—
—
—20 .
26,
20
14
11
у
8
6,5
—
—
ч Таблица 54. Состав растворов, насыщенных
по КСЮЯ, КС1 и NaCl при 0—80°
Твмпер«тур« *С
КСЮ, г!а
КС1 г}а
NiCl г/А
80
160
176
226
60
161
154
234
40
61
124
250
20
' 29
105
263 *
х 0'
20
90
270
На рис. 80 приведена кривая растворимости КСЮз и КС1
в насыщенном растворе NaCl при 16°. По этой кривой можно
определить содержание КС1, сделав анализ на СЮ'з без определения калия. Это имеет большое значение в производственных
условиях, так как определение калия продолжается минимум
несколько часов, а определение" CIO's продолжается всего
8—10 мин. (
Пользуясь диаграммой рис. 79, можно определить приблизительное содержание КСЮз и ЫаСЮз в горячем уваренном щелоке только по анализу на СЮ'з без определения калия. Пример:
в уваренном щелоке при 60° найдено СЮ'з 13,7 экв/л, а после
охлаждения щелока до 10° и отделения выпавших кристаллов
найдено СЮ'з 11,25 экв/л. По рис. 79 видно, что в уваренном
щелоке, насыщенном по NaCl и содержащем TJaClOs 100—200 г/л,
средняя растворимость КСЮз при 10° равна 1,37 экв/л. Поскольку в щелоке, охлажденном до 10°, мы нашли концентрацию
СЮ'з равной 11,25 экц/л, разница 11,25—1,37 = 9,88 экв/л будет
NaClOe. Содержание КСЮз в горячем щелоке (при 60°) будет
13,7 — 9,88 = 3,82 экв/л. Рассчитанные количества являются примерными, поскольку мы не учитываем изменения объема щелока
и концентрации в нем NaClOs, вызываемого охлаждением щелока.
176
Если при охлаждении щелока не выпало кристаллов, к- содержание КСЮз в нем меньше 1,37 экв/л или КСЮз совершенно
отсутствует.
Примечание. Если найденное в охлажденном щелоке количество
CIOs' меньше, чем должно быть по кривой рис. 79, то в щелоке нет NaCICh,
весь хлорат содержится в виде КСЮз и в щелоке еще содержится КС1,
концентрация которого рассчитывается, как указано выше (рис. 80).
/
/
/
■— Aioпборимостб при совместном присутствии
- Растворимость ё чистой боде
bumiopuMocmtKUbipecmtopeMaClcoSepMauteM
NaciOj НО г/л.
Исходя из рис. 79,
можно также определить
содержание №СЮз или КС1
в маточном щелоке после
^кристаллизации КСЮз, по
анализу на ClO'j без определения калия. Именно,
если СЮ'з найдено больше,
чем соответствует данной
температуре по кривой
рис. 79, то разница показывает содержание NaClO.-,
в щелоке. Например если
в маточном щелоке най-
Рис. 80. Расчет содержания КС1
Рис. 79. Растворимость КСЮд и NaCl при в растворах, насыщенных NaCl
температуре от —20 до 90°. и КСЮ, при 16° по количеству
С103, найденному анализом.
дено СЮ'з 5,0 экв/л, а по кривой рис. 79 должно быть 3,5 экв/л,
то содержание NaC10s = 5— 3,5= 1,5 экв/л. Если по анализу
определено меньше СЮ'з, чем соответствует данной температуре
по кривой рис. 79, то в щелоке содержится кроме КСЮз и NaCl
еще КС1, концентрация которого рассчитывается, как указано
выше (рис. 80).
» 4 '
12 Зш. 179. — Шрайбкак.
177
§ 12. Основные коэфициенты получения бертолетовой соли
каустическим и содовым методами
Табл. 55 составлена соответственно схеме, показанной на
рис. 72 (стр. 157). Количества NaCl, NaOH и NaClOs в рассоле,,
слабом каустике и хлорированном щелоке рассчитаны согласно
уравнениям (69) и (74) (стр. 163) с учетом 50% разложения NaCl
при электролизе. Принимаем увеличение объема при хлорировании в 9,5% (стр. 168) и уменьшение объема при кристаллизации в 10%. Объем щелока, поступающего на выпарку, и количества NaCl, NaClOj и КСЮз в нем (п. 4)
рассчитаны как сумма этих данных в хлорированном и маточном щелоках (пп. 3 и 8). Концентрация НаС1 в уваренном
щелоке- (.п. 5) и КСЮз в маточном щелоке (п. 8) взяты
соответственно их растворимости в данных условиях (стр. 177).
Объем бертолетового щелока и количества NaCl и КСЮз в нем
рассчитаны из данных для уваренного щелока и раствора КС1.
Данные для перекристаллизации бертолетовой соли те же, что
в табл, 39 .(стр. 147).
Табл. 56 составлена соответственно схеме, показанной на
рис. 73 (стр. 160). Количества №гСОз, NaClOs и NaCl в содовом
растворе и в хлорированном щелоке рассчитаны согласно уравнениям (80) и (81). Принимаем увеличение объема при хлорировании в 6% (стр. 170). Данные для щелока, поступающего на
выпарку (п. 3), рассчитаны, исходя из данных хлорированного
и маточного щелоков (пп. 2 и 7). Данные пп. 6—7 те же, что
в табл. 55.
Практический объем щелоков и количества NaCl, NaOH,
ШгСОз и КСЮз в производственных растворах при каустическом и содовом методах рассчитываются, исходя из приведенных в табл. 55 и 56 данных и баланса потерь. На одном из хло-
ратных заводов, работавшем по каустическому методу в течение нескольких лет, потери по хлорату (т. е. и по хлору и по
NaOH) составляли 10—12%, что соответствует расходу 1,95—
2,0 т хлора и 2,2—2,3 г NaOH на 1 т КСЮз; расход КС1 был
0,65—0,67 т на 1 г КСЮз.
Практический состав и плотность производственных растворов не зависят от потерь, а только от налаженности режима
работы производства.
По вопросам каустического и содового методов производства хлоратов
см. статьи автора в журналах:
1. Ж. X. П. 1934 г., № 6, стр. 49—68; 2. Химстрой 1933 г., № 5,
стр. 2239—2246; 3. Военная химия 1932 г., № 5—6, стр. 10—14.
См. также стр. 195.
12*
Таблица 55. Состав и количества1 производственных растворов для получения КСЮ3
по каустическому методу
с
Б
X
Какие растворы
Объем 1
в л»
Состав в г}л
Всего тонн 1
Плотность
NaCI
NaOH
NaCIO,
КС1
ксю,
NaCI
NaOH
NaCIO.
KCI
ксю,
Уд. вес
°Боме
Температура вС
1
Рассол .
18,45
310
5,72
1,18
22
60
ъ
Слабый каустик . . .
16,6
172
118
—
—
—
2,86
1,96
—
—
—
1,20
21
60
3
Хлорированный щелок
18,18
289
—
48
—
—
5,25
—
0,87
—
—
1,19
23
70
4
Щелок, поступающий
на выпарку ...»
24,26
285
—
36
—
16
6,93
—
0,87
—
0,40
1.22
26
40
5
Уваренный щелок . •
5,01
240
—
174
—
80
1,20
—
0,87
—
0,40
1,34
36,6
60
.6
Раствор КС1
1.74
—
—
—Г
_35Э
—
—
—
—
0,61
—
1*17
21
80
7
Бертолетовый щелок .
6,75
249
—
—
—
208
1,68
—
—
—
1,40
1,26
29,8
60
8
Маточный щелок . .
6,08
276
—
—
—
66
1,68
—
—
—
0,40
1,28
31,5
10
г*
Таблица $6. Состав и количества1 производственных растворов для получения КС108
по содовому методу
Б
Б
X
Какие растворы
Объем 1
в мш
Состав в г[л
Всего тонн 1
Плотность
Na.CO,
NaCIO,
NaCI
KCI
КСЮ,
Na,CO,
NaCIO,
NaCI
KCI
ксю,
Уд. вес
® Боме
Температура °С
1
Содовый раствор . .
13
200
2,6
1.18
22
20
2
Хлорированный щелок
13,78
—
63
174
—
—
—
0,87
2,39
—
—
1,14
17,6
60
3
Щелок, поступающий
на выпарку ....
19,86
—
44
205
—
20
—
0.87
4,07
—
0,40
1,16
19,9
40
4
Уваренный щелок . .
5,01
:
174
240
—
80
—
0,87
1,20
—
0,40
1,34
36,6
60
5
Раствор КС1
1,74
—
—
—
350
—
. —
—
—
0,61
—
1,17
21
80
6
Бертолетовый щелок
6,75
—
—
219
—
208
—
—
1,68
—
1,40
1,26
29,8
60
7
Маточный щелок . .
6,08
—
—
276
—
66
1,68
0,40
1,28
31,5
10
3 1 Объем и количества тонн рассчитаны на получение 1 т КСЮ3 при кристаллизации.
ГЛАВА 14
ПОЛУЧЕНИЕ БЕРТОЛЕТОВОЙ СОЛИ ХЛОРИРОВАНИЕМ MgO,
ZnO и KsCOa. ХЛОРИРОВАНИЕ СаСОз
§ 1. Применение окиси магния для получения бертолетовой соли
Этот метод разработан Муспратом и Эшельманом (герм. пат.
26698, 27729, 27730 1883 г.) и Вельдоном (англ. пат. 2389 1871,
1898—1883 гг.). Много улучшений внес в этот метод Печиней.
В основном схема этого метода идентична схеме известкового
метода по варианту Либиха или по варианту Печинся (стр. 34),
только вместо известкового молока хлорируют магнезиальное
молоко, содержащее взвесь Mg(OH)2.
MgO получается обжигом магнезита. Температура обжига
магнезита на 150—200° ниже, чем известняка (стр. 37). При
слишком высокой температуре обжига получается MgO
в виде «.перепала», трудно поддающегося гашению и
хлорированию. Примесь MgCk увеличивает активность MgO
к гашению. Хлорирование взвеси Mg(OH)2 протекает аналогично
хлорированию CaCOs (см. ниже стр. 184); это объясняется тем,
что ввиду плохой растворимости Mg(OH)2 в хлорируемом щелоке
все время хлорирования имеется слабокислая среда от избытка
растворенного хлора. Хлорат образуется постепенно в течение
всего времени хлорирования. Выход хлората при равных условиях выше, чем при хлорировании Са(ОН)2, и на хлорирование
не так сильно сказывается влияние температуры. Содержание
гипохлорита зависит от температуры хлорирования и может
дойти до 1—1,5 экв/л. Однако при хранении такого щелока гипохлорит разлагается с образованием хлората и хлорида, так что
устойчивых белильных растворов нельзя получить хлорированием магнезиального молока. Тепловой эффект реакции хлорирования Mg(OH)2 несколько ниже, чем Са(ОН)2. При низкой температуре хлорирования магнезиального молока часто получаются
осадки оксихлоридов (MgO + MgCl2 + НгО). Суммарное уравнение реакции хлорирования Mg(OH)2 будет:
6Mg(OH)2 + 6С12 = Mg(C103)2 + 5MgCl2 + 6Н20. (82)
При выпарке хлорированного щелока Юриш1 рекомендует
добавлять небольшое количество MgO, что уменьшает коррозию
выпарных аппаратов. Выпарку щелока, содержащего Mg(C103)2
и MgCl2, производят до удельного веса 1,25—1,28, после чего
' к щелоку прибавляют КС1 для обменной реакции и полученный
бертолетовый щелок охлаждают для выделения КСЮз. При
большей концентрации увариваемого щелока при охлаждении
могут выделиться кристаллы MgCl2 • 6НгО (47% MgCl2). Обменную реакцию надо производить без избытка КС1, так как
последний может при кристаллизации образовать карналлит
(КС1 • MgCl2 • 6Н20), загрязняющий получаемую бертолетову соль.
В маточном щелоке остается меньше КСЮз, чем при соответ-
180
ствующем щслокс с Cad», так как влияние MgCI2 па растворимость КСЮя больше, чем СаС1» (при 10—20’ в маточнике
остается КСЮя 10—15 г/л, см. табл. 35, стр. 130). При варианте
Печинея упаривают щелок, содержащий MgCl2 и Mg(C10a)2, до
уд. веса 1,38 (39,7° Боме), после чего охлаждают до 10°; при
этом выделяется 50—60% хлорида. При большей концентрации
уваренный щелок по охлаждении целиком затвердевает.
Маточный щелок, получающийся после кристаллизации
КСЮя, может быть использован для получения плавленого хлористого магния (содержание MgCb равно 46—48%), для чего
упаривают его до температуры кипения ~ 150°. Предварительно
можно использовать хлорат маточного щелока для получения
хлора из соляной кислоты (стр. 14Г)). Упариваемый щелок очень
сильно корродирует железо, частично образуя Fed». Для очистки от последнего Юриш1 рекомендует по окончании уварки
прибавить KNOfl и продувать горячий плав воздухом, после чего
прибавить MgO, отчего образуется Ре(ОН)я. При отстое горячего плава (Оседают ;Бе(ОН)я, избыток MgO и другие нерастворимые примеси. Осветленный плав сливают в барабаны.
Вельдон разработал способ регенерации Mg(OH)2 из MgCk,
содержащегося в маточном щелоке, с одновременным получением серы из остатков производства соды по Леблану (англ,
пат. 98, 99, 100 1883 г.). Схематически реакции этогб процесса
происходят по следующим уравнениям:
2CaS + 2НЮ = Са(ОН)2 + Ca(SH)*. (83)
Ca(SH)2 + MgCl2 +' 2НЮ = Mg(OH)2 + GaCl» + 2H2S. (84)
Полученный H2S утилизируется для получения серы.
Из MgCk маточного щелока можно также получить MgO и
хлор, что было разработано Вельдоном и Печинеем. Для этого
маточный щелок упаривают до концентрации MgCU в 50%.
К горячему плаву прибавляют MgO (в эквивалентном количестве), перемешивают и дают остыть. Остывшую массу — ЗГокси-
хлорид» — измельчают и высушивают горячим воздухом при
150—200°, чем удаляют до 60% влаги, содержащейся в оксихлориде. Высушенный оксихлорид прокаливают при 900—1000°
при пропускании над прокаливаемым продуктом воздуха. При
прокаливании большая часть MgCl2, реагируя с кислородом воздуха, разлагается, образуя MgO и хлор:
MgCl2 + О = MgO + С12. (85)
Поскольку в прокаливаемом продукте все же содержится влага,
частично образуется также НС1. Хлор и HQ уносятся в виде
весьма разбавленного газа воздухом, пропускаемым над прокаливаемым продуктом. По Юришу1 при этом процессе удается
утилизировать до 78% хлора, содержавшегося в маточном щелоке ' в виде MgCl2 (Юриш1 приводит также описание аппаратуры для разложения оксихлорида). .
181
Литература по магнезиальному мешоОу
Ю р и ш 1; Л унте2; Г мел и u Jber. chcm. Tcchn. 1884 г., стр. 352;
J. Soc. Chcm. Ind. 1887 г., стр. 248—319 и 782; Морозов53.
§ 2. Применение окиси цинка для получения бертолетовой соли
Метод получения КСЮз хлорированием взвеси окиси
цинка в воде разработан Байером (герм. пат. 81804 1894 г.;
англ. пат. 17978 1894 г.). Выгода этого метода заклю¬
чается в получении в виде отхода ценного ZnCh. Схема этого
метода в общем идентична схеме известкового метода. На хлорирование поступает взвесь ZnO в воде или лучше в растворе
КС1 (0,33 моля КС1 на 1 моль ZnO). По Байеру хлорирование
ведут при температуре в 100°. Выделение кислорода при хлорировании весьма незначительно и выход хлората при хлорировании равен 99—99,5%. Процесс хлорирования проходит аналогично хлорированию MgO: образование хлората происходит
в течение всего времени хлорирования, возможно образование
оксихлоридов и т. д. При выпарке хлорированного щелока целесообразно добавить небольшое количество ZnO. Растворимость
КСЮз в маточном щелоке после кристаллизации примерно равна
растворимости в воде (как и в растворах NaCl и ВаСЬ). Маточный щелок, полученный после кристаллизации КСЮз, упаривают
до удельного веса ~2 и охлаждают, отчего получается твердый
продукт, представляющий собой в основном ZnCU • 6Н2О.
Уравнение получения KQlOs по этому методу будет:
3ZnO + 3CU + КС1 = КСЮз +: 3ZnCl2. (86)
t Литература по методу Байера
Лунге8; Гмелнн4-88; J. Soc. Chem. Ind. 14 (1895) 658 и (1903) 296;
Jber. chem. Techn. (1895) 447; Ch. Zeit. (1904) 763; Zeit. ang. Ch. 21 (1908) 137.
§ 3. Применение поташа для получения бертолетовой соли -
Хлорирование КгСОз для получения бертолетовой соли в лабораторных опытах применялось еще Граамом (1841 г.). В промышленном масштабе этот метод не нашел применения, поскольку КгСОз дороже СаО. Однако в,начале развития произ-
, водства бертолетовой соли в СССР метод с применением КгСОз
имел ряд сторонников, поскольку до начала разработки Соликамских калийных залежей цоташ был наиболее доступной калийной солью в наших условиях, а КС1, который получился бы
как отход при этом Методе, являлся бы более ценным продуктом, чем расходуемый поташ. Поэтому в 1927—1930 гг. производили обменную реакцию Са(СЮз)г, п.олучаемого хлорированием
известкового молока с КгСОз, а не с КС1, а. проф. Шпитальский
с сотрудниками исследовал в лабораторных условиях процесс
хлорирования КгСОз с целью полного перевода производства
182
бертолетовой соли на поташный метод (доклад на Менделеевском Съезде в 1925 г., а также статья в Журнале прикладной химии, т. I, вып. 3—4, 1924 г.). Первый завод, построенный в СССР,
также был рассчитан на обменную реакцию с ноташем и па частичное хлорирование раствора КгСОз (в абсорбере). С развитием
добывания хлористого калия в Соликамске вопросы применения
поташа в производстве бертолетовой соли отпали, так как хлористый калий оказался дешевле и доступнее поташа.
Хлорирование раствора КгСОз проходит идентично хлорированию раствора Г4агСОз (стр. 169). Выход хлората, по нашим
исследованиям, имеет те же зависимости от концентрации КгСОз
и температуры, как и при хлорировании 1ЧагСОз. При концентрации КгСОз 200—400 г/л выход хлората при температуре хлорирования 70—80° равен 97—98% от теоретически возможного.
Суммарное уравнение реакции хлорирования будет:
ЗК2С03 + ЗС12 = КС108 + 5КС14- ЗСО, +17,2 ккал. (87)
3-282 80 5-100 3-94,4
Как и при NaaCOe, оптимальной температурой хлорирования
является 70—80°; поэтому поташный раствор до хлорирования
•следует подогреть, так как тепловой эффект хлорирования
очень мал. В действительности хлорирование происходит не
сразу по уравнению (87), а сначала образуются гипохлорит и
бикарбонат и т. д. (стр. 163).
Разделение получающихся при хлорировании КСЮз и КС1
довольно сложно, поскольку изменение температуры изменяет
растворимость обоих компонентов (см. рис. 61—64; стр. 130).
I
!
§ 4. Хлорирование СаСОз
При известковом методе производства хлоратов наиболее
значительной примесью в известковом молоке является СаСОз
в виде недопала или СаСОз, образующегося из извести и СО*
воздуха. При исследовании остатков шлама, остающегося после
хлорирования молока высокой концентрации, основной его составной частью (нерастворимой в воде) оказывается СаСОз.
Однако при хлорировании молока низкой концентрации, содержащего небольшое количество СаСОз (до 5—10 г/л), в шламе
часто не содержится СаСОз (Ж. X. П. № 25—27 за 1930 г.,
стр. 1563, табл. 7). Поэтому весьма интересно было изучить процесс хлорирования СаСОз как такового тем более, что среди
ряда производственников распространено преувеличеннее мнение
о вреде СаСОз, не только как балласта, остающегося после
хлорирования в виде шлама, но и как примеси, понижающей
выход хлората, и т. д. Юриш1 указывает, что при опытах
пропускания хлора через трубку с кусочками известняка,
облитыми водой, из трубки выходила только хлорная вода. Мы
ставили опыты не с кусочками известняка, а с известняком,
измельченным-в тонкий порошок, и получали совершенно другие
результаты. Первые опыты мы поставили с известковым моло-
■' 183
КОМ, содержащим СаО 100 г/л, куда был i«:i
образный известшгк 10 r/л. Ряд опыту» хлорирования чакою
молока (барботажом
хлоргаза). показывал неизменно после 3—5 мин.
перехлорирования получение щелока, нс содер-'
жащего осадка СаСОз и
с выходом хлората, одинаковым для хлорирования молока без СаСОз.
Далее были поставлены
опыты хлорирования
взвеси измельченного известняка в воде. Опыты
производились в лабораторной установке бар-
бо оо ботажем хлоргаза без
дополнительного перемешивания. Абгаз из сосуда для хлорирования
пропускался через раствор МаОН для улавливания из него хлора. Пробы хлорируемого щелока и раствора
NaOH для улавливаний хлора из абгаза отбирались через каждые 5 мин. ^Полученные данные приведены на рис. 81 и
в табл. 57.
20 30 40 50 60
бр€мя 6 минутах
Рис. 81. Кривые поглощения хлора и образования СЮ' и CKV при хлорировании взвеси
СаСОз в воде (200 г/л) при 30—36°.
Таблица 57. Опытные данные по хлориров а'ни ю взвеси
СаС03 вводе
и
опытов
СаСО,
г!л до
,опыта
Процент про-
скока'хлора (по
отношению к
поглощенному
хлору)
Состав щелока- в экв/л
Процент
СаС1а
о
Ca(CIOtV
всего
хлора
выхода
потери *
*
1
100
130
1,55
1,65
1,825
90.4
9.6
2
100
—
1,50
1,62
1.77
91,5
8,5
3
200
120
3,04
3.48
3,62
96,1
3.9
4
200
—
3,06
3,52
3,65
96,4
3,6
.Из данных рис. 81 и табл. 57 ©идно, что СаСОз поддается
хлорированию с образованием СаСЬ, Са(ОЮ)г и Са(С10з)г.
Отличием от хлорирования Са(ОН)г является меньший подъем
температуры, меньшая максимальная концентрация гипохлорита
и образование хлората в течение всего времени хлорирования.
1 Содержание Са(СЮ3)з дано в окислительных эквивалентах; 1 экв. >
17.25 z Са (СЮ3)2. 4
а Расчет процента выхода и потери см. стр. 90.
184
Таблица 58. Основные теоретические козфнциенты подучения KUO, разными методами
п роизводства
•
Расходуется 1
_
Получается в виде отходов 1
С
в
X
Метод производства
ш
KCI
Хлор
СаО 1
MgO
ZnO
Na.CO,
NaOH
кон
СаС1,
М*С1,
ZnCl,
NaCl
со,
KCI
На
•
1
1
Известковый метод
(Либиха)
0,608
1,736
1,37
—
—
—
—
—
2,72
—
—
—
—
—
—
2
Метод ,с MgO . . . .
о т-
-Ъ987
—
—
— '
Ч-
-wa*-
—
—
—
—
3
Метод с ZnO (Байера)
0,608
1,736
—
—
1,97
—
—
—
—
—
3,33
—
—
—
—
4
Содовый метод . . .
0,608
1,736
—
—
—
2,596
—
—
—
—
—
2,857
1,075
—
—
5
Каустический метод
(с NaOH)
0,608
1,736
—
/
-ч
—
1,958
—
—
—
—
2,857
—
—
—
6
Метод с хлорированием КОН
1,736
—
—
—
—
2,75
—
—
—
—
—
3,04
—
7
Электролитический
метод2
0,608
1 Количества тонн продуктов на 1т КС103.
2 Не показана трата электроэнергии, практически равная 5—б тыс. кв-ч на 1 т КСЮ3. imn
Расчетыданных таблицы сделаны, исходя из следующих суммарных уравнений реакции получения КСЮ3:
1. 6Са (ОН), + 6CU + 2КС1 = 2КСЮ3 + 6СаС1г + 6Н,0;
2. 6Mg(OH).> + 6СГ, + 2КО = 2КС103 + 6MgCU + 6Н20;
3. в2п (ОН>2 + 6С1.Ч- 2КС1 = 2КСЮ3 + 6ZnCl2 + 6Н0О;
4. 3Na2C08 + ЗС1,, + KCI = КСЮ3 + 6NaCi + ЗСО,;
5. 6NaOH 4- 3CI, + КС1 = КСЮ3 + 6NaCl + ЗН,0;
6. 6КОН + 30, = КС103 + ока + ЗН,0:
7. Ка 4- ЗН,0 4- 6(+) 4- 6Й = КСЮ, 4- ЗН,.
В этом отношении хлорирование СаСОл более похоже на хж\ *,i
рование NasCOs (стр. 169), что объясняется тем, что при обоих
процессах происходит выделение СОг. При этом, благодаря малой растворимости СаСОз, щелок «о все время хлорирования
имеет слабокислую реакцию от растворенного хлора. Так же как
и при хлорировании Са(ОН)з и №гСОз, выход хлората больше
при более высокой концентрации СаСЬ (стр. 64). Проскок хлора
происходит в течение всего времени хлорирования, составляя
120—140% от количества хлора, прореагировавшего с СаСОз.
Суммарное уравнение реакции хлорирования СаСОз будет:
бСаСОз + 6CU = Са(СЮз)г + 5СаСЬ + 6СОз. (88)
6*288 168,2 5*206,5 6*94,4
Исходя из теплот образования исходных и получающихся
веществ при хлорировании, тепловой эффект хлорирования
будет:
Теплота образования исходных веществ равна бСаСОз =
•= 6 • 288 == 1728 к кал.
Теплота образования получающихся веществ равна
Са(СЮз)г + 5СаС12 + 60 02 = 168,2 + 5 * 206,5 + 6 * 94,4 =
= 1767,1 ккал.
Выделится на 6 молей СаСОз • 1767,1 —1728 = 39,1 ккал
OQ 1
или на 1 г СаСОз 6 0,0652 ккал.
На этом заканчиваем описание методов получения КСЮз
химическим путем*. В заключение приводим табл. 58, в которой
сведены расходные коэфициенты и количества получаемых отходов при основных описанных методах получения КСЮз.
Для удобства сравнения в таблицу включены также коэфициенты
электролитического получения КСЮз, описание которого будет
дано в гл. 20.
ГЛАВА 15
ХЛОРАТ НАТРИЯ
После бертолетовой соли хлорат натрия является 'наиболее
употребляемой солью хлорноватой кислоты и, особенно в последнее время, его применение с каждым годом расширяется.
Действительно хлорат натрия имеет перед бертолетовой солью
ряд преимуществ, из которых основное — это гораздо большая
растворимость, а также большая окислительная способность
(содержание кислорода на 6% больше, чем в КСЮз); кроме того
для производства Г4аСЮз применяется поваренная соль, которая
менее ценна, чем КС1, являющийся исходным продуктом в производстве КСЮз. Однако в то время как первая фабрика КСЮз
начала работать в 1847 г., производство NaClOs в промышленном масштабе началось только в 1883 г. Это произошло из-за
сложности разделения NaClOs и NaCl, в виде совместного раствора которых получается щелок при всех промышленных методах производства NaClOs. Основным толчком к началу про-
186
мышленного производства NaClCb послужила потребность
в концентрированных растворах хлората для красочной промышленности (анилин-чсрный).
§ 1. Физические и химические свойства
Процентный состав NaClOa следующий: натрия 21,6%, хлора
33,3% и кислорода 45,1%. Молекулярный вес NaClOa равен
248—264 *. Теплота образования NaClOa из элементор
84,8—86,7 ккал. Теплоемкость для . твердой соли 0,281
и для расплавленной соли 1 0,581 ккал. . Коэфициент
расширения' NaClOa равен 0,006. Удельная электропровод-
1 По данным разных авторов.
187
Рис. 83. Влияние NaCl на раствори*
мость NaC10a при 20°. .
;
ьо
40
® о too 555 300 400 ЗЙО 600 ТОО «00 too л:
Na.Ct.Oj 1/л. i
Рис. 84. Влияние NaC10;t на растворимость NaCl при 95—100°.
ность расплавленного NaClOa
при 265° равна 0,653 обрат- \
ных ома. ;
Разложение NaClOa при ;
нагреве выше температуры !
плавления, влияние примесей *
и каталитическое действие |
некоторых веществ на разло- {
жение NaClOj, взаимодействие |
NaClOa с кислотами и дру- '
гие химические свойства з
NaClOa в общем сходны с |
соответствующими свойствами i
КСЮз (стр. 19). Растворимость ?
NaClOa в воде гораздо значи- г
тельнее, чем КСЮз. Однако |
температурный коэфициент ;
растворимости NaClOa мень- !
ше, чем температурный коэ- *
фициент растворимости КСЮз. \
Концентрация и состав насы- ;
щенных растворов NaClOa
при температуре от —15
до 122° показаны в табл. 59.
В присутствии NaCl ^>ас- <
творимость NaClOs значитсль- $
но уменьшается (рис. 82 данные автора, рис. 83 данные
Винтелера Zeit. Electroch.,
том 7, стр. 360). В свою очередь NaClOa уменьшает раст- ;
воримость NaCl (рис. 82 и 84). |
В спирту NaClOa мало раство- j
1
188
Таблица 59. Плотное ть и концентрация растворов NaCI03, насыщенных при температурах от —15 до Г22°м-5
Температура
в® С
Содержание
Плотность
°!о
г/кг Н,0
г/л раствора
Уд. вес
® Боме
—* 15
41.9
721
578 .
1,380
39.7
0
44,1
789
612 •
1,389
40,4
10
.47,4
901
668
1,409
41,8
20
50,2
1008
718
1,430
43,4
30 ‘
53,1
1132
770
1,451
44,9
40
55,8
1262
821
1,472
46,3
50
58,2
1392
869
, 1Д93
47,7
60
60,8
1551
920
' 1,514
49,0 .
70
63,1
1710 1
969
1,536
50,4 4
80
65,4
1890
1019
1,559
51,8
90
67,6
2086
1069
1,581
53,1
100
69,7
2307
1118
1,604
54,3
110
72,0
2577
1170
1,625
55,5
122
74,1
2861
1225
1,654
57,1
рим. В спирто-водных смесях NaClOs тем меньше 'растворим, чем
больше процент спирта. Температурный коэфициент растворимости NaClCh в спирто-водных смесях очень мал (рис. 85).
В жидком аммиаке NaClOs хорошо растворим. В гидразине
растворимость NaClOs равна 40%. i
Вязкость растворов NaClOs по отношению к воде три 15,
25 и 40° будет2в**10:
/Концентрация NaC103 в молях
на 1000 г Н20
. 0!25
0,50
1,00
2,50
4,50
Вязкость при 15°
1,012
1,028
1,067
1,24
1,61
. „ 25°
1,021
1,041
1,086
1,265
1,625
. „ 40°
—
1,10
1,285
1,64
Упругость паров насыщенного раствора NaClOs при 100°
равна 410 ш рт. ст. Для растворов разной концентрации понижение упругости паров при температуре 100° будет:
г —
г NaC103 на 100 г Н20 .
9,02
23,93
29,34
46,22
57,00
85,70
121,28
160,16
ММ рт. ст
19,7
54,7
67,5
107,3
132,1
197,4.
242,9
290,0
NaClOs принадлежит к солям, . имеющим две температуры
кипения: насыщенный раствор кипит при 132°, а пересыщенный
раствор кипит при 135°. Для растворов с разной концентрацией
NaClOs температура кипения следующая":
NaC103 г/л .... .
165
512
815
990
1120
1210
Температура кипе*'
ния °е ..... .
/
101,2
106,4
110,7
115
118
121,5
189
Понижение температуры замерзания растворов NaUO;; м<//мн>
рассчитать по формуле: 3,5812 М — 1,3040 Л*2, где М — концентрация NaClOa в молях на 1000 г НгО.
Эквивалентная электропроводность в обратных омах показана в Табл. 79 (стр. 244).
Степень диссоциации <* при 18е равна:
0,101!.
!
! o/jorn
0,513
1,0 И
2,082
4,161
0,8'.’ 1
: 0,773
i
0,700
0,<i21
0,517
0,556
При, освещении растворов NaClOa ультрафиолетовыми лучами хлорат целиком разлагается на хлорид и кислород. При
обычном освещении раствор NaClOa вполне устойчив. NaaOs и
КМп(>4 в кислой среде и Н2О2 в нейтральной или щелочной
среде не окисляют NaClOa. ШгБгОа окисляет растворенный
NaClOa в NaCIO*. Эта реакция каталитически ускоряется AgNOa.
Н2О2 в кислой среде и SO2 восстанавливают СЮ'* в СГ.
Муравьиная кислота в концентрированных растворах NaClOa
образует СЮг.
n § 2. Получение хлората натрия из бертолетовой соли
1. Кремнефтористый способ. Этот способ был предложен Велером еще в 1817 г. К раствору КСЮз прибавляют HaSiFe, отчего
получается осадок KaSiFe, а в растворе остается НСЮз.
Последнюю нейтрализуют прибавлением ЫагСОа и полученный
раствор NaClOa концентрируют выпариванием и кристаллизуют.
Видоизменением этого способа является кипячение раствора
КСЮз с NaaSiFe, отчего выделяется осадок KaSiFe и в растворе
остается NaClOa. Из осадка KaSiFo можно регенерировать HaSiFe,
обрабатывая промытый •осадок серной кислотой и улавливая
водой выделяющийся SiF* (см. Лунге3).
2. Способ с виннокаменной кислотой. Этот способ был предложен Витштейном в 1838 г. Прибавляют горячий насыщенный
раствор КСЮз к раствору H2C4H4OG и нейтрализуют содой. Получающийся осадок КНСШЮв отделяют, а раствор NaClOa упаривают и кристаллизуют. Полученный отход KHQHiOe регенерируют в HaCihUOe.
3. Способ с КСЮз и NaaSO.i. К горячему раствору 100 г
КСЮз в 600 см3 воды прибавляют 60 г NaaSO*. Во время охлаждения раствора прибавляют 300 ел3 спирта и оставляют на
двое суток. Выделившийся K2SO4 отделяют от жидкости и промывают 30%-ным спиртом. Жидкость, слитую с осадка KaSC^,.
и промывные воды упаривают и кристаллизуют.
4. Способ с КСЮз н (NH4)aS04. К раствору 5 ч. КСЮз и 3 ч.
(NH4)sSC>4 в 15 ч. воды прибавляют 4-кратное количество
спирта. Отделяют выделившийся осадок K-SO* и отгоняют спирт
из получившегося раствора NH4CIO3. Прибавляют NaaGOa, выпа-
180
ривают досуха и подгоняют (ЬШфСОз. Остаток представляет
•собой NaClOs с примесями, почему его необходимо нерекри-
сталлизовать.
5. Способ с квасцами. Способ основан на меньшей растворимости калиевых квасцов, чем натриевых, и состоит в обменной
реакции КСЮз и натриевых квасцов. Получаемый по этому
способу хлорат натрия загрязнен примесями квасцов.
§ 3. Известковый метод Печинея
Этот способ, разработанный Печинеем [герм. пат. 15493
(1881); Jber. ch. Techn. (1881) 296], вытеснил получение хлората
натрия другими вышеизложенными способами, исходящими из
КСЮз. Схема этого метода получения NaClCh, показанная на
рис. 86, аналогична способу получения КСЮз, описанному на
стр. 34. Маточный щелок, полученный после выделения большей части СаСЬ, разбавляют до удельного веса 1,30—1,35, подогревают до 30—35° и прибавляют теплый (35—40°) раствор
Na2SO<1 для обменной реакции с Са(С10з)г и СаСЬ. Получившийся осадок гипса отделяют и промывают горячей водой,
после чего он является отходом.2 По нашим данным целесообразно массу после обменной реакции подогреть до 80—90',
при каковой температуре выдержать несколько часов, отчего
образуются крупные кристаллы гипса, которые легче отделить
от щелока и легче промыть. Можно также проводить обменную
реакцию с ШгСОз. Щелок, отделенный от гипса, и промывные
воды обрабатывают, как будет указано ниже (§ 10). Этот способ сохранил свое значение по настоящее время.
Можно также получать хлорат натрия известковым методом,
аналогичным способу получения КСЮз по Либиху, проводя
обменную реакцию NajSCb и №гСОз с хлорированным щелоком
без предварительного выделения СаСЬ. Однако такой способ
получения NaClOs уступает способу Печинея: больше (в 2—3
раза) расход Na2S04 (или NagCCb); сложнее отделение большего
количества гипса (или мела), образующегося при обменной реакции; больше потери хлората с гипсом; больше NaCl (в 2—3
раза) приходится выделить из щелока после обменной реакции.
§ 4. Магнезиальный метод
Этот способ разработан Муспраттом и Эшельманом [герм,
пат. 27729 (1883); Dingl. J. 254 (1884) 37]. Схема этого способа
аналогична магнезиальному способу получения. КСЮз, описанному на стр. 180, и вышеописанному способу Печинея. Хлори-
* Технический сульфат натрия часто содержит свободную H:SO<, которую надо нейтрализовать.
1 CaSO*, растворенный в полученном растворе NaCl и NaClOa, осаждают
прибавлением NatCO* соответственно содержанию Са. Для предохранения
железных частей аппаратуры от коррозии прибавляют NaOH из расчета
1—2 г/л раствора.
191
^зВшстшок
Толли 9o
Горяча* Вод*
ВВоаз Воз Ci*
Жлороаз Воздал
РоактиВЫ
ллсрат натрия
Рис. 86. Схема производства хлората натрия известковым методом по Печинею.
руют взвесь Mg(OH)a в воде. Хлорированный щелок упаривают
до удельного веса 1,38 и охлаждают, отчего выделяется 50 7«
MgCb, бывшего в хлорированном щелоке. Маточный щелок после отделения от (выделившегося хлористого магния подогревают и прибавляют ИагСОз или NaOH для обменной реакции.
Получающийся осадок MgCOs или Mg(OH)2 промывают и
используют для хлорирования и т. д. Щелок, отделенный
от осадка MgCOs или Mg(OH)2, и промывные воды упаривают,
.как будет описано ниже (§ 10).
§ 5. Метод с окисью цинка
Этот способ, разработанный Фридерих, Маллет и Гувэ [Ch.
Zeit. 28 (1904) 763], аналогичен способу получения КСЮз, описанному на стр. 182.
На хлорирование подают взвесь ZnO в растворе NaCl и получают ‘в виде отхода ZnCU. Уравнение реакции получения
NaClOs по этому способу будет:
. ' 3ZnO + NaCl + ЗС12 NaClOs + 3ZnCl2.
Как указывают авторы способа, прибавляя избыток NaCl,
можно благодаря гидролитической диссоциации ZnCU получить
NaClOs больше, чем по уравнению (89). Полученный после хлорирования щелок, содержащий ZnCU и NaClOs, упаривают и обрабатывают, как обычно (см. также стр. 182 и 231).
§ 6. Методы с NaMnOi, Na2CrO« и бурой
Хлорируя раствор NaMn04, получают №гМпО« и NaClOs
[Болтов, Вильде и Ауэр, англ. пат. 8217 (1887) и 10193 (1888);
J. Soc. Chem. Ind. 7 (1888) 437,8 (1889) 706].
Хлорируя раствор NasCrOs, получают раствор №гСгг07 и
NaClOs:
6Na2Cr04 + 3Ch = 3NasCHOr + &NaCl + NaClOs (90)
Полученный раствор упаривают для выделения NaCl, а потом разделяют ИагСтгОт и NaClOs дробной кристаллизацией
[Гиббс, герм. пат. 164881 (1904)].
Хлорируя раствор буры, получают борную кислоту и NaClOs
[Флеминг, англ. пат. 4736 (1912); С. А. (1913) 3397; Флеминг и
Миллер, ан?л. пат. 23101' (1912); С. А. (1914) 1193].
<
§ 7. Каустический метод
I х
Хлорируя раствор NaOH, получают щелок, содержащий
ЛаСЮз и NaCl. Можно также получить NaClOs, хлорируя
13 Зыс. 17». - ШраИбмая. *• <. , 193
Рис. 87. Схема производства хлората натрия каустическим методом,
ЛроаитЬ/и яерех/юриробам*
нЫи щелоМ
раствор NaOH -f- NaCl, получающийся при электролизе раствора
NaCl. Схема этого способа, показанная на рис. 87, проверенная
при непосредственном участии автора на одном из современных
заводов, дала хорошие результаты в отношении расходных ко-
эфициентов, технологического режима и качества продукции
(стр. 207).
■ § 8. Способы с №гСОз
Д-р Мук [герм. пат. 25785 (1883)] предложил хлорировать
раствор соды, полученный щелок упарить досуха, из сухого
остатка выщелочить NaClC>3 подогретым маточным щелоком от
предыдущего цикла производства и, охлаждая жидкость после
•процесса выщелачивания, выделить из нее МаСЮз. Маточник,
остающийся после кристаллизации, используется для выщелачивания в новом цикле производства. При выпарке досуха часть
NaClOs разлагается, почему практически этот метод не нашел
широкого распространения. На
рис. 88 (Ульман в“®) показана установка Гаргривса [англ,
пат. 16257 (1895), герм. пат.
92474 (1896); J. Soc. Chem. Ind.
15 (1896) 719; Ch. Ind. 20 (1897)
224]. Процесс ведется в башне А, футерованной кирпичом.
Кальцинированная сода смешивается с небольшим количеством воды и в виде кашицы подается в В, где имеются колосники С. Хлоргаз входит через £*■
и хлорирует соду. Образовавшийся NaCl нерастворим1 в небольшом количестве получающейся жидкости и сбрасывается
по окончании операции в F.
Жидкость, содержащая большую
часть образовавшегося NaClOs,
спускается по трубе G в приемник J, где очищается пропусканием через твердую соду и направляется либо на выпарку,
либо обратно в башню. Жидкость, стекающая с NaCl в F, поступает в сборник Н, откуда передается на выпарку.
Рис. 88. Схема установки для получения хлората натрия по Гаргрив-
су.
А — башня, В — шахта, куда поступает кашица из соды и воды, С — тарелки, распределители кашицы, Е— вход хлоргаза,
F— сборник NaCl, О — шелокопровод, I —
приемник щелока, И — сборник щелока,
стекающего из F.
Примечание. Этот метод производства хлората натрия проверялся
Грибановским. Однако выделение Оа при хлорировании кашицы из соды
и воды было значительным и выход хлората составлял всего 80—85%
вместо 95—97%, полученных нами при хлорировании раствора NaeCOa
(см, стр. 170). ' , •
Г *
13*
195
§ 9. Электролитическое получение NaClO.»
Совершенно отдельно стоит метод получения NaCICb электролизом раствора NaCl, который будет разобран в гл. 21 (стр. 282).
Этим методам в данное время получается большая часть мирового производства хлората натрия. Получаемый после электролиза щелок, содержащий NaClOe и NaCl, дальше перерабатывается как щелок после обменной реакции при известковом методе (см. выше п. 3) или щелок от хлорирования растворов
NaOH или №г(Юз (см. выше пп. 7 и 8).
§ 10. Переработка на^риево-хлоратных щелоков
При всех современных методах производства хлората натрия
получаются щелока, содержащие NaClOe и NaCl, раздельное получение которых в возможно более чистом виде и составляет
цель дальнейших стадий производства (выпарка, кристаллиза-
Рис. 89. Схема переработки натриевс-хлоратных щелоков.
ция и т. д.). Щелока, полученные при известковом, магнезиальном, каустическом, содовом или электролитическом методе, отличаются между собой только концентрацией *и соотношением
содержащихся в них №СЮз и NaCl, что однако не меняет схемы
переработки этих щелоков. В общем эта схема состоит в следующем (рис. 89): выпаривают_щелок для тог(о, чтобы увеличить концентрацию. NaClOs « выделить большую часть ,NaCl,
содержащегося в щелоке до выпарки. Пределы уд. веса' щелока
при конце выпарки колеблются в зависимости от температуры
выпарки (под вакуумом или под давлением) и от количества
примесей,.. Обычно упаривают до удельного веса 1,48—1,{>1
(47—49° Боме).. Щелок, поступающий на выпарку, должен со-
196 ' , / ’ ч , ^ '
держать NaOH 3—5 г/л для уменьшения коррозии железных частей аппаратуры и трубопроводов. Выделяющаяся при выпарке
«обратная соль» (NaCl) отжимается на нутч-фильтрах от щелока
и промывается горячей водой. Промытая «обратная соль»
является отходом производства (см. табл. 63, стр. 203). Промывные воды направляют обратно на выпарку.
Уваренный щелок, отделенный от выпавшей NaCl, охлаждают для выделения части NaCJOj в виде кристаллов. NaCl
не выделяется при охлаждении уваренного щелока, так как растворимость NaCl не уменьшается, а даже увеличивается благодаря уменьшению концентрации NaClOs (рис. 82 и 84). Выделившиеся кристаллы NaClOs отделяются на центрофугах или на
нутч-фильтрах бт маточного щелока. Последний возвращается
обратно на выпарку. Чем ниже температура кристаллизации, тем
меньше NaClOs остается в маточном щелоке. Однако, поскольку
маточный щелок возвращается в цикл производства, количество
остающегося в нем NaClOs не имеет особенно большого значения и обычно искусственного охлаждения не применяют.
Хлорат, отделенный от маточного щелока, содержит некоторое количество примесей, обычно в сумме до 1%. Основной
примесью является NaCl. Количество примесей можно значительно уменьшить, промывкой хлората холодным конденсатом
или маточным щелоком от перекристаллизации. При отделении
хлората на нутч-фильтрах промывку вести удобнее и удаление
примесей происходит полнее (стр. 204), чем1 при отделении хлората на центрофугах. Если нужен более чистый продукт, производят перекристаллизацию хлората из воды: растворяют хлорат в горячей воде, отстаивают и декантируют полученный
горячий раствор от нерастворимых примесей, охлаждают отде-
кантированный раствор и отделяют выделившиеся кристаллы
NaCICb от маточного щелока. Примеси почти целиком остаются
в последнем, а полученный перекристаллизованный хлорат
обычно очень чист. Маточный щелок от перекристаллизации
можно использовать еще 1—2 раза на следующие циклы перекристаллизации (а также на промывку хлората 1-й. кристаллизации), после чего он обогащается примесями и его направляют
на выпарку как маточник 1-й кристаллизации (табл. 69, стр. 208).
Отжатый от маточника хлорат сушится, просеивается для отделения комочков и упаковывается. Эти последние стадии процесса не отличаются от соответствующих стадий в производстве
бертолетовой соли (см. гл. 10, стр. 137).
Поскольку маточные щелока от кристаллизации ИаСЮз содержат на единицу NaClOs во много раз меньше NaCl, чем
«слабые» щелока до выпарки, луч}пе упаривать их отдельно от
начальных «слабых» щелоков.
§ 11. Изучение выделения хлорида по Печинею
Как указано на стр. 34, способ Печинея предусматривает три
варианта выделения хлорида: в виде СаСЬ • 6HzO из хлорированных щелоков, уваренных до удельного веса 1,50, в виде окси-
'197
хлорида из хлорированного щелока и в виде оксихлорида ил
маточного щелока, остающегося после выделения СаСЬ • 61ЬО.
Ниже приводим некоторые данные наших исследований по этим
вопросам.
а) Выделение СаСЬ • 6НгО из у варенных
хлорированных щелоков
А
В табл. 60 приведены данные выделения хлорида из щелоков,
уваренных до разной концентрации. При расчетах применены
следующие формулы:
• % выделения СаС1а= 100—^?,
% потери Са(СЮа)г с выделившимся хлоридом равен:
2,90 • [% выделения СаСЬ] • [% Са (СЮ3)2 в кристаллах]
' [% СаС13 в кристаллах] ’
где К — обозначает отношение СаСЬ: Са(СЮз)г в маточном щелоке, а 2,90 обозначает. это отношение в уваренном щелоке.
Таблица 60. Выделение хлорида в виде СаС1,• 6Н20 из тело*
ков, уваренных до уд. веса 1,44—1,60
J*
опытов |
'А
2
3
4
5
/
б
7
8
3—5 1
Уваренные |
’ Удельный вес • .
1,439
1,468
1,490
1,500
1,510
1,530
1,563
1,598
1,486
щелока при {
СаС12 г/л*« • • •
, Са(С103)2 г/л » .
522
560
601
612
622
644
681
740
612
95—100° \
Выделившиеся, 1
180
193
207
211
215
222
235
255
211
®/о СаС12 • • • •,
48,5
48,7
50,3
50,5
50,6
52
54
56
50,3
кристаллы' |
[ ®/о Са(СЮ3)а • • •
0,38
0,47
0,54
0,70
0,64
1.0
1,9
4,1
0,62
г Удельный вес . .
1,490
463
1,510
1,590
1,600
1,607
1,616
1,616
1,643
1,598
Маточные
СаС12 г/л ....
475
487
460
468
512
518
496
472
щелок!а при <
Са(СЮ3)2 г/л . .
236
263
402
451
463
423
425
506
435
12—16°
ш* СаС12
(,А — Са(СЮ3)2 ‘ ’
1,96
1,81
1,21
1,02
1,01
1,21
1,22
0,98
1,08
% выделения СфС12 . • • . . х.
32
38
58
65
65
58
58
66
63
% потери хлората
1
0,7
1Д
1,8
2,6
2,4
3,2
5,9
14
2,3
1 Средние данные опытов 3—5.
Из данных табл. 60 видно, что при удельном весе уваренных щелоков 1,490—1,510 (47,5—48,5° Боме) процент ,<СаСЬ
в выделившихся кристаллах почти равен теоретическому для
состава СаСЬ • 6Н*0, выделение СаСЦ равно 58—65% и потеря
Са(СЮ»)* равна 1,8—2,6%. При щелоках, уваренных до более
низкого уд. веса, содержание Са(СЮз)г в выделившихся кристаллах ниже, но одновременно сильно понижается процент
выделения СаСЬ., При более' высокой концентрации уварен-
198 /
ных щелоков процент выделения СаСЬ нс увеличивается,
но сильно возрастает процент Са(С10з)г в выделившихся кристаллах.
Параллельно проведенные опыты, отличающиеся между собой тем, что при одних опытах кристаллизация хлорида из уваренных щелоков производилась при спокойном состоянии щелоков, а при других опытах при перемешивании, показали разницу
только в величине выделившихся кристаллов, но не в проценте
выделения СаСЬ и не в проценте Са(СЮз)з в отжатых кристаллах.
Опыты, приведенные в табл. 60, проведены при температуре
конца кристаллизации в 12—16°. Для щелоков, уваренных до
удельного веса 1,49—1,51, кристаллизация начинается при 23—
26° и интенсивно увеличивается до 10—12°. Дальнейшее понижение температуры увеличивает выделение СаСЬ, но уже не так
значительно. Вместе с тем, чем ниже температура, тем больше
вязкость маточного щелока и труднее отделение его от выделившихся кристаллов, почему последние содержат больше хлората. Поэтому, применяя охлаждение до низкой температуры,
следует вести ее в две "стадии*— сначала охладить до 10—12° и
отделить выделившиеся кристаллы, а затем уже охладить маточник до '5—15° ниже нуля для дополнительного выделения
кристаллов. При охлаждении маточного щелока, полученного
при опытах 3—5, до —10° мы получали маточник, содержащий
СаСЬ 330 т/л и Са(СЮз)г 535 г/л, т. е. выделение СаСЬ было
равно 79%.
Промывая выделенный хлорид холодной водой, удается
уменьшить содержание в нем Са>(СЮз)2 в несколько раз. Однако
благодаря большой растворимости СаСЬ при промывке большое
его количество переводит в промывные воды. Промывку надо
вести на нутч-|фильтрах, а не на центрофугах, и добавлять жидкость для .промывки небольшими порциями. Промывные воды
надо использовать несколько раз, пока в них концентрация
хлората достигнет около Yz той величины, которую имеет концентрация хлората в маточнике, от которого отжат промываемый хлорид. Заканчивать промывку надо холодной водой. При
таких условиях мы получали хлорид с содержанием хлората
в 0,1% и меньше; при этом в промывные воды переходило
10% промываемого хлорида. 4
б) Выделение СаСЬ из хлорированных
щелоков в виде оксихлоридов х
В табл. 61 приведены данные выделения оксихлоридов из
хлорированных щелоков разной концентрации при условии прибавления разного количества извести и охлаждения до температуры 10, 0 и —10°. Известь прибавлялась в виде пушонки
к щелоку, нагретому до 80—85° при энергичном перемешивании.
По охлаждений массы до необходимой темлературы образовавшиеся оксихлориды отделялись от маточных щелоков и по-
199
слсдние анализировались. Процент выделении
вался по формуле
юо-*шо
1UU 2,85 ’
рЗСС'НП'Ы
где К обозначает отношение СаСЬ : Са(СЮз)г в маточном щелоке, а 2,85 обозначает это же отношение для хлорированных
щелоков, которое было одинаково для всех опытов.
Таблица 61. Выделение хлорида из хлорированных иуело-
KOfeB виде, оксихлоридов
Влияние кон
центрании
в щелоках
•
Влияние
количества
СаО
Влияние
температуры
охлаждения
м
/
опытов
1
2
а
4
б
6
3
6
7 i
8
Хлорированные 1
СаС1а z/л • • • •
111
157
210
262
210
210
210
210
210
210
щелока при 20° |
[ Са(С103)2 21л • •
39
55
74
92
74
' 74
74
74
74
74
Прибавлено молей СаО на'
1 моль СаС12 .
3
3
3
3
1
2
3
2
2
2
Температура
Г
охлаждения , • ,
10°
10°.
10°
10°
10°
10°
10°
10"
0°
-10°
СаС1а z/a ■ • • •
98
139
89
202
161
132
89
132
119
114
Маточные
Са(СЮ^)а zJa . •
сослал?' •
38
65
111
190
I
79
125
111
125
126
123
щелока
2,58
2Д4
0,80
1,06
2,04
1,06
0,80
1,06
0,94
0,93
% выделения СаС1а
10
25
72
63
28
63
72
63
67
67
Из данных табл. 61 видно, что максимум СаСЬ (72%) выделяется при щелоке, содержащем СаСЬ 210 г/л„ к которому прибавлена известь в количестве 3 молей СаО на 1 моль СаСЬ
(опыт 3). При меньшей концентрации щелока (опыты 1 и 2) выделяется меньше СаСЬ. Большая концентрация щелока не увеличивает выделения СаСЬ, но делает всю массу более вязкой,
отчего от нее труднее отжимать маточный щелок. Хотя максимум СаСЬ выделяется от прибавления 3 молей СаО на
1 моль СаСЬ, мы считаем более целесообразным прибавлять
только 2 моля СаО на 1 моль СаСЬ. Правда, при этом несколько
уменьшается процент выделения СаСЬ (с 72 до 63%), однако
значительно облегчается отделение маточника от оксихлоридов
и Уменьшается количество маточника, остающегося в отделенном оксихлориде. Считаем также нецелесообразным охлаждение ниже. 10°, так как это очень мало увеличивает процент выделения СаСЬ и, повышая вязкость массы, ухудшает отделение
маточника. Таким образом наиболее целесообразным является
прибавка 2 молей СаО на 1 моль СаСЬ к щелоку, содержащему
СаСЬ ~ 200 г/л, и охлаждение полученной массы до 10°.
в) Выделение оксихлоридов из маточных щелоков щ.о'сле-'Ьыделения СаСЬ • 6НЮ
. В табл. 62 приведены данные о выделении оксихлоридов из
маточных щелоков после выделения СаСЬ * 6Н2О, разбавленных
200
до разной концентрации и мри разном количестве прибавленной извести. Был взят маточный щелок от опытов 3—5 (табл. 60)
и разбавлен до содержания СаСЬ 200, 265 и'320 г/л. К разбавленному щелоку, подогретому до 80—85°, прибавлялась пушонка из
расчета 1, 1у5 и 2 молей СаО на 1 «моль СаСЬ. Полученная масса
охлаждалась до 10°, после чего отделялись оксихлориды. Процент выделения СаСЬ рассчитан по формуле:
100
К • 100
1,08 ’
где К обозначает отношение СаСЬ: Са(СЮз)? в маточном щелоке после отделения оксихлоридов, а 1,08 обозначает это отношение в щелоках до прибавления извести. Разбавление да
концентрации СаСЬ ниже 200 г/л, прибавление СаО больше 2
молей на 1 моль СаО* и охлаждение ниже 10° не применялось,
на основании опытов, приведенных выше в табл. 61.
Таблица 62. Выделение хлорида в виде оксихлоридов из
маточников, полученных после выделения СаС12*6Н20
№ опытов
».
2
3
4
5
6
7
8.
9
Щелок до при- 1
СаС12 г/л . . . .
4 l
200
\
265
1
320
бавления СаО \
t Са(СЮз)2 zfA . •
185
245
296
Прибавлено молей СаО на 1 моль
1
1,5
i
1,5
l;$
1
1,5
2
1
2
Щелок после
отделения
СэС12 zjA . • . •
220
198
235
208
141
238
213
143
Ca(C103)2 z/л . .
j. CaCl2
A “Ca(C103)2 * ‘
272\
315
386
310
353
446
335
380
476
оксихлоридов
0,81
0,63
0,34
0,76
0,59
0,32
0,71
0,56
0,30
.% выделения СаСЬ в вйде оке и-
30
72
хлоридов 1
25
32
68
45
70
34
48
Суммарный °/п выделения СаС12
в виде СаС12*6Н20 и в виде
оксихлоридов 2 . . . . ^ . . .
70
77
j 87
72
78
88
74
79
89
1 По отношению к взятому для опытов щелоку после выделения
СаС1а • 6Н20. 1
2 По отношению к хлорированному щелоку # до выделения СаС12-6Н20.
Из данных таблицы -видно, что максимум СаСЬ выделяется:
в случае прибавления 2 молей СаО (на 1 моль СаСЬ. Изменение
концентрации СаСЬ в начальном щелоке от 200 до 320 т/л не
имеет большого влияния на процент выделения СаСЬ, но сильно
увеличивает вязкость маточного щелока и количество маточного
щелока, удерживаемого в отжатом оксихлориде. Поэтому наиболее целесообразным является {как и при хлорированном щелоке) прибавка 2 молей СаО на 1 моль СаСЬ к щелоку, разбавленному до содержания СаСЬ 200 г/л. >
Примечание. Промывкой уменьшить содержание хлората в отжатых оксихлоридах не удается, ибо при промывке оксихлориды разрушаются. Процент выделения СаСЬ по отношению 'к щелоку до выделения,
СаС1; • 6НгО. рассчитывается по вышеприведенной формуле, только в знаменатель вместо 1,08 вставляется йоэфициент 2,90 или другой соответствующий:
отношению СаСЬ: Са(СЮ«)» в хлорированных щелоках.
< ' • ^ . 20 i
§ 12, Изучение вьпы;растворов NaQO.t | NaCi
и кристалл».buuw NaCIO;»
На рис. 90 показана зависимость между удельным весом увариваемого раствора 1МаС10з и NaCl и содержанием в нем NaCICh
<при ,70°). Хлористым натрием щелок насыщен (концентрацию
УЛД NaCLo$
г/л.
1,50
- 800
■: %
- Г 73(Г
- — 700
•4^46-
ч • Г
v°-:
330 1
I
!v
*
|до
I
1,26
690
600
900 &
- 400
tr»U |,
•€■ 300. *|
Рис. 91. Выделение NaCl при выпарке *
натриево-хлоратных щелоков.
- 290
F- 200
Рис. 90. Содержание NaC|03 в уваренных щелоках
разного уд. веса,
насыщенных NaCl.
NaCl см. рис. &4 стр. 188). Температура 70°
выбрана как близкая к практически наблюдаемой при выпарке под вакуумом.
На рис. 91 показано выделение NaCl
из увариваемого раствора, содержавшего
Йо выпарки NaClOe 50 г/л. и NaCl 294 г/л.
з рисунка видно, что при выпарке выделяется 9&1—97% NaCl, бывшего в начальном щелоке. При других соотношениях
NaCl и NaClC>3 в начальном щелоке получаются другие данные, чем по кривой рис. 91, но общий характер выделения NaCl не изменяется.
В табл. 63 приведены данные об отделении и промывке па
нутч-фильтрах соли (NaCl), выделяющейся при выпарке щелоков на производственной вакуум-выпарной установке. Из приведенных данных видно, что промывка проходит хорошо и
в промытой соли остается очень немного хлората. Исходя из
количеств выделяющегося NaCl, по рис. 91 и из данных табл. 63
мы находим, что общее количество хлората, теряемого в промытой соли, равно 2—4 кг, а общее количество промывных вод
равно 0,3—0,5 ж* на 1 г готового, хлората.
•202
Таблица 63. Некоторые данные об отделении и промывке
с о Л'М, выделяющейся при р ы парке натриево-хлоратных
щ е л о к о в
N \
Уваренные щелока (70°)
Состав обратной ооли в °/0
Промывные воды (65—60®)
удельный
вес
состав в г/л
до промывки
после промывки
л{кг промытой СОЛИ
удельный
вес
состав в г/л
О
о
св
2
NaC!
NaOH
«*
О
и
<0
2
NaOH
NaCl
о
и
се
2
NaOH
NaCl
т
о
и
се
2
о
d
2
NaOH
1,29
224
* 248
11
1.7
0,09
91,1
0,07
0,03
93,6
0,33
1,20
48
280
2.1
1,32
347
209
16
3,6
0,16
88,4
0,10
0,03
93,2
0,38
1,21
102
269
4.4
1,37
462
184
21
6,2
0,25
84,4
0,13
0,05
92,2
0,46
1,215
142
251
5.1
1,44
586
144
26
8,7
0,36
81,7
0,16
0,05
92,1
0,58
1,22
159
246
6,4
1,50
702
112
31
17.4
0,51
77,4
0,22
0,07
90,8
0,71
1,25
261
228
8.0
В табл. 64 приведены данные по кристаллизации NaClO.i из
щелокё, насыщенного по NaClOs и NaCl при 70° по мерс охлаждения щелока до —10°. Температура 70" выбрана как близкая
к практически наблюдаемой при вакуумвыпарке. Содержание
NaCl по мере охлаждения щелока увеличивается, поскольку из-
за выделения NaClOs и охлаждения объем щелока уменьшается,
а растворимость NaCl увеличивается по мере уменьшения концентрации NaClOs (см. рис. 82 и 84 стр. 187 и 188).
Таблица 64. Кристаллизация NaC103 из щелока, насыщенного
NaClOg и NaCl при 70°
х
Температура
eb®
60®
40®
30®
20®
10®
0®
-10®
У
NaC103 г/л • . .
737
679
627
576
526
475
428
386
NaCl г/л ....
99
103
\
106
110
114
118
122
127
Уменьшение объема щелока можно рассчитать по увеличению концентрации NaCl или других примесей, не выделяющихся при кристаллизации, если таковые присутствуют (NaOH
и т. д.). Например по табл. 64 при охлаждении с 60 до 10° концентрация NaCl повысилась с 99 до 118 г/л; отсюда рассчитываем
{118 99) • 100
уменьшение объема в - 118- =16,1%. Согласно рассчи¬
танному уменьшению объема и концентрации NaClOs до и после кристаллизации рассчитывается количество NaClOs, выделившееся при кристаллизации. Например по данным табл. 64 при
охлаждении с 60 до 10° концентрация NaClOs уменьшается
с 737 до 475 r/\t, а объем уменьшается (как рассчитано выше)
на 16,1%. Отсюда рассчитываем выделение NaClOs в
737—-475 • 9,839 = 338 г из' 1 л щелока или ^737°° =46%.
203
Практическое уменьшение объема и выделение NaClo.i оо.п.пк
рассчитанных вышеуказанным методом, поскольку п отжатом
хлорате всегда остается часть неотжатой маточной жидкости.
Выделение NaCIO» при кристаллизации может быть увеличено
донасыщением маточного щелока хлористым натрием, поскольку, как видно из сравнения данных табл. 64 и рис. 82, маточный щелок не насыщен хлористым натрием.
На рис. 92 приведено влияние NaOH на содержание NaClOa
в уваренных щелоках, насыщенных NaCl при 70° и в маточниках при 10°. Маточные
щелока взяты как полученные кристаллизацией
при обычных условиях
(т.е. ненасыщенные NaCl),
так и донасыщенные
NaCl. Эти данные имеют
практический интерес,
поскольку щелок, поступающий на выпарку,
обычно содержит некоторое количество NaOH,
прибавляемого для предохранения выпарной
установки от коррозии
(стр. 346).
В табл. 65 приведены
данные о промывке хлората натрия 1-й кристаллизации на нутч-фильтре.
Промывка проводилась небольшими количествами воды из расчета примерно 3% воды от веса промываемой соли на каждую
промывку. Из приводимых данных видно, что 3—4 промывок
достаточно, чтобы уменьшить содержание NaCl до 0,1%. Содержание других растворимых примесей уменьшается ‘ соответственно уменьшению NaCl. Уменьшение содержания NaCl
ниже 6,1—0,15% уже проходит более медленно сопровождается вымыванием значительного количества хлората. При'
•3—4 промывках указанным . количеством воды вымывается
всего 5—6% промываемого хлората.
0 «О 10 30 40 30 W п м #о юо
С7 Содпо*они4 МаОн ё г//г.
Рис. 92. Влияние NaOH на содержание NaC103
в'натриево-хлоратных щелоках.
М промывок „
1
2
3
4
5
NaCl г/л промывных вод . . .
103
86
34
6,2
1.3,
о/о NaCl в промытом хло-
t
рате1
.1 -
0,49
0,21
0,09
0,07
0,0$
1 До лромывкр.хлорат натрия содержал 0,86% NaCl*4
• * * 1/ , \
204
В табл. G6 приведены данные о перекристаллизации хлората
натрия. Для опытов был взят непромытый хлорат натрия 1-й
кристаллизации, содержащий примеси: NaCl 0,53%, NaOH и
Na«COs 0,14% и NaaSOi 0,08%. Пи опыте 1 растворение хлората
производилось 'в воде, а при опыте 2 растворение хлората производилось в маточном щелоке от опыта 1. В щелок, приготовленный растворением хлората, прибавлялась разбавленная соляная кислота для нейтрализации NaOH и NazOOs.
Таблица 66. Некоторые данные по перекристаллизации
технического хлората натрия
J*
опы¬
тов
Горячий щелок (100—105°)
Состав хлората натрия
В °/о
Маточный щелок (5 -10°)
удельный
вес
состав в г/л
удельный
вес
состав в г/л
О
и
св
Z
О
я
Z
X
О
5
О
3
Z
С?
О
Я
Z
G
я
Z
X
О
я
Z
о
со
•В
«в
Z
6
0
я
Z
G
я
*
X
о
П
*
сГ
я
Z
1
2
1,549
1,546
990
9§0
4,3
9,7
1.4
1.3
0,8
1.7
99,95
99,92
0,03
0,06
иет
нет
следы
следы
1,411
1,408
664
628
5,9
12 2
0,16
0,11
\
1,1
2,1
Уменьшение объема щелока при 2-й кристаллизации больше,
чем при 1-й. Расчет уменьшения объема и количества выделившегося NaClOs при 2-й кристаллизации можно делать так, как
указано для 1-й кристаллизации (стр. 203)v Можно произвести
этот расчет так же, исходя из содержания №СЮз на 1 г воды,
содержащейся в горячем и холодном щелоке; надо узнать,'
сколько выделилось NaClOs, а отсюда рассчитать вес маточного
щелока, получающегося из 1 Iл горячего щелока, и, зная удельный вес маточного щелока, рассчитать его объем. Например для
опыта 1 табл. 66 содержание NaClOs равно 1,79 г на 1 г НгО
в горячем щелоке и 0,90 г на 1 г НгО в маточном щелоке. Поскольку количество воды не изменяется при кристаллизации, на
I г НгО выделилось 1,79 — 0,90 = 0,89 г NaClOs. Всего НгО в 1 л
горячего щелока было 552,5 г. Отсюда общее количество NaClOs,
выделившееся из 1 л горячего щелока, равно 552,5 • 0,89 =
, — 490 г/ или —ggg—=49,5%. Вес маточного щелока из 1 л
горячего щелока будет 1549 — 490=1059 г. Объем маточного'
щелока будет -рщ- = 0,75 от объема горячего щелока, т. е.
уменьшение объема при 2-й кристаллизации равно 25%.
В табл. 67 приведен состав хлората натрия (высушенного
в вакуум-сушилке при 70°), полученного на производственной
установке при каустическом методе производства при разном
составе щелоков, поступающих на кристаллизацию. Температура
конца кристаллизации была 5°. Кроме NaClOs и NaCl щелока
содержали NaOH и Nas80«. Выкристаллизовавшийся NaClOs отжимался от маточного щелока на центрофугах, а при опыте
205
2 дополнительно шромывался холодной водой в количестве 0,2 jr
на 1 кг хлората. Опыты 1 и 2 проведены со щелоком обычного
для данной установки состава. Опыт 3 проведен со щелоком
с повышенным содержанием NaCl, а опыт 4 проведен при повышенном содержании 'Na2S04.
Таблица 67. Состав технического х ората натрия
м
опытов
'•V.
Состав хлората натрия в °/0'
Состав щелоков до кристаллизации в ?/д
NaClO,
NaCl
NaOH
.N»»SO,
влага
нераство¬
рим.
остаток
NaClO,
NaCl
NaOH
Na,SO«
1
99,16
0,56
0,14
0,08
0,05
0,01
703
96
26
7
2
99,87
0,06
0,01
0,02
0,03
0,01
702
96
26
7
3
97,51
2,14
0,14
0,07
0,13
0,01
533
151
23
6
4
97,33
0,79
0,32
1,38
0,17
0,01
641
93
42
31
Из данных таблицы видно, что при нормальном составе щелока, поступающего на кристаллизацию (опыты 1 и 2), получается хлорат с незначительным количеством примесей, которое
сильно уменьшается промывкой. При щелоке, содержащем повышенное количество сульфата (опыр 4), часть последнего выделяется вместе с кристаллизующимся NaClOa (несмотря на то,
что маточный щелок далеко,не насыщен NaaSCU).
В табл. 68 приведены данные об изменении содержания влаги
(«увлажняемости») в химически чистом и техническом хлорате
натрия при хранении в Атмосфере, насыщенной влагой при 15—
20° (под колоколом с водой). Для сравнения приводятся также
Таблица 68. Изменение влажности (в°/п) хлоратов натрия
и калия при хранении в атмосфере, насыщ е,н ной парами
воды ,
Количество
суток
Хлорат натрия
Бертолетова соль техническая4,'
технический
химвч. чистый
I
№ 2/
нз |
№ 4
№ 5
*& 6
V
{
0
0,08
0,04
0,06
0,05
0,05
0,07
5
3,6
4Д х
4,8
5,0
0,68
0,73 *
10
5,4
6,3 г
8,1
3.6
0,99
1,01
ч 15 л
8,8
9.6
11,8
11,5
1,28
1,26
20^
11,3
12,0
14,1
13,8
1.47
1,43
25
13,6
14,8
16,4
15,9
1,63
1,56
30
15,9
’ 16,9
18,9
18,2
1,72.
% 1,64
40
17,9
19,7
22,9
24,0
1,82
1,71 .
50
20,3
21,2
26,7
27,1
1,94
1.77
60
23,0
23,9
30,9
*
31,8
2,0
1,81
Примечание. .При дальнейшем хранении пробы хлората натрия про;
должали поглощать власу, постепенно превращаясь в раствор.
206 Г
данные для технической бертолетовой соли. Необходимо отметить, что при хранении в обычных атмосферных условиях с относительной влажностью в 50—60% хлорат натрия отдавал
свою влагу быстрее и полнее, чем бертолетова соль, и в нем
оставалось не больше сотых долей процента влаги. После
сушки в течение 1—1,5 часа в вакуум-сушилке (рис. 65, стр. 134)
при 70° бертолетова соль с общим содержанием примесей
в 0,1% показывала при сушке при 190° 0,2—0,25% влаги, а хлорат натрия с содержанием примесей в 0,5% при тех же условиях показывал всего 0,06—0,10% влаги.
§ 13. Основные коэфициенты получения хлората натрия
Табл. 69 составлена соответственно схеме производства, показанной на рис. 87 (стр. 194). Количества NajSCb, NaCl и NaClOj
•в пп. 1—2 рассчитаны согласно уравнению (80). Принимаем
6%-ное увеличение объема при хлорировании (стр. 170) и
18%-ное увеличение объема при кристаллизации (стр. 203).
Объем щелоков, поступающих на выпарку, и количества NaCl и
NaClOs в них (п. 3) рассчитаны как сумма этих данных для хлорированного и маточного щелоков (пп. Ч и 5). Концентрация
NaCl в уваренном щелоке и NaClOb в маточном щелоке взяты
соответственно их растворимости (сТр. 187 и 188).
Практический объем щелоков и количества ШгСОз, Na’Cl и
NaClOe в них будут несколько иные, чем по табл. 69 — соответственно производственным потерям. Практический состав щелоков и их плотность не зависят от производственных потерь,
а только от правильности, режима работы.
На одном хлоратйом заводе, получавшем NaClOs каустическим методом (в общем идентичным содовому методу, см.
стр. 194), производственные потери были в пределах 10—13%,
что соответствует расходу 2,2—2,3 г хлора и 2,5—2,6 т NaOH
на 1 т NaClOs.
Понятно, что приведенные в табл. 69 соотношения количеств
уваренного и маточного щелоков (пп. 4 и 5) устанавливаются
постепенно по мере развертывания производства. При пуске
производства количества уваренного и маточного щелоков будут вначале меньше приведенных в табл. 69; так же количество
NaClOs, выделяющегося при кристаллизации, будет вначале
меньше 1 т. Количества, приведенные в табл. 69, устанавливаются, начиная с 9—10-го цикла производства.
Табл. 70 составлена соответственно 'схеме производства, показанной на рис. 86 (стр. 192). Количества СаО, Са(СЮз)г и СаСЬ
•в пп. 1—3 рассчитаны согласно уравнениям (37) и (63). Увеличение объема при хлорировании принимаем в 4,2% (стр. 68).
Выделение СаСЬ в виде гидратов принимаем в 65% (стр. 198) и
в виде оксихлоридов в'65% (стр. 200). Концентрацию СаСЬ в маточном щелоке пррле выделения СаСЬ • 6Н2О (п. 4) принимаем
в 470 г/л (стр. 198); концентрацию СаСЬ в маточном щелоке после, выделения оксихлоридов (п. 6) принимаем в 135 г/л (стр. 200).
' - ; ' 207
Таблица 69. Состав и количества производственных
растворов при получении NaClOj содовым методом
-
Состав в г/л
Количество в т 1
Плотность
В
с
Z
Какие растворы
■ а
X
£
о
м
о
Ч
я
z
NaClOj
NaCl
С*
О
Ч
я
г
NaClOj
б
Я
г
Удельный
вес
• Боме
Темпера¬
тура
1
Содовый раствор
14,9
200
2,98
1,18
22°
20°
2
Хлорированный
щелок ....
15,8
_
63
174
1,0
2,75
1,14
17,6°
60°
3
Щелока, поступающие на выпарку ....
18,14
по
167
2,0
3,04
1,17
21°
40°
4
Уваренный щелок
2,86
700
100
■2,00
0,286
1,50
48,1°
70°
3
Маточный щелок
1-й кристаллизации . . • •
со
с*
428
122
1,00
0,286
1,38
39,7°
0°
«
Разваренный щелок ®
2,05
1000
10
_
2,05
0,0205
1,55
51,2°
100°
7
Маточный щелок
2-й кристаллизации ....
1,64
640
12,5
1,05
0,0205
1,41
41,9°
10°
Ч'
1 Объемы и количества в тоннах рассчитаны на выделение 1 т NaClOj
при кристаллизации.
* „Разваренные щелока* обозначают горячий раствор хлората натрия,
поступающий на 2-ю кристаллизацию. *
Количество Са(СЮз)з принимаем неизменяющимся при выделении СаСЬ - 6НгО и оксихлоридов. Количества NaCl и NaClOs
в щелоке после обменной реакции (п. 7) рассчитаны соответственно количествам СаСЬ и Са(СЮз)2 в щелоке до обменной
реакции (п. 6). Объем щелока после обменной реакции взят согласно нашим исследованиям. Данные объема щелока, поступающего на выпарку {п. 8), и количества NaCl и NaClOs в нем
рассчитаны как сумма этих данных для щелока после обменной
реакции (п. 7) и маточника после кристаллизации NaClOs (п. 10).
Данные пп. 9 и 10 взяты те же, что в табл. 69.
Практически состав щелоков и количества хлората и хлорида
в них могут колебаться в широких пределах соответственно
производственным потерям.
В заключение приводим табл. 71, в которой сведены расходные коэфициенты и получаемые отходы при основных методах получения NaClOs химическим путем, исходя из суммарных
уравнений реакций, процессов производства. Для удобства
сравнения в таблицу включены также коэфициенты электролитического получения -NaClOs, описание которого будет дано
в гл. 20.
■208
чт«9»»*Щ-Ч1Т -wa Н
Таблица 70. Состав и количества производственных р*а с т в о р.о в при п оьл у-4ч е нви и №С10з
известковым методом по Печинею
•4
Состав в г/л
Всего тонн 1
Плотность
*
#
i '
*
Какие растворы *
а
Ж
С?
|
т
с?
a
5
4>
s
а.
а.
е я
1
О
т
и
О
О
€
л
О
У
Z .
NaCl
О
и
о
"т
О
СаС!
и
<9
Z
NaC
2s
О
ia
о
а с.
se-
•
1
Известковое молоко . . .
14,4
по
1,58
1,083
11°
20°
2
Хлорированный щелок
15,0
—
65
174
—
—
—
0,97
2,60
—
—
1.17
21°
40э
3
Уваренный кальциево-
хлоратный щелок . . .
4,33
224
600
—
-
—
0,97
2,60
—
—
1,50
48,1°
О
О
1—
4
Маточный щелок А после
выделения СаС1а*6Н20
1,93
—
500
470
—
—
—
0,97
0,91
—
—
1,61
54,7°
10°
5
Разбавленный маточный
щелок А -ж .
4,55
212
.2С0
—
—
—
0,97
0,91
—
—
1,29
32,5°
20°
6
Маточный щелок Б после
-
выделения оксихлори-
дов .
2,36
—
410
135
—
—
—
0,97
0,32
—
—
1,30
33,3°
10°
7
Щелок после обменной
реакции с Na2S04. . .
4,20
—
—
—
238
81
—
—
—
1,00
0,34
1,18
22°
40°
8
Щелок, поступающий на
выпарку
6,54
—
—
\
305
96
—
—
—
2,00
0,63-
1,19
23°
30э
9
/
Уваренный натриевохло-
рагный щелок ....
2,86
—
—
—
700
1С0
—
—
—
2,00
0,29
1,50
48,1°
70°
10
Маточный натриевохло-
ратный щелок
2,34
—
—
—
428
122
—
—
—
1,00
0,29
1,38
39,7"
0°
1 Расчеты объемов и количеств продуктов в тоннах
сделаны на получение I т NaC103 при кристаллизации.
Таблица 71. Теоретические коэфицненты получения КлСЮ*
разными метода
Расходуется
1
Получается 1
1
i
*
Какие растворы
т
и
о*
о
«Г
55
X
о
«4
55
О
«в
и
о
««
Z;
NaCl
О
О
«4
Z.
NaCl
о
о
X
т
G
«
и
о
(Л
я
и
1
Содовый метод .
2,0
2,98
1,00
2,75
1,24
2
Каустический метод
2,0
2,25
1,00
2,75
-
. _
3
Известковый метод по Либиху
2,0
1,58
4,0
1,00
2,75
1
3,83
4
Известковый метод поПечинею
2,0
1,58
1,08
1,00
0,89
1,69
1,03
5
Электролитический метод2 . .
—
-
—
—
0,55
1,00
—
0,056
—
—
1 Количества тонн продуктов на 1 т NaClOj.
* Не показана затрата электроэнергии (практически 6—7 тыс. квт-ч на 1 т
NaC10a).
Расчеты величин в табл. 71 сделаны, исходя из следующих суммарных
уравнений реакции получения NaC103:
1. 3Na,CO„ 4- ЗС1, = NaClO, + 5NaCl + 3C02;
2. 6NaOH + 3C12 = NaC103 + 5NaCl + 3H20;
3. 6Са(ОН)г + 6C12 + 6Na2S04 = 2NaC103 + 6CaS04 + lONaCl + 6H20;
4. 6Ca(OH)2 + 6C12 + (6—n) Na2S04 = 2NaC103 + nCaCl, + (6 —n) CaS04 +
+ (5 — n) 2 • NaCl + 6H20 (где n равно 4,385, т. e. 87,7% от 5 молей СаС1а,
образующихся при хлорировании).
' 5. NaCl + ЗН20 + 6® + 60 = NaCIO, + ЗН3.
Литература
Гмелин4-*1; Абегг®-*; Лунге®.
Также см. статьи автора в журналах:
Военная химия 1932 г., № 5—6, стр. 10—14. Химстрой 1933 г., Hi 5,
стр. 2239—2246. Ж. X. П. 1934 г., № 6, стр. 49-58 и 1930 г. № 31-33,
стр. 1911. / _
ГЛАВА 16
ХЛОРАТ БАРИЯ И ХЛОРАТ КАЛЬЦИЯ
, Хлорат бария
Основными потребителями хлората бария являются производства сигнальных составов, поскольку хлорат бария дает при
сгорании зеленый огонь. Хлорат бария применяют также для
получения большинства .других хлоратов путем обменной
'реакции с сернокислыми или углекислыми солями и для получения хлорноватой кислоты.' Хлорат бария применяется также
в красочной и вдекоторых других отраслях промышленности.
210
§ 1. Физические и химические свойства 1
Хлорноватокислый барий или хлорат бария образует моно-
клинические призмы состава Ва(СЮз)2 • Н20. Молекулярный нес
кристаллического хлората 322,3, а безводного Ва(СЮз)2 304,3.
Содержание кристаллизационной воды равно 5,6%. Содержание
кислорода в Ва(СЮз)г равно 31,5%, т. е. меньше, чем у КСЮз
(39,16%) и чем у NaClOe (45,1%). Обезвоживание хлората бария
происходит при 120°. Удельный вес Ва(СЮз)г • Н20 2,988—3,179 2.
Температура начала разложения обезвоженного хлората
300—310° *. При этой температуре* выделяется 11 % кислорода
с образованием перхлората и хлорида:
2Ва(СЮз)2 = Ва(СЮ4)2 + ВаСЬ + 202. (91)
•
Кроме того образуются также следы ВаО, т. е. выделяется и
хлор. Дальнейший нагрев разлагает и перхлорат.
При быстром нагреве или ударе хлората бария в смеси с горючими веществами происходит взрыв.
Теплота образования Ва(СЮз)2Н*0 из элементов равна но»
Томсону 77,570 ккал. Теплота растворения в 600 молях Н20
равна минус 11,240 ккал.
В воде хлорат бария растворяется больше, чем КСЮз, но
меньше,'чем NaClOs (см. табл. 77). 4
По Этарду растворимость Ва(СЮз)2 в пределах температуры
от 0 до 100° рассчитывается по формуле:
% Ва(СЮз)2 = 19 + 0,382 Т°.
В табл. 72 приводим данные о растворимости Ва(СЮз)2 при
0—105,6°.
'Таблица 72. Плотность и концентрация растворов Ва(СЮ,)3
насыщенных при температурах от 0 до 105,6°34-5
4
Температур!
Плотность
Ba(CIOe)t
Удельный вес |
"Боме
г\л раствора
°/о
*/** н,о
0
1,195*
23,5
229
19,2
236 а
10
1,234
27,4
284
23
298 '
20 ,
1,274
31 ,
339
26,6
363
30
1,315
34,6
398
30,3
435
40
1,355
37,8
459
33,9
513
-50
1,395
40,9
51%
37,2
592
60
1,433
43,6
576
40,2
672
70
1,470
46,1
629
42,8
748
80
1,508
> 4*,6
683
45,3
828
90
• 1,545
51,1
738
47,8
915
100
1,580
53
792
50,1
1004
105,6
1,600
54,1
824
51,5
1062
1 Приводимые данные о свойствах1 хлората бария взяты из Абегг 6—2
и Гмелин 4г“80.
• По данным разных авторов. 1
i
14*
211
Приводим также данные о системе Ма(СЮа)--|-BaCU 4* IW*
при 20° по Gass, 58, 1928, 250 (Гмслин 4_30).
% Ва(С10а)з. . .
0
5,20
8,80
12,30
16,50
18,13
21,08
23,04
23,76
% BaClj ....
21,34
20,55
20,46
18,77
16,03
16,67
14,42
6,56
0
% нго
7 8,66
74,25
70,74
68,93
66,87
65,20
61,50
70,40
76,21
7*
Температура кипения насыщенного раствора Ва(СЮз)з равна
111°. -В спирту хлорат бария трудно растворим. По Агсру2*
(т. 1, стр. 751) в горячем спирту растворяется 1 :35, а в холодном спирту 1 :400 частей. Понижение упругости ларов растворов Ва(С10з)з равно при 100°
Ва(СЮ8)2 моль/л
0,5
1
2
3
а мм Hg
15,8
33,3
70,5
108,2
§ 2. Получение хлората бария из бертолетовой соли
1. К раствору КСЮз прибавляют HsSiFe. Получающийся оса-
• док K2SiFe отфильтровывают. Фильтрат, содержащий НСЮз, нейтрализуют прибавлением ВаСЮз. Полученный раствор Ва(СЮз)з
концентрируют, после чего при охлаждении выделяются кристаллы Ва(СЮз)г • НгО.
2. Смешивают 1000 г измельченного сернокислого глинозема
с 160 г серной кислоты и 160 г воды. Смесь охлаждают и прибавляют понемногу (небольшими количествами) при перемешивании 370 г КСЮз. К полученной массе прибавляют воды до
консистенции жидкой кашицы и подогревают на водяной бане
до 35° (но не выше 40°). Обменная реакция происходит по следующему уравнению:
2КСЮз 4- Al2(SO«)s 4- H2SO4 = A12(SO«)s • K2S04 4- 2.НСЮ3. (92)
Оставляют на 30—40 мин., после чего охлаждают и понемногу прибавляют при перемешивании 2,5 объема спирта. Дают
отстояться осадку АЦБОфКгЮ*, сливают раствор и промывают
осадок 1,5 объемами 60%-ного спирта. Снова сливают раствор
и отфильтровывают осадок через стеклянную вату (но не через
бумагу).
К спиртовому раствору НСЮз прибавляют 350 г Ва(ОН)г и
еще раствора Ва(ОН)г до щелочной реакции.' Образовавшийся
осадок BaSO« отфильтровывают, а раствор упаривают до полной
отгонки спирта. При кристаллизации получается около 475 г
Ва(СЮз)*Н*0 (по Агеру**).
212
3. По Ванино 22 хлорат бария получают из KClOj следующим
образом: 3 части (NH^SOi и 5 частей КСЮз растноряют
в 15 частях, горячей воды и упаривают до кашицеобразной
консистенции. Охлаждают и прибавляют 4-кратный объем
80%-ного спирта. Отделяют фильтрацией выделившийся осадок K2SO4, который промывается 80%-ным спиртом. Из
фильтрата отгоняют спирт, к водному раствору прибавляют
Ва(ОН)г до сильно щелочной реакции и нагревают до
удаления запаха NH3. Получаемый при этом сухой остаток растворяют в воде, через раствор пропускают СОг для осаждения
избытка Ва(ОН)г. Отделяют осадок ВаООз, а раствор упаривают
для кристаллизации хлората.
§ 3. Получение хлората бария из хлората натрия
На рис. 93 показана разработанная автором схема получения
хлората бария, исходя из обменной реакции NaClOe и ВаСЬ. Из
технического хлористого бария приготовляют раствор, насыщенный при 20—25°. Полученному раствору дают отстояться от
нерастворимых примесей, затем его декантируют и подогревают
до 60—80°. В горячий раствор вносят хлорат натрия из расчета
150—200% от количества, теоретически соответствующего содержанию ВаСЬ. При охлаждении полученного щелока выделяется
большая часть Ва(СЮз)г в виде кристаллов Ва(СЮз)г • НгО. Выделившуюся соль отделяют от маточного щелока на центрофугах
или нутч-фильтрах. Полученная соль содержит по 2—3% NaCl и
NaClOs. Промывкой на нутч-фильтрах можно получить продукт,
содержащий ПаСЮз и NaCl по 0,1—0,2% (0,2—0,3 л промывных
вод на 1 кг соли). .Если нужен еще более чистый продукт, производят перекристаллизацию.
Оставшийся маточный щелок, содержащий NaCICb, NaCl и
Ва(СЮз)г, упаривают до удельного веса 1,45—1,50. Во время выпарки выпадает большая часть NaCl, бывшего в маточном щелоке. Выделившуюся NaCl отделяют и промывают на нутч-
фильтрах от уваренного щелока, после чего она представляет
собой отход производства. Промывные воды поступают обратно
на выпарку. Уваренный щелок охлаждают; выделяется смесь
NaClOs и Ва(СЮз)г • НгО, которую используют для новой обменной реакции. Маточный щелок поступает обратно на выпарку.
Если хлорат бария получают на заводе, основной продукцией которого является хлорат натрия, то возможна иная схема
переработки маточного щелока с целью избежать необходимости в установке для упаривания щелоков, содержащих
Ва(СЮз)г. Для этого осаждают из маточного щелока барий
в виде 'BaSC>4 путем добавления теплого раствора Na2SC>4 и оставшийся раствор, содержащий NaClOs и NaCl, используют в производстве хлората натрия. Полученный BaS04 является ценным
отходом. Уравнение обменной реакции будет:
ВаСЬ + 2NaCKDs = Ва(СЮз)* + 2NaCl.
(93)
Выделение Ва(СЮз)г происходит ввиду меньшей его растворимости (молярной), чем NaClOa, BaCl* и NaCl (рис. 94). Обмен¬
ную реакцию можно производить также, прибавляя NaClOa
к холодному раствору ВаСЬ. Однако получаемые при этом кристаллы . Ba(CIOa)t*. HtO настолько мелки, что их весьма трудно
214 /
Рис. 93. Схема получения хлората бария, исходя , из обменной реакции ВаС12 + 2NaC10j = Ва(С103)2 -f- 2NaCl.
l?r>0 n
Рис. 94. Растворимость Ba(C10j)8i NaC10e, ВаС1а и NaCl в воде при ; 0—100°.
I
Рис. 95. Влияние NaC108 на раство* Рис. 96. Кристаллизация Ва(СЮ8)а из '
римость Ва(С10з)2. J растворов, содержащих NaCl и NaClO*.
215
отделить и промыть от маточного щелока. Концентрация С л
в щелоке после обменной реакции нс должна превышать
3,1 экв/л, иначе при кристаллизации выделяется также и часть
хлорида. Концентрация NaClOa не должна превышать 4,8—
5,0 экв/л во избежание выделения части NaClOa при кристаллизации.
На рис. 95 показано влияние NaClOa на растворимость
Ва(СЮз)г в воде и в растворе NaCl при 5, 20 и 25°. На рис. 96
показан ход кристаллизации Ва(С10з)г при охлаждении от 80
до —10°.
§ 4. Известковый метод получения хлората бария
По Печинею • хлорат бария может быть получен путем
обменной реакции горячего раствора ВаСк с подогретым
маточным щелоком, получаемым после выделения большей
части СаСк. По охлаждении выделяется хлорат бария с примесью 10% ВаСЬ, от которой освобождаются перекристаллизацией. Маточный щелок не содержит солей бария, но содержит
еще часть Са(СЮз)з, которую используют для получения КСЮ*.
или NaClOa. По нашим данным выделение Ва(СЮз)« • НгО проходит лишь при концентрации СаСк в щелоке после обменной
реакции не свыше 2 экв А; при большей концентрации СаСк
при охлаждении выделяется ВаСк.
§ 5. Получение хлората бария хлорированием баритового
молока
Имеются также указания на получение хлората бария, исходя
из хлорирования баритового молока с последующим разделением путем выпарки и дробной кристаллизации Ва(СЮз)г и
ВаСк, полученных при хлорировании (А. Р. 1391858, Е. Р. Schochj.
Уравнение получения Ва(СЮз)г этим методом будет:
, 6Ва(ОН)з + 6CkN= Ва(СЮз)* + 5ВаСк + 6НЮ. (94)
Получаемый при этом методе хлористый барий является
весьма ценным отходом, окупающим расход Ва(ОН)г. Недостатком этого метода является малое распространение в природе ВаО
и ВаСОз, являющихся исходным сырьем при этом методе производства. По нашим данным при хлорировании раствора
Ва(ОН)з происходит более значительное выделение Ог, чем при
хлорировании Са(ОН)г, NaOH и т. д. Разделение Ва(СЮз)г и
ВаСк благодаря их близкой растворимости представляет значительные трудности.
Примечание. Метод получения хлората бария электролизом см. стр. 283.
S 6. Основные коэфициенты получения хлората бария
Табл. 73 составлена соответственно схеме производства, показанной на рис. 93. Количества Bad*, NaClOs, Ва(СЮз)г и NaCl
в растворе ВаСк и в горячер* щелоке после обменной реакции
(пп, 1 и 2) рассчитаны согласно уравнению (93) с учетом при-
216
бавлсния при обменной реакции 80% избытка NaClO.-t и остатка
и маточном щелоке (и. 3) 25% хлората, содержавшегося » щелоке
до кристаллизации (п. 2). Концентрация раствора ПаСЬ (н. 1)
соответствует насыщению при 20°. Исходя из наших практических данных, принимаем 31% увеличения объема при обменной реакции и 18% уменьшения объема при кристаллизации.'
Таблица 73. Состав и количества производственных растворов при получении Ва(С10а)4 методом обменной реакции
NSClOj с ВаСЬ
«9
Состав ив г/л
Всего тонн 1
Плотности
i
%
Какие растворы
Объем в м
т
9
со
а
G
'«в
m
NaCIO,
G
«
й
*1
G
<4
CQ
|
*
CQ
NaCIO,
NaC! j
Удельный
вес
° Боме
Темпера-
1 тура
1
%
Раствор ВаС12 •
2,76
330
0,913
_
1,28
31,5
20°
2
Горячий щелок
после обменной
реакции . .
3,62
369
206
142
1,333
0,747
0,513
1,47
46,2
80°
3
Маточный щелок
после кристаллизации . . .
2,96
— -
113
252*
173
— ‘
0,333
0,747
j
0,513
1,32
35
1?о
1 Расчеты объемов и* количеств продуктов в тоннах сделаны па 1 т
Ва(С103)2, выделяющегося при кристаллизации.
1 Утилизация хлората, остающегося в маточнике, см. стр. 213.
В табл. 74 приведены расходные коэфициенты и получаемые
отходы при получении .хлората бария хлорированием Ba(OH)i,
методом из NaCIOs и ВаСЬ и электролитическим методом.
Таблица 74. Теоретические коэфициенты получения хлората
бария р-азными методами
Расходуются 1
Образуются 1
с
с
*
Метод производства
т
9
в
О
G
£
Л
X
ъ
т
G
*
G
в
9
Z
•«
G
«в
в
£
1
Электролитический
0,039>
2
метод *
Метод, исходящий
из хлорирования
0,684
1,0
«г
3
Ва(ОН>2 ......
Метод, исходящий из
—
—
3,38*
1,40
1,0
3,42
—
NaClOe
0,684
0,70
““
1,0
0,384
1 Количества тонн продуктов на 1 т Ва(С103)2.
* Не показана трата электроэнергии, практически равная 5—7 т квт-ч»
на 1 т Ва(СЮ,)*.
Расчеты данных таблицы сделаны, исходя из следующих суммарных уравнений реакции получения Ва(СЮ|)г:
1. BaCU + 6Н,0 + 1204-120 = Ва(СЮа), + 6Н2;
2. 6Ba(OH)j + 6CU = Ва(С10Л + 5ВаС1, + 6HjO;
3. BaClj+2NaClO, = Ba(C10l)g + 2NaCl.
%U
Литература
А б е г г e-s; Ульман г,_2; Д а м м е р 1; Г м е л ни П е ч и н с I! *;
Агер a_l; Ванино82; Лунгс3; англ. пат. 1391858 (1920); герм. нат.
89844 (1906).
Хлорат кальция
Из всех хлоратов, получаемых химическими методами, наиболее дешевым должен быть хлорат кальция, поскольку на его
изготовление тратится кроме хлора только известь, являющаяся
самой дешевой и доступной щелочью. Однако получение хлората кальция в виде готового продукта наталкивается на ряд
трудностей, почему до последнего времени хлорат кальция применялся- лишь как промежуточный продукт (в виде хлорированного щелока) для получения КСЮз и отчасти NaClO.-» путем
’обменной реакции с солями калця или натрия. Основная трудность получения Са(СЮз)г заключается в отделении его от '
СаСЬ, с которым он совместно получается при хлорировании.
Кроме того хлорат кальция обладает большой гигроскопичностью и сравнительно низкой температурой разложения.
Последние годы в иностранных специальных журналах появился ряд патентов на средства борьбы с сорняками (гербесиды)
на железных дорогах и в земледелии. Основным действующим
веществом в гербесидах является Са(СЮз)г. При этом для устойчивости и облегчения производства, а также из патентных соображений эти средства содержат кроме Са(СЮз)г еще СаСЬ, NaCl
и другие индиферентные вещества.
:В условиях СССР при большой длине наших железных дорог
область применения хлоратов как гербесидов огромна, и вопрос
сводится только к стоимости, простоте производства и устой-
/ чивости данного продукта.
$ 7. Физические и химические свойства хлората кальция (по
Абеггу 6-2 и Гмелину 4_28)
Хлорноватокислый кальций образует моноклинические или
ромбические кристаллы с двумя молекулами кристаллизационной
воды Са(СЮз)г • 2НгО. Молекулярный вес Са(СЮз)г равен 207.
■ Эквивалентный вес в реакциях окисления равен 17,25. Са(СЮз)г
содержи^Са = 19,3%, хлора 34,3% и кислорода 46,4%.
При быстром нагреве кристаллы плавятся в своей кристаллизационной воде, образуя при застывании стекловидную массу,
показывающую при растворении щелочную реакцию. При 290°
jtfApaT разлагается со взрывом. Безводная соль разлагается при
' 340°.1 При медленном нагревании до 110° удается получить безводный Са(СЮз)г, который при дальнейшем нагреве выделяет
кислород и следы хлора. Данных о теплоте образования
Са(СЮз)г из элементов в литературе нами не найдено. По нашим
Жданным она равна примерно 168,2 ккал. Растворимость Са(СЮз)г
1 По данным ГИПХА (Ж. X. П. № 4, 1934 г.).
\ 218 '
в иоде весьма. большая. При 18° насыщенный раствор имеет
удельный вес 1,729 (60,8° Боме) и содержит Са(СЮя)2 04%, или
1110 r/л раствора, или 1780 г/кг НгО; при 100' растворимость
Са(СЮз)г равна 78,5% *. ра(СЮз)г также хорошо растворяется
в спирту. Спиртовый раствор горит красивым красным пламенем.
В табл. 75 приведена плотность, растворов Са(СЮз)з разной концентрации.
Таблица 75. Плотность растворов Са(Cl03)j при 18° 2,-г’
Са (СЮ,),
ПЛ01 (ГОСТЬ
Са (С10|)9
Плотность
°!о
г/4
Уд. вес
°Боме
°/о
г/л
Уд. пес
®Боме
2
20,3
1,0135
2Э
18
206
1,1469
18,4°
4
41,1
1,0288
40 /
20
233
1,1656
20,5°
/ 6
62,8
4 1,0444
' 6,25
22
261
1,1848
22,4°
8
84,8
1,0604
8,За
24
, 289
1,2045
24,4°
* 10
107,7
1,0768
10,3°
26
' 318
1,2247
26,5°
12
131,2
1,0936
12,3°
28
348
1,2454
28,5°
14
155,5
1,1109
14,4®
30
380
1,2665
30,4°
16
180,5
1,1286
16,4°
ч
■Как и другие хлораты» Са(СЮз)г — физиологический яд. Его
свойство убивать протоплазму используется для борьбы с сорняками.
* »
§ 8. Способы получения хлората кальция
В лабораторных условиях хлорат кальция может быть получен нейтрализацией раствора НСЮз прибавлением Са(ОН)г или
порошка СаООз с последующей выпаркой полученного раствора
•Са(СЮз)2 на водяной бане. И. Б. Фрайман разработал способ
.получения продукта, содержащего Са(01Оз)г с небольшой примесью СаСЬ, кристаллизацией из уваренного маточного щелока,
полученного после выделения большой части СаСЬ по Печинею
(стр: 34). Нами разработан способ получения твердого продукта, содержащего 25—27% Са(СЮз)г. Схема этого способа показана на рис. 97. К подогретому до 90—100° маточному щелоку,
полученному после выделения большей части СаСЬ по Печинею
(стр. 34 и 197), прибавляют при. энергичном перемешивании
измельченную известь из такого расчёта, чтобы количество СаО
равнялось 60% от суммы количеств Са(СЮз)г и СаСЬ. Происходит гашение извести с испарением части воды. Продолжают некоторое время перемешивание, отчего масса покрывается твердой и хрупкой коркой и отстает от стенок реакционного котла.
После полного остывания затвердевшую массу измельчают и
> По данным ГИПХА (Ж.'х.
/
Л. № 4, 1934 г.).
219
сушат. В высушенном массе остается 14—15% и,uni, uu иаш.,.
в виде гидратнон воды. Сушку можно производить и храпением
в открытом виде на воздухе с относительной влажностью не
больше 50—60%. Кроме Са(СЮя)г и влаги продукт содержит
СаСЬ и СаО. Продукт этот имеет порошкообразную форму, не
Маточник посла ёыдолчния Узмелбчепнаа избшстё
Рис. 97. Схема получения продукта, содержащего 25—27% Са(СЮ3)2.
слеживается, мало гигроскопичен, не взрывчат и не разъедает
тары при обычных условиях хранения. Состав продукта до и
после сушки показан в табл. 76.
Таблица 76. Состав продук та, с о д е р ж а5ц его 25— 27% Са(СЮ3)2
•/о СаО
«/о СаС1,
®/о 08(00,),
°!о Н,0
4* примеси
Продукт до сушки
' 26,2
20,2
21,7
31,9
Продукт, высушен- [ 2 часа .
32,1
24,7
26,6
16,6
ный при темпе- <
ратуре 105° 1 2 сут. .
32,3^
24,9
26,?
16,0
— щ
а - — ■ ■ ■
•
1 CaSO«, СаСО» и т. д., всего 1—2%.
§ 9. Некоторые коэфициенты получения хлората кальция
При хлорировании известкового молока согласно уравнению 37 (стр. 59) получаются следующие коэфициенты на 1 г
Са(СЮа)*:
Расходуются: ' *
6СаО __ _ 1 со m р.л
Ca(C10j)a~“ 207 1,62/Я СаО >
и.
6С ' 70,92 Л
— —> 2,06 т хлора.
Са(СЮз)з 207
Получается в виде отхода
= -УД — 2,68 т CaCL.
Са(СЮ,)2 207
229
Исходя из метода получения твердого хлората кальции
в виде смеси с известью и СаС1г (§ 8), выводим следующие
коэфициенты на 1 г СА(СЮз)г:
Расходуются СаО 2,7 т и хлора 2,06 т.
Получается отход в 1,88 т СаСЬ в виде СаСЬ • 6НгО.
Готовый продукт получается в количестве 4,3 т до сушки и
.3,5 т после сушки.
I Литература
\
А б je гг*—*; Ульман*-*.*; «Гм ел им*-**; Ж.Х.П. № 4, 1934 г.
ГЛАВА 17
ХЛОРАТЫ ДРУГИХ МЕТАЛЛОВ, ХЛОРНОВАТАЯ КИСЛОТА
Как уже указывалось, наибольшее применение имеют хлораты
К, Na, Ва и Са. Другие хлораты ввиду их малой устойчивости
и трудности изготовления применяются редко и в сравнительно
небольших количествах. Получение этих хлоратов основано
обычно либо на обменной .реакции соответствующих сульфатов
или карбонатов с раствором Ва(СЮз)г, либо растворением окисей
или карбонатов в растворе НСЮ».
Ниже приводим данные о хлоратах большинства металлов,
располагая их соответственно периодической системе элементов.
§ 1. Хлораты лития, рубидия, цезия, меди, серебра, аммония
I. Хлорат лития 1 ЕлСЮз. Раствор LiClOs может быть получен
внесением сульфата или карбоната лития в раствор Ва(СЮз)з
или нейтрализацией раствора ЫСЮз окисью или карбонатом
лития. Полученный раствор сгущают, отчего из него выделяются
кристаллы хлората лития. При сгущении на водяной бане выделившийся хлорат содержит примесь хлорида вследствие частичного разложения ЫСЮз. При сгущении над серной кислотой
под вакуумом при комнатной температуре выделившийся хлорат
не содержит примеси хлорида. Кристаллы, выделившиеся при
50° и выше, не содержат гидратной воды; при кристаллизации
при более низкой температуре выделяются кристаллы состава
LiClOs • ViHjO и LiClOs • УзНгО. При сушке при 55° и выше
гидрат переходит в безводный LiCIO». Последний плавится при
124° и начинает разлагаться при 140°. Однако до 270° разложение LiClOs весьма незначительно, и до 323° выделяется всего
1 Библиография см. Г We л и и *-*>; Абег'г*—*;
цинш.
\ ; • ’
СТЭ **—5,6; п О т Ы Л И-
fcn
i
~3% кислорода. Максимум кислорода выделяется при 41Г> —
416°. При разложении ЫСЮз сначала образуется перхло|)ат (см.
стр. 22), который при дальнейшем нагреве также разлагастсй.
Кроме кислорода при разложении LiClOa выделяется также немного хлора, а в остатке после разложения содержится кроме
LiCl также небольшое количество L12O.
Кристаллы хлората лития весьма гигроскопичны; при хранении в открытом виде они в одну минуту поглощают влагу в количестве до 1Уг% от своего веса (Z. anorg. Chem. 155, 1926, 311).
Растворимость УСЮз весьма большая. Раствор, насыщенный
ЫСЮз при 18°, содержит 75,8% УСЮз, что равно 3,135 г ЫСЮз
на 1 /1 НзО, или 1 моль ЫСЮз на 1,6 моля НгО. Такой концентрации при 18° не имеет ни одий раствор другой неорганической
соли. В спирту ЫСЮз также хорошо растворим; спиртовые растворы 1лСЮз сильно взрывчаты.
Приводам некоторые свойства водных растворов ЫСЮз.
Удельный вес растворов UCIO3 и
*>/о Li СЮ,
‘1
1 2 1
I-«1
1 6 1
1 8
10
12
14 |
1 18
, 18 1
138,1 |
76,8
dj*
1,0048
1,0111
1,0237
1,0365
1,0495
1,0628
1,0764
1,0903
1,1045
1,1190
1,2921
1,815
Понижение те м'п ературы замерзания растворов
LiClOg «-6 и иг
Молей ЫС10а на 100<j> .молей Н,0 | 2 | 2,5 | 3,0 | 3,5 | 4,0 | 4,5
5,0 | 5)5 | 6,0 | 6,5
Молярная депрессия
4,42
4,49
4,61
4,80
5,02
5,26
5,50
5,72
5,94
6,18
Эквивалентная электропроводжгсть растворов LiCl03
при 25° в-г •
Литров НаО на 1 моль UC10*
33 |
6* |
128 |
266 |
512 |
1024
Эквивалентная электропроводность
в обр. омах . .
91,5
94,2
96,8
99,4
100,4
. 101,5
Коэфициент внутреннего трения « при 25° для растворов
LiClOg
Эка/л |
1 Ч» 1
. 8,60 |
'6,45 |
; ю,5
15,1
т
0,01033
0,01270
0,02118*
0,08263
0,5373
Теплоемкость с растворов LiC103 при 18° 4
-20
Экв/л
0,5 ' |
| 1,0
| • 3,0
4,0
с
0,9582
4 •
< Ч
0,9204
0,8511
0,7906
0,7860
2. Хлорат рубидия1 RbClOa. Мол. нес 168,9. Растнор КЬСЮз
получается ннесением Rb2SC>4 в раствор Ва(С10я)2. Хлорат рубидия образует безводные кристаллы уд. веса 3,19. При сильном
нагреве RbClOa разлагается на RbCl и 02. Переходным продуктом
разложения RbClOa является RbClOa Приводим растворимость
RbClOa в воде при разной температуре и уд. вес растворов
RbClOs при 19,5°.
Растворимость RbC103 вводе при разной темпера-
\ туре 28-6 « юн
Температура |
°* |
1 10* 1
1 1
30
40е |
50е |
60е
70е |
1 «• 1
| <ю° |
100*
Молей RbC108 на 1000 г
. Hjp-
0,127
0,201
0,319
0,474
0,680
0,946
1,32
1,75
2,26
2.88
3,82
«/о RbQ08
2,1
3,3
5,0
7,4
10,3
13,8
18,4
22,8
27,6
32,7
39,3
Удельный вес растворов RbClOg * ui
°/о RbCIO, |
1
2
3 1
4
rfi9’5
1,0057
1,0122
1,0192
l;0260
Эквивалентная электропроводность раствора, содержащего
1 моль RbClOa на 1024 J воды, будет при 25° 144,2 обр. ома.
Хлорат цезия2 СвСЮз. Мол. вес 216,27. CsClOs получается
внесением CS2SO4' в раствор Ва(СЮ*)г.- Хлорат цезия образует
безводные кристаллы уд. веса 3,57. Приводим растворимость
CsClOs в воде при разной температуре и уд. вес растворов
CsClOs при 19,5°.
Растворимость CsClOg вводе п р ит р а з н о й т е м п ejp а- ■*
туре 6 и 106
Температура |
°* 1
1 10* 1
20°
30е
40е |
50*
60е |
70* |
80е
90е
100е
Молей СзСЮ8 на 1000 г
НвО .........
% CsClOj .......
0,114
0,178
0,293
0,445
0,642
0,900
1,21
1,58
2ДЗ
2,81
3.64
2,4
3,7
6,0
8,8
12,2
16,3
20,8
25,5
31,6
37,8
43,1
Удельный вес растворов CsClOs 2з~б и 111
»/, СвСЮ, |
1 1
2 1
3
4
5
rf}9-5
1,0057
1,0132
1,0208
1,0285
1,0363
Эквивалентная электропроводность раствора, содержащего
1 моль RbClOs на 1024 л воды, равна 147 обр. ома.
1 Библиографию см. Абегг*-*; СТЭ2*-5*6.
библиографию см. Абег^*-*; СГЭ2*-*.*.
223
Растворимость Си (СЮ3)3 в воде при разной температуре 2з-6 й 91
еч
0
r-ito
N
-t to
г-н Ь-
-t*
<п
a> r-
<о
o^aT
со
h
Х'У
cKco
00
CO V
00
ь
1-H CO
к
& oq
t^oo
со
h
N м
CO
СЧ
о
со ^
<°‘8
о
CSO>
•
о
J
’ 00 Ю
U0t^“
to
' . ■
00
*
ю со
«в
'So •
О.
£
0£ • •.
О.
U j*>
■ в
ЛоО
д
°8u
ggo
S/,*3r
#
224
S
4. Хлора г меди
с?
&
СЧ
Си(СЮя)2. Мол. пес
г—<
230,49. Си(СЮ,)2 полу¬
со
чается при взаимодей¬
Я
о>
со
сч
ствии CuSOi с раство-
Г-Н
ром Ва(С10з)г; также
о
можно получить рас¬
8
-г
00
твор Си(СЮз)г нейтра¬
1—»
лизацией раствора
НСЮз окисью или кар¬
00
СП
сч
СО
бонатом меди. Раствор
1—»
Г-Н
Си(СЮз)г имеет голу¬
бовато-зеленый цвет.
со
г+*
По Wachtler’y при кон¬
гН
центрации раствора
—
Си(СЮз)г под ваку¬
S
<м
умом над серной кис¬
л
V*
сч
лотой выделяются тем¬
i
00
1
1-4
нозеленые кристаллы
A
в-
Си(СЮз)г • бНгО, на
6
**
§
воздухе расплываю¬
и
Г-Н
щиеся. Точка плавле¬
3
KJ
С-
ния этих кристаллов
n
о
3
0
равна 65°. При 100°
о ,
Q.
г-н
кристаллы начинают
О
ш
н4
разлагаться (с выде-
о
СО
С--/
S
\ лением кислорода,
си
00
<§
хлора и хлорокиси).
о
4>
п
.
По данным Meusser’a
«3
05
кристаллы хлората ме¬
2
S
со
о
ди представляют со¬
•0
5
1—г
бой четырехводный
£
оо
гидрат с температурой
1-Н
плавления в 73°.
2
г-н
Теплота образова¬
ния Си(СЮз)г в раз¬
S
бавленном растворе
е«
»—t
О.
равна по Бертелло:
*-•
Си -f 2С1 -f 60 + aq =
ао
= Си(С10з)г aq -f-
+ 28,6 к кал.
*-н
Приводим раствори¬
мость Си(СЮз)г в воде
при разной темпера¬
^2
туре и уд. вес раство¬
о
0
ров Си(СЮз)г при 18°.
в
у
в
о
1 Библиографию си.
{
А б е г г *-ч Мел-
>
4
1
лор *•-«; СТЭ 28-5,6.
I
Понижение температуры замерзания раствора, содержащего
2,106% Си(СЮз)г, равна 0,485° (молярная депрессия = 58,1°)
(Mcusser »1).
Основной хлорат меди. При ' обработке раствора
Си(СЮз)г едким кали или едким натром выпадают малорастворимые голубоватые моноклинические призмы уд. веса 3,55
состава 4СиО • СЬОг, • 3HzO, т. е. Си(СЮз)г • ЗСи(ОН)г. Эта соль
получается также при электролизе раствора КСЮз, подкисленного H2SO4, переменным током между медными электродами.
В разбавленной азотной кислоте соль хорошо растворима без
разложения — в растворе не образуется мути от прибавления
AgNOs. Раствор соли в разбавленной соляной кислоте пахнет
хлором.
Комплексные аммиачные соединения. Образуются пропусканием NH3 в насыщенный водный раствор
Си(СЮз)г, прибавлением спиртового раствора NHs к водному
раствору Си(СЮз)2, нагревом хлората меди в струе аммиака
и т. д. Эти соединения легко взрываются от удара.
Си(С10з)в • 4NHs образует кристаллы в виде голубых игл уд.
веса 1,81, мол. объема 164,9. Теплота образования Си(СЮз)г •
. 4NH3 равна 15,0 ккая. Упругость диссоциации этой соли равна
36 мм при 97°, 55 мм при 116° и 715 мм при 158°. При нагреве
в открытой трубке соль взрывает .при 208°, при нагреве в закрытой трубке соль взрывает при 289°.
Си(С10з)г • 6NH3 образует густо голубые кристаллы. Теплота
образования Си(СЮз)г • 6NH3 равна 9,8 ккая. Упругость диссоциации этой соли равна 201 мм при 15°, 286 мм при 1°, 380 мм
при 10°, 491 мм при 20° и. 628 мм при 31°. При нагреве в открытой трубке соль взрывает при 201°, а в закрытой трубке при
249°.
5. Хлорат серебра1 AgClOs. Мол. вес 191,34. AgC103 получается растворением окиси серебра в растворе HClOs, а также
при хлорировании водной взвеси Ag20 или AgsCOs (при хлорировании выпадает в осадок образующийся AgCl, a AgClOj
остается в растворе). По Гендрихсону (Hendrixon) AgClOs получается при обработке тонкоизмельченного металлического
серебра раствором НСЮз по Уравнению:
6Ag + 6НСЮ3 = AgCl + 5AgC10p + ЗН2О. (95)
Хлорат серебра существует в двух модификациях:, а) устойчивые, белые, непрозрачные тетрагональные призмы; уд. вес
кристаллов равен 4,40—4,44 (при 23°); отношение осей а : с равно
4 1:0,9325; б) неустойчивые кубические кристаллы уд. веса 4,21.
Устойчивая модификация AgClOs не изменяется при хранении
в открытом виде как в сухой, так и во влажной атмосфере.
В воде AgClOs сравнительно с большинством других хлоратов мало растворим. В спирту AgClOs хорошо растворим.
1 Библиографию см. Абе гг*—•; М е л л орСТЭ*8-*••.
. 15 Зм. 171. — ШрМЬбтк.
226
Приводим растворимость AgClOs в воде при равной температуре, уд. вес растворов AgClOs при 16° и молярную электропроводность растворов AgClOs при 25°.
Растворимость AgC103 в воде при разной темпе-
р а т у р е 28-6 и Ю7
Температура
0е
10*
20е
40е'
60е
80е j 100е
Мелей AgClOs на
1000 г НаО....
«/о AgClOs
0,0097
0,18
0,0165
0,31
0,0236
0,43
0,0397
0,71
0,061
1,05
0,088
1,44
0,123
1.91
Уд. вес растворов AgClOj и **
°/о AgCIO,
1
2
4
6
8
и\ь
«А
1,0074
1,0158
1,0327
1,0503
j 1,0683
’Молярная электропроводность (в о б р. омах) водных
растворов AgC10s при 25°
Молей AgCIO, в л
раствора
0,025
0,015
- 0,007
0,003
0,0015
0,Х08 ^
Молярная электропроводность в обр.
омах
111,7
117,9
120,1
123,1
124,1
124,3
- Число переноса аниона для 0,2 N раствора AgNOs равно 0,505.
Температура плавления AgClOj равна 230°; при 270° начинается разложение AgClOs с образованием AgCl и Ог. При быстром нагреве AgClOs разложение может произойти со взрывом.
Из аммиачного раствора AgClOs выделяются кристаллы состава AgClOs • 2NHs с температурой плавления ~ 100°.
6. Хлорат аммония1 NH4CIO3. Мол. зес 101,46. Раствор’
NH4CIO3 получается внесением сульфата или карбоната аммония-
в раствор Ва(СЮз)г или внесением кремнефтористоводородного
или виннокислого аммония в раствор КСЮз или нейтрализацией
раствора НСЮ$ аммиаком (последняя реакция сопровождается
уменьшением объема).
; При сгущении раствора NH4CIO3 над серной кислотой до уд.
веса 1,25 выделяются мелкие кристаллы в виде игл или табличек
уд. веса 1,80. ;
1 Библиографию см. А б е г г 6—1*; Г м е л и н м е л л о р *•—*;
Ann. . 12 (1803), 433; J. S0c. Chem. Ind. 16 (1896), 161.
. - - /
226
t
Gibb,
Растворимость NH4CIO3 в воде при разной температуре будет
(Gibb, Ann. 12, 1803, 433) следующая:
Температура
0е
15*
30*
45е
60*
\
75*
% NH4C10j ....
22.3
28.0
34,8
41.8
48,4
53,5
Раствор, насыщенный NH4CIO3 и NHj при 15,5°, содержит
2,115 моля NH4CIO3 и 1,342 моля NH3 на 100 г НгО.
В чистом спирте NH4CIO3 почти нерастворим; в водном
спирте NH4CIO3 тем больше растворим, чем меньше процент
спирта.
Хлорат аммония является сильно взрывчатым веществом.
Данные разных авторов о температуре плавления и о температуре разложения противоречивы; многие авторы указывают
температуру начала разложения в 102°. При быстром нагреве
NH4CIO3 взрывается при более низкой температуре. Взрыпает от
удара, трения и т. д. Даже при комнатной температуре хлорат
аммония при хранении постепенно разлагается. Однако химически чистый NH4CIO3 в запаянных трубках можно хранить долгое время без разложения. Если хранить хлорат аммония тонко
насыпанным слоем, с тем чтобы продукты разложения (СЮг)
удалялись, то взрыв не наступает.
Приводим следующие данные о влиянии количества NH4CIO3
и температуры нагрева на время наступления взрыва4-23:
Температура
40е
70е
90е
100е
120*
140*
Взято граммов
NH4CIO3 . • .
3.0
0,5
0,3 '
0,1
0,3
0,1
0.3
0.3
Продолжительность нагрева
до взрыва . . .
11 час.
45 мин.
6 мин.
lo¬
3—
51-
20—
ll мин.
372мин.
62 сек.
22 сек.
Концентрированные растворы NH4CIO3 при хранении также
постепенно разлагаются (особенно при нагреве) и может произойти самопроизвольный взрыв. Разбавленные растворы можно
безопасно кипятить; раствор, содержащий NH4CIO3 405 г/л,
взрывает при кипячении с обратным холодильником в течение
1 часа; более концентрированные растворы взрывают еще скорее.
Devis (J. Soc. Chem. Ind., 15, 1896, 161) описывает взрыв, происшедший при’выпаривании водного раствора NH.ClOj в эмалированном котле, обогреваемом паром; 'взрыв разрушил здание, где
производилась выпарка.
15*
/
227
§ 2. Хлораты бериллия, магния, стронция, цинка кадмия, ртути
1. Хлорат бериллия1 Ве(СЮз)г. Мол. вес 175,94. Раствор
Ве(СЮз)г получается при внесении свежеосажденной Ве(ОН)г
в раствор НСЮз или BeSOe в раствор Ва(СЮз)г. В твердом виде
хлорат бериллия не получен, так как разлагается даже при сгу-
тцении над серной кислотой под вакуумом при комнатной температуре.
Приводим уд. вес и молярный объем растворов Ве(СЮз)з при
15° и концентрацию водородных ионов в растворах Ве(СЮз)*
при 20°.
Уд. вес растворов Be(С10з)з28-5"22
' «I. Be (СЮ,),
1
2
3
46
1,0053
1,0114
1,0175
Молярный объем растворов
Be(Ciqs), при 15° 4~2*
^ ' •/, Ве(СЮЛ
1,949
2,565
3,310
Мол. объем .
69,9
69,3
70,2
Кислотность при 20’(±0,02°) растворов Be(C10sfo4_2S
Молей Ве(С1ОД
в 1 л раствора
1
0,5
0,2
0,1
0,05
0,02
0,01
0,005
0,002
0,001
pH' . . . .
pH"
1,35
1,799
1,85
2,386
2,40
2,746
2,90
3,047
3,05
3,37
3,40
3,62
3,65
3,95
4,25
4,65
pH' — определено потенциометрически хннгидроновым электродом.
pH" — определено колориметрически,
1 2. Хлорат магния2 М£(СЮз)з. Мол. вес 191,24. Раствор
М£(СЮз)* может быть получен внесением MgSO* в раствор
Ва(СЮз)*, а также нейтрализацией раствора НСЮз, окисью
1 Библиографию см. А б е г г *—*; Г м е л и н *-*6; М е л л о р ••—■;
СТЭ **-*.
* Библиографию см. А б е г г *—М е л л о р *»—2; СТЭ **-*.*.
228
ч
или карбонатом магния, взаимодействием'
КСЮз с фторосилика-
том магния и т, д.
При сгущении раствора
Mg(C10s)2 над серной кислотой выделяются кристаллы шестиводного гидрата
Mg(C103)2 • 6Н2О; уд.
вес кристаллов 1,80.
При хранении в от-„
крытом виде кристаллы Mg(C103)2 • 6Н2О
расплываются. При 35°
кристаллы Mg(C103)2 •
• 6НО2 плавятся и переходят в Mg(ClC>3)2 •
. 4HgO (по другим данным при 40°). При 65е
образуется двухводный гидрат Mg(C10s)2 -
.•;2НгС>. Безводный хлорат магния не удается
получить.
Температура начала
разложения хлората
магния равна 120°.
Раствор смеси
Mg(C10s)2 и. MgCl2
может быть получен
хлорированием взвеси MgO или MgCOs'
в горячей воде (см.
стр. 180)j
Приводим состав
насыщенных водных
растворов Mg(C103)2
при разной температуре и удельный вес
растворов Mg(C10s)2
при 18°.
Молярная депрес-
сия растворов, содержащих 1,496 и 1,871
моля Mg(C10*)2 на
1000 г НгО, будет
5,35 и 6,41° (Meus-
ser »»•; СТЭ **“♦}.
S
8
8
а
»о
I
«3
а
8
о
о.
о
со
н
о
«5
а
о
о
а
<s
а
я
Л *
К'
а>
>>
со
00
229
1,0135 1,0287 1,0441 1,0597 1,0758 1,0922 1,1091 1,1264 1,1442 1,1624 1,1810 1,2001 1,2196 1,2395 1,2598
Удельный вес растворов Sr(C103)2 28-5 и 92
<*
* 3
1,839
8
1,2935
а
1,2348
я .
1,1800
00
1,1593
ю
1,1394
1,1203
со
о
о
о
1,0825
00
1,0647
л
<0
1,0476
\
ч*
1,0310
со
ь-
г}*
§
§
3.
м
230
к
о.
с
О
о
о.
о
со
н
и
«в
а
и
3
в
*
О
ю
S
S
в
со
в
в
о
о
о
S
е*
»А
В
о
с
о
н
О
л
н
о
о
X
et
О
ю
о
о.
с
о
о*
н
в
0>
*
СП
3,951
О ОО
CN ОО
НЮС4
‘4
0,09335
47,26
0,446
)
■ I
О
а’
°Й°
5
о
0,03245
65,70
0,620
0,1975
0,01463
74,07
: 0,699
о
! 0,00783
79,34
: 0,748
h
Si
(Л
г>
CI
*-
' }
к
«э
>;
о
&
о u
. п
о.
о
о *■*
о
в g
в 5
н о
о а
2 о
5
5 с
2 °
В о
? Н !
СХ us s
С В t
о ;
О.В 2
н в 5
£ § <
» £ 2
и с
ОС О) '
S я :
зв|
8 * j
>•<1 в
\
3. Хлорат стронция 1
Sr(ClOa)2. Мол. исс
254,55. Растяор
Sr(C10j)2 может быть
получен нейтрализацией раствора НСЮз
окисью или карбонатом стронция, а также электролизом раствора SrCb. Элскт-
ррлиз производится
с добавкой хромата
(см. стр. 264). По герм,
пат. 202500 (1906 г.)
при электролизе целесообразно подкислять электролит хлор-
газом, что уменьшает
выделение кислорода.
Раствор смеси
Sr(C10*)2 и SrCb можно получить хлорированием взвеси Sr(OH)2
в воде.
. При сгущении раствора Sr(C10n)2 над
серной кислотой выделяются безводные
кристаллы хлората
стронция. Кристаллы
Sr(C10s)2 бывают нескольких модификаций. При кристаллизации из сильно охлажденных растворов
(при—20—40°) выделяется гидрат Sr(C10s)2 •
• ЗНгО (Потылицын пз).
При хранении при
комнатной температуре гидрат выветривается, превращаясь в
безводную соль.
Уд. вес Sr(C10i)2
-равен 3,152 (Рри комнатной температуре).
' 1 Библиографию см.
А б е г г 6—в; Г и е-
лин *—*►; М е л л о р
СТЭ »-*.
Молекулярный объем равен
81,1-
При 290° Sr(C103)2 плавится и начинает разлагаться с выделением О»: сначала проходит стадия образования перхлората, хлорида и Ог, а затем стадия
разложения образовавшегося перхлората. Первая
стадия проходит по уравнению:
' И Sr(C103)2 = 9SrCl2 +
+ 2Sr(C104)2 + 250г. (96)
Растворимость Sr(ClOj)*
в воде при 18° равна
63,6% (174,9 г на 100 г НгО '
или 1 моль хлората на
9,3 моля НгО).
Приводим удельный вес,
электропроводность' и степень диссоциации водных
растворов 5г(СЮз)г.
4. Хлорат цинка1 Zn(C10j)2.
Мол. вес 232,3. Раствор
2п(С10з)г может быть получен внесением ZnS04 или
ZnCOs в раствор Ва(СЮз)г
нейтрализацией раствора
НСЮз окисью или карбонатом цинка, реакцией фто-
росиликата цинка с КСЮз
и т. д. Раствор Zn(C103)2,
сгущенный над серной кислотой, выделяет кристаллы
хлората цинка. При темпе- .
ратуре ниже 14,5° выделяются расплывающиеся на \
воздухе кристаллы шестиводного гидрата Zn(C10s)2 •
• 6НзО. При температуре
выше 14,5° выделяются кри- ,
сга^лы четырехводного гидрата Zn(C10s)2 • 4НзО. При
1 Библиографию см. Гме-
лин4-®; А бег г*—*; ,Мел-
Д Q р 8 J стэ »-*.«.
О)
о.
н
аз
Си
<и
С
о
н
о
X
<п
03
О,
S
О*
с
О
О
с
N
а
о
о*
о
со
н
о
аз
. а
и
2
X
X
о
2
о
X
a
СО
н
о
о
U
<
о
м !
я
jZ
сч
о
со ll\ д*
сою ™
Г-Ч г- О
0
• N
о
8
10.96
71,8
о
'Г
<N О •
о> ^ i
СО ^
•ч
о
8
О
о
8
2 *
00 со
со
2)
§о.
ОО *т
со
о
О
ев
о
6*
2^0
О
«ООО
•
8
1
\ с?ю
ю ю“
ю
св • • *
. Я . . .
«в
О,
н
ев
О,
4)
|
^ . . .
О •
• Oo-SS
с = 0|.
N U
С' к
н
§2-52
S эн
8
ю
I
8
U
с
N
a
о
CU
о
со
н
о
. аз
си
и
о
a
ш |
со
«
ю
сож
гн
со
в
о
ГО
СП.
сч
гм
8
с 1
со
СЧ
со
8
СО
а
00
1 —
»о
СО
со
со
о
CD
ев
g
«—•
*4
со
о
(N
оо
о
2
,х
‘ л
к
о
•=(
>»
• со
г-
тг
о
1,0309
2
о
*
о
о
«в
а
N
в"
2 31
55° Zn(C10j)2 • 4HzO плавится и при дальнейшем нагрсио до О » ш»-
степенно переходит в двухводный гидрат Zn(C10:t)2 • 2НгО. Уд. вес
2п(С10з)г • 4НгО равен 2,15. Безводной соли получить нс удается.
Приводим растворимость Zn(COfo)2 в воде при разной температуре и удельный вес растворов Zn(C10s)2 при 18°.
Молярная депрессия водных растворов, содержащих 1,555 и
1,87 моля Zn(CK)a)2 на-1000 г НгО, равна 5,79 и 6,95° (Meusser91;
СТЭ28, т. 6, стр. 386).
В спирту хлорат цинка хорошо растворим (образуя взрывчатый раствор).
Аммиачные соединения хлората цинка. Шестиаммиачный хлорат цинка гп(СЮз)г • 6NH3 получается из четырехаммиачного хлората цинка (см. ниже). Теплота образования
равна 9,8 ккял на 1 моль NH3. Упругость диссоциации этой соли
равна 225 мм при —15°, 270 мм при —10°, 388 мм при :—2е’,
427 мм три 0°j 550 мм при 6°, 690 мм при 10°, 747 мм при 11°.
Температура плавления равна 60°.
Четырехаммиачный хлорат цинка Zn(C10s)2 • 4NH3 выделяется при пропускании NH3 через охлаждаемый насыщенный
раствор Zn(C10s)*. Теплота образования Zn(ClOa)* равна 18,6 ккал
(по формуле Периста). Образует бесцветные кристаллы уд. веса
1,84чмол. объема 163,2 с температурой плавления 55°. Упругость
разложения этой соли с выделением NH3 равна 16 мм при 114°,
32 мм при 140°, 50 мм при 165°, 88 мм при 177°, 760 мм при 216°.
В открытом сосуде взрывает яри 205°, а в закрытом — при 289°.
При ударе молотком взрывает. При хранении на воздухе соль
теряет часть NH3, которая заменяется влагой — образуется трех-,
аммиачный гидрат Zn(C10d)2 • 3NH3 • Н2О.
5. Хлорат кадмия1 С<1(С10з)г. Мол. вес 279,33. Раствор Сб(СЮз)г
получается внесением CdSOi в раствор Ва(ОЮз)г. При сгущении
раствора Сб(С10з)2 над H2SO* выделяются весьма гигроскопичные,
призматические кристаллы Сб(С10з)г • 2НгО. По Wachter’y кристаллы плавятся при 80° с разложением. По Meusser’y температура плавления кристаллов Сб(С10з)г • 2НгО равна 79°..
Приводим растворимость Сб(С10з)г в воде при разной температуре, уд. вес раствора Сс1(С10з)2 и понижение упругости паров
воды над растворами Сб(СЮз)2.
Молярная депрессия растворов, содержащих 1,27 и 3,935%
Сс1(СЮз)г, равна 5,1 и 3,3°.
В спирту хлорат кадмия хорошо растворим, в ацетоне —
мало растворим.
Аммиачные соединения хлората кадмия. Шестиаммиачный хлорат С<1(С10з)2 • 6NHs получается при пропускании NHs через концентрированный раствор Cd(C10s)2; NH3 пропускают, пока образовавшийся вначале осадок не растворится.
Выделяются мелкие кристаллы с запахом NH3. Теплота образо-
ч вания аммиачного хлората равна 14 ккал на 1 моль NH3. Удель-
1 Библиографию си. Г м'«лин|г-**; Абегг*-*; Меллор**-*;
СТЭ»-М.
232
^о став насыщенных растворов Cd (СЮз)3 при разной температуре и ei
^ Температура
-20е
0е
20*
40е
65*
Молей Cd(C103)a на
1000 2 Н20 . . . •
% Cd (С103)а ....
Твердая фаза«...
12,4
78,0
14,1
79,8
15,9
81,8
Cd (С1С
18,1
83,5
>з)а-2НаО
21,4
85,7
23,4
86,7
1 Удельный вес растворов Cd (СЮ3)2 я“5 и 95
1, Cd (СЮ,),
2
4
6
8
10
• 12
14
16
18
20
25
30
35
40
^18
«4
1,0147
1,0313
1,0483
1,0659
1,0839
1,1025
1,1217
1,1415
1,1620
1,1831
1,2394
1,301
1,363
1,441
Понижение упругости паров Н20 над растворами Cd (С103)3 29~6 и 91
a Cd (СЮ,), на 100 г Н,0
13,38
^ 28,98
39,08
54,76
74,84
152,59
Понижение упругости
паров НхО в мм Hg.
ч
16,7
• 42,1
59,6
91,1
135,3
310,9
иый лес равен ~ 1,78. При нагреве в открытом сосуде взрывает
при 184°; при нагреве в закрытом сосуде взрывает при 300'.
Упругость разложения этой соли с выделением NHs равна: 89 мм
при 69°, 156 miи при 82°, 241 мм при 94°, 330 мм при 103,5°,
530 мм при 116,5°, 772 мм при 122°.
Четырехаммиачный хлорат Сс1(С10з)2 • 4NHa получается при
120° из шестиаммиачного хлората. Теплота образования равна
15,4 к кал на 1 моль NH3. Упругость разложения этой соли с выделением NH3 равна: 117 мм при 116,5°, 174 мм при 125,5°, 355 мм
при 136°.
6. Хлорат ртути При взаимодействии закиси ртути и раствора НСЮз получается раствор НдСЮз. При выпаривании этого
раствора при 80° выделяются белые безводные ромбические
призмы, легко растворимые в воде, спирте, уксусной кислоте.
В соляной кислоте осаждается HgCl. При нагреве до 250°
HgClOs разлагается, образуя О2, HgO, Hg2<D, HgCb.
При растворении в хлорноватой кислоте окиси ртути и сгущении полученного раствора Hg(C103)2 над серной кислотой
выделяются бипирамидальные ромбические кристаллы основного
хлората окисной ртути состава Hg(C103)« • Hg(OH)2. Уд. вес кристаллов равен 5—5,15 (по данным разных авторов); на воздухе
кристаллы расплываются. При растворении в воде кристаллы разлагаются на Hg(OH)2 и Hg(C108)2. Применяются в медицине
в виде патентованных средств.-*.
, Traube (Zeit. f. anorg, Chem. 1895 г., т. 8,.стр. 12) приводит
следующий уд. вес растворов Hg(C103)2.
!
\—
о/,нг(сюв)в
1
2
3
45 ■ •
1,0080
1,0170
1,0260
$ 3. Хлораты алюминия, скандия, иттрия, эрбия, таллия,.
I циркония, олова, свинца, висмута
1. Хлорат алюминия2 А1(С103>. Мол. вес 277,35, Раствор
А1(СЮз)з получается внесением хлората бария в раствор
АЦЭОф. При сгущении раствора А1(СЮз)з над H2SO4 (на холоду под вакуумом) выделяются кристаллы А1(СЮз)з • 9НгО
в виде мелких игл, трудно отделимых от маточника. Кристаллы
хлората алюминия гигроскопичны и растворимы в спирту. При
нагреве соль разлагается; при быстром нагреве выделяется хлор
и образуется хлорид и основной перхлорат 2А1(С1С>4)з • АЬОз;
при медленном нагреве постепенно образуется СЮг и происходит взрыв (при температуре выше ,100°).
* Библиографию см. Абегг*-®; Меллор**-®; СТЭ*-®.
*• Библиографию см. Гнедин *—•*; А б е г г в-®; М е л л о р *•—2.
234
Шестиводный гидрат А1(СЮз)з • СИгО получается при кристаллизации из горячего раствора. Образует весьма гигроскопические кристаллы. При нагреве разлагается, как и дсвятиводиый
гидрат.
Безводный хлорат алюминия получить нс удается. Водный
раствор А1(СЮз)э показывает кислую 'реакцию на лакмус. При
осторожном нагреве раствор А1(СЮз)з можно упаривать Почти
досуха.
Приводим молярную депрессию и степень гидролиза растворов А1(СЮз)з разной концентрации.
Молярная депрессия растворов А1 (С103)3 гв-в
г Л1 (СЮ*), на 100 г Н,0
0,3594
0,7470
2,5032
5,4251
11,586
19,705
Молярная депрессия х
5,98
5,70
5,66
5,93
6,46
7,74
Степень гидролиза хлората алюминия в растворах разной концентрации
А1 (СЮ,), моль!л
0,2
0,1
0,05
0,02
0,01
o/fl гидролиза при 20° .
. 0,590
0,667
0,847
1,33
1,89
Примечание. Раствор сернокислого алюминия в растворе КСЮ» применяется при крашении материи.
2. Хлорат скандия1 Sc(C103)3. Мол. вес 295,48. Внесением
гидроокиси скандия в раствор НСЮз получают прозрачный бесцветный раствор 8с(СЮз)з; при выпариванйи полученного раствора, хлорат разлагается с выделением хлора.
3. Хлораты иттрия и эрбия2 У(СЮз)з и Ег(СЮз)з. Получаются
внесением сульфатов иттрия и эрбия в раствор Ва(СЮз)з. Выделяются восьмиводные гидраты, сильно расплывающиеся на воздухе.
4. Хлорат таллия2 Т1СЮз. Мол. вес 287,85. Получается растворением металлического таллия в растворе НСЮз или внесением сульфата таллия в раствор Ва(СЮз)г. Выделяются длинные
игловидные безводные кристаллы, малорастворимые <в холодной
воде. Уд. вес Т1СЮз равен 5,5047. При нагреве ТГСЮз разлагается, образуя хлорокись и перхлорат.
1 Библиографию см. Me л лор®*'-®.
1 Библиографию см. А б е г г ®—®; М е л л о р —*;
• Библиографию см. Аб е г г®—®; М е л ло р •*—*; СТЭ 28 ®.
' 235
Приводим растворимость Т1СЮз при 10—80° и электропроводность растворов TIClOs разной концентрации при 25°.
Растворимость TIClOg в воде при разной темпера-
туре 28-е и м
Температура
10е
20*
30е
40е
60е
t
80*
Молей Т1СЮ< на
1000 г НаО . .
% TIClOg . . . -
0,090
2,5
0,137
3,8
0,210
5,7
0,302
8,0
0,640
15,5
1,14
24,7
Электропроводность растворов TIClOg разной концентрации при 250/
А Н.0 на 1 моль
нею.
32
64
128
256
512
1024
Эквивал. электропроводность в
обр. омах . . .
123,6
127,8
129,8
132,1
134,2
135,4
5. Хлорат циркония1. Раствор хлората циркония получается
при внесении сульфата циркония в раствор Ва(СЮз)г. При сгу-
шении полученного раствора испарением под вакуумом над
HiSOg или КОН выделяются кристаллы гидрата основной соли
ZrO(CK>3)2.6Н2О. Средняя соль не выделяется вследствие ее
сильного гидролиза. В воде хлорат циркония хорошо растворим;
в спирте также растворим, в эфире нерастворим.
6. Хлорат олова2. При внесении свежеосажденного Sn(OH)2
в раствор HClOa образуется закисная соль Sn(C10j)2, которая
однако быстро (через несколько минут) разлагается, образуя
Sn(OH>4, SnCU и НСЮз.
При растворении металлического олова в растворе НСЮз
образуется Sn(C103>4 без выделения водорода.
7. Хлорат свинца3 РЬ(С103)2. Мол. вес 374,1. Раствор РЬ(СЮз)г
получается при нейтрализации раствора НСЮз строго эквивалентным количеством РЬО. Для получения твердого хлората выпаривают полученный раствор РЬ(СЮз)г почти досуха, разбавляют водой, содержащей НСЮз, снова выпаривают, охлаждают
и разбавляют спиртом. Выделяются моноклинические призмы
РЬ(СЮз)г • НгО, изоморфные кристаллам хлората бария. На воздухе кристаллы устойчивы; уд. вес равен 3,89.
1 Библиографию см. А б е г г 6—3; М е л л о р *■'-*. >
* Библиографию, pi. М е л л о р *•“*.
* Библиографию см. А б е г г ®—3; М е л л о р в»—*. %
236
При нагревании до температуры 190—2G0° Pb(ClOj)* разлагается по следующим 'параллельно идущим реакциям:
РЬ(СЮз)2 = РЬС12 + 302. (97)
РЬ(С10*)2 — РЬО-2 -[- CI2 -j- 2O2. (98)
При нагреве в открытом сосуде реакция (97) проходит в 7 раз
быстрее, чем реакция (98). При нагреве в условиях, когда образующемуся хлору некуда удалиться, происходит вторичная
реакция:
РЬОз + С12 = РЬС1г + Ог. (99)
В смеси с легко окисляемыми веществами хлорат свинца
сильно взрывает. Растворимость РЬ(СЮз)г в воде большая. На
1 кг НгО растворяется РЬ(СЮз)2 1513 г при 18° и 2547 г при 25,1°.
Удельный вес этих растворов равен 1,947 и 2,346.
Если прибавлять к раствору НСЮз больше РЬО, чем необходимо для нейтрализации, то образуются кристаллы малорастворимого основного хлората свинца.
8. Хлорат висмута *.• При внесении гидроокиси висмута в раствор НСЮз получается В1(СЮз)з. При упаривании полученного
раствора хлорат разлагается. По Гмелину 4_~1в можно получить в виде кристаллов основной хлорат висмута ВЮСЮз следующим методом: 24,42 г азотнокислого висмута вносят в горячий
раствор 97,6 г NaClOs в 100 г НгО. Получается прозрачный раствор, из которого по охлаждении выделяются игольчатые кристаллы ВЮСЮз, которые высушиваются на глиняной пластинке.
При нагреве кристаллов ВЮСЮз вместе с KCN получается взрыв.
При нагреве с порошком магния или алюминия получается самовозгорание. В смеси с серой, углем или обоими вместе ВЮСЮз
не взрывает. Растворимость в кипящей воде 1.: 40. В спирте,
ацетоне и эфире он нерастворим.
I
§ 4. Хлораты хрома, урана, марганца, железа, кобальта, никеля
1. Хлорат хрома2. При внесении хромовых квасцов CrK(SO«)2 •
• 12НгО в раствор Ва(СЮз)2 или сульфата хрома в раствор
КСЮз получается фиолетовая жидкость, содержащая хлорат
хрома Сг(СЮз)з. Раствор- Сг(С10з)з неустойчив и даже на холоду
пахнет хлором; при нагреве до 65° раствор зеленеет, выделяя
СЮ; при нагреве до 100° хлорат разлагается полностью и в жидкости остается только хромовая кислота. В твердом виде хлорат
хрома не получен. Раствор Сг(СЮз)з является сильным окислителем и предложен для применения в красочной промышленности.
1 Библиографию см. Г м е л и я А б е г г *-*•. •
* Библиографию см. А б егг*—*; М е л л о р в»—*.
237
2. Хлорат урана Ч При внесении гидроокиси урана (IV) и раствор НСЮз получается раствор хлората урана, который быстро
разлагается с выделением хлора и образованием в растворе
уранилхлората.
Уранилхлорат иОг(СЮз)г можно получить обменным разложением уранилсульфата с раствором Ва(СЮз)г; полученный раствор
кгущают под вакуумом над серной кислотой при низкой температуре— выделяются кристалы и0г(С10з)2 • хНгО легко растворимые в воде; кристаллы неустойчивы и весьма легко
разлагаются.
3. Хлорат марганца2. В твердом виде хлорат марганца получить не удается. Раствор Мп(СЮз)2 получается внесением сульфата. марганца в раствор Ва(СЮз)г. При сгущении раствора
Мп(С10з)г под вакуумом над серной кислотой до значительной
концентрации хлорат разрушается с образованием осадка
Мп(ОН)г.
4. Хлорат железа*. При внесении сульфата закиси железа
в холодный раствор Ва(СЮз)з получается бесцветный раствор
Fe(C10s)a. Однако re(ClOs)a неустойчив даже в разбавленном
растворе, разлагаясь с образованием РебС10з)з, FeCU и основного хлората железа. При температуре (г это разложение проходит медленно, но уже при комнатной температуре оно проходит весьма быстро.
При растворении металлического железа в растворе НСЮз
образуются Ре(С10з)з и FeCU.
•При реакции хлората аммония с раствором [Fe(NH:i)«]
(СНзСОО)г получается раствор [Fe(NH3)e](C10s)2. В твердом
виде эту соль не удается выделить. При хранении раствора хлорат постепенно разлагается с образованием осадка Fe(OH)3.
. Fe(C103)s.
При внесении сульфата окиси железа в раствор Ва(СЮз)г
получается раствор Fe(ClC>3)s. В твердом виде выделить хлорат
железа не удается. Теплота образования Ре(СЮз)з по Томсону
равна 16,165 икал, согласно следующей реакции:.
Fe(OH)3 -1- ЗНСЮз aq = Fe(Q10j)3 aq + 16,165 ккал.
Раствор, содержащий Ре(СЮз)г и FeCU, получается при хлорировании водной суспензии свежеосажденного Fe(OH)s.
5. Хлорат кобальта4 Со(СЮз)ё. Мол. вес 225,86. Раствор
Со(СЮз)* получается внесением C0SO4 в раствор Ва(СЮз)г. При
сгущении раствора Со(010з)2 под вакуумом над H2SO4 п.ри низкой температуре выделяются крупные темнокрасные октаэдрические и кубические кристаллы Со(СЮз)г • 6НЮ уд. веса 1,92.
‘Библиографии см. Гм един*-*5; Абегг*—Меллер**-8.
* Библиографию см. б е г г *“*; М е л л о р ®*-8.
• Библиографию.см.Тиелия4г-®9; Меллор**~*.
4 Библиографию см. Гмеляя4—*•; Меллор6*-8.
V ' ' '
/
238
При 18,5° шестиподный '
хлорат переходит в четырехводный Со(СЮз)г •
• 4Н2О. При нагреве до
о
3
о "
гг* со
«-•
50° соль плавится, а при
61° образуется двух-
водныйхлоратСо(СЮз)г • к
. 2НгО при одновремен- "
I
О ю
со -г
ном начале разложения. а
При 100° хлорат пол- £.
ностыо .разлагается с >,
выделением СЬ, Ог и НгО £
и образованием окиси ~ °*
кобальта. Двухводный с
хлорат Со(СЮз)г • 2НгО *
может быть также полу- н
чен сушкой Со(СЮз)г • в
• 4НгО над пятиокисью *
фосфора. Стойкость хло- «
рата кобальта тем мень- 2,
ше, чем меньше он содер- s
к
ю Q
Ю Ч*
ooi
о
9
о
^ и'
оГ ьГЛ
со W
k
8,56
65,8
житгидратной воды. Но о.
даже в растворе, Со(СЮз)* в
постепенно разлагается. "S
Приводим раствори- ' §
к
N.
СМ
о ■+
°°‘з
мость хлората кобальта ^
в воде при разной тем-' и
пературе и уд. вес рас- »
гворов Со(СЮз)2 при 18°. ®
Раствор, содержащий о
Со(СЮз)2 29,97%, замер- ‘
зает при —12°, раствор, °
содержащий Со(СЮз)г 2.
37,40%, замерзает' при и
—22°. а
Молярная депрессия. 2
растворов, содержащих ®
1,894 и 2,645 моля ^
О
.О
о ю
СО
6
О
со
^со
JJ4
о
7
со
о
9 б
ЮЮ о
Со(СЮз)г на 1000 ,г НгО, 2
равна 6,34 и 8,32°. £
X л о р а т - а м м и н ы
кобальта1. 1) Гекса- «
О
3
1
5,10
53,5
амминокобальт хлорат 2
Co(NH,)e(C10a), • НгО по- о
лучается пропусканием и
*в
е
«я
• * *
«...
5 • • •
00 я
О)
а* '
^о*©*
1 Библиографию см. Г м е-
В
Я
и W
лин4, № 58—В, стр. 55, 83,
в»
И-
|§з|
2 ©В
S ©“Н .
93, 136, 146, 154, 173^ 1&.
192, 206, 213, 232.
/ . ■ t
Q.
cj
O)
a
<s
2
/ x
л
>>
о
NT
п
£
СО
•о
со
о
оо
00
»о
о
*0
со
еч
С 1
—*
04
8
г-
сг>
СО •
22
ю
*—«
—
со
(О
со
(М
зо
-
СО
о>
CS
сл
ов
о
00
0
—,
01
00
_
см
г-
90
3
о
о
СО
ч*
о
—
ч*
ч4
N ^
ож
..
Т-Г
•а
О
00
0
«-* ч
о
у
23$
При 14° имеется следующая зависимость удельного веса и
содержания НСЮз в ее растворах.
Удельный вес , . .
1,0059
1,0145
1,0255
1,0520
1,128
1,161
% НСЮ8
1,06
2,09
4.12
8,03
19
33,82
На холоду растворы НСЮз не имеют запаха, при нагревании имеют колющий запах, напоминающий запах азотной
кислоты. Вкус растворов НСЮз сильно кислый.
Молекулярный вес НСЮз — 84,46. Теплота образования из
элементов равна 23,9 ккая (по Бертелло). Теплота нейтрализации
НСЮз в разбавленном растворе равна 13,8 ккая. Полунормаль-
ный раствор НСЮз диссоциирован на 88%. НСЮз химически
весьма активна. Спирт и эфир окисляются НСЮз в уксусную кислоту. Особенно активна смесь соляной кислоты и раствора НСЮз.
Если смочить такой смесью фильтровальную бумагу, то последняя вспыхивает (растворы НСЮз фильтруют через асбест). Магний, цинк и алюминий растворяются в растворе НСЮз с выделением водорода. Железо, медь, висмут и другие металлы растворяются без выделения водорода.
§ 6. Сводные таблицы свойств хлоратов
Таблица 77. Молекулярные и уд. веса, температура плавления,,
устойчивость при хранениина воздухеи растворимость
при 18° некоторых хлоратов
Формула
Молекуляр
ный вес'
безводной
4°
Температура плавления
Устойчивость при
хранении
У — устой¬
Растворимость при 18*
(безводных солей)
соли
°С
чивый
Р — разла¬
°/о
г/л
гается
AgClOs
191,34
4,43
230
У
11
115
Ва (СЮз^. Н.О .
Са (С108)з • 2Н,0
304,30
ЗД79
120
У
26
335
207
. —
Р
64
1097
Cd (СЮ3)2 • 2HlO
279,33
—
80
Р
81,5
—
Со (СЮ3)- • 6Н20
225,86
1,92
61
Р
63,5
г—
CsClOg
216,27
3,57
—
—
—
Си (СЮ»), • 6НаО
230,48
—
65
Р
62
—
HgClOj ....
284,07
ч —
250 разл.
/
—
—
КСЮ3
122,56
2,32
368,4
У
6,2
64
LiC103 • V3H2O .
90,40
—
65
—
—
—
UCIO3
90,40
—
129
Р
76
, 1380
Mg(C10,)3.6H,0
191,24
1,80
35
Р
56
900
NaClOj
106,46
2,49
248
У
49
680
NH4CIO, ....
Г41(ао,)..6НзО .
101,46
225,61
2,07
00 взр.
80
р
56
I
n2h4 • нею, . .
116,51
80 взр.
—
—
—
РЬ(СЮ,)2 . . .
374,12
3,89
—
У
60
—
S®*:1!?:
374,12
168,90
3,19
110 разл.
—
4,7
—
Sr(C10.). . . .
Zn (СЮзЬ^НзО
.'ч
254,54
3,15
120 разл.
р
64
1170
•• •
232^0
2,15
\
р.
65
1839
' > ‘
242
Таблица 78. Растворимость некоторых хлоратов в воде при разной температуре 2а~6
н
ол.
N
. Формула
Допус
°/o
Молей вещеотва на» 1000 г HJ> при температуре
к
— 20е
-10е
0е
10°
20е
30е
40е
50°
60е
70е
80е
100*
1
TIClOa
it 4
0,090
0,137
0,210
0,302
0,640
—
1,14
2
Zn(aOa)a
it3
5,36
—
6,10
7,П
8,62
9,0
9,62
10,96
—
—
'—
—
3
CdfClOsfe . . .
±3
12,4
—
14,1
—
15,9
—
18,1
—
21,4
—
—
—
4
Си(СЮа;2 . . . ..
it3
\58
5,88
.,6,52
6,62
7,06
7,60
8.18
8,94
9,94
13,8
—
—
5
Agao3 ......
:t 5
—
—
0,0097
0,0165
0,0236
—
0,0397
—
0,061
—
0,088
0,123
6
Со(СЮз)а
+ 2
5,10
5,43
5,98
7,09
8,02
8,56
9,37
10,55
13,0
—
—
—
7
Ni(CIOj)a
it 2
4,30
4,60
4,93
5,37
5,94
6,9
8,5
9,4
9.8
10,5
13,8
—
8
Mg(CIOa)j
±3
5,54
5,71
5,96
6,30
6,87
8.03
—
—
—
—
—
—
9
Ва (CI03)2 .....
—
—
—
0,65
038
1,11
1Л7
1,64
—
2,20
—
2,79
3,48
10 .
NaC10s
it3
—
—
7,5
9,2
—
ИД
—
13,4
—
16,1
19,4
И
ксю, ....
it 3
—
0,270
0,400
0,582
0,828
1,156
—
2,02
3,13
4,61
12
CsCIO,. . . .
it 2
—
—
0,114
CJ78
0,293
0,442
0.642
9
0,900
1,21
1,58
2,13
3,64
Таблица 79. Эквивалентная э л е к т р о п р о в о д и о с ;
Формула
Темпе-
Концентрация хлората в тысячных
' хлората
parg)a
0,6
1
2
5
10
20
50
НСЮ3 ....
18
i
•
I
НСЮ3 . . ! .
25
■ —
ч —
—
400
396
391
382 |
Т1(С103)2 . . .
25
—
135,1
133,8
131,4
129
125,8
- «
v2 Ztf(C103)2 •
18
—
—
—
—1
—
—
-1
Va Cd (С103Ь .
18
—
—
—
т-
—
—
Va Си (СЮ,), .
18
—
—
—
—
—
—
&
AgC103. . . .
25
—
124,1
123,5
121,8
119,7
113,2
i-
\
т- Н
i/j Со (CIO,), .
18
—
—
—
—
—
•
-
l/a Ni (C103)a .
18
—
\
—
—
—
—
-г |
V, Mg (CIO,), .
18
—ч
—
—
—
—
i/2 Ca(C103)2 .
18
—
—
—
—
—
—
~~ 1
t/aSr(CI03)8 .
18
У*
—
—
. —
_ ё
»/aBa(C103)2 .
18
—
—
—
—
—
—
“1
Va В a (C103)j .
30
—
—
—
—
—
—
щ
UC108 ....
18
—
—
—
—
— ’
—
1
" j
53,•;
LiC103/. . . .
25
—
101,3
100,4
98,4
96,0
—
NaClOj.. . '. .
0
• — '
59,8
59,6
58,9
57,6
56,1
NaC10„.', ...
18
96,3
95,6
*94,6
92,8
91
88,7
NaC103....
25
— .
113
111,4
108,8
106,4
103,4
*{
NaC10a. . . .
35
—
—
134
132
124
125
119 1
KCIO, ....
0
74,8
74,3
73,4
72,2
71
68,8
G4
Кею, ....
18
117,5
116,7
115,7
113,7
111,5
108,7
103
KCIO, . i . .
•
25
435,7
134,4
132
129,6
125,7
111*. 1
KCIO, ....
30
162
161
158
154
; 150
14.
244
>
sB обратных омах) растворов хлоратов®-4
долях моля на литр раствора
| 70
> 100
200
500
700 f
1000
2000
3000
4000
347,6
343,6
334,6
’ 316,6
306,2 '
(
291,4
246,7
205
379
375
366
352
—
—
—
—
—
—
—
~
—
—
—
—
—
—
73,9
69
61,7
58,4
54,3
44 7
35,4
28,7
—
75
69,9
62,1
58,6
543
43,6
34,6
27,3
—
75,7
70,6
*
62,7
59,2
34,7
43,5
34,5
—
*■
ттш
—
—
61,7
58,2
54,2
43,7
35,1
27,9
—
—
—
61,9
58,4
54,2
43,6
34,6
27,5
—
76,1
70,6
62,7
59,2
54,8
44,3
35,6
28,4
—
79,9
75
68
64,8
60,6
49,9
41
33,7
—
1 79,2
73,8
65,4
61,9
57,8
46,9
37,6
—
—
79,5
73,8
64,7
61
56,4
44,7
^ — ■
. —
-
• —
933
82
77
70,9
55,7
—
—
-
74,5
70
62,7
59,5
55,7
46,9
—
—
: “
—
—
—
—
—
—
— *
52,6
51,3
483
43,6
—
—
—
—
t —
82,9
803
. 76,4
69,1
65,8
61,8
51,7
43,5
ч
36,1
-
94
883
793
—•
—
—
—
—
—
113
109
96
— ‘
—
—
64
62,6
—
—
, —
—
—
—
—
101,5
99
93,6
—
—
—
—
—
. —
116,4
пзз
—
—
—
—
—
—
135
' ■
■
245
Таблица 79а. Кристаллические формы некоторых х л о р а . * п
(Г мел иг 4-f: Qmti 2. сто. 76. 10Г>. ;u, v?v
№
пп.
Формула
Кристаллическая форма
Примечание
1
2
3
■' 4
" 5
6
V
7
8
9
10
11
12
13
14
LiC103
NaClOg
NaC103
Неизвестно
а) Кубическая
б) Ромбоэдрическая "ч
NaClOg
NaC103
KClOg
в) Ромбическая
г) Моноклнническая
Монокл и и ическая
RbC103
CsClOg
NH4CIO3
AgC103
TIClOa
ж?0-
Sr (С10з)з
Sr(C108)2
Sr (C10j)a
Ва(С10зЬ
Ва(С10зЬ-НаО
Pb (ClOaVHaO
Hg (CIO.) OH
Cr(C108)0H -
а) Тетрагональная
б) Кубическая
% **
Кубическая
а) Ромбическая
б) Моноклнническая ~
в) Ромбическая
Монокл ин ич еская
Ромбическая
Моноклнническая
Изоморфны NaBr03
Метастабильны; подобны
NaN03
Метастабильны
Метастабильны
Единственная модификация
Неизоморфны NaClO.3
Изодиморфны КВг03
Изоморфны с КСЮ3
Изоморфны с КС103
Вероятно изоморфны
с КВг03
Изоморфны с AgBrO.3
Стабильны при нагреве;
изоморфны с N&CIO3
Изодиморфны с КСЮ3
Подобны Sr(N03)2
Стабильны при нагреве
Нестабильны
Нестабильны
Подобны Ba(Ni03)2
Изоморфны друг с другом и
с Sr (ВЮ3)а • Н2Ъ,РЬ (Вг03)2 •
• Н20, Ва (Ю3)2 • Н20,
РЬ(Вг03)2-Н20
Изоморфяы с Hg(Br03)0H
Изоморфны с Cua(N08) (ОН)з
ЧАСТЬ ТРЕТЬЯ
ЭЛЕКТРОЛИТИЧЕСКИЕ МЕТОДЫ ПОЛУЧЕНИЯ
ХЛОРАТОВ
Практика электролитических методов получения хлоратов,
несмотря на пятидесятилетнее существование этого производства,
еще менее освещена в литературе, чем получение хлоратов
химическим путем. Ферстер10, Билитер “•12, Ульман5 и др.
указывают на отсутствие подробных и достаточных данных о
заводской практике получения хлоратов электролизом и большей частью приводят лишь данные старых патентов. Теоретически процессы получения хлоратов электролизом более или
менее изучены и опубликованы, но и тут полного освещения
вопроса еще нет и во всяком случае опубликованные материалы
.оставляют очень много неясного. В СССР вопросами получения
хлоратов электролизом занимались П. П. Федотьев, Н. Н. Воронин, Шпитальский, Соколов .и Кацен, Памфилов и другие.
В 1920—1925 годах работала руководимая Н. Н. Ворониным небольшая заводская установка 27-г.
Исторические сведения. Впервые об образовании хлората при
электролизе водных растворов хлоридов щелочных металлов
упоминается в работах Берцелиуса в 1808 г. и Стадиона
в 1816 г., но лишь Колбе в 1847 г. более подробно исследовал
этот процесс и твердо установил содержание NaC103 при электролизе раствора NaCl. Однако и после исследования Колбе пона-
Добились еще десятки лет, пока методы электролитического
получения хлоратов были достаточно изучены для рентабельного
осуществления в промышленном масштабе.
Первый патент на способ электролитического получения хлоратов и аппарат для этого способа был взят Чарльзом Уаттом
в Англии в 1851 г. Однако, хотя этот патент предусматривал мно-'
гое из того, что было впоследствии осуществлено, он не вызвал в жизнь организации производства и вскоре был даже забыт, так как общие технические и экономические условия того
времени были еще недостаточны для развития таких производств (отсутствие достаточно мощных источников дешевой
электроэнергии, недостаточное развитие электротехники и т. д.).
Лишь через 35 лет после -патента Уатта в 1886 г. французские
инженеры Галль и Монтлор' организовали по разработанному
247
ими методу заводскую установку для получения хлоратов алсктро-
лизом. С этого времени начинается быстрый рост этой отрасли промышленности, и уже через 10—15 лет после начала
работы первой установки больше 50% мирового производства
хлоратов производилось электролитическим путем. Кроме Галля
и Монтлора основными пионерами в области развития этой промышленности были Карлсон в Швеции, Гибс, Франшо и Гертер
в Америке, Корбэн и Ледерлэн во Франции и др. Основные теоретические работы по получению хлоратов электролизом были
опубликованы уже после промышленного осуществления, именно
в конце 90-х и начале 900-х годов Ферстером и его учениками,
а также Эттелем, Вольвиллом, Броше, Мюллером, Ймгоффом,
Корбэном и другими.
ГЛАВА 18
ЭЛЕКТРОЛИЗ С ПЛАТИНОВЫМИ АНОДАМИ
§ 1. Электролиз нейтрального раствора хлорида
Для электролитического получения хлората щелочного металла подвергают электролизу раствор хлорида того же металла.
Ход процессов электролиза в значительной степени зависит от
материала электродов. В настоящей главе мы рассмотрим процесс с платиновыми электродами.
При прохождении тока через раствор хлорида на аноде разряжаются ионы хлора (выделяется хлор), а на катоде разряжаются ионы водорода и образуется щелочь.' Суммарная реакция процесса выражается уравнением (69):
2NaCl + 2НаО + 20+2© = С1й + Н2 + 2NaOH. (69)
При производстве хлора и каустика необходимо изолировать
друг от друга образующиеся при электролизе С12 и NaOH. При
производстве хлоратов необходимо, наоборот, создать условия,
благоприятствующие реагированию хлора и щелочи. Это реагирование проходит в две стадии по следующим уравнениям:
' С12 + NaOH = НСЮ + Nad. (100)
НСЮ + NaOH = NaCIO -f Н20 (101)
Суммарное уравнение обеих стадий взаимодействия хлора со
щелочью будет:
Cl2 + 2NaOH = NaCIO + NaCl+, Н20. (71)
Таким образом при электролизе раствора NaCl благодаря
взаимодействию образующихся при электролизе хлора и щелочи [уравнения (69) и (71)]1 продуктом электролиза должен
быть только гипохлорит. В действительности в электролите
содержится еще НСЮ и растворенный хлор вблизи анода и щелочь вблизи катода, так как реакции (100) и (101) протекают
248
только постепенно и образование гипохлорита по уравнению (Нп>
происходит лишь в некотором отдалении от анода.
Образовавшийся гипохлорит, электролитически диссоциируя,
дает в электролите ионы СЮ', принимающие участие в переносе
тока и разряжающиеся на аноде, причем одновременно с этим
разряжается на катоде водородный ион воды:
NaClO^Na+ClO'. (102)
6С10' + ЗНаО + 6© = 2С108' + 4С1' + 6Н' +1 »/гОа. (103)
6НЧ-60Н' + 6© = ЗН9 + 60Н'. (104)
Таким образом результатом всего процесса будет анодное
образование хлората и кислорода и катодное образование водорода.
Все ионы СЮ', достигающие анода, разряжаются (ур. 103),
поскольку разряд СЮ' происходит легче, чем разряд С1, который обладает более высоким анодным потенциалом. Как указано, гипохлорит образуется в некотором отдалении от анода,
почему анода достигают не все образовавшиеся ионы СЮ'. Количество 'ионов СЮ', достигающих анода, и количество ионов,
остающихся в электролите неразряженными, определяется концентрацией хлорида и гипохлорита в растворе, числами переноса и диффузией. В начале электролиза концентрация СЮ'
в электролите повышается соответственно количеству прошедшего тока, затем начинается разряд СЮ' и повышение концентрации СЮ' замедляется; наконец наступает момент, начиная
от которого концентрация ОКУ становится постоянной, поскольку количество образующихся ионов СЮ' становится равным количеству разряжающихся ионов СЮ'. При наступившем
стационарном состоянии электролиза дальнейшее прохождение
тока вызывает только увеличение количества хлората и кислорода.
Складывая вышеприведенные уравнения согласно коэфициен-
там, необходимым для получения 2C1CV, получаем суммарное
уравнение следующего вида:
2NaCl + 9НаО +18©+18© = 2NaC10s+9Ha + 1‘/г02. (105)
По закону Фарадея на 6 атомов кислорода, содержащихся
в 2 молекулах хлората, образовавшихся по уравнению (105),
должно было быть затрачено 12 фарадёев электричества. Поскольку по уравнению (105) тратится 18 фарадеев электричества
на 2C1CV, выход тока на хлорат равен
12-100 с с что I
—-— == 66,67°/0,
а 33,33% тока расходуется на образование газообразного кислорода.
Таким образом при электролизе нейтрального раствора хлорида теоретический выход хлората по току равен 66,67%. Практический выход по току отклоняется от теоретического бдаго-
249-
даря протеканию при электролизе побочных реакции, из которых основные это разложение и восстановление гипохлорита
и хлората, разряд ионов ОН', химическое образование хлоратов
без затраты тока. Примерный ход основных побочных реакций
при электролизе следующий:
1. Гипохлорит и НСЮ, участвующие в процессе электролиза
как малоустойчивые соединения, частично разлагаются с выделением кислорода:
Это разложение увеличивается с повышением температуры и
■от присутствия катализаторов, каковыми являются окислы и
соли большинства металлов, имеющих по несколько степеней
валентности, особенно Со и Ni (см табл. 82 и 86 стр. 257 и 262).
Таким же катализатором может быть и металл электрода. Щелочная среда уменьшает это разложение.
2. Восстановление гипохлорита, а в меньшей степени и хлората происходит в присутствии большинства восстановителей.
В условиях электролиза особенно опасным является катодное
восстановление гипохлорита и хлората образующимся водородом. Газообразный водород не имеет таких восстанавливающих
свойств. Вероятно восстановление на. катоде происходит благодаря «атомному» состоянию водорода в момент его образования
(im statu nascendi). Обычно катодное восстановление изображается
следующими уравнениями: '
Величина катодного восстановления гипохлорита зависит от
температуры электролита, кислотности или щелочности его,
материала катода, присутствия каталитически действующих примесей (см. табл. 92, стр. 267) и т. д. Например при электролизе
нейтрального раствора хлорида с железным катодом без особых
добавок восстановление достигает до 60% и больше от общего
расхода токах. Катодное восстановление хлората обычно мало
по сравнению с восстановлением гипохлорита.
3. Хотя нормальный электродный потенциал разряда ОН'
ниже, чем для разряда СГ, расход тока на разряд ОН' при
электролизе нейтрального раствора хлорида практически ничтожен, поскольку концентрация ОН' при нейтральной среде весьма
мала и разряд ОН' сопровождается большим перенапряжением
для кислорода.
Разряд CIOs' происходит только при значительном понижении
концентрации СГ в электролите, поскольку потенциал разряда
CIOs' положительнее, чем для потенциала разряда СГ и СЮ'.
1 Об условиях защиты от като оного восстановления см. стр. 264.
нсю -v нс1 + у2о2.
NaC10-*NaCl + У2Ог.
(106)
(107)
СКУ + 2Н’ + 2© = СГ + НаО.
С10'8 + 6Н- + 6© = СГ + ЗН20.
(108)
(109)
250
Реакции разряда ОН' и С10з' проходят по следующим
уравнениям:
4. Поскольку вблизи анода и при электролизе нейтрального
раствора хлорида образуется кислая среда и содержится НСЮ
[уравнения (100) и (110)], частично происходит образование
хлората без затраты тока — чисто химическим путем. Это
образование хлората заключается в окислении СЮ' хлорноватистой кислотой. При этом НСЮ восстанавливается до НС1,
которая реагирует с СЮ', образуя СГ и снова НСЮ. Вновь
образовавшаяся НСЮ окисляет новое количество СЮ' в СЮз',
опять восстанавИиваясь сама до НС1. Так процесс продолжается
до перевода почти всех ионов СЮ' в CIOs'. Реакция идет по следующим уравнениям:
Суммарно уравнения (112) и (113) показывают самоокисление
гипохлорита:
3C1Q' = СЮз' + 2СГ. (114)
Как установил Ферстер, такое самоокисление гипохлорита
возможно и без наличия НСЮ, по уравнениям:
Суммарно уравнения (115) и (116) дают то же уравнение
(114), что и реакции с участием НСЮ. Практически, скорость
реакции (115) так мала, что обнаружить в электролите СЮг' не
удается, так что образование хлората по уравнениям (115) и
(116) можно считать практически отсутствующим.
Ниже приводим некоторые исследования по электролизу
нейтрального раствора хлорида с платиновыми анодами при
разных условиях температуры, концентрации и плотности тока,
перемешивания электролита, платинирования анода.
1. Рис. 98 показывает ход электролиза нейтрального раствора
NaCl с платиновыми и платинированными анодами (Ферстер10).
Электролизу подвергался раствор, содержащий NaCl 5,1 моля
в литре и NasCrC>4 0,2% *. Сила тока была 2А, анодная плотность тока — 0,067 А/с*2, температура электролита 12—13°.
Кривые электролиза с платинированным анодом (сплошные
линии) показывают следующее:
Первые 2—3 часа электролиза образование гипохлорита
идет почти .по теоретической кривой, выделение Ос и образова-
1 Роль добавки хромата см. стр. 264.
4OH' + 4H'-f-40 = 2H2O + 4H' + O2. (ПО)
2Cl03, + Ha0 + 2© = HC103 + HC104. (111)
СЮ' + 2НСЮ = СЮз' + 2НС1.
2СЮ' + 2НС1= 2С1' +; 2НСЮ.
(П2)
(ИЗ)
(115)
(116)
251
ние хлората весьма малы, выход по току на активный кислород1 весьма высок. При дальнейшем ходе электролиза
образование хлората и выделение Ог начинают расти, выход по
току падает и примерно через 4—5 час. наступает стационарное состояние электролиза, т. е. концентрация гипохлорита,
образование хлората и О* и выход по току становятся'
постоянными.
Рис. 98. Кривые образования гипохлорита, хлората и газообразного кислорода и выхода по току при электролизе нейтрального раствора NaCl с платинированным и платиновым анодом.
Кривые электролиза с гладким платиновым анодом (пунктирные линии) показывают несколько иной ход электролиза,
поскольку потенциал разряда иона хлора на таком аноде поло-
ж'ительнее на 0,6 V по сравнению с платинированным анодом.
Разряд СЮ', выделение Os и образование хлората начинаются
почти с самого начала электролиза. Стационарное состояние
электролиза наступает несколько раньше и при более ризкой
концентрации гипохлорита. Выход по току в начале электролиза
ниже, но при стационарном состоянии электролиза почти одинаков, как при платинированном аноде,
1 Активным кислородом называют сумму кислорода, содержащегося
в хлорате и гипохлорите.
252
Таблица 80. В л и я и и с перемешивания э л с к т р о л im а, копией
-грации NaCl, температуры и плотности тока па ход
электролиза нейтрального раствора NaCl с л л а т и и о и ы м и
и платинированными анодами 1и
М опытов
NaCl
экв/д
Темпе¬
ратура
•С
Плотнооть
тока
А 1см*
Максимум ги-
похлоритного
кислорода
в zfл
Расход тока
в °/о°/о на выделение 0,
Содержат».* пм<*
ХЛОрИТПОГО
рода п ?!л при
Ю’/о-пой потере по
току
А1 В
А 1
1 в
А1 | В
Анод вертикальный сплошной; электролит не перемешивается
1
5.0
14
0,014
3.4
'5,4
33-34
35
1,4
3,0
2
5,0
14
0,034
5,2
7,7
33—34
33—34
3.3
6,0
3
5,0
14
0,110
7.4
10,2
33—34
33—34
, 5,4
9,3
4
5.0
14
0,440
9.7
10,8
33—34
33-34
* 6,5
9,9
5
5.0
30
0,014
2,7
3,6
33—34
?
U
2,7
6
5,0
30
. 0,110
6.1
7,7
33—34
33,5
3,7
6,3 •
7
5,0
70
0,057
1.8
—
30
—
0,9
8
2,0
17
0,036
4,7
5,9
33
>35
3,0
5/2
9
2,0
17
0,440
7,4
—
35—36
—
3,8
10
1Д,
17
0,110
5,3
>5,4
33—34
35-36
1,4
И
1Д
30
0,110
5,1
4,4
34—35
38—39
1.5
2,9
12
1Д
45
0,110
4,1
—
35—36
—
1.6
Анод сетчатый; электролит перемешивается
13
4.34
10
0,004
0,33—
0,35
39-35
35-36
0,15
14
4,34
10
0,013
0,23
0,56
£з
34-35
15
4,34
50
0,004
0,21—
0,06
36
47—48
0,14
16
4,34
50
0,013
0,15
0,2
36—37
36
17
2,17
10
0,004
0,05
—
37
18
2,17
10
0,013
0,16
—
34—35
19
2,17
50
0,004
0,02
—
43
2. Рис. 99 показывает данные Ферстера и Мюллера69 о влиянии температуры на ход электролиза нейтрального раствора
NaCl. Из кривых этой диаграммы видно, что при 50° максимальная концентрация гипохлорита ниже, стационарное состояние электролиза устанавливается быстрее и выход по току выше,
чем при 10—18°. Такая разница в основном объясняется ускорением образования хлората химическим путем по уравнению
(114) с повышением температуры. Характер кривых катодного восстановления указывает при обеих температурах на
связь его с концентрацией гипохлорита, а не хлората, что подтверждает, чро в основном восстанавливается гипохлорит, а не
хлорат.
1 А—данные дда платиновых анодов, В —данные для платинированных
анодов.
253
Номцшмтра. ция
3. Табл. 80 прнм>дпт
Прауснитца74 о влиянии перемешивания электролита при разных
условиях температуры, плотности
тока и концентрации NaCl на
электролиз с платинированным и
гладким платиновым анодом.
Из данных таблицы можно
сделать следующие выводы:
Перемешивание облегчает доступ СЮ' к аноду и разряд СЮ',
вследствие чего понижается максимальная концентрация гипохлорита и повышается выделение Ог
по сравнению со спокойным состоянием электролита.
Платинирование анода увеличивает, а повышение температуры
и снижение концентрации NaCl
уменьшают концентрацию СЮ'
как при спокойном состоянию
электролита, так и при его перемешивании.
Повышение плотности тока
увеличивает концентрацию СЮ'
при спокойном состоянии электролита и мало влияет при перемешивании.
Рис. 99. Кривые образования г и- Примечания: а) Уменьшение кон-
. похлорита, хлората и газообраз- центрации СЮ' при опытах 13—19 объяс-
. ного кислорода и величина катод- няется еще сетчатой формой анода в этих
. ного восстановления при элек- опытах; б) наблюдаемый при некоторых
г тролизе нейтрального раствора опытах расход тока на выделение О»
■ NaCl при 10—18° и при 50° (влия- меньше 33,3% объясняется образование температуры). нием хлората химическим путем.
§ 2. Электролиз щелочного раствора хлорида
При электролизе раствора хлорида, содержащего щелочь,
процессы электролиза проходят иначе, чем выше описано для
нейтрального раствора. Основная причина этого отличия заключается в том, что поскольку раствор, поступающий на-
электролиз, содержит щелочь, образование гипохлорита про-
, исходит не в некотором отдалении от анода, как в нейтраль-
' ном растворе, а у самого анода, почему разряд СЮ' начинается сразу же лоецр-ч^ачала электролиза. Поэтому максимальная концентрация гииЪхЛ^рита ниже и стационарное состояние
' электролиза наступает раныЪё, чем при нейтральном растворе.
Так же «выше и процент выделения кислорода и ниже процент
выхода по току,, поскольку химического образования хлората
v почти совсем нет и есть расход тока на разряд. ОН'. Эти отлили •' , ■ .* ''
р-р NaCl при W-1V
N*umptvth*biuр-р ttaCL при **50 •
чия от электролиза нейтрального раствора тем резче выражены,
чем больше щелочность раствора, поступающего на электролиз.
При большой концентрации щелочи в начале электролиза
идет только разряд ОН'; разряд СГ начинается лишь
С одёр*#а ниш И а ОН для kpuBbtx шарообразного кислорода
i 0 0,116» 0,19» 0,375» 0,3»
’ Содержание к л ОН длр kpuihtx, гипохлорита *
«• СопохлоритнЫй кислород г/л
~~ Газообразный кислород^ рас гола mokaj
ч>
О
Рис. 100. Кривые образования гипохлорита и газообразного кислорода
при электролизе раствора NaCl с разным содержанием NaOH при
18, 45 и 75° (влияние
щелочности).
через некоторое время после того, как повышается перенапря-
жение для кислорода. На гладких платиновых анодах перенапряжение кислорода больше, чем на платинированных, почему
больше образование хлората — меньше разряд ОН'. Малая
плотность тока и повышение температуры уменьшают перенапряжение кислорода, почему увеличивается разряд ОН' и уменьшается
разряд СГ и СЮ'.
Влияние щелочности электролита при различных условиях хорошо иллюстрируется следующими
работами некоторых исследователей.
1. Рис. 100 показывает влияние
возрастающей щелочности электролита на концентрацию гипохлорита и процент расхода тока
на выделение Ог при температуре
электролиза в 75, <45 и 18° *. Для
большей наглядности, влияние щелочности в интервале 0,25—0,1 N на
концентрацию гипохлорита пред-'
ставлено на отдельной диаграмме. Электролит содержал >в литре
4,3 моля NaCl и 0,2% К*СЮ« при анодной плотности тока
Рис. 101. Кривые содержания гипохлорита и хлората при электролизе раствора NaCl с разным
содержанием NaOH при 6—8°.
‘Nilsen, Dissertation, Dresden 1911, Muller, Zeit. anorg. Chem. 2% 57
(1900).
255-
0,057 Л/см2 И аноде ИЗ гладком платины. Cll.'l<>m;:u4i;
дано влияние щелочности электролита на концентрацию пшо-
хлоритного кислорода при стационарном состоянии электролиза.
Пунктирными линиями показано влияние щелочности на процент тока, - расходуемого на выделение кислорода. Абсциссу
надо в этом случае отсчитывать по верхней шкале.
2. Рис. 101 показывает зависимость количества сантиграммов
активного кислорода в виде гипохлорита и хлората от щелочности электролита при постоянном количестве пропускаемого
тока. Электролит содержал NaCl 200 г/л; температура Г»—8°;
анодная плотность тока 400 А/тг; продолжительность электролиза 60 мин.1 По мере роста щелочности кривая содержания
гипохлорита все больше снижается, а при NaOH 15—17 г/л
содержание гипохлорита
равно ~ 0,1 г/л. Содержание хлората увеличивается
с ростом щелочи до
'Рис. 102. Кривые содержания гипохлорита
и хлората и выхода по току при электролизе щелочного раствора NaCl при температуре от 0 до 80°.
личение концентрации щелочи уже снижает содержание хлората.
Такое направление кривой содержания хлората
объясняется тем, что при
сравнительно небольшой
щелочности в основном
ток расходуется на разряд
CIO' с образованием хлората и кислорода, каковая
реакция происходит тем
'скорее, чем больше щелочность; при слишком большой щелочности разряд QH' делается все более значительным, отчего уменьшается количество тока, который тратится на разряд СЮ' и СГ.
3. Рис. 102 показывает влияние повышения температуры на
.электролиз щелочного раствора NaCl', чем выше температура,
тем ниже выход по току и меньше количество образующегося
хлората. Концентрация гипохлорита с повышением температуры
увеличивается ввиду уменьшения перенапряжения кислорода,
-отчего увеличивается разряд ОН' и уменьшается разряд СЮ'.
4. Табл. 81 показывает влияние платинирования анода и плотности тока на электролиз раствора, содержащего в литре 3,6
моля NaCl и 1 моль NaOH при 17° (Ферстер и Мюллерв#). На
гладком платиновом аноде перенапряжение кислорода выше, чем
' на платинированном аноде, почему меньше разряд ОН' и больше
разряд СЮ' — меньше концентрация СЮ' и больше образование
хлората и выход по току. Уменьшение плотности тока с 0,067
до 0,017 А /см* несколько уменьшает перенапряжение кислорода,
•Foerster «Muller, Zeit. anorg.
Chem. 22, 73 (1899).
256
почему увеличивается концентрация СЮ' и уменьшается образование хлората.
Таблица 81. Влияние платинирования и анодной плотности-
тока на электролиз в слабощелочной среде10
Анод
X
о
и
• 3
6 5 ..
Анодная плот¬
<\’п тока на вы¬
г кислорода в виде
Сила
в ам!
Прод
жит. с
в час
ность тока
в А 1см*
деление О,
хлората
гипохлорита
Платинированный .
2
0,067
/
70
1,136
0,0872
Гладкий
2
б</4
0,067
58
1,639
0,0012
я
—%
0,5
24
0,017
58
1,586
0,0032
5. Табл. 82 приводит данные Броше о влиянии добавления
некоторых окислов на электролиз раствора КС1, содержащего
небольшие количества КгСгО, и КОН. Из данных таблицы видно,
что добавка окислов Cr, Al, Zn и Fe почти не влияет на выход
по току; добавка окислов Си и РЬ уменьшает выход по току на
9—13%; добавка окислов Hg, N1 и Со весьма сильно влияет на
электролиз, направляя его почти целиком на выделение Ог. Самым большим является влияние добавки, окислов Со.
Таблица 82. Влияние добавок некоторых окислов на
электролиз растворов КС1 115
L—.
Добавлено
гидроокиси
Со
N1
Hg
Pb
Cu
Fe
Zn
Al
Cr
без
доба¬
вок
о/о выхода
по току .
2,1
5,5
-U
10,1
52,2
56,8
63,4
64,4
65,9
69,6
65,3
' § 3. Электролиз слабокислого раствора хлорида
Как указывалось на стр. 251 при электролизе нейтрального раствора хлорида происходит частичное образование хлората химическим путем [ho уравнению (114)] за счет НСЮ и
ионов СЮ', имеющихся вблизи анода. Однако поскольку количество свободной НСЮ при электролизе нейтрального раствора
хлорида ничтожно, химическим путем образуется лишь небольшая часть хлората, а основное количество хлората образуется
электролитически по уравнению (103). Так как химическое образование хлората происходит без затраты, тока, оно
является весьма желательным, почему и возникла мысль^ о создании при электролизе слабокислой среды путем подкисления всего
электролита с целью получения условий; максимально благоприятных для химического образования хлората из СЮ'. При таких условиях ббльшая часть образующегося при электролизе
гипохлорита самоокисляется в хлорат [уравнение (114)] и лишь
17 ВМС. 179. «*■ Шрайбмаа. 257
незначительная часть его разряжается на аноде по уравнение,
(103). С другой стороны, поскольку в слабокислой среде концентрация ионов ОН' незначительна, разряда таковых почти не происходит и ток почти целиком расходуется только на .разряд
СГ, а выход по току достигается весьма высокий (до 90—95%) —
гораздо больший, чем при электролизе нейтрального раствор;!
хлорида, при котором выход обычно не выше 65%.
Чем больше кислотность электролита и выше его температура и чем ниже концентрация тока, тем меньше концентрации
СЮ' в электролите, тем скорее и полнее СЮ' переходит в СЮ*'
химическим путем. Однако при электролизе в кислой среде образующийся по уравнению (69) хлор частично выделяется в виде
газа1 и вместо электролиза NaCl начинается электролиз HCI
тем больше, чем больше кислотность электролита. Поэтому
существует определенный оптимум кислотности, выше которого вред от выделения СЬ превышает пользу от ускорения перехода СЮ' в СЮ*' химическим путем. Обычно в производственных условиях наилучший выход по току получается при кислотности электролита в 0,03—0,05 N. Ферстер ,0’
устанавливает кислотность электролита такой, чтобы соотношение НСЮ и NaCIO в электролите было от 1:2 до 2:1. Для
постоянства такого отношения в течение всего времени электролиза периодически или непрерывно к электролиту1 добавляют
разбавленную соляную кислоту. Начальную кислотность электролита обычно устанавливают добавкой бихромата (служащего
и для защиты от катодного восстановления), который гидроли-
зуясь, образует Н*, что обусловливает кислую среду.
Сг207" + Н20 — 2Сг04"+2Н’ (118)
Примечание. Во время электролиза реакция по уравнению (118) проходит полностью вправо и раствор имеет желтый цвет (CrOt). При остановке электролиза гидролиз почти прекращается, реакция по уравнению
(118) проходит влево и раствор делается оранжевым (CrsCh).
Зависимость скорости реакции химического образования хлората по уравнению (114) от содержания НСЮ и температуры выражается формулой:
—1^21 = К • [СЮ'] • [НСЮ]2.
/
Как показано в диаграмме Книббса (рис. 22, стр. 60), зависимость скорости реакции химического образования хлората от
температуры очень велика, особенно начиная с температуры 40°
и выше. Так например величина константы К вышеприведенной
формулы при 80° больше, чем при 20°, почти в 100 раз.
Подкисление электролита возможно пропусканием СО* или
прибавлением бикарбоната (герм. пат. 83536 и 89444 и шведск.
пат. 3614). Так же можно достигнуть кислотности электролита
1 Кроме того в кислой среде, благодаря взаимодействию хлорноватистой
кислоты с соляной идет образование молекулярного хлора:
нао + на-*С1* + н,о. (пя-
258
добавкой солей Са или Mg, образующих при электролизе у катода осадки Са(ОН)г и Mg(OH)2, отчего выводится из системы
часть ОН' и в электролите получается некоторое количество свободных ионов Н‘, т. е. кислая среда (см. табл. 85—87). Прибавка
солей Ва не дает такого эффекта, поскольку Ва(ОН)г имеет значительную растворимость.
Ниже приводятся данные некоторых авторов о влиянии на
электролиз: степени кислотности электролита, различных добавок (бихромата, СаСЬ и др.) к электролиту, плотности тока, концентрации СГ и СЮз'.
1. Табл. 83 приводит влияние добавок соляной кислоты на
ход электролиза 500 мл раствора NaCl, содержащего КгСгО*
2 г/л, при гладких платиновых анодах. Начальный раствор содержал НО 0,025 N. Добавляемая НС1 предварительно разбавлялась 10 мл воды.
Таблица S3. Электролиз растворов NaCl при разной кислотности и при разной температуре11
L
Температура J
<1
S
S
ц»
*
т
о.
с
«•
ЗС
Прибавлено
НС1 в г
Прошло часов от начала
электролиза
Процент использования
тока
Содержание О, в г[л раствора
Потеря
от улетучивания
С1,
иа восстановление
на выделение О*
на образование
акт.
хлора
в виде
NaClO
в виде
нею
NaClO
Кяв нею
15°
1
0,0
3,5
96,5
2,04
0,16
13
'
—
2
0,0
7,3
92,7
4,04
<М6
25
—
—f
3
0,0
11,9
88,1
5,52
0,16
• 35
—
—
4
0,0
26,7
73.3
6,62
0,16
41
—
Ю
1—н
—
24
4.2
22,6
73,2
6,СО
0,16 .
38
0,0019
Ю
0,4
243Д
—
—
—
1
1
S
26
v6,3
18,1
75,6
5,56
0,8
7
—
0,4
—
—
—
—
—
—
—
27
6,0
13,2
80.8
3,94
1,32
3
—
0,4
—
—
—
| —
30
2,9
7,2
89,9
1,58
#
| 1J8
0,9
—
50—
.
1
2,8
5,2
92,0
1,44
0,24
6
51°
>
—
2
" 6,0
8,3
85,7
• 2,28,
0,2*
9,5
—
•
<о
6
7,2
• 10.4
82,4
%
60
-
1
—
237<
6,9
9,4
83,7
t
—
0,0055
0,4
__
26
' 4,0
5,0
91,0
—
0,011
48
2,5
5,3
92,2
0,8
0.4
2
0,040
81—
>
1
~~8,6
5,9
85,5
0,38
0,25
1,5
8?°
00 .
0,08
—
—
о>
со
—
372
6,9
6,4
, 86,7
— .
\ —
—
—
1
0,08
—
—
—
__
—
}2
“7^
% 4
6,2
5,5
88,3
0,12
0,34
0,35
0,023
*
СО
: 22
0,0
7,3
92,7
0,54
«0,24
2,2
0.Q245
..V
17*
I
259
Из приводимых данных видно, что по мерс хода электролиза нейтрального раствора выход по току понижался
(главным образом за счет увеличения выделения Ог). Прибавка
НС1 понижает как выделение 02, так и катодное восстановление,
повышая выход по току. При 50—5F выход по току (при прочих равных условиях) значительно выше, чем при 15°.
2. Рис. 103 показывает данные Шпитальского и др.60 о влиянии степени кислотности электролита на процент выхода по току
и количество хлора, выделяющегося в виде газа. Электролиз начат с раствором NaCl, содержавшим NazCKX По ходу электролиза
через равные промежутки времени
добавлялась разбавленная соляная
кислота в количестве, соответствующем переводу 10% CrCV' в
СГ2О7" по обратному уравнению (118).
Из кривых диаграммы авторы
делают вывод, что оптимальной
является кислотность, при которой
отношение СГ2О7" : СЮ4" близко
к 1 : 1. Большая кислотность значительно увеличивает выделение СЬ, не изменяя заметно процента выхода по току, а меньшая кислотность сильно снижает
выход по току.
■3. В табл. 84 приведены данные Шпйтальского и др.60 о влиянии величины добавки бихромата, из которых видно, что для
’■ Таблица 84. Процент выхода по току и процент восстановления при электролизе 25%-ных растворов NaCl,содержа щ и х 0,2, 3 и 5% NajC^Pf^
Количество вмпер-чвеов
0-10
10—20
20-30
30—4oj 40-50
50-80
80-80
90-130
130-150
'5
. О
И . -
= 5?
При 0,2% Na2Cr207
ч
95
93
89
85
79*
_
в *
Н Н
1 с
При 3% Na2Cr207
91 '
95
94,5
94,5
94
94
93
—
—
sз с
о
о*
С 1
При 5% Na2Cr207 %
88
92
92
96
96
96
96
95
93
•
га
и «
о —
ш =
При 0,2% Na2Cr207
2
2'
4
а
9
•V
—
—
—
—
<D
£ ч
s а
При 3% Na2Cr207
' 2
2
1.5
/
1,5
1
1
Is
—
—
go
Iх
С ,
При 5%/Na2Cr207
%
1 ,4 —~~
1
3
4
'4
1
1
\
0
0
0
0
1 Плотность тока один A/cxt1, концентрация тока один А/200 мл, т-ра 65—70°
Рис. 103. Влияние кислотности
электролита на выход по току и
на выделение С12 при электролизе
раствора NaCl с платиновым анодом.
продолжительного ведения электролиза добавка бихромата
в 0,2% не дает устойчивых результатов и необходима большая
концентрация бихромата.
4. В табл. 85 приведены данные исследований Эттсля о влиянии различных добавок на ход электролиза раствора NaCl'npH
10 и 50°. Из приводимых данных видно, что добавка NaOH,
Са(ОН)г, СаСЬ и NaHCOs повышает выход по току в основном
за счет уменьшения катодного восстановления. Наибольший выход (78%) получается при добавке СаСЬ. Еще выше в!>1ход по
току (82%) при электролизе раствора, содержащего только
СаСЬ. При 50° при большинстве добавок уменьшается процент
восстановления, но увеличивается процент выделения СЬ. Количество гипохлоритного кислорода при 50° большей , частью
ниже, чем при 10°.
Таблица 85. Данные Эттеля об электролизе растворов КаС1
содержащего примеси NaOH, Са(ОИ)2, СаС12, НаНСОя 11 и 656
о.
о
в
g
'*
^1>аств<^
Колич,
' часов
Процент
выхода
Процент
восста¬
новления
Процент
выделения О,
г гипохлоритного
кислорода
(па весь раствор)
ю» 1
50е
10е
*50®
10* |
50®
10® |
50®
10®
50®
1
25 г NaCl (нейтр.) . . .
7
4
32,3
33,1
51,4
54,5
16,3
12.4
2,76
1,15
2
25 г NaCl + l°/n NaOH .
3 .
3
5V
52,8
10.3
\л
31,6
46
—
—
3
25 г NaCl + 3 г Са(ОН)2
7,5
5
42,3
50,6
40,8
29,1
17
20,3
2,65
1,54
4
25 г NaCl + 2,5 г СаС12 .
4,5
—
78,1
—
13,8
—
8,1
—
0,97
5
25 г NaCl -f- 0,8 г NaHCO,
5
5
51,9
41,2
34,7
36,8
14,2
22
1,42
1,42
6
25 г NaCl -f- 2,4 г NaHCOj
—
5
—
51,6
—
23,2
25,8
0,24
7
30 г СаС12
0
4
-ч»—
4
85,2
82,6
3,5
6^
1U
10,9
2,54
0,90
Примечание. 10 и 50° показывают температуру проведения опытов
Для опытов с прибавкой Са(ОНЬ и NaHCOj 0,8 г температура была не 10°,
5. Табл. 86 показывает данные исследований Бергер-Карлсона
о влиянии разных добавок на ход электролиза, из которых
видно влияние СаСЬ, бихромата, хромата, кислоты и т. д. Из
данных таблицы видно, что наибольший выход по току (93%)
получается в опыте 15 при добавке К2СГ2О7 и СаСЬ. Хороший
выход (90%) получается также в опытах И и 14 при добавке
СаСЬ или К2СЮ4 и СаСЬ. Добавки NaOH и СаО понижают процент восстановления (опыты 5—9), но в некоторых случаях повышают процент выделения Ог; чем выше концентрация
NaOH, тем больше выделение О2. Кислая среда без добавки хромата или СаСЬ уменьшает выделение Ог, но сильно увеличивает
восстановление, так что в общем процент выхода по току падает. Добавка FeCb сильно увеличивает выделение Ог. При добавке СоСЬ процент выхода падает до нуля.
,6. Табл. 87 приводит данные Эттеля 056 по электролизу раствора СаСЬ, из которых видно, что улучшение использования
тока происходит постепенно (в основном от уменьшения восстановления), именно по мере, постепенного образования осадка
261
1
Таблица ДО. Данные Бергер-Карлсона об электролите р а с т »»<. -
ров NaCl и KGI с добавками Ка^гй04, FcCl,, CoCI3, NaOH, CaO, MCI, C.iOl
MgCl* КаСг207ь^ и 12
°;0 использования тока
а
о
е
g
*
Раствор
/
Реакция
на
образован.
| акт. хл.
на восстановление
на
выделение
о.
-1
Л
6
Ш
1
300 г КС1
ней¬
тральная
45
35
20
4,1
2
300 г КС!+2 г К2СЮ4
■
64
0-1
36
4,5
3
300 г КС1+2 г FeCl,
•
20
56
24
4,0
4
300 г КС1 + 2 г СоСЦ ' .
»
0
5-10
60-100
3,9
5
300 г NaCl + 4 г NaOH ......
щелочи.
40
35
25'
4,3
6
300 г NaCl+ 12 г NaOH .....
п
59
2
39
4,6
7
300 г NaCl + 40 г NaOH
п '
36
2
1 62 .
1 27
4.0
8
300 г NaCl + 8 г СаО
в
. 60
13
5.1
9
300 г КС1 + 8 г СаО
\
т
47
27
16
5.3
10
250 г КС1 + 2 г НС1
KHCJL
28
65
7
4,3
11
300 г КС1+4 г СаС12
п
90
2
8
4.6
12
250 г КС1 + 2 г MgCl2
»
41
49
10
4,2
13
300 г КС1+2 г К2Сг207+1 г НС1
300 г КС1 + 4 г К2Сг04 + 4 г СаС12
п
87
1,5
11,5
4,6
v 14
п
90
0—0,5
10
4.4
15
300 г КС1 + 4 г К,Сг207 4- 4 г СаС12
93
0-1
7
4,6
16
300 г КС14- 2 г К2СЮ4 4- 4 г MgCl2
п
85
2
13
4,6
ч
Примечание. Опыты проводились с 500 мл раствора (в стеклянной
колбе при 70°. Анод платиновый, катод медный, сила- тока 7 А.
Са(ОН)г по ходу электролиза. Плотность тока при опытах
Эттеля была 990 А /л2, температура 75°, напряжение 3,8—4 V.
>
Таблица 87. Данные Эттеля об электролизе раствора
СаС1а и и «и
Количество часов от начала электролиза ...
хи
Чг
1
3
. 5
8
10
22
\
Процент выхода по току .
/ ,
71,8
76,3
78,2
79,7
83,1
81,1
81,9
83,3
Процент восстановления
24,1
12,3
9.3
3,8
4,0
6,4
6,7
4,2
7. Табл. 88 показывает данные Шпитальского й др. *® о влиянии анодной плотности тока на ход электролиза и у на расход
'Энергии при электролизе раствора NaCl, содержащего бихромат
(данные средние за 80 час.). Из данных таблицы видно, что выделение Oi почти одинаково для,всех взятых величин плотности
262 ,
тока, а катодное носстановленис увеличивается при плотности
тока 0,08 А/с/и2. Последнее объясняется по Праузнитцу74 малой
прочностью хроматной диафрагмы при столь низкой плотности
тока. Расход.энергии повышается с увеличением плотности тока,
хотя и не прямо пропорционально. Для уменьшения площади анодов (ввиду дороговизны платины) согласно данных таблицы 88,
оптимальной плотностью тока следует считать 0,5 А/см*.
Таблица 8S. Влияние анодной плотности тока на электролиз
раствора NaCl с платиновыми анодами
1
Плотность тока в А/ел* . . .'
1
0,08
0,5
1.0
2,0
Процент выхода по току
82,4
91,2
89,7
91
Процент восстановления
9,3
1.8
2.0
1,3
Процент выделения Оо
Относител! ная поверхность анода (принимая за 100 поверхность при плот¬
8,3
7.0
8.3
7,7
ности тока в 0,5 А /см*
625
100
50
25
Расход квт-ч на 1 кг NaCICV
6,3
6,4
7,3
7,2
Стационарная концентрация гипохлорита
0,03
0,05
0,09
0,22
8. Табл. 89 показывает данные Шпитальского и др.60 о влия-1
нии концентрации хлорида и хлората на выход по току при
электролизе раствора NaCl, содержащего бихромат. Из этих
данных видно, что снижение концентрации NaCl ниже 15%
сильно уменьшает выход по току и что рост, концентрации
хлората при условии донасыщения электролита хлоридом
почти не отражается на выход но току.
Таблица 89. Влияние концентрации NaG и NaClOj на выход по
току (плотность то.ка 0,6 А/емг, концентрация тока 5А/л, температура 65—70°) **#
Процент NaCl* . .
23
21
18,5
15
11,8
8,9
24
22
, NaC103 . .
4
7
10
16
21,5
26
27,5
30
' , выхода по
току
94
94,5
93,5
93
88
77,5
91
91
9. Значительное влияние на выход по току имеет также концентрация тока1, поскольку при прочих равных условиях концентрация СЮ' тем ниже, чем меньше концентрация тока. Это
влияние изучали Мюллер и Коппе7S, которые нашли, что при
электролизе раствора NaCl, содержащего 0,2% бихромата при
;10°, выход по току был 93% при концентрации тока в 1,4 А/л и
87% при 8,4 А//, т. е. повышение концентрации тока в 6 раз
Дало снижение выхода по току на 6%. Однако Кацен и Соко-
*'Сила тока V амперах, деленная на объем электролита в литрах, обозначается в А/л.
263
ловe2h нашли, что при электролизе с большей концентрацией
бихромата (1,3%) и при более повышенной температуре концентрация тока не имеет такого влияния, и получили выход около
92% при концентрации тока в 4 и 8 А/л.
§ 4. Материал катодов и защита от катодного восстановления
При лабораторном получении хлоратов электролизом большей частью применяют платиновые электроды. В промышленной
практике стремятся заменить платину более дешевым материалом. В промышленности для катодов применяют большею частью железо или чугун,—реже медь, латунь, никель, графит
и т. д. Однако при электролизе растворов хлоридов без особых
добавок, катоды из железа, меди и подобных материалов быстро '
разъедаются и приходят в состояние, негодное для ведения
электролиза *.
Для уменьшения разъедания катодов и катодного восстановления в начале развития электролитического получения хлоратов электролиз вели в щелочной среде и в ваннах с диафрагмами. Однако щелочная среда, уменьшая катодное восстановление, увеличивает выделение О* (см. табл. 85, опыт 2, стр. 2(H),
а диафрагмы повышают вольтаж ванн, т. е. расход энергии. Поэтому эти способы борьбы с разъеданием катодов и катодным
восстановлением были оставлены и заменены прибавкой к электролиту особых примесей, имеющих защитное действие.
Особо удачным и наиболее распространенным в данное время
является предложенная Имгоффом2 и подробно исследованная
МюЛлером67 прибавка бихромата. Механизм реакции прибавки
бихромата полностью еще не изучен и по настоящее время кроме
вышеуказанного подкисляющего действия (стр. 258). Предполагается, что на катоде образуется пленка хромихромата, препятствующая соприкосновению ионов СЮ' с металлом катода и
атомным водородом, отчего прекращается или во всяком случае
уменьшается катодное восстановление (табл. 84 и опыты 13—16,
табл. 86) и коррозия кйтодов. В щелочной среде защитной
пленки почти не образуется (табл. 86, опыт 5); в сильно кислой
среде действие бихромата также неполно, так что прибавка бихромата наиболее эффективна при электролизе в слабокислой
среде.
Примерно такое же действие, как прибавка бихромата, оказывает прибавка солей кальция или магния. Как уже указывалось
выше, соли кальция при электролизе образуют у катода мало-
1 На меди, как и на платине, восстановление гипохлорита происходит
только .в нейтральной и кислой среде и не происходит в щелочной среде.
На железе восстановление происходит в любой среде. Повышение температуры усиливает катодное восстановление^ Катодное восстановление хлората
во много раз меньше, чем гипохлорита, и при этом на железе больше, чем
на меди.
*• Герм. пат. 110420.
264 . '
/
растворимый осадок Са(ОН)г, который оседает на катоде,
образуй на нем защитную пленку. Уменьшение катодного восстановления при электролизе с прибавкой CaCU изучено »ттс-
лем и др. хорошо видно из табл. 85, 86 (опыты 11 и 12) и 87.
Из табл. 86 (опыт 15) видно также, что наивысший выход по току получен при комбинировании добавки бихромата
и СаСЬ.
Кроме бихромата и солей Са и Mg применяется добавка и
других веществ. Хорошее действие оказывает прибавка к электролиту солей ванадия (хлорид, сульфат или нитрат *), которое
не ослабляется от продолжительности электролиза и не требует
кислой'среды. При электролизе с добавкой солей ванадия.концентрация гипохлорита во все время электролиза весьма мала,
и например при опыте, приведенном в табл. 91, была всего
0,14 г/л при общей
концентрации хлора в
виде гипохлорита и
хлората в 64,2 г/л.
Также применяются ‘
добавки хлористого
церия 2 и ряда других
веществ. Однако по
Биллитеру в данное
время в промышленности чаще всего применяется добавка бихромата или солей ванадия.
Добавка бихромата имеет и отрицательную сторону, состоящую в том, что она вызывает некоторое загрязнение и желтоватую окраску получаемого хлората. Поэтому
Грубе и Борхардт78 предложили вместо добавки хромовых солей работать с хромированными катодами. При этом матово-
хромированные катоды оказались лучшими, чем глянцево-хромированные, что очевидно объясняется тем, что окисляющее
действие гипохлорита на хромирующий слой (с образованием
защитной пленки хромихромата) происходит легче на неровной матовой поверхности, чем на глянцевой. Практически при
продолжительном электролизе, как установили Кацен и Соколов,
матово-хромированные катоды дают все же худший эффект,
чем прибавки к электролизу бихромата.
Влияние добавок бихромата и солей Са и Mg уже было приведено при изучении электролиза в слабокислой среде
(табл. 84—87). Ниже приводим некоторые данные о влиянии на
катодное восстановление и на общий ход электролиза прибавок
к электролиту солей ванадия и некоторых других веществ и при-
Количество амп./час.
Рис. 104. Влияние некоторых веществ на процент восстановления по ходу электролиза нейтрального раствора КС1 с платиновыми электродами.
‘Герм, пат.'174128. %
* Франц, пат. 421618 я герм. пат. 235706.
, :бб
меиеиия хромированных и нехромиропанных железных, медных
и никелевых катодов с добавкой бихромата и без таковой.
1. Табл. 90 и рис. 104 показывают данные Шлеттера 7$ о влиянии некоторых солей, не участвующих в процессе электролиза,
на процент выхода по току при электролизе раствора с концентрацией КС1 в 220 г/л с платиновыми анодами. Номера линий на
рис. 104 относятся к порядковым номерам солей на табл. 90.
Уменьшение выхода по току в основном вызывалось увеличением процента катодного восстановления.
Таблица 90. Влияние примеси некоторых солей на электролиз растворов КС1626
Какая примесь
CuCI,
РЬОа
TICI.
SbCIs
SnCla
HgCI,
MCI.
AgCl
CdCla
ZnCl,
ММ по порядку
‘ 1
* 1
3 1
* 1
в 1
1 6 1
7
8 1
» 1
10
Количество
лримесн в г/л
0,5
0,21
0,50
0,50
0,50
0,37
0,50
0,25
0,14
0,12
Расход тока
1035
в ампер-часах
Процент выхо¬
1410
1785
1754
832
1031
705
1736
682
881
да по току .
91
88.2
75,4
66,9
66,6
64
63,5
37.8
37,4
37,i
I
Таблица 91. Влияние примеси соле
ванадияна электролиз раствора
NaCl
й
и
M
Количество изра¬
Содержание
Процент исполь¬
. опытов
сходованных
ампер-часов
кислорода в газах
зования тока
50
6,0
81,8
1
40
5,8
96,5
50
6,а
93,1
N
Всего 140
С
в среди. 90
60
6,0
94,5
II
60
6,0
90,5
70
5,0
—
Всего 190
ч . •
' —
в среди. 92,5
• 1
120
_
85,5
90
—
85,1
III
1 1
120
_
85
90
82,6
120
—
76,0
Всего 540
в среди. 83,0
IV*
126
13
74,0
126
•
7,5
. 84,8
'* Щелочной раствор.
266 '
По дополнительным данным Шлеттера действие этих солеи
зависит также от их концентрации (отнесенной к поверхности
электрода) и от природы материала катода.
2, Табл. 91 показывает влияние прибавки к электролиту солей ванадия. В опыте III выход по току стал падать ввиду разложения больше 50% хлорида и начала кристаллизации хлората в ванне.
3. Табл. 92 показывает опыты Грубе и Борхардта78 о влиянии на катодное восстановление материала к'атода, матового и
Таблица 92. Влияние материала катода, хромировании и добавки хромата на восстановление при электролизе
раствора NaCl 5,1 N при анодах из гладкой платины.626
Какой метала
Процент восстановления
в нейтральной среде
Процент восстановления
в кислой среде
чистый
металл
_
хромирование
добавка
хрома¬
та
чистый
металл
хромирование
добавка
хрома¬
та
глянце¬
во.?
мато¬
вое
глянце-
воо
мато¬
вое
Железо
64 4
33,4
1.2
1.0
32,6
11,8
0
1.7
Медь
65,4
8,9
0,5
33,2
27,5
—
1.0
Никель
и
58,3
9,8
27,4
14,6
глянцевого хромирования и прибавки хромата при электролизе
5,1 N, раствора NaCl и анодах из гладкой платины.
Из данных табл. 92 видно следующее: при нехромированных
катодах без прибавки хромата «катодное восстановление велико, но в кислой среде восстановление почти в два раза ниже,
Таблица 93. Электролиз 25%-ного раствора NaCl с матово-
хромированным железным катодом при 50°
Расход тока в ампер-час.
0-10
20-30
30—40
40—50
50—60
60—70
70—80
80-90
90—100
100-110
Процент
выходапо
току
88,1
81,1
94
92,7
1
96,5
88,7
91,3
90.5
92,0
91,3
Процент
восстано¬
вления
6,5
4.9
1.3
2,2
0,8
1.0
2,1
2,3
2,1
0,5
П р и м е ч а н и е. До начала электролиза к электролиту было приба-
„ влево 3 мл ' 1 Ы раствора НС1; после 30 ампер-часов был сделан
перерыв в электролизе на сутки.
Л
267
чем в нейтральной среде: для Fe 32,6 *и 64,4%, для меди 33,2 и
65,4% и для Ni 27,4 и 58,3%.
Матовое хромирование, как и прибавка хромата, даст почти
одинаковый эффект полного или почти полного прекращения
катодного восстановления.
.Глянцевое хромирование лишь отчасти уменьшает катодное
восстановление.
4. Табл. 93—95 показывают данные Кацена и Соколова 620 об
изменении эффективности снижения катодного восстановления
хромированными катодами при длительном электролизе и о влиянии перерывов в электролизе и прибавок кислоты к электролиту. Электролизу подвергался 25%-ный раствор NaCl (по
500 мл) при температуре 50°, анодной и катодной плотности
тока в 0,25 А/см2, силе тока в 2 А, концентрации тока в 4 А /л и
анодах из гладкой платины.
Таблица 94.Электролиз 25°/0-ного раствора NaCl с глянцево-хромированным железным катодом при 50° ^
Расход тока в ампер-часах . . .
2
4
5
6,5
8
10
47
51,5
53,5
Процент выхода
по току ....
13,5
48,4
51,7
52
4 24
32,1
94
94,8
95,1
Процент восстановления . . .
81,5
47,2
'45,8
43,2
71,6
63,2
2,9
2
2,8
Примечание. До начала электролиза к электролиту было прибавлено 10 мл 1 N раствора НО; после расхода 2 и 47 ампер-часов прибавлено
еще по 5 лл 1 N раствора НС1. После расход» 10 ампер-часов был сделан
перерыв в подаче тока на 30 мин.; напряжение на ванне было .3,92—4 V;
содержание гипохлорита в электролите было 0,13—0,15 экв/л.
Таблица 95. Электролиз 25%-ного раствора NaCl с матово-
хромированным медным катодом при 50°
Расход тока в ампер-
часах . . •
‘ 2
4
7
*
8,5
11,5/
■7
46
50
52
Процент/выхода по току
79
86,2
90
77,1
95,2
95,6
95,6
96,8
Процент восстановле-
i ния
18,6
10
13,4
19,6
1
0
0.9
0,5
Примечание. До начала электролиза прибавлено 10 мл 1 N раствора НС1 и (после 49 ампер-часов еще 5 мл; после 8,5 ампер-часов был
сделан перерыв в подаче тока на несколько минут; напряжение на ванне
было 3,7—3,78 V; содержание гипохлорита в электролите было 0,12—
0,16 экв/л.
Во всех трех’опытах электролит к концу желтел и хром сходил с катодов. Авторы делают выцод, что действие хромирован-
268 . / , • • * ; * v'
ных катодов заключается в растворении слоя хрома в электролите с образованием хромовой соли, которая дальше действует
как обычная прибавка ее; перерывы в подаче тока благоприятствуют растворению этого слоя; при матовой неровной поверхности катода растворение происходит быстрее, чем при глянцевой поверхности. Общий вывод авторов заключается в нецелесообразности замены прибавки хромата хромированием катодов.
§ 5. Общие замечания по электролизу с платиновыми анодами
Исходя из изложенного в параграфах 1—4, можно сделать
следующие выводы об оптимальных условиях получения хлоратов электролизом при условии применения платиновых
анодов.
1. Электролиз должен вестись с содержанием хромовой соли
в 10—20 г А и в слабокислой среде так, чтобы отношение
СГ2О7" к СЮ4" было близко к 1 :1.
2. Ввиду выделения хлора из ванн надо для поддержания
в электролите вышеуказанного отношения CrgCV : С1О4" в течение всего времени ведения электролиза периодически или
непрерывно добавлять в ванну разбавленную соляную
кислоту.
3. Для уменьшения выделения хлора из ванн электроды
должны быть целиком погружены в электролит и покрыты как
можно более толстым слоем электролита.
4. Температура электролита должна поддерживаться в пределах 75—80°.
5. Концентрация хлорида в электролите не должна опускаться ниже 14—15%.
6. Концентрация хлората в электролите не должна доходить
До состояния, близкого к насыщению для данной температуры
электролиза во избежание возможного короткого замыкания
кристаллами, оседающими между электродами.
7. Аноды лучше применять из гладкой платины, так как платинированные аноды менее стойки. Анодная плотность тока желательна не ниже 0,5 А/ся2.
8. При указанных условиях кислотности и концентрации би-
.хроматов (п. 1) катоды из железа и меди достаточно стойки;
катодная плотность тока обычно 0,2 А/ся2.
9. При содержании бихромата 10—20 т/л и температуре электролита в 75—80° концентрацию тока можно держать до
8—10 А /л.
При соблюдении вышеприведенных условий
катодное восстановление сводится к нулю, вы-
- деление газообразного кислорода минимально
и выход.по току на хлорат достигает 90—95%.
•I
2Б9
ГЛАВА 19
ЭЛЕКТРОЛИЗ С МАГНЕТИТОВЫМИ, УГОЛЬНЫМИ
И ГРАФИТОВЫМИ АНОДАМИ
§ 1. Электролиз с магнетитовыми анодами
В то время как катоды почти с самого возникновения
электролитического получения хлоратов делались не из платины,
для анодов платина долго применялась как единственный материал, с которым получались достаточно хорошие результаты
электролиза. Однако вследствие необходимости крупных капитальных затрат на платину и частичного износа платины при
электролизе, давно стали изыскивать другие подходящие материалы Для анодов. Такими материалами, больше всего нашедшими себе применение на многих промышленных установках,
являются магнетит и графит.
Впервые магнетитовые аноды были изготовлены Блекманом
в 1896 г. и для получения хлоратов впервые применены в 1910 г.
фирмой Грисгейм Электрон в Германии1. Аноды состоят из
сплавленной закиси-окиси железа (Fe3<>4) с небольшим количеством примесей (кремнекислота и др.), сравнительно дешевы и
очень стойки в условиях электролиза — обычно через 3—4 года
употребления на таких анодах не обнаруживается заметного износа. Основными недостатками магнетитовых анодов являются:
хрупкость, растрескивание при резкой перемене температуры,
большое удельное сопротивление (порядка 0,03—0,05 ома на ел2),
каталитическое ускорение разложения СЮ' с выделением Ог,
меньшее перенапряжение для разряда ОН', чем на платиновых
анодах. Чем выше плотность тока при электролизе с магнетитовыми анодами, тем больше выделение Ог и тем меньше стойкость анодов, почему обычно рекомендуется держать анодную
плотность тока всего 0,01—0,02 А /см2. Однако известно применение в промышленной практике и гораздо более высокой плотности тока без сильного износа анодов.
Для избежания разряда ОН' электролиз надо вести в слабокислой среде. При этом увеличивается химическое образование
хлората и понижается концентрация СЮ', что благоприятствует
уменьшению каталитического разложения СЮ' с выделением О»
и уменьшается разряд ионов СЮ'. Увеличению химического
образования хлората благоприятствует также ведение электролиза при повышенной температуре (65—70°). Для уменьшения
омического сопротивления аноды делают полыми с покрытием
их внутри электролитически осажденной медью или в массу магнетита забивают стержни или сетку из хорошо проводящего ток
1 Эта фирма долгое время была монополистом изготовления магнетитовых аиодов. В настоящее время эти аноды изготовляются еще в Бусси
в Италии, в Земковицах в Польше, в Швеции. Большое исследование по
изготовлению их проведено Н. Н. Ворониным' и в последнее время ГИПХ'ом.
270 < -
металла. При электролизе слабокислого электролита при 65—
70° и низкой плотности тока указанное выделение Ог делается
небольшим и выход по току может достигнуть 90%.
Исходным материалом для приготовления магнетитовых анодов могут служить любые продукты, содержащие технически
чистый ИегОз (например колчеданные огарки и т. п.). Такие продукты плавят в электропечи и полученный плав сливают в специальные формы. По охлаждении полученные электроды подвергаются отжигу. Во время плавки происходит образование
Fea04 из БегОз и одновременно улетучивается большинство примесей (магнетит плавится при 1600°). Фогель85 считает весьма
важным для получения хорошо устойчивых анодов, чтобы примесь кремнекислоты в магнетите не превышала 3% и чтобы применялась тщательная закалка .
медиа* ши^а^
анодов. — i
По некоторым данным хоро-
шие аноды получаются сжига- 'мт ^ Маг£тит
нием железных опилок в струе \
кислорода. П. П. Федотьев15 раз- Рис. 105. Магиетитовый анод,
работал метод приготовлений
магнетитовых анодов, исходя из окисления железных стержней
или труб водяным паром при 1000—1100°; при этом слой магнетита образуется на поверхности неокисленного железа, которое
служит проводником тока. Механическая прочность анодов,
изготовленных по П. П.- Федотьеву, достаточно высока и
благодаря большей гомогенности в их структуре они менее
чувствительны к колебаниям температуры. Большим недостатком таких анодов является их пористость.
Ульман5 приводит рисунок полого магнетитового анода
(рис. 105). Для подводки тока к внутренней поверхности анода
прикреплена медная шинка. Полость анода заполнена асфальтом или другим подходящим материалом.
Применяются аноды и в виде плит, стержней, прямоугольных
карманов и.т. д.
Приводим некоторые исследования Грубе и Пфундера 77 по
электролизу с магнетитовыми анодами при разных условиях.
1. Рис. 106 показывает ход электролиза 5,1 N раствора NaCl
(содержащим 0,3% хромата) при температуре 12°, силе тока 0,6 А
и анодной плотности тока 0,015 А /см*.
Как видно из кривой выхода тока, последний составлял в начале электролиза 86%, но затем постепенно снизился до 41%.
Такое снижение выхода тока доказывает, йто при электролизе
с магнетитовым анодом происходят побочные реакции с выделением Ог (разряд ОН', разложение СЮ'), поскольку восстановления не было совсем (благодаря хромату), а разряд СЮ' по
уравнению (103) даёт 66,7 % выхода по току.
2. Табл. 96 прказываёт влияние плотности тока при электро¬
лизе нейтрального 5,1 АГ раствора NaCl (содержащим 0,3% хромата) при 12®. , 1
' ! . , . • Ч
271
Из данных таблицы видно,
тем ниже выход по току и.
Рис. 106. Выход по теку и образование гипохлорита и кислорода при
электрслизе нейтрального раствора
NaCl при 12° и анодной плотности
тока, равной 0,015 А/сж8 с магне-
титовым анодом.
что чем выше плотность тока,
выше вольтаж, а также что
при любой плотности тока
% выхода по току снижается по
мере продолжения электролиза.
3. Табл. 97 приводит данные
электролиза слабокислого раствора NaCl (содержащего бихромат 2 г/л) при 65° и анодной
плотности тока 0,01 А/an2. Напряжение на клеммах ванны
было 3,4—3,6 V.
Данные этой таблицы показывают, что в условиях слабокислой бихроматной среды и
повышенной температуры получается высокий выход по
току, мало изменяющийся
при продолжительном электролизе.
Таблица 96. Влияииё плотности тока на электролиз с магнетит о в ы м-и анодами нейтрального раствора NaCl 5,1 N, со-
держащего 0,3% хромата при 12°686
Плотность
тока А/см2
0,08
-
0,05
0,С2 ;
0,01
Прошло
часов от
начала
электролиза
0,5
3
1
2
4
6
10
2
6
10
16
21
1
6
И
*
Процент
выхода по
току
63
52
69
61
56
52
49
87
82
76
68
60
88
80
75
Гипохло-
рнтный кислород
в г/л
0,42
5,02
ИДО
1,52
)
2,.64
4,16
0,56
и'г
2,24
3,12
5,04
5,68
0,80
3,44
5,60
Напряже¬
ние
в вольтах
8,6
8,7
7,8
1
7,9
1
4,4
4,5
4,2
§ 2. Электролиз с угольными и графитовыми анодами
Попытки замены платиновых анодов угольными были сделаны
Карлсоном еще*в самом начале развития электролитического получения хлоратов. Однако' угольные аноды весьма быстро изна-
' > ' 4'
272 * ,
Таблица 97. Электролиз слабо кислого рлстпора NaCl 5,1 N
с м а г и е т и т о в ы м и а н о д а м и п р и 65° и анодной плотности тока 0,01
А/см* т
Прошло часов ст начала
электролиза
Vl
2*
3
5
7
9*
11
14
18*
20
25.
Процент выхода по току .
87
86
90
91
91
92
91
91
91
90
91
Хлоратный кислород в г/л
—
2
2,6
4.6
5,7
7
8.7
11,7
15,5
16
19.6
Гипохлоритный кислород
в г/л
—
0,32
0,56
0,48
0,40
0,42
0,64
0,48
0,24
0,16
0,16
* Пвсле 2, 9 и 18 часов прибавлено по 0,5 мл концентрированной соляной кислоты.
шивались, а получаемый хлорат загрязнялся и окрашивался
в темный цвет продуктами разрушения анодов.
Гораздо более устойчивыми, чем угольные аноды, оказались
графитовые аноды, которые были впервые предложены Гиббсом
в 1905 г.1 и применены в заводской хлоратной установке Гас-
лингером в 1908 г.
Электролиз с графитовыми ил№ч угольными анодами проходит несколько иначе, чем с платиновыми или магнетитовыми
анодами. Основные отличия зависят от того, что в то время как
при платиновых и магнетитовых анодах разряд ионов происходит только на поверхности анодов, при графитовых или угольных анодах разряд ионов происходит и внутри анодов, поскольку последние пористы. Однако плотность тока сильно падает по мере перехода от поверхности вглубь электрода. Внутри пор электролиз идет с незначительной плотностью тока,
что благоприятствует разряду ОН', выделению кислорода и
разрушению анодов. Кроме того смешение электролита внутри
пор анодов с электролитом, содержащимся во всей ванне,
затруднительно, почему в порах анодов получается обеднение
электролита ионами хлора; последнее обстоятельство вызывает усиление разряда СЮ' по уравнению (103) и разряда ОН'
по уравнению (ПО), т. е. увеличение расхода тока на образование Ог за счет меньшего образования хлората.
Получающийся Ог не весь уходит в хлоргаз, а частично
реагирует с углем, который сгорает, образуя ООг. Такое действие
кислорода является весьма вредным в отношении износа анодов, тем более что химический износ анодов от образования
СОг сопровождается механическим разрушением их с образованием угольного шлама.
Образование Ог и износ анодов тем больше, чем выше температура электролиза и зависит от плотности тока. С ростом,
'* Ам. пат. 82772 0905). .
2 Начиная с, определенного оптимума.
v
18 За*. 179. —Шрайбман.
273
лоследнс." из:.ос спадали Понижается, затем расти' И’.фс
анодов (особенно мфсаничсЫий) тем больше, чем мугчс с<(рт
угля и чем неравномеЬнее структура угля.
Образующаяся СОь приносит и некоторую пользу, црекольху,.
растворяясь в электролите, .обусловливает кислотностг последнего, что увеличивает химическое образование хлоратФ Одна|ко
вред от расхода тока на 1 образование Ог значительно превышает пользу от подкисления электролита образующимся
СОг, почему выход тйка при! электролизе нейтрального раствора
NaCl ниже при уголь [ых и Графитовых анодах, чем при платиновых. В случае ела юкиелфго раствора NaCl, образование 02-
при электролизе на yi эльнь!Х и графитовых анодах уменьшается
(но не так значитель ю как, при платиновых анодах) И общий
выход по току мо; ет достигнуть 90% и даже несколько
выше. Поэтому и п и графитовых анодах электролиз ведут
в слабокислой бихро атной йреде с добавкой по ходу электро1
лиза разбавленной се [яной кислоты. По данным некоторых последователей кислотн 1сть при электролизе с графитовыми анодами должна быть вшше, ч$м при платиновых анодах!, в 3--4
раза (ср. рис. 103 и 1(1)7). • * ,
Углерод в условиях электролира не реагирует с хлором, fjo
если в угле содержатся битумы и т. п. соединения, то они образуют с хлором солянуЧо кислоту и хлорорганические соединения
по следующему схематическому уравнению (Ферстер 10, стр. 087):
СоНш -|4 С12 -v CnH(m_uCl + НС1. i. (119)
Практически обычно в применяемых графитовых аИодах содержание битумов и других хлорируемых органических [веществ
ничтожно, но в них часто Содержатся вещества, применяемые
длй импрегнирования анодов. Последнее применяется для устранения электролиза в лорах анодов (пропитка парафином, льняным маслом, смолой г другими веществами). Однако образование НС1 по уравнении (119)'из импрегнированных анодов тоже
весьма мало, тем бол< е, что электроды после импрегнйрования
обычно подвергаются особой обработке (хлорирование и т. д.)
для увеличения стойк >сти импрегнирующего вещества в ванне.
Повышение темпер ггуры увеличивает химический и механический износ графитовых анодов, почему при электролизе
обычно поддерживаю! температуру не выше 40—50°. Еще более низкая температура уже замедляет химическое образование
хлората (см. рис. 22, стр. 60).
Плотность тока при графитовых анодах обычно применяют
более низкую, чем при платиновых анодах, — именно 0,03 —
0,05 А /см2, так как пфи более высокой плотности тока износ
анодов больше.
Хотя выход по току даже при слабокислой среде и 40 — 50’
при графитовых анодак обычно несколько ниже, чем прй платиновых анодах, расход энергии обычно меньше при графитовых
анодах, так как благодаря применению в последнем случае меньшей плотности тока меньше и напряжение (обычно 3,4—3,6 V).
Ф
274 ' •
Графитовые аноды хорошего качества расходуются в количестве 10—30 лт на тонну хлората. Колебания зависят от обработки анодов (импрегнирование и т. д.) и условий электролиза
(температура, плотность тока, концентрация тока *, кислотность).
Поскольку качество анодов имеет весьма важное значение
для электролиза, необходимо их испытание. Ферстер10 предложил следующую методику испытания графитовых и угольных анодов. Из испытуемого анода вырезают пластинку размерами в 7 X 4,5 си. В одну из торцевых сторон пластинки ввинчивают графитовый стерженек или платиновый нипелечск, служащий для подвеса пластинки и для подводки тока. Электролиз ведут в стеклянном сосуде, плотно закрывающемся пробкой и имеющем приспособления для подвода тока, для отвода
газов (выделяющихся при электролизе) и для отбора проб электролита. В этот электролизер наливают 250 ил раствора, содержащего NaCl 250 г/л и Na2CrO« 2 г/л (но не ШгСггОт), и
помещают пластинку испытуемого анода так, чтобы она целиком была погружена в раствор. Электролиз ведут при 60°
6'час., периодически анализируя выделяющиеся газы на СОг, О?
и Н*, а электролит на содержание активного кислорода. Количество прошедшего тока измеряют по медному кулонометру,
включаемому последовательно с электролизером. По данным
кулонометра и количеству активного кислорода в электролите
рассчитывают процент выхода по току. По анализу газов рассчитывают расход тока на анодное окисление и на катодное
восстановление. Общий износ графита определяют по разнице
веса промытой й просушенной пластинки до и после опыта.
Износ от механического разрушения определяется по весу
промытого и высушенного шлама, образовавшегося при электролизе.
Примечание. Быстрый метод испытания графитовых электродов
разработали Сирак и Иоффе {в ГИПХ’е). Метод состоит в электролизе
/ с образцом данного электрода разбавленного раствора НС1 10 г/л в ячейке
с проточным электролитом без диафрагмы. (Однако этот метод не имеет
целью исследование 'Пригодности электродов для электролитического получения хлоратов).'
Ниже приводим некоторые исследования Ферстера, Бенцига,
Арндта и Кацена и Соколова по электролизу с графитовыми и
угольными анодами.
1. Табл. 98 показывает данные Ферстера10 по испытанию нескольких угольных и графитовых анодов вышеописанным методом. Опыты проводились каждый по 6 час. (370 ампер-ча!:.)
с раствором NaCl 250 r/л и NajCrOi 2 г/л при силе тока в 2,1 А и
температуре 60°. Катодов было 2, поверхность каждого из которых была равна поверхности анода.
Из данных таблицы видно, что наилучшим оказался анод из
Ачессоновского графита.
1 См. стр. 263, примечание. ’
18*
275
Таблица 98. Д а н и ы е Ф е р с т с р а по испытанию у г о л mi ы х и графитовых анодов при электролизе нейтрального раствора NaCl при 60°10
м
' Материал анодов
Объем
пор В °/о
использования
тока для образования
Потери пега
анода в г от
образования
пп
к объему анода
золы
актнвн.
о,
газообразного Оа
СО,
шлама
1
Ачессоновский графит
#
22,9
0,8
69
7,5
2
Искусственный графит от Le
Carbon (Париж)
23,2
3,0
54
‘ 16
_
„ ,
3
Ретортный уголь очень плотный,
таблитчатого строения . . .
11,2
0,4
63
12
7,3
3,7
4
Ретортный уголь плотный, мелкозернистый >
12,6
2,3
52
24
10,4
3,4
5
Искусственный уголь, плотный
мягкий
22,2
1,8
61
20
_
6
Искусственный уголь очень
мелкозернистый, твердый . .
21.1
2,3
56
27
13
10,6
7
Искусственный уголь очень
твердый
,
6,1
45
31
_,
1
8
Искусственный уголь весьма
твердый
22,5
1,1
46
37
16
5
9
Искусственный уголь мягкий
# легко обрабатываемый . .
27,8
42
44
41
16,1
32,5
2. По исследованиям Бенцига1в при лабораторном исследовании электролиза подкисленного 5,1 N раствора* NaCl при плотности тока 0,05 А/см*, расход тока на сжигание графитового, анода
в ОО* составлял 1,5% при 40° и 5% ери 50°. /
д Рис. 107. Влияние кислотности электролита на
выход по току и на выделение С1а при электролизе раствора NaCl с графитовым анодом.
3. Табл. 99 и рис. 107 показывают данные Кацена и Соколова о влиянии степени кислотности раствора на выход
хлората при электролизе с графитовым анодом. Электролит до
электролиза содержал NaCl 25% и NajCr^O 1,3%. Концентрация
тока была 4 А'/л, анодная плотность тока 0,05 А/ом2, сила
той! 4 А, анод был приготовлен из смеси естественного гра-
276 ' ;
Таблица 99. Влияние кислотности паэлектроли.1 25’У0-ного раствора NaCl с графитовыми анодами
Процейт перевода СгаО?
в СгО*
0
10
20
30
40
50
60
70
80
90
100
Процент окисления ....
84,7
88,5
89,3
87,1
83,5
83,3
82,5
78,9
79,4
79,1
76,1
/
Выделёние С1а мг/час . .
18
7,7
6.2
1
0,9
0,45
—
—
—
—
—
фита с нефтяным коксом и пеком. Изменение кислотности
электролита достигалось периодической добавкой щелочи в таком количестве, чтобы 10% бихромата переводились в хромат
по уравнению: \
Na2Cr207 + 2NaOH = 2Na2CrO« + НгО (120)
Из данных таблицы и диаграммы видно, что оптимальная
кислотность получается при отношении СггО?" к СгО«", как 4:1,
т. е. когда в электролите содержится 20% хромата и 80% бихромата. При отношении СггСЬ"
к СггО*" меньше чем 4:1. умень- *
шается процент тока на окисление \го
ввиду увеличения выделения СОг. §
4. Рис. 108 показывает данные
Ферстера10 об образовании Ог при ,
электролизе нейтрального 20%-ного
раствора КС1, содержащего К2СЮ4
2 r/л при низкой температуре
с платиновым и угольным анодом.
Анодная плотность тока была
0,033 А/см2 на угле и 0,043 А/с/и2
на платине. Концентрация гипохлорита достигла при стационарном состоянии электролиза 0,42 г на платине и всего 0,2 г
на угле.
Из кривых диаграммы видно, что выделение 02 происходит
различно для начала электролиза и после установления стационарного состояния. В начале электролиза выделение 02 больше
на угле, чем на платине, а при стационарном состоянии электролиза выделение 02 больше на платине, чем на угле. Такая разница получается потому, что по мере продолжения электролиза
при угольном аноде электролит становится слабокислым от растворения образующейся СОг, отчего увеличивается химическое
образование хлората. При платиновом аноде электролит остается
все время нейтральным, почему химическое образование хлората
не увеличивается.
время $ часах
Рис. 108. Образование кислорода
по ходу электролиза нейтрального раствора КС1 при низкой
температуре с угольным и с пла
тиновым анодом.
277
Примечание. Как далее указывает Фсрстер, лри более высокой
температуре электролиза разряд ОН' в порах угля настолько увеличивается,
что выделение Оа становится ббльшим при угле, чем при платине, и после
установления стационарного состояния электролиза.
5. Табл. 100 показывает данные Кацена <и Соколова62* о влиянии плотности тока на разрушение графитовых анодов при электролизе 25%-ного раствора NaCl.
Таблица 100. Влияние аноднойплотности тока на разрушение графитовых анодов при электролизе 25%-ного раствора
NaCl
Плотность тока в А/см2
0,04
0,14 .
0,50
Потеря веса анода в г на\ кг NaC103
59,1
121,2
140,0
» * . . , на 1000 А/час
13,8
61,1
68,3
Процент химического разрушения .
60
4 1,5
3,8
• . механического
40
58,5
96,2
Из данных таблицы видно, что с повышением плотности тока
химический износ анода уменьшается, но механический износ
настолько увеличивается, что общий износ анода значительно
возрастает (хотя и непрямо пропорционально увеличению плотности тока).
Зависимость разрушения анода от количества протекшего
тока показывает также табл. 101 Арндта и Фезе7в.
Таблица 101. Данные Арндта и Фезе о разрушении графитовых анодов при электролизе 25%-н ого раствора NaCl п ри 60°
(Анодная плотность тока = 0,1 А /см2)
Y
Процентлотери веса после пропускания
151 ампер-час.
302 ампер-час.
403 ампер-час.
Потеря веса в виде шлама .
, !.3
5,0
8,4
Потеря веса от образования
N
СО*
1,3
6,5
10,4
Общая' потеря веса . .
2,6
11,5
18,8
6. Табл. 102 показывает данные Кацена и Соколова62*
об электролизе с графитовыми анодами при 30, 50 и 70°. Аноды
были взяты фирмы Кребс. Сила тока 0,25 А, концентрация тока
1 А/л, анодная плотность тока 0,04 А/см2.
j Из данных таблицы видно, что оптимальной является темпе-
* ратура в 50°, так как выше 50° сильно возрастает химическое
разрушение' и общий износ анода и уменьшается выход по току,
а при 30° износ анодов лишь немного ’ ниже, чем при 50°, но
сильно понижается выход по току (ввиду уменьшения скорости
- химического образования .хлората, см. рис. 22).. {
278
Таблица 102. Влияние температуры на разрушение графитовых анодов при электролизе 20 ’/(,-н ого раствора NaCl
Температура . : .
30°
501
70\
Потеря веса анода в г
на 1 кг NaClOa
8,74
9,73
22,8
на 1000 ампер-час
4,4
6
13,1
Процент химического разрушения . ?
—
61
91
. ' механического разрушения .
; .—
39
6
„ выхода по току
74,6
92,9
84,4
7. Табл. 103 показывает данные Арндта и Фезе7® о влиянии
на стойкость анодов процента графитирования. Последний определялся по разработанной Арндтом кривой зависимости удельного сопротивления от процента графитирования в угле. Электролит содержал NaCl 250 г/л и хромата 2 r/л. Анодная плот-
юность тока была 0,067 А /см*.
Таблица 103. Электролиз с угольными анодами с разным процентом графитирования024
Процент графита
0
44
70
75
100
. золы
7,63
' 0,69
0,19
0,36
0,24
. объема пор ....
21,4
26,7
24,4-27,7
22,2
22,8
• потери веса ....
8,1
4,2
4,2 •
^,2
3,1
. выхода по току . . .
72,7
76,7
75,1
80,2
78,6
углекислоты в газе .
13,2
8,7
9.4
3,3
5,0
• кислорода в газе . .
10,4
13,4
14,1
16,0
14,4
. хлора в газе ....
2,5
0.9
2,5
0,8
0,7
Из данных таблицы, Арндт и Фезе делают вывод, что 75%
графитирования достаточно для получения электродов хорошей
стойкости; также весьма важным является гомогенность и грубо-
.зернистость строения электрода. /
ГЛАВА 20
СХЕМЫ ЭЛЕКТРОЛИТИЧЕСКОГО ПОЛУЧЕНИЯ ХЛОРАТОВ,
КЛАССИФИКАЦИЯ ВАНН, ПРОИЗВОДСТВЕННЫЕ
КОЭФИЦИЕНТЫ
%
§ 1. Общие данные- режима работы
Поступающий в ванны раствор должен содержать хлорид
.в концентрации несколько меньшей, чем концентрация насыщения при температуре электролиза. Кроме хлорида раствор дол-'
-жен содержать- хромат (натрия или калия) в количестве
; 279
Ю—20 г/л и H‘ • ■ и,05 экп/л. Содержание небольшого количества примесей Оа или Mg нс является вредным дли
электролиза и по* них стадий производства. Содержание
сульфатов является i *»м.
В течение электрол.. ‘'прерывно или периодически в электролит прибавляют силмк •бавленную соляную кислоту, чтобы
компенсировать уменьшен ' лотности, происходящее вследствие выделения некоторого лчества СЬ из электролита. Кислотность электролита во врем>. электролиза должна соответствовать при платиновых анодах отношению HCIO к NaCIO от
2:1 до 1:2 (по Ферстеру10) или отношению СГ2О7" к СЮ4",
как 1 :1 (по Кацену и Соколову в2в.
При графитовых анодах кислотность должна быть несколько
больше, чем при платиновых, — по Кацену и Соколову должна
соответствовать отношению СГ2О7" к СЮ<", как 4:1. При магне-
титовых анодах кислотность электролита обычно держат примерно такой же, как цри платиновых.
Температуру электролита во время электролиза рекомендуется
держать 70—80° при платиновых анодах, 65—70° при магнетито-
вых анодах и 40—50° при графитовых анодах. При платиновых
и магнетитовых анодах джоулева тепла, выделяющегося при
электролизе, обычно достаточно для поддержания в электролите
необходимой температуры. При графитовых анодах обычно
применяют искусственное охлаждение (по змеевикам, вставленным в ванны, и т. п.).
Анодная > "плотность тока рекомендуется в пределах
0,08—2 А/см2 при платиновых анодах, 0,03—0,05 А/см2 при графитовых анодах и 0,01—0,02 А/см2 при магнетитовых анодах.
В случаях периодически действующих ванн убыль воды, получающуюся от испарения и от участия НгО в реакциях электролиза, компенсируют, периодически дрливая в ванну раствор
клорида, что замедляет уменьшение концентрации хлорида, которая не должна опускаться много ниже 150 г/л.
Электролиз обычно прекращают, когда концентрация хлората
достигает почти насыщенного состояния, после чего горячий
раствор оставляют на некоторое время до перехода желтого
. цвета жидкости в оранжевый, что наступает благодаря переходу
гипохлорита в хлорат1 и хромата в бихромат. Дальше раствор
охлаждают, отчего выделяется ббльшая часть хлората в виде
кристаллов. Последние отделяются от маточного щелока, промываются холодной водой и дальше обрабатываются, как
обычно при химических методах производства (перекристаллизация, сушка и т. д. — см. главы 9 и 10). Маточные щелока,
отделенные от кристаллов, донасыщают хлоридом и направляют
оЛять на электролиз. Таким образом хлорат, остающийся, в ма-
' * Что очень валЛю для предупреждения коррозия трубопроводов и ап¬
паратуры от НСЮ.
280 ' :
точных щелоках, не является потерей, вследствие чего кристаллизацию обычно производят с охлаждением только до 10—20°.
без применения вымораживания.
§ 2. Получение КСЮз электролизом раствора КС1
Содержание КС1 в растворе, поступающем на электролиз,,
обычно равно у 250 г/л, а содержание K2G2O7 около 12 г/л.
Электролизх прекращают то достижении концентрации хлората
в 150—200 г/л. При кристаллизации при 10—20° в маточном ще¬
локе остается растворенным 15—20 г КСЮз на литр щелока, при
вымораживании до —10° только 6—8 г/л. По Биллитеру11
можно достигнуть остатка КСЮз в маточнике в 3 г/л (см. также
стр. 126 рис. 59 и 60).
Рис. 109 показывает примерную схему этого метода производства КСЮз.
§ 3. Получение КСЮ3 электролизом раствора NaQ
с последующей обменной реакцией с КС1
^ Содержание NaCl в растворе, поступающем на электролиз,,
равно ~ 270 г/л. Электролиз прекращают при концентрации
NaClOs в 300—350 г/л. Полученный NaClOe переводят в КСЮз
прибавлением соответствующего количества КС1. При охлаждении щелока, полученного после обменной реакции с КС1, до
10—20° в маточной жидкости остается КСЮз 60—80 г/л; при вымораживании до —10° в маточной жидкости остается 30—40 г/т
(см. табл. 53 и 54 и рис. 79 и 80 на стр. 176—177).
Для уменьшения остатка КСЮз в маточнике можно мри
обменной реакции добавлять избыток КС1 (сгр. 176). Маточный
щелок поступает^ обратно на электролиз без донасыщения хло¬
берсолЬ .
Рис. 109.' Схема получения КС103 электролизом раствора КС1.
ристым натрием, так как доиасыщение происходит от образования NaCl при обменной реакции. Вели концентрация МаООз
в щелоках после электролиза превышает 300—350 г/л, сумма
NaCl, образующегося при обменной реакции, и NaCl, остающегося неразложенным при электролизе, превысит растворимость
NaCl, и часть её выпадает в осадок, загрязняя получаемую
бертолетову соль.
Стадии обменной реакции и кристаллизации при этом методе
производства КСЮ# почти идентичны * этим же стадиям при
каустическом методе, описанном в гл. 13 (стр. 158).
Рис. 110 показывает примерную схему этогЪ метода производства.
Лова
Развавл. соляная
кислота'
Хлористый
Готовая.
версалб
Маточник от перокри*' _ f
сталлилации на промывку сЫрои
Рерсоли
Рис. 110. Схема^олучения КСЮ8 электролизом раствора bjaCl.
Преимущества и недостатки этого метода перед методом непосредственного электролиза раствора КС1 следующие.
Преимущества: а) возможность вести электролиз до большей .
концентрации хлората; б) меньшая примесь хлорида в получаемой бертолетовой соли (NaCl лучше отмывается, чем КС1))
в) меньшая потеря по КС1, поскольку в циркулирующих щелоках
в основном содержится NaCl, а не КС1.
Недостатки: а) вводится добавочная операция обменной реакции; б) в маточном щелоке после кристаллизации остается
больше KClOs, что увеличивает количество КСЮз, циркулирую-
.щего <в производстве, и его потери.
' § 4. Получение NaGOs
' На электролиз поступает раствор, содержащий NaCl ~ 270 г/л.
Электролиз прекращают после достижения в электролите концентрации NaClOj в 700—750 г/л1 (47—49° Боме) при 70—75° С
•’ *• л "*^
4 Отдельные фабрики ведут электролиз до концентрации NaCIO» 300—
400 I/л, после чего щелок упаривают до уд. веса 1,51—1,53 (40-60° Боме).
232 * / ' ‘
и при концентрации хлорида (NaCl) в 100—120 г/л. При охлаждении полученногб щелока до 10—15° выделяется Г>0—70%
хлората. Маточный щелок донасыщастся хлористым натрием и
поступает обратно на электролиз. Содержание NaClOs в маточном щелоке равно 350—450 г/л.
Стадии кристаллизации, перекристаллизации и сушки NaClOj
идентичны таковым при получении ИаСЮз химическим путем
(см., гл. 15, стр. 196).
Следует отметить также возможность получения NaClOs как
побочного продукта при электролитическом получении СЬ и
NaOH в ваннах Грисгейм-Электрон (с неподвижным электролитом). При этом процессе около 11% тока расходуется на образование NaClOs, около ‘/в которого диффундирует в католит,
а остальные 5/в остаются в анолите и из последнего могут быть
получены обычным путем дробной выпарки и кристаллизации
(Н. Н. Воронин м, Биллитер п, Ферстер 10). -Состав анолита, приводимый Н. Н. Ворониным*1, следующий:
Состав
NaCIO,
NtCl
NaCIO + Cl,
N«,SO,
Ca (OH),
Pc (OH),
Mn
п
г/л
130 i
265
1.2
6,8
0,53
0.1—0.2
следы
§ 5. Получение NaClOs и КСЮз из бикарбонатов
Гмелин4-21 приводит патенты получения хлоратов электролизом смешанных растворов хлорида и бикарбоната натрия или
жалия. Электролиз производится в ваннах с диафрагмой при 60—
70°. Суммарное уравнение реакции электролиза следующее:
' NaCl + 6NaHC03+ЗНаО + 6© + 6© = NaC103+6СОа +
+ 6NaOH + 3H2 1 (121)
При этом в анодном пространстве образуется NaClOs и выделяется СОг, а в катодном пространств^ образуется NaOH и
выделяется Нг.
Плотность тока 5—тЮ А/дц2. Напряжение до 5 V. Выход
тока по NaClOs ~ 50,%, а по NaOH ~ 90%.
§ 6. Получение хлоратов лития, бария и кальция
Исходят из электролиза растворов соответствующих хлоридов. Ввиду трудности разделения хлоридов и хлоратов этих
солей при совместном «х присутствии в растворах, электролиз
ведут до почти полного истощения хлорида в электролите. При
повышенной температуре и плотности тока (до 0,1 А /си2)
образование перхлората ничтожно даже при снижении концентрации СГ в электролите до 0,1—0,2 экв/л.. При получении хлоратов Li' и Са на электролиз подают насыщенный на холоду
раствор их хлоридов, содержащий бихромат. При получении
Ва(СЮз)г применять бихромат нельзя ввиду образования осадка
ЛА . ■■ ) 283
ВаСгОч. По Форстеру10 при электролизе раствора ВаСЬ при 70—
80° при высокой катодной плотности тока, достигаемой применением катода в виде платиновой решетки, и при анодной плотности тока меньше 0,1 А/см^ получают Ba(ClOs)* с выходом по
току в 65—70% (см. также герм. пат. 89844, 1896 г. и Forschritte
in der anorgan. Chem. Ind., Berlin 1921 г., том. 1, crp. 320).
о
§ 7. Классификация ванн, применяемых для получения хлоратов
I электролизом
*
Ванны, применяемые для получения хлоратов электролизом,
можно разделить по их основным характерным особенностям на
ряд групп.
1. Ванны могут иметь диафрагмы для разделения анодного и
катодного пространства или не иметь таковых. Диафрагмы применялись главным образом в целях защиты от катодного восстановления и от коррозии катодов. В настоящее время в промышленности применяются только ванны без диафрагм, так как
последние усложняют конструкцию ванн и вызывают повышенный вольтаж ванн, а защитой от катодного восстановления сложит прибавка бихромата к электролиту.
Из ванн с диафрагмами ниже описываем ванны Галля и Монт-
лора, Блюменберга, Спилкера и Леве, Гертера, Брука.
j. 2. Электроды ванн могут быть включены монополярно и биполярно. Последнее удобно тем, что электроды целиком погружены в электролит (исключая крайних двух). В настоящее время
в промышленности обычно применяются только ванны с моно-
полярными электродами.
Ниже описываем ванну Корбена и Ледерлэна с биполярными
платиновыми электродами.
3. Расположение электродов в ванне может быть горизонтальное или вертикальное. Большая часть промышленных ванн
имеет вертикальное расположение электродов. ч
К ваннам с горизонтальным 'расположением электродов отно-
/ сится нижеописанная ванна Ауссигского союза.
4. По материалу Применяемых анодов ванны можно разделить на группы с платиновыми, магнетитобыми и графитовыми
анодами. Ванны с анодами из иных материалов весьма редки.
Наиболее распространенными в настоящее время являются ванны
с графитовыми анодами. Из нижеописанных ванн платиновые
аноды имеют ванны Карлсона, Nat. Electric Со. Корбэна и Ладер-
лэна, Alby Nya Kloratfabriken; магнетитовые аноды имеют ванны
Карлсона, Bussi, Воронина; графитовые аноды имеют ванны
Гиббса, Гаслингера, Баркера, Ангела, ‘ Ауссигского союза.
5. Ванны могут работать непрерывно (с проточным электро¬
литом) или периодически (с неподвижным электролитом) с перерывом электролиза для смены электролита. Последние могут
работать с кристаллизацией внутри ванн или кристаллизацией
в^е ванн. / ;
284
В промышленности в настоящее время применяются как непрерывно действующие ванны, так и периодически действующие.
Кристаллизация хлората в ваннах в настоящее время не применяется.
§ 8. Коэфициенты электролитического получения хлоратов
20 42 '
Теоретически 1 амлёр-час образует = 0,762 г КСЮз;
1 г КСЮз требует затраты ^ 1»31 ампер-часа. Теоретиче¬
ское напряжение, необходимое для электролитического образования хлората из хлорида, равно по Абелю и Лютеру
1,43 вольта. Таким образом теоретический расход энергии для
получения 1 кг КСЮз равен 1,31 • 1,43 = 1,87 квт-ч.
Ниббс и Пальфримен определили напряжение образования
хлората при 90° в ваннах без диафрагмы равным около 2 вольт.
Отсюда расход энергии на 1 КСЮз равен 1,31 -2 = 2,62 квт-ч.
Биллитер11 приводит теоретический расход энергии на 1 кг
КСЮз в 2,91 квт-ч. * (что соответствует, вышеприведенному
расходу энергии в 1,87 квт-ч с учетом выхода по току в 66,7%
при электролизе в щелочной среде!).
( Практическое напряжение, необходимое для получения хлората, равно 3,5 — 5 вольт; практический расход энергии равен
6—7 квт-ч на 1 кг КСЮз (колебания объясняются изменениями
величин напряжения, выхода по току и механических потерь).
Суммарное уравнение получения КСЮз будет:
КС1 + ЗН20 + 6® +,60 = КС103 + ЗН2. (75)
Согласно уравнению (75) на 1 г КСЮз расходуется 0,608 г КС1
и 0,44. г НгО и получается 0^049 г Н*. Практический расход КС1
равен 0,61—0,65 г на 1 г КСЮз. /
Кроме КС1 и энергии при электролитическом получении
КСЮз расходуются: бихромат 1—2 кг на 1 г КСЮз и соляная
кислота 10—20 кг на 1 т КСЮз.
\ На получение 1 г NaClOs теоретически требуется затрата
17 75
1,51 ампер-часа; 1 ампер-час образует =0,663 г NaClOs.
При теоретическом напряжении в 1,43 вольта, теоретический расход энергии на 1 кг NaC10s=l,51 • 1,43 = 2,195 квт-ч.
Практический расход энергии на 1 кг NaClOs равен 7—8 квт-ч.
Суммарное уравнение получения NaClOs будет:
NaCl + ЗН20 + 60 -f 6© = NaClps 4- ЗН9. (122)
По уравнению (122) на 1 г NaClOs расходуется 0,55 г NaCl
и 0,477 г НгО и получается 0,056 r Ht. Практический расход
NaCl равен 0,65—0,70 г на 1 г NaClOs.
* Первичными процессами при электролизе раствора хлорида являются
разряд ионов хлора и иунов водорода с образованием хлора, водорода «
щелочи. Напряжение разложения для этого процесса равно для KG1 —
2,28 вольта. Отсюда расход энергии на1 кг КСЮа будет 2,91квт/ч. При и. ред.
285
Ангел67 приводит следующие данные о расходных коэфн-
циентах и элементах себестоимости 1 т бертолетовой соли
в Швеции. 1
Хлористый калий
Соляная кислота и бихромат
Электроды 1 . .
Электроэнергия 2
Уголь для выпарки . . . . .
Зарплата
Ремонт
Амортизация *,
Разные
650 кг
26 долл.
22"/„
—
•А7
•
2.3"/о
40 .
20
я
17%
13.2»/,,
6821,5 квт-ч
15,6
я
250 кг
1,7
п
М%
0,025 уел. дней 3
20
я
17%
—
7
я
5.9%
—
15
я
12,7%
—
10
я
3.5%
\
Итого ..... . 118 4 дслл. 100%
, ГЛАВА 21
ОПИСАНИЕ ОТДЕЛЬНЫХ СПОСОБОВ И ВАНН, ПРИМЕНЯЕМЫХ
ДЛЯ ПОЛУЧЕНИЯ ХЛОРАТОВ ЭЛЕКТРОЛИЗОМ
■Л
§ 1. Ванна Уатта 6
Английский химик-инженер Чарльз Уатт взял в 1851 г. паг
тент, впервые описывающий способ и ванну для получения хлоратов электролитическим 'путем. Хотя этот патент не получил
промышленного осуществления, однако примененные через 40
лет первые электролитические ванны хлоратных фабрик имели
много общего с описанием в патенте Уатта. На рис; 111 приводим изображение аппарата Уатта.
На электролиз поступает теплый, почти насыщенный раствор
КС1, содержащий примесь щелочи— 10% от количества хлорида. Электролиз производится в сосуде В, наполненном электролитом с погруженными в электролит электродами Е. Сосуд
окружен рубашкой А, через которую проходит пар для подогрева. Электроды Е изготовлены из платины и установлены
горизонтально — внизу анод и вверху катод. Подводка тока
к -электродам производится через клеммы е. Для показаний
температуры в сосуд вставлен термометр G.
Во время электролиза хлорид разлагается — на аноде выделяется хлор, а на катоде образуются NaOH и Нг. Хлор, поднимаясь от анода, перемешивается со щелочью, образуя гипохло-
1 Применялись имлрегнированные графитовые электроды Ачесоиа.
3 Включая расход энергии на моторы и потерю тока при трансформировании.
в Повидимому опечатка. Надо думать/~что. имеется в виду 2,5 раб. дня-
4 В этой же статье Ангел приводит для сравнения калькуляцию стоимости
бертслетовой соли при известковом методе производства с выводом, что при
известковом методе тонна хлората' стоит дешевле на 56 долларов благодаря
побочному получению NaOH.
4 К е р ш а у *, англ. пат. 1S785 (1851 г.)..
286
рит, который переходит в хлорат и хлорид. Последний вновь
разлагается током на хлор и щелочь.
Электролиз прекращают после разложения 2/з хлорида. После
этого электролит охлаждается для выделения хлората.
Рис. 111. Ванна Уатта для электролитического
, получения хлоратов.
А — паровая рубашка; а — отвод пара, В — электролит,
' С—выпуск'электролита, d—подвод пара, £ — электроды,
ее — клеммы, О — термометр. ^
(
§ 2. Способ и эанны Галля и Монтлора1
Французские инженеры Галль и Монтлор разработали и осуществили заводской способ получения хлоратов электролитическим путем и за свои исследования в этой области получили
премию французской Академии Наук.
Первая опытная установка была ими пущена в 1886 г. в-'Vil-
lers Seinte Sepulcre в Швейцарии и работала до 1891 г., когда
ими была пущена крупная фабрика в Vallorbe (Французские
Альпы). В 1896 г. ими была пущена еще одна крупная фабрика
в St. Michel. .
Ванны Галля и Монтлора имели диафрагму, расположенную
между катодами и анодами. Электроды были расположены горизонтально. Аноды были из платины или сплава платины
с 10% иридия. Толщина анодов — 1 мм. Катоды были из никеля.
На электролиз поступал раствор КС1, содержащий щелочь.
Электролит непрерывно подавался из катодного пространства
в анодное по трубопроводу, расположенному вне ванны. По патенту ванны могут быть изготовлены из кирпичам керамики
1 Керш а у Билли тер11; фр. пат. 179413 (1886 г.); 340697 и 340699
(1894 г.); англ. пат. 13795 (1964 г.); аи. пат. 492003 (1896 г,).
287
я т. п. Диафрагма делалась из особого материала, устойчивого против хлора и гипохлорита. Температура электролита
поддерживалась в 45 — 50° подогревом посредством опущенной
в электролит платиновой спирали. Анодная плотность тока была
0,5 А /ем2. Напряжение на 65 ваннах было 330 вольт, т. е. •
—> 5 вольт на каждую ванну. Хлорат выкристаллизовывался
в самих ваннах, откуда вычерпывался эмалированными ложками.
Впоследствии горизонтальное расположение электродов было
изменено на вертикальное. В 1897 г. отказались и от диафрагмы
заменив ее асбестовым кожухом вокруг катода (фр. пат. 242073).
Хотя при щелочном электролите разъедание катодов бывает
меньше, чем при нейтральном, рекомендовалось вынимание катодов уз ванн при остановках электролиза.
Получение NaClOs описано Галлем и Монтлором в фр.
пат. 249698. Жидкость после Электролиза упаривалась до концентрации хлората в 750 т/м.
В первые годы работы указанных установок выход по току
яе превышал 25—30%. Однако при тогдашних ценах на хлорат
производство было рентабельно. и при таких . выходах. Уже
к 1900 г. на фабриках в Vallorbe и St. Michel вырабатывалось
в год до 3000 т хлоратов.
\
§ 3. Способ Карлсона 1
Такую же роль, как Галль и Монтлор сыграли для развития
промышленного электролитического получения хлоратов во
.•Франции, сыграл вШ1Ьеции Карлсон, проведший ряд исследований в этой области и организовавший две крупные установки по
'своему способу (в Мансбое и Альби).
Карлсон применял электролиз щелочного раствора хлорида
без диафрагмы 2. Ванны применялись открытые с вертикальным
расположением электродов. Сначала применяли угольные аноды
и железные катоды. Вскоре однако отказались от угольных анодов и перешли к платиновым. Электролиз велся прерывно с кристаллизацией хлората вне ванн. Выделяющийся при электролизе
водород благоприятствовал перемешиванию электролита.
Температура при электролизе поддерживалась не выше
40 — 50° во избежание усиления образования Ofe. «По достижении
Достаточной концентрации по активному кислороду (гипохлорит
и хлорат) электролиз прекращали, спускали жидкость из ванн,
подогревали для разложения гипохлорита и затем охлаждали
для Выделения хлората. Так как электролиз раствора КС1 давал
худшие результаты, чем раствора NaCl, то для производства
КСЮз исходили из электролиза раствора NaCl с последующей
‘Keipniiay*, Ульман*, Б и л лите р п, швед. пат. 3614 и 8149 (1890 г.),
11Э711 (1896 г), 197,15 (1903 г.}, Вассерман*4, Стасинг** и Карлсоню. • :
8 Интересно отметить, что именно такой принцип работы — электролиз
в щелочной среде и без диафрагмы—предложил в сво^ время Уатт.
288'.'.' ■ -- ■
обменном реакцией с КС1. Для получения NaCIO» жидкоеп> or
электролиза раствора NaCl подвергали упариванию.
Первоначальное исследование и проработка вопросов электролиза хлоридов для получения хлоратов были проведены
Карлсоном на Стокгольмской суперфосфатной фабрике в 1892 г.
В 1893 г. были проведены опыты на полузаводской установке
в Гедвиге (возле Стокгольма).
Сначала 'прибавляли в электролит Са(ОН)г. С 1898 г. стали
прибавлять СаСЬ (швед. пат. 11371). С 1903 г. стали прибавлять
кроме СаСЬ еще и хромат (шв. пат. 19715). В настоящее
время все пять установок проводят электролиз в слабокислой
среде.
В 1894 г. была пущена крупная фабрика в Мансбое (Mansboe)
(8 генераторов по 1200 ампер и 115 вольт), а в 1898 г. в Альби
(Alby, Швеция). К 1901 г. обе эти фабрики уже давали 1500 т
хлоратов в год. С 1903 г. эти две фабрики перешли к Шведскому Спичсиндикату, организовавшему еще установку в Тролд-
гатене (Troldhaten), а в 1926 г. значительно расширившему ycta-
новку в Альби. Этот же синдикат контролирует хлоратные
установки на Иматре (Финляндия) и в Радоха (Польша). Мощность этих пяти фабрик в 1928 г. была 2000, 2000, 4000, 2000
и 1000 i в год,'т. е. всего 11 000 г в год (хлораты Na, К, Ва
и перхлораты).
§ 4. Способ Блюменберга 1
, Электролиз производился в ваннах, изображенных на
рис, 112, разделенных диафрагмой В на анодное и катодное про-,
странство Е й F. В отличие от способа Галля и Монтлора в ванне
Блюменберга получавшийся у анода хлоргаз отводился под да-
„ влением по трубопроводу Н в катодное пространство, где реагировал со щелочью.
Аноды D из платины; катоды С из железа, никеля, кобальта
■ или тоже из ‘платины. Анодное пространство Е герметично закрыто крышкой; катодное пространство F открытое.
Размеры ванны 2,5 X 1,2 X 1,5 лг. Материал ванн в патенте не
. указан, но по Д э н л о п у89 ванны были железные эмалированные. Для уменьшения восстановления катод С во время электролиза приводился в движение. Температура жидкости в катодном
пространстве ~ 50°. Напряжение на ванне 4,5 вольт. Хлорат пе-
рекристаллизовывался в эмалированных сосудах.
Установка по опособу Блюменберга работала на Ниагаре
в 1896 —1898 гг. и прекратила работу после большого пожара
в 1898 г. В 1897 <г. работало 60. ванн, которые: давали до 1 т
хлората в сутки.89 „ ,
• • к /
&Керщау”, Овербери86, Дэнлоп88; амер. рат. 5Г9400 (1894 г!),
. 536848 и 537179 (1895 г.), 565324 (1896 г.), герм. пат. 80395, фр. пат. 238&0;
англ. пат. 9129 (1894 г.).
19 За*. 179. — Шрайбман.
289
Рис. 112. Ванна Блюменберга для электролитического
получения хлоратов.
, В — диафрагма, Я — анодное пространство, — катодное простран¬
ство, Н — хлоропровод, D — анод, С — катод
§ 5. Способ Nat. Electric Со.1
Этот способ и аппарат разработали канадские инженеры
Гиббс и Франшо. Основное лабораторное исследование проведено ими в 1892 г., после чего они организовали в Букингеме
(Квебек) полузаводскую установку. Для промышленной эксплоа-
тации разработанного ими способа была пущена в 1898 г. крупная хлоратная установка на Ниагарском водопаде. Первоначально разработанная конструкция ванн была впоследствии
изменена и ниже нами описывается ванна на основе англ, и
амер. пат. 1901 т. (рис. 113).
Авторы исходят из того, что при электролизе выход по току
уменьшается по мере обогащения электролита продуктами электролиза из-за частичного разложения последних. Поэтому предлагаемый ими способ предусматривает непрерывное протекание
электролита через ванну с тем, чтобы концентрация хлората не
превышала 2—3%.
Так как расход энергии зависит весьма сильно от сопротивления, авторы отказываются от диафрагмы, располагают
электроды на расстоянии между собой не более 2—3 мм и рабо-
.*■ К ерш а у*, Биллитер*1, Рихард с®7; англ. пат. 4869; фр. пат.
288460 н ам. лат. 493023 (1893 г.), ам. лат. 665426 и 665427 (1901 г.); англ. пат.
'ЗЭЗ (1901 г.). •
290
тают с повышенной температурой электролита. Для уменьшения восстановления (которое должно увеличиться из-за отсутствия диафрагмы) авторы применяют катод в виде медных
проволок или стержней (с диаметром не более 6
Ряд электролитических ячеек соединяется вместе наподобие
рам фильтрпресса. К источнику тока присоединяются только
электроды крайних ячеек (рис. 113).
Каждая ячейка состоит из деревянной рамы ,выложенной
изнутри свинцом В. С одной стороны рамы (на рис. 113 слева)
укрепляется катод С, состоящий из ряда вертикальных медных
проволок или стержней, поддерживаемых горизонтальными
стержнями О из изоляционного материала. С другой стороны
рамы укрепляется свинцовая пластина D с натянутым на нее (на
Рис. 113. Ванна Nat. Electric. Со. для электролитического получения хлоратов.
А — деревянная рама, В—свинцовая обкладка рамы, С — катод, О — стержни для укрепления
катода, Е — анод из платиновой фольги, D — свинцовая обшивка рамы со стороны анода, L —
выступы рам для их соединения, т — шины для соединения с источником тока, /Си/— метал-
лические плиты для укрепления ванны, F— резиновая прокладка — изоляция между анодом и
катодом отдельных ячеек, О — воронки для питания рассолом, Н — выход электролита и водорода.
рис. 113 справа) листом платиновой фольги £. Несколько таких
ячеек (на рис. всего 5) соединяются вместе болтами через выступы L, имеющиеся у каждой рамы, и, укрепляются двумя металлическими плитами I и К, изолированными от ячеек ванны.
Между рамами двух соседних ячеек имеется резиновая прокладка F для взаимной изоляции друг от друга катода и анода,
так что проводником тока в этом месте служит электролит. Питание рассолом производится отдельно в каждую ячейку
через воронки G, нижние концы которых доходят-почти до дна
ячеек. Выход электролита и водорода производится через отверстия Н, имеющиеся в верху ячеек и соединяющиеся в один
трубопровод для каждой ванны. Таким образом электролит поступает внизу “ячеек и выходит сверху, по пути омывая электроды. Одна крайняя ячейка ванны (на рис. 113 левая) оканчи-
19* j
291
вастси илитон D, обтянутой платиновом фольгой /;. Другая
крайняя плита (на рис. 113 справа) оканчивается простой плитой D без платинового покрытия. Эти две крайние плиты D
присоединяются к шинам т, расположенным сверху ванны и
соединенным с источником тока.
Размеры рам 46 X 66 X 8 см. Анодная плотность тока
0,55 А/слг2. Сила тока 1650 А. Напряжение 4,5 вольта. Объем
электролита 2,5—5,0 мл на 1 см2 поверхности электродов. Струя
рассола регулируется так, чтобы концентрация хлората была нс
больше 3% и чтобы температура была достаточна для быстрого
разложения гипохлорита на хлорат и хлорид. В среднем через
каждую ячейку 'проходит 28 л/мин.
Рис. 114 показывает общую схему установки. Холодный рассол поступает из Т по шлангу X в ванны Р, где происходит
электролиз и получается хлорат.
Из ванн Р электролит вытекает
в кристаллизаторы R, снабженные змеевиками Q для искусственного охлаждения, где выделяется большая часть КООя.
Маточный щелок из R перекачивается в Т, где донасыщается
хлористым калием, откуда
опять передается в Р на электролиз. Жидкость из Т через X
протекает в Р непрерывно. Процессы охлаждения, отделения
хлората и донасыщения хлористым калием могут быть непрерывными, или периодическими.
Способ Нац. Электр. К° разработан для производства КСЮя.
При производстве NaClC>3 и др. хлоратов более растворимых,
чем их хлориды, авторы предлагают концентрировать хлорат
упаркой, выделяя часть хлорида, после чего выделяется часть
хлората охлаждением щелока.
ч • Вначале Гиббс и Франшо предлагали катоды делать из СиО
для того, чтобы образующийся при электролизе водород связывался материалом самого катода (СиО +'Нг = Си + НгО) и
не восстанавливал бы гипохлорит. При этом предполагалось
электролиз вести прерывно, периодически вынимая из ванн
•катоды, восстановившиеся в металлическую медь, для их обратного окисления в СиО пропусканием над ними струи теплого
воздуха. Однако операция вынимания катодов и их окисления
оказалась весьма неудобной и дорогой, почему отказались от
тайих катодов и перешли к вышеописанным медным стержням.
Ричардс87 в статье «Ниагара как центр электрической промышленности» указывает, что выход по току на этой установке
был сначала 60%, но после ряда усовершенствований достиг
Рис. 114. Схема установки для электролитического получения хлоратов по способу Nat. Electric. Со.
Г—аппарат для донасыщения KCI, Л-—-сифон для питания ванн, р — ванна, /? — кристаллизаторы, Q — змеевики для охлаждения,
S — насос.
70%. Температура электролита была 60—70°. Расстояние между
электродами было 0,4 мм.
Биллитер11 указывает, что в настоящее время вероятно нигде
не работают на ваннах фильтрпрессного типа.
§ 6. Способы и ванны Гертера, Брука, Кельнера, Спилкера и
Лове, Гиббса, Зильбермана и Имгоффа
1, Аппарат Гертера.1 Отличием этого аппарата, изображенного на рис. 115, является расположение нескольких ванн одна
над другой, работающих как один аппарат, и то, что катодами
служат чугунные стенки ванн. - Рассол поступает в верхнюю
ванну у q, откуда по трубе Е переходит в нижерасположенную
и т. д., и выходит у Н из самой нижней
ванны. При этом жидкость, входящая
в каждую ванну, попадает в нижний
слой почти у дна ванны, а выходящая
жидкость отводится сверху ванны. Посредине каждой ванны имеется платиновый анод G. Чугунные стенки ванн, служащие катодами, изнутри выложены
пористым материалом В, являющимся
диафрагмой. Ток подводится к аноду
D А
*—С'
Ванны Гертера
Ванны 6рука.
Рис. 115. Ванны Гертера и Брука для электролитического получения хлоратов.
А — сУенки ванн (катод), В — диафрагма, D — изоляция между ваннами, Е— переливные трубы
для рассола внутри ванн, F — изоляция переливных труб, О — платиновый анод, И — выход эле*
ктролита, q — поступление рассола. Ванны Брука (справа). А — стенки ванн (катод), А'— анод, С—
переходные рассолопроводы, С — выход электролита, а — диафрагма.
верхней ванны и отводится от стенки нижней ванны. Электролитом служил щелочной раствор хлорида. Температура жидкости
при электролизе равна 60—80°. \
2. Аппарат Брука.2 Отличием от аппарата Гертера является
горизонтальное террасообразное расположение ванн, что имеет
/К ерша у* англ. пат. 15396 (1893); амер. пат. 587437'(1897) г.); англ,
пат. 9002 (1898 г.); J.. Soc. Cbem. Ind. VII, 71*9.
* К ерш а у*, айгл. пат. 15396 (1893'г.); амер. пат. 587437 (1897 г.); англ,
пат. 9002 (1898 г.).
293
преимущества и отношении ремонта, выключения отдельных
ванн и т. д. (рис. 115).
Способ был осуществлен в Bay City (США). Однако впоследствии на этой фабрике перешли к ваннам другого типа и способу электролиза в слабокислой среде. . '
3. Способ Кельнера.1 На электролиз подается раствор хлорида, содержащий 1—3% Са(ОН)г. Вместо Са(ОН)г можно применять и Mg(OH)s. Более подробного описания способов работы
и конструкции ванн патенты Кельнера нс дают.
4. Способ и аппарат Спилкера и
Лове2. Этот способ пытается разрешить
задачу одновременного получения хлората и едкой щелочи.
Как видно из рис. 116, ванна имеет
диафрагму D. Катодом является железная стенка ванны. Для уменьшения
явления поляризации в ванне имеется
приспособление, не дающее пузырькам
водорода прилипать к стенкам ванны.
В анодном пространстве находится насыщенный раствор КС1, содержащий
Са(ОН)г. Последний периодически добавляется, так что фактически в анодном ‘пространстве образуется только
гипохлорит и хлорат кальция. В катодном пространстве содержится 2%-ный
раствор КС1 и образуется КОН. Католит
выпаривается для получения твердого
едкого кали как отхода производства.
5. Способы Гиббса, Зильбермана и
Имгоффа. Отличием способа Гиббса
(амер. пат. 827721, 1905 г.) является
применение графитовых анодов. Для
увеличения продолжительности работы
анодов температура электролиза не должна превышать 37°.
Ввиду такой низкой температуры по окончании электролиза
получается жидкость с большим содержанием гипохлорита,
разложение которого достигается нагревом после слива из
ванны.
Отличием способа Зильбермана (герм. пат. 205019, 1907 г.)
является то, что, применяя ванну с диафрагмой, слабую кислотность электролита достигают посредством непрерывного изъятия части католита во время электролиза.
Отличием способа Имгоффа (англ. пат. 1014, 1899 г.)
является прибавление к электролиту фосфата натрия, окиси
>’алюминия и других соедннеий, реагирующих с кислотой или со
Рис. 116. Ванны Спилкера
и Лове для электролитического получения хлоратов.
А — анод, D —диафрагма, К — катод (стенки ванны).
‘Кершау*, герм. пат. 9060 (1890 г.); англ. пат.. 23591 (1895 г.).
' ‘Кершау*, англ. пат. 14494 (1887 г.); герм. пат. 73221 (1892 г.),
49627 и 65127 (1888 г.); фр. пат. 192593 (1888). \
294 / !■ ' '"у
щелочью, что улучшает выход по току, уменьшая побочные
реакции при электролизе. Реакции, происходящие в случае
добавления к электролиту окиси алюминия, по патенту Имгоффа
выводятся следующим образом:
в катодном пространстве АЬОз реагирует со щелочью
АЬОз + 2КОН = 2 КАЮг + НгО. (123)
Образовавшийся КАЮг в анодном пространстве реагирует
с хлором, образуя обратно АЬОз и гипохлорит и хлорид:
2 КАЮ* + СЬ = КС1+ КСЮ + АЬОз. (124)
§ 7. Способы и ванны Корбэна и Ледерлэна 1
Корбэн и Ледерлэн внесли очень много в промышленность
электролитического получения хлоратов и впервые осуществили
в заводском масштабе электролиз в слабокислой среде с добавлением бихромата. Фабрика, основанная по их способу
в 1896 г. в Шедде (Chedde), во Франции, являлась до войны
крупнейшей в мире и уже к 1900 г. давала 4000 т хлоратов
в год. Ими же было много сделано и в области применения
хлоратов, в частности разработано и осуществлено производство
взрывчатого хлоратного вещества «шеддит».
Первый патент Корбэна (фр. пат. 226257, 1892 г.) описывает
ванны с платиновыми анодами и цинковыми катодами. Аноды
были в виде весьма тонких платиновых листов В (или платиновой сетки G), которые во избежание изгиба были включены
в эбонитовые рамы С и Ci, из которых одна сплошная и одна
сетчатая. От одного из верхних углов анода В отходило платиновое ушко А в 10 раз большей толщины, чем сам анод.
Аи В могут- быть соединены сваркой или вывальцованы из одного
куска. Анод В целиком погружен в электролит. Эбонитовые
рамы С и Ci также целиком погружены в электролит или выдаются из него на 2—3 см. К платиновой шине А на высоте
2—3 см над урйвнем электролита припаивается медная шина D,
соединенная с источником тока. А и D проходят через отросток
эбонитовых рам £, в котором и укреплены. Таким образом верхняя часть платиновой шины А и целиком вся медная шина D не
соприкасаются с электролитом, что весьма важно в отношейии
разъедания D и припоя между А и D. Плотность тока в ушке А
равна 20 А/дм2. Способы соединения анода и токоподводящей
шины показаны на рис. 117.
В желобках, имеющихся в стенках ванны, укреплены полосы е, удерживающие цинковый катод Н в вертикальном положении параллельно аноду. Катод имеет также две ножки у. Полосы е и ножки у обтянуты каучуком или покрыты лаком. Общая
действующая ^поверхность анода и катода одинаковы. Катод, так
‘Кершау1, Биллитер11; фр. пат. 226257 (1892 г.), 238612 (1894 г.)
я 309361 (1901 г.); англ. пат. 17320 (1901 г.), 14387 (1902 г.); герм. пат. 136678
(1901 г.)
/
/
295
же как и анод, погружен целиком в электролит, откуда выдастся
только токоподводящий отросток.
Патент 226257 приводит разрез и горизонтальную проекцию
ванны Корбэна (рис. 118 и 119).
Сама ванна сделана из непроводящего материала (камень,
керамика и т. д.). Изнутри ванны облицованы плитами К и Ki
из непроводящего материала, имеющими свёрху желобки для
\
. Рис. 117. Детали электродов ванн Корбэна.
А — платиновое ушко анода, В — анод в виде платинового листа,
С и С' — эбонитовые рамы анодов, D и F — медные шнны анодов,
Е — отросток эбонитовых рам, G — анод в виде платиновой сетки,
Н — цинковый катод, ёе — полосы для опоры катода, У — ножки
для опоры катода.
укрепления (рам анодов С и Ci и полос е катодов; благодаря
такому устройству электроды очень легко вынимать из ванн.
Рассол входит в ванну снизу под давлением и выходит по всему
верху ванны в желоба L. Ванны установлены на арках, как показано на рис. 118.
В 1894 г. Корбэн взял патент (фр. пат. 238612) на ванну с биполярными платиновыми электродами. Такая ванна изображена
на рис. 120. * *
296
Биполярный электрод С работает обеими плоскостями —
одной как анод и другой как катод. Электрод заключен в эбонитовую раму В, в основном предназначенную дли предохранения
от рассеивания силовых линий (что вызвало бы неравномерную
Рис. 118. Схема установки для электролитического получения хлоратов по Корбэну.
А — вход рассола, В — анод, D — шина анода, Н — катод, '
К и А'| — керамиковые плитки облицовки изнутри ванн.
L — жёлоба для выхода электролита, М — подводка- тока.
нагрузку электродов) и для предохранения от изгиба весьма
тонких электродов (0,1 мм). Рамы В удерживаются в вертикальном положении полосами qи Н,проходящими вдоль всей ванны;
благодаря такому устройству электроды легко вынимать из
ванн. Снизу рамы оканчиваются несколько выше дна ванн для
возможности обтекания их электролитом. Сверху рамы выдаются над поверхностью жидкости на 1—2 см; сами электроды
целиком погружены в жидкость. Расстояние между электродами
297
должно быть как можно меньше, но сближать их меньше
12—15 мм практически нельзя, поскольку для большей устойчивости эбонитовые рамы не могут быть слишком тонкими. Рассол
может входить снизу ванны, как показано на рис. 118, или
сверху, как на рис. 120. В последнем случае вставляются специальные плиты-перегородки, образующие огороженные пространства, усиливающие циркуляцию электролита.
Против крайних электродов в стенках ванны делаются отверстия R, закрываемые металлическими плитами S, обтянутыми
платиновой фольгой; плиты устанавливаются строго параллельно
электродам. Между 8 и стенкой ванны помещается каучуковая
Ьрокладка Т. Поверхность 8 равна поверхности крайнего электрода. Ток проходит по болту W через 'отверстие R к плите S,
затем проходит через платиновую фольгу, покрывающую
I
Рис. 120. Ванна Корбэна с биполярными электродами.
А — вход рассола. В — эбонитовая рама электрода, С — биполярный электрод,
q и Н — опорные полосы для рам, Q — выход электролита, /? — отверстие против
крайних электродов, 5 — металлическая плита, обтянутая платиновой фольгой,
• Т — каучуковая прокладка, W — подводка тока.
плиту 8, и дальше по электролиту и электродам. Направление
тока можно менять, что очищает электроды от осевших на них
веществ.,
Фабрика в Шедде работала с биполярными электродами по
1900 г. С 1901 г. ввиду перехода на электролиз в слабокислой
среде, содержащей хромат, в которой катоды из Fe, Си и других
материалов уже не разъедаются, перешли обратно на ванны
с монополярными электродами. Об изменениях в конструкциях
ванн в патентах указано очень мало, а главным образом описываются условия подкисления электролита и т. д. 'Приводим описание процесса в заводском масштабе по герм. пат. 136678,
\ 1901 г. Ледерлэна.
Опыт 1. Получение КСЮз при слабокислом' электролите.
Работала серия в 42 ванны. Аноды платиновые с поверхностью
в 1000 см*. Катодов по два на каждой анод (из железа, меди,
, бронзы, латуни и других материалов) с общей поверхностью
298 / ■
в 3200 см2. Сила тока 2400 А. Напряжение 230 V. Анодная плотность тока 2,4 А/см2 и среднее напряжение на ванну 5,4—5,5 V.
Электролит до 1-й операции содержал КС1 240 г/л и К2СГ2О7
~ 13 г/л. Электролиз продолжался до повышения уд. веса
электролита до 1,285 (32° Боме). Температура электролита 75'.
После электролиза жидкость содержала бихромата ~ 8 г/л и
примерно столько же хромата, а активного хлора 0,9—1,2 г/л.
По прекращении электролиза к жидкости прибавляли разбавленную соляную кислоту из расчета перевода всего хромата в бихромат. При этом никогда не выделялось хлора, а через 1,5 часа
жидкость не содержала и активного хлора, что очень важно,
так как уменьшает корр'озию кристаллизаторов, трубопроводов
и т. д. Жидкость после «обесхлорирования» охлаждалась — выделялась большая часть КСЮз (остаток 13 г/л). Маточник дона-
сыщался хлористым калием и опять подвергался электролизу.
После 40 таких операций, продолжавшихся 60 суток, катоды
не имели даже следов разъедания и были покрыты беловатым
налетом из Са(ОН)» и Mg(OH)*, получившимися от примесей
в хлористом калии и воде. Вбего было пропущено тока
134 400 000 ампер-часов и получено в виде твердой соли и маточного щелока 93 г. КСЮз. Таким образом на 1 ампер-час получено
93
-.-■■т- =0,69 г КСЮз, что соответствует утилизации тока в
i
*4
0,69 • 100
0,763
= 90%.
Опыт 2. Получение КСЮз при нейтральном электролите.
Работа велась на описанной при опыте 1 установке при той же
силе и плотности тока, но без подкисления электролита. Общая
продолжительность опыта 17 суток, за которые проведено 8 операций. Каждая операция длилась дольше, чем при опыте 1,
ввиду более медленного роста концентрации КСЮз из-за худших выходов по току. После 17 суток работу пришлось, прекратить из-за того, что катоды от сильного разъедания пришли
в полную негодность. Указанной при опыте 1 пленки на катодах не было. Электролит уже после второй операции сделался
грязножелтым от частиц разъедаемых катодов. Активного хлора
в электролите было 6,5 г/л. Всего было пропущено тока
39360 000 ампер-часов и получено в виде соли и в маточных
щелоках 15,75 г КСЮз. Таким образом на 1 ампер-час получено
~Щ- = 0,40 г KCIOS, или —^^1^ = 52,5% выхода по затраченному току.
Опыт 3. Получение NaClOs при слабокислом электролите.
Установка и общие условия те же, что при опыте 1, исключая
следующие моменты.
, 1) начальный рассол содержал NaCl 270 г/л и Na2Cr2C>7
' ~13 г/л и имел уд. вес на холоду 1,185 (22,5° Боме);
2) электролиз продолжали до уд. ^еса электролита в 1,51
(49° Боме) при температуре 75°. Поэтому каждая операция
/ ■ —У
. / 299
длилась дольше, чем при КСЮз, и подкисление производили не
по окончании операции, а через каждые 24 часа;
3) понижение уровня жидкости в ванне от испарения воды
и выделения водорода компенсировали приливанием раствора
NaCl.
•К концу операции электролит содержал NaCl 120 г/л,
№гСг2С>7~13 г/л, КаСЮз~750 г/л и активного хлора 1 .г/л.
Несмотря на такое высокое содержание хлората, в электролите
не содержалось перхлората. «Обесхлорироваиие» производилось,
как при первом опыте. После кристаллизации в маточном щелоке оставалось NaClOe ~ 450 г/л. Этот маточник донасыщал'ся
хлористым натрием и направлялся опять на электролиз.
Работа продолжалась 60 суток, за которыми проведены
13 операций, пропущено 135 000 000 ампер-часов и получено
в виде соли и щелоков 78,3 т NaClOs. Таким образом на 1 ампер-
час получено - = 0,58 г NaClC>3 и выход равнялся =
= 87% от затраченного тока.
Катоды, как и при первом опыте, после 60 суток нс имели
и следов разъедания и были покрыты беловатым налетом.
Опыт 4. Получение NaClOs при нейтральном электролите.
Из-за сильнейшего разъедания катодов работа продолжалась
только 19 суток. За это время проведена всего одна операция,
ибо из-за плохого выхода по току концентрация №СЮз повышалась медленно. Электролит уже после 48 час. электролиза
сделался грязножелтым от ржавчины катода. Содержание активного хлора в электролите было ~ 4 г/л.
Всего за 19 суток было пропущено 42 820 000 ампер-часов и
получено №СЮз 15 т. Таким образом на 1 ампер-час получено
~42 82 г- NaClOs и выход равнялся 0’о^ббз°^ ~ 52,5% от
затраченного тока.,
§ 8. Способ Гаслингера1
Гаслингер осуществил в заводском масштабе электролиз
с графитовыми анодами. По этому методу в 1908 г. была основана хлоратная фабрика в Шваце (Австрия). Ванны имели герметично закрывающиеся крышки для избежания потерь хлора,
поскольку электролиз велся в кислой среде. Подкисление было
автоматическим2. Пористость применяемых анодов и кислая
среда благоприятствовали переходу гипохлорита в хлорат химическим путем [уравнение (114)]. В ванну не должен был иметь
доступа воздух, чтобы разбавлением хлоргаза над электролитом
не уменьшать парциального давления СЬ, так как при уменьшении парциального давления уменьшилась бы концентрация HCIO
в жидкости.
1 Биллитер11; герм. пат. 202962 (1906 г.). f
* Благодаря разряду ОН' в.порах графитовых анодов происходило под-
. кнеление., Прны. ред.
300 1 /
Ванны были цилиндрические (из каменного топара) диаметром в 70 хм и высотой в 75 см и работали силой тока в 2000 А
В каждой ванне имелись 32 электрода, вертикально установленные в 4 секции но 8 шт. Электроды каждой секции стояли параллельно на расстоянии в 15—20 мм друг от друга. Каждая секция в 8 электродов была перпендикулярна двум другим секциям
и параллельна противоположной секции. Середина ванн оставалась свободная.
Размеры графитовых анодов были 2,5 X 16 X 75 см. Анодная
плотность тока была 800—1000 А/м2. Температура электролита
по патенту должна была быть ~ 60°, но практически была
70—75°, почему аноды разрушались весьма быстро (через 3 мес.),
поэтому результаты работы фабрики в Шваце были сперва плохие. Впоследствии эта фабрика перешла к Ауссиговскому обществу и давала на графитовых анодах хорошие результаты.
Гаслингер также доказал возможность биполярной работы
графитовых электродов, что упрощает аппаратуру (электроды
целиком погружены, уменьшается количество контактов и т. д.).
| 9. Современные ванны Баркера, Ангела, Ауссигского союза;
Alby Nya Kloratfabriken, Воронина
1. Ванна Баркера.1 Ванна Баркера, изображенная на рис. 121,
представляет собой четырехугольный железный бак размером
2,4 X 0,4 X 1,2 м. Изнутри внизу и наверху ванна облицована
цементом аг. В крышке ванны по всей ее длине установлены два
ряда графитовых анодов (импрегнированных) £, не доходящих
до дна ванны, а вверху висящих на асбестоцементной крышке G
при помощи эбонитовых штифтов. Катодом служат необложен-
ные цементом стенки ванны и проходящий между анодами железный змеевик F, служащий одновременно для поддержания
температуры электролита в пределах 35—40°. Во избежание короткого замыкания внизу анодов между ними и катодами вставлены стеклянные палочки. Ванна работает непрерывно. Вход
рассола по трубе через крышку вднны; выход электролита также
вверху ванны через трубу t. Подводка тока производится по
шине /, соединяющей аноды. Нагрузка ванны 1500 А.
2. Ванна Ангела.2 На рис. 122 изображена ванна Ангела.
Корпус ванны представляет собой железный изнутри освинцованный ящик. Аноды Е укреплены в крышке ванны при помощи
круглых стержней и имеют форму параллелепипеда. Аноды Е
графитовые, но могут применяться и магнетитовые. Катоды F
сделаны из железной сетки и укреплены в раме D из поЛосового
железа, так что могут быть все сразу вынуты из ванны. Катоды
несколько расширяются! кверху, чтобы компенсировать падение
напряжения на анодах и сделать равномерным износ анодов по
всей их высоте. Над электродами имеется значительный слой
электролита, что благоприятствует уменьшению потери хлора
1 Англ. пат. 173028 (1920 г.).
* Бил литер12, Ульман*-*.
301
(из-за выделения его из ванны). Между отдельными группами
' электродов также оставляется большой объем электролита.
? Рис. 121. Ванна Баркера для электролитического получения хлоратов.
Ж А — железный корпус ванны (катод), а% — цементная футеровка дна н верха ванны, Е — графито-
вые аноды, F — змеевики (катод), / — выход электролита, О — крышка ванны, / — токоподводя-
7* щая шинка.
Внизу ванны оставляется свободное пространство для оседания
Л графитового шлама, образующегося при работе ванны.
I
v Рис. 122. Ванна Ангела для электро- f
литического получения хлоратов.
А — анодная шина, С — крышка из керамики,
I ' D — подвеска для катодов, Е — графитовые
аноды, Z5*— катоды из железной сетки.
< ’ Ванны работают с периодическим опорожнением, но могут
работать и непрерывно. В последнем случае температура электролита регулируете# (не врше 50°) величиной струи рассола,
' 302 / / ' - / /
поступающего в ванну. Анодная плотность тока 0,04 А
Импрегнированные графитовые аноды выдерживают около года
работы.
3. Ванна Ауссигскогб общества.1 Основное отличие этой
ванны (рис. 123) заключается в горизонтальном расположении
электродов и значительной высоте жидкости над электродами.
Катоды 2 из листового железа чередуются с графитовыми анодами 3, имея между собой в качестве изоляции цементные подставки. Все катоды 2 каждой ванны соединяются сборной шиной 5, а все аноды 3 присоединены при помощи горизонтального графитового блока к графитовому стержню 4. Шина 5
и стержень 4 выходят из ванны с двух противоположных концов
и соединяются с источником тока. Благодаря высокому слою
жидкости над электродами хлор почти совсем не выделяется
из ванны, а выделяющийся водород перемешивает жидкость, что
благоприятствует химическому образованию хлората из гипо-
Рис. 123. Ванна Ауссигского союза для электролитического
/ получения хлоратов. /
/ — бетонный корпус ванны, 2 — катоды, 3 — аноды, 4 — графитовый стержень,,
соединяющий аноды, 5 — графитовый стержень для подвода тока к анодам,
5 — сборная шина к катодам
хлорита [уравнение (114)]. Неудобством ванны является возможность короткого замыкания от оседания графитового шлама
между электродами.
4. Ванна Alby Nya Kloratfabriken 2 (рис. 124). Корпус ванны
представляет собой деревянный ящик размером 6200 X 200 X
X 170 мм, выложенный свинцом. Катодом служит свинцовая
обшивка ванны. Аноды сделаны из сплава платины с 10% иридия
и представляют собой сетку из плоских проволок, которые припаяны свинцом к многочисленным железным полосам. Последние
имеют вид опрокинутой буквы Т, на нижних освинцованных
частях которых покоятся стеклянные крышки ванны. Сборными
шинами служат две полосы из коробчатого железа, согнутые
вокруг ванны в виде лодковы.
Сила тока на ванну равна 3200 А. Анодная плотность тока
0,6 А/ся2. Напряжение на клеммах ванны — около 5 V. Электролиз производится периодически и электролит сменяется два раза
----- ■ ... — .
1 Герм, пат/418946 (1927 г.); Биллитер1*; Ульман5-*.
1 Ульман5-*. ■
303
в сутки. При этом в один конец ванны пускают свежий электролит, отчего через перелив в другом конце ванны сливается
щелок, обогащенный хлоратом.
Таким образом три смене электролита ванна не опорожняется
и ее отключать от тока не нужно.
Рис. 124. Ванна Alby Nya Kloratfabriken для электро-
' литического получения хлоратов.
А _ сборная железная анодная шина (200.75 мм), В— сборная катодная
железная шина (200.75 мм). С,— анод из платиновой сетки, D — свинцовая футеровка (катод), £— деревянный ящик, медная шина,
О — планка для выключения катода, Н — плоская железная полоса для
подвески анодов, / — стеклянная крышка ванны
I
Примерный состав электролита, входящего и выходящего из
«ванны, виден из следующих производственных анализов (состав
дан, в т/л). '
* '
NaCl
Г нпохло-
рит и хлор
NaC10t
НС1
К,Сг.О,
Темпера¬
тура
•*
^Электролит, входя¬
щий в ванну . . .
230—240
0,8
40-50
+ 1.3
2.5
20—30°
.Электролит, выходя¬
/
щий из ванны . .
7.0
115-140
— 0.7
2,5
60-70°
Как видно из анализов, выделение СЬ при электролизе было
таковым, что электролит, содержащий НС1 до входа в ванну
1,3 г/л, выходил слабощелочным (—0,7 г/л в пересчете на НС1).
Это надо объяснить слишком высокой концентрацией тока
в электролите, благодаря чему в ванне была высокая концентрация хлорноватистой кислоты.
Выход по току был 74—80%. Расход соляной кислоты составлял ~ 90 кг на 1 т хлората.
5. Ванна Воронина1 (рис. 125). Ванна представляет собой керамическую трубу, заделанную в железобетонный каркас. Сверху
1 Эта ванна применялась в СССР несколько лет на небольшой установке | •
304 . i
Медное.
комтакное
кольцо—"
Слой *ецдц
Фланец
Железный
катод
панна закрыта бетонной крышкой, через которую н шишу опускаются несколько анодно-катодных элементов, состоящих каждый из магнетитового анода и железного катода. Анод представляет собой полый закрытый снизу стержень
круглого сечения длиной 760 мм,
диаметром 57 мм и толщиной стенок- 7 мм. Изнутри анод покрыт
тонким слоем электролитически осажденной меди, благодаря чему ток
подводится равномерно ко всей поверхности магнетита. Катод представляет собой цилиндрическую трубу
высотой в 550 лтуи и диаметром
в 120—140 мм, сваренную из листового железа толщиной в 2 мм. Для
увеличения плотности тока катод по
всей своей поверхности имеет отверстия (перфорирован). Для подвода
тока к верхнему краю катода приварено ушко из толстого котельного
железа.
Анод должен быть расположен
строго по оси катода. Электролиз
велся с большой плотностью тока —
около 0,12 А/см2 на аноде и около
0,13 А/смг на катоде, но при желании
можно эту плотность тока увеличить на 50%. Температура жидкости
при электролизе держится в пределах 60—70°.
Сила тока на ванну зависит от
количества анодно-катодных элементов. Применялись ванны на 120, 360
и 600 А.'Напряжение на. ванну было
от 3,6 до 4,3 V. Утилизация тока на
хлорат составляла 70—75%, а временами достигала 85%. Расход энергии
колебался от 6000 до 7200 квт-ч на
1 т хлората. Работа велась периодически. На электролиз поступал раствор, содержащий КС1 230 т/л и
КгСгЮт 13 г/л и небольшое количество КСЮз, получившегося после до-
насыщения хлористым калием и подкисления соляной кислотой маточной
жидкости от предыдущей операции.
Выпуск, электролита производился
через керамический кран, имевшийся
внизу ванны. Отвод газов произво-
20 9». 17». — хйраМмк.
Магнетитобый
анод
J
Рис. 125. Элемент ванны Воронина для электролитического
получения хлоратов.
305
дился через штуцер, имевшийся вверху ванны и соединенный
с вентиляционной линией.
Устройство анодно-катодного элемента ‘показано на рис. 125.
Основная литература по электролитическим методам получения
хлоратов
4 1. Керша у2. 2. Ферстер10. 3. Биллитер11. 4. Биллитер12.
5. Ульман *—*. 6. Г м е л и н 1м. 7. Федотьев15 и 1в. 8. М а н т е л л ,7.
9. Ряд журнальных статей и патентов, указанных в тексте и п.я. 60- 89
в перечне литературы.
ЧАСТЬ ЧЕТВЕРТАЯ
s '
КОНТРОЛЬ ПРОИЗВОДСТВА, ТЕХНИКА БЕЗОПАСНОСТИ,
ПОТРЕБИТЕЛИ ХЛОРАТОВ, ПРОИЗВОДСТВЕННЫЕ
ИНСТРУКЦИИ
ГЛАВА 22
ЛАБОРАТОРНЫЙ КОНТРОЛЬ ПРОИЗВОДСТВА ХЛОРАТОВ
§ 1. Наиболее частые аналитические определения, применяемые
при контроле производства хлоратов
1. СаО. Определяется в извести, в известковом молоке, в не-
дохлорированных щелоках, фильтрпрессном шламе и т. д.
Определение основано на нейтрализации СаО раствором НС1 по
реакции:
СаО + 2НС1 = СаСЬ + НгО. (125)
Титрование производят в присутствии 3—4 капель раствора
фенолфталеина до обесцвечивания. Титрование проходит медленно, так как СаО .в воде плохо растворим. Для ускорения титрования рекомендуется в колбочку для титрования вложить
стеклянные бусы, а также вести титрование теплой жидкости
(разбавление пробы горячей водой). Пробы для определения СаО
надо хранить закрытыми, так как СаО поглощает из воздуха
СОг и влагу. При наличии в пробе с СаО (недохлорированный
щелок и т. п.) Са(С10)г необходимо до начала титрования разложить Са(СЮ)г 3%-ным раствором НгОг, так как гипохлорит разрушает индикатор.
2. CIO'. Определяется в' абгазном щелоке, недохлорированном
и перехлорированном щелоке. Это определение производится
весьма часто и имеет большое значение для контроля поглощения хлора из абгаза, контроля процессов хлорирования и
контроля обезвреживания. Применяются три метода определения
СЮ': а) по Пено, б) иодометрически и в) газоволюметрически.
а) Определение СЮ' по Пено. Пробу, содержащую
СЮ', разбавляют в 2—3 раза водой в фарфоровой чашечке и
при непрерывном перемешивании титруют раствором AszOs.
При титровании As*Os окисляется гипохлоритом в As*Os:
As*Os + 200' = AsiOe + 20',. (126)
. ' *
'20*
Конец титрования узнают, перенося но капле титруемой жидкости на полоску иодкрахмальной бумажки; пока в жидкости спь
СЮ', на бумажке получается синее пятно от реакции выделившегося иода с крахмалом:
СЮ' + 2KJ + Н20 == С1' + 2КОН + J2. (127)
б) Иодометрическое определение СЮ'. 11робу
жидкости, содержащей СЮ', переносят в коническую колбочку
и прибавляют 5 мл 10%-ного раствора KJ, 2—3 мл раствора
крахмала и 5—10 мл раствора СНзСООН ~ 2 N. Если жидкость
была щелочная, то раствора СНзСООН
прибавляют больше, так чтобы
ее был избыток. Закрыв колбочку
пробкой, оставляют ее на 5—10 мин.
для полноты реакции, после чего
титруют выделившийся иод 0,1 N
раствором Na»S*03 до . обесцвечивания. Выделение иода происходит
по уравнению (127). Титрование гипосульфитом происходит по уравнению:
J2 + 2Na2S2Oa = 2NaJ + Na2S4Oe. (19)
Необходим параллельный контрольный опыт, так как применяемый
KJ часто выделяет некоторое количество иода и при отсутствии СЮ',
а применяемая уксусная кислота
иногда содержит примеси минеральных кислот, разлагающих хлорат,
часто содержащийся в пробах.
в) Г азоволюметрическое
определение СЮ'. Определение основано на выделении кисло-
с НЮг:
Рис. 126. Аппарат для газволю-
метрнческих определений.
А — уравнительная склянка, В — измерительная бюретка, С — реакционный сосуд, D — бюретка для реактивов, Е — трехходовой кран.
.рода при реакции СЮ'
СЮ' + НгОг = С1' + НгО + Ог
(128)
Определение производится в аппарате, показанном на рис. 126,
состоящем из уравнительной склянки А (на 200 мл), измерительной бюретки В (на 100 мл), бюретки для раствора Н202 D (на
*15—20 мл) и реакционного сосуда С (на 50—100 мл). Измерительная бюретка В сверху закрывается трехходовым краном Е,
соединяющим ее с воздухом и (резиновой трубкой) с реакционным сосудом С. Снизу бюретка В соединяется резиновой трубкой с уравнительной склянкой А. Бюретка D вставлена в резиновую пробку, закрывающую реакционный сосуд С; сверху
бюретка D закрыта резиновой пробочкой с вставленной в нее
стеклянной трубочкой, соединенной с трубкой, соединяющей
В и С. В уравнительную склянку А наливают 150 мл раствора
NaCl и наполняют им бюретку В. В бюретку D наливают 3%-ный
308 / /' '•
раствор Н2О2. И сосуд С вносят пробу для определения СК> .
Поставив кран Е в положение, при котором сосуд С и бюретка В
соединены между собой, открывают кран е, впуская понемногу
раствор Н2О2 в сосуд С. Кислород, выделяющийся от реакции
Н2О2 с СЮ', вытесняет раствор NaCl из бюретки В в склянку А.
После прекращения выделения кислорода приводят жидкость
в В и А к одинаковому уровню и отсчитывают в бюретке В
объем выделившегося Ог.
1 мл Ог при 0° и атмосферном давлении равен 1,4289 мг
(0,0001786 экв.) кислорода; поскольку по реакции (ур. 128) на
2 эквивалента гипохлоритного кислорода выделяется 4 эквивалента газообразного кислорода, надо отсчитанный объем Ог
в бюретке разделить на 2 (кроме того надо сделать поправку на
температуру и упругость водяных паров).
Примечание. Наиболее быстрым и 'простым является газоволюметрическое определение СЮ', не требующее титрованных растворов, бюреток
и т. д. При методе Пено мешает наличие в титруемой жидкости большого
количества щелочи, ибо щелочь реагирует с выделяющимся иодом, вследствие чего нс получается синего пятна на иод-крахмальной бумажке.
3. Хлорат. Определяется в хлорированных, бертолетовых и
маточных щелоках, в фильтрпрессном шламе, в готовой бертолетовой соли и т. д. Обычно применяется перманганометриче-
ский метод, описанный на стр. 28 (§ 4, п. 4) *. При наличии
в анализируемой пробе СЮ' он также реагирует с FeSO« и определяется совместно с СЮз':
CIO' -f 2FeS04 + H2SO4 = СГ +: Fe2(S04)3 + Н2О. (129)
Поэтому в таких случаях надо к анализируемой пробе добавить раствор AS2O3 в количестве, соответствующем найденному
по п. 2 содержанию СЮ', либо вычесть найденное по п. 2 содержание СЮ' из суммы СЮз' + СЮ', определенной перманга-
нометрически. Для более ясного получения розового окрашивания при конце титрования рекомендуется к титруемой жидкости
прибавлять 10 мл раствора Рейнгарда. (К раствору 67 г
MnSC>4 • 4НгО в 500 мл воды добавляют 138 мл фосфорной кислоты уд. веса 1,7 и 130 мл серной кислоты уд. в. 1,84 и доводят
водой до 1 л.)
4. Хлорид. Хлорид определяется во всех щелоках, в готовой
бертолетовой соли и т. д. Определение производится по методу
Мора или по методу Фольгарда.
а) Определение СГ по Мору. К пробе щелока или
к раствору соли прибавляют 3—4 капли раствора К2СЮ4 и титруют 0,1 N раствором AgNOs до появления не исчезающего при
перемешивании оранжевого окрашивания. От прибавления раствора' AgNOs образуется белый осадок AgCl:
СГ.+ AgNOs = AgCl + NO»', (130)
1 См. также .журнал «Заводская лаборатория» № 4, 1936 г., стр. 425.
* /
309
Когда весь Cl осажден, избыток прибавляемого AgNOa образует с КгСЮ4 оранжевый осадок AgsCrOc
СЮ4" + 2AgN03 = Ag2Cr04 + 2NO»'. (131)
Поскольку Ag2Cr04 имеет большую растворимость, чем AgCl,
пока в растворе еще есть СГ, получившийся Ag2Cr04 при перемешивании вступает в обменную реакцию с СГ, образуя AgCl
и СЮ4".
В кислой среде Ag2Cr04 растворяется, в щелочной среде образуется черный осадок Ag20, затемняющий титрование. Поэтому
перед началом титрования жидкость должна быть нейтрализована, что производится раствором HNO» и СаСОз, поскольку
избыток последнего нерастворим и не мешает титрованию.
Следует иметь в виду, что СЮ' частично тоже титруется
с AgNOj. Поэтому до титрования восстанавливай^ СЮ' в СГ прибавлением 3%-ного раствора Н2О2. В полученные данные вносят
поправку на СЮ'.
б) Определение СГ по Фольгарду. К пробе, содержащей СГ, прибавляют раствор AgNOs в избытке против содержания СГ и 1—2 мл раствора железоаммониевых квасцов. Избыток AgNOs определяют титрованием раствором NH4CNS (или
KCNS) до получения красного окрашивания от образующегося
Fe(CNS)s. Осаждение AgCl проходит по уравнению (130). Реакция избытка AgNO* с NH4CNS проходит по уравнению:
v AgNOa + NH4CNS = AgCNS + NH4NO3. (132)
Когда в растворе больше нет Ag’, дальнейшее прибавление
NH4CNS вызывает красное окрашивание:
6NH4CNS + Fe2(S04)3 = 3(NH4)aS04 + 2Fe(CNS)a. (133)
При не слишком, большой концентрации HNO3 в растворе квасцов хлорат не восстанавливается и не мешает определению СГ.
Примечание. Если в титруемом растворе содержится СЮ', который
также частично реагирует с AgNOj, то надо до начала титрования восстановить СЮ' 3%-ным раствором HtOt. 'При подсчете содержания СГ надо
в результат титрования внести поправку «а количество СГ, образовавшееся
от восстановления СЮ' (1 экв. СГ соответствует двум окислительным эквивалентам СЮ').
Содержащийся в растворе хлорат не мешает определению СГ.
Необходимо только применять раствор квасцов с не слишком
высокой концентрацией HNO3.
5. Кальций. Определение кальция при небольшом его содержании обычно производится весовым путем, -как оно описано
в учебниках аналитической химии. При определении кальция
в хлорированных и бертолетовых щелоках можно .пользоваться
следующим простым и быстрым методом: к нейтральной анализируемой пробе прибавляют этиловый спирт в количестве
Уз—У* от, объема пробы и 3—4 капли раствора фенолфталеина,
после чего титруют 0,5 N раствором ЙагСОз (не содержащим
NaOH) до покраснений- Последнее происходит после осаждения
N ‘ ' / - / . • \
310 А •
нечто Са » нндс СаСОз и появлении в жидкоеm пним.дио, ■>
Na2CO:). Спирт необходим для подавления гидролиза СаС( Ь, вследствие которого покраснение жидкости наступило бы при неполном осаждении Са. При повышенной температуре титрование проходит лучше. При наличии в анализируемой жидкости СЮ' его
надо восстановить раствором Н2О2. При содержании Н или ОН'
жидкость должна быть нейтрализована до определения Са.
Количество Са в щелоках может быть определено также расчетом по содержанию в них СГ, СЮ' и СЮз'. При выражении состава щелока в экв/л количество Са равно
С1Ч-
СЮ' . сю/
2 ' 6 ‘
Так же как и Са, рассчитывается и «общий хлор», т. е. хлор,
содержащийся в щелоках в виде хлорида, гипохлорита и хлората. Аналитически общий хлор определяется после восстановления СЮ' и СЮз' раствором FeSC>4 в присутствии H2SO4 или
KNO2 в присутствии HNOs и т. п.
6. Калий. Определение калия является кропотливым и сложным. Однако правильный контроль обменной реакции и 'кристаллизации требует частого определения калия, почему мы его и
приводим. Метод определения калия выбираем кобальтгексани-
тритный, вполне оправдавший себя в нашей практике. Приводим
весовой и объемный вариант этого метода.
а) Весовой способ. Раствор, содержащий 0,05—0,1 г
соли калия, перенося* в фарфоровую чашечку, упаривают до
сиропообразной' консистенции и прибавляют 15 мл реактива —
раствора кобальтгексанитрита (см. ниже примеч. 2), перемешивая
жидкость в чашечке стеклянной палочкой. Происходит образование труднорастворимого K2NaCo(N02)e • Н2О по уравнению:
2К‘ + Co(N02)e + 7NaN02 + 2СН3СООН = K2NaCo(N02)eH20 +
+ 2NaNOs + 2Na’ + 2CH3COONa + NO. (134)
Оставляют на несколько часов (лучше на сутки), после чего
фильтруют через взвешенный тигель Гуча с асбестом или через
тигель Шотта со стеклянным фильтром. Осадок с чашечки смывают в фильтр 20%-ным раствором СНзСООН, которым и промывают осадок до получения вполне бесцветной промывной
жидкости и отрицательной реакции промывной жидкости на СГ.
После этого отмывают уксусную кислоту с осадка 10—15 мл
спирта и затем 10—15 мл эфира, после чего сушат тигель при
95—100° (не выше) до постоянного веса.
Пблученный осадок K2NaCo(N02)e • Н2О имеет молекулярный
вес 454,23. Таким образом количество калия равно
А ■ 78,2 -100 А • 17,2 0/ А • 78,2 ■ 1000 _ А ■ 4.4экв\л
навеска • 454,23 — навеска /о ИЛИ Б • 454*23 • 39,1 Б ’
где А обозначает вес полученного осадка, а Б обозначает взятое
для определения количество мл раствора (поскольку 'расчет
ведется по калию — эквивалент КСЮз равен 122,56 г).
311
6) О б ь с м и ы ii с п о с о и. Прибавление реактивов производится, как при иссопом способе. Нагрей на бане производи гея
(при частом перемешивании) до получения пастообразной массы.
Выделившийся осадок отфильтровывают через тигель Гуча,
в который вместо асбеста вкладывают два кружочка из фильтровальной бумаги. Промывку осадка производят, как при весовом способе. Тигель с осадком «переносят в стакан с доведенным до кипения раствором 80 мл 0,1 N КМп04, разбавленным
250 мл воды, и медленно при перемешивании жидкости в стакане
приливают 30 мл раствора H2S04 1 :3. При этом происходит
следующая реакция:
10K2NaCo(N02)« + 22КМп<Э4 + 33H2S04 = 2OKNO3 + lONaNO* +
+ 10Co(NOs)2 + 11K2S04 + 22MnS04 + 5N2Os + 33H20. (135)
Продолжают кипятить раствор 5—10 мин., после чего к горячей жидкости прибавляют по каплям при непрерывном перемешивании 80 мл 0,1 N раствора НгСгС^ для реагирования с избытком КМп04:
2KMn04 + 5Н2С*04 + 3H2S04 = K*S04 +
+ 2MnS04 -f 10CO2 + 8H20. (136)
Обычно после прибавления H2S04 1:3 в растворе остаются
черные крупинки Мп02, частично образовавшегося от разложения
КМп04. Раствор Н2С204 приливают до полного растворения этих
крупинок Мп02, после чего дают еще избыток (всего 80 мл).
Прозрачную жидкость опять подогревают (до 70—80°) и титруют
0,1 N раствором КМп04 до порозовения.
Как видно из уравнения (135), 10 молей K2NaCo(N02)e реагируют с 22 молями КМп04, т. е. 20 эквивалентов калия реагируют
с 22 • 5= 110 эквивалентов КМп04 или 1 экв. КМп04 = 0,182 экв.
калия = 0,182 • 39,1 = 7,12 г калия. Отсюда содержание калия
равно:
А- 0,0712 0, А- 0,00182
% ИЛИ ^
навеска 10 Б
ЭКВ {Л,
где А обозначает количество мл 0,1 N раствора КМп04, ушедшее
на титрование избытка Н2Сг04 (соответствующее количеству мл
0,1 N раствора КМп04, прореагировавшее с осадком), а Б обозначает количество мл раствора, взятое для анализа (поскольку
расчет производится по калию, эквивалент КСЮз равен 122,56).
Примечание 1. При определении следует придерживаться изложенной последовательности операции. Внесение тигля с осадком в воду до прибавления КМпО( вызывает частичное разложение осадка по уравнению:
К,NaCo(NO,).'-*• 2KNOj + NaNOa + Co<NOj)a+ NO, (137)
т. e. один эквивалент NOt окисляется до NOa, вследствие чего меньше прореагирует КМпОа. Тайнее нельзя прибавлять раствор HiS04 1:3 до внесе-
нияосадка в раствор КМпОа во избежание улетучивания образующейся
HN()-_\ чю *i'ci к ж г ирммодст к уменьшению колнчесша прорешгироьшщнп»
KMnOi. Кипячение осадки с рлепюром KMnOt больше 0,5 1 мин. не реко¬
мендуется, так как при этом образуются большие крупинки МпОг, труднее
•реагирующие с ЫаОО*.
Примечание 2. Реактив на калий, представляющий собой
NaaCo(N02)e • 0,5 Н20, готовят следующим образом. Растворяют 150 •'
NaN02 в 150 мл теплой воды. Фильтруют и к фильтрату прибавляют 50 г
Co(N03)2 • 6НгО и (при непрерывном помешивании) 50 мл 50%-ного раствора
СНзСООН. Полученный раствор продувают воздухом для освобождения от
NO и оставляют в закрытой склянке в темном месте на 1-2 суток, отчего
выделяется осадок от примесей калия, содержащихся и применяемых реактивах, который отфильтровывают. При хранении этот раствор довольно
быстро разлагается (через несколько дней). Твердую соль, устойчивую при
хранении, получают следующим образом {по Берль-Лунгедо). К жидкости,
отделенной от осадка (~ 250 мл), прибавляют 210 мл 96° спирта, отчего выделяется осадок Na3Co(N02)e. Осадок отжимают на воронке Бюхнера и промывают 4 раза по 15 мл спирта и 2 раза по 25 мл эфира. Промытый осадок
растворяют в воде (1 : 1,5) и осаждают прибавлением спирта; отсасывают на
воронке Бюхнера, промывают спиртом и эфиром и сушат между листами
фильтровальной бумаги. Такая соль при хранении в темном месте не изменяется очень длительное время. Для определения калия прибавляют свежеприготовленный раствор 1 г реактива в 5 мл воды.
7. Натрий. Определение натрия производится периодически
в хлористом кали (стр. 314, <п. 3), маточных щелоках и плавленом хлористом кальции (стр. 319, п. 5). Определение лучше всего
производить уранил-ацетатным методом (Берль-Лунге30 русский
перевод, том 2, часть I, вып. 2, стр. 437).
§ 2. Анализы сырья при производстве бертолетовой соли
известковым методом
1. Известь. Состав и свойства извести описаны на стр. 39—40.
При текущем контроле в извести определяют СаО и СаСОз.
Более подробный анализ делается из средне-месячных проб, при
получении крупной партии извести, при получении извести из
нового месторождения и т. д. Особое внимание надо уделять
правильности отбора проб извести, так как она часто неоднородна. Во избежание поглощения СОг и влаги из воздуха пробы
извести надо хранить в банках с притертыми пробками.
Определение СаО производится, как описано на стр. 307, п. 1:
1 мл 1N раствора НС1 соответствует содержанию 2,8% СаО
в извести. Определение СаСОз производится путем прибавления
избытка 0,1 N раствора НС1 к жидкости от титрования СаО и
оттитровывания избытка НС1, остающегося после растворения
СаСО* 0,1 N раствором NaOH; 1 мл 0,1 N раствора НС1 соответствует' содержанию 0,05% СаСОз в извести. Более точно СаСОз
определяется газоволюметрически, как описано на стр. 308,
наливая в бюретку D соляную кислоту (см. также Берль-Лунге*1,
стр. 237); 1 мл выделяющейся СО* весит 0,00198 г (при 0° и 760 мм);
если брать навеску в 4,5 г извести, то 1 мл выделившейся СОг
будет соответствовать содержанию 0,1% СаСОз.
Иногда определяют также количество негасящейся части
извести и скорость гашения извести (см.ОСТ’ы 2843 и 5810).
\7
313
2. Хлоргаз. Состав к свойства хлоргаза описаны nacip. 43 Ь
Наиболее часто в хлоргазс определяется, только пропейi СЬ.
Периодически определяется также содержание СЮ», С)», II»,
влаги и т. д. Анализ хлоргаза обычно производится аппаратом
Орса, последовательным поглощением газов реактивами. При
хлоргазе с высокой концентрацией СЬ количество и состав примесей СОг, Ог и +12 более точно определяются в пробе «ие-
хлора» — остатка после поглощения хлора из хлоргаза. Подробный анализ описан в книге автора 1 (см. также аналитическую
химию Тредвелла, т. II, ч. 2 и руководства но газовому анализу
Францена, Лидова, Гродзовского).
3. Хлористый калий. Состав и свойства хлористого калия описаны на стр. 49. При текущем контроле производства обычно
определяют только процент КС1 титрованием СГ 0,1 N раствором AgNOs (см. стр. 309, п. 4). Периодически производят также
следующие определения: процента КС1 по калию (стр. 311), примесей нерастворимых веществ, соединений Na, Mg, SO4, Fe и Al,
содержания! воды и т. д.
4. Аммиачная вода. Применяется для обезвреживания перс-
хлорированных щелоков от СЮ' (стр. 95). При текущем контроле
определяется только содержание NH4OH титрованием раствором
НС1. Периодически производится более полный анализ по ОСТ
3754 и 6449.
5. Гипосульфит. Часто применяется для обезвреживания пе-
рехлорированных щелоков от СЮ' (наряду или вместо аммиачной воды). Процент NajS20s определяется титрованием 0,1 N
раствором иода. Более подробный анализ производится по
ОСТ 6703.
§ 3. Анализы производственных растворов, получаемых при
производстве бертолетовой соли известковым методом -
1. Известковое молоко. Приготовление, состав и свойства
известкового молока описаны на стр. 56. При текущем контроле
в известковом молоке определяются СаС, СаСОз и его уд. вес.
Если для приготовления известкового молока применяют производственные промывные воды, то определяют еще содержание СГ и СЮз'. Примеси соединений Mg, SO4 и т. д. определяются
в известковом молоке лишь по особому заданию. Так как
известковое молоко при хранении расслаивается, то правильная
средняя проба получается лишь при отборе из тщательно перемешанного известкового молока.
Обычно уд. вес определяется ареометром. При известковом
молоке высокой концентрации, которое имеет большую вязкость, определение уд. веса ареометром затруднительно; опре-
1 Контроль производства хлора и каустика, М., 19Э4.
2 Считаем наиболее удобным выражать состав производственных растворов в экв/л, что, упрощает, расчет состава, сравнение состава разных
растворов, расчет выходов и потерь и т. д.
314
деление можно произнести взвешиванием литровой мерной
колбы пустой и с известковым молоком.
СаО и СаСО» определяют в 5—10 мл известкового молока,
как описано на стр. 307. Определение СГ и CIOs' производят
в 10 мл известкового молока, как описано на стр. 309. Следует
развести известковое молоко в 3—4 раза водой, переболтать,
дать отстояться и брать для определения СГ и СЮ»' часть прозрачной отстоявшейся жидкости, так как Са(ОН)г, взвешенный
в молоке, затрудняет определение СГ и CIOs'.
2. Недохлорированные щелока. Эти щелока получаются при
улавливании СЬ из абгаза, а также по ходу хлорирования и содержат Са(ОН)г, Са(СЮ)г, СаСЬ и, реже, еще Са(СЮ»)г. Обычно
определяют только содержание СЮ' (стр. 307). Определение СГ и
CIOs' производят в 1 мл щелока, разведенного водой в отношении 1 : 10, как указано на стр. 309. Определение Са(ОН)г производят, как в известковом молоке (стр. 314, п. 1), после предварительного восстановления СЮ' 37«-ным раствором НгОг. Расчет
процента выхода СЮ' см. стр. 91.
3. Перехлорированные щелока. Эти щелока получаются но
окончании хлорирования. Щелока содержат в основном Ca(dO»)s
и СаСЬ и в виде примеси Са(СЮ)г и растворенный хлор. Суммарное содержание СЮ' определяют в 10 мл щелока, как указано на стр. 307; СГ и СЮ»' определяют (в 10 мл щелока, разведенного водой в отношении 1 : 10), как указано на стр. 309. Кислотность щелока (Н‘) можно определить титрованием 10 мл
щелока 0,1 N раствором NaOH после предварительного восстановления СЮ' нейтральным 3%-ным раствором НгОг.
Восстановление СЮ' раствором НгСЬ происходит по уравнению:
Раздельное содержание Са(СЮ)г и растворенного хлора рассчитывается соответственно определенному содержанию СЮ' и
Н' по формулам:
Са(СЮ)г = (А—В) экв/л или (А—В)35,75 г/л.
Растворенный хлор = В экв/л или В 35,46 г/л,
где А « В обозначают найденное, как указано выше, содержание
СЮ' и Н' в экв/л щелока.
Раздельное содержание свободного хлора и хлорноватистой
кислоты можно определить иодометрическим методом (стр. 308),
подкисляя пробу титрованным раствором НС1 и титруя жидкость
сначала гипосульфитом, а затем 0,1 N раствором NaOH. Определение основано на том, что хлорноватистая кислота при реакции
с KJ образует иод и КОН, а свободный хлор образует только
Са(СЮ)2 +-2НгОг = СаСЬ + 2НгО + 20г
НСЮ -f НС1 + НгОг = 2НС1 + НгО + Ог
038)
(139)
иод:
НрО + 2KJ = КС1 + КОН + J»
/ СЬ + 2KJ — 2КС1 + J*.
(140)
(141)
./
315
(См. Бсрль-Лунге 30 русский иср., том. 2, часть 1, вып. 2, стр. 38,S).
Примечание. Впиду того что кислотность нерехлорироианного
щелока и содержание в нем СЮ' обычно очень малы, целесообразно отбирать большие пробы щелока н определение проияподить и 100 m.i щелока.
Определение Н' и СЮ' надо производить сразу после отбора пробы,
так как растворенный хлор постепенно улетучивается из проб щелока.
4. Обезвреженные хлорированные щелока. Эти щелока получаются после обезвреживания от СЮ' перехлорированных щелоков. В этих щелоках определяются СГ и СЮз' в 10 т щелока,
разведенного водой в отношении 1 : 10, как указано на стр. ЗОН.
Часто еще определяют уд. вес (ареометром) и объем осадка.
Последний обычно определяется путем отстоя пробы перемешанного щелока в мерном цилиндре на 100 мл и наблюдения количества мл отстоявшегося осадка через определенный промежуток времени (через 1 час и т. д.).
Расчет процента выхода хлората см. стр. 90.
5. Уваренные щелока. Эти щелока получаются .после выпарки
обезвреженных щелоков (стр. 103). Обычно в них определяются
СГ и CIOs'. Определение производится, как в обезвреженных щелоках (см. выше п. 4), только надо брать в два раза меньше щелока (5 мл из щелока, разведенного водой 10:100), поскольку
концентрация этих щелоков более высокая.
Расчет процента выхода хлората см. стр. 90.
6. Раствор хлористого калия. Этот раствор приготовляется
растворением хлористого калия в производственных промывных
жидкостях и служит для обменной реакции с уваренным хлорированным щелоком (стр. 107). В нем кроме КС1 обычно содержатся еще КСЮз и СаСЬ (перешедшие из промывных жидкостей). Обычно в нем определяется только КС1 по СГ. Определение ведется титрованием с 0,1 N раствором AgNOe 10 мл
раствора, разведенного водой в отношении 10 :100 (т. е. в 1 мл
раствора), как описано на стр. 309. Определение СЮя' производится как в обезвреженном щелоке (см. выше п. 4).
7. Бертолетовые щелока. Эти щелока получаются после обменной реакции уваренного хлорированного щелока с раствором
КС1 (стр. 107). Щелока содержат СаСЬ и КСЮз и в виде примеси
КС1 или Са(СЮз)г. Определение СГ и СЮз' производится, как
в уваренных щелоках (см. выше п. 5). Часто определяют еще
калий; определение производится в 10 мл щелока, разведенного
водой, в отношении 10 : 500 (т. е. в 0,2 мл щелока), как описано
на стр. 311. Расчет раздельного содержания КСЮз и Са(СЮз)г,
как и СаСЬ и КС1, а также расчет процента выхода хлората и
процент избытка или недодачи КС1 производится, как указано
на стр. 111.
Надо иметь в виду возможность выделения кристаллов КСЮз
и КС1 при охлаждении отобранной пробы щелока.
8. Маточный щелок 1-й кристаллизации. Эти щелока получаются после кристаллизации КСЮз. Кроме СаСЬ они содержат
еще КСЮз и КСГили Са(СЮз)*. Определение СаСЬ производится
в 5 мл из, разведенного водой щелока в отношении 10 :100 (т. е.
/
в 0,5 мл щелока). Определение СЮз производится и К) ли щелока, разведенного водой 10: 100 (т. е. в 1 мл щелока). Иногда
определяют еще содержание калия; для определения К' берут
10 мл разведенного водой щелока в отношении 10 : 100 (г. е.
в 1 мл щелока). Расчет процента потери хлората с маточным щелоком см. ст.р. 132. Расчет процента избытка или недостатка КСЛ
при обменной реакции, см. стр. 111. Для правильного определения СЮз' и К' отобранные пробы щелока не должны содержат!»
взвешенных кристаллов.
9. Разваренные щелока. Так называются горячие щелока,
полученные растворением бертолетовой соли для ее перекристаллизации (стр. 115). В этих щелоках определяют СГ и СЮз',
а также уд. вес. Определение СГ производится в 10 мл щелока.
■Определение СЮз' производится в 10 м щелока, разведенного
водой <в отношении 10 :100 (т. е. в 0,2 мл щелока).
При отборе проб этих щелоков надо иметь в виду быстрое
выделение из них кристаллов КСЮз при охлаждении во время
отбора и переноски пробы.
10. Маточные щелока 2-й кристаллизации и промывные воды.
В этих жидкостях обычно определяются СГ и СЮ'», Определение СГ производится в 10 мл жидкости. Определение СЮ'з производится в 10 мл щелока, разведенного водой в отношении
10:100 (т. е. в 1 мл жидкости).
В заключение этого, параграфа приводим примеры расчетов
по анализу недохлорированных щелоков.
СаО. Для определения взято 5 мл перемешанного щелока.
Ушло на титрование 6,8 мл 1 N раствора НС1. Содержание СаО
равно 6,8 • 0,2= 1,36 экв/л, или 1,36 • 28 = 38,1 г/л.
CIO'. Определение произведено иодометрическим методом
(стр. 308) в 10 мл щелока. При титровании ушло 13,8 мл 0,1 N
раствора NasSsOs. Содержание СЮ' равно 13,8 • 0,1 = 1,38 экв /л.
СГ. Определение произведено по Мору в 1 мл щелока (разбавленного водой в отношении 1 : 10) после восстановления СЮ'-
в СГ раствором Н*Ог. При титровании ушло 31,1 мл 0,1 N раствора AgN03. Содержание хлора в виде хлорида и гипохлорита
равно 31,1 -0,1=3,11 экв/л. Содержание СГ равно
3,11 — ^ = 2,42 экв/л.
CIOs'. Определение произведено в 1 мл щелока (разведенного
водой в отношении 1 :10) без восстановления CIO' раствором
НгОг. .Связалось 31,8 мл 0,1 N раствора FeSO«. Содержание
СЮ'+ CIOs' равно 31,8-0,1=3,18 экв /л. Содержание CIOs'
равно 3,18—1,38=1,80 экв/л.
Общий хлор. Содержание хлора в виде хлорида, гипохлорита и хлората рассчитывается по формуле
п» | С1СК | СЮ.'
, Cl Н 2 I ~ С
и будет равно , •
'' 2,42 + -^ + =3.41 экв/л.
317
Расчет выходов и потерь при хлорировании:
1/0* 100 С.О Q0 /
выход хлората равен— —— = 52,8°/();
1 38 • 100
выход гипохлорита ’ 3 41— = 40,5°/„;
потеря от выделения Оз равна 100 — (52,8 + 40,5) ~ 6,7%.
§ 4. Анализы отходов, получаемых при производстве
бертолетовой соли известковым методом
1. Абгаз. Абгаз получается в результате поглощения известковым молоком хлора из хлоргаза. Состав и свойства абгаза
описаны на стр. 89. Практически абгаз является отбросом, а нс
отходом. Лишь при содовом Методе производства бертолетовой
соли абгаз содержит так много СО», что становится рентабельным его использование (стр. 159). Анализ абгаза на СЬ, ССЬ,
Нг и Ог производят аппаратом Орса. Более точно можно определить содержание СЬ протягиванием большого объема абгаза
через склянки с раствором KJ с последующим титрованием
выделившегося иода, раствором гипосульфита. Можно также
протянуть абгаз через раствор гипосульфита или AsaOs с последующим титрованием нелрореагировавшего избытка гипосульфита. Таким же образом можно определить и содержание
ССЬ .протягиванием абгаза через раствор щелочи.
Литературу по газовому анализу см. стр. 314, п. 2.
Расчет процента потери хлора с абгазом и потери при хлорировании по анализам хлоргаза и абгаза см. стр. 91—92.
2. Шлам от очистки известкового молока. Этот шлам получается в результате отделения примесей от известкового молока
и содержит Са(ОН)г, СаО, СаСОз и т. д. (стр. 99). Обычно в нем
определяется только содержание суммы Са(ОН)г и СаО. Для
определения разбавляют 100 г шлама горячей водой до 500 мл
и 50 мл разведенного шлама (10 г шлама) титруют 1 N раствором
НС1 (стр. 307). Если в этом шламе много СаО, его выщелачивают.
3. Шлам от хлорированного щелока. Этот шлам получается
при отстое или фильтрации хлорированного щелока от нерастворимых примесей и содержит кроме нерастворимых примесей
(СаСОз, песок и т. д.) еще СаСЬ и Са(СЮз)з, а иногда и СаО
(стр. 99). Для анализа разбавляют 100 г шлама горячей водой
до 500 мл. Нерастворившиеся вещества отделяют, промывают и
высушивают. Этот осадок иногда подвергают дальнейшему
анализу. В отфильтрованном растворе определяют Са(СЮз)г и
СаСЬ. Если в этом шламе содержится значительное количество хлората, производится промывка или выщелачивание
шлама. Если в нем содержится мало хлората, то шлам является
отбросом.
4. Вымороженные маточные щелока 1-й кристаллизации. Эти
щелока получаются после охлаждения до низкой температуры
и отделения выкристаллизовавшихся кристаллов КСЮз (стр. 115).
Их анализ производится, как описано выше в п. 8 (стр. 316).
318 • •/
5. Плавленый хлористый кальций. Этот продукт является
единственным ценным отходом производства бертолетовой соли
известковым методом.
Состав и свойства его см. стр. 141. На этот продукт имеется
ОСТ 4100 (стр. 352), имеющий однако ряд серьезных недостатков. Для более полного представления о составе продукта, в нем
необходимо определять содержание калия (стр. 311), по которому можно рассчитать содержание КСЮз и КС1 (стр. 111) и натрия (стр. 313), по которому можно рассчитать содержание
NaCl.
По составу плавленого хлористого кальция можно также рассчитать %
избытка или недостатка КО при обменной реакции и % потери KCIO*
с маточными щелоками — см. стр. 111 и 132..
Многие потребители прокаливают получаемый продукт при 400—500°.
В такой продукте обычно КСЮз уже нет, так как при прокаливании ои разлагается на KCI и кислород.
§ 5. Контроль готовой бертолетовой соли
а) Отбор проб
1. Отбор пробы на заводе, производящем бертолетову соль.
Бертолетова соль обычно упаковывается в деревянные бочонки
весом нетто 50 кг соли. От одной операции сушки обычно получают 10—20 бочонков соли (стр. 134). От каждого бочонка
отбирается проба щупом, доходящим до */я глубины бочонка.
Пробы, взятые от одной партии, соединяются в. одну среднюю пробу, хранимую в банке с притертой пробкой.
2. Отбор пробы потребителями. Пробы отбираются щупом,
доходящим до У я глубины бочонков не менее как от 10% бочек
испытуемой партии. Отобранные пробы от бочонков одной партии (~ 1,5 кг соли) тщательно перемешиваются и насыпаются
в три банки с притертыми пробками. 'Проба одной банки анализируется, а две другие банки хранятся как контрольные.
б) Технические условия
- ОСТ на техническую бертолетову соль пока нет; имеются
только проекты ОСТ. В основном требования к бертолетовой
соли зависят от целей потребления. Для спичек обычно допускается соль, содержащая до 0,5% примесей. Для взрывчатых и т. п. целей требуется соль, содержащая очень мало примесей (в сумме до 0,1 %) и не дацнцая увлажняемости больше 0,1 % <
при хранении в сыром, месте. Медицина требует также очень
чистую соль. В данное время большей частью выпускают соль
двух сортов (1-й и 2-й кристаллизации) примерно следующего
состава
1-й сорт 2-й сорт
1. Хлоридов не больше 0,05% 0,30%
2. Щелочи не больше нет 0,05%
3. Сульфатов не больше следы 0,05%
1 Состав бертолетовой соли, применяемый как реактив, см. стр. 348.
Часто еще обусловливают величину кристаллов технической бертолетовой
соли (например, чтобы через сито в 100 меш проходило не меньше, 95%
соли и т. д.).
31?
5. Нерлстпоримых и иоде соединений нс больше
6. Органических примесей не больше
7. Унлажпиемость не спышс
8. КСЮ3 (по разнице) не ниже . . . .
1. Промлмж нс больше . . . .
Содержание влаги, определенной высушиванием пробы соли
при 105—110°, должно быть не свыше 0,10% для 1-го сорта и
0,30% для 2-го сорта. При известковом методе получения КСЮа
примеси рассчитываются как соединения Са. При каустическом
методе примеси рассчитываются как соединения Na. При методе, исходящем из электролиза раствора КС1, примеси рассчитываются как соединения К. «Следы» обозначают количественное содержание меньше 0,01%.
1. Определение щелочи. 10 г соли растворяют в 50—60 ли
воды, прибавляют 1—2 капли метилоранжа и титруют 0,1 N раствором НС1; 1 ли- 0,1 N раствора НС1 соответствует 0,028% щелочи в расчете на СаО.
2. Определение хлоридов. 10 г соли растворяется в 50—60 ли
воды и определяют СГ, как указано на стр. 309, п. 4; 1 «л 0,1 N
раствора AgNOs соответствует содержанию 0,0555% хлорида
в расчете на СаСЬ.
3. Определение нерастворимого в воде остатка. 50 г соли
растворяют в 200—250 мл горячей воды. Раствор нагревают на
бане 1 час и фильтруют через взвешенный высушенный при 110°
фильтр. Остающийся на фильтре осадок тщательно промывают
горячей водой. Промытый фильтр с осадком высушивают до
постоянного веса. Содержание в соли нерастворимых примесей
равно А • 2%, где А обозначает вес осадка в граммах.
4. Определение сульфатов. Фильтрат и промывные воды от
предыдущего определения подогревают до кипения, прибавляют
1 мл 1W раствора НС1 и по каплям прибавляют 10 мл кипящего
10%-ного раствора ВаСЬ. Оставляют раствор на водяной бане
на 50—60 мин., после чего сливают отстоявшуюся прозрачную
жидкость через беззольный фильтр. К, остатку жидкости с осадком прибавляют 50—400 мл горячей воды, перемешивают, дают
отстояться и декантируют отстоявшуюся жидкость на фильтр.
Остаток с осадком сливают на фильтр, смывая его горячей водой, после чего фильтр с осадком тщательно промывают горячей
водой. Промытый фильтр высушивают при 110°, переносят во
взвешенный тигель, сжигают и прокаливают. Охладив прокаленный тигель в эксикаторе, взвешивают его и, смочив осадок
1—2 каплями H*S04 уд. веса 1,84, высушивают и снова прокаливают, охлаждают и взвешивают. Содержание сульфатов в соли
будет А • 1,1656% в пересчете на CaSO« и А ■ 1,2168% в пересчете
на NasSO*, где А обозначает вес осадка в граммах.
5. Органические примеси. Высушенный остаток, нерастворимый. в воде (п. 3), переносят в стакан, прибавляют 15—20 мл
в) Количественные определения
йоды и затем 5 мл соляной кислоты уд. нес 1,19, нагревают до
кипения, отфильтровывают через беззольный фильтр и тщательно промывают горячей водой до отрицательной реакции
.на СГ. Промытый фильтр высушивают при 100—110° до постоянного веса, после чего сжигают, прокаливают, охлаждают и
взвешивают. Содержание органических примесей в соли равно
2 (А—Б)%, где А обозначает вес остатка, нерастворимого *в соляной кислоте, а Б — вес прокаленного остатка.
6. Бромат. 1 г соли растворяют в 45 мл воды. К раствору
прибавляют 1 мл 5%-ного раствора KJ и 'А мл раствора крахмала.
Перемешивают и прибавляют еще 5 Мл 0,1 N раствора H2SO4.
Синее окрашивание должно наступить не раньше чем при контрольном опыте с раствором 1 ч. х. ч. КСЮз и 0,2 мг KBrOs при
анализе соли 1-го сорта и 1 мг КВгОз при анализе соли 2-го сорта.
Примечание. По Тредвелл-Голлу (Курс аналитической химии, т. I,
стр. 477, над. 1933 г.) берут 2 г хлората, растворяют в 100 мл воды и прибавляют 5 мл 10%-ного раствора KJ, 5 мл раствора крахмала и 5 мл 1 N
раствора НС1 (см. также Каст и Метц0*, стр. 319). По нашим данным при
таком методе определения бромата быстрое синее окрашивание наступает и
при химически чистом хлорате, заведомо «с содержащем бромата (по этому
вопросу ом. также статью В. Л. Пешкова в журнале «Заводская лаборатория» Мг 10, 1933 г.).
По И. М. Коренману (журнал «Заводская лаборатория» № 4, 1935 г.,
стр. 427) берут 2 мл 1%-ного раствора испытуемого хлората, прибавляют
1 мл 3 'N раствора НС1 и 3 капли раствора метилоранжа 0,015%. При содержании в хлорате 0,1% KBrOi раствор обесцвечивается через несколько се-
жунд.
7. Влага. Навеску в 10 г соли сушат при 105—110° до постоянного веса. Уменьшение веса в граммах, умноженное на 10,
показывает процент влаги.
Примечание. Химически чистая бертолетова соль показывает очень
малую разницу .в уменьшении в весе отри сушке при 105—?-110° и при 180—
*200°. Некоторые сорта технической бертолетовой соли показывают разницу в 0,2—0,3%. (См. прим. стр. 18).
8. Увлажняемость. Поставить под колокол рядом с сосудом
с водой бюксу с навеской в 10 г анализируемой соли и бкжсу
с навеской в 10 г химически чистой соли. Пробы обеих солей
предварительно должны быть высушены при 105—110°. Через
24 часа вынуть бюксы из-под колокола и взвесить. Увлажняемость анализируемой соли при данной температуре равна 10
(<4 — Б)%,. где А обозначает привес бюксы с айализируемой
солью, а Б — привес бюксы с химически чистой солью.
т) Качественные пробы на ч и с f о т у соли высшего
качества (по Мерку)
v
1. Щелочность. Раствор 1 г соли в 40 мл теплой воды не должен давать окрашивания от прибавления фенолфталеина и не
должен менять окраску розовой лакмусовой бумажки.
2. Хлорид. К раствору 1 г соли в 40 мл теплой воды прибавляют
1—2 каплй азотнбй кислоты удГ веса 1,15 и 1 мл 0,1 N раствора
;AgNOs. Не должно получиться мути.
21 Зак. 179. — Шрайбщьа.
321
3. Сульфаты. 5 г соли растворить в 150 мл воды, прибавить-
1 мл 1 N раствора MCI и 5 мл 10%-ного раствора ВаСЬ. Через
5 час. не должно выпасть ни осадка, ни мути.
4. -Гипохлорит. К раствору 2 г соли в 100 мл воды прибавить
5 мл 10%-ного раствора KJ и 3 мл раствора крахмала. Не должно
получиться даже слабого посинения.
§ 6. Особенности контроля производства бертолетовой соли
каустическим, содовым и электролитическим методами
а) Контроль производства бертолетовой соли
, каустическим методом
Схема каустического метода производства изложена в гл. 13,
стр. 156. Основным отличием контроля этого способа от контроля производства при известковом методе является отсутствие
контроля стадии приготовления известкового молока и отделения шлама и то что в большинстве анализов приходится иметь
дело с солями натрия, а не кальция. Однако при этом методе,
производства добавляется контроль «слабого каустика», поступающего на хлорирование, и «обратной соли», выделяющейся
при выпарке. Наиболее частыми определениями, которые приходится делать при контроле производства, остаются- определения СГ, CIO', ClO'j и калия. Производят эти определения так же,
как н при известковом методе (см. стр.. 307—312).
1. Слабый каустик. Поступающий на хлорирование слабый
каустик содержит в основном NaOH и NaCl. В качестве примесей в нем обычно содержатся ИагСОз, NaClOs и реже NaClO.
Обычно Na*COs определяется совместно с NaOH и рассчитывается как NaOH.
10 мл слабого каустика разводят водой в мерной колбе до
100 мл; 10 мл раствора титруют в присутствии метилоранжа
0,1 N растворам НС1, 1 мл которого соответствует содержанию
NaOH 0,1 экв/л (4 г/л). Хлорид определяют в других 10 м/
раствора, как указано на стр. 309, п. 4; 1 мл 0,1 N раствора AgNOe
соответствует содержанию NaCl 0,1 экв/л (5,846 г/л). Хлорат
определяют в 10 мл неразбавленного слабого каустика, как указано на стр. 309, п. 3, осторожно нейтрализовав NaOH кислотой
(без избытка); 1 мл 0,1 N раствора FeSO« соответствует содержанию хлората ИаСЮз в 0,01 экв/л. Гипохлорит определяют
в 10 мл неразбавленного слабого каустика иодометрическим методом, как указано на стр. 308.
При содержании в слабом каустике СЮ' его разрушают при-
; давлением 3%-ного раствора Н2О2 перед определением NaOH и
NaCl (при расчете учесть образование СГ из СЮ').
2. Обратная соль. Выделяющаяся при выпарке хлорированных и маточных щелоков «обратная соль» состбит в основном
из NaCl, а в качестве примесей содержит хлорат, щелочь и влагу
(см. табл. 63, стр. 203).
Щелочь определяют в раствбре 10 г соли титрованием 0,1 N
раствором НС1 с метилоранжем; 1 мл 0,1 N раствора НС1 соответ-
' / 4 1 - '
322 -л '
ствует содержанию 0,04% щелочи и пересчете на NaOlI. Хлорат определяют тоже в растворе 10 г соли обычным путем (см.
стр. 309, и. 3); 1 мл 0,1 N раствора FeSO.t соответствует содержанию 0,020% КСЮз. Хлорид определяется по Мору или
Фольгарду в 10 мл раствора 10 г соли в 500 мл воды; 1 мл 0,1 N
раствора AgNOa соответствует содержанию 2,92% NaCl.
3. Щелока. Хлорированные щелока и раствор КС1 анализируются так же, как и при известковом методе (см. стр. 315—316).
При анализе уваренных бертолетовых и маточных щелоков необходимо только иметь в виду, что содержание хлората в них
больше, чем в соответствующих щелоках при известковом методе, почему для определения СЮ'з надо брать меньше раствора:
в уваренных и бертолетовых щелоках по 0,2 мл, а в маточных
щелоках 0,5 мл. В уваренных бертолетовых и маточных щелоках
обычно содержится еще щелочь, а при обезвреживании гипосульфитов еще сульфат. Определение щелочи производится, как
в слабом каустике (см. выше). Определение сульфата производится в 10 мл щелока: нейтрализуют, прибавляют 20 мл 0,5 N
раствора ВаСЬ, 30 мл спирта и 3—4 капли раствора фенолфталеина, подогревают и титруют избыток ВаСЬ 0,5 N раствором
ЙагООз (см. стр. 310, п. 5); 1 мл 0,5 раствора ВаСЬ соответствует содержанию Na2SC>4 в 0,05 экв/л (3,55 г/л).
Расчет выходов и потерь по анализам щелоков производится,
как указано на стр. 90. Расчет раздельного содержания NaClOs
и КСЮз или КСЮз и КС1 без анализа на калий см. стр. 176;
расчет изменения объема при кристаллизации см. стр. 203; расчет содержания хлоратов в уваренном щелоке по его уд. в. см.
стр. 175.
4. Хлоргаз и абгаз. Анализ хлоргаза и абгаза одинаков при каустическом и известковом методах производства (см. стр. 314 и 318).
5. Готовая соль. В общем определения делаются так же, как
и .при известковом методе. Примеси хлоридов, сульфатов и т. д.
рассчитывают как натриевые соли. В готовой соли 1-й кристаллизации иногда еще содержится NaClCb, для расчета содержания
которого приходится делать анализ соли на натрий. Соединения
Са и Mg обычно в соли отсутствуют. Содержание броматов
в соли,, полученной каустическим методом, обычно несколько'
больше, чем в соли, полученной известковым методом, так как
благодаря характеру данного метода (стр. 156) бромистые соединения, попадающиеся в цикл производства при обменной реакции, не удаляются в процессе производства и их количество
поэтому увеличивается.
б)Ко1ггроль производства бе'ртолетовой соли
содовым методом
В общем контроль производства при содовом методе отличается от контроля производства при каустическое методе
только контролем .раствора, поступающего, на хлорирование, и
контролем хлорируемого щелока. В остальном никакой разницы
нет^схщяу содового метода см.., стр. J59).
21*
323
В поступающем на хлорирование растворе соддо кроме Na-COj
надо определять еще примеси NaCl и хлората. Определение ЫагСОз производится титрованием 10 мл раствора, разбавленного водой 10:100, 0,1 N раствором НС1 с метилоранжем.
Определение NaCl и NaClOs производится, как в слабом каустике
(см. выше, стр. 322).
В хлорируемом щелоке иногда требуется произвести анализ
щелока по ходу хлорирования (см. стр. 169). Определяют ШгСОз,
NaHCOs, NaClO, NaClO.i и NaCl. Для определения! ЫагСОз и
NaHCOs разрушают NaClO прибавлением 3%-ного раствора Н2О2,
после чего определение ведут, как обычно, титруя 0,1 N раствором НС1 при индикаторах фенолфталеине и метилоранже.
Определение -СЮ' производят иодометрически (стр. 308). Определение NaCOa и NaCl производят, как обычно (см. стр. 309,
п. 3 и п. 4).
в) Контроль производства КСЮз, получаемой
электролитическим методом
Анализируют поступающий на электролиз раствор, газы,
выделяющиеся из электролизеров, щелок после электролиза,
щелок до и после кристаллизации и получаемую соль. В щелоках до и после электролиза определяют КС1 (или NaCl), КСЮз,
CIO', Н’, СЮ4" (и СГ2О7"). В газах; выделяющихся из электролизеров, определяют СЬ, Ог, СОг, Нг. В щелоках до и после
кристаллизации определяют главным образом КСЮз. Готовая
соль анализируется, как обычно, только с добавкой определения соединений хрома. Методы определения СЮ',_СЮ'з и т. д.
идентичны таковым при контроле производства известковым
методом.
§ 7. Контроль производства хлората натрия и хлората бария.
а) Контроль производства хлората натрия
(гл. 15, стр. 186)
Контроль перйых стадий производства идентичен контролю
соответствующих стадий при получении бертолетовой соли.
Контроль выпарки натриево-хлоратных щелоков (стр. 196) и дальнейших стадий производства исходит из щелоков, содержащих
в основном NaClOs и NaCl. В виде примесей обычно содержится
щелочь (NaOH и ШгСОз) и NaaSCU. В готовом)хлорате натрия
делаются те же определения, что и в бертолетовой соли
(стр. 319), рассчитывая все соединения как соли натрия. Если
имеется подозрение на попадание в хлорат натрия примеси
КСЮз, надо определить калий (см. стр. 311), по которому рас:
считывают содержание КСЮз. s
б) Контроль производства хлората бария
,. (гл. 16, стр. 2Ю)
Определения СКУ^л СЮ'з делаются, обычным путем. Определения СГ производят по' Фольгардту. При желании определить
324 ^
СГ по Мору надо предварительно осадить Ва' ' прибавлением
избытка раствора ШгСОя, после чего отделить осадок и в фильтрате определить СГ. При получении хлората бария методами,
исходящими из NaClOa или КСЮз, надо примеси их определять
в готовом продукте. При методе производства, исходящем из
обменной реакции NaClOa с ВаС1г, в щелоках и готовой соли
могут содержаться одновременно Ba(QO*)* и NaClOa или NaCl
и ВаС1*. Их расчет производится из сравнения найденного содержания Ва'', СЮ'з и СГ. Приводим пример таких расчетов.
при¬
мера
Какие щелока
Найдено анализом
экв/л
Содержится ji щелоках экв/л
Ва-
СКУ,
СГ
Ва (СЮ,),
NaCIO,
NaCl
Bad,
1
До кристаллизации ......
2,42
4,35
2,42
2,42
1,93
2,42
Нет
2
После кристаллизации
0,74
3,10
2,96
0,74
236
2.96
Нет
'3
До кристаллизации
2,42
2,02
2,42
2,02
Нет
202
0,40
4
После кристаллизации
1,19
0,70
2,94
0,70
Нет <
2,43
0,49
Примечание^. Содержание СЮ'-, приводится в нормальных эквивалентах (не окислительных); 1 экв. Ва (СЮ3)2 = 152,15 г.
Литература
1. Шрайбиан, Контроль производства хлора и каустика, М. 1934,
особенно стр. 76—102 и 173—174. „
2. Каст и Метц".
i 3. Б е р л ь-Л у н г е *°. \
4. Б е р л ьтЛ у н г е ". '
5. Руководства - по аналитической химии Кольтгоффа, Тредвелла и др.
ГЛАДА 23
ТЕХНИКА БЕЗОПАСНОСТИ, ОХРАНА ТРУДА И ПРОТИВО-
' ПОЖАРНЫЕ МЕРОПРИЯТИЯ
При производстве бертолетовой соли кроме мер безопасности, обычных для любого завода, приходится учитывать еще
специфические особенности работы с хлоргазом, отравляюще
действующим на организм (а при некоторых условиях образую-
щим( взрывчатые смеси), и с бертолетовой солью, являющейся
весьма опасной в отношении возможности пожаров и взрывов.
В этой главе приводим данные об опасности бертолетовой соли
и хЛоргаза, описываем некоторые аварии, случившиеся на производствах бертолетовой соли, и. приводим основные мероприя¬
тия, необходимые для уменьшения опасности и предотвращсчшя
аварий.
Почти все нижеизложенное остается в силе и для производства хлората натрия, хлората бария и др.
§ 1. Влияние хлора на организм и личные меры
предосторожности
Хлор является веществом, отравляюще действующим па живой организм. По Леману содержание но вдыхаемом воздухе
0,0001% (по объему) хлора имеет раздражающее действие; содержание 0,001% хлора имеет значительное раздражающее действие и делает невозможной нормальную работу. Концентрация
хлора в 0,01% и выше опасна для жизни, работа без противогаза становится совершенно невозможной, ибо наступает быстрое отравление и при непрекращении вдыхания такого
воздуха наступает смерть от кровоизлияния в легких и
от удушья.
Древе21 дает Несколько иную градацию действия хлора на
человеческий организм. При содержании хлора в 0,0001—0,0005
вес. процента — отчетливое раздражение дыхательных органов,
при 0,0015—0,0030 вес. процента — воспаление дыхательных
органов и легочной ткани, при 0,004—0,006 вес. процента через
3%—5 час. наступает отек легких, при содержании хлора в воздухе больше 0,006 вес: процента — быстрая смерть. Концентрация хлора в воздухе в миллионных долях процента безвредна
для организма и даже полезна при некоторых болезнях. При длительной работе с хлором большинство людей привыкает к хлору
и может переносить концентрацию хлора в несколько раз большую, чем не привыкшие, вплоть до 0,001%. Хлор действует
отравляюще также на животных, рыб и т. д. и на растения. При
нормальном режиме работы и исправном состоянии оборудования в атмосфере рабочих помещений хлоратных заводов не бы-’
вает даже следов хлора и не требуется ни работа в противогазах, ни сокращенный рабочий день, спецпитание и т. д. При
таких условиях появление хлора в атмосфере бывает редко —
только в аварийных случаях. При неисправности, изношенности,
плохом монтаже, плохом ремонте оборудования или неправильности в режиме работы наличие хлора в помещении становится
частым явлением, вызывая частую или даже постоянную надобность в противогазах и т. д. На случай аварщ^ в помещениях
хлорирования, улавливания хлора из абгаза и обезвреживания
должны соблюдаться следующие правила.
1. Эти помещения как подверженные возможности заражения
атмосферы хлоргазом должны быть отделены брандмауэрными
„ стенами от помещений, в которых выполняются другие стадии
’производства.
2. Весь пёрсонал этих стадий производства должен уметь
пользоваться противогазами и быть проверенным на способность длительной работы в противогазах в атмосфере хлоргаза.
326 / >'
3. Весь персонал этих стадий производства должен быть
снабжен индивидуальными противогазами. Сумки с последними
должны быть всегда надетыми на работающих или храниться на
видных и легко доступных местах, непосредственно у мест
работы.
4. Противогазы должны периодически проверяться на
исправность.
5. При отравлении хлором необходимо сейчас же обратиться
в пункт первой помощи. Основными лечебными мероприятиями
являются: покой на свежем воздухе, вдыхание кислорода, паров
спирта или паров смеси спирта и раствора NHs, прием эфирновалериановых капель и т. д.
§ 2. Влияние содержания хлора в атмосфере производственных
помещений на ход производства
Кроме вреда для здоровья работающего персонала содержание хлора в атмосфере производственных помещений
приносит также огромный вред производству, вызывая резкое
падение производительности труда работающих в противогазах.
Кроме количественной стороны тут имеет еще большое значение
качественная сторона этого момента — ухудшается наблюдение
за оборудованием и процессами и т. д. При частом содержании
хлора в атмосфере производственный режим обычно расстраивается полностью, увеличиваются потери, ускоряется износ оборудования и вообще производство приходит в упадок. При
этом портится оборудование, и не имеющее прямого отношения
к процессам хлорирования и т. п., особенно электрооборудование, коммуникация и т. д. Поэтому при появлении в помещении
хотя бы малейшего запаха хлора основное внимание должно
быть обращено не на продолжение работы, хотя бы в противогазах, а на нахождение источника пропуска хлора (раствором
аммиака и т. п.) и устранение его в возможно более короткий
срок. Если для этого необходима остановка хлорирования, то
лучше таковую произвести сразу, а не* пытаться продолжать
работу в противогазах до случайной остановки производства по
какой;либо другой причине. Задержка ликвидации аварии приносит, возможно не оразу заметный, но в, общем гораздо больший вред, чем кратковременная остановка, а именно: указанную
Ныше порчу оборудования, расстройство режима работы1 и т. д.
$ 3. Наиболее 'частые причины содержания хлора в атмосфере
производственных помещений
Появление хлора в атмосфере производственных помещений,
.при хорошо смонтированном оборудовании и правильном режиме хлорирования случается только при авариях и т. п. Ниже
приводим замеченные в практике хлоратных производств: наиболее частые причины появления хлора, зависящие от неправильностей в режиме работы или от неисправности аппаратуры — при
' схеме хлорирования барботажем в башнях (см. стр. 80).
4 I . 327
а) Причины, зависящие от неправильностей
в режиме производства
1. При перебоях или недостаточном орошении абгазной колонки известковым молоком в период перехлорирования хлор
проскакивает через абгазную колонку в атмосферу. Такой абгаз
весьма сильно разъедает вентилятор, который в таких случаях
быстро выходит из строя. Кроме того хотя выпуск абгаза производится вне помещения, хлор частично все же попадает в рабочие помещения.
2. Если гидравлические затворы абгазного коллектора или
абгазной колонки не залиты водой, абгаз, содержащий хлор,
может попасть непосредственно в помещение.
3. Если в абгазной системе создается давление, то абгаз может выбросить воду из гидравлических затворов и попасть
в атмосферу помещений. Обычно давление получается от засорения абгазной колонки или абгазопроводов.
4., При открытии лнжа башни, не продутой воздухом и не
отсоединенной заглушками от хлоропррвода и абгазопровода,
хлоргаз выходит в атмосферу.
4 5. При создании тупика в хлоропроводе, если закрыть хлор¬
ный вентиль в прохлорированную башню, не открыв хлорный,
вентиль в башню со овежезалитым известковым молоком.
б) Причины, зависящие от неисправности
аппаратуры
1. Пропуск сальников хлорных вентилей.
2. Пропуск хлора через флянцевые соединения хлоропрово-
дов и абгазопроводов.
3. Пропуск хлора через пружинные манометры.
4. Местные разъедания хлоро- и абгазопроводов, вплоть до
образования в них отверстий.
5. Остановка работы вентиляторов для отсоса абгаза или
насоса, откачивающего абгазный щелок, при продолжении поступления хлора на хлорирование. ^
6. При смене хлорных вентилей или'частей хлоро- и абгазопроводов.
Примечание. Набивка сальников хлорных (вентилей должна производиться .при закрытом вентиле на пустой башне заблаговременно, т. е.
4 ранее начала пропуска хлора от износа сальника. n
Смену вентилей или частей хлоро- и абгазопровода надо производить
после предварительного переключения хлора © хлоропровод, идущий непосредственно к абгазной колонке, и отсоса остатка хлоргаза из башен и абгазного коллектора. »
§ 4. Опасность образования взрывчатых смесей в абгазе.
При содержании в хлоргазе водорода, в абгазе после хлорирования могут получиться соотношения между содержанием
Нг и О* или Н, и СЬ, вызывающие образование взрывчатой
смеси. Возможное?!?, образования взрывчатой газовой смеси
обусловливается наличием водорода в хлоргазе. Образованию
взрывчатой смеси благоприятствуют: i
'г . ;
328
1. Высокая концентрация CU н хлоргазе, содержащем Hi.
2. Выделение Ог при хлорировании.
3. Создание данленин к абгазпом пространстве ;п
4. Наличие п известковом молоке СаСОя, у,,
вспенивание, что повышает давление.
Практически при перечисленных условиях мы и.
частые взрывы как при хлорировании на абсорберах, ..
башнях (барботажем). При абсорберах обычно взрывы выв
только сры» свинцовых газопроводов между абсорберами. ./)/.
один раз (XII 1928 г.) мы наблюдали взрыв большей си.;
разрушивший керамиковую абгазную колонку, стоявшую за абсорберами. На башнях (при барботаже) взрывы большей частью
вызывали только выброс воды из гидравлического затвора
абгазного коллектора. Однако если нет гидравлического затвора
или он' забился, то взрыв может причинить и больший вред.
Описываем один такой взрыв значительной силы, случившийся
на опытной установке в 1932 г.
Хлорирование, производилось барботажем в башне. Абгаз
отводился под давлением в 0,1—0,15 ат в другую башню для
нового барботирования через известковое молоко с целью поглощения остаточного хлора. Из второй башни абгаз отсасывался вентилятором. Хлоргаз содержал СЬ~90% и Нг— 1%. На
башнях не было гидравлических затворов. Геометрический
объем башен был яо 9 **. Известкового молока заливали по
3 я* с концентрацией СаО ~ 240 г/л. В момент перехлориров' - •
сопровождавшегося сильным вспениванием, произошел ы; !лв.
сорвавший с первой башни чугунную крышку весом ~ 1 г и
приподнявший ее на высоту —2 л. Из башни было выброшено
около % всей жидкости, которая в ней содержалась. Силой
удара газов и жидкости была сорвана часть крыши здания площадью в, 20—25 л2. Корпус башни не пострадал. Оставшийся
щелок показал выход хлората в 35%, т. е. разложилось 65%.
Для 3 л* известкового молока с СаО в 240 г/л это соответствует-
~ 41 л3 кислорода.
При всех случаях взрывов как на абсорберах, так и на башнях, если сила взрыва даже небольшая и взрываются только
газопровод или выбрасывается гидравлический затвор, происходит потеря хлоргаза в атмосферу и т. д. Средствами борьбы, со
взрывами являются:
1) мероприятия (в производстве хлора) д^я получения хлоргаза, содержащего минимум водорода;
' 2)‘ разбавление воздухом хлоргаза, содержащего Нг больше
0,2—0,3%;
3) снижение количества Ог, выделяющегося при хлорировании, путем соблюдения температурного режима и т., д.;
4) недопущение создания давления в абгазной системе.
§ 5. Пожаро- и взрывоопасность бертолетовой соли и ее растворов:
В основном* бертолетова. соль является опасной в отношении
пожаров и взрывов только в сухом виде и в смеси с окнеляю-
■ ' v 329
1ЦИМИСЯ веществами. Однако от сильного удара или толчка
может взорваться и чистая бсртолстовая соль •'и и 3\ Раст поры
бертолетовой соли опасны только в том отношении, что, попадая на оборудование, части 'здания и т. д. и испаряясь, оставляют слой твердой бертолетовой соли. Особенно опасно обливание растворами КСЮз предметов, впитывающих эти растворы
(деревянные предметы, ткани и т. д.).
По степени опасности в отношении взрывов и пожаров отдельные стадии производства бертолетовой соли могут быть
расположены в следующей последовательности:
1. Размол сухой бертолетовой соли. Бертолетова соль подвергается ударам при одновременном разогревании. Наличие
примесей металлических частиц, органических веществ и т. п.
почти неизбежно вызывает взрыв.
2. Сушка бертолетовой соли. Если лопасти мешалки аппарата
для перемешивания задевают стенки аппарата, то при наличии
указанных выше примесей может произойти взрыв.
3. Перекристаллизация бертолетовой соли. Разваренный бер-
толетовый щелок содержит КСЮз ~ 350 т/л. Попадая на оборудование и здание, этот щелок уже по охлаждении оставляет
значительный слой твердой бертолетовой соли.
4. Центрофугирование. Если бертолетова соль попадает на
приводные ремни, подшипники и т. п., то возможны взрыв или
пожар от трения.
5. Бертолетовые щелока. Содержат КСЮз до 140—150 г/л,
т. е. в 2—2,5 раза меньше, чем разваренный щелок (п. 3). Кроме
-Того эти щелока содержат СаСЬ в 2,7—2,9 раза больше, чем
КСЮз (380—400 г/л). Поэтому при обливании ими оборудования
или здания они опасны, но менее, чем например разваренные
щелока (п. 3).
6. Хлорированные щелока. Содержат вместо КСЮз хлорат
кальция Са(СЮз)* — весьма гигроскопичный. Одновременно
в этих щелоках содержится СаСЬ в 2,7—2,8 раза больше хлората.
Поэтому нет опасности получения твердого хлората от высыха-
,ния или испарения на облитых щелоком предметах, и стадии
работы с этими щелоками гораздо менее опасны в отношении,
взрывов и пожаров.
7. Отдельно стоит вопрос о взрывах и пожарах, которые
могут возникнуть — при ремонте оборудования, пропитанного
или 'покрытого слоем бертолетовой соли, в любых стадиях производства — от ударов молотка, рубки зубилом, применения
газовой или электросварки и т. п.
I \
§ 6. /Описание некоторых аварий в производстве бертолетовой
соли
1. Скопившиеся под центрофугой частицы бертолетовой соли
и масла вспыхнули от искры, образовавшейся при задевании
за кронштейн осевшего шкива на валу центрофуги. Загорелись
:ремни и деревянная площадка центрофуги. Подсар быллокали-
330
зонам применением нескольких огнетушителей и струей .-‘.оды m
пожарного рукава.
2. Попавшая в подшипник сушилки Пассбурга бертолетова
соль, смешавшись со смазочным маслом, взорвалась от сотрясения сушилки, которое произошло благодаря задеванию лопастей вала за стенки аппарата. Причиной такого задевания была
недоброкачественная сборка аппарата.
3. От попадания бертолетовой соли и трения вала воспламенились фибровые кольца, одно время применявшиеся для лабиринтового уплотнения между подшипниками вала и крышкой
сушилки. Вспышка была локализована огнетушителем через
лючок в крышке сушилки, который случайно был в это время
открыт, поскольку вспышка произошла в период выгрузки солй
из сушилки.
4. Рабочий отделения кристаллизации вышел из завода
в спецодежде — хлопчатобумажном пиджаке. От случайно закуренной папиросы искра попала на пиджак, который моментально вспыхнул; рабочий получил тяжелые ожоги.
5. От удара молотком о гвоздь получилась искра, попавшая
на рабочего из отделения сушки бертолетовой соли. Одежда
рабочего, которая очевидно была пропитана бертолетовой
пылью, вспыхнула. Рабочий получил такие ожоги, что скончался
;через несколько часов.
6. При заварке трещины в кристаллизаторе Цана отскочившая искра попала на деревянную площадку, которая находится
над кристаллизаторами. Хотя площадка перед этим была вымыта водой, она вспыхнула и загорелась. Имевшиеся в помещении огнетушители оказались негодными, и огонь быстро
распространился, охватив деревянную крышу здания. Очевидно
крыша и особенно, площадка были пропитаны бертолетовой
солью, почему мытье поверхности площадки не предохранило ее от вспышки. Пожар был потушен лишь после больших усилий работников производства и прибывшей пожарной
команды.
7. От удара топором вспыхнула разбираемая деревянная площадка над обменниками. Очевидно, площадка была также пропитана бертолетовой солью. Огонь был потушен огнетушителем
и водой пожарного рукава.'
8. При ремонте помещения выпарки деревянная балка, сброшенная со 2-го этажа, от удара об землю вспыхнула. Очевидно
балка была пропитана бертолетовым щелоком, который высох
и дал отложения KClOj.
^ 9. Деревянная вагонетка, наполненная- сырой бертолетовой
солью, получила толчок об стену здания, отчего получилось вос-
пламенение стенок вагонетки. Пламя было потушено струей воды
из пожарного рукава.. Соль, содержавшаяся в вагонетке, не взорвалась. Очевидно загорание произошло из-за КСЮ$, пропитав-
лпего деревянные стенки вагонетки.
. 10. Самый‘крупный взрыв, описанный в литературе произошел 14/V 1899 г. на хлоратной фабрике в Сен-Элен (Англия).
331
Точные причины взрыва остались неизвестными, так как весь
персонал фабрики погиб при взрыве. Взрыв произошел в 10 час.
утра, уже после нескольких часов работы завода. Сила взрыва
была настолько большая, что им был разрушен близлежащий
завод серной кислоты и через минуту после взрыва.на территории заводов потекли 800 т серной кислоты. Взрыв был слышен на 20 миль в окрестности. На 1600//и в окрестности сор-,
вало крыши, выбило стекла и т. д.
Необходимо отметить, что помещение и большая часть баков
производства были деревянные и что при работе с открытым
огнем на заводе не применяли особых предосторожностей. Силу
и последствия взрква особенно увеличило совершенно недопустимое хранение в производственных помещениях большого запаса готовой бертолетовой* соли (больше 50 т)
§ 7. Меры предосторожности против взрывов и пожаров
1. В помещениях сушки, размола, кристаллизации, перекристаллизации и склада готовой соли совершенно не должно быть
деревянных 'предметов или частей оборудования (включая двери,
окна, крышу). Пол в помещении сушки и размола должен быть
из материала, не дающего искр при ударе.
2. Оборудование и внутренние стены здания этих помещений
должны быть покрыты антикоррозийным огнеупорным лаком,
чтобы не могло .произойти загорание и коррозия их, вследствие
которой было бы возможно попадание в бфтолетову соль продуктов коррозии.
3. В рабочих помещениях этих стадий должна соблюдаться
особая чистота. Не должны быть допущены течи и расплескивание растворов, .рассыпка или распыление твердой бертолетовой
соли и т. д. Стены, пол и потолок помещений должны не реже
одного раза в смену смываться или вытираться влажной тряпкой.
4. Должна быть обеспечена невозможность попадания посторонних предметов в твердую бертолетову соль (как сырую, так
и сухую); должны применяться крытые вагонетки, сита над
приемными бункерами, общие меры по чистоте и т. д.
5. Совершенно запрещается' применение открытого огня и
хранение огнеопасных и взрывоопасных предметов. Запасы твердой бертолетовой соли должны храниться в особом складе,
далеко отстоящем от территории производства.
6. Световое и силовое электрооборудование должно быть
герметичным и предусматривать наличие повышенной влажности
в окружающей атмосфере. /
7. Работа должна производиться исключительно в спецодежде, которая должна быть выстирана и высушена по окончании работы каждой смены. Обувь не должна иметь железных
гвоздей. Выход из завода в спецодежде должен быть категорически запрещен.
8. Центрофуги для отжатия бертолетовой соли j»t щелоков
• iChem. Ind. 1899 г., стр. 443 -444 и Zeit. angew, Cheiq. 1899 г., стр. 537;
Блинов, Ж, Х.П. 1937,.№ 2, сгр. 119.
332 ' 4 /
должны быть на одном палу с моторами, чтобы избежать применения приводных ремней. В случае необходимости ь таковых
(особенно при большой скорости движения) надо применять
резиновые ремни, а не кожаные, так как последние вызывают
образование электрических разрядов с искровыделением. Для
отжатия соли от щелоков лучше применять нутч-фильтры.
9. Матерчатые рубашки центрофуг должны быть подрублены
-так, чтобы нитки их не могли попасть в бертолетову соль.
10. Подшипники центрофуг, насосов и т. д., в которые возможно попадание бертолетовой соли или бертолетовых щелоков, должны быть закрытые, чтобы ни бертолетова соль не
могла попасть в подшипники, ни масло из подшипников не могло
попасть в бертолетову соль.
11. При ремонте оборудования предварительно должны быть
тщательно смыты все следы бертолетовой соли или щелоков.
12. Все помещения должны быть полностью обеспечены
огнетушителями, пожарными кранами и т. п. противопожарным
оборудованием. Персонал этих стадий производства должен
уметь обращаться с противопожарным оборудованием, чтобы
в случае пожара суметь быстро локализовать его, не дав огню
распространился. Сохранность и годность противопожарного
оборудования должны как можно чаще проверяться.
13. В помещении сушки и размола целесообразно ставить
открытые ванны с водой, чтобы в случае загорания одежды
можно было сразу окунуться в воду. Кроме того в каждом помещении должен быть водяной душ.
14. 'Должно быть\ запрещено ношение бороды, усов и длинных волос. Женский персонал должен завязывать головы косынками.
15. Обслуживающие помещения должны быть расположены
таким образом, чтобы никто ' не мог , уйти с завода, не сняв
рабочей одежды. 1
N
ГЛАВА 24
ОСНОВНЫЕ ПОТРЕБИТЕЛИ ХЛОРАТОВ
§ 1. Применение бертолетовой соли в производстве спичек
Производство спичек является в данное время наиболее круп-
дым потребителем бертолетовой соли как в СССР, так и в других странах. Общее количество мирового расхода бертолетовой
соли на производство спичек равно не менее 20—25 тыс. т в год.
СССР является одним из крупнейших в мире потребителей спичек, поскольку спички являются предметом широчайшего обихода. Вся потребность СССР в спичках покрывается за счет собственного производства и кроме того значительное количество
спичек экспортируется.
В настоящее время применяются почти исключительно безопасные «шведские» спички, основными химическими реагентами
333
которых являются бертолетова соль и красный фосфор. Реже
применяются вместо бертолетовой соли другие хлораты (хлорач
бария и др.), а также иные виды спичек.
Литература
1. Ильокий и Хавин, Химическая технология производства спичек,
1931 г.
2. Халин, Производство спичек, 1932 г.
3. Штерн, Химия п спичечном производстве, 1933 г.
4. J. Kellner, Handbuch der Ziindwahren Fabrikatiom
5. William, Hepwortz, Dixon, The Math. Industry, 1925.
^ 6, Ульман *-1■*.
§ 2. Применение хлоратов для приготовления взрывчатых веществ, воспламенительных составов, фейерверков и т. д.
Производства этих веществ являются и в мирное время
весьма крупными потребителями бертолетовой соли и хлората
натрия и самыми крупными потребителями хлората бария.
В военное время потребление хлоратов для этих целей особенно
возрастает (в годы 1914—1918 потребление хлоратов в основных воюющих странах доходило до 100 тысяч тонн в год). Применение хлоратов для этик целей основано на < их быстром
разложении с отдачей кислорода. Однако это же является и причиной недостаточной устойчивости хлоратов против тепла и
удара, что ограничивает их применение. Наибольшее применение
имеют КСЮз и 1ЧаСЮз. В значительном количестве применяется
еще хлорат бария и реже хлорат стронция. В сравнительно небольших количествах применяются для воспламенительных составов
еще органические производные хлорноватой кислоты. Значительные количества КСЮз и -NaClOs расходуются на получение
перхлоратов К’, Na‘ и NtU', имеющих применение для взрывчатых веществ. - . .
1. Хлоратные взрывчатые вещества. Смеси хлоратов с серой,
углем, сахаром и т. п., отчасти применявшиеся в XIX столетии
как «хлоратные пороха», в данное время отставлены ввиду их
малой стабильности. В данное время обычно применяются зернистые смеси хлоратов с пластическими массами и другими обволакивающими веществами. Значительное распространение имеют
смеси «шеддиты». Содержание хлората (КСЮз и NaClOs) в шед-
дитах равно 75—90% и лишь 10—15% составляют другие вещества. В качестве последних применяются динитротолуол, нитронафталин, пикриновая кислота, нитроглицерин, нитробензол,
древесные опилки, касторовое масло, терпентин, канифоль и т. д.
Иногда применяются патроны, содержащие только хлорат и
обмакиваемые непосредственно перед применением в керосин.
Шеддиты выпускаются в виде зерен, запрессованных в патроны,
а также в гранатах, как минный порох и т. д. Особенно широко
применяются «шеддиты» в виде патронов для горных работ.
2.. Ударные срставы. Большая часть ударных составов представляет собой смеси 85—90% гремучей ртути и 10—15% бертолетовой'солис небольшим (количеством гуммиарабика (1—2%).
/ .: :
J
334
Реже прибавляются еще небольшие количества KNCh, тринитротолуола и др. Основная роль КОСЬ — это облегчение воспламенения, но она также служит связующим веществом.
3. Воспламенительные составы. Большая часть таких составов
содержит -в основном гремучую ртуть, сурьму, бертолетову соль
и небольшое количество шеллака, желатины, молотого стекла
и т. п., но имеются составы и не содержащие гремучей ртути.
Твердый остаток составов, содержащих КСЮз, корродирует дула
орудий. Поэтому предложены составы, где бертолетова соль заменена перекисью бария или свинца и т. п. веществами. Однако
такие составы мало распространены.
4. -Составы для запалов. Для электрозапалов применяются
составы, содержащие сравнительно небольшое количество бертолетовой соли. Основной массой для таких составов служат пироксилин или сернистая медь и в меньших количествах гремучая ртуть, сурьма, порошки меди, алюминия, магния и т. д. Эти
составы применяются непрессованными, обернутыми бумажными
оболочками или обволакивающими веществами. Вариации рецептуры зависят от рода принятой передачи тепла: накалом платиновой проволочки, искрового промежутка и т. д.
5. Составы для пистонов, гремучих пробок, фитилей и т. д.
Эти составы обычно содержат те же вещества, что и вышеописанные. Весьма распространено применение состава из красно/ о
фосфора, и хлората.
6. Фейерверочные составы. Эти составы имеют широкое применение для военных осветительных и иных сигналов, для петард
и сигналов на железных дорогах, для увеселительных ракет
и т. д. Основной массой таких составов являются хлораты К, Na
и Ва, нитраты Na, К, Ва, Са, Sr и сера. В меньших количествах
применяются мел, каломель, сурьмянистые соединения, пороховая мякоть,- соединения меди, уголь (сажа), опилки, порошки
металлов и т. д. Цвет горения зависит от металла солей смеси:
Ва дает зеленый цвет, Sr — красный, Са — оранжевый, Na -i-
желтый. Голубой цвет получается от примеси медноаммонийной
соли; искры получаются от примеси угля или опилок металла.
' !
Литература
1. Esc ales, Chloratsprengstoffe Лейпциг, \1910.
{ 2. Corbin, Conference sur les Exposifs chlorates et perchlorates,.
П&риж, 1916.
3. Ульман e—5.
4. Г. Каст35.
б. Г. Каст и Л. Метци.
6. Спутник практика — техноэкономические рецепты. Инж. Е. С.
и С. С. Г у ре вич, под ред. лроф. Вальгиса, 1930 г., стр. 982—1032.
7. Блинов, «Килий» 1937 г. JSfe 10, стр. 19—30.
§ 3. Применение хлоратов в качестве гербесидов
Гербесидами называют химические вещества, которые применяются как средства борьбы с сорняками. Применение гербесидов имеет перед ручной полкой следующие преимущества: ма«
■ /
335>
лую трату рабочей силы, большую продолжительность действия,
меньшую стоимость. Последнее верно только при не слишком
высоких ценах на гербесиды. В западной Европе и в Америке
гербесиды нашли широкое применение. Больше всего применение гербесидов привилось для борьбы с сорняками на жел.
дор. пблотне. В земледелии применение гербесидов выгодно
только при более дорогих культурах (сады, хлопковые поля
и г. д.) и на сильно засоренных участках (например на куртинах).
Также применяют гербесиды для очистки от сорняков игЛюдро-
•мов, спортплощадок и т. д. Чем больше засоренность участка,
тем больше эффективность применения гербесидов перед ручной полкой.
По характеру действия на растения гербесиды можно разделить на тип наружного действия и тип внутреннего действия.
Первые (серная кислота, щелочи и т. д.) убивают только надземные части сорняков, не влияя на корни' и прочие подземные
части, вторые (хлораты, мышьяковистые соединения и т. д.) убивают и надземные и подземные части сорняков. Хлбраты принадлежат к гербесидам внутреннего действия и являются самыми
распространенными из таковых. Действие хлоратов основано на
■влиянии иона СЮ'з, почему могут быть применены все хлораты
и выбор зависит только от цены и удобства употребления. В данное время наибольшее применение имеют хлорат натрия и хлорат кальция в виде смесей с соответствующими хлоридами. Последнее выгодно, поскольку получение такой смеси технически
проще и дешевле, чем получение чистых продуктов, и кроме
того хранение и работа со смесями безопаснее в отношении по-
.жаров и взрывов. Наличие в применяемом гербесиде кроме хлората еще хлористого кальция Делает гербесид эффективнее, поскольку благодаря своей гигроскопичности о« образует в почве
гербесидный раствор. Применение чистой NaClOs увеличивает
потери от распыления его ветром и т. д.
Хлораты действуют на сорняки как протоплазматический яд.
Действие это развивается постепенно. Обычно через 1—2 суток
йадземные части сорняков желтеют, через 3—4 суток они буреют и наконец через 6—12 суток отмирают.
То же происходит с подземными частями сорняков. Быстрота
. действия хлоратов зависит от влажности почвы. Дожди весьма
ускоряют действие хлоратов.
Хлораты не абсорбируются почвой. Обычно через 4—8 мес.
после применения хлоратов анализом уже не обнаруживается
содержание ОО'з в почве. Поэтому в земледелии лучше всего
применение хлоратов как гербесидов производить осенью с тем,
чтобы весной производить посев культуры (после отрицательного анализа почвы на СЮ'з). Дожди благоприятствуют скорей-
• шему вымыванию хлоратов из почвы. На жел.-дор. путях лучше
всего применять хлораты весной перед максимумом дождей (но
после достаточного роста сорняков).
Обычно применяют обрызгивание 10—15%-ным раствором
хлората, Расход хлората варьирует в зависимости от степени
/ . '
• &6 / •»
1
засоренности участка в пределах 100—600 кг на га (10—GO г на
1 м2). На 1 км жел.-дор. пути расходуют 80—120 кг хлората.
Можно также применять опыливание сорняков порошком хлората. Опыливание даже экономичнее, чем обрызгивание раствором гербесида, так как дает меньший расход продукта. Наилучшим для опыливания является хорошо высушенный порошок
сильно гигроскопической смеси.
/ На применение хлоратов в качестве гербесидов имеется много
патентов, перечень некоторых из них приводим.
Французские патенты: 547599, 566459, 573527, 631734, 644166,
659957, 660245 (1922—1928 гг.).
Германские патенты: 460546, 549645, 553617, 558951 (1927—
1932 гг.).
4 Американские патенты: 1854405, 1887405, 1887809, 1893740
<1930—1932 гг.).
Швейцарский патент: 129209 (1928 г.).
В большинстве' этих патёнтов приводятся смеси Са(С10а)г
с СаСЬ или NaClOj с СаСЬ (в количествах, близких к эквивалентным). Реже приводятся смеси хлоратов с NaCl, Na*COa,
KiCOs, K*Crg07, тальком, песком и т. д.
Примечание. По вопросам применения хлоратов в качестве гербе-
ендов ®- последние годы опубликован ряд , статей в сборниках ВИЗР
(Всесоюзный Ин-т Защиты Растений), журналах «Железнодорожный' путь»,
«Железнодорожное дело», «Плодоовощное хозяйство» и Ж.Х.П.
ГЛАВА 25
НЕКОТОРЫЕ ДАННЫЕ ПО РЕЖИМУ РАБОТЫ ОСНОВНЫХ
СТАДИЙ ПРОИЗВОДСТВА ч
§ 1. Хлорирование на абсорберной установке
Предполагаем, что хлорирование ведется на установке, описанной на Стр. 77 (рис. 36 и 37), и что хлорируется известковое
.молоко слабой концентрации, так что не требуется искусственного охлаждения во время хлорирования.
1. Поступающее на хлорирование известковое молоко должно
содержать СаО 100—110 г/л. Большая концентрация СаО вызывает превышение оптимальной температуры конца хлорирования
(см. п. 6), отчего увеличиваются химические потери (выделение Ог) и получается большой осадок в готовом щелоке. Более
низкая концентрация невыгодна, так как увеличивается количество воды, которую необходимо выпарить ^из хлорированных
щелоков. ^
2. Молоко, -поступающее на хлорирование, должно иметь температуру ~ 20°. Более высокая температура вызывает превышение- оптимума температуры конца хлорирования (см. ниже п. 6).
Более низкая температура молока, увеличивая его- вязкость,
ухудшает -перем^щивание в 1-м1 абсорбере, отчего уменьшается
.абсорбция хлора..
22 ,3*к. 179. ШрвДбман.
/
337
3. Питание абсорбсрной установки известковым молоком
должно производиться непрерывно и равномерной струей, соответствующей полному поглощению хлора из поступающего
хлоргаза. Слишком большая струя молока вызывает получение
недохлорированных щелоков. Слишком малая струя молока вызывает появление хлора в абгазе. Совершенно недопустимы
остановки поступления молока или хлоргаза, и если останавливается одно, надо тотчас же остановить и другое. Такие перебои всегда вызывают расстройство хрежима работы, отчего некоторое время получаются недохлорированные щелока и т. д.
4. Щелок, выходящий из 4-го абсорбера, должен быть псрс-
хлорирован: пахнуть хлором, быть ярко розовым и содержать
лишь небольшой, быстро оседающий нерастворимый остаток.
Получение недохлорированных щелоков весьма затрудняет дальнейшую работу производства.
5. Абгаз после 1-го абсорбера не должен содержать хлора
или во всяком случае содержание хлора в нем не должно
превышать десятых долей процента. Абгаз, содержащий хлор,
должен обязательно пропускаться через абг.азную установку, так
как ОН (к тому же насыщенный влагой и имеющий повышенную
температуру) очень сильно разъедает вентиляцию и абгазопро-
воды, отравляет атмосферу и кроме того вызывает потерю хлора.
- 6. Температура щелоков должна равномерно повышаться походу молока (табл. 20) с тем, чтобы в 4-м абсорбере не превышать 80—85°. Большая-температура увеличивает химические потери при хлорировании (выделение Ог), а также вызывает технологические затруднения (вспенивание и т. д.). Большая температура во 2-м и 3-м абсорберах вызывает местные перегревы,
что тоже увеличивает химические потери. Для замера температуры должны быть вставлены термометры во все переходные
щелокопроводы между абсорберами и до 1-го и после 4-го абсорбера.
7. В газопроводах до и после всех абсорберов должно быть-
разрежение, все увеличивающееся по ходу хлоргаза. Для измерения разрежения во всех переходных газопроводах между
абсорберами, а также в хлоропроводе и абгазопроводе должны
быть установлены манометры. Появление давления в газопроводах доказывает, что где-либо произошло засорение линии
и т. д., что необходимо немедленно устранять во избежание
расстройства режима хлорирования и появления хлора в атмосфере.
8. Регулирование хлорирования для получения из 4-го абсорбера лёрехлорированного щелока и выхода, из 1-го абсорбера
\абгаза, не содержащего хлора, производится регулированием
струи молока, поступающего в 1-й абсорбер. При превышении
концентрации СаО в молоке 110 г/л необходимо производить,
охлаждение щелока в 2-м и 3-м абсорберах проточной водой по
кожухам абсорберов и т. п.
1 Нумерация абсорберов ведется по. ходу молока.:
338
§ 2. Хлорирование барботажем в башнях
Предполагаем, что хлорирование производится в установке,
описанной на стр. 81 (рис. 38), причем хлорируется известковое
молоко слабой концентрации, для того чтобы во время хлорирования не Применять искусственного охлаждения. Хлоргаз должен поступать (после сушки в башнях, орошаемых серной
кислотой) под давлением в 0,4—0,5 ат.
1. Известковое молоко, заливаемое в башни, должно быть
тщательно перемешано и содержать СаО 100—ПО г/л. Большая концентрация СаО (при отсутствии искусственного охлаждения) вызывает увеличение химических потерь, увеличение
количества осадка в готовом щелоке и т. д.
2. Температура молока до начала хлорирования должна быть
не выше 25° и не ниже 20°,. Если в башню заливается молоко,
частично прохлорированное на абгазной установке, то температура должНа быть ниже 80° примерно на 0,6° на 1 г непрохлори-
рованного СаО в литре щелока.
3. ‘Молоко должно заполнять не больше 50% и не меньше
40% геометрического объема башни. Превышение 50% почти
всегда вызывает выбрасывание жидкости из башни к концу хлорирования, уменьшение заполнения ниже 40% невыгодно, ибо
уменьшается продолжительность операции, увеличивается стоимость обслуживания и т. д.
4. После начала заливки известкового молока в башню надо
немедленно пустить воздух в барботер, чтобы не было оседания
Са(ОН)г в башне. Пуск воздуха остановить только после пуска
хлора.
5. Хлорирование одной операции надо вести без перерывов
в пуске хлора. Перерывы приводят обычно к ухудшению хлорирования, возможному выделению оксихлоридов и т. д.
6. Конец хлорирования узнают по прекращению подъема
температуры щелока (термометр устанавливают к патроне, имеющемся в крышке люка башни), а также по пробе щелока, взятой
из пробного краника (розовый цвет, запах хлора), и по началу
подъема температуры щелока на абгазной установке.
7. При перехлорировании, продолжительность которого
должна быть 3—5 мин., должны быть открыты хлорные вентили как в башню с перехлорируемым щелоком, так и в башню
со свежим молоком. Это уменьшает количество хлора, попадающего в абгазную установку. ,
8. После 3—5 мин. перехлорирования щелока закрывается
хлорный вентиль и открывается воздушный вентиль для продувки щелока.
9. При продувке щелока возможность поступления в башню
хлора или известкового молока должна быть исключена. Иначе
■ продувка бесполезна, ибо от известкового молока щелок станет
щелочным, т. е. -растворенный хлор перейдет в Са(СЮ)*, который
не выдувается, а от поступления хлора щелок убудет получать
все время вместо, выдуваемого хлора новое количество его.
>^22*
I
339
10. При отсутствии доступа хлора и молока и достаточной
струе воздуха уже через 10—15 мин. продувки в щелоке должно
содержаться СЮ' не больше 0,01—0,015 экв/л, а в выдуваемых
из башни газах должны содержаться только следы хлора.
Только после этого прекращают продувку.
11. По окончании продувки щелок необходимо сразу выкачать из башни. Излишнее задерживание перехлорированного щелока в башне увеличивает коррозию башни и особенно ее металлических частей.
12. Во время хлорирования в башне должно всегда быть разрежение — примерно в 5—10 яш вод. ст. Это создается работой
вентилятора после абгазной установки. Наличие давления
в башне доказывает засорение абгазного коллектора и т. п. и
должно быть немедленно ликвидировано.
13. Гидравлический затвор абгазного коллектора должен
быть всегда залит водой. ,
14. Если анализ хлоргаза показывает содержание водорода
больше десятых долей процента, то при концентрации СЬ выше
70—80% его надо разбавить путем пуска в башню одновременно
с хлоргазом и воздуха (во избежание возможности создания
.взрывчатой газовой смеси — см. стр. 328). ч
§ 3. Улавливание хлора из. абгаза
■ Нижеприводимые правила даны для работы колонки, описанной на стр. 86 (рис. 42) при ведении основного хлорирования
барботажем в башнях (см. выше § 2).
1. Известковое молоко должно поступать на колонку непрерывно и равномерно в количестве, достаточном для поглощения
всего хлора, поступающего на хлорирование. В 'противном случае во время перехлорирования хлор может проскочить в абгаз
после колонки.
2. Поступающее на колонку молоко должно содержать СаО
100—110 г/л-и иметь температуру в пределах 20—30°.
3. Абгазный щелок, вытекающий из колонки в приемный бак,
должен непрерывно откачиваться для основного хлорирования.
4. В периоды перехлорирования хлоргаз должен поступать
в Две башни: в одну с перехлорируемым щелоком и в другую со
свежим известковым молоком, в противном случае температура
в абгазной колонке слишком высоко поднимется (что увеличивает химические потери), и кроме того хлор может проскочить
в абгаз, уходящий из колонки.
5. Температура выходящего из колонки абгазного щелока не
должна превышать 50?, а в абгазах после колонки не должно
чбыть и следов хлора, в противном случае надо немедленно увеличить струю поступающего на колонку известкового молока.
6. Один раз в смену, в один, из периодов начала хлорирования башни со свежим известковым молоком, колонку промывают сильной струей воды.
7. Если колонка оставляется неработающей (резервная и т. п.),
ее надо промыть* известковым молоком/ (для защиты от коррозии).
8. В напорный и приемный бакй колонки должен все время
поступать воздух для непрерывного перемешивания молока.
§ 4. Перекристаллизация бертолетовой соли
Правила относятся к схеме перекристаллизации соли, описанной в главе 9.
1. При перекристаллизации, имеющей основною целью очистку бертолетовой соли от примесей, в помещении и во всей
аппаратуре особо тщательно должна соблюдаться чистота.
2. Надо строго следить за правильным и последовательным
применением промывных вод и маточников, иначе получится
либо недостаточный оборот и использование их (больше потерь),
либо ухудшится качество бертолетовой соли (много СаСЬ).
Жидкость для разварки при правильном обороте не должна содержать СаСЬ выше 5—10 г/л. \
3. Кроме промывных вод и маточников -для приготовления
разваренного щелока можно применять только конденсат. Применение сырой воды вносит в щелока примеси, Обычно содержащиеся в сырой воде (сульфаты и т. д.).
4. Разваренные щелока должны иметь удельный вес 1,17—1,18
(21—22° Боме) при температуре в 95—100°, что отвечает содержанию KClOs в 330—360 г/л. Ббльший уд. вес или более низкая
температура угрожают началом кристаллизации при отстое, перекачках и в напорной коробке.
5. На кристаллизацию надо пускать разваренный щелок, хорошо отстоявшийся от нерастворенных примесей. Слишком длительный отстой вреден — возможно выделение кристаллов от
охлаждения щелока. v
6. При центрофугировании надо как можно лучше отжать
соль. При нормальной ( работе jb отжатой бертолетовой соли
должно быть не больше 4—5% влаги. Чем больше влаги в бертолетовой соли, тем больше в ней водорастворимых примесей — хлоридов и других.
§ 5. Сушка бертолетовой соли
, Правила даны для схемы сушки, описанной на стр. 137, и
аппарата для суФки, показанного на рис. 65.
1. Бертолетова соль, загружаемая в сушильный аппарат, ни
в коем случае не должна содержать механических примесей
в виде кусочков железа или дерева и т. п., так как от удара* или
трения таких кусочков о сухую бертолетову соль может произойти взрыв.
2. Перед началом загрузки необходимо проверить полную
исправность сушилки. При вращении вала лопасти не должны
скрести по стенкам аппарата, подшипники должны быть смазаны, предохранительные карманы подшипников должны быть
промыты водой, приводные ремни должны быть вполне
исправны. Последнее очень важно, ибо даже временная остановка перемешивания соли (особенно в начале сушки) вызывает
прикипание соли к стенкам сушилки, и в таких случаях прихо-
' . ' ' , С ' 341
дится соль выгружать, чистить стенки, лопасти и вал аппарата,
а иногда и вынимать мешалку и промывать аппарат водой и т. д.
3. Загрузку соли надо производить после пуска мешалки,
благодаря чему загружаемая соль равномерно 'распределяется по
всей сушилке.
4. Нельзя загружать бертолетову соль (выше паспортного рабочего объема (обычно 50% геометрического объема) сушильного барабана.
5. По окончании загрузки бертолетовой соли в аппарат закрывают загрузочный люк, пускают вакуум-насос и затем пар.
Последовательность этих операций обязательна.
6. Во время сушки в аппарате должен поддерживаться максимально возможный вакуум — не меньше 650 мм рт. ст. Давление пара в рубашке аппарата должно равняться 1,5—2 ати.
7. Проба хорошо высушенной соли не должна приставать
к стеклу и должна легко сдуваться с ладони, не оставляя видимых следов. Если'условия сушки и состав соли более или менее
постоянны, то конец сушки определяют по часам, согласно установленным опытным данным.
Примечание. Конец сушки можно также узнать по 'Понижению температуры отходящих газов из сушилки «виду прекращения выделения паров
НЮ из сушймой соли. Для этого помещают термометр в патрон, вделанный в трубопровод, соединяющий сушильный аппарат и ловушку бертолетовой пыли перед вакуум-насосам.
Для отбора пробы соли останавливают вакуум-насос, открывают воздушный вентиль аппарата и снимают крышку загрузочного люка. Мешалку останавливать нельзя.
8. Продолжительность сушки завйсит от давления пара, степени вакуума, содержания влаги и СаСЬ в соли, величины кристаллов и т. д. В среднем продолжительность сушки равна
1,5—2 часам, включая время загрузки и выгрузки.
9. По окончании сушки останавливают пар и затем вакуум.
Работу мешалки останавливают только по окончании выгрузки
бертолетовой соли.
10. Температура бертолетовой соли в аппарате и температура
подшипников не должны превышать 50—60°. • Все время сушки
конденсат должен непрерывно выходить из паровой рубашки.
Также необходим периодический спуск воздуха из паровой рубашки. .
И. Сырая соль обычно содержит 4—7% влаги. Сухая соль
при нормальной работе аппарата должна показывать при последующем анализе сушкой до постоянного веса при 105° содер-
, жание влаги не выше 0,1%.
12. Не реже 1 раза в месяц надо (производить очистку вала,
лопастей и внутренних стенок аппарата от образовавшейся на
них корки бертолетовой соли. Последняя содержит по ’ анализу
около 99,9% КСЮз, но обычно имеет большую твердость.
Очистку производят промывкой горячей водой и механическим
соскабливанием. Корка от очистки аппарата используется в отделении перекристаллизации.
Приложение 1
ЗАМЕЧАНИЯ ПО КОРРОЗИИ АППАРАТУРЫ
Вопросы коррозии имеют в производстве бертолетовой соли весьма
•большое значение как в отношении износа аппаратуры, так и в отношении
загрязнения полупродуктов (щелоков) и готовой продукции. Последнее
особенно нежелательно ввиду возможного каталитического .воздействия
некоторых продуктов коррозии на бертолетову соль в отношении увеличения ее взрыво- и пожароопасности (см. табл. 6, стр. 24). Практически
75—80% стоимости ремонтов- в производстве бертолетовой соли вызывается
коррозией. Помимо увеличения затрат на ремонты, явления коррозии вызывают увеличение механических потерь (течь щелоков и т. п.)* простой
аппаратуры и вообще нарушение нормального хода (Процесса из-за простоев
ремонтируемых аппаратов и т. д. Особенно усугубляет важность вопросов
коррозии в производстве бертолетовой соли то, что наиболее распространенный материал для аппаратуры и трубопроводов — железо — является
весьма сильно подверженным коррозии. Например железные трубопрбводы
.для иерехлорированных щелоков практически приходится менять через
каждые 3—4 мес. г.
Наиболее опасными в отношении коррозии являются аппараты, где
имеется хлоргаз или щелока, содержащие растворенный хлор (башни, обез-
вреживателн), а затем аппараты, в которых имеются горячие хлорированные и бертолетовые щелока. Температура имеет весьма сильное влияние
на величину коррозии; аппараты, в которых обрабатываются холодные
щелока (например вымораживатели), мало корродируют*/ Меньше всех корродируют аппараты с жидкостями, содержащими Са(ОН)г.
Таким образом основные аппараты можно по степени увеличения коррозии расположить в следующем, порядке.
1) Аппараты Мика и Русселя и остальные аппараты с известковым
молоком; 2) .абгазная колонку -и остальные аппарат^ с абгазным щелоком;
3) -вымораживатели, декантеры, сборники промывных вод и др. аппараты
с холодными щелоками; 4) отстойники и выщелачиватели шлама от хлорированных щелоков, .питатели выпарных аппаратов и отстойники уваренных
щелоков, кристаллизаторы и др. аппараты, где температура' щелоков не
превышает 50—60°; 5) .выпарные аппараты-, растворители хлористого калия
и бертолетовой соли для перекристаллизации; 6) обезвреживатели; 7) башни
для хлорирования.
Устойчивыми .против всех щелоков и хлоргаза являются керамика,
диабаз, бакелиты и т. д. Мы наблюдали в течение пяти лет башни для
хлорирования и обезвреживатели, выложенные кислотоупорным кирпичом
и работавшие без сильного износа. Из металлов наиболее устойчивы
против горячих щелоков медь, нержавеющая сталь, а затем свинец. Для
большей чистоты готовой продукции обменники, декантерьг и растворители
хлористого калия и бертолетовой соли и отстойники растворов КС1 и
КСЮз целесообразно выложить изнутри свинцом.
В заключение приводим на рис. 127, 128 и 129 результаты некоторых
наших исследований по вопросам коррозии в производствах хлоратов.
Примечание. По вопросам коррозии в производстве хлоратов авто*
ром опубликованы работы в следующих журналах.
1. Химстрой № 4, 1930 <г., стр. 475—476. 7
2. Химстрой № И, 1932 г., стр. 1883—1889.
. 3. "Химстрой № 8, 1936 г., стр. 460—461.
4. Калий JVe 5, 1936 г* стр. 41. л J
5. КалийNt 2,, 1937-г., стр. 20-23.
• t . ’ X ' 1
у •' ■ ;. 343
р мд j*т»т*н**ь
Уменьшение Веса пластинок б */**
Раствор с добавкой
NaHC03
\
же^ныт В*И"ННе добаво" NaHCOj. NaaCOs и NaOH на коррозию-
железны* пластинок при 100“ в растворе, содержащем NaCl 252 г\лг
f >' NaClOg 41 г/л, KClOg 29 г/л и NagSOj 5,6 г/л (эа 9 суток).
осты
Приложение 2
СССР
ОБЩЕСОЮЗНЫЙ СТАНДАРТ
ост
7174
Народвый комиссариат
тяжелой промышленности
КАЛИЙ ХЛОРНОВАТОКИСЛЫЙ
(реактив)
НКТП
468
Комитет стандартизации
КСЮ3; форм. мол. вес 122,56*;
log—08835
Химпром
А. КЛАССИФИКАЦИЯ
\
По количеству содержащихся в препарате примесей различают «чистый
для анализа» и «чистый» препараты,
Б. ТЕХНИЧЕСКИЕ УСЛОВИЯ
а) Препарат «представляет собой бесцветные блестящие кристаллы, растворимые в воде.
б) Содержание KClOs должно быть не менее 99%.
в) Наибольшие количества допустимых примесей:
Допустимые примеси
1. Нерастворимые в воде вещества
12. Хлориды (С1')
■3. Сульфаты (SO/')
4. Броматы (ВгОа') . • •
5. Тяжелые металлы группы H2S . .
6. Железо (Fe) > . .
7. Кальций (Са)
8. Магний (Mg)
Мышьяк (As)
.Чистый
для анализа*
.Чистый*
'в °/о
0,005
0.01
0,002
0,005 *
0,005
0.01
0,005
0,01
0,001
0,002
0,0005
0,001
0,002
0,005
0,002
0,005
0,00005
0,0001
В. УПАКОВКА и МАРКИРОВКА
Препарат упаковывают в стеклянные банки с хорошо притертыми
стеклянными или хорошими корковыми пробками по 0,1; 0,25; 0,5; 1; 2 и
5 кг нетто. Корковые пробки снизу защищают пергаментной бумагой. Сверху
пробки покрывают .пергаментной бумагой или эластичной капсулой. Каждая
банка имеет этикетку с обозначением наименования треста и завода, названия препарата и его квалификации «чистый для анализа» или «чистый»,
а также количества препарата, номера серии, номера анализа, знака кон-
ОСТ 7174
тролера я __w.
* По атомным весам Американской комиссии 1933 г.
V •
347
I
Г. ПРАВИЛА ПРИЕМКИ
а) Отбор проб
1. Каждую банку всей партии, 'подлежащей сдаче, подвергают наруж-
ному^осмопру, после чего в зависимости от размера -партии отбирают по
усмотрению приемщика от 20 до 5% общего числа банок. Из каждой отобранной банки берут в чистую, сухую банку с притертой пробкой равные
или пропорциональные количества препарата общим весом не менее 0,5 Kt
и тщательно перемешивают.
2. Среднюю пробу разделяют на 3 части, которые помещают в три
стеклянные с хорошо притертыми пробками, чистые, сухие банки. Банки
опечатывают .печатями поставщика и потребителя. На каждой байке наклеивают этикетку с обозначением наименования завода, названия препарата,
номера серии, места и даты отбора пробы. Одну банку передают для анализа, другую потребителю, а третью хранят на складе поставщика в течение трех месяцев на случай арбитражного анализа.
Место отбора проб и «выбор лаборатории для арбитражного анализа
устанавливаются соглашением сторон.
* б) Методы испытаний
Определение содержания КСЮз
Точную навеску препарата (около 0,5 г) расторяют в мерной колбе на
100 мл и объем доводят водой до метки. 10 мл этого раствора вводят
в круглодонную колбу, предварительно наполненную GOa и содержащую
25 мл раствора закисного сернокислого железа.
Закрывают колбу резиновой пробкой, снабженной бунзеновским клапаном, кипятят раствор в течение 10 минут, охлаждают, к охлажденному раствору прибавляют 10 мл раствора сернокислого марганца и титруют
0,1 N раствором -перманганата до изменения окраски. Число, миллилитров
0,1 N раствора перманганата, затраченное на Нитрование, — а.
25 мл раствора закисного сернокислого железа титруют тем же 0,1 К
раствором перманганата. Число мл 0,1 N раствора перманганата, затраченное на титрование, — б.
Тогда (б — а) дает число мл 0,1 N раствора пермаганата, отвечающее
Сбдержанию действующего начала в препарате:
(б— а)» 10-0,0020426.100
где. в — навеска препарата.
1 1 мл 0,1 N раствора перманганата отвечает 0,0020426 г КСЮз; log—31019.
' Примечание 1. Для приготовления раствора закисного сернокислого железа берут 5 г FeS04*7H20, растворяют в 90 мл воды и прибавляют 10 мл „х. ч.* серной кислоты (уд. в. 1,84). .✓
. Примечание 2. Для приготовления раствора сернокислого марганца берут 10 г „х. ч.* MnS04-oH20, растворяют в 95 мл воды и 5 мл „х.
^ ч.“ серной кислоты (уд. в. 1,84).
Определение примесей*
1. Нерастворимые в воде вещества. 20 г препарата растворяют при нагревании в 300 'мл воды, раствор нагревают на .водяной бане,
в течение 1 часа, фильтруют через стекляйный тигель Шотта (№ 4), фарфоровый с пористым дном (Ai) или тигель Гуча, остаток промывают горячей водой, сушат при 105—110° С и взвешивают. Вес -остатка не должен
превышать:
для препарата «чистый для анализа* 1,0 мг
, » «чистый* 2,0 *
А Л
348
При определении примесей навески препарата берут с точностью до 0,1 г
2. Хлориды (СГ)- 1 г препарата растворяют при нагревании в 40
воды, раствор охлаждают, прибавляют 0,5 мл «х. ч.» азотной кислоты (уд
в. 1,15) и 1 мл 0,1 N раствора азотнокислого серебра. Образовавшаяся/через
10 минут опалесценция не должна быть интенсивнее опалесценции типового
раствора, содержащего в том же объеме 0,5 мл «х. ч.» азотной кислоты
(уд. в. 1,15), 1 мл 0,1 N раствора азотнокислого серебра и:
для препарата «чистый для анализа- . . . 0,02 мг С1'
, „ „чистый- 0,05 „ СК
Примечание. Для приготовления типа С1' растворяют в воде 0,824 г
предварительно слегка прокаленного химически чистого хлористого натрия и полученный раствор доводят водой до 1 л—раствор А.
20 мл раствора А разбавляют до 200 жл—раствор Б. 1 мл раствора
Б содержит 0,05 мг С1'.
3. Сульфаты (SO"«). 10 г препарата растворяют при нагревании
о 200 мл воды, если надо, фильтруют, раствор нагревают до кипения, прибавляют 2 мл соляной кислоты (уд. в. 1,125), 10 мл 10% раствора хлористого бария и оставляют стоять 18 часов; выпавший осадок отфильтровывают через фарфоровый тигель с пористым дном (Ai) или тигель Гуча,
промывают горячей водой до исчезновения реакции на хлор-ион, сушат,
прокаливают до постоянного веса и взвешивают.
Вес прокаленного остатка не должен превышать:
для препарата .чистый для анализа- 1,2 мг
/ . , .чистый- 2,4 .
Фактор для пересчета веса сернокислого бария на вес SO<" 0,41153;
log —61440.
4. Броматы (ВгОз). 1 г препарата растворяют (на холоду) в 45 мл
воды, раствор переводят в цилиндр на 50 мл с притертой пробкой, прибавляют, 1 мл 2% раствора йодистого калия, не содержащего йодатов, и 5 мл
1,0 N раствора серной кислоты. Появляющаяся через 30 минут окраска не
должна быть интенсивнее окраски типового раствора, содержащего в том
же объеме 1 мл 2% раствора йодистого калия, 5 мл 1,0 N раствора серной
кислоты и:
для препарата .чистый для анализа- 0.05 мг ВЮ3
„ „ .чистый- 0,1 „ Вг03
Примечание. Для приготовления типа ВгОз растворяют 1,306 г
предварительно высушенного в эксикаторе над серной кислотой бромноватокислого калия и доводят раствор водой до 1 л—раствор А.
10 мл раствора А разбавляют водой до 200 мл—раствор Б.
1 мл раствора Б содержит 0,05 мг Вг08.
5. Тяжелые металлы группы H2S. 20 г препарата растворяют
в 100 мл воды и 60 мл соляной кислоты (уд. в. 1,19) (не содержащей мышьяка—см. п. 9) в фарфоровой чашке на 250 мл, прикрывают часовым стеклом и нагревают на .водяной бане до прекращения выделения пузырьков
газа; стекло снимают, внутреннюю поверхность стекла смывают 5 мл воды
н раствор выпаривают досуха; сухой остаток растворяют в 100 мл воды;
25 мл раствора (отвечающие 5 г препарата) нейтрализуют 10% аммиаком
в присутствии кусочка лакмусовой бумаги, объем доводят до 40 мл, прибавляют 0,5 мл сх. ч.» уксусной кислоты и 10 мл свежеприготовленной
сероводородной воды; получающаяся через 10 минут темная окраска не
должна быть интенсивнее окраски типового раствора, содержащего в том
же объеме 0,5 мл «х. ч.» ледяной уксусной кислоты, 10 мл сероводородной
воды, и:
- для препарата „чистый для анализа* ...... 0,05 мг РЬ
. . ' я * .чистый- . v. . . • ..... *0^1 • РЬ
349
Примечание 1. Оставшиеся 75 мл раствора сохраняют дан определения кальция, магния, железа и мышьяка.
Примечание 2. Для приготовления типа свинца растворяют 1.831 г
свсженерекристаллизованного „х. ч." уксуснокислого свинца РЬ (CII:jCOO>> •
• ЗН20 в воде, подкисленной 1 мл ледяной уксусной кислоты, и доводят
объем до 1 л—раствор А. 20 мл раствора А разбавляют водой до 1 л —
раствор Б. 1 мл раствора Б содержит 0,02 мг РЬ.
6. Ж е л ечз о '(Fe). 5 мл раствора (см. п. 5, прим. 1) «переводят в цилиндр
с «притертой пробкой емкостью на 50 млЛ прибавляют 0,5 мл 4,0 N серной
кислоты, 4 мл 4,0 N раствор роданистого аммония, 10 мл изоамилоиого
спирта, доводят объем до метки, хорошо взбалтывают и сравнивают получившуюся окраску спиртового слоя с окраской спиртового слоя типового
раствора, содержащего те же количества воды, серной кислоты, роданистого аммония н кзоамилового спирта, к которому из бюретки прибавляют
•по каплям до уравнения окраски слоев спирта, типовой раствор железа,
содержащий 0,01 мг Fe в 1 мл. Сравнения окрасок производят всякий раз
после взбалтывания содержимого обоих цилиндров. По числу прибавленных миллилитров типового раствора 1вычисляют содержание Fe.
Примечание» Для приготовления типа Рс растворяют 0.864 г „х. ч.а
железоаммонийных квасцов в воде, подкисленной 4. мл серной кислоты
(уд. в. 1,84), и доводят объем до 1 л—раствор А.
10 мл раствора разбавляют водой до 100 мл—раствор Б, 1 мл раствора 1>
содержит 0,01 мг Ре. Раствор Б годен только в день его приготовления.
7.1 Кальций (Са). 25 мл раствора (отвечающие 5 г препарата, см. п. 5,
прим. 1) нейтрализуют в присутствии лакмусовой бумаги 10% раствором
аммиака и прибавляют избыток его в 1 мл и 0,5 г «х. ч.» хлористого аммония и 1 лл «насыщенного раствора щавелевокислого аммония и «нагревают
до кипения. Образовавшийся через 30 минут осадок не должен быть
больше осадка типового .раствора, содержащего в том же объеме 3 г
«х. ч.» хлористого калия без кальция, 1 мл раствора аммиака 10%, 0,5 г
«х. ч.> хлористого аммония, 1 мл насыщенного раствора щавелевокислого
аммонжк ■: , •
для препарата „чистый для анализа" ..... . 0,10 'мг Са
» . „ „чистый" 0,25- „ Са
Через 3 часа осадок щавелевокислого кальция отфильтровывают и
фильтрат употребляют для определения магния.
Примечание. Для получения типа Са растворяют в 20 мл „х. ч.“
\ соляной кислоты (1:10)0,624 г „х. ч.“ углекислого кальция, высушенного
при 100°С, и раствор доводят до 1 л.
1 мл этого раствора содержит 0,25 мг Са, см. также прим. 2, п. 8.
8. Магний (Mg). К фильтрату, оставшемуся от определения кальция,
прибавляют 4 мл раствора аммиака (10%), 2 мл раствора фосфорнокислого
аммония (10%) н оставляют на 18 часов. Выделившийся осадок не должен
быть больше осадка типового -раствора, содержащего в том же объеме
3 г хлористого калия без магния и кальция, 5 мл раствора аммиака (10%)„
1 мл насыщенного раствора щавелевокислого аммония, 2 мл раствора фосфорнокислого аммония (10%) и:
‘ для, препарата „чистый для анализа* 0,1 мг Mg
; „ „чистый" 0,25 „ Mg
/ Примечание 1. Для приготовления типа Mg растворяют в 30 мл
соляной кислоты (1:10) 0,332 г „х. ч.“ прокаленной окиси магния и раствор доводят водой до 1 л.
1 1мл этого раствора содержит 0,2 мг Mg.
Примечание 2. Если не имеется препарата хлористого калия, не
^ содержащего Са и Mg, берут 18 г хлористого калия, растворяет в 150 мл
воды, прибавляют, 3 г „х. ч.* хлористого аммония, 6 мл раствора аммиака
(10%) и 6 мл насыщенного раствора щавелевокислого аммония и нагревают
^ до кипения.
350
/
/ Выделившийся черев 3 часа осадок отфильтровывают и для каждом»-
типового раствора на кальций берут 27 мл фильтрата. К оставшийся 1U8
мл фильтрата прибавляют еще 16 мл 10 % раствора аммиака и 8 мл
раствора фосфорнокислого аммония (10*V0) и оставляют па 8 часов Выделившийся осадок отфильтровывают и для каждого типового раствора на
магний берут 33 мл фильтрата.
9. Мышьяк (As). К 25 мл раствора (см. <п. 5, прим. 1), отвечающим
5 г препарата, прибавляют 45 мл воды и 10 мл серной кислоты (уд. о. 1,84),
раствор охлаждают, вводят в аппарат Зангер-Блэка *, прибавляют 2 капли
10% раствора двухлористого олова и 3 г цинка без мышьяка; через 1—1,5-
часа окрашивание бумажки, пропитанной сулемой, не должно быть интенсивнее получающегося в тех же условиях в том же объеме типового раствора, содержащего те же количества кислоты, цинка, двухлористого
олова и:
для препарата .чистый для анализа* 0.0025 мг As
•чистый* 0,005 . As
Примечание 1. Если употреблявшаяся при разложении препарата
(см. п.,5) соляная .кислота содержала мышьяк, то для приготовления типовых растворов берут 32 мл той же кислоты и обрабатывают по ОСТ
359.1Охлажденную жидкость доводят водой до 145 мл, прибавляют 15 мл
„х. ч.* серной кислоты (уд. в. 1,84) и для каждого типового раствора берут половину жидкости, прибавляя к ней тип As. '
Примечание 2. Для приготовления типа As растворяют 0,660 г
возогнанного .х. ч.* As203 в небольшом количестве 10% раствора едкого
натра и раствор доводят водой до 1 л—раствор А.
4\мл раствора А доводят водой до 1 л—раствор Б. 1 мл раствора Ь
содержит 0,005 мг As.
С.С.С.Р.
ОБЩЕСОЮЗНЫЙ СТАНДАРТ
S-4100"-
Совет труда в обороны
КАЛЬЦИЙ ХЛОРИСТЫЙ
Всесоюзный комитет
технический
по стандартизации
(плавленый)
А. ОПРЕДЕЛЕНИЕ
Хлористый кальций технический плавленный представляет собой хлористо-водородную соль кальция, расплавленную в своей кристаллизационной
•оде.
. Б. ТЕХНИЧЕСКИЕ УСЛОВИЯ
1-й сорт
2-й сорт
3-й сорт
1. Хлористого кальция (СаС12) безвод-
ногсУ не менее
2. Хлористого магния (MgCla) не более
3. Хлористого натрия (NaCl) не более
4. Хлорноватокислого калия (КСЮ3)
, не более .......
5. Нерастворимого в воде' остатка
(прокаленного) не более
6* Хлорного' железа в пересчете на
Ее не более
72,00/о
1,3%
2,0% •
Отсутствие
0,2 %
Отсутствие
66,0%
1.3%
2.0%
Отсутствие
0,2%
0,03%
67,0»/о
Не корм.
Не норм.
1.5%
•,2*/.
0,07% -
• Тре двелл, т. II, стр. 166, «за 1927.
•• Утвержден всесоюзным Комитетом по стандартизации при СТО
26 декабря 193^ г. хак обязательный с 1 февраля 1932 г.
351
В. УПАКОВКА И МАРКИРОВКА
Хлористый кальций упаковывают в железные барабаны весом 160 кг.
На каждом барабане должно быть обозначено: наименование треста и завода, название продукта, вес брутто и нетто и ОСТ 4100.
Г. ПРАВИЛА ПРИЕМКИ
% * а) Отбор проб
1. Для приготовления проб отбирают не менее 2% подлежащих сдаче
барабанов. Ударами молота по стенкам барабана разрыхляют его содержимое, вскрывают барабан по продольному шву и быстро отбирают пробу
из разных мест. Крупные куски при этом разбивают на небольшие и помещают их в банку с притертой пробкой.
2. Взятые пробы быстро перемешивают и отбирают среднюю пробу вепсом около 1,5 кг, которую помещают в три чистые и сухие банки с притер*'
тыми пробками.
3. Банки запечатывают печатями поставщика и покупателя. Одна банка
остается у поставщика, другую передают покупателю, а третья хранится
у поставщика «а случай экспертного анализа. Выбор лаборатории для
экспертного анализа, срок хранения экспертной пробы и место отбора проб
устанавливаются соглашением сторон.
\ б) Методы испытаний
1. О <п р е д е л е н и с нерастворимого остатка. Навеску хлористого кальция около 20 г, взятую в стаканчике с притертой пробкой, переносят в Небольшой стакан и растворяют >в воде. Нерастворившийся в воде
остаток собирают на бензольном фильтре и промывают водой до исчезновения реакции на хлор. Фильтрат собирают в мерную колбу на 1 л, дополняют водой до метки и оставляют для последующих определений.
Фильтр с осадком сжигают в тигле, затем тигель прокаливают и по охлаждении В’ эксикаторе взвешивают.
2. Определение хлористого кальция. 50 <\ма фильтрата,
после определения нерастворимого остатка (а 1), разбавляют горячей во-
дрй до 200 cjk3 и, прибавив 20 еле3 10% раствора NH4CI, нагревают до кипения. К горячему раствору прибавляют 15 см3 8% раствора щавелевой кислоты, 5 см3 соляной кислоты (уд. в. 1,19), несколько капель метилоранжа
и небольшими порциями—при постоянном помешивании и продолжая подогревание раствора — разбавленный раствор аммиака лишь до появления
желтого окрашивайия (избыток аммиака вредит). После этого приливают
10 cjk3 горячего 4% раствора щавелевокислого аммония, дают стоять 4 часа,
затем отфильтровывают щавелевокислый кальций и промывают, теплым 1 %
раствором щавелевокислого аммония. В полноте промывки убеждаются по
отсутствию осадка от азотнокислого серебра, «прибавляемого к небольшой
порции фильтрата, подкисленной азотной кислотой. Осадок подсушивают
в сушильном, шкафу, затем переносят вместе с фильтратом в поместительный платиновый тигель и сжигают. При этом необходимо быть олень осторожным, так как при быстром выделении окиси углерода могут произойти
потери.
После сгорания фильтра тигель закрывают и сильно нагревают сначала на обычном пламени горелки и наконец на паяльном огне в течение
2Q минут.
ч Взвешивание тигля как с осадком, так и без него производится в стаканчике с «притертой пробкой, который ставится при охлаждении тигля
в эксикатор рядом с тиглем. Прокаливание, охлаждение и взвешивание
повторяют до получения постоянного веса. Привес а тиА*е СаО пересчитывают на СаС12, умножая на 1,9793.
3. Определение хлористого магния. Фильтрат от второго
определения выпаривают в платиновой или фарфоровой чашке и прокаливанием удаляют аммонийные соли. Полученный остаток растворяют в небольшом количестве разбавленной соляной кислоты, и выделившийся углерод.
отфильтровывают и промывают. Фильтрат нсйтралиауют аммиаком, :югл<
чего прибавляют 1 с.v3 сочиной кислоты (уд. в. 1,19), К) с.ч'л 10% раствора
NaaHl’Oi. 12 НЮ, иагрепают до кипения и прибавляют сразу */* oi-ьомп
всей жидкости 10% раствора аммиака; дают ох.чл чи гьси, мерса некоторое
время фильтруют, промывают 21{*% раствором аммиака и, высушив осадок
насколько 1ПОЗМОЖНО, переносят его во взвешенным тигель. Фильтр с/кн-
гают в платиновой спирали и золу присоединяют к главной массе, находящейся в тигле. После этого тигель, .прикрыв крышкой, нагревают сначала
на малой пламени до исчезновения запаха аммиака, затем сильнее и наконец на паяльном огне. Полученный привес «в тигле пересчитывают на MgCb,
умножая на 0,8552.
• 4. Определение железа. Из колбы пипеткой отбирают 10 г.*3
фильтрата после определения нерастворимого остатка (п. Г), добавляют
15 с.ч3 воды, 0,5 с.ч3 не содержащей железа азотной кислоты (уд. в. 1,2),
нагревают до кипения, охлаждают и переносят в цилиндр с притертой
пробкой на 50 ел3, прибавляют 0,5 ел3 соляной кислоты (уд. в. 1,19), 15 r.w3
изоамилового спирта, 5 ел3 10% раствора роданистого аммония и хорошо
взбалтывают.. '
В другой такой же цилиндр берут те же количества воды, соляной
и азотной кислот, роданистого аммония и спирта и из бюретки прибавляют
типовой раствор железа, содержащий в 1 ел* 0л01 мг Fe, до уравнения
окраски слоев спирта в обоих цилиндрах. Сравнение окрасок производится
каждый раз после взбалтывания содержимого обоих цилиндров, Равенство
объемов в цилиндрах поддерживают прибавлением , поды.
Примечание. Для приготовления типового раствора Fe раство-
ряют 0,864 г х. ч. железных квасцов в воде, подкисленной 4 с.ч3 сорной
кислоты (уд. в. 1,84), и доводят водой до 1 л. 10 см9 этого раствора
доводят водой до 100 с.ч3. J см9 последнего (разбавленного) раствора
содержит 0,01 лг Fe. Разбавленный раствор годен в день его приготовления.
5. Определение хлористого натрия. 50 см3 фильтрата после
определения нерастворимого остатка (п. 1) вливают в мерную колбу на
200 см9, подкисляют слегка азотной кислотой и добавляют избыток титрованного 0,1 JV раствора азотнокислого серебра, после чрго колбу закрывают пробкой и взбалтывают до тех пор, пока осадок хлористого серебра
не соберется в комки, а находящийся «ад ним раствор не станет прозрачным. ^ '
После этого уолбу дополняют водой до -метки, перемешивают и фильтруют через сухой фильтр. Первые 10 см9 фильтрата отбрасывают. 'Для
титрования берут 50 см9, прибавляют к ним 1—2 см9 раствора железо-аммонийных квасцов и оттитровывают обратно избыток серебра 0,1 N раствором роданистого аммония. Общее процентное содержание хлора определяют по формуле:
где А — количество куб. сантиметров 0,1 JV раствора азотнокислого серебра;
р — количество куб. сантиметров 0,1 JV (раствора роданистого аммония, пошедших на титрование 50 см3 фильтрата; В — навеска.
Процентное содержание хлористого натрия определяют по формуле:
[х ^ (% СаС13 • 0,6390 + % MgCl2 • 0,7446-f % Fe • 1,9051)1 • 1,6486, (2)
где 0,6390 — коэфициент для пересчета СаСЬ на хлор; 0,7446 — коэфициент
для пересчета MgCla на хлор; 1,905Г—коэфициент для пересчета Fe на'
хлор; 1,6486—коэфициент для пересчета хлора на NaCI; х—процентное
содержание хлора, вычисленное по формуле (1).
6. Определение хлората кал^ия (хлорновато-кислого калия —
КСЮэ). Необходимые растворы: 1) 0,1 N раствор As*Os (готовится обычным
способом с прибавлением ^NaHCOa. Т р е д в е л л, т. II, ч. 2, 128 стр.,
2-е изд.); 2) 0,1 N раствор бромата'калия (КВгО*).
0,003546 (А — Ар) • 20.100
В
<1)
353
К 50 см* раствора As^O:» в колбе Эрленмепсра прибавляю» р ч t
2 i* испытуемого хлористого кальция в 25 см* воды, 0,05 г бромискно капп,
и соляной кислоты (уд. в. 1,19) из расчета, чтобы на каждые 7 см нейтрализованной жидкости был прибавлен 1 см* соляной кислоты (уд в 1,19),
затем кипятят «на слабом огне в течение 15 минут, прикрыв колбу воронкой.
После этого жидкость охлаждают до 60° С и, прибавив несколько капель метилоранжа, оттитровывают избыток AszOa броматом до исчезновения розовой окраски. Титрование ведут медленно, приливая бромат по
каплям и с паузами, особенно к концу титрования. Бели температура во
время титрования падает ниже 50° С, то раствор подогревают. Коэфиииент
для Пересчета на КСЮ* — 0,002043.
Приложение li
ДОПОЛНИТЕЛЬНЫЕ РИСУНКИ И ТАБЛИЦЫ.
На ри-с. ИЗО приеден,1 номограмма, показывающая коэфициенты расхода СаО, хлора и КС1 на < ■ *,:iy получаемого КСЮа при разном проценте
выхода хлората. Выход счи*»(м по отношению к теоретическим количествам согласно уравнению (Ь3>.
Расход СС*
°асход СаО
А%
!СД-
90 —
-<,39
05 — —
07-
06'
93 —»
Г-
94 —
03 —
92
9<
904
89
66-
' 67
72 ——1,90
*“4,30
62
6< — -
Тонн А % I Тонн
СаО (СаО
30-
79 —
7,
<;<LQ
-1,45
77 —
76
75
74-
73
-1,59
—да
71
70-
69-
-<,35
66 —Г
66 —
-—<,60
85—
64—-
67 —
Со —
65
64
- \
~уэ
83—{— Г;65 и _Ь
62-
61 — ZL
--<,70
60 —' 60—
—1,95
“2,00
—2,05
—2,<0
—2,20
Г"**25
Расход HCL
As
А'А,
<00-
сэ —
—
96 — -
—0,61
Тонн А*/,
на
со-
Тонн
на
^;7б .
4-
79 —
76-
н
77 —j
93 —
а
. _1
04— j
с,ез
C.3-J
02—Г
91 —
90-
89 —
66 —
X __
07 —
66 —
85-
64 —
ез —
62 —
в<
30
—0,70
66 —
65 —
64 —
63 —
62 —(—
“0.75 Ci —
60
—0,00
76
75
74
73 —
72 —
7< —
70 — _
69—~
58-
— —0,90
67 —
-0,65
-0,95
—<.00
-
Рис. 130. Коэфициенты расхода СаО, хлора n KG1 на'1 т КС108
при разном проценте выхода хлората. *
3W
355
На рис. 1Ж1 показана схема установки дли лабораторного хлорирование
На рис. 132 приведена аппаратурная схема производства бертолетовой
холи известковым методом с применением выпарки.
К схеме можно сделать следующие общие замечании.
Бакам, в которых должен происходить отстой щелоков от шлама, и
вообще бакам, где имеются взвешенные твердые частицы, целесообразно
придать форму цилиндра с коническим дном. Такая форма уменьшает возможность создания мертвых -пространств, облегчает перемешивание воздухом и т. д.
Рабочие объемы аппаратуры желательно сделать кратными друг другу
и подобрать размеры так, чтобы объемы выражались целыми числами (ля),
что весьма облегчает учет. С этой же целью баки, служащие' мерниками,
целесообразно сделать с переливными трубами и т. п. устройством.
Рйс. 131. Лабораторная установка для хлорирования.
Баки, в которых не должно происходить охлаждения жидкости, необ-
' ходимо покрыть снаружи тейловой изоляцией, также необходима тепловая
изоляция вымораживателей.
Перекачки щелоков производятся центробежными насосами. Целесообразно применение для всех перекачек стандартных насосов одного размера, что весьма упрощает вопросы ремонта н замены одного насоса другим. Для перекачки известкового молока в бак для орошения абгазной
колонки, откачки абгазного щелока из баков и откачки перехлорирован-
ного щелока из башен обязательно ставить по 2 насоса- (один резервны^).
На остальные перекачки резервное -насосы не обязательны.
/.
Таблица 101. Указатель дан и ы х о* свойст н л х х л и р а т о и
по справочнику технической э п ц и к л о и од и н
Показатели
Том
№
Какие хлораты и стр.
Аммиакаты
10
Взрывные свойства
Вязкость водного раствора . . .
Давление пара водного раствора .
Диэлектрическая постоянная . .
Дисперсия
10
10
6
4
8
Изменение объема при плавлении
Магнитная восприимчивость . . .
Оптическая^вращательная способ
ность
Осмотическое давление .....
Отражение
Лиэзоэлектрическая константа . .
Плотность водного раствора . . .
6
4
8
10
8
5
5
*
Плотность твердой соли
1
Поверхность натяжения в растворе .
Повышение точки кипения в рас-
творе .......
Понижение давления пара водного
раствора . . .
10
6
5
Понижение точки затвердегвания
• водного раствора
Преломления показатель водного
раствора
Преломления показатель твердой
соли ......
6
\
8
ч\ '
1
Рассеивание света комбинационное
8
Растворимость в воде
6
Рентгенографический анализ • . .
Свободная энергия
Сжимаемость водного раствора • .
Скорость растворения в воде . . .
Температура плавления . . . . . \
• разложения
• перехода
Теплопроводность
Теплота образования,
Теплота плавления . .
• ч удельная видного раствора
\
/
Хлораты Ni, Ag, Си и Zn; стр.
186. 196, 202, 220
Хлорат аммония, стр. 353
Хлораты К. Na п U; сгр. 95 и 98
Хлораты К и Na, стр. 74 и 76
Хлорат калия, стр. 270
Хлораты Li, Со, Ni, Си, стр. 117
и 118
Хлорат калия, стр. 99
Хлорат калия, стр. 105
Хлорат натрия, стр. 158
Хлорат калия, стр. 156
Хлораты К, Na, Ва, Ag; стр. 17;
Хлорат натрия, стр. 115
Хлорать! К, Na, Ва, Са, Li, Со
Ni, Mg, Sr, Pb, Ag, Cu, Rb, Tl, Zn,
стр. 205—242 и 258—261
Хлораты К, Na, Ва, Sr, стр. 182,
183, 187, 192
Хлораты К и Na, стр. 47
Хлораты К, Na и Ва, стр. 26, 27
Хлораты К, Na, Ва, Cd, стр. 458,
460, 461, 462
Хлорат!>1 К, Na, Ва, Li, Со, N1,
Mg, Ag, Си, Zn, стр. 386—391
Хлораты Na, Ва, Са, Li, Со, Ni,
Mg, Sr, Си и Zn, стр. 82—85
Хлораты К, Na, Ва, Sr, стр.
182—192
Хлораты К, Na, Ва, NH*, стр.
315, 316, 317
Хлораты К, Na, Ва, Са, Li, Со,
Ni, Mg, Sr, Pb, Ag, Си, Rb, Tl и
Zn, стр. 350—370
Хлорат натрия, стр. 77
Хлорат калия, стр. 346
Хлорат6 калия, стр. 351
Хлорат натрия, стр. 240, 243
Хлораты ;К, Na, Ва, стр. 183,
187, 192
Хлорат бария, стр. 183 *
Хлораты К, Li, стр. 94
Хлорат натрия, стр. 454, 474
Хлораты JK, Na, Ва, Ag, Си,
стр. 396, 39$, 419, 425, 432
Хлораты К и Na, стр. 323
Хлорат калия, стр. 309
357
Показатели
Том
№
Kai и с хлораты и стр.
Теплота удельная твердой соли . .
7
Хлораты К, Na, Ва, Li, стр. 288,
289, 295, 309
Число переноса
Электропроводность водного рас-
4
Хлораты К, Ag, стр. 346, 447
твора
4
Хлораты К, Na, Ва, Са, Li, Со,
Ni, Mg, 5r, Ag, Rb, Tl, Zn, стр. 367,
370, 371, 372, 373, 374, 381
Электропроводность твердой соли .
4
Хлораты К, Na, Ag, стр. 347,
349, 381
ЛИТЕРАТУРА *
1. Jurisch, Chlorsaurcs Kali (Берлин 1888 г.).
2. Kerschaw, Die elcktrolytische Chloratindustrie (Галле 1905 г.).
3. Lunge, Handbuch der Sodaindustrie, т. 3, стр.567—591 (1909г.).
4. Gmellns Handbuch der anorganischen Ctiemie (особенно т. 6, 21, 22).
5. Ull man n, Encyclopedie der technischen Chemie (особенно том 3.
стр. 278 — 299, изд. 1929 г.). . ^
4 6. A b b е g, Handbuch der anorganischen Chemie.
6a. Me 11 о г, A comprehensive treatise on inorganic and theoretical chemistry, vol. II.
7. D'ammer, Technologie der Neuzeit (особенно т. 3, стр. 286—292, изд.
1927 г.).
8. Musspratt, Technische praktische und analvtische* Chemie.
9. Pechincy, Encyclop. chem. u. Fremy. том.'5, ч. 1, стр. 189—216.
10. Foerster, Elektrochemie wasseriger Losungen (изд. 1923 г.).
11. В ill iter, Technische Elektrochemie,-том 2 (1924 г.).
12. Б и л л и т е р, Новейшие достижения технической электрохимии
(пер. с немецкого изд. 1934 г.).
13. Би л л и т е р, Технический электролиз хлористых солей щелочных металлов (перевод с немецкого изд. 1930 г.).
14. Любавин, Техническая химия.
15. Федотъев, Химико-технологические очерки (изд. 1930 г.).
16. Ф е д о т ь е в, Конспект к лекциям по технич. электрох. (Л. 1909 г.).
17. С. L. Man tell, Производство угольных электродов (пер. с англ. Л.
1926 г.).
18. Askonasy, Einfiihrung in der technische Elektrochemie, тома 1 и 2
(изд. 1910 и 1916 г.г.).
19. Г р у б е, Основы электрохимии (пер. с нем. Л. 1932 г.).
20. А л м а н д, Основы прикладной электрохимии (пер. с англ., тома 1 и 2,
изд. 1926 и 1935 гг.).
21. Drews, Verdichtete und verfliissigte Gase. (1928 г.)
22. V a n i п о, Praparative Chemie.
23. Hager, Фармацевтическая и медико-химическая практика.
24. Ост, Химическая технология (пер. с нем. изд. Л. 1927 г.).
25. Сасс-Тисовский, Производство хлора (изд. Л. 1933 г.).
26. Г. Ангел, Электролиз хлористых солей щелочных металлов.
27. Техническая энциклопедия.
28. Справочник физич., химич. U технология, величин Технической Энциклопедии.
#
* Ссылки в, тексте на литературу даны в виде, цифр (мелким шрифтом).
Первая цифр^'указывает порядковый № данвого указателя вторая М» тома.
х» •' . ' ;
29. Chcmikor Kalcndcr ил 1933 г. и Спуптк химика пая. 1931—1935 гг.
30. Вег 1-Lung с, Cliemisch-technische Untersucliungsmetlmdeii (изд. 3
1931 г., и 2 т. русского изд.
3U В е р л ь - Л у и г о, Справочник по [основной хнмич. промышл. (пер.
с немецкого, 2-ое издан. 1937 г Л
32. Landolt-Bdrnsteln, Physikalisch-chemische Tabellcn.
33. Вольфкович, Производство хлористого калия.
34. Деркачев, Поташное производство (изд. М. 1932 г.).
35. Каст, Взрыв, вещества и средства воспламенения (пер. сном. 1932 г.)
36. Каст и Мет Ц. Химическое исследование взрыв, веществ, М. 1931 г
. 37. С л 11 о ж и и к о в, Техника безопасное гм и основном хнмич. промышленности (см. также книгу Лазарева' и Астраханцева „Хим. вредные
вещества в промышленности").
38. Ильский и Хани и, Химич.технология производства спичек (1931 г.,
см. также книги по вопросам произвол, спичек: Быстрова, Штерна, Сапожникова).
39. М е г i n g, Das chlorsaure Kali, seine physiologischen, toxischen und the-
rapeutischen Wirkungen (Берлин 1885 г.).
40. Б н p к г а н, Центрофуги (Mi 1934 г.). Сушилки в химич. промышленности (1934 К).
41. Г а у с б р а и д, Выпаривание, конденсация и охлаждение.
42. Бедж ер и Мак-Кеб, Основные процессы и аппараты хнмич.
промышленности (М. 1933 г.).
43. Л у к ь я и о в П. М., Курс химич. технологии минеральных веществ.
44. Дммчишин, Производство хлористого бария (Л. 1933 г.).
45. Гольдштейн, Производство кальцинированной соды (1934 г.).
46. Г ен ин, Глазков к Хомяков, Производство хлора в ваннах с
диафрагмой. (М. 1936 г.)
47. На mm 11, Journ. Soc. ghem. Ind. (англ.) 1889 г., стр. 168г-172—0 вымораживании бертолетовых маточников.
48. Lunge, Die chem. Ind. (нем.) 1885г.,$стр. 4 — о коррозии при выпарке,
Z. f. angew. Chem. (нем.) 1899 г., Стр. 537 — взрыв в St. Helens.
49. Dolner, Chem. Ind. 1899 г., стр. 443—444 — взрыв в St. Helens.
59а. Мацетисс, Annalen chimica aplicata 1929г., т. 19, стр. 273—282; система СаС12 Са (СЮзЬ КС1, КСЮ3, Н20.
506. Osaka и Nischio, Bull. chem. Soc. Japan № 5, 3183, 1930 г., система
Са(СЮ3)2, КС1, КСЮ3, CaCi2, HzO.
51. О взрываемости бертолетовой соли: 1) Berthelot, Comptes rendus
т. 129, стр. 926; 2) Dupr£, Chemical Trade Journal 11/X1 1899 r.
52. Морозов, Известия ГИПХА 1932 г. X® 15, стр. 46—56 — магнезиальный метод получения КС103.
53. Шпитальский и др., Ж. Пр. Хим. 1924 г. (М.) том I, вып. 3—4, получение КСЮ3 из поташа.
54. Н о в а к о в с к а я Ж. X. П. 1937, № 3, стр. 207.
55. Пупко, Ж. X. П.№ 23/24 1929 г. Получение берсоли химическим путем.
56. Щербаков, и др. Ж. X. П. 1931 г. №/3/4 Хлорирование известкового молока высокой концентрации.
57. Ангел. Ж. X. П. 1927 г. № 11. Экономика, химич. и электрол. получение хлоратов.
58. Блинов, Ж „Калий* 1937 г., № 10 и Ж. X. П. 1937 г.. № 2.
59. Шрайбман, Исследование вопросов производства КСЮ3 и NaC103
известковым, каустическим и содовым методом и коррозии аппаратуры при
этих производствах: Ж. X. П. 1930 г. №№ 25—33, 1934 г. № 6 и 1937 г. № 5
Химстрой 1930 г. № 4, 1931 г. № 1, 1932 г. № 2 и № 11,1933 г. № 5 и № 8
и 1934 г. № 8; Военная химия № 5—6 1932 г* Калий 1936 г. № 5 и 1937 г.
№ 2 и 5—6. Заводская лаборатория 1936 г. № 4.
60. Шпитальский и др., Ж. Пр. Хим. (М.): а) том 1; вып. 1—2,£б)том2;
вып. 3—4 (1924 г.); в) том 2, вып. 1—2“ (1925 г.).
61. Воронин, Ж. X. П., 1925 г. № 3, стр. 61 и 1930 г. № 14/15.
62. Каце н и Соколов: а) Ж. X. П. 1932 г. № 1; б) Ж. Пр. Хим. (Л)
1931 г. том IV, стр. $45—566; в) Ж. Пр. Хим. 1932 т. том V, стр. 902—928.
63. Панфилов и др., Известия Иваново-Вознес.Полит.Института 1921 г.
№ 4 и том VII, вып. 1, стр. 79. *
, • / »
359
64. Алсксеевский, Ж. Р. Ф. X. О. том 63, стр. 323.
65. Octt el. Z. f. E.:i: a) 1—474; б) V—1 и 16; в) VII-310.
66. W о h 1 w i 1, Z. f. E. V—52.
67. Muller Z. f. EV—469; VII—398; VIII—409.
^ 63. F о e r s t e r u. Sonne n born, Z. f. E. VI—579.
69. F о e r s t e г u. Muller, Z. f. E. VI — 579
70. F о e r s t e г u. J о г г e, Z. f. prakt. Chem. 21, 59, 53 # 63—141.
71. Spresser, Z. f. E. VII—971, 987, 1012, 1027, 1071, 1083.
72. Wintelir Z. f. E.: a) V—10, 49 и 217; б) VII—360; в) IX—49, 217.
73. Muller u. Koppe, Z. f. E.XVII—421.
74. P г a s s n i t z Z. f. E. XVIH—1025; XIX- 676.
75. S c h 011 e г Z. f. E. XXVI—394.
76. Arnd u. Felisc Z. f. E. XXVIII—376.
77. G г u b e u. Plunder Z. f. E. XXIX—150. \
78. G г u b e u. Burchardt, Z. f. E. XXX-67.
79. L i e b г i c h, Z. f. E. XXX.—344.
80. Bun net, Bull. Soc. Franc. Electric. VIII—798 (1928).
' 81; Jo'st, Dissert. Dresden 1910 г., стр. 41—49 и 57—64.
82. I mil off, герм. пат. 110420 и англ. пат. 1017.
83. Vogeb F., MetallbOrse XIX, № 28, стр. 761.
84. H a s s e r m a n, Dingl. Polytechn. J. 28/VII 1900 r.
85. Carlson, Z. f. E. VI—471.
86. Stassing, Teknisk Tidskrift 1894 — 95 r.
87. Richards, Electrochemical Industry IX—1902 r. 0
88. Overbury, Cassiers Magazin. VII—1897 r.
89. Dunlap, The Electrician, том 37—661 стр.
90. M u 1 i ц s u. Funk, Ber. 30, 1716 (1897).
91. Meusser, Ber. 35, 1414 (1902).
92. Traube, Ztschr. anorg. u. allg. Chem. 8, 12 (1895).
93. Hcydweiller, Ztschr. anorg. u. allg. Chem. 116, 42 (1921).
94. H e у d we i 11 e r, Annalen der Physik, 30, 873 (1909).
95. H e у d we i 11 e r, Annalen der Physik, 37, 739 (1912).
96. M u i r, J. chem. Soc. (London), 29, 857 (1876).
97. Noyes and Falk, J. Am. Soc. 32, 1011 (1909).
98. Noyes and Bray, Am. Soc. 33, 1643 (1911).
99. К г a u s, J. Am. Soc. 49, 1226 (1927).
100. Carlson, Klason Festkrift 247 (191,0).
101. Be у her, Ztschr. physikal. Chem. 26, 744 (1888).
102. Bakhuis Roozeboom, Ztsch. physikal. Chem. 8, 531 (1891).
103. Trautz u. Anschutz, Ztsch. physikal. Chem. 56, 236 (1906). 9
104. J a h n, Ztschr. physikal. Chem. 59, 31 (1907).
105. FI tig el, Ztschr. physikal. Chem. 79, 577 (1912)
106. Cal zo lari, Gazz. chim. (italiana). 42/11, 85 (1912).
107. Levi, Gazz. chim. (italiana). 53, 522 (1923),
108. Ressig, Ann. chem. 12^, 38 (1863).
109. Bourgeois, Bull. Soc. Chim. 19, 949 (1898).
110. Rankin u. Taylor, Trans, of the Royal Society of Edinburg 45,397 (1906).
111. Buchanan, Trans, of the Royal Soc. of Edinburg, 49, 1 (1912).
112. Kraus, Brown University (частное сообщение).
113. Поты л ицын, Ж. Р. Ф. X. О., т. 20/1, 1888 г., стр. 541., т.21/1,1889 г„
стр. 451.
114. Ф е д о т ь е в, Физико-химические таблицы.
115. В rochet, Bull. Soc. chim. (4), 3, 548 (1908).
116. Knibs, Trans. Faraday Soc. 1921 г., ч. 2, стр. 402.
117. Ricci u. Janick. J. Amer. Chem. Soc. 59 (1937)№8. стр. 491—496.
118. Engelbracht, Ch. Ztg. 1918, 150.
119. Billiter, Monatscheft f. chemie 41 (1920) № 4, стр. 287.
120* Пешков, Заводская лаборатория № 10^1933 г.
* Ztschr. f. Elektrochem. Римские цифры доказывают номера томов, а араб*
ские цифры — страницу* *
ИМЕННОЙ УКАЗАТЕЛЬ
Абегг 13, 20, 42, 48, 50, 218, 221,
✓223, 224, 225, 226, 228, 230, 231,
232, 234, 235, 236, 237, .238, 239,
240, 241. V
Агер 218, 358
Алексеевский 359
Ангел 48, 284, 286, 301, 359 „
Арндт 275, 279, 360
Байер 16, 162, 193
Беллами 23
Бенциг 275, 276
Беркер 284, 301
Вертело 25, 359
Бертолле 15, 58
Берцелиус 15, 17, 247
Биллитер 33, 34, 42, 48, 70, 259, 281,
283, 300, 301, 303, 306
Блекман 270 . /
Блинов 336, 359 .
Блюменберг 284, 289 \
Борхардт 265, 267
Броше 248, 257 '
Брук 284, 293 j
Вельдон 180, 181 ч
Вильдерман 72, 84, 106, 108
Винтелер 126, 188
Вольвилл 248
Вольфкович 50
Воронин 17, 247, 270, 283, 284, 301,
304
Ворс 42
Галль 247, 284, 287
-Гаммил 15
Гаргривс 196
Гаслингер 273, 284, 300
Гей-Люссак 15,, 58
Генин 48, 87, 91
Гертер 248, 284, 293
Гиббс 248, 273, 284, 290, 292, 294
Гмелин 13, 18, 20, 29, 42, 48, 156,
218, 221, 223, 224, 225, 226, 228,
230, 231, 232, 236, 237, 238, 239,
240, 241, 283, 306-
Гольдштейн 42
Грубе 265, 267, 271, 276*
Даммер 50, 218 s
Диксон 334
Древе 44
Дюпре 25
Дюфло 142
, Дэви 43
Заславский 128, 130
Зильберман 294
^Ильинский 18
Имгофф 248, 264, 294
Иоффе^ 275
Карлсон 268, 272, 284, 288
Каст 135, 321, 325, 336
Кацен 18, 247, 263, 268, * 275, 276,
278, 280
Кершав 13, 18, 286, 287, 288, 289,
290, 293, 294, 295, 306
Кельнер 294
. Книббс 60, 258
Кольбе 248
Копне 263
Коренман 321 \
Корбэн 248; 284, 295, 335
Кунгейм 75
' Кюльман 75
Ледерлэн 248, 284, 295
Либих 15, 16, 58, 191
Леве 284, 294
Лукьянов 36, 42
Лунге 13, 32, 35, 58, 70, 146, 182, 35а
Любавин 13, 37, 41, 50
Мантелл 306
Мацетис 128 ч
Меринг 29 ^
Монлор 247, 284, 287
Морозов 182
Мук 195
Муспрат 16, 58, 75. 180, 191
Мюллер 253, 256, 263, 264
Нильсен 255
Нишио 128
Нов айовская 16
361
Ост 42, 358
Осака 128
Панфилов 18, 247
Печиней 15, 18, 33, 34, 70, 85, 105,
191, 197, 216
Праусниц 253, 254
Пфундер 271
Розе 37
Ричардс 292
Сасс-Тисовский 48
Сирак 275
Соколов 18, 247, 263, 268, 275, 276,
278, 280
Спилкер 284, 294
Стадион 247
Уатт 247 286
Ульман 13, Д8, 34, 70,' 88, 108, 166,
218, 221, 241, 262; 301, 803, 334,
336
Фсзс 270
Фсрстер 5S, 247, 251, 255, 258, 258.
274, 275, 277, 280, 283. 284, 306
Федотьев 18, 247, 270, 306
'Фогель 271
Фрайман 61, 73, 108, 219
Фрсйденберг 283
Франшо 248, 290, 292
Фобелль 283
Харгревс 156, 195
Шеслс 43
Шлеттер 266, 267
Шпитальский 18, 182, 247, 260, 262,
263
Шульц 16
Шультесс ^1
Эскалес 335
Эттель 248, 261, 262
Эшельман 180, 191
Юриш 13, 18, 19, 23, 70, 106, 146,
182, 183
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
Абгаза анализ 318
— опасность взрыва 328
— получение и состав 89
— улавливание 340
Абсорбера устройство 77 j}
1— режим работы 338
Аварии в пр-ве хлоратов 330
Алюминия хлорат 234, 358
Аммиака анализ 314
— применение в производстве хлоратов 95
Аммиакаты 361 у
Аммония хлорат 226, 242, 358
Анализ абгаза 318
— аммиачной воДы 314
— бертолетдрой соли 27, 319, 348
— бертолетовых щелоков 316
•— извести 313
— известкового молока 314
— маточных щелоков 316
— обратной соли 322
— плавленого хлористого кальция
319, 352
— слабого каустика 322
— хлората бария 325
натрия 324
— хлоргаза 314
— хлористого калия 314
— хлорированных щелоков 315
— шлама от хлорированных щелоков 318
-Аппарат Кунгейма 75
— Кюльмана 75
Мика 50, 54
Аппарат Русселя 53
—: Шультесса 41, 55 *
Аппаратура для выпарки 105
кристаллизации 113 )
обезвреживания 97
«— г- обменной реакции 109
— — сушки бертолетовой соли \34
' хлорирования 70
Аппаратурная схема по Биллите-
РУ 33
— — по известное, методу 357
по Лунге 32
Арагонит/37
Байера метод пр-ва КСЮя 16, 182
NaCI03 193
Баланс потерь в пр-ве КСЮя 149
Барботаж как способ хлорирования 80
Бария хлорат анализ 325
получение 210, 283
свойства 211, 242, 358
Барий хлористый, состав, свойства,
•получение 142
Башня абгазная 8Г>, 340
-V- барботажная 80, 339
— Вильдермана 84
— Гаргривса 195
— с распылением 86
Берилия хлорат 228, 242, 351
Биполярные электроды 298, 300
Бромат в бертсоли 319, 321, 340
Вагонетки для бертсоли 137
Ванадий, влияние на электролиз 266
Ванны-электролизеры Alby Nya Kl.
303
Ангела 301 .
Ауссигского союза 303
Беркера 301
Блюменберга 289
Брука 293
Воронина 304
Ворса 43
— Галля и Монтлора 287
Гаслингера 300
Гертера 293
Карлсона 288
Корбэна и Ледэрлена 295
Нац. Электр. Комп. 290
Спилкера и Лове 294
Уатта 286
Варианты получения КСЮя известковым методом 29, 35 •
— / каустическим методом 159
электролизом 281
Взрываемость хлоратов 25, 27, 330,
334
Взрывчатые вещества как потребители хлоратов 334
Взрывы абгаза 329
363
Внльдермана способ хлорирова*
ни я 84
Висмута хлорат 237
Влага в хлоргазе 45, 48
бертсоли 319, 321
Водород 43, 46, 314, 328
Восстановление СЮ' и CIOs' 250,
264 , *
Выделение Os при хлорировании
60, 61
Вымораживание маточников 16,31,
114, 115, 158
Вымораживатели 114
Выпарка при известковом методе ,
31, 103
-—i каустическом методе 158,174
производстве ИаСЮз 196,202
Высаливание КСЮз прибавкой КС1
16, 176
— NaCIOs прибавкей NaCl 186
Выход хлората при хлорировании
64, 65, 90, 167, 170, 318
— кристаллизации 126, 13В
Вязкость растворов KClOi 22
NaCIOs 189
— хлорированных щелоков 70
Газы, свойства 46
Гашение извести 42
Гербесиды 336
Гигроскопичность КСЮз и NaCIO*.
^ 21/206, 321
Гипосульфит, анализ 314
— — применение в производств
хлоратов 96, 150
Гипохлорит, анализ 307, 308 \
— образование 59, 162, 248
— расчет выхода 91
Графитовые электроды 272, 284
Графические таблицы,- см. Номограммы
Двойное хлорирование 72
Дезинтегратор Матодор 136
Декантеры 114 -
’Диссоциация СаСОз при обжиге 37
— КСЮз в растворе 22 '
— хлоратов в растворах 358
Доломиты 36
Дорра классификатор 52
Железа хлорат 238
Избыток КС1 при обменной реак- *
ции 16, 108, 120
Известковое молоко анализ 314 !т
получение и свойства 50
Известковый метод пр-ва КСЮз 29
NaCIOs 191
— Ba(C10e)t 216 /• , .
Известняк свойства и состав 36
— хлорирование 18$ >. х ;
364 : ' 'Ах / '
Известь анализ 313
— получение и свойства 38
Изменение объема при кристаллизаций 132, 208, 217
хлорировании 68, 168, 170
Итрия хлорат 235
Кадмия хлорат 232
Калий хлористый анализ 314
получение, свойства .48
применение в производстве
КСЮз 107
Калия определение 311
Калькуляция бертолетовой соли 154
Кальций хлористый плавленый 141
свойства 139
Кальцит 37
Кальция хлората получение 219,
283
свойства 218, 243, 361
Каталитическое разложение хло-
* ратов 23, 84, 106
Катодное восстановление СЮ и
СЮз 250, 264
Катоды для электролитического
•получения хлоратов 264'
Каустический метод получения
КСЮз 16, 156
NaCIOs 193
Качественные реакции на СЮз 25
Кислород — выделение при хлорировании 60, 61
•Кислотность — влияние на электролиз 260, 277
Классификатор Дорра 52
Классификация ванн для электролиза 284
Кобальта хлорат 238, 243, 361
Количественное определение СЮ*
27, 319, 348
Колонка для поглощения Ch 86,
340
Контроль произв. КСЮз 307
NaCIOs 324 (см. Анализы)
Коррозия аппаратуры 54, 105, 158,
196, 344, 346 v ч
<Коэфициенты обезвреживания 98
/ Коэфициенты получения Ва(СЮз)
217
—I— Са(С10з)2 220
М— КСЮз 146, 153, 178, 185, 285
' NaCIOs 207, 210
хлоратов электролизом 285
— хлорирования Са(ОН)2 68
— хлорирования NaOH и NatCO*
171
Кристаллизаторы прерывного действия 114
— Цана 113
Кристаллизация Ва(СЮз)* 215
— КСЮз 30, 112, 122, 175
— NaCIOs . 196, 202
Кристаллические формы* хлоратов
246
Лабораторная установка хлорирования 61, 357
Лабораторные опыты по свойствам КСЮа 26
Лабораторный контроль производства 307 ^
Либиха метод получения КСЮа
15, 29 .
Лития хлорат 221, 243, 362
Ловушка при выпарке 105
сушке бертсоли 136, 137
Магнезиальный метод пр-ва КСЮа
16, 180
NaClOa 191
Магнетитовые электроды 270, 284
Магнитная восприимчивость 358
Магнитный сепаратор 136
Магния хлорат 180, 191, 228, 242,
358
Марганца-хлорат 238
Материал для катодов 264
Маточники от производства КСЮа
121, 138, 176, 316
Меди хлорат 224, 242, 361
Меласса — применение в производстве хлоратов 97
Мельница для размоЛа бертсоли
136
Мергеля 36
Метод получения хлоратов Байера
v 16, 182, 193
—' Либиха 15, 28
Муспрата- 16, 180, 191
’Печинея 15, 24, 1919, 197
Мика аппарат 50, 54
Молекулярные веса хлоратов 242
Муспрата метод производства хлоратов 16, 180, 191
Натрия хлорат, анализ 324
— —•получение 186, 282
свойства 187,. 242, 358
Недопал 38, 51
Никеля хлорат 240, 243, 358
Номограммы и графич. таблицы
. 57, 68, 93, 125, 172, 175, 356
Нутч-фильтры 115, 122, 202, 204 , V
Обезвреживание от СЮ' 30, 94
Объема изменение при кристаллизации 132, 208, 217
хлорировании 68, 168, 170
Обжиг известняка 38 \ -
Обменная реакция Ca(ClOs)* с КС1 /
30, 107 '
—» КгСОз 107
Na*£04 Ю7, 191
NaClOa с Ва(СЮа)* 213
—КС1 158, 281
Обращая соль анализ М2
... — (получение при ,»р-вс KCIOi
158, 174
— - NaClOa 196, 202
Оксихлориды 34, 40, 66, 181, 200
. Окта гоны 74
7 Олова хлорат 236
Определение As 350
— Ва* * 325
— ВгОл' 321, 350
— Са*’ 310, 351 4
— СаО 307
— CV 309, 350
— СЮ' 307
— CIOs' 28, 309
— О*, СО*, О* !и Н* 314
Fe 351
— К* 311, 324 v
— Mg 351
/— Na* 313, 319 *
4 _ S04" 320, 350
(См. также анализ)
Оптическое вращение 358
Осмотическое давление 358
ОСТ на аммиачную воду 314
бертолетову соль 319, 348
гипосульфит 314
ОСТ на известь 313
плавленый хлористый кальций 319, 352
Отделение шлама от известкового
молока 52
хлорированных щелоков
99
Отстой известкового молока 56
/ — хлорированных щелоков 67,
100
Патент Байера 16, 182, 193
— Вельдона 180, 181
— Вильдермана 84
— Гаргривса 195
— Гаммила 15
— Муспрата 16, 180, 191
— Шульца 16
Патенты по электролизу, см.
Ванны
Перекристаллизация бертсоли 114,
158
— хлората натрия 197, 205
; Перхлората образование 22, 211,
: 231
Печи для обжига известняка 38
Печинея метод пр-ва КСЮэ 15, 24,
191, 197
Плавленый хлор, кальций 141, 154,
319, 352
Плотность раствора AgClOs 226
Bad* 145
’ Ва(СЮа)* 211
Be(ClOs)* 228
* CaClt 140
365
Плотное!». раствора Са(С10а)г 219
Сс1(СЮя)а 233
Со(СЮз)> 239
CsClOs 223
Си(С10з)г 224
— НСЮз 242
Hg(CI0s)2 234
КС1 49, 111
КС Юз 20
LiClO.i 222
Мк(С10я)з 229
NaC103 189 ,
Ni(C10»b 241 1
Sr<C10a)a 230
Zn(C103)2 231
Повышение температуры кипения
361
Понижение температуры замерзания 22, 222, 361
—1 упругости паров растворов
хлоратов 22, 189, 233, 361 \ '
Потеря хлора с абгазом 92
Потеря хлората баланс 149
при кристаллизации 132
отделении шлама 104
хлорировании 91
Поташ 107, 182
Потребители хлоратов 333
Промывка бертсоли 121 х
— обратной соли 203
— хлората натрия 204
Просеивание бертсоли 136
— извести 42
Пушонка 41, 56, 84
Разложение хлората ;в маточнике
127 f
: *при выпарке 106
нагрева 23
— хлоратов 242
Размол бертсоли 136
Рассол для электролиза 166, 281
Растворимость ВаСЬ в воде 145,
212
— CaCU в воде 140
в спирту 139
•— СаО в воде 40
—■ КСЮз в воде 20, 243 }
‘ в водных смесях спиртами
ацетона 21
в присутствии CaCU 124
КС1 126 ,
, КС1 и CaCU 127 1
К8СОз, KNOa, КОН,
MgClt 130
— —• NaCl 176
NaCl и KC1 176, 177
—,-r-1 NaClOa 130, 176
— NaClOa в воде 187, 189
в присутствии / Ва(СЮз)* 212
г NaCl 187, 188
— NaOH 204
/ /
Растворимость NaCl: и смесях ел ;:-
та и *поды 188
— хлора и поде и растворах NaCl
44
— хлоратов (сводная таблица) (см.
также Плотность) 243
Расчеты выхода кристаллизации
133
хлорирования 90, 318
— к-иа NH.i для обезвреживания
98
— •потери хлора с абгазом 92
— содержания Са и общ. хлора
91, 317
— состава бертолетовых щелоков
111
недохлорированиых щелоков 317
Реакции получения КСЮя 185
' NaCIO» (см. также Химизм)
210
Режим кристаллизации 116
— обезвреживания 98
— обменной реакции 109
— отделения шлама 101
— перекристаллизации 341
— ‘поглощения CU из абгаза 340
— сушки бертсоли 342
— хлорирования в абсорберах 337
башнях 339
Ртути хлорат 234, 342
Рубидия хлорат 223, 242
Русселя аппарат 53
Свинца хлорат 236, 243
Свойства газов, входящих в состав
хлоргаза 46
— извести 39
, — известняков 36
— хлора 43
, — хлората бария 211*
кальция 218
калия 18
натрия 187
— хлоратов (сводные таблицы) 242
' — хлористого бария 140
— — кальция 139
калия 50
Серебра хлорат 225, 242
Системы Са(С10з)*, KCI, CaCU,
КСЮз 130—132
Сита для бертсоли 136
Слабый каустик 158, 193
Содовый метод производства
КСЮз 159
NaC103 195
Состав абгаза 89
— бертолетовой соли 118, 319
— бертолетовых щелоков 111
— извести 39
— известкового молока 56
— известняков 36
366
/'
^*i\; о rv»'iii!>;\ то.мжоп 121
-.'.V? v » U' \ *op клльЦия 141
- V\v'i'! .:.u 4.“
-- \.u'pnpoiumu>!\ me u'koh 66, 79,
I ГД IS4
— хлористого калин 4S
Спичек производство*— потребитель хлоратов 233
Сравнение известковых методов
производства КСЮя 35
— - и каустических методов
165
электрохимических методов 286
— способов хлорирования в абсорберах и башнях 82
Стандарты — см. ОСТы
Степень диссоциации растворов
КСЮя 22
NaClOa 190
— хлоратов 361
Стронция хлорат 229, 242, 361
Суцгильный аппарат 134
Сушка бертолетовой соли 134, 137,
342
хлората натрия 197, 206
Схема кристаллизации КСЮз 117
— лабораторной установки хлорирования 357
Схема обменной реакции 110
— отделение шлама 101, 102
— получения извести 38
известкового молока 55 /
хлора, NaOH 43
хлората бария 214
кальция 220
— получения хлората калия известковым методом ЗР, 32, 33,
.«357 ' .
каустическим методом
157, 161
— содовым методом 160,
162
электрохимическим методом 281, 282
натрия известковым методом 192
каустическим методом
194
плавленого хлористого кальция 141
— хлористого бария 144
Тара для бертолетовой соли 138
Температура замерзания растворов
СаСЬ 140
—1 растворов хлоратов 358
хлорированных щелоков 70
Температура кипения растворов
CaClt 140 .
— — растворов хлоратов 358
—хлорированных щелокбв 70
Те v! ю;* л tv о а кристалл изпин
КО^ ПО, 1 >2. 174
NaCJO» 202
:«.*.имеинч хлор .поп 242
р мложеннч KOIOi 24
- ч.юрпронлннч tn, hi4
Тепловой эффект хлорирования
Са(ОН)з 61
СаСОя 1S5
- - NaOH и Na>COn 164
Теплота образования 358
--- удельная 222, 35S
Техника безопасности 325
Увлажняемость бертсоли 206, 321
— хлората натрия 206
Углекислота получение из СаСОя
38
— при хлорировании растворов
Na»COs и КгСОя 159, 183
—(свойства 46
Угольные электроды 272
Удельная теплота 222, 261
Удельные веса хлоратов 242
Удельная электропроводность 20,
244
Уменьшение объема при кристаллизации 132, 208, 217
Упругость паров растворов хлоратов 22, 233, 358
Урана хлорат 238
Утилизация КСЮя из маточников
145 '
Феррат кальция 67
— натрия 158
Физико-химические свойства, см.
Свойства
Физиологические свойства хлора
326
хлоратов 25
Фильтрпресса 100
Фильтрпрессный шлам 103, 318
Химизм обезвреживания 95
— обменной реакции 107
— хлорирования взвеси в воде
Ва(ОН)2 216
Са(ОН)2 58
СаСОя 183
MgO 180
ZnO 182
растворов К2СО3 182
NaOH 163
ИазСОз 163
— электролитического образования
хлоратов 248
Хлораты — сводные таблицы
свойств 242—4, 358
Хлоринатор 87
Хлорирование в абсорберах 77,
337
\
367
Хлорирование в башнях барботажем 90, 339
Вильдермаиа 84
— в лабораторной установке 61,
357
— методом распыления 86
Хлорирования реакции — см. Химизм
Хлорноватая кислота 241
Хрома хлорат 237
Хромат — защита от восстановления 260, 264
Хромирование катодов 267
Цезия хлорат 223 ^ /
Центрофуги 114, 122, 204
Цинка хлорат 231, 242, 358
Циркония хлорат 236
Шадиэры 32
Шедднты 334
Шлам от и;нкч Iсомого м - •>, \ *
хлорированных щелоков 9ч
Штат производства бсртсоли 154
Шультеса аппарат 41, 55
Щелочь* как защита от коррозии
196, 346
Электролиз в кислом среде 257
нейтральной среде 24S
щелочной среде 254
— с графитовыми анодами 272
магнетитовыми анодами 270
платиновыми анодами 248
Электролитическое получение СЬ,
NaOH и Н8 43
хлоратов 17,\ 248
Электропроводность КСЮ* 20
— растврров хлоратов 244
Эрбия хлорат 235