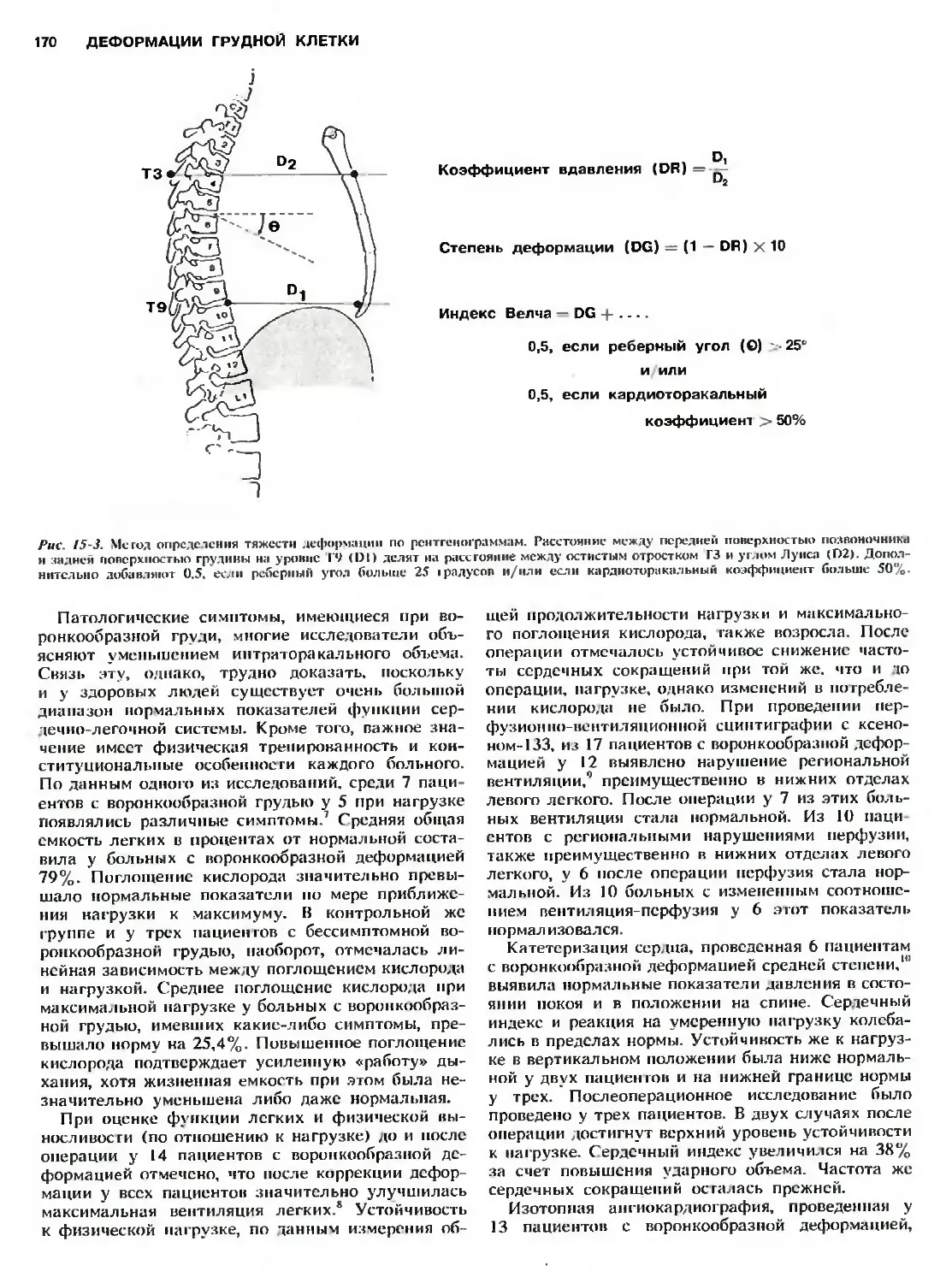
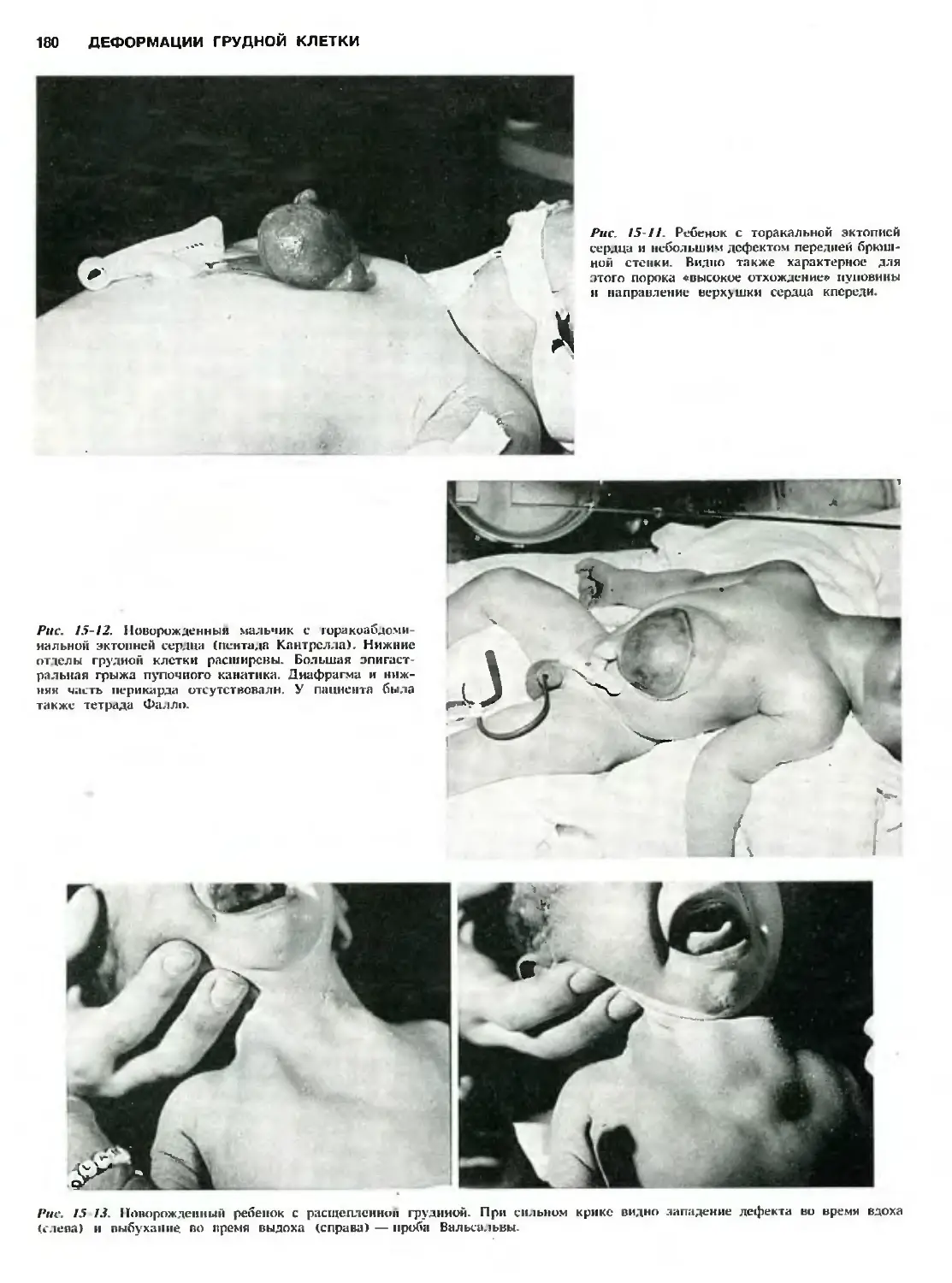
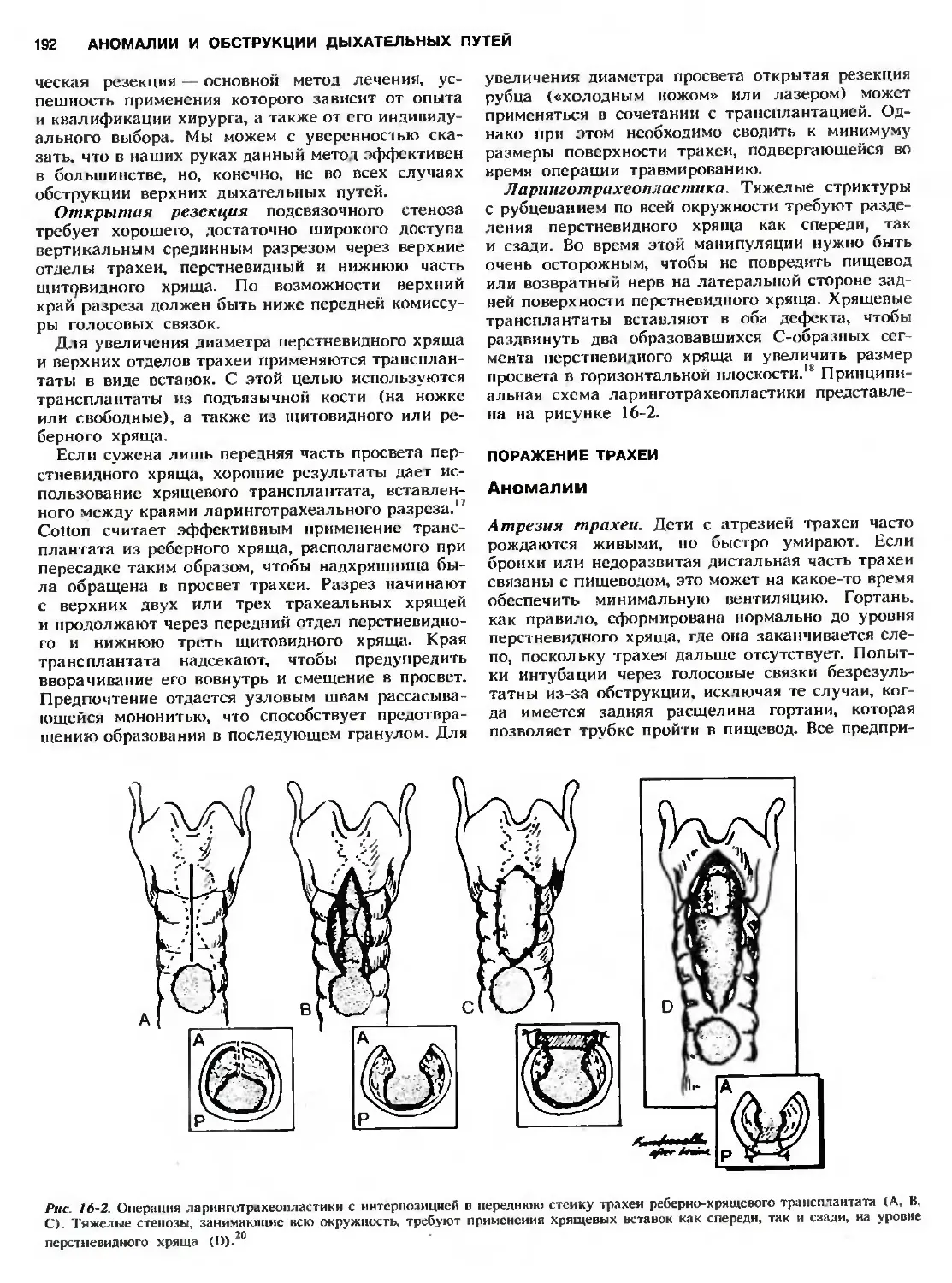
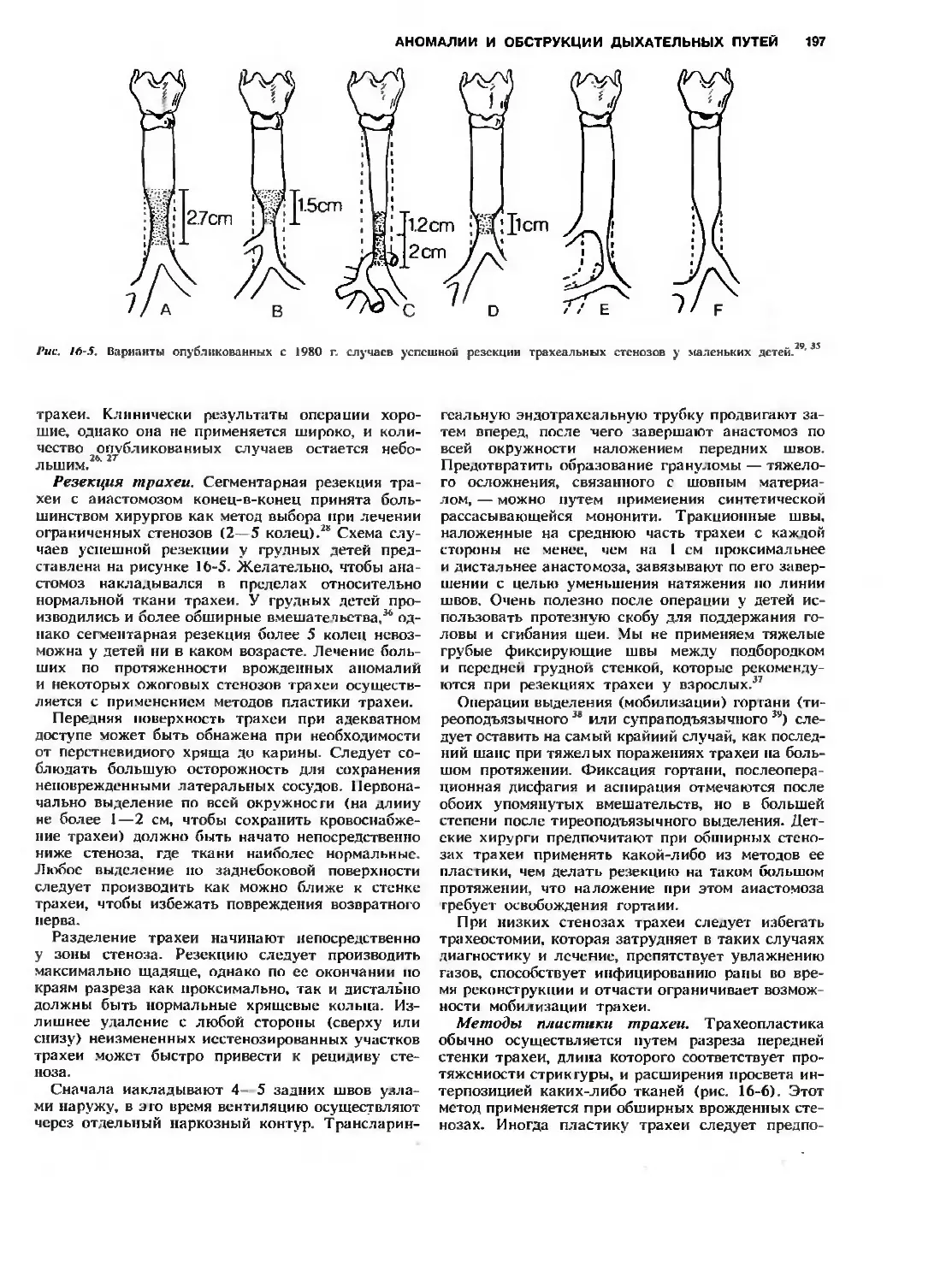
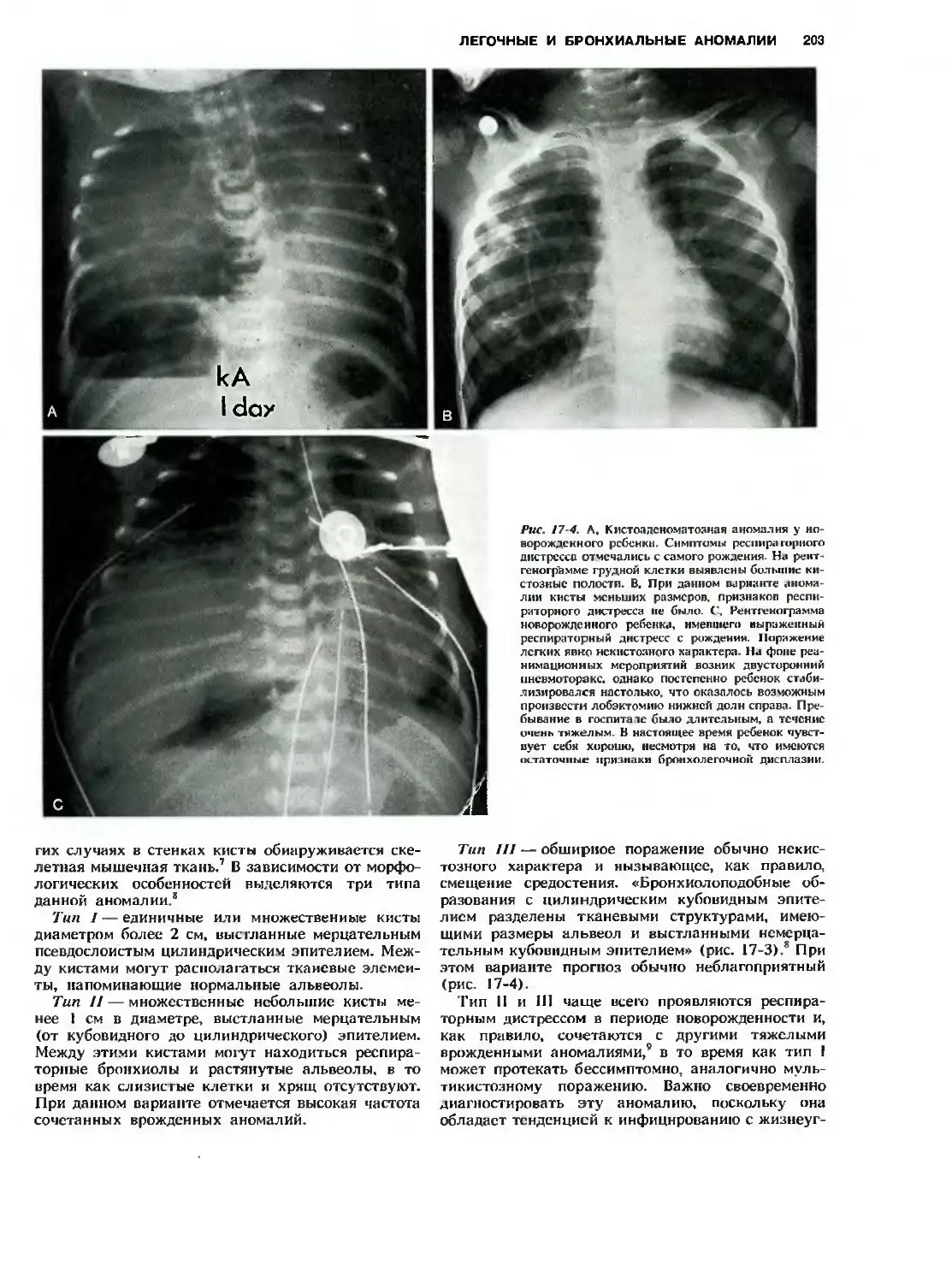
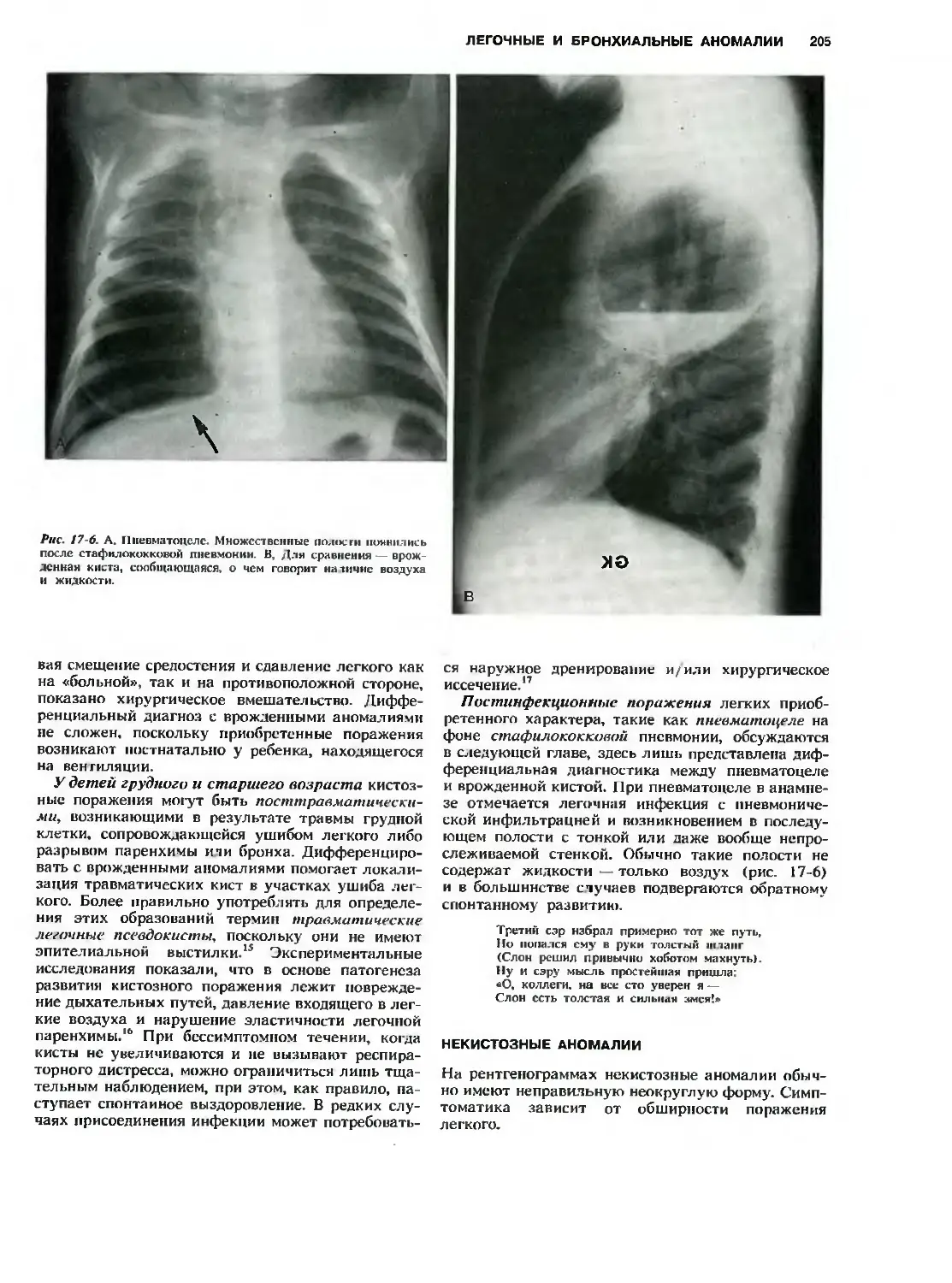
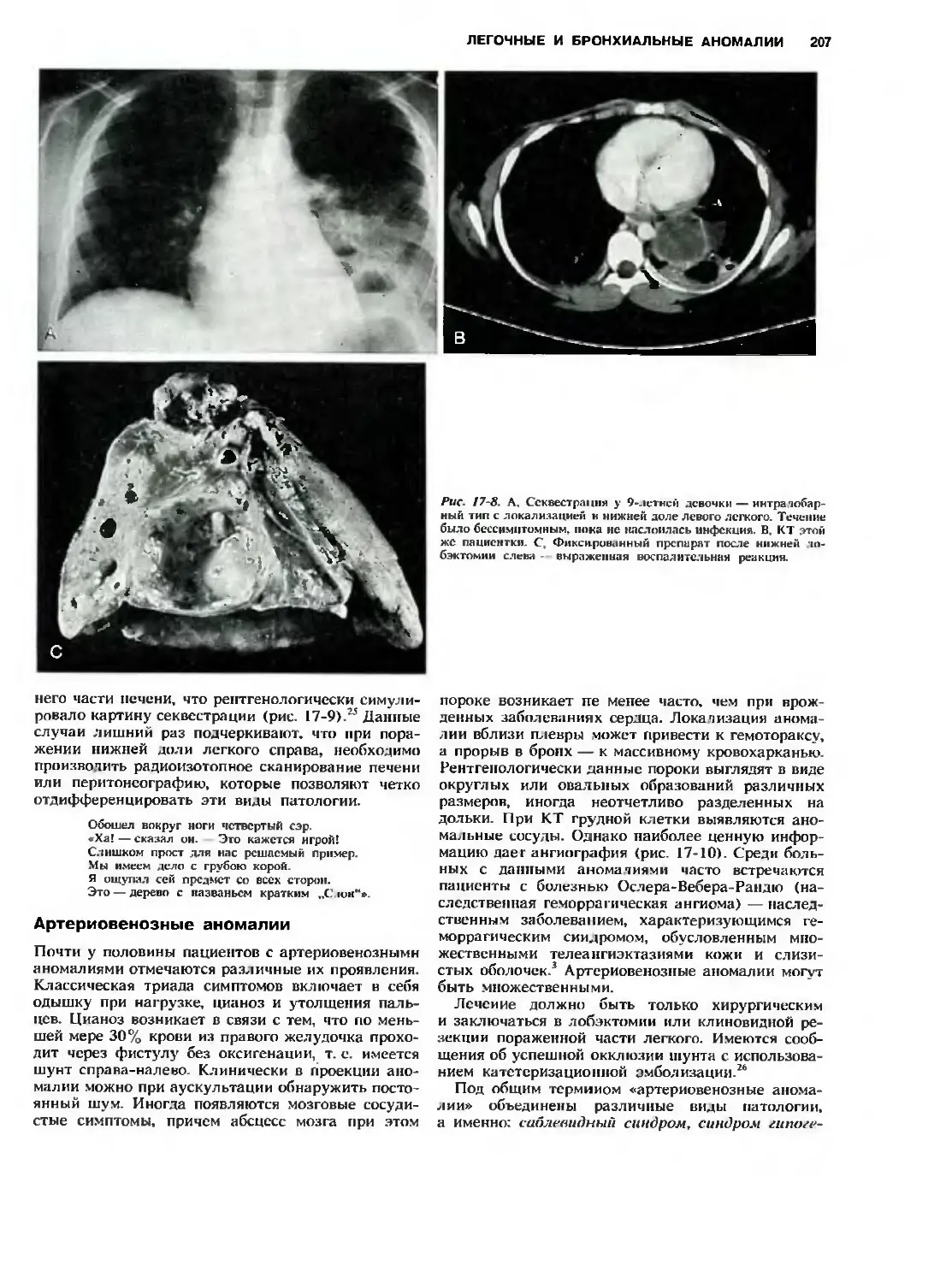
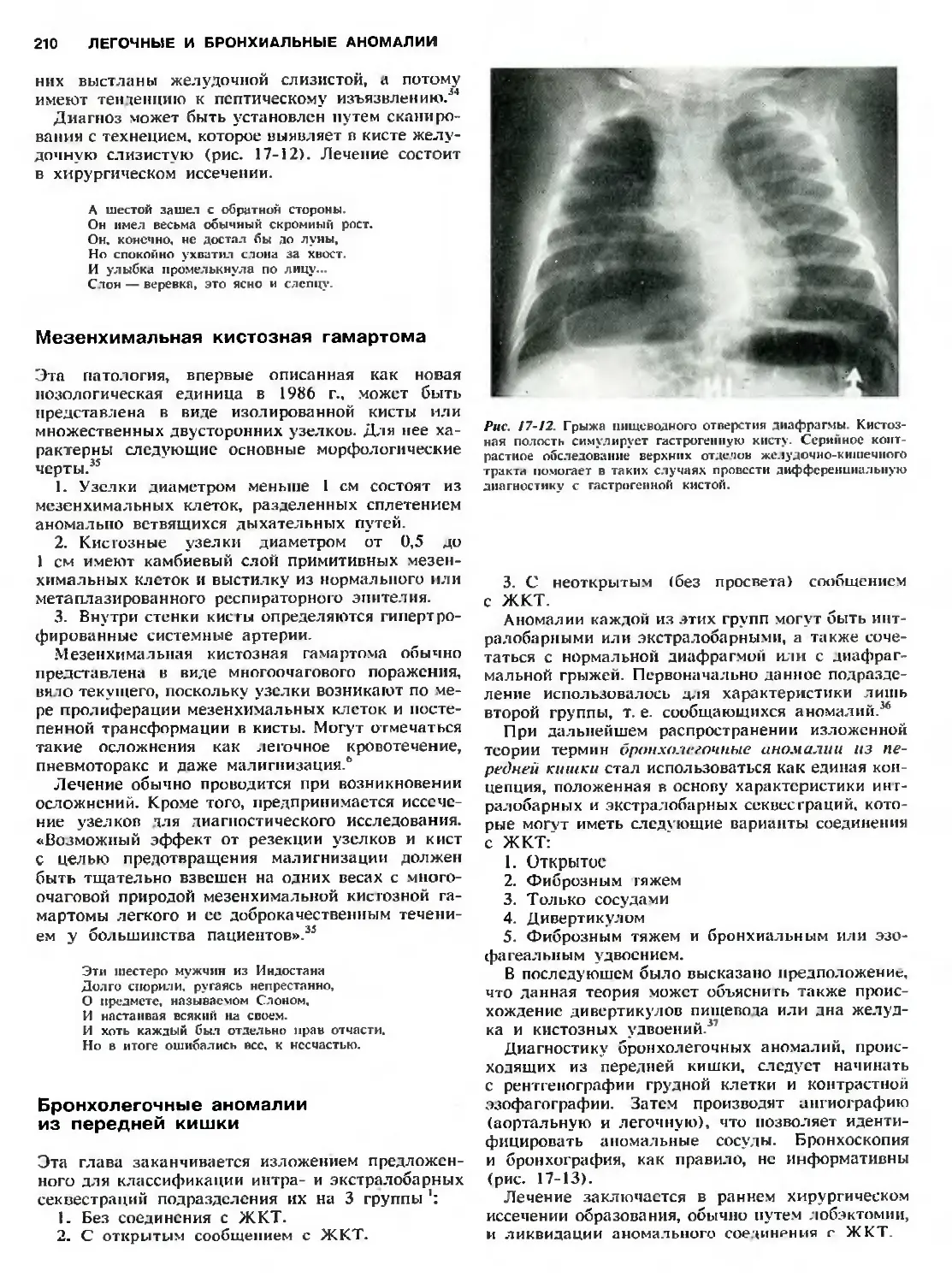
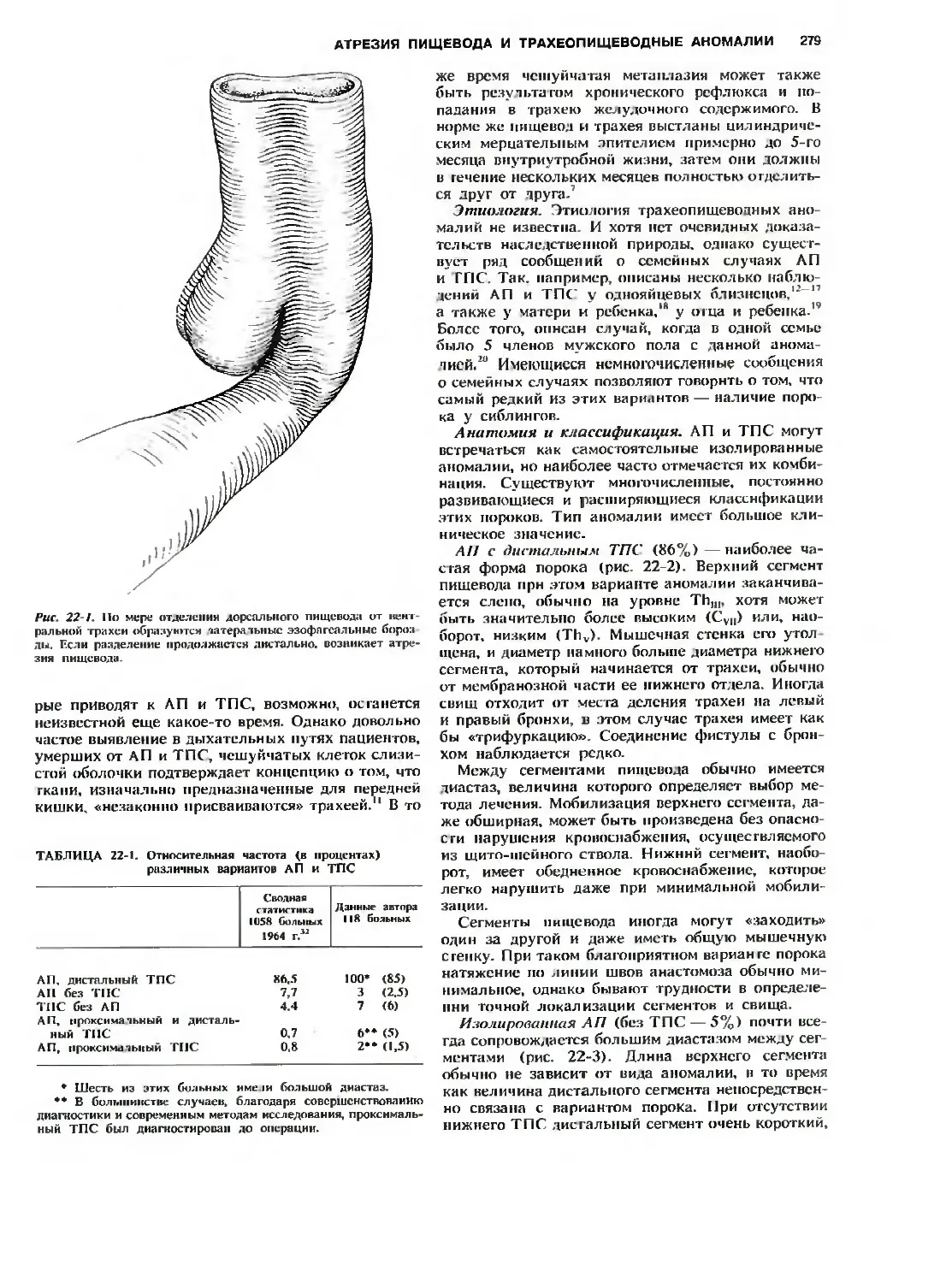
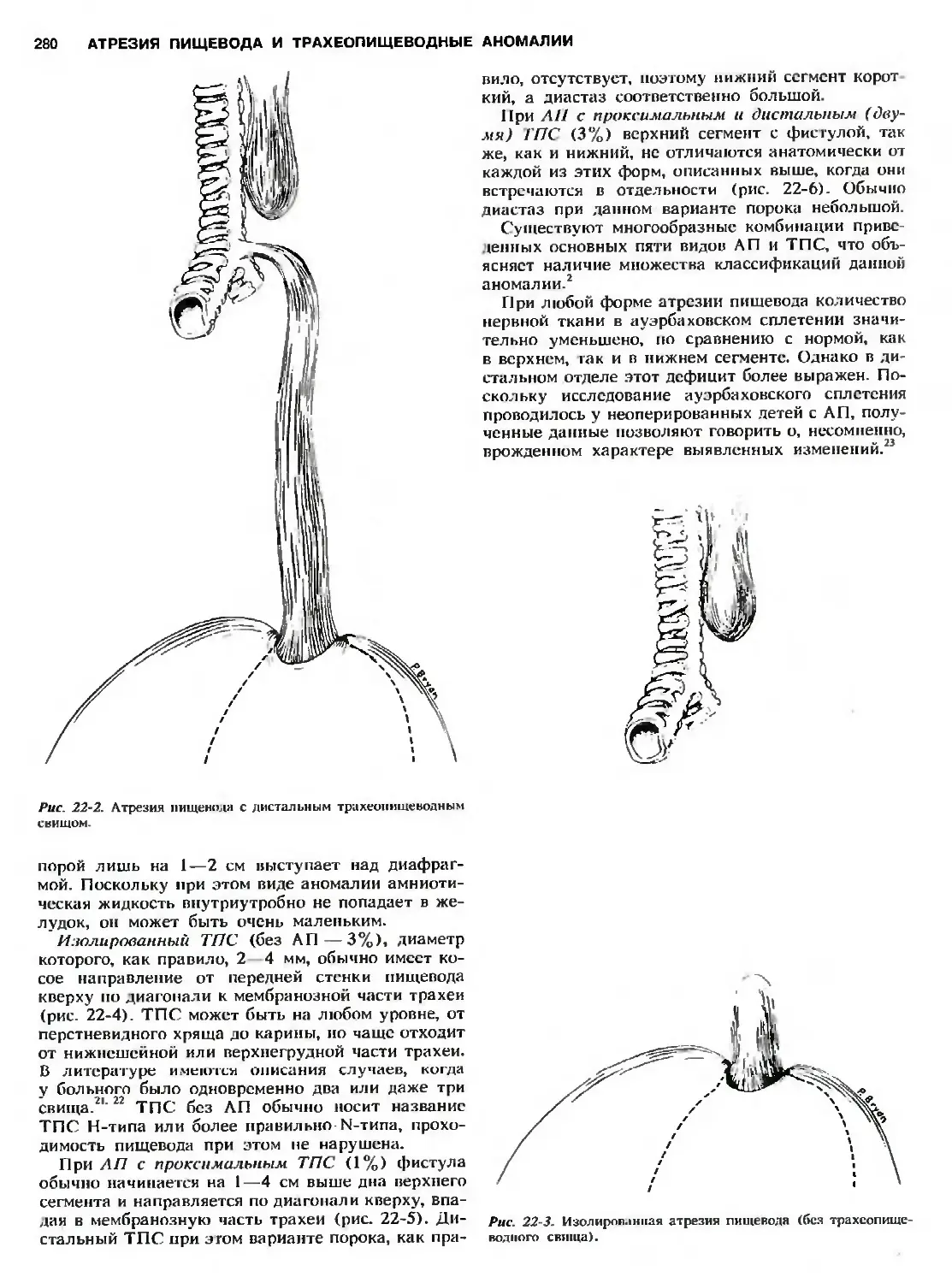
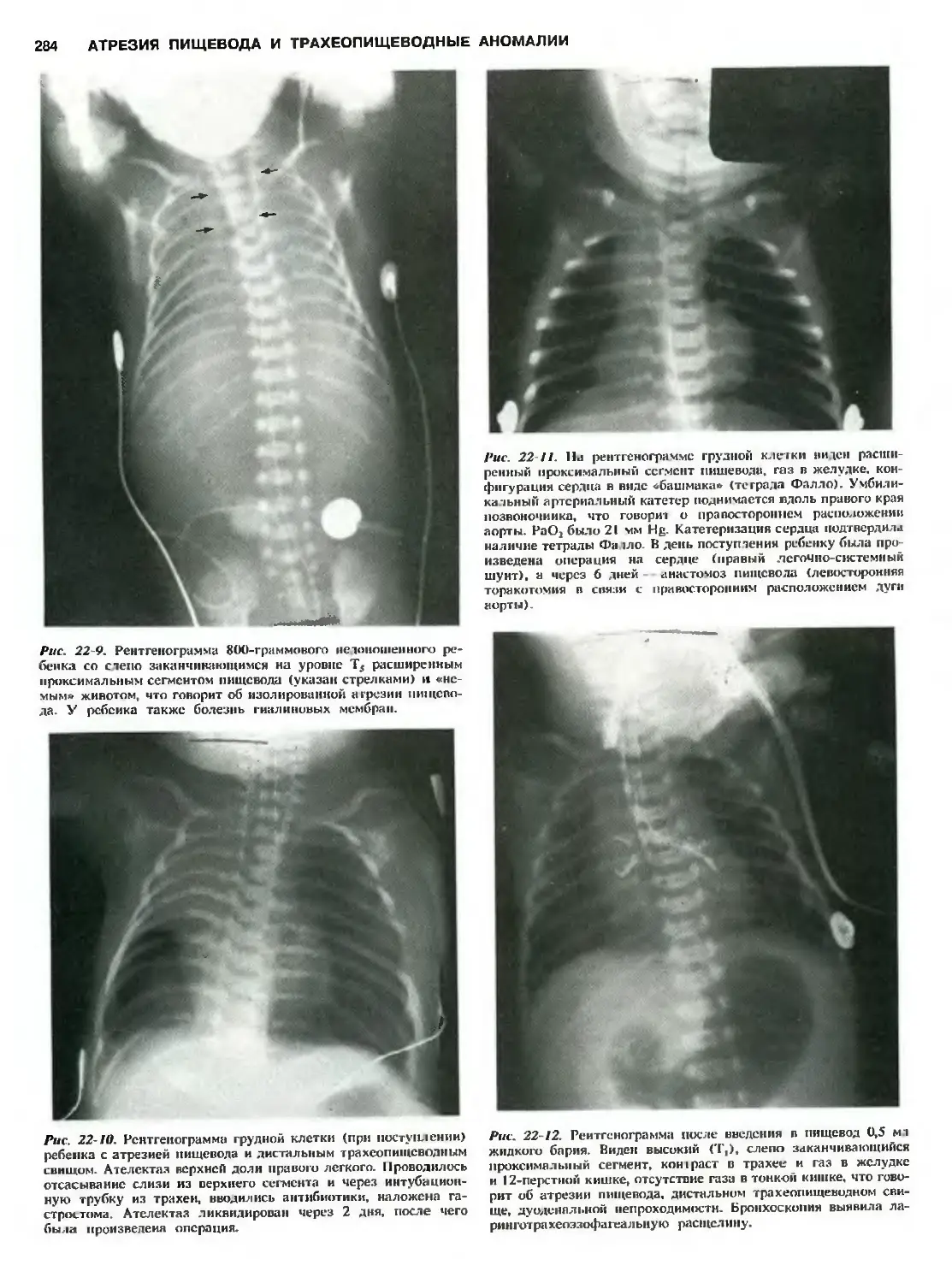
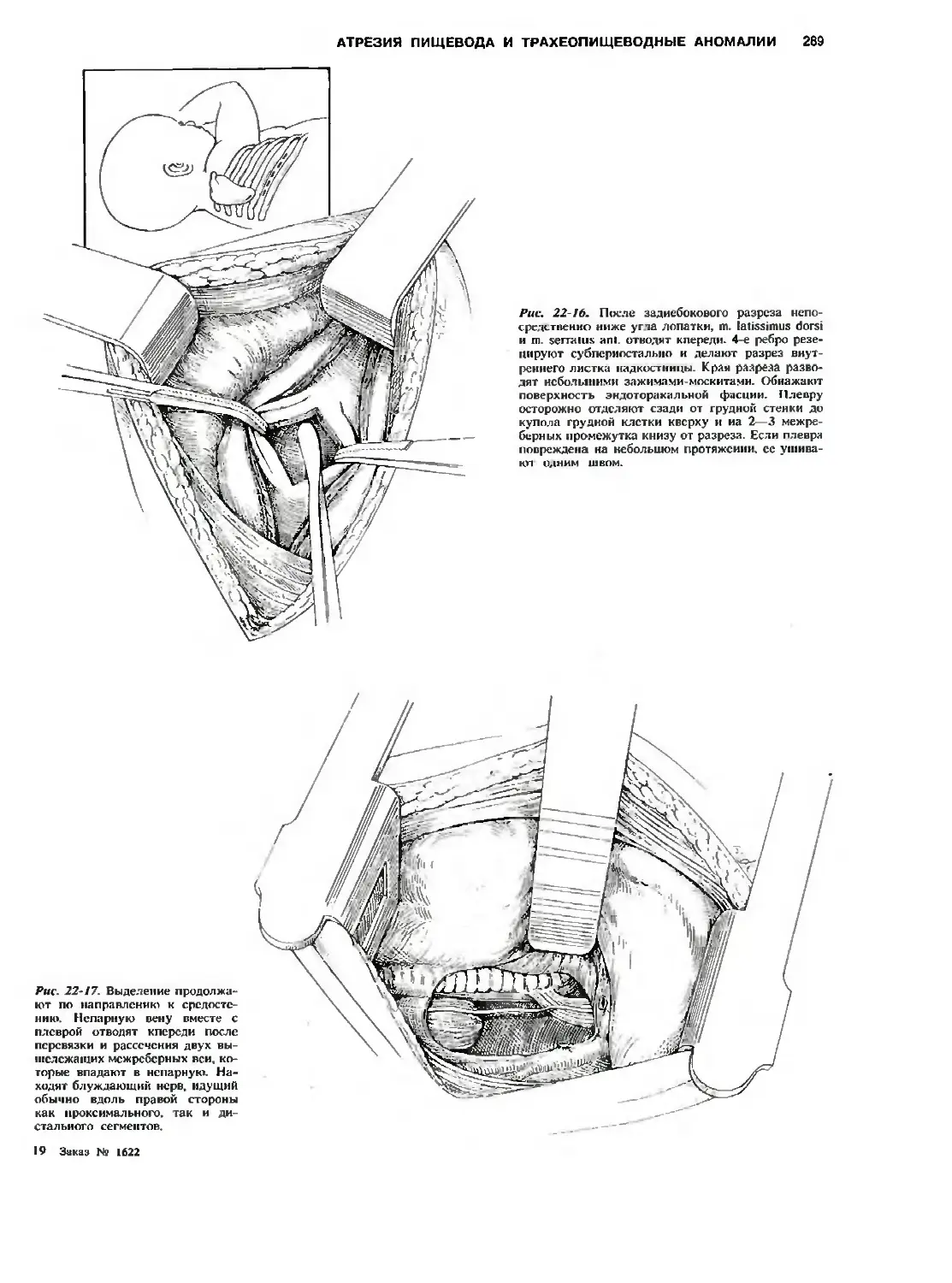
Автор: Холдер Т.М. Ашкрафт К.У.
Теги: медицина хирургия практическая медицина педиатрия детская хирургия
ISBN: 5-90131-10-10
Год: 1996
Текст
К. У. Ашкрафт, Т. М. Холдер
ДЕТСКАЯ ХИРУРГИЯ
Первое издание на русском языке
ИЧП «Хардфорд»
Санкт-Петербург
1996
Перевела и подготовила к изданию на русском языке
канд. мед. наук Т. К. Немилова
Детская хирургия. — СПб., Хардфорд. 1996. — 384 с.
ISBN 5-90131-10-10
Руководство охватывает все разделы детской хирургии. В его напи-
сании принял участие большой коллектив авторов — наиболее известных
специалистов в США. в каждой конкретной области детской хирургии.
Издание на русском языке осуществляется в трех томах.
В первом томе представлены вопросы физиологии ребенка, питания,
методов обезболивания и вентиляции легких, нарушений функции почек
при хирургической патологии. Широко освещены вопросы всех видов
травмы (за исключением повреждений опорно-двигательного аппарата).
Несколько глав посвящены проблемам торакальной хирургии (деформации
грудной клетки, диафрагмальные грыжи, врожденная и приобретенная
патология дыхательных путей, легких и плевры, опухоли средостения).
Включены также вопросы хирургии пищевода, желудка, пороков развития
кишечника, мекониевой болезни. В отдельной главе подробно рассматри-
вается проблема гастроэзофагеального рефлюкса.
Каждая глава снабжена большим количеством ярких иллюстраций,
а также обширным библиографическим указателем.
Руководство предназначено для детских хирургов, педиатров и врачей
всех специальностей, принимающих участие в диагностике хирургической
патологии у детей и ее лечении.
ЛР № 032244 от 03.12.93 г.
Сдано в набор 07.02.96. Подписано в печать 09.04.96 г. Формат 60X90 */г
Бумага мелованная. Гарнитура Тип Таймс. Печать офсетная. Усл. печ. л. 48.
Тираж 5000 экз. Заказ No 1622.
ИЧП «Хардфорд», Санкт-Петербург, пр. Космонавтов, д. 19.
П111 < Печатный Двор» Комитета Российской Федерации по печати.
197110, Санкт-Петербург, Чкаловский пр., 15.
ISBN 5-90131-10-10
© Перевод Немилова Т. К., 1996
© Издательство «Хардфорд», 1996
© СП «Пнг — Тал», 1996
Оглавление
Глава / Физиология ребенка. 5. D. Smith,
М. I. Rowe II
Новорожденные с низкой для срока
гестации массой тела II
Недоношенные дети II
Физиологические особенности новорожденных
детей 1I
Жидкость и электролиты 15
Легочная и сердечно-сосудистая системы
новорожденного 17
Шок 22
Глава 2. Энтеральное и парентеральное питание.
A. G. Согап 29
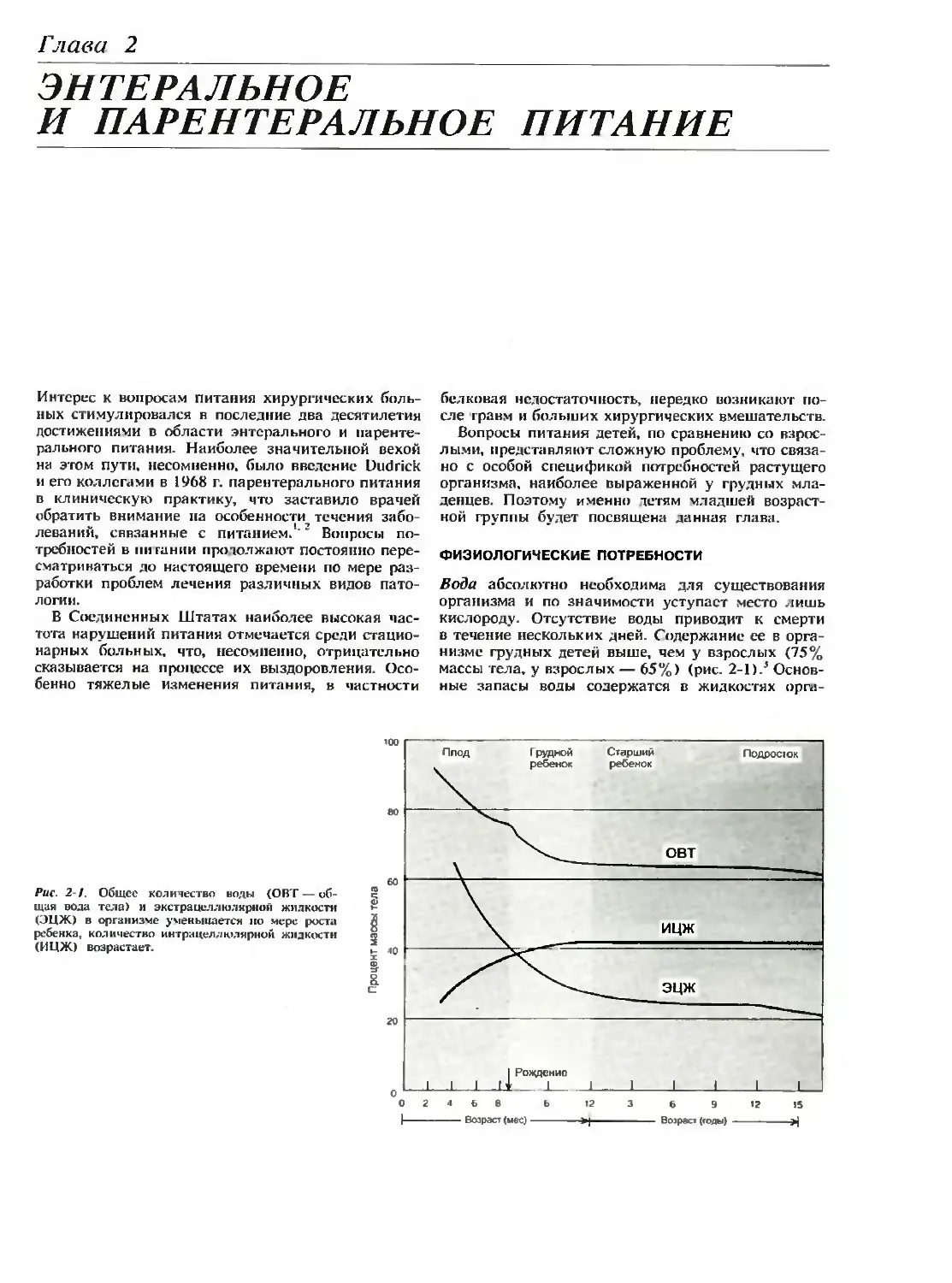
Физиологические потребности 29
Гормональная и метаболическая реакция на
стресс у новорожденных 31
Оценка состояния питания 33
Энтеральное питание 36
Полное парентеральное питание 38
Контроль за проведением питания 43
Осложнения парентерального питания 45
Синдром короткой кишки 48
Парентеральное питание в домашних
условиях 49
Глава 3. Методы обезболивания. R. Е. Binda,
Р. Н. Mestad 52
Предоперационная подготовка 52
Анестезия при амбулаторных операциях 53
Ведение амбулаторных больных
в послеоперационном периоде 54
Особенности обезболивания у недоношенных
детей 55
Мониторинг 55
Боль 57
Глава 4. Искусственная вентиляция легких.
Р. В. Manning 60
Физиология легких 60
Оценка больного 63
Мониторинг и способы вентиляции 64
Искусственная вентиляция 67
Осложнения 70
Глава 5. Нарушение функции почек.
S. Hellerstein, U. Alon, В A. Warady 72
Регуляция содержания воды в организме 72
Оценка функции почек 73
Лечение больных с послеоперационным
нарушением функции почек 75
Острая почечная недостаточность
у новорожденных 78
Обструктивные уропатии 80
Глава 6. Этические проблемы в детской хирургии.
A. Shaw, /. A. Shaw 82
Глава 7. Укусы. Ch. W. McGill 86
Столбняк 86
Укусы собак и бешенство 86
Укусы змей 88
Человеческие укусы 91
Укусы перепончатокрылых насекомых 91
Укусы коричневого паука 92
Укусы черного паука 93
Глава 8. Инородные тела. S. L. Gans,
Е. Austin 95
Инородные тела гортани 95
Инородные тела трахеобронхиального
дерева 95
Инородные тела пищевода 97
Инородные тела желудочно-кишечного
тракта 98
Безоары 100
Инородные тела кожи и мягких тканей 100
Глава 9. Ожоги. R. J. Sharp 102
Оценка ожоговой травмы и классификация
ожогов 105
Инфузионная терапия 106
4
ОГЛАВЛЕНИЕ
Питание больного с ожогом IU6
Местное лечение ожоговых ран 107
Обезболивание 108
Хирургическое лечение 108
Поражение дыхательных путей 111
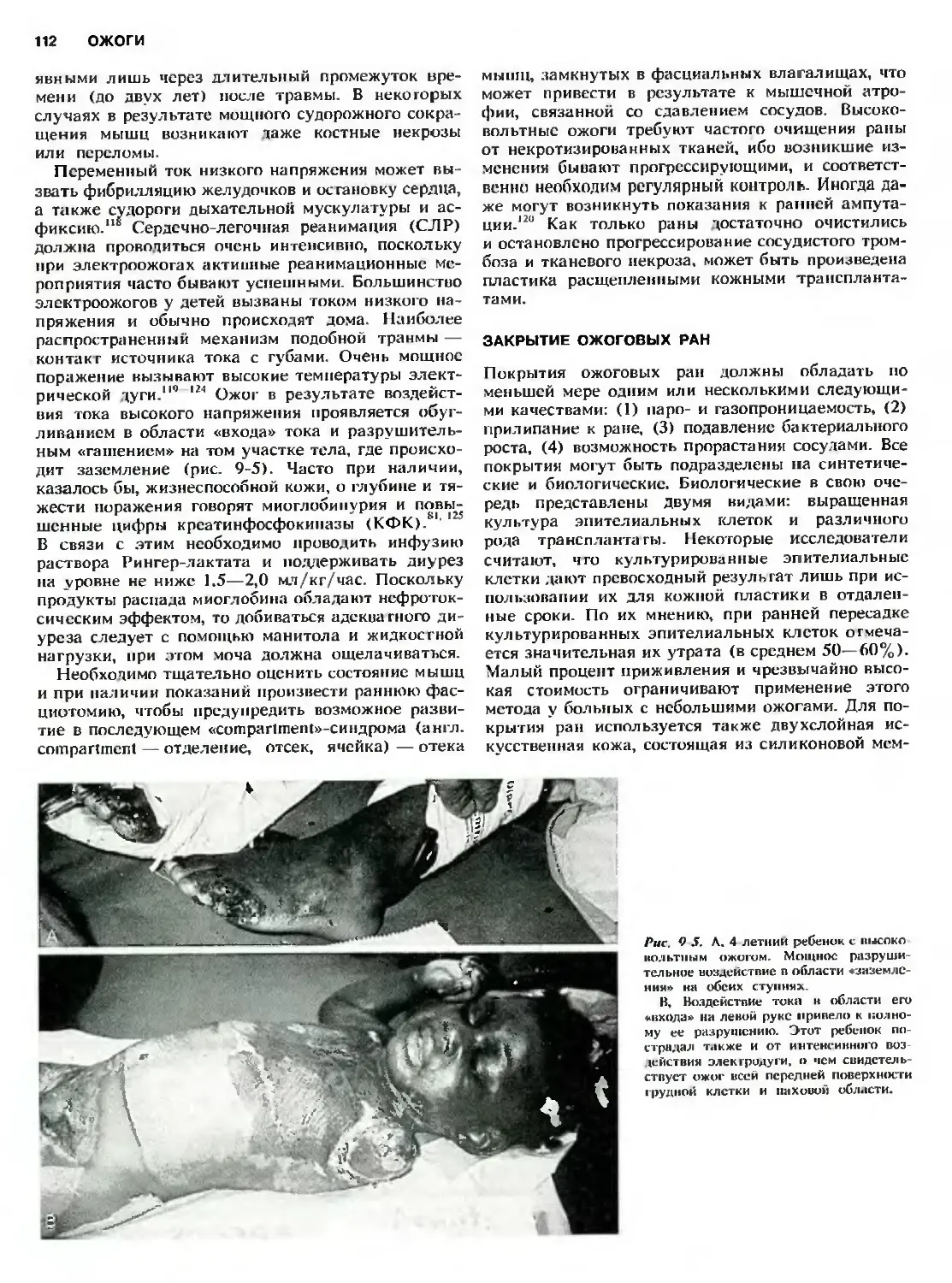
Электроожоги 111
Закрытие ожоговых ран 112
Реабилитация 113
Осложнения 113
Прогноз и профилактика 114
Глава 10. Эпидемиология травмы. 13. L. Heaver,
J. A. Haller 118
Летальность при травмах 119
Механизмы травмы и профилактика 120
Служба неотложной медицинской помощи
детям 122
Профилактика травматизма 124
Этические проблемы «Положения о смерти
и искусственном поддержании жизни» 125
Глава 11. Оценка и лечение травмы в остром
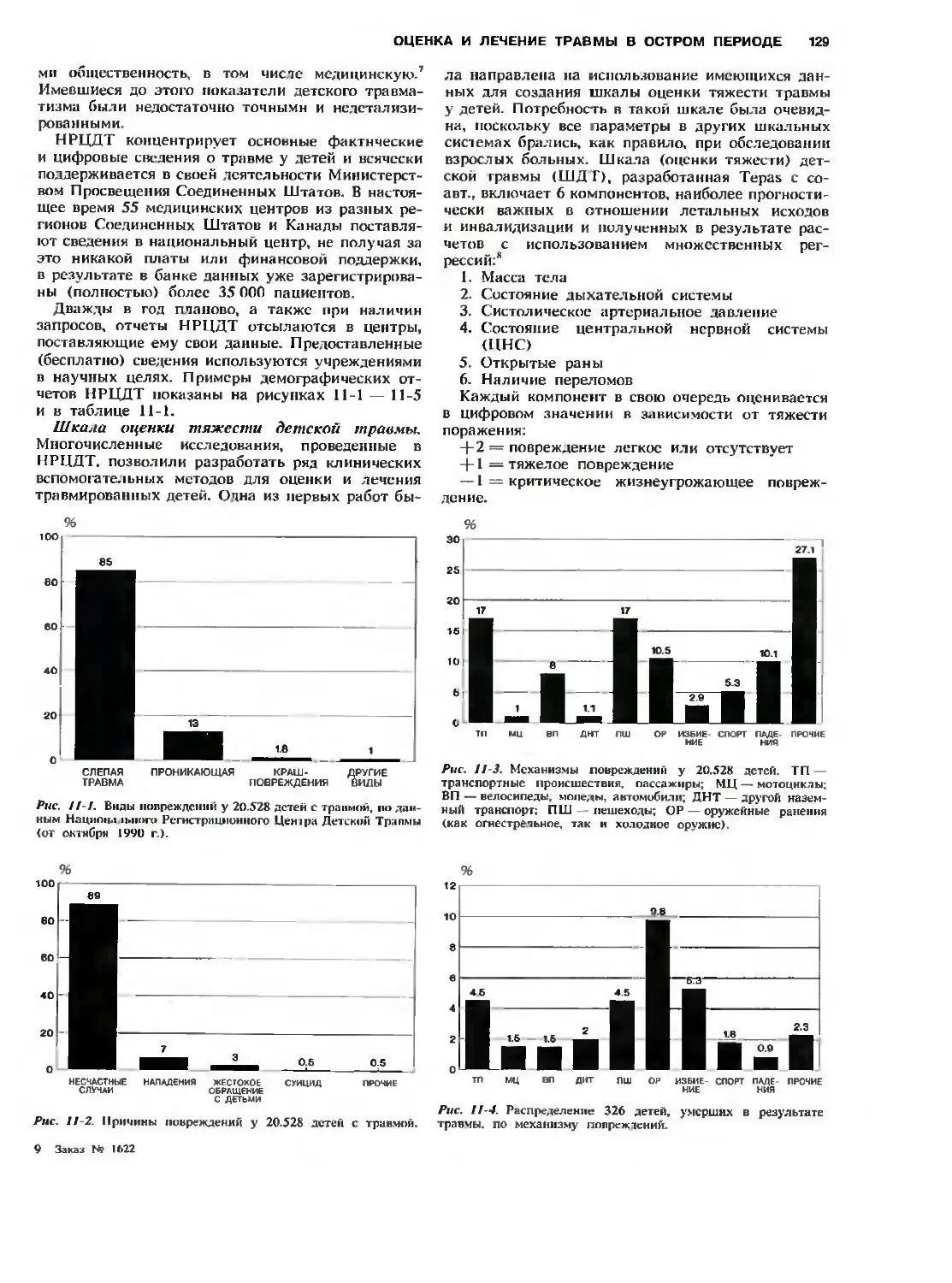
периоде. М. L. Ramenofsky 127
Национальный регистрационный центр
детской травмы 128
Предварительное планирование экстренной
помощи детям при травме 131
Начальная оценка ребенка с травмой:
первичное обследование 132
Вторичное обследование 136
Окончательная постановка диагноза и выбор
метода лечения 138
Заключение 139
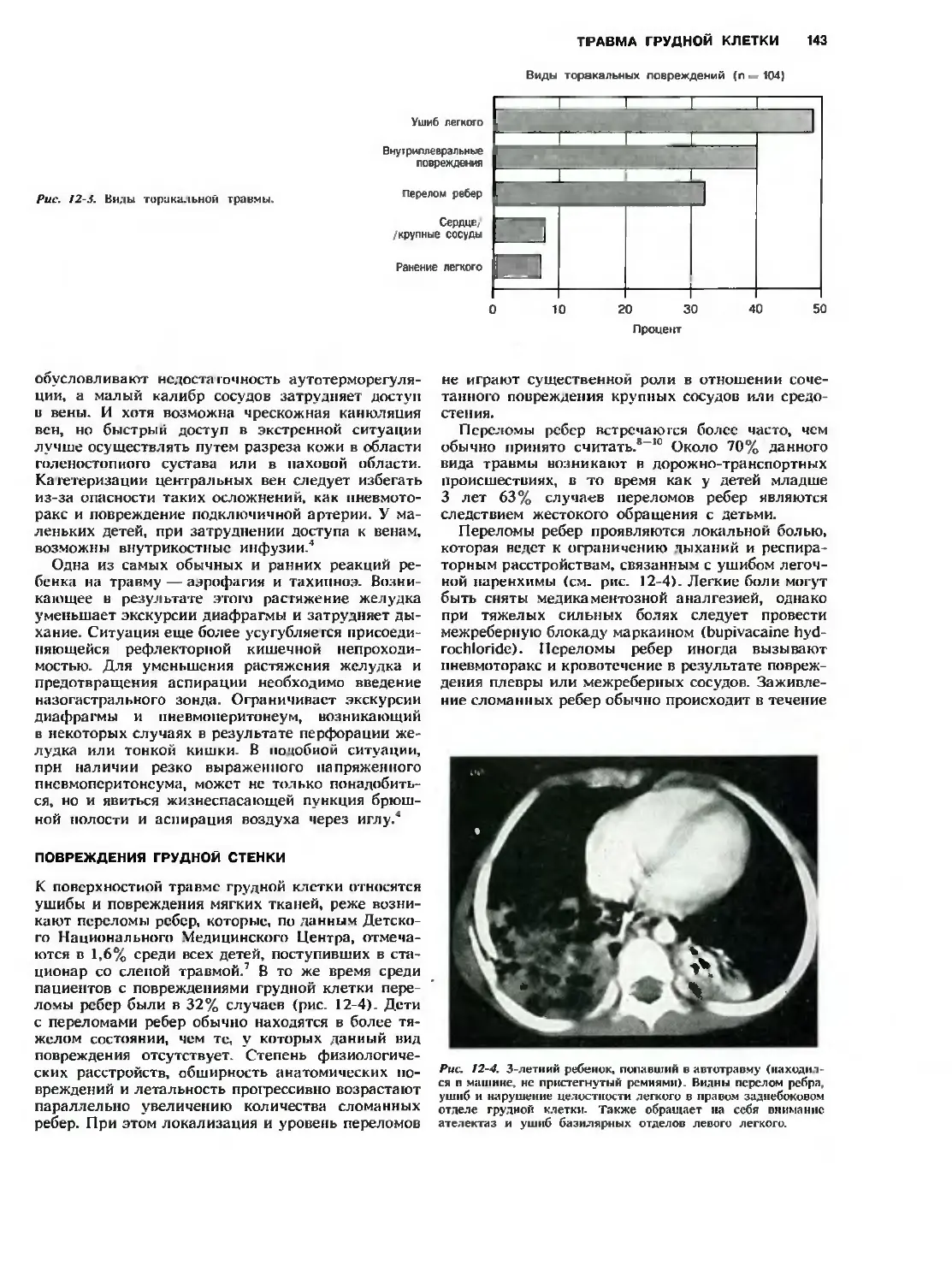
Глава 12. Травма грудной клетки.
М. Eichelberger 141
Повреждения грудной стенки 143
Ушиб легкого 144
Внутриплевральные повреждения 146
Хилоторакс 148
Повреждения трахеи и бронхов 148
Травматическая асфиксия 148
Повреждения аорты 149
Сердце 149
Диафрагма 150
Повреждение грудной клетки
у новорожденных 150
Глава 13. Травма живота и мочевых путей.
М. Peclet, Р. Murphy 153
Селезенка 154
Печень 155
Поджелудочная железа и 12-перстная
кишка 156
Повреждение полых органов 157
Проникающие ранения 157
Травма почек 158
Повреждение мочеточников 159
Повреждение мочевого пузыря 159
Повреждение уретры 159
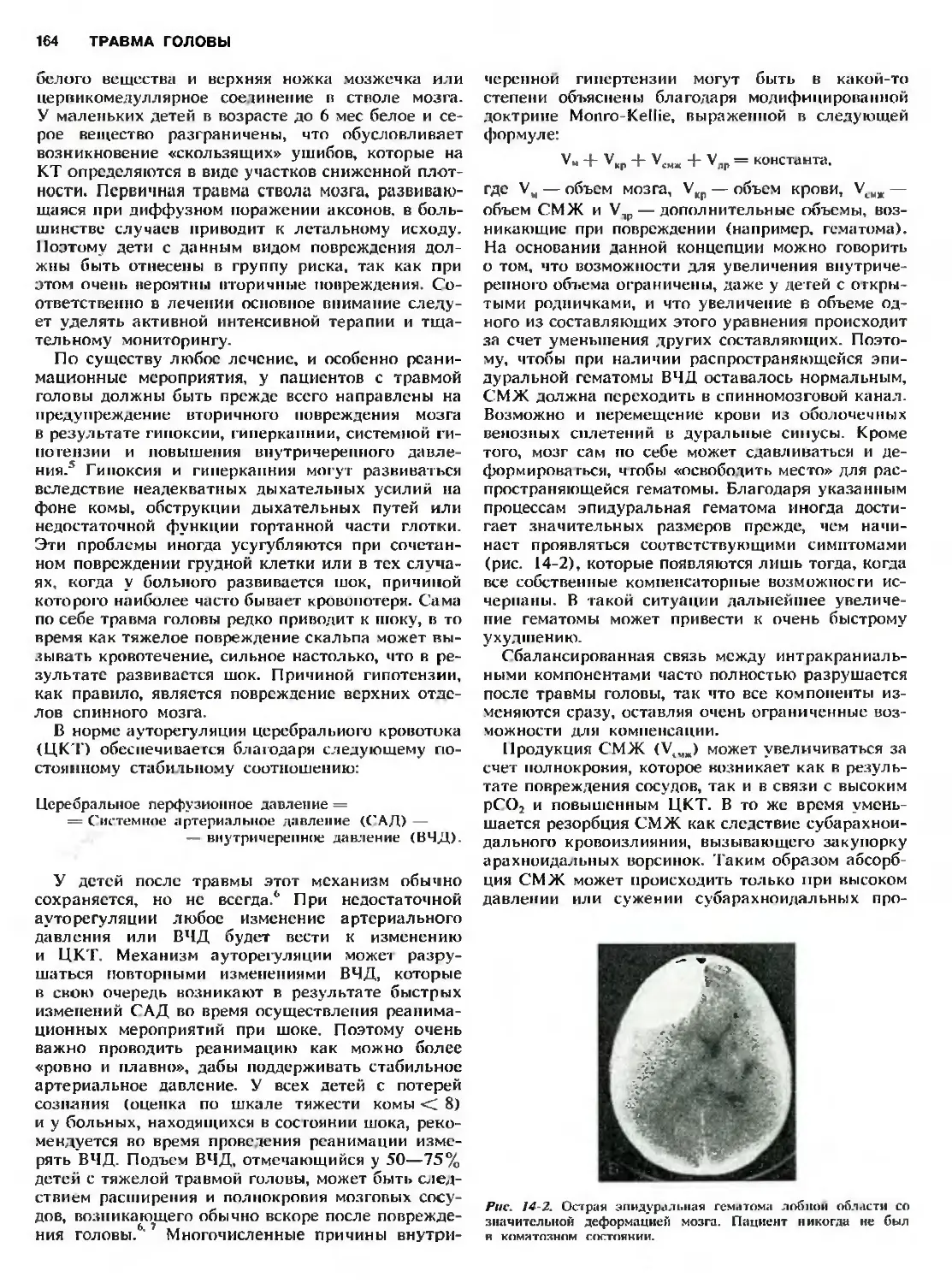
Глава 14. Травма головы. D. A. Bruce 162
Обследование, реанимация, лучевые методы
исследования 165
Хирургическое лечение 166
Неоперативное лечение 166
Результаты 167
Глава 15. Деформации грудной клетки.
R. С. Shambcrger, К. J. Welch 168
Воронкообразная грудь 168
Килевидная деформация грудной клетки 174
Синдром Поланда 176
Дефекты грудины 176
Деформации грудной клетки при диффузных
скелетных расстройствах 181
Асфиксическая торакальная дистрофия
(болезнь Jeune) 181
Спондилоторакальная дисплазия (синдром
Jarcho-Levin) 183
Глава 16. Аномалии и обструкции дыхательных
путей. D. G. Johnson 185
Атрезия хоан 185
Интраоральная обструкция 185
Обструкция гортани 186
Аномалии 186
Кисты и опухоли 186
Приобретенные обструкции 187
Диагностика 189
Хирургические вмешательства
и результаты 189
Поражение трахеи 192
Аномалии 192
Приобретенные обструкции трахеи 194
Диагностика структурных
аномалий 195
Хирургические вмешательства
и результаты 195
Глава 17. Легочные и бронхиальные аномалии.
В. Othersen 200
Кистозные аномалии 200
Врожденные аномалии 200
Приобретенные аномалии 204
Некистозпые аномалии 20г5
Секвестрация легкого 206
Артериовенозные аномалии 207
Смешанные аномалии 209
Агенезия легкого 209
Гастрогенные кисты 209
Мезенхимальная кистозная гамартома 210
ОГЛАВЛЕНИЕ 5
Бронхолегочные аномалии из передней
кишки 210
Дальнейшие направления в диагностике
и лечении 211
Глава 18. Приобретенные заболевания легких
и плевры. R. L. Telander, С. R. Moir 213
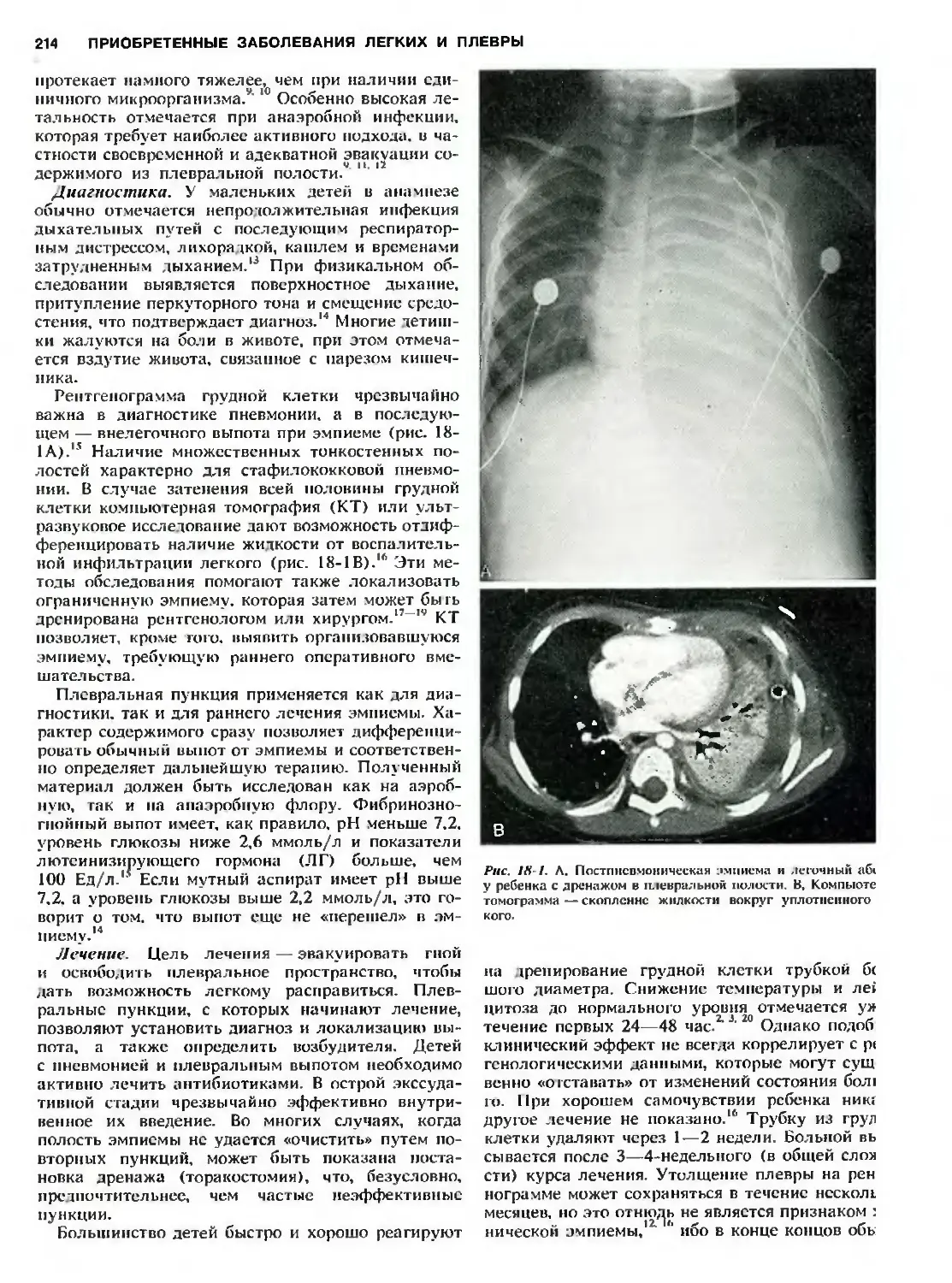
Эмпиема 213
Пневматоцеле 216
Бронхоэктазы 217
Абсцесс легкого 219
Хилоторакс 220
Кистофиброз 221
Легочный туберкулез 222
Поражение, вызванное атипичной
микобактерией 222
Актиномикоз 222
Нокардиоз (атипичный актиномикоз) 222
Гистоплазмоз 223
Диффузные легочные заболевания 223
Идиопатические хронические
интерстициально-альвеолярные
пневмонии 225
Глава 19. Диафрагмальные грыжи.
A. A. de Lorimier 229
Врожденная диафрагмальная грыжа
(ВДГ) 233
Ретростернальные грыжи 240
Эвентрация диафрагмы 240
Глава 20. Опухоли средостения.
W. J. Pokorny 244
Опухоли паравертебральной борозды 246
Опухоли центрального средостения 247
Опухоли переднего средостения 249
Тератома и дермоид 251
Опухоли, локализующиеся в любом отделе
средостения 252
Г зава 21. Пищевод. К. W. Aschcraft 255
Химические ожоги пищевода 255
Инородные тела пищевода 258
Врожденный стеноз пищевода 261
Функциональные расстройства пищевода 261
Стриктуры пищевода 263
Послеожоговые стенозы 263
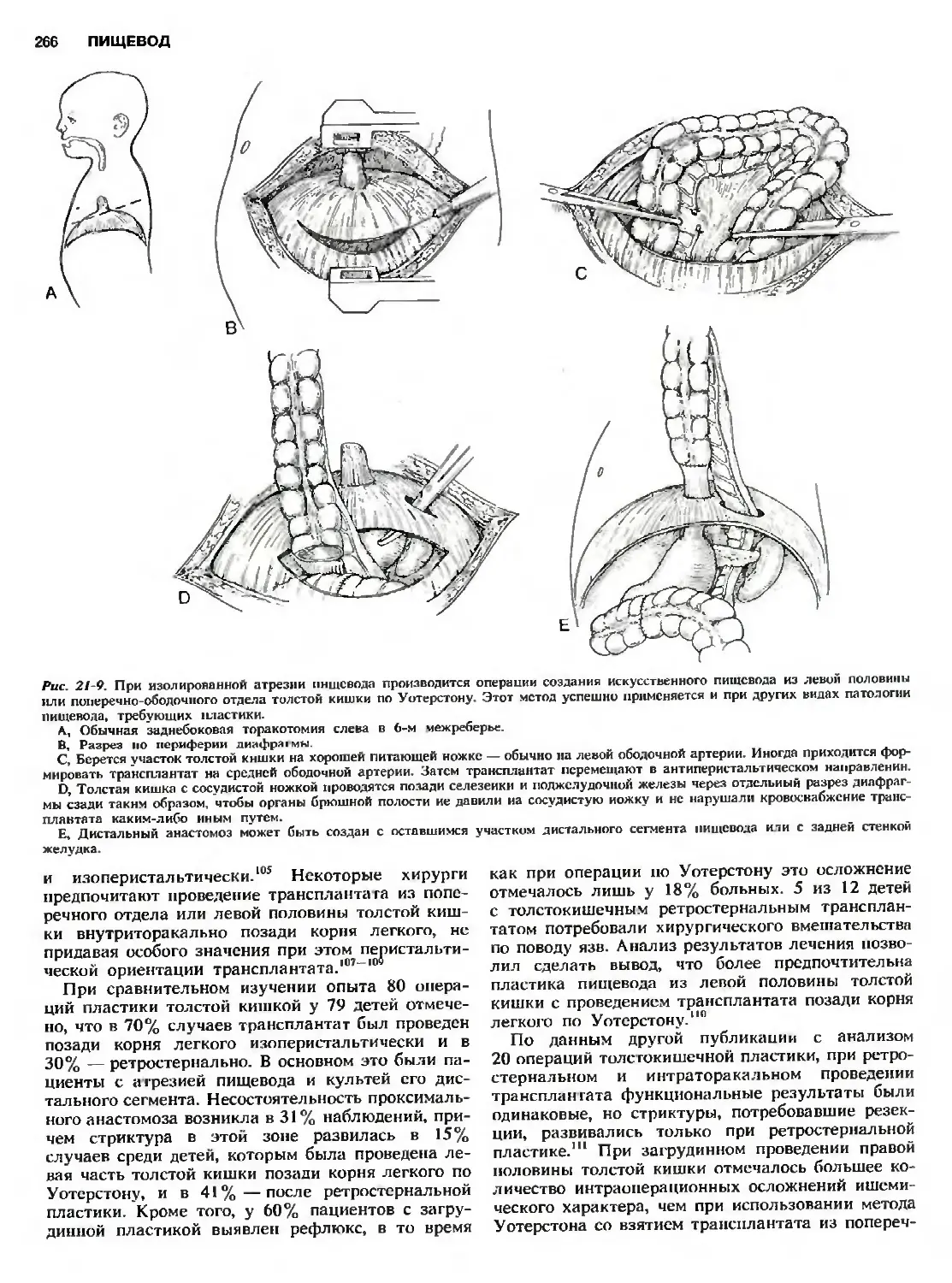
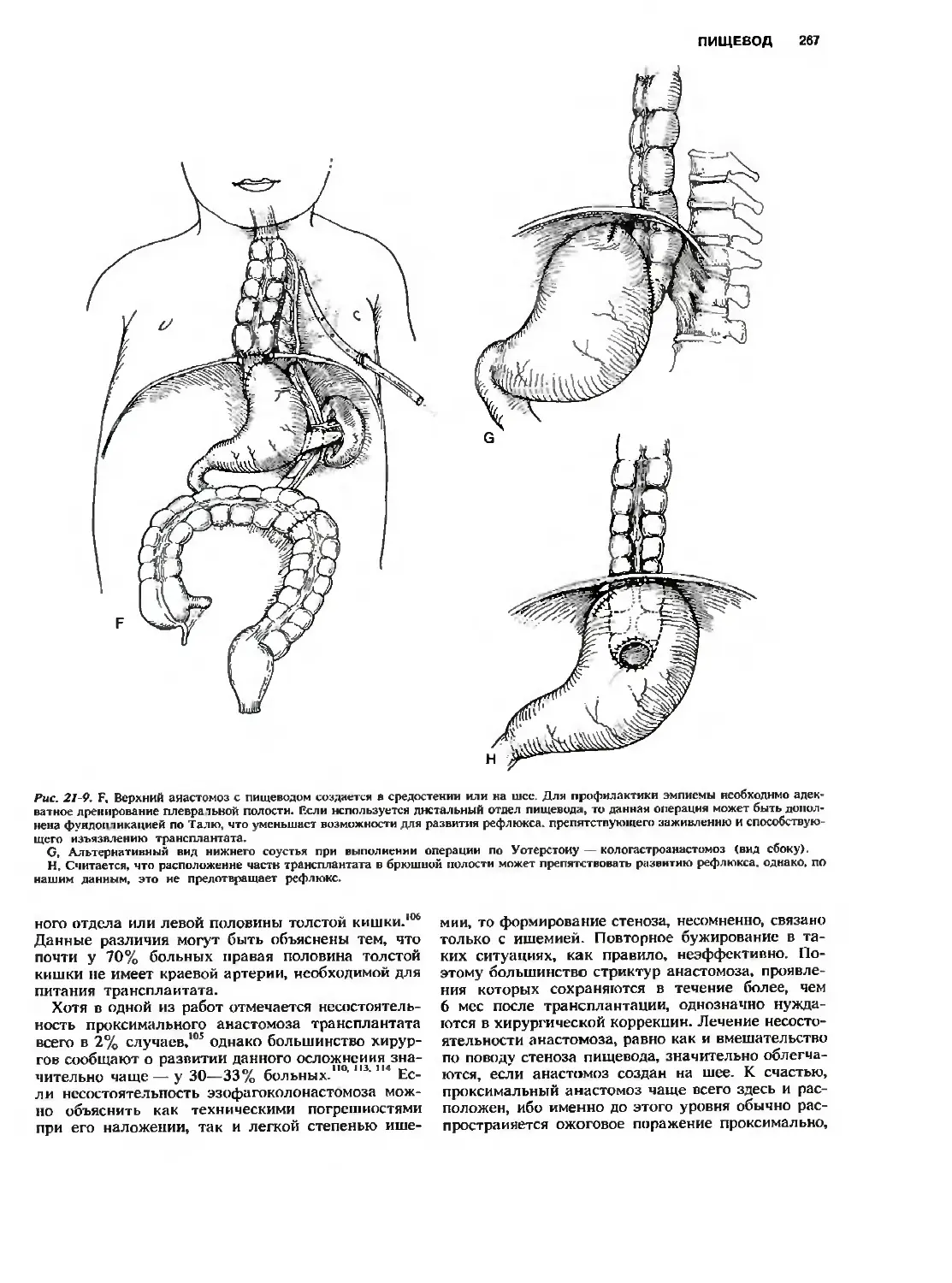
Пластика пищевода 264
Толстокишечная пластика 264
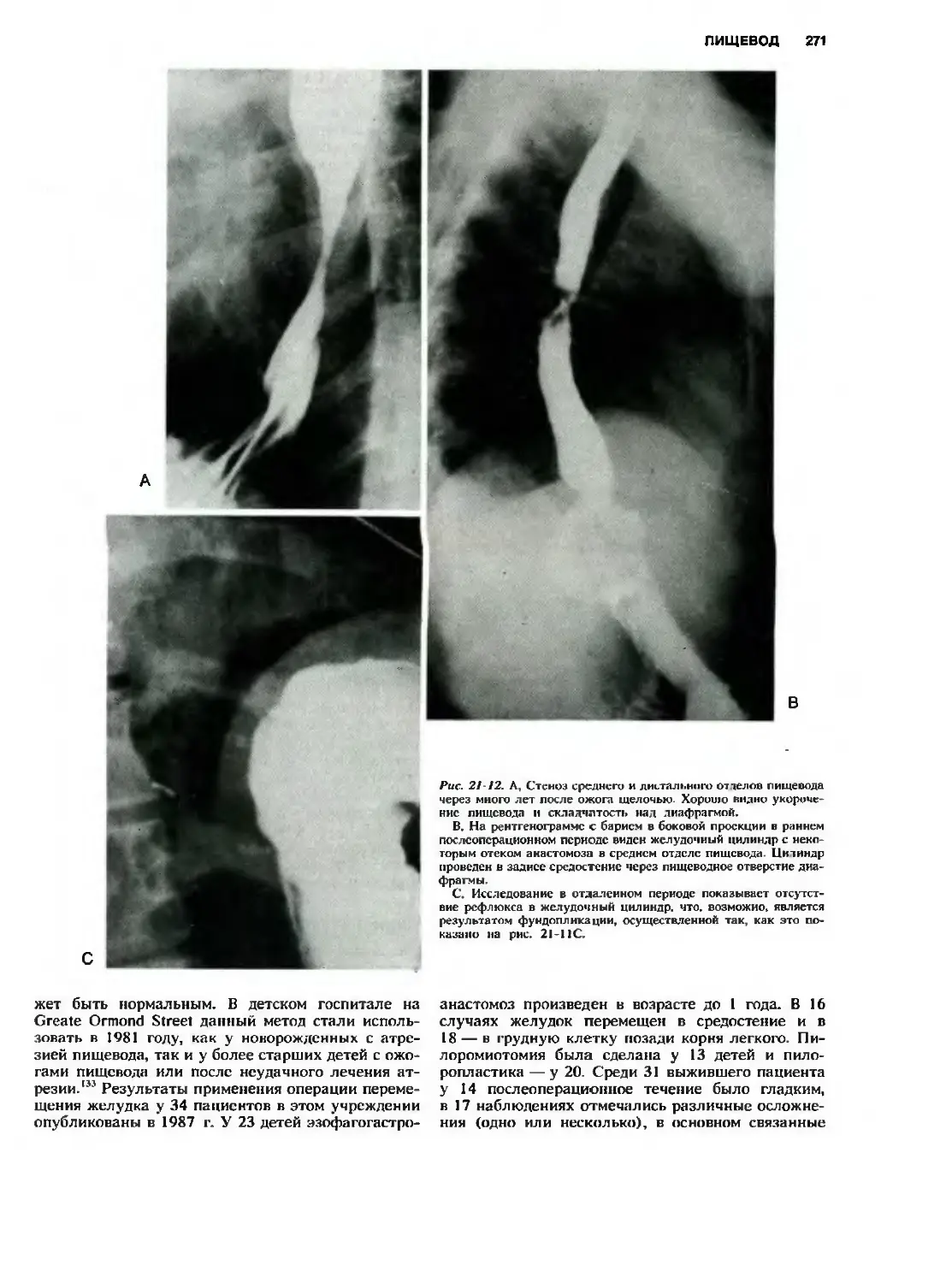
Пластика пищевода желудочным
цилиндром 269
Перемещение желудка 270
Пластика тощекишечным
трансплантатом 272
Осложнения пластики пищевода 272
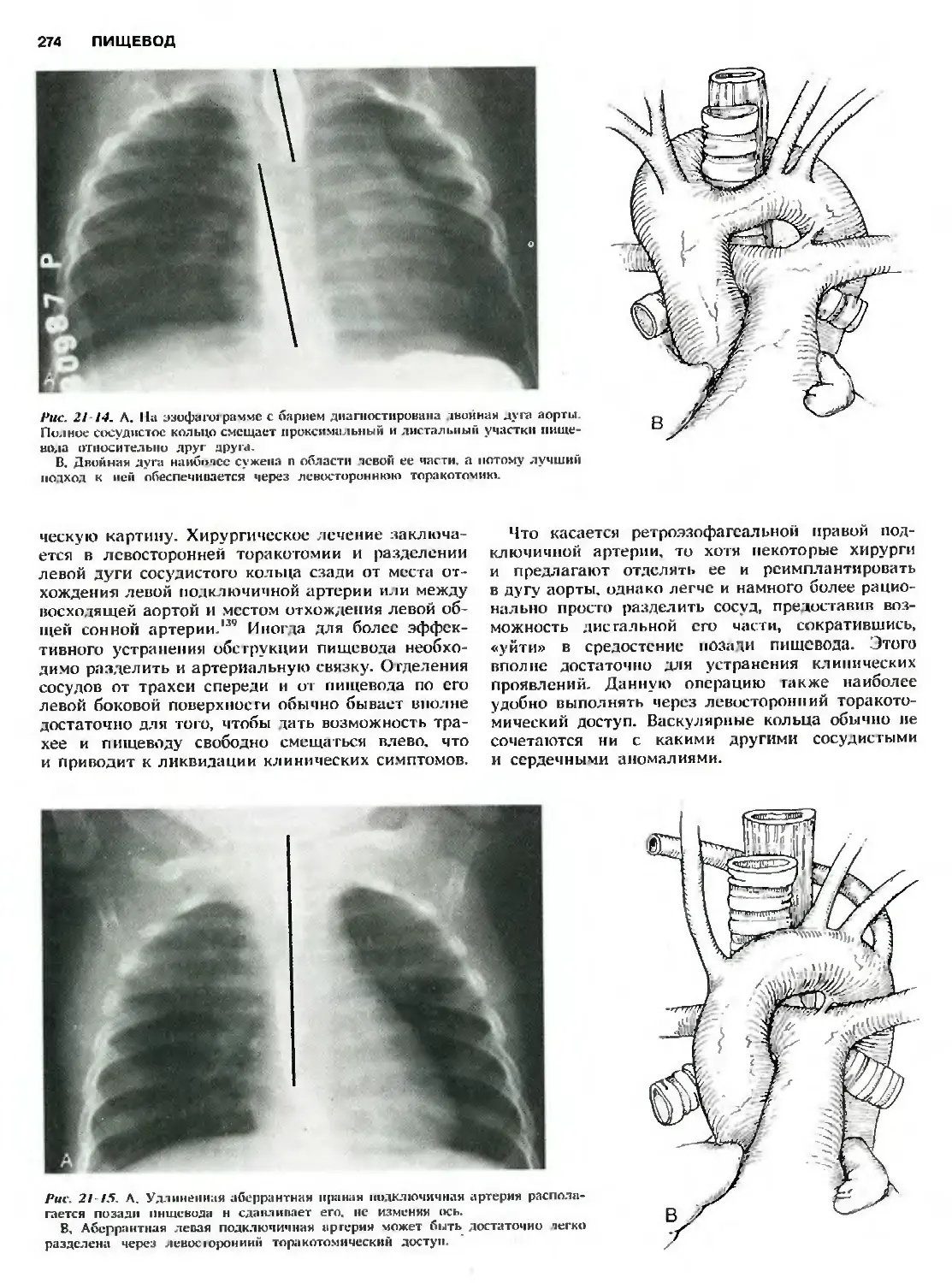
Сосудистое кольцо 273
Глава 22. Атрезия пищевода и трахеопищеводные
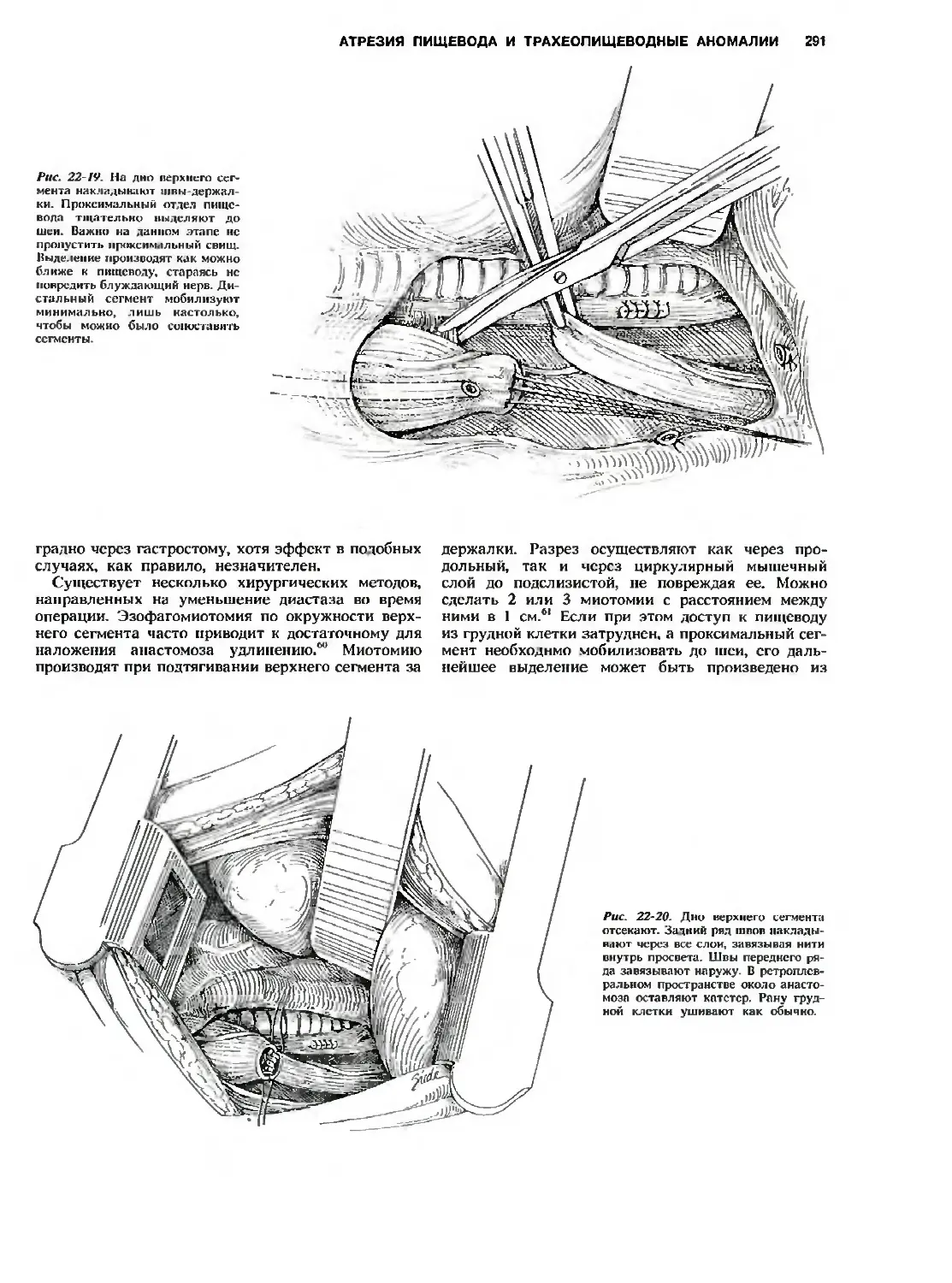
аномалии. Th. М. Holder 278
Атрезия пищевода и трахеопищеводный
свищ 278
Ларинготрахеоэзофагеальная расщелина 296
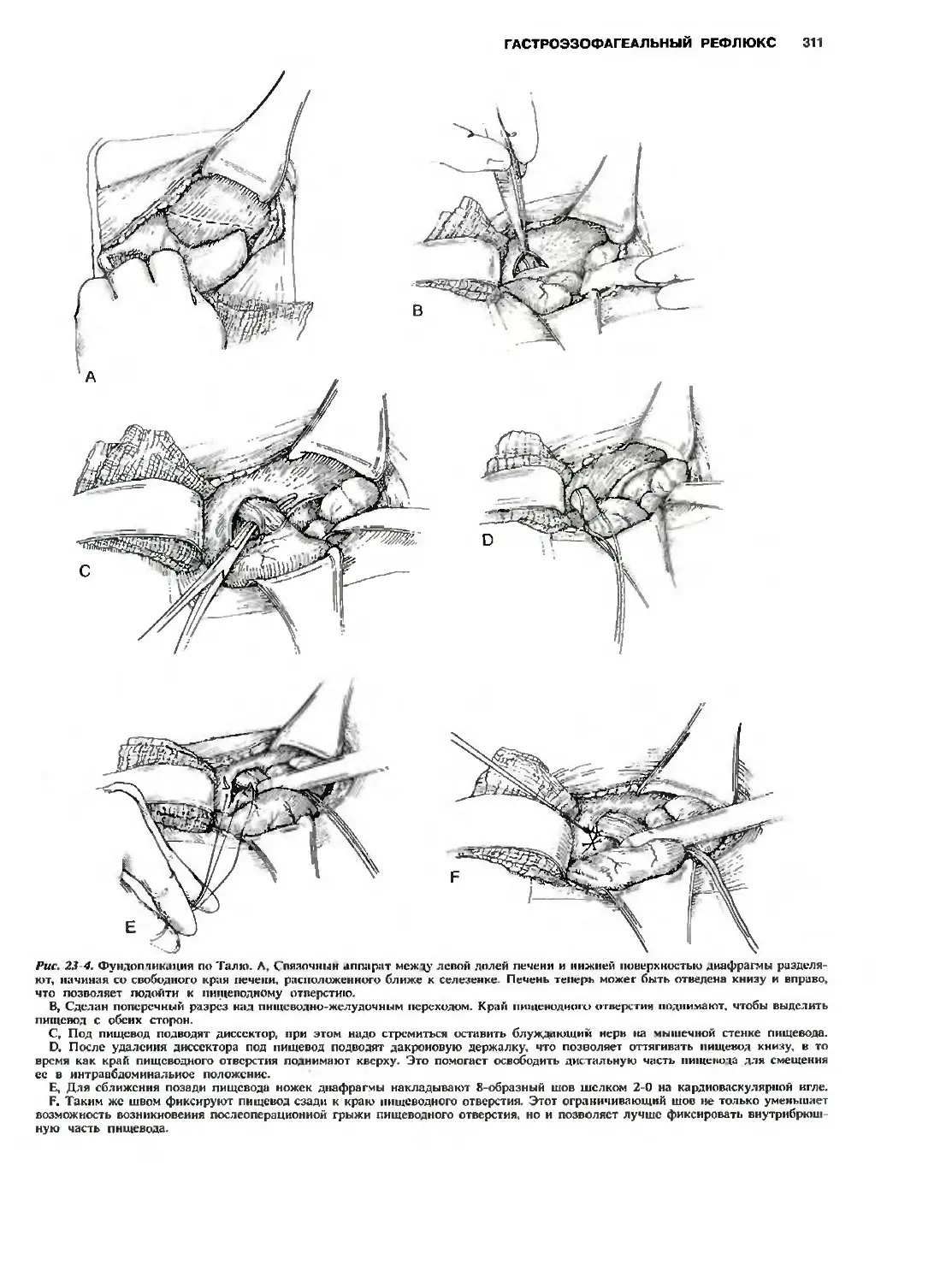
Глава 23. Гастроэзофагеальный рефлюкс.
К. W. Aschcraft 300
Глава 24. Заболевания желудка.
D. L. Dudgeon 322
Непроходимость желудка 322
Гипертрофический пилоростеноз 322
Мембрана антрального отдела
желудка 327
Дискинезия антрального отдела
желудка 327
Атрезия привратника 328
Удвоение желудка 329
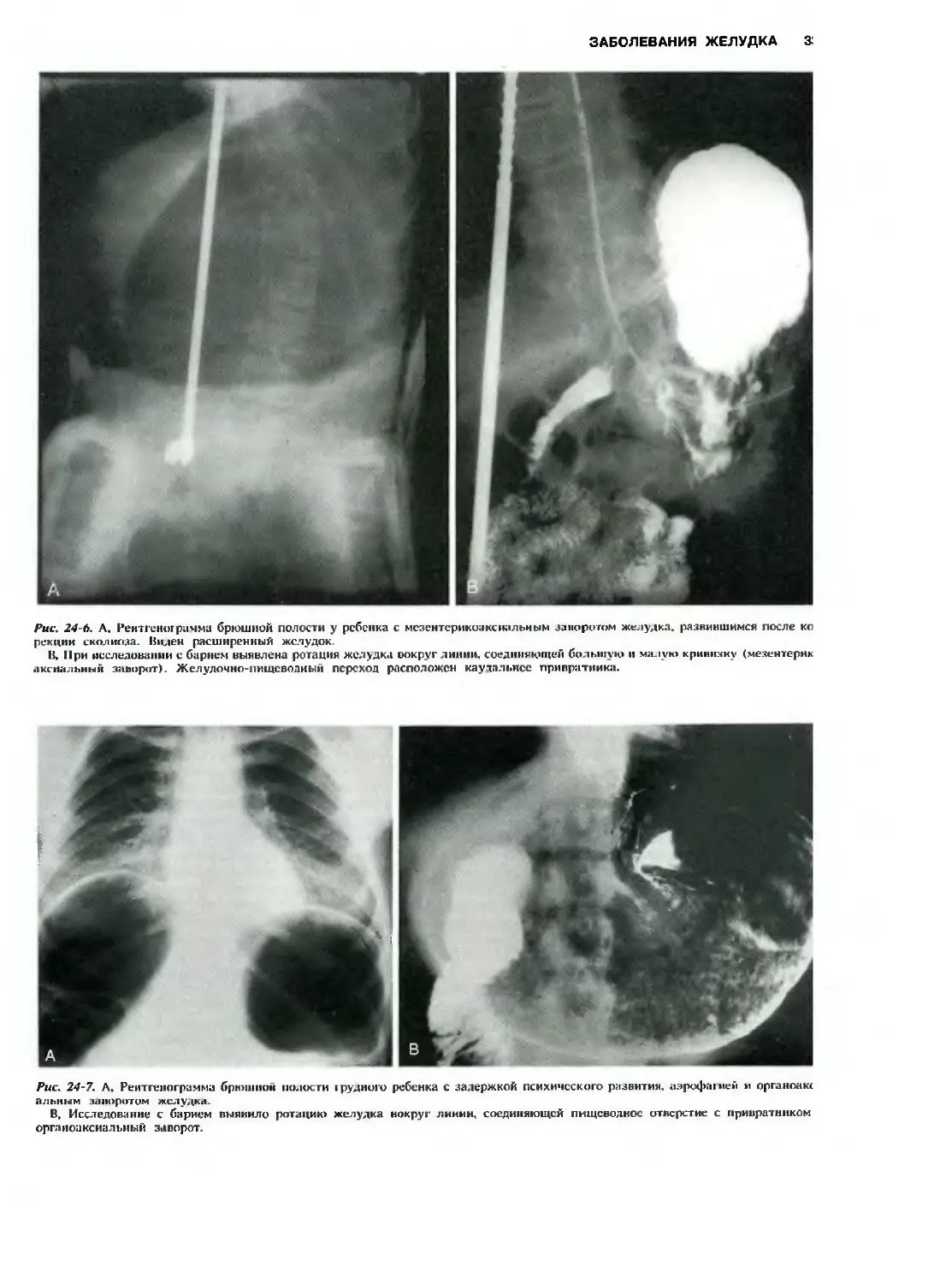
Заворот желудка 329
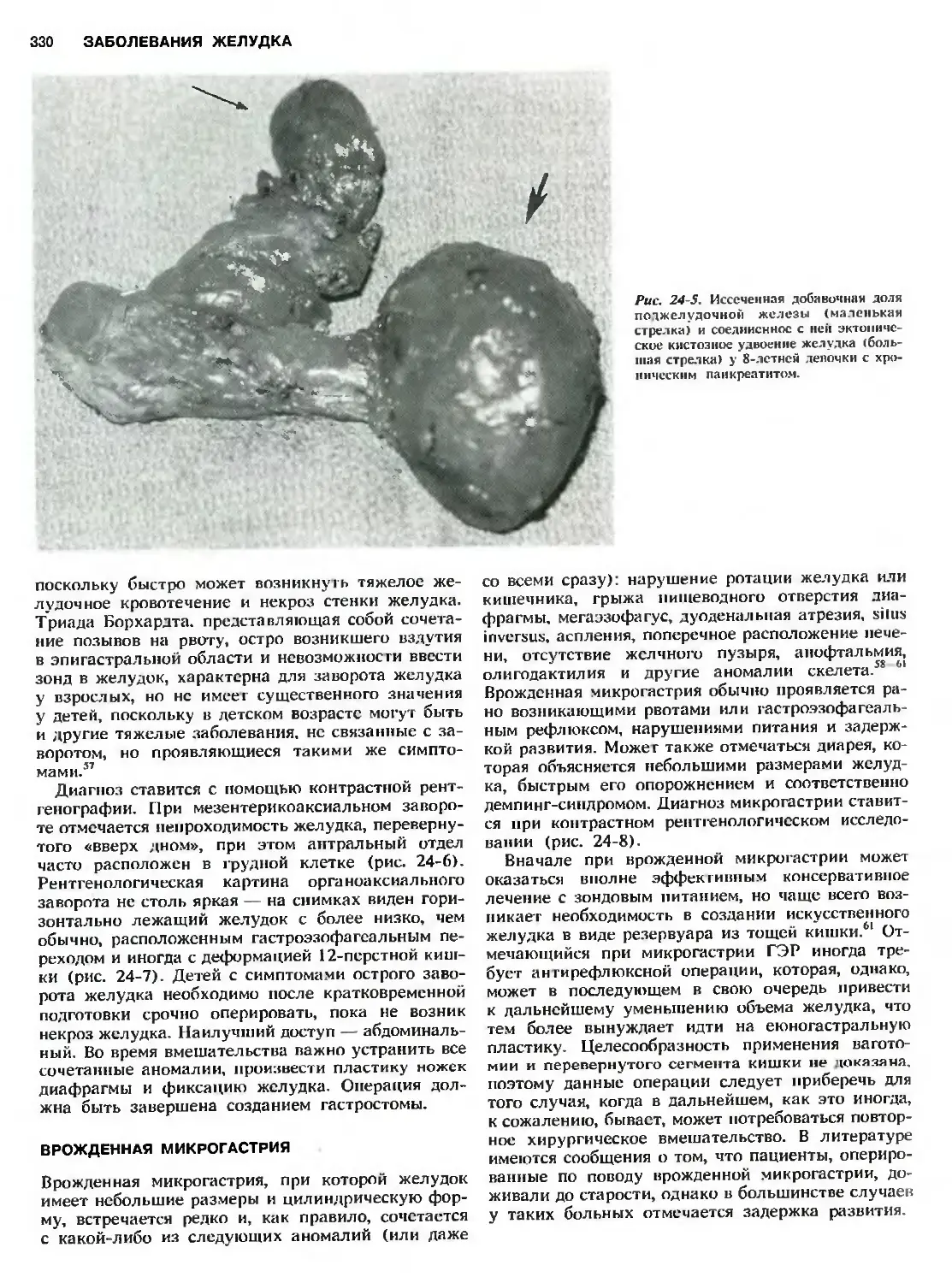
Врожденная микрогастрия 330
Пептические язвы 332
Перфорация желудка 333
Гастростомия 334
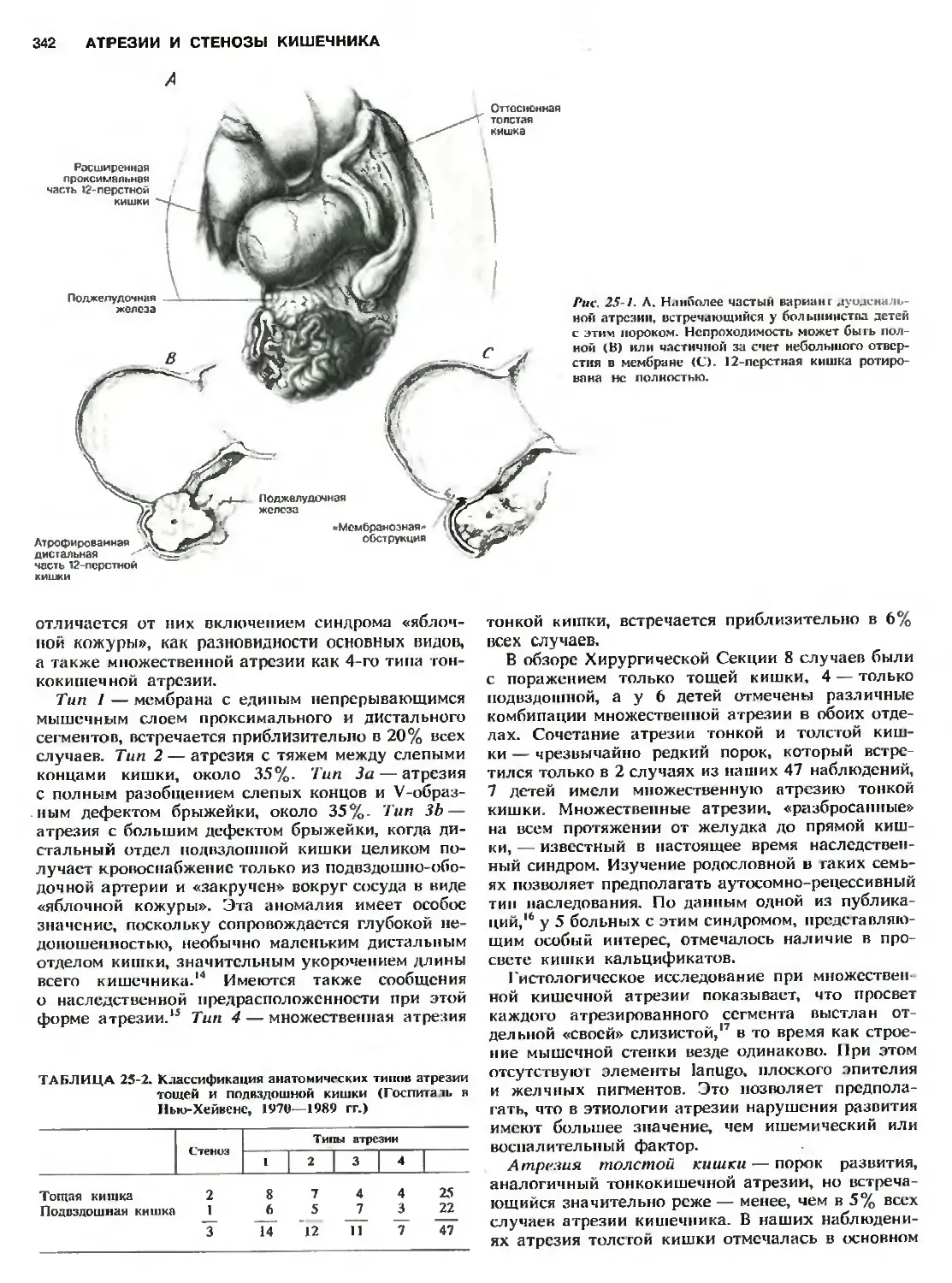
Глава 25. Атрезии и стенозы кишечника.
R. J. Touloukian 341
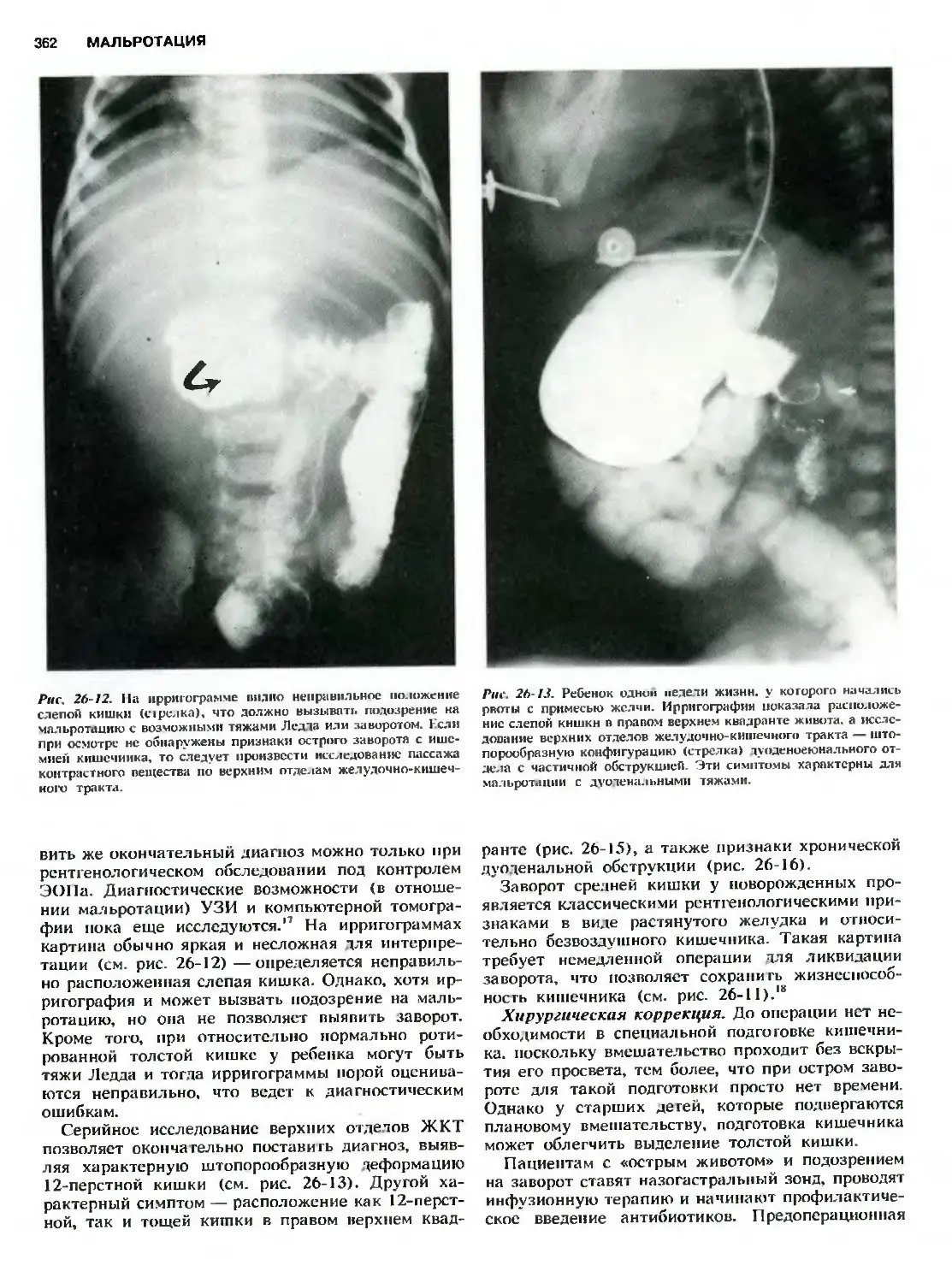
Глава 26. Мальротация. D. Groff III 357
Глава 27. Мекониевая болезнь: ме кон новый ил eye,
синдром мекониевой пробки,
мекониевый перитонит. R. J. Andrassy,
J. G. Hirgiotis 366
Мекониевый илеус 366
Эквивалент меконнового илеуса 372
Синдром мекониевой пробки 372
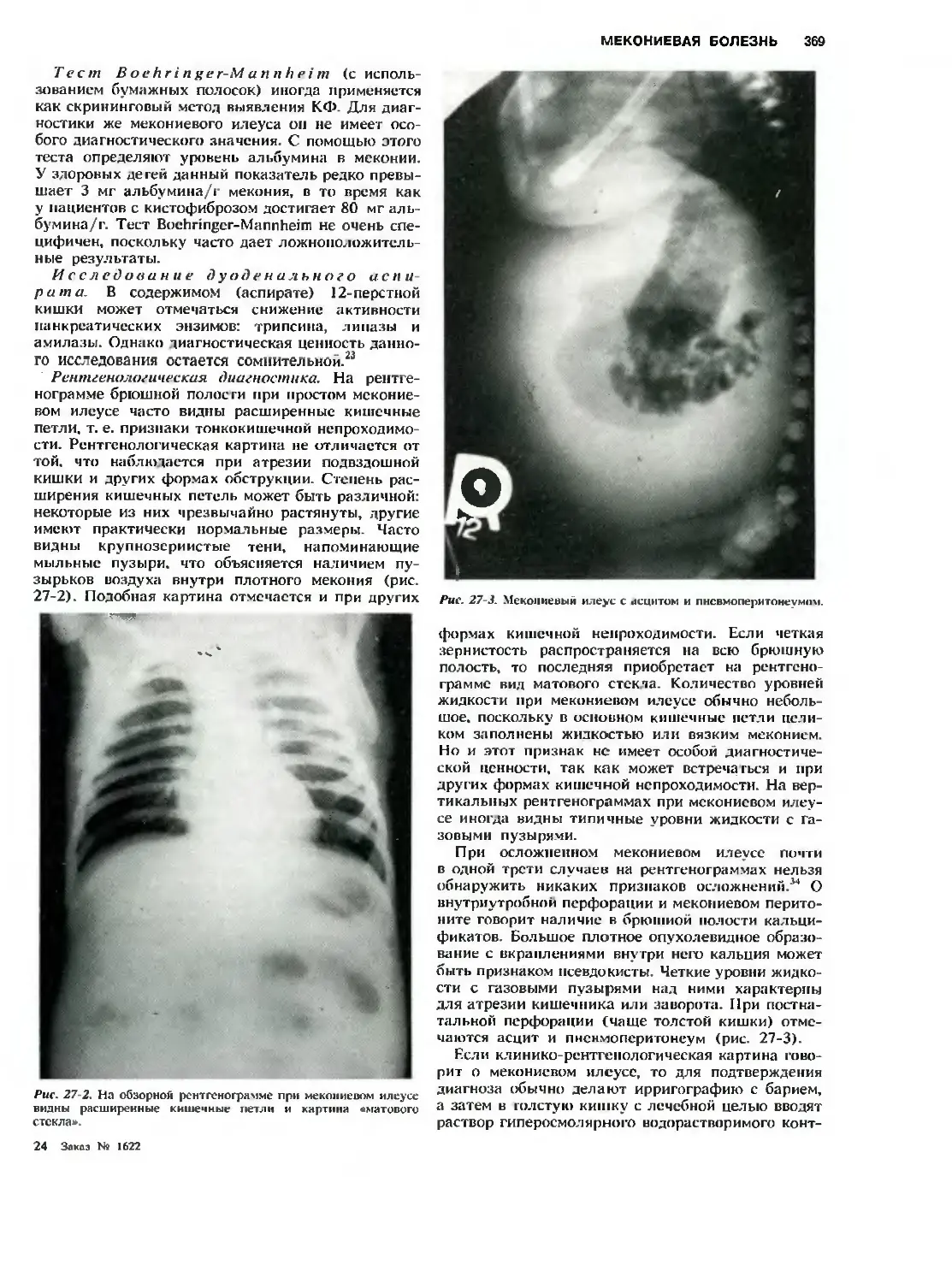
Мекониевый перитонит 373
Заключение 375
Предметный указатель 377
Предисловие к русскому изданию
Отечественная детская хирургия, будучи
по сути очень «молодым» разделом медици-
ны, сделала за последние 3 4 десятилетия
очень мощный рывок. Вероятно, ее развитие
было бы еще более стремительным, если бы
мы имели возможность пользоваться инфор-
мацией о достижениях в этой области зару-
бежных коллег. Однако в силу разных обсто-
ятельств, связанных с общей обстановкой
в стране и трудностями издания любой спе-
циальной литературы в последние годы, та
кой возможности отечественные детские
хирурги, особенно работающие в стороне от
столичных медицинских учреждений, прак-
тически были лишены. Информационный го-
лод существует не только в отношении
зарубежной литературы. И отечественные
последние крупные руководства по детской
хирургии вышли в свет уже много лет
назад. Поэтому смею надеяться, что первое
издание на русском языке «Детской хирур-
гии» под общей редакцией К.Ашкрафта
и Т. Холдера станет немаловажным собы-
тием для детских хирургов нашей страны.
Данное руководство издано во многих стра-
нах и является основной настольной книгой
детских хирургов всего мира. В его написа-
нии принимал участие мощный коллектив
авторов — ведущих специалистов Соединен-
ных Штатов. Именно поэтому каждая конк-
ретная проблема освещена очень подробно,
с изложением истории вопроса, этиологии
заболевания или порока, патогенеза, класси-
фикации, осложнений, методов диагностики
и лечения, как консервативного, так и опе-
ративного. Кроме того, в конце каждой гла-
вы приведен подробный библиографический
указатель, который может оказать неоце-
нимую помощь детским хирургам, занимаю-
щимся научной работой.
Руководство охватывает практически все
разделы детской хирургии. Нельзя не подпер
кнуть удивительную доскональность и от-
кровенность в изложении материала, с об
суждением в каждой главе осложнений и оши-
бок как самого автора, так и других хирур-
гов, с мнением которых автор порой несо-
гласен. Книга богато иллюстрирована. Дан-
ное издание (второе на английском языке)
вышло в свет в 1993 году. В нем на самом
современном уровне отражены все новейшие
технологические достижения в детской хи-
рургии, включая вопросы трансплантации,
техники лучевых методов исследования и
вмешательств (эндо-, лапаро- и торакоско-
пических), антенатальной хирургии.
В процессе перевода руководства и подго-
товки его русского издания было сделано все
для того, чтобы, с одной стороны, предельно
точно и максимально близко к тексту, на-
сколько это только возможно, сохранить пре-
красный и очень отличающийся у разных ав-
торов стиль изложения, а, с другой стороны,
создать такой вариант руководства, кото-
рый был бы не только понятным, но и инте-
ресным для русскоязычного читателя, как
с профессиональной, так и с литературной
точки зрения. Хочется надеяться, что эту
задачу удалось выполнить достаточно ус-
пешно.
Не со всеми положениями и концепциями
авторов можно согласиться безоговорочно,
но в любом случае их мнение не может быть
безынтересным для нас, ибо трудно продви-
гаться вперед в любой области, и в том чис-
ле в детской хирургии, если мы не знаем, что
делается нашими коллегами в соседней боль-
нице, в соседних городах, в соседних странах.
Русское издание «Детской хирургии» К. Аш-
крафта и Т. Холдера будет осуществлено
в трех томах. Нам показалось, что это
удобнее чисто в практическом пиане, ибо
некоторым узким специалистам может ока-
заться более интересным не столько все
руководство, как определенная часть его.
Так, во втором томе очень широко будут
представлены, кроме прочих проблем, вопро-
сы урологии, а в третьем томе — детской
онкологии.
Все отзывы и замечания, касающиеся рус-
ского издания, несомненно, помогут при под
готовке 2-го и 3-го томов и будут приняты
с благодарностью и признанием.
Канд. мед. наук доцент Т. К. Немилова
Предисловие
Порой почти невозможно очертить
границы детской хирургии, ибо круг во-
просов, относящихся к ней, различается
не только в разных странах, но даже
в больницах и медицинских учреждениях
одного и того же города. А потому не
менее сложно было, планируя издание
данного руководства, с одной стороны
удовлетворить ожидания каждого чита-
теля, а с другой — сделать так, чтобы
здесь не оказалось ничего «лишнего».
Второе издание «Детской хирургии»
претерпело очень существенные измене-
ния по сравнению с первым. В основном
это касается вопросов травмы, кото-
рым здесь уделено значительно больше
места, в то же время меньше внимания
во всех разделах обращено на общие во-
просы. Поскольку многие детские хирур-
ги в Соединенных Штатах и в других
странах все чаще и больше сталкива-
ются с вопросами урологии, осветить
проблемы этой области было одной из
главных наших задач. То же самое можно
сказать об аномалиях и обструктивных
поражениях дыхательных путей.
Наша главная задача состояла в том,
чтобы написать книгу, в которой было
бы представлено не только четкое и яс-
ное объяснение каждой проблемы, но
чтобы это было еще сделано и в очень
доступном «читабельном» стиле. Мы не
пытались, поскольку это практически
невозможно, осветить абсолютно весь
материал по детской хирургии, равно
как и не всегда были согласны с точкой
зрения каждого из авторов данного руко-
водства. Тем не менее, выбор авторов
определялся прежде всего тем, что имен-
но эти специалисты признаются наибо-
лее компетентными в данной области
большинством своих коллег.
Мы чрезвычайно признательны нашему
секретарю Кэти Смит, без помощи и
участия которой эта книга не вышла
бы в свет.
СПИСОК УСЛОВНЫХ СОКРАЩЕНИЙ (РУССКИХ)
ААП — Американская Академия Педиат- рии
АВСДЕ Алгоритм, определяющий после- довательность проведения экст- ренных мероприятий при оказа- нии помощи травмированному ре- бенку (см. гл. 11)
АДГ — Аптидиуретический гормон
АКТГ — Адренокортикотропный гормон
АМА — Американская Медицинская Ассо- циация
АП — Атрезия пищевода
A PC — Антирабическая сыворотка
АТФ — Аде низ и нтр ифосфа т
АУП — Анелгезия, управляемая пациентом
БГМ — Болезнь гиалиновых мембран
ВЛД — Бронхолегочная дисплазия
BACK — Бремя активного свертывания крови
вв — Время вдоха
вдг — Врожденная диафрагмальная гры- жа
ВИЧ — Вирус иммунодефицита человека
ВнВП — Внутривенная пиелография
вчд — Внутричерепное давление
вч и вл — Высокочастотная ИВЛ
вчи ивл — Высокочастотная струйная (ин жекционная) ИВЛ
вчо ивл — Высокочастотная осцилляционпая ИВЛ
вчпд ивл — Высокочастотная с положитель- ным давлением ИВЛ
ГЭР — Гастроэзофагеальп ы й рефлюкс
ДАВГ — Длительная артериовенозная ге- мофильтрация
две — Диссеминированное внутрисосу- дистое свертывание
дгэпт — Догоспитальная экстренная по- мощь при травме
дпл — Диагностический перитонеальный лаваж
ДПП — Домашнее парентеральное пита-
ние
Ас
жк г
и вл
ил
и РАС
ит
ицж
кис
кил
кт
КТр
КТТр
КФ
КФК
KJA
лг
лдг
лип
Л 0-50
момс
мт
HAT
ИМИ АВС
НМП-Д
нпс
НПТ-АВС
НРЦДТ
— Дифтерийно-столбнячный анаток-
син
— Желудочно-кишечный тракт
— Искусственная вентиляция легких
— Интерлейкин
— Идиопатический респираторный
дистресс-синдром
— Инфузионная терапия
— Интрацеллюлярная жидкость
— Коклюшно-дифтерийно-столбняч-
ная вакцинация
— Кумулятивный индекс легально-
сти
— Компьютерная томография (томо-
грамма), компьютерный томограф
— Коэффициент травмы
— Коэффициент тяжести травмы
— Кистофиброз
Крсатинфосфоки на за
— Карциноэмбриональный антиген
— Лютеинизирующий гормон
— Лактатдегидрогеназа
Лимфоцитарная интерстициаль-
ная пневмония
— Процент ожога (от общей поверх-
ности тела), дающий летальность
у 50% больных
— Синдром множественной органной
малтротации
— Масса тела
— Наземный автотранспорт
Неотложная медицинская помощь,
первые три (АВС) звена (то же
НПТ-АВС)
— Неотложная медицинская помощь
детям
— Нижний пищеводный сфинктер
(то же НЭС)
Неотложная помощь при травме,
первые три (АВС) звена (то же
НМП АВС)
— Национальный Регистрационный
Центр Детской Травмы
СПИСОК УСЛОВНЫХ СОКРАЩЕНИЙ (РУССКИХ) 9
нецз — Национальный Статистический Центр Здоровья спид
нэс — Нижний эзофагеальный сфинкгер (то же НПО еппвл
овт — Общая вода тела
ОЖУС Острое жизнеугрожающее состоя- ние ссс
оит — Отделение интенсивной терапии сэпт
онф — Фактор опухолевого некроза
опн — Острая почечная недостаточность ТПП
оцк Объем циркулирующей крови
ПАХГ — Передвижной Армейский Хирур- 1ический Госпиталь тпе УЗИ
ПБЭ — Подострый бактериальный эндо- кардит ФАТ
пвд — Правая верхняя доля (легкого) ФР
пдв — Пик давления на вдохе (то же PIP) ФСК-ГМ
пдкв — Положительное давление конца выдоха ФЭ цвл
плгн — Персистирующая легочная гипер- тензия новорожденного цкз цкт
пмн — Полиморфно-ядерные нейтрофи- лы цмв цис
пнд — Правая нижняя доля (легкого) чдкв
поит — Педиатрическое отделение интен- сивной терапии ЧРИГ
пп — Парентеральное питание
ппвл — Перемежающаяся принудительная вентиляция легких (IMV) чсс чтж
ппд — Постоянно положительное давле- ние
ппшо Пневматическая противошоковая одежда чхг
псд — Правая средняя доля (легкого) чэг
пени — Постспленэктомическос наслое- ние инфекции чэсн
псе — Периферическое сосудистое сопро- тивление шдт
ПТА — Почечный тубулярный ацидоз
ПФК — Персистирующее фетальное кро- вообращение шкг
РДС — Респираторный дистресс-синдром штт
РЛФ — Ретролентальная фиброплазия ЭКГ
PH — Ретинопатия недоношенных
РСН — Рекомендуемая Суточная норма (витаминов и т. д.) экмо
САД — Системное артериальное давление ЭМИ
свс — Синдром внезапной смерти эоп
свсд — Синдром внезапной смерти детей
едд — Среднее давление в дыхательных путях )ППТ
СКФ — Скорость клубочковой фильтра- ции ЭрМ эцж
СЛР — Сердечно-легочная реанимация оэг
СНП — Специалист но неотложной помо- щи ЯМР
СП ж — Спинномозговая жидкость
— Синдром приобретенного иммуно-
дефицита
— Синхронизированная перемежаю-
щаяся принудительная вентиля-
ция легких
— Систем и ое сосудистое сопротивле-
ние
— Специализированная экстренная
помощь при травме
— Полное (тотальное) парентераль-
ное питание
Трахеопищеводный свищ
— Ультразвуковое исследование
— Фактор, активирующий тромбоци-
ты
— Физиологический раствор
— Фактор, стимулирующий колонии
гранулоцитов-макрофагов
Фракционная экскреция
— Центральное венозное давление
— Центр Контроля Заболеваемости
— Церебральный кровоток
— Цитомегаловирус
— Центральная нервная система
— Человеческая диплондноклеточ-
пая вакцина
— Человеческий рабический имму-
ноглобулин
— Частота сердечных сокращений
— Частично торакальный (частично
расположенный в грудной клетке)
желудок
— Человеческий хорионический го-
надотропин
— Чрескожная эндоскопическая гаст-
ростомия
Чрескожные электростимуляторы
нервов
— Шкала (оценки тяжести) детской
травмы
Шкала (тяжести) комы, разрабо-
танная в Глазго
— Шкала тяжести травмы
— Электрокардиограмма
(кардиограф, кардиография)
— Экстракорпоральная мембранная
оксигенация
— Эквивалент меконневого нлеуса
— Электроннооптический преобразо-
ватель
— Эффективный почечный плазмо-
ток
— Эритроцитарная масса
— Экстрацеллюлярная жидкость
— Электроэнцефалография
(ЭЭграмма)
— Ядерный магнитный резонанс
СПИСОК УСЛОВНЫХ СОКРАЩЕНИЙ (ЛАТИНСКО-АНГЛИЙСКИХ)
A-а Ог
СаСЪ
CBCs
СО2
ЕСНО-вирусы
FIO2
FRC
1MV
MG
P-50
PaCOj
PaOi
PCOj
— Альвеолярно-артериальная разни-
ца по кислороду
Содержание кислорода в артери-
альной крови
— Взятие на анализ капиллярной
(артериализированной кропи)
— Двуокись углерода (углекислый
газ)
— Энтероцитопатогенные («сирот-
ские») вирусы человека
— Концентрация кислорода во вдь1
хаемом воздухе
— Функциональная остаточная
емкость
— Перемежающаяся принудительная
вентиляция легких (то же ППВЛ)
— Myasthenia gravis — миастения
— Показатель уровня кислорода,
при котором из гемоглобина вы-
свобождается 50% кислорода
— Напряжение углекислоты в арте-
риальной крови
— Напря'хепие кислорода в артери-
альной крови
— Парциальное давление (напряже-
ние) двуокиси углерода
FH
PIP
SaO2
SGOT
SGPT
SvO2
TLC
TMZ
VATER
VACTER
VACTERL
v/Q
vo2
— Показатель концентрации водо-
родных ионов
— Пик давления на вдохе (то же
ПДВ)
— Степень насыщения гемоглобина
кислородом в артериальной крови
— Глютаматоксалоацетагная транса-
миназа
Гл ютаматпиру ватная трансамина
за
— Степень насыщения гемоглобина
кислородом в венозной крови
(смешанная венозная сатурация)
— Общая емкость легких
Три метопр и м-сул ьфа метоксазол
— Сочетание аномалий (вертебраль-
ные, ануса, трахеопищеводные,
эзофагеальные, лучевой кости, ре-
нальные)
— К комбинации VATER добавлены
кардиальные пороки
— К комбинации VACTER добавле-
ны пороки конечностей (ПшЬ)
— Соотношение вентиляция/перфу-
зия
— Потребление кислорода
Глава 1
ФИЗИОЛОГИЯ РЕБЕНКА
Особое внимание в данной главе будет уделено
новорожденному ребенку, поскольку в течение
именно первого месяца жизни происходят особенно
значительные и быстрые изменения всех физиоло-
гических характеристик организма, что связано
прежде всего с приспособлением к внеутробиой
окружающей среде и продолжающимся созрева-
нием органов и систем.
В зависимости от степени зрелости и физичес-
кого развития новорожденные дети могут быть
подразделены на 4 группы.
1. Доношенные новорожденные — гестационный
возраст больше 38 недель, масса тела (МТ) превы-
шает 2,5 кг.
2. Недоношенные дети — гестационный возраст
меньше 38 недель, МТ соответствует этому воз-
расту.
3. Новорожденные с низкой массой но отноше-
нию к гестационному возрасту — гестационный
возраст больше 38 недель, МТ меньше 2,5 кг.
4. Новорожденные с большой по отношению
к гестационному возрасту массой — МТ больше
долженствующей к данному сроку (или выше 90%
перцентильной кривой), у доношенного ребенка
МТ превышает 4 кг.
НОВОРОЖДЕННЫЕ С НИЗКОЙ
ДЛЯ СРОКА ГЕСТАЦИИ МАССОЙ ТЕЛА
Для новорожденных детей, «маленьких к сроку»,
характерна внутриутробная задержка физического
развития в результате различных причин, связан-
ных с недостаточностью плаценты, некоторыми со-
стояниями матери или плода (рис. 1-1). У ново-
рожденных этой группы низкая масса тела обычно
сочетается с относительно нормальными для срока
гестации длиной тела и окружностью головы. Для
того, чтобы отнести новорожденного в группу «ма-
леньких к сроку», гестационный возраст должен
быть установлен с учетом клинических признаков,
суммированных в таблице 1-1.
Хотя новорожденные, «маленькие к сроку», мо-
гут иметь такую же массу тела, как и недоношен-
ные дети. однако физиологические характеристики
у них различны. Жировая ткань у «маленьких
к сроку» часто составляет менее 1% общей массы
тела. Столь выраженный недостаток «изоляцион-
ного материала» резко увеличивает риск переох-
лаждения. Для них характерно, по сравнению с до-
ношенными и недоношенными детьми, более ран-
нее и быстрое развитие гипогликемии, что связано
с высокой метаболической активностью и снижен-
ным уровнем гликогена печени, а также значи-
тельное повышение гематокритного показателя.
Увеличение числа эритроцитов у новорожденных
«маленьких к сроку» часто ведет к полицитемии
и повышению вязкости крови. Длина тела у этих
детей соответствует гестационному возрасту, внут-
риутробное развитие легких также не имеет, в
сравнении с доношенными детьми, особенностей,
н функция легких обычно не нарушена.
НЕДОНОШЕННЫЕ ДЕТИ
К недоношенным относят новорожденных с отно-
сительно низкой массой тела, родившихся раньше
38-й недели беременности. Кожа недоношенных
детей тонкая и прозрачная, подошвенные складки
отсутствуют, пальцы мягкие и легко сгибаются,
ушные хрящи развиты слабо. У девочек малые по-
ловые губы выглядят увеличенными, а большие —
маленькими. У мальчиков яички обычно не опу-
щены в мошонку, сама же мошонка недоразвита.
Для недоношенных детей характерны слабый соса-
тельный рефлекс, снижение резорбции питатель-
ных веществ в пищеварительном тракте, высокая
частота открытого артериального протока, болезни
гиалиновых мембран, внутрижелудочковых крово-
излияний, охлаждения организма.
ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ
НОВОРОЖДЕННЫХ ДЕТЕЙ
Метаболизм глюкозы и кальция. Благодаря сво-
бодной диффузии через плаценту, концентрация
глюкозы в крови плода поддерживается на уровне
11
12 ФИЗИОЛОГИЯ РЕБЕНКА
МТ (ГРАММЫ)
СРОК ГЕСТАЦИИ (НЕДСПИ)
Рис. I I. Виды цитологии, вызывающие отклонения внутриут-
робного физического развития плода. Локализация «клеток» по
отношению к вертикальной и горизонтальной линиям обознача-
ет приблизительную массу тела при рождении и гестационный
возраст, которые чаще всего отмечаются при наличии данной
патологии.
70—80% от значений этого показателя в организ-
ме матери. В поздних стадиях внутриутробного
развития в печени, скелете и сердечной мышце
плода образуются запасы гликогена, однако коли-
чество его очень невелико. Прекращение после
рождения снабжения глюкозой через плаценту
делает новорожденного ребенка целиком зависи-
мым от гликолиза до тех пор, пока глюкоза не
начнет поступать из экзогенных источников.
В отличие от взрослых людей, имеющих эффек-
тивно работающую систему гликогенеза, возмож-
ности новорожденных по использованию жиров
и белков как субстрата для синтеза глюкозы суще-
ственно ограничены. В течение 2—3 часов после
рождения ребенок исчерпывает запасы гликогена
печени и становится зависимым от гликонеогенеза.
Скорость снижения уровня глюкозы сыворотки за-
висит от сс запасов, определяющихся гестацион-
ным возрастом, а также от энергетических потреб-
ностей ребенка. Дети «маленькие к сроку» имеют
очень высокий риск развития гипогликемии. Симп-
томы ее неспецифичны и могут включать слабый
или наоборот громкий крик, цианоз, апноэ, беспо-
койство, вялость или судороги. В некоторых слу-
чаях может не быть никаких клинических проявле-
ний, несмотря на чрезвычайно низкий уровень
глюкозы в крови.
Гипогликемией новорожденных считают содер-
жание глюкозы менее 1,9 ммоль/л у доношенных
и менее 1,4 ммоль/л у детей с низкой МТ. Через
72 часа после рождения уровень глюкозы должен
быть 2,5 ммоль/л или больше.1 Новорожденные
с высоким риском развития гипогликемии требуют
частого мониторинга концентрации глюкозы. С
целью ранней диагностики определение уровня
глюкозы в крови может быть осуществлено непо-
средственно в отделении новорожденных у постели
больного с помощью индикаторной бумаги, про-
ТАБЛИЦА 1-1. Клинические признаки, лежащие к псноке разделения детей с низкой МТ иа недоношенных и «маленьких
к сроку»
Клинические признаки 36 недель (недоношенный) 37 38 недель («пограничный» недоношенный) 39 недель (доношенный)
Подошвенные складки Редкие, поверхностные Пятка гладкая На всей подошве
Размеры молочных желез Волосы на голове Ушная раковина Меньше 3 мм, не пальпируются Пушковые Плохо сформирована, медлен но расправляется, хрящ ма- ленький, мягкий 4 мм Видны при осмотре (7 мм) Шелковистые, каждую прядь МЪжно отделить Расправляется быстро. Хряш плотный
Мужские наружные половые Небольшая мошонка, складча- Яички опустились в мо- Мошонка с выраженной склад
OpIaiHN тость нс выражена, яички ие опустились шонку чатостью, яички опустились полностью
ФИЗИОЛОГИЯ РЕБЕНКА 13
питанной реактивом. Для увеличения точности
исследования данный способ может дополняться
калориметрическим методом, что позволяет качест-
венную реакцию преобразовать в количественную,
выразив содержание глюкозы в ммоль/л.
Поскольку большинство новорожденных, нужда-
ющихся в хирургическом лечении, имеют риск раз-
вития гипогликемии, целесообразно сразу при по-
ступлении ребенка провести пробу с индикаторной
бумагой и при положительных результатах начи-
нать введение 10% глюкозы, параллельно отпра-
вив кровь в лабораторию для точного определения
уровня глюкозы в крови. Цель ранней инфузии
глюкозы — предотвратить развитие клинических
проявлений гипогликемии и поддержать уровень
глюкозы выше 2,5 ммоль/л. При падении концент-
рации глюкозы ниже 2,2 ммоль/л, а также при
наличии любых симптомов гипогликемии, внутри-
венно вводят I—2 мл/кг 50% глюкозы. В течение
первых 36—48 часов после больших операций во-
дно-электролитный баланс, как правило, претерпе-
вает быстрые изменения. В этот период содержа-
ние декстрозы во внутривенно вводимых растворах
должно поддерживаться в пределах от 5% до 15%
в зависимости от показателей концентрации глю-
козы в крови и в моче.
Гипергликемия довольно часто возникает у не-
зрелых новорожденных со сроком гестации менее
38 недель и массой тела до 1,1 кг, находящихся на
парентеральном питании. Эго обычно дети первых
трех дней жизни, получающие 10% глюкозу в дозе
1(H) мл/кг/сут.2 Причиной гипергликемии, по-види-
мому, является пониженная инсулиновая реакция
на вводимую глюкозу. В результате гиперглике-
мии может развиться внутрижелудочковое крово-
излияние, а также почечные потери жидкости
и электролитов, связанные с глюкозурией. Для
предотвращения гипергликемии скорость инфузии
и концентрация глюкозы должны регулироваться
в зависимости от уровня глюкозы в сыворотке.
Чтобы обеспечить таким детям адекватную кало-
рийную поддержку, увеличение концентрации и
объемов глюкозы должно быть очень медленным
и постепенным. Например, можно начать с 5%
раствора декстрозы в обьеме 100 мл/кг/сут, нара-
щивая концентрацию ежедневно или через день на
1% в отличие от общепринятого повышения на
2,5% или 5% ежедневно.
Кальций. Плод постоянно снабжается кальцием
через плаценту. Из общего количества кальция,
полученного таким путем, 75% транспортируется
после 28 недель гестации.3 Это обстоятельство от-
части объясняет высокую частоту гипокальциемии
у недоношенных детей. При рождении имеется
естественная тенденция к гипокальциемии, обу-
словленная уменьшением запасов кальция, незре-
лостью почек и относительным гипопаратирео-
идизмом, связанным с высоким уровнем кальция
у плода. Содержание кальция у новорожденного
обычно максимально снижается через 24—48 часов
после рождения. Гипокальциемией считается уро-
вень ионизированного кальция менее 0,25 ммоль/л.
Наибольший риск гипокальциемии имеют недо-
ношенные дети, новорожденные с хирургической
патологией, а также родившиеся у женщин с ослож-
ненным течением беременности, например с диабе-
том, либо от матерей, получавших инфузии би-
карбоната.
Заменные переливания или массивные трансфу-
зии цитратной крови могут привести к образова-
нию кальциево-цитратных комплексов и соответ-
ственно падению уровня кальция в сыворотке. Бо-
лее позднее развитие гипокальциемии (после 48
часов от рождения) редко отмечается в настоящее
время, поскольку большинство получаемых ново-
рожденными смесей имеют низкое содержание
фосфата.
Симптомы гипокальциемии, так же, как и гипо-
гликемии, неспенифичны и заключаются в общей
возбудимости и приступообразном беспокойстве.
Повышенный мышечный тонус у детей с гипокаль-
циемией помогает в дифференциальной диагности-
ке с гипогликемией. Наибольшее значение имеет
определение уровня ионизированного кальция в
крови. Лечение детей с клиническими проявле-
ниями гипокальциемии заключается во внутривен-
ном введении 10% раствора кальция глюконата
в количестве 1—2 мл/кг в течение 10 минут на
фоне постоянного ЭК Г-мониторинга. Пациентам
с бессимптомной гипокальциемией кальций назна-
чают в дозе 50 мг/кг/сут в виде кальция глюко-
ната, который добавляют к инфузионным раство-
рам (1 мл 10% раствора кальция глюконата содер-
жит 9 мг кальция). Кальций нс следует смешивать
с натрия бикарбонатом. Метаболизм кальция вза-
имосвязан с обменом магния. Поэтому при нали-
чии риска гипокальциемии всегда имеется и риск
гиломагнезиемии. Если у ребенка с судорогами,
расцениваемыми как проявление гипокальциемии,
нет эффекта от введения кальция, следует заподо-
зрить гипомагнезиемию и подтвердить или исклю-
чить ее, проведя исследование уровня магния в
сыворотке. Лечение заключается в срочном внутри-
мышечном введении 50% раствора магния суль-
фата в дозе 0,2 мг/кг, при необходимости эту дозу
можно повторять каждые 4 часа.
Объем крови. Общее число эритроцитов подни-
мается при рождении до своего максимума. Пока-
затели объема крови у недоношенных и доношен-
ных новорожденных, а также у детей старше ме-
сяца жизни представлены в таблице 1-2. К трем
месяцам жизни общий объем крови на кг массы
тела достигает величин, характерных для взрос-
лых людей.
Общий объем крови в периоде новорожденности
варьирует в зависимости от зрелости ребенка, его
размеров, а также плацентарной трансфузии. По-
скольку плацента при рождении содержит 75—
125 мл крови, то при отсроченной перевязке пупо-
ТАБЛИЦА 1-2. Показатели объема кропи
Недоношенные дети 85 100 мл/кг
Доношенные новорожденные 85 мл/кг
> I месяца 75 мл /кг
3 месяца — взрослые 70 мл/кг
14 ФИЗИОЛОГИЯ РЕБЕНКА
вины уровень гемоглобина у новорожденного будет
более высоким.4 Пре (отвратить плацентарную транс-
фузию или искусственно «создать» анемию можно,
если перед перевязкой пуповины подержать ре-
бенка выше уровня плаценты.
Изначально высокое гематокритное число (боль-
ше 50%) может быть использовано как ориентиро-
вочный показатель имевшейся плацентарной
трансфузии. Уровень гемоглобина больше 220 г/л
в сочетании с гематокритным числом выше 65%
в течение 1-й недели жизни должен расцениваться
как полицитемия. По достижении гематокритным
числом уровня 65%, дальнейшее его повышение
приводит к быс(рому существенному увеличению
вязкости крови. Полицитемия новорожденных ха-
рактерна для детей, родившихся от женщин с диа-
бетом, токсикозом беременности, а также для «ма-
леньких к сроку». Лечение полицитемии осуществ-
ляется путем частичного заменного переживания
свежей крови или 5% раствора альбумина.
Причины анемии при рождении могут быть объ-
единены в 3 большие группы: кровопотеря, гемо-
лиз и сниженная продукция эритроцитов. Одной из
важных причин тяжелой хронической анемии, ко-
торая иногда может привести даже к летальному
исходу, является фетальный эритробластоз или
изоиммунизация. Это заболевание возникает в том
случае, когда эритроциты резус-положительного
плода проникают в кровоток резус-отрицательной
матери. Последующий переход IgG резус-антител
от матери в кровоток плода ведет к гемолизу, ко-
торый и обусловливает тяжелые проявления пато-
логии. Наиболее частые признаки гемолитической
болезни новорожденных — желтуха, бледность,
увеличение селезенки или печени. В особо тяже-
лых случаях возникают массивные отеки, не свя-
занные непосредственно с уровнем гемоглобина.
Лечение фетального эритробластоза должно
быть сосредоточено на профилактике иммуниза-
ции матери введением антирсзусного иммуногло-
булина каждой резус-отрицательной женщине, пе-
ренесшей роды резус-положительным ребенком
или аборт. В тяжелых случаях при положитель-
ной пробе Кумбса, уровне гемоглобина в пуповин-
ной крови ниже 105 г/л или билирубина выше
80 ммоль/л, показано срочное заменное перелива-
ние. У менее тяжелых детей заменное переливание
производят в том случае, когда общий уровень не-
прямого билирубина превышает 340 ммоль/л.
Фетальный и «взрослый» гемоглобин. Пои
уровне кислорода 27 мм рт. ст. из «взрослого» ге-
моглобина освобождается 50% кислорода (Р-50).
Таким образом, Р-50 «взрослого» гемоглобина
равно 27 мм рт. ст. Снижение способности гемо-
глобина связывать кислород позволяет большему
количеству освобожденного кислорода при данном
его уровне переходить в ткани.
Показатель Р-50 фетального гемоглобина на 6—
8 мм рт. ст. ниже, чем «взрослого» гемоглобина.
Относительно низкий уровень Р-50 фе.ального ге-
моглобина способствует более эффективному по-
ступлению кислорода из плаценты в ткани плода.
В этой ситуации кривая, отражающая насыщение
гемоглобина кислородом, смещается влево. Умень-
шение Р-50 отчасти связано с меньшей способно-
стью фетального гемоглобина, по сравнению со
«взрослым», связывать 2,3-дифосфоглицерат.5 К
4—6-месячному возрасту у доношенных детей кри-
вая насыщения гемоглобина кислородом посте-
пенно уклоняется вправо и показатели Р-50 при-
ближаются к значениям «взрос юго» гемоглобина.
Желтуха. Билирубин — жирорастворимое веще-
ство, образующееся в результате распада гемо-
глобина. При конъюгации в гепатоцитах с глюку-
роновой кислотой он становится водорастворимым.
При нарушении механизма связывания непрямой
билирубин накапливается и действует как нейро-
токсический яд, вызывая поражение нервной сис-
темы в виде ядерной желтухи. При тяжелых ее
формах могут развиться такие осложнения как
церебральный паралич, потеря слуха и т. д.
Сразу после рождения экскреторная функция
печени у новооожденых значительно снижена.
Поэтому даже у здоровых доношенных детей мо-
гут отмечаться подъемы уровня непрямого билиру-
бина, достигающего максимума (170 ммоль/л) к
4-му дню жизни и возвращающегося к нормаль-
ным показателям к 6-му дню. Повышение у доно-
шенного ребенка уровня общего билирубина более
200 ммоль/л должно заставлять искать причину
гипербилирубинемии (табл. 1-3).
ТАБЛИЦА 1-3. Наиболее частые причины затянувшейся
гипербилирубинемии (за счет непрямого
билирубина)
Желтуха у дпеи, находящихся на грудном вскармливании
Гемолитическая болезнь
Гипотириоидизм
Пилоростеноз
Синдром Крш лер-Найяра
Желтуха при массивных кровоизлияниях
Лечение гипербилирубинемии, в значительной
мере определяющееся массой гела ребенка, начи-
нают с фототерапии: (1) у новорожденных с мас-
сой тела меньше 1500 г, когда уровень билирубина
достигает 85 ммоль/л, (2) при массе тела 1500—
2000 г и повышении уровня билирубина до
140 ммоль/л, (3) при МТ 2000—2500 г, когда уро-
вень билирубина достигает 220 ммоль/л. У доно-
шенных детей, находящихся на искусственном
вскармливании и не имеющих признаков гемоли-
тической болезни, фототерапию начинают, когда
уровень билирубина достигает 250 ммоль/л. При
гипербилирубинемии, связанной с гемолитической
болезнью, фототерапию рекомендуют проводить, ес-
ли показатели билирубина превышают 170 ммоль/л
к 12 часам после рождения, 200 ммоль/л — к 18 ча-
сам, 240 ммоль/л — к 24 часам и 255 ммоль/л —
в более поздние сроки.6 До настоящего времени
остается спорным вопрос — какой уровень билиру-
бина должен являться показанием к заменному пе-
реливанию крови.
Ретинопатия недоношенных (PH) возникает
в результате нарушений развития (его активной
ФИЗИОЛОГИЯ РЕБЕНКА 15
фазы) сосудов сетчатки в течение первых 3—4 ме-
сяцев жизни. В больших отделениях новорожден-
ных детей (например, в госпитале г. Питсбурга)
PH обнаруживается у 1,9% недоношенных.’ Вы-
явить факторы риска в отношении PH трудно, од-
нако две причины, несомненно, играют существен-
ную роль в патогенезе PH — воздействие кислорода
и недоношенность. Американская Педиатрическая
Академия считает необходимым у каждого недоно-
шенного ребенка, получавшего кислород, обследо-
вать сетчатку в возрасте 6—8 недель.8 Рет-
ролентальная фиброплазия (РЛФ) проявляется
изменениями в сетчатке и стекловидном теле, на-
ступающими после острой стадии ретинопатии
(3—6 мес. после рождения). Исследование резуль-
татов применения криотерапии в лечении PH 9 по-
казало, что данный метод достаточно эффективен
и способствует профилактике таких осложнений,
как отслойка сетчатки и фиброз стекловидного
тела
Терморегуляция. Относительно большая поверх-
ность тела по сравнению с массой у новорожден-
ного ребенка в значительной степени объясняет
трудности самостоятельного поддержания постоян-
ной температуры тела. Потери тепла могут воз-
никнуть в связи с испарением (мокрый ребенок
или лежащий на влажном белье), непосредствен-
ной отдачей тепла (прямой контакт кожи с холод-
ной поверхностью), конвекцией (движение воз-
душных потоков) и радиацией (организм излучает
тепло по направлению к более холодным поверх-
ностям, даже если они не находятся в прямом кон-
такте с этим организмом). Именно радиация наи-
более трудно контролируема и управляема. Увели-
чение теплопродукции у новорожденных может
быть обеспечено активацией метаболизма, повы-
шением мышечной активности (подобно взрослым
людям), либо благодаря липолизу бурого жира. Од-
нако жировой термогенез бывает существенно
ограничен малыми запасами бурого жира (при ис-
тощении) 12, а также возможной его дезактивацией
в результате блокирования при использовании не-
которых лекарств (сосудосуживающие препара-
ты10 или анестетики11).
Оптимальной температурой окружающей среды
для новорожденного считается та, при которой ре-
бенок может поддерживать постоянную температу-
ру тела путем вазомоторной регуляции при мини-
мальной скорости обменных процессов. Под крити-
ческой температурой подразумеваются те ее пока-
затели, при дальнейшем снижении которых для
восстановления теплопотерь ребенку необходимо
изменение метаболизма. Невозможно рекомендо-
вать какой-либо единый температурный режим
в кувезе, подходящий для любого ребенка. Опти-
мальная (нейтральная) температура устанавлива-
ется с учетом массы тела и возраста новорожден-
ного (рис. 1-2 и 1-3). Для маловесных детей пер-
вых 6 недель жизни она обычно составляет 34—
35°, после 6 до 12 недель —31—32°. Для более
крупных доношенных новорожденных с МТ 2—
3 кг нейтральная температура колеблется в преде-
лах 31—34° в первый день жизни и 29—31° —
Рис. 1-2. Нейтральный температурный режим для новорожден-
ных первой недели жизни.
в последующем до 12-го дня. Наилучшим образом
необходимую температуру обеспечивают двустен-
ные кувезы. Что касается нагревательных прибо-
ров, они не могут предотвратить конвекцию, что
в результате приводит порой к высоким экстраре-
нальным потерям воды.
ЖИДКОСТЬ И ЭЛЕКТРОЛИТЫ
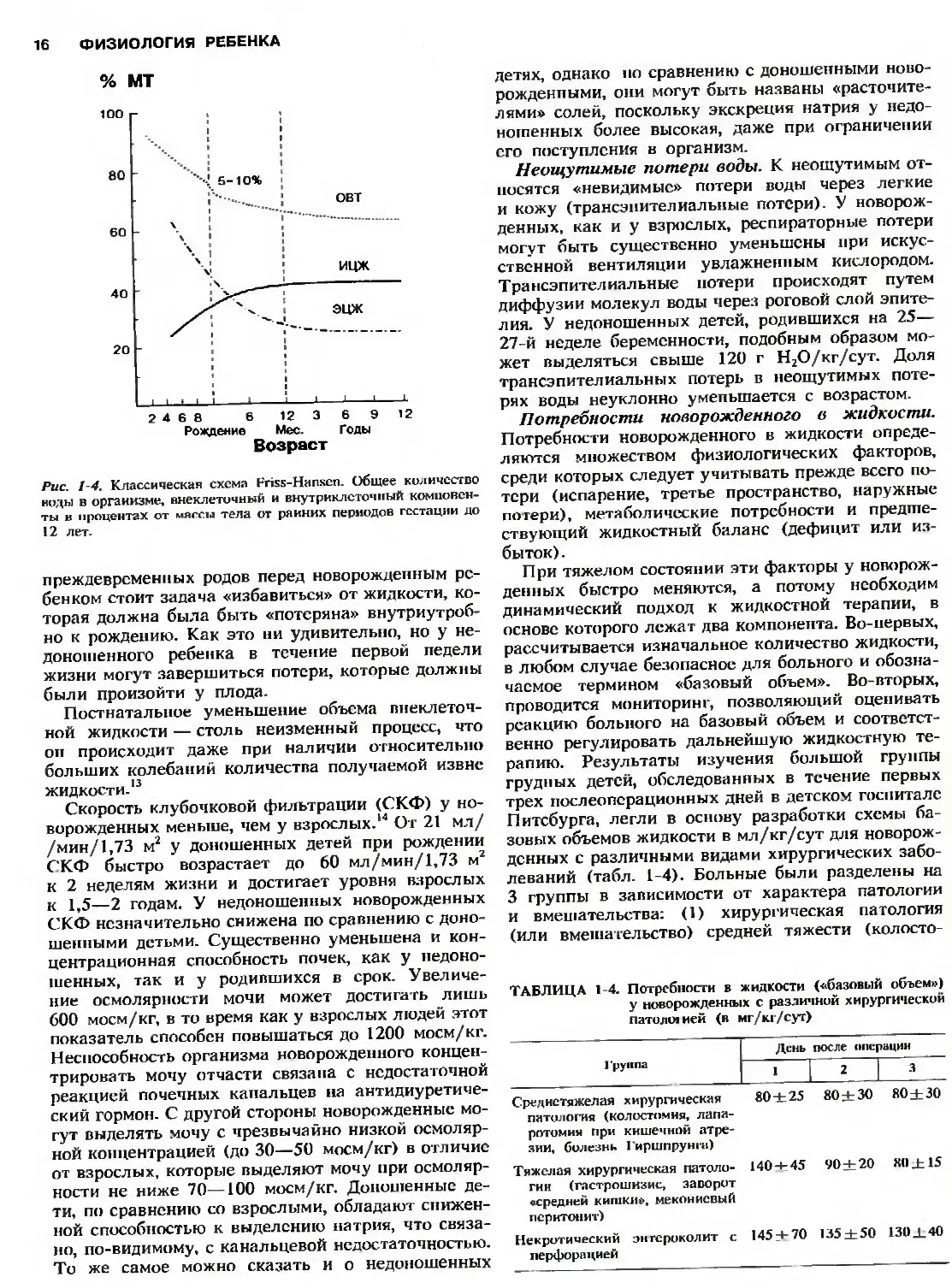
На 12-й неделе внутриутробного развития содер-
жание воды составляет 94% массы тела плода. Это
количество уменьшается до 80% к 32-й неделе
и до 78% — к рождению (рис. 1-4). В первые 3—
5 дней постнатальной жизни происходит дальней-
шее снижение на 3—5% от общей МТ. В последу-
ющем количество воды продолжает уменьшаться
и к полутора годам жизни достигает уровня взрос-
лых. Параллельно, к 1—3 годам уменьшается
и внеклеточный компонент. Подобные изменения
происходят уже внутриутробно, а потому в случае
Постнатальный возраст (дни)
Рис. 1-3. Нейтральный температурный режим СС) для ново-
рожденных в возрасте с 7-го по 35-й дни жизин. Температура
для детей с массой тела больше 2 кг рассчитывается путем экст-
раполяция.
16 ФИЗИОЛОГИЯ РЕБЕНКА
% МТ
Рождение Мее. Годы
Возраст
Рис. 14. Классическая схема Friss-Hanscn. Общее количество
коды в организме, внеклеточный и внутриклеточный компонен-
ты в процентах от массы тела от ранних периодов гестации до
12 лет.
преждевременных родов перед новорожденным ре-
бенком стоит задача «избавиться» от жидкости, ко-
торая должна была быть «потеряна» внутриутроб-
но к рождению. Как это ни удивительно, но у не-
доношенного ребенка в течение первой педели
жизни могут завершиться потери, которые должны
были произойти у плода.
Постнатальное уменьшение объема внеклеточ-
ной жидкости — столь неизменный процесс, что
он происходит даже при наличии относительно
больших колебаний количества получаемой извне
жидкости.13
Скорость клубочковой фильтрации (СКФ) у но-
ворожденных меньше, чем у взрослых.14 От 21 мл/
/мин/1,73 м2 у доношенных детей при рождении
СКФ быстро возрастает до 60 мл/мин/1,73 м2
к 2 неделям жизни и достигает уровня взрослых
к 1,5—2 годам. У недоношенных новорожденных
СКФ незначительно снижена по сравнению с доно-
шенными детьми. Существенно уменьшена и кон-
центрационная способность почек, как у недоно-
шенных, так и у родившихся в срок. Увеличе-
ние осмолярности мочи может достигать лишь
600 мосм/кг, в то время как у взрослых людей этот
показатель способен повышаться до 1200 мосм/кг.
Неспособность организма новорожденного концен-
трировать мочу отчасти связана с недостаточной
реакцией почечных канальцев на антидиуретиче-
ский гормон. С другой стороны новорожденные мо-
гут выделять мочу с чрезвычайно низкой осмоляр-
ной концентрацией (до 30—50 мосм/кг) в отличие
от взрослых, которые выделяют мочу при осмоляр-
ности не ниже 70—100 мосм/кг. Доношенные де-
ти, по сравнению со взрослыми, обладают снижен-
ной способностью к выделению натрия, что связа-
но, по-видимому, с канальцевой недостаточностью.
То же самое можно сказать и о недоношенных
детях, однако по сравнению с доношенными ново-
рожденными, они могут быть названы «расточите-
лями» солей, поскольку экскреция натрия у недо-
ношенных более высокая, даже при ограничении
его поступления в организм.
Неощутимые потери воды. К неощутимым от-
носятся «невидимые» потери воды через легкие
и кожу (трансэпителиальные потери). У новорож-
денных, как и у взрослых, респираторные потери
могут быть существенно уменьшены при искус-
ственной вентиляции увлажненным кислородом.
Трансэпителиальные потери происходят путем
диффузии молекул воды через роговой слой эпите-
лия. У недоношенных детей, родившихся на 25—
27-й неделе беременности, подобным образом мо-
жет выделяться свыше 120 г Н2О/кг/сут. Доля
трансэпителиальных потерь в неощутимых поте-
рях воды неуклонно уменьшается с возрастом.
Потребности новорожденного в жидкости.
Потребности новорожденного в жидкости опреде-
ляются множеством физиологических факторов,
среди которых следует учитывать прежде всего по-
тери (испарение, третье пространство, наружные
потери), метаболические потребности и предше-
ствующий жидкостный баланс (дефицит или из-
быток) .
При тяжелом состоянии эти факторы у новорож-
денных быстро меняются, а потому необходим
динамический подход к жидкостной терапии, в
основе которого лежат два компонента. Во-первых,
рассчитывается изначальное количество жидкости,
в любом случае безопасное для больного и обозна-
чаемое термином «базовый объем». Во-вторых,
проводится мониторинг, позволяющий оценивать
реакцию больного на базовый объем и соответст-
венно регулировать дальнейшую жидкостную те-
рапию. Результаты изучения большой группы
грудных детей, обследованных в течение первых
трех послеоперационных дней в детском госпитале
Питсбурга, легли в основу разработки схемы ба-
зовых объемов жидкости в мл/кг/сут для новорож-
денных с различными видами хирургических забо-
леваний (табл. 1-4). Больные были разделены на
3 группы в зависимости от характера патологии
и вмешательства: (1) хирургическая патология
(или вмешательство) средней тяжести (колосто-
ТАБЛИЦА 1-4. Потребности в жидкости («базовый объем»)
у новорожденных с различной хирургической
патолыией (в мг/кс/сут)
I руина День после операции
1 2 I 3
Средиетяжелая хирургическая 80 ± 25 80 ±30 80 ±30
патология (колостомия, лапа-
ротомия при кишечной атре-
зии, болезнь Гиршпруш-и)
Тяжелая хирургическая патоло- 140-*-45 90±20 Х0±15
гии (гастрошизис, заворот
«средней кишки», меконисвый
перитонит)
Некротический энтероколит с 145±70 135±50 130±40
перфорацией
ФИЗИОЛОГИЯ РЕБЕНКА 17
1АБЛ1ЩА 1 5. «Идеальный» диурез (мл/кг/сут)
у но ни рож де иных с различной хирургической
на гологнен
Группа
День после операции
Средпетяжеянм хирургмче 2 ±0.96 2.63 ± 1.71 2.38 ±0.92
скмя патология (колосто-
мия. лапаротомия при
кишечной атрезии, бо-
лезнь Гиршпрунга)
Тяжелая хирургическая па- 2.67 10.92 2.96 ±0.54 2.9б± 1.0
тология (гастрошизис,
запорот «средней» киш-
ки, мекониеиый перито-
нит)
Некротический онгероко- 2.58±1.04 3,17 ±1,67 3.46±1.46
лит с перфорацией
мия, лапаротомия, кишечная атрезия), (2) тяжелая
патология (заворот средней кишки, гастрошизис)
и (3) некротический энтероколит с перфорацией
нли некроз кишки, требующий оперативного вме-
шательства.
У всех обследованных новорожденных мочевы-
деление было нарушено в той или иной степени.
Оптимальным («идеальным») диурезом считается
тот объем мочи, который необходим, чтобы боль-
ной справился с осмолярной нагрузкой, сохранив
осмолярность мочи на изотоническом уровне —
280 мосм/л. В указанных трех группах больных
с хирургической патологией поддерживалась «иде-
альная» скорость мочеиспускания от 2 мл/час до
3 мл/час (табл. 1-5). Столь широкий диапазон
был связан с непостоянством экскреции осмолярной
нагрузки, которая колебалась от 13 мосм/кг/сут
до 21 мосм/кг/сут.
После введения базового объема жидкости в те-
чение 4—8 часов, в зависимости от характера
патологии, производится оценка эффективности
терапии на основании показателей диуреза и кон-
центрации мочи, позволяющих в большинстве слу-
чаев определить состояние гидратации и реакцию
организма на базовый объем. У тяжелых больных
необходимо определение в динамике концентрации
в сыворотке натрия, остаточного азота, креатинина,
осмолярности, а также концентрации натрия, креа-
тинина и осмолярности мочи, что позволяет более
точно оценить жидкостный баланс и реакцию на
проводимую терапию и рассчитать жидкостную
нагрузку на следующие 4—8 часов.
Иллюстративные примеры.
Обезвоживание. У недоношенного ребенка с мас-
сой тела 1 кг в течение первых 8 часов после опе-
рации при базовом объеме жидкости 120 мл/кг/су г
скорость мочеотделения была 0,3 мл/кг/час, удель-
ный вес мочи 1025. Остаточный азот в крови
увеличился с 2,9 ммоль/л до 5,7 ммоль/л, показа-
тели гематокрита возросли с 35 до 37% (гемотранс-
фузия не производилась). Приведенные данные
были расценены как признаки внутрисосудистого
обезвоживания. Необходимо на следующие 4 часа
увеличить объем жидкости до 160 мл/кг/сут и из-
мерять диурез и концентрацию мочи для того, что-
бы вновь оценить жидкостный баланс.
Неадекватная реакция на жидкостную нагруз-
ку. У новорожденного с диафрагмальной грыжей
с массой тела 3 кг в первые 8 часов после опера-
ции при исходном объеме жидкости 120 мл/кг/сут
скорость мочевыделения 0,2 мл/кг/час, осмоляр-
ность мочи 360 мосм/л. Осмолярность сыворот-
ки уменьшилась с 300 мосм/л до операции до
278 мосм/л, остаточный азот — с 8,5 ммоль/л до
5,7 ммоль/л. Трактовка — неадекватная реакция
на жидкостную нагрузку. Лечение — уменьшение
объема жидкости па следующие 4—8 часов со
120 мл/кг/сут до 90 мл/кг/сут с повторным лабо-
раторным обследованием.
Гипергидратация. Ребенок с гастрошизисом,
массой тела 3 кг, через 24 часа после операции
имел скорость мочеиспускания 3 мл/кг/час (за
последние 3 часа). В течение предыдущих 4 часов
жидкость вводилась из расчета 180 мл/кг/сут.
Удельный вес мочи уменьшился до 1006. остаточ-
ный азот — 2,8 ммоль/л, гематокрит 30% (до опе-
рации 35%), общий белок сыворотки 2,9 ммоль/л
(до операции 3,2). Трактовка — избыточная жид-
костная нагрузка (гипергидратация). Лечение —
уменьшение объема жидкости на следующие 4 ча-
са до 80 мл/кг/сут с повторной оценкой диуреза
и концентрации мочи.
ЛЕГОЧНАЯ И СЕРДЕЧНО-СОСУДИСТАЯ
СИСТЕМЫ НОВОРОЖДЕННОГО
Дихотомическое разделение бронхиального дерева
обычно заканчивается к 16-й неделе внутриутроб-
ного развития. До 24 26-й недели альвеолы прак-
тически нс развиты, поэтому при рождении ре-
бенка в эти сроки аэрогематическая поверхность
для диффузии газа очень ограничена. Между 24-й
и 28-й неделями кубовидные и цилиндрические
клетки дифференцируются в клетки 1-го и/или
2-го (пневмоцигы> типа. Между 26-й и 32-й
неделями гестации развитие терминальных аль-
веол приводит к формированию аэрогемагического
барьера. С 32-й по 36-ю неделю этот процесс про-
должается и альвеолы становятся многочислен-
ными. В то же самое время поверхностно-активные
фосфолипиды или легочный сурфактант, продуци-
руемый клетками 2-го типа, начинает выстилать
альвеолярную поверхность. Этот фактор стано-
вится чрезвычайно важным в поддержании ста-
бильности альвеол. Для оценки степени зрелости
легких плода используется определение в амнио-
тической жидкости фосфолипидов или соотноше-
ния лецитин : сфингомиелин. Соотношение более
2,0 говорит о функциональной зрелости легких.
Наличие адекватного количества сурфактанта край-
не важно для постнатальной адаптации легких.
При недостаточных его запасах может развиться
болезнь гиалиновых мембран (БГМ) или респира-
торный дистресс-синдром. Ы’М является одной из
ведущих причин летальности (30%) среди недоно-
шенных детей в США. Возникновению дыхатель-
ных расстройсгв у новорожденных способствуют
2 Заказ No 1622
18 ФИЗИОЛОГИЯ РЕБЕНКА
также замедленная абсорбция в легких плода или
синдром влажных легких, внутриутробная аспира-
ционная (мекониевая аспирация) или интранаталь-
ная пневмония. При всех этих состояниях гипок-
сия, накопление СО2 или апноэ .могут потребо-
вать интубации и И ВЛ.
Интубацию производят через рот или нос.
Диаметр трубки должен соответствовать размеру
ноздрей или мизинца ребенка. Длина трахеи от
голосовых связок до карины варьирует от 2,6 см
у маловесных недоношенных детей до 6 см у доно-
шенных. Запомнить, па какую глубину (от губ)
следует вводить трубку, помогает следующий мне-
монический прием: идеальная глубина составляет
«7—8—9» см у детей с МТ 1, 2 и 3 кг соответ-
ственно.
ИВЛ — один из самых главных методов лечения
дыхательной недостаточности у новорожденных.
Большинство вентиляторов для новорожденных —
это респираторы, циклированные по давлению,
в которых вдох продолжается до достижения в си-
стеме респиратор — больной определенного задан-
ного давления, после чего происходит переключе-
ние на выдох. Избыточное повышение давления
предупреждаете» автоматически. Скорость потока
газа может регулироваться так же, как и время
выдоха, что позволяет устанавливать необходимое
соотношение вдох/выдох.
Чтобы понять механизм действия ИВЛ на легкие
новорожденного, необходимо обладать знаниями
механики дыхания. У новорожденных с БГМ наи-
более существенным нарушением легочной меха-
ники является уменьшение податливости легких
(рис. 1-5), которая выражает зависимость между
объемом и давлением газа, введенного в альвеолы
(мл/см Н2О). Податливость легких зависит от их
эластических свойств, меняющихся в зависимости
от легочного объема, а также наличия воспаления
легочной ткани или отека легких. Податливость
снижается при коллапсе альвеол или их перерастя-
жении. При одинаковом градиенте давления дыха-
тельный объем у новорожденных с БГМ уменьша-
ется. Или наоборот — давление должно быть более
высоким для того, чтобы поддержать нормальный
дыхательный объем.
Рис. 1-5. Схематическое соотношение давлсиие/объем норма-
льных легких и при респираторном дистрссс-снн <роме (РДС)
В основе этого соотношения — юдат.1иность, при ее снижении
у ребенка с РДС соответственно снижается и объем, и давление.
Болес высокое давление необходимо нс только
для того, чтобы преодолеть упругость легочной
гкани, но и для форсирования продвижения возду-
ха по дыхательным путям. Скорость наполнения
легких воздухом определяется сопротивлением ды-
хательных путей в сочетании с легочной податли-
востью. Сопротивление у детей высокое, что объ-
ясняется небольшими размерами (диаметром) ды-
хательных путей. Произведение сопротивления
и податливости и их воздействие на наполнение
легких воздухом определяются термином «постоян-
ная» времени.
Постоянная времени (сек) =
= сопротивление (см Н2О/л/сек) X
X податливость (л/см Н2О)
Нарушение как сопротивления, так и податливо-
сти, ведет к изменению постоянной времени. Лег-
кие со сниженной податливостью, например при
БГМ, совершают вдох и выдох за более короткий
промежуток времени, чем в норме. Поскольку у де-
тей с БГМ постоянные времени уменьшены во вре-
мя пика болезни, длительность вдоха и выдоха
могут приближаться друг к другу.
В середине 70-х годов для ИВЛ при болезни
гиалиновых мембран использовались вентиляторы
с малой частотой, высоким потоком и большим
давлением, по это приводило к баротравме и брон-
холегочной дисплазии. В настоящее время отмеча-
ется тенденция к применению комбинации высокой
частоты (40—60 дых. в мин), малой скорости га-
зового потока (5—10 л/мин) и низкого давления.
Цель вспомогательной вентиляции — обеспечить
эффективный газообмен. Ряд исследований позво-
лили сделать заключение, что оксигенация у детей
зависит в основном от среднего давления в дыха-
тельных путях,15-17 которое повышается при уве-
личении: пика давления на вдохе, соотношения
вдох : выдох и положительного давления конца
выдоха (ПДКВ). Удаление углекислоты из орга-
низма зависит главным образом от альвеотярной
вентиляции, которая определяется следующим
образом:
Альвеолярная вентиляция = (дыхательный объем —
объем мертвого пространства) X
X частота дыхания
Поскольку объем мертвого пространства оста-
ется относительно постоянным, повышение дыха-
тельного объема или частоты приводит к увеличе-
нию альвеолярной вентиляции. При ИВЛ дыха-
тельный объем зависит от податливости легких
и градиента давления (пик давления на вдохе —
Р1Р). Очень короткий вдох может также умень-
шить дыхательный объем при данном градиенте
давления.
Сурфактант. Сурфактантная недостаточность
считается одной из главных причин болезни гиа-
линовых мембран, а потому повысить эффектив-
ность оксигенации можно с помощью нового мето-
да — замещающей терапии. Существуют три вида
сурфактантных препаратов, которые подвергаются
в настоящее время тщательному исследованию:
ФИЗИОЛОГИЯ РЕБЕНКА 19
(1) сурфактанты, полученные из легких животно-
го (быка или свиньи). (2) сурфактанты человека,
экстрагированные из амниотической жидкости
и (3) искусственные сурфактанты. Результаты
сравнительного применения сурфактантов из бы-
чьих легких 18 и искусственных препаратов 14 пока-
зали, что у детей, получавших бычьи сурфактанты
(в виде однократной дозы в интубационную труб-
ку в среднем через 12 минут после рождения), от-
мечались менее тяжелые изменения в легких на
рентгенограммах через 24 часа после рождения,
чем у новорожденных, получавших плацебо. В то
же время через 7 и 28 дней разницы в клиническом
статусе в этих двух группах не было. Эффектив-
ность искусственных синтетических сурфактантов,
вводимых в виде однократной дозы недоношенным
детям, также оценивалась в сравнении с контроль-
ной группой. Результаты исследования показали
значительное уменьшение при использовании сур-
фактантов частоты летальных исходов, связанных
С Б ГМ, легочной недостаточности, потребности
в кислороде, среднего давления в дыхательных пу-
тях. При лечении сурфактантами доношенных де-
тей с пневмонией и мекониевой аспирацией полу-
чены аналогичные данные — существенное улуч-
шение оксигенации после введения сурфактанта.20
Хотя подобные сообщения многообещающи, одна-
ко необходимо дальнейшее серьезное изучение
с целью определения наиболее эффективной дозы,
количества вводимых доз и выбора оптимального
времени для лечения сурфактантами. Сурфактант-
терапия — очень важное дополнение к лечебным
мероприятиям при легочной патологии у недоно-
шенных детей.
Контроль за сердечно-легочной деятельно-
стью болыюго в отделении интенсивной тера-
пии. Постоянный контроль за функцией жизненно
важных органов позволяет фиксировать измене-
ния, на основании которых можно судигь об эф-
фективности проводимой терапии. Мониторинг
предоставляет также возможность предупредить
катастрофу и своевременно осуществлять направ-
ленные на спасение жизни мероприятия. Многие
эпизоды «внезапного ухудшения» состояния тяже-
лых больных возникают, по данным ретроспектив-
ной оценки, на фоне предшествующих, не столь
критических изменений, которые могли при пра-
вильной их трактовке позволить оказать своевре-
менную помощь и предотвратить катастрофу.
Газы артериальной крови. Напряжение кисло-
рода в артериачьной крови (РаО2) представляет
собой разницу парциального давления между си-
стемной капиллярной кровью и тканями и легоч-
ной капиллярной кровью и альвеолами. Наиболее
распространенный способ определения РаО2— из-
мерение парциального давления кислорода в арте-
риальной крови. Недостаток этого метода — не-
обходимость применения инвазивной процедуры
(пункция или катетеризация артерии) и получение
лишь периодической информации.
При лечении новорожденных часто используют-
ся заборы капиллярной крови, которую можно «ар-
териализовать» с помощью местных вазодилатато-
ров или тепла, увеличивающих приток крови к пе-
риферии. Кровь должна течь свободно и быть
взята на анализ очень быстро, чтобы предотвра-
тить ее контакт с окружающей атмосферой. Мед-
ленный ток крови и воздействие на нее атмосфер-
ного кислорода дают ложное увеличение показате-
лей РаО2 капиллярной крови, особенно при низких
его значениях (40—60 мм рт. ст.).21 РСО2 и pH
капиллярной крови хорошо коррелируют с этими
показателями в артериальной крови, за исключе-
нием тех случаев, когда имеется сниженная перфу-
зия. РаО2 — наименее надежный из всех показате-
лей газов крови. У пациентов, получающих кисло-
род, когда артериальное РаО2 превышает 60 мм
рт. ст., капиллярное РаО2 плохо коррелирует с ар-
териальными показателями.
Нормальное напряжение кислорода в артериаль-
ной крови зависит от степени зрелости и возраста
ребенка. У новорожденного можно говорить о ги-
поксии при значениях РаО2 ниже 55 мм рт. ст. Ги-
пероксия диагностируется при повышении РаО2
более 80 мм рт. ст. Показатели газов артериальной
крови не обладают ни чувствительностью, ни спе-
цифичностью, поскольку слишком много внелегоч-
ных факторов влияет на газообмен, изменяя РаО2.
Чтобы осуществлять повторные заборы крови для
определения РаО2, необходим постоянный катетер.
У новорожденных детей первого месяца жизни
очень удобно использовать для этих целей пупоч-
ную артерию, доступ к которой осуществляется че-
рез пуповинный остаток либо через разрез кожи
ниже пупка. Катетер продвигают в аорту до тех
пор, пока его кончик не достигнет уровня диафраг-
мы или третьего поясничного позвонка (либо ниже
его). Можно использовать и катетеризацию луче-
вой артерии. При любом из этих способов есть
риск таких осложнений, как септицемия, эмболия,
тромбоз и т. д. Заборы артериальной крови с целью
определения оксигенации имеют еше два недо-
статка — необходимость повторных заборов крови
и возникающую иногда в связи с этим анемию.
Изменения оксигенации происходят порой на-
столько быстро н часто, что при периодических
заборах крови критические эпизоды гипоксии или
гипероксии могут быть пропущены. Кроме того,
запоздалое взятие крови и соответственно запозда-
лая информация о происходящих изменениях бы-
вают причиной принятия неправильного решения
на основании уже «устаревших» данных. Учитывая
недостатки мониторинга путем взятия крови, в на-
стоящее время стали применяться мониторные си-
стемы, предусматривающие исключение инвазив-
ных процедур.
Пульсоксиметры я. Сатурация (SaO2> — показа-
тель степени насыщения гемоглобина кислородом.
Под воздействием парциального давления кисло-
рода его молекулы переходят в легочных капилля-
рах в кровь и соединяются с молекулами гемогло-
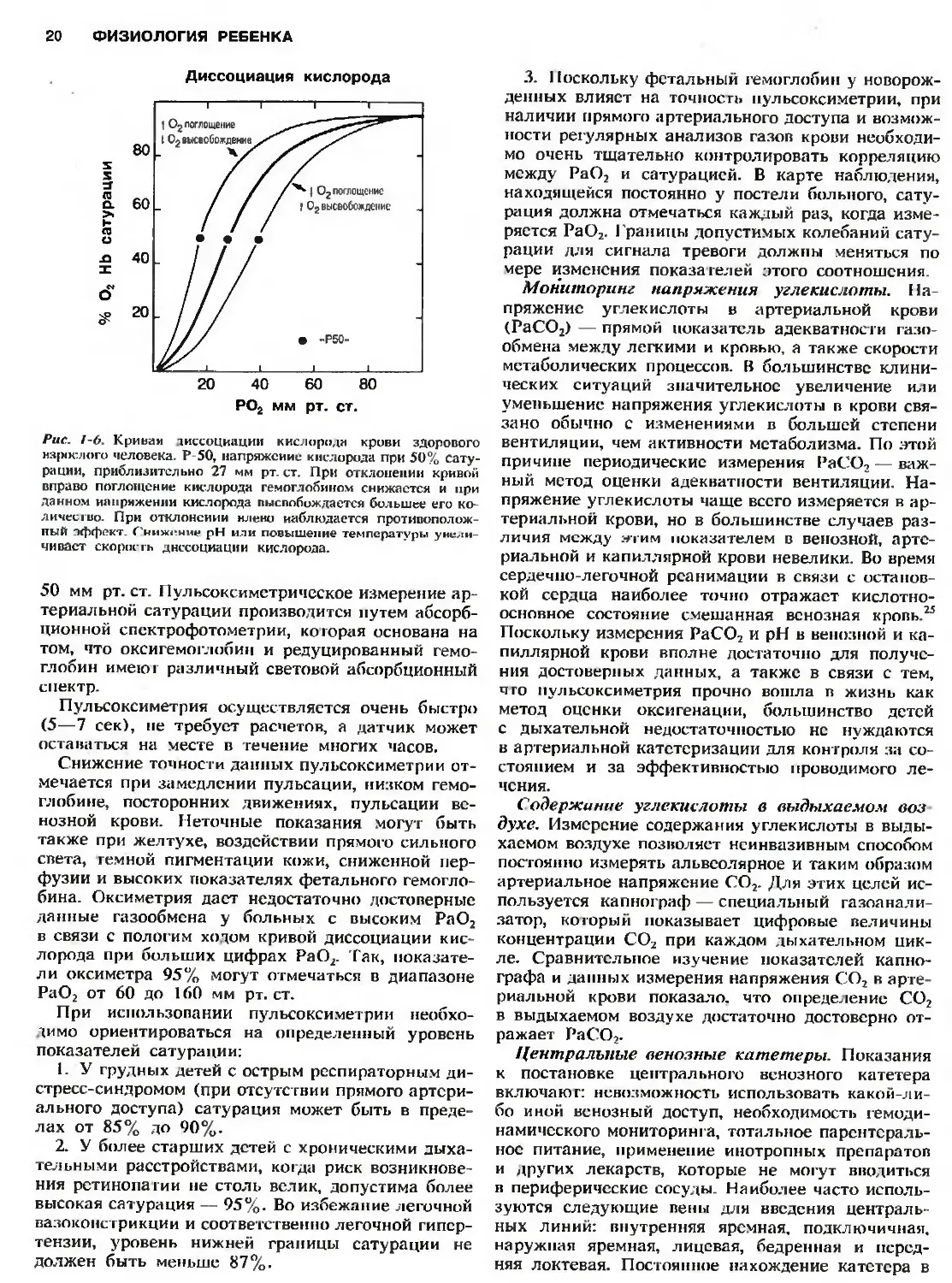
бина. Кривая, отражающая насыщение кислородом
гемоглобина и его диссоциацию, имеет S-образную
форму (рис. 1-6). Согласно этой кривой гемогло-
бин на 50% насыщен кислородом при показателях
РаО2 25 мм рт. ст. и на 90% при РаО2
20 ФИЗИОЛОГИЯ РЕБЕНКА
Рис. 1-6. Крива» диссоциации кислорода крови здорового
взрослого человека. Р 50, напряжение кислорода при 50% сату-
рации, приблизительно 27 мм рт. ст. При отклонении кривой
вправо поглощение кислорода гемоглобином снижается и при
данном напряжении кислорода высвобождается большее его ко-
личество. При отклонении влево наблюдается противополож-
ный аффект. Снижение pH или повышение температуры уншш-
чиваст скорчи ь диссоциации кислорода.
50 мм рт. ст. Пульсоксимстрическое измерение ар-
териальной сатурации производится путем абсорб-
ционной спектрофотометрии, которая основана на
том, что оксигемоглобин и редуцированный гемо-
глобин имеют различный световой абсорбционный
спектр
Пульсоксиметрия осуществляется очень быстро
(5—7 сек), не требует расчетов, а датчик может
оставаться на месте в течение многих часов.
Снижение точности данных пульсоксиметрии от-
мечается при замедлении пульсации, низком гемо-
глобине, посторонних движениях, пульсации ве-
нозной крови. Неточные показания могут быть
также при желтухе, воздействии прямого сильного
спета, темной пигментации кожи, сниженной пер-
фузии и высоких показателях фетального гемогло-
бина. Оксиметрия дает недостаточно достоверные
данные газообмена у больных с высоким РаО2
в связи с пологим ходом кривой диссоциации кис-
лорода при больших цифрах РаО2. Так, показате-
ли оксиметра 95% могут отмечаться в диапазоне
РаО2 от 60 до 160 мм рт. ст.
При использовании пульсоксиметрии необхо-
димо ориентироваться на определенный уровень
показателей сатурации:
1. У грудных детей с острым респираторным ди-
стресс-си ндромом (при отсутствии прямого артери-
ального доступа) сатурация может быть в преде-
лах от 85% до 90%.
2. У более старших детей с хроническими дыха-
тельными расстройствами, когда риск возникнове-
ния ретинопатии не столь велик, допустима более
высокая сатурация — 95%. Во избежание легочной
вазоконстрикции и соответст венно легочной гипер-
тензии, уровень нижней границы сатурации не
должен быть меньше 87%.
3. 11оскольку фетальный гемоглобин у новорож-
денных влияет на точность пульсоксиметрии, при
наличии прямого артериального доступа и возмож-
ности регулярных анализов газов крови необходи-
мо очень тщательно контролировать корреляцию
между РаО2 и сатурацией. В карте наблюдения,
находящейся постоянно у постели больного, сату-
рация должна отмечаться каждый раз, когда изме-
ряется РаО2. Границы допустимых колебаний сату-
рации для сигнала тревоги должны меняться по
мере изменения показателей этого соотношения.
Мониторинг напряжения углекислоты. На-
пряжение углекислоты в артериальной крови
(РаСО2) — прямой показатель адекватности газо-
обмена между легкими и кровью, а также скорости
метаболических процессов. В большинстве клини-
ческих ситуаций значительное увеличение или
уменьшение напряжения углекислоты в крови свя-
зано обычно с изменениями в большей степени
вентиляции, чем активности метаболизма. По этой
причине периодические измерения РаСО2 — важ-
ный метод оценки адекватности вентиляции. На-
пряжение углекислоты чаше всего измеряется в ар-
териальной крови, но в большинстве случаев раз-
личия между этим показателем в венозной, арте-
риальной и капиллярной крови невелики. Во время
сердечно-легочной реанимации в связи с останов-
кой сердца наиболее точно отражает кислотно-
основное состояние смешанная венозная кровь.23
Поскольку измерения РаСО2 и pH в венозной и ка-
пиллярной крови вполне достаточно для получе-
ния достоверных данных, а также в связи с тем,
чго пульсоксиметрия прочно вошла в жизнь как
метод оценки оксигенации, большинство детей
с дыхательной недостаточностью нс нуждаются
в артериальной катетеризации для контроля за со-
стоянием и за эффективностью проводимого ле-
чения.
Содержание углекислоты в выдыхаемом воз
духе. Измерение содержания углекислоты в выды-
хаемом воздухе позволяет нсинвазивным способом
постоянно измерять альвеолярное и таким образом
артериальное напряжение СО2. Для этих целей ис-
пользуется капнограф — специальный газоанали-
затор, который показывает цифровые величины
концентрации СО2 при каждом дыхательном цик-
ле. Сравнительное изучение показателей капно-
графа и данных измерения напряжения СО2 в арте-
риальной крови показало, что определение СО2
в выдыхаемом воздухе достаточно достоверно от-
ражает РаСО2.
Центральные венозные катетеры. Показания
к постановке центрального венозного катетера
включают: невозможность использовать какой-ли-
бо иной венозный доступ, необходимость гемоди-
намического мониторинга, тотальное парентераль-
ное питание, применение инотропных препаратов
и других лекарств, которые не могут вводиться
в периферические сосуды. Наиболее часто исполь-
зуются следующие вены для введения централь-
ных линий: внутренняя яремная, подключичная,
наружная яремная, лицевая, бедренная и перед-
няя локтевая. Постоянное нахождение катетера в
ФИЗИОЛОГИЯ РЕБЕНКА 21
центральной вене позволяет измерять центральное
венозное давление (ЦВД), используемое прн вы-
числении многих показателей, связанных с гемоди-
намикой. Измерение ЦВД основано на предположе-
нии, что существует непосредственная пропорцио-
нальная связь между функцией правого и левого
желудочков. Соответственно, с помощью катетера,
помещенного в верхнюю полую вену или правое
предсердие, определяется давление в правой поло-
вине сердца, которое отражает эти показатели
и в левой половине. Однако порой имеются рас-
хождения между давлением в левом и правом пред-
сердии, например при заболеваниях легких, тяже-
лом сепсисе или сердечной патологии. Чтобы
использовать мониторинг более эффективно, необ-
ходимы серийные измерения ЦВД. Центральное
венозное давление может повышаться при вентиля-
ции с положительным давлением, пневмотораксе,
вздутии живота, тампонаде сердца.
Катетеризация легочной артерии. Внедрение
в клиническую практику метода катетеризации ле-
гочной артерии внесло существенные изменения
в лечение детей с тяжелой сердечно-легочной па-
тологией, благодаря предоставленной возможности
прямого измерения показателей деятельности сер-
дечно-сосудистой системы непосредственно у по-
стели больного. Показания для катетеризации ле-
гочной артерии представлены в таблице 1-6. Этот
метод позволяет измерять ЦВД, давление в легоч-
ной артерии, давление заклинивания и сердечный
выброс. Катетер (двух- или трехпросветный)
обычно вводится у детей, как и у взрослых, мето-
дом чрескожной пункции, за исключением малень-
ких пациентов, у которых иногда приходится де-
лать разрез. Когда кончик катетера находится
в дистальном отделе легочной артерии, показатели
давления точно соответствуют давлению в левом
предсердии, поскольку легочные вены не имеют
клапанов. Это давление заклинивания представ-
ляет давление наполнения левого желудочка, кото-
рое используется как показатель преднагрузки.
Низкие его значения свидетельствуют о том, что
для поддержания адекватного сердечного выброса
и улучшения кровотока необходимо увеличение
объема крови. Высокое иди нормальное давление
заклинивания при наличия сохраняющихся при-
знаков шока говорит о нормальном объеме крови
и адекватном наполнении левого желудочка, но
нарушении при этом функции сердца.
Сердечный выброс — количество крови, достав-
ляемой к периферическим тканям в единицу вре-
ТАБЛИЦА 1-6. Показания к катетеризации легочной артерии
Неадекватная системная перфузия при наличии повышенного
ЦВД
Жидкостная терапия при отеке легких некардиогеиного проис-
хождения
Оценка эффективности таких лечебных мероприятий как изме-
нение ПДКВ, использование вазоактивных препаратов, искус-
ственное кровообращение
Оценки гемодинамики у детей с легочной 1инер1ензмей
Тяжелые заболевания легких с глубокой гипоксемией
мени, обычно выражается в литрах в минуту. У
детей сердечный выброс рассчитывается на поверх-
ность тела с последующим преобразованием в сер-
дечный индекс, представляющий собой попросту
сердечный выброс, разделенный на поверхность
тела. Сердечный индекс позволяет оценивать ра-
боту сердца независимо от размеров тепа, в покое
он обычно составляет 3,5—4,5 л/мин/м2. В клини-
ческой практике широко распространено определе-
ние сердечного выброса термодилюционным мето-
дом. хорошо коррелирующим с другими способами.
Достоинствами термодилюционного метода явля-
ются быстрота измерения и точность при отсутст-
вии шунтирования крови.
В настоящее время развиваются другие методы
измерения сердечного выброса, позволяющие избе-
жать инвазивной процедуры введения катетера
в легочную артерию. Допплеровское определение
скорости аортального тока предоставляет возмож-
ность вычислить сердечный выброс по следующей
формуле:
Сердечный индекс (мл/мин) =
=средняя скорость аортального кроногока (см/сек) X
X площадь поперечного сечения аорты (см2) X 60
Площадь поперечного сечения аорты определя-
ется с использованием стандартной ультразву-
ковой техники. Допплеровское измерение скорости
аортального кровотока проводится с помощью дат-
чика, помещаемого в надгрудинную ямку, в пище-
вод или в трахею (со специально модифицирован-
ной эидотрахеалыюй трубкой). Полученные дан-
ные этих двух методов используются для расчета
сердечного выброса. Проводились различные ис-
следования для определения корреляции между
показателями сердечного выброса, измеренного
с применением указанной техники и с использова-
нием термодилюционного метода. В 1989 г. было
опубликовано сообщение о том, что сердечный
выброс, измеренный Допплеровским методом (в су-
прастернальной ямке), не был достаточно достове-
рен по сравнению с термодилюционной методикой,
а потому не рекомендуется его использование для
гемодинамического мониторинга/'
Импедансная реография (биоимпеданс)—еще
один неинвазивный метод, используемый для изме-
рения ударного объема и основанный на регистра-
ции изменений электропроводности грудной клет-
ки, возникающих при соответствующих изменени-
ях объема и скорости кровотока в грудной аорте.
Попытки применения этой техники у критически
больных пациентов были недостаточно успешны,28
однако последние усовершенствования формы
электрода, алгоритмов и микропроцессоров позво-
лили получить более ощутимые результаты. Дан-
ные экспериментальных исследований на живот-
ных продемонстрировали хорошую корреляцию
сердечного выброса, определенного методом био-
импеданса, с данными термодилюционной тех-
ники.29 Необходимо дальнейшее клиническое изуче-
ние достоинств и недостатков этого метода с целью
выяснения целесообразности его применения в пе-
диатрической практике.
22 ФИЗИОЛОГИЯ РЕБЕНКА
Намерение венозной сатурации (венозная ок-
симетрия). Процесс транспорта кислорода вклю-
чает не только доставку его в эритроциты и ткани,
но и утилизацию кислорода на периферии, а затем
возвращение десатурированной крови в правую
половину сердца. Потребление кислорода представ-
ляет собой его количество, утилизированное тка-
нями, и отражается в формуле Fick:
Потребление О2 = сердечный выброс X
X артерио-пенозная разница по кислороду
Смешанная венозная сатурация — показатель аде-
кватности обеспечения кислородом потребностей
в нем перфузируемых тканей. Современным мето-
дом, позволяющим осуществлять постоянную ве-
нозную оксиметрию, является спектрофотометрия.
Данная техника основана на преобразовании све-
товых волн разной длины в волны определенной
интенсивности. Для этой цели используется специ-
альный катетер, вводимый в легочную артерию.
Нормальные показатели смешанной венозной са-
турации (68—77%) говорят о равновесии между
снабжением кислородом и потребностью в нем при
условии, что сосудистая регуляция не нарушена
и распределение периферического кровотока пор
мальное. Значения выше 77% обычно отмечаются
при синдромах нарушения сосудистой регуляции,
например при сепсисе. Некомпенсированные из-
менения сатурации О2, уровня гемоглобина или
сердечного выброса ведут к уменьшению SvO2. Дли-
тельное снижение SvO2 больше, чем на 10%, тре-
бует измерения SaO2, уровня гемоглобина и сер-
дечного выброса для выяснения причины умень-
шения венозной сатурации/0 Наиболее частым
источником ошибок в определении SvO2 является
неправильная калибровка и смещение катетера.
Важное достоинство метода — возможность прово-
дить постоянные измерения, и таким образом свое-
временно предупреждать различные изменения и
осложнения.31
ШОК
Шок — это состояние острой сердечно-сосудистой
дисфункции, при котором снабжение кислородом
и питательными веществами тканей недостаточно
для обеспечения их метаболических потребностей.
Сердечно-сосудистая функция определяется пред-
нагрузкой, сократительной способностью миокарда
и постнагрузкой.
Пред нагрузка представляет собой объем крови,
возвращающейся к желудочкам, и состоит из сово-
купности объемов правого и левого предсердий.
11 реднагрузка обычно соответствует объему крови,
но в связи с трудностями его измерения предна-
грузка определяется давлением в правом или левом
предсердии. В большинстве клинических ситуаций
показателем преднагрузки является давление в
правом предсердии или ЦВД. В тех случаях, ког-
да нарушена податливость левого или правого же-
лудочка или при некоторых врожденных пороках
сердца, показатели давления в правом предсердии
могут быть выше или наоборот ниже, чем в левом
желудочке, что может ввести в заблуждение и обу-
словить недостоверность измерений. У детей кар-
диоваскулярный шок развивается, как правило,
в результате снижения преднагрузки на фоне по-
терь жидкости, например при диарее или рвоте.
Первый шаг в лечении шока — обеспечить адекват-
ный внутрисосудистый объем, контролируя его из-
мерением давления в правом или левом, или в обо-
их предсердиях. Пока не восстановлен адекватный
интраваскулярный жидкостный объем, инотропные
препараты не должны применяться.
Сократительная способность миокарда отра-
жает возможность мышечных волокон сердца уко-
рачиваться. Ударный объем — наиболее важный
клинический показатель сократительной способно-
сти миокарда. У детей снижение сократительной
способности отмечается при некоторых формах
врожденных пороков сердца или при сочетании
гипоксемии и ацидоза. Задача лечения шока ино-
тропными препаратами — улучшение сократитель-
ной способности сердца.
Постнагрузка представляет собой силу, с кото-
рой левый желудочек должен сокращаться, чтобы
«выбросить» кровь. Постпагрузка связана с сис-
темным сосудистым сопротивлением (ССС) и на-
пряжением сердечной мышцы. ССС определяется
как разница между системным средним артери-
альным давлением и правым артериальным давле-
нием, деленная на сердечный выброс. Системное со-
судистое сопротивление и постпагрузка влияют на
сократительную способность миокарда. Увеличение
постнагрузки, как правило, уменьшает сердечный
выброс, в то время как снижение постнагрузки по-
вышает сократительную способность миокарда.
Адренергические рецепторы играют важную роль
в регуляции обмена кальция, который в свою оче-
редь влияет на сократительную способность мио-
карда. А- и В-рецспторы представляют собой
липопротеиновые комплексы, входящие в состав
гладкомышечных клеток сердца и сосудов. В, -ре-
цепторы преимущественно содержатся в сердце
и их стимуляция приводит к увеличению сократи-
тельной способности миокарда. В2-рецепторы пре-
обладают в гладкомышечной мускулатуре дыха-
тельных путей и сосудов, их стимуляция способ-
ствует бронхо- и вазодилатации. А, -адренергиче-
ские рецепторы располагаются в гладких мышцах
степки сосудов, их стимуляция приводит к суже-
нию сосудов. А2 -рецепторы в основном находятся
в симпатических нервных окончаниях. Использу-
ется также понятие «допаминергические рецепто-
ры», позволяющее объяснить кардиоваскулярный
эффект допамина, не связанный с А- и В рецепто-
рами. Активация допаминергических рецепторов
приводит к уменьшению сопротивления сосудов
почек и брыжейки и таким образом к увеличению
в них объемного кровотока.
Фармакология развивающегося организма. Опи-
саны разные варианты реакций на положительное
и отрицательное воздействие инотропных препара-
тов в зависимости от стадии развития организма.
Так, у молодых собак выявлена невосприимчи-
вость к инотропному действию допамина. Уста-
ФИЗИОЛОГИЯ РЕБЕНКА 23
новлено также, что сосочковые мышцы сердца
новорожденных кроликов менее чувствительны к
инотропному эффекту изопротеренола.33 Незрелая
сердечно-сосудистая система, в отличие от сфор-
мировавшейся, более восприимчива к негативному
инотропному эффекту верапамила. У новорожден-
ных поросят действие верапамила зависит как от
возраста животного, так и от дозы препарата.34
Возрастные изменения в симпатической иннерва-
ции, соотношении сокращающихся и несокраща-
ющихся элементов и регуляции формирования
мышц желудочков сердца помогают объяснить раз-
личия в реакции развивающихся организмов на
одни и те же препараты.
Специфические инотропные препараты (табл.
1-7). Адреналин — эндогенный катехоламин с А-
и В-адренсргическим эффектом. Низкие дозы пре-
парата обладают преимущественно В-адренерги-
ческим воздействием, вызывая увеличение сокра-
тительной способности миокарда и сердечного
выброса. Возрастает и кровяное давление в связи
с увеличением не только сердечного выброса, ио
и сопротивления периферических сосудов. Послед-
ний эффект отмечается при использовании боль-
ших доз, оказывающих А-адренергическое дейст-
вие. Увеличивается частота сердечных сокраще-
ний. Ренальный кровоток может возрастать, либо
оставаться неизменным или даже уменьшаться,
в зависимости от соотношения между увеличенным
сердечным выбросом и изменением сопротивления
периферических сосудов, которое ведет к местному
перераспределению кровотока. При введении адре-
налина, особенно в больших дозах, может отме-
чаться сердечная аритмия. Дозы, применяемые тля
лечения нарушений функции сердечно-сосудистой
системы, колеблются от 0,05 до 0,5 мкг/кг/мин.
Изопротеренол — В-адрснергическии агонист. Он
увеличивает сократительную способность сердца
и частоту сердечных сокращений, незначительно
влияя на сопротивление сосудов. В-адренсргиче-
ское воздействие на периферические сосуды и от-
сутствие А-адренергического эффекта позволяют
уменьшить постнагрузку для левого желудочка.
Сильное хронотропное действие изопротеренола
ограничивает его использование при тахикардии.
Изопротеренол вводится внутривенно в дозе от
0,05 до 0,5 мкг/кг/мин.
Допамин — эндогенный катехоламин с В- и А-ад-
ТАЬЛИЦА 1-7. Вазоактннные препараты, обычно используемые у новорожденных
Вазоа истинный препарат Основной принцип действия Основной гемодинамический эффект Способ введения и дозы Показания
Адреналин А- и В-агопист Увеличивает ЧСС' и со- кратительную способ- ность миокарда путем активации В|-рсцеп- торон 0,1 мл/кг 1:10 000 раст- вора вн/в, внутрисер- дечно или эндотрахеаль- ко; 0,05—1,0 мкг/кг/мин нн/в Сердечная реанимация; кратковременное при- менение при тяжелой сердечной недостаточ- ности и отсутствии эф- фекта от других пре- паратов
Допамин Низкие дозы Стимулирует допамино- вые рецепторы Снижает сопротивление сосудов внутренних органов, почек и моз- га До 2 мкг/кг/мин ин/в Кардиогенный или гипо- волемический шок, после кардиоло!«че- ски х операций
Допамин ('редине дозы Стимулирует Bj-рсцеп- торы, высвобождает норадреналин Инотропный 2—10 мкг/кг/мин пн/п Отсутствие изменения артериального давле- ния в ответ на низкие дозы
Допамин Высокие дозы Стимулирует А-рецеп- торы Увеличивает сопротив- ление перифериче- ских и почечных СО- СУДОВ > 10 мкг/кг/мип пн/п Септический шок с низ- ким системным сосуди- стым сопротивлением
Добутамин Синтетический В।-аго- нист при низких до- зах. А и В2 эффект При высоких дозах Увеличивает минутный объем сердца, арте- риальное давление; в меньшей степени, чем допамин, повы- шает ЧСС 1 10 мкг/кг/мнн вн/в Альтернативный по от- ношению к допамину препарат в ситуациях, когда нежелательно увеличение ЧСС
Изопротеренол В|- и В2-агонист Увеличивав! минутный объем сердца и ве- нозный возврат, бла- годаря положитель- ному инотропному и хронотропному дей- ствию; обычно СМИ жаст системное и ле- гочное сосудистое со- противление 0.05 0.5 мкг/кг/мин пн/н Низкий минутный объем сердца, особенно н со- четании с уменьшены ем ЧСС
Натрия нитро Вазодилататор прямот Уменьшает постна груз- 1 —10 мкг/кг/мин вн/в (В Гипсртензионпыи криз.
пруссид действия, расслабля- ет гладкие мышцы стенок артериол и вен ку; снижает артсри альнос давление течение до 10 мин); 0.5—2 мкг/кг/мип ин/в сосудорасширяющая терапия
24 ФИЗИОЛОГИЯ РЕБЕНКА
ренергическим эффектом, равно как и с юпами-
нергическим. Он является и прямым и непрямым
В а ренергическим агонистом. Допамин обладает
положительным инотропным и хронотропным эф-
фектом, благодаря прямому взаимодействию с В-рс-
цепторами (прямое действие.) и путем стимуляции
высвобождения из симпатических нервных оконча-
ний норадреналина, который взаимодействует с
В- рецензорами (непрямое действие). Низкие дозы
(менее 2 мкг/кг/мин) вызывают преимущественно
допаминер! ический эффект, приводя к умень-
шению сопротивления почечных и брыжеечных
сосудов и увеличению кровотока в соответствую-
щих органах. В-адренергический эффект стано-
вится преобладающим при средних дозах (2—
10 мкг/кг/мин), вызывая повышение сердечного
выброса. При относительно высоких дозах (боль-
ше 15—20 мкг/кг/мин) преобладает Л-адрснсрги-
ческий эффект, приво (ящий к сокращению перифе-
рических сосу дов.
В педиатрической практике применение допа-
мина эффективно при необходимости увеличения
кровяного давления. Однако точные дозы, дающие
желаемый оптимальный гемодинамический эффект,
окончательно нс опрс (елены. Воздействие низких
доз допамина на кровяное давление, частоту сер-
дечных сокращений и функцию почек изучалось
у 18 недоношенных детей с гипотензией.31 Влияние
на кровяное давление и диуретический эффект
были отмечены при дозах 2, 4 и 8 мкг/кг/мин.
Увепичение частоты сердечных сокращений выяв-
лялось лишь при дозе 8 мкг/кг/мин. Для более
точного выяснения фармакокинетики и фармакоди-
намики допамина у детей, особенно новорожден-
ных, необходимы дальнейшие исследования.
Добутамин, синтетический катехоламин, обла-
дает преимущсствсчно В-адренергическим дейст-
вием с минимальным А адренергическим эффектом.
Изучение влиянш добутамина на гемодинамику
при шоке у детей 36 показало, что он значительно
увеличивает сердечный и ударный индекс, умень-
шая в то же время системное сосудистое сопро-
тивление. Этот препарат более эффективен при
лечении кардиогенного шока, чем септического.
Преимущества добутамина перед изопротерено-
лом заключаются в меньшем хронотропном эф-
фекте и способности поддерживать системное дав-
ление. Преимущество перед допамином — в мснсс
выраженном сужении периферических сосудов.
Обычные дозы добутамина колеблются от 2 до
15 мкг/кг/мин. В реанимации и интенсивной тера-
пии все чаще используется комбинация допамина
и добутамина, однако сведений о применении
этого сочетания у детей пока недостаточно
Лечение шока. Фактически все виды шока у де-
тей связаны со значительным внутрисосудистым
и интерстициальным дефицитом жидкости. Гипо-
волемия приводит у уменьшению венозного воз-
врата к сердцу. Прсднагрузка сокращается, падает
сердечный выброс, и в результате уменьшается
тканевая перфузия. Тяжелый инфекционный про-
цесс и гиповолемия — наиболее частые причины
шока у детей, как и у взрослых. Первый шаг в ле-
чении всех видов шок<1 — ликвидация имеющегося
дефицита жидкости. Скорость и объем инфузии
определяются реакцией больного на проводимую
терапию, особенно изменениями в кровяном давле-
нии, частоте пульса, диуреза, ЦВД. При шоке, свя-
занном с острой кровопотерей, вводят болюс рас-
твора Рингер-лактата в дозе 10—20 мл/кг. При
отсутствии эффекта повторяют введение кристал-
лоидного раствора При необходимости производят
гемотра псфузию.
Болес труден выбор жидкости для инфузии при
шоке, развившемся на фоне сепсиса или потерь
экстрацеллюлярной жидкости, например при пери-
тоните, кишечной непроходимости, панкреатите.
У старших детей мы начинаем обычно с введения
раствора Рингер-лактата, а у новорожденных —
с половинного раствора Рингера. Несмотря на
наше отрицательное отношение к использованию
при шоке коллоид-содержащих растворов, мы
делаем исключение для крайне тяжелых новорож-
денных или недоношенных детей с септицемией.
Чтобы восполнить дефицит таких компонентов
сыворотки как фибронектин и комплемент, мы
переливаем свежезамороженную плазму. Скорость
и объем переливаемых растворов определяются в за-
висимости от реакции больного на первоначаль-
ную инфузию, после которой адекватность вое
полнения дефицита жидкости оценивается по вели-
чине диуреза, концентрации мочи, кислотности
плазмы, оксигенации, артериального давления, ЦВД
и, если необходимо, давления заклинивания. При
сердечной недостаточности продолжающееся вве-
дение больших объемов жидкости вызывает увели-
чение преднагрузки на ослабленный миокард и
усугубляет таким образом тяжесть состояния. В
подобных ситуациях применяют инотропные препа-
раты с мониторингом функции сердца и легких,
как описано выше.
Септический шок — распространенная форма шо-
ка, которая отличается от других его видов. Кар-
диогенный, экстракардиальный обструктивный и
гиповолемический шок ведут к уменьшению минут-
ного объема, в то время как септический шок вызы-
вает значительное снижение резистентности сосу-
дов и генерализованное перераспределение кро-
ви.37 Патофизиологический механизм септического
шока начинается с очага инфекции. Инфекцион-
ные агенты могут проникать в кровяное русло
или, размножаясь в очаге, высвобождать различ-
ные медиаторы, которые поступают в кровоток.
В настоящее время со всей очевидностью доказано,
что экзогенные вещества (например те, что проду-
цируются микроорганизмами — липосахариды, эн-
дотоксин, экзотоксин, расщепленные жиры и др.)
могут вызывать септический шок, стимулируя вы-
свобождение эндотоксинов в организме больного
(цитокинины, лейкотриены и эндорфины).
Из эндогенных медиаторов центральную роль
в реакции организма на инфекцию играют цитоки-
нины. Эндотоксин, мурамил-дипептид и экзоток-
син могут способствовать высвобождению фактора
опухолевого некроза (ОНФ) и, возможно, именно
через этот эндогенный медиатор оказывать свое
ФИЗИОЛОГИЯ РЕБЕНКА 25
токсическое воздействие.38-40 Антитела против
ОНФ защищают животных от эндотоксина и бак-
териальной агрессии. ' ОНФ представляет собой
157-аминоацид-гормон, продуцируемый «моноцита-
ми, микрофагами, лимфоцитами, клетками-килле-
рами и Купферовскими клетками печени. Эффек-
тивными стимуляторами продукции ОНФ явля-
ются эндотоксин, энтеротоксин, вирусы, С5а —
фрагмент комплемента, грибковые и паразитарные
антигены, интерлейкин-1 (ИЛ-1) и сам ОНФ.
ОНФ обладает разнообразным эффектом, в том
числе высвобождает фактор, стимулирующий ко-
лонии гранулоцитов-макрофагов (ФСК ГМ), ин-
терферон и интерлейкин-1, а также вызывает из-
менения в сосудистом эндотелии.
Интерлейкин-1 (ИЛ-1) продуцируется макрофа-
гами и другими клетками в ответ на воздействие
эндотоксина и иных бактериальных компонентов.
ИЛ-1 известен также, как эндогенный пироген,
играющий центральную роль в стимуляции разно-
образных реакций организма, включая температур-
ную реакцию, активацию лимфоцитов и стимуля-
цию эндотелиальных клеток, которые увеличи-
вают прокоагулянтную активность. ИЛ-1 вызывает
также индукцию ингибитора активации тканевого
плазминогена и продукцию ФСК-ГМ. Эти эф-
фекты уравновешиваются высвобождением фак-
тора, активирующего тромбоциты (ФАТ) и мета-
болиты.
Интерлейкин-2 (ИЛ-2) продуцируется активи-
зированными Т-лимфоцитами. Клинически его
действие выражается в тахикардии, гипотензии,
увеличении сердечного индекса, уменьшении сис-
темной сосудистой резистентности и левожелу-
дочковой фракции сердечного выброса. "
ФАТ продуцируется нейтрофилами, базофилами,
макрофагами, тромбоцитами и эндотелиальными
клетками. Этот фактор обладает разнообразным
действием, включая активацию и агрегацию тром-
боцитов, сокращение гладких мышц, гипотензию,
увеличение проницаемости сосудов. В модели грам-
отрицательного сепсиса, вызванного эндотоксином
у животных, профилактическое лечение антагони-
стом ФАТ значительно предотвращало уменьше-
ние системного артериального давления и дав-
ления в левой половине сердца, а также сердечного
выброса.45 В то же время антагонист ФАТ оказы-
вал незначительное воздействие на легочную ги-
пертензию. Эти данные подтверждают положение
о том, что при септическом ниже ФАТ играет
важную роль в возникновении изменений перифе-
рической гемодинамики, но поражение легких при
этом связано скорее всего с другими медиаторами.
Эндотоксин — липополисахарид, обнаруживае-
мый в наружной мембране грамотр и нательных бак-
терий. Функционально его молекула разделена на
3 части: (1) высоко вариабельная боковая це-
почка атомов О-полисахарида (придает ссротипи-
ческую специфичность бактерии и может акти-
вировать альтернативный путь комплемента); (2)
центральная часть (мало вариабельная у различ-
ных грамотрицательных бактерий, антитела к этой
части могут быть перекрестно защищены); и (3)
липид А (именно он и обеспечивает главным об-
разом токсичность эндотоксина), который сти-
мулирует ОНФ и может непосредственно акти-
визировать классический путь комплемента при
отсутствии антител. Клиническое исследование,
проведенное в Ю88 г. и основанное на серийных
определениях уровня эндотоксина у 100 пациентов
с септическим шоком, выявило повышенное содер-
жание эндотоксина у 43 больных.46 Эндотоксемия
сопровождалась высокой летальностью. Однако
лишь 26% пациентов из тех, у кого был высокий
уровень эндотоксина, имели подтвержденную грам-
отринательную бактериемию. Эти данные позво-
ляют говорить о том, что эндотоксин играет важ-
ную роль в патогенезе септического шока, причем
не только при грамотрицателыюм сепсисе. Иссле-
дования последних лет сосредоточены на разра-
ботке антител к эндотоксину для использования их
в лечении септического шока
Особенности септического шока в незрелом
организме. Исследования, проведенные в экспери-
менте на животных (собаки), подтвердили, что
септический шок, вызванный кишечной палочкой,
сопровождается у незрелых животных большей
летальностью и что механизм поражения тканей
при одинаковой дозе на единицу массы тела может
быть различен по сравнению со зрелыми осо-
бями.4 Особенности реакции незрелых животных
на инфузию живой кишечной палочки были следу-
ющими.
1. У незрелых животных отмечается раннее (че-
рез I час) падение артериального давления с не-
большим восстановлением через 2 часа, однако
с последующим ухудшением к 4-му часу. У взрос-
лых собак снижение артериального давления вы-
являлось через 2 часа, и затем наступал период
стабилизации, который длился до конца 6-часового
периода наблюдения.
2. У незрелых животных через 1 час падала
ЧСС, а затем отмечалась постоянная тахикардия,
вплоть до смерти. У взрослых собак ЧСС была
стабильной в течение всех 6 часов эксперимента.
3. У незрелых животных отмечалось первона-
чальное (1 час) увеличение концентрации глю-
козы, которое сменялось резким сс падением в тече-
ние 4 часов. У взрослых собак после постепенного
снижения этого показателя в течение первых 4 ча-
сов наблюдалась последующая стабилизация.
4. У незрелых животных выявлялось значитель-
ное снижение pH с выраженным ацидозом через
4 часа. У зрелых собак падение pH было уме-
ренным.
5. У незрелых животных развивалась гипоксия,
не отмечавшаяся у зрелых особей.
6. Незрелые животные жили в среднем 3,1 часа,
зрелые— 18,5 часа.
Посмертное макроскопическое исследование вы-
являло бледность кишечной слизистой с участками
некротизированных клеток в криптах у незрелых
собак. У взрослых животных отмечались геморра-
гии с некрозом сосочков и крипт. Эти данные под-
черкивают существование количественных и/или
26 ФИЗИОЛОГИЯ РЕБЕНКА
качественных различий в медиаторах септического
шока у детей и взрослых.
Защитные механизмы новорожденного могут
успешно противостоять обычной микробной агрес-
сии. При массивном бактериальном внедрении воз-
можности самозащиты ограничены, чем и объясня-
ется высокая летальность при тяжелом сепсисе.
Иммунная система состоит из 4 основных компо-
нентов: клеточный иммунитет (Т-клетки), система
комплемента, иммунитет, обусловленный антите-
лами (В-клетки), и фагоцитарная система макро-
фагов/нейтрофилов. Дефицит двух наиболее важ-
ных из этих звеньев (количественные и качествен
ныс изменения в фагоцитарной системе и дефекты
в иммунитете, обусловленном антителами) увели-
чивает риск бактериального сепсиса у новорож-
денных.
Нейтрофильная недостаточность. Скорость
пролиферации гранулоцитов-макрофагов очень вы-
сока.48 Однако у новорожденных запасы нейтро-
филов значительно уменьшены по сравнению со
взрослыми, поэтому при внедрении бактериальной
инфекции новорожденные не в состоянии ни уве-
личить клеточную пролиферацию, ни использо-
вать скудные нейтрофильные запасы. Разнообраз-
ные отклонения обнаруживаются in vitro у ново-
рожденных в полиморфно-ядерных нейтрофилах
(ИМИ), особенно в стрессовых ситуациях или при
наличии инфекции.49 Эти нарушения включают
пониженную способность к деформации, хемотак-
сису, уничтожению бактерий и фагоцитозу, сниже-
ние уровня СЗ-компонента комплемента. Хемотак-
сис ослабляется в нейтрофилах новорожденного
в ответ на действие различных бактериальных ор-
ганизмов и комплексов антиген-антитело.50 Хотя
установлено, что фагоцитоз также нарушен у но-
ворожденного, однако эти изменения возникают
вторично в результате снижения опсоничсской ак-
тивности, а не являются врожденным дефектом
11М Н новорожденного. 1 52
Гуморальная и опсоническая недостаточность.
Как у недоношенных, так и у доношенных ново-
рожденных отмечается ослабленная реакция на
различную антигенную ' стимуляцию, сниженный
уровень при рождении гаммаглобулинов и недоста-
точное снабжение материнским иммуноглобулином
через плаценту. Почти у 33% детей, родившихся
с массой тела меньше 1500 г, развивается выра
женная гиногаммаглобулинемия с показателем IgG
меньше 200 мг%.53 IgA и IgM также находятся на
низком уровне из-за сниженной способности этих
двух иммуноглобулинов проходить через плаценту,
с чем связана подверженность новорожденных
пиогенной бактериальной инфекции, поскольку
прежде всего именно IgA и IgM опсонируют кап-
сулярные антигены пиогенных бактерий. Неспо-
собность новорожденных продуцировать специфи-
ческие антитела вторична по отношению к ос-
лаблению дифференцировки В-лимфоцитов на
иммуноглобулин-секретирующие клетки плазмы и
Т-лимфоциты, являющиеся медиаторами, которые
способствуют синтезу антител. ' У доношенных
новорожденных общая гемолитическая активность
комплемента, отражающая классический путь, со-
ставляет 50% значений этого показателя у взрос-
лых.56 Активность альтернативного пути компле-
мента также уменьшена у новорожденных.57 Фиб-
ронектин (плазменный протеин, который способ-
ствует ретикулоэндотелиальному очищению от
внедрившихся микроорганизмов) содержится в не-
достаточном количестве в пуповинной плазме.58
Методы усиления защитных механизмов но
ворожденных. При клинических испытаниях эф-
фективности трансфузий гранулоцитов новорож-
денным в возрасте до 28 дней с массой тела более
800 г и признаками тяжелого сепсиса проводилось
либо поддерживающее лечение в сочетании с транс-
фузией лейкоцитов, либо то же самое поддержива-
ющее лечение, но в сочетании с внутривенным
введением иммуноглобулина. Значительное повы-
шение выживаемости отмечено в группе, получав-
шей трансфузии лейкоцитов, при этом никаких от-
рицательных реакций нс зарегистрировано.” От-
носительно ПМН-трапсфузий при лечении сепсиса
новорожденных остается несколько нерешенных
вопросов: (1) в какой группе септических больных
наиболее целесообразно применение этого метода?
(2) оптимальное количество ПМН? (3) частота
трансфузий? (4) роль факторов плазмы, таких,
как внутривенно вводимый гаммаглобулин?
Группа детей с массой тела 1500 г и меньше
получала 500 мг/кг иммуноглобулина внутривен-
но еженедельно в течение 4 недель и сравнивалась
с детьми, которые не получали иммуноглобулин.60
Летальность составила 16% среди получавших
иммуноглобулин и 32% в контрольной группе.
Факторы, стимулирующие колонии. — это семей-
ство гликопротеинов, которые способствуют про-
лиферации и дифференциации кроветворных кле-
ток различного происхождения. ФСК-ГМ и ФСК-
гранулоцитов обладают одинаковым действием. И
тот и другой стимулируют пролиферацию клеток
костного мозга, индуцируя освобождение его ней-
трофильных запасов и усиливая функцию зрелых
нейтрофилов.61, 62 Предварительное изучение при-
менения ФС’К I М у новорожденных животных по-
казывает увеличение нейтрофильного окислитель-
ного метаболизма так же, как и стимуляцию
способности нейтрофилов новорожденного к хемо-
таксису и уничтожению бактерий. Как ФСЖ-ГМ,
так и ФСК-Г после интраперитонеального введе-
ния индуцируют в периферической крови нейтро-
филию, которая отмечается в течение 2—6 часов,
а затем, через 24 часа, количество нейтрофилов
возвращается к исходному уровню.63 Эти предвари-
тельные исследования позволяю г говорить о важ-
ной роли лимфокинов в лечении сепсиса новорож-
денных в будущем.
ФИЗИОЛОГИЯ РЕБЕНКА 27
ЛИТЕРАТУРА
1. Cornblath М. Schwartz R: Disorders of Carbohydrate Metaba
lism in Infancy, second edition. WB Saunders, Philadelphia,
1976.
2. Dweck IIS. Cassady G: Glucose intolerance in infants of very
low birth weight. I. Incidence of hyperglycemia in infants of
birth weights 1,110 grams or less. Pediatrics 53; 189—195.
1974.
3. Ziegler EE. O’Donnell AM. Nelson SF, et al.: Body composition
of reference fetus. Growth 40:329, 1976.
4. Colozzi AE: Clamping of the umbilical cord. Ils effect on the
placental transfusion. N Engl J Med 250:629, 1954.
5. Bauer C, Ludwig I, Ludwig M: Different effects of 2.3-diphos-
phoglyceratc and adenosine triphosphate on the oxygen affinity
of adult and fetal human hemoglobin. Life Sei 7:1339, 1968.
6. Osborn LM, Lenarsky C, Oakes RC, Reiff MI; Phototherapy in
full-term infants with hemolytic disease secondary to ABO in-
compatibility. Pediatrics 73:520 526, 1984.
7. Biglan AW, Cheng KP, Brown DR: Update on retinopathy of
prematurity. Intern Ophthalmol Clin 29:2—4. 1989.
8. Brann AW Jr. Cefato RC: Guidelines for perinatal care. Am
Acad Pediatr Am Col Obstct Gynecol 216, 1983.
9. National Institutes of Health: Cryotherapy for retinopathy of
prematurity cooperative group. Multicenter trial of cryotherapy
for retinopathy of prematurity. Arch Ophthalmol 106:471—479.
1988-
10. Karlbcrg P. Moore RE, Oliver TK: The thermogenic response of
the newborn infant to noradrenaline. Acta Paediatr Scand
51:284, 1962.
II. Stein L Chou H, Lee M, et al.: Effects of muscle relaxants, se-
datives, narcotics and anesthetics on neonatal thermogenesis. In
Pannell M (Editor). Surgical Forum, volume 38. American Col-
lege of Surgeons, Chicago, p 76, 1987.
12. Landsberg L, Young JB: Fasting, feeding and regulation of the
Sympathetic nervous system. N Engl J Med 198:1295, 1978.
13. Lorenz JM, Kleinman LI, Kotagal UR, et al.: Water balance in
very low birth weight infants: Relationship to waler and sodium
intake and effect on outcome. J Pediatr 101:423 432, 1982.
14. Aperia A, Brobcrger O, Herin P, el al.: Postnatal control of
water and electrolyte homeostatis in pre-term and full-term in-
fants. Acta Paediatr Scand 305:61—65, 1983-
15. Boros SJ: Variation in inspiratory: expiratory ratio and airway
pressure wave form during mechanical ventilation: The signifi-
cance of mean airway pressure. J Pediatr 94:114—117, 1979.
16. Ciszek TA, Modanlon HD, Owings D, et al.: Mean airway pres-
sure significance during mechanical ventilation in neonates.
J Pediatr 99:121 126, 1981.
17. Raincr I, Hernandez J, Accurso F: Low peak inspiratory pressu-
res for ventilation of infants with hyaline membrane disease.
J Pediatr 100:802—804, 1982-
18. Soil RF, Holkstra RE, Fangman JJ, et al.: Multicenter trial of
single-dose modified bovine surfactant extract (Survanta) for
prevention of respiratory distress syndrome. Pediatrics
85:1092—1102, 1990.
19. Corbet A. Bucciarelli R, Goldman S, et al.: Decreased mortality
rate among small premature infants treated at birth with a single
dose of synthetic surfactant: A multicenter controlled trial. J Pe-
diatr 118:277—284, 1991.
20. Aulen RL, Notter RH, Kendtg JW, ct al.: Surfactant treatment of
full-tenn newborns with respiratory failure. Pediatrics 87:101
107, 1991.
21. Garg AK: “Arlerialized" capillary blood. (Letter) Can Med
Assoc J 104:16, 1972.
22. Glasgow JF, Flynn DM, Swyer PR: A comparison of descending
aortic and “arlerialized ” capillary blood in I he sick newborn.
Can Med Assoc J 106:660, 1972.
23. Siggniird-Andersen O: Acid-base and blood gas parameters —
arterial or capillary blood? Scand J Clin Lab Invest 21:289.
1968.
24. Reynolds GJ, Yu VYH: Guidelines for rhe use of pulse oximetry
in the noninvasive estimation of oxygen saturation in oxygcndc-
pendent newborn infants. Aust Paediatr J 24:346—350. 1988.
25. Weil MH, Rackow EC. Trevino R, ci al.: Difference in acidbase
state between venous and arterial blood during cardiopulmonary
resuscitation. N Engl J Med 315:153—156, 1986.
26. McEvcrdy BAB, McLeod ME, et al.: End-tidal carbon dioxide
measurements in critically ill neonates: A comparison of sidestre-
am capnometers. Can J Anacsth 37:322—326, 1990.
27. Nonerman DA, Castello FV, Steinberg C, et al.: A comparison of
thermodilution and pulsed Doppler cardiac output measurement
in critically ill children. J Pediatr 115:554—560, 1989.
28. Van de Water JM, Phillips PA, Thouin LG, et al.: Bioelectric
impedance: New developments and clinical application. Arch
Surg 102:541, 1971.
29. Spinalc FG: Relationship of bioimpedance to themodilution and
electrocardiographic measurements of cardiac function. Cril Ca-
re Med 18:414 418, 1990.
30. Nelson LD: Application of venous saturation monitoring. In
Civetta JM, Taylor RW, Kirby RR (Editors). Critical Care.
J В 1 ippincott, Philadelphia, pp 327—334, 1988.
31. Norfleet EA. Watson CB: Continuous mixed venous oxygen
saturation measurement: A significant advance in hemodynamic
monitoring? J Clin Monit 1:245—258. 1985.
32. Driscoll DJ, Gillette PC, Ezrailson EG. et al.: Inotropic response
of the neonatal canine myocardium to dopamine and dobutamine
in the newborn dog. Pediatr Res 13:1006—1009, 1979.
33. Park MK. Sheridan PH, Morgan WW, et al.: Comparative inot-
ropic response of newborn and adult rabbit papillary muscles to
isoproterenol and calcium. Dev Pharmacol Ther 1:70—82. 1980.
34. Jarenwattananon M, Buckley BJ. Goolman N, et al.: Agedepen-
dent cardiovascular effects of verapamil in newborn swine. Pcdi-
alr Res 20:428—432, 1986.
35. DiSessa TG, Leitner M, Ti CC, et al.: The cardiovascular ef-
fects of dopamine in the severely asphyxiated neonate. J Pediatr
99:772 776, 1981.
36. Perkin RM, Levin DL, Webb R, et al.: Dobutamine: A hemody-
namic evaluation in children with shock. J Pediatr 100:977—
983, 1982.
37. Parrillo JE: Septic shock in humans. Advances in the understan-
ding of pathogenesis, cardiovascular dysfunction, and therapy.
Ann Intern Med 113:227—242. 1990.
38, Tracey KJ, Lowry SF, Ccrami A: Chacheciin: A hormone that
triggers acute shock and chronic cachexia. J Infect Dis
157:413 420, 1988.
39. Nedwin GE, Svedersky LP, Bringman TS: Effect of inlerleu-
kin-2, interferon-gamma and mitogens on the production of tu-
mor necrosis factors alpha and beta. J Immunol 135:2492—
2497, 1985.
40. Jupin C. Anderson S, Damais C, et al.: Toxic shock syndrome
toxin I as an inducer of human tumor necrosis factors and gam-
ma interferon. J Exp Med 167:752—761, 1988.
41. Tracey KJ, Fong Y, Hesse DG, el al.: Anli-cachectin/TNF mo-
noclonal antibodies prevent septic shock during lethal bacterae-
mia. Nature 330:662—664, 1987.
42. Bcutlcr Ba Milsaark IW, Cerami AC: Passive immunization aga-
inst cachectin/tumor necrosis factor protects mice from the let-
hal effects of endotoxin. Science 229:869— 871, 1981.
43. Rosenstein M, Ellinghausen SE, Rosenberg SA: Extravasation
of intravascular fluid mediated by the systemic administration of
recombinant interleukin-!. Immunol 137:1735, 1986.
44. Ognibene FP, Rosenberg SA, Lotze M, el al.: lnlerleukin-2 ad-
28 ФИЗИОЛОГИЯ РЕБЕНКА
ministration causes reversible hemodynamic changes and left
ventricular dysfunction similar to those seen in septic shock.
Chesl 94:750, 1988.
45. Toyofuku T, Kubo K, Kobayashi T, et al.: Effects of
ONO-6240, a platelet-activating factor antagonist, on endotoxin
shock in unanesthetized sheep. Prostaglandins 31:271—281,
1986.
46. Danner R. Elin RJ. Hosline KM, el al.: Endotoxin determinati-
ons in 100 patients with septic shock. Clin Res 36:453A, 1988.
47. Pryor RW, Hinshaw LB: Sepsis/septic shock in adults and chil
dren. Pathol Immunopalhol Res 8:222 230. 1989.
48. Christensen RD, Harper ТЕ, Rothstein G: Granulocyte-macro-
phage progenitor cell (CFU-GM) in term and preterm neonates.
J Pediatr 109:1042 1051. 1986.
49. Hill HR: Biochemical, structural and functional abnormalities of
polymorphonuclear leukocytes in the neonate. Pediatr Res
22:375—382, 1987.
50. Miller M: Chemotactic function in the human neonate: Humoral
and cellular aspects. Pediatr Res 5:487 492, 1971.
51- Miller MF: Phagocytosis in the newborn: Humoral and cellular
factors. J Pediatr 75:255—259, 1969.
52. Forman ML, Stiehm ER: Impaired opsonic activity but normal
phagocytosis in low-birth-weight rhfa'nis. N Engl J Med
281:926—931, 1969.
53. Cates KL, Rowe JC, Ballow M: The premature infant as a comp-
romised host. Curr Probl Pediatr 13:1 63. 1983.
54. Baskhurst AP, Morilo T, Williams RC: Studies of human cord
blood and adult lymphocyte interactions with in vitro immuno-
globulin production. J Clin Invest 64:990—995, 1979.
55. Nagaoki T, Mitawaki T, Ctorbaru R. et al.: Maturation of В cell
differentia lion ability and T cell regulatory function during child
growth assessed in a Nocardia water-soluble mitogen-drive sys-
tem. J Immunol 126:2015—2019, 1981.
56. Anderson DC. Hughes BJ. Edwards MS, el al.: Impaired chemo-
laxigeiicsis by type ill group В streptococci in neonatal sera:
Rcintionship to diminished concentration of specific anticapsular
antibody and abnormalities of serum complement. Pediatr Res
17:496—502. 1983.
57. Slossel TP, Alpcr CH, Rosen F: Opsonic activity in the new-
born: Role of properdin. Pediatrics 52:134 137, 1973.
58. Gerdes JS. Yoder M<\ Douglas SD, et al.: Decreased plasma
fibronectin in neonatal sepsis. Pediatrics 72:877—88 L 1983.
59. Cairo MS, Sender L, Worcester C, et al.: A prospective randomi-
zed trial demonstrating the importance of bone marrow reserves
and the advantage of PMN transfusion vs. intravenous gamma-
globulin or supportive care in neonatal sepsis: Preliminary obser-
vations and expansion of previous study population. Abstracted.
Pediatr Res 23:471 A. 1988.
60. Chirico G, Rondini G, Plebani A. et al.: Intravenous gamma-
globulin therapy for prophylaxis of infection in high-risk neona-
tes. J Pediatr 110:437—442, 1987.
61. Clark SC, Kamen R: The human hematopoietic colony-stimula-
ting factors. Science 236:1229—1237, 1987.
62. Sieff CA: Hematopoietic growth factors. J Clin Invest 79:1549,
1987.
63. Cairo MS. Van de Ven C. Toy C, et al.: Lymphokines: Enhance-
ment by granulocyte-macrophage and granulocyte colonystimu-
laling factors of neonatal myeloid kinetics and functional activa-
tion of polymorphonuclear leukocytes. Rev Infect Dis 12(suppl)
4:S492—497, 1990.
Глава 2
ЭНТЕРАЛЬНОЕ
И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
Интерес к вопросам питания хирургических боль-
ных стимулировался в последние два десятилетия
достижениями в области энтерального и паренте-
рального питания. Наиболее значительной вехой
на этом пути, несомненно, было введение Dud rick
и его коллегами в 1968 г. парентерального питания
в клиническую практику, что заставило врачей
обратить внимание на особенности течения забо-
леваний, связанные с питанием.'* ~ Вопросы по-
требностей в питании продолжают постоянно пере-
сматриваться до настоящего времени по мере раз-
работки проблем лечения различных видов пато-
логии.
В Соединенных Штатах наиболее высокая час-
тота нарушений питания отмечается среди стацио-
нарных больных, что, несомненно, отрицательно
сказывается на процессе их выздоровления. Осо-
бенно тяжелые изменения питания, в частности
белковая недостаточность, нередко возникают по-
сле гравм и больших хирургических вмешательств.
Вопросы питания детей, по сравнению со взрос-
лыми, представляют сложную проблему, что связа-
но с особой спецификой потребностей растущего
организма, наиболее выраженной у грудных мла-
денцев. Поэтому именно тетям младшей возраст-
ной группы будет посвящена данная глава.
ФИЗИОЛОГИЧЕСКИЕ ПОТРЕБНОСТИ
Вода абсолютно необходима для существования
организма и по значимости уступает место лишь
кислороду. Отсутствие воды приводит к смерти
в течение нескольких дней. Содержание ее в орга-
низме грудных детей выше, чем у взрослых (75%
массы тела, у взрослых — 65%) (рис. 2-1)/ Основ-
ные запасы воды содержатся в жидкостях орга-
Рис. 2-1. Общее количество воды (ОВТ — об-
щая вода тела) и экстрацеллюлярной жидкости
(ЭЦЖ) в организме уменьшается по мере роста
ребенка, количество интрацеллюлярной жидкости
(ИЦЖ) возрастает.
30 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
низма, однако часть ее обеспечивается за счет про-
цессов окисления пиши и тканей. Грудной ребенок
нуждается в значительно большем количестве во-
ды на единицу массы тела, чем,взрослый. Если же
воду рассчитывать на 100 получаемых килокало-
рий, то необходимое количество будет одинаковым
у детей и взрослых (табл. 2-1).
ТАБЛИЦА 2-1. Суточные потребности в жидкости
Масса тела Объем
<2 кг 150 мл/кг
2 10 кг ИИ) мл/кг
10 20 KI 1000 мл -J-50 мл на каждый кг свыше 10 кг
> 20 кг 1500 мл -j- 20 мл и» каждый кг свыше 20 кг
Суточное потребление жидкости у здорового ре-
бенка равно 10—15% массы тела, в то время как
у взрослого человека всего 2—4% МТ. Кроме того,
пища, употребляемая детьми, содержит намного
больше воды, чем пища взрослых. Тс фрукты
и овощи, которые обычно входят в пищевой ра-
цион ребенка, состоят почти на 90% из воды. Од-
нако лишь 0,5—3% получаемой детьми жидкости
удерживается в организме, в то время как около
50% выводится почками, 3—10%—желудочно-
кишечным трактом и 40—50% входит в состав не-
ощутимых потерь.
Килокалории. Энергетические потребности де-
тей существенно различаются в зависимости от
возраста и ряда других обстоятельств (табл. 2-2).
Хорошо сбалансированная диета должна включать
в себя 15% белка, 35% жира и 50% углеводов.
Взрослый человек нуждается в 150 небелковых ки-
локалориях на каждый грамм полученного азота.
Потребность в белке увеличивается в состояниях
стресса и травмы, однако до настоящего времени
не известно, каким должно быть при этом соотно-
шении небелковых килокалорий и азота. Прове
денные исследования показали достоверно одно —
у маленьких детей после больших операций это
соотношение должно быть как минимум 230; I.4
Белки. Потребности в белках у грудных детей
определяются необходимостью не только поддер-
жания организма, но и роста. Белки составляют
20% массы тела взрослого человека, азот — 2%
МТ у маленького ребенка и 3% — у взрослого.
Наибольший рост содержания азота в организме
происходит в течение первого года жизни. Пита-
тельная ценность белка определяется содержанием
в нем не только азота, но и аминокислот. Из 20 из-
вестных аминокислот 9 являются эссенциальными,
т. е. необходимыми грудному ребенку (табл. 2-3).
ТАБЛИЦА 2-2. Потребности в энергии и белках
Возраст (и годах) Ккал/кг Белок г/кг
0—1 90 120 2,0—3,5
1—7 75—90 2,0—2.5
7—12 60—75 2,0
12—18 30 60 1,5
>18 25—30 1,0
ТАБЛИЦА 2-3. Эссенциальные аминокислоты
Треонин
Лейцин
И золей ЦИII
Валин
Лизин
Мет конин
Фенилаланин
Триптофан
Гистидин •
Тирозин ••
Цистин ••
• необходим только грудным детям
• • может быть необходим недоношенным детям
Новая ткань не может образовываться в организ-
ме, если все эссенциальные аминокислоты не по-
ступают одновременно. Отсутствие даже одной из
них приводит к отрицательному азотистому и бел-
ковому балансу. Общий уровень белков плазмы
колеблется у здоровых детей от 60 до 75 г/л, с не-
сколько более низкими показателями у новорож-
денных и недоношенных.
Углеводы. Наибольшая часть энергетических по-
требностей обеспечивается углеводами, запасы ко-
торых состоят главным образом из гликогена в пе-
чени и мышцах. Однако, поскольку у грудного
ребенка относительная масса печени и мышц зна-
чительно меньше, чем у взрослого, то и гликоген-
ные запасы существенно снижены по сравнению со
взрослыми. Гликоген превращается в глюкозу в
печени и затем преобразуется в тканях, либо ана-
эробным путем в молочную кислоту либо аэроб-
ным — в углекислоту и воду. В результате аэроб-
ного метаболизма образуется значительно больше
энергии в виде аденозинтрифосфата (АТФ).
Жиры — еще один вид существенных запасов
небелковых калорий. Жиры, как находящиеся в
организме, так и поступающие с нищей, состоят
в основном из простых липидов, преимущественно
триглицеридов. Натуральные жиры содержат жир-
ные кислоты, насыщенные и ненасыщенные.
Человеческий организм не синтезирует линоле-
вую кислоту, поэтому она считается незаменимой
и соответственно должна содержаться в пище. Ее
дефицит проявляется сухостью и утолщением кожи
с типичными высыпаниями и шелушением. Если
ребенок получает 1 —2% килокалорий в виде ли-
нолевой кислоты, недостаточность ее не возникает.
Вопрос о необходимости для организма линолено-
вой кислоты продолжает оставаться спорным, хотя
дети, находящиеся на длительном парентеральном
питании жировыми эмульсиями, содержащими 78%
линолевой кислоты и лишь 0,5% линоленовой, мо-
гут давать неврологические расстройства, которые
удается купировать введением эмульсий, содержа
щих 54% линолевой кислоты и 8% линоленовой.5
Минералы и витамины. Быстро растущий ребе-
нок нуждается в большем количестве минералов,
чем взрослый, особенно это касается фосфора
и кальция. Содержание минералов в организме
плода низкое, к моменту рождения они составляют
лишь 3% массы тела, постепенно увеличиваясь
в течение всего детства. При этом растет как абсо-
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 31
ТАБЛИЦА 2-4. Электролитные добавки, рекомендуемые при ТПП (потное парентеральное питание)
Электролиты Грудные дети (<_ 10 кг) Старшие дети (10 30 кг) Подростки о 30 кг)
Кальций 0.5 3,0 мэкв/кг/сут 5 20 мэкв/сут 10—15 мэкв/сут
Магний 0,5—1,0 мэкв/кг/сут 4 24 мэкв/сут 8 24 мэкв/сут
Калий 2—4 мэкв/кг/сут 20—240 мэкв/сут 90—240 мэкв/сут
Натрий 2—4 мэкв/кг/сут 20 150 мэкв/суг 60 150 м.экп/сут
Ацетат 2 8 мэкв/кг/сут 20- 120 мэкв/сут 80 120 мэкв/сут
Хлор 4 12 мэкв/кг/сут 20 150 мэкв/сут 60 150 мэкв/сут
Фосфор 0,5—1,(1 ммоль/кг/сут 6—50 ммоль/сут 30—50 ммоль/сут
лютное, так и относительное количество минера-
лов, в результате у взрослого человека их в 40 раз
больше, чем у новорожденного, в то врем и как мас-
са тела взрослого лишь в 23 раза превышает МТ
новорожденного. На каждый грамм белка в орга-
низме откладывается около 0,3 грамма минералов.
Наиболее важные электролиты, требующиеся для
организма — кальций, магний, калий, натрий, фос-
фор, сера, хлор (табл. 2-4). Железо, йод и ко-
бальт имеются в организме в составе различных
органических комплексов. Что касается микроэле-
ментов, то характер участия в метаболизме неко-
торых из них известен, например фтора, меди,
цинка, марганца. В то же время селен, кремний,
бор, никель, алюминий, мышьяк, молибден и строн-
ций требуются для организма, но их специфиче-
ское метаболическое действие недостаточно изу-
чено (табл. 2-5).
Витамины для нормального клеточного метабо-
лизма необходимы в минимальных количествах.
Они должны поставляться полностью или час-
тично извне. Витамины группы В действуют как
коэнзимы в различных биохимических реакциях,
специфический же тип действия других витаминов
пока еще недостаточно известен. К жирораствори-
мым витаминам относятся А, Д, К и Е, к водора-
створимым — тиамин, рибофлавин, фолиевая кис-
лота, вит. В12, пиридоксин, никотиновая кислота,
биотин, пантотеновая кислота и вит. С. Поскольку
у человека имеются запасы жирорастворимых ви-
таминов, их избыточное введение может вызывать
различные расстройства. Кроме того, к дефициту
жирорастворимых витаминов приводит нарушение
абсорбции жира (табл. 2-6).
висят от характера и длительности эндокринной
и метаболической реакции на стрессовую ситуа-
цию. Результатом этой реакции могут быть такие
осложнения, как тяжелая гипотрофии, сердечно-
легочная недостаточность, тромбоэмболия, стрессо-
вые язвы желудка, а также ослабление иммунного
статуса и резко замедленное выздоровление. 617
В то время как у взрослых людей гормональная
и метаболическая реакция на стресс была предме-
том лабораторных и клинических исследований на
протяжении всего последнего столетия, у новорож-
денных детей такое изучение не проводилось. Ме-
таболические изменения или осложнения, вызван-
ные стрессом, могут нарушить хрупкий метаболи-
ческий баланс новорожденного и без того уже
вовлеченного в сложный процесс адаптации к
постнатальной окружающей среде. Нормальные
резервы питательных веществ у новорожденного
ограничены, а нуждающиеся в энергии быстрый
рост и созревание дополняются операцией, предъ-
являющей организму новые требования. Экспери-
ментальные данные показывают более тяжелое по-
слеоперационное течение и летальность у ново-
рожденных по сравнению со старшими детьми или
взрослыми, перенесшими одинаковые хирургиче-
ские вмешательства. ’ При лечении новорожден-
ных необходимо знание специфических особенно-
стей их реакции на стресс.
Реакция эндокринной системы ни хирургиче-
ское вмешательство. Suits и Bottsford 10 описали
нейроэндокринный рефлекторный механизм, кото-
рый приходит в действие под влиянием тяжелого
стресса. Компонентами этого механизма являются
афферентная дуга, состоящая из возбудителей, вы-
ГОРМОНАЛЬНАЯ И МЕТАБОЛИЧЕСКАЯ РЕАКЦИЯ
НА СТРЕСС У НОВОРОЖДЕННЫХ
У взрослых пациентов группы высокого риска тя-
жесть течения послеоперационного или посттрав-
матического периода, равно как и летальность, за-
тлели ЦА 2-5. Рекомендуемые суточные добавки
микроэлементов при ТПП
Микроэлемент Количество (мкг) для детей Количество (мкг> для подростков (шрослых)
Цинк (сульфат) 300 5.0
Медь (сульфат) 20 1.0
Марынец (сульфат) 10 0,5
Хром (хлорид) 0,2 0.010
Селен (в виде селеновой 1.2 0.060
кислоты)
ТАБЛИЦА 2-6. Рекомендуемые суточные добавки витаминов
при ТПП
Витамин Дети Кол-во в сутки Подростки (взрослые) Кол-во в сутки
Аскорбиновая кислота 80 мг 100,0 г
Витамин А 2300 ME 3300 ME
Витамин Д 400 MF 200 ME
Тиамина хлорид (BI) 1,2 мг 3,0 мг
Рибофлавин (В2) 1,4 мг 3.6 мг
Пиридоксина хлорид (Вб) 1.0 мг 4,0 мг
Никотинамид 17 мг 40 мг
Пантотеновая кислота 5 мг 15,0 мг
Витамин Е 7 ME 10.7 ME
Биотин 20 мкг 60 мкг
Фолиевая кислота 140 мкг 400 мкг
Цнанокобаламин (BI2) 1 .мкг 5 .мкг
Фитонадион (К1) 200 мкг 1 мг
32 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
зывающих метаболические реакции, и эфферент-
ная дуга, регулирующая восстановление объема
и продукции энергетического субстрата. Хирурги-
ческий стресс инициирует нейроэндокринный реф-
лекс непосредственно через сигналы по нервным
путям в центральную нервную систему (ЦНС) и
опосредованно, благодаря выработке катехолами-
нов — главных медиаторов гиперметаболических
реакций, и адренокортикоидов — основных актива-
торов этих реакций. Компоненты афферентной ду-
ги, вовлеченные в данный процесс, представтены
периферическими болевыми хемо- и барорецепто-
рами, которые посылают сигналы в гипоталамус,
где, объединяясь, и формируют физиологическую
реакцию на стрессовую ситуацию.
Эфферентная дуга, образующаяся в гипоталаму-
се, имеет ветви, проходящие через автономные
участки ствола мозга и гипофиз. Эти стволовые
структуры посылают тфферептные волокна через
парасимпатическую и симпатическую нервную си-
стему к периферии, действуя на нервномышечные
синапсы и органные рецепторы, которые в свою
очередь стимулируют высвобождение перифериче-
ских гормонов. Реакция же гипофиза заключается
в повышенном выделении адренокортикотропного
гормона (АКТГ), вазопрессина, гормона роста
и высвобождении пролактина.
Новорожденные имеют хорошо развитые боле-
вые нервные проводящие пути." Количество чув-
ствительных нервных окончаний в коже новорож-
денного практически такое же, как у взрослых.
Эти рецепторы обнаруживаются но всей поверхно-
сти кожи и слизистых даже у плода около 20-й не-
дели гестации.12 Таким образом, уже в ранней
внутриутробной жизни имеется начальный компо-
нент афферентной дуги, а соответственно и спо-
собность «запуска» стрессовой реакции.
Эндокринная реакция взрослого пациента на
операционную и неоперационную травму характе-
ризуется прежде всего существенным уменьшени-
ем концентрации основного анаболического гормо-
на — инсулина. Выраженность и продолжитель-
ность этой реакции, в частности изменений кон-
центрации в плазме кортизола, катехоламинов,
глюкагона, гормона роста и вазопрессина, пропор-
циональны тяжести повреждения и послеопераци-
онных осложнений. Возникающие гормональные
сдвиги могут оказывать серьезное воздействие на
метаболический и почечный гомеостаз, гемодина
мику, иммунный статус, функцию ЖКТ, а также
на поведение и психику больного. Возможности
регуляции нарушений метаболизма, вызванных
стрессовыми гормональными изменениями, обсуж-
даются в следующем разделе.
Значительно меньше изучена гормональная ре-
акция на стресс у новорожденных 1етей. Известно
лишь, что она носит преимущественно катаболи-
ческий характер с достоверно установленным по-
вышением уровня катехоламинов и эндорфинов.
Изменения концентрации глюкагона, инсулина,
а также кортизола, полученные при обследовании
новорожденных, нс соответствуют таковым у
взрослых. Эти различия, возможно, связаны с не-
зрелостью организма, однако многие аспекты гор-
мональной реакции на хирургический и нехирур-
гический стресс пока еще недостаточно исследова-
ны в группе новорожденных детей.
Метаболическая реакция на хирургическое
вмешательство (табл. 2-7). На фоне многочис-
ленных исследований метаболической реакции
взрослых на хирургическое вмешательство и трав-
му, у новорожденных эта проблема разработана
недостаточно. Мало подобных исследований и у
грудных детей, что связано отчасти с трудностями
Таблица 2-7. Метаболическая реакция на операционный стресс у взрослых и новорожденных
Метаболиты Взрослые Новорожденные
Скорость метаболизма н | Кратковременно, затем f | По сравнению со взрослыми (минимальные нз-
потребление кислорода менения по сравнению с контрольной группой такого же возраста)
У глеводы f Гипергликемическая реакция f Глюконеогенез и | утилизация глюкозы f Глюкоза 2 X сразу после операции (менее стой- кое f, чем у взрослых) Возможно вторично в результате в большей степени гликогенолиза, чем f глюконеогенеза новорожденные могут быть не н состоянии осу- ществлять печеночный глюконеогенез в связи с недос г«1 точностью основных энзимов
Всяки Отрицательный азотистый баланс Слегка f распад белка — зависит от тяжести стресса; f с увеличением тяже- сти | Синтез белка но внепеченочных тканях f У гилизация аминокислот для глюконео- генеза f Выделение изо га — н течение периода до 5 дней Отрицательный азотистый баланс в течение 72—96 час после операции f Потери азота у новорожденных по сравнению со старшими детьми f Мышечный распад белка, нарушенная утилиза- ция азота, гранзиторное ♦ выделение азота | (R противоположность взрослым) образовав- шихся в результате глюконеогенеза аминокислот в плазме
Жиры Липолиз жировой ткани —► мобилизация не- эстерифици роваи пых жирных кислот и f образования кетоновых тел Kioncy (1970) — 75—90% потребностей в послеоперационном периоде обеспечи- ваются за счет жирового метаболизма (10—25% за счет белка) f Липолиз кетогенез (? в результате стимуляции катехоламинами) -* f общие кетоновые тела f глицерин, f иеэстсрифицироваиные жирные КИСЛОТЫ Утилизация жира в послеоперационном периоде превышает скорость высвобождения свободных жирных кислот
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 33
в проведении длительного наблюдения, а также
в значительной степени с этическими ограничения-
ми в отношении многократных заборов немалых
количеств крови для анализов. В то же время не
вызывает сомнения, что послеоперационное лече-
ние могло быть намного более эффективным, если
были бы понятны механизмы воздействия стресса
на обмен веществ. Ясно лишь, что новорожденные
часто реагируют на стресс и травму совершенно
иначе, чем старшие дети и взрослые пациенты.
У взрослых после травмы или хирургического
вмешательства отмечается увеличение потребле-
ния кислорода (VO2). следующее за коротким пе-
риодом сниженной скорости метаболизма. " VO2
доношенного новорожденного, находящегося на
обычном вскармливании, неоперироваиного, уве-
личивается с возрастом примерно до 2-й или
3-й недели жизни.15 Исследования показывают,
что после операций, особенно больших, у новорож-
денных в некоторых случаях отмечаются более
низкие показатели VO2, чем можно было бы ожи-
дать при данном возрасте и массе тела. Ito с со-
авт. 15 установили, что VO2 у новорожденных по-
сле операции в большей степени зависит от количе-
ства получаемых калорий, чем от тяжести хирур-
гического вмешательства. Эти данные находятся
в глубоком противоречии с результатами исследо-
ваний у взрослых, выявляющими ускорение у них
скорости обменных процессов.
Возникающие в ответ на стресс изменения в ор-
ганизме нацелены на удовлетворение возросших
в послеоперационном периоде энергетических и
метаболических запросов. Гипергликемическая ре-
акция направлена на обеспечение увеличенных по-
требностей поврежденных тканей в глюкозе.16
Протеолитический компонент стрессового ответа
способствует образованию аминокислот, необходи-
мых для репаративного синтеза белка, а также
продукции разнообразных веществ печенью.
Ускорение липолиза и кетогенеза, как один из
компонентов стрессовой реакции, ведет к созданию
альтернативных запасов метаболической пищи тля
таких тканей, как мозг и скелетные мышцы, а от-
мечающийся глюконеогенез вызывает увеличение
снабжения глюкозой тех жизненно важных орга-
нов, деятельность которых зависит в значительной
мерс именно от глюкозы. ' Однако указанные
метаболические изменения могут привести и к не-
желательным эффектам в послеоперационном пе-
риоде или к дальнейшему усилению стрессовой ре-
акции. К таким негативным последствиям относят-
ся состояние гиперметаболизма с соответствующим
повышением VO2, энергетических потребностей,
температуры и сердечного выброса, нарушение
или замедление воспалительной и иммунной ре-
акции.
Многочисленными исследованиями показано,
что взрослые больные, попавшие в ситуацию тяже-
лого травматического стресса, чрезвычайно склон-
ны к таким осложнениям, как сердечная и легоч-
ная недостаточность, инфаркт миокарда, наруше-
ние функции печени или почек, стрессовые язвы
желудка, сепсис. Подобная бурная реакция орга-
низма может быть жизнеугрожающей, особенно ес-
ли вызванная стрессом катаболическая активность
в течение длительного периода остается высокой
или нераспознанной. Выявить с большой степенью
достоверности группу больных с риском летально-
го исхода можно на основании анализа ряда плаз-
менных субстратов, появляющихся в крови за
9 дней до смерти.7
Регулирование иди замедление катаболической
реакции на стрессовую ситуацию может быть до-
статочно эффективным. Изучение вопросов после-
операционного обезболивания показало, что адек-
ватное лечение болевого синдрома приводило
к уменьшению потерь белка и сокращению сроков
выздоровления.19' 0
Новорожденные, даже недоношенные, способны
отвечать на хирургический стресс эндокринной
и метаболической реакцией. К сожалению, многие
аспекты этой проблемы, достаточно хорошо разра-
ботанные у взрослых, слабо исследованы у ново-
рожденных. Что касается взрослых, то их реакция
на стресс является первоначально катаболической
по своей природе, поскольку гормональные изме-
нения состоят в ускоренном освобождении катабо-
лических гормонов, таких как катехоламины, глю-
кагон, кортикостероиды, в сочетании с подавлени-
ем периферической резистентности к действию
основного анаболического гормона — инсулина.
Катехоламины могут играть главную роль в по-
добной ситуации, оказывая влияние на остальные
звенья реакции на стресс, как гормональной, так
и метаболической, включая задержку высвобож-
дения инсулина, значительную гипергликемию и
истощение у новорожденного запасов углеводов,
белков и жиров. Эти изменения в конечном счете
приводят к освобождению глюкозы, неэстерифици-
рованных жирных кислот, кетоновых тел и амино-
кислот. И хотя побочные продукты метаболизма
необходимы для удовлетворения увеличенных
энергетических запросов организма, тяжелая или
длительная метаболическая реакция может резко
негативно сказаться на состоянии новорожденного,
который и без того имеет ограниченные резервы
питательных веществ, что связано как с болезнью,
так и с высокими метаболическими потребностями,
обусловленными ростом, созреванием органов и
адаптацией к постнатальной окружающей среде.
Предварительные исследования показывают, что
введение в практику анестезиологии таких препа-
ратов, как фторотан и фентанил, равно как
и управление иммунным ответом организма на
стресс, может значительно уменьшить интенсив-
ность катаболической реакции. ' “ Дальнейшее
углубленное изучение различных аспектов реак-
ции на стресс у новорожденных может предоста-
вить возможности управления этой реакцией и та-
ким образом будет способствовать уменьшению ча-
стоты осложнений и снижению летальности.
ОЦЕНКА СОСТОЯНИЯ ПИТАНИЯ
Оценка состояния питания должна быть основой
общей оценки состояния любого больного с хирур-
3 Закиз № 1622
34 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
гической патологией, особенно подвергшегося
стрессовому воздействию. Тяжелые нарушения пи-
тания могут быть выявлены при обычном первич-
ном осмотре, даже без антропометрических иссле-
дований и лабораторных анализов. Однако при
средней степени этих изменений порой даже опыт-
ным докторам приходится сталкиваться с серьез-
ными диагностическими трудностями. Раннее вы-
явление пациентов группы риска тяжелых наруше-
ний питания — первая важная ступень в обеспече-
нии адекватного лечения. К счастью, большинство
пациентов с хирургической патоло! ней получают
хорошее питание в процессе лечения, что способст-
вует профилактике возможного стресса при трав-
мах, ускоряет процесс выздоровления, обеспечива-
ет рост организма.
При назначении питания учитываются такие
основные показатели как рост, масса тела, окруж-
ность головы, уровень альбумина и общего белка.
При развитии в послеоперационном периоде ги-
потрофии отмечается медленное заживление ран.
изменение иммунного статуса, высокая частота
осложнений, повышение летальности. Полная
оценка состояния питания должна включать ана-
лиз факторов риска, анамнез, клиническое иссле-
дование, в том числе основные антропометриче-
ские показатели и лабораторные данные, опреде-
ление энергетических потребностей и при необхо-
димости непрямую калориметрию.
Факторы риска обусловлены характером основ-
ного заболевания и перенесенного оперативного
вмешательства. При больших открытых ранах су-
ществует опасность значительных потерь питатель-
ных веществ и соответственно увеличения мета-
болических потребностей. Высокие энергетические
запросы возникают и при обширных ожогах,
тупой закрытой травме, гипертермии. При предше-
ствовавшей потере 10% массы тела или более,
а также предполагаемой невозможности кормления
через рот в течение более, чем 7 дней, следует
начинать поддерживающее питание.
Анамнестические данные о вскармливании ре-
бенка имеют важное значение в оценке состояния
питания. Применение в прошлом специальной дие-
ты, нарушения вкуса и аппетита могут быть при-
знаками серьезных изменений. Клиническое обсле-
дование играет не менее существенную роль. Кро-
ме того, в каждом случае важно учитывать, будет
ли полноценной или нет функция желудочно-ки-
шечного тракта в ближайшем послеоперационном
периоде (24 48 час). Например, после больших
вмешательств на забрюшинном пространстве или
спинном мозге можно ожидать выраженный парез
кишечника, а потому, как правило, требуется дли-
тельное парентеральное питание.
Показатели питания. Поскольку каждая мо-
лекула белка играет определенную жизненную
функцию и поскольку в организме не существует
запасов белка, снижение его содержания свиде-
тельствует о нарушении питания. Именно белко-
вый статус больного является прямым показателем
резервных возможностей реакции на стресс, осо-
бенно когда уменьшены запасы жира и гликогена.
Поэтому для оценки состояния питания более все-
го важно содержание белка, как соматического
(мышечного), так и висцерального (нсмышечно-
го). Однако нет единого теста или показателя,
который изолированно мог бы достоверно отразить
состояние питания больного. С другой стороны,
нет необходимости у каждого больного применять
все существующие методы исследования.
Масса тели. МТ — один из наиболее простых
и важных показателей. Потеря се, часто отражаю-
щая использование белка организма (т. е. ткани
мышц или органов) в качестве субстрата для мета-
болизма, может происходить очень быстро в после-
операционном периоде, если поступление калорий
существенно ограничено. Измеряемая масса тела
больного должна сопоставляться с обычной для не-
го МТ, се динамикой в последнее время и с иде-
альной МТ для данного роста.
Кожная складка плеча. Измерение кожной
складки в области трехглавой мышцы плеча — хо-
роший показатель запасов жира (калорий) в орга-
низме, так как около 50% жировой ткани локали-
зуется в подкожной клетчатке.
Окружность плеча (мышечная). Этот показа-
тель отражает соответствие калорических запасов
и мышечной массы. Окружность плеча измеряется
в средней трети. Часть подлежащей жировой ткани
(кожная складка) вычитается по стандартной фор-
муле. При этом измеряется именно мышечная
окружность плеча, поскольку толщина кости нс
берется в расчет. Кроме этого в формуле преду-
сматривается то, что плечо по форме нс совершен-
но круглое, а сжимаемость жирового слоя может
быть разная (сжимаемость больше у лиц женского
пола и у полных людей).
Висцеральный белок. Энзимы, факторы сверты-
вания, альбумин, глобулины, транспортные белки
и клеточные структуры внутренних органов состо-
ят из висцерального (немышечного) белка, дефи-
цит которого неблагоприятно влияет на иммун-
ную реакцию и раневое заживление. Недостаточ-
ность сывороточного альбумина и трансферрина
отражает нарушение синтеза в печени в результа-
те ограниченного снабжения субстратрм. Сыворо-
точный альбумин в связи с большим периодом по-
лураспада (20 дней) не может быть достоверным
показателем гипотрофии или белкового дефицита.
Намного более чувствительным индикатором бел-
кового статуса является трансферрин (белок,
транспортирующий в организме железо), имею-
щий период полураспада 9 дней, однако его опре-
деление более дорогостояще, сложно и не имеет
смысла при сепсисе или железо-дефиците. Основ-
ным показателем возможности пациента реагиро-
вать на инфекцию является общее количество лим-
фоцитов. Лимфоциты быстро разрушаются, и для
образования новых клеток требуется белок. Соот-
ветственно абсолютное число лимфоцитов помога-
ет определить состояние белковых резервов.
Белок требуется также для синтеза клеток и ме-
диаторов, участвующих в реакции на различные
кожные антигены. Хотя реактивность, определяе-
мая с помощью кожных тестов, отражает лимфо-
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 35
цнт-опосредованный иммунитет, однако в большей
степени она является показателем общего состоя-
ния защитных сил, а не только самой лимфоци-
тарной активности. У больных с острыми и хрони-
ческими нарушениями питания диапазон измене-
ний может быть очень велик — от реактивного
состояния до анергии. Реактивность может быть
восстановлена, благодаря избыточному питанию,
а потому различные кожные тесты являются не-
прямыми показателями состояния питания. Ней-
трофильный хемотаксис (или недостаточность его)
коррелирует с кожной чувствительностью к упомя-
нутым антигенам, подтверждая, что результаты
и других иммунологических тестов могут также
быть непрямыми показателями состояния питания
больного?7
Определение азотистого баланса — способ еже-
дневного контроля потребностей больного в азоте,
так же, как и эффективности проводимого пита-
ния. Для роста или выздоровления у подростков
н взрослых суточный положительный баланс дол-
жен составлять 4—6 г, у детей, в том числе груд-
ных — соответственно меньше. Определение су-
точного баланса бывает несколько затруднено
в связи с необходимостью измерения суточного ди-
уреза. Для расчета азотистого баланса должно
очень тщательно учитываться количество получае-
мого как энтералыю, так и парентерально, белка.
Скорость метаболизма или энергетические по-
требности больного в послеоперационном периоде
могут быть рассчитаны по номограммам, методом
респирометрии или непрямой калориметрии. Но-
мограммы обычно позволяют определить основной
расход энергии в зависимоеги от возраста, роста
и массы тела, а также энергетические траты, свя-
занные с дополнительными факторами, изменяю-
щими основной расход энергии, такими, как после-
операционный стресс, множественная травма, ги-
пертермия, тяжелая инфекция. В таблице 2-8 и на
рисунке 2-2 представлены примеры номограмм,
используемых в настоящее время.
Практически во всех прежних исследованиях по-
требности в питании как здоровых людей, так
и больных, рассчитывались на основе вычислений
энергетических расходов. Ясно, что получаемые
таким образом показатели недостаточно точны.
Наиболее распространенный в настоящее время
метод, достоверно отражающий метаболические
нужды организма, — непрямая калориметрия, ба-
ТЛБЛИЦА 2-8. Скорость осноыких» нбмгиз у хдорокых детей
Возраст в годах Мальчики ккал/ы /час Девочки ккал/м*/час
1 5.5 53
2—3 52 52
4 5 50 49
6—7 48 46
8 9 46 43
10—1 1 44 42
12 13 42 41
14 15 42 39
16 17 41 37
18—19 40 36
Площадь ожога
5
£
ио
Ю5
- - то%
60%
t
Перелом длинных трубчатых костей
Состояние после операции
Перитонит
Незначительная
потеря МТ
I
Комбинированная травма
(пациент на ИВЛ?
Тяжелая инфекция,
комбинированная травма
Рис. 2-2. В. । инн нс различных заболеваний на скорость основ-
ного обмена.
зирующаяся на положении о том, что количество
кислорода, поглощаемого при прохождении через
легкие, равняется его количеству, которое расходу-
ется в метаболических процессах. Этот основной
принцип равенства Fick помогает понять, почему
кислородное потребление является важным показа-
телем метаболизма, даже у пациентов с наруше-
нием функции легких. Энергия, высвобождаемая
в результате оксигенации различных пищевых
компонентов, определяется прямыми измерениями.
Скорость метаболизма, выражаемая в см1 кислоро-
да в мин, может быть переведена в калории в час
или в сутки, если пищевые субстраты известны.
В практических целях принято считать, что 5 ки-
локалорий энергии соответствуют литру потреб-
ленного кислорода. При подобных расчетах ско-
рость метаболизма оказывается несколько выше
ис!ипной, но полученные таким образом цифры
намного более точны, чем показатели, определяе-
мые по диаграммам или таблицам- При использо-
вании метода непрямой калориметрии у грудных
детей со спонтанным дыханием отмечаются более
широкие колебания энергетических затрат у паци-
ентов с той же МТ и гестационным возрастом, чем
при применении номограмм и таблиц, которые
36 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
обычно дают заниженные по меньшей мере до 70%
показатели.’"
Респирометрия — довольно простой метод, при-
меняемый у неинтубированпых пациентов, находя-
щихся на самостоятельном дыхании. Однако мно-
гие тяжелые больные, как правило, интубированы
и находятся на ИВЛ, что затрудняет использова-
ние респирометрии. Для непрямой калориметрии
апробирован миниатюрный прибор, который по-
мещается между респиратором, циклированным по
давлению, и эндотрахеалыюй трубкой, что значи
тельно упрощает измерение потребления кислоро-
да и продукции углекислоты у детей, находящихся
на ИВЛ.’Г
Потребление кислорода может быть определено
следующими способами: (1) измерение прямых из-
менений объема в спирометрической системе с аб-
сорбером углекислоты; (2) измерение объема и со-
става выдыхаемого газа при известном составе
и объеме вдыхаемого и (3) измерение содержания
кислорода в артериальной и смешанной венозной
крови, а также сердечного выброса, с расчетом
затем на основании равенства Fick потребления
кислорода периферическими тканями. Последний
метод требует катетеризации легочной артерии, од-
нако применение его стало более реальным прак-
тически, благодаря добавлению миниатюрных ок-
симетров к небольшим катетерам Swan-Ganz.32
Анализ смешанного выдыхаемого газа — простей-
ший метод у обычных больных, но мало приемле-
мый у пациентов, находящихся на вспомогатель-
ной или искусственной вентиляции, из-за неболь-
ших во время респираторного цикла изменений
вдыхаемого объема и концентрации кислорода.
Прямая объемная спирометрия, лучший способ из-
мерения потребления кислорода, может быть ис-
пользована для одновременного определения про-
дукции углекислоты с помощью капнометра. По
данным VO2 и продукции углекислоты можно вы-
числить дыхательный эквивалент и калорические
расходы, используя уравнение Weir.
Вышеупомянутые методы используются для
оценки состояния питания больного во время опе-
рации, травмы или тяжелых заболеваний. Приме-
няемое с этой целью тщательное клиническое об-
следование порой не менее точно, чем более слож-
ные и дорогостоящие лабораторные и антропо-
метрические измерения.34 Определение клеточной
массы тела показало, что нарушения питания не
могут быть достоверно выявлены на основании со-
отношения рост:МТ, кожной складки, окружности
плеча, силы руки, концентрации альбумина, уров-
ня общего белка." Лишь измерение непосредствен-
ных показателей скорости метаболизма — лучший
метод контроля за состоянием питания у тяжело
больных пациентов.
Таким образом, измерение и опенка скорости
метаболических процессов занимают важное место
в лечении критически больных пациентов. Как ми-
нимум необходимо ежедневно определять суточ-
ный энергетический баланс, а также скорость ме-
таболизма и совокупный калорийный баланс.
У взрослых пациентов с острыми заболеваниями
при дефиците, превышающем 10 000 калорий, на-
много более высок риск летальных исходов, чем
у больных с положительным калорийным балан-
сом.36 Подобные исследования должны быть прове-
дены у детей, в том числе грудных.
ЭНТЕРАЛЬНОЕ ПИТАНИЕ
Человек, который до хирургического вмешательст-
ва или травмы был здоров, может безболезненно
выдержать 5—7 дней без энергетических поставок
извне при условии, что затем будет начато адек-
ватное питание. Однако сохранить массу тела не
так уж трудно. Более важно избежать осложнений,
обычно сопровождающих у критически больных
детей тяжелые нарушения питания, на предотвра-
щение которых и должно быть направлено лечеб-
ное питание. Характер его зависит от формы и вы-
раженности стресса. Вряд ли стоит доказывать, что
с точки зрения физиологичности, эффективности,
усвоения, а также стоимости лечения энтеральное
питание должно быть всегда предпочтительным
и стоять на первом месте среди методов питания
у больных с нормальной функцией ЖКТ. ' Если
же пациент не может усваивать энтеральное пита-
ние, показано полное парентеральное питание
(ТПП).
Энтеральное питание начинают после разреше-
ния послеоперационного пареза, о чем говорит ис-
чезновение примеси желчи и зелени в желудочном
содержимом, количество которого уменьшается,
и наличие регулярного стула. Появление при аус-
культации кишечных шумов — признак, подтверж-
дающий восстановление перистальтики кишечника
у старших детей и подростков, однако в грудном
возрасте этот симптом не столь надежен и достове-
рен. У маленьких пациентов питание начинают
с небольших количеств подслащенной воды или
разбавленных смесей через рот или назогастраль-
ный зонд. У старших детей можно начинать с про-
стых жидкостей малыми порциями, помня о том,
что в восстановительный после стресса период
ЖКТ быстрее приспосабливается к увеличению
объема, чем к повышению осмолярности. В процес-
се наращивания концентрации смесей и/или пищи
до нормальной по возрасту могут возникнуть на-
рушения приспособления к увеличивающейся
осмолярности, что проявляется спазматическими
болями и расстройством стула, в то время как о по-
ниженной толерантности к возрастающему объему
обычно свидетельствует рвота или повышение ко-
личества отделяемого по желудочному зонду.
Стремясь как можно раньше начать энтеральное
питание, нередко используют введение жидкой пи
щи и готовых смесей через назогастральные труб-
ки. Однако резиновые и пластиковые зонды не
очень хорошо переносятся детьми, часто вызывая
раздражение пищевода и желудка и ощущение ди-
скомфорта в носоглотке. В настоящее время появи-
лись новые зонды для питания из более мягких
материалов (силиконовая резина), обработанные
специальным смазывающим веществом. Они име-
ют маленький калибр и вводятся значительно лег-
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 37
че, Некоторые трубки имеют на конце ртутный
утяжелитель, который позволяет проводить их
в 12-перстную или начальный отдел тощей кишки.
Например, зонды для питания Dohbhoff, Nuiraflex
и Entriflex намного лучше переносятся, чем более
жесткие трубки для декомпрессии желудка. Если
пациенту предстоит абдоминальная операция и за-
ранее предполагается, что невозможно будет в
ранние сроки начать кормление, предотвратить
дискомфорт, связанный с длительным стоянием
назогастрального зонда, помогает гастро- или
еюностомня для питания. Сторонники еюностомии,
накладываемой с этой целью, подчеркивают необ-
ходимость ее осуществления непосредственно во
время основной операции и с использованием спе-
циальной техники катсгсризационной еюностомии.
Они указывают также, что достоинством этой ме-
тодики является возможность очень раннего нача-
ла питания, часто в первые 24 часа после боль-
шого абдоминального хирургического вмешатель-
37, 39
ства.
Множество готовых смесей используется для
обычного и специального питания, и каждый год
появляются все новые и новые препараты. Суще-
ствуют и разнообразные классификации питатель-
ных растворов.** Гак, они иногда подразделяются
в зависимое ги о г состояния функции Ж КТ на те,
что могут применяться при интактном Ж КТ, и на
смеси, которые используются при нарушении фун-
кции кишечника. Последние требуют для своего
переваривания значительно меньших затрат. Как
правило, при тяжелых заболеваниях или стрессе
часто развивается недостаточность лактазы, поэто-
му начинать энтеральное питание целесообразно
с безлактозной диеты. После обширных резекций
кишечника и создания стом либо при наличии
спонтанно открывшихся кишечных свишей, когда
невозможно осуществлять оральное питание, необ-
ходимо интубировать стому или свищ с проведени-
ем зонда дистально. Специальные питательные
растворы, вводимые таким путем, могут усваивать-
ся полностью, даже если осталось всего 30—40 см
тонкой кишки. Отделяемое из проксимального сви-
ща можно также вводить в дистальный отдел, что
значительно упрощает задачу восполнения жидко-
стных и электролитных потерь.
Энтеральное питание может быть более эффек-
тивным при соблюдении некоторых правил. Во
первых, как уже было сказано, Ж КТ легче приспо-
сабливается к увеличивающемуся объему, чем
к возрастающей осмолярности. Спазматические бо-
ли, жидкий стул и соответственно нарушение аб-
сорбции можно предотвратить, начиная питание
с разбавленных (в 2 или даже в 4 раза) смесей
с постепенным увеличением их концентрации. Во-
вторых, при капельном введении, по сравнению
с дробным, усвоение лучше, а также значительно
меньше угроза гастроэзофагеального рефлюкса,
рвоты и последующей аспирации. В-третьих, не-
обходимо тщательно следить, чтобы смеси не были
загрязнены ни во время приготовления, ни у посте-
ли больного. Важно обращать внимание на сроки
изготовления, предпочитая свежие растворы. Лече-
ние больных с синдромом короткой кишки с при-
менением Pectin, Mctamucii, Lomotil, Paregoric
и Imodium позволяет достигать значительных успе-
хов, в то время как отсутствие хотя бы одного из
этих препаратов обрекает энтеральное питание
в таких случаях на неудачу. Постепенное расши-
рение диеты и «тонкая настройка» ее — ключ
к успеху в сложных случаях.
Как только принято решение о необходимости
проведения зондового питания, следует опреде-
лить, в зависимости от риска аспирации, куда це-
лесообразнее поставить зонд — в желудок или
в тощую кишку. Всегда предпочтительнее питание
в желудок, поскольку это обеспечивает наиболее
приближенный к нормальному пищеварительный
процесс, адекватную гормональную реакцию, луч-
шую усвояемость больших осмотических нагрузок,
меньшую частоту вздутия живота, спазматических
болей, расстройства стула, не говоря о простоте
введения трубки в желудок по сравнению с тощей
кишкой. Проведение еюнальной трубки через пи-
лорический отдел показано больным с высоким
риском аспирации, например при задержке опо-
рожнения желудка, гастроэзофагеальном рефлюк-
се, сниженном рвотном рефлексе, а также у паци-
ентов, находящихся в коме.
Перед началом кормления следует проверить
местонахождение зонда. Просто введение в него
с этой целью воздуха и аускультация над желуд-
ком иногда дают ложные результаты, ибо звук мо-
жет передаваться даже при случайном попадании
трубки в бронхиальное дерево. Многие из совре-
менных специальных зондов для питания столь ма=
лы, что могут пройти через голосовые связки
и трахею, не вызывая каких-либо изменений голо-
са и дыхания. Естественно, растворы, введенные
в легкие через ошибочно поставленную трубку,
могут вызвать не только пневмонию, но и внезап-
ную смерть. Простейший способ убедиться в пра-
вильном расположении трубки — аспирация желу-
дочного содержимого небольшим шприцем, кото-
рую следует осуществлять очень деликатно, по-
скольку мягкие трубки с небольшими отверстиями
могут спадаться при создании отрицательного дав-
ления. Если при отсасывании не удается получить
желудочное или тонкокишечное содержимое, необ-
ходимо рентгенологически подтвердить правиль-
ность стояния зонда. Большинство из применяю-
щихся в настоящее время трубок рентгеноконтра-
стны, а потому достаточно для этих целей обычной
обзорной рентгенограммы брюшной полости.
Для постановки зонда за пилорический отдел
трубку с ртутным утяжелителем сначала вводят
в желудок. Затем пациента укладывают на правый
бок, чтобы во время перистальтики желудка облег-
чить прохождение кончика зонда через пилорус
в 12-перстную кишку. Если трубка нс проходит
в 12-перстную кишку в течение 8—24 часов, мож-
но дать больному церукал для стимуляции опорож-
нения желудка. Иногда трубку в 12-перстную киш-
ку проводят под рентгенологическим контролем,
используя струну или хорошо смазанный провод-
ник, применяющимся для аортографии.4' Опти-
38 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
мальная локализация для транспилорического зон-
да— непосредственно за связкой Трейца.42 Это
положение гарантирует при проведении питания
минимальный рефлюкс через пилорус.
Гастростомия для питания — более надежный
и лучше управляемый метод в тех случаях, когда
заранее предполагается длительное зондовое пита-
ние (более 8 недель), например при тяжелой трав-
ме головы. Если больному производится абдоми-
нальное оперативное вмешательство, то гастросто-
мия должна быть осуществлена непосредственно
во время операции. При этом в начальной стадии
гастростомичсская трубка обеспечивает декомпрес-
сию желулка, а в последующем через нес можно
проводить энтеральное питание.
Безопасность и целесообразность гастростомии
для питания у детей с хирургической патологией
хорошо известна. ' В то же время при непра-
вильно произведенной гастростомии могут возни-
кать достаточно тяжелые осложнения (табл. 2-9).
Перед наложением гастростомы для питания не-
обходимо оценить больного с точки зрения гастро-
эзофагеального рефлюкса, ибо при его нали-
чии после введения гастростомической трубки
рефлюкс нередко усугубляется.4’ Это обстоятель-
ство особенно важно учитывать у детей с пораже-
нием мозга, для которых неуправляемый рефлюкс
чрезвычайно опасен.48 .Пооперационная диагности-
ка ГЭР показана во всех случаях и состоит в рент-
генологическом обследовании с барием верхних от-
делов ЖКТ. При отсутствии рефлюкса на рентге-
нограммах необходимо суточное определение pH
Если по данным хотя бы одного из этих методов
обнаружен рефлюкс, во время гастростомии дол-
жна быть произведена фундопликация. Если же
при обследовании выявлено снижение сократи-
тельной способности желудка и замедление его
опорожнения, операцию необходимо дополнить пи-
лоропластикой.
Наиболее простой и безопасный метод гастро-
стомии— операция Штамма.49 Е.сли гастростомия
предпринимается как самостоятельное вмешатель-
ство, то се осуществляют через небольшой разрез
по средней или парамедианной линии, па желудок
накладывают 2—3 кисетных шва и трубку, вве-
денную в центре, выводят наружу через отдельный
прокол брюшной стенки. Наиболее целесообразно
использовать для этих целей катетер Пеццера со
сплошной головкой и двумя дополнительными от-
верстиями, позволяющий хорошо фиксировать из-
нутри желудок к передней брюшной стенке. Кроме
того, правильно поставленный катетер Пеццера
практически нс смешается, в отличие от других
катетеров. Как катетер Пеццера, так и уступаю-
щий ему катетер Малеко, обладают преимущества-
ми перед катетером Фолея, баллон которого через
10-14 дней может спадаться, давать «протечку»
либо проходить через пилорус, вызывая непрохо-
димость выходного отдела желудка.
В настоящее время у детей стала применяться
чрескожная эндоскопическая техника введения га-
стростомической трубки для питания, что исклю-
чает необходимость лапаротомии. Процедура
осуществляется с помощью гибкого эндоскопа
и в опытных руках является безопасным и эффек-
тивным вмешательством. Современным усовершен-
ствованным вариантом гастростомической трубки
является гастростомическая «пуговица», представ-
ляющая собой ареактивный силастиковый клапан,
который после введения располагается почти вро-
вень с передней брюшной стенкой и может пере-
крываться в промежутках между использованием.
По данным некоторых авторов, в тех случаях,
когда производится оперативное вмешательство на
органах брюшной полости, одним из относительно
безопасных способов обеспечения энтерального
питания является катстеризационная еюностомия.
Однако мы предпочитаем комбинацию раннего па-
рентерального питания с последующим, при необ-
ходимости, питанием через назогастральный зонд.
В тех же случаях, когда из-за гастроэзофагеально-
го рефлюкса или сниженной перистальтики желуд-
ка показано еюнальное питание, мы проводим
трубку в тощую кишку через предварительно со-
зданную по методу Штамма гастростому. Обеспе-
чить при проведении трубки через гастростому
в тощую кишку оптимальное положение кончика
зонда помогает осуществление этой процедуры под
контролем рентгеновского экрана или с помощью
гибкого эндоскопа.53
Таким образом, быстрое развитие высоких тех-
нологий и фармакологии позволяет обеспечивать
более эффективное энтеральное питание с лучшей
абсорбцией и меньшими побочными эффектами по
сравнению даже с тем, что было всего несколько
лет назад. В настоящее время в большинстве слу-
чаев энтеральное питание может быть начато
в значительно более ранние сроки, чем прежде,
что позволяет обеспечить больных белками и дру-
гими пищевыми компонентами с меньшими финан-
совыми затратами, чем при полном парентераль-
ном питании.
Питание через назоэнтеральный зонд показано
в большинстве случаен, когда невозможно питание
через рот. При необходимости длительного энте-
рального питания наиболее приемлемый способ —
гастростомия Категеризационная еюностомия, при
которой инфузию осуществляют за пилорус, уме-
ньшает риск аспирации и позволяет проводить
энтеральное питание в раннем постпаретическом
периоде. Использование рентгеноскопии и гибких
эндоскопов при введении трубок для питания в раз-
личные отделы ЖКТ часто позволяет избежать
дополнительных оперативных вмешательств и
ускорить переход от парентерального к полному
энтеральному питанию.
ПОЛНОЕ ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
История внутривенного питания началась с
1665 г., когда Christopher Wren впервые ввел внут-
ривенно спирт. Изучение вопросов парентерально-
го введения жиров животным проводилось в
1869 г. Menzel и Регсо. После безуспешных попы-
ток, предпринятых в Японии в 20-х и 30-х годах
нашего века, первое эффективное введение жиро-
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 39
ГДБЛИЦЛ 2-9. Возможные осложнения при зондовом питании и их профилактика
Ос тожнения Возможные причины Лечение
Диарея Осмотическая перегрузка Непереносимость лактозы Инфицирование рас тора или инфузионной сис- темы Нервное напряжение, боль Чрезмерный бактериальный рост, реакция на орально получаемые лекарственные препараты Уменьшение концентрации растворов, иногда примене- ние антиднарейных препаратов Капельное, а нс дробное, введение растворов Переход на растворы, нс содержащие лактозу Замена раствора и инфузионной системы: четкое со- блюдение всех правил инфузии Обеспечение спокойной окружающей обстановки Посев кала; пересмотр лекарственном ера и и и и ее побочных эффектов
Тошнота Перегрузка жидкостью Уменьшение общего объема раствора, скорое ги ин- фузии
Pkoi.1 Кишечная непроходимость Болезненные или просто излишние движения сразу после кормления Обслслонание ЖКТ (рентгенограммы); обеспечение состояния покоя в течение 45 мин после кормления
Схваткообразные Непереносимость лактозы Переход на растворы, не содержащие лактозу
боли, замедлен- ное опорожне- ние желудка
Запоры Недостаточная жидкостная нагрузка, снижение перистальтики кишечника Увеличение жидкостной нагрузки; но возможности уве- личение физической ilKTMBIIOCIH
Дегидратация 1k-.irK.ra гоч на я жидкостная на грузка Увеличение жидкостной нагрузки Введение дополнительно половины общего объема пи т;шня к виде воды
1 iiiicpi мдратация Чрезмерная жидкостная нагрузка Почечная, сердечная или легочная недостаточ- ность Уменьшение объема вводимой жидкости Лабораторный контроль содержания электрод и гон, сни- жение дозы натрия; переход на растворы, применяю- щиеся при поражении органа, функция которого на- рушена
Аспирация Быстрое введение питательных растворов Горизонтальное положение больших» во время или после кормления Смещение зонда Рио га после кормления Уменьшение скорости введения Приподнять верхнюю час1Ь i ул они щи на 30 градусов во время капельного введения растворов и и тече- ние 1 часа после дробного кормления Контроль положения зонда перед началом кормлении и при появлении приступов кашля Завести зонд ла пилорус: не проводить никаких лечеб- ных манипуляций иепосрсдс! пенно до, во время или сразу после кормления
биохимические Избыточная или недостаточная жидкостная па- Определение уровня глюкозы, остро возникшая непере- носимость глюкозы может быть симптомом сепсиса; контроль за электролитами (нагрузка и выведение) и динамикой массы тела, соответствующая коррекция питания
сленги ।рузка Низкое содержание натрия в растворах или излишек свободной воды
Изменение уровня глюкозы, элект родитов, нече- Органная недостаточное» ь Заболевания печени или почек могут кызшыь необхо- димое in уменьшения содержания белка в пита тель- ных расворах
ночных и по- чечных биохи- мических пока- зателей
Недостаточные прибавки МТ Энергетическая (калорийная) недостаточность Высокая скорость метабол нзма Мальабсорбция Увеличение концентрации и/или обт>ема вводимых рас- творов Может быть подтверждена непрямой калориметрией и увеличением калорической нагрузки Изменит состав питательных смесей
большие быстрые Энертс гичсская перегрузка Уменьшить калорическую нагрузку
прибавки МТ Нарушение водно-электролитною баланса Контроль получаемых и выделяемых электролитов, массы тела
Депрессии, «уход и себя», агрес- сивное новеде (1сихологичсскис нарушения Обеспечение с<и»т нетсгвующей социально-психплогиче- ской обстановки во время кормления; двигательная активность, эмоциональная поддержка
ине Отсутствие удовольствия от приема нищи через рот Отсутствие информации о цщях и длительности проводимого питания Если ист противопоказаний — леденцы, жевательная резинка, не содержащая сахара; регулярная обработ- ка полости рта Объяснять смысл проводимого лечения пациенту и род- ным; сообща 1Ь о положительной динамике в состоя- нии; привлекать больного к обсуждению плана лече- ния в отношении питания и хода выполнении этого плана
40 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
вых эмульсий было осуществлено в 50-х годах
в США, когда осуществлялись клинические испы-
тания липомула. Однако полученная тяжелая ток-
сическая реакция послужила причиной исчезнове-
ния этого препарата из поля зрения. Реальностью
применение жировых эмульсий становится в
1962 г., когда Wrctlind начал использовать интра-
липид — масляную эмульсию, приготовленную из
соевых бобов.54
В 1904 г. впервые внутривенно был введен эн-
зимный гидролизат белка. Наиболее часто исполь-
зуемые белковые гидролизаты приготавливаются
из казеина и фибрина. Однако гидролизаты усту-
пают место растворам аминокислот.
Хотя первое сообщение о полном (тотальном)
парентеральном питании (ТПП) у детей было
опубликовано в 1944 году, ' первый успешный его
результат, полученный сначала у щенков, а в по-
следующем у детей и взрослых,1'2 описан лишь
в 1968 г. Dudrick с соавт.
Опыт, накопленный во всем мире, подтверждает
возможность сохранения жизни детям с нарушени-
ями функции ЖКТ с помощью ТПП. При объек-
тивном отборе больных для ТПП, тщательном со-
блюдении всех технических правил и постоянном
мониторинге осложнения ТПП могут быть сведены
к минимуму, а эффективность увеличена макси-
мально.
Pudrick, проводя инфузионную терапию (ИТ),
использовал введение высокогипертонических ра-
створов глюкозы и аминокислот через централь-
ный венозный катетер. Данный метод все еще ши-
роко используется многими медицинскими учреж-
дениями. Однако в последние два десятилетия
появились новые способы ИТ, которые предусмат-
ривают введение через периферические вены ме-
нее гипертонических растворов глюкозы с или без
жировых растворов.5”-62 По сути 3 способа 1111 мо-
гут быть использованы у детей: (1) инфузии ги-
пертонических растворов глюкозы в центральные
вены; (2) инфузии в периферические вены средне-
гипертонических растворов глюкозы вместе с жи-
ровыми эмульсиями; (3) инфузии в перифериче-
ские вены среднсгипсртонических растворов глю-
козы в больших объемах. Каждый из этих способов
достаточно эффективен, и в процессе лечения тя-
желых больных все три метода могут быть приме-
нены в течение длительного периода времени.
Показания. Тотальное парентеральное питание
показано в тех случаях, когда питание через ЖКТ
невозможно, неадекватно или даже опасно. Для
некоторых пациентов, например маленьких детей
с хронической неспецифической диареей, полезно
дать «отдых» ЖКТ в течение длительного проме-
жутка времени. У других восстановление соответ-
ствующего питания может быть осуществлено
лишь с помощью оперативного вмешательства. Об-
щие показания к ТПП включают хроническую
спаечную кишечную непроходимость, перитоне-
альный сепсис, кишечные свищи, синдром корот-
кой кишки, хроническую тяжелую диарею, обшир-
ные ожоги, состояния после хирургического лече-
ния опухолей брюшной полости, рентгенотерапию.
химиотерапию. Хотя ТПП предназначается в
основном для детей, у которых уже есть наруше-
ния питания, однако оно может быть начато и про-
филактически в тех случаях, когда заранее пред-
полагается невозможность энтерального питания
в течение длительного времени. Яркий пример по-
добной ситуации — гастрошизис.
По мере накопления опыта и развития различ-
ных методов появились новые показания к ТПП.
Так, оно применяется у глубоко недоношенных де-
тей, которые, несмотря на нормальную функцию
Ж К Г, дают постоянные рвоты и срыгивания при
питании через назогастральный зонд или через га-
стростомическую трубку. Кроме того, гиперали-
менгация используется при лечении уремии , пе-
ченочной недостаточности и сепсиса/"1 ’’
ТПП следует начинать у грудных детей, не по-
лучающих по тем или иным причинам адекватного
энтерального питания в течение больше, чем 4—
5 дней. Старшие дети и взрослые более длительно
могут относительно безболезненно переносить не-
полноценное питание. Причем возможности при-
способления к неблагоприятным условиям в значи-
тельной мере зависят от исходного состояния их
питания перед началом болезни или оперативным
вмешательством. Каждый раз, приступая к прове-
дению ТПП, следует тщательно сопоставить пока-
зания и ожидаемую эффективность с риском воз-
можных осложнений этого метода, прежде всего,
конечно, таких, как катетеризационный сепсис.
Состав растворов. Питание через централь-
ные вены. Состав основного раствора, содержаще-
го 25% глюкозу для питания в центральную вену,
используемого в детском госпитале в Анн-Арбо-
ре (шт. Мичиган, США), представлен в табли-
це 2-10. Небольшое количество калия содержится
в растворе кристаллических аминокислот, но в
основном электролиты в соответствующих коли-
чествах должны добавляться Инфузия 100—
110 мл/кг/сут этого раствора в центральную вену
обеспечивает поступление глюкозы, аминокислот
и других пищевых компонентов в количествах, до-
статочных для удовлетворения нормальных по-
требностей грудного ребенка в строительном мате-
риале для восстановления тканей и для роста. Ука-
занный объем может быть введен и старшим детям,
хотя их потребности в калориях меньше. В первые
I—2 дня парентерального питания раствор разбав-
ляется равным объемом 5% декстрозы (в воде),
чтобы дать больному возможность адаптироваться
к осмотической нагрузке и таким образом предот-
вратить осмотический диурез и гипертоническую
дегидратацию. По мере привыкания ребенка к на-
грузке, о чем можно судить по уменьшающейся
глюкозурии, переходят к неразбавленному раство-
ру. При отсутствии диабета в добавлении инсули-
на нет необходимости. Количество электролитов,
указанное в таблице 2-10, обеспечивает основные
потребности детей любого возраста. При наличии
патологических потерь количество электролитов
должно быть увеличено. У детей с нормальной
функцией ночек, получающих этот раствор, редко
бывают нарушения уровня электролитов в сыво-
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 41
ТАБЛИЦА 2-10. Состав основного раствора для ПП
в центральную вену у грудных детей *
Кол-но (на кг в сутки)
Глюкоза 15 30 г
Белки 2.0 4.0 г
Натрин 2,4 мэкп
Калий 2.4 мэкв
Хлор 3—6 мэкв
Магний 0,5 -1.0 мэкв
Кальции 0,5 3.0 мэкв
Фосфор 0.5—1.0 ммоль
Микроэлементы •• 0,1 мл/0.3 мл для попорол
М ул ьти в и та м и и ими инфу- денных 1 фл (ралвсденный до 3 мл)
зат •••
Гепарин 1.0 МЕ/мл
Глюкозо-бел коны и объем 60 112 мл
Жиры 1 4 г
1(1% жировая эмульсия (объ- 10—40 м.1
см)
Общий объем 70—154 мл
Общее количество ккал 70 — I54 ккал
• Каждая 1UUU мл стандартного раствора прмготан 1ива-
ется путем смешения 500 мл 50% водного раствора декстрозы
с 500 мл 7% аминокислот, с конечном концентрацией декстро-
зы— 25%. аминокислот 3.5%. Электролиты. ни (амины и
микроэлементы добавляются в количестве, соответствующем
МТ больного.
Каждая 0.1 мд раствора .микроэлементов содержит
цинк 1(H) мкг. мель 20 мкг, марганец 10 мкг, хром 0,2 мкг и се-
лен 1,2 мкг. Специальный раствор микроэлементов для ново
рожденных содержит 3U0 мкг цинка в 0.3 мл и такое же коли-
чество других элементов,
♦♦♦ Каждый флакон (разбавленный до 3 мл) детского
МОИ содержит витамин А 2300 МГ, витамин Д 400 MF, аскор-
биновую кислоту 80 ME. тиамин (витамин BI> 1,2 мг. рибофла-
вин (витамин В2) 1,4 мг, никотинамид 17 мг. пиридоксин (нита-
мин В6) 1 мг. декснангенол 5 мг, нитамин Е 7 ME. фолиевую
кислоту 140 мкг. циапокобаламин (витамин В12) I мкг, фитона-
дион (витамин KI) 200 мкг и биотип 20 мкг.
ротке. Однако в тех случаях, когда имеется сниже-
ние функции ночек или метаболические расстрой-
ства, необходима осторожность в проведении па-
рентерального питания. Потребности в железе
обеспечиваются еженедельным внутривенным вве-
дением декстрана железа. Микроэлементы добав-
ляются к основному раствору как обычно. Эссен-
циальные жирные кислоты вводятся в виде неболь-
ших количеств готовых жировых эмульсий или
иногда путем ежедневных аппликаций с подсол-
нечным маслом на грудную клетку ребенка.66
Питание через периферические вены. Раствор
для парентерального питания через перифериче-
ские вены состоит из равных количеств 4% кри-
сталлических аминокислот и 20% водного раство-
ра глюкозы, таким образом, в нем содержится 2%
аминокислот, 10% глюкозы и 0.40 ккал/мл. Элек-
тролиты добавляются к ин фу за ту в количествах,
необходимых для обеспечения суточных потребно-
стей и дополнительных нужд, связанных с состоя-
нием больного (табл. 2-11). Концентрация элект-
ролитов и витаминов по существу такая же, как
рекомендуется для питания через центральные ве-
ны. Для профилактики флебита к раствору добав-
ляется гепарин в дозе 1 ЕД/мл. Если жировая
эмульсия не вводится, то основная часть эссенци-
альных жирных кислот поставляется путем еже-
дневных аппликаций с подсолнечным маслом на
грудную клетку ребенка.66 Для грудных детей
общее кол ичестно растворов соста вляе г 160—
200 мл/кг/сут. что обеспечивает 64—80 ккал/сут.
У старших четей объем уменьшается соответствен-
но калорическим потребностям.
При включении в инфузат жировой эмульсии
(10% или 20%) грудной ребенок получает 4 г
жира на кг/суг, соответственно на этот объем
уменьшается количество других, нс содержащих
жнра растворов. Такой инфузат обеспечивает
102—121 ккал/кг/сут, что превышает количество
энергетического материала, необходимого грудно-
му ребенку для увеличения МТ и роста (рис. 2-3).
У старших детей жиры назначаются из расчета
2—3 г/кг/сут, нежировые растворы обеспечивают
остальные калорические потребности. В жировых
эмульсиях содержатся все необходимые для орга-
низма жирные кислоты. 20% жировая эмульсия
особенно показана у детей с заболеваниями почек,
сердца или легких, когда необходимо ограничение
жидкостной нагрузки.67
Витамины, микроэлементы и железо вводятся
так же, как при питании в центральные вены.
Методы. Питание через центральные вены.
Во избежание воспаления и тромбоза перифериче-
ских вен гипертонические инфузаты должны вво-
диться в центральные вены. С этой целые произво-
дится катетеризация верхней полой вены путем
кожного разреза и введения катетера во впутрен-
ТА БЛИЦА 2-11. Состав раствора с добавлением жиров для
1111 через периферическую «сну у грудных
детей *
Кол-во (на кг в сутки)
Глюкоза
Белки
Натрий
Калий
Хлор
Магний
Кальции
Фосфор
Микроэлементы ** ***
Мультивитаминный инфу-
зат (МВИ) “““
Гепарин
Глюкозо-белковый объем
Жиры
10% жировая эмульсия (объ-
ем)
Общий объем
Общее количество ккал
15 20 г
2,0 4,0 г
2—4 мэкв
2—4 мэкв
3 6 мэкв
0,5 1.0 мэкв
0.5- 3.0 мэкв
0,5 1.0 ммоль
0,1 мл (0,3 мл для новорож-
денных
1 фл (разбавленный до 3 мл)
1,(1 МЕ/мл
120 160 мл
4 г
40 мл
160—200 мл
102 121 ккал
• Каждая ЮОО .мл стандартного раствора приготавлива-
ется путем смешения 500 мл 20% водного раствора декстрозы
с 500 мл 4% аминокислот, с конечной концентрацией декстро-
зы — 10% и аминокислот 2%. Электролиты, витамины и
микроэлементы добавляются в количестве, соответствующем
МТ больного.
•* Каждые 0,5 мл раствора микроэлементов содержат
цинк 100 мкг, медь 20 мкг, марганец 10 мкг и хром 0,2 мкг.
*** Каждый мл МВИ содержит вит. А 2000 ME, вит. Д
200 ME, аскорбиновую кислоту 100 ME, тиамин (вит. В1) 10 мг,
рибофлавин (вит. В2) 2 мг. никотинамид 20 мг. пиридоксин
(пит. В6) 3 мг, дскспантенол 5 мг и вит. Е I Mli.
42 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
Поступление небелковых калорий
30 детей в возрасте до года
НО -
90-
70-
ь-
&
| 50-
ГО
*
30-
10-
Угле-
воды
Амино-
кислоты
Всего кал
Колебания
Средняя
прибавка МТ-
18 г/сут
Калории, необходимые
для нормальных
весовых прибавок
Рис. 2-3. Распределение калорий при парентеральном питании
с использованием жиров. Как видно из графика, без жировых
калорий не может быть достигнута прибавка МТ, поскольку
общее количество калорий прн отсутствии жиров недостаточно
для получения у нормального грудного ребенка весовых при
банок.
нюю или наружную яремную вену либо с исполь-
зованием чрескожной пункции подключичной или
внутренней яремной иены. Эту манипуляцию луч-
ше проводить в операционной или в специальной
кардиологической катетеризационной лаборато-
рии, где есть соответствующие асептические усло-
вия и инструменты. Для предупреждения инфици-
рования кровеносного русла катетер проводят в
подкожном туннеле таким образом, чтобы or места
его вхождения в кожу до вены было бы 5—10 см.
Катетер вы котят наружу на грудной клетке меди-
альнее правого грудного соска. Глубокая v. epigast-
rica inf. может быть успешно использована у детей
для доступа в нижнюю полую вену, когда ее кате-
теризация невозможна через какой-либо иной
сосуд.6*
Катетеризацию центральной вены можно прово-
дить как под местной, так и под общей анестезией.
Мы обычно предпочитаем общее обезболивание
(рис. 2-4). Антибиотики, как правило, не вводятся.
Каждые 2 дня меняется мазевая стерильная повяз-
ка, фиксирующая катетер. При смене ее кожа об-
рабатывается антисептиками. Для повязки исполь-
зуется мазь Povidone-iodine (Bctadinc), действую-
щая как на бактерии, так и на грибки. Специ-
альный микрофильтр включается в инфузионную
систему для удаления чрезвычайно мелких частиц,
таких, как соли кальция или микроорганизмы, ко-
торые могут оказаться в растворе. Необходимо ис-
пользовать градуированные сосуды, чтобы точно
определять количество вводимого раствора. В си-
стему может быть включена инъекционная трубка
для внутривенного введения лекарственных препа-
ратов асепгично под фильтром. Все трубки инфу-
зионной системы и сосуд для инфузата меняются
ежедневно. Поскольку высокое содержание сахара
в переливаемых растворах способствует росту бак-
терий и дрожжевых организмов, наружная поверх-
ность всех элементов инфузионной системы дол-
жна раз в день обрабатываться Povidone-iodine для
удаления инфузата. который в небольшом коли-
честве случайно может попасть из сосуда на труб-
ки. Ко всем местам соединений в системе прикла-
дывают мазь Povidone-iodine для предотвращения
проникновения микроорганизмов.
Ипфузат должен вводиться с равномерно за-
данной скоростью, что у маленьких грудных детей
обеспечивается с помощью постоянного инфузи-
онного насоса. Желательно, чтобы пациенты, по-
лучающие парентеральное питание, находились
Рис. 2-4. Катетеризация центральной вены у грудных детей
осуществляется путем чрескожной пункции подключичной или
ину 1 ремней яремной пены или с использованием кожного разре-
за через наружную или внутреннюю яремную вену. Кате-
тер выводи гея через туннель на грудную кпетку мсдиальнее
правого соска.
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 43
в отделении интенсивной терапии, однако это не
всегда возможно. Чтобы оптимально обеспечить
проведение ПП, мы формируем специальную инфу-
зионную бригаду, состоящую из медицинской се-
стры, диетолога и фармацевта, которые наблюда-
ют за лечением каждого больного, находящегося
на парентеральном питании. Эта бригада делает
обходы дважды в день и производит смену трубок,
инфузионных систем и повязок.
Питание через периферические вены с примене-
нием жиров. У грудных детей производят пункцию
периферической вены, обычно на голове. Трубка
от флакона с аминокислотами соединяется с пунк-
ционной иглой- Трубка же от флакона с жировой
эмульсией соединяется с трубкой от первого фла-
кона ближе к ее концу. Инфузия из обоих флако-
нов осуществляется в течение 24-часового периода
с использованием отдельной для каждого флакона
градуированной бюретки и постоянного инфузион-
ного насоса. Микрофильтр помещается в трубку
системы, содержащей раствор аминокислот, про-
ксимальнее места введения в нее жирового раство-
ра. поскольку фильтр не пропускает жиры. Внут-
ривенная игла требует замены каждые 2 3 дня
в связи с возникающей обычно инфильтрацией,
которая, как правило, незначительна и не флеби-
тического происхождения. Аналогичная техника
ПП применяется у старших детей и взрослых,
с той разницей, что у них чаще используются при
этом вены не головы, а дорсальной поверхности
кисти или другой локализации.
Питание через периферические вены без приме-
нения жиров. Техника этого вида IIП такая же,
как при питании с жировыми эмульсиями. Весь
раствор содержится в одном флаконе и перелива-
ется через небольшую иглу, введенную в перифе-
рическую вену на голове или конечноеги. Также
используется микрофильтр, и инфузия осуществ-
ляется в течение 24 часов по причинам, представ-
ленным выше. У грудных детей применение инфу-
зионного насоса абсолютно необходимо, у старших
детей — желательно. Иглу обычно меняют каждые
24—48 часов или чаще, если появляются признаки
инфильтрации или флебита. На инфильтрирован-
ную кожу накладывают согревающие компрессы
для уменьшения отека. В редких случаях, при бо-
лее выраженных изменениях кожи, местное лече-
ние обычно способствует достаточно быстрому за-
живлению.
КОНТРОЛЬ ЗА ПРОВЕДЕНИЕМ ПИТАНИЯ
С самого начала проведения энтерального или па-
рентерального питания необходимо оценивать его
эффективность на основе исследования состояния
метаболизма, которое включает в себя прежде все-
го клинические показатели: ежедневное взвешива-
ние, у грудных и маленьких детей — еженедельное
измерение длины тела и окружности головы, точ-
ный учет получаемых и выделяемых объемов. В мо-
че определяют сахар и ацетон, сначала — в каждой
порции, а затем, когда достигнута стабилизация
состояния больного, — раз в сутки. В таблице 2-12
ТАБЛИЦА 2 12. Показатели крови, которые не»бх<цяммп
контролировать при потом парентеральном
питании <ТПП)
В канале ТПП и затем еженедельно в начале ТПП и затем каждые 2 нсдети 11л показаниям
Натрий, калий, хлор SGOT (Глинамиг- Медь
МО*1С!Ш!<<1 оксало-ацетатная Цинк
Глюкоза т ра кеа ми низа) Железо
Магний Ллктктдегидрогенлза Аммиак
Кальций 1 Цепочная фосфа газа Осмоляр-
Фосфор Билирубин (примой/ НОС ГЬ
Альбумин 1 емоглобин Гематокрит Лейкоциты Тромбоциты общий) Креатинин pH
перечислены рекомендуемые исследования и ча-
стота их проведения. У некоторых больных, на-
пример с заболеваниями почек и печени, может
понадобиться более частый контроль отдельных
параметров. Однако важно разумно и бережно от-
носиться к заборам крови для анализов у грудных
и маленьких детей, учитывая малый общий объем
крови у них и риск возникновения анемии, которая
может потребовать даже гсмотрансфузии. В допол-
нение к различным лабораторным данным необхо-
димо очень внимательно следить за субъективны-
ми и объективными клиническими симптомами.
Например, улучшение мышечного тонуса, ранево-
го заживления, функции легких, затухание инфек-
ционного процесса и восстановление самостоятель-
ного дыхания — все это вместе свидетельствует
и об улучшении состояния питания.
Изменения массы тела во время 1111 обычно па-
раллельны изменениям общего состояния ребенка.
Если к началу лечения отмечались тяжелые нару-
шения питания, то в течение нескольких дней мо-
жет нс быть существенных прибавок МТ. Паци-
енты же, у которых не было отклонений в питании
или сепсиса, могут давать весовые прибавки, срав-
нимые с таковыми у здоровых детей (рис. 2-5).
Увеличивающиеся метаболические затраты, на-
пример при тяжелой травме или сепсисе, приводя!
к значительному уплощению весовой кривой. Нор-
мальные прибавки массы тела должны в среднем
составлять 15—25 г/сут у новорожденных и груд-
ных детей и 0,5 общей МТ/кг/сут — у более стар-
ших пациентов и подростков. Более интенсивное
увеличение МТ говорит об избыточной жидкост-
ной нагрузке и задержке жидкости. Положитель-
ный азотистый баланс и синтез белка зависят в не-
которой степени от активности пациента (рис. 2-6
и 2-7), поэтому важны занятия лечебной физ-
культурой, поскольку физические упражнения спо-
собствуют восстановлению мышечной силы и фун-
кции сердечно-сосудистой системы.
Диурез должен поддерживаться на уровне
1 мл/кг/час или больше, уд. вес мочи — от 1005
до 1015. Нс следует допускать глюкозурии. Боль-
шие количества внутривенно вводимой глюкозы
при постепенном наращивании хорошо усваивают-
ся большинством детей, при этом нет необходимо-
44 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
сти в применении инсулина. Уровень глюкозы
в крови обычно нс выхолит за пределы верхней
границы нормы. Если возникает гипергликемия
и глюкозурия, то, как правило, бывает достаточно
снизить скорость инфузии или временно умень-
шить концентрацию глюкозы, если только у боль-
ного нет сепсиса. ТПП приводит к большей, по
сравнению с энтеральным питанием, экскреции
с мочой растворенных веществ. Эта повышенная
нагрузка, однако, не превышает концентрацион-
ных возможностей здоровой почки. Водный баланс,
даже при большой скорости ТПП, как правило,
удерживается на нормальном уровне.
Переход от парентерального к орально-энте-
ральному питанию — очень важный и часто труд-
ный этап в лечении больных. Если во время этого
периода нс проводить адекватную терапию, то па-
циент может потерять половину того, что приобрел
за время парентерального питания. При длитель-
ном ТПП могут развиваться вкусовые и обонятель-
ные расстройства или гипертрофированное сосре-
доточение на еде. С другой стороны, ТПП часто пол-
ностью подавляет аппетит. Врач должен убедить
больного, вселить в него уверенность в том, что
аппетит и вкусовые ощущения восстановятся по
мере ухода от парентерального питания и прекра-
БАЛАНС АЗОТА
Рис. 2-6. Метаболический баланс у ребенка с гастрошизисом, оперированного с применением силонового покрытия экентрнрован
пых органов. Заштрихованные участки соответствуют положительному балансу, черные — отрицательному. В течение 38 дней ПП
\ больного отмечался положительный баланс азота (Л) и калия (В).
Октябрь Ноябрь
ДНИ BHOHtjrtiTH r»x2t и 1 • з л ь « » вокнонкиип
В
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 4S
А/с. 2-7. Кумулятивный азотистый баланс у
больного, представленного на рис. 2-6.
20.000
19.000
iaooo
17.000
16000
15.000
14000
13000
12000
£ 11.000
о 10.000
СО
< 9000
аооо
7000
6.000
5.000
4.000
3000
2000
1.000
о
Октябрь Ноябрь
ДНИ 11 12 13 14 15 16 17 16 W 20 21 22 23 24 25 26 27 2529 30 31 I 2 3 4 5 6 7 в 9 Ю И 12 13 М 15 16 17
щения его. Поскольку при ПП калорические по-
требности удовлетворяются полностью, то, прежде
чем прекратить парентеральное питание, следует
уменьшить его объем наполовину для того, чтобы
стимулировать у пациента аппетит и желание при-
нимать пнщу. Питание начинают, как правило,
с простых жидкостей. Они легко воспринимаются
большинством пациентов, поэтому можно быстро
переходить к более «вкусной» пище (леденцы, го-
товые безлактозные смеси, печенье, яйца, взбитые
с молоком и сахаром, и т. д.). Во время переходно-
го к энтеральному питанию периода необходимо
подсчитывать калораж для контроля за динами-
кой состояния питания больного, что, к сожале-
нию, не всегда четко осуществляется в стационаре.
Поэтому целесообразно привлечь к данному заня-
тию. если возможно, пациента или его родственни-
ков, что часто к тому же оказывает существенное
положительное влияние на психоэмоциональное
состояние как больного, так и ухаживающих за
ним родных.
ОСЛОЖНЕНИЯ ПАРЕНТЕРАЛЬНОГО ПИТАНИЯ
Технические осложнения. Так же, как почти все
инвазивные методы лечения, Г1Л1 и, в меньшей
степени, энтеральное питание имеют свой круг
осложнений (табл. 2-9 и 2-13), которые .могут
быть успешно предупреждены, если осуществляет-
ся тщательный контроль за проведением ПП.65 Ча-
стота технических осложнений при постановке
центральных венозных катетеров у детей сущест-
венно снизилась благодаря четкому соблюдению
всех правил осуществления этих манипуляций и
рентгенологическому контролю положения катетера.
Сердечной аритмии, связанной с раздражением ка-
тетером, можно избежать, если кончик катетера
устанавливать в месте впадения верхней полой ве-
ны в правое предсердие, а не в полость сердца
Рентгенологический контроль положения катетера
позволяет исключить такое осложнение, как некроз
печени в результате инфузии гипертонических
растворов непосредственно в печеночные вены.
С заменой поливиниловых катетеров на силико-
новые снизилась частота реакций на катетер, как
на инородное тело, реже возникают перфорация ве-
ны и тромбоз подключичной или верхней полой
вены. Подшивание катетера к коже в месте его
входа и контроль положения при каждой перевяз-
ке, производимой через день, значительно умень-
шают возможность случайного смещения катетера.
Однако даже при правильном его положении мо-
жет возникнуть тромбоз вены, особенно у тяжелых
больных с сепсисом и замедленной циркуляцией.
Тромбоз верхней полой вены в редких случаях мо-
жет привести к синдрому верхней полой вены, не
представляющему серьезной проблемы.
Хотя при патологоанатомическом исследовании
детей, у которых стоял катетер в верхней полой
вене, иногда обнаруживается тромбоэмболия, кли-
нические ее проявления возникают чрезвычайно
редко. Легочная эмболия также описана как редкое
осложнение у грудных и маленьких пациентов
с длительным стоянием центрального венозного
катетера. При па ренте рал ьном питании через
периферические вены удается избежать больший-
46 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
ТАБЛИЦА 2-13. Возможные метаболические осложнения полного парентерального питания
Электролитные нарушения
Осложнения, связанные с ппеденмем углеводов
Осложнения, связанные с введением белков
Осложнения, связанные с введением липидов
Гинер/гипонатриемия
Г и пер/1 инокалиемия
Гнпер/гипохлоремня
Гинер/гинокальцисмия
I ‘hi iep/ ги । юм<1 rne:iиемия
Гмпер/гинофосфа гемин
Гниср/гмногликемия
Гиперосмолярпос! ь с осмотическим диурезом и дегидратацией с исходом
в пикетогенную гипергликемическую кому
Хол ее гатн ческая желтуха
Азогсмня
I иперхлоремическии метаболический ацидоз
Гиперлипидемия
Нарушение функции легких
Замещение билирубина, связанного альбумином, свободными жирными
кислотами плазмы
Синдром перегрузки, характеризующийся гиперлипидемией, гипертермией,
сгуиорозным состоянием, поражением печени и коагуляционными рас-
стройствами — описан у взрослых, но очень редко встречается у детей
11едоста точное гь микроэлементов
Цинк
Медь
Хром
Недостаточность эссенциальных жирных кислот
В том случае, если липиды нс применялись; проявляется кожной сыпью
ства технических осложнений, присущих цент-
ральным венозным катетерам. Наиболее частые
нежелательные последствия катетеризации перифе-
рических вен — флебиты и поверхностные инфиль-
траты, которые можно предупредить путем одно-
временной инфузии жировых эмульсий. Кроме
уменьшения осмолярности и увеличения pH инфу-
зата, добавление жиров обеспечивает непосредст-
венную механическую защиту вены от флебита.
Септические осложнения. Сепсис — одно из
наиболее частых и серьезных осложнении паренте-
рального питания у детей через центральные ве-
ны. Достоверно установлено, что при длитель-
ном нахождении в центральной вене катетер мо-
жет быть источником бактериемии и септицемии.
Микроорганизмы попадают в кровоток непосредст-
венно с катетера, из инфицированных растворов
либо из удаленных септических очагов. Однако
в последнем случае катетер, являясь инородным
телом, фокусирует на себе бактериальный рост.
Наиболее важные факторы, способствующие умень-
шению частоты септических осложнений, — поста-
новка катетера в строго асептических условиях
и тщательный уход за ним со сменой повязок че-
рез день. Кроме того, свести до минимума риск
инфицирования позволяет использование катетера
только для парентерального питания, исключая за-
боры крови через этот катетер, переливание пре-
паратов крови или введение лекарственных ве-
ществ. Создание специальной инфузионной брига-
ды в нашем госпитале и строгое соблюдение всех
правил парентерального питания привели к умень-
шению частоты сепсиса с 16% до 3,2% в течение
первых же 2,5 лет работы бригады.74 За последние
10 лет существования этого коллектива частота
сепсиса при ТПП через центральные вены состав-
ляет в среднем 4,5%.
Катетсризационцый сепсис у больных, получаю-
щих парентеральное питание, проявляется лихо-
радкой, лейкоцитозом, «необъяснимой» глюкозу-
рией или любой комбинацией этих симптомов. Ин-
фекция подтверждается высевом микроорганизмов
из крови, взятой из катетера или из любой другой
вены. При отсутствии интоксикации катетер дол-
жен быть оставлен в вене на первые 24—48 часов
после выявления бактериемии, поскольку около
50% лихорадящих больных, у которых стоит кате-
тер в центральной вене, имеют иные причины ли-
хорадки. Если не обнаружены никакие другие оча
ги сепсиса, катетер следует удалить. Возможен
и альтернативный подход — сразу после получе-
ния положительных результатов посева крови на-
чать внутривенное введение через этот катетер ан-
тибиотиков. Во многих случаях центральный ве-
нозный катетер может быть «спасен» с помощью
5—10-дневного курса внутривенного (через этот
катетер) введения антибиотиков.
Поскольку именно лихорадящие пациенты чаще
всего нуждаются в парентеральном питании, важ-
но очень четко контролировать и документировать
у них все, что связано с использованием катетера.
Парентеральное питание никогда не является экст-
ренным мероприятием, а потому при наличии по-
казаний к ПП у лихорадящего больного он должен
быть тщательно обследован для выяснения причин
лихорадки перед тем. как приступить к ПП в цент-
ральные вены. Парентеральное питание ни в коем
случае нс следует начинать на ранних стадиях
тяжелой инфекции, особенно при рецидивирующей
септицемии. Если же ПП проводится па фоне ли-
хорадки, необходимы регулярные посевы крови до
тех пор, пока больной нс перестанет лихорадить
(каждые 1—3 дня).
Парентеральное питание через периферические
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 47
иены позволяет избежать многих септических и
технических осложнений, свойственных централь-
ным венозным катетерам. Мы не наблюдали у де-
тей ни одного случая катетер изацион него сепсиса,
связанного с парентеральным питанием через пе-
риферические вены как с использованием жиров,
так и без них.75 77
Метаболические осложнения. Все известные
метаболические нарушения могут возникнуть при
ТПП, наиболее частые из них представлены в таб-
лице 2-13. Если эти осложнения остаются долгое
время нераспознанными, развиваются серьезные
последствия. Однако тщательный контроль парен-
терального питания с соответствующей коррек-
цией позволяет большинству пациентов достаточ-
но легко приспосабливаться к ТПП.
Гипергликемия. В начальных стадиях паренте-
рального питания может отмечаться повышенный
уровень глюкозы крови, что лечения нс требует,
если не приводит к глюкозурии 4+ или значи-
тельному осмотическому диурезу- При повышении
скорости инфузии или концентрации глюкозы в
течение 48—72 часов парентерального питания
включаются эндогенные механизмы секреции ин-
сулина и уровень глюкозы крови возвращается
к норме. Если гипергликемия не проходит за этот
период, то к инфузату следует добавить инсулин.
Дети, не страдающие диабетом, редко нуждаются
во введении инсулина. Пациенты, у которых на
фоне стабилизации состояния при парентеральном
питании внезапно увеличивается уровень глюкозы
крови более 10 ммоль/л или которые но иным
причинам требуют дополнительных повышенных
доз инсулина, должны быть тщательно обследова
ны с целью выявления возможных других причин
гипергликемии, в частности — сепсиса.
Гипогликемия. Хотя такие симптомы гипоглике-
мии, как обильное потоотделение, спутанное со-
знание или возбуждение, описаны при внезапном
прекращении парентерального пи гания, мы редко
наблюдаем это осложнение у детей. Тем не менее,
в любом случае, когда ТПП по тем или иным при-
чинам внезапно прерывается, необходимо вводить
10% декстрозу. При прекращении парентерально-
го питания «уходить» от него следует постепенно.
Пациенты, подвергающиеся большим хирургиче-
ским вмешательствам, часто становятся менее то-
лерантными к глюкозе в связи с секрецией эндо-
генных гормонов или инсулиновой резистент-
ностью. Поэтому мы рекомендуем при проведении
ПП сокращать вдвое скорость инфузии или вовсе
ее прекращать, когда больной берется в операци-
онную. Скорость инфузии может быть восстанов-
лена до предоперационных показателей через 48
часов после операции при условии, что концентра-
ция глюкозы в крови возвратилась к обычному
уровню.
Гиперкалиемия. У пациентов, получаюших па-
рентеральное питание, может отмечаться повыше-
ние уровня калия сыворотки, если в силу анаболи-
ческой недостаточности вводимый калий нс ути-
лизируется полностью. Гиперкалиемия может раз-
виваться также в результате снижения функции
почек или сердечного выброса с метаболическим
ацидозом при тканевом некрозе или системном
сепсисе. В таких ситуациях количество калия в ин-
фузате должно быть уменьшено либо его вовсе
следует исключить, пока гиперкалиемия не будет
ликвидирована.
Гипокалиемия. Для ассимиляции вводимых при
парентеральном питании растворов и синтезе бел-
ка в организме требуется повышенное количество
внутриклеточного калия. Поэтому калий необхо-
димо вводить внутривенно из расчета 2—
4 ммоль/кг/сут для грудных и маленьких пациен-
тов или 40 ммоль/л для более старших детей и по-
дростков. Могут потребоваться и более высокие
дозы, показания к применению которых возникают
на основе результатов регулярного исследования
концентрации калия в сыворотке.
Гипокальциемия/гиперкальциемия, гипофосфа-
темия/гиперфосфатемия. Эти состояния, опи-
санные у пациентов, получающих ТПП, обычно
возникают, когда к растворам для ТПП добавля-
ются неадекватные количества кальция и фосфо-
ра. ’ Подобных редких осложнений можно избе-
жать, тщатечьно контролируя уровень кальция
и фосфора в сыворотке. В связи с продолжающимся
ростом дети, но сравнению с подростками и взрос-
лыми, нуждаются в относительно больших количе-
ствах кальция и фосфора.80
Гипомигнелиемия. Подобно калию и фосфору,
магний требуется при ускоренных процессах ана-
болизма и синтеза белка. Гипомагнезиемия может
проявляться галлюцинациями, головокружениями,
кишечной непроходимостью и гиперрефлексией.
Добавление соответствующего количества магния
к инфузату полностью устраняет это осложнение.
IIедостаточность микроэлементов. 11едоста-
точность цинка нередко возникает при длительном
парентеральном питании, обычно у детей с диа-
реей. Клинические проявления заключаются в вы-
падении волос, себорейном дерматите с локализа-
цией вокруг носа и рта и иногда в кишечной непро-
ходимости. Дефицит меди приводит к гипо- или
нормохромной анемии, нейтропении, депигмента-
ции кожи и волос, гипотонии, задержке психомо-
торного развития и остеопорозу. Недостаточ-
ность хрома встречается чрезвычайно редко и мо-
жет вызывать диабетоподобный синдром. Дефицит
селена — возможное осложнение очень длительного
парентерального питания проявляется мышечны-
ми болями и кардиомиопатией. Недостаточность
этих микроэлементов редко возникает у больных,
получающих добавки микроэлементов к инфузату.
Н едостаточност ь жирных кислот / г и п ерл ип и -
демия. Лабораторные признаки выраженной недо-
статочности эссенциальных жирных кислот обыч-
но развиваются не раньше, чем через 2 3 недели
безжирового парентерального питания, и заключа-
ются в повышении в сыворотке содержания 5, 8,
11-триеновой кислоты, низком уровне линолевой
и арахидоновой кислот и увеличении выше 0,4 со-
отношения триеновой-тетраеновой кислот. Клини-
ческие симптомы, как правило, появляются не
раньше, чем через 2—3 месяца лечения без жиро-
48 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
вых эмульсий,83 и включают в себя чешуйчатый
эритематоз, папулезную кожную сыпь, преимуще-
ственно в области конечностей, грудной клетки
и лица. В предыдущем разделе уже было указано,
что с этой сыпью можно справиться введением как
минимум 4% суточных калорических потребно-
стей в виде линолевой кислоты. Благодаря тому,
что при парентеральном питании часть суточных
калорийных потребностей обычно вводится внут-
ривенно в виде жиров, недостаточность жирных
кислот развивается редко.
Большинство больных, получающих жировые
эмульсии, имеют нормальный уровень триглицери-
да и холестерина в сыворотке. В некоторых редких
случаях у пациентов, получающих парентеральное
питание дольше месяца, содержание триглицерида
в сыворотке может колебаться в пределах 3,5—
4,0 ммоль/л (в норме 0,6—1,7 ммоль/л), а показа-
тели холестерина—4,0—6,5 ммоль/л (в норме
2,5—4,0 ммоль/л). Эти изменения редко вызыва
ют какие-либо последствия, и показатели возвра-
щаются к норме обычно сразу после прекращения
инфузий жиров.84
Нарушения функции печени. Хотя имеются со-
общения о нарушениях функции печени, возника-
ющих со 2-го до 14-го дня после начала ТПП, та-
ких как повышение в сыворотке уровня глютама-
токсалоацетатной трансаминазы (SGOT) и лак-
та гдегидрогеназы (ЛДГ), глютаматпируватной
трансаминазы (SGPT) и билирубина, однако ги-
стологическое исследование печеночной ткани не
выявляет каких-либо патологических изменений.
Указанные отклонения обычно преходящи, и в боль-
шинстве случаев показатели возвращаются к
норме сразу после прекращения парентерального
питания. Возникающие изменения, как правило, нс
зависят от того, получает пациент внутривенно
жировые добавки к инфузату или нет. Гистологи-
чески у большинства больных, получающих жиры
внутривенно дольше 1 месяца, в печени в клетках
Купфера обычно обнаруживаются жировые пиг-
менты. Роль подобного депонирования пигментов
пока еще недостаточно ясна.
Холестатическая желтуха, связанная с ТПП, бо-
лее часто встречается у недоношенных детей, чем
у старших пациентов, что, по-видимому, связано
с незрелостью билиарной экскреторной системы.
Хотя холестатическая желтуха обычно исчезает
через 2—3 недели после прекращения паренте-
рального питания, однако в некоторых осложнен-
ных случаях может развиться печеночная недоста-
точность. иногда даже с летальным исходом.
Патофизиология подобного тяжелого поражения
печени не ясна, однако не исключено, что опреде-
ленную роль здесь играет полное отсутствие энте-
рального питания, а соответственно и отсутствие
энтеральной стимуляции выделения желчи, приво-
дящее к ее застою.
Аллергические реакции. Для детей, получаю-
щих регулярно интралипид, довольно характерно
развитие в периферической крови эозинофилии
в пределах 5—10%. В редких случаях этот показа-
тель может достигать 35%. Подобные изменения
не имеют особого клинического значения, если не
сопровождаются кожной сыпью или другими про-
явлениями аллергии, и обычно исчезают, как толь-
ко прекращается введение интралипида.76
Гипергидратация и дыхательная недоста-
точность. Гипергидратация, сопровождающаяся
отеком легких, периферическими отеками или сер-
дечной недостаточностью, редко возникает в тех
случаях, когда соблюдаются все правила, описан-
ные выше, а парентеральное питание осуществля-
ется по строгим показаниям и с тщательным конт-
ролем. Проведенные в нашей клинике исследова-
ния с применением нерадиоактивных изотопов
окиси дейтерия показали, что общее содержание
воды в организме во время парентерального пита-
ния не повышается, а даже уменьшается парал-
лельно с ростом МТ. Эти данные подтверждают
гипотезу о том, что весовые прибавки при паренте-
ральном питании связаны в большей степени
с увеличением тканевой массы, чем с задержкой
6». 70. 87
воды.
У пациентов с нарушениями функции легких
значительная нагрузка декстрозой при паренте-
ральном питании может способствовать развитию
дыхательной недостаточности. Подобное осложне-
ние объясняется повышенной продукцией углекис-
лоты, связанной с углеводным обменом (1 моль
СО, продуцируется на каждый моль поглощенного
кислорода: RQ—1), что требует увеличения дыха-
тельной активности. Если такие больные уже на-
ходятся на ИВЛ, то переход на самостоятельное
дыхание бывает затруднен. Лечение заключается
в уменьшении нагрузки декстрозой и в замещении
декстрозных калорий жировыми (RQ=0,7). Дан-
ное осложнение подчеркивает необхо щмость точ-
ного расчета соотношения калорий, обеспечивае-
мых глюкозой, белками и жирами. Подобные
расчеты достаточно хорошо разработаны для взрос-
лых 88 и продолжают разрабатываться в настоящее
время для грудных и маленьких детей.
СИНДРОМ КОРОТКОЙ кишки
Лечение грудных детей с синдромом короткой
кишки — одна из наиболее трудных проблем, тре-
бующая большого опыта и терпения со стороны
хирургов, педиатров, специалистов по питанию
и медсестер. У доношенных детей длина тонкой
кишки при рождении около 200 см. Хотя нс опре-
делено достоверно, какая минимальная длина ки-
шечника совместима с жизнью, однако большин-
ство детских хирургов считает, что при сохранен-
ном илеоцекальном угле ребенок может жить на
оральном питании при длине тонкой кишки более
25—30 см. При отсутствии же илеоцекального уг-
ла для выживания необходимо не менее 50 см
тонкой кишки. В литературе встречаются сообще-
ния о детях, выживших при наличии меньшей дли-
ны кишечника, но это скорее исключение, чем пра-
вило.
В случаях, когда диагностирован синдром корот-
кой кишки, необходимо составить программу веде-
ния пациента. Это чрезвычайно сложная задача,
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 49
особенно если учесть, что нет и нс может быть
единого «рецепта». Лечение такого больного требу-
ет комбинации парентерального и диетического
питания со специальными смесями. Переход на эн-
теральное питание осуществляется постепенно,
в течение нескольких недель, и даже месяцев. По-
стоянно должны учитываться потребности, связан-
ные нс только с наличием короткого кишечника,
но и обусловленные ростом и развитием ребенка.
При использовании каких бы то ни было питатель-
ных смесей парентеральное питание должно обес-
печивать всеми необходимыми калориями углево-
дов, жиров и белков. Внутривенное питание посте-
пенно сокращается по мере адаптации ЖКТ
к оральному питанию.
Поскольку маленькие дети с короткой кишкой
обладают очень низкой толерантностью, даже
к умеренно гипертоническим препаратам, готовые
смеси, такие как Pregestimil. должны вводиться
в очень разбавленном виде. Объем увеличивают
постепенно в течение нескольких дней, и даже не-
дель. Только после того, как ребенок стал усваи-
вать соответствующий объем, можно начать мед-
ленное увеличение концентрации. Если эти препа-
раты не усваиваются ни в какой концентрации,
можно назначить самые простые элементарные
смеси в разбавленном виде, такие, как Vivonex. По
мере роста грудных детей, получающих все необ-
ходимые калории внутривенно, их кишечник начи-
нает приспосабливаться путем удлинения, расши-
рения и гипертрофии кишечных ворсинок, поэтому
в последующем к оральной диете ребенок адапти-
руется быстрее.
Обычно такие больные периодически госпитали-
зируются на период от нескольких месяцев до года,
и даже больше. В течение этого времени ребенок
может иметь несколько «подъемов и падений»,
и это часто обескураживает родителей н медицин-
ский персонал, что в свою очередь приводит к сни-
жению внимания к важным деталям и скрупулез-
ности в уходе, необходимых при лечении таких
больных. Одна из самых важных задач в подобных
ситуациях — поддерживать морально-психологи-
ческое состояние всех, кто осуществляет уход за
этими пациентами: врачей, специалистов по пита-
нию и среднего мсдпсрсоната.
ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ В ДОМАШНИХ
УСЛОВИЯХ
У некоторых больных с синдромом короткой киш-
ки, кишечной псевдообструкцией, хроническими
воспалительными заболеваниями кишечника мо-
жет возникать необходимость в частичном или
полном парентеральном питании в домашних
условиях. Домашнее парентеральное питание
(ДНИ), несомненно, имеет психологические, со-
циальные и экономические преимущества перед
длительным пребыванием в стационаре. Важно
очень скрупулезно отобрать детей для ДПП, обу-
чить их самих и родителей, осуществляя во время
ДПП внимательное наблюдение. Основные по-
казания к ДПП следующие: (1) заболевания, ха-
рактер которых исключает возможность нормаль-
ного роста и развития без дополнительного парен-
терального питания, и (2) необходимость паренте-
рального питания в течение 30 дней или больше.
Как только поставлен силиконовый катетер в цен-
тральную вену, для каждого больного и семьи со-
ставляется детальная подробнейшая карта, в кото-
рой в мельчайших деталях, шаг за шагом, указы-
ваются методы инфузии и ухода за катетером. Как
только пациент приспособился к усвоению опти-
мального суточного парентерального объема с со-
ответствующей концентрацией, начинается адап-
тивная фаза, которая состоит в уменьшении про-
должительности инфузии до 2 часов каждый день
с сохранением прежнего общего суточного объема
за счет увеличения скорости инфузии. При этом
используется электрический инфузионный насос
с сигналом тревоги и устройством для автомати-
ческого выключения при попадании воздуха в си-
стему, окклюзии катетера или трубки и окончании
раствора. Иногда больные приспосабливаются к
инфузии всего суточного объема ночью в течение
10—12 часов. Промывание катетера гепаринизиро-
ванным физиологическим раствором и отключение
системы позволяют ребенку днем вести обычный
образ жизни. Растворы для питания могут приго-
тавливаться в больничной аптеке или поставляться
больному непосредственно на дом одним из пред-
приятий, изготавливающих или торгующих этими
препаратами.
Стоимость проведения такой программы состав-
ляет от половины до трети стоимости стационарно-
го парентерального питания. Экономия может уве-
личиваться. когда больные или родственники
овладевают умением приготавливать (смешивать)
питательные растворы дома.
В нашем госпитале обучение программе ДПП
проводится фармацевтами и медсестрами из специ-
альных бригад по парентеральному и энтерально-
му питанию. Продолжительность курса обучения
в стационаре составляет 2 недели. Осложнения
ДПП удивительно редки, и дети могут существо-
вать с этими катетерами в течение столь же дли-
тельного времени, как и взрослые. Психологиче-
ские и социальные выгоды ДПП для детей, не-
сомненно, чрезвычайно велики. Один из наших
пациентов, живя на домашнем-парентеральном пи-
тании, с постоянным катетером, закончил колледж
и женился.
При проведении у детей ДПП возникает ряд
специфических проблем. Такие пациенты нужда-
ются во внимательном профессиональном наблю-
дении за технической стороной инфузий, в обеспе-
чении тщательного ухода, постоянном контроле,
выборе необходимых растворов. Все это должно
способствовать быстрому физическому развитию
ребенка и позволить ему вести днем активный пол-
ноценный образ жизни. Участие бригад по пита-
нию в этом процессе обязательно, причем бригада
должна работать в тесном контакте со всеми спе-
циалистами, имеющими отношение к данному
больному. К пациенту и его семье «прикрепляется»
доктор, который незамедлительно решает все воз-
4 Заказ № 1622
50 ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ
никаюшие проблемы. Состав растворов для парен-
терального питания, результаты периодически
проводимых лабораторных исследований, измене-
ния физического развития пациента должны конт-
ролироваться регулярно, с определенными времен-
ными интервалами.
ЛИТЕРАТУРА
1. Dudrick SJ. Wilmore DW, Vars HM, and Rhoads JE: Longterm
parenteral nutrition with growth, development, and positive nit-
rogen balance. Surgery 64:134—142. 1968.
2. Dudrick SJ, Wilmore DW, Vars HM, and Rhoads JE: Can intra-
venous feeding as the sole means of nutrition support growth in
the child and restore weight loss in an adult: An affirmative
answer. Ann Surg 169:974—984. 1969.
3- Coran AG. Drongowski RA: Body fluid compactment chan-
ges following neonatal surgery. J Pediatr Surg 24:829—832.
1989.
4. Benner JW, Coran AG, Weintraub WH, Wesley JR: The impor-
tance of different calorie sources in the intravenous nutrition of
infants and children. Surgery 86:429—433, 1979.
5. Holman RT, Johnson SB, Hatch TF: A case of human linolenic
acid deficiency involving neurological abnormalities. Am J Clin
Nutr 35:617—623, 1982.
6. Kchlet H: Stress-free anaesthesia and surgery. Acta Anesthes
Sea nd 23:503—504. 1979.
7. Moyer E, Cerra F, Cheiner R, Peters I), et al.: Multiple systems
organ failure. VI. Death predictors in the trauma septic state —
the most critical determinants. J Trauma 21:862—869. 1981.
8. Rackow H, Salanitre E, Green LT: Frequency of cardiac arrest
associated with anesthesia in infants and children. Pediatrics
28:697—704, 1961.
9. Schweiss JF, Pennington DG: Anesthetic management of neona-
tes undergoing palliative operations for congenital heart defects.
Clev Clin Quart 48:153—165, 1981.
10. Suits GS, Boltsford JE Jr: The metabolic response to trauma.
Res Staff Phys 33:21—29, 1987.
IL Anand KJS, Hickey PR: Pain and its effects in the human neo-
nate and fetus. N Engl J Med 317:1321 —1329. 1987.
12. Valman HB, Pearson JF: What the fetus feels. Br Med
J 280:233- 234, 1980
13. Cuthbertson DP: Post-shock metabolic response. Lancet
1:433—437. 1942.
14. Cuthbertson DP: Protein metabolism in relation to energy needs.
Metabolism 8:787—808, 1959.
15. Ito T. I у omasa Y, Inoue T: Changes of the postoperative mini-
mal oxygen consumption of the newborn. J Pediatr Surg
11:495 503, 1976.
16. Im MJC, Hoopes JE: Energy metabolism in healing skin wounds.
J Surg Res 10:459—466, 1970.
17. Wilmore DW: Glucose metabolism following severe injury.
J Trauma 21:705—707. 1981.
18. Elliott M. Albert KG MM: The hormonal and metabolic response
to surgery and trauma, In Kleinberger G, Deutsh E (Editors).
New Aspects of Clinical Nutrition. Karger. Basel, pp 247 270,
1983.
19. Kerri-Szanto M: Demand analgesia. Br J Anesthesia 55:919
920, 1983.
20. Brandt MR, Fernandez A, Mordhurst R. Kehlet II: Epidural
analgesia improves post-operative nitrogen balance. Br Med
J 1:1106—1108, 1978.
21. Anand KJS, Brown MJ, Causon RC, et al.: Can the human neo-
nate mount an endocrine and metabolic response to surgery?
J Pediatr Surg 20:41—48, 1985.
22. Anand KJS, Brown MJ, Bloom SR, Aynsley-Green A: Studies on
the honnotal regulation of fuel metabolism in the human new-
born infant undergoing anesthesia and surgery. Hormone Res
22:115 128, 1985.
23. Anand KJS, Sippell WG. Aynsley-Green A: Randomised trial of
fentanyl anesthesia in preterm babies undergoing surgery: Ef-
fects on the stress response. Lancet 8527:243—248, 1987.
24. Anand KJS, Sippell WG. Schofield NM, Aynsley-Green A: Does
halothane anesthesia decrease the metabolic and endocrine
stress responses of newborn infants undergoing operation? Br
Med J 296:668—672» 1988.
25. Anand KJS. Aynsley-Green A: Metabolic and endocrine effects
of surgical ligation of patent ductus arteriosus in the human
preterm neonate: Are there implications for further improvement
of post-operative outcome? Mod Probl Paediatr 23:143—157,
1985.
26. Anand KJS: Metabolic and Endocrine Effects of Surgery an
Anesthesia in the Human Newborn Infant. D Phil. Thesis.,
University of Oxford, 1985.
27. Christou NV, McLean APH, Meakins JL; Host defense in blunt
trauma: Interrelationships of kinetics of energy and depressed
neutrophil function, nutritional status, and sepsis. J Trauma
20:833—841. 1980.
28. Dechert RE, Wesley JR, Schafer LE, et al.: A water-sealed indi-
rect calorimeter for measurement of oxygen consumption (Vo2),
carbon dioxide production (Vco2), and energy expenditure in
infants. J Parent Enteral Nutr (In press).
29. Dechert R, Wesley JR, Schafer L, et al.: Comparison of oxygen
consumption (Vo2), carbon dioxide production (Vco,), and res-
ting energy expenditure (REE) in premature and full-term in-
fants. J Pediatr Surg 20:765—771, 1985.
30. Mendeloff E, Wesley JR, Dcckert RE, et al.: Comparison of
measured resting energy expenditure (REE) versus estimated
energy expenditure (EEE) in infants. J Parent Enteral Nutr
10: (Supplement) 65, 1986.
31. Heiss K, Hirschl R, Ciiley R, et al.: Measuring infant metabo-
lism: Design and testing of a miniature gas exchange monitor
J Pediatr Surg (In press).
32. Hirschl R, Heiss K, Hultquist K, ct al.: Right atrial venous satu-
ration: What role can in play in the mechanically ventilated
neonate? Presented at the Society for Pediatric Research, To-
ronto, Ontario, September 27, 1987.
33. Wesley JR, Tse Y, Dechert R: Indirect calorimetry on mechani-
cally ventilated rabbits. Presented at lhe European Society of
Parenteral and Enteral Nutrition, Paris. September 17, 1987.
34. Baker JP, Detsky AS, Wesson D, et al.: Nutritional assessment:
A comparison of clinical judgement and objective measurements.
N Engl J Med 306:969—972, 1982.
35. Forse RA, Shizgal HM: 1'hc assessment of malnutrition. Surgery
88:17 24, 1980.
36. Bartlett RH, Dechert RE, Mault JR, et al.: Measurement of me-
tabolism in multiple organ failure. Surgery 92:771—779, 1982.
37. Randall HT, Bauer RH, Hickey MD, et al.: Early post-operative
feeding. (Symposium.) Contcmp Surg 30:97—130, 1987.
38. Heymsfield SB, Bethel RA, Ansley JO, et al.: Enteral hyperali-
mentation — an alternative to central venous hyperalimentation.
Ann Intern Med 90:63—71, 1979.
39. Delany HM, Carnevale N. Garvey JW, et al.: Post-operative
nutritional support using needle catheter feeding jejunostomy.
Ann Surg 186:165—170, 1970.
40. Steffee WP, Krey SH: Enteral hyperalimentation of the cancer
patient. In Newell GR, Ellison NM (Editors). Nutrition an
Cancer: Etiology and Treatment. Raven Press, New York, pp
7—31, 1981.
ЭНТЕРАЛЬНОЕ И ПАРЕНТЕРАЛЬНОЕ ПИТАНИЕ 51
41. McLean GK: Radiologic technuquc of gastrointestinal intubati-
on. tn Rombeau JI , Caldwell ND (Editors). Entered and lube
Feeding. WB Saunders Co, Philadelphia, pp 240—252, 1984.
42. Gustke RF, Vaina RR, Soergel KM: Gastric reflux during perfusi-
on of the small bowel. Gastroenterology 59:890 895. 1970.
43. Meeker I A. Snyder WH: Gastrostomy for the newborn surgical
patient: A report of 140 cases. Arch Dis Child 37:159—Ifift,
1962.
44. Berg RB. Schuster SR. Colodny AH: The use of gastrostomy
feeding premaiure infanis. Pediatrics 33:287—289. 1964.
45- Haws EB, Sieber WK, Kiesewetter WB: Complications of tube
gastrostomy in infants and children; 15-year review of 240 ca-
ses. Ann Surg 164:284—290„ 1966.
46. Gallagher MW, Tyson KRT, Aschcraft KW: Gastrostomy in
pediatric patients; An analysis of complications and techniques.
Surgery 74:536—539. 1973.
47. Canal DF. Vane DW. Seiichi G: Reduction of lower esophageal
sphincter pressure with Stamm gastrostomy. J Pediatr Surg
22:54—57. 1987.
48. Wesley JR. Coran AG, Sara han ГМ, et al.: The need for evalua-
tion of gastroesophageal reflux in brain-damaged children re-
ferred by feeding gastrostomy. J Pediatr Surg 16:866 871,
1981.
49. Rombeau JI , Barot I R, Low DW, et aL: Feeding by lube ente-
rostomy. In Rombeau JL, Caldwell MD (Editors). Enteral an
Tube Feeding. WB Saunders Co, Philadelphia, pp 275—291.
1984.
50. Gauderer ML, Ponsky JL, Izant RJ Jr: Gastrostomy without
laparotomy: A percutaneous endoscopic technique. J Pediatr
Surg 15:872-875, 1980.
51. Bchkov KJ. Kazlow PG. Wave JD, et al.: Percutaneous endosco
pic gastrostomies in children. Pediatrics 177:248—250, 1986
52. Gauderer ML, Picha GJ, Izant RJ: The gastrostomy «button* —
a simple skin-level, non-refluxing device for long-term enteral
feedings. J Pediatr Surg 19:803 805. 1984.
53. Mukherjee D, Emmcns RE, Putnam ГС: Non-operative conversi-
on of gastrostomy to feeding jejunostomy in children and adults.
Surg Gynecol Obstet 154:881 —882. 1982.
54 Lee HA: Parenteral Nutrition in Acute Metabolic Illness. Aca-
demic Press, New York, 1974.
55. Hclfrick FW, Abelson NM: Intravenous feeding of a complete
diet in a child; Report of a case. J Pediatr 25:400—403,
1944.
56. Filler RM. Eraklis AJ. Rubin VG, Das JB: Long-term parenteral
nutrition in infants- N Engl J Med 281:589 594, 1969.
57. Hcird WC, Winters RW; Total parenteral nutrition: The slate of
the art. J Pediatr 86:2—16, 1975.
58. Borresen HC, Coran AG, Knutrud O: Metabolic results of pa-
renteral feeding in neonatal surgery: A balanced parenteral
feeding program based on a synthetic L-aminu acid solution
and a commercial fat emulsion. Ann Surg 172:291 301. 1970.
59. Coran AG: The intravenous use of fat for the total parenteral
nutrition of the infant. Lipids 7:455—458, 1972.
60. Coran AG: The long-term intravenous feeding of infants using
peripheral veins. J Pediatr Surg 8:801—807, 1973.
61. Coran AG: Total intravenous feeding of infants and children
without the use of a central venous catheter. Ann Surg
179:445—449, 1974.
62. Fox HA, Krasna IH: Total intravenous nutrition by peripheral
vein in neonatal surgical patients. Pediatrics 52:14—20, 1973.
63. Dudrick SJ, Steiger E, Long JM: Renal failure in surgical pati-
ents: Treatment with intravenous essential amino acids and hy-
pertonic glucose. Surgery 68:180 186, 1970.
64. American College of Surgeons. Ballinger WF, Collins JA, Dru-
cker WR. ct al. (Editors): Manual of Surgical Nutrition. WB Sa-
unders. Philadelphia. 1975.
65. Wesley JR, Khalidi N, Faubion WC. el al.: The University о
Michigan Hospitals Parenteral and Enteral Nutrition Manual,
fourth edition. Abbott Laboratories, Hospital Products Division,
Chicago, HI., 1986
66. Press M, Напор PJ, Prottey C: Correction of essential fattyacid
deficiency in man by the cutaneous application of sunflower
seed oil. Lancet 1:579—580, 1974.
67. Coran AG, Drongowsiki R, Sarahan TM. et al.: Studies on the
efficacy of a new 20% fat emulsion in pediatric parenteral nut-
rition. J Parent Enteral Nutr 6:222—225. 1982.
68. Fonkalsrud E.W, Berquist W. Burke M. et ah: Long-term hype-
ralimentation in children through saphenous central venous ca-
theterization. Am J Surg 143:209—211. 1982.
69. Rhodin AGJ, Coran AG, Weintraub WH, et al.: Total body wa-
ter changes during high-volume peripheral hyperalimentation.
Surg Gynecol Obstet 148:196—200. 1979.
70. Coran AG. Drnngowski RA. Wesley JR: Changes in total body
waler and extracellular fluid volume in infanis receiving total
parenteral nutrition. J Pediatr Surg 19:771—776, 1984
71. Buck JR. Connors RH, Coon WW. et al.: Pulmonary embolism in
children. J Pediatr Surg 16:385—391, 19X1.
72. Wesley JR, Keens TG, Miller SW, ct al.: Pulmonary embolism in
the neonate: Occurrence during the course of total parenteral
nutrition. J Pediatr 93:113—115, 1978.
73. Curry CR, Quic PG: Fungal septicemia in patients receiving
parenteral hyperalimentation. N Engl J Med 285:1221 —1225,
197L
74. Faubion WC. Wesley JR, Khalidi N, ct al.: TPN catheter sepsis:
Impact of the team approach. J Parent Enteral Nutr 10:642—
645, 1986.
75. Coran AG: The long-term intravenous feeding of infants using
peripheral veins. J Pediatr Surg 8:801—807, 1973.
76. Coran AG: Total intravenous feeding of infanis and children
without the use of central venous catheter. Ann Surg 179:445
449, 1974.
77. Coran AG, Weintraub WH: Peripheral intravenous nutrition
without fat in neonatal surgery. J Pediatr Surg 12:195—199,
1977.
78. Shils ME: Guidelines for total parenteral nutrition. JAM
220:1721 — 1728. 1972.
79. Travis SF. Sugar man 11 J, Ruberg R1 . et al.: Alterations of red-
cell glycolytic intermediates and oxygen transport as a consequ-
ence of hypophosphatemia in patients receiving intravenous hy-
peralimentation. N Engl J Med 285:763—768. 1971.
80. Knutrud O: The water and electrolyte metabolism in the new-
born child after major surgery. Norwegian Monographs on
Medical Science, Oslo, 1965.
81. Ashkenazi A, Levin S, Djaldetti M, et al.: The syndrome of neo-
natal copper deficiency. Pediatrics 52:525—533, 1973.
82. Karpcl JT, Peden VH: Copper deficiency in long-term parente-
ral nutrition. J Pediatr 80:32 36. 1972.
83. Paulsrud JR, Pensler L, Whitten CF, et al.: Essentia! fatty acid
deficiency in infanis induced by fat-frec intravenous feeding. Am
J Clin Nutr 25:897- -904, 1972.
84. Coran AG, Edwards B, Zalesk R: The value of heparin in the
hyperalimentation of infants and children with a fat emulsion.
J Pediatr Surg 9:725—732, 1974.
85. Merritt RJ: Cholestasis associated with total parenteral nutriti-
on. J Pediatr Gastroenterol Nutr 5:9—21. 1986.
86. Drongowski RA. Coran AG: An analysis of factors contributing
to development of total parenteral nutrition-induced cholestasis.
J Parent Enteral Nutr 13:586—589, 1990.
87. Polley TZ, Benner JW, Rhodin AGJ, et al.: Changes in total
body water in infants receiving total intravenous nutrition.
J Surg Res 26:555—559, 1979.
88. Askanazi J. Rosenbaum SH. Hyman Al, ct al.: Respiratory
changes induced by the large glucose loads of total parenteral
nutrition. JAMA 243:1444—1447, 1980.
89. Cannon A, Byrne J, Ament E, ct al.: Home parenteral nutrition
in infants. J Pediatr 96:1098—1104, 1980.
90. Goldberger H, DuLuci G, Wesselhoeft W, et al.: A home pro-
gram of long-term total parenteral nutrition in children. J Pedi-
atr 94:325—328, 1979.
Глава 3
МЕТОДЫ ОБЕЗБОЛИВАНИЯ
ПРЕДОПЕРАЦИОННАЯ ПОДГОТОВКА
Оценка состояния больного на данный момент, ре-
шение вопроса о его готовности к хирургическому
вмешательству и выбор наиболее рационального
метода анестезии определяются многими факто-
рами.
Ценную информацию дает анамнез, в частности
сведения о наличии в прошлом у больного или его
родственников анестезиологических осложнений,
таких как псевдохолинэстеразная недостаточность,
злокачественная гипертермия или порфирия. Од-
нако отсутствие в анамнезе данных осложнений
не исключает возможности их возникновения.
В частности 33% больных со злокачественной ги-
пертермией не имеют обычно никаких осложнений
во время предыдущих обезболиваний. Могут раз-
виться также аллергическая реакция и побочные
эффекты на применение различных анестетиков.
Нередко при слишком настойчивом выяснении
анамнеза родители ребенка начинают говорить об
аллергии, которая раньше ими отрицалась. Поэто-
му вопрос об аллергии не следует задавать упорно
и многократно. Абсолютно необходимы сведения
о недавно перенесенных заболеваниях.
Каждый пациент перед операцией должен быть
обследован. Уже на основании общего осмотра
обычно создается впечатление о том, может ли
данный больной быть подвергнут оперативному
вмешательству или нет. При наличии насморка
или кашля, если эти явления носят хронический
характер и отсутствуют какие-либо другие симпто-
мы, например снижение аппетита или активности,
больной может быть прооперирован. Если же на-
сморк начался недавно, или есть другие симптомы
заболевания (снижение активности, аппетита, по-
вышение температуры), операцию лучше отло-
жить до выздоровления. Никогда нс следует игно-
рировать подъем температуры и, пока достоверная
причина этого повышения не найдена, заболевание
правильнее расценивать как острое и соответст-
венно воздержаться от операции.
Продолжает оставаться спорным вопрос о необ-
ходимости лабораторного обследования всех боль-
ных. Практика показывает, что обычные анали-
зы дают мало новой информации и их резуль-
таты в большинстве случаев не отражаются на
принятии решения о характере обезболивания.
В 1987 г. Американским Обществом Анестезиоло-
гов было введено положение о том. что при подго-
товке к анестезии нет необходимости в обычных
лабораторных анализах и скрининговых тестах.
Решение о показаниях к лабораторному обследова-
нию должно приниматься индивидуально в каждом
конкретном случае в зависимости от особенностей
данного больного и предполагаемого характера
оперативного вмешательства. При таком подходе
уменьшается травма для больного и косвенно для
родителей, а также стоимость медицинских мани-
пуляций, которые часто оказываются совершенно
бесполезными.
Медикаментозная подготовка, безусловно, пока-
зана при планировании эфирного наркоза. Пред-
варительное обезболивание частично уменьшает
риск ларингоспазма и сокращает время, требующе-
еся для введения больного в наркоз. Однако ис-
пользуемые в настоящее время анестетики лишены
присущих эфиру недостатков, а потому при их
использовании отпадает необходимость в медика-
ментозной подготовке. Хорошо «обставленное» до
операционное посещение анестезиологом больного
может сделать очень многое для снятия страха
и тревоги пациента и родителей и быть во многих
случаях нс менее эффективным, чем применение
лекарств.
Тем не менее для некоторых больных медика-
ментозная подготовка полезна, например, перед
кардиохирургическими операциями и особенно
у нервных детей. Такая подготовка может быть
осуществлена любым способом, желательно лишь
избегать внутримышечного введения препаратов.
Мидазолам в дозе 0,3 0,5 мг/кг орально доста-
точно эффективен и притом нс столь длительно
действует, как диазепам. Могут быть также ис-
пользованы синтетические опиаты в каком-либо не-
стандартном виде, например, фентаниловые леден-
цы или суфентанил интраназально. Метогекситал
продолжает успешно использоваться ректально
МЕТОДЫ ОБЕЗБОЛИВАНИЯ 53
как для индукции, так и для премедикации. В не-
которых медицинских учреждениях существуют
специальные индукционные комнаты, где родите-
лям разрешают присутствовать при введении ре-
бенка в наркоз, что оказывает порой не менее бла-
гоприятное воздействие, чем фармакологические
препараты. Из возможных нежелательных проб-
лем, возникающих в связи с медикаментозной под-
готовкой, следует прежде всего назвать гипоксию
и длительный выход из наркоза при чрезмерной
седатации.
Многие дети, которым предстоит хирургическое
вмешательство, находятся на лечении различными
лекарствами по поводу имеющихся у них забо-
леваний. В таких случаях лечение, включая
оральные и аэрозольные препараты, должно быть
продолжено вплоть до операции. Возможным иск-
лючением является дигоксин (ланоксин) у кардио-
хирургических больных. Не прекращая проводив-
шееся лечение, можно избежать обострения болез-
ни, а также обеспечить более гладкое и безопасное
течение анестезии.
Часто дети с пороками сердца подвергаются опе-
рациям на других органах и системах. Некоторые
из них имеют риск развития подострого бактери-
ального эндокардита (ПБЭ), профилактика кото-
рого необходима/
Аспирационная пневмония может быть осложне-
нием любой анестезии. Частота ее, по данным ис-
следований 1986 и 1988 гг., уменьшается. ’ Глав-
ный способ снизить риск аспирации — воздержи-
ваться от приема пищи и питья перед операцией
с целью уменьшения объема желудка. Однако воз-
держание от питья и еды часто вызывает состояние
дискомфорта у ребенка и беспокойство у родите-
лей. а иногда даже ведет к дегидратации и ги-
погликемии.6 Не следует поэтому держать ребенка
без пищи и питья длительное время. Последний
прием чистой жидкости вполне допустим за 2—
3 часа до операции. ’ Однако соблюдение медпер-
соналом сроков голодания перед операцией в усло-
виях стационара довольно сложно. В связи с этим
наиболее разумно установить время последнего
кормления с некоторой перестраховкой — 4 часа
до операции для питья (чистая жидкость) и 6 ча-
сов для пищи, включая молоко.
Риск аспирации можно уменьшить путем сниже-
ния кислотности желудочного содержимого или
уменьшения объема желудка. С этой целью с успе-
хом применяются блокаторы Н2-рецепте ров, такие
как ранитидин. Для достижения максимального
эффекта препарат следует принимать по меньшей
мере за 90 мин до операции, хотя оптимальное
время для его приема — вопрос спорный и слож-
ный. Ускорению опорожнения желудка и уменьше-
нию его объема способствует применение церука-
ла. В плане снижения pH желудочного содержимо-
го эффективны буферообразующие препараты, та-
кие как цитрат натрия. Специальные медикамен-
тозные средства этой группы в настоящее время ие
рекомендуются до операции, но у больных с ри-
ском аспирации, особенно при срочных вмешатель-
ствах, они могут быть использованы.
АНЕСТЕЗИЯ ПРИ АМБУЛАТОРНЫХ ОПЕРАЦИЯХ
В использовании преимуществ амбулаторных опе-
раций при лечении детей с хирургической патоло-
гией отмечаются радикальные изменения. В нача-
ле 80-х годов амбулаторная детская хирургия
в большинстве медицинских учреждений ограничи-
валась больными, которые не имели более или ме-
нее серьезных заболеваний, или теми, кому были
показаны лишь минимальные малые вмешательст-
ва. В настоящее время 60—70% всех операций
в большинстве детских госпиталей страны произ-
водится в амбулаторных условиях. Дети с доста-
точно тяжелыми заболеваниями (диабет, астма,
врожденные пороки сердца), но находящиеся в ста-
бильном состоянии, подвергаются наркозу для
весьма сложных процедур и вмешательств (тон-
зиллэктомия. уретропластикэ, бронхоскопия) и от-
пускаются домой в тот же чень. Стремительный
рост частоты амбулаторных операций вызвал не-
обходимость модификации и развития методов
анестезии, а также новых лекарственных препара-
тов. применяющихся для этих целей. В настоящее
время проведение анестезии многим больным, под-
вергающимся самым разнообразным вмешательст-
вам, стало более безопасным и эффективным.
Вопрос о том, можно ли данного ребенка опери-
ровать амбулаторно, должен решаться с учетом
многих факторов. При этом необходима согласо-
ванность действий хирурга и анестезиолога. Инди-
видуальные особенности пациентов могут быть са-
мыми разнообразными, поэтому нет каких-либо
единых определенных правил анестезии для всех
больных. При наличии у ребенка тяжелого систем-
ного заболевания течение его должно тщательно
контролироваться. Необходимо сделать все, чтобы
это заболевание нс сказалось неблагоприятно на
течении послеоперационного периода. Оператив-
ные вмешательства, оказывающие серьезное воз-
действие на важнейшие системы организма, не
должны осуществляться в амбулаторных условиях.
Согласованность в действиях хирурга и анестезио-
лога очень существенна в принятии решений в по-
добных ситуациях. Выбор пациентов для амбула-
торных вмешательств определяется также семей-
ными и социальными обстоятельствами. Важно
выяснить — будет ли ребенку обеспечен уход до-
статочно разумными и заботливыми взрослыми
людьми? Не будет ли ребенок на руках у единст-
венного родителя, который к тому же вынужден
работать? Насколько далеко придется ребенку до-
бира гься до медицинского учреждения, если пона-
добится стационарная помощь? Эти и ряд других
факторов должны быть оценены прежде, чем при-
нимается решение с возможности осуществления
хирургического вмешательства в амбулаторных
условиях.
Анестезиологи обладают широкими возможно-
стями в выборе анестетиков для амбулаторной
хирургии. Достаточно популярным остается до
настоящего времени фгоротан, который хорошо
переносится больными и имеет минимум побочных
эффектов. Несколько более тяжело переносят дети
54 МЕТОДЫ ОБЕЗБОЛИВАНИЯ
изофлюран, хотя в принципе это ценный и безо-
пасный анестетик. Часто используются синтетиче-
ские наркотические анальгетики короткого дейст-
вия, фентанил и суфентанил, в сочетании с инга-
ляционными препаратами. Алфентанил имеет бо-
лее короткую продолжительность действия, чем
фентанил. Все три препарата могут применяться
для обезболивания процедур длительностью 30—
60 мин. В некоторых учреждениях при амбулатор-
ных вмешательствах используют регионарную
анестезию, в частности спинальную.’ При решении
вопроса о контроле за проведением анестезии
и вмешательства и об уходе в послеоперационном
периоде, амбулаторных больных необходимо также
внимательно обследовать и обсуждать, как и ста-
ционарных пациентов. После вводного наркоза це-
лесообразно поставить катетер в вену для частич-
ной регидратации, а также для обеспечения воз-
можности введения лекарственных препаратов и
обезболивания в послеоперационной палате. В те-
чение всего времени, пока стоит интравенозная ли-
ния, мы стараемся вводить не меньше 30 мл/кг
кристаллоидов. Этот объем, обеспечивающий аде-
кватную гидратацию, позволяет уменьшить ораль-
ную нагрузку в послеоперационном периоде и со-
ответственно предотвратить тошноту, нередко воз-
никающую после хирургических вмешательств.
ВЕДЕНИЕ АМБУЛАТОРНЫХ БОЛЬНЫХ
В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ
Период выздоровления после хирургических вме-
шательств в детском возрасте может быть более
тяжелым и неожиданным, чем у взрослых паци-
ентов. Хотя риск интраоперационных осложнений
одинаков у взрослых и детей, частота серьезных
осложнений в послеоперационном периоде состав-
ляет у детей 3 -4%, в то время как у взрослых
только 0,5 %.'°'11
Учитывая все большее распространение амбула-
торных операций с выпиской в тот же день и более
высокий процент осложнений у детей, клиницисты
должны знать о возможных осложнениях.
При появлении боли в послеоперационном пери-
оде амбулаторного больного следует лечить так
же, как и стационарного. Хороший эффект в таких
случаях оказывает местная блокада.12 Обеспечить
на 12—24 час. обезболивание можно с помощью
Bupivacaine, что позволяет к тому же избежать
в послеоперационном периоде применения нарко-
тических препаратов.
Рвота после операции возникает у 2—5% детей,
иногда — чаще.11 Например, у подростков после
любых вмешательств рвота отмечается в два раза
чаще, чем у детей любого другого возраста. Ха-
рактерна рвота и для больных с задержкой опо-
рожнения кишечника в анамнезе, а также после
вмешательств на глазных мышцах.13 Не следует
ожидать прекращения рвоты и стремиться начать
поить ребенка перед выпиской из госпиталя. Важно
лишь удостовериться в том, что больной хорошо
гидратирован перед выпиской. Это, как правило,
обеспечивается внутривенным введением жидкости
во время операции. Детям, имевшим в анамнезе
рвоту после предыдущих операций, а также в тех
случаях, когда производится оперативное вмеша-
тельство. которое само по себе может вызывать
тошноту и рвоту (операции по поводу косоглазия,
стоматологические вмешательства, тонзиллэкто-
мия, операции на среднем ухе), мы вводим интра-
операционно внутривенно дропсридол (50—
70 мкг/кг). При этом ребенок может быть в день
операции, как обычно, без задержки выписан домой.
Различные дыхательные нарушения — наиболее
частая проблема послеоперационного периода,
свойственная детям всех возрастных групп. По
данным Cohen, при исследовании псриоперацион-
ных осложнений обструкция дыхательных путей
встретилась в среднем в 3% случаев. У наших
больных частота была такой же — около 2%.
Обычно указанные изменения отмечаются преиму-
щественно у пациентов, поступающих в послеопе-
рационную палату еще в глубоком наркозе, без
механической вентиляции.
Другая нередкая проблема, связанная с дыха-
тельными путями — постинтубационный круп.
Когда амбулаторная детская хирургия начала вхо-
дить в практику, многие медицинские центры дли-
le.ibHO пытались избегать амбулаторных операций
под интубационным наркозом именно в связи
с этим осложнением. И если требовалась операция
под интубационным наркозом, то это считалось
противопоказанием к амбулаторному вмешатель-
ству. По мерс накопления опыта отмечено, что
постинтубационный круп, в отличие от вирусного,
непродолжителен и па фоне лечения адреналином
не сопровождается реактивным отеком.14 Постепен-
но стало довольно обычным проведение амбула-
торных операций под интубационным наркозом,
если он показан, и этот вид обезболивания пере-
стал считаться показанием к обязательному стаци-
онарному ведению послеоперационного периода.
Постинтубационный круп отмечается в среднем
в 1 — 6% всех наблюдений. Наиболее часто он
возникает после операций на голове и шее у ма-
леньких детей (1—4 года), при травматической
интубации или повторных ее попытках, после уси-
ленного кашля или мышечного напряжения на ин-
тубационной трубке.15 Лечение обычно ограничива-
ется применением адреналина в аэрозоле (0,5 мл
в 2,5 мл физиологического раствора), хотя некото-
рые анестезиологи рекомендуют назначать стерои-
ды.16 В настоящее время, если больной получил
адреналин, мы наблюдаем его в течение 2 часов
и затем отпускаем домой. Родителям объясняем
симптомы и признаки нарастающего стридора
и/или нарушений дыхания и четко инструктируем
в отношении того, куда и к кому обращаться, если
это вдруг произойдет. За последние 5 лет среди
20 000 больных, оперированных нами амбулатор-
но, лишь 3 ребенка вернулись в госпиталь из дома
для дальнейшего лечения крупа.
Еще одно осложнение, которое мы отмечали
примерно у 3% детей в послеоперационной пала-
те — это снижение сатурации, встречающееся, как
правило, в тех случаях, когда ребенок поступает
МЕТОДЫ ОБЕЗБОЛИВАНИЯ 55
в послеоперационную палату в состоянии еще глу-
бокого наркоза. У таких больных бывает трудно,
по непонятным причинам, достичь адекватной са-
турации (95%) без кислорода. В подобных ситуа-
циях мы даем ребенку кислород, контролируем са-
турацию в течение нескольких часов и, если состо-
яние улучшается, ребенок выписывается, если
нет — поступает на ночь в стационар.
ОСОБЕННОСТИ ОБЕЗБОЛИВАНИЯ
У НЕДОНОШЕННЫХ ДЕТЕЙ
У детей, родившихся недоношенными, в последую-
щем при амбулаторных операциях могут отмечать-
ся различные особенности и осложнения, не свой-
ственные пациентам, родившимся в срок.17 Наи-
большую опасность представляет апноэ, возникаю-
щее обычно в течение первых 12—18 часов после
операции. Недостаточно понятно, какие факторы
способствуют этому, но, вероятно, определенную
роль играет незрелость нервной системы, особен-
но дыхательного центра ствола мозга, и недоста-
точное развитие мускулатуры диафрагмы, объяс-
няющее быстро развивающуюся утомляемость.18
Все, кто занимался изучением проблем, связанных
с амбулаторными операциями у недоношенных де-
тей, ' сходятся в том. что это пациенты высокого
риска в отношении послеоперационного апноэ, но
расходятся во мнениях относительно возраста,
к которому этот риск уже исчезает. Большинство
исследователей считают, что к возрасту 44—46 не-
дель после зачатия (гестационный возраст 4- воз-
раст после рождения) уже нет высокого риска ап-
ноэ и дети .могут быть подвергнуты амбулаторному
оперативному вмешательству. Однако существует
и иное мнение — о небезопасности операций рань-
ше, чем в возрасте 60 недель после зачатия.21
Сложно сделать какое-либо заключение на основа-
нии этих исследований в связи с очень разнообраз-
ным материалом у авторов, как в отношении воз-
раста детей, так и характера операций, а также
методов диагностики апноэ. Предпринимались по-
пытки определить факторы риска, которые могли
бы помочь в выявлении детей, склонных к апноэ.
Мы проспективно анализировали течение периода
новорожденности у 100 детей, родившихся недоно-
шенными. Наличие у них в анамнезе апноэ или
заболеваний легких, по-видимому, должно предрас-
полагать к послеоперационному апноэ.23 К сожале-
нию, небольшой материал в данном исследовании
не позволяет сделать какие-либо серьезные выво-
ды. Ни один из методов анестезии не обладает
существенными преимуществами перед любым
другим, хотя достаточно очевидно, что наибольшие
достоинства присущи спинальной анестезии.23 Так
же, как и никакие медикаментозные средства не
могут предупредить эпизоды апноэ, хотя кофеин
в этом плане в какой-то степени обнадеживает.2 *
Споры продолжаются. Во многих учреждениях
тактику в большей степени определяют принятые
установки, чем объективные фактические данные.
Пока нс будет получена достоверная дополнитель-
ная информация, разумно ограничить амбулатор-
ные оперативные вмешательства, проводя их у тех
недоношенных детей, возраст которых после зача-
тия больше 44—46 недель. Недоношенных паци-
ентов меньшего возраста целесообразно госпита-
лизировать после операции и наблюдать в отноше-
нии апноэ в течение 18—24 часов, осуществляя
мониторинг.
МОНИТОРИНГ
До 1960 г. интраоперационный мониторинг огра-
ничивался неинвазивным измерением давления
и частоты сердечных сокращений, катетеризация
сердца к тому времени использовалась не более
10 лет, а интраоперационный инвазивный монито-
ринг был вообще в зачаточном состоянии. В сере-
дине 70-х годов некоторые ведущие детские ане-
стезиологи продолжали считать, что в обычных
случаях для мониторинга достаточно прекордиаль-
ного стетоскопа.
В 1961 г. Dripps опубликовал данные о том. что
87% всех периоперационных летальных исходов
связаны исключительно с медицинскими ошибка-
ми.26 Более того, около 80%, а возможно, даже все
100% этих ошибок могли быть предотвраще-
ны.27-29 Хотя это сообщение было шокирующим,
однако автор не давал никаких специальных реко-
мендаций, не считая предупреждения о необходи-
мости особой настороженности со стороны анесте-
зиолога. Все более широкое внедрение сложных
методов мониторинга относится к 70-м годам. Тем
не менее повторное изучение причин «анестезио-
логических» смертей в 1978 г. показало, что 82%
по-прежнему были связаны с допущенными ошиб-
ками и что более 50% этих ошибок явились след-
ствием неопытности, поспешности, невнимательно-
сти или просто усталости анестезиолога-29
Наиболее частым фактором, являющимся причи-
ной анестезиологических неудач, была интраопе-
рационная гипоксемия.50 При дальнейшем изуче-
нии установлено, что частота падения сатурации
ниже 90% во время анестезии отмечалась в 10—
50% наблюдений. При этом не имело значения,
применялось ли общее обезболивание или местная
анестезия с внутривенной седатацией.31 Эпизоды
гипоксемии возникали даже при, казалось бы, бе-
зупречно проводимой анестезии. Однако серьезные
осложнения, вплоть до летальных исходов, отмеча-
лись, как правило, в тех случаях, когда гипоксемия
была нераспознана или не лечилась соответствую-
щим образом.
В 80-х годах в клиническую практику вошли
мониторы, которые стали применяться и для полу-
чения информации о состоянии больного, находя-
щегося в наркозе. Были предприняты попытки
уменьшить риск применения анестетиков путем
установления стандартов, касающихся пути их
введения и обязательности использования монито-
ров определенного типа.
В 1985 г. Отделение Анестезиологии Гарвард-
ской Медицинской Школы установило стандарты
для всех служб, где применяется анестезия.32 Лю-
бое помещение, в котором используются анестети-
56 МЕТОДЫ ОБЕЗБОЛИВАНИЯ
ки, должно иметь адекватное освещение, доста точ-
ное пространство и электророзетки, два источника
кислорода, наркозный аппарат, приспособление
для срочной транспортировки и функциональную
систему связи.
Через год Американским Обществом Анестезио-
логов было разработано положение об интраопера-
ционном мониторинге. Согласно этому положению
наркозный аппарат должен быть снабжен кисло-
родным анализатором, сигналом тревоги, измери-
телем сатурации и кровяного давления (автомати-
ческим), клинографом, температурным датчиком
и электрокардиографом (ЭКГ).
Страховые компании быстро отреагировали на
введение этих стандартов и требуют четкого со-
блюдения установленных правил, предоставляя
большие скидки тем анестезиологам, которые не-
уклонно следуют в своей работе всем рекоменда-
циям.
Для того, чтобы выяснить, действительно ли эти
рекомендации оказывают влияние на частоту
анестезиологических неудач, в 1988 г. Отделени-
ем Анестезиологии Гарвардской Медицинской
Школы был проведен ретроспективный анализ
750 000 операций, осуществленных до введения
указанных стандартов, и 244 000 вмешательств,
сделанных после внедрения их в практику.33 Обна-
ружено, что частота анестезиологических неудач
до применения мониторинга была 1 : 75 000, а по-
сле его введения — 1 : 244 000. Это же исследова-
ние выявило, что летальность, связанная исключи-
тельно с анестезиологическим пособием и состав-
лявшая 1 : 150 000, полностью исчезла с введением
мониторинга. И хотя полученные данные не под-
тверждены статистически (в связи с малой часто-
той изучавшегося показателя), невозможно нр
заметить несомненного влияния введения мони-
торинга на частоту осложнений, связанных с ане-
стезией.
Когда мы переносим полученные данные на де-
тей, следует помнить, что в детском возрасте инт-
раоперационные осложнения встречаются так же
часто, как и у взрослых. В среднем частота любой
интраоперационной проблемы составляет около
10% во всех возрастных группах. Среди детей
наибольший риск осложнений отмечается у ново-
рожденных. В нашем госпитале частота эпизодов
гипоксемии (сатурация ниже 90%) выявляется
в 5% всех наблюдений, а среди новорожденных —
в 38%.
Можем ли мы категорически утверждать, что
сложные и дорогостоящие мониторы, применяемые
в настоящее время, существенно уменьшают риск
неудач и ошибок, связанных с проведением анесте-
зии? Безусловно, нет. По мнению Arthur Keats, ис-
тинная частота анестезиологических ошибок и
осложнений неизвестна в значительной степени
в связи с субъективностью исследователей. Он так-
же считает, что врачи порой «создают» новые
проблемы с той же скоростью, с которой решают
старые. Кроме того, существует «риск ложной ин-
формации или ложной интерпретации достоверной
информации, что может привести к неправильному
решению и соответственно нежелательным послед-
ствиям». Однако результаты исследований
Гарвардской Медицинской Школы и сообщения
компаний, обеспечивающих многоплановое страхо-
вание, об уменьшении числа исков против анесте-
зиологов говорят о том, что анестезия всех видов
и во всех регионах страны становится все более
надежным и безопасным методом.
Специальные мониторы, их возможности и недо-
статки в плане увеличения безопасности анесте-
зии — предмет дальнейшего обсуждения.
ЭКГ монитор используется в течение многих
лет и первоначально применялся для определения
нарушений ритма и наличия или отсутствия ише-
мии сердца. Наиболее значимые аритмии — это
брадиаритмии и экстрасистолии. В нашей практи-
ке за последние 2 года мы наблюдали три случая
полного сердечного блока во время анестезии у де-
тей, не имевших ранее никаких симптомов. Даль-
нейшее кардиологическое обследование выявило
не определявшиеся прежде нарушения проводи-
мости.
Поскольку большинство анестезиологических
осложнений — результат гипоксемии, появление
надежного монитора сатурации кислорода было
воспринято как чрезвычайно важное достижение.
В одном из интересных исследований проводилась
оценка целесообразности применения этого мони-
тора во время общей анестезии.36 В половине на-
блюдений анестезиологи следили по монитору за
показателями сатурации, а в другой половине —
были лишены такой возможности. В тех случаях,
когда анестезиологи не могли контролировать са-
турацию, ее уменьшение ниже 90% отмечено
у 32% больных. При наблюдении за сатурацией
значительное ее снижение было лишь в 14% слу-
чаев.
Остается спорным вопрос о целесообразности
применения капнографа или спектрометра — бо-
лее дорогого монитора Сторонники его использо-
вания подчеркивают возможность с помощью кап-
нографа определять колебания СО2, подтверждая
таким образом правильное расположение эндотра-
хеальной трубки и соответственно уменьшая риск
интубации пищевода. Кроме того, каннограф отра-
жает артериальное РСО2, помогая тем самым осу-
ществлять адекватную вентиляцию и уменьшая не-
обходимость определения газов артериальной кро-
ви. Когда минутная вентиляция постоянна, СО2
конца выдоха может быть использовано как пока-
затель легочного кровотока, что, в свою очередь,
очень ценно в детской кардиохирургии, а также
в диагностике легочной воздушной эмболии при
некоторых нейрохирургических операциях. Дан-
ные капнографии в детском возрасте могут быть
не совсем точны в связи с небольшими дыхатель-
ными объемами у детей.
Автоматические неинвазивные мониторы кровя-
ного давления существенно повысили уровень ане-
стезиологической помощи, освободив анестезиоло-
гов от необходимости мануального измерения кро-
вяного давления в критических ситуациях, а также
обеспечив объективную информацию о функции
МЕТОДЫ ОБЕЗБОЛИВАНИЯ 57
жизненно важных систем и органов в обычных
случаях.
Вероятно, определенной склонностью нашего об-
щества к перестраховке можно отчасти объяснить
оснащение наркозных аппаратов слишком боль-
шим количеством сигналов тревоги, которые пре-
дупреждают о любых малейших изменениях конт-
ролируемых характеристик. Эти сигналы с одной
стороны, увеличивают безопасность и надежность
аппаратов, а с другой — их звуки, одинаковые по
характеру и времени, порой не позволяют быстро
понять, какой же из сигналов включился. Правда,
это не столь серьезный недостаток на фоне суще-
ственных преимуществ. Кроме того, эта проблема,
несомненно, будет разрешена изготовителями ап-
паратов в ближайшем будущем.
В заключение следует сказать, что положитель-
ная роль мониторов в повышении безопасности
анестезиологических пособий нуждается в под-
тверждении. К сожалению, достаточно трудно про-
вести научную оценку современного мониторного
«взрыва», поскольку этически невозможно исполь-
зование контрольной группы. Поэтому мы вынуж-
дены положиться на информацию, полученную
в результате таких серьезных исследований, как
те, что были проведены в Гарвардской Медицин-
ской Школе, а также на данные страховых ком-
паний.
БОЛЬ
Болевой синдром в послеоперационном периоде
возникает у детей столь же часто, как и у взрос-
лых. Около 75% детей предъявляют жалобы на
боли в день операции и 17% отмечают сильные
боли в первый послеоперационный день.’7
Почему боль недостаточно лечится у детей? То-
му есть много причин, но четыре из них четко из-
вестны и всегда присутствуют независимо от того,
в каком учреждении ребенок получает медицин-
скую помощь.
Во-первых те, кто вовлечен в оказание помощи
детям, порой считают, что если ребенок нс беспо-
коится, то он и нс чувствует боль. Формированию
такого отношения способствовали некоторые на-
блюдения и исследования, проведенные у новорож-
денных. Новорожденные, даже после больших опе-
раций, обычно беспокоятся в течение короткого
промежутка времени, а затем успокаиваются без
всяких лекарств.38 Микроскопическое изучение
анатомических болевых проводящих путей у ново-
рожденных показало, что таламокортикальные пу-
ти бывают не полностью миелинизированы и пред-
ставляют собой рудиментарные образования?9 У
новорожденных обнаружена также более высокая,
чем у старших детей, концентрация эндогенных
опиоидов в плазме и спинномозговой жидкости
(СМЖ).40 Эти данные привели многих клиници-
стов к заключению, что дети, особенно новорож-
денные, нс имеют нормальной реакции на боль
и не требуют серьезного послеоперационного обез-
боливания. В настоящее время со всей очевид-
ностью показано, что это не так — новорожденные
чувствуют боль. И эти болевые ощущения могут
приводить при отсутствии лечения к серьезным по-
следствиям. Научные наблюдения за характером
крика, выражением лица, движениями, показате-
лями деятельности сердечно-сосудистой системы
подтверждают наличие отрицательной реакции но-
ворожденных на болезненные процедуры, которая
аналогична той, что отмечается у взрослых.
Вторая причина — недостаточная осведомлен-
ность врачей относительно современных представ-
лений о своеобразии и сложности фармакокинети-
ки у детей. Новорожденные в этом плане суще-
ственно отличаются от более старших детей
и взрослых. Новорожденные более чувствительны
к подавляющему действию наркотиков на дыха-
тельную систему. У детей этой возрастной группы,
по-видимому, меньше Ми-1 рецепторов, ответствен-
ных за анелгезию, и большее количество Ми-2 ре-
цепторов, являющихся медиаторами в процессе
угнетения дыхания/1
Очевидно также, что распределение наркотиков
в организме новорожденных, особенно недоношен-
ных детей, более широкое, а период полураспада —
более длительный. Так, период полураспада фен-
танила у взрослых — 129 мин, в то время как у но-
ворожденных — более 230 мин. Как проявление
этих особенностей у новорожденных отмечается
повышенный уровень в СМЖ наркотических ве-
ществ в течение более длительного промежутка
времени. Некоторые исследователи считают, что
применение наркотиков у новорожденных должно
быть ограничено теми случаями, когда предполага-
ется наблюдение в условиях отделения интенсив-
ной терапии либо когда планируется проведение
И ВЛ в послеоперационном периоде.42 Различия
в фармакокинетике исчезают около 5—6 мес
и в дальнейшем характер действия наркотиков
у детей такой же, как у взрослых.
Третья проблема, связанная с лечением боли
в детском возрасте, это трудность оценки самой
боли. Многие дети могут реагировать на боль эмо-
циональным «отключением», что иногда неверно
воспринимается как проявление состояния комфор-
та. В ответ на вопрос о характере и степени боли
ребенок может дать ложную информацию из-за
боязни дальнейших болезненных процедур либо
из-за неспособности понять, что от него хотят
услышать. Для того, чтобы «перехитрить» ребенка
и разрешить эти проблемы, в практику введены
несколько схем, позволяющих оценить степень бо-
лезненных ощущений и отражающих описание ти-
пичного поведения ребенка при этом. Эти схемы
применяются с различной долей успеха, поскольку
порой трудны для выполнения, требуют времени
и рассчитаны на определенную степень понимания
пациента.
Четвертая общая проблема в лечении боли
в детском возрасте — индивидуальные представле-
ния медиков о боли у детей. Эти представления
исходят порой из убеждения в том, что боль — это
естественная реакция на оперативное вмешатель-
ство и что в связи с опасностью угнетения дыхания
и привыкания к наркотикам следует ограничивать
послеоперационное обезболивание.
58 МЕТОДЫ ОБЕЗБОЛИВАНИЯ
Если учитывать все эти трудности в лечении ре-
бенка, испытывающего боль, то что же все-таки
делать клиницисту? Главной опорой в терапии все
равно остаются наркотики. Важно лишь сделать
правильный выбор из большого арсенала наркоти-
ческих веществ и методов их введения.
Стандартом, по которому сверяют и оценивают
большинство других видов лечения, остается мор-
фин. Чтобы увеличить эффективность применения
некоторых фармакологических форм, их важно не
только знать, но и понимать механизм действия.
Хотя период полураспада морфина в плазме такой
же, как и у других наркотиков, продолжительность
его действия может быть значительно большей
в связи с низкой растворимостью в жире. Попав
в СМ Ж, он уходит из нее очень медленно. В ре-
зультате действие его и выведение могут быть
очень различными и не связанными с уровнем
в плазме. Длительную или даже короткую эффек-
тивную анелгезию осуществить морфином трудно.
Это один из тех препаратов, который больной, ис-
пытывающий дискомфорт, может вводить себе сам
с помощью специального устройства. Доза в таком
случае составляет от 60 до 200 мкг/кг. Если про-
изводится постоянная инфузия, то доза колеблется
от 10 до 30 мкг/кг/час.
Очень популярным обезболивающим стал фен-
танил. Он используется в широком диапазоне от
0,3 до 4 мкг/кг для снятия послеоперационной бо-
ли и очень легкой седатации. Фентанил может вво-
диться традиционно или путем самовведения боль-
ными. У детей клиренс этого наркотика выше, чем
у взрослых.43
Налбуфин (нубаин) — смешанный наркотиче-
ский агонист/антагонист, который, как показал
опыт, очень эффективен в педиатрии для после-
операционного обезболивания.44 Мы применили
этот препарат в послеоперационном периоде бо-
лее, чем в 10 000 случаях в дозе 0,1—0,5 мг/кг
и получили хороший результат в 95% случаев.
Весьма высокий уровень седатации при использо-
вании этого препарата сочетается с очень редким
угнетением дыхания. У подростков он. по-видимо-
му, не столь эффективен.
Как было упомянуто, существует много новых
методов медикаментозного снятия боли. Один из
наиболее популярных в детском возрасте — анел-
гезия, управляемая пациентом (АУП). Больные
в возрасте 6 лет и старше способны вводить ле-
карство сами с помощью специального инфузион-
ного устройства. Доказано, что этот способ эффек-
тивен и безопасен. Мы его использовали более,
чем у 300 пациентов, с прекрасной анелгезией
ЛИТЕРАТУРА
I. Roizen MF: Preoperative laboratory testing what is necessa-
ry? International Anesthesia Research Society Review Course
Lecluies, 1989, pp 29—35.
2. Leonard JV, Clayton BE, Colley JR Г: Use of biochemical profile
in Children’s Hospital: Results of two controlled trials. Br Med
J 21:662—665, 1975.
3. Shulman ST, ct al.: Prevention of bacterial endocarditis; a state-
в 99% наблюдений. Частота осложнений чрезвы-
чайно низка. Менее, чем у 5% больных, отмечался
зуд, и только в одном случае возникло угнетение
дыхания.
У взрослых очень эффективное послеоперацион-
ное обезболивание достигается путем введения
препаратов через эпидуральный катетер. По срав-
нению с АУП этот способ обеспечивает более на-
дежное снятие боли, но связан со значительным
числом осложнений. Эпидуральная анестезия мо-
жет быть использована и у детей.45
Многие препараты включая наркотики, могут
вводиться трансдермально с помощью специальной
техники. Хотя фентанил в настоящее время приме-
няется не так часто, но он является одним из пре-
паратов, использование которого данным способом
дает хорошие результаты.
Еще один метод послеоперационного обезболи-
вания — проводниковая анестезия, которая может
быть специфически индивидуальной, например
илиоингвинальная (подвздошнопаховая) или ане-
стезия полового члена (пениальная). В то же вре-
мя существуют общепринятые способы блокады
больших проводящих путей, в частности спиналь-
ная и эпидуральная анестезия. При использовании
илиоингвинальной или пениальной блокады боль
уменьшается в 90% случаев.46 По нашему опыту,
эти виды блокад наиболее эффективны у детей
в возрасте до 6 мес. Однако дополнительное меди-
каментозное обезболивание в этой возрастной
группе было необходимо почти у 40% больных.
У детей в возрасте до 6 мес отмечается стабиль-
ность деятельности сердечно-сосудистой системы,
даже во время высокой эпидуральной и спиналь-
ной анестезии, что делает эти методы вполне при-
емлемыми для интра- и послеоперационного обез-
боливания Дозы при каудальной блокаде для низ-
кой поясничной и крестцовой локализации —
0,5 мл/кг, тля низкого торакального уровня —
I мл/кг и для среднеторакального уровня —
1,25 мл/кг.47 У взрослых эпидурально вводимые
комбинации местных анестетиков, наркотиков,48
или адренергических агонистов, подобных клофе-
лину,45 обеспечивают очень эффективное после-
операционное обезболивание.
Таким образом, за исключением новорожден-
ных, потребность детей в обезболивании и их ре-
акция на наркотики такая же, как у взрослых,
а потому в педиатрии следует придавать этой
проблеме нс меньшее значение. У новорожденных
необходимо учитывать особенности фармакокине-
тики, обеспечивая безопасное и эффективное обез-
боливание и в этой группе больных.
meat for health professionals by the committee on Rheumatic
Fever and Infective Endocarditis of the Council on Cardiovascu-
Jar Disease in the Young. Circulation 70:1123A— 1127A. 19X4.
4. Olson GL, Hallcn B, Hambraeus-Jonzon K: Aspiration during
anesthesia: A computer aided study of 185,35» anaesthetics.
Acta Anacsthesiol Sea nd 30:84—92, 1986.
5. Tiret L, Ilivoche Y, Halton F, Desmonts JM, Vourc’h G: Com-
МЕТОДЫ ОБЕЗБОЛИВАНИЯ 59
plications related to anesthesia in infants and children. A pro-
spective survey of 40,240 anaesthetics. Br J Anaesth 61:263—
269. 1988.
6. Welborn LG. McCail WA, Hanna Hah RS, et al.; Perioperative
blood glucose concentrations in pediatric outpatients. Anesthesi-
ology 65:543—547, 1986.
7. Splinter WM, Stewart JA, Muir JC: The effect of prcopcntiivc
apple juice on gastric contents, thirst, and hunger in children.
Can J Anaesth 36:55—58, 1989.
8. Schreiner MS, Triebwasscr A. Keon TP: Ingestion of liquids
compared with preoperalivc fasting in pediatric outpatients.
Anesthesiology 72:593- 597, 1990.
9. Broadman 1 M: Regional anesthesia for the pediatric outpatient.
Ancsthes Clin North Am 5:53— 72. 1987
10 Cohen MM. et al.: A survey of 112.000 anesthetics .it one te-
aching hospital (1975—1983). Can Anaesth Soc J 33:22—31.
1986.
11. Cohen MM. et al.: Pediatric morbidity and mortality in the peri-
operative period. Anesth Analg 70:160—167. 1990.
12. Shamlling B, Steward DJ: Regional analgesia for postoperative
pain in pediatric outpatient surgery. J Pediatr Surg 15:477.
1980.
13. Abramowitz MD, et al.: Antiemeiic effectiveness of intraoperati-
vely administered droperidol in pediatric strabismus outpatient
surgery. Anesthesiology 53:5323, 1980.
14. Koka BY, et al.: Postintubation croup in children. Anesth Anal
56:501. 1977.
15. Gregory C (Editor): Pediatric Anesthesia, 2nd edition. Chur-
chill Livingstone, New York, p 635. 1989.
16. Goddard JE, et al.: Betamethasone for prophylaxis of pustittlu-
bation inflammation. Anesth Analg 46:348, 1967.
17. Steward DJ: Preterm infants are more prone to complications
following minor surgery than are term infants. Anesthesiology
56:304—306, 1982.
18. Rigatto H, Brady JP: Periodic breathing and apnea in preterm
infants. Evidence for hypoventilation possibly due to central
respiratory depression. Pediatrics 50:202 218, 1972.
19. Liu LM. Cote CS. Goudsouzian NG. et al.: Life-threatening
apnea in infants recovery from anesthesia. Anesthesiology
59:506—510. 1983
20. Welborn LC, Ramirez N, Oh TH. ct al.: Postancsthctic apnea
and periodic breathing in infants. Anesthesiology 65:658—661.
1986.
21. Kurth CD, Spitzer AR. Broennlc AM, Downes JJ: Postoperative
apnea in preterm infants. Anesthesiology 66:483—488, 1987.
22. Mcstad PH, Glcnski J A. Binda RE Jr: When is outpatient surge-
ry safe in preterm infants? Anesthesiology 69:A744. 1988.
23. Welborn L, et al.: Postoperative apnea in former preterm in-
fants: Prospective comparison of spinal and general anesthesia.
Anesthesiology 72:838—842. 1990.
24. Welborn LG. DeSoto H, Hannallah RS, el al.: The use of caffei-
ne in the control of postanesthetic apnea in former premature
infants. Anesthesiology 68:796—798, 1988.
25. Welborn LG, Hannallah RS. Fiwle R, et al.: High-dose caffeine
suppresses postoperative apnea in former premature infants.
Anesthesiology 71:347—349, 1989.
26. Dripps RD, cl al.: The role of anesthesia in surgical mortality
JAMA 178:261 266, 1961.
27. Macintosh, RR: Deaths under anesthetics. Br J Anaesth
21:107—136. 1948.
27a. Wylie WD: «There, but for the grace of God...* Ann Roy Coll
Surg Engl 56:171 180. 1975.
28. Marx C, et al.: Computer analysis of postancsthctic deaths-
Anesthesiology 39:54 58, 1973.
29. Cooper JB, ct al.: Preventable anesthesia mishaps. Anesthesiolo-
gy 49:399—406. 1978.
30. Green RA. Taylor TH: An analysis of anesthesia medical liabili-
ty claims in the United Kingdom 1977 1982. Inr Anesthesiol
Clin 22:73—90. 1984
31. Bailey PL, et al.: Respiratory effects of midazolam and fentanyl.
Potent inicractors producing hypoxemia and apnea. Anesthesio-
logy 69:A8I3, 1988.
32. Lichhorn JH. el al.: Standards for patient monitoring during
anesthesia at Harvard Medical School. JAMA 256:1017—1020,
1986.
33- Eichhorn JH: Prevention of intraoperative anesthesia accidents
and related severe injury through safely monitoring. Anesthesio-
logy 70:572—577, 1989.
34. Keats A: Anesthesia mortality in perspective. Anesth Analg
71:113—199. 1990»
35. Keats A: Whai do we know about anesthetic mortality? Anesthe-
siology 50:387-392, 1979.
36. Cote CJ, et al.: A single-blind study of pulse oximetry in child-
ren. Anesthesiology 68:184—188, 1988.
37. Mather I, Mackie J: I he incidence of postoperative pain in
children. Pain 15:271—282. 1983.
38. Hatch DJ: Analgesia in the neonate. Br Med J 294:920, 1987.
39. Filney F. Rosseti J: The value of brain lipoids in an index of
brain development. Bull Neurological Institute NY 1:28—71,
I93L
40. Orlokowski JP: Cerebrospinal fluid endorphines and the infant
apnea syndrome. Pediatrics 78:233—237, 1986.
41. Pasternak GW. ct al.: Developmental differences between high
apd low affinity opiate binding sites: Their relationship to anal-
gesia and respiratory depression. Life Sci 27:1185—1190. 1980.
42. Lloyd-Thomas AR; Pain management in paediatric patients. Br
J Anaesth 64:85—104, 1990
43. Singleton MA, et al.: Plasma concentrations of fentanyl in in-
fants. children and adults. Can J Anaesth 34:152—155, 1987.
44. Bikhazi OB: Comparison of morphine and nalbuphine in post-
operative pediatric patients. Anesihesiol Rev 5:34—36, 1978.
45. Dcsparmet J, et al.: Continuous epidural infusion of bupivacaine
for postoperative pain relief in children. Anesthesiology
67:108-110, 1987.
46. Casey W. et al.: Comparison between bupivacaine instillation
versus ilioinguinal/iliohypogastric nerve block for postoperative
analgesia following inguinal herniorrhaphy in children. Anesthe-
siology 72:637—639, 1990.
47. Da lens B: Regional anesthesia in children. Anesth Analg
68:654 672, 1989.
48. Lopez KA, et al.: Epidural morphine provides greater pain relief
than patient-controlled intravenous morphine following cholecys-
tectomy. Anesth Analg 69:826 828, 1989.
49. Bonner F. ct al.: Clonidine-induced analgesia in postoperative
patients: Epidural versus intramuscular administration. Anesthe
siology 72:423 427, 1990.
Глава 4
ИСКУССТВЕННАЯ
ВЕНТИЛЯЦИЯ ЛЕГКИХ
Повышение выживаемости четей с хирургической
патологией в значительной мере связано с дости-
жениями в лечении дыхательной недостаточности,
касающимися двух основных аспектов. Во-первых,
в последние годы существенно расширились зна-
ния физиологии и патофизиологии легких, в част-
ности специфических особенностей у детей, в том
числе маленьких. Во-вторых, произошел резкий
технологический скачок как в плане самой венти-
ляции, так и методов контроля. Беспрерывно про-
должающаяся интеграция и оптимизация этих двух
направлений способствует значительному улучше-
нию результатов лечения.
В данной главе рассматривается физиология
легких, описываются современные виды контроли-
рующих и вентиляционных систем, а также пред-
ставлены основные направления в лечении детей
с учетом самых разнообразных патофизиологиче-
ских и терапевтических аспектов.
ФИЗИОЛОГИЯ ЛЕГКИХ
Главные задачи искусственной вентиляции —
адекватное выведение углекислоты, обеспечиваю-
щее баланс кислотно-основного состояния, и под-
держание достаточной артериальной оксигенации.
Первая цель достигается путем улучшения альвео-
лярной вентиляции, вторая — деликатной регуля-
цией баланса альвеолярной вентиляции и легочной
перфузии. Чтобы контролировать этот процесс, не-
обходимо прежде всего понимать основы анатомии
и функции легких в норме и патологии.
Анатомии развивающегося организма. Значи-
тельные различия существуют между строением
и функцией легких и грудной клетки у недоно-
шенных новорожденных и взрослых людей. Про-
водящие дыхательные пути, выстланные мерца-
тельным эпителием, разветвляются между 4-й и
16-й неделями гестации. Газообмен при рождении
происходит в гроздьевидпых мешочках респира-
торных бронхиол. Дыхательные анатомические
структуры (бронхиолы, альвеолярные протоки
и альвеолярное дерево) развиваются и увеличива-
ются в количестве в течение первых 18 месяцев
жизни. В результате быстрой постнатальной про-
лиферации 20 млн альвеол, существующих при
рождении, «размножаются» приблизительно до
300 млн к 8 годам жизни, когда этот процесс оста-
навливается. В то же время коллатеральная венти-
ляция внутри респираторных структур (интрааль-
веолярные поры Коха и бронхиоло-альвеолярные
каналы Ламберта), поддерживающая альвеоляр-
ную вентиляцию при обструкции бронхиол и ста-
билизирующая таким образом легочные сегменты,
предотвращая ателектазы, не развивается до 1 го-
да жизни или позже. Трахея новорожденного ко-
роткая и широкая, непропорционально большая по
сравнению с размерами легкого и самого ребенка.
По мере ее роста легочный объем увеличивается
почти в 30 раз. Поэтому в отличие от взрослых,
у которых проксимальные дыхательные пути обра-
зуют первичный компонент легочной резистенции,
у детей этот компонент формируется в перифери-
ческих дыхательных путях/ Указанный фактор
объясняет высокую подверженность детей респира-
торному дистрессу при заболеваниях мелких дыха-
тельных путей, таких как бронхиолиты или отек
легких.
Грудная клетка новорожденного по своей меха-
нике значительно отличается от таковой у взрос-
лых, будучи в поперечном сечении более округлой,
чем элипсоидной, что уменьшает ее возможности
в плане увеличения интраторакального объема за
счет сокращения межреберных мышц. Особенности
прикрепления диафрагмы у детей объясняют дви-
жение при вдохе нижних ребер больше внутрь, чем
кнаружи. В связи с этими двумя факторами увели-
чение интраторакального объема в детском возра-
сте зависит преимущественно от экскурсий диа
фрагмы.
Абдоминальные вмешательства или вздутие жи-
вота могут соответственно крайне неблагоприятно
влиять па самостоятельное дыхание у новорожден-
ных. Ребра, будучи более «мягкими», имеют мень-
шую способность при снижении легочной податли-
вости сопротивляться внутреннему коллапсу во
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ 61
время вдоха и удерживать легочный объем в конце
выдоха, что ведет к прогрессированию ателекта-
зов. Дыхательная мускулатура у детей имеет отно-
сительно меньшую массу и намного быстрее «уста-
ет». Количество медленно сокращающихся воло-
кон 1-го типа в диафрагме у недоношенных ново-
рожденных составляет лишь 10%, в то время как
у доношенных — 25%, а у взрослых — 50%.4
Легочная механика. Поступление газа из атмо-
сферы в альвеолы происходит за счет градиента
давления. Это может быть достигнуто либо расши-
рением грудной полости в результате работы ды-
хательной мускулатуры, что приводит к созданию
отрицательного по отношению к окружающей сре-
де интраплеврального давления (спонтанная вен-
тиляция), либо в результате обеспечения положи-
тельного (относительно альвеолярного) давления
В проксимальных отделах дыхательных путей
(вспомогательная вентиляция). Возвращение газа
в атмосферу — пассивный акт в любой ситуации.
Некоторые особенности дыхательной системы
обеспечивают противостояние поступлению газа
в альвеолы. Так, эластичность легких и грудной
клетки лежит в основе свойства податливости,
определяемой как способность к изменению объема
на единицу изменения давления. На рисунке 4-1
представлена кривая статической податливости
у новорожденного с нанесенными на нее петлями
сверхснльного динамического объема газотока. По-
датливость является мерой крутизны этой кривой.
Нормальная вентиляция происходит в центральной
крутой части кривой, где изменения давления эф-
фективно приводят к изменению объема. Различ-
ные патологические состояния могут сдвинуть эту
кривую в ту или другую сторону, отражая ситуа-
цию, когда для достижения такого же дыхательно-
го объема требуется большее давление.
Понимание сути свойства податливости и пред-
ставление о том, на какую часть кривой прихо-
дится состояние больного в данный момент, важно
для правильного регулирования вентиляции. При
низком объеме в конце кривой положительное дав-
ление конца выдоха (ПДКВ) может помочь рас-
править ателектазнрованные сегменты, увеличив
таким образом легочный объем и улучшив подат-
ливость. В противоположной ситуации удлинение
экспираторной фазы может уменьшить проблемы,
связанные с пере растяжением.
Силы трения между воздушными молекулами
н стенками дыхательных путей препятствуют току
газа в легкие и описываются как свойство сопро-
тивления. Сопротивление зависит от объема газо-
тока, его физических свойств (плотность и вяз-
кость). длины пути, по которому проходит газ и,
что особенно важно, — от внутреннего диаметра
этого пути. Как было сказано выше, у детей, осо-
бенно грудных, дыхательные пути имеют малые
размеры, что способствует увеличению сопротив-
ления. Процессы, ведущие к изменению просвета
дыхательных путей, могут затруднять вентиляцию.
У интубированного больного эндотрахеальная
трубка иногда значительно повышает сопротивле-
ние, особенно когда она частично закупорена сек-
ретом.
Константа времени легких определяется подат-
ливостью и сопротивлением. Константа времени
выдоха показывает, как быстро легкие могут про-
изводить выдох или сколько времени требуется
Для уравновешивания давления между альвеолами
н проксимальными дыхательными путями. За одну
константу времени эвакуируется 63% общего ды-
хательного объема, к концу трех констант — 95%.
Для нормального ребенка с податливостью, рав-
ной 0,005 л/см Н2О и сопротивлением 30 см Н2О/
/л/сек константа времени будет равна 0,15 сек.
Таким образом, за трн константы времени или
0,45 сек эвакуируется 95% общего дыхательного
объема. Использование вентиляционных систем,
рассчитанных на выдох меньше, чем за 0,45 сек,
может вести к перерастяжению легких и сдвигу
к высокому объему и низкой податливости (конец
кривой)—ситуации, относящейся к «неумышлен-
Рис. 4-1. Кри пая статической податливости
при различных состояниях с петлями динами-
ческого объема газотока. Обращают на себя
внимание дне области низкой податливости
(А и С), соответствующие ателектазам (или
коллапсу) и перераздуванию. (TLC — общая
емкость легких, FRC — функциональная оста-
точная емкость).
Давление
62 ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ
ному ПДКВ».5 Этот фактор уменьшает эффектив-
ность вентиляции и увеличивает риск баротравмы.
При состояниях низкого объема и сниженной по-
датливости, часто наблюдающихся у детей после
оперативных вмешательств, короткая константа
времени выдоха может позволить с целью улучше-
ния газообмена пролонгировать фазу вдоха так,
что она становится продолжительнее времени вы-
доха (обратное соотношение вдох : выдох — ин-
вертный режим вентиляции).
Легочный газообмен. Обмен углекислоты, обла-
дающей способностью к быстрой диффузии, почти
целиком зависит от объема вдыхаемого и выдыхае-
мого в единицу времени газа или от минутной
вентиляции. Минутная вентиляция определяется
скоростью дыхания и дыхательным объемом. Ма-
нипулирование этими параметрами непосредствен-
но отражается на элиминации СО2.
Обмен кислорода, в отличие от углекислоты, бо-
лее сложен. Хотя он в какой-то степени зависит
и от минутной вентиляции, однако более важную
роль играет соотношение вентиляции и перфузии.
Нарушение этого соотношения (V/Q), особенно
недостаточная вентиляция перфузируемых (шун-
тируемых) участков — одна из самых частых при-
чин гипоксемии при многих заболеваниях. Когда
шунтируемая фракция достигает приблизительно
30%, увеличение концентрации О2 во вдыхаемом
воздухе в процентах (FIO2) уже не приводит к
улучшению оксигенации.6 Ситуации, которые умень-
шают функциональную остаточную емкость (FRC)
или увеличивают закрытую емкость (легочный
объем, в котором проводящие воздушные пути
в зависимых частях легкого начинают спадаться),
обычно приводят к увеличению шунтируемой
фракции и к гипоксемии. Примеры таких ситуаций
перечислены в таблице 4-1. Только в том случае,
когда поддерживается на должном уровне соотно-
шение V/Q, может быть улучшенг! оксигенация
либо изменением параметров вентиляции, либо
с помощью мер, направленных на лечение патоло-
гии, лежащей в основе дыхательных расстройств.
Легочный кровоток. При рождении происходят
быстрые и глубокие изменения в характере легоч-
ного кровообращения. С первыми вдохами легкие
растягиваются, сопротивление легочных сосудов
падает, а легочный кровоток увеличивается. Затем
закрываются внелегочные шунты плода (артери-
ТАБЛИЦА 4-1. Ситуации, увеличивающие шунтируемую
фракцию и вызывающие гипоксемию
Увеличенная закрытая емкость Уменьшенная FRC
Нормальный грудной ре- бенок Бронхиолит Астма БЛД Кистофиброэ Положение лицом вверх Вздутие живота Вмешательство на грудной клетке или брюшной полости Ателектаз Травми грудной клетки НДС- Отек легких Утопление Пневмония (диффузная)
альный проток, овальное отверстие). Сопротивле-
ние легочных сосудов у новорожденного сущест-
венно меняется в зависимоеги от напряжения О2.
Гипоксемия может вызвать серьезный спазм легоч-
ных сосудов — ситуация, потенцируемая ацидозом.
При возникновении сосудистого спазма в легких
может возобновиться шунтирование справа-налево
через артериальный проток или овальное окно,
что приводит к уменьшению легочного кровотока,
усугубляя гипоксемию и ацидоз. Этот феномен
определяется как персистирующая легочная гипер-
тензия новорожденного (ПЛГН) или персистирую-
щее фетальное кровообращение (ПФК). ПЛГН —
главный компонент легочных расстройств при
врожденной диафрагмальной грыже, гак же, как
и при ряде других заболеваний новорожденных, не
требующих хирургического вмешательства. Про-
филактика ПЛГН у больных группы риска или
лечение уже возникших расстройств состоит из
(1) усиления оксигенации, (2) создания алкалоза
с помощью дыхательных (гипервентиляиия) или
метаболических (инфузия бикарбоната) средств
и (3) инфузий назоактивных препаратов. В тяже-
лых случаях, при отсутствии реакции на перечис-
ленные меры, может быть с успехом применена
экстракорпоральная мембранная оксигенация
(ЭКМО).
Физиология кислотно-основного обмена. Как
уже говорилось ранее, одна из главных функций
вентиляции — выведение СО2. Поскольку альвео-
лярная СО2 находится в равновесии с плазменной
концентрацией двууглекислых и водородных
ионов, как представлено в равенстве Henderson-
Hasselbalch, вентиляция играет главную роль
в кислотно-основном гомеостазе. Легкие выделяют
из организма в 100 раз больше кислот, чем почки.
В течение заболевания или его лечения Рго
и концентрация бикарбоната могут подниматься
или снижаться. Эти нарушения, изолированные
или в комбинации, ведут к соответствующим изме-
нениям кислотно-основного состояния. Анализ га-
зов артериальной крови позволяет определить по-
казатели PLO, концентрацию бикарбоната и pH,
что в свою очередь помогает охарактеризовать
кислотно-основное состояние больного.
Индивидуальные изменения кислотно-основного
статуса могут возникнуть в трех вариантах;7
1. В результате какого-либо изолированного
физиологического процесса — например, обычный
респираторный или метаболический ацидоз или
алкалоз. В частности, при упорной рвоте может
развиться метаболический алкалоз.
2. Изолированный физиологический процесс
иногда приводит к отклонениям, которые устраня-
ются благодаря физиологической компенсации.
Так, гипервентиляция (респираторный алкалоз)
может быть компенсирована метаболическим аци-
дозом.
3. Несколько физиологических процессов могут
привести к отклонениям независимо друг от друга,
с соответствующей компенсацией или без нее.
При оценке кислотно-основного состояния по га
зам крови важно помнить, что компенсаторный ме-
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ 63
ханизм, направленный на нормализацию pH, ни-
когда не может полностью корригировать первич-
ные нарушения, а поэтому, когда, например, изо-
лированный процесс сопровождается компенса-
цией, pH непременно показывает, какая патология
первична, а какая — вторична.
По газам артериальной крови можно определить
респираторные и метаболические компоненты кис-
лотно-основного дисбаланса. Большинство газо-
анализаторов автоматически вычисляют дефицит
оснований (т. е. метаболический компонент), упро-
щая тем самым анализ- Отклонения чисто метабо-
лические или чисто респираторные распознать не-
трудно. При метаболическом ацидозе или алкало-
зе Рго равняется 40 мм рт. ст. Изменения pH
связаны исключительно с метаболическими причи-
нами. При чисто респираторном алкалозе или аци-
дозе дефицит оснований нулевой. Оценивая pH.
Рсо2 и дефицит оснований, можно оценить относи-
тельную долю респираторных и метаболических
компонентов в кислотно-основном дисбалансе, а
соответственно предположить, какой процесс пер-
вичен. Сопоставление этих данных с клинически-
ми проявлениями позволяет проводить адекватное
лечение и планировать дальнейшее обследование.
Обмен кислорода: поступление и потребление.
Главная цель лечения любого больного, находяще-
гося в критическом состоянии — поддержать адек-
ватную оксигенацию тканей. Достижение этой це-
ли возможно лишь в том случае, если поступление
О2 достаточно для удовлетворения потребностей
в нем тканей. Четкое представление о том, что
такое потребление О2 и его поступление и какие
факторы определяют эти понятия — главное усло-
вие понимания сложностей сердечно-легочной реа-
нимации.
Потребление кислорода отражает скорость мета-
болизма у данного пациента. У больных людей эта
скорость может быть увеличена при мышечной ак-
тивности, сепсисе, повышении температуры тела,
уменьшении температуры окружающей среды
(особенно у новорожденных, которые с падением
температуры окружающей среды от 33 до 31 °C
могут потреблять в 2 раза больше О2) и при дру-
гих состояниях.
Поступление кислорода обеспечивается увеличе-
нием содержания его в крови за счет скорости до-
ставки или сердечного выброса. Содержание кис-
лорода в артериальной крови (Сао) выражается
формулой:
CaOj (см3/100 мл) =
= (%О2 sat X ПЬ X 1,34) + (0.003 X РаОг>.
где % О2 sat — процент насыщения гемоглобина
кислородом,- НЬ — концентрация гемоглобина; 1,34
представляет собой кислородонесущую часть гемо-
глобина в см3О2 на грамм гемоглобина; 0,003 —
коэффициент растворимости кислорода в крови
и Рао — напряжение О2 в артериальной крови.
Как явствует из этой формулы, Рао мало влияет
на содержание О2 в кровн в связи с его ограничен-
ной растворимостью. Таким образом, главные ком-
поненты, определяющие содержание О2 — концен-
трация гемоглобина и процент сатурации.
В норме снабжение кислородом в 4—5 раз пре-
вышает потребность в нем тканей. Исследования
на животных показали, что когда снабжение пада-
ет в два раза ниже скорости потребления, то по-
требление О2 само по себе становится ограничен-
ным, и начинает действовать анаэробный метабо-
лизм с развитием лактат-ацидоза и тяжелыми
нарушениями в организме.8
Поскольку в норме потребляется только 20—
25% поступающего кислорода, то остальной О2
остается в венозной крови. Таким образом, измере-
ние содержания О2 в смешанной венозной крови
наиболее достоверно отражает баланс поступления
и потребления О2. Нормальная артериальная сату-
рация близка к 100%, следовательно, нормальная
сатурация смешанной венозной кровн должна быть
75—80%. Падение смешанной венозной сатурации
до 50% говорит о критически низком уровне по-
ступления кислорода. Сатурация О2 смешанной ве-
нозной крови находится в прямой зависимости от
содержания О2 и может быть измерена путем ана-
лиза крови из легочной артерии через фиброоп-
тический катетер. У детей, в том числе новорож-
денных, уровень сатурации в правом предсердии
достоверно отражает показатели смешанной веноз-
ной крови. В настоящее время появляются фибро-
оптическне катетеры соответствующих размеров
для использования в детском возрасте. Такой мо-
ниторинг может скоро стать довольно обыденным
в лечении критически больных детей.9
ОЦЕНКА БОЛЬНОГО
Цель искусственной вентиляции — обеспечить
альвеолярную вентиляцию с адекватным удалени-
ем СО2 и адекватную оксигенацию, а также умень-
шить «работу» дыхания. У каждого конкретного
больного может возникнуть необходимость решить
любую из этих задач или все вместе.
Лежащие в основе дыхательной недостаточности
патофизиологические механизмы обычно мульти-
факториальны. Повреждение дыхательного «насо-
са», обеспечивающего физическое движение газов,
может быть связано с поражением ЦИС (апноэ,
лекарственные препараты, кровоизлияние, травма,
энцефалопатия), периферической нервной системы
(повреждение или заболевание спинного мозга, па-
ралич диафрагмального нерва) или грудной клет-
ки и мускулатуры (миопатия, деформации, трав-
мы, наружные силы, препятствующие дыханию).
Кроме того, может быть патология самих дыха-
тельных путей, как проксимальных (хоанальная
атрезия, ларингомаляция, синдром Пьера-Робена,
подсвязочный стеноз, трахеомаляция, шейнолице-
вая травма, инородные тела), так и дисталь-
ных (реактивные заболевания дыхательных путей,
закупорка слизью) вплоть до альвеол (пневмония,
контузия, сурфактантная недостаточность, гипо-
плазия легких, отек легких). Одна из возможных
причин — нарушение легочной перфузии (врож-
64 ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ
денные синие пороки сердца, персистирующее фе-
тальное кровообращение, легочная эмболия, сер-
дечная недостаточность). Хирургическое вмеша-
тельство или травма также могут быть этиологиче-
ским фактором в любой из вышеперечисленных
групп.
Поскольку дыхательная недостаточность иногда
развивается в результате нескольких причин, дей-
ствующих одновременно, показания для ИВЛ так-
же могут быть множественными. Наиболее частое
показание для ИВЛ — неадекватная самостоятель-
ная вентиляция или оксигенация. ИВЛ может по-
надобиться при нарастающем внутричерепном дав-
лении в связи с необходимостью гипервентиляции,
или при низком сердечном выбросе для принятия
на себя «работы» дыхания и таким образом умень-
шения потребности миокарда. Необходимость кон-
троля за состоянием дыхательных путей сама по
себе может также быть первичным показанием для
ИВЛ. как, например, при обструкции проксималь-
ных отделов дыхательных путей или с целью сана-
ции трахеобронхиального дерева.
Необходимость перехода на ИВЛ обычно опреде-
ляется по клиническим показателям, но более ча-
сто — на основании анализа газов артериальной
крови. Нарастающая частота дыхания, особенно
в сочетании с увеличением мышечных усилий, ци-
аноз, не снимаемый дополнительной подачей О2,
учащение пульса, признаки низкого сердечного
выброса — все это является показанием для пере-
хода на ИВЛ. Очевидные признаки угнетения
ЦНС нередко затушевываются симптомами гипо-
ксемии и гиперкапнии. Примеры тому — нарастаю-
щие апноэ и брадикардия у недоношенных детей,
возбуждение при множественной травме или в по-
слеоперационном периоде. При явных клиниче-
ских признаках нарушения функции дыхания дол-
жна быть немедленно проведена оценка состояния
больного с использованием наиболее объективных
методов, среди которых на первом месте — анализ
газов артериальной крови.
Оксигенация считается неадекватной при
меньше 50 60 мм рт. ст. на фоне F1O2 больше
60%. Указанные цифры соответствуют величине
шунтируемой фракции около 30%, когда дальней-
шее увеличение концентрации О2 во вдыхаемом
воздухе уже не помогает в борьбе с гипоксемией.
Альвеолярно-артериальная разница по кислороду
(А-аО2) больше, чем 300, при FIO2 около 100%
говорит об аналогичной ситуации. При неадекват-
ной вентиляции Р{(, обычно больше, чем 55 —
60 мм рт. ст. или plf меньше 7,25. У недоношен-
ных детей с массой тела до 1500 г нельзя допу-
скать повышения РГ1) больше 50 мм рт. ст. в связи
с опасностью при этом расширения мозговых сосу-
дов и соответственно риском внутрижелудочкового
кровоизлияния.
МОНИТОРИНГ И СПОСОБЫ ВЕНТИЛЯЦИИ
Чтобы оптимизировать ИВЛ и свести к минимуму
ее осложнения, врачу важно иметь информацию,
отражающую адекватность вентиляции и оксигена-
ции. Хотя клиническая оценка всегда остается од-
ним из основных компонентов, однако необходимы
более точные и объективные показатели функции.
Этим целям служат как инвазивные, так и неинва-
зивиые методы, каждый из которых имеет свои,
присущие ему, достоинства и недостатки, ограни-
чения к применению и возможные осложнения,
возникающие порой непосредственно в процессе
получения информации.
Анализ газов артериальной крови, pH, Pto, Ро
и концентрация бикарбонатов остаются фундамен-
том, на котором «строится» ИВЛ. Заборы крови
могут осуществляться путем периодической пунк-
ции периферических артерий или с помощью по-
стоянных катетеров, позволяющих также осущест-
влять постоянный контроль артериального давле-
ния. Чрескожное введение катетеров в лучевую,
локтевую, заднюю большеберцовую и тыльную
артерии стопы возможно, даже у глубоко недоно-
шенных детей. Постановке катетера должна пред-
шествовать клиническая оценка состояния коллате-
рального кровообращения конечности. В некото-
рых случаях необходим разрез сосуда, чаще
всего лучевой артерии. У новорожденных пер-
вых двух недель жизни иногда канюлируют пу-
почную артерию. Катетер может быть поставлен
высоко (кончик между IX и X грудными позвонка-
ми, над чревной артерией) или низко (кончик
между III и IV поясничными позвонками, ниже по-
чечных артерий). При высоком положении есть
риск эмболических осложнений, вовлекающих со-
суды внутренних органов. Для низкого расположе-
ния характерна более высокая частота осложне-
ний, однако в основном малых.
Наиболее важные показатели, получаемые при
анализе газов крови и отражающие альвеолярную
вентиляцию и кислотно-основной статус, это pH,
Рсо и бикарбонат. Ро не имеет существенного
значения для определения О2 в артериальной
крови.
При заборах артериализированной капиллярной
крови (CBGs) путем пункции пятки теплой конеч-
ности может быть проведен такой же анализ, как
и при взятии артериальной крови. При хорошей
перфузии имеется высокая корреляция между pH
и Рсо капиллярной и артериальной крови. При
Ро, превышающем 60 мм рт. с г., исследование ка-
пиллярной крови дает не очень точные результа-
ты, но ниже этого уровня корреляция достаточная,
при этом капиллярные показатели обычно на
10 мм рт. ст. ниже артериальных.
Сатурация оксигемоглобина смешанной веноз-
ной крови — лучший индикатор баланса поступле-
ния и потребления О2,’ отражающий не только ле
точный обмен О2, но и изменения сердечного
выброса. В настоящее время существуют фиброоп-
тические катетеры, с помощью которых оксиметр
вводится в легочную артерию у взрослых и стар-
ших детей и в правое предсердие — у маленьких
пациентов, позволяя постоянно контролировать
эту быстро меняющуюся величину.
Неинвазивные способы мониторинга имеют
двойное преимущество: меньший риск осложнений
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ 65
и возможность постоянного получения чрезвычай-
но важной информации.
Транскутанные датчики О2 и СО2 измеряют РОп
и Рсо подлежащей кожи,12 хорошо коррелируя
с артериальным Ро и Рсо в обычных клинических
ситуациях. В обоих случаях требуется согревание
подлежащей кожи до 43—45 °C с целью создания
вазодилатации, которая приближает напряжение
О2 и СО2 кожи к артериальному. При такой темпе-
ратуре могут возникнуть ожоги 1 и II степени,
особенно у новорожденных, у которых как раз наи-
более часто эти мониторы и используются. В на-
стоящее время появляются приборы, позволяющие
измерять оба параметра с помощью одного дат-
чика.
Постоянная пульсоксиметрия для измерения са-
турации оксигемоглобина артериальной крови ста-
ла обыденным методом почти во всех операцион-
ных и отделениях интенсивной терапии. Она дает
очень точные показатели в большинстве ситуаций
и, в отличие от транскутанного измерения Ро, не
требует согревания кожи. Результаты пульсокси-
мстрии недостаточно достоверны у пациентов с по-
вышенной двигательной активностью и у больных
со сниженным кровотоком при сужении перифери-
ческих сосудов.
Показатели Рсо выдыхаемого газа в конце вы-
доха (СО2 конца выдоха) приближаются к альвео-
лярному РСХ)2, которое, в свою очередь, находится
в равновесии с артериальным Рсо. Концентрация
С02 в выдыхаемых газах может постоянно измерять-
ся с помощью инфраспсктроскопии. Однако приме-
нение этого метода ограничено у маленьких детей
из-за низкого дыхательного объема и высокой ча-
стоты дыхания у них, что снижает точность полу-
чаемых показателей. Кроме того, некоторые систе-
мы измерения СО2 конца выдоха увеличивают мер-
твое пространство, что по сути ведет к задержке
у новорожденных СО2.13
Обычные вентиляторы. Механические вентиля-
торы — «рабочие лошади» И ВЛ. Существует много
различных моделей, у каждой из которых есть
свои достоинства и недостатки. Но принципиально
вентиляторы могут быть разделены на 2 основные
группы: вентиляторы объема и вентиляторы давле-
ния. В основе данного подразделения лежат пара-
метры, непосредственно регулируемые при венти-
ляции. С технической точки зрения вентиляторы
различаются по способу циклирования или тем па-
раметрам, которые определяют конец фазы вдоха.
Вентиляторы, циклированные по объему, заканчи-
вают фазу вдоха, когда достигнут установленный
дыхательный объем. Вентиляторы, циклированные
по давлению, заканчивают вдох, когда достигнут
пик давления на вдохе (PIP). Вентиляторы, цикли-
рованные по времени, переключаются на выдох по
истечении установленного времени вдоха. Послед-
няя группа обычно имеет ограничения и по давле-
нию, т. е. в этих аппаратах устанавливается и пик
допустимого давления, однако нет триггерного
окончания газотока. При использовании циклиро-
ванных по времени и ограниченных по давлению
вентиляторов, если пик давления достигнут до то-
5 Заказ № 1622
ТАБЛИЦА 4-2. Классификация вентиляторов по способу
циклирования
Циклированные по объему Циклированные по давлению Циклированные по времени
Siemens 900С Babybird Bear Cub
Bennett Ma 1 Emerson 3PV Bournes LS 104—150 Biomed MVP 10 Seachrist IV 100 Healthdyne 100 Bournes BP 200
го, как кончилось время вдоха, возникает плато на
кривой давления. Поскольку в основе работы вен-
тиляторов, регулируемых как по давлению, так
и по времени, лежит первичный параметр — PIP,
оба этих аппарата обычно относятся к «вентилято-
рам давления». В таблице 4-2 представлены ряд
вентиляторов, распределенных в зависимости от
способа их циклирования.
Способ вентиляции относится к алгоритму,
с помощью которого вентилятор либо целиком
обеспечивает дыхание больному, либо помогает па-
циенту в его собственном дыхании. Существует
множество методов ИВЛ. При использовании
вентиляторов давления может проводиться переме-
жающаяся принудительная вентиляция легких
(ППВЛ или IMV — intermittent mandatory venti-
lation) с постоянно положительным давлением
(ППД). Суть метода ППВЛ заключается в обес-
печении дыхания с положительным давлением че-
рез определенные заданные промежутки времени.
Этот способ показан у больных с недостаточно
эффективным самостоятельным дыханием. При
ППД пациент полностью «ответственен» за дыха-
тельный объем, но при этом в вентиляционном
цикле постоянно поддерживается положительное
давление.
Увеличивающаяся техническая сложность венти-
ляторов, циклированных по объему, позволяет ис-
пользовать дополнительные способы вентиляции,
например, Siemens 900С допускает 8 различных ме-
тодов ИВЛ. Наиболее частый дополнительный спо-
соб работы вентиляторов по объему - вспомога-
тельная вентиляция. При этом методе ИВЛ авто-
матически прекращается приведением в действие
триггерного устройства каждой попыткой самосто-
ятельного вдоха пациента. ППВЛ вновь устанав-
ливается, если количество самостоятельных дыха-
ний пациента в заданный промежуток времени
недостаточно. Достоинство вспомогательной венти-
ляции в том, что пациенты могут сами устанавли-
вать минутную вентиляцию, регулируя таким об-
разом кислотно-основной баланс. Кроме того, тео-
ретически при этом исключена возможность дс-
синхронизации в системе «больной-вентилятор»,
которая при возникновении обычно приводит к
неудовлетворительной вентиляции и состоянию
дискомфорта. При синхронизированной ППВЛ
(СППВЛ) принудительный вдох не подается через
заранее установленные промежутки времени, а
совпадает с определенным вдохом больного.
В зависимости от вида аппарата перед началом
ИВЛ должны быть установлены определенные па-
66 ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ
рамстры вентиляции, FIO2 и выбран се способ.
В вентиляторах объема частота дыхания и дыха-
тельный объем — два главных показателя, кото-
рые предварительно необходимо определить. До-
полнительные параметры также могут быть полез-
ны: дыхательное соотношение вдох : выдох, состав
вдыхаемой смеси, пределы давления. При исполь-
зовании вентиляторов давления в дополнение ко
времени вдоха и скорости газотока предвари-
тельно устанавливаются ПДВ и ПДКВ. Дыхатель-
ный объем (в мл) может быть измерен по формуле:
16,7 X ВВ (сек) X ток/л (мин),
где В В — время вдоха, ток — газоток, 16,7 — фак-
тор поправки для перевода в соответствующие еди-
ницы. Следует заметить, однако, что данные изме-
рения дыхательных объемов у детей, находящихся
на вентиляторах давления, часто неточны, что свя-
зано с подтеканием воздуха вокруг эндотрахеаль-
ной трубки и потерей объема в результате податли-
вости контура и сжимаемости газа в контуре. Ког-
да пик давления достигнут до окончания времени
вдоха, объем «уходит» из контура через предохра-
нительный клапан.
Взаимоотношение параметров, установленных
на вентиляторах давления, лучше всего объясня-
ется их индивидуальным воздействием на кривую
давления на вдохе (рис. 4-2). Изменения, которые
повышают амплитуду волны или удлиняют время
вдоха, увеличивают минутную вентиляцию; изме-
нения, которые увеличивают область под кривой,
повышают среднее давление в дыхательных путях.
У критически больных пациентов, особенно ново-
рожденных, среднее давление в дыхательных пу-
тях является главным фактором, определяющим
оксигенацию.
Во многих стационарах используются вентиля-
торы по давлению и объему, но вентиляторы дав-
ления применяются исключительно у детей. Пре-
имущество вентиляторов объема в том, что уста-
новленная минутная вентиляция не меняется при
изменениях легочной податливости. Различные
способы вспомогательной ИВЛ возможно приме-
нять только на вентиляторах объема, в связи с не-
обходимостью наличия реагирующих на давление
клапанов.
Вентиляторы давления всегда ограничивают
ПДВ, уменьшая риск баротравмы у детей. Их ме-
ханика относительно проста, они компактны, недо-
роги и менее сложны в употреблении. Контур вен-
тиляторов давления предполагает низкий объем
и низкую податливость, а соответственно они бо-
лее подходят для ИВЛ у детей. Поскольку эти ап-
параты требуют постоянного тока О2, то их приме-
нение ограничивается использованием у детей
с массой тела до 15 кг при максимальной допусти-
мой скорости тока 30 л/мин. В вентиляторах дав-
ления объем меняется в зависимости от податливо-
сти легких, что требует более внимательного отно-
шения к больным, позволяющего избежать гипо-
или гипервентиляции.
Высокочастотная ИВЛ (ВЧ ИВЛ) относится
к группе методов, при которых применяется боль-
шая частота дыхания (до 2400 дых/мин) и низкие
дыхательные объемы, нередко равные объему мер-
твого пространства или даже меньше него.1 Пре-
имущество этих методов в способности поддер-
живать адекватную альвеолярную вентиляцию,
используя низкие давления и таким образом умень-
шая риск баротравмы. Истинный механизм газооб-
мена в таких ситуациях недостаточно ясен. Для
его объяснения предложен ряд теорий, однако, по-
видимому, имеется комбинация нескольких фак-
торов
ВЧ ИВЛ может быть применена в трех различ-
ных вариантах. Первый — высокочастотная венти-
ляция с положительным давлением (ВЧПД ИВЛ)
30-1
Рис. 4-2. Кривая давления на вдохе.
Сроднее давление в дыхательных путях
может быть увеличено пятью способами:
(1) более высокая скорость потока газа
ведет к более «плоской» конфигурации
волны; (2) увеличение пика давления иа
вдохе; (3) пролонгированное время вдо-
ха без изменения частоты (увеличенное
или обратное соотношение вдох: вы-
дох); (4) увеличение ПДКВ и (5) уве-
личение частоты без изменения времени
вдоха (уменьшение времени выдохи и
таким образом повышенное или обрат-
ное соотношение вдох : выдох).
Т
О
-----1------
1
Время (сек)
2
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ 67
осуществляется с помощью обычных вентиляторов
с использованием частоты дыхания 60—150 в ми-
нуту и дыхательных объемов, значительно умень-
шенных по сравнению с нормой. Эксплуатацион-
ные возможности большинства обычных вентиля-
торов при этом увеличиваются, а поставляемый
пациенту объем ниже рассчитанного для этих ап-
паратов. Второй метод, высокочастотная струйная
(инжекционная) вентиляция (ВЧИ ИВЛ), создает
периодическое поступление газа через канюлю,
находящуюся в просвете эндотрахеальной трубки.
Ее проводят с частотой 100—900 дых. в мин. Как
и при ВЧПД ИВЛ экспираторная фаза в данном
случае пассивная и зависит от эластической «отда-
чи» легких и грудной клетки. При третьем способе,
высокочастотной осцилляционной ИВЛ (ВЧО
ИВЛ), создаются объемы, меньшие по величине
объема мертвого пространства, с частотой дыхания
от 400 до 2400 в минуту. В отличие от других ви-
дов ВЧ ИВЛ, при данном методе выдох активный,
ВЧ ИВЛ остается пока еще экспериментальной
техникой, хотя предпринимается множество клини-
ческих испытаний для выяснения ее достоинств
и недостатков. Благодаря возможности осуществ-
лять при использовании этого метода эффектив-
ную альвеолярную вентиляцию, применяя низкие
пики давления в дыхательных путях, ВЧ ИВЛ про-
пагандируется при синдромах выхода воздуха из
легких, таких как бронхоплевральная фистула,
травма верхних дыхательных путей и пневмото-
ракс. ВЧ ИВЛ рекомендуется также при дыхатель-
ной недостаточности у новорожденных, характери-
зующейся персистирующей легочной гипертен-
зией, в том числе при врожденной диафрагмальной
грыже. Благодаря возможности более эффективно-
го выведения СО2, ВЧ ИВЛ позволяет достичь ги-
первентиляции и алкалоза в тех случаях, когда
обычные методы ИВЛ неэффективны.
К отрицательным сторонам большинства мето-
дов ВЧ ИВЛ относится трудность оценки давления
в дыхательных путях, отражающего альвеолярное
давление. При струйной ВЧ ИВЛ задержка возду-
ха может создать «неумышленное ПДКВ», если ле-
гочная константа времени слишком продолжитель-
на и препятствует адекватному выдоху. Эта проб-
лема не существует при осцилляционной ВЧ ИВЛ
в связи с активным характером выдоха. Кроме то-
го, во время проведения ВЧ ИВЛ отмечаются ате-
лектазы в зависимых легочных сегментах, попыт-
ки предотвращения которых путем использования
перемежающихся вдохов приводят к высокой ча-
стоте пневмотораксов. В ряде сообщений также
описываются иные неожиданные осложнения, паи
более часто встречающиеся при струйной В1!
ИВЛ — некротический трахеит, иногда тяжелая
воспалительная реакция в месте поступления газа
в проксимальные дыхательные пути.15
Экстракорпоральная мембранная оксигена
ция. Экстракорпоральная мембранная оксигенация
(ЭКМО) — метод реанимации, который подразу-
мевает перевод ребенка на сердечно-легочный об-
ходной путь. При этом легким предоставляется
«отдых» на низких параметрах вентиляции при
адекватном поступлении О2 и удалении СО2.16
Этот метод получил широкое распространение
в лечении доношенных и недоношенных детей, на-
ходящихся в критическом состоянии, и не может
уже считаться экспериментальным в этой группе
больных. Описано успешное его применение и у
старших детей, и взрослых. Детальное обсуждение
ЭКМО представлено в главе 77.
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ
При возникновении у больного дыхательной недо-
статочности помощь должна быть оказана неза-
медлительно. Нередко вначале достаточно бывает
относительно консервативных мероприятий для
улучшения газообмена, включая активную физио-
терапию на грудную клетку и отсасывание слизи,
лечение бронходилататорами, коррекцию метабо-
лических нарушений, применение лекарств, дейст-
вующих на ЦНС. Если эти меры не помогают,
показана ИВЛ.
Интубация. Метод доступа в дыхатепьные пу-
ти — первая проблема, возникающая при переходе
на ИВЛ. Эндотрахеальная интубация позволяет
проводить вентиляцию с положительным давлени-
ем, контролировать секрецию и обеспечивает об-
ходной путь при обструкции проксимальных дыха-
тельных путей. Вначале больной должен быть ста-
билизирован, чего почти всегда можно достичь
с помощью мешочно-масочной вентиляции. После
этого выполняется оро- или назотрахеальная инту-
бация, кроме того, может быть произведена трахе-
остомия. Размер трубки выбирается в зависимости
от «размеров» пациента. Используются трубки
наибольших диаметров, дабы уменьшить до мини-
мума сопротивление, что обеспечивает лишь лег-
кую утечку воздуха при высоких давлениях и со-
ответственно предупреждает некроз от давления
(табл. 4-3). Манжеточные трубки не применяются
у грудных и маленьких детей, поскольку наличие
манжетки требует значительного уменьшения диа-
метра самой трубки.
Оротрахеальная интубация — технически наибо-
лее простой метод доступа в дыхательные пути,
поэтому именно ей должно быть отдано предпочте-
ние в экстренной ситуации. Главный недостаток
оротрахеальной трубки — ее нестабильное поло-
жение, особенно у маленьких детей, у которых да-
ТАБлИЦА 4-3. Выбор размера эндотрахеальной трубки
в зависимости от возраста
Возраст Размер трубки (наружный диаметр)
С 30 пел (гестационный возраст) 2,5
30 недель (доношенные) 3,0
Новорожденные — 5 мое 3,5
6—18 мсс 4.0
2 -4 года 5,0
4—6 лет 5.5
6—8 лет 6,0
8—10 лет 6.5
>•10 лет 6,5 или больше, с манжеткой
68 ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ
же небольшое смещение трубки может затруднять
интубацию или привести к самопроизвольной экс-
тубации. Кроме того, нестабильность трубки уве-
личивает риск подсвязочного стеноза при длитель-
ной интубации. Старшие дети могут сжимать зуба-
ми оротрахеальную трубку, что приводит к ее
окклюзии.
Назотрахеальная интубация, хотя и требует боль-
шего опыта для введения трубки, но зато обеспе-
чивает ее стабильность, трубка нс может быть ок-
клюзирована зубами, кроме того, легче осуществ-
лять гигиенические мероприятия в полости рта.
При длительной назотрахеальной интубации воз-
можно развитие некроза носовой перегородки.
Трахеостомия позволяет достичь тех же целей,
что и трансларингеальная интубация, но без риска
повреждении гортани и подсвязочной области,
а также обеспечивает стабильность трубки. У
взрослых и детей старшего возраста вопрос о тра-
хеостомии следует ставить в тех случаях, когда
больной интубирован уже в течение 7—10 дней
и ясно, что интубация потребуется еще на значи-
тельный период времени. У грудных и маленьких
пациентов высокая частота осложнений трахеосто-
мии вынуждает оставлять ребенка на трансла-
рингеальной интубации в течение месяца и более.
Возможные осложнения трахеостомии включают
гранулему и стеноз трахеи, трахеомаляцию, обра-
зование фистулы между трахеей и сосудами, трав-
матический трахеопищеводный свищ.
Трахеостомию следует проводить под наркозом,
с интубацией больного. Ребенок должен нахо-
диться в таком положении, чтобы шея была слег-
ка разогнута. Посередине между надгрудинной
ямкой и перстневидным хрящом гортани делается
поперечный разрез. Подкожная клетчатка и пла-
тизма разделяются электрокаутером, длинные
мышцы разъединяются по средней линии. Перед-
няя стенка трахеи очищается, при этом порой не-
обходимо отвести краниально перешеек щитовид-
ной железы. С обеих сторон от средней линии на-
кладывают тракционные швы проленом 3-0, чаще
на уровне 4-го трахеального кольца. Эти нити
оставляют длинными и завязывают в виде нетель.
Подтягивание за них помогает раскрыть операци-
онное поле во время трахеотомии при первичной
канюляции, а также в том случае, когда в раннем
послеоперационном периоде возникает необходи-
мость в рсканюляции. Продольная трахеотомия
производится через 3-е и 4-е (и, если необходимо,
5-е) трахеальные кольца, и в тот момент, когда
анестезиолог подтягивает эндотрахсальную трубку
проксимально, вводят трахеостомическую трубку.
У детей никогда не иссекают ткань трахеи, так же,
как и не создают лоскуты из-за риска последую-
щего трахеального стеноза или трахеомаляции. Нс
производят в детском возрасте и поперечную тра-
хеотомию, при которой рана имеет тенденцию рас-
ширяться, особенно у маленьких детей, и, кроме
того, есть риск полного пересечения трахеи. Уши-
вание раны при трахеотомии обычно не требуется.
Трахеостомическую трубку укрепляют завязками.
Вентиляционная поддержка. Перед началом
ИВЛ необходимо попытаться понять патофизиоло-
гические механизмы, лежащие в основе дыхатель-
ной недостаточности у данного пациента, что по-
могает правильно выбрать параметры вентиляции.
Хотя вмешательство в организм путем ИВЛ может
вносить определенные изменения в патофизиоло-
гические процессы, вентиляция — это все-таки
только поддержка. Основные усилия в терапии
должны быть направлены на лечение первопричи-
ны, и одновременно с этим следует осуществлять
вентиляционную поддержку.
При переводе ребенка на ИВЛ необходимо иметь
параметры, отражающие состояние функции лег-
ких и сердечно-сосудистой системы. Важно знать,
какова податливость легких и грудной клетки,
и понимать, чем вызвана низкая податливость —
рестриктивной болезнью и низкими легочными
объемами или обструктивными факторами и высо-
кими легочными объемами? (см. кривую податли-
вости, рис. 4 1). У большинства хирургических
больных уменьшаются и податливость, и легочные
объемы. Снижают податливость грудной стенки то-
ракальные и абдоминальные разрезы, а также
вздутие живота. Поверхностное дыхание у боль-
ных в подобных ситуациях и индуцированная ле-
карствами гиповентиляция ведут к возникновению
массивных ателектазов, уменьшая таким образом
податливость и повышая шунтируемую фракцию.
При врожденной диафрагмальной грыже увеличен-
ная мышечная масса в легочных артериолах пред-
располагает больного к тяжелой и иногда фаталь-
ной ПЛГН, наслаивающейся на сниженную подат-
ливость гипоплазированного легкого. Обструкция
дыхательных путей, ведущая к уменьшению подат-
ливости и увеличению легочных объемов, возни-
кает при астме, бронхолегочной дисплазии, синд-
роме мекониевой аспирации.
В большинстве случаев в клипической медицине
лечение любого больного вначале основывается на
имеющейся информации о его состоянии, а затем,
в зависимости от реакции на первичные мероприя-
тия («обратная связь»), проводится коррекция.
ИВЛ в этом плане нс является исключением. Пер-
воначальные параметры вентиляции устанавлива-
ются близкими к физиологическим. Дополнитель-
но проводится коррекция с учетом диагностиро-
ванной или предполагаемой патологии. Затем по
данным клинического обследования и измерения
различных мониторных показателей производят
оценку эффективности ИВЛ и корректировку пара-
метров вентиляции, если к этому времени не
достигнуто улучшение состояния больного.
Основные параметры для начальной вентиляции
даны в таблице 4-4. Можно первоначальные пара-
метры установить иным способом, особенно у но-
ворожденных — вентилируя больного с помощью
мануального мешка и наблюдая за степенью подъ-
ема грудной клетки при вдохе, за объемом и пиком
требующегося давления, сатурацией О2, а затем
использовать полученные таким образом показа-
тели при работе с вентилятором.
При наличии низких легочных объемов в нача-
ле ИВЛ может быть показано более высокое
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ 69
ТАБЛИЦА 4 4. Начальные параметры вентиляции
Вентиляторы объема
Способ НО2 Частота сппвл 100% 12—15 дых/мин (старшие дети)
Дыхательный объем 15—20 дых/мин 20—30 дых/мин 12—15 см3/кг (младшие дети) (грудные дети)
ПДКВ Вентиляторы Способ Н()2 Частота PIP давления 3—5 мм рт. ст. ппвл 1<Ю% 20 30 дых/мин 20- 30 мм рт. с
ПДКВ Соотношение вдох : выдох 3 5 «и рт. ст. 1:2
ПДКВ. При обструктивной болезни дыхательных
путей и высоких легочных объемах должна быть
удлинена экспираторная фаза. Важно также кон-
тролировать сердечный выброс и при необходимо-
сти поддерживать его инотропами.
После короткого периода стабилизации на на-
чальных параметрах вентиляции (10—15 мнн)
определяют газы артериальной крови и в зависи-
мости от результатов исследования проводят даль-
нейшую корректировку.
Регуляция Рсо, (или pH при дыхательном аци
дозе/алкалозе). Для корректировки Р(;о2 должна
быть изменена минутная вентиляция. При исполь-
зовании вентиляторов объема этот параметр регу-
лируется дыхательным объемом и скоростью вен-
тиляции. Прн работе с вентиляторами давления
существенное влияние на Рсо оказывают измене-
ния частоты дыхания и PIP. Изменения потока
и времени вдоха также воздействуют на дыхатель-
ный объем, а соответственно и на минутную венти-
ляцию. При достижении предела давления допол-
нительный объем газа теряется из контура через
выпускной клапан, ограничивая таким образом
воздействие этих параметров на обмен СО2. Высо-
кие уровни ПДКВ вызывают подъем Рсо в ре-
зультате снижения амплитуды кривой давления на
вдохе и уменьшения дыхательного объема.
Регуляция Рог Увеличение концентрации вдыха-
емого кислорода (FIO2) в некоторой степени улуч-
шает артериальную кислородную сатурацию. Од-
нако у большинства больных, которые требуют
вентиляционной поддержки, воздействие на окси-
генацию повышения FIO2 может быть значительно
ограничено за счет шунтирования в недостаточно
вентилируемых сегментах легких.
Изучение рядом исследователей проблемы дыха-
тельной недостаточности показало, что главным
фактором, определяющим оксигенацию при ИВЛ,
является среднее давление в дыхательных путях
(СДД). СДД может быть корригировано изме-
нением ряда параметров вентиляции. В частности,
как бы значительны ни были индивидуальные ко-
лебания, однако увеличение ПДКВ с последующим
возрастанием PIP и соотношения вдох : выдох, как
правило, оказывает существенное влияние на еди-
ницу увеличения СДД. Благоприятное воздействие
на оксигенацию постоянно повышенного давления
происходит благодаря ряду факторов:
— В результате расправления ателсктазирован-
ных участков увеличивается FRC.
— Сопротивление воздушных путей имеет тен-
денцию к снижению, поскольку растяжение легко-
го приводит к уменьшению периферических дыха-
тельных путей.
— Возрастает податливость, нбо эффект, связан-
ный с расправлением ателектазов, «перевешивает»
любую потерю податливости в результате перерас-
тяжения нормальных легочных сегментов.
— Отмечается и защитное воздействие на сур-
фактант, который при наличии нерасправленных
ателектазов поглощается с большой скоростью
в участках альвеолярного коллапса.
Однако высокие давления при ИВЛ обладают
и пбгенциальными побочными эффектами, в част-
ности, увеличивают риск баротравмы. Кроме того,
обратное соотношение вдох: выдох может вести
к неумышленному ПДКВ и задержке воздуха, осо-
бенно в участках легких с удлиненной константой
времени. Повышение СДД порой отражается на
функции других органов. В результате нарушения
венозного возврата в грудную клетку может па-
дать сердечный выброс, особенно при гипово-
лемии. Отмечается и независимое негативное
инотропное воздействие на сердце, по-видимому,
опосредованное простогландинами.19 Прямой комп-
рессионный эффект на русло легочных капилляров
может поднимать легочное сосудистое сопротивле-
ние, увеличивая таким образом риск экстрапуль-
моиарного шунтирования справа налево (откры-
тый артериальный проток нли овальное окно).
Улучшение оксигенации путем увеличения СДД
может активно способствовать снятию легочного
артериального сосудистого спазма. Очевидная
сложность сердечных и легочных реакций на вен-
тиляционные манипуляции подчеркивает важность
измерения сатурации О2 смешанной венозной кро-
ви в тех случаях, когда давление достигает уров-
ней, при которых можно ожидать побочных эф-
фектов.
Смешанная венозная сатурация О2 позволяет не-
прерывно оценивать воздействие ИВЛ и на дыха-
тельную, и на сердечно-сосудистую систему-
Снятие с искусе таенной вентиляции — это пе-
риод, когда вентиляционная поддержка постепенно
прекращается, соответственно пациент начинает
все больше обеспечивать собственное дыхание са-
мостоятельно. В большинстве случаев это сложный
испытательный период, когда важно определить,
находятся ли процессы, лежащие в основе респира-
торного дистресса, под контролем или уже ликви-
дированы. Начать «отлучение» больного от ИВЛ
можно лишь в том случае, если податливость близ-
ка к нормальной, нет признаков сердечной недо-
статочности (о чем говорит минимальная потреб-
ность в инотропах, или даже отсутствие необходи-
мости в их применении), а сепсис, если он был
у больного, «идет на убыль». При всех этих усло-
виях шунтируемая фракция становится незначи-
тельной, и F1OZ может быть быстро уменьшена.
70 ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ
В некоторых случаях нет необходимости в посте-
пенном снятии больного с ИВЛ, например при
кратковременной вентиляции после операции, ког-
да ИВЛ проводят лишь до прекращения действия
анестетика.
При снятии с вентиляции в первую очередь дол-
жны быть уменьшены те параметры, которые наи-
более склонны давать побочные эффекты. При ис-
пользовании вентиляторов давления, по мере улуч-
шения легочной податливости, если не уменьшить
PIP и время вдоха, то дыхательный объем возра-
стает. Соответственно «неснижение» этих парамет-
ров у ребенка с уже нормально функционирующи-
ми легкими несет риск значительного их перераз-
дувания и баротравмы. ПДКВ следует уменьшать
до физиологического уровня (3—5 мм рт. ст.), но
никогда не снимать сразу полностью. Снятие с ап-
парата с помощью ППВЛ применяется при исполь-
зовании вентиляторов давления, поскольку ника-
кие другие способы «отлучения» здесь нс пригод-
ны. Однако этот метол часто используется и при
ИВЛ вентиляторами объема. При снятии с аппара-
та путем ППВЛ постепенно уменьшают частоту
принудительных вдохов, заставляя пациента брать
на себя все больший объем работы по обеспечению
дыхания. Часто непосредственно перед экстуба-
цией применяют «постоянно положительное давле-
ние в дыхательных путях» (ППД) или увеличива-
ют мертвое пространство вентилятора («Т-трубоч-
ная проба»). В течение этого периода пациенты
полностью выполняют работу дыхания сами. Од-
нако целесообразность проведения ППД-пробы
достаточно сомнительна. Дополнительное сопро-
тивление в дыхательных путях, связанное с нахож-
дением там интубационной трубки, особенно у
грудных и маленьких детей, может потребовать от
больного более напряженной работы, чем н том
случае, когда он был бы экстубирован.20 Эти про-
бы должны быть ограничены очень короткими пе-
риодами. Свободное ненапряженное дыхание в
процессе снятия с ИВЛ и наличие нормальных по-
казателей Рсо, и pH говорят о готовности больно-
го к экстубации.
Описан ряд параметров, которые помогают
оценить дыхательные резервы больного и соответ-
ственно являются критериями, позволяющими осу-
ществить успешную экстубацию (табл. 4-5).21 От-
рицательная сила вдоха — простой показатель
максимального отрицательного давления, которое
больной может создать в случае внезапной окклю-
зии дыхательных путей во время вдоха. Этот пока-
затель возможно определить у детей любого возра-
ста, включая новорожденных, однако в младшей
возрастной группе трактовка полученных дан-
ных иногда затруднена. Допустимые значения от-
рицательной силы вдоха — 30 мм рт. ст. или боль-
ше применительно ко всем возрастам.
ТАБЛИЦА 4-5. Критерии, позволяющие прекратить ИВЛ
Отрицательная сила вдоха
Жизненная емкость
Жизненная емкость
>30 мм рт. ст.
И) -15 см3/кт
2 X дыхательный объем
При длительно проводимой ИВЛ снятие с венти-
ляции может представить серьезную проблему.
Успешное решение ее возможно лишь в том слу-
чае. когда состояние питания больного достаточно
стабильно, а «отлучение» от аппарата производит-
ся неспешно. Один из методов снятия с ИВЛ пред-
полагает короткие периоды перехода на минималь-
ные параметры вентиляции, первоначально в тече-
ние нескольких минут каждый час или два. Эти
периоды постепенно (на протяжении многих дней)
удлиняются до тех пор, пока пациент не укрепил
в достаточной степени дыхательную мускулатуру
и не приобрел таким образом стойкие резервы для
осуществления самостоятельного дыхания. 11екото-
рыс новые вентиляторы объема предлагают метод,
называемый поддержка давления, при котором
определенное давление на вдохе поддерживается
сразу, как только больной прекращает самостоя
тельный вдох. Уровень поддержки в этом случае
может постепенно снижаться в процессе отлучения
от вентиляции. Существенное преимущество спо-
соба поддержки давления в том, что он позволяет
сохранять синхронность системы пациент-вентиля-
тор, с одной стороны, поддерживая каждое дыха-
ние, а с другой — отлучая одновременно больного
от аппарата.
Вслед за экстубацией необходимо уделять самое
пристальное внимание тщательному туалету дыха-
тельных путей с целью предупреждения скопления
секрета и возникновения ателектазов. Отек горта-
ни. наблюдающийся порой сразу после экстуба-
ции, может привести к выраженному стридору,
особенно у грудных детей. В таких случаях часто
эффективен адреналин в аэрозоле. Иногда отек
может быть снят парентеральным введением перед
экстубацией стероидов (дексаметазон 1 мг/кг каж-
дые 6 час).
ОСЛОЖНЕНИЯ
Кислород - это лекарство и, как всякое лекарство,
несет в себе потенциал серьезных побочных эф-
фектов.22 Токсичность кислорода может быть свя-
зана как с его концентрацией, так и с продолжи-
тельностью воздействия. При использовании
60% ПО2 нарушение функции легких может на-
блюдаться не раньше, как минимум, 24-часового
воздействия. В высоких концентрациях кислород
вызывает повреждение всех типов клеток, с кото-
рыми он контактирует, опосредованное, по-види-
мому, реактивными свободными радикалами. Наи-
более чувствительны к неблагоприятному воздей-
ствию О2 прежде всего капиллярный эндотелий,
а также пневмоциты I и II типов. В дополнение
к прямому повреждению клеток высокие концент-
рации вдыхаемого О2 могут усугубить ателектазы
в недостаточно вентилируемых участках за счет
эффекта вымывания азота. Азот замещается О2,
который в конечном счете полностью абсорбиру-
ется, что приводит к коллапсу участков с бедным
газообменом.
С положительным давлением, применяемым в
механических вентиляторах, снязап ряд синдромов
ИСКУССТВЕННАЯ ВЕНТИЛЯЦИЯ ЛЕГКИХ 71
утечки воздуха. Наиболее часто это пневмоторакс,
легочная интерстициальная эмфизема, пневмоме-
диастинум, пневмоперикард и подкожная эмфизе-
ма. Однако риск утечки воздуха в большей степе-
ни связан обычно с тяжестью основной легочной
патологии, чем с уровнем PIP и ПДКВ. Пневмото-
ракс и пневмоперикард — жизнеугрожаюшие со-
стояния, требующие срочной диагностики и лече-
ния. Легочная интерстициальная эмфизема при
значительной ее выраженности фактически делает
невозможной вентиляцию и является причиной
очень высокой летальности.
Бронхолегочная дисплазия (БЛД) — хрониче-
ское поражение легких, возникающее приблизи-
тельно у 15% грудных детей, находящихся на
ИВЛ. ‘ Что является при этом первичным этио-
логическим фактором — сам кислород или высокое
давление, вопрос спорный. БЛД, начинаясь с не-
кроза клеток, интерстициального отека и воспале-
ния. склонна к прогрессированию, что выражается
в фибропролиферативных изменениях в интерсти-
ции, чешуйчатой метаплазии дыхательных путей,
гладкомышечной гипертрофии, перерастяжении,
разрыве и иногда эмфизематозных изменениях на
альвеолярном уровне. Рецидивирующая инфекция,
легочный отек и правосторонняя сердечная недо-
статочность — хронические последствия этой бо-
лезни, ведущие к 30%-ной лета т внести у детей
первого года жизни.
Сепсис — частое осложнение ИВЛ у критически
больных пациентов. Интубация и механическая
вентиляция «прорывает брешь» в важном звене за-
щитного механизма больного. Респираторный эпи-
телий у тяжелых пациентов «жадно» задерживает
на себе грамотрицательные организмы, превраща-
ясь таким образом в гнездо (очаг), являющийся
благоприятной основой для развития серьезных
инфекционных осложнений.25 Для снижения риска
возникновения осложнений необходимо обращать
самое строгое внимание на соблюдение правил
асептики и элементарное мытье рук при проведе-
нии ИВЛ.
ЛИТЕРАТУРА
1. Hislop A. Reid L. Development of the acinus in the human lung.
Thorax 29:90—94. 1974.
2. Dunhill MS: Postnatal growth of the lung. Thorax 17:329—333,
1962.
3. Hogg JC, Williams J. Richardson JB, et al.: Age as a factor in
the distribution of lower airway conductance and in the patholo-
gic anatomy of obstructive lung disease. N Engl J Med
282:1283—1287. 1970.
4. Keens TG, Bryan AC, Levison H, lanuzzo CD: Developmental
pattern of muscle fiber types in human ventilatory muscles.
J Appl Physiol 44:909—917, 1978.
5. Bancalari E: Inadvertent positive end-expiratory pressure during
mechanical ventilation. J Pediatr 108:567—569, 1986.
6. Puntoppidan H, Laver MB, Geffin B: Acute respiratory failure
in the surgical patient. Adv Surg 4:163 254, 1970.
7. Davenport HW: The ABC of Acid-Base Chemistry, 6th edition.
The University of Chicago Press, (’hicago, 1974.
8. Cilley RE, Polley TZ Jr. Zwishenbergcr JB. et al.: Independent
measurement of oxygen consumption ans oxygen delivery.
J Surg Res 47:242—247, 1989.
9. Dedell G, Cornish JD, Bartlett RH: What constitutes adequate
oxygenation? Pediatrics 85:39—41, 1990.
10. Harris MS. Little GA: Umbilical artery catheters: High, low, or
no? J Perinai Med 6:15—21, 1978.
11. Mokrohisky S, Levine R, В him ha gen J. et al.: Low positioning of
umbilical artery catheters increases associated complications in
newborn infants. N Engl J Med 299:561, 1978.
12. Cassady G: Transcutaneous monitoring in the newborn infant.
J Pediatr 103:837—848, 1983.
13- Epstein MF, Cohen AR, Feldman HA, Raemer l)B: Estimation of
Paco2 by two noninvasivc methods in the critically ill newborn
infant. J Pediatr 106:282—286, 1985.
14. Wetzel RC, Gioia ER: High frequency ventilation. Pediatr Clin
North Am 34:15 38, 1987.
15. Boros SJ, Mammel MC, Coleman JM, el al.: Neonatal highfrequ-
ency jet ventilation: Four years’ experience. Pediatrics 75:657—
663, 1985.
16. Hirschl RB. Bartlett RH: Extracorporeal membrane oxygenation
support in cardiorespiratory failure. Adv Surg 21:189, 1987.
17. Boros SJ: Variations in inspiratory: expiraiorv ratio and airway
pressure wave form during mechanical ventilation: The signifi-
cance of meam airway pressure. J Pediatr 94:114—117, 1979.
18. Stewart AR, Finer NN, Peters KL: Effects of alterations of ins-
piratory and expiratory pressures and inspiratory/expiratory
ratios on mean airway pressure, blood gases, and intracranial
pressure. Pediatrics 67:474 481, 1981-
19. Manny J, Grindlinger G, Mafhe AA, Hechfman 1IB: Positive
end-expiratory pressure, lung stretch, and decreased myocardial
contractility. Surgery 84:127—133. 1978.
20. Kim EH: Successful extubation of newborn infants without pre-
extubation trial of continuous positive airway pressure. J Perinai
9:72 76, 1989.
21. Sahn SA: Bedside criteria for discontinuation of mechanical
ventilation. Chest 63:1002—1005, 1973.
22. Winter PM, Smith G: The toxicity of oxygen. Anesthesiology
37:210—241, 1972.
23. Monin P. Vert P: The management of bronchopulmonary dys-
plasia. Clin Perinalol 14:531—549. 1987.
24. Goetzman BW: Understanding bronchopulmonary dysplasia. Am
J Dis Child 140:332—334, 1986.
25. Johanson WG, Higuchi JH, Chaudhuri TR, Woods DE: Bacteri-
al adherence to epithcli.il cells in bacillary colonization of the
respiratory tract. Am Rev Rcsp Dis 121:55—63, 1980.
Глава 5
НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК
РЕГУЛЯЦИЯ СОДЕРЖАНИЯ ВОДЫ В ОРГАНИЗМЕ
Эффективно функционирующие почки поддержи-
вают нормальный объем и состав жидкости в орга-
низме, даже при значительных колебаниях диеты,
внепочечных потерь воды и растворенных веществ.
Баланс воды и электролитов достигается благода-
ря экскреции мочи с определенным объемом и со-
ставом, что обеспечивается клубочковой ультра-
фильтрацией плазмы в сочетании с последующей
канальцевой реабсорбцией и секрецией.' Выделя-
емая конечная моча представляет собой лишь не-
большую часть клубочкового ультрафильтрата,
измененного в процессе прохождения по нефрону.
Капилляры клубочков свободно пропускают воду
и растворенные вещества низкого молекулярного
веса, задерживая в то же гремя форменные эле-
менты и макромолекулы. Стенка клубочкового ка-
пилляра функционирует в отношении макромоле-
кул как барьер, «отбирающий» их по размерам,
форме и величине заряда Изменение клубочкового
фильтра га в процессе его прохождения через ка-
нальцы осуществляется путем транспортировки
некоторых всшсств как активной (в просвет ка-
нальцев или из просвета), так и пассивной. По-
следняя обусловлена осмотическим и электрохими-
ческим равновесием и различной пропускной спо-
собностью отдельных сегментов нефрона. Система
транспорта ионов в клетках почечного эпителия
в основном не отличается от функции любых дру-
гих эпителиальных клеток. Однако почечная
транспортная система обеспечивает общее содер-
жание в организме воды, солей и кислотно-основ-
ной гомеостаз, в то время как местные процессы,
происходящие в других эпителиальных клетках,
регулируют лишь отдельные «фрагменты» водно-
солевого обмена, например, объем жидкости и аб-
сорбцию продуктов метаболизма.
Для того, чтобы почка эффективно регулирова-
ла баланс воды и растворенных веществ, клубоч-
ковый фильтрат должен иметь адекватный объем.
Почечный кровоток составляет 20—30% сердечно-
го выброса. Из общего ренального плазмотока
92% плазмы проходит через функционирующую
экскреторную ткань и опре [еляется как эффектив-
ный почечный плазмоток (ЭППТ). Скорость клу-
бочковой фильтрации (СКФ) обычно составляет
1/5 часть ЭППТ, в результате фильтрационная
фракция равна 0,2.
Скорое ть ультрафильтрации через клубочковые
капилляры, СКФ. обусловлена теми же фактора-
ми, которые опреде ,яют трансмуральное движение
жидкости и в других капиллярных сетях организ-
ма,3 а именно — градиентами транскапиллярного
гидравлического и осмотического давления и про-
ницаемостью капиллярной стенки. Механизм ре-
нальной ауторегуляции дает почке возможность
поддерживать относительное постоянство кровото-
ка при наличии изменяющегося давления, как си-
стемного артериального, так и ренального перфу-
зионного.' Этот механизм, по-видимому, опосреду-
ется в нефронах за счет канальцево-клубочковой
обратной связи через macula densa (область в нача-
ле дистального канальца, примыкающая к клу-
бочку), а также приводящие и отводящие артерио-
лы. Уменьшение артериолярного сопротивления
в приводящих артериолах с сохранением его на
стабильном уровне в отводящих позволяет поддер-
живать гидродинамическое давление в клубочке,
несмотря на падение системного и почечного арте-
риального давления.
Реабсорбция воды, а также реабсорбция и секре-
ция растворенных веществ при прохождении филь-
трата через нефрон, служит в норме поддержанию
жидкостного гомеостаза в организме. В здоровом
нерастущем организме поступление и выведение
воды и растворенных веществ равны, и таким
образом гидроионный баланс нулевой. Механиз-
мы регуляции функции почек могут меняться
под влиянием различных заболеваний как систем-
ных, так и почечных, а также при воздействии
самых разнообразных лекаре гвенных веществ,
таких как вазопрессоры и вазодилататоры, не-
стероидные противовоспалительные препараты, ди-
уретики и антибиотики. Нарушение функции по-
чек в послеоперационном периоде наиболее часто
проявляется гипоксией и снижением ренальной пер-
фузии.
НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК 73
ОЦЕНКА ФУНКЦИИ ПОЧЕК
Оценка функции почек начинается с тщательного
сбора анамнеза и осмотра больного, а затем лабо-
раторного обследования, направленного на опреде-
ление скорости клубочковой фильтрации и функ-
ции почечных канальцев. Серьезные нарушения
выделительной и концентрационной способности
почек очевидны порой уже из анамнеза. Иссле-
дование мочевого осадка может выявить прямые
признаки поражения клубочков или почечной па-
ренхимы. Определение содержания в сыворотке
электролитов, кальция и фосфора является ценным
скрининговым методом, характеризующим каналь-
цевые нарушения, концентрация же креатинина —
главный показатель СКФ.
Объем мочи. Часто в самых разнообразных кли-
нических ситуациях очень важно определить, адек-
ватный ли объем мочи выделяет больной. Ответ на
вопрос, какой же диурез является адекватным, —
очень непрост, поскольку этот показатель зависит
от нескольких факторов: водного баланса в орга-
низме в настоящий момент, жидкостной нагрузки
и экстраренальных потерь, а также облигатной на-
грузки растворимым веществом. Больным с нару-
шениями концентрационной способности почек,
например при серповидно-клеточной анемии (у
старших детей и взрослых) и при постобструктив-
ной уропатии, требуется больший минимальный
объем мочи для экскреции облигатной нагрузки
растворимым веществом, чем пациентам с нор-
мальной концентрационной функцией почек.
Хотя определение «адекватности» объема мочи
в большинстве случаев вызывает много сложно-
стей, тем не менее всегда важно по меньшей мере
выяснить вопрос — имеется ли у больного при дан-
ном диурезе олигурическая почечная недостаточ-
ность или нет. Решение этого вопроса основано на
знании минимального объема мочи, необходимого
для выведения облигатной нагрузки растворимым
веществом. Вычисление производится с пересчетом
на 100 метаболизированных калорий или на
100 мл нагрузки Н2О, что позволяет осуществлять
расчеты независимо от массы тела. Физиологиче-
скую потребность в воде удобно определять для
этой цели с использованием метода Holliday и Se-
gar (табл. 5-1).4 Норма в 100 мл/кг/сут примени-
тельна к детям с массой тела только до 10 кг.
Ребенок с МТ 15 кг имеет потребность в воде
83 мл/кг/сут, а при МТ 30 кг — 57 мл/кг/сут.
Минимальный объем мочи, необходимый для экс-
креции облигатной нагрузки растворимым веще-
ством, вычисляется с учетом следующих условных
положений и допущений.
1. Облигатная нагрузка растворимым вещест-
вом, условно принятая для пациента с ишемиче-
ТАБЛИЦА 5-1. Физиологические потребности в воде
Масса тела Потребности в воле * 10
2,5—К) кг 100 мл/кг
10 20 кг 1000 мл 4- 50 мл/кг L> 10 кг
20 кг 1500 мл + 20 мл/кг >-20 кг
ТАБЛИЦА 5-2. Минимальные объемы мочи, необходимые
для экскреции облигатной нагрузки
растворимым веществом
Возраст Условно принятые показатели Объем мочи (мл)
Нагрузки рас- творимым веществом (моем/100 кал) Макс, концент- рация мочи (моем/ кг) на 100 мл физ. потребности в Н2О б сутки j в час
1 нел—2 мес 25 (?) 800 31,3 1,3
2 мес—2 года 30 1000 25,0 1,0
2 года 30 1200 20,8 1.0
ской острой почечной недостаточностью (ОПН),
будет больше, чем минимальная эндогенная на-
грузка растворимым веществом, составляющая ги-
потетически 10—15 моем на 100 метаболизирован-
ных калорий (или на 100 мл полученной воды)
и меньше, чем 40 моем на 100 калорий, получен-
ных с пищей при обычной диете.4 Примерно
30 моем облигатного растворимого вещества на
100 мл калорий будут приняты нами как облигат-
ная нагрузка растворимым веществом у детей
в возрасте 2 мес и старше.
2. Концентрационная способность почек быстро
возрастает в течение 1-го года жизни и на втором
году жизни достигает уровня, характерного для де-
тей старшего возраста, (1200—1400 мосм/кг) на
втором году жизни-5, Максимальная концентраци-
онная способность почек доношенного ребенка
в возрасте от 1 недели до 2 мес колеблется от
600 до 1100 мосм/кг, а к возрасту 10—12 мес она
в среднем несколько выше 1000 мосм/кг. В табли-
це 5-2 представлены минимальные объемы мочи,
которые позволяют больному справиться с обли-
гатной нагрузкой растворимым веществом, обес-
печивая таким образом соответствующую физио-
логическую реакцию на ренальную гипоперфузию.
При ишемической ОПН диурез обычно значитель-
но снижен. Объем мочи рассчитывается по следую-
щей формуле:
Объем мочи =
Нагрузка растворимым веществом (моем)
Концентрация растворенного вещества (моем)
Ишемической ОПН, как правило, нет у ребен-
ка в возрасте до 2 мес жизни при объеме мо-
чи >1,25 мл/час/100 мл полученной жидкости,
так же как и у пациента более старшего возраста
с диурезом ^1,0 мл/час/100 мл. Дети, имеющие
объемы мочи ниже указанных уровней, соответст-
венно нуждаются в дальнейшем обследовании
и оценке на предмет олигурической почечной не-
достаточности. Неолигурическая почечная недо-
статочность— серьезная патология, которая воз-
никает почти так же часто, как и олигурическая
почечная недостаточность, и диагностируется в тех
случаях, когда при нормальном диурезе имеются
другие явные признаки снижения СКФ, чаще всего
повышенная концентрация креатинина сыворотки
или сниженный клиренс креатинина.
Скорости клубочковой фильтрации. Скорость
клубочковой фильтрации — наиболее важный во
многих отношениях показатель функции почек.
74 НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК
поскольку он отражает объем ультрафильтрата
плазмы, поступающего в канальцы.7 Снижение
СКФ — основное функциональное нарушение как
при острой, так и при хронической почечной недо-
статочности. Определение СКФ необходимо не
только для оценки функции почек как таковой, но
и для правильного выбора антибиотиков и других
лекарственных препаратов.
Метод определения клиренса инулина для изме-
рения СКФ обладает рядом недостатков. Концент-
рация мочевины в сыворотке не используется как
показатель СКФ из-за больших колебаний в зави-
симости от поступления азота с пищей. Для оцен-
ки СКФ в практике наиболее широко применяется
измерение концентрации сывороточного креатини-
на и его клиренса. Ряд обстоятельств необходимо
учитывать при использовании этого метода. На-
пример, потребление пиши, содержащей большое
количество белка (мясо, птица, рыба) повышает
уровень креатинина сыворотки через 2 часа на
22 мм.оль/л и увеличивает скорость экскреции
креатинина на 75% в течение последующих 3—
4 часов.6 Соответственно при измерении концент-
рации креатинина в сыворотке и его клиренса ука-
занные продукты должны быть исключены из пи-
щи. Кроме того, уровень креатинина в сыворотке
может повышаться в результате приема некоторых
лекарств, например триметоприма, который «кон-
курирует» с креатинином в процессе канальцевой
секреции. Триметоприм, не оказывая влияния на
СКФ, изменяет концентрацию креатинина в сыво-
ротке, что может вызвать сложности в оценке
больного с нарушением функции почек, поскольку
при этом фракция креатинина мочи за счет ка-
нальцевой секреции увеличивается, в то время как
СКФ падает.
Концентрация креатинине! сыворотки новорож-
денного в течение первой недели жизни соответст-
вует материнскому уровню, а со 2-й недели до
2 лет составляет в среднем 35+3,5 ммоль/л. В те-
чение этого возрастного периода концентрация
креатинина сыворотки относительно постоянна,
поскольку в процессе роста нет больших измене-
ний процентного содержания мышц в организме.
Повышение продукции эндогенного креатинина,
коррелирующее с мышечной массой, идет парал-
лельно с увеличением СКФ. В течение первых
двух лет жизни СКФ, выраженная в мл/мин на
единицу поверхности тела, возрастает с 35—
45 мл/мин/1,73 м2 до уровня взрослого челове-
ка— 80—170 мл/мин/1,73 м2. Нормальные пока-
затели концентрации креатинина сыворотки уве-
личиваются после 2 лет по мере полового со-
зревания, в то время как СКФ остается весьма
постоянной величиной при расчете на единицу по-
верхности тела. Это объясняется развитием мы-
шечной массы в процессе роста ребенка, а соответ-
ственно повышением продукции креатинина, кото-
рая опережает по своим темпам увеличение СКФ
на единицу массы тела. В таблице 5-3 представ-
лены средние показатели уровня креатинина в
плазме или сыворотке в различном возрасте.
Фракционная экскреция (ФЭ) натрия и бикар-
ГАЬЛИЦЛ 5-3. Уровень креатинина плазмы к разном
возрасте
Возраст Креатинин плазмы (ммоль/л)
В среднем | Колебания (+2 SD) *
Кровь ПУПОВИНЫ 66.3 45,1 - 87,5
0—2 нед 44,2 30.1 58,3
2- 26 нед 34,5 20.3 48.6
26 нед—1 год 28.3 15,9- 40.7
2 года 28,3 17,7- 38,9
4 года 32,7 22.1 43.3
6 дет 38,0 23,9 52,2
8 лет 42.4 27,4 57,5
10 лет 46,0 30.1 61,9
12 лет 52,2 36,2- 69,0
Взрослые (муж.) 85,7 63,6 107,8
Взростые (жен.) 68,1 46.9 89,3
• SD среднее квадратичное отклонение.
боната. Фракционная экскреция — показатель
функции почек, важный в оценке некоторых кли-
нических состояний и представляющий собой то
количество (фракция) профильтрованного в поч-
ках вещества, которое выведено с мочой. Фракци-
онная экскреция измеряется с использованием кли-
ренса креатинина, определяющего СКФ, и концен-
трации данного вещества в сыворотке и моче.
Количество профильтрованного вещества вычисля-
ется умножением концентрации его в сыворотке на
СКФ, а выведенное количество — умножением
концентрации вещества в моче на объем мочи.
Следовательно, фракционная экскреция натрия
рассчитывается следующим образом:
Э = Na выделенный * =
Na профитьтрованныи
UK„ X V X 100 UN РСг
= —------------= — X — X 100,
иСг X V иСг
+ X
Р.
где UNa и Uc, — концентрация натрия и креатинина
в моче, соответственно Рх>1 и РГг — их концентра-
ция в плазме или сыворотке. Поскольку объемы
мочи в числителе и знаменателе сокращаются
и «уходят» из формулы, фракционная экскреция
может быть рассчитана на основании определения
лишь концентрации натрия и креатинина в забо-
рах крови и мочи, взятых примерно в одно и то же
время.
Фракционная экскреция натрия. ФЭ№ обычно
меньше 1%, но может увеличиваться при повы-
шенном потреблении соли, при адаптации к хрони-
ческой почечной недостаточности и при введении
диуретиков. При снижении ренального перфузи-
онного давления, обычно характерном для гипово-
лемии и сердечной недостаточности, почки, адап-
тируясь к возникшим нарушениям, значительно
увеличивают канальцевую реабсорбцию натрия
и воды, в результате чего моча выделяется кон-
центрированная и в небольшом количестве. Таким
образом, ФЭК| < 1 % является физиологической
реакцией на уменьшение ренальной перфузии.
При ишемической ОПП ФЭ№ обычно > 2%.
При использовании ФЭН„ для дифференциаль-
ной диагностики между преренальной азотемией
НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК 75
и ОПН полученные данные могут быть недосто-
верны, если незадолго до исследования больной
получал диуретики. Преренальная азотемия может
развиться у пациентов с предшествующим хрони-
ческим почечным заболеванием, при уровне
ФЭ№> 1% как проявлении адаптации к хрониче-
ской почечной недостаточности- Когда у этих
больных имеется гиповолемия, то именно с ней
могут быть частично связаны повышенный уро-
вень мочевины и креатинина сыворотки и высокая
ФЭ№. ФЭХ<? так же, как и другие «диагностические
показатели», используемые при дифференциаль-
ной диагностике преренальной азотемии с ишеми-
ческой ОПН, не является патогномоничной ни для
одного, ни для другого из этих видов патологии.
Однако ФЭ^ дает очень важную информацию, ес-
ли анализируется в комплексе общей клинической
оценки.
Фракционная экскреция бикарбоната. Почеч-
ный тубулярный ацидоз (ПТА) —термин, опреде-
ляющий группу расстройств, при которых метабо-
лический ацидоз возникает в результате наруше-
ния реабсорбции профильтрованного НСО3 или
экскреции ионов водорода, при отсутствии суще-
ственного уменьшения СКФ." Обычно ПТА дол-
жен входит в перечень видов патологии, диффе-
ренцируемых у пациентов с метаболическим аци-
дозом, нормальной анионной разницей сыворотки
(гиперхлоремический метаболический ацидоз) и
при pH мочи выше 6,0. У пациентов с проксималь-
ным ПТА, развивающимся вследствие замедления
канальцевой реабсорбции НСО/, pH мочи может
быть меньше 6,0. когда концентрация НСО3
в плаз.ме ниже почечного порога его реабсорбции.
При IV типе ПТА (вариант дистальной формы)
метаболический ацидоз при нормальной анион-
ной разнице сыворотки сочетается с гиперкалие-
мией и кислой реакцией мочи (см. объяснение
дальше). Когда при проксимальном типе ПТА кон-
центрация в плазме НСО нормализуется адекват-
ным введением натрия бикарбоната, в дистальном
нефроне повышается содержание НСО3 и моча
становится высоко щелочной. Диагноз нарушения
проксимальной канальцевой реабсорбции HCOJ"
ставится при показателе ФЭ НСО3 выше 15%,
когда концентрация ПСО3 в сыворотке увеличена
до нормы. При обычной диете весь фильтруемый
НСО^ реабсорбируется и ФЭ НСО^" равна нулю.
PH мочи 6,2 нлн меньше говорит о том, что
содержание НСО^~ в моче совершенно незначи-
тельно.
РСО2 мочи или разница рСО2 мочи и крови
(U—В рСО2). Дистальный ПТА в его классиче-
ском варианте характеризуется гиперхлоремиче-
ским метаболическим ацидозом, pH мочи выше 6,0,
неизмененной или сниженной концентрацией HCOf
сыворотки и ФЭ НСО, <с5^>1гпри нормальном
уровне сывороточного НСО3. ' Причиной клас-
сического дистального ПТА является неспособ-
ность клеток нефрона секретировать Н в про-
свет канальцев, где при наличии НСО] образуется
угольная кислота (Н,СО3). Замедленное дегидра-
тирование Н2СО3 в медуллярных собирательных
протоках, почечной лоханке и мочевом пузыре
приводит к повышению рСО2 мочи, что характерно
для нормальной дистальной секреции Н , когда
содержание НСО3 в моче высокое (те. рСО2 мо-
чи >-80 мм рт. ст. или /U—В рСО2/> 30 мм
рт. ст.). Определение рСО2 мочи производится по-
сле введения одной дозы натрия бикарбоната (2—
3 ммоль/кг) или диакарба (17+2 мг/кг). Если
во время обследования уровень HCOf сыворотки
у больного значительно снижен, лучше использо-
вать нс диака рб, а натрия бикарбонат. Оценка
рСО2 мочи производится только после того, как pH
мочи превысит 7,4 и/или концентрация HCOj- бу-
дет больше 40 мэкв/л.
Тип IV ПТА (вариант дистального ПТА), со-
четающийся с низким pH мочи (<Г 6,0) и гиперка-
лиемией, при котором в дистальных канальцах
нарушена секреция как Н+, так и К*, связан с не-
способностью почек реабсорбировать натрий, что
благоприятствует развитию отрицательного потен-
циала в просвете канальцев или «вольтаж-зависи-
мого» дефекта. Данная форма из всех вариантов
ПТА наиболее часто встречается как у взрослых,
так и у детей. Отмечается при этом также и на-
рушение почечного синтеза аммония. Посколь-
ку при гиперкалиемии ингибируется аммониоге-
нсз, это приводит к снижению содержания ам-
мония, служащего буфером мочи и соответственно
к уменьшению pH мочи вместо снижения секреции
1Г (NH3 + Н+ = NH^). Тип IV ПТА физиологи-
чески является эквивалентом недостаточности аль-
достерона, которая может быть одной из причин
данной патологии. У детей этот тип ПТА бывает
проявлением истинного гипоальдостеронизма, но
намного чаще встречается при паренхиматозном
поражении почек, особенно при обструктивных
уропатиях. После ликвидации обструктивных рас-
стройств проявления ПТА IV типа уменьшаются
в течение нескольких недель или месяцев.
ЛЕЧЕНИЕ БОЛЬНЫХ С ПОСЛЕОПЕРАЦИОННЫМ
НАРУШЕНИЕМ ФУНКЦИИ ПОЧЕК
Патофизиология острой почечной недостаточ-
ности. ОПН характеризуется резким снижением
почечной функции. Поскольку причиной ее явля-
ется падение СКФ, то первичные клинические про-
явления заключаются в подъеме концентрации
мочевины и креатинина сыворотки и снижении диу-
реза. С повышением уровня неонатальной и педи-
атрической службы отмечается уменьшение часто-
ты ОПН, связанной с лекарственной терапией
и оперативными вмешательствами. Среди детей
с хирургической патологией нарушение функции
почек чаще всего отмечается после вмешательств
на сердце и легких.13’ 14
Наиболее важный фактор в патогенезе после-
операционной почечной недостаточности — умень-
шение почечной перфузии, которое в ранней своей
фазе приводит к падению СКФ. В ответ на ука-
занные нарушения увеличивается реабсорбция на-
трия и воды в канальцах. Это клиническое состоя-
ние определяется как преренальная азотемия.
76 НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК
Анализ мочи показывает высокую осмоляль-
ность > 300 мосм/кг Н2О, соотношение концен-
трации мочевины в моче и плазме >5 и концен-
трацию натрия в моче 20 ммоль/л. Наиболее
важный показатель канальцевой реакции на ре-
нальную гипоперфузию при интактной функции
почек — ФЭКо. Этот тест, однако, недостоверен, ес-
ли больной получал диуретики перед взятием мочи
на анализ. Когда при гипоперфузии функция поч-
ки не нарушена, показатель ФЭНл у доношенных
детей ниже 1%, а у недоношенных — меньше
2,5%.15 У большинства пациентов с преренальной
азотемией клинически достаточно четко отмечает-
ся гиповолемия. Однако у больных со сниженным
сердечным выбросом (насосная недостаточность)
клиническая оценка сниженной ренальной перфу-
зии иногда затруднена, поскольку масса тела
и ЦВД могут наводить на мысль о жидкостной
перегрузке. Явными признаками снижения «эф-
фективного» внутриартериального объема являют-
ся уменьшение АД, тахикардия и замедленное на-
полнение капилляров.
Преренальная азотемия может быть корригиро-
вана за счет улучшения ренальной перфузии, вос-
полнения внутрисосудистого объема жидкости, ли-
бо повышения сердечного выброса. Восстановление
функции почек проявляется в увеличении диуреза
и нормализации концентрации мочевины и креати-
нина сыворотки. Однако при длительно существу-
ющей гипоперфузии или при воздействии каких-
либо нефротоксических факторов может развиться
паренхиматозная почечная недостаточность. К
факторам, предрасполагающим к возникновению
ОПН, могут быть отнесены врожденные аномалии
почек и мочевыделительной системы, септицемия,
гипоксемия, гемолиз, рабдомиолиз, гиперурикемия,
применение некоторых токсичных лекарств и
рентгеноконтрастных веществ.
Лекарственное лечение. Ребенок с послеопера-
ционной олигурией и повышенной концентрацией
креатинина в сыворотке должен быть оценен на
предмет возможной преренальной азотемии. Если
у больного выявлена гиповолемия, то, как пра-
вило, внутривенно быстро вводят 20 мл/кг фи-
зиологического раствора или плазмы. Однако
в большинстве случаев физиологически выгоднее
вводить раствор, содержащий бикарбонат в количе-
стве 25—40 ммоль/л анионов в жидкостном болю-
се (1/2 изотонического раствора в 5% глюкозе
с добавлением 25—40 ммоль/л 1 М NaHCOj). Ес-
ли ребенок не отреагировал на терапию и остается
все еще дегидратированным, указанная доза может
быть введена повторно. Когда в ответ на восполне-
ние жидкости появился достаточный диурез, ребе-
нок должен продолжать получать поддерживаю-
щую инфузионную терапию с тщательным мони-
торингом. Необходимо постоянно контролировать
массу тела, диурез, концентрацию мочевины, креа-
тинина и электролитов в сыворотке.
Если после введения жидкостного болюса диурез
остается неадекватным, следует добавить внутри-
венно фуросемид в дозе 1 мг/кг. При почечной
недостаточности могут потребоваться более высо-
кие дозы — до 5 мг/кг. При отсутствии реакции
на первое введение фуросемида, вторая, более вы-
сокая доза, может быть введена через 1 час. В не
которых случаях для поддержания достаточного
диуреза необходимо вводить фуросемид каждые
4—8 час. У’ пациентов с олигурией после кардио-
логических операций в ряде клиник успешно ис-
пользовался метод постоянной инфузии фуросеми-
да в количестве 0,1 мг/кг/час с увеличением дозы
на 0.1 мг через 2 часа, если объем мочи оставался
.меньше 1 мл/кг/час.”’ Максимальная лоза состав-
ляет 0,4 мг/кг/час.
Очень важен тщательный контроль жидкостно-
электролитного статуса. При отсутствии реакции
на фуросемид существует опасность перегрузки
больного жидкостью. Переусердствование в отно-
шении инфузионной терапии во время наркоза
и операции и частое введение больших жидкост-
ных объемов для лечения длительной гипоперфу-
зии, с одной стороны, и уменьшенный диурез —
с другой, могут привести к гиповолемии, гипертен-
зии, сердечной недостаточности и отеку легких.
В некоторых случаях количество жидкости должно
быть уменьшено до того минимума, который не-
обходим лишь для введения лекарственных препа-
ратов. В менее тяжелых случаях при нарушении
функции почек у больных с нормоволемией общая
жидкостная нагрузка должна состоять из суммы
нечувствительных потерь воды, диуреза и суще-
ственных экстрарснальных потерь жидкости. Диу-
рез необходимо измерять и отмечать ежечасно,
а эффективность жидкостной терапии оценивать
клинически каждые 4—12 час. Важную информа-
цию об общем жидкостном балансе пациента дает
тщательный мониторинг АД, пульса и массы тела.
Измерение этих показателей до операции служит
основой, исходными данными для послеоперацион-
ной оценки динамики. В идеале гемодинамический
статус больного должен оцениваться с помощью
центральной венозной линии и измерения ЦВД.
У кардиологических больных с осложненным тече-
нием заболевания следует использовать катетер
Swan-Ganz для измерения давления заклинивания
в легочной артерии.
Гинергидратация может вести к гипонатриемии.
Поскольку в большинстве случаев общий нат-
рий в организме остается нормальным или высо-
ким, лучший путь нормализовать концентрацию
натрия в сыворотке — ограничить жидкостную на-
грузку и увеличить диурез. У пациентов с острой,
проявляющейся клинически, гипонатриемией осто-
рожная инфузия 3% раствора натрия хлорида
(512 ммоль Na/л или 0,5 ммоль/мл) может способ-
ствовать коррекции гипонатриемии. Быстрое вве-
дение со скоростью 1—2 ммоль/час в течение 2—
3 час с увеличением уровня натрия в сыворотке на
4—6 ммоль/л является адекватным и обычно хо-
рошо переносится больными. Инфузия 3% натрия
хлорида в дозе 6 мл/кг увеличивает концентра-
цию натрия в сыворотке примерно на 5 ммоль/л.
Длительная гипонатриемия, продолжающаяся бо-
лее 24—48 час, не должна быть корригирована со
скоростью большей, чем 0,5 ммоль/час.
НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК 77
ТАБЛИЦА 5-4. Лечение гиперкалиемии
Кардиальная защита
Глюконат кальция 10%, 0,5 мл/кг вн/в медленно в течение
5—10 мин с постоянным измерением частоты сердечных со-
кращений
Перемещение калия во внутриклеточное пространство
Натрия бикарбонат, I—2 ммоль/кг вн/в в течение 10 20 мин,
при условии, что нет солевой и водной перегрузки
Глюкоза 1 r/кг и инсулин 1 ЕД на каждые 4 г глюкозы вн/в
в течение 20—30 мин
Стимуляторы В2 — адренергических рецепторов (напр., сальбу-
тамол) вн/в или в виде ингаляций
Удаление избытков калия
Катионообменная смола, натрия полистирол сульфонат, I г/кг
орально или ректально в 20 30% сорбитоле или 10% глю-
козе, 1 г смолы/4 мл
Дополнительно, при появлении запоров. 70% сироп сорбитола
Диализ, перитонеальный или гемодиализ
У детей с ОПН часто развивается гиперкалие-
мия. Высокий уровень калия в сыворотке отрица-
тельно воздействует на сердечную деятельность
с ранним появлением признаков кардиотоксично-
сти, что отражается на ЭКГ в виде подъема зуб-
ца Т. Дальнейшее повышение уровня калия может
вызвать фибрилляцию желудочков и остановку
сердца. Принципы лечения гиперкалиемии у па-
циентов с ОПН представлены в таблице 5-4. Не-
отложная быстрая коррекция гиперкалиемии пока-
зана в тех случаях, когда концентрация калия
в сыворотке достигает 7,0 ммоль/л или при по-
явлении изменений на ЭКГ.
У детей с ОПН быстро развивается метаболи-
ческий ацидоз, поскольку в связи со снижением
функции почек выделяется меньше водородных
ионов. Накапливающиеся в организме органиче-
ские кислоты вызывают затем уменьшение концен-
трации бикарбоната в сыворотке. Если ребенок нс
имеет при этом дыхательных расстройств, то он
может самостоятельно достичь частичной компен-
сации путем гипервентиляции. Однако при нали-
чии нарушений функции легких или гиперкатабо-
лическом состоянии имеется риск тяжелого ацидо-
за. Лечение метаболического ацидоза обычно про-
водится введением натрия бикарбоната, при этом
важно не передозировать натрий. Поскольку у
многих пациентов с ОПН развивается также гипо-
кальциемия, то при лечении щелочными препара-
тами следует не допустить гипокальциемических
судорог. Для того, чтобы предотвратить неблаго-
приятное воздействие на организм ацидемии,
обычно нет необходимости в полной коррекции ме-
таболического ацидоза. Достаточно бывает, как
правило, увеличения концентрации бикарбоната
сыворотки до 15 ммоль/л.
Диализ. При отсутствии эффекта от медикамен-
тозного лечения водно-электролитных расстройств
или нарушений кислотно-основного равновесия,
вызванных почечной недостаточностью, следует
проводить диализ.
Показания к экстренному диализу:
Длительная олигоанурия
Гиперкалиемия
Метаболический ацидоз
Жидкостная перегрузка
Тяжелые электролитные расстройства и на-
рушения обмена минералов
Уремический синдром
Наиболее частым показанием для диализа у де-
тей в послеоперационном периоде является гипер-
волемия, вызванная инфузионной реанимационной
терапией, введением различных медикаментозных
препаратов и тотальным парентеральным питани-
ем. Повторные интенсивные (сильной струей) про-
мывания катетера и лаваж эндотрахеальной труб-
ки могут добавить значительное количество воды
и растворимых веществ к общей жидкостной на-
грузке.18 Перегрузка жидкостью после операции
может вызвать у больного отек легких и, реже,
гипертензию.
Данный метод лечения включает три варианта:
гемодиализ, гемофильтрацию и перитонеальный
диализ. Последний наиболее часто используется
у детей. Его эффективность определяется несколь-
кими внутренними факторами, такими как перито-
неальный кровоток и сосудистая проницаемость,
а также величиной поверхности брюшины.19 В то
время как удаление до 50% перитонеальной по-
верхности (при резекциях) не отражается сущест-
венно на эффективности диализа,20 гипоперфузия
перитонеальной мембранной сосудистой сети эту
эффективность резко снижает.21 * * Диализ у больных
после операции осуществим, даже при наличии пе-
ритонита, а также в ранние сроки (сразу) после
больших хирургических вмешательств на брюш-
ной полости. Увеличение внутрибрюшного дав-
ления при введении диализной жидкости может
вызвать нарушения дыхания и способствовать под-
теканию жидкости через хирургические разрезы
и место входа перитонеального катетера. В таких
случаях используются катетеры самых маленьких
размеров. С увеличением сроков, прошедших по-
сле операции, катетеры могут быть заменены на
более широкие. К наиболее частым осложнениям,
связанным с перитонеальным диализом, относятся
перитонит, инфекция места постановки катетера,
подтекание диализата, закупорка катетера, грыжи
брюшной стенки и очень редко перфорация орга-
нов брюшной полости.24
Раствор диализата с 1,5% концентрацией глю-
козы имеет осмоляльность 350 мосм/кг Н2О. буду-
чи. следовательно, умеренно гипертоничным по от-
ношению к нормальной плазме (280—295 мосм/кг
Н2О). С увеличением концентрации глюкозы в диа-
лизном растворе осмотическое давление повыша-
ется, достигая 490 мосм/кг Н2О при концентрации
глюкозы 4,25% —максимальная концентрация го-
товых растворов. При прочих равных условиях,
чем выше осмотическое давление диализата, тем
больше объем ультрафильтрата (жидкость, удаляе-
мая из организма). В связи с быстрым прохождени-
ем воды и глюкозы через перитонеальную мембра-
ну, эффект перитонеального диализа в отношении
удаления жидкости из организма максимальный
в том случае, когда проводятся кратковременные
78 НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК
сеансы диализа продолжительностью 20—30 мин.
При использовании растворов с концентрацией
глюкозы выше 1,5%, необходим тщательный конт-
роль уровня глюкозы в сыворотке. Если развива-
ется гипергликемия с уровнем глюкозы выше
11 ммоль/л. следует добавить инсулин либо к диа-
лизному раствору, либо вводя его внутривенно ка
пельно. Объем жидкости, удаляемой при диализе
за сутки, нс должен превышать 500 мл у новорож-
денного, 1000—1500 мл — у маленьких детей и
3000 мл — у больных с МТ больше 30 кг.23 Эффек-
тивность диализа в отношении удаления раство-
ренных веществ зависит в основном от длительно-
сти стояния катетера в брюшной полости и моле-
кулярного веса вещества. Следующие сравнитель-
ные скорости диффузии характерны для наиболее
распространенных веществ: мочевина > калий >
> натрий > креатинин > фосфор > мочевая кис-
лота > кальций > магний/’ Стандартный диализ-
ный раствор не содержит калия. Поэтому коррек-
ция гиперкалиемии может быть достигнута за
несколько часов эффективного перитонеального
диализа.
ОСТРАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ
У НОВОРОЖДЕННЫХ
Следующее определение олигурической почечной
недостаточности у новорожденных является обще-
принятым:
1. Диурез ниже 1 мл/кг/час в течение более,
чем 24 часа.
2. Отсутствие увеличения диуреза в ответ на
жидкостную нагрузку
3. Сочетание двух предыдущих факторов с уров-
нем креатинина в сыворотке выше 130 ммоль/л.27
Хотя у большинства маленьких детей с ОПН
диурез снижен, однако у некоторых больных при
нормальной скорости мочеотделения отмечается
задержка растворенных веществ, что отражается
в подъеме уровня креатинина в сыворотке (неоли-
гурическая почечная недостаточность). Частота
олигурической ОПН у новорожденных колеблется
от 1 до 6% среди всех пациентов отделений интен-
сивной терапии. Причины ОПН традиционно
делятся на 3 группы: преренальные, ренальные
и постренальные (табл. 5-5). Данное деление,
основанное на локализации поражения, имеет важ-
ное значение, поскольку оценка, лечение и про-
гноз в этих трех группах могут быть совершенно
различными.
Преренальная острая почечная недостаточ-
ность. Наиболее частая причина ОПН в периоде
новорожденности — нарушение ренальной перфу-
зии, встречающееся у 70% детей с олигурией.28
Преренальная ОПН может возникнуть при любой
клинической ситуации, когда имеется гипоперфу-
зия почки, нормальной во всех других отношениях.
Хотя быстрая коррекция состояния низкой перфу-
зии обычно восстанавливает почечную функцию,
однако, при несвоевременно начатой инфузионной
терапии может развиться паренхиматозное пора-
жение почки.
ТАБЛИЦА 5-5. Этиология острой почечной недостаточности
у новорожденных
Преренальные причины
I. Уменьшенный объем плазмы; кровотечение, дегпдратяция,
сепсис
2. Другие причины ренальной гипоперфузии: гипоксия, респи-
раторный дистресс-синдром, застойиаи сердечная недостаточ-
ность, шок
Ренальные причины
1. Врожденные аномалии почек: днусгоронняя агенезия, двусто-
ронний мультикистоз (дисплазия), поликистоз
2. Сосудистые поражения: тромбоз почечной артерии или вены
3. Ишемические: шок, кровотечение, дегидратация, сепсис, ги-
поксия, респираторный дистресс-синдром
4. Нефротоксические: аитнбиотики-аминогликозиды
5. Мочевая кислота: гнпсруриксмия новорожденного
Постренальные причины
1. Двусторонняя обструкция: клапан задней уретры, гравма
уретры, врожденный фимоз, дивертикул уретры, нейроген-
ный мочевой пузырь, синдром мегацистис мегауретер
2. Обструктивное поражение единственной функционирующей
почки: обструкция лоханочно-мочеточникового сегмента
Ренальная острая почечная недостаточ-
ность. При ренальной ОПН нарушение функции
почки связано с поражением паренхимы на кле-
точном уровне. Обычно это один из следующих
4 видов патологии: ишемия (острый канальцевый
некроз), нефротоксическое поражение (аминогли-
козиды), врожденные аномалии почек (поликис-
тоз), сосудистые нарушения (тромбоз почечной ар-
терии или вены, особенно единственной ночки).
Постренальная острая почечная недостаточ-
ность. Постренальная ОПН развивается при на-
личии препятствия току мочи из обеих почек или
из единственной почки. Наиболее частые причины
постренальной ОПН у новорожденных — клапан
задней уретры или двусторонняя обструкция пу-
зырно-мочеточникового сегмента.30 Хотя эти виды
обструкции обычно корригируемы, однако при
длительном внутриутробном их существовании мо-
гут развиться различной степени необратимые из-
менения почечной функции. ОПН возникает в ре-
зультате лежащей в ее основе аномалии, но, с дру-
гой стороны, уже имеющаяся ОПН может привести
ко вторичному поражению паренхимы.
Клинические проявления ОПН у новорожден-
ного проявляется клинически симптомами, харак-
терными прежде всего для лежащей в ее основе
патологии, например, сепсиса, шока, дегидратации,
тяжелого респираторного дистресс-синдрома и т. д.
Часто имеются и нсспецифические симптомы, свя-
занные с уремией, а именно — гипотрофия, резкая
вялость, рвота, судороги, гипертензия, анемия.
Диагностика. Оценка новорожденного с ОПН
должна начинаться с тщательного сбора анамнеза
как самого больного, так и семьи и осмотра. При
подозрении на преренальные причины острой оли-
гурии увеличение жидкостной нагрузки с фуросе-
мидом или без него имеет как диагностическое, так
и терапевтическое значение. Если в ответ на ука-
занные мероприятия диурез нс увеличился, необ-
ходимо дальнейшее более глубокое определение
функции почек.
НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК 79
Лабораторное исследование включает в себя
полный анализ крови, определение концентрации
в сыворотке мочевины, креатинина, электролитов,
мочевой кислоты, кальция и фосфора. Уровень
креатинина в сыворотке в течение первых несколь-
ких дней жизни ребенка соответствует материнско-
му, а после 1-й недели составляет у доношенного
новорожденного 35—44 ммоль/л.31 Наличие в мо-
че эритроцитов, белка, цилиндров характерно для
паренхиматозного поражения почек.
В дифференциальной диагностике ренальной по-
чечной недостаточноеги и преренальной азотемии
у больного с олигурией наиболее ценным показа-
телем является ФЭкп. Использование этого теста
основано на предположении, что почечные каналь-
цы плохо перфузируемой почки жадно реабсорби-
руют натрий, в то время как почка с паренхима-
тозным или канальцевым поражением неспособна
к реабсорбции натрия. Соответственно в большин-
стве случаев олигурической почечной недостаточ-
ности у новорожденных, развившейся на фоне ре-
нальных причин, показатель ФЭКа больше 2.5%.
ФЭ^, должна быть измерена до введения фуросеми-
да. Кроме того, у глубоко недоношенных детей,
которые и в норме имеют высокую ФЭК;1, результа-
ты этого теста следует интерпретировать с осто-
рожностью.
УЗИ является чрезвычайно ценным методом об-
следования, позволяющим определить размеры по-
чек, их форму и локализацию, а также расширение
выделительной системы и состояние мочевого пу-
зыря. При подозрении на клапан задней уретры
или пузырно-мочеточниковый рефлюкс показана
микционная цистоуретрография. Может понадоби-
ться и антеградная пиелография для выявления
обструкции уретеровезикального сегмента. Однако
снижение СКФ и канальцевой функции у новорож-
денных обусловливает плохую визуализацию по-
чек и мочевого тракта при внутривенной пиелогра-
фии в течение первых нескольких недель жизни.
Кроме того, некоторые рентгеноконтрастные веще-
ства обладают нефротоксичностью.32 Поэтому луч-
ше всего функцию почек обследовать с помощью
радиоизотопного сканирования, используя техне-
ЦИЙ-99ГП.
Лечение. Лечение ОПН у новорожденных дол-
жно производиться параллельно с диагностически-
ми мероприятиями. У детей с преренальной олигу-
рией жидкостная нагрузка с фуросемидом или без
него обычно увеличивает диурез и улучшает фун-
кцию почек. При клапане задней уретры необходи-
мо срочно поставить мочевой катетер, в то время
как при других обструктивных поражениях у ново-
рожденных может понадобиться «высокое» хирур-
гическое дренирование (нсфро- или уретеросто-
мия). Жидкостная нагрузка осуществляется из рас-
чета 20 мл/кг изотонического раствора, содержа-
щего 25 ммоль/л натрия бикарбоната с инфузией
указанного объема в течение 1—2 час. Если за это
время не восстанавливается достаточный диурез
(2 мл мочи или более на кг за 1—2 часа), показа-
но внутривенное введение фуросемида в дозе 2—
5 мг/кг. Отсутствие увеличения диуреза после
жидкостной нагрузки у новорожденного с нормаль-
ным сердечным выбросом (а значит, нормальной
ренальной перфузией) при отсутствии обструкции
мочевых путей говорит о наличии паренхиматоз-
ного поражения почек и требует соответствующего
лечения олигурической или анурической почечной
недостаточности.
Поддержание жидкостного баланса — основа ле-
чения больного с ОПН. Суточная жидкостная на-
грузка должна быть равна сумме нечувствитель-
ных потерь воды, диуреза и внепочечных потерь
жидкости. У доношенных детей нечувствительные
потери воды составляют 30—40 мл/кг/сут, в то
время как недоношенные дети могут потребовать
до 70 мл/кг/сут.33 При проведении жидкостной те-
рапии очень важно часто измерять массу тела но-
ворожденного. Электролитный состав вводимой
жидкости определяется данными регулярного лабо-
раторного обследования. Нечувствительные потери
воды не содержат электролитов, а потому должны
быть восполнены просто водным раствором глю-
козы.
В результате ОПН могут возникать такие серь-
езные вторичные нарушения, как гиперкалиемия,
гипонатриемия, гипертензия, гипокальциемия, ги-
перфосфатемия и метаболический ацидоз. Поэтому
у пациентов с ОПН прежде всего должны быть
исключены экзогенные источники поступления
в организм калия. Тем не менее у многих отмеча-
ется повышение уровня калия в сыворотке, что тре-
бует немедленного активного лечения во избежа-
ние кардиотоксического эффекта.34 При прогресси-
рующем росте концентрации калия в сыворотке
терапия должна начинаться с применения натрий-
калиевых ионообменных смол (натрия полисти-
рол-сульфонат в сорбитоле, 1 г/кг ректально
в клизме) (см. табл. 5-4). В неотложных ситуациях
для предотвращения или лечения уже возникшей
сердечной аритмии показано внутривенное введе-
ние натрия бикарбоната (1—2 ммоль/кг), 10%
раствора глюконата кальция (0,5 мл/кг) и глюко-
зы (0,5—1,0 г/кг) с последующим введением ин-
сулина (0,1- 0,2 ЕД/кг).
У детей с олигурией при гипергидратации могут
развиваться гипонатриемия и гипертензия, что
требует прежде всего ограничения жидкостной на-
грузки. Эффективным может быть применение вы-
соких доз фуросемида внутривенно (5 мг/кг). При
стойкой бессимптомной гипертензии добавляют
парентерально апрессин (0,25—0,5 мг/кг каждые
6 час). Если же упорные значительные подъемы
АД сопровождаются клиническими проявлениями,
внутривенно вводят диазоксид (5 мг/кг).
Гиперфосфатемия (уровень фосфора в сыворот-
ке больше 2 ммоль/л), которая часто бывает при-
чиной сочетанной с ней гипокальциемии, требует
использования молочных смесей с низким содер-
жанием фосфора (S-M-A, Симилак РМ 60/40 ),
а также кальция карбоната, связывающего фосфат
(50 100 мг/кг/сут).33 Применение с этой целью
(связывание фосфата) алюминия гидроокиси про-
тивопоказано в связи с токсичностью алюминия
у детей при почечной недостаточности36
80 НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК
В результате задержки водородных ионов может
развиться метаболический ацидоз, что требует
применения натрия бикарбоната. Его доза рассчи-
тывается следующим образом:
1 /2 (желаемый уровень бикарбоната — имеющийся) X
X МТ в кг X 0,5 = ммоль натрия бикарбоната.
Эта доза может быть применена орально или до-
бавлена к инфузионным растворам и введена в те-
чение нескольких часов.
Питание больного (внутривенное или энтераль-
ное) должно обеспечивать поступление 100—
120 калорий и 1 -2 г белка/кг/сут. Для новорож-
денных, усваивающих энтеральное питание, реко-
мендуются смеси с низким содержанием фосфора
и алюминия, такие как S-M-A или Симилак РМ
60/40. Активное проведение адекватного питания
в значительной мере способствует восстановлению
функции почек, обеспечивая необходимые энерге-
тические потребности на клеточном уровне.54
Хотя у большинства новорожденных с ОПН про-
водится консервативная терапия, тем нс менее
в редких случаях для лечения метаболических
осложнений жидкостной перегрузки может потре-
боваться перитонеальный диализ или длительная
артериовенозная гемофильтрафия (ДАВГ). Ле-
тальность в этой группе больных обычно превы-
шает 60%. В нашем госпитале за последние 6 лет
мы проводили перитонеальный диализ у 17 ново-
рожденных с ОПН В основном это были паци-
енты, перенесшие операцию на открытом сердце.
Хотя, по данным литературы, летальность у таких
больных составляет 90—100%, по нашему опыту
раннее начало перитонеального диализа и обеспе-
чение адекватного питания позволили снизить ле-
тальность в последнее время до 38%.
ОБСТРУКТИВНЫЕ УРОПАТИИ
Обструктивные уропатии у новорожденных наибо-
лее часто развиваются при наличии клапана зад-
ней уретры или обструкции лоханочно-мочеточ-
никового сегмента,30 требующих своевременной
диагностики и лечения во избежание поражения
функции почек. При уже возникших вторичных па-
ренхиматозных расстройствах изменения СКФ, ре-
нального кровотока и канальцевой функции могут
сохраняться, несмотря на хирургическое вмеша-
тельство и устранение обструкции.37 Поражение
почечных канальцев, в свою очередь, приводит
к потере почками способности реабсорбировать
натрий, концентрировать мочу и секретировать ка-
лий и водород. Каждое из этих функциональных
расстройств может иметь тяжелые клинические
проявления. Иногда нарушается также реабсорб-
ция и других растворенных веществ, таких как
магний, кальций и фосфор.
Возможность восстановления после устранения
обструкции способности канальцев реабсорбиро-
вать соли и воду зависит от того, была обструкция
одно- или двухсторонней. При одностороннем пора-
жении проксимальные канальцы юкстамедулляр-
ных нефронов не способны к реабсорбции солей
и воды, в то время как в поверхностных нефронах
фракционная реабсорбция солей и воды увеличи-
вается.” Однако благодаря поддержанию каналь-
цево-клубочкового баланса, количество натрия,
выделяемого почкой, которая имела обструкцию,
такое же, как и экскретируемое контрлатеральным
органом. И наоборот, устранение двухсторонней об-
струкции приводит к значительному увеличению
абсолютных показателей потерь натрия и воды.
Отчасти эти изменения являются результатом
осмотического диуреза, связанного с накоплением
мочевины.30 Имеет значение и влияние натрий-
уретического фактора, уровень которого в плазме
при наличии обструкции повышается.37 Снижение
реакции почечного мозгового вещества и гидроди-
намической проницаемости мочевых путей в ответ
па действие антидиуретического гормона способст-
вует поражению концентрационной способности
почек.3’
Описанные изменения проявляются симптомами
вторичного нефрогенного несахарного диабета
и гипонатриемической дегидратации. Соответст-
венно лечение следует направить на обеспече-
ние адекватной жидкостной и солевой нагрузки.
Количество назначаемой жидкости должно быть
равно сумме нечувствительных потерь, диуреза
и внепочечных потерь при постоянном контроле
и учете динамики массы тела. Нагрузка натрием
определяется показателями уровня электролитов
в сыворотке и моче.
Обструкция мочеточника может привести к на-
рушению секреции водорода и калия и синдрому
гиперкалиемического гиперхлоремического мета-
болического ацидоза или IV типу почечного тубу-
лярного ацидоза.40 Данные изменения являются
результатом сниженной реакции дистальных по-
чечных канальцев па воздействие альдостерона.
У части пациентов с подобными клиническими
проявлениями ФЭКв нормальная, а ФЭК снижена
непропорционально по отношению к высокому
уровню калия в сыворотке. Лечение должно быть
направлено на устранение хирургическим путем
аномалии, лежащей в основе обструкции, так же,
как и на обеспечение организма натрия бикарбона-
том для коррекции метаболического ацидоза и ги-
перкалиемии.
Устранение двухсторонней обструкции мочеточ-
ника у детей старшего возраста приводит к неспе-
цифическому повышению экскреции калия. Этот
эффект отчасти связан с увеличением поступления
натрия в дистальные канальцы, что ускоряет нат-
рий-калиевый обмен.41 Во избежание развития ги-
покалиемии необходим тщательный мониторинг
уровня калия в сыворотке для определения потреб-
ности в нем и адекватного проведения замести-
тельной терапии.
НАРУШЕНИЕ ФУНКЦИИ ПОЧЕК 81
ЛИТЕРАТУРА
I. Brenner ВМ. Dworkin LD. Kchikawa L: Glomerular ultrafiltrati-
on. hi Brenner BM. Rector FC Jr (Editors): The Kidney, 3rd
edition, volume 1, WB Saunders, Philadelphia, pp 124 144.
1986.
2. Hogg RJ, Stapleton FB: Renal tubular function, hi Holliday MA,
Barrall TM, Vernier Rl (Editors). Pediatric Nephrology, 2nd
edition. Williams & Wilkins, Baltimore, pp 59—77. 1987.
3. Yared A. Ichikawa I: Renal blood flow and glomerular filtration
rale. In Holliday MA, Barratt TM, Vernier Rl. (Editors). Pedi-
atric Nephrology. 2nd edition. Williams & Wilkins. Baltimore,
pp 45—58, 1987.
4. Holliday MA. Scgar WE: The maintenance need for water in
parenteral fluid therapy. Pediatrics 19:823—832, 1957.
5. Edelmann CM Jr. Barnett HL: Role of the kidney in water meta-
bolism in young infants. J Pediatr 56:154—179, 1960.
6. Polacek B. Voccl J. Ncugcbauerova L. et al.: The osmotic con-
centrating ability in healthy infants and children. Arch Dis
Child 40:291 295, 1965-
7. Chantler C, Barratt TM: Laboratory evaluation, hi Holliday
MA, Barratt RM, Vernier Rl. (Editors). Pediatric Nephrology,
2nd edition, Williams & Wilkins, Baltimore, pp 282—299. 1987.
8. Hellerstein S, Hunter JL. Warady BA: Creatinine excretion
rates for evaluation of kidney function in children. Pediatr Ne-
phrol 2:419 424, 1988
9. , Hellerstein S, Holliday MA. Grupe WE, et al.: Nutritional mana-
gement of children with chronic renal failure. Pediatr Nephrol
1:195—211. 1987.
10. Steiner RW: Interpreting the fractional excretion of sodium Am
J Med 77:699—702. 1984.
11. Halperin ML. Goldstein MB, Stinebaugh BJ, Richardson RM A:
Renal tubular acidosis. In Maxwell MH, Klceman CR. Narirts
RG (Editors). Clinical Disorders of Fluid and Electrolyte Meta-
bolism, 4th edition. McGraw-Hill, New York, pp 675—689,
1987.
12, Rodrigucz-Soriana J. Vallo A: Renal tubular acidosis. Pediatr
Nephrol 4:268 275, 199(1.
13. Rigden SPA, Barratt TM. Dillon MJ, et al.: Acute renal failure
complicating cardiopulmonary bypass surgery. Arch Dis Child
57:425—430. 1982.
14. Gomcz-Campadra FJ, Maroto-Alvaro E. Galinancs M. et al.:
Acute renal failure with cardiac surgery. Child Nephrol Urol
9:138 143, 1989.
15. Siegel NJ, Gaudio KM: Pathogenesis and treatment of acute
renal failure. Pediatr Clin North Am 34:771—787, 1971.
16. Singh N, Kissoon N, AI-Mofada S, et al.: Furosemide infusion
versus furosemide bolus in the postoperative pediatric cardiac
patient. Pediatr Res 27:35A, 1990.
17. Feld LG, Cachero S. Springate JE: Fluid needs in acute renal
failure. Pediatr Clin North Am 37:337—350. 1990.
18. Noble-Jamieson CM. Kuzim P. Airede KI: Hidden sources of
fluid and sodium intake in ill newburns. Arch Dis Child
61:645—696, 1986.
19. Gruskin AB, Morgenstern BZ, Perlman S: Kinetics of peritoneal
dialysis in children, hi Fine RN. Grustin AB (Editors). En
Stage Renal Disease in Children. WB Saunders. Philadelphia,
pp 95—117. 1984,
20. Alon U, Bar-Maor JA, Ваг-Joseph G: Effective peritoneal dialy-
sis in an infant with extensive resection of the small intestine.
Ain J Nephrol 8:65—67, 1988.
21. Erbe RW, Greene J A Jr, Weller JM: Peritoneal dialysis during
hemorrhagic shock. J A ppi Physiol 22:131 —135, 1967.
22. Fine RN: Peritoneal dialysis update. J Pediatr 100:1—7, 1982.
23. I'zamaloukas AH, Garclla S, Chazan JA: Peritoneal dialysis for
acute renal failure after major abdominal surgery. Arch Surg
106:639—643. 1973.
24. Matthews DF, West KW, Rescoria FJ, et al.: Peritoneal dialysis
in the first 60 days of life. J Pediatr Surg 25:111 —116, 1990.
25. Chan JCM: Peritoneal dialysis for renal failure in childhood:
clinical aspects and electrolyte changes as observed in 20 cases.
Clin Pediatr 17:349 354. 1978.
26. Miller RB. Tassistro CR: Peritoneal dialysis. New Engl J Med
17:945—948. 1969.
27. Stapleton FB, Jones DP, Green RS: Acute renal failure in neona-
tes: incidence, etiology and outcome. Pediatr Nephrol 1:314
320, 1987.
28. Norman ME. Asadi FK: A prospective study of acute renal failu-
re in the newborn infant. Pediatrics 63:475—479. 1979.
29. Chevalier RL. Campbell F. Norman A, Brcnbridgc AG: Prognos-
tic factors in neonatal acute renal failure. Pediatrics 74:265
272. 1984.
30. Elder JS. Duckett JW: Management of the fetus and neonate
with hydronephrosis delected by prenatal ultrasonography. Pe-
dialr Ann 17:19—28. 1988.
31. Feldman H. Guignard J-P: Plasma creatinine in the first month
of life. Arch Dis Child 57:123—126, 1982.
32. Gruskin AB. Oetliker O. Wolfish NM. et al.: Effects of angi-
ography on renal function and histology in infants and piglets.
J Pediatr 76:41—50, 1970.
33. Roy NR, Sinclair JC; Hydration of the low birth weight infant.
Clin Pcrinatol 2:393—410. 1975.
34. Gaudio KM, Siegel NJ: Pathogenesis and treatment of acute
renal failure. Pediatr Clin North Am 34:771—787, 1987.
35. Alon U, Davidai G. Bcntur L. el al.: Oral calcium carbonate as
phosphate binder in infants and children with chronic renal
failure. Miner Electrolyte Mct«ib 12:320—325. 1986.
36. Scdnuin AB, Miller NL, Warady BA. cl al.: Aluminum loading in
children with chronic renal failure. Kidney Int 26:201 204.
1984.
37. Klahr S. Harris K. Purkcrson ML: Effects of obstruction on
renal functions. Pediatr Nephrol 2:34—42. 1988.
38. Harris RH, Yarger WE: The pathogenesis of postobsiructive
diuresis: the role of circulating natriuretic and diuretic factors,
including urea. J Clin Invest 56:880 887. 1975.
39. Hanley MJ, Davidson K: Isolated nephron segments from rabbit
models of obstructive nephropathy. J Clin Invest 69:165—174.
1982.
40. Rodriguez-Soria no J, Vallo A, Oliveros R, Castillo G: Transient
pscudohypoaldostcronism secondary to obstructive uropathy in
infancy. J Pediatr 103:375—380, 1983.
41. Yarger WE, Buerkeri J: Effect of urinary tract obstruction on
renal tubular function. Semin Nephrol 2:17—30. 1982.
6 Заказ № 1622
Глава 6
ЭТИЧЕСКИЕ ПРОБЛЕМЫ
В ДЕТСКОЙ ХИРУРГИИ
* Следует ли воздерживаться от экстракорпо-
ральной мембранной оксигенации у ребенка
с диафрагмальной грыжей, если у него, кроме
того, синдром Дауна?
* Следует ли принимать во внимание нежелание
12-летнего ребенка подвергнуться почечному
диализу?
* Имеют ли право родители 500-граммового но-
ворожденного с тяжелыми аномалиями потре-
бовать полноценного жизнеобеспечения с
применением всех реанимационных меропри-
ятий?
* Можно ли считать мозг ребенка с анэнцефа-
лией «умершим», чтобы на законных основа-
ниях взять его органы для пересадки?
* Следует ли накладывать гастростому ребенку
с декортикацией?
* Не следует ли сделать платными плановые не-
большие операции при некоторых видах пато-
логии, например таких, как грыжи, косогла-
зие, для того, чтобы государственная казна,
обладающая скудными возможностями, сэко-
номленные таким образом деньги могла выде-
лить на обеспечение пересадок печени и
сердца?
По мере того, как в хирургии появляются новые
современные технические и иные возможности, по-
зволяющие вылечивать все более сложных боль-
ных, врачи все чаще сталкиваются с этическими
проблемами, порой запутанными и трудно решае-
мыми.
С V-ro века до нашей эры вплоть до настоящего
времени основой, определяющей отношения между
врачом и больным, а также коллегами, остается
клятва Гиппократа, в которой отражены главные
этические принципы — «делай хорошо» и «не на-
вреди». В XVIII и XIX веках представления о вра-
че и его деятельности получили дальнейшее разви-
тие в этическом кодексе, принятом в Англии, а за-
тем в аналогичном кодексе, принятом Американ-
ской Медицинской Ассоциацией (АМА) при ее
основании в 1846 г. Эти кодексы, господствовав-
шие в медицине вплоть до XX века, были направ-
лены на то, чтобы свести к минимуму конфликты
в различных ситуациях, довольно своеобразно
и однозначно определяя роли и ответственность
врача и больного: врач назначает лечение, а боль-
ной лишь беспрекословно следует этим назначе-
ниям.
Главенствующее, «родительски-покровител вет-
венное» отношение врача к больному, закреплен-
ное в этих кодексах, постепенно менялось на более
уважительное, когда за больным стало признавать-
ся преимущественное право на решение вопроса
о лечении. Более современные кодексы этических
принципов, включая кодекс АМА, не только пред-
писывают врачу «помоги» и «не навреди», но
и учитывают право больного на участие в решении
различных вопросов, связанных с лечением.
Право взрослого человека на принятие самосто-
ятельного решения было в последующем закрепле-
но в виде легальных прав, краеугольным камнем
которых является право больного на полноценную
информацию и основанное на ней согласие. Запад-
ное общество достигло в этом отношении значи-
тельного прогресса, утвердив ряд положений в
многочисленных юридических формах и законах.
Права «недееспособных» пациентов, таких, как
больные, находящиеся в коматозном состоянии или
со старческим слабоумием, менее четко очерчены.
Однако выводы, сделанные в результате ряда су-
дебных расследований в подобных ситуациях, по-
зволили и для таких больных принять законополо-
жения, учитывающие завещание больного и выска-
зывавшиеся им ранее пожелания, что часто упро-
щает механизм принятия медицинских решений
и в таких непростых случаях.
Намного более сложные этические проблемы по-
добного рода возникают перед педиатрами и дет-
скими хирургами. Механизм принятия медицин-
ских решений в отношении детей и младенцев ча-
сто далек от оптимального уровня, несмотря на
продолжающиеся постоянные попытки многих спе-
циалистов, включая профессионалов в области
биоэтики, усовершенствовать этот процесс.
ЭТИЧЕСКИЕ ПРОБЛЕМЫ В ДЕТСКОЙ ХИРУРГИИ 83
Чем отличается принятие медицинского решения
в отношении детей и младенцев от этой же ситуа-
ции в отношении взрослых? Главное различие со-
стоит в том, что взрослый, в противовес ребенку,
имеет юридическое право согласиться или нс со-
гласиться на избранный метод лечения, а также
обладает возможностью заставить врачей принять
его мнение во внимание. Врачи, в свою очередь,
имеют право отказаться проводить лечение, вы-
бранное пациентом, но, с точки зрения врача, не-
целесообразное (в данном случае), либо нелегаль-
ное, либо не являющееся лучшим в конкретной
ситуации. Право взрослых иметь собственный вы-
бор в отношении лечения ценится и уважается все-
ми слоями нашего общества, независимо от куль-
туры, религии и социального положения.
Поскольку западное общество не считает детей
дееспособными личностями, за исключением юри-
дически самостоятельных подростков, медицинское
решение в отношении ребенка обычно принимается
родителями либо опекунами, которые, естественно,
практически всегда действуют в интересах детей.
Этические принципы, с учетом которых принима-
ется медицинское решение в отношении детей, за-
креплены в своде принципов медицинской этики
Американской Ассоциации Детских Хирургов, где
членам Ассоциации предписывается «... выбирать
из равно эффективных методов те, которые наиме-
нее сложны, наименее болезненны, наименее доро-
гостоящи...». Обязанность родителей или опекунов
ребенка — чтить эти принципы, выбирая из пред-
ложенных именно тот метод лечения, который наи-
лучшим образом отвечает интересам ребенка. Если
«интересы ребенка» положить в основу механизма
принятия решения педиатрами и детскими хирур-
гами, то возникают два практических вопроса. Как
в каждой конкретной ситуации определить, каковы
же эти самые «интересы ребенка»? Кому может
быть доверено представлять эти интересы?
К счастью, для детских хирургов, большинство
«сценариев» течения болезни, как правило, относи-
тельно просты (диагностика — операция — выздо-
ровление) и не связаны с этическими конфликта-
ми. При этом обычно совершенно ясно, что необхо-
димо делать в интересах ребенка (ликвидировать
трахеопищеводный свищ, удалить аппендикс,
устранить кишечную непроходимость), и соответст-
вующее принятие решения несложно и очевидно
для матери и отца при консультации с врачом
и в содружестве с ним. Однако в последние годы,
вместе с изменением отношения нашего общества
к ребенку, который стал восприниматься как лич-
ность с соответствующими правами, сложность
этических проблем неуклонно возрастает. Это свя-
зано в значительной мере с внедрением и успеш-
ным применением новых технологий. Указанные
проблемы постоянно возникают в больницах и за-
лах суда, ими бывают заполнены страницы печат-
ных изданий. В результате стали подвергаться со-
мнению прежние основополагающие представле-
ния о том, что же такое «интересы ребенка» и кто
должен быть защитником этих интересов.
Невозможно представить здесь во всей глубине
множество этических дилемм, которые возникают
в настоящее время перед детскими хирургами как
в теоретической сфере, так и в клинической прак-
тике. Можно лишь проиллюстрировать, как при
обсуждении некоторых, наиболее сложных, вопро-
сов возникает ряд трудностей, связанных с необхо-
димостью соблюдения этических принципов в об-
ществе, где спектр мнений может колебаться
в огромном диапазоне. Анализ с точки зрения эти-
ки сложных спорных вопросов часто приводит
к рекомендациям действий, диаметрально противо-
положных. и хотя в каждом решении соблюдены
этические принципы, но приоритеты везде различ-
ны, в частности, например, религиозные и обще-
ственные.
Всегда ли осуществление жизнесохраняющих
операций при атрезии пищевода или кишечника
соответствует интересам новорожденного? Ответы
на этот вопрос детских хирургов, юристов и роди
телей варьируют от безоговорочного «да» до
условного «нет». Второе мнение может быть осно-
вано на том, что при наличии сопутствующей па-
тологии, тяжелой или инкурабельной, осуществле-
ние жизнесохраняющих вмешательств не всегда
соответствует интересам ребенка, а потому с эти-
ческой точки зрения не показано. Существуют аб-
солютно противоположные взгляды на эту пробле-
му. Одни считают, что «всякое живое существо»,
независимо от того, полноценно оно или нет. дол-
жно быть спасено. Другие придерживаются иной
точки зрения. Эти диаметральные представления
отражены в упрощенной формуле «неприкосновен-
ность жизни или качество жизни?» и «право жить
или право умереть?». Упрощение сложных этиче-
ских вопросов до этой простейшей формулы отра-
жает полярные позиции, исключая огромный
спектр промежуточных ситуаций, в котором как
раз и лежат обычно совершенно особые индивиду-
альные интересы каждого конкретного больного
ребенка.
Хотя решение в пользу операции у новорожден-
ного с пороками развития или против нее всегда
принималось родителями на основании совета вра-
чей, этот процесс существенно изменился после
того, как общественному вниманию были пред-
ставлены этические дилеммы неонатальной хирур-
гии, связанные со случаем Baby Doe. Это была
новорожденная девочка с атрезией пищевода и
синдромом Дауна, которая родилась в 1982 году.
Родители и врач решили отказаться от операции,
и девочка умерла. Данный случай заставил Депар-
тамент Здоровья обратиться к Правительству
США с требованием вмешательства в националь-
ную неонатальную службу для постановки вопроса
о защите гражданских прав больных новорожден-
ных. Впоследствии, когда представление Департа-
мента Здоровья не было поддержано Верховным
Судом, Конгресс США все-таки настоял на введе-
нии в национальное законодательство ряда поло-
жений об ущемлении прав ребенка, которые были
включены в государственную программу обеспече-
ния заботы о детях. Согласно государственным за-
конам «Baby Doc» отказ от жизнеспасающих one-
84 ЭТИЧЕСКИЕ ПРОБЛЕМЫ В ДЕТСКОЙ ХИРУРГИИ
раций у новорожденных возможен только лишь
в одной из следующих трех ситуаций:
1. Ребенок длительно находится в необратимо
коматозном состоянии.
2. П танируемая операция может лишь отсро-
чить летальный исход, либо направлена на коррек-
цию только одного из нескольких сочетанных жиз-
неопасных видов патологии.
3. Операция заведомо не обеспечит выживания
ребенка, а, соответственно, лечение в таких обстоя-
тельствах было бы негуманным.
Дополнения к федеральному закону рекоменду-
ют образовывать в больницах наблюдательные ко-
митеты, которые следят за тем, как закрепленные
в законах принципы претворяются в жизнь. Вклю-
чение в круг людей, ответственных за принятие
решений, юристов, законодателей и представите-
лей комитетов по этике, а также гласность, несо-
мненно, обеспечивают принятие оптимальных ре-
шений.
Многие врачи считают вышеперечисленные кри-
терии, позволяющие отказаться от операции,
слишком ограниченными. Столь узкий перечень
противопоказаний к операции вынуждает прово-
дить лечение с реанимацией и поддержанием жиз-
ни во многих случаях, когда характер патологии
и логика врачебного мышления, основанная на
опыте, говорят о необходимости применения абсо-
лютно противоположных действий. Спорный во-
прос о том. должны ли всегда, у любого ребенка
проводиться питание и жидкостная терапия, как
предписывают правила «Baby Doe», или с этиче-
ской точки зрения можно подходить к этому из-
бирательно, вызывает очень бурные дебаты. В не-
которых случаях юристы разрешают прекращать
питание взрослых больных, находящихся в терми-
нальном состоянии, если они сами просили об этом
ранее, предвидя подобную ситуацию. Детские же
хирурги порой вынуждены соглашаться с требова-
ниями постановки центрального венозного катете-
ра или осуществления гастростомии, даже с фун-
допликацией, чтобы продлить существование ре-
бенка, у которого давно отсутствуют минимальные
проявления функции коры головного мозга.
Значительные достижения жизнеобеспечиваю-
щих технологий, таких как парентеральное пита-
ние, экстракорпоральная мембранная оксигенация,
трансплантация, помогают продлевать жизнь боль-
ным и улучшать ее качество, но одновременно
и усложняют многие вопросы для детских хирур-
гов. Особенно трудно в настоящее время выбрать
из многочисленных критериев те, которые необхо-
димо учитывать, чтобы принять наилучшее реше-
ние, оптимальное и в этическом отношении. Слож-
ность усугубляется еше и тем, что, согласно афо-
ризму, наилучший в этическом плане совет можно
дать только в том случае, когда знаешь на основа-
нии «фактов», как этот совет подействует. Однако
в каждой конкретной ситуации сначала дается со-
вет, а потом уже появляются «факты», и никогда
с уверенностью нельзя сказать, каковы будут ре-
зультаты следования этому совету. Трудности ре-
шения этических проблем бывают связаны еще
и с тем, что наравне с общепринятыми традици-
онными методами лечения существуют новые, по-
рой лучшие, но не утвердившиеся в практике,
а потому являющиеся в какой-то степени «экспе-
риментальными». Представляя родителям ребенка
информацию о его состоянии, на основании кото-
рой они принимают решение, врач должен быть
абсолютно честен, говоря не только о риске и про-
гнозе, но и о том, является ли данный метод лече-
ния условно традиционным или новым, экспери-
ментальным. К сожалению, нередко требуется
очень много времени для того, чтобы новый про-
грессивный метод лечения, довольно широко уже
применяемый в жизни, стал официально обще-
признанным.
В большинстве стран законы по защите прав
ребенка неудачный выбор лечения вменяют в вину
родителям, считая, что именно они должны были
обеспечить использование наиболее эффективных
методов лечения. Однако истории известны слу-
чаи, когда попытки некоторых религиозных и
культовых групп отказываться от медицинского
лечения, подменяя его нетрадиционными метода-
ми непроверенной эффективности, приводили не
только к инвалидности, но и к смерти детей.
Возлагая главную ответственность на родителей,
судебные органы тем не менее традиционно благо-
склонно относятся к докторам, которые по жизнен-
ным показаниям назначают трансфузии крови де-
тям, несмотря на возражения (по религиозным мо-
тивам — Свидетелей Иеговы) их родителей. И все
же в большинстве государственных законов о за-
щите прав ребенка существуют статьи, освобожда-
ющие от ответственности родителей в тех случаях,
когда неудачный результат лечения ребенка был
связан с применением, по религиозным мотивам,
нетрадиционных методов, и даже в случаях отказа
родителей от жизнсспасающих операций по тем
же мотивам. Американская Педиатрическая Ака-
демия твердо настаивает на необходимости исклю-
чения из законов подобных статей. Правда, статьи
такого рода не защищают родителей в том случае,
если их ребенок умирает при оказании помощи
религиозными целителями, использующими кри-
минальные методы, что иллюстрируется случаем,
происшедшим в Бостоне в 1990 г. Родители-хри-
стиане ребенка, который умер от кишечной непро-
ходимости после того, как его лечил религиозный
целитель, были осуждены за непредумышленное
убийство.
Некоторые специалисты по этике все больше
поднимают голос за участие детей в принятии ре-
шения о их лечении в виде согласия самого ребен-
ка, признавая и уважая возрастающую по мере
взросления способность ребенка к принятию реше-
ний. Это предложение, широко поддерживаемое
в том, что касается его сути, находит, однако, про-
тивников среди тех, кто считает, что такой подход
может быть вредным для отношений в семье, уве-
личивая самостоятельность ребенка в ущерб авто-
ритету родителей. В любом случае пока не ясно,
как в условиях детской хирургии должна «рабо-
тать» эта концепция согласия самого ребенка. Вряд
ЭТИЧЕСКИЕ ПРОБЛЕМЫ В ДЕТСКОЙ ХИРУРГИИ 85
ли хирург должен спрашивать согласия ребенка на
операцию или лечение, поскольку ребенок не име-
ет реальной возможности выбора. И хотя за стар-
шими детьми, почти взрослыми, доктора и юристы
признали право на принятие самостоятельного ре-
шения, однако трудно следовать этому решению,
когда ребенок, например, отказывается от жизнен-
но необходимого лечения.
Кодексы этических принципов, аналогичные
принятому Американской Ассоциацией Детских
Хирургов, помогают определить некоторые обязан-
ности детских хирургов и установить «норму» их
моральной ответственности. Но как и все другое,
наши представления о том, что этично, а что нет,
постоянно пересматриваются в зависимости от
того, с какой точки зрения мы смотрим на эту
проблему.
Достижения медицины последних лет застав-
ляют пересмотреть ряд мотивов в связи с введе-
нием новых методов лечения, одобряемых одними
и отвергаемых другими как с этических, так
и с клинических позиций. Вот некоторые, лишь
немногие из них: генетический скрининг, пе-
ресадка печени от живых доноров, взятие органов
и тканей (для трансплантации) у новорожденных
С анэнцефалией, дооперационное серологическое
тестирование на СПИД, забор крови (или других
сред) для исследований, не связанных непосредст-
венно с лечением. Этические вопросы невероятной
сложности возникают и в связи с неясным стату-
сом плода. Является ли плод личностью? А если
является, то обладает ли правами пациента и экс-
периментального объекта? В го время, как детские
хирурги доказывают, что некоторые угрожающие
жизни аномалии, такие как диафрагмальная гры-
жа, могут быть корригированы внутриутробно, пе-
ред юристами в подобной ситуации может встать
очень сложный вопрос, ибо возникает реальная
основа для серьезного конфликта между правом
плода на лечение и нравом матери на сохранение
в тайне ее беременности («врачебная тайна»),
т. е. фактически ее правом отказаться от хирурги-
ческого вмешательства («внедрения» в ее тело для
операции у плода).
Еще в 1975 г. детские хирурги пришли к пол-
ному согласию относительно необходимости от-
крытых дискуссий по поводу этических проблем
и выразили надежду, что эта тенденция будет раз-
виваться, дабы помочь в принятии решений в слож-
ных случаях. С тех пор, как начали публиковаться
в широкой печати материалы по этой проблеме,
стали популярными всенародные дискуссии. Более
того, к решению некоторых наиболее сложных
вопросов в детской хирургии теперь привлекаются
юристы, судьи, психологи, члены Парламентских
Комиссий, Конгресса и многие другие специалисты
медицинских и немедицинских профессий. Не оста-
ются в стороне и комитеты по этике и защите прав
человека. Трудно сказать, помогает или мешает
в каждом случае столь мощно разросшийся меха-
низм, но по меныней мерс одно преимущество не-
сомненно — открытость и гласность в обсуждении.
Другой спорный вопрос — проблема источников
финансирования медицины. С одной стороны мно-
гие считают, что должны быть установлены лими-
ты иа трату денег из государственной казны для
обеспечения медицинской помощи, а с другой —
этические принципы, такие как справедливость
и честность, подразумевают отсутствие ограниче-
ний в использовании средств, направленных на ох-
рану здоровья. В настоящее время предпринима-
ются попытки, как, например в шт. Орегон, сде-
лать приоритетными граты национальных ресур-
сов на медицинские нужды.
В обществе, где возрастает убежденность в не-
обходимости установления лимита относительно
траты денег на здоровье, трудно удовлетворить по-
требности в хирургическом лечении всех нуждаю-
щихся — плодов, детей, взрослых людей. Тем не
менее, детские хирурги, основываясь на этических
принципах, не должны позволять, чтобы традици
онные ценности, определяющие их действия в ин-
тересах больного, замещались финансовыми инте-
ресами.
Глава 7
УКУСЫ
Укусы животных и насекомых — один из самых
частых пидов травмы у детей. Частоту укусов на-
секомых по понятным причинам установить прак-
тически невозможно. Что же касается укусов со-
бак, то в Америке на их долю приходится пример-
но 500 000 травм в гол.1 От 6000 до 8000 пациентов
обращаются ежегодно по поводу укусов змей.2 Ча-
сто при укусах проблему представляют не только
и не столько сами по себе раны от укусов, сколь-
ко последствия воздействия яда, вторичная инфек-
ция и опасность бешенства.
СТОЛБНЯК
Каждый врач, который лечит загрязненные раны,
должен быть насторожен в отношении столбняка.
Бактериологическая контаминация большинства
ран от укусов и широкая распространенность
возбудителя столбняка (Clostridium tetani) требу-
ют, чтобы лечение данного вида травмы включало
в себя профилактику столбняка.
При чистых ранах с небольшим повреждением
тканей и раннем обращении (непосредственно по-
сле укуса) за медицинской помощью риск заболе-
вания столбняком очень мал. В тех же случаях,
когда имеются загрязненная рана, нежизнеспособ-
ные ткани или пациент поздно (больше, чем через
24 часа после травмы) обратился к врачу, риск
заражения столбняком наибольший. Кроме опасно-
сти, связанной непосредственно с видом рапы,
большое значение имеет характер предыдущей им-
мунизации больного. Достаточную иммунную за-
щиту от столбняка имеют, как правило, дети, по-
лучившие в течение первого года жизни 3-крат-
ную вакцинацию против коклюша, дифтерии и
столбняка (КДС) с промежутком между привив-
ками в 2 мес, затем — ревакцинацию через год по-
сле законченной вакцинации и через 4—5 лет,
т. е. перед тем, как ребенок идет в школу. В после-
дующем профилактика столбняка осуществляется
путем ревакцинации каждые 10 лет.
Пациент с низким риском раневого заражения
и неполной анамнестически вакцинацией или от-
сутствием сведений о прививках должен получить
дозу столбнячного анатоксина [дети до 6 лет —
дифтерийно-столбнячного (ДО анатоксина]. Им-
мунизация завершав гея последующим введением
двух доз анатоксина. Ребенку с высоким риском
раневого заражения и неполной или неизвестной
вакцинацией необходимо ввести дозу столбнячного
или ДС анатоксина и 250—500 международных
единиц (ME) столбнячного иммуноглобулина. Гло-
булин и анатоксин должны быть введены в разные
места во избежание их нейтрализации друг дру-
гом. Затем иммунизация завершается по схеме.
Больной, который получил раньше полную вак-
цинацию и через 10 лет ревакцинацию, достаточно
хорошо иммунизирован против столбняка, незави-
симо от тяжести травмы. 'Гем не менее, если рана
высокой степени загрязнения и прошло более 5 лет
после ревакцинации, должна быть введена 1 доза
анатоксина, а если при этом с момента травмы
прошло более 24 час, следует добавить 250—
500 ME иммуноглобулина.
Ребенок, который был полностью вакцинирован,
но нс получил ревакцинацию через 10 лет, при
наличии раны с низким риском заражения должен
получить одну дозу анатоксина, а при высоком
риске раневой контаминации — одну дозу анаток-
сина и 250—500 ME иммуноглобулина.3
УКУСЫ СОБАК И БЕШЕНСТВО
Укусы собак. Центрами контроля заболеваемости
(ЦКЗ) установлено, что частота укусов собак
в США составляет в год 200 на 100 000 населения.
Изучение этого показателя в западном Техасе по-
казало в 6 раз большую цифру. Около 40% укусов
отмечаются у детей в возрасте от 5 до 14 лет. Хотя
частота укусов собак очень велика, летальные ис-
ходы редки и обусловлены в основном кровотече-
нием. Ни один из легальных исходов не был свя-
зан с бешенством.4
Обработка раны и местное лечение. При уку-
се собакой рану обрабатывают тах же, как любую
УКУСЫ 87
другую загрязненную рану. При локализации ее
в косметически важной области ткани должны
быть по возможности сохранены, однако явно не-
жизнеспособные следует удалить. Края небольших
(по типу колотых) ран конечностей и незначимых
в косметическом отношении участков тела иссека-
ют и рану оставляют открытой. Лоскутные и рва-
ные раны обрабатывают таким же образом и оби-
льно промывают водным или физиологическим
раствором с мылом. Составы, содержащие аммоний
(Zephiran), в настоящее время не рекомендуется
применять для этих целей, ибо они не обладают
преимуществами перед простыми мыльными рас-
творами.5
Профилактика столбняка должна быть проведе-
на соответственно анамнезу в отношении прививок
и степени загрязненности раны. Флора полости рта
у собак содержит множество бактерий, включая
обычно стрептококки, стафилококки, актиномице-
ты, различные виды Pastcurclla, грам отри натель-
ные бактерии и некоторые анаэробные микро-
организмы. Пенициллин или цефалотин воздей-
ствуют иа большинство из перечисленных возбу-
дителей, однако предпочтительнее применять
амоксициллин в сочетании с аугментином в связи
с их действием на Pasteurella multocida и золоти-
стый стафилококк. Раны, полученные при укусах
собак, следует ревизовать повторно через 24—
48 час после травмы для того, чтобы не пропустить
присоединение инфекции.6 8
Бешенство. Наибольшую опасность при укусах
собак представляет возможность заражения бешен-
ством. Около 80% укусов, в результате которых
развивается бешенство у домашних животных, —
это укусы собак. Однако сообщения о бешенстве
у домашних собак стали стремительно уменьшать-
ся с введением обязательной вакцинации домаш-
них животных.9 Хотя реальная опасность зараже-
ния бешенством от домашних животных невелика,
решение о том, следует ли проводить соответству-
ющее лечение или нет, должно быть принято очень
быстро. Лечение бешенства является профилакти-
ческим, и для того, чтобы оно было эффективным,
начинить его необходимо как можно раньше, ибо
смертность от бешенства чрезвычайно высока.5
Вопрос об антирабическом лечении должен ре-
шаться в зависимости от характера травмы, вида
животного, а также с учетом факторов риска. Ви-
рус бешенства находится у животных в слюне, а по-
тому угроза этого заболевания существует только
в том случае, когда рана загрязнена слюной.
Если животное было иммунизировано по всем
правилам, риск для пострадавшего очень невелик.
Лечение в таком случае не следует начинать, но за
животным необходимо установить наблюдение.
При отсутствии сведений о вакцинации собаки ее
наблюдают по меньшей мере 10 дней. Если в тече-
ние этого срока животное остается здоровым, то
наблюдение может быть прекращено, ибо позже
опасности заболевания бешенством уже практиче-
ски не существует. Если покусавшую собаку по
тем или иным причинам умерщвляют, то ее мозг
должен быть исследован методом флюоресцирую-
щих антител. 11 сотому способ уничтожения живот-
ного не должен задеть мозг.
Исследование мозга подтверждает диагноз бе-
шенства у большинства животных, за исключени-
ем летучей мыши. Поэтому все пациенты, полу-
чившие укусы летучих мышей, должны получать
лечение, поскольку летучие мыши представляют
собой очень серьезный источник вирусов бешенст-
ва. Риск при укусе дикими животными, передаю-
щими бешенство, намного выше, чем домашними.
Из всех опубликованных в литературе случаев бе-
шенства 70% были вызваны укусами диких жи-
вотных, поэтому животное после укуса, если толь-
ко это возможно, должно быть уничтожено, а мозг
его подвергнут исследованию. Если метод антител
дает отрицательные результаты, лечение постра-
давшего можно не проводить или прекратить, если
оно было уже начато. Полезно знать, какие виды
диких животных являются источником бешенства
в данном регионе. ЦКЗ могут представить такую
информацию. В США не было зарегистрировано
случаев бешенства человека от укусов кроликов,
белок, морских свинок, бурундуков, мышей. Поэто-
му укусы перечисленных животных не требуют
профилактики бешенства. Носителями и передат-
чиками вируса среди диких животных нередко яв-
ляются скунсы (вонючки), лисы, койоты (луговые
волки), еноты, собаки, кошки и летучие мыши.
Соответственно их укусы более часто требуют ан-
тирабического лечения.
У бешеных животных отмечается изменение
походки, обильная саливация, несвойственное дан-
ному виду агрессивное поведение. Внезапное не-
спровоцированное нападение на человека обычно
спокойного животного должно вызывать у врача
подозрение на возможность бешенства. Однако
тщательный сбор анамнеза и деликатный опрос
показывают, что большинство укусов собак, как
правило, спровоцированы и являются проявлением
естественных агрессивных защитных инстинктов.
Соответственно подобное поведение в таких ситуа-
циях должно рассматриваться как нормальное.
Необходимо учитывать и другие факторы риска.
Гак, заражение бешенством более характерно
именно для детского возраста. Кроме того, раны
в обильно иннервируемых областях или близкие
по локализации к центральной нервной системе
(ЦИС) чаще являются очагом для развития бешен-
ства, благодаря быстрому передвижению вируса по
нервным путям. В этом отношении особенно опас-
ны раны головы и шеи. Важно учитывать и ха-
рактер рамы, ибо чем больше тканей подверглось
деструкции при укусе, тем выше шансы иа зараже-
ние. Любой больной, имеющий два или более из
следующих четырех наиболее важных факторов
риска, должен немедленно начать получать лече-
ние для профилактики бешенства:10
1. Возраст меньше 10 лет.
2. Раны головы и шеи.
3. Глубокие раны.
4. Укусы жияотными, сведений о вакцинации
которых нет или они недостоверны и сомнительны.
В ситуации высокого риска заражения бешенст-
88 УКУСЫ
вом лучшие результаты дает одновременно прово-
димая как активная, так и пассивная иммунизация.
Препаратам лошадиной сыворотки следует пред-
почесть изготовленные из человеческой сыворот-
ки. Активная иммунизация проводится человече-
ской диплоидноклеточной вакциной (ЧДКВ). Со-
гласно схеме, принятой в США, 1 мл вакцины
вводится вн/м на О, 3, 7, 14 и 28-й дни. В европей-
ских странах применяется еще и 6-я доза. Обязате-
лен внутримышечный путь введения, предпочти-
тельнее — в дельтовидную мышцу. У 25% паци-
ентов возникает местная реакция на инъекцию.
Легкие общие симптомы (тошнота, недомогание,
мышечные боли) отмечаются у 20% детей. Описа-
на и тяжелая неврологическая реакция, в частно-
сти синдром Гийепа-Барре (острый первичный
идиопатический полирадикулоневрит), однако это
чрезвычайно редкое осложнение. Среди тех паци-
ентов, которые позже получают реиммунизацию,
у 6% отмечается реакция иммунокоч.плекса, но без
опасных для жизни проявлений. Реиммунизацию
проводит ь не рекомендуется, за исключением слу-
чаев повторных укусов, а также тех пациентов,
которые постоянно, в силу своей профессии, кон-
тактируют с животными, потенциально могущими
заболеть бешенством.
Пассивная иммунизация осуществляется челове-
ческим рабическим иммуноглобулином (ЧРИГ),
вводимым в то же время, что и ЧДКВ. Только
в том случае, когда пациент был ранее вакциниро-
ван, ЧРИГ можно не применять, а использовать
две дозы вакцины на 0 и 3-й дни. ЧРИГ предпоч-
тительнее лошадиной антирабической сыворотки
(АРС), гак как он дает наименьшее количество
реакций и осложнений. ЧРИГ применяется в дозе
20 ME на кг массы тела (40 МЕ/кг АРС). Поло-
виной этой дозы обкалывается рана, оставшееся
количество вводится вн/м в другом месте. ЧРИГ
и ЧДКВ не должны вводиться в одно и то же мес-
то. Каждый препарат может использоваться без
другого, если один из них отсутствует, но в любом
случае лечение необходимо начинать как можно
быстрее.5
УКУСЫ ЗМЕЙ
Частота. Несколько тысяч укусов змей регистри-
руются ежегодно в США. Несмотря на ауру смер-
ти, окружающую все, что связано с этим видом
травмы, летальные исходы, согласно статистике,
отмечаются менее, чем в 1 % случаев. От I/3 до
половины жертв укусов ядовитых змей имеют ма-
лые проявления воздействия змеиного яда или во-
обще не имеют их." 13
Биология. Из всех видов змей, встречающихся
на территории США, лишь четыре (10%) пред-
ставляют интерес в медицинском аспекте. К ним
относятся семейства Micrurus (аспиды), Crotalus
(большая гремучая змея), Sistrurus (земляная
и карликовая гремучая змея) и Agkistrodon (мока •
синовия змея или водяной и медноголовый щито-
мордник).11
Аспиды (или ядовитые ужи, к которым относит-
ся кобра) имеют короткие неподвижные ядовитые
зубы. Это небольшие змеи, обычно 60—90 см
в длину, с окраской в виде поперечных полос крас-
ного, черного и желтого (или белого цвета). По по-
следовательности расположения этих полос можно
отличить аспида от безвредного американского до-
мового ужа. Чередование полос ужа следующее'
красная, черная, желтая, черная и красная. У аспи-
да черный нос, а полосы распределены в ином
порядке: черная, желтая, красная, желтая, черная.
Эти различия легко запоминают в Америке, зная
рифмованный стишок:
“Red on yellow kills fellow.
Red on black won’t hurt Jack”
("Красная на желтую убивает, красная на черную
не причинит вреда").
Только 2% змеиных укусов в США приходится
на аспидов, но воздействие их нейротоксического
яда может быть смертельным.14
Гремучие или ямкоголовые змеи (к ним отно-
сятся гадюки) имеют два ядовитых зуба, похожих
на иглы для подкожных инъекций, через которые
они могут впрыскивать свой яд. Голова у них тре
угольная с характерной, расположенной между ноз-
дрей и глазом ямкой, не имеющей чешуи и давшей
название (ямкоголовые) этим змеям. Глаза с вер-
тикальным эллиптическим зрачком. У неядовитых
змей зрачки круглые. Любой укус ямкоголовой
змеи должен оставлять следы ядовитых зубов. Рас-
стояние между колотыми ранками в какой-то сте-
пени отражает размеры змеи. Чем больше это рас-
стояние, тем больше змея, а чем больше змея —
тем больше риск гяжетого поражения змеиным
ядом. Ядовитые зубы при изнашивании и поломке
замещаются новыми, которые постоянно заклады-
ваются и находятся на разных стадиях развития.
Таким образом, змея всегда имеет активно функ-
ционирующие ядовитые зубы.
Характеристика яда. Состав змеиного яда сло-
жен. В него входят от 10 до 15 ферментов и от 3 до
12 неферментных белков и пептидов. Кумулятив-
ный эффект ферментов в сочетании с действием
продуктов распада клеток чрезвычайно токсичен.
Все неферментные составляющие змеиного яда
(нейротоксины, кардиотоксины, геморрагины) яв-
ляются полипептидами.
Полипептиды. Геморрагины действуют местно
и оказывают влияние на легкие, вызывая наруше-
ние проницаемости капилляров за С“ет разруше-
ния ктеточных связей эндотелия. Они также за-
медляют at грегацию тромбоцитов, что способству-
ет возникновению кровотечения. Кардиотоксин
низкомолекулярный полипептид, который может
деполяризовать клеточные мембраны, особенно в
сердечной мышце. Кроме того, он усиливает дейст-
вие фосфолипазы А в других тканях. Нейротоксин,
в основном присущий яд) аспидов, является не де-
поляризующим кура реподобным токе том
Ферменты. Фосфолипаза А может проникать
через клеточную стенку, вызывая лизис эритроци-
тов и локальную деструкцию гканей. Протеазы
оказывают антикоагулянтное действие, благодаря
УКУСЫ В9
своим фибринолитическим и антитромбопласгиче-
ским свойствам, а также являются плазминогенны-
ми активаторами. Хотя протеазы не усиливают
внутрисосудистое свертывание, однако яды, содер-
жащие небольшое количество протеаз и значи-
тельное — а миноа пи дзете раз, обладают этим эф-
фектом, высвобождая прокоагулянт и активируя
фактор X или превращая фибриноген в фибрин.
Эти же самые эстеразы высвобождают брадики-
нин, главный медиатор шока, развивающегося сра-
зу после поражения змеиным ядом. Эстеразы, со-
держащиеся в змеином яде, не всегда вызывают
аггрегацию тромбоцитов и активацию или разру-
шение факторов V или VIII; таким образом, гепа-
рин сам по себе не играет существенной роли
в этой форме внутрисосудистого свертывания. Ан-
тидотом змеиному яду является антивенин. Змеи-
ный яд очень стоек и постоянно, пока существует
в организме, вызывает свертывание крови, благо-
даря действию эстераз, и фибринолиз за счет эф-
фекта протеаз.’ '
Клиническая картина. Сила воздействия зме-
иного яда прямо пропорциональна полученной до-
зе и зависит от размера змеи, количества яда, ме-
ста укуса и размеров жертвы. Чем меньше жертва,
тем больше относительная доза яда и соответст-
венно тяжелее его воздействие.
Местная реакция включает боль, отек, образова-
ние волдыря, некроз и геморрагии вокруг ранки.
Особое значение, отражающее степень заражения
и возможность дальнейшего его прогрессирования,
имеет характер припухлости или отека в зоне уку-
са и в пораженных областях.
Общая реакция начинается с тошноты и рвоты,
затем появляются более жизнеопасные симптомы:
кровотечение, сердечная аритмия, шок в связи
с падением сосудистого тонуса, кровопотерей
и значительным накоплением отечной жидкости.
Кровотечение не представляет особой опасности,
если возникает лишь из места укуса, однако оно мо-
жет быть легочным или любой другой локализации
и тогда это уже перерастает в серьезную пробле-
му. Первичное поражение ферментами в сочетании
с эффектом токсических продуктов, высвобождаю-
щихся при воздействии яда на ткани, усиливает
потери жидкости и крови, вызывая гемолиз и гипо-
тензию и в конечном счете почечную недостаточ-
ность. 15‘16
Лечение. Ключ к оптимальному лечению жерт-
вы укуса змеи лежи! прежде всего в правильной
опенке местных и общих изменений. Наличие сле-
дов от двух ядовитых зубов позволяет предполо-
жить укус гремучей змеи, а анамнез (словесное
описание змеи) или сама змея (если ее удалось
убить) делают предположение несомненным. Аспи-
ды не оставляют характерных следов ядовитых
зубов, ибо для того, чтобы поразить жертву ялом,
они должны сначала как бы «жевать» ее зубами
(несколько раз), и соответственно после их укуса
имеется множество ранок.11 Если у пострадавшего
есть следы ядовитых зубов, он должен наблюдать-
ся не менее 4 часов после укуса.
Первая помощь, оказываемая на месте, иногда.
к сожалению, осложняет дальнейшее лечение, а
порой наоборот, существенно облегчает состояние
пострадавшего, что бывает значительно реже. Не-
медленно после укуса яд может быть удален из
ранки с помощью разреза места укуса и отсасыва-
ния яда либо путем иссечения краев ранки. ’
Данная процедура, если она производится, должна
быть осуществлена только специалистом. Однако
изучение результатов ранней санации раны пока-
зывает меньшую эффективность этого метода по
сравнению с лечением только антивенином.1 “ 19
Поэтому лучше, если первая помощь на месте
ограничивается иммобилизацией пораженной об-
ласти и срочной транспортировкой больного в ста-
ционар. Жгуты в большинстве случаев накладыва-
ются неправильно, и связи с чем целесообразность
их применения многими ставится под большое со-
мнение, тем более, что опасность переноса яда че-
рез капилляры по лимфатическим путям в общий
кровоток преувеличена. Кроме того, отек, возника-
ющий при поражении ядом, вовлекает не только
лимфатическую систему, но все ткани, подвергши-
еся воздействию токсинов, а потому действенность
жгута во время транспортировки чрезвычайно ма-
ла, если она вообще существует. Наилучший вари-
ант следовательно — обойтись без жгута. Холод
к конечности также не следует прикладывать.15
Каждому пострадавшему от укуса ядовитой змеи
необходимо проводить профилактику столбняка.
Хотя бактериальная контаминация у таких паци-
ентов обычно меньше, чем при человеческих уку-
сах, однако при явно загрязненных ранах следует
начать лечение антибиотиками. В подобных случа-
ях эффективны ампициллин и цефалотин.16
Лечение при змеиных укусах должно быть преж-
де всего сосредоточено на тех пациентах, которые
получили заражение ядом, о чем свидетельствует
наличие вокруг раны отека в сочетании с болез-
ненностью. Если через 4 часа после укуса припух-
лости нет, это говорит об отсутствии заражения,
и больной может быть выписан.
Как только поставлен диагноз поражения змеи-
ным ялом, необходимо взять кровь на группу и со-
вместимость, сделать общий ее анализ с уровнем
фибриногена, электролитов, остаточного азота, мо-
чевины и протромбиновым временем. Берется так-
же анализ мочи. Определение группы крови и со-
вместимости должно быть сделано как можно
раньше, так как при тяжелом заражении змеиным
ядом клетки крови повреждаются настолько стре-
мительно и значительно, что очень быстро резуль-
таты этого исследования могут стать совершен ио
искаженными и недостоверными, а порой даже са-
мо исследование просто невозможным. Внутривен-
ное переливание жидкости при подозрении на тя-
желое заражение начинают сразу через две вн/в
линии (одна для антивенина, другая — для других
лекарств и иной терапии). В течение первых
24 часов полностью исключается энтеральное пи-
тание, поскольку среди наиболее ранних общих
симптомов тошнота и рвота стоят на первом месте.
Кровотечение и потери жидкости в «третье про-
странство» леча г так же, как при любых других
90 УКУСЫ
травматических повреждениях. Инфузионную тера-
пию первоначально проводят сбалансированными
солевыми растворами. При необходимости добав-
ляют кровь и фибриноген. Необходим тщатель-
ный контроль диуреза и функции жизненно важ-
ных органов. ЭКГ у детей обычно не требуется.
Лечение должно быть дифференцированным
в зависимости от тяжести или степени поражения.
Подразделение по степени заражения змеиным
ядом, наиболее универсальное и широко использу-
емое, представлено в таблице 7-1. ’
Проводимая терапия в основном преследует
3 главные цели: (1) удаление яда или ограничение
его распространения, (2) нейтрализация яда и (3)
смягчение воздействия яда на организм.
Местная припухлость может быть достаточно
массивной, а при тяжелом заражении — захваты-
вать всю конечность и лаже части туловища на
стороне поражения. Если отек прогрессирует до
такой степени, что вызывает препятствие оттоку
крови, следует произвести фасциотомию, необхо-
димость в которой обычно не возникает, если сра-
зу и в эффективной дозе введен антивенин.15 Без
фасциотомии не удается все-таки обойтись, когда
при осмотре очевидно, что поражены все тканевые
слои. Поэтому разрез, при наличии показаний,
должен быть произведен не только через кожу, но
и через подлежащие ткани. Поверхностная (под-
кожная) фасциотомия неэффективна и бессмыс-
ленна.22
Удаление яда путем разреза и отсасывания или
иссечения краев раны было раньше методом выбо-
ра. Однако эта процедура эффективна лишь
в том случае, когда она сделана немедленно после
укуса (и то не всегда). Кроме того, при иссечении
краев раны остается дефект, который позже требу-
ет пластики. Против этого метода убеждают
и осложнения, связанные с кровотечением и после-
дующей утратой или повреждением тканей. Все
эти проблемы могут быть решены с помощью ан-
тивенина, применение которого исключает необхо-
димость подключения какого-либо дополнительно-
го лечения.
Если имеются показания к применению антиве-
нина, то первая его доза назначается соответствен-
но степени поражения, определяемой по таблице
7-1. Независимо от метода обработки раны, при
наличии признаков заражения 2-й, 3-й или 4-й
степени антивенин абсолютно необходим. Следует
соблюдать осторожность во избежание его передо-
зировки, ибо антивенин сам по себе может вызы-
вать сывороточную болезнь или анафилаксию.
При воздействии на организм змеиного яда терми-
нальному состоянию всегда предшествуют общие
симптомы, поэтому при отсутствии таких симпто-
мов в течение двух часов после укуса антивенин
может не потребоваться.23
Рекомендуемые дозы антивенина даны в табли-
це 7-1. Для уменьшения местного отека, коррекции
нарушений свертываемости, а также при наличии
гемолиза и тканевых расстройств, может понадо-
биться увеличение дозы. 30% пациентов, которым
показан антивенин, нуждаются в повторном его
введении. Дети с массой тела меньше 45 кг требу-
ют антивенина иа 50% больше, чем указано в таб-
лице, поскольку за счет относительно малых раз-
меров тела степень заражения у них больше.15
Поливалентный антивенин против яда ямкоголо-
вых змей — препарат, приготовленный из лиофи-
лизированной лошадиной сыворотки. Перед его
использованием необходимо провести кожный тест
на чувствительность. Однако эта проба должна
применяться только после того, как принято реше-
ние о необходимости использования антивенина,
ибо пациент не должен быть сенсибилизирован
к лошадиной сыворотке без определенных к тому
показаний.2,1 Кожный тест осуществляется инъек-
цией 0,02 мл 1:10 раствора лошадиной сыворотки,
что может выявить анафилактическую реакцию,
но не сывороточную болезнь. Последняя довольно
распространена и отмечается у 40% пациентов, не
являясь противопоказанием к применению антиве-
нина25
Антивенин должен быть введен внутривенно,
а не в место укуса, или вокруг раны подкожно.
Инфузия осуществляется на протяжении 2 часов.
При этом сначала медленно в течение нескольких
минут вводят контрольную пробную дозу (1 доза
в 500 мл физиологического раствора — разведение
1:50). Если в течение 5 минут нет аллергической
реакции, концентрация антивенина может быть
увеличена добавлением необходимого его количе-
ства к исходным 500 мл физиологического раство-
ра, разведение при этом не должно быть меньше,
чем 1:4 Увеличивают и скорость введения (мед-
ленная инфузия нецелесообразна). Эффективность
проводимого лечения определяют по исчезновению
припухлости. Необходимо контролировать про-
тромбиновое время и уровень фибриногена. При
лечении коагулопатий у пораженных змеиным
ядом применения только антивенина, как правило,
бывает вполне достаточно. Добавление гепарина
ТАВЛИЦА 7-1. Степени тяжести поражения змеиным ядом
Степень Местные симптомы Общие симптомы Антивенин
0 Заражения нет, следы зубов, но без отека Нет Нет
1 Следы зубов с развитием отека от 2,5 до 12,5 см в диаметре в течение 12 час Нет Нет
2 Следы зубов, отек 15—30 см в течение 12 час Ранние общие симптомы (тошнота и рппта) 2—5 доз
3 Следы зубов, отек больше 30 см Общие симптомы и нарушения коагуляции 5—10 доз
4 Следы зубов с некрозом и образованием вол дыря, отек иа пораженной стороне распросгра- Гипотензия, тяжелые нарушения коагуля- ции 10 20 доз
няется на туловище
УКУСЫ 91
показано лишь при поражении ядами с сильными
прокоагулянтными свойствами, обусловленными
наличием в их составе эстераз. Однако наиболее
распространенный яд больших гремучих змей
обычно не требует применения гепарина.17 15
Даже если у пациента отмечается аллергическая
реакция на лошадиную сыворотку, применение ан-
тивенина тем не менее возможно. В этом случае
рекомендуется предварительное введение 50—
100 мг димедрола и затем медленная инфузия раз-
веденного раствора антивенина. При анализе
650 случаев не отмечено ни одного летального ис-
хода, связанного с анафилаксией.24’ Оказание помо-
ши больным в подобных ситуациях целесообразно
осуществлять с участием в их лечении региональ-
ных токсикологических центров.
ЧЕЛОВЕЧЕСКИЕ УКУСЫ
Хотя при человеческих укусах нет того риска, ко-
торый наблюдается при поражении змеиным ядом,
однако бактериальное загрязнение может принести
к достаточно тяжелым последствиям, ибо флора
полости рта человека содержит большое количе-
ство разнообразных патогенных микроорганизмов,
включая стафилококки, стрептококки, спирохеты,
спириллы и т. д.
Существуют три вида механизма повреждений,
приводящих к человеческим укусам: укус другим
человеком, повреждение зубами руки при ударе ею
«в зубы» и «прикус» языка или губ, который чело-
век наносит сам себе, как правило, случайно.
Все эти раны необходимо тщательно ревизовать
и определить их глубину. Затем рану очищают
и санируют. Показана профилактика столбняка.
Человеческие укусы требуют лечения антибиоти-
ками, при этом достаточно бывает пенициллина
или цефалоспорина.
Рана языка должна быть очищена от нежизне-
способных тканей, а в том случае, если она боль-
шая, очень глубокая или идет через край языка —
ушита до сопоставления краев. Иногда ушивание
может понадобиться и для остановки кровотечения.
До тех пор, пока рана не заживет, рекомендуются
27, 2Я
частые гигиенические полоскания рта.
УКУСЫ ПЕРЕПОНЧАТОКРЫЛЫХ НАСЕКОМЫХ
Частота. На укусы перепончатокрылых насеко-
мых (пчелы, осы, шершни, термиты) приходится
50% всех смертей от заражения ядом в США.2’
Ежегодно сообщается о 40 летальных исходах от
укусов насекомых, что значительно^превышает ко-
личество смертей от укусов змей.
Главная опасность укусов насекомых — в аллер-
гической реакции, которую они могут вызывать,
хотя имеются сообщения и о смерти в результате
непосредственно токсического воздействия при на-
личии множественных укусов. Но для того, чтобы
наступил летальный исход в результате прямого
токсического эффекта, насекомое должно нанести
где-то около 500 укусов. Большинство смертей
приходится на взрослых, но тяжелые генерализо-
ванные реакции отмечены в основном у постра-
давших в возрасте до 20 лет. Соотношение мужчин
и женщин 60:40.14 Установлено, что 8 из 1000 лю-
дей дают аллергическую реакцию на укусы насе-
комых, причем 4 из 1000 — тяжелую.0
Перепончатокрылые — наиболее распространен-
ный вид в животном мире. Их яды нс идентичны,
но имеют некоторые.общие свойства. Онн содер-
жат вазоактивные кислоты, протеазы, поверхност-
но-активные вещества и кинины. Количество ядо-
витого вещества, передаваемое одним укусом,
обычно составляет от 0,3 до 0,6 мг.32
Фосфолипаза А, преобладающая у всех перепон-
чатокрылых, считается главным аллергеном. Мел-
литин, на который приходится 50% объема пче-
линого яда — пептид, который воздействует на
клеточные мембраны. Именно он, вместе с лизоле-
цитином, способствует высвобождению гистамина.
Хотя основное количество клинически активного
гистамина освобождается из тучных клеток по-
страдавшего человека, однако гистамин, допамин
и норадреналин содержатся и в большинстве
ядов.32
Клиническая картина. Первоначальная ло-
кальная реакция на укус — жгущая боль с зудом
и припухлость вокруг места укуса, что связано
с высвобождением гистамина. Если появляются
общие симптомы, то, как правило, не сразу, а че-
рез 30 мин.32 К ним относятся обычные проявле-
ния аллергии, генерализованные отеки и крапив-
ница. Может развиться, хотя довольно редко, и от-
сроченная аллергическая реакция (крапивница,
поражение лимфатических узлов, полиартрит).
Подобный симптомокомплекс после укуса может
быть предвестником анафилаксии, которая может
возникнуть в ответ на следующий укус. Однако
сила последующей реакции уменьшается с увели-
чением временного промежутка между укусами.33
Общая аллергическая реакция варьирует от лег-
кой до очень тяжелой. Умеренно выраженная ре-
акция обычно заключается в ощущении спазмов
в горле, болях в животе, головокружении, свистя-
щем дыхании, генерализованных отеках. При тя-
желой реакции развивается слабость, затрудненное
дыхание, спутанное сознание. При анафилактиче-
ской реакции отмечается шок и потеря сознания.
От пациента, имеющего аллергический анамнез,
можно, соответственно, ожидать более выраженной
реакции. И хотя она имеет иммунологическую
основу, однако ее тяжесть может быть связана так-
же и с количеством укусов.
Лечение. Немедленно начатое лечение пациента
с аллергической реакцией на укус направлено
прежде всего на борьбу с общими проявлениями.
При легкой выраженности симптомов все, что не-
обходимо больному — это адреналин для воздей-
ствия на вазомоторы и бронхи и антигистамин —
для снятия зуда. Обычно для подростков и взрос-
лых достаточной дозой является 0,2- 0,5 мл
1:1000 раствора адреналина подкожно. Для аллер-
гически настроенных детей максимальная доза
0,3 мл. Если симптомы сохраняются, адреналин
92 УКУСЫ
вводится повторно каждые 15—20 мин. Антигиста-
минные препараты, например димедрол (25—
50 мг) или хлорфснирамин (50—100 мг), приме-
няют внутримышечно, что помогает уменьшить
зуд. При тяжелой анафилактической реакции мо-
жет потребоваться ИВЛ и инфузионная терапия.
Иногда для снятия бронхоспазма в дополнение
к адреналину следует назначить эуфиллин.
Люди, подверженные аллергическим реакциям,
должны быть очень осторожны, избегая повторных
укусов. Для этого важно знать излюбленные места
распространения и скопления пчел, ос, шершней
и, соответственно, стараться не попадать в эти ме-
ста, а, оказавшись там невольно, хотя бы не поль-
зоваться парфюмерией с сильным запахом и не
носить яркую одежду. Несмотря на попытки избе-
жать контактов с насекомыми, повторные укусы
всегда возможны, поэтому пациентам, склонным
к аллергическим реакциям, рекомендуется посто-
янно иметь при себе специальный набор, который
содержит шприц с 1:1000 адренатином и антиги-
стаминные таблетки, а также носить какой-либо
опознавательный знак (например специально изго-
тавливаемый для этих целей браслет), чтобы
и окружающие также были насторожены в отноше-
нии возможной у них аллергической реакции.
Многие из связанных с аллергией летальных исхо-
дов происходят каждый год из-за того, что окружа-
ющие не могут правильно оказать неотложную по-
мощь (хотя это часто возможно и не гак уж слож-
но), поскольку не в состоянии понять происходя-
щее, ибо не знают о склонности данного человека
к подобным реакциям.
Десенсибилизация трудна, проводится в течепие
длительного периода времени (несколько лет) и не
всегда эффективна.30 Для определения аллергенов
требуются многократные кожные пробы, однако
выявить специфический аллерген очень сложно.
И хотя есть сообщения об эффективности десенси-
билизации, что выражается в снижении тяжести
общих реакций через 3 года,14 однако считается,
что такое снижение на протяжении нескольких лет
происходит и естественным путем, без десенсиби-
лизации.33
В результате проведения одной из работ по ис-
пользованию человеческих сывороток носителей
яда пчел были выделены фракции IgG, обладаю-
щего активностью против фосфолипазы А. Эти
препараты специфических антител использовались
при лечении некоторых пациентов с повышенной
аллергической реакцией. Подобная терапия хотя
и считается целесообразной, но не должна приме-
няться изолированно как единственный метод ле-
чения.35
УКУСЫ КОРИЧНЕВОГО ПАУКА
Loxosceles reclusa, североамериканский коричне-
вый паук-отшельник, не был известен как источ-
ник токсических укусов до первых сообщений, поя-
вившихся в конце 50-х годов. Этот паук распро-
странен в южных и центральных штатах, как
в городской, так и в сельской местности. Его часто
обнаруживают в помещениях, где он выбирает су-
хие места. Частота укусов неизвестна, по предпо-
лагается, что они отмечаются менее часто, чем
укусы черного паука. Однако укусы коричневого
паука могут представить значительно более слож-
ную в медицинском аспекте проблему, чем укусы
его черного собрата.36
Биология. Коричневый наук имеет средние раз-
меры, длина его тела 8—9 мм. Цвет варьирует от
светло- до темнокоричневого. Главная характерная
отличительная черта — темное пятно в виде
скрипки, расположенное дорсально на спинном
щитке и переходящее в тонкую линию по направ-
лению вперед к брюшку. Данный «знак» объясняет
часто употребляющееся для этого паука название
«скрипичная спинка».37
Яд имеет сложный состав, в него входят протеа-
за, гиалуронидаза, гемолизин и другие цитотокси-
пы, которые вызывают деструкцию, воздействуя
в основном на клеточную стенку (эритроцитов, эн-
дотелия, клубочков) ' Больше всего поражается
эндотелий, что приводит к микрососудистому
тромбозу, являющемуся причиной тканевых ин-
фарктов с последующим асептическим некрозом,
на фоне которого может возникнуть вторичное ин-
фицирование.37 39
Клиническая картина. Пострадавший может
первоначально не почувствовать укус и соответст-
венно не знать о нем. Чаще всего паук кусает че-
ловека, когда тот надевает одежду, которая долго
лежала без использования и не встряхивалась пе-
ред тем, как ее надели.
Поражение по степени может быть подразделено
на: (1) только зуд, (2) образование пузырька с не-
крозом диаметром менее I см, (3) некроз более
4 см без общих симптомов, (4) некроз более 4 см
с общими симптомами.'10
Общие симптомы — лихорадка, ДВС-синдром,
гемоглобинурия и почечная недостаточность в ре-
зультате токсического воздействия на эритроциты
и клубочки. Маленькие дети в большей степени,
чем взрослые люди, склонны к общим проявле-
ниям. '
Некроз вокруг укуса развивается в течение не-
скольких дней. Сначала на этом месте может быть
только серо-голубой ободок, обусловленный лока-
льным сокращением сосудов. Затем через 5—
7 дней формируется струп. На участках тела
с большим количеством жировой ткани, образовав-
шиеся язвы могут длительное время не заживать
в связи с высокой токсичностью яда и благоприят-
ными условиями для вторичной инфекции.
Если диагноз неясен, может оказать помощь им-
мунологический тест, выявляющий повышение ти-
мидина в лимфоцитах, подвергшихся воздействию
паучьего яда Обычно проходит от одной до двух
недель, прежде чем данное исследование дает ре-
зультаты.38
Лечение. Лечение укусов коричневого паука
ограничивается, как правило, лишь уходом за ра-
ной. Небольшие ранки заживают путем грануля-
ции и эпителизации. При больших их размерах
может потребоваться кожная пластика. При 1-й и
УКУСЫ 93
2-й степени поражения ядом достаточно хорошие
результаты бывают при исключительно местном
лечении. Необходимо назначать антибиотики ши-
рокого спектра действия для профилактики вто-
ричного инфицирования раны.
3-я и 4-я степень поражения иногда требуют ис-
сечения пораженного участка и кожной пластики.
Однако прежде чем производить это вмешатель-
ство. необходимо дождаться появления демаркаци-
онной линии и ограничения, дабы не пришлось
иссекать повторно?6
Выраженные общие симптомы, такие как гемо-
глобинурия, требуют инфузионной терапии для
обеспечения адекватного диуреза и уменьшения
таким образом шансов на поражение почечных ка-
нальцев. При развитии тяжелого гемолиза или
ДВС-синдрома необходимо переливание крови и
свежезамороженной плазмы.41
УКУСЫ ЧЕРНОГО ПАУКА
Среди укусов паукообразных укусы черного пау-
ка-ткача встречаются наиболее часто. Опасны
только самки, с чем и связано еше одно название
этого паука — «черная вдова». Для него характер-
но красное пятно на брюшке в виде песочных
часов.
Яд обладает в основном нейротоксическим дей-
ствием, вызывая как локальные, так и общие судо-
роги. В месте укуса сразу появляется боль, вол-
дырь и эритема. Вскоре после этого начинаются,
быстро и широко распространяясь, судороги, в том
числе мышц живота. При этом боли в животе
могут быть более интенсивными, чем в области
укуса. В подобной ситуации живот из-за рш на-
нести мышц иногда даже невозможно пропальпи-
ровать.
Укус черного паука редко приводит к смерти, но
сильная боль может продолжаться от 24 до 48 ча-
сов. Лечение обычно симптоматическое, включая
наркотические анальгетики и иногда для снятия
судорог глюконат кальция внутривенно. В чрезвы-
чайных ситуациях может быть применен, при на-
личии показаний, антивенин, приготовленный из
лошадиной сыворотки.24
ЛИТЕРАТУРА
1. Newman ЕС: Animal bites as a public health disease. Tex Med
73:49. 1977.
2. Strickland NE; Snake bile: A review. J Arkansas Med Soc 73:69.
1976.
3. Report of the Committee on Infectious Diseases, 21st edition.
American Academy of Pediatrics, Elk Grove Village, IL,
p 409 414. 1988.
4. Winkler WG: Human deaths induced by dog bites. United States
1974—75. Public Health Rep 92:425. 1977.
5. Report of the Committee on Infectious Diseases, 21st edition.
American Academy of Pediatrics, Elk Grove Village. IL,
p 344—350, 1988.
6. Graham WP, Calabreita AM, Miller SH: Dog biles. Am Fnm
Physician 15:132, 1977.
7. Saphir DA, Carter GR: Gingival flora of the dog with special
reference io bacteria associated with biles. J Clin Microbiol
3:344, 1976.
8. Goldstein EJ: Infectious complications and therapy of bile wo-
unds. J Am Pediatr Med Assoc 79:486, 1989.
9. Public Health Advisory Committee on Immunization Practices.
Rabies: Risk, management, prophylaxis, and immunizations. Ann
Intern Med 86:452. 1977.
10. Robinson DA: Dog bites and rabies: An assessment of risk. Br
Med J 1:1066, 1976.
11. Van Mierop LHS: Poisonous snakebite: A review. 1 Snakes and
their venom. J Fla Med Assoc 63:191, 1976.
12. Nelson BK: Snake envenomation. Incidence, clinical presentation
and management. Med Toxicol Adverse Drug Exp 4:17. 1989,
13. Litovitz TL. Martin TG, Schmitz B: 1986 Annual Report of the
American Association of Poison Control Centers National Data
Collection Svstcm. Am J Emcrg Med 5:405, 1987.
14. Strickland NE: Snake biles: A review. J Arkansas Med Soc
73:69. 1976.
15. Wingert WA. Chan L: Rattlesnake bites in southern California
and rationale for recommended treatment. West J Mr<l 148:37,
1988.
16- Van Mierop LHS: Poisonous snakebite: A review. 2. Symptoma-
tology and treatment. J Fla Med Assoc 63:201, 1976.
17. Huang TT, Lynch JB, Larson K, Lewis SR; The use of excisio-
nal therapy in the management of snakebite. Ann Surg 179:598,
1974.
18. Snyder CC, Pickins JE, Knowles RP, ct al.: A definitive study
for snakebite. J Fla Med Assoc 55:330, 1968.
19. Stewart RM. Page CP. Schwesingcr WH. el al.: Antivenin and
fasciotomy/debridement in the treatment of the severe rattles-
nake bite. Am J Surg 158:543, 1989.
20. Wood JT, Hoback WW, Green TW: Treatment of snake venom
poisoning with ACTH and cortisone. Virginia M Month 82:130,
1955.
21, McCollough NC. Gennaro JF: Treatment of venomous snake
bites in the United Slates. Clin Toxicol 3:483, 1970.
22. Carter JM, Bevin AG: Venomous snakebites of the extremities.
NC Med J 37:651, 1976.
23. Sabbaack MS. Cunningham ER. Fitts CT: A review of the tre-
atment of poisonous snakebite in 45 patients. Rev Surg 34:358.
1977.
24. White BD. Rodgers GC. Maty nu mas NJ, Allen F: Copperhead
snakebites reported to the Kentucky Regional Poison Control
Center 1986 Epidemiology and treatment suggestions. J Ky Med
Assoc 86:61. 1988.
25. Parrish HM, Hayes RH: Hospital management of pit vjper veno-
mations. Clin Toxicol 3:501, 1970.
26. Russell FE: Snake Venom Poisoning. Scholium International,
Great Neck, New York. 1983.
27. Chuinard RG. D*Ambrosia RD: Human bite infections of the
hand. J Bone Joint Surg 59:416. 1977,
94 УКУСЫ
28. Paton ВС: Biles; Human, dog, spider, snakes. Surg Clin North
Am 43:549. 1963.
29. Cavagnol RM: The pharmacological effects of Hymenoptera
venoms. Am Rev Pharmacol Toxicol 17:479, 1977.
30, Frazier CA: Insect stings — a medical emergency. JAM
235:2410, 1976.
31. Reisman RE: Studies of the natural history of insect sling aller-
gy. Allergy Proc 10:97, 1989.
32. Ilikin 1: Bee sting. Am Fam Physician 13:124. 1976.
33- Golden DB: Epidemiology of allergy to insect venoms and stings.
Allergy Proc 10:103, 1989.
34. Mueller HL: Maintenance of protection in patients treated for
stinging insect hypersensitivity: a booster injection program.
Pediatrics 59:773, 1977.
35. Lcssof MH, Sobotka AK, Lichtenstein LM: Protection against
anaphylaxis in Hymcnoptcra-sensitive patients by passive immu-
nization. Mvnogr Allergy 12:253, 1977.
36. Young VL, Pm P: The brown recluse spider bite. Am Plast Surg
20:447, 1988.
37. Hufford DC: The brown recluse spider and necrotic arachni-
dism. A current review. J Arkansas Med Soc 74:126, 1977,
38. Anderson PC: What’s new in loxoscelism? Mo Med 74:549,
1978.
39. Majeski JA, Durst GG: Necrotic arachnidism. South Med
J 69:887. 1976.
40 Aver Al, Hershey FB: Surgery for necrotic biles of the brown
spider. Arch Surg 108:612, 1974.
41. Arnold RE: Brown recluse spider biles: Five cases with a review
of the literature. J Am Coll Emcrg Physicians 5:262, 1976.
Глава 8
Инородные тела
Природное, неосознанное и вполне естественное
стремление малышей исследовать окружающую
среду и несколько авантюрный, без мыслей об от-
ветственности за свои действия дух эксперимента-
торства, свойственный более старшим детям, объ-
ясняют то широкое разнообразие как самих ино-
родных тел, так и органов и тканей организма
ребенка, куда они попадают. Наибольшее количе-
ство чужеродных предметов и веществ оказывают-
ся в бронхиальном дереве и пищеварительном
тракте, реже они внедряются в мягкие ткани. Мно-
гие подобные инциденты заканчиваются, к сча-
стью, лишь малыми неприятностями, некоторые же,
к сожалению, приводят к тяжелым катастрофам.
ИНОРОДНЫЕ ТЕЛА ГОРТАНИ
Не гак много видов патологии и состояний в дет-
ском возрасте, которые были бы столь же опасны,
как те, что приводят к дыхательной обструкции.
Это всегда острая ситуация, почти не дающая вре-
мени для диагностики и оказания своевременной
грамотной помощи. Подобные эпизоды могут быть
прежде всего результатом попадания в гортань
инородного тела. Типичные симптомы — внезап-
ное удушье, потеря голоса, одышка, иногда с раз-
витием инспираторного стридора. Наиболее часто
в подобных случаях роль инородных тел у детей
играют детали игрушек, булавки, монеты, кусочки
пищи (непрожеванного яблока или мяса) или скор-
лупа яиц, косточки рыбы и птицы. Очень важно по
возможности точно установить характер инородно-
го тела и давность происшествия, а также правиль-
но оценить тяжесть имеющихся симптомов. Если
речь идет о пище, притом относительно мягкой, то
ее можно извлечь, перевернув ребенка вниз го-
ловой и достаточно интенсивно поколачивая по спи-
не, либо с помощью модифицированного приема
Хеймлиха (выталкивание застрявшего комка пищи
из горла резким толчком кулака в живот в эпига-
стральной области). Если таким образом не уда-
ется достичь успеха, то показана ларингоскопия,
которую производят непосредственно в приемном
покое или в операционной, с удалением инородно-
го тела щипцами или отсасыванием.
Твердые или остроконечные предметы требуют
более «медицинского» подхода. Желательно в та-
ких случаях провести седатацию с добавлением
местного обезболивания аэрозольными препарата-
ми-анестетиками. Иногда показано и общее обез-
боливание.
Ларингоскопия. Эту процедуру никогда не сле-
дует делать в одиночку, а только бригадой, в со-
став которой должны входить анестезиолог, две
медсестры (одна из них операционная) и человек,
который будет держать голову ребенка. Под рукой
необходимо иметь набор щипцов для извлечения
инородного тела. Предварительно ставят катетер
в вену и подключают монитор. Больного надежно
фиксируют на столе в положении с согнутой к гру-
ди шеей и вытянутой головой. Ларингоскоп вводят
слегка вправо от средней линии, направляя клинок
к надгрудинной ямке. Для быстрой оценки состоя-
ния корня языка и верхних дыхательных путей
клинок продвигают к вершине надгортанника, за-
тем подходят под него, после чего поднимают кпе-
реди, чтобы осмотреть гортань и голосовые связки.
Па любом этапе этой процедуры, как только ино-
родное тело попало в поле зрения, его удаляют,
захватывая щипцами целиком или фрагментируя
по кусочкам (например, раскалывая клиновидную
рыбью кость).
ИНОРОДНЫЕ ТЕЛА
ТРАХЕОБРОНХИАЛЬНОГО ДЕРЕВА
Хотя инородные тела могут быть обнаружены
в любом отделе трахеобронхиального дерева, одна-
ко над карнной они локализуются редко, мсисс,
чем в 10% случаев. Большинство же попадает
в правый главный бронх. Разнообразие аспирируе-
мых предметов бесконечно — от пищи (например,
орехи, кусочки моркови, бекона и рыбные или ку-
риные кости) до карандашей, разного рода метал-
лических изделий, деталей игрушек, пуговиц,
фольги и даже зубов. Указание в анамнезе на ха-
96 ИНОРОДНЫЕ ТЕЛА
Рис. 8-1. Телескопический бронхоскоп. Телескоп
(Л) расположен в корпусе бронхоскопа (В) с про-
типоза потека ющей трубкой (В,> и соединен с фиб
рооптичсскнм источником света (Р).
Щипцы (С) введены в просвет и негру мента,
и захватывающие зубчики (С,) выдвинуты впере-
ди телескопического объектива. Воздух неболь-
шим потоком осторожно вводит впереди телеско-
пического объектива через соединительный кла-
пан <Е) и нротииоз.1потепа1ощую трубку (Bt>_
Проксимальная световая призма (ГЛ использу-
ется в том случае, когда телескоп удален. На ри-
сунке не виден расположенный напротив световой
призмы большой клапан для подсоединении аппа-
рата для наркоза или вентиляции.
В + В1
рактср инородного тела помогает в диагностике.
Клиническая картина включает в себя судорож-
ный кашель, позывы на рвоту, удушье, затруднен-
ное дыхание. «Попытка» слизистой и бронхов
«приспособиться» к возникшей ситуации может со-
провождаться бессимптомным интервалом, что
иногда производит ложное впечатление, будто
инородное тело вышло при кашле наружу или что
ребенок проглотил его. Постоянно затрудненное
дыхание, а также явные признаки эмфиземы или
ателектаза являются показанием для дальнейшего
обследования. Рентгенография подтверждает подо-
зрения и нс только выявляет рентгеноконтрастное
инородное тело, но и устанавливает его локализа-
цию. Обнаружить неконтрастные предметы помо-
гает УЗИ. При неясном диагнозе или серьезных
сомнениях показана бронхоскопия. Попавшее в
дыхательные пути инородное тело, которое нс уда-
лось извлечь, может привести к пневмонии, абсцес-
су легкого, бронхоэктазам, легочному кровотече-
нию или эрозии и перфорации бронха. Чем раньше
поставлен диагноз и удалено инородное тело, тем
меньше вероятности развития указанных ослож-
нений.
Бронхоскопия. Для удаления инородных тел эта
процедура должна проводиться только под общим
наркозом, ибо она может оказаться очень трудной
и длительной, а потому любые потенциальные не-
достатки общей анестезии существенно «переве-
шиваются» практической целесообразностью и эф-
фективностью бронхоскопии, а также значитель-
ным уменьшением для ребенка при этом виде
обезболивания анатомической и психической
травмы.
Здесь следует придерживаться тех же принципов
работы бригадой, как и при ларингоскопии. Обес-
печение при этом доступа в вену и мониторинга
имеет не меньшее, если не большее значение, чем
при ларингоскопии. Первая цель при бронхоско-
пии—дойти до входа в трахею, как это описано
в разделе ларингоскопии.
Голосовая щель достигается ларингоскопом, за-
тем через голосовые связки в трахею прово 1ят
осторожно бронхоскоп, держа его как карандаш
в правой руке. Ларингоскоп извлекают и продол-
жают обследование. Удаление инородных тел —
это искусство, которое требует большого опыта
и творческого подхода.
Значительным достижением, радикально усовер-
шенствовавшим этот метод, явилось создание
бронхоскопа, снабженного телескопическим
устройством и фиброоптикой,1 что обеспечивает
широкое поле зрения (даже через маленький ту-
бус) и прекрасную визуализацию, позволяя в то
же время осуществлять адекватную вентиляцию
легких и беспрепятственно манипулировать инст-
рументами (рис. 8-1 и 8-2).
В тубус телебронхоскопа вставляют специально
разработанные для этого аппарата щипцы, кото-
рые могут применяться и самостоятельно, без
бронхоскопа, если просвет последнего слишком
мал для их проведения (рис. 8-3). Эти щипцы
можно использовать, вводя и в бронхоскоп или
эзофагоскоп большего размера. Щипцы позволяют
mm] I I I I I
О ю 20 30 40 50
Рис. 8-2. Дейсткне захватывающих щипцов впереди телескопи-
ческого объем типа (крупный план).
ИНОРОДНЫЕ ТЕЛА 97
Рис. 8-3. Инструмент, сочетающий в себе телескоп
и щипцы, успешно применяющийся для удаления ино-
родных тел из дыхательных ну гей у маленьких детей.
удалять инородное гели и извлекать его одной ру-
кой под непосредственным контролем глаза, остав-
ляя тубус эндоскопа на месте.
С обычными бронхоскопами маленьких размеров
работать трудно, поскольку поле зрения чрезвы-
чайно ограничено. Но даже это небольшое поле
зрения еще более уменьшается прн введении через
просвет аппарата инструмента. В результате «за-
хват» инородного тела производится «на ощупь»,
полувслепую, если не совсем даже вслепую.
Миниатюрным телескопическим бронхоскопом
можно вой ги даже в самый маленький бронх, сразу
сориентироваться и быстро провести обследование.
Когда инородное тело обнаружено, аппарат позво-
ляет свободно манипулировать щипцами, не сме-
щая при этом поле зрения. Если инородное тело нс
удается захватить, то через просвет бронхоскопа
вводят катетер Фогэрти, осторожно проводя его за
инородное тело дистально, надувают баллончик
и извлекают катетер вместе с инородным телом.
Из возможных осложнений следует прежде всего
упомянуть сохраняющуюся частичную обструк-
цию, связанную, как правило, с отеком или выде-
лением слизи и крови, либо с комбинацией этих
причин. Возможна перфорация с пневмотораксом
или пневмомедиастинумом. Неадекватно проводи-
мая вентиляция или сохраняющаяся обструкция
дыхательных путей может привести к гипоксии
мозга и даже остановке сердца. Ведение послеопе-
рационного периода включает в себя постоянный
мониторинг и обычное общее лечение, а также са-
нацию, аэрозоли и. при наличии показаний, стеро-
идную терапию.
ИНОРОДНЫЕ ТЕЛА ПИЩЕВОДА
Маленькие дети глотают почти все, что могут по-
ложить в рог, чаще всего — предметы, находящие-
ся непосредственно рядом с ними, когда они полза-
ют по полу. Как уже было упомянуто, это бывают
обычно булавки, небольшие детали женских укра-
шений, пуговицы, монеты, игрушки, все виды ме-
таллических изделий, ключи, семечки, батарейки.
Более старшие в семье дети порой дают малышу
совершенно неподходящую для него пищу или са-
ми заглатывают случайно то, что держат во рту.
Иногда этому способствует падение или шлепок по
спине. Кусочек кости рыбы или куры может быть
проглочен ребенком любого возраста»
От размера и формы инородного тела зависит -
застрянет оно в пищеводе или пройдет в же-
лудок. Играют роль и другие факторы — анатоми-
ческие сужения (врожденные, воспалительного ха-
рактера, послеоперационные) и спазм. Наиболее
частые симптомы — боль, обильное слюноотделе-
ние и невозможноегь проглотить пищу. Если попа-
дание инородного тела в пищевод не было замече-
но, поводом для обращения служат развившаяся
аспирационная пневмония, температура, кашель,
симптомы перфорации пищевода или возникшего
трахеопищеводного свища.
Контрастное инородное тело может быть выяв-
лено при рентгенографии, которую необходимо
проводить в двух проекциях с обяза тельным захва-
том шеи. При попадании нерентгеноконтрастного
инородного тела показано исследование с барием,
помогающее обнаружить подозреваемую обструк-
цию. Должны быть сделаны рентгенограммы и
брюшной полости, чтобы определить, не прошло
ли инородное тело в желудок.
Успешность проведения процедуры удаления
инородного тела из пищевода зависит от правиль-
ности выбора инструмента, знания анатомии ре-
бенка и техники данного вмешательства, а также
о г комбинации опыта врача и владения этим, по-
рой сложным, искусством.
Неострое инородное тело, недавно проглочен-
ное, например монета или пуговица, иногда может
7 Заказ № 1622
9В ИНОРОДНЫЕ ТЕЛА
быть удалено после седатации больного, под конт-
ролем экрана с помощью катетера Фолея, прове-
денного за инородное тело дистальнее. Баллончик
раздувают каким-либо рентгеноконтрастным рас-
твором, и инородное тело извлекают вместе с кате-
тером. Во всех других случаях удаление осуществ-
ляют под непосредственным контролем глаза, при-
меняя эзофагоскопию.
Эзофагоскопия. Эту процедуру проводят под об-
щим наркозом бригадой того же состава и при тех
же условиях, что были описаны в предыдущих раз-
делах (ларингоскопия и бронхоскопия). Для пред-
отвращения обструкции, связанной с закупоркой
как инородным телом, так и эндоскопом, необходи-
ма интубация. Общая анестезия, как и при бронхо-
скопии, позволяет тщательно, не спеша, осущест-
вить процедуру наиболее безопасным и удобным
для больного и хирурга путем.
После введения пациента в наркоз и иммобили-
зации его на операционном столе шею сгибают
к груди, а голову вытягивают. Головной коней сто-
ла опускают или удаляют. Открывая рот больного
(релаксированного) и защищая зубы левой рукой,
хирург очень деликатно манипулирует эзофагоско-
пом над корнем языка, осторожно приподнимая
кпереди гортань, чтобы открыть вход в пище-
вод. Деликатные движения концом эндоскопа
позволяют ввести его в шейный отдел пищевода.
Характер дальнейшего исследования и манипуля-
ций зависит от конфигурации и положения ино-
родного тела.
Как и при бронхоскопии, телескопический эндо-
скоп обладает несомненными преимуществами пе-
ред обычным, обеспечивая четкое, яркое, увеличен-
ное изображение и позволяя манипулировать при
непосредственном контроле глаза (рис. 8-4). Ино-
родные телгт пищевода обычно превышают по раз-
мерам аспирированные предметы. Для пищевода,
имеющего больший диаметр и более расширенно-
го, следует подбирать эндоскоп соответствующих
размеров. Под рукой всегда должен быть набор
разнообразных щипцов и зондов. Телескоп удаля-
ют, если он препятствует введению большего по
размерам инструмента. Процедуру тогда произво-
дят через открытую трубку, используя для освеще-
ния проксимально расположенный источник света
(см. рис. 8-1). Некоторые острые предметы (на-
Рис. 8-4. Вит ип эндоскопии прокрашенного барием колесика
от игрушки, проглоченного 3 дня назад. Инородное тело было
захначсно щипцами и удалено.
пример открытая булавка) могут при извлечении
воткнуться в противоположную стенку, поэтому их
лучше осторожно продвинуть в желудок (см. след,
раздел «Инородные тела желудочно-кишечного
тракта»). Проглоченные батарейки от слуховых
аппаратов, компьютеров, фотооборудования и фо-
нариков представляют собой особую проблему
в связи с возможностью их коррозийного воздей-
ствия. Они должны быть срочно удалены до того,
как вызовут перфорацию, медиастинит и даже тра-
хеопищеводный свищ. Очень трудно бывает захва-
тить тяжелые предметы с гладкой поверхностью,
например шарики от детских игр (рис 8-5). В та-
ких случаях через просвет телескопического эндо-
скопа, предназначенный для инструментов, вводят
катетер Фогэрти за инородное тело дистально, об-
ходя его Слегка надувают баллончик и извлекают
катетер вместе с инородным телом.
Осложнения могут быть прежде всего в виде
перфорации пищевода, вызванной самим инород-
ным телом либо возникшей при попытках его уда-
тения.
ИНОРОДНЫЕ ТЕЛА
ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
Способность детей проглатывать все, что только
они могут положить в рот, уже упоминалась в раз-
деле об инородных телах пищевода. Говорилось
также и о чрезвычайном разнообразии предметов.
Застрянет инородное тело в пищеводе или пройдет
в желудок, зависит, как правило, от его размеров,
формы и вида. Исход в каждом случае может быть
предсказан достаточно точно, в зависимости от
этого и проводится либо наблюдение, либо лече-
ние. Попав в желудок, проглоченные инородные
тела чаще всего безболезненно проходят через же-
лудочно-кишечный тракт и выходят наружу в те-
чение 24—48 часов.
Округлые, овальные, кубовидные предметы без
острых краев или выступов должны вызывать наи-
меньшее беспокойство врачей. Наиболее часто
проглатываемые детьми монеты, маленькие игруш-
ки, пуговицы, шарики от детских игр или закры-
тые английские булавки относятся именно к этой
группе. Ребенок в таком случае не нуждается
в госпитализации и может быть отпущен домой, но
если позже появились боли в животе, рвота, кровь
в стуле или если проглоченный предмет не вышел
естественным путем в течение 4—5 дней, необходи-
мо повторно обратиться в стационар. Рентгеноло-
гическое исследование позволяет определить поло-
жение инородного тела и убедиться в том. вышло
ОНО уже или нет. Показаниями для хирургического
удаления являются продолжающиеся боли в живо-
те, рвота, кровь в стуле. При отсутствии указан-
ных симптомов операция необходима в том случае,
когда инородное тело остается в желудочно-ки-
шечном тракте в течение 4—5 недель. Иногда уда-
ление можно произвести с помощью гибкого гас-
троскопа, но чаще требуется лапаротомия.
Другая группа инородных тел желудочно-ки-
шечного тракта — это предметы с острыми краями
ИНОРОДНЫЕ ТЕЛА 99
Рис. 8-5. Переднезадним
и пищеводе.
(А) и боковая (В) рентгенограммы грудной клегки
Виден шарик от детской шры, застрявший
или копчиком, размеры которых позволяют им
пройти через пищевод. К ним относятся открытые
английские булавки, иглы, гвозди, кусочки стекли
или игрушек. В подобных случаях ребенка необхо-
димо госпитализировать и внимательно наблю-
дать. Не рекомендуется назначать какую-либо осо-
бую диету, способствующую защите слизистой
и прохождению инородного тела. При каждом опо-
рожнении кишечника каловые массы должны тща-
тельно осматриваться. Ежедневно следует прово-
дить рентгенологическое исследование для опреде-
ления положения инородного тела. Грозными сим-
птомами являются боли в животе, напряжение
мышц брюшной стенки, подъем температуры и ки-
шечное кровотечение, которое хоть и отмечается
редко, но тем не менее может возникнуть. Наибо-
лее частая причина незначительного кровотече-
ния— легкая травма слизистой или небольшое
изъязвление. Выявляемое при обследовании быст-
рое продвижение инородного тела является показа-
нием к консервативному лечению и наблюдению.
Хирургическое вмешательство производится лишь
при выраженном кровотечении или признаках пе-
ритонита, а также в тех случаях, когда инородное
тело не продвигается свободно и быстро. Среди
наших 132 наблюдений инородных тел желудочно-
кишечного тракта было девять остроконечных бу-
лавок и игл, и три открытые английские булавки.
Все они вышли самостоятельно и безболезненно.
Ни один пациент нс имел серьезного кровотечения
или признаков перитонита, и никто не был опери
рован.
Некоторые дети проглатывают длинные тонкие
инородные тела. В наших наблюдениях это были
заколки для волос, части карандашей или даже
целые карандаши, ручки, длинные гвозди, инстру-
менты (рис. 8-6), куриные кости. Многие из этих
предметов также проходили беспрепятственно, но
при проглатывании именно таких инородных тел
отмечается наибольшая частота осложнений или
отсутствие их самостоятельного пассажа. Чаще
всего они застревают в пилорическом отделе,
12-перстной кишке, в области связки Троица
и в илеоцекальном углу. Пройти через указанные
изгибы мешает таким предметам нс только то, что
они твердые, но в основном препятствуют прохож-
дении! кончики, которые, даже будучи незаострен-
ными, могут внедряться в кишечную стенку, по-
вреждая и перфорируя ее. В подобных случаях
пациенты должны наблюдаться в стационаре. Опе-
рация показана при наличии болей в животе, кро-
вотечения или напряжения мышц брюшной стенки,
а также если в течение суток инородное тело нс
меняет своего положения. Среди наших наблюде-
ний четверо больных с такими инородными телами
были оперированы.
Проглоченные батарейки должны быть удалены
хирургическим ну гем. если по данным рентгено-
грамм, производимых каждые 6 часов, они не про=
двигаются.
100 ИНОРОДНЫЕ ТЕЛА
Рис. 8-6. Небольшая отвертки, располагающаяся и 12-персгпой
кишке у годовалого ребенка. Кровь в стуле и отсутствие при-
знаков продвижения инородною села послужили показанием
для оперативного вмешательства.
Как правило, мы не ограничивали детей в пита-
нии и не меняли диету, так же, как и не применяли
лекарств. Лишь в редких случаях назначали мине-
ральное масло, чтобы ускорить пассаж инородного
тела больших размеров. Использование в таких
ситуациях средств, усиливающих перистальтику
кишечника, противопоказано. Для извлечения ме-
таллических инородных тел мы не любим приме-
нять трубки с магнитами на конце, ибо небольшие
предметы подобного рода выходят самостоятельно
и без этого. Большие же предметы опасно извле-
кать таким образом ретроградно вслепую из-за уг-
розы возможного повреждения пищевода. Для этих
целей мы использовали гибкие эндоскопы, но из
5 наблюдений только в одном манипуляция была
успешной. Этот метол помогает лишь в исключи-
тельных случаях, к тому же большинство предме-
тов, которые могут быть свободно извлечены через
пищевод, обычно и сами безболезненно проходят
по желудочно-кишечному тракту.
Осложнения инородных тел желудочно-кишеч-
ного тракта включают кровотечение, перфорацию,
перитонит, внутрибрюшные или забрюшинные аб-
сцессы, кишечные свищи. Руководствуясь показа-
ниями к Операции, которые были представлены
выше, мы не имели ни одного из перечисленных
осложнений среди 132 наблюдений. Хирургическое
вмешательство (7 операций и одна лапароскопия)
было проведено всего у 8 детей (6,0%).
К поздним осложнениям недиагиостироваиного
или диагностированного, но оставшегося в желу-
дочно-кишечном тракте инородного тела относят-
ся последствия длительного его пребывания в чер-
веобразном отростке или дивертикуле Меккеля,
а также выхождение из кишечника в свободную
брюшную полость или забрюшинное пространство.
БЕЗОАРЫ
Безоар представляет собой конгломерат проглаты-
ваемых детьми волос (трихобезоар) или рас-
тительных волокон (фитобезоар), или комбинацию
того и другого (трихофитобезоар). Чаще всего это
дети (преимущественно девочки), обладающие
причудливыми эксцентричными пристрастиями,
имеющие эмоциональные расстройства или задер-
жку психического развития. Обычно безоары фор-
мируются в желудке, по могут распространяться
и в тонкую кишку.
В клинической картине отмечаются боли в живо-
те, анорексия или рвота, анемия и гипотрофия раз-
личной степени. Менее часто возникает непрохо-
димость или перфорация. Иногда же безоар фор-
мируется абсолютно бессимптомно. Обследование
выявляет признаки гипотрофии, а пальпация —
«опухоль» в эпигастральной области. На рентге-
нограммах с барием видно образование, обтекае-
мое контрастным веществом.
Как только поставлен диагноз безоара, необхо-
димо оперативное вмешательство, позволяющее
предотвратить такие осложнения, как непроходи-
мость, кровотечение, изъязвление, перфорация, пе-
ритонит, и постепенно справиться в последующем
с гипотрофией. Безоары желудка и начальных от-
делов тонкой кишки обычно удаляют из гастрото-
мического разреза. Во время операции необходимо
ревизовать и кишечник, в котором могут быть от-
дельные комки волос.
ИНОРОДНЫЕ ТЕЛА КОЖИ И МЯГКИХ ТКАНЕЙ
Самые разнообразные инородные тела внедряются
самостоятельно или вводятся детьми в кожу и мяг-
кие ткани обычно во время ползания или игр. Эти
предметы чаще всего загрязнены, а потому коло-
тые раны должны в большинстве случаев рассмат-
риваться как инфицированные. Следовательно, не-
обходимо назначать антибиотики, руководствуясь
при этом размерами раны и степенью ее загрязне-
ния. Проводится также профилактика столбняка,
определяемая характером ранее полученных ре-
бенком прививок.
Часто возникает вопрос — удалять или не уда-
лять инородное тело? Как правило, если после
травмы прошло немного времени и инородное тело
четко определяется, оно должно быть удалено.
С другой стороны, при отсутствии симптомов риск
операции, производимой с целью удаления, превы-
шает риск, связанный с нахождением инородного
тела, а поэтому лучше оставить его на месте.
В любом случае решение этого порой непростого
вопроса зависит от характера инородного тела
и его локализации.
Диагноз обычно ставится на основании анамне-
за. Однако порой ребенок или родители не увере-
ны, действительно ли имелась травма. Обычная
ИНОРОДНЫЕ ТЕЛА 101
рентгенограмма выявляет не все инородные тела.
Существенную помощь в обнаружении стекла,
пластмассовых предметов и деревянных щепок мо-
жет оказать ксеро (элекгро) рентгенография и мяг-
котканная рентгенография. Исследование в прохо-
дящем свете (трансиллюминацня) небольших ча-
стей тела, таких как пальцы, рука, нога, кисть,
ступня, также помогает определить наличие и ло-
кализацию щепок и заноз. R тех случаях, когда
инородное гело находится глубоко в мышцах нли
подкожно-жировой клетчатке, исследование обяза-
тельно должно быть проведено в двух проекциях,
независимо от тот, какой метод применяется.
Если только инородное тело расположено не со-
всем поверхностно, то у маленьких детей наиболее
эффективно и наименее травматично удалять его
под общим наркозом. У пациентов старшего возра-
ста при манипуляциях на кисти и ступне можно
применить регионарную блокаду. Местной инфи-
льтрации анестетиками следует однако избегать,
ибо она приводит к возникновению припухлости,
иногда небольшого кровотечения, а также некото-
рого смещения тканей, что может осложнить и без
того нелегкую задачу. Особенно трудны для удале-
ния маленькие короткие остроконечные предметы,
такие, как иглы, поскольку во время операции они
легко смещаются и мигрируют в глубину. Намного
проще и целесообразнее удалять их, используя об-
щий наркоз и проводя вмешательство под контро-
лем экрана в операционной. Разрез должен быть
небольшим. Через него вводят зажим, направляя
прямо к игле, которую захватывают и, осторожно
маневрируя, извлекают.
Древесные инородные тела. Дерево почти все-
гда загрязнено, а потому для предупреждения ин-
фекции его кусочки, попавшие в мягкие ткани,
должны быть удалены. Вокруг входного отверстия
обычно отмечается болезненность и гиперемия ко-
жи. Если щепка видна, можно использовать мест-
ную анестезию и извлечь ее, захватив зажимом
либо путем иссечения тканей через небольшой
разрез непосредственно над ней. Глубоко располо-
женные щепки или остатки частично удаленных
инородных тел должны быть прежде всего четко
локализованы с помощью ксеро- или мягкотканной
рентгенографии. При наличии множественных
мелких кусочков рациональнее не разыскивать
каждый, а иссечь раневой канал и все пораженные
мягкие ткани, содержащие инородные тела, если
локализация позволяет это сделать. Занозы под
ногтями пальцев руки или ноги должны быть уда-
лены путем клиновидного иссечении покрывающе-
го инородное тело ногтя. Это превращает анаэроб-
ную рану в аэробную и, кроме того, весь фрагмент
при таком способе может быть удален без труда.
Металлические осколки по размерам обычно
меньше древесных щепок и вызывают менее выра-
женную реакцию. Они особенно трудны для обна-
ружения, так как могут проникать глубоко в мяг-
кие ткани. Рентгенография практически всегда вы-
являет металлические инородные тела. Если же
они не определяются четко, то удалять их не сле-
дует.
Иглы или части игл при локализации в мягких
тканях в области ладони или ступни могут причи-
нять серьезное беспокойство. Они входят через не-
большую ранку и способны проникать глубоко,
мигрируя при любом движении. Если рентгеноло-
гически инородное тело обнаружено, конечность
Сразу должна быть иммобилизована. Для успешно-
го удаления необходимы общий наркоз, наложение
жгута, что позволяет выполнять .манипуляцию бес-
кровно, и возможность использования рентгенов-
ского экрана, как было описано выше.
Иногда в мягких тканях остается сломавшаяся
во время медицинской манипуляции инъекционная
игла. Этн иглы обычно стерильны и не требуют
срочного удаления за исключением тех случаев,
когда их извлечение не представляет сложности
или когда у больного появились какие-либо симп-
томы.
Если обломившаяся при люмбальной пункции
игла осталась в области позвоночника, то после
рентгенологического контроля производят опера-
цию, которая может оказаться не только длитель-
ной, но иногда даже потребовать удаления дужки
позвонка или остистого отростка.
Рыболовные крючки обычно внедряются в паль-
цы или в ладонь. Их зубцы очень затрудняют уда-
ление. Рыболовный крючок может быть извлечен
без особых сложностей, если продвинуть его
острым кончиком вперед, выколоть через кожу
и срезать зубец.
Кусочки стекла часто внедряются у детей
в кисть или стопу. В некоторых случаях мелкие
фрагменты, попавшие «брызгами» на лицо или те-
ло, могут быть удалены с помощью липкого пла-
стыря. Ксерорентгенография обычно выявляет в
мягких тканях кусочки стекла лишь значительных
размеров. Однако их чрезвычайно трудно бывает
обнаружить на операции. И поскольку они сопро-
вождаются обычно минимальным воспалением, то
их удаляют позже, если появится боль или стойкие
признаки инфекции.
ЛИТЕРАТУРА
1. Gans SI., Berci G: Advances in endoscopy of infants and child-
ren. J Pediatr Surg 6:199—233, 1971.
Глава 9
ожоги
История. Самое раннее описание лечения ожогов
было обнаружено на папирусах, относящихся при-
мерно к 1500 году до н. э.: «Лечение шаг за шагом
на протяжении пяти дней описано очень образно;
в первый день черная грязь, на второй — телячий
навоз, перемешанный с дрожжами, на третий —
засохшая смола акации, смешанная с ячменным
тестом и маслом. На четвертый (ень жирный воск
и папирус, прокипяченный с бобами, и на пятый
день, завершающий лечение, микстура с колонхоэ,
красной охрой, листьями и кусочки меди».1 Египтя-
не для облегчения боли использовали аппликации
на рану растительной смолы и натирание лягуш-
кой, нагретой в масле.2,1
Гиппократ в 430 г. до н. э. рекомендовал приме-
нять в качестве повязки кусочек ткани с нанесен-
ным на него топленым свиным салом, смешанным
со смолой и битумом и подогретым на огне.’ Ни-
трат серебра (ляпис), который применяется еще
и в настоящее время, был впервые предложен
в 1821 г.4
Местное лечение ожогов резко продвинулось
вперед после корейской войны, когда Дуглас Линд-
сей открыл мафснид (сульфамилон). А благодаря
открытию Чарльзом Фоксом в 1968 г. сульфадиа-
зина серебра, появились препараты столь же эф-
фективные. но с меньшими побочными эффектами.
Местное применение этих новых мощных лекарств
способствовало значительному снижению деталь
ности при ожогах, но, с другой стороны, отсрочило
введение в практику так широко используемого
в настоящее время раннего хирургического ле-
чения. '
Частота и эпидемиология. Травма — ведущая
причина детской смертности, ожоги стоят па вто-
ром месте среди детей в возрасте до 5 лет
в США-6 Каждый год 2500 детей умирают от
ожогов и 10 000 остаются тяжелыми инвалидами.
Наиболее часто отмечаются ожоги кипящей или
очень горячей жидкостью, из них 48% - пи-
щей.’ 12 Грудные дети получают ожоги в основном
во время купания. Малыши, начинающие ходить,
преимущественно обжигаются, проливая (или ро-
няя) на себя горячую пищу или воду из-под крана.
Ожоги рта от соприкосновения с электропроводами
отмечаются исключительно- в этой возрастной
группе. У дошкольников, проявляющих активный
интерес к спичкам и зажигалкам, увеличивается
частота ожогов пламенем. В более старшем и под-
ростковом возрасте дети нередко пытаются экспе-
риментировать со смесями из огня и летучих ве-
ществ, в этой же возрастной группе растет и коли-
чество электроожогов.’
В Англии частота ожогов кипящей жидкостью за
последние 10 лет несколько увеличилась.” В то же
время в Германии отмечается прогрессивное сни-
жение этого показателя — на 50% за последние
17 лет, что является результатом планомерно про-
водимой просветительской деятельности.
Ожоги отмечаются в 10—20% всех официально
зарегистрированных случаев жестокого обращения
с детьми, причем наиболее часто в возрасте до
5 лет (в среднем 1.5 года). Для такого механизма
термической травмы почти патогномоничны одно-
временные глубокие ожоги ягодиц, промежности
и обеих стоп. Поэтому сочетание очевидных при-
знаков жестокого обращения, двустороннего сим-
метричного поражения и позднего обращения за
медицинской помощью должно вызывать подозре-
ние на данную причину ожоговой травмы.
Анатомия. Кожа — самый большой орган чело-
веческого тела, играющий наиважнейшую роль
в обеспечении жизнедеятельности организма и со-
ставляющий примерно 15% общей массы тела.
Структура и толщина ее очень варьируют на раз-
ных участках тела, а также у людей разного воз-
раста и пола. Образована кожа пятью основными
слоями: эпидермис, дермо-эпидермальное соедине-
ние, эпидермальные придатки, дерма (собственно
кожа) и подкожный слой (рис. 9-1). Базальный
слой представлен исключительно пролифератив-
ными клетками внутри эпидермиса. Базальная
мембрана дермо-энидермального соединения слу-
жит барьером, препятствующим проникновению
макромолекул. Сосочковый слой состоит из мел-
ких волокон соединительной ткани, густо окружен-
ОЖОГИ 103
Рис. 9 /. Нормальная анатомия кожи.
Bosal Cell Lcyer^jf/
Stratum Corneum
Melanocytes
(Clear Cells)
Prickle Cell Layer
(Stratum Molpighu)
Stratum Lucidum
Granular Layer
(Stratum Granulosum)
11 Dermol
ных основным веществом. Сосочковый и более глу-
бокий сетчатый слои разделены нервными сплете-
ниями и кровеносными сосудами.
Кровоснабжение кожи чрезвычайно богато. У
мужчин с массой тела 70 кг скорость кожного кро-
вотока составляет в среднем от 200 до
500 мл/мин, возрастая до 7000 8000 мл/мин при
нагревании и уменьшаясь до 20—50 мл/мин при
значительном охлаждении. Этот широкий диапа-
зон колебаний скорости кровотока — важный фак-
тор, смягчающий тяжесть термической гравмы.
Придатки кожи представляют собой функциони-
рующие выпячивания эпидермиса и сосочковой
дермы в ретикулярный и подлежащий жировой
слои. Они состоят из волосяных фолликулов, пото-
вых (экзокринных и апокриновых) и сальных
желез.
После термического поражения эпидермальные
придатки служат источником не только регенера-
ции клеток эпидермиса, но и бактериального за-
грязнения, поскольку глубоко в протоках этих
структур обитает флора, присущая нормальной ко-
же. Кожный покров выполняет функцию естест-
венного барьера, препятствующего инвазии бакте-
рий. Постоянное шелушение кожи способствует
удалению микроорганизмов, находящихся как на
поверхности, так и в ее толще. В сухом наружном
слое кожи гибнут многие вирусы и грамотрица-
тельные микроорганизмы. В норме ее pH колеблет-
ся между 4 и 6, задерживая рост ряда бактерий.
Покрывающая кожу тонкослойная пленка из жир-
ных кислот является бактерио- и фунгистатиче-
ской. Неинвазивные бактерии, населяющие кожу,
способны вытеснять более инвазивные организмы
путем выработки антибиотиков, «перехвата» пита-
тельных веществ, необходимых для их жизнедея-
тельности, а также создавая неблагоприятное pH.
Все перечисленные факторы и процессы образуют
самую первую жизненно важную линию иммунной
защиты организма. Именно ее в первую очередь
и разрушает термическое поражение.18 20
Патофизиология. Термическое поражение раз-
рушает клетки или вызывает нарушение их функ-
ции. Степень ожога зависит от температуры и про-
должительное г и воздействия термического агента,
толщины кожи и проводимости тканей. ' Па ри-
сунке 9-2 графически изображена эта температур-
но-временная связь. Ожоговая рана может быть
схематически представлена в виде грех концентри-
ческих зон (рис. 9-3). В центре — наибольшая сте-
пень поражения. Клетки и сосуды здесь разруше-
ны. «Выживание» зоны стаза зависит от факторов,
которые могут бы гь во власти хирурга, но иногда
и не подвластны ему.22 24 В результате гибели
этой зоны частичный по глубине некроз может
охватить всю толщу кожи. Периферическая зона
гиперемии —это область повреждения, поддающа-
яся лечению и заживающая в течение 7—10 дней.
Ожоги делятся прежде всего на две группы:
(а) частичное поражение кожи (1-я и 2-я степени)
и (б) поражение всех ее слоев, на всю глубину
(3-я степень).25 Первые в свою очередь подразде-
ляются на поверхностные (1 степень) и глубокие
(2 степень). Ожоги l-й степени распространяются
до базального слоя эпидермиса. Их отличительные
признаки — образование пузырей, эритема, острая
боль. Заживление происходит в течение 10—
14 дней. Ожог 2-й степени разрушает эпидермис
и распространяется в дерму на различную глуби-
ну. Благодаря глубоким эпидермальным придат-
кам некоторые из этих ран медленно заживают
в течение нескольких недель, часто с выраженным
рубцеванием. Ожог 3-й степени вызывает полную
деструкцию эпидермиса, термы и дермальных при-
датков. Раны при этом часто сухие, плотные, без-
болезненные и самостоятельно не заживают.17
104
ОЖОГИ
Рис. 9-2. Соотношение глубины ожога,
температуры термического лгеитн и дли
тельности его воздействия.
** - выше этого уровня ожоговая поверхность — бледная
* - только до этого уроння можно применять водопроводную воду
Воспалительная реакция на ожоговую гравму
проходит через сосудистую и клеточную фазы
Сначала в течение короткого периода времени воз-
никает вазоконстрикция, сменяющаяся активной
дилатацией. В ожоговой ране существенно увели-
чивается проницаемость сосудов. Медиаторами
этого процесса могут быть гистамин, серотонин,
комплемент, лейкотриены, простагландины и кис-
лородные радикалы. Повышенная проницаемость
сосудов способствует быстрому проникновению
в ожоговую рану белков и других макромолекул
сыворотки, чем и объясняется фаза отека воспали-
тельной реакции. При ожоге более, чем 30% по-
верхности тела, возникает отек и неповрежденных
ожогом тканей, причины которою пока не нашли
достаточно логичного объяснения.26 28 Одновре-
менно с сосудистой реакцией происходит миграция
в рану и скопление в ней нейтрофилов, моноцитов
и тромбоцитов. Эти клетки высвобождают медиа-
торы, модулирующие сосудистую проницаемость,
клеточную миграцию, неспецифическую и специ-
фическую иммунную реакцию. Моноциты могут
играть центральную роль в управлении воспали-
тельной реакцией, а также направлять по опреде-
ленному руслу многие фазы процесса заживления
раны. Существует предположение, что послеожо-
говый гиперметаболизм является результатом дей-
ствия медиаторов, высвобождаемых из макро-
фагов. ‘
Стимуляция процесса свертывания крови и акти-
визация комплемента вызывают блокаду лимфоот-
тока и активизируют клеточную миграцию, вме-
шиваясь в течение сосудистой фазы.
Иммунная реакция. При нарушении структур-
Рис. 9-3. Зоны ожогового поражения.
Подкожная
ткань
Кожа
с дермальными *-
сосочками
Ц| Зона коагуляции
Г ,1 Зона стаза
га Зона гиперемии
ОЖОГИ 105
ной целостности кожи на защиту от повреждения
встает нсспсцифическая иммунная система. Эго
вторая линия защиты, представленная клеточными
и сывороточными компонентами. Первыми из них
являются нейтрофилы и макрофаги. К сывороточ-
ным элементам относятся коагуляционно фибрипо-
литическая система, комплемент и фибронектин.
Сразу после ожоговой травмы активизируются
процесс свертывания крови, а также фибринолити-
ческая и комплементарная системы. Компоненты
СЗА и С5А комплемента увеличивают сосудистую
проницаемость и играют роль хемоаттрактантов,
притягивающих на себя в зону поражения цирку-
лирующие нейтрофилы и моноциты. Сывороточ-
ные факторы действуют как опсонины, которые
усиливают фагоцитоз (нейтрофилами и моноцита-
ми) проникших в ожоговую рану организмов. Фак-
торы свертывания способствуют концентрации лим-
фоцитов и замедлению эфферентного кровотока,
локализуя внедрившиеся микроорганизмы и «под-
готавливая» их к деструкции клеточными элемен-
тами.
Третья линия защиты — специфический имму-
нитет, обеспечиваемый тимус-зависимыми и кост-
номозговыми лимфоцитами. В-лимфоциты диффе-
ренцируются в клетки, образующие специфиче-
ские антитела, способные атаковать бактерии или
клетки, подготавливая их к фагоцитозу клеточны-
ми элементами, или передавать их комплементар-
ной системе, непосредственно лизирующей микро-
организмы без участия фагоцитарных клеток.
Макрофаги передают антиген Т-лимфоцитам, ак-
тивизируя их, в результате чего высвобождаются
лимфокины, стимулирующие В-клегки к продук-
ции специфических антител. Эти активированные
l'-клетки также имеют возможность высвобождать
медиаторы, ускоряющие макрофагальный фагоци-
тоз и продукцию как «клеток-убийц», которые
уничтожают покрытые антителами клетки-мише-
ни, так и цитотоксических Т-клеток. Функция ак-
тивированных Т-лимфоцитов регулируется хел-
перными и супрессорными Г-клетками. При увели-
чении выделения Т-супрессоров подавляется про-
цесс «обработки» антигена, а соответственно и
освобождения лимфокина, что приводит к замедле-
нию и ослаблению иммунной реакции.35 30
Подавление иммунной реакции у ожоговых
больных — хорошо доказанный феномен. Наруше-
ния иммунной системы при этом включают в себя
снижение уровней нейтрофильного фагоцитоза
и хемотаксиса, киллерных свойств нейтрофилов,
макрофагальной активности, лимфоцитарной реак-
ции на митогенную стимуляцию, интерлейкина-2,
фибронектина и гамма-глобулина, а также увели-
чение активности супрессорных Т-клеток. Даль-
нейшая разработка методов управления иммунной
реакцией и уточнение характера циркулирующих
иммунных токсинов может значительно уменьшить
г- 4. 37—50
летальность от сепсиса у ожоговых больных.
ОЦЕНКА ОЖОГОВОЙ ТРАВМЫ
И КЛАССИФИКАЦИЯ ОЖОГОВ
При ожоговой травме прежде всего непосредствен-
но на месте происшествия должно быть как можно
быстрее устранено воздействие повреждающего
агента. В случае химического ожога рану следует
промыть большим количеством воды. Кольца и ча-
сы с рук сразу же необходимо снять, чтобы избе-
жать в последующем сдавления ими. Рану закры-
вают, и больного немедленно транспортируют, обя-
зательно согревая во время транспортировки. При
поступлении пациента с ожогом первую помощь
оказывают ему но всем правилам, принятым для
больных с любой травмой. Серьезное внимание
всегда должно быть уделено дыхательным путям,
тем более если есть указания на ожог пламенем
в закрытом помещении. Обструкция верхних дыха-
тельных путей, особенно у маленьких детишек, мо-
жет возникнуть очень быстро. Больному подается
100% кислород. Должен быть обеспечен доступ
в иену и начато переливание раствора Рингер-лак-
тата из расчета 20 мл/кг за первые 30 мин. Во
всех случаях больших ожогов необходимо поста-
вить назогастральный зонд, а в мочевой пузырь —
катетер Фолея. После оказания первой экстренной
помощи и проведения первичных реанимационных
мероприятий следует тщательно собрать анамнез
и провести детальное обследование. Необходимо
точно определить площадь и глубину ожога. Ис-
пользование при этом правила девяток, как это
делается у взрослых, у детей неприменимо из-за
совершенно иных соотношений размеров частей
тела. 'Гак, голова у новорожденных, по отношению
к поверхности тела, почти в три раза больше, чем
у взрослых, в то время как конечность — в два
раза меньше. Для определения площади пора-
жения следует использовать таблицу Ланда-Брау-
дера (рис. 9-4).51’52 Ребенка необходимо взве-
сить (желательно без одежды и до наложения по-
вязок).
Внутривенно вводят обезболивающие средства.
Внутримышечные и подкожные инъекции у ожого-
вых больных часто не только неэффективны, но
и опасны. Показаниями для госпитализации явля-
ются ожоги 1—2-й степени площадью более 10%
и 3-й степени — более 2%, а также, независимо от
площади, любые ожоги рук, лица, ступней и про-
межности, дыхательных путей, все электро- и хи-
мические поражения и все случаи подозрения на
жестокое обращение с детьми как причину терми-
ческой травмы.17
Лабораторное обследование при поступлении
включает в себя клинический и биохимический
анализ крови и анализ мочи. Производится также
рентгенография грудной клетки. Если подозрева-
ется ожог дыхательных путей или элсктротравма,
необходимо определить газы крови и уровень кар-
боксигемоглобнна, а также сделать ЭКГ.
При отсутствии показаний к госпитализации ле-
чение ожога осуществляется амбулаторно. Имму-
низация против столбняка должна быть проведена
каждому больному, у которого после вакцинации
106 ожоги
Причина «хотя
Дата ожога _
Время «ан»* ______
BoipttcT
Пол _________
Рис. 9-4. Таблица Lund Browder.
(или ревакцинации) прошло более 5 лет, а также
в том случае, когда дата последней иммунизации
нс известна. Те, кто не был ранее иммунизирован
или иммунизирован, но неадекватно, должны по-
лучить 250 ЕД столбнячного иммуноглобулина.
Следует начать курс активной иммунизации. В тех
случаях, когда ребенок госпитализируется, прово-
дят обработку раны, осторожно промывая ее вод-
ным мыльным раствором и удаляя все нежизне-
способные ткани и пузыри. На ладонях и ступнях
пузыри можно не удалять. После того, как рапа
очищена, на нее обильно наносят сульфалиазин
серебра (сульфаден) или другие препараты. При
локализации ожога на конечности, накладывают
свободную повязку. Во всех случаях циркулярных
ожогов следует произвести разрезы струпа, кото-
рые можно осуществить непосредственно в палате,
у постели больного, без анестезии, используя ост-
роконечный термокаутер.
ИНФУЗИОННАЯ ТЕРАПИЯ
Диапазон растворов, применяемых при инфузион-
ной терапии у ожоговых больных, чрезвычайно
широк — от чистых коллоидов до комбинации кол-
лоидов-кристаллоидов и^о исключительно крис-
таллоидных растворов. ' ' В составе любого
из переливаемых растворов обязательно должен
быть натрий. Принципы, используемые для расче-
тов необходимого объема жидкости у взрослых па-
циентов, пс могут быть перенесены в педиатрию.
Совершенно иные соотношения поверхности тела
и массы и более высокая скорость метаболических
процессов в детском возрасте приводят к значи-
тельным ошибкам, когда эти расчеты применяются
у детей. Наиболее рационально использование мо-
дифицированной формулы Паркланда, предусмат-
ривающей ежедневное введение раствора Рингер-
лактата из расчета 3—4 мл/кг/% ожога. Полови-
на этого объема дается за первые 8 часов, вторая
половина за оставшиеся 16 часов. Данная схема
теласт инфузионную терапию простой в практиче-
ском применении, недорогостоящей и безопасной.
Введение в схему коллоидных растворов увеличи-
вает стоимость лечения, не предоставляя при этом
никаких особых преимуществ. При использовании
гипертонических растворов требуются относитель-
но малые объемы жидкости и в меныней степени
развиваются отеки, однако существует значитель-
ный риск возникновения гипернатриемии, гиперос-
молярной комы, почечной недостаточности и алка-
лоза.53 В литературе существует даже описание
случая центрального понтинного миелинолиза при
гиперосмолярной коме у ожогового больного.5" Ин-
фузионную терапию необходимо постоянно регу-
лировать и корригировать. В каждой данной ситуа-
ции ребенок может, в зависимости от реакции на
лечение, потребовать больший или меньший объем
жидкости. Более глубокие ожоги и поражение ды-
хательных путей значительно увеличивают по-
требности в жидкости.59
При проведении инфузионной терапии следует
ориентироваться прежде всего на состояние функ
ции жизненно важных органов, величину диуреза
и самочувствие больного Диурез должен поддер-
живаться на уровне не ниже 1 мл/кг/час у детей
с массой тела до 30 кг и не меньше 30 40 мл/час
при массе тела выше 30 кг. Надежным индикато-
ром успешности проведения жидкостной терапии
является отсутствие нарушений функции внутрен-
них органов. Этот показатель имеет большее зна-
чение, чем ориентация на поддержание определен-
ного уровня центрального венозного давления.
Потеря жидкости, связанная с увеличением про-
ницаемости капилляров, отмечается в наибольшей
степени в первые 12 часов после ожога и прогрес-
сивно уменьшается п последующие 12 часов. Поэ-
тому коллоиды необходимо вводить со вторых су-
ток, в дальнейшем ежедневно повторяя их введе-
ние для поддержания альбумина сыворотки на
уровне не ниже 290 мкмоль/л. Скорость введения
кристаллоидов может быть уменьшена до поддер-
живающего уровня и регулироваться в зависимо-
сти от диуреза.69 В течение вторых суток после
ожога вводят 5% декстрозу в физиологическом
растворе. Через 12 часов после травмы начинают
питание через зонд, что улучшает функцию ки-
шечника и стимулирует иммунные процессы.
ПИТАНИЕ БОЛЬНОГО С ОЖОГОМ
Метаболическая реакция организма ребенка на
тяжелую ожоговую травму может быть рассмотре-
на во временной последовательности.41 Первые
ОЖОГИ 107
24- 48 часов характеризуются как период относи-
тельного гиперметаболизма, который сменяется
фазой выраженного катаболизма и массивной по-
тери тканевого белка и жира. Эта фаза продолжа-
ется до тех пор, пока остается открытой рана, и ее
течение нередко усугубляется эпизодами инфек-
ции, ознобов, стресса, боли, беспокойства и опера-
тинными вмешательствами. Как только раны
закрыты, метаболизм начинает нормализоваться,
и в этом периоде доминируют анаболические про-
цессы с восстановлением белковых запасов в тка-
нях и органах.
Для катаболической фазы ожоговой травмы ха-
рактерно увеличение уровня кортизона, адренали-
на, норадреналина, глюкагона, альдостерона и ан-
тидиуретического гормона.64 Скорость основного
обмена может при этом возрастать вдвое. У детей
с низкими запасами жира и небольшой мышечной
массой быстро развиваются нарушения белкового
обмена, если не обеспечено адекватное пита-
7. 65. 66
нис, поскольку через ожоговую рану происхо-
дят значительные потери белка.
Для удовлетворения калорических потребностей
обожженных детей существуют различные пита-
тельные растворы и смеси, ” которыми обычно
обеспечивают поступление 1800 ккал/м2 плюс
2200 ккал/м2 ожоговой поверхности.60 Энергетиче-
ские затраты больного в покос достаточно точно из-
67. 69. 71
меряются методом непрямой калориметрии.
Данные исследований, проведенных у детей пер-
вых 3 лет жизни с ожогами более 50% поверх-
ности тела, показали, что потребности в питании
могут быть удовлетворены обеспечением 120—
200% показателей скорости основного обмена
в покое.70 Эти цифры даже несколько меньше тех,
что предусмотрены большинством растворов, при-
меняемых у данной категории больных.
Белок должен составлять 20—25% общего кало-
ража, углеводы — 40—50% и жиры — оставшиеся
калории.7,72,73 Применение современных модифи-
цированных питательных растворов и смесей сни-
жает иммунную супрессию, интенсивность метабо-
лических реакций и летальность, уменьшает дли-
тельность пребывания больного в стационаре
и укрепляет барьерные (в отношении проникнове-
ния бактерий) свойства желудочно-кишечного
тракта (ЖКТ).74 76 Эти растворы покрывают 20%
энергетических потребностей за счет сыворото-
чного белка, 2% — аргинина, 0,5% — цистина,
0,5% — гистидина и 15% —за счет липидов. По-
ловина жировых калорий обеспечивается рыбьим
жиром и 50% — растительным (сафлоровым) мас-
лом. Оставшиеся калорические потребности удов-
летворяются за счет углеводов.
Оптимальным способом питания является, несо-
мненно, энтеральный, требующий в большинстве
случаев постановки желудочного зонда.76 Зондовое
энтеральное питание лучше усваивается в тех слу-
чаях, когда альбумин сыворотки удерживается на
уровне 360 мкмоль/л или даже выше. Если при
данном способе питание не усваивается, то необхо-
димо переходить к парентеральному методу, тре-
бующему обычно постановки центрального катете-
ра, поскольку через периферические вены редко
можно обеспечить адекватный калораж.77 Необхо-
димо ежедневное измерение массы тела и расчет
получаемого калоража. У больных, находящихся
на зондовом питании или парентеральной гипера-
лиментации, следует также ежедневно определять
уровни сывороточных электролитов, .мочевины,
креатинина, альбумина, глюкозы, фосфора, каль-
ция, гемоглобина, гематокрит, глюкозу мочи. Еже-
недельно исследуются показатели функции пече-
ни, преальбумин, трансферин, магний, холестерол,
тригл и церин.
Все обожженные дети должны получать по мень-
шей мере минимальную рекомендуемую суточную
норму (РСН) витаминов, минеральных веществ
и микроэлементов. Витамин С добавляется к вво-
димым растворам или смесям в количестве 5—
10 РСН, цинк — 2 РСН, витамины группы В не
меньше 2 РСН.72
МЕСТНОЕ ЛЕЧЕНИЕ ОЖОГОВЫХ РАН
Большинство (95%) ожогов у детей небольшие
и могут лечиться амбулаторно. Перевязку произво-
дят дважды в день—рану промывают, очищают,
наносят полимиксин В сульфат (полиспорин) или
бацитрацин и накладывают марлевую повязку. За-
живление обычно происходит в течение 10—
14 дней.57 Поверхностные небольшие ожоги можно
также лечить с применением полупроницаемых
синтетических пленок, которые облегчают домаш-
r 7R. 79
нии уход и уменьшают боль.
При ожогах третьей степени, когда глубина
поражения не вызывает сомнений, показана некрэк-
томия с закрытием раны аутотрансплантатом. Вме-
шательство осуществляется сразу, как только ста-
билизирована гемодинамика. Однако важно отме-
тить, что в ранние сроки бывает трудно опреде-
лить глубину поражения, особенно при ожогах
горячей жидкостью, которые как раз и встречают-
ся у детей наиболее часто. В то же время раннее,
слишком активное хирургическое лечение всех ран
при ожогах 3-й степени (даже при наличии сомне-
ний в правильности определения глубины ожога)
чревато потерей значительного количества тканей,
причем порой и в тех случаях, когда рана могла
бы зажить и самостоятельно без выраженного руб-
цевания. Поэтому при неясной глубине ожога не-
обходимо, воздержавшись от некрэктомии, дважды
в день производить перевязку (туалет раны, мест-
ные препараты) до тех пор, пока не станет воз-
можным (по появившимся четким признакам) до-
стоверно определить глубину поражения (это за-
нимает обычно 10—14 дней).6’
Идеальные средства для местного лечения дол-
жны при использовании не вызывать болезненных
ощущений и аллергических реакций, предотвра-
щать высыхание, глубоко проникать в ожоговую
рану и обладать бактерицидно-бактериостатиче-
скими свойствами. Препарат не должен ни препят-
ствовать эпител изаци и, ни отрицательно воздейст-
вовать на жизнеспособные клетки.80 Сильваден,
хотя и не является идеальным средством, но отве-
108
ОЖОГИ
чает почти всем перечисленным требованиям
в большей степени, чем любой другой препарат.
Его применение безболезненно, дает минимальные
побочные эффекты, он незначительно абсорбиру-
ется и обладает хорошим антибактериальным
спектром.*11 81 При обширных ожогах более эффек-
тивна комбинации нитрата церии и сульфадиазина
серебра. Компонент церия препятствует развитию
грамотрицатсльных организмов, а сульфадиазин
серебра оказывает влияние на грибковую и грам-
положительную флору. Ценным препаратом про-
должает оставаться мафенид, благодари своей спо-
собности проникать через ожоговый струп и актив-
но воздействовать как на грамотрицатсльную, так
и на грамположительную флору.82 Противогрибко-
выми свойствами он, однако, не обладает. Некото-
рые другие лекарства для местного применении
перечислены в таблице 9-1, где в отношении каж-
дого из них указаны преимущества, ограничения
и показания к применению.
Важный аспект ухода за раной, особенно при
ожогах кисти, — обеспечение конечности опреде-
ленного положения. Сопутствующие ожогу отек,
воспаление и ограничение движений — три глав-
ные силы, которые ведут к нарушению функции,
а потому требуют соответствующих профилакти-
ческих мероприятий. Лечебная гимнастика, возвы-
шенное положение конечности, адекватная иммо-
билизация шиной и раннее закрытие раны способ-
ствуют снижению инвалидизации Шину накла
дывают в функциональном положении кисти. Под-
нимание и активные упражнения руки должны
начинаться в очень ранние сроки. Со всеми суста-
вами надо заниматься активно и пассивно несколь-
ко раз в день.
Глубокие ожоги промежности нс требуют хирур-
гического отведения мочи и кала. Анализ 20-лет-
него опыта лечения ожогов данной локализации не
выявил увеличения инфекционных осложнений,
связанного с отказом от наложения кишечных
и мочевых свищей.5
ОБЕЗБОЛИВАНИЕ
К сожалению, обезболивание у детей редко осуще-
ствляется должным образом. Восприятие боли
ребенком часто существенно отличается от вос-
приятия боли как собственной, так и чужой, меди-
цинским персоналом, принимающим участие в ле-
чении детей.84 86
Обезболивание может проводиться как нсфар-
макологи вескими, так и фармакологическими сред-
ствами. Разной степенью эффективности в этом
плане обладают гипноз, иглоукалывание, приме-
нение чрескожных электростимуляторов нервов
(ЧЭСН). Большое значение имеет и вспомога-
тельный нефармакологический подход к снятию
боли у детей,85 дающий хорошие результаты
и включающий следующие ключевые компоненты.
1. Перед перевязкой ребенку рассказывают, что
ему собираются делать, и продолжают беседовать
с ним во время манипуляции.
2. Необходимо сделать акцент па том, что для
успешного проведении перевязки абсолютно необ-
ходима помощь самого пациента.
3. Важно объяснись и постараться убелить ре-
бенка в том. что в данном случае для лечения вы-
браны методы, наиболее подходящие и наилучшие
именно для него.
4. Медсестра, принимающая участие в перевяз-
ке, должна поддерживать психологическую «игру»,
отвлекая периодически внимание ребенка и говоря
в частности о том, сколько времени займет про-
цедура и что это самая малая продолжительность,
какая только возможна.
5. Внимание ребенка фокусируют на задаче бы-
стрейшего выздоровления, при этом ему может
быть разрешено смотреть на обожженную поверх-
ность и ее обработку с акцентом в разговоре на
явно положительную динамику.
6. Ребенка чаще надо хвалить во время перевяз-
ки, говоря о том, какую неоценимую помощь он
оказывает своим активным участием.
7. Необходимо всегда назначать время следую-
щей перевязки, чтобы ребенок знал об этом, а нс
пребывал в состоянии тревожно-неопределенного
ожидания.
8. Очень важно понимать, что ни одного ребен-
ка никакого возраста нельзя заставить (и не надо
пытаться) делать что-либо, если он не хочет или
нс готов к этому.
Не следует скупиться на введение наркотиков
при проведении болезненных процедур и про-
сто при усилении самостоятельных болей. Естест-
венно, дети намного больше предпочитают ораль-
ное введение внутримышечному. Для внутривенно-
го применения достаточно эффективен и меньше
всего вызывает угнетение дыхания налбуфин (ну-
баин). При наличии устойчивости к нему может
быть использован морфин. Эффективным препара-
том морфина для орального введения является рок-
санол. При показаниях к применению наркотиков
длительного действия для снятия упорных посто-
янных болей препаратом выбора считается мета-
дон. Меперидин (демерол), хотя и является нарко-
тиком короткого действия, однако может вызывать
продолжительную выраженную токсическую реак-
цию. Фентанил — чрезвычайно эффективный нар-
котический анальгетик, который следует «прибе-
речь» для использования при сильных болях. Кро-
ме тою, его применение ограничивается быстрым
развитием привыкания, а также высокой стоимо-
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
Методы обезболивания. Анестезиолог всегда
должен быть готов к возможной массивной и бы-
строй кровопотере. Постоянного внимания требует
и поддержание нормальной температуры тела
и температуры в операционной на уровне 29—
32 °C. Подогреваемая одежда и грелки должны
быть под рукой и в рабочем состоянии. Если не
предполагаются манипуляции на голове, она дол-
жна быть закрыта для предотвращения потери теп-
ожоги
109
ТАБЛИЦА 9-J. Препараты для местною лечения
Препарат KOHUCtt- Гр.ЩИЯ •lai iuia применения Метол ведения рины Преимущества Недостатки, побочные эффекты, ограничения к применению Камерна илыи спектр Показания
Сульфа- диазин серебра 1% каждые 12 час Откры- тый или Незначительная абсорбция, редкие побоч- Повышенная чувстви- тельность к препарату в 4 8% случаев, по- давляет лейкоциты, к Грамиол. кокки. Грамотр. флора устойчива к
закры тый ные реакции, широкий ан- тимикробный спектр препарату, включая кншеч ную палочку, Fschvrichia coli и грибы
препарату устойчивы грамм рица тельные организмы, особенно enierobacter. нс эф- фективен при ожогах площадью > 60%
Мафе- на мид 10% каждые 12 час Откры- тый или ми ни- молы» Быстрое про- никновение через орун, широким бак- териальный снек гр Бактериальная уеюйчм- воегь к препарату, особенно Providciicia stuarii и грибов. Метабол, ацидоз, ды Широкий i рамен р. и Грамши, спектр. Не дей- ствует па гриб- ковую флору.
закры- тый хательная недоста точи., болезненность и быстрая абсорбция Особенно эф {ректипеп в от- ношении Pseudomonas
Н и।ра। серебра <1.5% смачи- вать каждые 2 часа Закры- тый Устойчивость к препарату от- мечается ред- ко, безболез- ненность Чрезвычайно «пачкаю- щий» рану и белье; гипонатриемия, гипо- калиемия; из-за ок раски препа ра том трудно определять со- стояние раны Грампол., грибы, некоторые грамотр.
Гентами- цин 0.1% каждые 12 час Хорошо дейст- вует на грам- отр. флору, особенно PxEudoinonax Высокая скорость аб- сорбции до токсиче- ского уровня, развитие устойчивости к препа- рату Грамотр.
Первоочередной пре-
парат при обшир-
ных ОЖОГ. IX
Инфицированные
ожоговые раны или
небольшие по ило
щади глубокие ожо-
ги, например, элек
гроожш и
Oxoi и площадью до
50%. для профи-
лактики, у больных
с аллергической ре
акцией на сулыра-
нил.тмиды
Церия нитрат — суль- фа дин- зип серебра 2.2% 1% каждые 12 час Закры- тый Низкая токсич- ность. слабая абсорбция, эффективен при обшир- ных ожошх Такие же. как у сульфа- В дополнение к
диазина серебра спектру суль- фа д низ и >ы се- ребра прекрас- ным грамотр. згффект
Povidone/ iodine 1% каждые 12 час Откры гый или за крыт ыи Широкий бак термальный спектр Инактивируется экссу- датом, болезненный, быстрая абсорбция с мысоким уровнем йода, метаболический ацидоз Широкий
Scarlet red (азо- краси- тель) 5% Закры- тый Безболезнен- ность. може । ускорять эни- тслизацию Метгемоглобинемия, ду- бильное действие на кожу и рану, очень «пачкающий» препа- рат Действует бактс- риостатически, создавая низ- кое pH окруж. среды
Нитро- фура- зоп (фура- ЦН.1ИН) каждые 24 часа 1 hviyau- кры гый Нет Инактивируется ране- вым экссудатом Ограничен
Кратковрем. лечение
небольших ижплн!,
инфицированные
раны у бальных с
аллерг. реакцией на
сульфа пил амиды,
должен контролиро-
ваться уровень пре
unpaid в крови
Обширные ожоги
60 80%
Нсоспо- по мере Откры- Можно испоив Достигает токсического
рип/ необ- тый зовать па ли- уровня при больших
Бацит- ходи- или за- це. не токен ожогах
рацин мости крытым чем тля глаз
Небольшие ожоги, мо-
жет быт эффекти-
вен при «мягких»,
трудных для иссече-
ния ранах, в тече-
ние 24 час до иссе-
чения
Донорские участки,
возможно исполь-
зование при поверх-
ностных ожогах у
амбулат. больных
Небольшие поверх
пос гн. ОЖОП1 с ма-
лом возможное гью
инфицирования, ал-
лергия к сульфа
и ила мидам, на сет-
ча тыс ।ранспланта
ты
Поверхностные ожоги
у амбулат. больных
и ожоги лица при
лечении открытым
способом
110 ожоги
ла. При большинстве обширных процедур у ожого-
вых больных снижение температуры тела почти
неизбежно. Если тщательно контролировать и под-
держивать температуру окружающей среды и
внутривенно вводимых растворов, то гипотермию
можно свести к минимуму. Четкая организация
проведения опсраиии и координация действий всех
участников укорачивают ее продолжительность
и соответственно уменьшают потери тепла. Дол-
жны быть поставлены две внутривенные линии
(с широким просветом). В ряде клинических ситу
аций могут возникнуть показания к постановке
и артериального (или центрального венозного) ка-
тетера, а также уретрального.
У ожоговых больных иногда отмечается необыч-
ная реакция на некоторые лекарственные препара-
ты.*’ Так, деполяризующие мышечные релаксанты,
такие как дитилин, могут вызвать быстрое высво-
бождение калия. Устойчивость же к действию не-
деполяризующих препаратов возрастает с увеличе-
нием процента ожоговой поверхности. У больных
с ожогами отмечается также невосприимчивость
к тиопенталу, которая сохраняется длительное вре-
полного заживления
ожоговых
мя даже после
ТО. 90—97
ран.
Анестезия, обширная обработка раны, пластика
и гипотермия — все эти факторы, будучи объеди-
нены, усиливают метаболический стресс. При этом
вслед за общей анестезией и оперативным вмеша-
тельством отмечается значительный подъем уров-
ня катехоламинов и сопутствующее увеличение
продукции мочевины.™ Ослабить эту стрессовую
реакцию можно путем ограничения длительности
операции, объема кровопотери и колебаний темпе-
ратуры.
В послеоперационной палате продолжаются все
те мероприятия, которые проводились в операци-
онной. Особенно важно поддержание нормальной
температуры тела и адекватного дыхания. Фарма-
кологическая «загруженность» больного, сдавлива-
ющие повязки и гипотермия могут способствовать
снижению эффективности вентиляции.
Оперативное лечение. Хирургическое лечение
показано при ожогах 2-й и 3-й степени. Раннее
иссечение и пластика сокращают длительность
пребывания больного в стационаре, исключают необ-
ходимость частых болезненных перевязок и умень-
4. 99, К <
шают среднюю стоимость лечения.
Три вида нскрэктомии наиболее широко приме-
няются в клинической практике.61 Первый заклю-
чается в последовательном иссечении струпа и под-
разумевает ежедневное очищение раны и 1 или
2 раза в неделю сеансы иссечения ножом (с огра-
ничителем) наиболее плотных участков. Подобная
тактика приводит к очищению гранулирующего
ложа через 2—3 недели, после чего и производят
пластику. Данный метод можно использовать в тех
случаях, когда изначально невозможно определить
глубину ожога.
Второй метод — первичное иссечение до фасции
электрокаутером или скальпелем. При этом спосо-
бе меньше кровопотеря, и пластика производится
на гарантированно жизнеспособное ложе. Кроме
того, точное определение глуоины поражения
здесь не так важно, как при последовательном ис-
сечении. Данный метод к тому же может быть ис-
пользован не столь опытным хирургом. Этот вид
иссечения нс должен применяться на руках, лице,
шее, поскольку получается значительный космети-
ческий дефект. Р.го можно использовать на прокси-
мальных участках конечностей и на туловище. Но
даже в этих областях функциональные и космети-
ческие результаты иссечения до фасции часто неу-
довлетворительные. В одном из обобщенных ана-
лизов применения этого способа в течение первых
24 часов после травмы у 594 детей, отмечено сокра-
щение кровопотери в два раза. Кроме того, всегда
было возможно полностью закрыть дефект сетча-
тым трансплантатом, перфорированным в соотно-
шении 1 : 3, и сверху гомотрансплантатом. Участ-
ки, недостаточно прикрытые аутотрансплантатом,
закрывались гомотрансплантатом. Длительность
пребывания в стационаре, количество болезненных
перевязок и частота присоеди нения инфекции бы-
ли значительно снижены. Однако существенного
уменьшения летальности нс отмечено.
Третий вид операции — тангенциальное иссече-
ние, которое подразумевает последовательное уда-
ление тонких слоев ожогового струпа до тех пор,
пока не достигается чистое жизнеспособное ложе.
Эта техника требует большого опыта, позволяю-
щего определить — когда же глубина иссечения до-
статочна. Значительное преимущество этой техни-
ки в том, что часто могут быть сохранены при ожо-
гах 2-й степени элементы дермы, а при ожогах
3-й степени — жировая ткань. Если глубина ожога
нс ясна и остается нежизнеспособная ткань, ауто-
трансплантат, столь ценный, утрачивается. Танген-
циальное иссечение может сопровождаться массив-
ной кровопотерей. Для ее уменьшения мы на ко-
нечностях традиционно используем жгут. При
вмешательствах на туловище снизить кровопотерю
помогает введение под струп адреналина в раство-
ре Рингер-лактата. Тангенциальную некрэкгомию
обычно ограничивают 15—20% поверхности тела
за один сеанс. Используя жгут и введение под
струп раствора адреналина мы обычно производи-
ли значительно более обширное иссечение, при
этом с кровопотерей, вполне допустимой по
объему.
Большинство иссеченных ран могут быть сразу
закрыты кожным трансплантатом. При наличии
тяжелого кровотечении или неуверенности в адек-
ватной глубине иссечения, раны можно закрыть
мелкосетчатой марлей и толстой влажной повяз-
кой. Трансплантация откладывается при этом на
сутки.
В любой области, где берется трансплантат,
можно ввести подкожно раствор Рингер-лактата,
что делает поверхность кожи плотной и облегчает
таким образом взятие трансплантата. Применение
для введения раствора специального насоса умень-
шает продолжительность процедуры и позволяет
вводить жидкость с определенной температурой
(температурой тела). При этом подкожная инфиль-
трация всей спины может быть осуществлена ме-
ОЖОГИ 111
нее, чем за 10 мин. Трансплантаты перфорируют
в соотношении 1 : 1,5 или более (в зависимости от
необходимой величины аутотрансплантата) и под-
шивают на подготовленное ложе. Если трансплан-
таты растянуты очень широко, например в соотно-
шении 1 : 3 или 1:4, то сверху накладывают гомо-
трансплантат.
Перфорированные трансплантаты должны быть
покрыты мелкосетчатой марлей и толстой повяз-
кой. С помощью катетеров, поставленных изна-
чально через повязку, можно в течение первых
4—5 дней увлажнять трансплантаты раствором
антибиотиков (в тройной дозе). Используя данную
методику, мы отмечаем прекрасное приживление
трансплантатов. Главная причина утраты транс-
плантата — недостаточно подготовленное (иссе-
ченное) ложе, инфекция, высыхание и механиче-
ский разрыв.
Общераспространенным методом становится в
настоящее время использование выращенной куль-
туры эпителиальных клеток. Другое перспектив-
ное направление — иммунносупрессивная терапия,
позволяющая более широко использовать гомо-
трансплантаты. Если бы можно было обеспечить
иммунную толерантность, то гомотрансплантаты
могли быть использованы как постоянное покры-
тие. Эти развивающиеся технологии очень важны
и перспективны, особенно в лечении детей с об-
ширными ожогами, у которых возможности взятия
аутотрансплантатов чрезвычайно ограничены.
ПОРАЖЕНИЕ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Ингаляционные поражения отмечаются у 15 18%
больных с ожогами, поступающих в стационар,
и именно они являются причиной от 30 до 80%
всех летальных исходов при ожогах.1<и 110
Ингаляционные ожоги возникают в результате
прямого действия высокой температуры и/ил и ток-
сического химического поражения. Сухой воздух
с температурой 500* С охлаждается почти до
50° С за время, пока он достигает карины. Что же
касается химических веществ, среди них есть те,
что вызывают токсический эффект в результате
абсорбции, и те, что повреждают трахеобронхиаль-
ную выстилку при непосредственном контакте
с ней." Наиболее токсичны окись углерода и циа
ниды, быстро приводящие к фатальному исходу."2
Токсические химические вещества прямого кон-
тактного действия разнообразны. В обгоревших
материалах и резине обнаруживается поливинил
хлорид, который является источником альдегида,
соляной кислоты и хлора. При сгорании нейлона,
резины, шелка, продуктов нефти высвобождается
аммиак. Все эти и различные другие вещества вы-
зывают непосредственное повреждение слизистой
дыхательных путей.
Оценка больного с ожогом дыхательных путей
должна прежде всего включать в себя тщательное
выяснение анамнеза. К линически отмечается боль
в горле, хрипота, дисфагия, кашель, выделение
мокроты с примесью гари, стридор, гиперемия но-
са, тахипноэ, беспокойство, спутанность сознания
или возбуждение. При обследовании можно обна-
ружить опаленные волосы в носу, ожоги лица^при
аускультации — хрипы и свистящее дыхание.
Иногда же тяжелые ингаляционные повреждения
протекают нс только бессимптомно, но даже с нор-
мальными лабораторными показателями."6
В первые сутки может развиться острая дыха-
тельная недостаточность с переходом в отек лег-
ких и пневмонию. Наиболее точно ингаляционную
травму можно диагностировать с помощью бронхо-
скопии (гибким бронхоскопом) или ксенон-133-
IO7. 114, 117
сканирования.
Лечение ингаляционных поражений начинают
на месте происшествия. Необходимо прежде всего
обеспечить подачу 100% кислорода, который уско-
ряет элиминацию окиси углерода фактором 5.
Увлажнение вдыхаемого газа, подача кислорода
и тщательный туалет дыхательных путей — глав-
ные компоненты неотложной терапии. Стероиды
не следует применять при лечении ингаляционных
поражений. Антибиотики используют только в тех
случаях, когда есть явные, объективно подтверж-
денные признаки инфекции. Показанием к интуба-
ции и вентиляционной поддержке является любой
из следующих симптомов и факторов: (1) нараста-
ющий стридор с явными признаками отека верх-
них дыхательных путей и обструкции; (2) гипоксе-
мия; (3) невозможность освобождения дыхатель-
ных путей от мокроты; (4) неэффективность само-
стоятельного дыхания, несмотря на рассечение
струпа при циркулярных ожогах грудной клетки;
(5) повышение внутричерепного давления в ре-
зультате гипоксии мозга."6
При ингаляционном поражении потребность
больного в жидкости может увеличиваться на 50%.
А потому неадекватная инфузионная терапия спо-
собствует развитию осложнений и может усугу-
бить тяжесть ожоговой травмы и иммуннологиче-
ских нарушений.
ЭЛЕКТРООЖОГИ
В большинстве ожоговых отделений на электро-
травму приходится менее 5% всех термических по-
ражений. Тяжесть электроожога зависит от силы
тока, напряжения и длительности воздействия.
В тканях, обладающих значительной сопротивляе-
мостью, таких как сухая кожа и кости, высоко-
вольтный ток генерирует очень высокую темпера-
туру. В результате термического поражения, диф-
фузных сосудистых расстройств и интенсивного
отека мышц, заключенных в фасциальные влага-
лища, возникает мышечный некроз. Сосудистые
изменения носят прогрессирующий характер
вплоть до развития в последующем аневризмы
аорты.
Неврологические нарушения могут вылиться
в кому, эпилептиформные припадки и перифериче-
ские невриты. Поздние неврологические расстрой-
ства иногда являются следствием прогрессирующей
сосудистой окклюзии и демиелинизации. Причем
симптомы перечисленных проявлений электроожо-
гов со стороны нервной системы норой становятся
112 ОЖОГИ
явными лишь через длительный промежуток вре-
мени (до двух лет) после травмы. В некоторых
случаях в результате мощного судорожного сокра-
щения мышц возникают даже костные некрозы
или переломы.
Переменный ток низкого напряжения может вы-
звать фибрилляцию желудочков и остановку сердца,
а также судороги дыхательной мускулатуры и ас-
фиксию.11* Сердечно-легочная реанимация (СЛР)
должна проводиться очень интенсивно, поскольку
при электроожогах активные реанимационные ме-
роприятия часто бывают успешными. Большинство
электроожогов у детей вызваны током низкого на-
пряжения и обычно происходят дома. Наиболее
распространенный механизм подобной транмы —
контакт источника тока с губами. Очень мощное
поражение вызывают высокие температуры элект-
рическои дуги. Ожог в результате воздейст-
вия тока высокого напряжения проявляется обуг-
ливанием в области «входа» тока и разрушитель-
ным «гашением» на том участке тела, где происхо
дит заземление (рис. 9-5). Часто при наличии,
казалось бы, жизнеспособной кожи, о глубине и тя-
жести поражения говорят миоглобинурия и повы-
шенные цифры креатинфосфокиназы (КФК).
В связи с этим необходимо проводить инфузию
раствора Рингер-лактата и поддерживать диурез
на уровне не ниже 1.5—2,0 мл/кг/час. Поскольку
продукты распада миоглобина обладают нефроток-
сическим эффектом, то добиваться адекватного ди-
уреза следует с помощью манитола и жидкостной
нагрузки, при этом моча должна ощелачиваться.
Необходимо тщательно оценить состояние мышц
и при наличии показаний произвести раннюю фас-
циотомию, чтобы предупредить возможное разви-
тие в последующем «сотрагНпепи-синдрома (англ,
compartment — отделение, отсек, ячейка) — отека
мышц, замкнутых в фасциальных влагалищах, что
может привести в результате к мышечной атро-
фии, связанной со сдавлением сосудов. Высоко-
вольтные ожоги требуют частого очищения раны
от некротизированных тканей, ибо возникшие из-
менения бывают прогрессирующими, и соответст-
венно необходим регулярный контроль. Иногда да-
же могут возникнуть показания к ранней ампута-
ции.12" Как только раны (Остаточно очистились
и остановлено прогрессирование сосудистого тром-
боза и тканевого некроза, может быть произведена
пластика расщепленными кожными транспланта-
тами.
ЗАКРЫТИЕ ОЖОГОВЫХ РАН
Покрытия ожоговых ран должны обладать по
меньшей мере одним или несколькими следующи-
ми качествами: (1) паро- и газопроницаемость, (2)
прилипание к рапе, (3) подавление бактериального
роста, (4) возможность прорастания сосудами. Все
покрытия могут быть подразделены па синтетиче-
ские и биологические. Биологические в свою оче-
редь представлены двумя видами: выращенная
культура эпителиальных клеток и различного
рода трансплантаты. Некоторые исследователи
считают, чго культурированиые эпителиальные
клетки дают превосходный результат лишь при ис-
пользовании их для кожной пластики в отдален
пые сроки. По их мнению, при ранней пересадке
культурированных эпителиальных клеток отмеча-
ется значительная их утрата (в среднем 50—60%).
Малый процент приживления и чрезвычайно высо-
кая стоимость ограничивают применение этого
метода у больных с небольшими ожогами. Для по-
крытия ран используется также двухслойная ис-
кусственная кожа, состоящая из силиконовой мем-
Рис. Я 5. Л, 4 летний ребенок с высоко
вольтным ожогом. Мощное разруши-
тельное воздействие о области «заземле-
ния» на обеих ступнях.
В, Воздействие тока в области его
«входа» на левой руке привело к полно-
му ее разрушению. Dtot ребенок по-
страдал также и от интенсивного воз
(ейстния элекгродуги, о чем свидетель
стпует ожог всей передней поверхности
грудной клетки и паховой области.
ОЖОГИ 113
б раны и коллагеновой основы. Рана после иссече-
ния закрывается этим материалом и, как только
произошла достаточная васкуляризация коллаге-
новой основы (обычно примерно за 30 дней), сили-
коновая пленка удаляется и замещается тонко-
слойным аутотрансплантатом или культивирован-
ными эпителиальными клетками. Считается, что
при использовании двухслойной искусственной ко-
жи в меньшей степени образуются контрактуры,
а рубцевание происходит не столь грубое.
Еще один метод закрытия ожоговых ран заклю-
чается в нанесении культуры эпителиальных кле-
ток на механически деэпитслизиронаиную труп-
ную кожу, которая играет таким образом роль
коллагеновой основы. Это покрытие, по данным
литературы, дает незначительное рубцевание н хо-
рошие косметические результаты — трансплантат
очень близок по внешнему виду к нормальной
коже. И совсем новый пластический материал пред-
ставлен культурой эпителиальных клеток, нанесен-
ных на дермальную основу, сделанную из культу-
рированных человеческих фибробластов, инкорпо-
рированных в коллагеновую неклеточную глюко-
за ми игл и каповую мембрану.126
Синтетические и биологические покрытия требу-
ют очень тщательного наблюдения за больными.
В литературе имеются сообщения о синдроме ток-
сического шока у детей, лечившихся с применени-
ем синтетических раневых покрытий и трансплан-
татов из чужеродных материалов.127
РЕАБИЛИТАЦИЯ
При лечении ожогов преследуются две главные це-
ли — сохранение жизни больного и снижение фи-
зической и эмоциональной инвалидизации. Меро-
приятия, направленные на решение этих задач, на-
чинаются с момента поступления обожженного
ребенка. «Качество выживания» детей с ожогами
зависит от возможности свести к минимуму физи-
ческую и эмоциональную инвалидизацию. Актив-
но участвовать в достижении поставленных целей
должна вся ожоговая «команда», ведущими «игрока-
ми» в которой, несомненно, является персонал, зани-
мающийся с ребенком трудотерапией и лечебной
физкультурой. Несколько факторов определяют
степень физической инвалидизации в результате
ожоговой травмы. Их можно условно разделить на
внутренние и внешние- К внутренним относятся:
(1) анатомическая локализация ожога, (2) глубина
поражения, (3) качество заживления, (4) генетиче-
ская предрасположенность к образованию рубцов,
(5) физиологическая сократительная способность
тканей, (6) степень зрелости организма и (7) воз-
раст. С глубиной ожога, возрастом пациента и ге-
нетическими качествами связаны возможность раз-
вития гипертрофических рубцов и скорость зажив-
ления ожоговых ран. Чем меньше ребенок, тем
больше склонность к образованию гипертрофиче-
ских рубцов. Причем у маленьких детей рубцы
формируются намного метл с инее, чем у более
старших пациентов. Внешние факторы включают
в себя: (I) оперативные вмешательства (ранняя
некрэктомия, пластика), (2) диспансерное наблю-
дение и (3) выполнение пациенто.м и родителями
всех назначений. В этом плане очень важны посто-
янные регулярные занятия (активные и пассивные
упражнения), соответствующее положение и меро-
приятия, направленные на уменьшение отека.
После того, как ожоговые раны полностью за-
крылись, необходимо продолжать иммобилизацию
(шинирование), применение давящих повязок (или
специальной одежды), активных и пассивных
упражнений, приспособительных устройств и ап-
паратов и всевозможные мероприятия, направлен-
ные на ускорение адаптации ребенка к повседнев-
ной нормальной жизни. Для предотвращения фор-
мирования гипертрофических рубцов достаточно
эффективно используется специально изготовлен-
ная для этих целей «сдавливающая» одежда.
ОСЛОЖНЕНИЯ
При первичном осмотре ожоговых больных серь-
езные ингаляционные поражения могут отчетливо
не проявляться. Поэтому при наличии в анамнезе
указаний на возможность (по механизму травмы)
ожога дыхательных путей следует быть чрезвы-
чайно внимательным, обследуя больного. В первые
48 час после ожога часто возникает гипонатрие-
мия, связанная отчасти с повышенным выделением
анти диуретического гормона (АДГ) и гипотониче-
ской жидкости. При обширных глубоких ожогах,
особенно циркулярных, следует помнить о возмож-
ности развития «сотраггтепг»-син()рома. Доппле-
ровская пульсомстрия при этом имеет относитель-
ную ценность, поскольку выраженный compart-
ment-синдром может существовать достаточно
длительное время, прежде чем начнет исчезать
артериальный пульс. Практически все циркуляр-
ные ожоги требуют разрезов струпа. Однако пока-
зания к фасциотомии возникают редко, если не
считать элек гроожоги. Циркулярные ожоги груд-
ной клетки также могут потребовать рассечения
струпа с целью улучшения механики дыхания, осо-
бенно у маленьких детей. Большое значение для
профилактики осложнений имеет раннее начало
зондового кормления, что способствует поддержа-
нию нормального pH в желудке и предотвращению
кровотечения из верхних отделов ЖКТ.
В более поздние сроки, через 7—10 дней после
ожога, наибольшей проблемой может стать сепсис,
источником которого является, как правило, ожо-
говая рана.4 Тяжелое ингаляционное поражение
и сепсис — особенно неблагоприятное сочетание,
приводящее обычно к мультиорганной недостаточ-
ности и смерти.128 Одним из источников сепсиса,
о котором часто забывают, может быть септиче-
ский тромбофлебит, развивающийся у 4—5%
больных с обширными ожогами. При отсутствии
лечения летальность при этом осложнении при-
ближается к 100%. При подозрении на септиче-
ский тромбофлебит необходимо тщательно обсле-
довать вес места, где до этого стояли венозные
катетеры. Аспирация содержимого из этих участ-
ков, к сожалению, помощи в постановке диагноза
8 Заказ № 1622
114 ОЖОГИ
не оказывает. При наличии малейшего отделяемо-
го в области стояния катетера вена должна быть
открыта, желательно с применением анестезии. Ес-
ли получен гной, то всю вену следует удалить
и рану оставить открытой. У септических ожого-
вых больных необходимо также помнить о возмож-
ности развития сепсиса, синусита, хондрша и уро-
сепсиса, связанных с постоянным пребыванием
в венах катетеризационных линий.4 Почечная не-
достаточность может возникнуть как следствие
реанимационных, неадекватно проводимых меро-
приятий, сепсиса или токсического воздействия
миоглобина или лекарственных препаратов. Гипер-
тензия — проблема, с которой приходится сталки-
ваться при ожогах почти исключительно только
в детском возрасте. Она может возникнуть непо-
средственно после ожога или спустя значительный
промежуток времени (до 3 мес) после полного за-
крытия ран. Причиной данного осложнения, по
всей видимости, является повышенное выделение
ренина. Лечение проводится с помощью фуросеми-
да (лазикс) и гидралазина (апрсссин). Гипертен-
зия может быть достаточно тяжелой и иногда, при
отсутствии лечения, приводит к неврологическим
расстройствам.
Как только раны закрыты, может возникнуть
проблема, которая у детей явтястся юстаточно
серьезной, а именно — зуд Детишки часто расче-
сывают себя с голь яростно, что раздирают зажив-
шие уже к этому времени донорские места и уча-
стки, куда были пересажены трансплантаты К со-
жалению, не существует никаких надежных
эффективных средств против зуда. В какой-го
степени могут помочь димедрол и гидроксизин
(атаракс) в сочетании с увлажняющими кремами
и применением давящей одежды. Дети склонны
также к развитию тяжелых гипертрофических
рубцов.31',6' 120 Использование специальной давя-
щей одежды и четкое выполнение реабилитацион-
ной программы позволяют в некоторой степени
предотвратить это осложнение. Не менее серьез-
ную проблему представляет гетеротопическая
кальцификация'30 которая может быть связана
с переусердствованием в лечебной физкультуре,
что иногда приводит к кровоизлияниям в мягкие
ткани с последующим обызвествлением гематом.
В литературе имеются даже сообщения о развитии
в очень поздние сроки после травмы озлокачеств-
ления ожоговых рубцов. Это, как правило, проис-
ходит в тех случаях, когда раны, закрывшись
в процессе заживления, вновь неоднократно откры-
ваются или просто очень плохо, медтенно и дли-
тельно заживают.131
ПРОГНОЗ И ПРОФИЛАКТИКА
В 1898 г. Wyeth высказал предположение о том,
что при разрушении одной трети поверхности ко-
жи выздоровление практически невозможно.3 Этот
мрачный взгляд на ожоги на рубеже нашего века
значительно изменился за последние несколько
лет. Тем не менее лечение обширных ожогов про-
должает оставаться сложной проблемой. И вес же
показатель ЛО-50 (летальный ожог), который
представляет собой процент ожога (по отношению
к обшей поверхности тела), дающий летальность
у 50% больных, постоянно прогрессивно увеличи-
вается До 1950 г. ЛО-50 составлял 30%. Анализ
результатов лечения ожогов с 1978 по 1985 г. по-
казал, что ЛО-50 повысился до 64%, а в некото-
рых центрах в 1991 г. эта планка была поднята до
90%.'” На рисунке 9-6 графически изображено
соотношение летальности и площади ожога у де-
тей и взрослых.7’ Площадь ожога по-прежнему яв-
ляется главным фактором, обусловливающим ис-
ход при этом виде травмы. Кроме того, по данным
однш-о из исследований, практически 100%-ную
корреляцию с летальностью имеет процент задер-
жки жидкости в организме в течение первых
48 часов реанимации.132
Рис. 9-6. Эпидемиология ожогов
у детей.
Эпидемиология ожогов у детей — выживаемость в зависимости
от возраста, 1964-1984 (п = 29,492)
ОЖОГИ 115
Профилактика. Наиболее эффективный «метод
лечения» ожогов — это их профилактика. В
I985 г. 47% смертей от ожогов у детей приходи-
лось на малышей в возрасте до 4 лет. Три четвер-
ти из этих летальных исходов могли бы быть пред-
отвращены, если бы имелись в наличии и исполь-
зовались домашние огнетушители, детекторы
дыма, безопасные (непозгорающиеся) сигареты
и специальные зажигалки, которые не могут быть
зажжены ребенком. Безопасные сигареты, для про-
изводства которых необходим соответствующий
закон, могли бы предотвратить большое количе-
ство детских смертей, а детекторы дыма — умень-
шить летальность от ожогов в детском возрасте
почти наполовину. Около 24% ожогов горячей
жидкостью, требующих госпитализации, это ожоги
водой из-под крана. Подобные повреждения можно
предотвратить, применяя специальные противо-
ожоговые устройства, а также регуляторы темпера-
туры в водных нагревательных приборах.’ Одним
из важнейших направлений в профилактике ожо-
гов является санитарное просвещение, необходи-
мость и эффективность которого четко продемон-
стрированы в Германии, где за последние 17 лет
частота ожогов горячей жидкостью уменьшилась
на 50%.1'< 13 Для регионов, где риск ожогов по тем
или иным причинам особенно высок, должны быть
разработаны специальные программы по профи-
лактике термической травмы. Данные переписи
населения показывают отчетливую корреляцию
между высокой частотой ожогов и такими факто-
рами, как бедность, частые переезды, безработица,
пользование старыми электроприборами. Элект-
роожоги у молодых людей в возрасте до 2(1 лет
могут быть в значительной степени предотвраще-
ны с помощью целенаправленного образования
и строгого соблюдения мер безопасности.1"1
Жизненно важный раздел работы ожоговых
бригад — активное участие в санитарном просвеще-
нии и законодательных разработках, направлен-
ных на профилактику ожогов.
ЛИТЕРАТУРА
1 Robotti ЕВ: The treatment of burns: an historical perspective
with emphasis on the hand. Hand Clin 6:163—190, 1990.
2. Romm S: Burns in art. Clin Plast Surg 13:3—8, 1986.
3. Pinnegar MD, Pinnegar FC: History of burn care. A survey of
important changes in the topical treatment of thermal injuries.
Burns 12:508—517, 1986.
4. Lu ter man A, Dacso CC, Curreri PW: Infections in burn pati-
ents. Am J Med 81:45—52, 1986.
5. Alghanem AA, McCauley RL, Robson MC, et al.: Management
of pediatric perineal and genital burns: twenty-year review.
J Burn Care Rehab 11:308—311, 1990
6- Schubert W, Ahrenholz DH, Solcm LD: Burns from hot oil and
grease: A public health hazard. J Burn Care Rehab 11:558—
562, 1990.
7. Ilarmel RP, Vane DW, King DR: Burn care in children: special
considerations. Clin Plast Surg 13:95—105 1986.
8. Rossignol AM, Boyle CM, Locke J A, et al.: Hospitalized burn
injuries in Massachusetts: an assessment of incidence and pro-
duct involvement. Am J Public Health 76:1341 —1343, 1986.
9. McLoughlin E, McGuire A: The causes, cost, and prevention of
childhood burn injuries. Am J Dis Child 144:677—683, 1990.
10. Chatterjee BP, Barancik JI, Fraiiannc RB, et al.: Northeastern
Ohio trauma study. V. burn injury. J Trauma 26:844 847,
1986.
11. Rossignol AM, 1 ocke JA, Burke JF: Paediatric burn injuries in
New England, USA. Burns 16:41 48. 1990.
12. Hong QL, Zamboni W, Eriksson E, et al.: Burns in patients
under 2 and over 70 years of age. Ann Plast Surg 17:39—44,
1986.
13. Bradshaw C, Hawkins J, Leach M, el al.: A study of childhood
scalds. Burns 14:21—24, 1988.
14. Elberg JJ, Schroder HA, Gleni-Madsen L, ct al.: Burns: epide-
miology and the effect of a prevention programme. Burns
13:391—393, 1987.
15. Lyngdorf P: Epidemiology of scalds in small children. Burns
12:250—253. 1986.
16. Purdue GF, Hunt JL. Prescott PR: Child abuse by burning: an
index of suspicion. J Trauma 28:221—224, 1988.
17. Coren CV; Bum injuries in children. Pediatr Ann 16:328—339,
1987.
18. Holbrook KA, Byers PH, PinncII SR; The structure and func-
tion of dermal connective tissue in normal individuals and pati-
ents with inherited connective tissue discorders. Scan Electron
Microsc 4:1731 — 1744. 1982.
19. Lewis GM. Wheeler C: Practical Dermatology, third edition.
WR Saunders, Philadelphia, pp 1-—103. 1967.
20. Smith DJ, Robson MC, Heggers JP: Frostbite and other cold-
induced injuries. In Auerbach PS, Gcchr EC (Editors). Mana-
gement of Wilderness and Environmental Emergencies» second
edition. CV Mosby, St. Louis, pp 101 —118, 1990.
21. Cerra FB: Hypermetabolism, organ failure and metabolic sup-
port. Surgery 101:1—14, 1987.
22. Kaufman Г. Neuman RA, Weinberg A: Is postburn dermal
ischaemia enhanced by oxygen free radicals? Burns 15:291 —
294. 1989.
23. Niwa Y: Lipid peroxides and superoxide dismutase (SOD)
induction in skin inflammatory diseases, and treatment with
SOD preparations. Dermatologiea 1:101 —106, 1989-
24. Rockwell WB, Ehrlich HP: Fibrinolysis inhibition in human
burn blister fluid. J Burn Care Rehab 11:1 —6, 1990.
25. Hendricks WM: Commentary: The classification of burns. J Am
Acad Dermatol 22:838—839, 1990.
26. Rubin WD, Mani MM, Hiebert JM: Fluid resuscitation of the
thermally injured patient. Current concepts with definition of
clinical subsets and their specialized treatment. Clin Plast Surg
13:9—20. 1986.
27. Baxter CR: Fluid volume and electrolyte changes in the early
post burn period. Clin Plast Surg 1:693—709, 1974.
28. Demling R; Fluid and electrolyte management. Critical Care
Clinics 1:27 45. 1985-
29. Cerra F: Critical care: State of the art. Soc Crit Care Med
11:15—30, 1990.
30. Rohrich RJ: Wound healing and closure/abnormal scars/enve-
nomation and extravasation injuries. Selected Readings in Plas-
tic Surgery 6:1—3. 1990.
31. Moore FD, Davis CF: Monocyte activation after burns and
endoloxemia. J Surg Res 46:350—354, 1989.
32. Baker CC, Yamada AH, Fiiist E, et al.: Interleukin-1 and
T cell function following injury. J Burn Care Rehab 8:503—
508. 1987.
33. Hansbrough JF. Field TO Jr, Gadd MA. el al.: Immune respon-
se modulation after burn injury: T cells and antibodies. J Burn
Care Rehab 8:509 -512, 1987.
34. Deitch EA: Immunologic considerations in the burned child- In
116 ожоги
Carvajal GF, Parks DH (Editors). Burns in Children Pediatric
Burn Management. Medical Year Book Publishers. Chicago,
pp 195—212. 1988.
35. Moran K. (Munster AM; Alterations of the host defense mecha-
nism in burn patients. Surg Clin North Am 67:47—56, 1987.
36. Tcodorczyk-Injcyan J A, Sparkes BG, Mills GB, el al.: Impaired
expression of interleukin-2 receptor (IL2R) in the immuno-
suppressed burned patient: reversal by exogenous IL2. J Trau-
ma 27:180 -187, 1987.
37. Lazarou SA, Barbul A, Wasscrkrug HL, et al.: The wound is
a possible source of posttraumatic immunosuppression. Arch
Surg 124:1429—1431, 1989.
38. Ogle CK, Alexander JW, Nagy H, cl al.: The patient with
burns. J Burn Care Rehab 11:105 111, 1990.
39. Kim Y, Goldstein E. Lippert W, cl al.: Polymorphonuclear
leucocyte motility in patients with severe burns. Burns 15:93—
97, 1989.
40. Bjerknes R, Vindenes H. I aerum OD: Altered neutrophil func-
tions in patients with large burns. J Blood Cells 16:127—141.
1990.
41. Bjerknes R. Vindenes H, Pilkancn J, et al.: Altered polymor-
phonuclear neutrophilic granulocyte functions in patients with
large burns. J Trauma 29:847—855, 1989.
42. Ferrara JJ. Dyess DL, Lulerman A, et al.: In vitro effects of
complement inactivation upon burn-associated cell mediated
immunosuppression. Am Surg 56:571—574, 1990.
43. Utoh J, Utsunomiya T, Imaniura T. et al.: Complement activati-
on and neutrophil dysfunction in burned patients with sepsis —
a study of two cases. Jpn J Surg 19:462—467, 1989.
44. Ferrara JJ, Peterson RD, Hester R, et aL: Inhibition of lympho-
cyte blastogcncsis caused by suppression of interleukin-2 re-
ceptor sites after thermal injury. J Burn Care Rehab 10:119—
124. 1989.
45. Klimpel GR, Herndon DH, Stein MD: Peripheral blood lym-
phocytes from thermal injury patients arc defective in their
ability to generate lymphokinc-activated killer cell activity.
J Clin Immunol 8:14- 22, 1988.
46. Ferrara JJ, Dyess DL, Luterman A, et al.: The suppressive
effect of subeschar tissue fluid upon in vitro cell-mediated im-
munologic function. J Burn Care Rehab 9:584—588, 1988.
47. Echinard CE: Immunity of the burned patient. Scand J Plast
Reconstr Surg Hand Surg 21:317—321, 1987.
48. Ozkan AN, Hoyt DB, Ninnemann JL: Generation and activity
of suppressor peptides following traumatic injury. J Burn Care
Rehab 8:527—530, 1987.
49- Asko-Seljavaara S: Granulocyte kinetics in burns. J Burn Care
Rehab 8:492—495, 1987.
50. Ninnemann JL: Trauma, sepsis, and the immune response.
J Burn Care Rehab 8:462—468, 1987.
51. Warden GD: Outpatient care of thermal injuries. Surg Clin
North. Am 67:147—157, 1987.
52. Wilson GR, Fowler CA, Housden PL: A new burn area assess-
ment chart. Burns 13:401—405, 1987.
53. Rubin WD, Mani MM. Hiebert JM: Fluid resuscitation of the
thermally injured patient. Current concepts with definition of
clinical subsets and their specialized treatment. Clin Plast Surg
13:9—20. 1986.
54. Aharoni A, Moscona R, Kremerman S, et al.: Pulmonary comp-
lications in burn patients resuscitated with a low-volume colloid
solution. Burns 15:281—284. 1989-
55. Graves TA, Cioffi WHG, McManus WF, et al.: Fluid resuscita-
tion of infants and children with massive thermal injury. J Tra-
uma 28:1656—1659, 1988.
56. Aharoni A, Mascona R, Kremerman S, et al.: Pulmonary comp-
lications in burn patients resuscitated with a low-volume colloid
solution. Burns 15:281—284, 1989.
57. Bowser-Wai lace BH, Caldwell FT: Fluid requirements of seve-
rely burned children up to 3 years old: hypertonic Lactated
saline vs. Ringer’s lactate-colloid. Burns 12:549—555, 1986.
58. McKee AC, Winkelman MD, Banker BQ: Central pontine mye-
linolysis in severely burned patients: Relationship to serum
hyperosmolality. Neurology 38:1211 —1217, 1988.
59. Navar PD, Saffle JR, Warden GD: Effect of inhalation injury
on fluid resuscitation requirements after thermal injury. Am
J Surg 150:716—720. 1985.
60. Hildreth MA, Ilerndon DN, Parks DH, et al.: Evaluation of
a caloric requirement formula in burned children treated with
early excision. J Trauma 27:188—189, 1987.
61. Burkc JF. Quinby WC, Bondoc CC: Primary excision and
prompt grafting as routine therapy for the treatment of thermal
burns in children. Hand Clin 6:305 317. 1990.
62. Bonale PL: Pathophysiology and pharmacokinetics following
burn injury. Clin Pharmacokinet 18:118—130, 1990.
63. Jahoor F. Desai M, Herndon DN, et al.: Dynamics of the prote-
in metabolic response to burn injury. Metabolism 37:330 337,
1988.
64. Crum RL, Dominic W, Ilansbrough JF, et al.: Cardiovascular
and neurohumural responses following burn injury. Arch Surg
125:1065—1069, 1990.
65. Wolfe RR, Herndon DN, Jahoor F. et al.: Effect of severe burn
injury on substrate cycling by glucose and fatty acids. N Engl
J Med 317:403 408, 1987.
66. Wolfe RR. Herndon DN, Peters EJ, et al.: Regulation of lipoly-
sis in severely burned children. Ann Surg 206:214— 221, 1987.
67. Cunningham JJ, Lydon MK, Russell WE: Calorie and protein
provision for recovery from severe burns in infants and young
children. Am J Clin Nutr 51:553—557, 1990.
68. Sarubin J: Increased requirement of alcuronium in burned pati-
ents. Anaeslhesist 31:392—395, 1982.
69. Matsuda T, Clark N, Hariyani GD. et al.: The effect of burn
wound size on resting energy expenditure. J Trauma 27:115
118, 1987.
70. Allard JP, Pichard C, Hoshino E, et al.: Validation of a new
formula for calculating the energy requirements of burn pati-
ents. J PEN 14:115—118, 1990.
71. Allard JP, Jcejheebhoy KN, Whitwell J, el al.: Factors influ-
encing energy expenditure in patients with burns. J Trauma
28:199—202, 1988.
72. O’Neil CE, Hutsler D. Hildreth MA: Basic nutritional guideli-
nes for pediatric burn patients. J Burn Care Rehab 10:278—
284, 1989.
73- Baxter CR: Metabolism and nutrition in burned patients.
Compr Ther 13:36—42, 1987.
74. Gotlschlich MM, Jenkins M, Warden GD, et al.: Differential
effects of three enteral regimens on selected outcome variables.
Procedures Am Sue Parent Entcrol Nutr 14:225—236, 1990.
75. Alexander JW, (rottschlich MM: Nutritional immunomodulation
in burn patients. Crit Care Med 18:149—153, 1990.
76. Jenkins M, Gotlschlich M, Alexander JW, et al.: Effect of im-
mediate entcrol feeding on the hypermelabolic response follo-
wing severe burn injury. 13th Clinical Congress Program Book,
Am Soc Parent Enterol Nutr, 1989.
77. Merrell SW, Saffle JR. Sullivan JJ, et al.: Fluid resuscitation
in thermally injured children. Am J Surg 152:664—669,
1986.
78. Phillips LG, Robson MC, Smith DJ el al.: Uses and abuses
of a biosynthetic dressing for partial skin thickness burns. Burns
15:254-256, 1989.
79- Patterson DR, Questad KA. Bollwood MD; Hypnotherapy as
a treatment for pain in patients with burns: research and clini-
cal considerations. J Burn Care Rehab 8:263 268, 1987.
80. Wachtel TI: Topical antimicrobials. In Carvajal HT. Parks
DH (Editors). Burns in Children: Pediatric Burn Manage-
ment. Year Book Medical Publishers, Chicago, pp 106—118,
1988.
81. Miller L, Hansbrough J, Slater H, el al.: Sildimac: a new deli-
very system for silver sulfadiazine in the treatment of full thick-
ness burn injuries. J Burn Care Rehab 11:35—41, 1990.
82. Monafo WW, West MA: Current treatment recommendations
for topical bum therapy. Drugs 40:364—373, 1990.
ОЖОГИ 117
83. Beasley RW; Secondary repair of burned hands. Hand Clin
6:319—341. 1990.
84. Van dor Docs AJW: Patients' and nurses’ ratings of pain and
anxiety during burn wound care. Pain 39:95—101, 1989.
85. Osgood PF, Szyfelbein SK: Management of burn pain in child-
ren. Pediatr Clin North Am 36:1001 —1013, 1989.
86. Choiniere M, Melzack R, Rondeau J, et al: The pain of burns:
characteristics and correlates. J Trauma 29:1531 —1539. 1989.
87. Patterson DR. Questad KA, Bollwood MD: Hypnotherapy as
a treatment for pain in patients with burns: research and clini-
cal considerations- J Burn Care Rehab 8:263—268, 1987.
88. Lewis SM, Clelland J A, Knowles CJ. cl a!.: Effects of auricular
acupuncture-like transcutaneous electric nerve stimulation on
pain levels following wound care in patients with burns: a pilot
Study. J Burn Care Rehab 11:322—329, 1990.
89. Martyn JA. Green bl a It DJ. Hagen J, ei al.: Alteration by burn
injury of the pharmacokinetics and pharmacodynamics of cime-
tidine in children. Eur J Clin Pharmacol 36:361 367, 1989.
90. Mills AK. Martyn JA: Neuromuscular blockade with vecuroni-
um in paediatric patients with burn injury. Br J Clin Pharmacol
28:155—159. 1989.
91- D’Eramo C, Stocchetti N, Vczzani A: Clinical evaluation of
atracurium bcsylate in patients at risk: major burns. Minerva
Anestesiol 56:121 —125, 1990.
92. Martyn JA. Goudsouzian NG. Matico RS. et al.: Metocurinc
requirements and plasma concentrations in burned paediatric
patients. Br J Anaesth 55:263-—268, 1983.
93. Mills AK. Martyn JA: Evaluation of atracurium neuromuscular
blockade in paediatric patients with burn injury. Br J Anaesth
60:450—455. 1988.
94. Cote CJ, Petkau AJ: 1 hiopenral requirements may be increased
in children reanesthetized al least one year after recovery from
extensive thermal injury. Anesth Analg 64:1156—1160. 1985.
95. Brown TC, Bell B: Electromyographic responses to small doses
of suxamethonium in children after burns. Br J Anaesth
59:1017—1021, 1987.
96. McCauley RL, Beraja V, Rutan RL. et al.: I ongiludinal
assessment of breast development in adolescent female patients
with burns involving the nipple-areolar complex. Plasf Re-
constr Surg 83:676—680, 1989.
97. Mills AK, Martyn JA: Evaluation of atracurium neuromuscu-
lar blockade in paediatric patients with burn injury, Br J Ana-
esth 60:450—455, 1988.
98. Balogh D, Bauer M, Hortnagl H: Effect of surgery and anest-
hesia on the plasma catecholamine level and rate of urea pro-
duction in severely burned patients. Anacslliusist 32:105 110.
1983.
99. Heimbach DM; Early burn excision and grafting. Surg Clin
North Am 67:93 -107, 1987.
100. Chicarilli ZN, Cuono CB, Heinrich J J, el al.: Selective aggressi-
ve burn excision for high mortality subgroups. J Trauma
26:18—25, 1986.
101. Clarke H. Winpenn GP, McLeod AM. et al.: Acute manage-
ment of pediatric hand burns. Hand Clin 6:221—231. 1990.
102. Bos wick JA: Management of the burned hands. Hand Clin
6:297 303, 1990.
103. Desai MH. Herndon DN, Broemeling L, ct al.: Early burn
wound excision significantly reduces blood loss. Ann Surg
211:753 762, 1990.
104. Herndon DN, Parks DH: Comparison of serial debridement
and autografting and early massive excision with cadaver skin
overlay in the treatment of large burns in children. J Trauma
26:149—152, 1986.
105. Herndon DN. Thompson PR, Hugo AL, et al.: Incidence, mor-
tality, pathogenesis and treatment of pulmonary injury. J Burn
Care Rehab 7:184—191. 1986.
106. Herndon DN, Barrow RE, Linares IIA, ct al.: Inhalation injury
in burned patients: effects and treatment. Burns 14:349—356,
1988.
107. Waxman K: Pulmonary management. In Achaucr BM (Editor),
Management of the burned Patient. Appleton & Lange. Nor-
walk, Connecticut, pp 149—160. 1987,
108. Deskin RWQ, McCracken MM. Hokanson J A, el al.: Longterm
airway sequelae in a pediatric burn population. Laryngoscope
98:721—725, 1988
109. Shirani KZ. Pruitt BA, Mason AD: The influence of inhalation
injury and penunion ia on burn mortality. Ann Surg 205:82—
87, 1987.
110. Thompson PB, Herndon DN, Traber DI , el al.: Effect on mor-
tality of inhalation injury. J Trauma 26:163—165, 1986.
111. Burns TR, Greenberg SD. Cartwright J, et al.: Smoke inhala-
tion: an ullrastruciurai study of reaction to injury in the human
alveolar wall. Environ Res 41:447—457, 1986.
112, Silverman SH, Purdue EG. Hunt JL, et al.: Cyanide toxicity in
burn patients. J Trauma 28:171—176, 1988.
113. Crapo RO: Causes of respiratory injury. In Haponik EF, Mun-
ster AM (Editors). Respiratory Injury Smoke Inhalation an
Burns. McGraw-Hill, New York, pp 47—59. 1990.
114. Parish RA: Smoke inhalation and carbon monoxide poisoning
in children. Pediatr Emergency Care 2:36—39, 1986.
115. Traber DI., Herndon DN: Pathophysiology of smoke inhala-
tion. In Haponik EF. Munster AM (Editors). Respiratory
Injury Smoke Inhalation and Burns. McGraw-Hill. New York,
pp 61—71, 1990.
116. Blinn DL, Slater H, Goldfarb IW: Inhalation injury with burns:
a lethal combination. J Emergency Med 6:471—473, 1988.
117. Herndon DN. Langner F. Thompson P, et al.: Pulmonary
injury in burned patients. Surg Clin North Am 67:31—46.
1987.
118. Gordon MWG, Reid WH, Awwaad AM; Electrical burns —
incidence and prognosis in western Scotland. Burns 12:254—
259, 1986.
119. Sadove AM, Jones JE, Lynch TR, et al.: Appliance therapy for
perioral electrical burns: a conservative approach. J Burn Care
Rehab 9:391—395, 1988.
120. Hanumadass ML, Voora SB. Kagan RJ, el al.: Acute electrical
burns: a 10 year clinical experience. Burns 12:427—431, 1986.
121. Pensler JM, Rosenthal A; Reconstruction of the oral commissu-
re after an electrical burn. J Burn Care Rehab 11:50 53.
1990.
122. Vorhies JM: Electrical burns of the oral commissure. Angle
Orthod 57:2 17, 1987.
123. Palin WE, Sadove AM, Jones JE, el al.: Oral electrical burns in
a pediatric population. J Oral Med 42:17—34. 1987.
124. Schneider PE; Infant commissural burn management with re-
verse pull headgear. Pediatr Dent 10:34—38, 1988.
125. Ahrenholz DH. Schubert W, Solcm l,D: Creatine kinase as
a prognostic indicator in electrical injury. Surgery 104:741
747. 1988
126. Hergrueier CA, O’Connor NE: Skin substitutes in upper extre-
mity burns. Hand Clin 6:239—242, 1990.
127. Egan WC, Clark WR: The toxic shock syndrome in a bum
victim. Burns 14:135 138, 1988.
128. Aikawa N, Shinozawa Y. Ishibiki K. ct al.: Clinical analysis of
multiple organ failure in burned patients. Burns 13:103—109,
1987.
129. Smith CJ, Smith JC, Finn MC: The possible role of mast cells
(allergy) in the production of keloid and hypertrophic scarring.
J Burn Care Rehab 8:126—131, 1987.
130. Blassingame WM, Bennett GB, Helm PA, ct al.: Range of moti-
on of the shoulder performed while patient is anesthetized.
J Burn Care Rehab 10:539 542, 1989.
131. Bartle EJ, Sun JH, Wang XW, et al.: Cancers arising from burn
scars: A literature review and report of twenty-one cases.
J Burn Care Rehab 11:46—49, 1990.
132. Carlson RG, Miller SF, Finley RK, et al.: Fluid retention and
burn survival. J Trauma 27:127—135, 1987.
133. 1 иске J A, Rossignol AM, Boyle CM, el al.: Socioeconomic
factors and burn rates in persons hospitalized for burns in
Massachusetts. Public Health Rep 101:389- 395. 1986.
Глава 10
ЭПИДЕМИОЛОГИЯ ТРАВМЫ
William Haddon определит понятие «травматиче-
ское повреждение» как «повреждение организма,
вызванное таким изменением энергии окружаю-
щей среды, сила которого превышает силу упруго-
сти человеческого тела».1 Термин «повреждение»
чаще встречается в литературе не столько клини-
ческой, сколько научно-популярной медицинской,
в то время как понятие «травма» в основном ис-
пользуется для определения повреждения организ-
ма преимущественно в экстренных (экстремаль-
ных) ситуациях, либо в хирургических и даже бое-
вых обстоятельствах. В любом случае два этих
термина «травматическое повреждение» и «трав-
ма» употребляются как взаимозаменяемые при
описании клиники, статистики и мер профилакти-
ки самых разнообразных процессов, являющихся
результатом повреждения.2
Повреждение — ведущая причина летальности
среди детей и подростков в возрасте до 15 лет.
Ежегодно около 20 000 смертей обусловлены трав-
мой. И хотя в общей популяции в Америке глав-
ными причинами смерти являются кардиоваску-
лярные заболевания, злокачественные опухоли и
легочная патология, однако в детском возрасте ве-
дущую роль, определяющую летальность, играет
именно травма (рис. 10-1).3 Повреждения вызыва-
ют около 44% всех смертей у детей в возрасте от
I года до 4 лет, 51 % — в возрасте от 5 до 9 лет
и 58% —в возрасте от 10 до 14 лет.4 Наиболее
ярко значение легальности, связанной с травмой
среди детей и молодежи, отражено в том факте,
что в Америке травма превосходит все основные
большие группы заболеваний как ведущая причи-
на преждевременного ухода из жизни в детском
возрасте. '
Смерть здорового ребенка — всегда трагедия.
И это, разумеется, главное, когда речь идет о трав-
ме. Но не меньшее значение и влияние на все
звенья системы здравоохранения оказывает инва-
лидизация детей, оставшихся живыми после по-
вреждения, и необходимость соответствующей реа-
билитации. Расходы средств, связанные с пере-
численными факторами, занятость персонала и
экономические потери, обусловленные исключены
ем из трудовой деятельности потенциального рабо-
тника, которым мог бы стать ребенок, если бы
травма не сделала его тяжелым инвалидом, столь
огромны, что нс идут ни в какое сравнение с поте-
рями, возникающими в результате травм у взрос-
лых. Различия эти усугубляются тем, что необ-
ходимость длительной реабилитации маленьких
детей, перенесших травму, наслаивается на пробле-
Соединенные Штаты, 1986
КОЛИЧЕСТВО УМЕРШИХ
Рис. 10 1. Основные причины детской
смертности.
ЭПИДЕМИОЛОГИЯ ТРАВМЫ 119
мы, связанные с продолжающимся ростом и разви-
тием. Кроме того, адаптация ребенка к тяжелой
инвалидности крайне затрудняется восприятием
им самого себя как неполноценного человека. При-
чем эти психологические проблемы могут выйти
на первый план и стать подавляющими, если в об-
щем реабилитационном процессе не участвуют, по-
мимо врачей и сотрудников лечебных учреждений,
целенаправленно обученные квалифицированные
профессионалы самых разных специальностей, ра-
бота которых связана с воспитанием и развитием
детей.
Десятилетиями и даже веками история накап-
ливала и регистрировала все эти «столкновения
с энергией окружающей среды», которые приводят
к повреждениям. Слишком широкое повсеместное
распространение травм и большое их количество
часто затушевывают важность этой проблемы, вое
питывая в обществе отношение к повреждениям
как к обычному, само собой разумеющемуся, не-
избежному явлению. И в результате общественный
интерес к травматическим повреждениям в детском
возрасте не пробуждается, как правило, до тех пор,
пока возрастающая частота травм не начинает вы-
зывать увеличение статистических показателей
летальности.
ЛЕТАЛЬНОСТЬ ПРИ ТРАВМАХ
В основе различных делений травм, в отличие от
болезней, лежат совершенно иные факторы, в том
числе, в частности, характер событий, предшество-
вавших повреждению, и даже намерения постра-
давшего. Большинство классификаций смерти в
результате травм включают убийство, самоубий-
ство, непреднамеренное (случайное) повреждение
и травму с неизвестным механизмом. Хотя проис-
шествия, ведущие К преднамеренному и неумыш-
ленному повреждению, часто существенно разли-
чаются, механизм травмы и повреждения сами по
себе могут быть не только похожими, по и абсо-
лютно идентичными.6 Например, выстрел из ружья
приводит к одинаковому результату, хотя спектр
случившегося несчастья может колебаться от пол-
ного отсутствия намерения, когда пострадавший
вообще не знает о наличии и состоянии (заряжено
или дозаряжено) оружия до полностью противопо-
ложной ситуации, а именно — запланированной
попытки самоубийства. И какими бы ни были
«сценарии» фатальных повреждений, основная
стратегия профилактики травмы почти всегда оди-
накова. В частности строгое соблюдение закона об
ограничении распространения, ношения и приме-
нения личного оружия может снизить количество
как непреднамеренных, так и суицидных смертей.
Информация о летальности за 1980—1985 гг.,
использованная в настоящей главе, основана на
данных Национального Статистического Центра
Здоровья (НСЦЗ), Департамента Здоровья США
и Министерства Здравоохранения.4 Смерти детей
в результате травм классифицированы по 23 при-
чинам согласно разделу «Травма» Международной
Классификации Болезней.
ТАБЛИЦА 10 1. Летальность при различных видах травм
у детей (о г 0 до 14 лет). Соединенные
Штаты. 19X0 85 гг.
Характер травмы Кол-во умерших еи-й за 198U 85 гг. Средняя цс- laihiKKTh на МИНИН) насе- ления в год
Автотранспортные и парни 22.174 7.2
Пассажиры 9746 3,2
Пешеходы (в ширни) 7489 2.4
Велосипеды 2194 0.7
Пешеходы (не в аварии) 1276 0.4
Могоцик 1Ы 690 0.2
Другие автомашины 729 0.2
Утопленмм 8568 2.8
Пожары 7021 2.3
У бимс nut 5722 1,9
Удушения 2279 0.7
Неумышленные огнестрельные ра- 1700 0.6
нения
Падения 1332 0,4
Аспирация (пищевая) 1248 0,4
Суициды 1214 0.4
Аспирация (непищевая) 983 0.3
Отравление (твердым/жидким нс- 539 0.2
ществом)
Сельхозмашины 508 0,2
Электрический ток 432 0.1
Яд газообразный 384 0,1
Авиакатастрофы 348 0.1
Другие виды неумышленных травм 3473 1,1
Неизнестные причины 1237 0.4
Метицинския/хирургическая 539 0.2
Всего 59.711 19.3
Дальнейшее подразделение по .механизму трав-
мы неумышленных повреждений, приведших к
смерти, представлено в таблице 10-1, которая
включает 23 категории повреждений у детей в Со-
единенных Штатах? В течение 6-летнего периода
(1980—85 гг.) около 10 000 детей в возрасте от
0 до 14 лет умирали ежегодно от травмы. Из них
37% погибли в транспортных авариях (включая
велосипедные травмы и гибель детей-пешеходов).
Из других причин наиболее частыми были утопле-
ния (14%), домашние пожары (12%) и убийства
(10%). Если же взять не единую группу автоава-
рий, а разделить ее по виду транспортных средств
и происшествий, то характер травм с летальным
исходом распределится по убывающей частоте сле-
дующим образом: (1) пассажир автомашины,
(2) утопление, (3) пешеход в автоаварии, (4) до-
машние пожары и (5) убийства.
В Соединенных Штатах среди детей в возрасте
от 0 до 14 лет среднее ежегодное количество смер-
тей в результате травм составляет 19,3:100 000
(см. табл. 10-1).7 Частота летальных исходов, так
же, как и характер повреждений, меняется в зави-
симости от возраста (рис. 10-2).7
Мальчики получают травмы в два раза чаще
девочек, а при таких видах повреждений, как само-
убийство, неумышленные огнестрельные ранения,
мотоциклетная травма и аварии на сельхоз. маши-
нах, это соотношение мальчики:девочки возраста-
ет до 4:1.
Если рассмотреть частоту смертей от травм в на-
циональном аспекте, то и здесь отмечаются разли-
120 ЭПИДЕМИОЛОГИЯ ТРАВМЫ
< 1 года (33,9 смерти/100,000)
Возраст 1—4 года (25,4 смертей'100,000)
Возраст 5—9 лет (14,4 смертей/100,000)
Транспортные
аварии
Утопления
Возраст 10—14 лет (16,2 смерти/100,000)
Транстортные аварии
Рис. IU 2. Детская смертность при трапме с процентным распределением по причинам травмы.
чия, а именно — распределение по возрастающей
будет следующим: уроженцы Востока = белые <
<. черные < коренные американцы. Причем для
каждой из этих групп характерны спои особенно-
сти травм. Гак, среди уроженцев Востока наиболь-
шее число травм у детей возникает в результате
падений. Черные детишки чаще всего становятся
жертвами пожаров, убийств и автомобильных ава-
рий (как пешеходы). Жизни детей белых и корен-
ных американцев обычно прерываются в автоката-
строфах, когда они находятся в машинах как пас-
сажиры.’
Разумеется, летальность при травмах не может
быть классифицирована только по национальному
признаку без учета возраста детей и территори-
альных особенностей регионов страны. Между от-
дельными штатами существуют значительные
«географические» различия в отношении частоты
и механизма травм. Как правило, наибольшая ле-
тальность при любом виде повреждений приходит-
ся на горные и южные штаты, в то время как са-
мый низкий ее уровень отмечается в Новой Анг-
лии, на Среднеатлантическом побережье и на
Среднем Западе.3,
МЕХАНИЗМЫ ТРАВМЫ И ПРОФИЛАКТИКА
Транспортные происшествия (пассажиры, пе-
шеходы, мотоциклы, велосипеды, другие авто-
машины). Дети, гибнущие в транспортных авари-
ях, будучи внутри автомашины или грузовика, мо-
гут находиться там либо как пассажиры, либо быть
за рулем. Эта группа включает также все падения
в результате столкновения с движущимся транс-
портом. Среди детей в возрасте от 1 год;| до 14 лет
летальность в автодорожных происшествиях, когда
дети находятся внутри автомашин, превышает по
частоте все другие повреждения и заболевания как
главная причина смерти в детском возрасте в Сое-
диненных Штатах. '
Смерти пешеходов в транспортных авариях
включают все происшествия, когда дети получают
удар, иногда смертельный, от автотранспорта на
больших дорогах, порой будучи не просто пешехо-
дами, а катаясь на роликовых коньках, досках
и т. д. Естественно, частота данного вида травм
с летальными исходами намного выше в городских
местностях. Пик летальности в этой группе прихо-
дится на возраст от 5 до 9 лет.7
Смерти детей-«пешсходов», не связанные с до-
рожно-транспортными происшествиями, отмечают-
ся в самых разных местах в стороне от больших
дорог (например, подъездная аллея возле частного
дома, парковая стоянка). Естественно, данный ме-
ханизм превалирует в сельских местностях. Мно-
гие неправильно относя г указанный вид травм
в рубрику транспортных происшествий. Уровень
летальности при данном характере повреждений
самый высокий среди детей в возрасте от 1 года до
4 лет. Наиболее часто жертвами становятся малыши.
ЭПИДЕМИОЛОГИЯ ТРАВМЫ 121
которые только начинают холить. Их сбивают лич-
ные автомашины или грузовики, выезжающие зад-
ним ходом из гаража либо со стоянки на дорогу.7
В группу травм с летальными исходами в мото-
циклетных авариях включены все повреждения
у детей, находившихся на мотоцикле. независимо
от места происшествия. Более 2/3 фатальных ис-
ходов при этом механизме травмы возникает в тех
случаях, когда дети непосредственно управляют
мотоциклом. Данный вид травмы преобладает
в возрастной группе от 10 до 14 лет.
К велосипедным авариям отнесены происшест-
вия, связанные с любыми педальными транспорт-
ными средствами. Большинство этих смертей
(95%) являются результатом столкновения с авто-
мобилями. Велосипедисты, получающие легальные
повреждения, относятся, как правило, к возрастной
группе 10 14 лет. ‘
Весь наземный автотранспорт (HAT), — кроме
автомашин и грузовиков, как причина травм с ле-
тальными исходами, а именно: снегоуборочные ма-
шины, мопеды, минивслосипеды, моторные самока-
ты — включен в подраздел «другие автомашины».
Утопления происходят чаше всего либо при ка-
тании на лодках (5% детских утоплений) либо
при купании в ванной (8%), причем наибольшая
частота данного вида травмы, включая происше-
ствия в плавательных бассейнах, приходится на
возраст от 1 года до 4 лет. Следует отметить, что
белые дети тонут в два раза чаще черных. Однако
в возрасте 10—14 лет отмечается обратное соотно-
шение — черные дети тонут в два раза чате, чем
белые. В географическом аспекте утопления пре-
обладают в западных и южных штатах/’
Домашние пожары. На домашние пожары при-
ходится 92% всех летальных исходов, обусловлен-
ных непреднамеренными ожогами или иными по-
вреждениями, связанными с огнем. Это наиболее
частая причина смерти черных детей в возрасте от
1 года до 9 лет, отмечающаяся преимущественно в
южных и восточных штатах. В результате домаш-
них пожаров черные дети в любых возрастных груп-
пах до 10 лет гибнут в 3 раза чаще, чем белые?'
Убийства. Значительное количество летальных
исходов в детском возрасте обусловлено убийства-
ми, включая жестокое обращение с детьми, поджо-
ги и любые другие умышленные повреждения,
в том числе с применением огнестрельного и хо-
лодного (ножи) оружия, а также удушения и утоп-
ления. Убийство—ведущая причина смерти от
травматических повреждений детей первого года
жизни, независимо от национальной принадлежно-
сти. Частота огнестрельных ранений продолжает
упорно расти, поскольку оружие, к сожалению, все
более широко распространяется. Причем черные
дети в возрасте от 0 до 14 лет намного чаще стано-
вятся жертвами убийств. ’
Удушение возникает в тех случаях, когда обту-
рируются рот и нос либо снаружи перекрывается
доступ кислорода. Более 33% случаев удушения
детей происходят в постели или детской кроватке.
В редких, но очень тяжелых, случаях (3%) данный
вид травмы связан с попаданием ребенка в безвоз-
душное замкнутое пространство (холодильник,
сундуки, чемоданы). Сюда же включена странгуля-
ция различными предметами (веревки, одежда,
детали одежды). Норой в данную группу непра-
вильно относят синдром внезапной смерти (СВС),
хотя достаточно ясно, что это совершенно иная
категория/'
Неумышленные огнестрельные ранения. В Со-
единенных Штатах около 40% всех огнестрельных
ранений детей в возрасте от 0 до 14 лет с леталь-
ными исходами являются неумышленными. Часто-
та данного вида фатальной травмы значительно
преобладает среди мальчиков-подростков, особен-
но в южных и северо-западных штатах. В литера-
туре существует описание более 400 случаев не-
преднамеренных огнестрельных ранении, по-
влекших за собой смерть.
Падения. Наиболее частый вид повреждений —
падения, которые редко приводят к летальным ис-
ходам, не считая падений на ребенка больших тя-
жестей или ударов головой о твердую поверхность.
При данном механизме травмы смерть или тяже-
лая инвалидность чаше всего связана с падением
маленьких детей из окон или в пролеты лестниц.
Более высокая летальность в этой группе отмеча-
ется в возрасте до 5 лет. На городские регионы,
в частности Нью-Йорк, приходится особенно зна-
чительное количество подобных случаев.
Аспирация. Аспирировать ребенок может как
пищу, так и различные другие предметы и веще-
ства. Обструкция дыхательных путей очень опасна
и порой стремительно приводит к смерти. Наибо-
лее часто «вдыхаются» округлые предметы (вино-
градинки, сосиски, орехи, твердые конфеты, шари-
ки от детских игр, крышки от бутылок). Кроме
того, дети нередко аспирируют семечки и зерныш-
ки, кусочки резиновых воздушных шаров и пласт-
массовых игрушек. В эту же группу отнесены слу-
чаи аспирации пищи при регургитации у больных
детей или у детей, отстающих в психическом раз-
витии, когда имеется склонность к рвотам или ды-
хательным расстройствам. Этот ви^ травмы чаще
встречается в возрасте до 5 лет. ’
Суициды. К сожалению, частота суицидов в
юношеском возрасте продолжает расти в нашей
стране, причем среди белых детей 10—15 лет ле-
тальность при этом виде травмы значительно вы-
ше, чем среди темнокожих пациентов того же воз-
раста.
Отравления (твердыми/жидкими вещества
ми). Отравления, приводящие к смерти, могут
быть связаны с употреблением лекарственных пре-
паратов или наркотиков (антидепрессанты, сердеч-
но-сосудистые средства, метадон, кокаин), а также
продуктов перегонки нефти. У старших детей
(10—14 лет) отравление чаще всего бывает умыш-
ленным. Смерть относят к разряду суицидных
в тех случаях, когда имеются несомненные данные
о преднамеренном самоотравлении. ’
Под летальными исходами, включенными в
группу «другие виды неумышленных травм», по-
дразумеваются те повреждения, которые не укла-
дываются в предыдущие категории. Сюда относят-
122 ЭПИДЕМИОЛОГИЯ ТРАВМЫ
ся смерти в результате падения на ребенка каких-
либо предметов, ожоги (исключая домашние пожа-
ры), железнодорожные аварии, редкие случаи
гибели от столкновения со спортивными снарядами
или непосредственно со стремительно движущими-
ся спортсменами, с животными, с велосипедом.3
Причинные факторы детской травмы. В этио-
логическом аспекте при повреждениях у детей ту-
пая травма значительно преобладает над проника-
ющей. Опасные для жизни повреждения в детском
возрасте, возникающие в результате воздействия
тупой силы (примерно 00%), условно подразделя-
ются на раздавливание (краш-повреждение), сдав-
ление (компрессия) и воздействие силы резкого
торможения.’ Краш-повреждение характеризуется
придавливанием тела ребенка к твердой поверхно-
сти (платформа, стена) или резким сдавлением его
тела движущимся тяжелым крупным предметом.
Данный механизм травмы отличается от компрес-
сионного повреждения, при котором на тело обыч-
но воздействует векторная сила движения (напри-
мер, переезд через ребенка автомобильного коле-
са). Травма при этом усугубляется нс только
дополнительным фактором движения, но и мощ-
ным, невероятно пугающим ребенка стрессовым
воздействием подобного вида повреждения.
Наиболее тяжелую травму вызывает воздейст-
вие сил резкого торможения или ускорения. При
этом не только весь организм ребенка оказывается
под влиянием мощного силового фактора, но и от-
дельные органы и системы приводятся в движение
совершенно по-разному в зависимости от их мас-
сы. Действующие внутри тела «рассекающие-раз-
рывающие» силы могут привести к разрыву тканей
и структур в участках фиксации («опорных точках
организма»), в частности в области связки Трейца,
илеоцекального угла, ligamcntum arteriosum груд-
ной аорты. В результате возникает деваскуляриза-
ция или отрыв кишечника (или аорты) с последую-
щей перфорацией.
Различные виды деваскуляризационпых повреж-
дений могут затронуть также паренхиматозные ор-
ганы и любые сосудистые структуры. Три указан-
ных этиологических силовых фактора (краш-по-
вреждение, сдавление, силы ускорения-торможе-
ния) воздействуют при травмах, связанных с авто-
мобильными авариями, падениями (слепая травма)
и проникающими повреждениями.’
Частота повреждений различных органов и
систем. Тупая травма влечет за собой ряд обстоя-
тельств, которые порой существенно осложняют
лечение пострадавших детей. Прежде всего, любые
тупые повреждения, как правило, сочетаются
с травмой головы — наиболее частым видом по-
вреждений. В результате при оценке состояния
больного, находящегося нередко в полукоматозном
состоянии, возникает серьезная проблема, связан-
ная с невозможностью установления контакта с по-
страдавшим. Отсутствие же отчетливой обратной
связи с ребенком, который, будучи в спутанном
сознании, не в состоянии отвечать на поставлен-
ные врачом вопросы, резко затрудняет диагности-
ку повреждений других органов и систем.
Вслед за выявлением симптомов (или при их от-
сутствии) травмы головы важно адекватно оценить
имеющиеся очевидные наружные повреждения ске-
лета и мягких тканей, стоящие по частоте травми-
рования на втором месте. Копа нет явных видимых
внешних признаков травмы опорно-двигательного
аппарата и мягких тканей, или они незначитель-
ны, необходимо следующим этапом определить на-
личие или отсутствие опасных для жизни повреж-
дений внутренних органов. Очень широкий диапа-
зон возможной травмы различных внутренних ор-
ганов и многообразие сочетаний диктуют необходи-
мость оценки состояния травмированного ребенка
высокоопытными профессионалами, которые все-
гда должны быть в составе подразделений служб
экстренной помощи, так же как и все необходимое
оснащение для первичной оценки, помощи и реа-
нимации. К сожалению, в действительности нередко
ситуация оказывается обратной — первичная оцен-
ка детей, получивших травму, осуществляется
наименее опытными членами бригад скорой помо-
щи.10 Это положение должно быть пересмотрено,
и соответственно штаты всех звеньев неотложной
медицинской помощи детям (НМП-Д) следует все-
мерно полноценно укреплять опытными професси-
оналами. Постоянные штатные квалифицирован-
ные сотрудники экстренной медицинской помощи
всегда должны быть в первых рядах на самых ран-
них этапах при лечении травмированных детей,
так же, как и при обучении и контроле за повыше-
нием квалификации менее опытных специалистов.
СЛУЖБА НЕОТЛОЖНОЙ
МЕДИЦИНСКОЙ ПОМОЩИ ДЕТЯМ
Система НМП-Д представляет собой единую орга-
низационную структуру, состоящую из нескольких
звеньев и решающую задачи транспортировки
и оказания высококвалифицированной помощи де-
тям при тяжелых повреждениях или острых, угро-
жающих жизни состояниях и заболеваниях. Звенья
этой структуры включают в себя системы связи,
транспорта, срочной медицинской помощи на ме-
сте происшествия (НПТ-АВС— неотложная по-
мощь при травме, первые три ABC-звена), дет-
ский травматологический центр 1 го уровня,
и далее отделения: педиатрическое интенсивной
терапии (ПОИТ), промежуточное и реабилита-
ционное." 13
В идеале экстренная помощь должна начинаться
с момента повреждения одновременно с констата-
цией факта травмы. Все диагностические и ле-
чебные мероприятия необходимо осуществлять в
строгой последовательности, заранее четко разра-
ботанной и нс менее четко организованной. Не-
медленно после получения по системе связи сигна-
ла о травме выехавшая на место происшествия
травматологическая бригада начинает активную
догоспитальную реанимацию. Ребенок должен быть
быстро и тщательно оценен по определенной схеме
(первичное обследование) в отношении жизнс-
опасных повреждений. Начальная «сортировка»
и принятие квалифицированного решения о том.
ЭПИДЕМИОЛОГИЯ ТРАВМЫ 123
куда рациональнее всего транспортировать данно-
го больного, осуществляются бригадой специали-
стов по неотложной помощи (СНП) после кон-
сультации (по системе связи) с медицинским «ко-
ординационным центром». К сожалению, в этой
схеме оказания первичной неотложной помощи
еще недостаточно используются различные суще-
ствующие специальные методы количественно-
балльной оценки тяжести травмы, такие как напри-
мер Шкала оценки тяжести Детской Травмы
(ШДТ). В любом случае главная цель догоспи-
тальной помощи — быстрая и безопасная транс-
портировка с места происшествия в соответствую-
щее лстское травматологическое медицинское уч-
реждение.
Центр, где оказывается помощь пострадавшим
от различных повреждений, должен иметь сформи-
рованную квалифицированную детскую травмато-
логическую бригаду. При получении сигнала
о транспортировке в данное учреждение травмиро-
ванного ребенка эта бригада обязана в полной
готовности ожидать прибытия пострадавшего в от-
делении экстренной помощи, где продолжается
осуществление жизнеобеспечения и лечебно-диа-
гностических мероприятий.
Пребывание больного в стационаре длится до
тех пор, пока не ликвидированы все проявления
и последствия травмы и не достигнут тот статус,
в котором ребенок был до получения повреждения.
В некоторых ситуациях процесс заживления и реа-
билитации может потребовать нескольких месяцев
и даже нескольких лет (рис. 10-3).9 14
Рис. 10 3. Системный подход к оказанию помощи при детской
травме-
В большинстве регионов Соединенных Штатов
травматологическая помощь пока еще недостаточ-
но развита либо не централизована. В 1982 г. бы-
ли определены ведущие направления развития
звеньев НМП-Д и сформулированы основные спе-
цифические положения системы детской травмато-
логической помощи — Нормативы по оказанию
помощи критически пострадавшим детям. Этот
документ разработан Американской Корпорацией
Хирургов и входит составной частью в Правила
оказания оптимальной помощи травмированно-
му ребенку на госпитальном и догоспитальном
этапах. Указанные документы были одобрены
Американской Ассоциацией Детских Хирургов
и Комиссией по травме Американской Корпорации
Хирургов.1’ Государственная система лечения жиз-
неопасных повреждений у детей наиболее хорошо
развита в Мэриленде, где опа успешно функциони-
рует в течение последних 17 лет (1975 1992 гг.).
Данные по этому региону и использованы в насто-
ящем разделе.
С июля 1989 г. по июнь 1990 г. травму получи-
ли 950 детей, 513 из них поступили в Мэриленд-
ский региональный детский травматологический
центр. Здесь мы используем данные лишь о 462
пациентах, где информация была наиболее полной
и, кроме того, травма зарегистрирована в Нацио-
нальном Регистрационном Центре по инвалидно-
сти и реабилитации после детской травмы.1*'
Все дети были в возрасте до 15 лет (средний
возраст 7, 8 лет). Соотношение мальчики : девочки
равнялось 2: 1 (табл. 10-2). Транспортировка по-
страдавших осуществлялась вертолетом (42%)
или наземным транспортом (58%). Большинство
детей (81%) были доставлены непосредственно
с места происшествия. Характер повреждений (ту-
пая травма — проникающая), так же, как и меха-
низм травмы, представлены в таблице 10-3.
Тупую травму дети чаще всего получали при
падениях (28%). На втором месте по частоте меха-
низма травмы стоят автомобильные аварии, в ко-
торых пострадавшие были в роли пешеходов
(23%), далее по убывающей следуют велосипед-
ные травмы, остальные — транспортно-наземные
и мотоциклетные (11%). У оставшихся 73 паци-
ентов отмечались спортивные травмы (24), по-
вреждения при жестоком обращении-насилии (36),
краш-синдром и ожоги (13).
ТАБЛИЦА 10-2. Распределение пациентов с травмой по полу
и возрасту
Пил Количество Процент
Мальчики 295 64
Девочки 167 36
462 100
Возраст
До 1 года 22 4,8
1 год — 5 лет 157 34
6 10 лет 159 34
II —15 лет 123 27
16 20 лет 1 0,2
— ————
462 100
124 ЭПИДЕМИОЛОГИЯ ТРАВМЫ
ТАБЛИЦА 10-3. Механизм и вины повреждений
Тупая травма Количество Процент
Автомобильные аварии (пешеходы) 105 23
Автомобильные аварии (пассажиры) 79 17
Автомобильные аварии (велосипед [41]. 50 11
другие виды наземною гранспорта [6],
мотоциклы (3])
Падения 128 28
Другие 73 15
Проникающие ранения
Огнестрсл ьв ыс 16 4
Ножевые 9 2
Другие (спортивные, насилие) 2 0.4
Проникающие повреждения отмечались редко,
но зато, как правило, заканчивались смертью. По
частоте поражения различных органов травма рас-
пределялась следующим образом; ЦНС (86%),
скелет (60%), мягкие ткани (24%), живот (20%),
грудная клетка (7%).
Средняя летальность среди 462 пациентов была
2,2% (10 больных). Из умерших де гей: 5 получили
повреждения в авгонроисшествиях, 3 -- при паде-
нии. и 2 летальных исхода были связаны с прони-
кающими ранениями. Непосредственной причиной
смерти у 70% детей была закрытая гравма головы,
причем 7 пациентов умерли сразу при поступле-
нии, остальные трое — в течение раннего госпи-
тального периода.
ПРОФИЛАКТИКА ТРАВМАТИЗМА
При анализе летальности, связанной с травмой,
среди детей от 0 до 14 лет в Соединенных Штатах
за 1980—1985 гг., отмечено несомненное ее сниже-
ние, особенно существенное в младшем возрасте
(до 9 лет) и касающееся почти всех видов повреж-
дений. Если принимать во внимание пять самых
«фатальных» механизмов травмы, то наибольшее
снижение выявлено в группе утоплений и группе
автодорожных происшествий, где детишки были
пешеходами. Частота травм в автомобильных ава-
риях, когда пострадавшие дети находились в ма-
шине, уменьшилась в общем па 14%. Имеется за-
метная разница в темпах снижения травматизма
в разных возрастных группах: у детей в возрасте
до 1 года уменьшение на 32%, 1—4 года — на
22%, 5—9 лет — на 11 % и 10—14 лет — всего на
3%. К сожалению, не снижается летальность, свя-
занная с суицидными повреждениями, среди детей
в возрасте от 10 до 14 лет.
Профилактическая работа с детьми в догравма-
тическом периоде должна стоять па одном из пер-
вых мест в детской травматологии и в обществе
в целом,2 ибо во все времена остается актуальной
формула «Легче болезнь предупредить, чем потом
ее лечить».
Каждый год в стране более 250 000 детей полу-
чают травмы и соответственно госпитализируют-
ся.1, Необходимость в экстренной реанимации, так
же, как и в длительной реабилитации, cyuiei гнев-
но увеличивает нагрузку на нашу и без того пере-
груженную систему здравоохранения. До тех пор,
пока не будет серьезных изменений в профилакти-
ке травматизма и в системе оказания экстренной
помощи, мы будем продо, 1жать наблюдать это
«кровавое истребление» детей в результате травм!
Ежегодно более 78 000 детей госпитализируются
по поводу травмы головы, что составляет около
трети всех экстренных госпитализаций при трарме
в детском возрасте. На лечение такого количества
больных только в остром периоде затрачивается
27 млн долларов.1’ Кроме того, хорошо известны
тяжелые последствия травмы головы у детей, по-
следствия физические, неврологические и психоло-
гические. И хотя скудна информация о травме го-
ловы малой и средней тяжести, однако можно
предположить, что и здесь психосоциальн»1е и по-
веденческие последствия удлиняют сроки необхо-
димого диспансерного наблюдения. Вес это обу-
словливает существование непреходящих проблем,
стоящих перед системой здравоохранения в связи
с детским травматизмом, что уже неоднократно на-
ми подчеркивалось.18' 20
В 1951 г. Американская Академия Педиатрии
(ААП) разработала законопроект, предусматрива-
ющий обязательное получение элементарного об-
разования по детскому травматизму врачами и
другими работниками здравоохранения, равно как
и населением страны. Это были первые шаги на
поприще законодатели гва по профилактике
травм, их контролю и лечению.21
Что касается промышленности, то в прежние
времена мало кто проявлял интерес и стремился
к лидерству в развитии стандартов для производ-
ства безопасных товаров, используемых детьми.
Если :аже такие стандарты и существовали, то не
было средств для их соблюдения и претворения
в жизнь, да и не ясно было, кто должен был выпол-
нять эти предписания С увеличением же осведом-
ленности населения о возрастающей частоте дет-
ской травмы и летальности в обществе начали
понимать, что добровольных общественных усилий
и действий в этом направлении явно недостаточно.
Необходимо было легализовать некоторые положе-
ния не только для работников промышленности,
что обязывало бы их производить безопасные то-
вары. но и для населения, которому следует пони-
мать необходимость соблюдения ряда правил, обсс
почивающих самосохранение и безопасность.
Первоначально три элемента казались необхо-
димыми для избавления общества от детского
травматизма: законодательство, прокладывающее
путь для соответствующих технологий, и образо-
вание, обеспечивающее все остальные аспекты
этой проблемы. Однако очень быстро стало ясно,
что подобный подход к профилактике травматизма
явно недостаточен. Необходим был еще один ком-
понент — обязательное контролируемое проведе
ние в жизнь этих намерений. Раннее федеральное
законодательство, направленное на решение этих
задач, до 1965 г. носило в основном «реактивный»
характер и вступало в действие лишь после свер-
ЭПИДЕМИОЛОГИЯ ТРАВМЫ 125
шения трагедий» преследуя довольно специфиче-
ские цели. Примерами таких «исторических памят-
ников» может служить ряд актов по правилам
безопасности при использовании легко воспламе-
няющихся тканей, эксплуатации холодильников
и т. д.21 И хотя намерения, обусловившие появление
на свет этих законов, были похвальными, однако
эффект отмечался слишком кратковременный. И
только в 1973 г., после 20 лет дебатов. Конгрессом
была наконец создана Потребительская Комиссия
по контролю за качеством и безопасностью това-
ров. Это позволило довести до конца дело, не за-
вершенное в свое время Федеральной Комиссией
Предпринимателей. Федеральный А кт-перечень
опасных веществ потребовал многочисленных по-
правок и дополнений.
Важной вехой в профилактике травм была боль-
шая работа, проведенная объединенными усилиями
правительства и медиков А АП, по маркировке
и разработке специальных форм и упаковок сали-
цилатов, применяемых в педиатрии. Дальнейшим
шагом на пути уменьшения травматизма и смерт-
ности в результате транспортных аварий явилось
создание при правительстве в середине 60-х годов
Национального Управления по безопасности до-
рожного движения.21 В задачи данной структуры,
укрепленной для этих целей специальными штата-
ми, входит контроль за соблюдением норм, стан-
дартов и программ, обеспечивающих безопасность
на всех уровнях, начиная с промышленного про-
изводства автомобилей, правил дорожного движе-
ния и т. д. Сюда же относятся и такие меры, как
тестирование водителей на содержание алкоголя
в крови, использование мотоциклетных касок, при-
вязных ремней, откидных рулевых колонок и дру-
гих приспособлений, а также программы специаль-
ного обучения для полиции, водителей транспорта
и персонала скорой медицинской помощи. Целена-
правленное осуществление всех этих мероприятий,
начатое на федеральном уровне, первоначально,
в 60-х годах, было довольно хаотичным и неравно-
мерным в разных штатах.
Со временем отмечаются значительные достиже-
ния на пути профилактики детского травматизма,
но, к сожалению, не повсеместно. И порой чрезвы-
чайно трудно легализовать некоторые достаточно
простые, но важные меры. Например, к настояще-
му времени только в одной местности в Соединен-
ных Штатах (Говард, Мэриленд) принят закон,
обязующий юных велосипедистов (в возрасте до
16 лет) носи1ь защитные шлемы.
В заключение необходимо еще раз подчеркнуть,
что профилактика травматизма должна начинать-
ся задолго до травмы. И эффективное обеспечение
детской безопасности может быть достигнуто лишь
при объединении усилий правительства (как феде-
рального, так и местного), профессионалов-меди-
ков, работников системы образования, представи-
телей духовенства и родителей.
ЭТИЧЕСКИЕ ПРОБЛЕМЫ
«ПОЛОЖЕНИЯ О СМЕРТИ
И ИСКУССТВЕННОМ ПОДДЕРЖАНИИ ЖИЗНИ»
Проблема определения понятия смерти и выработ-
ки критериев, позволяющих ее констатировать, ни
в одном из разделов медицины не стоит так остро
и не вызывает столько споров, как в травматоло-
гии, особенно детской. С точки зрения социальной
и законодательной, так же, как и непосредственно
медицинской, факт смерти должен устанавливать-
ся только в том случае, когда этот «диагноз» аб-
солютно несомненен и неопровержим.22 Однако
главная сложность заключается в том, что, с одной
стороны, основным и широко распространенным
определением понятия смерти является «смерть
мозга», а потому многочисленные и разнообразные
исследования направлены на выявление и установ-
ление наиболее достоверных и объективных ее
признаков. С другой же стороны, ведущим направ-
лением развития медицины вообще и особенно та-
ких ее разделов, как травматология и реанимация,
является всестороннее совершенствование методов
искусственного поддержания жизни. Резко обостри-
лась данная проблема с приходом в медицину но-
вого раздела — трансплантологии, использующей
в качестве доноров трупы. Начало этому направ-
лению было положено в 50-х годах текущего сто-
летия, когда человеку впервые была пересажена
почка, затем в 60-х гг. последовала транспланта-
ция сердца, а последние два десятилетия — печени
и поджелудочной железы, а также кишечника, изо-
лированно либо в сочетании с паренхиматозными
органами. Параллетьно стремительному развитию
трансплантологии в неотложной клинической ме-
дицине резко возрос интерес к проблеме «смерти
мозга».
Трансплантация может быть успешной лишь
в том случае, когда пересаживаемый орган интак-
тен. Однако его пригодность для трансплантации
стремительно уменьшается по мере остановки ды-
хания и кровообращения. Иначе говоря, наиболее
подходящим донорским органом является тот, ко-
торый взят от молодого здорового организма,
умершего непосредственно после травмы головы.
Если же проводится интенсивная терапия, то орга-
ны потенциального донора «портятся». Таким об-
разом. решающий и в то же время особенно слож-
ный вопрос — определить на самой ранней стадии
тот момент, когда мозг пациента перестал функци-
онировать, притом необратимо. В действительно-
сти же, на практике, лишь в очень небольшом про-
центе случаев взятие органов для трансплантации
осуществляется с учетом критериев смерти мозга.22
Не удивительно, что при решении вопроса о вре-
мени наступления смерти медики руководствуются
в меньшей степени желанием облегчить транс-
плантологам пересадку органов, чем стремлением
оказывать соответствующую оптимальную помощь
больному, искусственно поддерживая жизнь «до
последнего», когда пациент находится на грани
смерти. Именно такое отношение врача к больно-
126
ЭПИДЕМИОЛОГИЯ ТРАВМЫ
му пользуется наибольшим уважением и понима-
нием в обществе. С другой стороны, нельзя не при-
нимать во внимание, что порой использование
дорогостоящей и имеющейся в недостаточном коли-
честве аппаратуры для интенсивной терапии у па-
циента с нефункционирующим мозгом может не
только бессмысленно продлевать положение нео-
пределенности и страдания убитых горем родст-
венников, но и оставить в это время без надлежа-
щей помощи больных с обратимыми состояниями.22
Если эта проблема иногда почти неразрешима, да-
же у взрослых пациентов, то у маленьких детей
сложность вопроса определения времени смерти
мозга возрастает до предела.
ЛИТЕРАТУРА
1. Haddon W Jr: Advances in epidemiology of injuries as a basis
for public policy. Public Health Rep 95:411—21, 1980.
2. Jacobs LM, Jacobs BB: Injuries: Statistics, prevention, and costs.
In Manox KL, Moore EE, Feliciano DV (Editors). Trauma.
Appleton & Lange, East Norwalk, CT, pp 15—33, 1988.
3. Baker SP, Waller AE: Childhood Injury State-by State Morta-
lity Facts. The Johns Hopkins Injury Prevention Center. Janua-
ry. 1989.
4. National Center for Health Statistics: Vital Statistics of the Uni-
ted States, 1984. US Dept of Health and Human Services. Pub-
lic Health Service, NCI IS, Hyattsville, MD. 1987.
5. National Research Council and Institute of Medicine. Committee
on Trauma Research. Commission on Life Sciences: Injury in
America, a continuing public health problem. National Academy
Press, Washington, DC, 1985.
6. Overview of injury mortality. In Baker SP, O’Neill B. Karpf RS
(Editors). Injury Fact Hook. Lexington Books. Lexington. MA,
pp 17—37. 1984.
7. Waller AF., Baker SP, Szocka A: Childhood injury deaths: Nati-
onal analysis and geographic variations. Am J Public Health,
79:310—314, 1989.
8. Beaver BL, Moore VL, Peclet M. et al.: Characteristics of pedi-
atric firearm fatalities. J Pediatr Surg 25:97—100, 1990.
9. Haller JA, Beaver BL: Overview of pediatric trauma. In Toulou
kian RJ (Editor). Pediatric Trauma, second edition. CV Mosby,
St. Louis, pp 3—13, 1990.
10. Morse TS: Triage, technicians and leaching in a children’s
emergency room. J Pediatr Surg 8:70!—7U4, 1973.
11. Haller J A, Beaver BL: Emergency medical systems for children’s
trauma. In Dieckman RA (Editor). Planning and Managin
Systems fur Pediatric Emergency Care. Williams and Wilkens,
Baltimore, 1992.
12. Ramenoksky ML: Emergency medical services for children and
pediatric trauma system components. J Pediatr Surg 24:153—
155, 1989.
13. Haller J A (Editor): Emergency medical services for children.
Report of the 97th Ross Conference on Pediatric Research. Ross
Laboratories, Columbus, OH, 1989.
14. Haller J A: Toward a comprehensive emergency medical system
for children. In Coran AG, Harris BII, (Editors). Pediatric
Trauma: Proceedings of the Third National Conference. J В
Lippincott, Philadelphia, pp 1—5, 1990.
15. American College of Surgeons: Resources for Optimal Care о
the Injured Patient. Chicago, October, 1989.
16. National Institute on Disability and Rehabilitation Research:
Pediatric Trauma Registry Phase 2. September 5, 1990.
17. MacKcnzic EJ, Morris JA. DeLissovoy GV, el al.: Acute hospi-
tal costs of pediatric trauma in the United States: How much
and who pays? J Pediatr Surg 25:970—976, 1990.
18. Wesson DE, Williams JI, Spence LJ, et al.: Functional outcome
in pediatric trauma. J Trauma 78:497—502, 1988.
19. Levin HS, Eisenberg HM: Neuropsychological outcome of clo-
sed head injury in children and adolescents. Childs Brain
5:281—292, 1979.
20. Casey R, 1 .udwig S, McCormick MC: Morbidity following minor
head trauma in children. Pediatrics 78:497—502, 1986.
21. McIntire M (Editor): Injury Control for Children and Youth.
Committee on Accident and Poison Prevention, American Acade-
my of Pediatrics, Elk Grove Village, IL, 1987.
22. President's Commission fui the Study of Ethical Problems in
Medicine and Biomedical and Behavioral Research: Defining
death: A report on the medical, legal and ethical issues in the
determination of death. U.S. Government Printing Office, Was-
hington, DC, July, 1981.
Глава 11
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ
В ОСТРОМ ПЕРИОДЕ
История. С древних времен человек нередко ста-
новился объектом как несчастных случаев, так
и умышленных повреждений, что обусловливало
потребность в срочной помощи, особенно возрас-
тавшую во время войн, когда травму получали
огромные количества как воинов, так и граждан-
ских лиц.
Фундамент современной хирургии в значитель-
ной степени и во многих отношениях был заложен
во время войн,1 3 которые всегда, во все времена
являлись для врачей школой хирургии, позволяв-
шей приобрести ни с чем нс сравнимый опыт. Так,
Джон Гюнтер (1728—1793), основоположник со-
временной хирургии, описал огнестрельные раны
живота, груди и головы, основываясь на опыте,
полученном во время кровавых войн Британской
империи в середине XVIII века. А Алексис Кэррел
разработал технику сосудистых анастомозов, при-
меняемую и сегодня. Война служила школой для
приобретения опыта лечения самых разнообраз-
ных видов повреждений, и хирург всегда был ря-
дом с полем сражения, поскольку часто возникала
потребность в срочном восстановлении анатомии,
так же, как и физиологического гомеостаза.
Травма всегда была и остается хирургической
патологией, поскольку для диагностики и лечения
повреждений необходимы навыки и опыт именно
хирургические.
На протяжении всей истории Соединенных Шта-
тов лечение воинов с травмой всегда хорошо доку-
ментировалось. По данным Военного Департамен-
та, во время Гражданской Войны от полученных
ранений погибли 620 000 участников с обеих сто-
рон. ’ 25% из тех, кто не умер сразу, скончались
от ранений позже. Столь ошеломляюще высокая
летальность частично объясняется сложностью
и длительностью транспортировки раненых в ме-
дицинские учреждения, которые к тому же не везде
имелись. Так в битве Bull Run средняя продолжи-
тельность транспортировки составляла 72 часа. Во
время 1-й мировой войны появились моторизован-
ные медицинские пункты, что привело к сокраще-
нию длительности транспортировки до 8 часов.
Соответственно и летальность сразу упала до
8,2%.
Во время 2-й мировой войны с целью оказания
хирургической помощи медики были непосредст-
венно введены в состав вооруженных сил. Именно
они обеспечили возможность использования плаз-
мы, морфина, местных сульфамидных препаратов,
а в последние годы войны — пенициллина. По ме-
рс расширения сети дорог, позволявших с меньши-
ми сложностями осуществлять транспортировку,
стали стремительно развиваться моторизованные
медицинские пункты. К концу войны для началь-
ных этапов транспортировки начали использовать
вертолеты. Летальность составляла в то время 4%,
а продолжительность транспортировки —* в сред-
нем 4 часа.
Корейская война привнесла новые значительные
изменения в лечение повреждений. В качестве
транспортных средств широко использовались вер-
толеты. Для оказания экстренной помощи ране-
ным непосредственно около линий фронта стали
разворачиваться передвижные армейские хирур-
гические госпитали (ПАХГ). Опытные хирурги,
работавший в ПАХГ, обеспечивали высококвали-
фицированную помощь. Во время корейской войны
смертность уменьшилась до 2.1%, а длительность
транспортировки — до 1,2 часа.
В деле оказания помощи раненым как по каче-
ству, так и по объему, Вьетнам, по данным Армей-
ских Служб, явился кульминацией.3 Штаты высоко-
квалифицированных хирургов, среднего медицин-
ского персонала и медиков других специальностей
были во Вьетнаме укомплектованы полностью.
Транспортировка вертолетами, усовершенствован-
ная как в авиационно-техническом, так и в меди-
цинском плане, позволяла обеспечивать специализи-
рованное обслуживание, качественное и быстрое.
Смертность снизилась до 1,9%, а время транспор-
тировки — в среднем до 27 мин.
Во время войны еще один фактор повлиял на
оказание помощи раненым — постоянно совершен-
ствующиеся системы связи, с помощью которых не
только решались военные задачи, но также про-
120 ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ
изводились поиски раненых и оказание им догос-
питальной помощи/ С первых же дней использова-
ния в коммуникационных сооружениях спутнико-
вых систем связи резко возросли возможности
непосредственного лечения «на расстоянии*.
Внедрение в жизнь четко отработанной системы
травматологической помощи способствовало сни-
жению летальности благодаря прежде всего сокра-
щению времени транспортировки, формированию
травматологических бригад, всегда находящихся
в состоянии готовности, и, конечно же, использова-
нию современных средств связи. Стремительно
улучшающиеся результаты лечения травм во вре-
мя войны стимулировали в Соединенных Штатах
и «гражданский сектор» обратить более присталь-
ное внимание на травму среди мирного населения.
Национальная Академия Наук в 1966 г. опублико-
вала работу «Смерть и нетрудоспособность в ре-
зультате несчастных случаев — запущенная бо-
лезнь современного общества».* Это был перший
серьезный шаг подобного масштаба, заставивший
общество в целом и представителей как медицин-
ских, так и иных профессий, заняться проблемами,
связанными с травмой. Почти все «невоенные» до-
стижения в травматологии за последние 2,5 деся-
тилетия обязаны своим появлением упомянутой
работе, ставшей теперь классической.
Успехи в травматологической помощи, однако,
в большинстве своем невольно касались преимуще-
ственно взрослой молодежи, поскольку основное
количество травм происходит именно в этой воз-
растной группе. Оказание помощи при травме де-
тям осуществлялось так же, как и у взрослых лю-
дей, поскольку считалось, что дети не нуждаются
в каких-либо специфических мерах помощи. Со
временем было доказано, что подобный подход не
правилен. Такие факторы, как рост и развитие,
дозы и характер применяющихся в детском возра-
сте лекарственных веществ, размеры инструмен-
тов, аппаратов и оборудования, физиологические
и анатомические различия, необходимость в специ-
альном обучении персонала, совершенно особое
положение и отношение к детям в семье — все это
требует принципиально иного подхода к обеспе-
чению высококвалифицированной травматологиче-
ской помощи в детском возрасте.
Курс специализированной экстренной помощи
при травме. Травматологическая помощь в Сое-
диненных Штатах, так же, как и почти во всем
мире, заметно улучшилась в 1978 г., когда Амери-
канской Корпорацией хирургов был разработан
для врачей курс специализированной экстренной
помощи при травме (СЭПТ). Инициатором его со-
здания была небольшая группа хирургов-энтузи-
астов из Линкольна (штаг Небраска), осознавших
потребность каждого, любого врача в овладении
простым, воспроизводимым и легко воспринимае-
мым при обучении методом оказания помощи
больному с тяжелыми повреждениями при жизне-
угрожающих состояниях в течение первого часа
после травмы. Понимание такой необходимости
возникло на почве личной трагедии одного из этих
хирургов, который на собственном печальном опы-
те убедился в том, насколько недостаточно препо-
давались в медицинских институтах вопросы трав-
матологической помощи и на каком низком уровне
эта помощь оказывалась на практике во многих
регионах страны.5
Курс СЭПТ стал преподаваться повсеместно
в Соединенных Штатах, а также в Канаде, Мекси-
ке, Центральной и Южной Америке, Великобри-
тании, Израиле, Австралии и Ирландии. Более,
чем 130 000 врачей прошли обучение на этом кур-
се. Дальнейшее развитие СЭПТ привело к созда-
нию дополнительного курса -догоспитальной эк-
стренной помощи при травме (ДГЭПТ), разрабо-
танного Национальной Ассоциацией Специалистов
по Неотложной Медицине.6
СЭПТ подразумевает прежде всего последова-
тельность мероприятий при лечении травмы, осно-
ванную на необходимости устранения, в первую
очередь, жизнеопасных повреждений, которые мо-
гут привести к смерти или тяжелой инвалидности.
Например, вряд ли можно добиться хороших ре-
зультатов, если перелом конечности лечится до то-
го, как обеспечена функция пораженных дыхатель-
ных путей. Кроме того, в курсе предусмотрено обу-
чение методам стабилизации состояния больного
при жизнеугрожающих повреждениях на раннем
этапе, до того, как пациенту начнут оказывать
квалифицированную помощь в медицинском либо
каком-то ином специализированном учреждении.
Порядок срочности в проведении тех или иных
мероприятий основан прежде всего на знании того,
какое из полученных повреждений быстрее всего
может привести к смерти. Так, при отсутствии ле-
чения поражение дыхательных путей приводит
к летальному исходу за 3—4 минуты. Если дыха-
тельные пути проходимы, но больной не может
дышать по каким-то иным причинам, смерть на-
ступает за 5—7 минут. Тяжелый гиповолемиче-
ский шок обусловливает летальный исход при от-
сутствии лечения примерно за 10 мин. Для упро
щения задач, стоящих перед врачом, оказывающим
первую помощь, мы используем алгоритм в виде
первых букв алфавита — ABCDE, определяющий
последовательность проведения экстренных меро-
приятий:
А — Airway В — Breathing — дыхательные пути — дыхание
С — Circulation — циркуляция
D — Disability — состояние ЦНС (краткое неврологическое обследова- ние)
Е — Expose — полный осмотр (раздеть больного полностью, ста- раясь при этом избежать
его охлаждения)
НАЦИОНАЛЬНЫЙ РЕГИСТРАЦИОННЫЙ
ЦЕНТР ДЕТСКОЙ ТРАВМЫ
В 1985 г. Национальный регистрационный центр
детской травмы (НРЦДГ) впервые начал собирать
данные о повреждениях у детей и знакомить с ни-
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ 129
ми общественность, в том числе медицинскую-7
Имевшиеся до этого показатели детского травма-
тизма были недостаточно точными и нелегализи-
рованными.
НРЦДТ концентрирует основные фактические
и цифровые сведения о травме у детей и всячески
поддерживается в своей деятельности Министерст-
вом Просвещения Соединенных Штатов. В настоя-
щее время 55 медицинских центров из разных ре-
гионов Соединенных Штатов и Канады поставля-
ют сведения в национальный центр, не получая за
это никакой платы или финансовой поддержки,
в результате в банке данных уже зарегистрирова-
ны (полностью) более 35 000 пациентов.
Дважды в год планово, а также при наличии
запросов, отчеты НРЦДТ отсылаются в центры,
поставляющие ему свои данные. Предоставленные
(бесплатно) сведения используются учреждениями
в научных целях. Примеры демографических от-
четов НРЦДТ показаны на рисунках 11-1 — 11-5
и в таблице 11-1.
Шкала оценки тяжести детской травмы.
Многочисленные исследования, проведенные в
НРЦДТ. позволили разработать ряд клинических
вспомогательных методов для оценки и лечения
травмированных детей. Одна из первых работ бы-
ла направлена на использование имеющихся дан-
ных для создания шкалы оценки тяжести травмы
у детей. Потребность в такой шкале была очевид-
на, поскольку все параметры в других шкальных
системах брались, как правило, при обследовании
взрослых больных. Шкала (оценки тяжести) дет-
ской травмы (ШДГ), разработанная Tepas с со-
авт., включает 6 компонентов, наиболее прогности-
чески важных в отношении летальных исходов
и инвалидизации и полученных в результате рас-
четов с использованием множественных рег-
рессий?
1. Масса тела
2. Состояние дыхательной системы
3. Систолическое артериальное давление
4. Состояние центральной нервной системы
(ЦНС)
5. Открытые раны
6. Наличие переломов
Каждый компонент в свою очередь оценивается
в цифровом значении в зависимости от тяжести
поражения:
+2 = повреждение легкое или отсутствует
-|-1= тяжелое повреждение
— 1 = критическое жизнеугрожающее повреж-
дение.
Рис. Н-1. Виды повреждений у 20.528 детей о травмой, по дан-
ным Национа ibnoro Регистрационного Ценцм Детской Травм и
(от октября 1990 г.).
ВП — велосипеды, мопеды, автомобили; ДНТ — другой назем-
ный транспорт; ПШ - пешеходы; ОР — оружейные ранения
(как огнестретьное, так и холодное оружие).
9 Заказ № 1622
Рис. П-4. Распределение 326 детей,
травмы, по механизму попрежтений.
умерших в результате
130 ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ I ОСТРОМ ПЕРИОДЕ
Для упрощения оценки показатели объединены
в таблицу (табл. 11-2). Для каждого компонента
выбирается одно цифровое значение, а затем вы-
числяется общая сумма. Оценка по ШДТ может
колебаться от +12 при отсутствии повреждения
или незначительной его тяжести до —6 при прак-
тически абсолютно фатальной травме. Чем ниже
оценка по ШДТ, тем больше тяжесть повреждения.
Между оценкой по ШДТ и летальностью имеется
обратная линейная корреляция (см. табл. 11-1).’'
ШДТ может быть использована в качестве про-
стого и эффективного метода определения очеред-
ности и последовательности мероприятий при ока-
зании помощи. По существу у пациентов с оцен-
кой по ШДТ 9 и выше летальных исходов не
бывает. Возможность наступления смерти появля-
ется на уровне 8 по ШДТ (критический, погра-
ничный коэффициент) и прогрессивно увеличива-
ется по мере снижения цифровых значений (см.
табл. 11-2). Соответственно при критической оцен-
ке 8 и более низких показателях ШДТ необходимо
транспортировать ребенка в го медицинское уч-
реждение, где помощь может быть оказана на са-
мом высоком уровне.’ Использование этой крити-
ческой оценки способствовало тому, что 25% детей
были направлены именно в те больницы, где обес-
печивалась наиболее квалифицированная помощь.
Еще одно достоинство ШДТ состоит в том, что
в ней по сути заложены и сконцентрированы
основные положения C31IT.
ТАБЛИЦА 11-1. Летальность при травме в зависимости от
оценки по шкале тяжести детской травмы
(общее количество детей 13.162)
Оценка по ШДТ Летальность (%) % больных с данной оценкой среди общею числа пациентов
<- 2 96,6 0,21
— 1—0 70,9 0,78
1—2 39,3 1.49
3—4 28.1 2,54
5-6 11,7 5,45
7—8 0,9 14.63
9 10 0,1 30,56
11 — 12 0.0 44,3
Причины смерти. НРЦДТ обладает в числе
прочих показателей данными о частоте и соотно-
шении изолированной и сочетанной травмы у де-
тей. Были подтверждены существовавшие и ранее
представления о том, что дети чаще страдают от
множественных повреждений, возникновению ко-
торых способствуют малые размеры тела и бли-
зость расположения органов и систем друг к дру-
гу. Поэтому, при наличии хотя бы одного явного
повреждения, врач обязан провести полное обсле-
дование.
Главная причина смерти детей — травма голо-
вы Важные данные были получена НРЦДТ о том,
что хотя повреждение ЦНС и является одним из
наиболее частых танатогенных факторов, однако
не обязательно именно первичная травма головы
обусловливает летальный исход. ' Не менее ча-
сто к смерти приводит не первичное, а вторичное
поражение или повреждение ЦНС, которое возни-
кает в тех случаях, когда не лечатся быстро и со-
ответствующим образом гиповолемический шок
или гипоксия.
При уменьшении артериального давления или
повышении внутричерепного церебральное перфу-
зионное давление падает ниже интракраниального,
в результате чего уменьшается перфузия мозга.
ТАБЛИЦА 11-2. Шкала тяжести детской травмы
Величины
Компонент +2 +1 — 1
Масса тела Дых. пути ЦНС (сознание) Систол- АД Открытые раны Переломы >20 кг Норма В сознании >90 мм Hg Нет Нет 10—20 кг Нарушения корриги- руемы Спутанное 50—90 мм Hg Небольшие Единичный закрытый <10 кг Нарушения некорригируе- мы Коматозное <50 мм Hg Большие или проникающие Открытый или множествен- ные
И ТОГО = ШДТ________
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ 131
И вне зависимости от того, внезапно или на протя-
жении длительного промежутка времени происхо-
дит падение рО2, мозг, перфузируемый кровью
и являющийся абсолютно аэробным органом, под-
вергается при этом вторичному, порой очень
тяжелому, повреждению. Оптимальный метод ле-
чения в подобной ситуации — обеспечение аде-
кватной перфузии мозга хорошо оксигенированной
кровью.
Согласно данным НРЦДТ, половина смертен,
связанных с тр’авмой ЦНС, по сути вызваны вто-
ричным поражением ЦНС, чему, как правило,
способствует несоблюдение принципов алгоритма
ABCDE.
Летальность и выживаемость. По четко доку-
ментированным данным НРЦДТ ежегодно 25 000
детей умирают от повреждений, что составляет
1,9% всех видов травм в детском возрасте. Среди
же всех госпитализированных детей (нс только с
травмой) от повреждений погибают 3%. Разни-
ца в цифровых показателях объясняется тем, что
часть получивших травму пациентов умирает до
поступления в стационар, т. е. непосредственно на
месте происшествия.
Оценка результатов лечения травмы в детском
возрасте затрудняется тем, что при анализе обыч-
но используются принципы, применяемые для
взрослых пациентов. Кроме того, низкая смерт-
ность среди детей с травмой (3%) по сравнению
с этим показателем у взрослых (10%) таит в себе
опасность неоправданно спокойного отношения
к летальности в детском возрасте, ибо при исполь-
зовании критериев, применяемых в общей травма-
тологии, летальность у детей кажется вполне «при-
емлемой», а соответственно не вызывает беспокой-
ства и необходимости что-либо предпринимать для
ее снижения. Все это заставило разработать новый
способ оценки летальности у детей — Кумулятив-
ный Индекс Летальности (КИЛ).12
КИЛ определяется путем умножения частоты
процентного распределения травмированных детей
с каждым цифровым значением коэффициента
111ДТ НРЦДТ на разницу между смертностью
в данном госпитале и этим показателем НРЦДТ
для того же коэффициента ШДГ. В результате
этого расчета получается дифференцированный
индекс летальности. Сумма всех дифференциро-
ванных индексов летальности для каждого показа-
теля ШДТ представляет собой КИЛ.
КИЛ может иметь как положительные, так и от-
рицательные цифровые значения- Нулевой (0) по-
казатель принят за общенациональную норму
НРЦДТ. Если госпитальный КИЛ имеет положи-
тельное значение, это означает, что в данном гос-
питале результаты лечения травмы у детей лучше,
чем общенациональные. Отрицательный КИЛ со-
ответственно говорит о худших результатах. Для
оценки качества лечения детей с травмой любой
госпиталь может определить дифференцированный
индекс летальности для каждого цифрового коэф-
фициента ШДТ, что позволяет увидеть, насколько
результаты в данном медицинском учреждении от-
личаются от общенациональных.
ПРЕДВАРИТЕЛЬНОЕ ПЛАНИРОВАНИЕ
ЭКСТРЕННОЙ ПОМОЩИ ДЕТЯМ ПРИ ТРАВМЕ
Травма по своей природе всегда относится к экст-
ренной медицине. К сожалению, несчастные слу-
чаи нельзя планировать и предвидеть и они про-
исходят в большинстве своем в самое «неподходя-
щее время». Поступление больного с травмой
в госпиталь, и без того работающий в напряжен-
ном ритме, вызывает обычно нарушение заведен-
ного существующего порядка. Чтобы свести к
минимуму возникающую при этом «сутолоку», каж-
дая больница, которая занимается оказанием помо-
щи пострадавшим, должна иметь заранее подго-
товленный, хорошо продуманный план всех не-
обходимых в подобной ситуации мероприятий.
Учреждение, принимающее активное участие
в общей системе детской травматологии, обязано
детально разработать конкретную схему обеспече-
ния соответствующего лечения и сделать это не-
обходимо до того, как ребенок поступает в госпи-
таль. Подобный план подразумевает выбор сотруд-
ников, их обучение и обеспечение соответствую-
щими официальными удостоверениями, развитие
реанимационной службы, приобретение необходи-
мого оборудования, установку местных и наруж-
ных систем связи, четкую разработку схемы взаи-
модействия со всеми службами экстренной медици-
ны, в том числе региональными.
В любом крупном госпитале существуют обычно
6 отделений, где возможно осуществление квали-
фицированного обследования и лечения детей
с травмой. Это отделения реанимации, интенсив-
ной терапии, операционная, детское отделение,
рентгенологическое и отделение медицинской реа-
билитации. В течение первого часа оказания помо-
щи ведущую роль играет, разумеется, отделение ре-
анимации.
Наиболее эффективно лечение ребенка с по-
вреждениями проводит специализированная трав-
матологическая бригада, в состав которой должны
входить медицинские работники самых разных
профилей.13 Педиатрическая травматологическая
бригада обычно состоит из руководителя, хирур-
гов, врачей — специалистов по неотложной меди-
цине, представителей среднего хирургического зве-
на, медсестры (с травматологической подготовкой)
и парамедицинского персонала. Поскольку травма
является хирургической патологией, руководите-
лем бригады должен быть травматолог, выполняю-
щий в данном случае роль общего координатора
(«директора») всего процесса лечения. Этот чело-
век ответственен за все, в том числе за общую
оценку состояния ребенка, обеспечение примене-
ния оптимальных, наиболее быстрых и точных
методов диагностики и лечения, за объективную
интерпретацию и синтез всей получаемой информа-
ции и, наконец, за составление как кратковре-
менного, так и перспективного плана лечения.
Руководитель бригады должен определить, адек-
ватна ли проводимая реанимация, и уловить тот
момент, когда возникает необходимость в опера-
тивном вмешательстве. Он (или она) координиру-
132 ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ
ет лечение, предлагаемое специалистами смежных
хирургических дисциплин (ортопедами, нейрохи-
рургами и т я.), и, кроме всего прочего, должен
быть постоянно полностью и четко информирован-
ным об общем состоянии ребенка. Командующий
хирург обязан определить, какое хирургическое
вмешательство предпочтительнее в данной ситуа-
ции, и, более того, показана ли вообще какая-либо
операция.
Другие члены травматологической бригады дол-
жны быть соответствующим образом обучены ме-
тодам оказания помощи осбенку с повреждениями.
Каждый специалист обязан прежде всего уметь вы-
брать наилучший подход к данному виду травмы
со своей точки зрения как узкого специалиста. Од-
нако лечение, оптимальное для изолированного
поражения какой-либо системы, может быть совер-
шенно невыгодным и даже неприемлемым при со-
четанной травме Поэтому любой специалист дол-
жен подчиняться решению руководящего хирурга.
Вне зависимости от собственной специальности
любой член педиатрической травматологической
бригады должен принимать участие в СЭПТ. Обу-
чение на курсе СЭПТ способствует тому, что связь
между членами бригады осуществляется наилуч-
шим образом, ибо все они одинаково воспринима-
ют порядок срочности проведения мероприятий
при лечении жизнсугрожающих повреждений.
Медсестры, работающие в составе травматологиче-
ской бригады, также должны пройти курс СЭПТ.
К сожалению, большинство госпиталей не име-
ют достаточных и удобных площадей для работы
травматологических бригад. Тем не менее для
экстренного обследования и реанимации ребенка
с травмой должно быть отведено специальное по-
мещение. Обычно это может быть палата в отделе-
нии неотложной помощи достаточно больших раз-
меров, чтобы вместить травматологическую брига-
ду и необходимое оборудование, которое должно
постоянно там находиться.
Очень важно наличие а чекпатпого освещения
в реанимационных палатах, которые должны рас-
полагаться рядом с операционной или иметь свой
операционный зал, где может быть при необходи-
мости произведено экстренное хурургическое вме-
шательство. Оснащение этих палат должно вклю-
чать находящиеся в постоянной готовности для
использования стерильные широкопросветные
внутривенные (вн/в) катетеры, укладки для вено-
секции и торакотомии, трубки для торакоцентеза
с дренирующими устройствами, а также средства
для тщательного контроля температуры как боль-
ного, гак и окружающей среды, инфузаторы (боль-
шого объема, подогретые, позволяющие осуществ-
лять быструю инфузию», упаковки с консервирован-
ной кровью и особенно с эритроцитарной массой
гр\ппы 0(1) Rh~.
Кроме того, необходимо иметь мониторы для
определения сатурации и СО2 конца выдоха, поми-
мо многоканальных физиологических мониторов
и автоматических аппаратов для постоянного из-
мерения артериального давления, а также оборудо-
вание для дефибрилляции сердца. В полной готов-
ности, «пол рукой» должно быть все, что может
понадобиться для эндотрахеальной интубации,
крикотирготсмии, трахеостомии и т. д. Наиболее
полный перечень необходимого оборудования
опубликован Комитетом по Травме Американской
Корпорации Хирургов.14
НАЧАЛЬНАЯ ОЦЕНКА РЕБЕНКА С ТРАВМОЙ:
ПЕРВИЧНОЕ ОБСЛЕДОВАНИЕ
Первичная оценка состояния ребенка с травмой
проходит несколько ступеней, так же, как и у
взрослых пациентов, однако у детей есть ряд
специфических аспектов принципа ABCDE. На-
чальный осмотр преследует цель выявления и ле-
чения жизнеопаеных повреждений.
Оценка состояния дыхательных путей и шей
ного отдела позвоночника. При оценке состоя-
ния дыхательных путей необходимо прежде всего
убедиться в их проходимости и, кроме того, обеспе-
чить защиту шейного отдела позвоночнике! таким
образом, чтобы в случае его повреждения (неди
агностированный перелом позвоночника в этом от-
деле) не вызвать непреднамеренной травмы спин-
ного мозга.
Наиболее жизнеопасным повреждением дыхате-
льных путей, требующим экстренной диагностики,
является их обструкция. При этом абсолютно
необходимо знание особенностей анатомии. Над-
связочное пространство у маленьких детей чрез-
вычайно узкое, что обусловлено значительными
размерами языка и большим количеством тонзил-
лярной и аденоидной ткани. Гортань сама по себе
небольшая, «мягкая» и локализуется на шее вы-
соко и кпереди. Голосовые связки располагаются
в переднезаднекаудальном направлении. Благода-
ря выступающему затылку голова ребенка, ле-
жащего на спине, обычно слегка согнута. Все эти
факторы способствуют «открытию входа» в дыха-
тельные пути, даже маленькие по размерам, в то
время как излишнее сгибание или разгибание го-
ловы в области шеи обусловливает закупорку цы-
хательных путей.
О |ним из первых мероприятий у ребенка с трав-
мой должно быть очищение дыхательных путей от
крови, рвотных масс и иного содержимого. Глотку
ребенка санируют путем осторожной аспирации.
Как только дыхательные пути освобождены, начи-
нают обязательную подачу кислорода, независимо
от тяжести травмы.
Дыхательные пути «открывают» наклоном голо-
вы слегка вперед в позицию «нюханья», что по-
зволяет «вывести» гортань.
У ребенка, находящегося в бессознательном со-
стоянии, можно использовать оральный во здухо-
вод, который, однако, не следует применять, если
пациент в сознании, так как это может способство-
вать возникновению рвоты и аспирации желудоч-
ного содержимого. Воздуховод вводят вдоль «спин-
ки» языка.
У ребенка с сохраненным сознанием может быть
использован назофарингеальный воздухово i со-
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ 133
ответствующего размера, проведенный до глотки,
в чем необходимо удостовериться.
Если проходимость дыхательных путей возмож-
но поддержать указанными методами, это позволя-
ет далее достаточно достоверно оценить состояние
дыхания ребенка. В том же случае, когда эти мето-
ды нс эффективны, либо если по данным анамнеза
или обстсдования подозревается наличие повреж-
дения, требующего ИВЛ, необходимо провести эн-
дотрахеальную интубацию.
Трахея у маленьких детей короткая, длиной
5 см и растет так быстро, что к возрасту 1,5 лет
достигает длины 7,5 см. Трахея и главные бронхи
в детском возрасте — податливые и сдавливаемые
структуры. Мембранный отдел трахеи тонкостен-
ный и легко травмируемый. Как только ребенок
перестает расти в длину, трахея и бронхи приобре-
тают структурально и анатомически конфигура-
цию, свойственную взрослым людям.
В случае необходимости проведения ИВЛ очень
важно, чтобы эндотрахеальная трубка была соот-
ветствующего размера. Эндотрахеальные трубки
с манжетками у детей не используются в связи
с гем, что податливые дыхательные пути могут
повреждаться даже при низком давлении в ман-
жетке. В какой-то степени роль этой манжетки
играет перстневидное кольцо — наиболее узкая
часть дыхательных путей ребенка. Эндотрахеаль-
ная трубка, диаметр которой должен приблизи-
тельно соответствовать толщине мизинца ребенка,
должна свободно проходить через голосовые связ-
ки. В противоположном случае, при введении ее
с усилием, голосовые связки ребенка могут быть
очень легко повреждены. При интубации и ИВЛ
почти, как правило, возникает «утечка» воздуха,
которую более желательно компенсировать увели-
чением потока, а ис путем использования более
широкой, плотно вводимой трубки. Эндотрахеаль-
ную трубку не следует заводить в трахею слишком
глубоко, поскольку при этом может быть за инту-
бирован главный бронх. Как только трубка прове-
дена за голосовые связки и укреплена, следует
обязательно прослушать аускультативно дыхание,
особенно в подмышечных областях (не говоря уже
о визуальном осмотре грудной клеткн), дабы удо-
стовериться в правильном стоянии трубки и соот-
ветственно в адекватной вентиляции легких. Для
подтверждения положения трубки производится
рентгенограмма грудной клетки.
Контроль за состоянием шейного отдела по
звоночника. Позвоночник ребенка, как и другие
отделы скелета, имеет не столь плотную структу-
ру, как у взрослых людей, и более гибок. Позвонки
у детей клиновидно расширяются кпереди, межпоз-
воночные соединения плоские, а связочный аппа-
рат очень податлив. Переднею! и невидная конфи-
гурация способствует возникновению ложного под-
вывиха шейных позвонков, который встречается
только и исключительно в детском возрасте (рис.
11-6, 11-7).
При манипуляциях на дыхательных путях ре-
бенка следует иметь в виду возможность поврежде-
ния шейного отдела спинного мозга, которое мо-
Рис. П-6. Ьокопая рентгенограмма шейного отдела позпоноч
ника 14-месячного ребенка. Ложный нодвыних С-2,3. Обращает
на себя внимание легкое сгибание головы (ребенок лежит на
спине).
жет быть вызвано интенсивным сгибанием или
разгибанием головы. Поэтому, если предполагает-
ся наличие травмы шейного отдела позвоночника,
то во время манипуляций на дыхательных путях
должна осуществляться его мануальная иммоби-
лизация а выпрямленном («в линию») положении.
Для этого существуют различные приспособления,
но они не всегда могут обеспечить полную иммо-
билизацию.
Дыхание. Разнообразные виды травмы грудной
клетки могут привести к следующим фатальным
поражениям легких:
* напряженный пневмоторакс
♦ открытый пневмоторакс
* массивный гемоторакс
• тампонада сердца
* «болтающаяся» грудная клетка (потеря кар-
касных свойств грудной клетки вследствие
перелома грудины и/или ребер)
* массивный упгиб легких.
Оценить состояние дыхания у ребенка с травмой
бывает проще, чем у взрослых, благодаря меныпей
толщине грудной стенки у детей. Обычный осмотр
уже дает ценную информацию о характере рас-
правления легких. Аускультацию грудной клетки
лучше проводить в подмышечных областях, по-
скольку они анатомически наиболее удалены от
магистральных дыхательных путей. Очень важно
134 ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ
Рис. П-7. Тот же ребенок (см. рис. 11-6). Рентгенограмма по-
вторена в положении «нюханья» (с вытянутой головой). Лож-
ный подвывих исчез, шейный отдел выглядит нормально.
применение мониторов, позволяющих точно опре-
делить кислородную сатурацию и СО2 конца выдо-
ха. Эти мониторы должны быть подключены как
можно раньше, при первичном осмотре.
Средостение ребенка очень мобильно, и даже не-
большие изменения внутриплеврального давления
приводят к его смещению в ту или другую сторо-
ну. При значительном смещении возникает задер-
жка венозного притока к сердцу. Таким образом,
даже простой пневмоторакс, если он просмотрен,
потенциально может стать гибельным для ребенка.
Пневмоторакс или гемоторакс требуют дрениро-
вания плевральной полости. Напряженный пнев-
моторакс, являющийся жизнеугрожающим состоя-
нием, должен быть немедленно переведен в откры-
тый, что лучше всего достигается декомпрессией
плевральной полости с помощью иглы (с надетым
на нее катетером), вводимой во втором межреберье
но среднеключичной линии. Дренажная же трубка
может быть поставлена несколько позже (но, разу-
меется, чем раньше, тем лучше), в более подхо-
дящих условиях. Открытый пневмоторакс (при
проникающей травме) требует постановки трубки,
после чего на рану накладывают повязку.
При «болтающейся» грудной клетке терапия
у детей, как и у взрослых, должна быть направле-
на на лечение ушиба легкого. Если в результате
массивного ушиба нарушено дыхание, необходима
эндотрахеальная интубация. При этом следует по-
мнить, что небольшая но диаметру трубка может
обтурироваться кровью, если не обеспечено адек-
ватное увлажнение кислорода. При «болтающем-
ся» сегменте самостоятельное дыхание иногда за-
труднено из-за сильных болей. В таком случае по-
казана межреберная блокада. Тампонада сердца
рассматривается в следующем разделе.
Кровообращение. Оценка циркуляторного ста-
туса требует знания физиологии сердечно-сосуди-
стой системы, что способствует своевременной диа-
гностике скрытого кровотечения, которое может
привести к развитию гиповолемического шока.
Объем крови ребенка варьирует в зависимости
от возраста. У новорожденного он составляет
90 мл/кг, уменьшаясь до 80 мл/кг к году жизни
и достигая показателей взрослого человека
(70 мл/кг) в раннем юношеском возрасте.
Реакция сердечно-сосудистой системы на гипо-
волемию у большинства людей возникает по од-
ним и тем же законам, независимо от возраста.
Разница отмечается лишь между реакцией у очень
маленьких детей и взрослых пациентов средних
лет, причем состоит она не столько в медиаторах,
вступающих в действие при шоке, сколько в сосу-
дах, обеспечивающих поддержание объема крови.
Наиболее простой и клинически легко измеряе-
мый показатель реакции сосудистой системы на
потерю 15 -25% объема крови.— тахикардия, со-
провождающаяся прогрессивным снижением сер-
дечного выброса и увеличением периферического
сосудистого сопротивления (ПСС). Молодой орга-
низм способен поддерживать относительно ста-
бильное давление при нарастающей гиповолемии
благодаря увеличению ПСС в результате адренер-
гического сокращения артерий среднего и малого
калибра в ответ на гиповолемию. С возрастом раз-
вивается ишемическая болезнь сердца и атероскле-
роз периферических сосудов, утрачивающих воз-
можность сокращаться при потере объема крови.
Поэтому у взрослых часто отмечается лишь незна-
чительное повышение систолического давления,
в то время как дети поддерживают нормальное
давление до тех пор, пока потеря объема крови не
превысит возможности периферических сосудов
сокращаться. Обычно это происходит при потере
40% объема крови, когда констриктивная способ-
ность сосудов тотально падает и давление быстро
снижается.
«Органы первой важности» при гиповолемиче-
ском шоке — это сердце, мозг, почки и кожа. Каж-
дый из них может быть использован для выявле-
ния изменений объема циркулирующей крови
(табл. 11-3).
Оценка циркуляторного статуса при травме
включает в себя определение характера пульса на
центральных и периферических сосудах, частоты
сердечных сокращений, капиллярного наполнения,
цвета кожи и перфузии. Важно также отмечать
уровень сознания пациента. При тяжелом шоке
для измерения диуреза необходимо поставить мо-
чевой катетер.
Продолжающееся кровотечение должно быть
остановлено непосредственным прижатием крово-
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ 135
ТАБЛИЦА 11-3. Реакция на кровопотерю различных органон и систем у детей
Ранняя кровопотеря -<25% объема Пре1 ишиензивная 25% объема Гипотензивная >40% объема
Сердце Слабость, слабый пульс, увеличе- ние ЧСС Увеличение ЧСС Гипотензия, тахикардия, переходя- щая в брадикардию
ЦИС Сонливость, возбуждение, спутан- ное сознание, агрессивность Спутанное сознание, слабая реак- ция на боль Коматозное состояние
Кожа Холодная, липкая Цианоз, сниженное наполнение капилляров, холодные конеч- ности Бледная, холодная
Почки Сниженный диурез Повышение азота мочевины кропи Анурия
Жидкостная терапия 20 мл/кг 20 мл/кг (Х2) ЭрМ ПО мл/кг. XI. Х2) 20 мл/кг (Х2) ЭрМ (10 мл/кг) и срочная транс- портировка в операционную
точащего места. Этот простой способ предпочти-
тельнее слепого наложения зажимов в ране в на-
дежде на то, что в зажим попадет кровоточащий
сосуд. Особенно большие трудности возникают
при остановке внутрибрюшного кровотечения, свя-
занного с переломом таза. В таких случаях опреде-
ленную помощь может оказать применение специ-
альной пневматической противошоковой одежды
(1И1ШО).
Как только кровотечение остановлено, продол-
жают проведение мероприятий, направленных на
восстановление объема. Если же кровотечение
остановить не удается, показано оперативное вме-
шательство — единственный способ прекращения
кровопотери в подобной ситуации.
Тампонада сердца возникает в основном при
проникающей травме грудной клетки и проявля-
ется так же, как гиповолемический шок и напря-
женный пневмоторакс. Поскольку перикард при
Этом заполнен кровью, возможность наполнения
правой половины сердца ограничена, в результате
падает сердечный выброс. Яремные вены расширя-
ются, так как затруднен венозный возврат в пра-
вую половину сердца (преднагрузка). Расширение
яремных вен характерно и для напряженного пнев-
моторакса, при котором оно связано с повышением
внутриплеврального давления на стороне пораже-
ния. Сердечные тоны становятся приглушенными,
но триада Бека (сочетание повышенного ПВД, ас-
цита, а также рентгенологических и гемодинамиче-
ских признаков гипокинезии сердца) отмечается
редко. Лечение заключается в перикардиоцентезе
иглой с надетым на нее катетером. Игла оставля-
ется в перикардиальной полости на время транс-
портировки больного в операционную.
Лечение. Как только выявлена гиповолемия, не-
обходимо поставить в вены широкопросветные ка-
тетеры, определить группу крови, совместимость,
сделать соответствующие анализы. Сразу должна
быть начата быстрая инфузия кристаллоидов.
Обычно для этих целей используется раствор Рии-
гер-лактата.
Распределение вен для катетеризации в порядке
предпочтения следующее:
1. большая подкожная в области голеностопного
сустава
2. срединная подкожная в области локтевого су-
става
3. V. ccphalica в области верхней трети плеча
4. наружная яремная
5. внутрикостное введение (до 6 лет)
6. подключичная (с использованием большого
венозного проводи ика).
Исходная инфузия предполагает замещение 25%
циркулирующего объема. С этой целью первона-
чально быстро вводят кристаллоидный раствор в
количестве 20 мл/кг.5 Часто гемодинамический
статус ребенка сразу начинает нормализоваться.
Повторная оценка функции жизненно важных ор-
ганов и состояния периферической гемодинамики
позволяет говорить об эффективности инфузии.
Если после некоторой стабилизации вновь появля-
ются признаки ухудшения состояния, предприни-
мается повторное быстрое введение кристаллоидов
в объеме 20 мл/кг. Постоянная оценка эффектив-
ности проводимой терапии является основой, опре-
деляющей дальнейшую тактику. Если сохраняется
необходимость введения дополнительных объемов,
то теперь уже производится гемотрансфузия.
Цельная кровь не всегда бывает в наличии, кро-
ме того, в настоящее время она вытесняется компо-
нентными препаратами, которым отдается пред-
почтение. В отделении реанимации необходимо
постоянно иметь запас консервированной эритроци-
тарной массы (ЭрМ). Если нет в наличии типо-
специфической крови (соответствующей по группе
и резус-фактору крови больного), следует перели-
вать кровь 0(1) Rh-.15 Первоначальный объем ге-
мотрансфузии должен составлять 10 мл/кг. Очень
важно помнить о том, что если для переливания
используется кровь (а не ЭрМ) 0(1) Rh-, то ее
следует переливать в течение всего времени, пока
больному требуются трансфузии, ие переходя на
переливание типоспецифической крови (по груп-
пе и резусу больного). Существуют описания мас-
сивного гемолиза при трансфузии типоспецифи-
ческой кровн после использования цельной крови
0(1). Плазма в этой ситуации является носителем
антител, поэтому всегда предпочтительнее транс-
фузия ЭрМ.
Физиологическая реакция пациента на воспол-
нение объема — важный индикатор, определяю-
136 ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ
щий показания к оперативному вмешательству.
Если восполнение объема по вышеописанной схе-
ме не приводит к быстрой нормализации состояния
больного, то дальнейшие инфузии, как правило,
оказываются бесполезными до тех пор, пока не
остановлено кровотечение.
Оценки характера повреждения нервной сис-
темы. Реакция ребенка на повреждение ЦНС зна-
чительно оттичается от таковой у взрослых. Ран-
ние проявления неврологических расстройств
включают апноэ, рвоту и потерю сознания. Эти
симптомы отмечаются даже при нетяжелой трав-
ме и в детском возрасте возникают чаще, чем
у взрослых.
Поражения, вызванные первичной травмой, так-
же имеют у детей свои особенности, как количс-
ственные, так и качественные. В детском воз-
расте реже возникают суб- и эпидуральные гема-
томы, в то время как простое сотрясение мозга
очень часто и типично. Нередко развиваются суба-
рахноидальные кровоизлияния, проявляющиеся
обычно головной болью, ригидностью затылочных
мышц и небольшими подъемами температуры.
Повреждение ЦНС может быть симулировано
поражением других органов и систем." ' Напри-
мер, нарушение сознания иногда отмечается при
гиповолемии или гипоксии. Наиболее просто и до-
стоверно определить, есть ли поражение ЦНС,
можно с помощью восстановления нарушенных
функций в определенной последовательности со-
гласно принципу ABCDE.
Неврологическая оценка больного при оказании
первой помон,и должна быть сосредоточена на
двух основных показателях — уровне сознания
и состоянии зрачков. Шкала (тяжести) комы, раз-
работанная в Глазго (ШКГ). обычно не применя-
ется при оказании первой помощи. Уровень созна-
ния может быть оценен с использованием мнемо-
нической схемы AVPU:
А = Alert — оживленный и ориентированный
V = Verbal — реагирует на слова
Р = Painful — реагирует на боль
U = Unresponsjve — отсутствие реакции.
Состояние и реакция зрачков оцениваются путем
осмотра их при ярком освещении.
Лечение первичного поражения ЦНС начинается
лишь после оказания первоочередной помощи по
схеме ABCDE. Легкое повреждение головы может
значительно усугубиться, если его лечением зани-
маются до того, как произведена оценка состояния
дыхательных путей, спонтанной вентиляции, цир-
куляции и осуществлены необходимые мероприя-
тия по устранению выявленных нарушений.
Как уже говорилось, всегда важно у любого ре-
бенка с травмой предполагать возможность нали-
чия множественных повреждений.10 И хотя ЦНС
при травме страдает особенно часто, и именно ее
поражение является главной причиной смерти де-
тей, тем не менее при травме головы необходимо
сначала убедиться в том, что мозг хорошо перфу-
зируется достаточно оксигенированной кровью.
Поэтому раннее лечение первичной травмы голо-
вы заключается прежде всего в лечении поврежде-
ний других органов и систем, способных привести
к гипоксии и/или гиповолемии.
Общий осмотр бе итого и окружающая среда.
Полная оценка характера травмы не может быть
проведена адекватно, пока ребенок в одежде Всю
одежду следует удалить очень быстро, при первом
же осмотре. Важно при этом обратить 1нимание на
температуру в реанимационной палате. 1 йпотер-
мия часто вызывается ятрогенно, когда больного
раздевают в холодном помещении или переливают
растворы, имеющие температуру ниже температу-
ры тела ребенка. И хотя обсуждение проблемы ги-
потермии находится за пределами задач этой гла-
вы, необходимо все же подчеркнуть, что эффектив-
ная реанимация трудна, а порой лаже невозможна,
если ребенок находится в состоянии гипотермии
Поэтому использование теплых растворов для ин-
фузии и соотвстс гвующая температура в помеще-
нии, где проводится реанимация, — основа как для
адекватной первой помощи, так и для дальнейшего
лечения.
Рентгенологическое обследование при оказа
нии первой помощи. Три рентгенограммы имеют
наиболее важное значение, а потому должны быть
сделаны, если позволяет время, при оказании пер-
вой помощи. Это боковая рентгенограмма шейного
отдела позвоночника с подтягиванием рук вниз та-
ким образом, чтобы хорошо были видны все шей-
ные и первый грудной позвонки (см. рис. 11-6,
11-7); рентгенограмма грудной клетки, особенно
если больной интубирован или уже поставлена
дренажная трубка в плевральную полость; и рент
генограмма брюшной полости, на которой, кроме
всего прочего, следует обратить пристальное вни-
мание на кости таза.
Повторная оценка для определения эффек-
тивности проводимой терапии. Как только ока-
зана первая помощь, необходимо и, более того,
жизненно важно повторно оценить имеющиеся на-
рушения. При этом вновь соблюдается принцип
ABCDE, помогающий убедиться в том, что прово-
димая реанимация адекватно решает проблемы,
связанные с дыхательными путями, дыханием
и циркуляцией. Если нарушения, на ликвидацию
которых направлена первая помощь, сохраняются,
то переход ко второму этапу обследования больно-
го не разумен. Некоторые повреждения, "ыявлен-
ные при первичном осмотре, могут быть корриги-
рованы только в операционной, хирургическими
методами.
ВТОРИЧНОЕ ОБСЛЕДОВАНИЕ
Цель вторичного осмотра — определить сопутству-
ющие повреждения и другие нарушения и измене-
ния нетравматического происхождения, которые,
нс угрожая непосредственно в данный момент жиз-
ни больного, в дальнейшем, будучи пропущенны
ми, могут привести к осложнениям или даже смер-
ти. В большинстве случаев только 90% поврежде-
ний идентифицируются в течение первых 24 часов
после травмы.
Вторичное обследование включает в себя осмотр
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ 137
больного «с головы до пят», оценку рентген»! рамм
и данных других диагностических методов, а так-
же составление плана дальнейшего лечения.
Осматривать ребенка следует самым тщатель-
ным образом, начиная «с макушки» и продвигаясь
шаг за шагом вниз. При вторичном обследовании
врач обычно имеет больше времени, чем при пер-
вичном осмотре, для подробного выяснения меха-
низма травмы и характера повреждений.
Голова и лицо. При осмотре головы и лица сле-
дует обратить внимание на уровень сознания, на
наличие ран, ссадин, субапоневротических гема-
том, кровоизлияний позади ушной раковины в об-
ласти сосцевидного отростка (признак Бзтла, воз-
никающий при переломе основания черепа), на
выделение из носа или ушей крови или ликвора.
Необходимо также детально осмотреть глаза,
желательно при этом (разумеется, если позволяет
состояние больного), провести калорическую про-
бу — определение функции вестибулярного аппа-
рата путем раздражения наружного слухового про-
хода горячей или холодной водой, что вызывает
возбуждение вестибулярного аппарата, приводя-
щее к нистагму. Используется также прием «ку-
кольных глаз» (в горизонтальном положении боль-
ного его глаза закрыты, в вертикальном — откры-
ваются). Осмотр глаз завершается пальпацией,
повторной оценкой состояния зрачков и исследова-
нием функции черепно-мозговых нервов.
Травма челюстно-лицевой области достаточно
редко встречается в детском возрасте. Если эти
повреждения не связаны с обструкцией дыхатель-
ных путей, то лечение их должно проводиться
после того, как состояние больного полностью
стабилизировано и устранены жизнеопасные по-
вреждения.
Шея. Все пациенты с повреждениями, локализу-
ющимися выше уровня ключиц, должны рассмат-
риваться как больные с возможным поражением
шейного отдела позвоночника и спинного мозга до
тех пор, пока этот диагноз не исключен, а потому
очень важно с самого начала защитить шею от
дальнейшего травмирования.
Травма спинного мозга у детей может не иметь
рентгенологических проявлений, в связи с чем дан-
ные рентгенографии должны внимательно сопо-
ставляться с неврологическим статусом.17 Следует
помнить и о том, что физиологический подвывих
позвонков в детском возрасте часто неправильно
интерпретируется как повреждение шейного отде-
ла позвоночника. Поэтому нельзя в процессе диа-
гностики основываться только на данных обычной
боковой рентгенограммы шейного отдела, даже ес-
ли на ней видны все семь шейных позвонков.
О нормальном состоянии позвоночника можно
с уверенностью говорить лишь при отсутствии оча-
говой неврологической симптоматики и напряже-
ния шейных мышц в сочетании с нормальной кар-
тиной шейного отдела на боковой рентгенограмме.
Наиболее достоверная диагностика поражения
шейного отдела обеспечивается обычным осмотром
шеи в комбинации с неврологическим обследова-
нием и компьютерной томографией (КТ).
Грудная клетка. Исследование грудной клетки
проводится с целью подтверждения травмы, обна-
руженной при первичном осмотре, а также для вы-
явления других, более скрытых нарушений. Чтобы
оценить состояние спины, ребенка следует осто-
рожно перевернуть на живот («перекатить, как
бревно») и тщательно пропальпировать весь позво-
ночник, стараясь определить переломы, гематомы
и т. д.
Живот. Внугрибрюшное кровотечение, будучи
довольно значительным, может представлять боль-
шие трудности для диагностики. Кроме того, во
время падения дети обычно заглатывают большое
количество воздуха, что может привести к выра-
женному растяжению желудка, затрудняющему
в свою очередь дыхание. Подобная ситуация ино-
гда симулирует повреждение органов брюшной по-
лости.
Декомпрессия желудка является одним из перво-
очередных мероприятий и производится с по-
мощью назогастрального зонда. Однако при нали-
чии явных повреждений в области головы и шеи
лучше провести орогастральиое зондирование,
чтобы избежать такого редкого, но возможного
осложнения, как введение трубки в полость черепа
через перелом решетчатой кости. Осмотр, аускуль-
тация и пальпация живота позволяют диагностиро-
вать травму органов брюшной полости.
Промежность и прямая кишка. Диагностика
повреждений промежности и прямой кишки осуще-
ствляется путем обычного осмотра и ректального
исследования. При этом может быть выявлена
кровь в наружном отверстии мочеиспускательного
канала, что говорит о возможном разрыве уретры.
Кровь, визуально определяемая в мошонке или
больших половых губах, свидетельствует о внутри-
брюшном кровотечении или переломе таза. При
ректальном исследовании можно выявить высокое
расположение предстательной железы, что иногда
является одним из симптомов разрыва уретры.
Осмотр конечностей и выявление переломов.
Конечности должны быть тщательно осмотрены
с целью выявления ушибов, деформаций и измене-
ний длины. При осторожной пальпации в области
обнаруженной деформации можно определить кре-
питацию, подтверждающую наличие перелома. Не-
обходимо также оценить характер пульса. Типич-
ными для детей являются надломы и переломы,
вколоченные либо по типу зеленой ветки.18 В диа-
гностике переломов таза помогает прием, заключа-
ющийся в надавливании спереди назад на передне-
верхние подвздошные ости.
Неврологический статус. По анамнестическим
данным относительно характера происшествия
и поведения при этом пострадавшего ребенка мож-
но порой судить об уровне сознания пациента не-
посредственно после травмы (например, крик или
плач сразу после травмы, благополучный интер-
вал с последующей потерей сознания и т. д.).
Всестороннее неврологическое обследование
включает повторное определение уровня сознания
пациента и реакции зрачков, двигательных функ-
ций и чувствительности. Именно в это время обыч-
138 оценка и лечение травмы в остром периоде
но производится оценка по ШКГ. Стандартная
ШКГ должна быть модифицирована для примене-
ния ее у маленьких детей в возрасте до 4 лет
(табл. 114). ШКГ является, кроме того, достаточ-
но точным методом контроля за изменениями
уровня сознания пациента и неврологического ста-
туса.
ОКОНЧАТЕЛЬНАЯ ПОСТАНОВКА ДИАГНОЗА
И ВЫБОР МЕТОДА ЛЕЧЕНИЯ
Большинство диагностических алгоритмов, испо-
льзуемых при травме у детей, подразумевают дви-
жение от общих представлений о деятельности ор-
ганизма к знаниям специфических особенностей
органов и систем. После проведения реанимацион-
ных мероприятий и стабилизации состояния ребен-
ка все внимание должно быть направлено на вы-
явление повреждений отдельных органов. Напри-
мер, у ребенка с гиповолемическим шоком прежде
всего необходимо лечить шок. Вторая задача —
точно определить его причину, третья — ликвиди-
ровать изменения, к которым привело основное по-
вреждение, чтобы окончательно остановить про-
цесс.
Эти принципы можно проиллюстрировать на
примере разрыва селезенки с возникшим в резуль-
тате этого внутрибрюшным кровотечением и шо-
ком, Сначала все усилия в таком случае должны
быть направлены на лечение шока. Когда достиг-
ТАБЛИЦА 11-4. Шкала оценки тяжести комы (Глазго),
модификация для применения у детей
(ШКГ)
Глаза открываются Оценка
Спонтанно 4
В о гнет па речь 3
В ответ на боль 2
Пет реакции 1
Двигательная реакция
Спонтанная (выполняет словесные команды) 6
Локализует боль 5
Реакция отдергивания к отпет на боль 4
Резкие сгибание в отпет на боль
(поза декортикации) 3
Резкое разгибание п отпет на боль
(поза децеребрации) 2
Нет реакции 1
Вербальная реакция
Улыбается, ориентируется на звук, следит
за предметами, контактен 5
План
Успокаивается в ответ на
утешение
Периодически успокаивается
Безутешный
Нет реакции
ОБЩАЯ СУММА ПИК
Возможность контакта
Реакция
неадекватная 4
Стонет 3
Раздражительный,
беспокойный 2
Нет реакции I
3—15
нута достаточная стабилизация состояния, необхо-
димо проводить дальнейшую диагностику, чтобы
выявить повреждение внутренних органов. Наибо-
лее часто с этой целью производится КТ с контра-
стированием. Решение о показаниях к оперативно-
му вмешательству принимается в зависимости от
состояния гемодинамики и степени повреждения
селезенки. Если, однако, не удастся достичь ста-
билизации, то не следует откладывать операцию
в надежде на спонтанную остановку кровотечения.
В большинстве детских травматологических цен-
тров КТ активно используется для диагностики
повреждений органов брюшной полости. Практи-
чески любой КТ-аппарат дает сегодня столь каче-
ственное изображение, что степень разрыва по-
врежденных органов, таких, как селезенка или пе-
чень, определяется очень точно. Консервативное
лечение может проводиться, как правило, без осо-
бых опасений и преимущественно оказывается эф-
фективным. Операция показана лишь в тех случа-
ях, когда невозможно легко и быстро восстановить
нормальную гемодинамику. Соответственно, если
после введения крови в объеме 20 мл/кг, гемоди-
намика остается нестабильной, должно быть пред-
принято хирургическое вмешательство.
Если лечение шока дает лишь временное улуч-
шение, но состояние ребенка тем не менее упорно
продолжает оставаться тяжелым, либо в тех случа-
ях, когда нс установлен источник кровотечения,
полезным оказывается перитонеальный лаваж, ко-
торый не должен откладываться для того, чтобы
сделать КТ, ибо во время проведения КТ пациент
находится вне постоянного контроля травматоло-
гов и нс может, как правило, получить немедлен-
ную помощь. При наличии длительной или реци-
дивирующей гемодинамической нестабильности
оперативное вмешательство должно быть срочным.
Повреждение селезенки чаще всего может лечить-
ся неоперативным путем.” Консервативный метод
особенно показан в тех случаях, когда для стаби-
лизации состояния не потребовалось даже перели-
вание крови.
Опасности и преимущества, связанные с вы-
бором метода лечения. Консервативное лечение
повреждений внутренних органов, как правило, об-
ладает преимуществами перед стандартными хи-
рургическими методами. В частности, например, при
консервативном лечении травмы селезенки умень-
шается, по сравнению с хирургическим лечением,
риск, связанный с анестезиологическим пособием,
самим оперативным вмешательством и постспле-
нэктомичсским наслоением инфекции (ПСНИ). Но-
лес того, даже в случае безуспешности консерва-
тивного ведения, возможность развития различных
осложнений и последствий значительно ниже, чем
при оперативном вмешательстве. Поэтому, прини-
мая решение о выборе метода лечения, хирург дол-
жен тщательно взвесить опасности, которые могут
возникнуть в результате лапаротомии, гсмотранс-
фузии (гепатит А и В, СПИД) и ПСНИ,21 понимая
при этом, что риск при консервативном лечении по
меньшей мере не превышает риска, связанного
с хирургическим вмешательством.
ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ 139
Принятие решения о переводе ребенка в со-
ответствующее медицинское учреждение. Как
только завершено первичное и вторичное обследо-
вание, начаты соответствующие реанимационные
мероприятия и поставлен диагноз (иногда предпо-
ложительный), необходимо принять решение о
том, где ребенку может быть оказана дальнейшая
наиболее квалифицированная помощь — в данном
стационаре или в каком-либо ином. В большинстве
лечебных учреждений есть все условия для обеспе-
чения любой помощи при травме. Однако если
в стационаре, где ребенок находится, такие воз-
можности отсутствуют, пострадавший должен быть
переведен туда, где эту помощь могут оказать иаи-
лучшим образом.
ЗАКЛЮЧЕНИЕ
Организация системы травматологической помощи
как в данном регионе в целом, так и в отдельных
медицинских учреждениях, подразумевает обеспе-
чение возможности госпитализации ребенка с
травмой именно в тот стационар, где ему будет
оказана необходимая помощь на самом высоком
уровне соответственно характеру и степени по-
вреждения.22-24 Чрезвычайно расточительно для
специализированных Травматологических Педиат-
рических Центров 1 Уровня принимать большое
количество детей с легкой травмой. И наоборот,
госпитализировать тяжело травмированных детей
в учреждения, неспособные оказать необходимую
помощь, не только неразумно, но и вредно. Непра-
вильно также транспортировать ребенка с жизнеуг-
рожающей травмой на большие расстояния, когда
близрасположенное учреждение может оказать
в данном случае квалифицированную помощь.
Лучшее решение в любых подобных ситуациях по-
зволяет принять ярусная система травматологиче-
ской помощи.
Ярусная система включает в себя соответствую-
щую подготовку персонала, оказывающего помощь
ребенку на догоспитальном этане, связь до-
и внутригоспитальных звеньев, быструю и без-
опасную транспортировку ребенка с травмой в
медицинское учреждение.
Курс СЭПТ для врачей, сочетающийся с обуче-
нием методам оказания помощи на догоспитальном
этапе (в частности курс ДГЭПТ — догоспитальная
экстренная помощь при травме), позволяет наи-
лучшим образом обеспечивать помощь ребенку
с травмой в данном регионе. Этому способствует
единое понимание терминологии всеми специали-
стами, участвующими в лечении, и одинаковый
подход при том или ином повреждении. Пациенты
обследуются и получают необходимую помощь на
самом раннем этапе, непосредственно на месте
происшествия и транспортируются в соответствую-
щее учреждение, где может быть оказана наиболее
квалифицированная помощь.
Ярусная система травматологической помощи
обеспечивает последовательное и непрерывное
проведение необходимых мероприятий при жизне-
угрожающих повреждениях и дает наилучшис ре-
зультаты лечения любых видов травмы у детей.
ЛИТЕРАТУРА
1. Adams GW: Doctors in Blue. Collier Books. New York, 1961.
2. Blaisdell FW: Medical advances during the Civil War; Presi-
dential address. Arch Surg 123:1045—1050, 1988.
3. Heaton LD: Army medical service activities in Vietnam. Milil
Med 131:646. 1966.
4. Accidental death and disability: The neglected disease of mo-
dern society. National Academy of Sciences/National Research
Council, Washington. DC. 1976.
5. Ramenofsky MI , et al (Editors): Advanced Trauma Life Sup-
port Student Manual. American College of Surgeons, Committee
on Trauma. Chicago. 1989.
6. Pre Hospital Trauma Life Support, second edition. Educational
Direction. Akron. 1990.
7. Tcpas JJ, Ramen of sky ML, Barlow B. et al.: National Pediatric
Trauma Registry. J Pediatr Surg 24:156—158. 1989.
8. Tepas JJ, Mollitt, DI , Talbert JI., et al: Pediatric Trauma Score
as a predictor of injury severity in the injured child- J Pediatr
Surg 22:14—18. 1987.
9. Ramenofsky Ml., Ramenofsky MB. Jurkovich, GJ. ei al.: The
predictive validity of the Pediatric Trauma Score. J Trauma
28:1038 1042. 1988.
10. Tepas JJ. DiScala C. Ramenofsky ML. Barlow B: Mortality and
head injury: The pediatric perspective. J Pediatr Surg 25:92—
96, 1990
11. Gcnnarelli TA, Champion HR, Sacco WJ, et al.: Mortality of
patients with head injury and extracranial injury treated in
trauma centers. J Trauma 29:1193—1209, 1989.
12. Tepas JJ, Wears RL, DiScala C, et al.: Mortality experience in
13.162 injured children: The development of national outcome
norms fur childhood injuries. J Trauma. In press.
13. Ramenofsky, ML: How can we address the differences in trauma
versus illness systems? The 97th Ross Conference on Pediatric
Research, Ross laboratories. Columbus. OH. 1989.
14. American College of Surgeons: Committee on Trauma: Reso-
urces for optimal care of the injured patient. 1990.
15. Schwab CW, Shayne JP, Turner J: Immediate trauma resuscita-
tion with type О uncrossmatched blood: A two-year prospective
experience. J Trauma 26:897—902. 1986.
16. Bruce DA: Outcome following severe head injuries in children.
J Neurosurg 48:697, 1978.
17. Pang D. Wilbergcr JE: Spinal cord injury without radiographic
abnormality. J Ncurosurg 57:114—129. 1982
18. Rubin P: Dynamic Classification of Hone Dysplasias. Medical
Year Bonk Publishers. Chicago, 1964.
140 ОЦЕНКА И ЛЕЧЕНИЕ ТРАВМЫ В ОСТРОМ ПЕРИОДЕ
19. Pearl RH, Wesson DE, Spence 1Д. et al.: Splenic injury:
5-year update with improved results and changing criteria for
conservative management. J Pediatric Surg 24:121 —125, 1989.
20. Bunrain WI , Gould HP, MauII KI: Prediction of splenic salvage
by computed tomography. J Trauma 28:24- -34, 1988.
21. Luna GK, Dellinger EP: Honoperative observation therapy for
splenic injuries: A safe therapeutic option? Am J Surg 153:462—
468, 1987.
22. Boyd DR: Trauma — A controllable disease of the 1980's.
J Trauma 20:14—24. 1980.
23. Boyd DR: Emergency medical services systems development:
A national initiative. IEEE TRANS VEHICULAR TECH MOL.
VT 25:104—115, 1976.
24. Ramenofsky ML, Luterman A, Curreri PW, et al.: EMS for pe-
diatrics: Optimum treatment or unnecessary delay? J Pediatric
Surg 18:498 504, 1983.
АННОТАЦИИ К ЛИТЕРАТУРЕ
I. Tepas JJ. DiScala C, Ramenofsky ML. Barlow B: Mortality and
head injury: The pediatric perspective. J Pediatric Surg 25:92—
96. 1990.
С печью выяснения характера повреждения головы у детей
н влияния травм других органов на ЦНС. были проаналн
,шровапы данные На пиона эьного Регистрационного Центра
Детской Травмы о 10.098 детях. Для сравнения использова-
ны также сведения о 16.524 взрослых пациентах с травмой
головы. Результаты исследований показали, что прн одних
и тех же (по характеру и тяжести) повреждениях леталь-
ность в детском возрасте ниже, чем у взрослых. Наличие
сопутствующих внекраниальиых повреждений значительно
уменьшает шансы иа благополучный исход. Поражение
ЦНС как первичное, так и вторичное, является преобладаю-
щей и самой частой причиной смерти детей с травмой-
Глава 12
ТРАВМА ГРУДНОЙ КЛЕТКИ
Тяжесть повреждений. Повреждения у дегей
продолжают будоражить общество, заставляя при-
нимать активные меры по предупреждению и лече-
нию детской травмы, анализ 2086 случаев кото-
рой позволил выявить основные факторы, опреде-
ляющие результаты лечения торакальных повреж-
дений?
Главным и решающим аспектом реанимации при
травме у тетей является эффективная вентиляция?
Торакальная травма требует прежде всего особого
внимания к состоянию (проходимости) дыхатель-
ных путей и к механике дыхания.
Травма грудной клетки у детей, будучи редким
повреждением (104/2086 пациентов, 4,4%), обу-
словливает высокую летальность (26%). Основной
механизм, приводящий к неблагоприятным исхо-
дам, это очень резкое торможение во время дорож-
но-транспортных происшествий? Проникающее
ранение грудной клетки встречается менее часто
и вызывается такими предметами, как осколки зер-
кала, камни, огнестрельное и холодное оружие.
Все виды повреждений грудной клетки по меха-
низму травмы можно объединить в три главные
группы: автомобильно-пешеходная травма, автомо-
бильно-пассажирская и проникающие ранения.
Наиболее часто торакальные повреждения возни-
кают в тех случаях, когда ребенка сбивает машина
(37%), затем следует травма автомобильно-пасса-
жирская (ребенок попадает в аварию, будучи пас-
сажиром автомобиля — 31%). Средний возраст де-
тей с травмой грудной клетки 6,2 года, причем
47% из них — младше 4 лет?
Тяжесть травмы у детей с повреждениями груд-
ной клетки очень высока, поскольку в 82% случа-
ев имеется сочетанное множественное поражение
разных органов и систем. А кроме того, в 58%
случаев отмечается комбинация с повреждениями
головы. По нашим наблюдениям, у детей с тора-
кальной травмой повреждения обычно более серь-
езные, чем у пациентов, не имеющих поражения
органов грудной клетки. Разница становится осо
бенно очевидной, если учитывать ннзкий в детском
возрасте средний коэффициент травмы (КТр —
= 10,8 против 14,8 у взрослых) при высоком сред-
нем коэффициенте тяжести травмы (КГТр = 26,7
против 7,3), что говорит о большей степени у де-
тей по сравнению со взрослыми физиологических
расстройств и анатомических повреждений. Хотя
дети с торакальной травмой значительно чаще
других пациентов требуют госпитализации в отде-
ления интенсивной терапии (ОПТ) (71,2% против
19.1%), однако длительность их пребывания в
ОПТ и в стационаре в целом существенно не отли-
чается от этого показателя среди пациентов, не
имеющих повреждений органов грудной клетки.
В то же время летальность у детей примерно
в 20 раз выше при торакальной травме, чем при
других повреждениях (26% против 1,5%)?
Среди детей с торакальной травмой, полученной
в дорожно-транспортных происшествиях, средние
значения КТр меньше II, а средний КТТр — око-
ло 30, летальность же составляет 30%. Наиболее
тяжелые повреждения грудной клетки возникают
при жестоком обращении с детьми. При этом меха-
низме средний коэффициент травмы равняется 8,
в то время как летальность — 50%. Наименее тя-
желые повреждения грудной клетки с нулевой ле-
гальностью отмечаются при падениях. Если су-
дить но среднему коэффициенту тяжести травмы
(КТТр), то среди детей с торакальными поврежде-
ниями прогностическая вероятность выживаемости
составляет всего 0,701 (рис. 12-1)?'3 Данный пока-
затель, статистически достоверный, говорит о том,
что с возникновением у детей травмы органов
грудной клетки резко увеличивается общая тя-
жесть повреждения.
По нашим данным, летальность среди детей
с торакальной травмой достигает 26%. Смерть
обычно наступала в первые 3 дня после травмы,
в более поздние сроки летальные исходы были
редки. При множественных торакальных повреж-
дениях летальность возрастала до 50% (рис. 12-2),
в то время как при изолированной травме грудной
клетки она составляла 5,3%, при повреждении
двух областей тела — 28,6%, а при травме трех
и более областей — 32,6%. Комбинация поврежде-
142 ТРАВМА ГРУДНОЙ КЛЕТКИ
LETT
Дети с торакальной травмой (п = 104)
Рис. 12-1. Шкала тяжести травмы <ШТТ> — за-
висимость предполагаемого исхода от тяжести по-
вреждения у 104 детей с торакальной травмой.
Каждая точка может представлять более, чем
одного ребенка.
нии грудной клетки и головы давала повышение ле-
тальности до 35%, тогда как при сочетании тора-
кальных повреждений с травмой других органов
и систем летальность была 13,6%. Оперативное
лечение потребовалось лишь в 7% случаев тора-
кальной травмы, в основном при огнестрельных
ранениях.
Повреждения грудной клетки у детей отличают-
ся от аналогичной травмы у взрослых как по ха-
рактеру (рис. 12-3), так и по исходам. При срав-
нении больших групп пострадавших с торакальной
травмой отмечено, что у взрослых пациентов пере-
ломы ребер отмечаются в 75% случаев, в то время
как у детей, по нашим данным, — только в 32%.6
«Болтающаяся» грудная клетка встретилась у 10%
взрослых и менее, чем в 1% — у детей (по данным
Детского Национального Медицинского Центра
в Вашингтоне). Важно отметить, что в детском
возрасте повреждение легких и средостении может
возникать и при отсутствии переломов ребер, чему
способствует высокая эластичность костно-хряще-
вых структур грудной клетки у детей. Приблизи-
тельно 20% летальных исходов у взрослых отме-
чаются в поздние сроки, в то время как у детей
этот показатель (поздние смерти), по нашим дан-
ным, составляет менее 1 %. Однако общая смерт-
ность у детей почти в два раза выше, чем
у взрослых.
Анатомические особенности. Структура груд-
ной клетки ребенка существенно отличается от ее
строения у взрослого человека. Грудная клетка
в детском возрасте чрезвычайно податлива благо-
даря высокой эластичности костей и большому ко-
личеству хрящевой ткани. Переднезадние разме-
ры грудной полости ребенка меньше, по сравне-
нию со взрослыми. При слепой травме у детей
может возникать тяжелое поражение внутренних
органов без повреждения при этом скелетных
структур. Средостение, особенно у детей младшего
возраста, более подвижно, поэтому возникающий
иногда при травме грудной клетки напряженный
пневмоторакс вызывает значительное смещение
сердца, что приводит к перегибу крупных сосудов,
уменьшению системного венозного возврата к сер-
дцу и сердечного выброса, а это в свою очередь
снижает периферическую перфузию. Кроме того,
смещение средостения вызывает сдавление проти-
воположного легкого и перегиб трахеи, что еще
больше усугубляет тяжесть состояния ребенка.
Небольшие общие размеры организма ребенка
Количество торакальных повреждений
Рис. 12-2. Зависимость летальности от «количе-
ства» повреждений в грудной клетке.
ТРАВМА ГРУДНОЙ КЛЕТКИ 143
Рис. 12-Л. Виды торакальной травмы.
обусловливают недостаточность аутотерморегуля-
ции, а малый калибр сосудов затрудняет доступ
в вены. И хотя возможна чрескожная канюляция
вен, но быстрый доступ в экстренной ситуации
лучше осуществлять путем разреза кожи в области
голеностопного сустава или в паховой области.
Катетеризации центральных вен следует избегать
из-за опасности таких осложнений, как пневмото-
ракс и повреждение подключичной артерии. У ма-
леньких детей, при затруднении доступа к венам,
возможны внутрикостные инфузии.4
Одна из самых обычных и ранних реакций ре-
бенка на травму — аэрофагия и тахипноэ. Возни-
кающее в результате этого растяжение желудка
уменьшает экскурсии диафрагмы и затрудняет ды-
хание. Ситуация еще более усугубляется присоеди-
няющейся рефлекторной кишечной непроходи-
мостью. Для уменьшения растяжения желудка и
предотвращения аспирации необходимо введение
назогастрального зонда. Ограничивает экскурсии
диафрагмы и пневмонеритонеум, возникающий
в некоторых случаях в результате перфорации же-
лудка или тонкой кишки. В подобной ситуации,
при наличии резко выраженного напряженного
пнсвмопсритонсума, может не только понадобить-
ся, но и явиться жизнеспасающей пункция брюш-
ной полости и аспирация воздуха через иглу.4
ПОВРЕЖДЕНИЯ ГРУДНОЙ СТЕНКИ
К поверхностной травме грудной клетки относятся
ушибы и повреждения мягких тканей, реже возни-
кают переломы ребер, которые, по данным Детско-
го Национального Медицинского Центра, отмеча-
ются в 1,6% среди всех детей, поступивших в ста-
ционар со слепой травмой.7 В то же время среди
пациентов с повреждениями грудной клетки пере-
ломы ребер были в 32% случаев (рис. 12-4). Дети
с переломами ребер обычно находятся в более тя-
желом состоянии, чем те, у которых данный вид
повреждения отсутствует. Степень физиологиче-
ских расстройств, обширность анатомических по-
вреждений и летальность прогрессивно возрастают
параллельно увеличению количества сломанных
ребер. При этом локализация и уровень переломов
не играют существенной роли в отношении соче-
танного повреждения крупных сосудов или средо-
стения.
Переломы ребер встречаются более часто, чем
обычно принято считать.8 10 Около 70% данного
вида травмы возникают в дорожно-транспортных
происшествиях, в то время как у детей младше
3 лет 63% случаев переломов ребер являются
следствием жестокого обращения с детьми.
Переломы ребер проявляются локальной болью,
которая ведет к ограничению дыханий и респира-
торным расстройствам, связанным с ушибом легоч-
ной паренхимы (см- рис. 12-4). Легкие боли могут
быть сняты медикаментозной аналгезией, однако
при тяжелых сильных болях следует провести
межреберную блокаду маркаином (bupivacaine hyd-
rochloride). Переломы ребер иногда вызывают
пневмоторакс и кровотечение в результате повреж-
дения плевры или межреберных сосудов. Заживле-
ние сломанных ребер обычно происходит в течение
Рис. 12-4. 3-летний ребенок, попив ши и в автотравму (находит-
ся п машине, не пристегнутый ремнями). Видны перелом ребра,
ушиб и нарушение целостности легкого в правом заднебоковом
отделе грудной клетки. Также обращает на себя внимание
ателектаз и ушиб базилярных отделов левого легкого.
144 ТРАВМА ГРУДНОЙ КЛЕТКИ
6 недель. Перелом грудины у детей возникает
очень редко.
«Болтающаяся» грудная клетка. Множествен-
ные переломы соседних ребер, встречающиеся до-
вольно редко, приводят к образованию «болтающе-
гося» сегмента грудной клетки, что проявляется
парадоксальными дыха тельными движениями этой
части грудной стенки, затруднением дыхания и ги-
потензией. Видимые признаки ушиба грудной
стенки или экхимозы помогают в распознавании
переломов ребер, являющихся причиной возникно-
вения «болтающегося» сегмента. Парадоксальные
дыхательные движения этой части грудной клетки
обусловлены характерным для данной травмы от-
рицательным внутригрудным давлением на вдохе
и положительным — на выдохе. Недостаточная
вентиляция приводит к гипоксии. Возникающее
в этой ситуации смещение подвижного средостения
вызывает ухудшение системного венозного возвра-
та к сердцу и сдавление противоположного легко-
го. Ушиб легкого на стороне поражения ведет
к дальнейшему ухудшению газообмена. Лечение
заключается в эндстрахеальной интубации, венти-
ляционной поддержке и оксигенации.
УШИБ ЛЕГКОГО
Слепая травма грудной клетки может вызвать
ушиб легкого с паренхиматозным кровотечением
и огеком.11 Результатом этого вида повреждения
является гипоксия и увеличение внутрилегочного
шунтирования, что ведет к развитию дыхательной
недос гаточности. Поражение паренхимы обуслов-
ливает транссудацию жидкости и крови в альвео-
лы, что в свою очередь нарушает соотношение
вентиляции/перфузии и ухудшает оксигенацию
(рис. 12-5). Попытки в данной ситуации улуч-
шить вентиляцию путем увеличения инфляционно-
го давления догут привести к баротравме и в ко-
нечном счете — к легочному фиброзу.
Во избежание жидкостной перегрузки и дальней
шего ухудшения состояния поврежденного легкого
необходимо катетеризовать легочную артерию, что
позволяет осуществлять мониторинг легочно-ка-
пиллярного давления заклинивания. Хороший эф-
фект оказывает ьндотрахеальная интубация и
искусственная вентиляция с положительным давле-
нием конца выдоха. Закрепить успешность прове-
дения вентиляционной терапии, которая может
потребоваться в течение длительного периода вре-
мени, помогает нейромышечная блокада. При тя-
желом ушибе легкого иногда необходимо лечение,
направленное на поддержание осмолярности сыво-
ротки в пределах 290—300 моем. Характер анти
биотикотерапии, преследующей цель лечения ин-
фекции поврежденной паренхимы, определяется
флорой, высеваемой из легочного аспирата.
Наиболее объективное подтверждение травмы
легочной паренхимы обеспечивается компьютер-
ной томографией (рис. 12-5, 12-6). В частно-
сти, при КТ-исследовании становится очевидным
пневмоторакс, который может быть не диагно-
стирован по обычным обзорным рентгенограммам
(см. рис. 12-6С1.12, 13 Что касается клинических
симптомов, которые должны вызывать подозрение
на внутрилегочное поражение, то к ним относятся
Рис. 12-5. А, 2-летний ребенок, сбитый автомашиной. На рент-
генограмме при поступлении изменений нет, однако рО, было
50 мм Hg при подаче 100% О2. В, Компьютерная томограмма
выявляет двухсторонний ушиб ле1ких, ателектаз и раннее фор-
мирование кисты.
ТРАВМА FF
Рис. 12-6. А, 1,5-гндов«’-1ыЛ ребенок был на руках у матери, когда их сбила автомашина. На рентгено!
менений нет. В и С. Компьютерная томография показывает базилярный ателектаз с ушибом и ранение»'
ронний бази |ярный ателектаз с пневмотораксом.
прежде всего признаки гипоксии (Ро2<100 мм
Hg и F1O2=1) на фоне нормальной картины на
обычной рентгенограмме грудной клетки.
По данным Детского Национального Медицин-
ского Центра ушиб легкого — наиболее частое то-
ракальное повреждение в детском возрасте
(см. рис. 12-3).3 Летальность при ушибе одной до-
ли составляет 15%т при поражении нескольких до-
лей она возрастает до 43 %,
дыхательных путей в сочста
позволяет предупредить рази
вреждепном легочном сегмент
ляемого из трахеи способе
целенаправленной антибиот
ранних этапах лечения.
10 Заказ № 1622
146 ТРАВМА ГРУДНОЙ КЛЕТКИ
Рис. 12-7. 5-летняя девочка «вылетела* из автомашины во время аварии и была обнаружена по прибытии «скоро
правым передним колесом (придавлена в эпигастральной области). А-Е, Видны признаки травматической асфиксии
пневмоторакса, ушиба легкого и раны печени с гематомой.
ВНУТРИПЛЕВРАЛЬНЫЕ ПОВРЕЖДЕНИЯ
Пневмоторакс, гемоторакс и гемопневмоторакс
встречаются при травме грудной клетки с одинако-
вой частотой, однако при наличии крови в плев-
ральной полости отмечается наибольшая деталь-
ность (57,1%).’
Пневмоторакс. 1Ihciimo торакс в дет
сте иногда протекает бессимптомно, а
является тяжелым дистрессом. При
физикальном обследовании можно выя
вы грудной стенки, подкожную эмфиз
ленис или отсутствие дыхания на стор<
ния и гиперрезонанс при перкуссии. Йт
ГРАВМА ГРУДНОЙ КЛЕТКИ 147
F
Рис, 12-7 (продолжение). F, Сканпропанне печени и селезенки через 6 мес после травмы — полное излечение.
тиво определяется смещение трахеи в противопо-
ложную сторону. Из признаков дыхательной недо-
статочности отмечаются тахипноэ, бледность и циа-
ноз. Рентгенограмма грудной клетки выявляет воз-
дух в плевральной полости и коллабироваиное
легкое (рис. 12-7А). Торакоцентез и дренирование
сразу улучшают состояние ребенка (рис. 12-7В).
Травма грудной клетки может сопровождаться
травматической асфиксией (рис. 12-7С, D). Ино-
гда при этом повреждаются и прилежащие органы
брюшной полости.
При бессимптомном пневмотораксе, когда легкое
спадается менее, чем на 15% своего объема, пока-
зано наблюдение без дренирования, поскольку воз-
дух может спонтанно рассосаться. Если же име-
ются признаки гипоксии или респираторного ди-
стресса, а также в тех случаях, когда необходима
искусственная вентиляция, следует поставить дре-
наж в плевральную полость, выбрав трубку соот-
ветствующего диаметра (у старших детей French
трубка N20—24, у маленьких — N12).
Напряженный пневмоторакс (см. рис. I2-7A)
приводит не только к коллапсу легкого на стороне
поражения, но и к смешению средостения, а также
сдавлению противоположного легкого и опущению
диафрагмы на стороне поражения. Значительная
дислокация медиастинальных структур ведет к пе-
регибу полой вены, уменьшению системного веноз-
ного возврата к сердцу и сердечного выброса,
а также к потенциально летальному сердечно-со-
судистому коллапсу. В подобной ситуации необхо-
дима очень срочная пункция плевральной полости
и аспирация воздуха с незамедлительным введени-
ем дренажной трубки. Напряженный пневмоторакс
следует подозревать у любого ребенка с травмой
грудной клетки при наличии признаков респира-
торного дистресса и шока. Напряженный пневмо-
торакс иногда развивается не сразу, а несколько
позже, вслед за интубацией, поскольку при венти-
ляции у детей со скрытым повреждением легочной
паренхимы может развиться положительное дав-
ление.
Проникающая травма иногда приводит к такому
редкому поврежден ню, как открытый пневмоторакс
или «подсасывание» воздуха через рану грудной
стенки. При наличии сквозного отверстия в груд-
ной стенке воздух как входит в плевральную по-
лость, так и выходит наружу, в результате чего не
может быть создано отрицательное внутригрудное
давление, что ведет к серьезным нарушениям вен-
тиляции. В таком случае необходимо ушивание ра-
ны с целью восстановления герметичности грудной
клетки, постановка дренажной трубки через от-
дельный прокол в стороне о г раны и введение ан-
тибиотиков.
Гемоторакс. Повреждение крупных сосудов не
характерно для детского возраста, поскольку у де-
тей редко бывают проникающие ранения. Однако
гемоторакс может возникнуть и в результате пере-
лома ребра с повреждением межреберной артерии.
Массивная кровопотеря в грудную полость приво-
дит к выраженной гипотензии. При лечении гемо-
торакса очень важно до постановки тор<1костоми-
ческой трубки обеспечить доступ в вену, ибо бы-
страя эвакуация крови из плевральной полости
может усугубить гиповолемию и даже привести
к остановке сердца. Развитие у ребенка с травмой
грудной клетки гипотензии без каких-либо види-
мых признаков кровопотери должно вызывать по-
дозрение на гемоторакс, часто сочетающийся
с пневмотораксом.
Эвакуацию крови из плевральной полости луч-
ше всего осуществлять через торакостомическую
трубку, введенную по среднеаксиллярной линии.
Адекватное дренирование способствует расправле-
нию легкого и позволяет контролировать кровопо-
терю. Выделение крови через трубку со скоростью
1—2 мл/кг/час требует торакотомии для осуще-
148 ТРАВМА ГРУДНОЙ КЛЕТКИ
ствлсния непосредственного гемостаза. При нали-
чии «по ( рукой» реинфузионной системы возмож-
на аутотрансфузия аспирированной крови. При не-
адекватном дренировании оставшаяся в грудной
клетке кровь может привести в последующем
к фибротораксу с поражением легкого и развитию
сколиоза. Для профилактики этих осложнений
иногда требуется операция декортикации плевры,
осуществляемая с цетыо удаления из плевральной
полости организовавшейся крови.
ХИЛОТОРАКС
Проникнув из брюшной полости в грудную, лим-
фатический проток располагается справа от аорты,
пересекая затем среднюю линию слева от средней
трети пищевода 14 и вливаясь в венозную систему
в области слияния левой подключичной и внутрен-
ней яремной вен. Травматический хилоторакс воз
пикает как результат разрыва грудного протока
при псрсразгибании туловища. При проникающей
травме проток повреждается редко. Он может так-
же быть травмирован ятрогенно во время опера-
ции, когда осуществ |яется мобилизация пищевода
с целью ликвидации трахеопищеводного свища
или при кардиохирургическом вмешательстве
Разрыв гру (ного протока приводит к скоплению
лимфы в средостении или в плевральной поло-
сти.15 Диагноз, как правило, ставится поздно, по-
скольку для того, чтобы вызвать дыхательные рас-
стройства, лимфа должна накопиться в значитель-
ном количестве. Диагноз хилоторакса становится
очевидным, когда при аспирации из грудной клет-
ки выделяется бе пая мутная жидкость, Содержа-
щая жир.
Первоначальное лечение состоит в дренирова-
нии плеврадьной полости в сочетании с оральным
введением триглицеридов или тотальным паренте-
ральным питанием с целью уменьшения лимфото-
ка. Эмпиема при хилотораксс возникает редко, по-
скольку лимфа обладает бактериостатическими
свойствами. Если в течение 4- -6 недель консерва-
тивное лечение оказывается безуспешным, то по-
казана операция перевязки грудного протока. До-
ступ осуществляется с той стороны грудной клет-
ки, где отмечается подтекание лимфы. Обнаружить
поврежденный проток помогают такие приемы, как
назначение перед вмешательством жирной пищи,
введение синьки Эванса до операции в бедренную
кость или интраоперационно в пищеводное отвер-
стие диафрагмы, либо заполнение плевральной по-
лости физиологическим раствором. Иногда поиски
с применением указанных методов оказываются
безуспешными. В этом случае необходимо перевя-
зать проток сразу над диафрагмой со стороны пра-
вой половины грудной клетки.
Хроническая постоянная потеря лимфы приводит
к значительному уменьшению количества лим-
фоцитов и в результате — к иммунной недостаточ-
ности. В конечном счете развивается лимфоцито-
пения и истощение. На этом фоне ребенок стано-
вится объектом агрессивной грибковой инфекции,
чаще всего кандидозной.
ПОВРЕЖДЕНИЯ ТРАХЕИ И БРОНХОВ
В связи с низкой частотой проникающих ранений
у детей, повреждение трахеи и главных бронхов
встречается редко и возникает, как правило, '
при раздавливающей (краш) травме, когда на
грудную клетку ребенка падают какие-либо очень
тяжелые предметы. Разрыв трахеобронхиального
дерева следует подозревать в тех случаях, когда
через торакостомическую трубку, поставленную
в связи с пневмотораксом, отмечается постоянное
массивное выделение воздуха. Другие признаки
этого повреждения — медиастинальная или под-
кожная эмфизема, кровохарканье, напряженный
пневмоторакс и обширный ателектаз.”
Для постановки диагноза необходимо проведе-
ние бронхоскопии, причем методом выбора явля-
ется исследование ригидным бронхоскопом с ане-
стезией. Если же ребенок интубирован, то целесооб-
разно применение фиброоптического бронхоскопа.
Трахеобронхиальное повреждение выявляется при
осмотре трахеи и бронхов. Однако в тех случа-
ях, когда данный вид травмы очевиден по клиниче-
ским признакам и диагноз не вызывает сомнений,
может понадобиться немедленная торакотомия без
предварительной бронхоскопии. При поражении
верхних отделов трахеи производится ее ушивание
и трахеостомия. При низких трахеальных или
бронхиальных повреждениях лучшим доступом яв-
ляется срединная стернотомия. Обширное пораже-
ние бронха иногда требует резекции соответствую-
щей доли легкого. Поздним осложнением подобно-
го вмешательства может быть стеноз дыхательных
путей.18
ТРАВМАТИЧЕСКАЯ АСФИКСИЯ
Травматическая асфиксия возникает в результате
непосредственного сдавления грудной клетки или
верхних отделов живота,” что происходит в тех
случаях, когда на упавшего ребенка наступают но-
гами (давка в толпе) или он попадает под колеса
машины (см. рис. 12-7). В такой ситуации состоя-
ние надвигающегося ужаса обычно приводит к
рефлекторному закрытию голосовой щели, напря-
жению торакоабдоминальных мышц и глубокому
вдоху. Давление, оказываемое на грудную клетку,
передается в нижнюю и верхнюю полые вены, по-
скольку в легочных венах отсутствуют клапаны.
Лицо и шея становятся цианотичными, а на голове,
шее. грудной клетке и иногда на руках появляются
петехии (см. рис. 12-7С). Часто развивается пери-
орбитальный отек, а также геморрагии, субконъ-
юнктивалытые и в сетчатку (см. рис. 12-7D). Ре-
бенок нс ориентируется в пространстве, отмечается
тахипноэ, кровохарканье или дыхательная недо-
статочность. Диагноз обычно очевиден, поскольку
именно для травматической асфиксии характерно
несоответствие внешнего вида головы и шеи по
сравнению с нижней частью туловища: верхние
отделы выглядят полнокровными, в то время как
нижние — бледными. Данный вид травмы может
сочетаться с ушибом легкого, сердца, повреждени-
ТРАВМА ГРУДНОЙ КЛЕТКИ 149
см печени (см. рис. 12-7F). Травматическая ас-
фиксия обычно самостоятельно купируется и в те-
чение нескольких недель се признаки исчезают.20
ПОВРЕЖДЕНИЯ АОРТЫ
Разрыв аорты у детей встречается редко/' посколь-
ку ткани и структуры средостения у них чрезвы-
чайно податливы, что способствует ограничению
повреждения пределами ligamentum arleriosum. По-
вреждение аорты обычно возникает в автомобиль-
ных авариях или при падении на ребенка тяжелых
предметов. Клинические проявления заключаются
в гипертензии верхних отделов туловища и расши-
рении средостения на рентгенограмме грудной
клетки или КТ (рис. 12-8А). Аортография, кото-
рую необходимо произвести перед хирургическим
вмешательством, позволяет определить протяжен-
ность поражения. Операция заключается в непо-
средственном ушивании сосуда и предотвращении
таким образом разрыва возникающей при травме
псевдоаневризмы, неизбежно ведущего к смерти
(рис. 12-8В). В некоторых случаях при значитель-
ном диастазе между концами поврежденного сосу-
да требуется вшинанис трансплантата.21 Эта опе-
рация осуществляется в условиях экстракорпо-
рального кровообращения.
СЕРДЦЕ
Тампонада сердца возникает в результате скопле-
ния крови в перикардиальном пространстве при
повреждении миокарда. К тампонаде может также
привести проникновение воздуха в перикард при
баротравме. Уменьшению венозного возврата и со-
кращению сердечного выброса способствует недо-
статочная эластичность перикардиальной сумки.
У маленьких детей (иагноз тампонады сердца по-
ставить трудно.22 Признаками этого вила травмы
являются гипотензия, сохраняющаяся, несмотря на
адекватно проводимую после травмы инфузион-
ную терапию, расширение шейных вен, повышение
центрального венозного давления и сужение пери-
ферических кровеносных сосудов. Парадоксальный
пульс, характерный для тампонады сердца, у детей
определить трудно. Рентгенограмма грудной клет-
ки также обычно не дает никакой полезной инфор-
мации. Достоверно выявить жидкость в полости
перикарда и установить ее количество помогает
ультразвуковое исследование. При отсутствии воз-
можности использования данного метода показана
диагностическая пункция перикарда. Аспирация
крови нли воздуха приводит к быстрому улучше-
нию функции сердечно-сосудистой системы. К со-
жалению, классические проявления тампонады
с парадоксальным пульсом, расширением вен шеи,
приглушенными сердечными тонами и увеличени-
ем сердца на рентгенограмме в детском возрасте
редки. Более часто у ребенка возникает проникаю-
щая травма средостения, ведущая к шоку.
Ранение миокарда. Повреждение сердца ножом
или огнестрельное ранение требует оперативного
вмешательства и ушивания раны.23 Показанием
к срочной торакотомии является наличие у детей
Рис. I2-S. А, 9-лстний мальчик, катавшийся на велосипеде, был сбит грузовиком. На рентгенограмме при поступлении отмечается
широкое средостение. В. Произведена аортография, выявившая повреждение аорты н области ligamentum artcriosum. В связи с про-
должавшимся из селезенки кровотечением была произведена спленэктомия, а затем ушивание аорты с применением трансплантата
в виде вставки.
150 ТРАВМА ГРУДНОЙ КЛЕТКИ
с проникающими ранениями к области грудины
стойкой гипотензии или электромеханической дис-
социации. При «входе» в грудную клетку виден
напряженный перикард, имеющий голубоватую
окраску. При вскрытии его (продольным разрезом)
важно не повредить диафрагмальный нерв. После
эвакуации крови оценивают состояние сердца. На-
давливание пальцем обычно останавливает крово-
течение и позволяет стабилизировать циркуляцию.
Использование тампонов, закрепленных швами,
помогает предотвратить повреждение миокарда во
время ушивания раны, особенно в области тонко-
стенного предсердия. Летальность при этом редком
виде повреждения сердца и больших сосудов со-
ставляет 75 %.3
Ушиб миокарда. При слепой травме у дегей
ушиб миокарда возникает редко.24 Обычно он до-
статочно локализован и проходит спонтанно. На
электрокардиограмме (ЭКГ) при этом отмечается
изменение зубцов ST-T или признаки наруше-
ния проводимости. Наиболее чувствительный по-
казатель повреждения сердца — повышение актив-
ности креатинфосфокиназы (КФК), но следует
помнить, что бывают ложноположитсльные резуль-
таты данного метода исследования. Обширность
повреждения определяется с помошью эхокардио-
графии и радионуклидной ангиографии.25 Хотя
большинство ушибов проходят без последствий,
однако в некоторых случаях может развиться тя-
желая аритмия или сердечная недостаточность.
В связи с этим при подозрении на ушиб сердца
у всех детей должен проводиться длительный мо-
ниторинг сердечного ритма, неоднократное иссле-
дование в динамике ЭКГ и определение уровня
КФК-изоэнзимов.
Непосредственная прямая травма сердца может
вызвать разрыв миокарда, что обычно приводит
к смерти Разрыв сосочковых мышц сердечных
клапанов или межжелудочковой перегородки так-
же является летальным повреждением, если диа-
гноз не поставлен сразу и не проведено соответст-
вующее лечение. Данные виды травмы у детей
наиболее юстоверно диагностируются с помощью
эхокардиографии.
ДИАФРАГМА
Тяжелая тупая травма нижних отделов грудной
клетки или верхних — живота может привести
к повреждению диафрагмы, наиболее часто с левой
стороны.26 Это повреждение возникает чрезвычай-
но редко и, как правило, в дорожно-транспортных
происшествиях на высокоскоростных магистралях.
Очень мощное повышение внутрибрюшного давле-
ния приводит к разрыву диафрагмальной мышцы,
в результате чего органы брюшной полости пере-
мещаются в грудную клетку. Иногда при этом про-
исходит их ущемление или развиваются дыхатель-
ные расстройства. Изменение на вертикальной
рентгенограмме контуров диафрагмы или непра-
вильное местоположение назогастрального зонда
подтверждает диагноз (рис. 12-9). В некоторых
случаях нераспознанного повреждения диафрагмы
Рис. 12-4. 10 летний мальчик, сбитый Мишиной, поступил с та-
хипноэ и ослаблением дыхания слева. На рентгенограмме вид-
ны симптомы травматической диафрагмальной грыжи: отсутст-
вие контуров шафрЯ1мы и смещение желудка и кишечника
в левую половину грудной клетки.
респираторные расстройства или ущемление орга-
нов брюшной полости могут развиться значитель-
но позже и потребовать при этом срочной опера
ции. Данная травма редко приводит к смещению
в грудную полость селезенки, но если это прои-
зошло, то селезенка в свою очередь может быть
повреждена во время постановки торакостомиче-
ской трубки. При повреждении диафрагмы опера-
тивное вмешательство лучше производить из лапа-
ротомического доступа, что позволяет не пропус-
тить сочетанную травму органов брюшной полости.
При колотых и огнестрельных ранениях нижних
отделов грудной клетки (ниже сосковой линии)
может быть задета не только диафрагма, но и
полые органы брюшной полости.
ПОВРЕЖДЕНИЕ ГРУДНОЙ КЛЕТКИ
У НОВОРОЖДЕННЫХ
С широким внедрением в лечение респираторного
дистресса искусственной вентиляции легких стала
стремительно расти частота ятрогенной травмы
грудной клетки у недоношенных детей. Подобные
повреждения обычно вызываются высоким давле-
нием при ИВЛ, отсосными катетерами, неосторож-
но вводимыми через эндот рахеальную трубку не-
ТРАВМА ГРУДНОЙ КЛЕТКИ 151
посредственно в легочную паренхиму, или перфо-
рацией легкого при постановке в плевральную
полость торакостомической трубки.
Поскольку при проведении механической венти-
ляции легких, эффективного метода лечения дыха-
тельной недостаточности у маленьких детей, часто
требуется применение высокого инфляционного
давления и положительного давления конца выдо-
ха, возникновение напряженного пневмоторакса
в такой ситуации является достаточно закономер-
ным и отмечается в 25% всех случаев ИВЛ у ново-
рожденных. Развитие этого осложнения объясняет-
ся тем, что при высоком вентиляционном давлении
воздух проникает вдоль перибронхиального про-
странства и вызывает разрыв висцеральной плев-
ры.27 Ранняя своевременная диагностика пневмото-
ракса жизненно важна, поскольку у новорожденных
он практически всегда бывает напряженным. По-
становка торакостомической трубки у новорожден-
ных — не такая простая манипуляция, как многим
кажется. Она требует определенного опыта и учета
ряда важных деталей. Поэтому если диагностиро-
ван напряженный пневмоторакс, но у врачей, на-
ходящихся в данный момент возле ребенка, нет
соответствующих навыков, то лучше сделать гора-
коцентез обычным катетером N 22 для вн/в инъ-
екций с тем. чтобы стабилизировать состояние па-
циента. Постановка же дренажной трубки в плев-
ральную полость может быть затем осуществлена
более опытным человеком и в подходящих услови-
ях. Во избежание повреждения легкого, отмечаю-
щегося при этой манипуляции в 25% случаев,28
для проникновения в грудную клетку целесообраз-
но использовать изогнутый зажим. Применение
с этой целью троакара увеличивает вероятность
травмирования легкого, поэтому троакар не следу-
ет использовать. Как только трубка введена
в грудную полость, ее конец сразу должен быть
направлен вверх к куполу плевральной полости.
Еще одно возможное осложнение вентиляцион-
ной терапии — перфорация бронха отсосным кате-
тером, когда его вводят новорожденному в инту-
бационную трубку слишком глубоко.29 Ятрогенную
перфорацию бронха следует подозревать у малень-
кого ребенка, состояние которого ухудшается
вслед за отсасыванием из интубационной трубки,
либо если санируется кровянистая мокрота нлн,
наконец, в том случае, когда после санации отсос-
ным катетером возникает пневмоторакс и из вве-
денной в грудную клетку дренажной трубки посто-
янно продолжает выделяться воздух. Бронхоплев-
ральные свищи у новорожденных обычно дают
высокую летальность. Лечение заключается в то-
ракотомии и у шипа нии поврежденного легкого.
Показаниями к операции являются постоянное
массивное выделение воздуха, стойкий коллапс
легкого и прогрессирующая гипоксия, несмотря на
адекватное дренирование плевральной полости.
Предупредить перфорацию бронха отсосным кате-
тером возможно, если помнить схему, отражаю-
щую величины срокарииалыюго и на.зокариналь-
ного расстояния у детей с разной массой и разме-
рами тела.
Грубое введение назогастральной трубки у ново-
рожденных может привести к перфорации пищево-
да,16 которая обычно происходит в нижнем отделе
глотки, где волокна перстневидно-глоточной мыш-
цы располагаются крестообразно, образуя при вхо-
де в пищевод острый угол. Перфорация на данном
уровне может рентгенологически симулировать ат-
резию пищевода, поскольку назогастральная труб-
ка при этом останавливается в верхних отделах
шеи илн средостения. Лечение перфорации шейно-
го отдела пищевода может быть консервативным.
Пазогастральная трубка, естественно, удаляется
и обеспечивается введение антибиотиков широкого
спектра. Если пснстрация сразу не обнаружена
и диагноз поставлен поздно, то в таком случае
показано хирургическое дренирование шеи. Через
неделю проводится обычное контрастное исследо-
вание пищевода и при отсутствии изменений начи-
нают энтеральное питание. Перфорация внутри-
грудного отдела пищевода обычно приводит к
пневмотораксу, требующему обязательного соот-
ветствующего лечения во избежание развития ме-
диастинита и сепсиса.
ЛИТЕРАТУРА
1. Eichelberger MR, Goischall CS, Feely HB. ci al.: Parental atti-
tudes and knowledge of child safely — a National Survey. Am
J Dis Child 144:714 720, 1990.
2. Peclet MH, Newman KD, Eichelberger MR, ct al.: Patterns of
injury in children. J Pediatr Surg 25:85 91. 1990.
3. Pccict MH, Newman KD. Fichclbcrgcr MR. ct al.: Thoracic
trauma in children: an indicator of increased mortality. J Pediatr
Surg 25:961-966. 1990.
4. Young GM, Eichelberger MR: Initial resuscitation of the child
with multiple injuries. In Grossman M, Dickmann RA (Editors).
Pediatric Emergency Medicine: A Clinician’s Reference^ JB
Lippincott. Philadelphia, pp 230—236, 1940.
5. Eichelberger MR, Mangubat EH. Sacco WS, et al.; Outcome
analysis of blunt trauma in children. J Trauma 28:1109—1117,
1988.
6. Shorr RM, Grincndcn M. Indck M: Blunt thoracic trauma: ana-
lysis of 515 patients. Ann Surg 306:200—205, 1987.
7. Garcia VF, Goischall CS, Eichelberger MR, Bowman LM: Rib
fractures in children: a marker of severe trauma. J Trauma
30:695—700, 1990.
8. Smyth ВТ: Chest trauma in children. J Pediatr Surg 14:41—47,
1979.
9. Metier JL, Little AG. Shermeta DW: Thoracic trauma in child-
ren. Pediatrics 74:813—819, 1984.
10. Schweich P, Fleisher CS: Rib fractures in children. Pediatr Fmerg
Care 1:187—189. 1985.
H. Wagner RB, Crawford WO Jr, Schimpf PP: Classification of
parenchymal injuries of the lung. Radiology 167:77 82. 1988.
12. Sivil CJ, Taylor GA, Eichelberger MR: Chest injury in children
with blunt abdominal trauma: evaluation with CT. Radiology
171:815 818. 1989.
13. Wat! SD, Federle MP. Brett C.M: CT diagnosis of unsuspected
pneumothorax after blunt abdominal trauma. AJR 141:919—
921, 1983.
152 ТРАВМА ГРУДНОЙ КЛЕТКИ
14. Randolph JR, Gross R: Congenital chylothorax. Arch Surg
74:405. 1957.
15. Ramzy A, Rodriguez A, Cowley RA: Pitfalls in the management
of chylothorax. J Trauma 22:513—515, 1982.
16. Eichelberger MR, Randolph JG: Thoracic trauma in children.
Surg Clin North Am 6:1181 —1197, 1981.
17. Grover FJ, Ellested C, Arom KU: Diagnosis and management of
major tracheobronchial injuries. Ann Thorac Surg 28:384- 391,
1979.
18 Kaiser LR. Cooper JD: Tracheobronchial injuries, hi Turney
SZ, Rodriguez A, Cowley RA (Editors). Management of Curdi-
othuracic Trauma, Williams & Wilkens, Baltimore, 1990.
19. Haller JA, Donahoo JS: Traumatic asphyxia in children: patho-
physiology and management. J Trauma. 11:453—457. 1971.
20. Gorenstein 1, Blair GR. S handling B: The prognosis of trauma-
tic asphyxia in childhood. J Pediatr Surg 21:753—756. 1986.
21. Townsend RN, Colella JJ, Diamond DL: Traumatic rupture of
the aorta. J Trauma 30:1169—1174, 1990.
22. Galladay ES, Donahoo JS. Haller JA: Special problems of cardi-
ac injuries in infants and children. J Trauma 19:526—531,
1979.
23. Ordog GJ, Wasserberger J, Schatz 1, et al.: Gunshot wounds in
children under 10 years of age. A new epidemic. Am J Dis Child
142:618 622, 1988.
24. Tellelz DW, Harden WD, Takchaski M, et al.: Blunt cardiac
injury in children. J Pediatr Surg 22:1123—1128, 1987.
25. Langer JC. Winthrop AL, Wesson DE, et al.: Diagnosis and
incidence of cardiac injury in children with blunt thoracic trau-
ma. J Pediatr Surg 24:1091 — 1994, 1989.
26. Adeymi SD, Stephens CA: Traumatic diaphragmatic hernia in
children. Can J Surg 24:355—359, 1981.
27. Grosfeld JL, Lcmans JL, Ballantine TV, et al.: Emergency tho-
racotomy for acquired bronchopleural fistula in the premature
infant with respiratory distress. J Pediatr Surg 15:416, 1980.
28. Wilson AJ, Krous HF: Lung perforation during chest lube place-
ment in the stiff lung syndrome. J Pediatr Surg 9:213, 1974.
29« Anderson KD, Chandra R. Pneumothorax secondary to perfora-
tion of sequential bronchi by suction catheters. J Pediatr Surg
11:687, 1976.
Глава 13
ТРАВМА ЖИВОТА
И МОЧЕВЫХ ПУТЕЙ
На травму живота и мочевых путей как слепую,
так и проникающую, приходится 5% всех повреж-
дений у детей, поступающих в стационар по пово-
ду травмы. Повреждения органов брюшной поло-
сти и мочевой системы возникают в транспортных
авариях, при падениях, ударах в живот, жестоком
обращении с детьми, а в последние годы все более
частыми становятся проникающие ранения. Леталь-
ность среди детей с травмой живота составляет
14%. Это намного больше средней летальности
(2.4%) при любых других повреждениях в детском
возрасте.
При тупой гравме, на которую приходится 97%
всех повреждений у детей, тщательное исследова-
ние живота особенно важно, при этом следует
обращать внимание на его вздутие, наличие экхи-
мозов, ссадин или следов от привязных ремней —
каждый из этих симптомов может говорить о воз-
можном повреждении живота. Напряжение или ри-
гидность мышц брюшной стенки — также важный
признак абдоминальной травмы, хотя иногда он
может ввести в заблуждение, ибо отмечается и при
переломах нижних ребер, таза, ушибах брюшной
стенки или расширении желудка. Исследование
живота, включающее визуальный осмотр и паль-
пацию обоих флангов и спины, часто бывает за-
труднено, если ребенок плачет, кричит или на-
ходится в состоянии возбуждения. Физикальное
обследование при тупой абдоминальной травме до-
полняется стандартной рентгенографией грудной
клетки и таза. Кроме того, обязательно делается
анализ мочи (макро- и микрогсматурия).
Окончательный диагноз травмы живота ставится
с помощью контрастной компьютерной томогра-
фии (КТ), позволяющей достоверно оценить как
структуру, так и функцию большинства органов
брюшной полости. Поскольку многие повреждения
у детей могут лечиться консервативно, то при об-
следовании более важно определить нс столько
сам факт наличия гемоперитонеума, сколько вы-
явить источник кровотечения.
КТ — надежный метод диагностики внутри-
брюшных повреждений у детей, позволяющий
к тому же локализовать травму, определить ее тя-
жесть и обширность. 5 Из органов брюшной поло-
сти наиболее часто повреждается селезенка, четко
определяемая на КТ. Довольно нередко травмиру-
ются также печень и почки. Из всех внутренних
паренхиматозных органов наименее часто повреж-
дается поджелудочная железа, причем ее травму
трудно определить с помощью КТ.6 Диагностиро-
вать повреждение кишечника и поджелудочной
железы помогает контрастное исследование желу-
дочно-кишечного тракта, которое должно быть
включено в план обследования ребенка с абдоми-
нальной травмой.7
Выявление на КТ повреждения селезенки, пече-
ни и почек еще нс говорит о необходимости хи-
рургического вмешательства. Менее 20% детей
с диагностированной по данным КТ абдоминаль-
ной травмой требуют опера гииного лечения.2 4 Ге-
моперитонеум сам по себе также нс является пока-
занием к хирургическому вмешательству, хотя
понятно, что чем массивнее внутрибрюшное кро-
вотечение, тем чаще приходится прибегать к опе-
ративному лечению.2
При слепой травме живота у детей повреждение
кишечника возникает редко и вызывает порой диа-
гностические трудности- Однако и здесь сущест-
венную помощь оказывает КТ. Наличие пневмопе-
ритонеума иногда вводит в заблуждение. Следует
помнить о том, что источником свободного газа
в брюшной полости может быть не только травма
полого органа, но и такие причины, как проникно-
вение воздуха из грудной клетки при торакальной
травме или «остатки» его от проводившегося пери-
тонеального лаважа. Указанные источники пнев-
моперитонеума должны быть исключены при про-
ведении дифференциальной диагностики. О воз-
можном повреждении кишечника может также го-
ворить наличие жидкости в животе при отсутствии
данных за повреждение паренхиматозных орга-
нов.8 Внимательный анализ механизма травмы,
знание ее особенностей и тщательное наблюдение
за ребенком продолжают оставаться наиболее на-
дежными методами диагностики повреждений ки-
шечника при слепой травме живота.
Более половины всех детей со слепой травмой
154 ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ
живота имеют сочетанные повреждения головы,
груди и конечностей. Поэтому КТ-обследование
должно проводиться лишь после осуществления
первичных реанимационных мероприятий и стаби-
лизации состояния ребенка. Компьютерная томог-
рафия показана в следующих случаях:
— при подозрении по данным анамнеза и обсле-
дования на тяжелое повреждение органов брюш-
ной полости при обязательном условии стабильной
на данный момент гемодинамики;
— когда состояние больного требует проведения
массивных инфузий, но при этом источник крово-
потери остается неясным:
— при комбинированных повреждениях, особен-
но в сочетании с травмой головы.
Диагностический перитонеальный лаваж (ДПЛ),
являясь ценным методом для выявления гемопсри-
тонеума, не позволяет, однако, определить источ-
ник кровотечения. ДПЛ может быть использован
избирательно в некоторых случаях подозрения на
повреждение полых органов. ДПЛ также показан
при тяжелой травме черепа, когда невозможно ста-
билизировать состояние ребенка и требуется сроч-
ная трепанация черепа, которую, естественно, нель-
зя откладывать и задерживать, чтобы провести КТ
живота. Однако с введением в практику сверхбы-
стрых КТ-сканеров ДИЛ в подобных ситуациях
применяется намного реже.
Лечение. Консервативное лечение при поврежде-
нии паренхиматозных органов обычно проводится
в тех случаях, когда гемодинамика и систоличе-
ское АД стабилизированы, а потребность в транс-
фузии при этом не превышает 50% объема цирку-
лирующей крови. Лапаротомия, как правило, про-
изводится у детей, состояние которых не удается
стабилизировать, и при наличии более высокого
коэффициента тяжести травмы (КТТр) по сравне-
нию с теми больными, которые лечатся консерва-
тивно. В среднем лапаротомии требуют менее
10% детей с повреждением паренхиматозных орга-
нов и менее 15% — с гсмоперитонеумом. Опера-
тивное вмешательство необходимо при наличии
следующих показаний:
— острое ухудшение состояния во время прове-
дения или после завершения реанимационных ме-
роприятий;
— проникающие ранения огнестрельным или
холодным оружием;
— явные признаки перфорации желудочно-ки-
шечного тракта;
— невозможность стабилизировать гемодинами-
ку при очень массивной или продолжающейся кро-
вопотере;
— потребность в гемотрансфузии, превышаю-
щей половину объема циркулирующей крови дан-
ного ребенка (или более 40 мл/кг).
К несомненным признакам повреждения полого
органа, являющимся показанием к срочной опера-
ции, относятся пневмоперитонеум и выхождение
в свободную брюшную полость контрастного веще-
ства при рентгенологическом обследовании. При
выборе метода лечения для каждого ребенка дол-
жны быть четко оценены потенциальные возможно-
сти реакции на гемотрансфузию и инфицирования
при се проведении. Для достижения успеха при
консервативном лечении повреждений паренхима-
тозных органов необходимо самое тщательное
и непрерывное наблюдение за детьми в условиях
медицинского учреждения, имеющего соответству-
ющее оборудование и квалифицированный пер-
сонал
СЕЛЕЗЕНКА
При лечении на современном уровне повреждений
селезенки у детей необходимо учитывать три глав-
ных фактора. Во-первых, во многих случаях к то-
му времени, когда производится лапаротомия, кро-
вотечение из ран селезенки, как правило, уже пре-
кращается. Во-вторых, благодаря исследованиям
последних лет, иммунологическая значимость се-
лезенки стремительно возросла в нашем сознании.
И в- третьих, широкое распространение КТ сдела-
ло возможным точно локализовать повреждения
паренхиматозных органов брюшной полости, что
позволило в частности разработать классифика-
цию разрывов селезенки. Однако необходимость
в хирургическом вмешательстве определяется не
только установленной по данным КТ протяжен-
ностью разрыва. Решение вопроса о том. опериро-
вать или не оперировать ребенка с травмой селе-
зенки, зависит в большей степени от его гемодина-
мического статуса.
Если состояние ребенка с выявленным на КТ
повреждением селезенки стабильно, го больной по-
мещается в отделение интенсивной терапии и в те-
чение 5 7 дней находится на строгом постельном
режиме (рис 13-1). Показатели гемодинамики
и гематокрита исследуются тщательно и часто.
У ребенка со стабильной гемодинамикой вопрос
о том, при каком уровне гемоглобина необходимо
производить гемотрансфузию, решается строго ин-
Рис. 13-1. Компьютерная томограмма маленькой девочки со
слепой травмой живота, полученной в автомобильной аварии.
Ранение среднего отдела селезенки (стрелка). Хирургическое
пмешатетъетво не потребовалось. Спонтанное заживление.
ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ 155
дивидуально. Если гемоглобин стойко держится
в пределах 70—80 г/л. то от переливания крови
лучше воздержаться. Гемотрансфузия показана
в тех случаях, когда продолжающаяся кровопотеря
приводит к гипотензии или тахикардии. Если при
переливании крови в количестве, не превышаю-
щем 50% объема циркулирующей крови, достигну-
та стабилизация состояния, консервативное лече-
ние продолжают.
Показаниями к операции являются очевидные
признаки кровопотери, продолжающейся, несмотря
на адекватно проводимые оптимальные реанима-
ционные мероприятия, а также сочетанная травма
других органов брюшной полости, требующая хи-
рургического вмешательства. При отсутствии на
операции видимого кровотечения и сопутствующих
повреждений, которые делают нежелательным уд-
линение оперативного вмешательства, селезенку
следует сохранить, ушив ее разрывы. Существуют
различные методы остановки кровотечения из се-
лезенки. К ним относятся; наложение обычных
швов, применение местных гемостатических
средств, подшивание к месту разрыва сальника
или специальной рассасывающейся сетки и, нако-
нец, частичная резекция селезенки. Хотя некото-
рыми хирургами рекомендуется оставлять и имп-
лантировать кусочки селезеночной ткани, однако
вопрос о роли этих фрагментов в предотвращении
постспленэктомического сепсиса остается весьма
спорным.9
Наблюдение и обследование в динамике дечей,
перенесших травму селезенки, показывают, что за-
живление ее разрывов происходит не ранее, чем
через месяц после травмы. А потому при успешном
консервативном лечении ребенок должен быть
ограничен в физической активности в течение I —
3 месяцев, до тех пор, пока полное заживление
селезенки не будет подтверждено на КТ.
Многочисленными исследованиями доказано,
что после консервативного лечении травмы селе-
зенки функция ее совершенно нормальна. Уровень
IgM у детей с зажившими разрывами селезенки
близок к показателям в контрольной группе и зна-
чительно выше, чем у пациентов после спленэкто-
мии.10 Аналогичные данные получены и в экспери-
менте. При пневмококковом заражении крыс,
у животных с зажившими ранами селезенки отме-
чался более высокий бактериальный клиренс и ре-
акция антител, чем у тех, которые были подверг-
нуты спленэктомии.11
У детей, перенесших спленэктомию по поводу
травмы селезенки, летальность от сепсиса в 58 раз
выше, чем в общей популяции.7 Поэтому в тех
случаях, когда показана спленэктомия, необходимо
соблюдать ряд предосторожностей, помогающих
предотвратить развитие постспленэктомического
сепсиса. В частности, ребенок должен быть имму-
низирован поливалентной пневмококковой вакци-
ной. Кроме того, против половины микроорганиз-
мов, вызывающих эту форму сепсиса, вполне
эффективным оказывается профилактическое вве-
дение антибиотиков — пенициллина или ампицил-
лина.
Хирург обязан предупредить родителей о воз-
можности развития постспленэктомического сепси-
са и насторожить в этом плане педиатра или дру-
гого врача, постоянно наблюдающего данного па-
циента после выписки из стационара. При любом
заболевании с температурой выше 38,5° ребенок
должен быть обязательно осмотрен врачом, и лече-
ние (если нс ясен диагноз — симптоматическое)
следует начинать незамедлительно. Существуют
также специальные медицинские брастсты, кото-
рые рекомендуется носить таким детям, чтобы
сталкивающиеся с ними медики могли сразу ви-
деть, что данный ребенок перенес спленэктомию.
Родителям следует консультироваться со специа-
листами относительно мер профилактики пост-
спленэктомического сепсиса регулярно, не реже,
чем раз в 3 года, поскольку с течением времени,
ростом ребенка и развитием медицины рекоменда-
ции могут меняться.
ПЕЧЕНЬ
С появлением и внедрением в клиническую прак-
тику КТ стало ясно, что печень повреждается при
травме так же часто, как и селезенка, обусловли-
вая наибольшую летальность по сравнению со все-
ми другими абдоминальными повреждениями. До
40% детей с тяжелой травмой печени умирают до
поступления в стационар.12 Нестабильность гемо-
динамики при повреждении печени требует актив-
ной реанимации и срочного хирургического вме-
шательства. Высокая летальность отмечается так-
же у детей при тупой травме живота с повреждени-
ем печеночных вен или нижней полой вены.13
В некоторых случаях травму печени можно лечить
консервативно. Показания к использованию этого
метода следует определять сугубо индивидуально.
Избирательный отказ от хирургического вмеша-
тельства основывается на опыте, показывающем,
что у 45% детей, оперирующихся по поводу тупой
травмы живота с повреждением печени, требуется
только лишь дренирование, поскольку ко времени
хирургического вмешательства рана печени уже не
кровоточит.
Консервативное лечение подтвержденных на КТ
повреждений печени показано у детей со стабиль-
ной гемодинамикой. Терапевтические мероприятия
должны быть такими же, как и при травме селе-
зенки. Больной лечится в отделении интенсивной
терапии. На 7—10 дней назначают постельный ре-
жим. Проводится постоянный тщательный монито-
ринг показателей гемоглобина и гематокрита. При
наличии показаний осуществляется гемотрансфу-
зия в объеме до 50% ОЦК с целью поддержания
стабильности гемодинамики. По данным многочис-
ленных исследований разных авторов, от 40 до
90% детей с повреждениями печени излечиваются
без оперативного вмешательства.14-1’ При успешно
осуществляемой консервативной терапии ограни-
чение активности рекомендуется на период от 6 до
8 недель. Для подтверждения заживления раны пе-
чени производят повторную КТ.
Оперативное лечение показано при наличии
156 ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ
глубоких гемодинамических расстройств, явных
признаков продолжающейся, несмотря на оптималь-
но проводимую реанимацию, кровопотери, а также
при сочетанных повреж щниях, требующих лапа-
ротомии. Остановка кровотечения, являющаяся
целью вмешательства, может осуществляться раз-
личными способами Большинство поверхностных
ран требуют просто дренирования или прошивания
кровоточащих сосудов, определяемых в паренхиме.
Иноыа целесообразна сегментарная резекция пе-
чени. Однако обширная резекция при тупой трав-
ме сопровождается высокой летальностью, поэтому
к данному вмешательству следует прибегать лишь
в чрезвычайных или каких-то необычных обстоя-
тельствах, в частности в тех случаях, когда при
повреждениях печени задета печеночная вена.
У некоторых детей глубокая рана печени, про-
должающая кровоточить, может быть затампони-
рована. В таком случае тампон выводят через
брюшную стенку и удаляют путем ретапаротомии
через 24—48 часов после первого вмешательства.
Метод тампонады обычно применяется при тяже-
лых обширных повреждениях печени, а также для
остановки продолжающегося во время операции
кровотечения. Хирургические вмешательства при
повреждениях печени у детей часто сопровож-
даются охлаждением ребенка и осложняются ко-
агулопатией. Поэтому во время операции важно
поддерживать нормальную температуру тела и
адекватно восполнять кровопотерю переливанием
эритооиитарной массы и свежих препаратов —
корректоров свертывающей системы крови.
ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА И
12-ПЕРСТНАЯ КИШКА
Наиболее частой причиной повреждений поджелу-
дочной железы у детей является тупая травма жи-
вота, которая к тому же вызывает более 50% всех
случаев панкреатита.1* Благодаря глубокому рас-
положению в относительно защищенной области
поджелудочная железа и 12-перстная кишка по-
вреждаются реже, чем любые другие органы брюш-
ной полости и забрюшинного пространства, но
травма эта обычно приводит к очень тяжелым по-
следствиям. Поджелудочная железа при тупой
травме сдавливается преимущественно в той ее ча-
сти, где она «пересекает» позвоночник. Поврежде-
ния поджелудочной железы и 12-псрстной кишки
возникают, как правило, в дорожно транспортных
происшествиях, при падении на руль велосипеда
или при ударе кулаком в живот. У детей, пере-
несших подобную травму, а также при наличии
клинических признаков, характерных для повреж-
дения этих органов, должно быть проведено тща
тельное обследование на предмет травмы поджелу-
дочной железы.
Наиболее важный метод диагностики травмы
поджелудочной железы — опреде (ение амилазы
в сыворотке. Помощь в подтверждении диагноза
может оказать также анализ сыворотки на липазу
и соотношение амилаза — креатинин. Выявить отек
и разрыв паренхимы поджелудочной железы в ка-
кой-то степени помогает ультразвуковое исследо-
вание и КТ. Очень тяжело протекает у детей раз-
вивающийся в результате повреждения травмати-
ческий панкреатит.
Как только у ребенка установлен диагноз по-
вреждения поджелудочной железы, в большинстве
случаев начинают консервативное лечение, состоя-
щее из декомпрессии желудка через назогастраль-
ный зонд, инфузионной терапии и парентерально-
го питания. По мерс восстановления функции же-
лудочно-кишечного тракта и снижения уровня
амилазы в сыворотке переходят к энтеральному пи-
танию. Если держатся постоянные боли в животе
или отмечается подъем уровня амилазы в сыворот
ке, необходимо провести повторное ультразвуко-
вое обследование и КТ для того, чтобы исключить
возможное развитие флегмоны или .ожной кисты
поджелудочной железы.
Разрыв выводного протока поджелудочной желе-
зы редко возникает у детей. При его повреждении
дистальнее верхнебрыжеечных сосудов производят
операцию дистальной панкреатэктомии. Желате-
льно при этом сохранить селезенку, если только
позволяет интраоперационная ситуация. Таким же
образом лечатся и более проксимальные разрывы
протока, когда они выявлены в острой стадии,
и при условии, что остается достаточное количе-
ство жизнеспособной паренхимы поджелудочной
железы.
Псевдокисты поджелудочной железы могут раз-
виваться в результате травматического панкреати-
та или разрыва выводного протока (рис. 13-2).
Частота их формирования при тупой травме под-
желудочной железы колеблется, по данным разных
авторов, от 26 до 78%.18-22 Поч ги в 60% всех слу-
чаев травматических псевдокист отмечается спои-
Рис. 13-2. Компьютерная томограмма 10-летнего мальчика со
слепой травмой живота, полученной при игре в футбол. Боль-
шая псевдокиста поджечудочной железы в области малого саль-
ника (стрелка). В течение нескольких месяцев наблюдения не
было никакой положительной динамики, в связи с чем потребо-
валось внутреннее дренирование.
ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ 157
тайное выздоровление. Хирургическое лечение по-
казано лишь в тех ситуациях, когда спонтанное
выздоровление нс наступило в течение 4—6 не-
дель или если прогрессирующие клинические про-
явления не позволяют продолжать наблюдение.
Существует несколько методов хирургического
дренирования панкреатических кист: чрескожное
наружное, лапаротомия с наружным или внутрен-
ним дренированием.
Наибольшее распространение из перечисленных
вмешательств получило внутреннее дренирова-
ние — цистогастростомия или цистоеюностомия,
обеспечивающие хорошее опорожнение кисты и
низкую частоту рецидивов (менее, чем в 10% слу-
чаев).19 Чрескожное наружное дренирование может
быть целесообразным у детей с обструктивными
симптомами, продолжающимся перитонитом или
СТОЙКИМИ болями. В тех случаях, когда, несмотря
на проводимое лечение, состояние ребенка клини-
чески нс улучшается или отмечается рецидив псев-
докисты,19 необходимо провести исследование ана-
томического строения выводного протока поджелу-
дочной железы.
Тупая травма живо га может привести к возник-
новению гематомы стенки 12-перстнон кишки, что
проявляется расширением желудка, рвотой с
желчью и иногда появлением опухолевидного об-
разования в эпигастральной области. Диагностика
повреждения 12-перстной кишки очень трудна. Не-
оценимую помощь здесь может оказать КТ. Диа-
гноз подтверждается контрастным исследованием
верхних отделов желудочно-кишечного тракта, вы-
являющим «обрубленную» 12-нерстную кишку или
спиралевидную ее конфигурацию (рис. 13-3). Ле-
чение заключается в декомпрессии желудка с по-
мощью назогастрального зонда и в парентераль-
ном питании. Большинство дуоденальных гематом
рассасываются в течение 10 дней — 3 недель после
травмы. Необходимость в оперативном вмешатель-
стве возникает очень редко, в основном в тех слу-
Рис. 13-3. Контрастное исследование выянляет сужение
12-перстной кишки, вызванное интрамуральной гематомой
(стрелка).
чаях, когда консервативными мерами не удается
остановить кровотечение в просвет 12-перстной
кишки.
ПОВРЕЖДЕНИЕ ПОЛЫХ ОРГАНОВ
Из полых органов чаще всего у детей поврежда-
ются тонкая кишка и мочевой пузырь. Травма же-
лудка и толстой кишки встречается реже, но пред-
ставляет порой очень сложную проблему. Повреж-
дение кишечника может возникать при следующих
механизмах травмы: (1) раздавливание (между пе-
редней брюшной стенкой и позвоночником) —
краш-травма, (2) резкое торможение с разрывом
(отрывом) брыжейки или кишечной стенки по
брыжеечному краю, (3) разрыв перерастинутой ки-
шечной петли.7 Третий механизм травмы характе-
рен и для повреждений мочевого пузыря.
В остром периоде диагноз повреждения полого
органа установить порой сложно и своевремен-
ность диагностики зависит в значительной мере от
нацеленности клинициста на поиски данного вида
травмы. В клинической картине иногда отмечают-
ся симптомы перитонита, но чаще они появляются
лишь через несколько часов после травмы. При
разрывах брыжейки или других повреждениях
с деваскуляризацией кишечника перфорация мо-
жет развиться через 3—4 дня. Ценную помощь
в диагностике травмы полого органа иногда оказы-
вает КТ, при этом важно проводить исследова-
ние в динамике, даже если при поступлении ре-
бенка не обнаружено никаких данных за этот вид
повреждения.
Среди детей, которым осуществляется лапарото-
мия по поводу травмы, слепые повреждении желу-
дочно-кишечного тракта выявляются в 5—15%
случаев всех наблюдений.' Наиболее частая их ло-
кализация — проксимальный отдел тощей кишки
возле связки Трейца, затем следует дистальный
отдел подвздошной кишки. При травме у детей,
пристегнутых в автомобиле поясными ремнями,
может возникнуть довольно характерный для этого
вида повреждений «комплекс поясных ремней»,
при котором отмечаются ссадины брюшной стенки
и боковых флангов живота, перфорация кишки
и повреждение поясничного отдела позвоночника.
Приблизительно от 37 до 50% детей с абдоминаль-
ной травмой требуют хирургического вмешатель-
ства.2" 2*
Ежегодно в Соединенных Штатах 1,9 млн детей
становятся жертвами физического насилия, не свя-
занного с несчастными случаями?4 Наиболее часто
из внутренних органов у детей, подвергающихся
побоям, повреждаются кишечник, брыжейка и подже-
лудочная железа. Этот механизм травмы обусловли-
вает, как правило, значительную тяжесть поврежде-
ния и нередко ведет к неблагоприятному исходу.25
ПРОНИКАЮЩИЕ РАНЕНИЯ
При проникающем ранении (огнестрельном, ноже-
вом или при падении на острые предметы) может
быть поврежден любой орган брюшной полости
158 ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ
как паренхиматозный, так и полый. У детей реже
всего травмируются толстая и прямая кишка. Лече-
ние травмы прямой кишки, возникающей, как пра-
вило, при огнестрельных ранениях или в тех ситу-
ациях, когда ребенок «садится» на острый предмет,
осуществляется по гем же принципам, что и у
взрослых, и обычно состоит в наложении колосто-
мы и тщательном пресакральном дренировании,
которое проводится до полного заживления.
Проникающие ранения внутрибрюшной части
толстой кишки у детей бывают преимущественно
ножевыми или огнестрельными. Если данный вид
травмы не сочетается с другими повреждениями
и рана единичная, желательно ограничиться ее
ушиванием. При множественном поражении пред-
почтительно выведение толстой кишки (повреж-
денного ее участка). Хирургическая тактика обыч-
но одинакова, независимо от того, какой отдел
поврежден — правая или левая половина. При про-
никающих ранениях тонкой кишки производится
ушивание или резекция с анастомозом, если пер-
вичное ушивание по каким-либо причинам ка-
жется нецелесообразным.
Лечение проникающей травмы паренхиматозных
органов, часто выявляемой лишь во время лапаро-
томии, должно быть индивидуальным. Главная
цель его — остановить кровотечение. Наибольшие
сложности в решении вопроса о тактике возника-
ют в тех случаях, когда в результате ранения
в свободную брюшную полость поступает желчь
или панкреатический сок. В подобных ситуациях
особенно важно осуществить адекватное эффек-
тивное дренирование, желательно и предпочти-
тельнее — закрытое, поскольку этот метод способ-
ствует профилактике сепсиса и некроза кожи на
месте выхода дренажа — осложнений, довольно
характерных для открытого способа.
ТРАВМА ПОЧЕК
Повреждения почек у детей обычно возникают при
слепой травме, причем детские почки больше под-
вержены травмированию, поскольку костно-мы-
шечные структуры, их окружающие, ие так выра-
жены, как у взрослых, и соответственно в меныпей
степени выполняют защитную функцию. Опухоли,
аномалии положения и слияния, врожденные об-
струкции отмечаются в 20% случаев повреждений
почек у детей. Почки при травме поражаются бо-
лее часто, чем любой другой орган мочеполовой
системы.
Почки не очень прочно фиксированы в ретропе-
ритонеальном пространстве, а поэтому прямой
удар может как прижать почку к ребрам или по-
звоночнику, так и вызвать травму паренхимы. При
падении иногда возникает разрыв прилоханочного
отдела или повреждение почечной ножки. Одним
из наиболее редких видов травмы является тром-
боз почечной артерии при высоковольтной электро-
травме.
При осмотре ребенка с травмой почки никаких
внешних признаков повреждения обнаружить
обычно не удается, однако напряжение мышц, на-
личие опухолевидных образований и экхимозов
в боковых и верхних отделах живота, симптомы
шока должны вызывать подозрение. Главным при-
знаком повреждения почки, обнаруживаемым у
80—90% больных с ренальной травмой, является
гематурия, степень которой, однако, часто не отра-
жает тяжесть повреждения. Лишь нарастание гема-
турии в динамике обычно говорит о серьезной
травме. У 10—20% детей повреждение почки
протекает без гематурии. В работах некоторых
авторов этот показатель значительно ниже —
2-3%Л“
КТ живота — самый точный метод диагностики,
который позволяет не только выявить травму поч-
ки, но и определить ее степень. Следующее под-
разделение по тяжести повреждений, основанное
на данных КТ, принято в клинической практике.
Степень I — небольшое паренхиматозное повреж-
дение без признаков субкапсулярного или около-
почечного скопления жидкости, либо выявленная
аномалийная (но неповрежденная) почка; степень
II — частичное ранение почки или небольшое ко-
личество жидкости в субкансулярном или околопо-
чечном пространстве; степень III — выраженное
повреждение (разрыв) или значительное перире-
налыюе скопление жидкости; степень IV — «вдре-
безги разбитая» почка; степень V — повреждение
(любое) сосудов.2’
Цель лечения травмы почки — максимальное со-
хранение функционирующей паренхимы Около
85% повреждений ночек представлены ушибами
и ушибленными ранами, которые можно (и нужно)
лечить консервативно. При небольших поврежде-
ниях (I и II степень) назначается постельный ре-
жим до прекращения макрогематурии, после чего
только через 6 недель разрешается более или ме-
нее активный образ жизни. Всякие ограничения
полностью снимаются лишь тогда, когда исчезает
микрогематурия. Наблюдение должно проводиться
на протяжении 6—8 недель после травмы. По
меньшей мере в течение года необходимо периоди-
чески определять артериальное давление, брать
анализы мочи и проводить КТ или внутривенную
пиелографию (ВнВП). Тяжелые повреждения (сте-
пень IV и V), особенно при наличии гипотензии,
обычно требуют хирургического вмешательства.
При травме сосудов почки операция может быть
эффективной лишь в том случае, когда она про-
изводится в периоде «теплой ишемии», т. е. нс по-
зже, чем через 2 часа после травмы.
Споры относительно тактики при тяжелых по-
вреждениях почки (степень III и иногда IV) про-
должаются до настоящего времени. Некоторые
хирурги предлагают активный хирургический под-
ход — трансабдоминальный доступ, соответствую-
щее найденным изменениям вмешательство на со-
судистой ножке и по возможности максимальное
сохранение почечной ткани. Однако при такой
тактике нефрэктомия производится намного чаще,
чем при консервативном лечении. Показаниями
к операции при повреждениях почки должны яв-
ляться лишь следующие ситуации: продолжающая-
ся гематурия ипи кровотечение в околопочечное
ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ 159
пространство, массивное паренхиматозное пораже-
ние, инфицирование паранефралыюй клетчатки,
обструкция мочевых путей. Вмешательство по по-
воду кровотечения желательно отложить, если
только это возможно, на 3—4 дня. Порой за этот
период возникает четкое демаркационное отграни-
чение нежизнеспособной ткани. Кровотечение при
этом чаще всего останавливается, и операцию мож-
но произвести забрюшинным доступом. После пе-
ренесенной травмы почки все дети должны наблю-
даться в течение года, с регулярным измерением
артериального давления, взятием анализов мочи
и проведением лучевых методов обследования.
ПОВРЕЖДЕНИЕ МОЧЕТОЧНИКОВ
Мочеточники у детей повреждаются редко, обычно
при слепой травме и преимущественно в прило-
ханочном сегменте. При переломах таза может
произойти повреждение пузырно-мочеточникового
отдела. Следует быть очень настороженным в от-
ношении этого вида травмы, чтобы не пропус-
тить его.
Проникающее ранение иногда приводит к попе-
речному разрыву, ушибу мочеточника или даже
утрате его сегмента на протяжении (рис. 13-4). Во
Рис. 13-4. Внутривенная пиело! рафин Ю-летнего мальчика
с огнестрельным ранением нижних отделов живота и таза. Вы-
ход контрастного вс шест ил в области дистального отдела право-
го мочеточника и мочевого пузыря. Диагносгировано проникаю-
щее ранение дистального отдела мочеточника и моченого пузы-
ря, потребовавшее реимплантации мочеточники. Выздоронлсняс
без осложнений.
многих случаях целостность мочеточника может
быть восстановлена первично, если сохранилось
достаточное количество жизнеспособной ткани.
При повреждениях приложи ночного сегмента обыч-
но производится пиелопластика. Если мочеточник
травмирован на протяжении, то сопоставление его
концов иногда осуществляют за счет мобилизации
почки или лоханочного лоскута. Если этот вари-
ант по каким-либо причинам невозможен, то аль-
тернативой является уретерокаликостомия (нало-
жение анастомоза между мочеточником и нижней
почечной чашечкой).30
В большинстве случаев мочеточник при повреж-
дениях может быть восстановлен во время первич-
ной операции. Иногда для этой цели требуется
мобилизации почки и смещение ее вниз, что позво-
ляет наложить уретеральный анастомоз без натя-
жения. Повреждения дистальных отделов моче-
точника корригируются, как правило, путем уре-
тероцистонеостомии. Если собственной длины
мочеточника не хватает для сопоставления его кон-
цов. то может быть использован лоскут из по-
ясничной мышцы или мочевого пузыря.31 Из
других методов, применяющихся иногда для восста-
новления целостности поврежденного мочеточни-
ка, следует упомянуть трансуретероуретеросто-
мию. аутотрансплантацию или замещение моче-
точника сегментом подвздошной кишки.
ПОВРЕЖДЕНИЯ МОЧЕВОГО ПУЗЫРЯ
Повреждения мочевого пузыря обычно возникают
при наполненном пузыре в результате сдавления
нижних отделов туловища привязными ремнями во
время автомобильной аварии. Причиной этого ви-
да травмы может быть и проникающее ранение
промежности или живота. Клиническая симптома-
тика заключается в основном в гематурии, которая
обычно выявляется при введении в мочевой пузырь
катетера. Повреждение мочевого пузыря может
быть компонентом травмы, связанной с переломом
таза. В подобной ситуации необходима цистогра-
фия, однако следует быть очень осторожным при
введении катетера, поскольку при этом можно усу-
губить частичный разрыв уретры, превратив его
в полный. Экстраперитонеальный разрыв пузыря
успешно лечат консервативно с помощью дрениро-
вания, как в большинстве случаев при переломах
таза.32, 33 Если гравма пузыря внутриперитонеачь-
ная (рис. 13-5), то чаще всего показано хирурги-
ческое вмешательство — ушивание раны.34 Прони-
кающее ранение мочевого пузыря следует лечить
только хирургическим путем, так как при данном
механизме травмы очень высока вероятность по-
вреждения окружающих пузырь органов и тка-
ней.
ПОВРЕЖДЕНИЕ УРЕТРЫ
Повреждение мочеиспускательного канала у детей
наиболее часто происходит в области задней урет-
ры.37 Этот вид травмы в большинстве случаев со-
160 ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ
Рис. 13-5. Выход контрас i вещества (стрелка) на цисто-
граммс говорит о перфорации мочевого пузыря.
чстастся с тяжелыми переломами таза. Передняя
часть уретры обычно повреждается в тех ситуаци-
ях, когда при расставленных ногах бульбарная
часть уретры придавливается к лонной кости.38
Еще одной причиной повреждений уретры с после-
дующим развитием стриктуры может быть инстру-
ментальное обследование. В острой фазе диагноз
ставится с помощью ретроградной уретрографии.
Если подозрение на повреждение таза или уретры
возникает изначально, на основании анамнестиче-
ских данных о механизме травмы, ретроградная
урстрограмма должна быть сделана до введения
катетера в мочевой пузырь. Выход контрастного
вещества из просвета в окружающие ткани, несо-
мненно, доказывает наличие значительного по-
вреждения уретры (рис. 13-6). При ушибах урет-
ры на уретрограмме видны неровные контуры сли-
зистой. Повреждения уретры могут приводить
в последующем к развитию стриктуры.
В большинстве случаев при разрыве уретры
у детей необходимо наложить цистостому с после-
дующим отсроченным восстановлением целостно-
сти уретры. Мы придерживаемся именно этой так-
Рис. 13-6. Выход контрастного вещества (стрелка) из просвета
уретры при ее разрыве, с сочетанном переломом таза.
тики. При данном подходе частота развития таких
осложнений, как недержание мочи и импотенция,
значительно ниже, чем при иных тактических ре-
шениях.3’ Стриктуры на небольшом протяжении
могут быть устранены эндоскопически, но более
значительные стенозы иногда требуют открытого
хирургического вмешательства. При сужениях в
области задней уретры операция может осуществ-
ляться как промежностным, так и чрезлобковым
37. 40-42
доступом.
ЛИТЕРАТУРА
I Pcclei МН. Newman КО, Eichelberger MR, et al.: Patterns of
injury in children. J Pediatr Surg 25:85—91, 1990.
2. Taylor GA, Fallal ME, Potter BM, et al.: The role of computed
tomography in blunt abdominal trauma in children. J Trauma
28:1660—1664. 1988.
3. Haftel AJ, Lev R, Mahour GH. el al.: Abdominal. CT scanning
in pediatric blunt Irauma. Ann Emerg Med 17:684 689, 1988.
4. Kane NM, Cronan JJ, Dorfman GS, et al.: Pediatric abdominal
trauma: Evaluation by computed tomography. Pedi.atrics 82:11 —
15, 1988.
5. Brody AS, Seidel FG. Kuhn JP: CT evaluation of blunt abdomi-
nal irauma in children: Comparison of ultrafast and conventional
CT. AJR 153:803—806, 1989.
6. Jeffrey RB. Federle MP, Crass RA: Computed tomography of
pancreatic trauma. Radiology 147:491—494, 1983.
7. Schiff man MA: Non-operative management of blunt abdominal
irauma in pediatrics. Emerg Med Clin North Am 7:519—535.
1989.
8. Bulas DI, Taylor GA, Eichelberger MR: The value of CT in
detecling bowel perforation in children after blunt abdominal
trauma. AJR 153:561—564, 1989.
9. Moore GE, Stevens RE, Moore EF., et al.: Failure of splenic
implants to protect against fatal post-splenectomy infection.
JAMA 146:413—414, 1984.
10. Linne T, Frikson M, I annegren K, et al.. Splenic function after
nonsurgical management of splenic rupture. J Pediatr 105:263—
265, 1984.
11. Karp MP. Guralnick-Schcff S, Schiffman G, et al.: Immune con-
sequences of non-operative I realment of splenic irauma in the
rat model. J Pediatr Surg 24:112—117, 1989.
ТРАВМА ЖИВОТА И МОЧЕВЫХ ПУТЕЙ 161
12. Buntain Wl., Lynch FP, Ramcnofsky ML: Management of the
acutely injured child. Adv Trauma 2:43- 86. 1987.
13. Hollands MJ, Little JM: Hepatic venous injury after blunt abdo-
minal trauma. Surgery 107:149—152, 1990.
14. Karp MP, Cooney DR, Pros GA, et al.: Non-operativc manage-
ment of pediatric hepatic trauma. J Pediatr Surg 18:512—518,
1983.
15. Cywcs S. Rode H. Millar A: Blunt liver trauma in children: Non-
operative management. J Pediatr Surg 20:14—18, 1985.
16. Giacomanionio Mo Filler RM, Rich RH: Blunt hepatic trauma in
children: Experience with operative and non-operalive manage-
ment. J Pediatr Surg 19:519—522, 1984.
17. Oldham KT, Guice KS, Ryckman F, ct al.: Blunt liver injury in
childhood: Evolution of therapy and current perspective. Surge-
ry- 100:542—549. 1986.
18. Warner RL, Olhcrscn HB. Smith CD: traumatic pancreatitis
and pseudoeyst in children: Current management. J Trauma
29:597 601, 1989.
19. Rescorla FJ, Cory- D, Vane DW, ei al.: Failure of percutaneous
drainage in children with traumatic pancreatic pseudocysts.
J Pediatr Surg 25:1038—1042. 1990.
20. Bass J, DcLorcnzo M. Desjardins JG, et al.: Blunt pancreatic
injuries in children: 1'he role of percutaneous external drainage
in the treatment of pancreatic pscudocysts. J Pediatr Surg 33:
721—724. 1988.
21. Synn AY, Mulvihill SJ, Fonkalsrud EW: Surgical management of
pancreatitis in childhood. J Pediatr Surg 22:628—632, 19X7.
22. LcGay DA. Petrie DP. Alexander DI: Flexion-distraction injuri-
es of the lumbar spine and associated abdominal trauma. J Tra-
uma 30:436—444. 1990.
23. Reid AB. Letts RM, Black GB: Pediatric fractures: Association
with rntra-abdominal injuries and seat belt use. J Trauma
30:384 391, 1990.
24. Sfraus MA, Geller RJ, Steinmetz SK: Behind Closed Doors:
Violence in the American Family. Anchor, New York,
1980.
25. Sivit CJ, Taylor GA, Eichelberger MR: Visceral injury in batte-
red children: A changing perspective. Radiology 173:659—661,
1989.
26. Orsay CP Merloni G, Abc<iri<m H. ct al.: Colorectal trauma. Dis
Col Reel 32:188—190, 1989.
27. Shannon FL. Moore EE: Primary- repair of the colon; When is it
a safe alternative? Surgery 98:851—859. 1985.
28. Stalker HP, Kaufman RA. Stedje K: The significance of hematu-
ria in children after blunt abdominal trauma. AJR 154:569—
571, 1990.
29. Karp MP. Jewett Jr TC, Kuhn JP, et al.: The impact of compu-
ted tomography scanning on the child with renal trauma. J Pcdi-
dlr Surg 21:617—623, 1986.
30. Duckett JW. Pfister RR: Urctcrocalicostomy for renal salvage.
J Orel 128:98—101. 1982.
31. Ehrlich RM, Melman A, Skinner DG: The use of vesico-psoas
hitch in urologic surgery. J Urol 119:322*—325, 1978-
32. Richardson JR, I eadbetter GW: Non-operativc treatment of the
ruptured bladder J Urol 114:213—216, 1975.
33. Weigel JW: Bladder and urethral trauma. AUA Update Series
1:1—7. 1982.
34. Berger PE, Munschauer RW, Kuhn JP: Computed tomography
and ultrasound jf renal and perirenal diseases in infants and
children. Pediatr Radiol 9:91—99, 1980.
35. Brereton RJ, Philip N, Biiyukpamukcu N: Rupture of the urina-
ry bladder in children. The importance of the double lesion. Br
J Urol 52:15—20. 1980.
36. Livine PM, Gonzales ET: Genitourinary trauma in children.
Urol Clin North Am 12:53—65, 1985.
37. Glassbcrg KI: Urethral trauma. Dialog Pediatr Urol 3:4—5,
1980.
38. Kiracofe HI , Pfister RR, Peterson NE: Management of nonpe-
nctrating distal urethral trauma. J Urol 114:57—62. 1975.
39. Morehouse DD. MacKinnon KJ: Management of prostatomcm-
branous urethral disruption: 13-ycar experience. J Urol
123:174 174, 1980.
40. Brock WA, Kaplan GW: Use of the transpubic approach for
urethroplasty in children. J Urol 125:496—501, 1981.
41. Harshman MW, Cromie WJ, Wein AJ, et al.: Urethral stricture
disease in children. J Urol 126:650—654, 1981.
42. Kramer SA, Furlow WL, Barrett DM, et al.: Transpubic ure-
throplasty in children. J Urol 126:767—769, 1981.
11 Заказ № 1622
Глава 14
ТРАВМА ГОЛОВЫ
В детском возрасте частота травмы головы, требу-
ющей госпитализации, составляет 1 ; 4300 детей
в год, причем один из восьми пациентов с этим
видом повреждений погибает, что вполне объясня-
ет непреходящее внимание медиков к травме голо-
вы. Наиболее частой причиной являются падения.
Особенно тяжелую травму головы дети получают
обычно в автомобильных авариях,1 а к возрасте до
года — при жестоком обращении. На убийства
приходится 17% смертей в этой группе, в то время
как у взрослых данный показатель составляет все-
го тишь 1%. Нетьзя не отмстить одну опасную
тенденцию — если доля аварий как причины ле-
тальных исходов снижается, то частота смертей
в детском возрасте от насилия возросла за послед-
ние 4 года на 25%.
Клиническая картина. Наиболее частая причи-
на кровотечения при травме головы — поврежде-
ние скальпа. Очень опасны небольшие колотые ра-
ны, которые, с одной стороны, могут быть нс заме-
чены. а с другой — являются порой единственным
признаком проникающего ранения мозга. При
оценке характера повреждения волосистой части
головы необходимо всегда учитывать механизм
травмы, помня о том, что кажущаяся поверхност-
ной рана иногда проникает до кости. А потому
прежде, чем зашивать рану, нужно тщательно ее
ревизова ь.
Переломы черепа могут быть простыми или от-
крытыми. Кроме того, они делятся на линейные
и вдавленные. Несколько отдельно стоят переломы
основания черепа. Линейные переломы чаще всего
возникают у грудных и маленьких детей и редко
сочетаются с травмой мозга Если такой перелом
проходит через основание черепа, го могут отме
чаться экхимозы вокруг глаз (симптом енота) или
отсроченные кровоизлияния за ухом (признак Бат-
ла). Эти симптомы иногда появляются через не-
сколько часов и даже дней после травмы. Линей-
ные переломы черепа порой дают острые проявле-
ния в виде кровотечения или выделения спинно-
мозговой жидкости (СМЖ) из ушей или носа.
Характер шнейных переломов и их протяженность
очень важны, поскольку отражают интенсивность
воздействия повреждающего агента и возможность
наличия эпидурального кровоизлияния. Особенно
тяжелых проявлений следует ожидать при перело-
мах, проходящих через заднюю черепную ямку
или мозговые синусы.
При вдавленных переломах пальпация черепа
позволяет определить углубление («ямку»). Необ-
ходимо помнить, что припухлость и уплотнение
galea aponeurotica по краям участка поврежденного
скальпа может симулирова гь вдавленный перелом,
которого на самом деле нет. При открытых перело-
мах иногда через кожную рану видна мозговая
ткань или СМЖ. До ушивания любой раны
волосистой части головы необходимо тщательно
пропальпировать подлежащую кость, дабы убеди-
ться в том. что она интактна.
Повреждения самого мозга могут быть разнооб-
разными — от сотрясения или комы до локальных
повреждений, таких как ушиб и гематома. Важным
показателем сотрясения является длительность пост-
гравматической амнезии Этот параметр, однако,
сложно определять у грудных и маленьких детей,
у которых сотрясение мозга клинически может
проявляться в виде бледности, возбуждения и рво-
ты. Предпринимались попытки выделить различ-
ные степени сотрясения, но это имеет практиче-
ское значение в основном при лечении спортсме-
нов с легкой или средиетяжелой травмой. Для
детей с тяжелыми повреждениями подобные клас-
сификации не имеют особого смысла.
Эпидуральные гематомы не сопровождаются,
как правило, серьезной первичной травмой подле-
жащей ткани мозга. У трети пациентов отмечается
период полного благополучия, сменяющийся по-
явлением головной боли, рвоты, сонливости, рас
ширения зрачка (обычно на стороне гематомы) и
гемипареза. При отсутствии лечения может раз-
виться децеребрация, двустороннее расширение
зрачков, брадикардия, гипертензия и, наконец,
остановка дыхания и сердца. Одна треть детей
с эпидуральной гематомой не теряет сознания ни
в острой стадии, ни в последующем. Еще одна
ТРАВМА ГОЛОВЫ 163
треть пациентов, наоборот, находится в бессозна-
тельном состоянии с моменте! травмы — в таких
случаях поражение обычно не ограничивается
лишь эпидуральной гематомой.
Острая субдуральная гематома, как и внутри-
мозговая, обычно сочетается с диффузным повреж-
дением мозга н наиболее часто обнаруживается
у детей, находящихся в коматозном состоянии.
Операция нс всегда является методом выбора. По-
казания к хирургическому вмешательству опреде-
ляются размерами и локализацией гематомы.
И субдуральная и внутримозговая гематома может
быть причиной развития прогрессирующих невро-
логических расстройств. При тяжелом диффузном
поражении мозга дети, как правило, находятся
в состоянии комы (табл. 14-1).
Травма, полученная при жестоком обращении
с маленькими детьми, очень трудно диагностиру-
ется, ибо в таких случаях обычно нет анамнеза
либо уровень сознания ребенка не соответствует
механизму и тяжести повреждения. Дети в подоб-
ных ситуациях внезапно, «необъяснимо» (по сло-
вам нанесших травму) теряют сознание или отме-
чается столь же «непонятная» остановка дыхания.
Поскольку детишки в возрасте до года обычно
ограничены в подвижности и не могут «увернуть-
ся» от побоев и других видов насилия, тяжелая
травма головы в этом возрасте стремительно ведет
к смерти, особенно если нет свидетелей, которые
могут в какой-то степени уберечь и защитить ре-
бенка или оказать первую помощь. Поэтому любой
ребенок с нарушенным сознанием должен рассмат-
риваться при проведении дифференциальной диа-
гностики как возможная жертва насилия. К сожа-
лению, эта проблема существует в любых расовых
и социально-экономических слоях общества и по-
вреждения в результате жестокого обращения диа-
гностируются лишь в том случае, когда врач дума-
ет о возможности подобной травмы/
Повреждение спинного мозга нетрудно распо-
знать у ребенка, находящегося в сознании и
предъявляющего жалобы на потерю чувствитель-
ности. Произвольные движения при этом отсутст-
вуют. Понятно, чго в том случае, когда ребенок
без сознания, жалоб он, естественно, не предъяв-
ТАБЛИЦА 14-1. Шкала оценки тяжести комы (Глазго)
Оценка
Глаза Открывает Спонтанно 4
По команде 3
На боль 2
Нет реакции 1
Реакция на болевое Локализует боль 5
раздражение С гнбанис-отдергикишс 4
Сгибание аномальное 3
Разгибание 2
Пег реакции 1
Словесная реакция Ориентирован и отвечает Дезориентирован, но 5
отвечает 4
Ilccoo’i не гс гнукнцие слова 3
Непонятные звуки 2
Нет реакции 1
/*«<•. 14-1. Компьютерная томит рамма в первый лень была нор-
Mii.-ihiion. А. Я терныи магнитный резонанс головы через 3 дня
после травмы средней тяжести. В, Оценка ио 111 КГ (ко время
КГ) — 15. Поражение базально-фронтальной области.
ляет и тогда диагноз может быть установлен на
основании лишь данных клинического обследова-
ния. Характер н механизм травмы иногда являются
главными показателями, позволяющими предполо-
жить возможность повреждения спинного мозга.
Патофизиология. Классификация травмы моз-
га, основанная на данных компьютерной томогра-
фии (КТ) и характере патологии, выделяет фо
кальные и диффузные повреждения. Наличие од-
ного из этих видов нс исключает другого. К фо-
кальным повреждениям относят гематомы, ушибы,
раны и инфаркты. Гематомы могут быть эпиду-
ральными, субдуральными или внутримозговыми.
Эпидуральные гематомы нередко сочетаются с
ограниченным диффузным повреждением мозга.
Хирургическое опорожнение гематомы обычно да-
ет прекрасные клинические результаты, если оно
осуществляется до того, как произойдет выбухание
через намет мозжечка.4 В 50% случаев имеется
перелом черепа. Субдуральная гематома возника-
ет. как правило, при тяжелых травмах, связанных
с резким изменением скорости, и сочетается с диф-
фузным повреждением белого вещества или аксо-
нов и ушибом нли ранением коры. Ребенок обычно
находится при этом без сознания. Внутримозговые
гематомы у детей располагаются преимущественно
в глубоких ядрах н также сочетаются с диффуз-
ным повреждением белого вещества. Ушибы мозга
в детском возрасте возникают нс так часто, как
у взрослых. С более широким внедрением в клини-
ческую практику ядерного магнитного резонанса
(ЯМР) значительно чаще стали диагностироваться
при травме головы ушибы коры и основания мозга
в области глазницы и передневисочных отделов.
Данные ЯМР имеют очень важное значение при
оценке отдаленных результатов (рис. 14-1).
Диффузное повреждение аксонов возникает в
результате натяжения или разрыва миелиновой
оболочки или самих аксонов. Обычно при травме,
связанной с резким изменением скорости, клиниче-
ские проявления побых диффузных повреждений
достаточно ярки. Прежде всего это потеря созна-
ния, возникающая сразу после травмы. Наиболее
часто поражаются мозолистое тело, глубокие слои
164 ТРАВМА ГОЛОВЫ
белого вещества и верхняя ножка мозжечка или
цервикомедуллярное соединение в стволе мозга.
У маленьких детей в возрасте до 6 мес белое и се-
рое вещество разграничены, что обусловливает
возникновение «скользящих» ушибов, которые на
КТ определяются в виде участков сниженной плот-
ности. Первичная травма ствола мозга, развиваю-
щаяся при диффузном поражении аксонов, в боль-
шинстве случаев приводит к летальному исходу.
Поэтому дети с данным видом повреждения дол-
жны быть отнесены в группу риска, так как при
этом очень вероятны вторичные повреждения. Со-
ответственно в лечении основное внимание следу-
ет уделять активной интенсивной терапии и тща-
тельному мониторингу.
По существу любое лечение, и особенно реани-
мационные мероприятия, у пациентов с травмой
головы должны быть прежде всего направлены на
предупреждение вторичного повреждения мозга
в результате гипоксии, гиперкапнии, системной ги-
по гензии и повышения внутричерепного давле-
ния.5 Гипоксия и гиперкапния могут развиваться
вследствие неадекватных дыхательных усилий на
фоне комы, обструкции дыхательных путей или
недостаточной функции гортанной части глотки.
Эти проб 1смы иногда усугубляются при сочетан-
ном повреждении грудной клетки или в тех случа-
ях, когда у больного развивается шок, причиной
которого наиболее часто бывает кровопотеря. Сама
по себе травма головы редко приводит к шоку, в то
время как тяжелое повреждение скальпа может вы-
зывать кровотечение, сильное настолько, что в ре-
зультате развивается шок. Причиной гипотензии,
как правило, является повреждение верхних отде-
лов спинного мозга.
В норме ауторегуляция церебрального кровотока
(ЦКТ) обеспечивается благодаря следующему по-
стоянному стабильному соотношению:
Церебральное перфузионное давление =
= Системное артериальное (явление (САД)
— внутричерепное давление (ВЧД).
У детей после травмы этот механизм обычно
сохраняется, но нс всегда.6 При недостаточной
ауторегуляции любое изменение артериального
давления или ВЧД будет вести к изменению
и ЦК Г. Механизм ауторегуляции может разру-
шаться повторными изменениями ВЧД, которые
в свою очередь возникают в результате быстрых
изменений САД во время осуществления реанима-
ционных мероприятий при шоке. Поэтому очень
важно проводить реанимацию как можно более
«ровно и плавно», дабы поддерживать стабильное
артериальное давление. У всех Детей с потерей
сознания (оценка по шкале тяжести комы < 8)
и у больных, находящихся в состоянии шока, реко-
мендуется во время проведения реанимации изме-
рять ВЧД. Подъем ВЧД, отмечающийся у 50—75%
детей с тяжелой травмой головы, может быть след-
ствием расширения и полнокровия мозговых сосу-
дов, возникающего обычно вскоре после поврежде-
ния головы.6. Многочисленные причины внутри-
черепной гипертензии могут быть в какой-то
степени объяснены благодаря модифицированной
доктрине Monro-Kellie, выраженной в следующей
формуле:
v- + \г + Чмж + V„p = константа.
где Ум — объем мозга, VKp — объем крови, У%ж —
объем СМЖ и Vlp— дополнительные объемы, воз-
никающие при повреждении (например, гематома).
На основании данной концепции можно говорить
о том, что возможности для увеличения внутриче-
репного объема ограничены, даже у детей с откры-
тыми родничками, и что увеличение в объеме од-
ного из составляющих этого уравнения происходит
за счет уменьшения других составляющих. Поэто-
му, чтобы при наличии распространяющейся эпи-
дуральной гематомы ВЧД оставалось нормальным,
СМЖ должна переходить в спинномозговой канал.
Возможно и перемещение крови из оболочечных
венозных сплетений в дуральные синусы. Кроме
того, мозг сам по себе может сдавливаться и де-
формироваться, чтобы «оснобо лть место» для рас-
пространяющейся гематомы. Благодаря указанным
процессам эпидуральная гематома иногда дости-
гает значительных размеров прежде, чем начи-
нает проявляться соответствующими симптомами
(рис. 14-2), которые появляются лишь тогда, когда
все собственные компенсаторные возможности ис-
черпаны. В такой ситуации дальнейшее увеличе-
ние гематомы может привести к очень быстрому
ухудшению.
Сбалансированная связь между интракраниаль-
ными компонентами часто полностью разрушается
после травмы головы, так что все компоненты из-
меняются сразу, оставляя очень ограниченные воз-
можности для компенсации.
Продукция СМЖ (VlMM) может увеличиваться за
счет полнокровия, которое возникает как в резуль-
тате повреждения сосудов, так и в связи с высоким
рСО, и повышенным ЦКТ. В то же время умень-
шается резорбция СМЖ как следствие субарахнои-
дального кровоизлияния, вызывающего закупорку
арахноидальных ворсинок. Чаким образом абсорб
ция СМЖ может происходить только при высоком
давлении или сужении субарахноидальных про-
Рис. 14-2. Острая эпидуральная гематома лобной области со
значительной деформацией мозга. Пациент никогда не был
я коматозном состоянии.
ТРАВМА ГОЛОВЫ 165
странств в результате набухания и деформации
мозга.
Церебральный объем крови (VKp) увеличивается
при вазодилатации, а также за счет ауторегуля-
торного механизма или при нарушении венозного
оттока.
Объем мозга (V4) изменяется в результате отека
и внутрипарейхимигодного кровоизлияния. И на-
конец, Vlp нарушается при возникновении суб- или
эпидуральных гематом. Таким образом все интра-
краниальные компоненты могут увеличиваться в
объеме одновременно. Меняются и эластические
свойства интракраниального пространства. Травма
головы приводит к тяжелым нарушениям функции
нормальных механизмов, которые обеспечивают
баланс между внутричерепным объемом и давлени-
ем. В результате часто возникает вторичный подъ-
ем ВЧД и вторичное поражение как следствие вы-
бухания («грыжевого выпячивания») или ишемии
мозга либо сочетания этих факторов. Синдромы
выбухания мозга развиваются при наличии фо-
кальных гематом или повышения ВЧД (табл. 14=2).
Деформация мозга при этих синдромах и ло-
кальная церебральная ишемия в результате сдав-
ления сосудов приводят к повреждению мозговой
ткани. В таблице 14-2 указаны и сосуды, которые
сдавливаются при синдромах выбухания мозга раз-
ной локализации.
Одной из дополнительных причин повреждений
мозга может быть действие нейромедиаторов, вы-
свобождаемых в результате ишемии, судорог и оте-
ка мозга. До настоящего времени, к сожалению,
нет никаких препаратов, позволяющих эффектив-
но бороться с этими медиаторными субстанциями.
Тем не менее, если у больного через час после
травмы сохраняется судорожная готовность, необ-
ходимо применить противосудорожные препараты
с тщательным контролем их уровня в крови и
показателей электроэнцефалографии (ЭЭГ). Тя-
жесть поражения, вызванного локальной ишемией,
может усугубляться при высоком уровне глюкозы
крови. Соответственно следует контролировать
глюкозу крови и не допускать ее повышения.
ОБСЛЕДОВАНИЕ, РЕАНИМАЦИЯ,
ЛУЧЕВЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Обследование. Неврологическое обследование при
травме должно быть быстрым и целенаправлен-
ным. Главные задачи при этом — установить уро
вень сознания больного, выявить фокальные не-
врологические симптомы и установить локализа-
цию каждого из очагов поражения (кортикальный,
субкортикальный, ствол мозга, медуллярный,
спинной мозг, периферические нервы). Обследова-
ние следует регулярно повторять и каждый раз
фиксировать в истории болезни. Во много раз бо-
лее важна именно динамика состояния (улучше-
ние, ухудшение или отсутствие изменений), а не
данные однократного обследования. У детей стар-
ше 2 лет быстрым и надежным способом определе-
ния уровня сознания является шкала тяжести комы
(ШКГ — см. табл. 14-1), позволяющая оценить
ТАБЛИЦА 14-2. Синдромы выбухания («грыжевого
выпячивания») мозга
Локализация
СН1ЦЦЮМ
Субссрповидным
1 |озадикрыловид-
»1ЫЙ
Тргшстеиторжыь-
II ый
Тонзиллярный
С одной стироны н<1 дру-
гую под серпонидным
отростком
От фронтальной к сред
ней имки над малым
крылом клиновидной
кости
Через вырезку намета
мозжечка
В большое затылочное
отверстие
<'скулы
(слепливаемые)
Передние цереб-
ральные
Сонная артерия
Задние церсб
ральныс
Базилярная арте-
рия (прободаю-
щие ветви)
Задней ижн не
мозжечковые
функцию коры, используя речь, понимание и про-
извольные движения.
ШКГ предоставляет возможность охарактеризо-
вать взаимодействие подкорки и коры, исследовать
реакцию на боль и динамику мышечного гонуса,
в частности разгибательные и сгибательные дви-
жения. Этот метод позволяет также сравнить фун-
кцию левой и правой стороны, что помогает лока-
лизовать очаг повреждения мозга. А сопоставление
движений в проксимальных и дистальных отделах
(реакция на боль в ногах и руках) делает возмож-
ной оценку состояния спинного мозга.
В дополнение к ШКГ важно обследование глаз-
ного дна, особенно у детей в возрасте до 2 лет,
при этом признаки кровоизлияний в сетчатку
всегда должны вызывать подозрение на механизм
травмы, не связанный с несчастным случаем. Ре-
зультаты данного обследования могут быть един-
ственным ключом к постановке диагноза, посколь-
ку в подобных ситуациях истинный характер по-
вреждения обычно скрывается.* 8 Исследование ре-
акции зрачков и их размеров позволяет оценить
функцию отделов мозга, прилежащих к намету
мозжечка, и верхних стволовых структур. Однако
нс следует использовать в таких случаях прием
«кукольных глаз», поскольку состояние шейного
отдела позвоночника, как правило, неизвестно,
а при его поражении данный прием противопока-
зан. Для оценки функции моста мозга применяется
калорическая проба. Прежде, чем орошать наруж-
ный слуховой проход холодным физиологическим
раствором или кодой, необходимо убедиться в том,
что он не обтурирован сгустками, а барабанная
перепонка интактна и нет признаков подтекания
СМ Ж. Если сознание у ребенка сохранено, то ир-
ригация холодным раствором вызывает отклонение
глаз в сторону охлаждения с быстрым нистагмом
обратно к средней линии. Прн кортикальной дис-
функции способность к нистагму утрачивается
и возникает топическое кои тегированное отклоне-
ние глаз в сторону охлаждения. Одностороннее
или двустороннее отсутствие отклонения глаз от
средней линии может отмечаться при поражении
мостовой части ствола мозга. Это грозный при-
знак, говорящий об особо тяжелом поражении моз-
166 ТРАВМА ГОЛОВЫ
га. Состояние медуллярной функции оценивается
по дыхательным движениям и рвотной реакции.
Реанимация. Одновременно с неврологическим
осмотром проводится реанимация и общее физи-
кальное обследование с целью выявления травмы
других органов и систем. Шок нс следует связы-
ва1ь с травмой головы. Глубокая гипотензия при
отсутствии каких-либо явных причин может быть
результатом повреждения шейного отдела спинно-
го мозга.
Реанимация проводится но стандартной схеме
«ЛВС...». Ес специфические особенности при по-
вреждении мозга еле (уюшие.
Положение головы. Оптимальное положение го-
ловы по средиеи линии, при этом грудная клет-
ка и голова должны быть слегка приподняты. Пока
ис исключен диагноз повреждения позвоночника,
целесообразно использовать фиксацию шеи с по-
мощью воротника.
Артериальное СО,. В связи с частым ранним
возникновением полнокровия, РаСО2 должно под-
держиваться на уровне около 28 мм рт. с г. Ребе-
нок с оценкой по ШКГ меньше 8 обычно требует
интубации с последующей гипервентиляцией
100% кислородом, применением иедсполяризую-
щих мышечных релаксантов и внутривенным вве-
дением барбитуратов У ослабленных больных
с гипотензией барбитураты можно нс применять.
Жидкость. В связи с высоким риском неадекват-
ной секреции антидиуретического гормона (ЛДГ)
инфузионная терапия должна производиться очень
осторожно во избежание гипергидратации. Необхо-
димо применять сбалансированный солевой рас-
твор (Рингер-лактат).
В последнее время считается, что при травме
головы нет необходимости в применении кортико-
стероидов. Они не играют существенной роли
в снижении ВЧД во время реанимации. У ребенка
с нарушением сознания вполне эффективны для
достижения этой цели осмотические диуретики, та-
кие как маннитол, которые могут снижать ВЧД
достаточно длительно для того, чтобы можно было
произвести КТ, установить диагноз и транспорт»
ровать ребенка в операционную.
При остром повреждении спинного мозга у
взрослых эффективен Solu-Medrol, особенно если
он применяется в первые 6 час после травмы. Хотя
нет данных о применении этого препарата в дет-
ском возрасте, возможно, стоит все-таки использо-
вать стероиды у детей при повреждении спинного
мозга <30 мг/кг начальная доза, 5,4 мг/кг —
каждый час X 23 часа).’
Лучевые методы исследования. Наиболее цен-
ным радиологическим методом диагностики острой
травмы мозга является КТ, при этом нет пеобходи
мости обычно во внутривенном введении контра-
стных веществ. Данный метод позволяет четко
увидеть кос1и черепа, мозг и все острые измене-
ния, которые в свою очередь определяют лечебные
мероприятия. Иногда внутричерепная гематома по-
является уже после проведения первичной КТ.
Кроме того, изначально небольшие кровоизлияния
могут увеличиваться в динамике. Поэтому любое
значительное ухудшение состояния ребенка или
изменение ВЧД являются показанием для повтор-
ной КТ. Небольшие изменения, не определяемые
на КТ, могут быть выявлены с помощью ЯМР.
Данное обследование проводится после того, как
состояние ребенка стабилизируется. При тяжелой
травме у детей обычные рентгенограммы черепа
чаще всего не дают никакой дополнительной ин-
формации. В то же время боковую рентгенограмму
шейного отдела позвоночника рекомендуется сде-
лать как можно раньше в процессе проведения реа-
нимационных мероприятий. Однако следует по-
мнить, что от 25 до 60% повреждений спинного
мозга у детей никак не проявляются рентгенологи-
чески."1 Травма спинною мозга встречается в 50—
100 раз реже, чем повреждение головы. При пере-
ломах верхних шейных позвонков боковая рент-
генограмма может дать ложное впечатление об
отсутствии повреждения, особенно если снимок де-
лается при нейтральном положении головы. Реани-
мационные мероприятия, включая эндотрахеаль-
ную интубацию, не должны откладываться до того,
чтобы сделать рентгенограмму шеи. При интуба-
ции следует избегать псреразгибания шеи. ЯМР
наименее инвазивный и наиболее ценный скринин-
говый мето ( диагностики острых повреждений
спинного мозга, требующих хирургической коррек-
ции. В то же время тяжелую костную травму по-
звоночника лучше всего оценивать по данным КТ
с введением или без введения в СМЖ контрастно-
го вещества.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
В острой фазе повреждений мозга у детей хирурги-
ческое лечение ограничивается эвакуацией скопле-
ний крови, обработкой ран и вмешательствами при
проникающей травме и вдавленных переломах че-
репа. Иногда для предотвращения повышения ВЧД
может понадобиться хирургическое дренирование
СМЖ. Однако подобные повреждения отмечаются
лишь в 20—30% всех наблюдений тяжелой травмы
головы. В любом случае жизненно важно выявить
кровоизлияния, которые подлежат удалению хирур-
гическим путем, как можно раньше, в процессе их
образования. При хирургическом вмешательстве
неврологическое улучшение отмечается очень бы-
стро, часто непосредственно во время эвакуации
кропи и сгустков.
НЕОПЕРАТИВНОЕ ЛЕЧЕНИЕ
Консервативная терапия должна быть интенсивной
и в основном направленной на поддержание нор-
мальных показателей функции жизненно важных
систем и ВЧД. Если возникают судороги, лечение
проводится очень активно. Не менее важна профи-
лактика вторичной инфекции, а также поддержа-
ние нормальной функции легких и лечение любых
сочетанных повреждений. Вторичные подъемы
ВЧД с уменьшением ЦКТ — наиболее частая при-
чина смерти при травме головы, поэтому очень
важно предупредить развитие внутричерепной ги-
ТРАВМА ГОЛОВЫ 167
пертензии. Данная цель достигается сочетанием
профилактических мер (осторожная инфузионная
терапия, частое определение электролитов и осмо-
лярности. положение головы, адекватная вентиля-
ция) и своевременно осуществляемых корригирую-
щих мероприятий (гипервентиляция, осмотические
диуретики, седативные препараты для снижения
скорости мозговых метаболических процессов, мы-
шечные релаксанты тля проведения вентиляции).
РЕЗУЛЬТАТЫ
Среди детей с оценкой по ШКГ от 5 до 8 отмеча-
ется низкая летальность (0—35%) и относительно
малая частота последствий травмы (20%). При
каждом данном показателе ШКГ исходы значи-
тельно хуже при сочетанной гравме. Важно под-
черкнуть, что полное выздоровление, в том числе
и в плане умственной деятельности, может быть
даже после перенесенной комы. В ранние сроки
после тяжелой травмы головы (оценка по ШКГ
< 8) у всех детей выявляется замедление мысли-
тельных процессов и особенно снижение кратко-
временной памяти." Подобные, но непродолжи-
тельные нарушения могут наблюдаться даже после
легкого сотрясения мозга. На это необходимо обра-
тить внимание прежде, чем ребенку будет разре-
шено вернуться в школу. Дети с оценкой по ШКГ
3—4 имеют летальность от 23 до 70%, а невроло-
гические последствия обнаруживаются у 50% вы-
живших. Тем не менее полное восстановление со-
циального статуса и всех жизненных функций от-
мечается в 70—90% случаев. Этот показатель
составляет всего 30% среди детей, получивших
травму при жестоком обращении.
Очень большое внимание необходимо уделять
реабилитационным мероприятиям, которые дол-
жны включать в себя разнообразные методы, на-
правленные н«1 психосоциальную адаптацию, вос-
становление познавательной деятельности и физи-
ческое развитие. При «физическом» выздоровле-
нии детей после тяжелой травмы головы (исклю-
чая последствия синдрома опасного обращения
с детьми) степень поведенческого и познаватель-
ного восстановления значительно различается у
пациентов с приблизительно одинаковой тяжестью
травмы. Причины подобных различий пока еще не
ясны.
Результаты лечения никогда никоим образом не
могут быть сравнимы с результатами профилакти-
ки травмы в детском возрасте. И ответственность
за планомерное проведение в жизнь профилакти-
ческой программы лежит на всех, кто принимает
участие в воспитании детей.
ЛИТЕРАТУРА
1. Waller АЕ. Baker SP. Syocha A: Childhood injury deaths, nati-
onal analysis and geographic variations. Am J Public Health.
79:310—315. 1989
2. Cri Stoffel KK: Homicide in childhood: A public health problem
in need of attention. Am J Public Health 74:68—70, 1984.
3. Du ha i me AC, Gennarclli TA, Thibault LE, ct al.: The shaken
baby syndrome: A clinical, pathological and biomechanical stu
dy. J Ncurosurg 66:409—415. 1987.
4. Molloy CJ. McCaul KA. McLean AJ, et al.: Extradural hemor-
rhage in infancy and childhood: A review of 35 years experience
in South Australia. Child Nerv Syst 6:383—387, 1990.
5. Bruce DA: Head injuries in the pediatric population. Cuff Probl
Pediatr 20:61—107, 1990.
6. Muizclaar JP, ct al.: Cerebral blood flow and metabolism in se-
verely head-injured children. Pans I and 2. J Ncurosurg 71:67—
76, 1989=
7. Bruce DA, Alavi A. Bilaniuk LT. ct al.: Diffuse cerebral swelling
following head injuries in children: The syndrome of “malignant
brain edema.*’ J Ncurosurg 54:170 178. 1981.
8. Bruce DA: Pathophysiology of intracranial pressure, hi Asbury
AK. McKhann GM. McDonald Wl (Editors). Diseases of the
Nervous System. WB Saunders, Philadelphia, 1986.
9. Bracken MB, Shepard MJ, Collins WF. ct al.: A randomized,
controlled trial of methylprednisolone or naloxone in the tre-
atment of acute spinal cord injury. N Engl J Med 322:1405 -
1411. 1990.
10. Pang I). Wifbergcr JE: Spinal chord injuries without radio-
graphic abnormalities in children. J Neurosurg 57:114 129,
1982.
11. 1 evin IIS, High WM Jr, Ewing-Cobbs I . et al.: Memory functio-
ning during the firs! year after closed head injury in children
and adolescents. Neurosurgery 22:1043 1052. 1988.
Глава 15
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
Врожденные деформации грудной клетки обычно
подразделяются на 5 видов: воронкообразная грудь
(pectus excavalum), куриная грудь (pectus carina-
lum), синдром Поланда, (ефекты грудины и сме-
шанные дисплазии или торакальные деформации
при диффузных скелетных расстройствах. Боль-
шинство поражений не представляют опасности
для жизни, и функциональные нарушения при них
незначительны. В то же время некоторые редкие
варианты, например, такие, как торакальная экто-
пия сердца или асфиксическая торакальная дист-
рофия Jeune, почти всегда абсолютно фатальны.
ВОРОНКООБРАЗНАЯ ГРУДЬ
/Торошпюбразная груЛь — наиболее часто встреча-
ющаяся деформация грудной клетки. Грудина при
этом вогнута кзади к позвоночнику, так же, как
и нижние реберные хрящи (рис. 15-1). Воронко-
образная деформация в большинстве случаев
(86%) видна уже при рождении или становится
явной в течение первого года жизни и лишь в не-
большом количестве наблюдений появляется по-
зже.' У мальчиков эта деформация встречается
в три раза чаще, чем у девочек. Этиология неизве-
стна, ио определенную роль, безусловно, играет ге-
нетический фактор, ибо у 37% больных были слу-
чаи воронкообразной деформации в семье. Около
15% пациентов имеют сколиоз, причем в 11% на-
блюдений сколиоз есть и у других членов семьи.
Наиболее тяжелый вариант воронкообразной де
формации отмечается при синдроме Марфана
(рис. 15-2), который следует искать у всех наци
енгов с тяжелой воронкообразной деформацией,
особенно если это мальчик и деформация сочета-
ется со сколиозом. Поэтому в таких случаях не-
обходимо проводить офтальмологическое обследо
ванне для выявления подвывиха хрусталиков —
патологии, патогномоничной для синдрома Марфа
на. При подозрении иа этот синдром показано
УЗИ сердца. Расширение начальной части аорты
и регургитация через аортальный или митральный
клапан подтверждают диагноз.
Воронкообразная грудь у 2% пациентов сочета-
ется с врожденными пороками сердца. В большин-
стве случаев вмешательство по поводу сердечной
аномалии следует осуществлять до принятия реше-
ния о необходимости коррекции деформации. В тех
же ситуациях, когда кардиальный порок корриги-
руется через стернотомический доступ, операция
по поводу деформации грудной клетки должна
быть проведена до вмешательства на сердце, ибо
в противном случае после коррекции воронкооб-
разной груди сердце может испытывать давление
вогнутой кзади грудины.2
У некоторых пациентов с воронкообразной или
куриной грудью выявляется астма. Но данным
сводной статистики, среди 694 пациентов с дефор-
мацией грудной клетки астма отмечена у 35 боль-
ных (5,2%). При сравнении этих показателей с ча-
стотой астмы в общей популяции (среди детского
населения) не выявлено очевидных данных ни
о причинной роли астмы в развитии деформаций
грудной клетки, ни об отрицательном влиянии де-
формации на течение астмы.
Максимально точная оценка тяжести воронкооб-
разной деформации чрезвычайно важна как для
выявления показаний к оперативному вмешатель-
ству, так и для сравнения до- и послеоперацион-
ных данных. Предложены несколько методов опре-
деления тяжести вдавления. Все они используют
соотношение расстояния между грудиной и позво-
ночником и ширину верхнего и нижнего отделов
грудной клетки.3 На рисунке 15-3 представлен
один из этих методов — метод Велча (Welch).'
Влияние деформации на сердечно-легочную си-
стему. Но мнению некоторых исследователей, во-
ронкообразная деформация не вызывает измене-
ний со стороны сердечно-сосудистой и легочной
систем.' Однако это представление не согласовыва-
ется с общераспространенными клиническими дан-
ными, свидетельствующими, что у большинства
больных после хирургической коррекции деформа-
ции значительно улучшается физический статус.
Это подтверждено комплексным обследованием па-
циентов.''
ДЕФОРМАЦИИ ГРУДНОЙ КЛ
Рис. IS I. А, 7 летний мальчик с симметричной воронкообразной деформацией грудной клетки до операции.
В. После операции полностью откорригиропяпная деформации.
Рис. 15-2. А, 8-летняя девочка с синдромом Марфана и тяжелом пором (сообразной деформацией грудной к тетки
Виден рубец ink тс стернотомии, предприми гон в грудном возрасте с целью коррекции митрального порока.
В. После операции — полная коррекция деформации.
170 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
D,
Коэффициент вдавления (DR) =
°!
Степень деформации (DG) = (1 — DR) х 10
Индекс Велча - DG + ....
0,5, если реберный угол (О) 25‘
и или
0,5, если кардиоторакальный
коэффициент > 50%
Рис. 15-3. Метод определения тяжести деформации по рентгенограммам. Расстояние между передней поверхностью позвоночника
и задней поверхностью грудины на уровне Г9 < I) 1) делят на расстояние между остистым отростком ГЗ и углом Луиса (02). Допол-
нительно добавляют 0.5. если реберный угол больше 25 (ралусоп н/или если кардиоторакальный коэффициент больше 50%.
Патологические симптомы, имеющиеся при во-
ронкообразной груди, многие исследователи объ-
ясняют уменьшением интраторакального объема.
Связь эту, однако, трудно доказать, поскольку
и у здоровых людей существует очень большой
диапазон нормальных показателей функции сер-
дечно-легочной системы. Кроме того, важное зна-
чение имеет физическая тренированность и кон-
ституциональные особенности каждого больного.
По данным одного из исследований, среди 7 паци-
ентов с воронкообразной грудью у 5 при нагрузке
появлялись различные симптомы’ Средняя общая
емкость легких в процентах от нормальной соста-
вила у больных с воронкообразной деформацией
79%. Поглощение кислорода значительно превы-
шало нормальные показатели но мере приближе-
ния нагрузки к максимуму. В контрольной же
группе и у трех пациентов с бессимптомной во-
ронкообразной грудью, наоборот, отмечалась ли-
нейная зависимость меж iy поглощением кислорода
и нагрузкой. Среднее поглощение кислорода при
максимальной нагрузке у больных с воронкообраз-
ной грудью, имевших какие-либо симптомы, пре-
вышало норму на 25,4%. Повышенное поглощение
кислорода подтверждает усиленную «работу» ды-
хания, хотя жизненная емкость при этом была не-
значительно уменьшена либо даже нормальная.
При оценке функции легких и физической вы-
носливости (по отношению к нагрузке) до и после
операции у 14 пациентов с воронкообразной де-
формацией отмечено, что после коррекции дефор-
мации у всех пациентов значительно улучшилась
максимальная вентиляция легких8 Устойчивость
к физической нагрузке, по данным измерения об-
щей продолжительности нагрузки и максимально-
го поглощения кислорода, также возросла. После
операции отмечалось устойчивое снижение часто-
ты сердечных сокращений при той же. что и до
операции, нагрузке, однако изменений в потребле-
нии кислорода не было. При проведении пер-
фузионно-нентиляционной сцинтиграфии с ксено-
ном-153, из 17 пациентов с воронкообразной дефор-
мацией у 12 выявлено нарушение региональной
вентиляции,” преимущественно в нижних отделах
левого легкого. После операции у 7 из этих боль-
ных вентиляция стала нормальной. Из 10 наци
ентов с региональными нарушениями перфузии,
также преимущественно в нижних отделах левого
легкого, у 6 после операции перфузия стала нор-
мальной. Из 10 больных с измененным соотноше-
нием вентиляция-перфузия у 6 этот показатель
иормал изовался.
Катетеризация сердца, проведенная 6 пациентам
с воронкообразной деформацией средней степени,"'
выявила нормальные показатели давления в состо-
янии покоя и в положении на спине. Сердечный
индекс и реакция на умеренную нагрузку колеба-
лись в пределах нормы. Устойчивость же к нагруз-
ке в вертикальном положении была ниже нормаль-
ной у двух пациентов и на нижней границе нормы
у трех. Послеоперационное исследование было
проведено у трех пациентов. В двух случаях после
операции достигнут верхний уровень устойчивости
к нагрузке. Сердечный индекс увеличился на 38%
за счет повышения ударного объема. Частота же
сердечных сокращений осталась прежней.
Изотопная ангиокардиография, проведенная у
13 пациентов с воронкообразной деформацией,
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ 171
позволила неинвазивным способом оценить состоя-
ние ссртсчной деятельности в вертикальном поло-
жении. в покое и при нагрузке па ветосипетс."
Хотя после операции не было изменений сердечно-
го выброса и его лсвожслудочковой фракции, од-
нако отмечено существенное увеличение как пра =
во-, так и левожелудочкового объема, что, безу-
словно, подтверждает устранение сдавления сердца.
При обследовании этих пациентов с нагрузкой
10 из 13 сумели до операции достичь заданной
частоты сердечных сокращений, причем четверо —
без каких-либо симптомов. После же операции
у всех, кроме одного, отмечена заданная частота
сердечных сокращений во время упражнений и у 9
из 13 больных не было при этом никаких патоло-
гических симптомов.
Результаты исследований в этой области порой
противоречивы. Для достоверной оценки характе-
ра воздействия воронкообразной деформации на
функцию сердечно-легочной системы необходимо
использовать простые и воспроизводимые количе-
ственные методы исследования.
История хирургического лечения. Первые опе-
рации по поводу воронкообразной деформации
грудной клетки были осуществлены Meyer и Sau-
erbruch в 1911 г. и 1913 г. С тех пор методы кор-
рекции существенно изменились.1 1 Ravilch в
1949 г. описал вмешательство, включавшее: (1)
иссечение всех деформированных реберных хря-
щей с надхрящницей, (2) отделение мечевидного
огростка от грудины, (3) отделение от грудины
межреберных мышечных пучков и (4) поперечную
остеотомию грудины. Эта операция позволяла сме-
стить грудину кпереди с помощью спиц Кирш-
нера.14
В 1958 г. Welch описал метол коррекции ворон-
кообразной деформации, подчеркнув необходи
мость полного сохранения футляров (реберных
хрящей) из надхрящницы и верхних межреберных
мышечных пучков. Он производил остеотомию
грудины и переднюю фиксацию ее шелковыми
швами.'5 При использовании данного метода были
получены прекрасные результаты.1 Другие авторы
применяли фиксацию грудины с помощью подпор-
ки, дабы обеспечить раннюю ее стабильность в
передней позиции. ‘ К сожалению, не было про-
ведено ни одного выборочного исследования по
сравнению этих двух методов и их отдаленных
результатов. Сообщалось лишь о результатах
(одинаковых) каждого из этих методов в отдельно-
сти: в одной публикации говорилось о 92% удов-
летворительных исходов при использовании под-
порок у 1112 больных, а в другой серии — о 91 %
удовлетворительных результатов применения ме-
тода без подпорок у 392 пациентов. 1 Некоторые
исследователи сделали выводы о гом, чю внутрен-
няя подпорка не обладает дополнительными преи-
муществами, зато иногда вызывает серьезные
осложнения. Однако справедливость подобного за-
ключей ия у многих вызывала сомнения. Опи-
сан также метод фиксации на «треножнике»,
подразумевающий заднюю остеотомию грудины,
субперихондральную резекцию нижних деформиро-
ванных реберных хрящей и косое разделение нор-
мальных второго и третьего реберных хрящей.5
Эти разделенные в косом направлении хрящи по-
мещаются и укрепляются с захождением труг на
друга, что обеспечивает поддержку грудины в пе-
реднем положении. Имеются сообщения о 100%
удовлетворительных результатов (45 пациентов)
при использовании данного метода.
Была также описана техника «поворота» груди-
ны,21 22 использованная первоначально в Японии.
Грудина при этим играла роль «свободного транс-
плантата», который ротировался на 180 градусов
и прикреплялся к реберным хрящам, от которых
грудина сначала отделялась.25 У детей с воронко-
образной деформацией применение столь ради-
кального подхода было ограничено из-за риска
серьезных осложнений в случае присоединения ин-
фекции, а также в связи с наличием альтернатив-
ных, менее сложных методов.
До настоящего времени в арсенале хирургиче-
ского лечения воронкообразной деформации по-
прежнему остается много методов, однако ни один
из них не принят всеми как оптимальный. При
каждом имеется риск поздних рецидивов, которые
не могут не вызывать беспокойства хирургов, за-
нимающихся лечением этой патологии. Применяе-
мый нами способ реконструкции показан на ри-
сунке 15-4.
Вторичная реконструкция рецидивных деформа-
ций технически значительно более сложна, чем
первичная, в связи с наличием рубново-изменен-
ных и деформированных реберных хрящей. По-
вторные операции сопровождаются также большей
кровопотерей и послеоперационными дыхательны-
ми расстройствами. Для обеспечения благоприят-
ных исходов в подобных случаях решающую роль
играет прочная фиксация грудины в передней по-
зиции. Рецидив — частое осложнение в таких си-
туациях, поскольку реберные хрящи плохо регене-
рируют после повторных операций и не способны
поддерживать грудину, когда удаляются подпорки.
Результаты и осложнения. Круг осложнений
после хирургической коррекции воронкообразной
деформации достаточно невелик. Пневмоторакс
возникает редко и требует лишь аспирации возду-
ха. Если это частичный пневмоторакс, можно огра-
ничиться тщательным наблюдением. Повреждение
легкого с длительным подтеканием воздуха, требу-
ющее постановки дренажа в плевральную полость,
встречается не часто. Редко развивается и раневая
инфекция, гематома или расхождение краев раны.
Кровохарканье, гсмоперикард или перикардиаль-
ный выпот отмечаются в основном в тех случаях,
когда производится ретростс риал иная фиксация.
При первичной реконструкции с применением
электро коагулятора гемотрансфузия требуется
редко, при повторных же вмешательствах необхо-
димость в ней возникает, как правило. Частота тя-
желых рецидивов, по данным литературы, состав-
ляет 3—5%, небольшие рецидивы с развитием
центрально расположенной «впадины» грудной
клетки возникают у 5—10% больных.
172 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
Рис. 15-4. А, Поперечный разрез проводят ниже и кнутри от сосковых линий на месте будущей складки пол молочными железами.
Большую грудную мышцу вместе с частью малой грудной и передней зубчатой мышцы отделяют от грудины и поднимают.
В. Лоскут грудной мышцы отделяют путем введения рукоятки от скальпе зя в направлении прямо к реберному хряшу после
того, как поднята медиальная часть мышцы. Рукоятку ножа перемешают вместе с изогнутым крючком, которым оттягивают мышцу
кпереди. Переднее отведение мышц во время разделения позволяет определить бессосудистую зону в околососкопой области и избе-
жать внедрения в межребериые мышечные пучки.
С, Субперихондральная резекция реберных хрящей разрез надхрящницы спереди. Надхрящницу отделяют от реберных хря-
щей в бессосудистой зоне. Дополнительные разрезы надхрящницы под углом в 90 градусов (к продольному разрезу) в каждую сто-
рону в месте се соедннеиия с грудиной (вставка) позволяют «подойти» к задней стенке реберного хряща.
D, Хрящи в области соединения их с грудиной отделяют скальпелем, используя перихондральный элеватор Велча (Welch), кото-
рый держат сзади, полнимая им хрящ и защищая средостение (вставка). Отделенный хрящ можно затем захватить зажимом Аллиса
(Allis), поднять и «оторвать» от костио-хрящевого соединения.
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ 173
Н ДО ПОСЛЕ
-.J- 1-1- • Лоскуты
m. pect. major
ушиты над грудиной
Peet. m. подшита
к влагалищу
прямых мышц
Рис. 15-4.
Е. Остеотомию гру хины осуществляют на уровне последнего
деформированною хряща (в основном третьей), иногда второго)
и заднего изгиба грудины. Два поперечных разреза грудины на
расстоянии 2—4 мм друг от друга производят пневматической
дрелью.
F. Подняв шумя зажимами нижнюю часть грудины, отделяют
от нее электрокоагулятором мечевидный отрос гак. что позволя-
ет войти и ретростсриальное пространство и уже под контри юм
глаза, избегая повреждения плевры, отделить шестой и седьмой
перихондральные футляры.
G, Грудину в области остеотомии ушнвают несколькими тол-
стыми шелковыми швами, при этом ассистент приподнимает
грудину большим пальцем или каким-либо инструментом.
Н, Коррекция деформации грудины достигается благодаря
клиновидной остеотомии, перенодяшей грудину кпереди в поло-
жение гипсркоррскцин.
I, Грудные мышцы ушивают по средней линии, полностью
закрывая ими всю грудину. Прямые мышцы затем подшивают
к грудным.
174 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
КИЛЕВИДНАЯ ДЕФОРМАЦИЯ
ГРУДНОЙ КЛЕТКИ
Килевидная деформация, представляющая собой
выступание грудной стенки кпереди, встречается
менее часто, чем воронкообразная, и, по нашим
данным, составляет около 15% всех деформаций
грудной клетки. Килевидная грудь включает в себя
несколько компонентов деформации, при этом по-
ражение реберных хрящей может быть одно- или
двусторонним, а грудина выступает кпереди в вер-
хнем или нижнем отделе. «Куриная» грудь бывает
также одним из компонентов «смешанных» дефор-
маций, с западением хрящей на одной стороне
и выступанием на другой или с ротацией грудины.
В клинической практике наиболее часто встречает-
ся вариант, когда имеется симметричное выступа-
ние нижних реберных хрящей и тела грудины — гру-
дино-хрящевой (chondrogladiolar) вид (рис. 15-5В).
Реже отмечаются асимметричные деформации с
односторонним выступанием реберных хрящей
и совеет редки смешанные деформации. При нео-
бычном варианте верхней или «рукояточно-хря-
щевой» (chondroinanubrial) деформации рукоятка
грудины и верхние реберные хрящи выступают
кпереди, а тело грудины по отношению к выступа
ющим отделам западает (рис. 15-5Л).
Этиология килевидной деформации неизвестна.
Встречаясь у мальчиков в три раза чаще, чем у де-
вочек. она обычно проявляется в детском и юноше-
ском возрасте, в отличие от воронкообразной гру-
ди, которая видна, как правило, уже при рождении
Гис. /5-5. Л. 14 летпии мальчик с высокой (рукояточно-хряще-
вой) килевилной деформацией грудной клетки. Виты выступа-
ющие вперед рукоятка грудины, верхние — второй и третий ре-
берные хрящи и относительное западение кзади нижней части
грудины. В. 19-лстний юноша с симметричной низкой (груднно-
хрящевой) килевидной деформацией грудной клетки.
или в течение первого года жизни. Килевидная же
деформация при рождении отмечается у трети
больных, имеющих эту патологию, и почти у поло-
вины она проявляется лишь после начала пубер-
татного «рывка» в росте.21 У 26% пациентов с ку-
риной грудью деформации грудной клетки имеют-
ся и у других членов семьи. Частота сочетания со
сколиозом такая же, как и при воронкообразной
деформации — у 15% больных, а в семье сколиоз
отмечается у 12% пациентов.
У маленьких детей с килевидной грудью, осо-
бенно если она сочетается со сколиозом или имеет
очень тяжелую степень деформации, следует подо-
зревать синдром Марфана.
Состояние сердечно легочной системы. Изме-
нений со стороны сердечно-легочной системы при
килевидной деформации обычно не отмечается,
а потому принятие решения об операции основыва-
ется лишь на тяжести деформации. Иногда паци-
ен гы могут предъявлять жалобы на повышенную
чувствительность или болезненность и области вы-
ступающей грудины, что, как правило, связано
с локальной травмой.
История хирургического лечения. Все 4 послед-
них десятилетия, с тех пор, как впервые была осу-
ществлена коррекция килевидной деформации, ме-
тоды хирургического лечения продолжали неук-
лонно развиваться. Пионером на этом пути был
Равич, который в 1952 г. произвел вмешательство
при «рукояточно-хрящевом» варианте порока пу-
тем резекции множественных деформированных
реберных хрящей и двойной остеотомии грудины.2'
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ 175
Грудино-хряшевая (90.8%)
Смешанная деформация
В (вид спереди) — 9,2%
Рис. /5-6. Л. Лечение грудини-хрящепой деформа-
ции. Единичная или двойная остеотомия imcie об-
нажения и резекции реберных хрящей производит-
ся так же. как при воронкообразной деформации.
Это позволяет сместить грудину кзади в нормаль-
ное положение.
В. Лечение комбинированном деформации груд-
ной клетки. Полная и симметричная резекция ре-
берных хрящей (от третьего до седьмого) с после-
ду кмцей поперечной коррекцией (О—10 градусов)
путем клиновидной остеотомии грудины. Ушива-
ние грудины позволяет осуществить как переднее,
так и ротационное ее смешение.
С Рукояючно-хряшевая (очень редкий вид)
С. Деформированная грудина в боковой проек-
ции. Схема широкой клииопидной остеотомии, ко-
торую производят в области перехода тела груди-
ны в рукоятку. После завершения остеотомии верх-
нюю час!ь грудины смещают кзади, и фиксация
ее обеспечивается только за счет прикрепления
к первому ребру. Нижняя часть грудины гиперкор-
рнтируется на 20—35 градусов (справа).
Последующие операции включали резекцию пе=
родней части грудины и даже поднадкостничную
резекцию всей грудины.2* Подобные попытки кор-
рекции деформации в основном оказались без-
успешными.
Методы, распространенные в настоящее время
и впервые примененные в 1963 г., заключаются
в резекции реберных хрящей (субперихондраль-
ной) и нижнего отдела грудины с перемещением
прямых мышц к оставшейся части грудины.27 В по-
следующем, в 1973 г., были предложены способы,
подразумевавшие субперихондральную резекцию
выступающих реберных хрящей и сохранение при
этом всей грудины. Переднее же ее выступание
корригировалось путем передней поперечной ос-
теотомии и перелома задней части, что позволяло
переместить грудину кзади.2* Данная техника про-
должает использоваться и сегодня, с прекрасными
резуль га гами (рис. 15-6).24
Результаты и осложнения. Современные мето-
ды коррекции дают в общем хорошие результаты.
Необходимость в интраоперационной гемотранс-
фузии возникает редко. Пневмоторакс является не-
частым осложнением и требует, как правило, лишь
аспирации воздуха. Рецидивы развиваются редко
и обычно у тех пациентов, которые подвергаются
оперативному вмешательству до полного заверше-
ния роста и развития и при этом производится
лишь односторонняя резекция пораженных ребер-
ных хрящей. В подобных ситуациях в процессе
продолжающегося роста может развиться выступа-
ние хрящей на противоположной стороне. Стойкая,
трудно поддающаяся исправлению деформация от-
мечается также после неадекватно проведенной
первоначальной резекции деформированных отде-
лов. В таких случаях деформация обусловлена
обычно нижними реберными хрящами, образующи-
ми реберную дугу.
176 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
СИНДРОМ ПОЛАНДА
Синдром Поланда представляет собой сочетание
аномалий, включающее отсутствие большой и ма-
лой грудной мышц, синдактилию, брахидактилию,
ателию (отсутствие соска молочной железы)
и/или амастию (отсутствие самой молочной желе-
зы), деформацию или отсутствие ребер, отсутствие
волос в подмышечной впадине и снижение толщи-
ны подкожно-жирового слоя (рис. 15-7). Этот син-
дром (отдельные его компоненты) впервые был
описан в 1826 г. и в 1839 г. " соответственно во
французской и немецкой литературе, однако на-
зван именем английского студента-медика Аль-
фреда Поланда, который в 1841 г. опубликовал
частичное описание данной деформации, встретив-
шейся ему на секции.’1 Полная характеристика де-
формации со всеми ее компонентами появилась
в литературе лишь в 1895 г.32
У каждого пациента имеются различные компо-
ненты синдрома Поланда, который встречается
спорадически, с частотой 1 на 30 000 — 1 на 32 000
новорожденных и редко носит семейный харак-
тер. Поражение кистей варьирует по обширно
сти и тяжести. Предполагается, что в этио-
логии синдрома Поланда играет роль аномальная
миграция эмбриональных тканей, образующих
грудные мышцы, гипоплазия подключичной арте-
рии или внутриутробное повреждение. Ни одна те-
ория до сих пор не нашла, однако, достоверного
подтверждения
Деформация грудной стенки при синдроме По-
ланда варьирует от легкой гипоплазии ребер и ре-
берных хрящей на стороне поражения до аплазии
передней части ребер и всех реберных хрящей
(рис. 15-8). Так, по данным одного из исследова-
ний, среди 75 больных с синдромом Поланда
у 41 не было деформации грудной стенки, 10 име-
ли гипоплазию ребер без локальных участков
вдавления, у 16 отмечалась деформация ребер с за-
ва юанем, причем у 11 из них западение было зна-
чительным. И наконец, в 8 наблюдениях выявлена
аплазия ребер.35 Важно отметить, что между сте-
пенью деформации кисти и грудной клетки нс об-
наружено корреляции
Хирургическое лечение при синдроме Поланда
требуется лишь у небольшой части пациентов,
обычно при аплазии ребер или деформации с вы-
раженным вдавлением (рис. 15 9).3' У больных со
значительным западением на противоположной
стороне часто имеется килевидная деформация ре-
берных хрящей (рис. 15-8В), которую также мож-
но корригировать во время операции 1 Равич ис-
пользовал для реконструкции расщепленные ре-
берные трансплантаты с тефлоновым покрытием.37
Другие хирурги в дополнение к реберным транс-
плантатам применяли лоскуты из широчайшей
мышцы спины. У девочек важно осуществить
коррекцию деформации грудной клетки до вмеша-
тельства но поводу гипоплазии или аплазии мо-
10ЧНОЙ железы, что позволяет обеспечить опти-
мальные условия для хирургического увеличения
в последующем размеров железы (рис. 15-10). Ро-
тания широчайшей мышцы спины редко использу-
ется у мальчиков, в го время как у девочек эта
операция может с успехом применяться при необ-
ходимости реконструкции молочной железы.
ДЕФЕКТЫ ГРУДИНЫ
Дефекты грудины представляют собой широкий
спектр редких аномалий грудины, сердца и верх-
них отделов брюшной стенки. Наиболее часто рас-
сматриваются 4 нозологические формы этого поро-
Рпс. 15-7. А. 17-лстиий юноша с otcvtcibhcm большой и малой грудных мыши и легкой гипоплазией соска. Контуры грудной
клетки не нарушены. В, 8-Летний мальчик с аплазией третьей»— пятого ребра и косым положением грудины. Видна также тяже-
лая сочетанная деформация руки с той же сгороны.
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
177
Рис. 1.5-Я. Аномалии грудной клетки при синдроме Пиланда. А, Наиболее часто реберный каркас совершении нормальный, лишь
отсутствуют грудные мышцы.
В, Западение пораженной стороны грудной стенки с ротацией и (часто) западением i рудник. Нередко с противоположной
стороны имеется килевидная деформация.
С. Гипоплазия ребер на пораженной стороне, но без существенного вдавлен ня. Этот вариант обычно не требует хирургической
коррекции.
D, Атазия одного и 1и нескольких ребер обычно сочетается с западением прилежащих ребер на пораженной стороне и рота
имей грудины.
ка. которые могут в какой-то степени сочетаться
или «перекрещиваться» друг с другом. В основе
данного подразделения лежит характер тканей, по-
крывающих сердце.
Торакальная эктопия сердца представляет со-
бой классическое «обнаженное сердце», не прикры-
тое спереди никакими тканями. Верхушка его
обычно обращена кпереди или кверху (рис. 15-11).
Часто при этом имеются кардиальные пороки,
особенно такие, как тетрада Фалло, стеноз легоч-
ной артерии, транспозиция магистральных сосудов
и дефекты межжелудочковой перегородки.^ Ниже
стернального дефекта может располагаться грыжа
пупочного канатика, которая в подобных случаях
прилежит к сердцу, но грыжевые оболочки не по-
крывают его. Лечение торакальной эктопии сердца
почти всегда безуспешно. В литературе имеется
описание лишь трех случаев хирургической кор-
рекции с благоприятным исходом. Ни у одного из
этих детей не было аномалий сердца (эктопиро-
ванное сердце было «непорочным»). Сердце, воз-
вращенное на свое «законное» место, плохо адап-
тируется в грудной клетке, что объясняется в
основном торсией крупных сосудов и сдавлением
сердца. Спасение жизни детям.с торакальной экто-
пией сердца возможно лишь при разработке ка-
ких-либо совершенно новых, иных подходов, пре-
дусматривающих реконструкцию грудной стенки
вокруг спереди расположенного сердца, а не воз-
вращение его в грудную клетку.
IIIей на я эктопия сердца. Пациенты с шейной
эктопией сердца отличаются от больных с тора-
кальной эктопией лишь расстоянием, на которое
перемещено сердце. Обычно в таких случаях име-
ется слияние между верхушкой сердца и ртом
и другие тяжелые аномалии. В литературе нет ни
единого сообщения о выживании детей с данным
пороком.
Торакоабдоминальная эктопия сердца. При
этом варианте аномалии имеется расщелина ниж-
ней части грудины, а сердце покрыто мембраной,
напоминающей оболочки грыжи пупочного кана-
тика, или тонкой, иногда пигментированной кожей
(рис. 15-12). Обычно нс бывает тяжелой передней
ротации сердца, как при торакальной его эктопии.
У таких пациентов, как правило, имеются карди-
альные пороки, наиболее часто тетрада Фалло, ди-
вертикул левого желудочка и дефекты межжелу-
дочковой перегородки.40 Торакоабдоминальная эк-
топия сердца может быть компонентом пентады
Кантрелла, которая включает в себя, кроме того,
дефекты диафрагмы и перикарда, аномалии груди-
ны, сердца и брюшной стенки. Лечение торакоаб-
доминальной эктопии обычно намного более
успешно, чем при торакальной эктопии. Первона-
чально хирургическое вмешательство должно быть
12 Заказ № 1622
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ 179
Рис. IS-10. Компьютерная гомшра.ммя 24-лстнси пацмешки с синчромач Ноланда. Видны идавление ребер на пораженной стороне
(сптошная стрелка) н килеви иная деформация с противоположной стороны (полая стрелка). Молочная железа на стороне пораже-
ния гнпоплазирована.
Рис. 15-9. А. Поперечный разрез производят ниже сосков
и между ними, у девочек — на месте формирующемся в после-
дующем складки под молочными железами.
В, Схематическое изображение деформации с ротацией груди-
ны, западением хрящей на пораженной стороне и килевидным
выстоянном с противоположной стороны.
С, При аплазии ребер эндоторака п>ная фасция находится
непосредствен ио под истонченным подкожным слоем и пскто-
ральной фасцией. Поднимают грудную мышцу на «здоровой*
стороне вместе с пскторальиой фасцией (если ина есть) на по-
раженной стороне. Выполняют субпсрихонтральную резекцию
реберных хрящей, как показано пунктирной линией. В редких
случаях резекцию производят до уровня второго реберною
хряща.
D. Ниже второго реберного хряща производят поперечную
корригирующую клиновидную стернотомию. После ушивания
грудины толстой шелковой нитью устраняется как заднее сме-
щение, так и ротация грудины.
Е. При аплазии ребер расщепленные реберные трансплан-
таты берут с противоположных пятого или седьмого ребер и
укрепляют на стороне поражения металлическими швами меди-
ально в предварительно созданные выемки грудины, а лате-
рально—к соответствующим ребрам. Ребра расщепляют, как
показано на рисунке, чтобы максимально обеспечить их меха-
ническую прочность.
в основном направлено на закрытие дефекта кожи
над сердцем и брюшной полостью. После иссече-
ния оболочек грыжи желательно ушить кожу, что
позволяет избежать инфекции и медиастинита. Об-
легчает закрытие дефекта мобилизация лоскутов
с боковых от де юв брюшной стенки или использо-
вание синтетических материалов. Однако имеются
сообщения и об успешном консервативном лечении
с применением местных вяжущих средств, способ-
ствующих вторичной элите тизации. Полную кор-
рекцию порока сердца лучше осуществлять до то-
го, как сердце будет прикрыто каким-либо проте-
зирующим материалом.
Расщепление или раздвоение грудины является,
несомненно, корригируемым пороком. При данной
аномалии сердце обычно нормально развито («не-
порочное»), грудина расщеплена частично или
полностью, а перикард, так же, как и кожа, покры-
вающая грудину, интактны (рис. 15-13). Расщели-
на грудит»1 никогда не сочетается с грыжей пу-
почного канатик.!. Частичный дефект грудины
обычно локализуется в верхней ее части и в обла-
сти рукоятки, в противоположность торакальной
или торакоабдоминальной эктопии, при которой
расщеплена преимущественно нижняя часть груди-
ны.4,1 У большинства больных при неполном рас-
щеплении грудины нижняя се треть и мечевидный
отросток интактны. Методы лечения представлены
на рисунке 15-14. Важно устранить этот дефект
180 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
Рис 15-11. Ребенок с торакальной эктопией
сердца и небольшим дефектом передней брюш-
ной стенки. Видно также характерное для
этого порока «высокое отхождение» пуповины
и направление верхушки сердца кпереди.
Рис. 15-12. Новорожденным мальчик с торакоабдоми-
нальной эктопией сердца (пентада Кантрелла). Нижние
отделы грудной клетки расширены. Большая эпигаст-
ральная грыжа пупочного канатика. Диафрагма и ниж-
няя часть перикарда отсутствовали. У пациента была
также тетрада Фалло.
Рис. 15 13. Новорожденный ребенок с расщепленной грудиной. При сильном крике видно западение дефекта во время вдоха
(слепа) и выбухание по время выдоха (справа) — проба Вальсальвы.
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ 181
Рис. 15-14. К. Дефекты грудины
обычно локализуются в верхнем
ее отделе, как показано на схеме.
Продольный разрез кожи прово-
дят но всю длину дефекта.
В. Непосредственно ниже под-
кожного слоя нмдны «половинки»
грудины с отходящими от их ла-
теральных поверхностей грудны-
ми мышцами. Сразу под ними
расположены эндоторакальная
фасция и перикард.
С. Эндотора кал ьную фасцию
отделяют сзади от грудины с обе-
их сторон путем слепой препа-
ровки таким образом, чтобы мож
но было безопасно наложить
швы. Сближение стернальных
пл at тонок облегчается благодари
клиновидному иссечению хряща
в нижнем отделе. Коррекцию
лучше производить в периоде но-
ворожден н ости. когда грудная
стенка гибкая и податливая.
D. Ушивание дефекта произво-
дят Tevdek или полидиоксапопо-
выми швами 2-0.
Перикард
и эндоторакальная фасция
в грудном возрасте, когда грудная клетка податли-
ва и половины расщепленной грудины могут быть
сближены без трудностей. Если же коррекция осу-
ществляется у старших детей, то иногда требуется
даже хондротомия в косом направлении, что позво-
ляет увеличить (расширить) размеры грудной
клетки и предотвратить тем самым сдавление серд-
ца, которое может возникнуть после ликвидации
дефекта грудины.41
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
ПРИ ДИФФУЗНЫХ
СКЕЛЕТНЫХ РАССТРОЙСТВАХ
Асфиксическая торакальная дистрофия
(болезнь Jeune)
Jeune первым в 1954 г. описал новорожденного
с узкой ригидной грудной клеткой и множествен-
ными аномалиями хрящей.42 Пациент умер вскоре
после рождения. Причиной смерти явилась дыха-
тельная недостаточность. В последующем другими
исследователями была дана подробная характери-
стика этой формы остеохондрочистрофии, имею-
щей разнообразные проявления со стороны скеле-
та. Болезнь Jeune — наследственное заболевание,
передающееся аутосомно-рецессивным путем и не
связанное с хромосомными аномалиями.43 Наибо-
лее существенными ее признаками являются узкая
грудная клетка, имеющая форму колокола, и вы-
ступающий живот. Грудная клетка сужена как
в поперечной, так и в сагиттальной плоскости.
Из-за горизонтального направления ребер дыха-
тельные движения резко ограничены (рис. 15-15).
Ребра короткие и широкие, а их утолщенные ко-
стнохрящевые соединении едва достигают перед-
ней подмышечной линии. Реберные хрящи непра-
вильной формы напоминают рахитические четки.
Микроскопическое исследование костно-хрящевых
соединений выявляет беспорядочную и плохо вы-
раженную эндохондральную оссификацию, кото-
рая и приводит к укорочению длины ребра.
Сочетанные скелетные аномалии, которые быва-
ют при этом синдроме, включают короткие корена-
стые конечности с относительно укороченными
и широкими костями. Ключицы фиксированы
182 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
Рис. Ребенок с асфиксической торакальной дистрофией
(синдром Jeune). На рентгенограмме видны короткие горизон-
тально расположенные ребра и узкая грудная клетка с умень-
шенным объемом yteiKHx.
Рис. /5-16. Рентгенограмма ребенка со
с нон дилотора калькой дисплазией (синд-
ром Jure ho-Levin). Тяже гая аномалия
позвоночника с множественными полу-
позвонка ми и крабообразными ребрами,
вплотную сближенными сзади и расхо-
дящимися спереди.
ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ 183
в приподнятом положении, а гипиплазированный
таз небольшой по размерам, с прямоугольными
подвздошными костями.
Данный синдром сам по себе, так же, как и пора-
жение легких при нем, бывает разной степени вы-
раженности. Первые случаи, описанные в литера-
туре, заканчивались всегда смертью ребенка в пе-
риод новорожден ноет и. Однако в последующем
в разных сообщениях был представлен очень
широкий диапазон процентов выживаемости среди
больных с этим синдромом.44 Данные аутопсии
вариабельны и показывают разнообразные анома-
лии легких, хотя в большинстве случаев раз-
витие бронхов нормальное и отмечаются лишь
различные вилы уменьшения альвеолярного де-
ления.45
Хирургические вмешательства при этой патоло-
ги и очень редко бывают успешными. Все они за-
ключаются в продольном расщеплении грудины
и расширении расстояния между двумя ее полови-
нами с целью увеличения интратора кал ыюго объ-
ема. Для удержания и фиксации расщепленной
грудины использовались реберные трансплантаты,
распорки из нержавеющей стали, трансплантаты
из подвздошной кости с металлической фиксирую-
щей пластинкой и метилметакрилатовые протезы.
Однако результаты всех хирургических вмеша-
тельств зависят прежде всего от степени первич-
ной легочной гипоплазии.
Спондилоторакальная дисплазия
(Синдром Jarcho-Levin)
Спондилоторакальная дисплазия — аутосомно-ре-
цессивный тип деформации, включающий в себя
множественные аномалии позвонков и ребер- Дети
с данной патологией обычно погибают в раннем
возрасте от пневмонии и дыхательной недостаточ-
ности.46 При этом синдроме имеются множествен-
ные перемежающиеся пол у позвонки с поражением
большей части, а иногда и всего торакального
и поясничного отделов позвоночника. Центры
оссификации позвонков редко пересекают сред-
нюю линию. Множественные слияния ребер сзади,
так же как и значительное укорочение грудного
отдела позвоночника, обусловливают крабообраз-
ную форму грудной клетки на рентгенограммах
(рис. 15-16). Одна треть пациентов имеет соче-
танные аномалии, включая врожденные пороки
сердца и почек. Строение костей у этих больных
нормальное. Данный синдром впервые был описан
у детей в пуэрто-риканских семьях (15 случаев из
18 опубликованных).47
Деформация грудной клетки при спондилотора-
кальной дисплазии по сути вторична по отноше-
нию к аномалии позвоночника, которая обусловли-
вает сближение начальных отделов ребер сзади.
Большинство детей с этой патологией умирает
в возрасте до 15 мес. Никакие попытки хирурги-
ческого лечения не только не предпринимались, но
и не предлагались.48
ЛИТЕРАТУРА
1. Shamberger RC, Welch KJ: Surgical repair of pectus excavuium.
J Pediatr Surg 23:615—622, 1988.
2. Shamberger RC, Welch KJ. Castaneda AR. et al.: Anterior chest
wall deformities and congenital heart disease- J Thorac Cardio-
vasc Surg 96:427—432. 1988.
3- Haller JA Jr, Kramer SS, Lietman SA: Use of CT scans in se-
lection of patients lor pectus excavatum surgery: A preliminary
report. J Pediatr Surg 22:904-—906, 1987.
4. Welch KJ: Chest wall deformities, /л Holder TM, Ashcraft KW
(Editors). Pediatric Surgery. WB Saunders. Philadelphia,
pp 162—182. 1980.
5. Hailer J A. Peters GN, Mazur D, et al.: Pectus excavatum:
A 20-year surgical experience. J Thorac Cardiovasc Surg
60:375- 383. 1970.
6. Shamberger RC, Welch KJ: Cardiopulmonary function in pectus
excavatum Surg Gynecol Obstct 166:383 391, 1988.
7. Castile RG, Staats BA. Westbrook PR: Symptomatic pectus de-
formities of the chest. Am Rev Respir Dis 126:564 568, 1982.
8. Cahill JL, Lees GM, Robertson HT: A summary of preopcraiive
and postoperative cardiorespiratory performance in patients un-
dergoing pectus excavatum and carinatum repair. J Pediatr Surg
19:430—433, 1984.
9. Blickmaii JG, Rosen PR, Welch KJ, et al.: Pectus excavatum in
children: Pulmonary scintigraphy before and after corrective
surgery. Radiology 156:781—782, 1985.
10. Beiser GD, Epstein SE. Stampfcr M, et al.: Impairment of cardi-
ac function in patients with pectus excavatum, with improvement
after operative correction. N Engl J Med 287:267—272. 1972.
11. Peterson RJ, Young WG Jr, Godwin JD, et al.: Noninvasive as-
sessmenl of exercise cardiac function before and after pectus
excavatum repair. J Thorac Cardiovasc Surg 90:251—260.
1985.
12. Meyer I.: Zur chirurgischen Behandlung der angeborenen Tri-
chtcrbrusl. Verh Berliner Med 42:364—373, 1911.
13. Sauerbruch F: Die Chimrgie der Brustorgane. Verlag von Julius
Springer. Berlin, pp 440—444. 1920.
14. Ravitch MM: The operative treatment of pectus excavatum. Ann
Surg 129:429—444, 1949.
15. Welch KJ; Satisfactory surgical correction of pectus excavatum
deformity in childhood: A limited opportunity. J Thorac Surg
36:697—713, 1958.
16. Rehbcin F, Wernicke IIH: The operative treatment of (he funnel
chest. Arch Dis Child 32:5 8, 1957.
17. Adkins PC. Blades B: A stainless steel strut for correction of
pectus excavatum. Surg Gynecol Obstcl 113:111—113, 1961.
18. Willital GH: Operationsindikation-Operationslechnik bci Brusl-
korbdeformicrungen- Z Kindcrchir 33:244—252, 1981.
19. Hecker WCh, Procher G, Dietz HG: Results of operative correc-
tion of pigeon and funnel chest following a modified procedure
of Ravitch and Haller. Z Kinderchir 34:220—227, 1981.
184 ДЕФОРМАЦИИ ГРУДНОЙ КЛЕТКИ
20. Oelsniiz G: Fehlbildungen des Brusikorbes. Z Kindcrchir
33:229- 237, 1981.
21. Judel J, Judel R: Thorax en entonnoir: Un procede operatoire.
Rev Orthop 40:248—257. 1954.
22. Jung A: Le traitement du thorax en entonnoir par le “relourne-
ment pcdicule” de lit cuvette sterno-chondrale. Mem Acad Chin
82:242—240, 1956.
23. Wada J. Ikeda K, Ishida T, et al.: Results of 271 funnel chest
operations. Ann Thorac Surg 10:526- 532, 1970.
24. Shamberger RC, Welch KJ: Surgical correction of pectus carina
turn. J Pediatr Surg 22:48—53, 1987.
25. Ravitch MM: Unusual sternal deformity with cardiac symptoms.
Operative correction. J Thorac Surg 23:138—144, 1952.
26. 1 ester CW: Pigeon breast (pectus carinalum) and other protru-
sion deformities of the chest of developmental origin. Ann Surg
137:482—489. 1953.
27. Roblcsek F, Sanger PW. Taylor FH„ et al.: The surgical tre-
atment of chondroslernal prominence (pectus carina him). J Tho-
rac Cardiovasc Surg 45:691—701, 1963.
28. Welch KJ, Vos A: Surgical correction of pectus carinatum (pige-
on breast). J Pediatr Surg 8:659-—667. 1973.
29. Froriep R: Beobachtung eines Failes Von Mangel der Bru st drib
sc. Notizen aus dem Gebiete der Natur- und Heiikunde 10:9
14, 1839.
30. Lallemand LM: Ephcrmcrides Medicates de Montpellier.
1:144—147, 1826.
31. Poland A: Deficiency of the pectoral muscles. Guys Hosp Rep
6:191 193. 1841.
32. Thomson J: On a form of congenital thoracic deformity. Tcrato-
logia 2:1 — 12, 1895.
33. Frcire-Maia N, Chautard EA, Opitz JM, et al.: The Poland syn-
drome — Clinical and genealogical data, dermaloglyphic analy-
sis, and incidence. Hum Hered 23:97 104, 1973.
34. McGillivray BC, Lowry RB: Poland syndrome in British Co-
lumbia: Incidence and reproductive experience of affected per-
sons. Am J Med Genet 1:65 74. 1977.
35. Shamberger RC, Welch KJ, Upton J III: Surgical treatment of
thoracic deformity in Poland’s syndrome. J Pediatr Surg
24:760 766, 1089.
36. Haller JA Jr, Colombani PM, Miller D, et al.: Earty reconstructi-
on of Poland’s syndrome using autologous rib grafts combined
with a latissimus muscle flap. J Pediatr Surg 19:423—429, 1984.
37. Ravitch MM: Atypical deformities of the chest wall — absence
and deformities of the ribs and costal cartilages. Surgery
59:438 449, 1966.
38. Urschel HC Jr, Byrd HS. Sethi SM. et al.: Poland's syndrome:
Improved surgical management» Ann Thorac Surg 37:204—211,
1984.
39. Fodor PB, Khoury F: I atissimtis dorsi muscle flap in reconstruc-
tion of congenitally absent breast and pectoral is muscle. Ann
Plast Surg 4:422—425, 1980.
40. Shamberger RC, Welch KJ: Sternal defects. Pediatr Surg Ini
5:156—164, 1990.
41. Sabiston DC Jr: The surgical management of congenital bifid
sternum with partial ectopia cordis. J Thorac Surg 35:118—122,
1958.
42. Jeune M. Carron R, Beraud C, et al.: Polychondrodyslrophie
avec blocage thoracique d’evolution fatale. Pediatrie 9:390 -
392, 1954.
43. Tahernia AC, Stamps P: «Jeune syndrome* (asphyxiating thora-
cic dystrophy): Report of a case, a review of the literature, and
an editor’s commentary. Clin Pediatr 16:903—-908, 1977.
44 Kozlowski K, Masel J: Asphyxiating thoracic dystrophy without
respiratory disease: Report of two cases of the latent form. Pedi-
atr Radiol 5:30—33, 1976.
45. Williams AJ, Vawter G, Reid LM: Lung structure in asphyxia-
ting thoracic dystrophy. Arch Pathol I ab Med 108:658—661,
1984.
46. Jarcho S, Levin PM: Hereditary malformation of the vertebral
bodies. Bull Johns Hopkins Hosp 62:216—226, 1938.
47. Hcilbronncr DM, Renshaw TS: Spondylolhoracic dysplasia.
J Bone Joint Surg 66A:302—303, 1984.
48. Roberts AP, Conner AN, Tolmie JL, et al.: Spondylothoracic
and spondylocostal dysostosis: Hereditary forms of spinal de-
formity. J Bone Joint Surg 70B:123—126, 1988.
Глава 16
АНОМАЛИИ И ОБСТРУКЦИИ
ДЫХАТЕЛЬНЫХ ПУТЕЙ
АТРЕЗИЯ ХОАН
Врожденная обструкция задней носовой хоаны мо-
жет быть костной или мембранозной, одно- или
двусторонней. Односторонняя атрезия, как прави-
ло, не проявляется тяжелыми симптомами и может
быть заподозрена лишь по увеличению водяни-
стых выделений из одной половины носа. Двусто-
ронняя хоанальная атрезия иногда вызывает пери-
одически повторяющуюся асфиксию, обычно во
сне или при попытках кормления. Большинство
детей в норме дышат носом. Когда же носовые
ходы непроходимы, адекватный воздухообмен осу-
ществляется только в том случае, если ребенок не
спит и плачет. Нормальное кормление и сосание
обычно невозможны, поскольку при этом быстро
развивается асфиксия.
Диагноз может быть заподозрен уже при рожде-
нии в связи с невозможностью проведения катете-
ра в носоглотку через один из носовых ходов. Для
подтверждения диагноза необходимо контрастное
исследование носа и/или компьютерная томогра-
фия (КТ). Существенную помощь оказывает так-
же прямое исследование фиброназофарингоскопом.
Адекватная вентиляция при атрезии хоан впол-
не может быть обеспечена за счет ротоглоточных
дыхательных путей. Однако при этом необходимо
постоянное наблюдение, позволяющее избежать
эпизодов гипоксии. Некоторых детей можно кор-
мить с ложки или пипетки, но зондовое питание
обычно наиболее эффективно.
Некоторые дети с двусторонней атрезией хоан
достаточно хорошо чувствуют себя, что позволяет
отложить специальное лечение на месяцы, а порой
и годы. Другие имеют тяжелые обструктивные
симптомы и требуют иногда даже трахеостомии
или радикальной коррекции в первые недели жиз-
ни. Прямое иссечение перегородки может быть
осуществлено через носовой или небный доступ,
в зависимости от возраста ребенка. При мембра-
нозной обструкции возможно иссечение лазером,
однако этот метод редко применяется, поскольку
окклюзия преимущественно бывает костной. К со-
жалению. ни один из хирургических методов не
гарантирует от развития послеоперационного сте-
ноза. Адекватная резекция кости, закрытие кост-
ных краев лоскутами слизистой и различные спо-
собы расширения носовых ходов — вот те основ-
ные факторы, которые способствуют профилакти-
ке этого осложнения. Однако многие специфиче-
ские детали реконструкции при атрезии хоан не
входят в задачи обсуждения в данном руководстве.
ИНТРАОРАЛЬНАЯ ОБСТРУКЦИЯ
Нарушение проходимости дыхательных путей на
уровне ротовой полости может быть вызвано раз-
личными опухолевидными образованиями. Одной
из причин бывает и гипоплазия нижней челюсти,
например при синдроме Пьера Робена или Trea-
cher Collins, когда язык имеет нормальные разме-
ры, но его западение вызывает обструкцию надсвя-
зочпых отделов дыхательных путей. Обструкция
может быть вызвана также ненормально большим
языком при лимфангиоме, нейрофиброматозе или
простой мышечной гипертрофии, связанной с
синдромом Беквит-Видемана. Многие дети чувст-
вуют себя вполне удовлетворительно в положении
на животе лицом вниз, поскольку язык при этом
направлен кпереди и не западает. Обструкция воз-
никает обычно во время сна или при движениях
языка в процессе сосания.
Старые методы в виде попыток фиксировать
язык кпереди подшиванием его к подбородку или
нижней губе большинством хирургов оставлены
в связи с неэффективностью. В настоящее время нс
вызывает сомнений тот факт, что трахеостомия,
которой раньше боялись и старались избегать,
уменьшает летальность и сокращает длительность
госпитализации.1 Иногда может понадобиться на-
ложение гастростомы для питания. Реконструктив-
ные операции на языке или нижней челюсти не
следует производить в первые месяцы жизни.
Внутриротовые опухоли, такие как лимфангио-
мы, тератомы, краниофарингеомы, аберрантные
щитовидные железы, рабдомиосаркомы, а иногда
186 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
даже гетеротопическая ткань мозга, могут вызвать
обструкцию дыхательных путей и потребовать ис-
сечения. Характер вмешательства зависит от вида
и локализации опухоли, но в любом случае иссече-
ние проводится на фоне эндотрахеальной интуба-
ции или трахеостомии.
ОБСТРУКЦИЯ ГОРТАНИ
Аномалии
Ларингомаляция — наиболее частая обструктив-
ная аномалия дыхательных путей у грудных детей,
главное проявление которой — инспираторный
стридор. Данная патология существует с самого
рождения, но симптомы инспираторного стридора
и частичной обструкции могут отсутствовать в те-
чение нескольких дней и даже недель. В ряде слу-
чаев после первых месяцев жизни обструкция про-
грессирует в своей тяжести.
Термин ларингомаляция обозначает анатомиче-
скую аномалию надсвязочного отдела гортани, вклю-
чающую в себя удлиненный изогнутый (внутрь)
надгортанник, свободно висящий утолщенный или
отечный черпаловидный хрящ, иногда перегибаю-
щийся даже через среднюю линию, слабые черпа-
лонадгортанные складки и функциональный про-
лапс всех этих структур на вдохе, что и вызывает
субтотальную обструкцию голосовой щели.
Инспираторный оридор варьирует по степени
и тяжести. Дыхание на вдохе часто грубое и отры-
вистое. Стридор может отсутствовать в состоянии
покоя и бурно нарастать при возбуждении и уси
ленном дыхании. Интенсивность симптомов зави-
сит также от положения ребенка. Проявления
обычно минимальны, когда малыш лежит на живо-
те с вытянутой шеей.
Рентгенологическое исследование шеи помогает
исключить другие причины имеющихся симптомов.
На боковой рентгенограмме иногда видно опуска-
ние на вдохе черпалонадгортанной складки. Окон-
чательный диагноз устанавливается лишь при не-
посредственном прямом обследовании гортани.
Наилучшис результаты дает осмотр гортани от
уровня надгортанника (при спонтанном дыхании)
с применением гибкого бронхоскопа, введенного
трансназально. Подъем надгортанника клинком
ларингоскопа обычно устраняет инспираторную
обструкцию. Гортань ниже надгортанника может
выглядеть совершенно нормальной. Бронхоскопия
при стридоре требуется в основном для того, чтобы
исключить другие возможные причины обструк-
ции, локализующиеся ниже голосовых связок. Что
касается типичной ларингомаляции, то при ней го-
лосовые связки, гортань ниже голосовой щели
и трахеобронхиальное дерево выглядят нормаль-
ными.
Никакой специфической причины, вызывающей
данную патологию, не выявлено, не считая откло-
нений в развитии структуральной ригидности
и контуров падсвязочной части гортани. В боль-
шинстве случаев специальное лечение не требует-
ся. По мере роста гортани, к 2 3 годам жизни
состояние ребенка улучшается и симптомы исчеза-
ют. В более тяжелых случаях отмечается тенден-
ция к развитию обструкции и накоплению СО2 во
время сна. Иногда до созревания гортани может
понадобиться трахеостомия. В редких наблюдениях
это созревание затягивается на несколько лет, за-
вершаясь порой к 6 годам.
Мембраны гортани представляют собой тонкие
перегородки, обычно локализующиеся на уровне
голосовой щели, но иногда несколько выше или
ниже. Симптомы часто появляются сразу после
рождения в виде обструкции дыхательных путей
и слабого крика. Диагноз может быть поставлен
с помощью ларингоскопии, но порой при располо-
жении мембраны в подсвязочном пространстве тре-
буется бронхоскопия.
Характер вмешательства зависит от толщины
мембраны. Толстые и массивные перегородки тре-
буют до их иссечения предварительной трахеосто-
мии. Тонкие мембраны могут быть удалены эндо-
скопически обычным иссечением либо с помощью
лазера или высокочастотного тока.
Атрезия. При атрезии гортани ребенок не мо-
жет родиться живым, если только нет сочетанного
трахеопищеводного свища или расщелины, доста-
точно большой, чтобы поддерживать вентиляцию.
Данная патология требует немедленной трахеосто-
мии, если, разумеется, трахея сама по себе не атре-
зирована.
Кисты и опухоли
Ларингоцеле. Наполненные только жидкостью
или воздухом и жидкостью кисты гортани могут
вызывать рецидивирующую обструкцию надсвя-
зочных отделов дыхательных путей. Эти образова
ния часто подвижны и меняют свое положение
в течение респираторного цикла. Стридор и об-
струкция обычно отмечаются на вдохе и порой рез-
ко выражены
Термин ларингоцеле применим к тем кистам, ко-
торые возникают как расширение мешочк<1 гортан-
ного желудочка. Прямая ларингоскопия обычно до-
статочна для диагностики, хотя исследование гиб-
ким или жестким бронхоскопом позволяет более
тщательно детализировать имеющиеся изменения.
Срочное лечение включает в себя эндотрахеаль-
ную интубацию, обеспечивающую восстановление
проходимости дыхательных путей, и декомпрессию
кисты путем аспирации через иглу или с помощью
хирургического вскрытия ее («срезание верхуш-
ки»), которое может быть произведено лазером.2
Лимфангиома и гемангиома. Лимфатические
кисты, вызывающие частичную или полную об-
струкцию дыхательных путей, обычно являются
частью больших лимфангиом шеи, распространяю-
щихся в гортань через дно полости рта. Как прави-
ло, эти образования требуют этапного иссечения,
которое редко может быть осуществлено без вре-
менной трахеостомии. Встречаются в дыхательных
путях и изолированные кисты. В таких случаях
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
187
лечение ограничивается деструкцией внутрипро-
светной части кисты.
Гемангиомы подсвязочного пространства могут
быть жизнеопасными и даже фатальными. Это
редкая патология, встречающаяся обычно у детей
первого года жизни. Примерно у 50% больных
с подсвязочными гемангиомами имеются также ге-
мангиомы кожи. Расположение этих образований
в подсвязочном пространстве обычно асимметрич-
ное— с одной или с другой стороны. Они относи-
тельно сдавливаемы, имеют консистенцию доста-
точно плотной губки и почти всегда покрыты нор-
мальной слизистой, которая часто «скрывает»
истинный характер подлежащего образования. Диа-
гностическая биопсия порой бывает серьезно за-
труднена, ибо поверхностное взятие бион га га дает
неизмененную слизистую, а глубокая биопсия мо-
жет вызвать значительное кровотечение. По дан-
ным одного из сообщений, точные морфологиче-
ские результаты при биопсии были получены
лишь в четырех случаях из семи?
У 85% детей симптомы в виде стридора как
инспираторного, так и экспираторного, появляют-
ся в первые 6 мес жизни. Может также отмечаться
осиплость голоса, одышка, затруднения при корм-
лении и плохая прибавка массы тела.
Иногда наблюдается спонтанная регрессия ге-
мангиом гортани. В других случаях тяжелая сте-
пень обструкции может заставить прибегнуть
к трахеостомии или иным методам лечения. Во-
прос о целесообразности общего применения сте-
роидов в таких ситуациях продолжает оставаться
очень спорным, ибо высокая их эффективность со-
четается со значительной частотой побочных эф-
фектов при длительном лечении. По данным одно-
го из исследований, у трех пациентов, получавших
несколько коротких, от 3 до 6 недель, курсов лече-
ния стероидами, вслед за регрессией наступил бы-
стрый рецидив и лишь у четвертого пациента от-
мечен стойкий продолжительный эффект. Криоте-
рапия, открытое или эндоскопическое иссечение
также успешно используются теми, кто обладает
опытом в применении данных методов. Однако при
иссечении существует опасность, связанная с кро-
вотечением, а в некоторых случаях — нарастанием
стеноза в результате образования послеоперацион-
ного рубца.
В прошлом для лечения подсвязочных гемангиом
была предложена лучевая терапия (низкие дозы),
данные об эффективности которой очень противо-
речивы. Тем не менее известный риск индуцирова-
ния у детей при этом опухолей щитовидной желе-
зы делает метод облучения противопоказанным
для применения в детском возрасте.
Папилломы. Папилломатоз гортани — доброка-
чественное новообразование, развитие которого
стимулируется, по существующим предположени-
ям, человеческими паповавирусами, хотя бывает
очень трудно получить подтверждение этой тео-
рии высевами культуры. Симптомы наиболее часто
появляются в возрасте от полутора до пяти лет.
При папиллома гозе « органи у де гей в 60% случа-
ев в родах у матери диагностируется остроконеч-
ная кондилома. По данным литературы, малигни-
зация папиллом возникает у 1—2% больных.4
Пролиферация папиллом вызывает обструкцию
дыхательных путей, которая проявляется симпто-
мами осиплости, стридора и одышки. В тяжелых
случаях распространение опухоли вниз приводит
к обструкции трахеобронхиального дерева.
Хирургическое удаление остается главным мето-
дом лечения папиллом, несмотря на то, что реци-
дивы являются фактически правилом, ибо мани-
пуляции ниже места расположения образования
несут в себе риск распространения опухоли глуб-
же — в трахею и бронхи. Удаление папиллом про-
изводится кусачками либо с применением криохи-
рургических методов или углекислотного лазера.
По литературным данным, эффективным может
быть использование аутовакцины. Лечение интер-
фероном в дополнение к иссечению пока еще нахо-
дится в стадии клинических испытаний, однако
предварительные результаты подтверждают, что
прекращение лечения этим препаратом приводит
к рецидиву папилломатоза.5 Оценка эффективно-
сти любого метода затрудняется тем, что никогда
нельзя исключить вероятность спонтанной регрес-
сии папиллом, которая возникает с непредсказуе-
мой частотой.
Приобретенные обструкции
Острый эпиглоттит. Эпиглоттит представляет
собой клинический синдром, возникающий при
остром воспалительном отеке надсвязочного отде-
ла гортани. Надгортанник, черпалонадгортанные
связки, черпаловидные хрящи и ложные голосовые
связки — каждое из этих образований может быть
вовлечено в процесс и вызывать обструкцию
дыхательных путей. Этиологическим фактором
обычно является Haemophilus influenzae В, хотя
иногда встречаются пиогенный стафилококк и бе-
та-гемолитические стрептококки группы А. Для
данной патологии характерен длительный инспи-
раторный стридор, нарастающий в положении ре-
бенка на спине. Болезнь быстро прогрессирует,
приводя в конечном счете к респираторному кол-
лапсу. Большинство детей находятся в состоянии
тяжелого токсикоза. Они стараются сесть прямо,
выдвинув подбородок вперед и высунув наружу
язык. Такое положение сопровождается обильным
слюнотечением. Заболевание в основном поражает
детей в возрасте от 2 до 6 лет. но иногда встреча-
ется даже у 5-мссячных малышей, а порой и у
взросл ых.
При любых манипуляциях у ребенка с эпиглот-
титом очень высок риск стремительного возник-
новения полной обструкции. Поэтому никакие
попытки осмотра гортани или задней стенки глот-
ки не должны предприниматься вне стен операци-
онной. На боковой рентгенограмме шеи (с исполь-
зованием режима визуализации мягких тканей)
иногда виден отечный надгортанник, однако рент-
генологическое обследование можно производить
лишь в том случае, когда состояние ребенка позво-
ляет это сделать.
188 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Основной метод экстренной помощи — эндотра-
хеальная интубация (на короткий период време-
ни), производимая в операционной и обычно под
общей анестезией. Введение интубационной труб-
ки может быть затруднено из-за массивного отека.
В такой ситуации условия операционной обеспечи-
вают возможность общей анестезии, мышечной ре-
лаксации и канюляции дыхательных путей. К сча-
стью, показания к трахеостомии возникают редко.
Воспалительный процесс быстро и тет на убыль
при внутривенном введении антибиотиков. Обычно
больной находится на интубационной трубке не
больше 3 дней.
Круп. Вирусное воспаление и отек верхних ды-
хательных путей, определяемое терминами
острый ларинготрахеобронхит или инфекцион-
ный круп, встречается намного более часто, чем
эпиглоттит, и вызывает меньшие трудности при
лечении. Главные этиологические факторы — ви-
русы парагриппа А и В, но среди возбудителей
этого заболевания также могут быть респиратор-
но-синцитиальный вирус, аденовирус, Коксаки-ви-
рус А, ЕСНО-вирусы (энтероцитопатогенныс «си-
ротские» вирусы человека) и вирус кори. В основе
поражения лежит подсвязочный отек с различны-
ми компонентами трахеобронхиального воспа-
ления.
Средний возраст больных с крупом — от 3 мес
до 3 лет, причем девочки поражаются в два раза
чаще мальчиков. У ребенка отмечается лающий
кашель, хриплое дыхание, инспираторный и экс-
пираторный стридор, втяжение эпигастральной об-
ласти. Пациенты выглядят ослабленными, но без
признаков интоксикации. Нет и слюнотечения,
а стридор не нарастает в положении на спине.
Переднезадняя и боковая рентгенограммы шеи
могуг подтвердить клинические данные, говорящие
о наличии подсвязочного стеноза, а кроме того,
позволяют исключить другие причины обструкции
дыхательных путей.
Неотложная помощь заключается прежде всего
в увлажнении окружающего воздуха, что обычно
достигается помещением ребенка в специальную
«палатку» для больных с крупом. Быстрое дейст-
вие может оказать рацемический адреналин в
аэрозоле, снимающий стридор и обструкцию дыха-
тельных путей. Иногда для закрепления достигну-
того эффекта требуется повторное его примене-
ние.6 Вопрос о целесообразности использования
кортикостероидов продолжает оставаться весьма
спорным.7 В редких случаях может понадобиться
назотрахеальная интубация. Что же касается тра-
хеостомии, то необходимость в ней в настоящее
время снизилась почти до нуля.
Инородные тела. Обструкция гортани инород-
ным телом может быть чрезвычайно жизнеопас-
ной. При тяжелой ее степени отмечается инспира-
торный стридор, афония, цианоз, гипоксия и ино-
гда, в конечном счете, остановка сердца Если это
случается не в медицинском учреждении или ря-
дом нет человека, который может срочно и пра-
вильно использовать прием Хеймлиха (резкий тол-
чок кулаком в живот) или осуществить крикотире-
отомию, то ребенок обычно умирает. Инородные
тела больших размеров, полностью обтурирующие
дыхательные пути, застревают, как правило, над
голосовыми связками. У старших детей наиболее
часто это комки пищи. Своевременно (немедлен-
но) произведенный удар по спине или прием Хей-
млиха обеспечивает быстрое устранение обструк-
ции. Маленькие дети «вдыхают» самые разнооб-
разные твердые и мягкие инородные тела, однако
извлечь их из дыхательных путей бывает намного
труднее, чем у пациентов старшего возраста.
Если обструкция частичная и какое-то количе-
ство воздуха продолжает поступать, пусть даже
с трудом, то почти всегда безопаснее сначала огра-
ничиться поддерживающей вентиляцией кислоро-
дом (дыхание мешком или маской, рот в рот или
любым другим способом) на то время, пока ребе-
нок транспортируется в операционную, где есть
необходимое эндоскопическое и наркозное обеспе-
чение. Слепые манипуляции на обтурированных
дыхательных путях недостаточно опытным персо-
налом и при отсутствии соответствующего обору-
дования могут привести к большой беде
При полной обструкции и отсутствии поступле-
ния воздуха немедленно должен быть использован
прием Хеймлиха. Если он оказался безуспешным
после трех или четырех толчков, показана срочная
крикотиреотомия. К сожалению, обструкция может
возникнуть в ситуации, когда нет под рукой инст-
рументов, необходимых для крикотиреотомии. И
тогда жизнь ребенка зависит от того, насколько
успешно используется прием резкого голчка в эпи-
гастральную область, а у грудных детей — надав-
ливания на нижнюю часть грудной клетки либо
удара по спине.
Инородные тела, которые проникают за голосо-
вые связки, как правило, не настолько велики, что-
бы вызвать полную обструкцию дыхательных пу-
тей. Большинство из них обычно проходят в один
из бронхов — правый или левый, так что при этом
вполне может поддерживаться адекватная вентиля-
ция. Однако в некоторых случаях инородное тело,
пройдя через голосовые связки своей продольной
осью, может затем повернуться и обтурировать
верхние отделы трахеи. Кроме того, предметы с не-
ровными контурами, такие, например, как драпи-
ровочные гвоздики, иногда частично проходят
своей ножкой, а головка при этом застревает над
голосовыми связками.
Срочная помощь должна быть всегда направле-
на прежде всего на освобождение дыхательных пу-
тей от инородного тела, что достигается иногда
простыми способами — ударом по спине, сдавлени-
ем эпигастральной области или нижних отделов
грудной клетки. Если эти приемы не помогли, то
прежде, чем применить дыхание рот в рот или ма-
ской-мешком, необходимо предпринять попытку
выдавить инородное тело пальцем сзади со сторо-
ны глотки. В том случае, когда усиленная вентиля-
ция обеспечивает прохождение воздуха вокруг
инородного тела, ее следует продолжать до тех
пор, пока не будет подготовлено все для оказания
дальнейшей помощи. Если же усиленная вентиля-
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ 189
ния нс эффективна, то единственный шанс на спа-
сение жизни ребенка — немедленная крикотирео-
томия.
Способ удаления в операционной инородных тел
из гортани или верхних отделов грахеи зависит от
формы, характера и локализации пред мега, а так-
же от опыта хирурга. В большинстве случаев наи-
более безопасно и точно осуществить эту манипу-
ляцию позволяет использование жесткого детского
бронхоскопа (с управляемым дыханием), снабжен-
ного оптическим телескопом и оптическими щип-
цами (см. главу 8).
II остинтубационный подсвязочный стеноз.
Повреждение дыхательных путей в детском возра-
сте, связанное с интубацией, обычно происходит
на уровне перстневидного хряща единственного
хряща, образующего в нормальных дыхательных
путях полностью замкнутое кольцо. Диаметр тра-
хеи у детей на этом уровне — наименьший. Поэто-
му эндотрахеальную трубку подбирают, как пра-
вило, соответственно диаметру именно перстневид-
ного кольца. Механическая травма подсвязочной
области может быть связана с некрозом в резуль-
тате давления, вызванного слишком плотно стоя-
щей трубкой, а также излишней се подвижностью,
обусловленной недостаточной фиксацией или пуль-
сирующими толчками при ИВЛ циклированным
аппаратом. Развивающийся рубцовый стеноз обыч-
но локализуется на уровне перстневидного хряща,
но может распространяться и па голосовые связки
или вниз на верхние отделы трахеи.
По данным литературы, в 1965—76 гг. частота
постинтубационного подсвязочного стеноза коле-
балась от 1,6 до 6,7%.в Эти тревожно высокие
цифры обусловили необходимость разработки по-
ложений и правил, соблюдение которых позволяло
избежать плотного вставления интубационных
трубок, обеспечивало надежную их фиксацию,
а также было направлено на профилактику инфек-
ции и сокращение длительности пребывания боль-
ного на интубационной трубке. Последовавшее
уменьшение частоты интубационных повреждений
было отчетливым — в некоторых отделениях ново-
рожденных они вообще практически перестали
возникать. Однако это осложнение, к сожалению,
не может совершенно исчезнуть до тех пор, пока
дети с различными видами патологии требуют
лечения с применением интубационных трубок.
Диагностика
Лучевые методы исследования практически не
информативны при диагностике приобретенных
обструкций гортани, поскольку в большинстве слу-
чаев стенозы не видны на рентгенограммах. Диа-
гноз непроходимости дыхательных путей основы-
вается на клинических симптомах, таких как стри-
дор, одышка, снижение сатурации, и данных эндо-
скопического обследования, которые позволяют
подтвердить диагноз и установить уровень об-
струкции, ее степень и причину.
Эндоскопия. Грансназальное исследование гиб-
ким эндоскопом обеспечивает наилучший обзор
надсвязочного отдела гортани. Эт,а процедура важ-
на также для оценки динамики развития патологии
дыхательных путей, вторичной по отношению
к ларингомаляцни. *
При поражении на уровне голосовых связок
или ниже более эффективно как для уточнения
диагноза, так и для осуществления различных
небольших лечебных манипуляций, исследование
жестким бронхоскопом с тслсоптикой. Самые ма-
ленькие детские бронхоскопы последних моделей
имеют наружный диаметр тубуса 4—5 мм. Если
у любого ребенка старше периода новорожден по-
сти таким бронхоскопом невозможно пройти без за-
труднений, это говорит о выраженном стенозе.
В тех же случаях, когда имеется особо тяжелое
сужение, ввести через просвет удастся лишь же-
сткий телескоп диаметром 2,8 мм. без тубуса. Эта
процедура позволяет определить протяженность
и диаметр стенозированного участка. Для оценки
любого сужения с просветом меньше 2,8 мм может
понадобиться трахеостомия. Дальнейший осмотр
производят с помощью гибкого эндоскопа, вводи-
мого через трахеостому, таким же путем, как и при
обследовании выше места обструкции.
Хирургические вмешательства
и результаты
Трахеостомия. Перед вмешательством при тяже-
лых хронических обструкциях верхних дыхатель-
ных путей обычно требуется трахеостомия, кото-
рая у маленьких детей достаточно сложна и не
должна осуществляться вне операционной. До тра-
хеостомии, если только это возможно, ребенка не-
обходимо за интубировать. Общая анестезия облег-
чает процедуру и повышает ее безопасность. Тех-
ника трахеостомии, которую мы применяем, нс
отличается принципиально от той, что описана
в главе 4.
В редких случаях обструкция дыхательных пу-
тей инородным телом или в результате травмы
делает невозможной интубацию или вентиляцию
мешком и .маской. В подобных обстоятельствах
временное введение иглы с большим просветом
или канюли через перстнещитовидную мембрану
может обеспечить удовлетворительную вентиля-
цию и позволить подготовить ребенка к трахеосто-
мии в более благоприятных условиях. Срочная
трахеостомия у грудных детей с короткой толстой
шеей — очень сложная процедура и вне операци-
онной может быть предпринята только в том слу-
чае, если это единственный шанс для спасения ре-
бенка. В экстренных ситуациях почти всегда более
простым и безопасным способом является интуба-
ция или мешочно-масочная форсированная венти-
ляция.
При наложении трахеостомы у детей никогда не
следует иссекать хрящ из передней трахеальной
стенки, ибо это может привести к нестабильности
трахеи и вызвать в последующем сложности при
190 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
деканюляции. Нерациональны и поперечные раз-
резы трахеи, поскольку давление при этом труб-
кой изнутри вызывает деформацию трахеального
кольца выше трахеостомы, что также может за-
труднить деканюляцию.
Очень важно предотврати |ь возможность слу-
чайного смещения трахеостомической трубки. По-
этому она должна быть надежно фиксирована
в том положении, в котором изначально поставле-
на во время операции. Данная процедура облегча-
ется, если при завязывании вокруг шеи трахеосто-
мических тесемок держать голову ребенка в поло-
жении сгибания кпереди, чтобы тесемки плотно
облегали шею. Тракционные швы вокруг третьего
трахеального кольца фиксируются к передней
грудной стейке и оставляются на 4—5 дней, что
помогает выйти из положения в случае смещения
трахеостомической трубки.
При смене трахеостомической трубки лучше ис-
пользовать не обтуратор, а отсосный катетер, ко-
торый вводят через трубку в трахею. Трахеостоми-
ческую трубку затем извлекают. Применение для
этих целей обтуратора может быть опасным, осо-
бенно если ход трахеостомы не сформировался до-
статочно хорошо. Короткий кончик обтуратора
в таком случае может, не пройдя в трахею, остано-
виться спереди около се стенки. Если подобная
ситуация не распознана до начала вентиляции, то
средостение будет при вентиляции наполняться
воздухом, трахея тогда «уходит» в глубь раны
и трахеостомическая трубка оказывается слишком
короткой, чтобы достичь трахеостомы. Исходом
может быть смерть ребенка. Описанное осдожне-
Ги<. 16-1. Эндоскопическое иссечение пнутрипросветной грану-
лемы или подсвязочвой рубцовой пиши с помощью детского
уретрального резектоскопа.
ние более надежно предотвращается, если исполь-
зуется катетер, а не обтуратор.
Деканюляция трахеи. Попытка деканюляции
должна производиться у детей только после обяза-
тельного эндоскопического обследования дыхатель-
ных путей. Трудности деканюляции, за редким
исключением, связаны, как правило, с непол-
ностью ликвидированной механической обструк-
цией. Если дыхательные пути имеют нормальный
просвет и причина, послужившая показанием к тра-
хеостомии, устранена, трахеостомическая трубка
удаляется без осложнений. Однако нередкой на-
ходкой при этом бывает гранулема, которая растет
в просвете дыхательных путей вокруг краниальной
части трубки, распространяясь вниз. И если
у взрослого человека для его дыхательных путей
большого калибра это не имеет особого зна-
чения, то гранулома таких же размеров у ребенка
может вызвать субтотальную обструкцию дыха-
тельных путей.
При наличии обтурирующей грануломы исполь-
зование старых методов деканюляции, таких как
переход на трубку меньших размеров или с не-
сколькими отверстиями, а также временная окклю-
зия трубки, является лишь пустой тратой времени,
а иногда может быть и опасным. Если имеется
обструкция просвета, го никакие попытки деканю-
ляции не удаются до тех нор, пока обструкция не
устранена. В тех же случаях, когда проходимость
дыхательных путей не нарушена, трубка удаляется
легко.
Внутрипросветная гранулома может быть удале-
на без сложностей путем эндоскопической резек-
ции с помощью детского уретрального резектоско-
па (рис. 16-1), а иногда и того проще — используя
экстракцию полипоидной массы грануломы через
стому с проведением, если необходимо, небольшого
гемостаза. Эту процедуру следует осуществлять
под эндоскопическим контролем.
Более сложно лечить посттра хвостом и ческу ю
обструкцию, связанную с коллапсом трахеи на
вдохе в результате нестабильности передней ее
стенки. Иногда приходится даже хирургическим
путем ушивать трахеостомическое отверстие во-
круг внутренней трубки, которую оставляют на
месте до того, как рана начнет закрываться (24—
48 час). В более тяжелых случаях локальной тра-
хеомаляции или деформации хрящей необходимо
использование какого-либо из методов реконструк-
ции трахеи, описанных ниже. Передняя пластика
трахеи со вставкой из хрящевого трансплантата
эффективно восстанавливает деформированную
или нестабильную трахеальную стенку, придавая
ей прочность.
Хирургическое лечение подсвязочного стеноза.
Дилатация и инъекция стероидов. Дилатация
стенозированной гортани жестким бронхоскопом
или бужами была в прежние времена основным
методом лечения. Она и до сих нор довольно часто
эффективна при легких стенозах или обтурации
мембранозными перегородками, но, как правило,
безуспешна в большинстве случаев выраженных
фиброзных стриктур. Некоторые дети тяжело по-
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ 191
реносят бужирование, которое проводится порой
месяцами и годами, но при этом с минимальным
эффектом.
Для смягчения рубца и усиления эффекта бужи-
рования предложена инъекция стероидов непосред-
ственно в зону стеноза. И хотя не было планомер-
ных целенаправленных исследований относитель-
но местного и общего их применения, однако
многочисленные клинические сообщения подтвер-
ждают несомненную эффективность этого метода
при использовании его в сочетании с бужировани-
ем 9 либо с бужированием и применением расширя-
ющих трубок-протезов (стентов),’0 а также в ком-
бинации с эндоскопической резекцией.11
В сочетании с бужированием или различными
типами резекции, при подсвязочных стенозах ис-
пользуются многообразные внутрипросветные рас-
ширяющие трубки-протезы. В зависимости от об-
стоятельств и опыта хирурга это может быть Г-сю-
разная трубка Монтгомери или килевидная из
силастика, «швейцарский цилиндр» Эванса, стент
Aboulker и т. д. В качестве кратковременных стен-
тов применялись и обычные эндотрахеальные
трубки, хотя они сами по себе могут вызывать
повреждение, которое приводит к стенозу.
Независимо от вида стента, образование вокруг
него грануляционной ткани представляет иногда
достаточно серьезную проблему, часто требуя по-
сле его удаления эндоскопической резекции грану-
ляций. При использовании любого протеза бывают
как успехи, так и неудачи. Что касается продолжи-
тельности его пребывания в трахее, то рекомендуе-
мые сроки колеблются от 3 недель до 13 месяцев.
Осложнения возникают нередко и довольно серь-
езные.
Расщепление перстневидного хряща. В тех
случаях, когда из-за подсвязочного отека, наличия
грануляций или изъязвлений попытки эндотрахе-
алыюй экстубации оказываются безуспешными,
в качестве альтернативы трахеостомии у грудных
детей может быть использован метод расщепления
перстневидного хряща, рекомендованный Cotton
и Seid в 1980 г. Разрез при этом проводится через
перстневидный хрящ и два вышерасположенных
кольца трахеи.13 После первой публикации показа-
ния к этому вмешательству и объем операции рас-
ширялись. В одном из исследований сообщалось о
17 (из 26) успешных случаях эндотрахеальной эк-
стубации после переднего расщепления перстне-
видного хряща. Возрасг больных был от 6 до
9 мес. Достигнутое увеличение диаметра трахеи
поддерживалось после операции с помощью проте-
за в течение 7—26 дней. Эта процедура доста-
точно проста и стоит о ней помнить как об аль-
тернативе трахеостомии при легких подсвязочных
стенозах.
Электрохирургическая и лазерная резекция.
Метод прямой внутрипросветной резекции подсвя-
зочного стеноза привлекателен по своей идее, но
практическое его применение ограничено опреде-
ленными видами сужений. Так, данный способ ред-
ко эффективен в случаях прогрессирующих проли-
феративных стенозов, а при выраженных сужениях
(толщина стенки >2 мм) после резекции часто
образуются рубцы. В то же время стенозирующие
перегородки из рубцовой ткани, относительно тон-
кие (<С 1—2 мм) и зрелые, часто хорошо подда-
ются внутрипросветной резекции.
Наш собственный опыт прямой резекции пока-
за 1, что наиболее обнадеживающие результаты да-
ет электрохнрургическая техника в виде повтор-
ных кратковременных сеансов высокочастотного
тока с использованием петлевого электрода от дет-
ского уретрального резектоскопа.15 Длительность
воздействия тока необходимо свести к минимуму,
а коагулирующий ток применяться вообще не дол-
жен. Вентиляция, проводимая через ирригацион-
ный канал эндоскопа, обычно вполне достаточна
для поддержания нормальной сатурации О2, разу-
меется, если вмешательство осуществляется квали-
фицированно и быстро. Непосредственно на время
резекции кислород должен быть отключен.
Резекция лазером — один из возможных методов
лечения, используемый в тех случаях, когда зона
поражения доступна для воздействия луча угле-
кисло того лазера. Однако применение гибких во-
локонных световодов ограничивается невозмож-
ностью пропускания через иих лазерного излучения
с той длиной волны, которая в таких ситуациях
наиболее эффективна благодаря деструктивному
ее действию. А лазерные лучи с волнами того диа-
пазона. который можно применять через гибкие
моноволоконные световоды, не эффективны для
этих целей. Нет сомнений, что в будущем техниче-
ски усовершенствованный лазер с простым воло-
конным концевым манипулятором может стать ме-
тодом выбора для внутрипросветной резекции.
Небольшие перегородки и ограниченные стено-
зы. если просвет при этом не меньше 4 мм, могут
быть резецированы без предварительной защитной
трахеостомии. Резецировать нужно по квадрантам
(четверть окружности), чтобы избежать слишком
большого отека за один раз. Мы считаем также,
что не следует производить резекцию сзади по
средней линии. В случаях осложненных стенозов
необходимо до резекции наложить защитную тра-
хеостому. Если предполагается резекция лазером,
трахеостомическая трубка должна быть металли-
ческой или вделанной в металлическую «обшив-
ку», чтобы предупредить случайное воспламе-
нение.
В нашей клинике электрохирургическая резек-
ция при стенозах с последующей инъекцией стеро-
идов оказалась эффективной и позволила успешно
деканюлкровать 30 из 38 больных, у которых при-
менялся только этот метод. Длительность лечения
колебалась от 2 месяцев до 3 лет (в среднем
9 мес). У 18 других пациентов после первичного
эндоскопического обследования и оценки были
применены иные методы — от простого бужирова-
ния с инъекцией стероидов до резекции лазером,
разреза перстневидного хряща и трахеи со встав-
кой трансплантата, а также сегментарной резек-
ции стенозированной трахеи с анастомозом ко-
нец-в-конец.*6
При ранних полсвязочных стенозах эндоскопи-
192 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
ческая резекция — основной метод лечения, ус-
пешность применения которого зависит от опыта
и квалификации хирурга, а также от его индивиду-
ального выбора. Мы можем с уверенностью ска-
зать, что в наших руках данный метол эффективен
в большинстве, но, конечно, не во всех случаях
обструкции верхних дыхательных путей.
Открытая резекция подсвязочного стеноза
требует хорошего, достаточно широкого доступа
вертикальным срединным разрезом через верхние
отделы трахеи, перстневидный и нижнюю часть
щитовидного хряща. По возможности верхний
край разреза должен быть ниже передней комиссу-
ры голосовых связок.
Для увеличения диаметра перстневидного хряща
и верхних отделов трахеи применяются трансплан
тэты в виде вставок. С этой целые используются
трансплантаты из подъязычной кости (на ножке
или свободные), а также из щитовидного или ре-
берного хряща.
Если сужена лишь передняя часть просвета пер-
стневидного хряща, хорошие результаты даег ис-
пользование хрящевого трансплантата, вставлен-
ного между краями ларинготрахеального разреза.17
Cotton считает эффективным применение транс-
плантата из реберного хряща, располагаемого при
пересадке таким образом, чтобы надхрящница бы-
ла обращена в просвет трахеи. Разрез начинают
с верхних двух или трех трахеальных хрящей
и продолжают через передний отдел перстневидно-
го и нижнюю треть щитовидного хряща. Края
трансплантата надсекают, чтобы предупредить
вворачивание его вовнутрь и смещение в просвет.
Предпочтение отдастся узловым швам рассасыва-
ющейся мононитью, что способствует предотвра-
щению образования в последующем гранулом. Для
увеличения диаметра просвета открытая резекция
рубца («холодным ножом» или лазером) может
применяться в сочетании с трансплантацией. Од-
нако при этом необходимо сводить к минимуму
размеры поверхности трахеи, подвергающейся во
время операции травмированию.
Ларииготрахеопластика. Тяжелые стриктуры
с рубцеванием по всей окружности требуют разде-
ления перстневидного хряща как спереди, так
и сзади. Во время этой манипуляции нужно быть
очень осторожным, чтобы нс повредить пищевод
или возвратный нерв на латеральной стороне зад-
ней поверхности перстневидного хряща. Хрящевые
трансплантаты вставляют в оба дефекта, чтобы
раздвинуть два образовавшихся С-образных сег-
мента перстневидного хряща и увеличить размер
просвета в горизонтальной плоскости.18 Принципи-
альная схема ларинготрахеопластики представле-
на на рисунке 16-2.
ПОРАЖЕНИЕ ТРАХЕИ
Аномалии
Атрезия трахеи. Дети с атрезией трахеи часто
рождаются живыми, но быстро умирают. Если
бронхи или недоразвитая дистальная часть трахеи
связаны с пищеводом, это может на какое-то время
обеспечить минимальную вентиляцию. Гортань,
как правило, сформирована нормально до уровня
перстневидного хряща, где она заканчивается сле-
по, поскольку трахея дальше отсутствует. Попыт-
ки интубации через голосовые связки безрезуль-
татны из-за обструкции, исключая те случаи, ког-
да имеется задняя расщелина гортани, которая
позволяет трубке пройти в пищевод. Все предпри-
Рис. 16-2. Операция ларинготрнхеонластики с интерпозицией в переднюю стейку трахеи реберно-хрящевого трансплантата (А, В,
С). Тяжелые стенозы, занимающие всю окружность, требуют применения хрящевых вставок как спереди, так и сзади, на уровне
перстневидного хряща (D).20
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ 193
н имевшиеся до настоящего времени немногочис-
ленные попытки реконструкции с созданием дыха-
тельных путей из пищевода были безуспешными.
Трахеомаляция представляет собой «размягче-
ние» трахеальной стенки, вызванное неправиль-
ным формированием хрящевых колец, которые,
создавая в норме каркас трахеи, удерживают ее
просвет открытым. Первичная трахеомаляция, не
связанная с какими-либо видами наружного сдавле-
ния — чрезвычайно редкая патология. В большин-
стве клинических наблюдений имеется вторичная
трахеомаляция, причина которой — давление сна-
ружи иа формирующиеся хрящи в процессе внут-
риутробного их развития.
В норме трахеальные кольца изогнуты подобно
букве С, обращенной выпуклостью кпереди. Кон-
цы хряща почти прилежат друг к другу и соедине-
ны мягкотканным мостиком, образующим заднюю
трахеальную стенку. Когда С-образный хрящ ста-
новится выпрямленным и окружность образуется
в основном за счет мягкотканной задней стенки,
просвет дыхательных путей оказывается менее
стабильным и, что очень важно и неблагоприятно,
диаметр его меняется параллельно колебаниям
давления на вдохе и выдохе.
Сдавление трахеи пищеводом. Чаще всего
встречающаяся вторичная трахеомаляция различ-
ной степени тяжести обычно сочетается с атрезией
пищевода, слепо заканчивающийся верхний сег-
мент которого в процессе развития сдавливает зад-
ние отделы дыхательных путей, в результате чего
и развивается трахеомаляция на протяжении, со-
ответствующем длине верхнего сегмента. При тя-
желой деформации трахеальных колец мягкая зад-
няя стенка грудной части трахеи может во время
выдоха прилегать к распрямленной передней стен-
ке, препятствуя движению воздуха, что объясняет
появление странного лающего звука на выдохе
и выраженного респираторного дистресса. Даже
обычное прохождение пищи вниз по пищеводу мо-
жет вызвать славление трахеи сзади и дыхатель-
ные расстройства.
Состояние большинства детей с симптомами тра-
хеомаляции, сочетающейся с атрезней пищевода,
со временем и развитием дыхательных путей улуч-
шается. Однако в некоторых случаях клинические
проявления настолько тяжелы, что оправдывают
применение операции фиксации дуги аорты к гру-
дине. Наличие фиброзных тканей, связывающих
большие сосуды и трахею, позволяет путем фикса-
ции дуги аорты подтягивать вперед и стенку тра-
хеи и тем самым поддерживать ее просвет откры-
тым, противодействуя таким образом давлению пи-
щевода сзади. В тяжелых случаях, когда операция
фиксации неэффективна, Filler предложил исполь-
зовать наружное протезирование трахеи.19 Олиако
применение этого метода остается весьма ограни-
ченным.
Сосудистые кольца. Сдавление трахеи при
врожденных аномалиях дуги аорты хорошо изве-
стно как причина стридора, приступов цианоза,
рецидивирующей инфекции верхних дыхательных
путей и дисфагии.
Сосудистые кольца могут в процессе развития
вызывать сдавление трахеи по всей ее окружности,
что порой приводит к трахеомаляции в результате
размягчения хряща и утраты им нормальной фор-
мы или к фиксированному хрящевому стенозу тра-
хеи, при котором иногда трахеальные хрящи име-
ют вид полностью замкнутых колец. При анома-
лии, представляющей собой двойную дугу аорты,
вокруг верхней части пищевода и трахеи образу-
ется плотное полное сосудистое кольцо. Этот по-
рок дает, как правило, наиболее яркую по сравне-
нию со всеми другими сосудистыми аномалиями
клиническую картину. Неполные кольца обычно
проявляются менее выраженными симптомами. Не
все подобные случаи требуют хирургической кор-
рекции. Сдавление дыхательных путей иногда вы-
зывается безымянной артерией при аномальном ее
отхождении от дуги аорты, поскольку артерия при
этом перекидывается через трахею. При правосто-
ронней дуге аорты и левосторонней нисходящей ее
части трахея может сдавливаться спереди левой
подключичной и сонной артерией.20
Лечение трахеомаляции, связанной с сосудисты-
ми кольцами, заключается в устранении причины
стеноза. Однако остающаяся после этого нестабиль-
ность мягких дыхательных путей может потребо-
вать допоинитсльной коррекции — передней фик-
сации трахеи или каких-либо иных методов внут-
реннего или наружного укрепления ее каркаса.
Трахеальный стеноз иногда связан с синдромом
петли легочной артерии, когда этот сосуд отходит
аномально высоко от правой легочной артерии
и идет затем между трахеей и пищеводом к левому
легкому. При этом нередко отмечается формирова-
ние полных хрящевых колец. Коррекция в таких
случаях заключается в транспозиции легочной ар-
терии и резекции трахеи. Лечение фиксированных
стриктур трахеи описывается ниже.
Синдром петли аномальной левой легочной ар-
терии существует в двух вариантах. У больных
1-й группы симптомы трахеальной компрессии
обусловлены лишь сосудистым сдавлением, а со-
ответственно оперативное лечение ограничивается
разделением и реанастомозом аномального сосуда.
Этого вмешательства однако недостаточно у паци-
ентов 2-й группы (5 больных из четырех учрежде-
ний), которые кроме сосудистой петли имеют еще
и трахеальный стеноз на значительном протяже-
нии, вызванный полными О-образными хрящевы-
ми кольцами трахеи.21 Устранение в такой ситуа-
ции только сосудистой аномалии не приводило
к ликвидации респираторных нарушений. Если до
операции диагностирована первичная патология
трахеи, то рекомендуется одновременная коррек-
ция как сосудистого, так и трахеального компо-
нента стеноза.
Врожденные трахеальные стенозы, описанные
в 1964 г. (на основании анализа 24 случаев),22
встречаются в трех основных вариантах: (1) диф-
фузная генерализованная гипоплазия (30%), (2)
воронкообразный (20%) и (3) сегментарный сте-
ноз (50%).23 Последний вид может локализоваться
примерно с одинаковой частотой в подперстневид-
13 Заказ № 1622
194 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Рис. 16-3. Верхний ряд — три типа трахеальных стенозов, описанных Кантреллом: генерализованная гипоплазия, воронкооб-
разный и сегментарный стеноз. Ннжний ряд — варианты анатомии кольца-петлн левом легочной артерии.21’22
ной области, центральном отделе трахеи и над ка-
риной (рис. 16-3).
Приобретенные обструкции трахеи
Обструкция в результате аспирации инородных
тел. Инородные тела, которые проходят через гор-
тань, обычно застревают в одном из бронхов, а по-
тому редко вызывают жизнеопасную гипоксию или
полную обструкцию дыхательных путей. Однако
в редких случаях предметы значительных разме-
ров, проникнув через узкий просвет перстневидно-
го хряща, оказываются слишком большими, чтобы
дальше пройти в бронх. Возникающая в результа-
те обтурация трахеи жизненно опасна и нс может
быть устранена без крикотиреотомии или трахе-
остомии. В таких ситуациях лучшим способом эк-
стренной помощи является трансназальная или
трансоральная интубация с форсированной венти-
ляцией (в надежде на то, что воздух будет прони-
кать вокруг инородного тела), которую следует
проводить до тех пор, пока ребенок не будет до-
ставлен в соответствующее учреждение, где есть
жесткий бронхоскоп и все необходимое оборудова-
ние для оказания квалифицированной помощи.
Большинство инородных тел бронхов не вызыва-
ют тяжелых клинических проявлений, если только
они не находятся там длительное время и в резуль-
тате нс осложнились вторичной инфекцией и пнев-
монией. Поэтому эндоскопическое их удаление —
не столь срочная процедура и может быть отложе-
но как минимум до тех пор, пока не опорожнится
желудок, что уменьшит вероятность аспирации во
время анестезии. Мы удаляли кусочки арахиса, об-
турировавшие бронх, через 3 месяца после аспира-
ции. Часто обтурация инородным телом диагности-
ровалась лишь через 3—10 дней после его попада-
ния в дыхательные пути.
У ребенка с инородным телом бронха обычно
имеются признаки частичной обструкции, проявля-
ющейся затрудненным шумным хрипящим дыхани-
ем на выдохе. Тотальная обтурация бронха вызы-
вает ателектаз соответствующего сегмента легкого
и смещение средостения в сторону поражения. Од-
нако многие инородные тела, застревающие в
бронхе, дают возможность воздуху проходить во-
круг них в обоих направлениях. Рентгенологиче-
ские данные в таких случаях минимальны, а порой
и вовсе отсутствуют. Показания к бронхоскопии
часто целиком основываются на анамнезе, в кото-
ром есть указание на внезапное появление удушья
и кашля во время еды (чаще всего орехов). Сохра-
няющиеся одышка и кашель или необъяснимая ли-
хорадка вслед за подобным эпизодом оправдывают
проведение бронхоскопии, даже при отсутствии па-
тологии на рентгенограммах.
Обычная рентгенограмма грудной клетки редко
помогает в диагностике инородного тела бронха.
Для более достоверного выявления смещения сре-
достения и задержки пассажа воздуха должны
быть сделаны снимки на вдохе и выдохе или про-
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ 195
ведсно обследование средостения под контролем эк-
рана. По нашим данным, при наличии в анамнезе
указаний иа попадание инородного тела и полном
отсутствии рентгенологических проявлений мы об-
наруживали инородные тела в 60% случаев.
Посттрахеостомический стеноз трахеи.
Причиной стеноза трахеи на месте трахеостомы
являются обычно технические погрешности при ее
наложении. Иссечение хряща или его некроз в ре-
зультате давления, когда стома сделана слишком
маленькой, может вызвать нестабильность или кон-
трактуру передней стенки. Узость стомы ведет так-
же к фиксированной внутренней деформации рас-
положенного выше кольца трахеи, что связано
с давлением от трубки. Это осложнение часто воз-
никает в тех случаях, когда делается поперечный
разрез трахеи маленького диаметра.
Некоторые стенозы на месте трахеостомы корри-
гируются путем разреза трахеи и вставки из хря-
щевого трансплантата. При тяжелых стриктурах
рациональнее производить сегментарную резек-
цию с анастомозом конец-в-конец.
Постинтубационный стеноз» Повышенное
давление от баллонной манжетки на трахеостоми-
ческой или эидотрахеальной трубке может вызвать
некроз трахеальной стенки, что приводит к стрик-
туре в шейном или верхнегруцном отделе трахеи.
К. счастью, такие «манжеточные* стриктуры стали
редкими с введением в клиническую практику ман-
жеток с большим объемом, но низким давлением.
Именно этот вид повреждений стимулировал раз-
витие техники трахеальных резекций. В подобных
ситуациях операцией выбора является резекция
с прямым анастомозом.
Наружная травма и ингаляционные поврежде-
ния. Травматические повреждения, хотя и являют-
ся преобладающей причиной смерти в детском воз-
расте, однако редко вызывают стеноз дыхательных
путей. К развитию сужения может привести нерас-
познанная травма трахеи или бронха. Прямое
краш-повреждение, а также проникающее ранение
гортани или трахеи иногда происходят при авари-
ях, связанных с роликовыми досками, мопедами,
снегоочистительными и другими машинами. Выбор
метода лечения определяется протяженностью и
локализацией поражения соответственно принци-
пам, изложенным ниже. Наиболее серьезное по-
вреждение дыхательных путей возникает при тя-
желых ингаляционных ожогах. Реконструкция при
этом бывает очень сложной, а результаты ие вызы-
вают оптимизма.
Наружное сдавление кистами и опухолями.
Кисты и опухоли средостения могут вызвать у де-
тей любого возраста наружное сдавление дыха-
тельных путей. В переднем средостении обычно
локализуются тератомы, значительно реже — опу-
холи, исходящие из вилочковой железы. В цент-
ральном средостении чаще всего располагаются
у грудных детей бронхогенные кисты, а у паци-
ентов старшего возраста—лимфомы. Сдавление
дыхательных путей лимфомой требует особой
срочности в лечении, поскольку тля этих образова-
ний характерен быстрый рост. В заднем средосте-
нии дыхательные пути могут сдавливаться нейро-
генными опухолями и нейроэнтеральными киста-
ми, располагающимися, как правило, у выхода из
грудной клетки. Лимфангиомы или гемангиомы
встречаются в любом отделе средостения, а иногда
занимают его целиком, но они редко вызывают
сдавление дыхательных путей.
Лечение обструкции дыхательных путей заклю-
чается в удалении образования, вызывающего на-
ружное сдавление. Описание деталей не входит
в задачи данной главы (см. главу 20).
Диагностика структурных аномалий
Прямые методы лучевой диагностики. Контраст-
ная рентгенография верхних отделов, желательно
с увеличением, плюс обследование под контролем
экрана с ЭОПо.м в двух проекциях дают достаточ-
но четкую информацию о состоянии дыхательных
путей ребенка. Протяженность сужения может
быть точно измерена с помощью КТ, но лучшим
методом, занимающим ведущее место в диагности-
ке, безусловно, является ядерный магнитный резо-
нанс (ЯМР), несомненные достоинства и преиму-
щества которого — лучи высокого качества, отсут-
ствие ионизирующей радиации и неинвазивность
процедуры.1
Бронхографии старались в прошлом избегать,
считая ее опасным методом и небезосновательно,
поскольку раньше применялись гиперосмолярные
контрастные вещества. Однако в настоящее время,
с появлением новых, водорастворимых, неосмоти-
ческих контрастных препаратов, этот метод стал
достаточно безопасным. Бронхография высоко ин-
формативна в диагностике обструкции дыхатель-
ных путей, тем нс менее ее не следует применять
у детей, находящихся в крайне тяжелом состоянии.
Бронхоскопия — очень ценный и точный метол
диагностики трахеальных стенозов. При резко вы-
раженных стриктурах бронхоскоп не следует про-
водить через зону сужения, если не планируется
одновременное корригирующее вмешательство,
ибо неразумные, неосторожные бронхоскопические
манипуляции могут резко усугубить острую об-
струкцию.
Дополнительные методы обследования. Эзо-
фагография с барием может быть применена в ка-
честве предварительного метода обследования, по-
зволяющего выявить косвенные признаки сдавле-
ния, связанного с сосудистой аномалией. Кривая
инспираторно-эксп ираторного потокового объема
помогает определить состояние функции легких.
При подозрении на сосудистое кольцо показано
УЗИ сердца и иногда ангиография.
Хирургические вмешательства
и результаты
Общие принципы. Не все случаи врожденного
и приобретенного трахеального стеноза требуют
хирургического вмешательства. Выбор метода ле-
196 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
чения зависит от степени сужения. Опыт показы-
вает, что поражения, которые ранее считались нс-
корригируемыми, в настоящее время успешно из-
лечиваются хирургическим путем, а показания
к резекции или пластической реконструкции тра-
хеи неуклонно расширяются.
Вряд ли есть необходимость объяснять, насколь-
ко важно обеспечение во время оперативного вме-
шательства адекватной вентиляции легких. До
операции заранее должны быть приготовлены до-
полнительный стерильный дыхательный контур,
запасной наркозный аппарат и все необходимое
для высокочастотной струйной вентиляции. В бо-
льшинстве случаев сегментарной резекции венти-
ляция может быть надежно обеспечена путем вре-
менной интубации дистальных отделов трахеи или
бронха через операционную рану до тех пор, пока
не начнется наложение швов анастомоза При рез-
ко выраженных стенозах рекомендуется примене-
ние струйной вентиляции, что исключает необхо-
димость рискованной в такой ситуации форсиро-
ванной дилатации до введения в наркоз. Для
проведения струйной вентиляции тонкий катетер
проводится через зону стеноза и остается на месте
до и во время резекции. Применение особо слож-
ных методов резекции и пластической реконструк-
ции трахеи может потребовать экстракорпорально-
го кровообращения, которое в данной ситуации
наиболее рационально.
Стандартные разрезы для реконструкции трахеи
показаны на рисунке 16-4. Нижний поперечный
шейный доступ наиболее удобен для коррекции
большинства постинтубационных стенозов трахеи
и некоторых высоких врожденных стриктур сег-
ментарного характера. Низкие врожденные стено-
зы обычно требуют либо стернотомии, либо ниж-
него шейного воротникового разреза, дополненно-
го верхней стернотомией. Доступ к сегментарным
стенозам, локализующимся возле или ниже кари-
ны. может быть лучше всего обеспечен заднебо-
ковой торакотомией.
Фиксация трахеи. Фиксация передней стенки
трахеи, направленная на устранение ее коллапса,
связанного с трахеомаляцией, осуществляется пу-
тем подшивания дуги аорты к подлежащей поверх-
ности грудины. Доступ может быть как через раз-
рез спереди в третьем межреберье слева, так и пу-
тем частичного расщепления грудины с продолже-
нием разреза в третье межреберье. Доли тимуса
должны быть отделены и отведены или частично
удалены. Дугу аорты фиксируют к грудине нерас-
сасываюшнмися швами, которые накладывают на
аорту около отхождения от ее дуги безымянной
и левой общей сонной артерий. Швы могут быть
наложены непосредственно на стенку аорты или
на предварительно подшитую к ней дакроновую
заплату. Следует избегать разделения аорты и
трахеи, дабы не разрушить соединительнотканную
«подвешивающую связку» трахеи («suspensory li-
gamentum»).
Показанием к этой операции являются повторя-
ющиеся приступы апноэ, связанные с коллапсом
Рис. 16-4. Техника резекции сегментарного трахеального стеноза (объяснения в тексте) В зависимости от локализации суже-
ния применяются различные доступы: поперечный шейный, верхняя стернотомия, правый заднебоковой или комбинированный.
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ 197
Рис. 16-5. Варианты опубликованных с
1980 г. случаев успешном резекции трахеальных стенозов у маленьких детей.29, 33
трахеи. Клинически результаты операции хоро-
шие, однако она не применяется широко, и коли-
чество опубликованных случаев остается Небо-
26, 2Т
льшим.
Резекция трахеи. Сегментарная резекция тра-
хеи с анастомозом конец-в-конец принята боль-
шинством хирургов как метод выбора при лечении
ограниченных стенозов (2—5 колец).28 Схема слу-
чаев успешной резекции у грудных детей пред-
ставлена на рисунке 16-5. Желательно, чтобы ана-
стомоз накладывался в пределах относительно
нормальной ткани трахеи. У грудных детей про-
изводились и более обширные вмешательства,36 од-
нако сегментарная резекция более 5 колец невоз-
можна у детей ни в каком возрасте. Лечение боль-
ших по протяженности врожденных аномалий
и некоторых ожоговых стенозов трахеи осуществ-
ляется с применением методов пластики трахеи.
Передняя поверхность трахеи при адекватном
доступе может быть обнажена при необходимости
от перстневидного хряща до карины. Следует со-
блюдать большую осторожность для сохранения
неповрежденными латеральных сосудов. Первона-
чально выделение по всей окружности (на длину
не более 1—2 см, чтобы сохранить кровоснабже-
ние трахеи) должно быть начато непосредственно
ниже стеноза, где ткани наиболее нормальные.
Любое выделение по заднебоковой поверхности
следует производить как можно ближе к стенке
трахеи, чтобы избежать повреждения возвратного
нерва.
Разделение трахеи начинают непосредственно
у зоны стеноза. Резекцию следует производить
максимально щадяще, однако по ее окончании по
краям разреза как проксимально, так и дистально
должны быть нормальные хрящевые кольца. Из-
лишнее удаление с любой стороны (сверху или
снизу) неизмененных иестенозированных участков
трахеи может быстро привести к рецидиву сте-
ноза.
Сначала накладывают 4 5 задних швов узла-
ми наружу, в эго время вентиляцию осуществляют
через отдельный наркозный контур. Трансларин-
гсальную эндотрахеальную трубку продвигают за-
тем вперед, после чего завершают анастомоз по
всей окружности наложением передних швов.
Предотвратить образование гранулемы — тяжело-
го осложнения, связанного с шовным материа-
лом, — можно путем применения синтетической
рассасывающейся мононити. Тракционные швы,
наложенные на среднюю часть трахеи с каждой
стороны не менее, чем на I см проксимальнее
и дистальнее анастомоза, завязывают по его завер-
шении с целью уменьшения натяжения по линии
швов. Очень полезно после операции у детей ис-
пользовать протезную скобу для поддержания го-
ловы и сгибания шеи. Мы не применяем тяжелые
грубые фиксирующие швы между подбородком
и передней грудной стенкой, которые рекоменду-
ются при резекциях трахеи у взрослых.37
Операции выделения (мобилизации) гортани (ти-
реоподъязычного 38 или супра подъязычного w) сле-
дует оставить на самый крайний случай, как послед-
ний шанс при тяжелых поражениях трахеи на боль-
шом протяжении. Фиксация гортани, послеопера-
ционная дисфагия и аспирация отмечаются после
обоих упомянутых вмешательств, но в большей
степени после тиреоподъязычного выделения. Дет-
ские хирурги предпочитают при обширных стено-
зах трахеи применять какой-либо из методов ее
пластики, чем делать резекцию на таком большом
протяжении, что наложение при этом анастомоза
требует освобождения гортани.
При низких стенозах трахеи следует избегать
трахеостомии, которая затрудняет в таких случаях
диагностику и лечение, препятствует увлажнению
газов, способствует инфицированию раны во вре-
мя реконструкции и отчасти ограничивает возмож-
ности мобилизации трахеи.
Методы пластики трахеи. Трахеопластика
обычно осуществляется путем разреза передней
стенки трахеи, длина которого соответствует про-
тяженности стриктуры, и расширения просвета ин-
терпозицией каких-либо тканей (рис. 16-6). Этот
метод применяется при обширных врожденных сте-
нозах. Иногда пластику трахеи следует предпо-
198 АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
честь резекции и при некоторых приобретенных
поражениях. Трансплантат, вшиваемый в разрез,
может быть представлен самыми разнообразными
тканями или материалами, включая реберный
хрящ, твердую мозговую оболочку, танталовую
сетку и кожу, перикард, а также комбинацию пери-
карда и реберного хряща. Делались попытки осу-
ществить и задний разрез трахеальных колец
с подшиванием в этот разрез передней стенки пи-
щевода. Опубликованы данные о трех подобных
вмешательствах, причем один из пациентов про-
40
жил после операции довольно долго.
Первая успешная реконструкция субтотального
стеноза трахеи у 12-месячного ребенка путем со-
здания полных трахеальных колец из трансплан-
татов была описана в 1982 г. Затем появились
сообщения еще о 3 пациентах, у которых был при-
менен этот метод. У первого больного на протяже-
нии 7 лет наблюдения не было отмечено никаких
заболеваний дыхательных путей. Ежегодное брон-
хоскопическое обследование выявило увеличение
просвета трахеи в процессе роста.41
Несмотря на успех первых операций хрящевой
пластики, более простым методом, впервые опубли-
кованным в 1984 г., все-таки является использова-
ние заплат из перикарда. Его результаты по срав-
нению с другими способами лечения тотальных
стенозов трахеи такие же, а иногда и значительно
лучше.42 Поддержание адекватного газообмена во
время операций облегчается при использовании
экстракорпорального кровообращения, хотя сто-
ронники метода хрящевых трансплантатов предпо-
читают интубацию дистальных отделов дыхатель-
ных путей или струйную вентиляцию. Послеопера-
ционные осложнения в виде симптомов, подобных
проявлениям трахеомаляции, могут быть сведены
к минимуму с помощью фиксации трансплантата
из безымянной артерии, который в свою очередь
фиксируют подшиванием к грудной стенке во вре-
мя закрытия грудины.41 Для придания создавае-
мому трахеальному каркасу еще большей стабиль-
ности использовалось вшивание комбинации хря-
щевых трансплантатов и заплаты из перикарда.
Однако существуют разногласия относительно це-
лесообразности добавления хряща к перикарду.
П ротезирование трахеи. У детей предприни-
мались попытки использования протезных мате-
риалов для формирования колец или сегментов
трахеальной стенки с целью обеспечения ее ста-
бильности и поддержания при сегментарной трахео-
маляции. У взрослых в течение короткого перио-
да времени также применялись протезные сегмен-
ты силиконовой трахеи.43 Однако в литературе
пока не было сообщений о замещении протезом
всей трахеи у детей.
ЛИТЕРАТУРА
1. Monroe CW, Ogo К: Treatment of micrognathia in the neonatal
period: Report of 65 cases. Plast Rcconstr Surg 50:317—325,
1972.
2. Booth JB, Birck JIB: Operative treatment and postoperative
management of saccular cyst and laryngocele. Arch Otolaryngol
107:500—502, 1981.
3. I.eikensohn JR, Benton C, Cotton R: Subglottic hemangioma.
J Otolaryngol 5:487—492, 1976.
4. Cotton RT, Richardson MA: Advances in head and neck surgery
in children. Head Neck Surg 3:424—437, 1981.
5. McCabe BF, Clark KF: Interferon and laryngeal papillomatosis.
Ann Otol Rhinol Laryngol 92:2—7, 1983,
6. Fogel JM, Berg IJ, Berger MA, et al.: Racemic epinephrine in the
treatment of croup: Nebulization alone versus nebulization with
intermittent positive pressure breathing. J Pediatr 101:1028—
1031, 1982.
АНОМАЛИИ И ОБСТРУКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ 199
7. Leipzig В. Oski FA, Cummings CW, et al.: A prospective rando
mixed study to determine the efficacy of steroids in the treat-
ment of croup. J Pediatr 94:194—196, 1979.
8. Parkin JL. Stevens MH, Jung AL; Acquired and congenital sub-
glottic stenosis in the infant- Ann Otol Rhinol Laryngol
85:573—581, 1976.
9. Gnanapragasam A: Intralcsional steroids in conservative mana-
gement of subglottic stenosis of the larynx. Int Surg 64:63—67,
1979.
10. Birck HG: Endoscopic repair of laryngeal stenosis. Trans Am
Acad Ophthalmol Otolaryngol 74:140—143, 1970,
11. O’Neill JA Jr: Experience with iatrogenic laryngeal and tracheal
stenoses. J Pediatr Surg 19:235—238, 1984.
12. Zalzal GH: Use of stents in laryngotracheal reconstruction in
children: indications, technical considerations, and complicati-
ons. Laryngoscope 98:849- 854, 1988.
13. Cotton RTr Seid AB: Management of the extubation problem in
the premature child. Ann Otol Rhinol laryngol 89:508—511,
1980.
14. Anderson GJ. Tom LW. Wetmore RF, ct al.: The anterior cricoid
split: the Children’s Hospital of Philadelphia experience. Ini
J Pediatr Otorhinolaryngol 16:31—38, 1988.
15. Johnson DG, Stewart DR: Management of acquired tracheal
obstructions in infancy. J Pediatr Surg 10:709—717, 1975.
16. Johnson DG: Tracheal stenosis in infants and children. In Fallis
JC. Filler RM, LeMoinc G (Editors). General Thoracic Surgery.
Elsevier, New York, 1991.
17. Colton RT: Pediatric laryngotracheal stenosis. J Pediatr Surg
19:699—704. 1984.
18. Cotton RT, Gray SI), Miller RP: Update of the Cincinnati expe-
rience in pediatric laryngotracheal reconstruction. Laryngoscope
99:1111—1116, 1989,
19. Filler RM. Buck JR, Bahoric A, Steward DJ: Treatment of seg-
mental tracheomalacia and bronchomalacia by implantation of
an airway splint. J Pediatr Surg 17:597—603, 1982.
20. Smith RJH, Smith MCF, Glossop I ,P, et al.: Congenital vascular
anomalies causing tracheoesophageal compression. Arch Otola-
ryngol 110:82—87, 1984.
21. Berdon WE, Baker DH, Wung JT. et al.: Complete cartilagering
tracheal stenosis associated with anomalous left pulmonary arte-
ry: tlie ring-sling complex. Radiology 152:57—64, 1984.
22. Cantrell JR. Guild HG: Congenital stenosis of the trachea. Am
J Surg 108:297 - 305, 1964.
23. Landing BH: Congenital malformations and genetic disorders of
the respiratory tract. (Larynx, trachea, bronchi, and lungs.) Am
Rev Respir Dis 120:151 185, 1979.
24. Vogl T. Wilimzig C. Bilan ink LT, ct al.; MR imaging in pediatric
airway obstruction. J Compul Assisi Tomogr 14:182—186,
1990.
25. Fletcher BD. Cohn RC: Tracheal compression and the innomina-
te artery: MR evaluation in infants. Radiology 170:103—107,
1989.
26. Schwartz MZ, Filler RM: Tracheal compression as a cause of
apnea following repair of tracheoesophageal fistula: Treatment
by aortopexy. J Pediatr Surg 15:842—848, 1980.
27. Cohen D: Tracheopexy—aortotracheal suspension for severe
tracheomalacia. Aust Paediatr J 17:117—121. 1981.
28. Grillo HC. Zannini P: Management of obstructive tracheal dise-
ase in children. J Pediatr Surg 19:414—416, 1984.
29. Harrison MR. Hcldt GP, Brasch RC, et al.: Resection of distal
tracheal stenosis in a baby with agenesis of the lung. J Pediatr
Surg 15:938 943, 1980.
30. Mansfield PB: Tracheal resection in infancy. J Pediatr Surg
15:79—81, 1980.
31. Mattingly WT Jr, Belin RP, Todd EP: Surgical repair of conge-
nital tracheal stenosis in an infant. J Thorac Cardiovasc Surg
81:738—740. 1981.
32. Weber TR, Eigen H, Scott PH, et al.: Resection of congenital
tracheal stenosis involving the carina. J Thorac Cardiovasc Surg
84:200—203, 1982.
33. Nakayama DK, Harrison MR. DcLonmicr A A, et al.: Reconst-
ructive surgery for obstructing lesions of the intrathoracic trac-
hea in infants and small children. J Pediatr Surg 17:854—868.
1982.
34. Minatu N, Itoh K, Ohkawa Y, et al.: Surgical treatment of con-
genital distal tracheal stenosis involving the carina. Ann Thorac
Surg 42:326—328, 1986.
35. Healy GB, Schuster SR, Jonas RA. McGill TJ: Correction of
segmental tracheal stenosis in children. Ann Otol Rhinol La-
ryngol 97:444—447, 1988
36. Longaker MT, Harris-on MR. Adzick NS: Testing the limits of
neonatal tracheal resection. J Pediatr Surg 25:790—792, 1990.
37. Grillo HC, Mathisen DJ: Surgical management of tracheal stric-
tures. Surg Clin North Am 68:511—524, 1988.
38. Dedo HII, Fishman NH: I aryngeal release and sleeve resection
for tracheal stenosis. Ann Otol Rhinol I aryngol 78:285 -296,
1969.
39. Loeff DS, Filler RM, Vinagrad I, el al.: Congenital tracheal
stenosis: A review of 22 patients from 1965 to 1987. J Pediatr
Surg 23:744—748, 1988.
40- Montgomery WW; Suprahyoid release for tracheal stenosis.
Arch Otolaryngol 99:225—260, 1974.
41. Tsugawa C, Kimura K, Muraji T. et al.: Congenital stenosis
involving a long segment of the trachea: Further experience in
reconstructive surgery. J Pediatr Surg 23:471—475, 1988.
42. Idriss FS, DeLeon SY, llbawi MN, et al.: Tracheoplasty with
pericardial patch for extensive tracheal stenosis in infants and
children. J Thorac Cardiovasc Surg 88:527—536, 1984,
43. Neville WE, Bolanowski PJP. Soltanzadch H: Prostlictic recon-
struction of the trachea and carina. J Thorac Cardiovasc Surg
72:525-538, 1976.
Глава 17
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ
АНОМАЛИИ
Каждый вит патологии, описанный в данной главе,
относительно редок, однако если взять их все вме-
сте, то эти аномалии достаточно часто встречают-
ся в практике детских хирургов. Пороки развития
бронхов и легких, представленные здесь, не вклю-
чают в себя аномалии, вызывающие обструкцию
дыхательных путей (глава 16), а также приобре-
тенные заболевания легких (глава 18). Различия
между пороками развития и приобретенными забо-
леваниями часто достаточно призрачны. Например,
кистозные образования могут быть врожденными,
но когда присоединяется инфекция, то выстилка из
псевдослоистого мерцательного цилиндрического
эпителия разрушается, и микроскопические при-
знаки, позволяющие провести дифференциальную
диагностику, исчезают. Кроме того, врожденные
кисты могут сообщаться с бронхами, что приводит
к образованию уровня жидкости с газовым пузы-
рем — признака, характерного для легочных абс-
цессов. Поскольку первичная передняя кишка яв-
ляется закладкой и легочной системы, и прокси-
мальных отделов желудочно-кишечного тракта
(ЖКТ), то не удивительно, что аномалии развития
легких и ЖКТ могут сочетаться и «пе-
реплетаться». Вот почему для определения таких
пороков, как секвестрация, кистозное удвоение пе-
редней кишки, дивертикулы пищевода, был пред-
ложен термин врожденные бронхолегочные анома-
лии передней кишки 1
Детальное описание процесса внутриутробного
развития легких и патогенеза кистозных аномалий
представляет интерес, но не имеет особого клини-
ческого значения, поэтому мы ограничимся здесь
лишь краткими сведениями из эмбриологии2 3
Врожденные пороки легких и бронхов, по-видимо-
му, являются результатом отклонений в развитии
на двух стадиях: (1) между 3-й и 6-й неделями
гестации, когда появляется дивертикул трахеи
в виде вентрального выступа на передней кишке
на уровне четвертого сомита, каудальное по отно-
шению к фарингеальным карманам (зачатки пра-
вого и левого легкого и их долей возникают не-
сколькими днями позже), и (2) между 6-й и 16-й
неделями, когда происходит быстрое деление брон-
хов дистальнее субссгменгарного уровня.2
Этот процесс определяет деление легочных по-
ражений, проявляющихся клинически, на кистоз-
ные и некистозные аномалии, с дальнейшим под-
разделением на врожденные и приобретенные.
Приобретенная патология включена в данную гла-
ву лишь в связи с тем, что се приходится диффе-
ренцировать с врожденной. Между кистозными
и некистозпыми аномалиями имеется существенное
сходство, зависящее в значительной мере от того,
чем заполнено образование — жидкостью или воз-
духом. Дифференциальная диагностика базируется
на клинических данных и является основой для
решения вопроса о характере лечения.
Это были шесть мужчин из Индостана
С жаждой знания, святой и неустанной.
Изучать Слона они явились утром райо.
Но смотрети на него немного странно.
Озирая все от неба до травы,
Так как были все незрячие, увы.
КИСТОЗНЫЕ АНОМАЛИИ
Врожденные аномалии
Бронхогенные кисты. Врожденные кистозные
аномалии обычно определяются термином бронхо-
генные кисты и могут быть по расположению цен-
тральными (около ворот легких или средостения)
или периферическими. Они возникают в результа-
те отделения (в процессе почкования и ветвления)
небольших групп клеток, которые превращаются
в изолированную нефункционирующую тканевую
массу. Если образовавшаяся киста расположена
центрально, го она, как правило, единичная и про-
текает бессимптомно, пока нс присоединяется ин-
фекция, что может привести к появлению крово-
харканья, температуры, кашля или к выделению
гноевидной мокроты. Эти образования обычно
округлой формы и при наличии сообщения с дыха-
тельными путями могут быть наполнены воздухом.
Если же такого сообщения пет, то кисты на рентге-
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ 201
Рис. 17-1. А. Бронхогенная, центрально расположенная киста соединена с бронхом, о чем говорит уровень жидкости. В, Соединения
с бронхом нет, поэтому киста заполнена только жидкостью. С, КТ кисты, показанной на рис. В.
нограммах грудной клетки выглядят как безвоз-
душные паренхиматозные образования. Кисты, на-
полненные и воздухом и жидкостью, проявляются
в виде уровней жидкости с газовыми пузырями
(рис. 17-1).
Лечение состоит в удалении кисты. При бессим-
птомном течении трудно бывает решиться на опе-
рацию, но всегда имеющаяся неблагоприятная пер-
спектива возможных тяжелых осложнений, кото-
рые нельзя ни прогнозировать, ни предотвратить,
вполне оправдывает хирургическое вмешатель-
ство. Подобно кистам щитовидно-подъязычного
протока и околоушным, легочные кисты могут ин-
фицироваться. Если при этом имеется сообщение
с бронхом, то быстрое увеличение напряженной
кнеты иногда приводит к острому развитию респи-
раторного дистресса и даже к пневмотораксу (рис.
17-2).4 Необходимость иссечения врожденных кист
основывается, кроме того, и на возможности их
озлокачествления, о чем имеются сообщения в ли-
тературе. ’
Периферические кисты образуются в результате
нарушения развития на 6—16-й неделе гестации
и, в противоположность центральным кистозным
образованиям, могут быть множественными и бо-
льшими. При наличии нескольких кист респира-
торный дистресс, иногда с летальным исходом,
возникает порой вскоре после рождения. Соедине-
ние с бронхом обычно характерно для перифери-
ческих кист с уровнями жидкости и газовыми пу-
зырями. Именно в подобных случаях особенно
быстро развивается инфекция. По данным рентге-
нологического обследования грудной клетки необ-
ходимо провести дифференциальную диагностику
с врожденной кисгоаденоматозной аномалией и да-
же с диафрагмальной грыжей, а при кистах, растя-
нутых воздухом, — с лобарной эмфиземой и напря-
женным пневмотораксом. Диафрагмальную грыжу
обычно можно исключить на основании анализа
клинических проявлений, а внимательная оценка
рентгенограмм грудной клетки позволяет отверг-
нуть диагноз пневмоторакса, для которого харак-
202 ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ
Рис. 17-2. Ai, Бронхогенная напряженная киста со смещением средостения и поджатым (кинзу) легким. В. Вид на операции
киста исходит из левой верхней доли.
терно наличие спавшегося легкого и острого, хоро-
шо определяемого реберно-диафрагмального угла,
в то время как легкое, славленное кистой или пе-
рерастянутой долей, проявляется затемнением ре-
берно-диафрагмального синуса.4 В тех случаях,
когда клинически трудно провести дифференци-
альную диагностику между лобарной эмфиземой,
напряженной кистой и большим кистоадсноматоз-
ным образованием, не следует для этого прилагать
героические усилия, поскольку все перечисленные
аномалии требуют хирургического вмешательства
по срочным показаниям. Радикальное удаление об-
разования обычно может быть осуществлено пу-
тем лобэктомии.
Первый сэр шагнул так близко, что о ляшку
Он ударился, упал и охнул тяжко.
Встал, пошарил по неровной твердой коже
И промолвил, первый опыт подытожив:
«Мне ясна природа этого Слона
Эго может быть забор или стена!»
Кистоаденоматозная аномалия представляет
собой образование, состоящее из множественных
кист в легочной ткани, в котором есть признаки
пролиферации бронхиальных структур за счет
альвеол. Кисты выстланы кубовидным или цилин-
дрическим эпителием. Эта патология скорее и в
большей степени относится к локальным легочным
дисплазиям, чем к гамартомам, поскольку во мно-
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ 203
Рис. 17-4. к, Кистоадсноматозная аномалия у но-
ворожденного ребенка. Симптомы респираторного
дистресса отмечались с самого рождения. На рент-
генограмме грудной клетки выявлены большие ки-
стозные полости. В. При данном варианте анома-
лии кисты меньших размеров, признаков респи-
раторного дистресса не было. С, Рентгенограмма
новорожденного ребенка, имевшего выраженный
респираторный дистресс С рождения. Поражение
легких явно кекистозного характера. Пл фоне реа-
нимационных мероприятий возник двусторонний
пневмоторакс, однако постепенно ребенок стаби-
лизировался настолько, что оказалось возможным
произвести лобэктомию нижней доля справа. Пре-
бывание в госпитале было длительным, а течение
очень тяжелым. В настоящее время ребенок чувст-
вует себя хороши, несмотря на то, что имеются
остаточные признаки бронхолегочной дисплазии.
гих случаях в стенках кисты обнаруживается ске-
летная мышечная ткань.7 В зависимости от морфо-
логических особенностей выделяются три типа
данной аномалии.8
Тип 1— единичные или множественные кисты
диаметром более 2 см, выстланные мерцательным
псевдослоистым цилиндрическим эпителием. Меж-
ду кистами могут располагаться тканевые элемен-
ты, напоминающие нормальные альвеолы.
Тип 11— множественные небольшие кисты ме-
нее 1 см в диаметре, выстланные мерцательным
(от кубовидного до цилиндрического) эпителием.
Между этими кистами могут находиться респира-
торные бронхиолы и растянутые альвеолы, в то
время как слизистые клетки и хрящ отсутствуют.
При данном варианте отмечается высокая частота
сочетанных врожденных аномалий.
Тип 111 — обширное поражение обычно некис-
тозного характера и нызывающее, как правило,
смещение средостения. «Бронхиолоподобные об-
разования с цилиндрическим кубовидным эпите-
лием разделены тканевыми структурами, имею-
щими размеры альвеол и выстланными немерца-
тсльным кубовидным эпителием» (рис. 17-3).8 При
этом варианте прогноз обычно неблагоприятный
(рис. 17-4).
Тип II и III чаще всего проявляются респира-
торным дистрессом в периоде новорожденности и,
как правило, сочетаются с другими тяжелыми
врожденными аномалиями,9 в то время как тип I
может протекать бессимптомно, аналогично муль-
тикистозному поражению. Важно своевременно
диагностировать эту аномалию, поскольку она
обладает тенденцией к инфицированию с жизнеуг-
204 ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ
рожающими осложнениями. При отсутствии инфи-
цирования компьютерная томография (К Г) выяв-
ляет множественные кисты с тонкими стенками.
В случае же инфицирования картина иная — ки-
стозные образования чередуются с тканевыми
структурами, четкие границы между ними отсутст-
вуют."
Лечение заключается в хирургическом иссече-
нии, в том числе и при бессимптомном течении.
Лобарная эмфизема представляет собой
«...постнатальное перерастяжение одной или не-
скольких долей гистологически нормального лег-
кого, возникающее в результате недосга точного
развития хрящей трахеобронхиального дерева».7
Существуют и другие определения данной патоло-
гии, в частности ее характеризуют как порок раз-
вития бронхов и альвеол с персрастяжснисм одной
или нескольких легочных долей. Согласно класси-
ческим представлениям, лобарная эмфизема явля-
ется врожденной аномалией, развивающейся в ре-
зультате бронхомаляции, которая вызывает об-
струкцию клапанного типа, когда воздух заполня-
ет нормально сформированную долю легкого, но
не выходит обратно." Данная патология представ-
ляет собой симптомокомплскс с множеством лежа-
щих в его основе причин.’2 Это поражение бывает
также приобретенным и наблюдается тем чаще,
чем больше маленькие дети подвергаются вентиля-
ции в течение длительного промежутка времени
Различные формы псрерастяжения доли легкого
могут встречаться как в сочетании с интерстици-
альной эмфиземой и бронхолегочной дисплазией,
так и без них.
Диагностика обычно не сложна. Очень важно
сделать КТ и определить вентиляционно-перфу-
зионные (V/Q) показатели для того, чтобы вы-
яснить, насколько адекватно ребенок может пе-
ренести оперативное вмешательство.13 В тех
случаях, когда эмфизема является врожденной
и отсутствуют очевидные признаки другой патоло-
гии легких, показана лобэктомия. В литературе
отмечается высокая часгога соче1аниых пороков
сердца (рис. 17-5).14 Эта комбинация аномалий мо-
жет потребовать срочной операции. У детей
с приобретенными формами лобарной эмфиземы
к выздоровлению может привести и консерватив-
ное лечение. Такие пациенты обычно находятся
в отделении интенсивной терапии и часто на вен-
тиляции с тщательным мониторингом. В подобной
ситуации селективная бронхиальная интубация со
«здоровой стороны» может «изолировать» пора-
женное легкое, ускорив таким образом выздоров-
ление.
У вториги было правило свое.
Он пошел другим, извилистым п\тсм
И, на бивень наскочив (на острие).
Закричал: «Имеем тело мы с копьем!
Это круглое и гладкое копье
Есть iiniii С тон. Вот мнение мое!»
Приобретенные аномалии
В неонатальном периоде, особенно у недоношен-
ных детей, находящихся (или находившихся! на
вентиляции, может возникнуть интерстициальная
эмфизема, лобарная эмфизема и паренхиматозные
кисты. Каждый из этих видов патологии способен,
как было отмечено ранее, спонтанно подвергнуться
обратному развитию, требуя лишь тщательного
наблюдения. Если поражение прогрессирует, вызы-
Рис. /7-5. А, Врожденная лобарная эмфизема. На рентгенограмме видно перерастяжение правой верхнее доля <ПВД>. Пыла про-
изведена правосторонняя верхняя лобэктомия. В, Растяжение правой средней доли (ПСД) со славлением ПВД и ИНД. У этого
ребенка был также дефект межжелудочковой перегородки и коарктация аорты.
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ 205
вая смещение средостения и сдавление легкого как
на «больной», так и на противоположной стороне,
показано хирургическое вмешательство. Диффе-
ренциальный диагноз с врожденными аномалиями
не сложен, поскольку приобретенные поражения
возникают пост натально у ребенка, находящегося
на вентиляции.
У детей грудного и старшего возраста кистоз-
ные поражения могут быть пост травматически-
ми, возникающими в результате травмы грудной
клетки, сопровождающейся ушибом легкого либо
разрывом паренхимы или бронха. Дифференциро-
вать с врожденными аномалиями помогает локали-
зация травматических кист в участках ушиба лег-
кого. Более правильно употреблять для определе-
ния этих образований термин травматические
легочные псевдокисты, поскольку они не имеют
эпителиальной выстилки.15 Экспериментальные
исследования показали, что в основе патогенеза
развития кистозного поражения лежит поврежде-
ние дыхательных путей, давление входящего в лег-
кие воздуха и нарушение эластичности легочной
паренхимы.16 При бессимптомном течении, когда
кисты не увеличиваются и не вызывают респира-
торного дистресса, можно ограничиться лишь тща-
тельным наблюдением, при этом, как правило, на-
ступает спонтанное выздоровление. В редких слу-
чаях присоединения инфекции может потребовать-
ся наружное дренирование и/или хирургическое
иссечение.17
Постинфекционные поражения легких приоб-
ретенного характера, такие как пневматоцеле на
фоне стафилококковой пневмонии, обсуждаются
в следующей главе, здесь лишь представлена диф-
ференциальная диагностика между пневматоцеле
и врожденной кистой. При пневматоцеле в анамне-
зе отмечается легочная инфекция с пневмониче-
ской инфильтрацией и возникновением в последу-
ющем полости с тонкой или даже вообще непро-
слеживаемой стенкой. Обычно такие полости не
содержат жидкости — только воздух (рис. 17-6)
и в большинстве с ту чаев подвергаются обратному
спонтанному развитию.
Третий сэр избрал примерно тот же путь.
Но попался ему в руки толстый шланг
(Слон решил привычно хоботом махнуть).
Ну и сэру мысль простейшая пришла;
*0, коллеги, на все сто уверен я —
Слон есть толстая и сильная змея!»
НЕКИСТОЗНЫЕ АНОМАЛИИ
На рентгенограммах некистозные аномалии обыч-
но имеют неправильную неокруглую форму. Симп-
томатика зависит от обширности поражения
легкого.
206
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ
Секвестрация легкого
В клинической практике распространено следую-
щее определение секвестрации легкого: «Кистоз-
ное образование нефункционирующей легочной
ткани, не имеющее явной связи с трахеобронхи-
альным деревом и получающее артериальное кро-
воснабжение целиком (или почти целиком) из ано-
мально развитых системных сосудов». ' Некото-
рые исследователи считают, что правильнее упо-
треблять термин спектр легочной секвестрации,
поскольку в литературе описаны самые разнооб-
разные варианты комбинаций системного и легоч-
ного артериального кровоснабжения и венозного
дренажа как нормальной, так и аномальной легоч-
ной ткани.19 Кроме того, (1) нормальная легочная
ткань может получать кровь из аномальных сосу-
дов системного происхождения, в то время как
(2) аномальная легочная ткань, подобная той, что
обнаруживается при секвестрации, может быть
и без аномального кровоснабжения.20 Многообра-
зие и количество описанных комбинаций этих ви-
дов поражений, включая и сочетанные с ними ано-
малии, такие как бронхогенные кисты, просто не-
сметно.21-23 Хотя основные клинические проявле-
ния секвестрации связаны с дыхательной системой,
однако выраженная симптоматика бывает и со сто-
роны сердца, что может быть обусловлено не толь-
ко сочетанным врожденным кардиальным пороком,
но и наличием мощных шунтов.23
При дальнейшем изложении секвестрация будет
подразделена на интралобарную, при которой
аномальная ткань находится внутри нормального
легкого, и экстралобарную, при которой секвест-
рированный участок отделен от нормальной легоч-
ной доли и расположен вне висцеральной плевры
(рис. 17-7). Описан также порок, определяемый
термином псевдосеквестрация
Интралобарная секвестрация прсимуществен-
но обнаруживается в нижних долях, наиболее ча-
сто слева, и в заднем базальном сегменте. Рентге-
нологические проявления разнообразье от затене-
ния до кистозного поражения паренхимы с уровня-
ми жидкости и воздушными пузырями. Аномаль-
ное кровоснабжение обычно представлено боль-
шим сосудом, отходящим от аоргы выше или ниже
диафрагмы. Часто не один, а несколько сосудов
подходят к секвестрированной ткани, а отток
обычно осуществляется через легочную вену, ино-
гда — в систему V. azygos.
Диагноз ставится при обнаружении в одной из
нижних долей образования, не меняющегося в ди-
намике. Некоторую помощь в диагностике может
оказать КТ. Однако наиболее ценный метод в та-
ких случаях — легочная или аортальная ангиогра-
фия, позволяющая четко установить диагноз, бла-
годаря выявлению аномальных сосудов. Данные
этого обследования, кроме всего прочего, очень
важны для хирурга, которому необходимо знать
локализацию сосудов во избежание их поврежде-
ния в процессе операции (рис. 17-8). Большинство
летальных исходов, связанных с оперативным вме-
шательством, возникает именно в результате кро-
вотечения из незамеченных аномальных сосудов.
Лечение заключается в лобэктомии пораженной
доли, хотя иногда (в редких случаях) можно обой-
тись сегментэктомией.24
Экстралобарная секвестрация представляет
собой поражение, локализующееся вне доли легко-
го. Диагноз устанавливается так же, как и при
интралобарном расположении. Если внедолевая
локализация не вызывает сомнений, и при этом
отсутствуют проявления со стороны сердечно-сосу-
дистой системы, лечение может быть консерватив-
ным, поскольку инфекция в таких случаях обычно
не возникает. Однако экстралобарная секвестрация
часто сочетается с другими аномалиями, особенно
с диафрагмальной грыжей. '
Интересное наблюдение описано у трех детей,
имевших дефект диафрагмы с выбуханием через
Рис. 17-7. Легочная секвестрация. Схема ано-
малии и локализации внутри легкого и вне
Висцеральной плевры.
Intralobar
Extralobar
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ 207
Рис. 17-8. А, Секвестрация у 9-.1стнсй девочки — интра попар-
ный тип с локализацией и нижней доле левого легкого. Течение
было бессимптомным, пока не наслоилась инфекция. В, КТ этой
же пациентки. С, Фиксированный препарат после нижнем ло-
бэктомии слева выраженная воспалительная реакция.
него части печени, что рентгенологически Симули-
ровало картину секвестрации (рис. 17-9).25 Данные
случаи лишний раз подчеркивают, что при пора-
жении нижней доли легкого справа, необходимо
производить радиоизотопное сканирование печени
или перитонсографию, которые позволяют четко
отдифференцировать эти виды патологии.
Обошел вокруг ноги четвертый сэр.
«Ха! — сказал он. Эго кажется игрой!
Слишком прост для нас решаемый пример.
Мы имеем дело с грубою корой.
Я ощупал сей предмет со всех сторон.
Это — дерево с названьем кратким „Слои*4*.
Артериовенозные аномалии
Почти у половины пациентов с артериовенозными
аномалиями отмечаются различные их проявления.
Классическая триада симптомов включает в себя
одышку при нагрузке, цианоз и утолщения паль-
цев. Цианоз возникает в связи с тем, что по мень-
шей мере 30% крови из правого желудочка прохо-
дит через фистулу без оксигенации, т. е имеется
шунт справа-налево. Клинически в проекции ано-
малии можно при аускультации обнаружить посто-
янный шум. Иногда появляются мозговые сосуди-
стые симптомы, причем абсцесс мозга при этом
пороке возникает пе менее часто, чем при врож-
денных заболеваниях сердца. Локализация анома-
лии вблизи плевры может привести к гемотораксу,
а прорыв в бронх — к массивному кровохарканью.
Рентгенологически данные пороки выглядят в виде
округлых или овальных образований различных
размеров, иногда неотчетливо разделенных на
дольки. При КТ грудной клетки выявляются ано-
мальные сосуды. Однако наиболее ценную инфор-
мацию даег ангиография (рис. 17-10). Среди боль-
ных с данными аномалиями часто встречаются
пациенты с болезнью Ослера-Вебера-Рандю (на-
следственная геморрагическая ангиома) — наслед-
ственным заболеванием, характеризующимся ге-
моррагическим синдромом, обусловленным мно-
жественными телеангиэктазиями кожи и слизи-
стых оболочек.3 Артериовенозные аномалии могут
быть множественными.
Лечение должно быть только хирургическим
и заключаться в лобэктомии или клиновидной ре-
зекции пораженной части легкого. Имеются сооб-
щения об успешной окклюзии шунта с использова-
нием катетеризационной эмболизации.26
Под общим термином «артериовенозные анома-
лии» объединены различные виды патологии,
а именно: саблевидный синдром, синдром гипоге-
208
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ
Рис, 17 9. А. Псевдисеквестрация. Кажется, что образование расположено о легком, на самом деле это эвентрация диафрг
с находящейся в грыжевом выпячнваннн печенью. В. На ангиограмме видно, что артерии окружают образование, ио нс пронш
в него.
незии легкого и врожденный венолобариый синд-
ром. Хоти название «саблевидный синдром» корот-
кое и не носит описательного характера, однако
именно этот термин используется наиболее часто.
Данный синдром включает в себя наличие умень-
шенного в размерах, неправильно сформировапно-
1*0 правого легкого, аномальный венозный возврат
от правого легкого в нижнюю полую вену и пороч-
ное артериальное кровоснабжение, обычно из си-
стемного круга кровообращения.3 Поскольку этот
синдром описан при многих аномалиях, трудно до-
статочно достоверно объяснить возникновение его
в эмбриогенезе. Правое легкое обычно неправк
но развито — в той или иной степени. Класс»
ским признаком аномального венозного дрен,
является серповидная (саблевидная) тень на pt
генограмме легких в центре правой нижней д<
Однако подобная типичная картина определи»
лишь в трети случаев. Аномальная вена инс
небольшая. Артериальное снабжение правого .
кого может быть обеспечено за счет легочной
системной циркуляции. Легочная артерия по
отсутствует или гипоплазировапа и тогда сие,
ное кровоснабжение осуществляется из груд
Рис. 17-10. К* Артериовенозные аномалии. На рентгенограмме видны двусторонние тени неправильной формы, клинически
культативио) проявляющиеся шумом. В. Ангиограмма выявила фистулы.
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ 209
аорты или даже от се отделов, расположенных ни-
же диафрагмы. Отмечается высокая частота (при-
близительно одна четвертая часть всех наблюде-
ний) сочетанных сердечно-сосудистых аномалий.5
Рентгенологически правая половина грудной
клетки небольшая но размерам, с высоким стояни-
ем купола диафрагмы и описанной выше сабле-
видной тенью. Катетеризация сердца и ангиогра-
фия помогают в установлении правильного диа-
гноза и в обнаружении аномальных артериальных
и венозных сосудов. Выбор метода лечения зави-
сит от вида порока. В классическом варианте ано-
мальную вену трансплантируют в левое предсер-
дие. иногда может потребоваться пневмонэктомия.
Пятый был весьма высок и потому
Дотянулся он до уха. Не в момент.
Методично, постепенно по всему
Уху долго шарил и сказал: «Брезент!
Я не знаю, для чего он здесь висит.
Но, как толстый веер. Слои имеет вид».
СМЕШАННЫЕ АНОМАЛИИ
Агенезия легкого
Односторонняя агенезия легкого совместима с
жизнью, но часто сочетается с тяжелыми врожден-
ными аномалиями, подобными тем, что встречают-
ся при VATER-синдроме (вертебральные пороки,
атрезия ануса, трахеопищеводный свищ, дисплазия
лучевой кости и почек).27 29 Нередко выявляются
и другие сопутствующие пороки. Предпринима-
лись попытки объяснить возникновение агенезии
легкого поражением в эмбриогенезе нервного
гребня.30
Различные вилы легочной агенезии наиболее
точно могут быть охарактеризованы следующим
образом: агенезия — полное отсутствие бронха
и легкого; аплазия — «недоразвитое» легкое с ру-
диментарным бронхом; гипоплазия — рудиментар-
ное легкое с нормальным бронхом.31
Диагноз поставить обычно нс сложно, но иногда
агенезия может быть принята за ателектаз, осо-
бенно если затенение половины грудной клетки
обнаруживается поздно и прн этом нет ни одного
ранее сделанного снимка. При отсутствии правого
легкого сердце ротировано по часовой стрелке, что
проявляется в виде декстрокардии. Грудная клетка
на пораженной стороне запавшая, с ослабленными
дыхательными движениями (рис. 17-11).
Лечение, разумеется, должно быть направлено
только на коррекцию сочетанных пороков, таких
как атрезия пищевода и трахеопищеводный свищ.
Главная цель при этом — максимальное сохране-
ние дыхательных «единиц». Некоторые хирурги
являются сторонниками первичных радикальных
вмешательств по поводу трахеопищеводных ано-
малий,32 в то время как другие пропагандируют
этапное их лечение.33
Двусторонняя агенезия легкого не совместима
с жизнью.
Гастрогенные кисты
Гастрогенные кисты напоминают центральные
бронхогенные кисты, однако в отличие от послед-
Рис, 17-11. Л. Агенезия правого легкого. Ротация сердца со смещением его в правую половину грудной клетки. В, Легочная ангио-
грамма подтверждает диагноз.
14 Закса № 1622
210 ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ
них выстланы желудочной слизистой, а потому
имеют тенденцию к пептическому изъязвлению/4
Диагноз может быть установлен путем сканиро-
вания с технецием, которое выявляет в кисте желу-
дочную слизистую (рис. 17-12). Лечение состоит
в хирургическом иссечении.
А шестой зашел с обратной стороны.
Он имел весьма обычный скромный рост.
Он. конечно, не достал бы до луны.
Но спокойно ухватил стона за хвост.
И улыбка промелькнула по лицу...
Слон — веревка, это ясно и слепцу.
Мезенхимальная кистозная гамартома
Эта патология, впервые описанная как новая
нозологическая единица в 1986 г., может быть
представлена в виде изолированной кисты или
множественных двусторонних узелков. Для нее ха-
рактерны следующие основные морфологические
черты.33
1. Узелки диаметром меньше 1 см состоят из
мезенхимальных клеток, разделенных сплетением
аномально ветвящихся дыхательных путей.
2. Кистозные узелки диаметром от 0,5 до
1 см имеют камбиевый слой примитивных мезен-
химальных клеток и выстилку из нормального или
металлизированного респираторного эпителия.
3. Внутри стенки кис гы определяются гипертро-
фированные системные артерии.
Мезенхима тьная кистозная гамартома обычно
представлена в виде многоочагового поражения,
вяло текущего, поскольку узелки возникают по ме-
ре пролиферации мезенхимальных клеток и посте-
пенной трансформации в кисты. Могут отмечаться
такие осложнения как легочное кровотечение,
пневмоторакс и даже малигпизация.”
Лечение обычно проводится при возникновении
осложнений. Кроме того, предпринимается иссече-
ние узелков тля диагностического исследования.
«Возможный эффект от резекции узелков и кист
С целью предотвращения малигнизации должен
быть тщательно взвешен на одних весах с много-
очаговой природой мезенхимальной кистозной га-
мартомы легкого и ее доброкачественным течени-
ем у большинства пациентов».33
Эти шестеро мужчин из Индостана
Долго спорили, ругаясь непрестанно,
О предмете, называемом Слоном.
И настаивая всякий на своем.
И хоть каждый был отдельно прав отчасти.
Но в итоге ошибались вес, к несчастью.
Бронхолегочные аномалии
из передней кишки
Эта глава заканчивается изложением предложен-
ного для классификации иптра- и экстралобарных
секвестраций подразделения их на 3 группы
I. Без соединения с ЖКТ.
2. С открытым сообщением с ЖКТ.
Рис. /7-/2. Грыжа пищеводного отверстия диафрагмы. Кистоз-
ная полость симулирует гастрогенную кисту. Серийное конт-
растное обследование верхних отделов желудочно-кишечного
гранта помогает в таких случаях провести дифференциальную
диагностику с гастрогенной кистой.
3. С неоткрытым (без просвета) сообщением
с ЖКТ.
Аномалии каждой из этих групп могут быть ипт-
ралобарными или экстралобарными, а также соче-
таться с нормальной диафрагмой или с диафраг-
мальной грыжей. Первоначально данное подразде-
ление использовалось для характеристики лишь
второй группы, т. е. сообщающихся аномалий.36
При дальнейшем распространении изложенной
теории термин бронхолегочные аномалии из пе-
редней кишки стал использоваться как единая кон-
цепция, положенная в основу характеристики инг-
ралобарных и экстралобарных секвестраций, кото-
рые могут иметь следующие варианты соединения
с ЖКТ:
1. Открытие
2. Фиброзным гяжем
3. Только сосудами
4. Дивертикулом
5. Фиброзным тяжем и бронхиальным или эзо-
фагеалыгым удвоением.
В последующем было высказано предположение,
что данная теория может объяснить также проис-
хождение дивертикулов пищевода или дна желуд-
ка и кистозных удвоений.37
Диагностику бронхолегочных аномалий, проис-
ходящих из передней кишки, следует начинать
с рентгенографии грудной клетки и контрастной
лзофагографии. Затем производят ангиографию
(аортальную и легочную), что позволяет иденти-
фицировать аномальные сосуды. Бронхоскопия
и бронхография, как правило, не информативны
(рис. 17-13).
Лечение заключается в раннем хирургическом
иссечении образования, обычно путем лобэктомии,
и ликвидации аномального соединения с ЖКТ.
ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ 211
Рис. 17-13. А. Бронхолегочном аномалия, происходящая из передней кишки. На обзорной рентгенограмме — затенение ясной
половики грудной клетки со смещением сердца влево. В. На эзофагограмме ин дно, что левый бронх идет от пищевода. Бронхо-
грамма практически не информатиння, однако отсутствие на ней культи левого бронха позволяет говорить об агенезии. Аортальная
янгнограмма выявляет аномальное кровоснабжение.
ДАЛЬНЕЙШИЕ НАПРАВЛЕНИЯ
В ДИАГНОСТИКЕ И ЛЕЧЕНИИ
Ультразвук стал в акушерской практике фактиче-
ски рутинным методом исследования. Имеются со-
общения о внутриутробной ультразвуковой диа-
гностике бронхолегочных аномалий с последую-
щим оперативным лечением у новорожденного.38
Большие кисты, обнаруженные на ранней стадии
пренатально, могут быть дренированы даже внут-
риутробно, что позволяет предотвратить дальней-
шее сдавление и гипоплазию нормальной ле-
гочной ткани.39 Иссечение этих образований у но-
ворожденных должно производиться с максималь-
ным сохранением респираторных «единиц».
О! Как часто в спорах искренних о Боге,
Иногда их доводящих до войны.
Люди спорили, нс ведая дороги
И решений, что противникам видны.
Так мы вечно спорим о Слоне.
Чю нс виден ни тебе, ни им, ни мне.
John Godfrey Saxe
Перевод Я. Дольского
ЛИТЕРАТУРА
1. Gerle RD. Jaretzki A, Ashley СА, cl al.: Congenital broncho-
pulmonary-foregut malformation. N Engl J Med 278:1413—
1419. 1968.
2. Shamji FM. Sachs HJ. Perkins DG: Cystic disease of the lungs.
Surg Clin North Am 68:581—620. 1988.
3. Heilzman ER: Embryology of the lung and pulmonary abnorma-
lities of developmental origin. In Heilzman ER (Editor). The
Lung. Radiologic-Pathologic Correlations, second edition. CV
Mosby. Si- I.ouis. pp 13 15. 1984.
4. Fan LL Strain JD. Foley IC. et al.: Radiological case of the
month—giant pulmonary cyst simulating pneumothorax. Am
J Dis Child 142:189 -190. 1988.
5. Shariff S. Thomas JA. Shelly N, et al.: Primary pulmonary rhab-
domyosarcoma in a child, with a review of literature. J Surg
Oncol 38:261—264. 1988.
6. Hedlund GL. Bissei GS. Bo\e KE: Malignant neoplasms arising
in cystic Inimanomas of the lung in childhood. Radiology
173:77—80. 1989.
7. Buniain WL. Isaacs H. Payne VC. et al.: Lobar emphysema,
cystic adenomatoid malformalion, pulmonary sequestration, and
bronchogenic cyst in infancy and childhood. J Pediatr Surg
9:85—93. 1974.
8. Siocker JT, Made well JE, Drake RM: Congenital cystic adeno-
matoid malformalion of the lung. Hum Pathol 8:155—171, 1977.
9. Gwinn JL. Barnes GR. Kaufman HJ: Radiological case of the
month—cystic adenomatoid malformation of lhe upper lobe of
the right lung. Am J Dis Child 112:61 62. 1966.
10. Shackelford GD. Siegel MJ: CT appearance of cystic adenoma-
toid malformations. J Compui Assisi Tuniugr 13:612—616. 1989.
11. Hendren WH. McKee D; Lobar emphysema of infancy. J Pedi-
alr Surg 1:24—39. 1966.
12. Henderson R. Hislop A. Reid L: New pathological findings in
emphysema of childhood. Thorax 26:195—205. 1971.
13. Markowitz Rl. Mercurio MR, Vahjen GA. el al.: Congenital
lobar emphysema. Clin Pediatr 28:19—23. 1989.
14. Jones HC. Almond CH. Snyder HM. el al.r Lobar emphysema
212 ЛЕГОЧНЫЕ И БРОНХИАЛЬНЫЕ АНОМАЛИИ
and congenital heart disease in infancy. J Thorac Cardiovasc
Surg 49:1, 1965.
15. Co ML, Rosner IK, Berkmen YM, et al.: Radiological case of
the month—traumatic pulmonary pseudocyst. Am J Dis Child
143:841—842, 1989.
16. Moohen SF: Mechanical production of cavities in isolated lungs.
Arch Pathol Lab Med 19:825—832. 1935.
17. Kato R. Horinouchi H, Maenaka Y: Traumatic pulmonary pseu-
docyst. J Thorac Cardiovasc Surg 97:309—312, 1989.
18. Bunlain WL, Woolley MM, Ma hour GH, ct al.: Pulmonary sequ-
estration in children: a 25-year experience. Surgery 81:413—
420, 1977.
19. Sade RM, Clouse M, Ellis Fl I: The spectrum of pulmonary sequ-
estration. Ann Thorac Surg 18:644—658, 1974
20. Heitzman ER: Embryology of the lung and pulmonary abnorma-
lities of developmental origin. In Heitzman ER (Editor). The
Lung, Radiologic Pathologic Correlations, second edition. CV
Mosby, St. Louis, p 17, 1984.
21. Savic B, Birtel FJ, Tholen W: Lung sequestration: report of se-
ven cases and review of 540 published cases. Thorax 34:96—
101, 1979.
22. Black TL, Fernandes ET, Wrenn EL, et al.: Extralobar pulmo-
nary sequestration and mediastinal bronchogenic cyst. J Pediatr
Surg 23:999—1001, 1988.
23- Gupta SK, Abraham KA, Ganesh KM: Intralobar sequestration
of upper lohe of right lung case reports. Angiology 39:1056—
1060, 1988.
24. White JJ, Donahoo JS, Ostrow PT, et al.: Cardiovascular and
respiratory manifestations of pulmonary sequestration in child-
hood. Ann Thorac Surg 18:286 294, 1974.
25. Macpherson RI, Whytehead L: Pseudosequestration. J Can As-
soc Radiol 28:17—25, 1977.
26. Taylor BG, Cockerill FM, Manfredi F, Klatte EC: Therapeutic
embolization of the pulmonary artery in pulmonary arterioveno
us fistula. Am J Med 64:360— 365, 1978.
27. Knowles S, Thomas RM. Lindenbaum RH, et al.: Pulmonary
agenesis as part of the VACTERL sequence. Arch Dis Child
63:723—726, 1988.
28. Davies RP, Kozlowski K, Wood BP: Radiological case of the
month—right upper lobe esophageal bronchus. Am J Dis Child
143:251 253. 1989.
29. Dennis WW; Correspondence. J Pediatr Surg 23:389, 1988.
30. Osborne J. Mascl J, McCredie J: A spectrum of skeletal anomali-
es associated with pulmonary agenesis: possible neural crest inju-
ries. Pediatr Radiol 19:42*5—432. 1989.
31. Booth JB, Berry CL: Unilateral pulmonary agenesis. Arch Dis
Child 42:361—374. 1967.
32. Hoffman MA, Superina R, Wesson DE: Unilateral pulmonary
agenesis with esophageal atresia and distal tracheoesophageal
fistula: report of two cases. J Pediatr Surg 24:1084- 1085,
1989.
33. Black PR, Welch KJ: Pulmonary agenesis (aplasia), esophageal
atresia, and tracheoesophageal fistula: a different treatment
strategy. J Pediatr Surg 21:936—938, 1986.
34. Macpherson RI. Reed MH, Ferguson CC: Intrathoracic gastro-
genic cysts: a cause of lethal pulmonary hemorrhage in infants.
J Can Radiol 24:362- 369, 1973-
35. Mark EJ: Mesenchymal cystic hamartoma of the lung. N Engl
J Med 315:1255—1259, 1986.
36. Leithiser RE, Capitanio MA, Macpherson RL el al.: Communi
eating bronchopulmonary foregut malformations. AJR 146:227—
231, 1986.
37. Heilhoff KB, Sane SM, Williams HJ: Bronchopulmonary foregut
malformations. AJR 126:46—55, 1976.
38. Siffring PA, Forrest TS, Hill WC: Prenatal sonographic diagno-
sis of bronchopulmonary foregui malformation. J Ultrasound
Med 8:277—280, 1989.
39. Bion M, Nicolaides KH, Greenough A: Postnatal respiratory
function after chronic drainage of fetal pulmonary cyst. Am
J Obstct Gynecol 159:858—859, 1988.
Глава 18
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ
ЛЕГКИХ И ПЛЕВРЫ
Благодари планомерно проводимой всеобщей им-
мунизации детей и применению в клинической
практике антибиотиков, значительно уменьшилась
частота легочных инфекционных заболеваний,
ведущих к эмпиеме, абсцессам легких, бронхоэкта-
зам и пневматоцеле. И хотя перечисленные ослож-
нения в настоящее время относительно редки, од-
нако иногда при их возникновении требуется
хирургическое вмешательство. Среди детей с эпми-
емой и пневматоцеле летальность остается доволь-
но высокой.
На фоне общего снижения в детском возрасте
частоты интраторакальной инфекции, наиболее тя-
желые легочные инфекционные заболевания отме-
чаются у детей с ослабленным иммунитетом или
хроническими болезнями. Химио- и иммуносупрес-
сивная терапия при трансплантации способны при-
водить к развитию инфекции, вызванной условно
патогенной флорой. Наслоение этих и других ин-
фекционно-соматических заболеваний у хирурги-
ческих больных представляет порой довольно серь-
езную проблему.
ЭМПИЕМА
Эмпиема возникает при скоплении гноя в плев-
ральной полости, являясь у большинства детей ре-
зультатом инфицирования выпота, связанного с
некупирующимся легочным сепсисом или пневмо-
нией. Очень маловероятно возникновение инфек-
ции плеврального пространства при наличии «здо-
ровых» и полностью расправленных легких. С раз-
витием эффективных методов антимикробной те-
рапии летальность снижается. Тем не менее еже-
годно умирает большое количество детей, в том
числе и грудных. Средняя летальность от эмпиемы
плевры в детском возрасте за последние два деся-
тилетия, по данным разных авторов, составля-
ет 8% 1 s
Патогенез. Эмпиема в своем развитии проходит
через три стадии: (1) экссудативная или острая
стадия, когда скопление жидкости в плевре (с pH
в основном ниже 7,2) незначительное и удаляется
из грудной полости без трудностей; (2)фибриноз-
но-гнойная стадия, с образованием большого коли-
чества полиморфноядерных клеток и отложениями
фибрина, снижением pH и уровня глюкозы, с фор-
мированием множественных полостей и (3) стадия
организации, в которой экссудат становится гус-
тым. а фибрин пронизывается фибробластами.
Эмпиема подразделяется также на острую и хро-
ническую. Острая фаза переходит в хроническую
через 4—6 недель. Эмпиема может быть диффуз-
ной и вовлекать все плевральное пространство или
ограничиваться пределами одной доли, областью
диафрагмы или парамедиастинальными отделами.
Из микроорганизмов, наиболее часто вызывающих
эмпиему у детей, следует назвать золотистый
стафилококк, пневмококк, Haemophilus influen-
zae, лишенный стрептококк и Klebsiella pneumo-
nine* По данным одного из исследований,6 треть
бактерий, выделенных в группе из 72 детей с эм-
пиемой, были анаэробы, в том числе бактероиды,
анаэробные палочки и Fusobacterium. Хотя золо-
тистый стафилококк остается наиболее распро-
страненным среди высеваемых организмов и у
взрослых и у детей, однако достижения антимик-
робной терапии в педиатрии привели к некоторому
возрастанию среди возбудителей (в процентном
отношении) Haemophilus influenzae. В то же время
частота, с которой встречаются пневмококки и Дру-
гие бактерии, не изменилась.6
Анализ 227 наблюдений эмпиемы у пациентов
в возрасте до 15 лет показал, что 71% больных
были грудного или младшего возраста, из них поч-
ти половина — от 7 мес до 2 лет.3
У детей с пневмонией, вызванной золотистым
стафилококком, стрептококком или Н. influen-
zae, внелегочный выпот появляется в 50—95%
случаев.2, э*7' н В то же время эмпиема развивается
лишь в одном наблюдении из 155 (по данным свод-
ной статистики — 3248 детей с пневмонией).2
Столь незначительная частота эмпиемы, безуслов-
но, и непосредственно связана со своевременно
(как можно раньше) начинающейся при пневмо-
нии и планомерно проводимой специфической ан-
тимикробной терапией.
Эмпиема, вызванная смешанной флорой, часто
214 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
протекает намного тяжелее, чем при наличии сди
ничного микроорганизма?'10 Особенно высокая ле-
тальность отмечается при анаэробной инфекции,
которая требует наиболее активного подхода, в ча-
стности своевременной и адекватной эвакуации со-
держимого из плевральной полости? " '
Диагностика. У маленьких детей в анамнезе
обычно отмечается непродолжительная инфекция
дыхательных путей с последующим респиратор-
ным дистрессом, лихорадкой, кашлем и временами
затрудненным дыханием.^ При физикальном об-
следовании выявляется поверхностное дыхание,
притупление перкуторного тона и смещение средо-
стения, что подтверждает диагноз.14 Многие детиш-
ки жалуются на боли в животе, при этом отмеча-
ется вздутие живота, связанное с парезом кишеч-
ника.
Рентгенограмма грудной клетки чрезвычайно
важна в диагностике пневмонии, а в последую-
щем — внелегочного выпота при эмпиеме (рис. 18-
1А).15 Наличие множественных тонкостенных по-
лостей характерно для стафилококковои пневмо-
нии. В случае затенения всей половины грудной
клетки компьютерная томография (КТ) или ульт-
развуковое исследование дают возможность отдиф-
ференцировать наличие жидкости от воспалитель-
ной инфильтрации легкого (рис. 18-1 В).1'’ Эти ме-
тоды обследования помогают также локализовать
ограниченную эмпиему, которая затем может быть
дренирована рентгенологом или хирургом ' ” КТ
позволяет, кроме того, выявить организовавшуюся
эмпиему, требующую раннего оперативного вме-
шательства.
Плевральная пункция применяется как для диа-
гностики. так и для раннего лечения эмпиемы. Ха-
рактер содержимого сразу позволяет дифференци-
ровать обычный выпот от эмпиемы и соответствен-
но определяет дальнейшую терапию. Полученный
материал должен быть исследован как на аэроб-
ную, так и на анаэробную флору. Фибринозно-
гнойный выпот имеет, как правило. pH меньше 7.2.
уровень глюкозы ниже 2,6 ммоль/л и показатели
лютеинизирующего гормона (ЛГ) больше, чем
100 Ед/л.1 Если мутный аспират имеет pH выше
7,2. а уровень глюкозы выше 2,2 ммоль/л, это го-
ворит о том. что выпот еще не «перешел» в эм-
пиему.14
Лечение. Цель лечения — эвакуировать гной
и освободить плевральное пространство, чтобы
дать возможность легкому расправиться. Плев-
ральные пункции, с которых начинают лечение,
позволяют установить диагноз и локализацию вы-
пота, а также определить возбудителя. Детей
с пневмонией и плевральным выпотом необходимо
активно лечить антибиотиками. В острой экссуда-
тивной стадии чрезвычайно эффективно внутри-
венное их введение. Во многих случаях, когда
полость эмпиемы нс удастся «очистить» путем по-
вторных пункций, может быть показана поста-
новка дренажа (торакостомия), что, безусловно,
предпочтительнее, чем частые неэффективные
пункции.
Большинство детей быстро и хорошо реагируют
Рис. Hi I. К. Постпнсвмоиичсская эмпиема и легочный аб<
у ребенка с дренажом в плевральной полости. В, Компыоте
томограмма — скопление жидкости вокруг уплотненного
кого.
на дренирование грудной клетки трубкой б<
итого диаметра. Снижение температуры и лет
цитоза до нормального уровня отмечается у»
течение первых 24—48 час.2”1' Однако подоб
клинический эффект не всегда коррелирует с рт
генологическими данными, которые могут сущ
венно «отставать» от изменений состояния болт
го. При хорошем самочувствии ребенка ник.
другое лечение не показано.16 Трубку из груд
клетки удаляют через 1—2 недели. Больной вь
сывается после 3—4-неделыюго (в общей слоя
сти) курса лечения. Утолщение плевры на рен
нограмме может сохраняться в течение нссколт.
месяцев, но это отнюдь не является признаком :
нической эмпиемы,1 6 ибо в конце концов обь
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 215
Рис. 18-2. А, Рентгенограмма грудной клетки в вертикальном
положении 13-летней девочки с тератомой средостения — пи-
ра пневмонический выпот и пневмонические изменения в языч-
коно.м сегменте слепа. В. Переход в левостороннюю эпмисму со
сдавлением легкого и смещением средостения вправо. С. Через
три месяца после декортикации слева и удаления тератомы сре-
достения с прилежащим абсцессом язычкового сегмента.
наступает полное «рентгенологическое выздоров-
ление».
Если же в течение нескольких дней нет суще-
ственного клинического улучшения, многие дет-
ские хирурги предпринимают торакотомию и де-
кортикацию. ' Однако у маленьких детей
с эмпиемой необходимость в этой операции возни-
кает редко, ' в то время как у пациентов старше-
го возраста, особенно при анаэробной инфеку^ии^
декортикация бывает показана более часто/
В нашей клинике с 1975 по 1990 г. из 26 детей
с эмпиемой 58% потребовали торакотомии и де-
коргикации. В основном это были пациенты стар-
шего возраста (средний возраст 8 лет), которые
лечились до поступления в госпиталь в течение
нескольких (до 6) месяцев. 10 из 15 больных, по-
требовавших декортикации или «эмпиемэктомии»,
имели «фоновую» патологию, которая и обуслови-
ла хроническое течение инфекции (рис. 18-2), а
именно — послеоперационную стафилококковую
пневмонию, тератому средостения, прорыв (через
диафрагму) под диафрагмального абсцесса, стафи-
лококковый септический артрит, эндокардит.
При наличии организовавшейся эмпиемы произ-
водят миниторакотомию путем разреза длиной
5 см над проекцией эмпиемы. Подлежащее ребро
резецируют.30 После эвакуации гнойного содержи-
мого спайки разделяют отсосным катетером или
рукой. Полуорган изовавшисся массы удаляют с
помощью промывания или анатомическим пинце-
том. Дренажную трубку в грудную клетку ставят
через отдельный разрез.
Результаты. При анализе результатов лечения
227 детей с постппевмонической эмпиемой3 выяв-
лено, что средняя летальность составила 8,4%.
Большинство смертей приходилось на грудных де-
гей с эмпиемой, вызванной золотистым стафи-
лококком, Цифры летальности, приводимые раз-
ными авторами, колеблются в большом диапазо-
не — от О до 30%. В некоторых исследованиях
этот показатель был меньше 8%/' 4‘14 16 По нашим
216 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
данным, длительность пребывания больных в ста-
ционаре после декортикации составляла 9 дней.
В ряде учреждений смертности вообще не было
и пациенты выписывались через 7—10 дней после
хирургического вмешательства. А если к тому же
учесть, что при проведении консервативного лече-
ния антибиотиками больные находятся в стациона-
ре в среднем 4—5 недель, становится понятным,
почему декортикация так привлекает внимание хи-
рургов. Естественно, что уменьшение продолжи-
тельности госпитализации и периода выздоровле-
ния после этого вмешательства выгодны как для
пациента, так и для его семьи.
Наблюдение в отдаленном периоде (в сроки до
15 лет) показало, что у детей, которым дренирова-
ние (любым методом) производилось в поздних
стадиях болезни, могут развиваться плевральные
рубцы и обструктивные легочные заболевания.21
И тем нс менее прогноз в отношении возможности
восстановления нормальной функции легких впол-
не благоприятный. Исследование функции легких
у 15 детей в сроки от 5 до 16 лет после успешного
лечения эмпиемы показало отсутствие у них раз-
ницы по сравнению со здоровыми детьми в этих
семьях.23 В большинстве случаев не бы то выявлено
ни фиброторакса, ни деформации грудной клетки.
ПНЕВМАТОЦЕЛЕ
Пневматоцеле наиболее часто развивается у очень
маленьких детей при пневмонии, вызванной золо-
тистым стафилококком. Пневматоцеле
это тонкостенные, наполненные воздухом кисты
легкого, при которых хирургическое вмешатель-
ство обычно не требуется, если не возникает за-
труднения дыхания, связанного со сдавлением лег-
кого или прорывом кист в плевральную полость.13
Этиология. В острой фазе стафилококковой
пневмонии пневматоцеле обнаруживаются у 42—
85% пациентов. s Менее часто кисты возникают
у маленьких детей с пневмонией, вызванной стреп-
тококком (8%) или Н. influenzae (5%).3
Патология. К развитию пневматоцеле приводит
некроз и расплавление легочной паренхимы. Ста-
филококковая пневмония вызывает тяжелый вос-
палительный процесс, связанный отчасти с мощным
деструктивным воздействием стафилококкового
экзотоксина на легочную ткань.13 Воздух выхо-
дит через разрушенные стенки альвеол субплев-
рально, в результате чего и образуется типичная
тонкостенная киста. Гистологическое исследование
подтверждает наличие обструктивного клапанного
механизма, который позволяет воздуху входить
в кисту, но препятствует его движению в обратном
направлении.32 Большинство легочных кист отно-
сительно невелики по размерам, но порой могут
разрываться и тогда возникают такие осложнения,
как пневмоторакс, бронхоплевральный свищ и эм-
пиема.13
Диагностика. Выявить пневматоцеле позволяет
рентгенограмма грудной клетки (рис. 18-3). КТ
предоставляет более точную информацию, однако
на практике этот метод нс может применяться еже-
дневно, а порой и ежечасно, для контроля за дина-
микой увеличения кисты. Очень важно дифферен-
цировать пневматоцеле с другими легочными ки-
стами.14'33'3 6 Врожденные кисты являются истин-
ными. Соответственно они выстланы цилиндриче-
ским мерцательным эпителием, а потому не могут
исчезать спонтанно, оставаясь обычно постоянны-
ми в размерах и с более толстыми стенками.13
Пневматоцеле, расположенные в задних базаль-
ных сегментах, могут быть приняты за диафраг-
мальную грыжу с поздним началом ее проявлений.
В таких случаях требуется контрастное исследова-
ние ЖКГ. Помогает также в дифференциальной
диагностике наличие четко прослеживаемого ин-
тактного купола диафрагмы. Множественные не-
большие пневматоцеле могут симулировать кисто-
аденоматозную аномалию, тем более что и та
и другая патология связаны с инфекцией.
Рис. 18-3. А. Стафилококковая пневмония у 3 летнего мальчика. Большая киста в нижней дозе левого легкого с пневмониче-
скими изменениями над ней. В. Киста уменьшилась в размерах, пневмония идет иа убыль.
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 217
Лечение. При быстро нарастающих пневматонс-
лс может понадобиться срочная декомпрессия с по-
мощью катетера. Описанные в литературе леталь-
ные исходы почти всегда связаны с дыхательной
недостаточностью, вызванной большими пневмато-
целе на фоне прогрессирующей пневмонии.
Увеличение кисты в такой ситуации с последую-
щим разрывом приводит к напряженному пневмо-
тораксу, что и является, как правило, причиной
смерти. Эта катастрофа может быть предупрежде-
на путем дренирования плевральной полости или
непосредственно кисты. Хотя практически каж-
дая четвертая из всех пневматоцеле прорывается,26
однако большинство кист все же небольшие, а по-
тому их разрыв не приводит к напряженному пнев-
мотораксу. В связи с этим профилактическое дре-
нирование кисты показано только у больных с бы-
стро увеличивающимися кистами, сопровождаю-
щимися дыхательной недостаточностью.
При пиопневмотораксе и бронхоплевральных
свищах, возникших в результате разрыва кисты,
эффективным, как правило, оказывается дрениро-
вание грудной клетки в сочетании с антимикроб-
ной терапией. Открытое дренирование, декортика-
ция или ушивание места «протечки» воздуха редко
бывают необходимы при лечении пневматоцеле.
Прогноз. По мере стихания острого инфекцион-
ного процесса пневматоцеле обычно уменьшаются
в размерах. Анализ 127 случаев из Нигерии, опуб-
ликованный в 1984 г.,31 показал, что 12,6% пнев-
матоцеле первоначально увеличивались в разме-
рах, а затем, примерно к 14-му дню. прекращали
расти. Летальность была 2,4%, причем во всех
случаях неблагоприятный исход отмечался при
стафилококковой пневмонии с эмпиемой. У 45%
больных приблизительно через 6 недель отмечено
полное исчезновение пневматоцеле. У остальных
детей для этого потребовалось до 12 месяцев. Са-
мый большой срок излечения был 1,5 года.
БРОНХОЭКТАЗЫ
Бронхоэктазы впервые были описаны Laennec
в 1810 г. В те времена они встречались довольно
часто. За последние 30 лет активное применение
антибиотиков способствовало резкому снижению
частоты возникновения этого серьезного осложне-
ния пневмонии у детей.
Патология. Бронхоэктазы представляют собой
длительно текущий воспалительно-деструктивный
процесс на уровне мерцательного эпителия и пе-
рибронхиальных тканей. Утрата мышечной элас-
тичности является причиной неспособности дыха-
тельных путей освобождаться от слизи. Застой
гнойного секрета приводит к рецидиву пневмонии
и дальнейшей деструкции. В результате происхо-
дит расширение бронхов различной! вида; цилинд-
рическое, веретенообразное или мешотчатое. В хи-
рургическом плане имеет значение лишь мешотча-
тая форма. Цилиндрические бронхоэктазы, обна-
руживаемые иногда на бронхограммах после ост-
рой пневмонии, способны подвергаться обратному
развитию.3*’ 34
Этиология. К развитию бронхоэктазов могут
привести самые разнообразные виды патологии,
в основном приобретенного характера. Обструкция
бронхиального дерева как изнутри, так и снару-
жи, вызывает ателектазы с наслоением инфекции
в соответствующих сегментах легких, расположен-
ных дистальнее. В результате возникают непрехо-
дящие изменения. У маленьких детей основной
причиной бронхоэктазов является бактериальная
или вирусная легочная инфекция. Определенная
роль традиционно отводится также перенесенным
кори, гриппу и коклюшу. Однако в развитых стра-
нах эти заболевания в настоящее время редко яв-
ляются этиологическим фактором. Тем не менее
в мире они все же остаются самой распространен-
ной причиной бронхоэктазов, равно как и кисто-
фиброз с множественным двусторонним инфекци-
онным процессом б легких.
Картагенер в 1933 г. описал синдром, включаю-
щий в себя синусит, обратное расположение внут-
ренних органов и бронхоэктазы. Около 20% паци-
ентов с situs inversus и декстрокардией имеют
бронхоэктазы, в го время как их максимальная
частота в общей популяции составляет всего
0,5 %.40 По данным одного из исследований, среди
106 пациентов с обратным расположением внут-
ренних органов 19 имели синдром Картагенера
(рис. 18-4).41 Существует описание интересного
наблюдения комбинации синдрома Картагенера
с генетической аномалией подвижности реснитча-
того эпителия и спермы, что привело к необычно-
му продвижению слизи в дыхательных путях
и очищению бронхов, но одновременно и к муж-
скому бесплодию.44 43
Рис. 18-4. Синдром Картагенера с бронхоэктазами: обратное
расположение органов, усиление легочного рисунка в базаль-
ных отделах, характерное для бронхоэктазов.
218 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
ТАБЛИЦА 18-1. Причины бронхоэктазов у 40 детей,
перенесших резекцию легкого
Причины Количество больных
Инфекция 26
Иммунодефицит 5
Аллергия 4
Анатомические аномалин 3
Инородные тела 0
Кисгофнброз 0
Неизвестные причины 2
Всего 40
Из других нидов патологии, предрасполагающих
к развитию бронхоэктазов, следует назвать ино-
родные тела бронхов,” аллергический легочный
аспергиллез,44 недостаточность альфа,-антитрип-
сина45 и IgA с повышением IgE, ' агаммагло-
булинемию и дисгаммаглобулинемию, саркоидоз,
туберкулез с лимфоаденопатией, острую лейке-
мию, абсцессы, опухоли, локализованные кисты,
астму и различные виды аллергии (табл. 18-1).
Доказано, что гастроэзофагеальный рефлюкс при-
водит к возникновению рецидивирующей лего-
чной инфекции, но бронхоэктазы при этом разви-
ваются редко. Примером наружного сдавления,
вызывающего бронхоэктазы, может быть синдром
средней доли, связанный с увеличением лимфо-
узлов.5"
По данным одного из исследовании, из 170 детей
с бронхоэктазами 40 потребовали резекции легко-
го. Наиболее частой причиной развития бронхо-
эктазов у этих 40 пациентов была бактериальная
и вирусная пневмония (65%). Легочная инфекция
обычно возникала в раннем возрасте. Синдром
Картагенера обнаружен у одного ребенка, а соче-
танные врожденные кисты — у двух. Иммунодефи-
цит выявлен у 5 детей среди тех, кому была про-
изведена резекция легкого.15
Клинические аспекты. У дегей с бронхоэктаза-
ми обычно отмечается хронический кашель, иногда
сочетающийся с кровохарканьем. Наиболее часгая
причина кровохарканья в детском возрасте —
именно бронхоэктазы. Характерно то, что очаги
рецидивирующего легочного сепсиса (в случае его
возникновения) локализуются в тех же отделах
легкого, что и бронхоэктазы,
Диагностика. Дети с бронхоэктазами почти
всегда имеют изменения на рентгенограмме груд-
ной клетки. Информативной может быть и брон-
хография (рис. 18-5). Однако наиболее предпо-
чтительна КТ, позволяющая определить форму
заболевания, локализацию, распространенность и
тяжесть изменений. После острого воспалительно-
го процесса в легком иногда возникает обратимая
цилиндрическая дилатация трахеобронхиального
дерева. Поэтому после обострения легочного сеп-
сиса рекомендуется отсрочить рентгенологическое
обследование на несколько недель, чтобы избежать
диагностической ошибки, хотя нсспсцифическое
цилиндрическое расширение бронхов обычно не-
сложно дифференцировать от мешотчатых бронхо-
эктазов.
Иммунологическое обследование ребенка с брон-
хоэктазами должно включать полный анализ кро-
ви с лейкоцитарной формулой, кожную пробу на
выявление повышенной чувствительности и коли-
чественную оценку уровня иммуногтобутипов
(IgG, IgA, IgM и IgE).
Наиболее характерная локализация бронхоэкта-
зов у детей — нижние доли, но мы не менее часто
наблюдали вовлечение язычкового сегмента и пра-
вой средней доли (табл. 18-2).
Лечение. Если после курса полноценного лече-
ния антибиотиками и постуральным дренировани-
ем инфекция продолжается, но отграничивается,
следует рассмотреть вопрос об иссечении поражен-
ной легочной ткани.5 При бессимптомном течении
небольших бронхоэктазов резекция легкого обыч-
но нс требуется. Наилучшие результаты хирурги-
ческое вмешательство даег в тех случаях, когда
Рис. Бронхограмма 14-летней девочки. Ме-
шотчатые бронхоэктазы в верхних долях обоих
легких.
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 219
ТАБЛИЦА 18-2. Локализация бронхоэктазов у 50 детей,
перенесших резекцию легкого
Локализация Количество больных
Правая верхняя доля 4
Пряная средняя доля 12
Припая нижняя доля И
Левая верхняя шля 3
Язычковый сегмент ч
Л спая нижняя доля и
Всего 50
заболевание одностороннее и вовлекает лишь одну
долю легкого.52 Бронхоэктазы обычно не распро-
страняются в прилежащие сегменты. Основное по-
казание к резекции легкого — продуктивный ка-
шель (65%).55 Из других показаний следует на-
звать рецидивирующую пневмонию, лихорадку,
невозможность для ребенка из-за болезни посто-
янно посещать школу, повторяющееся кровохар-
канье и зловонный запах изо рта. У тех детей, кото-
рым мы производили резекцию легкого, средняя
длительность заболевания равнялась почти 8
годам.
Операцией выбора является резекция сегмента
или доли легкого. Если процесс двусторонний, то
интервал между операциями должен быть не менее
2—3 месяцев. Сначала оперируют с той стороны,
которая наиболее тяжело поражена. Часто после
первой операции состояние ребенка улучшается
настолько, что дальнейшее вмешательство не тре-
буется. При вовлечении в процесс базилярных сег-
ментов нижней доли сегментарная резекция неже-
лательна, лучше произвести лобэктомию. При тя-
желых бронхоэктазах нижней доли слева часто
поражен и язычковый сегмент. Поэтому при дан-
ной локализации требуется тщательная его реви-
зия и удаление, если необходимо, вместе с нижней
долей. У детей, имеющих выраженные бронхоэкта-
зы в правой нижней доле, нередко в процесс вовле-
кается и средняя доля. В старшем детском возра-
сте, как и у взрослых с бронхоэктазами, бронхиаль-
ные артерии обычно расширены, что может вызвать
технические сложности во время операции.
По данным клиники Мауо,15 у 40 детей с бронхо-
эктазами, подвергшихся резекции легкого, быти
произведены 42 торакотомии: 35 лобэктомий,
15 сегментэктомий и две пневмонэктомии. У 7 па-
циентов вместе с левой нижней долей был удален
и язычковый сегмент, а у двух — вместе с правой
нижней долей удалена и средняя.
Результаты. В тех случаях, когда процесс ло-
кализован. хорошие результаты после хирургиче-
ского иссечения части легкого с бронхоэктазами
отмечаются у 80% пациентов.54 Если же пораже-
ние диффузное, только 36% детей избавляются от
клинических проявлений, хотя состояние улучша-
ется приблизительно у 50%. ' “ По данным одного
из исследований, из 242 пациентов с бронхоэктаза-
ми у 85% после резекции легкого отмечалась по-
ложительная динамика, а летальность была всего
0.4%/° Эмпиема и сочетанные бронхоплевральные
свищи возникают у 3—5% больных.
По нашим данным, хорошие результаты резек-
ции с отсутствием клинических рецидивов были
у 33 из 37 пациентов (89%). удовлетворитель-
ные— у 4 больных (11%). Сроки наблюдения от-
даленных результатов составляли от нескольких
месяцев до 12 лет. После резекции ни у одного
пациента не отмечалось распространения бронхо-
эктазов в другие доли. Летальных исходов не бы-
ло. У одного ребенка после резекции легкого раз-
вилась эмпиема. Трое детей имели ателектазы,
ликвидированные бронхоскопически.
АБСЦЕСС ЛЕГКОГО
Легочным абсцесс образуется в том случае, когда
при локализованной инфекции происходит нагное-
ние легочной паренхимы с образованием полости.
По мерс внедрения в клиническую практику анти-
биотикотерапии частота первичных легочных абс-
цессов уменьшилась. Обычно приходится сталки-
ваться со вторичными абсцессами, которые возни-
кают у тяжелых больных с ослабленным иммуни-
тетом, а также у детей младшего возраста.57
Этиология. Факторы, которые могут рассматри-
ваться как причинные в отношении первичных ле-
гочных абсцессов, включают в себя операции на
верхних отделах дыхательных путей, в частности
такие, как тонзиллэктомия и экстракция зубов,
а также аспирацию инородных тел, длительное
пребывание ребенка в бессознательном состоя-
пииЛ58 По другим данным, у детей с первичными
легочными абсцессами (25 больных) перечислен-
ные предрасполагающие факторы встречаются
редко.5’ В этих наблюдениях 75% абсцессов были
в верхнем сегменте правой нижней доли, заднем
сегменте правой верхней доли или верхнем сегмен-
те левом нижней доли. Устойчивый к пенициллину
пиогенный стафилококк наиболее часто вызывает
как первичные, так и вторичные легочные абсцес
сы у детей. Кроме того, встречаются альфа- и бе-
тагемолитические стрептококки, Pseudomonas-
микроорганизмы и кишечная палочка.59
Вторичные абсцессы могут быть множественны-
ми. Они являются обычно осложнением системных
заболеваний, не имеют склонности к какой-либо
определенной локализации и наиболее часто вы-
званы стафилококками, но иногда встречаются
и Pseudomonas. Klebsiella и кишечная палочка.
Тщательное бактериологическое обследование6
10 детей с легочными абсцессами выявило ана-
эробную флору абсолютно у всех, при этом у 9 па-
циентов одновременно обнаружены и аэробные
микроорганизмы. Наиболее частыми возбудителя-
ми, встречавшимися изолированно, были Peptost-
rcptococcus* Peptococcus5 Pacteroides melaninogf-
nicus* и Hacteroides fragilis*
Клинические аспекты. Почти у всех детей с ле-
гочными абсцессами отмечаются подъемы темпера-
туры, слабость, отсутствие аппетита. Кроме того,
нередко бывают кашель и плевральные боли в об-
ласти грудной клетки. Может появляться крово-
220
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
харканье часто с выделением мокроты. При нали-
чии сочетанной стафилококковой пневмонии отме-
чаются и другие клинические проявления, вплоть
до септического шока, особенно если абсцесс про-
рывается в плевральную полость.
На ранних стадиях болезни рентгенограмма
грудной клетки может быть неинформативной. Ло-
кализованный очаг пневмонии внача ie выглядит
как участок затенения с последующим развитием
характерной картины полостей. Множественные
абсцессы, как правило, бывают вторичными. При
возникновении сообщения с бронхом появляется
уровень жидкости с воздушным пузырем. Инфици-
рованные пневматоцеле при стафилококковой пнев-
монии у маленьких детей относительно тонкостен-
ные и достаточно легко могут быть дифферен-
цированы от более толстостенных, длитепьно
существующих легочных абсцессов. Даже выражен-
ные изменения на рентгенограммах часто пол-
ностью исчезают после проведения активной комп-
лексной терапии. Очень ценную информацию дает
КТ, демонстрирующая полость абсцесса, его лока-
лизацию и толщину стенок.
При отсутствии лечения легочный абсцесс через
несколько недель переходит в хроническую ста-
дию, становясь особенно толстостенным и устойчи-
вым к воздействию антибиотиков.
Лечение. Антибиотикотерапия должна быть дли-
тельной. Первоначально обычно назначают пени-
циллин G в течение 2—4 недель парентерально,
а затем орально. Очень важен правильный вы-
бор соответствующего антибиотика, осуществляе-
мый на основе результатов посевов и определения
чувствительности. Но данным одного из исследо-
ваний, 84 пациента с легочным абсцессом, вызван-
ным анаэробными организмами, получали лечение
пенициллином G или клиндамицином с одинако-
вым эффектом, ни один из этих больных нс потре-
бовал операции.’ Клиндамицин, по нашему мне-
нию, следует «приберечь» для тех пациентов, у ко-
торых имеются противопоказания к применению
пенициллина G. Если из абсцесса высеваются ста-
филококки. необходимо назначать полусинтетиче-
ские пенициллины. При активной антибиотикоте-
рапии абсцесс в течение 4—5 недель превращается
в тонкостенную полость, а затем, к концу трех
месяцев, 75% всех полостей полностью ИСЧСЗа-
ют. У маленьких детей на ранних стадиях бо-
лезни очень эффективна лечебная бронхоскопия
с аспирацией содержимого. Фиброоптическую
бронхоскопию следует проводить всем пациентам,
прежде всего для подтверждения диагноза и, если
окажется необходимым, с лечебной целью.
Хирургическое вмешательство рекомендуется в
тех случаях, когда хронический толстостенный аб-
сцесс имеет размеры, превышающие 4X6 см,
а также у пациентов младшего возраста при отсут-
ствии эффекта от активной антибис .икотерапии
в течение нескольких недель и более.*’2’*’ Обычно
требуется лобэктомия, хотя иногда оказывается
возможным иссечение только самого абсцесса. Из
других показаний к операции следует назвать про-
грессирование заболевания с переходом в эмпиему
и массивное кровохарканье.24 У маленьких детей
с ослабленным иммунитетом, которые не в состоя-
нии самостоятельно продуктивно кашлять, уже на
ранних стадиях болезни следует рассмотреть во-
прос о целесообразности трансбронхиальной аспи-
рации, которая помогает предупредить развитие
большого, нсподддющсгося лечению, хронического
легочного абсцесса.
Результаты. Летальность при первичных ле-
гочных абсцессах почти нулевая,64 в то время как
при нюричных поражениях она остается чрезвы-
чайно высокой — от 75% до 90%.59 65
ХИЛОТОРАКС
Хилезный плевральный выпот может появиться
у новорожденных спонтанно, обычно, по существу-
ющим предположениям, при врожденных аномали-
ях грудного протока или родовой травме.66 Однако
анализ 34 наблюдений врожденного хилоторакса
не выявил его связи с характером родов. При анте-
натальной диагностике на УЗИ гидроторакса пло-
да отмечена его связь с другими врожденными ано-
малиями.67 У старших детей хилогоракс иногда
возникает после травмы и кардиохирургических
вмешательств. Повреждению грудного протока во
время операции в некоторой степени способствует
аномальный его ход, отмечающийся белее, чем
у 50% пациентов. Вызвать хилоторакс могут так-
же опухоли. В частности, лимфомы и нейробласто-
мы иногда приводят к обструкции грудного прото-
ка, а при лимфангиома гозе хилезный выпот по-
является порой как в плевральной, так и в брюш-
ной полости.
Клинические проявления. Первым проявлением
может быть nt трый респираторный дистресс, преж-
де всего в виде тахипноэ и цианоза. Длительная
потеря лимфы приводит к нарушениям питания,
гипопротеинемии, метаболическому ацидозу,66 во-
дным, электролитным и иммунным расстройствам.
Массивный и юлироваппый хилоторакс, диагности-
рованный антенатально, может вызвать тяжелый
респираторный дистресс уже при рождении и со-
ответственно потребовать экстренной плевральной
пункции.66
Диагностика. Симптомы респираторного дист-
ресса при хилотораксе сочетаются с плевральным
выносом, определяемым па рентгенограмме груд-
ной клетки. При аспирации выпота получают про-
зрачную соломенно-желтую (если ребенок нс кор-
мился) жидкость, которая приобретает молочный
цвет у детей, ранее кормившихся. Анализ обычно
выявляет повышенное содержание общего жира
(более, чем 4 г/л) и белка 0 50 г/л). Преобла-
дают лимфоциты, а уровень триглицерида превы-
шает 1,3 ммоль/л. Данные показатели подтверж-
дают, что «молочная» жидкость является лимфой.
Лечение и результаты. Лечение начинают
с обычной плевральной пункции и прекращения
кормления, что часто позволяет справиться с хило-
тораксом. Назначение диеты, содержащей тригли-
цериды, может способствовать снижению продук-
ции лимфы и заживлению места ее «протечки».
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 221
Если повторные плевральные пункции и измене-
ние диеты оказываются неэффективными, необхо-
димо поставить дренаж в грудную клетку. Тоталь-
ное парентеральное питание при этом приводит
фактически к прекращению образования лимфы.
Врожденный хилоторакс у новорожденных обыч-
но поддастся лечению плевральными пункциями
или дренированием грудной клетки. Нетравмати-
ческий хилоторакс у детей часто бывает связан
с серьезными заболеваниями или малигнизацией.
При травматическом хилотораксе консервативное
лечение, как правило, эффективно. Но если поло-
жительной динамики нет на протяжении более
14 дней, или если развиваются нарушения пита-
ния, то показано оперативное вмешательство.
Правосторонняя торакотомия с перевязкой груд-
ного протока на уровне диафрагмы обычно оказы-
вается достаточно эффективной.' ' При проши-
вании лимфатического свища так же, как и при
перевязке протока в области диафрагмы, поиски
грудного протока и места «протечки» облегчаются,
если непосредственно перед операцией больной
получает с пищей нейтральные жиры с лимфочув-
ствительной краской. Прошивание мы с успехом
сочетаем с применением фибринного клея.70 Неко-
торые авторы в дополнение к этой процедуре про-
изводят еще и частичную плеврэктомию.71 В тяже-
лых случаях может быть осуществлено временное
плевроперитонеальное шунтирование. Имеются со-
общения и об антенатальном плевроамниотичс-
ском шунтировании в эксперименте.6’
КИСТ0ФИБР03
Кистофиброз (КФ) — наследственное нарушение
функции экзокринных желез. Заболевание пора-
жает поджелудочную железу и ведет к раннему
развитию фиброкистозного ее перерождения. Во-
влекаются также железы легкого, секретирующие
слизь. Кроме того, отмечается аномалия экзокрин-
ных желез кожи, что приводит к повышению уров-
ня электролитов в поту.
Заболевание передается генетически по аутосом-
но-рецессивиому пути. Ген КФ картирован на
длинном плече хромосомы 7.7? Частота в общей
популяции приблизительно 1 на 2000 новорожден-
ных. Около 5% всего населения являются носите-
73. 74
лями гена КФ.
Патология. Изменения в железах организма,
продуцирующих слизь, способствуют образованию
густого и вязкого секрета, часто вызывающего об-
струкцию выводных протоков. При рождении лег-
кие ребенка, как правило, интактны, однако на
протяжении первого года жизни развивается кли-
ническая симптоматика поражения легких.51 Имен-
но легочная недостаточное гь — наиболее частая
причина смерти. Возникающая вначале обструкция
бронхиол вязкой слизью приводит к ателектазам,
сепсису, бронхиту, перибронхиту, бронхоэктазам
с образованием полостей и абсцессов.
Клинические аспекты. Респираторные проявле-
ния КФ у маленьких детей связаны с обструкцией
мелких бронхиол, являющейся причиной ателекта-
зов в этих участках и эмфизематозных изменений
в прилежащих отделах легкого. Развивается
острый и хронический сепсис, поскольку деструк-
ция бронхов и бронхиол приводит к формирова-
нию бронхоэктазов и абсцессов. У старших детей
возникает расширение грудной клетки в передне-
заднем направлении и барабанообразнос утол-
щение пальцев. Часто развивается пневмоторакс,
требующий экстренного дренирования грудной
клетки. В терминальной стадии отмечается крово-
харканье, гипертрофия правого желудочка (легоч-
ное сердце), субплевральное скопление выпота
в виде пузырьков, пневмоторакс и дыхательная не-
достаточное гь.
На рентгенограммах отмечается преимуществен-
ное поражение правого легкого, особенно верхней
его доли.
Диагностика. КФ следует подозревать у детей
с повторной инфекцией дыхательных путей, аст-
мой в раннем возрасте, синуситами, хроническим
кашлем, бронхитом, пневмонией. Любые очевид-
ные проявления недостаточности поджелудочной
железы, кишечная непроходимость или меконие-
вый илеус подтверждают подозрения. Наиболее
важный диагностический тест — потовая проба,
которая показывает при КФ увеличение уровня
натрия и хлора выше 60 ммоль/л.
Лечение легочной формы заключается прежде
всего в поддерживающей терапии, которая «смяг-
чает» или замедляет развитие осложнений инфек-
ции. Цель лечения —обеспечить ребенку относи-
тельно активную нормальную жизнь и возмож-
ность посещать школу. Основные компоненты этой
терапии — перкуторный массаж грудной клетки,
постуральный дренаж, дыхательная гимнастика
(глубокое дыхание), применение механических
вибраторов. Очень важно периодически использо-
вать аэрозольные ингаляции в сочетании с ан-
тибиотиками.75 У более тяжелых больных нередко
показана длительная терапия антибиотиками широ-
кого спектра. При пневмотораксе необходимо дре-
нирование грудной клетки, причем дренаж остав-
ляют надолго (много дней), ибо нередко пневмо-
торакс возникает повторно. Иногда возникают
показания к абразивному плевродезу с резекцией
апикальных пузырьков. Однако если пациент яв-
ляется кандидатом на трансплантацию комплекса
сердце/легкие. то следует ограничиться только
апикальным плевродезом.
Резекция легкого обычно не показана, поскольку
поражение почти всегда диффузное и двусторон-
нее. Однако в некоторых случаях, в частности при
массивном кровохаркайьи, локализованных брон-
хоэктазах, длительно существующих сегментар-
ных ателектазах или абсцессах, резекция может
Г 76, 77
потребоваться.
Результаты. В настоящее время дети с КФ
обычно доживают до 15—20 лет, хотя некоторые
умирают в раннем возрасте, а иные живут (в ред-
ких случаях) дольше 30 лет.78
222 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
ЛЕГОЧНЫЙ ТУБЕРКУЛЕЗ
Туберкулезная инфекция преимущественно бывает
легочной, вызывается туберкулезной палочкой
и перелается от больных с активной формой ту-
беркулеза.
В большинстве случаев первичная инфекция не
оставляет после себя следов поражения легкого.
Достаточно быстрое заживление первичного очага,
по-видимому, связано с положительным микробным
балансом в организме человека, что объясняется
как естественной его устойчивостью, так и прово-
димой вакцинацией.
Первичный туберкулез обычно следует подозре-
вать по данным проводимых рутинно туберкулино-
вых кожных проб или при наличии в анамнезе
контакта с туберкулезными больными. Рентгеног-
рамма грудной клетки помогает выявить первич-
ный процесс. У детей обычно отмечается типичная
картина уплотнения паренхимы в сочетании с уве-
личением лимфоузлов в области ворот легкого.
Окончательно диагноз легочного туберкулеза
устанавливается, кома из мокроты или промыв-
ных вод желудка высевается туберкулезная па-
лочка
Лечение детей с первичным легочным туберку-
лезом начинают с изониазида в дозе 10—
20 мг/кг/сут. Кроме того назначают этамбутол
и рифампин. Уменьшить продолжительность необ-
ходимой медикаментозной терапии позволяет ни-
разина.мид, ’ максимальная общая суточная доза
которого составляет 400 мг.80 При активной форме
первичного легочного туберкулеза у детей пора-
женные участки легкого расплавляются и подвер-
гаются казеозному некрозу.
В ряде случаев может произойти диссеминация
процесса с распространением по бронхам и возник-
новением новых очагов легочного туберкулеза. Од-
нако это случается редко, если при первичном по-
ражении ребенок получает полноценную медика-
ментозную терапию.81
Необходимость в хирургическом лечении возни-
кает в настоящее время значительно реже, чем
в прошлом, поскольку современная антибактери-
альная терапия достаточно эффективна. Тем не
менее при тяжелом поражении легочной ткани мо-
жет потребоваться оперативное вмешательство, ко-
торое должно быть максимально щадящим. Обыч-
но предпринимается клиновидная или сегментар-
ная резекция, а иногда — лобэктомия.
ПОРАЖЕНИЕ, ВЫЗВАННОЕ
АТИПИЧНОЙ МИКОБАКТЕРИЕЙ
Легочные инфильтраты и нагноение лимфоузлов,
особенно подчелюстных, могут быть вызваны ати-
пичной микобатерией.
Клинические проявления. Хотя наиболее типич-
ная форма данного заболевания протекает с пора-
жением преимущественно подчелюстных лимфоуз-
лов, однако иногда может быть вовлечено и легкое.
У детей эта патология встречается очень редко.83
Диагностика. Диагноз устанавливается только
на основании неоднократных высевов атипичных
бактерий из мокроты, промывных вод желудка или
из ткани.
Лечение. Противотуберкулезная лекарственная
терапия обычно достаточно эффективна. Однако,
к сожалению, возбудители часто не чувствительны
к ней. При лечении шейных лимфаденитов, вы-
званных атипичными микобактериями, с успехом
применялся рифампин.84 Если показано хирургиче-
ское вмешательство, то инфицированные лимфо-
узлы иссекают полностью, после чего рану ушива-
ют наглухо. При легочном поражении, даже если
произведено хирургическое вмешательство, все же
главную роль играет антимикробная терапия.
У детей необходимость в резекции легкого возни-
кает очень редко.
АКТИНОМИКОЗ
Актиномикоз и нокардиоз (атипичный актиноми-
коз), в прошлом рассматривавшиеся как грибковые
инфекции, на самом деле по своей природе явля-
ются бактериальными.
Клинические проявления. При наиболее распро-
страненной форме данной инфекции поражаются
преимущественно лицо и шея. Однако легочная
форма встречается с неменыпей частотой. Общие
проявления такие же, как при остром легочном
сепсисе, включая бронхопневмонию и образование
острых легочных абсцессов. На рентгенограммах
грудной клетки картина напоминает таковую при
легочных абсцессах. Дети с ослабленным иммуни-
тетом должны быть отнесены в группу риска.
Диагностика часто трудна, поскольку и у здо-
ровых людей в мокроте и слюне могут обнаружи-
ваться актиномицеты. При высеве возбудителя из
легочной ткани или плевральной полости произво-
дят микроскопическое исследование с целью обна-
ружения зеленовато-желтых зерен. Хотя это и не
главный диагностический признак актиномикоза,
однако наличие зерен в значительной мерс под-
тверждает диагноз.
Лечение пенициллином является методом выбо-
ра. При вовлечении грудной стенки может понадо-
биться иссечение пораженных тканей на фоне при-
менения больших доз пенициллина. В редких слу-
чаях показана декортикация или дренирование
эмпиемы или абсцесса.
НОКАРДИОЗ
(АТИПИЧНЫЙ АКТИНОМИКОЗ)
Возбудитель хронического нокардиоза Nocardia
asteroides поражает, как правило, легкие. Nocardia
часто встречается как условно патогенная флора
у больных ослабленных или с иммунной недоста-
точностью.68 Поэтому при лечении именно таких
пациентов, особенно лихорадящих и имеющих из-
менения на рентгенограмме грудной клетки, следу-
ет помнить о нокардиозе.
Клинические проявления. У детей данное забо-
левание встречается редко. Клиническое течение,
так же, как и данные рентгенологического истлело-
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 223
вания грудной клетки, напоминает картину легоч-
ного туберкулеза.
Диагностика. Диагноз устанавливают на осно-
вании высева возбудителя из мокроты, биопта та
(берется путем соскоба специальным катетером)
или аспирата, взятого из легкого чрескожно или
транс грахеально. Иногда требуется и открытая
биопсия легкого, если все другие попытки устано-
вить диагноз оказываются безрезультатны мн. Счи-
тается, что Nocardia не может примешиваться во
время исследования, поэтому диагноз часто уста-
навливают по результатам рутинного посева на
грибковые или микобактериологические среды.
Лечение и прогноз. Лечение начинают с сульфо-
намидов. Редко возникающая эмпиема требует
дренирования, а абсцесс грудной клетки — иссе-
чения.
ГИСТОПЛАЗМОЗ
Гистоплазмоз — наиболее распространенная в дет-
ском возрасте системная и легочная грибковая ин-
фекция. Возбудитель Ifistoplasma capsulation оби-
тает в эндемических очагах в долине Миссисипи.
В основном заболевание является доброкачест-
венным.
Клиническая картина гистоплазмоза чрезвы-
чайно вариабельна и может напоминать тубер-
кулез. Наиболее частое проявпение — солитарный
легочный очаг, определяемый на рентгенограмме
грудной клетки. Увеличение медиастинальных лим-
фоузлов может быть причиной синдрома средней
доли, слипчивого перикардита и прогрессирующе-
го фиброзного медиастинита.
Диагностика. Реакция связывания комплемен-
та — наиболее важный серологический тест, кото-
рый говорит об активной стадии заболевания.
Лечение. У больных со сформировавшимися при
гистоплазмозе полостями или диссеминированной
формой заболевания хорошие результаты, в том
числе и отдаленные, дает применение амфотерици-
на В или кето кон а зол а/2 Однако при использова-
нии этого препарата отмечаются различные побоч-
ные эффекты, которые должны быть учтены
и тщательно сопоставлены с возможными потенци-
альными его достоинствами.
В тех с ту чаях, когда образовались полости, хи-
рургическое вмешательство неэффективно. При
синдроме же средней доли может потребоваться
лобэктомия. В редких случаях констриктивного пе-
рикардита показана перикардэктомия.
ДИФФУЗНЫЕ ЛЕГОЧНЫЕ ЗАБОЛЕВАНИЯ
Инфекционные и неинфекционные. Помощь дет-
ских хирургов иногда может понадобиться и на
соматических отделениях при диагностике и лече-
нии у детей диффузных легочных процессов. Диа-
пазон подобных ситуаций очень велик — от мед-
ленно прогрессирующего диффузного легочного
поражения до критических состояний, требующих
искусственной вентиляции легких. Порой детских
хирургов привлекают для осуществления открытой
легочной биопсии. Детальное изложение огромно-
го множества легочных интерстициальных инфиль-
тративных заболеваний, при которых может ока-
заться необходимым морфологическое или бак-
териологическое исследование ткани легких, не
является целью данной главы. Мы ограничимся
лишь описанием типичных ситуаций, чтобы позна-
комить читателя с основными принципами, кото-
рыми должен руководствоваться хирург в подоб-
ных случаях.
У детей с подавленным иммунитетом, иммуноде-
фицитом или просто ослабленных может потребо-
ваться срочная открытая диагностическая биопсия.
У таких пациентов условно-патогенные микроор-
ганизмы, например PneumocyStis carinii. иногда
вызывают диффузную интерстициальную пневмо-
нию (рис. 18-6). Экстренная диагностика в подоб-
ной ситуации позволяет осуществлять соответству-
ющую целенаправленную терапию.
Открытая биопсия порой нужна также для уста-
новления диагноза интерстициальной пневмонии
(десквамативной, лимфоидной, гигантоклеточной)
и идиопатического легочного гемосидероза. Иногда
она может потребоваться при любом грибковом за-
болевании, злокачественных поражениях, таких
как гистиоцитоз X,w и других видах патологии
легких, которые обычно диагностируются с по-
мощью посевов мокроты.
Диагностика. Рутинные посевы мокроты редко
выявляют Р. carinii, цитомегаловирус (ЦМВ) нли
Legionella. Более диагностически значимы посевы
содержимого плевральной полости. Но особенно
велика роль фибробронхоскопии с диагностиче-
ским бронхоальвеолярным лаважем. При ее прове-
рке. 18-6. По ла иным открытой легочной биопсии диффуз-
ная нитерстиии<1 1ън.1я легочная инфильтрация, вызванная Pne-
umocystis carinii.
224 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
Рис. lti-7. Л, Ребенок с лейкемией и диффузными легочными инфильтративными изменениями. Открытая легочная биопсия вы-
явила Pneumocystis carinii. Проведено лечение, в результате чего легкие «очистились». В, Рентгенограмма того же ребенка через
5 месяцев — вновь возникла диффузная легочная инфильтрация. На этот раз открытая легочная биопсия показала лейкемическую
инфильтрацию.
дснии у 72 пациентов с синдромом приобретенного
иммунодефицита (СПИД) и легочным заболева-
нием86 Р. carinii (пневмоцисты) обнаружена в 94%
случаев, ЦМВ — в 67% и Mycobacterium avium
в 62%.*’ Достаточно широко применяемая у взрос-
лых трансбронхоскопичсская легочная биопсия
у детей обычно не используется.
Среди тяжелых больных смертность, связанная
с открытой легочной биопсией, по данным литсра-
гуры, ооычно низкая. Однако описаны ред-
кие случаи гибели пациентов непосредственно во
время процедуры.90 Тем не менее нельзя переоце-
нить значение этого метода диагностики у детей со
СПИДом, когда образовавшийся в легком инфиль-
трат обусловлен лимфоцитарной интерстициаль-
ной пневмонией (ЛИП). Дело в том, что ЛИП
очень хорошо поддастся стероидной терапии, а по-
тому открытая легочная биопсия играет здесь клю-
чевую роль, позволяя проводить целенаправленное
лечение (рис. 18-7).
В различных группах детей с искусственно по-
давленным иммунитетом, например у пациентов,
перенесших трансплантацию костного мозга, от-
крытая легочная биопсия имеет ограниченное при-
менение,90 поскольку Р. carinii у таких больных
встречается редко, что объясняется профилактиче-
ским применением у них тримеТоп рим-сульфаме-
токсазола (TMZ). Наличие у ребенка в возрасте до
13 лет ЛИП в сочетании с выявлением ВИЧ (вирус
человеческого иммунодефицита) является основа-
нием для установления диагноза СПИД.91
При обследовании 21 ребенка с ВИЧ-инфекцией,
потребовавших хирургического вмешательства, у
11 больных была сделана открытая биопсия.9
В трех случаях из пяти, где подозревалось нали-
чие Р. carinii, диагноз был подтвержден данными
открытой биопсии. У 6 пациентов с лимфоцитар-
ной интерстициальной пневмонией также потребо-
валось диагностическое подтверждение с помощью
легочной биопсии прежде, чем была начата стеро-
идная терапия.
Раньше применялась пункционная легочная био-
псия, однако она связана с опасностью развития
пневмоторакса и кровотечения и нс позволяет по-
лучить необходимое количество ткани. Кроме того,
при слепой биопсии есть риск взятия материала не
из патологического очага. По этим причинам у де-
тей предпочтительнее производить открытую ле-
гочную биопсию.
Для выявления толстостенных цист Р carinii
биоптат окрашивают толуидиновым синим и сереб-
ром. Результаты получают через несколько часов
(рис. 18-8).
Лечение и результаты. Применение пентака-
рината (pentamidine isethionate) в лечении эндеми-
ческого детского типа пневмоцистоза оказалось
чрезвычайно успешным и позволило снизить ле-
тальность с 50% до 3% и меньше.93 Л при том же
варианте заболевания на фоне подавленного имму-
нитета и у взрослых пациентов 100%-ная в про-
шлом летальность уменьшилась до 25%-ной. У де-
тей с лейкемией летальность при пневмонии, вы-
званной Pneumocystis, составляет 5%.м Наиболее
эффективным препаратом, обладающим минима-
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 225
льным побочным действием, является, безусловно,
TMZ, в то время как при лечении пентамидином
частота побочных эффектов высокая. Поэтому
у пациентов, которые не могут принимать лекарст-
ва орально, TMZ должен быть препаратом выбора
для начальной терапии инфекции, вызванной
I’, carinii/'94 Не менее важно параллельно прово-
дить коррекцию глубокой гипоксии. Напряжение
кислорода в артериальной крови необходимо под-
держивать на нормальном уровне, при этом FIO2
не должно превышать 50%, что позволяет предот-
вратить токсичное воздействие кислорода.
На и худший прогноз отмечается у детей со
СПИДом. Показатель летальности после первич-
ной атаки Р. carinii составляет в этой группе
39%.95 И даже те, кто выживают в раннем периоде,
почти в 100% случаев погибают в течение 2 лет
(или в начале 3-го года) после первой атаки бо-
лезни, несмотря на активно проводимое медика-
ментозное лечение.
ИДИОПАТИЧЕСКИЕ ХРОНИЧЕСКИЕ
ИНТЕРСТИЦИАЛЬНО-АЛЬВЕОЛЯРНЫЕ
ПНЕВМОНИИ
В этой редкой группе заболевании, протекающих
с образованием легочных инфильтратов, для по-
становки правильного диагноза часто бывает не-
обходима открытая легочная биопсия89 (рис. 18-9).
Описаны несколько гистологических типов данной
патологии, в том числе обычная интерстициальная
пневмония, десквамативная,96’9 лимфоидная и ги-
гантоклеточная. Рентгенологические проявления
нередко аналогичны тем, что отмечаются у паци-
ентов С легочно-альвеолярным диспротеинозом,
идиопатическим легочным гемоси^еррзом^ и легоч-
но-альвеолярным микролитиазом. Не все-
гда можно провести и четкую гистологическую
грань между различными типами диффузных ин»
терстициальных пневмоний и фиброзов, поскольку
многие из них имеют общие черты.
Риг. /8-8. А. Пневмония, вызванная Pneumocystis
carinii. Альвеолярные пространства заполнены ny-
зырно-клсточнымн элементами. Воспалительные
клетки отсутствуют. Большие альвеолярные ннсв-
моциты содержат внутриклеточные включения тел
цитомегаловирусов (пематоксилин-эозик, X 250).
В, Пневмония, вызванная Pneumocystis carinii.
Окраска серебром выявляет различные организмы
и альвеолярный экссудат. Микроорганизмы не-
большие и многие из них имеют нечеткую конфи-
гурацию «шлема* (окраска метенамином серебра.
X 250).
15 Заказ № 1622
226 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
Рис. 18-9. А, Техника открытой легочной биопсии, осуществляемой обычно под общим наркозом. Положение больного на спине
с приподнятым на 45° боком. Разрез производят под молочной железой, чтобы войти в i рудную клетку в 4-м или 5-м межреберье.
В, Вставляют ранорасширитель и после общего осмотра и пальпации берут тот участок легочной ткани (2 3 см>. который макро-
скопически наиболее изменен. С, Для более быстрого иссечения используют сшивающий аппарат. При расправлении легкого опре-
деляют - нет ли «протечки» воздуха. 1), В плевральную полость вводят небольшой катетер, который обычно удаляют на следую-
щий день. Если пациент после операции нуждается в ИВЛ, то дренаж оставляют на весь период проведения ИВЛ. Иногда может
быть осуществлено более тщательное обследование легких и плевральной полости (после соответствующего расширения разреза),
однако в этом, как правило, нет необходимости. При наличии показаний берут также для исследования жидкость из полости пери-
карда и плевры.
ЛИТЕРАТУРА
1. Adeyemo АО, Adejuyigbe О, I'aiwo ОО: Pleural empyema in
infants and children: analysis of 298 cases. J Natl Med Assoc
76:799 805, 1984.
2. Chonmailree T, Powell KR: Parapneumonic pleural effusion and
empyema in children. Review of a 19-year experience, 1962—
1980. Clin Pediatr (Phila) 22:414- 419, 1983.
3. Freij В J, Kusmiesz H, Nelson JI), McCracken GH: Parapneumo-
nic effusions and empyema in hospitalized children: a retrospec-
tive review of 227 cases. Pediatr Infect Bis Line 3:578—591,
1984.
4. Jess P, Brynitz S, Mollar AF: Mortality in thoracic empyema.
Scand J Thorac Cardiovasc Surg 18:85—87, 1984.
5. Stiles QR. Lindesmith GG, Tucker BL, ct al.: Pleural empyema
in children. Ann Thorac Surg 10:37- -43, 1970.
6. Brook I: Microbiology of empyema in children and adolescents.
Pediatrics 85:722—726. 1990.
7. Ginsberg CM, Howard JB, Nelson JD: Report of 65 cases of
Haemophilus Influenza В pneumonia. Pediatrics 64:283 286,
1979.
8. Taryle DA. Potts DE. Sahn SA: The incidence and clinical cor-
relate of parapneumonic effusions in pneumococcal pneumonia.
Chest 74:170—173. 1978.
9. Bartlett JG, Finegold SM: Anaerobic plcuro pulmonary infecti-
ons- Medicine (Baltimore) 51:413—450, 1972.
10. Bartlett JG, Gorbach SL; Penicillin or clindamycin for primary
lung abscess (editorial). Ann Intern Med 981:546, 1983.
11. Brook 1, Finegold SM: Bacteriology and therapy of lung abscess
in children. J Pediatr 94:10—12, 1979.
12. Kosloske AM: Empyema. In Welch KJ, Randolf JG, Ravitch
MM, et al. (Editors). Pediatric Surgery. Medical Year Book
Publishers, Chicago, ррббб—669, 1986.
13. Telander RL: Empyema thoracis in pediatric surgery. In Holder
TM, Ashcraft KW (Editors). Pediatric Surgery. WE Saunders,
Philadelphia, pp213—214, 1980.
14. Avery B: Pleural effusion and empyema. In Avery B, First LR
(Editors). Pediatric Medicine. Williams & Wilkins, Baltimore,
pp273—274, 1989.
15- Light RW: Parapneumonic effusions and empyema. Clin Chest
Med 6:55 59, 1985.
16. Foglia RP, Randolph J: Current indications for decortication in
the treatment of empyema in children. J Pediatr Surg 22:28—33,
1987.
17. Collins JD, Byrd SE0 Bassett LW: Thoracentesis under fluo-
roscopic control. JAMA 237:2751—-2752, 1977.
ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ 227
IS. Stark DD, Fcdcric MD, Goodman PC: Radiographic assessment
of СГ and tube thoracostomy. AJR 141:253—258. 1983.
19. VanSonпспberg E. Ferrucci JTO Mueller PR. et al.: Percutaneous
drainage of abscesses and fluid collections: technique, results,
and applications. Radiology 142:1 —10, 1982.
20. De La Rocha AG: Empyema thoracis. Surg Gynecol Obstcl
155:839—845, 1982.
21. Hartl H: Pleuropulmonary suppurations. Prog Pediatr Surg
10:257—266. 1977.
22. McLaughlin FJ. Goldmann DA. Rosenbaum DM. et ul.: Empye-
ma in children. Clinical course and long term follow up. Pedi-
atrics 73:587 593. 1984.
23. Wise MB. Beaudry DH0 Bates DV: I ong term follow-up of stap-
hylococcal pneumonia. Pediatrics 38:398—401, 1966.
24. Kosloskc AM, Cartwright КС: The controversial role of decorti-
cation in the management of pediatric empyema. J Thorac Car-
diovasc Surg 96:166—170. 1988.
25. Cattanco SM. Kilman JW: Surgical therapy of empyema in child-
ren. Arch Surg 106:564 567, 1973.
26. Ryckmau FC. Roscnkraniz JG: Thoracic surgical problems ul
infancy and children. Surg Clin North Am 65:1443—1446
1985.
27. Golladay ES. Wagner CW: Management of empyema in child-
ren. Am J Surg 158:618 621, 1989.
28. Gustafson RA. Murray GF, Warden HE. et al.: Role of lung
decortication in symptomatic empyemas in children. Ann Thorac
Surg 49:940 947, 1990.
29. VanWay C. N.irrod J, Hopeman A: The role of early limited
thoracotomy in the treatment of empyema. J Thorac Cardiovasc
Surg 96:436 439, 1988.
30. Raffcnsbcrgcr JG. Luck SR. Shkolnik A. Ricketts RR; Miniiho-
racoiomy and chest tube insertion for children with empyema.
J Thorac Cardiovasc Surg 84:497—504, 1982.
31. Oviawe O, Ogundipe O: Pneumatoceles associated with pneumo-
nia: incidence and clinical course in Nigerian children. Trop
Geogr Med 37:264 269. 1985.
32. Quigley NJ, Fraser RS: Pulmonary pneumatocele pathogenesis.
AJR 150:1275—1277. 1988.
33. Burrows PE, Leahy FA. Reed MH: Neonatal pulmonary infarc-
tion. A cause of "cysilike" hicencies on the chest roentgenog-
ram. Am J Dis Child 137:61—64, 1983.
34. Godwin JD, Merten DF„ Baker ME: Paramediastinal pneumato-
cele: alternative explanations to gas in the pulmonary ligament.
AJR 145:525—530. 1985.
35. Wagner RB, Crawford WO. Schimpf PP: Classification of pa-
renchyma injuries of the lung. Radiology 167:77—82. 1988.
36. Woodring JH, Vandiviere HM, Fried AM, el al.: Update: the
radiographic features of pulmonary tuberculosis. AJR 146:497—
506, 1986.
37 Asplund MW. Beckwith PS. Soltanzadeh H: Successful trans-
thoracic drainage of infected traumatic pneumatocele (letter).
Chest 90:788, 1986.
38. Blades B. Dugan DJ: Pseudobronchiectasis. J Thorac Surg
13:40—48, 1944.
39. Crausaz PH: Bronchiectasies reversibles ou dilatations bronchi-
ques temporarircs. Rev Med Suisse Romande 90:45—54, 1970.
40. Kartage пег M. Slucki P: Bronchiectasis with situs inversus. Arch
Pediatr 79:193 207. 1962.
41. Miller RD, Diverlie MB: Kartagener’s syndrome. Chest
62.130—135. 1972.
42. Afzelius BA: A human syndrome caused by immotile cilia. Sci-
ence 193:317—319, 1976.
43. Eliasson R, Mossberg B, Cummer P, Afzelius BA: The immotile-
cilia syndrome: A congenital ciliary abnormality as an etinlogic
factor in chronic airway infections and male sterility. N Engl
J Med 297:1—6. 1977.
44. Hart RJ, Patterson R, Sommers H: Hypcrimmunoglobulinemia
E in a child with allergic bronchopulmonary aspergillosis and
bronchiectasis. J Pediatr 89:38 41, 1976.
45. Scott JH. Anderson CL. Shankar PS, Stavridcs A: Alpha,-anti-
trypsin deficiency with diffuse bronchiectasis and cirrhosis of
the liver. Chest 71:535 538. 1977
46. Bragger C. Seger RA. Aeppli R, et al.: lgG2/IgG4 subclass
deficiency in a patient with chronic mucocutaneous candidiasis
and bronchiectasis. Eur J Pediatr 149:168 169, 1989.
47. Yadav M, Thong YH, Sinniah D: Decreased serum immunoglo-
bulin. A level in a patient with bronchiectasis. Med J Malaysia
31:292- 295. 1977.
48. Halal F. Brochu P, Delage G. et al.: Severe disseminated lung
disease and bronchiectasis probably due to Mycoplasma pneu-
moniae. Can Med Assoc J 117:1055—1056. 1977.
49. Kearney PJ, Kershaw CR, Stevenson PA; Bronchiectasis in acu-
te leukaemia. Br Med J 2:857 859. 1977.
50. Brodman RF: Congenital chylothorax: Recommendations for
treatment. NY Stale J Med 75:553—557. 1975.
51. Dogan R. Alp M, Kaya S. et al.: Surgical treatment of bronchi-
ectasis: a collective review of 487 cases. J Thorac Cardiovasc
Surg 37:183—1X6, 1989.
52. Snell JD. Jr, IIoIimii CW: Suppurative lung disease*. Lung abs-
cess and bronchiectasis, in Holman CW. Muschenheim C (Edi-
tors). Bronchopulmonary Diseases and Related Disorders. Har-
per & Row, Hagerstown. MD. pp34l—356. 1972.
53. Irwin RS. Curley FJ, French CL: Chronic cough. The spectrum
and frequency of causes, key components of the diagnostic eva-
luation, and outcome of specific therapy. Am Rev Rcspir Dis
141:640—647. 1990.
54. Sealy WC. Bradham RR. Young WG, Jr: The surgical treatment
of multisegmentaf and localized bronchiectasis. Surg Gynecol
Obstcl 123:80-90. 1966.
55. Ripe E: Bronchiectasis. 1. A follow-up study after surgical tre-
atment. Scand J Resp Dis 52:96—112, 1971.
56. Sanderson JM, Kennedy MCS, Johnson MF. Marley DCE: Bron-
chiectasis: Results of surgical and conservative management:
A riview of 393 cases. Thorax 29:407—416. 1974.
57. Ncild JE. Eykyn SJ, Phillips 1: Lung abscess and empyema.
Q J Med 57:875—882, 1985.
58. Bernhard WF, Malcolm J A, Wylie RH: Lung abscess: A study of
148 cases due io aspiration. Dis ('best 43:620—630, 1963.
59. Mark PH, Turner JAP: Lung abscess in childhood. Thorax
23:216—220, 1968.
60. Levine MM. Ashman R. Heald F; Anaerobic (putrid) lung abs-
cess in adolescence. Am J Dis Child 130:77 81. 1976.
61. Weiss W, Cherniack NS: Acute nonspecific lung abscess: A cont-
rolled study comparing orally and parenterally administered
penicillin G. Chest 66:348—351, 1974.
62. Nonaynamu A: Surgical treatment of pulmonary abscess of chil-
dren under 10 years of age. Chest 85:356, 1984.
63. Potts WJ. Riker WL: Differentiation of congenital cysts of the
lung and those following staphylococcic pneumonia. Arch Surg
61:684—695. 1950.
64. Asher MI. Spcir S. Beland M, et al.: Primary lung abscess in
childhood. The long-term outcome of conserved management.
Am J Dis Child 136:491. 1982.
65. Sabiston DC. Jr. Hopkins EH, Cooke RE. Bennet IL. Jr: The
surgical management of complications of staphylococcal pneumo-
nia in infancy and childhood. J Thorac Cardiovasc Surg
38:421—431. 1959.
66. Vain NF, Swanner OW, Cha CC: Neonaiat chylothorax; a re-
port and discussion of nine consecutive cases. J Pediatr Surg
15:261—265, 1980.
67. Seeds JW, Azizkhan RT (Editors): Congenita/ Malformations.
Antenatal Diagnosis, Perinatal Management and Counseling.
Aspen Publisher. Rockville, MD. 1990.
68. Sicgler RL. Pearce MB: Metabolic acidosis from the loss of tho-
racic lymph. J Pediatr 93:465—466. 1978.
69. Ross JK; A review of the surgery of the thoracic duct. Thorax
16:12—21, 1961.
70. Stenzel W: Treatment of postsurgical chylothorax with fibrin
glue. J Thorac Cardiovasc Surg 31:35, 1983.
71. Azizkhan RG, Canfield J. Alford BA„ et al.: Pleuroperitoneal
228 ПРИОБРЕТЕННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ И ПЛЕВРЫ
shunts in the management of neonatal chylothorax. J Pediatr
Surg 18:842—850, 1983.
72. Ballantine TVN, Grosfeld JL, Knapek RM, Baehner RL: Inters-
titial pneumonitis in the immunologically suppressed child: An
urgent surgical condition. J Pediatr Surg 12:501—508, 1977.
73. Chong GL, Thibodeau SN: A simple assay for the screening of
the cystic fibrosis allele in carriers of the Phc508 deletion muta-
tion.'Mayo Clin Proc 65:1072 1076. 1990.
74- Dawson DB, Cummins LA, Schaid DJ, et al.: Carrier identificati-
on of cystic fibrosis by recombinant DNA techiques. Mayo Clin
Proc 64:325—334, 1989.
75. Rubio TT: Infection in patients with cystic fibrosis. Am J Med
81 (Suppl 1A):73, 1986.
76. Schuster SR, Fellows KE: Management of major hemoptysis in
patients with cystic fibrosis. J Pediatr Surg 12:889—896, 1977.
77. Stcinkamp G. von dcr Hardt H, Zimmerman HJ: Pulmonary
resection for localized bronchiectasis in cystic fibrosis. Report of
three cases and a review of the literature. Acta Paediatr Scand
77:569—575, 1988.
78. Taussig 1 M, Kattwinkel J. Friedewald WT, di Sant’Agnese PA:
A new prognostic score and clinical evaluation system for cystic
fibrosis. J Pediatr 82:380 388, 1973.
79. O’Brian RJ, Snider DE: Tuberculosis drugs old and new. Am
Rev Respir Dis 131:309, 1985.
80- Hsu KHK: Isoniazid in the prevention and treatment of tubercu-
losis: A 20-year study of the effectiveness in children. JAM
229:528—533, 1974.
81. McConville JH, Rapoport MI: Tuberculosis management in the
mid-1970’s. JAMA 235:172—176, 1976.
82. Stamm AM, Dismukes WE: Current therapy of pulmonary and
disseminated fungal disease. Chest 83:9—11, 1983.
83. Lincoln EM, Gilbert LA: Disease in children due to mycobacte-
ria other than Mycobacterium tuberculosis. Am Rev Resp Dis
105:683—714, 1972.
84. Mandell F, Wright PF: Treatment of atypical mycobacterial
cervical adenitis with rifampin. Pediatrics 55:39 43, 1975.
85. Bonafils-Roberts EA, Nickodem A, Ncalon TF, Jr: Retrospective
analysis of the efficacy of open lung biopsy in acquired immuno-
deficiency syndrome. Ann Thorac Surg 49:115—117, 1990.
8b. DeBlic J, Blanche S, Diuicl C, cl dl.. Dionchoalveolar lavage in
HIV infected patients with interstitial pneumonitis. Arch Dis
Child 64:1250 1256, 1989.
87. Stover DE. Zaman MB, Hajdu SI, et al.: Diagnosis of pulmonary
disease in acquired immune deficiency syndrome (AIDS): Role
of bronchoscopy and bronchoalveolar lavage. Am Rev Respir
Dis 130:659. 1984.
88. Hewitt Cl, Hull D, Keeling JW: Fibrosing alveolitis in infancy
and childhood. Arch Dis Child 52:22—37. 1977.
89. Hewitt CJ, Hull D, Keeling JW: Open lung biopsy in children
with diffuse lung disease. Arch Dis Child 49:27—-35, 1974.
90. Shorter NA, Ross AJ, August C, cl al.: The usefulness of open
lung biopsy in the pediatric bone marrow transplant population.
J Pediatr Surg 23:533—537, 1988.
91. Murray JF, Garay SM, Hopewell PC, el al.: NHI.BI workshop
summary: Pulmonary complications of the acquired immunodefi-
ciency syndrome: An update report of the second national heart,
lung, and blood institute workshop. Am Rev Respir Dis 135:504,
1987.
92. Beaver BL, Hill JL, Vachon DA, el al.: Surgical intervention in
children with human immunodeficiency virus infection. J Pediatr
Surg 25:79 84, 1990.
93. Wolff LJ. Barlctt MS, Bachner RL, et al.: The causes of intersti-
tial pneumonitis in immunocompromised children: An aggressive
systemic approach to diagnosis. Pediatrics 60:41—45, 1977.
94. Hughes WT. Feldman S, Chaudhary S, et al.: Comparison of
trimethoprim-sulfamcthoxazole (TMP-SMZ) and pentamidine
(PNT) in the treatment of Pneumocystis carinii pneumonitis
(PCP). Pediatr Res (Abstr) 10:399, 1976.
95. Bernstein TJ, Rye MR, Rubinstein A: Prognostic factors and life
expectancy in children with acquired immunodeficiency syndro-
me and Pneumocystis carinii pneumonia. Am J Dis Child
143:775—778, 1989.
96. Carrington CB, Gaensler EA, Coutu RE, cl al.: Natural history
and treated course of usual and desquamative interstitial pneu-
monia. N Engl J Med 298:801—809, 1978.
97. Stillwell PC, Norris DG, O’Connell EJ, el al.: Desquamative in-
terstitial pneumonitis in children. Chest 77:165, 1980.
98. Bradham RR, Sealy WC, Young WG, Jr: Chronic middle lobe
infection: Factors responsible for its development. Ann Thorac
Surg 2:612 616, 1966.
Глава 19
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
Грыжевое выпячивание в грудную клетку органов
брюшной полости может возникать в пяти участ-
ках диафрагмы.
1. Наиболее часто отмечаются грыжи пищевод-
ного отверстия, при которых в средостение прола-
бирует желудок.
2. Врожденный дефект в заднелатеральном от-
деле является результатом нарушения развития
диафрагмы.
3. Аномальное прикрепление диафрагмы к гру-
дине и прилежащим ребрам бывает причиной об-
разования в этом участке отверстия, через которое
кишечник может проникать в средостение.
4. Сочетание эпигастральной грыжи пупочного
канатика с ретростернальным дефектом в диафраг-
ме и перикарде (пентада Кантрелла) приводит
к грыжевому выпячиванию органов брюшной по-
лости в перикард.
5. Истончение (вследствие недостаточного раз-
вития) сухожильной или мышечной части диа-
фрагмы обусловливает ее эве нт рацию.
К грыжевому выпячиванию содержимого брюш-
ной полости в грудную клетку по типу эвен грации
может также приводить паралич мышц диафрагмы
в результате травмы диафрагмального нерва или
при врожденном дефекте клеток переднего рога
шейного отдела спинного мозга (С-3,4), как это
бывает при болезни Верднига-Гоффмана.
Анатомия диафрагмы. Диафрагма представля-
ет собой куполообразную фиброзно-мышечную пе-
регородку, которая разделяет грудную и брюшную
полости, играя принципиально важную роль в акте
дыхания. Фиброзная часть диафрагмы (сухожиль-
ный центр) расположена больше кпереди, чем цен-
трально, и занимает 35% всей ее поверхности.
Мышечный отдел состоит из (1) коротких мышеч-
ных волокон, начинающихся от мечевидного отро-
стка, (2) части, идущей от б нижних ребер, (3)
мышц, отходящих от медиальной и латеральной
дугообразных связок, покрывающих соответствен-
но m. psoas и т. guadratus lumborum, (4) позвоноч-
ной части — ножек, идущих от первых трех пояс-
ничных позвонков (рис. 19-1 А). У 80% людей су-
ществует диастаз между мышцами, идущими от
латеральной дугообразной связки, и теми, что на-
чинаются от реберной дуги. Эта щель, покрытая
фиброзной мембраной, носит название вертебро-
косталыюго или люмбокостального треугольника
(рис. 19-1 А, а). Богдатек установил, что слабость
именно этого отдела является причиной возникно-
вения врожденных заднелатеральных диафрагмаль-
ных грыж.
В норме в диафрагме имеются три наиболее
«важных» отверстия: (1) полая вена проходит че-
рез сухожильный центр справа от средней линии;
(2) пищеводное отверстие расположено слева от
средней линии и слегка кзади от полой всиы;
и (3) аорта лежит на телах позвонков, ограничен-
ная правой и левой ножками диафрагмы, пересека-
ющимися спереди о г нее. В литературе нет описа-
ний случаев грыжевого выпячивания органов через
отверстие аорты или полой вены, в то время как
пролабирование желудка через пищеводное отвер-
стие встречается часто, и частота эта с возрастом
увеличивается.
Эмбриология диафрагмы. Диафрагма образует-
ся из четырех закладок: (1) поперечная перегород-
ка, (2) парные плевроперитонеальные мембраны
на каждой стороне грудной стенки и средостения,
(3) мезенхима, примыкающая к пищеводу, (4) вра-
стание внутрь мышц из стенки туловища. По-
перечная перегородка впервые становится видимой
на 3-й неделе гестации (эмбрион 2 мм) и представ-
ляет собой мезенхимальное уплотнение, возникаю-
щее из перикарда. В это время развивающееся сер-
дце расположено снаружи и кпереди от эмбриона.
Постепенно, с ростом вентральной полости оно
занимает положение внутри грудной клетки
(рис. 19-2). Поперечная перегородка по своему
происхождению относится к уровню шейных соми-
тов, однако по мере удлинения дорсальных частей
эмбриона возникает ее связь и с нижнегрудными
позвонками. Поперечная перегородка дает начало
большинству мембран, которые отделяют брюш-
ную и плевроперикардиальную полости, однако
она не распространяется к дорсальной стенке туло-
вища.
Плевроперикардиальные складки возникают из
230 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
Рис. /9-7. Нижняя поверхность диафрагмы.
А. Нормальная диафрагма — люмбокостальная треугольная теть (а) обусловлена расхождением в разных направлениях мышц,
начинающихся oi латеральном сухожильной дуги и 12-го ребра.
В. (а) Отверстие Морганьи, образованное диастазом между мышцами, идущими от грудины и ребер. (Ь) Небольшой задне-
латеральный дефект диафрагмы, обусловленным нарушением слияния поперечной перегородки и плевроперитонеальных складок.
С. (а) Перитонеально-перикардиальным дефект диафрагмы и расщелина грудины, сочетающиеся с пентадой Кантрелла. (Ь) Бо-
льшой заднелатеральный дефект диафрагмы, распространяющийся до латеральной поверхности грудной стоики, однако сзади име-
ется калик диафрагмы.
D. Агенезия левого купола диафрагмы с отсутствием аортальных и дзофагеальных ножек — очень редкий вариант.
латеральной стенки туловища, которая содержит
главные вены, сходящиеся вместе в венозный си-
нус в заднем отделе поперечной перегородки. Эти
складки впервые заметны у эмбриона 5 мм. С ро-
стом эмбриона они становятся треугольными мемб-
ранами с основанием, располагающимся вдоль ла-
теральной стенки туловища, и верхушкой — в ве-
нозном синусе. Основание плевроперитонеальных
мембран перемешается каузально, пока не дости-
гает 11-го и 12-го ребер сзади. Полное отделение
плевральной и перитонеальной полостей происхо-
дит в начале 8-й недели гестации (эмбрион 19—
20 мм). Поперечная перегородка, медиастинальная
мезенхима и плевроперитонеальные мембраны сое-
диняются вместе. В последнюю очередь они сли-
ваются в том участке, который носит название
плевроперитонеального канала. Врожденная диа-
фрагмальная грыжа возникает в случае персисти-
рования этого канала, что приводит к формирова-
нию дефекта в заднелатеральной части диафраг-
мы, встречающегося слева в 5 раз чаще, чем
справа, поскольку правый плевроперитонеальный
канал, благодаря расположенной там печени, за-
крывается быстрее.4
Мышцы диафрагмы могут развиваться из трех
источников, прежде всего — из миобластов, обра-
зующих стенку туловища. По мере развития груд-
ной клетки эта стенка отделяется от внутреннего
абдоминального слоя мышц, которые затем мигри-
руют, образуя диафрагму.’ Данным процессом
можно объяснить, почему в грудной клетке суще-
ствуют только два межреберных мышечных слоя,
в то время как в брюшной стенке — три Некото-
рые эмбриологи считают, что миобласты развива-
ются in situ внутри эмбриональных диафрагмаль-
ных мембран? И, наконец, высказывается еще од-
но предположение о том, что миобласты имеют
«шейное» происхождение, сопровождая диафраг-
мальный нерв в качестве компонента диафраг-
мального «опускания» в процессе дифференци-
ации.
Эмбриогенез заднелатеральной диафрагмаль-
ной грыжи и легочной гипоплазии. Заднелате-
ральные диафрагмальные грыжи очень широко
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 231
2 мм 3,6 мм 11 мм
25 мм
Рис. 19-2. Соотношение в эмбриогенезе печени (заштрихованная часть) и диафрагмы (черная сплошная линия). По мере диффе-
ренциация и роста эмбриона диафрагма занимает более каудальное положение. Пунктирная линия показывает распространение
плевроперитонеальных тяжей и медиастинальной мезенхимы.
варьируют как по размерам, так и по локализации.
Это лишний раз подтверждает предположение, что
причиной возникновения данного порока могут
быть самые разнообразные нарушения эмбриогене-
за, а также слияние как одной, так и всех диафраг-
мальных закладок.3-5 Отверстие иногда представ-
ляет собой маленькую щель с широким реберным
ободком диафрагмы (рис. 19-1 В, Ь, 19-3), а в дру-
гих случаях это полное отсутствие диафрагмы,
в том числе ее ножек, т. е. картина агенезии всех
четырех компонентов грудобрюшной перегородки
(рис. 19-10). В норме плевроперитонеальное от-
верстие должно закрываться иа 8-й неделе геста-
ции. Кишечник же начинает быстро удлиняться
уже на 5-й неделе. В связи с небольшим пока объ-
емом брюшной полости ои выпячивается в пупоч-
ный каиатик. Простая U-образиая первичная ки-
шечная петля с желточным стебельком (диверти-
кул Меккеля) на верхушке быстро удлиняется
и поворачивается против часовой стрелки. К 10-й
неделе гестации, через 2 недели после закрытия
плевроперитонеального отверстия, брюшная по-
лость увеличивается настолько, что удлиненные
кишечные петли имеют возможность возвратиться
в живот и продолжать там ротацию против часо-
вой стрелки вокруг брыжейки.
Если дефект в диафрагме персистирует, кишеч-
ник может выпячиваться в грудную клетку. Мы
проводили с помощью ультразвука исследование
плодов с врожденной диафрагмальной грыжей во
время 2-го и 3-го триместра гестации. В некоторых
случаях выпячивание кишечника в грудную клет-
ку было преходящим, а именно — при первичном
осмотре грудная клетка была заполнена кишечны-
ми петлями, а через неделю или позже кишечника
там уже не было. Вероятно, это соответствует тем
известным наблюдениям из клинической практики,
когда при рождении на рентгенограммах в груд-
ной клетке нет органов брюшной полости, не-
смотря на наличие значительного дефекта диа-
фрагмы, но затем, через несколько месяцев или
лет, развивается грыжевое выпячивание/ Если
грыжа возникает рано в фетальном периоде, то
неизбежно имеется мальротация или отсутствие
фиксации средней кишки, в то время как при раз-
витии выпячивания в поздние сроки гестации или
после рождения отмечается нормальная фиксация
брыжейки к задней брюшной стенке. Естественно,
что при завершенном процессе ротации кишечника
и фиксации брыжейки, в грудной клетке располо-
жено меныпее количество кишечных петель.
Степень развития легкого — один из ключевых
моментов, определяющих выживаемость при задне-
латеральных диафрагмальных грыжах.7 На 26—
33-й дни гестации (4,0—4,5 мм) из передней
кишки образуется дивертикул трахеи, который
расщепляется на два легочных зачатка. Последую-
щее развитие дыхательных путей проходит через
несколько фаз: железистую, каналикуляркую и
терминальную мешотчатую или альвеолярную/ В
железистой фазе (от 52-го дня до конца 16-й неде-
ли) в результате дихотомического деления конце-
вых зачатков формируются бронхолегочные сег-
менты. Они выстланы кубическим эпителием бла-
годаря чему гистологически напоминают железу.
Между 10-й и 16-й неделями гестации дихото-
232 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
Рис. 19 -3. Небольшой дефект диафраг-
мы (стрелка), который был ушит нс-
рассаеываютимися ш пами.
мическое деление прогрессирует и теперь уже об-
разуются не 4, а минимум 15 ветвей в верхней
доле и 25 бронхиальных ветвей в язычковом сег-
менте и нижней доле.
Каналикулярная фаза длится от 17-й до 26-й не-
дели гестации и характеризуется продолжающимся
почкованием периферических воздушных про-
странств, в результате чего формируются бронхи
и альвеолы. Кроме того, происходит интенсивное
врастание капилляров внутрь воздушных про-
странств. Контакт капилляров с эпителиальной
выстилкой ацинусов приводит к трансформации
цитоплазмы эпителиальных клеток в тип I пневмо-
цигов с тонкими мембранами, выстилающими воз-
душные пространства. На этой стадии образуется
также и тип II пневмоци гоп, которые, начиная
с 24-й недели гестации, продуцируют сурфактант.
Альвеолярная фаза или терминальный мешотча-
тый период продолжается с 26-й недели до конца
внутриутробного развития и даже после рождения.
На этой стадии прогрессивное удлинение и размно-
жение тонкостенных воздушных пространств про-
исходит дистальнее промежуточных протоков, рес-
пираторных бронхиол и альвеолярных мешочков.
Жизнеспособность плода зависит от величины
поверхности альвеолярных мешочков (конечных
альвеол), выстилающих подлежащие слои и ка-
пиллярное русло. При рождении имеется около
24 миллионов мешочков, из которых развиваются
перегородки и в результате формируются отдель-
ные альвеолы. В течение первых трех лет жизни
альвеолы быстро растут по количеству, но не по
размерам, а между 3 и 8 годами они продолжают
увеличиваться и в количестве, и в размерах. К 8 го-
дам и позже насчитывается от 200 до 600 миллио-
нов альвеол, при этом они увеличиваются по мере
расширения объема грудной клетки, но новые аль-
веолы не образуются.
Легочные артерии состоят из тех, что сопровож-
дают бронхиальные ветви, обычных легочных ар-
терий и интраальвсолярных, которые называют
еще дополнительными («сверхкомплектными»).’
Последние ответвляются от обычных сосудов от-
дельно от бронхиальных ветвей. Количество их
в два раза превышает число обычных артерий.
В норме стенка проксимальных легочных артерий
до уровня 7-го бронхиального деления состоит
преимущественно из эластических волокон. Дис-
тальнее мышечный слой приобретает спиральную
конфигурацию, «закручиваясь» вокруг сосуда, и по
ходу его становится все тоньше. Иногда сосудистая
стенка только с одной стороны состоит из мышц,
поскольку спиралевидные мышцы уменьшаются по
количеству. Такие артерии (лишь частично имею-
щие мышечную стенку) возникают на уровне тер-
минальных бронхов. Они сохраняют постоянный
диаметр в течение всей гестации и до взрослого
возраста.
У плода «мышечные» (целиком) артерии имеют
более толстую по отношению к диаметру сосуда
мышечную стенку, чем у старших детей и взрос-
лых.’ В норме к 3-му дню после рождения некото-
рые из мышечных артерий уже становятся по тол-
щине такими же, как у взрослых людей, что явля-
ется результатом мышечной атрофии, а также
расширения сосудов. Эта утрата толщины мышц
связана с самим фактом рождения, но не с гестаци
онным возрастом.
Легочная гипоплазия возникает в том случае,
когда развивающиеся легкие плода сдавлены лю-
бым образованием, занимающим пространство,
предназначенное для легких, в частности — кишеч-
IV. 11
ником, выпячивающимся в грудную клетку.
Легочная гипоплазия, сочетающаяся с врожденной
диафрагмальной грыжей (ВДГ), характеризуется
уменьшением количества бронхиальных ветвей и
альвеол.|? Поражена также и сосудистая сеть лег-
ких. 12 А поскольку число ветвей легочной артерии
соответствует количеству бронхов, го и этот пока-
затель уменьшен при легочной гипоплазии.13 Кро-
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 233
ме того, артерии имеют меньший диаметр и более
толстую мышечную стенку. Мышечный слой рас-
пространяется в небольшие артерии, расположен-
ные дистальнее терминальных бронхиол, подобно
тому, как это бывает у маленьких детей с первич-
ной легочной гипертензией, мскониевой аспира-
цией и синдромом гипоплазии левых отделов
сердца.9
У маленьких детей с гипоплазией легких часто
возникает легочная гипертензия, причинами кото-
рой являются: уменьшение количества легочных
сосудов и объема капиллярного русла, повышенная
резистентность аномально толстой мышечной ар-
териальной стенки и патологически обостренная
реакция артериальной мускулатуры на гипоксию,
гиперкапнию, ацидоз и другие медиаторы сосуди-
стого тонуса.11
История. В 1579 г. Ambroise Раге (1510—
1590) сообщил о двух случаях травматической
диафрагмальной грыжи.и По данным работы The-
ophil Bonet (1620 1689), опубликованной в
1679 г., первое наблюдение ВДГ принадлежало
Lazare Riviere (1589—1655). который обнаружил
дефект диафрагмы у 24-летнего мужчины при по-
смертном исследовании.14 В 1769 г. Giovanni Batlis-
la Morgagni (1682—1771) суммировал сообщения
о различных видах диафрагмальных грыж и опи-
сал первый случай субстернальной диафрагмаль-
ной грыжи.14 В этом обзоре он, кроме всего проче-
го, ссылался иа Stehelinus. который при аутопсии
плода обнаружил левостороннюю диафрагмальную
грыжу, при этом левое легкое имело одну долю
и размеры его были в три раза меньше, чем право-
го легкого.
В 1848 г. Vincent Alexander Bochdalek (1801 —
1883), анатом, сообщил о двух случаях ВДГ, кото-
рая, как он считал, была вызвана разрывом мемб-
раны в люмбокостальном треугольнике.’5 Однако
основанием данного треугольника является 12-е
ребро и при самых различных посмертных иссле-
дован иях нередко отмечается слабое развитие
именно этого участка. В иллюстрациях же Когда-
лека в одном случае был ясно показан сзади от
дефекта ободок диафрагмальной мышцы, а не
12-е ребро, что не соответствовало предложенной
им трактовке причины возникновения ВДГ
В 1902 г. Broman опубликовал данные детально-
го исследования эмбриогенеза диафрагмы. Он
установил, что грыжевое выпячивание является ре-
зультатом недостаточного слияния поперечной пе-
регородки и плевроперитонеальных складок.1 И
хотя врожденная заднелатеральная диафрагмаль-
ная грыжа традиционно считается выпячиванием
через щель Богдалека, однако ясно, что не Богда-
лек установил механизм развития данного порока
(он считал причиной разрыв мембраны) и ие
в люмбокостальном треугольнике (как это звучало
в его трактовке) локализуется обычно дефект.
В 1888 г. Naumann из Швеции впервые сообщил
об оперативном лечении ВДГ у взрослого челове-
ка. Однако больной умер.14 Первое успешное вме-
шательство было осуществлено Heidenhain в
1902 г. у 9-летнего мальчика.16 Для закрытия де-
фекта из трансторакального доступа этот хирург
использовал марлю, пропита иную трийодметаиом
(йодоформ). Однако возник рецидив, в связи с чем
больной был повторно оперирован уже через жи-
вот. В 1928 г. Bettman и Hess оперировали 3,5-ме-
сячного ребенка, который выжил, а в 1940 г. Ladd
и Gross успешно восстановили диафрагму у ребен-
ка в возрасте 40 часов от рождения.14 Harrison с со-
авт. были первыми, кто оперировал ВДГ внутри-
утробно. После 1L неудач последующие три опе-
рации были у них успешными — дети родились
жизнеспособными.17
ВРОЖДЕННАЯ ДИАФРАГМАЛЬНАЯ ГРЫЖА (ВДГ)
ВДГ встречается с частотой 1 на 2000 рождений,
включая мертворожденных. Истинная природа
ВДГ стала значительно более попятной с тех пор,
как в практику было широко внедрено ультразву-
ковое обследование плода. Из всех случаев ВДГ,
выявленных внутриутробно, 70—75% связаны с
многоводием.18 Этот показатель частоты многово-
дия, возможно, несколько завышен, поскольку од-
ним из основных поводов для ультразвукового ис-
следования являются именно большие размеры
матки, не соответствующие гестационному сроку,
т. е. женщины с многоводием более часто подверга-
ются обследованию. Тем не менее не вызывает со-
мнений тот факт, что при наличии многоводия ле-
тальность среди детей с ВДГ особенно высокая
и составляет 72—89%.18 При отсутствии же много-
водия этот показатель ниже, но до настоящего вре-
мени все еще превышает 50%.18 Многие из детей
с ВДГ и многоводием у матери умирают сразу по-
сле рождения от легочной недостаточности, не-
смотря на оптимально проводимые реанимацион-
ные мероприятия. Причина многоводия, по-видимо-
му, заключается в перегибе гастроэзофагеального
перехода и/или пилоруса, когда желудок выпячи-
вается в грудную клетку, что препятствует продви-
жению заглоченной амниотической жидкости. При
пролабировании в плевральную полость желудка
летальность обычно более высокая, чем в тех слу-
чаях, когда желудок расположен и а своем месте
в брюшной полости.19 Желудок является содержи-
мым грыжи, как правило, у больных, имеющих
.медиально расположенный большой дефект диа-
фрагмы. Ясно, что чем больше количество переме-
щенных в грудную клетку органов, тем более недо-
развито легкое.
При ВДГ часто встречаются сочетанные анома-
лии других органов и систем, поскольку неблаго-
приятное воздействие на эмбрион возникает в ран-
нем периоде формирования внутренних органов
(на 8-й неделе гестации). Из всех детей с ВДГ
32% рождаются мертвыми. Около 36% умирают
до поступления в Центр хирургии новорожден-
ных.20 Почти у всех мертворожденных и тех, кто
умирает вскоре после рождения, обнаруживаются
тяжелые аномалии нервной системы, такие как
анэнцефалия, миеломенингоцеле, гидроцефалия, эн-
цефалоцеле и тяжелые сердечные пороки, а также
трисомия 13 и 18-20 Около 65% умирающих рано
234 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
ТАБЛИЦА 19-1. Медиаторы легочного артериального
.давления у новорожденных
Вазоконстрикции Вазодилатация
Низкие РаОа
Высокое P«iCO2
Низкое pH
Гипотермия
Норадреналин
Серотонин
Тромбоксан
Лейкотриены
Адреналин
Проча нол ол
Серотонин
Эндотелии
Высокое РаО2
Низкое Ря(’О2«<30 мм Hg
Высокое pH 7> 7,5
Закись азога
Толазолин
Кураре
Гистамин
Простагландины D. Е. F. I
Нитропруссид
Ацетилхолин
А ГФ-MgClj
Аминазин
Фторотан
Глюкагон
детей — недоношенные, родившиеся раньше 36 не-
дель гестации с массой тела меньше 2500 г.20
Эта комбинация тяжелых аномалий и недоношен-
ности и обусловливает высокую летальность. Боль-
шинство новорожденных, которые доживают до
оперативного вмешательства, как правило, доно-
шенные и не имеют других аномалий.
Хотя причины возникновения ВДГ неизвестны,
однако нельзя исключить, что определенную роль
играет генетический фактор, ибо имеются сообще-
ния о ВДГ у однояйцевых близнецов, сиблингов
и двоюродных родственников.21 Девочки поража-
ются почти в два раза чаше мальчиков.
Дефект диафрагмы может представлять собой
небольшую шель или тотальное отсутствие всех
компонентов грудобрюшной преграды, включая
ножки (см. рис. 19-1). ВДГ в 80% случаев, по
данным самых разных авторов, встречается сле-
ва, в 1% — с двух сторон. Интактный плевропери-
тонеальный грыжевой мешок имеется у 20— 40%
больных. Когда он ограничивает пролабирование
кишечника, дети, как правило, выживают.
Патофизиология. При рождении ребенка воз-
никают трудности прохождения воздуха в легкие,
поскольку отсутствует наиболее важный механизм
вдоха — сокращение диафрагмы, а, кроме того,
средостение смещено в противоположную сторону
и соответственно сдавленными оказываются оба
легких. Отрицательное давление, развивающееся
во время вдоха, способствует еще большему выпя-
чиванию кишечника в грудную клетку Имеет зна-
чение и то. что при респираторном дистрессе ре-
бенок заглатывает большое количество воздуха,
который растягивает кишечник, а это приводит
к дальнейшему сдавлению легкого. Грыжа сама по
себе, даже при нормально развитых легких, может
привести к дыхательной недостаточности. А любая
степень легочной гипоплазии вызывает тяжелые
нарушения оксигенации и выведения углекислоты.
В гипоплазированных легких снижен газообмен за
счет уменьшения поверхности как альвеол, так
и капиллярного русла. Эти легкие мало податливы
и медленно расправляются. Количество ветвей ле-
гочной артерии уменьшено, поэтому правый желу-
дочек вынужден с усилием проталкивать кровь че-
рез небольшое сосудистое русло, что приводит
к расширению легочной артерии и увеличению
давления в правом сердце.
Легочные артерии имеют необычно толстые мы-
шечные волокна, распространяющиеся дистальнее
герминальных бронхиол. Этот мышечный слой
особенно восприимчив к медиаторам вазоконстрик-
ции (табл. 19-1) В результате развиваются нару-
шения газообмена и легочного кровотока, легочная
гипертензия и правожслудочковая недостаточ-
ность. Возникает также шунтирование крови спра-
ва-налево через артериальный проток и овальное
окно, что усугубляет системную гипоксию, гипер-
капнию и ацидоз и приводит к нарастанию суже-
ния легочных сосудов. Гели клинически сужение
легочных сосудов уже наступило, то корригиро-
вать его чрезвычайно трудно. Поэтому, как только
установлен диагноз ВДГ. необходимо незамедли-
тельно начинать очень активное лечение.
Диагностика. Диагноз может быть установлен
пренатально при ультразвуковом обследовании бе-
ременных женщин. Наличие многоводия или рас-
тянутого желудка, расположенного в грудной клет-
ке, говорит о плохом прогнозе. Если диагностиро-
вана ВДГ, то необходимо обследовать плод на
наличие других пороков, тщательно осматривая
голову, позвоночник, сердце и почки. Для выявле-
ния хромосомных и обменных аномалий произво-
дят амниоцентез или хорион-биопсию. Если ВДГ
является единственной изолированной аномалией,
то следует рассмотреть вопрос о возможности и
критериях для коррекции порока внутриутробно у
плода (см. главу 82).
После рождения диагноз устанавливают по на-
личию затрудненного дыхания, цианоза, ладьевид-
ного живота, смещения тонов сердца, а также от-
сутствию дыхания на стороне грыжи. Смешение
трахеи в сторону ог средней линии и кишечные
шумы в грудной клетке обычно не определяются.
Тяжесть перечисленных симптомов имеет большой
диапазон: около 65% всех детей с ВДГ умирают
вскоре после рождения, в то время как 5% и боль-
ше иногда живут бессимптомно месяцы и годы,
прежде чем устанавливается диагноз.20-23 Перед
рентгенографией грудной клетки (основной метод
диагностики) желательно ввести в желудок зонд.
Если рентгенограмма делается до того, как воздух
заполнил кишечник, то грудная клетка на стороне
поражения затенена, но трахея и сердце смещены
в противоположную сторону и контрлатеральное
легкое уменьшено в размерах. Чаще всего кишеч-
ник заполнен воздухом, причем иногда эти воз-
душные тени ошибочно принимаются за различ-
ные формы легочных кист (рис. 19-4).
ВДГ с поздним началом проявлений. По дан-
ным разных авторов, от 5 до 25% диафрагмальных
грыж выявляются после периода новорожденно-
сти — в возрасте от 1 месяца до поздней старо-
сти.20-23 Диагноз иногда устанавливают случайно,
при рентгенологическом исследовании грудной
клетки у пациентов с бессимптомным течением
грыжи. Если же появляются симптомы, то они мо-
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 235
Рис. 19-4. Рентгенограмма грузной клетки —
хи юл ценный газом кишечник находится и ле-
ном половине грудной клетки. Трахея, коите-
рирующийся воздухом пи щеп о а и сердце сме-
щены вправо настолько, чго лишь небольшая
часть правого легкого остается воздушной.
гут быть очень легкими либо, наоборот, чрезвы-
чайно тяжелыми — как со стороны дыхательных
путей в виде респираторного дистресса, так и со
стороны ЖКТ — в виде непроходимости. Респира-
торные симптомы иногда напоминают проявления
легочной инфекции с температурой и кашлем.
Сдавление легких может вызывать укорочение ды-
хания. Данные физикального и рентгенологическо-
го обследований помогают отдифференцировать
плевральный выпот, эмпиему или кисты легких.
Боли в животе, тошнота, рвота бывают связаны со
сдавлением кишечника в отверстии диафрагмы,
что приводит к непроходимости, либо с нарушени-
ем кровообращения кишечника (с заворотом или
без него). Если на рентгенограмме грудной клетки
диафрагма контурируется нечетко, определяются
«легочные кисты», а при исследовании пассажа
контрастного вещества по желудочно-кишечному
тракту видно проникновение тонкой кишки через
диафрагму, операцию необходимо осуществлять из
тра нса бдом и нал ь но го доступа.
Дооперационное лечение. Новорожденный ребе-
нок с ВДГ и проявлениями дыхательной недоста-
точности требует эндотрахеальной респираторной
поддержки. Не следует начинать вентиляцию ма-
ской, поскольку при этом воздух нагнетается в же-
лудок и кишечник. Как только больной за интуби-
рован и переведен на ИВЛ, необходимо вводить
миорелаксанты, чтобы исключить необходимость
участия самого ребенка в борьбе за эффективное
дыхание и предотвратить дальнейшее смещение
кишечника в грудную клетку. Обязательно прово-
дят декомпрессию желудка назогастральным зон-
дом, который подсоединяют к вакуум-о гсосу. Вен-
тиляционное давление должно быть снижено до
уровня менее, чем 45 мм рт. ст., поскольку гипо-
плазированное легкое очень легко повреждается
при высоком давлении.
Ставят катетеры в пупочную артерию и в правое
предсердие. Желательна катетеризация правой лу-
чевой артерии, позволяющая определять разницу
РаО2 в аорте проксимальнее и 1истальисе артери-
ального протока. Если РаО2 в дистальной аорте
ниже, чем в правой лучевой артерии, это говорит
о наличии легочной гипертензии и/или гипопла-
зии. Поскольку при ВДГ превалирует шунтирова-
ние справа-налево, РаО2 в диета тьной аорте часто
ниже 40 мм рт. ст., что приводит к печеночной,
кишечной и почечной ишемии. Во избежание ги-
поксии нижних отделов туловища, FIO2 должно
быть на уровне 1,0, при этом РО2 в правой лучевой
артерии может превышать 100 мм рт. ст.; показа-
тель разницы РО2 часто выше 200 мм рт. ст.
В прошлом неонатологи считали, что преду-
ктальное РаО2 выше 100 мм рт. ст. может вызы-
вать ретролентальную фиброплазию (РЛФ), соот-
ветственно уменьшали ПО2, чтобы поддерживать
РаО2 ниже указанного уровня. Однако это сниже-
ние FIO2 у детей, требующих любой вентиляци-
онной поддержки,— большая ошибка. Мы никогда
не видели развития РЛФ у детей с ВДГ’. В первые
несколько дней после рождения даже незначитель-
ное снижение FIO2 обычно приводит к тяжелой
внезапной легочной вазоконстрикции. Возникаю-
щие в результате гипоксия, гиперкапния и ацидоз
очень трудно корригируются и требуют для этого
длительного промежутка времени. Поэтому одина-
ково важен мониторинг как РаО2, так и pH, ибо
механика вентиляции должна быть отрегулирова-
на таким образом, чтобы индуцировать гипокап-
нию и алкалоз. Главная цель— поддержать но-
стдукталыюе РаО2 больше 40 мм рт. ст.. РаСО2
меньше 30 мм рт. ст- и pH выше 7,5, что позволяет
достичь максимальной легочной вазодилатации.м
Чтобы вызвать алкалоз, может понадобиться вве-
дение соды или tromethamine.
236 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
Обычно у детей с ВДГ отмечается сужение сосу-
дов и гиповолемия в результате выхода плазмы из
капилляров в ткани в ответ на гипоксию. Поэтому
необходимо введение больших объемов раствора
Рингср-лактага. РО2 должно поддерживаться на
уровне около 40 мм рт. ст. до тех пор. пока име-
ется нормальная тканевая перфузия, состояние ко-
торой измеряется непрямыми способами и зависит
от адекватности объема крови и функции сердца.
Важно осуществлять мониторинг давления в пра-
вом предсердии. Быстрое его повышение во время
болюсного введения раствора Рингер-лактата по-
зволяет определить, адекватна ли наполненность
венозного руста и нет ли недостаточности функ-
ции правых отделов сердца. Системное кровяное
и пульсовое давление также отражают состояние
объема крови и функции сердца.
Разница в содержании кислорода в аорте и пра-
вом предсердии (DA—VO2)* должна быть в преде-
лах 5 мл/100 мл.
DA—VO2=a,39XHb)X(SaO2 SvOj)
* Hb — гемоглобин; SaO2 — артериальная сатура-
ция; SvO2 — венозная са гурация.
Более высокие значения этого показателя гово-
рят о замедленной тканевой перфузии. Смешанная
венозная (правопредсердная) сатурация также от-
ражает поступление и выведение кислорода тканя-
ми и должна поддерживаться на уровне выше 65%.
Восстановление капиллярного кровотока после
сдавления кожных капилляров должно происхо-
дить в течение 3 сек, если у ребенка нормальная
температура, а температура окружающей среды —
28 °C или больше. Эхокардиография может выя-
вить снижение сократительной способности сердца
и увеличение правых его отделов с легочной и три-
куспидальной регургитацией, что говорит о высо-
ком давлении в легочной артерии. Чем длительнее
период гипоксии, тем выше опасность развития ги-
поксической кардиомиопатии, почечной и печеноч-
ной недостаточности и выхода плазмы из капил-
ляров в ткани.
Возникновение легочной гипертензии и шунтиро-
вания справа-налево представляет серьезную проб-
лему при лечении детей с ВДГ. В таблице 19-1
представлены многочисленные факторы, которые
могут изменять тонус легочных сосудов.21 30 К со-
жалению, нет таких препаратов, которые бы изби-
рательно расширяли легочные сосуды, не вызывая
одновременно и системной вазодилатации Многие
отдают предпочтение толазолину, ' который
(так же, как кураре и морфин) приводит к расши-
рению сосудов, благодаря высвобождению из тка-
невых запасов гистамина. Поэтому данный препа-
рат способствует выходу крови из капилляров
в ткани и соответственно развитию гиповолемии
и системной гипотензии. Однако при повторном
его применении сосудорасширяющий эффект бы-
стро и прогрессивно снижается и вообще становит-
ся непредсказуемым. Кроме того, из побочных дей-
ствий и осложнений применения толазолина изве-
стно развитие пептических язв с кровотечением
и даже перфорацией.
Изучались и другие препараты, такие как про-
стагландины и ацетилхолин, но при их использо-
вании в периоде новорожденное™ уменьшению ле-
гочной вазоконстрикции сопутствует и системная
гипотензия.211 В эксперименте предпринимались по-
пытки вводить в легочную артерию аденозин-три-
фосфат (АТФ-MgClj). Он действительно вызывал
избирательно только легочную вазодилатацию, по-
скольку быстро метаболизировался до того, как
попадал в системное кровообращение. Однако све-
дений об его использовании у новорожденных в ли-
тературе нет.30 Вазодилатации и уменьшению ле-
гочной вазоконстрикции способствует также добав-
ление к дыхательной смеси закиси азота. Особенно
выраженный эффект отмечается при этом у детей
с хорошо развитым легочным сосудистым руслом.
Закись азота быстро разрушается, поэтому систем-
ная гипотензия не возникает.31 В настоящее время
наилучшим способом улучшения газообмена и сни-
жения легочной гипертензии является экстракор-
поральная мембранная оксигенация (ЭКМО).
При нормальном плазменном объеме, но снижен-
ной функции сердца, может потребоваться инфузия
добутамина и/или допамина (2—15 мгк/кг/мин)
при постоянном мониторинге его воздействия на
правое предсердие и системное давление.
Вентиляционная поддержка может осуществля-
ться путем обычной ИВЛ либо высокочастотной
(ВЧ ИВЛ) — осцилляционной или струйной. При
обычной вентиляции давление на вдохе/конце вы-
доха должно быть не выше 45/6, что позволяет
избежать баротравмы. Частота дыхания поддержи-
вается на уровне 125 дых/мин, что способствует
снижению РСО,. Если обычная ИВЛ не эффектив-
на, то следует применить ВЧ ИВЛ с частотой бо-
лее 400 дых/мин и низким вентиляционным давле-
нием.31,1 После того, как установлен оптимальный
режим вентиляции, показатели предуктального и
постдуктал ьного РО2, РСО2 и pH позволяют либо
прогнозировать благоприятный исход, либо ста-
вить показания к проведению ЭКМО." 13
В прошлом считалось, что главное в коррекции
вентиляционной недостаточности при ВДГ — это
срочное хирургическое вмешательство с низведе-
нием кишечника и ликвидацией грыжи. И сразу
после операции у многих детей действительно от-
мечались нормальные показатели газов крови при
FIO2 меньше 1,0 и низком вентиляционном давле-
нии. Однако позже, через несколько часов и даже
дней возникало прогрессирующее ухудшение пока
зателей газов крови с шунтированием справа-нале-
во в результате интенсивного спазма легочных ар-
терий. Ухудшение, наступавшее вслед за светлым
промежутком («медовым месяцем»), отмечавшимся
непосредственно после операции, обусловлено не-
сколькими факторами, такими, как повышение
внутрибрюшного давления с недостаточностью
висцеральной и периферической перфузии, огра
ниченис экскурсий диафрагмы, псрерастяжение
альвеол в гипоплазированном легком с уменьше-
нием альвеолярно-капиллярного кровотока, осво-
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 237
бождеиие вазоактивных цитокинов. Кроме того,
после хирургического вмешательства отмечается
снижение податливости легких.32
В настоящее время оперативное лечение обычно
откладывается на 24 часа и более. За этот период
устанавливается оптимальный режим вентиляции,
что позволяет надеяться на сведение к минимуму
или даже на ликвидацию реактивной легочной ги-
пертензии/ ’ И хотя, согласно обычным законам
логики, кажется, что дли улучшения механики вен-
тиляции необходимо уменьшить грыжевое выпячива-
ние, однако в действительности оперативное вме-
шательство может ухудшить состояние больного.
Когда ребенок релаксирован, самые разнообразные
способы механической вентиляции могут обеспе-
чить достаточно эффективный газообмен и без
уменьшения диафрагмальной грыжи.
В тех же случаях, когда нет положительной ди-
намики, несмотря на оптимальный режим вентиля-
ции, поддержание объема крови и функции серд-
ца, ребенок должен быть переведен на ЭКМО. По-
скольку при этом легкие больного «отдыхают», то
может быть предпринята операция ликвидации
грыжи. Однако сравнительное изучение исходов
при экстренных и отсроченных вмешательствах не
выявляет различий относительно выживаемости,
поэтому можно говорить о том, что в срочной опе-
рации нет особой необходимости.34
Экстракорпоральная мембранная оксигенация
(ЭКМО). При ЭКМО кровь пациента перфузиру-
ется через мембранный оксигенатор, где происхо-
дит газообмен, и затем возвращается к пациенту
(см. главу 77). Кровь может быть взята из правого
предсердия и возвращена в венозное русло (через
бедренную вену) — вено-венозное шунтирование,
ио наиболее часто ее возвращают в артериальную
систему — венозно-артериальная циркуляция. Пу-
тем разреза на шее осуществляют доступ к глубо-
кой яремной вене, через которую в правое пред-
сердие вводят катетер большого диаметра (10—
16 French) с множественными отверстиями. Арте-
риотомия общей сонной артерии позволяет прове-
сти канюлю (8—14 French) в дугу аорты. Венозная
кровь оттекает в резервуар, где пропускается
через силиконовую мембрану, проницаемую для
кислорода и углекислоты. Движение кислорода
и углекислоты внутри мембраны регулируется
таким образом, чтобы газы в возвращающейся
крови поддерживались на оптимальном уровне
(РО3= 100 мм Hg, РСО2=30 мм Hg).
Пока пациент находится на обходном кровообра-
щении, легкие вентилируются со скоростью 10 раз
в мин (FIO2= 0,21) Пик давления иа вдохе (PIP)
поддерживается на уровне 20 см Н2О, а положи-
тельное давление конца выдоха (ПДКВ) — 5 см
Н2О. Это давление помогает легким «отдохнуть» до
того времени, когда они смогут расправляться при
идеальных кровотоке и вентиляции. Скорость за-
бора крови от больного первоначально должна
быть около 100 мл/кг/мин (нормальный сердеч-
ный выброс колеблется от 120 до 300 мл/кг/мин).
Если обходное кровообращение превышает 80%
сердечного выброса, то кривая артериальной вол-
ны уплощается. Тщательно измеряют показатели
газов артериальной крови, что позволяет регули-
ровать в оксигенаторе соотношение кислород/уг-
лекислота/воздушная смесь и скорость перфузии.
Постдуктальное РО2 в идеале должно быть 60—
80 мм Hg, в то время как сатурация в правом
предсердии — 65—75%. При этих показателях
обеспечивается достаточное поступление в орга-
низм кислорода.
После периода в 24 часа или более объем заби-
раемой от пациента крови может быть уменьшен,
поскольку легочная перфузия улучшается. Частота
вентиляции и FIO2 регулируются таким образом,
чтобы легкие имели возможность поддерживать
вентиляцию независимо от ЭКМО. Критерии для
снятия с ЭКМО не ограничены какими-либо жест-
кими рамками. Например, ЭКМО может быть пре-
кращена, когда на обходную циркуляцию при-
ходится менее 15% сердечного выброса, а легкие
при этом обеспечивают уровень РаО2 выше 60,
РаСО2—меньше 40, при PIP ниже 0,3 и частоте
дыхания менее 30 в 1 мин.
При проведении ЭКМО возникают еще две важ-
ные проблемы — необходимость общего примене-
ния гепарина и опасность возникновения ишемии
мозга. Доза гепарина устанавливается таким обра-
зом, чтобы поддержать время активного свертыва-
ния крови (BACK) на уровне 3—4 мин (норма
1,5—2,0 мин). BACK определяют ежечасно и на
основании полученных результатов регулируют
лозу гепарина. В связи с указанными обстоятель-
ствами всегда существует риск развития кровоте-
чения как вследствие вентиляционного поврежде-
ния легких, так и спонтанного кровотечения любой
локализации. Иногда возникает и внутричерепное
кровоизлияние, которое отчасти может быть связа-
но с внутричерепной венозной гипертензией в ре-
зультате канюлирования яремной вены. Поэтому
ежедневно следует проводить УЗИ мозга. Внутри-
черепное кровоизлияние чаще отмечается у недо-
ношенных детей, родившихся раньше 35-й недели
гестации. В этой группе ЭКМО может быть проти-
вопоказана. Еще одна опасность при использова-
нии данного метода — аггрегация тромбоцитов в
местах соединения трубок и на мембране. При ко-
личестве тромбоцитов меньше 80 000 производится
их трансфузия. В результате окклюзии общей сон-
ной артерии может возникнуть ишемия мозга. Од-
нако это редкое осложнение, поскольку^ коллате-
ральное кровообращение из позвоночных артерий,
противоположной сонной и Виллизиевого круга
достаточно интенсивное. Следует лишь иметь в ви-
ду, что неврологические нарушения отмечаются
у многих пациентов в течение длительного вре-
мени в отдаленном периоде, но это, как правило,
связано не собственно с ЭКМО, а с исходной
гипоксией, которая и потребовала проведения
ЭКМО.45 46
ЭКМО обычно применяют для спасения тех па-
циентов, у которых имеются прогностические кри-
терии неэффективности вентиляции и соответст-
венно неблагоприятного исхода (табл. 19-2). К со-
жалению, не существует методов, которые возводя-
238 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
ТАБЛИЦА 19-2. Прогностические факторы при ВДГ
Показатель Величины Прогноз Литература
РаСОа 50 мм Hg Плохой 35-39 pH <7,2 Плохой 35 39 A-aDO2* Постдукт. > 600 мм Hg Плохой 39. 4U Продукт. >200 мм Hg Плохой 39, 40 Индекс ИВ <1000; РаСО2<40 Хороший 41, 42 вентиляции И В >1000; I,aCUa>40 Плохой** 41, 42 (ИВ) ИВ>1000; РаСОа<40 Промежу- 41, 42 точный Индекс >0.4 Плохой 43 окснгс нации (ИО)" Индекс >84 Хороший 43 оксигенации/ <4 Фаталь- 43 венти л яци и и ы и (ИОВ)Л Высш, постдукт. >100 мм Hg Хороший 43 РаОа <100 мм Hg Плохой 43
* A-aD02 = FIO, — (РаСО, — 47) - РаО2.
Fl2 = FO2 X барометрическое давление.
ИВ = частота веи1Ш1Яции X среднее давление в дыхательных
путях.
* ИО = FIO2 X среднее давление в дыхательных путях —РаО2.
* ИОВ = РаО2 - ИВ X 100.
• Во время лечения многие, выжившие в последующем, имеют
ИВ>1000 и РаСО2>40.“
ли бы при диафрагмальной грыже четко опреде-
лить — имеются ли у ребенка легкие, маленькие
настолько, что неспособны поддерживать эффек-
тивное дыхание, либо тяжесть состояния связана
с обратимой реактивной легочной гипертензией.
Хотя ЭКМО может продолжаться в течение 2 не-
дель и более, однако и столь длительный период
бывает недостаточным для того, чтобы позволить
гипоплазированному легкому достичь в результате
роста и развития нормального уровня вентиляци-
онной функции, если эта функция была нарушена
в течение первых нескольких дней жизни. Поэтому
главная задача ЭКМО в другом — дать ребенку
возможность пережить то время, пока имеется ре-
активный легочный сосудистый спазм.
ЭКМО при диафрагмальной грыже должна при-
меняться с большой осторожностью и критерии от-
бора больных для ЭКМО достаточно (возможно
даже слишком) строгие.47-50 Если до начала ЭКМО
градиент A-aDO2 (см. табл. 19 2) удерживается на
уровне >600 в течение более, чем 4—8 час,
и РО2 — менее 40 мм Hg в течение более 2 час,
неизбежно развивается длительная гипоксия, даже
если тканевая перфузия при этом нормальная.
А столь продолжительная гипоския, несомненно,
оказывает неблагоприятное влияние на мозг, серд-
це, функцию почек и определяет соответствующий
прогноз с летальностью, превышающей 80%. Не
менее серьезны бывают последствия гипоксическо-
го поражения и у выживших детей. Риск же воз-
никновения этих осложнений при использовании
ЭКМО намного ниже. Соответственно ЭКМО дол-
жна применяться в тех случаях, когда с помощью
различных методов вентиляции при F1O2 1,0 и дав-
лении, приближающемся к 40 см Н2О, не удается
в течение часа обеспечить РаО2 выше 40 мм Hg,
РСО2 меньше 40 мм Hg и pH — больше 7.4.
Отсрочка в оперативном вмешательстве при
ВДГ дает время и возможность для выявления по-
требности в ЭКМО. Из больных, которым прово-
дится обычная ИВЛ и экстренное вмешательство,
более половины требуют ЭКМО после операции,
причем у многих отмечается тяжелая гипоксия во
время вмешательства и после него, пока не начи-
нается ЭКМО. Из тех пациентов, у которых на
фоне проведения ИВЛ операция откладывается,
около 10% имеют столь недостаточно развитые
легкие, что умирают в ранние сроки, а из выжив-
ших более, чем половина, требуют ЭКМО. У одной
трети детей, помещенных на ЭКМО, состояние не
улучшается в течение 3 дней и эти больные, как
правило, умирают, когда их снимают с ЭКМО. Те
же пациенты, у которых легочная гипертензия об-
ратима, могут быть сняты с ЭКМО. После ЭКМО
и ликвидации ВДГ у половины пациентов возника-
ет рецидив легочного сосудистого спазма, приводя-
щий к смерти.'’'1 Следовательно, выживаемость мо-
жет быть повышена за счет ранней операции в тех
случаях, когда функция легких улучшается, пока
ребенок находится еще на ЭКМО. Если же по-
сле операции вновь наступает ухудшение с легоч-
ным вазоспазмом, то ЭКМО в течение еще не-
скольких дней позволяет спасти большинство этих
детей. В среднем ЭКМО увеличивает выживае-
мость при ВДГ на 15%.
Хирургическое лечение. Как только состояние
ребенка стабилизировалось, производится опера-
тивное вмешательство. Наркоз общий с использо-
ванием фторотана и павулона (pancuronium bromi-
de), что помогает свести к минимуму сосудистую
реакцию. Наиболее рационален поперечный раз-
рез в эпигастральной области. Из этого доступа
легче извлечь кишечник, растянуть брюшную
стенку, чтобы уместить кишечник в брюшной по-
лости, сформировать при необходимости вентраль-
ную грыжу и выполнить по показаниям дополни
тельные вмешательства, такие как гастростомия
или фундопликация, если есть основания предпо-
лагать развитие в дальнейшем гастроэзофагеаль-
ного рефлюкса.
После извлечения органов из грудной клетки
грудная полость тщательно осматривается на на-
личие грыжевого мешка, который может присутст-
вовать более, чем в 20% случаев. Мешок должен
быть иссечен.
Если дефект диафрагмы представляет собой уз-
кую щель, ее ушивают нерассасывающимися шва-
ми 2-0 или 3-0. Большие дефекты, шириной в не-
сколько сантиметров, хотя в принципе и могут
быть ушиты, однако в результате диафрагма упло-
щается и ее экскурсии при дыхании становятся
либо ослабленными, либо вовсе отсутствуют. В
связи с этим грудная полость увеличивается, что
способствует чрезмерному перерастяжению альве-
олярных пространств. Уменьшается также емкость
брюшной полости. Поэтому большой дефект луч-
ше закрывать каким либо пластическим материа
лом.53 Мы предпочитаем использовать тефлоновую
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 239
сетку, к которой со стороны живота приклеиваем
заплату из специального материала (ЗМ drape),
предотвращающего подпаивание кишечника к сет-
ке. Сетку вырезают таким образом, чтобы ее раз-
меры слегка превышали величину дефекта диа-
фрагмы. Это обеспечивает выбухание купола в
грудную клетку, возможность расширения брюш-
ной полости, а также сводит к минимуму перерас-
тяжение легкого. Прежде, чем ушивать диафрагму,
в грудную клетку ставят дренаж, который вы-
водят наружу через одно из нижних межреберий.
При больших дефектах задний валик диафраг-
мы может быть плохо выражен или вообще отсут-
ствовать. Тогда швы проводятся вокруг нижнего
ребра. Тефлоновая сетка быстро приживает как
к краям диафрагмы, так и к грудной стенке. С ро-
стом ребенка она имеет тенденцию к уплощению,
в то время как сама диафрагма растет. Именно
поэтому некоторые хирурги предлагали использо-
вать для закрытия дефекта широчайшую мышцу
спины и лоскуты из мышц брюшной стенки на
ножке. Однако мы считаем, что это вмешательство
неоправданно сложное и связано с излишней до-
пол иител ьной тра вмой.
После восстановления диафрагмы брюшную
стенку растягивают руками, чтобы увеличить ем-
кость брюшной полости и возможности для распо-
ложения в ней кишечника. Если слои брюшной
стенки не .могут быть сопоставлены без существен-
ного повышения внутрибрюшного давления, что
обычно связано с растяжением кишечных петель
воздухом, то к краям раны подшивают силиконо-
вое покрытие, формируя таким образом вентраль-
ную грыжу. В течение недели после операции эго
покрытие уменьшают в размерах, постепенно пере-
вязывая как мешок, все ближе и ближе к брюшиой
стенке. Когда же достигнуто такое состояние, что
края раны могут быть сближены без существенно-
го натяжения, производят вторичное ушивание ра-
ны брюшиой стенки.
Послеоперационное лечение. Дренирование
плевральной полости осуществляют с использова-
нием пассивного оттока (водяной затвор), а не ва-
куума, ибо легкие у этих детей легко рвутся при
повышении эндобронхиального давления. При пас-
сивном оттоке по мере относительного постепенно-
го расширения легких воздух и жидкость оттекают
из плевральной полости. При спонтанном же ды-
хании или кашле воздух слишком интенсивно вы-
ходит из интраплеврального пространства и может
возникнуть значительное разряжение в плевраль-
ной полости. При этом наступает перерастяжение
альвеол, нарушение легочной капиллярной перфу-
зии, ухудшение показателей газов крови. В такой
ситуации для уменьшения перерастяжения воздуш-
ных пространств может понадобиться инстилляция
воздуха обратно в плевральную полость. В после-
операционном периоде «здоровое» легкое расправ-
ляется первым, смещая средостение к средней ли-
пни или даже на сторону грыжи. Позже растягива-
ется и растет и ипсилатеральное легкое, однако
оно не всегда увеличивается настолько, чтобы сме-
стить средостение к средней линии. Баротравма
с пневмотораксом может возникнуть как на сторо-
не грыжи, так и на противоположной. В такой си-
туации показатели концентрации газов крови вне-
запно снижаются и прогноз соответственно значи-
тельно ухудшается,53
Для поддержания гипокапнии и уровня pH боль-
ше 7,5 вентиляционную поддержку продолжают
и после операции. Всякую коррекцию режимов
вентиляции, в частности, снижение давления, ча-
стоты или FlOj, следует проводить очень медлен-
но, поскольку малейшие изменения могут резко
усилить легочную вазоконстрикцию.
В первые 24—48 часов после операции интраве-
нозные инфузии должны проводиться раствором
Рингер-лактата в связи с выраженной чрескапил-
лярной потерей плазменного объема. При тяжелой
предшествовавшей гипоксии могут возникнуть
кардиомиопатия и почечная недостаточность. По-
этому при внутривенном введении жидкости необ-
ходим мониторинг давления в правом сердце
и иногда эхокардиография. Если возникает повы-
шение давления в правом сердце, может потребо-
ваться инфузия допамина или добутамина.
Результаты лечения. Среди детей, которые
рождаются живыми непосредственно в медицин-
ском центре, где производится оперативное ле-
чение, летальность превышает 60—65%. Из па-
циентов, имеющих с рождения симптоматику и
относительно благополучно перенесших транспор-
тировку в детские хирургические центры, умирают
35—50%.............. У детей, требующих экст-
ренного хирургического лечения в течение первых
6—24 час жизни, летальность, по сравнению с бо-
лее старшими пациентами, намного выше. Столь
высокие показатели летальности мало менялись
в течение 10 лет, предшествовавших 1985 г., не-
смотря на значительные достижения в тот период
в области неонатальной интенсивной терапии.
У большинства детей легкие были столь тяжело
гипоплазированы, что достичь адекватной венти-
ляции не представлялось возможным. Увеличение
выживаемости иа 10—15% может быть обеспечено
благодаря использованию высокочастотной венти-
ляции и ЭКМО, что позволяет, отложив опе-
ративное вмешательство, корригировать за это
время состояние легочных артерий.
У некоторых из выживших пациентов отмеча-
ется задержка умственного развития и неврологи-
ческие расстройства. Естественно, что с повышени-
ем выживаемости детей с ВДГ (благодаря активно
проводимым, порой героическим реанимационным
мероприятиям) эта проблема становится все более
актуальной.55 Определенное значение в возникно-
вении этих последствий имеют сочетанные анома-
лии мозга, однако главную роль чаще играет ги-
поксия, связанная с длительным периодом неадек-
ватной вентиляции и нарушением перфузии мозга.
У детей, выписывающихся из стационара, состо-
яние легких в последующем может варьировать
в значительных пределах. В тех случаях, когда до-
и послеоперационный период протекал относите-
льно благополучно, легкие функционируют нор-
мально, в то время как при тяжелых формах ле-
240 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
точной гипоплазии отмечаются нарушения венти-
ляционной функции, а потому в первые несколько
месяцев таких пациентов следует тщательно обе-
регать от наслоения респираторной инфекции.
Ни в одном центре, к сожалению, не оказалось
возможным провести изучение отдаленных резуль-
татов абсолютно у всех пациентов, выживших по-
сле лечения ВДГ. Однако, по имеющимся данным,
рост тканевых легочных элементов продолжается
(притом ускоренно) вплоть до 8 10 лет, позволяя
компенсировать задержку развития, отмечавшуюся
при рождении. При рентгенологическом обследова-
нии выявляется нормальное положение средосте-
ния и обычная картина в легких. В некоторых
сообщениях указывается, что в 20% случаев опре-
деляется уменьшение легочного объема и повы-
шенная прозрачность ипсилатерального легкого,
обусловленная эмфизематозными изменениями
или нарушением васкуляризации.56, 9 Радиоизо-
топное вентиляционно/перфузионное сканирова-
ние показывает почти равный объем обоих легких.
По данным некоторых авторов, на стороне грыжи
отмечается нарушение перфузии/7' 6 Общая ем-
кость легких нормальная или уменьшена, а оста-
точный объем и функциональная остаточная ем-
кость увеличены соответственно до 136% и 122%
по отношению к норме. Показатели жизнен-
ной емкости, объема форсированного выдоха и
максимальной вентиляции легких варьируют от
нормальной до уменьшенной, что объясняется об-
структивным компонентом поражения легких, свя-
занным с резидуально небольшими по размерам
воздушными путями.” 60 Тесты с нагрузкой пока-
зали неизмененные значения максимального по-
ступления кислорода и уровня газов капиллярной
крови. УЗИ сердца выявляет обычное состояние
его полостей и функции клапанов, а также отсут-
ствие признаков остаточной легочной гипертензии.
Клинически у пациентов не отмечается каких-либо
отклонений от нормы, и они обычно не ограничива-
ют себя в плане физической нагрузки, которую
переносят безболезненно.
РЕТРОСТЕРНАЛЬНЫЕ ГРЫЖИ
Существуют две формы ретростернальных грыж.
При пентаде Кантрелла в ретростерналыюм от-
деле диафрагмы и перикарде имеется врожден-
ный дефект, который сочетается с эпигастраль-
ным диастазом или грыжей пупочного канатика
(см. рис. 19-1 Qi).61 6 Часто при этом дистальная
часть грудины короткая или расщеплена, а также
отмечаются пороки сердца, обычно дефект межже-
лудочковой перегородки, тетрада Фалло или ди-
вертикул миокарда, исходящий из левого желудоч-
ка. Лечение этой формы аномалии состоит в под-
шивании диафрагмы к грудине. В некоторых слу-
чаях может понадобиться заплата из тефлона или
дакрона, которой можно также прикрыть большой
дефект брюшной стенки в эпигастральной области.
Второй вид ретростернальной грыжи носит на-
звание парастернальной или грыжи через отвер-
стие Морганьи (см. рис. I9-1B, а). При данном ва-
рианте грыжевое выпячивание происходит через
щель между стернальным и реберным краями
диафрагмы, представляющий в норме маленькое
отверстие, через которое проходят сосуды (epigast-
ric/internal mammary). Эти грыжи могут быть как
одно-, так и двусторонними. В отличие от грыжи
при пентаде при парастернальном выпячивании
имеется грыжевой мешок. Большинство случаев
этой формы ретростернальных грыж описаны
у взрослых, имевших ожирение или перенесших
в анамнезе травму. Жировая ткань может как бы
вклиниваться в небольшой диафрагмальный де-
фект, «раскрывая» его и прокладывая путь для по
следующего внедрения печени и кишечника. У боль-
шинства взрослых течение, как правило, бессим-
птомное и диагноз ставится случайно по данным
рентгенограммы грудной клетки, сделанной по
другому поводу.
У детей парастернальные грыжи встречаются
с частотой 1 на 20 врожденных заднелатеральных
диафрагмальных грыж,63 и, в отличие от их те-
чения у взрослых, имеют обычно клинические
проявления, вызывая кашель, удушье, рвоту и не-
приятные ощущения в эпигастральной области.
Нередко отмечаются разнообразные сочетанные
аномалии, особенно врожденные пороки сердца
и трисомия 21. Правая сторона поражается в 5 раз
чаще левой. Грыжевым содержимым могут яв-
ляться (в порядке убывающей частоты) часть пе-
чени, тонкая кишка, толстая кишка, селезенка
и желудок (рис. 19-5).
Оперативное лечение осуществляю! путем лапа
ротомии, торакотомии или комбинированного то-
ракоабдоминального доступа. При большом дефек-
те задний его край может быть расположен очень
близко к диафрагмальному нерву, а потому при
такой локализации предпочтителен торакальный
доступ, позволяющий избежать повреждения нерва
при наложении швов на диафрагму. Двустороннш
грыжи требуют трансабдомипального доступа.
ЭВЕНТРАЦИЯ ДИАФРАГМЫ
Эвентрация диафрагмы может быть обусловлена
нейрогенными причинами или дефектом развития
сухожильного центра либо мышечной части диа-
фрагмы. Нейрогенные причины включают в себя
врожденное отсутствие клеток переднего рога (бо-
лезнь Верднига—Гоффмана) или повреждение диа-
фрагмального нерва. ' Наиболее часто нерв по-
вреждается вследствие растяжения шеи и плеч при
прохождении ребенка через родовые пути при
осложненных родах. Обычно в таких случаях име-
ется и сочетанный паралич плечевого сплетения
(паралич Эрба—Дюшена или Клюмпке). Эвентра-
цию диафрагмы может вызвать травма диафраг-
мального нерва во время операций па шее и средо-
стении, а также воспалительные процессы или
опухоли, локализующиеся вблизи него.
Что касается врожденной эвентрации, то она
иногда ограничивается небольшим участком диа-
фрагмы, а порой охватывает всю грудобрюшную
преграду, так чтл имеется лишь плевроперитоне-
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 241
Рис. 19-5. Рентгенограммы грудной клетки и брюшном полости в переднезадней (А) и боковой (В) проекциях. Виден барии в же-
лудке, расположенном ниже диафрагмы, и в тонкой кишке, которая находится в праной половине грудной клетки (грыжевое выпя-
чивание через правое отверстие Морганьи).
альная мембрана. В этом случае различие между
эвентрацией и ВДГ с грыжевым мешком весьма
условно. Врожденная эвентрация встречается бо-
лее часто слева, однако описано и двустороннее
поражение. Значительное по размерам грыжевое
выпячивание может привести внутриутробно к
развитию легочной гипоплазии. Другие сочетан-
ные аномалии редки, хотя описаны наблюдения
трисомии 13—15 и 18.
При положительном внутрибрюшном давлении
свободно «висящая» диафрагма выпячивается в
грудную клетку, что усугубляется в положении
больного на спине. Во время вдоха отрицательное
внутриторакальное давление приводит к парадок-
сальному увеличению грыжевого выпячивания ор-
ганов в грудную клетку и смещению средостения
в противоположную сторону. Обычные клиниче-
ские проявления — респираторный дистресс и
пневмония. Иногда развиваются симптомы со сто-
роны ЖКТ, такие как неприятные ощущения
в эпигастральной области, рвота и даже заворот
желудка с соответствующей симптоматикой.
Диагноз устанавливают с помощью рентгеногра-
фии грудной клетки, выявляющей высокое стояние
диафрагмы. А при исследовании под экраном или
на УЗИ можно увидеть парадоксальные ее движе-
ния во время вдоха и выдоха. Для дифференци-
альной диагностики эвентрации с опухолями.
врожденными кистами легкого, секвестрацией, вос-
палительным легочным инфильтратом и плевраль-
ным выпотом рекомендуется применять пневмопе-
ритонеум, изотопное сканирование печени, конт-
растное исследование ЖКТ и компьютерную то-
мографию.
В случае приобретенного паралича диафраг-
мального нерва лечебная тактика может быть вы-
жидательной. Однако если вентиляционная под-
держка необходима в течение более 2-х недель
следует предпринять хирургическое вмешатель-
ство. Небольшая локальная эвентрация, протекаю-
щая бессимптомно, не требует операции. В тех же
случаях, когда вовлечена большая часть диафраг-
мы, это неблагоприятно влияет на функцию лег-
ких, а потому должна быть предпринята хирурги-
ческая коррекция. Операция осуществляется через
торакотомический доступ в 7-м межреберье. Диа-
фрагму гофрируют в складки широкими швами
нерассасывающимся материалом. Если поражена
часть диафрагмы, иннервируемая диафрагмальным
нервом, трансторакальный доступ позволяет визу-
ализировать веточки нерва и избежать его повреж-
дения во время наложения швов. При вовлечении
значительной части диафрагмы, особенно в случа-
ях, когда имеется паралич нерва или двусторонняя
эвентрация, наиболее эффективно транса бдоми-
нальное вмешательство.
16 Закнз № 1622
242 ДИАФРАГМАЛЬНЫЕ ГРЫЖИ
ЛИТЕРАТУРА
1. Вготап 1: Uber die Entwicklung des Zwerchfells beim Men-
schen. Verh Anat Ges 16:9—17, 1902.
2. Wells. 1J: Development of the human diaphragm and pleural
sacs. Contr Embryol Carneg Insin 35:107—137. 1954.
3. Iritani I: Experimental study on embryogenesis of congenital
diaphragmatic hernia. Anat Embryol 169:133—139. 1984.
4. Kluth D, Petersen C, Zimmerman HJ: The developmental anato-
my oi the diaphragm. Paediatr Surg Int 2:322—326, 1987.
5. Bremer JL: The diaphragm and diaphragmatic hernia. Arch
Pathol 36:539—549. 1943.
6. Coca MA, Landin F: Malformations congenitales multiples avec
absence presque complete de diaphragm. Sent Hop Paris
33:3839. 1957.
7. Roe BB. Stephens HB: Congenital diaphragmatic hernia and
hypoplastic lung. J Thorac Surg 32:279—290, 1956.
8. Boyden EA: Hodson WA (Editor). Development and growth of
the airways. In Development of the Lung. Marcel Dekker, New
York, pp 3—35, 1977.
9. Hislop A. Reid LM: Formation of the pulmonary vasculature. In
Hodson WA (Editor). Development of the Lung. Marcel Dek-
ker, New York, pp 37—86, 1977.
10. Areechon W, Ried L: Hypoplasia of the lung with congenital
diaphragmatic hernia. Br Med J 1:230 233. 1963.
11. de lorimier AA, Tierney DF, Parker MR: Hypoplastic lungs in
fetal lambs with surgically produced congenital diaphragmatic
hernia. Surgery 62:12—17, 1967.
12. Kitigawa M, Hislop A, Boyden EA, Ried LM: Lung hypoplasia
in congenital diaphragmatic hernia: A quantitative study of air-
way, artery, and alveolar development. Br J Surg 58:342—346,
1971.
13. Geggel RL. Murphy JD, Langleben D, et al.: Congenital diaph-
ragmatic hernia; arterial structural changes and persistent pul-
monary hypertension after surgical repair. J Pediatr 107:457—
464, 1985.
14. Puri P, Dewan P: Historical review. In Puri P (Editor). Conge-
nital Diaphragmatic Hernia, Volume 24. Karger, Basel, pp 1 —
6, 1989.
15. Bochdalek VA: Einigc Betrachtungen iiber die Entstehung des
angelborenen Zwerchfellbruchcs. A Is Bietrag zur pathologi-
schen. Anatomie der Hernien. Vjsch Prakt Heik 19:89 97.
1848.
16. Heidenhain L: Geschichte eines Failes von chronischer. Incarce-
ration des Magens in einer angehorenen Zwerchfellherme wel-
cher durch Laparotomie geheilt wurde, mitanschiessenden Be-
rne rk ungen iiber die Moglichkert, das Kardiacarcinom der Spci-
serohre zu reseciren. Dl Z Chir 76:394—403, 1905.
17. Harrison MR, Langer JC, Adzick NS. et al.: Correction of di-
aphragmatic hernia in utero V. Initial clinical experience. J Pe-
diatr Surg 25:47—-55, 1990.
18. Nakayama DK. Harrison MR, Chinn DH et al.: Prenatal di-
agnosis and management of the fetus with congenital diaphrag-
matic hernia: Initial clinical experience. J Pediatr Surg 20:118
124, 1985.
19. Hatch El, Kendall J: Stomach position as an in-utero predictor
of neonatal outcome in left-sided diaphragmatic hernias. J Pedi-
atr Surg (In print).
20. Puri F: Epidemiology of congenital diaphragmatic hernia. In
Puri P (editor). Congenital Diaphragmatic Hernia, Volume
24. Basel. Karger, pp 22—27, 1989.
21. Misha lany H. Gordo J: Congenital diaphragmatic hernia in mo-
nozygotic twins. J Pediatr Surg 21:372-—-374, 1986.
22. Newman BM, Afshani E. Karp MP. et al.: Presentation of conge-
nital diaphragmatic hernia past the neonatal period. Arch Surg
121:813—816, 1986.
23- Berman L, Stringer D. Ein SI I. Shandling B: The late-prescn-
ting pediatric Bochdalek hernia: A 20-year review. J Pediatr
Surg 23:735 -739. 1988.
24. Drummond WH. Gregory GA. Heyinann MA, Phibbs RA: The
independent effects of hyperventilation, tolazoline and dopamine
on infants with persistent pulmonary hypertension. J Pediatr
98:603 611, 1981.
25- Ein SH. Barker G, Olley P, et al.: The pharmacologic treatment
of newborn diaphragmatic hernia — A 2-year evaluation. J Pe-
diatr Surg 15:384—394, 1980.
26 Reynolds M, Luck SR, Lappen R: The “critical” neonate with
diaphragmatic hernia. A 21-year perspective. J Pediatr Surg
19:364 369, 1984
27. Meadow W, Bern A, Giardini G: Clinical correlates do not pre-
dict Pao2 responses after tolazoline administration in hypoxic
newborns. Crit Care Med 14:548 551, 1986.
28. Soifer S, Clyman RI, Heymann MA: Effects nf prostaglandin
D2 on pulmonary artery pressure and oxygenation in newborn
infants with persistent pulmonary hypertension. J Pediatr
112:774—777, 1988.
29. Ein SH, Barker G: The pharmacologic treatment of newborn
diaphragmatic hernia—update, 1987. Pacdiair Surg Int 2:341 —
345, 1987.
30. Paidas CN. Dudgeon DL, Haller JA, Clemens MG: Adenosine
triphosphate: A potential therapy for hypoxic pulmonary hy-
pertension. J Pediatr Surg 23:1154 1160, 1988.
31. Frostell C, Fratacci M, Wain JC, et al.: Inhaled nitric oxide.
A selective pulmonary vasodilator reversing hypoxic pulmonary
vasoconstriction. Circulation 83:2038, 1991.
31a. Boros SJ, Mammel MC: A practical guide to high-frequencj
ventilation. Pediatr Ann 17:508- 516, 1988.
32. Sakai H, Tamura M, Bryan AC, et al.: The effect of surgical
repair on respiratory mechanics in congenital diaphragmatic her-
nia. J Pediatr 111:432—458, 1987.
33. I anger JC, Filler RM. Bohn DJ, el al.: Timing of surgery for
congenital diaphragmatic hernia: Is emergency operation neces-
sary? J Pediatr Surg 23:731 — 734. 1988.
34. Wilson JM, Lund DP. Lillehei CW, el al.: Delayed surgery and
preoperative ECMO docs not improve survival in high risk con-
genital diaphragmatic hernia. J Pediatr Surg (In print).
35. Boix-Ochoa J, Peguero G, Seijo G. el al.: Acid-base balance and
blood gases in prognosis and therapy of newborn infants with
diaphragmatic hernia. J Pediatr Surg 9:49—57, 1974.
36. Mishalany HG, Nakada K, Woolley MM: Congenital diaphrag-
matic hernias; eleven years’ experience. Arch Surg 114:1118—
1123, 1979.
37. Ruff SJ, Campbell JR, Harrison MW, Campbell TJ: Pediatric
diaphragmatic hernias. Am J Surg 139:641—645, 1980.
38. Dibbins AW, Wiener ES: Mortality from diaphragmatic hernia.
J Pediatr Surg 9:653—662, 1974.
39. Harrington J, Raphaely RC, Downs JJ: Relationship of alveolar-
arterial oxygen tension difference in diaphragmatic hernia of
the newborn. Ancsthcsiolngy 56:473—476, 1982.
40. Krummel TM, Greenfield LJ, Kirkpatrick BV, et al.: Alveolar-
arterial oxygen gradients versus the neonatal pulmonary insuf-
ficiency index for the prediction of mortality in ECMO candida-
tes. J Pediatr Surg 19:380 384, 1984.
41. Bohn DJ: Ventilatory and blood gas parameters in predicting
survival in congenital diaphragmatic hernia. Pacdiat Surg Int
2:336—340, 1987.
42. Bohn DJ, Tamura M, Perrin D, et al.: Ventilatory predictions of
pulmonary hypoplasia in congenital diaphragmatic hernia, con-
firmed by morphometry. J Pediatr 111:423—431, 1987.
43. W'ilson JM, Lund DP, Lillehei CW, et al.: Congenital diaphrag-
matic hernia: Predictors of severity in the ECMO era. J Pediatr
Surg 26:1028—1033, 1991.
44- Newman KD, Anderson KD, Van Meurs K, cl al.: Exlracnrpore-
al membrane oxygenation and congenital diaphragmatic hernia:
Should any infant be excluded? J Pediatr Surg 25:1049—1053,
1990.
ДИАФРАГМАЛЬНЫЕ ГРЫЖИ 243
45. Andrews AF. Nixon CA, Cillev RE, ei al.: Onc-to-three-year
outcome for 14 neonatal survivors of extracorporeal membrane
oxygenation. Pediatrics 78:692 698, 1986.
46. Towne BH Loti IT. Hicks DA, Healey T: Long-term followup
of infants and children with extracorporeal membrane oxygena-
tion (ECHO): A preliminary report. J Pediatr Surg 20:410
414. 1985.
47. Langham M, Krummel TM. Bartlcll RH, et al.: Mortality with
extracorporeal membrane oxygenation following repair of conge-
nital diaphragmatic hernia in 93 infants. J Pediatr Surg
22:1150—1154. 1987.
48. Johnston PW. Bushncr В, I iberman R, cl al.: Clinical use of
extracorporeal membrane oxygenation in the treatment of persis-
tent pulmonary hypertension following surgical repair of conge-
nital diaphragmatic hernia. J Pediatr Surg 23:908 912, 1988.
49 Redmond C. Heaton J. Calix J. ct al.: A correlation of pulmona
ry hypoplasia, mean air way pressure, and survival in congenital
diaphragmatic hernia treated with extracorporeal membrane
oxygenation, J Pediatr Surg 22:1143—1149. 1987.
50 Slolar C. Dillon P. Reyes C: Selective use of cxiracurpureal
membrane oxygenation in the management of congenital diaph-
ragmatic hernia. J Pediatr Surg 23:207—211, 1988.
51. Connors RH, Ггасу T, Bailey PV, et al.: Congenital diaphrag-
matic hernia repair on ECMO. J Pediatr Surg 25:1043—1047,
1990.
52. Bax NMA. Collins DL: The advantages of reconstruction of the
dome of the diaphragm in congenital posterolateral diaphragma-
tic defects. J Pediatr Surg 19:484—487, 1984.
53. Srouji MN. Buck B, Downs JJ: Congenital diaphragmatic hernia:
Deleterious effects of pulmonary interstitial emphysema and ten-
sion cxtrapulmonary air. J Pediatr Surg 16:45—54, 1981.
54. Adzick NS. Harrison MR. Glick PL. et al.: Diaphragmatic her-
nia in the fetus: Prenatal diagnosis and outcome in 94 cases.
J Pediatr Surg 20:357—361. 1985.
55. Chatrath RR. Ei Shafic M, Jones RS: Fate of hypoplastic lungs
after repair of congenital diaphragmatic hernia. Arch Dis Child
46:633—635, 1971.
56. Grotte G, Bjure J, Bratteby L, et al.: Posterolateral diaphragma-
tic hernia—Long-term results. Prog Pediatr Surg 10:35 44,
1977.
57. Ried IS, Hutcherson RJ: Long-term follow-up of patients with
congenital diaphragmatic hernia. J Pediatr Surg 11:937—942,
1976
58. Wohl ME, Griscom NT. Strcidcr DJ. ct at: The lung following
repair of congenital diaphragmatic hernia. J Pediatr 90:405—
414, 1977.
59. Landaw LI, Phelan PD. Gillam GL. et al.: Respiratory function
after repair of congenital diaphragmatic hernia. Arch Dis Child
52:282—286. 1977.
60. Thurlbeck WM. Kidn K. Langston C, ct al.: Postnatal lung
growth after diaphragmatic hernia. Thorax 34:338—343, 1979.
61. Cantrell JR, Haller JA, Ravilch MM: A syndrome of congenital
defect involving the abdominal wall, sternum, diaphragm, peri-
cardium and heart. Surg Gynecol Obstet 107:602—614 1958.
62. Milne LW. Moroson AM. Campbell JR. Harrison MW: Pars
sternalis diaphragmatic hernia with omphalocele: A report of
two cases. J Pediatr Surg 25:726—730. 1990.
63. Pokorney WJ, McGill CW, Harberg FJ: Morgagni hernias du-
ring infancy. Presentation and associated anomalies. J Pediatr
Surg 19:394—397, 1984.
64. Mellins RB, Hays AP, Gold AP, et al.: Respiratory distress as
the initial manifestation of Werdnig-Hoffmann disease. Pedi-
atrics 53:33—40, 1974.
65. Smith CD, Sade RM, Crawford FA, Olhersen HB: Diaphragma-
tic paralysis and eventration in infanis. J I'horac Cardiovasc
Surg 91:490—497, 1986.
КРАТКИЕ АННОТАЦИИ
Puri P (Editor): Congenital Diaphragmatic Hernia, volume 24. Mo-
dern Problems in Pediatrics. Karger, Basel, 1989. Работа напи-
сана несколькими авторами. В ней отражены вопросы исто-
рии, эпидемиологии, патологии, лечения (и его результа-
тов) диафрагмальной грыжи и эвентраиии диафрагмы у ма-
леньких детей.
Anderson KD: Congenital diaphragmatic hernia, fn Welch KJ. el
al. (Editors). Pediatric Surgery. 4th edition. Medical Year Book
Publishers, Chicago, pp 589 601, 1986. В этой главе пред-
стаплсн всеобъемлющий обзор современной литературы по
диафрагмальным грыжам.
Глава 20
ОПУХОЛИ СРЕДОСТЕНИЯ
Большинство опухолей грудной клетки у детей
исходят из средостения, что отчасти объясняется
редкостью новообразований легких в цетеком воз-
расте. Кроме истинных опухолей средостения у де-
тей часто встречаются разнообразные врожденные
аномалии и кисты. Медиастинальные опухоли мо-
гут вызывать жизнсопасное сдавление дыхатель-
ных путей, особенно у малышей первого года жиз-
ни. Если нс принимать во внимание лимфомы, то
частота малигнизации колеблется от 20 до 30%.1
С учетом же лимфом этот показатель возрастает
до 57%?'4 Риск сдавления дыхательных путей
и высокая частота малигнизации обусловливают
необходимость ранней диагностики и своевремен-
ного лечения детей с любыми опухолями средо-
стения.
Частота и клинические проявления. На рисун-
ке 20-1 показана сравнительная частота опухолей
средостения в детском возрасте и в общей популя-
ции. Примерно одна треть медиастинальных опу-
холей выявляется у детей в возрасте до 2 лет. Со-
отношение доброкачественных и злокачественных
образований обычно одинаковое в младших и стар-
ших возрастных детских группах. Однако дети до
2 лет со злокачественными медиастинальными
опухолями имеют в среднем лучший прогноз, чем
более старшие пациенты. Эта разница может быть
объяснена большим количеством у маленьких де-
тей нейробластом, имеющих благоприятные исхо-
ды, и более высокой частотой у старших детей не-
ходжкинских лимфом и недифференцированных
сарком.
У детей младше 2 лет типичным проявлением
медиастинальных опухолей является выраженный
респираторный дистресс, часто появляющийся
вскоре после рождения. ‘ Симптомы дыхательных
расстройств объясняются тем, что у маленьких де-
тей трахеальные и бронхиальные кольца легко
сдавливаются. Что же касается старших детей
с доброкачественными опухолями, то среди них
лишь одна треть имеет проявления со стороны
дыхательных путей, притом значительно менее тя-
желые. Как правило, респираторные симптомы
бывают особенно выраженными при наслоении
острой инфекции дыхательных путей.
Классификация. Опухоли, исходящие из средо-
стения, могут быть классифицированы соответст-
венно анатомическому делению средостения на три
части, четко определяемые на боковой рентгено-
грамме грудной клетки: переднее средостение, цент-
ральное и паравертебральная борозда (рис. 20-2).6
Переднее средостение ограничено грудиной, верх-
ней апертурой грудной клетки и передней поверх-
ностью сердца. Центральное средостение располо-
жено между передней поверхностью тел позвонков
и передним средостением. Паравертебральная бо-
розда, которая локализуется кзади от передней по-
верхности тел позвонков, не является по сути ана-
томическим отделом средостения, но она включена
сюда, поскольку нейрогенные опухоли возникают
именно в этой области. Болес 90% медиастиналь-
ных образований у детей располагаются в одном
из этих трех отделов. Субсгернальные опухоли
щитовидной и паращитовидной желез, которые
встречаются в верхнем средостении у взрослых,
в детском возрасте чрезвычайно редки.
Диагностика медиастинальных опухолей начи-
нается с тщательного выяснения анамнеза и фи-
зикального обследования. Если у маленького ре
бенка, здорового во всех других отношениях, в
анамнезе отмечается лишь стойкое тахипноэ в те-
чение длительного периода времени, то следует
думать о доброкачественной опухоли больших раз-
меров, например о кистозной тератоме или лим-
фангиоме. Шумное или стридорозное дыхание,
появляющееся сразу или вскоре после рождения,
типично для доброкачественных образований,
сдавливающих трахею или бронхи, таких, как
бронхогенная киста или кистозная гигрома. Разви-
тие симптомов сдавления дыхательных путей или
окклюзии верхней полой вены в школьном возра-
сте характерно для не-ходжкинской лимфомы. ''
При стертом начале заболевания и длительных
(в течение недель и месяцев) лихорадке, недомога-
нии и потере массы тела необходимо подозревать
болезнь Ходжкина или хроническое инфекционное
ОПУХОЛИ СРЕДОСТЕНИЯ 245
г 4 6 8 Ю 1г 14 16 18 20 22 24 26 26 30 32 34 36 38
НЕЙРОГЕННЫЕ ОПУХОЛИр^^^^/^^^
ОПУХОЛИ ТИМУСА^^ 3 -| |в
ТЕРАТОМЫ К
ЛИМФОМЫ
КИСТЫ из ПЕРЕДНЕЙ КИШКИ
WSS/TSSS/ASW
ОПУХОЛИ ИЗ ЗАРОДЫШЕВЫХ КЛЕТОК
Кол-во (сводная статистика)
^ЯЕТИ
ГД БОЛЬНЫЕ
'—' ВСЕХ
ВОЗРАСТОВ
МЕЗЕНХИМАЛЬНЫЕ ОПУХОЛИ,___
ВКЛЮЧАЯ АНГИОЛИМФОМЫ С_________" 1т
ЭНДОКРИННО-ФУНКЦИОНИРУЮЩИЕ1 -
ОПУХОЛИ! --------16 *
IZ СЛУЧАЯ
ПЕРИКАРДИАЛЬНЫЕ КИСТЫ}--------
564
2729
* Процент вычисляется из меньшего кол-ва. чем
в сводной статистике, поскольку данный вид был
представлен не во всех работах
Г j'Z
Рис. 20-1. Распределение по частоте медиастинальных опухолей (по данным сводной статистики) у пациентов всех возрастов
(СМ. литературу 1, 2, 4. 43, 44, 47, 64. 84).
заболсвание, например гистоплазмоз или тубер-
кулез.
При осмотре маленьких детей с лимфангиомами
и более старших с лимфомами обычно видно опу-
холевидное образование над ключицей. При ге-
мангиомах наблюдаются соответствующие измене-
ния кожи. У детей с нейробластомами могут отме-
чаться такие симптомы, как некоординированные
движения глаз, атаксия, неврологические проявле-
ния сдавления спинного мозга или синдром Гор-
нера.
Рентгенограммы грудной клетки в переднезад-
ней и боковой проекциях позволяют определить
локализацию опухоли в средостении, ее размеры,
форму, наличие кал ьцифи катов. Относительно
ограниченная по размерам опухоль в центральном
средостении характерна для кисты, происходящей
из передней кишки. На ззофагограмме эта киста
имеет вид округлого образования, расположенного
вне пищевода. Эзофагография под контролем эк-
рана позволяет оценить функцию пищевода и та-
кие особенности опухоли, как пульсация, подвиж-
ность, смешаемость. Иногда может быть информа-
тивной сцинтиграфия с технецисм-OOm. особенно
246 ОПУХОЛИ СРЕДОСТЕНИЯ
при диагностике кишечного удвоения, содержаще-
го слизистую желудка.
Компьютерная томография (КТ) или ядерный
магнитный резонанс (ЯМР) показаны почти по
всех случаях, когда после первичных рентгено-
грамм грудной клетки диагноз, локализация и раз-
меры опухоли остаются неясными.8 Как КТ, так
и ЯМР обладает большими достоинствами во мно-
гих специфических ситуациях. При проведении ис-
следования с ЯМР больной не подвергается иони-
зирующей радиации и не требуется внутривенное
введение контрастных веществ. У этого метода
лишь два недостатка — длительность исследова-
ния и высокая стоимость. КТ особенно точно по-
зволяет идентифицировать кальцификаты малень-
ких размеров, которые обычно определяются в
нейробластоме. Небольшие пакеты лимфоузлов
и бронхиальные аномалии также лучше выявля-
ются на КТ. Что же касается диагностики сосуди-
стых аномалий, то хотя ЯМР превосходит в этом
плане КТ-изображение, однако если КТ дополнить
внутривенным введением контрастных веществ, то
этот метод не уступает по информативности ядер-
ному магнитному резонансу. В случае применения
КТ, позволяющей точно установить анатомические
особенности, необходимость в бронхоскопии и эзо-
фагоскопии возникает редко. Тем не менее в нео-
бычных клинических ситуациях, когда трудно от-
дифференцировать сдавление дыхательных путей
опухолью снаружи от обструкции инородным те-
лом или образованием, расположенным внутри
просвета, может быть показана бронхоскопия Эта
процедура должна производиться только в опера-
ционной и в присутствии хирурга, готового осуще-
ствить экстренное вмешательство для ликвидации
сдавления дыхательных путей, поскольку бронхо-
скопия иногда усугубляет обструкцию.
Острая обструкция дыхательных путей при
введении в наркоз. Большинство хирургов реко-
мендуют удалять медиастинальные опухоли и ки-
сты сразу, как только они обнаружены, независимо
от того, есть клинические проявления или нет.
Консервативно лечатся лишь лимфомы. Гистоло-
гический диагноз обычно устанавливается путем
биопсии опухоли (из шейного доступа). Наш опыт
работы в Техасском Детском Госпитале показал,
что торакотомии (для адекватной биопсии) требу-
ют менее 5% детей с лимфомами. Уточнение вида
клеток лимфомы важно в основном для выбора
наиболее эффективного метода химиотерапии (см.
гл. 69).
В литературе существуют многочисленные сооб-
щения о случаях остро возникающей тотальной
обструкции дыхательных путей в результате их
сдавления при введении в наркоз детей с больши-
ми опухолями средостения.' Поэтому очень важ-
но до операции с помощью КТ определить, име-
ется ли сдавление трахеобронхиального дерева
и насколько оно выражено (рис. 20-3). Такие дети
должны получать стероиды, химио- и рентгеноте-
рапию до операции для того, чтобы уменьшить
размеры опухоли и восстановить проходимость ды-
хательных путей до вмешательства.’' 1 13 К сожа-
лению, н подобных ситуациях достоверная иденти-
фикация в последующем вида клеток уменьшив-
шейся опухоли бывает невозможной. Это часто
означает, что ребенок получил более высокую дозу
химиотерапии, чем следовало бы назначить.
ОПУХОЛИ ПАРАВЕРТЕБРАЛЬНОЙ БОРОЗДЫ
Из опухолей средостения у детей наиболее часто
встречаются нейробластомы и ганглионевромы.
Почти все опухоли паравертебральной борозды
нейрогенного происхождения и развиваются из
симпатических ганглиев?'4 Подробно они описаны
в главе 66.
Передние торакальные менингоцеле. Интра-
торакальные менингоцеле — очень редкая патоло-
гия, но о ней нельзя забывать, когда проводится
дифференциальная диагностика при опухолях зад-
него средостения. Согласно сводной статистике
(1965 г.) только 4 из 49 пациентов с данным ви-
дом поражения были моложе 16 лет. Считается,
что интраторакальные менингоцеле являются не
«рожденными, а развиваются в результате дегене-
ративных изменений. По данным одной из пуб-
ликаций, из 5 наблюдений этой патологии у детей
в 4 случаях отмечалась выраженная деформация
грудного отдела позвоночника. Трое пациентов
имели неврологические проявления, включая па-
раплегию, генерализованные судороги и полное
отсутствие движений в нижних конечностях.”' 2
В основном считается, что менингоцеле — прогрес
сирующая патология и соответственно подлежит
оперативному лечению.22 Однако авторы, наблю
давшие в течение от года до 10 лет шестерых па-
циентов, не отмечали увеличения опухоли ни у од-
ного из них.18 Диагноз устанавливается с помощью
ЯМР или миелографии.
Нейрогенные кисты. Это редкие кистозные об-
разования заднего средостения, которые могут
быть в различной степени связаны с центральной
нервной системой (ЦНС) и желудочно-кишечным
трактом (ЖКТ). Их называют гастроэнтеральны-
ми кистами, гастроцитомами, энтерогенными кис-
тами или медиастинальными кистами из передней
кишки. Нейрогенные кисты, по-видимому, развива-
ются в тех случаях, когда в процессе эмбриогенеза
не происходит отделение хорды от передней
кишки.
Гистологически в нейрогенных кистах отсутст-
вует серозный слой, но имеются хорошо развитые
мышечные слои и слизистая пищеварительного
тракта, в частности — желудка. Обычно стенка ки-
сты воспалена и изъязвлена, что связано с воздей-
ствием пепсина и кислоты. Симптомы часто по-
являются в раннем детском возрасте и обусловле-
ны воспалительным процессом и увеличением ки
сты. Это боли, анемия, одышка, неврологическая
симптоматика, включая параплегию в результате
сдавления спинного мозга, и другие признаки его
поражения.
Диагноз подтверждается при выявлении сочета-
ния опухоли заднего средостения с аномалиями
спинного мозга, особенно в нижпешеином и верх-
ОПУХОЛИ СРЕДОСТЕНИЯ 247
Рис. 20-3. КТ 11-летней девочки с не-
хцржкинской лимфомой, с та вливающей
трахею и области кмрины.
негрудном отделах (рис. 20-4). такими как spina
bifida anterior, полупозвонок, неполное слияние ду-
жек. Наличие желудочной слизистой может быть
обнаружено путем сцинтиграфии с технением-99т,
что подтверждает происхождение кисты из перед-
ней кишки.23 Связь опухоли с позвоночником
и спинным мозгом лучше всего определяется с по-
мощью ЯМР или КТ-миелографии (рис. 20-4, В
и С).
При ранней диагностике и своевременном вме-
шательстве прогноз прекрасный. Если же наблю-
дать таких детей и воздерживаться от хирургиче-
ского лечения, то осложнения могут быть фаталь-
ными, а именно — изъязвление с перфорацией
и инфекцией ЦНС, особенно в случае возникнове-
ния свища между кистой и спинномозговым ка-
налом.24
ОПУХОЛИ ЦЕНТРАЛЬНОГО СРЕДОСТЕНИЯ
У детей в возрасте до 2 лет в центральном средо-
стении очень редки любые виды опухолей. Но если
они все же встречаются, то это, как правило, брон-
хогенные кисты, протекающие обычно с клиниче-
ской симптоматикой. У детей старше 2 лет в цент-
ральном средостении наиболее часто бывают лим-
фомы.
При этапном хирургическом лечении болезни
Ходжкина с последующей активной химио- и рент-
генотерапией отдаленные результаты прекрас-
ные. Оперативные вмешательства должны быть
ограничены тем минимальным объемом, который
необходим для установления диагноза и стадии за-
болевания (см. главу 69).
Кистозное удвоение передней кишки. Бронхо-
генные кисты и кистозное удвоение пищевода —
аномалии эмбриогенеза, локализующиеся в цент-
ральном средостении и имеющие общее происхож-
дение, — из передней кишки.27 Они примыкают
к пищеводу и трахее, располагаясь обычно около
бифуркации, но редко бывают непосредственно
связаны с ними.28 Эти кисты отличаются от нейро-
генных тем, что позвоночник при них сформиро-
ван правильно. Бронхогенные кисты обычно тон-
костенные, заполнены густой вязкой жидкостью,
выстланы респираторным эпителием, а в стенке
содержат небольшое количество гладких мышц
и иногда — хрящи.
У старших детей эти кисты обычно протекают
бессимптомно и на рентгенограммах грудной клет-
ки имеют вид гомогенного опухолевидного образо-
вания.29 У маленьких же пациентов сразу после
рождения отмечаются эпизоды выраженных дыха-
тельных расстройств. Диагностика может быть
трудна, что связано с большим разнообразием
рентгенологических проявлений. Так, почти у 50%
маленьких детей, имеющих клинические симпто-
мы, опухолевидное образование в средостении на
рентгенограмме грудной клетки может не опреде-
ляться, а отмечаются лишь участки ателектазов
или тяжелого перерастяжения ткани легкого возду-
хом.' ‘ Дифференциальную диагностику следует
проводить с лобарной эмфиземой, пневмонией,
инородными телами, бронхиальным стенозом, га-
мартомой легких и пневмотораксом. Имеются со-
общения о бронхогенных кистах, сочетавшихся
у детей с другими аномалиями трахеобронхиаль-
ного дерева.32 Хотя эзофагограмма и может под-
твердить диагноз, показывая смещение пищевода
кзади, однако этот метод полностью вытеснен
компьютерной томографией (рис. 20-5). КТ прак-
тически устранила необходимость проведения
бронхоскопии и эзофагоскопии у пациентов с
бронхогенными кистами.8 У некоторых маленьких
детей отмечается односторонняя эмфизема, в гаких
случаях необходимо исключить инородное тело.
Иссечение кисты должно проводиться очень
тщательно и осторожно, чтобы избежать поврежде-
248 ОПУХОЛИ СРЕДОСТЕНИЯ
пия стенки бронхов или пищевода. Небольшие ки-
сты, расположенные около карины, могут быть нс
видны до тех пор, пока не вскрыта задняя меди-
астинальная плевра, нс отодвинуто кпереди легкое
и не обнажен проксимальный отдел главного брон-
ха. В тех случаях, когда киста, вызывающая об-
струкцию, остается нераспознанной, хирурги, к со-
жалению, иногда производя г резекцию легочной
ткани, ошибочно принимая обнаруженную патоло-
гию за аденоматозную аномалию легкого или ло-
барную эмфизему/"
Удвоения пищевода составляют примерно 15%
всех удвоений пищеварительного тракта. В проти-
воположность бронхогенным кистам, которые
встречаются, как правило, в раннем возрасте,
у большинстве! детей с удвоениями пишевода симп-
томы появляются в возрасте после 10 лет. Эти уд-
воения бывают двух типов; кисты пищевода и эн-
теральные удвоения. Кисты пищевода — редкий
порок развития. Они, естественно, связаны с пище-
водом, могут располагаться i
слизистую респираторного т
пые элементы в стенке.53 Эти
хогенным, возникают из ано
редней кишки и проявляются
птомами в раннем возрасте.4
тальком иссечении, если т
Иногда киста и пищевод т
в такой ситуации можно ог
слизистой выстилки удвоени
не трогать, оставив ее ипта
Энтеральные удвоения яв;
воениями и соответственно
тую мышечную стенку с а у;
ем и выстланы слизистой ш
кишечника.27 Тс опухолевид
рального средостения, котор,
ними вертебральными аном
собой нейроэнтсральные кис
ются сообщения о выявлен
ОПУХОЛИ СРЕДОСТЕНИЯ 249
Рис. 20'5. Рентгенограмма (А) и КТ (В)
грудной клетки. Видна хорошо очерчен-
ная бронхогенная киста, сдавливающая
трахею.
нервной ткани.34 Эти нейроэнтеральные кисты, по-
видимому, являются результатом неполного отделе-
ния передней кишки от хорды эмбриона.35 Они мо-
гут быть ограничены пределами грудной клетки
и в этом случае обычно не соединяются с пищево-
дом, а порой, имея вид слепого мешка, достигают
больших размеров или прорастают в прилежащие
органы и ткани, что приводит к катастрофическим
осложнениям.36 Благодаря наличию в большинстве
этих удвоений эктопированной слизистой желудка,
диагноз может быть поставлен с помощью сцин-
тиграфии с технецием-99ш?7
В редких случаях, по данным литературы, тора-
кальные удвоения ЖКТ распространяются ниже
диафрагмы, где заканчиваются слепо или соединя-
ются с кишечником?8 Со времени первого описа-
ния в 1950 г. этого варианта патологии опублико-
вано всего 20 наблюдений торакоабдоминальных
удвоений?9 Половина больных были новорожден-
ными и почти все остальные — в возрасте до года.
У новорожденных отмечались респираторные сим-
птомы, у более старших детей — анемия, боли за
грудиной или в эпигастральной области, пептиче-
ские язвы. Все удвоения, за исключением одного,
локализовались в правой половине грудной клет-
ки.40 Почти 60% торакоабдоминальных удвоений
соединялись с нормальным ЖКТ ниже диафрагмы,
а одно - с шейным отделом пищевода?9 В боль-
шинстве случаев отмечались аномалии шейного
или верхне грудного отдела позвоночника. Удвое-
ние следует удалять целиком за одну операцию.
Если это невозможно, хирург должен четко уста-
новить расположение шейной и сублиафрагма ль-
нов части образования, что позволяет избежать
оставления слепого мешка, выстланного слизистой
желудка, секретирующей кислоту (см. главу 35).
ОПУХОЛИ ПЕРЕДНЕГО СРЕДОСТЕНИЯ
Опухоли переднего средостения редки у детей
и представлены обычно лимфомами, особенно лим-
фобластомами, неоплазмами из зародышевых кле-
250 ОПУХОЛИ СРЕДОСТЕНИЯ
ток, поражениями тимуса и мезенхимальными опу-
холями.4*' 42 Хотя злокачественные поражения про-
текают. как правило, с клиническими проявления-
ми, однако наличие симптомов не является спсци-
фичным для малигнизации. При злокачествен-
ных опухолях переднего средостения отмечаются
боли в грудной клетке, кашель, одышка, дисфагия,
осиплость голоса, кровохарканье, связанные со
сдавлением или прорастанием опухоли в смежные
органы и ткани.45 При доброкачественных пораже-
ниях обычно наблюдаются респираторные симпто-
мы в результате сдавления трахеи. Из пациентов
с респираторным дистрессом, вызванным опухолью
переднего средостения, более 75% — детишки
младше двух лет. Около 80% этих маленьких де-
тей имеют симптомы сдавления трахеи.
Тимус. Распознавание аномалий тимуса может
представлять большие трудности, поскольку в ран-
нем детстве он и в норме имеет значительные раз-
меры.46 Однако физиологическое увеличение ви-
лочковой железы не должно вызывать респиратор-
ные симптомы. Чтобы отдифференцировать его от
опухолей переднего средостения, может быть на-
значен короткий курс преднизона (1,5 мг/кг/сут
в течение 5 дней), способствующий сокращению
нормальной вилочковой железы.47 Использование
этого диагностического теста следует ограничить
лишь теми маленькими детьми, у которых нет
серьезных подозрений на лимфому.
Опухоли тимуса. Тимомы у детей редки. Злока-
чественные тимомы следует дифференцировать
с лимфобластомами. Прогноз у детей при этих
опухолях особенно тяжелый. Из взрослых пациен-
тов с миастенией у 8 15% обнаруживается тимо-
ма. Самый ранний возраст, по данным литературы,
в котором миастения сочеталась с тимомой, был
19 лет.
Кисты тимуса обычно протекают бессимптомно
и обнаруживаются случайно на рентгенограммах
грудной клетки, сделанных по иному поводу. Эти
киегы, как правило, могут быть резецированы без
труда.
Хирургическое лечение ювенильной миасте-
нии. Миастения (myasthenia gravis — MG) — бо-
лезнь нервной и мышечной систем, характеризую-
щаяся прогрессирующей слабостью и патологичс
ской утомляемостью различных групп мышц. Око-
ло 10% пациентов с миастенией — дети.51 MG
встречается у них в виде трех вариантов. Во-пер-
вых, транзиторная миастения новорожденных, ко-
торая возникает у детей, родившихся от матерей
с MG. У этих новорожденных отмечается транзи-
торная мышечная слабость. Собственно же болезнь
возникает только у 15% детей, родившихся от ма-
терей с MG, и, по-видимому, связана с транспла-
центарной передачей антител IgG против рецепто-
ров ацетилхолина. Клинические проявления редко
бывают при рождении, а развиваются в течение
первых нескольких дней и держатся несколько не-
дель. Затем ребенок полностью выздоравливает.
Второй вариант — врожденная миастения — воз-
никает у детей, родившихся от матерей, не страда-
ющих данным заболеванием. При этой форме
ТАБЛИЦА 20-1. Степени тяжести миастении — классификация
Остермана
I Слабость глазодвигательных мыши без прогрессиро-
вания
II Генерализованная слабость, бульбарная и скелетная
Легкая
Средней степени
111 Острая резкая слабость с тяжелыми бульбарными про-
явлениями
IV Поздняя, тяжелая миастения
V Мышечная атрофия
у новорожденных отмечается общая слабость,
а в более позднем периоде — глазодвигательные
нарушения. Симптомы обычно легкие. Лечение
проводится антихолинергическими препаратами.
Тимэктомия не показана ни при какой форме MG
у маленьких детей.
Третья, ювенильная (юношеская) форма MG
обычно начинает проявляться после 10 лет. Так,
по данным литературы, у 74% больных (из
35) клинические симптомы возникали после
10 лет и только у двух пациентов — в возрасте до
6 лет.51 Ювенильная MG поражает девочек намно-
го чаще, чем мальчиков. Выделение степеней тяже-
сти MG основано па характере и выраженности
симптомов (табл. 20-1).
MG вызывается нарушением передачи нервно-
мышечного импульса в результате блокады рецеп-
торов ацетилхолина специфическими антителами,
которые определяются в сыворотке у большинства
(85%) пациентов с миастенией.52 Иммунный ответ
на рецепторы ацетилхолина опосредуется лимфо-
цитами.5 6 * В ' гСчитается, что тимус сенсибилизируе!
специфические лимфоциты к продукции антител
к рецепторам ацетилхолина. К сожалению, уровень
этих антител как до, так и после лечения, не все-
гда отражает тяжесть симптомов или реакцию на
лечение.55
В настоящее время существуют 4 метода, позво-
ляющие успешно лечить больных с миастенией:
(1) антихолинэстеразные препараты — пиридо-
стигмина бромид (местинон) и нсостигмин (про-
стигмин), которые ускоряют передачу нейромы
шечного импульса; (2) иммунносупрессия (стерои
ды), подавляющая иммунную реакцию; (3) плаз-
моферез (удаление циркулирующих антител); (4)
тимэктомия, устраняющая главный источник про-
дукции антител.
По данным сводной статистики, у 80 — 90%
взрослых больных с MG после тимэктомии мышеч-
ная сила возрастает. Что касается пациентов
младшего возраста, то если продолжительность за-
болевания небольшая (меньше года), тогда после
тимэктомии легче достигается улучшение или да
же полная ремиссия. Однако и при отсутствии ре-
миссии все-таки после тимэктомии отмечается бо-
лее выраженная положительная реакция на приме-
нение ингибиторов холинэстеразы.5’
Обзор результатов лечения детей с MG подтвер-
ждает важную роль тимэктомии. Однако
механизм воздействия тимэктомии на иммунную
систему в раннем возрасте остается до сих пор
ОПУХОЛИ СРЕДОСТЕНИЯ 251
ТАБЛИЦА 20-2. Результаты тимэктомии при миастении —
шкала Оссермана
А Полная ремиссия без ацетилхолина на протяжении
более, чем 3 мес
В Заметное улучшение на фоне применения уменьшаю-
щихся доз ацетилхолина
С Клиническое улучшение на фоне продолжения медика-
ментозной терапии (в прежних дозах)
D Нет улучшения, но дозы препаратов снижаются
Е Нет изменений
F Ухудшение
неясным. По этой причине оперативное лечение
у детей рационально ограничить теми случаями,
когда заболевание прогрессирует, несмотря на
применение ингибиторов холинэстеразы.59
Хотя трансстернальный доступ всеми принят,
как лучший при лечении тимом, однако некоторые
хирурги нс считают его рациональным у больных
с MG. Результаты тнмэктомин у больных с миасте-
нией представлены в таблице 20-2. Поскольку нс
только тимэктомия, но и многие другие факторы
влияют на течение заболевания после операции,
трудно сравнивать результаты при разных досту-
пах — шейпом и чрезгрудинном. Факторы, опреде-
ляющие исход, включают тяжесть и длительность
заболевания, характер симптомов (генерализован-
ные или окулярные), сроки наблюдения отдален-
ных результатов. У пациентов с тяжелыми про-
явлениями тимэктомия менее эффективна. С дру-
гой стороны, у больных с окулярными симптомами
результаты хирургического вмешательства не
столь отчетливы по сравнению с теми пациентами,
которые имели до операции генерализованные
проявления. Мем больше период наблюдения после
тимэктомии, тем чаще выявляется ремиссия. В на-
стоящее время, учитывая все множество факторов,
влияющих на результаты лечения, трудно в от-
даленные сроки говорить о преимуществах того
или иного хирургического доступа.
Сторонники шейной тимэктомии говорят о более
легком течении послеоперационного периода, хотя
результаты не отличаются от тех, что наблюда-
ются при трансстернальной тимэктомии. ’ Сто-
ронники же медиастинотомин утверждают, что
именно этот доступ обеспечивает наилучший обзор
переднего средостения, позволяя четко удостове-
риться в полном удалении тимуса. По нх мнению,
рецидив MG после тимэктомии обычно связан с не-
достаточно полным удалением тимуса во время
первой операции из шейного доступа.50,56,61
ТЕРАТОМА И ДЕРМОИД
Вторая по частоте (после крестцово-копчиковой
области) локализация тератом у детей — средосте-
ние. Если не считать редкие наблюдения располо-
жения тератом в заднем средостении, то большин-
ство этих опухолей наблюдается в переднем его
отделе, будучи непосредственно связанными с ти-
мусом, из которого они и возникают. При анализе
58 случаев тератом у детей выявлено, что 17 опу-
холей первично исходили из средостения.62 В
1969 г. был опубликован обзор литературы по
этой теме, объединивший 120 наблюдений меди-
астинальных тератом в детском возрасте, из кото-
рых 23% были злокачественными.63 В отличие от
тератом крестцово-копчиковой области, которые
встречаются преимущественно у девочек в возра-
сте до года, медиастинальные тератомы отмечают-
ся одинаково часто как у мальчиков, так и у дево-
чек, и во всех возрастных группах.64 Однако ма-
лигнизированные тератомы обнаруживаются почти
исключительно у мальчиков раннего возраста.
В большинстве случаев тератомы представляют
собой простые кистозные образования, содержа-
щие дериваты более, чем одного зародышевого
слоя. Обычно преобладают зачатки эктодермы,
и часто встречаются аморфные кальцификаты.
Как и другие доброкачественные опухоли средо-
стения, тератома у грудных детей проявляется рес-
пираторными симптомами двух типов. Во-первых,
эти опухоли могут вызывать дыхательные рас-
стройства, связанные со сдавлением дыхательных
путей.65 Чаще всего это шумное, временами стри-
дорозное дыхание, подобное тому, что отмечается
при трахеомаляции. Второй тип проявлений харак-
терен для пациентов с очень большими кистозны-
ми образованиями, которые сдавливают и смещают
легочную паренхиму. У этих больных опухоль мо-
жет протекать бессимптомно, если не считать та-
хипноэ. Поскольку тератома, а соответственно
и тахипноэ, имшотси с рождения, то родители по-
рой нс обращают внимания на учащенное дыхание
ребенка, принимая его за «норму». Эти опухоли
могут быть столь большими, что иногда вызывают
асимметрию грудной клетки.
У старших детей медиастинальные тератомы
обычно обнаруживаются как случайная находка на
рентгенограмме грудной клетки. Прорыв тератомы
средостения в соседние органы и ткани может
иметь катастрофические последствия.63 Данные
рентгенографии иногда неправильно расценивают-
ся как плевральный выпот. Одна четверть доброка-
чественных тератом содержит кальцификаты, как
правило, бесформенные, но иногда бывают видны
зубы и кости. КТ грудной клетки обычно выявляет
кистозное образование, в котором участки различ-
ной плотности перемежаются с жировой тканью
и мышцами- В дополнение к рентгенологическому
обследованию необходимо до операции провести
анализ сыворотки на опухолевые маркеры, вклю-
чая альфа-фетопротеин, карциноэмбриональный
антиген (КЭА) и человеческий хорионический го-
надотропин (ЧХГ).
Несмотря на значительные размеры, большин-
ство доброкачественных кистозных тератом иссе-
каются без осложнений и рецидивов. Однако пред-
шествующая инфекция или интимное расположе-
ние опухоли вблизи крупных сосудов или пери-
карда могут вызвать большие технические трудно-
сти во время операции. Если тератома находится
в перикарде, то существует опасность развития
тампонады сердца. Опухоль нередко васкуляри-
зируется от крупных сосудистых стволов. Терато-
мы, расположенные в заднем средостении, могут
252 ОПУХОЛИ СРЕДОСТЕНИЯ
Рис. 20-6. КТ ребенка с шейной кис-
тозной гигромой, распространяющейся в
грудную клетку.
иметь непосредственную связь с аортой?7 При по-
добной локализации или при любой связи с сосу-
дами, целесообразно произвести дооперационную
аортографию.
ОПУХОЛИ, ЛОКАЛИЗУЮЩИЕСЯ
В ЛЮБОМ ОТДЕЛЕ СРЕДОСТЕНИЯ
Кистозная гигрома — врожденная аномалия, раз-
вивающаяся в том случае, когда не происходит
дренирование первичного лимфатического мешка
в венозную систему. Окончательная локализация
кистозной гигромы зависит от того, к какой анато-
мической структуре окажется прикрепленным сек-
вестрировавшийся мешок.68 Эти опухоли, как пра-
вило, возникают на шее и у 2 -3% пациентов мо-
гут проникать в средостение.69 Они составляют
всего лишь 5—6% всех опухолей средостения
и обычно локализуются спереди, иногда в цент-
ральном и редко — в заднем средостении” По-
скольку большинство кистозных гигром средосте-
ния представляют собой лишь часть шейиомеди-
астинальной опухоли, то обычно они располага-
ются в верхнем средостении.1 2 3 4 Однако при очень
больших размерах может быть вовлечен любой от-
дел средостения, от диафрагмы до верхней аперту-
ры грудной клетки.
Обычно гигромы обнаруживаются у детей млад-
ше трех лет, причем, как правило, кроме медиасти-
нальной локализации, отмечаются также шейные
и подмышечные узлы. Поэтому у всех пациентов
с шейной или подмышечной кистозной гигромой
должна быть сделана рентгенограмма грудной
клетки для исключения внутриторакального рас-
пространения опухоли. Если локализация в груд-
ной клетке несомненна или подозревается, необхо-
димо произвести и КТ, которая позволяет четко
определить контуры опухолевидного образования
(рис. 20-6). Изолированная локализация в средо-
стении (без шейных и подмышечных узлов) встре-
чается намного реже.
Большинство кистозных гигром протекают бес-
симптомно. Иногда, при близком их расположении
к легко сдавливаемым жизненно важным органам,
могут возникать клинические проявления, доста-
точно грозные и опасные, например, такие, как рес-
пираторный дистресс, хилоторакс или хилопери-
кард. В редких случаях отмечается дисфагия в ре-
зультате сдавления пищевода в области нижней
апертуры грудной клетки. В связи с риском респи-
раторных осложнений оптимальным методом лече-
ния является раннее тотальное иссечение опухоли.
Если ее не удалить полностью, то существует
опасность рецидива. С другой стороны, при иссече-
нии не должны повреждаться соседние жизненно
важные органы. Поэтому в тех случаях, когда все
же опухоль невозможно иссечь целиком, не затро-
нув прилежащие анатомические образования,
определенный эффект может оказать снятие ее эн-
дотелиальной выстилки с обработкой подлежащих
тканей склерозирующими веществами, такими как
йодная настойка, тетрациклин или концентриро-
ванная глюкоза.
ЛИТЕРАТУРА
1. Ellis Jr FH, DuShane JW: Primary mediastinal cysts and neo-
plasms in infanis and children. Am Rev Tuberc 74:940—953,
1956.
2. Heimburger IL. Batterby JS: Primary mediastinal tumors of
childhood. J Thorac Cardiovasc Surg 50:92—103. 1965.
3. Bower RJ. Kicscwelter WB: Mediastinal masses in infants and
children. Arch Surg 112:1003 1009, 1977.
4. Pokorny WJ, Sherman JO: Mediastinal masses in infants and
children. J Thorac Cardiovasc Surg 68:869—875, 1974.
5. King RM. Telander RL. Smilhson WA, ct al.: Primary mediasti-
nal tumors in children. J Pediatr Surg 5:512—520. 1982.
6. Shields TW: Primary Tumors ami Cysts of the Mediastinum.
Lea & Febiger. Philadelphia, p 108. 1972.
7. Janin Y, Becker J, Wise L. et al.: Superior vena cava syndrome
in childhood and adolescence: a review of the literature and
report of three cases. J Pediatr Surg 17:290—295. 1982.
8. Snvder ME, Luck SR, Hernandez R, cl al.: Diagnostic dilemmas
of mediastinal cysts. J Pediatr Surg 20:810—815, 1985.
ОПУХОЛИ СРЕДОСТЕНИЯ 253
9. Aziz к han RG, Dudgeon DL, Buck JR, el al.: Life-threatening
airway obstruction as a complication to the management of me-
diastinal masses in children. J Pediatr Surg 20:816—822, 1985.
10. Bergman NA: Reduction in resting end expiratory position of the
respiratory system with induction of anesthesia and neuromus-
cular paralysis. Anesthesiology 57:14—17, 1982.
II. Bray RJ. Fernandes FS: Mediastinal tumor causing airway ob-
struction in anesthetized children, /\nesthesiology 37:571—575.
1982.
12. Northrip DR. Boh man BK, Tsueda K: Total airway occlusion
and superior vena cava syndrome in a child with an anterior
mediastinal tumor. Ancsth Analg 65:1079—1082. 1986.
13. Keen TP: Death on inducation of anesthesia for cervical node
biopsy. Anesthesiology 55:471—472, 1981.
14. Kirks DR, Fram EK. Vock P. et al.: Tracheal compression by
mediastinal masses in children and adolescents. Radiology
145:361—364, 1982.
15. Mandell GA. Laniicri R. Goodman CR: Tracheobronchial comp-
ression in Hodgkin's Ivmphoma in children. AJR 139:1167—
1170, 1982.
16. Neuman GG. Weingarter AE. Abramowitz RM. et al.: The anes-
thetic management of the patient with an anterior mediastinal
mass. Anesthesiology 60:144—147. 1984.
17. YaDcan RE. Clagett TO. Divcnic MD: Intrathoracic meningoce-
le. J Thorac Cardiovasc Surg 49:202—209. 1965.
18. Miles J, Pennybacker J, Sheldon P: Intrathoracic meningocele:
Its development and association with neurofibromatosis. J Neu-
rol Neurosurg Psychiatry 32:99—110. 1969.
19. Nanson I-M: Thoracic meningocele associated with neurofibro-
matosis. J Thorac Surg 33:650—662, 1957.
20. Herrman C. Mulder DG. Fonkalsrud EW: Thjmeclomy for my-
asthenia gravis. Ann Surg 158:85 92, 1963.
21. Kessel AW: Intrathoracic meningocele, spinal deformity and
multiple neurofibromatosis. J Bone Joint Surg 33:87—93. 1951.
22. Weimann RB. Hallman GL, Bahar D, el al-: Intrathoracic me-
ningocele: A case report and review of rhe literature. J Thorac
Cardiovasc Surg 46:40—49, 1963.
23. Kropp J. Emons D. Winkler C: Nuurcntcric cyst diagnosed by
techneiium-99m pertechnetate sequential scintigraphy. J Nucl
Med 28:1218 1220, 1987.
24 Piramoon AM. Abbassioun K: Mediastinal cnterogenic cyst with
spinal cord compression. J Pediatr Surg 9:543—545. 1974.
25 Aisenberg AC: Primary management of Hodgkin's disease.
N Engl J Med 278:93—95, 1968.
26. Glatstein E, Guernsey JM. Rosenberg SA. Kaplan HS The va-
lue of laparotomy and splenectomy in the staging of Hodgkin's
disease. Cancer 24:709—718. 1968.
27. Ochsner JL. Ochsner SF: Congenital cysts of the mediastinum.
Ann Surg 163:909 920. 1966.
28. Hardy LM: Bronchogenic cysts of the mediasrinum. Pediatrics
4:108—113, 1949.
29. Grafe WR. Goldsmith EI, Redo SF: Bronchogenic cysts of lhe
mediastinum in children. J Pediatr Surg 1:384 393, 1966.
30. Eraklis AJ. Griscom NT, McGovern JB: Bronchogenic cysts of
lhe mediastinum in infancy. N Engl J Med 281:1150—1155.
1969.
31, Operman HA, Abell MR: Neurogenous neoplasms of the media-
stinum. Cancer 13:882—898, 1960.
32. Black TL, Fernandes ET. Wrenn Fl , Magill HL: Extra lobar
pulmonary sequestration and mediastinal bronchogenic cyst-
J Pediatr Surg 23:999 1001, 1988.
33. Kissanc JM: Pathology of Infancy and Childhood, 2nd edition.
CV Mosby. Si. Louis, p 56. 1975.
34. Beardmore HE, Wigglcswurth FW: Vertebral anomalies and
alimentary duplication. Pediatr Clin North Am 5:457 473.
1958.
35. Fallon M, Gordon ARG, Lend rum AD: Mediastinal cysts of fore-
gut origin associated with vertebral anomalies. Br J Surg
41:520—533, 1954.
36. MacPherson Rl, Reed MH, Ferguson CC: Intrathoracic gastro-
genic cysts: A cause of lethal pulmonary hemorrhage in infants.
J Can Assuc Radio I 24:362, 1973.
37. Ferguson CC, Young LN. Sutherland JBD ct al.: Intrathoracic
gastrogenic cyst: Preoperative diagnosis by technetium pertech-
netate scan. J Pediatr Surg 8:827, 1973.
38. Gross RE, Ncuhauscr EBD, Longino LA: Thoracic diverticula
which originate from the intestine. Ann Surg 131:363—375.
1950.
39. Pokorny WJ, Goldstein IR: Enteric thoracoabdominal duplicati-
ons in children. J Thorac Cardiovasc Surg 87:821—824, 1984.
40. Me! etc hie NGB, Purves JK. Saunders RL. et al.: The genesis
of gastric and certain intestinal diverticula and enterogenous
cysts. Surg Gynecol Obstet 99:135—141. 1954,
41. Gooncraine S, Keh P, Sreekanlh S, et al.: Anterior mediastinal
endodermal sinus (yolk sac) tumor in <i female infant. Cancer
56:1430—1433, 1985.
42. Hawkins EP. Finegold MJ. Hawkins HK. et al.: Nongerminoma-
tous malignant germ cell tumors in children. Cancer 58:2579
2584. 1986,
43. Wychulis AR. Payne WA. Clagett Г0. Woolhcr LB: Surgical
treatment of mediastinal tumors: A forty-year experience. J Tho-
rac Cardiovasc Surg 62:379—391, 1971.
44. Oldham HN, Sabiston DC: Primary tumors and cysts of the
mediastinum. Monogr Surg Sci 4:243—279. 1967.
45. Mullen B. Richardson JD: Primary anterior mediastinal tumors
in children and adults. Ann Thorac Surg 42:338—345, 1986.
46. Malone PS. Fitzgerald RJ: Aberrant thymus: a misleading medi-
astinal mass. J Pediatr Surg 22:130—131, 1987.
47. Haller Jr JA, Major DA. Morgan Jr WW: Diagnosis and mana-
gement of mediastinal masses in children. J Thome Cardiovasc
Surg 59:385—393. 1969
48. Blalock A, Mason MF. Morgan HF. et al.: Myasthenia gravis
and tumors of the thymic region. Ann Surg 110:544—561.
1939.
49- Fonkalsrud EW, Herrmann C Jr. Mulder DG: Thymectomy for
myasthenia gravis in children. J Pediatr Surg 5:157—165, 1970.
5(1 . Youssef S: Thymectomy for myasthenia gravis in children. J Pe-
din tr Surg 18:537 541, 1983.
51. Millichap JG, Dodge PR: Diagnosis and treatment of myasthenia
gravis in infancy, childhood, and adolescence. Neurology <Min-
neap) 10:1007 1014. I960.
52. King D, Goodman J, Hawk T, et al.: Dumbbell neuroblastomas
in children. Arch Surg 110:888—891, 1975.
53. Kao I, Drachman DB: Myasthenic immunoglobulin accelerates
Ach receptor degradation. Neurology (Minncap) 27:364 365,
1977.
54. Гоука KV. Drachman DB, Guffin DE. et al.: Myasthenia gravis:
study of humoral immune mechanisms by passive transfer to
mice. N Engl J Med 296:125—131, 1977.
55. Campbell JR. Bisio JM, Harrison MW. Campbell TJ: Surgical
treatment of myasthenia gravis in childhood. J Pediatr Surg
18:857—861, 1983.
56. Mulder DG. Herrman C. Keesey J. Edwards H: Thymectomy for
myasthenia gravis. Am J Surg 146:61—66, 1983.
57. Papatestas AE. Genkins G. Kornfeld P. et al.: Effects of thy-
mectomy in myasthenia gravis- Ann Surg 206:79—88. 1987.
58. Papaiesias AE. Alpert LI. Osscrman KE. cl ill.: Studies in my-
asthenia gravis: Effect of thymectomy. Am J Med 50:465—474.
1971
59. Sarnat HB. McGarry JD. Lewis Jr JE: Effective treatment of
infantile myasthenia gravis by combined prednisone and thy-
mectomy. Neurology 27:550 553, 1977.
60. Scybold ME. Howard FM. Duane DD, et al.: Thymectomy in
juvenile myasthenia gravis. Arch Neurol 25:385—392, 1971.
61. Simpson J A: An evaluation of thymectomy in myasthenia gravis.
Brain 81:112—144, 1958.
62. Carney JA, Thompson DP. Johnson CL, Lynn HB: Teratomas
in children: Clinical and pathologic aspects. J Pediatr Surg
7:271 282. 1972.
63. Thompson DP. Moore TC: Acute thoracic distress in childhood
254 ОПУХОЛИ СРЕДОСТЕНИЯ
due to spontaneous ruptures of a large mediastinal teratoma.
J Pediatr Surg 4:416—423, 1969.
64= Whittaker LD„ Lynn HB: Mediastinal tumors and cysts in the
pediatric patient. Surg Clin North Am 53:893—904. 1973.
65. Stinnett DM, Pokorny WJ. Harberg FJ: Anterior mediastinal
teratomas in infants and children. Cardiovasc Dis 5:224—228,
1978.
66. Aldousany AW. Joyner JC, Price RA, et al.: Diagnosis and tre-
atment of intra pericardia I teratoma. Pediatr Cardiol 8:51—53,
1987.
67. Karl SR, Dunn J: Posterior mediastinal teratomas. J Pediatr
Surg 5:508—510, 1985.
68. Goetch E: Hygroma colli cysticum and hygroma axilla re. Arch
Surg 36:394—479, 1938.
69- Childress ME, Baker CP, Samson PC: Lymphangioma of the
mediastinum. J Thorac Surg 31:338—348. 1956.
70. Curley SA, Ahlin DS, Kosioske AM: Grant cystic hygroma of the
posterior mediastinum. J Pediatr Surg 24:398—400, 1989.
71. Gross RE, Hurwitt ES: Cervicomediastinal and mediastinal cys-
tic hygromas. Surg Gynecol Obstet 87:599—610, 1948.
72. Grosfcld JL. Weinberger M, Kilman JW, el al.: Primary medi-
astinal neoplasms in infants and children. Ann Thorac Surg
12:179 190, 1971.
73. Gross RE: The Surgery of Infancy and Childhood. Its Princip-
les and Techniques. WB Saunders, Philadelphia, pp 762—784,
1953.
74. Jaubert de Beaujeu MJ, Mol lard P Campo-Paysaa A: Tumours
chirurgicales du mediastin de Penta nt. Ann Chir Infant 9:177—
191. 1968.
75. Rubush JL, Gardner IR, Boyd WC. Ehreiihaft JL: Mediastinal
tumors: Review of 186 cases. J Thorac Cardiovasc Surg
65:216—222, 1973.
76. Benjamin SP. McCormack I J, EffJer DB, Groves LK: Primary
tumors of the mediastinum. Chest 62:297—303, 1972.
77. Boyd DP, Midell Al: Mediastinal cysts and tumors: An analysis
of 96 cases. Surg Clin North Am 48:493—505. 1968.
78. Fontenelle LJ, Armstrong RG, Stanford W, et al.: The asympto-
matic mediastinal mass. Arch Surg 102:98—102, 1971.
79- Harrington SW: Intrathoracic extrapulmonary tumors: Diagnosis
and surgical treatment. Postgrad Med 6:6—21, 1949.
80. Herlitzka AJ, Gale JW; Tumors and cysts of the mediastinum-
Thorax 13:294—307, 1958.
81. Key JA; Mediastinal tuiiiours. Suig Clin Nuith Лш 34=959—978,
1954.
82. LeRoux ВТ: Cysts and lumors of the mediastinum. Surg Gyne-
col Obstet 115:695—703, 1962.
83. Morrison IM: Tumors and cysts of the mediastinum. Thorax
13:294—307. 1958.
84. Ringerlz N. Lidholm SO: Mediastinal tumors and cysts. J Tho-
rac Surg 31:458—487. 1956.
Глава 21
ПИЩЕВОД
Эмбриология. Пищевод и трахея развиваются из
первичной кишки эмбриона. Их разделение начи-
нается в области карины и продолжается в крани-
альном направлении. При нарушениях этого слож-
ного процесса могут возникнуть такие пороки, как
атрезия пищевода (глава 22) и атрезия трахеи
(глава 16). Поскольку трахея в норме имеет хря-
щи. то при аномалиях развития пищевода он. как
правило, тоже имеет в своей стенке хрящевые
остатки. Кистозное поражение стенки пищевода
может быть представлено полным кистозным его
удвоением или бронхогенными кистами, в стенке
которых содержится как слизистая дыхательных
путей, так и хрящи.
Мышечная стенка пищевода состоит из внутрен-
ней циркулярной и наружной продольной мускула-
туры. Пищевод не имеет серозной оболочки. Верх-
няя его треть, представленная поперечнополосаты-
ми мышцами, находится под произвольным конт-
ролем, в то время как две дистальные трети,
состоящие из гладких мышц, управляются авто-
номно. Слизистая пищевода снабжена своими соб-
ственными железами, которые при наличии острой
обструкции продуцируют большое количество
слизи.
С хирургической точки зрения в пищеводе могут
быть выделены шейная, грудная и абдоминальная
части. Шейный отдел интимно связан с гортанью.
Наиболее тонкая стенка у пищевода непосредст-
венно ниже и кзади от перстневидно-глоточных
мышц. Эта часть пищевода, где особенно высок
риск перфорации, получает кровоснабжение от
щнтовидно-шейных сосудов.
Торакальная часть пищевода огибается с лате-
ральной стороны дугой аорты и при аномалии, но-
сящей название сосудистого кольца, оказывается
значительно сдавленной. В этом отделе пищевод
интимно соприкасается с аортой и перикардом, ко-
торые соответственно также могут поражаться при
инородных телах или химических ожогах пищево-
да. Средняя его часть имеет с латеральной или
дорсальной стороны сегментарное кровоснабжение,
легко повреждаемое при слишком активной моби-
лизации этого отдела, что может неблагоприятно
повлиять на заживление анастомоза.
Абдоминальная часть пищевода обеспечивает
механизм действия нижнего пищеводного сфинкте-
ра — НГ1С (см. главу 23) и обильно кровоснабжа-
ется из диафрагмальных ветвей и желудочных со-
судов. Разрыв слизистой этого отдела в результате
сильных рвот (синдром Бурхаве) и развитие вари-
коза при портальной гипертензии — потенциаль-
ные источники обильной кровопотери из нижней
трети пищевода. В литературе существуют работы
с детальным описанием эмбриологии и анатомии
пищевода.1
ХИМИЧЕСКИЕ ОЖОГИ ПИЩЕВОДА
Природное любопытство детей и их стремление
все попробовать «на вкус» в комбинации с насы-
щенностью окружающей среды различными хими-
катами являются благодатной почвой, на которой
возникают химические ожоги пищевода. Щелочи
намного чаще, чем кислоты, приводят к пораже-
нию пищевода. Существующие в продаже чистя-
щие вещества, щелоки домашнего приготовления,
сильные средства для мытья посуды — вот основ-
ные агенты, которые особенно часто вызывают хи-
мический некроз пищевода.2 Концентрированные
щелочные растворы «скользкие» и потому, попав
в рот, быстро проникают в пищевод. В отличие от
жидких щелочей, сухие каустические препараты
задерживаются в ротовой полости, прилипая к сли-
зистой, вызывают сильную боль и саливацию и,
благодаря этому, в конце концов растворяются.
Довольно нередко ребенок, к счастью, выплевыва-
ет сухие щелочи, не успевая их проглотить. При
поражении жидкой щелочью травма пищевода мо-
жет быть и без поражения слизистой рта. Контакт
щелочи со слизистой пищевода вызывает интен-
сивный его спазм, способствующий воздействию
каустического агента по всей окружности пищево-
да, суженного вследствие спазма. В результате воз-
никает расплавление и некроз стенки. Если доза
щелочи значительна, то «разъедаются» слизистый,
256 ПИЩЕВОД
подслизистый и мышечный слои, причем этот про-
цесс продолжается до тех пор, пока «разведение»
каустического агента не приблизит pH раствора
к нейтральным показателям. В эксперименте на
кошках с интактным пищеводом и открытой груд-
ной клеткой, измерение с помощью поверхностных
электродов показало, что в различных местах во-
круг средостения отмечается подъем pH. По всей
видимости, изменения pH более связаны с феноме-
ном диффузии, чем с сосудистой дисперсией. Ин-
тенсивность поражения как пищевода, так и средо-
стения, зависит в основном от концентрации гид-
роксильных ионов.
В местах естественных сужений пищевода (об-
ласть перстневидно-глоточных мышц, дуги аорты
и кардиального жома) даже небольшое количество
щелочи может вызвать ожог по всей окружности.
Часто, однако, поражение пищевода бывает значи-
тельным и в среднем его отделе.
Кислота вызывает намного менее тяжелое пора-
жение пищевода, чем щелочь, если, конечно, это
не очень сильная кислота. Ожоги кислотой наибо-
лее часто локализуются у входа в желудок, где
возникает некроз слизистой и интрамуральное вос-
паление, в результате чего развивается антраль-
ный стеноз.
Каустическое воздействие на пищевод приводит
к образованию рубца (рис. 21-1). Интенсивность
рубцевания, а соответственно и прогноз, определя-
ются глубиной ожога. Если возникает тишь эрите-
ма слизистой, серьезных последствий обычно не
возникает. При некрозе слизистой по всей окруж-
ности, когда процесс достигает мышечного слоя,
образуется сужение, но не циркулярное. Если же
поражение захватило все слои и распространилось
па средостение с деструкцией его тканей под воз-
действием гидроксильных ионов, то может раз-
виться медиастинит и иногда перфорация пищево-
да в прилежащие органы. Особенно большую опас-
ность в этом плане представляет, конечно, аорта
(рис. 21-2)?
Лечение в остром периоде. К сожалению, пора-
жение пищевода происходит обычно мгновенно.
При небольшой дозе химического агента он может
пройти в желудок, где разбавление его кислотой
желудочного сока до нейтральной реакции предот-
вращает дальнейшее воздействие. В течение мно-
гих лет в качестве первой помощи маленькому ре-
бенку, проглотившему щелочь, рекомендовалось
(и широко пропагандировалось) искусственно вы-
звать рвоту. Однако в этом случае щелочь с рвот-
ными массами возвращается обратно в пищевод
и получает возможность вновь воздействовать на
его слизистую. К сожалению, любой разбавляю-
щий агент, чтобы оказывать эффективное дейст-
вие, должен быть введен в таких больших количе-
ствах, что это неизменно вызывает рвоту. В част-
ности, введение уксусной кислоты, нейтрализую-
щей щелочь, как правило, вызывает рвоту. Все это
объясняет, почему первая помощь оказывается
обычно малоэффективной, если вообще можно го-
ворить о каком-либо ее значении. Более того, она
Рис. 21-1. Сужение пищевода в результате ожога щелочью,
наиболее выраженное на участке от уровня аорты до дисталь-
ной части ввутригрулного отдела пищевода. Поскольку через
зону стеноза прошло лишь небольшое количество бария, то
невозможно определить — поражены или нет желудок и дис-
тальная часть пищевода. Оба этих фактора очень важны для
выбора метода лечения при обширных химических ожогах пи-
щевода щелочью.
может даже привести к дальнейшему поражению
слизистой пищевода.2
Обычно при поступлении ребенка в приемный
покой в анамнезе есть четкое указание на то, что
он проглотил именно щелочь. Знать химический
состав поражающего агента очень важно. При упо-
треблении ребенком таких широко распространен-
ных в быту веществ, как, например, отбеливатели,
не требуется ни эндоскопия, ни дальнейшее на-
блюдение. При проглатывании жидкой гидроокиси
натрия, гидроокиси калия (как жидкой, так и в по-
рошке) или порошкообразных моющих средств не-
обходимо проведение диагностической эндоскопии.
Состояние слизистой полости рта практически не
имеет прогностического значения и не отражает
характер и степень ожога пищевода. А вот эндо-
скопия, если она проводится в течение 24 час по-
сле травмы, четко показывает, поражен пищевод
или нет. Линейный ожог пищевода не имеет суще-
ственного клинического значения, ибо, если пора-
жение не циркулярное, то оставшаяся интактной
стенка обычно полностью замещает обожженный
участок. Общее лечение, в частности инфузионная
терапия, должно быть начато немедленно при по-
ступлении, как можно раньше, до любых диагно-
стических процедур.
Для оценки характера поражения пищевода мы
ПИЩЕВОД 257
Рис. 21-2. А, Рентгене»рамма [рудной клетки ребенка сразу
после ироглатынания щелочного раствора.
В3 Тот же больной через 4 дин Более шаровидные контуры
сердца говорят о наличии выпота в полости перикарда.
С, Рентгенограмма с барием через 2 недели после ожога. Вид-
ны неровные контуры слизистой шнценода, но особенно тре-
вожным симптом — большое шаропидкое сердце.
D, Вскоре после предыдущего рентгенологического обследова-
ния ребенок умер от кровотечения. Па аутопсии выявлена об-
ширная перфорация пищевода в аорту.
предпочитаем использовать жесткий эзофагоскоп.
Главная цель исследования — определить, цирку-
лярный ожог или нет.
В течение долгих лет считалось, что антибиоти-
ки предотвращают развитие медиастинита, а об-
щее применение стероидов способствует профи-
лактике рубцевания пищевода. Однако оценка
глубины поражения и его степени с делением на
1-ю» 2-ю и 3-ю, как это принято при ожогах кожи,4
всегда была достаточно трудной. Несомненно, что
характер образования рубца определяется глуби-
ной ожога. Выявить при этом роль стероидной те-
рапии и долю ее участия в достижении тех или
иных клинических результатов чрезвычайно слож-
но. Исследование эффективности применения сте-
роидов при лечении ожогов пищевода щелочью
17 Заказ N? 1622
258 ПИЩЕВОД
проводилось в эксперименте на кошках.5 В конт-
рольной группе помощь животным не оказывалась
(течение ожога было «пущено на самотек»). Там
же, где проводилось лечение, применялся только
один из следующих методов: бужирование, стерои-
ды или антибиотики. И, наконец, исследовалась
эффективность использования стероидов в совета
нии с антибиотиками. Животные, леченные по-
следним способом (комбинация стероидов и анти-
биотиков), в наименьшей степени, чем все другие,
теряли массу тела и лишь немногие из них умерли
от истощения, однако проводимая терапия не пред-
отвращала развития стриктуры.
В клинических условиях результаты лечения
комбинацией стероидов и антибиотиков изучались
у 69 пациентов с ожогом пищевода.6 В 8 наблюде-
ниях (12%) развился стеноз, потребовавший дли-
тельного бужирования. Необходимость в пластике
пищевода не возникла ни в одном случае. Восемь
же пациентов, лечившихся в других госпиталях
и не получавших в остром периоде стероиды с ан-
тибиотиками, были направлены в поздние сроки
для пластики пищевода или длительного бужиро-
вания. Создается совершенно определенное впе-
чатление, что терапия стероидами с антибиотика-
ми уменьшает частоту стенозов, но не предотвра-
щает их полностью. Данный метод принят повсе-
местно, и можно с уверенностью говорить о том,
что если только стероиды не применяются слиш-
ком долго, то результаты обычно бывают хороши-
ми. Дальнейшие исследования подтверждают, что,
несмотря на лечение стероидами с антибиотиками,
стриктуры все же развиваются.7 Целенаправленное
изучение эффективности применения стероидов
у детей с химическими ожогами пищевода показа-
ло, что при ожогах щелочью нет статистически
достоверных явных преимуществ использования
кортикостероидов.'
Лечение обширных тяжелых ожогов в остром
периоде. Если, по данным анамнеза, ребенок про-
глотил большое количество концентрированной
щелочи ' (малыши — случайно, старшие дети
и подростки иногда при суицидных попытках), то
должен быть срочно рассмотрен вопрос о показа-
ниях к эзофагэктомии и, возможно, гастрэктомии.
Конечно, не известно, предотвратит ли такой ак-
тивный подход возникновение аортоэзофагеально-
го свища (в результате продолжающегося действия
щелочи на ткани средостения), однако некоторые
наши данные, экспериментальные и клинические,
полученные при лечении взрослых, подтверждают,
что подобная тактика может быть рациональ-
ной.11’lz При случайном проглатывании щелочи
детьми наиболее стандартный и общепринятый
подход — наложение гастростомы для питания
и бужирования. При проглатывании большого ко-
личества щелочи следует сделать верхнюю лапа-
ротомию, чтобы оценить состояние стенки желудка
и убедиться в наличии каустического поражения
и его распространенности. Когда препарат имеет
высокую концентрацию или большой объем, он
обычно достигает желудка и вызывает поражение
его стенки. В таких случаях пищевод, как правило.
полностью разрушен и должен быть удален. Если
же нет серьезного ожога желудка, следует нало-
жить гастросгому.13
Лечение каустических ожогов в подостром пе-
риоде. Наиболее общепринятый подход к лечению
каустических ожогов в подостром периоде — это
наблюдение в динамике, цель которого — опреде-
лить, разовьется стриктура или нет. Чаще всего
она все же развивается.
Как в эксперименте,14 так и по клиническим дан-
ным у детей1518 и взрослых, хороший эффект в фа-
зе заживления оказывает использование стен-
тов — специальных временных приспособлений-
протезов (катетеры, трубки) для расширения про-
света пищевода и предотвращения его сужения
в процессе заживления. Эта методика была пред-
ложена 25 лет назад, однако не нашла широкого
распространения. То же самое можно сказать
и о лечении ожогов (щелочью), полученных в экс-
перименте бета-аминопропионитрилом, описан-
ном 20 лет назад, но не нашедшем применения
в клинической практике.
Лечение стриктур пищевода, развивающихся
в поздние сроки после тяжелых каустических ожо-
гов, будет представлено ниже.
ИНОРОДНЫЕ ТЕЛА ПИЩЕВОДА
Из инородных тел, вызывающих иногда поврежде-
ние пищевода, дети чаще всего проглатывают мо-
неты, которые в большинстве своем безболезненно
проходят через весь пищеварительный тракт, при-
чем родители часто даже нс знают о случившемся.
Инородные тела и способы их извлечения из пи-
щевода обсуждались в главе 8. Здесь лишь пред-
ставлены проблемы, связанные с отдаленными по-
следствиями застрявшего в пищеводе и вызвавше-
го его повреждение инородного тела.
Отношение докторов к оказанию первой помощи
ребенку, проглотившему монету, бывает очень раз-
ным —- от полного пренебрежения к происшед-
шему21 до немедленной реакции в виде экстренного
рентгенологического контроля, включающего не
только обзорные рентгенограммы, но даже конт-
растное исследование.22 В зависимости от массы
тела и роста самого ребенка и размеров прогло-
ченной монеты, шансы на то. что она застрянет
в пищеводе, различны. Если монета небольшая
и прошла в желудок, не остановившись в местах
естественных сужений пищевода (перстневидно-
глоточное, дуга аорты, дистальный отдел пищево-
да), то маловероятно, что она застрянет в других
суженных участках ЖКТ, таких, как пилориче-
ский отдел, связка Трсйца и илеоцекальная за-
слонка. При наличии в анамнезе указаний на то,
что ребенок проглотил монету, следует, как прави-
ло, сделать обзорную рентгенограмму грудной
клетки и живота.2 По данным одного из исследо-
ваний, 52 детям, проглотившим монеты, были сде-
ланы рентгенограммы. При наличии симптоматики
монеты удалялись. Из 30 пациентов, у которых
монета была в пищеводе, в 9 случаях (30%) тече-
ние было бессимптомным.24 В трех наблюдениях
ПИЩЕВОД 259
Рис. 21-3. А. Видно попадание бария из пищевода в дыхательные Пути у 4-лстнсго ребенка с хроническим кашлем.
В, На боковой рентгенограмме определяется небольшое инородное тело в пищеводе, проникающее н в трахею. Приблизительно
за 4 месяца до установления диагноза приобретенного трахеопищеводного свища ребенок проглотил кусочек волана от бадминтона.
монета в течение 24 часов не прошла в желудок,
а потому была удалена. В другом обзоре, прове-
денном одновременно с предыдущим и в том же
городе, отмечено, что лишь очень небольшая часть
родителей, позвонивших в госпиталь, чтобы сооб-
щить о проглатывании их ребенком монеты, согла-
сились сделать предложенную врачом обзорную
рентгенограмму. У 20% из этих детей монета нахо-
дилась в пищеводе. В большинстве случаев из тех,
где монета застряла в пищеводе, имелись клиниче-
ские проявления — стридор или слюнотечение.'
Последствия нахождения в пищеводе нераспоз-
нанного инородного тела, даже такого гладкого,
как монета, могут быть очень тяжелыми.26-2’ Хотя
некоторые хирурги советуют проталкивать монету
в желудок,2’ большинство все же предпочитают из-
влекать гладкие инородные тела с помощью кате-
тера Фолея.30-32
Повреждение пищевода чаще всего возникает
в результате прокатывания острых инородных
тел, включая отрывные сегменты крышек жестя-
ных банок с напитками.3 Поскольку эти предме-
ты нередко бывают рентгенологически мало или
совсем неконтрастными, то диагноз порой ставится
поздно, когда уже появляются симптомы стеноза
пищевода.
В некоторых редких ситуациях в результате
проглатывания инородного тела возникает трахео-
пищеводный свищ.35 У нас был один подобный слу-
чай — ребенок проглотил кусочек (диаметром
13 мм) пластикового волана для бадминтона. Ино-
родное тело вызвало пролежень стенки пищевода
и в конце концов проникло в трахею (рис- 21-3)
Намного более серьезными бывают последствия
проглатывания батареек, используемых в кальку-
ляторах, часах и других небольших электронных
аппаратах.36. Повреждение пищевода при этом
обусловлено одним из трех или всеми тремя ме-
ханизмами: (1) некроз в результате давления,
(2) поражение щелочью или иным химическим ве-
ществом, входящим в состав электролитного аген-
са, и (3) воздействие от электрического тока не-
разряженной батарейки. Некоторые считают, что
разряженные («мертвые») батарейки вызывают
меньшее повреждение.3’ В литературе описаны
2 случая пенетрации батарейки в аорту. Эти
сообщения были среди первых публикаций о про-
глатывании батареек.
Хотя некоторые и считают, что опасны лишь
батарейки размерами 22 м.м по окружности и бо-
лее, однако риск повреждения зависит прежде все-
го от размеров пищевода и возможности батарейки
пройти в желудок.-36 Кроме того, батарейки, кото-
рые задерживаются в желудке, всего за 2 часа вы-
зывают поражение слизистой. Может ли подобная
травма приводить к перфорации желудка — не из-
вестно. Батарейки, помещенные в эксперименте
в физиологический раствор, быстро вызывают по-
вышение pH до 12.0. А батарейки, находившиеся
в пищеводе в течение нескольких дней, приводили
к тяжелому трахеопищеводному эрозированию.37
Этот тип поражения напоминает ожог каустиче-
ским агентом, поскольку после удаления инородно-
го тела и соответственно прекращения его непо-
средственного воздействия в нескольких случаях
продолжалось прогрессирование процесса.
260 ПИЩЕВОД
Удаление батареек из пищевода может быть
произведено с помощью катетер;! Фолея или маг-
нитных устройств, под рентгенологическим конт-
ролем.44 Извлечение из желудка и даже из верхних
отделов тонкой кишки также осуществляется с ис-
пользованием магнитов или через гастростому.'”
Если батарейка прошла через пилорус, она вряд
ли вызовет повреждение в нижележащих отделах.
Однако описан случай перфорации батарейкой
дивертикула Меккеля через 3 дня после проглаты-
вания.43 Подход к выбору метода лечения трахео-
пищеводных свищей или перфорации пищевода,
возникших в результате травмы инородным телом,
должен быть строго индивидуальным. Поврежде-
ние батарейкой с образованием свища между пи-
щеводом и трахеей лечится нс так просто, как,
казалось бы, можно было лечить этот вид травмы,
ибо степень и тяжесть деструкции тканей обычно
более серьезны, чем поражение в результате не-
кроза от простого давления.
У новорожденных детей может произойти ят-
рогенное повреждение пищевода, как интактного,
так и при наличии необычных форм его поро-
ков— атрезии и трахеопищеводных свищей.
Осложнения при отсасывании слизи и интубации
также бывают причинами перфорации пищевода.
В большинстве подобных случаев необходимо осу-
ществить немедленное хирургическое дренирова-
ние,48 однако при поздней диагностике и «доброка-
чественном» течении в отдельных редких ситуаци-
ях можно обойтись лечением антибиотиками без
40
дренирования.
В литературе имеется сообщение о спонтанной
перфорации пищевода у новорожденного ребенка,
которому не производились никакие манипу-
ляции.50
Другие виды ятрогенной травмы включают пер-
форацию пищевода инструментами, например при
пневматической дилатации (при ахалазии) бал-
лонным расширителем, который может достигать
размеров, соответствующих 108 French катетеру.
В подобной ситуации (при таких больших разме-
рах расширителя) повреждение пищевода не уди-
вительно. Наш печальный опыт ятрогенных перфо-
раций пищевода состоит из двух случаев. В одном
это было бужирование пищевода у ребенка со стри-
ктурой в результате ожога щелочью (рис. 21-4),
в другом — повторные бужирования у пациента
с пептическим стенозом пищевода в дистальном
отделе. При подобных поражениях может происхо-
дить спонтанное дренирование в просвет пищево-
да, что подтверждается рентгенологически — вы-
ходящий из просвета пищевода контраст довольно
быстро исчезает на отсроченных рентгенограммах.
В таких случаях, когда внутреннее дренирование
несомненно и сочетается с доброкачественным
клиническим течением, следует воздержаться от
активного хирургического дренирования.52
Стандартный подход, однако, подразумевает
обязательность дренирования при любом виде пер-
форации пищевода. Клинические проявления
включают боли и подъем температуры. Рентгено-
грамма грудной клетки, сделанная вскоре после
Рис. 21-4, Перфорация верхнегрудного отдела пищевода, воз-
никшая после бужирования нослеожогового стеноза. На повтор-
ной рентгенограмме, сделанной через несколько часов. ибнару
жеио. что весь барий, который располагался вне пищевода, воз-
вратился d его просвет, поэтому решено н<».< (рржаться от дрени-
рования. Больному в конечном счете потребовалась пластик»
пишспода, но не в связи с перфорацией, а по поводу7 стеноза.
перфорации, редко выявляет воздух в средостении.
До 10% случаев перфорации пищевода дают лож-
ноотрицательныс результаты контрастного иссле-
дования — контраст не выходит из просвета, хотя
перфорация есть. * В зависимости от характера
основной патологии, на фоне которой произошла
перфорация, может быть предпринято либо пер-
вичное ушивание пищевода, либо только дрениро-
вание.52'55-57 Иногда, особенно в некоторых редких
необычных ситуациях, когда по каким-либо причи-
нам очень малы шансы на самостоятельное зажив-
ление пищевода, рационально сразу идти на ради-
кальную его резекцию.58
Баротравма пищевода обычно развивается у де-
тей, которые попадают в какие-то приспособле-
ния-аппараты с повышенным давлением. Повреж-
дение пищевода при этом бывает очень тяжелым.59
При синдроме Бурхаве в результате сильной рво-
ты может возникнуть пищеводно-плевральный
свищ, чаще на левой стенке пищевода. Если свищ
диагностирован рано, необходимо произвести пер-
вичное ушивание пищевода и дренирование.
ПИЩЕВОД 261
Каждый случай перфорации пищевода требует
индивидуального подхода, обязательного лечения
антибиотиками широкого спектра действия, адек-
ватного дренирования, если оно показано, и иногда
хирургического вмешательства. Операция может
включать мобилизацию окружающих тканей и
укрепление ими стенки пищевода или трахеи.
К сожалению, многие пациенты, у которых про-
исходит повреждение пищевода, имеют какую-ли-
бо его патологию, требующую инструментальных
методов лечения. Эти факторы, несомненно, игра-
ют очень важную роль в выборе метода лечения
перфорации и часто затрудняют это лечение.
ВРОЖДЕННЫЙ СТЕНОЗ ПИЩЕВОДА
Врожденное сужение пищевода трудно диагности-
руется и нередко проходит под диагнозом пепти-
ческого стеноза, выявляемого у детей необычно ра-
но для этой патологии — до 1,5-годовал ого возра-
ста. В тех случаях, когда имеется истинный врож-
денный стеноз, в стенке пищевода могут быть
остатки хрящей дыхательных путей, что нехарак-
терно для пептических стриктур.611 Из 27 детей
с врожденным стенозом, по сводной статистике,
у большинства сужение локализовалось в дисталь-
ном отделе пищевода.61 Мы наблюдали одного из
этих пациентов и, кроме того, ребенка с необычной
стриктурой шейного отдела пищевода, в задней
стенке которого имелась большая хрящевая
бляшка.
Диагноз наиболее часто ставится непосредствен-
но во время резекции пищевода. Хотя врожденные
стенозы обычно небольшие по протяженности, но
они не поддаются повторным бужированиям.
ФУНКЦИОНАЛЬНЫЕ РАССТРОЙСТВА ПИЩЕВОДА
Диффузный спазм пищевода редкое состояние,
которое обозначается также термином «первичные
нарушения двигательной активное ги».62 Ориги-
нальное описание этой патологии очень точно
отражает ее суть63 — обычно возникают спастиче-
ские боли в пищеводе, сопровождающиеся дисфа-
гией. Со времени первого описания патогенез диф-
фузного спазма пищевода был уточнен — выявле-
на циркулярная мышечная гипертрофия, в основ-
ном в нижних двух третях пищевода. Этиология,
однако, остается неизвестной.
Мы наблюдали лишь одного ребенка с данной
патологией (рис. 21-5). Ему не потребовалась ми-
отомия. Большинство же взрослых больных, со-
гласно данным литературы, были подвергнуты ми-
отомии на значительном протяжении, с хорошими
результатами.
Склеродермия пищевода представляет собой не-
обычное заболевание коллагеновой ткани в дет-
ском возрасте, когда дистальные две трети пище-
вода, имеющие гладкую мускулатуру, нс могут
нормально перистальтировать. При этом почти
всегда отмечается гастроэзофагеальный рефлюкс.
При склеродермии, как правило, возникает пепти-
ческий стеноз пищевода.64 Фундопликация у мио-
Рис. 21-5. Диффузный спазм пищакъш у 8-летнего ребенка.
Гастроэзофагеального рефлюкса в данном случае не было, как
не было н эффекта от бужиролаиня пнщепода. При последнем
осмотре ребенка он мог есть только супы и протертую пищу,
гих из этих больных дает клиническое улучшение,
несмотря на то, что не устраняет лежащую в осно-
ве системную патологию. Мы не наблюдали детей
с поражением пищевода при склеродермии.
Дивертикулы пищевода встречаются у детей
чрезвычайно редко. При отсутствии диффузного
эзофагеального спазма нечасты они и у взрослых.
В литературе имеется лишь одно сообщение о ре-
бенке с синдромом Элерса-Данлоса, у которого бы-
ли обнаружены дивертикулы пищевода, желудка,
толстой кишки и мочевого пузыря.65
Ахалазия пищевода. Этиология ахалазии неиз-
вестна. Гистопатологическое изучение мышечной
стенки дистального отдела пищевода 24 больных
детского возраста выявило полное отсутствие нер-
вных сплетений у двух пациентов и ганглиозных
клеток - у 10. Однако в 7 случаях ганглиозные
клетки были нормальными. У 5 больных в гангли-
озных клетках обнаружены признаки хронически-
262 ПИЩЕВОД
го воспаления. Волокна же гладких мышц выгляде-
ли обычно.66 Клинические симптомы появлялись
в самом разном возрасте — от 5 дней до 15 лет.
Ахалазия, тем не менее, болезнь преимущественно
взрослых людей, причем симптомы также начина-
ют появляться лишь в зрелом возрасте, что позво-
ляет сомневаться во врожденном характере заболе-
вания. Теоретически можно предположить, что
к спазму нижнего отдела пищевода приводит га-
строэзофагеальный рефлюкс, а это в конце концов
вызывает клиническую картину ахалазии. Наблю-
даются семейные случаи заболевания. В таких
ситуациях у некоторых членов семьи выявлялся
пилоростеноз,67 при котором первоначальные сим-
птомы те же, что и при гастроэзофагеальном реф-
люксе. Частая ошибка в диагностике ахалазии
связана как раз с тем, что ее симптомы расце-
ниваются как проявления гастроэзофагеального
рефлюкса.6’
Мы наблюдали одного пациента, который про-
шел именно такой путь. Ему сделали фундоплика-
цию, но он по-прежнему не мог глотать. Фундопли-
кация была произведена до того, как установлен
диагноз ахалазии. Затем последовала эзофагомио-
томия с повторной фундопликацией по Талю
(Thai). Позже потребовалась пилоропластика, по-
скольку в возрасте 5 лет появились признаки пи-
лоростеноза.
При обследовании с барием детей с ахалазией
выявляется значительное расширение и ослабле-
ние перистальтики проксимального отдела пище-
вода, при этом лишь небольшая часть контрастно-
го вещества проходит в желудок (рис. 21-6). По-
добная рентгенологическая картина позволяет
установить диагноз ахалазии. У детей пет необхо-
димости в проведении манометрии для подтверж-
дения диагноза.
Рис. 21-ff. Ахалазия у З-летнегч ребенка. Произведено опера-
тивное вмешате 1ьство — миотомия по Геллеру с фундоплика
иней ио Галю. Получен прекрасный результат.
Диагноз ахалазии может быть установлен на
основании исследования с барием. У взрослых, од-
нако, желательно подтвердить диагноз с помощью
манометрии, которая выявляет отсутствие пери-
стальтики пищевода и отсутствие расслабления
(или незначительное расслабление) кардиального
жома.
Измерение pH в дистальном отделе пищевода
может обнаружить гастроэзофагеальный рефлюкс.
Но это исследование при диагностике ахалазии
проводилось редко.
Лечение ахалазии хирургическое. Для уменьше-
ния спазма кардиального жома у детей с подтверж-
денной ахалазией показано применение блокато-
ров кальциевых каналов (нифедипин), однако их
эффект непостоянен. Поэтому не следует ограни-
чивать терапию использованием лишь этих препа-
ратов на протяжении длительного периода вре-
мени.70
Много работ в литературе посвящено вопросам
хирургического лечения ахалазии у взрослых.
Сравнение результатов и возникающих при этой
патологии проблем показывает, что лечение аха-
лазии у взрослых и детей практически одинако-
вое.” Бужирование или баллонная дилатация ино-
гда дает клинический эффект, но частота перфора-
ций при этом доходит до 12%.72 Хотя 50% боль-
ных в течение 4 лет после дилатации не имеют
клинических проявлений, однако у 30% отмеча-
ется гастроэзофагеальный рефлюкс с соответству-
ющими симптомами и у 20% —дисфагия. В упо-
мянутой работе подчеркивается, что любая опера-
ция, которая дает от 20 до 50% неблагоприятных
результатов с плохими отдаленными последствия-
ми, не может быть расценена как приемлемый ра-
циональный способ лечения.
Основной общепринятый метод лечения ахала-
зии — миотомия пищевода, предложенная Гелле-
ром 70 лет назад. Торакальные хирурги обычно
пользуются торакальным доступом, общие хирур-
ги — абдоминальным. Очень важно рассечь как
продольный, так и циркулярный мышечный слой,
до подслизистой, как это делается при пилоромио-
томии. У взрослых миотомию осуществляют на
протяжении 10—12 см, у детей длина разреза дол-
жна быть соответственно меньшей.
Мы делаем миотомию у большинства детей на
протяжении последних 2,5—5 см пищевода, при-
крывая место миотомии с помощью передней фун-
допликации, чтобы предотвратить гастроэзофаге-
альный рефлюкс. Учитывая то, что операция Гел-
лера, когда она применяется как изолированное
единственное вмешательство, осложняется реф-
люксом с клиническими проявлениями, вопрос
о правильном выборе хирургического метода лече-
ния ахалазии продолжает оставаться непростым
и актуальным.74 Из 19 пациентов, которым была
произведена только эзофагомиотомия, эзофагомио-
томия с фундопликацией по Ниссену или только
фундопликация по Ниссену, непроходимость как
следствие фундопликации развилась у одной трети
больных и гастроэзофагеальный рефлюкс — также
у одной трети. У остальных эзофагомиотомия бы-
ПИЩЕВОД 263
ла произведена неадекватно (недостаточное рассе-
чение). У тех пациентов, которые ранее не лечи-
лись, упомянутые авторы использовали комбина
цию эзофагомиотомии и фундопликации по Белеи
(Belsey). Среди наблюдавшихся и обследованных
в отдаленные сроки после операции у 88% резуль-
таты были очень хорошими, что подтверждалось
отсутствием жалоб, данными определения pH
и манометрии. Авторы сделали вывод, что перед-
няя фундопликация и эзофагомиотомия — методы
выбора при ахалазии у взрослых. Другие хирурги
утверждают, что правильно сделанная эзофагомио-
томия, когда разрез не заходит на желудок. — абсо-
лютно адекватное вмешательство при ахалазии.
Если же разрез распространяется на желудок, то
следует дополнить операцию фундопликацией,
причем предпочтительнее создание полумуфты,
а не полной муфгы.7* Большинство клиницистов
считают, что эзофагомиотомия в сочетании с пе-
редней фундопликацией — идеальная операция при
ахалазии.66 ,6 79
В одной из работ сообщалось, что при лечении
21 ребенка только у 5 пациентов была сделана
фундопликация (во всех случаях — по Ниссену).
Получены хорошие результаты.71 По данным дру-
гих авторов, изучавших проблемы фундопликации
по Ниссену в детском возрасте, 50% детей, кото-
рым делается эзофагомиотомия по поводу ахала-
зии, нуждаются в последующем в фундопликации,
причем предпочтительнее вмешательство по Талю.”
Наш собственный опыт представлен 15 пациента-
ми, которым произведена эзофагомиотомия в соче-
тании с фундопликацией по Талю. Во всех случаях
получены прекрасные отдаленные результаты.
СТРИКТУРЫ ПИЩЕВОДА
У детей практически не бывает стриктур пищево-
да, связанных со злокачественными процессами.
Причинами же доброкачественных стенозов могут
быть гастроэзофагеальный рефлюкс, химические
ожоги и рубцы в зоне анастомоза. Анастомотиче-
ские стриктуры иногда усугубляются гастроэзофа-
геальным рефлюксом. Поэтому во многих случаях
лечение должно заключаться не только в устране-
нии непроходимости, но и в предупреждении ее
рецидива путем ликвидации гастроэзофагеального
рефлюкса. Сужения в зоне анастомоза обычно не-
большие по протяженности, в то время как стено-
зы, вызванные ожогами, могут охватывать пище-
вод на значительном протяжении Пептические
стриктуры пищевода локализуются, как правило,
в нижней его трети, длина их небольшая, тем не
менее они очень трудно поддаются лечению.
Стенозы пищевода известны с давних времен,
а лечение их бужированием представляет собой
чрезвычайно увлекательную историю."1 Дилатация
циркулярных стриктур обычно направлена на то,
чтобы «разорвать» рубцовую ткань, и если бужи-
рование сочетается с местной инъекцией триамци-
нолона, то эффект, как правило, отчетливый.’2"84
Применяемые в настоящее время методы дилата-
ции очень разнообразны. Это прежде всего прове-
дение струны, по которой вводятся расширители
Tucker.” Используются также бужи Hurst с ртут
пым наполнителем, нити и проводники, расшири-
тели Savary с проволочным проводником и. нако-
нец, наиболее современные баллонные расширите-
ли. При сравнении (в отношении как осложнений,
так и отдаленных результатов) метода тангенци-
ального расширения бужами с радиальным бужи-
рованием баллонами. наибольшее число сто-
ронников находят второй способ (баллонное бужи-
рование) более безопасным и эффективным."" Ем)
отдаем предпочтение и мы.
Любой метод дилатации несет в себе риск разви-
тия септицемии, вплоть до образования абсцессов
мозга.8’ В одной из работ сообщалось о том, что
при бужировании 9 пациентов у четверых из крови
высевался золотистый стафилококк. Авторы
считают поэтому, что больные, подвергающиеся
бужированию пищевода, должны получать соот-
ветствующую защиту антибиотиками. Кроме того,
всегда существует угроза перфорации пищевода,
однако ею приходится пренебрегать, поскольку
слишком уж велико значение бужирования.
Кроме стриктур в зоне анастомоза, наложенного
при атрезии пищевода, сужения могут также воз-
никать на любом из концов пересаженного транс-
плантата толстой кишки. Хотя в некоторых случа
ях бужирование подобных стенозов бывает эффек-
тивным, однако часто из-за рефлюкса кислого
желудочного содержимого проблема таких стрик-
тур продолжает на протяжении многих лет оста-
ваться очень серьезной и требует повторных бужи-
рований. В редких публикациях приводятся приме-
ры успешного бужирования проксимального эзо-
фагоколоанастомоза, что способствовало заживле-
нию шейного свища.™ Однако, по нашему опыту,
такие свищи обычно требуют ревизии и резекции,
без чего спонтанное заживление невозможно.
Пептические стенозы дистального отдела пише-
вода успешно лечатся бужированием и консерва-
тивной терапией рефлюкс-эзофаги га. Однако бо-
льшинство хирургов, занимающихся лечением
этой комбинации (пептический стеноз 4- рефлюкс-
эзофагит), дополняют дилатацию фундоплика-
цией, что способствует устранению рефлюкса.”-’4
Если сравнивать эффективность фундопликации
(в сочетании с дилатацией) и первичной пластики
пищевода, го оказывается, что фундопликация да-
ет лучшие результаты и меньшее количество позд-
них осложнений (рис. 21-7) ’’
В редких случаях сужение пищевода развивается
у больных с эпидермолизом. В подобных ситуаци
ях обычно требуется пластика пищевода, посколь-
ку основное заболевание не позволяет проводить
бужирование из-за опасности разрыва слизистой.96
ПОСЛЕОЖОГОВЫЕ СТЕНОЗЫ
Послеожоговые стенозы могут быть успешно изле-
чены бужированием. Эффект лечения более стой-
кий, если бужирование сочетается с введением
в рубец стероидов.” Одна из сложных проблем,
возникающих при таком подходе к послсожоговым
264 ПИЩЕВОД
Рис. 21 7 У 8-летнего ребенка с запущенным нелеченным рсф
люксом пилен расширенный проксимальный отдел пишеиода.
резко ныражениое сужение и нонан складчатость в пищеводе
над диафрагмой. Целесообразно произвести фундопликацию
о сочетании с бужированием. Возможно, потребуется пластика
дистальною отдела пищевода. Выбор метода хирургического
лечения в данном случае зависит от тою. насколько легко и аф-
фективно будет проходить бужирование. Нередко вопрос о ха-
рактере вмешательства может быть решен тишь интраппераци-
оиио. Готовиться же следует тем не менее либо к пластике диа-
фрагмы по поводу грыжи пищеводного отверстия с фундоплика-
цией либо к замещению дистального отдела пищевода тем или
иным способом.
стриктурам, состоит в том, что, когда пищевод
продолжает функционировать как путь для про-
хождения пиши, то с течением лет на месте пора-
жения можег развиться эпителиальная карцинома.
В литературе существуют сообщения в общей
сложности более, чем о 130 подобных наблюдени-
ях. Клинически при этом у ребенка со стриктурой,
леченной бужированием на протяжении долгого
времени, через 20 40 лет развивается прогрессы
рующая дисфагия. Эпителиальная карцинома по-
сле тяжелых ожогов возникает, как правило, на
уровне дуги аорты.” 1,12 Согласно данным одного
из исследований, среди 63 пациентов с карцино-
мой, иозникшей после лечения бужированием ожо-
говой стриктуры, 24 были кандидатами на хирур-
гическое лечение. Только v 20 была произведена
резекция, из них 5 умерли. Из 15 выживших пяте-
ро жили в течение 5 лет. А среди тех, кто получал
рентгенотерапию, 10% жили 5 лет и 5% —7 лет.
Сравнение с другими пациентами с карциномой
пищевода (без ожога и бужирования в анамнезе)
позволяет говорить, что в этой группе (у детей
с ожогами и развившейся впоследствии карцино-
мой) результаты резекции пищевода обнадежива-
ют в большей степени. Лучший прогноз, возможно,
связан с тем. что дисфагия у таких больных по-
является раньше, поскольку из-за рубцовых изме-
нений пищевод менее растяжим. Кроме того, рубец
в пищеводе препятствует раннему местному рас
пространснию опухоли.112
В нашей практике (и у некоторых других авто-
ров)"1’ не было ни одного случая карциномы после
ожога пищевода. В связи с этим следует подчерк-
нуть. что при послеожоговых рубцовых изменениях
пищевод не должен использоваться по своему на-
значению (как проводник пищи) у оставшихся в жи-
вых пациентов. Пластика пищевода со всеми при-
сущими ей трудностями, вероятно, все же лучший
способ лечения, чем использование пищевода как
тракта для прохождения пиши. Оставлять или ре-
зецировать пораженный пищевод при проведении
трансплантата — этот вопрос остается дискута-
бедьным.
ПЛАСТИКА ПИЩЕВОДА
Мой собственный подход к пластике пищевода
определяется следующими главными четырьмя
принципами.
1. Пищевод — лучший проводник для пиши, ес-
ли, разумеется, он нормально функционирует и не
имеет склонности к злокачественному росту, как
это бывает при ожогах щелочью или при пищеводе
Барретта.
2. Наилучший трансплантат — прямой, без из-
гибов и поворотов. Очень важно, чтобы он обладал
этими свойствами, поскольку часто требуется эзо-
фагоскопия и дилатация. Почти нее трансплантаты
функционируют в большей степени как пассивные
проводники, чем за счет собственной двигательной
активности и перистальтики.
3. Используя любой метод пластики пищевода,
жела тельно предотвратить рефлюкс из желудка
в трансплантат, а потому лучшие виды замещения
пищевода — те, при которых дистальный нормаль
ный отдел пщцевода с пищеводно-желудочным со-
единением остается действующим и интактным.
4. Чрезвычайно важна надежность пластики, ко-
торая должна быть проведена таким образом, что-
бы не возникала необходимость бужирования ана-
стомоза (на концах трансплантата), за исключени-
ем фазы заживления. Стриктуры после трансплан-
тации следует лечить только хирургическим пу-
тем. Если по завершении пластики пищевода
трансплантат не функционирует достаточно хоро-
шо. может и должна быть произведена реконструк-
ция с целью создания и обеспечения наиболее пря-
мого и надежного пути для прохождения пищи.
Толстокишечная пластика
(рис. 21-8, 21-9)
В США наиболее популярно замещение пищевода
правой половиной толстой кишки.104 В Англии ча-
ще для этих целей используется ее левая полови-
на. 1олстая кишка может быть перемещена
как в ан гиперистальтическом направлении,'04 так
ПИЩЕВОД 265
Рис. 21 -ti. А, При любом поражении пищевода, когда предполагается пластика, показана гастростомия. Гастростома должна быть
наложена по малой кривизне желудка на уровне его вырезки (incisura) таким образом, чтобы при проведении трансплантата как из
толстой кишки (левой или правой половины), так и из желудочного цилиндра, не возникли бы нарушения кровообращения.
В, Выделены правая половина толстой кишки и терминальный отдел подвздошной, получающие питание от аркад и средней обо-
дочной артерии.
С, Толстая кишка на сосудистой ножке проведена через малый сальник и помещена загрудинно в нзопсристальтичсском на-
правлении.
D, В большинстве случаев производится резекция терминального отдел.» поднздопнюй и слепой кишки. Дистальный отдел
трансплантата очень аккуратно сопоставляется и анастомозируется с антральным отделом желудка таким образом, чтобы он
был прямым, без изгибин. Операция дополняется пи юропластикон. но может быть выполнена и без нее. Если производится дрени-
рующее вмешательство, то частота развития клинически проявляющегося гастроэзофагеального рефлюкса, как правило, умень-
шается.
266 ПИЩЕВОД
Рис. 21-9. При изолированной атрезии пищевода производится операции создания искусственного пищевода из левом половины
или поперечно-ободочного отдела толстой кишки по Уотерстону. Этот метод успешно применяется и при других видах патологии
пищевода, требующих пластики.
А, Обычная заднебоковая торакотомия слева в 6-м межреберье.
В, Разрез по периферии диафрагмы.
С, Берется участок толстой кишки на хорошей питающей ножке — обычно на левой ободочной артерии. Иногда приходится фор-
мировать трансплантат на средней ободочной артерии. Затем трансплантат перемещают в антиперистальтическом направлении.
D, Толстая кишка с сосудистой ножкой проводятся позади селезенки и поджелудочной железы через отдельный разрез диафраг-
мы сзади таким образом, чтобы органы брюшной полости ие давили на сосудистую иожку и не нарушали кровоснабжение транс-
плантата каким-либо иным путем.
Е, Дистальный анастомоз может быть создан с оставшимся участком дистального сегмента пищевода или с задней стенкой
желудка.
и изоперистальтически.105 Некоторые хирурги
предпочитают проведение трансплантата из попе-
речного отдела или левой половины толстой киш-
ки внутриторакально позади корпя легкого, не
придавая особого значения при этом перистальти-
ческой ориентации трансплантата.10’-10
При сравнительном изучении опыта 80 опера-
ций пластики толстой кишкой у 79 детей отмече-
но, что в 70% случаев трансплантат был проведен
позади корня легкого изоперистальтически и в
30% — ретростернально. В основном это были па-
циенты с атрезией пищевода и культей его дис-
тального сегмента. Несостоятельность проксималь-
ного анастомоза возникла в 31% наблюдений, при-
чем стриктура в этой зоне развилась в 15%
случаев среди детей, которым была проведена ле-
вая часть толстой кишки позади корня легкого по
Уотерстону, и в 41%—после ретростернальной
пластики. Кроме того, у 60% пациентов с загру-
динной пластикой выявлен рефлюкс, в то время
как при операции по Уотерстону это осложнение
отмечалось лишь у 18% больных. 5 из 12 детей
с толстокишечным ретростернальным трансплан-
татом потребовали хирургического вмешательства
по поводу язв. Анализ результатов лечения позво-
лил сделать вывод, что более предпочтительна
пластика пищевода из левой половины толстой
кишки с проведением трансплантата позади корня
легкого по Уотерстону.110
По данным другой публикации с анализом
20 операций толе токи шечной пластики, при ретро-
стернальном и интраторакальном проведении
трансплантата функциональные результаты были
одинаковые, но стриктуры, потребовавшие резек-
ции, развивались только при ретростернальной
пластике."1 При загрудинном проведении правой
половины толстой кишки отмечалось большее ко-
личество интраоперационных осложнений ишеми-
ческого характера, чем при использовании метода
Уотерстона со взятием трансплантата из попереч-
ПИЩЕВОД 267
Рис. 21-9. F, Верхний анастомоз с пищеводом создается в средостении или на шсс. Для профилактики эмпиемы необходимо адек-
ватное дренирование плевральной полости. Если используется дистальный отдел пищевода, то данная операция может быть допол-
нена фундоп ликацией по Талю, что уменьшает возможности для развития рефлюкса, препятствующего заживлению и способствую-
щего изъязвлению трансплантата.
G, Альтернативный вид нижнего соустья при выполнении операции по Уотерстону — кологастроанастомоз (вид сбоку).
Н. Считается, что расположение части трансплантата в брюшной полости может препятствовать развитию рефлюкса, однако, по
нашим данным, это не предотвращает рефлюкс-
ного отдела или левой половины толстой кишки.106
Данные различия могут быть объяснены тем, что
почти у 70% больных правая половина толстой
кишки не имеет краевой артерии, необходимой для
питания трансплантата.
Хотя в одной из работ отмечается несостоятель-
ность проксимального анастомоза трансплантата
всего в 2% случаев,105 однако большинство хирур-
гов сообщают о развитии данного осложнения зна-
чительно чаще — у 30—33% больных.110,1,3‘1,4 Ес-
ли несостоятельность эзофагоколонастомоза мож-
но объяснить как техническими погрешностями
при его наложении, так и легкой степенью ише-
мии, то формирование стеноза, несомненно, связано
только с ишемией. Повторное бужирование в та-
ких ситуациях, как правило, неэффективно. По-
этому большинство стриктур анастомоза, проявле-
ния которых сохраняются в течение более, чем
6 мес после трансплантации, однозначно нужда-
ются в хирургической коррекции. Лечение несосто-
ятельности анастомоза, равно как и вмешательство
по поводу стеноза пищевода, значительно облегча-
ются, если анастомоз создан на шее. К счастью,
проксимальный анастомоз чаще всего здесь и рас-
положен, ибо именно до этого уровня обычно рас-
пространяется ожоговое поражение проксимально,
268 ПИЩЕВОД
и здесь же находится короткий верхний сегмент
пищевода при изолированной атрезии.
Среди наших больных была одна девочка, кото-
рой в возрасте 3 лет была произведена тодстоки-
шечная пластика по поводу послеожогового стено-
за. Несмотря на периодически рецидивировавшие
проявления верхней анасгомо1ической стриктуры,
она чувствовала себя вполне прилично до 18 лет,
когда возник свищ на шее. Первично анастомоз
накладывался между шейным отделом пищевода
и терминальной частью подвздошной кишки. Для
ликвидации позднего пищеводно-шейного свища
была сделана стернотомия и разрез вдоль tenia для
удлинения сегмента толстой кишки, что позволило
убрать терминальный отдел подвздошной кишки
и слепую кишку. Затем был наложен анастомоз
между пищеводом и восходящим отделом толстой
кишки. После этой операции клинические прояв-
ления исчезли. При первом описании упомянутого
метода удлинения загрудинного голегокишечного
трансплантата предлагалось иссечение tenia.115 Од-
нако множественные разрезы tenia более легки
в исполнении и не менее эффективны.116
Рефлюкс в толстокишечный трансплантат обыч-
но минимальный, если сохранен дистальный О1дел
пищевода и с ним анастомозирован трансплантат.
Считается, что предотвратить рефлюкс можно
и в том случае, когда трансплантат из левой поло-
вины толстой кишки соединяется с желудком низ-
ко на задней стенке. Однако, по нашему мнению,
это не так.’17 Хотя и высказывается мнение, что
интраабдоминальная локализация сегмента транс-
плантата длиной 10 см эффективно предотвраща-
ет рефлюкс, рентгенологическое исследование с
контрастным веществом под контролем экрана
н манометрия нс подтверждают это предполо-
жение 18
Профилактике рефлюкса в трансплантат эффек-
тивно служит создание туннеля в подслизистом
слое,1” обеспечивающего антирсфлюксный меха-
низм.120 Что же касается фундопликации Ниссена
вокруг передней полуокружности кологастроана-
стомоза, то хотя она и дает хорошие результаты
в эксперименте на животных, однако у людей не
всегда предотвращает рефтюкс. Авторы этих экс-
периментальных работ считают, что лучший метод
профилактики рефлюкса 121 — создание колоэзо-
фагоанастомоза по Уотерстону.1117
Изучение влияния кислоты желудочного сока на
дистальный кологастроаиастомоз установило, что
щелочной секрет толстой кишки имеет тенденцию
центра шзовать кислоту и проталкивать ее обрат-
но в желудок до того, как возникнут какие-либо
осложнения, с ней связанные 2 'Гем нс- менее, язвы
дистальных отделов трансплантата, если они воз-
никают, являются результатом воздействия кисло-
го желудочного содержимого. Большинству паци-
ентов, у которых развились язвы, пластика пище-
вода не дополнялась пилоропластикой или пилоро-
миотомией, цель которых — улучшить опорожне-
ние желудка. Результаты данного исследования
лишний раз подтверждают, что в тех случаях, ког-
да накладывается кологастроаиастомоз, необходи-
мо одновременно производить дрепиоование же-
лудка.
Изучение двигательной активности толстоки-
шечного и других трансплантатов пищевода пока-
зало, что толстая кишка хорошо продвигает пище-
вой комок, несмотря на то, что нет четких призна-
ков координированной перистальтики.1 Исследо-
вание более отдаленных результатов позволяет
говорить о том, что не имеет особого значения —
изо- или антиперистальтически пересажена тол-
стая кишка. В любом случае она достаточно бы
стро теряет способность продвигать содержимое
и служит лишь как пассивный проводник для пи-
щи.|Г| Не было никакой разницы и в плане процес-
са глотания при обследовании 00 пациентов, две
трети которых имели антиперистальтический тол-
стокишечный трансплантат. Рефлюкс из желудка
в дистальные отделы трансплантата отмечался
также независимо от перистальтической его ори-
ентации. А вот если была сделана пилоропласти-
ка, то осложнения встречались реже.124 Подобные
же результаты получены и другими авторами, ко-
торые у 84 больных производили как изо-, так
и антиперистальтическую толстокишечную транс-
плантацию.125
Функциональное исследование толстокишечного
трансплантата с молоком, меченным изо гопом, по-
казало. что у пациентов, не имевших никаких жа-
лоб. опорожнение трансплантата наступало мепее,
чем за 45 мин, а гастроэзофагеальный рефлюкс
при этом отсутствовал. У больных же с теми или
иными клиническими проявлениями обнаружена
задержка опорожнения трансплантате! в сочетании
с рефлюксом или только рефлюкс. В общем функ-
ция толстокишечного трансплантата, по данным
этого исследования, оценена как удовлетворите
льная.126
Из поздних осложнений следует назвать избы-
точный рост трансплантата, что может даже при-
вести к его завороту и непроходимости, как было
описано в одном из наблюдений.12' Изъязвление
трансплантата иногда способствует его прободе-
нию в перикард. Мы наблюдали пациента, у ко-
торого в результате изъязвления трансплантата
развился контактный остеомиелит грудины, его
лечение представило чрезвычайные сложности
(рис. 21-Ю).128
Одна из проблем, определяющая, в сочетании
с другими факторами, выбор метода пластики пи-
щевода, — возможность развития у пациента при-
обретенных заболеваний сердца, которые иногда
требуют хирургического вмешательства через
стернотомический доступ. В тех случаях, когда бы-
ла сделана загрудинная пластика, этот доступ
к сердцу чрезвычайно сложен. И наоборот, если
первоначально ребенок был оперирован на сердце
через сгернотомический доступ, необходимо поду-
мать об ином, альтернативном (не загрудинном)
методе пластики пищевода.
Выбор сроков пластики пищевода. В тех случа
ях, когда имеется атрезия пищевода без дистально-
го трахеопищеводного свища и решено нс пред-
принимать попыток удлинения сегментов, толсто-
ПИЩЕВОД 269
Рис. 21-10. Избыток загрудинно проведенной толстой кишки
иногда представляет сложную проблему и требует осторожного
перекраивания (с целью укорочения) дистального ее отдела,
при этом важно не нарушить кровоснабжение верхних участков.
кишечная пластика может быть произведена в пе-
риоде новорожденное™.130 Однако большинство
детских хирургов в подобных ситуациях делают
шейную эзофа гостом у и гастростому, а пластику
пищевода толстой кишкой выполняют после 6 мес.
Некоторые же откладывают эту операцию даже до
1 1,5 лет. И тот и другой вариант имеет свои
преимущества как в теоретическом, так и в прак-
тическом плане. В большинстве публикуемых ра-
бот рекомендуется более позднее вмешательство.
Однако, если ребенок не кормится через рот в те-
чение многих месяцев, то после пластики пищево-
да он может так и не захотеть есть. Поэтому при
наличии гастростомы кормление через нее должно
сочетаться с «бутафорским» кормлением через рог,
чтобы наполнение желудка ассоциировалось у ре-
бенка с приемом пищи через рот и глотанием.
В тех случаях, когда попытки удлинения сегментов
пищевода или наложения анастомоза при АП
с нижним ТИС при большом диастазе потерпели
неудачу, а также при каустических ожогах, пла-
стика пищевода, естественно, производится после
периода новорожден пости.
Пассивное или активное дренирование должно
сопровождать любой анастомоз пищевода, где бы
он ни накладывался — на шее нли в грудной
клетке.
Что касается нашего подхода к толстокишечной
пластике, то мы предпочитаем брать левую поло-
вину толстой кишки и использовать метод Уотер-
стона с проведением ножки трансплантата позади
поджелудочной железы. Дистальный анастомоз,
если это возможно, создаем с дистальным отрезком
пищевода. У большинства этих больных мы также
производим фундопликацию по Талю, дабы укре-
пить кардиальный жом и предотвратить гастроэзо-
фагеальный рефлюкс в трансплантат. Но в прин-
ципе мы предпочитаем использовать замещение
пищевода желудочным цилиндром, который прово-
дим вверх через естественное пищеводное отвер-
стие диафрагмы и анастомозируем с проксималь-
ным (шейным или медиастинальным) отделом пи-
щевода, дистальную часть которого резецируем.
Пластика пищевода
желудочным цилиндром
Пластика пищевода желудочным цилиндром стала
производиться у детей в начале 70-х годов.
Однако количество таких операций у каждого ав-
тора значительно меньше, чем опыт толстокишеч-
ной пластики. Это объясняется по меньшей мере
двумя обстоятельствами. Во-первых, большинство
хирургов пользуются в основном замещением пи-
щевода толстокишечным трансплантатом. Во-вто-
рых, уменьшилось количество больных, нуждаю-
щихся в пластике пищевода, что связано с боль-
шей настороженностью в отношении опасности
каустических препаратов, а также с изменениями
химического состава тех веществ, которые име-
ются в продаже.
Желудочные цилиндры стали популярны преж-
де всего в связи с тем, что могут быть созданы
очень быстро, с использованием сшивающих аппа-
ратов. Кроме того, они конструируются как из ант-
рального отдела вверх, так и из дна желудка вниз.
К тому же длина их может быть настолько велика,
что ее хватает для перемещения желудочного ци-
линдра до шеи.132 Желудочные цилиндры прово-
дятся за грудин но или за корнем легкого как спра-
ва, так и слева. При сравнительном изучении их
функции выявлено, что результаты вмешательств
были одинаковы, независимо от того, проведен
трансплантат трансторакально или загрудинно.
Отдаленные результаты при использовании желу-
дочного цилиндра намного лучше, чем при толсто-
кишечной трансплантации, не говоря уже о том,
что формирование желудочного цилиндра техниче-
ски значительно проще.132
Использование данного метода может сопровож-
даться развитием язв как в самом цилиндре, так
и в области его соединения с проксимальным отде-
лом пищевода. По существующим представлениям,
изъязвление скорее всего связано с застоем содер-
жимого в искусственном пищеводе. Поэтому всем
больным, которым производится замещение пище-
вода желудочным цилиндром, должна быть сдела-
на пи лоро пластика.132 Проблема рефлюкса обычно
не возникает, если хотя бы как минимум 6 см же-
лудочного цилиндра расположены в брюшной по-
лости.
Мы предпочитаем во всех случаях, если только
это возможно, перемещать желудочный цилиндр
через пищеводное отверстие диафрагмы позади
корня легкого, дополняя вмешательство фундопли-
кацией, как это показано на рисунке 21-11. Функ-
ция желудка в зоне подобной фундопликации пре-
270 ПИЩЕВОД
Рис. 21-11. Ку Пластику желудочным цилиндром, согласно на-
шему опыту, лучше делать в антнпсристальтическом направле-
нии, используя участок большой кривизны желудка. До того,
как приступают к формированию цилиндра, необходимо очень
тщательно оценить характер кровоснабжения.
В. Цилиндр формируется с помощью сшивающих аппаратов,
используемых при операциях иа ЖКТ. Важно избежать ятро-
генного сужения искусственного пищевода. Использование тол-
стого перфорированного резинового катетера может предотвра-
тить развитие этого осложнения. Следует также помнить о воз-
можности перекручивания большой кривизны, что иногда быва-
ет причиной несоответствия длины задней и передней стенок
желудка. Для создания цилиндра, достаточного по протяженно-
сти. редко возникает необходимость в перевязке и разделении
коротких желудочных сосудов.
С, Для анастомозирования в средостении или на шее с остав-
шейся проксимальной частью пищевода желудочный цилиндр
может быть перемещен в переднее средостение загрудинно или
через пищеводное отверстие диафрагмы. Создание задней не-
полной манжетки, как это показано на рисунке, эффективно
предотвращает рефлюкс содержимого желудка в созданный ци-
линдр и уменьшает вероятность изъязвления и стенозирования
анастомоза.
красная (рис. 21-12). Мы не делаем, как это обыч-
но принято, пилоропластику или пилоромиотомию.
Изучение отдаленных результатов перемещения
желудочного цилиндра показывает, что у наших
больных намного меньше любых проблем, чем по-
сле толстокишечной пластики.
Использование эзофагопластики желудочным
цилиндром ограничено, к сожалению, возрастом
ребенка и может применяться лишь у старших де-
тей, поскольку для создания хорошего искусствен-
ного пищевода должна быть взята столь значи-
тельная часть желудка, что это не позволяет осу-
ществлять данное вмешательство у очень малень-
ких детей.
Перемещение желудка
Мобилизация желудка с его перемещением в сре-
достение не применялась у растущих детей по
принципиальным соображениям, ибо считалось,
что после этой операции развитие ребенка не мо-
ПИЩЕВОД 271
С
В
Рис. 21-12. А, Стеноз среднего и листального отделов пищевода
через много лет после ожога щелочью- Хорошо видно укороче-
ние пищевода и складчатость нал диафрагмой.
В, На рентгенограмме с барием в боковой проекции в раннем
послеоперационном периоде виден желудочный цилиндр с неко-
торым отеком анастомоза в среднем отделе пищевода. Цилиндр
проведен в заднее средостение через пищеводное отверстие диа-
фрагмы.
С. Исследование в отдаленном периоде показывает отсутст-
вие рефлюкса в желудочный цилиндр, что, возможно, является
результатом фундопликации, осуществленной так, как это по-
казано на рис. 21-11С.
жет быть нормальным. В детском госпитале на
Create Ormond Street данный метод стали исполь-
зовать в 1981 году, как у новорожденных с атре-
зией пищевода, так и у более старших детей с ожо-
гами пищевода или после неудачного лечения ат-
резии.133 Результаты применения операции переме-
щения желудка у 34 пациентов в этом учреждении
опубликованы в 1987 г. У 23 детей эзофагогастро-
анастомоз произведен в возрасте до 1 года. В 16
случаях желудок перемещен в средостение и в
18 — в грудную клетку позади корня легкого. Пи-
лоромиотомия была сделана у 13 детей и пило-
ропластика —у 20. Среди 31 выжившего пациента
у 14 послеоперационное течение было гладким,
в 17 наблюдениях отмечались различные осложне-
ния (одно или несколько), в основном связанные
272 ПИЩЕВОД
с неправильным кормлением до пластики. У одно-
го ребенка развилась несостоятельность сюносто-
ма, что потребовало повторной лапаротомии.
У всех детей на время послеоперационного зажив-
ления обязательно накладывалась еюностома для
питания. Важно, что всего лишь у 6 детей из 23,
наблюдавшихся как минимум в течение года после
операции, отмечалось отставание в массе тела
и росте. Остальные дети развивались практически
нормально.
Сравнение результатов применения в этом гос-
питале данного метода со 112 наблюдениями тол-
стокишечной пластики по Уотерстону, проведен-
ной в 1952—81 гг., показало, что легальность
была одинаковой, однако частота гибели транс-
плантата, несостоятельности шейного анастомоза,
его стеноза и «качество жизни» были значительно
лучше после перемещения желудка.
Мы применили этот метод только у одного ре-
бенка, который перенес неудачную толстокишеч-
ную трансплантацию, а затем также неудачную
пластику желудочным цилиндром. В конце концов
ему был перемещен желудок через правую полови-
ну грудной клетки позади корня легкого с создани-
ем эзофагогастроанастомоза. Получен хороший
результат (рис. 21 13).
Пластика тощекишечным трансплантатом
Тощая кишка в качестве трансплантата пищевода
используется гораздо чаще у взрослых, чем у де-
тей. В детском же возрасте этот метод применяется
обычно лишь после неудачных попыток пластики
пищевода другими способами. В литературе име-
ются сообщения о 19 детях, которым была сделана
еюнальная пластика среднего отдела пищевода
с проведением трансплантата через правую поло-
вину грудной клетки. У 12 пациентов прослежены
отдаленные результаты: в одном случае выявлен
стеноз и в одном — избыточный рост транспланта-
та с его удлинением. Хирурги, как правило, сохра-
няли после неудачной пластики по Уотерстону ди-
стальный отдел пищевода, а потому требовался
сегмент тощей кишки длиной всего лишь 10—
12 см. Однако для выкраивания столь небольшого
по протяженности трансплантата приходится жер-
твовать участком тощей кишки длиной в 40 см.
В результате утраты столь значительного по про-
тяженности отдела гонкой кишки у некоторых
больных бывают проблемы с пищеварением.134
Наиболее часто тощая кишка используется в ви-
де свободного трансплантата с микрососудистым
анастомозом на шее у взрослых больных с карци-
номой. Имеются сообщения об использовании это-
го метода с хорошими результатами у 101 больно-
го, однако у детей он, конечно, не должен использо-
ваться.135 Мы сделали только одну тощекишечную
пластику со вшиванием трансплантата между шей-
ным отделом пищевода и желудком, с хорошим не-
посредственным результатом. Ребенок в дальней-
шем исчез из поля нашего зрения, и отдаленные
результаты поэтому не были прослежены.
Рис. 21-13. Ребенок после эзофагогастроаиастомоза, произве-
денного после безуспешной трансплантации толстой кишки
и неудачной пластики желудочным цилиндром. Во время опера-
ции создания эзофагогастроанастомоза была также сделана nit-
лоропластика.
Осложнения пластики пищевода
Замещение пищевод;! может повлечь за собой ряд
вполне предсказуемых осложнений, наиболее серь-
езным из которых является нарушение кровоснаб-
жения трансплантата. Как уже упоминалось ранее,
это осложнение чаще встречается при толстоки-
шечной пластике и может быть распознано во вре-
мя операции по таким признакам, как изменение
окраски трансплантата и пульсации сосудов. При
наличии этих симптомов следует ослабить натяже-
ние трансплантата или устранить перекрут его
ножки. Если данные манипуляции оказались безу-
спешными, то от трансплантации следует отка-
заться, ибо надежда на то, что кровообращение
восстановится в послеоперационном периоде,
обычно не оправдывается.
После пластики хорошо васкуляризированным
трансплантатом иногда через несколько дней по-
ПИЩЕВОД 273
является лихорадка, возрастает лейкоцитоз и уве-
личивается количество отделяемого сверху из зо-
ны проксимального анастомоза. Контрастное ис-
следование выявляет изменение состояния сли-
зистой трансплантата. При подобной ситуации
следует удалить трансплантат, восстановить шей-
ную эзофа гостом у и в последующем произвести
какой-либо другой вид пластики. Многие хирурги
имеют опыт успешного использования левой поло-
вины толстой кишки после неудачной пластики
правой половиной. Мы считаем, что в таких случа-
ях вряд ли стоит жертвовать столь большим коли-
чеством толстой кишки, и предпочитаем использо-
вать либо желудочный цилиндр, либо перемеще-
ние желудка.
Изъязвление как желудочного цилиндра, так
и толстокишечного трансплантата может развить-
ся в результате рефлюкса и застоя содержимого
в искусственном пищеводе, чему способствует на-
личие в нем изгибов, а также задержка опорожне-
ния желудка. В более поздние сроки иногда возни-
кают осложнения, обусловленные поражением
блуждающего нерва вследствие вовлечения его
в процесс после химического ожога или предше-
ствовавших неудачных попыток пластики пищево-
да. Остается спорным вопрос о том, чем целесо-
образней дополнять пластику пищевода — пило-
ропластикой иди иными вмешательствами, спо-
собствующими ускорению опорожнения желудка.
Разумеется, очень важно для профилактики изъязв-
ления устранить во время пластики все изгибы,
которые могут быть резервуарами для скопления
и задержки пищи. Но если это осложнение все же
возникло, то ревизию нижнего отдела толстоки-
шечного трансплантата для устранения избыточ-
ных петель и изгибов следует делать с очень боль-
шой осторожностью, дабы не повредить сосуди-
стую ножку, что может привести к потере всего
трансплантата.
У одного из наших пациентов после загрудин-
ной толстокишечной пластики развился рецидиви-
рующий стеноз верхнего анастомоза и тяжелый
гастроэзофагеальный рефлюкс в нижний отдел
трансплантата. Мы выделили оба конца транс-
плантата через комбинированный доступ (право-
сторонняя торакотомия и лапаротомия), опустили
трансплантат снова в брюшную полость, а затем
провели его позади корня правого легкого, реана-
стомозировали с верхним отделом пищевода, уко-
ротили и анастомозировали с нижним отрезком
пищевода, завершив операцию фундопликацией по
Талю. Результаты были отличными. Разумеется,
столь обширная повторная операция редко бывает
необходимой, но тем не менее она вполне осуще-
ствима и может радикально помочь при неудовлет-
ворительных результатах первичной пластики.
СОСУДИСТОЕ КОЛЬЦО
Сосудистые аномалии, в которые вовлечена дуга
аорты и ее главные ветви, известны под названием
сосудистых колец. В данной главе излагаются
только те варианты подобных пороков, которые
могут вызвать стеноз пищевода. К ним относятся:
полное кольцо (двойная дуга аорты), неполные
кольца (чаще всего добавочный подключичный со-
суд, располагающийся сзади от пищевода), а так-
же поперечная дуга аорты, которая, проходя поза-
ди пищевода, спускается на сторону, противопо-
ложную локализации восходящей аорты. Непол-
ные кольца часто связаны с артериальной связкой
или артериальным протоком, ограничивающими
пространство, предназначенное для трахеи и пи-
щевода. Эти пороки, будучи редкой причиной дис-
фагии. на контрастных (с барием) эзофагограммах
встречаются довольно часто. Еще одна тяжелая
аномалия типа сосудистого кольца, известная под
названием «петля легочной артерии», часто рас-
сматривается в разделе пороков развития трахеи,
но редко вызывает симптомы со стороны пище-
вода.
В большинстве случаев васкулярное кольцо про-
является дисфагией. Специальный термин dyspha-
gia lusoria (дисфагия загадочная) существует для
обозначения симптомов, возникающих при нали-
чии добавочной правой подключичной артерии,
которая проходит позади пищевода, направляясь
к правой подмышечной впадине. Однако в клини-
ческой практике этот аномальный сосуд редко вы-
зывает дисфагию.
Поскольку непроходимость пищевода при сосу-
дистых кольцах частичная, то выраженность симп-
томов зависит в основном от того, насколько «жад-
но» ест ребенок и какова консистенция пищи (гу-
стая, твердая, жидкая). Поэтому часто аномалии
данной группы не проявляются до тех пор, пока
ребенок не начинает есть обычную пищу взрос-
лых, не прожевывая ее при этом как следует.
Диагностика. Диагноз почти всегда устанавли-
вается лишь при исследовании пищевода с барием,
которое обычно предпринимается в связи с дисфа-
гией. Типичная рентгенологическая картина двой-
ной дуги аорты заключается в наличии изгиба или
отклонения продольной оси пищевода. Это харак-
терно именно для двойной дуги аорты (рис. 21-14),
в то время как в случае добавочной правой под-
ключичной артерии ход пищевода обычный (про-
дольная ось нс изменена), но имеется выемка или
сдавление его стенки (рис. 21-15). Хотя эхокарди-
ография,136 ангиография 137 или магнитный резо-
нанс338 могут подтвердить диагноз, однако в их
применении обычно нет необходимости.
Хирургическое лечение. В норме формирование
дуги аорты происходит в результате резорбции до-
рсальной четвертой правой дуги с образованием из
правой подключичной и общей сонной артерий бе-
зымянной артерии, которая является первым сосу-
дом, отходящим от аортальной дуги. При наруше-
нии хода этого резорбционного процесса и возни-
кает двойная дуга аорты. При данной аномалии
правая дуга почти всегда больше, левая же. обра-
зующая переднюю часть кольца, как правило, сте-
нозирована в различной степени или даже фиброз-
но изменена. Правая дуга идет позади пищевода,
а левая сдавливает пищевод спереди или препятст-
вует его расширению, что и обусловливает клини-
18 Заказ № 1622
274 ПИЩЕВОД
Рис. 21 14. N. Ла озофаго! раммс с барием диагностирована двойная дуга аорты.
Под ное сосудистое кольцо смещает проксимальный и дистальный участки пище-
вода относительно друг друга.
В, Двойная дуга наиболее сужена п области левой ее части, а потому лучший
подход к ней обеспечивается через левостороннюю торакотомию.
ческую картину. Хирургическое лечение заключа-
ется в левосторонней торакотомии и разделении
левой дуги сосудистого кольца сзади от места от-
хождения левой подключичной артерии или между
восходящей аортой и местом отхождения левой об-
щей сонной артерии.139 Иногда для более эффек-
тивного устранения обструкции пищевода необхо-
димо разделить и артериальную связку. Отделения
сосудов от трахеи спереди и от пищевода по его
левой боковой поверхности обычно бывает вполне
достаточно для того, чтобы дать возможность тра-
хее и пищеводу свободно смещаться влево, что
и приводит к ликвидации клинических симптомов.
Что касается ретроэзофагеальной правой под-
ключичной артерии, то хотя некоторые хирурги
и предлагают отделять ее и рсимп л актировать
в дугу аорты, однако легче и намного более рацио-
нально просто разделить сосуд, предоставив воз-
можность дистальной его части, сократившись,
«уйти» в средостение позади пищевода. Этого
вполне достаточно для устранения клинических
проявлений. Данную операцию также наиболее
удобно выполнять через левосторонний торакото-
мический доступ. Васкулярные кольца обычно не
сочетаются ни с какими другими сосудистыми
и сердечными аномалиями.
Рис. 2115. Л, Удлиненная аберрантная н рана я подключичная артерия распола-
гается позади пищевода и сдавливает его, нс изменяя ось.
В, Аберрантная левая подключичная артерия может быть достаточно легко
разделена через Левосторонний торакотомическмй доступ.
ПИЩЕВОД 275
ЛИТЕРАТУРА
I. Am our у КА: Structure and function of the esophagus in infancy
and early childhood, hi Ashcraft KW, Holder TM (Editors):
Pediatric Psophageal Surgery. Grunc & Stratton, Orlando,
ppi 28, 1986.
2. Leapc LL, Ashcraft KW, Scarpelli DG. et al.: Hazard to
health liquid lye. N Engl J Med 284:578—581. 1971.
3. Ashcraft KW, Padula RT: Effect of dilute corrosives on the
esophagus. Pediatrics 53:226 232, 1974.
4. Webb WR. Ko u Iras P. Ecker RR. el al.: An evaluation of stero-
ids and antibiotics in caustic burns of the esophagus. Ann Tho-
rac Surg 9:95—102, 1970.
5. Haller JA, Bachman BA: Comparative effect of current therapy
on experimental caustic burns of the esophagus. Pediatrics
34:236—245, 1964.
6. Haller JA. Andrews HG. White JJ. et «il.: Pathophysiology
and management of acute corrosive burns of the esophagus:
Results of treatment in 285 children. J Pediatr Surg 6:578—584,
1971.
7. MtKizam F, Talbert JI . Miller D. et al.: Caustic ingestion and
its sequelae in children. Smith Med J 80:187 190, 1987.
8. Anderson KD. Rouse TM, Randolph JG: Controlled trial of cor
ticosteroids in children with corrosive injury of the esophagus.
N Engl J Med 323:637 640, 1990.
9. Edmonson MB: Caustic alkali ingestions by farm children.
Pediatrics 79:413 416. 1987.
10. Shaw AN, Garvey J, Miller B: Lye burn requiring total gastrec-
tomy and colon substitution for esophagus and stomach in
a two-year-old boy. Surgery 65:837—844, 1969.
11. Estrera A, Taylor W, Mills LJ, et al.: Corrosive burns of the
esophagus and stomach: A recommendation for an aggressive
surgical approach. Ann Thorac Surg 41:276—283, 1986.
12- Gago O, Ritter FN, Martel W, et al.: Aggressive surgical tre-
atment for caustic injury of the esophagus and stomach. Ann
Thorac Surg 13:243—250, 1972.
13. Ashcraft KW: Correspondence. Ann Thorac Surg 14:221. 1972.
14. Reyes HM. Lin CY. Schlunk FF, et al.: Experimental tre-
atment of corrosive esophageal burns. J Pediatr Surg 9:317—
327. 1974.
15. Reyes HM, Hill U: Modification of the experimental stent
technique for esophageal burns. J Surg Res 20:65—70, 1976.
16. Hill I J, Norberg HP, Smith MD, cl al.: Clinical technique
and success of the esophageal stent to prevent corrosive strictu-
res. J Pediatr Surg 11:443—450, 1976.
17. Wijblirg FA, Heymans HSA, Urban us NAM: Caustic esophageal
lesions in childhood: Prevention of stricture formation. J Pediatr
Surg 24:171 — 173, 1989.
18. Mills LJ, F sir era AS, Platt MR: Avoidance of esophageal
stricture following severe caustic burns by the use of an intralu-
minal stent. Ann Thorac Surg 28:60 65, 1979.
19. Madden JW, Davis WM, Butler C, et al.: Experimental esopha-
geal lye bums. Correcting established strictures with betaami-
nopropionitrile and bougienage. Ann Surg 178:277—284, 1973.
20. Davis WM. Madden JW, Peacock EE: A new approach to
lhe control of esophageal stenosis. Ann Surg 176:469—476.
1972.
21. Joseph PR: The pediatric forum. Management of coin ingestion.
Am J Dis Child 144:449. 199(1
22. Smith PC. Swischuk LE, Fagan CJ: An elusive and often unsits
pected cause of stridor or pneumonia (the esophageal foreign
body). Am J Kad I'her Nucl Med 122:80—89, 1974.
23. Foster DI.: The pediatric forum. Pediatric coin ingestion.
Am J Dis Child 144:450—451. 1990
24. Schunk JE, Cumuli H. Bolte R: Pediatric coin ingestions.
Am J Dis Child 143:546 548, 1989
25. Caravati EM. Bennett DL. McElwee NF: Pediatric coin ingesti-
on. A prospective study on the utility of routine roentgeno-
grams. Am J Dis Child 143:549—551. 1989.
26. Fernandes E Г, Holfabaugh RS. Boulden T: Mediastinal mass
and radiolucent esophageal foreign body. J Pediatr Surg
24:1135—1136, 1989.
27. Beal SM: Sudden infant death associated with an oesophageal
problem. Med J Aust 2:91, 1979.
28. Woods I Swan PK: Tracheal occlusion following oesophageal
foreign body removal. Anacsth Intensive Care 17:346 348,
1989.
29. Bonadio WA. Jona JZ, Glicklich M, el al.; Esophageal bougie-
nage technique for coin ingestion in children. J Pediatr Surg
23:917—918, 1988.
30. Bigler FC: The use of a foley catheter for removal of blunt
foreign bodies from lhe esophagus. J Thorac Cardiovasc Surg
51:759 760. 1966.
31. Campbell JB, Foley CL: A safe alternative to endoscopic remo-
val of blunt esophageal foreign bodies. Arch Otolaryngol
109:323- 325, 1983.
32. Campbell JB. Condon VR: Catheter removal of blunt esophage-
al foreign bodies in children. Pediatr Radiol 19:361—365, 1989.
33. Burrington JD: Aluminum "pop tops" a hazard to child health.
JAMA 235:2614—1617. 1976.
34. Spitz J. Hirsig J: Prolonged foreign body impaction in lhe
oesophagus. Arch Dis Child 57:551—553, 1982.
35. Takano H, Okada A, Munden Y, et al.: Unusual case of acqui-
red benign tracheoesophageal fistula caused by an esophageal
foreign body. J Thorac Cardiovasc Surg 99:755—756. 1990.
36. I itovitz TL: Button battery ingestions. A review of 56 cases.
JAMA 249:2495—2500. 1983
37. Voiteler TP, Nash JC, Rutledge JC: The hazard of ingested
alkaline disk batteries in children. JAMA 249:2504—2506,
1983.
38. Sigalct D. Lees G: 1 racheoesophagcal injury secondary to
disc battery ingestion. J Pediatr Surg 23:996 998, 1988.
39. Moves MD. Carithers JS. Birck HG: Esophageal burns secon-
dary to disc battery ingestion. Ann Olol Rhino) L.tryngol
93:364 369, 1984.
40. Shabino DL, Feinberg AN: Esophageal perforation secondary to
alkaline battery ingestion. J Am Coll Enter Phys 8:360—362,
1979.
41. Vaishnav A. Spitz I : Alkaline ballcry-induced Iracheo-oeso-
phageal fistula. Br J Surg 76:1045, 1989.
42. Blatnik DS, Toohill RJ. 1 ehman RII: Fatal complication from an
alkaline battery foreign body in the esophagus- Ann Olol
. «6:611—615, 1977.
43- Rumack BH. Rumack CM: Disk battery ingestion. JAM
249:2509—2511. 1983.
44. Voile E, Beyer P. Kaufmann JH. Therapeutic approach to inges-
ted button-type batteries. Magnetic removal of ingested button-
type batteries. Pediatr Radiol 19:114 118, 1989.
45. Willis GA, Ho WC: Perforation of Meckel’s diverticulum by
an alkaline hearing battery. Can Med Assoc J 126:497 498.
1982.
46. Wells SD. Leonidas JC. Conklc D. cl al-: Traunutitc preverteb-
ral pharyngoesophageal pseudodiveniculum in the newborn
infant. J Pediatr Surg 9:217- 222, 1974.
47. Cohen RC, Myers NA: Traumatic oesophageal pseudodi vert i-
cufum. J Pediatr Ausi 23:125—127, 1987.
48. Nagaraj HS, Mullen P Groff DB: Iatrogenic perforation of the
esophagus in premature infants. Surgery 86:583—589. 1979.
49. Grosfeld: Discussion. In Nugaraj JS. Mullen P, Groff DB. el
al.: Iatrogenic perforation of the esophagus in premature infants.
Surgery 86:588 599, 1979.
50. Tolslcdt GE. Tudor RB: Esophagopleural fistula in a newborn
infant. Arch Surg 97 780 781 1968.
51. Adams H. Roberts GM, Smith PM: Oesophageal tears during
pneumatic balloon dilatation for the- treatment of achalasia.
Clin Radiol 40:53—57, 1989.
276 ПИЩЕВОД
52. Bolooki Н: A discussion. In Attar S, Hankins JR. Suter CM,
ct al.: Esophageal perforation: A therapeutic challenge. Ann
Thorac Surg 50:50, 1990.
53. DcMccster TR: Perforation of the esophagus. Ann Thorac
Surg 42:231—232, 1986.
54. Bladergroen MR, I owe JH, Postlelhwait RW: Diagnosis and
recommended management of esophageal perforation and ruptu-
re. Ann Thorac Surg 42:235—239, 1986.
55. Aja tat GM, Mulder DG: Esophageal perforations. Arch Surg
119:1318—1320, 1984.
56. Cohn HE, Hubbard A, Patton G: Management of esophageal
injuries. Ann Thorac Surg 48:309—314, 1989.
57. Michel L, Grillo HC, Malt RA: Esophageal perforation. Ann
Thorac Surg 33:203 210, 1982.
58. Hendren WH. Henderson BM: Immediate esophagectomy for
instrumental perforation of the thoracic esophagus. Ann Surg
168:997—1002. 1968.
59. Conlan AA. Wessels A. Hammond CA, cl al.: Pharyngoesopha-
geal barotrauma in children: A report of six cases. J Thorac
Cardiovasc Surg 88:452—456, 1984.
60. Domini R. Appignani A Ceccarelli PL, ct al.: Congenital esop-
hageal stenosis due to ectopic cartilaginous tissue: a case report.
Ital J Pediatr Surg Sei 2:87—89, 1988.
61. Scherer LR, Grosfeld JL: Congenital esophageal stenosis, esop-
hageal duplication, neurcnleric cyst and esophageal diverticu-
lum. In Ashcraft KW, Holder TM (editors): Pediatric Fsoph
ageal Surgery. Grunc & Stratton. Orlando, pp53—71, 1986.
62. Henderson RD, Davidson JW: Primary disordered motor ac-
tivity of the esophagus (diffuse spasm). Ann Thorac Surg
18:327 336. 1974.
63. Moersch HJ. Camp J I): Diffuse spasm of the lower part of
the esophagus. Ann Otorhinolaryngology 43:1165 1173, 1934.
64. Henderson RD, Henderson RF, Marryatl GV: Surgical manage-
ment of 100 consecutive esophageal strictures. J Thorac Cardio-
vasc Surg 99:1 7, 1990.
65. Toyohara T. Копека Г, Araki H. et al.: Giant epiphrenic di-
verticulum in a boy with Ehlers-Dan I os syndrome. Pediatr
Radiol 19:437, 1989.
66. Nihoul-Fekele C, Bawab F, Lorial-Jacob S, et al.: Achalasia of
the esophagus in childhood: Surgical treatment in 35 cases with
special reference to familial cases and glucocorticoid deficiency
association. J Pediatr Surg 24:1060—1063, 1989.
67. Tryhus MR, Davis M, Griffith JK, et al.: Familial achalasia
in two siblings: Significance of possible hereditary role. J Pedt-
alr Surg 24:292—295. 1989.
68. Rosenzweig S, Traube M: The diagnosis and misdiagnosis
of achalasia. J Clin Gastroenterol 11:147—153, 1989.
69. Shoenut P, Trenholm BG, Micflikier AB, et al.: Reflux patterns
in patients with achalasia without operation. Ann Thorac
Surg 45:303—305, 1988.
70. Smith II, Buick R. Booth 1, ct al.: I eiters to the editor. J Pe-
diatr Gastroenterol 7:146. 1988.
71. Vane DW, Cosby К» West K. ct al.: Late results following
esophagomyolomy in children with achalasia. J Pediatr Surg
23:515-519» 1988.
72. Sauer L, Pellegrini CA, Way LW: The treatment of achalasia.
Arch Surg 124:929—932, 1989.
73. Richardson JD: Discussion. In Sauer L, Pellegrini CA, Way
LW: The treatment of achalasia. Arch Surg 124:932, 1989.
74. Little AG, Soriano A, Ferguson MK. et al.: Surgical Ireatniciit of
achalasia: Results with esophagomyolomy and Belsey repair.
Ann Thorac Surg 45:489—494. 1988.
75. Ellis FH: Treatment of achalasia: A continuing controversy.
Ann Thorac Surg 45:473, 1988.
76. Jekler J, Lhotka J: Modified Heller procedure to prevent posto-
perative reflux esophagitis in patients with achalasia. Am J Surg
113:251—254, 1967.
77. Skinner DB: Myotomy and achalasia. Ann Thorac Surg 37:
183—184, 1984.
78. Murray GF, Batlaglini JW, Keagy BA0 et al.: Selective applicati-
on of fundoplicalion in achalasia. Ann Thorac Surg 37:185—
188, 1984.
79. Pai GP. Ellison RG, Rubin JW. et al.: Two decades of experi-
ence with modified Heller’s myotomy for achalasia. Ann Tho-
rac Surg 38:201—206, 1984
80. Fonkalsrud E: Discussion. In Vane DW, Cosby K, West K.
cl al.: Late results following esophagomyolomy in children
with achalasia. J Pediatr Surg 23:519. 1988.
81. Bolstad DS: The management of strictures of the esophagus.
Ann Otolaryngol 75:1019—1028, 1966.
82. Ashcraft KW, Holder TH: The experimental treatment of esop-
hageal strictures by intralesional steroid injections. J Thorac
Cardiovasc Surg 58:685—691, 1969.
83. Gandhi RP, Cooper A, Barlow BA: Successful management of
esophageal strictures without resection or replacement. J Pedi-
atr Surg 24:745 750, 1989.
84. Holder TH, Ashcraft KW, Lcape L: The treatment of patients
with esophageal strictures by local steroid injections. J Pediatr
Surg 4:646—653, 1969.
85- Fonkalsrud EW: Initial esophageal dilatation in infants with
benign esophageal stricture. Surgery 59:883—885, 1966.
86. Tytgat Guido NJ: Dilation therapy of benign esophageal
stenoses. World J Surg 13:142 — 148, 1989.
87. Shemesh E, Czcrniak A: Comparison between Savary-Gilliard
and balloon dilatation of benign esophageal strictures. World
J Surg 14:518—522, 1990.
88. Hoffer FA, Winter IIS, Fellows KE, ct al.: The treatment of
post-operative and peptic esophageal strictures after esophage-
al atresia repair. Pediatr Radiol 17:454 -458, 1987.
89. Golladay ES, Tepas 111 JJ, Pickard LR, et al.: Bacteremia after
esophageal dilation: A clinical and experimental study. Ann
I'horac Surg 30:19 23, 1980.
90- Musher DR. Boyd A: Esophagocolonic stricture with proximal
fistulae treated by balloon dilation. Am J Gastroenterol
83:445—447, 1988.
91. Little AG, Naunheim KS. Ferguson MK, et al.: Surgical ma-
nagement of esophageal strictures. Ann Thorac Surg 45:144
147, 1988.
92. Paulson DL: Benign stricture of the esophagus secondary to
gastroesophageal reflux. Ann Surg 165:765—-778, 1967.
93. Ohhama U, Tsunoda A, Nishi T, et al.: Surgical treatment
of reflux structure of the esophagus. J Pediatr Surg 25:758
761, 1990.
94. Henderson RD, Henderson RF, Marryatl GV: Surgical manage-
ment of 100 consecutive esophageal strictures. J Thorac Cardio-
vasc Surg 99:1—7, 1990.
95. I.xolaiiri J, Nordback I. Markkula II: Surgery for reflux strictu-
re of the oesophagus. Ann Chir Gynaecol 78:120—123, 1989.
96. Fonkalsrud EW, Ament ME: Surgical management of esophage-
al stricture due to recessive dystrophic epidermolysis bullosa.
J Pediatr Surg 12:221—226, 1977.
97. Imre J, Kopp M: Arguments against long-term concervativc tre-
atment of oesophageal strictures due to corrosive burns. Tho-
rax 27:594- 598, 1972.
98. Kiviranla UK: Corrosion carcinoma of tne esophagus: 381 ca-
ses of corrosion and nine cases of corrosion carcinoma. Acta
Otolaryngol (Stockh) 42:89—95. 1952.
99. Alvarez AF, Colbert JG: Lyc stricture of the esophagus compli-
cated by carcinoma. Can J Surg 6:470—476, 1963.
100. Bigger I A, Vinson PP: Carcinoma secondary to burn of the
esophagus from ingestion of lye. Surgery 28:887—889, 1950.
101. Bigelow Nil: Carcinoma of the esophagus developing at the
site of lye stricture. Cancer 6:1159—1164, 1953.
102. Appelqvist P, Salnio M: Lye corrosion carcinoma of the esop-
hagus. Cancer 43:2655—2658, 1980.
103. Mansour KA, Hansen HA. Hersh T, el al.: Colon interposition
for advanced nonmalignant esophageal stricture: Experience
with 40 patients. Ann Thoras Surg 32:584—592, 1981.
104. Gross RE, Firestone FN: Colonic reconstruction of the esopha-
gus in infants and children. Surgery 61:955- 964. 1967
ПИЩЕВОД 277
105. Belscy R. Clagell ОТ: Reconstruction of the esophagus with
left colon. J Thorac Cardiovasc Surg 49:33—54. 1965.
106. Kelly JP. Shackelford GD, Roper Cl.: Esophageal replacement
with colon in children: Functional results and long-term
growth. Ann Thorac Surg 36:634—644. 1983.
107. Waterston DJ: Replacement of oesophagus with colon in child-
hood. In Rob C, Smith R (Editors). Operative Surgery, volume
2, second edition. Butterworths. London, pp367—374, 1968.
108. German JC, Waterston DJ: Colon interposition for the replace-
ment of the esophagus in children. J Pediatr Surg 11:227—234,
1976.
109. Azar H, Chrtspin AR. Waterskin DJ: Esophageal replacement
with transverse colon infants and children. J Pediatr Surg
6:3 9. 1971.
110. Mitchell IM. Goh DW. Roberts KD, el a!.: Colon interposition
in children. Br J Surg 76:681—686. 1989.
III. Lindahl H. Louhimo 1, Virkola K. Colon interposition or gast-
ric lube? Follow-up study of colon-esophagus and gastric tube-
esophagus patients. J Pediatr Surg 18:58- 63. 1983.
112. Huang MH. Sung CY, Hsu HK. cl al.: Reconstruction of (he
esophagus with the left colon. Ann Thorac Surg 48:660 -664,
1989.
113. Stone MM. Ma hour GH, Weitzman JJ, et al.: Esophageal repla-
cement with colon interposition in children. Ann Surg
203:346- 351, 1986.
114. West KW. Vane DW. Grosfeld JL: Esophageal replacement in
children: Experience with thirty-one cases. Surgery 100:751 —
757. 1986.
115. Najafi H. Beattie E: Excision of teniae coli for repair of esop-
hagocolic stricture following colon transplant: case report. Ann
Surg 162:1097—1099, 1965.
116. Lynn H: Simple method of elongating a colonic segment for
esophageal replacement. J Pediatr Surg 8:391—393, 1973.
117. Belscy R: Discussion. In Kelly JP, Shackelford GD. Roper CL:
Esophageal replacement with colon in children: Functional re-
sults and long-term growth- Ann Thorac Surg 36:641 -642.
1983.
118. Sieber AM, Sieber WK: Colon transplants «is esophageal repla-
cement: Cincradiographic and manometric evaluation in child-
ren. Ann Surg 168:116—122, 1968.
119. Guzzctta PC, Randolph JG: Antireflux cologastric anastomosis
following colonic interposition for esophageal replacement.
J Pediatr Surg 21:1137—1138, 1986.
120, Larsson S, Lycke G, Rad berg G: Replacement of rhe esopha-
gus by a segment of colon provided with an antireflux valve.
Ann Thorac Surg 48:677—682, 1989.
121. Butterfield WC. Massi J: Gastric reflux in colon interpositions.
A method of treatment. J Thorac Cardiovasc Surg 64:229—
234, 1972.
122. Jones EL, Skinner DB, Demccstcr TR, et al.: Response of
the interposed human colonic segment to an acid challenge.
Ann Surg 177:75—78, 1973.
123. Moreno-Osset E. Tumas-Ridocci M, Paris F, ct «if.: Motor acti-
vity of esophageal substitute (stomach, jejunal, and colon seg-
ments). Ann Thorac Surg 41:515—519, 1986.
124. Isolauri J: Colonic interposition for benign esophageal disease.
Long-term clinical and endoscopic results. Am J Surg
155:498 502. 1988.
125. Neville WE. Najem AZ: Colon replacement of the esophagus
for congenital and benign disease. Ann Thorac Surg 36:626—
633. 1983.
126. Sutton R. Sutton DM. Ackcry DM, et al.: Functional assess-
ment of colonic interposition with Tc“ labeled milk. J Pediatr
Surg 24:874—881, 1989.
127 Sterling RP, Kuykendall C, Carmichael MJ, et al.: Unusual
sequelae of colon interposition for esophageal reconstruction:
Late obstruction requiring reopera lion. Ann Thorac Surg
38:292 295. 1984.
128. Pantelides ML. Fitzgerald MD: I -eft ventriculo-colic fistula —a
late complication of colonic interposition for the oesophagus.
Postgrad Med J 64:710 712. 1988.
129. Choh JH, Balderman SC, Bingham D. ei al.: Parasternal int-
rapleural colon interposition: An alternative pathway for the
colon graft. Ann Thorac Surg 31:474—477, 1981.
130. Bentley John FR: Primary colonic substitution for atresia
of the esophagus. Surgery 58:731—736. 1965.
131. Anderson KD. Randolph JG: The gastric lube for esophageal
replacement in children. J Thorac Cardiovasc Surg 66:333—
342. 1973.
132. Cohen DH. Middleton AW, Fletcher J: Gastric tube esopha-
goplasty. J Pediatr Surg 9:451 • 460, 1974.
133. Spitz L. Kiely E, Spanion T: Gastric transposition for esopha-
geal replacement in children. Ann Surg 206:69 73. 1987.
134 Saeki M, Tsuehi da Y„ Ogata T, et al.: Long-term results of
jejunal replacement of the esophagus. J Pediatr Surg 23:483—
489. 1988.
135. Coleman JJ, Tan КС. Searles JM, el al.: Jejunal free autograft:
Analysis of complications and their resolution. Plast Rccunslr
Surg’84:589—595, 1989.
136- Murdison KA, Andrews BA, Chin AJ: Ultrasonographic display
of complex vascular rings. J Am Coll Cardiol 15:1645
1653, 1990.
137. Chcrin MM, Pond GD, Bjclland JC. et al.: Evaluation of double
aortic arch and aortic coarctation by intravenous digital subt-
raction angiography. J Cardiovasc Surg 28:58!—584, 1987.
138. Kastlcr B, Livolsi A. Germain P, el al.: Magnetic resonance
imaging in congenital heart disease of newborns: preliminary
results in 23 patients. Eur J Radiol 10:109 117. 1990.
139. Backer CL, Ilbawi MN, Idriss FS, et al.: Vascular anomalies
causing tracheoesophageal compression. Review of experience
in children. J Thorac Cardiovasc Surg 97:725—731, 1989.
Глава 22
АТРЕЗИЯ ПИЩЕВОДА
И ТРАХЕОПИЩЕВОДНЫЕ
АНОМАЛИИ
Атрезия пищеиоди (АП), обычно сочетающаяся
с трахеопищеводным свищом (ТПС), неизбежно
приводит к смерти, если диагноз нс поставлен, ли-
бо ребенок по каким-то причинам не оперирован.
Наиболее частый вариант аномалии (АП со сви-
щом между дистальным сегментом пищевода и
трахеей) был впервые описан в 1696 г. Thomas
Gibson,1 который представил подробнейшее скру-
пулезное изложение клинической и патологоана-
томической картины порока. К сожалению, после
этого первого описания последовали 243 го да неу-
дачных попыток лечения АП и только в 1939 г.
Ladd 4 и l.even 3 независимо друг от друга получи-
ли по одному благоприятному результату этапной
коррекции аномалии, а в 1941 г. Haight и Tows-
ley6 впервые успешно прооперировали ребенка
с АН радикально. Операция заключалась в разде-
лении и ушивании свища и первичном анастомозе
пищевода. Данное вмешательство и в настоящее
время является методом выбора. Хотя в лечении
больных с атрезией пищевода постоянно отмеча-
ются немалые достижения, однако для всех, кто
имеет дело с этим сложным пороком, до сих пор
остается много нерешенных проблем, в том числе
и чисто технических.
Нс меньшие во всех отношениях сложности для
клинициста представляет ларинготрахеоэзофагс-
альная расщелина, встречающаяся, к счастью, па
много реже, чем обычные трахеопищеводные ано-
малии.
АТРЕЗИЯ ПИЩЕВОДА
И ТРАХЕОПИЩЕВОДНЫЙ СВИЩ
)мбриология. Около 19-го дня гестации передняя
кишка человеческого эмбриона представлена одно-
слойной трубкой, расположенной между глоткой
и желудком. Через несколько дней вентральная
часть этой кишки начинает утолщаться и образует
желоб, выстланный многослойным мерцательным
цилиндрическим эпителием, который становится
в последующем слизистой оболочкой дыхательных
путей. Отделение дорсальной части передней киш-
ки (пищевод) от вентральной (трахея) происходит
сначала в области карины и затем распространя-
ется в головном направлении. Около 26-го дня ге-
стации эти две структуры становятся полностью
разделенными до уровня гортани.’ Нарушение
дальнейшего разъединения приводит к формирова
нию ларинготрахеоэзофатеальной расщелины
Бронхи развиваются из заднебоковых зачатков
трахеи и растут каждый в свою сторону.
Прерывание по тем или иным причинам процес-
са разделения пищевода и трахеи ведет к образо-
ванию ТПС.
Значительно более трудно объяснить механизм
возникновения АП. Smith установил, что «лате-
ральные пищеводные борозды» (естественно обра
дующиеся области сужения, очень похожие на
гребни эпителиальной пролиферации, формирую-
щей перегородку между трахеей и пищеводом) мо-
гут развиваться дорсально (рис. 22-1), что и при-
водит к образованию АП.8 Grunewald и некоторые
другие авторы считают, что причиной возникнове-
ния АП является первоначально (до АП) сформи-
ровавшийся ТПС. По мнению этих исследовате-
лей, трахея так быстро растет в каудальном на
правлении, что если пищевод фиксирован свищом
к трахее, го дорсальная его стенка вы гягипается
вперед и вниз, чтобы «поспеть» за трахеей
и остаться соединенной с ней, что и приводит к об-
разованию АП. Теория наружного давления на пи-
щевод аберрантных сосудов или каких-либо иных
образований практически опровергнута. Механизм
возникновения АП, установленный Smith, считает-
ся в настоящее время наиболее вероятным и при-
нимается большинством исследователей.
АП с ТПС может быть компонентом комбинации
пороков, обозначаемой аббревиатурой VACTERL,
включающей в себя аномалии позвонков, ануса,
сердца, трахеи и пищевода, почек и конечностей.
Высокая частота и разнообразие сочетанных ано-
малий пищевода и трахеи подтверждает предполо-
жение о сложных нарушениях органогенеза, лежа-
щих в основе этих пороков (табл. 22-1).
Точная природа нарушений эмбриогенеза, кото-
278
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 279
Рис. 22-1. По мере отделения дорсального пищевода от вент-
ральной трахеи образуются латеразьныс эзофагсаявные борол
ды. Если разделение продолжается дистально, возникает атре-
зия пищевода.
рые приводят к АП и ТПС, возможно, останется
неизвестной еще какое-то время. Однако довольно
частое выявление в дыхательных путях пациентов,
умерших от АП и ТПС, чешуйчатых клеток слизи-
стой оболочки подтверждает концепцию о том, что
ткани, изначально предназначенные для передней
кишки, «незаконно присваиваются» трахеей.11 В то
ТАБЛИЦА 22-1. Относительная частота (в процентах)
различных вариантов АП и ТПС
Сводная статистика 1058 больных 1964 г." Данные автора 1 |Я больных
АП, дистальный ТПС «6.5 100» (85)
АП без ТПС 7,7 3 (2,5)
ТИС без АП 4.4 7 (6)
АП, проксимальный и дисталь- ный ТПС 0,7 6** (5)
АП, проксимальный ТПС 0.8 2** (1,5)
* Шесть из этих больных имели большой диастаз.
** В большинстве случаев, благодаря совершенствованию
диагностики и современным методам исследования, проксималь-
ный ТПС был диагностирован до операции.
же время чешуйчатая метаплазия может также
быть результатом хронического рефлюкса и по-
падания в трахею желудочного содержимого. В
норме же пищевод и трахея выстланы цилиндриче-
ским мерцательным эпителием примерно до 5-го
месяца внутриутробной жизни, затем они должны
в течение нескольких месяцев полностью отделить-
ся друг от друга-7
Этиология. Этиология трахеопищеводных ано-
малий не известна. И хотя нет очевидных доказа-
тельств наследственной природы, однако сущест-
вует ряд сообщений о семейных случаях АП
и ТПС. Так. например, описаны несколько наблю-
дений АП и ТПС' у однояйцевых близнецов,12’ 17
а также у матери и ребенка. ** у отца и ребенка.19
Болес того, опнеан случай, когда в одной семье
было 5 членов мужского пола с данной анома-
лией,20 Имеющиеся немногочисленные сообщения
о семейных случаях позволяют говорить о том, что
самый редкий из этих вариантов — наличие поро-
ка у сиблИНГОВ.
Анатомия и классификация. АП и ТПС могут
встречаться как самостоятельные изолированные
аномалии, но наиболее часто отмечается их комби-
нация. Существуют многочисленные, постоянно
развивающиеся и расширяющиеся классификации
этих пороков. Тип аномалии имеет большое кли-
ническое значение.
АН с дистальным ТПС (86%) —наиболее ча-
стая форма порока (рис. 22-2). Верхний сегмент
пищевода при этом варианте аномалии заканчива-
ется слепо, обычно на уровне Thtu, хотя может
быть значительно более высоким (CVN) или, нао-
борот. низким (Thv). Мышечная стенка его утол
(цена, и диаметр намного больше диаметра нижнего
сегмента, который начинается от трахеи, обычно
от мембранозной части ее нижнего отдела. Иногда
свищ отходит от места деления трахеи на левый
и правый бронхи, в этом случае трахея имеет как
бы «трифуркацию». Соединение фистулы с брон-
хом наблюдается редко.
Между сегментами пищевода обычно имеется
диастаз, величина которого определяет выбор ме-
тода лечения. Мобилизация верхнего сегмента, да-
же обширная, может быть произведена без опасно-
сти нарушения кровоснабжения, осуществляемого
из щито-шейного ствола. Нижний сегмент, наобо-
рот, имеет обедненное кровоснабжение, которое
легко нарушить даже при минимальной мобили-
зации.
Сегменты пищевода иногда могут «заходить»
один за другой и даже иметь общую мышечную
стенку. При таком благоприятном варианте порока
натяжение по линии швов анастомоза обычно ми-
нимальное, однако бывают трудности в определе-
нии точной локализации сегментов и свища.
Изолированная АП (без ТПС — 5%) почти все-
гда сопровождается большим диастазом между сег-
ментами (рис. 22-3). Дл н на верхнего сегмента
обычно не зависит от вида аномалии, в то время
как величина дистального сегмента непосредствен-
но связана с вариантом порока. При отсутствии
нижнего ТПС дистальный сегмент очень короткий.
280 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
Рис. 22-2. Атрезия лищекода с дистальным трахеопищеводным
СВИЩОМ.
вило, отсутствует, поэтому нижний сегмент корт
кий, а диастаз соответственно большой.
При ЛИ с проксимальным и дистальным (дву-
мя) ТПС (3%) верхний сегмент с фистулой, так
же, как и нижний, нс отличаются анатомически от
каждой из этих форм, описанных выше, когда они
встречаются в отдельности (рис. 22-6). Обычно
диастаз при данном варианте порока небольшой.
Существуют многообразные комбинации привс
денных основных пяти видов АП и ТПС, что объ-
ясняет наличие множества классификаций данной
аномалии.2
При любой форме атрезии пищевода количество
нервной ткани в ауэрбаховском сплетении значи-
тельно уменьшено, по сравнению с нормой, как
в верхнем, гак и в нижнем сегменте. Однако в ди-
стальном отделе этот дефицит более выражен. По-
скольку исследование ауэрбаховского сплетения
проводилось у кооперированных детей с АП, полу-
ченные данные позволяют говорить о, несомненно,
врожденном характере выявленных изменений.23
порой лишь на 1—2 см выступает над диафраг-
мой. Поскольку при этом виде аномалии амниоти-
ческая жидкость внутриутробно не попадает в же-
лудок, он может быть очень маленьким.
Изолированный ТПС (без АП—3%), диаметр
которого, как правило, 2 4 мм, обычно имеет ко-
сое направление от передней стенки пищевода
кверху по диагонали к мембранозной части трахеи
(рис. 22-4). ТПС может быть на любом уровне, от
перстневидного хряща до карины, но чаше отходит
от нижнешейной или верхнегрудной части трахеи.
В литературе имеются описания случаев, когда
у больного было одновременно два или даже три
свища 21 77 ТПС без ЛП обычно носит название
ТПС Н-типа или более правильно-N-типа, прохо-
димость пищевода при этом не нарушена.
При ЛП с проксимальным ТПС (1%) фистула
обычно начинается на 1—4 см выше дна верхнего
сегмента и направляется по диагонали кверху, впа-
дая в мембранозную часть трахеи (рис. 22-5). Ди-
стальный ТПС при этом варианте порока, как пра-
Рис. 22-3. Изолированная атрезия пищевода (бея трахеопище-
водного свища).
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 281
Патофизиология. При атрезии пищевода слюна
и пища (если при медиа тестированном пороке ре-
бенка начали кормить) не прохотят в желудок
и аспирируются. При наличии проксимального
ТПС содержимое верхнего сегмента попадает
в трахею еще и через свищ. В результате возника-
ют нарушения дыхания, ателектазы, пневмония.
Через дистальный ТПС воздух и жидкость могут
проходить в обоих направлениях. Если ребенок
кричит, кашляет, напрягается, то повышается йи-
тратрахеальное давление и воздух выталкивается
через фистулу в пишевод. Желудок и тонкая киш-
ка, наполняясь при этом воздухом, рас1ягиваются,
результатом чего является высокое стояние диа-
фрагмы. Рефлюкс воздуха и кислого желудочного
содержимого из растянутого желудка через фисту-
лу в трахею ведет к трахеобронхиту, предраспола-
гая к развитию ателектазов и бактериальной пнев-
монии. При изолированном ТПС эти осложнения
менее выражены, поскольку воздух имеет возмож-
ность эвакуироваться через проксимальную часть
пищевода наверх.
Рис. 22-4. Изолированный трнхеопищеиодный свищ (Н-тип или
N-тип) без атрезии пищевода.
Рис. 22-5. Атрезия пищевода с проксимальным трахсопишевод
ным свищом.
Перистальтика пищевода при АП и/или ТПС
изменена. У детей с изолированным ТПС предопе-
рационная эзофагография показывает нарушение
перистальтики.24 По данным манометрии, функция
верхнего пищеводного сфинктера нормальная, в то
время как перистальтические сокращения очень
слабые или вовсе отсутствуют.25 Дооперационная
манометрия у детей с АП (верхний сегмент через
ротовую полость, нижний — через гастростому)
выявляет некоординированные движения в обоих
сегментах.26 Подобные изменения сохраняются и
после операции.
При АП и ТПС уже внутриутробно нарушается
развитие трахеи и легких, чему способствуют два
обстоятельства. Во-первых, верхний сегмент атре-
зированкого пищевода растягивается заглоченной
амниотической жидкостью и давит на развиваю-
щуюся трахею, результатом чего является наруше-
ние развития хрящевых колец (трахеомаляция).
Во-вторых, амниотическая жидкость из легких по-
ступает через дистальный свищ в кишечник, ио
282 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
Рис. 22-6. Ат резня пищевода е проксимальным и дистальным
трахеопищеводными свищами.
под меныпим, чем в норме, давлением, а поэтому
естественное растяжение дыхательных путей из-
нутри уменьшается. Большее значение в этиоло-
гии трахеомаляции имеет сдавление снаружи. Од-
нако более низкое, чем в норме, внутриутробное
интрабронхиалыюе давление также немаловажно,
поскольку может быть причиной нарушения ветв-
ления бронхов и альвеол.” Именно этот механизм
может объяснить наличие у некоторых больных
с изолированным ТПС глухого лающего кашля
и трахеомаляции, хотя сдавление дыхательных пу-
тей снаружи в этих случаях (при ТПС без АП)
отсутствует.
Клиническая картина. «Кажется, что ребенок
очень хочет есть и с жадностью хватает ртом все,
что дают ему с ложки, но когда собирается прогло-
тить, то пища как будто наталкивается на препят-
ствие и не проходит внутрь, а возвращается через
рот и нос, при этом ребенок впадает в состояние,
подобное судорожному припадку».1 Это первое
описание Gibson (1696) поведения ребенка с атре-
зией пищевода представляет ценность до настоя-
щего времени.
Первый симптом АП обильное выделение
слюны, которую ребенок не может проглотить. Ес-
ли новорожденного начинают кормить, то он да-
вится, кашляет, часто при этом появляется цианоз
и регургитация. В динамике нарастают дыхатель-
ные расстройства, наиболее выраженные при нали-
чии дистального ТПС.
Изолированный ТПС проявляется более сгла-
женными симптомами. Поскольку пищевод при
этом варианте аномалии проходим, ребенок мо-
жет глотать. Однако лишь в редких случаях дети
с изолированным ТПС могут длительно жить от-
носительно благополучно, с минимальными симп-
томами. Обычно же во время кормления у ребенка
развивается кашель и удушье. В более старшем
возрасте эти симптомы чаще появляются во время
приема жидкой, а не густой пищи, поскольку
жидкости легче пройти через свищ. Нередко раз-
вивается рецидивирующая пневмония, отмечается
вздутие живота. В некоторых случаях увеличение
живота столь выражено, что может даже вызвать
подозрение на болезнь Гиршпрунга.30
АП и ТПС встречаются с частотой 1:3000 но-
ворожденных, являясь одним из самых распростра-
ненных пороков. Эта аномалия корригируема,
но без лечения неизбежно приводит к смерти.31 АП
почти одинаково часто встречается как у мальчи-
ков, так и у девочек. Новорожденные с АП нередко
рождаются недоношенными, 34% детей с этим по-
роком весят при рождении менее 2,5 кг.32 Прежде-
временным родам отчасти способствует многово-
дие, характерное для АП. особенно при отсутствии
дистального ТПС.33
Диагноз АП может быть поставлен антенаталь-
но, если на УЗИ выявляется многоводие и при
этом не виден желудок плода. Иногда определя-
ется расширенный проксимальный отдел пищево-
да, что гем более подтверждает АП. Наличие ком-
понентов VACTERl.-ассоциации должно быть по-
казанием к особенно тщательному поиску АП.’4
У новорожденных с такими относительно легко
диагностируемыми видами патологии, как недоно-
шенность, атрезия ануса, ирожденные пороки серд-
ца, аномалии верхних конечностей и позвоноч-
ника, многоводие у матери, также необходимо по-
дозревать и активно искать атрезию пищевода,
которая часто сочетается с перечисленными анома-
лиями.
Диагностика. Наиболее простым и быстрым,
хотя и не самым точным, методом диагностики ат-
резии пищевода является его зондирование. При
наличии АП обнаруживается препятствие па рас
стоянии 9—13 см. Если катетер проходит ниже
этого уровня, атрезия маловероятна, хотя тонкий
мягкий зонд может свернуться в расширенном вер-
хнем сегменте, поэтому в любом случае необхо-
димо рентгенологически подтвердить положение
зонда.
Рентгенологическое исследование необходимо
также, чтобы определить наличие или отсутствие
газа в ЖКТ. Воздух в желудке у ребенка с АП
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 283
Рис. 22-7. На рентгенограмме виден расширенный проксималь-
ный сегмент пищевода (указан стрелками). Катетер, заведен-
ный до его дна, подтверждает атрезию пищевода на уровне тре-
тьего грудного позвонка. Газ в желудке говорит о диета аьном
ТПС. В тонкой кишке также большое количество газа.
говорит о наличии дистального ТПС (рис. 22-7),
отсутствие при этом газа в тонкой кишке может
быть признаком сочетанной дуоденальной атрезии,
которая не является редкостью у новорожден пых
С АП (рис. 22-8). «Немой» живот характерен для
атрезии без свища (рис. 22-9), хотя в редких слу-
чаях подобная картина бывает у детей с узким
нижним ТПС или у очень ослабленных новорож-
денных.
На рентгенограммах необходимо обратить вни-
мание и на состояние легких, наличие пневмонии,
ателектазов (рис. 22-10). признаков идиопатиче
ского респираторного дистресс-синдрома (см. рис.
22-9). Увеличение размеров сердца или необычная
его конфигурация могут быть симптомами врож-
денного порока (рис. 22-11). Нередко выявляются
также аномалии позвоночника.
Исследование с барием, даваемым ребенку через
рот, не рекомендуется из-за риска бариевой аспи-
рации, однако осторожное введение через зонд под
контролем экрана 0.5 мл жидкой бариевой взвеси
позволяет, избежав этого осложнения, точно лока-
лизовать по рентгенограммам уровень атрезии,
а также выявить проксимальный ПК’ (рнс. 22-
12). Попадание контрастного вещества в грахею
может быть признаком проксимального ГПС, ла-
ри и готра хеоэзофагеальной расщелины, а также
просто аспирации. Анатомический вариант порока
можно уточнигь бронхоскопически непосредствен-
но на операционном столе перед операцией. Неко-
торые хирурги считают, н не без основания, что
бронхоскопия показана всем новорожденным с АП
для выявления проксимального ТПС. расщелины
или трахсомаляции. В определении диастаза
между сегментами может помочь сагиттальная
компьютерная томография (КТ).37
Изолированный ТПС иногда можно выявить при
обычном обследовании с барием во время глотания
или еще лучше на видеоэзофагограммах с введени-
ем бария через зонд в положении больного на жи-
воте лицом вниз (рис. 22-13)/" при этом хорошо
определяется и нарушение перистальтики. Для
диагностики изолированного ТПС используется
и бронхоскопия,2" во время которой можно увидеть
трахеальный конец фистулы, располагающийся
обычно в мембранозной части трахеи (рис. 22-14).
Если при этом через ТПС провести уретральный
Рис. 22-S. На рентгенограмме пилен значительно расширенный
проксимальный сегмент пмтенола (указан стрелками), заканчи-
вающийся на уровне Tv Газ определяется только в желудке
и отсутствует ниже 12-перегной кишки, что говорит об атрезии
пищевода с дистальным трахеопищеводным свищом и дуоде-
нальной атрезией.
284 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
Рис. 22 9. Рентгенограмма 800-граммового недоношенного ре-
бенка со степс заканчивающимся на уровне Г5 расширенным
проксимальным сегментом пищевода (указан стрелками) it «не-
мым» животом, что говорит об изолированной а грезии пищево-
да. У ребенка также болезнь гиалиновых мембран.
Рис. 22-10. Рентгенограмма грудной клетки (при поступлении)
ребенка с атрезией пищевода и дистальным трахеопищеводным
свищом. Ателектаз верхней доли правого легкого. Проводилось
отсасывание слизи из верхнего сегмента и через интубацион-
ную трубку из трахеи, вводились антибиотики, наложена га-
стростома. Ателектаз ликвидирован через 2 дня, после чего
была произведена операция.
Рис. 22-11. Iki рентгенограмме грудной клетки виден расши-
ренный проксимальный сегмент пищевода, газ в желудке, кон-
фигурация сердца в виде «башмака» (тсграда Фалло). Умбили-
ка.тьныГг артериальный катетер поднимается вдоль правого края
позвоночника, что говорит о правостороннем расположении
аорты. РаО2 было 21 мм Hg. Катетеризация сердца подтвердила
наличие тетрады Фа «ло. В день поступтения ребенку была про
изведена операция на сердце (правый легочно-системный
шунт), а через 6 дней анастомоз пищевода (левосторонняя
торакотомия п сняли с правосторонним расположением дуг»
аорты).
Рис. 22-12. Рентгенограмма после введения в пищевод 0,5 m i
жидкого бария. Виден высокий (Т,). слепо заканчивающийся
проксимальный сегмент, кончраст в трахее и газ в желудке
и 12-перстной кишке, отсутствие газа в тонкой кишке, что гово-
рит об атрезии пищевода, дистальном трахеопищеводном сви-
ще, дуоденальной непроходимости. Бронхоскопия выявила ла-
ринготрахеоззофагеальную расщелину.
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 285
Рис. 22-/3. Киноэзофагограмма с введением бария в прокси-
мальный cei мент пище вода. Контрастное вещество попадает
в трахею через трахеопищеводный свищ (стрелка).
катетер и извлечь его конец из пищевода, то на
рентгенограмме точно виден уровень свища (рис.
22-15).
Выявление свищей, особенно рецидивных, может
быть порой затруднено. Дополнительным методом
исследования в таких случаях является обтурация
баллонами верхнего и нижнего отделов пищевода
с введением барня между ними. Можно также вве-
сти в эндотрахеальную трубку метиленовый си-
ний, осматривая пищевод через эндоскоп, при этом
во время форсированного дыхания краситель мо-
жет появиться в пищеводе. Если есть подозрения
иа ТПС, особенно рецидивный, очень важна на-
стойчивость в проведении диагностических меро-
приятий. В одной из серий наблюдений 30 больных
с изолированным ТПС, только у 22 пациентов
свищ был выявлен при первичной эзофагографии,
в двух случаях фистула обнаружена лишь во вре-
мя третьего обследования.30 Другими авторами,
описавшими 23 рецидивных ТПС, представлено
наблюдение, когда у одного больного потребова-
лось 6 исследований с барием, чтобы выявить
свищ.38
Сочетанные аномалии. Примерно половина де-
тей с АП и ТПС имеют сопутствующие аномалии,
нередко тяжелые и неблагоприятно влияющие на
результаты лечения. Сочетанная патология значи-
тельно чаще, чем сама АП, является причиной
смерти. Сопутствующие аномалии более характер-
ны для недоношенных детей с АП. Так, у новорож-
денных с массой тела менее 2000 г сочетанные
пороки встречаются в 2,5 раза чаще, чем у детей
с массой тела больше 2500?' В 1973 г. была описа-
на ассоциация VATER, в состав которой входит
АП. Данное названне образовано из первых букв
соответствующих английских терминов [вертеб-
ральные дефекты, скальная атрезия, трахеопище-
водный свищ и атрезия пищевода (esophageal atre-
sia), радиальная-лучевая и ренальная диспла-
зия]40 Если сочетание пороков обозначается аб-
бревиатурой VACTER. то к VATER-комбинации
добавляются еще и кардиальные (cardiac) поро-
ки — наиболее часто сочетающиеся с АП и опреде-
ляющие в большинстве случаев неблагоприятный
исход. Также нередко при АП встречаются анома-
лии конечностей (limb) и тогда термин приобретает
наиболее современное звучание—VACTERL. ’
У детей с VACTERL-ассоциацией как правило от-
мечается высокий проксимальный сегмент пищево-
да, осложненное течение, более высокая леталь-
ность, чем у новорожденных с АП без этого соче-
тания/3 VACTERL-ассоциация—не синдром
(если подразумевать под синдромом обязательное
сочетание всех компонентов), но и не случайная
комбинация. При наличии у ребенка одной из ано-
малий, входящих в данную ассоциацию, следует
подозревать и искать другие. Частота ассоциации,
по данным разных авторов, широко варьирует
в зависимости от количества наблюдений и числа
включенных в ассоциацию компонентов. Так, пол-
ная VATER-ассоциация может встречаться в 1.5%
случаев среди новорожденных с АП и ТПС/5 а три
компонента VACTERL-ассоциации — в 17,5%.
Сочетанные аномалии играют важную роль при
оценке состояния и лечении тетей с АП и ТПС
и в значительной степени определяют исход.
Среди 118 новорожденных с АП и ТПС, наблю-
давшихся в Детском Госпитале Милосердия (Кан-
зас-Сити, шт. Миссури) с 1973 по 1990 гг.3
у 62 пациентов (52,5%) выявлены 123 аномалии
(табл. 22-2). Эти данные о частоте сочетанных
с АП и ТПС пороков соответствуют цифрам, при-
водимым многими авторами. ° — Порок серд-
Рис. 22-/4. Бронхоскопия. Видно отверстие трахеопищеводного
свища о мембранозной чисти трахеи на 2,5 см выше карины.
286 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
Рис. 2215. Рентгенограмма ребенка с решим-
ном трахеопищеводного свища. Уретральный
катетер во время бронхоскопии проведен из
трахеи в пищевод и извлечен с помощью эзо-
фагоскопа. Нижняя часть петли катетера пока-
зывает уровень свища (Т,).
ца — наиболее тяжелая сопутствующая аномалия,
нередко определяющая летальный исход. Пороки
ЖКТ встречаются часто, но, как правило, подда-
ются коррекции. Другие самые разнообразные ано-
малии могут быть как мало значимыми, так
и очень серьезными. Некоторые из них представ-
ляют порой непосредственную угрозу для жизни
ребенка и даже требуют лечения в первую очередь,
до вмешательства на пищеводе и грахее. Однако
большинство сочетанных аномалий не препятству-
ют экстренному лечению детей с АП и ТПС.
Предоперационная подготовка. Предопераци-
онная подготовка состоит из: (а) подтверждения
диагноза и установления типа аномалии; (б) оцен-
ки состояния легких и, при наличии поражения
(ыхательной системы, соответствующего лечения;
(в) выявления и, если необходимо, лечения соче-
танной патологии.
Диагностические процедуры, описанные выше,
должны быть осуществлены сразу, как только про-
изведена первичная оценка состояния больного
и оказана первая необходимая помощь. После зон-
ТАБЛИЦА 22-2. Сочетанные врожденные аномалии j 62 из
ПК пациентов с АП и ТПС
лнпма ши Количество больных
Сердца 29
Дыхательной системы 21
Желудочно-кишечного тракта 18
Скелета 19
Центральной периной системы 16
Мочеполовой системы 11
Брюшиой стенки 5
Хромосомные 4
123
шрования пищевода проводится обзорная рентге-
нография (переносным аппаратом) с зондом в вер-
хнем сегменте. У недоношенных детей исследова-
ние лучше проводить под контролем ЭОЛа. Наи-
лучшая визуализация достигается путем введения
через зонд 0,5 мл (нс более!) жидкого бария с по-
следующей рентгенографией переносным аппара-
том. Барий затем сразу отсасывается.
Состояние легких оценивается по частоте дыха-
ния, характеру одышки, наличию цианоза, хрипов
и по данным рентгенографии. Иногда необходим
контроль са гурации и газов крови. Для предотвра-
щения дальнейшей аспирации производится час-
тое отсасывание слюны и слизи из носоглотки
Ребенок должен находиться в возвышенном поло-
жении. Катетер, введенный в верхний сегмент пи-
щевода, присоединяется к постоянному отсосу.
Приподнятый головной конец помогает уменьшить
заброс желудочного содержимого через дисталь-
ный ТПС в трахею, ибо при таком положении кар-
диальный отдел находится выше уровня жидкости
в желудке и таким образом происходит в основном
регургитация воздуха, а не жидкости. Всем паци-
ентам вводят антибиотики, обычно ампициллин
и гентамицин (с четким контролем концентрации
их в крови). Если есть достоверные данные о зна-
чительных ателектазах или пневмонии, то под об-
щей анестезией производится декомпрессионная
гастростомия по 111 гамму, что позволяет предот-
вратить рефлюкс и его последствия. В то время,
как одни хирурги утверждают, что дооперационная
пневмония не влияет на выживаемость, и соответ-
ственно не придают особого значения ее лечению
4> 40. 4». 31
до операции. другие, к которым присое-
диняемся и мы, придерживаются иного мнения, по-
лагая, что значительное улучшение состояния лег-
ких в результате лечения ателектазов и пневмонии
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 287
перед большими торакальными вмешательствами
обеспечивает более гладкое течение как самой опе-
рации, так и послеоперационного периода.45,52
Обычно дооперационная подготовка лает эффект
за 24—72 часа, после чего производится операция.
Наиболее частая причина смерти детей с АН —
сопутствующая патология, которую необходимо
тщательно оценить во всей полноте, особенно если
она представляет риск для жизни новорожденного
и требует специфической терапии. Прежде всего
это касается различных вариантов пороков сердца,
идиопатического респираторного дистресс-си ндро-
ма (ИРДС), атрезии кишечника и анального отвер-
стия, некоторых видов аномалий дыхательных
путей и. наконец, недоношенности со всеми харак-
терными ее проявлениями, такими, например, как
внутричерепные кровоизлияния.
Каждому ребенку с признаками сердечной недо-
статочности, цианозом, увеличением размеров сер-
дца или сердечными шумами необходимо произве-
сти УЗИ сердца. В некоторых случаях, при нали-
чии показаний, до операции по поводу АП и ТПС
производится катетеризация сердца. Если порок
сердца представляет больший риск для жизни, чем
трахеопищеводная аномалия, необходимо в первую
очередь произвести операцию на сердце, радикаль-
ную или паллиативную.
ИРДС" иногда требует ИВЛ с высокими парамет-
рами вентиляции. Поступление при этом воздуха
через ТПС в желудок может вызывать растяжение
желудка и кишечника, высокое стояние диафраг-
мы, что в свою очередь делает вентиляцию неэф-
фективной. В подобных ситуациях описана даже
перфорация желудка.55 Если в таких случаях желу-
док «разгрузить» с помощью гастростомии, то это
позволит предотвратить его растяжение и рефлюкс
желудочного содержимого в трахею, но сброс воз-
духа при этом из трахеи через фистулу не позво-
ляет удерживать необходимое интратрахеальное
давление и соответственно адекватную вентиля-
цию. ’ Поэтому гастростомическую трубку целе-
сообразно подключить к активной аспирации,
установив давление на 2—3 см водн. ст. ниже, чем
в дыхательной системе, что позволяет осуществ-
лять ИВЛ, а также предотвратигь разрыв желудка
и гастроэзофагеальный рефлюкс.56 Вентиляция
у таких больных может быть облегчена, если фи-
стулу временно обтурировать бронхоскопически
с помощью баллонного катетера Фогэрти. Более
надежная окклюзия осуществляется путем экстрен-
ной операции разделения и ушивания ТИС.”
Из видов кишечной непроходимости при АП
и ТПС наиболее часто встречается дуоденальная
атрезия, которую несложно диагностировать на
первичных рентгенограммах (см. рис. 22-8). В та-
кой ситуации необходима как минимум срочная
гастростомия, чтобы предотвратить рефлюкс со-
держимого желудка в трахею через ГНС. Дуоде-
нальная атрезия можег быть устранена одновре-
менно с наложением гастростомы с последующим
отсроченным вмешательством на пищеводе. Такой
подход, по нашему мнению, является наиболее
правильным. Однако возможны и два других так-
тических решения: сначала операция по поводу
АП и ТПС, затем — дуоденальной атрезии, либо
одновременная коррекция обоих пороков.
Атрезия анального отверстия при отсутствии
промежностного нли вагинального свища, доста-
точно широкого для эффективного опорожнения
кишечника, является показанием к колостомии, од-
новременно с операцией на пищеводе.
Ларинготрахеоэзофагеальная расщелина, так
же, как и врожденный подсвязочный стеноз, соче-
танные с АП и ТПС, обычно требуют срочной
трахеостомии.
Проводимая предоперационная подготовка, как
правило, способствует улучшению состояния тяже-
лых недоношенных детей, у которых причина тя-
жести недостаточно ясна, а также новорожденных
с проявлениями сепсиса. В таких случаях, как
и при тяжелых сочетанных аномалиях, целесооб-
разно произвести гастростомию для предотвраще-
ния гастроэзофагеального рефлюкса и его послед-
ствий. поставить центральный венозный катетер
для парентерального питания и осуществлять ан-
тибактериальную терапию и остальные соответст-
вующие лечебные мероприятия, как хирургиче-
ские, так и консервативные. Когда в результате
этих мероприятий состояние больного стабилизи-
руется, а затем начнет улучшаться, операция по
поводу АП и ТПС будет наиболее безопасной.
Очень важно правильно выбрать время для опера-
тивного вмешательства.
Клинические группы и сроки оперативных
вмешательств. Среди детей с АП н ТПС могут
быть выделены 3 клинические группы, что помога-
ет правильно определить характер и длительность
предоперационной подготовки (табл. 22-3). Наи-
большая (количественно) группа включает в себя
исходно «здоровых# детей (если не считать АП
и ТПС), которых целесообразно срочно опериро-
вать, причем операцией выбора является анастомоз
пищевода. В гастростомии обычно нет необходимо-
сти. 59 (50%) наших больных относились к этой
категории.
Вторая, наименьшая группа (19 больных —
16%), включает новорожденных, у которых из со-
путствующей патологии на первый план выступа-
ют пневмония и ателектазы. На фоне примене-
ния антибиотиков, отсасывания слизи из верхнего
сегмента и разгрузочной гастростомии, состояние
легких у таких больных обычно улучшается в те-
чение 1—3 дней, после чего может быть преднри-
ТАБ.1ИЦА 22-3. Клинические группы и предоперационная
тактика у 118 больных с АП и ГПС
«Здоровые» де» и 59 больных (50%) Срочный нериич- ный анастомоз
11 иен мои и я/ателектаз 19 больных (16%) Гастростомия Антибиотики Анастомоз после 24 72-часовом НОДП1ТСП1КИ
«Больные» лети 40 Больных (34%) Лечение сочетай-
тяжелые сочегян- I астростом ия ной патоло-
ные пороки, ИРДС. Полное парсите- гни — отсро-
сепсис, недоношен- ные (индивидуально) ральное питание чеиный анасто- моз
288 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
нита операция прямого анастомоза с хорошими,
как правило, результатами.
Третья группа включает «больных» детей
(40 пациентов—34%). Это группа наибольшего
риска, который обусловлен не столько АП и ТПС,
сколько сочетанной патологией, жизнсугрожающи
ми аномалиями, нс поддающейся лечению пнев-
монией, ИРДС или сепсисом. Сюда же относятся
тяжелые недоношенные дети, причем не просто
имеющие небольшую массу тела или малый геста-
ционный возраст, а тяжелые по своему физиологи-
ческому статусу. («Крепкие» недоношенные дети
переносят первичную радикальную операцию впол-
не удовлетворительно.) Декомпрессионная гастро-
стомия, отсасывание слизи из верхнего сегмента,
питание через центральный венозный катетер позво-
ляют стабилизировать состояние таких пациентов,
выявить сону гствующую патологию и проводить
соответствующую предоперационную подготовку.
Разделение и ушивание свища, как самостоя-
тельная первичная операция, редко бывает необхо-
димым и показано лишь в тех случаях, когда
ИРДС требует ИВЛ, однако при функционирую-
щем "ТПС не удается достичь адекватной вентиля-
ции. Коррекция сочетанных аномалий может быть
произведена как до вмешательства на пищеводе,
так и после него (табл. 22-4). При наличии сопут-
ствующей нехирургической патологии длительность
предоперационной подготовки, естественно, увели-
чивается. В любом случае ликвидация АП и ТПС
у детей, относящихся к третьей группе, предприни-
мается, как только улучшится общее состояние ре-
бенка.
Оперативное лечение. Операция производится
под общим наркозом. ТПС может затруднить прове-
дение ИВЛ, ибо вентиляция с применением жест-
ких параметров у новорожденных без гастростомы
ведет к растяжению желудка и кишечника. Если га-
стростома наложена, то гастростомическая трубка
во время операции должна быть открыта. Однако
при широком ТПС, особенно при наличии откры-
той гасгростомы, вентиляция бывает крайне за-
труднена до тех пор, пока не ликвидирован свищ.
Операционный доступ — заднебоковая торакото-
мия на стороне грудной клетки, противоположной
расположению дуги аорты. М. latissimus dorsi
и m. serratus разделяются или отводятся кпереди.
Подходить к средостению транс- или экстраплев-
рально — дело выбора хирурга. Трансплевраль-
ный доступ более быстрый, простой и достаточно
безопасный,46'47 в то же время ретроплевральный
доступ дает лучший обзор, но что более важно —
при любой несостоятельности анастомоза ограни-
чивает процесс ретроплевральным пространством,
предотвращая тем самым эмпиему. Соответствен-
но некоторые хирурги считают наиболее безопас-
ным именно ретроплевральный доступ.42'52
К рстроплевральному пространству можно по-
дойти либо после резекции 4-го ребра, что проще,
либо без резекции через 4-е межреберье. Когда
в ране появилась эндоторакальная фасция, начи-
нают осторожное отделение плевры (рис. 22-16).
По достижении средостения разделяют две са-
мые верхние межреберные вены, после чего v. azy-
gos отподят кпереди вместе с плеврой. Разделение
продолжают кверху. Медиастинальную плевру от-
водят от трахеи кпереди. N. vagus, который по
своим относительным размерам значительно боль-
ше у детей, чем у взрослых, также отводят
(рис. 22-17). Нижний сегмент пищевода, обычно
расположенный непосредственно под п. vagus, вы-
деляют кверху до соединения его с трахеей. На
свищ непосредственно у трахеи накладывают
швы-держалки, после чего его рассекают как мож-
ТАБЛИЦА 22-4. Операции по поводу сочетанных аномалий
До операции иа пищеводе После операции на пищеводе
Сердце Системный легочный шунт 3* ОАП 2
Дыхательные пути Перевязка ОАП 3 Коарктация/ОАП 1 Трахеостомия по поводу Трахеостомия 4
Желудочно-кишечный тракт ларииготрахеоэзофаг. расщелины 1 Колостомия/атрезия ануса 5 Трахеомаляция 3 Субаортальный стеноз 1 Аортопексия 2 6 Г1 нлоростеноз 1
Дуоденальная непроходимость 4 Дуоденальная непроходимость 1
Центральная нервная система Резекция при нскротич. энтеро- колите 1 Шу нт/гидроцефал ия 1 • Мембрана желудка I Фундопликация 7 10 Шупт/ввутрнчерспное кровоиз-
Мочеполовая система Брюшная стенка Гастрошизис (раднкнльво) 1 лияиис I Стеноз уретры I Г рыжа 4
Всего 20 Всего 24
Одна смерть в каждой из этих групп.
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 289
Рис. 22-16. После заднебокового разреза непо-
срсдственмо ниже у па лопатки, m. latissimus dorsi
и т. serralus ant. отводят кпереди. 4-е ребро резе-
цируют субпериоста л ьн о и делают разрез внут-
реннего листка надкостницы. Края разреза разво-
дят небольшими зажимами москитами. Обнажают
поверхность эндоторакалькой фасции. Плевру
осторожно отделяют сзади от грудной стенки до
купола грудной клетки кверху и на 2—3 межре-
берных промежутка книзу от разреза. Если плевра
повреждена на небольшом протяжении, се ушива-
ют ОДНИМ ШВОМ.
19 Заказ № 1622
Рис. 22-17. Выделение продолжа-
ют по направлению к средосте-
нию. Непарную вену вместе с
плеврой отводят кпереди после
перевязки и рассечения двух вы-
шележащих межреберных вси, ко-
торые впадают в непарную. На-
ходят блуждающий нерв, идущий
обычно вдоль правой стороны
как проксимального, так и ди-
стального сегментов.
290 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
но ближе к трахее. Отверстие на трахее ушивают
несколькими швами тонкой нерассасывающейся
нитью (рис. 22-18).
Верхний сегмент находят после введения в него
(анестезиологом) катетера. На верхушку прокси-
мального отдела накладывают швы-держалки. Сег-
мент тщательно выделяют до шеи. В области груд-
ной или шейной части трахеи можно натолкнуться
на недиагностированную проксимальную фистулу,
поэтому необходимо особенно внимательно выде-
лясь сегмент по передней стенке (рис. 22-19). Ди-
стальный отдел мобилизуют лишь настолько, что-
бы можно было сопоставить сегменты без натяже-
ния. Следует избегать обширной мобилизации ди-
стального сегмента в связи с опасностью наруше-
ния кровообращения.
Верхушку проксимального сегмента отсекают,
и концы пищевода сопоставляют. При наложении
анастомоза часто приходится сталкиваться с раз-
личными трудностями. Так, почти всегда есть на-
тяжение, большее, чем хотелось бы. Диаметры сег-
ментов существенно различаются — проксималь-
ный в 2-—4 раза шире дистального. Пищевод, не
имеющий серозного покрытия, не «держит» швы
достаточно хорошо. В прошлом был популярен те-
лескопический анастомоз по Haight. Однако сегод-
ня большинство хирургов предпочитают одноряд-
ный анастомоз отдельными швами через все слои
(рис. 22-20). Можно применять как шелковые, так
и синтетические рассасывающиеся нити. При ис-
пользовании шелка чаще бывают послеоперацион-
ные осложнения. В ретроплевральном про-
странстве около анастомоза оставляют катетер,
чтобы в случае несостоятельности можно было
осуществлять дренирование.
Значительные сложности возникают при нали-
чии между сегментами большого диастаза, отме-
чающегося у всех больных, не имеющих дисталь-
ной фистулы, у новорожденных с высоким (корот-
ким) проксимальным сегментом или с низким (на
уровне карины) дистальным ТПС. Среди наших
118 пациентов с АП у 5 не было дистального
ТПС, а среди 100 детей с АП и нижним ТПС
у 6 было значительное расстояние между сегмента
ми (см. табл. 22-1). Если большой диастаз диа-
гностирован до операции, то растяжение верхнего
сегмента дважды в день введением в него под неко-
торым давлением широкого катетера или бужа
обычно приводит к удлинению проксимального от-
дела за период от 3 до 6 недель.5* Иногда просто
время играет роль в удлинении сегмента (удлине-
ние без бужирования за счет самостоятельного ро-
ста).5’ При отсутствии дистального ТПС можно
проводить удлинение и нижнего сегмента ретро-
Рис. 22-18. Нижний сегмент берут на дер-
жалку и выделяют до соединения с задней
стенкой трахеи. На трахеальный конец сви-
ща накладывают швы-держалки и свищ
пересекают непосредственно у трахеи- Важ-
но не сузить при этом трахею. Трахе-
альный коней свища ушивают отдельными
швами, которые прикрывают, если это воз-
можно, прилежащими тканями.
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 291
Рис. 22-19. На дно верхнего сег-
мента наклады№iют швы-держал-
ки. Проксимальный отдел пище-
вода тщательно выделяют до
шеи. Важно на данном этапе НС
пропустить проксимальный свищ.
Выделение производят как можно
ближе к пищеводу, стараясь нс
повредить блуждающий нерв. Ди-
стальный сегмент мобилизуют
минимально, лишь настолько,
чтобы можно было сопоставить
сегменты.
градно через гастростому, хотя эффект в подобных
случаях, как правило, незначителен.
Существует несколько хирургических методов,
направленных на уменьшение диастаза во время
операции. Эзофагомиотомия по окружности верх-
него сегмента часто приводит к достаточному для
наложения анастомоза удлинению.00 Миотомию
производят при подтягивании верхнего сегмента за
держалки. Разрез осуществляют как через про-
дольный, так и через циркулярный мышечный
слой до подслизистой, не повреждая ее. Можно
сделать 2 или 3 миотомии с расстоянием между
ними в 1 см.61 Если при этом доступ к пищеводу
из грудной клетки затруднен, а проксимальный сег-
мент необходимо мобилизовать до шеи, его даль-
нейшее выделение может быть произведено из
Рис. 22-20. Дно верхнего сегмента
отсекают. Задний ряд швов наклады-
вают через все слои, завязывая нити
внутрь просвета. Швы переднего ря-
да завязывают наружу. В рстроплсв-
ральном пространстве около анасто-
моза оставляют катетер. Рану груд-
ной клетки ушивают как обычно.
292 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
нижнего шейного доступа, что способствует макси-
мальной мобилизации кверху и прекрасно «откры-
вает» место для миотомий.
В редких случаях, когда концы пищевода воз-
можно сблизить для наложения анастомоза, но
натяжение слишком велико, может быть использо-
ван метод «фистулообразующего» центрального
шва 61 Для этого нижний сегмент ушивают от-
дельными шнами нерассасывающейся нитью. За-
тем через верхушки обоих сегментов и их просве-
ты накладывают шов шелком 2-0, который проч-
но завязывают. Для укрепления этого центрально-
го шва вокруг него накладывают мышечные швы,
сближающие сегменты. Через несколько дней цен-
тральный шов прорезается, образуя свищевое сое-
динение между верхним и нижним сегментами. Ча-
сто при этом возникает несостоятельность, однако
в большинстве случаев «анастомоз» самостоятель-
но заживает. Данный метод, естественно, подразу-
мевает обязательное бужирование.
Если сегменты не могут быть сопоставлены,
то нижний отдел ушивают и фиксируют к пери-
вертебральной фасции, чтобы предотвратить его
сокращение и укорочение. Верхний сегмент выво-
дят наружу через разрез в надключичной обла-
сти и подшивают к коже. Пластику пищевода
производят позже, в возрасте от 6 до 12 мес
(см. главу 21).
Послеоперационный период. В послеоперацион-
ном периоде в течение нескольких дней вводят ан-
тибиотики. Крупные «здоровые» дети могут быть
дезинтубированы вскоре после операции. У мало-
весных, «больных» новорожденных обычно требу-
ется ИВЛ. Интубационную трубку удаляют по
мерс восстановления самостоятельного дыхания
(см. главу 4). При развитии ателектазов, чему
способствует сохраняющаяся секреция, показана
санация трахеи через интубационную трубку. Не-
обходимо частое отсасывание слизи из носоглотки
до тех пор, пока ребенок не начнет глотать слюну.
Чтобы исключить возможность повреждения ана-
стомоза при отсасывании, используют отсосный
катетер с маркировкой. Метка ставится на расстоя-
нии, равном расстоянию от носа до мочки уха.
Дренажную трубку в грудной клетке оставляют
на 10 дней, так как именно в течение этого
времени может произойти несостоятельность ана-
стомоза.
Введение через рот небольших порций жидкости
начинают сразу, как только ребенок стал глотать
слюну. Затем переходят к смесям или молоку, рас-
считывая их количество соответственно возрасту
и массе тела. Если наложена гасгростома, то пита-
ние через нее обычно начинают на следующий
день после операции
Некоторые хирурги перед началом кормления
проводят рентгенологическое исследование пище-
вода, а перед выпиской — контрольное бужирова-
ние. По нашему мнению, контрастная рентгеногра-
фия показана и должна быть проведена обязатель-
но лишь в случаях затруднений глотания, рво-
ты или подозрения на несостоятельность анасто-
моза.
В послеоперационном периоде проводят также
лечение сопутствующей патологии. Поскольку при
АП нередко встречаются аномалии мочевой систе-
мы, перед выпиской всем больным покт1зано УЗИ
почек. Как только пациент стал получать полный
объем энтерального питания по возрасту, глотать
без затруднений и прибавтять в весе, родителей
инструктируют о правилах ухода за ребенком
и малыша выписывают домой. Гастростомическую
трубку, если была наложена гастростома, обычно
удаляют перед выпиской.
Осложнения. Наиболее опасное послеопераци-
онное осложнение — несостоятельность анасто-
моза, диагноз которой обычно несложен, посколь-
ку при наличии дренажной трубки через нес начи-
нает поступать слюна. Если есть какие-либо со-
мнения, то через рот вводя г раствор метиленового
синего, который при несостоятельности появляется
в дренаже. Для подтверждения диагноза, определе-
ния характера и локализации несостоятельности
целесообразно исследование с барием. Всем боль-
ным дают антибиотики. Если несостоятельность
массивная и ранняя (первые три дня после опера-
ции), показано повторное вмешательство. При
этом редко удается ушить отверстие в анастомозе
(с последующим консервативным лечением). Чаще
всего при полном расхождении анастомоза ушива-
ют дистальный отдел, а проксимальный выводят
на шею.
При частичной небольшой несостоятельности
анастомоз обычно заживает самостоятельно (спон
танно). Независимо от гого. каким был доступ —
транс- или экстраплевральным, необходимо эф-
фективное дренирование грудной полости. Способ-
ствует заживлению пищевода декомпрессионная
гастростомия, предупреждающая рефлюкс, а также
обеспечивающая адекватное питание (парентераль-
ное или через трубку, проведенную через гастросто-
му в тонкую кишку). Никогда не следует проводить
питание непосредственно в желудок, поскольку это
может способствовать возникновению рефлюкса,
который в свою очередь будет препятствовать за-
живлению анастомоза. В результате несостоятель-
ности может развиться сепсис и рецидив ТПС.
Среди наших наблюдений было 9 случаев несо-
стоятельности анастомоза, диагностированной в
раннем послеоперационном периоде. У 7 пациен-
тов анастомоз зажил спонтанно на фоне проводи-
мого (описанного выше) лечения. Двое детей
умерли. У одного из них вмешательство осуществ-
лялось трансплевральным доступом. После опера-
ции в связи с подсвязочным стенозом ребенок по-
лучал стероиды, в последующем развилась эмпие-
ма и сепсис. Второй недоношенный новорожден-
ный с врожденным пороком сердца, гидронефрозом
и почечной недостаточностью был оперирован
в первый день жизни по поводу коарктации аорты
и АП (перевязан ТПС). Однако возник рецидив
ТПС. и ребенок умер от сепсиса. Было также одно
наблюдение несостоятельности не анастомоза, а
ушитой культи дистального сегмента (при боль-
шом диастазе). Данное осложнение не было свое-
временно распознано, поскольку дренажная трубка
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 293
была уже удалена. Пациент умер от сепсиса. Та-
ким образом, во всех грех летальных исходах при-
чиной смерти были несостоятельность и сепсис.
Рецидив ТПС был еще у 5 пациентов с нераспоз-
нанной несостоятельностью. Таким образом, всего
отмечено 14 случаев несостоятельности (12%). Ре-
цидив ТПС выявлен в 5% всех наблюдений.
Рецидив ТПС обычно возникает в раннем после-
операционном периоде, но часто не распознается
месяцами и даже годами. Проявления рецидивного
свища такие же, как и врожденного: кашель во
время питья, рецидивирующая пневмония и ате-
лектазы. Эти симптомы в послеоперационном пе-
риоде могут также возникать в случаях недиагно-
сти рован кого, и соответственно не ликвидирован-
ного проксимального ТПС, стеноза зоны анасто-
моза, гастроэзофагеального рефлюкса, снижения
сократительной способности пищевода или трахео-
маляцин. Диагностика может быть очень трудна
и проводится при рецидивном свище так же, как
и при врожденном. Крайне редко рецидивный ТПС
может закрыться спонтанно. Предпринимались по-
пытки ликвидации свища с помощью лазера, одна-
ко лучшие результаты достигаются все же при хи-
рургическом вмешательстве.38
Если состояние больного позволяет ждать, то
лучше произвести операцию после того, как будет
купирован или пойдет на убыль местный воспали-
тельный процесс (обычно для этого требуется 3
6 мес). В течение этого времени ребенка кормят
через гасгростому. Многие трахеопищеводные сви-
щи (расположенные на уровне Т2_3 или выше)
могут быть ликвидированы из шейного доступа.
ТПС на уровне карины или около нее (Т4) лучше
достигается из трансплеврального доступа.
Проведение уретрального катетера через фисту-
лу позволяет подтвердить ее уровень рентгеноло-
гически и помогает определить точную локализа-
цию свища во время операции (см. рис. 22-15).
Тщательное ушивание (после рассечения) обоих
концов ТПС и интерпозиция тканей между ними
обеспечивают наилучшие шансы на успех. В тяже-
лых случаях повторного рецидива целесообразно
осуществлять операцию с противоположной, «коо-
перированной», стороны, что обеспечивает наибо-
лее простой доступ, меньшее образование рубцов
и лучшие результаты. 4 из 5 рецидивных свищей
были ликвидированы нами оперативно (рассече-
ние и ушивание). У одного ребенка свищ рециди-
вировал трижды, что в конце концов потребовало
пластики пищевода толстокишечным трансплан-
татом.
Стеноз пищевода в зоне анастомоза — доста-
точно обычное осложнение, которое проявляется
затруднением глотания, аспирацией (нарушения
дыхания, апноэ, пневмония), задержкой физиче-
ского развития, а в более поздние сроки — обтура-
цией пищевода пищевыми массами. Диагноз ста-
вится на основании рентгенографии с барием. Ле-
чение — бужирование пищевода. Если есть показа-
ния, то одновременно проводится и лечение гастро-
эзофагеального рефлюкса (ГЭР).
Роль ГЭР в развитии стриктуры анастомоза чет-
ко установлена.64 Рефлюкс кислого желудочного
секрета в сочетании с замедленным опорожнением
пищевода в результате нарушения его внутренней
двигательной активности предрасполагает к эзо-
фагиту и стриктуре анастомоза. С тех пор. как мы
стали активно лечить ГЭР, стриктуры анастомоза
встречаются реже. Важная роль ГЭР была подтвер-
ждена также в одном из сообщений о 30 пациен-
тах, потребовавших резекции зоны стриктуры
(троим резекция была произведена дважды). Толь-
ко 10% пациентов со стриктурами нуждались в ре-
зекции.63
Среди наших 118 больных стриктура анастомоза
развилась у 31 ребенка (25%). У 13 детей одно-
кратное бужирование дало хороший результат,
в то время как в 1 8 случаях потребовалось 2 се-
анса бужирования и больше. Двух пациентов при-
шлось оперировать — резецировать зону сужения.
Гастроэзофагеальный рефлюкс. ГЭР часто от-
мечается у детей с АП и ТПС. Так, при pH-метрик
у 22 пациентов через 6—33 года (в среднем
15 лет) после операции. ГЭР средней и тяжелой
степени выявлен у 59% обследованных?9 По дан-
ным других авторов, обследовавших 25 пациентов
через 3 мес—7 лет после операции, выраженный
ГЭР прн контрастной рентгенографии выявлен
в 72% случаев, при пищеводной р! 1-метрии—
у 68%, при сцинтиграфии — у 65%. Из тех детей,
у которых отмечались периодические рвоты, дыха-
тельные расстройства или эзофагит. 83% имели
объективно документированный рефлюкс?6 В на-
шей серии из 118 больных у 48 детей (41%) вы-
явлены симптомы рефлюкса, подтвержденного при
обследовании.
Причина рефлюкса недостаточно ясна. С одной
стороны, натяжение в зоне анастомоза может вести
к укорочению интраабдоминальной части пищево-
да и деформировать вход в желудок.66 Однако в эк-
сперименте на животных ни торакальная вагото-
мия, ни симпатэктомия, ни разделение пищевода,
ни наложение анастомоза не приводили к наруше-
нию функции нижнего пищеводного сфинктера?7
Кроме того, есть сообщения о ГЭР у пациентов
с изолированным ТПС, при котором нет укороче-
ния пищевода или натяжения его во время опера-
ции. Эти данные подтверждают предположение
о том, что в развитии ГЭР определенную роль
играет врожденная дисфункция пищевода?8
Симптомы рефлюкса включают рвоту, апноэ, ас-
пирацию, пневмонию, отсутствие прибавки веса,
эзофагит, сужение в зоне анастомоза пищевода.
Диагноз наиболее достоверно ставится на основа-
нии 24-часовой пищеводной pH-метрии. Большое
значение имеет рентгенологическое исследование
с барием, позволяющее не только диагностировать
ГЭР, но также определить наличие и характер су-
жения пищевода и оценить его двигательную ак-
тивность. Наличие симптомов со стороны дыха-
тельных путей является показанием к бронхоско-
пии для исключения ТПС или трахеомаляции.
Лечение рефлюкса такое же, как при ГЭР, не
связанном с АП и ТПС (см. главу 23). Однако
подход должен быть несколько более активным
294 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
ТАБЛИЦА 22-5. ГЭР (с клиническими проявлениями)
у больных (118) с АП и ТПС
Консервативное лечение Фундопликация 15 33
При первичной госпитализации Повторная фундопликация 7 6
По Ниссену По Талю 2 из 4 4 из 29
48
как п хирургическом плане, так и в отношении
медикаментозной терапии, поскольку рефлюкс
у этих больных более стойкий и может вести к
стенозу в зоне анастомоза.6’ У 15—45% пациен-
тов с ГЭР после операции по поводу АП и ТПС
консервативная терапия оказывается неэффек-
тивной^ а потому требуется хирургическое лече-
ние. • Среди наших больных с АП и ГНС
ГЭР был вылечен консервативно у 15, в то время
как 33 ребенка потребовали фундопликации (табл.
22-5). Нарушения двигательной активности пище-
вода после операций но поводу АП играют боль-
шую роль у больных, которым производится фун-
допликация по Ниссену.70
В одном из исследований 5 из 14 больных
(36%), оперированных по Ниссену, имели выра-
женные стойкие симптомы дисфагии, несмотря на
нормальное сокращение нижнего пищеводного
сфинктера (НПС). Дисфагия, по-видимому, была
связана со сниженной сократительной способно-
стью пищевода и с замедленным его опорожнением
из-за сопротивления образованной в результате
фундопликации по Ниссену полной «муфты».™
У наших 33 пациентов, которым была сделана
фундопликация «полумуфтой», двое (6%) имели
постоянную дисфагию, чго потребовало наложения
гастростомы для питания. При операциях по Thai,
Dor-Nissen или Boix-Ochoa, когда создается «полу-
муфта». по-видимому, возникает меныпее сопро-
тивление опорожнению пищевода. Таким образом,
в этой группе пациентов операции по созданию
«полумуфт» могут иметь преимущества перед
«полномуфтовыми».
Рецидив ГЭР после фундопликации у детей
с АП встречается чаще, чем у других больных.
В одной из серий наблюдений рецидив ГЭР был
основанием для повторной операции у 6 из
13 (46%) больных, которым была произведена
операция Ниссена.73 Среди наших 29 пациентов
с фундопликацией по Талю четверо (14%) потре-
бовали повторной операции, в то время как из
4 больных с фундопликацией по Ниссену повторно
оперированы двое (50%). У некоторых больных со
стойким ГЭР развивается пищевод Барретта. Па-
циенты с упорным рефлюксом должны быть обсле-
дованы эндоскопически на предмет метаплазии
и возможного наличия опухоли.73
Обструкция трахеи. Сдавление трахеи аортой
или безымянной артерией, ' " часто сопровождаю-
щее трахеомаляцию, — одна из причин послеопера-
ционных дыхательных расстройств при АП и
ТПС. Некоторые исследователи считают, что бо-
лее важный компонент, вызывающий трахеальную
обструкцию у этих детей, — необычная податли-
вость трахеи при трахеопищеводных аномалиях.76
Гистологическое исследование трахеи у пациентов,
умерших после операций но поводу АП и ТПС.
показывает, что в 75% случаев хрящи были коро-
че, чем в норме, а мембранозная часть шире в том
сегменте трахеи, который был предрасположен
к спадению в переднезаднем направлении.77
Клиническая картина заключается в цианозе,
брадикардии и апноэ, часто возникающими во вре-
мя кормления или непосредственно после него. На-
чало симптомов обычно приходится на 2—3-й ме-
сяц жизни, но иногда они могут появиться и в ран-
нем послеоперационном периоде.7'1 Аналогичный
комплекс симптомов бывает также при сужении
пищевода, снижении его двигательной активности,
аспирации, рецидиве ТПС или при ГЭР. Диа-
гноз устанавливается с помощью бронхоскопии
и КТ трахеи.78 При проведении дифференциальной
диагностики должны быть исключены не только
вышеперечисленные, но и другие виды патологии,
проявляющиеся подобной клинической картиной.
Если симптомы настолько выражены, что вызы-
вают апноэ, должна быть предпринята аортопек-
сия. Менее тяжелые проявления имеют тенденцию
к исчезновению в возрасте 1—2 лет, что связано
с увеличением плотности трахеальных хрящей
в процессе роста и развития. В одной из серий
наблюдений 8 больным была сделана аортопексия.
у 7 пациентов были хорошие результаты, в одном
же случае имелось недиагностированное во время
операции сосудистое кольцо, и улучшение наступи-
ло лишь после его ликвидации (см. главу 21).”
Среди наших пациентов аортопексия была произ-
ведена двум больным с хорошим результатом
в обоих случаях.
В двух наших набиодениях двусторонний пара
лич голосовых связок, вызывавший трахеальную
обструкцию, явился показанием к трахеостомии.
У этих детей отмечался стридор. Оба ребенка пе-
ренесли операцию прямого первичного анастомоза
с обычным выделением проксимального сегмента
до шеи Трудно сказать, была ли это врожденная
аномалия или послеоперационное осложнение.
Результаты. Летальность при АП и ТПС год
от года неуклонно снижается, и в настоящее время
риск, связанный с сочетанной патологией, стано-
вится больше, чем риск, связанный непосредствен-
но с АП и ТПС. Возрастающая выживаемость
в значительной мере обусловлена общим улучше-
нием результатов лечения новорожденных, дости-
жениями реанимации, анестезиологии, кардиохи-
рургии, развитием методов парентерального пита-
ния. Большую роль в снижении летальности при
АП сыграли активное лечение сочетанной патоло-
гии, особенно респираторного дистресс-синдрома,
и хирургическая коррекция сердечных и гастроин-
тестинальных аномалий.
В наших наблюдениях из 118 больных четверо
умерли до операции по поводу АП от сочетанных
аномалий и трое — вскоре после вмешательства от
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 295
ТАБЛИЦА 22-6. Летальные исходы в периоде
новорожденное™
Не связанные с АП-ТПС
До операции
Недоношенность
Пороки сердца
Тяжелое внутричерепное кровоизлияние
Гидроцефалия
Связанные с АП и ТПС
I !ссостоятельпость анастомоза
Недоношенность
Сочетанные аномалии
осложнений, связанных с коррекцией АН и ТПС
(табл. 22-6). Все семеро были из группы «боль-
ных» детей, и все — недоношенные. Общая выжи-
ваемость составила 94%, послеоперационная —
97,5% (табл. 22-7). У 4 новорожденных, умерших
до операции по поводу АП, имелись множествен-
ные аномалии, причем двое детей потребовали хи-
рургического лечения сочетанной патологии: у од-
ного ребенка была произведена операция на серд-
це в связи со сложным синим пороком, у другого
(масса тела 800 г) — резекция кишечника по по-
воду некротического энтероколита (этот ребенок
умер через несколько недель от тяжелого внутри-
черепного кровоизлияния). Три послеоперацион-
ные смерти были связаны с несостоятельностью
анастомоза.
Большинство из 14 поздних летальных исходов
были обусловлены сочетанными аномалиями
(табл. 22-8), в том числе—пороками сердца
(4 пациента). Больной с сердечным блоком (и кар-
диостимулятором) умер от аритмии.
Причиной смерти одного ребенка явилась реци-
дивирующая пневмония (без какой-либо анатоми-
ческой причины). Двое других пациентов умерли
внезапно дома в возрасте 5 и 6 мес. Один из этих
больных имел слегка положительную рН-пробу
и лечился по поводу ГЭР (специальное положение,
питание частыми малыми дозами), у другого была
диагностирована трахеомаляция, умеренно выра-
женная. Все эти три внезапные смерти, по-видимо-
му, были связаны с дисфункцией трахеи и/или пи-
щевода. Более активная хирургическая тактика,
возможно, могла бы предотвратить два последних
летальных исхода. Одна смерть наступила непо-
средственно после пластики пищевода (в первые
сутки) в результате несостоятельности анастомоза
ТАБЛИЦА 22-7. Выживаемость (118 пациентов)
Кол-во пациентов Умгрли Выжили (%)
«Здоровые» дети 59 0 59 (100)
Пневмония/ ателектаз 19 0 19 (100)
«Больные* дети 40 7 33 (82,5)
Всего 118 7 111 (94)
До операции по поводу АП 4
После операции 114 3 111 (97)
ТАБЛИЦА 22-8. Поздние летальные исходы
Врожденный пирок сердца 4
Трисомия 2
Внезапная смерть 3
Блокада сердца 1
Консервативное лечение ГЭР 1
Трахеомаляция I
Трахеоэзофагеальная расщелина I
Кишечная непроходимость I
Салмонеллезный сепсис 1
Рецидивирующая пневмония 1
Несостоятельность анастомоза
после пластики пищевода 1
14
и медиастинита, чему способствовала слишком
энергичная санация глотки немаркированным ка-
тетером.
Отдаленные результаты лечения АП и ТПС пре-
имущественно хорошие. Отмечаются лишь некото-
рые незначительные последствия. Так, у многих
больных (95%) изменена двигательная активность
пищевода.* 27 ПЭР (неоперированный) сохраняется
у 60%.27 Довольно частое явление у детей после
операций на пищеводе — обтурация пищевода ино-
родными телами, требующая их удаления.
Несмотря на имеющиеся нарушения двигатель-
ной активности пищевода, большинство больных
приучаются жить достаточно комфортно, прини-
мая пищу в вертикальном положении, медленно
и тщательно пережевывая ее и запивая большим
количеством жидкости непосредственно во время
еды. При оценке отдаленных результатов хирурги-
ческого лечения 58 пациентов в сроки от 13 до
27 лет после операции, только у одного отмечена
выраженная дисфагия, у 17 были лишь эпизоды
дисфагии, связанные, как правило, с быстрой едой
без тщательного разжевывания.
У половины больных в ранние сроки отмечались
выраженные симптомы стеноза. 18 пациентам по-
требовалось однократное бужирование; в 10 случа-
ях произведена резекция зоны сужения; один ребе-
нок оперирован по поводу рецидива ТПС. 40 паци-
ентов (69%) на момент обследования не имели
никаких затруднений глотания.79
Симптомы со стороны дыхательной системы
в первые годы после операции отмечались доволь-
но часто, но затем становились все более редкими.
Из 100 пациентов, обследованных в Королевском
Детском Госпитале Мельбурна (Австралия), 78%
среди детей до 3 лет не меньше 3 раз в год болели
бронхитом, в то время как из пациентов старше
8 лет только у 48% были столь частые бронхиты.
48% больных как минимум однократно лечились
стационарно по поводу пневмонии.
У пациентов, обследованных через 12—21 год
после операции и перенесших в раннем детстве
объективно подтвержденную пневмонию, отмеча-
лось статистически достоверное снижение жизнен-
ной емкости легких, сравнительно с теми, кто не
имел ранее пневмонии. Между этими данными
и наличием ГЭР не было корреляции.80
296 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
Для большинства тетей были характерны те или
иные хронические нарушения питания, в частно-
сти 19 пациентов имели рост ниже положенного.
Причем эти изменения были одинаковы как
в группе детей, родившихся с массой тела больше
2500 г., так и среди тех, кто весил при рождении
меньше 2500 г. У пациентов старше 5 лет получены
такие же данные, как и у более младших. Однако
к 13 годам хронические нарушения питания отме-
чались значитетьно реже, то есть к этому возрасту
дети «догоняли» в развитии своих сверстников.*
С течением времени пациенты с АН и ТПС чув-
ствуют себя, как правило, все лучше Отмечающи-
еся в ранние сроки симптомы со стороны пищево-
да, легких и нарушения питания постепенно умень-
шаются или исчезают. До юношеского возраста
могут иногда сохраняться тишь изменения двига-
тельной активности пищевода и ГЭР Практически
все пациенты ведут нормальную активную жизнь.
ЛАРИНГОТРАХЕОЭЗОФАГЕАЛЬНАЯ РАСЩЕЛИНА
Ларинготрахгоэзофагеальная расщелина — редкая
аномалия. Этот порок не только эмбриологически
связан с АП и ТПС, но и фактически может соче-
таться с аномалиями пищевода и трахеи.* Рас-
щелина располагается по средней линии между
задними отделами гортани-трахеи и передними от-
делами пищевода. Расщелина I типа (41% паци-
ентов) распространяется вниз через межчерпало-
видную щеть до нижней части перстневидного
хряща. Тип II (42%) характеризуется вовлечением
части мембранозного отдела трахеи. Тип III поро-
ка (17%) — полная расщелина, достигающая кари-
ны.и Тип IV очень редок, расщелина при этом
варианте аномалии распространяется за карипу
в один или оба бронха. 5
Тяжесть клинической картины зависит от протя-
женности расщелины. В большинстве случаев сим-
птомы появляются сразу после рождения. Редкие
пациенты с небольшой расщелиной могут годами
не иметь никаких проявлений. Хронический ка-
шель, дыхательные нарушения и аспирация обыч-
но возникают во время кормления. У некоторых
больных отмечается обильное выделение слизи,
стридор, связанный с вялостью черпалонадгортан-
ных складок, или слабый крик в результате недо-
статочности черпаловидной мышцы, или замедлен-
ного смыкания голосовых связок. Симптомы могут
быть тяжелыми и жизнеопасными.
Диагностика. Диагностировать данную патоло-
гию трудно.82 ( имптомы могут быть такими же,
как при АП и ТПС, а кроме того, эти виды патоло-
гии могут сочетаться.83 Диатноз АП исключают,
если зонд проходит в желу ток. При обследовании
с барием, которое лучше проводить под контролем
ЭОПа, можно выявить попадание контрастного
вещества в грахею, однако установить при этом
место соединения пищеварительного тракта с ды-
хательными путями практически невозможно. Во
всех случаях, когда контрастное вещество попада-
ет в трахею, необходимы ларинго- и трахеоскопия.
Однако расщелины трудно диагностировать и эн-
доскопически, поэтому даже после специальною
квалифицированного обследования диагноз ста
вится не всегда. ! Для того, чтобы исключить рас
щелину. необходимо убедиться в интактности теж-
черпаловидной складки. При наличии расщелины
надавливание кончиком жесткого бронхоскошт кза-
ди. когда он располагается на уровне перстневид-
ного хряща или непосредственно над ним. позволя-
ет пройти аппаратом дальше и увидеть расщелину.
Лечение. При небольших расщелинах лечение
не требуется. Минимальные симптомы с ростом ре-
бенка проходят. При выраженных симптомах лече-
ние необходимо.
При тяжелом поражении у новорожденных мо-
жет потребоваться экстренная интубация или тра-
хеостомия. При III типе аномалии в связи с от-
сутствием задней стенки трахеи бывает трудно,
но очень важно, правильно установить интубаци-
онную или трахеостомическую трубку и удержать
ее в этом положении. В таких ситуациях может
помочь бифуркационная трубка специальной кон-
струкции. ' ‘ Трахеостомия необходима во время
операции ликвидации расщелины.
При тяжелом поражении целесообразно нало-
жить гасгросюму как для декомпрессии желудка,
так и для питания. При расщелинах II и III типа
неблагоприятное влияние на заживление в послео-
перационном периоде может оказывать Г ЭР, поэ-
тому его следует ликвидировать то операции по
поводу расщелины. Соответственно, при наличии
ГЭР до основной операции производится фундо
пл икания и гастростомия. ' Тип IV расщелины
обычно сочетается с микрогастрией (желудок
крайне малого размера), при которой фундоплика-
ция не производится.83
Хирургическое течение Лечение малых расще-
лин может быть осуществлено одним из двух спо-
собов. Передний доступ с разделен ием перстневид-
ного хряща и верхней части трахеи дает хороший
обзор и позволяет избежать повреждения нервов.
Изнутри трахеи делается разрез трахеопищеводно-
го соединения, соответствующий длине расщели-
ны. Передняя стенка пищевода и задняя ларинго-
трахеи последовательно ушиваются.82
Более часто используется боковая фаринготомия
через нижний переднебоковой шейный разрез
справа. Находят возвратный и верхний гортанный
неовы и последний отводят кпереди. Резекция ла-
теральной трети подъязычной кости может облег-
чить этот доступ.
После того, как произведена боковая фарингото-
мия. видны расщелина и гортань. Делают верти-
кальный разрез пищевода кзади от трахеопище
водной борозды, чтобы иметь достаточно тканей
для реконструкции мембранозной части трахеи. Из-
нутри пищевода делают разрез на левой его сторо
нс также кзади от трахеопищеводной расщелины.
Затем закрывают гортань и трахею, начиная снизу
вверх. Пищевод ушивают двухрядным швом (сли-
зистая, затем мышечный слой) также в направле-
нии снизу вверх. После этого ушивают потку.
Прилежащие ткани или мышечные волокна про-
кладывают между линиями швов на пищеводе
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 297
и трахее.’6 Данный шейный доступ целесообраз-
но применять при расщелинах, которые на полови-
ну своей длины распространяются вниз на трахею.
При полной расщелине необходима дополни-
тельная правосторонняя торакотомия для адекват-
ного подхода к нижней части. Существует сообще-
ние об успешном лечении расщелины, когда разрез
пищевода был сделан справа по трахеопищеводной
борозде, а слева — изнутри пищевода на 1 см кза-
ди от борозды, таким образом трахея ушивалась
справа от центра, а пищевод — слева.sY
После операции питание первоначатьно осуще-
ствляется через гастростому или назогастральный
зонд. Некоторые хирурги у пациенюв с расщели-
ной III типа в течение 2 недель после операции
производили вентиляцию через специальную раз-
двоенную эндотрахеал ьную трубку, однако в по-
следующем стала использоваться специальная
изогнутая пол углом трахеотомическая трубка,
предназначенная тля предупреждения давления на
заднюю ушитую стенку трахеи.84
Результаты. По сводной статистике среди
102 пациентов с ларинготрахеоэзофагеальной рас-
щелиной легальность при I типе порока составила
31%, при II — 30%, при III — 82%. Согласно же
данным одной из последних публикаций, среди
17 пациентов, трос из которых имели III тип рас-
щелины, умер лишь один?3 Большинство детей,
выживших после операции по поводу расщелины,
чувствуют себя хорошо.
ЛИТЕРАТУРА
1. Gibson Т: The Anatomy of Humane Bodies Epitomized. sixth
edition. Awnsham and Churchill, London. 1703.
2. Ashcraft KW, Holder TM: The story of esophageal atresia
and tracheoesophageal fistula. Surgery 65:332 340. 1969.
3. Myers NA; The history of oesophageal atresia and tracheoe-
sophageal fistula. Prog Pedi.Hr Surg 20:106—157. 1986.
4. I add WE: The surgical treatment of esophageal atresia and
tracheoesophageal fistula. N Engl J Med 230:625. 1944
5. I.even NL: Congenital atresia of the esophagus with tracheoe-
sophageal fistula: Report of successful extrapleural ligation
of fistulous comiiiuiucation and cervical esophagostomv. J Tho-
r.tc Surg 10:648, 1940.
6. Haight C. Towslcy HA: Congenital atresia of the esophagus
with tracheoesophageal fistula; extrapleural ligation of fistu-
la and end-fn-end anastomosis of esophageal segments. Surg
Gynecol Obstet 76:672. 1943.
7. Hopkins WA: The esophagus. In Gray SW. Skandalakis JL
(Editors). Embryology for Surgeons. WB Saunders. Philadelp-
hia. 1972.
8. Smith EI: The early development of the trachea ««nd esophagus
in relation to al res in of the esophagus and tracheoesophageal
fistula. Contrib Embryol Carnegie Inst Wash 36:41, 1957.
9. Grucnwald P: A case of atresia of the esophagus combined
with tracheoesophageal fistula in a 9 mm. human embryo and
its embryological explanation. Anal Rec 78:293, 1940.
10 Quan L, Smith DW: The VATER association: Vertebral defects,
anal atresia, T-E fistula with esophageal atresia, radial and
renal dysplasia: A spectrum of associated defects. J Pediatr
104:7. 1973.
IL Emery JL. Haddadin AJ: Squamous epithelium in respiratory
tract of children with tracheo-oesuphageal fistula. Arch Dis
Child 46:236. I97L
12. Blank RH, Prillaman PE Jr, Minor GR: Congenital esophageal
atresia with tracheoesophageal fistula occurring in identical
twins. J I'horac Cardiovasc Surg 53:192—196. 1967.
13. David TJ. О’Callaghan SE: Twinning and esophageal atresia.
Arch Dis Child 49:660, 1974.
14. Farha SJ. Diener CH. Block PR: Esophageal atresia and
tracheoesophageal fistula occurring in multiple births. J Kans
Med Soc 72:386 388. 1971.
15. Forrester RM, Cohen SJ: Esophageal atresia associated with
an anorectal anomaly and probable laryngeal fissure in three
siblings. J Pediatr Surg 5:674—675, 1970.
16. Ohkuma R: Congenital esophageal atresia with tracheoesopha-
geal fistula in identical twins. J Pediatr Surg 13:361 362,
1978.
17. Wooley MM. Chinnock RF. Paul RH: Premature twins with
esophageal atresia and tracheoesophageal fistula. Acta Pediatr
50:423. 1961.
18. Engel PM A. Vos UM. DeVries JA, Kuijjer PJ: Esophageal atre-
sia with tracheoesophageal fistula in mother and child. J Pedi-
air Surg 5:564—565. 1970.
19. Kashuk JL. Lilly JR: Esophageal atresia in father and son.
J Pediatr Surg 18:621 622. 1983.
20. Schimke RH. Leape LL, Holder TM: Familial occurrence of
esophageal atresia: A preliminary report. Birth Defects 8:22
23. 1972.
21. Klulh D: Atlas of esophageal atresia. J Pediatr Surg 1L90I —
919, 1976.
22. Eckstein HB. Somasuudarani: Multiple tracheoesophageal fistu-
las without atresia, report of a case. J Pediatr Surg 1:381
383. 1966.
23. Nakazato Y. Landing BH. Wells IR: Abnormal Auerbach ple-
xus in the esophagus and stomach of patients with esophageal
atresia and tracheoesophageal fistula. J Pediatr Surg 21:831 —
837. 1986.
24. Johnston PW. Hustings N: Congenital tracheoesophageal fistu-
la without esophageal atresia. Am J Surg 112:233- 240, 1966.
25. Grundy SR, Orringer MB: Esophageal motor dysfunction in an
adult with a congenital tracheoesophageal fistula. Arch Surg
120:182—183. 1985.
26. Romeo G. Zuccarello B, Proietlo F, Romeo C: Disorders of the
esophageal motor activity in atresia of the esophagus. J Pediatr
Surg 22:120-124, 198*7
27. Orringcr MB. Kirsh MM. Sloan H: Long-term esophageal functi-
on following repair of esophageal atresia. Ann Surg 186:436—
443. 1977.
28. Filston HC, Rankin JS. Kirks DR: The diagnosis of primary and
recurrent tracheoesophageal fistulas: Value of selective cathete-
rization. J Pediatr Surg 17:144—148„ 1982.
29. Davies MRQ. Cywes S: The flaccid trachea and tracheoesopha-
geal congenital anomalies. J Pediatr Surg 13:363—367. 1978.
30. Beasley SW. Myers NA: The diagnosis of congenital tracheoe-
sophageal fistula. J Pediatr Surg 23:415—417. 1988.
31. Holder TM. Ashcraft KW: Esophageal atresia and tracheoe-
sophageal fistula. Curr Probl Surg August: 1—68, 1966.
298 АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ
32. Holder TM, Cloud DT, Lewis JE Jr, Pilling GP IV: Esophageal
atresia and tracheoesophageal fistula. A survey of its members
by the Surgical Section of the American Academy of Pediatrics.
Pediatrics 34:542 549,1964.
33. Scott JS, Wilson JK: Hydramnios as an early sign of oesophage-
al atresia. Lancet 2:569, 1957.
34. Hertzbcrg BS, Bowie JD: Fetal gastrointestinal abnormalities.
Radiol Clin North Am 28:101 — 114. 1990
35. Kosloske AM, Jewell PF, Cartwright КС: Crucial bronchoscopic
findings in esophageal atresia and tracheoesophageal fistula.
J Pediatr Surg 23:466—470, 1988.
36. McKinnon 1J. Kosloske AM: Prediction and prevention of ana-
stomotic complications of esophageal atresia and tracheoesop-
hageal fistula- J Pediatr Surg 25:778—781, 1990.
37. Tam PKH, Chan FL, Saing H: Direct sagittal CT scan: A new
diagnostic approach for surgical neonates. J Pediatr Surg
22:397—400. 1987.
38. Ein SH, Stringer DA. Stephens CA. ct al.: Recurrent tracheoe-
sophageal fistulas. Sevenleen-year review. J Pediatr Surg
18:436- 441. 1983.
39. German JC, Ma hour GH, Woolley MW: Esophageal atresia and
associated anomalies. J Pediatr Surg 11:299—306, 1976.
40. Orvan L, Smith DW; I'he VATFR association: Vertebral de-
fects, anal atresia, T-E fistula with esophageal atresia, radial
and renal dysplasia: A spectrum of associated defects. J. Pedi-
atr. 104:7. 1973.
41. Manning PB. Morgan RA, Coran AG el al.: Fifty years’ experi-
ence with esophageal atresia and tracheoesophageal fistula.
Ann Surg 204:446 453. 1986.
42. Heyman MB, Berquist WE, Fonkalsrud EW. el al.: Esophageal
muscular ring and the VACTERL association: A case report.
Pediatrics 67:683—686, 1981.
43. Touloukian RJa Keller MS: High proximal pouch esophageal
atresia with vertebral, rib, and sternal anomalies: An additional
component to the VATER association. J Pediatr Surg 23:76—
79. 1988.
44. Weber TR, Smith W. Grosfcld JL: Surgical experience in infants
with the VATER association. J Pediatr Surg 15:849—854.
1980.
45. Spitz L. Kiely E. Brereton RJ: Esophageal atresia: Five year
experience with 148 cases. J Pediatr Surg 22:103 108, 1987.
46. Louhimo I, Lindahl H: Esophageal atresia: primary results of
500 consecutively treated patients. J Pediatr Surg 18:217—
229. 1983.
47. Bishop PJ, Klein MD, Philippart Al, et al.: Transpleural repair
of esophageal atresia without a primary gastrostomy: 240 pati-
ents treated between 1951 and 1983. J Pediatr Surg 20:823—
828. 1085.
48. Randolph JG. Newman KD, Anderson KD: Current results in
repair of esophageal atresia with tracheoesophageal fistula
using physiologic status as a guide to therapy. Ann Surg
209:524—531, 1989.
49. Fin SH. Shandling B. Wesson D. Filler RM: Esophageal atresia
with disial tracheoesophageal fistula: associated anomalies and
prognosis in the 1980’s. J Pediatr Surg 24:1055—1059, 1989.
50. Sillen U, Hagberg S. Rubenson A, Werkmaster K: Management
Of esophageal atresia: Review of 16 years’ experience. J Pedi-
atr Surg 23:805 809, 1988.
51. Wise WE. Caniano DA, Harmel RP Jr: Tracheoesophageal ano-
malies. In Waterston C: Neonates: A 30-ycar perspective. J Pe-
diatr Surg 22:526—529, 1987.
52. Holder TH, Ashcraft KW. Sharp RJ. Amoury RA: Care of in-
fants with esophageal fistula and associated anomalies. J I'ho-
rac Cardiovasc Surg 94:828—835, 1987.
53. Jones ТВ, Kirchner SG, Lee FA. Heller RM: Stomach rupture
associated with esophageal atresia, tracheoesophageal fistula
and ventilatory assistance. AJR 134:675—677, 1980.
54. Filston HC, Chitwood WR Jr, Schkolne B. Blackmon LR: The
Fogarty balloon catheter as an aid to management of the infant
with esophageal atresia and tracheoesophageal fistula complica-
ted by severe RDS or pneumonia. J Pediatr Surg 17:149—151.
1982.
55. Templeton JM, Templeton JJ, Schnaufer L, el al.: Management
of esophageal atresia and tracheoesophageal fistula in the neo-
nate with severe respiratory distress syndrome. J Pediatr Surg
20:394—397, 1985-
56. Fann JI, Hartman GE. Shochal SJ: “Walerseal” gastrostomy in
the management of premature infants with tracheoesophageal
fistula and pulmonary insufficiency J Pediatr Surg 23:29—31,
1988
57. Chiltmittrapap 8. Spitz L. Kiely EM, Brereton RJ: Anastomotic
stricture following repair of esophageal atresia. J Pediatr Surg
25:508—511. 1990.
58. Howard R, Myers NA: Esophageal atresia: A technique for elon-
gating the upper pouch. Surgery 58:725—727, 1965.
59. Puri P. Blake N, O’Donnell B, Guincy J: Delayed primary ana-
stomosis following spontaneous growth of esophageal segments
in esophageal atresia. J Pediatr Surg: 16:180—183, 1981.
60. l.ivaditis A: Esophageal atresia: A method of overbridging large
segmental gaps. Z Kinderchir 13:298—306. 1973.
61. deLorimier AA. Harrison MR: Long gap esophageal atresia.
J Thorac Cardiovasc Surg 79:138—141, 1980.
62. Shafer AD, David ТЕ: Suture fistula as a means of connecting
upper and lower segments in esophageal atresia. J Pediatr Surg
9:669 673. 1974.
63. Schullinger JN, Vinocur CD, Santulli TV: The suture fistula
technique in the repair of selected cases of esophageal atresia.
J Pediatr Surg 17:234—236, 1982.
64. Picretii R. Shandling B. Stephens CA: Resistant esophageal
stenosis associated with reflux after repair of esophageal atre-
sia: A therapeutic approach. J Pediatr Surg 9:355 357, 1974.
65. Myers NA, Beasley SW, Aukhsi AW: Secondary esophageal
surgery following repair of esophageal atresia with distal trac-
heoesophageal fistula. J Pediatr Surg 25:773—777, 1990.
66. Joley SG, Johnson DG. Roberts CC. el al.: Patterns of gastroe-
sophageal reflux in children following repair of esophageal
atresia and distal tracheoesophageal fistula. J Pediatr Surg
15:857—862, 1980.
67. Shermeta DW, Whitington PF, Seto DS, et al.: Lower esophage-
al sphincter dysfunction ib esophageal atresia: nocturnal re-
gurgitation and aspiration pneumonia. J Pediatr Surg 12:871 —
876. 1977.
68. Parker AF, Christie DL. Cahill JL: Incidence and significance of
gastroesophageal reflux following repair of esophageal atresia
and tracheoesophageal fistula and the need for anti-reflux pro-
cedures. J Pediatr Surg 14:5—8, 1979.
69. Ashcraft KW, Goodwin CD Amoury RA. Holder TM: Early
recognition and aggressive treatment of gastroesophageal ref-
lux following repair of esophageal atresia. J Pediatr Surg
12:317—321. 1977.
70. Curci MR, Dibbins AW: Problems associated with a Nissen fun-
doplication following tracheoesophageal fistula and esophageal
atresia repair. Arch Surg 123:618—620, 1988.
71. Thai AP: A unified approach to surgical problems of the esop-
hagogastric junction. Ann Surg 168:542—550, 1968.
72. Boix-Ochoa J: The physiologic approach Io the management of
gastric esophageal reflux. J Pediatr Surg 21:1032—1039. 1986.
73. Lindahl II. Rintala R. Louhimo I: Failure of ihe Nissen fundo-
plicalion to control gastroesophageal reflux in esophageal atre-
sia patients. J Pediatr Surg 24:985 987, 1989.
74. Filler RM. Rossel Io PJ. I ebowiiz RL: Life-threatening anoxic
spells caused by tracheal compression after repair of esophage-
al atresia: Correction by surgery. J Pediatr Surg 11:739—748.
1976.
75. Schwartz MZ, Filler RM: Tracheal compression as a cause of
apnea following repair of tracheoesophageal fistula: treatment
by aortopexy. J Pediatr Surg 15:842—848. 1980.
76. Benjamin B, Cohen D, Glasson M: Tracheomalacia in associati-
on with congenital tracheoesophageal fistula. Surgery 79:504—
508. 1976
АТРЕЗИЯ ПИЩЕВОДА И ТРАХЕОПИЩЕВОДНЫЕ АНОМАЛИИ 299
77. Wai loo MP, Emery JL: The trachea in children with tracheoe-
sophageal fistula. Histopathology 3:329—338, 1979.
78. Kimura K, Soper RT, Kao SCS, et al. Aortos tern ореху for trac-
heomalacia following repair of esophageal atresia: Evaluation
by Cinc-CT and technical refinement. J Pediatr Surg 25:769
772, 1990.
79. Myers NA: Oesophageal atresia with distal taclico-oesophagcal
fistula—a long-term follow up. Prog Pediatr Surg 10:5—17,
1977.
80. LeSoucf PN. Myers NA, I andau LI: Etiologic factors in long-
term respiratory function abnormalities following esophageal at-
resia repair. J Pediatr Surg 22:918 922, 1987.
81. Andrassy RJ, Patterson RS, Ashley J, et al.: Long-term nutritio-
nal assessment of patients with esophageal atresia and/or trac-
heoesophageal fistula. J Pediatr Surg 18:431—435, 1983.
82. Wolfson PJ, Schhins MD, Guttman FM, et al.: Laryngotrachcoc-
sophagcal cleft: An easily missed malformation. Arch Surg
119:228—230, 1984.
83. Hof E. Hirsig J, Giedion A. ct al.: Deleterious consequences of
gastroesophageal reflux in cleft larynx surgery. J Pediatr Surg
22:197—199, 1987.
84. Donahoe PK. Gee PE: Complete laryngotracheoesophageal
cleft: Management and repair. J Pediatr Surg 19:143—148.
1984.
85. Ryan DP, Miehrake, DD, Doody DP. ct al.: Laryngotracheoe-
sophageal cleft (type IV): Malignant repair of lesions beyond
the carina. J Pediatr Surg 26:962 970, 1991.
86. Hendren WH: Repair of laryngotracheoesophageal cleft using
interposition of a strap muscle. J Pediatr Surg 11:425—429,
1976.
Глава 23
ГАСТРОЭЗОФА ГЕ А ЛЬНЫЙ
РЕФЛЮКС
История. Гастроэзофагеальный рефлюкс (ГЭР)
представляет собой функциональное нарушение
с осложнениями, которые порой не имеют отноше-
ния к пищеводу. Как заболевание, а не просто
функциональное расстройство, ГЭР стал известен
педиатрам и детским хирургам сравнительно не-
давно. Классическое описание в 1947 г. данной па-
тологии и ее позиционной терапии (полусидячее
положение) принадлежит Neuhauser и Berenberg,
которые назвали эту болезнь термином «халазия».1
Наиболее ранние исследования Г ЭР в большин-
стве своем были проведены профессором Ivo Car-
re — педиатром, который работал в детском госпи-
тале Бирмингема (Англия), а в последующем
в течение многих лет — в Королевском детском
госпитале Белфаста. До того, как Карре описал
симптомы и объяснил их происхождение, для обо-
значения поздних проявлений ГЭР использовался
термин «врожденно короткий пищевод», посколь-
ку данная патология расценивалась как врожден-
ная аномалия пищевода.
Карре и его коллеги-рен ггенологи начали свою
работу с того, что стали обследовать детей с упор-
ными рвотами, с кровавыми рвотами и с отстава-
нием в развитии. Среди тех, у кого определялся
ГЭР, были выделены два типа больных. У боль-
шинства детей желудок частично располагался
в грудной клетке (ЧТЖ — частично торакальный
желудок) — патология, которую мы теперь назы-
ваем грыжей пищеводного отверстия диафрагмы.
У меньшей части больных с повторными рвотами
рентгенологически никакой анатомической патоло-
гии обнаружено не было, причем если эти паци-
енты находились преимущественно в вертикаль-
ном положении, то рвота у них не отмечалась.
Однако порой с течением времени развивался эзо-
фагит с укорочением и стенозом пищевода. В неко-
торых случаях наблюдалась рецидивирующая ле-
гочная инфекция.2 В первые годы работы Карре
хирургическое лечение при ГЭР проводилось ред-
ко, а потому имелась возможность наблюдать есте-
ственное течение процесса, которое тщательно ав-
тора м и доку менти рова л ось.3
Карре считал, что у 2/3 пациентов ГЭР исчезает
с введением твердой пищи, то есть обычно в возра-
сте около 2 лет. У одной же трети больных со вре-
менем не только не было улучшения, несмотря на
переход на твердую пищу, но даже отмечалось
ухудшение. Патологические симптомы при этом
держались и после 4 лет, причем в 5% случаев
развивался стеноз пищевода, а у остальных детей
отмечались рецидивирующая пневмония, анемия,
нарушения питания. 5% пациентов с ГЭР (не счи-
тая тех, что имели стеноз пищевода) умирали
именно от рефлюкса и вызванных им осложнений.3
В Великобритании ГЭР выявлялся и описывался
более часто, чем в США. Дело в том. что в Англии
родители стараются укладывать детишек спать
в положении на спине, что поддерживает ГЭР.3
В результате отсутствия представлений об этом
патологическом процессе появились публикации
о большом количестве пациентов, лечившихся
хирургическим путем в Детском Госпитале Лон-
дона (на Great Ormond Street) еще до того, как
данное заболевание стало распознаваться в этой
стра не.
Карре продолжал изучать эффект от введения
твердой пищи и позиционной терапии (полусидя-
чее положение) даже после того, как появились
публикации об успешном хирургическом лечении.
Около 1975 г. был описан способ рентгенологиче-
ского обследования, позволявший более тщательно
и достоверно диагностировать ГЭР.’ К этому вре-
мени были уже хорошо разработаны методы хи-
рургического лечения ГЭР и грыжи пищеводного
отверстия диафрагмы у взрослых.’ 1 Что же каса-
ется детей, то при хирургическом течении у них
отмечалась значительно более низкая летальность,
чем при длительной безуспешной консервативной
терапии.3 И хотя первая публикация серии наблю-
дений данной патологии (из Бостона) появилась
еще в 1944 г.,12 однако в ряд наиболее распростра-
ненных и серьезных хирургических заболеваний
у детей ГЭР был поставлен лишь после выхода
в печати в 1974 г. работы с анализом результатов
хирургического лечения большого количества слу-
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 301
чаев ГЭР в Детском Национальном Медицинском
Центре Вашингтона.13
Анатомия и функция пищеводно-желудочного
перехода. В отличие от сфинктеров, которые обра-
зованы анатомическими структурами, нижний эзо-
фагсальный сфинктер (НЭС) представляет собой
физиологический клапан, состоящий из трех ком-
понентов. Первый компонент — пищеводное отвер-
стие диафрагмы, а именно ее мышечные пучки,
огибающие это отверстие. Функция данной части
НЭС может нарушаться при грыже пищеводного
отверстия диафрагмы или при наличии неврологи-
ческих расстройств. Второй компонент клала иного
«устройства» — острый угол между желудком и
нижним отделом пищевода, известный как угол
Гиса, который при грыже пищеводного отверстия
увеличивается и вследствие этого не функциони-
рует как запирательный механизм. Третий и наи-
более важный компонент НЭС — зона высокого
давления в дистальном отделе пищевода, которая
никак не проявляется анатомически, но может
быть установлена манометрически, Частично эта
зона высокого давления расположена в средосте-
нии, непосредственно над пищеводным отверстием
диафрагмы, но основная, функционально важная
ее часть локализуется в брюшной полости.14
К рождению НЭС сформирован не полностью,
что является причиной часто наблюдающихся
у новорожденных срыгиваний. К 6 месяцу жизни
формирование НЭС заканчивается, а потому симп-
томы его дисфункции в более позднем возрасте,
как клинические, так и лабораторные, могут уже
рассматриваться как патологические.15
В ряде случаев ГЭР может расцениваться как
норма. Длительное измерение pH в пищеводе по-
казывает, что рефлюкс кислого желудочного со-
держимого в пищевод может возникать и у здо-
ровых людей под влиянием различных обстоя-
тельств. Однако в норме кислота быстро возвраща-
ется в желудок. Патологический рефлюкс может
быть частично обусловлен недостаточностью дви-
гательной активности пищевода.14 16
Два аспекта, анатомический и функциональный,
связанные с НПО, должны быть подчеркнуты.
Первый — роль в этиологии ГЭР грыжи пищевод-
ного отверстия диафрагмы или частичного распо-
ложения желудка в грудной клетке. Карре до сих
пор считает, что внимания заслуживает только тот
рефлюкс, который сочетается с ЧТЖ 17— точка
зрения, которая в значительной степени препятст-
вовала развитию методов активного и эффектив-
ного лечения ГЭР у детей. И даже если учитывать
существенно отличающиеся возможности разных
рентгенологов в отношении выявления грыжи пи-
щеводного отверстия диафрагмы, то в любом слу-
чае у большинства детей, имеющих рефлюкс
с клиническими проявлениями, рентгенологически
грыжа пищеводного отверстия диафрагмы не опре-
деляется. Второй фактор, касающийся функции
НПС, связан с положением, в котором дети спят.
ГЭР, несомненно, поддерживается и провоцируется
в положении на спине. Интересно, что безотноси-
тельно к ГЭР предпочтительнее положение ребен-
ка на живого, поскольку оно в принципе увеличи-
вает продолжительность и глубину сна и уменьша-
ет период беспокойства и плача 18
Патофизиология. Механизм действия НПС за-
ключается в том, что он пропускает пищевые мас-
сы в желудок и препятствует регургитации, удер-
живая тем самым кислоту в желудке. Каждый из
этих функциональных компонентов очень важен.
Недостаточность функции НПС приводит к разно-
образным клиническим проявлениям, которые
можно объединить в 3 группы симптомов: респира-
торные нарушения, расстройства питания и при-
знаки воспаления со стороны пищевода. Рентгено-
логическое исследование показывает, что в ряде
случаев рефлюкс бария в нижний отдел пищевода
может наблюдаться как нормальное явление у лю-
дей. подвергающихся обследованию верхних отде-
лов ЖКТ по поводу симптомов, нс имеющих отно-
шения к ГЭР. И 24-часовое измерение pH также
подтверждает, что кислое желудочное содержимое
может забрасываться в пищевод у здоровых
(в плане ГЭР) людей. Физиологический рефлюкс
от патологического отличает комбинация «дозы»
кислоты и скорости, с которой пищевод, благодаря
перистальтике, возвращает кислоту в желудок, не
давая ей возможности и времени для неблагопри-
ятного воздействия. Поэтому рефлюкс, который не
вызывает клинических проявлений, может рас-
сматриваться как физиологический. Патологиче-
ский же рефлюкс дает клиническую симптоматику.
Разнообразные механизмы, за счет которых реф-
люкс оказывает патологическое влияние, являются
предметом многочисленных клинических и лабора-
торных исследований.
Осложнения. Только тс больные, у которых есть
осложнения или симптомы ГЭР, нуждаются в об-
следовании и лечении. У большинства пациентов
обычно имеется не один симптом ГЭР, а некоторые
больные имеют все три проявления: эзофагит, рес-
пираторные осложнения и нарушения питания.
Респираторные проявления ГЭР обычно вклю-
чают апноэ,19 аспирационную пневмонию, кашель,
обструктивные заболевания дыхательных путей
и иногда бронхолегочную дисплазию.20,21 Бронхо-
легочные осложнения ГЭР были основным показа-
нием к хирургическому лечению примерно 55%
наших пациентов на ранних стадиях практики ле-
чения ГЭР (табл. 23-1).22
Механизмы, путем которых ГЭР вызывает ши-
рокий спектр респираторных расстройств, во мно-
гих случаях трудно объяснимы. По данным некото-
рых исследований, рефлюкс небольшого количест-
ва кислоты в нижние отделы пищевода приводит
к рефлекторному ларингоспазму и в результате
к обструктивному апноэ.23 Аутопсия детей, умер-
ших при явлениях синдрома внезапной смерти
(СВСД), подтверждает, что смерть могла насту-
пить в результате удушья. Установлено, что ла-
рингоспазм, возникающий в конце фазы выдоха,
быстро ведет к тяжелой гипоксии и СВСД.25 Со-
ответственно лари и гос паз м, вызванный рефлюк-
сом именно в этот важный момент респираторной
фазы, безусловно, может быть причиной внезапной
302 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
ТАБЛИЦА 23-1. Гастроэзофагеальный рефлюкс: симптомы-
ослож нения-показания операции
Покздення к операции Процент
Апноэ 22
Ложный круп кашель — удушье 11 52
Рецидивирующая пневмония 19
Боли в области пищевода 2
Кровотечение, анемия 1 7
Стеноз пищевода 4
Упорная рвота 35
Нарушения питания 19)
Неврологическая патология 6) 6
смерти при ГЭР. С другой стороны, ряд исследова
ний, проведенных среди детей, умерших при СВСД
или имевших тяжелое апноэ, расцененное как ост-
рое жизнеугрожающее состояние (ОЖУС), показа-
ли, что хотя ГЭР и мог быть у этих пациентов.
не обязательно совпадал с
но по времени он
апноэ.26'2
ГЭР выявляется, как правило, у детей, которые
дают апноэ во время пробуждения.28 У некоторых
из этих пациентов в анамнезе отмечалась гипоксе-
мия, связанная с эпизодами ГЭР,29 у других — ап-
ноэ, совпадавшее по времени со снижением внут-
рипросветного pH.
В группе пациентов с тяжелым апноэ, у которых
измерялось pH, у одной трети было отчетливое
снижение pH в пищеводе непосредственно перед
началом апноэ.30 Консервативное лечение оказа-
лось эффективным у 8 больных. Шестеро опериро-
ваны. У всех детей приступы апноэ прекратились.
Родители ребенка, лечившегося в течение 4 меся-
цев с применением позиционной терапии, прер-
вали лечение, несмотря на рекомендации врачей,
и через несколько дней ребенок умер при явлениях
СВСД.
В другой группе из 20 больных, умерших при
СВСД, ГЭР при жизни отмечался во время про-
буждения у 18 пациентов и во время сна — у 13,
хотя приступов апноэ в течение периода наблюде-
ния не было.31
ГЭР может быть причиной не только апноэ, но
и рефлекторного бронхоспазма или других реак
тивных состояний со стороны дыхательных пу-
тей.32 При обследовании 43 больных с обструктив-
ными бронхитами во всех случаях обнаружен сни-
женный тонус НПС. Из этих пациентов 20 лечи-
лись консервативно по поводу ГЭР с отчетливым
улучшением.33 В другом исследовании при хрони-
ческих заболеваниях дыхательных путей ГЭР (по
данным двух или более методов обследования) вы-
явлен в 63% наблюдений. Консервативное или хи-
рургическое лечение оказалось успешным и приве-
ло к ликвидации астмоподобного синдрома.3
Аспирация кислоты или желудочного содержи-
мого может быть причиной рецидивирующей пнев-
монии. Обследование больных с рецидивирующей
пневмонией выявило большую частоту у них ГЭР.
У этих пациентов тенденция к возникновению
рефлюкса и замедлению опорожнения пищевода от
кислоты отмечалась чаще всего во время сна. Воз-
можно, это как раз именно та самая категория па-
циентов, которые кашляют или дают приступы
удушья во время сна, либо засыпают хорошо, но
пробуждаются с симптомами ложного крупа, или
у которых периодически отмечается упорно реци-
дивирующая пневмония. s
Косвенным доказательством того, что хрониче-
ская пневмония может быть связана с ГЭР, явля-
ются наши собственные данные, касающиеся 154
больных с рецидивирующей пневмонией, у кото-
рых был выявлен ЮР и произведена фундоплика-
ция Почти у 92% детей пневмония в последую-
щем нс возникала. Именно такое процентное коли-
чество хороших исходов отмечено и в двух других
сериях исследований результатов хирургического
лечения ГЭР. По данным разных авторов, у
взрослых пациентов с повторными аспирациями
выявляется снижение показателей внутрипросвет-
ного pH, кислотный привкус во рту или кашель
и эпизоды удушья. Почти у 75% этих больных
отмечается также замедление опорожнения пище-
вода от кислоты, особенно в положении на спине.38
Очевидно, что для возникновения аспирационного
синдрома необходимо не только наличие рефлюк-
са, но сочетание его с нарушением перистальтики
пищевода. Хирургическая ликвидация рефлюкса
приводит к устранению аспирации.
Нарушения питания. ГЭР может быть столь
тяжелым, что проглоченная пища забрасывается
обратно из желудка в пищевод при самом мини-
мальном повышении внутрибрюшного давления.
В результате из-за срыгиваний маленькие дети не
получают достаточного количества пищи. Калори-
ческие потери, связанные с несостоятельностью
НПС, иногда приводят к задержке роста и разви-
тия ребенка. Однако такие дети относятся к той
категории пациентов, которые могут «перерасти»
рефлюкс. По мере роста они учатся есть помень-
ше, быть менее активными после еды и своевре-
менно распознавать (уметь чувствовать) возникно-
вение регургитации, что позволяет им снова по-
вторно проглотить пищу, не допустив рвоты.
У тех пациентов, которые изначально тщатель-
но разжевывают пищу и, почувствовав регургита-
цию, повторно проглатывают пищевой комок, рас-
познать рефлюкс не так-то легко. У таких боль-
ных никогда не бывает рвоты и кажется, что они
никогда не бывают голодными. Но аппетит у них
обычно все-таки снижен, поскольку содержимое
желудка постоянно рефлюксирустся и снова про-
глатывается, а соответственно нет нормального
опорожнения.
У некоторых пациентов ГЭР проявляется обыч-
ной рвотой. Это, как правило, малыши, начинаю-
щие ходить, или более старшие дети, которые без
каких-либо предвестников внезапно «выдают» же-
лудочное содержимое в виде рвоты. Нарушений
питания при этом может и не быть. И хотя в по-
добных ситуациях единственное проявление реф-
люкса является проблемой не столько медицин-
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 303
ской, сколько социальной (естественно, что повто-
ряющаяся рвота неприятна как для ребенка, так
и для родителей, и окружающих), тем не менее
хирургическое лечение требуется достаточно час-
то. Симптомы нарушения питания были главным
осложнением ГЭР у 40% наших больных (см.
табл. 23-1).22
Симптомы со стороны пищевода. Кислота
очень быстро вызывает раздражение слизистой пи-
щевода. У многих пациентов с ГЭР морфологиче-
ские проявления эзофагита могут быть подтверж-
дены с помощью биопсии. При тяжелой степени
эзофагита возникают боли в нижних отделах гру-
ди и верхних отделах живота, у маленьких детей
боли носят приступообразный характер. При от-
сутствии лечения прогрессирующий эзофагит, а
соответственно повторяющийся процесс воспале-
ния и рубцевания, может привести к развитию
стриктуры. Редко встречаются два других проявле-
ния тяжелого рефлюкса — укорочение пищевода
и замещение его слизистой в нижнем отделе слизи-
стой желудочного типа.
Го, что раньше определялось термином «врож-
денно короткий пищевод», в действительности ино-
гда является приобретенной патологией в виде со-
четания расширенного пищеводного отверстия
диафрагмы и мышечного укорочения пищевода,
недостаточно прочно фиксированного в нижней
части. У ребенка подобная ситуация может возник-
нуть с поразительной быстротой. Ни один из на-
ших двух пациентов с коротким пищеводом не
имел стриктуры пищевода. Оба были успешно из-
лечены, благодаря трансабдоминалыюй пластике
пищеводного отверстия и фундопликации. Не-
сколько описанных ранее случаев короткого пище-
вода, возможно, были связаны с его укорочением
в результате эзофагита, поскольку в этих наблю-
дениях иногда имелась стриктура.
Метаплазия слизистой нижнего отдела пищево-
да, когда она замещается желудочной слизистой,
вызывается, согласно существующим предположе-
ниям, рефлюксом и известна под названием «пи-
щевод Барретта». Данная патология отличается от
врожденно короткого пищевода тем, что при ней
желудочно-пищеводный переход располагается на
своем месте, а не над диафрагмой, как при врож-
денно коротком пищеводе. Есть сообщения о том,
что успешное лечение ГЭР приводит к восстанов-
лению нормальной слизистой пищевода/9 однако
возможность подобного преобразования признает-
ся не всеми.40
Другое необычное проявление эзофагита изве-
стно как синдром Сандифера (Sandifer). Считает-
ся, что он связан с рефлюкс-эзофагитом.41 Этот
синдром выражается в принятии больным причуд-
ливой позы и в произвольных («извивающихся»)
движениях головы, шеи и иногда туловища. По-
добные дистонические движения способствуют
улучшению перистальтики нижнего отдела пище-
вода.42 От этого необычного состояния можно изба-
виться, если вылечить эзофагит, что было проде-
монстрировано в исследованиях из Госпиталя на
Great Ormond Street и двумя другими авторами.
облагавшими небольшим количеством наблюде-
ний. 1 J 4 Подтверждено это также и нашим соб-
ственным скромным опытом.
По мнению многих хирургов, равно как и по
моему собственному (см. главу 21), при отсутст-
вии адекватного лечения ГЭР может привести
к ахалазии.45
У 8% наших больных показанием к лечению
ГЭР послужил эзофагит (см. табл. 23-1).22
Связь ГЭР с атрезией пищевода. Симптомы
ГЭР со стороны пищевода иногда возникают у де-
тей. оперированных по поводу атрезии пищевода
и трахеопищеводного свища. Рефлюкс кислоты
в пищевод может вызвать рецидивирующий стеноз
зоны анастомоза. ' Предрасположенность к реф-
люксу и в результате к анастомотической стрикту
ре связана у этих детей как с укорочением пище-
вода, свойственным этим аномалиям, так и с нару-
шением перистальтики нижнего его отдела, прак-
тически всегда наблюдающимся у пациентов с АП
и ТПС. Выявление рефлюкса, если он есть, позво-
ляет намного более эффективно лечить стенозы
анастомоза.
В одном из сообщений описывались множествен
ныс эпизоды пневмонии у детей, перенесших опе-
ративные вмешательства по поводу АП и ТПС.4°
У этих больных, имевших низкий тонус НПС, от-
мечался хороший эффект при медикаментозном
лечении ГЭР.
Причины гастроэзофагеального рефлюкса. Бо-
льшинство детей с ГЭР нс имеют рентгенологиче-
ских симптомов грыжи пищеводного отверстия
диафрагмы. Что же за нарушения в таком случае
лежат в основе дисфункции НПС у этих пациен
тов? У больных с неврологическими расстройства-
ми причиной рефлюкса может быть замедленное
опорожнение желудка. К сожалению, при наличии
тяжелого ГЭР точное измерение скорости опорож-
нения резко затруднено. Поэтому для подобных
ситуаций была разработана специальная методика
исследования, цель которой — решить вопрос о
том, следует ли при лечении рефлюкса дополнять
фундопликацию вмешательствами, ускоряющими
опорожнение желудка, или нет.4’ Некоторые счита-
ют, что сочетание замедленного опорожнения же-
лудка и рефлюкса у неврологических пациентов
представляет собой часть общей проблемы, прису-
щей этим больным и связанной с нарушениями
двигательной активности всей «передней кишки».50
В любом случае замедленное опорожнение желуд-
ка установлено у 1/3 — 1/2 пациентов с ГЭР,
имевших клинические его проявления. К сожале-
нию, нет сведений о том. проводилось ли лечение
всех этих детей. Есть другая сторона данного во-
проса — если встать на ту точку зрения, что за-
медленное опорожнение желудка должно быть по-
казанием к выполнению соответствующего дрени-
рующего опера гивного вмешательства (направлен-
ного на ускорение опорожнения), то это может
привести к возникновению противоположной проб-
лемы, обусловленной развитием после операции
демпинг-синдрома (ускоренное опорожнение).19
Установлено, что гастростомия, производимая
304 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
как оперативным путем, так и с помощью эндоско-
пической техники, (1) увеличивает («открывает»)
угол Гиса, (2) понижает тонус НПС и (3) умень-
шает его длину (протяженность).' В одном из
исследований, проведенном у детей, оперирован-
ных по поводу АП и ТПС, отмечено, что из
25 больных, которым была сделана гастростома,
у 18 (72%) развился выраженный ГЭР, причем
10 из них потребовали оперативного вмешатель-
ства. Среди же 26 пациентов без гастростомы кли-
нически значимый ГЭР возник только у 8 (30%),
а операция потребовалась четверым. Таким обра-
зом, возникновение и частота ГЭР после лечения
АП могут быть связаны не только с укорочением
пищевода и нарушением его двигательной актив-
ности, но и непосредственно с фактом выполнения
гастростомии.53
К ГЭР склонны также больные с неврологиче-
скими расстройствами. Во многих публикациях от-
мечается, что большинство пациентов, требующих
хирургического лечения ГЭР, — неврологические
больные. Механизм возникновения у них ГЭР не
известен, хоти нет сомнения, что расстройства со
стороны ЦИС иногда оказывают влияние на двига-
тельную активность всей «передней кишки».50
Каков бы ни был механизм ГЭР у этих больных,
поводом для обращения к хирургу в большинстве
случаев является необходимость в наложении га-
стросгомы для питания. Гастростомия раньше де-
лалась до выявления ГЭР, который как раз и был
порой главным проявлением неврологических рас-
стройств двигательной активности. В результате
больные выписывались после операции с мини-
мальным улучшением питания, а иногда и наобо-
рот — с фатальными последствиями рефлюкса. За-
тем стало популярным во время наложения гастро-
стомы (для питания) делать фундопликацию («до-
полнять» гастростомию фундопликацией) для того,
чтобы предотвратить рефлюкс и избежать таким
образом повторной операции. Однако в послеопе-
рационном периоде очень большой проблемой
у этих детей стала задержка опорожнения желуд-
ка, которая была причиной рвот и нараставшего
истощения.
И в настоящее время продолжаются исследова-
ния, направленные на установление факторов, от-
ветственных за опорожнение желудка. Теперь всем
неврологическим больным, которым показано на-
ложение гастростомы для питания, проводится из-
мерение pH в верхних отделах ЖКТ и исследуется
характер опорожнения желудка, что позволяет ре-
шить вопрос о том, следует или нет дополнять
гастростомию вмешательством на кардиальном
или, наоборот, — на пилорическом отделе желуд-
ка. В одном из таких исследований, проведенном
у 46 неврологических больных, ГЭР выявлен
у 30 пациентов, соответственно во всех этих случа-
ях гастростомия была дополнена операцией Ниссе-
на. У троих из этих больных отмечался рецидив
рефлюкса, причину которого не удалось устано-
вить. У 16 из 46 пациентов при дооперационном
обследовании показатели pH были нормальными,
однако в четырех из этих наблюдений ГЭР развил-
ся после гастростомии, что но требовало в дальней-
шем фундопликации по Ниссену.4 В (ругой груп-
пе из 5 больных с нормальными показателями pH
до гастростомии ГЭР возник после операции
у всех без исключения, что соответственно явилось
показанием к фундопликации по Ниссену. Опера
ция была отложена в среднем на год до улучшения
состояния и достижения стойкой прибавки массы
тела.55
ГЭР отмечается у 10% больных с пилоростено-
зом.4 Кроме того, при обследовании 74 пациентов,
перенесших фундопликацию но Ниссену, у 40 па-
циентов были выявлены различные нарушения ро-
тации кишечника, выраженные в той или иной
степени.56 Большинству из этих больных потребо-
валась операция Ледда. Подобные наблюдения по-
зволяют высказать мысль о том, что пороки маль-
ротации могут играть определенную причинную
роль в отношении ГЭР.
Имеются сообщения и о том, что среди больных,
выживших после операции по поводу врожденной
диафрагмальной грыжи, почти у 3/4 выявлен ГЭР
и расширение пищевода, связанные, по-видимому,
с внутриутробно развившейся или ранней после-
операционной обструкцией кишечника.57
Диагностика. Обследование с целью выявления
или исключения ГЭР проводится обычно только
в том случае, когда предполагается, что ГЭР явля-
ется причиной имеющихся у больного симптомов.
Осложнения ГЭР столь разнообразны и часто, ка-
залось бы, настолько не связаны с функцией желу-
дочно-пищеводного перехода, что диагностика по-
рой требует в основном интуитивного подхода
и «полета» врачебной мысли в значительно боль-
шей степени, чем это присуще врачам догоспи
тального этапа. Именно поэтому некоторые педи-
атры утверждают, что «никогда не видят» больных
с ГЭР.
Очень важно иметь правильные клинические
представления о рефлюксе. Если малыш, сидящий
спокойно (просто сам или на коленях у мамы),
продолжает упорно срыгивать желудочным содер-
жимым на свой нагрудник (иногда даже через не
сколько часов после кормления), это означает, что
у него имеется ГЭР. Послужат ли осложнения или
симптомы этого рефлюкса основанием для обсле-
дования и лечения, зависит от того, насколько
тщательно собирается анамнез. С таким ребенком
родители могут прийти к педиатру на плановый
профилактический осмотр и в анамнезе при этом
не будет респираторных заболеваний, кратковре-
менных приступов удушья или любого иного про-
явления ГЭР. А другой ребенок иногда находится
под наблюдением детского хирурга по поводу па-
ховой грыжи, и у него в анамнезе отмечаются
явные, достаточно серьезно выраженные симпто
мы ГЭР
Пять методов диагностики наиболее широко
применяются при обследовании детей, у которых
подозревается ГЭР: рентгенологическое обследова-
ние пищевода с барием, мониторинг pH в пищево-
де, гастроэзофагеальная сцинтиграфия, эзофагс-
альная манометрия и эндоскопия (иногда с био-
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 305
пеней). Эти методы различаются по степени инва-
зивности, диагностическим возможностям и стои-
мости.
Эзофагография с барием была введена в прак-
тику в 1947 г.’ Если она производится опытным
рентгенологом^ *го диагностическая ценность ее
очень велика. Однако даже при наличии за-
ключения рентгенолога о том, что «данных за ГЭР
нет», клиницист все-гаки не должен снимать свои
подозрения, если заполненные барием пищевод
и желудок образуют фигуру «слона с поднятым
хоботом» (рис. 23-1) 60 или если на отсроченной
рентгенограмме барий остается все еще в пищево-
де, хотя виден уже и в тонкой кишке (рис. 23-2).
У больных с четкими клиническими данными за
рефлюкс (и его осложнения) рентгенологическое
исследование дает положительные результаты в
86% случаев, у остальных 14% пациентов рентге-
нологическая картина нормальная. При отсутствии
осложнений рефлюкса рентгенологически он под-
тверждается значительно реже — в 30—50% слу-
чаев. Это, конечно, не значит, что результаты об-
следования ошибочны — просто при наличии реф-
люкса он нс всегда улавливается в момент рентге-
Рис. 23-1. Конфигурация пищеводно-желудочного перехода в
виде туловища слона (в профиль) с поднятой головой — симп-
том «ревущего слона». (Rowen SJ, Gyepcs MT: The “irumpcting-
elephanf" sign of gastrocsophagcul reflux. Radiology 127:735—740,
197Я.)
Puc. 23-2. Исследование с барием. Барий хорошо заполняет
тонкую кишку, хотя все еще находится и н пищеводе = важный
признак, позволяющий заподозрить ГЭР. Подобная отсроченная
рентгенограмма обычно делается через 15—20 мин после дачи
бария.
нографии.61’62 Поэтому, если есть четкие анамне-
стические данные за выраженный рефлюкс, то
отсутствие его рентгенологических проявлений не
должно позволять снимать подозрения и требует
проведения повторного исследования. Если же кли-
нически отчетливый рефлюкс выявлен также
и рентгенологически, то обычно для подтвержде-
ния диагноза применяют дополнительные методы
обследования, хотя в подобных ситуациях в этом
нет особой необходимости.24 63
У детей с ГЭР необходимо также оценить ха-
рактер опорожнения желудка — выше говорилось
о замедлении этого процесса при ГЭР и о возмож-
ном сочетании рефлюкса с нарушениями рота-
ции. * Хотя исследование с барием и не является
количественным методом определения скорости
опорожнения желудка, однако опытные рентгено-
логи часто могут достаточно достоверно судить
о нарушениях двигательной активности антраль-
ного отдела, что, несомненно, оказывает опреде-
ленную помощь хирургу.
Измерение pH в просвете пищевода проводится
двумя способами. Во-первых, это может быть кратко-
временное исследование, называемое тестом Tuttle.
И во-вторых — более тщательное продолжитель-
ное измерение, впервые описанное в 1974 г.65
В последующем была предложена модификация
метода длительного мониторинга pH примснитель-
20 Заказ № 1622
306 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
66. 67
но к использованию его в педиатрии. В настоя-
щее время это исследование проводится на протя-
жении суток.
При суточном мониторинге врач, проводящий
исследование, отмечает эпизоды рефлюкса в дис-
тальный отдел пищевода, о чем обычно говорит
снижение показателей pH до 4 и меньше. Реги-
стрируется, как правило, общее количество реф-
люксов, число эпизодов продолжительностью бо-
лее 5 мин, длительность самого большого эпизода,
средняя продолжительность рефлюкса, а также об-
щее время исследования, в течение которого pH
было ниже 4. Для количественной оценки ГЭР эти
показатели учитываются в совокупности.
Контрольные исследования, проведенные у де-
тей в Мехико, позволили установить нормальные
показатели pH и верхние границы нормы, в срав-
нении с которыми и оценивались данные, получен-
ные у детей с подозрением на ГЭР.68 В ранние сро-
ки после приема пищи не выявлено статистически
достоверной разницы показателей pH у нормаль-
ных детей и «рефлюксирующих», но больные с па-
тологическим рефлюксом, в отличие от контроль-
ной группы, продолжали «рефлюксировать» даже
после того, как желудок, казалось бы, должен был
уже давно опорожниться.
Однако более современные исследования, прове-
денные у маленьких детей, выявили значительную
разницу в характере рефлюкса в раннем периоде
после приема пищи между контрольной группой
и пациентами, имевшими клинические проявления
ГЭР.6’ Эти данные меняют представление о значе-
нии измерения pH, позволяя говорить о достаточно
высокой чувствительности этого метода.
Прежние попытки установить специфичность
и чувствительность суточного измерения pH за-
труднялись тем, что раньше ни в одно из исследо-
ваний не были включены здоровые дети в качестве
контрольной группы. Тем не менее сейчас уже не
вызывает сомнения, что выявляемость ГЭР с по-
мощью этого теста составляет приблизительно
90 95%. Большинство исследователей считают,
что длительное измерение pH — лучший и единст-
венно достоверный метод оценки ГЭР. И главная
его ценность — в возможности усовершенствова-
ния. Однако корреляции между количественными
показателями и тяжестью симптомов не выявлено
ни по нашему опыту, ни по данным литера-
туры.70, 71
Попытки усовершенствовать метод длительного
измерения pH с целью установления соответствия
его показателей различным симптомокомплексам,
связанным с подозреваемым ГЭР, давали порой
очень противоречивые результаты. Например, из-
мерение pH с помощью 4-каналыюго телеметри-
ческого устройства, предназначенного для амбула-
торной практики, выявило у пациентов с респи-
раторными симптомами значительные изменения
показателей pH в верхних и средних отделах пище-
вода и почти нормальные — в дистальной его
части.
Объяснение этому феномену, возможно, лежит
в том, что дыхательные расстройства при ГЭР мо-
гут быть обусловлены нарушением двигательной
активности именно средних и верхних отделов
пищевода, в то время как дистальная его часть
быстро опорожняется от заброшенной туда кисло-
ты. Показатели pH ниже 4 в дистальном отделе
пищевода очень четко соответствовали данным
биопсии, выявившей в этой зоне эзофагит.74 У не-
врологических больных попытки сопоставления
показателей pH в среднем и дистальном отделе
пищевода с целью отдифференцировать патологи-
ческий рефлюкс от «физиологического» не позво-
лили получить сколько-нибудь значимых и убеди-
тельных данных в этом отношении.73
Мониторинг pH во время сна дает различные
результаты у больных с респираторными симпто-
мами и у тех, что имеют другие проявления ГЭР,
хотя современные исследования говорят о том, что
все пациенты именно ночью склонны иметь реф-
люкс более частый и выраженный. Техника изме-
рения pH не оказывает существенного влияния на
достоверность получаемых результатов, ибо ни
один из электродов или записывающих устройств
не обладает какими-либо преимуществами перед
другими. Доказано, что амбулаторные методы
мониторинга, такие, например как 4-канальная те-
леметрия, безусловно, являются высокоэффектив
ными и точными в оценке рефлюкса.
В диагностике ГЭР может использоваться также
эзофагеальная манометрия. Однако этот метод до-
ставляет неудобство больному, а потому редко при
меняется. Некоторые хирурги пользовались мано-
метрией для интраоперационной оценки эффектив-
ности фундопликации.80, 1 В настоящее время дан-
ное исследование редко применяется и с этой целью.
Эзофагеальная сцинтиграфия как метод диа-
гностики ГЭР и особенно выявления аспирации
желудочного содержимого, оценивается одними8
весьма высоко, другие83 же считают, что она не
имеет совершенно никакого значения. Истинная
ценность этого метода остается пока неясной.84
Эзофагоскопия, по нашему мнению, диагности
чески мало значима. Главная область ее примснс
ния выявление эзофагита и лечение стриктур
пищевода, связанных с ГЭР. Что же касается био-
псии пищевода, то она может быть сделана и без
эзофагоскопии с помощью специального вакуум
аспирационного устройства. Наиболее важное зна-
чение биопсия имеет при выборе метода хирурги-
ческого лечения, когда хирургу необходимо знать,
есть или нет у больного эзофагит, осложнением
которого, особенно при неадекватном лечении, мо-
жет быть стриктура пищевода.
Таким образом, наша диагностическая тактика
при подозрении на ГЭР предполагает прежде всего
эзофагографию с барием, которая проводится
рентгенологами, придерживающимися принципов
изложенных в работе Darling и McCauley.3’ Если
анамнестически проявления ГЭР слабо выражены
и рентгенологически рефлюкс не выявлен, этим
обследованием мы ограничиваемся. Если же кли-
нически ГЭР был значительным, то, независимо от
того, подтвержден он рентгенологически или нет,
мы в большинстве случаев проводим далее суточ-
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 307
ное измерение pH с целью количественной оценки
рефлюкса- Этот тест имеет особо важное значение
в тех случаях, когда имевшиеся симптомы ГЭР
сохраняются и после его лечения (консервативного
или хирургического). Наличие в такой ситуации
нормальных показателей pH говорит о том, что,
по-видимому, не рефлюкс был причиной клиниче-
ской симптоматики. Обязательно также обследова-
ние (с барием) желудка (скорости его опорожне-
ния) и 12-перстной кишки.
Даже при установленном диагнозе рефлюкса
имеющиеся у больного клинические симптомы мо-
гут быть проявлением совсем иной патологии. Об
этом особенно важно помнить при обследовании
детей с астмой или апноэ, когда предполагается,
что причиной данных респираторных расстройств
является рефлюкс.
выбор метода лечения при гастроэзофагеаль-
ном рефлюксе. Позиционная терапия. Как кон-
сервативный, так и хирургический метод лечения
ГЭР развивались в процессе наблюдения за есте-
ственным течением заболевания. К факторам, ко-
торые уменьшают проявления рефлюкса, относятся
вертикальное положение больного, снижение объ-
ема и увеличение густоты содержимого желудка,
изменение образа жизни, включая выбор опреде-
ленных видов пищи. Все эти составляющие позво-
ляют сделать симптомы ГЭР менее выраженными,
а порой даже приводят к их исчезновению. Осно-
вой консервативного лечения, безусловно, является
позиционная терапия.
Данные измерения pH показывают, что у боль-
ных с респираторными проявлениями рефлюкса он
чаще всего возникает, когда ребенок лежит в кро-
вати в горизонтальном положении на спине или
животе.’6 С началом активного применения пози-
ционной терапии стало ясно, что возвышенное по-
ложение (под углом в 60’), поддерживаемое круг-
лосуточно, у 65% больных отчетливо уменьшает
симптомы рефлюкса в любом состоянии (при про-
буждении, во время сна, во время еды). Наиболь-
шим антирефлюксным эффектом обладает поло-
жение лицом вниз с приподнятой на 30° верхней
частью туловища. ’ 7 Кроме того, такие положение
значительно уменьшает и беспокойство ребенка.88
Манометрическая оценка состояния НПС пока-
зала, что позиционная терапия никоим образом не
влияет на протяженность НПС. Следовательно, ее
эффект связан, по-видимому, с гравитационным
фактором. Подтверждается это и тем, что когда
позиционная терапия прекращается, рефлюкс воз-
никает с прежней интенсивностью.
Клиническое улучшение при проведении пози-
ционной терапии наступает довольно быстро. По-
этому некоторые исследователи считают, что если
имеющиеся симптомы нс исчезают в течение 2 не-
дель от начала лечения, то продолжать позици-
онную терапию не имеет особого смысла.89
Во время проведения позиционной терапии реко-
мендуется, не ограничиваясь клинической оценкой,
измерять также pH для тот, чтобы быстро устано-
вить — эффективно лечение или нет и соответст-
венно выделить больных, нуждающихся в хирурги-
ческом вмешательстве, и тех, кто хорошо подда-
ется консервативному лечению.90 Одна из проблем,
связанных с позиционной терапией, состоит в том,
что если уж она начата и эффективна, то должна
продолжаться неопределенно долго. Однако если
примерно до 6 мес жизни дети спят на специаль-
ном «антирефлюксном» щите или стульчике доста-
точно спокойно, то по мере роста и взросления
такое положение начинает их раздражать. Попыт-
ки найти компромисс, приподнимая головной ко-
нец обычной кроватки на 15 см, достаточно бес-
смысленны. поскольку гравитационный эффект
при таком небольшом наклоне мал или вообще
отсутствует. Кроме того, во время сна в обычной
кроватке, даже с приподнятым головным концом,
беспокойные детишки в поисках наиболее удобно-
го положения часто поворачиваются, оказываясь
в результате лежащими вообще поперек кроватки.
Возникновению рефлюкса, безусловно, способст-
вует повышение и нт ра гастрального давления, а
потому еще один важный компонент консерватив-
ной терапии ГЭР — употребление густой пищи не-
большими порциями, что в некоторой степени
уменьшает рефлюкс. Однако это порой не очень
полезно для больного и не всегда ему помогает.90
Кроме того, трудно регулировать («точно настро-
ить») эту терапию, подбирая именно ту по густоте
пищу, которая необходима данному больному, ибо
никем не проводилось сравнительное изучение по-
казателей pH у детей, питавшихся густой и обыч-
ной пищей. Кроме того, один из нежелательных
отрицательных побочных эффектов питания гус-
той пищей, особенно когда в качестве «загущаю-
щего» агента используется рис, состоит в том, что
иногда при таком питании развивается ожирение,
причем достаточно тяжелое.
Позиционная терапия в сочетании с употребле-
нием густой пищи может дать возможность ребен-
ку «перерасти» рефлюкс.85 В ряде работ, основан-
ных, правда, на небольшом материале, отмечается,
что у 90% детей симптомы при таком лечении
исчезали к 12—15 месяцам жизни. Поэтому сто-
ронники данного метода рекомендуют не предпри-
нимать попыток хирургического лечения раньше
15 месяцев.91 Они считают также, что добавлять
к проводимой терапии (с целью усиления ее эф-
фекта) лекарственные препараты опасно.
Лекарственное лечение. Медикаментозное ле-
чение ГЭР подразумевает применение антацидных
препаратов и группы лекарств, предназначенных
для усиления перистальтики пищевода, увеличе-
ния тонуса НПС и ускорения опорожнения желуд-
ка. Именно эти виды воздействия лекарственных
веществ особенно желательны.
В одной из ранних работ по изучению лекарст-
венной терапии при ГЭР у детей, лечившихся по-
зиционным методом, отмечался хороший эффект
при использовании эфира холина бетансхола (bet-
hanechol),92 который рекомендуется применять в
течение 3—4 месяцев. Этот препарат резко увели-
чивает тонус НПС и усиливает перистальтику пи-
щевода, что было- подтверждено и дальнейшими
исследованиями, * хотя некоторые авторы утвер-
308 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
ждают, что общая продолжительность рефлюкса
(по данным длительного измерения pH) сущест-
венно при этом не меняется. Большинство гастро-
энтерологов и детских хирургов считают, что бега-
нехол не обладает серьезным эффектом при ГЭР
у детей. Во всяком случае, нет очевидных доказа-
тельств его эффективности.
Для лечения больных с ГЭР применяется также
церукал, усиливающий перистальтику пищевода
и повышающий тонус НПС. Считается, кроме то-
го, что это — лучший из препаратов, способствую-
щих ускорению опорожнения желудка.’5 В проти-
вовес данному мнению, в некоторых исследованиях
показано, что этот препарат, обладая перечислен-
ными достоинствами, не приводит тем не менее
к существенному уменьшению рефлюкса.96
Церукал имеет серьезные побочные эффекты.
При проведении одного из обширных исследова-
ний, направленных на изучение его действия
с предполагавшимся двойным слепым контролем,
авторы вынуждены были исключить из планируе-
мой группы пациентов 2/3 больных, поскольку ро-
дители отказались от предложения дават» детям
этот препарат, ибо имели уже в прошлом нега-
тивный опыт его применения.” У троих из остав-
шегося небольшого количества детей, получавших
церукал (с двойным слепым контролем), лечение
пришлось прервать из-за побочных эффектов, за-
ключавшихся в заторможенности, диарее, экстра-
пирамидальных нарушениях, дистонии, которые
к тому же, как выяснилось, могут быть необрати-
мычи.’1-1™ Кроме того, хотя церукал и увеличива-
ет перистальтику пищевода, усиливает тонус НПС
и ускоряет опорожнение желудка, однако сущест-
венного снижения количества эпизодов рефлюкса
97
при этом не отмечается.
Уменьшает продолжительность наиболее дли-
тельных эпизодов рефлюкса,” нс оказывая сущест
венного влияния на количество этих эпизодов,100
нсхолинергический стимулятор перистальтики пи-
щевода и тонуса НПС cisapride. Этот препарат не
применяется в США, но интенсивно использовался
и изучался в Европе, при этом не обнаружено по-
бочных эффектов.” По данным одного из исследо-
ваний, лечение цизапридом привело к исчезнове-
нию рефлюкса и кашля в ночное время у 12 из
13 больных, имевших хронические респираторные
расстройства. Эти авторы, однако, применяли ci-
sapride не дольше 1 ме< яца. К сожалению, обследо-
вание в отдаленные сроки не было проведено, а по-
тому не известно, сохранился ли полученный эф-
фект после окончания лечения и полностью ли
были ликвидированы дыхательные расстройства.111
При проведении другой серии исследований дей-
ствие этого препарата изучалось у 22 маленьких
детей, имевших ГЭР (подтвержденный измерением
pH) с ночными проявлениями, причем у 8 паци-
103
ентов отмечались жизнеугрожающие состояния.
В процессе лечения эпизоды апноэ уменьшились
значительно. В одном случае применение цизапри-
да у ребенка, который лечился позиционным мето-
дом, было прокрашено. Больной умер через неде-
лю при картине СВСД.30 Будет ли когда-либо ci-
sapride выпушен для клинического применения
в США, пока не известно.
Результаты консервативного лечения ГЭР очень
вариабельны по данным разных авторов. Карре
продолжает считать, что даже при наличии у боль-
ных с ГЭР «анатомической» грыжи пищеводного
отверстия диафрагмы хирургическое лечение не
показано, за исключением редких случаев, когда
развиваемся стеноз пищевода.104 Другие авторы
при наблюдении в течение от 1 года до 12 лет за
детьми с грыжей пищеводного отверстия диафраг-
мы, диагностированной в раннем возрасте, отмеча-
ли, что во всех случаях, где наблюдался эффект от
консервативной терапии, он наступал довольно
быстро — в течение первых 2 недель лечения. По-
зиционное лечение проводилось у этих пациентов
на протяжении нескольких месяцев, однако 34 из
75 болы ых все же потребовали оперативного ле-
чения.105
В одной из более поздних работ дан анализ ре-
зультатов лечения 126 детей, у которых диагноз
рефлюкса был подтвержден рентгенологическим
исследованием с барием, данными эндоскопии,
сцинтиграфии и у некоторых пациентов — измере-
нием рП Позиционная терапия сочеталась с меди-
каментозным лечением с последующим длитель-
ным наблюдением. К 1,5-годовалому возраст'
у 81% детей симптомы исчезли. Оперативное вме
шательство в конце концов потребовалось 23 пащ
ентам (18%). Два ребенка продолжали получать
медикаментозную терапию более длительно, чем
рекомендовалось врачами, тем не менее симптомы
держались у них и после 2 лет.
По видимому, эти последние цифры (достаточно
высокие) более точно отражают реальное положе-
ние вещей в отношении ча< готы ГЭР, чем данные
многих других ранее проведенных исследований.
Подтверждается это и обзором, представленным
Институтом социальных исследований Гэллапа,
где указывается, что 13% взрослого населения
Америки страдает от изжоги, отмечающейся 2—
3 раза в неделю. Менее же частые эпизоды изжоги
возникают у намного большего числа людей.
Следующий пример иллюстрирует, насколько дли-
тельно симптомы ГЭР могут быть скрытыми и не-
распознанными, прежде чем проявляются яркой
клинической картиной.
Этот пример относится к тому времени, когда ГЭР еще нс
появился в клинической практике как самостоятельная нозоло
гическая единица. Значительно отстававший в развитии маль-
чик сам с детства приспособился предотвращать ерьпивавия,
принимая при их приближении более вертикальное положение.
В возрасте 10 лет впервые возникла пневмония, потребовавшая
госпитализации и применения пенициллина (вн/м 8 раз в день
через каждые 3 часа). Затем пневмония “Повторилась еще два-
жды. Оба раза проводилось стационарное лечение — в 17 лет
и в 23 года.
Хронический эзофагит давал иеодиократно резкие обостре
ния пекле нарушения диеты и употребления блюд индийской
кухни. Много ночей больной проводил, сидя в кресле и прини-
мая таблетки гавискона (гидроокись алюминия с трнсиликатом
магния) для того, чтобы уменьшить изжогу. Кульминацией бо-
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 309
ЛСЗКИ был эпизод л арннгоспазмн, который заставил обратиться
к врачу. В конце концов в возрасте 41 года пациент был про-
оперирован. Произведена фундопликация, приведшая к оконча-
тельному и полному излечению.
По понятным причинам количество (в процент-
ном выражении) американцев, у которых рефлюкс
возникает в детстве и продолжается в зрелом воз-
расте, не известно и нс может быть, к сожалению,
подсчитано.
Хирургическое лечение. Критерии, которыми
руководствуются хирурги при решении вопроса об
оперативном лечении ГЭР. настолько сложны
и многочисленны, что почти не поддаются анали-
зу. В детской хирургии практически нет, пожалуй,
никакой другой патологии, при которой столь раз-
ные факторы определяли бы показания к хирурги-
ческому вмешательству. Кроме того, существенное
влияние на решение вопроса об операции оказыва-
ет удовлетворенность или неудовлетворенность
врачей догоспитального этапа и гастроэнтерологов
результатами консервативной терапии вообще,
а не только у данного больного, а также отноше-
ние хирургов к оперативному лечению ГЭР. Это
отношение бывает очень разным. Одни хирурги
крайне неохотно соглашаются оперировать боль-
ных с ГЭР,106 в то время как другие с энтузиазмом
подходят к хирургическому лечению, считая, что
фундопликация — единственный способ эффектив-
ной коррекции данной патологии.’07
Выбор метода хирургического вмешательства
при ГЭР зависит от состояния (протяженности)
внутрибрюшного отдела пищевода. Соответствен-
но операция может заключаться просто в гастро-
пексии. с помощью которой пищеводу придается
нужное положение, без создания манжетки в обла-
сти дна желудка.108 Большинство вмешательств,
в том числе и гастропексия, обычно дополняются
пластикой диафрагмы, направленной на умень-
шение размеров пищеводного отверстия. При га-
стропсксии желудок фиксируют либо к передней
брюшной стенке (по Вогеша), либо кзади (по
Хиллу).
Что касается фундопликаций, направленных не
только на придание соответствующего положения
внутриабдоминальной части пищевода, но и на со-
здание угла Гиса, то существует два основных ви-
да подобных вмешательств — фундопликация по
Ниссену с «окутыванием» пищевода по всей окруж-
ности на 360° и фундопликации по Талю (Thai)
с созданием неполной манжетки. Операция Нис-
сена применяется более широко, однако в боль-
шинстве случаев при ней полностью устраняется
физиологический рефлюкс, а соответственно и воз-
можность возникновения рвоты. Операция Таля,
изначальным сторонником которой являюсь я и
мои коллеги, почти всегда сохраняет для больного
возможность (в случае необходимости) опорожне-
ния желудка путем рвоты. Сравнение результатов
и осложнений после этих двух вмешательств бу-
дет проведено в данной главе ниже. Однако сразу
следует подчеркнуть, что оценка эффективности
хирургического лечения очень существенно зави-
сит от трактовки и понимания хирургами сути дан-
ной патологии.
Задача детских хирургов при лечении ГЭР —
сделать так, чтобы ребенок стал настолько «нор-
мальным» в анатомическом и физиологическом от-
ношении, насколько это возможно. Мы считаем,
что операция Таля решает эту задачу наилучшим
образом. В сочетании с пластикой диафрагмы дан-
ное вмешательство позволяет уменьшить до «нор-
мы» размеры пищеводного отверстия, обеспечить
интраабдоминальное положение дистального отде-
ла пищевода и воссоздать угол Гиса. Таким обра-
зом, эта операция, в отличие от многих других
вмешательств, создает (восстанавливает) нормаль-
ные анатомо-физиологические взаимоотношения
внутренних органов. Кроме того, для пациента со-
храняется возможность возникновения не только
рвоты, но и физиологического рефлюкса. Этими
достоинствами операции 'Галя объясняется пред-
почтение, которое мы ей отдаем, а также наш
принципиально активный подход к хирургическо-
му лечению ГЭР.
Многие хирурги, производящие операцию Нис-
сена. также занимают активную позицию в отно-
шении хирургического течения ГЭР, понимая при
этом, что эффективность данного вмешательства,
как никакого другого, можно оценивать лишь
с учетом отдаленных результатов. Трудно сказать,
когда наиболее выгодно делать фундопликацию
у детей. Несомненно, ясно одно — при проведении
этой операции в детском возрасте значительно
меньше шансов на неудачу и развитие осложнений
в раннем послеоперационном периоде и в отдален-
ные сроки, чем при коррекции ГЭР у взрослых.
Что касается нашей «философии» в отношении
хирургического лечения ГЭР, то ее кратко выра-
зил Skinner. Он сказал, что главный спорный во-
прос не в том, создает ли фундопликация по Нис-
сену наиболее прочный антирефлюксиый меха-
низм (это доказано клиническими и эксперимен-
тальными исследованиями), а в том, может ли
менее «тесная» частичная фундопликация в соче-
гании с перемещением интактной стенки пищевода
в интраабдоминальное положение (что, как извест-
но, также играет роль в рсфлюкснохм механизме)
сделать го же самое, но при этом с меньшей опас-
ностью развития острого расширения желудка
и с сохранением возможности возникновения у
больного отрыжки и рвоты.11,1
Техника фундопликации по Ниссену детей опи-
сывалась многократно (рис. 23-3). ° Мы приме-
няем исключительно фундопликацию по Талю с
некоторыми модификациями (рис. 23-4). 1
Показания к оперативному лечению ГЭР под-
разделяются на «абсолютные» и «относительные».
К абсолютным мы относим эпизоды апноэ, требу-
ющие реанимации (это как раз те больные, кото-
рые умирают при явлениях СВСД или ЖУС), ре-
цидивирующую или длительно текущую пневмо-
нию, эзофагит (диагностированный клинически,
эндоскопически или но данным биопсии), неэф-
фективность консервативной терапии (позицион-
ное и медикаментозное лечение). Относительными
310 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
Рис. 23-3. Фундопликация по Ниссену.
А, Разрез брюшиой стенки поперечный
иди продольный. Дистальный отдел пище-
вода освобожден и пищеводное отверстие
ушито (сужено) вокруг пищевода, в кото-
ром находится буж соответствующего для
данного возраста размера. Селезенка от-
делена от желудка путем перевязки и про-
шивания (со стороны стенки желудка) ко-
ротких желудочных сосудов.
В, Дно желудка проведено позади внут-
рибрюшпого отдела пищевода.
С, Между желудком и передней стенкой
пищевода для их сближения наложены от
дельные серо-ссрозиые швы (2, 3 млн 4).
Следует избегать повреждения блуждающе-
го нерва.
D. Швы последовательно завязаны.
Ер Фундопликация закончена. Буж уда-
лен из пищевода.
показаниями являются астмоподобный синдром,
ложный круп, ночной кашель, эпизоды удушья,
хроническая рвота.
Поскольку после операции Таля, которую мы
применяем, практически нет летальности, а коли-
чество осложнений в ближайшие и отдаленные
сроки после операции невелико, врачи догоспи-
тальной службы в нашем регионе и гастроэнтеро-
логи не увлекаются длительной консервативной
терапией ГЭР и рано направляют пациентов на
хирургическое лечение.
Мы считаем, что длительное проведение (доль-
ше 6 мсс) позиционной терапии редко бывает эф-
фективным, вызывая к тому же состояние диском-
форта у ребенка и беспокойство у родителей, а по-
тому лучший метод лечения ГЭР у детей в возра-
сте старше 6 мес — хирургический. Операция, бе-
зусловно, не должна откладываться до 1—1,5 лет.
Большинство пациентов, обращающихся к нам,
обычно уже получали медикаментозное лечение
и позиционную терапию, но без эффекта. Однако
если до поступления консервативное лечение не
проводилось, разумеется, мы с него начинаем, ожи-
дая улучшения в течение 2 недель. Если за этот
срок симптомы ГЭР сохранились и эффекта от
консервативной терапии нет, то операцию прово-
щи сразу, не откладывая.
В обычных случаях ребенок, которому планиру-
ется фундопликация по Талю в нашем госпитале,
поступает утром, в день операции. Лично я счи-
таю, что назогастральный зонд следует ставить
только на время вмешательства и удалять его на
операционном столе по окончании операции. На
следующее утро ребенка начинают кормить и вы-
писывают через 48 час после вмешательства. Мои
коллеги, придерживающиеся более консерватив-
ных взглядов, оставляют назогастральный зонд на
ночь и приступают к кормлению через 24 часа.
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 311
Рис. 2.1-4. Фундопликация по Талю. Л, Связочный аппарат между левой полей печени и нижней поверхностью диафрагмы разделя-
ют, начиная со свободного края печени, расположенного ближе к селезенке. Печень теперь может быть отведена книзу и вправо,
что позволяет подойти к пищеводному отверстию.
В, Сделан поперечный разрез над пищеводно-желудочным переходом. Край пшценодною отнсрстия поднимают, чтобы выделить
пищевод с обеих сторон.
С, Под пищевод подводят диссектор, при этом надо стремиться оставить блуждающий нерв на мышечной стенке пищевода.
D. После удаления диссектора под пищевод подводят дакроиовую держалку, что позволяет оттягивать пищевод книзу, в то
время как край пищеводного отверстия поднимают кверху. Это помогает освободить дистальную часть пищевода для смещения
ее в ннтраабдоминальиое положение.
Е, Для сближения позади пищевода ножек диафрагмы накладывают 8-образный шов шелком 2-0 на кардиоваскулярной игле.
F. Таким же швом фиксируют пищевод сзади к краю пищеводного отверстия. Этот ограничивающий шов не только уменьшает
возможность возникновения послеоперационной грыжи пищеводного отверстия, но и позволяет лучше фиксировать внутрибрюш
ную часть пищевода.
2 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
Рис. 2Л-4 (продолжение).
G. Концы да кроновой держалки разводят таким образом, что-
бы желудок .между НИМИ МОЖНО было «индиинуты» 1121 пищевод
и подшить к переднем его стенке. При осуществлении фундоп-
ликации этим методом нет необходимости в перевязке коротких
желудочных сосудов.
Н, Собствен и о фундопликацию осуществляют с помощью не-
прерывного шва, который накладывают, начинах с большой
кривизны пищеводно-желудочного перехода и постепенно сбли-
жая свободную стенку желудка с пищеводом вдоль его левой
стороны, продвигаясь вверх к пищеводному отверстию. Для
этого шва мы предпочитаем использовать нить Gore-Tex.
I, В непрерывный шов захватываю! желудок, пищевод н край
пищеводного отверстия.
J. Непрерывный шов идет поперек передней стенки пищевода.
Каждый стежок соединяет желудок, пищевод и кран пищеводно-
го отверстия диафрагмы.
К, Непрерывный шов завершают иа малой кривизне пище-
вод но-желудочного перехода. Дииия шва имеет вид переверну-
той буквы Ь. Штриховые линии показывают положение пище-
вода по отношению к пищеводному отверстию и дну желудка.
Назогастральный зонд, который находится в желудке во время
операции, может быть удален сразу по окончании вмешатель-
ства либо оставлен до следующего дня. После удаления зоила
начинают кормление.
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 313
Иногда ребенка оставляют в больнице на 3 дня.
В процессе дальнейшего наблюдения за больным,
через 3—4 месяца после операции, проводится об-
следование с барием, цель которого — определить
состояние манжетки и убедиться в отсутствии реф-
люкса, а также в том, что не развилась параэзо-
фареальная грыжа пищеводного отверстия диа-
фрагмы (рис. 23-5). В тех случаях, когда после
операции вновь возникли какие-либо проявления
рефлюкса или имевшиеся симптомы ликвидирова-
ны не полностью, предпринимается исследование
pH. Если в отда пенные сроки (в любое время)
отмечается рецидив симптомов, которые были до
операции, либо возникают какие-то иные сложно-
сти, следует повторно, тщательно, с самого начала
проанализировать данный случай.
При оценке результатов хирургического лечения
ГЭР учитывается, во-первых, ликвидирован ли
рефлюкс, и, во-вторых, исчезли или нет его кли-
нические проявления. Мы изучали отдаленные
результаты в сроки от 1 года до 8 лет после опе-
рации, сопоставляя их с проявлениями рефлюкса,
послужившими показанием к хирургическому ле-
чению. Полученные данные представлены в табли-
це 23-2. Упорная рвота исчезала абсолютно у всех
детей сразу после операции. Нарушения питания
удалось полностью корригировать в 97% наблюде-
ний. Это позволяет предположить, что у осталь-
ных 3% больных эти нарушения были связаны нс
с рефлюксом, а с иными причинами. Ликвидация
апноэ (а соответственно профилактика СВСД
и Ж УС) достигнута в 95% наблюдений. Респира-
торные симптомы купированы у 92% из тех паци-
ентов, которые страдали от крупа, кашля или
удушья, и у 91% детей с хронической, тяжелой
или рецидивирующей пневмонией.
Менсе 1 % больных утратили после операции
возможность опорожнять желудок с помощью
рвоты. Кроме того, из 1150 наших пациентов, опе-
рированных к настоящему времени, у 2% возник
рецидив грыжи пищеводного отверстия диафрагмы
и еще у 2% — рецидив ГЭР, связанный с несостоя-
тельностью фундопликационных швов. В одном
случае сформировался небольшой перипликацион-
ный абсцесс, потребовавший повторной операции,
Рис. 23-5. Послеоперационное соотношение пищевод» и желуд-
ка имеет сходство с нормальным углом Гиса. Нижняя часть пи-
щевода располагается в брюшной полости, а желудок по отно-
шению к нему приподнят, что создает как бы клапанный меха-
низм.
во время которой швы были распущены, а абсцесс
дренирован. У одного больного отмечалось рас-
хождение краев раны брюшной стенки. В 6 наблю-
дениях (0,05%) развилась кишечная непроходи-
мость, один из этих пациентов умер. В двух случа-
ях возник синдром острого расширения желудка
(рис. 23-6), оба пациента были излечены путем
декомпрессии желудка с помощью назогастраль-
ного зонда на фоне уменьшения (в течение не-
скольких дней) объема энтерального питания.
Многие среди наших пациентов, которым произво-
дилась фундопликация, имели неврологические
расстройства. Специальные аспекты, касающиеся
этой категории больных, будут обсуждены позже.
Низкая частота развития у наших больных по-
слеоперационной кишечной непроходимости связа-
на, возможно, с тем. что мы (1) используем верхний
ТАБЛИЦА 23-2. Результаты фундопликации ип Талю у 335 пациентов
Кол-во больных Кол-во обследованных после операции Ошибки диагностики Неэффективность первой операции Первично хорошие результаты Окончательные удоЕл. результаты
кол-во процент кол-во процент? КОЛ-ВО процент кол-во процент
Апноэ 80 80 4 5 4 5 72 90 76 95 Кашель удушье—круп 49 42 2 5 2 5 38 90 40 95 Рецидивирующая пнев- мония 74 71 6 8 3 4 62 88 65 92 Эзофагит 26 26 1 4 2 8 23 88 25 96 Упорная рвота 58 54 0 3 6 51 94 54 100 Нарушения питания 66 57 2 3 3 5 52 92 55 97 Истощение 2 2 0 0 2 100 2 100 Нарушения со стороны ЦНС 7 7 0 0 7 100 7 100 Всего 362 335 15 5 17 5 303 90 320 95
314 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
Рис. 23-6. А, Через 3 суток посте операции у ребенка возникло острое расширение желудка (синдром большого газового пузырик
связанное с невозможностью опорожнения желудка рвотой- Кратковременная декомпрессия желудка позволила справиться с этой
ситуацией.
В. Обследование с барием через 6 мес не выявило ни стеноза, ни рефлюкса.
поперечный разрез при лапаротомии, (2) во время
операции постоянно «работаем» выше поперечно-
ободочной кишки, (3) стараемся не касаться тон-
кой кишки и делать так, чтобы она не появлялась
в ране, (4) не предпринимаем никаких дополни-
тельных вмешательств и (5) оперируем макси-
мально быстро.
Столь же низкая частота спаечной гонкокишеч-
ной непроходимости отмечается и после гастропек-
сии по Bogema в отличие от фундопликации по
Ниссену, после которой это осложнение развива-
ется значительно чаще.113 Так, по данным одного
из исследований, среди 156 больных, оперирован-
ных по Ниссену, тонкокишечная непроходимость
возникла в 10,3% случаев. Возможно, в большинст-
ве из этих наблюдений осложнение было связано
не с фундопликацией непосредственно, а с выпол-
нявшимися одновременно аппендэктомией, опера-
цией Ледда (при мальротации) или гастростомией.
У тех же больных, которым производилась только
операция Ниссена, ни с чем не сочетавшаяся, ки-
шечная непроходимость отмечена в 1,8% случа-
ев.64 В двух наблюдениях это осложнение привело
к летальному исходу. Согласно суммарным дан-
ным еще 6 серий исследований по изучению ре-
зультатов операции Ниссена, частота тонкокишеч-
ной непроходимости колебалась от 2,1% до
10% — среди 1319 больных осложнение развилось
у 43 (3,2%) пациентов (табл. 23-3).
В упомянутых 6 сериях исследований частота
послеоперационного рецидива грыжи пищеводного
отверстия диафрагмы или несостоятельности ман-
жетки после фундопликации по Ниссену колеба
лась от 1 до 27%. Среди 1114 больных эти два
у 79 пациентов, т. е- в сред-
5. 113 118 124
осложнения отмечены
нем в 6,4% случаев.
Истинную частоту развития после фундоплика-
ции по Ниссену синдрома острого расширения же-
лудка установить трудно, поскольку некоторые хи-
рурги у детей в возрасте до 3 лет одновременно
с операцией Ниссена традиционно накладывают
декомпрессионную гастростому на короткий, а по-
рой и на достаточно длительный промежуток вре-
мени. Другие же гастростомию не делают. В одном
из наблюдений среди 106 пациентов двоим потре-
бовалась повторная операция — гастростомия в
связи с синдромом острого расширения желудка.117
По данным других авторов, оперировавших 420
пациентов, гастростомия производилась всем детям
в возрасте до 3 лет, но несмотря на это, у 12 боль-
ных после удаления гастростомической трубки
развился данный синдром.104 Еще в одной работе
отмечается, что среди 100 больных проблемы, свя-
занные с расширением желудка в раннем или
позднем послеоперационном периоде, возникали
в 7% случаев.”6 А но данным авторов, анализиро-
вавших отдаленные результаты у 191 пациента,
два летальных исхода наступили в результате не-
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 315
ТАБЛИЦА 23-3. Осложнения фундопликации по Ниссену (по данным литературы)
Автиры Год Кол-во пациен- тов Послеопе- рационная грыжа пи- щеводного отверстия Несостоя- тельность манжетки Кишечная нспрохо- 1HMOCTI. Расширение желудка Смерть Примечания
Alriibcciih, cl al.118 1988 55 15 11 - — — В 14 из 15 случаев первоначально не были сделана пластика ножек диаф- рагмы
Davidson. Hurd, Jonstone 131 1987 20 — — 2 (10%) — — Включая 4 пациенток с пищеводом Барретта, у которых слизистая под- верглась обратному развитию
Dedinsky, et al.115 Fonkalsrud, ct al.109 1987 1989 429 408 11 29 (6,7%) 18 (4,2%) 9 (2.1%) 12 NA Многим больным с послеоперационной грыжей пищеводного отверстия пер- воначально ис делалась пластика но- жек диафрагмы
Lcape, Kamenofsky 1,6 1980 НЮ 1 (1%) — 3 (3%) 5 (5%) 1 (1%) У двух пациентов была несостоятель- ность in нов, потребовавшая повтор- ной операции
Spitz, Kiria ne 117 1985 IU6 7 (7%) — 5 (5%) 2 (2%) 5 (5%) По данным другой работы Spitz, часто- та кишечной непроходимости (в ре- зультате «других вмешательстве во вре- мя операции Ниссена) составила 10%
Jolley, et al.”4 1986 210 — — 13 (6,2%) Все случаи кишечной непроходимости были у пациентов, которым одновре- менно с операцией Ниссена произво- дилась гастростомия
Turnage, et al.124 ВСЕГО 1989 46 2 (6%) 2 (6%) 36 42 78/1144 (6,8%) 4 (13%) 42/1319 (3,2%) 3 (8%) 22/660 (3,3%) NA Только 35 пациентов обследовались в отдаленном периоде, по отношении! к этому количеству и высчитывались проценты
криза желудка, возникшего из-за невозможности
опорожнить его путем рвоты.119 Еще двое больных
умерли при явлениях кишечной непроходимости
после операции Ниссена, когда невозможность воз-
никновения рвоты привела к острому необратимо-
му расширению и некрозу желудка и 12-перстной
кишки.120 В одном из научных (и в какой-то степе-
ни философских) трудов, опубликованном в
1985 г., было высказано предположение, что синд-
ром расширения (или, как его еще называют, боль-
шого газового пузыря) желудка — не острое, а хро-
ническое состояние, связанное с операцией Ниссена.
Кстати, в подтверждение тому, в литературе есть
описание случая, когда ощущение дискомфорта,
вызванное этим осложнением, вынуждало больного
кусать губы (для того, чтобы не показать свои
страдания) до такой степени, что возникло их изъ-
язвление. Оперативное устранение произведенной
во время первого вмешательства фундопликации
ликвидировало это состояние дискомфорта, и паци-
ент перестал кусать губы. Все вышесказанное по-
зволяет говорить о том. что фундопликация в мень-
шем объеме,121 т. е. создание неполной манжетки
(в отличие от полной манжетки при операции Нис-
сена), является более разумным подходом при хи-
рургическом лечении ГЭР.
Наш опыт хирургического лечения ГЭР состоит
из 1166 фундопликаций (до 1990 г. включитель-
но): 16 — по Ниссену и 1150—по Талю. Двое
больных умерли от кишечной непроходимости, по
одному в каждой группе. У первого из этих паци-
ентов, оперированного по Ниссену, в результате
кишечной непроходимости возникла, несмотря на
наличие манжетки, рвота и аспирация, от которой
ребенок и умер. Второй больной через две недели
после операции Таля поступил в другой госпиталь
в связи с рвотами, о чем мы, к сожалению, не зна-
ли. У ребенка развилась механическая тонкоки-
шечная непроходимость, нераспознанная своевре-
менно и приведшая к гангрене кишки. К тому вре-
мени, когда с нами проконсультировали ребенка
и мы приготовились его повторно оперировать, со-
стояние уже было крайне тяжелым, с явлениями
нспоцдающегося коррекции ацидоза.
Результаты лечения ГЭР на первых этапах на-
шей работы в этом направлении в большинстве
случаев были оценены в отдаленные сроки после
операции, как это показано в таблице 23-2.
Хорошие результаты лечения ГЭР у детей с хро-
ническими легочными симптомами получены в
90—92% случаев, при упорных рвотах — в 100%,
при апноэ —около 90% и при эзофагите — около
100%. Те наблюдения, когда оперативное вмеша-
тельство не привело к улучшению состояния,
позволяют предполагать, что хотя эти больные
и были оперированы по поводу рефлюкса, однако
нельзя с уверенностью сказать (и это не было до-
стоверно доказано), что именно рефлюкс явился
316 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
Рис. 23-7. В возрасте 1 месяца
ребенку по поводу пилоростеноза
была произведена пнлоромиото-
мия, а в 2 месяца — фундопли-
кация по 'Галю. Эта рентгено-
грамма с увеличением сделана в
возрасте 10 лет. Видна полноцен-
ная фундопликация с размерами
почти как у взрослого человека.
причиной имевшихся до операции клинических
симптомов. Поскольку собственно
ГЭР ликвидирован практически у всех этих паци-
ентов, следовательно, неуспех операции связан ско-
рее всего с ошибками в определении показаний
к вмешательству, так как клинические симптомы,
по-видимому, были обусловлены не рефлюксом.
В литературе имеются сообщения о количествен
ной оценке результатов хирургического лечения,
в частности, путем определения функции НПС 125
и измерения pH.12* Полученные данные в общем
соответствуют результатам клинического обследо-
вания. Изучение эффективности фундопликации
в отдаленные сроки (более, чем через 10 лет после
операции) показывает, что созданный антиреф-
люксный механизм обычно выполняет свою функ-
цию в течение всего периода роста и развития
детей, и манжетка также растет вместе
с ростом ребенка (рис. 23-7).
Повторные операции. За все годы нашей рабо-
ты повторное вмешательство после операции Таля
потребовалось пяти пациентам, у которых сохраня-
лись патологические симптомы (у троих — респи-
раторные, у двоих с неврологическими расстрой-
ствами— упорная рвота). Всем этим детям при
повторном вмешательстве сделана операция Ниссе-
на, но нс потому, что были какие-либо проблемы
с наложенной во время первой операции манжет-
кой, а просто для большей надежности, поскольку
неполная манжетка по Талю у этих больных не
обеспечила ликвидации клинических проявлений
(табл. 23-4). Из 15 детей, оперированных по Нис-
сену (на ранних этапах нашей работы), по-
вторно оперировать пришлось двоих. Им была
«распущена» манжетка (в связи с выраженной об-
струкцией дистального отдела пишевода) и сдела-
на операция Галя. Кроме того, несколько больных
были оперированы нами повторно по Талю после
неудачного вмешательс гва по Ниссену, произве-
денного в других учреждениях. В литературе так-
же есть сообщение об отсутствии эффекта от фун-
допликации по Ниссену у 116 взрослых пациентов,
которым было произведено повторное вмешатель-
ство, но уже по Талю.12* По данным других авто-
ров. из 364 детей, перенесших фундопликацию по
поводу ГЭР, в 21 случае потребовалась повторная
операция. У 15 из этих больных первоначально
была сделана фундопликация по Ниссену, пяте-
ТАБЛИЦА 23-4. Обобщенный опыт по фуи допликацням
Children's Mercy Hospital 1973—1990 гг.
Kansas City, Missouri
1166 фундопликаций—1125 пациентов
Фундопликация по Талю — 1150
45 повторных операций (3,9%)
5 — но Ниссену*
40 — по Талю**
Фундопликация по Ниссену 16***
3 повторные операции (18,7%)
2 по Талю
1 — по Ниссену
* У двух тяжелых неврологических больных после опера-
ции по Талю были упорные рвоты, при повторном гмешатель-
стве сделана операция Ниссена с постоянной гастростомой.
•• У одного из этих пациентов была атрезия пищевода
с трахеопищеводным свищом и микрогастриев. Свищ трижды
рецидивировал. Ребенку 4 раза пе ,алась операция Таля. В кон-
це концов бг.ла сделана пластика тоастокишечним транспланта-
том и операция увеличения (п ластика) желудка. Двум тяжелым
невролщ ическим больным операция Таля производилась триж-
ды (каждому). Таким образом трем пациентам было сделано
10 операций Таля (из общего количества 1150).
*•* Включая 5 пациентов, которым после операции Таля
была сделана фундопликация по Ниссену.
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 317
рым из них при повторной операции манжетка по
Ниссену «переведена» в манжетку по Талю.
Стеноз пищевода. Больные с ГЭР, у которых
прогрессирующий эзофагит приводит к стриктуре,
после успешной а нт и рефлюкс ной операции часто
требуют длительной эндоскопической дилатации.
Проводить ее следует с большой осторожностью во
избежание «разрыва» манжетки. Лучшим метолом
бужирования в таких случаях является баллонная
дилатация. Дистальную часть баллона устанавли-
вают на уровне стриктуры, но нс ниже пищеводно-
го отверстия. Стенозы, которые не поддаются бу-
жированию и не могут быть резецированы с нало-
жением анастомоза, а потому требуют пластики
пищевода, обсуждаются в главе 21.
Метаплазия слизистой, вызванная рефлюксом
(пищевод Барретта), иногда после успешной фун-
допликации подвергается обратному развитию, од-
нако это может и не произойти.
В одной из работ, освещающей вопросы лечения
пищевода Барретта у 4 детей, после успешной фун-
топликации отмечена регрессия, подтвержденная
эндоскопически.131 Аналогичные результаты (вос-
становление нормальной слизистой, по данным эн-
доскопии и биопсии) были описаны и у 10 взрос-
лых пациентов.39 В других же исследованиях, в ча-
стности у авторов, оперировавших 88 взрослых
больных, подобный благоприятный исход не на-
блюдался.132 Более того, эти авторы рекомендуют
проводить больным с пищеводом Барретта ежегод-
ную эндоскопию для своевременного выявления
малигнизации.133
Микрогастрия. ГЭР, связанный с малыми раз-
мерами желудка, отмечается в основном у больных
с АП и ТПС. Среди наших наблюдений в одном
случае микрогастрия была причиной трехкратной
безуспешной фундопликации по Талю. Несмотря
на проведенные операции, клиническая симптома-
тика у этого ребенка продолжала нарастать. У па-
циентов с маленьким желудком, по-видимому, бо-
лее предпочтительна передняя фундопликация, по-
скольку в таких случаях желудка «не хватает» для
создания полной манжетки. ГЭР, сочетающийся
с АП, обсуждается в главе 22.
Неврологические расстройства. Осложнения
и симптомы ГЭР у детей с неврологическими рас-
стройствами бывают такими же, как и у невроло-
гически нормальных пациентов, однако осложне-
ния встречаются намного чаще. Некоторые иссле-
дователи утверждают, что нарушения со стороны
ЦНС ведут к генерализованным изменениям дви-
гательной активности верхних отделов пищевари-
тельного тракта.50 В ряде работ отмечается, что
среди детей, подвергавшихся фундопликации, бы-
ли исключительно больные с неврологическими
расстройствами, причем общее количество наблю-
дений у этих авторов достаточно большое. К хи-
рургу такие пациенты обычно направлялись в свя-
зи с показаниями к гастростомии для питания.
Установлено, что гастростома для питания, создан-
ная как эндоскопически чрескожным способом, так
и при обычной открытой операции, уменьшает то-
нус НПС, выпрямляет угол Гиса и тем самым спо-
собствует возникновению ГЭР. Мы уже прошли
через тот период, когда у любого неврологического
ребенка гастростомия для питания автоматически
дополнялась фундопликацией.
У некоторых больных развивался «желудочный
дистресс-синдром», который был, по-видимому,
вызван задержкой опорожнения желудка. Мы, как
и другие хирурги, в настоящее время у невроло-
гических больных, прежде чем наложить гастро-
стому для питания, проводим рентгенологическое
исследование с барием, 24-часовое измерение pH
и часто сци нт и граф» ию, чтобы определить скорость
опорожнения желудка и соответственно решить,
каким должен быть объем вмешательства: только
гастростомия, гастростомия с фундопликацией или
с фундопликацией и пилоропластикой.51 К сожале-
нию, очень трудно бывает предугадать — разо-
вьется рефлюкс или нет у больного, которому про-
изводится только гастростомия.134
Проблема аспирации у неврологических боль-
ных не ликвидируется путем фундопликации, по-
скольку аспирация слюны или проглоченной жид-
кости может продолжаться в той или иной степени
даже при отсутствии (по данным обследования)
рефлюкса.135 При измерении pH в пищеводе
у 32 детей с неврологической патологией, которым
были поставлены показания к гастростомии, у 23
(72%) выявлен выраженный ГЭР. Из этих боль-
ных 22 пациентам произведена фундопликация
и наложена гастростома для питания. У одного
ребенка с диагностированным при обследовании
рефлюксом антирефлюксная операция не была
сделана, в результате развилось тяжелое осложне-
ние в виде постгастростомического рефлюкса. Из
9 пациентов, не имевших по данным обследования
рефлюкса, у 6 он развился после операции, что
было подтверждено измерением pH. Таким обра-
зом, у неврологических больных, которым пока-
зана гастростомия, необходимо дополнять это вме-
шательство антирефлюксной операцией.
По данным других авторов, у всех 57 неврологи-
ческих больных (половина общего числа пациен-
тов за 4-летний период, которым была произведе-
на фундопликация) до операции наблюдалась рво-
та. Большинство детей отставали в физическом
развитии или имели рецидивирующую пневмонию.
Реже отмечались эзофагит, грыжа пищеводного
отверстии» диафрагмы, эпизоды апноэ или стрик-
тура пищевода. Стандартное консервативное лече-
ние ГЭР проводилось у 46 из 57 пациентов, однако
эффекта не было, что достаточно характерно для
неврологических больных. Постоянная гастростома
наложена 50 больным из 57. Четверым пациентам
была сделана фундопликация по Ниссену, однако
без достаточного эффекта, что потребовало в двух
из этих случаев повторной антирефлюксной опе-
рации (с хорошими окончательными результата-
ми — клинические проявления исчезли). Авторы
данного исследования рекомендуют дополнять га-
стростомию для питания фундопликацией по Нис-
сену.136
Обследование 90 неврологических больных, у
которых фундопликация по Ниссену сопровожда-
316 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
лась гастростомией, показало, что осложнений при
этом было не больше, чем после операции Ниссена
у неврологически здоровых детей.137 Другие же ис-
следователи утверждают, что у неврологических
пациентов осложнения развиваются в два раза ча-
ще и в 4 раза чаще требуются повторные опера-
ции.138 Хотя последние авторы и говорят о значи-
тельно более высоком проценте послеоперацион-
ных осложнений в данной группе больных, тем не
менее они считают, что не следует у этих паци-
ентов воздерживаться от фундопликации. По на-
шим данным, основанным на лечении 150 детей
с тяжелым отставанием в умственном развитии,
после фундопликации по Талю только в двух слу-
чаях рвоты были столь выраженными, что потре-
бовалась повторная операция (уже по Ниссену)
С удовлетворительными окончательными результа-
тами (оба ребенка имели постоянную гастросто-
му). Среди 116 пациентов, оперированных по Та-
лю, рецидивный рефлюкс развился в 16% наблю-
дений в группе неврологических больных и в
3%—у неврологически здоровых пациентов.139
В заключение следует сказать, что четко выпол-
ненная операция Ниссена, равно как и тщательно
произведенная операция Таля, одинаково успешны
при лечении ГЭР у детей. Пациенты, перенесшие
как то, так и другое вмешательство, растут и раз-
виваются совершенно нормально, а порой даже
опережают своих сверстников. Процент осложне-
ний выше после операции Ниссена, что может
быть отчасти связано с большим ее объемом, не-
обходимостью широкого доступа и иногда — с од-
новременно производимым дополнительным вме-
шательством. С дальнейшим развитием хирургии
некоторые сложности и проблемы, обусловленные
ГЭР у взрослых пациентов, возможно, удастся
предотвращать, если фундопликация будет произ-
водиться в детском возрасте.
ЛИТЕРАТУРА
1. Neuhauscr EBD, Berenberg W: Cardin-esophageal relaxation as
a cause of vomiting in infants. Radiology 48:480—483, 1947.
2. Carre IJ, Asticy R: Fate of the partial thoracic stomach in child-
ren. Arch Dis Child 35:484 486, 1960.
3. Carre IJ: The natural history of the partial thoracic stomach in
children. Arch Dis Child 34:344 353, 1959.
4. Carre IJ: A historical review of the clinical consequences of
hiatal hernia and gastroesophageal reflux. Report of 76th Ross
Conference on Pediatric Research, 1978.
5. Guttman FM: Experience and reason briefly recorded. Pediatrics
50:325—327, 1972.
6. Waterston DJ: Hiatus hernia. In Mustard WT, Ravitch MM, Sny-
der WH, et al. (Editors). Pediatric Surgery, Medical Year Book
Publishers, Chicago, pp 392—400. 1969.
7- Darling DR: Hiatal hernia and gastroesophageal reflux in infan-
cy and childhood. AJR 123:724—736, 1975.
8. Hill LD: An effective operation for hiatal hernia. Ann Surg
166:681 692, 1967.
9. Nissen R: The treatment of hiatal hernia and esophageal reflux
by fundoplication. In Nyhus L, Harkins D (Editors). Hernia.
JB Lippincott, Philadelphia, 1964.
10. Thai AP: A unified approach to surgical problems of esophago-
gastric junction. Ann Surg 163:542—550, 1968.
11. Vollenweider ER: The use of gastropexy in the management of
esophageal hiatus hernia. Surgery 66:264—268, 1966.
12. Filler RM, Gross RE: Esophageal hiatus hernia in infants and
children. J Thorac Cardiovasc Surg 47:551—565, 1964.
13. Randolph JG, Lilly JR, el al.: Surgical treatment of gastroe-
sophageal reflux in infants. Ann Surg 180:479—486. 1974.
14. Boix-Ochoa JB: Diagnosis and management of gastroesophageal
reflux in children. In Nyhus L (Editor). Surgery Annual, Apple
ion Century Crofts, Norwalk, 1981.
15. Boix-Ochoa J, Canals J: Maturation of the lower esophagus.
J Pediatr Surg 11:749—756, 1976.
16. Arana J, Tovar J A: Motor efficiency of the refluxing esophagus
in basal conditions and after acid challenge. J Pediatr Surg
24:1049—1054, 1989.
17. Carre IJ: Treatment of gastroesophageal reflux. J Pediatr
112:502—504, 1988.
18. Brackbill (J, Douthitt TC, West H: Psychophysiologic effects in
neonate of prone versus supine placement. J Pediatr 82:82—84,
1973.
19. Newell DJ, Booth IW, et al.: Gastro-esophageal reflux in pre-
term infants. Arch Dis Child 64:780—786, 1989.
20. Sindel BD, Maisels MJ, et al.: Gastroesophageal reflux to lhe
proximal esophagus in infants with bronchopulmonary dyspla-
sia. Am J Dis Child 143:1103 1106, 1989.
21. Jolley SG. Halpprr CT. et al - The. relationship of respiratory
complications from gastroesophageal reflux to prematurity in
infants. J Pediatr Surg 25:755 757, 1990.
22. Ashcraft KW, Holder TM, Amoury RA: Treatment of gastroe-
sophageal reflux in children by Thai fundoplication. J Thorac
Cardiovasc Surg 82.706—712, 1981.
23. Lcapc LL, Holder TM. et al.: Respiratory arrest in infants se-
condary to gastroesophageal reflux. Pediatrics 60:924—927,
1977.
24. Beckwith JB: The Sudden Infant Death Syndrome. Curr Probl
Pediatr 3:1, 1973.
25. Southall DP: Role of apnea in the sudden infant death syndro-
me: a personal view. Pediatrics 80:73—84, 1988.
26. Kahn A, Rebuffat E, et al.: Sleep apneas and acid esophageal
reflux in control infants and in infants with an apparent lifethre-
alening event. Biol Neonate 57:144—149, 1990.
27. Walsh JK, Farrell MK, et al.: Gastroesophageal reflux in
infants: relation to apnea. J Pediatr 99:197—201, 1981.
28. Spitzer AR, Boyle TT, Tuchman DN, et al.: Awake apnea as-
sociated with gastroesophageal reflux: A specific clinical synd-
rome. Pediatrics 104:200—205, 1984
29. Newman LJ, Berezin S, et al.: Gastroesophageal reflux-induced
hypoxemia in infants with apparent life-threatening event(s).
Am J Dis Child 143:951—954, 1989.
30. Herbst JJ, Minion SD, Book LS: Gastroesophageal reflux cau-
sing respiratory distress and apnea in newborn infants. J Pediatr
95:763—768, 1979.
31. Jeffery HE, Reid I, et al.: Gastro-esophageal reflux in “near
miss”sudden infant death infants in active but not quite sleep.
Sleep 3:393—399, 1980.
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 319
32. Orcnstein SR. Orenstein DM: Gastroesophageal reflux and res-
piratory disease in children. J Pediatr 112:847—858, 1988.
33. Danus O, Casar C. cl al.: Esophageal reflux an unrecognized
cause of recurrent obstructive bronchitis in children. J Pediatr
89:220—224, 1976.
34. Euler AR, Byrne WJ, Marvin EA, et al.: Recurrent Pulmonary
Disease in children: A complication of gastroesophageal reflux.
J Pediatr 63:47—51, 1979.
35. Paton JY. Macfadycn UM. Simpson H: Sleep phase and gastroe-
sophageal reflux in infants at possible risk of SIDS. Arch Dis
Child 64.264 269, 1989.
36. Jolley SG, Herbst JJ, Johnson DG, el al.: Surgery in children
with gastroesophageal reflux and respiratory symptoms. J Pcdi
atr 96:194—198, 1980.
37. Berquist WE, Rachelefsky GS. Kadden M, et al.: Gastroesopha-
geal reflux associated recurrent pneumonia and chronic asthma
children. J Pediatr 68:29—35. 1981.
38. Pellegrini CA, DcMccstcr TR. et al.: Gastroesophageal reflux
and pulmonary aspiration: Incidence, functional abnormality,
and results of surgical therapy. Surgery 86:110—119. 1979.
39. Brand DL, Ylvisakcr JT, et al.: Regression of columnar esopha-
geal (Barrett’s) epithelium after anti-reflux surgery N Engl
J Med 302:844—848. 1980.
40. Skinner DB: Controversies about Barrett's esophagus. Ann Tho-
rac Surg 49:523—524, 1990.
41. Kinsbourne M, Oxon DM: Hiatus hernia with contortions of the
neck. lancet May 16:1058—1061. 1964.
42. Puntis JWL, Smith Hl., et al.: Effect of dystonic movements on
oesophageal peristalsis in Sandifer’s syndrome. Arch Dis Child
64:1311 — 1313. 1989.
43. Bray PF, Herbst JJ, et al.: Childhood gastroesophageal reflux.
JAMA 237:1342 1345, 1977.
44. Mandel J, Tirosh E, Berant M: Sandifer syndrome reconsidered.
Acta Paediatr Scand 78:797—799, 1989.
45. Polk HC, Burford Til; Disorders of the distal esophagus in in-
fancy and childhood. Am J Dis Child 108:243—251, 1964.
46. Picretti R, Shandling B, Stephens CA: Resistant esophageal ste-
nosis associated with reflux after repair of esophageal atresia:
A therapeutic approach. J Pediatr Surg 9:355—357, 1974.
47. Ashcraft KW, Goodwin <*, et aL: Early recognition and aggressi-
ve treatment of gastroesophageal reflux following repair of eso-
phageal atresia. J Pediatr Surg 12:317—321, 1977.
48. Shcrmcta DW. Whilington DS, et al.: I owcr esophageal sphinc-
ter dysfunction in esophageal atresia: Nocturnal regurgitation
and aspiration pneumonia. J Pediatr Surg 12:871 876, 1977.
49. Jolley SG, Tunell WP, et al.: Gastric emptying in children with
gastroesophageal reflux. The relationship to retching symptoms
following antireflux surgery. J Pediatr Surg 22:927—930, 1987.
50. Papaila JG. Wilmot D, Grosfeld JI., et al.: Increased incidence
of delayed gastric emptying in children with gastroesophageal
reflux. Arch Surg 124:933—936, 1989.
51. Grunow JE, Al-Hafidh AS, Tunell WP: Gastroesophageal reflux
following percutaneous endoscopic gastrostomy in children.
J Pediatr Surg 24:42—45, 1989.
52. Grosfeld J: Discussion. In Grunow JE, Al-Hafidh AS, Tunell
WP: Gastroesophageal reflux following percutaneous endoscopic
gastrostomy in children. J Pediatr Surg 24:44. 1989.
53. Kiely E. Spitz L: Is routine gastrostomy necessary in the mana-
gement of oesophageal atresia. Pediatr Surg Int 2:6—9. 1987.
54. Molliti DI, Golladay ES, Seibert JJ; Symptomatic gastroesopha-
geal reflux following gastrostomy in neurologically impaired pa-
tients. Pediatrics 75:1124 1126, 1985.
55. Berezin S, Schwarz SM, et aL: Gastroesophageal reflux seconda-
ry to gastrostomy tube placement. Am J Dis Child 140:699 -
701. 1986.
56. Kumar D. Brereton RJ. ct al.: Gastro-oesophageal reflux and
intestinal ma I rotation in children. Br J Syrg 75:533 535. 1988.
57. Stolar CJH, Levy JP, Dillon PW, et al.: Anatomic and functional
abnormalities in esophagus in infants surviving congenital di-
aphragmatic hernia. Am J Surg 159:204—207. 1990.
58. Darling DB, Fisher JH, Gellis SS: Hiatal hernia and gastroe-
sophageal reflux in infants and children: Analysis of the inci-
dence in North American children. Pediatrics 54:450—455,
1974.
59. Darling DB. McCauley GK. et al.: Gastroesophageal reflux in
infants and children: Correlation of radiological severity and
pulmonary pathology. Radiology 127:735 740, 1978.
60. Rowen SJ, Gyepes MT; “The trumpeting elephant” sign of gast-
roesophageal reflux. Radiology 167:188, 1978.
61. Meyers WF. Roberts CC, et al.: Value of tests for evaluation of
gastroesophageal reflux in children. J Pediatr Surg 20:515—
520, 1985.
62. Benz LJ. Hootkin LA, Margulier S, el al.: A comparison of clini-
cal measurement of gastroesophageal reflux. Gastroenterology
62:1—5, 1972.
63. Fonkalsrud EW, Ament ME, Byrne WJ, et al.: Gastroesophageal
fundoplication for the management of reflux in infants and child-
ren. J Thorac Cardiovasc Surg 76:644—664. 1978.
64. Wilkins BM. Spitz L: Adhesion obstruction following Nissen
(undoplication in children. Br J Surg 74:777—779, I9§7
65. Johnson LF„ DeMeester TR: Twenty-four hour ph monitoring in
the distal esophagus. Am J Gastroenterol 62:325—332, 1974.
66. Hill JI . Pelligrini CA, el al.: Technique and experience with
24-hour esophageal ph monitoring in children. J Pediatr Surg
12:877—887, 1977.
67. Jolley SG, Johnson DG. Herbst J J, et al.: An assessment of gast-
roesophageal reflux in children by extended ph monitoring of
the distal esophagus. Surgery 84:16—22, 1978.
68. Jolley SG, Herbst JJ, Johnson DG, et al.: Patterns of postcibal
gastroesophageal reflux in symptomatic children. Am J Surg
138:946—950. 1979.
69. Drcizzen E, Escourrou P, Odievre M, et al.: Fsophagcal reflux
in symptomatic asymptomatic infants: Postprandial and circadi-
an variations. J Pediatr Gastroenterol Nutr 10:316—321, 1990.
70. Cucchiara S, Siaiano A, et al.: Value of the 24 hr intraoesopha-
gcal ph monitoring in children. Gut 31:129—133, 1990.
71. Dalt DA, Mazzoleni S, Montini G, et aL: Diagnostic accuracy of
monitoring in gastro-oesophageal reflux. Arch Dis Child
64:1421 1426, 1989.
72. Haase CM, Meagher DP, Goldson E. Falor WH: A unique tele-
iransmissinn system for extended four-channel esophageal ph
monitoring in infants and children. J Pediatr Surg 22:68—74,
1987.
73. Haase GM, Ross MN, et aL: Extended four-channel esophageal
ph monitoring: The importance of acid reflux patterns at the
middle proximal levels. J Pcdiair Surg 23:32—37, 1988.
74. Vandenplas Y, Granchx-Goossens A. et al.: Area under ph 4:
Advantages of a new parameter in the interpretation of esopha-
geal monitoring data in infants. J Pediatr Gastroenterol Nutr
9:34 39. 1989.
75. Ross MN, Haase GM, Rcilcy TT, ct al.: The importance of acid
reflux patterns in neurologically damaged children detected by
four-channel esophageal ph monitoring. J Pediatr Surg 23:573—
576, 1988-
76- Jolley SG, Herbst JJ. ct aL: Esophageal ph monitoring during
sleep identifies children with respiratory symptoms from gastroe-
sophageal reflux. Gastroenterology 80;150l—1506, 1981.
77. Vandenplas Y, Goyvaeris H. Hefvcn R: Do esophageal ph moni-
toring data depend on recording equipment and probes. J Pedi-
atr Gastroenterol Nutr 10:322 326, 1990.
78. Falor WH, Miller J, Kraus J, et al.: 24-hour monitoring of eso-
phagopharyngeal ph in outpatients. J Thorac Cardiovasc Surg
91:716—722, 1986.
79. Newman LJ, Berezin S, San Filippo JA, et aL: New ambulatory
system for extended esophageal ph monitoring. J Pediatr Gas-
troenterol Nutr 4:707—710, 1985.
80. Opie JC. Chayc H, Fraser GC: Fundoplication and pediatric
esophageal manometry: Actuarial analysis over 7 years. J Pedi-
atr Surg 22:935 938, 1987.
81. Christie DL. Mack DV, Parker AF, et al.: Use of intraoperative
320 ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС
esophageal manometries in surgical treatment of gastnx:sopha-
geal reflux in pediatric patients. J Pediatr Surg 12’648—652,
1978.
82. Berger D. Bischof Delaloye A, et al.; Esophageal and pulmona
ry scintiscanning in gastroesophageal reflux in children. Prog
Pediatr Surg 18:68 77, 1985
83. Fawcett HD, Hayden DK, el al.: How useful is gastroesopha-
geal reflux scintigraphy in suspected childhood aspiration. Pe-
diatr Radiol 18:311 313, 1988.
84. Berdon WE, Melins RB, Levy J: Commentary on how useful is
gastroesophageal reflux scintigraphy in suspected childhood as-
piration. Pediatr Radiol 18:309—310, 1988.
85. Carre IJ: Postural treatment of children with a partial thoracic
stomach. Arch Dis Child 35:569 580. 1960.
86. Meyers WF, Herbst JJ: Effectiveness of positioning therapy for
gastroesophageal reflux. Pediatrics 69:768—772. 1982.
87. Vandenplas Y, Smits L: Gastro-oesophageal reflux in infants.
Evaluation of treatment by ph monitoring. Fur J Pediatr
146:504—507, 1987.
88. Orcnstein, SR: Effects on behavior stale of prone versus seated
positioning for infants with gastroesophageal reflux. Pediatrics
85:756—767, 1990.
89. Prinsen JE: Hiatus hernia in infants and children: Long-term
follow-up medical therapy. J Pediatr Surg 10:97—102. 1975.
90. Ramenofsky JL, Powell RW, Curreri PW: Gastroesophageal
reflux. Ph probe-directed therapy. Ann Surg 203:531—536,
1984.
91. Guggenbichlcr JP, Menard G: Conservative treatment of gast-
roesophageal reflux hiatus hernia. Prog Pediatr Surg 18:78—
83, 1985.
92. Ftiler AR: Use of bethanechol for the treatment of gastroe-
sophageal reflux. J Pediatr 96:321—324, 1980.
93. Sondheimer JM, Arnold GL: Early effects of bethanechol on
the esophageal motor function of infants with gastroesophageal
reflux. J Pediatr Gastroenterol Nutr 5:47—51, 1986.
94. Orenstein SR, Lofton SW, Orcnslcin DM: Bethanechol for pedi-
atric gastroesophageal reflux. A prospective, blind, controlled
study. J Pediatr Gastroenterol Nutr 5:549—555, 1986.
95. Hyman PE, Abrams CE, Dubois A: Gastric emptying in infants:
response to metoclopramide depends on the underlying conditi-
on. J Pediatr Gasrtoenterol Nutr 7:181 — 184, 1988.
96. Tolia V, Calhoun J, Kuhns L, et al.: Randomized prospective
double-blind trial metoclopramide and placedo for gastroesop-
hageal reflux in infants. J Pediatr 115:141—145, 1989.
97. Machida HM, Forbes DA, et al.: Metoclopramide in gastroe-
sophageal reflux in unfancy J Pediatr 112:483—487, 1988.
98. Kearns GL, Pharm D, Fiser DH: Metoclopramide-induced
methemoglobinemia. Pediatrics 82:364—366, 1988.
99. Rode H, Stunden RD, Millar AJW, Cywes S: Esophageal pH
assessment of gastroesophageal reflux in 18 patients and the
effect of two prokinetic agents: Cisapride and metoclopramide.
J Pediatr Surg 22:931—934, 1987.
100. Richter JE: Efficacy of cisapride on symptoms and healing of
gastro-oesophageal reflux disease: A review. Scand J Gastro-
enterol 24:19—28, 1989.
101. Cucchtara S. Staiano A, et al.: Effects of cisapride on parame-
ters of oesophageal motility and on the prolonged intraoeso-
phageal ph test in infants with gastro-oesophageal reflux dis-
ease. Gut 31:21—25, 1990.
102. Sa ye Z, Forget PP: Effect of cisapride on esophageal ph moni-
toring in children with reflux-associated bronchopulmonary di-
sease. J Pediatr Gastroenterol Nutr 8:327—332, 1989.
103. Vandenplas Y, Deneyer M, el al.: Gastroesophageal reflux
incidence and respiratory dysfunction during sleep in infants:
Treatment with cisapride. J Pediatr Gastroenterol Nutr 8:31 —
36, 1989.
104. Carre IJ: Management of gastro-oesophageal reflex. Arch Dis
Child 60:71 75, 1985.
105. Shepherd RW, Wren J, et al., Gastroesophageal reflux in child-
ren. Clin Pediatr 26:55—60, 1987
106. Johnson DG: Current thinking on the role of surgery in gastroe-
sophageal reflux. Pediatr Clin North Am 32:1165—1179, 1985.
107. Nyhus LM: Surgical treatment of gastroesophageal reflux in
children. Surg Annu 21:96- 118, 1989.
108. Cahill J, Aberdeen E, Waterston DJ: Results of surgical ire-
atment of esophageal hiatal hernia in infancy and childhood.
Pediatr Surg 66:597—602, 1969.
109. Fonkalsrud EW. Fogiia RP. el al.: Operative treatment for the
gastroesophageal reflux syndrome in children. J Pediatr Surg
24:525—529, 1989.
110. Skinner D: Discussion. In Leonard! HK, Lee ME. el al.: An
experimental study of the effectiveness of various antireflux
operations. Ann Thorac Surg 24:224, ;977.
111. Ashcraft KW, Goodwin CD, et al.: Thai fundoplicalion: A sim-
ple operative ireatment for gastroesophageal reflux. J Pediatr
Surg 13:643 647, 1978.
112. Ashcraft KW, Holder TM, el al.: The Thai fundoplicalion for
gastroesophageal reflux. J Pediatr Surg 19:480—483, 19X4.
113. Jolley SG, Tunell WP, el al.: Postoperative small bowel ob-
struction in infants and children: A problem following Nissen
fundoplicalion. J Pediatr Surg 21 407—409, 1986.
114. Jolley SG, Tunell WP, et al.: Postoperative small bowel ob-
struction in infants and children: A problem following Nissen
fundoplicalion. J Pediatr Surg 21:407—409, 1986.
115- Dedinsky GK, Vane DW, ct al.; Complications and reopcration
after Nissen fundoplicalion in childhood. Am J Surg 153:177—
183, 1987.
116. Leape LL, Ramenofsky ML: Surgical treatment of gastroe-
sophageal reflux in children. Am J Dis Child 134:935—938,
1980.
117. Spitz L, Kirtane J: Results and complications of surgery for
gastro-oesophageal reflux. Arch Dis Child 60:743—747, 1985.
118- Alrabeeah A, Giacomantonio M, ct al.: Paraesophageal hernia
after Nissen fundoplicalion. A real complication in pediatric
patients- J Pediar Surg 23:766—768, 1988.
119. Beltex M, Oesch IO: Hiatus hernia saga: Ups and downs in
gastroesophageal reflux, present, and future perspectives. J Pe-
diatr Surg 18:670—680, 1983-
120. Glick PL, Harrison MR, et al.: Gastric infarction secondary to
small bowel obstruction: A preventable complication after Nis-
sen fundoplicalion. J Pediatr Surg 22:941—943, 1987.
121. Scharli AF: To Nissen or not to Nissen. Prog Pediatr Surg
18:96—100, 1985.
122. Pennell RC, 1 ewis E, Thomas V, et al.: Management of severe
gastroesophageal reflux in children. Area Surg 119:553—558,
1984.
123. St Lyr JA. Ferrara B, el al.: Treatment of pulmonary mani-
festations of gastroesophageal reflux in children two years of
age or less. Am J Surg 157:400—404. 1989
124. Turnage RH0 Oldham KT, et al.: Late results of fundoplicalion
for gastroesophageal reflux in infants and children. Surgery
105:457 463, 1989.
125. Takano U, Iwafuchi M: Evaluation of lower esophageal
sphincter function in infants and children following esophageal
surgery. J Pediar Surg 23: 410—414, 1988.
126. Jolley SCJ, Tunell WP, el al.: Intraoperative esophageal mano-
metry and early postoperative esophageal ph monitoring in
children. J Pediatr Surg 24:336—340, 1989.
127. Shirazi SS, Schulze K, Soper RT: Long-term follow-up for
treatment of chronic reflux esophagitis. Arch Surg 122:548—
552, 1987.
128. Pellerin D: Discussion. In Follette D, Fonkalsrud EW, et al.z
Gastroesophageal fundoplicalion for refljx in infants and chil-
dren. J Pediatr Surg 11:757—764, 1976.
129. 1 ow DE, Mercer CD, cl al.: Post-Nissen syndrome. Surg Gyne-
col Obstcl 167:1- 5. 1988.
130. Caniano DA, Ginn-Pease ME, King DR: The failed anlireflux
procedure. Analysis of risk factors and morbidity. J Pediatr
Surg 25:1022—1026, 1990.
131. Davidson BR, Hurd D, Jonslone MS. Nissen fundoplication
ГАСТРОЭЗОФАГЕАЛЬНЫЙ РЕФЛЮКС 321
pyloroplasty in the management of gastro-oesophugeal reflux
in children. Br J Surg 64:488—490, 1987.
132. Altorki NK, Skinner DB, Sega I in A, el al.: Indications for eso-
phagectomy nonmalrgnanl Barrett’s esophagus. A 10-year expe-
rience. Ann Thorac Surg 49:724 727, 1990.
133. Williamson WA. Ellis HF. et al.: Effect of aniircflux operation
on Barrett's mucosa. Ann Thorac Surg 49:537—542. 1990.
134- Langer JC. Wesson DE. Ein SH. et al.: Feeding gastrostomy
ncurologically impaired children: is an antirefiux procedure
necessary? J Pediatr Gastroenterol Nutr 7:837—841, 1988.
135. Bui IID, Dang CV, et al.: Does gastrostomy and fundoplication
prevent aspiration pneumonia in mentally retarded persons. Am
J Menl Retard 94:16—19, 1989.
136. Vunc DW, Harmel RP, et al.: The effectiveness of Nissen fun-
doplication in neurologically impaired children with gastro-
esophageal reflux. Surgery 98:662—667, 1985.
137. Stringel G. Delgado M. Guertin L, et al.: Gasrtostomy and
Nissen fundoplication in neurologically impaired children. J Pe-
diiitr Surg 24:1044—1048. 1989.
138. Pearl RH. Robie DK, Ein SH. et al.: Complications of gastro-
esophageal antireflux surgery in neurologically impaired vs.
neurologically normal children. Pediatr Surg 25:1169 1173.
1990.
139 Tuggle DW, Tunnel WP, el al.: Thai fundoplication in the
treatment of gastroesophageal reflux: The influence of central
nervous system impairment. J Pediatr Surg 23:638 — 640, 1988.
21 Заказ Ne 1622
Глава 24
ЗАБОЛЕВАНИЯ ЖЕ ЛУДКА
НЕПРОХОДИМОСТЬ ЖЕЛУДКА
Непроходимость желудка у детей проявляется сле-
дующими клиническими симптомами: рвота, боль,
тошнота, вздутие живота в эпигастральной обла-
сти. Из перечисленных симптомов на первом месте
стоит, безусловно, рвота без примеси желчи в рвот-
ных массах — главный отличительный признак
непроходимости желудка. Наиболее часто этот
симптом у детей говорит именно о гипертрофиче-
ском пилоростенозе. Однако признаки обструкции
могут быть также обусловлены и другими причи-
нами врожденного характера, которые встречаются
реже и не всегда проявляются остро. Это атрезия
привратника, атония желудка, мембрана антраль-
ного отдела, удвоение и даже острый заворот же-
лудка. При дифференциальной диагностике забо-
леваний, проявляющихся у детей прежде всего рво-
той без желчи, следует учитывать и нехирургиче-
ские причины, такие как нарушения питания
(перекармливание или неправильное вскармлива-
ние), «пилороспазм» (обычно непродолжительный
и самостоятельно проходящий), халазия или гаст-
роэзофагеальный рефлюкс (более длительно про-
текающий, но также купирующийся без лечения).
Симптомами хронической непроходимости выход-
ного отдела желудка могут проявляться и другие
приобретенные заболевания, например, язвенная
болезнь.
Гипертрофический пилоростеноз
Считается, что первое описание гипертрофическо-
го пилоростеноза у детей принадлежит Hildantis
и относится к 1627 г.', однако в данном клиниче-
ском случае было явное перекармливание ребенка,
который самостоятельно выздоровел.2 Более харак-
терная клиническая и патологоана гемическая кар-
тина гипертрофического пилоростеноза была пред-
ставлена Patrick Blair в его докладе Королевскому
обществу в Лондоне в 1717? В последующем ги-
пертрофический пилоростеноз был еще раз «по-
вторно открыт», а рассматриваться как нозологи-
ческая форма стал наконец лишь после того, как
в 1888 г Гиршпрунг дал подробное полное описа-
ние двух случаев этой патологии? Успешное хи-
рургическое лечение впервые осуществлено в
1898 г. Lober, который наложил при пилоростено-
зе гастроеюноанастомоз. А внесяилистая пилоро-
пластика впервые была произведена примерно в од-
но и то же время тремя авторами независимо друг
от друга: NicoII в 1906 г., Fredet в 1907 г. и Weber
в 1908 г. Однако каждый из упомянутых хирургов
сближал разделенные мышцы швами в поперечном
направлении. В 1911 г. Рамштедт описал технику
пилоромиотомии, которая применяется и в настоя-
щее время, являясь наиболее широко распростра-
ненным и общепринятым вмешательством, сопро-
вождающимся низкой летальностью 0,4% и да-
же меньше? История развития всех проблем, свя-
занных с этим заболеванием, наиболее полно
и тщательно представлена в работах Маск и Ra-
vich?'7
Частота гипертрофического пилоростеноза в Со-
единенных Штатах составляет 3:1000 новорожден-
ных, причем отмечаются определенные расовые
и этнические различия. Так, наиболее часто забо-
левание встречается у белых людей, особенно се-
вероевропейского происхождения, несколько ре-
же — у черных и совсем редко — у восточных на-
родов/ Отмечается преобладание пилоростеноза у
мальчиков — в соотношении (мальчики : девочки)
4:1. Заболевание может передаваться по наследст-
ву. Если пилоростеноз был у матери, то ча-
стота его возникновения у мальчиков составляет
19%, а у девочек — 7%. При наличии же пилоро-
стеноза у отца заболевание передается мальчикам
только в 5% и девочкам — в 2,5%.“’ Хотя счита-
ется, что наиболее вероятна передача пилоростено-
за первому мальчику в семье, однако не всеми
исследованиями это подтверждается." Пилоросте-
ноз часто встречается также у детей, оперирован-
ных по поводу атрезии пищевода с или без трахео-
пищеводного свища, в этих случаях частота его
колеблется от 1 до 10%.12
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 323
Многие факторы играют роль в развитии гипер-
трофического пилоростеноза. К ним относятся не-
зрелость и дегенеративные изменения нервных
элементов пилоруса,13 характер питания (в частно-
сти, кормление грудью),2 повышенный уровень
гастрина у матери или ребенка,2,14‘1 нарушение
взаимодействия гастрина-секретина.16 Но ни один
из этих факторов не считается достоверно этиоло-
гическим. Однако имеются данные исследований,
проведенных с использованием гистохимической
техники, которые выявили у пациентов с пилоро-
стенозом недостаточность нейропептидергической
иннервации.17 Более высокая частота этого заболе-
вания отмечается у детей с группой крови В и 0,'*
а также при наличии у матери в третьем три-
местре беременности стрессовых ситуаций.19
Spicer сообщил сведения о различных факторах,
связанных с возникновением пилоростеноза.2 Если
учесть определенную роль (о чем было сказано
выше) расы, пола, наследственности (семейных
случаев заболевания), атрезии пищевода, группы
крови, пренатального материнского стресса, нерв-
ной дисфункции, то можно сказать, что развитию
поражения пилоруса способствуют множественные
генетические (Х-сцетенные) факторы и/или фак-
торы окружающей среды.2 Однако в отличие от
достоверно генетически обусловленных аномалий,
пилоростеноз редко сочетается с другими порока-
ми. Из сону гствующих аномалий чаще всего встре-
чается грыжа пищеводного отверстия диафрагмы.20
которая может развиваться и вторично, в результа-
те хронических рвот. Пилоростеноз иногда сопро-
вождается желтухой, особенно если рвоты продол-
жаются в течение длительного промежутка време-
ни. У этих пациентов выявляется недостаточность
печеночной глюк урон илтрансферазы, как и у боль-
ных с синдромом Жильбера?1 После пилоромио-
томии желтуха спонтанно исчезает. Обычно это
происходит через несколько дней после возобнов-
ления нормального питания.
Считается, что гипертрофия мышечного слоя пи-
лоруса скорее всего развивается постнатально, по-
скольку симптомы пилоростеноза редко отмечают-
ся при рождении,22 а появляются обычно на 2—
5-й неделе жизни. Поэтому термин «врожденный
гипертрофический пилоростеноз» возможно недо-
статочно правилен. Существует однако описание
случая, когда при ультразвуковом пренатальном
исследовании был обнаружен резко расширенный
желудок, и сразу после рождения у ребенка паль-
пировался утолщенный пилорус, что, несомненно,
подтверждает наличие пилоростеноза в данном на-
блюдении уже внутриутробно.23 Высказывается
мнение о том, что в основе этого заболевания ле-
жит избыточность слизистой пилорического отде-
ла, отек которой и приводит к обструкции и вто-
ричному развитию мышечной гипертрофии.24 Дан-
ное предположение о патогенезе пилоростеноза
имеет клиническое подтверждение в том, что
с прекращением кормления детей с пилоростено-
зом обструктивные проявления исчезают. Именно
эти наблюдения обусловили попытки использовать
пехирургический метод лечения пилоростеноза, за-
ключающийся в длительном кормлении детей не-
большими количествами жидкости.25 Хотя при по-
добной консервативной терапии клинические про-
явления у большинства больных могут исчезнуть,
однако необходимость очень длительного лечения
и возникающие при этом осложнения нс позволи-
ли данному методу широко распространиться, да-
же в Европе, где он был впервые описан?1
Если охарактеризовать состояние пилоруса при
пил о росте козе, то он веретенообразно увеличен и не-
сколько асимметричен, с наибольшим утолщением
мышечного слоя спереди и сверху. Мышечная ги-
пертрофия в области пилорического отдела иногда
четко определяется при пальпации. Гипертрофиро-
ванные мышцы вдаются в 12-верстную кишку в виде
шейки, в результате чего дуоденальная слизистая
сидит внутри как шляпка на мышечном слое, со-
здавая нависающий свод по всей окружности тер-
минального отдела пилоруса (рис. 24-1А). Описан-
ная анатомическая ситуация обусловливает возмож-
ность повреждения дуоденальной слизистой при
слишком усердном разделении во время операции
дистальных волокон пилорической мускулатуры
(рис. 24-1 В). Проксимальная часть мышечного
слоя пилоруса плавно переходит в антральный от-
дел желудка, в котором также может возникать
вторичная мышечная гипертрофия. Мышечный
слой обычно очень плотный, у старших же детей
с длительным анамнезом — несколько размягчен-
ный. Гистологически определяется гипертрофия,
г. е. мышечные волокна увеличены в размерах без
значительного увеличения общего их количества.
После обычной пилоромиотомии гипертрофиро-
ванные мышцы при гистологическом исследовании
имеют нормальный вид лишь с небольшим оста-
точным линейным рубцом. Подобная морфологиче-
ская картина отмечается также и при спонтанном
выздоровлении в результате длительного нехирур-
гического лечения. Однако в поздние сроки после
проведения консервативной терапии могут отме-
чаться сохраняющиеся или вновь возникающие от-
сроченные симптомы пилорической обструкции?7
В типичных случаях рвота при пилоростенозе
появляется на 2—3-й неделе жизни, всегда без|
примеси желчи, сильная (подобно «выстрелу») и в
начале заболевания может временно прекратиться
или иметь очень неопределенный, «коварный» ха-
рактер. Рвота возникает через 30—60 мин после
кормления, ребенок в результате остается и выгля-
дит голодным даже непосредственно сразу после
эпизода рвоты. Хотя рвота всегда без примеси
желчи, однако рвотные массы могут иметь корич-
неватую окраску, а порой вид кофейной гущи, что
объясняется кровотечением, связанным с неизбеж-
но развивающимся проксимальным гастритом.
Имеются сообщения о том, что у детей, вскармли-
ваемых грудью, пилоростеноз развивается чаще?
Значительное увеличение тяжести и частоты эпи-
зодов рвот отмечается в тех случаях, когда ребенка
переводят на смеси, способствующие более интен-
сивному образованию в желудке творожистых
масс. И наоборот — частота рвот снижается, если
ребенку назначают декстроз но-водное питание.
324 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
Рис. 24-1. А, Сагиттальный срез при пилоростенозе через ди-
стальную часть антрального отдела желудка, гипертрофирован-
ный пилорус и проксимальный отдел 12-перстной кишки.
В. Разрез серозы и миотомия проксима зыю достигают ди
стальной части антрального отдела. На другом конце разреза
появляется «шляпка» слизистой 12-перстной кишки (I) с не-
большими мышечными волокнами (И), которые остаются между
слизистой пилоруса и шляпкой. Не следует предпринимать по-
пытки разделения этих волокон в связи с опасностью перфора-
ции слизистой 12-перстной кишки.
С. Сагиттальная проекция законченной миотомии. Видна
«шляпка» слизистой 12-псрстной кишки (I) и неразделенные
мышечные волокна дистального отдела привратника (II). Эти
волокна самостоятельно разделяются при первых же попытках
кормления в результате увеличения давления в просвете же-
лудка и его перистальтики.
Подозревая непереносимость смесей, поскольку
в ответ на их введение рвота усиливается, (егям
часто неоднократно меняют питание, что может
привести к значительным потерям массы тела,
а порой и к запорам, связанным с дегидратацией.
Однако в настоящее время вид детей с пилоро-
стенозом значительно отличается от той картины
умирающих пациентов, которая описывалась в
прошлом. Более высокая осведомленность педиат-
ров и общих врачей относительно клинической
картины пилоростеноз!» способствует ранней диаг-
ностике этой патологии и менее частому разви-
тию выраженных нарушений питания, тяжелой де-
гидратации и электролитного дисбаланса. У ослаб-
ленных недоношенных детей клинические прояв-
ления пилоростеноза могут быть столь коварны,
что диагноз часто даже не подозревается и лечение
в результате начинается слишком поздно.28
Дифференцировать пилоростеноз необходимо со
всеми хирургическими и соматическими видами
патологии, основным проявлением которых явля-
ется рвота без примеси желчи. Симулировать ги-
пертрофический пилоростеноз могут пилороспазм
с гастроэзофагеальным рефлюксом или без него,
первичная атопия желудка (с ГЭР или без него),
солетеряющая форма адреногенитального синдро-
ма, поражение центральной нервной системы с по-
вышением внутричерепного давления, первичный
ГЭР (халазия), мембрана антрального отдела, атре-
зия или кистозное удвоение пилоруса, эктопия ткани
поджелудочной железы в пилорус, аденома подже-
лудочной железы. Соответственно все перечислен-
ные виды патотогии должны быть исключены.
Диагноз пилоростеноза может быть поставлен
при обычном физикальном обе юдовании. Очень
помогает в диагностике кормление ребенка непо-
средственно во время осмотра (если ребенок доста-
точно активен и сосет самостоятельно), поскольку
при этом, как правило, появляется видимая пери-
стальтика желудка. Перистальтические волны в
эпигастральной области в проекции желудка про-
ходят слева направо и возникают непосредственно
перед рвотой. Характерна рвота фонтаном, бс-з
желчи, иногда с примесью коричневатой слизи.
Желудок при пилоростенозе обычно расширен не
равномерно, а за счет глубоких складок, и потому
рвота более эффективно его опорожняет от жидко-
го содержимого и воздуха, чем отсасывание через
зонд. Большое диагностическое значение имеет
пальпаторное определение «оливы» гипертрофиро-
ванного пилоруса. Пальпация облегчается, если
мышцы живота максимально расслаблены, а пото-
му ее следует провопить после опорожнения же-
лудка рвотой, спровоцированной кормлением (у
крепких детей), или зондированием и аспира-
цией— у ослабленных вялых детей. Гипертрофи-
рованный пилорус обычно плотный, подвижный,
длиной около 2 см, расположен непосредственно
над пупком и несколько справа от него. Иногда
пилорус локализуется выше и трудно доступен
пальпации из-за расположенной над ним печени.
Важно любыми способами успокоить ребенка, что-
бы он был в релаксированном состоянии, Это об-
легчает при легком пальпаторном надавливании
на брюшную стенку в краниальном направлении
обнаружение подвижного плотного опухолевид-
ного образования, которое при более глубокой
пальпации можно даже взягь пальцами, зафикси-
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 325
ровав между ними. Этот диагностический прием
возможен у 85% всех детей с пилоростенозом
и помогает достоверно поставить диагноз. Для об-
легчения проведения данного обследования может
быть использована медикаментозная ссдатация, но
в большинстве случаев в ней нет необходимости.
Если по анамнезу и клинической картине у ре-
бенка подозревается пилоростеноз, но пропальпи-
ровать пилорус не удается, следует прибегнуть
к другим диагностическим методам. В прошлом ча-
сто применялось рентгенологическое исследование
желудка с барием. В настоящее время ему на смену
пришел менее опасный и более безобидный ме-
тод — УЗИ живота. Опасность контрастного ис-
следования с барием состоит в том, что при после-
дующем введении перед операцией в наркоз может
возникнуть аспирация желудочного содержимого
и бария?4 Первоначальные сомнения относительно
точности определения пилоруса с помощью ультра-
звука были полностью развеяны после серии ис-
следований, заключавшихся в сравнении размеров
пилоруса по данным УЗИ и интраоперационного
измерения его толщины у детей с пилоростенозом
(рис. 24-2А).30 Диагноз может быть установлен
при диаметре пилоруса более 14 мм, толщине его
мышечного слоя, превышающей 4 мм, и длине —
более 16 мм. При указанных параметрах точность
диагностики достигает 91 —100%, причем чаще —
ближе к 100%.sn Если после УЗИ диагноз остается
неясным, показано контрастное рентгенологиче-
ское обследование. Рентгенологические признаки
пилоростеноза заключаются в увеличении желуд-
ка, замедленном его опорожнении, наличии стру-
нообразного или удлиненного суженного пилори-
ческого канала, обычно сочетающегося с симпто-
мом плечиков, образуемых округлыми краями ги-
пертрофированных мышц. Часто может быть виден
и симптом рельс, обусловленный выпячиванием
слизистой, в складках которой барий скапливается
в виде двух продольных полосок (рис. 24-2В).
После обследования необходимо опорожнить же-
лудок, удалив весь введенный барий, дабы пре-
дотвратить последующую аспирацию, о возмож-
ности возникновения которой было сказано выше.
Дегидратация, отмечающаяся у детей с пилоро-
стенозом, может быть выражена в разной степени
(от легкой до очень тяжелой) и зависит не только
от длительности заболевания, но и от частоты
рвот. Поскольку при рвотах теряется лишь желу-
дочное содержимое, то электролитные потери пер-
воначально касаются преимущественно Н и С1
и в меньшей степени Na и К В результате
указанных электролитных нарушений у ребенка
развивается гипохлоремия с метаболическим алка-
лозом. осложняющаяся в дальнейшем, к сожале-
нию, потерями К с мочой — реакция организма,
направленная на компенсацию ренальной реабсор-
бции Na , которая увеличивается в связи с внекле-
точными потерями жидкости.2 Алкалоз увеличива-
ется еще и в результате абсорбции в почках вместе
с натрием НСО^, что связано с истощением CL Ги-
покалиемия усугубляет алкалоз, который в свою
очередь усиливает гипокалиемию. Таким образом
возникает порочный круг, прервать который мож-
но только путем адекватного возмещения потерь
электролитов и внеклеточной жидкости на фоне
прекращения питания, что позволяет предотвра-
тить рвоту.
Экстренная предоперационная коррекция жидко-
стных и электролитных нарушений осуществляет-
Рис. 24~2. А, Сонографическое изображение пилоростеноза. Видны удлиненный привратник (обратите внимание на расстояние
между стрелками), утолщение его стенки и увеличение общего диаметра.
В, Классическая картина пилоростеноза при контрастном исследовании с барием. Виден увеличенный желудок, суженный пило-
рический канал (маленькая стрелка) и симптом «плечиков*, обусловленный пыпнч и мающимися гипертрофированными мышцами
в дистальном дуоденальном отделе привратника (большие стрелки).
326 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
ся путем как орального введения питательных рас-
творов (у менее тяжелых детей),24 так и паренте-
ральной жидкостной терапии (у более тяжелых
больных).2 Энтеральная терапия заключается в
применении простых сбалансированных электро-
литных растворов, содержащих глюкозу в виде 5%
декстрозы в растворе Рингер-лактата и назначае-
мых небольшими дозами — 30—60 мл каждые 1 —
2 часа. Однако этот метод может быть достаточно
утомительным и даст замедленную клиническую
реакцию, а потому чаще применяется инфузионная
(вн/в) терапия. Первоначально вводят физиологи-
ческий раствор (ФР) с добавлением 5% декстрозы
(Д5). Если у ребенка установился адекватный диу-
рез, то добавляют KCI в количестве 20 ммоль/л.
Д5/ФР.045 с добавлением KCI применяют в том
случае, когда уровень Na и С1“ начинает воз-
вращаться к норме и устанавливается адекватный
диурез. При тяжелом дефиците С1~ внутривенно
вводят хлористый аммоний, но необходимость
в этом возникает редко.
Длительность предоперационной подготовки оп-
ределяется в основном тяжестью жидкостных и
электролитных расстройств и у тяжелых больных
достигает 48 час. У маловесных детей, а также
при наличии рвот в течение длительного периода
или большой потери массы тела, может развиться
гипогликемия, поэтому у всех пациентов с пило-
ростенозом необходимо до операции определять
сахар в крови. Об эффективности подготовки го-
ворят следующие клинические параметры: нор-
мальные тургор кожи и родничковое давление,
влажные слизистые, диурез 2 мг/кг/час и соответ-
ствующий уровень электролитов сыворотки. Со-
держание НСОГ в сыворотке (наиболее важный
лабораторный показатель) меньше 300 ммоль/л
свидетельствует о надежной коррекции алкалоза
перед наркозом и операцией.
Предоперационная интенсивная терапия и адек-
ватное анестезиологическое пособие обеспечивают
в настоящее время безопасность и быстроту вме-
шательства. Местную анестезию не используют.
Для пилоромиотомии применяют самые разнооб-
разные доступы. Наиболее часто используют попе-
речный разрез в правом верхнем квадранте живо-
та, после которого образуется незаметный рубчик.
Фасцию рассекают продольно или поперечно, за-
тем разводят прямые мышцы Пилорус (нередко
расположенный под печенью) выводят в рану
и фиксируют между большим и указательным
пальцами. Серозу рассекают по передневерхней
поверхности в относительно бессосудистой зоне.
Разрез продлевают проксимально до антрального
отдела, а дистально заканчивают, не доходя при-
мерно 4 мм до пальпируемого терминального окон-
чания пилорических мышц (см. рис. 24-1 В).
Подлежащие мышцы раздвигают, начиная от
проксимального конца разреза, путем слепого раз-
деления продольных волокон, используя специаль-
ный инструмент либо тупой конец рукоятки скаль-
пеля. Мышцы разводят до тех пор, пока интактная
слизистая не начнет выбухать в разрез, при этом
особое внимание надо уделять полному разделе-
нию мышц в области антрального отдела желудка.
Затем мышцы раздвигают в дистальном направ-
лении таким образом, чтобы они полностью «разо-
шлись» в стороны. Не следует предпринимать по-
пытки разделять лишь последние небольшие мы-
шечные волокна дистального конца пилоруса,
поскольку это может привести к перфорации
(рис. 24-10. Эти волокна самостоятельно спон-
танно расходятся в результате перистальтики же-
лудка и опорожнения его при первых кормлениях
после операции.
Путем надавливания на желудок и наблюдения
за прохождением воздуха и жидкого содержимого
в кишечник необходимо убедиться в отсутствии
перфорации, которая, если возникает, то обычно
локализуется, как уже упоминалось, в области
12-перстной кишки. Перфорацию следует ушить
рассасывающимися швами, прикрыв их вторым ря-
дом швов, накладываемых на мышцы. Затем пило-
рус поворачивают на четверть— пол-оборота (90—
180°) и пилоромиотомию повторяют в другом ме-
сте. Некоторые хирурги считают, что в подобной
ситуации достаточно ушить слизистую, не ушивая
мышечный слой и не делая повторной пилоромио-
гомии. Однако всс-таки целесообразнее надежно
восстановить поврежденную слизистую двухряд-
ными швами и осуществить полную коррекцию пу-
тем повторной пилоромиотомии, тем более, что это
требует совсем немного операционного времени
и усилий. Минимальным кровотечением, отмечаю-
щимся при пилоромиотомии из разделенных краев
мышц и обусловленным венозным стазом, можно
пренебречь. Это подсачивание крови обычно само-
стоятельно прекращается, как только пилорус по-
гружают в брюшную полость. Брюшную стенку
послойно ушивают рассасывающимися швами.
Края кожи сближают подкожным рассасывающим-
ся швом или полосками стерильного пластыря, что
обеспечивает образование совсем незаметного руб-
чика.
Считается, что в течение первых 18 часов после
операции у ребенка отмечается атония желудка,31
но, по нашим наблюдениям, в неосложненных пер-
форацией случаях кормление небольшими порция-
ми глюкозы может быть начато уже через 8 часов
после пилоромиотомии. Затем переходят на сце-
женное грудное молоко или смеси, постепенно,
в течение 24—36 часов, увеличивая объем кор-
млений и промежутки между ними. Подобная так-
тика позволяет через 2—3 дня после операции
выписывать ребенка из больницы на полном энте-
ральном питании. Если интраоперационно прои-
зошла перфорация слизистой, то необходимо дре-
нировать желудок назогастральным зондом и тогда
кормление начинают через 24 часа после опе-
рации.
Из осложнений, наблюдающихся после пилоро-
миотомии, прежде всего следует отметить продол-
жающиеся рвоты и инфицирование операционной
раны, вызываемое, как правило, золотистым
стафилококком. Раневую инфекцию, расхождение
краев раны и послеоперационное кровотечение ча-
сто в прошлом связывали непосредственно с самим
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 327
оперативным вмешательством — пило ром иотомией
по Рамштедту.2 Однако в настоящее время опера-
ция производится та же самая» а частота ослож-
нений значительно снижается, что, скорее всего,
можно объяснить более ранней диагностикой, а со-
ответственно, реже возникающими до операции
тяжелыми нарушениями питания, а также совер-
шенствованием хирургической техники. При боль-
шой давности заболевания рвоты в послеопера-
ционном периоде отмечаются чаще, что обычно
требует более длительного пребывания ребенка
в стационаре. Сохранение рвот в течение более
чем 7 дней после операции, должно вызывать по-
дозрение на неполноценно проведенную пилороми-
отомию, но подобная ситуация бывает редко. Если
после операции ребенок длительно не усваивает
питание, это иногда вынуждает проводить конт-
растное рентгенологическое обследование. Однако
следует помнить, что это обследование имеет зна-
чение в основном в плане возможности неожиданно-
го выявления несостоятельности пилоруса и выхода
контрастного вещества из его просвета. Определить
же, полноценно ли была произведена пилоромио-
томия, достаточно сложно, ибо даже после успеш-
ной хирургической коррекции пилоростеноза пило-
рус может в течение нескольких недель после опера-
ции продолжать выглядеть так же. как и до нес.32
В редких случаях неполной пидоромйотомии»
проявляющейся послеоперационными рвотами, по-
вторная операция должна производиться не ранее
2—3-й недели. За это время проходит отек в зоне
вмешательства, что способствует снижению часто-
ты и интенсивности рвот, в результате чего не-
обходимость в повторном вмешательстве порой от-
падает. Если же все-таки операция потребуется, то
за этот 2—3-недельный срок уменьшается опас-
ность возникновения кровотечения во время вто-
рой операции. Осуществление повторной пилоро-
миотомии в другом участке (не на месте первой
пилоромиотомии) снижает шансы на повреждение
слизистой и развитие кровотечения. В любом слу-
чае при выписке ребенка из стационара родителей
следует предупредить, чтобы они старались давать
малышу возможность «отрыгнуть» воздух во время
и после каждого кормления. Это способствует
предотвращению рвот.
Поздние («хронические») послеоперационные
осложнения редко возникают после пилоромиото-
мии по Рамштедту, однако в одной из опублико-
ванных работ приводятся сведения об увеличении
у пациентов, оперированных по поводу пилоросте-
ноза, частоты язвенной болезни.33 Больше ни в ка-
ких других исследованиях, проводившихся с изуче-
нием отдаленных результатов, эти данные нс на-
шли достоверного подтверждения.34 В то же время
консервативное лечение пилоростеноза имеет чет-
кую связь с развитием в последующем пептиче-
ских язв.27
Мембрана антрального отдела желудка
Мембрана антрального отдела желудка обычно вы-
зывает частичную непроходимость с коварным те-
чением и порой поздним началом клинических
проявлений.35 Единственным симптомом в течение
хпительного периода времени может быть рвота
без примеси желчи. Иногда первым отклонением,
которое обращает на себя внимание врачей, явля-
ется отставание в физическом развитии и отсутст-
вие прибавки массы тела. У некоторых детей диаг-
ноз ставится очень поздно — в возрасте несколь-
ких (до 6) лет.36 А в литературе имеется даже
описание случая, когда диагноз был поставлен
у пациента на восьмом десятке жизни.37 У взрос-
лых больных поздняя и ошибочная диагностика
иногда связана с 1ем. что мембрана может быть
и приобретенной, образующейся вторично в ре-
зультате деформации, обусловленной рубцеванием
язвы при язвенной болезни.
Врожденная мембрана анатомически представля-
ет собой перегородку, расположенную в подслизи-
стом слое дистальной части антрального отдела
и покрытую слизистой желудочного типа. Что ка-
сается этиологии, то считается, что мембрана чаще
всего возникает в результате неполной реканали-
зации передней кишки в эмбриональном периоде.
Первыми симптомами являются боли в эпигастрии,
рвота после еды и отставание в развитии. Осмотр
обычно нс помогает в диагностике. Хотя диагноз
и может быть установлен при рентгенологическом
исследовании (с ЭОПом) верхних отделов желу-
дочно-кишечного тракта с использованием густого
бария (рис. 24-3), но чаще всего мембрана выявля-
ется при гастроскопии.38 Во время операции опре-
делить место расположения мембраны помогает
проведение за антральный отдел желудка катетера
с баллоном на конце, раздувание баллона и осто-
рожное подтягивание катетера назад (рис. 24-4).
□тот прием позволяет произвести продольный раз-
рез над местом расположения мембраны, иссечь
часть ее, если это необходимо, и ушить поперечно
для предотвращения стеноза. Поскольку мембрана
состоит из подслизистого и слизистого слоя (без
мышц), опа часто сокращается во время иссечения
настолько, что ее очень трудно определить даже
при непосредственном осмотре и хорошем доступе.
Операция приводит к излечению без каких-либо
последствий. И хотя в литературе имеются единич-
ные сообщения об успешной консервативной тера-
пии,39 тем нс менее хирургическое лечение оста-
ется методом выбора.
Дискинезия антрального отдела желудка
В литературе периодически появляются сообщения
о детях с хронической рвотой без примеси желчи,
которым сначала ставится диагноз ГЭР или хала-
зии, однако в конечном счете у них выявляется
дискинезия (нарушение двигательной активности)
антрального отдела желудка.40 Возраст этих паци-
ентов обычно до года. При рентгенологическом об-
следовании с барием у них отмечается задержка
опорожнения желудка, воронкообразная конфигу-
рация антрального отдела, отсутствие его пери-
стальтики и ГЭР. Эзофагеальная манометрия
и pH-проба позволяют исключить диагноз первич-
328 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
Рис. 24 3. Мембрана аитрального отдела желудка
у годовалого мальчика. В препилорическом отделе
видна тонкая перегородка, очерченная барием
(стрелка).
ного ГЭР. У большинства этих больных тоста точ-
но эффективным оказывается консервативное ле-
чение, заключающееся в переходе на частые корм-
ления малыми объемами густои пищи. Однако, по
данным литературы, 40% детей все-таки потребо-
вали пилоропластики, принесшей выздоровление.
Дискинезия антрального отдела — не такая частая
патология, однако о ней не следует забывать при
наличии у детей младшего возраста (но не ново-
рожденных) рвот без желчи.
Атрезия привратника
Пилорическая атрезия— достаточно редкая пато-
логия и встречается в 1 % среди всех атрезий же-
лудочно-кишечного тракта. У матери при этом,
как правило, отмечается многоводие. Клинически
данный порок проявляется рвотами без желчи. На
рентгенограммах виден заполненный воздухом же-
лудок и отсутствие газа дистальнее антрального
отдела. Иногда отмечается наследственный харак-
Рис. 24-4. Через гаетротомическос отверстие
видна мембрана антрального отдела желудка,
канюлированная катетером с баллоном на вер-
хушке. У этого мальчика 2,5 лет отмечались
хронические рвоты без примеси желчи после
кормления.
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 329
тер данной патологии— в литературе существует
описание 15 больных с пилорической атрезией
в 7 семьях.41 Атрезия привратника может также
быть компонентом синдрома Herliiz 42 — заболева-
ния, передающегося аутосомно-рецессивным путем
и проявляющегося пузырчаткой (сливающейся)
кожи и дефектом в десмосомной пластинке слизи-
стой желудка. Атрезия отличается от мембраны
полным разъединением стенки желудка на уровне
привратника. При оперативном вмешательстве
предпочтительно иссечение перегородки с попе-
речной пилороп ласти кой. Иногда показано нало-
жение гастродуоденоанастомоза. Следует по воз-
можности избегать создания гастроеюноанастомо-
за, чтобы уменьшить возможность развития таких
осложнений как анастомотическая язва. После
операции у детей часто отмечается небольшой диа-
метр 12-перстной кишки, задержка опорожнения
желудка и ГЭР, а соответственно проблемы, свя-
занные с аспирацией. Поэтому рекомендуется во
время вмешательства проводить катетер за зону
анастомоза, чтобы облегчить питание до тех пор,
пока не увеличится 12-псрстная кишка.
Удвоение желудка
Кистозное удвоение желудка в зависимости от
локализации может проявляться рвотой как с
желчью, так и без желчи. Киста обычно представ-
ляет собой продолжение стенки желудка и распо-
ложена, как правило, в области большой кривиз-
ны, но порой она отделена от желудка и прикреп-
ляется к поджелудочной железе.43 Четыре критерия
позволяют отнести образование к кистозному уд-
воению желудка: (1) внутренняя выстилка эпи-
телием пищеварительного тракта; (2) наличие
наружного гладкомышечного слоя; (3) кровоснаб-
жение от желудочных сосудов и (4) связь с же-
лудком (киста является как бы его продолжени-
ем).44 Если первые три признака имеются всегда,
то четвертым многие клиницисты пренебрегают
при постановке диагноза кистозного удвоения же-
лудка.
Эта патология чаще встречается у девочек
и в 50% случаев сочетается с другими пороками,
преимущественно с удвоением других отделов же-
лудочно-кишечного тракта (например, удвоение
или даже «утроение» пищевода) и вертебральными
аномалиями. Считается, что этиологическую роль
играет деформация хорды в виде ее расщепления.46
Удвоение имеет цилиндрическую или кистозную
форму, общую с желудком стенку и может сооб-
щаться (или не сообщаться) с просветом желудка.
Основным клиническим симптомом является рвота
без желчи. Более часто встречается кистозная фор-
ма удвоения, не сообщающегося с желудком. Этот
вариант патологии может проявляться желудочно-
кишечным кровотечением, развивающимся вторич-
но на Фоне изъязвления слизистой выстилки ки-
сты.47 4 Как при цилиндрической, так и при ки-
стозной форме иногда отмечаются боли в животе
и потеря массы тела. Из других проявлений следу-
ет назвать пневмонию, выпот в плевре и панкреа-
тит,50 которые непосредственно связаны с кистой,
ибо она иногда распространяется в грудную клетку
или имеет евнщевое соединение с поджелудочной
железой.51 Оба типа кист, если они связаны с же-
лудком, обычно имеют относительно большие раз-
меры (от 3 до 6 см) и часто пальпируются в виде
опухолевидного образования в животе.47-49
Цилиндрический тип чаще локализуется в обла-
сти большой кривизны желудка вблизи антрально-
го отдела. Кисты, которые нс связаны с желудком,
обычно прикрепляются к поджелудочной железе
или располагаются около нес, причем сама железа
при этом тоже аномально развита.52 Рвота у таких
больных связана, как правило, с панкреатитом,
а не с механической обструкцией.50 Рвотные массы
обычно имеют примесь желчи. Иссечение кисты
путем вылущивания се из общей с желудком стен-
ки или с частью подлежащей стенки желудка при-
водит к выздоровлению. Если киста выстлана же-
лудочной слизистой, но не связана со стенкой же-
лудка, то для полноценной коррекции может по-
требоваться и частичное иссечение закупоренной
или аномально развитой доли поджелудочной же-
лезы (рис. 24-5). Марсу пиал изация не должна
применяться при этой патологии, поскольку приво-
дит не только к осложнениям, но и к поздним ле-
тальным исходам, связанным с возможным пере-
рождением стенки кисты в карциноидную опу-
холь.53
Заворот желудка
Заворот желудка, впервые описанный Berti в
1866 г., редко возникает в детском возрасте —
в литературе представлен всего 51 случай.54 Эта
патология является результатом аномальной рота-
ции одной части желудка вокруг другой. Если ро-
тация происходит вокруг линии, соединяющей кар-
диальный отдел и пилорус, то за ворог носит на-
звание органоаксиального (по оси), если же вокруг
линии, соединяющей большую и малую кривиз-
ну — мезентерикоаксиального. В редких случаях
ротация возникает в обоих направлениях, и тогда
развивается смешанный заворот. Желудок в четы-
рех местах фиксирован связками к окружающим
его органам: диафрагме, печени, селезенке и обо-
дочной кишке. Примерно в 65% случаев заворот
желудка связан с аномалиями диафрагмы и недо-
статочностью фиксации желудка в области пище-
водного отверстия.54 Заворот желудка может соче-
таться и с другими пороками, такими как аспле-
ния,55 но бывает и идиопатическим.
Заболевание может протекать остро или носить
рецидивирующий характер. В 50% случаев, опи-
санных в литературе, заворот встретился у детей
до года жизни.54 Первыми симптомами являются
рвоты или позывы на рвоту и боли в животе. При
завороте нередко возникает расширение желудка,
в частности у больных с пилоростенозом или у па-
циентов с задержкой психического развития и
аэрофагией.56 Очень важна ранняя диагностика,
330 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
Рис. 24-5. Иссеченная добавочная доля
поджелудочной железы (маленькая
стрелка) и соединенное с ней эктопиче-
ское кистозное удвоение желудка (боль-
шая стрелка) у 8-лет ней лепочкн с хро-
ническим панкреатитом.
поскольку быстро может возникнуть тяжелое же-
лудочное кровотечение и некроз стенки желудка.
Триада Борхардта. представляющая собой сочета-
ние позывов на рвоту, остро возникшего вздутия
в эпигастральной области и невозможности ввести
зонд в желудок, характерна для заворота желудка
у взрослых, но нс имеет существенного значения
у детей, поскольку в детском возрасте могут быть
и другие тяжелые заболевания, не связанные с за-
воротом, но проявляющиеся такими же симпто-
мами.57
Диагноз ставится с помощью контрастной рент-
генографии. При мезентерикоаксиальном заворо-
те отмечается непроходимость желудка, переверну-
того «вверх дном», при этом антральный отдел
часто расположен в грудной клетке (рис. 24-6).
Рентгенологическая картина органоаксиального
заворота не столь яркая — на снимках виден гори-
зонтально лежащий желудок с более низко, чем
обычно, расположенным гастроэзофагеальным пе-
реходом и иногда с деформацией 12-перстной киш-
ки (рис. 24-7). Детей с симптомами острого заво-
рота желудка необходимо после кратковременной
подготовки срочно оперировать, пока не возник
некроз желудка. Наилучший доступ — абдоминаль-
ный. Во время вмешательства важно устранить все
сочетанные аномалии, произвести пластику ножек
диафрагмы и фиксацию желудка. Операция дол-
жна быть завершена созданием гастростомы.
ВРОЖДЕННАЯ МИКРОГАСТРИЯ
Врожденная микрогастрия, при которой желудок
имеет небольшие размеры и цилиндрическую фор-
му, встречается редко и, как правило, сочетается
с какой-либо из следующих аномалий (или даже
со всеми сразу): нарушение ротации желудка или
кишечника, грыжа пищеводного отверстия диа-
фрагмы, мегаэзофагус, дуоденальная атрезия, situs
inversus, аспления, поперечное расположение пече-
ни, отсутствие желчного пузыря, анофтальмия,
олигодактилия и другие аномалии скелета.58 61
Врожденная микрогастрия обычно проявляется ра-
но возникающими рвотами или гастроэзофагеаль-
ным рефлюксом, нарушениями питания и задерж-
кой развития. Может также отмечаться диарея, ко-
торая объясняется небольшими размерами желуд-
ка, быстрым его опорожнением и соответственно
демпинг-синдромом. Диагноз микрогастрии ставит
ся при контрастном рентгенологическом исследо-
вании (рис. 24-8).
Вначале при врожденной микрогастрии может
оказаться вполне эффективным консервативное
лечение с зондовым питанием, но чаще всего воз-
никает необходимость в создании искусственного
желудка в виде резервуара из тощей кишки.61 От-
мечающийся при микрогастрии ГЭР иногда тре-
бует ангирефлюксной операции, которая, однако,
может в последующем в свою очередь привести
к дальнейшему уменьшению объема желудка, что
тем более вынуждает идти на еюногастральную
пластику. Целесообразность применения вагото-
мии и перевернутого сегмента кишки не доказана,
поэтому данные операции следует приберечь для
того случая, когда в дальнейшем, как это иногда,
к сожалению, бывает, может потребоваться повтор-
ное хирургическое вмешательство. В литературе
имеются сообщения о том, что пациенты, опериро-
ванные по поводу врожденной микрогастрии, до-
живали до старости, однако в большинстве случаев
у таких больных отмечается задержка развития
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 3!
Рис. 24-6. А, Рентгенограмма брюшной полости у ребенка с мсзентсрикоакс мильным запоротом желудка, развинтимся после ко
рек пни сколиоза. Виден расширенны ft желудок.
В, При исследовании с барием выявлена ротация желудка вокруг ливни, соединяющей большую и малую кривизну (мезентернк
аксиальным запорот). Желудочно-пищеводный переход расположен каутальнсс привратника.
Рис. 24-7. А, Рентгенограмма брюшной полости iрудного ребенка с задержкой психического развития, аэрифагмеи и органоакс
альным запоротом желудкм-
В, Исследование с барием выявило ротацию желудка вокруг линии, соединяющей пищеводное отверстие с привратником
оргяиоаксиалъный запорот.
332 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
Рис. 24-8. Микрогастрия с небольшим цилиндрическим желуд-
ком и уменьшенной о диаметре 12-перстной кишкой.
ПЕПТИЧЕСКИЕ ЯЗВЫ
Пептические язвы у детей — довольно распростра-
ненная патология, но редко требующая оператив-
ного вмешательства, а соответственно ее, как пра-
вило, не относят в разряд хирургических заболева-
ний детского возраста.62 В связи с этим важно
отметить, что примерно у 2% взрослых больных
с язвенной болезнью первые симптомы появляются
в детстве.63 Разделение язв у детей на первичные
и вторичные очень важно для определения патоло-
гии, лежащей в основе язвенной болезни, и для
выбора адекватной терапии.64 Первичные язвы
развиваются при отсутствии фоновой патологии,
в то время как вторичные возникаю-) вследствие
таких стрессовых ситуаций, как: (1) обширные
ожоги (язвы Курлинга), (2) поражения, приводя-
щие к повышению внутричерепного давления (яз-
вы Кушинга), (3) прием ульцерогенных препа-
ратов.
Первичные язвы обычно имеют тенденцию
к хроническому течению, локализуются в
12-перстной кишке, более часто встречаются у па-
циентов с группой крови 0, обладают семейно-на-
следственным характером (40+%) 62 и возрастны-
ми особенностями, а также связаны с повышенной
секрецией желудочной кислоты. В течение первых
дней жизни отмечается физиологическое одновре-
менное увеличение продукции желудочной кисло-
ты и уровня гастрина сыноротки.65 Затем изна-
чально высокая секреция кислоты уменьшается и в
течение нескольких месяцев жизни достигает уров-
ня взрослых.66 Однако у детей с первичной язвен-
ной болезнью изменения кислотности желудочного
сока и скорости секреции непредсказуемы.67
Язвы, возникающие в первые 1—2 недели жиз-
ни, как правило, острые, чаше локализуются в же-
лудке и первыми их проявлениями обычно бывают
уже осложнения, такие как кровотечение и/или
перфорация. При кровотечении лечение проводит-
ся путем промывания желудка, применения анта-
цидных препаратов и, если необходимо, перелива-
ния крови. Хирургическое вмешательство показано
в тех случаях, когда кровопотеря за 24 часа дости-
гает объема циркулирующей крови. Операция за-
ключается в ушивании язвы без вмешательств, на-
правленных на уменьшение продукции желудоч-
ной кислоты Рецидив язвы у детей этой группы
чрезвычайно редок.64
У старших дегей первичные язвы желудка встре-
чаются относительно редко и проявляются болями
в животе неопределенного характера, потерей мас-
сы тела и плохим аппетитом 6’ Первичная язвен-
ная болезнь в детском возрасте часто (в 30%
случаев) носит наследственно-семейный харак-
тер.62 При желудочно-кишечном кровотечении и
подозрении на язву желудка эндоскопическое ис-
следование в 100% случаев позволяет поставить
точный диагноз.62 Если кровотечение вызвано еди-
ничной язвой, то его обычно удается остановить
с помощью лаважа желудка, применения антацид-
ных препаратов и П2-блокаторов, а потому к хи-
рургическому вмешательству редко приходится
прибегать. В большинстве случаев консервативная
терапия эффективна, однако часто возникает ре-
цидив язвы. И гем не менее хирургическое лечение
у детей применяется в редких случаях, особенно
у пациентов в возрасте до 8 лет, и строго по инди-
видуальным показаниям.70 Если оперативное вме-
шательство все же предпринимается, го оно заклю-
чается в селективной ваготомии, высокоселектив-
ной ваготомии или стволовой ваготомии с пило-
ропластикой, именно в таком порядке предпочте-
ния (по убывающей). Доказано, что антрэктомия
у детей влечет за собой возможность поздних
осложнений.71 Синдром Золлингера — Эллисона
редко встречается в детском возрасте72 и обычно
может быть диагностирован по уровню гастрина в
сыворотке с резкими изменениями кальция или
без них.73 В литературе существует описание
случая, когда применение Н2-блокаторов у паци-
ента с синдромом Золлингера Эллисона позво-
лило обойтись без тяжелого хирургического вме-
шательства.74
Как уже было сказано, у детей язвы обычно
вторичные и связаны со стрессом, например, язвы
Курлинга при ожогах или Кушинга при опухолях
и других поражениях головы, а также язвы, разви-
вающиеся как осложнение применения лекарствен-
ных препаратов — аспирина и стероидов. Все яз-
вы, за исключением язв Кушинга, являются ре-
зультатом не столько увеличенной продукции же-
лудочной кислоты, сколько нарушения защитного
механизма слизистой в отношении обратной диф-
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 333
фузии НЛ75, 7ft Вторичные язвы всегда острые, воз-
никают наиболее часто у детей в возрасте до 6 лет
и обычно проявляются желудочно-кишечным кро-
вотечением (81 %).62 Они поверхностные, множе-
ственные, речко требуют хирургического вмеша-
тельства, поскольку хорошо поддаются лечению
промыванием желудка и применением антацидных
препаратов, поднимающих уровень pH в желудке
выше 4,0. При язвах Кушинга (но не прн других
формах вторичных стрессовых язв) могут быть ис-
пользованы Н2-блокаторы. В одной из опублико-
ванных работ сообщается о необычно высокой ча-
стоте единичных стрессовых язв желудка у детей.77
При неэффективности консервативной терапии
у пациентов с острой кровоточащей язвой и поте-
рей кровн, превышающей 0,5 мл/мин, для обнару-
жения места кровотечения может потребоваться
артериография, которая в подобной ситуации бо-
лее информативна, чем эндоскопия.78 Оперативное
вмешательство на высоте кровотечения сопровож-
дается высокой летальностью (60%), а потому по-
казано у старших детей лишь при такой интенсив-
ности кровотечения, когда ребенок за 24 часа теря-
ет половину ОЦК.79
Нет какого-либо единого общепринятого метода
хирургического вмешательства при язвах, хотя
наиболее часто применяется лигирование кровото-
чащих сосудов, а при перфорации — ушивание
или закрытие дефекта серозным лоскутом с ваго-
томией и пилоропластикой. Имеются сообщения об
успешном применении у детей при кровоточащих
стрессовых язвах селективной интраартериальной
£0
инъекции вазопрессина.
ПЕРФОРАЦИЯ ЖЕЛУДКА
Перфорация желудка бывает двух типов: спонтан-
ная у новорожденных и посттравматическая. Спон-
танная нерфорация желудка обычно возникает
у здоровых новорожденных в возрасте от 2 до
7 дней. Этиология ее до сих пор остается не-
ясной. Одна из предполагаемых причин — врож-
денный дефект мускулатуры,53 однако нельзя иск-
лючить, что наблюдаемый в этих случаях дефект
может быть вторичным, образующимся в резуль-
тате сокращения мышц по краям уже возникшего
перфорационного отверстия. Подтверждением то-
му являются данные тщательного исследования
большого количества случаев перфорации, не об-
наружившего врожденного отсутствия желудочной
мускулатуры.81 Недоношенность н асфиксия ново-
рожденных также считаются возможными этиоло-
гическими факторами, но в большинстве наблюде-
ний, описанных в литературе, эти факторы отсут-
ствовали. Предполагается, что определенную роль
может играть обструктивное поражение дисталь-
ных отделов желудка с повышением внутриже-
лудочного давления, поскольку повреждение
желудка без перфорации обнаруживается при
обструкции, связанной с пилоростенозом.84 Однако
механическая обструкция также отсутствует у
большинства детей с перфорацией. Одной из
редких причин перфорации может быть повы-
шение внутрижелудочного давления при раздува-
нии воздухом во время масочной или мешочной
вентиляции.
Клинические проявления спонтанной перфора-
ции желудка у новорожденных обычно заключа-
ются в отказе от еды, вялости и вздутии живота.
В последующем развивается дыхательная недоста-
точность, связанная с высоким стоянием диафраг-
мы и ограничением ее экскурсий, а также мета-
болический ацидоз.81 Главный диагностический
симптом перфорации — пневмоперитонеум на рент-
генограммах. Для перфорации желудка характерно
наличие большого количества воздуха в свободной
брюшной полости. Гели воздуха немного, то он
наиболее отчетливо определяется на рентгенограм-
мах в вертикальном положении под диафрагмой,
на левой боковой рентгенограмме в горизонталь-
ном положении — в околопечеиочиом пространст-
ве, а в латеропозиции — в периумбнликальной об-
ласти.
Если пациент находится на ИВЛ с положитель-
ным интратрахеальным давлением, следует на
рентгенограммах внимательно рассмотреть средо-
стение, чтобы не пропустить наличие там воздуха.
У любого ребенка, а особенно у недоношенных
детей, может произойти разрыв альвеол с выходом
воздуха в средостение и затем через аортальное
отверстие диафрагмы в свободную брюшную по-
лость?6 Эту ситуацию трудно отдифференцировать
от истинной спонтанной перфорации новорожден-
ных, а потому при наличии сомнений показана
лапаротомия.
Травматическая перфорация желудочно-кишеч-
ного гракта возникает у детей довольно редко, по-
скольку в детском возрасте чаще бывает тупая
травма живота. Вторичное повреждение желудка
при тупой травме также встречается нечасто —
в 0,9—1,8% всех случаев слепой травмы.87 В боль-
шинстве наблюдений повреждение желудка возни-
кает обычно, когда желудок полный (вскоре после
еды), поскольку растянутый и заполненный пн щей
желудок легче травмируется, чем пустой.88 При
осмотре у ребенка с травматической перфорацией
имеются симптомы раздражения брюшины. На
рентгенограммах виден воздух в свободной брюш-
ной полости. Иногда помогает в диагностике рент-
генологическое исследование с водорастворимыми
контрастными веществами.
Как только поставлен диагноз перфорации поло-
го органа, необходимо срочно зондировать желу-
док для его декомпрессии. Иногда зонд выходит
через перфорационное отверстие желудка в брюш-
ную полость, что определяется на рентгенограмме.
После кратковременной интенсивной подготовки,
включающей, кроме всего прочего, антнбиотикоте-
рапию, производится срочная операция. Если
в процессе предоперационной подготовки повы-
шенное внутрибрюшное давление приводит к тя-
желому тахипноэ или дыхательным расстройствам,
то необходимо осуществить экстренную декомп-
рессию путем введения в брюшную полость иглы
или катетера. Поперечный разрез обеспечивает
прекрасный доступ и надежное послойное ушива-
334 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
ние брюшной стенки. При травматическом повреж-
дении у старших детей предпочтительна срединная
лапаротомия, позволяющая более тщательно реви-
зовать брюшную полость и корригировать сочетан-
ную травму внутренних органов. Чаще всего
встречается сопутствующее повреждение селезен-
ки и поджелудочной железы.
Спонтанная перфорация желудка у маленьких
детей наиболее часто происходит по переднебоко-
вой поверхности большой кривизны, ближе к кар-
диальному отделу. Если перфорационное отвер-
стие имеет иную локализацию, то его обычно до-
вольно трудно обнаружить. Поэтому необхо щмо
полностью мобилизовать желудок, чтобы тщатель-
но осмотреть всю заднюю стенку, уделив особое
внимание желуточпо-пищеводному переходу.88 Но
даже при таком подходе место перфорации во вре-
мя вмешательства не обнаруживается приблизи-
тельно у 10% детей. В большинстве случаев пер-
форационное отверстие имеет длину от 1 до 3 см,
края его неровные, истонченные и некротически
изменены. В брюшной полости обычно выявляется
большое количество мутного выпота и фибриноз-
ного экссудата. Измененные края должны быть ис-
сечены до жизнеспособных кровоточащих тканей,
после чего желудок послойно ушивают.8' В ряде
случаев целесообразно завершить вмешательство
гастростомией (с целью послеоперационной деком-
прессии), но показания к ней должны быть избира-
тельными и зависят, в основном, от того, какая
часть желудка осталась после иссечения. Необхо-
димое гь в классической резекции желудка возни-
кает редко и большинством хирургов это вмеша-
тельство не рекомендуется. В прежние годы ле-
тальность при данной патологии была 100%-ной.
В настоящее же время прогноз значительно улуч-
шился. О тако до 25% детей со спонтанной пер-
форацией желудка все-таки гибнут, что связано,
как правило, с тяжестью состояния до операции,
поздней диагностикой и септическими осложне-
ниями.81
Травматическая перфорация желудка обычно
происходит по передней его поверхности ближе
к малой кривизне, но может отмечаться и любая
другая локализация.’0 Важно во время операции
тщательно ревизовать весь желудок. Для осмотра
задней стенки необходимо войти в малый сальник
(через большой). Края перфорационного отвер-
стия иссекают и желудок ушивают 2-рядными
швами с или без декомпрессионной гастростомии.88
Прогноз определяется в основном пооперационным
состоянием ребенка и сочетанными повреждения-
ми, в частности, селезенки и поджелудочной же-
лезы. Травматическая перфорация желудка воз-
никает, как правило, в автомобильных авариях,
а потому относительно рано диагностируется
и вмешательство обычно производится достаточно
своевременно. Однако причиной этого поврежде-
ния могут быть и удары руками или ногами по
животу при жестоком обращении с детьми. В по-
добных ситуациях диагноз как повреждения же-
лудка, так и сочетанной травмы, обычно ставится
поздно, что обусловливает высокую летальность.90
В редких случаях возникает отсроченная перфора-
ция, когда вначале повреждаются желудочно-саль-
никовые сосуды, что приводит к последующему
локализованному некрозу желудка и перфо-
01
рации.
ГАСТРОСТОМИЯ
Гастростомия нередко создается у детей с невроло-
гической патологией для декомпрессии желудка
и кормления, а также широко используется как
первый этап при хирургическом лечении пациен-
тов с врожденным трахеопищеводным свищом.
Кроме того, она чрезвычайно популярна как метод
послеоперационной декомпрессии и энтерального
питания у детей с атрезией кишечника или состоя-
ниями. при которых возникает укорочение длины
кишечника, а соответственно ожидается длитель-
ная его дисфункция. Наиболее широко известны
два метода гастростомии: по Штамму и по Джей-
нуэю. Однако до настоящего времени постоянно
предпринимаются попытки модифицировать это
вмешательство, чтобы сделать его менее инвазив-
ным. При этом ставятся следующие цели: (1)
устранить необходимость в общем наркозе, (2) со-
кратить период послеоперационного выздоровле-
ния, (3) снизить частоту осложнений, связанных
с образованием спаек в брюшной полости, и (4)
уменьшить стоимость операции. Все эти цели
практически достигнуты, благодаря внедрению и
широкому распространению метола чрескожной эн-
доскопической гастростомии (ЧЭГ),92 а также
гастростомии без эндоскопии.93 Последний метол
заключается в чрескожном введении внугрижелу-
дочного спирального катетера без эндоскопии с по-
мощью рентгеноскопического (с ЭОПом) или ульт-
развукового исследования. Однако эта техника не
позволяет фиксировать желудок к брюшной стен-
ке, в результате чего в раннем послеоперационном
периоде может отмечаться подтекание желудочно-
го содержимого, причем не только наружу, но
и интраперитонеально. Поэтому неэндоскопиче-
ская чрескожная гастростомия применяется редко.
Значительное расширение показаний к гастро-
стомии вызывает у многих настороженность, по-
скольку приводит к возникновению новой пробле-
мы — увеличению частоты постгастростомическо-
го гастроэзофагеального рефлюкса с соответствую-
щими клиническими проявлениями 94 (см. гла-
ву 23). Неизбежное при наложении гастростомы
смещение желудка книзу может изменясь нормаль-
ный до этого угол Гиса, что объясняет частичную
утрату механизма, направленного на предотвраще-
ние патологического ГЭР.’’ Возможность развития
рефлюкса после гастростомии была продемонстри-
рована в эксперименте на животных и подтвержде-
на клиническими исследованиями, показавшими
высокую частоту ГЭР у пациентов, которые не
имели его до создания гастростомы.14 В настоя-
щее время для выявления ГЭР широко использу-
ется pH-мониторинг, имеющий важное диагности-
ческое значение. Следует помнить, что получен-
ные при этом показатели не всегда точны и в неко-
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 335
торых клинических ситуациях могут быть ниже
истинных, в частности, у детей с задержкой умст-
венного развития с элементами спастики. И хотя
гастростомия для питания все еще широко исполь-
зуется у неврологических больных со спастически-
ми проявлениями, однако при этом необходимо
проявлять большую осторожность, внимательно
и длительно наблюдая ребенка в послеоперацион-
ном периоде, даже если pH-исследование до опера-
ции не выявило патологического рефлюкса. Высо-
кая частота рефлюкса у неврологических больных
заставляет в большинстве случаев, даже у паци-
ентов, не имеющих никаких симптомов и жалоб,
проводить до операции тщательное исследование,
чтобы исключить диагноз ГЭР, а при его выявле-
нии дополнить гастростомию антирефлюксной
операцией.96
Операция Штамма наиболее часто применяется
с целью создания гастростомы для питания, как
временной, так и постоянной — на длительный пе-
риод. Данное вмешательство можно производить
под местной анестезией с седатацией, но при ис-
пользовании общего наркоза операция значитель-
но облегчается. Разрез производят верхнесредин-
ный с разделением левых прямых мышц живота
или левосторонний поперечный в верхнем квад-
ранте. В операционную рану выводят дно желудка
в области антрального отдела ближе к большой
кривизне. Место для гастростомии должно быть
достаточно удаленным от пилоруса, что предот-
вращает обструкцию выходного отдела желудка
головкой катетера. Некоторые хирурги предпочи-
тают вводить трубку ближе к малой кривизне, что-
бы избежать нарушения угла Гиса, о чем говори-
лось выше.* Однако наиболее часто для гастросто-
мии выбирается участок, расположенный на одной
трети расстояния от большой к малой кривизне.
Накладывают два кисетных шва, электроножом
рассекают серозно-мышечный слой, а затем прока-
лывают слизистую, которую очень важно вскрыть
отдельно. Эта предосторожность уменьшает риск
повреждения во время гастротомии противополож-
ной стенки желудка. Катетер (с головкой) соответ-
ствующего размера вводят в желудок, после чего
затягивают первый кисетный шов. Затем, слегка
надавливая трубкой вовнутрь, завязывают второй
шов, погружая при этом первый. Данный прием
позволяет создать вокруг трубки короткий туннель
из стенки желудка (рис. 24-9А), Трубку вывозят
наружу через отдельный прокол брюшной стенки
в подреберье таким образом, чтобы не было значи-
тельного натяжения желудка вниз или раздраже-
ния края ребер, что может привести к перихондри-
ту. Желудок фиксируют к брюшной стенке двумя
Рис. 24-9. А, Гастростомия „о Штамму. С помощью двойного кисетного ниш создастся желудочный туннель. Желудок надежно
фиксируют к брюшной стенке.
В. Гастростомия по Джен нуэю. Хирургическим путем формируют желудочную «ножку», которая проходит через брюшную
стенку в виде постоянного свища.
336 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
или четырьмя швами для предотвращения его от-
хождения и интраперитонеального подтекания со-
держимого. Трубку подшивают к коже, чтобы она
в дальнейшем не смещалась. Кормить через гаст-
ростому можно через 24—36 час.
В тех случаях, когда предполагается длительное
питание через гастростому, некоторые хирурги
операцией выбора считают гастростомию по Джей-
нуэю (рис. 24-9В). Преимущество этого метода
перед другими состоит в возможности периодиче-
ского введения трубки (только на время кормле-
ния) и отсутствии подтекания желудочного содер-
жимого при ее удалении. Кроме того, желудок
прочно фиксирован к брюшной стенке, поскольку
хирургически сконструированная желудочная
трубка идет от его дна через брюшную стенку
с выбуханием наружу небольшого сосочка полно-
слойной желудочной стенки. Но с другой стороны,
наличие этого «сосочка» способствует развитию
таких серьезных осложнений, как пролапс слизи-
стой желудка с ишемией и кровотечением. К тому
же трудно предотвратить подтекание желудочного
содержимого, если не ставить постоянный катетер,
особенно у маленьких детей Поэтому данное вме-
шательство не так популярно в детской хирургии,
как операция Штамма, тем более, что в последнее
время постоянно предлагаются и внедряются раз-
личные улучшенные варианты приспособлений
для стом (катетеры, приемники).
ЧЭГ является в настоящее время операцией вы-
бора у детей, нуждающихся в гастростоме для пи-
тания, но не имеющих данных за ГЭР и в прошлом
не оперированных.’2 Это в основном пациенты
с поражением нервной системы (без патологии
других органов и систем), которые не могут гло-
тать. ЧЭГ производят под седатацией и местной
анестезией или с общим обезболиванием. Наибо-
лее важный технический момент — чрескожное
проведение катетера (с прокалывающей иглой, ко-
торая затем извлекается) под визуальным контро-
лем через гибкий гастроскоп. В просвет катетера
вводят пить, захватывают ее в желудке гастроско-
пическими щипцами и выводят через рот. Специ-
альный катетер Пеццера с дополнительным ци-
линдрическим валиком прикрепляют к нити и вы-
тягивают антеградно через пищевод в желудок
и наружу через брюшную стенку. Положение ва-
лика и головки катетера в желудке проверяют ви-
зуально через гастроскоп. Второй валик помещают
снаружи и закрепляют в определенном положении,
чтобы предотвратить смещение трубки внутри же-
лудка (рис. 24-10). Эта операция очень широко
применяется и дает минимальное количество по-
слеоперационных осложнений.
Следующей важной ступенью на пути совершен-
ствования этого вмешательства явилась разработ-
ка и внедрение гастросгомичсской «пуговицы», ко-
торая представляет собой короткую силастиковую
трубку с клапаном на одном конце и укрепленным
колпачком для закрытия — на другом” (рис. 24-
11). Пуговица может быть поставлена через 6—
8 недель после гастростомии по Штамму либо пос-
ле ЧЭГ и служит для замещения длинной и отно-
Рис. 24-10. Эндоскопическая чрескожная гастростомия. Трубку
выводят антеградно через брюшную стенку. Фиксируют наруж-
ный валик. Положение и плотность прилегания к слизистой
желудка внутреннего валика контролируют путем осмотра че-
рез гастроскоп.
сительно большой гастростомической трубки. Иу
говицу вставляют амбулаторно, без анестезии. Для
этого удаляют гастростомическую трубку. Измеря-
ют толщину брюшной стенки. Данный показатель,
а также диаметр стоившей гастростомической
трубки позволяют правильно выбрать пуговицу
соответствующего размера, которую ставят с по-
мощью введенного в нее обтуратора. При этом пет
необходимости в какой бы то ни было повязке или
прокладке под ней. Осложнении вокруг стомы воз-
никают очень редко, так же, как и подтекание со-
держимого желудка. Пуговица незаметна под
Рис. 24-11. Гастростомическую пуговицу ставят вместо катетера
Фолея или Пеццера через хорошо сформировавшуюся гастро-
стому (по Штамму или ЧЭГ). Клапан на внутреннем конце
и наружная головка предотвращают подтекание через стому.
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 337
обычной одеждой, очень прочна и, „о нашему опы-
ту, требует смены в связи с изнашиванием клапана
не чаще, чем через каждые 6—9 мес.
Осложнения, и притом достаточно серьезные,
могут возникать при любом виде гастростомии,
сделанной как путем лапаротомии, так и без нес.
Однако совершенствование техники вмешательст-
ва позволило снизить частоту осложнений с 15%
до 7%, а летальность практически свести к ну-
лю.100 Наиболее тяжелое послеоперационное
осложнение — несостоятельность стомы с подтека-
нием желудочного содержимого в брюшную по-
лость и перитонитом. Как уже было сказано, это
обычно происходит при раннем отхождении желуд-
ка от брюшной стенки в результате недостаточной
его фиксации во время гастростомии или смещения
I рубки после операции.
Всякий раз, когда подозревается смещение вновь
поставленной трубки или по каким-либо причинам
производится ее замена в ранние сроки (до 3-й не-
дели после операции), кормление можно начинать
лишь после рентгенологического контроля. Это ис-
следование лучше осуществлять с введением не-
большого количества водорастворимого контраст-
ного вещества, что позволяет не только проконтро-
лировать стояние трубки, но и определить, нет ли
подтекания кои граегного вещества в брюшную по-
лость. Наличие свободного газа не всегда свиде-
тельствует о несостоятельности гастростомы, по-
скольку остаточный ноздух в небольшом количе-
стве может оставаться в брюшной полости в
течение нескольких недель после операции. Для
выяснения положения трубки не следует ограничи-
ваться ее промыванием с обратным отсасыванием
введенной жидкости (без рентгенологического кон-
троля). Эта процедура не позволяет достоверно
судить о положении трубки, поскольку вводимый
раствор иногда попадает во внежелудочную от-
граниченную полость, и тогда его можно при про-
мывании получить обратно, что создает ложное
впечатление о правильном стоянии трубки. При
неосложненной изолированной (без других вмеша-
тельств) гастростомии нормальная функция же-
лудка восстанавливается через 24—48 час. Поэто-
му наличие в более поздние сроки признаков не-
проходимости желудка (рвота, большое количе-
ство содержимого в желудке) служит показанием
к контрастному рентгенологическому обследова-
нию с целью контроля положения трубки.
Если трубка во время гастростомии поставлена
низко, около пилоруса, это может привести к об-
струкции выходного отдела желудка. При недоста-
точном гемостазе подслизистого или слизистого
слоя иногда возникает послеоперационное крово-
течение. Однако следует учесть, что небольшое ко-
личество крови в желудке вскоре после гастросто-
мии — явление нормальное. При значительном же
и упорном кровотечении необходимо исследование
свертывающей системы крови, и порой даже прихо-
ди гея прибегать к хирургическому вмешательству.
Воспаление послеоперационной раны с расхожде-
нием ее краев возникает редко и серьезную проб-
лему представляет обычно лишь в тех случаях.
когда гастростомическая трубка выведена наружу
через ла паротомический разрез. Расхождение
краев раны может привести к тяжелым осложнени-
ям и даже летальному исходу. Когда трубка выве-
дена через отдельный прокол брюшной стенки, то
воспаление раны (если оно возникает) обычно по-
верхностное и хорошо поддается местному лече-
нию с применением антибиотиков (или даже без
них). Более серьезные осложнения возникают
редко.
Местная гиперемия и/или воспаление подкож-
ной клетчатки более часто отмечается в тех случа-
ях, когда используется слишком широкая трубка,
которая давит на брюшную стенку, нызывая ише-
мию тканей вокруг стомы. В подобной ситуации
показано местное лечение и наблюдение. Антибио-
тики следует приберечь на тот случай, если будет
прогрессировать воспаление подкожной клетчатки
или появятся общие симптомы осложнения. Гипе-
ремия вокруг стомы в более позднем послеопера-
ционном периоде обычно связана с мацерацией
или раздражением кожи и хорошо поддается лече-
нию, направленному на «подсушивание» этой об-
ласти с помощью: (1) периодического удаления
трубки, (2) ведения открытым способом (без повя-
зок) и (3) применения местных лекарственных
препаратов.
Необходимость в применении антибиотиков воз-
никает редко — лишь в тех случаях, когда имеют-
ся признаки прогрессирующей инфекции. Поздно
появляющиеся симптомы обструкции выходного
отдела желудка почти всегда связаны с изменени-
ем и нтра гастрального положения трубки и смеще-
нием ее головки в пилорический канал. Иногда
слишком большой внутрижелудочный конец труб-
ки мигрирует в 12-перстную кишку. Маркирование
трубки на уровне кожи или измерение наружной
ее части (сразу после гастростомии) позволяет уха-
живающим за ребенком родственникам и персона-
лу быстро определять возникшее смешение и
устранять его, подтягивая трубку назад и устанав-
ливая ее в правильное положение. Данное ослож-
нение часто возникает у недоношенных и маловес-
ных детей. Предотвратить его можно путем обре-
зания утолщенной головки катетера Пеццера та-
ким образом, чтобы трубка осталась только с од-
ним отверстием и кромкой по окружности. Эта
кромка должна лишь слегка выдаваться в желудок
на небольшую глубину, тогда вероятность ее сме-
щения к пилорусу очень незначительна. Примене-
ние гастростомической пуговицы обычно уменьша-
ет шансы на развитие этого осложнения.
Обструкция желудка после гастростомии может
возникать также в результате вторичной антеград-
ной инвагинации слизистой (при нормальном по-
ложении трубки)."11 Кроме того, интенсивное (или
просто грубое) подтягивание за гастростом и ческ и й
катетер в попытке «прижать» желудок к брюшной
стенке, использование пуговицы неадекватного
размера или перегиб трубки в месте ее выхода
наружу — все это может вести к тканевому некро-
зу и развитию инфекции, в результате гастросто-
мическое отверстие увеличинастся и начинается
22 Заказ № 1622
338 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
подтекание желудочного содержимого иокруг ка-
тетере!.
Гастростомическая трубка в месте ее выхода на-
ружу должна поддерживаться в вертикальном по-
ложении по отношению к брюшной стенке. Для
этого можно использовать различные приспособле-
нии (например, соску от рожка), укрепляй их пла-
стырем, что позволяет предотвратить тканевой не-
кроз. Если гастростомическая пуговица давит на
подлежащие ткани, и в результате возникает гипе-
ремия, необходимо заменить ее на другую, более
подходящих размеров. Вокруг стомы могут так-
же развиться грануляции с выделением экссудата
и/или кровотечением. Избыточную воспалитель-
ную ткань прижигают нитратом серебра. При этом
нет необходимости в местной анестезии, поскольку
грануляционная ткань не имеет иннервации, а по-
тому данная манипуляция безболезненна. Прижи-
гание может проводиться повторно, неоднократно,
до тех пор, пока не будет достигнут эффект как
гигиенический, так и косметический.
После удаления трубки временные гастростомы
обычно закрываются самостоятельно в течение 4—
6 час. Ухаживающий за ребенком персонал или
родители должны быть обучены процедуре замены
(при необходимости, на время) гастростомической
трубки или пуговицы катетером Фолея таких же
размеров (с раздуванием баллона).
Если гастростома (обычная по Штамму, ЧЭГ
или пуговичная) существует в течение 3 мес и бо-
лее, желудочно-кожный канал начинает выстила-
ться эпи гелием слизистой. После удаления трубки
этот канал иногда может закрыться, но у некото-
рых пациентов продолжает функционировать как
свищ, что приводит к истощению больного. При-
жигание в таких случаях обычно неэффективно,
и тогда для закрытия свища показана небольшая
операция под местной или обшей анестезией.102, 103
Гастростома по Джсйнуэю, когда в ней уже нет
необходимости, требует для закрытия более серь-
езного оперативного вмешательства.
ЛИТЕРАТУРА
1. Fabry W: (Hildanus) Opera Quae Extant Omnia. Beyerus,
Frankfort, p 541, 1646.
2. Spicer RD: Infantile hypertrophic pyloric stenosis: a review. Br
J Surg 69:128—135, 1982.
3. Blair P: On the dissection of a child much emaciated. Phil Trans
30:631—632, 1717.
4. Hirschsprung H: Faile von angeborener Pylorus Stenose. Jb
Kinderhcilk 27:61, 1888.
5. Ramstedt C: Zur Operation der angeborenen Pylorus-Stenose.
Med Klinik 1702—1705, 1912.
6. Mack HCA: A history of hypertrophic pyloric stenosis and its
treatment. Bull Hist Med 12:465 595, 1942.
7. Ravitch MM: The story of pyloric stenosis. Surgery 48:1117—
1143. 1960.
8. Grant GA, McAIeer JJA: Incidence of infantile hypertrophic
pyloric stenosis. Lancet 1:1177, 1984.
9. Klein A, Cremin BJ: Racial significance in pyloric stenosis. S Afr
Med J 44:1131, 1970.
10. Carter CO, Evans KA: Inheritance of congenital pyloric steno-
sis. J Med Genet 6:233—254, 1969.
11. Huguenard JR, Staples GE: Incidence of congenital hypertrop-
hic pyloric stenosis within sibships. J Pediatr 81:45—49, 1972.
12. Louhimo L, Lindahl H: Esophageal atresia: Primary results of
500 consecutively treated patients. J Pediatr Surg 18:217 229,
1983.
13. Obiditsch-Mayer 1, Hclmemcr G: On the histology of congenital
hypertrophic pyloric stenosis. Wien Klin Wochenschr 71:968—
970, 1959.
14. Dodge JA: Production of duodenal ulcers and hypertrophic py-
loric stenosis by administration of pentagastrin to pregnant and
newborn dogs. Nature 225:284—285, 1970.
15. Wcrlin SL, Grand RJ, Drum DE: Congenital hypertrophic pylo-
ric stenosis: the role of gastrin re-evaluated. Paediatrics
61:883 885, 1978.
16. Moazam F, Rodgers BM, Talbert JL, ct al.: Fasting and po-
stprandial serum gastrin levels in infants with hypertrophic py-
loric stenosis. Ann Surg 188:623—625, 1978.
17. Malmfors G, Sandler F: Peptidergic innervation in infantile hy-
pertrophic pyloric stenosis. J Pediatr Surg 21:303—306, 1986.
18. Dodge JA: Abnormal distribution of ABO blood groups in infan-
tile pyloric stenosis. J Med Genet 8:468—471, 1971.
19. Dodge JA: Psychosomatic aspects of infantile pyloric stenosis.
J Psychosom Res 16:1—5, 1972.
20. Pellerin D, Berlin P, Tavar JA: Gastroesophageal reflux and
hypertrophic pyloric stenosis. Ann Chir Infant 15:7—14, 1974.
21. Woolley MM, Feisher BF, Asch MJ, et al.: Jaundice, pyloric
stenosis and hepatic ghicuronyl transfera.se. J Pedialr Surg
9:359—363, 1974.
22. Wallgren A: Preclinical stage of infantile hypertrophic pyloric
stenosis. Аш J Dis CZhild 72:371—376, 1946.
23. Katz S, Basel D, Brabski D: Prenatal gastric dilatation and in-
fantile hypertrophic pyloric stenosis. J Pediatr Surg 23:1021
1022. 1988.
24. Lynn HB: The mechanism of pyloric stenosis and its relations-
hip to preoperative preparation. Arch Surg 81:453— 459, I960.
25. Corner BD: Hypertrophic pyloric stenosis in infancy treated
with methyl scopolamine nitrate. Arch Dis Child 30:377—380.
1955.
26. Rasmussen L, Hansen LP, Pedersen SA: Infantile hypertrophic
pyloric stenosis: the changing trend in treatment in a Danish
county. J Pediatr Surg 22:953—955, 1987.
27. Steinicke-Nielson O. Roelsgaard M: Rocntgenologically demonst-
rable gastric abnormalities in cases of previous congenital pylo-
ric stenosis. Acta Radiol 45:273—280, 1956.
28. Tack ED, Perlman JM, Bower RJ, et a!.: Pyloric stenosis in the
sick premature infant: Clinical and radiologic findings. Am J Dis
Child 142:68—70, 1988.
29. Teelc RL, Smith EH: Ultrasound in the diagnosis of idiopathic
hypertrophic pyloric stenosis. N Engl J Med 296:1149—1150,
1977.
30. Keller H. Waldermann D, Greiner P: Comparison of preoperati-
ve sonography with intraoperative findings in congenital hy-
pertrophic pyloric stenosis. J Pediatr Surg 22:950—952, 1987.
31. Scharli AF, Leditschke JF: Gastric motility after pylorornyotomy
in infants: A reappraisal of postoperative feeding. Surgery
64:1133—1137, 1968.
32. Runstrom G: On the roentgen anatomical appearance of conge-
nital pyloric stenosis during and after the manifest stage of the
disease. Acta Pediatr Scand 26:383—433, 1939.
33. Solowiejczyk M, Holtzman M, Michowitz M: Congenital hyper-
trophic pyloric stenosis: A long-term followup of 41 cases. Am
Surg 46:567 571, 1980.
ЗАБОЛЕВАНИЯ ЖЕЛУДКА 339
34. Vilmunn Р, Hjortrup A. Altmann Р. el al.: A long-term gastro-
intestinal followup in patients operated on for congenital hy-
pertrophic pyloric stenosis. Acta Paediatr Stand 75156 158,
1986.
35. Woolley MM, Gwinn JI , Marcs A: Congenital partial gastric
antral obstruction. Ann Surg 180:265—273, 1974.
36. Blazek F. Boeckman CR: Prepyloric antral diaphragm: delays in
treatment. J Pediatr Surg 22:948 949, 1987.
37 Rona A, Sylvestre J: Prepyloric mucosal diaphragm. J Can As-
soc Radiol 26:291—294, 1975.
38. Schwartz Sr, Rowden DR, Dudgeon DI.: Antral mucosal diaph-
ragm. Gustrointcsl Endosc 24:33—34, 1977.
39» Tuncll WP. Smith EI: Antral web in infancy. J Pediatr Surg
15:152 155, 1980.
40. Byrne WJ, Kangarloo H, Ament ME. ct al.: Antral dysmutility:
an unrecognized cause of cltronic vomiting during infancy. Ann
Surg 193:521—524. 1981.
41. Olsen L, Grotle G: Congenital pyloric atresia: report of a famili-
al occurrence. J Pediatr Surg 11:181—184. 1976.
42. Weber M: Hernidesmosume deficiency of gastrointestinal muco-
sa demonstrated in a child with Herlitz syndrome and pyloric
atresia. Acta Derm Vencrol (Stockh) 67:360—362, 1987.
43. Schwartz DL, So HB, Becker JM, et al.: An ectopic gastric
duplication arising from the pancreas and presenting with pneu-
moperitoneum. J Pediatr Surg 14:187—188, 1979.
44. Bartels RJ: Duplication of rhe stomach. Case report and review
of the literature. Am Surg 33:747—752, 1967.
45. Milsom J. Unger S. Alford BA, Bradley MR: Triplication of the
esophagus with gastric duplication. Surgery 98:121 —125, 1985.
46- McLedtehie NGB; The genesis uf gastric and certain intestinal
diverticula and enterogenous cysts. Surg Gynecol Obstet
99:135—141, 1959.
47. Kremer RM, I epnff RB, Izant RJ Jr: Duplication of the stomach.
J Pediatr Surg 5:360—364, 1970.
48. Pruksapong C. Donovan RJ, Pinil A: Gastric duplication. J Pedi-
atr Surg 14:83 85, 1979.
49. Boww RJ, Sieber WK, Kicsewctter WB: Alimentary tract dupli-
cations in children. Ann Surg 188:669—674, 1978.
50. 1 avine JF. Harrison M, and Heyman MB: Gastrointestinal dup-
lications causing relapsing pancreatitis in children. Gastroente-
rology 97:1556—1558. 1989.
51- Schocat SJ, Strand RD, Fellows KF: Perforated gastric duplica-
tion with pulmonary communication: a case report. Surgery
70:370—374, 1971.
52. Spence RK, Schnaufer 1 , Mahboubi S: Coexistent gastric dupli-
cation and accessory’ pancreas: clinical manifestations, embryo-
genesis. and treatment J Pediatr Surg 21:68—70. 1986.
53. Hone H, Iwasaki I, Takahashi H: Carcinoid in a gastrointesti-
nal duplication. J Pediatr Surg 21:902- 904. 1986.
54. Cameron AEP, Howard ER: Gastric volvulus in childhood. J Pe-
diatr Surg 22:944 947, 1987.
55. Aoyama K, Talcishi K: Gastric volvulus in three children with
asplenic syndrome. J Pediatr Surg 21:307—310, 1986.
56. Ziprukowski MKN, Teele RL: Gastric volvulus in childhood. Am
J Radiol 132:921—925, 1979.
57. Borchardt M: Zur Pathologic und Therapic des Mogcnvolvulus.
Arch Klin Chir 74:243—250, 1904.
58. Schulz RD, Nieman F: Kongenitale Mikrogastric in Verbindung
mit Skclcfmissbildungcn — cin ncucs Syndrom. Hclv Paediatr
Acta 26:185—191. 1971.
59. Blank E, Chishholm AJ: Congenital microgastria, a case with
a 26-year followup. Pediatrics 51:1037—1041, 1973.
60. Hochberger O, Swoboda W: Congenital microgastria: a followup
observation over six years. Pediatr Radiol 2:207 208, 1974.
61- Anderson KD, Guzzetta PC: Treatment of congenital micro-
gastria and dumping syndrome. J Pediatr Surg 18:747—750,
1983.
62. Kumar I). Spitz I : Peptic ulceration in children. Surg Gynecol
Obstet 159:63—66, 1984.
63. Editorial: Peptic ulcer in childhood. Br Med J 1:584, 1970.
64. Schuster SR, Gross RE; Peptic ulcer disease in childhood. Am
J Surg 105:324, 1963.
65. Miller RA: Observations on lhe gastric acidity during the first
month of life. Arch Dis Child 15:22. 1941.
66. Agunod M. Yamaguchi N. Lopez R. ct al.: Correlative study of
hydrochloric acid, pepsin and intrinsic factor secretion in new-
borns and infants. Am J Dig Dis 14:400 414, 1969.
67. Ghai OP. Singh M, Walia BNS, et al.: An assessment of gastric
acid secretory response with “maximal” augmented histamine
stimulation in children with peptic ulcer. Arch Dis Child 40:77.
1965.
68. Curci MR, Little K, Sieber WK. et al.. Peptic ulcer disease in
childhood reexamined. J Pediatr Surg 11:329 335, 1976.
69. Seagram CGF. Stephens CA, Cumming WA; Peptic ulceration at
lhe Hospital for Sick Children, Toronto, during lhe 20-year
period 1949 1969. J Pediatr Surg 8:407, 1973.
70. Puri P. Boyd E. Blake N. cl al.: Duodenal ulcer in childhood:
a continuing disease in adult life. J Pediatr Surg 13:525—526.
1978.
71. Tsuchida Y, Makino S, Ishida M: A followup study of subtotal
gastrectomy in infancy and early childhood. J Pediatr Surg 9.
499 500, 1974.
72. Rosenlund ML: The Zollinger-Ellison syndrome in children:
a review. Am J Med Sci 141:884 892. 1967.
73. Abe K, Nukawa N, Sasaki H: Zollinger-Ellison syndrome with
Warden-Walker syndrome. Am J Dis Child 133:735 738, 1979.
74. Drake DP. Maclvcr AG, Atwell JD: Zollinger-Ellison syndrome
in a child: medical treatment with cimetidine. Arch Dis Child
55:226—228. 1980»
75. Cheung 1 Y, Chang N: The role of gastric mucosal blood flow
and II1 back-diffusion in the pathogenesis of acute gastric
erosions. J Surg Res 22:357—361, 1977.
76. Skillman JJ. Silen W: Stress ulcers. Lancet 2:1303—1306. 1972.
77. Grosfeld JL, Shipley F, Fitzgerald JF, et al.: Acute peptic ulcer
in infancy and childhood. Am Surg 44:13—19, 1978.
78. I-liegel CP, Herzog B, Signer E. et al.: Bleeding gastric ulcer in
<i newborn infant diagnosed by transumbilicai aortography.
J Pediatr Surg 12:589—590, 1977.
79. Williams JF. Pannell WP, Sherman RT: Curling’s ulcer in child-
ren. J Trauma 16:639 644, 1976.
80. Lerner AG, Meng CH, Schneider KM: Selective intra-arterial
vasopressin in the management of stress ulcers in childhood.
Pediatrics 51:126—128, 1973.
81» Rosser SB, Clark CH, Elechi F: Spontaneous neonatal gastric
perforation. J Pediatr Surg 17:390—394, 1982.
82. Tan CEL, Kielly EM, Agruwal M, ct al.: Neonatal gastrointesti-
nal perforation. J Pediatr Surg 24:888- -892, 1989.
83. Herbut PA; Congenital defect in the musculature of the stomach
with rupture in a newborn. Arb Pathol 36:91, 1943.
84. Abe Y, Araki S. Shimizu li, el al.: Seromuscular laceration of
the stomach associated with infantile hypertrophic pyloric steno-
sis in the newborn. Jpn J Surg 14:30—34. 1984
85. Garcia C, Markowitz Rl: Imaging case of lhe month: pneumope-
ritoneum and pncumoscrotum caused by gastric perforation. Am
J Perinatol 4:75—77, 1987.
86. Knight PJ, Abdenour G: Pneumoperitoneum in the ventilated
neonate: respiratory or gastrointestinal origin? J Pediatr
98:972 974, 1981.
87. Scwab CW, Shaikh DA, I'alucio RC: Injury to the stomach and
small bowel. In Mattox KL, Moore EE, Feliciano DV (Editors).
Trauma. Appleton-Lange. Norwalk. CT. pp 459—472. 1988.
88 Grosfeld J, Cuoney DR: Pancreatic and gastrointestinal trauma
in childhood. Pediatr Clin North Am 22:365—367, 1975.
89. Semel I., Fritelli G: Gastric rupture from blunt abdominal trau-
ma. New York Slate J Med 81:938 939. 1981.
90. Case MES, Nanduri R: 1 aceralion of the stomach by blunt trau-
ma in a child: a case of child abuse. J Forcnsis Sci 28:496—501.
1983.
91. Garfinklc SE. Matolo NM: Gastric necrosis from blunt abdomi-
nal truuma. J Trauma 16:406— 407, 1976.
340 ЗАБОЛЕВАНИЯ ЖЕЛУДКА
92. Gaudcrcr ML, Pensky JL, Izant RJ Jr: Gastrostomy without
laparotomy: a percutaneous endoscopic technique. J Pediatr
Surg 15:872—875, 1980.
93. Cory DA, Fitzgerald JF, Cohen MD: Percutaneous nonendosco-
pic gastrostomy in children. Am J Radiol 151:995—997. 1988.
94. Ravenlos JM, Kralcmann H, Gray DB: Mortality risks of mental-
ly retarded and mentally ill patients after feeding gastrostomy.
Am J Ment Defic 86:439—444, 1982.
95. Mollitt DL, Golladay ES. Seibert JJ: Symptomatic gastroesopha-
geal reflux following gastrostomy in neurulogically impaired pa-
tients. Pediatrics 75:1124 1126, 1985.
96. Jolley SG, Smith El. Tunell WP: Protective antireflux operation
with feeding gastrostomy. Experience with children. Ann Surg
201:736—740, 1985.
97. Jolley SG, Tunell WP, Hoelzer J, ct al.: Lower esophageal pres-
sure changes with lube gastrostomy; a causative factor of gast-
roesophageal reflux in children? J Pediatr Surg 21:624—627,
1986.
98. Papaila JG, Vane DW, Colville C, et al.: The effect of various
types of gastrostomy on the lower esophageal sphincter. J Pcdi-
atr Surg 22:1198—1202, 1987.
99. Gauderer MWL, Olsen MM, Stellate TA. el al.: Feeding gast-
rostomy button: experience and recommendations. J Pediatr
Surg 23:24 28» 1988.
100. Campbell JR, Asaki TM: Gastrostomy in infants and children:
an analysis of complications and techniques. Am Surg 9:505—
508, 1974.
101. Galea MH. Mayell MJ: Gastroduodenal mucosal intussuscep-
tion causing gastric outlet obstruction: a complication of gas-
trostomy tubes. J Pediatr Surg 23:980—981. 19X8.
102. Bishop HC: Simplified closure of the longstanding gastrostomy.
J Pediatr Surg 16:571—572. 1981.
103. Ducharme JC, Youssef S, Tilkin F: Gastrostomy closure: a
quick, easy and safe method. J Pediatr Surg 12:729 730,
1977.
Глава 25
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
Атрезия — наиболее частая при ч и на врожденной
кишечной непроходимости — составляет одну треть
всех пороков кишечника у новорожденных и встре-
чается одинаково часто как у мальчиков, так
и у девочек. Средняя частота рождения детей с ат-
резией кишечника приблизительно 1:2710 ново-
рожденных, причем этот порок отмечается в 2 раза
чаще атрезии пищевода и диафрагмальной грыжи
и в 3 раза чаше болезни Гиршпрунга.'
В отличие от атрезни, вызывающей полную об-
струкцию просвета кишки, врожденный стеноз
обусловливает частичную непроходимость, неред-
ко со значительно более поздними клиническими
проявлениями.
Несмотря на относительную частоту аномалии,
первые сообщения о тонкокишечной атрезии с бла-
гополучным исходом после наложения анастомоза
появились лишь в 1992 г.2 По данным сводной ста-
тистики, опубликованной в 1950 г. (1498 случаев
атрезии), выживаемость в то время была менее
10%.3 С введением в практику неонатологии со-
временных технических хирургических методов
и тотального парентерального питания выживае-
мость возросла почти до 90%.4 ь Так, из 110 детей
с атрезией и стенозом кишечника, оперированных
с 1970 по 1989 гг. в специализированном отделе-
нии интенсивной терапии новорожденных в Йель-
ском Госпитале (Нью-Хейвен, шт. Коннектикут),
выжили 93% (табл. 25-1).
Классификация. Дуоденальная атрезия и стеноз
могут быть как проксимальнее, так и дистальнее
Фатеровой ампулы, что клинически отражается
в характере желудочного содержимого, имеющего
или не имеющего примесь желчи. Преампулярная
обструкция встречается намного реже и, по свод-
ной статистике Хирургической Секции Американ-
ской Педиатрической Академии (1969), выявлена
лишь у 99 из 503 пациентов с врожденной дуоде-
нальной обструкцией.7 Мембрана с просветом была
обнаружена у 206 больных. Редкими причинами
обструкции были атрезия с тяжем между атрезиро-
ванными участками и полное отсутствие 12-перст-
ной кишки. Нечасто встречается и провисающая
мембрана, имеющая большое клиническое значе-
ние, поскольку она может быть принята за более
дистальную дуоденальную обструкцию, а также
в связи с возможным впадением аномального
5. 9
желчного протока вдоль медиального ее края.
Кольцевидная поджелудочная железа встрети-
лась в приведенной статистике у 21% пациентов.
Эта патология представляет собой эмбриологиче-
ски сложный порок, который обычно сочетается
с внутренней дуоденальной обструкцией, не явля-
ясь, однако, ее первопричиной (рис. 25-1). Теперь,
когда хирурги более тщательно обследуют место
обструкции, прежде чем осуществить хирургиче-
скую коррекцию, становится ясно, что истинная
частота кольцевидной поджелудочной железы и
аномалий билиарного тракта значительно выше,
чем предполагалось ранее.
Атрезия и стеноз тонкой кишки одинаково часто
встречаются на всем ее протяжении от связки
Трейца до илеоцекального угла (табл. 25 2). При
анализе 587 больных с данной аномалией 10 вы-
явлено следующее распределение обструкции по
локализации: проксимальные отделы тощей киш-
ки— 31%, дистальные — 20%, проксимальные
подвздошной — 13%, дистальные — 36%. Стенозы
были обнаружены примерно в 20% всех случаев.
Встречаются 4 различных типа атрезии
(рис. 25-2). Используемая нами здесь классифика-
ция подобна тем, что были предложены Louw
и Barnard,11 Hays,13 а также Martin и Zcrella,13 но
ТАБЛИЦА 25-1. Выживаемость при атрезии кишечника
(Госпиталь в Нью-Хейвене, 1970 -1989 гг.)
Локализация атрезии Кол-во больных Послеоперационная выживаемость
12 нерстная кишка Тощая и подвздошная 57 50/55* (93%)
кишка 47 44/47 (93%)
Толстая кишка 8 8/8 (100%)
112 102/110 (93%)
• 2 пациента с тяжелыми пороками сердца умерли до
операции
342 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
А
Оттесненная
толстая
кишка
Расширенная
проксимальная
часть 12-перстной
кишки
Поджелудочная
железа
Рис. 25-1. Л. Наиболее частый вариант дуоденаль-
ной атрезии, встречающийся у большинства детей
с этим пороком. Непроходимость может быть пол-
ной (В) или частичной за счет небольшого отвер-
стия в мембране (С). 12-псрстная кишка ротиро-
вана нс полностью.
Атрофированная
дистальная
часть 12-перстной
Поджелудочная
железа
Мембранозная-
обструкция
кишки
отличается от них включением синдрома «яблоч-
ной кожуры», как разновидности основных видов,
а также множественной атрезии как 4-го типа тон-
кокишечной атрезии.
Тип 1 — мембрана с единым непрерывающимся
мышечным слоем проксимального и дистального
сегментов, встречается приблизительно в 20% всех
случаев. Тип 2 — атрезия с тяжем между слепыми
концами кишки, около 35%. Тип За — атрезия
с полным разобщением слепых концов и V-образ-
ным дефектом брыжейки, около 35%. Тип ЗЬ—
атрезия с большим дефектом брыжейки, когда ди-
стальный отдел подвздошной кишки целиком по-
лучает кровоснабжение только из подвздошно-обо-
дочной артерии и «закручен» вокруг сосуда в виде
«яблочной кожуры». Эта аномалия имеет особое
значение, поскольку сопровождается глубокой не-
доношенностью, необычно маленьким дистальным
отделом кишки, значительным укорочением длины
всего кишечника.14 Имеются также сообщения
о наследственной предрасположенности при этой
форме атрезии.15 Тип 4 — множественная атрезия
ТАБЛИЦА 25-2. Классификация анатомических типов атрезии
тощей и подвздошной кишки (Госпиталь в
Нью-Хейвенс, 1970—1989 гг.)
Стеноз Типы атрезии
1 1 2 1 3 и
Тощая кишка 2 8 7 4 4 Z5
Подвздошная кишка 1 6 5 7 3 22
3 14 12 11 7 47
тонкой кишки, встречается приблизительно в 6%
всех случаев.
В обзоре Хирургической Секции 8 случаев были
с поражением только тощей кишки. 4 — только
подвздошной, а у 6 детей отмечены различные
комбинации множественной атрезии в обоих отде-
лах. Сочетание атрезии тонкой и толстой киш-
ки — чрезвычайно редкий порок, который встре-
тился только в 2 случаях из наших 47 наблюдений,
7 детей имели множественную атрезию тонкой
кишки. Множественные атрезии, «разбросанные»
на всем протяжении от желудка до прямой киш-
ки, — известный в настоящее время наследствен-
ный синдром. Изучение родословной в таких семь-
ях позволяет предполагать аутосомно-рецессивный
тин наследования. По данным одной из публика-
ций,“ у 5 больных с этим синдромом, представляю-
щим особый интерес, отмечалось наличие в про-
свете кишки кальцификатов.
Гистологическое исследование при множествен
ной кишечной атрезии показывает, что просвет
каждого атрезированного сегмента выстлан от-
дельной «своей» слизистой,17 в то время как строе-
ние мышечной стенки везде одинаково. При этом
отсутствуют элементы lanugo, плоского эпителия
и желчных пигментов. Это позволяет предпола-
гать, что в этиологии атрезии нарушения развития
имеют большее значение, чем ишемический или
воспалительный фактор.
Атрезия толстой кишки — порок развития,
аналогичный тонкокишечной атрезии, но встреча-
ющийся значительно реже— менее, чем в 5% всех
случаев атрезии кишечника. В наших наблюдени-
ях атрезия толстой кишки отмечалась в основном
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА 343
Мембранозная обструкция
Полное разделение сегментов
с дефектом брыжейки
344 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
в области поперечиоободочного отдела, причем
у одного пациента сочеталась с мальротацисй и за-
воротом средней кишки, а у двух детей при атре-
зии дистального отдела сигмовидной кишки была
также множественная тонкокишечная атрезия. Раз-
личные типы атрезии, описанные для тонкой киш-
ки, встречаются также и в толстой, но множест-
венная атрезия толстой кишки — чрезвычайная
редкость.
Патология. Наиболее важной особенностью
всех форм кишечной атрезии и стеноза является
значительное расширение проксимального сегмен-
та и резкое сужение дистального Разница в диа-
метре может быть от 2—3-кратной до 15—20-крат-
ной и зависит от того, является обструкция полной
или частичной, а также от локализации атрезии по
отношению к желудку. Протяженность расширен-
ного отдела тонкой или толстой кишки может быть
от 10 до 15 см. Гипертрофия мышечного слоя
и укорочение кишечных ворсинок на «дне» атрези-
рованного сегмента — результат внутриутробной
перистальтической «работы» и хронического рас-
тяжения кишки плода.
Экспериментальные исследования, подтвержден-
ные и при обследовании новорожденных, выявляют
нарушение координации перистальтики в расши-
ренной части,1 что можно объяснить выражен-
ной гиперплазией ганглиозных клегок в прокси-
мальном сегменте с инволюционными изменения-
ми в области максимального растяжения. У «вер-
хушек» как проксимального, так и дистального
сегментов, активность ацегилхолиплстеразы отсут-
ствует, холинергические ганглии и нервы не вы-
являются, а мышечные слои замещены рубцовой
тканью.19 Дистальные отделы ниже атрезии суже-
ны, поскольку были «выключены из работы», но
потенциально являются нормальными, как по раз-
мерам, так и функционально. Очевидных призна-
ков гипоплазии обычно нет, но нередко отмечается
некоторое укорочение общей длины кишечника.
В 18% случаев, обобщенных Хирургической Сек-
цией, кишечник был описан как «аномально ко-
роткий». Длина кишечника при атрезии 1 го типа
у большинства детей нормальная, при 2-м тине
кишечник может быть укорочен, а при 3-м и 4-м
типах тонкокишечной атрезии укорочение кишеч-
ника отмечается практически всегда.13
У новорожденных с атрезией часто имеются
признаки внутриутробного нарушения кишечного
кровообращения и мекониевого перитонита в ста
дни репарации или «свежего». Атрезия иногда
встречается в комбинации с сегментарным заворо-
том, мекониальной непроходимостью, гастрошизи-
сом, инвагинацией, ущемленной грыжей, запоро
том вокруг врожденных тяжей или незарашен-
ного желточного протока.20
Гистологическое исследование при атрезии то-
щей и подвздошной кишки выявляет гипертрофию
кишечных ворсинок в дистальном сегменте и нор-
мальные кишечные ворсинки в проксимальном.21
Кишечные ворсинки в дистальном сегменте не
только увеличены, но извиты и переплетаются, ча-
сто закупоривая узкий просвет дистального атре-
зированного участка (рис. 25-3). Характер этих
изменений аналогичен компенсаторной гипертро-
фии кишечных ворсинок после обширных резек-
ций кишечника, однако установить точный меха-
низм возникновения гипертрофии сложно из-за на-
личия обструкции и значительного укорочения
длины кишечника
Эмбриология и патогенез. Процессы, происхо-
дящие в эмбриогенезе и ведущие к возникновению
дуоденальной, тонко- и толстокишечной атрезии,
в настоящее время достаточно хорошо раскрыты.
Первое большое изменение дифференциации
12-нерстной кишки, гепатобилиарного дерева и
поджелудочной железы происходит около 3-й не-
дели внутриутробного развития, когда в месте сое-
динения передней и средней кишки образуются за-
кладки желчных путей и поджелудочной железы.
12-перстная кишка в это время представляет собой
скопление эпителия, подвергающегося вакуолиза-
ции, за которой следует реканализация и восста-
новление просвета кишечной трубки на 3—4-й не-
деле нормального развития. По теории Tandler,22
нарушения реканализации среднего отдела
12-перстной кишки могут приводить к врожденной
обструкции просвета и нередко — к сочетанному
неправильному развитию закладки поджелудочной
железы и терминальной части желчных путей.
Подтверждением этой концепции является высокая
частота кольцевидной поджелудочной железы, ко-
торая, no-видимому, представляет собой остатки
вентральной закладки pancreas в сочетании с внут-
ренней дуоденальной обструкцией. Посмертные
анатомические исследования отчетливо выявляют
нередкую комбинацию дуоденальных и билиарных
аномалий," особенно расщепление надвое желчно-
го протока, что может объяснять отмечаемое иног-
да наличие желчи как в проксимальной части
12-перстной кишки, так и в дистальных отделах
кишечника. Фатерова ампула может открываться
непосредственно в дуоденальную мембрану с меди
алыюй се стороны, что имеет как эмбриологиче-
ское, так и хирургическое значение.
Клинические и экспериментальные данные по
казывают, что атрезия тонкой и толстой кишки
1-го, 2-го и За типа возникает в результате ише-
мического поражения кишечника, причем после то-
го, как средняя кишка уже возвратилась в целоми-
ческую полость. Такой механизм и сроки развития
порока подтверждаются следующими доказатель-
ствами: (1) дистальнее уровня атрезии обнаружи-
ваются меконий, клетки чешуйчатого эпителия
и lanugo от заглоченной смазки (vernix caseosa);20
(2) различные стадии развития кишечной атрезии
выявляются у детей, родившихся с (а) инвагина-
цией,23 (б) заворотом, (в) грыжевым выпячиванием
кишечника через пупочное кольцо или через врож-
денные дефекты брыжейки и (г) с другими видами
локальной патологии воспалительного генеза (с
перфорацией или без) или с мекониевым перито-
нитом; 20 и (3) атрезия тощей, подвздошной или
толстой кишки может быть создана в эксперименте
путем деваскулязирации кишечника плода живот-
ных. Эти эксперименты, впервые произведенные
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
1И1466 4
р = П. S.
934+ 121ММ
р < 0.01
Рис. 25-3. А, При кишечной атрезии кишечные
ворсинки в проксимальном сегменте укороче-
ны. Их длина почти в 2 раза меньше длины
ворсинок в л метальном сегменте.
В, На микрофотограмме видны ворсинки в
проксимальном сегменте у новорожденного с
атрезией тощей кишки (увел. X 40).
С. Ворсинки в дистальном сегменте (у того
же больного) расширены, имеют неправильную
форму и извиты (увел. X 40).
346 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
на плодах щенков, были повторены на других жи-
вотных. Созданная у плодов кишечная атрезия
позволяет получить информацию о физиологиче-
ской адаптации в процессе внутриутробного разви-
тия при интестинальной обструкции
Изучению воздействия аномалий развития на
внутриутробный рост плода придавалось большое
значение. В результате установлено, что недоно-
шенные дети, имеющие массу тела, соответствую-
щую гестационному возрасту, физиологически от-
личаются от детей с меньшей по отношению к
гестационному возрасту массой.27 Выраженная ле-
гочная аспирация мекония и амниотической жидко-
сти, а также высокий риск гипогликемии у ново-
рожденных детей с массой тела, меньшей по отно-
шению к гестационному возрасту, являются при-
знаками, при которых следует ожидать хирургиче-
скую патологию, а потому эти факторы должны
быть предметом пристального внимания хирургов.
Высокая частота задержки внутриутробного раз-
вития отмечалась у детей с аноректальными и пи-
щеводными аномалиями.2’ Что же касается ново-
рожденных с атрезией кишечника, го значитель-
ная их часть также недоношенные, однако масса
тела при этом соответствует гестационному возра-
сту/ Нет очевидной разницы в распределении по
массе тела детей, родившихся с дуоденальной и то-
щеподвздошной непроходимостью (рис. 25-4).
Внутриутробное развитие таких детей одинаковое
как при многоводии, так и при нормальном коли-
честве амниотической жидкости.
Сочетанные аномалии. Одно из наиболее важ-
ных отличий дуоденальной атрезии от врожденной
кишечной непроходимости более дистальной лока-
лизации — сложная ее природа и высокая частота
трисомии 21 и множественных системных анома-
лий. Около 30% детей с дуоденальной атрезией
имеют один или несколько тяжелых сочетанных
пороков: сердца, ночек, опорно-двигательного ап-
парата, центральной нервной системы (ЦНС), в то
время как при тонкокишечной атрезии сопутству-
ющие серьезные аномалии отмечаются менее, чем
у 10% детей. Кроме того, среди наших пациентов
с дуоденальной атрезией в двух случаях была диа-
гностирована болезнь Гиршпрунга (в 10-дневном
возрасте) и еще у двух новорожденных — перфора-
ция желудка (как сопутствующая патология).
По сводной статистике Американской Педиатри-
ческой Академии,’ трисомия 21 отмечена у 30%
пациентов с дуоденальной атрезией и у 19 из
60 наших больных (31%). Поскольку среди таких
детей летальность высокая, а кроме того генетиче-
ская патология оказывает серьезное влияние на
рост, развитие и выживаемость, родители в подоб-
ных случаях должны быть подробно информирова
ны о характере патологии, и операция может быть
сделана только при их согласии. Если диагноз три-
сомии сомнителен, необходимо определение карио-
типа. До получения результатов исследования ре-
бенок обеспечивается парентеральным питанием
(через периферическую вену) и отсасыванием со-
держимого желудка.
Пороки сердца - самые частые из сопутствую-
щих аномалий при дуоденальной атрезии, они об-
наруживаются в 20% всех случаев. А у детей
с комбинацией дуоденальной атрезии и трисомии
21 почти в 80% отмечаются очень тяжелые сердсч
ные аномалии, такие как пороки группы AV-кана-
ла. Встречаются и другие, менее тяжелые и более
легко корригируемые пороки, например дефекты
перегородок или Боталлов проток.10
V А Т Е R-сипдром 29 — аббревиатура, обознача-
Рис. 25-4. Значительное количество больных с дуоденальной и тонкокишечной атрезией недоношенные, но их масса тела соответ-
ствует гестационному возрасту.
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА 347
ющая сочетание аномалий, состоящее из поро-
ков позвонков (vertebral), анальной атрезии (nnal),
трахеопищеводного свища (/racheo...) с атрезией
пищевода (esophageal), дисплазии луча (radial)
и пороков почек (renal). Известно и описано соче-
тание дуоденальной атрезии с этой комбинацией,
встретившееся у 5 из наших пациентов. Лечение
таких больных представляет особую сложность для
хирурга, который должен восстановить непрерыв-
ность пищевода в связи с его атрезией и нижним
трахеопищеводным свищом, а. кроме того, ликви-
дировать дуоденальную атрезию и аноректальный
порок.
У детей с атрезией тонкой кишки, имеющих
признаки мекониевого перитонита с внутриутроб-
ным заворотом и особенно при наличии суженной
толстой кишки, содержащей комочки мекониевой
СЛИЗИ, следует искать мекониальную непроходи-
мость. Содержимое тонкой кишки при этом более
вязкое, чем при неосложненной атрезии. Посколь-
ку, по данным большинства хирургов, при тонко-
кишечной атрезни мекониальная непроходимость
встречается в 20% случаев,зп всем тетям после опе-
рации по поводу атрезии кишечника следует про-
водить потовую пробу. Новорожденные с грыжей
пупочного канатика и гастрошизисом также могут
иметь атрезию тонкой или толстой кишки. Из
11 наших детей с толстокишечной атрезией четве-
ро имели гастрошизис.3’ Непроходимость в таких
случаях обычно выявляется во время операции
пластики брюшной стенки.
Диагностика. Пренатальная диагностика. Вы-
явление жизнеугрожающей патологии плода с по-
мощью скринингового метода определения уровня
альфафетопротеина, УЗИ, исследования амниоти-
ческой жидкости и крови плода на кариотип, не
только позволяет решить вопрос о необходимости
в ряде случаев прерывания беременности, но и вы-
явить группы риска (среди беременных женщин)
в отношении патологии как акушерско-гинеколо-
гической, так и неонатальной.
Многоводие отмечается в половине всех случаев
дуоденальной и высокой тощекишечной атрезии
и реже при атрезии подвздошной и толстой киш-
ки.32 Учитывая приведенные данные, многоводие
следует рассматривать как абсолютное показание
к УЗИ плода. Поскольку амниотическая жидкость
в норме абсорбируется в дистальных отделах тон-
кой кишки, то ее перераспределение или скопле-
ние должно наводить на мысль о возможной об-
струкции проксимальных отделов кишечника, что
подтверждается при амниоцентезе в 3-м триместре
беременности. Изучение состава амниотической
жидкости овец, у плодов которых была экспери-
ментально создана кишечная атрезия, не выявило
значительной разницы осмолярности, азота моче-
вины, электролитов, билирубина, амилазы и ли-
пазы по сравнению с контрольной группой жи-
вотных.25
Концентрация желчной кислоты в амниотиче-
ской жидкости при обследовании двух беременных
женщин с многоводием, у одной из которых ребе=
нок имел дуоденальную атрезию, а у другой —
атрезию подвздошной кишки, была соответст-
венно 30,3 и 83,1 ммоль/л (при норме 1,2
2,4 ммоль/л).33 Уровень же билирубина и амилазы
в амниотической жидкости был нормальным. Эт1
данные могут быть объяснены разницей между ду-
оденальным соком и амниотической жшкостью
больше в отношении концентрации желчной кис-
лоты, чем билирубина и амилазы, и более медлен-
ным «оборотом» желчной кислоты (в амниотиче-
ской жидкости) по сравнению с билирубином.
УЗИ беременных женщин имеет большие прей
мущсства перед иными диагностическими процеду-
рами, поскольку является неинназивным методом
и дает ценную информацию о раз винт сердца
и ЦНС плода, а также о состоянии желудочно-
кишечного тракта.34 С помощью ультразвука мо-
жет быть выявлено даже частичное обратное рас-
положение внутренних органов в комбинации
с дуоденальной атрезией и правосторонней диа-
фрагмальной грыжей (через щель Богдалека). Это
чрезвычайно редкое сочетание известно как
синдром множественной органной мальротации
(МОМ С).35 Пример одного из двух таких паци-
ентов, наблюдавшихся нами, приведен на рисунке
25-5.
Постнаталъная диагностика. Если диагноз
кишечной непроходимости был установлен прена-
тально, то после рождения его необходимо под-
твердить, поскольку данные УЗИ иногда непра-
вильно интерпретируются. С этой целью сразу по-
сле рождения должно быть проведено зондирова-
ние желудка и его опорожнение. Наличие в же-
лудке содержимого, окрашенного желчью, или
большое его количество, превышающее 25 мл,
должны вызывать подозрение на кишечную непро-
ходимость. При дуоденальной или высокой тоще-
кишечной атрезии сразу после рождения отмеча-
ется рвота с желчью, в то время как при более
низкой атрезии этот симптом появляется позже —
от нескольких часов до 1—2 дней. При кишечном
стенозе новорожденные могут плохо усваивать пи-
щу в течение нескольких недель и даже дольше, не
прибавлять в весе. Периодически у них появляется
рвота и аспирация.
Вздутие живота отмечается у 80% детей с не-
проходимостью, локализующейся ниже тощей
кишки. При этом может быть видна активная пе-
ристальтика растянутых кишечных петель. Значи-
тельное вздутие живота иногда приводит к респи-
раторным расстройствам, связанным с высоким
стоянием диафрагмы. Наличие рвоты с желчью
сразу после рождения у ребенка с ладьевидным
или нормальным животом позволяет обоснованно
заподозрить дуоденальную или высокую тощеки-
шечную непроходимость еще до того, как с по-
мощью других методов исследования диагноз бу-
дет окончательно установлен.
Отсутствие мекония подтверждает диагноз ки-
шечной непроходимости, однако у 30% пациентов
с дуоденальной атрезией и у 20% с тонкокишеч-
ной локализацией порока отмечается отхождение
нормального мекония в течение непродолжитель-
ного времени после рождения. Желтушность кожи
348 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
Рис. 25-5. А, УЗИ на 35-й неделе беременности
у женщины с многоводием. Видны кистопоаобиые
образования над и под правым куполом диа-
фрагмы.
В. Рен ггено! рамма ребенка через час после рож-
дения подтверждает диагноз дуоденальной атре-
зии, обратного расположения внутренних органов
и диафрагмальной грыжи (через щель Вогдалека).
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИК/
определяется почти у 40% детей с атрезией про-
ксимальных отделов кишечника и у 20% — с не-
проходимостью более дистальной. Желтуха объяс-
няется подъемом уровня непрямого билирубина,
что связано с наличием в кишечной слизистой но-
ворожденных В-глюкуронидазы. У детей с кишеч-
ной непроходимостью этот энзим освобождает свя-
занный билирубин и увеличивает его внутри пече-
ночную рециркуляцию.
Для подтверждения диагноза и уточнения уров-
ня непроходимости производят рентгенограммы
в прямой проекции (в горизонтальном и вертикаль-
ном положении) и в боковой. Наличие двух газо-
вых пузырей с уровнями жидкости (симптом двой-
ного пузыря — double bubble) подтверждает диа-
гноз дуоденальной обструкции, однако не обяза-
тельно атрезии. У детей с дуоденальным сте-
нозом иногда отмечается небольшое количество
газа дистальнее 12-перс гной кишки, при этом ха-
рактерные признаки непроходимости проксималь-
ных отделов могу г отсутствовать. Введение в
таких случаях 50 мл воздуха в желудок через назо-
гастральный зонд с последующей повторной рент-
генографией в положении лежа на животе до-
стоверно подтверждает наличие непроходимости.
Следует избегать обследования с барием. Однако
при остро возникшей непроходимости у маленьких
детей, даже нескольких дней жизни, исследование
с глотком бария может оказать ценную помощь
в диагностике обструкции. Такие признаки, как
клюво- или Z-образная конфигурация проксималь-
ных отделов тощей кишки или заполнение их в ви-
де спирали, очень характерны для мальротаиин
или заворота средней кишки. В таких случаях по-
казана срочная операция.
При атрезии проксимальных отделов тощей
кишки на рентгенограммах видно небольшое коли-
чество уровней жидкости с газовыми пузырями
и отсутствие газа в нижних отделах живота (рис.
25-6). Чем ниже атрезия, тем больше уровней
жидкости на рентгенограммах. Иногда наиболее
расширенный сегмент кишки не виден на обзорной
рентгенограмме, поскольку заполнен жидким со-
держимым (рис. 25-7). В таких случаях может
быть допущена ошибка в установлении уровня
и характера непроходимости. Имитировать атре-
зию подвздошной или толстой кишки могут бо-
лезнь Гиршпрунга, синдром мекониевой пробки
и мекониальная непроходимость. В большинстве
случаев дифференциальный диагноз с перечислен-
ными видами патологии может быть проведен с по-
мощью ирригографии с барием (рис. 25-8). Диа-
метр толстой кишки позволяет уточнить уровень
атрезии. При дуоденальной локализации порока
толстая кишка имеет нормальный диаметр, при ат-
резии дистальных отделов подвздошной кишки —
сужена (микрокодон).36 Особенно резкое сужение
толстой кишки отмечается у детей с мекониальной
непроходимостью.
Лечение. Предоперационная подготовка. Все
принципы неонатальной интенсивной терапии
применимы и к предоперационной подготовке де-
тей с кишечной атрезией. Особое внимание, одна-
Рис. 25-6. Атрезии Hexing юшнон кишки. Приводящий отд
ланшшдно расширен. Рентгенограммы в горизонтальном
вертикальном (В) положении.
ко, следует обратить на: (1) согревание (не
дить ребенка!) во время транспортировки, з<
крови для анализов и рентгенологического о
дования; (2) декомпрессию желудка назогаст
ным зондом (соответствующего диаметра)
предотвращения аспирации; (3) постановку
тера в вену и коррекцию потерей жидкости, а
350 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
Рис. 25-7. Иррнгография с барием при завороте и атрезии подвздошной кишки. Толстая кишка и терминальный отдел подвздошной
кишки сужены (А). Дистальная часть кишечника смешена кзади проксимальным отделом подвздошной кишки, заполненным
жидкостью и находящимся в завороте (В).
Рис. 25-8. Атрезия ободочной кишки. Ирригограмма
с барием. Дистальный отдел толстой кишки удлинен,
проксимальный расширен и заполнен воздухом.
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА 351
же электролитных нарушений. Очень важно пра-
вильно определить и восполнить потери, связан-
ные с секвестрацией жидкости в третьем простран-
стве (кишечник). Отделяемое по зонду желудочное
содержимое должно быть восполнено внутривен-
ным введением (1:1) раствора Рингер-лактата или
физиологического раствора. Дети, которые ко вре-
мени поступления уже имели большие потери
и в результате дегидратированы, должны получать
жидкость из расчета объема, равного 1% массы
тела в час до тех пор, пока не будут достигнуты
адекватные диурез и осмолярность мочи. В назна-
чении до операции антибиотиков нет необходимо-
сти, за исключением тех случаев, когда подозрева-
ется сепсис, а также если есть очевидные признаки
пневмонии или перитонита. Дети с перитонитом
требуют дополнительных жидкостных объемов
и антибиотиков. В таких ситуациях целесообразно
применение ампициллина 100 мг/кг/сут и гента-
мицина 5 мг/кг/сут. Как правило, определяют
группу крови больного, однако интраоперационная
трансфузия обычно нс требуется.
Оперативное лечение. Наркоз эндотрахеальный
с применением фторотана и мышечных релаксан-
тов. Функция жизненно важных органов контроли-
руется с помощью Допплеровского мониторинга
АД и ЭКГ, а также прекард нал ьного или эзофа ге-
ального стетоскопа. Гипотермии можно избежать,
применяя согревающие лампы, подогреваемый
матрац и специальное операционное белье. Даже
если все эти меры применяются, необходимо изме-
рять температуру тела с помощью ректального
зонда и телетермометра.
Правосторонний верхний поперечный разрез
обеспечивает прекрасный доступ ко всему желу-
дочно-кишечному тракту. Диагноз дуоденальной
атрезии подтверждается после разделения боль-
шого сальника, «вхождения» в полость малого
сальника и ревизии 12-перстной кишки до места
обструкции. В большинстве случаев для облег-
чения наложения анастомоза восходящий отдел
толстой кишки следует отвести медиально, а про-
ксимальный и дистальный отделы 12-перстной киш-
ки хорошо мобилизовать. Я предпочитаю одноряд-
ный дуоденодуодсноанастомоз бок-в-бок (рис. 25-9),
однако при большом диастазе между атрезирован-
ными сегментами показан дуоденоеюноанастомоз,
который за последние 10 лет мы накладывали
лишь у 4 из 32 больных.
После вскрытия проксимального сегмента необ-
ходима тщательная ревизия, как визуальная, так
и с помощью зонда, для того, чтобы исключить
провисающую мембрану. К сожалению, бывают
случаи наложения анастомоза дистальнее такой
перегородки, что требует повторной операции.
Альтернативой традиционному дуоденодуодсно-
анастомозу бок-в-бок является ромбовидный тип
этого соустья,37 который, по мнению некоторых хи-
рургов, позволяет рано начинать энтеральное пи-
тание и сокращает сроки пребывания больного
в стационаре?* Проведения за зону анастомоза
зонда (для питания) 39 следует избегать, предпочи-
тая кратковременное парентеральное питание че-
рез периферическую вену до тех пор, пока анасто-
моз не начнет функционировать, что обычно про-
исходит приблизительно на 4—7-й день после
операции?
При тонкокишечной атрезии необходимо реви-
зовать дистальные отделы кишечника для исклю-
чения множественных пороков. Это лучше всего
делать, вводя в просвет кишки сразу ниже атрезии
физиологический раствор или вазелиновое масло
и осторожно «выдаивая» содержимое в дистальном
направлении. Важно убедиться в том, что и тол-
стая кишка не изменена, ибо атрезия может быть
множественной и отмечаться на протяжении как
тонкой, так и толстой кишки.17
Мы вполне удовлетворены результатами ради-
кального лечения тех случаев кишечной атрезии,
когда отсутствуют нарушения кровообращения, пе-
ритонит и мекониевый илеус. Что же касается со-
временных представлений о выборе вида кишеч-
Рис. 25-9. Этапы формирования дуиденцдуоденоанастомоза. (А), Мобилизация проксимального и дистального сегментов по Кохеру
я их сопоставление.
В, Наложены сближающие шны таким образом, чтобы ширина анастомоза была 1.5—2,0 см. после чего сегменты вскрыты.
С, Завершен однорядный анастомоз бок-в-бок вворачивающими швами шелком 5-0.
352 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
12. 40
ных анастомозов, то последние 20 лет несо-
мненное предпочтение отдается первичному ана-
стомозу конец-в-конец, который даст лучшие ре-
зультаты по сравнению с широко применявшимся
раньше анастомозом бок-в-бок.
Возникающая порой длительная функциональ-
ная непроходимость зоны анастомоза может быть
предотвращена с помощью резекции (перед нало-
жением анастомоза) резко расширенного участка
кишки (обычно это 15 20 см) и создания анасто-
моза конец-в-конец с косым срезом (дистального
отдела) или других видов анастомоза, предусмат-
ривающих уменьшение размеров проксимального
сегмента.40 «Косое» соустье конец-в-конец исклю-
чает развитие синдрома слепой петли, часто воз-
никающего при анастомозе бок-в-бок. Расширен-
ную часть проксимального атрезированного сег-
мента необходимо резецировать всегда, в то время
как дистальный сегмент должен быть максимально
сохранен, ибо именно терминальный отдел под-
вздошной кишки играет наиболее важную роль
в процессе всасывания жирорастворимых витами-
нов и в кишечно-печеночной циркуляции желчных
кислот. Чтобы сгенки анастомозируемых сегмен-
тов были хорошо сопоставлены, косой срез следует
делать под углом 45° по отношению к противобры-
жеечному краю кишки с последующим продлением
разреза на необходимую длину. Анастомоз накла-
дывают одним рядом инвертированных (вворачи-
вающих) отдельных швов через все слои прокси-
мального и дистального сегментов кардиоваску-
лярным шелком 5-0 (рис. 25-10). Использование
таких инвертированных швов позволяет сопоста-
вить серозные поверхности без опасности сужения
просвета анастомоза.
При атрезии дистальной части 12-перстной
или проксимального отдела тощей кишки нало-
жение анастомоза представляет сложности из-за
значительной гипертрофии и дилатации кишки,
которую, однако, нельзя резецировать. Искусствен-
ное сужение приводящего сегмента тощей или
12-перстной кишки с помощью специальных аппа-
ратов 4 или путем интесгинопликации (создание
складок кишки) 41 позволяет уменьшить диаметр
просвета атрезированного отдела и способствует
более быстрому восстановлению перистальтики
и проходимости анастомоза. Из этих способов су-
жения проксимального отдела мы предпочитаем
интестинопликацию, достоинство которой состоит
в сохранении абсорбирующей поверхности слизи-
стой, что чрезвычайно важно в случаях разви-
тия после операции синдрома короткой кишки
(рис. 25-1 i).
Атрезия с синдромом яблочной кожуры создаст
особые проблемы при реконструктивных операци-
ях в связи с наличием при этом варианте патоло-
гии не только резко расширенной тощей кишки, по
и совершенно несвязанного с ней очень суженного
дистального отдела.14,1 В таких случаях следует
непременно сузить проксимальный сегмент и по-
пытаться наложить анастомоз консц-в-конец.
Альтернативным вмешательством в данной ситуа-
ции является создание еюноеюноанастомоза
бок-в-конец (кратсрообразного) с выведением при-
водящего отдела наружу в виде стомы.20 Такой
подход позволяет осуществлять полную декомпрес-
сию проксимального отдела тощей кишки с пита-
нием за зону анастомоза через катетер. Энтеросто-
му в последующем закрывают.43
В тех случаях, когда первичный анастомоз не
показан или наложить его невозможно, достаточно
эффективной оказывается порой двойная энтеро
стомия по Микуличу. Подобная ситуация может
встретиться у новорожденных с тяжелой гипотро-
фией, у недоношенных или при атрезии, сочетаю-
щейся с заворотом и мскониевым перитонитом. До-
стоинство двойной энтеростомии в том. что она
позволяет разгрузить кишку и добиться уменьше-
ния ее размеров до нормальных ко времени закры-
тия стом. При осуществлении этой операции про-
ксимальный и дистальный отделы сшиваются тон-
ким шелком по противобрыжсечному краю на
достаточно большом протяжении таким образом,
чтобы глубже апоневроза их стенки были сопостав-
лены друг с другом на протяжении не менее 1 —
2 см. Соединенные отделы выводят затем наружу
через отдельный разрез. Образование стомы может
быть завершено «вывертыванием» краев слизи-
стой. В большинстве случаев нет нсобхо (имости
в подшивании кишки к коже. Как только достиг-
нут положительный азотистый баланс и оптималь-
ная масса тела, стома может быть закрыта.
Рис. 25-10. Основные принципы наложения ко-
сого анастомоза при тонкокншечной атрезии;
(I) поперечная резекция колбообразио расши-
ренного проксимального сегмента; (2> косой
срез дистального сегмента; (3) дальнейшее
расширение просвета дистального сегмента пу-
тем рассечения его стенки по прогнвобрыже-
ечному краю; (4) «косой» однорядный анасто-
моз отдельными вворачивающими швами шел
ком 5-0; (5) ушивание дефекта брыжейки.
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА 353
Рис. 25-11. К, Типичная атрезия тощий кишки со значительным расширением тощей и 12-перстной.
В. Чрезвычайно расширенные тощая и 12-перстная кишка мобилизованы справа от перхнсбрыжссчных сосу дои и уменьшены в
размерах путем образования складки непрерывным ссрозномышечным швом с интервалом между стежками I см.
С. После создания складки операция завершается наложением косого анастомоза. Там. где образована складка, накладывается
U-образный шов между проксимальным и дистальным сегментами, чтобы предотвратить несостоятельность анастомоза в этом
месте.
При атрезии толстой кишки следует резециро-
вать наиболее расширенный участок проксималь-
ного сегмента и создать временную коицевую ко-
лостому. Анастомоз толстой кишки накладывают,
как правило, в возрасте года или даже раньше,
если диаметр проксимального отдела толстой киш-
ки быстро пришел к норме. Значительная разница
в размерах приводящего и отводящего («порабо-
тавшего») участков толстой кишки достаточно ти-
пична для этого варианта порока, но на восста-
новлении (после операции) функции кишечника
это обычно не сказывается.
Послеоперационное лечение. Основные принци-
пы послеоперационного лечения — адекватная де-
компрессия кишечника с помощью назогастрально-
го зонда (соответствующего размера) у всех боль-
ных и тотальное парентеральное питание у детей
с недоношенностью, мальабсорбцией (из-за умень-
шения всасывающей поверхности кишки), илн ког-
да непроходимость зоны анастомоза вынуждает от-
кладывать энтеральное питание более, чем на
5 дней. Парентеральное питание через перифери-
ческие сосуды обычно проводится всем этим детям,
начиная с 1-го дня после операции. Существует
прямая корреляция между потребностью в тоталь-
ном парентеральном питании, типом имевшейся
атрезии тонкой кишки и тяжестью послеопераци-
онной мальабсорбции, а также длиной оставшейся
кишки.*3 По нашим данным, только 20% детей
с 1-м и 2-м типом атрезии требуют тотального
парентерального питания, в то время как при
больших дефектах брыжейки, синдроме яблочной
кожуры или множественной атрезии все пациенты
требуют тотального парентерального питания от
10 дней до нескольких недель. Большое терпение
следует проявить, прежде чем решиться на повтор-
ную операцию у ребенка с «непроходимостью»
анастомоза, поскольку разница в диаметрах про-
светов вызывает длительную непроходимость или
анастомотическую дисфункцию, со временем спон-
танно проходящую. Стриктура правильно сконст-
руированного анастомоза — осложнение очень
редкое.
Когда содержимое желудка уменьшается в коли-
честве и становится светлым или буроватым,
а также неоднократно отходит нормальный меко-
ний или «голодный» стул, начинают энтеральное
питание, как правило, с подслащенной воды. Затем
детям с дуоденальной обструкцией мы обычно на-
значаем Nutramigen, имеющий мелкодисперсную
консистенцию. У пациентов с тонкокишечной ат-
резией Nutramigen и Pregestimil — препараты выбо-
ра. Питание начинаем с разбавленных растворов.
Объем и концентрацию постепенно увеличиваем,
пока не достигнем уровней, соответствующих нор-
мальной калорической потребности, и прибавки
массы тела. Как только ребенок начинает хорошо
усваивать питание, назначаем Enfamil (за несколь-
ко дней до выписки).
Необходимость проведения тотального паренте-
рального питания значительно увеличивает дли-
тельность пребывания детей в стационаре, не ока-
зывая тем не менее существенного влияния на
течение послеоперационного периода. Что же каса-
23 Заказ N? 1622
354 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
ется зависимости длительности госпитализации от
характера перенесенного оперативного вмешатель-
ства, то, по данным некоторых авторов, дети с дуо-
денодуодсноанастомозом выписываются намного
раньше (в среднем через 16 дней), чем пациенты
с дуоденоеюноанастомозом (28 дней).38 Аналогич-
ные данные получены и у наших больных.
Результаты лечения. Наиболее частые причи-
ны летальных исходов при дуоденальной атре-
зии — недоношенность, легочная патология или
сочетанные тяжелые аномалии, особенно пороки
сердца. Большие сложности могут возникать после
операции в связи с функциональной кишечной не-
проходимостью и дисфункцией анастомоза, что не
позволяет проводить энтеральное питание и требу-
ет инфузионной терапии. Однако указанные труд-
ности должны быть сведены к минимуму путем
выбора наиболее рациональных методов оператив-
ных вмешательств и ведения послеоперационного
периода.
При тонкокишечной атрезии, по данным литера-
туры, с 1969 г. до настоящего времени выживае-
мость возросла с 68% до 95%.1,1 Такому улучше-
нию результатов лечения способствуют следующие
основные факторы.
1. Пренатальная диагностика (почти 100%-ая)
дуоденальной атрезии и большинства случаев тон-
кокишечной непроходимости. При антенатальном
выявлении данного порока женщина должна быть
направлена в дородовое отделение для беременных
группы риска, а ребенок сразу после рождения —
в специализированный стационар для новорожден-
ных с хирургической патологией.
2. Лечение детей с врожденными аномалиями
целесообразно проводить в региональном неона-
тальном центре.
3. Своевременная диагностика и правильный
выбор сроков оперативного вмешательс гва у недо-
ношенных детей и новорожденных с тяжелыми со-
путствующими аномалиями.
4. Первичное радикальное лечение с примене-
нием современных хирургических методов и техни-
ческих приемов способствует снижению до мини-
мума частоты анастомотических осложнений, син-
дромов слепой петли и короткой кишки.
5. Адекватное неосложненное длительное то-
тальное парентеральное питание при замедленном
восстановлении функции анастомоза и у недоно-
шенных детей позволяет существенно уменьшить
число осложнений и нарушений питания, отмечав-
шихся раньше в таких ситуациях.
Летальность при атрезиях кишечника низкая
и в основном обусловлена тяжелыми сопутствую-
щими пороками сердца (такими, как аномалии
AV-канала с трисомией 21), хронической патоло-
гией легких или остро возникшей аспирацией,
в частности при послеоперационных язвах или ки-
шечной непроходимости. Выжившие дети развива-
ются нормально, однако при синдроме короткой
кишки может отмечаться задержка роста и разви-
тия в послеоперационном периоде и в течение 1-го
года жизни. Впоследствии такие больные, как пра-
вило, «нагоняют» своих сверстников.
Синдром короткой кишки. Синдром короткой
кишки — одно из наиболее серьезных осложнений,
отмечающихся при тяжелых формах тонкокишеч-
ной атрезии. Эго состояние является функциональ-
ным и обусловлено отсутствием значительной ча-
сти тонкой кишки, особенно герминального ее отде-
ла и илеоцекальной заслонки. Попытки энтераль-
ного питания в такой ситуации обычно приводят
к диарее, стеаторее, тяжелой дегидратации и в ко-
нечном счете к истощению. В ранней фазе
проявлений этого синдрома, при наличии диареи,
только тотальное парентеральное питание может
дать шансы на благоприятный исход.
При тонкокишечной атрезии 3-го и 4-го типа
синдром короткой кишки отмечается более часто,
поскольку при этих вариантах порока в ряде слу-
чаев уже внутриутробно кишечник значительно
укорочен либо во время операции необходима об-
ширная резекция в связи с заворотом, осложнен-
ным некрозом или мекониевым перитонитом с по-
ражением тонкой кишки на большом протяжении.
После резекции средних отделов тонкой кишки
прогноз лучше, чем при удалении илеоцекального
угла. Так, анализ 50 наблюдений обширной резек-
ции тонкой кишки показал, что при сохранении
илеоцекального угла шансы на благоприятный ис-
ход имеют дети, у которых осталось хотя бы 15 см
тонкой кишки Если же илеоцекальный угол уда-
лен, то для выживания ребенку необходимо иметь
не менее 40 см тонкой кишки.44
Гестационный возраст—второй важный фак-
тор, который влияет на исход при синдроме ко-
роткой кишки. Поскольку именно в 3-м триместре
внутриутробного развития происходит удвоение
длины кишечника,35 недоношенные дети с тяжелы-
ми формами атрезии или с послеоперационной
илеостомой имеют, как это ни парадоксально на
первый взгляд, больше шансов для адаптации ки-
шечника в связи с продолжающимся его ростом,
чем доношенные новорожденные с такой же дли-
ной оставшейся после резекции тонкой кишки. Эти
данные очень важно учитывать при планировании
лечения и определении прогноза, в том числе
и в разговоре с родителями. Достижения послед-
них лет в хирургической технике и возможность
проведения длительного тотального парентераль-
ного питания в домашних условиях позволяют
в настоящее время вылечивать детей, которые
раньше считались абсолютно безнадежными.
Если у пациентов с синдромом короткой кишки
в течение первых нескольких лет жизни эпизоды
диареи и дегидратации — довольно обычное явле-
ние, то в более поздние сроки метаболические
проблемы возникают редко. Пример тому — следу-
ющий случай из нашей практики.
Новорожденная девочка, родившаяся с массой
2,12 кг, оперирована по поводу множественной ат-
резии тощей и дистальных отделов толстой кишки.
В результате проведенного вмешательства оста-
лось 8 см проксимального отдела тощей и 7 см
терминального отдела подвздошной кишки В ди-
стальном отделе ободочной кишки была создана
колостома В течение 98 дней ребенок получал
АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА 355
тотальное парентеральное питание. В последую-
щем в течение почти двух лет, в связи с частыми
эпизодами диареи и с непереносимостью обычных
питатетьных растворов и молока, девочка получа-
ла только Nutramigen.
В возрасте 1,5 лет ребенку был поставлен диаг-
ноз рахита, обусловленного дефицитом витами-
на Д. Начато лечение (витамин Д и глюконат
кальция), что привело к заметному ускорению ро-
ста и развития. Дефицит фолиевой кислоты, вы-
явленный в возрасте 5,5 лет, ликвидирован назна-
чением фолата. Уровень витамина В|2 в это время
был на нижней границе нормы. В возрасте 6 лет
произведена брюшно-промежностная проктоплас-
тика. Во время операции отмечались признаки
нарушения свертываемости крови (увеличение
протромбинового времени), быстро и эффектив-
но устраненные внутривенным введением вита-
мина К.
Этот пример ярко показывает, что у детей
с чрезвычайно короткой кишкой, даже при устано-
вившемся нормальном развитии, в поздние сроки
могут появляться признаки недостаточности жи-
рорастворимых витаминов.
Важно и необходимо тщательно и очень дли-
тельно наблюдать детей с синдромом короткой
кишки. Кроме того, на весь период обычно чрезвы-
чайно долгого и трудного выздоровления семья та-
кого ребенка должна быть обеспечена социально-
психологической поддержкой.
ЛИТЕРАТУРА
I. Ravitch ММ, Barton ВЛ: The need for pediatric surgeons as
determined by the volume of work and the mode of delivery of
surgical care. Surgery 76:754. 1974.
2. Fockens P: Ein operativ geheilter Fall von kongeniialer duennd
Atresie. Zentralbl Chir 38:532. 1911.
3. Evans CH: Collective review: atresias of the gastrointestinal
tract. Surg Gynecol Obstet 92:1. 1951.
4. Grosfeld JL, Ballantine TVN, Shoemaker R: Operative manage
menl of intestional atresia and stenosis based on pathologic
findings. J Pediatr Surg 14:368, 1979.
5. Touloukian RJ: Intestinal atresia. Clin Perinatol 5:3, 1978.
6. Touloukian RJ: Intestinal atresia and stenosis. In Holder TM,
Ashcraft KW (Editors): Pediatric Surgery. WB Saunders, Phila-
delphia, pp 331—345, 1980.
7. Fonkalsrud EW, de I orimier ЛА, Hays DM: Congenital atresia
and stenosis of the duodenum. Л review compiled from the mem-
bers of the Surgical Section of the American Academy of Pedi-
atrics. Pediatrics 43:79, 1969.
8. Jona JZ, Belin RP: Duodenal anomnlics and the ampulla of Va-
ter. Surg Gynecol Obstet 143:565. 1976.
9. Rowe Ml, Buckner D, Clatworthy HW Jr: Windsock web of the
duodenum. Am J Surg 116:444, 1968.
10. de Lorimier A A, Fonkalsrud EW. Hays DM: Congenital atre-
sia and stenosis of the jejunum and ileum. Surgery 65:819,
1969.
11. l.ouw JH, Barnard CN: Congenital intestinal atresia: observati-
ons on its origin. Lancet 2:1065. 1955.
12. Hays DM: Intestinal atresia and stenosis. Cure Probl Surg
Year Book, 1969.
13. Martin I.W. Zerella JT; Jejunoileal atresia: a proposed classifi-
cation. J Pediatr Surg 11:399. 1976.
14. Dickson JAS: Apple |>eel small Ixiwel. An uncommon variant of
duodenal and jejunal atresia. J Pediatr Surg 5:595, 1970.
15. Seashore JH. Collins FS, Markowitz RE Familial apple peel
jejunal atresia: surgical, genetic, and radiographic aspects. Pedi-
atrics 80:540, 1987.
16. Guttman FM. Braun P, Bcnsoussan AL: The pathogenesis of
intestinal atresia. Surg Gynecol Obstet 141:203, 1975.
17. Puri P, Fujimoto T: New observations on the pathogenesis of
multiple intestinal atresias. J Pediatr Surg 23:221, 1988.
18. Tcpas JJ, Shcrmeta DW, Iron AE: Comparison of histochemical
studies of intestinal atresia in the human newborn and fetal
lamb application to clinical experience. J Pediatr Surg
14:376, 1979.
19. Hamdy MN, Man DWK, Bain D; Histochemical changes in in-
testinal atresia and its implications on surgical management:
a preliminary report. J Pediatr Surg 21:17, 1986.
20. Santulli TV. Blanc WA: Congenital atresia of the intestine: Pat-
hogeneis and treatment. Ann surg 154:939. 1961.
21. Touloukian RJ, Wright HK: Intrauterine villus hypertrophy with
jejunoileal atresia. J Pediatr Surg 8:779—1973.
22. Tandler J: Fntwicklungsgeshichte des menschlichen Duodenum
in foiihen Embry onalstudien. Gegerbarn Morph Jahrb 29:187,
1900.
23. Tndani T, I'abuchi K, Tanaka S: Intestinal atresia due to intra-
uterine intussusception. Analysis of 24 cases in Japan. J Pediatr
Surg 10:445. 1975.
24. Abrams JS: Experimental intestinal atresia. Surgery 64:185,
1968
25. Touloukian RJ: Composition of amniotic fluid with experimental
jejunoileal atresia. J Pediatr Surg 12:397, 1977.
26. Touloukian RJ: Antenatal intestinal adaptation with experimen-
tal jejunoileal atresia. J Pediatr Surg 13:468, 1978.
27. Battaglia FC, Lubchenco LO: A practical classification of new-
born infanis by weight and gestational age. J Pediatr 71:159,
1967.
28. Cozzi F. Wilkinson AW: Intrauterine growth rate in relation to
anorectal and oesophageal anomalies'. Arch Dis Child 44:59.
1969.
29. Temlamy SA Miller JD: Extending the scope of lhe VATER
association: definition of lhe VATER syndrome. J Pediatr
85:345, 1974.
30. Santulli TV, Chin CC, Schullingcr JN: Management of congeni-
tal atresia of the intestine. Am J Surg 119:542, 1970.
31. Boles ET Jr, Vassy I.E, Ralston M: Atresia of lhe colon. J Pedi-
atr Surg 11:69. 1976.
32. Lloyd JR. Clatworthy HW Jr; Hydramnios as an aid to the early
diagnosis of congenital obstruction of lhe alimentary tract.
A study of the maternal and fetal factors. Pediatrics 21:903,
1958.
356 АТРЕЗИИ И СТЕНОЗЫ КИШЕЧНИКА
33. Deleze G, Sidcropouios D, Paumgartner G: Determination of bile
acid concentration in human amniotic fluid for prenatal diagno-
sis of intestinal obstruction. Pediatrics 59:647, 1977.
34. Touloukian KJ, Hobbins JC: Maternal ultrasonography in the
antenatal diagnosis of surgically correctable fetal abnormalities.
J Pediatr Surg 15:373, 1980.
35. Adeyemi SD: Combination of annular pancreas and partial situs
inversus: a multiple organ malrotation syndrome associated with
duodenal obstruction. J Pediatr Surg 23:188,, 1988.
36. Bcrdon WE. Baker DH. Sanlilli TV: Microcolon in newborn
infants with intestinal obstruction. Radiology 90:878, 1968.
37. Kimura K, Tsugawa С» Ogawa K: Diamond-shaped anastomosis
for congenital duodenal obstruction. Arch Surg 112:1262, 1977.
38. Weber TR, 1 ewis Jt, Mooney D: Duodenal atresia: a compari-
son of techniques of repair. J Pediatr Surg 21:1133, 1986.
39- Wilkinson AW. Hughes EA, Stevens LH: Neonatal duodenal
obstruction: the influence of ireatment on the metabolic effects
of operation. Br J Surg 52:410, 1965.
40. Louw JH: Resection and end-to-end anastomosis in the manage-
ment of atresia and stenosis of the small bowel. Surgery 62:940,
1967.
41. de Lorimier AA. Harrison MR: Intestinal plication in the tre-
atment of atresia. J Pediatr Surg 18:734, 1983.
42. Zerella JT, Marlin LW: Jejunal atresia with absent mesentery
and helical ileum. Surgery 80:550, 1976.
43. Ahlgrcn I.S: Apple peel jejunal atresia. J Pediatr Surg 22:451.
1987.
44. Wilmore DW: Factors correlating with a successful outcome
following extensive intestinal resection in the newborn infant.
J Pcdiali 80:88, 1972.
45. Touloukian RJ, Smith GJW: Normal intestinal length in preterm
infants. J Pediatr Surg 18:720, 1983-
Глава 26
МАЛ ЬРОТЛЦИ}!
Пороки ротации и фиксации кишечника давно рас-
сматриваются как отдельные нозологические фор-
мы,1 5 имеющие очень разнообразные клинические
проявления. Аномалии этой группы нередко соче-
таются со многими другими пороками, включая ат-
резию 12-перстной и тощей кишки, инвагинацию,
атрезию пищевода, синдром дряблого живота и бо-
лезнь Гиршпрунга.4-” Мальротания является, как
правило, компонентом диафрагмальных грыж,
грыж пупочного канатика и гастрошизиса. При
острых проявлениях пороков ротации и заворота
важна экстренная диагностика и своевременная
операция, что позволяет предотвратить некроз
средней кишки. Хроническое течение мальротации
характеризуется отставанием ребенка в развитии
(по «непонятным причинам»), отсутствием прибав-
ки массы тела, периодическими рвотами и диа-
реей.10-14
Эмбриология. Для квалифицированного лечения
разнообразных анатомических проявлений .мальро-
тации хирургу необходимо знать эмбриологию ки-
шечника в первые 3 месяца развития плода.14-14
Изначально кишечный тракт от желудка до пря-
мой кишки представляет собой прямую трубку. По
мере того, как 12-перстная и будущая средняя
кишка (часть кишечника от связки Трейца до се-
редины ободочной кишки, кровоснабжаемая из
верхней брыжеечной артерии) удлиняются и вне-
дряются в основание пупочного канатика, они со-
вершают поворот на 180° вокруг формирующейся
верхней брыжеечной артерии (рис. 26-1). Затем
12-перстная кишка возвращается в брюшную по-
лость, проходя под верхней брыжеечной артерией
влево — туда, где будет впоследствии расположена
связка Трейца (рис. 26-2—26-5). Перемещаются
в живот и остальные отделы тонкой кишки, за
которой следует толстая, направляясь в левый вер-
хний квадрант. Затем толстая кишка ротируется
над верхней брыжеечной артерией и опускается
в правый нижний квадрант (рис. 26-6—26-9).
К этому времени 12-перстная кишка уже фиксиро-
вана к задней брюшной стенке. К 3-му месяцу
внутриутробного развития фиксированной оказы-
вается и закончившая ротацию толстая кишка как
Рис. 26-1. На представленной модели стер
жеиь, нернсняикулярным к доске, изображает
верхнюю брыжеечную артерию, ровная чисть
веревки, фиксированная к верхнему краю ле-
ски— дуодсносюнатьный отдел и крученая
часть веревки ниже артерии (стержня) — сле-
потолстокншечный от де i. На втором рисунке
части веревки ротированы на 270° против ча-
совой стрелки таким образом, что слепотолсто-
кишечный отдел (крученая веревка) теперь
лежит выше дуоденоеюна i иного отдела (ров-
ная веревка).
358 МАЛЬРОТАЦИЯ
Рис. 26-2. Схема 5-мм эмбриона (4 недели гестации). Кишечник
представляет собой удлиненную трубку с кровоснабжением из
верхней брыжеечной артерии (SNA), отходящей от аорты.
Стрелка на диске показы наст направление ротации от средней
линии (ао — аорта).
Рис. 26-4- По мере роста кишечника ротация вокруг верхней
брыжеечной артерии (SMA) продолжается, достигая 180° у
25-мм эмбриона (8 недель гестации). Этот непрерывный про-
цесс, представленный на схеме, происходит у эмбриона относи-
тельно быстро (ао — аорта).
Рис. 26-S. Схема 40-мм эмбриони (10 недель гестации). 12-
перстная кишка движется в левый верхний квадрант и фикси-
руется там после того, как совершит ротацию на 270° (диск
и стрелка).. (SMA— верхняя брыжеечная артерия, ао - аорта).
Рис. 26-3. Первая стадия ритацни начинается у 10-мм эмбриона
(5 недель гестации), когда удлиняющийся кишечник поворачи-
вается на 90‘ против часовой стрелки над верхней брыжеечнин
артерией (SMA) вправо от нее (ао — аорта).
МАЛЬРОТАЦИЯ 359
Рис. 26-6. На этой схеме 5-мм эмбриона слепоободочная петля
находится в положении исходной (нулевой) ротации (диск
и стретка) ниже верхней брыжеечной артерии (SMA) (соответ-
ствует положению крученой веревки на рис, 26-1). Дуоденоею-
нальный отдел здесь не изображен (ао — аорта).
Рис. 26 8. Схема 40-мм эмбриона. Слепоободочная петля про-
должает очень быстро ротироваться на 180° над Bepxxeif брыже-
ечной артерией (SMA).
Рис. 26-7. Схема 40-мм эмбриона. По мере возвращения тол-
стой и тонкой кишки из луночного канатика в брюшную по-
лость толстая кишка ротируется против часовой стрелки над
SMA (но аорта).
Рис. 26-9. Схема 40-мм эмбриона. Слспоободочпая исглм заиер
шила ротацию на 270" против часовой стрелки над верхней
брыжеечной артерией (SMA) и оказалась теперь в своем обыч-
ном положении н правом нижнем квадранте живота. В это время
12-перстная кишка фиксируется в левом верхнем отделе брюш-
ной полости у связки Трейца.
360 МАЛЬРОТАЦИЯ
правая, так и левая ее половины. Поскольку бры-
жейка тонкой кишки имеет широкое основание,
заворот ее практически невозможен или очень ма-
ло вероятен (рис. 26-10).
Знание закономерностей процесса развития ки-
шечника в эмбриогенезе необходимо для понима-
ния сути возникающих клинических проявлений
мальротации. но не имеет существенного значения
в диагностике и лечении разнообразных се вари-
антов. На практике важно отдифференцировать
острые симптомы от хронических и определить —
имеется ли при мальротации заворот или нет.
Мальротации с заворотом. При данном виде
аномалии клинические проявления могут быть
очень ранними, поскольку заворот на фоне маль-
ротации в некоторых случаях возникает уже внут-
риутробно. Считается, что в результате внутриут-
робного заворота иногда формируется тонкоки-
шечная атрезия, хотя экспериментальной модели
такой последовательности развития пороков не су-
ществует. Данное предположение во шик то в связи
с тем, что до 33% детей с еюнальной атрезией
и 50% с атрезией или стенозом 12-перстной киш-
ки имеют сочетанную мальротацию. Высказыва-
ется мнение о том, что и при мекониевом илеусе
внутриутробный заворот наполненной меконием
кишки, иногда сочетающийся с мальротацией, мо-
жет приводить к атреши Гак или иначе, но любая
мальротации, обнаруженная во время операции по
поводу кишечной атрезии, должна быть корриги-
рована.
Рис. 26-10. В результате нормальной ротации тонкой и толстой
кишки линия прикрепления брыжейки тонкой кишки имеет зна-
чительную длину (прямая линия), при этом 12-псрстная кишка
фиксирована у связки Трейца (заштрихованный кружок), а
толстая кишка ретроперитонеалыю (таштрихованные участ-
ки). Уменьшение протяженности линии фиксации (прямая ли-
ния на схеме) от связки Трейца до слепой кишки чрезвычайно
благоприятствует возникновению заворота тонкой кишки.
Фиксация брыжеики на небольшом протяжении
при мальротации позволяет тонкой кишке вра-
щаться вокруг узкой мезентериальной ножки, в ре-
зультате чего обычно и возникает заворот средней
кишки с острой обструкцией (см. рис. 26-10). Спо-
собствует этому и чрезмерное растяжение кишеч-
ника жидким содержимым или меконием.5 Хотя ча-
стота заворота (44%) ошнакова во всех возраст-
ных группах, однако у новорожденных детей он
чаще приводит к гангрене кишки, которую в ре-
зультате приходится резецировать.
Заворот проявляется острым началом, представ-
ляя собой неотложную хирургическую ситуацию,
которая требует экстренной диагностики и срочной
операции, что позволяет избежать гангрены киш-
ки. Рвота с примесью желчи в сочетании со взду-
тием живота, болями, выделением крови из прямой
кишки или в рвотных массах — классические симп-
томы заворота средней кишки. По мерс нараста-
ния ишемии кишечника развиваются шок и сепсис.
При наличии у ребенка вздутия живота, болезнен-
ности его при пальпации и сниженного газонапол-
нения кишечника на рентгенограммах, необходимо
исключить острый заворот (рис. 26-11). Дети
с описанными клиническими проявлениями и рент-
генологической картиной должны быть срочно (без
дальнейшего диагностического обследования) под-
вергнуты лапаротомии с целью ликвидации заво-
рота.4 Если клиника острого живота отсутствует,
необходимо провести обследование с контрастным
веществом верхних о)делов желудочно-кишечного
тракта, что обычно позволяет поставить диагноз
заворота, в то время как ирригография может
лишь вызвать подозрение на эту патологию
(рис. 26-12). Среди детей, которые требуют резек-
ции кишечника при завороте средней кишки, ле-
тальность составляет 50% и связана обычно с воз-
никающим после операции синдромом короткой
кишки.7
Хроническая форма заворота средней кишки
возникает менее часто, чем острая, и проявляется
периодическими болями в животе рвотой с при-
месью желчи или без нее. Нередко отмечается
мальабсорбция, приводящая к отставанию в разви-
тии. Серийное контрастное рентгенологическое об-
следование верхних отделов ЖКТ имеет важное
диагностическое значение. Хирургическая коррек-
ция в большинстве случаев приводит к изле-
чению. 1-15
Дуодена чъная непроходимость. Острая обст-
рукция (при мальротации) верхней трети 12-перст-
ной кишки вызвана обычно ее аномальной перито-
неальной фиксацией, связанной с недостаточным
прикреплением неправильно ротированной тол-
стой кишки к задней брюшной стенке. Почти
половина больных с этой аномалией имеют соче-
танный заворот средней кишки, что обусловливает
необходимость срочной диагностики. ' Наиболее
частый симптом — рвота после кормления. У 2/3
больных рвотные массы окрашены желчью. Меко-
ний обычно отходит, как и нормальный стул, но
иногда отмечаются запоры. ( ерийное контрастное
рентгенологическое обследование верхних отделов
МАЛЬРОТАЦИЯ 361
Рис. 26-11. Рентгенограммы новорожденного, у которого отмечались рвоты с примесью желчи, кровь в ciyne и напряжение живота.
Виден двойной пузырь, но при внимательном осмотре можно заметим, небольшое количество воздуха ниже (стречка на боковой
рентгенограмме), что говорит и частичной непроходимости и позволяет исключить диагноз туодсначыюй атрезии. Резко сниженное
газона иол пение кишечника очень характерно для заворота при мальротации.
ЖКТ — основной метод диагностики (рис. 26-13).
Хирургическое вмешательство должно быть сро-
чным.
Хроническая частичная дуоденальная непрохо-
димость может возникнуть в тюбом возрасте/ Ес-
ли она связана с заворотом, то иногда отмечаются
диарея и синдром мальабсорбции. Периодическая
рвота, сочетающаяся с болями в животе (или без
болей), должна быть показанием для серийного
обследования верхних отделов ЖКТ под контро-
лем ЭОПа, что позволяет выявить признаки об-
струкции.
Мезоколикопариетальные грыжи. Внутренние
грыжи возникают как следствие мальротации, ког-
да тонкая кишка в процессе поворота и ретропери-
тонеальной фиксации внедряется в мезоколон.м’15
Данная патология достаточно четко описана, и пра-
вильное ее название именно «мезоколикопарие-
тальные» грыжи. Применяемый иногда в подоб-
ных случаях термин «парадуоденальная» грыжа
неточен.15 При правосторонней грыже тонкая киш-
ка не совершает нормального поворота вокруг
верхней брыжеечной артерии, а остается в правом
верхнем квадранте и оказывается заключенной
справа позади мезоколон, при этом правая полови-
на толстой кишки ротируется и фиксируется рет-
роперитонеально на любом участке — от правого
верхнего квадранта до своего обычного местополо-
жения в правом нижнем квадранте (рис. 26-14).
Левая мезоколикопармстальная грыжа возникает
в том случае, когда тонкая кишка ротируется вле-
во и внедряется в мезоколон между нижней брыже-
ечной веной и забрюшинным пространством. Тол-
стая же кишка продолжает ротацию до нормального
положения, заключая тонкую в мешок мезоко-
лон, при этом нижняя мезентериальная вена обра-
зует довольно узкую шейку мешка (рис. 26-14).
Неопределенные боли в животе и хроническая рво-
та — наиболее частые симптомы данной патоло-
гии. При серийном рентгенологическом обследова-
нии верхних отделов ЖКТ с контрастным веще-
ством обнаруживают находящуюся в кармане
(мешке) тонкую кишку.
Рентгенологическая диагностика. Анамнез и
данные физикального обследования позволяют
лишь заподозрить мальротацию и заворот. Уста но-
362 МАЛЬРОТАЦИЯ
Рис. 26-13. Ребенок одной недели жизни, у когорого начались
рвоты с примесью желчи. Ирригографин показала расположе-
ние слепой кншкн в правом верхнем квадранте живота, а иссле-
дование верхних отделов желудочно-кишечного тракта — што-
порообразную конфигурацию (стрелка) дуоденоеюнального от-
дела с частичной обструкцией. Эти симптомы характерны для
мальрот.тии с дуоденальными тяжами.
Рис. 26-12. На ирригограмме видно неправильное положение
слепой кишки (сiредка), что должно вызывать подозрение на
мальротацию с возможными тяжами Ледла или заворотом. Если
при осмотре не обнаружены признаки острого заворота с ише-
мией кишечника, то следует произвести исследование пассажа
контрастного вещества по верхним отделам желудочно-кишеч-
ного тракта.
вить же окончательный диагноз можно только при
рентгенологическом обследовании под контролем
ЭОПа. Диагностические возможности (в отноше
нии мальротации) УЗИ и компьютерной томогра-
фии пока еще исследуются.1’ На ирригограммах
картингд обычно яркая и несложная тля интерпре-
тации (см. рис. 26-12)—определяется неправиль-
но расположенная слепая кишка. Однако, хотя ир-
ригография и может вызвать подозрение на маль-
ротацию, но она не позволяет выявить заворот.
Кроме того, при относительно нормально роти-
рованной толстой кишке у ребенка могут быть
тяжи Ледд<1 и тогда ирригограммы норой оценива-
ются неправильно, что ведет к диагностическим
ошибкам.
Серийное исследование верхних отделов ЖКТ
позволяет окончательно поставить диагноз, выяв-
ляя характерную штопорообразную деформацию
12-перстной кишки (см. рис. 26-13). Другой ха-
рактерный симптом — расположение как 12-перст-
ной, так и тощей кишки в правом верхнем квад-
ранте (рис. 26-15), а также признаки хронической
дуоденальной обструкции (рис. 26-16).
Заворот средней кишки у новорожденных про-
является классическими рентгенологическими при-
знаками в виде растянутого желудка и относи-
тельно безвоздушного кишечника. Такая картина
требует немедленной операции для ликвидации
заворота, что позволяет сохранить жизнеспособ-
ность кишечник?) (см. рис. 26-11).18
Хирургическая коррекция. До операции нет не-
обходимости в специальной подготовке кишечни-
ка. поскольку вмешательство проходит без вскры-
тия его просвета, тем более, что при остром заво-
роте для такой подготовки просто нет времени.
Однако у старших дегей, которые подвергаются
плановому вмешательству, подготовка кишечника
может облегчить выделение толстой кишки.
Пациентам с «острым животом» и подозрением
на заворот ставят назогастральный зонд, проводят
инфузионную терапию и начинают профилактиче-
ское введение антибиотиков. Предоперационная
МАЛЬРОТАЦИИ 363
CECUM
INFERIOR
MESENTERIC ARTERY
PROXIMAL
ILEUM
TERMINAL
ILEUM
INFERIOR
MESENTERIC VEIN
Puc. 26-14. А. Правосторонняя мсзоколнкопаристальная грыжа, при которой тонкая кишка заключена позади мезоколон (заштрихо-
ванная область), в то время как толстая (слепая) фиксирована к задней париетальной брюшине в правом верхнем квадранте. Ниж-
няя брыжеечная артерия образует левый край мезентериального мешка. Рассечение брюшины татератьнсе толстой кишки (пунк-
тирная линия) позволяет освободить толстую кишку и поместить ее в левый верхним квадрант, что высвобождает тонкую кишку,
которая остается в животе справа.
В и С, Левосторонняя мезоколикопариетальная грыжа развивается (В) по мере того, как совершакицая ротацию 12-перстная
кишка иивагинируется в пространство позади левой половины мезоколон, при этом верхняя брыжеечная вена располагается по
краю кармана (.мешка). Окончательно сформ и puna интим левосторонняя мелокол и ког триста я ышя грыжа (С) с узкими ворота-
ми, образованными верхней брыжеечной веной. Ликвидация этой грыжи должна быть осуществлена путем осторожного выделения
брыжеечной пены, что позволяет освободить тонкую кишку, которую помешают в пряную половину живота.
подготовка должна быть кратковременной, а опе-
рация экстренной, что позволяет предотвратить
ишемию кишечника, которая может потребовать
резекции н в результате привести к синдрому ко-
роткой кишки. При подозрении на заворот, но при
отсутствии картины «острого живота», предопера-
ционная подготовка не отличается от описанной
выше, но длительность ее можег быть увеличена
до 4—8 часов. Пациентам с хроническими проявле-
ниями мальротации операция проводится в плано-
вом порядке, а показания к ней ставятся сугубо
индивидуально и избирательно.
Разрез применяют поперечный справа, слегка
продлевая его за среднюю линию, или срединный.
Очень важно, особенно если есть заворот, эвентри-
ровать для осмотра весь кишечник. Цель вмеша-
тельства — возвратить кишечник в положение нор-
мальной незавершенной ротации, т. е. поместить
12-перстную и верхнюю часть тощей кишки в пра-
вый фланг живота, а слепую — в левый верхний
квадрант. * ' После извлечения кишечника
осматривают тяжи Ледда, идущие от слепой кишки
через 12-перстную (две верхние ее трети) к забрю-
шинному пространству. Слепая кишка на своем
месте обычно отсутствует, а 12-перстная может
быть замурована тяжами Ледда в основании бры-
жейки толстой кишки. 12-перстную кишку необхо-
димо отделить от слепой и поместить в правый
фланг живота.
При завороте по вскрытии брюшной полости
видна только тонкая кишка, а 12-перстная, слепая
и восходящий отдел толстой скрыты позади пе-
тель, находящихся в завороте. Заворот устраняют
путем поворота кишечника против часовой стрел-
ки на два, три или больше оборотов до тех пор,
пока не появятся слепая кишка и восходящий от-
дел толстой. Ишемические изменения после этого
(если они не были длительными), как праиило.
уменьшаются. Зате.м осторожно, острым и тупым
путем, разделяют все тяжи Ледда, после чего сле-
пая кишка должна быть помещена в левый верх-
ний квадрант. 12-перстную кишку освобождают
полностью таким образом, чтобы она «свешива-
лась» прямо вниз по направлению к правому ниж-
нему квадранту.
Если операция производится у новорожденного,
то следует обязательно исключить и внутреннюю
обструкцию 12-псрстной кишки. Для этого в
12-персгную кишку и далее в тощую проводят ка-
тетер Фолея (вводя его через рот), надувают бал-
лон и катетер подтягивают обратно в желудок.
Аппендэктомию следует производить всегда, так
как слепая кишка после операции по поводу маль-
ротации будет находиться в левом верхнем квад-
ранте и если отросток не удален, то при возникно-
вении острого аппендицита диагностика его может
вызвать очень большие трудности. Лучше осуще-
ствлять аппендэктомию инвагинационным спосо-
бом, который исключает необходимость вскрытия
просвета кишки, что нежелательно при операции
по поводу мальротации, всегда сопровождающейся
обширным выделением кишечника.20 В настоящее
364 МАЛЬРОТАЦИЯ
Рис. 26-15. Ребенок старшего возраста с хроническими болями
в животе и периодической рвотой. Рентгенограмма показывает
отсутствие связки Трейца и расположение начального отлета
тощей кишки в правом верхнем квадранте, что говорит о мать-
ротацни.
время считается, что при коррекции мальротации
нег необходимости и фиксации 12-персгной и сле-
пой кишки, как это рекомендовалось раньше.19
Операции при редких видах мальротации. Об-
ратная ротация толстой кишки (толстая кишка
при этом варианте ротируется по направлению
к левому верхнему квалранту вместо правого ниж-
него и прохолит под верхней брыжеечной арте-
рией) может быть корригирована п;,тем ра {деле-
ния аномальных брюшинных тяжей с отведением
их вниз и перемещения кишечника таким образом,
чтобы толстая кишка вышла из-под верхней бры-
жеечной артерии. Не следует пересекать толстую
кишку и реанастомозировать ее впереди артерии,
как это предлагается некоторыми хирургами.
При мезоколикопариетальных грыжах порой
трудно проводить коррекцию, поскольку стенка
грыжевого мешка образована брыжейкой толстой
кишки (см. рис. 26-14). Правостороннюю грыжу
устраняют путем выделения толстой кишки вдоль
правого фланга и перемещения ее в левую полови-
ну живота. В результате освобождается тонкая
кишка, которая теперь лежит в правой половине
живота (см. рис. 26-14А). При левосторонней гры-
же мезентериальная вена, образующая стенку
мешка (см. рис. 26-14В и С), должна быть выделе-
на по правому его краю, что позволяет извлечь
кишечник, который таким образом будет находить-
ся в правой половине живота.15
Заворот средней кишки с ишемией. Одна из
Рис. 2Л-К,. 9-лстний ребенок с повторными болями в животе,
хронической рвотой и потерей массы тела. Ирригография была
неинформативной, ио исследование верхних отделов показало
выраженную обструкцию средней и терминальной части
12-перстной кишки (стрстка) тяжами Лолла.
наиболее тяжелых ситуаций для хирурга — обна-
ружить во время лапаротомии при мальротации
тотальную гангрену средней кишки в результате
заворота. Самая экстренная операция при подозре-
нии на заворот помогает предупредить развитие
этого осложнения. Если гангренозные изменения
отмечаются на протяжении большей части средней
кишки, то резекция не должна производиться.
В такой ситуации следует ликвидировать заворот
и, ограничив этим операцию, ушить брюшную по-
лость. Через 12—24 час прои (водят релапарото-
мию с целью повторного осмотра кишечника. В не-
которых случаях состояние части его улучшается
настолько, что можно произвести резекцию с ана-
стомозом или наложением кишечного свища без
опасности развития синдрома короткой кишки.
В течение этого 12—24-часового периода ожида-
ния родители должны быть подготовлены к тому,
что кровообращение возможно и не восстановится,
а соответственно длина неизмененного кишечника
окажется недостаточной для того, чтобы ребенок
выжил. Если во время релапаротомии вся тонкая
кишка остается по-прежнему гангренозно изменен-
ной, то мой опыт подсказывает, что в такой ситуа-
ции правильнее ушить брюшную полость без ре-
зекции кишечника и полностью прекратить анти-
МАЛЬРОТАЦИЯ 365
биотикотсрапию. Больному лишь внутривенно вво-
дят жидкость и обезболивающие средства, посте-
пенно прекращая вентиляционную поддержку. Ес-
ли же продолжать ИВЛ и введение антибиотиков,
то новорожденные могут существовать довольно
долго, но неблагоприятный исход все равно неиз-
бежен и наступает обычно, когда уже исчерпаны
все возможности осуществлять доступ в вены.
Очень важно подчеркнуть, что лечение, разумеет-
ся, должно быть сугубо индивидуальным для каж-
дого конкретного пациента и каждой семьи.
Мальротация с бессимптомным течением. Ни
у одного больного не бывает абсолютно бессимп-
томного течения, ибо «случайно» мальротация об-
наруживается обычно при обследовании детей
в связи с наличием каких-либо неспецифических
симптомов со стороны ЖКТ 20 Тщательный ана-
лиз показывает, что именно ли симптомы и обу-
словлены мальротацией. К ним относятся кишеч-
ная колика, хроническая рвота, хроническая диа-
рея, неопределенные боли в животе, отставание
в физическом развитии.21 Если при обследовании
пациента с перечисленными симптомами диагно-
стирована мальротация, которой вполне можно
объяснить подобную клиническую картину, то
большинство хирургов в настоящее время рекомен-
дуют таких больных оперировать.5 7 Если же ано-
малия ротации обнаружена случайно во время вме-
шательства, производимого по иному поводу, то
она должна быть обязательно корригирована. Это
особенно важно сделать в тех случаях, когда в свя-
зи с основной патологией, послужившей показани-
ем к операции, предполагается наложение стомы,
анастомоза по Py-Y-образного либо создание
искусственного мочевого пузыря из сегмента киш-
ЛИТЕРАТУРА
1. Waugh GE: Congenita! malformation of lhe mesentery: A clini-
cal entity. Br J Surg 15:438—449» 1928.
2. Ladd WE: Congenital obstruction of the duodenum in children.
N Engl J Med 206:277—283. 1932.
3. Ladd WE: Surgical diseases of the alimentary tract in infants.
N Engl J Med 215:705. 1936.
4. Andrassy RJ, Mahour GIL Malrotation of lhe midgut in infants
and children. Arch Surg 116:158—160, 1981
5. Smith EI: Malrotation of lhe intestine. In Welch KJ. Randolph
JG, Ravitch MM (Editors): Pediatric Surgery, Year Book Medi-
cal Publishers, Chicago, pp 882—895. 1986.
6. Filston HC, Kirks DR: Malrolalion - the ubiquitous anomaly.
J Pediatr Surg 16:614 620, 1981.
7. Powell DM, Othersen HB, Smith CD; Malrolalion of the intesti-
nes in children; The effect of age on presentation and therapy.
J Pediatr Surg 24:777—780, 1989.
8. Brcrelon RJ. Taylor B, Hal! CM: Intussusception and intestinal
malrotation in infants: Waugh’s syndrome. Br J Surg 73:55—57,
1986.
9. Yanez R, Spitz L: Intestinal malrotation presenting outside the
neonatal period. Arch Dis Child 61:682 685, 1986.
10. Boulton JE, Ein SH, Reilly BJ, el al.: Necrotizing entercolilis
and volvulus in the premature neonate. J Pediatr Surg 24:901
905. 1989.
11. Jackson A, Bissel R. Dickson AP: Case report: Malrotation and
midgut volvulus presenting as malabsorption. Clin Radiol
40:536—537. 1989.
12. Howell CG, Vozza F, Shaw S. el al.: Malrotation, malnutrition,
ки. Если в подобной ситуации сначала не устра-
нить мал ь ротацию, то можно ошибочно взять не
тот сегмент кишки или провести его в антипери-
стальтическом направлении. Чрезвычайно слож-
ную проблему представляет иногда тиагностика
острого аппендицита у детей с нераспознанной
мал ьрота цией. К сча стью, а нома л и и поворота
очень редко встречаются у больных с аппендици-
том — нсего в 0,04% случаев. При сочетании ап-
пендицита с мальротацией отросток в 97,6% на-
блюдений расположен в правом верхнем квадранте
живота.22
Результаты. Послеоперационное ведение боль-
ных такое же, как после любой лапаротомии
и большого вмешательства на кишечнике. Леталь-
ность обусловлена в основном син дромом короткой
кишки после резекции при завороте средней киш-
ки с гангреной/ 7 Рецидив непроходимости или
заворота возникает редко.6, ‘ 1 Возобновление пос-
ле операции болей в животе, диареи или рвоты
чаще отмечается у пациентов, имевших до вмеша-
тельства хроническое течение патологии, чем
у больных с острыми симптомами.'
По данным одного исследования, из 70 больных
с мальротацией 8 умерли — 4 новорожденных
и 4 ребенка старше 1 месяца.7 Все смерти были
связаны с осложнениями длительного тотального
парентерального питания при синдроме короткой
кишки. Высокая частота легальных исходов при
гангрене средней кишки у детей с заворотом обу-
словливает необходимость очень срочного хирур-
гического вмешательства, которое должно прово-
диться сразу, как только заподозрен диагноз дан-
ной патологии.
and ischemic bowel disease. J Pediatr Surg 17:469—473. 1982.
13. Janik JS. Ein SH: Normnl intestinal rotation with nonfixaiion:
A cause of chronic abdominal pain. J Pediatr Surg 14:6, 1979.
14. Callander CL, Rusk GY. Netnir A: Mechanism, symptoms and
treatment of hernia into the descending mesocolon (left duode-
nal hernia). Surg Gynecol Obstet 60:1052 1071. 1923.
15. Willwerth BM, Zollinger RM, Izant RJ: Congenital mesocolic
(paraduodenal) hernia. Am J Surg 128:358—361, 1974.
16. Snyder WH. Chaffin 1 - Embryology and pathology of the intes-
tinal tract Presentation of 48 cases of malrotation. Ann Surg
140:368 380, 1954.
17. Loycr E. Eggli KI): Sonographic evaluation of superior mesente-
ric vascular relationship in malrotation. Pediair Radiol 19:173-
175, 1989.
18. Kassncr EG. Kottmeier PK: Absence and retention of small bo-
wel gas in infants with midgul volvulus: Mechanisms and signifi-
cance. Pediatr Radiol 4:28 30, 1975.
19. Stauffer UG. and Herrmann P: Comparison of late results in
patients with corrected intestinal malrotation with and without
fixation of the mesentery. J Pediatr Surg 15:9—12. 1980.
20. Bishop HC, Filston HC: Inversion-ligation technique for inci-
dental appendectomy. J Pediatr Surg 8:889- 892, 1973.
21. Kumar D, Brercton RJ, Spitz L. Hall CM: Gastro-oesophageal
reflux and intestinal malrotation in children. Br J Surg 75:533
536. 1988.
22. Collins DC: 71.000 Human appendix specimens: A final report,
summarizing forty years’ study. Am J Proctoi 14:365 381.
1963.
Глава 27
МЕКОНИЕВАЯ БОЛЕЗНЬ:
МЕКОНИЕВЫЙ ИЛЕУС,
СИНДРОМ МЕКОНИЕВОЙ ПРОБКИ,
МЕКОНИЕВЫЙ ПЕРИТОНИТ
Все заболевания, связанные с меконием, в какой-то
степени схожи между собой по клинической карти-
не, методам диагностики и лечения. И хотя среди
них трудно выделить метко очерченные нозологи-
ческие формы, мы попытались все-таки охаракте-
ризовать отдельно каждое из обозначенных в на-
звании главы заболеваний. Мекониевый илеус, мс-
конисвый перитонит и синдром мекониевой пробки
проявляются у новорожденных картиной кишечной
непроходимости. Мекониевый илсус обычно быва-
ет при кистофиброзе (КФ), хотя имеются сообще-
ния о мекониевом илеусе и без КФ. Синдром
мекониевой пробки, как правило, не связан с КФ,
но есть сообщения и о сочетании этих двух видов
патологии.3 Мекониевый илсус может быть «про-
стым» или осложненным. Во втором случае он про-
является картиной мекониевого перитонита.
КФ представляет собой наследственное заболе-
вание, характеризующееся генерализованным по-
ражением экзокринных желез. При мекониевом
илеусе отмечается внутренняя обструкция кишеч-
ника сгущенным меконием. Термином «эквивалент
мекониевого илеуса» (ЭМИ) обозначается механи-
ческая закупорка кишечника густыми, замазкопо-
добными, сгущенными каловыми массами, возни-
кающая у больных с КФ в любом возрасте, кроме
периода новорожденности. Синдром мекониевой
пробки проявляется у новорожденного толстоки-
шечной непроходимостью. Причина его лежит, по-
видимому не столько в самой мекониевой пробке,
сколько в снижении перистальтики толстой кишки.
Синдром мекониевой пробки порой ошибочно объ-
ясняется или вообще принимается за синдром су-
женной левой половины толстой кишки. Меконие-
вый перитонит представляет собой реакцию брю-
шины у новорожденного (по типу химической или
на инородное тело) в ответ обычно на пренаталь-
ную перфорацию кишечника. Мекониевый перито-
нит может быть вызван мскониевым илеусом или
любой другой причиной врожденной кишечной
непроходимости. Каждое из перечисленных в за-
главии состояний представляет собой лишь опре-
деленный спектр клинических симптомов, тем не
менее в данной главе они рассматриваются отдель-
но, в соответствующих подразделах.
МЕКОНИЕВЫЙ ИЛЕУС
История. Первое описание патологических изме-
нений в поджелудочной железе у новорожденных
с кишечной непроходимостью, вызванной сгущен-
ным меконием, было представлено в 1905 г. Lands-
teiner.'1 А кистофиброз (КФ) как сочетание недо-
статочности поджелудочной железы и хронической
болезни легких впервые описан в 1936.5 Двумя го-
дами позже появилось первое в литературе сооб-
щение о мекониевом илеусе как наиболее раннем
проявлении КФ.6 Необычная консистенция меко-
ния была объяснена образованием при КФ густого
вязкого секрета слизистых желез.
Хирургическое лечение мекониевого илеуса не
предпринималось до 1948 г., когда Hiatt и Wilson
достигли успешных результатов у 5 из 8 пациен-
тов, благодаря промываниям кишечника физиоло-
гическим раствором через илеостому.7 Gross в
1953 г. сообщил о ликвидации непроходимости пу-
тем резекции кишки и энтеростомии по Микули
чу.8 Bishop и Коор в 1957 г. описали резекцию
и анастомоз консц-в-бок с дистальной стомой,
предназначавшейся для послеоперационного про-
мывания кишечника.’ С тех пор применялись са-
мые разнообразные оперативные вмешательства
и растворы для «разрушения» густого мекония.
В 1969 г. Noblett предложил при простом меконие-
вом илеусе использовать для промывания кишеч-
ника и ликвидации обструкции гипсросмолярный
препарат meglumine diatrizoate (гастрографин).10
Благодаря ранней диагностике и совершенствова-
нию методов консервативного и хирургического
лечения послеоперационная летальность при меко-
ниевом илеусе снизилась за последние 25 лет
с 70 до 20%.“
Частота. Мекониевый илеус — наиболее ран-
нее клиническое проявление КФ, встречающееся
у 10—20% больных с этим заболеванием. По дан-
ным некоторых авторов, мекониевый илсус выяв-
МЕКОНИЕВАЯ БОЛЕЗНЬ 367
ляется у каждого третьего новорожденного с ки-
шечной непроходимостью.’2, ” Девочки и мальчики
подвержены этому заболеванию одинаково часто.
Мекониевый илеус редко встречается у темноко-
жих американцев и почти никогда у жителей Аф-
рики и Азии. Частота КФ у белого населения ко-
леблется от 1:1150 до 1:1500 живорожденных.14-16
Патогенез. Поскольку КФ передается аутосом-
но-рецессивным путем, то оба родителя могут быть
гетерозиготными носителями гена, сами не болея
при этом данным заболеванием. Каждый из их де-
тей имеет таким образом один шанс из четырех
заболеть этой болезнью. У белых людей КФ —
одно из наиболее частых среди генетически пере-
дающихся тяжелых заболеваний. Считается, что
приблизительно 5—6% населения в популяции яв-
ляются гетероз и гота ми.17 В семьях, где у первого
ребенка был мекониевый илеус, 29% последующих
детей с КФ также имеют мекониальную непрохо-
димость. Этот показатель составляет всего 6%
в тех случаях, когда у первого ребенка с КФ не
было мекониевого илеуса.*8, 19
Пациенты с мскониевым илеусом могут состав-
лять определенную группу, характеризующуюся
мультиаллелизмом (различные мутации одного
и того же локуса, например один—для КФ
и один — для мекониевого илеуса).20 Однако это
предположение не нашло достоверного подтверж-
дения во многих исследованиях.
КФ — системное заболевание с множественным
поражением экзокринных желез во всех частях ор-
ганизма. Наиболее тяжелые клинические проявле-
ния возникают в результате обструкции (необычно
густым и вязким слизистым секретом) дыхатель-
ных путей, протоков поджелудочной железы и ки-
шечника. Кроме того, могут поражаться потовые
и слюнные железы, печень, носовые слизистые
мембраны и репродуктивные органы.
Поражение поджелудочной железы начинается
пренатально с прогрессирующей обструкции ее
протоков, что приводит к ацинарной атрофии, сни-
жению секреции, иногда фиброзу и жировым из-
менениям ткани. В результате большинство па-
циентов с КФ имеют выраженную экзокринную
недостаточность поджелудочной железы.21, “ При-
близительно у 85—90% детей с КФ поражение
поджелудочной железы возникает в раннем детст-
ве, обусловливая отсутствие панкреатических эн-
зимов в дуоденальном содержимом.23 Выделение
слизи повышенной вязкости в кишечнике также
начинается пре натально. Уплотненный меконий
закупоривает кишечник уже внутриутробно. Меко-
ний при мекониевом илеусе содержит мало во^ы
и имеет измененный биохимический состав,
а именно — в нем отмечается высокое (по сравне-
нию с нормой) количество белков и сниженное —
углеводов. С этим связана густая консистенция ме-
кония. Излишний белок в основном представ-
лен альбумином,28 определение которого в меконии
используется как скрининг-тест на КФ.16 Возмож-
но, дефицит панкреатических энзимов —- не глав-
ная причина изменений мекония, о чем гонорит
отсутствие четкой корреляции между мекониевым
илеусом и тяжестью поражения поджелудочной
железы?0 Мекониевый илеус возникает прежде
всего как результат аномальной секреции в кишеч-
нике, а поражение поджелудочной железы стоит
при этом на втором плане?0
У детей с мекониевым илеусом легкие при рож-
дении имеют нормальную структуру и функцию,
но в результате закупорки слизью мелких дыха-
тельных путей и присоединения вторичной инфек-
ции развивается прогрессирующее диффузное их
поражение.
Уровень натрия и хлора в отделяемом потовых
желез начинает после рождения повышаться» но
это не связано ни с тяжестью заболевания, ни
с тем, какие органы поражены. Изменение содер-
жания электролитов в продукции потовых желез
вызвано непроницаемостью их эпителия для ионов
хлора. В то время как натрий активно абсорбиру-
ется из просвета железистых протоков, хлор оста-
ется внутри, удерживая таким образом в просвете
и натрий?1
Патология. Проксимальный отдел подвздошной
кишки при мекониевом илеусе утолщен, расширен
и забит вязким меконием. Дистальные отделы ки-
шечника сужены и содержат комочки серого, за-
мазкоподобного густого мекония, который часто
имеет вид шариков. Нефункционирующая толстая
кишка (микрокодон) недоразвита и также может
содержать небольшое количество мекония. Почти
у 50% детей с мекониевым илеусом возникает пер-
форация подвздошной кишки?2 причиной которой,
по-видимому, является заворот или локальная ганг-
рена, а иногда оба этих фактора. Встречаются так-
же атрезия кишечника, некроз, мекониевый пери-
тонит, псевдокисты или даже все перечисленные
виды патологии одновременно. Ишемический не-
кроз всего вовлеченного в заворот сегмента кишки
с выходом из просвета мекония и его разжижением
приводит к образованию псевдокисты (гигантский
кистозный мекониевый перитонит). Если заворот
и перфорация возникают постнатально, то разви-
вается бактериальный перитонит.
У детей с неосложненным мекониевым илеусом
клиническая картина может быть такой же, как
при аганглиозе, а потому иногда показана биопсия
кишечника с целью выявления ганглиев. И гисто-
логически мышечный слой кишки выглядит гипер-
трофированным как при мекониевом илеусе, так
и при болезни Гиршпрунга. К сожалении), нет ка-
кой-либо определенной классической гистологиче-
ской картины, характерной для мекониевого
илеуса.
Клиническая картина. Примерно от 10 до 33%
пациентов с мекониевым илеусом имеют родствен-
ников, страдающих кистофиброзом, который яв-
ляется генетической аномалией, передающейся
аутосомно-рецессивным путем.1 ’ 1 ’ Хотя дети
с мекониевым илеусом часто рождаются с внутри-
утробной гипотрофией, однако недоношенными
они бывают редко. Низкая масса тела при рожде-
нии отчасти объясняется тем, что в связи с кишеч-
ной непроходимостью, развивающейся при мекони-
евом илеусе внутриутробно, плод недополучает из
368 МЕКОНИЕВАЯ БОЛЕЗНЬ
амниотической жидкости питательные вещества.
Многоводие у матерей отмечается в 10—20% слу-
чаев, наиболее часто — при осложненных формах
мекониевого илеуса. Сочетанные врожденные ано-
малии встречаются редко. Тяжесть кишечной обст-
рукции бывает разной — от легких форм, с которы-
ми удается справиться клизмами, до рано возника-
ющей полной непроходимости. Простой мекониевый
илеус обычно проявляется в первые 24—48 часов
увеличением живота и рвотами с желчью. Меконий
не отходит. Через брюшную сгеику часто контури-
руются растянутые кишечные петли, имеющие при
пальпации тсстоватую консистенцию. Прямая
кишка и анальное отверстие обычно сужены, ма-
ленькие по размерам и это может быть не-
правильно интерпретировано как анальный стеноз
или даже атрезия.
Осложненный мекониевый илеус протекает бо-
лее тяжело и обычно начинается остро, в первые
24 часа после рождения, с прогрессирующего взду-
тия живота, иногда приводящего к респираторному
дистрессу (рис. 27-1). Могут отмечаться симптомы
перитонита с отеком и гиперемией перерастянутой
брюшной стенки, а на рентгенограмме пневмо-
перитонеум. Отек и гиперемия брюшной стенки
обычно говорят о наличии подлежащей псевдоки-
сты или о перитоните. Иногда развивается выра-
женная гиповолемия, появляются признаки сепси
са, состояние становится очень тяжелым.
Диагностика. Дифференциальная диагности-
ка. Предоперационный диагноз обычно устанавли-
вают на основании клинической картины, данных
физикального обследования и рентгенографии
(снимки в вертикальном и горизонтальном поло-
жении), а также семейного анамнеза. Имеющаяся
симптоматика иногда может быть ошибочно расце-
нена как проявление других видов врожденной не-
проходимости. В частности, такую же клиниче-
скую картину может давать врожденный агангли-
оз, особенно тотальный, толстой кишки, равно как
и гипотиреоз. Осложненный мекониевый илеус
с перфорацией и перитонитом бывает сложно от-
дифференцировать от иных видов патологии, при
которых развиваются такие же осложнения. При
появлении во время вмешательства подозрения на
тотальный аганглиоз толстой кишки, мы, как пра-
вило, направляем червеобразный отросток для ги-
стологического исследования на предмет наличия
ганглиев. Нельзя забывать о возможности и дру-
гих причин обструкции, включая синдром сужен-
ной левой половины толстой кишки, функциональ-
ную незрелость кишечника, a i резню толстой или
подвздошной кишки, синдром мекониевой пробки.
Диагностика кистофибрози. Потовая про
ба. Самый простой метод диагностики КФ — по-
товая проба, однако этот тест достаточно точен
лишь в течение первых нескольких дней жизни.
Кроме того, у маленьких детей порой невозможно
получить необходимое для исследования количе-
ство отделяемого потовых желез. Метод ионтофо-
реза с пилокарпином33 позволяет аккуратно со-
брать нужное количество незагрязненного пота
с предплечья ребенка, ноги или спины с последую-
щим количественным определением уровня натрия
и хлора.33 Пилокарпин — холинергический препа-
рат, стимулирующий продукцию йота. Раствор на-
носят на кожу и пропускают электрический ток
(3 4 мА), чтобы пилокарпин проник в кожу. Пот
собирают в течение часа на фильтровальную бума-
гу, которую укрепляют на участке, подвергнутом
воздействию тока, герметической повязкой для
предотвращения испарения. Диагноз устанавлива-
ется при концентрации натрия и хлора выше
60 ммоль/л (если собрано не меньше 100 мг по-
та). Гест рекомендуется повторить через 4—6 не-
дель, поскольку в первые несколько дней жизни
уровень электролитов пота может быть повышен
и в норме.
Рис. 27-1. Осложненный меко
ниеоый илеус со значитель-
ным вздутием жинота. гипе-
ремией и отеком брюшной
стенки.
МЕКОНИЕВАЯ БОЛЕЗНЬ 369
Тест Boehringer-Mannheim (с исполь-
зованием бумажных полосок) иногда применяется
как скрининговый метод выявления КФ. Для диаг-
ностики же мекониевого илеуса он не имеет осо-
бого диагностического значения. С помощью этого
теста определяют уровень альбумина в меконии.
У здоровых де гей данный показатель редко превы-
шает 3 мг альбумина/г мекония, в то время как
у пациентов с к и стофиброзом достигает 80 м г аль-
бумина/г. Тест Boehringer-Mannheim не очень спе-
цифичен, поскольку часто дает ложноположитель-
ные результаты.
Исследование дуоденального аспи
рата. В содержимом (аспирате) 12-перстной
кишки может отмечаться снижение активности
панкреатических энзимов: трипсина, липазы и
амилазы. Однако диагностическая ценность данно-
го иса-едования остается сомнительной.23
Рентгенологическая диагностика. На рентге-
нограмме брюшной полос ги при простом мсконие-
вом илеусе часто видны расширенные кишечные
петли, т. е. признаки тонкокишечной непроходимо-
сти. Рентгенологическая картина не отличается от
той. что наблюдается при атрезии подвздошной
кишки и других формах обструкции. Степень рас-
ширения кишечных петель может быть различной:
некоторые из них чрезвычайно растянуты, другие
имеют практически нормальные размеры. Часто
видны крупнозернистые тени, напоминающие
мыльные пузыри, что объясняется наличием пу-
зырьков воздуха внутри плотного мекония (рис.
27-2). Подобная картина отмечается и при других
Рис. 27-3. Мекониевый нлеус с асцитом и пневмоперитонеумом.
Рис. 27-2. На обзорной рентгенограмме при меклниевом илеусе
видны расширенные кишечные петли и картина «матового
стекла».
формах кишечной непроходимости. Если четкая
зернистость распространяется на всю брюшную
полость, то последняя приобретает на рентгено-
грамме вид матового стек па. Количество уровней
жидкости при меконлевом илеусе обычно неболь-
шое. поскольку в основном кишечные петли цели-
ком заполнены жидкостью или вязким меконием.
Но и этот признак не имеет особой диагностиче-
ской ценности, так как может встречаться и при
других формах кишечной непроходимости. На вер-
тикальных рентгенограммах при мекониевом илеу-
се иногда видны типичные уровни жидкости с Га-
зовыми пузырями.
При осложненном мекониевом илеусе почти
в одной трети случаев на рентгенограммах нельзя
обнаружить никаких признаков осложнений.54 О
внутриутробной перфорации и мекониевом перито-
ните говорит наличие в брюшной полости кальци-
фи катов. Большое плотное опухолевидное образо-
вание с вкраплениями внутри него кальция может
быть признаком псевдо кисты. Четкие уровни жидко-
сти с газовыми пузырями над ними характерны
для атрезии кишечника или заворота. При постна-
тальной перфорации (чаще толстой кишки) отме-
чаются асцит и пненмоперитонеум (рис. 27-3).
Если клинико-рентгенологическая картина гово-
рит о мекониевом илеусе, то для подтверждения
диагноза обычно делают ирригографию с барием,
а затем в толстую кишку с лечебной целью вводят
раствор гиперосмолярного водорастворимого конт- 24
24 Заказ № 1622
370 МЕКОНИЕВАЯ БОЛЕЗНЬ
растного вещества, рефлюкс которого в подвздош-
ную кишку позволяет определить место непрохо-
димости. Мы предпочитаем использовать как для
диагностики, так и для лечения, гипертонический
раствор контрастного вещества. На ирригограммах
выявляется чрезвычайно малый диаметр толстой
кишки (микроколоп), имеющей, однако, нормаль-
ную длину и незаполненной содержимым. В терми-
нальном отделе подвздошной кишки контурируют-
ся комочки (шарики) плотной слизи. При подозре-
нии на мекониевый илеус никогда не следует
давать контрастное вещество через рот.
Микроколон может быть обнаружена и при дру-
гих видах патологии, включая болезнь Гиршпрун-
га, синдромы мскониевой пробки и суженной левой
половины толстой кишки, атрезию толстой или
подвздошной кишки и функциональную незре-
лость кишечника. При болезни Гиршпрунга или
тотальном аганглиозе толстой кишки контрастное
вещество проходит через микроколон в расширен-
ную подвздошную кишку, в которой не видно ко-
мочков сгущенной слизи. Для определения нали-
чия или отсутствия ганглиев иногда может понадо-
биться ректальная биопсия. При мекониевом илеусе
скопления плотного мекония имеют на рентгено-
грамме вид больших дефектов наполнения, в то
время как при болезни Гиршпрунга кишечное со-
держимое более жидкое, а потому на рентгеног-
раммах в вертикальном положении видны уровни
жидкости с газовыми пузырями в расширенных
петлях тонкой кишки. При кишечной атрезии кон-
трастное вещество на ирригограммах не проходит
в атрезированный сегмент.
Атрезия и мекониевый илеус могут сочетаться,
что обычно выявляется только непосредственно во
время операции. В некоторых случаях осложнен-
ного мекониевого илеуса симптомы осложнений
(например, заворота) могут превалировать в кли-
нической картине, и тогда мекониальная непрохо-
димость, как правило, не диагностируется до вме-
шательства, а обнаруживается интраоперационно.
Бывают и такие наблюдения, когда диагноз меко-
ниевого илеуса устанавливается лишь патолого-
анатомами при морфологическом исследовании ре-
зецированной кишки или на аутопсии.
Лечение. Консервативное лечение. В 1969 г.
Nobletl предложила использовать в качестве кон-
сервативного метода лечения неосложненного ме-
кониевого илеуса гастрографиновую клизму. Под
неосложненным мекониевым илеусом она, как
и большинство хирургов, подразумевала те слу-
чаи, когда при наличии характерных признаков
этого заболевания у ребенка отсутствуют явные
клинические и рентгенологические симптомы та-
ких осложнений, как перфорация или перитонит.
Остальные пациенты (с заворотом, гангреной, пер-
форацией. перитонитом или кишечной атрезией,
т. е. с теми видами патологии, каждый из которых
может развиться в результате изначальной заку-
порки меконием) требуют срочной операции. Га-
стрографин представляет собой гипсросмолярный
водный раствор meglumine diatrizoate, содержа-
щий 0,1% разжижающего агента полисорбата 80
(Tween 80) и 37% йода. Гиперосмолярный раствор
(1900 мосм/л) «вытягивает» жидкость из плазмы
в просвет кишечника, что приводит к осмотиче-
ской диарее, прекращающейся после того, как га-
стрографин эвакуируется из кишечника.
Для предотвращения гиповолемии пациент дол-
жен получать адекватную гидратацию то и во вре-
мя процедуры. Перед проведением клизмы начина
ют также вводить антибиотики и тщательно обсле-
дуют больного. Гастрографин вводят через прямую
резиновую трубку, заведенную в прямую кишку.
Ягодицы при этом плотно сжимают. Процедуру
осуществляют под контролем ЭОПа. При введении
раствора может ощущаться сопротивление, по-
скольку толстая кишка сужена, до сих пор не фун-
кционировала и заполнена комочками слизи. Ког-
да контрастное вещество достигает терминального
отдела подвздошной кишки, оно очерчивает боль-
шую мекониевую npo6Kj После того, как гастрог-
рафип эвакуирован из прямой кишки, клизму по-
вторяют, чтобы очистить кишечник от оставшегося
мекония. После перевода ребенка из рентгеновско-
го кабинета в отделение новорожденных делают
клизму с теплым физиологическим раствором, со-
держащим 1% ацетилцистеина, с целью полного
очищения кишечника. При необходимости (если
продолжается растяжение кишечных петель или
сохраняется мскониевая обструкция) гастрографи-
новая клизма может быть повторена.
Чтобы предотвратить перфорацию прямой киш-
ки, рекомендуется использовать прямой резиновый
катетер без баллона. В одной из опубликованных
работ сообщается о перфорации кишечника у 5 из
22 больных при использовании баллонного катете-
ра.3’ Кроме того, имеются данные и о поздней пер-
форации подвздошной или слепой кишки через
12—48 час после проведения клизмы. Возможны-
ми причинами поздней перфорации могут быть
чрезвычайное перерастяжение кишечника в резуль-
тате осмотического процесса или повреждение
стенки кишки контрастным веществом. По нашим
данным, эти осложнения возникают редко, а пото-
му не представляют особой проблемы.
Оперативное лечение. Хирургическое лечение
показано при осложненном мекониевом илеусе ли-
бо при неэффективности консервативной терапии
(гастрографиновой клизмы). Цель операции при
простом мекониевом илеусе — полная эвакуация
мекония из кишечника. Для достижения этой цели
может быть использован один из многочисленных
методов — от простой энтеротомии с промыванием
кишки до резекции со стомой или без нее. Первые
случаи успешного хирургического лечения меко-
ниевого илеуса описаны в 1948 г.36 Это была энте-
ротомия с промыванием кишки и эвакуацией меко-
ния. Затем появились многочисленные модифика-
ции данного метода, заключавшиеся в применении
разнообразных растворов для промывания: 1 -4%
N-ацетилцистеин, раствор диатризоата, перекись
водорода, панкреатические ферменты, физиологи-
ческий раствор. От перекиси водорода быстро от-
казались в связи с опасностью перфорации и воз-
душной эмболии при ее использовании. Панкреа-
МЕКОНИЕВАЯ БОЛЕЗНЬ 371
тическис энзимы также мало приемлемы, посколь-
ку не обладают способностью быстро разжижать
кишечное содержимое.
На протяжении многих лет предлагались самые
разнообразные методы хирургического лечения ме-
кониевого илеуса. Gross® в 1953 г. сообщил об
успешном лечении кишечной непроходимости пу-
тем резекции расширенной подвздошной кишки
и создания энтеростомии по Микуличу. Bishop
и Кипр37 в 1957 г. предложили резекцию и анасто-
моз конец-в-бок с дистальной стомой, предназна-
ченной для послеоперационного промывания ки-
шечника. Saninlli в 1961 г. описал резекцию
и анастомоз по Ру с проксимальной энтеросто-
мией. Эта операция заключалась в резекции наи-
более расширенной части подвздошной кишки
и анастомозе бок-в-конец с выведением прокси-
мального сегмента в виде энтеростомы. Swenson 40
в 1962 г. рекомендовал производить резекцию,
интраоперационное промывание и анастомоз ко-
нец-в-конец, однако при использовании этого ме-
тола часто возникает несостоятельность анасто-
моза.
В 1963 г. Harberg предложил метод лечения,
заключавшийся в илеостом и и с использованием
Т-образной трубки. В 1981 г. он обобщил данные
о применении этой операции с подробным описа-
нием техники вмешательства.41 Т-образный French
катетер N14 вводят через илеостому одним концом
в проксимальный расширенный сегмент, другим —
в суженный дистальный отдел подвздошной киш-
ки, который содержит вязкий меконий. Т-образную
трубку и подвздошную кишку фиксируют к перед-
ней брюшной стенке. Трубку выводит наружу че-
рез отдельный прокол брюшной стенки в нижнем
квадранте живота. С первого дня после операции
кишечник начинают промывать панкреатическими
энзимами через Т-образную трубку, которую уда-
ляют на 10—14-й тень. По данным автора, у 9 из
11 больных меконий отходил между 1-м и 11-м
днем после операции. В двух случаях меконий не
отходил и картина кишечной непроходимости со-
хранялась. В одном из этих наблюдений потребо-
валась повторная операция, во время которой
Т-образная трубка была удалена и произведена
множественная энтеротомия для эвакуации меко-
ния. Другой ребенок умер от причин, нс связанных
с основной патологией. В 1970 г. O’Neill32 также
сообщил об успешном лечении непроходимости
с помощью трубчатой энтеростомии и послеопера-
ционного промывания.
Что касается нашего подхода к лечению меко-
ниевого илеуса, то при неэффективности консерва-
тивной терапии мы производим оперативное вме-
шательство после введения жидкости (внутривен-
но для адекватной гидратации), антибиотиков
и 1 мг витамина К. Лапаротомия осуществляется
обычным нижним поперечным разрезом. После
илеотомии в проксимальный и дистальный отделы
вводят катетер, через который кишечник промыва-
ют физиологическим раствором и ацетилцистеи-
ном. Иногда этой процедуры оказывается вполне
достаточно для освобождения кишки от мекония
и ликвидации непроходимоеги. Наш опыт показы-
вает, что настойчивые попытки «выдавливания»
мекония из кишки ведут к повреждению серозы
и кровотечению, поэтому, если не удается достичь
быстрого опорожнения кишечника, мы прекращаем
попытки промывания. В таком случае вводится
Т-образная French трубка N14, как пред лагал Har-
berg,41 и со следующего дня начинается промыва-
ние (рис. 27-4). Подобная тактика обычно дает
удовлетворительные результаты и избавляет от
необходимости повторного вмешательства для за-
крытия илеостомы. В течение ряда лет мы ни разу
не производили ни резекцию, ни энтеростом и ю.
Хорошие результаты мы получили и при ис-
пользовании у одного ребенка операции, описан-
ной Фицджеральдом.42 Это вмешательство заклю-
чается в аппендэктомии и промывании кишечника
через катетер, введенный в культю отростка. Пос-
ле эвакуации мекония культю ушивают. Хотя пос-
леоперационный период у нашего больного проте-
кал гладко, однако сама операция была несколько
более трудной, чем представлено автором в ее
описании Культю пришлось расширять, чтобы
извлечь комочки мекония из дистального отдела
подвздошной кишки. Кроме того, для удаления
плотного мекония мы вынуждены были усиленно
манипулировать на кишечнике. Операция закончи-
лась созданием временной трубчатой цекостомы.
Трубка удалена на 10-й день после вмешательства.
Большинство хирургов считает, что мекониевый
илеус без перфорации и атрезии может быть выле-
чен без стомы, с помощью одного из вышеописан-
ных методов.
Рис. 27-4. Т-трубочная илеостомия, накладываемая с целью по-
слеоперационного промывания кишечника.
372 МЕКОНИЕВАЯ БОЛЕЗНЬ
Если у ребенка имеется заворот, атрезия, перфо-
рация или гангрена кишки, мы предпочитаем
производить резекцию нежизнеспособного участка
с двойной концевой энтеростомией. Через стомы
по мере необходимости осуществляется промыва-
ние. Повторная операция с закрытием стом и нало-
жением анастомоза производится через 2—3 неде-
ли. Первичный анастомоз в подобных случаях мы
нс накладываем.
В послеоперационном периоде в течение не-
скольких дней больной получает антибиотики. На-
зогастральный зонд стоит до тех пор, пока содер-
жимое желудка не станет светлым, без примеси
желчи, и не уменьшится в количестве. Обычно
функция кишечника восстанавливается на протя-
жении 5—10 дней, после этого больного начинают
кормить. В течение периода, когда больной не мо-
жет получать «ничего-через-рот», назначают панк-
реатические энзимы, а питание обеспечивают па-
рентеральным путем через периферический или
центральный катетер. Если при введении пита-
тельных смесей ребенок их не усваивает, то пита-
ние осуществляют через трубку до тех пор, пока
не восстановится нормальная функция кишечника.
В течение всего послеоперационного периода
осуществляют тщательный контроль за состоянием
легких с постоянной эвакуацией бронхиального
секрета. Перед выпиской ребенка из стационара
неоднократно проводят анализ содержания хлори-
дов в отделяемом потовых желез с целью диагно-
стики КФ. Выживаемость в этой группе пациентов
и соответственно количество больных, выписывае-
мых из стационара, колеблется от 80 то 85%. Па-
циенты с КФ живут долго, но у многих из них
отмечаются серьезные легочные проблемы, кото-
рые либо постоянны, либо периодически рецидиви-
руют, а порой эти варианты сочетаются (обостре-
ния на фоне постоянных симптомов). Тяжесть ле-
гочных проявлений у наших пациентов колеблется
в очень широком диапазоне.
ЭКВИВАЛЕНТ МЕКОНИЕВОГО ИЛЕУСА
ЭМИ—термин, используемый для обозначения
частичной или полной кишечной непроходимости,
которая возникает у больных с КФ после периода
новорожденности. ЭМИ развивается в связи с на-
личием в терминальном отделе подвздошной и
правой половине толстой кишки необычно вязкого
кишечного содержимого. Впервые данная патоло-
гия была описана в 1941 г.,43 и в настоящее время
она диагностируется намного более часто, чем
раньше, особенно если пациенты с КФ длительно
наблюдаются. ЭМИ выявляется у 10—40% боль-
ных, находящихся на учете в специализированных
клиниках по лечению КФ.
У пациентов с острой формой ЭМИ отмечаются
боли, вздутие живота, рвота, запоры и признаки
кишечной непроходимости. Из перечисленных
симптомов наиболее характерны и часты интен-
сивные хронические или рецидивирующие колико-
подобные боли в животе, вздутие живота и уме-
ренно выраженные запоры.
Предрасполагающими к развитию ЭМИ факто-
рами в некоторых случаях являются внезапное
прекращение приема панкреатических препаратов,
обострение легочных процессов, дегидратация и
изменения диеты. Иногда ЭМИ может возникнуть
после хирургического вмешательства но поводу со-
вершенно иной патологии.
Hit обзорных рентгенограммах у этих больных
определяются зернистые тени (преимущес! пенно
в правой половине живота), а также расширение
тонкой кишки и уровни жидкости, обусловленные
тонкокишечной обструкцией.
Контрастное исследование с диатризоатом (га-
стрографин) не только подтверждает диагноз, но
и оказывает терапевтическое воздействие. Обсле-
дование с барием в таких случаях противопоказа-
но. ЭМИ может осложниться инвагинацией или
(реже) заворотом. Введение в подвздошную кишку
через Т-образную трубку раствора панкреазима
и 1% N-ацетилцистеина помогает «разжижить» гу-
стое кишечное содержимое.46 В некоторых слож-
ных ситуациях приходится прибегать к оператив-
ному вмешательству.
СИНДРОМ МЕКОНИЕВОЙ ПРОБКИ
Синдром мекониевой пробки — относительно ред-
кая причина кишечной непроходимости у новорож-
денных. Однако если знать об этой патологии и ее
клинических проявлениях, то она встречается на-
много чаще, чем принято считать. Данный синдром
был описан в 1956 г.,4’ причем к первому наиболее
точному оригинальному описанию вряд ли .можно
что-либо добавить: «Кишечная обструкция связана
с неспособностью толстой кишки самостоятельно
опорожниться от мекониевых остатков, которые
образовывались на протяжении девяти месяцев фе-
тальной жизни. Такие новорожденные встречаются
нередко». При синдроме мекониевой пробки харак-
тер мекониевых масс и двигательная активность
толстой кишки изменены настолько, что это при-
водит как к замедлению нормального процесса,
препятствующего уплотнению мекония, так и к за-
держке опорожнения пищеварительного тракта.*'
Clatworthy называл пациентов с этим состоянием
«закупоренные дети».
Спектр клинических проявлений определяется
именно, и прежде всего, наличием мекониевой проб-
ки. Однако для обозначения этого синдрома ис-
пользовались и продолжают использоваться такие
синонимы, как функциональная инертность тол-
стой кишки недоношенных, синдром суженной ле-
вой половины толстой кишки новорожденных, ле-
восторонняя микроколон и другие термины. Хотя,
согласно классическим представлениям, синдром
мекониевой пробки развивается у больных без КФ
и соответственно отличается от мекониевого илеу-
са, однако мы в редких случаях встречались с ти-
пичным синдромом мекониевой пробки у детей
с кистофиброзом. При подозрении на данный синд-
ром должна быть исключена болезнь Гиршпрунга
(с помощью ранней аспирационной биопсии). Сни-
жение двигательной активности толстой кишки
МЕКОНИЕВАЯ БОЛЕЗНЬ 373
может возникнуть в результате гипермагнезиемии,
при которой замедляется высвобождение ацетилхо-
лина, что приводит к нервно-мышечным расстрой-
ствам. Хотя существует описание комбинации син-
дрома мекониевой пробки и гипермагнезиемии
у детей, родившихся от женщин, получавших лече-
ние магнием по поводу эклампсии/8 однако эта
теория не нашла подтверждения в эксперименте на
животных.49 И большинство клинических случаев
этого синдрома не связаны с лечением магнием.
Снижение двигательной активности кишечника
может быть вызвано также повышенной продук-
цией глюкагона, индуцированной гипогликемией
у детей, матери которых страдают диабетом.50
Клинические аспекты. У детей с синдромом ме-
кониевой пробки отмечается вздутие живота. Ме-
коний отходит в небольшом количестве или вооб-
ще нс отходит. На обзорных рентгенограммах вид-
ны множественные раздутые кишечные петли. При
ирригографин с гастрографином под контролем эк-
рана можно выявить «пробку» в виде дефекта на-
полнения или суженную левую половину толстой
кишки с четко выраженной непроходимостью на
уровне левой половины colon или селезеночного
угла (рис. 27-5). При гипертонической клизме
обычно получают длинную плотную пробку (рис.
27-6). Это обследование может оказать также ле-
чебный эффект, и ребенок после него иногда начи-
нает самостоятельно опорожнять кишечник от ме-
кония. Пос по первоначального обследования с га-
стрографином отхождение стула стимулируется
в дальнейшем клизмами с теплым физиологиче-
ским раствором. Иногда требуется повторная клиз-
ма с гастрографином, чтобы вывести оставшийся
меконий. После опорожнения кишечника от меко-
Рис. 27-5. Синдром мекониевой пробки — видна большая меко-
миеная пробка в левой половине толстой и в прямой кишке.
Рис. 27-6. Мекониевая пробка, полученная после гасгрографи-
новой клизмы.
ния мы, как правило, провод им ректальную аспи-
рационную биопсию для исключения болезни Гир-
шпрунга, прежде чем выписать больного из стацио-
нара. Большинство пациентов в последующем не
имеют никаких проблем, если, конечно, у них нет
кистофиброза. Поэтому в план обследования мы
включаем также потовую пробу на хлор.
По нашему опыту, необходимость в оперативном
вмешательстве при синдроме мекониевой пробки
возникает чрезвычайно редко. Наиболее ранний
диагноз этой патологии был поставлен, согласно
данным литера гуры, при обычном ультразвуковом
исследовании плода в 3-м триместре беремен-
ности.51 Вслед за этим сделаны амниоцентез и а.м-
ниографин с урографином. Автор считает, что
урографин, заглоченный плодом, привел к ликвида-
ции кишечной непроходимости. Мы не использова-
ли этот метоп, поскольку постнатальное лечение
детей'с синдромом мекониевой пробки столь ре-
зультативно, что риск внутриутробного вмешатель-
ства как для матери, так и для плода, перевеши-
вает достоинства этой процедуры. При лечении
(ностнатально) клизмами с гастрографином и фи-
зиологическим раствором дети, как правило, дают
быструю положительную реакцию, так что через
несколько дней можно уже начинать энтеральное
кормление.
МЕКОНИЕВЫЙ ПЕРИТОНИТ
Мекониевый перитонит характеризуется как асеп-
тический, химический или реактивный (реакция
на инородное тело) и развивается в результате
попадания мекония в брюшную полость при внут-
374 МЕКОНИЕВАЯ БОЛЕЗНЬ
риугробнои перфорации кишечника. Этот синдром
впервые был описан Морганьи в J761 г. в De Sedi-
bus el Causis Morborum,52 а первая успешная хи-
рургическая коррекция произведена Agerlx в
1043 г.55
Причиной перфорации обычно является обструк-
ция кишечника при мекониевом илеусе, кишечной
атрезии, стенозе, завороте, внутренней грыже,
врожденных перитонеальных тяжах, инвагинации
или гастрошизисе.” В редких случаях перфорации
обструкция нс обнаруживается. В таких наблюде-
ниях может быть перфорация дивертикула Мекке-
ля, червеобразного отростка или наконец просто
идиопатическая перфорация. Мекониевый перито-
нит. связанный с КФ, может классифицироваться
и как осложненный мекониевый илеус. При любой
обструкции значительное скопление мекония в
проксимальном отделе приводит к ишемическому
некрозу и. как следствие, к перфорации. Часто сег-
мент кишки, заполненный меконием, перекручива-
ется, в результате чего возникает изолированный
заворот. Ишемизированный участок при завороте
может либо перфорироваться, либо самостоятельно
«восстановить» кровообращение с последующим
развитием стеноза или даже атрезии. Ишемиче-
ский некроз всего кишечника, вовлеченного в заво-
рот, с выходом из просвета в брюшную полость
мекония и его разжижением, приводит к образова-
нию псевдокисты (гигантский кистозный меконие-
вый перитонит) или развитию диффузного меко-
ниевого асцита.54
Перфорация толстой кишки может произойти
и дистальнее обструкции в результате, как прави-
ло. проведения бариевой клизмы под давлением
(рис. П-1).
Клинические проявления. Осложненный меко-
ниевый илеус или мекониевый перитонит обычно
проявляются сразу после рождения выраженным
прогрессирующим вздутием живота с гиперемией
и иногда отеком брюшной стенки Живот может
быть очень напряженным, порой при пальпации
определяется опухолевидное образование. Вздутие
живота часто ведет к дыхательным расстройствам.
В результате потерь жидкости в третье простран-
ство развивается гиповолемия.
Рентгенологическая картина зависит от причи-
ны перитонита. При внутриутробной перфорации
кишечника в животе или мошонке иногда видны
кальцификаты. Меконий, попадающий в брюш-
ную полость, кальцифицируется в течение 48 ча-
сов после перфорации.55 Однако кальцифициро-
ванный меконий может находиться и в просвете
кишки, и тогда он не связан с перфорацией, но
часто ошибочно принимается за проявление меко-
ниевого перитонита Дифференциация этих двух
типов кальцификатов важна для решения вопроса
о необходимости, сроках и объеме оперативного
вмешател ьства.
Патология. Описаны три типа мекониевого пе-
ритонита: фиброадгезивный, кистозный и генера-
лизованный.56 Первый из них (фиброадгезивный)
встречается наиболее часто. Стерильный меконий
вызывает интенсивно протекающий «химический»
Рис. 27 7. Мекониевый перитонит и перфорация толстой кишк
и области печеночного изгиба.
перитонит, индуцируемый пищеварительным
ферментами, содержащимися в меконии. В резулт
тате образуются плотные фиброзные спайки и ерт
щение петель кишечника. Интраоперационно мет
то перфорации часто не обнаруживается, посколт
ку оно прикрывается фиброзными и кальцифиш
рованными спайками, что и приводит к кишечно
непроходимости.
Кистозный мекониевый перитонит возникас
в тех случаях, когда фибропластическая реакци
недостаточно интенсивна для того, чтобы «з>
крыть» место перфорации, и меконий продолжав
поступать в брюшную полость. Псевдокиста пре/
ставляет собой плотно спаянные и частично некрт
тизированные кишечные петли, окружающие п<
лость с разжиженным меконием, находящимся вт
просвета кишки. Это образование в некоторы
участках местами покрыто кальцифицированнс
оболочкой.
При генерализованном мекониевом перитонит
меконии распределен по всей брюшной полост;
Спайки между кишечными петлями больше фибрт
нозные, чем фиброзные. Этот тип мекониевого п<
ритонита обычно возникает в том случае, кот/
перфорация происходит непосредственно перт
рождением или даже во время родов.
Лечение. Показанием к хирургическому вмени
гельству обычно является кишечная непроход!
мосты Наличие кальцификатов при отсутствг
МЕКОНИЕВАЯ БОЛЕЗНЬ 375
у ребенка других симптомов не требует оператив-
ного лечения. Характер вмешательства зависит от
этиологии мекониевого перитонита и интраопера-
ционных находок. Нежизнеспособные, атрезиро-
ванныс или резко перерастянутые кишечные петли
резецируются. Выделение их часто очень затрудне-
но и сопровождается кровотечением. Следует мак-
симально сохранить кишку, дабы предотвратить
развитие синдрома короткой кишки. Многим из
наших больных потребовалось наложение времен-
ной интестиностомы и гастрономы с целью раз-
грузки и питания. Для проведения тотального па-
рентерального питания ставят катетер в централь-
ную вену, поскольку обычное энтеральное питание
невозможно в течение длительного периода. Ре-
зультаты хирургического лечения, как правило,
хорошие, хотя несколько наших пациентов потре-
бовали повторной операции в связи с кишечной
непроходимостью.
ЗАКЛЮЧЕНИЕ
Описанные нами мекониевые синдромы ставят пе-
ред хир\ ргами-неонатологами широкий спектр
сложных проблем, связанных в частности с тем.
что некоторые больные могут потребовать повтор-
ных операций. Кроме того, серьезные диагностиче-
ские трудности возникают при развитии у детей
более старшего возраста эквивалента мекониевого
илеуса. У нас было несколько пациентов, у кото-
рых диагноз КФ не был поставлен до тех пор, пока
не развились осложнения кистофиброза, потребо-
вавшие оперативного вмешательства. Многие из
детей с КФ нуждаются в хирургическом лечении
в связи с вовлечением в процесс других органов
и систем, например при бронхоэктазах, кровохар-
каньи, пневмотораксе, поражении ЛОР-органов
или желудочно-кишечного тракта. Хирургическое
лечение перечисленных проявлений кистофиброза
представлено в соответствующих главах.
ЛИТЕРАТУРА
1. Dohin ТЕ, Touloukian RJ: Familial meconium ileus not associa-
ted with cystic fibrosis. J Pediatr Surg 9:821 -824, 1974.
2. Rickham PP. Boeckman CR: Neonatal meconium obstruction in
the absence of mucoviscidosis. Ann J Surg 109:173—177, 1965.
3. Vinograd 1. Mogle P, Pclcg O. et al: Meconium disease in pre-
mature infants with very low weight. J Pediatr 103:963—
966, 1983.
4. Landsteiner K: Darmvcrschluss durch cingcdicklex Meconium:
Pancreatitis. Zentralbl Allg Pathol 16:903. 1905.
5. Fanconi G. Vihlinger E, Knauer C: Das Coeiiakiessyndromc bei
angeborener zysfischer Pankrcasfihromatn.se und Bronchiektusi-
en. Wien med Wochenschr 86:753—756, 1936.
6. Andersen DH: Cystic fibrosis of the pancreas and its relation to
celias disease: A clinical and pathologic study. Am J Dis ('hiId
56:344—399, 1938.
7. Hiatt RB, Wilson PE: Celias syndrome: Therapy of meconium
ileus: Report of 8 cases with review of the literature. Surg Gy-
necol Obstet 87:317—327. 1948.
8. Gross RE: Intestinal obstruction in the newhnrn resulting from
meconium ileus. In The Surgery of Infancy and Childhood. WB
Saunders, Philadelphia, pp 175—191, 1953.
9. Bishop HC. Koop CE: Management of meconium ileus: Resec-
tion, Roux-cn-Y anastomosis and ileostomy irrigation with panc-
reatic enzymes. Ann Surg 145:410—414, 1957.
10. Noblett HR: Treatment of uncomplicated meconium ileus by
Gastrografin enema: A preliminary report. J Pediatr Surg
4:190—197, 1969.
II. Mobogunjc OA, Wang CI, Mahour GH: Improved survival of
neonates with meconium ileus. Arch Surg 117:37 40, 1982.
12. deLorimier AA. Fonkalsrud EW, Hays DM: Congenital atresia
and stenosis of the jejunum and ileum. Surgery 65:819—827,
1969.
13. Dey DL: The surgical treatment of meconium ileus. Med J Aust
50:179—180, 1963.
14. Danks DM, Allan J, Anderson CM: A genetic study of fibro-
cystic disease of the pancreas. Ann Hum Genet 28:323—356,
1965.
15. Kramm ER, Crane MM, Sirken MG. et al: A cystic fibrosis pilot
survey in three New Fngbind slates. Am J Public Health
52:2041—2057, 1962.
16. Stephan U. Busch EW, Kollberg H, et al: Cystic fibrosis defec-
tion by means of a test strip. Pediatrics 55:35—38, 1975.
17. Santulli TV: Meconium ileus. In Holder TM, Ashcraft KW (edi-
tors): Pediatric Surgery. WB Saunders, Philadelphia, pp 356
373, 1990.
18. Kcrcm E, Corey M, Kerem B, et al: Clinical and genetic compari-
sons of patients with cystic fibrosis, with or without meconium
ileus. J Pediatr 114:767—773, 1989.
19. Allan DL, Robbie M, Phelan PD. ct al: Familial occurrence of
meconium ileus. Eur J Pediatr 135:291—292, 1981.
20. Mornel E. Scrrc JL, Farrall M. et al: Genetic differences bet-
ween cystic fibrosis with and without meconium ileus. Lancet
1:376—378. 1988.
21. Farber SJ: Pancreatic function and disease in early life. V. Pat-
hologic changes associated with pancreatic insufficiency in early
life. Arch Pathol 37:23K 250, 1944.
22. Anderson DH: Cystic fibrosis of the pancreas. J Chron Dis
7:58 90. 1958.
23. Schwachman H, Lebenihal E, Khaw KT: Recurrent acute pan-
creatitis in patients with cystic fibrosis with normal pancreatic
enzymes. Pediatrics 55:86—95. 1975.
24. Di Sant’Agncsc PA, Davis PB: Research in cystic fibrosis.
N Engl J Med 295:481—485, 1976.
25. Emery JL: Laboratory observations of the viscidity of meconi-
um. Arch Dis Child 29:34—37, 1954.
26. Buchanan DJ, Rapoport S: Chemical comparison of normal me-
conium and meconium from a patient with meconium ileus. Pedi-
atrics 9:304—309, 1952.
27. DiSant’Agncsc PA. Dischc 7„ Danikzen KA: Physicochemical
differences of mucoproteins in duodenal fluid of patients with
cystic fibrosis of pancreas and controls: Clinical aspects. Pedi-
atrics 19:252—259, 1957.
28. Green MN, Clarke JTf Shwachman II: Studies in cystic fibrosis
of lhe pancreas. Prolein pattern in meconium ileus. Pediatrics
21:635—641, 1958.
29. Lloyd DA: Meconium ileus. In Welch KJ. Randolph JG, ct
al. (Editors). Pediatric Surgery. Year Book, Chicago, pp 849—
858. 1986.
30. Thomaidis TS. Arcy JB: The intestinal lesions in cystic fibrosis
of lhe pancreas. J Pediatr 63:444 453, 1963.
376 МЕКОНИЕВАЯ БОЛЕЗНЬ
31. Quinton PM, Bijman J: Higher bioelectric potentials due to dec-
reased chloride absorption in the sweat glands of patients with
cystic fibrosis. N Engl J Med 308:1185—1189, 1983.
32. O’Neill JA. Grosfeld JL. Boles ET. el al.: Surgical treatment of
meconium ileus. Am J Surg 119:99—105, 1970-
33. Cibson LE, Cooke RE: A lest for concentration of electrolytes in
sweat in cystic fibrosis of the pancreas utilizing pilocarpine by
iontophoresis. Pediatrics 23:545 549, 1959.
34. Leonidas JC, Berdon WE, Baker DH. et al: Meconium ileus and
its complications: A reappraisal of plain film roentgen diagnostic
criteria. Am J Roentgenol 108:598—609. 1970-
35. Ein S, Shandling B, Reilly B, ct al: Bowel perforation with nono-
perative treatment of meconium ileus. J Pediatr Surg 22:146—
147, 1987.
36. Hiatt RB, Wilson PE: Celias syndrome: Therapy of meconium
ileus: Report of 8 cases with review of the literature. Surg Gyne-
col Obstet 87:317—322, 1948.
37. Bishop HC. Koop CE: Management of meconium ileus: Resec-
tion, Roux-en-Y anastomosis and ileostomy irrigation with panc-
reatic enzymes. Ann Surg 145:410 414. 1957.
38. Santulli TV: Meconium ileus. In Mustard WT. Ravitch MM. Sny-
der Jr, WH et al. (Editors): Pediatric Surgery, second edition.
Year Book, Chicago, pp 851—860» 1969.
39. Santulli TV. Blanc WA: Congenital atresia of the intestine: Pat-
hogenesis and treatment. Ann Surg 154:939- 948, 1961.
40. Swenson O; Meconium ileus and peritonitis. In (Editor) Pedi-
atric Surgery, third edition. Appleton-Century-Crofts, New
York, pp 672 685. 1969.
41. Harberg FJ, Senekjian EK. Pokorny WJ: Treatment of uncompli-
cated meconium ileus via T-lube ileostomy- J Pediatr Surg
16:61—63, 1981
42. Fitzgerald R, Conlon K: Use of the appendix slump in the tre-
atment of meconium ileus. J Pediatr Surg 24:899—900, 1989.
43. Rasor GB, Stevenson WL: Meconium ileus equivalent. Rocky
Mount Med J 38:218 220, 1941.
44. O’Halloran SM, Gilbert J. McKendrick DM, ct al: Gastrografin
in acute meconium ileus equivalent. Arch Dis Child 61:1128—
1130. 1986.
45. Rosenslein BL l.angbaum TS; Incidence of distal intestinal
obstruction syndrome in cystic fibrosis. J Pediatr Gastroenterol
Nutr 2:299—301, 1983.
46. Pcrman J, Breslow L, Ingall D: Nonoperative treatment of meco-
nium ileus equivalent. Am J Dis Child 129:1210—1211. 1975.
47. Clatworthy HW, Howard WHR. Lloyd J: The meconium plug
syndrome. Surgery 39:131 —142. 1956.
48. Sakai MM. Koeiiigsberger MR. Rose JS. el al.: Neonatal hy-
permagnesemia and the meconium-plug syndrome. N Engl J Med
286:223—235, 1972.
49. Cooney DR. Rosevear W, Grosfeld JL: Maternal and postnatal
hypermagnesemia and the meconium plug svn drome. J Pediatr
Surg 11:167—172, 1976.
50. Stewart DR, Nixon GW. Johnson DG et al.: Neonatal small left
colon syndrome. Ann Surg 186:741—745, 1977.
51. Samuel N, Dicker D. Landman J, et al: Early diagnosis and
intrauterine therapy of meconium plug syndrome in the fetus:
Risks and benefits. J Ultrasound Med 5:425— 428, 1986.
52. Boix-Ochoa J: Meconium peritonitis. J Pediatr Surg 3:715—722,
1968.
53. Agerty HA: A case of perforation of the ileum in newborn infant
with operation and recovery. J Pediatr 22:233, 1943.
54. Moore TC: Giant cystic meconium peritonitis. Ann Surg
157:566—572, 1963.
55. Rickham PP: Intraluminal intestinal calcifications in the new-
born. Arch Dis Child 32:31 34, 1975.
56. Lorimer WS, Ellis DH: Meconium peritonitis. Surgery 6U:470—
475. 1966.
Предметный указатель
Абсцесс легкого, 219
Аварии автотранспортные, 119—
120
Аганглиоз толстой кишки. См.
Гиритрумги болезнь.
— тотальный, 368
Аденоматозные аномалии легких,
кистозные, врожденные, 202—204
Адреналин, при иостинтубацион-
ном крупе, 54
— при укусах перепончатокрылых,
92
— при шоке, 23
Адренергические рецепторы, 22
Азотемия прерснальная, 76
Азотистый баланс, 35
Актиномикоз, 222
Ал кал оз, гипока л иемнческий, при
пилоростенозе, 325—326
— респираторный, 69
Аллер! ичсская реакция, как ослож-
нение ТПП, 48
— на укусы перепончатокрылых,
91—92'
Алфентанил, в амбулаторной хи
рургии, 54
Альвеолярная вентиляция, 18
Амбулаторные операции, анесте-
зия, 53 54
— ведение послеоперационного пе-
риода, 54—55
Американского Общества анестезио-
логи, положение об интраопера-
ционном мониторинге, 56
Американской Ассоциации Детских
хирургов, свод этических прин-
ципов, 83—85
Американской Медицинской Ассо-
циации, этический кодекс, 82
Ами некиелота (ы), эссенциальная,
30
Ампициллин, до операции при ки-
шечной атрезии, 351
Аналгезия, в послеоперационном
периоде, 57
Анастомоз, пищевода, несостоятель-
ность, 292
— Py-Y-образный, при мсконневом
илеусе, 371
— тонкокишечный при атрезии,
351 353
Анемия, новорожденных. 14
Анестезия, 52—58
— индукция при обструкции дыха-
тельных путей, 246
— при ожогах, 108, ПО
Антибиотики, при атрезии пище-
вода до операции, 286287
— при легочных абсцессах, 220
— при химических ожогах пище-
вода, 257—258
— при эмпиеме плевры, 214
Антивенин, при змеиных укусах,
90—91
Антигистамин, при укусах перепон-
чатокрылых, 92
Антрального отдела желудка, дис-
кинезия, 327 328
— мембрана, 327
Анус, атрезия, 287
Аорта, аномалии дуги, 273—274
— разрыв, 149
Апноэ, при гастроэзофагеальном
рефлюксе. 301—302
— после операции у недоношен-
ных детей, 55
Аппендэктомия, при хирургическом
лечении мальротации, 363
Аппресин, при персистирующей ги-
пертензии. 79
Аритмия, как осложнение ТПП, 45
Артериальной крови газы, монито-
ринг, 19
Аспид, королевский (или уж ядови-
тый), 88
Аспирационная пневмония, как
осложнение анестезии, 53
Аспирация пищи, с летальным ис-
ходом, 119, 121
Астма, при воронкообразной груди,
168
Асфиксическая торакальная дист-
рофия (болезнь Jeune), 181—
183
Асфиксия, травматическая, 148
149
Асцит, при мекониевом илеусе, 369
Ателектаз, при атрезии пищевода.
287
Атрезия. См. по анатомическим об-
ластям, наир. Пищевода, атре-
зия.
Ауэрбаховскос сплетение, дефицит
нервной ткани, 280
AVPU, мнемоническая схема для
определения уровня сознания,
136
Ахалазия, пищевода, 261—263
Ацидоз, метаболический, лечение,
79
— почечный тубулярный, 75
— респираторный, 69
«Baby Doc»>, законы, КЗ—84
Бактериальный эндокардит, как
осложнение анестезии, 53
Барий, исследование с б., при ат-
резии подвздошной и толстой
кишки, 349 350
— и рн ГЭР, 305
— при пилоростенозе, 325
при трахеальной обструкции,
195
— при трахеопищеводном свище,
283, 285
Баротравма, пищевода, 260
Барретта, пищевод и ГЭР, 303, 317
Батарейки, травма пищевода при
проглатывании б., 259—260
Бацитрацин, при ожогах, 109
Безоар(ы), как инородное тело, 100
Беквит-Видемана, синдром, интра-
оральиая обструкция, 185
Белок (ки), висцеральный, 34 35
метаболическая реакция б. на
операционный стресс, 32
— потребности в б., у ожоговых
больных, 107
— — физиологические, 30
Бетанехол, при ГЭР, 307 308
Бешенство, 87—88
378 ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
Бикарбонат. См. также Натрин
бикарбонат.
— фракционная экскреция, 75
Биоимпеданс (импедансная кардио-
графия), 21
Биопсия легких, при легочных ин-
фильтратах, 225—226
Богдалека отверстие, грыжа. См.
Грыжа( и), диафрагмальная, врож
денная.
Boehringer-Mannheim, тест-пол иски,
в диагностике кистофиброза, 369
«Болтающаяся» грудная клетка, 134,
144
Боль, у амбулаторных больных, 54
— у обожженных детей, 108
— послеоперационная, 57 58
Большая масса тела (по отношению
к гестационному возрасту) у ново-
рожденных, 11
Богота гастрсм чексия. при ГЭР, 309
Борхардта триада, при завороте же-
лудка, 330
Бронх (и), аномалии, кистозные,
врожденные, 200—204
-----— приобретенные, 204 205
— — некистозные, 205 209
— смешанные, 209—211
— инородные тела, 194
Бронхогенная киста(м), 247—249
— врожденная, 200—202
Бронхолегочная дисплазия, 71
Бронхолегочные аномалии перед-
ней кишки, 210—211
— врожденные, 200
Бронхоскоп, телескоп, 96 97
Бронхоскопия, при инородных те-
лах, 96—98
при трахеальной обструкции,
195
Бронхоспазм, рефлекторный, при
ГЭР, 302
Бронхоэктазы, 217—219
Bupivacaine, при послеоперацион-
ных болях, 54
Бурхаве синдром, 255, 260
Велосипедист (ы), травма с леталь-
ным исходом, 119
Велча индекс, при воронкообразной
груди. 168—170
Венозная оксиметрия, 22
Вентиляторы, классификация, 65—
66
Вентиляционные параметры, 68—69
Вентиляция, 60 71
— альвеолярная, 18
— при диафрагмальной грыже,
235-237
— у недоношенных при дыхатель-
ной недостаточности, 18
— способы в., 64—67
Верднига-Гоффмана болезнь. 240
Висцеральный белок, 34—35
Витамин(ы), недостаточность при
кишечной атрезии, 354—355
— физиологические потребности,
31
Внезапной смерти детей синдром
(СВСД), при ГЭР, 301—302
Вода, потери неощутимые, у ново-
рожденных, 16
— содержание в организме, 72
— физиологические потребности,
29 -30, 73
Воронкообразная деформация груд-
ной клетки, 168—173
Времени константа, легких, 18. 61
Времени (по времени) — циклиро-
ванные вентиляторы. 65
Врожденная диафрагмальная гры-
жа (и). См. Грыжа(и), диафраг-
мальная, врожденная.
Врожденная микрогастрия. 330
Врожденно короткий пищевод, 300
(см. также ГЭР)
Врожденные кистоаденоматозные
аномалии, легких. 202—204
Врожден п ые пороки сердца, при
воронкообразной груди, 168
— при дуоденальной атрезии, 346
Врожденный венолобарный син-
дром, 208
Выдыхаемый воздух, содержание
углекислоты, 20
Выпот, плевральный, хилезный,
220—221
Высокочастотная вентиляция (ВЧ
ИВЛ), 66—67. См. Вентиляция.
— при диафрагмальной грыже. 236
Газового пузыря (большого) желуд-
ка синдром (острое расширение
желудка), после фундопликации,
313—315
Газообмен легочный, 62
Гамартома, кистозная, мезенхималь-
ная, 210
Га н гл ионеврома на равертебра л ьной
борозды, 246
Гангрена средней кишки, при маль
ротации с заворотом, 364—365
Гастрогенные кисты, 209—210
Гастрографиновая клизма, при ме-
кониевом илеусе» 370
— при синдроме мекониевой проб-
ки, 373
Гастропсксия, при ГЭР, 309
Гастростомия, 334—338
Гастроэзофагеальный рефлюкс
(ГЭР), 300 318
— после лечения атрезии пище-
вода, 293 - 294
— постгастростом и ческий, 334 -
335
Гемангиома, подсвязочпого прост-
ранства, 187
Гематокрит, у новорожденных, 14
Гематома(ы), дуоденальная, 157
— субдуральная, 162 163
— эпидуральная, 162 163
Гемоглобин, кривая диссоциации,
19-20
— фетальный, 14
Гемолитическая болезнь новорож-
денных, 14
Геморрагии, в змеином яде, 88
Гемоторакс, 147—148
Гентамицин, до операции при ки-
шечной атрезии, 351
— при ожогах, 109
Гестационный возраст, детей с
атрезией тонкой кишки, 346
Гиалиновых мембран болезнь, 17
19
Гипербилирубинемия. 14
Гипергидрачация, как осложнение
ТПП, 48
Гипергликемия, у новорожденных,
13
— как осложнение ТПП, 47
Гиперкалиемия, лечение, 77
— как осложнение ТПП, 47
Гиперкальциемия, как осложнение
ТПП. 47
Ги норма гнезиемия, как осложнение
ТПП, 47—48
Гипсроксия. 19
Гипертензия, интракраниальная
при травме головы, 164
— легочная при врожденной ди-
афрагмальной грыже, 233 234
— как осложнение ожоговой трав-
мы. 114
— системная, лечение, 79
Гиперфосфатемия, как осложнение
ТПП. 47
— смеси с низким содержанием
фосфора при г.. 79
Гипогенезии легкого синдром,
207 208
Гипогликемия, у новорожденных,
12 13
— как осложнение ТПП, 47
Гипокалиемический алкалоз, при
пилоростенозе, 325—326
Гипокалиемия, как осложнение
ТПП, 47
Гипокальциемия, у новорожденных,
13
— как осложнение ТПП, 47
Гипоксемия, интраоперационная,
55, 56
— причины г., 62
Гипоксия, определение понятия, 19
Ги пома гнезиемия, у новорожден-
ных, 13
— как осложнение ТПП, 47
Гипонатриемия, при гипергидрата-
ции, 76
— лечение г., 79
— как осложнение ожоговой трав-
мы, 113
Гипоплазия легкого, при врожден-
ной диафрагмальной грыже,
232 233
Гипофосфатемия, как осложнение
ТПП, 47
Гиршпрунга болезнь, при кишечной
атрезии, 346
Гистоплазмоз, 223
Глюкоза, метаболизм г. у новорож-
денных детей, 11 -13
применение г. при гиперкалие-
мии, 77
Голова, обследование г. при травме,
137
— травма г., 162—167
— ШКГ (шкала комы Глазго), 138
Гормональная реакция на стресс, 31
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ 379
Гортань, инородные тела, 95, 188—
189
— обструкция, при аномалиях,
186—187
— — хирургическое лечение, 189—
192
— отек после экстубации, 70
Гранулома, внутри просветная, эндо-
скопическое иссечение. 190
Грудина, дефекты, 176—181
ГрудинохрЯ1цевая деформация, при
килевидной грудной клетке,
174—175
Грудная клетка, «болтающаяся*,
лечение, 134
— деформации, 168—183
— дренирование, при эмпиеме,
214 —215
— исследование, при травме, 137
— механика, 60
— податливость, 61
рентгенологическое исследова-
ние, при АП и ТПС, 282 286
— — при эмпиеме, 214
— травма, 141 —151
Грыжа(и). См. также по названиям
(напр. Пупочная грыжа).
— диафрагмальная, 229—241
— мезоколикопариетальная, при
мальротации, 361, 363—364
— пищеводного отверстия, 210,
300—310
-----при пилоростенозе, 323
— — послеоперационная. 314 —
315
Давления вентиляторы, 65—66
Дауна синдром, 346
Двенадцатиперстная кишка, атре-
зия, 341—342. 344, 346—348,
351—352
— обструкция при мальротации,
360. 361
— травма, 156—157
Деканюляция трахеи, при обструк-
ции дыхательных путей, 190
Декортикация легких, при пораже-
нии легких, 215
Дексаметазон, при отеке гортани,
70
Декстроза, при гипергликемии, 13
Дермоид (ы) средостения, 251
Дети, доношенные, 11
— маленькие к гестационному воз-
расту, 11 12
— недоношенные, 11
— — особенности обезболивания,
55
Детской травмы шкала (ШДТ),
129—131
Дефекты грудины, 176—177, 179—
181
Диаксозид, при гипертензии, 79
Диализ, при острой почечной недо-
статочности, 77—78
Диафрагма, грыжа (и), 229—241
— травма, 150
Дивертикул(ы) пищевода, 261
Дилатация, при подсвязочном стено-
зе, 190—191
Димедрол, при укусах перепонча-
токрылых, 92
Диурез, у новорожденных, при раз-
личной хирургической патоло-
гии. 17
Добутамин, при шоке. 23—24
Догоспитальная экстренная помощь
при травме (ДГЭПТ), курс, 128,
139
Домашнее парентеральное питание,
49—50. См. также Питание и
ТПП.
Доношенные дети, классификация,
11
Допамин, при шоке, 23—24
Древесные инородные тела кожи н
мягких тканей, 101
Дроперндол, при послеоперацион-
ной рвоте, 54
Дуоденодуадеиоа настомоз, 351
Дыхание, оценка при травме. 133.
134
Дыхательная недостаточность. ИВЛ,
60—71
— как осложнение ТПП. 48
Дыхательные пути, обструкция.
185—198
— -— при введении в наркоз, 246
— — послеоперационная, 54
— — при травме, 132 -133
— при ожогах, 92
— сопротивляемость. 61
Дыхательный объем, 66
Желудок, заболевания, 322—333
— перемещение при пластике пи-
щевода, 270 272
— перфорация, 333—334
— — при дуоденальной атрезии,
346
— — у новорожденных, 287
Желудочно-кишечный тракт. См.
по его разделам и Желудок.
— инородные тела, 98—100
удвоения, торакоабдоминаль-
ные, 248, 249
Желудочный цилиндр, пластика пи-
щевода, 269—270
Жестокое обращение с детьми
(травма головы), 163
Живот, обследование при травме,
137
— травма, 153—158
Животных, укусы, 86. (См. также
Укусы).
Жидкость(и), у новорожденных де-
тей, 15 17
— при ожогах, 106
суточные потребности, 29—30
— при реанимации у травмирован-
пых детей, 135
Жизнеобеспечивающие технологии,
достижения, значение в принятии
этических решений, 84
Жир(ы), метаболическая реакция
на операционную травму, 32
— физиологические потребности,
30
Жирные кислоты, недостаточность
как осложнение ТПП. 47—48
Заворот, желудка, 329—330
— средней кишки при мальрота-
ции, 360
Защитные механизмы новорожден-
ного, 26
Змеиные укусы. 88 91
Золлингер — Эллисона синдром, 332
Игла(ы), как инородное тело кожи
и мягких тканей, 101
Идиопатический респираторный ди-
стресс-синдром (ИРДС). у ново-
рожденных. 287
Илеус мекониевый. См. Меконие-
вый илеус.
Илиоингвиналышя блокада при по-
слеоперационных болях, 58
Иммунизация, против бешенства,
87—88
Иммунная реакция на ожоговую
травму, 104—105
Импедансная кардиография (биоим-
педанс), 21
Ингаляционные ожоги. 111
Инородные тела, 95—101
— гортани. 188—189
— пищевода, перфорация, 259 -
261
— трахеобронхиального дерева,
194—195
Интенсивной терапии отделение,
кардиопульмонарный мониторинг,
19
Интерлейкин, 25
Intermittent mandatory ventilation
(1MV), 65. См. Перемежающаяся
принудительная вентиляция лег-
ких (ППВЛ).
Интубация, 67—68
Инфузионная терапия, при ожогах,
106
Iodine, при ожогах, 109
Искусственная вентиляция. См. так-
же Вентиляция.
— при диафрагмальной грыже,
236-237
— у новорожденных при дыхатель-
ной недостаточности, 18
Калории, потребности у ожоговых
больных, 106—107
Кальцификация гетеротопическая,
как осложнение ожогов, 114
Кальция глюконат, при гиперкалие-
мии, 77
— при гипокальциемии, 13
Кальция метаболизм, у новорож
денных, 13
Кантрелла пентада, 177, 180, 240
Кап нография, интраоперационная,
56
Кардиография импедансная, 21
Кардиотоксин, в змеином яде, 88
Картагенера синдром, с бронхоэкта-
зами, 217—218
Карцинома, эпителиальная, после-
ожоговая, 264
Катетеризация, вен центральных,
20—21
380 ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
легочной артерии, 21
Каудальная блокада, при амбула
торных операциях, 54
— при послеоперационных болях,
58
Каустические агенты, химические
ожоги, 255—958
Килевидная деформация грудной
клетки, 174— 175
Килокалории, потребности, 30
Кислород, напряжение, в аорте,
235—236
— артериальное, 19
— обмен, легочный, 62
потребление, 22, 36, 63
— сатурация, артериальная, 19—20
— токсичность к. как осложнение
ИВЛ, 70
Кислота(ы), амиио-к., эссенциаль-
ная, 30
— химические ожоги, 256
Кислотно-основной статус, 62—63
Кнста(ы), бронхогенная, 247—249
— гастрогенная, 209—210
— гортани, 186
— легочная, врожденная, 200 204
— — приобретенная, 204—205
— медиастинальная, нейроэнтераль-
ная, 246
— — сдавление трахеи, 195
тимуса, 250
Кисюаденоматозная аномалия, врож-
денная, легких» 202 204
Кистозная гамартома, мезенхималь-
ная, легких, 210
Кистозная гигрома, 252
Кистозный мекониевый пери гонит,
374
Кистофиброз, 221
— диагностика, 368 -369
— при мекониевого илеуса эквива-
ленте, 372
— при мекониевой пробки синдро-
ме, 372—373
— при мекониевом илеусе. См.
Мекониевый илеус.
— при мекониевом перитоните, 373
— передача по наследству, 366—
367
Кишечник. См. также отдельные
части кишечника, напр. Двенад-
цатиперстная кишка.
атрезия, 283, 287, 341 -355
— мальротация, 357—365
— непроходимость после фундопли-
кации, 313—315
— стеноз, 341—342
— эмбриологическое ра:*витие,
357—360
Кишка толстая, аганглиоз тоталь-
ный, 368 (см. также Гиршпрунга
болезнь).
— атрезия, 341—342, 344 346
— — лечение, 353
— — ирригографин с барием,
349—350
— обратная ротация, коррекция,
364
— перфорация и мекониевый пери-
тонит, 373 374
пластика пищевода, 264—269
Клизма гастрографиновин, при ме-
коннеком илеусе, 370
— при синдроме мекониевой проб-
ки, 373
Клюмпкс паралич, при эвентрация
диафрагмы, 240
Кожа, анатомия, 102 — 103
— инородные тела, Ю0—101
— реакция к. на кровопотерю, 135
Conipartment-синдром, как осложне-
ние ожоговой травмы. 113
Компьютерная томография (КТ),
при
— абдоминальной травме, 153—
154
— атрезии пищевода и ТПС, 283
— медиастинальных опухолях, 246
— мозговой травме, 163—165
— Поланда синдроме, 179
— эмпиеме плевры, 214
Конечности, осмотр при травме.
137
Коричневый паук, укус(ы), 92—93
Короткой кишки синдром, 48 -49
— при тонкокишечной атрезии,
354—355
Кровотечение, при травме, 134—
136
Кровоток легочный, 62
Кровь, артериальная, газы, монито-
ринг, 19
— кислорода содержание в к., 63
— объем к. у новорожденных,
13—14
Crotalids (ямкоголовые змеи), био-
логия, 88
Круп, инфекционный, 188
— постинтубационный, 54
Кумулятивный индекс летальности
(КИЛ), 131
Куриная грудь. См. Килевидная де-
формация грудной клетки.
Куря и и га язва, 332
Кушинга язва, 332
Лазер(ы), при подсвязочном сте-
нозе, 191
Ланда-Браудера таблица, при оцен-
ке площади ожога, 105 -106
Ларингомаляция. 186
Ларингоскопия, при инородных те-
лах, 95
Лариигоспазм, при рефлюксе,
301—302
Ларинготрахеобронхит, острый, 188
Ларинготрахсопластика, при подсвя-
зочном стенозе, 192
Л аринготрахеоэзофагеал ьная рас-
щелина, 296—297
Ларингоцеле, 186
Легкое(ие), аномалии, 200—211
— приобретенные заболевания,
213—226. См. также по нозоло-
гическим формам, иапр. Эм-
пиема.
— развитие л., выживаемость при
заднелатсрал ьн ы х диафрагмал ь-
ных грыжах, 231—233
— ушиб, 144—145
— физиология, 60—63
Легочная артерия, катетеризация,
21—22
— петли л. а. синдром, 193
Легочная биопсия, при легочной
инфильтрации, 223—224
Легочная гипертензия, при врож-
денной диафрагмальной грыже,
233- 234
Легочная гипоплазия, при врож-
денной диафрагмальной грыже.
232—233
Легочная система, развитие у ново-
рожденных детей, 17 22
Легочное артериальное давление,
у новорожденных, медиаторы.
234
Легочной утечки воздуха синдром,
70—71
Ледда тяжи, при мальротании,
362—364
Лекарственные препараты, при
ГЭР. 307 309
— инотропные, при шоке, 23—24
Лимфангиома гортани, 186—187
Лимфобластом» средин си ня, 249
250
Лимфома, лимфобластная, средосте-
ния, 249 250
Лицо, исследование при травме,
137
Лобарная эмфизема, врожденная,
204
Лоханочно-мочеточниковый сег-
мент, обструкция, 80
Loxosceles rcclusa, укус(ы), 92—
93
Магния сульфат, при гипомагне-
зисмии, 13
Малеко катетер, 38
«Маленькие» по отношению к геста-
ционному возрасту новорожден-
ные. 11 — 1?
Малигнизация ожоговых рубцов,
114
Мальротация кишечника, 357—365.
См. также Кишечник, мальро-
тация.
Манометрия эзофагеальная, при
ГЭР, 306
Марфана синдром, при воронкооб-
разной груди, 168—169
— при килевидной груди, 174
Масса тела, как показатель состоя-
ния питания, 34
Мафенамид, при ожогах, 109
Медь, недостаточность, как ослож-
нение ТПП, 47
Мсзоколиконариетальная грыжа (и),
при мальротации, 361, 363—
365
Мекониевого илеуса эквивалент,
366, 372
Мекониевой пробки синдром, 366,
372 373
Мекониевый илеус, 366—372
— при дуоденальной атрезии, 347
Мекониевый перитонит, 366, 373 —
375
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ 381
Мслиттин, в яде перепончатокры-
лых. 91
Мембрана (ы), гортани, 186
— желудка, антральная, 327
— провисающая, 341
Менингоцеле, торакальное, 246
Местные препараты, для лечения
ожогов, 107 109
Метаболизм, глюкозы, у новорож-
денных, II —13
— кальция, у новорожденных, 13
— скорость м. в послеоперацион-
ном периоде. 35 36
Метаболическая реакция, на опера-
ционную травму. 32—33
Метаболический ацидоз, лечение,
79—80
Металлические осколки, в коже и
мягких тканях, 101
Миастения (Myasthenia gravis), юве-
нильная, лечение, 250—251
Мидазолам, в предоперационной
подготовке, 52
Микобактериальная инфекция, ати-
пичная, 222
Микрогастрия, врожденная. 330
при гастроэзофагеальном реф-
люксе, 317
Микроэлементы, недостаточность,
как осложнение ТПП, 47
— рекомендуемые суточные добав-
ки, 31
Микулича энтеростомия, при меко-
ниевом илеусе, 371
— при тонкокишечной атрезин,
352
Минералы, физиологические потреб-
ности, 30—31
Миниторакотомия, при эмпиеме,
215
Миокард, сократительная способ-
ность, 22
травма, 149—150
Многоводие, при атрезин пищевода,
282
при врожденной диафрагмаль-
ной грыже, 233
— при дуоденальной атрезии, 347
Множественной органной мальрота-
ции синдром (МОМС). 347
Мозг, травма, 162—165 (см. также
Голова, травма)
Молочные смеси с низким содер-
жанием фосфора, при гиперфос-
фатемии, 79
Monro-Kellie доктрина, модифициро-
ванная, 164
Морганьи отверстие, грыжа. 240
Морфин, при послеоперационных
болях, 58
Мотоциклетная травма, леталь-
ность, 119—120
Мочевой пузырь, травма, 157, 159
Мочеточник (и), обструкция, 80
— травма, 159
Мочи объем, 73
Мягкие ткани, инородные тела,
100 101
Нагрузка (выносливость к и.) при
воронкообразной деформации
грудной клетки, 170
Назотрахеальная интубация, 68
Налбуфин (иубаин), при послеопе-
рационных болях, 58
Напряженный пневмоторакс, 134,
146—148
Наркотики, в лечении боли. 108
— прн послеоперационных болях.
58
Насекомых укусы, 86. См. также
Укусы.
Натрий, фракционная экскреция,
74—75
Натрия бикарбонат, при гиперка-
лиемии, 77
— при ОПН, 79—80
Натрия полнстирол-сульфонат, при
гиперкалиемии, 77
— при ОПН, 79
Национальный Регистрационный
Центр Детской Травмы (НРЦДТ),
128—131
Недоношенные дети, 11
— послеоперационное ведение. 55
11сй робласто.ма (ы), паравсртсбраль-
иой борозды, 246 247
Нейротоксин, в змеином яде. 88
Нейроэндокринный рефлекс, 31—
32
Нейроэнтеральная киста (ы), 246
247
Нейтрофильная недостаточность, у
новорожденных, 26
Неоспорим, при ожогах. 109
Нижний эзофагеальный сфииктер,
301
Низкофосфатные смеси, при гипер-
фосфатемии, 79
Ниссена фундопликация, прн ГЭР,
309—310
— осложнения, 314—318
Нитрофуразон, при ожогах, 109
Новорожденные, дети, острая почеч-
ная недостаточность, 78—80
— стресс, гормональная и метабо-
лическая реакция, 31—33
— торакальная травма, 150 151
— физиология, 11—26
Покардиоз, 222—223
Обработка, ожоговых ран, 107- 108
Обструкция, дыхательных путей. См.
Дыхательные пути, обструкция.
— кишечника. См. Кишечник.
Объем (по о.) — циклированные вен-
тнчяторы, 65
Огнестрельные ранения, неумыш-
ленные. 119, 121
Ожоги, 102—115
— ингаляционные, 195
— Курлинга язва, при о., 332
— химические, 255—258
Оксигенация, неадекватная, опре-
деление понятия, 64
— экстракорпоральная мембранная.
См. Экстракорпоральная мем
бранная оксигенация.
Олигурия, определение понятия, 78
Операции. См. также но названи-
ям о.
— амбулаторные. См. Амбулатор
ные операции.
— метаболическая реакция на опе-
рационный стресс, 32- 33
— эндокринная реакция на опе-
рационный стресс, 31 — 32
Опухоленого некроза фактор (ОНФ),
24—25
Опухоли. См. по названиям опухо-
лей и анатомических областей.
Оротрахеальная интубация, 67—68
Оса, укусы, 91—92
Основной обмен, в послеоперацион-
ном периоде, 35—-36
Оссермаиа, классификация степени
тяжести миастении, 250
— шкала, оценки результатов гим
эктомин, 251
Острая почечная недостаточность,
у новорожденных, 78—80
— послеоперационная, 75—78
Острое расширение желудка (газо-
вого пузыря большого синдром),
после фундопликации, 313—315
Отек (и), гортани, после экстуба-
ции, 70
— как осложнение ТПП, 48
Открытая резекция, при подсвязоч-
ном стенозе, 192
Отравление, змеиным ядом, 88 91
— летальность, 119, 121
Охлаждение, недоношенных детей,
15
Паденис(я), с летальным исходом,
119, 121
Панкреатит, травматический, 156—
157
Папиллома, гортани, 187
Паравертебральная борозда. 244—
245
— опухоли. 246 247
Паралич, плечевого сплетения, при
эвентрации диафрагмы, 240
Парастернальная грыжа, 240
Паркланда модифицированная фор-
мула, при ожогах, 106
Паук(и), укус(ы), 92—93
ПЛХГ (передвижной армейский хи-
рургический госпиталь), оказа-
ние помощи при травме, 127
Пациентом управляемая анелгезня,
при послеоперационных болях,
58
Пениальная блокада, при послеопе-
рационных болях, 58
Пептическая язва(ы), 332 333
Передняя кишка, кистозное удвое-
ние (я), центрального средосте-
ния, 246—249
Перелом (ы), ребер, 142—143
— черепа, 162
Перемежающаяся принудительная
вентиляция (ППВЛ), 65. См.
Intermittent mandatory ventilation
(/MV).
Перепончатокрылых укусы, 91 92
Перикарда тампонада, 135, 149
382 ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
Перистальтика, пищевода, при
ТПС, 281
Перитонеальный лаваж, диагности-
ческий, при травме живота, 154
Перитонит, мекониевый. См. Меко-
ниевый перитонит.
Перстневидный хрящ, расщепле-
ние, при подсвязочном стенозе,
191
Перфорация, желудка, 333—334
— толстой кишки, мекониевый пе-
ритонит, 374—375
Перфорированный (сетчатый) транс-
плантат, при ожогах, 111
Пеццера катетер, 38
— при чрескожной эндоскопической
гастростомии, 336
Печени, дифункция при ТПП, 48
— травма, 155—156
Пешеходов травма» летальность,
119—121
Пилоростеноз, 322—327
Пилоруса атрезия, 328—329
Пиразинамид, при туберкулезе, 222
Питание, домашнее парентеральное.
49—50
— при ожогах, 106—107
— при ОПН, 80
— тотальное парентеральное. См.
Тотальное парентеральное пи-
тание (ТПП).
— у хирургических больных, 29
50
— энтеральное, 36—38
Пищевод, 255—274
— атрезия, 278 297
— Барретта и ГЭР, 303- 317
— кистозное удвоение, 247—249
— свищ. См. Трахеопищеводный
свищ.
— сдавление трахеи (пищеводом),
193
Пищеводное отверстие, грыжа. См.
Грыжа(и), пищеводного отверстия.
Пищеводный сфинктер, нижний, 301
Плевра, приобретенные заболевания,
213—226. См. также но нозологи-
ческим формам, на пр. Эмпиема.
Плеча окружность, как показатель
состояния питания, 34
Плечевого сплетения паралич, при
эвентрации диафрагмы, 240
pH-мониторинг, при ГЭР, 305—306
Пневматоцеле, 216—217
— дифференциальная диагностика
с врожденной кистой, 205
Пнсвмония(и), при АП, 287 288
— аспирационная, как осложнение
анестезии, 53
-----при ГЭР, 302
— интерстициально-альвеолярные,
идиопатические, хронические,
225 226
Пневмоперитонеум, при мекониевом
илеусе, 369
Пневмоторакс, 146—148
— напряженный, 134
Pneumocystis carinii инфекция. 223—
225
РО2. См. Кислорода, напряжение.
Повидон, при ожогах, 109
Податливость, легких, 18, 61
Подвздошная кишка, атрезия. 341 —
344, 346—347, 349—354
Поджелудочная железа, при КФ.
См. Кистофиброз.
— псевдокиста, травма, 156—157
—- травма, 156—157
— экзокринная недостаточность,
367
Иодсвязочиая гемангиома, 186—187
Подсвязочиый стеноз, постинтуба-
ционный, 189
— хирургическое лечение, 190—
192
Пожары, детальные исходы, 119,
121
Позвоночник, шейный отдел, конт-
роль при манипуляциях на дыха-
тельных путях, 133—134
Позиционная терапия, при ГЭР,
307
Покрытия, ожоговых ран, 112 -113
Поланда синдром, 176—177, 179
Поливалентный антивенин, 90—91
Полипептид(ы), в змеином яде, 88
Полицитемия, у новорожденных, 14
Полых органов, повреждение, 157
Постнагрузка, как показатель сер-
дечно-сосудистой функции, 22
Потовая проба, в диагностике кисто-
фиброза, 368
Почечная недостаточность, острая.
См. Острая почечная ксдоста
точность.
— как осложнение при ожогах, 114
Почечный тубулярный ацидоз, 75
Почки, реакция на кровопотерю,
135
— травма. 158 159
— функции нарушение, 72—80
Поясных ремней комплекс, при пов-
реждении полых органов, 157
11 ре дна грузка, в определении сер-
дечно-сосудистой функции, 22
Преднизолон, при увеличенном ти-
мусе, 250
Промежность, обследование при
травме, 137
Протеазы, в змеином яде, 88—89
Протезирование трахеи, при обст-
рукции дыхательных путей, 198
Прямая кишка, исследование при
травме, 137
Псевдокис та (ы), легочная, травма-
тическая, 205
— панкреатическая, 156—157
Псевдосеквестрация, легочная,
206—208
П ульсоксиметрия, 19—20
Пчелиные укусы, 91—92
Пьера-Робена синдром, интраораль-
ная обструкция, 185
Раневые покрытия, при ожогах, 112
Ранение миокарда, 149 150
Расщепление (раздвоение) груди-
ны, 179—181
Рвота, без желчи, дифференциаль-
ная диагностика, 322
— при ГЭР, 300
— при пилоростенозе, 323
— послеоперационная, 54
— сильная, 255, 260
Реабилитация, после ожогов, 113
Ребер, перелом (ы), 143
Реберного каркаса, аномалии при
синдроме Поланда, 176—177
Ревущего слона синдром, при ГЭР,
305
Регионарная анестезия, в амбула-
торией хирургии, 54
Резекция лобарная, при бронхоэкта-
зах, 219
— при легочном абсцессе, 220
— трахеи, при обструкции дыха-
тельных путей, 197
Ренальные растворимые вещества,
экскреция, минимальные объемы
мочи, 73
Рентгенологическое исследование.
См. по отдельным видам.
— при АП и ТПС, 282—284
— при завороте, желудка, 330, 331
— — средней кишкн, с мальрота-
цией, 360—362
— при мекониевом илеусе, 369—
370
— при обструкции, гортани, 189
— — трахеи. 195
Респираторное поражение, при ин-
галяционных ожогах, 111
Респираторный алкалоз, 69
Респираторный ацидоз, 69
Респираторный дистресс-синдром.
См. Гиалиновых мембран бо-
лезнь.
Ретинопатия недоношенных, 14
15
Ретролентальная фиброплазии, 15
Ретростермальная грыжа, 240
Рефлюкс гастроэзофагеальный. См.
Гастроэзофагеальный рефлюкс.
Рин пер-лактат, раствор, при шоке,
24
Py-Y-образный анастомоз, при ме-
кониевом илеусе, 371
Рубцы гипертрофические, как ос-
ложнение ожогов, 114
Рукояточно-хрящевая деформация,
при килевидной груди, 174—175
Рыболовный крючок, как инород-
ное тело кожи и мягких тканей,
101
Саблевидный синдром, 207 208
Сандифера синдром, при ГЭР, 303
Свищ(н) трахеопищеводный, как ос-
ложнение инородных тел пище-
вода, 259
Связки Трейца повреждение, при
травме полых органов, 157
Секвестрация легочная, 206—207
Селезенки травма, 154—155
Селена недостаточность, как ос-
ложнение ТПП, 47
Сепсис, как осложнение, ИВЛ, 71
— — ожоговой травмы, 113—114
-----ТПП, 46—47
Септический шок, 24—26
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ 383
Сердечно-сосудистая система, у но-
ворожденных детей, 21—26
Сердца, повреждение при травме
грудной клетки, 149 150
— пороки, при дуоденальной атре-
зии, 346 347
— — при норонкообразной груди,
168
— реакция на кровопотерю, 135
Серебра нитрат, прн ожогах, 109
Серебра сульфадиазин, прн ожогах,
109
Синдром внезапной смерти детей
(СВСД), при ГЭР, 301—302
Синхронизированная перемежаю-
щаяся принудительная вентиля-
ция легких (СП ПЕЛ), 65
Скальпа повреждение, 162
Scarlei red, при ожогах. 109
Склеродермия пищевода, 261
Скорость клубочковой фильтрации
(СКФ), 72—74
— у новорожденных детей, 15 16
Смерть, причины, 119, 121
— — поданным НРЦДТ, 130—131
— от ожогов, 102
— определение понятия, этические
проблемы, 125—126
— после фундопликации, 315
Снятие с вентиляционной поддерж-
ки, 69—70
Сознание, определение уровня, мне-
моническая схема AVPU, 136
Сосудистого тонуса медиаторы. 234
Сосудистыми кольцами, обструкция
пищевода, 273—274
Спектрометр, интраоперационное
применение, 56
Специализированная экстренная по-
мощь прн травме (СЭПТ), курс
для врачей, 128
Спинальная блокада, при амбула-
торных операциях, 54
Спинного мозга повреждение, 163
Спленэктомия прн травме, 154—
155
Споидилоторакалышя дисплазия
(синдром Jarcho-Levin), 182—183
Средостение, опухоли. 244—252
— сдавление трахеи кистами с.,
195
Статической податливости кривая,
61
Стекла осколки, как инородные
тела кожи н мягких тканей, 101
Стеноз(ы), кишечника, 341—342
— пищевода, врожденный, 261
— трахеи, 193 195
Стернального «поворота* техника,
при лечении воронкообразной
груди, 171
Стероиды, инъекция при подсвязоч-
ном стенозе, 190—191
— при химических поражениях,
257- -258
Столбняк, при укусах, 86
Стресс, гормональная реакция на с.,
31—32
— метаболическая реакция на с.,
32—33
Субдуральная гематома(ы), 163
Суицид(ы), смерть от с., 119,
121
Сурфактантная недостаточность,
при болезни гиалиновых мем-
бран, 18 19
Сцинтиграфия ззофагеальная, при
ГЭР. 306
Т-трубчатая эптеростомия, прн ме-
кониевом илеусе, 371
Таля фундопликация, при ГЭР,
309 317
Гератома(ы) средостения, 251—252
Термиты, укусы, 91—92
Термические поражения. См.
Ожоги.
Терморегуляция, 15
Тимуса опухоли, 250
Тонкая кишка. См. Кишечник н от-
дельные его части, напр., Две-
надцатиперстная кишка.
— повреждение при травме, 157
Торакальная дистрофия асфиксиче-
ская (болезнь Jeune), 181 183
Торакальная эктопия сердца. 177,
180
Торакоабдоминальная эктопня серд-
ца, 177, 179, 180
Тотальное парентеральное питание
(ТПП), 38, 40 48
рекомендуемые суточные добав-
ки, витаминов, 31
— — микроэлементов, 31
— — электролитные, 31
Травма. См. также по анатомиче-
ским областям, напр.. Грудная
клетка, травма.
— желудка перфорация прн т..
333—334
— лечение, 127—139
— ожоговая. См. Ожоги.
— эпидемиология, 118—126
Травматологическая брнгаца, мно-
гопрофильная, 131 —132
Трансплантат, сетчатый, при ожо-
гах, 110—111
Транспортные происшествия, ле-
тальность. 119—120
Трахеомаляция, 193, 281—282
Трахеопищеводный свищ, 278—296
— и ГЭР, 303
— как осложнение инородных тел
пищевода, 259
Трахеостомия. при ИВЛ, 68
— при обструкции дыхательных пу-
тей, 189—190
Трахея, анатомия. 60—61
— — у маленьких детей особен-
ности, 133
— аномалии. 192—194
— деканюляция, при обструкции
дыхательных путей, 190
— инородные тела, 95 97
— обструкция, пекле лечения АП,
294
— — приобретенная, 194—198
— свищ. См. Трахеопищеводный
свищ.
— травма, 148
Treacher Collins синдром, с интра-
оралыюй обструкцией, 185
Трехглавая мыщца плеча, кожная
складка в области т. м. п. как
показатель запасов жира, 34
Трисомия 21, и дуоденальная атре-
зия, 346
Трихобезоар(ы) как инородное
тело, 100
Тромбофлебит септический, как ос-
ложнение ожоговой травмы,
113—114
Тромбоэмболия, как осложнение
ТПП, 45 46
Туберкулез, 222
ГиШе’а тест, 305
Убийства, 119, 121
Углеводы, метаболическая реакция
у- на операционный стресс. 32
— потребности в у., 30
Углекислота, легочный газообмен,
62
— рСО2 мочи, 75
— содержание в выдыхаемом воз-
духе, 20
Угол Гиса, 270—271
Удвоение кистозное, желудка, 329,
330
— передней кишки, 247—249
Удушение, смерть от у., 119, 121
Уж американский домовой, 88
Ультразвуковое исследование, бере-
менных при многоводии. 347
диагностическое, при ОПН. 79
— — при пилоростенозе, 325
Укус(ы), 86—93
Уретры, травма, 159—160
Утопление. 119. 121
Ушиб, легкого, 144 145
— миокарда, 150
VACTER-ассоциация, 285
VACTERL-ассоциация, 285
VATER-ассоциация, 285
VATER-синдром, 209
— прн д¥оденальной атрезии,
346-347
Фентанил, при послеоперационных
болях, 58
Фиброадгезивный мекониевый пери-
гон и г. 374
Фиброплазия, ретролеитальная, 15
Физиология ребенка, 11—26
Fick’а формула, 22
Фиксация трахеи, при обструкции
дыхатетьных путей, 196—197
Фитобезоар (ы), как инородное
тело, 100
Фолиевой кислоты недостаточ-
ность, при кишечной агрезнн,
355
Фосфолипаза А, в яде, змей, 88—89
— — перепончатокрылых, 91
Фототерапия, при гипербилирубине-
мии, 14
Фракционная экскреция, 74 -75
Friss-Hansen’a схема, общее содер-
жание воды в организме. 16
384 ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ
Фторотан, при амбулаторных опера-
циях, 53
Фундопликация, при ГЭР, 309—317
Фуросемида ни/в инфузия, при
ОПН, 76, 79
Халазия, 300. См. также Гастроэзо-
фагеальный рефлюкс.
Хеймлиха прием, 188
Хилла гастропексия, 309
Хилоторакс, 148, 220—221
Химические ожоги. См. Ожоги хи-
мические.
Хлорфенирамин. при укусах пере-
пончатокрылых, 91—92
Хоан атрезия, 185
Хрома недостаточность, как ослож-
нение ТПП, 47
Центральная нервная система
(ЦНС), оценка при травме,
135—136
Церебрального кровотока ауторегу-
ляция, 164
Церия нитрат — сульфадиазин се-
ребра, при ожогах, 109
Церукал, при ГЭР, 308
Цизаприд. при ГЭР, 308
Цинка недостаточность, как ослож-
нение ТПП, 47
Циркуляторный статус, при травме,
134—135
Частично торакальный желудок,
300
Человеческая диплоидоклсточная
вакцина (ЧДКВ), рабическая им-
мунизация, 88
Человеческий рабический иммуно-
глобулин (ЧРИГ), 88
Человеческий укус(ы), 91. См.
также Укус(ы).
Черепа перелом (ы), 162
Черного паука укус(ы), 93
Чрескожная эндоскопическая гастро-
стомия (ЧЭГ), 336—337
Шеи обследование при травме,
137
Шейная эктопия сердца, 177
Шейный отдел позвоночника, конт-
роль за его состоянием при трав-
ме. 133
Шершней укусы. 91—92
Шкала детской травмы (ШДТ),
129—131
Шкала комы Глазго (ШКГ), 163
— при травме, 138
Шкала тяжести травмы (ШТТ),
142
Шок, 22—26
Штамма гастростомия, 38. 334—336
Щелочи, химические ожоги, 228—
230
Эвентрация диафрагмы, 240 241
Эзофагеальная манометрия, при
ГЭР, 275
Эзофагеальная сцинтиграфия, при
ГЭР, 275
Эзофагсальный сфинктер, нижний,
270—271
Эзофагография, с барием. См.
также Барий, исследование.
— при обструкции трахеи, 195
Эзофагоскопия, при ГЭР, 275
— инородного тела удаление, 98
ЭКГ-монитор, интраоперационное
применение, 56
Экстракорпоральная мембранная ок-
сигенация (ЭКМО), 67
— при диафрагмальной грыже,
237—238
Электролиты, у новорожденных
детей, 15 17
Электроожог(и), 111—112
Элекгрохирургическая резекция,
при подсвязочном стенозе, 191 —
192
Эмпиема торакальная, 213 216
Эмфизема, лобарная, врожденная,
204
Эндокардит, бактериальный, как
осложнение анестезии, 53
Эндокринная реакция на операцион-
ную травму, 31—32
Эндоскопия. См. также но разделам
и Бронхоскопия.
— при обструкции гортани, 189
Эндотоксин, при септическом шоке,
25
Эндотрахеальная интубация, 133
— для ИВЛ, 67—68 '
— при остром эпиглоттитс, 188
Энзимы, в змеином яде, 88—89
Энтеральное питание, 36—38. См.
также Питание.
Энтеростомия, промывание кишки,
при мекониевом илеусе, 371
Эозинофилия, как осложнение
ТПП, 48
Энш лоттит, острый, 187—188
Эпидуральная гематома (ы), 162 —
163
Эпителиальная карцинома, на мес-
те ожога, 263—264
Эрба-Дюшена паралич, при эвен-
трации диафрагмы, 240
Эритробластоз, фетальный, 14
Эстераза(ы), в змеином яде, 88
89
Этические проблемы, в детской хи-
рургии, 82—85
Эффективный почечный плазмоток
(ЭППТ), 72
Яблочной кожуры деформация, при
тонкокишечной атрезии, 352
Яд, змей, 88—89
— пауков, 92—93
— перепончатокрылых, 91
Ядерная желтуха, 14
Ядерный магнитный резонанс
(ЯМР), при медиастинальных
опухолях, 246—247
— при травме мозга, 163, 166
Язва(ы), Курлинга, 332
— Кушинга, 332—333
— пептическая, 332—333
Языка укус(ы), самопроизвольный,
91
Ямкоголовые змеи (Crotalids), био-
логия, 88
Издательство приглашает к сотрудничеству
авторов, переводчиков
По вопросам реализации обращаться по телефону: (812) 251-01-67
FAX: 251-77-77
ГОТОВИТСЯ К ПЕЧАТИ
Содержание II тома
Содержание III тома
Глава 28. Некротический энтероколит.
Глава 29. Болезнь Гиршпрунга.
Глава 30 Атрезия ануса и клоакальные пороки
Глава 31. Экстрофия клоаки.
Глава 32. Аноректальный, запирательный меха-
низм и лечение запоров.
Глава 33 Приобретенные аноректальные рас-
стройства.
Глава 34 Инвагинация.
Глава 35. Удвоения пищеварительного тракта.
Глава 36. Дивертикул Меккеля.
Глава 37. Воспалительные заболевания кишеч-
ника.
Глава 38 Опухоли желудочно-кишечного тракта.
Глава 39 Аппендицит
Глава 40. Заболевания желчных путей и пор-
тальная гипертензия.
Глава 41. Трансплантация печени.
Глава 42. Заболевания поджелудочной железы.
Глава 43. Заболевания селезенки.
Глава 44 Грыжа пупочного канатика и гастро-
шизис.
Глава 45. Пупочные и другие грыжи брюшной
стенки.
Глава 46. Паховые грыжи и водянка яичка.
Глава 47 Аномалии развития и положения
почки.
Глава 48. Обструкция лоханочно-мочеточниково-
го сегмента.
Глава 49. Крипторхизм.
Глава 50. Заворот яичка.
Глава 51. Мочеточник.
Глава 52. Инфекция мочевых путей и пузырно-
мочеточниковый рефлюкс.
Глава 53. Мочевой пузырь и уретра.
Глава 54. Реконструктивные операции на моче-
вом тракте.
Глава 55. Клапаны уретры.
Глава 56 Экстрофия мочевого пузыря
Глава 57 Гипоспадия.
Глава 58 Обрезание крайней плоти.
Глава 59. Синдром «сливового» живота.
Глава 60. Лечение интерсексуальных аномалий.
Глава 61. Трансплантация почек.
Глава 62. Реноваскулярная гипертензия.
Глава 63 Опухоли почек
Глава 64 Атрезия влагалища и девственной
плевы.
Глава 65. Гемангиомы и лимфангиомы.
Глава 66. Нейробластомы.
Глава 67. Поражение печени.
Глава 68 Тератомы.
Глава 69. Лимфомы.
Глава 70 Рабдомиосаркома.
Глава 71. Пигментные пятна и меланомы.
Глава 72. Смешанные опухоли.
Глава 73. Аномалии и опухолевидные образова-
ния головы и шеи.
Глава 74. Поражение грудных желез.
Глава 75 Патология щитовидной и паращито-
видных желез.
Глава 76. Сросшиеся близнецы.
Глава 77. Экстракорпоральная мембранная ок-
сигенация
Глава 78 Катетеризация сосудов.
Глава 79. Доброкачественная гинекология.
Глава 80. Гемофилия и другие коагулопатии.
Глава 81. Вирус иммунодефицита человека.
Глава 82. Внутриутробные вмешательства.
Глава 83. Лазеры в детской хирургии, включая
эндоскопию, лапароскопию и торако-
скопию.
Издательство приглашает к сотрудничеству
авторов, переводчиков
По вопросам реализации обращаться по телефонам: Санкт-Петербург (812) 251-01-67
FAX: (812) 251-77-77