Автор: Лазарев А.И. Харламов И.П. Яковлев П.Я. Яковлева Е.Ф.
Теги: жилища химия аналитическая химия издательство металлургия
Год: 1976
Текст
СПРАВОЧНИК
ХИМИКА-
АНАЛИТИКА
МОСКВА «МЕТАЛЛУРГИЯ» 1976
УДК 643.06ЦС2 (03)
А. И. ЛАЗАРЕВ, И. П. ХАРЛАМОВ, П. Я. ЯКОВЛЕВ, Е. Ф. ЯКОВЛЕВА
УДК 543.061/62 (03)
Справочник химика-аналитика. Лазарев А. И.,
Харламов И. П., Яковлев П. Я-,
Яковлева Е. Ф. М.. «Металлургия». 1976, с. 184
Основное содержание справочника составляют
сведения, полезные для химика-аналитика заводской
лаборатории металлургических, машиностроительных,
приборостроительных и других предприятий и
отраслевых научно-исследовательских институтов.
Характер уже опубликованных справочников по
аналитической химии, например автора Ю. Ю. Лурье,
общий, рассчитан на читателя высокой квалификации.
В него не вошли многие полезные сведения, которые
необходимы химикам-аналитикам средней
квалификации в повседневной их работе. Табл. 105. Список лит.:
80 назв.
© Издательство «Металлургия», 1976 р.
31106—169
040(01)—76
СОДЕРЖАНИЕ
Что можно найти в справочнике . . 5
1. Периодическая система элементов
Д. И. Менделеева 6
1.1. Периодичность свойств в
системе Д. И. Менделеева 7
1.2. Химико-аналитическая звезда
элементов 8
2. Таблица атомных масс (на 1969 г.) 9
3. Атомные массы, массы наиболее
употребительных атомных групп
и соединений 12
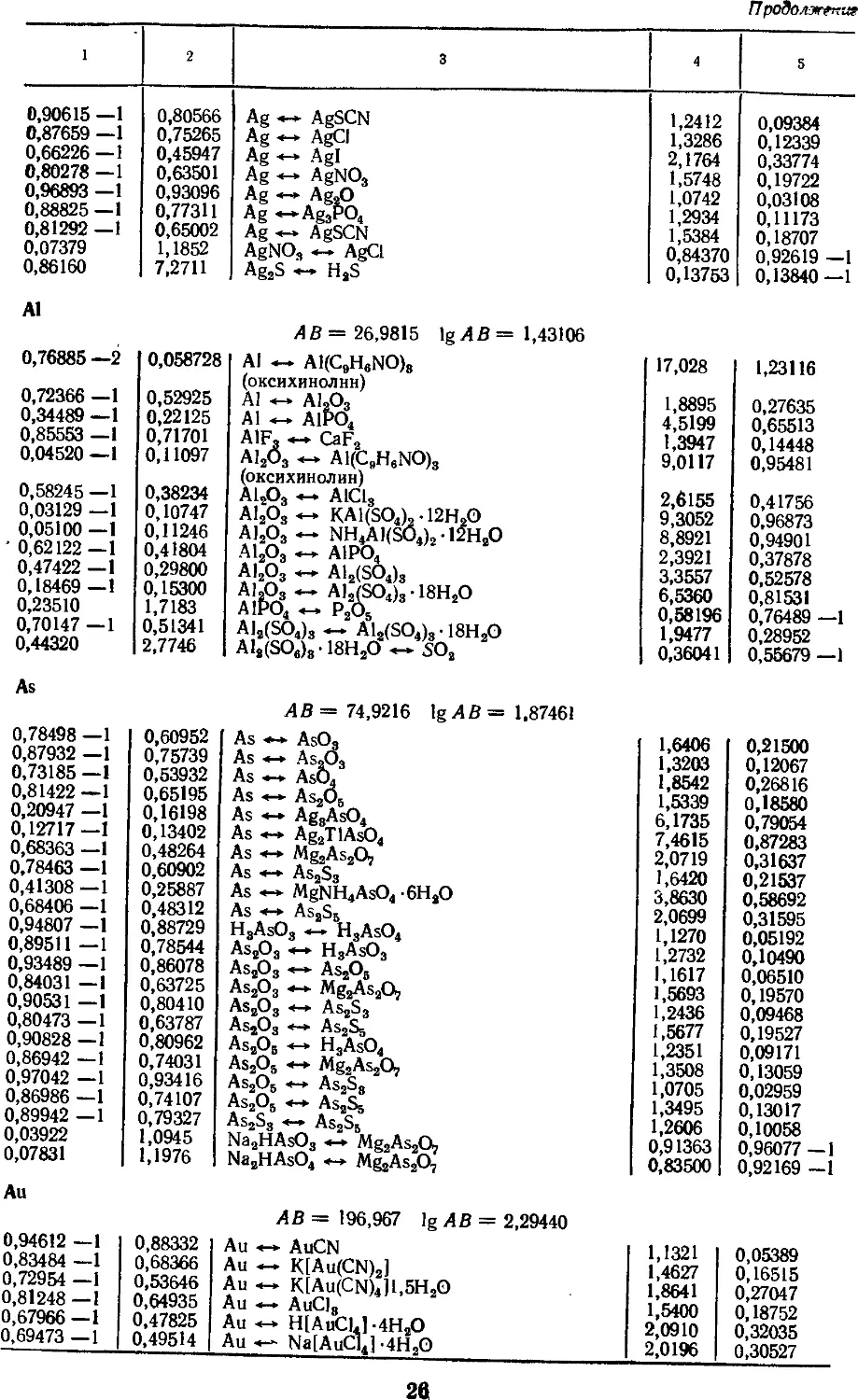
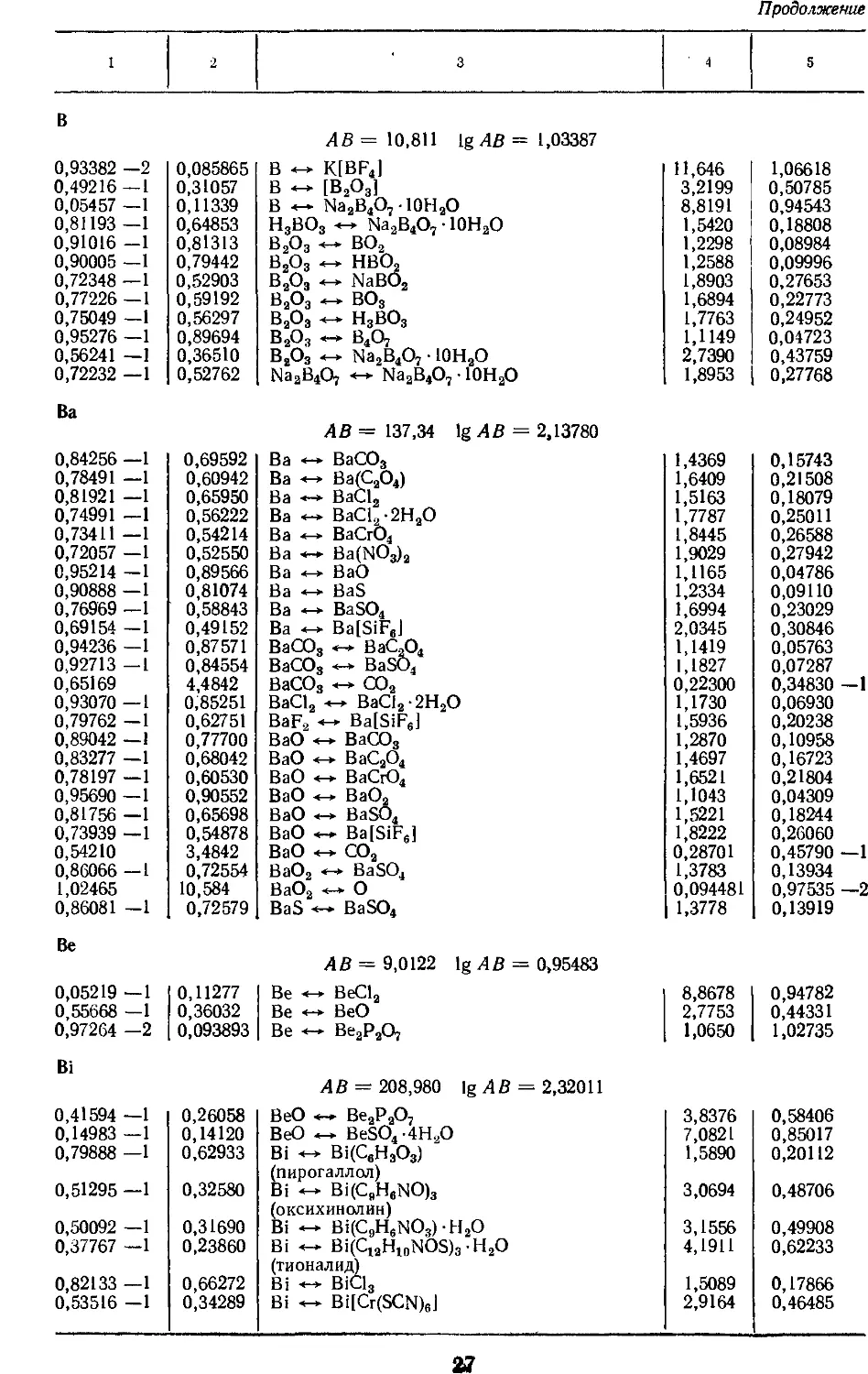
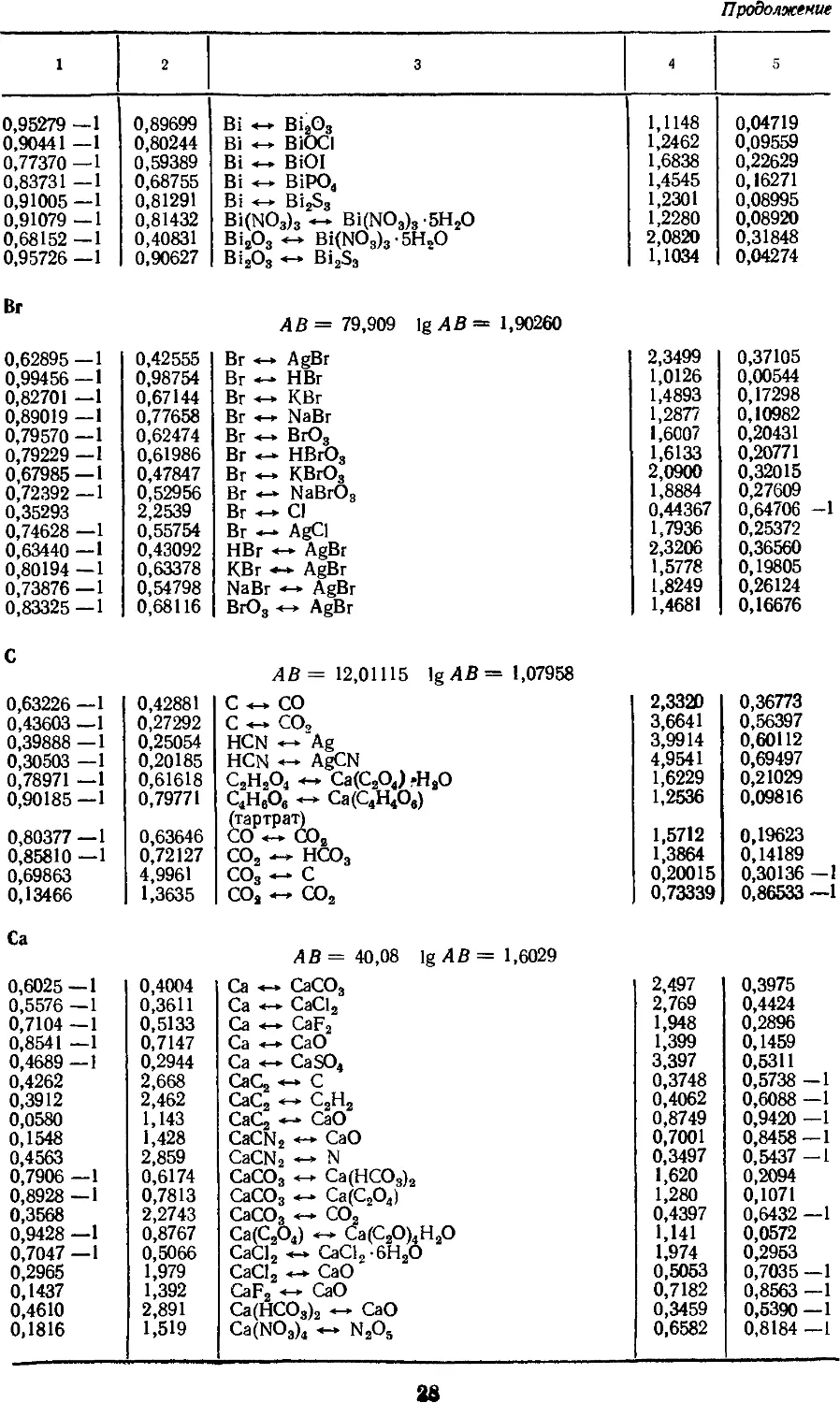
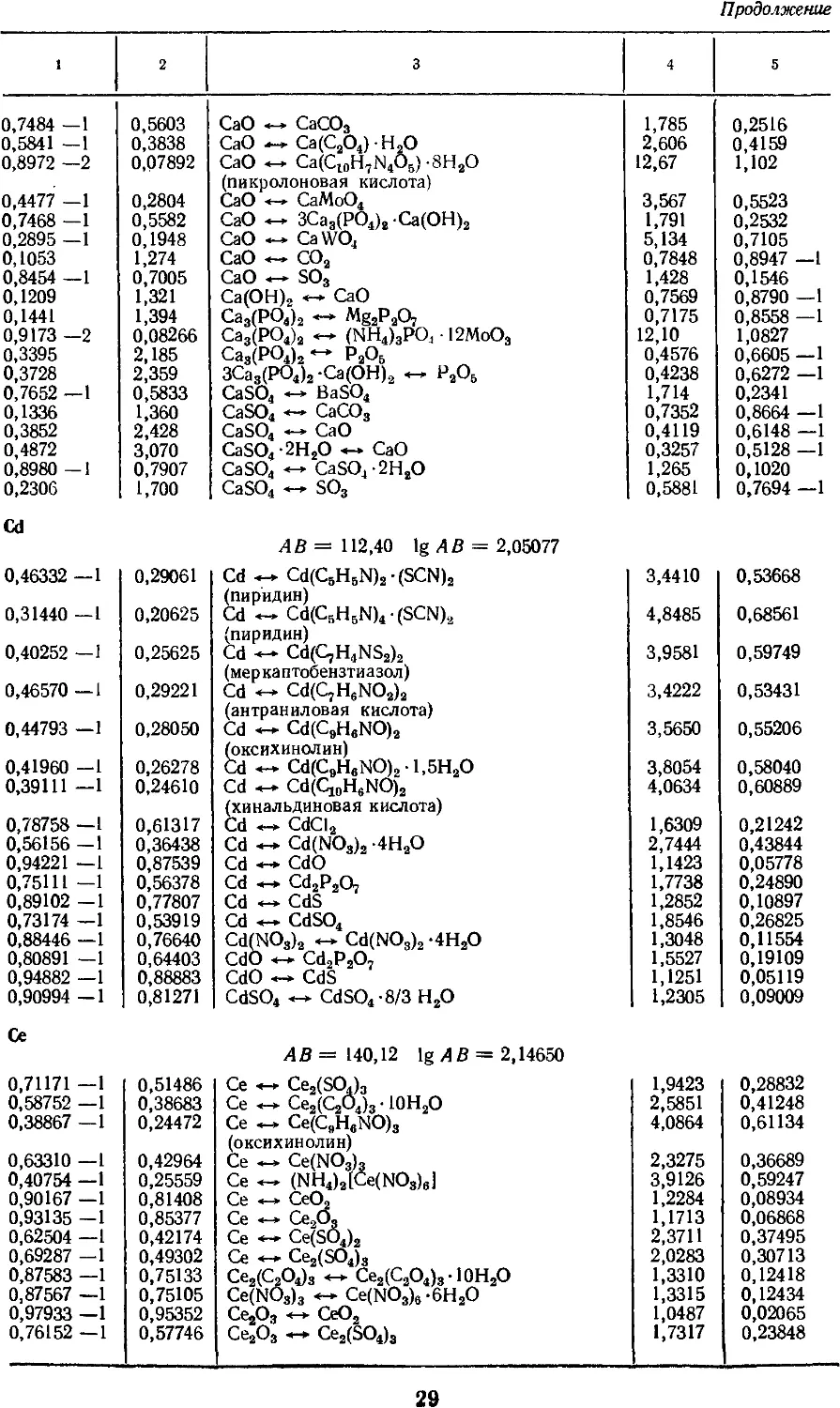
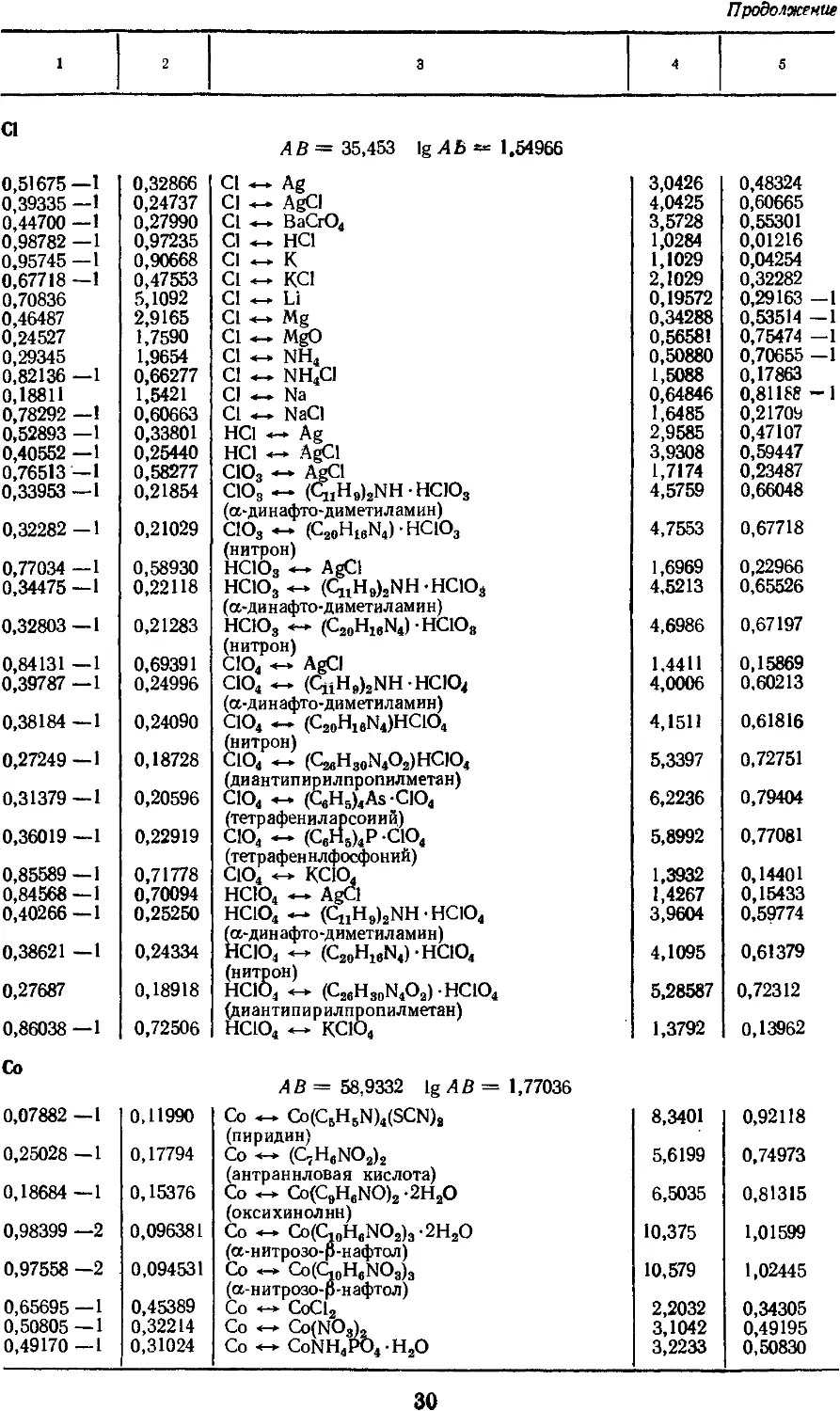
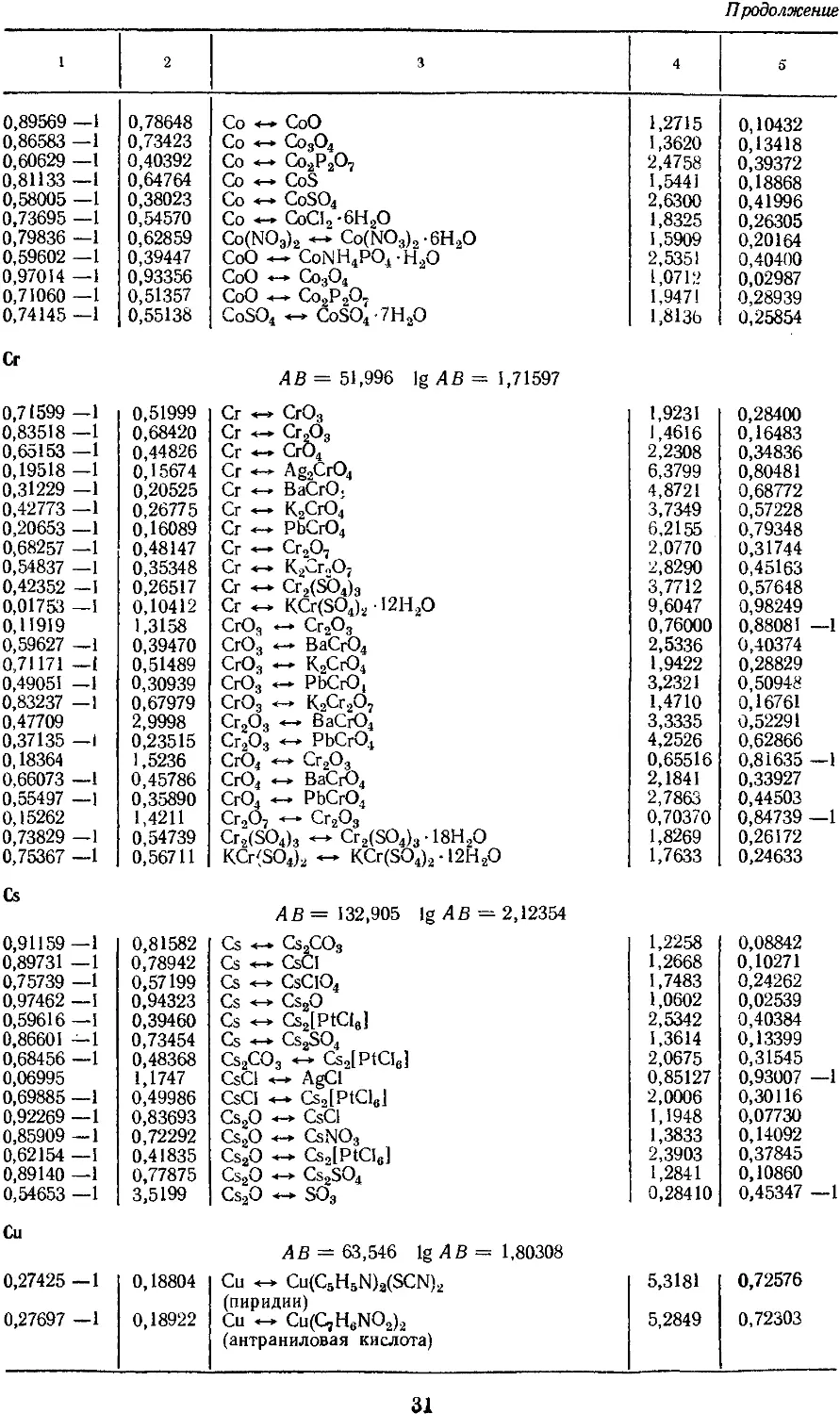
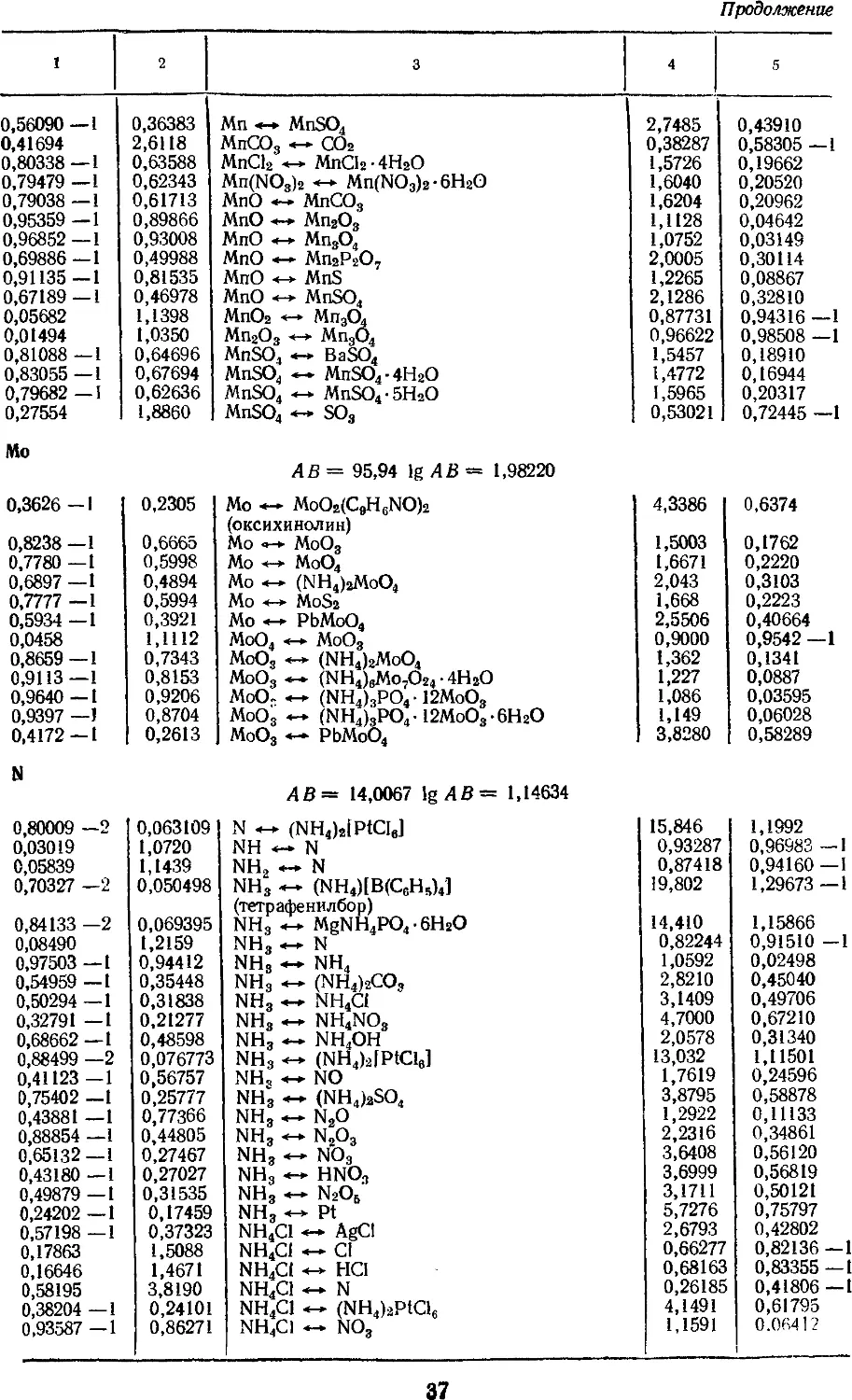
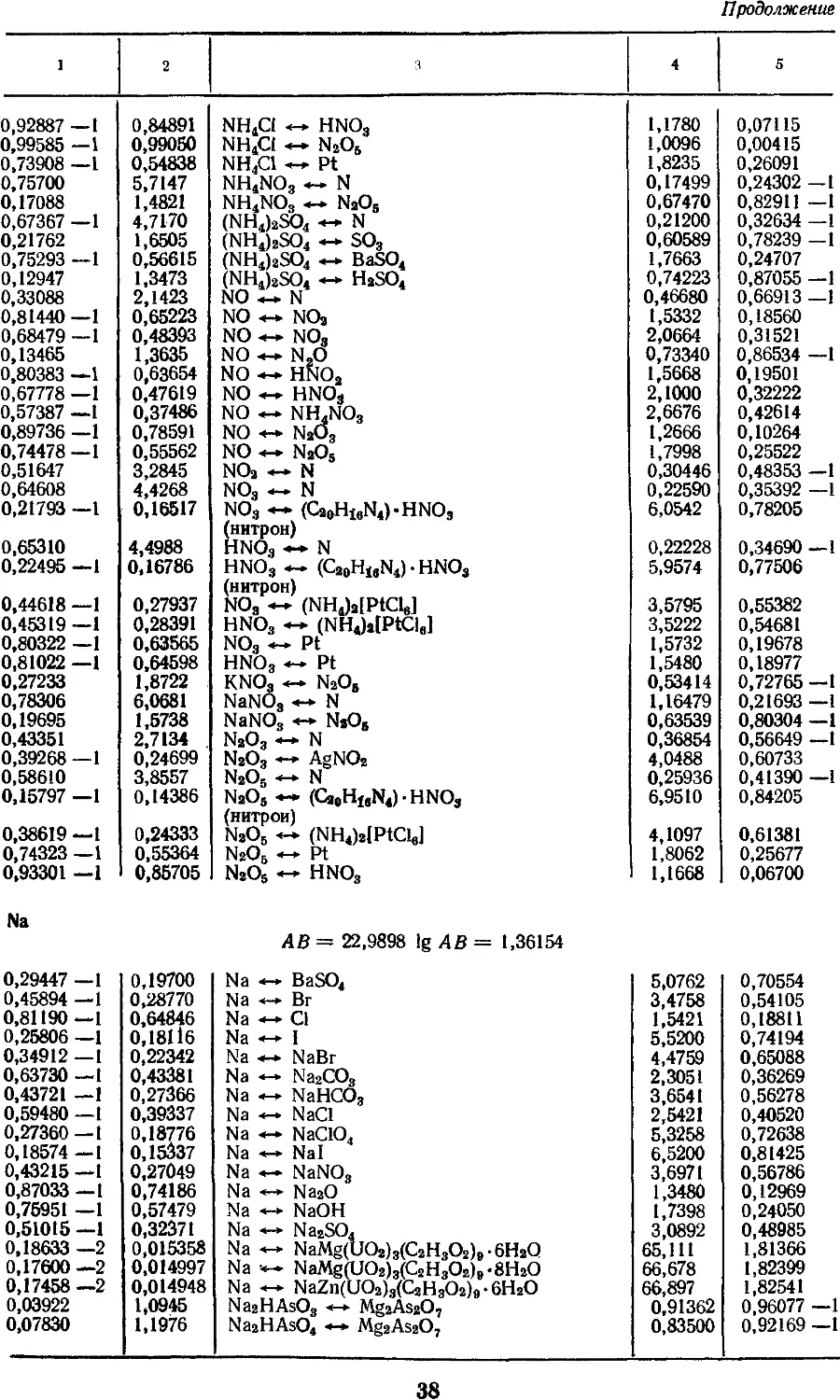
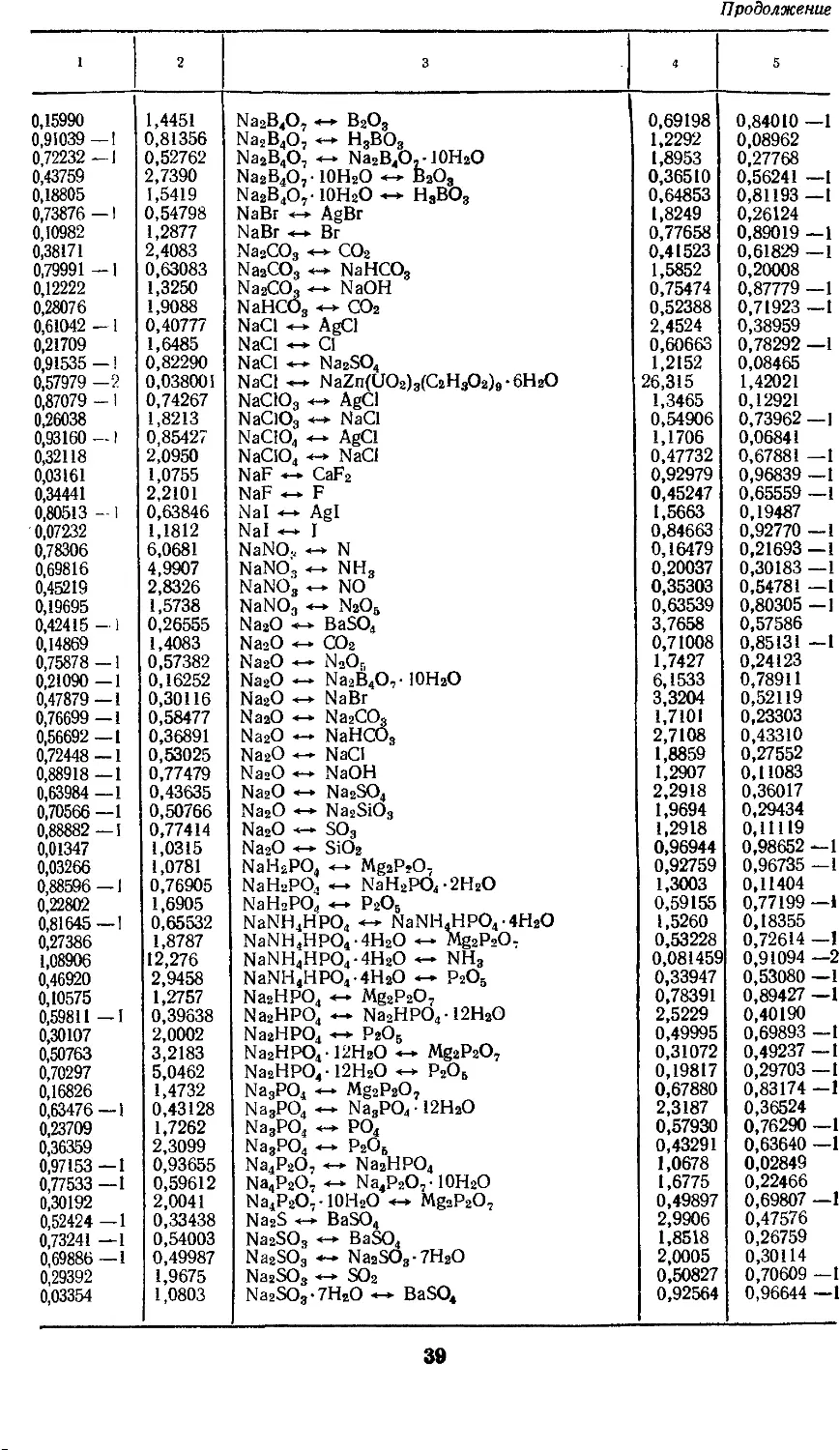
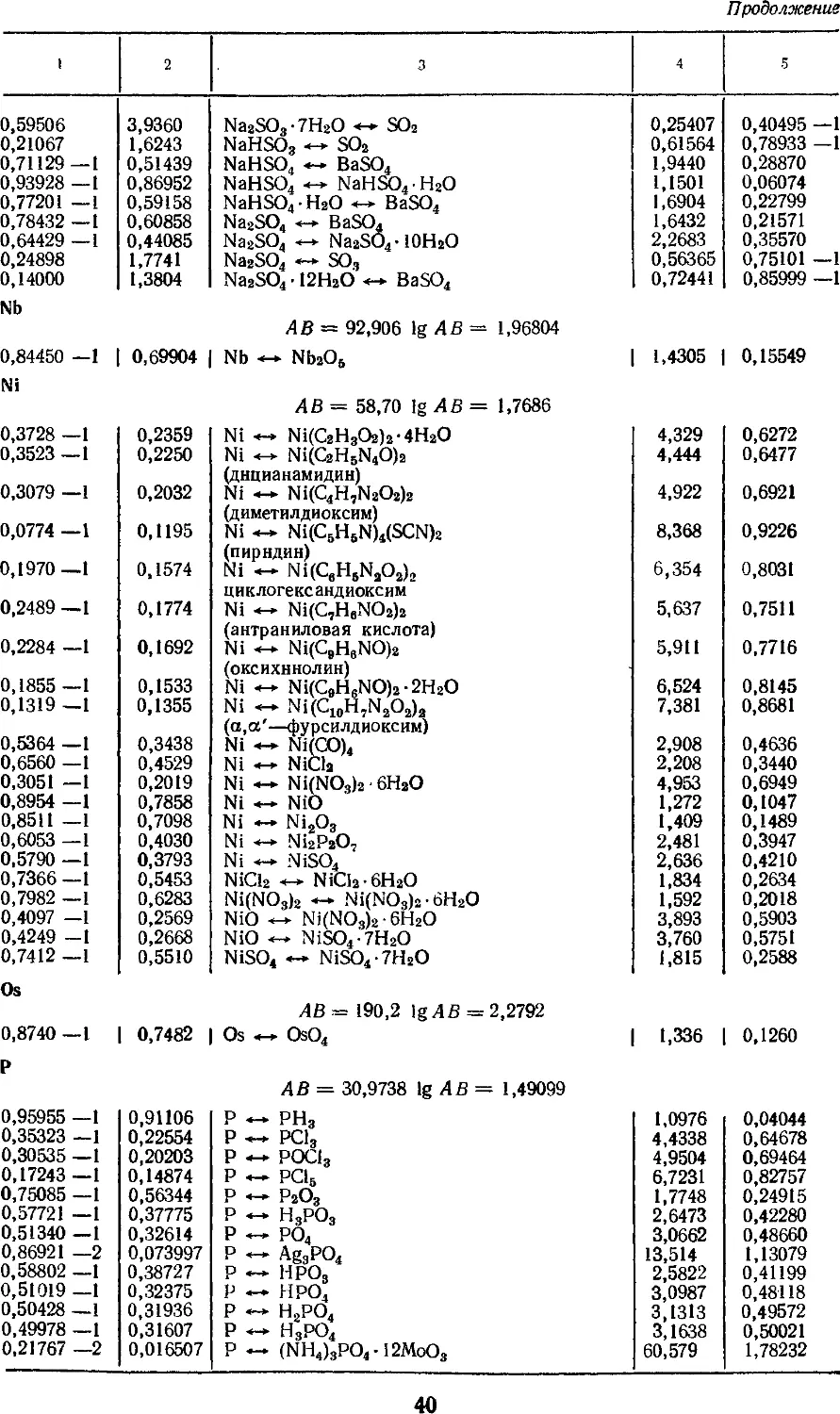
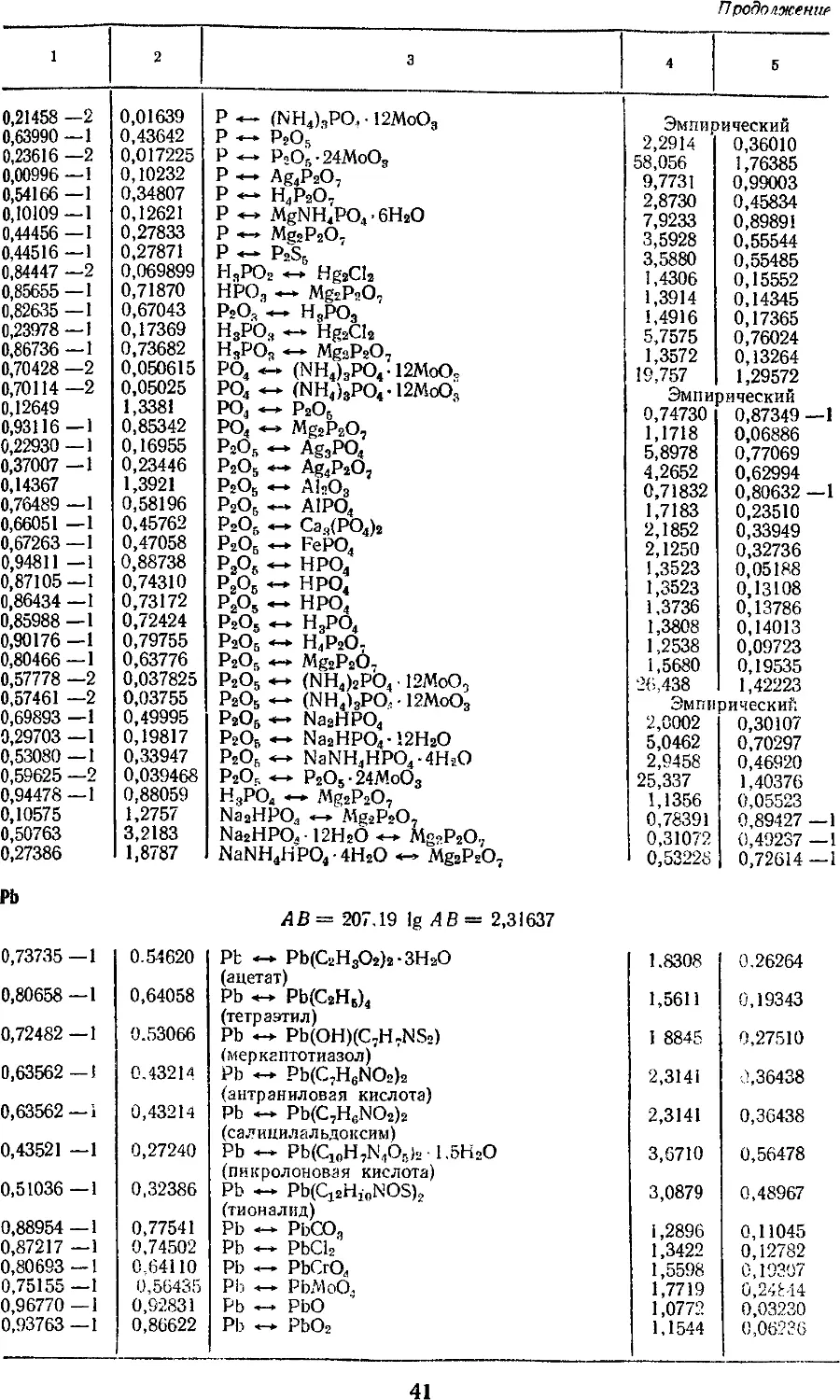
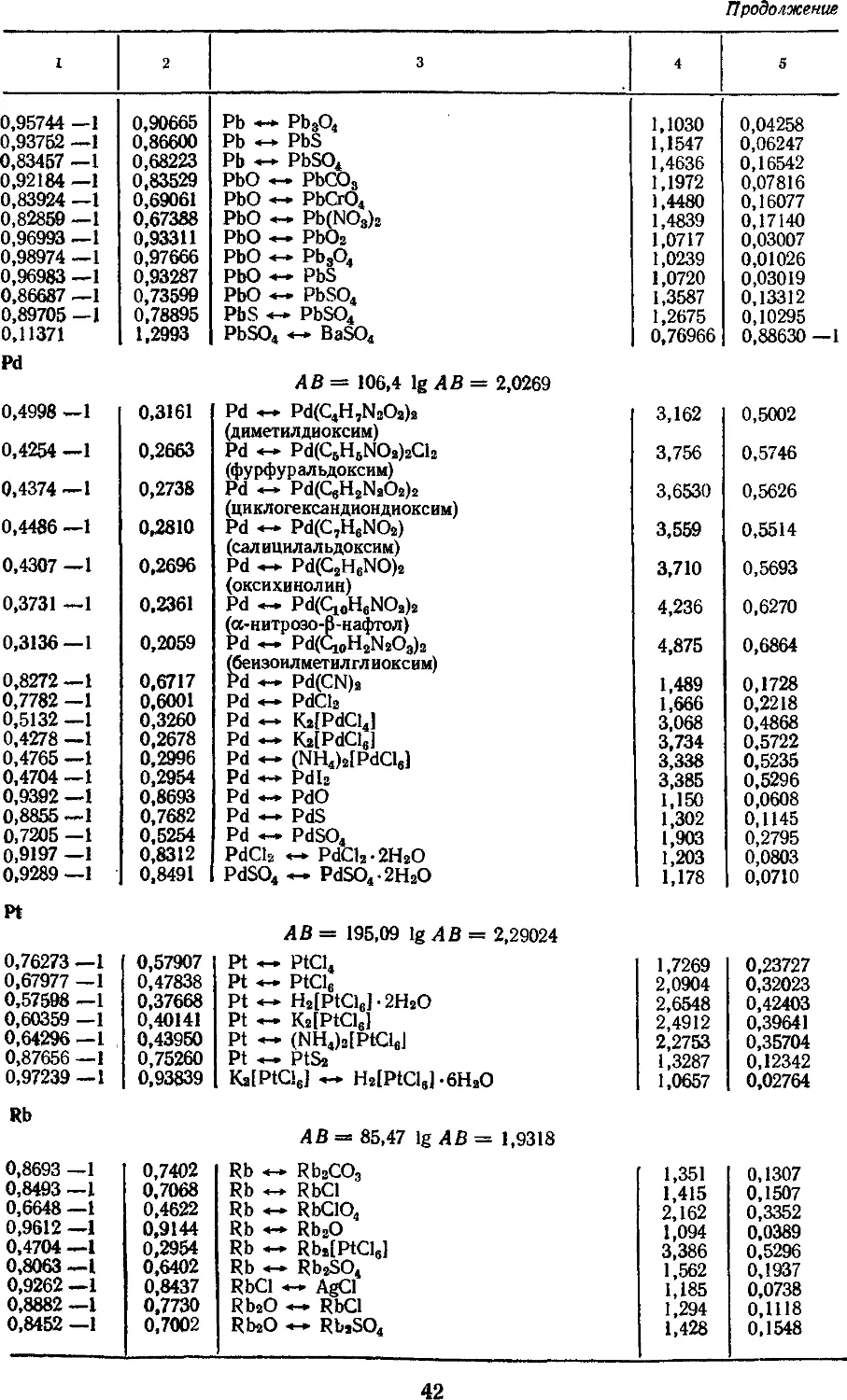
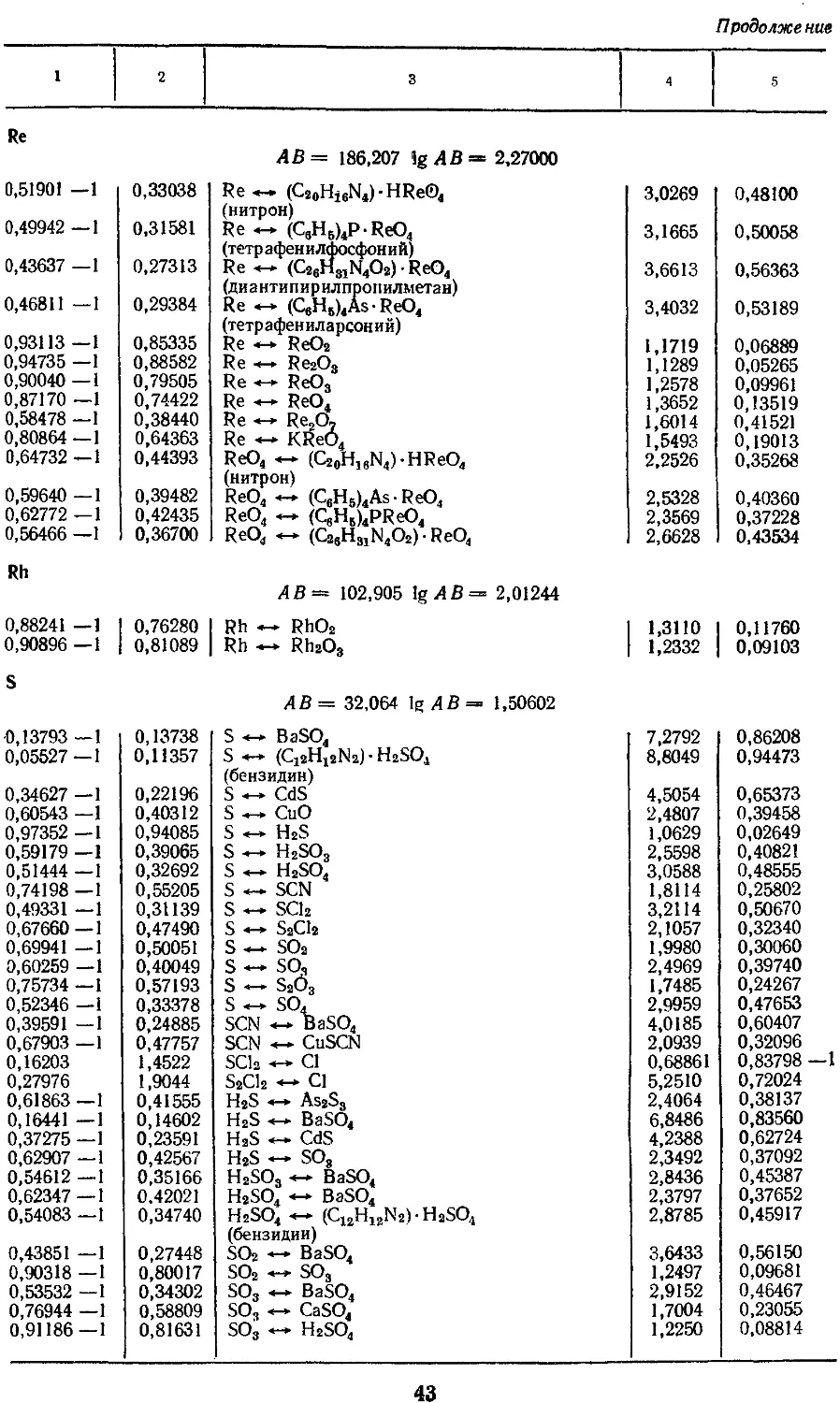
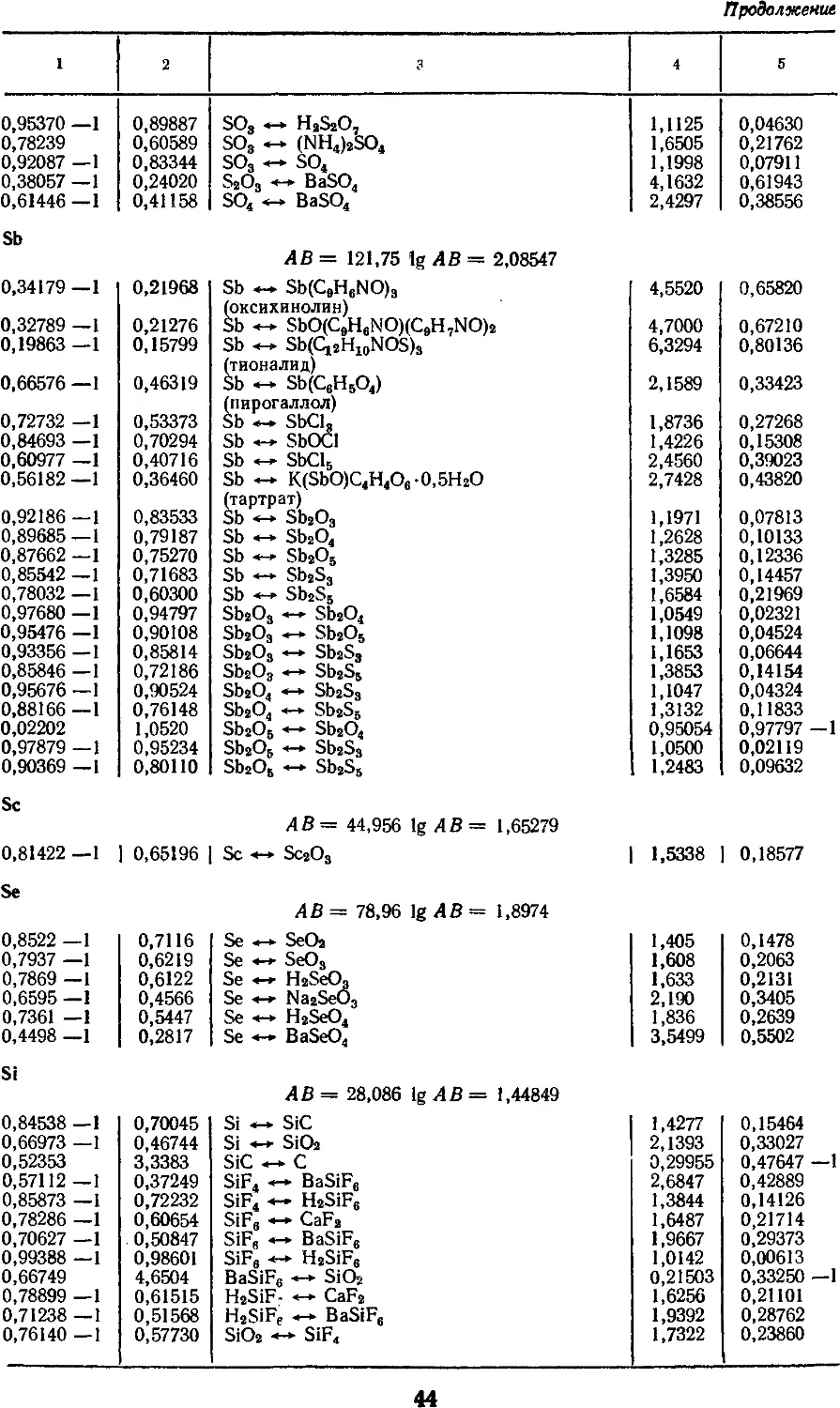
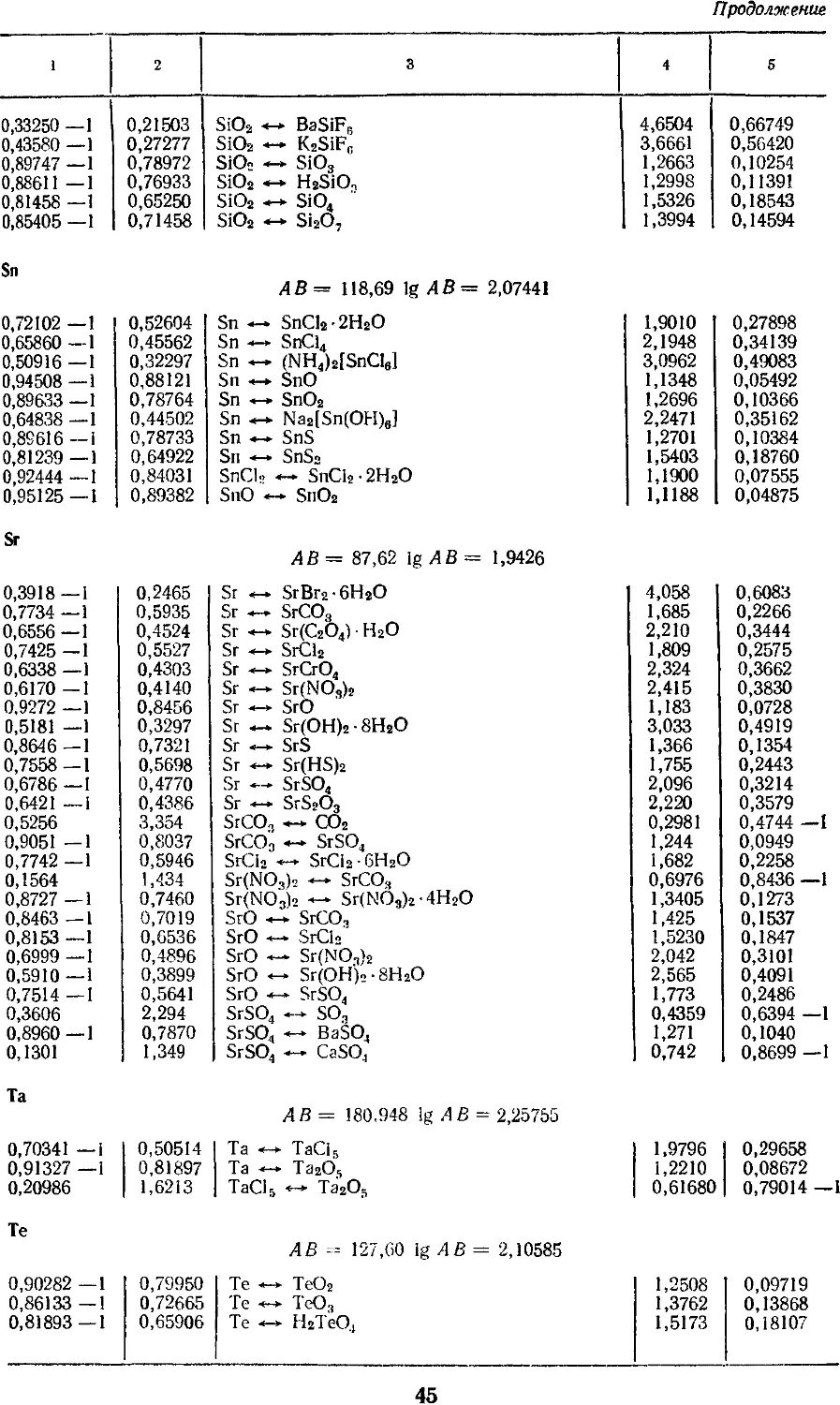
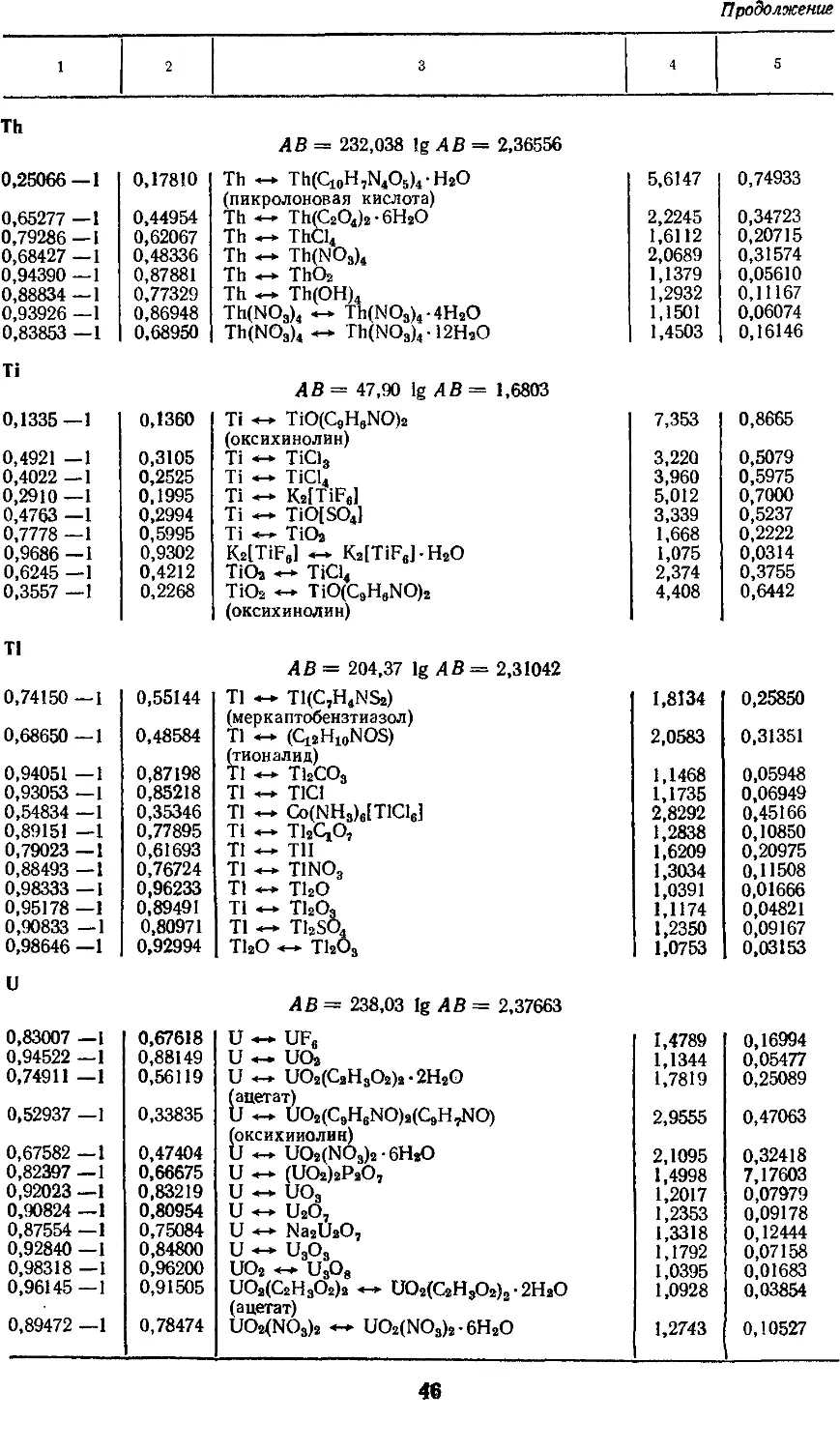
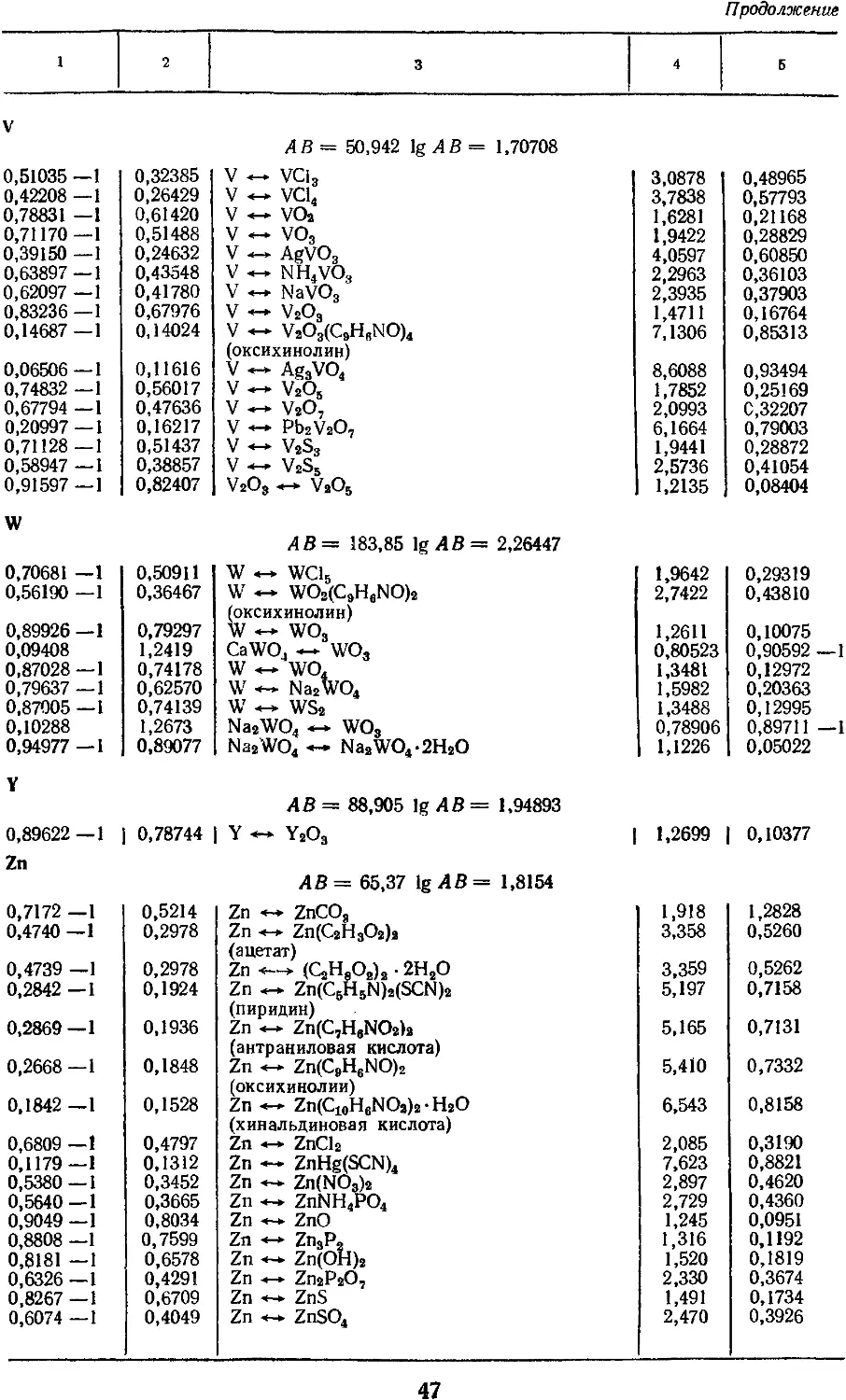
4. Факторы для пересчета химических
соединений 25
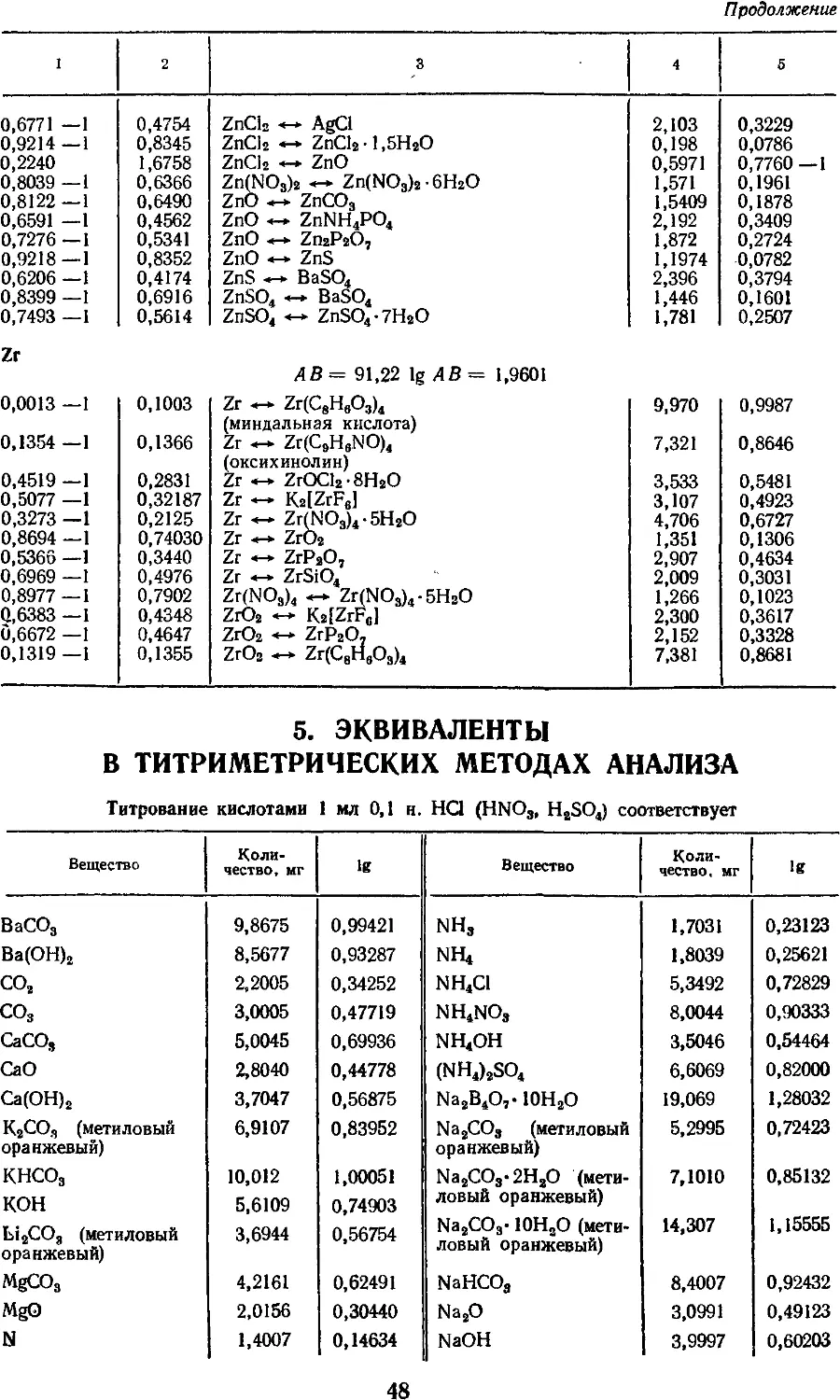
5. Эквиваленты в титриметрических
методах анализа 48
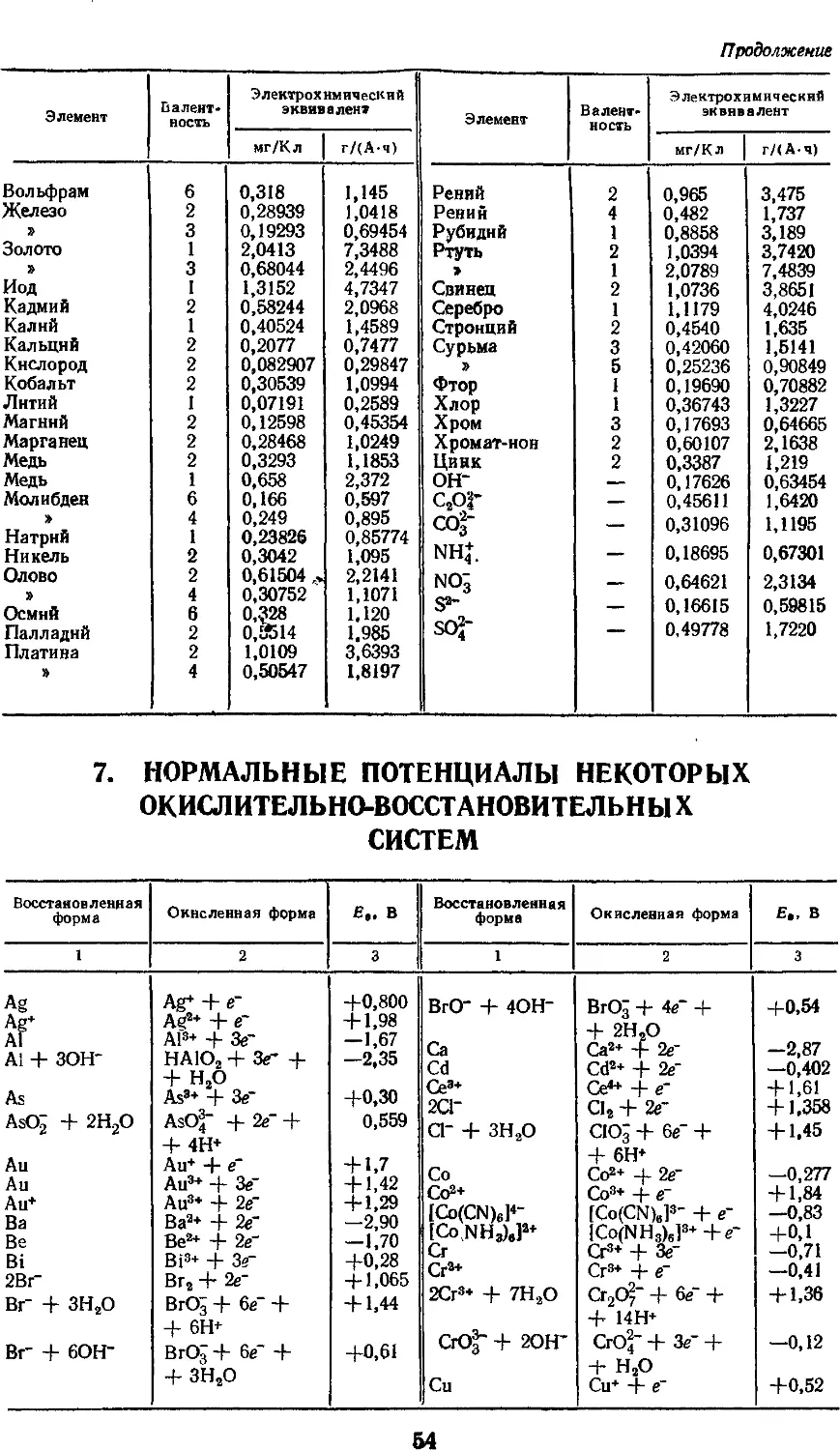
6. Электрохимические эквиваленты 53
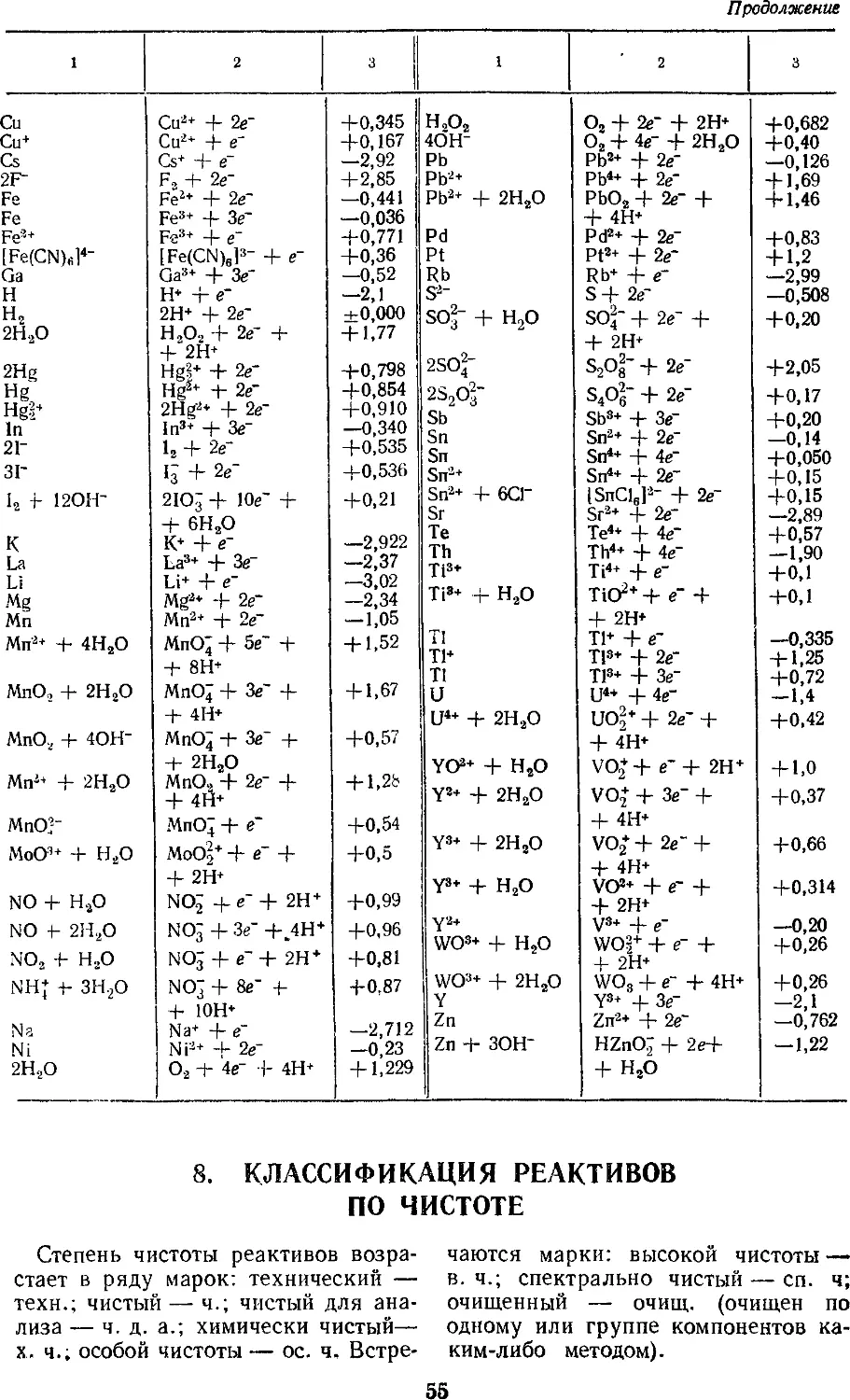
7. Нормальные потенциалы
некоторых
окислительно-восстановительных систем 54
8. Классификация реактивов по
чистоте 55
9. Характеристика некоторых
реактивов, применяемых в анализе
металлов 56
10. Рациональный ассортимент
органических реактивов для
определения неорганических ионов ... 66
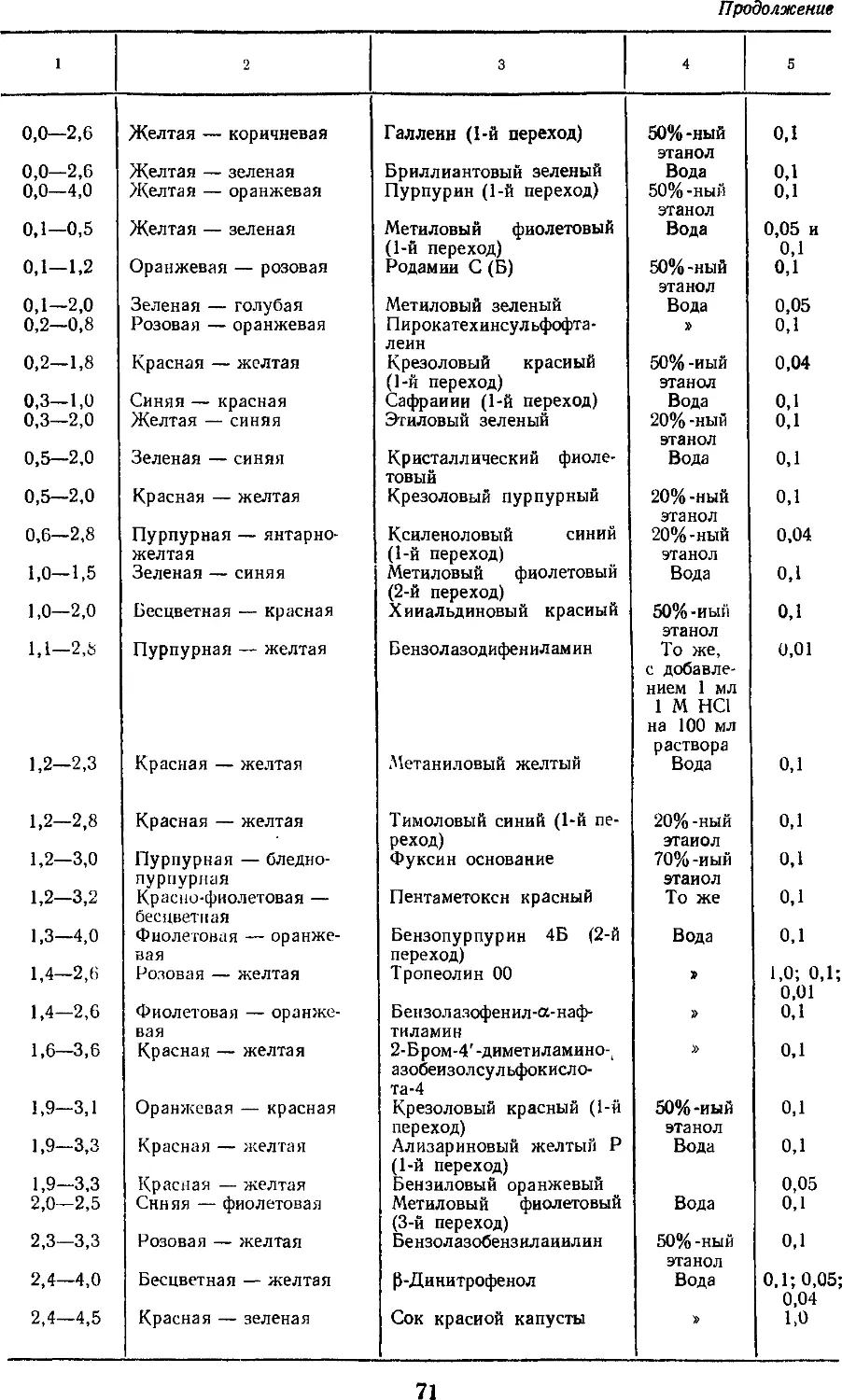
11. Индикаторы 70
11.1 Индивидуальные кислотно-
основные индикаторы ... 70
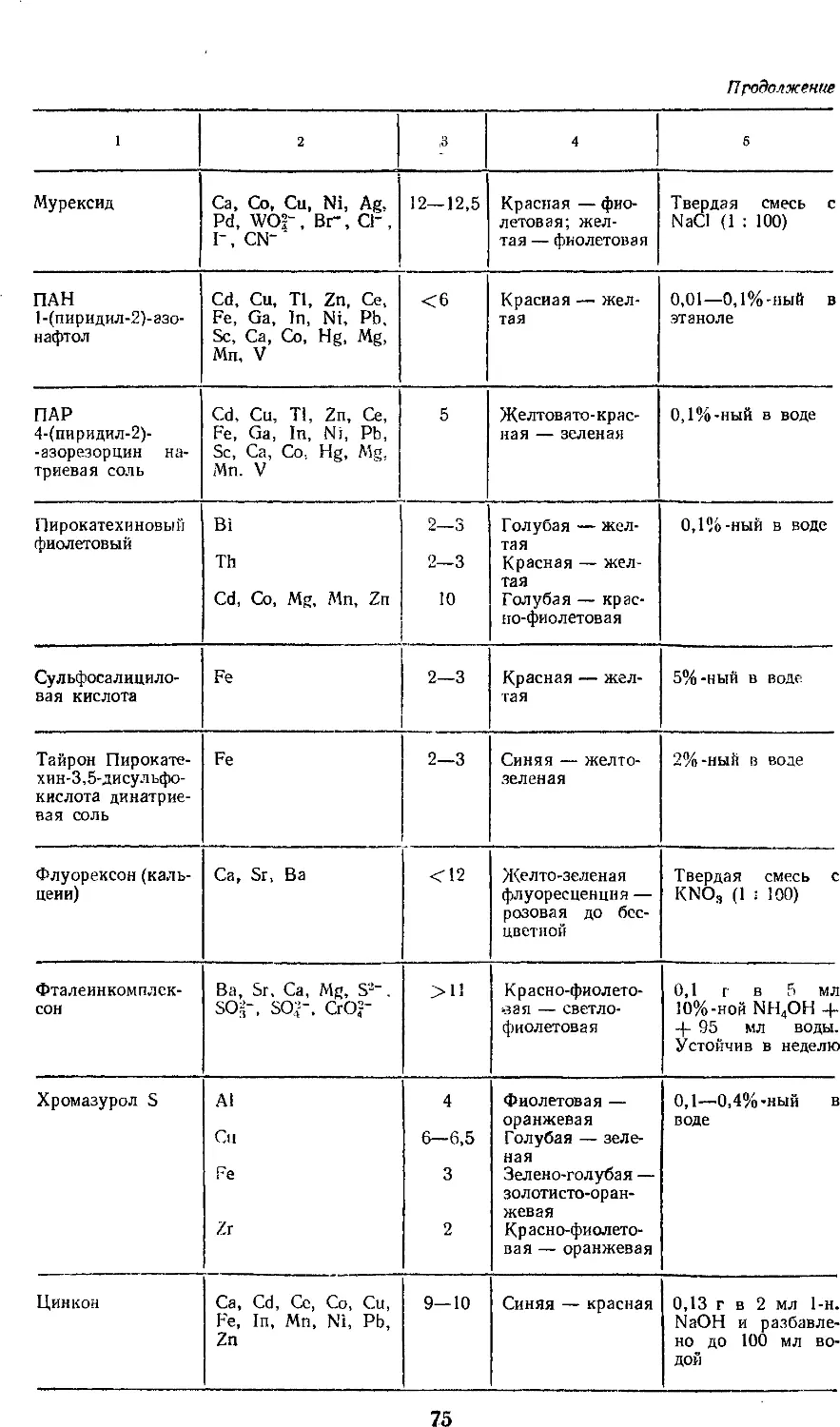
11.2. Индикаторы для комплекси-
метрического титрования 74
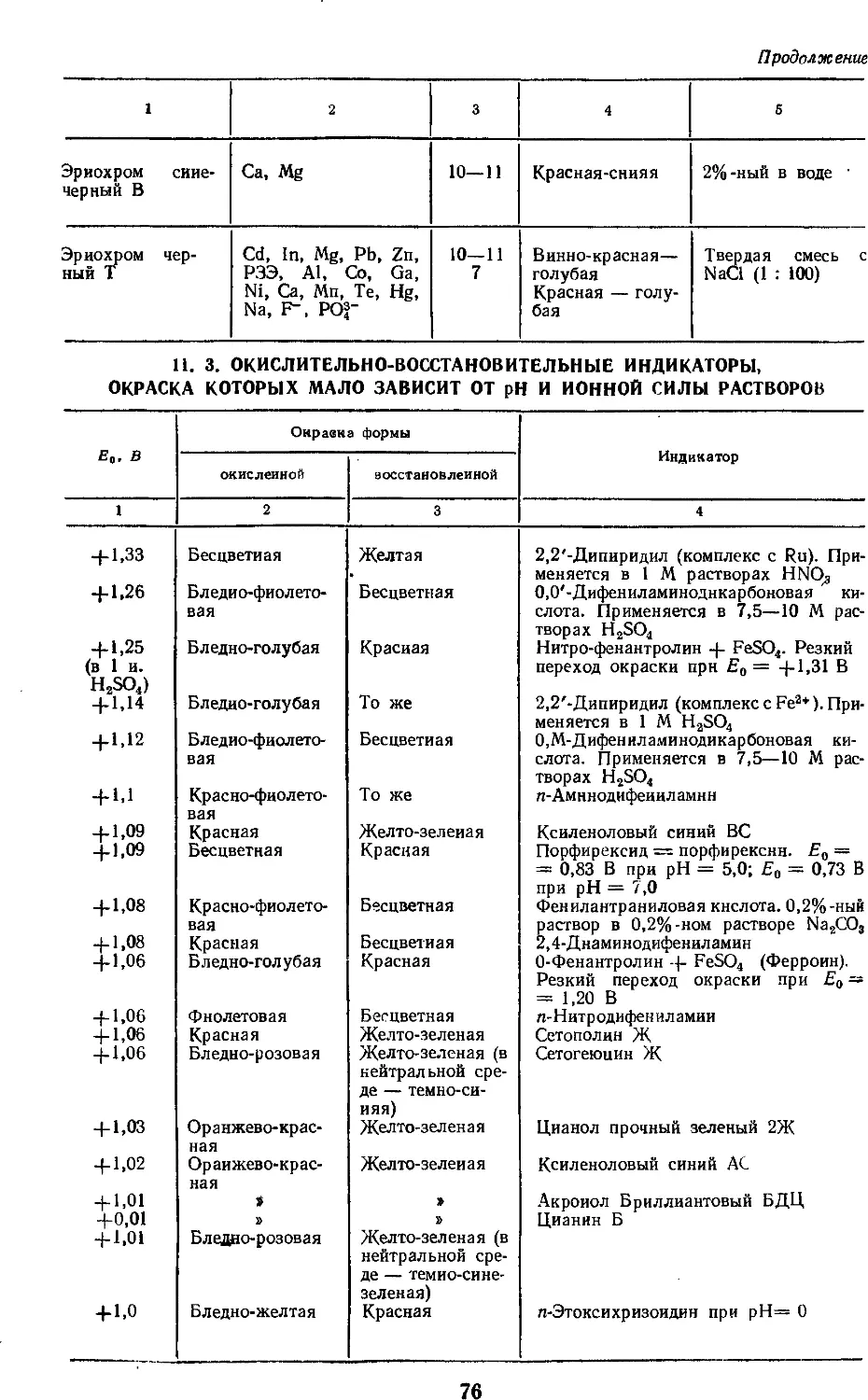
11.3. Окислительно -
восстановительные индикаторы,
окраска которых мало зависит от
рН и ионной силы
растворов 76
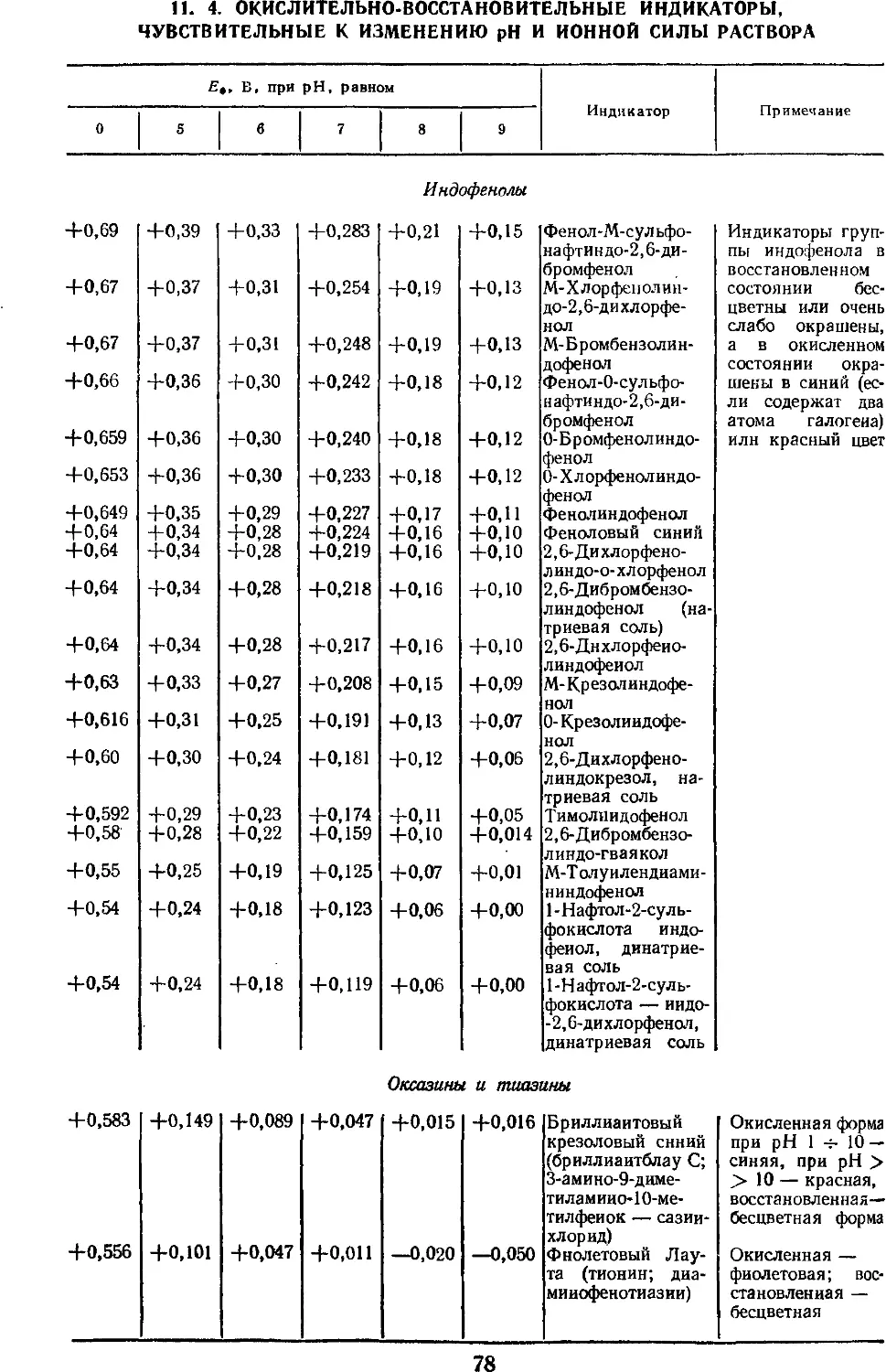
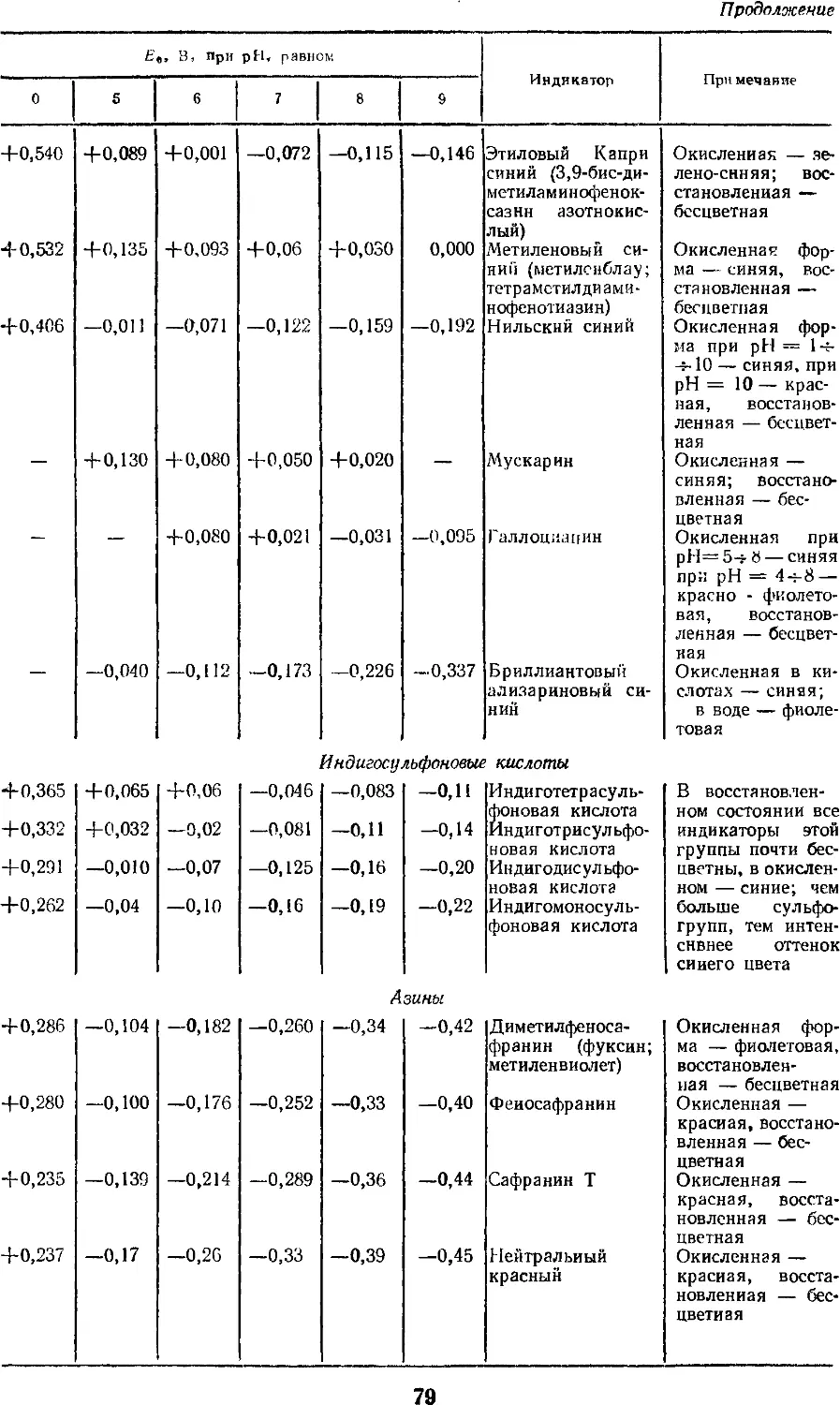
11.4. Окислительно -
восстановительные индикаторы,
чувствительные к изменению
рН и ионной силы' раствора 78
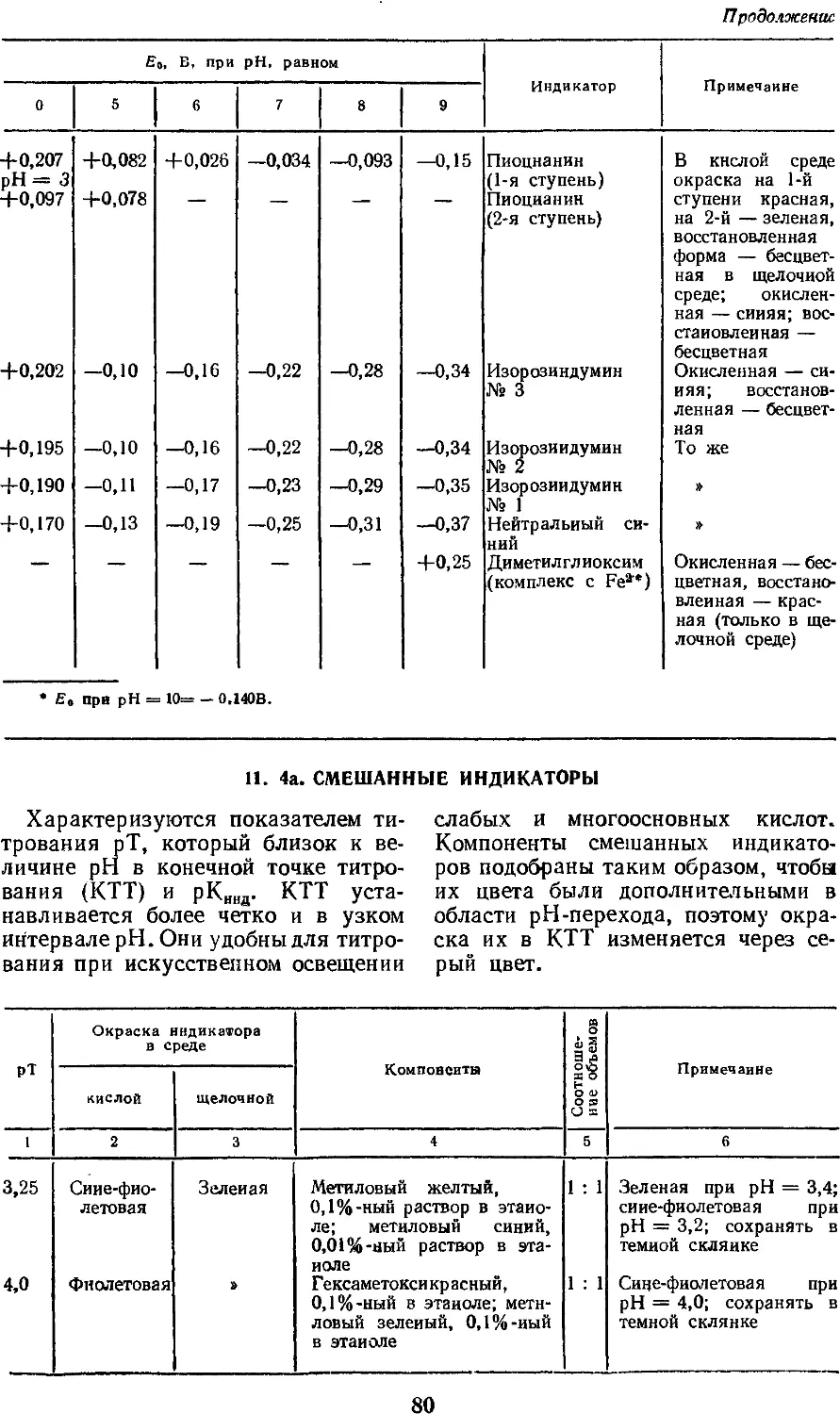
11.4а. Смешанные индикаторы. . 80
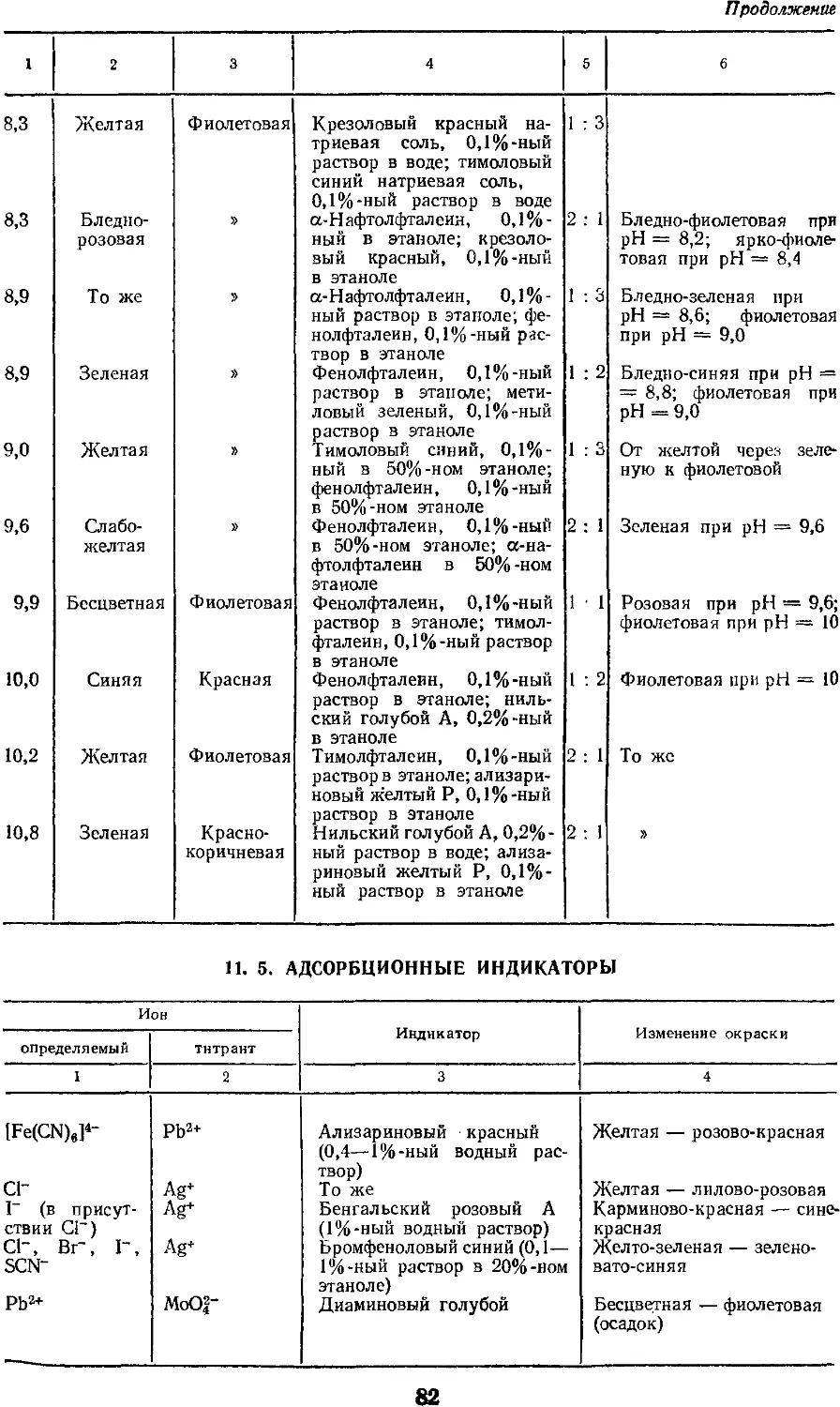
11.5. Адсорбционные индикаторы 82
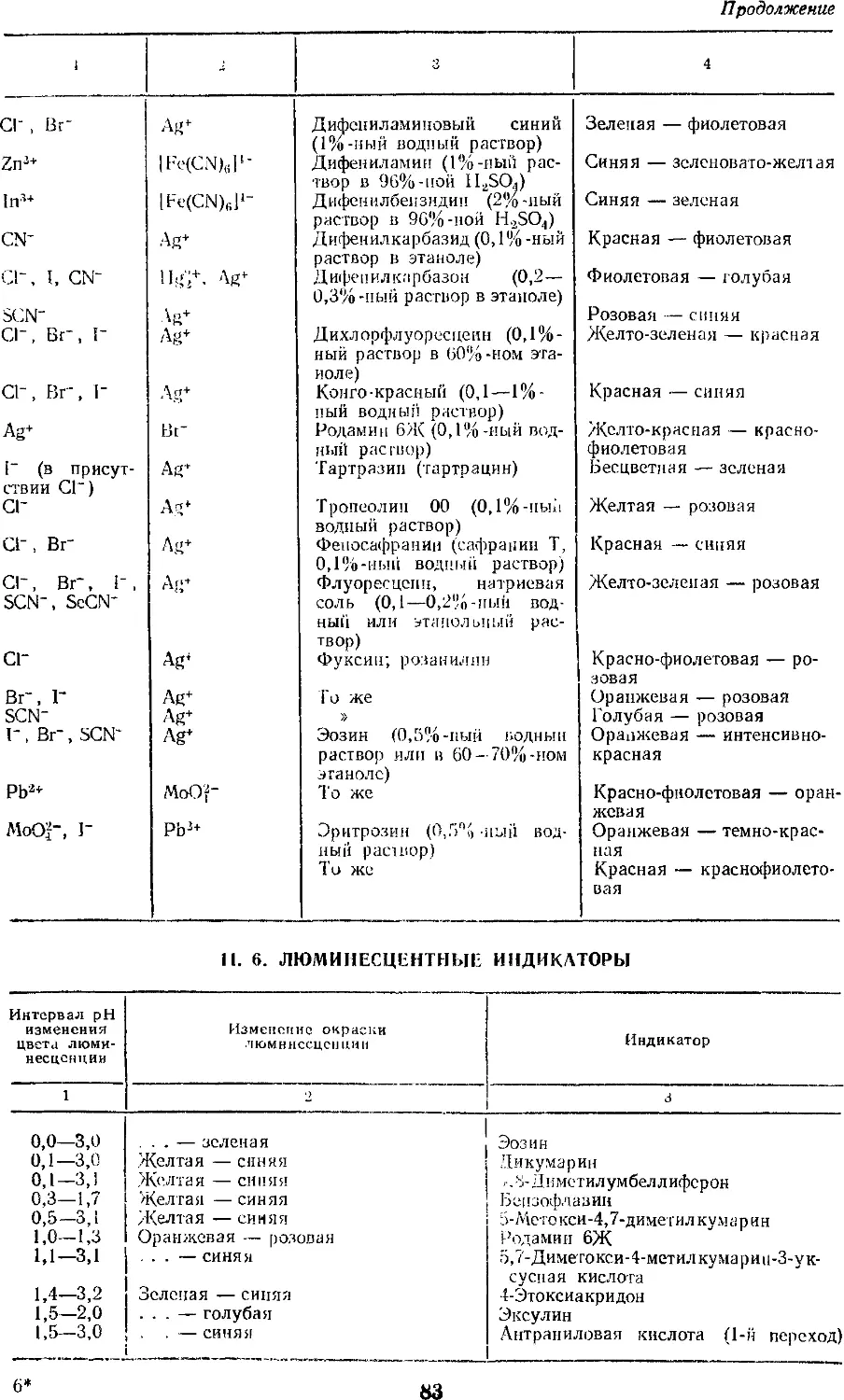
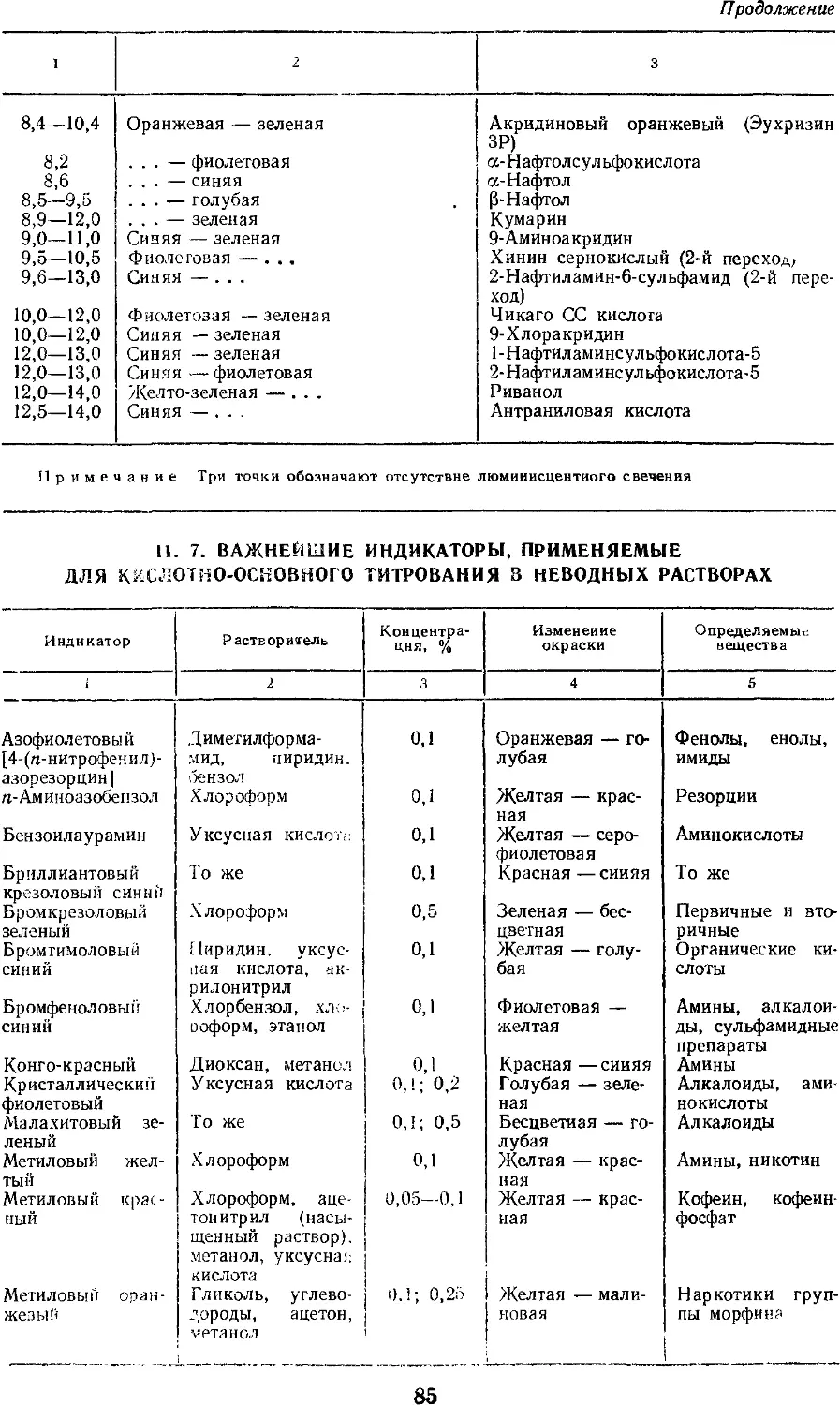
11.6. Люминесцентные индикаторы 83
11.7. Важнейшие индикаторы,
применяемые для кислотно-
основного титрования в
неводных растворах .... 85
11.8. Важнейшие индикаторы,
применяемые для
окислительно-восстановительного
титрования в неводных
растворах 86
12. Характеристика светопоглощения
растворителей и растворов
неорганических и
органических соединений 87
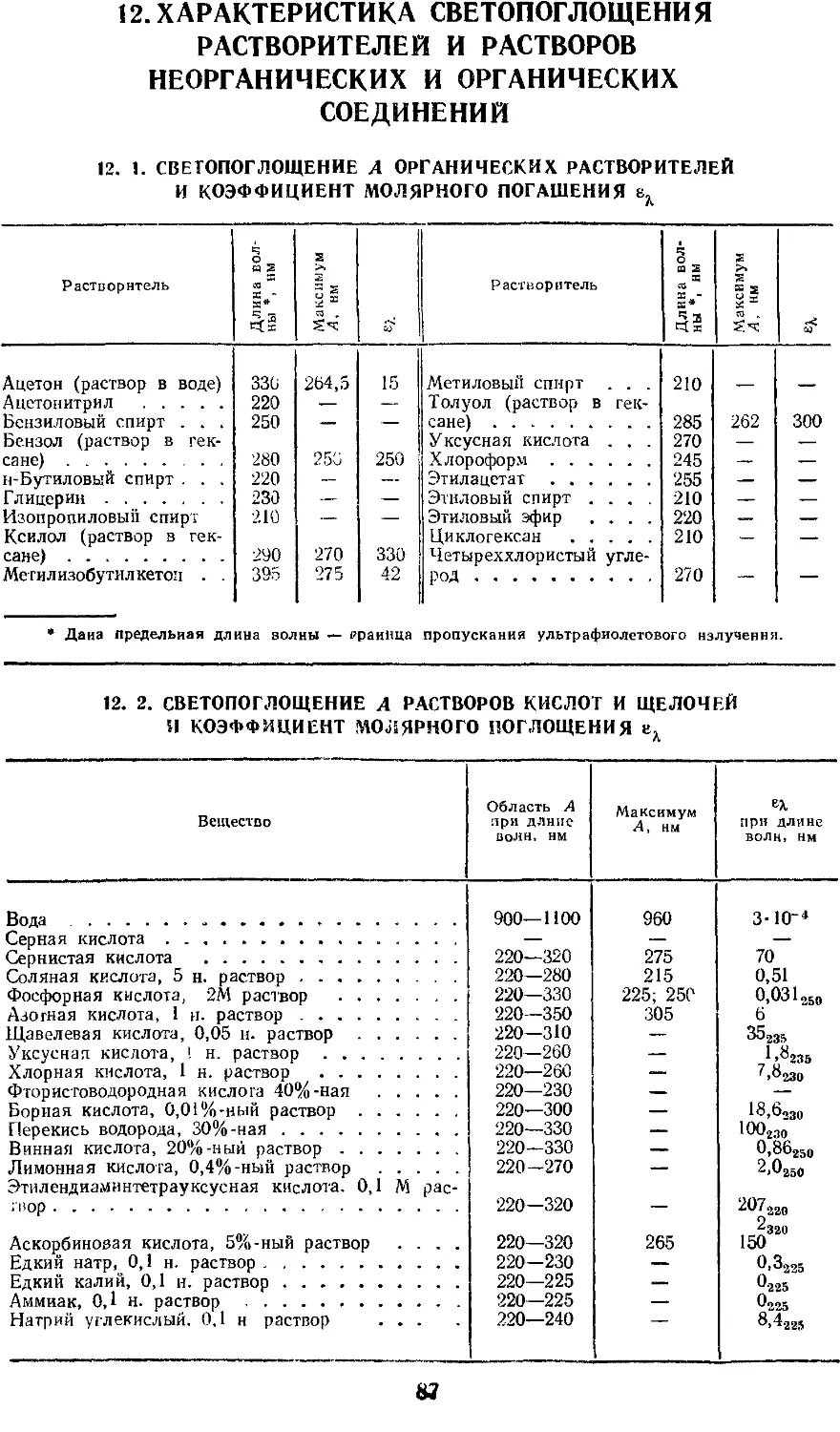
12.1. Светопоглощение А
органических растворителей и
коэффициенты молярного
погашения г% 87
12.2 Светопоглощение А
растворов кислот и щелочей и
коэффициент МОЛ%рВ01в ЙОГЕ-
шения £i 87
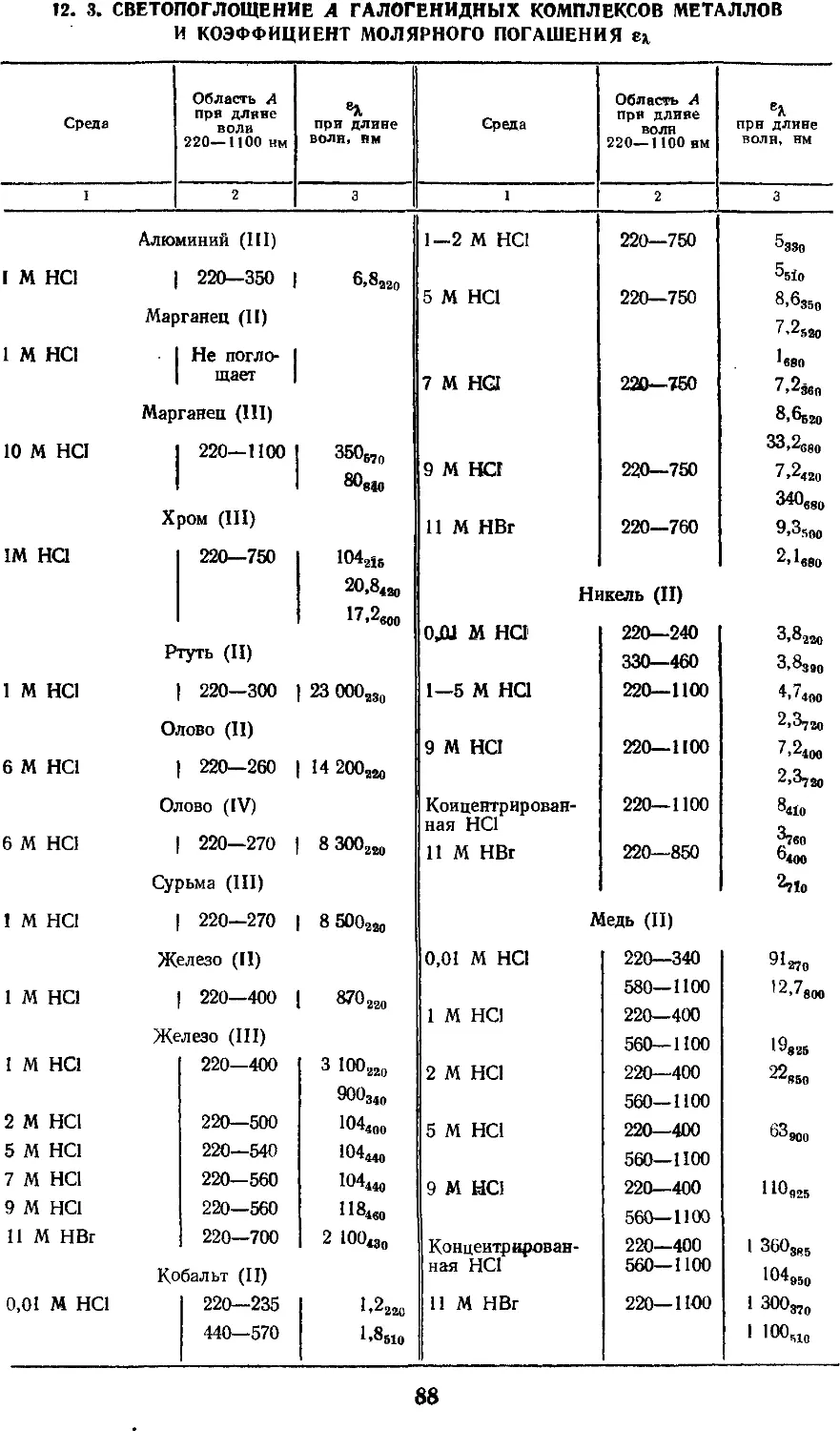
12.3. Светопоглощение А галоге-
нидных комплексов
металлов и коэффициенты
молярного погашения е\ . . . .
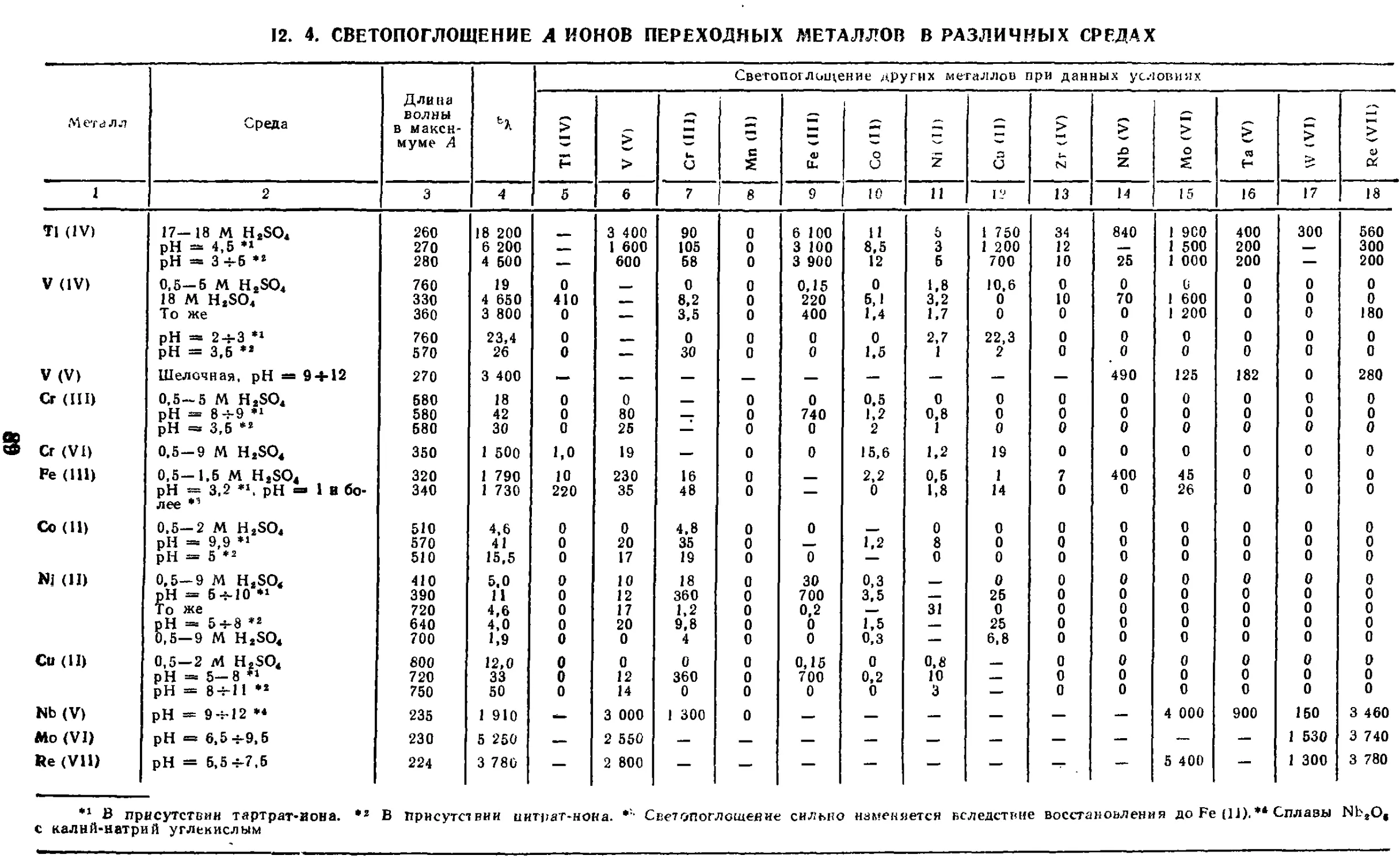
12.4. Светопоглощение А ионов
переходных металлов в
различных средах . . • . . .
13. Групповое разделение элементов
13.1. Выделение элементов на
ртутном катоде
13.2. Осаждение окисью цинка
13.3. Осаждение ацетатным
буферным раствором при
рН = 5,3
13.4. Осаждение янтарнокислым
(сукцинатным) буферным
раствором при рН = 4,2-=-4,6
13.5. Осаждение гексаметиленте-
траминовым (уротропино-
вым) буферным раствором
при рН = 5,4
13.6. Осаждение по Э. А.
Остроумову
13.7. Осаждение бензоатом
аммония
13.8. Осаждение купфероиом и
неокупфероном (среда 0,6—
2-н. соляная кислота или
1,8—5-н. серная кислота)
13.9. Осаждение арсоновыми
кислотами
13.10. Осаждение 8-оксихиноли-
ном рН полного осаждения
оксихинолинатов металлов
13.11. Осаждение элементов при
выпаривании с хлорной
кислотой
13.12. Осаждение тетрафенилар-
сонием (при любых
значениях рН)
13.13. Экстракционные методы
группового разделения
элементов
13.13.1. Экстракция
неорганических соединении ....
13.13.2. Экстракция хелатов . . .
14. Краткая характеристика наиболее
распространенных спектрофотоме-
трических методов определения
металлов
15. Маскирующие реагенты для
металлов и некоторых анионов . . .
16. Рациональные величины в
химическом анализе
16.1. Гравиметрический метод
анализа
16.2. Титриметрический метод
анализа
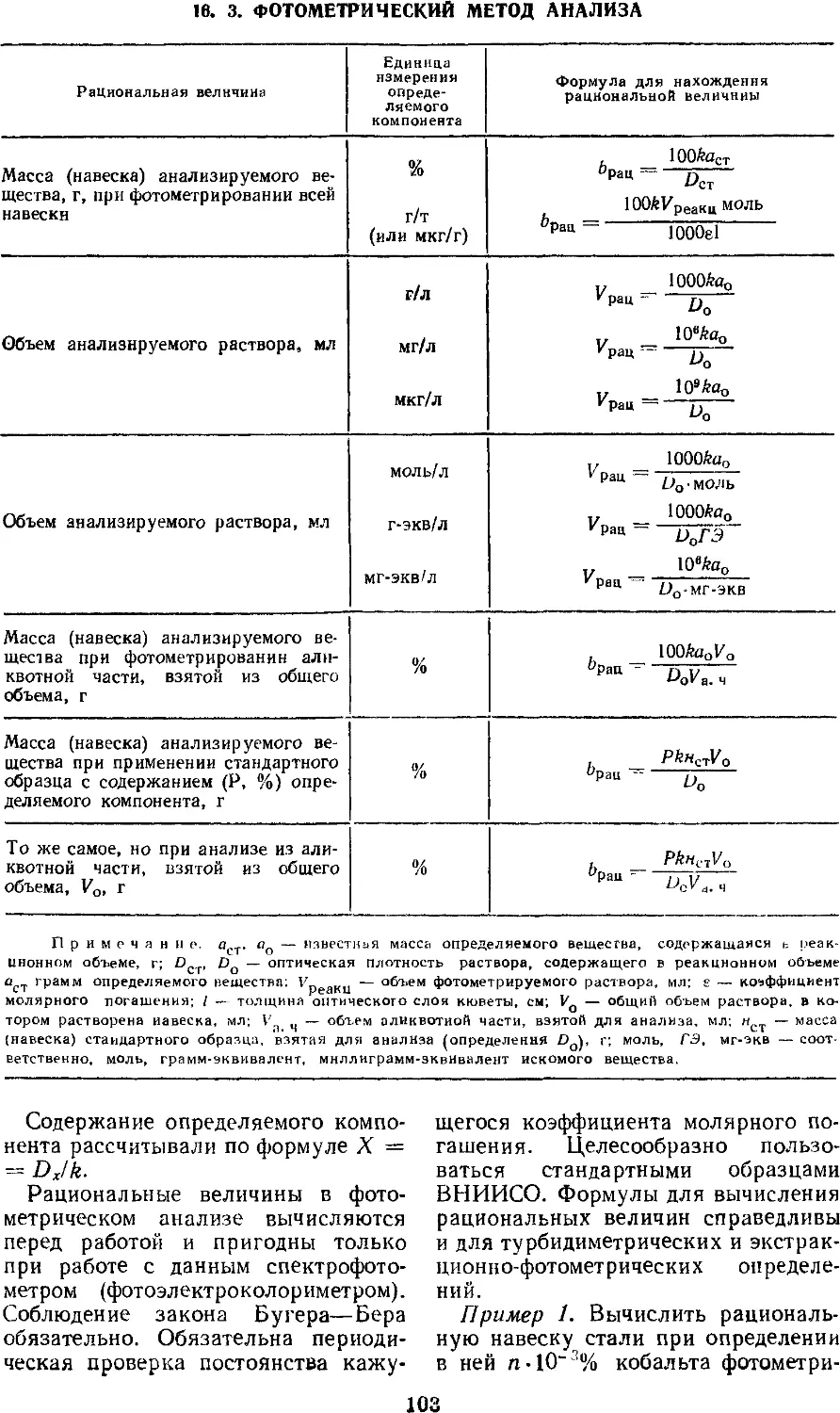
16.3. Фотометрический метод
анализа
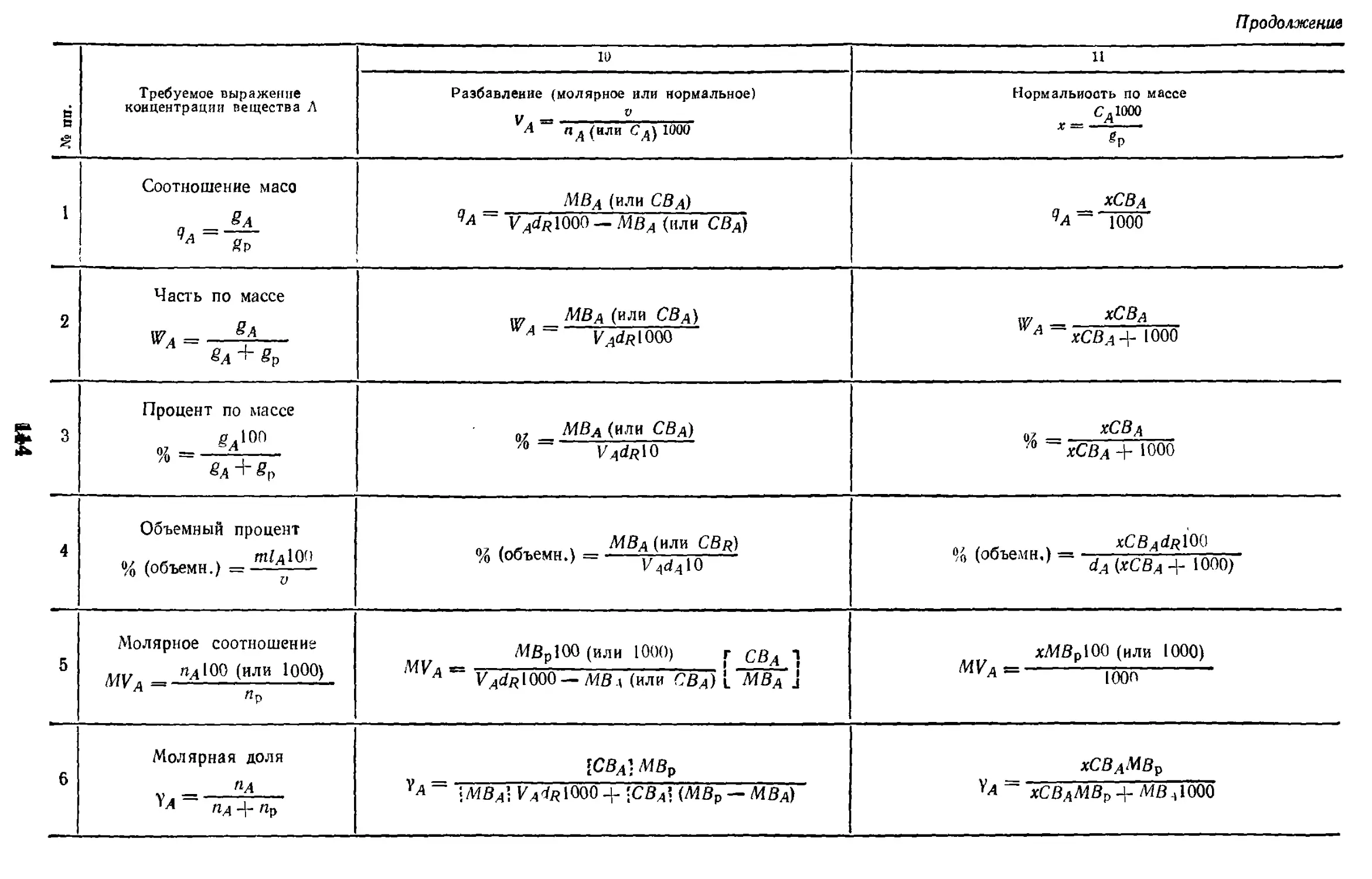
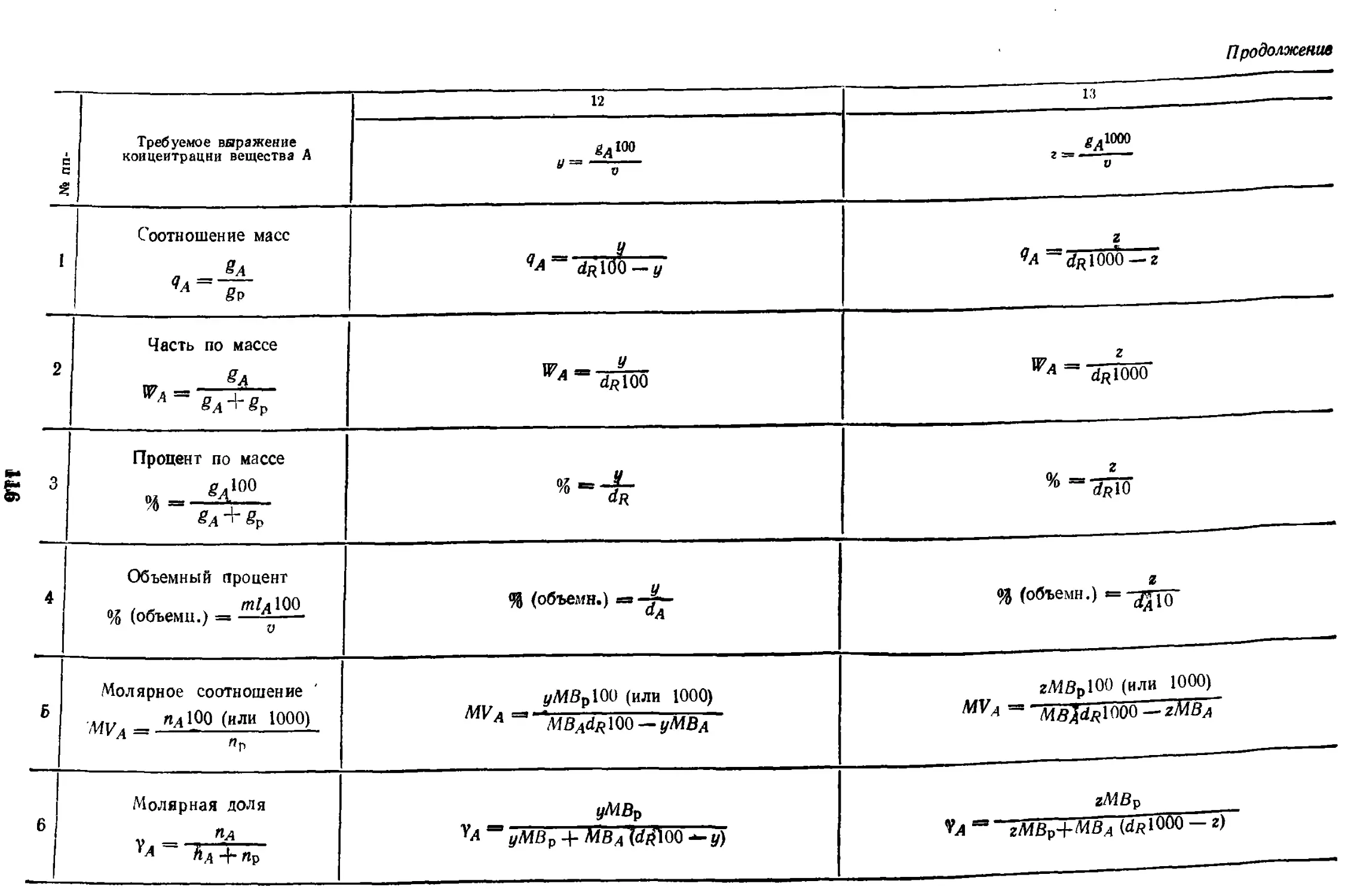
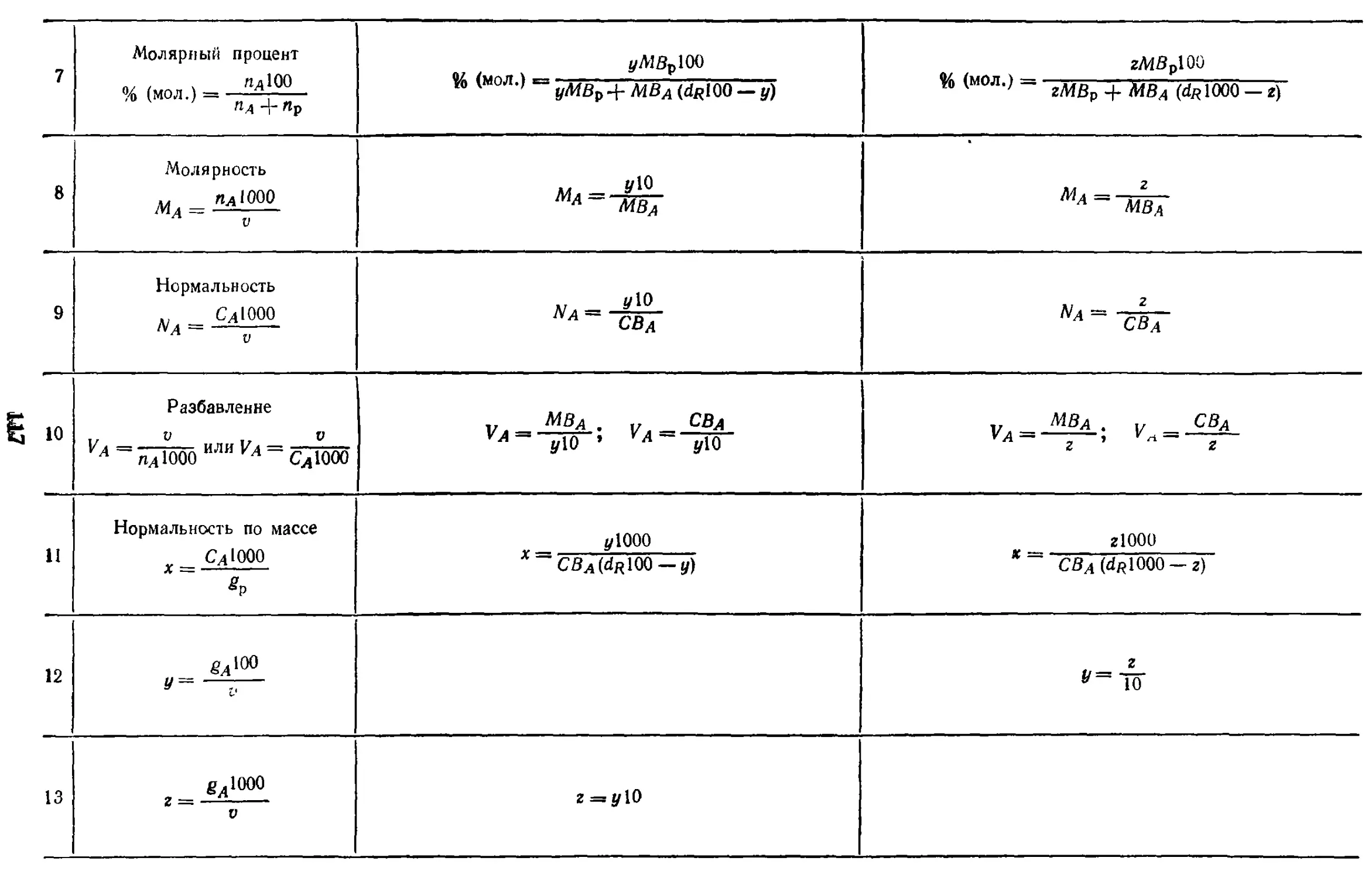
17. Растворы
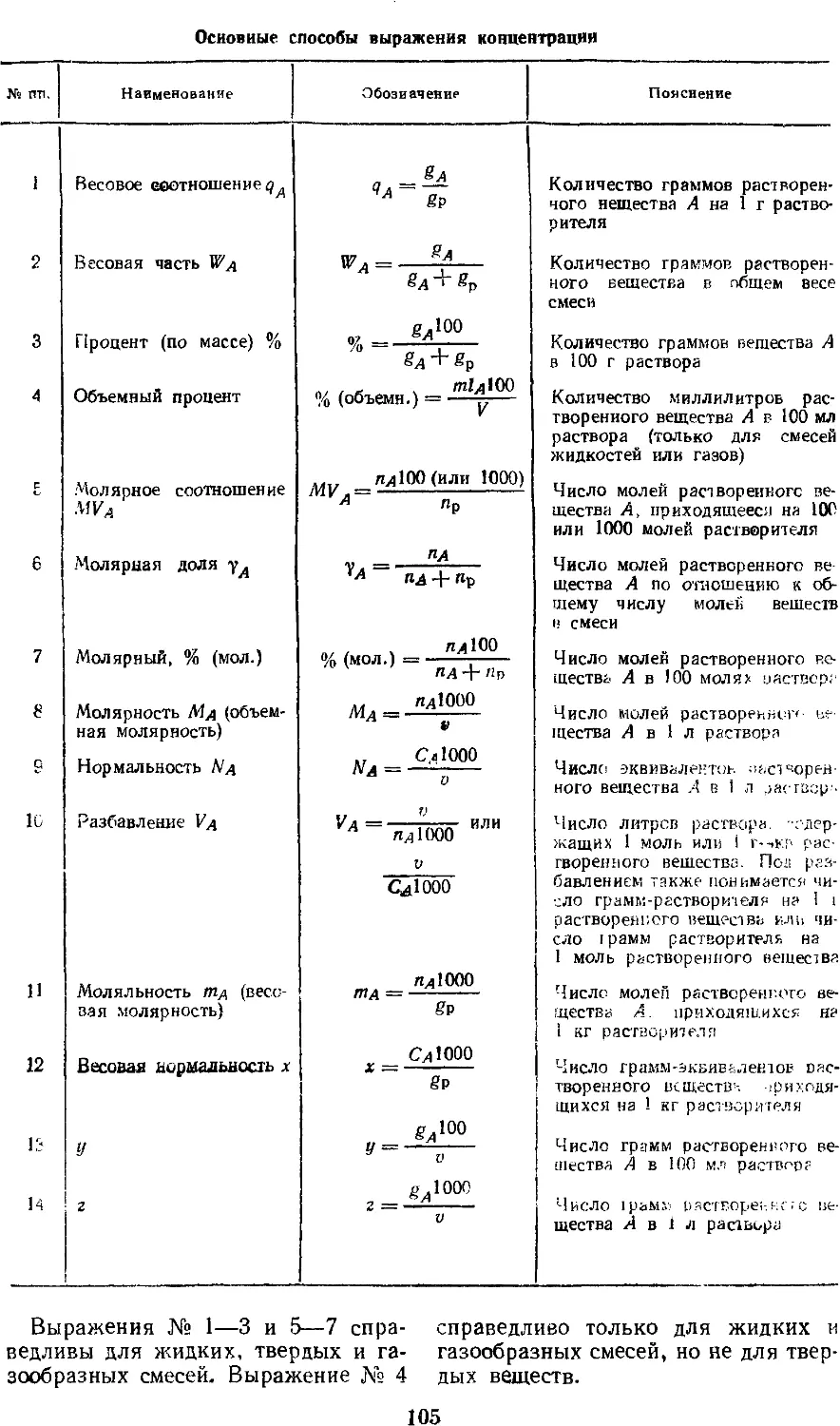
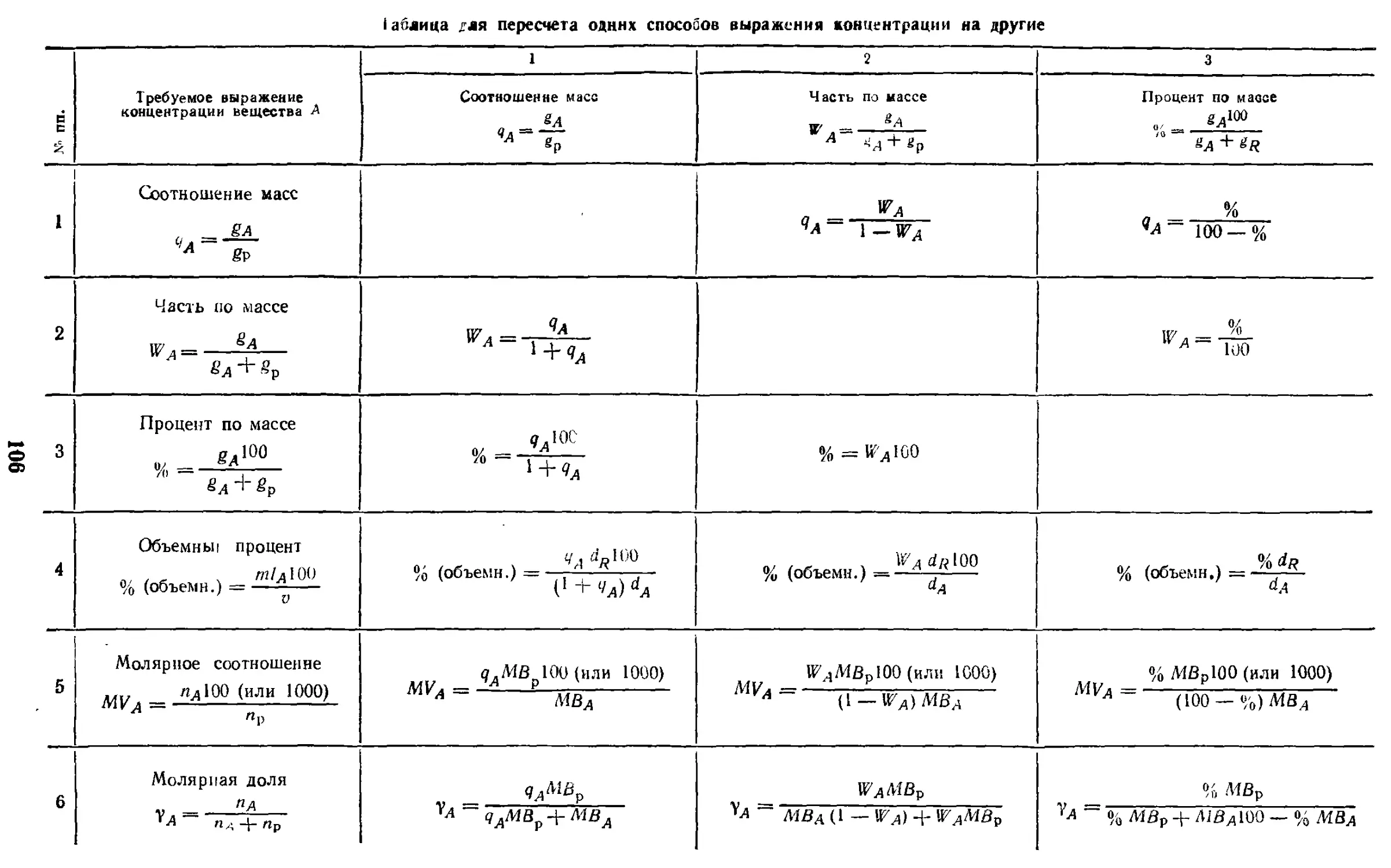
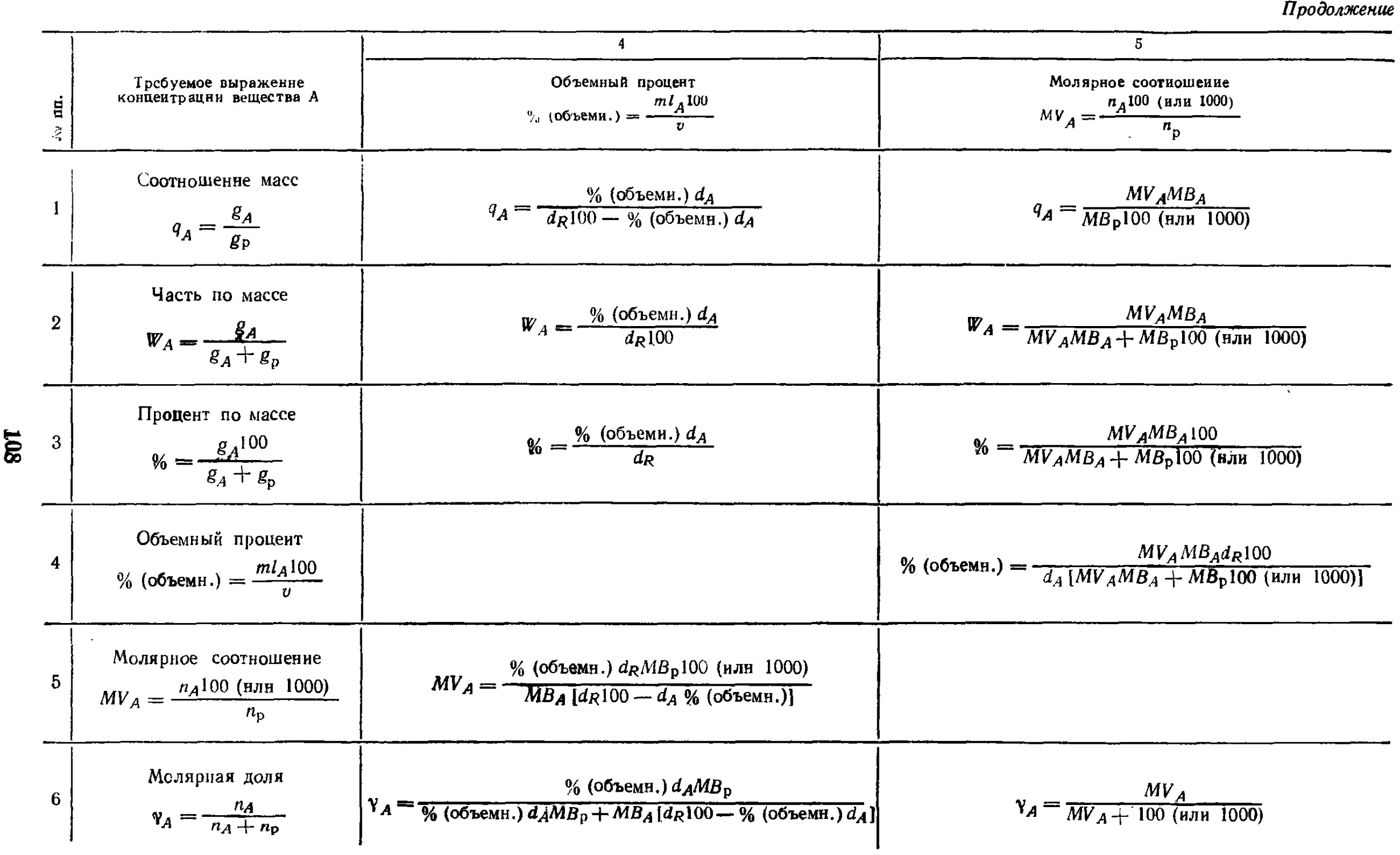
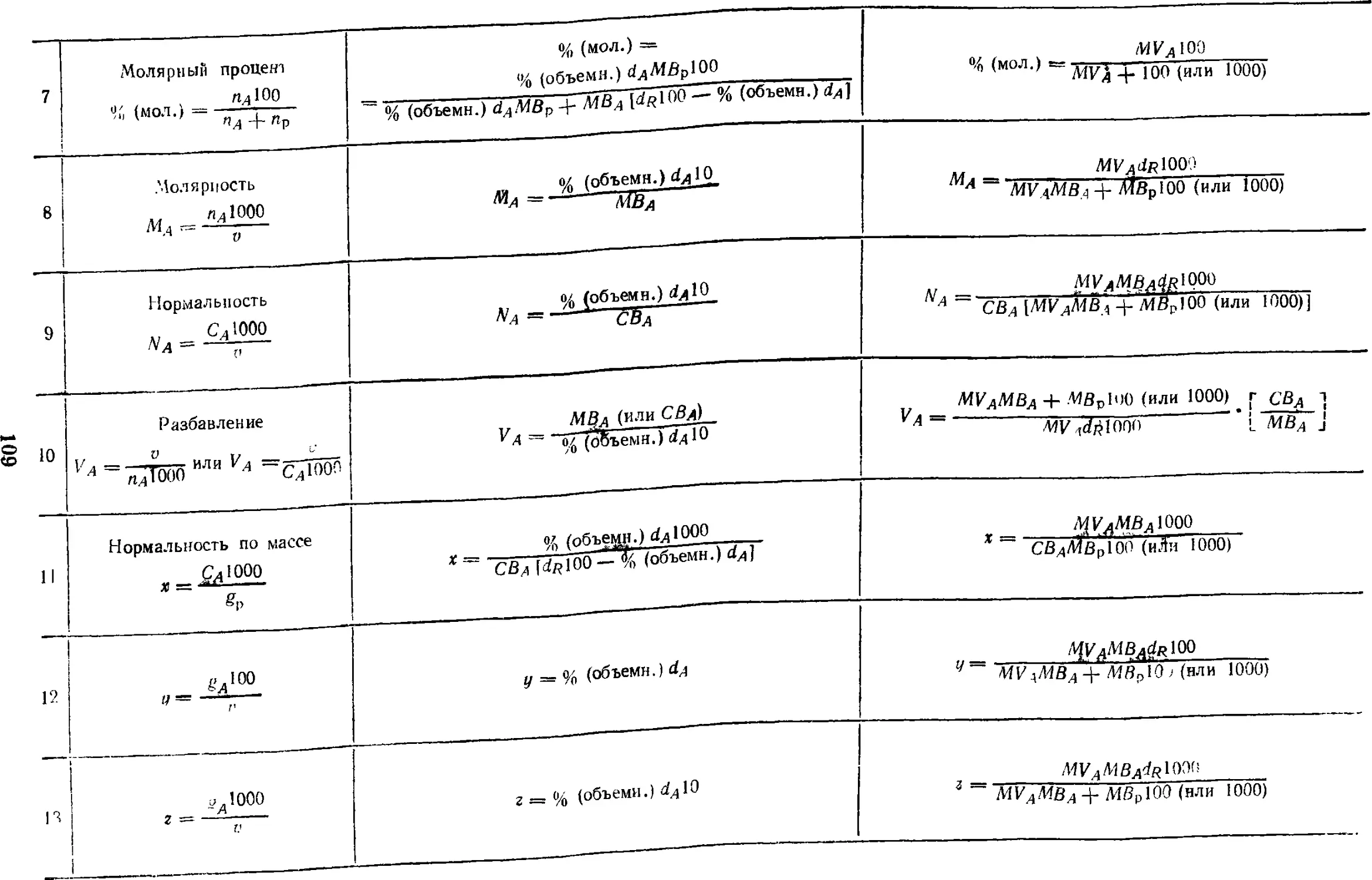
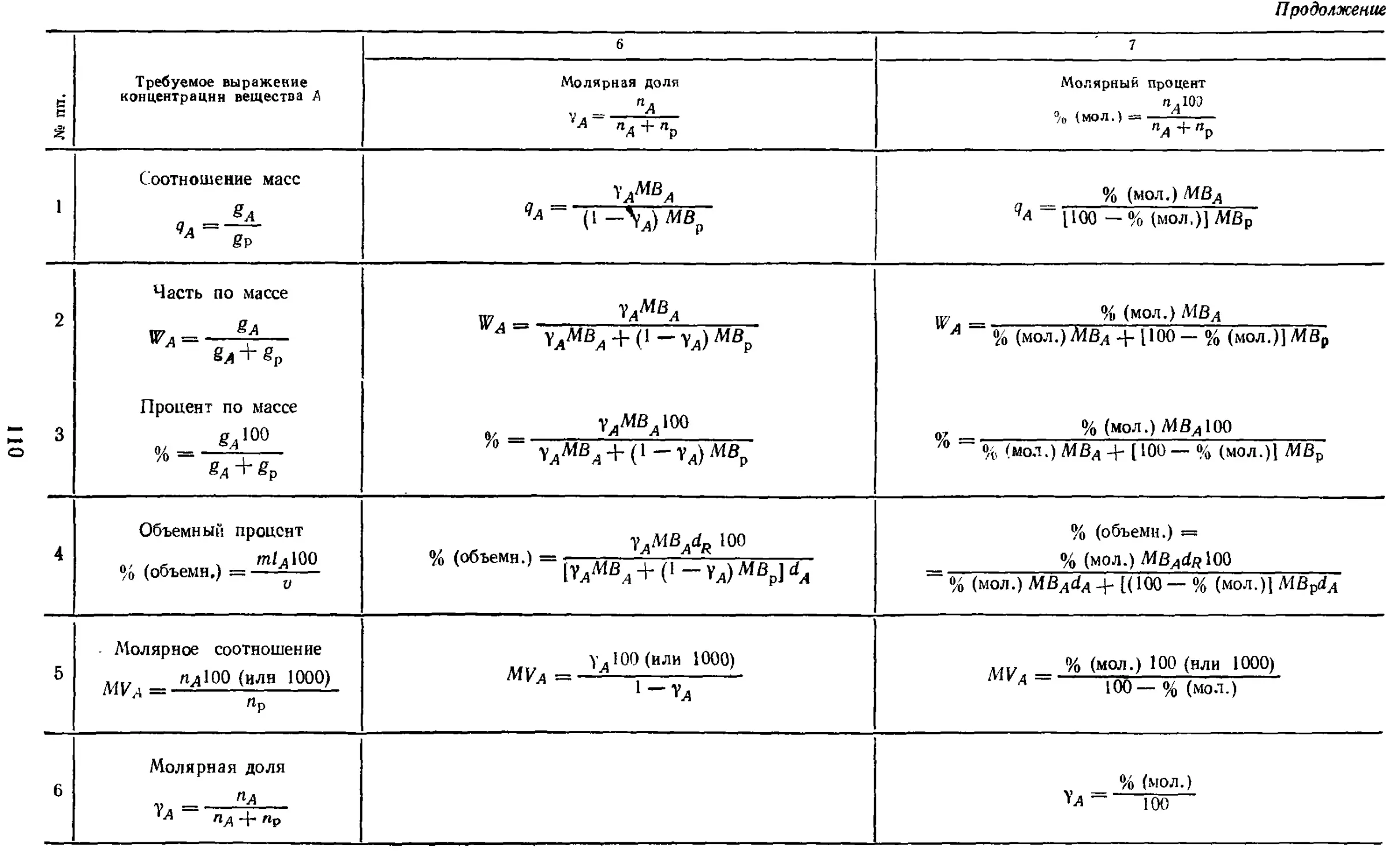
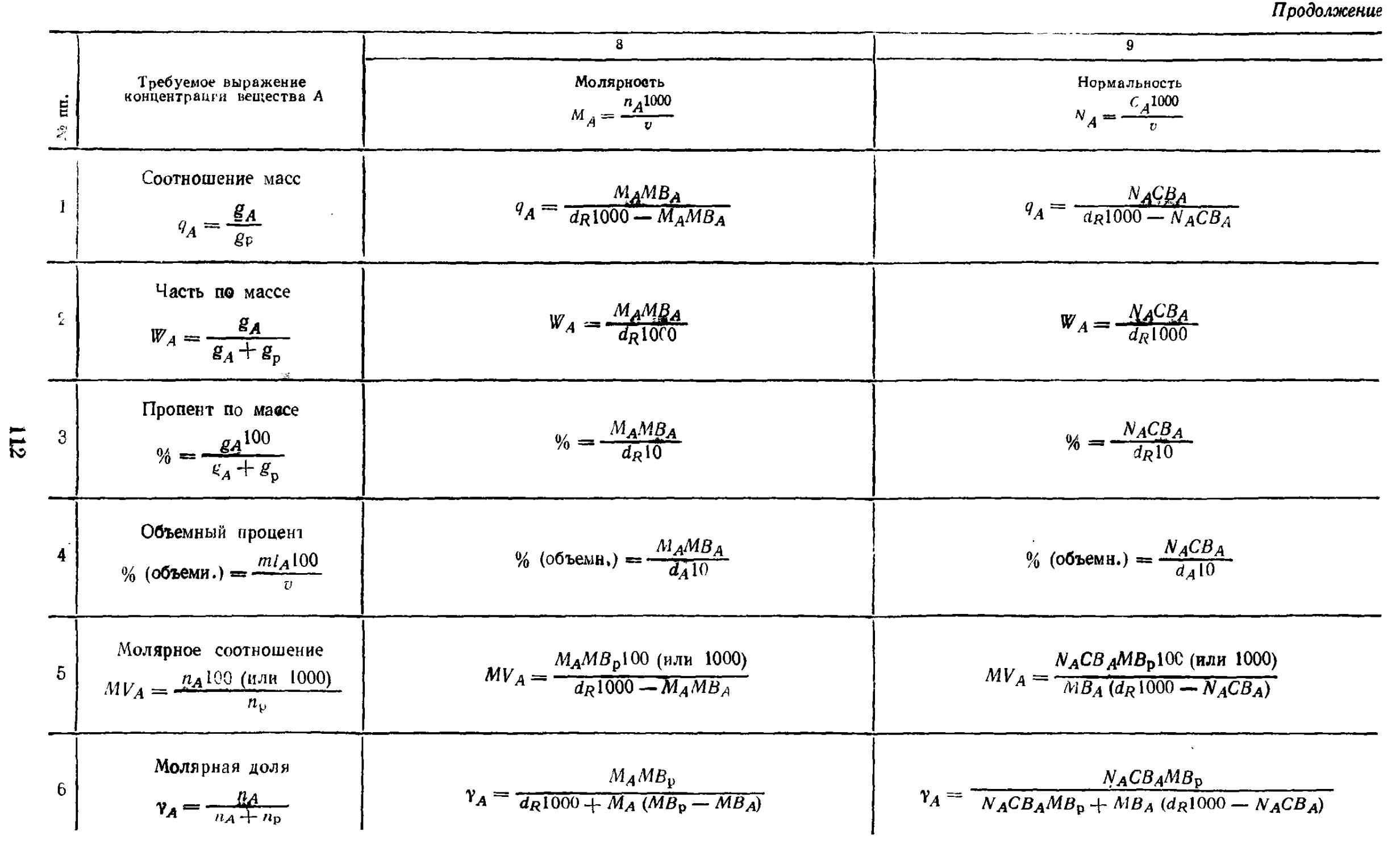
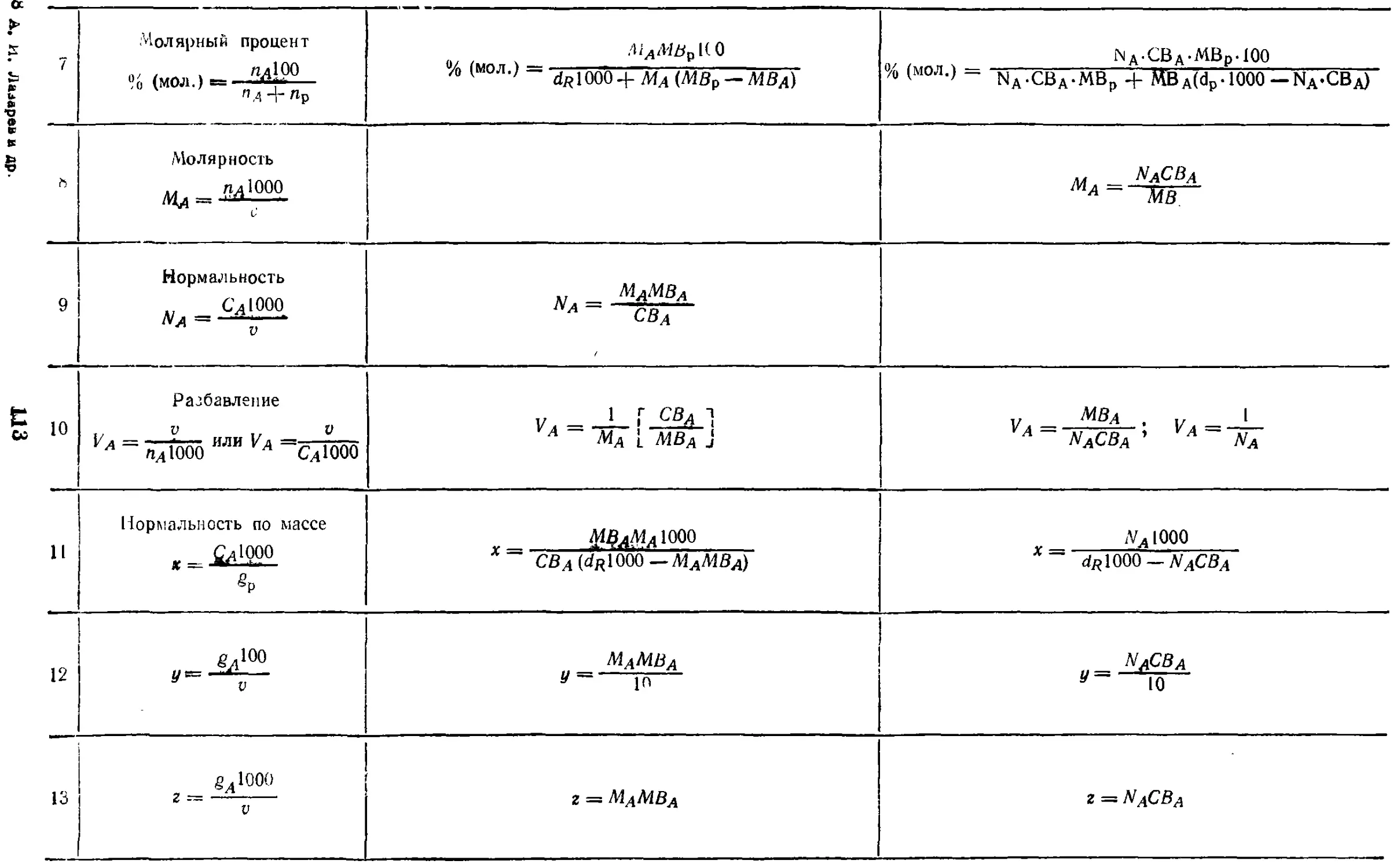
17.1. Способы выражения
концентрации и формулы
пересчета
17.2. Приготовление
стандартных (эталонных) растворов
(концентрация 10~2 М) 118
17.3. Способы перевода металлов
и некоторых их соединений
в раствор 130
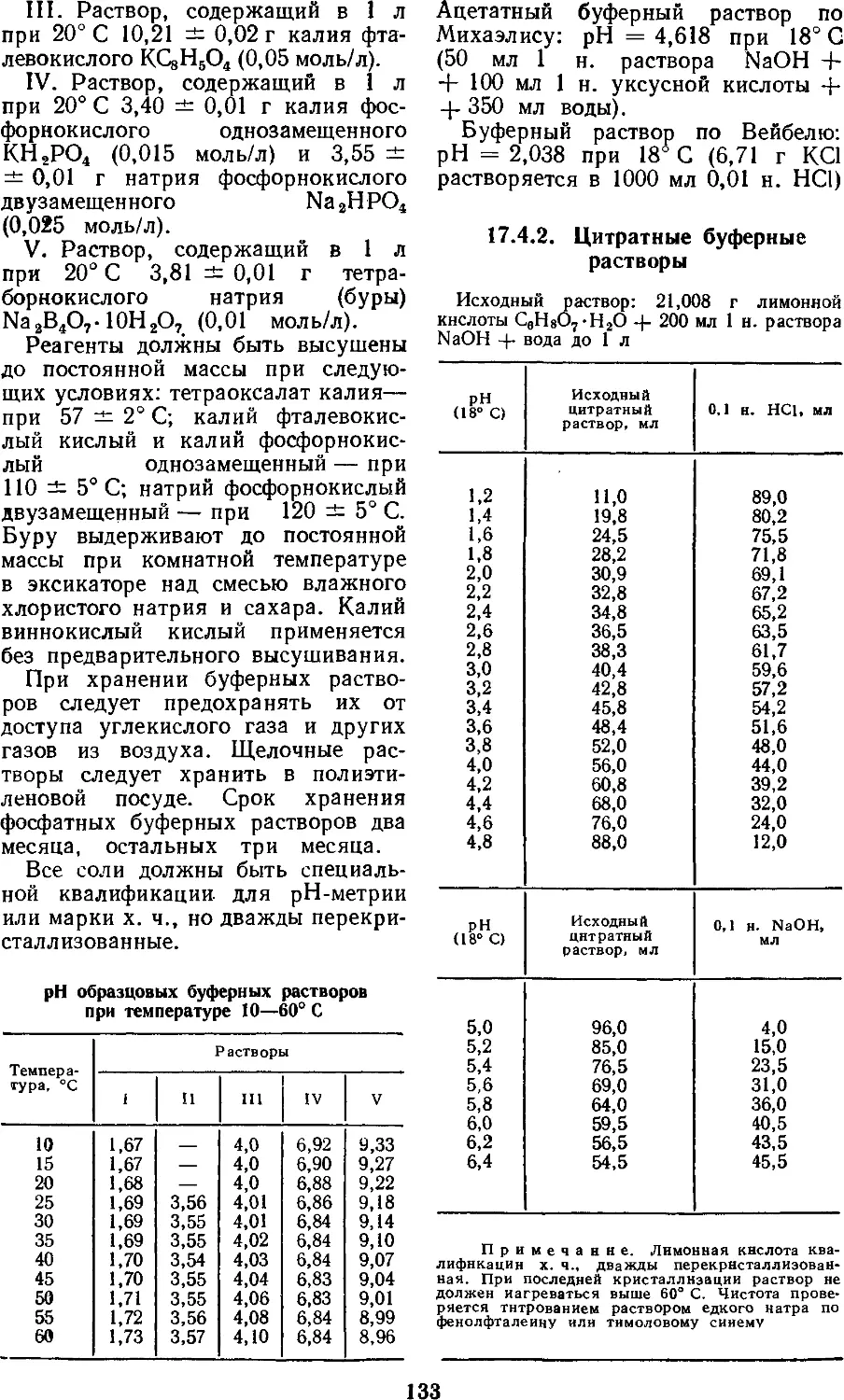
17.4. Буферные растворы ... 132
17.4.1. Образцовые
буферные растворы 132
17.4.2. Цитратные
буферные растворы 133
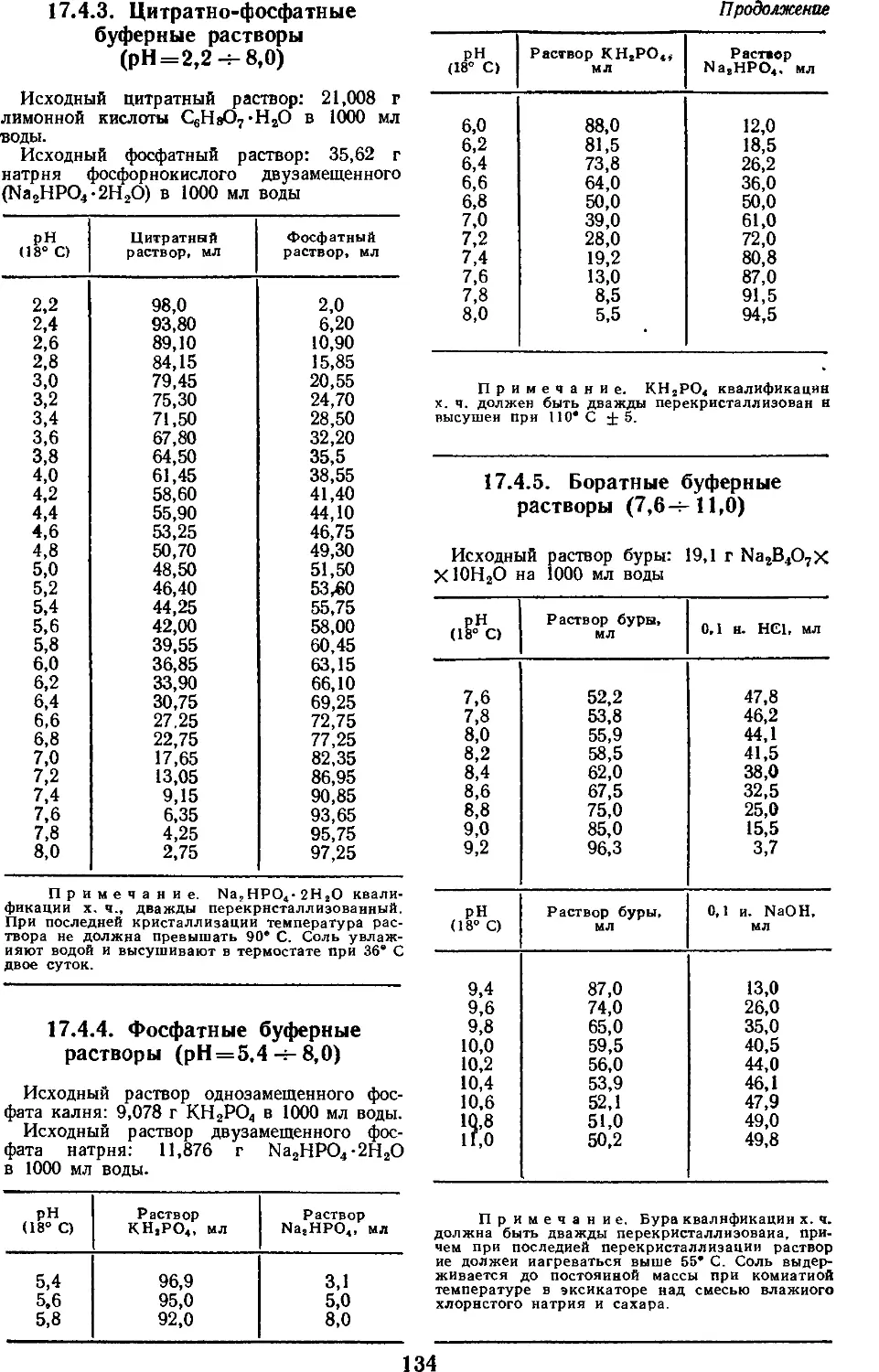
17.4.3. Цитратно-фосфат-
ные буферные
растворы 134
17.4.4. Фосфатные
буферные растворы 134
17.4.5. Боратные буферные
растворы ..... 134
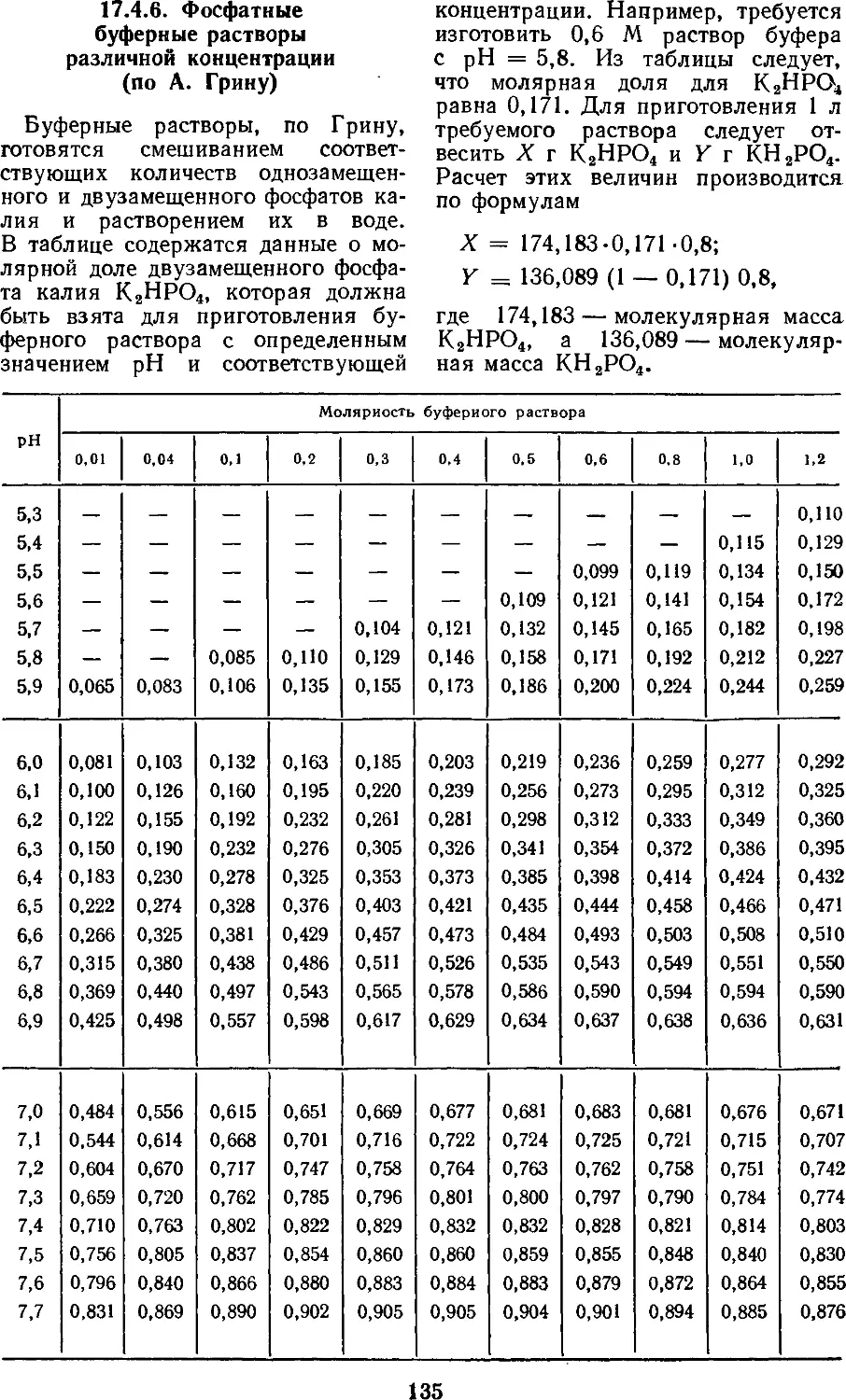
17.4.6. Фосфатные
буферные растворы
различной
концентрации 135
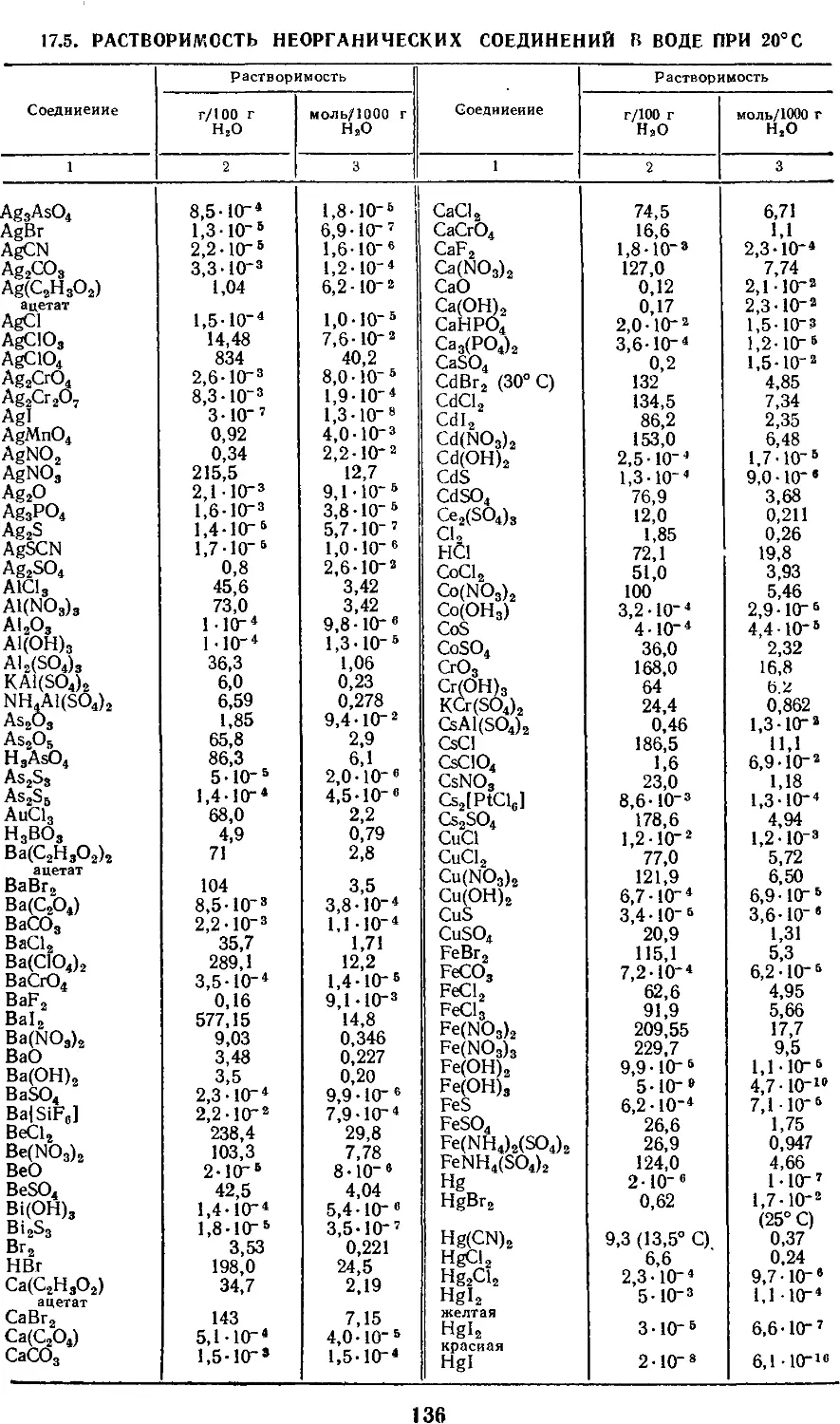
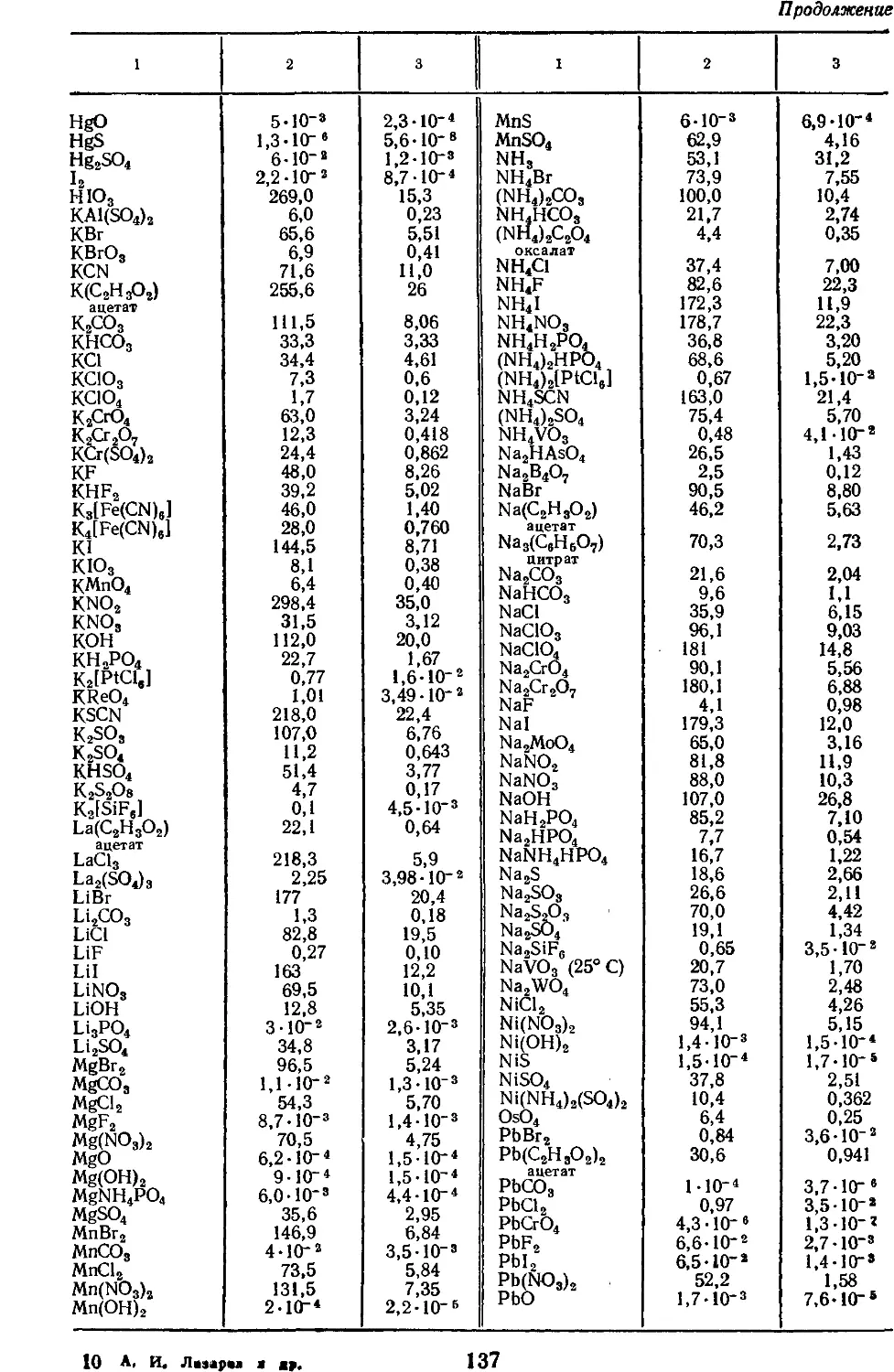
17.5. Растворимость
неорганических соединений в воде при
20° С 136
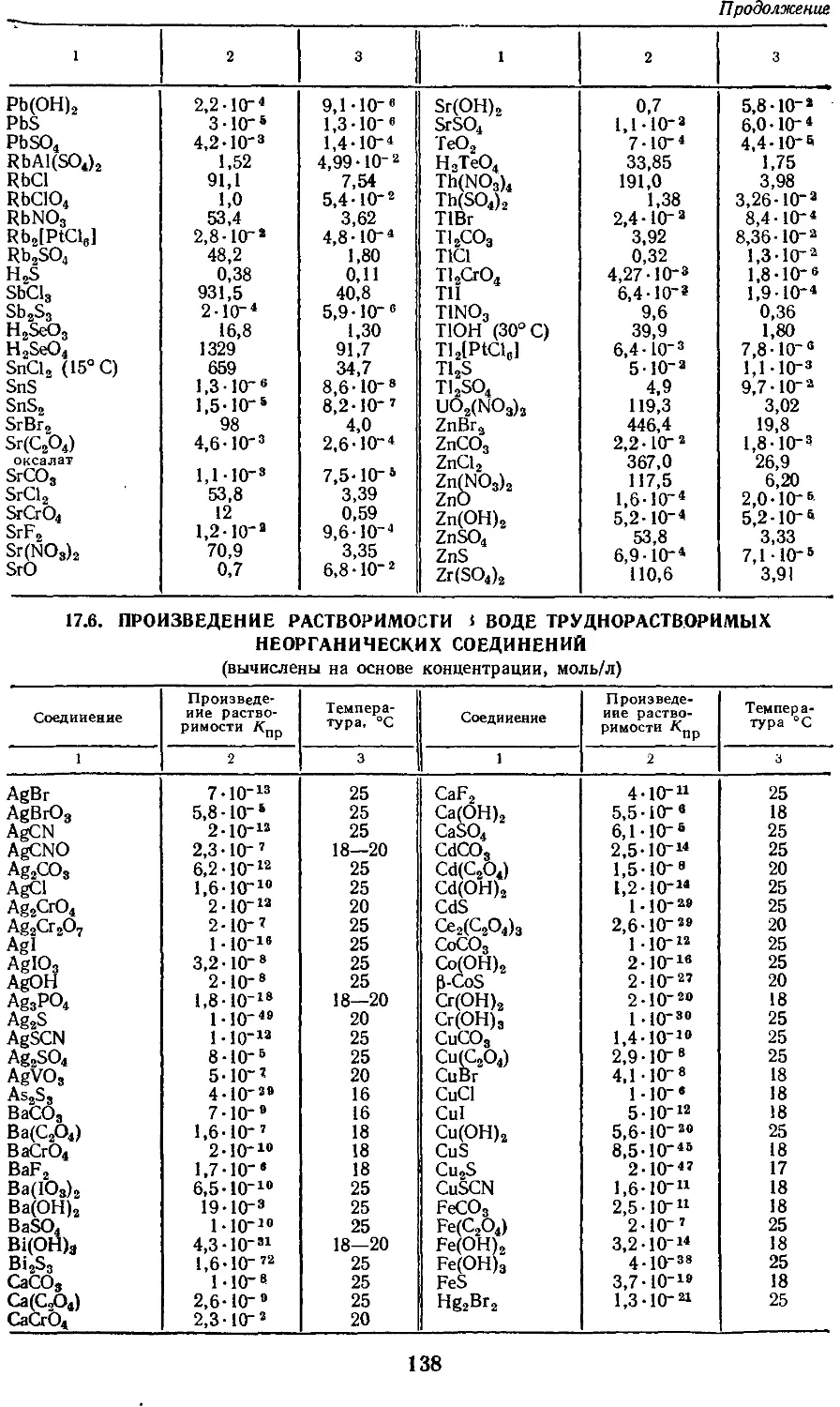
17.6. Произведение
растворимости в воде трудиораствори-
мых неорганических
соединений 138
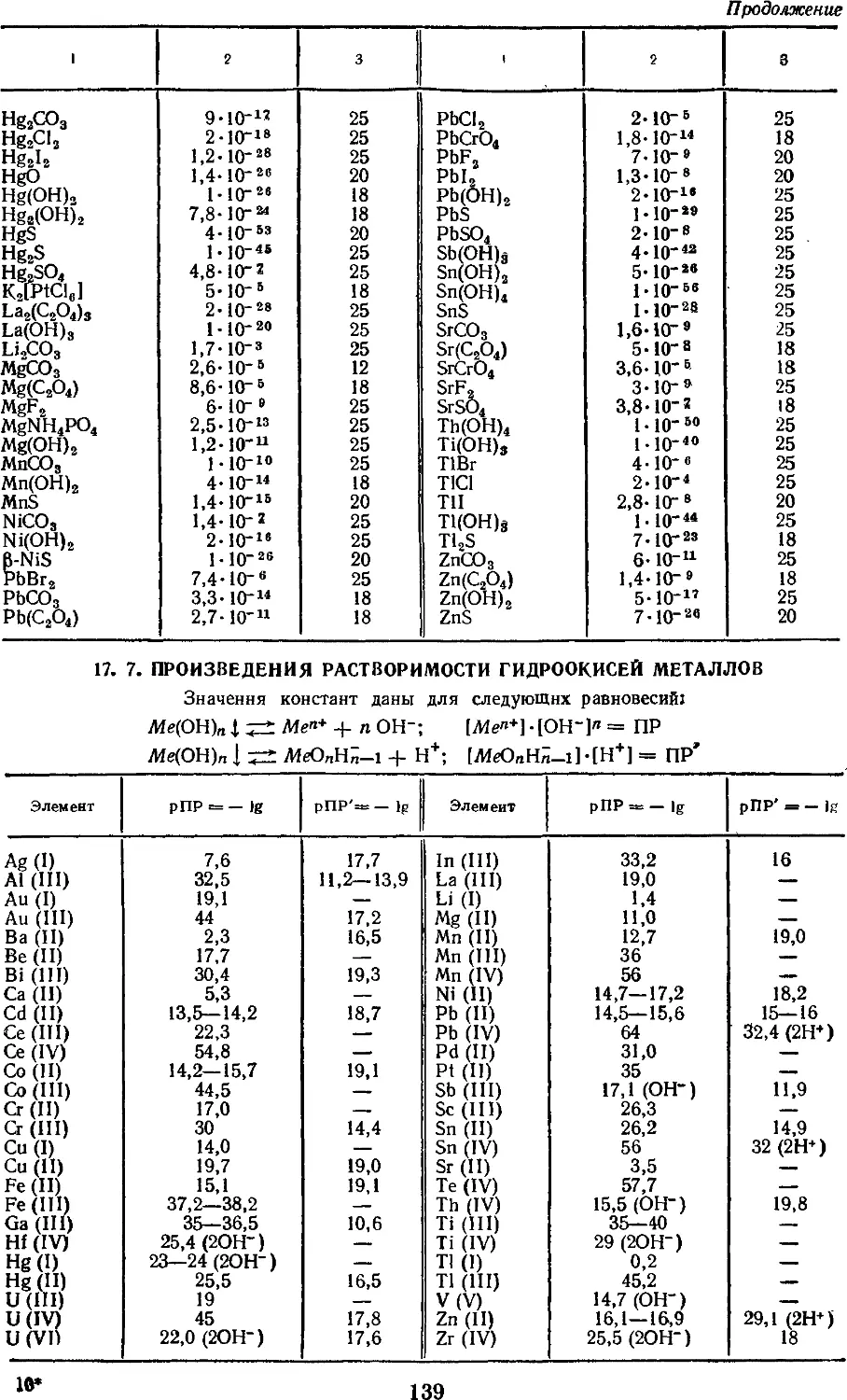
17.7. Произведения
растворимости гидроокисей металлов 139
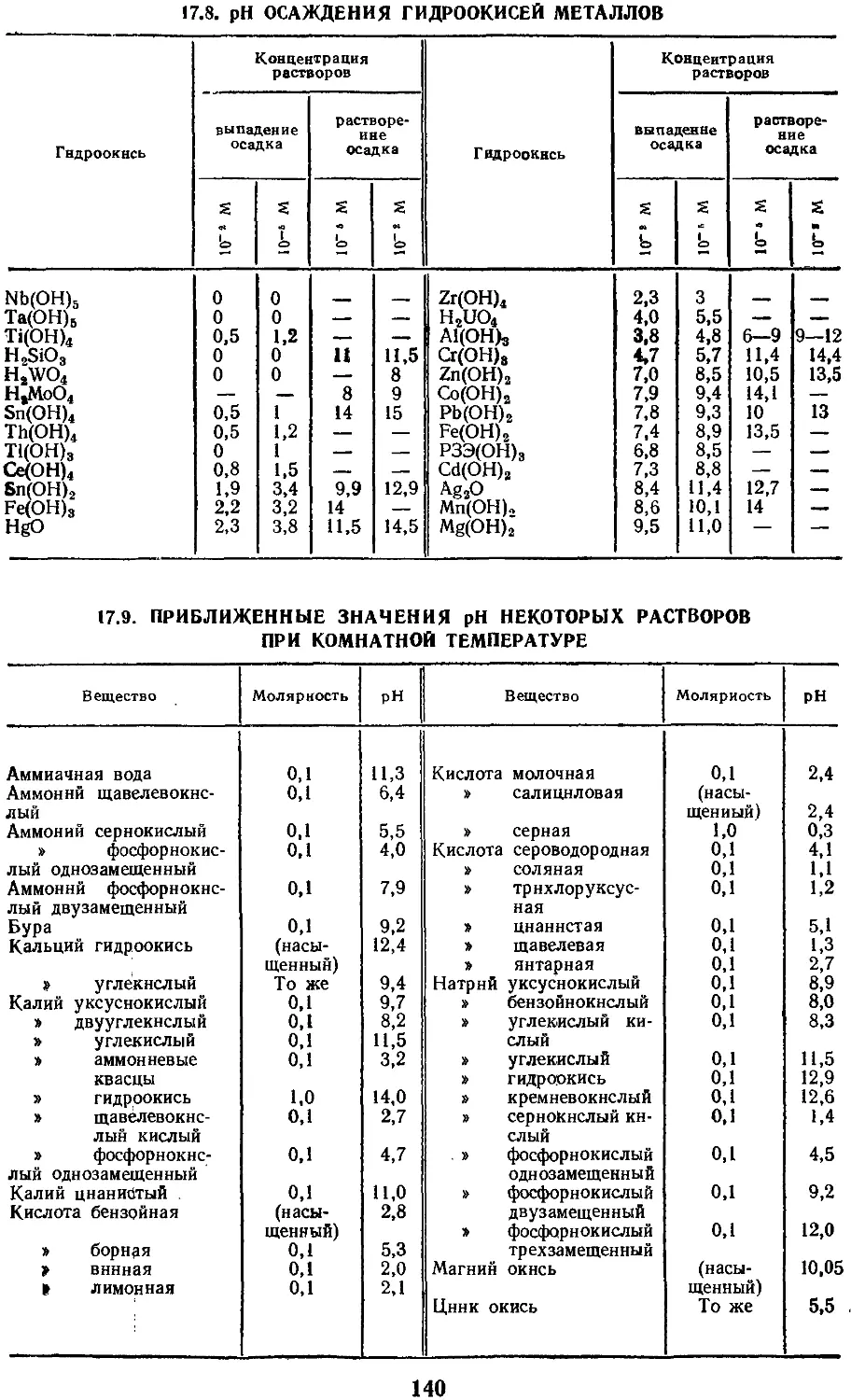
17.8. рН осаждения гидроокисей
металлов 140
17.9. Приближенные значения
рН некоторых растворов
при комнатной температуре 140
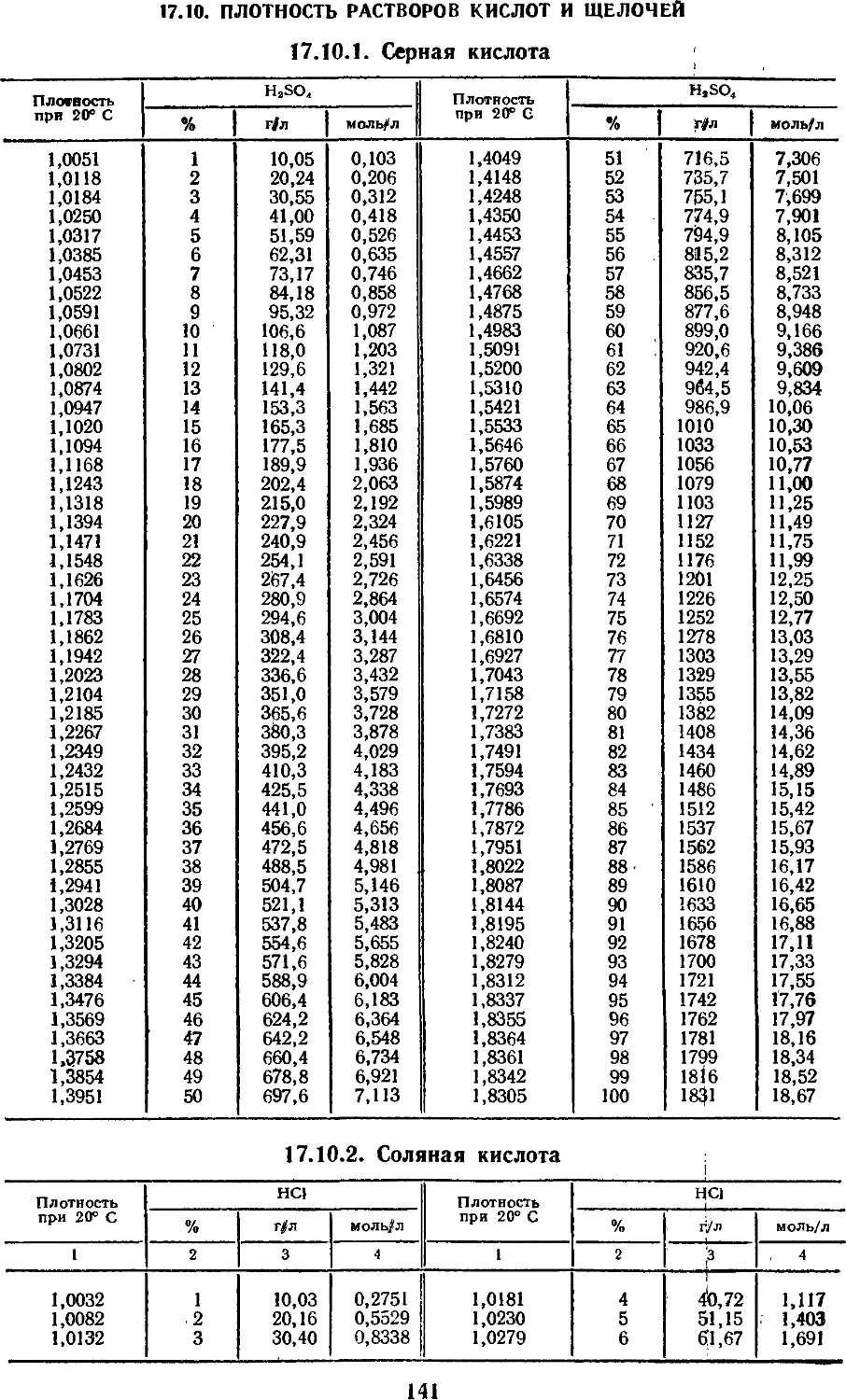
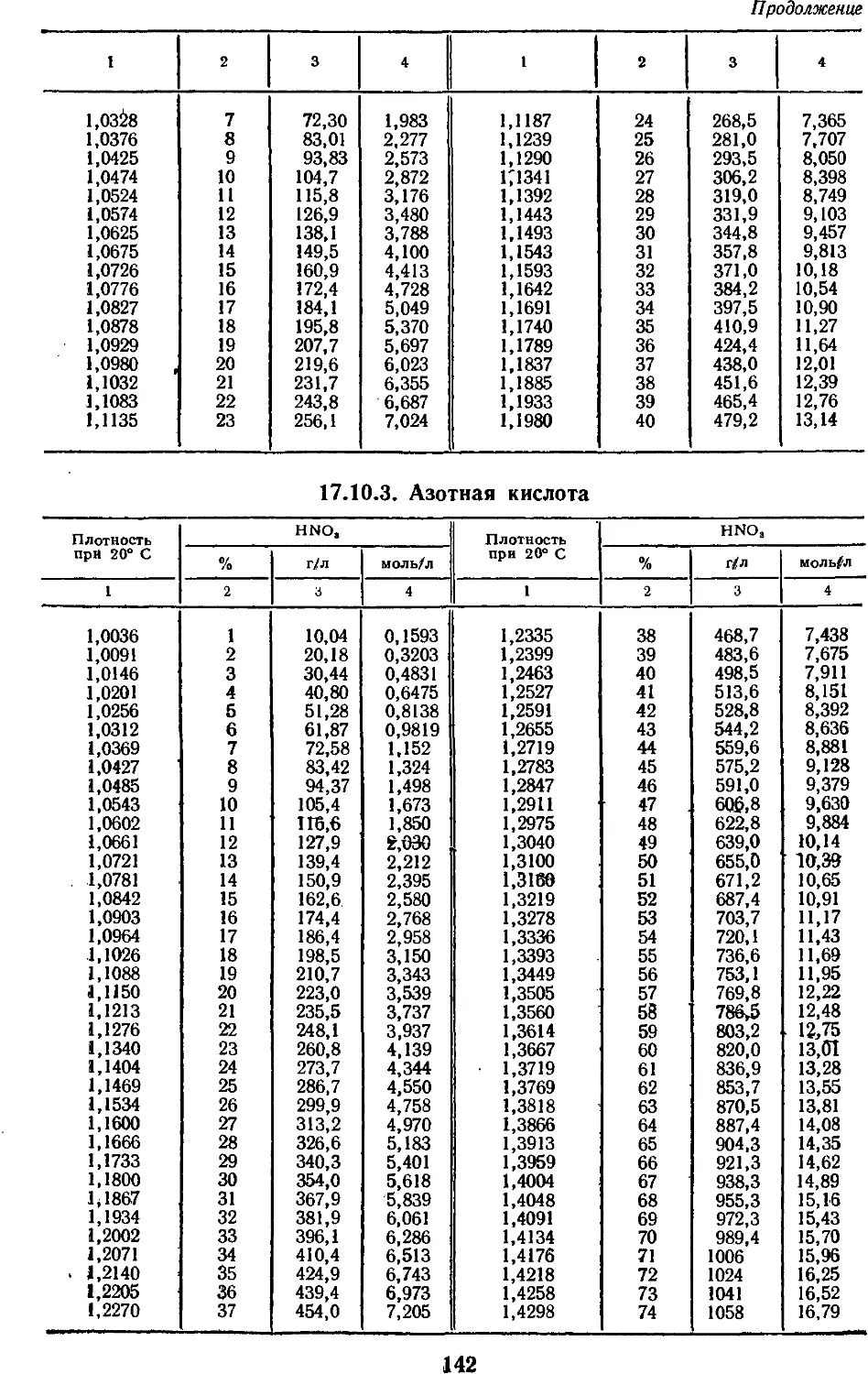
17.10. Плотность растворов кислот
и щелочей 141
17.10.1. Серная кислота 141
17.10.2. Соляная кислота 141
17.10.3. Азотная кислота 142
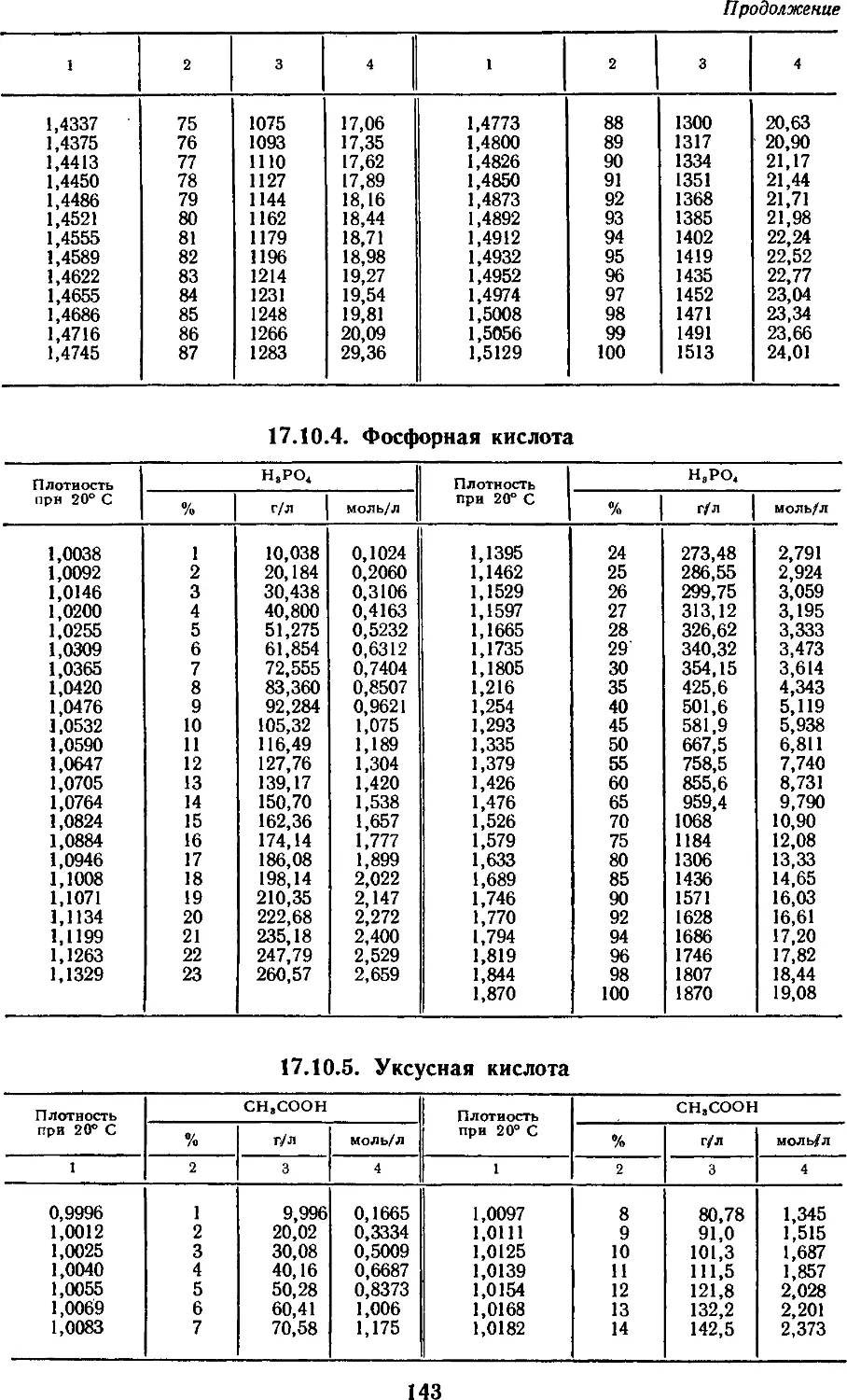
17.10.4. Фосфорная кислота 143
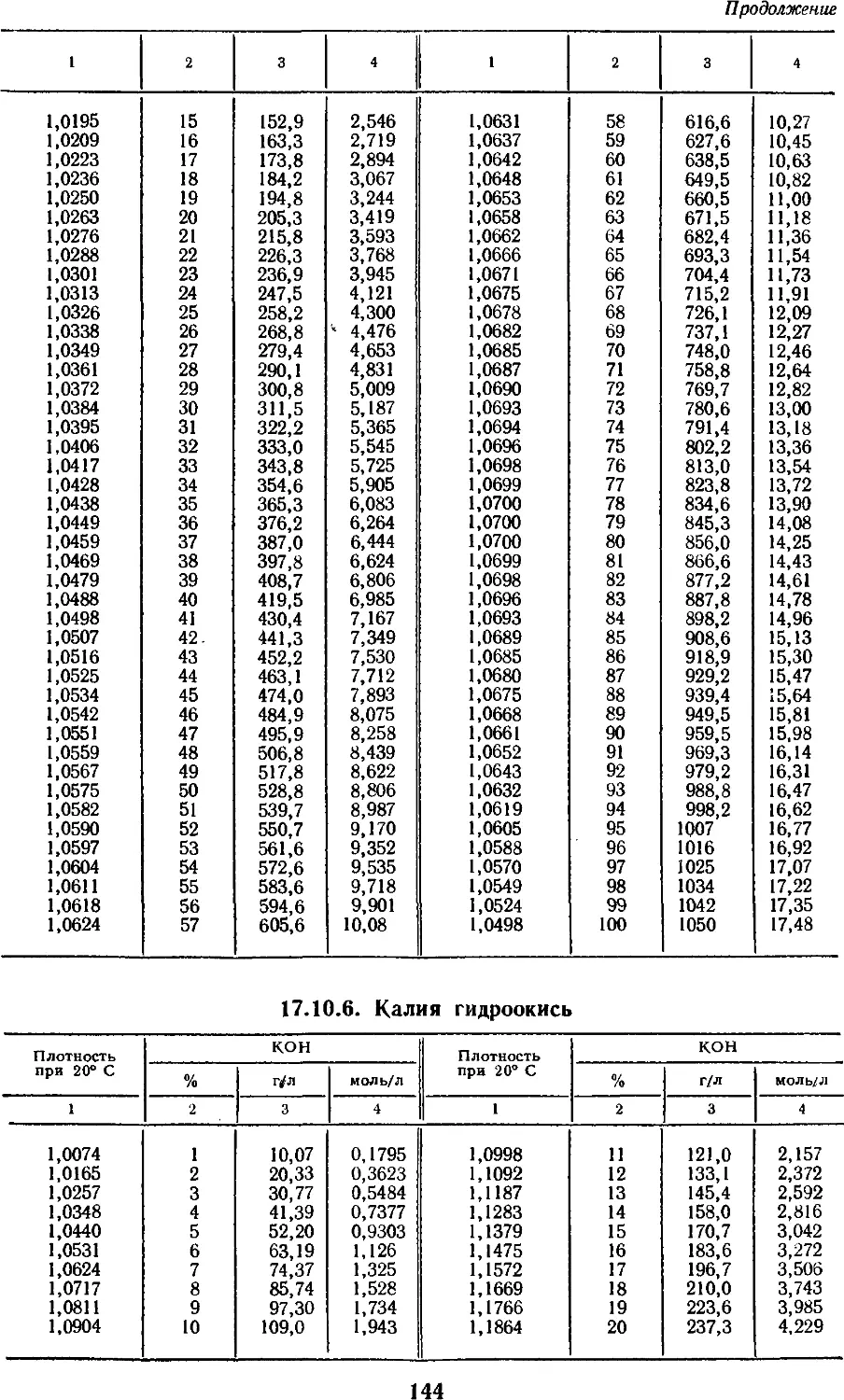
17.10.5. Уксусная кислота 143
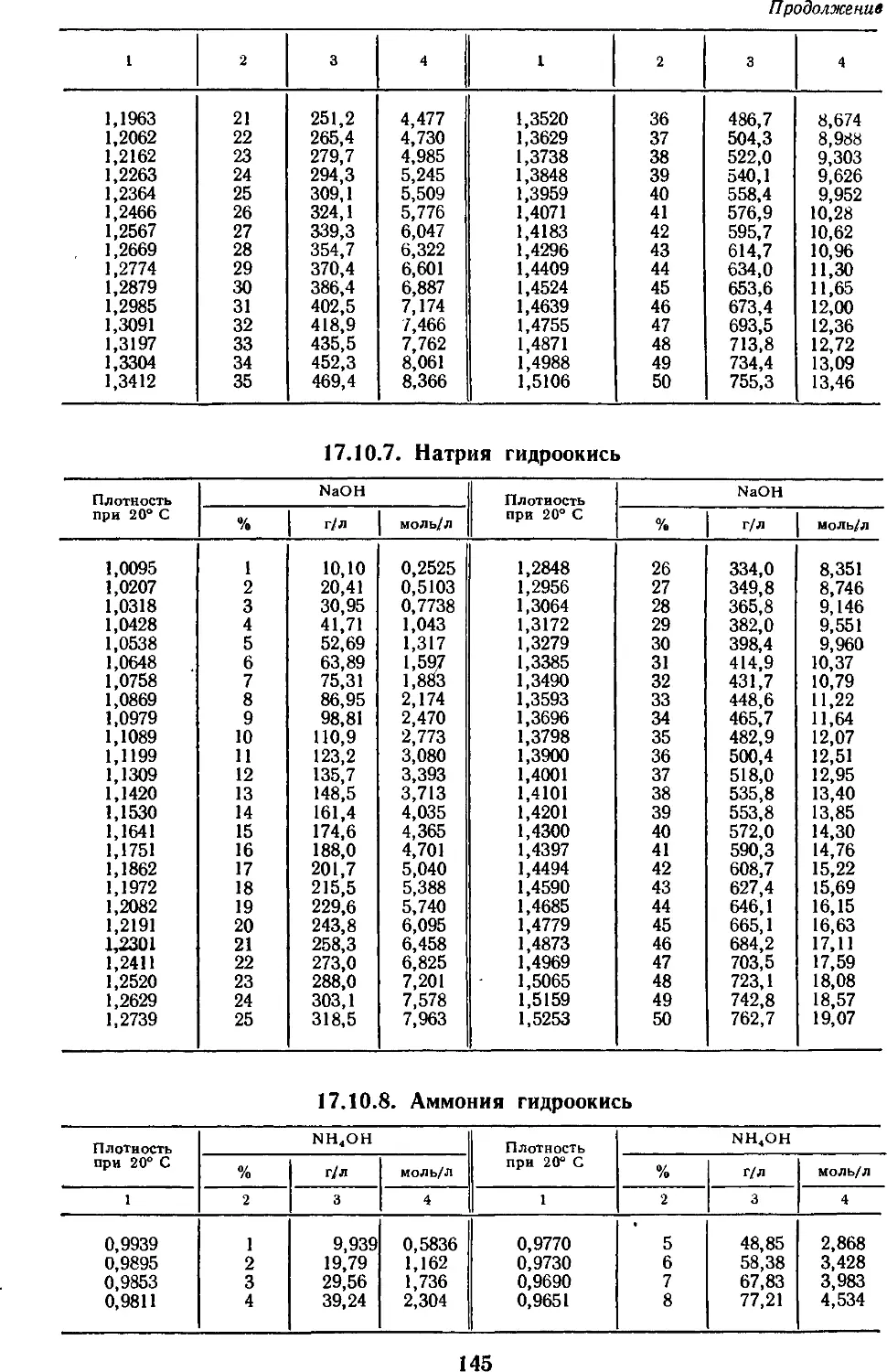
17.10.6. Калия гидроокись 144
17.10.7. Натрия гидроокись 145
17.10.8. Аммония
гидроокись 145
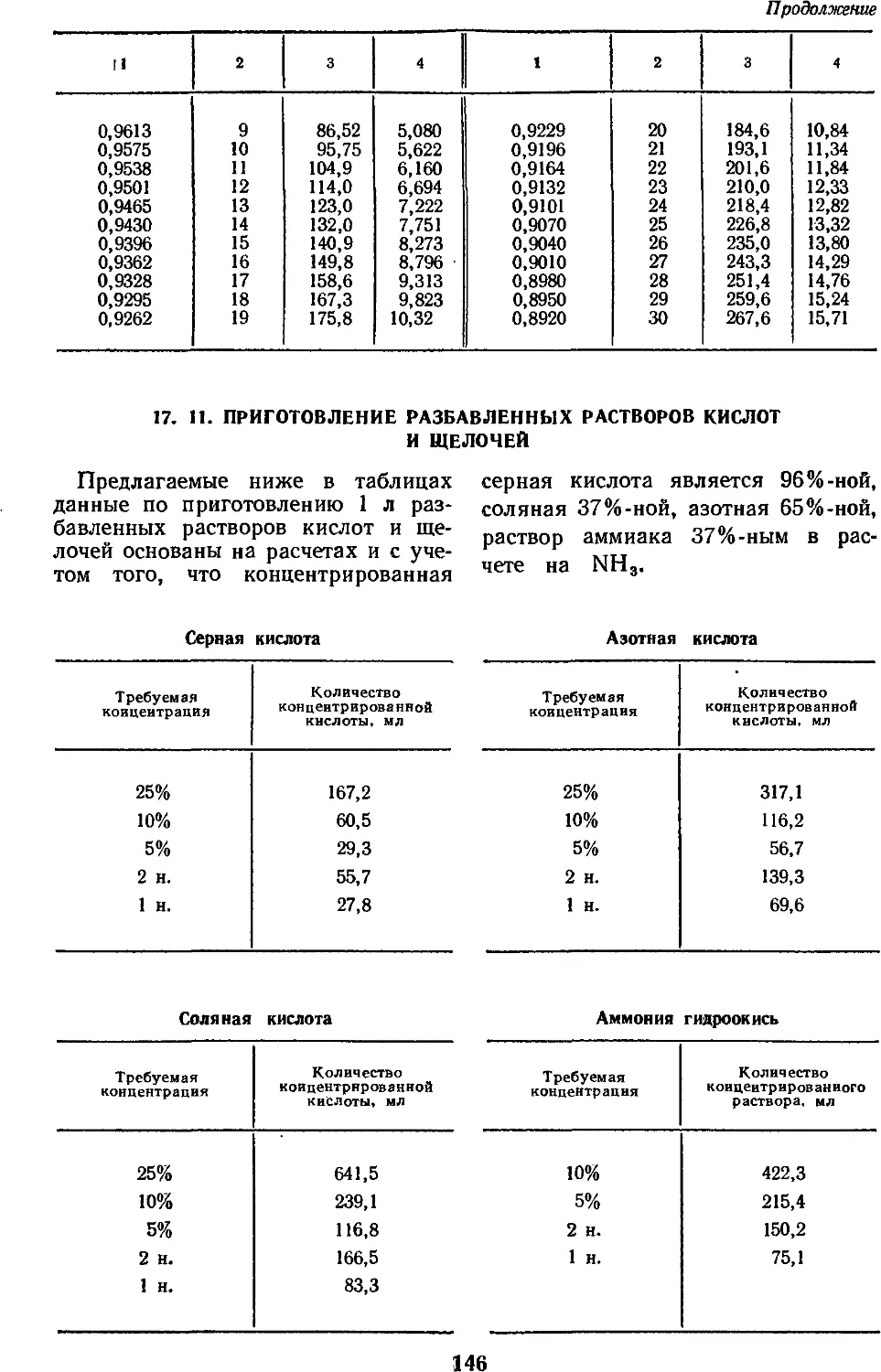
17.11. Приготовление
разбавленных растворов кислот и
щелочей 146
17.12. Правило креста 147
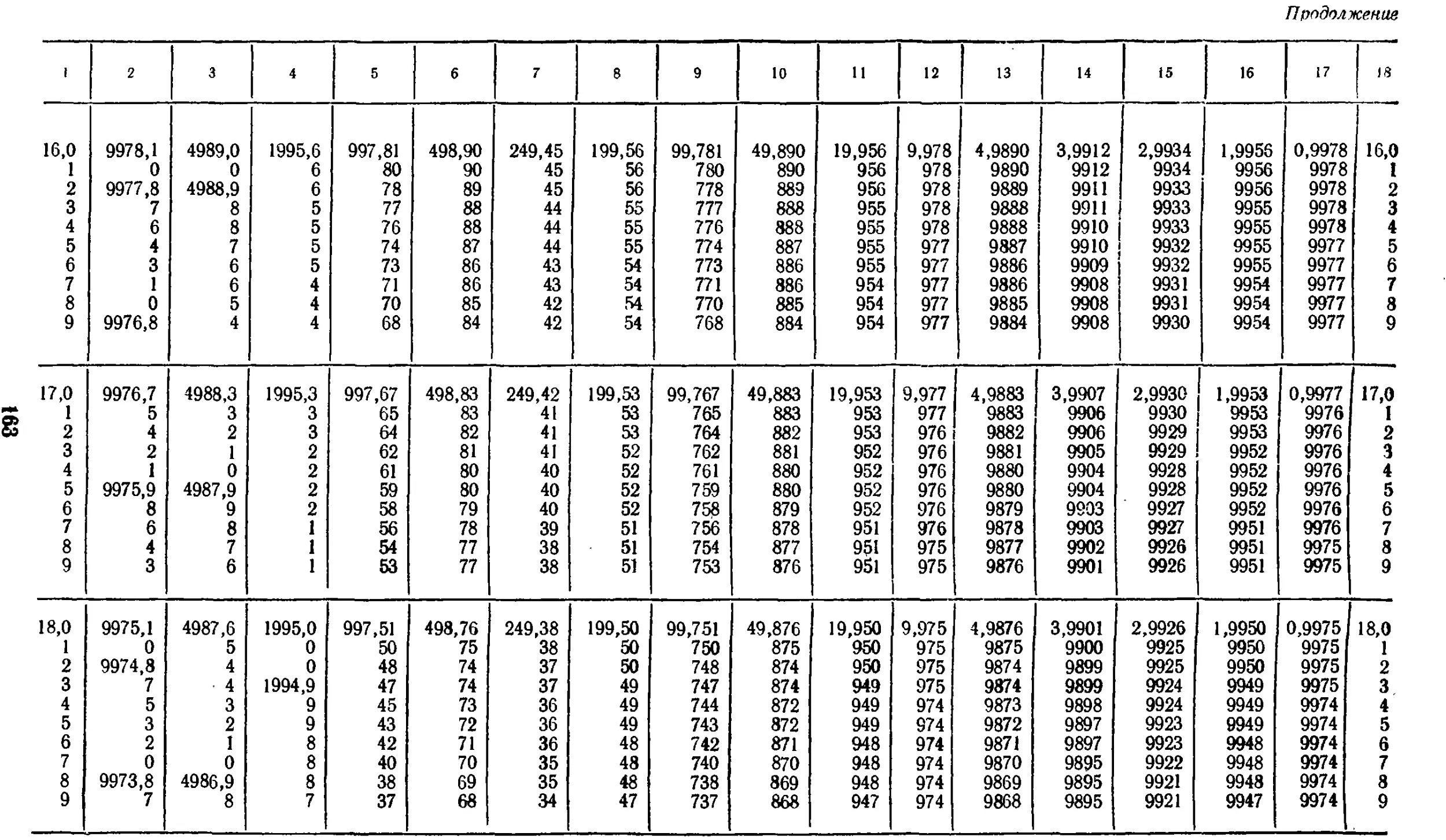
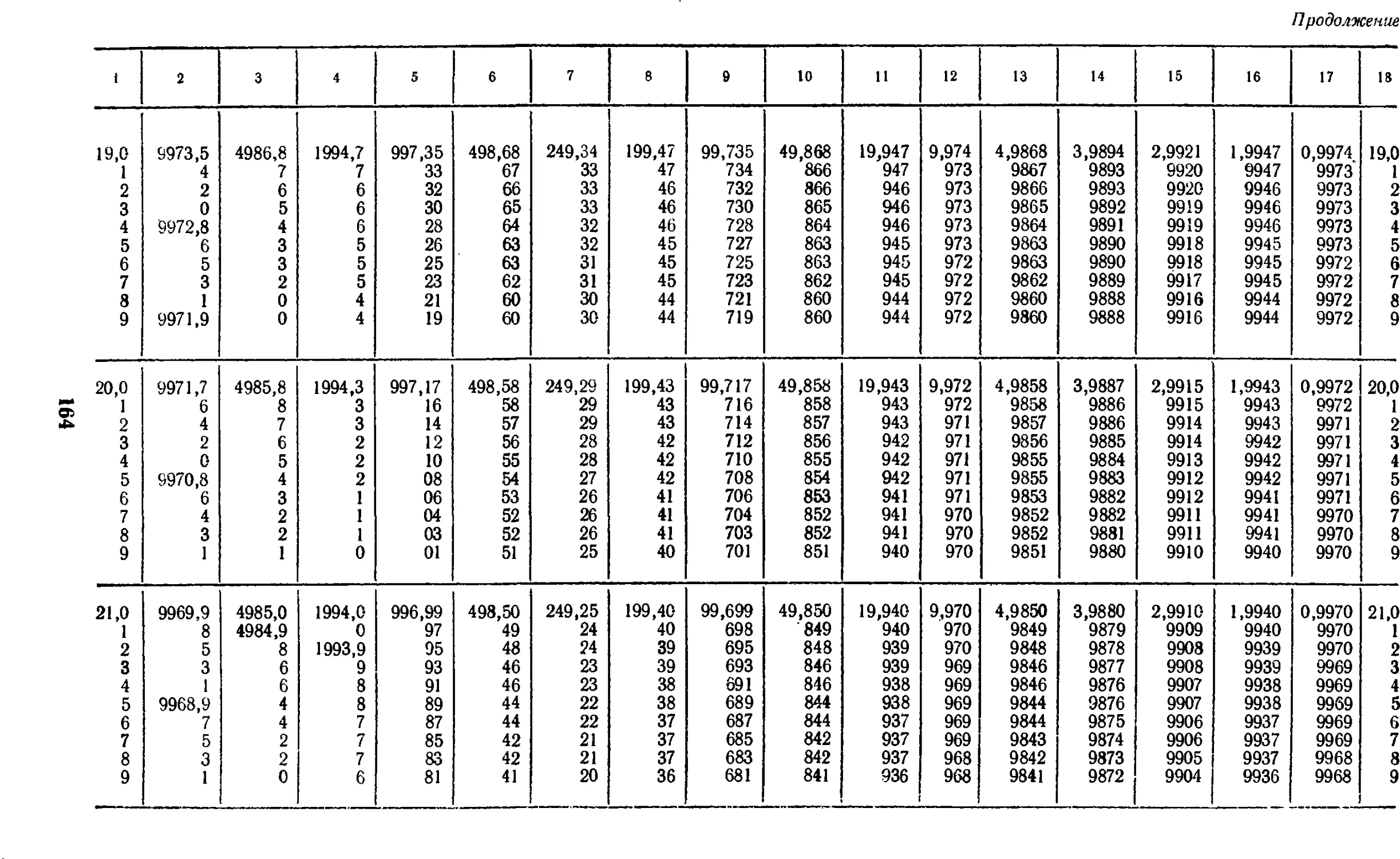
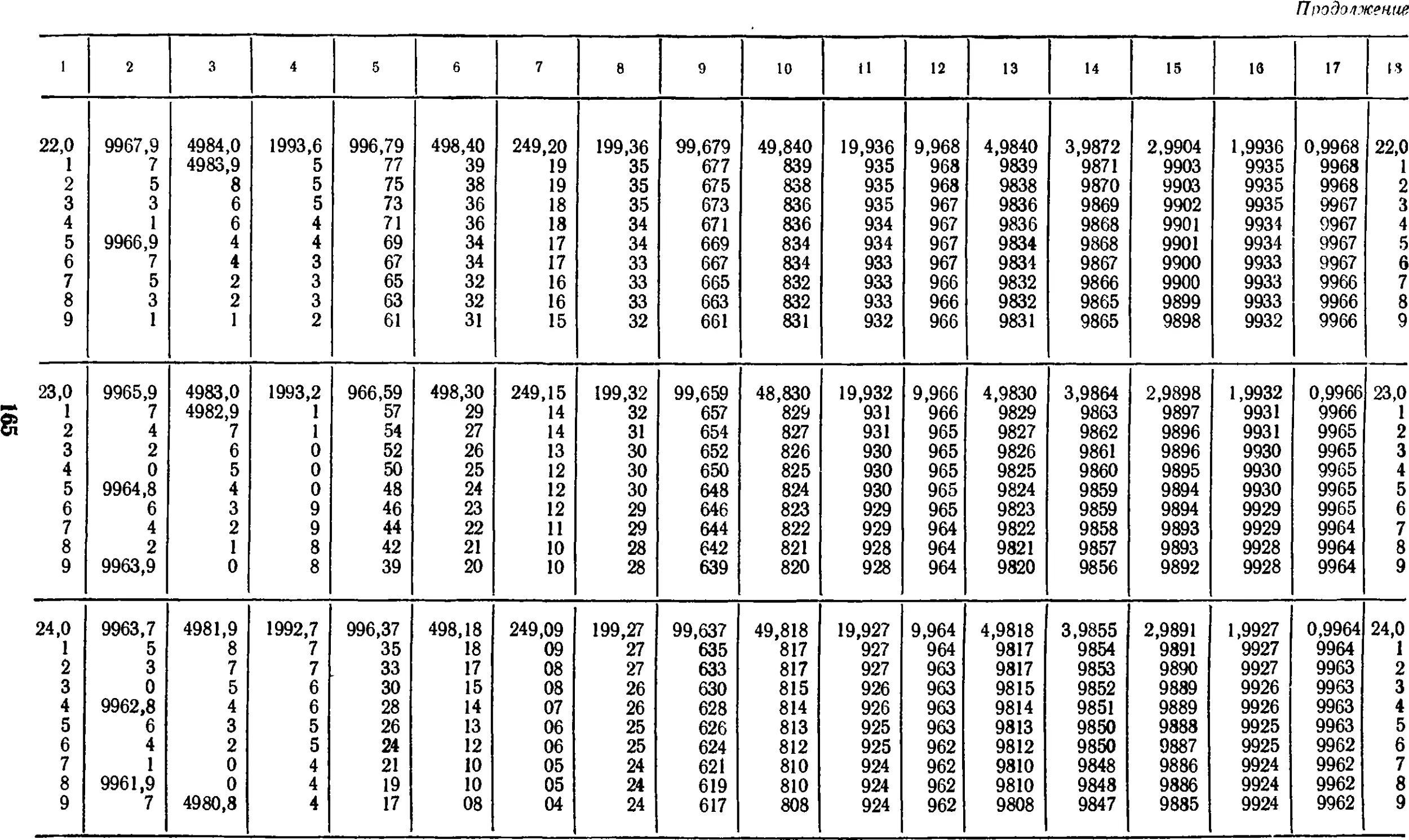
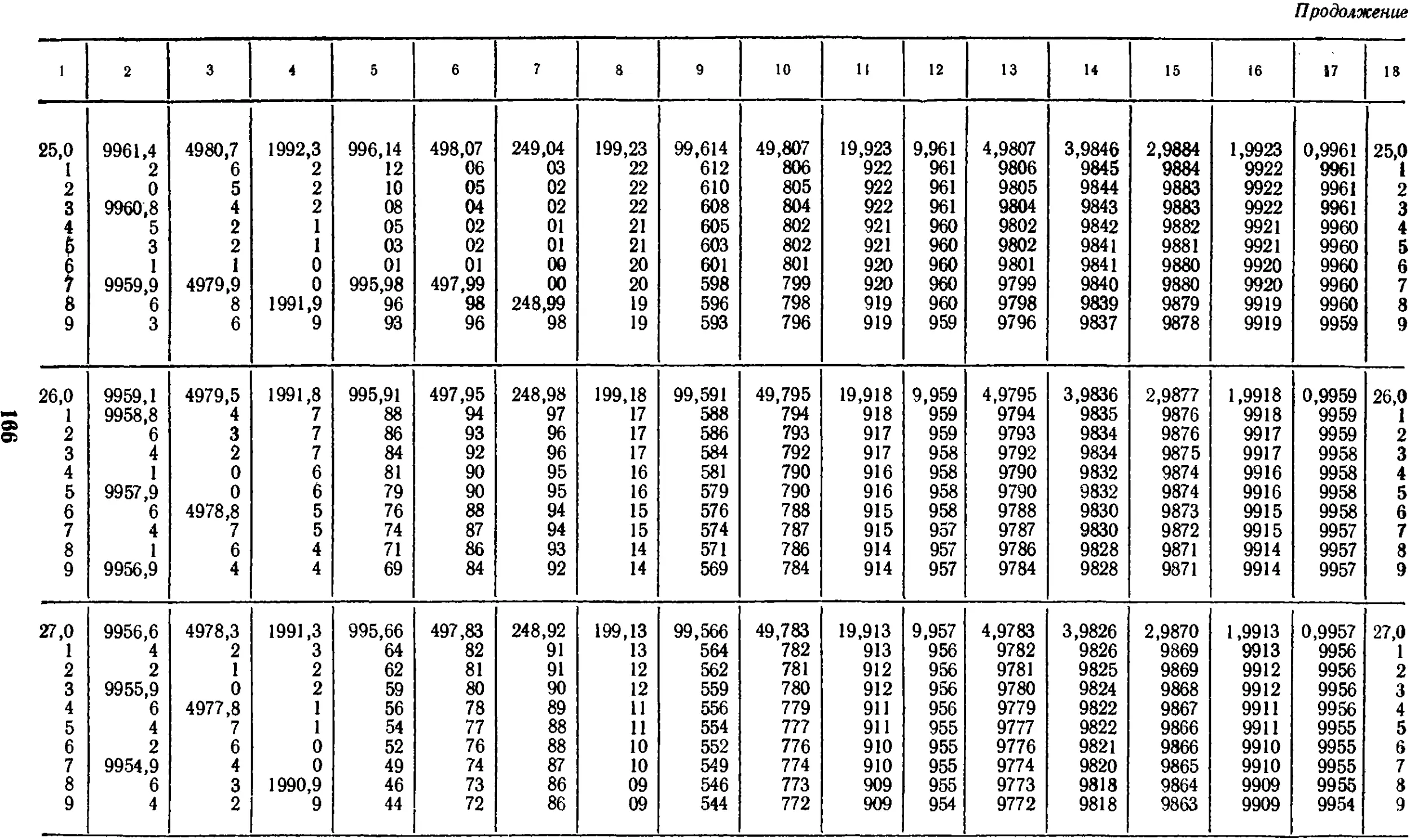
17.13. Плотность воды при
температурах от 0 до 50° С . . . 147
Газы и пары жидкостей 148
18.1. Способы получения газов 148
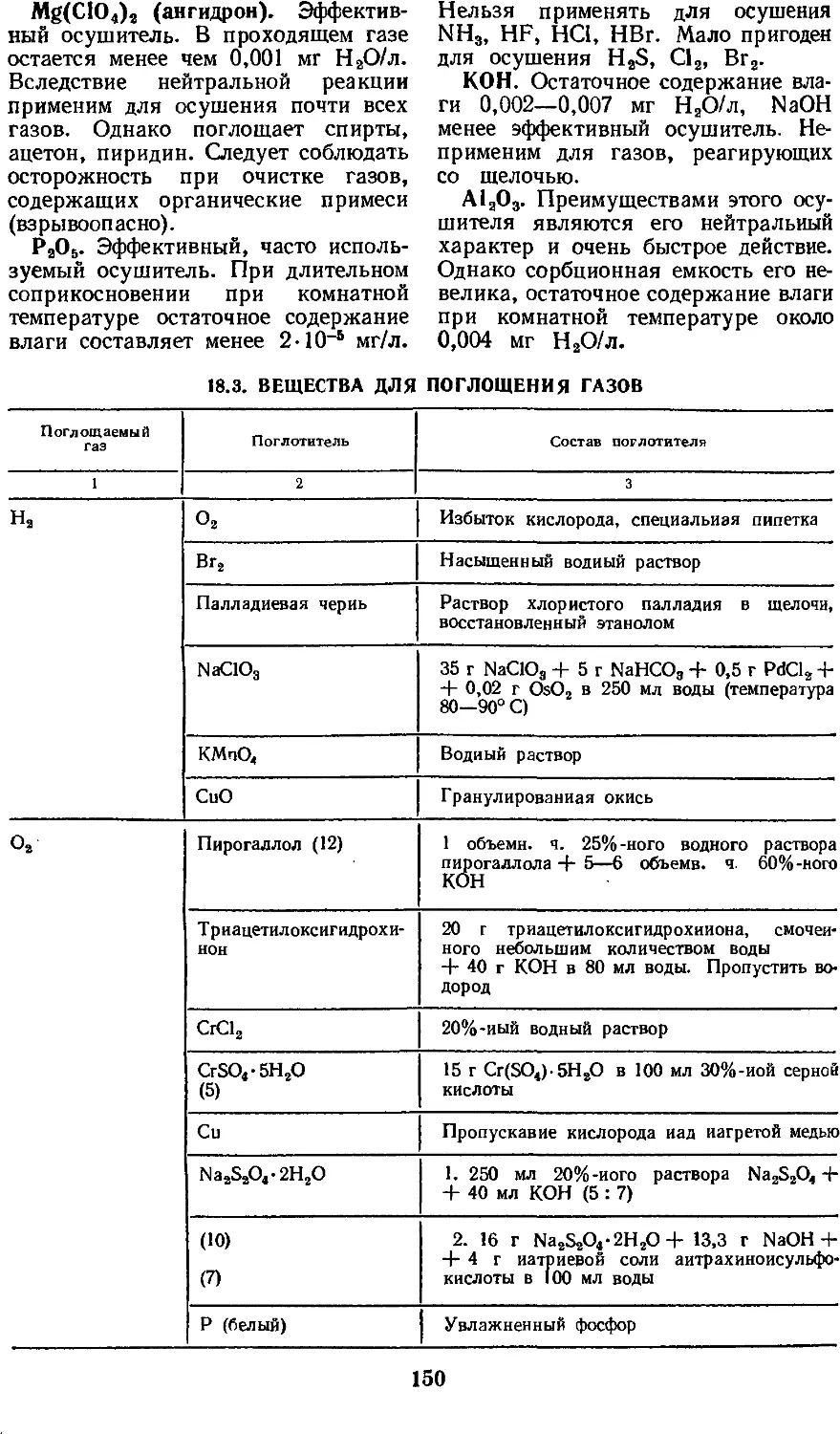
18.2. Осушители газов 149
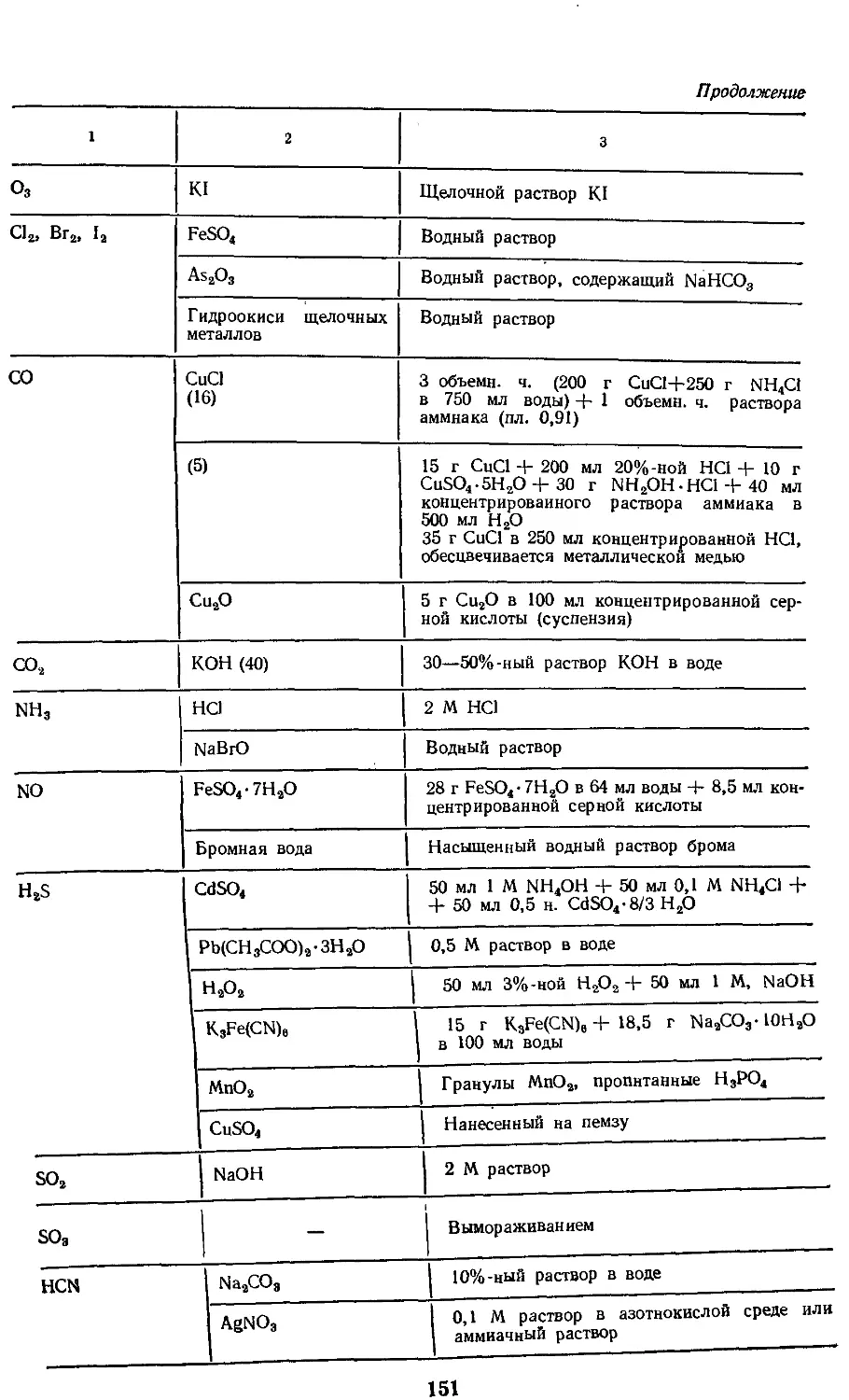
18.3. Вещества для поглощения
газов 150
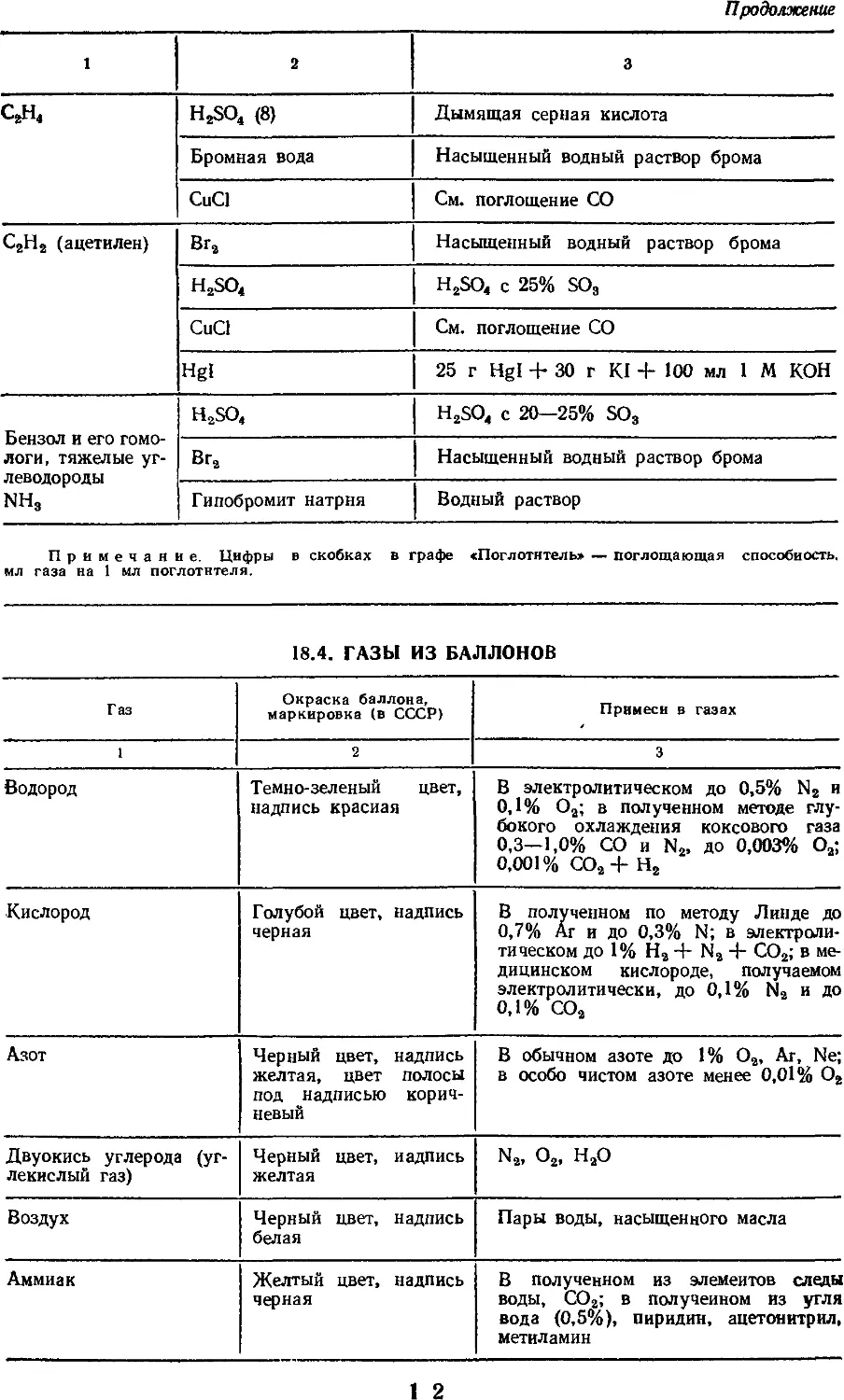
18.4. Газы из баллонов .... 152
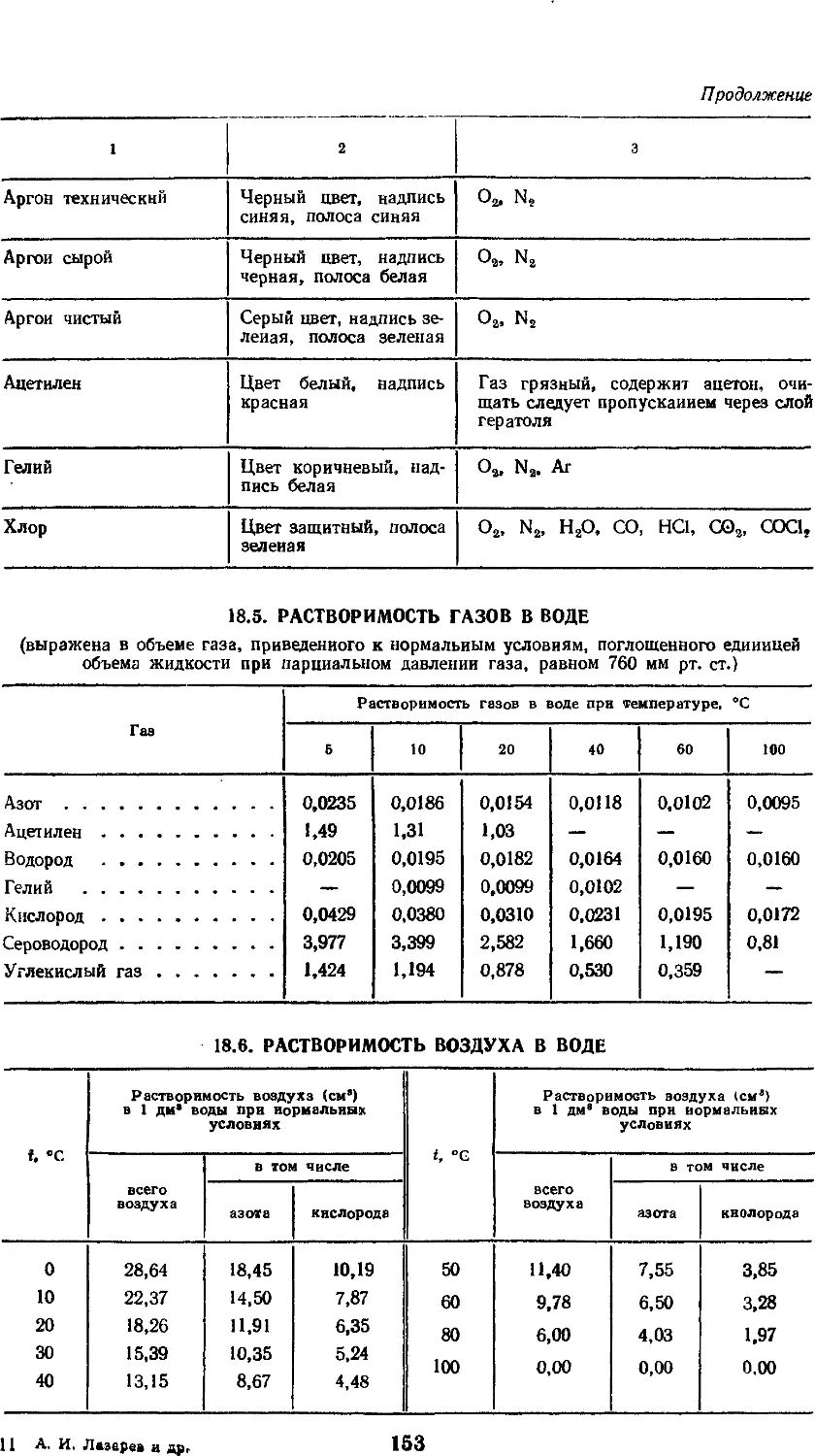
18.5. Растворимость газов в воде 153
18.6. Растворимость воздуха в
воде 153
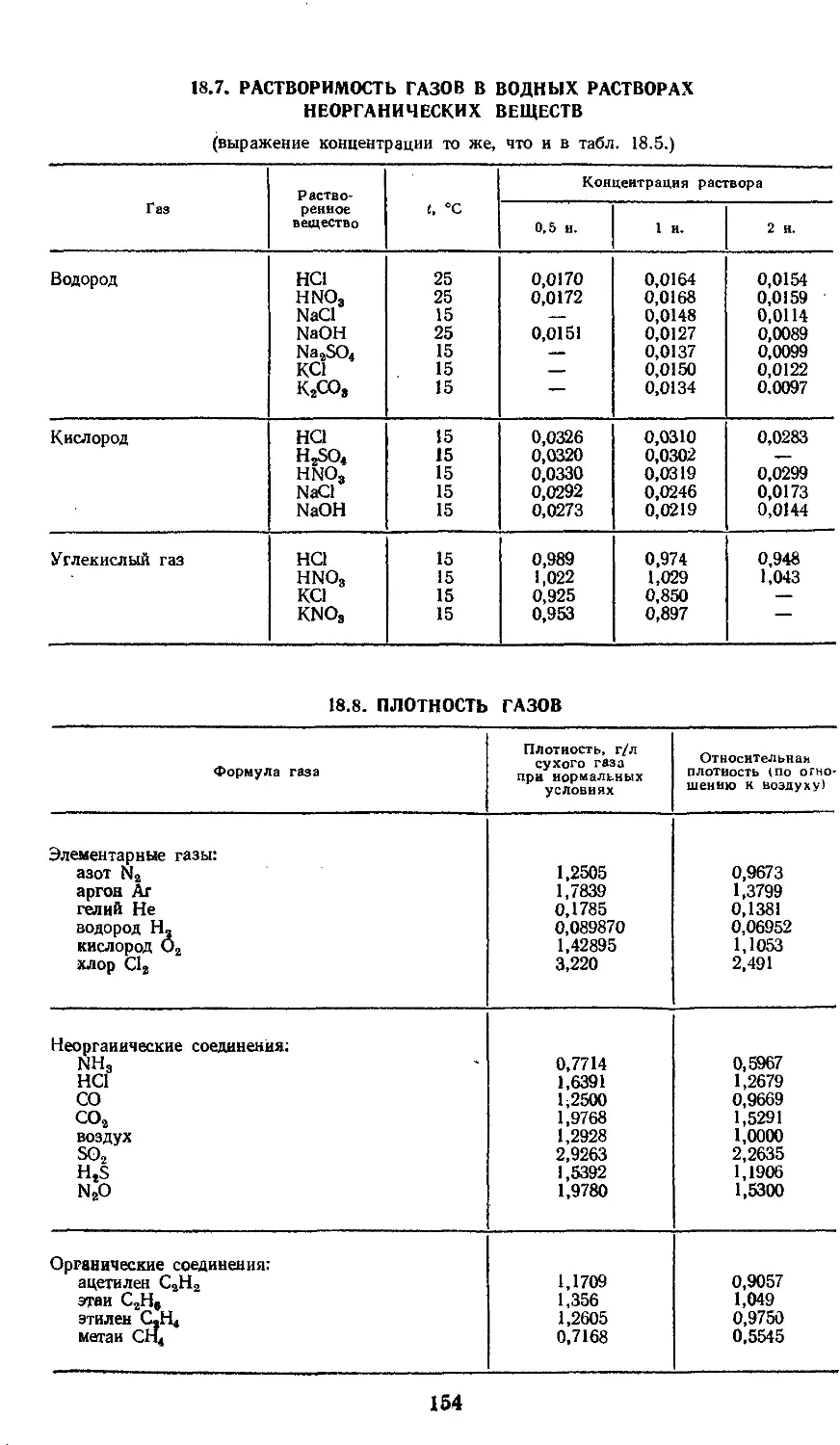
18.7. Растворимость газов в
водных растворах
неорганических веществ 154
18.8. Плотность газов 154
18.9. Несовместимые газы ... ,155
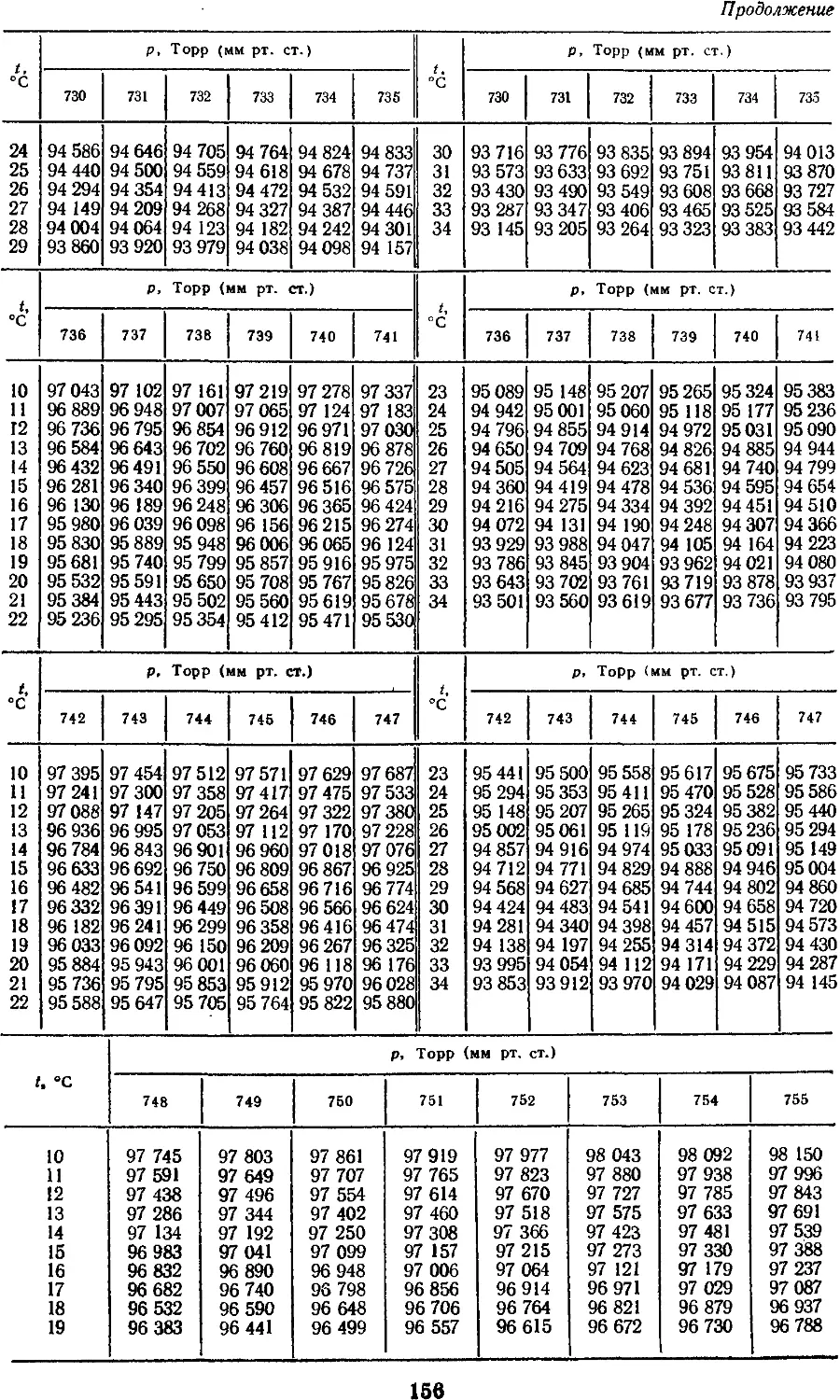
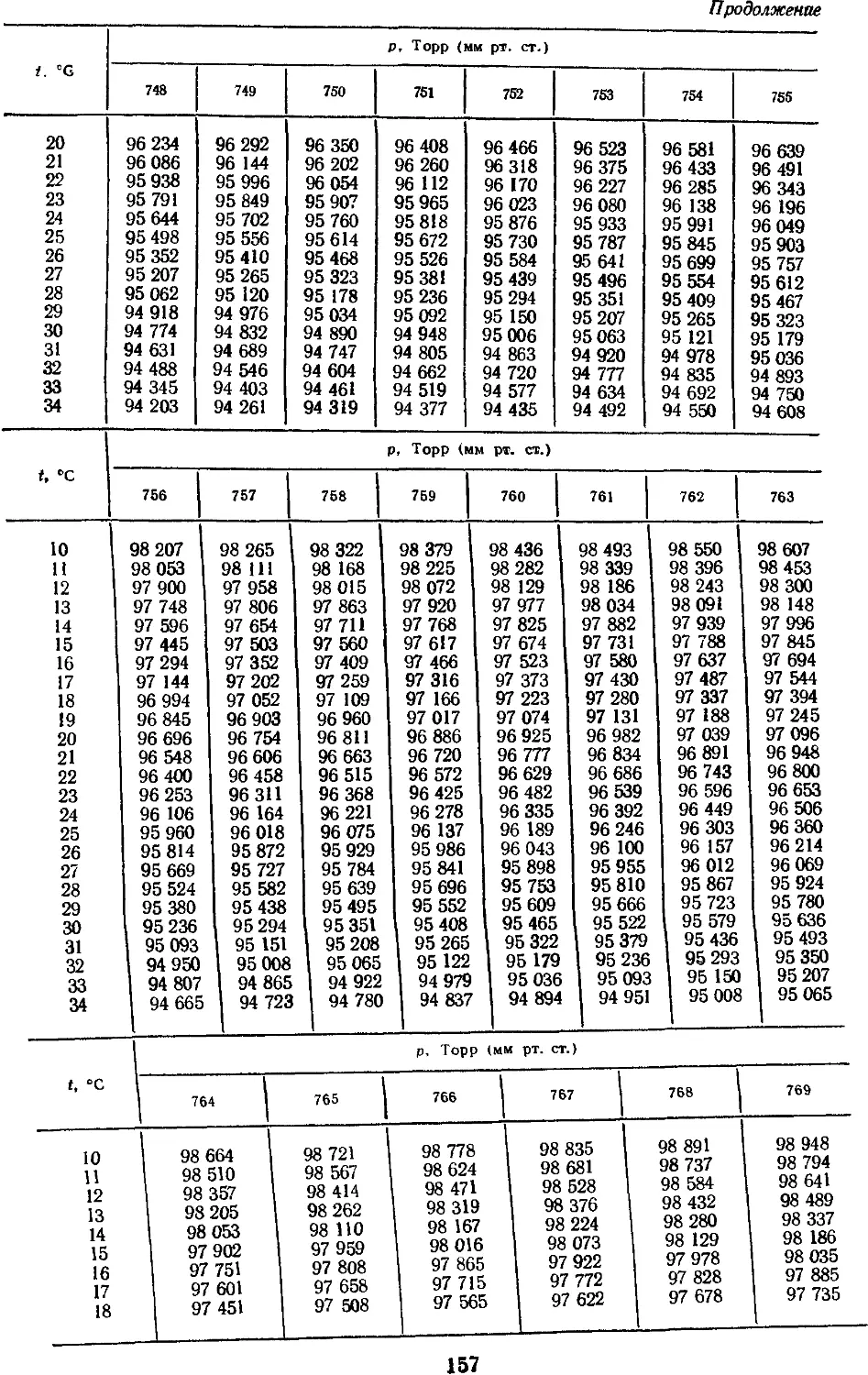
18.10. Приведение объема газов
к нормальным условиям 155
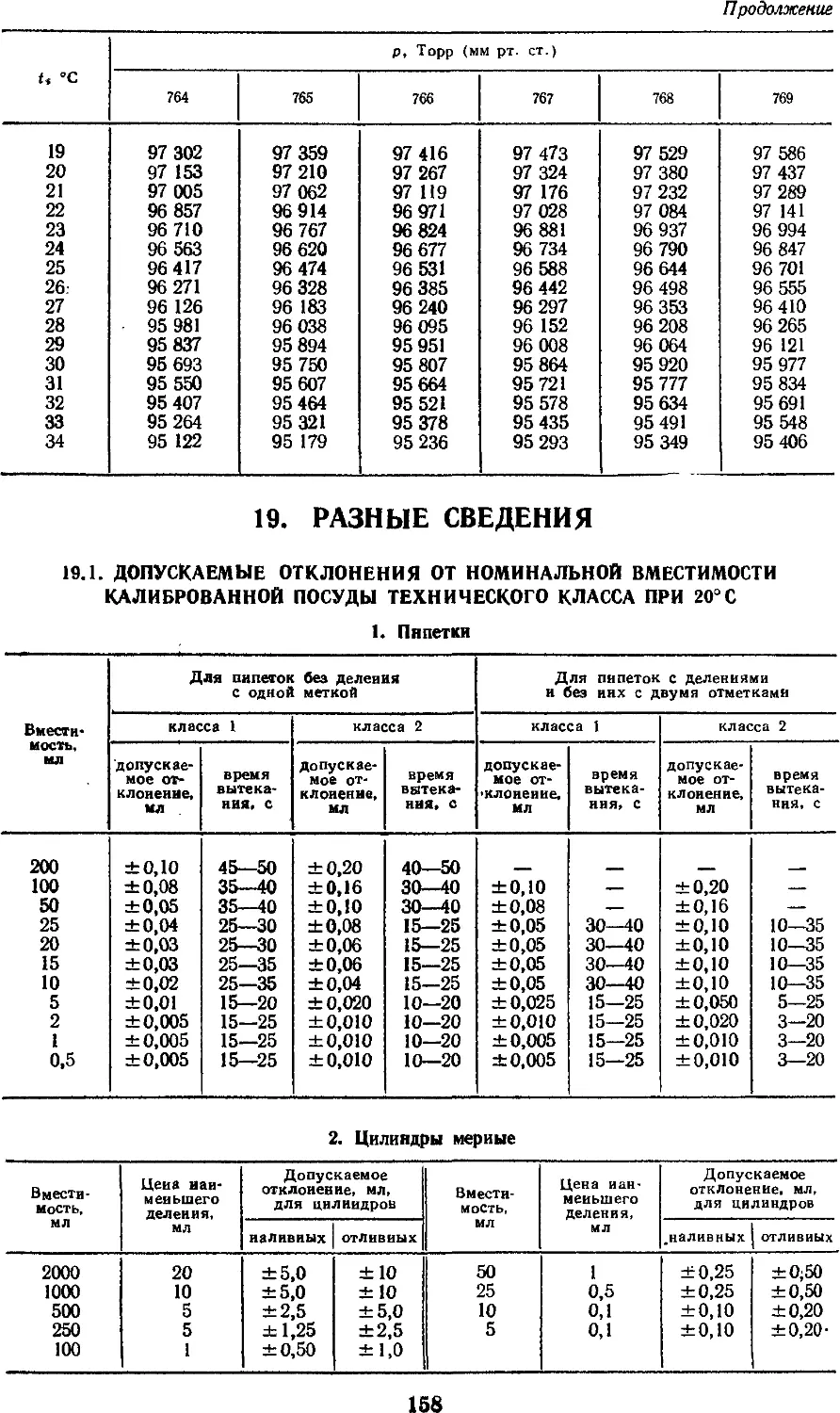
19. Разные сведения
19.1. Допускаемые отклонения
от номинальной
вместимости калиброванной посуды
технического класса при
20° С
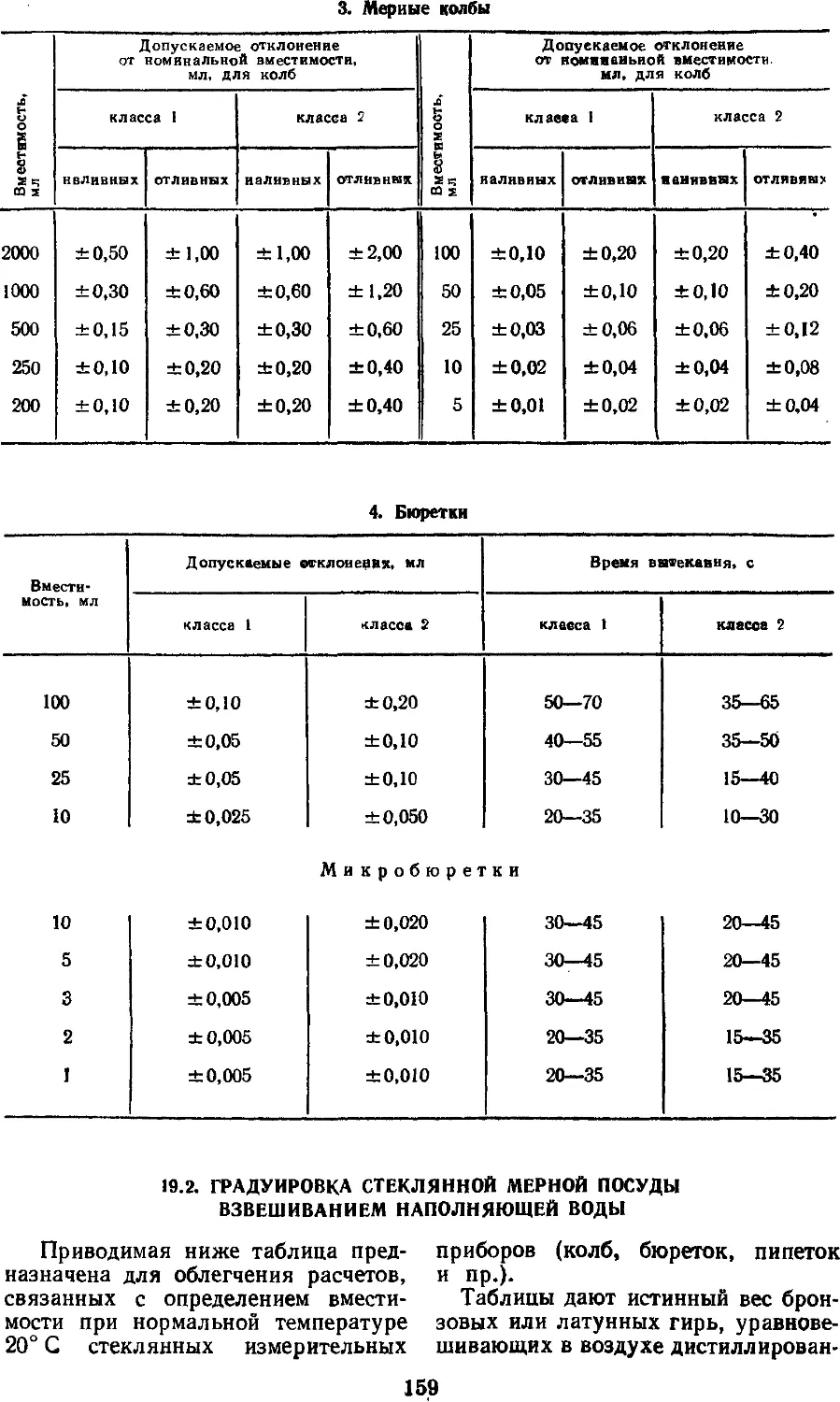
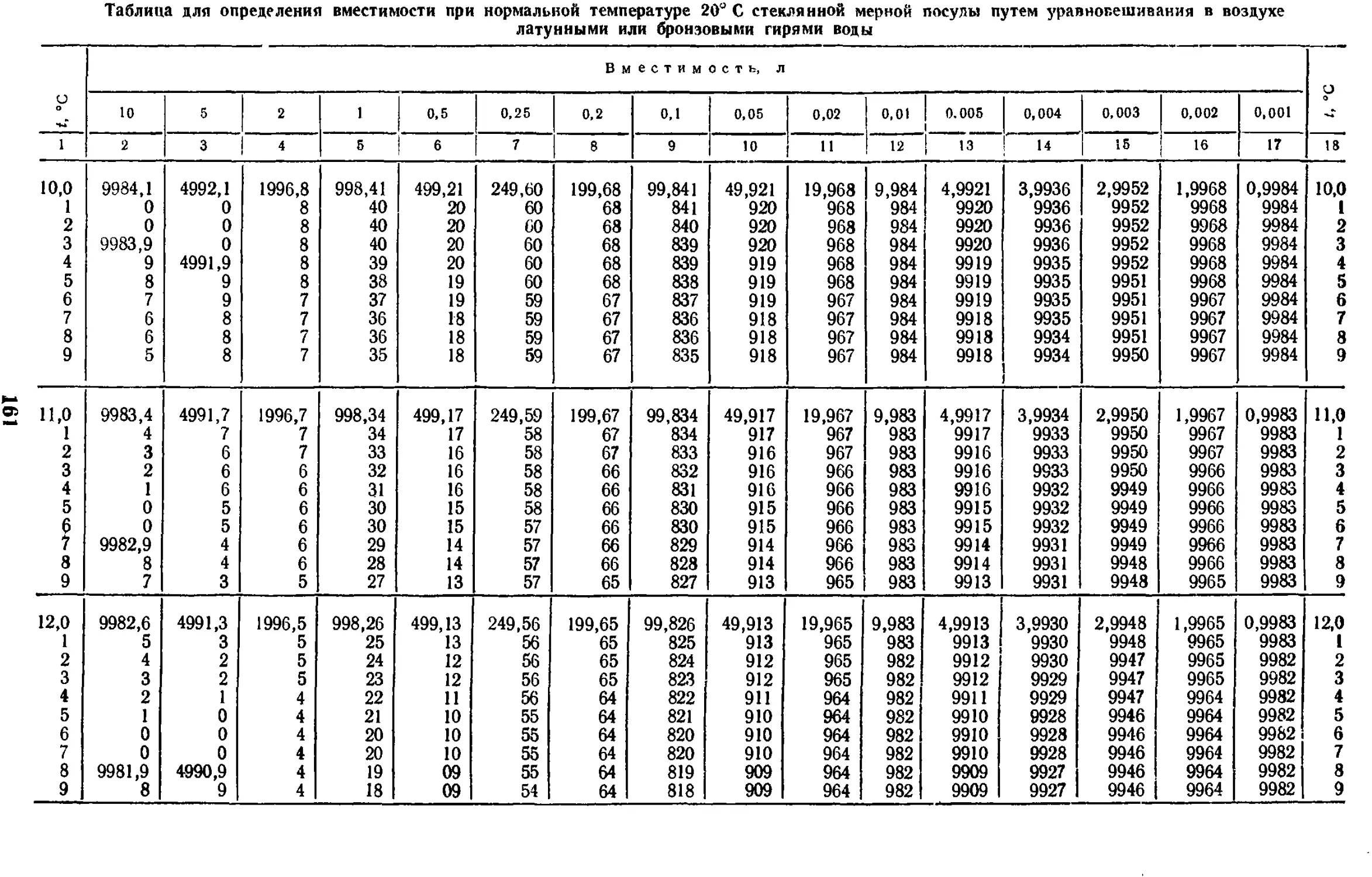
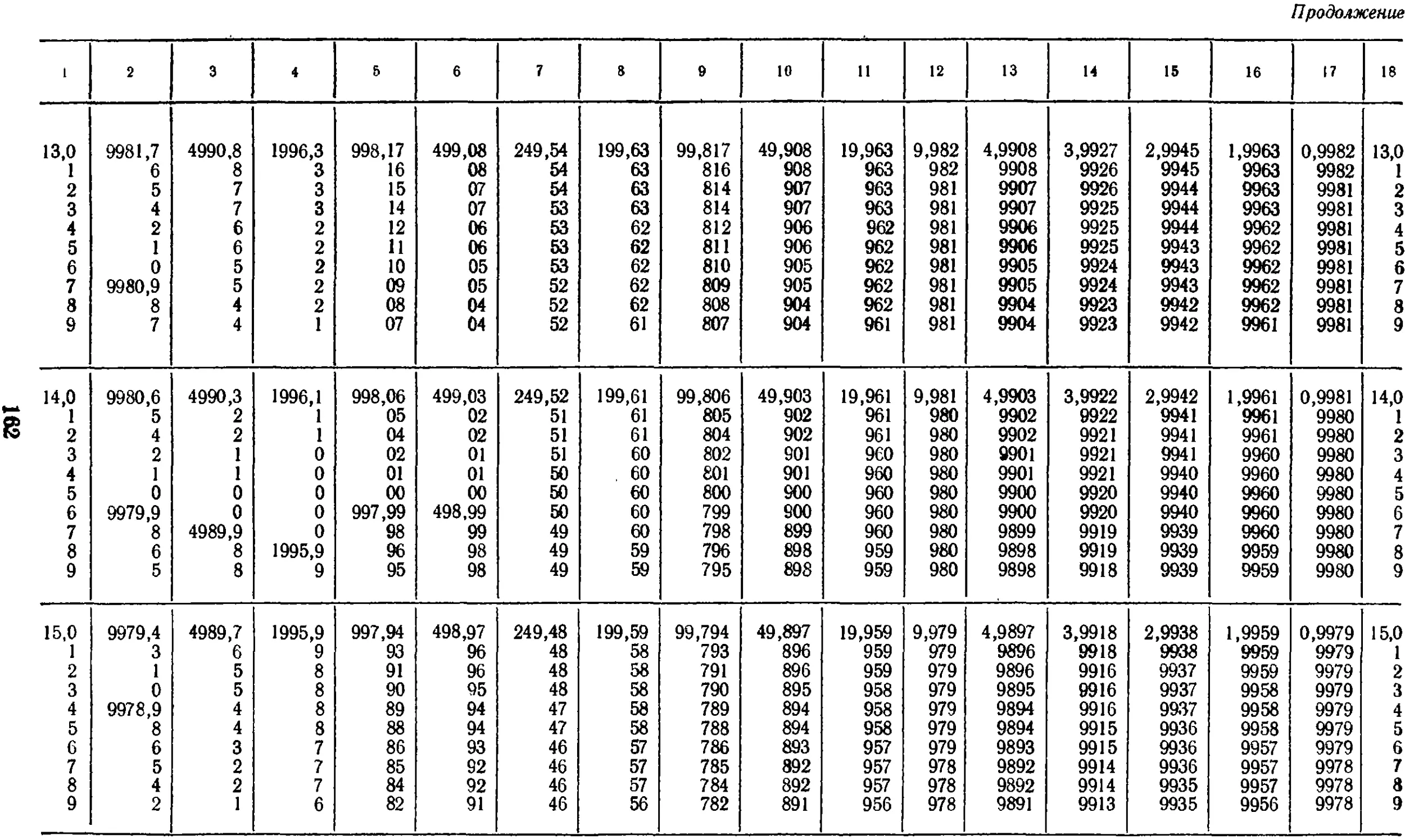
19.2. Градуировка стеклянной
мерной посуды
взвешиванием наполняющей воды
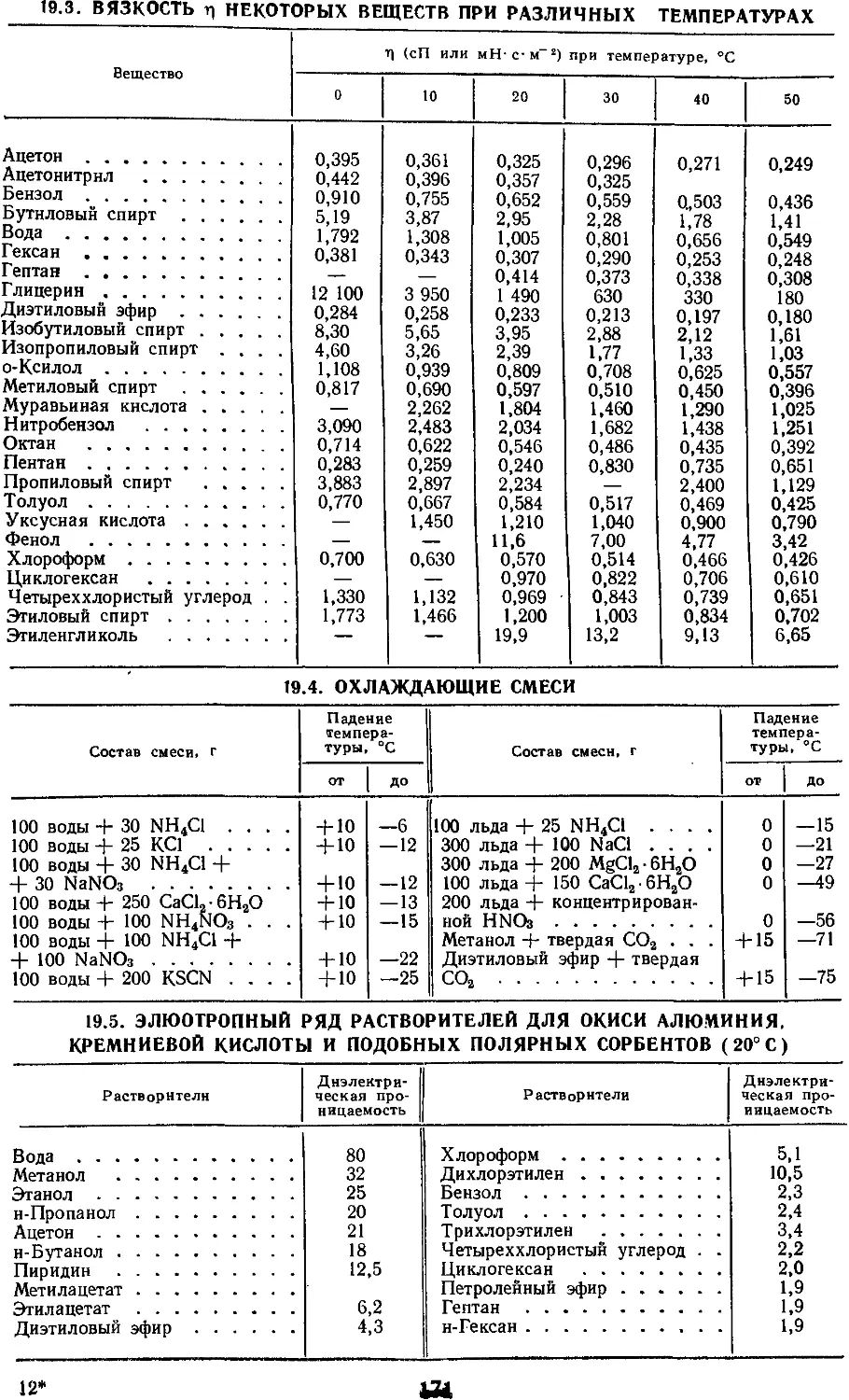
19.3. Вязкость (т|) некоторых
веществ при различных
температурах
19.4. Охлаждающие смеси . . .
19.5. Элюотропиый ряд
растворителей для окиси
алюминия, кремниевой кислоты
и подобных полярных
сорбентов (20° С)
19.6. Вычисление и обработка
результатов анализа . . .
19.6.1. Вычисление
результатов анализа и его
погрешности при
известном
коэффициенте вариации
19.6.2. Вычисление
результатов анализа и его
погрешности в
случае, когда
коэффициент вариации
неизвестен
19.6.3. Вычисление
количества
параллельных определений,
необходимых для
получения
результатов анализа с
погрешностью не выше
заданной
19.6.4. Выбор метода
анализа, точность
которого позволяет
получить
результаты с погрешностью
не выше заданной
19.6.5. Критерий
необходимости арбитражного
анализа
19.6.6. Оценка результатов
проверочных
анализов и
«шифрованных» проб ....
19.6.7. Правила действия с
приближенными
числами
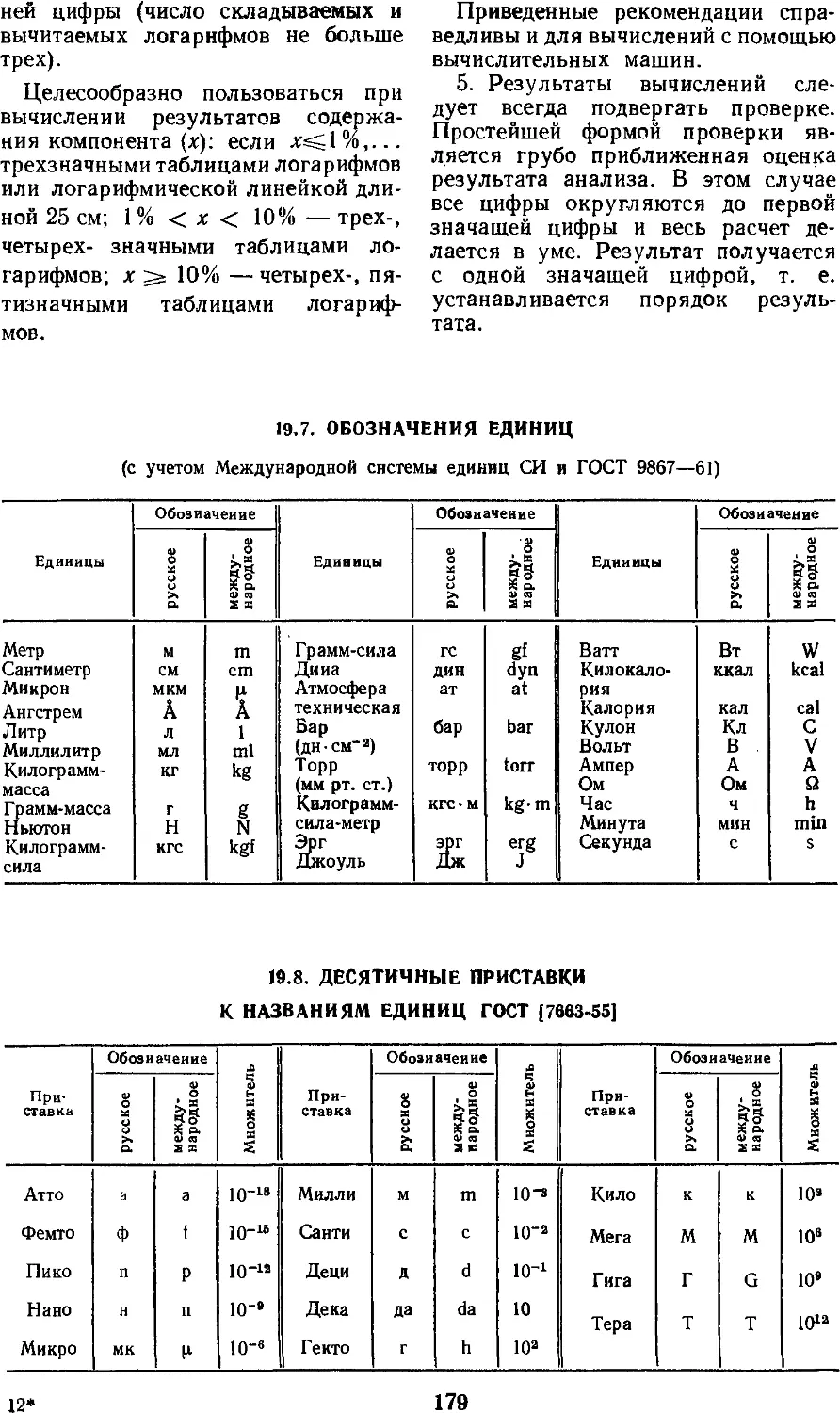
19.7. Обозначения единиц. . .
19.8. Десятичные приставки к
названиям единиц
[ГОСТ 7663—55] ....
19.9. Шкалы температур ....
19.10. Значения важнейших
универсальных констант. . .
19.11. Сведения о вредности и
опасности при работе с некоторыми
химическими реактивами ....
19.12. Список рекомендуемой
литературы
4
ЧТО МОЖНО НАЙТИ В СПРАВОЧНИКЕ
Справочник включает в себя
основные сведения по аналитической
химии, необходимые работнику
заводской химической лаборатории в его
повседневной работе.
Формально материалы
справочника можно разделить на четыре части.
В первой части приводятся сведения,
необходимые химику-аналитику при
использовании в практике наиболее
распространенных методов анализа:
гравиметрического, титриметрическо-
го и фотометрического, а также ряд
полезных сведений общего
характера.
Во второй части приведены
сведения, относящиеся к свойствам
растворов, в третьей — газов и паров
жидкостей. В четвертой части
помещены разные сведения, большей
частью относящиеся к смежным
областям науки.
Особенностью материала,
расположенного в первой части (1—17-й
разделы), является несколько
необычное для нашей литературы
построение таблиц. Например, факторы
пересчета химических соединений
расположены так, что допускается
как прямой, так и обратный пересчет
одной формы химического
соединения данного элемента в другую.
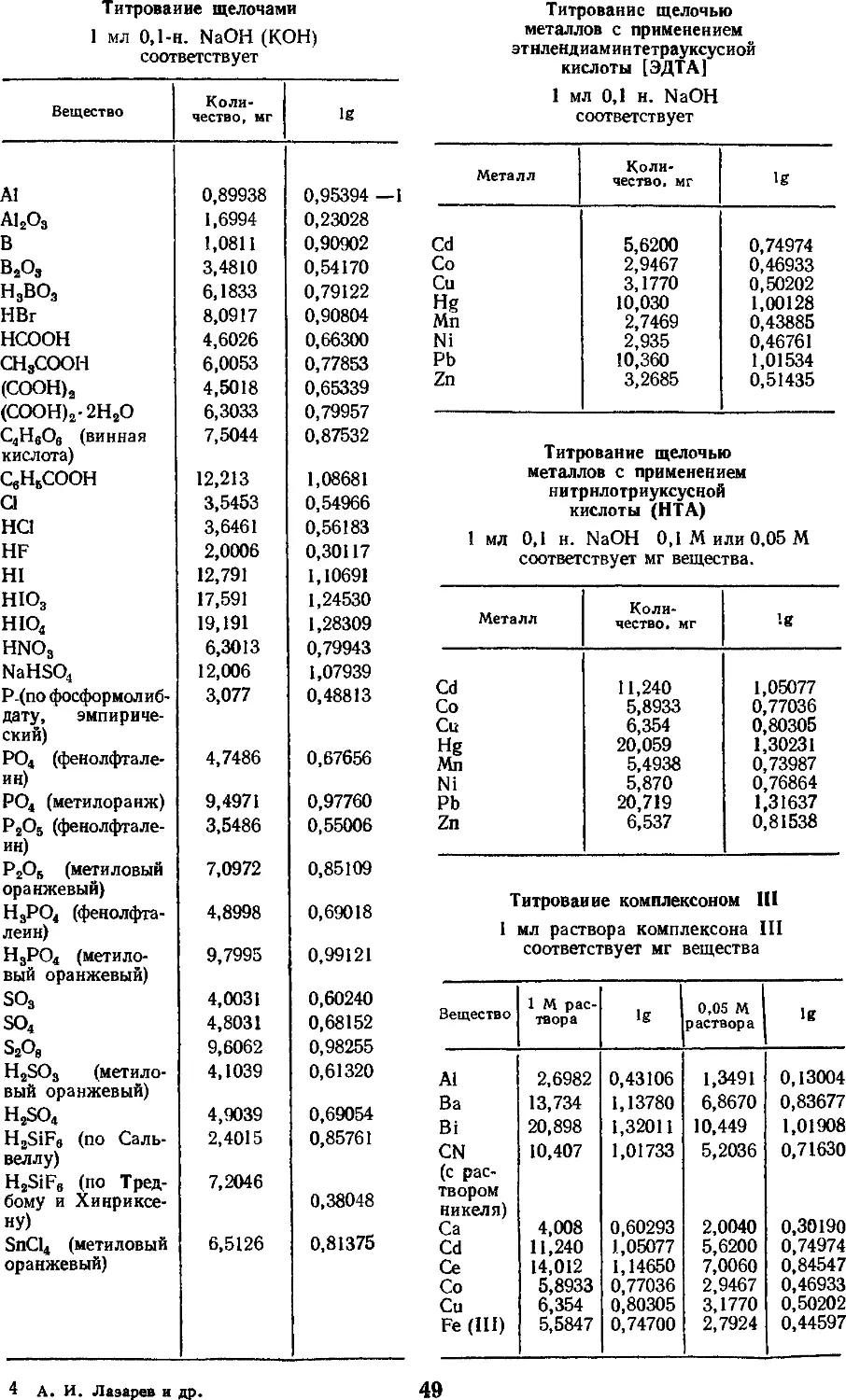
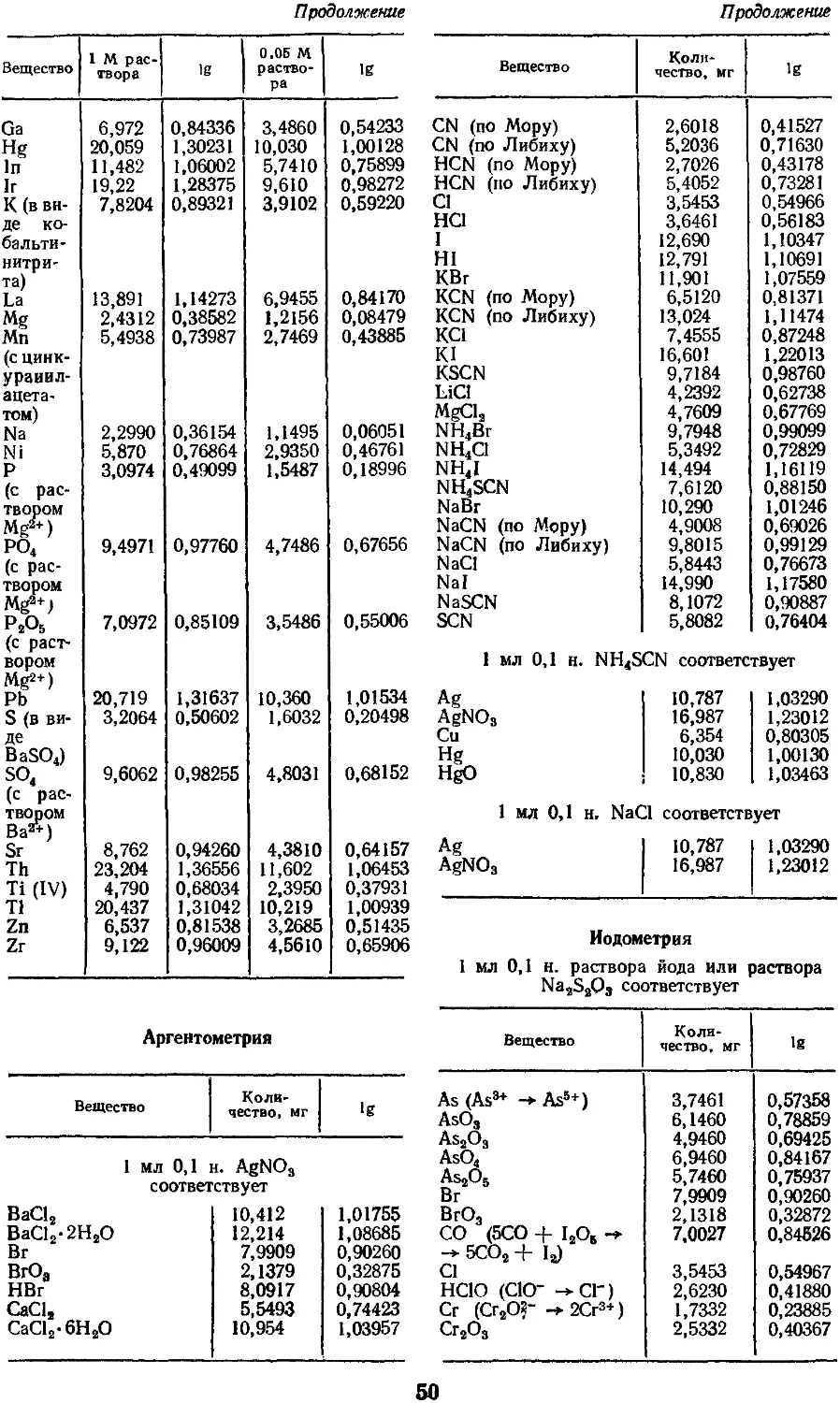
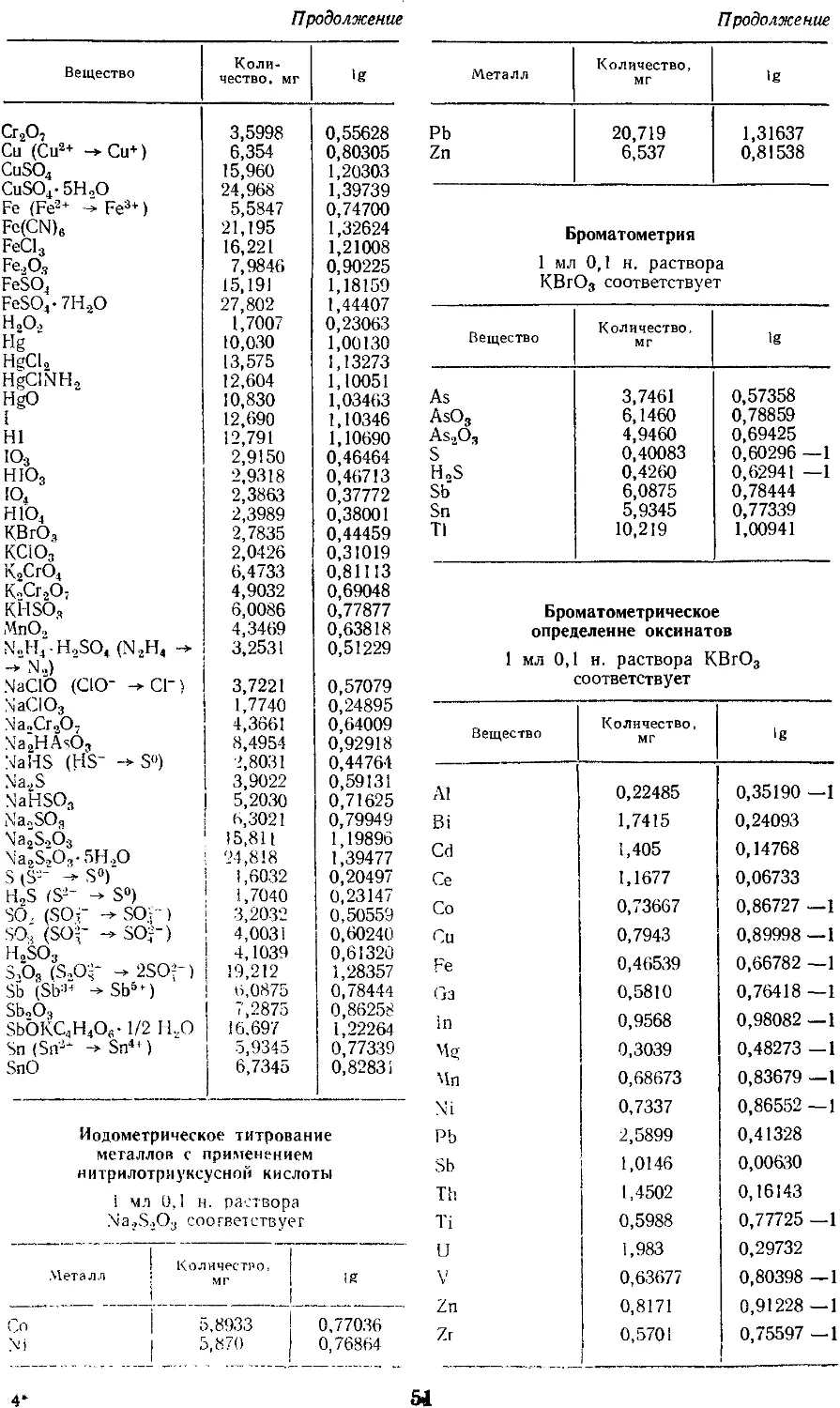
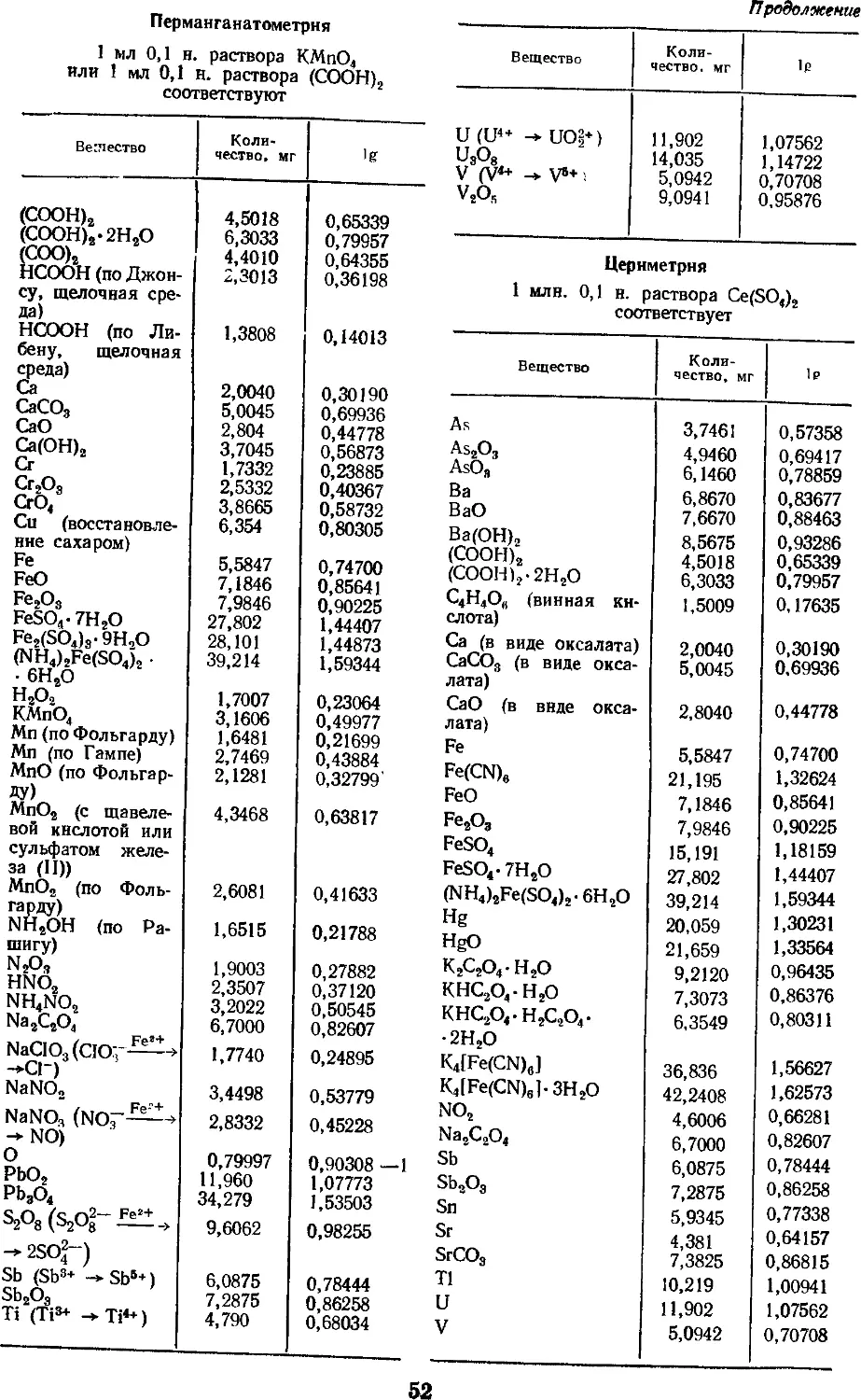
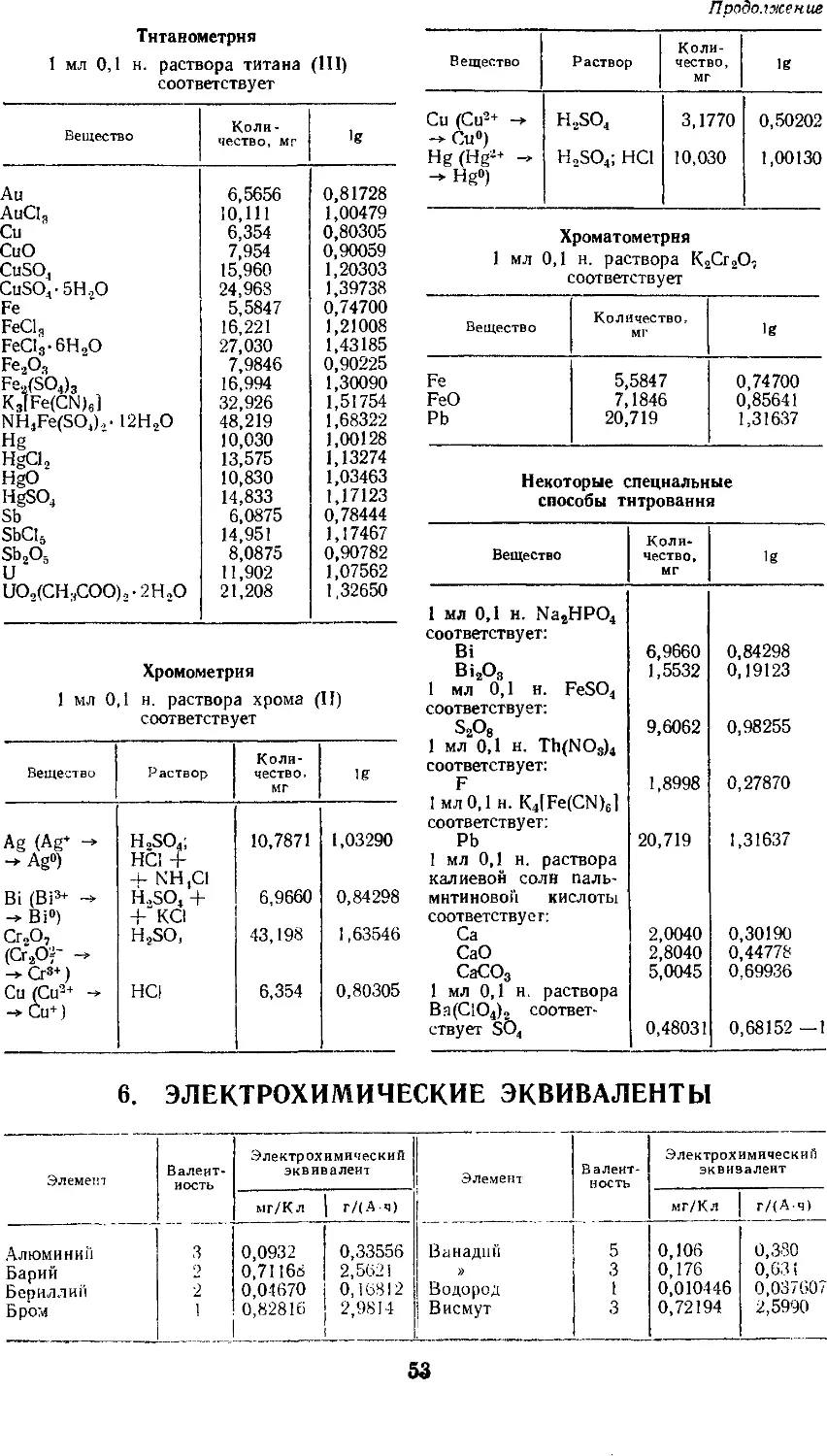
Эквиваленты в титриметрических
методах анализа даны в наиболее
приемлемой с практической точки зрения
форме, а именно: какому количеству
миллиграмм искомого вещества
соответствует 1 мл 0,1-н. раствора ти-
транта. Приведена классификация
реактивов по чистоте, а также
рациональный ассортимент
органических реактивов для определения
неорганических ионов, разработанный
ИРЕА (Москва).
Весьма полезными для читателя
будут данные по характеристике све-
топоглощения растворителей и
растворов неорганических и
органических веществ. Основное назначение
этих данных заключается в том, что
химик-аналитик всегда может
навести справку о величине светопогло-
щения (качественно или
полуколичественно) фона, на котором
осуществляется интересующая его
фотометрическая реакция.
В повседневной работе химику-
аналитику заводской лаборатории
иногда необходимо быстро решить
вопрос о возможности анализа
представленной ему пробы необычного
состава. В таких случаях будут
полезны сведения о групповом
разделении элементов, маскирующих
реагентах для металлов и некоторых
анионов, а также краткая
характеристика наиболее распространенных
фотометрических методов
определения металлов.
Из методов группового
разделения ионов рассмотрены способы
осаждения и экстракции, которые
широко используются в лабораториях
разной степени оснащенности
оборудованием. Описаны условия
разделения широко известными и
доступными реагентами.
В разделе 17 впервые в литературе
приводятся рекомендации по выбору
рациональной навески (или другой
величины) в химическом анализе.
Применение рациональных величин
позволяет значительно упростить
расчеты результатов анализа, так как
они непосредственно следуют из
показаний прибора, отмечающего
количественную сторону процесса
анализа, точнее его завершающей стадии
5
(показания весов при взвешивании
весовой формы, отсчет по бюретке
или на шкале фотоколориметра и
т. д.).
Во второй части (сведения,
относящиеся к свойствам растворов)
приводятся практически все возможные
в практике случаи пересчета одной
формы выражения концентрации
вещества в другую. Даны наиболее
доступные для условий заводских
лабораторий способы приготовления
стандартных (эталонных) растворов
концентрации 0,01 М, указаны
способы перевода металлов и некоторых
их соединений в раствор.
В настоящее время
химики-аналитики повсеместно пользуются для
проверки и установки рН
растворов специальными буферными
растворами, которые используются
также и для проверки показаний и
регулировки рН-метров.
Соответствующие сведения читатель найдет в
разделе 17.4. Приводятся также
сведения по плотности наиболее
распространенных кислот и щелочей,
приготовлению их разбавленных
растворов, приближенное значение рН
некоторых растворов, произведения
растворимости и растворимость
наиболее употребительных химических
соединений в химическом анализе.
Периодическая система элементов
Д. И. Менделеева — естественная
система химических элементов,
созданная Д. И. Менделеевым на основе
открытого им периодического закона
(1869 г.).
Формулировка закона данная
Д. И. Менделеевым в 1871 г., гласит:
«Физические и химические свойства
элементов, проявляющиеся в
свойствах простых и сложных тел, ими
образуемых, стоят в периодической
зависимости. . . от их атомного
веса».
Современная, более точная
формулировка периодического закона
отражает периодичность в измене-
В третьем разделе (газы и па ры
жидкостей) приводятся сведения о
способах получения газов,
осушителей для них и поглотителей,
данные о растворимости и плотности
газов, а также ряд других полезных
для химика-аналитика сведений.
Основным материалом четвертого
раздела (разные сведения) являются
сведения о калибровке мерной
посуды, допускаемых отклонениях от
номинальной вместимости
калиброванной посуды технического класса,
приемы вычисления и обработки
результатов анализа, обозначения
единиц, а также ряд полезных сведений
по элементарным математике и
физике.
Сведения по элементарной физике
включают данные по физическим
свойствам некоторых наиболее
употребительных в практике химика-
аналитика веществ, что избавляет
его от необходимости частого
обращения к специальным справочникам.
Справочник для химика-аналитика
заводской лаборатории издается в
нашей стране впервые. Неизбежные
при этом недостатки и критика будут,
безусловно, восприняты авторами
с благодарностью и учтены
издательством при выпуске такого рода
пособий для работников заводских
химических лабораторий в будущем.
нии свойств элементов от числа
электронов в атоме, определяемого
зарядом атомного ядра. Это число
равно порядковому (атомному)
номеру элемента в системе
Менделеева.
Периодическая система отображает
объективно существующую
взаимосвязь между химическими
элементами, поэтому она и была названа
Д. И. Менделеевым «естественной»
системой элементов. Периодическая
система и периодический закон
являются одним из наиболее широких
обобщений в области физики и
химии. Теория Бора, развитая в
дальнейшем А. Зоммерфельдом, качест-
1. ПЕРИОДИЧЕСКАЯ СИСТЕМА
ЭЛЕМЕНТОВ Д. И. МЕНДЕЛЕЕВА
6
венно объяснила и саму причину
периодичности в системе Менделеева.
Согласно этой теории, электроны
движутся вокруг ядра лишь
определенным образом, по «разрешенным»
орбитам. Иными словами, энергия
электрона в атоме может иметь ряд
определенных дискретных значений
(уровней энергии). В
многоэлектронном атоме электроны, заполняя
«разрешенные» орбиты, располагаются
слоями и оболочками. Чем дальше
от ядра находится оболочка (К, L,
Мит. д.), тем слабее связаны
с ядром входящие в ее состав
электроны. Эти периферические
(внешние) электроны и определяют
способность элементов к химическому
взаимодействию.
Причина периодичности свойств
элементов, открытая Д. И.
Менделеевым, заключается, следовательно,
в том, что по мере возрастания
числа электронов, окружающих
ядро, наступает такая стадия, когда
заканчивается заполнение данного
электронного слоя и начинается
заполнение следующего. При этом
элементы с одним, двумя, тремя и т. д.
электронами в этом новом наружном
слое воспроизводят химические
свойства элементов, имевших также один,
два три и т. д. электронов в
предшествовавшем, теперь уже
глубинном слое. Причина послойного
расположения электронов в атоме стала
ясна в 1925 г., когда Паули
сформулировал «принцип запрета», согласно
которому на одном энергетическом
уровне (в атоме, молекуле) может
находиться не более двух
электронов, причем эти электроны должны
иметь противоположно
ориентированные спины. Периодически
меняются не только химические свойства
элементов, но и многие их физические
свойства, такие как атомный объем,
коэффициент объемного сжатия,
коэффициент теплового расширения,
электропроводность, температура
плавления и т. п., т. е. именно те
свойства, которые связаны главным
образом с наружными электронными
слоями, тогда как свойства,
связанные с глубинными слоями, меняются
монотонно без какой-либо
периодичности (атомная масса,
характеристический рентгеновский спектр).
Распределение электронов по слоям дано
в разделе 2.
1. 1. ПЕРИОДИЧНОСТЬ СВОЙСТВ
В СИСТЕМЕ Д. И. МЕНДЕЛЕЕВА
Ионизационный потенциал
характеризует энергию связи электрона
в атоме. Периодичность хорошо
наблюдается на примере изменения
потенциала ионизации первого
электрона в зависимости от порядкового
номера элемента. Резкие максимумы
наблюдаются у атомов инертных
газов, обладающих наиболее
устойчивой конфигурацией. В минимумах
кривой находятся щелочные
металлы. В пределах одного периода
потенциал ионизации изменяется не
монотонно. На кривой наблюдаются
вторичные максимумы, менее резко
выраженные, соответствующие
заполнению s-оболочки у элементов II
группы — Be Mg, Zn, Cd и Hg.
Следующие максимумы наблюдаются
у элементов V группы — N, P, As,
что соответствует энергетически
выгодному половинному заполнению р-
оболочки, содержащей три неспа-
ренных электрона. В пределах одной
группы с увеличением порядкового
номера величина потенциала
ионизации в общем убывает, что связано
с увеличением расстояния от ядра
внешней электронной оболочки.
Периодически изменяется и сродство к
электрону, выражающее работу
присоединения электрона к
нейтральному атому.
Валентность — число электронов,
участвующих в образовании
химической связи. Наиболее четко
периодическая зависимость выявляется
на примере высшей положительной
валентности, равной числу
электронов в наружной электронной
оболочке атома. В малых периодах
она возрастает от 1 до 7 при переходе
от I к VII группе. У элементов
больших периодов высшая
положительная валентность изменяется
более сложно. Как правило, в первой
половине периода она возрастает от
1 до 8, затем при переходе к
побочной подгруппе II группы
уменьшается до 2 и вновь возрастает
7
к концу периода до 7. Некоторые
элементы проявляют аномально
высокую валентность, объясняемую
строением их атома. Так,
валентность Си, Ag и Аи доходит до 3.
Это, по-видимому, связано с
непрочностью 18-электронной оболочки,
формирование которой заканчивается
в середине большого периода. Для
лантанидов характерна высшая
положительная валентность 3,
соответствующая номеру группы. Однако
при начале формирования
^-оболочки образующие ее электроны связаны
не очень прочно. Вследствие этого
Се, Рг и отчасти Nd дают соединения,
в которых они четырехвалентны. Эта
оболочка заполняется в два приема,
и электронная конфигурация
седьмого элемента гадолиния оказывается
наиболее устойчивой. Однако
следующий за ним элемент тербий снова
проявляет высшую положительную
валентность 4.
Атомные оптические спектры
возникают при электронных переходах
в валентной оболочке.
Периодичность наблюдается не только в
спектрах атомов, но и в электронных
спектрах ионов металлов в
растворах. Способность вещества в растворе
поглощать свет определенных длин
волн является одним из свойств
химической системы, связанным с
энергетической характеристикой
валентных электронов атомов.
Наиболее четко периодичность наблюдается
у переходных металлов больших
периодов. В горизонтальном
направлении с увеличением заряда ядра
полосы поглощения смещаются в
длинноволновую область спектра. При
этом максимум достигается у
элементов в конце переходного периода,
а у элементов следующего периода
начинается вновь. Так, в ряду
ниобий (V) — молибден (VI) — тех-
нецкий (VII) максимум полос свето-
поглощения изменяется от 235 до
290 мм, а в ряду тантал (V) —
вольфрам (VI) — рений (VII) — от менее
216 до 226 нм.
Несколько сложнее проявляется
зависимость в ряду переходных
металлов 4-го периода. Смещение
максимума длины волны в
длинноволновую область прерывается на
марганце (II) ввиду особенностей
строения электронной оболочки этого
иона.
В вертикальном направлении с
увеличением заряда ядра полосы
поглощения смещаются в коротковолновую
область.
Атомные и ионные радиусы
элементов также изменяются
периодически с возрастанием порядкового
номера. Максимальные величины для
этих параметров приходятся на
щелочные металлы. В вертикальном
направлении сверху вниз величина
атомных и ионных радиусов
возрастает. Четкая закономерность
прослеживается для многих других
физических и химических свойств
элементов, например атомных объемов,
внешнего вида, кристаллической
структуры, температур плавления,
коэффициентов линейного
расширения и объемной сжимаемости в
кристаллическом состоянии,
характера окислов, водородных
соединений,
окислительно-восстановительных свойств элементов, их комп-
лексообразовання.
То, что между свойствами атомов
и свойствами химических систем,
содержащих эти атомы, существует
определенная взаимосвязь, является
основной для создания различного
рода классификаций
химико-аналитических свойств элементов на
основе периодического закона,
разработанных советскими химиками-
аналитиками И. П. Алимарнным,
Ф. М, Шемякиным, А. П. Крешко-
вым, Н. И. Блок и др.
I. 2. ХИМИКО-АНАЛИТИЧЕСКАЯ
ЗВЕЗДА ЭЛЕМЕНТОВ
Свойства элементов и их
соединений в периодической системе
элементов изменяются закономерно в
трех направлениях: вертикальном,
горизонтальном н диагональном
(только диагональ слева направо и
сверху вниз).
Элемент, расположенный на
пересечении этих направлений,образует
звезду с ближними и дальними
аналогами. Ближние аналоги являются
непосредственными соседями данного
8
элемента; дальние аналоги
расположены вслед за ближними по трем
направлениям (сечениям). Большим
сходством свойств обладают
ближние аналоги, этого элемента
сходство которых по разным сечениям
неодинаково.
Выделение звезды элемента и
рассмотрение совокупности его свойств
одновременно с ближними и
дальними аналогами дают возможность
сопоставить, а иногда и предсказать
ряд свойств, важных для анализа
данного элемента и его аналогов:
чувствительность, избирательность
метода, отношение к реагентам,
каталитические свойства и др.
Пример. Рассмотрим некоторые
свойства соединений рения,
используемых в анализе. Для этого выделим
его звезду с ближними (=) и
дальними (—) аналогами.
23
24
Сг
25
МП
42
Мо
Тс
та
73
W
74
43
: Re
75
OS
76
77
IT
107
Высшие окислы рения, технеция,
осмия, марганца обладают высокой
летучестью; труднее улетучиваются
окислы молибдена, вольфрама.
Следовательно, обычным методом
дистилляции эти аналоги разделить
затруднительно и необходимо использовать
другие методы или какие-либо
приемы, усиливающие различия в
летучести.
На основании аналогии в звезде
известная реакция осмия (ближнего
аналога рения и технеция) с тиомо
чевиной использована для разработ
ки фотометрического метода опреде
ления рения, а позднее и технеция
Таким образом, реагент, применяв
мый для анализа одного аналога
как правило, будет взаимодейство
вать и с другими элементами-анало
гами по звезде, и это необходимо
учитывать при характеристике
избирательности методов.
Роданидные комплексы рения (IV),
молибдена (V), вольфрама (V),
технеция (IV и V) широко используются
при их фотометрическом
определении.
Близость свойств комплексов
затрудняет анализ одного из них
при одновременном присутствии в
растворе других аналогов.
Реакции между теллуратом и се-
ленатом в кислой среде ускоряются
соединениями рения (<VII); эти же
реакции использованы для
определения малых содержаний
молибдена—аналога рения. Каждый из этих
аналогов будет мешать определению
другого.
Вызывают трудности разделение
на ионообменных смолах ионов—
аналогов молибдена, вольфрама,
рения, технеция.
Некоторые из методов анализа и
отделения рения и вольфрама могут
оказаться полезными при работе с их
ближним аналогом-элементом ю^Э.
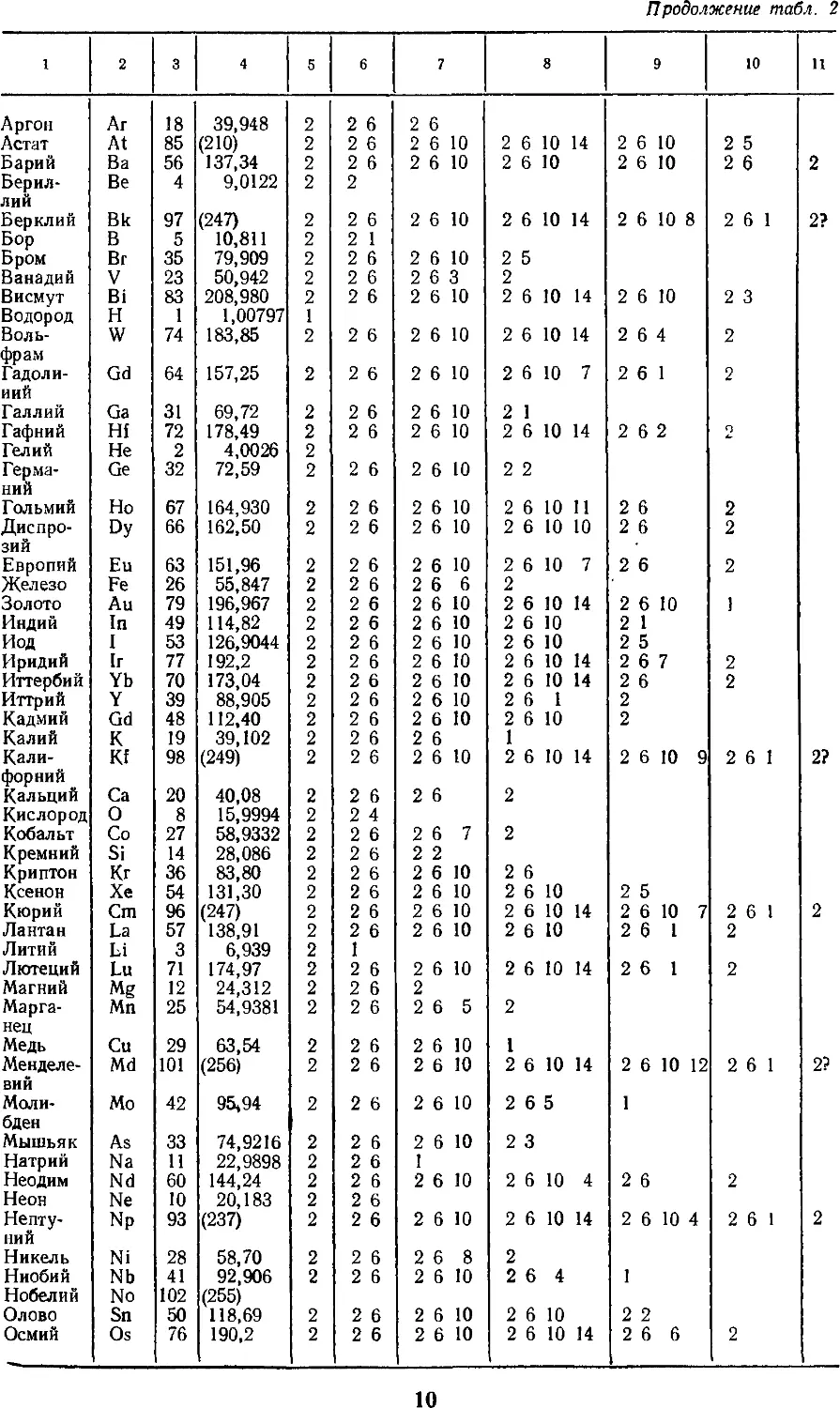
2. ТАБЛИЦА АТОМНЫХ МАСС
Название
элементов
1
Азот
Актиний
Алюминии
Америции
Символ
2
N
Ас
А1
Am
2 о.
S Ф
5; °
3
7
89
13
95
Атомная
масса
4
14,0067
(227)
26,9815
(243)
Распределение электронов по орбитам
Л
Is
5
2
2
2
2
L
2s2p
6
2 3
2 6
2 6
2 6
м
3s3p3d
7
2 6 10
2 1
2 6 10
N
4s4p4d4f
8
2 6 10 14
2 6 10 14
О
5s5p5d5/
9
2 6 10
2 6 10 7
р
6s6p6d
10
2 6 1
2 6
о
7?
11
■)
2
9
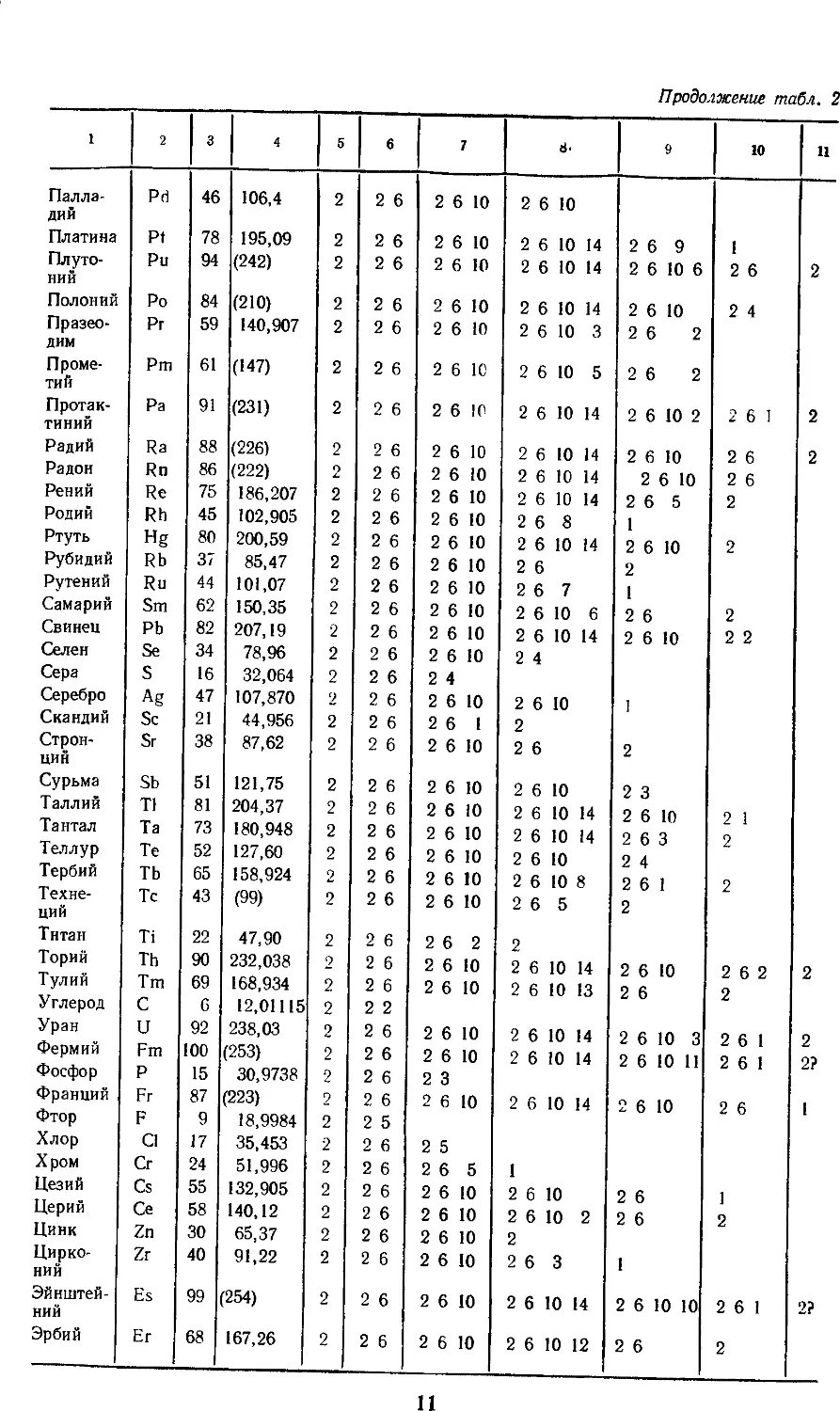
Продолжение табл. 2
1
Аргон
Астат
Барий
Бериллий
Берклий
Бор
Бром
Ванадий
Висмут
Водород
Вольфрам
Гадолиний
Галлий
Гафний
Гелий
Германий
Гольмий
Диспрозии
Европий
Железо
Золото
Индий
Иод
Иридий
Иттербий
Иттрий
Кадмий
Калий
Калифорний
Кальций
Кислород
Кобальт
Кремний
Криптон
Ксенон
Кюрий
Лантан
Литий
Лютеций
Магний
Марганец
Медь
Менделевии
Молибден
Мышьяк
Натрий
Неодим
Неон
Нептуний
Никель
Ниобий
Нобелий
Олово
Осмий
2
Аг
At
Ва
Be
Bk
В
Вг
V
Bi
н
W
Gd
Ga
Hf
Не
Ge
Но
Dy
Eu
Fe
Au
In
I
Ir
Yb
Y
Gd
К
Kf
Ca
0
Co
Si
Kr
Xe
Cm
La
Li
Lu
Mg
Mn
Cu
Md
Mo
As
Na
Nd
Ne
Np
Ni
Nb
No
Sn
Os
3
18
85
56
4
97
5
35
23
83
1
74
64
31
72
2
32
67
66
63
26
79
49
53
77
70
39
48
19
98
20
8
27
14
36
54
96
57
3
71
12
25
29
101
42
33
11
60
10
93
28
41
102
50
76
4
39,948
(210)
137,34
9,0122
(247)
10,811
79,909
50,942
208,980
1,00797
183,85
157,25
69,72
178,49
4,0026
72,59
164,930
162,50
151,96
55,847
196,967
114,82
126,9044
192,2
173,04
88,905
112,40
39,102
(249)
40,08
15,9994
58,9332
28,086
83,80
131,30
(247)
138,91
6,939
174,97
24,312
54,9381
63,54
(256)
95,94
74,9216
22,9898
144,24
20,183
(237)
58,70
92,906
(255)
118,69
190,2
5
2
2
2
2
2
2
2
2
2
1
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
6
2 6
2 6
2 6
2
2 6
2 1
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 4
2 6
2 6
2 6
2 6
2 6
2 6
1
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
7
2 6
2 6 10
2 6 10
2 6 10
2 6 10
2 6 3
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 6
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6
2 6 10
2 6
2 6 7
2 2
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2
2 6 5
2 6 10
2 6 10
2 6 10
2 6 10
1
2 6 10
2 6 10
2 6 8
2 6 10
2 6 10
2 6 10
8
2 6 10 14
2 6 10
2 6 10 14
2 5
2
2 6 10 14
2 6 10 14
2 6 10 7
2 1
2 6 10 14
2 2
2 6 10 11
2 6 10 10
2 6 10 7
2
2 6 10 14
2 6 10
2 6 10
2 6 10 14
2 6 10 14
2 6 1
2 6 10
1
2 6 10 14
2
2
2 6
2 6 10
2 6 10 14
2 6 10
2 6 10 14
2
1
2 6 10 14
2 6 5
2 3
2 6 10 4
2 6 10 14
2
2 6 4
2 6 10
2 6 10 14
9
2 6 10
2 6 10
2 6 10 8
2 6 10
2 6 4
2 6 1
2 6 2
2 6
2 6
2 6
2 6 10
2 1
2 5
2 6 7
2 6
2
2
2 6 10 9
2 5
2 6 10 7
2 6 1
2 6 1
2 6 10 12
1
2 6
2 6 10 4
1
2 2
2 6 6
10
2 5
2 6
2 6 1
2 3
2
2
о
2
2
2
1
2
2
2 6 1
2 6 1
2
2
2 6 1
2
2 6 1
2
li
2
2?
2?
2
2?
2
10
Продолжение табл. 2
1
Палладий
Платина
Плутоний
Полоний
Празеодим
Прометий
Протактиний
Радий
Радон
Рений
Родий
Ртуть
Рубидий
Рутений
Самарий
Свинец
Селен
Сера
Серебро
Скандий
Стронций
Сурьма
Таллий
Тантал
Теллур
Тербий
Технеций
Титан
Торий
Тулий
Углерод
Уран
Фермий
Фосфор
Франций
Фтор
Хлор
Хром
Цезий
Церий
Цинк
Цирконий
Эйнштейний
Эрбий
2
Pd
Pt
Pu
Ро
Pr
Pm
Pa
Ra
Rn
Re
Rh
Hg
Rb
Ru
Sm
Pb
Se
S
Ag
Sc
Sr
Sb
Tl
Та
Те
Tb
Тс
Ti
Th
Tm
С
U
Fm
P
Fr
F
CI
Cr
Cs
Ce
Zn
Zr
Es
Er
3
46
78
94
84
59
61
91
88
86
75
45
80
37
44
62
82
34
16
47
21
38
51
81
73
52
65
43
22
90
69
6
92
100
15
87
9
17
24
55
58
30
40
99 (
.
4
106,4
195,09
(242)
(210)
140,907
(147)
(231)
(226)
(222)
186,207
102,905
200,59
85,47
101,07
150,35
207,19
78,96
32,064
107,870
44,956
87,62
121,75
204,37
180,948
127,60
158,924
(99)
47,90
232,038
168,934
12,01115
238,03
(253)
30,9738
223)
18,9984
35,453
51,996
132,905
140,12
65,37
91,22
254)
167,26
5
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
9
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2
6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 2
2 6
2 6
2 6
2 6
2 5
2 6
2 6
2 6
2 6
2 6
2 6
2 6
2 6
7
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 1С
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 4
2 6 10
2 6 1
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 2
2 6 10
2 6 10
2 6 10
2 6 10
2 3
2 6 10
2 5
2 6 5
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
2 6 10
<j.
2 6 10
2 6 10 14
2 6 10 14
2 6 10 14
2 6 10 3
2 6 10 5
2 6 10 14
2 6 10 14
2 6 10 14
2 6 10 14
2 6 8
2 6 10 14
2 6
2 6 7
2 6 10 6
2 6 10 14
2 4
2 6 10
2
2 6
2 6 10
2 6 10 14
2 6 10 14
2 6 10
2 6 10 8
2 6 5
2
2 6 10 14
2 6 10 13
2 6 10 14
2 6 10 14
2 6 10 14
I
2 6 10
2 6 10 2
2
2 6 3
2 6 10 14
2 6 10 12
9
2 6 9
2 6 10 6
2 6 10
2 6 2
2 6 2
2 6 10 2
2 6 10
2 6 10
2 6 5
1
2 6 10
2
1
2 6
2 6 10
1
2
2 3
2 6 10
2 6 3
2 4
2 6 1
2
2 6 10
2 6
2 6 10 3
2 6 10 11
2 6 10
2 6
2 6
1
2 6 10 10
2 6
10
1
2 6
2 4
2 6 1
2 6
2 6
2
2
2
2 2
2 1
2
2
2 6 2
2
2 6 1
2 6 1
2 6
]
2
2 6 1
2
ll
2
2
2
2
2
2?
1
2?
11
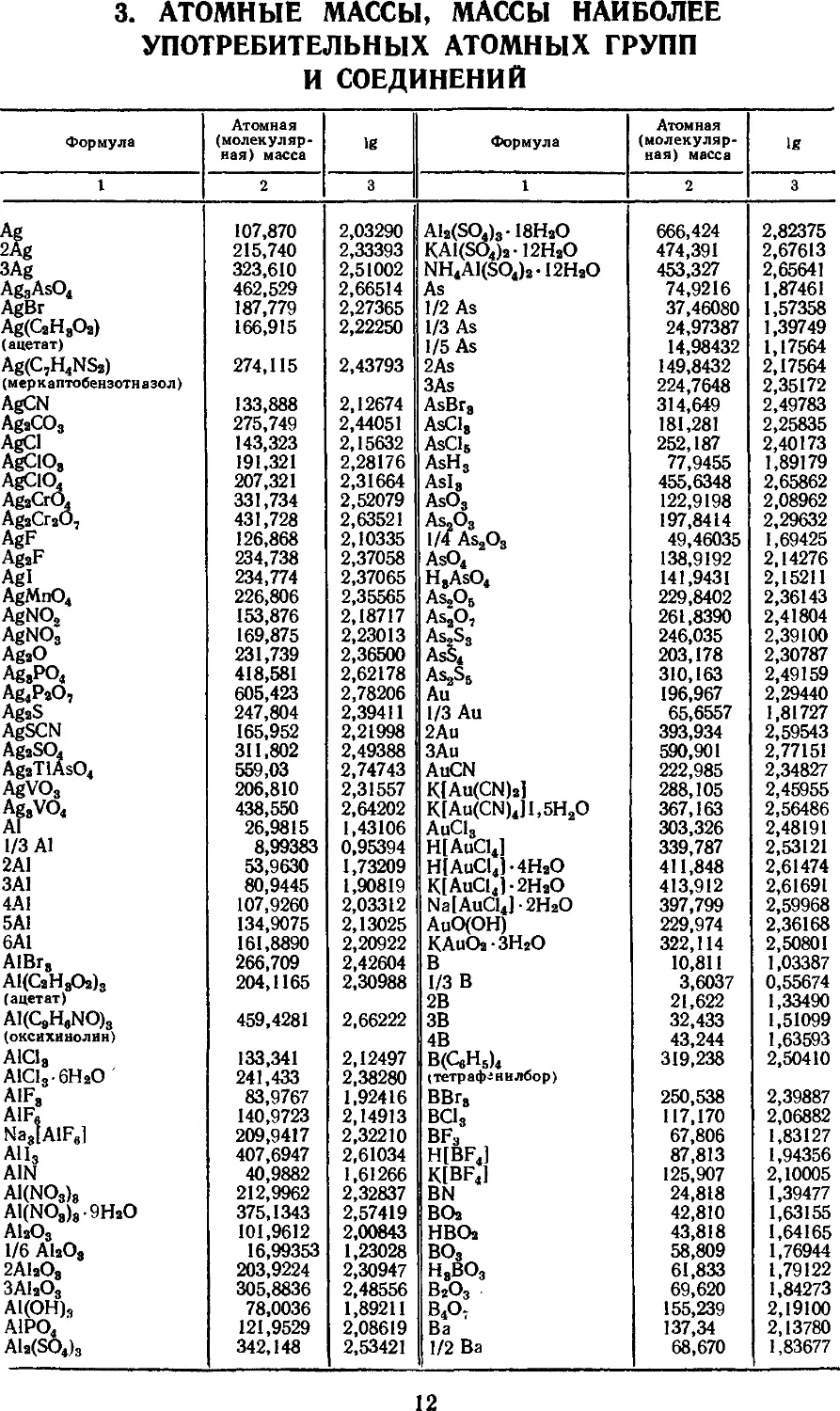
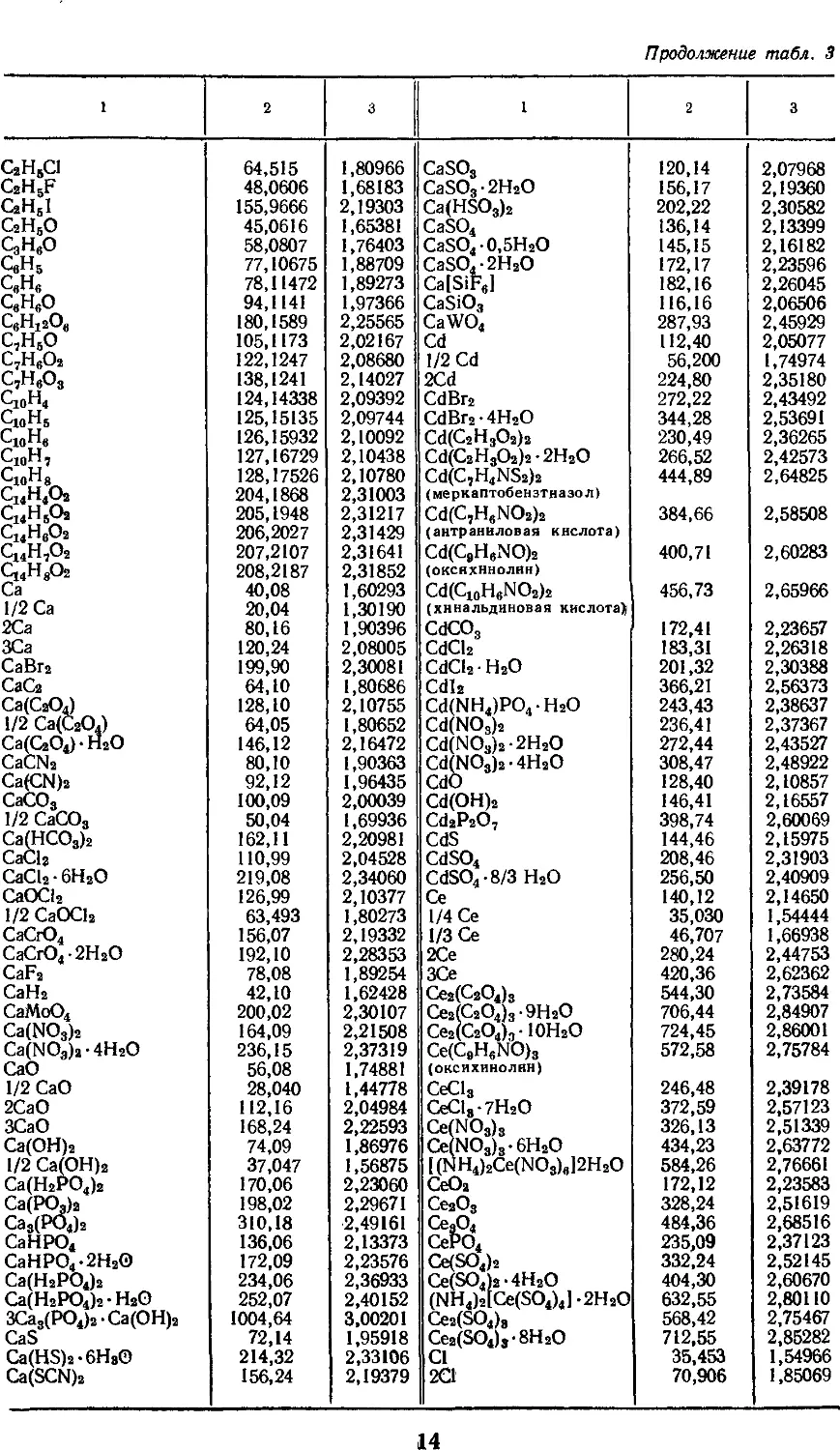
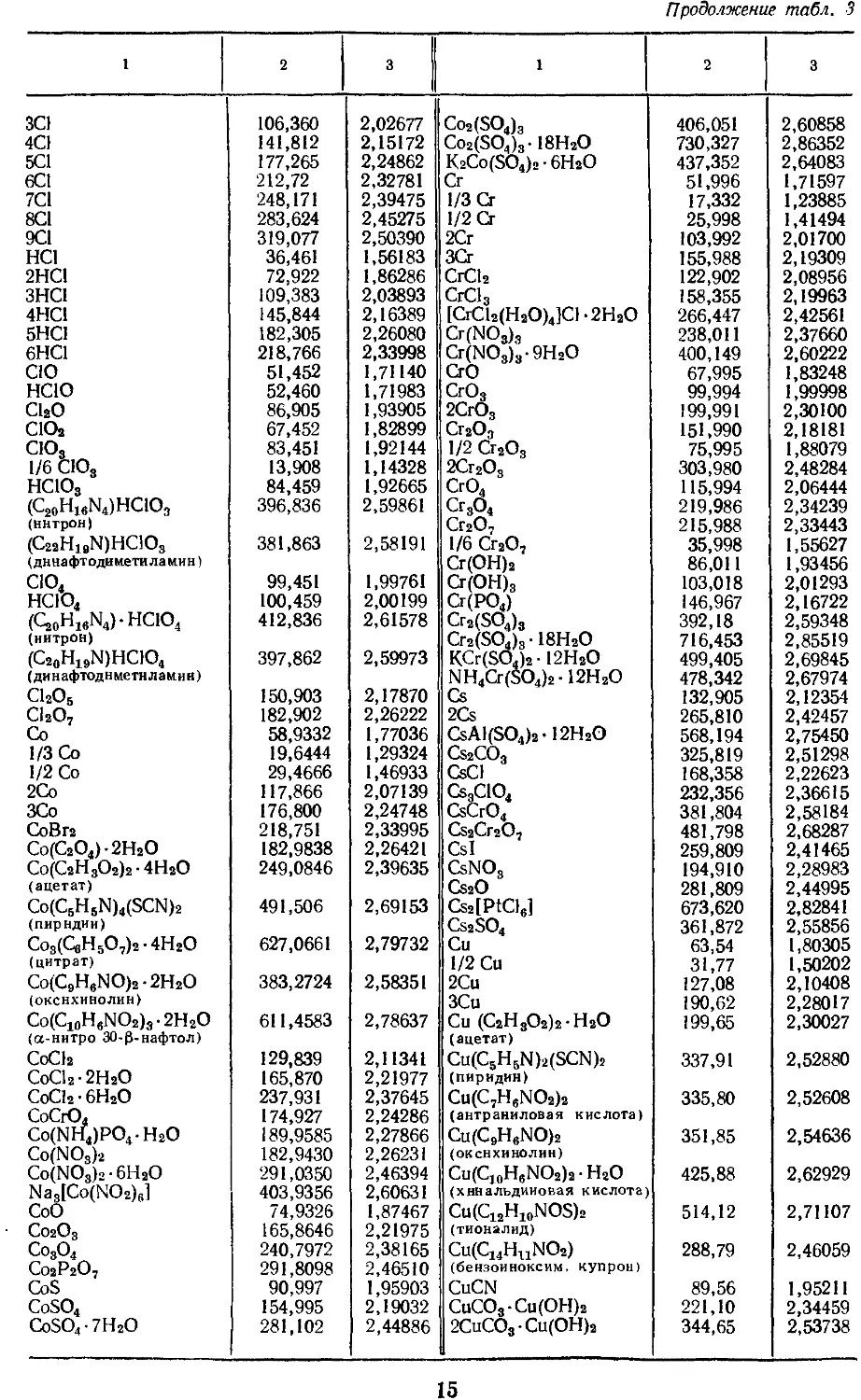
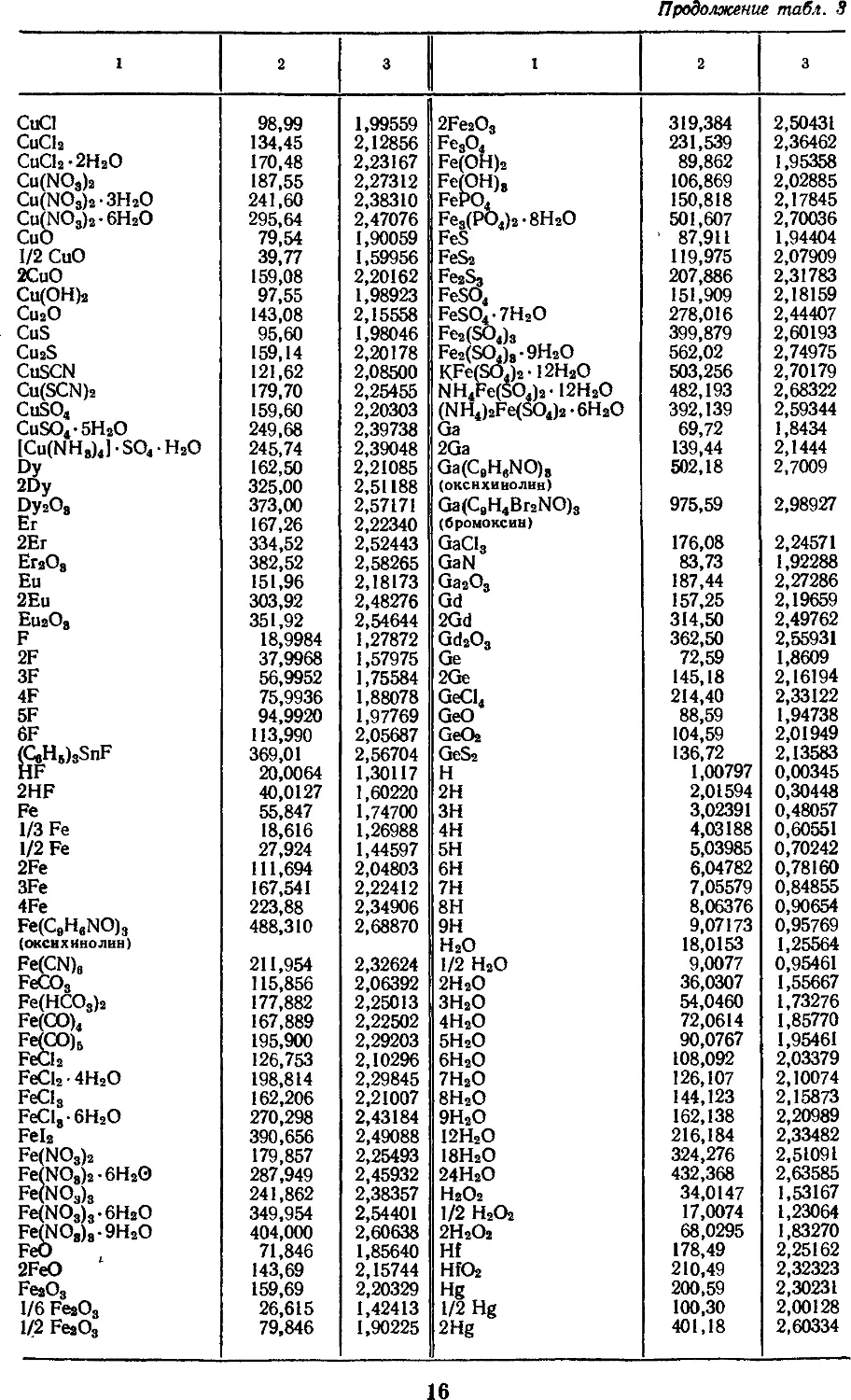
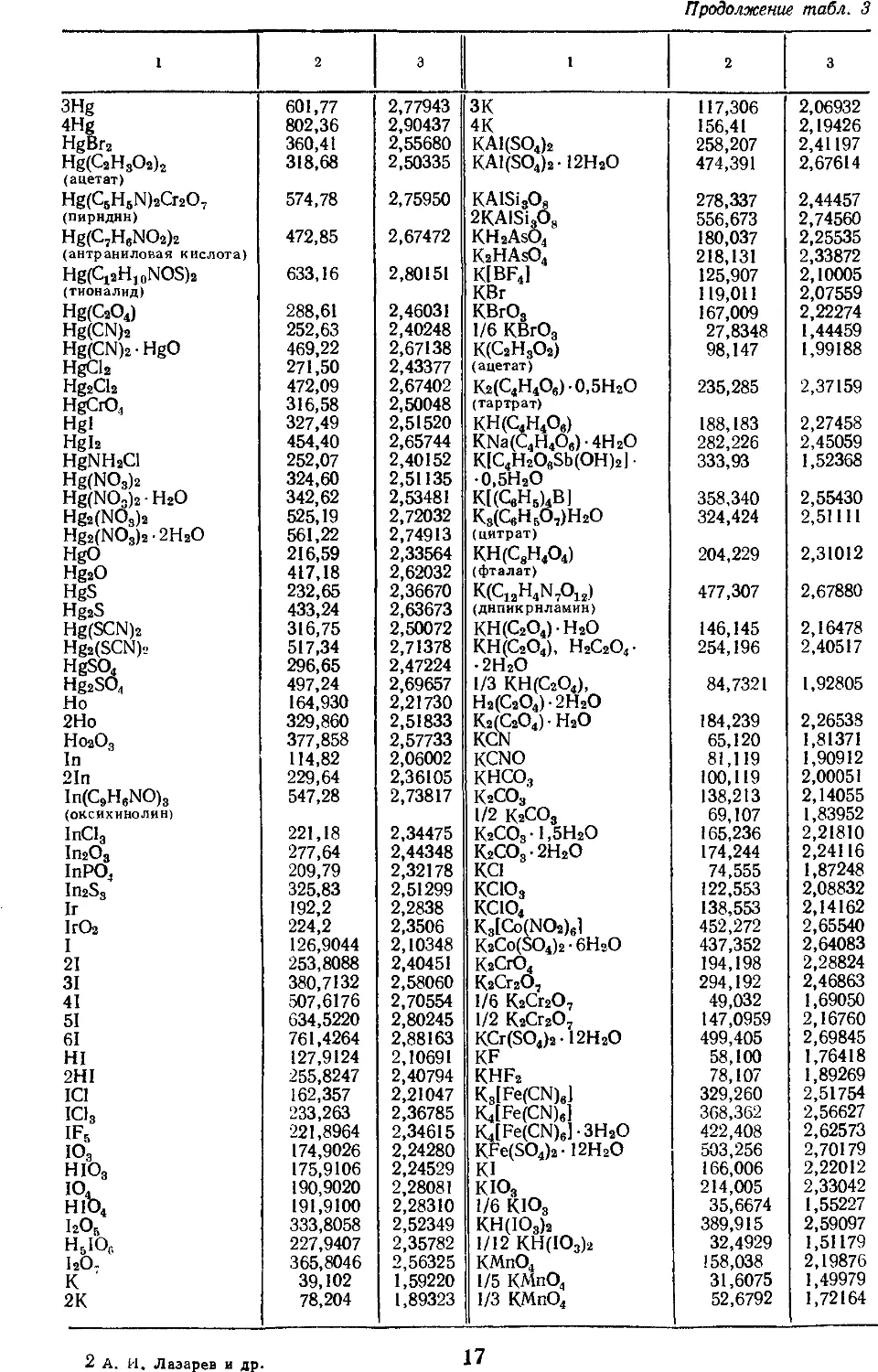
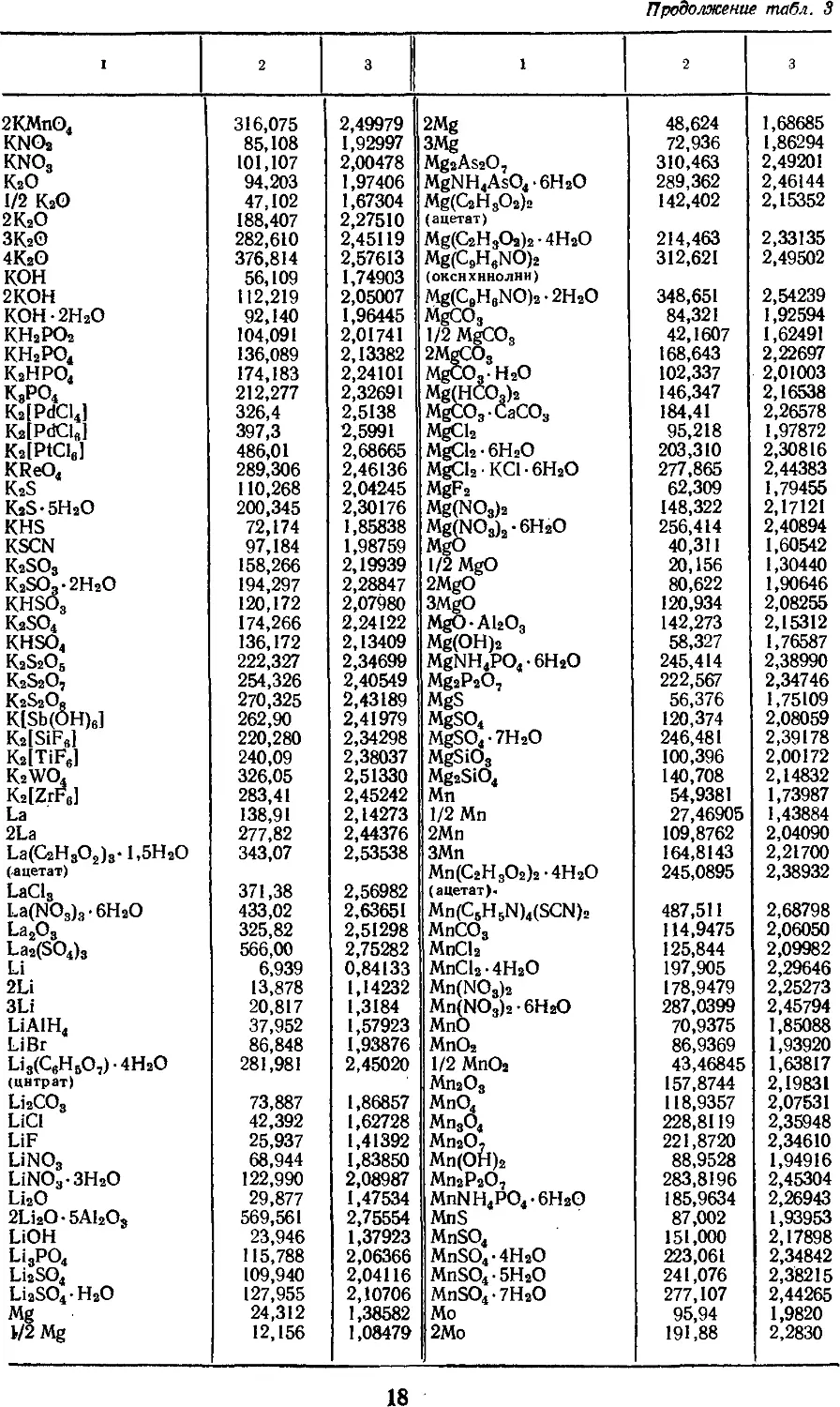
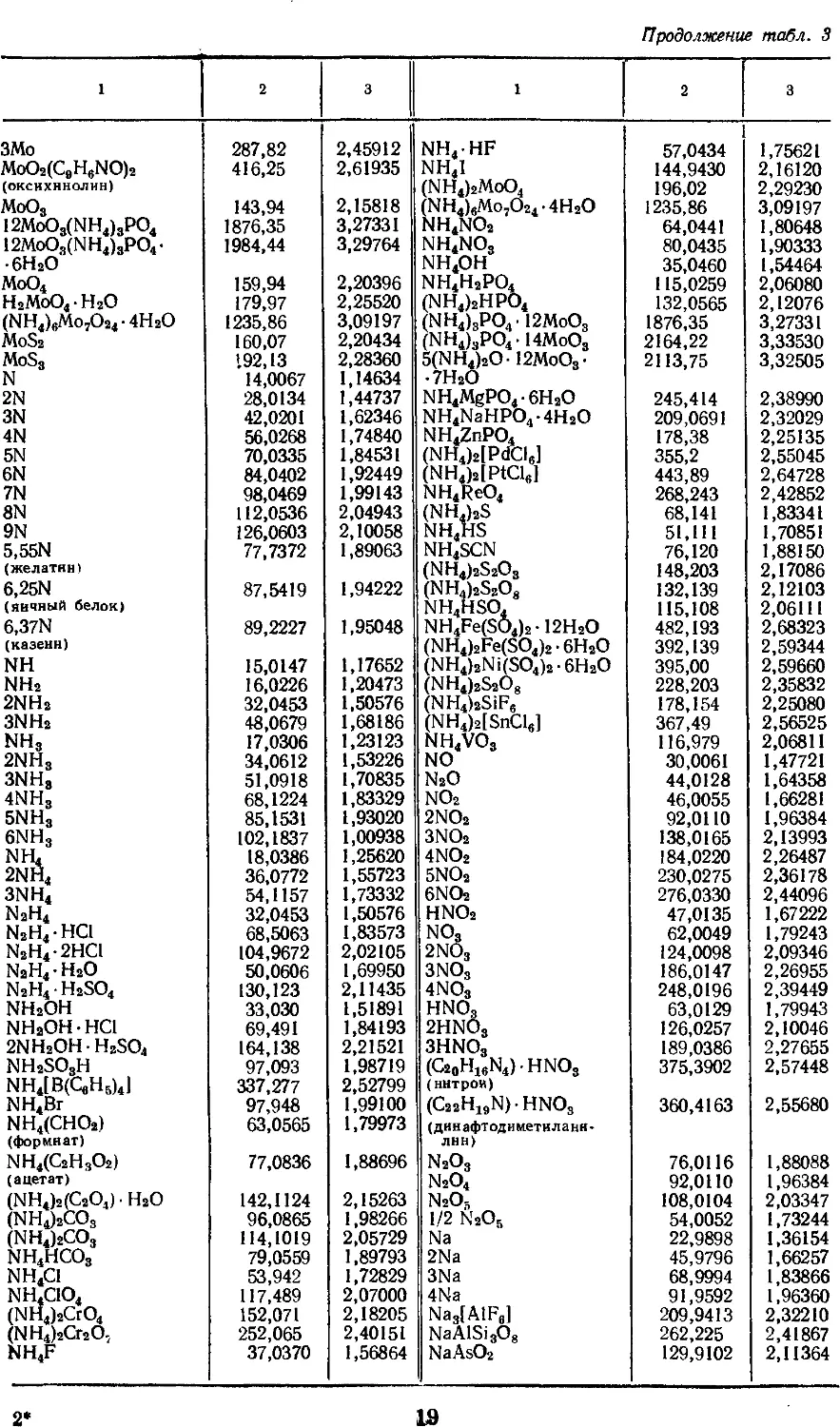
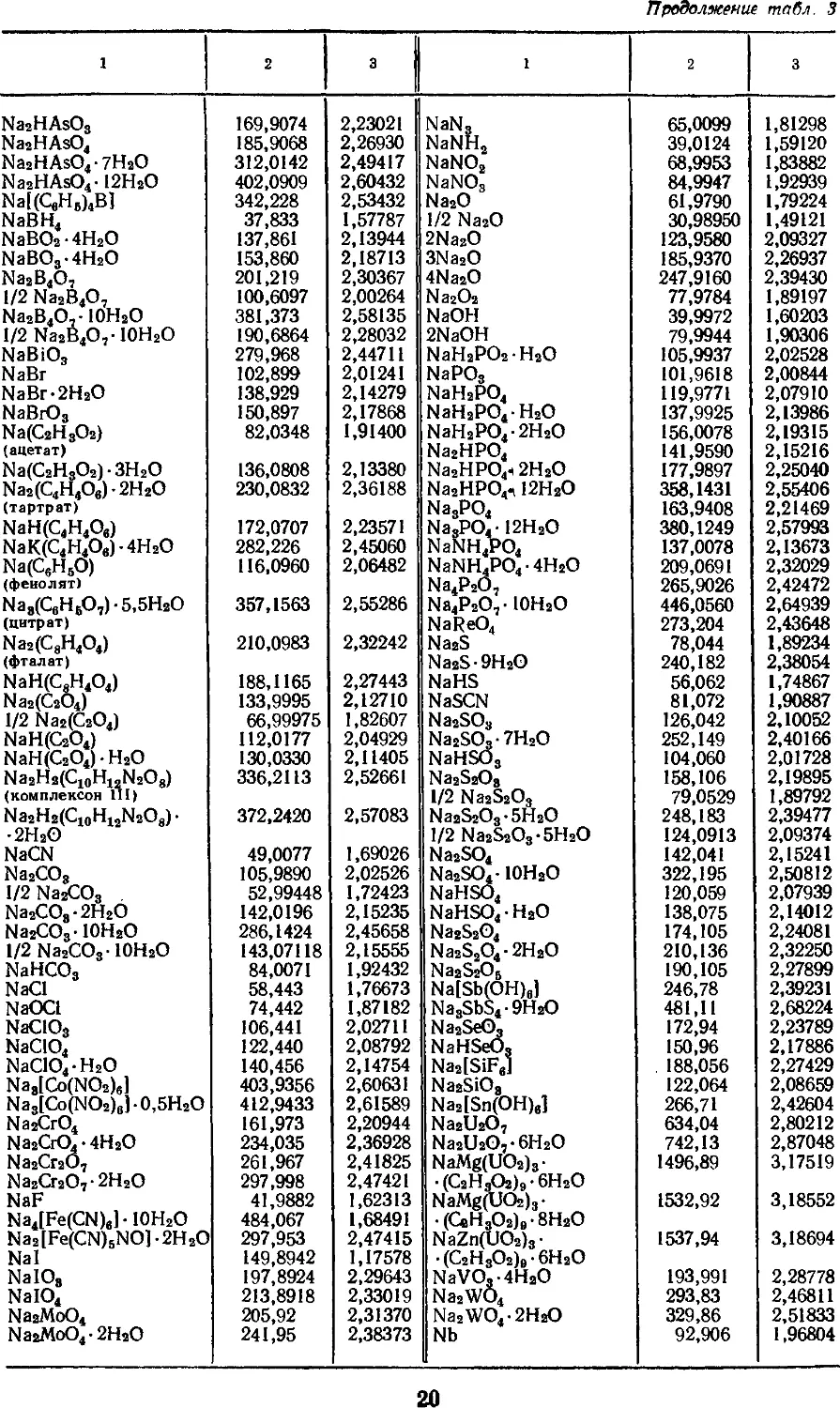
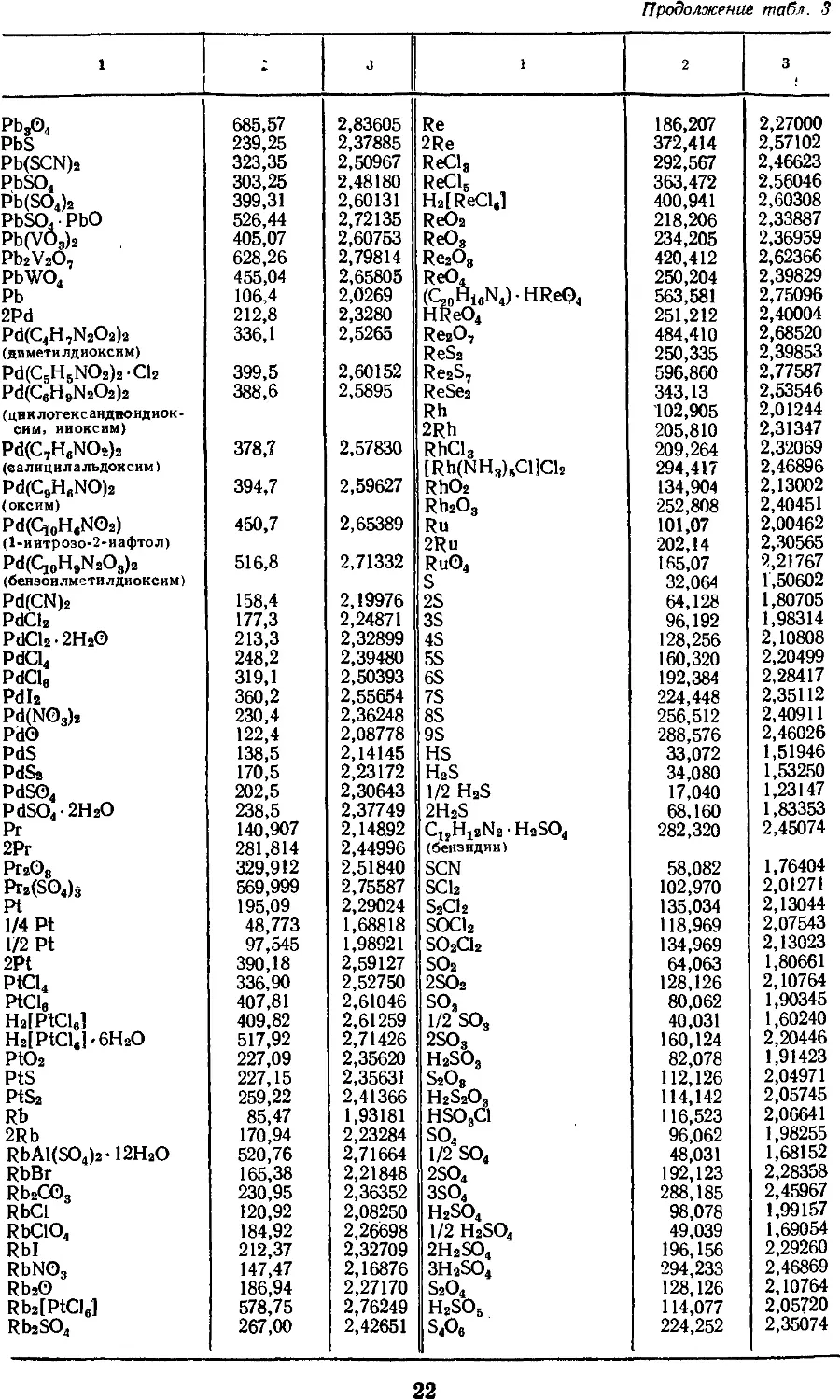
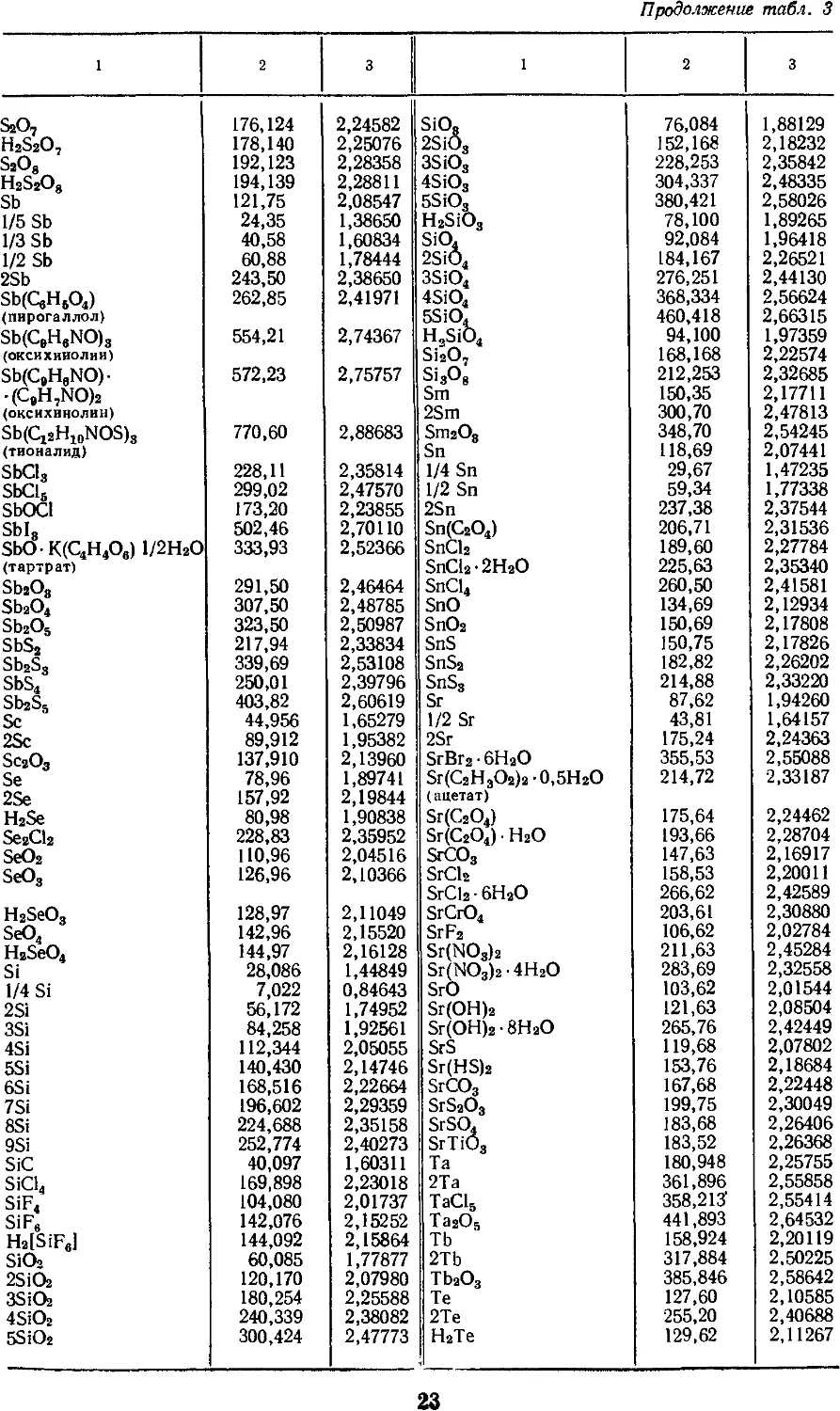
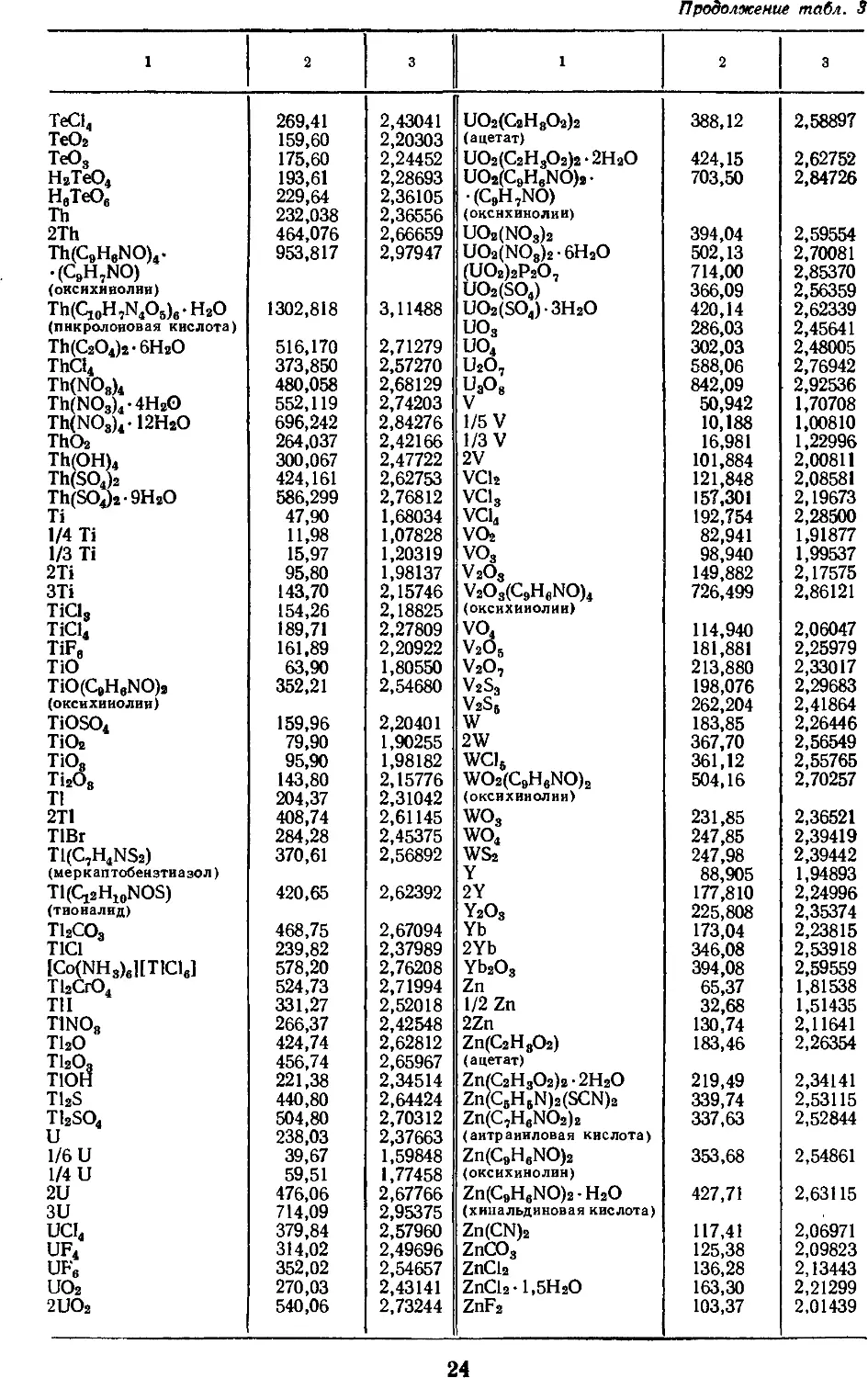
3. АТОМНЫЕ МАССЫ, МАССЫ НАИБОЛЕЕ
УПОТРЕБИТЕЛЬНЫХ АТОМНЫХ ГРУПП
И СОЕДИНЕНИЙ
Формула
г
гЬ
3Ag
Ag8As04
AgBr
Ag(CaH8Oa)
(ацетат)
Ag(C,H4NSa)
(меркаптобензотн азол)
AgCN
AgaCOs
AgCl
AgCl08
AgClO,
AgaCra
AgaCraO,
AgF
AgaF
Agl
AgMn04
AgNOs
AgNOs
AgaO
Ag8PO,
Ag4PaO,
AgaS
AgSCN
AgaSO,
AgaTlAs04
AgVOs
ApVO.
1/3 Al
2A1
3A1
4A1
5A1
6A1
AlBr„
Al(CaH80a)3
(ацетат)
Al(C9HeNO)3
(ОКСИХИНОЛИН)
A1C18
A1CU6H20
A1F8
A1F.
Na,[AlFf]
fl1»
A1N
A1(N08)8
Al(NO„)8-9HaO
AlaOs
1/6 AlaOs
2AlaO„
3AlaOs
Al(OH),
A1P04 '
Ala(S04)3
Атомная
(молекулярная) масса
2
107,870
215,740
323,610
462,529
187,779
166,915
274,115
133,888
275,749
143,323
191,321
207,321
331,734
431,728
126,868
234,738
234,774
226,806
153,876
169,875
231,739
418,581
605,423
247,804
165,952
311,802
559,03
206,810
438,550
26,9815
8,99383
53,9630
80,9445
107,9260
134,9075
161,8890
266,709
204,1165
459,4281
133,341
241,433
83,9767
140,9723
209,9417
407,6947
40,9882
212,9962
375,1343
101,9612
16,99353
203,9224
305,8836
78,0036
121,9529
342,148
lg
з
2,03290
2,33393
2,51002
2,66514
2,27365
2,22250
2,43793
2,12674
2,44051
2,15632
2,28176
2,31664
2,52079
2,63521
2,10335
2,37058
2,37065
2,35565
2,18717
2,23013
2,36500
2,62178
2,78206
2,39411
2,21998
2,49388
2,74743
2,31557
2,64202
1,43106
0,95394
1,73209
1,90819
2,03312
2,13025
2,20922
2,42604
2,30988
2,66222
2,12497
2,38280
1,92416
2,14913
2,32210
2,61034
1,61266
2,32837
2,57419
2,00843
1,23028
2,30947
2,48556
1,89211
2,08619
2,53421
Формула
г
Ala(S04)3-I8HaO
KAl(S04)a-12HaO
NH4Al(S04)a-I2HaO
As
1/2 As
1/3 As
1/5 As
2As
3As
AsBr8
AsCl8
AsCl5
AsH3
Asl8
As08
As„03
1/4 As2Os
As04
H8As04
Ass06
AsaO,
AS2^g
AsS4
As^
Au
1/3 Au
2Au
3Au
AuCN
K[Au(CN)a]
K(Au(CN)JI,5H20
AuCl3
H[AuCl4]
H(AuCl4]-4HaO
K[AuCl4]-2HaO
Na[AuClJ-2H20
AuO(OH)
КАиОа-ЗНгО
В
1/3 В
2B
ЗВ
4В
В(СвН5)4
(тетрафгннлбор)
ВВг8
ВС13
BF3
H[BF4]
K[BF41
BN
BOa
HBOa
BO.
н8во3
B203
в4о7
Ba
1/2 Ba
Атомная
(молекулярная) масса
2
666,424
474,391
453,327
74,9216
37,46080
24,97387
14,98432
149,8432
224,7648
314,649
181,281
252,187
77,9455
455,6348
122,9198
197,8414
49,46035
138,9192
141,9431
229,8402
261,8390
246,035
203,178
310,163
196,967
65,6557
393,934
590,901
222,985
288,105
367,163
303,326
339,787
411,848
413,912
397,799
229,974
322,114
10,811
3,6037
21,622
32,433
43,244
319,238
250,538
117,170
67,806
87,813
125,907
24,818
42,810
43,818
58,809
61,833
69,620
155,239
137,34
68,670
lg
з
2,82375
2,67613
2,65641
1,87461
1,57358
1,39749
1,17564
2,17564
2,35172
2,49783
2,25835
2,40173
1,89179
2,65862
2,08962
2,29632
1,69425
2,14276
2,15211
2,36143
2,41804
2,39100
2,30787
2,49159
2,29440
1,81727
2,59543
2,77151
2,34827
2,45955
2,56486
2,48191
2,53121
2,61474
2,61691
2,59968
2,36168
2,50801
1,03387
0,55674
1,33490
1,51099
1,63593
2,50410
2,39887
2,06882
1,83127
1,94356
2,10005
1,39477
1,63155
1,64165
1,76944
1,79122
1,84273
2,19100
2,13780
1,83677
12
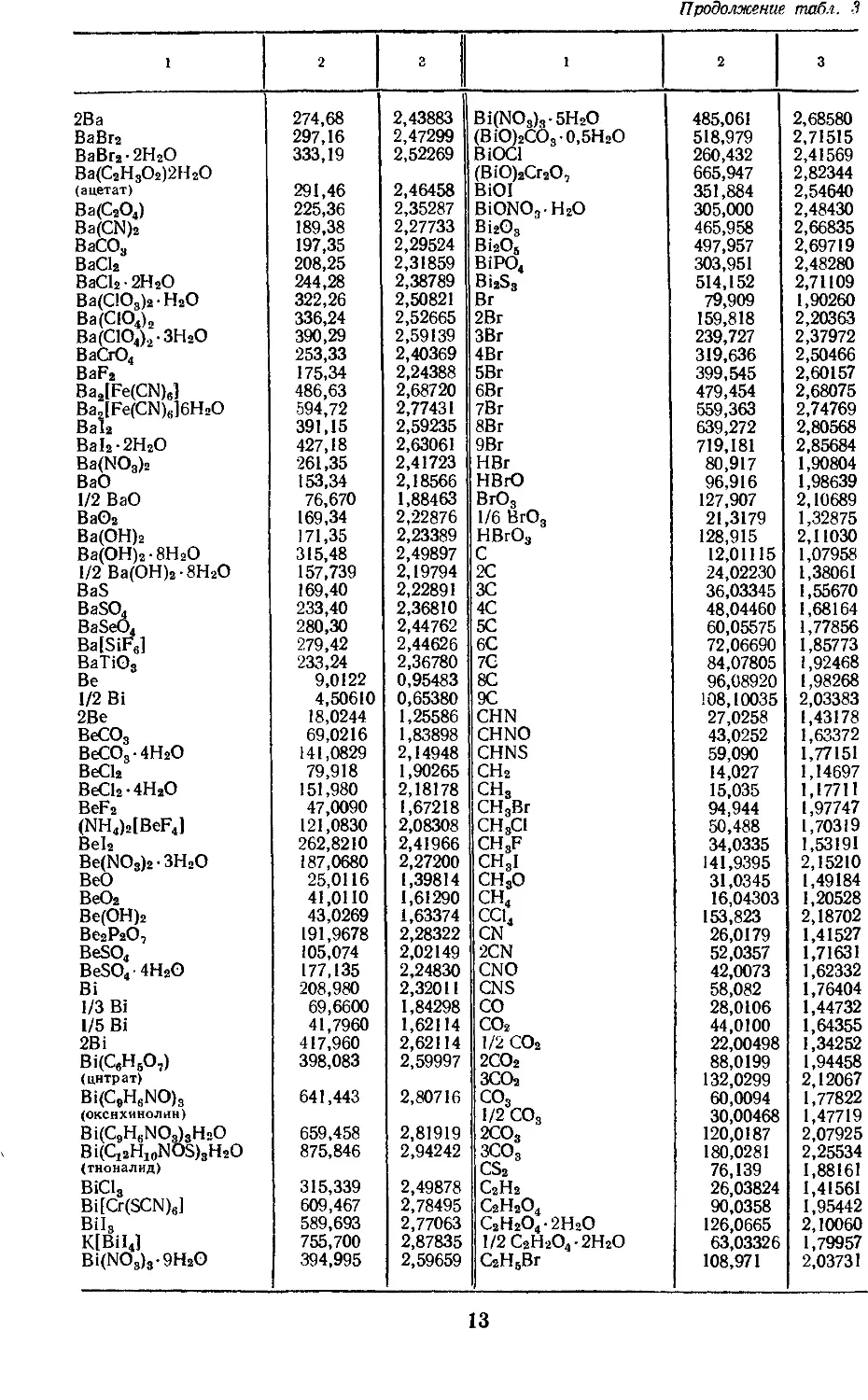
Продолжение табл. 3
1
2Ва
ВаВг2
ВаВг2-2Н20
Ва(С2Н302)2Н20
(ацетат)
Ва(С204)
Ba(CN)2
BaCOs
BaCU
ВаС12-2Н20
Ва(С!03)2Н20
Ва(СЮ4)2
Ва(СЮ4)2-ЗН20
ВаСЮ4
BaF2
Ba2[Fe(CN)e]
Ba,[Fe(CN)6]6H20
Bal2
ВаЬ-2Нг0
Ba(N03)2
BaO
1/2 BaO
Ba02
Ba(OH)2
Ba(OH)2-8H20
l/2Ba(0H)2-8H20
BaS
BaSO.
BaSeOj
Ba[SiF6]
BaTiO.
Be
1/2 Bi
2Be
BeCOs
ВеОЭ3-4Н20
BeCU
BeCl2-4H20
BeF2
(NH4)2[BeFJ
Beb
Be(N03)2-3H20
BeO
Be02
Be(OH)2
Ве2РгО,
BeS04
BeS04 4H20
Bi
1/3 Bi
1/5 Bi
2Bi
Bi(CeH50,)
(цнтрат)
Bi(C9H6NO)3
(ОКСНХИНОЛЙН)
Bi(C9H6N03)3H20
Bi(Cl2H10NOS)3H2O
(тноналид)
BiCl3
Bi[Cr(SCN)6]
BII.
K[BiI4]
Bi(N03)3-9H20
2
274,68
297,16
333,19
291,46
225,36
189,38
197,35
208,25
244,28
322,26
336,24
390,29
253,33
175,34
486,63
594,72
391,15
427,18
261,35
153,34
76,670
169,34
171,35
315,48
157,739
169,40
233,40
280,30
279,42
233,24
9,0122
4,50610
18,0244
69,0216
141,0829
79,918
151,980
47,0090
121,0830
262,8210
187,0680
25,0116
41,0110
43,0269
191,9678
105,074
177,135
208,980
69,6600
41,7960
417,960
398,083
641,443
659,458
875,846
315,339
609,467
589,693
755,700
394,995
О
2,43883
2,47299
2,52269
2,46458
2,35287
2,27733
2,29524
2,31859
2,38789
2,50821
2,52665
2,59139
2,40369
2,24388
2,68720
2,77431
2,59235
2,63061
2,41723
2,18566
1,88463
2,22876
2,23389
2,49897
2,19794
2,22891
2,36810
2,44762
2,44626
2,36780
0,95483
0,65380
1,25586
1,83898
2,14948
1,90265
2,18178
1,67218
2,08308
2,41966
2,27200
1,39814
1,61290
1,63374
2,28322
2,02149
2,24830
2,32011
1,84298
1,62114
2,62114
2,59997
2,80716
2,81919
2,94242
2,49878
2,78495
2,77063
2,87835
2,59659
l
Bi(N03)g-5H20
(BiO)2CO30,5H2O
BiOCl
(BiO)2Cr20,
BiOI
BiON03H20
Bi203
Bi205
BiP04
Bi2S3
Br
2Br
3Br
4Br
5Br
6Br
7Br
8Br
9Br
HBr
HBrO
Br03
1/6 Br03
HBr03
С
2C
3C
4C
5C
6C
7G
8C
9C
CHN
CHNO
CHNS
CH2
CH3
CH3Br
CH3C1
CH3F
CH3I
сн3о
CH4
CC14
CN
2CN
CNO
CNS
CO
C02
1/2 C02
2C02
3CCH!
co3
1/2 COs
2C03
3C03
CS2
C2H2
C2H204
C2H204-2H20
1/2C2H204-2H20
СгН5Вг
2
485,061
518,979
260,432
665,947
351,884
305,000
465,958
497,957
303,951
514,152
79,909
159,818
239,727
319,636
399,545
479,454
559,363
639,272
719,181
80,917
96,916
127,907
21,3179
128,915
12,01115
24,02230
36,03345
48,04460
60,05575
72,06690
84,07805
96,08920
108,10035
27,0258
43,0252
59,090
14,027
15,035
94,944
50,488
34,0335
141,9395
31,0345
16,04303
153,823
26,0179
52,0357
42,0073
58,082
28,0106
44,0100
22,00498
88,0199
132,0299
60,0094
30,00468
120,0187
180,0281
76,139
26,03824
90,0358
126,0665
63,03326
108,971
3
2,68580
2,71515
2,41569
2,82344
2,54640
2,48430
2,66835
2,69719
2,48280
2,71109
1,90260
2,20363
2,37972
2,50466
2,60157
2,68075
2,74769
2,80568
2,85684
1,90804
1,98639
2,10689
1,32875
2,11030
1,07958
1,38061
1,55670
1,68164
1,77856
1,85773
1,92468
1,98268
2,03383
1,43178
1,63372
1,77151
1,14697
1,17711
1,97747
1,70319
1,53191
2,15210
1,49184
1,20528
2,18702
1,41527
1,71631
1,62332
1,76404
1,44732
1,64355
1,34252
1,94458
2,12067
1,77822
1,47719
2,07925
2,25534
1,88161
1,41561
1,95442
2,10060
1,79957
2,03731
13
Продолжение табл. 3
1
С2Н5С1
C2H5F
С2Н51
с2н5о
С3НвО
СвН5
свнв
с„нво
CeHl2Oe
с,н5о
С7Нв02
CjHeOa
£ioH„
£ioH5
^10™в
^.10н,
-10" 8
CiiHjOa
S"5#
^i4™e02
С14Н,02
Q^Cfe
Са
1/2 Са
2Са
ЗСа
СаВгг
СаСа
Са(Са04)
1/2 Са(Сг04)
Са(С204)-НгО
CaCN2
Ca(CN)2
CaC08
1/2 CaCOg
Са(НС03)2
CaCU
CaCU-6H20
CaOCU
1/2 CaOCU
СаСЮ4
СаСЮ4-2Н20
CaF2
СаН2
СаМо04
Ca(NOs)a
Ca(NOa)a-4HaO
CaO
1/2 CaO
2CaO
ЗСаО
Ca(OH)a
1/2 Ca(OH)a
Ca(H2P04)a
Са(Р03)а
Са3(Р04)а
СаНЮ4
СаНР04-2НаО
Са(НаР04)а
Са(НаЮ4)а-НаО
ЗСа3(Р04)а-Са(ОН)а
CaS
Ca(HS)a-6H80
Ca(SCN)a
2
64,515
48,0606
155,9666
45,0616
58,0807
77,10675
78,11472
94,1141
180,1589
105,1173
122,1247
138,1241
124,14338
125,15135
126,15932
127,16729
128,17526
204,1868
205,1948
206,2027
207,2107
208,2187
40,08
20,04
80,16
120,24
199,90
64,10
128,10
64,05
146,12
80,10
92,12
100,09
50,04
162,11
110,99
219,08
126,99
63,493
156,07
192,10
78,08
42,10
200,02
164,09
236,15
56,08
28,040
112,16
168,24
74,09
37,047
170,06
198,02
310,18
136,06
172,09
234,06
252,07
1004,64
72,14
214,32
156,24
3
1,80966
1,68183
2,19303
1,65381
1,76403
1,88709
1,89273
1,97366
2,25565
2,02167
2,08680
2,14027
2,09392
2,09744
2,10092
2,10438
2,10780
2,31003
2,31217
2,31429
2,31641
2,31852
1,60293
1,30190
1,90396
2,08005
2,30081
1,80686
2,10755
1,80652
2,16472
1,90363
1,96435
2,00039
1,69936
2,20981
2,04528
2,34060
2,10377
1,80273
2,19332
2,28353
1,89254
1,62428
2,30107
2,21508
2,37319
1,74881
1,44778
2,04984
2,22593
1,86976
1,56875
2,23060
2,29671
2,49161
2,13373
2,23576
2,36933
2,40152
3,00201
1,95918
2,33106
2,19379
1
CaSOs
CaS03-2HaO
Ca(HS03)2
CaS04
CaSO40,5HaO
CaS04-2HaO
Ca[SiFel
CaSi03
CaW04
Cd
1/2 Cd
2Cd
CdBr2
CdBr2-4Ha0
Cd(C2H30a)a
Cd(CaH3Oa)a-2HaO
Cd(C,H„NSa)a
(меркаптобензтназол)
Cd(C,HeNOa)a
(антраниловая кислота)
Cd(C,HeNO)a
(окснхннолнн)
Cd(C10HeNOa)a
(хннальдиновая кислота)
CdC03
CdCU
CdCUHaO
Cdb
Cd(NH4)P04-HaO
Cd(NOs)a
Cd(NOs)a-2HaO
Cd(N03)a-4HaO
CdO
Cd(OH)a
CdaPaO,
CdS
CdS04
CdS04-8/3HaO
Ce
1/4 Ce
1/3 Ce
2Ce
3Ce
Ce2(Ca04)3
Cea(Ca04)3-9HaO
Cea(CaO4)310HaO
Ce(CeHeNO)3
(ОКСИХИНОЛНН)
CeCl3
CeCl8-7HaO
Ce(N03)3
Ce(N03)3-6HaO
[(NH4)2Ce(N03)e12H20
CeOa
CeaOg
Се.04
CeP04
Ce(S04)2
Ce(S04)i!-4H20
(NH4)2[Ce(S04)4]-2H20
Ce2(S04)8
Ce2(S04),-8H20
CI
2C1
2
120,14
156,17
202,22
136,14
145,15
172,17
182,16
116,16
287,93
112,40
56,200
224,80
272,22
344,28
230,49
266,52
444,89
384,66
400,71
456,73
172,41
183,31
201,32
366,21
243,43
236,41
272,44
308,47
128,40
146,41
398,74
144,46
208,46
256,50
140,12
35,030
46,707
280,24
420,36
544,30
706,44
724,45
572,58
246,48
372,59
326,13
434,23
584,26
172,12
328,24
484,36
235,09
332,24
404,30
632,55
568,42
712,55
35,453
70,906
3
2,07968
2,19360
2,30582
2,13399
2,16182
2,23596
2,26045
2,06506
2,45929
2,05077
1,74974
2,35180
2,43492
2,53691
2,36265
2,42573
2,64825
2,58508
2,60283
2,65966
2,23657
2,26318
2,30388
2,56373
2,38637
2,37367
2,43527
2,48922
2,10857
2,16557
2,60069
2,15975
2,31903
2,40909
2,14650
1,54444
1,66938
2,44753
2,62362
2,73584
2,84907
2,86001
2,75784
2,39178
2,57123
2,51339
2,63772
2,76661
2,23583
2,51619
2,68516
2,37123
2,52145
2,60670
2,80110
2,75467
2,85282
1,54966
1,85069
14
1 I 2 I 3
3C1
4C1
5C1
6C1
7C1
8C1
9C1
HC1
2HC1
3HC1
4HC1
5HC1
6HC1
CIO
нею
СЬО
СЮг
C103
1/6 СЮ3
НСЮ3
(C20HleN4)HClO3
(нитрон)
(C22HleN)HC103
(дннафтодиметиламин)
C104
нсю4
(C20HieN4)-HClO4
(нитрон)
(C2oH19N)HC104
(динафтоднметнламин)
C1205
ci2o7
Co
1/3 Co
1/2 Co
2Co
3Co
CoBr2
Co(C204)-2H20
Co(C2H302)2-4H20
(ацетат)
Co(C5H5N)4(SCN)2
(пиридин)
Co3(CeH50,)2-4H20
(цитрат)
Co(C9HeNO)2-2H20
(окенхинолин)
Co(C10HeNO2)r2H2O
(а-нитро 30-3-нафтол)
СоС12
CoCl2-2H20
CoCl2 • 6H20
С0СЮ4
Co(NH4)P04-H20
Co(N03)2
Co(N03)2-6H20
Na3[Co(N02)6]
CoO
Co203
Co304
Co2P20,
CoS
CoS04
CoS04-7H20
106,360
141,812
177,265
212,72
248,171
283,624
319,077
36,461
72,922
109,383
145,844
182,305
218,766
51,452
52,460
86,905
67,452
83,451
13,908
84,459
396,836
381,863
99,451
100,459
412,836
397,862
150,903
182,902
58,9332
19,6444
29,4666
117,866
176,800
218,751
182,9838
249,0846
491,506
627,0661
383,2724
611,4583
129,839
165,870
237,931
174,927
189,9585
182,9430
291,0350
403,9356
74,9326
165,8646
240,7972
291,8098
90,997
154,995
281,102
2,02677
2,15172
2,24862
2,32781
2,39475
2,45275
2,50390
1,56183
1,86286
2,03893
2,16389
2,26080
2,33998
1,71140
1,71983
1,93905
1,82899
1,92144
1,14328
1,92665
2,59861
2,58191
1,99761
2,00199
2,61578
2,59973
2,17870
2,26222
1,77036
1,29324
1,46933
2,07139
2,24748
2,33995
2,26421
2,39635
2,69153
2,79732
2,58351
2,78637
2,11341
2,21977
2,37645
2,24286
2,27866
2,26231
2,46394
2,60631
1,87467
2,21975
2,38165
2,46510
1,95903
2,19032
2,44886
Продолжение табл. З
1 2 3
Co2(SO„)3
Co2(S04)3-18H20
K2Co(S04)2 • 6H20
Cr
1/3 Cr
1/2 Cr
2Cr
3Cr
CrCU
CrCl3
[CrCl2(H20)4]Cl-2H20
Cr(N03)3
Cr(N03)3-9H20
CrO
Cr03
2CrOs
Сг2Оэ
1/2 Cr2Os
2Cr203
Cr04
Cr304
Cr207
1/6 Cr20,
Cr(OH)2
Cr(OH)3
Cr(P04)
Cr2(S04)3
Cr2(S04)3-18H20
KCr(SO„)2-12H20
NH4Cr(S04)2-12H20
Cs
2Cs
CsAl(S04)2-12H20
Cs2C03
CsCl
Cs3C104
CsCr04
Cs2Cr20,
Csl
CsN03
Cs20
Cs2[PtCle]
Cs2S04
Cu
1/2 Cu
2Cu
3Cu
Cu (C2H302)2-H20
(ацетат)
Cu(C5H6N)2(SCN)2
(пиридин)
Cu(C7HeN02)2
(антраниловая кислота)
Cu(C9HeNO)2
(окенхинолин)
Cu(C10HeNO2)2-H2O
(хннальдииовая кислота)
Cu(C12H10NOS)2
(тионалид)
Cu(C14HnN02)
(бензоиноксим, купрон)
CuCN
CuC03-Cu(OH)2
2CuCOs-Cu(OH)2
406,051
730,327
437,352
51,996
17,332
25,998
103,992
155,988
122,902
158,355
266,447
238,011
400,149
67,995
99,994
199,991
151,990
75,995
303,980
115,994
219,986
215,988
35,998
86,011
103,018
146,967
392,18
716,453
499,405
478,342
132,905
265,810
568,194
325,819
168,358
232,356
381,804
481,798
259,809
194,910
281,809
673,620
361,872
63,54
31,77
127,08
190,62
199,65
337,91
335,80
351,85
425,88
514,12
288,79
89,56
221,10
344,65
2,60858
2,86352
2,64083
1,71597
1,23885
1,41494
2,01700
2,19309
2,08956
2,19963
2,42561
2,37660
2,60222
1,83248
1,99998
2,30100
2,18181
1,88079
2,48284
2,06444
2,34239
2,33443
1,55627
1,93456
2,01293
2,16722
2,59348
2,85519
2,69845
2,67974
2,12354
2,42457
2,75450
2,51298
2,22623
2,36615
2,58184
2,68287
2,41465
2,28983
2,44995
2,82841
2,55856
1,80305
1,50202
2,10408
2,28017
2,30027
2,52880
2,52608
2,54636
2,62929
2,71107
2,46059
1,95211
2,34459
2,53738
15
Продолжены табл. 3
1
CuCl
CuCU
сиси-гнгО
Cu(N08)2
Cu(N03)2-3H20
Cu(N03)2-6H20
CuO
1/2 CuO
2CuO
Cu(OH)2
Cu20
CuS
Cu2S
CuSCN
Cu(SCN)2
CuS04
CuS04-5H20
[Cu(NH8)4]-S04H20
Dy
2Dy
Оу2о8
Er
2Er
Er208
Eu
2Eu
EuaOg
F
2F
3F
4F
5F
6F
geH5)3SnF
2HF
Fe
1/3 Fe
1/2 Fe
2Fe
3Fe
4Fe
Fe(CeHeNO)3
(окснхинолин)
Fe(CN)e
FeCOs
Fe(HCOs)2
Fe(CO)4
Fe(CO)6
FeCU
FeCl2-4H20
FeCl3
FeCl.-6H20
Feb
Fe(NOa)2
Fe(NO8)2-6H20
Fe(NOs)3
Fe(NOs)3.6HaO
Fe(NO,)8.9H20
FeO
2FeO
Fes03
1/6 Fe»Os
1/2 FesOs
2
98,99
134,45
170,48
187,55
241,60
295,64
79,54
39,77
159,08
97,55
143,08
95,60
159,14
121,62
179,70
159,60
249,68
245,74
162,50
325,00
373,00
167,26
334,52
382,52
151,96
303,92
351,92
18,9984
37,9968
56,9952
75,9936
94,9920
113,990
369,01
20,0064
40,0127
55,847
18,616
27,924
111,694
167,541
223,88
488,310
211,954
115,856
177,882
167,889
195,900
126,753
198,814
162,206
270,298
390,656
179,857
287,949
241,862
349,954
404,000
71,846
143,69
159,69
26,615
79,846
3
1,99559
2,12856
2,23167
2,27312
2,38310
2,47076
1,90059
1,59956
2,20162
1,98923
2,15558
1,98046
2,20178
2,08500
2,25455
2,20303
2,39738
2,39048
2,21085
2,51188
2,57171
2,22340
2,52443
2,58265
2,18173
2,48276
2,54644
1,27872
1,57975
1,75584
1,88078
1,97769
2,05687
2,56704
1,30117
1,60220
1,74700
1,26988
1,44597
2,04803
2,22412
2,34906
2,68870
2,32624
2,06392
2,25013
2,22502
2,29203
2,10296
2,29845
2,21007
2,43184
2,49088
2,25493
2,45932
2,38357
2,54401
2,60638
1,85640
2,15744
2,20329
1,42413
1,90225
1
2Fe2Oa
Fe304
Fe(OH)2
SB*
Fe3(P04)2-8H20
FeS
FeS2
Fe2S3
FeS04
FeS04-7H20
Fe2(S04)3
Fe2(S04)8-9H20
KFe(SO,)2-12H20
NH4Fe(S04)2-12H20
(NH4)2Fe(S04)2-6HaO
Ga
2Ga
Ga(CeHeNO)8
(ОКСНХИИОЛИН)
Ga(CeH4Br2NO)3
(бромоксин)
GaCl3
GaN
Ga2Os
Gd
2Gd
Gd203
Ge
2Ge
GeCl4
GeO
GeOs!
GeS2
H
2H
3H
4H
5H
6H
7H
8H
9H
н2о
1/2 H20
2H20
зн2о
4H20
5H20
6H20
7H20
8H20
9H20
I2H20
18H20
24H20
НаОг
1/2 Н2Ог
2H2Os
Hf
HfOs
Hg
1/2 Hg
2Hg
2
319,384
231,539
89,862
106,869
150,818
501,607
' 87,911
119,975
207,886
151,909
278,016
399,879
562,02
503,256
482,193
392,139
69,72
139,44
502,18
975,59
176,08
83,73
187,44
157,25
314,50
362,50
72,59
145,18
214,40
88,59
104,59
136,72
1,00797
2,01594
3,02391
4,03188
5,03985
6,04782
7,05579
8,06376
9,07173
18,0153
9,0077
36,0307
54,0460
72,0614
90,0767
108,092
126,107
144,123
162,138
216,184
324,276
432,368
34,0147
17,0074
68,0295
178,49
210,49
200,59
100,30
401,18
3
2,50431
2,36462
1,95358
2,02885
2,17845
2,70036
1,94404
2,07909
2,31783
2,18159
2,44407
2,60193
2,74975
2,70179
2,68322
2,59344
1,8434
2,1444
2,7009
2,98927
2,24571
1,92288
2,27286
2,19659
2,49762
2,55931
1,8609
2,16194
2,33122
1,94738
2,01949
2,13583
0,00345
0,30448
0,48057
0,60551
0,70242
0,78160
0,84855
0,90654
0,95769
1,25564
0,95461
1,55667
1,73276
1,85770
1,95461
2,03379
2,10074
2,15873
2,20989
2,33482
2,51091
2,63585
1,53167
1,23064
1,83270
2,25162
2,32323
2,30231
2,00128
2,60334
16
Продолжение табл. 3
1
3Hg
4Hg
HgBr2
Hg(C2H302)2
(ацетат)
Hg(C5H5N)2Cr207
(пирнднн)
Hg(C7HeN02)2
(антраниловая кислота)
Hg(Cl2H10NOS)2
(тионалид)
Hg(C204)
Hg(CN)2
Hg(CN)2-HgO
HgCl»
Hg2Cl2
HgCrO,
Hgl
Hgh
HgNH2Cl
Hg(N03)2
Hg(N03)2-H20
Hg2(N03)2
Hg2(N03)2-2H20
HgO
Hg20
HgS
Hg2S
Hg(SCN)2
Hg2(SCN)...
HgSO,
Hg2S64
Ho
2Ho
Hoa03
In
2In
In(C9HeNO)3
(ОКСИХИНОЛИН)
1пС13
ln208
InP04
In2S3
Ir
1гОг
I
21
31
41
51
61
HI
2HI
IC1
ICI.
IF»
I03
HI03
I04
НЮ4
ьо6
H5IOf,
I20-
K '
2K
2
601,77
802,36
360,41
318,68
574,78
472,85
633,16
288,61
252,63
469,22
271,50
472,09
316,58
327,49
454,40
252,07
324,60
342,62
525,19
561,22
216,59
417,18
232,65
433,24
316,75
517,34
296,65
497,24
164,930
329,860
377,858
114,82
229,64
547,28
221,18
277,64
209,79
325,83
192,2
224,2
126,9044
253,8088
380,7132
507,6176
634,5220
761,4264
127,9124
255,8247
162,357
233,263
221,8964
174,9026
175,9106
190,9020
191,9100
333,8058
227,9407
365,8046
39,102
78,204
3
2,77943
2,90437
2,55680
2,50335
2,75950
2,67472
2,80151
2,46031
2,40248
2,67138
2,43377
2,67402
2,50048
2,51520
2,65744
2,40152
2,51135
2,53481
2,72032
2,74913
2,33564
2,62032
2,36670
2,63673
2,50072
2,71378
2,47224
2,69657
2,21730
2,51833
2,57733
2,06002
2,36105
2,73817
2,34475
2,44348
2,32178
2,51299
2,2838
2,3506
2,10348
2,40451
2,58060
2,70554
2,80245
2,88163
2,10691
2,40794
2,21047
2,36785
2,34615
2,24280
2,24529
2,28081
2,28310
2,52349
2,35782
2,56325
1,59220
1,89323
1
3K
4K
KA1(S04)2
KA1(S04)2-12H20
KAlSi308
2KAlSi308
KH2As04
K2HAs04
KIBFJ
KBr
KBrOs
1/6 KBr03
K(C2H302)
(ацетат)
K2(C4H4Oe)0,5H2O
(тартрат)
КН(С4н4ов)
KNa(C4H4Oe)-4H20
K[C„H2OeSb(OH)2] •
•0,5Н2О
K[(QH5)4B]
K3(QH60,)H20
(цитрат)
KH(C8H404)
(фталат)
K(ClaH4N7Ol2)
(днпикрнламин)
КН(С204)-Н20
КН(С204), Н2С204-
•2Н20
1/3 КН(С204),
Н2(С204) • 2НгО
К2(С20„)-Н20
KCN
KCNO
кнсо3
КаС03
1/2 КаС03
КгС03-1,5Н20
КгС03-2Н20
КС1
ксю3
ксю4
K3[Co(N02)el
K2Co(S04)2 ■ 6HsO
КаСЮ4
КаСггО,
1/6 КгСггО,
1/2 КгСг207
KCr(S04)2-12H20
KF
KHF2
K3[Fe(CN)e]
KJFefCNbl
^[Ре^КЫ-ЗНгО
KFe(S04)2-12H20
KI
KIO3
1/6 КЮ3
KH(I03)2
1/12 KH(I03)2
KMn04
1/5 KMnO,
1/3 KMn04
2
117,306
156,41
258,207
474,391
278,337
556,673
180,037
218,131
125,907
119,011
167,009
27,8348
98,147
235,285
188,183
282,226
333,93
358,340
324,424
204,229
477,307
146,145
254,196
84,7321
184,239
65,120
81,119
100,119
138,213
69,107
165,236
174,244
74,555
122,553
138,553
452,272
437,352
194,198
294,192
49,032
147,0959
499,405
58,100
78,107
329,260
368,362
422,408
503,256
166,006
214,005
35,6674
389,915
32,4929
158,038
31,6075
52,6792
3
2,06932
2,19426
2,41197
2,67614
2,44457
2,74560
2,25535
2,33872
2,10005
2,07559
2,22274
1,44459
1,99188
2,37159
2,27458
2,45059
1,52368
2,55430
2,51111
2,31012
2,67880
2,16478
2,40517
1,92805
2,26538
1,81371
1,90912
2,00051
2,14055
1,83952
2,21810
2,24116
1,87248
2,08832
2,14162
2,65540
2,64083
2,28824
2,46863
1,69050
2,16760
2,69845
1,76418
1,89269
2,51754
2,56627
2,62573
2,70179
2,22012
2,33042
1,55227
2,59097
1,51179
2,19876
1,49979
1,72164
2 A. H. Лазарев и др.
17
Продолжение табл. 3
1
2КМп04
KNO*
KNOs
КгО
1/2 КгО
2КгО
ЗКгО
4К*0
кон
2 КОН
КОН-2ШО
КН2РОг
КН2Р04
КгНР04
к8ро4
K2[PdCl4]
K»[PdClel
K2[PtCle]
KReO,
K2S
KsS-5H20
KHS
KSCN
K2S03
K2SO.-2H20
KHSO3
K»S04
khso4
K2S205
Кг&О,
K2S2Os
KlSb(OH)e]
K2[SiFel
K2[TiFe]
k2wo4
K2[ZrFe]
La
2La
La(C2H302)3-I,5H20
(ацетат)
LaCl3
La(NOs)3.6H20
La2Os
La2(S04)3
Li
2Li
3Li
LiAlH,
LiBr
Li3(CeH60,)-4H20
(цитрат)
Li2COs
LiCl
LiF
LiNOs
LiN03-3H20
Li20
2Li20-5Al2Os
LiOH
Li3P04
Li2S04
Li2S04H20
Mg
W2Mg
2
316,075
85,108
101,107
94,203
47,102
188,407
282,610
376,814
56,109
112,219
92,140
104,091
136,089
174,183
212,277
326,4
397,3
486,01
289,306
110,268
200,345
72,174
97,184
158,266
194,297
120,172
174,266
136,172
222,327
254,326
270,325
262,90
220,280
240,09
326,05
283,41
138,91
277,82
343,07
371,38
433,02
325,82
566,00
6,939
13,878
20,817
37,952
86,848
281,981
73,887
42,392
25,937
68,944
122,990
29,877
569,561
23,946
115,788
109,940
127,955
24,312
12,156
3
1
2,49979 2Mg
1,92997
2,00478
1,97406
1,67304
2,27510
2,45119
2,57613
1,74903
2,05007
1,96445
2,01741
2,13382
2,24101
2,32691
2,5138
2,5991
2,68665
2,46136
2,04245
2,30176
1,85838
1,98759
2,19939
2,28847
2,07980
2,24122
2,13409
2,34699
2,40549
2,43189
2,41979
2,34298
2,38037
2,51330
2,45242
2,14273
2,44376
2,53538
2,56982
2,63651
2,51298
2,75282
0,84133
1,14232
1,3184
1,57923
1,93876
2,45020
1,86857
1,62728
1,41392
1,83850
2,08987
1,47534
2,75554
1,37923
2,06366
2,04116
2,10706
1,38582
1,08479
3Mg
Mg2As20,
MgNH4As04-6H20
Mg(C2H302)2
(ацетат)
Mg(CsHsOa)2-4HsO
Mg(C9HeNO)2
(окснхннолни)
Mg(C„HeNO)2-2H20
MgC03
1/2 MgCOs
2MgC03
MgC03H20
Mg(HC03)2
MgCOs CaC03
MgCU
MgCl2-6H20
MgCl2-KCl-6H20
MgF2
Mg(N03)2
Мб(Ы03)г-6Н20
MgO
1/2 MgO
2MgO
3MgO
MgO-Als03
Mg(OH)2
MgNH4P04-6H20
Mg2P20,
MgS
MgS04
MgS04-7H20
MgSiOs
Mg2Si04
Mn
1/2 Mn
2Mn
3Mn
Mn(CsH302)2-4H20
(ацетат)-
Mn(C5H5N)4(SCN)2
MnCOs
MnCU
MnCl2-4H20
Mn(N03)2
Mn(N03)2-6HaO
MnO
МпОг
1/2 МпОг
Mn203
MnO.
Mn304
Mn20,
Mn(OH)2
Mn2P20,
MnNH4P04-6H20
MnS
MnS04
MnS04-4H20
MnS04-5H20
MnS04-7H20
Mo
2Mo
2
48,624
72,936
310,463
289,362
142,402
214,463
312,621
348,651
84,321
42,1607
168,643
102,337
146,347
184,41
95,218
203,310
277,865
62,309
148,322
256,414
40,311
20,156
80,622
120,934
142,273
58,327
245,414
222,567
56,376
120,374
246,481
100,396
140,708
54,9381
27,46905
109,8762
164,8143
245,0895
487,511
114,9475
125,844
197,905
178,9479
287,0399
70,9375
86,9369
43,46845
157,8744
118,9357
228,8119
221,8720
88,9528
283,8196
185,9634
87,002
151,000
223,061
241,076
277,107
95,94
191,88
3
1,68685
1,86294
2,49201
2,46144
2,15352
2,33135
2,49502
2,54239
1,92594
1,62491
2,22697
2,01003
2,16538
2,26578
1,97872
2,30816
2,44383
1,79455
2,17121
2,40894
1,60542
1,30440
1,90646
2,08255
2,15312
1,76587
2,38990
2,34746
1,75109
2,08059
2,39178
2,00172
2,14832
1,73987
1,43884
2,04090
2,21700
2,38932
2,68798
2,06050
2,09982
2,29646
2,25273
2,45794
1,85088
1,93920
1,63817
2,19831
2,07531
2,35948
2,34610
1,94916
2,45304
2,26943
1,93953
2,17898
2,34842
2,38215
2,44265
1,9820
2,2830
18
Продолжение табл. 3
1
ЗМо
Mo02(C„HeNO)2
(оксихннолин)
Мо03
12MoOs(NH4)3P04
12Mo03(NH4)3P04-
•6Н2О
Мо04
Н2Мо04Н20
(NH4)eMo7024-4H20
MoS2
MoS3
N
2N
3N
4N
5N
6N
7N
8N
9N
5.55N
(желатин)
6.25N
(яичный белок)
6.37N
(казенн)
NH
NH2
2NH2
3NH2
NH3
2NH3
3NH8
4NH3
5NH3
6NH3
NH«
2NH4
3NH4
N2H4
N2H4HC1
N2H4-2HC1
N2H4-H20
N2H4H2SO„
NH2OH
NHaOH-HCl
2NH2OHH2SQ,
NH2S03H
NH4[B(CeH6)4]
NH4Br
NH4(CH02)
(формиат)
NH4(C2H302)
(ацетат)
(NH4)2(C204) ■ H20
(NH<i)2C03
(NH4)sC03
NH4HC03
NH4C1
NH,C104
(NH4)2CrO„
(NH4)2Cr20,
NH4F
2
287,82
416,25
143,94
1876,35
1984,44
159,94
179,97
1235,86
160,07
192,13
14,0067
28,0134
42,0201
56,0268
70,0335
84,0402
98,0469
112,0536
126,0603
77,7372
87,5419
89,2227
15,0147
16,0226
32,0453
48,0679
17,0306
34,0612
51,0918
68,1224
85,1531
102,1837
18,0386
36,0772
54,1157
32,0453
68,5063
104,9672
50,0606
130,123
33,030
69,491
164,138
97,093
337,277
97,948
63,0565
77,0836
142,1124
96,0865
114,1019
79,0559
53,942
117,489
152,071
252,065
37,0370
3
2,45912
2,61935
2,15818
3,27331
3,29764
2,20396
2,25520
3,09197
2,20434
2,28360
1,14634
1,44737
1,62346
1,74840
1,84531
1,92449
1,99143
2,04943
2,10058
1,89063
1,94222
1,95048
1,17652
1,20473
1,50576
1,68186
1,23123
1,53226
1,70835
1,83329
1,93020
1,00938
1,25620
1,55723
1,73332
1,50576
1,83573
2,02105
1,69950
2,11435
1,51891
1,84193
2,21521
1,98719
2,52799
1,99100
1,79973
1,88696
2,15263
1,98266
2,05729
1,89793
1,72829
2,07000
2,18205
2,40151
1,56864
1
NH4HF
NH4I
(NH4)2Mo04
(NH4)«Mo7024-4H20
NH4N02
NH4NOs
NH4OH
NH4H2P04
(NH4)2HP04
(NH4)3P04.12Mo03
(NH4)3P0414Mo03
5(NH4)20 12MoOs-
•7H20
NH4MgP04-6H20
NH4NaHP04-4H20
NH4ZnP04
(NH4)2[PdCle]
(NH4)2[PtClel
NH4Re04
(NH4)2S
NH4HS
NH4SCN
(NH4)2S203
(NH4)2S208
NH4HSO,
NH4Fe(S04)2-12H2O
(NH4)2Fe(S04)s-6H20
(NH4)2Ni(S04)2-6H20
(NH4)2S208
(NH4)2SiFe
(NH4)2[SnCle]
NH4VOa
NO
N20
N02
2N02
3N02
4N02
5N02
6N02
HN02
NOa
2N03
3NOs
4N03
HN03
2HN03
3HNOs
(C20HieN4)HNO3
(ннтрои)
(C22H19N)HN03
(динафтодиметилани-
лнн)
N203
N204
N205
1/2 NsOB
Na
2Na
3Na
4Na
Na3[AlFe]
NaAlSi308
NaAsQ2
2
1
57,0434
144,9430
196,02
1235,86
64,0441
80,0435
35,0460
115,0259
132,0565
1876,35
2164,22
2113,75
245,414
209,0691
178,38
355,2
443,89
268,243
68,141
51,111
76,120
148,203
132,139
115,108
482,193
392,139
395,00
228,203
178,154
367,49
116,979
30,0061
44,0128
46,0055
92,0110
138,0165
184,0220
230,0275
276,0330
47,0135
62,0049
124,0098
186,0147
248,0196
63,0129
126,0257
189,0386
375,3902
360,4163
76,0116
92,0110
108,0104
54,0052
22,9898
45,9796
68,9994
91,9592
209,9413
262,225
129,9102
3
1,75621
2,16120
2,29230
3,09197
1,80648
1,90333
1,54464
2,06080
2,12076
3,27331
3,33530
3,32505
2,38990
2,32029
2,25135
2,55045
2,64728
2,42852
1,83341
1,70851
1,88150
2,17086
2,12103
2,06111
2,68323
2,59344
2,59660
2,35832
2,25080
2,56525
2,06811
1,47721
1,64358
1,66281
1,96384
2,13993
2,26487
2,36178
2,44096
1,67222
1,79243
2,09346
2,26955
2,39449
1,79943
2,10046
2,27655
2,57448
2,55680
1,88088
1,96384
2,03347
1,73244
1,36154
1,66257
1,83866
1,96360
2,32210
2,41867
2,11364
2*
Id
продолжение табл. 3
1
Na2HAsOs
Na2HAs04
Na2HAs04-7H20
Na2HAsQ4- 12H20
Na[(CeH5)4B]
NaBH4
NaB02-4H20
NaB03-4H20
Na2B40,
1/2 Na2B40,
Na2B4O,10H2O
I/2Na2B4O,-I0H2O
NaBiOs
NaBr
NaBr-2H20
NaBrOs
Na(C2H302)
(ацетат)
Na(C2H302)-3H20
Na2(C„H4Oe)-2H20
(тартрат)
NaH(C4H4Oe)
NaK(C4H4Oe)-4H20
Na(CeH50)
(фенолят)
Na8(CeH607)-5,5Hi!0
(цитрат)
Na2(C8H404)
(фталат)
NaH(C8H404)
Na2(C204)
1/2 Na2(C204)
ЫаН(Сг04)
NaH(C204)-H20
Na»H»(C10Hli.N»Og)
(комплексон III)
Na2H2(C10Hl2N2O8)-
•2H20
NaCN
Na2COg
1/2 №гС08
Na2C08-2HsO
№гСО3-10Н2О
l/2Na2CO310H2O
NaHCOa
NaCI
NaOCl
NaC103
NaC104
NaC104-H20
Na8[Co(N02)e]
Na3[Co(NO2)e]0,5H2O
NaaCr04
Na2CrO4-4H20
Na2Cr207
Na2Cr20,-2H20
NaF
Na4[Fe(CN)e]-I0H2O
Na2[Fe(CN)5NO]-2H20
Nal
NalOg
NaI04
Na2Mo04
NaaMo04-2H20
2
169,9074
185,9068
312,0142
402,0909
342,228
37,833
137,861
153,860
201,219
100,6097
381,373
190,6864
279,968
102,899
138,929
150,897
82,0348
136,0808
230,0832
172,0707
282,226
116,0960
357,1563
210,0983
188,1165
133,9995
66,99975
112,0177
130,0330
336,2113
372,2420
49,0077
105,9890
52,99448
142,0196
286,1424
143,07118
84,0071
58,443
74,442
106,441
122,440
140,456
403,9356
412,9433
161,973
234,035
261,967
297,998
41,9882
484,067
297,953
149,8942
197,8924
213,8918
205,92
241,95
3
2,23021
2,26930
2,49417
2,60432
2,53432
1,57787
2,13944
2,18713
2,30367
2,00264
2,58135
2,28032
2,44711
2,01241
2,14279
2,17868
1,91400
2,13380
2,36188
2,23571
2,45060
2,06482
2,55286
2,32242
2,27443
2,12710
1,82607
2,04929
2,11405
2,52661
2,57083
1,69026
2,02526
1,72423
2,15235
2,45658
2,15555
1,92432
1,76673
1,87182
2,02711
2,08792
2,14754
2,60631
2,61589
2,20944
2,36928
2,41825
2,47421
1,62313
1,68491
2,47415
1,17578
2,29643
2,33019
2,31370
2,38373
l
NaN3
NaNH2
NaN02
NaNOs
Na20
1/2 NaaO
2Na20
3Na20
4Na20
NajOi!
NaOH
2NaOH
NaH2P02H20
NaPOs
NaH2P04
NaH2P04H20
NaH2P04-2H20
NasHP04
Na2HP04i 2H20
Na2HP04n 12H20
Na3P04
NasP04- 12H20
NaNH4P04
NaNH4PO„-4HsO
Na4P20,
Na4P2O,10H2O
NaRe04
Na2S
Na2S-9H20
NaHS
NaSCN
Na2SOs
Na2SO,-7H20
NaHSOa
Na2S208
1/2 Na2S2Os
Ыа28г08-5Н20
1/2 Na2S203-5H20
Na2S04
Na2SQ4- lOHssO
NaHS04
NaHS04H20
Na2S204
Na2S204-2H20
Na2Sa06
Na[Sb(OH)e]
Naj,SbS4-9Hi!0
Na2SeOs
NaHSeO.
Na2[SiFe]
Na2Si08
Na2[Sn(OH)„]
NassUiiO,
Na2U20,-6H20
NaMg(U02)8-
•(СгНзОг^-бНаО
NaMg^CbJs-
•(CeH302)e-8Hi!0
NaZn(U02)3-
•(C2H802)e-6H20
NaVO.-4H20
Na2W04
Na2W04-2Hi!0
Nb
2
65,0099
39,0124
68,9953
84,9947
61,9790
30,98950
123,9580
185,9370
247,9160
77,9784
39,9972
79,9944
105,9937
101,9618
119,9771
137,9925
156,0078
141,9590
177,9897
358,1431
163,9408
380,1249
137,0078
209,0691
265,9026
446,0560
273,204
78,044
240,182
56,062
81,072
126,042
252,149
104,060
158,106
79,0529
248,183
124,0913
142,041
322,195
120,059
138,075
174,105
210,136
190,105
246,78
481,11
172,94
150,96
. 188,056
122,064
266,71
634,04
742,13
1496,89
1532,92
1537,94
193,991
293,83
329,86
92,906
3
1,81298
1,59120
1,83882
1,92939
1,79224
1,49121
2,09327
2,26937
2,39430
1,89197
1,60203
1,90306
2,02528
2,00844
2,07910
2,13986
2,19315
2,15216
2,25040
2,55406
2,21469
2,57993
2,13673
2,32029
2,42472
2,64939
2,43648
1,89234
2,38054
1,74867
1,90887
2,10052
2,40166
2,01728
2,19895
1,89792
2,39477
2,09374
2,15241
2,50812
2,07939
2,14012
2,24081
2,32250
2,27899
2,39231
2,68224
2,23789
2,17886
2,27429
2,08659
2,42604
2,80212
2,87048
3,17519
3,18552
3,18694
2,28778
2,46811
2,51833
1,96804
20
Продолжение табл. 3
1
2Nb
NbCl5
Nb205
Nd
2Nd
Nd203
Ni
1/2 Ni
2Ni
Ni(C2H302)-4H20
(ацетат)
Ni(C2H5N40)2
(дициаиамидии)
Ni(C4H,N202)2
(диметилдиоксим)
Ni(C5H5N)4(SCN)2
(пиридин)
Ni(C,HeN02)2
(антраииловая кислота)
Ni(C,HeNO)2
(оксихииолин)
Ni(CeHeNO)2-2H20
NiC03
Ni(CO)4
NiCU
NiCl2-6H20
Ni(NOs)2
Ni(N03)2-6H20
NiO
NiCfe
Ni203
Ni2P20,
NiS
NiS04
NiS04-7H20
Ni(NH4)2(S04)2-6H20
0
1/2 0
20
30
40
50
60
70
80
90
OCH3
OC2H5
OH
20H
ЗОН
40H
50H
60H
Os
20s
OsCl4
Os02
Os04
P
1/5 P
1/3 P
2P
3P
2
185,812
270,171
265,809
144,24
288,48
336,48
58,70
29,35
117,40
248,85
260,79
288,93
491,27
330,96
347,01
383,04
118,71
170,74
129,61
237,71
182,71
290,80
74,70
90,70
165,41
291,35
90,76
154,76
280,87
394,99
15,9994
7,9997
31,9988
47,9982
63,9976
79,9970
95,9964
111,996
127,995
143,995
31,0345
45,0616
17,0074
34,0147
51,0221
68,0295
85,0369
102,0442
190,2
380,4
332,0
222,2
254,2
30,9738
6,19476
10,3246
61,9476
92,9214
3
2,26907
2,43164
2,42457
2,15909
2,46012
2,52696
1,7686
1,4676
2,0696
2,3959
2,41646
2,46080
2,69130
2,51979
2,54030
2,5832
2,0745
2,2323
2,1126
2,37605
2,2618
2,4636
1,8733
1,9576
2,2186
2,4644
1,9579
2,1897
2,4485
2,5966
1,20410
0,90308
1,50513
1,68122
1,80616
1,90307
1,98225
2,04920
2,10719
2,15835
1,49184
1,65381
1,23064
1,53167
1,70776
1,83270
1,92961
2,00879
2,27921
2,58024
2,52114
2,34674
2,40518
1,49099
0,79202
1,01388
1,79202
1,96812
l
4P
5P
6P
7P
8P
9P
PBr3
PC13
POCU
PC15
PH3
РОг
H3POa
P03
2P03
3P03
4P03
HP03
H3P03
P203
1/2 P203
P04
2P04
HP04
H2P04
H3P04
2H3P04
P205
1/2 P205
2P205
P205-24Mo03
P20,
H4P20,
p«s3
P2S5
Pb
1/2 Pb
2Pb
3Pb
PbBr2
РЬ(С2Н30г)2
(ацетат)
РЬ(С2Н302)2-ЗНгО
Pb(C2H5)4
Pb(OH)(C,H4NS2)
(меркаптобензтназол)
Pb(C,HeN02)2
(антраииловая кислота)
Pb№wH7N40,Ji-
• 1,5H20
(пикролоиовая кислота)
Pb(Cl2H10NOS)2
(тиоиалид)
рьсо3
2PbC03Pb(0H)2
PbCb
PbCl4
PbCr04
PbF4
Pbh
PbMoOj
Pb(N03)2
PbO
Pb02
Pb(OH)2
2
123,8952
154,8690
185,8428
216,8166
247,7904
278,7642
270,701
137,333
153,332
208,239
33,9977
62,9726
65,9965
78,9720
157,9440
236,9160
315,8880
79,9800
81,9959
109,9458
54,9729
94,9714
189,9428
95,9794
96,9873
97,9953
195,9906
141,9446
70,97230
283,8892
3596,46
173,9434
177,9753
220,087
222,268
207,19
103,60
414,38
621,57
367,01
325,28
379,33
323,44
390,44
479,45
760,60
639,76
267,20
775,60
278,10
349,00
323,18
245,19
461,00
367,13
331,20
223,19
239,19
241,20
3
2,09305
2,18996
2,26915
2,33605
2,39408
2,44524
2,43249
2,13777
2,18563
2,31856
1,53145
1,79915
1,81952
1,89747
2,19850
2,37459
2,49953
1,90298
1,91379
2,04118
1,74015
1,97759
2,27862
1,98218
1,98671
1,99121
2,29224
2,15212
1,85109
2,45315
3,55588
2,24041
2,25036
2,34259
2,34687
2,31637
2,01534
2,61740
2,79349
2,56468
2,51226
2,57902
2,50979
2,59155
2,68074
2,88116
2,80602
2,42684
2,88964
2,44420
2,54283
2,50944
2,38950
2,66370
2,56482
2,52009
2,34867
2,37874
2,38238
21
Продолжение табл. 3
1 1
рьа
PbS
Pb<SCN)2
PbS04
Pb(S04)2
PbSO.PbO
Pb(V03)2
Pb2V20,
PbW04
Pb
2Pd
Pd(C4H,N202)2
(диметилдиоксим)
Pd(C5H5N02)2-Ch
Pd(CeH9N202)2
(циклогександиондиок-
сим, ииоксим)
Pd(C,HeN02)2
(еалицилальдоксим)
Pd(C9HeNO)2
(ОКСИМ)
Pd(Q0HeNO2)
(1-иитрозо-2-иафтол)
Pd^HeN^g),
(бензоилметилдиоксим)
Pd(CN)2
PdCb
PdCU • 2H20
PdCl4
PdCle
Pdh
Pd(NOs)2
PdO
PdS
PdS2
PdS04
PdS04-2H20
Pr
2Pr
Pr208
Pr2(S04)3
Pt
1/4 Pt
1/2 Pt
2Pt
PtCl4
PtCle
H2[PtCle]
H2[PtCle]>6H20
Pt02
PtS
PiSa
Rb
2Rb
RbAl(S04)2-12HaO
RbBr
Rb2C03
RbCl
RbC104
Rbl
RbN03
Rb2©
Rb2[PtCle]
Rb2S04
-
685,57
239,25
323,35
303,25
399,31
526,44
405,07
628,26
455,04
106,4
212,8
336,1
399,5
388,6
378,7
394,7
450,7
516,8
158,4
177,3
213,3
248,2
319,1
360,2
230,4
122,4
138,5
170,5
202,5
238,5
140,907
281,814
329,912
569,999
195,09
48,773
97,545
390,18
336,90
407,81
409,82
517,92
227,09
227,15
259,22
85,47
170,94
520,76
165,38
230,95
120,92
184,92
212,37
147,47
186,94
578,75
267,00
i
2,83605
2,37885
2,50967
2,48180
2,60131
2,72135
2,60753
2,79814
2,65805
2,0269
2,3280
2,5265
2,60152
2,5895
2,57830
2,59627
2,65389
2,71332
2,19976
2,24871
2,32899
2,39480
2,50393
2,55654
2,36248
2,08778
2,14145
2,23172
2,30643
2,37749
2,14892
2,44996
2,51840
2,75587
2,29024
1,68818
1,98921
2,59127
2,52750
2,61046
2,61259
2,71426
2,35620
2,35631
2,41366
1,93181
2,23284
2,71664
2,21848
2,36352
2,08250
2,26698
2,32709
2,16876
2,27170
2,76249
2,42651
1
Re
2Re
ReCl8
ReCl5
H2[ReCle1
Re02
Re03
Re20„
Re04
(C,„HleN4)-HReQ4
HRe04
Re207
ReS2
Re2S,
ReSe2
Rh
2Rh
RhCl3
[Rh(NH3)llCl]Cb
Rh02
Rha03
Ru
2Ru
Ru04
S
2S
3S
4S
5S
6S
7S
8S
9S
HS
H2S
1/2 H2S
2H2S
C1}Hl2N2 • HaS04
(бензидии)
SCN
SC12
S2C12
SOCl2
S02Ch
so2
2S02
so3
1/2 S03
2S03
H2S03
SssOg
H2S203
HS03C1
so4
1/2 S04
2S04
3S04
H2S04
1/2 H2S04
2H2S04
3H2S04
S204
H„S05
s4oe
2
186,207
372,414
292,567
363,472
400,941
218,206
234,205
420,412
250,204
563,581
251,212
484,410
250,335
596,860
343,13
102,905
205,810
209,264
294,417
134,904
252,808
101,07
202,14
165,07
32,064
64,128
96,192
128,256
160,320
192,384
224,448
256,512
288,576
33,072
34,080
17,040
68,160
282,320
58,082
102,970
135,034
118,969
134,969
64,063
128,126
80,062
40,031
160,124
82,078
112,126
114,142
116,523
96,062
48,031
192,123
288,185
98,078
49,039
196,156
294,233
128,126
114,077
224,252
3
2,27000
2,57102
2,46623
2,56046
2,60308
2,33887
2,36959
2,62366
2,39829
2,75096
2,40004
2,68520
2,39853
2,77587
2,53546
2,01244
2,31347
2,32069
2,46896
2,13002
2,40451
2,00462
2,30565
Я.21767
1,50602
1,80705
1,98314
2,10808
2,20499
2,28417
2,35112
2,40911
2,46026
1,51946
1,53250
1,23147
1,83353
2,45074
1,76404
2,01271
2,13044
2,07543
2,13023
1,80661
2,10764
1,90345
1,60240
2,20446
1,91423
2,04971
2,05745
2,06641
1,98255
1,68152
2,28358
2,45967
1,99157
1,69054
2,29260
2,46869
2,10764
2,05720
2,35074
22
Продолжение табл. 3
1
SaO,
H2S20,
s2o8
H2S208
Sb
1/5 Sb
1/3 Sb
1/2 Sb
2Sb
Sb(QH604)
(пирогаллол)
Sb(CeHeNO)3
(ОКСИХИИОЛИИ)
Sb(C»HeNO)-
■(C„H,NO)2
(ОКСИХИНОЛИЫ)
Sb(Cl2H10NOS)3
(тионалид)
SbCl3
SbCU
SbOCl
Sbl8
SbOK(C4H4Oe)l/2H20
(тартрат)
Sb208
Sb204
Sb205
SbS2
Sb2S3
SbS4
Sb2S5
Sc
2Sc
Sc203
Se
2Se
H2Se
Se2Cl2
Se02
SeOs
H2SeOs
SeO,
H2Se04
Si
1/4 Si
2Si
3Si
4Si
5Si
6Si
7Si
8Si
9Si
SiC
SiCl4
SiF4
SiF6
H2[SiFe]
SiOa
2S1O2
3SiOi!
4Si02
5Si02
2
176,124
178,140
192,123
194,139
121,75
24,35
40,58
60,88
243,50
262,85
554,21
572,23
770,60
228,11
299,02
173,20
502,46
333,93
291,50
307,50
323,50
217,94
339,69
250,01
403,82
44,956
89,912
137,910
78,96
157,92
80,98
228,83
110,96
126,96
128,97
142,96
144,97
28,086
7,022
56,172
84,258
112,344
140,430
168,516
196,602
224,688
252,774
40,097
169,898
104,080
142,076
144,092
60,085
120,170
180,254
240,339
300,424
3
2,24582
2,25076
2,28358
2,28811
2,08547
1,38650
1,60834
1,78444
2,38650
2,41971
2,74367
2,75757
2,88683
2,35814
2,47570
2,23855
2,70110
2,52366
2,46464
2,48785
2,50987
2,33834
2,53108
2,39796
2,60619
1,65279
1,95382
2,13960
1,89741
2,19844
1,90838
2,35952
2,04516
2,10366
2,11049
2,15520
2,16128
1,44849
0,84643
1,74952
1,92561
2,05055
2,14746
2,22664
2,29359
2,35158
2,40273
1,60311
2,23018
2,01737
2,15252
2,15864
1,77877
2,07980
2,25588
2,38082
2,47773
l
SiO„
2SiOs
3Si03
4Si03
5SiOs
H2Si03
Si04
2Si04
3Si04
4Si04
5SiO,
H3Si04
SiaO,
Si308
Sm
2Sm
Sm2Og
Sn
1/4 Sn
1/2 Sn
2Sn
Sn(C204)
SnCU
SnCl2-2H20
SnCl4
SnO
Sn02
SnS
SnS2
SnS3
Sr
1/2 Sr
2Sr
SrBr2 • 6H20
Sr(C2H3O2)2-0,5H2O
(ацетат)
Sr(C204)
Sr(C204) • HaO
SrC03
SrCU
SrCl2 • 6H20
SrCr04
SrF2
Sr(N03)2
Sr(N03)2-4H20
SrO
Sr(OH)2
Sr(OH)2-8H20
SrS
Sr(HS)2
SrC03
SrS203
SrSO.
SrTi03
Та
2Ta
TaCl5
Ta2Os
Tb
2Tb
Tb203
Те
2Te
H2Te
2
76,084
152,168
228,253
304,337
380,421
78,100
92,084
184,167
276,251
368,334
460,418
94,100
168,168
212,253
150,35
300,70
348,70
118,69
29,67
59,34
237,38
206,71
189,60
225,63
260,50
134,69
150,69
150,75
182,82
214,88
87,62
43,81
175,24
355,53
214,72
175,64
193,66
147,63
158,53
266,62
203,61
106,62
211,63
283,69
103,62
121,63
265,76
119,68
153,76
167,68
199,75
183,68
183,52
180,948
361,896
358,2131
441,893
158,924
317,884
385,846
127,60
255,20
129,62
3
1,88129
2,18232
2,35842
2,48335
2,58026
1,89265
1,96418
2,26521
2,44130
2,56624
2,66315
1,97359
2,22574
2,32685
2,17711
2,47813
2,54245
2,07441
1,47235
1,77338
2,37544
2,31536
2,27784
2,35340
2,41581
2,12934
2,17808
2,17826
2,26202
2,33220
1,94260
1,64157
2,24363
2,55088
2,33187
2,24462
2,28704
2,16917
2,20011
2,42589
2,30880
2,02784
2,45284
2,32558
2,01544
2,08504
2,42449
2,07802
2,18684
2,22448
2,30049
2,26406
2,26368
2,25755
2,55858
2,55414
2,64532
2,20119
2,50225
2,58642
2,10585
2,40688
2,11267
23
Продолжение табл. 3
1
ТеС14
ТеОг
Те03
Н2Те04
НвТеОв
Th
2Th
Th(C9H,NO)4.
• (C9H,NO)
(оксихинолин)
Th<CwH7N40B)i'H.O
(пнкролоновая кислота)
Th(C204)2-6H20
ThCl4
Th(N08)4
Th(N03)4-4H20
Th(N03)4-12HaO
ThOa
Th(OH)4
Th(S04)2
■ЩБШг-ЭНаО
Ti
1/4 Ti
1/3 Ti
2Ti
3Ti
TiCl8
TiCl4
TiF,
ТЮ
TiO(C„HeNO)s
(оксихииолии)
TiOS04
TiOa
Ti08
Ti208
TI
2T1
TIBr
T1(C,H4NS2)
(меркаптобензтиазол)
TKQaH^NOS)
(тиоиалид)
TUC03
T1C1
lCo(NH3)e][TlCle]
Т12СЮ4
Til
TiN08
TUO
TUO.
TIOH
TUS
Tl2S04
и
1/6 U
1/4 U
2U
3U
UCI4
UF4
UF,
U02
2U02
2
269,41
159,60
175,60
193,61
229,64
232,038
464,076
953,817
1302,818
516,170
373,850
480,058
552,119
696,242
264,037
300,067
424,161
586,299
47,90
11,98
15,97
95,80
143,70
154,26
189,71
161.89
63,90
352,21
159,96
79,90
95,90
143,80
204,37
408,74
284,28
370,61
420,65
468,75
239,82
578,20
524,73
331,27
266,37
424,74
456,74
221,38
440,80
504,80
238,03
39,67
59,51
476,06
714,09
379,84
314,02
352,02
270,03
540,06
3
2,43041
2,20303
2,24452
2,28693
2,36105
2,36556
2,66659
2,97947
3,11488
2,71279
2,57270
2,68129
2,74203
2,84276
2,42166
2,47722
2,62753
2,76812
1,68034
1,07828
1,20319
1,98137
2,15746
2,18825
2,27809
2,20922
1,80550
2,54680
2,20401
1,90255
1,98182
2,15776
2,31042
2,61145
2,45375
2,56892
2,62392
2,67094
2,37989
2,76208
2,71994
2,52018
2,42548
2,62812
2,65967
2,34514
2,64424
2,70312
2,37663
1,59848
1,77458
2,67766
2,95375
2,57960
2,49696
2,54657
2,43141
2,73244
l
ио2(сгн8о2)2
(ацетат)
U02(C2H302)a-2H20
UOs(CeHeNO)s-
•(C„H,NO)
(ОКСИХИИОЛИИ)
U02(N03)2
U02(N08)2-6HaO
(U02)2P20,
U02(S04)
U02(S04)-3H20
uo3
uo4
U20,
u3o8
V
1/5 V
1/3 V
2V
vcu
vci3
VCld
VOs
vo3
V2Os
V203(C„HeNO)4
(оксихииолии)
V04
v2o5
V20,
v2s3
V2S6
w
2W
WC16
W02(CeHeNO)2
(оксихииолии)
wo3
wo4
W&
Y
2Y
Y203
Yb
2Yb
Yb203
Zn
1/2 Zn
2Zn
Zn(C2H802)
(ацетат)
Zn(C2H302)2-2H20
Zn(C5H6N)2(SCN)a
Zn(C,HeN02)2
(аитраииловая кислота)
Zn(CeHeNO)2
(оксихинолин)
Zn(C9HeNO)2 • H20
(хиыальдиновая кислота)
Zn(CN)2
ZnC03
ZnCb
ZnCla-l,5H20
ZnF2
2
388,12
424,15
703,50
394,04
502,13
714,00
366,09
420,14
286,03
302,03
588,06
842,09
50,942
10,188
16,981
101,884
121,848
157,301
192,754
82,941
98,940
149,882
726,499
114,940
181,881
213,880
198,076
262,204
183,85
367,70
361,12
504,16
231,85
247,85
247,98
88,905
177,810
225,808
173,04
346,08
394,08
65,37
32,68
130,74
183,46
219,49
339,74
337,63
353,68
427,71
117,41
125,38
136,28
163,30
103,37
3
2,58897
2,62752
2,84726
2,59554
2,70081
2,85370
2,56359
2,62339
2,45641
2,48005
2,76942
2,92536
1,70708
1,00810
1,22996
2,00811
2,08581
2,19673
2,28500
1,91877
1,99537
2,17575
2,86121
2,06047
2,25979
2,33017
2,29683
2,41864
2,26446
2,56549
2,55765
2,70257
2,36521
2,39419
2,39442
1,94893
2,24996
2,35374
2,23815
2,53918
2,59559
1,81538
1,51435
2,11641
2,26354
2,34141
2,53115
2,52844
2,54861
2,63115
2,06971
2,09823
2,13443
2,21299
2,01439
24
Продолжение табл. 3
1
ZnF2-4H20
ZnHg(SCN)4
Znb
Zn(NO„)2
Zn(N03)2-6H20
ZnO
Zn(OH)2
Zn3P2
Zn3(P04)2-4H20
ZnNH4P04
Zn2P20,
ZnS
ZnS04
ZnS04-7H20
ZnS04-(NH4)2S04
• 6H2O
2
175,43
498,29
319,18
189,38
297,47
81,37
99,38
258,06
458,11
178,38
304,68
97,43
161,43
287,54
401,66
3
2,24411
2,69748
2,50404
2,27733
2,47344
1,91046
1,99730
2,41172
2,66097
2,25135
2,48384
1,98869
2,20798
2,45870
2.W386
1
Zr
2Zr
ZrC
Zr(C9HeNO)4
(оксихииолин)
ZrCl4
ZrOCl2-8H20
ZrFe
Zr(NOs)4
Zr(N03)4-5H20
гю2
ZrP20,
ZrSa
Zr(S04)2
Zr(S04)2-4H20
ZrSi04
2
91,22
182,44
103,23
667,84
233,03
322,25
205,21
339,24
429,32
123,22
265,16
155,35
283,34
355,40
183,30
3
1,96009
2,26112
2,01381
2,82467
2,36741
2,50819
2,31220
2,53051
2,63278
2,09068
2,42351
2,19131
2,45231
2,55072
2,26316
4. ФАКТОРЫ ДЛЯ ПЕРЕСЧЕТА ХИМИЧЕСКИХ
СОЕДИНЕНИЙ
Ищут: эквивалентное ему
количество Ag2ONb, г.
Прямого пересчета по табличным
данным сделать нельзя, так как не
даются факторы для выражения
Ag20«— AgSCN. В таком случае
вначале используют выражение AgSCN *-*
*-*Ag для пересчета AgSCN в Ag,
а затем используют выражение Ag *-»
*-»Ag20 для пересчета Ag в Ag20:
0,5000 г AgSCN -0,65002 = 0 32501г
Ag,
0 32501 г Ag-1,0742 = 0,34913 г
Ag20.
Таким образом, искомое
количество Ag20 находят путем умножения
данного количества AgSCN на два
фактора:
0,5000 г AgSCN-0,65002-1,0742 =
= 0 34913 г. Следует оставить
0,3491 г AgaO.
lg фактора
1
Фактор
2
Пересчитываемые формы
3
Фактор
4
lg фактора
5
А В = 107,870 lg А В = 2,03290
0,84488 —1
0,75925 —1
0,54998 —1
0,69965
0,57445
0,39353
Ag —► AgsAs04
Ag ■«-»■ AgBr
Ag ~ Ag(C,H4NS2)
(мерка птобензтиазол)
1,4293
1,7408
2,5411
0,15512
0,24075
0,40502
Пользование таблицей поясняется
двумя нижеследующими примерами.
Пример 1.
Дано: 0,5000 г Ag3As04.
Ищут: содержание серебра, г.
В таблице находят выражение
Ag ** Ag3As04.
Так как ищут серебро, то
соответствующим фактором будет являться
0,69965:
0,5000 г Ag3As04- 0,69965 =
= 0,34983 г, следует оставить
0,3498 г Ag.
Дано: 0,34983 г Ag.
Ищут: эквивалентное ему
количество Ag3As04 г.
В этом случае 0,34983 Ag • 1,4293 =
= 0,50001 г Ag3As04.
Пример 2.
Дано: 0,5000 г AgSCN.
ш
Продолж&тие
0,90615 —1
0,87659 —1
0,66226 —1
0,80278 —1
0,96893—1
0,88825 —1
0,81292 —1
0,07379
0,86160
А1
0,76885 —2
0,72366
0,34489 ■
0,85553 •
0,04520 ■
0,58245 -
0,03129 -
0,05100 -
" 0,62122 -
0,47422 -
0,18469 -
0,23510
0,70147 -
0,44320
As
0,78498 -
0,87932 -
0,73185 -
0,81422 -
0,20947 -
0,12717-
0,68363 -
0,78463 -
0,41308 -
0,68406 -
0,94807 -
0,89511 -
0,93489 -
0,84031 -
0,90531 -
0,80473 -
0,90828 -
0,86942 -
0,97042 -
0,86986 -
0,89942 -
0,03922
0,07831
Au
0,94612 —1
0,83484 —1
0,72954 —1
0,81248 —1
0,67966 —1
0,69473 —1
0,80566
0,75265
0,45947
0,63501
0,93096
0,77311
0,65002
1,1852
7,2711
0,058728
0,52925
0,22125
0,71701
0,11097
0,38234
0,10747
0,11246
0,41804
0,29800
0,15300
1,7183
0,51341
2,7746
0,60952
0,75739
0,53932
0,65195
0,16198
0,13402
0,48264
0,60902
0,25887
0,48312
0,88729
0,78544
0,86078
0,63725
0,80410
0,63787
0,80962
0,74031
0,93416
0,74107
0,79327
1,0945
1,1976
0,88332
0,68366
0,53646
0,64935
0,47825
0,49514
Ag — AgSCN
Ag — AgCl
Ag — Agl
Ag *-» AgN03
Ag ~~Ag3P04
Ag — AgSCN
AgNO, — AgCl
Ag2S ~ H,S
»B=26,9815 lg А В = 1,43106
Al *- Al(CeHeNO)8
(оксихинолнн)
Al «— A1,03
Al *- AlP04
A1F, *-» CaF2
AlA ** Al(CBH6NO)3
(оксихинолнн)
A1C13
KA1(S04), • 12H,0
NH4A1(SQ4)2-12H20
A1203 •«-»
AlA <-»
AlA
A1203 — A1PO,
A1203 ** A12(S04)3
AlA — A12(S04)3 • 18H20
A1P04 — P205
A12(S04)3 *~ A12(S04)3-18H20
Al»(SOe)8-18H20 «~S02
AB = 74,9216 lg AB = 1.87461
As *-* AsO«
As *-► AsA
As — AsQ,
As — As265
As *-» Ag„As04
As *-► Ag2TlAs04
As — Mg2As2Q,
As *-► As2S3
As — MgNH4As04-6HsO
As ■*-* As8S5
H,AsOs *- H3As04
~ *-► H3As03
*» AsA
*-* MgjjAsA
* ' * AS2O3
*- As2S5
— H3As04
*■* Mg2As2Oj
*-* As,S.
AsA
As203
AsA-
AsA
AsA-
AsA
AsA
AsA
AsA
** AsjA
_ _ As2be
Na2HAs03 *-► Mg2As20,
Na2HAs04 *-* MggAsA
А В = 196,967 lg А В = 2,29440
Au — AuCN
Au *- K[Au(CN)2]
Au *-» K[Au(CN)4]l,5H20
Au *-► AuCl8
Au «-* H[AuClJ-4H20
Au ч-> Na[AuCl4] -4H20
1,2412
1,3286
2,1764
1,5748
1,0742
1,2934
1,5384
0,84370
0,13753
17,028
1,8895
4,5199
1,3947
9,0117
2,6155
9,3052
8,8921
2,3921
3,3557
6,5360
0,58196
1,9477
0,36041
1,6406
1,3203
1,8542
1,5339
6,1735
7,4615
2,0719
1,6420
3,8630
2,0699
1,1270
1,2732
1,1617
1,5693
1,2436
1,5677
1,2351
1,3508
1,0705
1,3495
1,2606
0,91363
0,83500
1,1321
1,4627
1,8641
1,5400
2,0910
2,0196
0,09384
0,12339
0,33774
0,19722
0,03108
0,11173
0,18707
0,92619 —1
0,13840—1
1,23116
0,27635
0,65513
0,14448
0,95481
0,41756
0.96873
0,94901
0,37878
0,52578
0,81531
0,76489 —1
0,28952
0,55679 —1
0,21500
0,12067
0,26816
0,18580
0,79054
0,87283
0,31637
0,21537
0,58692
0,31595
0,05192
0,10490
0,06510
0,19570
0,09468
0,19527
0,09171
0,13059
0,02959
0,13017
0,10058
0,96077
-1
0,92169 -1
0,05389
0,16515
0,27047
0,18752
0,32035
0,30527
26
Продолжение
1
2
3
' 4
5
В
АВ = 10,811 lgAB = 1,03387
0,93382 —2
0,49216—1
0,05457 —1
0,81193—1
0,91016 -1
0,90005 —1
0,72348 —1
0,77226 —1
0,75049 —1
0,95276 —1
0,56241 —1
0,72232 —1
Ва
0,84256 —1
0,78491 —1
0,81921 —1
0,74991 —1
0,73411 —1
0,72057 —1
0,95214 -1
0,90888 —1
0,76969 —1
0,69154 —1
0,94236 —1
0,92713 —1
0,65169
0,93070 —1
0,79762 -1
0,89042 —1
0,83277 —1
0,78197 —1
0,95690 —1
0,81756 —1
0,73939 —1
0,54210
0,86066—1
1,02465
0,86081 -1
Be
0,05219 —1
0,55668 —1
0,97264 —2
0,085865
0,31057
0,11339
0,64853
0,81313
0,79442
0,52903
0,59192
0,56297
0,89694
0,36510
0,52762
0,69592
0,60942
0,65950
0,56222
0,54214
0,52550
0,89566
0,81074
0,58843
0,49152
0,87571
0,84554
4,4842
0,85251
0,62751
0,77700
0,68042
0,60530
0,90552
0,65698
0,54878
3,4842
0,72554
10,584
0,72579
0,11277
0,36032
0,093893
В ~ K[BF4]
В ~ [В2031
В <— Na2B407 • 10Н2О
H3B03 -«->■ Na3B407 • 10Н2О
в2о3 *-* во2
В203 ^ НВ02
В203 •«-<■ NaB02
В203 ~ В03
В203 *-* Н3В03
ВаО, *— В40,
В203 <-> Na2B407 • 10Н2О
Na2B407 <-► Na2B407 • 10Н2О
АВ = 137,34 lg AB = 2,13780
Ва <-* ВаСОз
Ва «-^ Ва(С204)
Ва *— ВаС12
Ва — ВаС13-2Н20
Ва <-► ВаСЮ4
Ва «-» Ba(N03)2
Ва ^ ВаО
Ва •<-<■ BaS
Ва <-<■ BaSO„
Ва ^ Ba[SiFeJ
ВаС03 <— ВаС204
ВаС03 *-* BaS04
BaCOg —* С02
ВаС12 -е-> ВаС12-2Н20
BaF3 «— Ba[SiF6]
ВаО <->■ BaCOg
ВаО <— ВаС204
ВаО <->■ ВаСг04
ВаО <— Ва02
ВаО *-» BaS04
ВаО «-» Ba[SiF6]
ВаО <-► С02
Ва02 <-► BaS04
Ва02 *-* О
BaS «- BaS04
А В = 9,0122 lg А В = 0,95483
Be «— ВеС12
Be •— ВеО
Be *- Ве2Р207
11,646
3,2199
8,8191
1,5420
1,2298
1,2588
1,8903
1,6894
1,7763
1,1149
2,7390
1,8953
1,4369
1,6409
1,5163
1,7787
1,8445
1,9029
1,1165
1,2334
1,6994
2,0345
1,1419
1,1827
0,22300
1,1730
1,5936
1,2870
1,4697
1,6521
1,1043
1,5221
1,8222
0,28701
1,3783
0,094481
1,3778
8,8678
2,7753
1,0650
1,06618
0,50785
0,94543
0,18808
0,08984
0,09996
0,27653
0,22773
0,24952
0,04723
0,43759
0,27768
0,15743
0,21508
0,18079
0,25011
0,26588
0,27942
0,04786
0,09110
0,23029
0,30846
0,05763
0,07287
0,34830 — 1
0,06930
0,20238
0,10958
0,16723
0,21804
0,04309
0,18244
0,26060
0,45790 —1
0,13934
0,97535 —2
0,13919
0,94782
0,44331
1,02735
Bi
АВ = 208,980 \gAB = 2,32011
0,41594 —1
0,14983—1
0,79888 —1
0,51295 —1
0,50092 —1
0,37767 —1
0,82133 —1
0,53516 -1
0,26058
0,14120
0,62933
0,32580
0,31690
0,23860
0,66272
0,34289
ВеО «-» Ве2Р207
ВеО ^ BeSO„-4H20
Bi ^ Bi(CeH303)
(пирогаллол)
Bi ^ Bi(CBHeNO)3
(оксихинолин)
Bi ^ Bi(C9H6N03)-H20
Bi <-* Bi(C12H10NOS)3-H2O
(тионалид)
Bi *-+ BiCl3
Bi «- Bi[Cr(SCN)ej
3,8376
7,0821
1,5890
3,0694
3,1556
4,1911
1,5089
2,9164
0,58406
0,85017
0,20112
0,48706
0,49908
0,62233
0,17866
0,46485
27
Продолокение
1
0,95279 —1
0,90441 —1
0,77370 —1
0,83731 —1
0,91005 —1
0,91079 —1
0,68152 —1
0,95726 —1
2
0,89699
0,80244
0,59389
0,68755
0,81291
0,81432
0,40831
0,90627
3
Bi *-» Bi,03
Bi <->. BiOCl
Bi — BiOI
Bi ♦* BiPO„
Bi «->■ Bi^
Bi(N03)3*- Bi(N03)35H20
Bi203 *- Bi(N08)3-5H20
Bi2Os «-* Bi2S3
4
1,1148
1,2462
1,6838
1,4545
1,2301
1,2280
2,0820
1,1034
5
0,04719
0,09559
0,22629
0,16271
0,08995
0,08920
0,31848
0,04274
Br
0,62895 —1
0,99456—1
0,82701 —1
0,89019 —1
0,79570 —1
0,79229 —1
0,67985—1
0,72392—1
0,35293
0,74628 —1
0,63440 —1
0,80194 —1
0,73876 —1
0,83325—1
0,42555
0,98754
0,67144
0,77658
0,62474
0,61986
0,47847
0,52956
2,2539
0,55754
0,43092
0,63378
0,54798
0,68116
А В = 79,909 Ig AB = 1,90260
Br <-* AgBr
Br «- HBr
Br «-» KBr
Br -* NaBr
Br <-» BrOs
Br —* HB1O3
Br «-» KB1O3
Br *-» NaBr08
Br *- CI
Br — AgCl
HBr «-» AgBr
KBr *■* AgBr
NaBr -— AgBr
ВЮ3 -<-► AgBr
2,3499
1,0126
1,4893
1,2877
1,6007
1,6133
2,0900
1,8884
0,44367
1,7936
2,3206
1,5778
1,8249
1,4681
0,37105
0,00544
0,17298
0,10982
0,20431
0,20771
0,32015
0,27609
0,64706 -1
0,25372
0,36560
0,19805
0,26124
0,16676
С
AB= 12,01115 ]gAB= 1,07958
0,63226 —1
0,43603 —1
0,39888 —1
0,30503 —1
0,78971 —1
0,90185 —1
0,80377 —1
0,85810 —1
0,69863
0,13466
Ca
0,6025—1
0,5576 —1
0,7104 —1
0,8541 —1
0,4689 —1
0,4262
0,3912
0,0580
0,1548
0,4563
0,7906 —1
0,8928 —1
0,3568
0,9428 —1
0,7047 —1
0,2965
0,1437
0,4610
0,1816
0,42881
0,27292
0,25054
0,20185
0,61618
0,79771
0,63646
0,72127
4,9961
1,3635
0,4004
0,3611
0,5133
0,7147
0,2944
2,668
2,462
1,143
1,428
2,859
0,6174
0,7813
2,2743
0,8767
0,5066
1,979
1,392
2,891
1,519
С «- CO
С «— CO,
HCN *-*~Ag
HCN — AgCN
C2H204 *~ Ca(C204) .HjO
QHeOe ~ Ca(C4H4Oe)
(тартрат)
CO *- C02
co2 *- нсо3
C03 «~ С
cos *-* co2
AB= 40,08 \gAB = 1,6029
Ca <-* CaC03
Ca <—► CaCl2
Ca *-» CaF2
Ca *-* CaO
Ca <— CaS04
CaC2 ■«-» С
CaC2 <-► C2H2
CaC2 « CaO
CaCN2 «- CaO
CaCN2 «-* N
CaC03 «— Ca(HCOs)2
CaC03 «- Ca(C204)
CaC03 <-► C02
Ca(C204) ~ Ca(C20)4H20
CaClj, «— CaCl2-6H20
CaCl2 *-► CaO
CaF2 «— CaO
Ca(HCOs)2 — CaO
Ca(N03)4 *- N205
2,3320
3,6641
3,9914
4,9541
1,6229
1,2536
1,5712
1,3864
0,20015
0,73339
2,497
2,769
1,948
1,399
3,397
0,3748
0,4062
0,8749
0,7001
0,3497
1,620
1,280
0,4397
1,141
1,974
0,5053
0,7182
0,3459
0,6582
0,36773
0,56397
0,60112
0,69497
0,21029
0,09816
0,19623
0,14189
0,30136 -1
0,86533 —1
0,3975
0,4424
0,2896
0,1459
0,5311
0,5738 -1
0,6088 —1
0,9420 —1
0,8458—1
0,5437-1
0,2094
0,1071
0,6432 —1
0,0572
0,2953
0,7035 —1
0,8563 —1
0,5390 —1
0,8184 —1
28
Продолжение
1
0,7484 —1
0,5841 —1
0,8972 —2
0,4477 —1
0,7468 —1
0,2895 —1
0,1053
0,8454 —1
0,1209
0,1441
0,9173 —2
0,3395
0,3728
0,7652 —1
0,1336
0,3852
0,4872
0,8980-1
0,2306
2
0,5603
0,3838
0,07892
0,2804
0,5582
0,1948
1,274
0,7005
1,321
1,394
0,08266
2,185
2,359
0,5833
1,360
2,428
3,070
0,7907
1,700
3
CaO «-* CaC03
CaO *- Ca(C204)H20
CaO *- Ca(Cl0H7N4O5)-8H2O
(пикролоновая кислота)
CaO *-~ СаМо04
CaO <-» ЗСа3(Р04)2Са(ОН)2
СаО <-* CaW04
CaO *-~ СОа
СаО -* S03
Са(ОН)2 ~ СаО
Ca3(P04)2 ~ Mg2P20;
Са3(Р04)2 ~ (NH4)3POj • 12МоОэ
Са3(РОА)2— Р205
ЗСа3(Р04)2 -Са(ОН)2 <- Р205
CaS04 «-* BaS04
CaS04 ** CaC03
CaS04 «-* CaO
CaS04-2H20 «— СаО
CaS04 «- CaS04-2H„0
CaS04 *-* S03
4
1,785
2,606
12,67
3,567
1,791
5,134
0,7848
1,428
0,7569
0,7175
12,10
0,4576
0,4238
1,714
0,7352
0,4119
0,3257
1,265
0,5881
5
0,2516
0,4159
1,102
0,5523
0,2532
0,7105
0,8947 —1
0,1546
0,8790 —1
0,8558 —1
1,0827
0,6605 —1
0,6272 —1
0,2341
0,8664 —1
0,6148 —1
0,5128 —1
0,1020
0,7694 —1
0,29061
0,20625
0,25625
0,29221
0,28050
0,26278
0,24610
0,61317
0,36438
0,87539
0,56378
0,77807
0,53919
0,76640
0,64403
0,88883
0,81271
AB = 112,40 lg AB = 2,05077
Cd *- Cd(C5H5N)2-(SCN)2
(пиридин)
Cd *-Cd(C,H,N)4-(SCN)2
(пиридин)
Cd — Cd(C,H„NS2)2
(меркаптобензтиазол)
Cd ^-> Cd(C7H6N02)2
(антраниловая кислота)
Cd — Cd(C„HeNO)2
(оксихинолин)
Cd *~ Cd(C9HeNO)2l,5H20
Cd +~ Cd(C„H6NO)2
(хинальдиновая кислота)
Cd «-» CdCl2
Cd *-* Cd(N03)2 -4H20
Cd ** CdO
Cd *-* Cd2P20,
Cd *- CdS
Cd *- CdS04
Cd(N03)2 — Cd(NOs)2 -4H20
CdO «-» Cd2P207
CdO *-* CdS
CdS04
CdS04-8/3H,0
3,4410 0,53668
4,8485
3,9581
3,4222
3,5650
3,8054
4,0634
1,6309
2,7444
1,1423
1,7738
1,2852
1,8546
1,3048
1,5527
1,1251
1,2305
0,51486
0,38683
0,24472
0,42964
0,25559
0,81408
0,85377
0,42174
0,49302
0,75133
0,75105
0,95352
0,57746
AB = 140,12 lg/4B = 2,14650
Ce «- Ce2(S04)3
Ce «- Ce2(C204)3 • 10H2O
Ce ^-» Ce(C„HeNO)3
(оксихинолин)
Ce — Ce(N03)3
Ce ~ (NH4)2[Ce(N03)e]
Ce <-> CeO,
Ce «-» Ce203
Ce — Ce(S04)2
Ce — Ce2(S04)3
Ce2(C204)3 «- Ce2(C2O4)3-10H2O
Ce(N03)3 *-* Ce(N03)6 -6H20
Cej03 <-► Ce02
Ce203 *-► Ce2(S04)3
1,9423
2,5851
4,0864
2,3275
3,9126
1,2284
1,1713
2,3711
2,0283
1,3310
1,3315
1,0487
1,7317
0,28832
0,41248
0,61134
0,36689
0,59247
0,08934
0,06868
0,37495
0,30713
0,12418
0,12434
0,02065
0,23848
29
Продолжение
1
CI
0,51675—1
0,39335 —1
0,44700 —1
0,98782 —1
0,95745 —1
0,67718 —1
0,70836
0,46487
0,24527
0,29345
0,82136 —1
0,18811
0,78292 —1
0,52893 —1
0,40552 —1
0,76513—1
0,33953 —1
0,32282-1
0,77034 —1
0,34475 —1
0,32803 —1
0,84131 —1
0,39787 —1
0,38184 —1
0,27249 —1
0,31379—1
0,36019 —1
0,85589 —1
0,84568 —1
0,40266—1
0,38621 —1
0,27687
0,86038 —1
Со
0,07882 —1
0,25028 —1
0,18684—1
0,98399 —2
0,97558 —2
0,65695 —1
0,50805—1
0,49170 —1
2
3
АВ = 35,453 lg АЪ ** 1.54966
0,32866
0,24737
0,27990
0,97235
0,90668
0,47553
5,1092
2,9165
1,7590
1,9654
0,66277
1,5421
0,60663
0,33801
0,25440
0,58277
0,21854
0,21029
0,58930
0,22118
0,21283
0.69391
0,24996
0,24090
0,18728
0,20596
0,22919
0,71778
0,70094
0,25250
0,24334
0,18918
0,72506
Cl*- Ag
CI ~- AgCl
С1 — ВаСЮ4
CI *- HC1
С1 ^ К
С1 «- КС1
CI «- Li
CI — Mg
Cl — MgO
CI «- NH4
Cl *- NH4C1
Cl — Na
Cl — NaCl
HC1 — Ag
HC1 — AgCl
C103 ~- AgCl
C108— (СцН^зЫН-НСЮз
(а-динафто-диметиламин)
C103 — (C20HleN4)-HClO3
(нитрон)
HClOg *- AgCl
НС103 — (^HjJaNH-HClOj
(а-динафто-диметиламин)
НСЮ3 *-* (C20HleN4)HClO8
(нитрон)
С104 «- AgCl
СЮ4 *- (СцН^ЫН-НСЮ^
(а-динафто-диметиламин)
С104 *- (C20HieN4)HClO4
(нитрон)
С104 *- (C2eH30N4O2)HClO4
(диантипирилпропилметан)
С104 — (QH^iAs-ClO!
(тетрафениларсоиий)
С104 — (СвН5)4РС104
(тетрафеннлфосфоний)
С104 *-* КСЮ4
НС104 *- AgCl
НСЮ4 ~- (CUH9)2NH-HC104
(а-динафто-диметиламин)
НСЮ4 ** (C20HieN4)-HClO4
(нитрон)
НС104 *-* (C2eH3„N402)HC104
(диантипирилпропилметан)
НС104 — КСЮ4
А В = 58,9332 lg А В = 1,77036
0,11990
0,17794
0,15376
0,096381
0,094531
0,45389
0,32214
0,31024
Со *- Co(C5H5N)4(SCN)s
(пиридин)
Со «-* (C,HeN02)2
(антраннловая кислота)
Со *-* Co(C9HeNO)2 -2НаО
(оксихинолин)
Со *- Co(C,0HeNO2)3-2H2O
(а-нитрозо-р-нафтол)
Со *-» Co(Q0HeNO3)3
(а-нитрозо-р-нафтол)
Со *-*■ СоС12
Со *- Со(ЫОз)„
Со <->■ CoNH4P04-H20
А
3,0426
4,0425
3,5728
1,0284
1,1029
2,1029
0,19572
0,34288
0,56581
0,50880
1,5088
0,64846
1,6485
2,9585
3,9308
1,7174
4,5759
4,7553
1,6969
4,5213
4,6986
1,4411
4,0006
4,1511
5,3397
6,2236
5,8992
1,3932
1,4267
3,9604
4,1095
5,28587
1,3792
8,3401
5,6199
6,5035
10,375
10,579
2,2032
3,1042
3,2233
5
0,48324
0,60665
0,55301
0,01216
0,04254
0,32282
0,29163 -1
0,53514 -1
0,75474 -1
0,70655 -1
0,17863
0,81188 -1
0,21709
0,47107
0,59447
0,23487
0,66048
0,67718
0,22966
0,65526
0,67197
0,15869
0,60213
0,61816
0,72751
0,79404
0,77081
0,14401
0,15433
0,59774
0,61379
0,72312
0,13962
0,92118
0,74973
0,81315
1,01599
1,02445
0,34305
0,49195
0,50830
30
Продолжение
1
0,89569 —1
0,86583 —1
0,60629 —1
0,81133 —1
0,58005 —1
0,73695 —1
0,79836 —1
0,59602 —1
0,97014 —1
0,71060 —1
0,74145—1
2
0,78648
0,73423
0,40392
0,64764
0,38023
0,54570
0,62859
0,39447
0,93356
0,51357
0,55138
3
Со <-» СоО
Со *-*■ Со304
Со <г-* Со2Р207
Со «-► CoS
Со *-* CoS04
Со — СоС12 -6Н20
Co(N03)2 «- Co(N03)2-6H20
СоО — CoNH4P04-H20
СоО <-» Со304
СоО — Со2Р207
CoS04 «■ CoS04-7H20
4
1,2715
1,3620
2,4758
1,5441
2,6300
1,8325
1,5909
2,5351
1,0712
1,947!
1,813b
5
0,10432
0,13418
0,39372
0,18868
0,41996
0,26305
0,20164
0,40400
0,02987
0,28939
0,25854
Сг
АВ = 51,996 lg AB = 1,71597
0,71599—1
0,83518 —1
0,65153 —1
0,19518—1
0,31229 —1
0,42773 —1
0,20653 —1
0,68257 —1
0,54837 —1
0,42352 -1
0,01753 —1
0,11919
0,59627 —1
0,71171 —1
0,49051 —1
0,83237 —1
0,47709
0,37135 —1
0,18364
0,66073 —1
0,55497 —1
0,15262
0,73829 —1
0,75367 —1
Cs
0,91159—1
0,89731 —1
0,75739 —1
0,97462 —1
0,59616 —1
0,86601 —1
0,68456 —1
0,06995
0,69885 —1
0,92269 —1
0,85909—1
0,62154 —1
0,89140 —1
0,54653 —1
Си
0,27425 —1
0,27697 —1
0,51999
0,68420
0,44826
0,15674
0,20525
0,26775
0,16089
0,48147
0,35348
0,26517
0,10412
1,3158
0,39470
0,51489
0,30939
0,67979
2,9998
0,23515
1,5236
0,45786
0,35890
1,4211
0,54739
0,56711
0,81582
0,78942
0,57199
0,94323
0,39460
0,73454
0,48368
1,1747
0,49986
0,83693
0,72292
0,41835
0,77875
3,5199
0,18804
0,18922
Сг <-»■ Сг03
Сг *-* Сг203
Сг *-► Сг04
Сг —~ Ag2Cr04
Сг <- ВаСгО.
Сг *» К2СЮ4
Сг *-* РЬСЮ4
Сг «-» Сг207
Сг «-► К2Сго07
Сг «н* Cr2(Sb4)3
Сг *- KCr(S04)212H20
СЮ., «-* Сг20.,
СЮ3 — ВаСг04
Сг03 «-* К2СЮ4
Сг03 «- РЬСгО,
Cr03 *-* К2Сг207
Сг2Оэ ~ ВаСЮ4
Сг203 *-* РЬСг04
СЮ4 ^ Сг2Оэ
Сг04 ^- ВаСЮ4
Сг04 <-- РЬСгО,
Сг207 *- Сг203
Cr2(S04)3 *- Cr2(S04)3 • 18H20
KCr(S04)2 *» KCr(S04)2-12H20
AB = 132,905 lg AB = 2,12354
Cs ■*-* Cs2C03
Cs *— CsCl
Cs «-* CsCl04
Cs «-* CsaO
Cs «-* Cs2[PtCle]
Cs ■*-* Cs2S04
Cs2C03 «— Cs2[PtCl6]
CsCl «- AgCl
CsCl — Cs2[PtCl6J
Cs20 *-* CsCl
Cs20 +-* CsN03
Cs20 *■* Cs2[PtCl6]
Cs20 -*-» Cs2S04
CsaO *-* S03
AB = 63,546 lg AB = 1,80308
Си ** Cu(C5H5N)a(SCN)2
(пиридин)
Cu — Cu(C,H6N02)2
1,9231
1,4616
2,2308
6,3799
4,8721
3,7349
6,2155
2,0770
2,8290
3,7712
9,6047
0,76000
2,5336
1,9422
3,2321
1,4710
3,3335
4,2526
0,65516
2,1841
2,7863
0,70370
1,8269
1,7633
1,2258
1,2668
1,7483
1,0602
2,5342
1,3614
2,0675
0,85127
2,0006
1,1948
1,3833
2,3903
1,2841
0,28410
5,3181
5,2849
0,28400
0,16483
0,34836
0,80481
0,68772
0,57228
0,79348
0,31744
0,45163
0,57648
0,98249
0,88081 —1
0,40374
0,28829
0,50948
0,16761
0,52291
0,62866
0,81635 — 1
0,33927
0,44503
0,84739 —1
0,26172
0,24633
0,08842
0,10271
0,24262
0,02539
0,40384
0,13399
0,31545
0,93007 —1
0,30116
0,07730
0,14092
0,37845
0,10860
0,45347 — 1
0,72576
0,72303
(антраниловая кислота)
31
Продолжение
1
0,27679 —1
0,25670 —1
0,17377—1
0,09199 —1
0,34246 —1
0,71805 —1
0,90246 —1
0,94848 —1
0,82259 —1
0,90229 —1
0,60001 —1
0,40567 —1
0,81558—1
0,99984 —1
0,95380 —1
0,80565—1
0.49664
2
0,18922
0,18059
0,14920
0,12359
0,22002
0,52245
0,79884
0,88817
0,66464
0,79854
0,39812
0,25449
0,65400
0,99962
0,89908
0,63922
3.1379
3
Си «- Cu(C,HeN02)2
(салицилальдоксим)
Си *- Cu(CeHeNO)2
(оксихииолин)
Си «- Си(С50НвЫО2)2-НаО
(хииальдиновая кислота)
Си ♦* Cu(Cl2Hl0NOS)2H2O
(тионалид)
Си -е* Cu(Cj4HiiN02)
(бепзоиноксим)
Си «- CuSCN
Си -е* СиО
Си ■«-* Си20
Си •«• CuS
Си ** Cu2S
Си «— CuS04
Си -е* CuSO»-5Н„0
СиО «- CuSCN
СиО *— Cu2S
Си20 <-► Cu2S
CuS04 «-CuS04-5H20
CuS04-5H20«- Cu2S
4
5,2849
5,5375
6,7025
8,0913
4,5450
1,9141
1,2518
1,1259
1,5046
1,2523
2,5118
3,9295
1,5290
1,0004
1,1122
1 1,5644
I 0.31869
б
0,72303
0,74331
0,82624
0,90802
0,65753
0,28196
0,09753
0,05150
0,17742
0,09771
0,39999
0,59434
0,18441
0,00017
0,04618
0,19435
0,50337 — 1
F
AB = 18.9984 lg AB = 1.27871
0,83168 —1
0,92457 —1
0,68721 —1
0,97755 —1
0,68704 —1
0,65559 —1
n,73477 —1
0,86102 —2
0,86341 —1
0,90435 —1
0,61061 —1
0,89823 —1
0,71168—2
0,44576 —1
0.70966 —1
0,70950 —1
0,63306 —1
0,44356 —1
0,92069 —1
0,73634 —1
0,80503 —1
0,67870
0,84056
0,48664
0,94962
0,48645
0,45247
0,54296
0,072613
0,73015
0,80232
0,40795
0,79109
0,051485
0.27910
0,51246
0,51228
0,42960
0,27769
0,83307
0,54493
0,63831
F — AIF,
F— BF3
F «- CaF2
F«- HF
F — KHF2
F — NaF
F «- Na3[AlFe]
F «- PbCIF
F *- SiF4
F ~ SiFe
F «- Ba[SiFe]
F «- H2[SiF6]
F ~ (Q,H5)3SnF
(трифенилолово)
F*~ CaS04
HF ** CaF2
2HF «- KHF2
6HF *- Ba[SiFe]
2HF ~ H2[SiFe]
6HF *- H2[SiFe]
6HF +~ K2lSiFe]
6HF — Na2[SiFe]
1,4114
1,1897
2,0549
1,0531
2,0556
2,2101
1,8417
1,3772
1,3696
1,2464
2,4513
1,2641
19,423
3,5829
1,9514
1,9521
2,3278
3,6012
1,2004
1,8351
1,5666
0,16832
0,07544
0,31279
0,02247
0,31294
0,34441
0,26522
0,13899
0,13659
0,09566
0,38939
0,10178
1,28832
0,55424
0,29035
0,29050
0,36694
0,55644
0,07932
0,26366
0,19496
Fe
AB = 55,847 lg А В = 1,74700
0,05832 —1
0,42076 —1
0,45497 —1
0,64404 —1
0,53694 —1
0,25612 —1
0,89059—1
0,84475 —1
0,85950 —1
0,80296 —1
0,30294 —1
0,11437
0,26349
0,28508
0,44060
0,34430
0,18035
0,77730
0,69943
0,72360
0,63527
0,20088
Fe ~ Fe(C9HeNO)3
(оксихииолин)
Fe — Fe(CN)e
Fe «- Fe(CO)5
Fe — FeCl2
Fe •<— FeCl3
Fe -e* Fel2
Fe -e* FeO
Fe -* Fe2Os
Fe — Fe^
Fe ** FeS
Fe — FeS04-7H20
8,7437
3,7953
3,5078
2,2696
2,9045
5,5447
1,2865
1,4297
1,3820
1,5741
4,9782
0,94170
0,57925
0,54504
0,35595
0,46308
0,74388
0,10941
0,15525
0,14051
0,19703
0,69707
32
Продолжение
1
0,44610 —1
0,41234 —1
0,80452 —1
0,77822 —1
0,79248 —1
0,95415—1
0,96890 —1
0,91234 —1
0,26295 —1
0,65212 —1
0,69219 —1
0,29588 —1
0,01473
0,72380 —1
0,82316 —1
0,21903 —1
0,60136 —1
0,40996 —1
0,97144 —1
0,73751 —1
2
0,27932
0,26384
0,63755
0,60010
0,62013
0,89981
0,93090
0,81727
0,18322
0,44887
0,49225
0,19764
1,0345
0,52942
0,66552
0,16559
0,39935
0,25702
0,93635
0,56440
3
Fe «- Fe2(S04)3
Fe(CN)6 ♦* AgCN
FeC!2 «-* FeCl2 -4H20
FeCl3 — FeCl3-6Ha0
FeO «-* FeC03
FeO -<->- Fe2Os
FeO *- Fe304
FeO «— FeS
РЮ *- (NH4)2Fe(SO4)2-6H20
Fe203 *-* Fe(HC03)2
Fe203 ** FeCl3
FeA-— Fe(N03)3-9H20
Fe2Os «->. Fe304
Fe2Os «— FeP04
Fe203 «-» FeS2
Fe203 ♦* NH4Fe(S04)2.12H20
Fe203 — Fe2(S04)3
FeS2 «-* BaS04
FeS2 ** S02
FeS04 «- FeS04-7H20
4
3,5801
3,7901
1,5685
1,6664
1,6126
1,1113
1,0742
1,2236
5,4580
2,2278
2,0315
5,0597
0,96661
1,8889
1,5026
6,0390
2,5041
3,8908
1,0680
1,8301
5
0,55389
0,57865
0,19549
0,22178
0,20753
0,04583
0,03108
0,08764
0,73703
0,34788
0,30782
0,70412
0,98525 — 1
0,27621
0,17684
0,78097
0,39865
0,59004
0,02857
0,26247
0,1388
0,0715
0,7439
/46= 69,72 \gAB = 1,8434
Ga «- Ga(CeHeNO)3
(оксихинолин)
Ga «-* Ga(CeH4Br2NO)3
(дибромоксихинолин)
Ga *-» Ga203
7,203
13,99
1,3442
0,8575
1,146
0,1285
0,3386
0,6940
0,5309
/46= 72,59 lg/4S= 1,8609
Ge *- GeCl4
Ge «-* GeOa
Ge *-» GeS2
2,954 I 0,4704
1,441 I 0,1586
1,884 | 0,2750
8,9364
1,1260
1,0630
А В = 1,00797 lg А В = 0,00342
н2о«- н
H20 *- О
н2о2 *-+ o
0,11190
0,88810
0,94074
0,84798
0,17909
0,50718
0,21147
0,59810
AB = 178,49 lg AB = 2,25162
Hf — Hf02
Hf «-» Hf(C8He03),
(миндалат)
Hf — Hf(P20,)
Hf02 ** Hf(C8HeOs)4
(миндалат)
НЮ2 ~ Hf(P20,)
1,1793
5,5840
1,9711
4,7351
1,6720
0,07161
0,74694
0,29483
0,67533
0,22323
А В = 200,59 lg А В = 2,30231
0,54282 —1
0,84199 —1
0,62758-1
0,50080—1
0,86854 —1
0,34899
0,69502
0,42421
0,31681
0,73882
Hg ~ Hg(C5HBN)AA
(пиридин)
Hg *- Hg(C204)
Hg *~ Hg^HeNO,),
(антраниловая кислота)
Hg -* Hg(C12H10NOS)2
(тионалид)
Hg ~ HgCl2
2,8654
1,4388
2,3573
3,1565
1,3535
0,45718
0,15800
0,37242
0,49921
0,13146
3' A, Id. Лваасел и др.
33
Продолжение
1
0,92932 —1
0,96667 —1
0,98302 —1
0,93561 —1
0,80160 —1
0,06078
0,06707
0,04630
0,97118—1
0,96264 —1
0,96894 —1
0,94630 —1
0,99371 —1
2
0,84980
0,92613
0,96165
0,86220
0,63328
1,1502
1,1670
1,1125
0,93580
0,91758
0,93097
0,88369
0,98562
3
Hg — Hg2Cl2
Hg^HgO
Hg — HgaO
Hg — HgS
Hg ♦* Hg(SCN)2
HgCl2 — HgCl2
HgCl2 «- HgS
Hg2(NO,)2 ** Hg2Cl2
Hg2(NO,)2 — Не2(Ы03)а-2Н20
HgO — Hg2CI2
HgO ** HgS
Hg20 — Hg2Cl2
HgS — HgaCl,
4
1,1768
1,0798
1,0399
1,1598
1,5791
0,86941
0,85691
0,89889
1,0686
1,0898
1,0741
1,1316
1,0146
5
0,07071
0,03334
0,01699
0,06438
0,19841
0,93923 — 1
0,93294 — 1
0,95371 — 1
0,02882
0,03735
0,03104
0,05369
0,00630
0,20980
0,82711
0,54731
0,70478
AB = 114,82 lg AB = 2,06002
In *- In(C9H6NO)3
(оксихинолин)
In *-* ln203
In *■* 1пЮ4
In ■«-»■ In2S3
4,7664
1,2090
1,8271
1,4189
0,8573 | Ir
AB
lr02
192,2 lg AB = 2,2838
1,166
AB = 126,9044 lg AB = 2,10348
1,1765
0,88544
0,54054
0,78164
0,54404
0,57191
0,99212
0,72557
0,72141
0,66476
0,66127
0,76035
0,55674
0,69384
2,3854
0,70463
0,38308
0,77498
I ** Ag
I
1
I
I
I
I
I
1
I
I
I
I
I
1
1
I
•*—>
*-»
■*—>
<—*•
■*—>
<—¥■
<-+
-*—>
-*—>
<-+
4—>
<—¥■
4—>
«-*
*—■
■*—*■
Ю.
AgCl
Agl
ICI
ICI,
IF,
HI
IO,
HIO,
Ю,
HI04
I?05
H\lOfi
•A
Pd
Pdl,
Til
— Agl
0,85001
1,1294
1,8500
1,2794
1,8310
1,7485
1,0079
1,3782
1,3862
1,5043
1,5122
1,3152
1,7962
1,4413
0,41921
1,4191
2,6104
1,3423
AB = 39,102 lg AB = 1,59220
0,31854 —1
0,43857 —1
0,22409 —1
0,51662 —1
0,03790 —1
0,91340 —2
0,71972 —1
0,50387 —1
0,45059 —1
0,37205 —1
0,58742—1
0,20823
0,27282
0,16753
0,32856
0,10912
0,081922
0,52447
0,31906
0,28222
0,23555
0,38674
К -» AgBr
К — AgCl
К — BaS04
К ** KBr
К — K[B(QH5)4]
(тетрафенилбор)
К — K(C12H4N,012)
(дипикриламин)
К — KC1
К *- KClOg
К — KC104
К -— KI
К *- KN03
4,8023
3,6654
5,9690
3,0436
9,1642
12,207
1,9067
3,1342
3,5434
4,2455
2,5857
0,68145
0,56412
0,77590
0,48338
0,96210
1,08661
0,28028
0,49613
0,54942
0,62793
0,41258
34
Продолокение
1
0,91916—1
0,20659 —1
0,65202—1
0,60300—1
0,80194—1
0,17298
0,94910—1
0,38193
0,49700
0,96704 —1
0,45390 —1
0,12805
0,61490 —1
0,85926—1
0,71616—1
0,32282
0,78416—1
0,73086—1
0,48686 —1
0,88327 —1
0,93201 —1
0,53867
0,98530 —1
0,59196
0,88456—1
0,76392—1
0,17266
0,84948 —1
0,11664
0,95978 —1
0,22694
0,35011
0,13229
0,61917—1
0,85845
0,77355
0,27236
0,60596 —1
0,11873—1
0,59745 —1
0,83352—1
0,67252 —1
0,80056—1
0,53142—1
0,45291 —1
0,66826—1
0,92400—1
0,28742
0,73286 —1
0,68383—1
0,90952
0,67434—1
0,87311 —1
0,79857 —1
0,55457 —1
0,33778
0,29052
0,76599 —1
2
0,83016
0,16091
0,44876
0,40086
0,63378
1,4893
0,88939
2,4095
3,1405
0,92692
0,28438
1,3429
0,41200
0,72320
0,52019
2,1029
0,60835
0,53810
0,30680
0,76431
0,85508
3,4568
0,96672
3,9081
0,76658
0,58065
1,4882
0,70709
1,3081
0,91154
1,6863
2,2393
1,3561
0,41607
7,2185
5,9368
1,8722
0,40361
0,13144
0,39577
0,68158
0,47046
0,63177
0,33995
0,28373
0,46586
0,83946
0,19383
0,54057
0,48287
0,81193
0,47244
0,74664
0,62888
0,35856
2,1766
1,9522
0,58343
3
К ~ КгО
К *- Ka[PtCle]
К ~ K2S04
К *-* Pt
КВг <— AgBr
КВг «- Вг
КВгО, *-► AgBr
KCN -~ HCN
К2СОя *-* С02
КгСО'з <-* KCI
КгС03 ~ K2[PtCl6]
КНСО3 — КС1
кнсо, *-* кг[ргав]
КН(С4Н4Ов)-4Н20 — Са(С4Н406)-4Н20
(тартрат)
KCl ~ AgCl
KCl — Cl
KCl ** KC103
KCl ^- КСЮ4
KCl — K2[PtC!6J
KCl ** Pt
KO03 ~ AgCl
KC!03 — Cl
KC104 — AgCl
KC104 *- Cl
K2Cr04 — BaCrO,
КгСг207 *— BaCr04
KF ** CaF2
KI — Agl
KI •«- I
КЮ3 4- Agl
КЮЗ «- I
KNO3 *- N203
KN03 — KCl
KNO3 ~ K2[PtC!e]
KN03 ~ N
KNO3 ~ NH3
KNO, *- N205
K2O '«- BaS04
КЮ ** K[(C,H,)4B]
(тетрафенилбор)
КгО — КВг
КгО *-* КгС03
КгО — КНСОз
КгО «- КС1
КгО — КСЮ4
КгО — KI
КгО ~ KN03
КгО «- КОН
КгО ♦* KafPtClJ
КгО *-* KzSQ,
КгО *- Pt
КОН «- КгС03
K2S «- BaS04'
K2S04 *- BaS04
K2S04 — KC104
K2S04 «- KafPtCLJ
K2S04 — S03
KA1(S04)2-12H20 — K2[PtCle]
KHS04 *■* BaS04
4
1,2046
6,2146
2,2284
2,4946
1,5778
0,67144
1,1244
0,41502
0,31842
1,0788
3,5164
0,74466
2,4272
1,3827
1,9224
0,47553
1,6438
1,8584
3,2594
1,3084
1,1695
0,28929
1,0344
0,25588
1,3045
1,7222
0,67194
1,4143
0,76446
1,0970
0,59300
0,44656
0,73739
2,4034
0,13853
0,16844
0,53414
2,4776
7,6078
2,5267
1,4672
2,1256
1,5829
2,9416
3,5244
2,1466
1,1912
5,1592
1,8499
2,0710
1,2316
2,1167
1,3393
1,5901
2,7889
0,45942
0,51225
1,7140
5
0,08085
0,79341
0,34800
0,39700
0,19805
0,82701 —1
0,05092
0,61807 —1
0,50300 — 1
0,03294
0,54610
0,87196 —1
0,38511
0,14073
0,28384
0,67718 —1
0,21585
0,26914
0,51314
0,11674
0,06800
0,46134 —1
0,01469
0,40804 — 1
0,11544
0,23608
0,82733 — 1
0,15054
0,88336 — 1
0,04021
0,77305 —1
0,64988 — 1
0,86769 —1
0,38082
0,14154—1
0,22644 —1
0,72765 — 1
0,39403
0,88126
0,40256
0,16649
0,32748
0,19945
0,46858
0,54709
0,33175
0,07598
0,71259
0,26715
0,31618
0,09047
0,32566
0,12688
0,20143
0,44543
0,66221 —1
0,70948—1
0,23401
La
AB = 138,91 lg AB = 2,14273
0,93079—1 I 0,85268 I La-*->-La203 1 1,1728 I 0,06923
Продолжение
АВ = 6,939 lg АВ = 0,8413
2
0,1878
0,1637
0,4645
0,4873
0,1798
0,1262
1,6789
0,2718
0,8592
Li <-► Li2C03
Li -<->- LiCl
Li — Li20
Li — 2Li20-5Al203
Li *- Li3P04
Li «-* Li2S04
Li2C03 •<— СОг
Li20 «-* Li2S04
Li2S04 *■* Li2S04-H20
5,324
6,109
2,153
2,052
5,562
7,922
0,5956
3,6798
1,1639
0,077768
0,069732
0,28833
0,25533
0,60311
0,099065
0,21847
0,20197
1,9160
0,82395
0,75763
1,3429
0,46834
0,85563
2,4969
0,91595
0,47812
0,21859
0,14507
0,69112
0,16426
0,36224
0,40152
0,57298
0,56798
0,50350
0,51574
1,0817
0,48837
1,5035
X>3
AB = 24,312 lg AB = 1,38582
Mg ~ Mg(C9HeNO)2
(оксихинолин)
Mg — Mg(C9HeNO)2-2HaO
Mj_
Mg *-►
Mg-*
Mg~
Mg —*
Mg «-►
MgC03
MgC03
Mg^3
MgCb
MgO
MgNH4P04-6H20
Mg2P207
— MgC03-H20
MgC03 -* MgaPaO,
MgCb *-* CI
MgCla -* MgCU-6H20
MgCl2 ♦* MgaPaO,
MgCb-KCl-6HaO —► MgaPaO,
MgO — COa
MgO *- MgC03
MgO —»• MgC03-CaC03
MgO — MgCl2-KCl-6HaO
MgO *- Mg(OH)2
MgO — MgNH4P04-6H20
MgO *- Mg2P207
MgO «-* MgSi03
MgO -* MgaSi04
MgO *■* P205
MgO -* S03
MgS04 -* BaS04
Mg2P207
MgS04-7H20
~ SOs
MgS04
MgS04
MgS04
1,2859
1,4341
3,4679
3,9165
1,6581
10,094
4,5773
4,9512
0,52193
1,2137
1,3199
0,74467
2,1352
1,1687
0,40049
1,0918
2,0915
4,5747
6,8930
1,4469
6,0880
0,7606
2,4905
1,7453
1,7606
1,9861
1,9390
0,92448
2,0476
0,66511
А В = 54,9381 lg А В = 1,73987
0,05188 —1
0,67938 —1
0,64004—1
0,48715—1
0,88900—1
0,80067 —1
0,84259—1
0,69480 —1
0,85751 —1
0,54112—1
0,58786 —1
0,47044—1
0,80034 —1
0,11269
0,47794
0,43656
0,30701
0,77446
0,63193
0,69597
0,49522
0,72030
0,34763
0,38713
0,29542
0,63146
Mn — Mn(C5H5N)4(SCN)2
(пиридин)
Mn —» MnC03
Mn *-* MnCh
Mn -* Mn(NOs)2
Mn «-► MnO
Mn <-» Mn02
Mn *-* Mn203
Mn —► Mn207
Mn —»■ Mn304
Mn — KMn04
Mn «->■ Mn2P207
Mn — MnNH4P04-H20
Mn *-»■ MnS
8,8738
2,0923
2,2907
3,2573
1,2912
1,5825
1,4368
2,0193
1,3883
2,8767
2,5831
3,3850
1,5836
0,94811
0,32062
0,35997
0,51286
0,11100
0,11935
0,15740
0,30520
0,14248
0,45890
0,41214
0,52956
0,19965
36
Продолжение
12 3 4 5
0,56090—1
0,41694
0,80338—1
0,79479 —1
0,79038 —1
0,95359—1
0,96852—1
0,69886—1
0,91135—1
0,67189—1
0,05682
0,01494
0,81088 —1
0,83055—1
0,79682—1
0,27554
Mo
0,36383
2,6118
0,63588
0,62343
0,61713
0,89866
0,93008
0,49988
0,81535
0,46978
1,1398
1,0350
0,64696
0,67694
0,62636
1,8860
Мп ** MnS04
МпС03 -e* C02
MnCb «— МпС1г-4Н20
Mn(N03)2 — Mn(N03)2-6H20
MnO *- MnC03
MnO *-* Mn2Os
MnO «-* Mn304
MnO ■<-* Mn2P207
MnO -<->- MnS
MnO <-- MnS04
Mn02 — Mn304
Mn203 «-► Mn304
MnS04 *- BaS04
MnSO„ ** MnS04-4H20
MnS04 — MnS04-5H20
MnS04 *- S03
2,7485
0,38287
1,5726
1,6040
1,6204
1,1128
1,0752
2,0005
1,2265
2,1286
0,87731
0,96622
1,5457
1,4772
1,5965
0,53021
0,43910
0,58305 —1
0,19662
0,20520
0,20962
0,04642
0,03149
0,30114
0,08867
0,32810
0,94316—1
0,98508 — 1
0,18910
0,16944
0,20317
0,72445 —1
А В = 95,94 lg А В = 1,98220
0,3626 -
0,8238 -
0,7780 -
0,6897 -
0,7777 -
0,5934 -
0,0458
0,8659 -
0,9113-
0,9640-
0,9397 -
0,4172 -
-1
-1
-1
-1
-1
-1
-1
-1
-1
-1
-1
0,2305
0,6665
0,5998
0,4894
0,5994
0,3921
1,1112
0,7343
0,8153
0,9206
0,8704
0,2613
Mo -e* Mo02(CeH6NO)2
(оксихинолин)
Mo «-► Mo03
Mo *-» Mo04
Mo -e* (NH4)2Mo04
Mo *-* M0S2
Mo «— PbMo04
Mo04 -<-► Mo03
Mo03 — (NH4)2Mo04
Mo03 ** (NH4)eMo7024
4H20
MoO, «-* (NH4),P04-12Mo03
MoOs «- (NH4)3P04-12MoO,-6HaO
M0O3 — PbMo04
4,3386 1
1,5003
1,6671
2,043
1,668
2,5506
0,9000
1,362
1,227
1,086
1,149
3,8280
0,6374
0,1762
0,2220
0,3103
0,2223
0,40664
0,9542 —1
0,1341
0,0887
0,03595
0,06028
0,58289
N
AB= 14,0067 \gAB= 1,14634
0,80009 —2
0,03019
0,05839
0,70327 —2
0,84133 —2
0,08490
0,97503 —1
0,54959 —1
0,50294—1
0,32791 —1
0,68662 —1
0,88499 —2
0,41123—1
0,75402 —1
0,43881 —1
0,88854 —1
0,65132—1
0,43180 —1
0,49879—1
0,24202 —1
0,57198 —1
0,17863
0,16646
0,58195
0,38204 —1
0,93587 —1
0,063109
1,0720
1,1439
0,050498
0,069395
1,2159
0,94412
0,35448
0,31838
0,21277
0,48598
0,076773
0,56757
0,25777
0,77366
0,44805
0,27467
0,27027
0,31535
0,17459
0,37323
1,5088
1,4671
3,8190
0,24101
0,86271
N ~ (NH4)2[PtCle]
NH «- N
NH2 — N
NH3 ~ (NH4)[B(CeHs)4]
(тетрафенилбор)
NH3 «-* MgNH4P04-6H20
NH3 «-* N
NH3 «- NH4
NH3 -e* (NH4)2C0,
NH3 «- NH4C1
NH3 «-* NH4NOs
NH3 *~ NH4OH
NH3 *- (NH4)2fPtCle]
NH, ♦* NO
NH; «- (NH4)aS04
NH3 *- N20
NH3 «- N203
NH3 ~ N03
NH3 ~- HNOt
NH3 -e* N205'
NH3 «-* Pt
NH4C1 «- AgCI
NH4C1 -~ CI
NH4C1 -* HC1
NH4C! «- N
NH4C1 «- (NH4)2PtCl6
NH4C1 — N03
15,846
0,93287
0,87418
19,802
14,410
0,82244
1,0592
2,8210
3,1409
4,7000
2,0578
13,032
1,7619
3,8795
1,2922
2,2316
3,6408
3,6999
3,1711
5,7276
2,6793
0,66277
0,68163
0,26185
4,1491
1,1591
1,1992
0,96983 —1
0,94160 —1
1,29673—1
1,15866
0,91510 -1
0,02498
0,45040
0,49706
0,67210
0,31340
1,11501
0,24596
0,58878
0,11133
0,34861
0,56120
0,56819
0,50121
0,75797
0,42802
0,82136—1
0,83355—1
0,41806—1
0,61795
0.0R4I2
37
Продолжение
1
0,92887 —1
0,99585 —1
0,73908 —1
0,75700
0,17088
0,67367 —1
0,21762
0,75293 —1
0,12947
0,33088
0,81440 —1
0,68479 —1
0,13465
0,80383 —1
0,67778 —1
0,57387 —1
0,89736 —1
0,74478 —1
0,51647
0,64608
0,21793 —1
0,65310
0,22495 —1
0,44618 —1
0,45319—1
0,80322 —1
0,81022 —1
0,27233
0,78306
0.19695
0,43351
0,39268 —1
0,58610
0,15797 —1
0,38619 —1
0,74323 —1
0,93301 —1
2
0,84891
0,99050
0,54838
5,7147
1,4821
4,7170
1,6505
0,56615
1,3473
2,1423
0,65223
0,48393
1,3635
0,63654
0,47619
0,37486
0,78591
0,55562
3,2845
4,4268
0,16517
4,4988
0,16786
0,27937
0,28391
0,63565
0,64598
1,8722
6,0681
1,5738
2,7134
0,24699
3,8557
0,14386
0,24333
0,55364
0,85705
3
NH4C1 *- HN03
NH4C1 *-* N205
NH4C1 *•* Pt
NH4N03 *~ N
NH4NOs «- Na08
(NH4)2S04 *-. N
(NH4)2S04 — S03
(NH4)2S04 — BaS04
(NH4)2S04 — HaS04
NO ** N
NO ** NOa
NO — NOs
NO ** N,0
NO ** HN02
NO «- HNOs
NO «- NH4N03
NO ** Na03
NO <-* Na05
NOa «- N
N03 ** N
N03 ** (Ca0HleN4).HNO3
(нитрон)
HN03 ** N
HN03 ** (Ca0HleN4)-HNO3
(нитрон)
N03 ~ (NH4)2[PtCy
HNOs ** (NHJilPtCl.l
N03 ** Pt
HN03 ** Pt
KNO. «- N2O5
NaNO. «-+ N
NaN03 ** Ns05
Na03 — N
N203 *■* AgNOa
N205 — N
Na05— (C.eHleN4)-HNOi,
(нитрои)
N205 *■* (NH«)»IPtCg
N205 ** Pt
N205 ** HNOs
4
1,1780
1,0096
1,8235
0,17499
0,67470
0,21200
0,60589
1,7663
0,74223
0,46680
1,5332
2,0664
0,73340
1,5668
2,1000
2,6676
1,2666
1,7998
0,30446
0,22590
6,0542
0,22228
5,9574
3,5795
3,5222
1,5732
1,5480
0,53414
1,16479
0,63539
0,36854
4,0488
0,25936
6,9510
4,1097
1,8062
1,1668
5
0,07115
0,00415
0,26091
0,24302 —1
0,82911 —1
0,32634 —1
0,78239 — 1
0,24707
0,87055 —1
0,66913—1
0,18560
0,31521
0,86534 —1
0,19501
0,32222
0,42614
0,10264
0,25522
0,48353 —1
0,35392 — 1
0,78205
0,34690 — 1
0,77506
0,55382
0,54681
0,19678
0,18977
0,72765 —1
0,21693 —1
0,80304 —1
0,56649 —1
0,60733
0,41390 —1
0,84205
0,61381
0,25677
0,06700
AB = 22,9898 !g AB = 1,36154
5,29447 —1
3,45894 —1
Э.81190 —I
3,25806 —1
5,34912 —1
5,63730 —1
5,43721 —1
5,59480 —1
5,27360—1
5,18574—1
5,43215 —1
0,87033 —1
0,75951 —1
0,51015 —1
0,18633 —2
0,17600 —2
0,17458 —2
0,03922
0,07830
0,19700
0,28770
0,64846
0,18116
0,22342
0,43381
0,27366
0,39337
0,18776
0,15337
0,27049
0,74186
0,57479
0,32371
0,015358
0,014997
0,014948
1,0945
1,1976
Na *- BaS04
Na *■* Br
Na ** CI
Na ** I
Na «-* NaBr
Na — Na2O03
Na ** NaHC03
Na Ч-. NaCl
Na «- NaC104
Na «-» Nal
Na — NaN03
Na *-* Na20
Na *-* NaOH
Na — Na2S04
Na — NaMg(U02)3(C2H302)B-6H2Q
Na *~ NaMg(U02)3(C2H302)„-8H20
Na — NaZn(U02)3(C2H302)e-6HaO
Na2HAs03 —- Mg2As20,
Na2HAs04 *-► Mg2As207
5,0762
3,4758
1,5421
5,5200
4,4759
2,3051
3,6541
2,5421
5,3258
6,5200
3,6971
1,3480
1,7398
3,0892
65,111
66,678
66,897
0,91362
0,83500
0,70554
0,54105
0,18811
0,74194
0,65088
0,36269
0,56278
0,40520
0,72638
0,81425
0,56786
0,12969
0,24050
0,48985
1,81366
1,82399
1,82541
0,96077 —1
0,92169 —1
38
Продолжение
1
0,15990
0,91039—1
0,72232—1
0,43759
0,18805
0,73876 — 1
0,10982
0,38171
0,79991 —1
0,12222
0,28076
0,61042 — 1
0,21709
0,91535 —!
0,57979 -2
0,87079 -1
0,26038
0,93160 -1
0,32118
0,03161
0,34441
0,80513 -1
0,07232
0,78306
0,69816
0,45219
0,19695
0,42415-1
0,14869
0,75878 -1
0,21090—1
0,47879—1
0,76699—1
0,56692 —1
0,72448 — 1
0,88918—1
0,63984 —1
0,70566 —1
0,88882—1
0,01347
0,03266
0,88596—1
0,22802
0,81645—1
0,27386
1,08906
0,46920
0,10575
0,59811 —1
0,30107
0,50763
0,70297
0,16826
0,63476—1
0,23709
0,36359
0,97153—1
0,77533 —1
0,30192
0,52424 —1
0,73241 —1
0,69886 —1
0,29392
0,03354
2
1,4451
0,81356
0,52762
2,7390
1,5419
0,54798
1,2877
2,4083
0,63083
1,3250
1,9088
0,40777
1,6485
0,82290
0,038001
0,74267
1,8213
0,85427
2,0950
1,0755
2,2101
0,63846
1,1812
6,0681
4,9907
2,8326
1,5738
0,26555
1,4083
0,57382
0,16252
0,30116
0,58477
0,36891
0,53025
0,77479
0,43635
0,50766
0,77414
1,0315
1,0781
0,76905
1,6905
0,65532
1,8787
12,276
2,9458
1,2757
0,39638
2,0002
3,2183
5,0462
1,4732
0,43128
1,7262
2,3099
0,93655
0,59612
2,0041
0,33438
0,54003
0,49987
1,9675
1,0803
3
Na2B407 «— B203
Na2B407 *■+ H3B03
Na2B40, <-+ Na2B40,- 10H2O
Na2B407- 10H2O <— B203
Na2B407- 10H2O — H3B03
NaBr *■♦ AgBr
NaBr *♦ Br
Na2C03 ♦* C02
Na2C03 *■* NaHC03
Na2C03 — NaOH
NaHCOs ♦* СОг
NaCl ** AgC!
NaCl — CI
NaCl — Na2S04
NaCl — NaZn(U02)3(C2H302)9-6H20
NaC!03 *-* AgC!
NaCl03 <- NaCl
NaC104 ~- AgCl
NaCl04 — NaCl
NaF *-* CaF2
NaF <-» F
Nal *-* Agl
Nal — I
NaNO, —► N
NaNO; <-+ NH3
NaN08 — NO
NaN03 — N205
Na20 ** BaSQ,
Na20 — C02
Na20 — N20,
Na20 *- Na2B„O,-10H2O
Na20 «-* NaBr
Na20 ^- NaaCO,
Na20 — NaHC03
Na20 — NaCl
Na20 — NaOH
Na20 «- Na2S04
Na20 — Na2Si03
Na20 +-» S03
Na20 *- Si02
NaH2P04 *- Mg2P207
NaH2P04 «- №Н2РО*-2Н20
NaH2PO„ 4-. P2Os
NaNH4HP04 ** NaNH4HP04-4H20
NaNH4HP04-4H20 *- Mg2P207
NaNH4HP04-4H20 — NH3
NaNH4HP04-4H20 — РЮ5
Na2HP04 4-. Mg2P207
Na2HP04 — Na2HP04-12H20
NaaHP04 — P205
Na2HP04-12H20 *- Mg2P207
Na2HP04- 12H20 *~ P205
Na3P04 *- Mg2P207
Na3P04 — Na3P0412H20
Na3P04 — P04
Na3P04 ~ P205
Na4P20, *- Na2HP04
Na4P207 *-+ Na4P2O,-10H2O
Na4P2O,-10H2O — Mg2P207
Na2S *■* BaS04
Na2S03 *■* BaS04
Na2S03 *- Na2S03-7H20
Na2S03 *■* S02
Na2S03-7H20 — BaS04
4
0,69198
1,2292
1,8953
0,36510
0,64853
1,8249
0,77658
0,41523
1,5852
0,75474
0,52388
2,4524
0,60663
1,2152
26,315
1,3465
0,54906
1,1706
0,47732
0,92979
0,45247
1,5663
0,84663
0,16479
0,20037
0,35303
0,63539
3,7658
0,71008
1,7427
6,1533
3,3204
1,7101
2,7108
1,8859
1,2907
2,2918
1,9694
1,2918
0,96944
0,92759
1,3003
0,59155
1,5260
0,53228
0,081459
0,33947
0,78391
2,5229
0,49995
0,31072
0,19817
0,67880
2,3187
0,57930
0,43291
1,0678
1,6775
0,49897
2,9906
1,8518
2,0005
0,50827
0,92564
5
0,84010 —1
0,08962
0,27768
0,56241 — 1
0,81193—1
0,26124
0,89019 —1
0,61829 —1
0,20008
0,87779 —1
0,71923 —1
0,38959
0,78292 —1
0,08465
1,42021
0,12921
0,73962 —1
0,06841
0,67881 —1
0,96839 —1
0,65559 — 1
0,19487
0,92770 — 1
0,21693 —1
0,30183 —1
0,54781 —1
0,80305 — 1
0,57586
0,85131 — 1
0,24123
0,78911
0,52119
0,23303
0,43310
0,27552
0,11083
0,36017
0,29434
0,11119
0,98652 —
0,96735 —
0,11404
0,77199 —
0,18355
0,72614 —
0,91094 —!
0,53080 —
0,89427 —
0,40190
0,69893 —
0,49237 —
0,29703 —
0,83174 —
0,36524
0,76290 —
0,63640 —
0,02849
0,22466
0,69807 —
0,47576
0,26759
0,30114
0,70609 —
0,96644 —
39
Продолжение
1
0,59506
0,21067
0,71129—1
0,93928 —1
0,77201 —1
0,78432 —1
0,64429 —1
0,24898
0,14000
2
3,9360
1,6243
0,51439
0,86952
0,59158
0,60858
0,44085
1,7741
1,3804
3
Na2S03-7H20** S02
NaHS03 *-* S02
NaHS04 *- BaS04
NaHS04 *-* NaHS04H20
NaHS04H20 — BaS04
Na2S04 «-* BaSO,
Na2S04 *- Na2SO4-10H!!O
Na2S04 *~* SO,
Na2S04-12H20*- BaS04
4
0,25407
0,61564
1,9440
1,1501
1,6904
1,6432
2,2683
0,56365
0,72441
5
0,40495 —1
0,78933 —1
0,28870
0,06074
0,22799
0,21571
0,35570
0,75101 —1
0,85999 —1
AB = 92,906 lg А В = 1,96804
—1 | 0,69904 | Nb — Nb205
| 1,4305
0,2359
0,2250
0,2032
0,1195
0,1574
0,1774
0,1692
0,1533
0,1355
0,3438
0,4529
0,2019
0,7858
0,7098
0,4030
0,3793
0,5453
0,6283
0,2569
0,2668
0,5510
AB = 58,70 lg AB = 1,7686
Ni «- ЩС2Н302)2-4Н20
Ni «-* Ы1(СгН5Ы40)2
(днцианамидин)
Ni ** Ni(C4H,N202)2
(диметилдиоксим)
N1 *-*■ Ni(C5H5N)4(SCN)2
(пиридин)
Ni «- Ni(CeH5N202)2
циклогександиоксим
Ni -~ Ni(C,HeN02)2
(антраниловая кислота)
Ni — Ni(C„HeNO)2
(оксихннолин)
Ni ** Ni(CeH6NO)2-2H20
Ni — Ni(C10H7N2O2)2
(a,a'—фурсилдиоксим)
Ni *■» Ni(CO)4
Ni ** NiCIa
Ni *■» Ni(N03)2 - 6H20
Ni -e* NiO
Ni — Ni203
Ni *■* Ni2P20,
Ni — NiS04
NiCb *- NiCl2-6H20
Ni(N03)2 — Ni(N03)2-6H20
NiO «-* Ni(N03)2 • 6Н2О
NiO *- NiS04-7H20
NiS04 — NiS04-7H20
4,329
4,444
4,922
8,368
6,354
5,637
5,911
6,524
7,381
2,908
2,208
4,953
1,272
1,409
2,481
2,636
1,834
1,592
3,893
3,760
1,815
ЛВ= 190,2 lg^B = 2,2792
I 0,7482 I Os *- Os04
I 1,336 I
А В = 30,9738 lg А В = 1,49099
0,95955 —1
0,35323 —1
0,30535 —1
0,17243—1
0,75085 —1
0,57721 —1
0,51340 —1
0,86921 —2
0,58802 —1
0,51019—1
0,50428 —1
0,49978 —1
0,21767 —2
0,91106
0,22554
0,20203
0,14874
0,56344
0,37775
0,32614
0,073997
0,38727
0,32375
0,31936
0,31607
0,016507
P *- PH3
P *- PC13
P ** POCl3
P — PCI5
P — P203
P ~ H3P03
P «-* P04
P ~ Ag3P04
P « HPO3
P — HP04
P — H2P04
P — H3P04
P «- (NH„)3P04-12Mo03
1,0976
4,4338
4,9504
6,7231
1,7748
2,6473
3,0662
13,514
2,5822
3,0987
3,1313
3,1638
60,579
0,04044
0,64678
0,69464
0,82757
0,24915
0,42280
0,48660
1,13079
0,41199
0,48118
0,49572
0,50021
1,78232
40
Продолжение
0,01639
0,43642
0,017225
0,10232
0,34807
0,12621
0,27833
0,27871
0,069899
0,71870
0,67043
0,17369
0,73682
0,050615
0,05025
1,3381
0,85342
0,16955
0,23446
1,3921
0,58196
0,45762
0,47058
0,88738
0,74310
0,73172
0,72424
0,79755
0,63776
0,037825
0,03755
0,49995
0,19817
0,33947
0,039468
0,88059
1,2757
3,2183
1,8787
Р ■*- (NH4)3PCV12Mo03
Р ~* Р20, '
Р — Рг05-24Мо03
Р ~ Ag4P20,
Р «- Н4Р207
Р « MgNH4P(V6H20
Р « Mg2P20,
Р — P=S5
НяР02 — Hg2Cl3
НРОя *-* MgzPsO,
р2о3 ~ н3ро3
Н3РО, «-* Hg2Cl2
Н3Р03 *-* Mg2P207
Р04«- (NH4)sP04-12MoO,
Р04 *-* (NH4)3P04-12MoO;
Р04 — Р205
Р04 «■ Mg2P20,
P.O. ~ Ag3P04
Р205 *- Ag4PsO,
P206 ~ A!203
Р2Ой
A1P04
P2Os «- Cas(P04)s
P205 ** FeP04
P308 ~* HP04
P20E «• HP04
PA
РгО,
hpo4
H„POd
p2o5 *-» h;p2o7
P205 *-* Mg2P20,
P206 «-+ (NH4)2P04 • 12MoO,
Pa06 — (NH4)3PO, ■ 12Mo03
Pa05 *- Na2HP04
P205 *-* Na2HP04-!2H20
P20; <-* NaNH4HP04-4HaO
PsOs -и- P205-24Mo03
HsP04 *- MgsPaO,
Na2HP04 *- 'MgiPsO,
NaaHPO,- 12HgO +-» Mg«P207
NaNH4hfP04-4HaO *-» Mg2P20-
Эмпирический
2,2914
58,056
9,7731
2,8730
7,9233
3,5928
3,5880
1,4306
1,3914
1,4916
5,7575
1,3572
19.757
0,36010
1,76385
0,99003
0,45834
0,89891
0,55544
0,55485
0,15552
0,14345
0,17365
0,76024
0,13264
1,29572
Эмпирический
0,74730
1,1718
5,8978
4,2652
0,71832
1,7183
2,1852
2,1250
1,3523
1,3523
1,3736
1,3808
1,2538
1,5680
'2(5,438
0,87349 —1
0,06886
0,77069
0,62994
0,80632 —1
0,23510
0,33949
0,32736
0,05188
0,13108
0,13786
0,14013
0,09723
0,19535
1,42223
Эмпирический
2,0002
5,0462
2,9458
25,337
1,1356
0,78391
0,31072
0,53228
0,30107
0,70297
0,46920
1,40376
0,05523
0,89427 —1
0,49237 — 1
0,72614—1
AB= 207.19 lg /4 6= 2,31637
0,73735—1
0,80658 —1
0,72482 —1
0,63562—1
0,63562—i
0,43521 —1
0,51036—1
0,88954—1
0,87217 —1
0,80693—1
0,75155 —1
0,96770—1
0,93763 —1
0.54620
0,64058
0.53066
0.43214
0,43214
0,27240
0,32386
0,77541
0,74502
0,64110
0,56435
0,92831
0,86622
Pb — Pb(C2H302)2-3H20
(ацетат)
Pb «- Pb(C2H6)4
(тетраэтил)
Pb -* Pb(OH)(C,H-NS2)
(меркг птотиазол)
Pb — Pb(C,H6N02)a
(антраниловая кислота)
Pb «-> Pb(C,H6N02)2
(салицилальдоксим)
Pb «-» Pb(Ci„H7NA,)2'l.5H20
(пикролоновая кислота)
Pb «-* Pb(CjaHi„NOS)2
(тионалид)
Pb — Pb0O3
Pb «-* PbCb
Pb «-. PbCrQ,
Pb -~ PbMoO.
Pb «-. PbO
Pb «-* РЬОг
1.8308
1,5611
1 8845
2,3141
2,3141
3,6710
3,0879
1,2896
1,3422
1,5598
1,7719
1,0772
1,1544
0,26264
0,19343
0,27510
0,36438
0,36438
0,56478
0,48967
0,11045
0,12782
0,19307
0.24Ы4
0,03230
0,06236
41
Продолжение
1
0,95744 —1
0,93762 —1
0,83457 —1
0,92184 —1
0,83924 —1
0,82859 —1
0,96993 —1
0,98974 —1
0,96983 —1
0,86687 —1
0,89705 —1
0,11371
2
0,90665
0,86600
0,68223
0,83529
0,69061
0,67388
0,93311
0,97666
0,93287
0,73599
0,78895
1.2993
3
Pb — Pb3Q,
Pb «- PbS
рь *-* Pbsa
PbO — PbCD3
PbO — PbCr04
PbO — Pb(N03)2
PbO •*- PbOa
PbO *~ Pbs04
PbO — PbS
PbO ♦» PbS04
PbS *~ PbS04
PbS04 *~ BaS04
4
1,1030
1,1547
1,4636
1,1972
1,4480
1,4839
1,0717
1,0239
1,0720
1,3587
1,2675
0,76966
5
0,04258
0,06247
0,16542
0,07816
0,16077
0,17140
0,03007
0,01026
0,03019
0,13312
0,10295
0,88630 —1
0,3161
0,2663
0,2738
0,2810
0,2696
0,2361
0,2059
0,6717
0,6001
0,3260
0,2678
0,2996
0,2954
0,8693
0,7682
0,5254
0,8312
0,8491
AB = 106,4 lg AB = 2,0269
Pd •«■ Pd(C4H,N202)2
(диметилдиоксим)
Pd *~ Pd(C5H5N02)2Cl2
(фурфуральдоксим)
Pd «- Pd(CeH»N202)2
(циклогександиондиоксим)
Pd «-* Pd(C,H„N02)
(салицилальдоксим)
Pd ** Pd(C»H6NO)2
(оксихинолин)
Pd ** Pd^oHeNOa)^
(а-нитрозо-В-нафтол)
Pd «- Pd(CwHeN203)3
(беизоилметилгл иоксим)
Pd — Pd(CN)2
Pd — PdCla
Pd «- K2[PdCl4]
Pd — K2[PdCl6]
Pd *~ (NH4)2[PdCle]
Pd ♦* Pdh
Pd — PdO
Pd — PdS
Pd — PdS04
PdCb — PdCl2-2H20
PdS04 ** PdS04-2HaO
3,162
3,756
3,6530
3,559
3,710
4,236
4,875
1,489
1,666
3,068
3,734
3,338
3,385
1,150
1,302
1,903
1,203
1,178
0,57907
0,47838
0,37668
0,40141
0,43950
0,75260
0,93839
AB = 195,09 lg AB = 2,29024
Pt — PtCl4
Pt ■*-» PtCl
Pt — H2[PtCl6]-2H20
Pt «- K2[PtCl6]
Pt — (NH4)2[PtCl6j
Pt ** PtS2
Ki[PtCle] ~~ H2[PtCle]-6H20
1,7269
2,0904
2,6548
2,4912
2,2753
1,3287
1,0657
AB= 85,47 lgi4B= 1,9318
0,8693 —1
0,8493 —1
0,6648 —1
0,9612 —1
0,4704 —1
0,8063 —1
0,9262 —1
0,8882 —I
0,8452 —1
0,7402
0,7068
0,4622
0,9144
0,2954
0,6402
0,8437
0,7730
0,7002
Rb *~ Rb2C03
Rb *- RbCl
Rb *~ RbCIO,
Rb ** RbaO
Rb — Rba[PtCle]
Rb *~ Rb2S04
RbCl — AgCl
Rb20 — RbCl
Rb20 ** Rb»S04
1,351
1,415
2,162
1,094
3,386
1,562
1,185
1,294
1,428
0,1307
0,1507
0,3352
0.0389
0.5296
0,1937
0,0738
0,1118
0,1548
42
Продолже ние
0,33038
0,31581
0,27313
0,29384
0,85335
0,88582
0,79505
0,74422
0,38440
0,64363
0,44393
0,39482
0,42435
0,36700
АВ = 186,207 1gi4B= 2,27000
Re** (C2oHl6N4)-HRe04
(нитрон)
Re** (CeH5)4P-Re04
(тетрафенилфосфоний)
Re** (C26H31N402)Re04
(диантипирилпропилметан)
Re ** (CeH6)4As-Re04
(тетрафениларсоний)
Re «-► ReOa
Re *-* RezOg
Re ** Re03
Re — Re04
Re ** Re207
Re ** KRe04
Re04** (Ct^ieN4)-HRe04
(нитрон)
Re04** (C6H5)4As-ReO,
Re04 ** (QH^PReO,
ReO, ** (C2sH31N402)-Re04
3,0269
3,1665
3,6613
3,4032
1,1719
1,1289
1,2578
1,3652
1,6014
1,5493
2,2526
2,5328
2,3569
2,6628
0,48100
0,50058
0,56363
0,53189
0,06889
0,05265
0,09961
0,13519
0,41521
0,19013
0,35268
0,40360
0,37228
0,43534
0,76280
0,81089
AB= 102,905 lgAB= 2,01244
Rh ** Rh02
Rh ** Rh203
1,3110
1,2332
0,11760
0,09103
AB = 32,064 ]%AB= 1,50602
D, 13793 —1
0,05527 —1
3,34627 —1
0,60543 —1
3,97352 —1
0,59179 —1
0,51444 —1
0,74198 —1
0,49331 —1
0,67660—1
0,69941 —1
0,60259 —1
0,75734 —1
0,52346 —1
0,39591 —1
0,67903 —1
0,16203
0,27976
0,61863 —1
0,16441 —1
0,37275—1
0,62907 —1
0,54612 —1
0,62347—1
0,54083 —1
0,43851 —1
0,90318 —1
0,53532 —1
0,76944 —1
0,91186—1
0,13738
0,11357
0,22196
0,40312
0,94085
0,39065
0,32692
0,55205
0,31139
0,47490
0,50051
0,40049
0,57193
0,33378
0,24885
0,47757
1,4522
1,9044
0,41555
0,14602
0,23591
0,42567
0,35166
0.42021
0,34740
0,27448
0,80017
0,34302
0,58809
0,81631
S ** BaS04
S <- (Cl2Hl2N2)-H2S04
(бензидин)
S ** CdS
S ** CuO
S *-» H2S
s ** h2so3
S 4- H2S04
S — SCN
s *-» scu
S *-» S2C12
s*~ so2
s *-» so,
s -~ s263
s — so»
SCN ** BaS04
SCN ** CuSCN
SCh *•* CI
S2C12 ** CI
H2S «-► As2S3
H2S ** BaS04
H3S — CdS
H2S *-» SO,
H2S03 •<— BaS04
H2S04 *■» BaS04
H2S04 *■» (Ci2Hi2N2)-H2S04
(бензидии)
SCb *-* BaS04
so2 *-* so3
S03 ** BaS04
SO, — CaS04
S03 *-* H2S04
7,2792
8,8049
4,5054
2,4807
1,0629
2,5598
3,0588
1,8114
3,2114
2,1057
1,9980
2,4969
1,7485
2,9959
4,0185
2,0939
0,68861
5,2510
2,4064
6,8486
4,2388
2,3492
2,8436
2,3797
2,8785
3,6433
1,2497
2,9152
1,7004
1,2250
0,86208
0,94473
0,65373
0,39458
0,02649
0,40821
0,48555
0,25802
0,50670
0,32340
0,30060
0,39740
0,24267
0,47653
0,60407
0,32096
0,83798 —1
0,72024
0,38137
0,83560
0,62724
0,37092
0,45387
0,37652
0,45917
0,56150
0,09681
0,46467
0,23055
0,08814
43
Продолжение
1
0,95370 —1
0,78239
0,92087 —1
0,38057 —1
0,61446 —1
2
0,89887
0,60589
0,83344
0,24020
0,41158
з
SOs «— H2S2O,
503 «- (NH4)2S04
so3 ~* so4
S2O3 +-*■ BaS04
504 «— BaS04
4
1,1125
1,6505
1,1998
4,1632
2,4297
Б
0,04630
0,21762
0,07911
0,61943
0,38556
AB = 121,75 lg AB = 2,08547
0,21968 Sb *-» Sb(CeH6NO)3
(оксихинолин)
0,21276 Sb ** SbO(CeH6NO)(CeH7NO)2
0,15799 Sb ** Sb(Ci2H10NOS)3
(тионалид)
0,46319 Sb «- Sb(C6H504)
(пирогаллол)
0,53373 Sb *-r SbCl,
0,70294 Sb -* SbOCl
0,40716 Sb — SbCl6
0,36460 Sb *-* K(SbO)C4H4O6-0,5H2O
(тартрат)
0,83533 Sb <-» Sb203
0,79187 Sb «— Sb204
0,75270 Sb ** Sb205
0,71683 Sb «-*• Sb2S3
0,60300 Sb ** Sb2S5
0,94797 Sb2Os — Sb204
0,90108 Sb203 — Sb205
0,85814 Sb2Os ** SbiiSj
0,72186 Sb203 ** Sb2S5
0,90524 Sb204 «— Sb2S3
0,76148 Sb204 «-* Sb2S5
1,0520 Sb205 —•> Sb204
0,95234 Sb206 ** Sb2S3
0,80110 Sb2Os ** Sb2S5
4,5520
4,7000
6,3294
2,1589
1,8736
1,4226
2,4560
2,7428
1,1971
1,2628
1,3285
1,3950
1,6584
1,0549
1,1098
1,1653
1,3853
1,1047
1,3132
0,95054
1,0500
1,2483
0,65196
AB =
Sc ■*-»■ Sc203
44,956 lg,4B = 1,65279
1,5338
0,7116
0,6219
0,6122
0,4566
0,5447
0,2817
А В = 78,96 lg AB = 1,8974
Se *->■ SeOa
Se -* Se03
Se ** H2Se03
Se *->■ Na2Se03
Se ♦* H2Se04
Se ~~ BaSeO,
1,405
1,608
1,633
2,190
1,836
3,5499
А В = 28,086 lg А В = 1,44849
0,84538 —1
0,66973 —1
0,52353
0,57112—1
0,85873 —1
0,78286 —1
0,70627 —1
0,99388 —1
0,66749
0,78899 —1
0,71238 —1
0,76140 —1
0,70045
0,46744
3,3383
0,37249
0,72232
0,60654
0,50847
0,98601
4,6504
0,61515
0,51568
0,57730
Si «— SiC
Si ** SiCfe
SiC — С
SiF4 —► BaSiF6
SiF4 *- H2SiF6
SiFe *•► CaF2
SiFe ** BaSiF6
SiFe *-► H2SiF6
BaSiF6 «— SiOss
H2SiF- «— CaF2
H2SiFe ** BaSiF6
Si02 *- SiF4
1,4277
2,1393
0,29955
2,6847
1,3844
1,6487
1,9667
1,0142
0,21503
1,6256
1,9392
1,7322
0,15464
0,33027
0,47647 —1
0,42889
0,14126
0,21714
0,29373
0,00613
0,33250 —1
0,21101
0,28762
0,23860
44
Продолжение
1
0,33250 —1
0,43580—1
0,89747 —1
0,88611 —1
0,81458 —1
0,85405 —1
2
0,21503
0,27277
0,78972
0,76933
0,65250
0,71458
3
Si02 *-* BaSiF6
SiOa *-» K2SiFc
SiO= *- SiOs
Si02 «— HaSiO.,
Si02 — Si04
Si02 «— SiaO,
4
4,6504
3,6661
1,2663
1,2998
1,5326
1,3994
5
0,66749
0,56420
0,10254
0,11391
0,18543
0,14594
0,52604
0,45562
0,32297
0,88121
0,78764
0,44502
0,78733
0,64922
0,84031
0,89382
Sn —
Sn **
Sn «-»
Sn «-»
Sn *-*
Sn —
Sn —
Sn *-»
SnCb
ЛВ = 118,69 ]gAB
SnC!2-2H20
SnCl4
(NH4)2[SnC!e]
SnO
Sn02
Naa[Sn(OH)„]
SnS
SnSs
«- SnCb-2H20
SnO «— Sn02
2,07441
1,9010
2,1948
3,0962
1,1348
1,2696
2,2471
1,2701
1,5403
1,1900
1,1188
0,27898
0,34139
0,49083
0,05492
0,10366
0,35162
0,10384
0,18760
0,07555
0,04875
AB= 87,62 lg AB= 1,9426
-1
0,2465
0,5935
0,4524
0,5527
0,4303
0,4140
0,8456
0,3297
0,7321
0,5698
0,4770
0,4386
3,354
0,8037
0,5946
1,434
0,7460
0,7019
0,6536
0,4896
0,3899
0,5641
2,294
0,7870
1,349
Sr «-. SrBr2-6H20
Sr *-. SrCOs
Sr «-* Sr(C2b4) ■ НгО
Sr «-► SrCl2
Sr —► SrCr04
Sr — Sr(NO,)2
Sr ** SrO
Sr — Sr(OH)2-8H20
Sr *-. SrS
Sr *~ Sr(HS)2
Sr — SrS04
Sr •*-» SrS203
SrCO, <-* C02
SrCO'3 — SrS04
SrCla «-> SrCla-6HaO
Sr(NO,)2 *-» SrCO,
Sr(N03)2 — Sr(N03)2 •
SrO <-* srco,
SrO *-» SrCb
SrO *-~ Sr(NO,)s
SrO «- Sr(OHb-8H20
SrO — SrS04
SrS04 — SO,
SrS04 — BaS04
SrS04 -~ CaSO,
4H20
4,058
1,685
2,210
1,809
2,324
2,415
1,183
3,033
1,366
1,755
2,096
2,220
0,2981
1,244
1,682
0,6976
1,3405
1,425
1,5230
2,042
2,565
1,773
0,4359
1,271
0,742
0,6083
0,2266
0,3444
0,2575
0,3662
0,3830
0,0728
0,4919
0,1354
0,2443
0,3214
0,3579
0,4744 —I
0,0949
0,2258
0,8436 —1
0,1273
0,1537
0,1847
0,3101
0,4091
0,2486
0,6394 —1
0,1040
0,8699 —1
0,50514
0,81897
1,6213
AB = 180.948 lg А В = 2,25755
Та *- ТаС15
Та •*-» Taa05
ТаС15 —■ Та205
1,9796
1,2210
0,61680
0,79950
0,72665
0,65906
А В =-- 127,00 ]gAB= 2,10585
Те *-* Те02
Те -*— Те03
Те <-* НаТеО,
1,2508
1,3762
1,5173
0,09719
0,13868
0,18107
45
Продолжение
0,17810
0,44954
0,62067
0,48336
0,87881
0,77329
0,86948
0,68950
АВ = 232,038 lg А В = 2,36556
Th ** Th(C10H,N4O6)4-H2O
(пикролоновая кислота)
Th *- Th(C204)2-6H20
Th — ThCl4
Th — Th(N03)4
Th ** ThOs
Th — Th(OH)4
Th(N03)4 «- Th(N03)4-4H20
Th(NQ3)4 — Th(N03)4-12H30
5,6147
2,2245
1,6112
2,0689
1,1379
1,2932
1,1501
1,4503
0,1360
0,3105
0,2525
0,1995
0,2994
0,5995
0,9302
0,4212
0,2268
0,55144
0,48584
0,87198
0,85218
0,35346
0,77895
0,61693
0,76724
0,96233
0,89491
0,80971
0,92994
Ti
ДВ = 47,90 \gAB
+-» TiO(C9H„NO)2
(оксихинолин)
Ti
Ti
Ti
Ti
Ti
«-► TiCl3
«- TiCl4
— K2[TiF„]
** TiO[S04]
•^ Ti02
K2[TiF„] ** Kf[TlFJ-H,0
Ti02 ** TiCl4
TiOa ** TiO(C9H„NO)2
(оксихинолин)
TI
AB= 204,37 IgAB
** Tl(C.H4NSa)
(меркаптобензтиазол)
TI
«- (QgHioNOS)
(тионалид)
TI
TI
TI
11
11
TI
TI
TI
TI
— TlaCOs
** T1C1
♦* Co(NH3)JTlCl6]
«- TUCiO,
** Til
** T1N03
«- TlaO
«— ti2o3
«— TlaSQ,
T120 *-» T1203
1,6803
2,31042
7,353
3,220
3,960
5,012
3,339
1,668
1,075
2,374
4,408
1,8134
2,0583
1,1468
1,1735
2,8292
1,2838
1,6209
1,3034
1,0391
1,1174
1,2350
1,0753
А В = 238,03 lg А В = 2,37663
0,83007 —1
0,94522 —1
0,74911 —1
0,52937 —1
0,67582 —1
0,82397 —1
0,92023 —1
0,90824 —1
0,87554 —1
0,92840 —1
0,98318 —1
0,96145—1
0,89472 —1
0,67618
0,88149
0,56119
0,33835
0,47404
0,66675
0,83219
0,80954
0,75084
0,84800
0,96200
0,91505
0,78474
U**UF6
U** UOa
U ** U02(C2H302)2-2H20
(ацетат)
U ** UOs(CeHeNO)a(CeHTNO)
(оксихииолин)
U** U02(N03)2-6HaO
U — (U02)2PaO,
и — ио3
и *-* и2о,
U *-► Na2UaO,
и *~ и3о3
ио2 *-► и3о8
UOa(C2H302)2 ♦* иОгССгНзО^^гНЮ
(ацетат)
U02(N03)2 *■* U02(N03)2-6H20
1,4789
1,1344
1,7819
2,9555
2,1095
1,4998
1,2017
1,2353
1,3318
1,1792
1,0395
1,0928
1,2743
0,16994
0,05477
0,25089
0,47063
0,32418
7,17603
0,07979
0,09178
0,12444
0,07158
0,01683
0,03854
0,10527
Продолжение
1
2
3
4
Б
V
А В = 50,942 lg /4 В = 1,70708
0,51035 —1
0,42208—1
0,78831 —1
0,71170—1
0,39150 —1
0,63897 —1
0,62097 —1
0,83236—1
0,14687 —1
0,06506—1
0,74832 —1
0,67794 —1
0,20997—1
0,71128—1
0,58947 —1
0,91597 —1
W
0,70681 —1
0,56190 —1
0,89926 —1
0,09408
0,87028 —1
0,79637—1
0,87005 —1
0,10288
0,94977 —1
0,32385
0,26429
0,61420
0,51488
0,24632
0,43548
0,41780
0,67976
0,14024
0,11616
0,56017
0,47636
0,16217
0,51437
0,38857
0,82407
0,50911
0,36467
0,79297
1,2419
0,74178
0,62570
0,74139
1,2673
0,89077
V ~ VC13
V — VC14
V ч- VOa
v — vo3
V ~ AgV03
V <-* NH4V03
V «-» NaV03
V *-* v203
V ** V203(C9HeNO)4
(оксихинолин)
V ** Ag3V04
V ** V2Os
V ** V207
V ** Pb2V207
V ♦* V2S3
V ** V2S5
v2os ** vao5
А В = 183,85 lg А В = 2,26447
W ** WC16
W «-* WOs(C9H6NO)2
(оксихинолин)
w *-+ wo3
CaW04 — W03
W *- W04
W *-* Na2W04
W ** WS2
Na2W04 «- WOs
Na2W04 ** NaaW04-2H20
3,0878
3,7838
1,6281
1,9422
4,0597
2,2963
2,3935
1,4711
7,1306
8,6088
1,7852
2,0993
6,1664
1,9441
2,5736
1,2135
1,9642
2,7422
1,2611
0,80523
1,3481
1,5982
1,3488
0,78906
1,1226
0,48965
0,57793
0,21168
0,28829
0,60850
0,36103
0,37903
0,16764
0,85313
0,93494
0,25169
0,32207
0,79003
0,28872
0,41054
0,08404
0,29319
0,43810
0,10075
0,90592 — 1
0,12972
0,20363
0,12995
0,89711 — 1
0,05022
Y
AB = 88,905 lg AB = 1,94893
0,89622—1 I 0,78744 | Y «-* Y203 | 1,2699 | 0,10377
Zn
AB= 65,37 lg AB= 1,8154
0,7172 —1
0,4740—1
0,4739 —1
0,2842 —1
0,2869—1
0,2668 —1
0,1842—1
0,6809 —1
0,1179—1
0,5380 —1
0,5640 —1
0,9049 —1
0,8808 —1
0,8181 —1
0,6326 —1
0,8267 —1
0,6074 —1
0,5214
0,2978
0,2978
0,1924
0,1936
0,1848
0,1528
0,4797
0,1312
0,3452
0,3665
0,8034
0,7599
0,6578
0,4291
0,6709
0,4049
Zn *-* ZnCO,
Zn +-*■ Zn(C2H302)a
(ацетат)
Zn «-» (C2H.OB)2 • 2H20
Zn — Zn(C5H5N)2(SCN)2
(пиридин)
Zn — Zn(C,H„N02h
(антраниловая кислота)
Zn *- Zn(C,H6NO)2
(оксихинолин)
Zn <-~ Zn(C10H6NO8)2-H2O
(хинальдиновая кислота)
Zn «-► ZnCl2
Zn — ZnHg(SCN)4
Zn «-» Zn(NO,,)2
Zn — ZnNH4P04
Zn *- ZnO
Zn •<— Zn3P„
Zn *-* Zn(OH)2
Zn «— Zn2P20,
Zn *-* ZnS
Zn *-* ZnS04
1,918
3,358
3,359
5,197
5,165
5,410
6,543
2,085
7,623
2,897
2,729
1,245
1,316
1,520
2,330
1,491
2,470
1,2828
0,5260
0,5262
0,7158
0,7131
0,7332
0,8158
0,3190
0,8821
0,4620
0,4360
0,0951
0,1192
0,1819
0,3674
0,1734
0,3926
47
Продолжение
1
0,6771 —1
0,9214 —1
0,2240
0,8039 —1
0,8122 —1
0,6591 —1
0,7276 —1
0,9218—1
0,6206 —1
0,8399 —1
0,7493 —1
2
0,4754
0,8345
1,6758
0,6366
0,6490
0,4562
0,5341
0,8352
0,4174
0,6916
0,5614
3
ZnCl2 *- AgCl
ZnCl2 «- ZnCl2-l,5H20
ZnCls ** ZnO
Zn(N03)2 — Zn(N03)2-6H20
ZnO «— ZnC03
ZnO *-» ZnNH4P04
ZnO «— Zn2P20,
ZnO «— ZnS
ZnS «— BaS04
ZnS04 *-* BaS04
ZnS04 •<— ZnS04-7H20
4
2,103
0,198
0,5971
1,571
1,5409
2,192
1,872
1,1974
2,396
1,446
1,781
5
0,3229
0,0786
0,7760 —1
0,1961
0,1878
0,3409
0,2724
0,0782
0,3794
0,1601
0,2507
Zr
AB= 91,22 \gAB= 1,9601
0,0013 —1
0,1354 —1
0,4519 —1
0,5077 —1
0,3273 —1
0,8694 —1
0,5366 —1
0,6969 —1
0,8977 —1
Q.6383 —1
0,6672 —1
0,1319—1
0,1003
0,1366
0,2831
0,32187
0,2125
0,74030
0,3440
0,4976
0,7902
0,4348
0,4647
0,1355
Zr — Zr(C8HeO,)4
(миндальная кислота)
Zr — Zr(C9H„NO)4
(оксихинолин)
Zr «- ZrOCl2-8H20
Zr «-* K2[ZrF„]
Zr *- Zr(N03)4-5H20
Zr — Zr02
Zr «— ZrPaO,
Zr «- ZrSi04
Zr(N03)4 ** Zr(N03)4-5H20
гЮ2 — K2[ZrF0]
Zr02 •<— ZrP2Oj
ZrQ2 — Zr(C8He03)4
9,970
7,321
3,533
3,107
4,706
1,351
2,907
2,009
1,266
2,300
2,152
7,381
0,9987
0,8646
0,5481
0,4923
0,6727
0,1306
0,4634
0,3031
0,1023
0,3617
0,3328
0,8681
5. ЭКВИВАЛЕНТЫ
В ТИТРИМЕТРИЧЕСКИХ МЕТОДАХ АНАЛИЗА
Титрование
Вещество
ВаС03
Ва(ОН)2
сог
СОз
CaCOs
СаО
Са(ОН)2
К2С03 (метиловый
оранжевый)
КНСОз
КОН
Li2C08 (метиловый
оранжевый)
MgC03
MgO
N
кислотами
Количество, МГ
9,8675
8,5677
2,2005
3,0005
5,0045
2,8040
3,7047
6,9107
10,012
5,6109
3,6944
4,2161
2,0156
1,4007
1 мл 0,1 н.
lg
0,99421
0,93287
0,34252
0,47719
0,69936
0,44778
0,56875
0,83952
1,00051
0,74903
0,56754
0,62491
0,30440
0,14634
НО (HNOj, H2S04) соответствует
Вещество
NH,
NH4
NH4C1
NH4NOs
NH4OH
(NH4)2S04
Na2B40,- 10H2O
Na2C03 (метиловый
оранжевый)
№2С03-2Н20
(метиловый оранжевый)
Na2C03- 10НаО
(метиловый оранжевый)
NaHCOa
NasO
NaOH
Количество, мг
1,7031
1,8039
5,3492
8,0044
3,5046
6,6069
19,069
5,2995
7,1010
14,307
8,4007
3,0991
3,9997
lg
0,23123
0,25621
0,72829
0,90333
0,54464
0,82000
1,28032
0,72423
0,85132
1,15555
0,92432
0,49123
0,60203
48
Титрование щелочами
1 мл 0,1-н. NaOH (КОН)
соответствует
Вещество
А1
А1203
В
в2о,
н3во3
НВг
НСООН
СНзССЮН
(СООН)2
(СООН)2-2Н20
С4Н6Ов (винная
кислота)
СвН6СООН
а
НС1
HF
HI
ню3
ню,
HN03
NaHS04
Р-(по фосформолиб-
дату,
эмпирический)
Р04
(фенолфталеин)
Р04 (метилоранж)
Р20Б
(фенолфталеин)
Р205 (метиловый
оранжевый)
Н3Р04
(фенолфталеин)
Н3Р04
(метиловый оранжевый)
so3
S04
s2o8
H2S03
(метиловый оранжевый)
h2so4
H2SiFe (no Саль-
веллу)
H2SiFe (по Тред-
бому и Хинриксе-
ну)
SnCl4 (метиловый
оранжевый)
Количество, мг
0,89938
1,6994
1,0811
3,4810
6,1833
8,0917
4,6026
6,0053
4,5018
6,3033
7,5044
12,213
3,5453
3,6461
2,0006
12,791
17,591
19,191
6,3013
12,006
3,077
4,7486
9,4971
3,5486
7,0972
4,8998
9,7995
4,0031
4,8031
9,6062
4,1039
4,9039
2,4015
7,2046
6,5126
lg
0,95394 —1
0,23028
0,90902
0,54170
0,79122
0,90804
0,66300
0,77853
0,65339
0,79957
0,87532
1,08681
0,54966
0,56183
0,30117
1,10691
1,24530
1,28309
0,79943
1,07939
0,48813
0,67656
0,97760
0,55006
0,85109
0,69018
0,99121
0,60240
0,68152
0,98255
0,61320
0,69054
0,85761
0,38048
0,81375
4 А. И. Лазарев и др.
Титрование щелочью
металлов с применением
этнлендиаминтетрауксусиой
кислоты [ЭДТА]
1 мл 0,1 н. NaOH
соответствует
Металл
Cd
Со
Си
Hg
Мп
№
РЬ
Zn
Количество, мг
5,6200
2,9467
3,1770
10,030
2,7469
2,935
10,360
3,2685
lg
0,74974
0,46933
0,50202
1,00128
0,43885
0,46761
1,01534
0,51435
Титрование щелочью
металлов с применением
нитрнлотриуксусной
кислоты (НТА)
1 мл 0,1 н. NaOH 0,1 Мили 0.05М
соответствует мг вещества.
Металл
Cd
Со
Сц
Hg
Мп
№
РЬ
Zn
чество. мг
11,240
5,8933
6,354
20,059
5,4938
5,870
20,719
6,537
'■g
1,05077
0,77036
0,80305
1,30231
0,73987
0,76864
1,31637
0,81538
Титрование комплексоном III
1 мл раствора комплексона III
соответствует мг вещества
Вещество
А1
Ва
Bi
CN
(с
раствором
никеля)
Са
Cd
Се
Со
Си
Fe (III)
1 М
раствора
2,6982
13,734
20,898
10,407
4,008
11,240
14,012
5,8933
6,354
5,5847
lg
0,43106
1,13780
1,32011
1,01733
0,60293
1,05077
1,14650
0,77036
0,80305
0,74700
0,05 М
раствора
1,3491
6,8670
10,449
5,2036
2,0040
5,6200
7,0060
2,9467
3,1770
2,7924
lg
0,13004
0,83677
1,01908
0,71630
0,30190
0,74974
0,84547
0,46933
0,50202
0,44597
49
Продолжение
Продолжение
1 М
раствора
О,ОБ М
раствора
lg
Вещество
6,972
20,059
11,482
19,22
7,8204
13,891
2,4312
5,4938
2,2990
5,870
3,0974
9,4971
7,0972
20,719
3,2064
9,6062
8,762
23,204
4,790
20,437
6,537
9,122
0,84336
1,30231
1,06002
1,28375
0,89321
1,14273
0,38582
0,73987
0,36154
0,76864
0,49099
0,97760
0,85109
1,31637
0,50602
0,98255
0,94260
1,36556
0,68034
1,31042
0,81538
0,96009
3,4860
10,030
5,7410
9,610
3,9102
6,9455
1,2156
2,7469
1,1495
2,9350
1,5487
4,7486
3,5486
10,360
1,6032
4,8031
4,3810
11,602
2,3950
10,219
3,2685
4,5610
Аргентометрия
Вещество
Количество, мг
1 МЛ 0,1 н. AgN03
соответствует
0,54233
1,00128
0,75899
0,98272
0,59220
0,84170
0,08479
0,43885
0,06051
0,46761
0,18996
0,67656
0,55006
1,01534
0,20498
0,68152
0,64157
1,06453
0,37931
1,00939
0,51435
0,65906
lg
ВаС12
ВаС12-2Н20
Вг
Вг0а
НВг
СаС1,
СаС12-6Н20
10,412
12,214
7,9909
2,1379
8,0917
5,5493
10,954
1,01755
1,08685
0,90260
0,32875
0,90804
0,74423
1,03957
CN (по Мору)
CN (по Либиху)
HCN (по Мору)
HCN (по Либиху)
С1
НС1
I
HI
КВг
KCN (по Мору)
KCN (по Либиху)
КС1
KI
KSCN
ЫС1
MgCl3
NH4Br
NH4C1
NH4I
NH4SCN
NaBr
NaCN (no Mopy)
NaCN (no Либиху)
NaCl
Nal
NaSCN
SCN
Количество, мг
lg
2,6018
5,2036
2,7026
5,4052
3,5453
3,6461
12,690
12,791
11,901
6,5120
13,024
7,4555
16,601
9,7184
4,2392
4,7609
9,7948
5,3492
14,494
7,6120
10,290
4,9008
9,8015
5,8443
14,990
8,1072
5,8082
0,41527
0,71630
0,43178
0,73281
0,54966
0,56183
1,10347
1,10691
1,07559
0,81371
1,11474
0,87248
1,22013
0,98760
0,62738
0,67769
0,99099
0,72829
1,16119
0,88150
1,01246
0,69026
0,99129
0,76673
1,17580
0,90887
0,76404
1 мл 0,1 н. NH4SCN соответствует
Ag
AgN03
Cu
Hg
HgO
10,787
16,987
6,354
10,030
10,830
1,03290
1,23012
0,80305
1,00130
1,03463
1 мл 0,1 h, NaCl соответствует
Ag
AgN03
10,787
16,987
1,03290
1,23012
Иодометрия
1 мл 0,1 н. раствора йода или раствора
Na3SaOs соответствует
Вещество
As (As3* -* As5+)
AsOs
As203
AsO„
As205
Br
BrOs
CO (SCO + I205 -*
-* 5C02 + Is)
CI
HCIO (СЮ- -*СГ)
Cr (Cr20?" -»-2Cr3+)
Cr203
Количество, мг
3,7461
6,1460
4,9460
6,9460
5,7460
7,9909
2,1318
7.0027
3,5453
2,6230
1,7332
2,5332
lg
0,57358
0,78859
0,69425
0,84167
0,75937
0,90260
0,32872
0,84626
0,54967
0,41880
0,23885
0,40367
50
Продолжение
Продолжение
Вещество
Сг207
Си (Си2+ -* Си+)
CuS04
CuSCV 5Н„0
Fe (Fe'2+ -> Fe3+)
Fc(CN)6
FeCl3
Fe.,0,
FeS64
FeS04-7H20
H20.,
Hg "
HgCl2
HgClNH2
HgO
i
HI
Юз
НЮЗ
io4'
ню4
KBrO,
kcio3
К2СЮ4
KXr20,
khso,
MnO„
NsH;.H2S04(NaH4
(СЮ-
■СГ)
■ S°)
NaClO
N'aC103
.Ma„Cr„07
N'aJHAsO,
MaHS (MS
N!a4S
NaHS03
Na„SOs
\Ta2S,03
\a2S.203-5H.>0
SIS-' -S°f
H„S (S-~ -+ S°)
SO, (SOf -* SOf)
so;i (SOf -son
h2so3
S,Os (S.,Or ->• 2SOf)
Sb (Sb3+ -*Sb5M
Sb„03
SbbKC4H40„-1/2 H.,0
Sn (Sir5" -> Sn4+)
SnO
Количество. МГ
3,5998
6,354
15,960
24,968
5,5847
21,195
16,221
7,9846
15,191
27,802
1,7007
10,030
13,575
12,604
10,830
12,690
12,791
2,9150
2,9318
2,3863
2,3989
2,7835
2,0426
6,4733
4,9032
6,0086
4,3469
3,2531
3,7221
1,7740
4,3661
8,4954
'.',8031
3,9022
5,2030
6,3021
15,811
24,818
1,6032
!,7040
3,2032
4,0031
4,1039
19,212
6,0875
7,2875
16.697
5,9345
6,7345
0,55628
0,80305
1,20303
1,39739
0,74700
1,32624
1,21008
0,90225
1,18159
1,44407
0,23063
1,00130
1,13273
1,10051
1,03463
1,10346
1,10690
0,46464
0,46713
0,37772
0,38001
0,44459
0,31019
0,81113
0,69048
0,77877
0,63818
0,51229
0,57079
0,24895
0,64009
0,92918
0,44764
0,59131
0,71625
0,79949
1,19896
1,39477
0,20497
0,23147
0,50559
0,60240
0,61320
1,28357
0,78444
0,86258
1,22264
0,77339
0,82831
Иодометрическое титрование
металлов г применением
нитрилотриуксусной кислоты
1 мл 0,1 н. раствора
NajSjOj соответствует
Металл
Количестро,
IR
Металл
РЬ
Zn
Количество,
мг
20,719
6,537
ig
1,31637
0,81538
Броматометрия
1 мл 0,1 н. раствора
КВг03 соответствует
Вещество
As
As03
As20„
S
H„S
Sb
Sn
Tl
Количество.
мг
3,7461
6,1460
4,9460
0,40083
0,4260
6,0875
5,9345
10,219
ig
0,57358
0,78859
0,69425
0,60296 —1
0,62941 —1
0,78444
0,77339
1,00941
Броматометрическое
определение оксинатов
1 мл 0,1 н. раствора КВг03
соответствует
Ni
5,8933
5,870
0,77036
0,76864
Вещество
А1
Bi
Cd
Се
Со
Си
Fe
Оэ
in
М£Т
Мп
Ni
Pb
Sb
Th
Ti
U
м
Zn
Zr
Количество,
мг
0,22485
1,7415
1,405
1,1677
0,73667
0,7943
0,46539
0,5810
0,9568
0,3039
0,68673
0,7337
2,5899
1,0146
1,4502
0,5988
1,983
0,63677
0,8171
0,5701
ig
0,35190 —1
0,24093
0,14768
0,06733
0,86727 —1
0,89998 —1
0,66782 —1
0,76418 —1
0,98082 — 1
0,48273 — 1
0,83679 — 1
0,86552 — 1
0,41328
0,00630
0,16143
0,77725 —1
0,29732
0,80398 — 1
0,91228—1
0,75597 — 1
4*
54
Перманганатометрия
1 мл 0,1 н. раствора КМп04
или 1 мл 0,1 н. раствора (СООН)2
соответствуют
продолжение
Вещество
(СООН)2
(СООН)2-2Н.О
(СОО)г
НСООН (по
Джонсу, щелочная
среда)
(по Ли-
щел очная
НСООН
бену,
среда)
Са
CaCOs
СаО
Са(ОН)2
Сг
Сг2Оэ
СЮ4
Си
(восстановление сахаром)
Fe
FeO
Fe203
FeS04- 7НгО
Fee(S04)s- 9H,0
(NH4)2Fe(S04),, •
• 6Нг0
H202
KMn04
Мп(поФолыарду)
Мп (по Гампе)
МпО (по Фольга р-
ДУ)
МпОг (с
щавелевой кислотой или
сульфатом
железа (II))
Мп03 (по Фоль-
гарду)
NH2OH (по Ра-
шигу)
N,.0,
HNO.
NH4N02
Na2CA
NaC103(CIO:f—^
-*С1")
NaN0„
NaNO, (МОГ—^
-►NO)
О
РЬОг
Pb304
■ 2SQ2-
)
•Sb5+)
Sb (Sb3+
Sb2Oa
Ti (Ti3* -+Ti4+)
Количество, мг
4,5018
6,3033
4,4010
2,3013
1,3808
2,0040
5,0045
2,804
3,7045
1,7332
2,5332
3,8665
6,354
5,5847
7,1846
7,9846
27,802
28,101
39,214
1,7007
3,1606
1,6481
2,7469
2,1281
4,3468
2,6081
1,6515
1,9003
2,3507
3,2022
6,7000
1,7740
3,4498
2,8332
0,79997
11,960
34,279
9,6062
6,0875
7,2875
4,790
ig
0,65339
0,79957
0,64355
0,36198
0,14013
0,30190
0,69936
0,44778
0,56873
0,23885
0,40367
0,58732
0,80305
0,74700
0,85641
0,90225
1,44407
1,44873
1,59344
0,23064
0,49977
0,21699
0,43884
0,32799'
0,63817
0,41633
0,21788
0,27882
0,37120
0,50545
0,82607
0,24895
0,53779
0,45228
0,90308 —1
1,07773
1,53503
0,98255
0,78444
0,86258
0,68034
Вещество
U(U4+ -»-UO|+)
u3o8
V (V*+ -v V»+ i
VA
Количество, мг
11,902
14,035
5,0942
9,0941
ip
1,07562
1,14722
0,70708
0,95876
Цериметрия
1 млн. 0,1 н. раствора Ce(S04)2
соответствует
Вещество
As
As203
AsOj,
Ва
BaO
Ва(ОН)„
(СООН)2
(С00Н)2-2Н20
QH40„ (винная
кислота)
Са (в виде оксалата)
СаС03 (в виде
оксалата)
СаО (в виде
оксалата)
Fe
Fe(CN)„
FeO
FeA
FeS04
FeS04.7H20
(NH4)2Fe(S04)2-6H20
Hg
HgO
КгСг04-НгО
khca-h2o
Khca-h2ca-
•2H20
K4[Fe(CN)e]
К4[Ре(СМ)61-ЗНгО
N02
Na2CA
Sb
SbA
Sn
Sr
SrCOa
Tl
U
V
Количество, мг
3,7461
4,9460
6,1460
6,8670
7,6670
8,5675
4,5018
6,3033
1,5009
2,0040
5,0045
2,8040
5,5847
21,195
7,1846
7,9846
15,191
27,802
39,214
20,059
21,659
9,2120
7,3073
6,3549
36,836
42,2408
4,6006
6,7000
6,0875
7,2875
5,9345
4,381
7,3825
10,219
11,902
5,0942
le
0,57358
0,69417
0,78859
0,83677
0,88463
0,93286
0,65339
0,79957
0,17635
0,30190
0,69936
0,44778
0,74700
1,32624
0,85641
0,90225
1,18159
1,44407
1,59344
1,30231
1,33564
0,96435
0,86376
0,80311
1,56627
1,62573
0,66281
0,82607
0,78444
0,86258
0,77338
0,64157
0,86815
1,00941
1,07562
0,70708
52
Поодолжение
Титанометрия
1 мл 0,1 н. раствора титана (III)
соответствует
Вещество
Аи
АиС13
Си
СиО
CuS04
CuS04-5H20
Fe
FeCl3
FeCl3-6H,0
Fe,0,
Fe2(S04)3
K,[Fe(CN),]
NH4Fe(S04).,-12H20
Hg
HgCl2
HgO
HgS04
Sb
SbCl5
sb2o5
и
иО,(СНчСОО),-2Н„0
Количество, мг
6,5656
10,111
6,354
7,954
15,960
24,963
5,5847
16,221
27,030
7,9846
16,994
32,926
48,219
10,030
13,575
10,830
14,833
6,0875
14,951
8,0875
11,902
21,208
Ig
0,81728
1,00479
0,80305
0,90059
1,20303
1,39738
0,74700
1,21008
1,43185
0,90225
1,30090
1,51754
1,68322
1,00128
1,13274
1,03463
1,17123
0,78444
1,17467
0,90782
1,07562
1,32650
Хромометрия
1 мл 0,1 н. раствора хрома (II)
соответствует
Вещество
Ag (Ag* -»
-+Ag<>)
Bi (Bi3+ -»
-»Bi°)
Cr20,
(CraOr -*
^-Cr3+)
Cu (Cu3+ ->
->Cu+)
Раствор
H2S04;
HC1 -f
4- NH,C1
H,S04 +
-f KC1
H2SO,
HCI
Количество,
мг
10,7871
6,9660
43,198
6,354
ig
1,03290
0,84298
1,63546
0,80305
Вещество
Cu (Cu2+ -»•
->Cu°)
Hg(Hgi+ -
^Hg»)
Раствор
H2S04
HaS04; HCI
Количество ,
мг
3,1770
10,030
Ig
0,50202
1,00130
Хроматометрня
1 мл 0,1 н. раствора К2Сг20,
соответствует
Вещество
Fe
FeO
Pb
Количество,
мг
5,5847
7,1846
20,719
ig
0,74700
0,85641
1,31637
Некоторые специальные
способы титрования
Вещество
Количество,
мг
Ig
1 мл 0,1 н. Na2HP04
соответствует:
Bi
Bi203
1 мл 0,1 н. FeS04
соответствует:
S208
1 мл 0,1 н. Th(N03)4
соответствует:
F
1мл0,1н. K4[Fe(CN)6]
соответствует:
РЬ
1 мл 0,1 н. раствора
калиевой солн
пальмитиновой кислоты
соответствует:
Са
СаО
СаС03
1 мл 0,1 и. раствора
Ва(С104)2
соответствует S04
6,9660
1,5532
9,6062
1,8998
20,719
2,0040
2,8040
5,0045
0,48031
0,84298
0,19123
0,98255
0,27870
1,31637
0,30190
0,44778
0,69936
0,68152 —1
6. ЭЛЕКТРОХИМИЧЕСКИЕ ЭКВИВАЛЕНТЫ
Элемент
Алюминий
Барий
Бериллий
Бром
Валентность
3
2
2
1
Электрохимический
эквивалент
мг/Кл | г/(А-ч)
0,0932
0,7116а
0,04670
0,82816
0,33556
2,5021
0,16812
2,9814
Элемент
Ванадий
»
Водород
Висмут
Валентность
5
3
1
3
Электрохимический
эквивалент
мг/Кл | г/(Ач)
0,106
0,176
0,010446
0,72194
0,380
0,63!
0,037607
2,5990
53
Продолжение
Элемент
Вольфрам
Железо
»
Золото
»
Иод
Кадмий
Калий
Кальций
Кислород
Кобальт
Литий
Магний
Марганец
Медь
Медь
Молибден
»
Натрий
Никель
Олово
»
Осмий
Палладий
Платина
»
Валентность
6
2
3
1
3
I
2
1
2
2
2
I
2
2
2
1
6
4
1
2
2
4
6
2
2
4
Электрохимический
эквивалент
мг/Кл
0,318
0,28939
0,19293
2,0413
0,68044
1,3152
0,58244
0,40524
0,2077
0,082907
0,30539
0,07191
0,12598
0,28468
0.3293
0,658
0,166
0,249
0,23826
0,3042
0,61504 л
0,30752 '
0,?28
0.ЕЯ14
1,0109
0,50547
г/(А-ч)
1,145
1,0418
0,69454
7,3488
2,4496
4,7347
2,0968
1,4589
0,7477
0,29847
1,0994
0,2589
0,45354
1,0249
1,1853
2,372
0,597
0,895
0,85774
1,095
2,2141
1,1071
1,120
1.985
3,6393
1,8197
Элемент
Рений
Рений
Рубидий
Ртуть
>
Свиней
Серебро
Стронций
Сурьма
»
Фтор
Хлор
Хром
Хромат-ион
Цинк
он-
csor
СО?"
NHJ.
NOg
ga-
SOf
Валентность
2
4
1
2
1
2
1
2
3
5
1
1
3
2
2
—
—
__
—
—
—
Электрохимический
эквивалент
мг/Кл
0,965
0,482
0,8858
1,0394
2,0789
1,0736
1,1179
0,4540
0,42060
0,25236
0,19690
0,36743
0,17693
0,60107
0,3387
0,17626
0,45611
0,31096
0,18695
0,64621
0,16615
0,49778
г/(А-ч)
3,475
1,737
3,189
3,7420
7,4839
3,8651
4,0246
1,635
1,5141
0,90849
0,70882
1,3227
0,64665
2,1638
1,219
0,63454
1,6420
1,1195
0,67301
2,3134
0,59815
1,7220
7. НОРМАЛЬНЫЕ ПОТЕНЦИАЛЫ НЕКОТОРЫХ
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫ X
СИСТЕМ
Восстановленная
форма
1
Ag
Ag+
Al
Al + ЗОН-
As
AsO^ + 2H20
Au
Au
Au+
Ba
Be
Bi
2ВГ
Br + 3HaO
Br + 60H-
Окисленная форма
2
Ag+ + e"
Ag2+ + e
Af3+ + 3e~
HA102 +3er +
+ НгО
As3+ + 3e~
AsO|" +2e" +
+ 4H+
Au+ + e~
Au3* + 3e"
Au3+ + 2e-
Ba2+ + 2e-
Be2+ + 2e"
Bi3+ + 3g"
Br2 + 2e"
ВЮ3 + 6e" +
+ 6№
BrO^ + 6e" +
+ 3H.0
£,. В
3
+0,800
+ 1,98
—1,67
-2.35
+0,30
0,559
+ 1,7
+ 1,42
+ 1,29
—2,90
—1,70
+0,28
+ 1,065
+ 1,44
+0,61
Восстановленная
форма
1
BrO" + 40H-
Ca
Cd
Ce3+
гост + 3H20
Co
Co2*
[Co(CN)6]*-
[CoNHa),?*
Cr
Cr*
2Cr3+ + 7H30
СЮ^ + ЮгГ
Cu
Окисленная форма
2
ВгОд + 4e~ +
+ 2H.O
Саг+ + 2e"
Cd2+ + 2e"
Ce44- +e"
CI2 + 2e-
CIO3 + 6e" +
+ 6№
Co2+ + 2e"
Co3+ + er
[Co(CN)J3- + e-
ICo(NH3)6l3++e-
Cr3+ + 3e"
Cr3+ + e~
Cr20?" + 6e~ +
+ 14H+
CrOf + 3e~ +
+ нго
Cu+ + e-
E„ в
3
+0,54
—2,87
—0,402
+ 1,61
+ 1.358
+ 1.45
—0,277
+ 1,84
—0,83
+0,1
-0,71
—0,41
+ 1,36
—0,12
+0,52
54
Продолжение
1
Си
Си+
Cs
2F"
Fe
Fe
Fe3+
[Fe(CN)fil4"
Ga
H
2H,0
2Hg
Hg
Hgl+
In
21"
ЗГ
12 f 120H-
K
La
Li
Mg
Mn
Mn2+ 4- 4H20
MnO, + 2H20
MnO, + 40H-
Mni+ 4- 2H20
МпОГ
Mo03+ + H20
NO 4 HaO
NO +■ 2H20
N02 4 H20
NHt 4 3H.20
\ £
Na
Ni
2H.,0
2
Cu2+ + 2e-
Cu2+ + e-
Cs+ 4- <T
F2 4- 2e-
Fe2+ 4- 2e"
Fe3+ + 3e~
Fe3+ 4- e
[Fe(CN)ep- + e-
Qa3+ + Ъе
H* 4-e"
2H+ 4- 2e"
H202 -f 2e" +
4- 2H+
Hg?+ 4- 2e"
Hg2+ 4- 2e-
2Hg>* + 2e"
In3+ + 3e"
12 + 2e"
Ij + 2e"
2Ю3 4- 10e~ +
+ 6H30
K* 4-e-
La3+ + 3e"
Li+ 4- e-
Mg2+ 4- 2e~
Mn2+ 4- 2e
MnO; 4- 5e~ 4
4- 8H+
MnOJ 4- 3e~ +
4- 4H+
MnO^ 4- 3e" 4-
4- 2HaO
Mn02 + 2e~ +
+ 4H+
МПО4 4- e"
MoOi+ 4- e- +
4- 2№
NOj 4- e" + 2H +
NO3 4- Зе" +„4H+
NO3 4- e~+ 2H +
NOj 4- 8e~ 4
4- ЮН*
Na+ + e
Ni3+ 4- 2e"
02 4- 4e" f 4H+
3
4-0,345
4-0,167
—2,92
4-2,85
—0,441
—0,036
4-0,771
4-0,36
-0,52
—2,1
+0,000
4-1,77
4-0,798
4-0,854
+0,910
—0,340
4-0,535
4-0,536
4-0,21
—2,922
—2,37
—3,02
—2,34
—1,05
4-1,52
4-1,67
4-0,57
4-1,2b
4-0,54
+0,5
4-0,99
4-0,96
4-0,81
40,87
—2,712
-0,23
4-1,229
l
H202
40H-
Pb
Pbi+
Pb2+ 4- 2H20
Pd
Pt
Rb
S2"
SO^" + H20
2SO^
2S20a"
Sb
Sn
Sn
Sn2+
Sn2+ 4- 6C1-
Sr
Те
Th
Ti3+
Ti»* + H20
TI
Tl+
Tl
и
U4+ 4- 2H30
YO2* + H20
Y2+ + 2H20
Y3+ 4- 2H20
Y3+ 4- H20
y2+
W03+ 4- H20
W03+ 4- 2H20
Y
Zn
Zn 4- ЗОН-
2
Ог + 2e" + 2H*
02 4- 4e" + 2H20
Pb2+ + 2e"
Pb4+ 4- 2e~
Pb02 4- 2e- +
4- 4H+
Pd2+ + 2e
Pt3+ + 2e"
Rb+ 4- e"
S + 2e~
SO^ 4- 2e" +
4- 2H+
S20=- + 2e~
S40^ + 2e~
Sb3+ 4- 3e"
Sn2+ 4- 2e
Sn4+ 4- 4e"
Sn4* 4- 2e-
lSnCle]2- + 2e-
Sr2+ 4- 2e"
Te4+ 4- 4<r
Th4+ + 4e"
Ti4+ + e"
TiO2* 4- e" +
4- 2H+
Tl+ + e"
Tl3+ + 2e"
Tl3+ + 3e-
U4+ + 4e"
UO^ 4- 2e" 4-
4- 4H+
V02++ e-+ 2H+
V02+ 4- 3e" +
4- 4H+
V02+ + 2e" +
4- 4H+
УОг+ + r +
4- 2H+
V3+ 4- e-
WO|+ 4-e"4-
4- 2H+
W03 4- e~ 4- 4H+
Y3+ 4- 3e-
Zn2+ 4- 2e-
HZnOJ 4- 2e+
4- НгО
3
4-0,682
4-0,40
—0,126
+ 1,69
+ 1,46
4-0,83
+ 1,2
—2,99
—0,508
+0,20
+2,05
+0,17
+0,20
—0,14
+0,050
+0,15
+0,15
—2,89
+0,57
—1,90
+0,1
+0,1
—0,335
+ 1,25
+0,72
—1,4
4-0,42
+ 1,0
+0,37
+0,66
+0,314
—0,20
4-0,26
+0,26
-2,1
—0,762
— 1,22
КЛАССИФИКАЦИЯ РЕАКТИВОВ
ПО ЧИСТОТЕ
Степень чистоты реактивов
возрастает в ряду марок: технический —
техн.; чистый — ч.; чистый для
анализа — ч. д. а.; химически чистый—
х. ч.; особой чистоты — ос. ч.
Встречаются марки: высокой чистоты —
в.ч.; спектрально чистый — сп. ч;
очищенный — очищ. (очищен по
одному или группе компонентов
каким-либо методом).
55
Реактивы разных марок
отличаются содержанием основного вещества,
примесей и их числом, нормы
которых периодически пересматриваются.
Спектрально чистые реактивы
содержат примеси в количествах менее
чувствительности (%) спектрального
метода анализа существующими
способами.
Вещества особой чистоты в СССР
с 1965 г. классифицируются по
маркам в зависимости от числа
лимитируемых (контролируемых) в них
примесей и содержания суммы этих
примесей.
Особо чистые вещества, в которых
лимитируются только
неорганические примеси, маркируются
индексом ос. ч. и следующими за ними
двумя (через тире) цифрами: первая
из этих цифр показывает число
неорганических примесей; вторая —
отрицательный десятичный логарифм
показателя степени суммарного
процентного содержания этих примесей.
Например, в серной кислоте марки
ос. ч. 12—4 содержится
^контролируемых неорганических примесей с
суммарным содержанием «•10"4%.
Особо чистые вещества, в которых
лимитируются только органические
примеси, маркируются индексом о.п.
(органические примеси), затем (через
тире) цифрой, соответствующей
отрицательному десятичному
логарифму показателя степени суммарного
их содержания и буквами ос. ч. Так,
марка особо чистого вещества,
имеющего сумму органических примесей
2 • 10~2%, обозначается о. п. — 2
ос. ч.
Для особо чистых веществ, в
которых лимитируется содержание
органических и неорганических
примесей, учитывается содержание
примесей обеих групп, как описано
выше. Например, изо-пропиловый
спирт марки о. п.— 1 ос. ч. 11—5
содержит органические примеси в
сумме не более «•10"1%, 11
лимитируемых неорганических примесей с
суммой примесей не более га-10~6%.
Металлы высокой чистоты можно
встретить с другой классификацией.
По степени чистоты металлы особой
чистоты подразделяются на три
класса, каждый из которых
подразделяется на подклассы.
лассы
А-1
А-2
В-3
В-4
В-5
В-6
С-7
С-8
С-9
С-10
Сумма контролируемых-
примесей, %
(n = l-i-9,9)
п-10-1
п-10-'
п- Ю-'
п-10-4
n-10-s
п-10-»
n-I0-'
п-10-«
п-10-*
п-10-"
Класс А соответствует содержанию
примесей от 9,9-Ю-1 до 1-10"!%;
класс В — от 9,9-Ю-8 до ЫСТ^/о;
класс С—от 9,9 до 1.1(Г,0%.
Содержание основного металла в
металлах класса А можно
определять непосредственно анализом или
по разности. В металлах классов В
и С содержание основы определяется
вычитанием из 100% суммы
непосредственно определяемых примесей
(примеси, не обнаруживаемые при
существующей чувствительности
методами анализа, в расчет не
принимаются).
9. ХАРАКТЕРИСТИКА
НЕКОТОРЫХ РЕАКТИВОВ, ПРИМЕНЯЕМЫХ
В АНАЛИЗЕ МЕТАЛЛОВ
Аммоний хлористый
NH4C1, M = 53,497
Белый кристаллический порошок
при нагревании свыше 337° С
диссоциирует на пары NH8 и НС1,
которые улетучиваются и, соединяясь ных и промывных растворов.
вне сферы нагревания,.образуют
плотный белый «дым», состоящий из
мелких кристалликов. Легко растворим
в воде, с трудом — в этаноле.
Применяют для перевода в
растворы минералов как компонент буфер-
56
А с к а р и т
Лучший твердый поглотитель
двуокиси углерода, медленно
насыщается ею, при этом не отдает влагу.
Для приготовления в большой
фарфоровой чашке со 100 мл воды
растворяют 350 г NaOH, 25 г Na202,
присыпают асбестовую вату до тех
пор, пока асбест не перестанет
смачиваться теплой щелочью.
Высушивают при 170° С в течение 6 ч.
Если при этом масса разжижается,
то прибавляют еще асбестовую вату.
Высушенный аскарит охлаждают,
измельчают в ступке (в очках!) и
просеивают через сито с отверстиями
1—2 мм. Ссыпают в банку с
резиновой пробкой.
Алюминий хлористый
А1С13-6НаО, М = 241,43
Бесцветное кристаллическое
вещество. Гигроскопичен, на воздухе
расплывается и дымит вследствие
гидролиза. Растворяется в воде, этаноле,
диэтиловом эфире с выделением
тепла; продажный препарат содержит
около 90% А!С13-6Н20. В
растворах соотношение А13+ : СГ = 1 : 3.
Растворение безводного А1С13
сопровождается выделением тепла,
дымлением (НО), растворы готовят под
тягой добавлением небольших
порций к воде.
20%-ный раствор готовят
растворением 200 г безводного А1С13 или
360 г А1С13-6НаО в 700 мл Н20
и разбавлением до объема 1 л.
Содержание алюминия и хлора
контролируют известными методами.
Аммоний азотнокислый
NH4NOs, М = 80,04
Бесцветные кристаллы, хорошо
растворимые в воде; нейтральный
раствор получают растворением навески
препарата в свежепрокипяченной
охлажденной воде: 1) 25 мл
приготовленного раствора в присутствии
3 капель фенолфталеина должны
быть бесцветными; от 1—2 капель
0,1 н. раствора NaOH должна
появиться устойчивая розовая окраска.
Если окраска появляется сразу, то
необходимо по каплям прибавить
0,1 н. HN03 до обесцвечивания;
2) 2,5%-ный раствор готовят
нейтрализацией раствором NH4OH в
присутствии метилового красного.
Аммоний
надсернокислый
(NH4)2Sa08, M = 228,20
Бесцветные или зеленоватые
кристаллы, при нагревании разлагаются
с выделением кислорода; в
присутствии влаги постепенно разлагаются.
Водные растворы неустойчивы и
особенно при нагревании. Продажный
препарат ч. д. а. содержит 85%
(NH4)2S208. Применяют при
определении хрома, марганца и как
плавень. Предельный срок хранения 12—
25%-ных растворов — 4 суток.
Аммоний роданистый
NH4SCN, M = 76,12
Бесцветные кристаллы. Продажный
препарат содержит 98% NH4SCN.
Растворяется в воде, этаноле с
поглощением тепла.
Концентрированные водные растворы на свету
краснеют, хранить надо в склянках из
темного стекла. При нагревании до
70° С частично переходит в тиомо-
чевину.
Аммоний сернистый
(NH4)2S, M = 68,14
Известны растворы, желтеющие на
воздухе.
Аммоний
тетрароданомеркуриат
(NH4)2 [Hg (SCN)J, M ='468,99
Кристаллический порошок. Для
получения растворов, применяемых
при гравиметрическом определении
цинка, 32 г NH4SCN растворяют
в 200 мл воды. Затем при
помешивании прибавляют 27 г HgG2,
разбавляют водой до 1 л. Через двое
суток фильтруют, фильтрат хранят
в темной склянке.
57
Аммоний
молибденовокислый
(NH4) Мо7Ог4, М = 1235,8
Хранение на воздухе
сопровождается выветриванием аммиака.
Продажные препараты содержат
МоОэ: х. ч. 81%; ч. д. а. 80,5%;
ч. 80%. Растворим в воде, сильных
кислотах, щелочах.
1%-ный раствор: 10 г препарата
растворяют в 500 мл воды при
нагревании, охлаждают, доливают до
1 л водой, после суточного стояния
фильтруют.
Молибденовый раствор (жидкость)
для определения фосфора: 1) 150 г
мелкоистертого молибдата аммония
растворяют в 1 л горячей воды.
К мутному раствору вливают
раствор аммиака до просветления.
Охлаждают и вливают тонкой струйкой
при помешивании в 1 л раствора
азотной кислоты (1 + 1) (но не
наоборот!!). При добавлении первых
порций аммиачного раствора к
азотной кислоте выделяется белый осадок
молибденовой кислоты,
растворяющийся при перемешивании. Раствор
выдерживают в течение 8—10 дней,
после чего отфильтровывают от
желтого осадка в полиэтиленовую
посуду; 2) 55 г молибденового ангидрида
растворяют в смеси из 135 мл воды
и 80 мл концентрированного
раствора аммиака, растворение
ускоряется при нагревании. Охлаждают,
фильтруют, вливают 35 мл
концентрированной HN03. Полученный
раствор медленно вливают в холодный
раствор из 220 мл воды и 530 мл
воды, добавляют к нему 0,1 г
(NH4)2HP04. Через сутки раствор
фильтруют.
Раствор в серной кислоте для
фотометрического определения фосфора:
25 г препарата растворяют в 200 мл
горячей воды, фильтруют,
приготовленный охлажденный раствор
вливают в холодный раствор из
520 мл воды и 280 мл
концентрированной H2S04. После охлаждения
раствор доливают водой в мерной
колбе до 1 л.
Очистка молибдата аммония: 1.
Экстракцией от кремния, германия,
мышьяка, фосфора. Содержание
кремния в Na2Mo04 ч. 14 мгк/г; молиб-
дате аммония х. ч. 6 мкг/г. К 40 г
молибдата аммония (натрия) в
полиэтиленовом (фторопластовом)
сосуде приливают 100 мл нагретой
до кипения воды двойной перегонки,
размешивают полиэтиленовой
палочкой. После растворения фильтруют
через фильтр, помещенный иа
полиэтиленовую воронку, при
помешивании приливают к фильтрату азотную
или серную кислоту до рН = 1,5,
через 15 мин охлаждают до
комнатной температуры. Создают
кислотность, 3-н. по азотной или серной
кислотам, и проводят экстракцию
гетерополикислот бутанолом 40 мл +
4- 40 мл до тех пор, пока очередной
экстракт не будет бесцветным. Затем
водный слой сливают в
полиэтиленовый стакан, нейтрализуют до рН =
= 6,5 раствором в бидистилляте
NaOH, полученном из
металлического натрия.
В результате очистки получаются
молибдаты аммония и натрия с
содержанием 0,2 и 3 мкг/г, что
позволяет повысить чувствительность
определения Si, Ge, P, As в 3—5 раз.
2. Очистка перекристаллизацией
менее эффективна. 250 г молибдата
аммония (ч. д. а.) растворяют в 400 мл
горячей воды, добавляют аммиака
до отчетливого запаха, горячий
раствор фильтруют через плотный
фильтр в стакан, содержащий 300 мл
этанола. Охлаждают до 10° С. Через
1 ч фильтруют через воронку с
пористым дном № 2—3, кристаллы
промывают 20 + 20 мл этанола,
высушивают на воздухе.
Аммоний углекислый
(NH4)2C03-H20, M = 114,10
Бесцветные кристаллы с запахом
аммиака; при хранении на воздухе
переходит в NH4HCOg и (NH4)2COs.
1М раствор готовят растворением
96 г растертого порошка (NH4)2C03
в 1 л 2М NH4OH (смесь из 150 мл
концентрированного аммиака и
850 мл воды).
58
Аммоний
фосфорнокислый двухзамещенный
(NH4)2HP04) М == 132,06
Бесцветные кристаллы,
устойчивые ниже 111° С. На воздухе
медленно теряют аммиак, переходя в
однозамещенный фосфат.
10%-ный раствор в воде лучше
применять свежим; при хранении
растворов в стеклянных сосудах
рекомендуется подкислять фосфорной
кислотой.
Барий хлористый
ВаС12-2Н20, М = 244,28
Бесцветные кристаллы, при 100° С
теряют воду, во влажном воздухе
вновь поглощают ее. Полностью
обезвоживается при 160° С. Хорошо
растворим в воде, почти нерастворим
в соляной кислоте: в этаноле не
растворяется, но теряет
кристаллизационную воду. Сильный яд!!!
Применяют 10- и 5%-ные; 0,05:0,05 н.
растворы в воде. 0,1 н. раствор
готовят растворением 12,22 г ВаС12-
• 2Н20 в воде и доводят до 1 л.
Бром, М = 159,82
Темно-бурая жидкость с резким
запахом, плотность 3,12, пары брома
темно-красного цвета. При 0° С
растворяется 4,22 г/100 мл воды;
хорошо растворим в кислотах НС1,
НВг, растворах KB г, этаноле,
хлороформе, четыреххлористом
углероде и др. Температура кипения 58,8°С.
При —5,7° С затвердевает в желто-
зеленую массу, при —252° С
становится бесцветным. Пары брома
ядовиты. Бром хранят в склянках
из темного стекла с
предохранительным колпачком.
Бромная вода. Насыщенный
раствор брома в воде (~3%) желто-
бурого цвета. Сильный окислитель;
на воздухе выделяет пары брома.
50 г брома встряхивают с 1 л воды,
открывая при этом иногда пробку.
Избыток брома находится на дне.
Работу с бромной водой ведут под
тягой.
Бром в растворе бромида калия.
Применяют в анализе плавикового
шпата. 160 мл брома наливают в
склянку из темного стекла, вливают
700 мл 20%-ного раствора КВг,
перемешивают. По израсходовании
этого раствора в склянку приливают
600—700 мл 20%-ного раствора КВг
без брома и перемешивают.
Гидразин-гидрат
H2N—NH2-H20, M = 50,06
Бесцветная густая
гигроскопическая жидкость, дымит на воздухе,
плотность 1,03. Смешивается с водой,
этанолом. Не растворима в
хлороформе, диэтиловом эфире. Сильное
основание, из воздуха поглощает
С02. С кислотами образует соли.
Сильный восстановитель. При
действии окислителей может
взрываться!! Яд!!
Гидразин сернокислый
H2N—NH2-H2S04, M = 130,13
Бесцветные кристаллы, плотность
1,38. Растворяются в 100 мл воды
3,05 г при 22° С; 27,65 г при 60° С;
мало растворимы в этаноле.
Безводный чистый гидразин сернокислый
как основное вещество в иодометрии
и алкалиметрии получают
перекристаллизацией его из воды и
высушиванием при 140° С. Раствор титруется
раствором щелочи в присутствии
метилового красного, метанилового
желтого. Восстановитель. Яд!!
0,15%-ный раствор применяют при
фотометрическом определении
мышьяка: 0,15 г растворяют в 75 мл воды
и разбавляют до 100 мл водой.
Гидроксиламин NH4OH,
М = 33,03
Бесцветные кристаллы;
гигроскопичны, легко разлагаются, особенно
в присутствии примесей и щелочей.
При нагревании выше температуры
плавления взрывается.
Гидроксиламин
солянокислый
NH2OH-HCl, M =69,49
Бесцветные кристаллы.
Восстановитель. Яд!! Хорошо растворим в
69
воде, мало в абсолютизированном
этаноле, не растворим в эфире.
10%-ный раствор применяют в
качестве восстановителя. 10 г
препарата растворяют в 90 мл воды,
фильтруют.
1%-ный раствор, очищенный дити-
зоном: к 300 мл раствора добавляют
концентрированный аммиак до
щелочной реакции по феноловому
красному. Раствор переливают в
делительную воронку, встряхивают с
0,01% раствора дитизона в
хлороформе 10 мл + 10 мл + и т. д. до
тех пор, пока последняя порция
дитизона не будет иметь чисто
зеленый цвет. Промывают несколькими
порциями хлороформа до тех пор,
пока последняя порция хлороформа
не будет бесцветной.
Железо-аммонийные
К В Э С П Ы
Fe2(S04)3 • (NH4)2S04 • 24H 20,
М = 964,38
Кристаллы бледно-фиолетового
цвета, буреющие на воздухе
вследствие выветривания и образования
основных солей; плавятся при 39—
41° С. Безводный бурый порошок
получается при 750° С. Квасцы
хорошо растворимы в воде, легко
образуют пересыщенные растворы. Для
предотвращения гидролиза водные
растворы готовят с добавкой кислот;
не растворимы в этаноле.
Насыщенный на холоду раствор:
42 г препарата в виде порошка
растворяют в 100 мл воды.
Насыщенный красноватый раствор фильтруют
через складчатый фильтр и к
мутному фильтрату до просветления
прибавляют концентрированную HN03.
3%-ный раствор: 3 г квасцов
растворяют в 100 мл воды, содержащей
2 мл концентрированной H2S04.
Железо хлорное FeCl3 •
• 6Н20, М = 270,30
Красно-коричневая,
кристаллическая, влажная на ощупь и мягкая
масса; на воздухе расплывается.
Хорошо растворима в воде, этаноле,
глицерине, эфире. Заметно
улетучивается при 100° С; плавится при
37° С. Выше 250° С разлагается с
образованием Fe203, FeCl2, C12.
Растворы готовят с добавкой кислоты.
Раствор 150 г FeCl8 -6Н аО в 300 мл
20,3% -ной НС1 после разбавления
до 1 л водой применяют при
определении окислов железа в
присутствии железа для удаления
металлической меди.
Насыщенный раствор в соляной
кислоте применяют для надписей на
фарфоровых тиглях.
Калий йодистый KI»
М = 166,01
Бесцветные кристаллы, устойчивые
в сухом воздухе. Хорошо
растворяются в воде с поглощением тепла.
Растворы должны быть бесцветны
и храниться в темных склянках;
запасные растворы не готовят.
Раствор с аскорбиновой кислотой
применяют при фотометрическом
определении сурьмы. 1 г
аскорбиновой кислоты растворяют в 100 мл
воды и добавляют 12 г KI; раствор
должен быть бесцветным.
Калий — олово (II)
хлористый
К2 [SnClJ.2H20, M = 374, 74
25%-ный раствор в 5%-ной НС1
применяют для восстановления меди
(II), железа (III), при
фотометрическом определении молибдена,
вольфрама, рения, ниобия.
Калий роданистый KSCN,
М = 97,184
Бесцветные кристаллы,
гигроскопичны. Хорошо растворимы в воде
и этаноле. При 430° С синеют, после
охлаждения снова бесцветны.
Окрашенные растворы очищают от железа
(III) соосаждением с несколькими
миллиграммами соли алюминия,
осаждая аммиаком. Через сутки раствор
сливают сифоном.
Калий цианистый KCN,
М = 65,12
Белое кристаллическое вещество,
плотность 1,52. На воздухе расплы-
60
вается и пахнет синильной кислотой
(горьким миндалем) из-за
взаимодействия с влагой и СО а воздуха.
Яд!!] Следует остерегаться подкисле-
ния растворов цианидов!!
Хороший комплексант, применяют
для маскировки примесей, основы
и непосредственного анализа многих
элементов. Все работы проводить под
хорошей тягой!! Недопустимо
попадание на кожу, одежду.
1,5%-ный раствор: 15 г KCN и
5 г КОН растворяют в воде и
разбавляют водой до 1 л.
Кобальтовые
катализаторы
Применяют при титриметрическом
определении марганца, хрома:
1) кобальтовый катализатор: 0,5 г
CoS04-7H20 растворяют в 100 мл
воды;
2) кобальто-никелевый
катализатор: 0,5 г CoS04-7H2Oh l,5rNiS04-
• 7Н20 растворяют в 100 мл воды;
3) кобальто-медно-никелевый
катализатор: 0,25 г CoS04-7H20 +
+ 0,4 г NiS04-7H20 + 1 г CuS04 •
• 5Н20 растворяют в 100 мл воды.
Лучшим из них является последний;
4) при определении хрома
применяют в качестве катализатора
раствор 1 г CoS04-7H20 и 3 г NiS04 -
• 7Н20 в 100 мл воды. Во всех
случаях сначала растворяют соли
кобальта при нагревании до 50° С,
затем соли никеля и меди.
Калий иоднокислый
(п е р и о д а т)
КЮ4, М = 230,01
Белый кристаллический порошок,
устойчивый на воздухе. Плохо
растворяется в холодной воде, лучше
при нагревании. 5%-ный его раствор
в азотной кислоте (1 + 4) удобен
для окисления марганца (II) в
марганец (VII): 25 г препарата
растворяют в 400 мл HN03 (1 + 1),
доливают водой до 500 мл, перемешивают.
Применяется при определении
марганца, железа, никеля.
Кремнезем
(кварцевый порошок)
Si02, M = 60,085
Получают измельчением в тонкий
порошок кусочков кварца или
горного хрусталя. Прокаливают.
Кремнемолибденовая
кислота
Раствор применяют в качестве
индикатора при титровании железа (II)
бихроматом. Переход окраски от
синей к светло-зеленой. 0,17 г
кремнекислого натрия растворяют в 5 мл
воды, содержащей несколько капель
5%-ного раствора NaOH; раствор
вливают в раствор 0,44 г молибдено-
вокислого аммония в 15 мл воды,
добавляют воды до 25 мл и 1 мл
H2S04 (1 + 1). Раствор применяют
свежеприготовленный.
Магнезиальная смесь
Растворы, содержащиеMg2+ , NH+,
С1~, ОН-, применяют при
определении фосфора, мышьяка (V).
Аммиачный раствор: а)
растворяют 100 г MgCl2-6H20 и 125 г
NH4C1 в 150 мл воды и приливают
500 мл концентрированного аммиака;
б) растворяют 55 г MgCi2-6H20 и
и 105 г NH4C1 в воде, приливают
350 мл концентрированного аммиака
и воды до 1 л. Через 3 дня раствор
фильтруют.
Кислый раствор: а) 50 г
MgCl2-6H20 и 100 г NH4C1
растворяют в воде, добавляют несколько
капель НС1 и разбавляют водой до
1 л; б) растворяют 50 г MgCl2-6H20
и 100 г NH4C1 в 500 мл воды,
добавляют аммиак до запаха и через
12 ч фильтруют, прибавляют
соляную кислоту до кислой реакции по
метиловому красному и разбавляют
водой до 1 л.
Растворы хранят в склянках с
притертой пробкой.
Мочевина О-С (NH2)2,
М = 60,06
Бесцветные кристаллы, при
нагревании выше 100е С разлагаются, хо-
61
рошо растворяются в воде, метаноле:
почти нерастворимы в хлороформе,
эфире. Водные растворы имеют
нейтральную реакцию.
Применяется для удаления
нитритов, окислов азота из растворов,
как осадитель гидроокисей,
фосфатов при гомогенном осаждении.
Магний хлорнокислый
Mg (СЮ4)2, М = 229,23
Безводный магний — белая
пористая масса, чрезвычайно
поглощающая влагу. Способен поглощать
воду в количестве до 60% от
исходной массы, при этом переходит в
Mg (C104)a-3H20, не расплывается.
При смачивании с водой
наблюдаются разогревание и шипение.
Как нейтральное вещество
применяется для поглощения влаги,
осушки газов (Н2, Оа, Cl2, HC1, С02,
NH3 и др.).
Хранить нужно в склянке с
пришлифованной пробкой, залитой
парафином.
Магний хлористый
MgCl2-6HaO, M = 203,22;
MgCl2, M = 95,23
MgCl2-6HaO—кристаллы,
плотность 1,56. Легко растворимы в воде.
При нагревании теряют
одновременно воду и НС1, оставляя MgO.
Температура плавления 117,5° С;
разложения 151° С. Гигроскопичны и
должны храниться в плотно
закрытых банках.
MgCl2— пластинки с
перламутровым блеском, плотность 2,32.
Растворимы в воде, этаноле. Во
влажном воздухе расплываются. При
температуре белого каления в
атмосфере водорода возгоняются.
0,1 н. раствор: 10,17 rMgCl2-6H30
растворяют в воде, доливают до 1 л
водой.
Натрий сернистый
Na2S-9H20, M = 240,18
Бесцветные или слабоокрашенные
гигроскопичные кристаллы, хорошо
растворимые в воде, этаноле; при
хранении вследствие
гигроскопичности над кристаллами появляется
слой раствора. На воздухе
окисляется. Для приготовления
растворов отбирают крупные кристаллы под
раствором, слегка промывают их
водой, их состав близок к Na2S-9H20.
Растворы имеют щелочную реакцию.
10%-ный раствор: 100 г
кристаллов растворяют в 800 мл воды и
разбавляют водой до 1 л. Раствор
готовят пропусканием H3S в 63 мл
5М раствора NaOH до насыщения
и разбавляют водой до 1 л.
Натрия кобальтинитрит
Na3 tCo(N02)6] 0,5H2O,
М= 412,94
Желтый кристаллический
порошок, устойчив на воздухе; при
нагревании разлагается. Хорошо
растворяется в воде, неустойчив в
растворах. Не растворим в эталоле,
диэти ловом эфире.
Натрия перекись
Na202, М = 77,98
Белый или светло-желтый
порошок, при нагревании желтеет.
Соприкасаясь с водой, сильно
разогревается и растворяется с частичным
разложением; при кипячении
выделяется кислород. Гидрат— Na2Oa •
■ 8Н20, температура плавления
30° С. При длительном хранении
разлагается на NaOH, H20 и 02.
Натрий нитропруссид-
ный Na2 [Fe(CN)5NO]-2H20,
М = 297,95
Темно-красные кристаллы,
плотность 1,71. Растворим в воде;
водные растворы разлагаются даже на
рассеянном свету. В щелочном
растворе энергичный восстановитель.
Яд!!
10%-ный раствор применяют в
качестве индикатора при меркуриметри-
ческом определении С1". 10 г
препарата растворяют в 90 мл воды и
хранят в склянке темного стекла.
Если раствор приобрел зеленую
окраску, то он не пригоден.
62
Натрий
пирофосфорнокислый
Na4P207, M = 265,90;
Na4P2O7-10H2O, м = 446,05
Белые кристаллы, плотность 1,85,
растворимые в воде, нерастворимы
в этаноле. Водные растворы имеют
щелочную реакцию; при кипячении
переходят в HPOi-; применяют в
качестве комплексанта при
определении марганца, никеля и др.
Насыщенный раствор: 50 г
безводного пирофосфата или 85 г
кристаллогидрата растворяют в 980 мл воды
при нагревании и фильтруют
горячий раствор.
Калий пирофосфорнокислый
К4Р207-ЗН20 обладает лучшей
растворимостью в воде, чем натриевая
соль.
Натрий
сернистокислый
Na2S03-7H20, M = 252,15
Бесцветные кристаллы,
выветривающиеся на воздухе, окисляются
до Na2S04. При нагревании до 150° С
теряют кристаллизационную воду,
при дальнейшем нагревании
плавятся, образуя Na2S04 и Na2S.
Безводный сульфит натрия в
сухом воздухе не изменяется,
окисляется медленнее кристаллогидрата.
Насыщенный раствор: 250 г
безводного или 500 г кристаллического
сульфита растворяют в 500—700 мл
подогретой воды, фильтруют.
Натрий
тетраборнокислый
Na2B4O7-10H2O, M = 381,73
(тетраборат натрия,
бура)
Na2B4O-10H2O — твердые
призматические кристаллы, плотность
1,72. При нагревании сначала
плавятся, затем вспучиваются, теряя
кристаллизационную воду, и,
наконец, переходят в стекловидную
массу. До 200° С устойчив Na2B4Cy
• Н20; последняя молекула воды
полностью удаляется при 400—450°С.
Бура хорошо растворима в воде,
глицерине. Почти не растворима в
этаноле. Водный раствор имеет
щелочную реакцию. NaaB407—
бесцветные стекловидные кусочки
плотностью 2,37. На воздухе поглощает
влагу. Применяется в качестве
плавня, комплексанта, основного
вещества в ациди- и алкалиметрии, для
приготовления буферных растворов.
0.05М раствор в воде (19,072 г/л
Na2B407-10Н2О) имеет величину
рН =9,18 (25° С).
Натрий
фосфорноватисто-
кислый
NaH2P02, M = 106,01
Бесцветные кристаллы,
расплывающиеся на воздухе. Хорошо
растворимы в воде, этаноле. Энергичный
восстановитель. При нагревании
разлагается с выделением РН3, поэтому
безводный препарат не получен.
Водные растворы применяются в
качестве восстановителя при
определении мышьяка, олова и др.
По свойствам к нему близки
Ca(H2P02)2, NH4H2P02; первый в
отличие от других не рекомендуется
применять в растворах, содержащих
сульфаты.
Натрий
гидросернистокислый
(гидросульфит)
Na2S204-H30, M = 210,14
Белый кристаллический порошок,
легко растворим в воде, не
растворим в этаноле. Энергичный
восстановитель. Сухой устойчив на
воздухе в течение нескольких дней;
влажный быстро окисляется.
Безводный Na2S204 — мелкий, очень
твердый белый порошок.
Применяется в анализе кислорода, селена и др.
Натрий
пиросернистокислый
Na2S205
(метаб и сульфит натрия)
М = 190,11
Белый кристаллический порошок
или крупинки с запахом двуокиси
03
серы. Хорошо растворим в воде,
нерастворим в этаноле. Плавится при
100° С с разложением. На воздухе
постепенно окисляется до Na2S04;
в водных растворах окисляется
быстрее. Применяется в анализе
фосфатов, свинца, альдегидов, кетонов.
Натрий
висмутовокислый
NaBi03-2HaO (в и с м у т а т)
Аморфный порошок желтоватого
или коричневого цвета. Сильный
окислитель. Несколько
гигроскопичен. Нерастворим в воде; трудно
растворяется в HN03 на холоду,
легко при нагревании. Применяется
в качестве окислителя при
определении марганца, хрома и др.
Олово двухлористое
SnCl2.2H20, M = 225,62
Бесцветные кристаллы, плотность
2,17. Хорошо растворимо в воде,
этаноле. При 40° С плавится в
кристаллизационной воде, теряя ее при
дальнейшем нагревании.
Безводный SnCl2 хорошо
растворим в воде, этаноле, ацетоне,
пиридине, уксусноэтиловом эфире;
устойчив . на воздухе. Продажные
препараты ч. д. а. содержат 98% SnCl2-
•2Н20.
SnCl2-2H20 на воздухе, особенно
на свету, легко окисляется,
покрываясь непрозрачным слоем SnCl4.
25%-ный раствор применяется при
фотометрическом определении
молибдена, вольфрама, ниобия, рения.
250 г. SnCla-2HaO растворяют при
нагревании в 200 мл
концентрированной НС1 до просветления
раствора, охлаждают, вливают 800 мл воды.
Старые препараты требуют более
длительного нагревания для более
полного растворения. Растворы
окисляются на воздухе, поэтому в них
бросают кусочек олова, а еще лучше
особенно титрованные растворы
хранить в атмосфере инертных газов
(С02, N2, Ar).
10%-ный раствор из
металлического олова: 53 г олова в виде
гранул, фольги, порошка растворяют
в 1 л концентрированной НС1 при
нагревании и перемешивании. На
холоду растворение заканчивается
за несколько дней.
0,5%-ный раствор для
фотометрического определения кремния: 0,5 г
SnCla-2HaO растворяют в 10 мл
концентрированной НС1 и
разбавляют водой до 100 мл. Раствор
устойчив в темной склянке
несколько часов.
Раствор SnCla в фосфорной
кислоте применяют для определения
сульфатной серы иодиметрическим
методом.
Перекись водорода
H2Os, M = 34,02
Продажные растворы
(пергидроль) — бесцветная жидкость с
содержанием 21—31% На02, плотность
1,112. При хранении разлагается
с выделением 02, с разбавлением
устойчивость возрастает. Полностью
смешивается с водой, этанолом,
эфиром. Перекись водорода — сильный
окислитель, иногда реагирует как
восстановитель. Разбавлением
готовят растворы нужной концентрации.
Хранят растворы в темных
склянках, неплотно закрытых притертыми
пробками (не допускается
применение резиновых, корковых пробок).
При хранении растворы извлекают
из сосудов примеси, каталитически
ускоряющие разложение перекиси^
При попадании на кожу
пергидроля образуются ожоги в виде
белых пятен, пузырей.
Ртуть хлористая HgaCl8
М = 472,13
(хлорид ртути (I))
Белый порошок, плотность 7.15.
Нерастворима в воде, спирте, эфире,
разбавленных кислотах.
Растворяется в горячих концентрированных
HN03, H2S04 с образованием ртути
(II). Растворима в бензоле, пиридине.
Растворяется при кипячении в
растворах НС1, NH4C1, щелочей,
выделяя ртуть и HgCla. При постепенном
нагревании возгоняется без
предварительного разложения.
Температура плавления 543° С. Под
действием света темнеет вследствие вы-
64
деления металлической ртути.
Применяется при анализе олова,
заполнении каломельных стандартных
полуэлементов (электродов). Смесь
NaCl и Hg2CI2 для определения
олова: растирают в ступке смесь из
3 г Hg2Cl2 и 6 г NaCl. Для анализа
берут 0,1 г приготовленной смеси;
лучше предварительно приготовить
таблетки из смеси с массой 0,1 г.
Суспензия каломели в насыщенном
водном растворе КО: растирают
каплю ртути и небольшие количества
каломели, смоченные насыщенным
раствором КС1 до тех пор, пока не
получится совершенно гомогенная
масса. Так повторяют несколько раз,
пока не соберется достаточное
количество ее.
Ртуть хлорная HgCl.,,
М = 271,50
Бесцветные кристаллы, плотность
5,42. Температура плавления 275° С.
Ртуть хорошо растворима в горячей
воде, этаноле, эфире; хуже
растворима в холодной воде. В растворах
мало диссоциирована, летуча с
нарами воды.
Для получения HgCl2 растирают
20 г с водой в жидкую кашицу,
которую вносят в 75 мл 10?/о-ной
соляной кислоты. Раствор фильтруют,
выпаривают до образования
кристаллической пленки, дают
закристаллизоваться. Сильный яд!!
Насыщенный раствор (—4,5%):
45 г HgCl2 растворяют при
нагревании в 1 л воды, фильтруют.
Серебро азотнокислое
AgN03, M = 169,87
Бесцветные кристаллы, плотность
4,35. Чернеет на свету в присутствии
органических веществ. Яд!!
Хорошо растворимо в воде,
глицерине, спиртах; хуже в ацетоне,
бензоле; почти не растворяется в
концентрированной азотной кислоте.
Для повышения устойчивости
растворов добавляют (в процессе
разбавления) несколько капель
концентрированной азотной кислоты. Растворы
хранят в склянках из темного стекла.
Отработанные растворы, осадки
собирают в специальный сосуд для
регенерации серебра.
Снесь Циммермана —
Рейнгардта
Применяют при титровании
железа (II) перманганатом в растворах
НС1. Используемые реагенты не
должны содержать примесей, титруемых
перманганатом.
70 г MnS04-7H20 растворяют в
400 мл воды, приливают к раствору
130 мл концентрированной H2SCy
охлаждают, вливают 140 мл
фосфорной кислоты (1,70), разбавляют
водой до 1 л. MnS04 можно
заменить 50 г МпС1,-2НоО или
раствором 30 г МпСОз в "100 мл HaSO«
(1 : 6).
Соль Мора
FeSCv(NH4)aS04.6H20, M = 392,14
Голубовато-зеленые кристаллы,
плотность 1,87, при хранении не
изменяется. При 100е С теряет
кристаллизационную воду. 10 или 15%-
ные растворы: 100 или 150 г
препарата растворяют в 500 мл раствора
H2S04 (1 : 10 или 1 : 7), разбавляют
водой до 1 л, фильтруют.
Соль Рейнеке
NH, [Cr (NH3)2 (SCN)J,
М = 354,439
Красные кристаллы, при 100—
120е С теряют воду, при
дальнейшем нагревании разлагаются.
Хорошо растворимы в воде, этаноле,
эфире с образованием красных
растворов. В водном растворе
постепенно разлагается с выделением
HCN!!
1%-ный раствор 1 г соли
растворяют при нагревании до 50—60° С
в 100 мл 0,6М НС1, фильтруют.
Раствор применяют при
определении меди, кадмия и др.
Сурьма (V)
пятихлористая
SbClB, М = 292,02
Бесцветная или слабо-желтая
жидкость, плотность 2,39. Дымит на
5 А. И. Лаварев и др.
65
воздухе. Затвердевает на воздухе
при +49 С, кипит при 140° С с
частичным разложением на SbCl3 и С12.
На воздухе поглощает влагу и
затвердевает, образуя гидрат. В
вакууме перегоняется без разложения.
Применяют 0,5%-ный раствор в 4М
НС1,
Сурьма
(треххлористая)
SbCl», M = 228,11
Кристаллы, дымят на воздухе,
жадно ■ поглощая воду. Растворяются
в абсолютном этаноле; легко
растворимы в растворах НС1, винной
кислоты. Едко действует на кожу.
Смесь Эшке
Белый рыхлый порошок,
состоящий из смеси MgO и Na2C03,
свободных от серы, в соотношении 2:1.
(Рекомендуются и смеси других
составов, например MgO + Na C03 =
= 1:1; 1 :4-)
Титан (III)
сернокислый
Применяют в качестве
восстановителя при фотометрическом
определении вольфрама.
Хром (II) хлористый
СгС12-4Н20, М = 194,96
Прозрачные синие кристаллы,
хорошо растворимые в воде. Растворы—
энергичные восстановители,
поглощают кислород из воздуха и
окрашиваются в зеленый цвет. Растворы
применяют для восстановления
соединений U, W, V, Мо и т. д. .
Раствор Сг (II) получают путем
взбалтывания 5%-ной К2Сг207 в HCI
с амальгамой цинка до получения
раствора темно-синего цвета, б. 20 г
К2Сг207 нагревают со 150 мл
концентрированной HCI, кипятят до
удаления хлора, охлаждают, переносят
в колбу, добавляют стружки цинка.
Колбу закрывают пробкой с
клапаном Бунзена, оставляют стоять
до получения светло-голубого
раствора.
Раствор CrS04: 50 г Cr2 (S04)3-
•18Н20 в 1 л 1,5М H2S04
восстанавливают металлическим кадмием
или амальгамой цинка.
Цинка окись ZnO,
М = 81,37
Белый порошок с желтоватым
оттенком, плотность 5,42. В воде
растворяется незначительно. Растворим
в растворах кислот, щелочей,
аммиака, ядовит. Применяется в качестве
суспензии для отделения марганца
от других элементов.
ZnO прокаливают при 800° С и
испытывают на содержание Мп, 25 г
ZnO растирают в ступке с 25 мл
воды до густой консистенции,
добавляют 70—80 мл воды и перемешивают
до легко переливающейся массы.
Приготовленную суспензию хранят
в закрытой колбе. Аммиачный
раствор: осаждают Zn(OH)2 из соли
ZnCl2 раствором щелочи,
отфильтровывают, промывают водой,
растворяют в небольшом избытке аммиака.
Раствор устойчив в закрытой склянке.
10. РАЦИОНАЛЬНЫЙ АССОРТИМЕНТ
ОРГАНИЧЕСКИХ РЕАКТИВОВ ДЛЯ ОПРЕДЕЛЕНИЯ
НЕОРГАНИЧЕСКИХ ИОНОВ (ИРЕА, МОСКВА)
В зависимости от определяемого
элемента применяются
соответствующие реактивы и методы анализа
[приняты следующие условные
обозначения: гравиметрическое
определение (1), титриметрическое (2), спек-
трофотометрическое (3), люминис-
центное (4)1:
N — пирозалоновый реактив (3),
фенол (3), для NH+; нитрон
(1), дифениламин (3),
салициловая кислота (3), фенол-
2, 4-дисульфокислота (3) для
NOj, сульфаниловая
кислота -f 1-нафтиламин (3) для
NO;;
66
А1 — 8-оксихинолин (1), 2-окси-
3-нафтойная кислота (2),
ПАН (2), ализариновый
красный (3), алюминон (3),
алюмокрезон (3), стильба-
зо (3), сульфохром (3), хро-
мазурол S (3), салицилаль-
о-аминофенол (4), эриохром-
циапин R (3);
Ва - флуорексон (2), хлорфосфо-
назо III (3);
Be — 2,2'-диметилгександион-3,5
(1), 2-окси-1-нафтальдстид
(1), бериллон II (3), хлор-
фосфоназо III (3), морин
(4), 2-окси-З-нафтойная
кислота (4);
В — маннит (2), Аш-резориин ди-
натриевая соль (3), 1,1'-
диантримид (3), куркумин
(3), хинализарин (3),
бензоин (4), бутиловый эфир
родамина С или В (4)
Вг — дифенилкарбазон (2), мета-
ниловый желтый (2), 2-ни-
трозо-1 -нафтол (2), эозин
(2), феноловый красный (3),
фуксин (3);
V — диантипирилфенилметан (1),
купферон (1),
дифенилкарбазон (2), пирокатехиновый
фиолетовый (2), N-фенилан-
траниловая кислота (2),
алюминон (3), ванадокс (3),
8-оксихинолин (3), сульфо-
назо (3), N-фенилбензгидро-
ксамовая кислота (3);
Bi — ксиленоловый оранжевый
(2,3), пирокатехиновый
фиолетовый (2), дитизон (3), N,
N' -диэтилдитиокарбаминат
натрия (3), тиомочевина (3);
W — амидопирин (1), (3-нафтохи-
нолин (1), 8-оксихинолин
(1, 3), гидрохинон (3), ди-
тиол (комплекс с цинком)
(3);
Gd - салицнлфлуорон (1),
щавелевая кислота (1),
ксиленоловый оранжевый (2), арсе-
назо III (3);
Ga — диаптнпирилпропнлметан
(1, 2), ПАН (2), галлион (3),
люмогаллион (4), родамин С
(4);
Hf - миндальная кислота (1), фе-
ниларсоновая кислота (1),
кислотный хромчерный
специальный (2), ксиленоловый
оранжевый (2, 3), арсена-
зо 1 (1), морин (4);
Ge — 8-оксихинолин (1),
пирокатехин (2), резарсон (3, 4),
фенилфлуорон (3)
Но — салицнлфлуорон (1),
щавелевая кислота (1),
ксиленоловый оранжевый (2), арсе-
назо III (3)
Dy — салицнлфлуорон (1),
щавелевая кислота (1),
ксиленоловый оранжевый (2), арсе-
назо III (3), 1-(п-сульфофе-
нил)-3-метилпиразолон-5 (4);
Ей — салицилфлоурон (1),
щавелевая кислота (1),
ксиленоловый оранжевый (2), арсена
зо III (3), о-фенантролин -,-
-f- салициловая кислота (4),
о-фенантролин теноилтриф-
торацетон (4),
о-фенантролин -f- 2-фенилцинхонино-
вая кислота (4);
Fe — 5,7 - Дибром-8 - оксихинолин
(1), купферон (1), вариами-
новый голубой (2),
ксиленоловый оранжевый (2),
сульфосалициловая
кислота (2, 3), фенилантранило-
вая кислота (2), ферроин (2),
алюмокрезон (3), батофенан-
тролин (3), 2,2' -дипиридил
(3), тирон (3),
о-фенантролин (3), стильбексон (4);
Аи — тиогликолевая кислота (1),
щавелевая кислота (1),
аскорбиновая кислота (2),
гидрохинон (2), дитизон (2),
5- (п-диметиламинобензили-
ден)-роданин (3), пикрами-
новая кислота (3);
In — N, N'-диэтилдитиокарбами-
натнатрия (1), ксиленоловый
оранжевый (2), ПАН (2),
родамин С (3,4), родамин 6Ж
(4);
I — крахмал растворимый (2,3),
бриллиантовый зеленый (3)
для 12, таннин (3) для Ю;;
метаниловый желтый (2),
эозин (2) для I" ;
1г — гидрохинон (1,2), диантипи-
рилпропилметан (1),
тиомочевина (1), аскорбиновая
кислота (2), кристалличе.
скии фиолетовый (лейкоос-
нование) (3), ПАН (3);
Yb — салицилфлуорон (1),
щавелевая кислота (1), ксилено-
ловый оранжевый (2), арсе-
назо III (3);
Y — салицилфлуорон
(^.щавелевая кислота (I), арсеназо 1
(2,3), ксиленоловый
оранжевый (2), ализариновый
красный С (3), арсеназо III (3);
Cd — диантипирилметан (1), 0, 0-
диэтилдитиофосфат никеля
(I), кислотный хром черный
специальный (2), сульфар-
сазен (2,3), бромбензтиазо
(3), дитизон (3), хромпира-
зол II (3), 8-(бензолсуль-
фаниламино)-хинолин (4);
К — ди пир кил амин (1), тетрафе-
нилборат натрия (1);
Са — щавелевая кислота (I), ги-
дрон II (2), глиоксальбис-
-(2-оксианил) (2,3), каль-
цион (2,3), кислотный хром
темно-синий (2), флуорек-
сон (2, 4), азо-азоокси БН
(3);
О — крахмал растворимый (2),
индигокармин (3);
Со — ксиленоловый оранжевый
(2), 1-нитрозо-2-нафтол (3),
2-нитрозол-1-нафтол (3), ни-
трозо-Р-соль (3), ПАР (3),
рубеановодородная
кислота (3), салицилфлуорон (4);
Si — желатин (I), 1-амино-2-наф-
тал-4-сульфокислота (3),
аскорбиновая кислота (3);
La — салицилфлуорон (1),
щавелевая кислота (I),
ксиленоловый оранжевый (2),
арсеназо III (3);
L — нитроантранилазо (3) то-
рон (3);
Lu — салицилфлуорон (1),
щавелевая кислота (I),
ксиленоловый оранжевый (2),
арсеназо III (3);
Mg — 8-оксихинолин (I),
кислотный хром темно-синий (2),
кислотный хром черный
специальный (2), магнезон ХС
(2,3), феназо (3), N, N'-ca-
лицилальэтилендиамин (4),
люмомагнезон (4);
Мп — кислотнбгй хроти черный
специальный (2), метилтимоло-
вый синий (2), пирокатехи-
новьгй фиолетовый (2), N,
N'-диэтилдитиокарбаминат
натрия (3), формальдок-
сим (3), люмомагнезон (4);
Си — а-бензоиноксим (I), люми-
нор светло-зеленый 4961 (I),
2-меркаптобензотиазол (1),
8-оксихинолин (I), салици-
лальдоксим (I), хинальди-
новая кислота (I), мурексид
(2), ПАН (2), тетра (2),
бис - (циклогексанон) - окса-
лил-дигидразон (3), 2,9-ди-
метил-1,Ю-фенантролин (3),
8,8'-дихинолилдисульфид
(3), 2,2'-дихинолил (3), 2,2'-
дицинхониновая кислота,
N, N'-диэтилдит-иокарбами-
нат натрия (3), о-толидин
(3), люминол (4), люмокуп-
ферон (4), флуорексон (4);
Мо — а-Бензоиноксим (I),
8-оксихинолин (1, 2), дитиол
(комплекс с цинком) (3), дифе-
нилкарбазон (3);
As — кислотный хром черный
специальный (2), N, N'-диэтил-
дитиокарбаминат Ag (3);
Nd — салицилфлуорон (I),
щавелевая кислота (1),
ксиленоловый оранжевый (2),
арсеназо III (3);
IMS—диметилглиоксим (1,3), ци-
клогександион-1,2 - диоксим
(I), мурексид (2), сульфарса-
зен (2), а - бензилдиоксим
(3), ПАН (3), а-фурилдиок-
сим (3);
Nb — купферон(1), пироллидинди-
тиокарбаминат аммония (I),
таннин (I), фениларсоновая
кислота (I), N-фенилбензги-
дроксамовая кислота (I),
кислотный хром фиолетовый
К (3), ксиленоловый
оранжевый (3), ортонитрофенил-
флуорон (3), ПАР (3), суль-
фохлорфенол С (3);
Sn — ксиленоловый оранжевый
(2), дитиол (комплекс с
цинком) (3), п-нитрофенилфлуо-
рон (3);
Os — бензтриазол (1), тетрафенил-
арсония хлорид (I), тетра-
68
фенилфосфония бромид (1),
селеномочевина (3),
тиомочевина (3);
Pd - 5-бромбензтрназол (1), ди-
метилглиотссим (1), Р-фур-
фуральдоксим (1), цикло-
гександион-1,2-диоксим (1),
8-меркаптохинолин (3), 4-
нитрозо- N, N'-диметил-
анилин (3), п-нитрозодифе-
ниламин (3), 2-нитрозо-1-
нафтол (3), ПАН (3), ех-
фурилдиоксим (3);
Pt — висмутол II (1), гексамети-
лен-бис-(триметил аммоний
хлористый) (I), дитизон (2),
N, N'-дибензилдитиоокса-
мид (3), 5-( п-диметиламин-
бензилиден)-роданин (3);
Рг — салицилофлуорои (I),
щавелевая кислота (I), ксилено-
ловый оранжевый (2), арсе-
назо III (3);
Re — нитрон (I), тетрафениарсо-
ния хлорид (I), метиловый
фиолетовый (3), тиомочевина
(3), а-фурилдиоксим (3);
Rh — 2-меркаптобензимидазол (I),
тиомочевина (I), тионалид
(1,2), пиперидиндитиокар-
баминат натрия (2), 2-мерка-
тобензоксазол (3), 4-нитро-
зо-N, N'-диметиланилин (З),
ПАН (3);
Hg — ксиленоловый оранжевый
(2), сульфарсазен (2,3),
дитизон (3), тиурамат меди
(3);
Rb - дипикриламин (1), тетрафе-
нилборат натрия (I);
Ru ~ тиомочевина (1,3), тионалид
(1), гидрохинон (2), 4-ни-
трозо-N, N'-диметиланилин'
(3), рубеановодородная
кислота (3);
Sm — салицилфлуорон (1),
щавелевая кислота (1),
ксиленоловый оранжевый (2), арсе-
назо Ш(3),о-фенантролин +
-f теноилтрифторацетон (4);
РЬ — кислотный хром черный
специальный (2),
ксиленоловый оранжевый (2),
сульфарсазен (2,3), арсазен (3),
дитизон (3);
Se -- аскорбиновая кислота (1),
3,3'-диаминобензидин (3,4),
дитизон (3), 2,3-диамино-
нафталин (4);
S — карбоксиарсеназо (2), нит-
хромазо (2), флуорексон (2),
хлорфосфоназо III (2),
салицилфлуорон (комплекс
с торием) (4) для SO2-; диэти-
ламин гидрохлорид (3) для
CS2; N, N'-диметил-п-фени-
лендиамин дигидрохлорид
(3); тетрартутьацетатфлуо-
ресцеин (4) для S2""; фуксин
(3) для S02 и SOt;
Sc — винная кислота (1),
фитиновая кислота (1), мурексид
(2), ализариновый красный
С (3), ксиленоловый
оранжевый (3), пропилфлуорон
(3), сульфоназо (3);
Sr — метилтимоловый синий (2),
хлорфосфоназо III (3);
Sb — кристаллический
фиолетовый (метиловый фиолетовый)
(3), фенилфлуорон (3);
Т1 — диантипирилметан (1),
тионалид (1), ПАН (2),
метиловый фиолетовый (3), родамин
6Ж (4), родамин С (4);
Та — Купферон (1), таннин (1),
фениларсоновая кислота (1),
N - фенилбензгидроксамовая
кислота (1), диметилфлуо-
рон (3), метиловый
фиолетовый (3), пирогаллол (3),
родамин 6Ж (4);
Те — N, N'-диэтилдитиокарбами-
нат натрия (3), диантипирил-
про пилметан (3),
тиомочевина (3), бутиловый эфир
родамина С (4);
ТЬ — салицилфлуорон (1),
щавелевая кислота (1),
ксиленоловый оранжевый (2), арсе-
назо III (3), 1-(п-сульфофе-
нил)-3-метилпиразолон-5
(4), о-фенантролин -}-
салициловая кислота (4);
Ti -— 5,7 - дибром-8 - оксихинолин
(1), купферон (1), п-окспфе-
ниларсоновая кислота (1),
N -фенилбензгидроксамовая
кислота (1),
диантипирилметан (3), дисульфофенил-
флуорон (3), 2,7-дихлорхро-
мотроповая кислота (3), хро-
мотроповая кислота (3);
69
Th — фитиновая кислота (1),
щавелевая кислота (1), ксиле-
ноловый оранжевый (2), пи-
рокатехиновый. фиолетовый
(2), арсеназо I (3), а также
арсеназо III (3), торон I (3);
Тт — салицилфлуорон (1),
щавелевая кислота (1), ксилено-
ловый оранжевый (2),
арсеназо III (3);
С — дитизон (2), мурексид (2),
пирокатехиновый
фиолетовый (2) для CN-; 5-(Г-суль-
фо-8'-нафтилазо) - 8 - оксихи-
нолин (2), пиридин -f суль-
фаниловая кислота (3) для
CN" и SCN-; бромкрезоло-
вый пурпуровый (2), тропео-
лин 000 (2) для SCN";
U — купферон (1), 8-оксихино-
лин (I), арсеназо I (2),
арсеназо III (3), дибензоил-
метан (3), тиогликолевая
кислота (3), хлорфосфона-
зо III (3);
Р — кислотный хром черный
специальный (2), 8-оксихино-
лин (2), 1-амино-2-нафтол-4-
сульфокислота (3),
аскорбиновая кислота (3);
F — ализариновый красный С
(2,3), арсеназо I (2,3),
кислотный хром черный
специальный (2), ксиленовый
оранжевый (2), метил-
тимоловый синий (2),
ализарин-комплексон (3),
сульфохром (3);
С1 — бромнитрозол (2), дифенил-
карбазон (2,3), 2,7-дихлор-
флуоресцеин (2), метанило-
вый желтый (2) для
СГ; метиловый оранжевый
(2), о-толидин (3) для>С12;
Сг — ксиленоловый оранжевый
(2), N-фенилантраниловая
кислота (2), 1,5-дифенил-
карбазид (3), этилендиамин-
N, N, N', N'-тетрауксусная
кислота (3), триазинил—
стильбексон (4);
Cs — дипикриламин (1), тетрафе-
нилборат натрия (I);
Се — салицилфлуорон (1),
щавелевая кислота (1),
ксиленовый оранжевый (2),
арсеназо III (3), о-толидин (3),
тирон (3);
Zn — 8-оксихинолин (1),
кислотный хром черный
специальный (2), ксиленоловый
оранжевый (2), сульфарсазен
(2,3), дитизон (3), хромпи-
разол (3), 8-(п-толуолсуль-
фониламино)-хинолин (4);
Zr — миндальная кислота (1), фе-
ниларсоновая кислота (1),
кислотный хром черный
специальный (2), ксиленоловый
оранжевый (2,3), арсеназо I
(3), арсеназо III (3), морин
(4);
Ег — салицилфлуорон (1),
щавелевая кислота (I),
ксиленоловый оранжевый (2),
арсеназо III (3).
11. ИНДИКАТОРЫ
11. 1. ИНДИВИДУАЛЬНЫЕ КИСЛОТНО-ОСНОВНЫЕ ИНДИКАТОРЫ
Интервал рН
1
0,0—1,3
0.0—1.6
0,0—2,0
0,0—2,0
Переход окраски
2
Бесцветная — желтая
Розовая — желтая
Зеленая — синяя
Желтая — голубовато-
зеленая
Индикатор
3
Пикриновая кислота
Ализариновый синий АВ
(1-й переход)
Красно-фиолетовый 5Р
экстра
Малахитовый зеленый
(1-й переход)
Растворитель
4
Вода
»
•а
Концентрация, %
5
р о р о
70
Продолжение
1
0,0—2,6
0,0-2,6
0,0—4,0
0,1-0,5
0,1-1,2
0,1-2,0
0,2—0,8
0,2-1,8
0,3—1,0
0,3—2,0
0,5-2,0
0,5-2,0
0,6—2,8
1,0—1,5
1,0-2,0
1,1—2,8
1,2-2,3
1,2-2,8
1,2-3,0
1,2-3,2
1,3-4,0
1,4—2,6
1,4—2,6
1,6—3,6
1,9-3,1
1,9-3,3
1,9-3,3
2,0-2,5
2,3—3,3
2,4-4,0
2,4-4,5
2
Желтая — коричневая
Желтая — зеленая
Желтая — оранжевая
Желтая — зеленая
Оранжевая — розовая
Зеленая — голубая
Розовая — оранжевая
Красная — желтая
Синяя — красная
Желтая — синяя
Зеленая — синяя
Красная — желтая
Пурпурная — янтарно-
желтая
Зеленая — синяя
Бесцветная — красная
Пурпурная — желтая
Красная — желтая
Красная — желтая
Пурпурная — бледно-
пурпурная
Красно-фиолетовая —
бесцветная
Фиолетовая —
оранжевая
Розовая — желтая
Фиолетовая —
оранжевая
Красная — желтая
Оранжевая — красная
Красная — желтая
Красная — желтая
Снняя — фиолетовая
Розовая — желтая
Бесцветная — желтая
Красная — зеленая
3
Галлеин (1-й переход)
Бриллиантовый зеленый
Пурпурин (1-й переход)
Метиловый фиолетовый
(1-й переход)
Родамин С (Б)
Метиловый зеленый
Пирокатехинсульфофта-
леин
Крезоловый красный
(1-й переход)
Сафранин (1-й переход)
Этиловый зеленый
Кристаллический
фиолетовый
Крезоловый пурпурный
Ксиленоловый синий
(1-й переход)
Метиловый фиолетовый
(2-й переход)
Хинальдиновый красный
Б ензол азодифен и л ам ин
■Метаниловый желтый
Тимоловый синий (1-й
переход)
Фуксин основание
Пентаметоксн красный
Бензопурпурин 4Б (2-й
переход)
Тропеолин 00
Бензол азофенил-а-наф-
тиламин
2-Бром-4' -диметиламино-,
азобензолсульфокисло-
та-4
Крезоловый красный (1-й
переход)
Ализариновый желтый Р
(1-й переход)
Бензиловый оранжевый
Метиловый фиолетовый
(3-й переход)
Бензолазобензил анилин
Р-Динитрофенол
Сок красной капусты
4
50%-ный
этанол
Вода
50%-ный
этанол
Вода
50%-ный
этанол
Вода
»
50%-иый
этанол
Вода
20% -ный
этанол
Вода
20%-ный
этанол
20%-ный
этанол
Вода
50%-ный
этанол
То же,
с
добавлением 1 мл
1 М НС1
на 100 мл
раствора
Вода
20% -ный
этанол
70%-ный
этанол
То же
Вода
»
»
»
50%-ный
этанол
Вода
Вода
50%-ный
этанол
Вода
»
5
0,1
0,1
0,1
0,05 и
0,1
0,1
0,05
0,1
0,04
0,1
0,1
0,1
0,1
0,04
ОД
0,1
0,01
0,1
0,1
ОД
0,1
0,1
1,0; 0,1;
0,01
0,1
0,1
0,1
0,1
0,05
ОД
0,1
0.1; 0,05;
0,04
1,0
71
Продолжение
1
2,&-4,6
2,8—4,4
2,9-4,0
3,0—4,6
3,0-4,4
3,0-5,2
3,1—4,4
3,2-4,8
3,5-4,5
3,6—6,0
3,6-7,0
3,7-5,0
3,7—5,2
3,8-5,4
3,9-5,5
3,9—5,9
4,0—5,4
4,0-6,4
4,0—7,0
4,0—7,0
4,0-8,0
4,3-6,3
4,4-5,5
4,4-6,2
4,5-6,5
4,6-6,8
5,0—6,0
5,0—6,6
5,0—7,0
5,0—8,0
2
Красно-розовая
бесцветная
Бесцветная — желтая
Красная — желтая
Желтая —
сине-фиолетовая
Красная — оранжево-
красная
Сине-фиолетовая —
красная
Красная — оранжево-
красная
Желтая — синяя
Розовая — желтая
Розовая — фиолетовая
Коричневая — розовая
Красная — желтая
Желтая — буро-розовая
Желтая — синяя
Снняя — оранжевая
Бесцветная — желтая
Бесцветная — желтая
Красная — синяя
Желтая — зеленая
Оранжевая — желтая
Оранжевая — розовая
Бесцветная — желтая
Красная — синяя
Красная — желтая
Бесцветная — розовая
Оранжевая — розовая
Желтая — фиолетовая
Желтая — красная
Бесцветная — желтая
Красная — синяя
3
Гексаметоксикрасный
а-Динитрофенол
Метиловый желтый
Бромфеноловый синий
Метиловый оранжевнй
Конго-красный
Метиловый пурпурный
Бромхлорфеноловый
синий
Этиловый оранжевый
Красно-фиолетовый 5РС
Галлеин (2-й переход)
а-Нафтоловый красный
Ализариновый красный S
Бромкрезоловый
Оксиновый синий
8-Динитрофенол
у-Динитрофенол
Лакмонд
Пирокатехннсульфофта-
леин (2-й переход)
Хризоиднн
Пурпурин (2-й переход)
а-Динитрофенол
Лакмазол
Метиловый красный
Иодэозин
Карминовая кислота
(1-й переход)
Гематоксилин
Хлорфеноловый красный
о-Динитрофенол
Азолитмин
4
50% -ный
этанол
Этанол;
вода
90% -ный
ьтанол
20%-ный
этанол;
0,002 М
NaOH
в воде
Вода
»
50%-ный
этанол
20% -ный
этанол;
0,002 М
раствор
NaOH
в воде
Вода
»
50%-ный
этанол
70%-ный
этанол
Вода
20% -ный
этанол;
0,002 М
раствор
NaOH
в воде
50%-ный
этанол
Вода
»
Этанол
Вода
»
50%-ный
этанол
Вода
»
60%-ный
этанол
Вода;
70%-ный
этанол
Вода
90%-иый
этанол
20%-ный
этанол
50%-ный
этанол
То же
5
0,1
0,1; 0,04
и
насыщенный
0,1 и 0,01
0,1
0,1
0,1 и 1,0
0,1
0,04
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,2
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,5
0,1
0,1
0,1
72
Желтая — пурпурная
Желтая — красная
Желтая — красная
Синяя — фиолетовая
Бесцветная — желтая
Желтая — синяя
Желтая — синяя
Желтая — зеленая
Желтая — зеленая
Красная — желтая
Желтая — синяя
Красная — желтая
Желтая — красная
Бесцветная — желтая
Бесцветная — зеленая
Бесцветная —
фиолетовая
Синяя — розовая
Янтарно-желтая —
пурпурно-красная
Бесцветная —
сине-зеленая
Оранжевая — желтая
Желтая — буро-красная
Желтая — синяя
Желтая — пурпурная
Желтая — фиолетово-
синяя
Бесцветная — красная
Бесцветная — красная
Желтая — зеленая
Фиолетовая — синяя
Бесцветная — синяя
Бесцветная — синяя
Розовая — пурпурная
Фиолетовая — бледно-
желтая
Синяя — красная
Бледно красно-желтая
оранжевая
Бромкрезоловый
пурпурный
Бромфеноловый красный
Ализарин (1-й переход)
Индулин спиртораствори-
мый
п- Нитрофенол
Бромтимоловый синий
Бромксиленоловый синий
Ализариновый снннй АВ
(2-й переход)
Ализариновый синнй БС
(1-й переход)
Розоловая кислота
Нитразиновый желтый
Нейтральный красный
Феноловый красный
М-Динитрофенол
Гваяколовая настойка
Хннолиновый снний
Нильская голубая 2Б
Крезоловый красный
(2-й переход)
а-Нафтолфталеин
Тропеолин 000 (1-й
переход)
Куркумин (1-й переход)
Тимоловый синнй
Крезоловый пурпуровый
(2-й переход)
Кснленоловый синий
(2-й переход)
о- Крезолфталеин
Фенолфталеин
(2-й
а-Нафтолбензоин
переход)
Пирокатехинсульфофта-
леин (3-й переход)
п- Кснленолфталеин
Тимол фтал ей н
Галлеин (3-й переход)
Ализариновый красный S
(2-й переход)
Нильский голубой А
Ализариновый желтый
Р
73
Продолжение
1
10,1—12,1
10,2—11,8
10,2—12,5
10,3—12,0
11,0—13,0
11,0—13,0
11,0—13,0
11,0—13,5
11,0—14,0
11,5—13,2
11,6—14,0
12,0—13,4
12,0—14,0
12,2—14,0
2
Фиолетовая — пурпурная
Буро-красная —
оранжево-желтая
Синяя — зеленая
Желтая — красная
Оранжево-желтая —
зелено-синяя
Желтая — оранжевая
Зеленая — синяя
Зеленая — бесцветная
Фиолетовая — розовая
Бесцветная — оранжевая
Синяя — желтая
Бесцветная — оранжево-
красная
Лиловая — фиолетовая
Бесцветная — оранжевая
3
Ализарин (2-й переход)
Куркумин (2-й переход)
Пирокатехинсульфофта-
леин (4-й переход)
Тропеолнн 000 (2-й
переход)
Ализариновый синий
Тропеолин 0
Ализариновый снний БС
(2-й переход)
Малахитовый зеленый
Карминовая кислота (2-й
переход)
2,4,6-Тринитроголуол
Индигокармин
1,3,5-Трннитробензойная
кислота
Пурпурин (3-й переход)
1,3,5-Тринитробензол
4
50%-ный
этанол
90%-ный
этанол
Вода
»
»
»
»
»
»
90% -ный
этанол
50%-ный
этанол
Вода
50%-ный
этанол
Этанол
5
0,1
0,1
0,1
0,1
0,1
0,1
0,05
0,1
0,1
0,1
0,1
0,1
0,1
0,1
И. 2. ИНДИКАТОРЫ ДЛЯ КОМПЛЕКСИМЕТРИЧЕСКОГО ТИТРОВАНИЯ
Индикатор
1
Бромпирогалло-
вый красный
Вираминовый
голубой
З,3'-Диметил на-
фтндин
Кальконкарбоно-
вая кислота
Ксиленоловый
оранжевый
Метилтимоловый
синий
Определяемый
металл
2
РЗЭ
Bi
Pb
Cd, Co, Mn, Mg, Ni,
Pd, Tl, Fe, In, Ga,
V, Cu, Th
Fe
Zn, Al, Cd, Cu, Fe,
Ni, Pb
Ca
Zn, Ca, Cd, Ce, Co,
Cu, Fe, In, Mn, Ni,
Pb
Ba, Ca, Cd, Mg, Mn,
Pb, Sr, Zn, Bl, Co,
Cd, Hg, ba, Pb, Sc,
Th, Zn
pH
3
6—7
2—3
4
7—8
2—3
5
>12
9—10
11,5—
12,5
3—5
Изменение окраски
4
Синяя — красная
Красная — желто-
оранжевая
Сине-фиолетовая — красная
Сине-фиолетовая — желтая
Фиолетовая —
бесцветная
Винно-красная —
голубая
Снняя — красная
Синяя — серая
Синяя — серая
Раствор
индикатора
'5
0,5% -ный в
50%-иом этаноле
1%-ный в воде
1%-ный в уксусноС
кислоте
Твердая смесь с
Na2S04 (1 : 100)
0,13 г в 2 мл 1-н.
NaOH и
разбавленный водой до
100 мл
Твердая смесь о
KNO„ (1 : 100) или
0,1%-иый в воде
74
Продолжение
1
Мурексид
ПАН
1-(пиридил-2)-азо-
нафтол
ПАР
4-(пиридил-2)-
-азорезорцин
натриевая соль
Пирокатехиновый
фиолетовый
Сульфосалицило-
вая кислота
Тайрон Пирокате-
хин-3,5-дисулъфо-
кислота динатрие-
вая соль
Флуорексон (калъ-
цеин)
Фталеинкомплек-
сон
Хромазурол S
Цинкон
2
Са, Со, Си, Ni, Ag,
Pd, WOi", Br, C1-,
Г, CN"
Cd, Си, Tl, Zn, Ce,
Fe, Ga, In, Ni, Pb,
Sc, Ca, Co, Hg, Mg,
Mn, V
Cd, Си, Ti, Zn, Ce,
Fe, Ga, In, Ni, Pb,
Sc, Ca, Co. Hg, Mq,
Mn. V
Bi
Th
Cd, Co, Mg, Mn, Zn
Fe
Fe
Ca, Sr, Ba
Ba, Sr, Ca, Mg, S2" .
SO§-, SOr. CrOj"
Ai
Си
Fe
Zr
Ca, Cd, Ce, Co, Си,
Fe, In, Mn, Ni, Pb,
Zn
,3
12—12,5
<6
5
2—3
2—3
10
2—3
2—3
<12
>11
4
6—6,5
3
2
9—10
4
Красная —
фиолетовая;
желтая — фиолетовая
Красная —
желтая
Желтовато-красная — зеленая
Голубая —
желтая
Красная —
желтая
Голубая —
красно-фиолетовая
Красная —
желтая
Синяя — желто-
зеленая
Желто-зеленая
флуоресценция —
розовая до
бесцветной
Красно-фиолетовая — светло-
фиолетовая
Фиолетовая —
оранжевая
Голубая —
зеленая
Зелено-голубая —
золотисто-оранжевая
Кр асно-фиолето-
вая — оранжевая
Синяя — красная
5
Твердая смесь с
NaCl (1 : 100)
0,01—0,1%-ный в
этаноле
0,1%-ный в воде
0,1%-ный в воде
5%-ный в воде
2%-ный в воде
Твердая смесь с
KNOj, (1 i 100)
0,1 г в 5 мл
10%-ной NH4OH +
-f- 95 мл воды.
Устойчив в неделю
0,1—0,4%-ный в
воде
0,13 г в 2 мл 1-н.
NaOH и
разбавлено до 100 мл
водой
75
Продолжение
1
Эриохром сине-
черный В
Эриохром
черный Т
2
Са, Mg
Cd, In, Mg, Pb, Zn,
РЗЭ, Al, Co, Ga,
Ni, Са, Мп, Те, Hg,
Na, F", POf
3
10—11
10—11
7
4
Красная-снияя
Винно-красная—
голубая
Красная —
голубая
s
2%-ный в воде ■
Твердая смесь с
NaCl (1 : 100)
11. 3. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ИНДИКАТОРЫ,
ОКРАСКА КОТОРЫХ МАЛО ЗАВИСИТ ОТ рН И ИОННОЙ СИЛЫ РАСТВОРОВ
Е0, В
+ 1,33
+ 1.26
+ 1,25
(в 1 и.
H2S04)
+ 1,14
+ 1,12
+ 1.1
+ 1,09
+ 1,09
+1,08
+ 1,08
+ 1,06
+ 1,06
+ 1,06
+ 1,06
+ 1,03
+ 1,02
+ 1,01
+0,01
+ 1,01
+ 1,0
Окравка формы
окисленной
2
Бесцветная
Бледно-фиолетовая
Бледно-голубая
Бледно-голубая
Бледно-фиолетовая
Красно-фиолетовая
Красная
Бесцветная
Красно-фиолетовая
Красная
Бледно-голубая
Фиолетовая
Красная
Бледно-розовая
Оранжево-крас-
Оранжево-крас-
*
»
Бледно-розовая
Бледно-желтая
восстановленной
Желтая
Бесцветная
Красная
То же
Бесцветная
То же
Желто-зеленая
Красная
Бесцветная
Бесцветная
Красная
Бесцветная
Желто-зеленая
Желто-зеленая (в
нейтральной
среде —
темно-синяя)
Желто-зеленая
Желто-зеленая
»
»
Желто-зеленая (в
нейтральной
среде — темно-сине-
зеленая)
Красная
Индикатор
2,2'-Дипирндил (комплекс с Ru).
Применяется в 1 М растворах НЫОз
О,0'-Дифениламнноднкарбоновая
кислота. Применяется в 7,5—10 М
растворах H2S04
Нитро-фенантролин + FeS04. Резкий
переход окраски прн Е0 = +1,31 В
2,2'-Дипиридил (комплекс с Fe2+).
Применяется в 1 М H2S04
0,М-Дифениламнноднкарбоновая
кислота. Применяется в 7,5—10 М
растворах H2S04
я-Амннодифеииламнн
Ксиленоловый синий ВС
Порфирексид = порфирекснн. Е0 =
= 0,83 В при рН = 5,0; Е„ = 0,73 В
при рН = 7,0
Фенилантраниловая кислота. 0,2% -ный
раствор в 0,2%-ном растворе Na2C03
2,4-Днаминодифениламин
0-Фенантролин + FeS04 (Ферроин).
Резкий переход окраски при Е0 —
= 1,20 В
я-Нитродифениламин
Сетополин Ж
Сетогеюиин Ж
Цианол прочный зеленый 2Ж
Ксиленоловый синий АС
Акронол Бриллиантовый БДЦ
Цианин Б
я-Этоксихризоидин при рН= 0
76
Продолжение
I
+0,99
+0,9°
+0,99
+0,97
+0,94
4-0,92
+0,87
+0.85
+ 0,84
+0,8
+0,76
-4-0Л;
+0,/
+0,23
+0,21
+0,11
+0,06
+0,01
2
Оранжевая
»
»
Желто-зеленая
Бесцветная
Желтая (в
нейтральной среде —
темно-синяя)
Желтая (в
нейтральной
среде —
зелено-синяя)
Красная
Красно-фиолетовая
Бесцветная
Фиолетовая
»
Оранжево-красная
Голубая
Снняя (рН > 8,5)
или красноватая
(рН < 8,5)
Сине-фиолетова я
Фиолетовая
Голубая
3
Желтая (в
нейтральной среде —
синяя)
Желто-зеленая (в
нейтральной
среде — зеленовато-
синяя)
Желто-зеленая
(в нейтральной
среде — снняя)
Красная
Интенсивно-синяя
Бесцветная
»
»
»
Красная
Бесцветная
»
Желтая (в
нейтральных и
слабокислых
растворах — синяя)
Бесцветная
»
»
»
»
4
Ксиленцианол 2Ф
Патентный синий А
Эриоглюцин А
5,6-Диметнл-1,10-фенантролин
(комплекс с Fe2+)
Порфиринднн. £0 = 0,67 В при рН =
= 5,0; £„ = 0,57 В прн рН = 7,0
Бензндин. £0 = 0,86 В при рН = 1.0;
£0=0,80 В при рН = 2,0; £0 =
= 0,74 В при рН = 3,0
0-Толидин. £„ =0,81 В при оН =
= 1,0; £0=0,75 В при рН = 2,0;
£„ = 0,69 В при рН = 3,0
^-Дианизидин
Дифениламиносульфонат Na или Ва
Метиловый красный. Необратимый
индикатор
Дифенилбензндип сернокислый
Дифениламин сернокислый
Патентный синий Б
2,6-Дихлорфенолиндофенал Na-соль-
0,02%-ный раствор в воде
М-Крезолиндофенол. 0,02%-ный
раствор в 60%-ном этаноле
Толунленовый синий. 0,05%-ный рас
твор в 60%-ном этаноле
Тионин. 0,05%-ный раствор в 60%-ном
этаноле
Метнленовый голубой. 0,05%-ный
раствор в роде
77
11. 4. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ ИНДИКАТОРЫ,
ЧУВСТВИТЕЛЬНЫЕ К ИЗМЕНЕНИЮ рН И ИОННОЙ СИЛЫ РАСТВОРА
Е
0
s
+0,69
+0,67
+0,67
+0,66
+0,659
+0,653
+0,649
+0,64
+0,64
+0,64
+0,64
+0,63
+0,616
+0,60
+0,592
+0,58
+0,55
+0,54
+0,54
+0,39
+0,37
+0,37
+0,36
+0,36
+0,36
+0,35
+0,34
+0,34
+0,34
+0,34
+0,33
+0,31
+0,30
+0,29
+0,28
+0,25
+0,24
+0,24
+0,583
+0,556
+0,149
+0,101
». В, при
б
+0,33
+0,31
+ 0,31
+0,30
+0,30
+0,30
+0,29
+0,28
+0,28
+0,28
+0,28
+0,27
+0,25
+0,24
+0,23
+0,22
+0,19
+0,18
+0,18
+0,089
+0,047
рН, равном
7
8
9
Индофенолы
+0,283
+0,254
+0,248
+0,242
+0,240
+0,233
+0,227
+0,224
+0,219
+0,218
+0,217
+0,208
+0,191
+0,181
+0,174
+0,159
+0,125
+0,123
+0,119
+0,21
+0,19
+0,19
+0,18
+0,18
+0,18
+0,17
+0,16
+0,16
+0,16
+0,16
+0,15
+0,13
+0,12
+0,11
+0,10
+0,07
+0,06
+0,06
Оксазинъ
+0,047
+0,011
+0,015
—0,020
+0,15
+0,13
+0,13
+0,12
+0,12
+0,12
+0,11
+0,10
+0,10
+0,10
+0,10
+0,09
+0,07
+0,06
+0,05
+0,014
+0,01
+0,00
+0,00
t и muaai
+0,016
—0,050
Индикатор
Фенол-М-сул ьфо-
нафтиндо-2,6-дн-
бромфенол
М-Хлорфенолин-
до-2,6-дихлорфе-
нол
М-Бромбензолин-
дофенол
Фенол-0-сульфо-
нафтиндо-2,6-ди-
бромфенол
0-Бромфенолиндо-
фенол
0- X лорфенолиндо-
фенол
Фенолиндофенол
Феноловый синнй
2,6-Дихлорфено-
линдо-о- хлорфенол
2,6-Днбромбензо-
линдофенол
(натриевая соль)
2,6-Днхлорфено-
линдофенол
М-Крезолиндофе-
нол
0- Крезолиидофе-
нол
2,6-Дихлорфено-
линдокрезол,
натриевая соль
Тимолиндофенол
2,6-Дибромбензо-
линдо-гваякол
М-Толуилендиами-
ниндофенол
1-Нафтол-2-суль-
фокислота
индофенол, динатрие-
вая соль
1-Нафтол-2-суль-
фокислота — индо-
-2,6-дихлорфенол,
динатриевая соль
гны
Бриллиантовый
крезоловый синий
(бриллиаитблау С;
З-амино-9-диме-
тиламиио-10-ме-
тилфенок — сазин-
хлорид)
Фиолетовый
Лаута (тионин; диа-
мииофенотиазин)
Примечание
Индикаторы
группы индофенола в
восстановленном
состоянии
бесцветны илн очень
слабо окрашены,
а в окисленном
состоянии
окрашены в синий
(если содержат два
атома галогена)
илн красный цвет
Окисленная форма
при рН 1 -i- 10 —
синяя, при рН >
> 10 — красная,
восстановленная—
бесцветная форма
Окисленная —
фиолетовая;
восстановленная —
бесцветная
78
Продолжение
Еп, В, при рН, равном
0
+0,540
+0,532
+0,406
5
+0,089
+0,135
—0,011
+ 0,130
—0,040
6
+0,001
+0,093
—0,071
+ 0,080
+0,080
—0,112
7
—0,072
+0,06
—0,122
+0,050
+0,021
—0,173
8
—0,115
+0,030
—0,159
+0,020
—0,031
—0,226
S
—0,146
0,000
—0,192
—0,095
-0,337
Индикатор
Этиловый Капри
синий (3,9-бис-ди-
метиламинофенок-
сазнн
азотнокислый)
Метиленовый
синий (ыетилснблау;
тетрамстилдиами-
нофенотиазин)
Нильский синий
Мускарин
Галлоцианнн
Бриллиантовый
ализариновый
синий
При мечание
Окисленная — яе-
лено-снняя;
восстановленная —
бесцветная
Окисленная
форма — синяя,
восстановленная —
бесцветная
Окисленная
форма при рН = 1-s-
-=-10 — синяя, при
рН = 10 —
красная,
восстановленная —
бесцветная
Окисленная —
синяя;
восстановленная —
бесцветная
Окисленная при
рН=5-тй — синяя
np;i рН = 4-^8 —
красно -
фиолетовая,
восстановленная —
бесцветная
Окисленная в
кислотах — синяя;
в воде —
фиолетовая
+0,065
+0,032
—0,010
—0,04
+0,06
—0,02
—0,07
—0,10
—0,046
—0,081
—0,125
—0,16
Индигосульфоновые кислоты
Индиготетрасуль-
фоновая кислота
-0,083
-0,11
-0,16
-0,19
—0,11
-0,14
—0,20
—0,22
Йндиготрисульфо-
новая кислота
Ин дигодис ул ьфо-
новая кислота
Инднгомоносуль-
фоновая кислота
В
восстановленном состоянии все
индикаторы этой
группы почти
бесцветны, в
окисленном — синие; чем
больше сульфо-
групп, тем
интенсивнее оттенок
сниего цвета
Азины
+0,286
+0,280
+ 0,235
+0,237
—0,104
—0,100
—0,139
—0,17
—0,182
—0,176
—0,214
—0,26
—0,260
—0,252
—0,289
—0,33
—0,34
—0,33
—0,36
—0,39
—0,42
—0,40
—0,44
—0,45
Диметилфеноса-
франин (фуксин;
метиленвиолет)
Феиосафранин
Сафранин Т
Нейтральный
красный
Окисленная
форма — фиолетовая,
восстановленная — бесцветная
Окисленная —
красная,
восстановленная —
бесцветная
Окисленная —
красная,
восстановленная —
бесцветная
Окисленная —
красная,
восстановленная —
бесцветная
79
Продолжение
Е
0
+0,207
рН= 3
+0,097
+0,202
+0,195
+0,190
+0,170
5
+0,082
+0,078
—0,10
—0,10
—0,11
—0,13
о, В, при
6
+0,026
—0,16
—0,16
—0,17
—0,19
рН, равном
7
—0,034
—0,22
—0,22
—0,23
—0,25
8
—0,093
—0,28
—0,28
—0,29
—0,31
9
—0,15
—0,34
—0,34
—0,35
—0,37
+0,25
Индикатор
Пиоцнанин
(1-я ступень)
Пиоцианин
(2-я ступень)
Изорозиндумин
№ 3
Изорозиндумин
№ 2
Изорозиндумин
№ 1
Нейтральный
синий
Диметнлглиоксим
(комплекс с Fea'*)
Примечание
В кислой среде
окраска на 1-й
ступени красная,
на 2-й — зеленая,
восстановленная
форма —
бесцветная в щелочной
среде;
окисленная — синяя;
восстановленная —
бесцветная
Окисленная —
синяя;
восстановленная —
бесцветная
То же
»
»
Окисленная —
бесцветная,
восстановленная —
красная (только в
щелочной среде)
* £. при рН = 10= - 0,140В.
П. 4а. СМЕШАННЫЕ ИНДИКАТОРЫ
Характеризуются показателем
титрования рТ, который близок к
величине рН в конечной точке
титрования (КТТ) и рКинд. КТТ
устанавливается более четко и в узком
интервале рН. Они удобны для
титрования при искусственном освещении
слабых и многоосновных кислот.
Компоненты смешанных
индикаторов подобраны таким образом, чтоба
их цвета были дополнительными в
области рН-перехода, поэтому
окраска их в КТТ изменяется через
серый цвет.
рт
1
3,25
4,0
Окраска индикатора
в среде
кислой
2
Сине-фиолетовая
Фиолетовая
щелочной
3
Зеленая
»
Компоненты
4
Метиловый желтый,
0,1%-ный раствор в
этаноле; метиловый синий,
0,01%-аый раствор в
этаноле
Гексаметоксн красный,
0,1%-ный в этаноле;
метиловый зеленый, 0,1%-иый
в этаноле
10В
О 0J
о в
5
1 : 1
1 : 1
Примечание
6
Зеленая при рН = 3,4;
сине-фиолетовая при
рН = 3,2; сохранять в
темной склянке
Сине-фиолетовая при
рН = 4,0; сохранять в
темной склянке
80
Продолжение
Фиолетовая
Оранжевая
Винно-
красная
Крясно
фиолетовая
Фиолетовая
Зеленая
Желто-зеленая
Желтая
Ф ноле: obi;
Фиолегозо-
синяч
Розовая
Желтая
Зеленая
Сине-зеленая
Зеленая
Желто-зеленая
Фиолетовая
Сине-фио-
лстозая
То же
к/ЛПЯЛ
Зеленая
Фиолетовая
Метиловый оранжевый,
0,1%-ный в воде; инднго-
кармин, 0,25% -ный в воде
Метиловый оранжевый,
0,1%-ный в воде;
анилиновый синий, 0,1%-ный
в воде
Бромкрезоловый синий
натриевая соль, 0,1%-ный
в воде; метиловый
оранжевый, 0,02%-ный в воде
Бромкрезоловый зеленый,
0,1%-ный в этаноле;
метиловый красный,
0,2%-ный в этаноле
Метиловый красный,
0,2%-ный в этаноле;
метиловый синий, 0,1%-ный
в этаноле
Бромкрезоловый зеленый,
натриевая соль, 0,1%-ный
в воде; ализариновый
красный, S 0,1%-ный раствор
в воде
Хлорфеноловый красный
натриевая соль, 0,1%-ный
раствор в воде;
анилиновый синий, 0,1%-ный
раствор в воде
Бромкрезоловый синий
натриевая соль, 0,1%-ный
раствор в воде;
хлорфеноловый красный, 0,1%-ный
раствор в воде
Бромкрезоловый
пурпуровый натриевая соль,
0,1%-ный раствор в воде;
бромтимоловый синий
натриевая соль, 0,1%-ный
раствор в воде
Бромтимоловый синий
натриевая соль, 0,1%-ный
раствор в воде; азолитмин,
0,1%-ный раствор в воде
Нейтральный красный,
0,01%-ный в этаноле; ме-
гиленовый синий, 0,10%-
ный в этаноле
Нейтральный красный,
0,1%-ный в этаноле;
бромтимоловый синай, 0,1 % -ный
в этаноле
Цианин, 0,1%-ный раствор
з 50%-ном этаноле;
феноловый красный, 0,1% -ный
в 50%-ном этаноле
Бромтимоловый синий
натриевая соль, 0,1%-ный
раствор в воде; феноловый
красный, 0,1%-ный раствор
в воде
1 : 1
1 : 1
1 : 1
3 : 1
1 : 1
1 : I
: 1
2 : 1
1 : 1
Особенно удобен для ти-
трован.ия при
искусственном освещении;
сохранять в темной
склянке
Желтая при рН = 3,5,
зеленовато-желтая при
рН = 4,05;
слабо-зеленая при рН = 4,3
Очень резкое изменение
окраски
Красно-фиолетовая при
рН = 5,2; грязно-синяя
при рН = 5,4; грязно-
зеленая при рН = 5,6;
сохранять в темной
склянке
Красно-коричневая при
рН = 5,6
Бледно-фиолетовая
рН = 5,8
при
Сине-зеленая при рН =
= 5,4; синяя при рН =
= 5,8; сине-фиолетовая
при рН = 6,2
Желто-фиолетовая при
рН — 6,2; фиолетовая
при рН = 6,6;
сине-фиолетовая при рН = 6,8
Фиолетовая при рН
= 6J3
Фиолетовая при рН =
= 7,0 сохранять в
темной скляике
Розовая при рЫ = 7,0
Л. И. Лазарев и др.
81
Продолжение
1
8,3
8,3
8,9
8,9
9,0
9,6
9,9
10,0
10,2
10,8
2
Желтая
Бледно-
розовая
То же
Зеленая
Желтая
Слабожелтая
Бесцветная
Синяя
Желтая
Зеленая
3
Фиолетовая
»
»
»
»
»
Фиолетовая
Красная
Фиолетовая
Красно-
коричневая
4
Крезоловый красный
натриевая соль, 0,1%-ный
раствор в воде; тимоловый
синий натриевая соль,
0,1%-ный раствор в воде
а-Нафтолфталеин, 0,1%-
ный в этаноле;
крезоловый красный, 0,1%-ный
в этаноле
а-Нафтолфталеин, 0,1%-
ный раствор в этаноле;
фенолфталеин, 0,1%-ный
раствор в этаноле
Фенолфталеин, 0,1%-ный
раствор в этаноле;
метиловый зеленый, 0,1%-ный
раствор в этаноле
Тимоловый синий, 0,1%-
ный в 50%-ном этаноле;
фенолфталеин, 0,1%-ный
в 50%-ном этаноле
Фенолфталеин, 0,1%-ный
в 50%-ном этаноле; а-на-
фтолфталеин в 50% -ном
этаноле
Фенолфталеин, 0,1%-ный
раствор в этаноле; тимол-
фталеин, 0,1%-ный раствор
в этаноле
Фенолфталеин, 0,1%-ный
раствор в этаноле;
нильский голубой А, 0,2%-ный
в этаноле
Тимолфталеин, 0,1%-ный
раствор в этаноле;
ализариновый желтый Р, 0,1%-ный
раствор в этаноле
Нильский голубой А, 0,2%-
ный раствор в воде;
ализариновый желтый Р, 0,1%-
ный раствор в этаноле
5
1 : 3
2 : 1
1 :'д
1 : 2
1 :Ь
2: 1
1 ■ 1
1 : 2
2 : 1
2 : 1
6
Бледно-фиолетовая при
рН = 8,2;
ярко-фиолетовая при рН = 8,4
Бледно-зеленая при
рН = 8,6; фиолетовая
при рН = 9,0
Бледно-синяя при рН =
= 8,8; фиолетовая при
рН = 9,0
От желтой через
зеленую к фиолетовой
Зеленая при рН = 9,6
Розовая при рН = 9,6;
фиолетовая при рН = 10
Фиолетовая при рН = 10
То же
»
И. 5. АДСОРБЦИОННЫЕ ИНДИКАТОРЫ
Ион
определяемый
1
[Fe(CN)e]*-
С1-
1" (в
присутствии С!-)
CI", Br, Г,
SCN-
РЬ2+
тнтрант
2
РЪ2+
Ag+
Ag+
Ag+
MoOi"
Индикатор
3
Ализариновый красный
(0,4—1%-ный водный
раствор)
То же
Бенгальский розовый А
(1%-ный водный раствор)
Бромфеноловый синий (0,1—
1%-ный раствор в 20%-ном
этаноле)
Диаминовый голубой
Изменение окраски
4
Желтая — розово-красная
Желтая — лилово-розовая
Карминово-красная — сине-
красная
Желто-зеленая —
зеленовато-синяя
Бесцветная — фиолетовая
(осадок)
82
Продолжение
CI" , Br-
Zn3+
ln3+
CN-
Cl", I, CN-
SCN"
CI-, Br, I-
C1-, Br, Г
Ag+
1" (в
присутствии CI")
ci-
C1-, Вг-
СГ , Br, [" ,
SCN". SeCN-
A«*
|Fe(CN)(il'-
|Fe(CN)fij'-
Ад*
П^+. Ag1-
Ag+
Ag+
Bt-
Ag+
А?Г
ci-
Ag*
Br, 1-
SCN"
Г , Br, SCN-
Pb2+
MoOJ", I-
Ag+
Ag+
Ag+
MoO'f"
PbJ+
To же
»
Эозин (0,5%-ный воднын
раствор или и 60 —70%-ном
этаноле)
То же
Эритрозин (0,5% iiuii
водный расшор)
То же
Дифсниламиновый синий
(1%-ный водный раствор)
Дифениламин (1%-ный
раствор в 96%-пой 1I2S04)
Дифенилбелзидии (2% -ный
раствор в 90%-ной H.2S04)
Дифенилкарбазид (0,1%-ный
раствор в этаноле)
Дифепилкмрбазон (0,2 —
0,3%-ный раствор в этаноле)
Дихлорфлуоресцеин (0,1%-
ный раствор в 60%-ном
этаноле)
Конго-красный (0,1 — 1%-
ный водный раствор)
Родамин 6>К (0,1%-ный
водный расшор)
Тартразип (тартрацин)
Тропеолин 00 (0,1%-ный
водный раствор)
Фечосафранин (сафранин Т,
0,1%-ный водный раствор)
Флуоресцстш, натриевая
соль (0,1—0,2%-пый
водный или углполындй
раствор)
Фуксин; розанилин
Зеленая — фиолетовая
Синяя — зеленовато-желтая
Синяя — зеленая
Красная — фиолетовая
Фиолетовая — голубая
Розовая — синяя
Желто-зеленая — красная
Красная — синяя
Желто-красная — красно-
фиолетовая
Бесцветная — зеленая
Желтая — розовая
Красная — синяя
Желто-зеленая — розовая
Красно-фиолетовая —
розовая
Оранжевая — розовая
Голубая — розовая
Оранжевая — интенсивно-
красная
Красно-фиолетовая —
оранжевая
Оранжевая —
темно-красная
Красная — краснофиолето-
вая
II. 6. ЛЮМИНЕСЦЕНТНЫЕ ИНДИКАТОРЫ
Интервал рН
изменения
цвета
люминесценции
Изменение окраски
люминесценции
Индикатор
0,0—3,0
0,1—3,0
0,1—3,1
0,3—1,7
0,5-3,1
1,0—1,3
1,1-3,1
1,4—3,2
1,5—2,0
1,5—3,0
... — зеленая
Желтая — синяя
Желтая — синяя
Желтая — синяя
Желтая — синяя
Оранжевая — розовая
... — синяя
Зеленая — синяя
... — голубая
. — синяя
Эозин
Дикумарин
.-.Ч-Димстилумбеллифсрон
Бецзофдавии
5-Мстокси-4,7-диметил кумарин
Родамин 6Ж
5,7-Диметокси-4-метилкумариц-3-ук-
сусная кислота
4-Этоксиакридон
Эксулин
Антраниловая кислота (1-й переход)
6*
83
Продолжение
l
1,5-3,0
>2
>2
2,2-3,6
2,5-3,5
2,5-3,5
2,8-4,4
3,0-6,0
3,0—6,8
3,1-4,4
3,1-4,4
3,1-4,4
3,1-4,4
3,2—3,8
3,2-4,7
3,4-4,1
3,4-4,3
3,4—4,3
3,4—4,8
3,8-6,1
4,0-4,5
4,0-5,0
4,0—6,0
4,0-6,0
4,0-6,6
4,4-6,3
4,4-6,4
4,7—6,0
4,8-6,6
5,4-6,1
5,7-7,0
5,8-7,0
5,8-7,6
5,8-8,0
6,0-7,0
6,0—7,0
6,0—8,0
6,0—10,0
6,1-7,1
6,2-7,2
6,2-7,6
6,5-7,6
6,7-7,3
6,8-8,4
7,0—8,2
7,0-9,0
7,1-8,1
7,2-8,9
7,2—9,0
7,4-9,0
7,5-9,1
7,8
8,0—9,8
8,0—10,6
8,1—10,6
8,2—10,0
8,2—10,0
2
... — зеленая
... — оранжевая
... — желтая
... — синяя
... — синяя
... — синяя
... — фиолетовая
... — синяя
... — синяя
Зеленая — ...
... — фиолетовая
... — оранжевая
Зеленая — ...
Лиловая — оранжевая
Лиловая — сиреневая
... — зеленая
Желто-зеленая — голуба?
Желто-зеленая — синяя
... — синяя
Голубая — фиолетовая
... — зеленая
Желтая — синяя
Зеленая — синяя
Синяя — темно-синяя
... — зеленая
Синяя —...
Желтая — оранжевая
Зеленая — синяя
Зеленая — фиолетовая
Зеленая — фиолетовая
Зеленая — фиолетовая
... — синяя
... — синяя
... — сиияя
Желтая — синяя
... — синяя
Зеленая — желтая
Синяя — фиолетовая
Синяя — зеленая
... — голубая
... — голубая
... — синяя
Оранжевая — зеленая
Зеленая — фиолетовая
... — фиолетовая
... — фиолетовая
... — синяя
Синяя — желтая
... — зеленая
... — синяя
... — синяя
... — синяя
... — зеленая
Зеленая — синяя
Зеленая — синея
Желтая — зеленая
... — синяя
3
3-Амино-(1)-нафтойная кислота (1-й
переход)
Тимоловый синий
Ксиленоловый синий
Аш-кислота (1,8-аминоиафтол-3,6-ди-
сульфокислота)
а-Нафтойная кислота
Салициловая кислота
Р-Нафтиламин
Нафтяоновая кислота
З-Окси-2-нафтойная кислота
Морин (1-й переход)
5-Амииосалициловая кислота
0-фенилеидиамин
п-фенилендиамин
Диметилнафтейродин
Диэтилнафтейродин
Флуоресцеин
2-Метокси-6,9-дихлоракридяи
2-Метокси-7,9-дихлоракридии
а-Нафтиламин
Хииин сернокислый (1-й переход)
Эритрозин
Хинная кислота
3-амиио-(1)-нафтойная кислота (2-й пе-
Рех°Д)
Антраниловая кислота (2-й переход)
2,7-Дихлорфлуорсцеин
(5-Нафтохииолии
Резоруфин
9-ЭтиЛ-1,2-беиза кридин
Акридин
9-Метил-1,2-бенза кридии
9-Метил-3,4-беизакридин
Лакмоид
(5-Метилумбеллиферои
Кислота Шефера (2,6-нафтол-сульфо-
кислота)
Гидрохинондисульфокислота
Хромотроповая кислота
3,6-Д иоксифта л имид
Хинии
5-Фенил умбелл иферон
Хинолин
4,7-Диоксикумарин
Умбеллиферон
7-Аминоакридин
Феноловый красный
Розоловая кислота
Кислота Невиль—Винтера (1,4-иафтол-
сульфокисяота)
8-Аллилумбеллиферон
Кармин
Кумаровая кислота
Г-соль
Ж-кислота
Азолитмии
Морин (2-й перевод)
Р-еоль
Р-кислота (2-вафтол-3,6-дисульфоки-
слота)
Нафтол АС
3-Окси-1-наф*ойная кислота
84
Продолжение
I
8,4—10,4
8,2
8,6
8,5—9,5
8,9—12,0
9,0—11,0
9,5—10,5
9,6—13,0
10,0—12,0
10,0—12,0
12,0—13,0
12,0—13,0
12,0—14,0
12,5—14,0
2
Оранжевая — зеленая
... — фиолетовая
... — синяя
... — голубая
... — зеленая
Синяя — зеленая
Фиолетовая — ...
Синяя —.. .
Фиолетовая — зеленая
Синяя — зеленая
Синяя — зеленая
Синяя — фиолетовая
Желто-зеленая — ...
Синяя — ...
3
Акридиновый оранжевый (Эухризин
ЗР)
а- Нафтолсул ьфокислота
а-Нафтол
р-Нафгол
Кумарин
9-Аминоакридин
Хинин сернокислый (2-й переход,
2-Нафтиламин-6-сульфамид (2-й
переход)
Чикаго СС кислота
9-Хлоракридин
1-Нафтиламинсульфокислота-5
2-Нафтиламинсульфокислота-5
Риванол
Антраниловая кислота
Примечание Три точки обозначают отсутствие люмииисцентиого свечения
II. 7. ВАЖНЕЙШИЕ ИНДИКАТОРЫ, ПРИМЕНЯЕМЫЕ
ДЛЯ КИСЛОТИО-ОСКОВНОГО ТИТРОВАНИЯ В НЕВОДНЫХ РАСТВОРАХ
Индикатор
i
Азофиолетовый
[4-(я-нитрофенил)-
азорезорцин]
/г-Аминоазобепзол
Бензоилаурамин
Бриллиантовый
крезоловый синий
Бромкрезоловый
зеленый
Бромтимоловый
синий
Бромфеноловый
синий
Конго-красный
Кристаллический
фиолетовый
Малахитовый
зеленый
Метиловый
желтый
Метиловый
красный
Метиловый
оранжевый
Растворитель
1
Диметилформа-
мид, пиридин.
бензол
Хлороформ
Уксусная кислотг:
То же
Хлороформ
Пиридин,
уксусная кислота, ак-
рилонитрил
Хлорбензол,
хлороформ, этанол
Диоксан, метанол
Уксусная кислота
То же
Хлороформ
Хлороформ, аце-
тонитрил
(насыщенный раствор),
метанол, укеусна;:
кислота
Гликоль,
углеводороды, ацетон,
■метанол
Концентрация, %
3
0,1
0,1
0,1
0,1
0,5
0,1
0,1
0,!
0,!; 0,2
0,!; 0,5
0,1
0,05—0,1
0.1; 0,25
Изменение
окраски
4
Оранжевая —
голубая
Желтая —
красная
Желтая — серо-
фиолетовая
Красная — сиияя
Зеленая —
бесцветная
Желтая —
голубая
Фиолетовая —
желтая
Красная —сиияя
Голубая —
зеленая
Бесцветная —
голубая
Желтая —
красная
Желтая —
красная
Желтая —
малиновая
Определяемые
вещества
5
Фенолы, енолы,
имиды
Резорцин
Аминокислоты
То же
Первичные и
вторичные
Органические
кислоты
Амины,
алкалоиды, сульфамидные
препараты
Амины
Алкалоиды,
аминокислоты
Алкалоиды
Амины, никотин
Кофеин, кофеин-
фосфат
Наркотики
группы морфин?
85
Продолжение
1
Метиловый
фиолетовый
2-Нафтолбензеин
Нильский
голубой
Нитрофеиолы
я-Оксиазобензол
Пикриновая
кислота
Тимоловый синий
(тимолсульфофта-
леии)
Тимол фталеии
Тропеолин 00
Феноловый
красный
Фенолфталеин
2
Уксусна*
кислота, хлорбензол
Уксусная
кислота, изопропило-
вый спирт,
бензол — метанол
Бензол — метаиол
Хлорбензол,
анизол
Ацетон
Этилеидиамии
Диметилформамид.
метанол, этилен-
гликоль
Пиридин
Уксусная
кислота; метанол;
ацетон + пиридин
Этанол
Этанол ■+- бензол;
этанол + пиридин
3
0,1—1,0
0,1—0,5
0,1
0,1
0,1
0,1
0,1; 0,3
0,1
0,1 — 1,0
0,1
0,1
4
Зеленая —
желтая
Желтая —
зеленая
Красная — синяя
Желтая —
бесцветная
Бесветная —
желтая
Желтая —
бесцветная
Желтая — синяя
Светло-желтая —
голубая
Желтая —
фиолетовая
Красная —
желтая
Бесцветная —
малиновая
в
Производные
антипирина
Аминокислоты,
хинин
Дифенилфосфат
Основания
Карбоновые
кислоты
Фенолы
Соли аммония,
ацетилсалициловая кислота,
алкалоиды, найлон
Амины, ацетилен
Алкалоиды,
кофеин, салицилаты
Муравьиная
кислота
Жирные кислоты,
сульфамиды,
барбитуровая кислота
Четкость перехода окраски при
неводном титровании зависит от
концентрации индикатора, силы кислот
и оснований, концентрации ионов
и от изменения состава растворителя
в процессе титрования.
В неводном титровании находят
применение смешанные индикаторы.
Например, растворы 0,1%-ного ме-
тиленового синего и 0,2%-ного хи-
нальдинового красного в метаноле с
соотношением 1 : 1. Примечание: при
титровании в смеси нитрометана с
бензолом из щелочной среды в
кислую переход окраски пурпурная —>
—> синяя —» зеленая.
И. 8. ВАЖНЕЙШИЕ ИНДИКАТОРЫ, ПРИМЕНЯЕМЫЕ ДЛЯ ОКИСЛИТЕЛЬНО-
ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ В НЕВОДНЫХ РАСТВОРАХ
Индикатор
(определяемые вещества)
Растворитель
Концентрация,
%
Изменение окраски
Вариаминовый Б
(аскорбиновая кислота, гидрохинон, 0-
нафтол)
Дифениламин (гидрохинон)
Метиловый красный
(гидрохинон)
0-фенантролии + Fe2+ ферроин
(гидрохинон)
Янус зеленый (гидрохинон)
Пиридин
Ледяная
кислота
То же
уксусная
0,1
0,25
0,1
2
0,1
Бесцветная — синяя
Бесцветная — фиолетовая
Красная — желтая
Красная
Синяя — розовая
86
12. ХАРАКТЕРИСТИКА СВЕТОПОГЛОЩЕНИЯ
РАСТВОРИТЕЛЕЙ И РАСТВОРОВ
НЕОРГАНИЧЕСКИХ И ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
12. 1. СВЕТОПОГЛОЩЕНИЕ А ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ
И КОЭФФИЦИЕНТ МОЛЯРНОГО ПОГАШЕНИЯ е„
Растоорнтель
Растворитель
ол-
а S
s
в*
5=»
210
285
270
245
255
210
220
210
270
е
>.
В £
а: -
—
262
—
—
—
—
—
—
—
Ацетон (раствор в воде)
Ацетоиитрил
Бензиловый спирт . . .
Бензол (раствор в гек-
сане)
н-Бутиловый спирт . . .
Глицерин
Изопропиловый спирт
Ксилол (раствор в гек-
сане)
Метилизобутилкетоп . .
330
220
250
280
220
230
210
290
395
264,5
250
270
275
250
330
42
гек-
Метиловый спирт
Толуол (раствор в
сане)
Уксусная кислота
Хлороформ . .
Этилацетат . .
Этиловый спирт
Этиловый эфир
Циклогексан
Четыреххлориетый
углерод
300
Даиа предельная длина волны — рраинца пропускания ультрафиолетового излучения.
12. 2. СВЕТОПОГЛОЩЕНИЕ А РАСТВОРОВ КИСЛОТ И ЩЕЛОЧЕЙ
И КОЭФФИЦИЕНТ МОЛЯРНОГО ПОГЛОЩЕНИЯ е.
Вещество
Область А
при длине
волн, им
Максимум
А, нм
при длине
волн, нм
Вода
Серная кислота
Сернистая кислота
Соляная кислота, 5 н. раствор
Фосфорная кислота, 2М раствор
Азошая кислота, 1 и. раствор
Щавелевая кислота, 0,05 н. раствор
Уксусная кислота, ! н. раствор
Хлорная кислота, 1 н. раствор
Фтористоводородная кислота 40%-ная ....
Борная кислота, 0,01%-ный раствор
Перекись водорода, 30%-ная
Винная кислота, 20%-ный раствор
Лимонная кислота, 0,4%-ный раствор ....
Этилендиаминтетрауксусная кислота. 0,1 М рас
гпор
Аскорбиновая кислота, 5%-ный раствор . . .
Едкий натр, 0,1 н. раствор
Едкий калий, 0,1 н. раствор
Аммиак, 0,1 н. раствор
Натрий углекислый. 0,1 н раствор . . .
900—1100
220—320
220—280
220—330
220—350
220—310
220—260
220—260
220—230
220—300
220—330
220—330
220—270
220—320
220—320
220—230
220—225
220—225
220—240
960
275
215
225; 250
305
265
3-10-*
70
0,51
0,0312Б0
6
35гз5
1,8235
' >°230
18,6330
10023„
0,86250
2,0250
207220
''зао
150
0,3225
0а2Б
0225
8.422S
87
t2. 3. СВЕТОПОГЛОЩЕНИЕ А ГАЛОГЕНИДНЫХ КОМПЛЕКСОВ МЕТАЛЛОВ
И КОЭФФИЦИЕНТ МОЛЯРНОГО ПОГАШЕНИЯ е*
Среда
I
1 М НС1
1 М НС1
10 М HCI
iM на
1 М НС1
6М НС1
6 М НС1
1 М НС1
1 м на
1 м на
2 м на
5 м на
7 м на
э м на
11 М НВг
о,о1 м на
Область А
при длвве
вола
220—1100 нм
2
Алюминий (III)
| 220—350 |
Марганец (11)
1 Не погло- 1
| щает 1
Марганец (III)
1 220—1100
•
Хром (III)
220—750
Ртуть (II)
| 220—300
Олово (II)
| 220—260
Олово (IV)
| 220—270
Сурьма (III)
| 220—270
Железо (II)
| 220—400
Железо (III)
220—400
220—500
220—540
220—560
220—560
220—700
Кобальт (II)
220—235
440—570
8Ji
при длине
волн, нм
3
6,8Ю0
35°Б70
«•»
Ю4Й6
20,8420
1'>^воо
23 000aSo
14 200а20
8 3002ао
8 500220
870220
3 100220
900Э40
Ю44О0
Ю4440
Ю4440
П84в0
2 100430
1«88ю
Среда
1
1-2 м на
5 м на
7 м на
э м на
11 М НВг
Область А
при длине
волн
220—1100 нм
2
220—750
220—750
220—750
220—750
220—760
Никель (II)
0Д1 М НО
1—5 м на
9 м на
Концентрированная на
11 М НВг
N
o.oi м на
1 м на
2 м на
5 м на
9 м на
Концентрированная на
11 М НВг
220—240
330—460
220—1100
220—1100
220—1100
220—850
1едь (II)
220—340
580—1100
220—400
560—1100
220—400
560—1100
220—400
560—1100
220—400
560—1100
220—400
560—1100
220—1100
Ря
при длине
волн, нм
3
5ззо
5sio
8>6350
7,252о
'«80
7>2збо
8>6б80
33,2в80
7,242о
"40в80
9,3-ioo
*•'«во
3,8220
3,°зоо
*''400
2,3720
''^400
2,3720
841о
3?в0
6400
2710
91270
'^''800
19825
22
63 900
110П25
1 360SR5
Ю4950
1300з,0
1 100,M
88
12. 4. СВЕТОПОГЛОЩЕНИЕ А ИОНОВ ПЕРЕХОДНЫХ МЕТАЛЛОВ В РАЗЛИЧНЫХ СРЕДАХ
Металл
1
Т1 (IV)
VUV)
V(V)
Сг (III)
Сг (VI)
Ре (111)
Со (11)
Ni (11)
:u (id
Mb(V)
йо (VI)
»e(VII)
Среда
2
17-18 М H2S04
рН = 4,5 •»
рН — 3+5 ••
0,5-5 М H2S04
18 М H2S04
То же
рН — 2+3 *»
рН = 3,5 ••
Щелочная, рН = 9 + 12
0,5-5 М H2S04
рН = 8+9 «
рН = 3,5 *г
0.5-9 М H2S04
0,5-1.5 М HsS04
рН = 3,2 ". рН — 1 в
более *'
0.5-2 М H2S04
рН = 9,9 "
рН = 5 "-
0,5-9 М H2S04
рН = 5 + 10 "
То же
рН =. 5 + 8 »2
0,5—9 М H2S04
0,5—2 М H2S04
рН =. 5-8 *>
рН = 8 + 11 "
рН = 9 + 12 •«
рН = 6,5+9,5
рН = 5,5+7,5
Длина
волны
в
максимуме А
3
260
270
280
760
330
360
760
570
270
580
580
580
350
320
340
510
570
510
410
390
720
640
700
800
720
750
235
230
224
ч
4
18 200
6 200
4 500
19
4 650
3 800
23,4
26
3 400
18
42
30
1 500
1 790
1 730
4,6
41
15,5
5.0
11
4,6
4,0
1,9
12,0
33
50
1 910
5 250
3 780
>
5
-
0
410
0
0
0
—
0
0
0
1.0
10
220
0
0
0
0
0
0
0
0
0
0
0
—
—
-
>
>
6
3 400
1 600
600
-
_
—
0
80
25
19
230
35
0
20
17
10
12
17
20
0
0
12
14
3 000
2 550
2 800
U
7
90
105
58
0
8,2
3,5
0
30
—
—
—
16
48
4.8
35
19
18
360
1.2
9,8
4
0
360
0
1 300
—
—
Свегопоглищение др)
с
%
8
0
0
0
0
0
0
0
0
—
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
—
-
9
6 100
3 100
3 900
0,15
220
400
0
0
—
0
740
0
0
—
0
"о
30
700
0,2
0
0
0,15
700
0
—
—
—
о
и
10
11
8,5
12
0
5,1
1,4
0
1.5
—
0,5
1.2
2
15,6
2,2
0
1,2
0,3
3,5
1,5
0,3
0
0,2
0
—
—
—
гих металлов при данных ус
Z
11
ь
3
5
1,8
3,2
1,7
2,7
1
—
0
0,8
1
1.2
0,5
1,8
0
8
0
31
0,8
10
3
—
—
—
б
У-!
1 750
1 200
700
10.6
0
0
22,3
2
—
0
0
0
19
1
14
0
0
0
0
25
0
25
6,8
-
—
—
—
>
13
34
12
10
0
10
0
0
0
—
0
0
0
0
7
0
0
0
0
0
0
0
0
0
0
0
0
—
—
— .
>
Z
14
840
25
0
70
0
0
0
490
0
0
0
0
400
0
0
0
0
0
0
0
0
0
0
0
0
-
—
—
ОВИ'ЛХ
>
о
£
15
1 9С0
1 500
1 000
0
1 600
1 200
0
0
125
0
0
0
0
45
26
0
0
0
0
0
0
0
0
0
0
0
4 000
-
5 400
>
те
е-
16
400
200
200
0
0
0
0
0
182
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
900
-
—
>
17
300
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
150
1 530
1 300
>
ее
18
560
300
200
0
0
180
0
0
280
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
0
3 460
3 740
3 780
*' В присутствии тартрат-иона. *г В присутствии цитпат-нона. *:- Светопоглошевие сильно изменяется вследстние восстановления до Fe (11).** Сплавы NbsO,
с калий-натрий углекислым
13. ГРУППОВОЕ РАЗДЕЛЕНИЕ ЭЛЕМЕНТОВ
13.1. ВЫДЕЛЕНИЕ ЭЛЕМЕНТОВ
НА РТУТНОМ КАТОДЕ
Полностью осаждаются (в среде
0,1-н. серной кислоты) Си, Ag, Au,
Zn, Cd, Hg, Ga, In, Tl, Ge, Sn, Pb,
Bi, Cr, Se, Те, Mo, Po, Fe, Co, №,
Rh. Pd, Ir, Pt.
Частично осаждаются Mn, Sb, Ru,
As.
He осаждаются щелочные и
щелочноземельные металлы, Be, В, А1,
Sc, Y, La, РЗЭ, Si, Ti, Zr, Hf,
V, Nb, Та, W, Ra, Th, Ac, U.
Примечание. Селективность метода
повышается при проведении электролиза
при контролируемом потенциале. Если
потенциалы полуволн двух элементов на
капельном ртутном электроде различаются на
250—300 мб, то можно провести их
количественное разделение.
13.2. ОСАЖДЕНИЕ ОКИСЬЮ ЦИНКА
Полностью осаждаются Al, Ga, Tl,
In, Ti, Zr, Sn, Hf, Th, P, V, As,
Nb, Та, Bi, Pa, Сг, Те, W, Po,
U, Fe, Os.
Осаждаются частично Си, Ag, Au,
Be, Hg, Sc, Y, La, РЗЭ, Ac, Si, Ge,
Pb, Sb, Se, Mo, Ni, Ru, Rh, Pd,
Ir, Pt.
He осаждаются Li, Na, K, Rb, Cs,
Mg, Ca, Sr, Ba, Zn, Cd, Ra, B, Re,
Tc, Mn, Co.
Примечания: 1. Осаждение
ванадия (V) может быть неполным.
2. Большие количества меди и
молибдена частично захватывают с собой кобальт.
3. В присутствии хромат-ионов выпадает
осадок хромата марганца (II); железо (II)
следует предварительно окислять.
13.3. ОСАЖДЕНИЕ АЦЕТАТНЫМ
БУФЕРНЫМ РАСТВОРОМ ПРИ рН == 5,3
Осаждаются Ti (IV), Zr (IV), Th
(IV), Fe (III), Al, Cr (III).
В растворе остаются Со (И), Ni (II),
Mn (II), Zn, Mo (VI), W (VI).
Примечания: 1. Осаждение
алюминия и хрома (III) неполное.
2. Не следует применять метод для
выделения алюминия и хрома, если в растворе
не содержится значительно превосходящих
количеств железа (III).
13.4. ОСАЖДЕНИЕ ЯНТАРНОКИСЛЫМ
(СУКЦИНАТНЫМ) БУФЕРНЫМ
РАСТВОРОМ ПРИ рН == 4,2 -ь 4,6
Осаждается А1.
Остаются в растворе Mg, Ca, Ва,
Mn, Ni, Fe (II), Zn, Cd, Cu.
13. 5. ОСАЖДЕНИЕ
ГЕКСАМЕТИЛЕНТЕТРАМИНОВЫМ
(УРОТРОПИНОВЫМ) БУФЕРНЫМ
РАСТВОРОМ ПРИ рН == 5,4
Осаждаются Fe (III), Al, Ti (IV),
Zr (IV).
Остаются в растворе Ni, Co, Zn.Mn.
13.6. ОСАЖДЕНИЕ
ПО Э. А. ОСТРОУМОВУ
а. Пиридином при рН = 6,5
Осаждаются Fe (HI), Al, Cr (HI),
U, In, Ga, Ti, Zr, Th, Sc.
Остаются в растворе Mn, Co, Ni,
Zn, Cu, Cd.
б. Смесью пиридина и его
азотнокислой соли при рН = 4, l-r-4,2
Осаждаются Bi, Th.
Остаются в растворе Pb, Cu, Cd,
Се (III), РЗЭ.
в. ос-Пиколином при рН = 7,0
Осаждается Be.
Остаются в растворе Mn, Zn, Co,
Ni.
13.7. ОСАЖДЕНИЕ
БЕНЗОАТОМ АММОНИЯ
Осаждаются Al, Cr (III), Fe (III),
Ti (IV), Zr, Th, Се (IV), Bi, Sn (IV).
Остаются в растворе
щелочноземельные металлы, V (V), Со, Ni, Mn,
Zn, Cd, Hg (II).
13.8. ОСАЖДЕНИЕ
КУПФЕРОНОМ И НЕОКУПФЕРОНОМ
(СРЕДА 0,6 —2-н. СОЛЯНАЯ
КИСЛОТА ИЛИ 1,8 — 5-н.
СЕРНАЯ КИСЛОТА)
Осаждаются Nb, Та, Zr, Ti, Sn (IV),
Се (IV), Sb (III), W (VI), V(V),
Fe (III), Ga, U (VI).
В не слишком кислой среде
осаждаются также In, Cu, Мо (VI), Bi.
90
Остаются в растворе Al, Co, Pb,
As(III), Sb (V), Ni, Zn, Mn, U(VI),
P (V), Cr (III) и др.
(3.9. ОСАЖДЕНИЕ
АРСОНОВЫМИ КИСЛОТАМИ
а. Феииларсоновая кислота из I н.
НС1.
Осаждается Zr (IV).
В растворе остаются в присутствии
Н20» Ti (IV), при двукратном
осаждений Fe (III), Th (IV).
б. Феииларсоновая кислота в ук-
сусно-ацетатном растворе
Осаждаются Th (IV), Ti (IV), Zr
IV), Hf (IV), Се (IV), Sn (IV).
В растворе остаются Al, Ce (III),
РЗЭ.
в. п-оксифениларсоиовая кислота
из 0,6 н. НС1 или 3 н. H2S04
Осаждаются Ti (IV), Sn (IV),
Th(IV).
Остаются в растворе Al, Be, Ca,
Сг, Со, Fe (II), Fe (III), Mg, Mn,
Mo (VI), Ni, TI (III), U (VI), Pb, Cu,
Bi, Zr, Zn, As (III), Sb (III), Cd.
г. п-н Бутилфениларсоновая
кислота
Осаждаются и отделяются от всех
других катионов Fe (III), Zr, Th,
Ti (IV), Sn (IV), U (VI), Ce (IV).
13.10. ОСАЖДЕНИЕ 8-ОКСИХИНОЛИНОМ рН ПОЛНОГО
ОСАЖДЕНИЯ ОКСИХИИОЛИНАТОВ МЕТАЛЛОВ
(в скобках указаны данные других авторов)
Металл
А1
Be
V(V)
Bi
W(VI)
Ga
Fe (III)
In
Y
Cd
Ca
Co
La
Mg
Mn
Cu
Mo
рН осаждения
3s4,7 (4,4-9,8)
Щелочная среда
3-4,5(2,7-6,1)
3=6,5(35=5,2; 4,8-9,4)
3-3,5 (5,0-5,6; 5,0)
3,6-11,0
2,8-11,2(3*4,1)
2,5-3,0
3s3,8
3=5,5 (5,7-14,6)
35=9,2 (9,5-10)
35=4,9 (4,3-14,5)
Зэ=7,1
3*8,7 (3&8.2; 9,4-12,7)
5,9-9,5
5,3-14,5
3,6—7,3 (3,3—7,6)
Металл
Ni
Pd
Pu (IV)
Hg(I)
Hg (II)
Pb
Ag
Sc
sb (im
Tl (III)
Ti (IV)
Th (IV)
U (VI)
Ce(IH)
Zn
Zr
рН осаждения
38=4,6(4,6—10,0; 4,3—14,6)
HC1 разбавленная
~5
5,2-8,2
4,8-7,4
8,4—12,3
6,1 — 11,6
6,5-8,5
~6
4,0—8,0
4,8-8,6
4,4—8,8
5,0—9,0(5,7—9,8; 4,1—8,8)
^5,8(^9,4)
32=4,5 (4,6—ГЗ,4; i=-4,4)
4,7-12,5
13.11. ОСАЖДЕНИЕ ЭЛЕМЕНТОВ
ПРИ ВЫПАРИВАНИИ С ХЛОРНОЙ
КИСЛОТОЙ
Полностью выделяются из
раствора Si, Sn, Nb, Sb, Та, W.
Частично осаждаются К, Rb, Cs,
Ag, Ba, Ra, Ti, Ge, Zr, Hf, Pb,
Th, P, V, As, Bi, Pa, Cr, Se, Mo,
Те, Mn.
13.12. ОСАЖДЕНИЕ
ТЕТРАФЕНИЛАРСОНИЕМ
(ПРИ ЛЮБЫХ ЗНАЧЕНИЯХ рН )
Осаждаются СЮ; , MnO; , ReO;,
ТеО;, 10;, ICdClJ8-, [SnCI0]3-,
lPbCl6]2-, [PtBr6]2-.
13. 13. ЭКСТРАКЦИОННЫЕ
МЕТОДЫ ГРУППОВОГО
РАЗДЕЛЕНИЯ ЭЛЕМЕНТОВ
J3. 13. 1. Экстракция
неорганических соединений
Экстракция хлоридных
комплексов диэтиловым эфиром, очищенным
от спирта из 8 М. НС1:
хорошо экстрагируются
Ga (III), Au (III), Tl (III).
Sb (V), As (III), Ge (IV),
слабо экстрагируются
Sn(II), Sn(IV), Sb (III),
As(V), Cu(II), Hg(II),
Ni (II);
Fe (III),
Mo (VI),
Ce (IV);
Те (IV),
Ir (IV),
Zn (II),
91
не экстрагируются Se (TV). V (V),
Al, Bi, Cd, Cr (III), Co, Be, Fe (II),
Pb, Mn, Os (VIII), Pd (II), РЗЭ,
Rh, Ag, Th, Ti, W Li, Zr.
Для экстракции хлоридных
комплексов используют диизопропило-
вый эфир, метилизобутилкетон.
Экстракция бромидных комплексов
из 4 М. НВг диизопропиловым
эфиром: хорошо экстрагируются In,
Tl (III), Fe (III), Ga, Au (III),
Sn(II), Sn(IV), Sb(V), Mo (VI),
Pb (II).
Экстракция иодидных комплексов
из 2 н. серной кислоты метилизо-
бутилкетоном: хорошо
экстрагируются Си (II), As (III), Bi, Cd, Pb,
Sn(II), Sn(IV), Zn, Au(III), In,
Hg (II), Tl (III), Pd (II);
не экстрагируются щелочные и
щелочноземельные металлы, Fe (II),
Ni, Cr (III), Co, Mn, Ti (IV), Zr,
Th, Al, Be, U (VI), V (IV).
Экстракция роданидных
комплексов из 0,5М. НС1 диэтиловым эфиром,
метилизобутилкетоном:
хорошо экстрагируются Be, Zn,
Со, Se (IV), Ga, Nb, In, Tl (III),
Fe (III), Sn (IV), Mo (V), V (IV), Cu,
Bi, Sc;
не экстрагируются Th, Zr, Mn, Pd.
Экстракция фторидных
комплексов из 10—20 М HF диэтиловым
эфиром, метилизобутилкетоном:
хорошо экстрагируются Та (V),
Те (IV), Nb(V), Re (VII), U [VII.
Экстракция нитратных комплексов
из 8—10 М. HN03 эфирами, кето-
нами трибутилфосфатом:
хорошо экстрагируются U (VI),
Ри (VI), Np (VI), Am (VI), Zr (IV),
Се (IV);
слабо экстрагируются Fe (III),
Au (III), Sc, Pa, Tl (III), As (V), Bi,
Cr (VI), V (V).
13. 13.2. Экстракция хелатов
Экстракция диэтилдитнокарбаминатов
Экстрагируемый
элемент
рН водного
раствора
Органическая фплз
Ag
As (III)
Au (III)
Bi (III)
Cd (II)
Cd (II)
Co (II)
Cr (VI)
Cu (II)
Fe (II)
Fe (III)
Ga (III)
(извлечение неполное)
3
4—11
4; 0—5,8
4—11
4—11
1—10
4-11
3
4-11
0—6
1—3,5
4—11
4—11
4,0—9,8
0—10
5,5
3
Этилацетат
Четыреххлористый углерод
То же
Хлороформ; диэтиловый эфир
Четыреххлористый углерод
Этилацетат
Четыреххлористый углерод
Хлороформ
»
Четыреххлористый углерод
То же
»
Хлороформ
Четыреххлористый углерод
Этилацетат
Hg (II)
In (III)
In (III)
Mn (II)
Mo (VI)
Nb(V)
Ni (II)
Pb (II)
Pd (II)
3
4—11
4—10
3
6—9
0—5
3
4-5,5
0—10
4—11
4-11
-0,2
4—1!
»
Четыреххлористый углерод
To же
Этилацетат
Четыреххлористый углерод
Этилацетат
»
Четыреххлористый углерод
Хлороформ
Четыреххлористый углерод
То же
Этилацетат
Четыреххлористый углерод
92
Продолжение
Экстрагируемый
элемент
Re (VII)
Sb (III)
Se (IV)
Sn (IV)
Те (IV)
Tl (III), Tl (I)
V(V)
W(VI)
Zn
pH водного
pacTEopa
Конц. HCl
4—9,5
4—6,2
5-6
4—8,8
0,001-5 н.
соляная кислота
4—11
4—5,9
1-1,5
3
4—11
Органическая фаза
Этилацетат
Четыреххлористый углерод
То же
»
»
Хлороформ, бензол
Четыреххлористый углерод
То же
Этилацетат
»
Четыреххлористый углерод
Экстракция купферонатов
Sn (II)
3,5—9,5
0,5—8 н. H2S04
>3
2—12
>4,5
4-5
0,1—0,15 MH2S04
>4,5
2—10
2—10
1,5-12
Разбавленные
минеральные
кислоты
2-5
3-8
4—10
0-1,5
0-5
9—12
3—9
0—12
0—9
3—12
Разбавленные
минеральные
кислоты
рН= 0 +
+ 0,5%-ная
винная кислота
2,8—8,5
0—4
1,5-10
Кислые растворы
0,5-М. НС1
0-2,5
0-3
(экстрагируется
менее 25%)
>5
9—10,5
0—3
Хлороформ, метилизобутилкетон
Хлороформ
»
»
Бутилацетат, амилацетат
Хлороформ
Хлороформ, бензол
То же
Хлороформ, бензол
» , мегнлизобутилкетсн
Хлороформ
» , бензол
Хлороформ
»
Изоамнловый спирт
Хлороформ
»
»
Диэтиловый эфнр
Этилацетат
Хлороформ
Хлороформ, смесь бензола 4- амиловый спирт
Хлороформ
Экстракция 8 оксихииояинатов
8—9,5
4,5-11
Хлороформ, бензол,
толуол, хлорбензол
Хлороформ
четыреххлористый углерод
Не экстрагируется растворами оксина в хлороформе
№
Продолжение
Экстрагируемый
элемент
Ва (II)
Be (II)
Bi(III)
Са (II)
Cd (II)
Се (III)
Со (II)
Сг (III)
Си (II)
Fe (III)
Ga (III)
Ge (IV)
Hf (IV)
Hg(II)
In (III)
ba (III)
Mg(II)
Mn (II)
Mo (VI)
Nb(V)
Ni (II)
Pb (II)
Pd (II)
Rh (III)
Ru(III)
Sc (III)
Sn (IV)
Sr (II)
Ta(V)
Th (IV)
Ti (IV)
Tl (III)
U (VI)
V(V)
•
W(VI)
Y (III)
Zn (II)
Zr (IV)
pH водного
раствора
>10
(экстрагируется
частично)
6—10
2,5-11
>Ю,7
5,5—9,5
9,9—10,6
4,5—10,5
6—8
2—12
2—10
2,2—12
Экстрагируется
частично
2,0; 4,5—11
>з
3,0—11,5
7—10
10,7—13,6
6,5—10
1,0—5,5
6—9
4,0—10,0
6—10
0—10
6—9
6,4
4,5—10
2,5—5,5
>П,5
0—7 (частичная
экстракция)
4—10
2,5—9,0
3,5—11,5
5—9
2—6
2,5—3,5
7—10
4—5
1,5-4,0
Органическая фаза
Хлороформ
»
»
»
»
»
Хлороформ, бензол, изоамиловый спирт, етил-
ацетат, метилизобутилкетон
Хлороформ
»
Хлороформ, бензол, метилизобутилкетон, цикло-
гексанон, диэтиловый эфир, этилацетат
Хлороформ
Хлороформ
»
Хлороформ, бензол, изоамиловый спирч
Хлороформ
»
»
»
»
Хлороформ, бензол, толуол и др.
Хлороформ
»
»
»
»
»
Хлороформ, бензол, толуол и др.
Хлороформ, лучшие кислородсодержащие
растворители
Хлороформ, метилизобутилкетон
Хлороформ
»
Хлороформ, метилизобутилкетон
Хлороформ, бензол, четыреххлористый углерод,
амилацетат и др.
Хлороформ
»
Хлороформ, метилизобутилкетон
Хлороформ
14. КРАТКАЯ ХАРАКТЕРИСТИКА
НАИБОЛЕЕ РАСПРОСТРАНЕННЫХ
СПЕКТРОФОТОМЕТРИЧЕСКИХ МЕТОДОВ
ОПРЕДЕЛЕНИЯ МЕТАЛЛОВ
(R — реагент; е — коэффициент
молярного погашения; %<—
рекомендуемая длина волны, нм; ап —
коэффициент вариации, %, при
определении п мкг металла; НМ — не мешают
определению; М — мешают
определению).
1) А1Я— ализарин S; е = 16 000;
Я. = 485; аъ = 6,8; НМ —
небольшие количества Mn, Zn, Cd, Ni,
Со; М—Сг, Си, Fe, Mo, Sb, Sn.
2) R — алюминон; е = 11 000; К—
= 515; oc5 = 3,8; НМ — <0,1 г CI,
S04, N03) <0,25 г Mn(II), Ni,
94
Сг (III), Mo (VI); M — Fe (III), тар-
трат, цитрат.
3) R — хромазурол S; e = 30 000;
X = 540; a, = 3,5; HM — до 0,5 r
CI, Br, I, S04, N03, ацетата, Pb, Cd,
Zn, W (VI), Mn, Sri (II); M—более
чем по 5 мг оксалата, цитрата, тар-
трата, F, P04, As (V), Си (II), Ni,
Со, Ag, Hg (II), Sb (III), >1 мг
Fe (III), Cr (VI).
4) R — эриохромцианин R; s =
= 68 000; X = 535; a5 = 3,0; HM —
до 1 мг CI, S04, ацетата, Ni, Co, Cu,
Zn, Mn; M — железо (III)
маскируется тиогликолевой кислотой.
5) R — 8-оксихинолин; е =
= 5000; X = 410; a5 = 4,3; HM —
CI, N03, S04, ацетат, щелочные
металлы, Са, Сг; М — Bi, Cd, Co,
Cu, Fe, Hg, Mn, Ni, Pb, Sb, Sn, Zn,
тартрат.
N. R — Ы-1нафтил-1 1-этиленди-
аммонийдихлорид (для определения
нитрата); е = 41 000; X = 543; аъ —
= 5,4; НМ— до 0,2 г ацетата, С1,
цитоата, F, P04, S04, тартрата, Cd,
Pb,' Zn; M— I, Cu, Fe (HI), Ni,
W (VI).
Ba. R — o-крезолфталеин; e =
= 16 000; X = 575;
малоизбирательный реагент.
Be. 1) R — алюминон; е =
= 7600; X = 536; ce5 = 0,7; HM —
<1 r CI, Br, I, S04, N03, <0,2 r
Mn(II), Cd, Pb, Zn, W (VI); M —
>2 мг F, Fe (III), Ni, Co, Cu (II),
Al, Cr (VI).
2) R — хромазурол S; г =
= 11 700; л = 550; a5 = 4,5; HM —
до 1 r CI, Br, I, S04) N03, ацетата
и <1 мг Al; M— no 5 мг оксалата,
цитрата, тартрата, F, P04, Cu (II),
Ni, Co, Hg(II), Fe (III).
3) R — эриохромцианин R; e =
= 13 500; X = 512; a5 = 8,0; HM —
до 1 г CI, Br, 1, S03, SO.,, N03,
цитрата, ацетата, Сг (VI), W {VI);
M — от 10 мг и более Pb, Cd, Zn,
Mn (II), Al; no 2 мг Cu (II), Co,
Ni, Fe (III).
B. R— 1,Г-диантрамид; г =
= 8500; X = 620; a5 = 1,3
V. \ R — варнамшювый синий;
e = 5500; X = 570; a-y = 2,6; HM —
миллиграммовые количества Cr, Cu,
Fe, Mg, Mn, Ti, Zn; M — окислители.
Влияние некоторых из них может
быть устранено введением не
слишком большого избытка щавелевой
кислоты.
2) R — диэтилдитиокарбамин
натрия; е = 3800; X = 400; аь = 2,9;
М — Со, Cu, Fe, Ni, Mo, U.
3) R — Ы-бензоил^-фенилгидро-
ксиламин; е = 4800; X = 510, a5 =
= 2,0; HM — CI, N03, P04, а также
по 20 мкг цитрата, тартрата, А1,
Со, Cr, Cu, Fe, Mn, NH4, Ni, N02,
Zn; M — сильные окислители и
восстановители, а также Мо (VI),
Ti (IV), Zr (IV).
Bi. 1) R — висмутол 1, калиевая
соль; е = 12 000; X = 440; ос5 = 3,3;
2) R — ксиленоловый оранжевый;
е = 11 000; X = 545; а5 = 1,9; НМ—
алюминий, железо. После
добавления перекиси водорода не мешает
Мо (VI). Мешающее влияние сурьмы
или олова устраняется добавлением
лимонной кислоты; М — хлориды.
3) R — дитизон; е = 63 000; X =
= 505; аъ = 3,2; НМ — CI, Br, I,
CN, ацетат, цитрат, тартрат, Ag,
Au, Cd, Co, Cu, Hg, Pd, Zn, Ni;
M — сульфид, Pb, Sn, TI.
Fe. 1) R — тиогликолевая
кислота; e = 4000; X — 540; a5 = 2,3;
HM —до 100 мг CI, F, P04,
ацетата, цитрата, оксалата, тартрата,
щелочных и щелочноземельных
металлов, As; M — цианид, нитрат и
все элементы, которые дают осадок
с аммиаком.
2) R — сульфосалициловая
кислота; е = 5600; к = 420; аъ = 2,3;
НМ — щелочные и
щелочноземельные металлы, Cd, Zn и большинство
анионов, включая фосфат-ион; М —
марганец.
3) R— 1,10-фенантролин; е =
- 11 000; X = 508; ос5 --=■ 1,6; НМ —
до 25 мг Al, As, щелочных и
щелочноземельных металлов, Mn, Pb, Q,
ацетата, цитрата, нитрата, сульфата,
бромида, иоднда фторид-роданид-
ионов; М — цианид- и фосфат-ионы.
4) R — нитрозо-Р-соль, г =
= 23 000; X = 720; а5 = 1,1; М —
F, Co, Cr, Cu, CN, Ni, окислители.
5) R — 2,2'-дипиридил; s =
= 9000; X = 520; а5 = 4,5; М — Ag,
Hg, Cu, оксалат, если он
присутствует в преобладающих
количествах.
95
6) R — батофенан-тролян; p. ~
= 18 000; % = 533; аъ = 3,7; M —
сильные окислители, но действие их
может быть устранено аскарбиновой
кислотой.
Аи. 1) R — пиоктанин; е = 63;
К = 600; а5 = 9,0.
2) R — 0-толидии; е = 87 000; К =
= 437; аБ = 3,0; НМ — <0,5 мг
Ag, Си, Ni, Zn, Os, Ru и Fe могут
маскироваться фосфорной кислотой;
М — элементарный хлор, N02, Pd.
In. R — дитизон; е = 69 000;
К = 510; ов = 4,6; М — Р04, Ag,
Си, Hg, Pd. Мешающее влияние
многих катионов можно устранить,
если предварительно отделить их при
рН = 2.
Cd. R — дитизон; е = 65 000;
Ь=520;аБ = 4,2;НМ — по 1 гВг, I,
CI, S03, S04, NOs, ацетата, Bi, Zn,
Pb, Tl, Cu, Co, Ni, Hg (II), Fe (III),
Mn (II) мешают, но могут
удаляться предварительно дитизоном.
Са. R — мурексид; е =
= 10 000; А, = 490; а6 ==7; НМ —
ионы аммония Na, К, Al, Mn; M —
стронций в преобладающих
количествах, а также Mg, Ba, Fe.
Со. 1) R — 1-нитрозо-2-нафтол;
е = 34 000; К = 405; аБ = 3,8; НМ—
по 0,5 г F, C1, В г, I, S04, N03,
Р04, ацетата, тартрата, оксалата,
цитрата, Сг (VI), Cd, Pb, Zn, W (VI),
Fe (III), Mn (II), As (V), Al, Mo (VI),
V(V); M —no 50 мг Cu (II), Sn,
Sb (III), Ag.
2) R — 2-нитрозо-1 -нафтол; е =
= 14 400; % = 530; аБ = 1,3; НМ —
no 1 г Fe, CI, Br, I, S04, S03, N03,
P04, ацетата, тартрата, оксалата,
цитрата. По 0,1 г А1, V (V), Pb,
Cd, Mo (VI), Sn (IV), Sb (III); no
0,5 г Zn, W, Fe(III), Mn (II), Ag,
As(V), Cr(Vl), Ni; M—no 0,1 г
Hg(II), Cu(II).
3) R — нитрозо-Р-соль; е =
= 14 000; % = 500; аБ = 1,5; НМ —
no 1 г CI, Br, I, Fe, S04, N03, P04,
ацетата, цитрата, тартрата, Pb, Cd,
W, Mn, As, Mo, Al; M— более 0,1 г
S03, оксалата Gr (VI), Zn, Ni,
Fe (III), Cu (II), Sn(II), Sb (III),
Hg, Ag (I), V (V).
4) R — рубеано-водородная кисло-
та; е = 12 000; A, = 410; а5 = 1,3;
НМ— по 1 г О, Br, F, S03, S04,
NOs, Р04, ацетата, тартоата; <0,2 г
V (V), Мо (VI), As (V); '/А — иодид-
ион, питрат, оксалат, Ci, Pb, Zn,
Cd, Ni, Fe, Cu, Sn, Sb, Al, Hg, Ag.
Mg. R — эриохром черный Т; г—
= 23 000; Я = 530; аь = 3,7; М —
А1, Са, Со, Cu, Fe, Mn, Zn.
Mn. 1) R — формальдоксим; е =
= 11 000; % = 450; a6 = 2,4.
2) R — диэтилдитиокарбаминат
натрия; e = 4000; К — 505; аБ =
= 5,7; M^- никель и хром. Мешают
равные количества Со, Cu, Fe, Mo,
V и урана, но эти элементы могут
быть отделены экстракцией в виде
роданидных комплексов смесью те-
трагидрофурана с эфиром (1 : 1).
Си. 1) R — 2,2'-дихинолил; е =
= 6300; X = 546; осБ = 4,7; НМ —
по 2 г С1, В г, F, S04, цитрата,
тартрата. По 0,5 г Al, As (V), Сг (VI),
Мп (VII), Мо (VI), Ni, Pb, V. По 2 г
сильных окислителей, если их
восстановить аскорбиновой кислотой;
М — Ag, Cd, Co, Sn, Hg, Sb. >0,3 г
железа и >0,2 г S03, P04, оксалата.
2) R—2,9-диметил-1,10-фенан-
тролин (неокупроин); е = 7600;
К = 457; аБ = 7,5; НМ — по 2 г
перманганата, нитрата и других
окислителей, если их восстановить
избытком аскорбиновой кислоты. По
2 г С1, В г, I, S03, S04, P04, цитрата,
тартрата; по 0,5 г Al, As (V), Сг
(VI), Мп (II), Мо (VI), Ni, Pb, V.
По 1 г W (VI), Zn (II); М —Ag,
Cd, Co, Hg, Sb, Sn, >0,3 г Fe и
>0,2 г оксалата.
3) R — батокупроин; е = 12 000;
X = 460; аБ = 10,0; НМ — по 2 г
перманганата, нитрата и других
окислителей, если их восстановить
избытком аскорбиновой кислоты. По
2 г С1, В г, I, SOs, S04, P04, цитрата,
тартрата; по 0,5 г Al, As (V), Сг (VI),
Мп (II), Мо (VI), Ni, Pb, V. По 1 г
W(VI), Zn(II); M —Ag, Cd, Co,
Hg, Sb, Sn, >0,3 г Fe и >0,2 г
оксалата.
4) R — диэтилдитиокарбаминат
свинца; е = 12 000; I = 436; a5 =
= 2,3; HM— no 2 г CI, Br, I, F,
S03, S04, N03, P04, цитрата,
тартрата, оксалата, Fe (III), Mo (VI),
Pb, Zn, Al, As (V), Cr (VI), Ni,
W (VI); <0,2 г Sb (III), Cd, Sn,
V(V); M —Co, Ag, Hg, Mn(VII).
96
5) R — диэтилдитиокарбаминат
диэтиламмония; е = 12 700; К = 440;
a5 = 5,0; HM—• по 2 г F, CI, Br,
I, S04, S03, N03, P04, ацетата,
тартрата, цитрата, оксалата, Pb, Cd.
Zn, As (V), <§0,2 г Al, Ni, Mn, Sri;
M — no 1 мг W, Ag, Mo, Co, V, Hg,
Fe, Sb.
6) R — диэтилдитиокарбаминат
натрия; е = 16 000; % = 436; a5 =
= 5,5; HM— no 2 г CI, Br, I, F,
503, S04, N03, P04, оксалата,
цитрата, тартрата, Mo, Pb, Zn; <1 r
As, Cd, Sn, W, Al; M— Ag, Co, Cr,
Fe, Hg, Mn, Ni, V.
7) R — рубеановодородная
кислота; e = 10 000; К = 400; a5 = 1,3;
HM—по 2 г CI, Br, I, F, NO,,
504, P04, цитрата, оксалата,
тартрата, W, Pb, Mo, Cd, As; M — S03,
V, Ni, Mn, Fe, Cr, Co, Sn, Zn, Al.
Mo. 1) R — фенилфлуорон; е =
= 24 000; К = 510; аБ = 2,9;
2) R — 3,4-толуолдитиол(дитиол)-;
e = 23 000; К = 670; аь = 0,9; HM—
по 10 мг CI, F, цитрата, тартрата,
оксалата, Al, Ва, Са, Се, Со, Сг (III),
Fe (II), К, Mg, Mn(II), NH4, Nb,
Ni, Pb, Se, Si, Sr, Та, Th, Ti, U (VI),
V, Zn, Zr; M— Ag, As, Bi, Cr (VI),
Cu, Fe (III), Hg, Pd, Sb, Sn, N03.
Добавлением лимонной кислоты
можно устранить мешающее влияние
этих элементов.
As. R — диэтилдитиокарбаминат
серебра; е = 13 500; К = 538; ос5 =
= 2,5; НМ—большие количества
С1, В г, I, S04, P04, цитрата,
тартрата, оксалата, Na, К, NH4, Ва,
Sr, Ca, Al, Fe, Zn, Cd. Нитраты
удаляются серной кислотой, а
сульфиды улавливаются ацетатом свинца;
М — медь; мешающее влияние
небольших количеств сурьмы можно
устранить увеличением хлорида
олова (II).
Ni. R — диметилглиоксимна-
триевая соль; е = 16 000; % = 450;
аь = 1,1; М—>1 мг А1, Со, Си,
Fe, Mn, Zn.
Nb. R — 4-(2 - пиридил - азо) - pe-
зорцин-(ПАР); е = 9200; % = 550;
oc5 = 3,1; M- U (VI), V (V), РОГ.
Sn. R — фенилфлуорон; е =
= 56 000; К = 510; cc5 = 4,2; M —
сильные окислители, а также AsOl",
Cr, Fe, Mo, Pb. Sb, Та, Ti, P04.
Os. R — дифенилкарбазид; s =
= 62 000; к = 560; cs5 = 4,5; HM —
небольшие количества Cr (VI)., Ni,
Mo (VI), CI; M—Au, Cu, Fe (III).
Pd. 1) R — висмутол I; г = 7000;
л = 400; a5 — 2,8; M — нитрат и
нитрит; Au, Rh no 10 мкг.
2) R — нитрозо-Р-соль; е =
= 14 000; к = 510; a5 = 2,1; M —
Co, а также по 100 мг Ag, Cu, Fe,
Hg, Ni, Se, Sn, Zn.
Pt. R — дитизон; e = 27000; К =
= 710; a5 = 6,1; влияние Ag, Cu
и Hg устраняется добавлением
соляной кислоты. НМ — Bi, Cd, Co, Fe,
In, Mn, Ni, Pb, TI, Zn. M — Au, Pd.
Rh. R — 1 - (2-пиридил-азо) - 2-
нафтол(ПАН); е = 5700; % = 598;
a5 = 6,6; M — иридий дает подобную
реакцию.
Hg. R — дитизон; е = 68 000;
% = 485; a5 — 3,5; HM —
миллиграммовые количества СГ, CN",
SCH~, Bi, Cd, Co, Cu, Fe, Ni, Sn,
TI, Zn; M—I", S2-, S2Or, Ag,
Au, Pd, Pt.
Pb. 1) R — дитизон; е =
= 62 000; К = 520; ax = 6,2; HM —
no 1 г Br, I, CI, F, S03, S04, N03,
P04, цитрата, тартрата, ацетата,
оксалата, если после установки
рН = 7-i-8 добавить еще 0,3—0,5 мл
15%-ного раствора аммиака; М —
Bi (III), Cr (VI), Fe (III), Mn (II),
TI (I).
2) R — диэтилдитиокарбаминат
натрия; е = 11 000; К = 436; a5 =
= 4,0; HM— no 1 г CI, Br, I,
N03, S03, S04, ацетата, цитрата,
тартрата, оксалата, фосфата, если
установить аммиаком рН = 11-^12.
Большие количества Cd, Zn, Ni, Cu,
Mn и Al можно маскировать цианид-
ионом; М — по 5 мг Fe (III), Sn (II),
Sb (III), Hg, Ag, Co (II).
Se. R — 3,3'-диаминобензидин-
тетрахлорид; е = 8000; К = 420; a5=
= 3,7; HM—CI, Br, N03, P04,
S04, цитраты, тартраты, оксалаты,
<5 мг Ag, As, Au, Co, Cr (III),
Cu (II), Hg, Ni; M— >1 мг Те,
а также сильные окислители.
Sc. R — ализариновый красный
S; е = 5400; X = 520; ос5 = 8,0; М —
А1, Ва, Be, Bi, Са, Cu, Fe, Hg, К,
Pb, Pt, Sn, TI, РЗЭ.
7 А. И. Лазарев и др-
97
Sb. 1) R — родамин В; е =
= 82 000; К = 565; аъ = 1; НМ —
миллиграммовые количества Ag, A1,
Cd, Со, Сг (III), Cu, Fe (II), Hg (II),
Mg, Mn, Ni, Pb, F, CI, N03, S04;
M—Au, Cr(VI), Fe (III),. Tl, U,
V, W.
2) R — диэтилдитиокарбаминат
серебра; е = 17 500; К = 507; oc5 =
= 6,5; НМ — большие количества
CI, Br, I, S04, P04, цитрата, тар-
трата, оксалата, Na, К, NH4, Ba,
Sr, Ca, Al, Fe, Zn, Cd; M — нитраты
(можно удалить серной кислотой).
Tl. 1) R — бриллиантовый
зеленый; е = 90 000; X = 632; ос5 = 6,1.
2) R — кристаллический
фиолетовый; е = 90 000; К = 595; осБ = 1,4.
Ti. 1) R — диантипирилметан
(+роданид); е = 60 000; К = 420;
а5 = 3,2; НМ — до 10 мг фторидов,
фосфатов, комплексонатов. Железо
(III) и медь (II) восстанавливаются
хлоридом олова.
2) R — дихлорхромотроповая
кислота; е = 11 200; К = 490; а5 = 1,6;
М— фториды, окислители.
Cr. R — дифенилкарбазид; е =
= 34 000; К = 540; аъ = 0,2; М —
N03, Ag, Al, Co, Cu, Hg, Ni,
Pb, Zn.
Се. R — 8-оксихинолин; e=
= 6000; A, = 505; a5 = 7,3; HM —
миллиграммовые количества Al, As,
Bi, Co, Cr, Cu, Hg, Mo, Ni, Pb, Sb,
Se, Sn, Те, Ti, V, W, Zr; M—
фториды.
Zn. 1) R — дитизон; е — 95 000;
К = 538; a5 = 11; НМ —
миллиграммовые количества Au, Ag, As,
Co, Cu, Cd, Fe, Hg, In, Mn, Ni,
Pb, Tl.
2) R — 1-(2-пиридилазо)-2-нафтол
(ПАН); е = 48 000; К = 540; a5 =
= 2,2; HM — до 0,2 мг Co, Fe, Ni.
Zr. 1) R — фенилфлуорон; е =
= 55 000; К => 540; ab = 3,5; HM —
до 1 мг F, Fe, As, Sb, фосфата,
оксалата.
2) R — ксиленоловый оранжевый;
e = 12 800; К = 535; a5 = 3,2; HM —
миллиграммовые количества Al, Bi,
Cd, Co, Cr, Cu, Fe, Hg, Mn, Ni,
Pb, Sn.
15. МАСКИРУЮЩИЕ РЕАГЕНТЫ ДЛЯ МЕТАЛЛОВ
И НЕКОТОРЫХ АНИОНОВ
Ag—CN~, NH3, S202r,
Br", I", CI", тиоглико-
левая кислота;
Al — F"", C2O4-, ацетат-ион-
цитрат, тартрат,
комплексов III, ОН-,
2,3-димеркапто-1-пропа-
нол, триэтаноламин,
глюконат, ацетилаце-
тон, силициловая, суль-
фосалициловая
молочная кислота, фосфат,
пирофосфат;
As — S2", ОН", 2,3-димер-
капто-1 -пропанол;
Au — CN", Br", S203~;
В — F", оксикислоты, гли-
коли;
Ва — комплексен III, цитрат,
тартрат, нитрилтри-
уксусная кислота, SC>4~
Be — F~, цитрат, тартрат,
COj-", сульфосалици-
ловая, салициловая
кислоты;
Bi — цитрат, тартрат, кем
плексон III, 1~, С1~
нитрилтриуксусная
кислота, тиомочевина:
триэтаноламин, 2,3-ди
меркапто-1-пропанол,
тиогликолевая кислота
Са — комплексен III, цитрат,
тартрат, пирофосфат,
нитрилтриуксусная
кислота, F~;
Cd — комплексен III, CN
S203~, SCN~, Г, цит
рат, тартрат, нитрил
триуксусная кислота
унитиол, тиогликоле
вая кислота;
Се — F", комплексен III,
нитрилтриуксусная
кислота, цитрат,
тартрат, тайрон, сахара;
Со — NH3, NOr, SCN-, CN,
Н2О2, S203_,
комплексен III,
нитрилтриуксусная кислота, цит-
98
Сг(Ш)
Си
Fe (III)
рат, тартрат, этилен-
диамин, 2,3 - димер -
капто-1-пропанол, 2,2';
2"- триаминотриэтила -
мин, полиамины;
— комплексон III (при
нагревании), нитрил-
триуксусная кислота,
цитрат, тартрат, три-
этаноламин,
аскорбиновая кислота;
- NH3, SCN-, Г, CN",
S2O3-, тиомочевина,
комплексон III, S2-, ди-
этилдитиокарбаминат,
цитрат, тартрат, нит-
рилтриуксусная
кислота, тиогликолевая
кислота, триэтанола-
мин, полиамины;
-F-, РОГ, Р20?~, ни-
трилтриуксусная
кислота, комплексон III,
диэтилдитиокарбами-
нат, цитрат, тартрат,
2,3-димеркапто -1 - про ■
панол, SCN-, S2( '
s2or
Ge
Hf
Hg
'■+
In
Ir
QOr, CN~, тайрон,
аскорбиновая кислота,
тиомочевина, 1,10-фе-
нантролин, S2-,
тиогликолевая кислота,
триэтаноламин, а, а'-
дипиридил, глюконат,
сульфосалицилат, гли-
коли;
- СгОГ, F~, гликоли,
ЭДТА;
- F~, ILO2, SO4", цитрат,
тартрат, митрилтри-
уксусная кислота,
комплексон III, РгОГ,
РОГ, САГ,
триэтаноламин;
Г, SCt, СгГ, СГ,
S2Or, цитрат, тартрат,
тиогликолевая кислота,
комплексон III,
триэтаноламин, унитиол, тио-
семикарбазид, нитрил
триуксусная кислота,
тиомочевина;
■ тиогликолевая кислота;
SCN", цитрат, тартрат,
тиомочевина;
So
Mg — нитрилтриуксусная
кислота, комплексон
III, СгОГ, цитрат,
тартрат, ОН-, РгОт-,
гликоли, F";
Mn - F~, C£t, P20?-,
нитрилтриуксусная
кислота, комплексон III
триэтаноламин, цитрат,
тартрат, окисляющие
реагенты;
Мо — SCN", С2ОГ, Н-А,
цитрат, тартрат,
комплексон III,
нитрилтриуксусная кислота,
тайрон;
Nb — F~, ОН", Н202, GOr,
цитрат, тартрат,
тайрон, гликоли;
Ni — CN", SCN", NH3,
цитрат, тартрат,
комплексон III,
нитрилтриуксусная кислота;
Os — CN", SCN-,
Pb — Г, ацетат, S203~,
цитрат, тартрат,
комплексон III,
нитрилтриуксусная кислота,
SO4-, унитиол,
тиогликолевая кислота, ме-
тафосфат;
Pd — CN~, Г, NH3, NOT,
SCN", S2Ol~, цитрат,
тартрат, ацетилацетон
нитрилтриуксусная
кислота, комплексон
III, триэтаноламин;
Pt— NH3, Г, CN", N07,
SCN-, S20r, цитрат,
тартрат,
нитрилтриуксусная кислота,
комплексон III, метафос-
фат;
Rh — тиомочевина, цитрат,
тартрат;
Sb — цитрат, тартрат;
F-, Г, S2", S20JT,
диаминобензидин,
тартрат, цитрат,
восстановители;
Sn — цитрат, тартрат, F~, I~t
О-ОГ, ОН-,
триэтаноламин, тиогликолевая
кислота, РОГ. гликоли;
и его
анионы
7*
99
Tl
Sr — S04~, нитрилтриуксус-
ная кислота, комплек-
сон III, цитрат, тар-
трат, гликоли;
Та — F", ОН, цитрат, тартрат;
Th — F~, нитрилтриуксус-
ная кислота,
комплексен III, цитрат, тартрат,
триэтаноламин, ацетат;
SOl-, OH~, Н202, F",
нитрилтриуксусная
кислота, комплексон III,
цитрат, тартрат, тайрон,
триэтаноламин, глюко-
нат, молочная, сульфо-
салицилат, гликоли;
С1~, CN~,
нитрилтриуксусная кислота,
комплексон III, цитрат,
тартрат, триэтаноламин
тиогликолевая кислота;
TI
U
л2—
•\2—
Н2О2,
f-, cor, Qoa
цитрат, тартрат;
V - CN-, Н202, F",
комплексон III, тайрон,
триэтаноламин;
W — тайрон, F\ SCN", Н202,
цитрат, тартрат, окса-
лат;
2п — CN~, шгЕрилтриуксус-
ная кислота,
комплексон III, цитрат,
тартрат, SCN~, ОН",
NH3, гликоли, уни-
тиол, тиогликолевая
кислота, полиамины;
Zr — F~, SOl-, цитрат,
тартрат, нятрилтриуксус-
ная кислота,
комплексон III, Н202, Р20?-,
РОГ, СгО!-,
триэтаноламин;
GI- - Hg2+;
CN~ — НСНО, переходные
металлы;
F" — Н3В03, Al, Be, Ti, Zr,
Nb, Та, Fe(III);
I- - Hg2+;
S2" —S;
S — CN~, S2-, S02r;
sot— Hg2^ нсно.
16. РАЦИОНАЛЬНЫЕ ВЕЛИЧИНЫ
В ХИМИЧЕСКОМ АНАЛИЗЕ
Рациональные величины (навески,
объемы, титры, аликвотные части
и пр.) позволяют получать
результаты анализа непосредственно по
показаниям измерительного прибора
(весов, шкалы бюреток,
гальванометра, шкалы фотоколориметра и
т. д.). В некоторых случаях
результаты анализа получаются из простых
расчетных действий, обычно
производимых в уме.
16.1. ГРАВИМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА
Рациональная величина
Масса (навеска), анализируемого
вещества, г
Объем анализируемого раствора, мл
Единица
измерения
определяемого
компонента
%
г/л
г-экв/л
мг-экв/л
моль/л
Формула для нахождения
рациональной величины
6рац = ЮОкФ
Vpaa = 100<М:Ф
10ШФ
' рац — рд
10вЙФ
Р™1 "" МГ-ЭКВ
„ 10006Ф
1 раи моль
Примечание. Ф — фактор пересчета в гравиметрическом методе анализа; k —
коэффициент, необходимый для обеспечения нужной точности анализа. Обычно I > k > Ю-*. Величина *
зависит от величины Ф и содержания определяемого компонента; Ь„ — рациональная масса (вес)
вещества, взятого на анализ, р; V — рациональный объем раствора анализируемого вещества,
взятый для анализа, мл; ГЭ, мг-экв и моль — грамм-эквивалент, милнграмм-эквнвалеит и молекулярная
масса анализируемого вещества соответственно.
100
Расчет содержания определяемого
компонента производят по формуле
X = alk, где а — масса (вес)
полученного осадка, г (с учетом
холостой пробы).
Пример 1. Найти рациональную
навеску для определения никеля
гравиметрическим методом с осаждением
его диметилглиоксимом.
Анализируется сталь, содержащая примерно
3% никеля. Расчет производится
по формуле Ьраа = 100&Ф.
Фактор пересчета для взвешиваемого
осадка на металлический никель
Ф = 0,2032. Если принять
коэффициент k равным 1, то величина
рациональной навески будет равна
20,32 г. Но это нереально. Если
считать достаточной и удобной величину
взвешиваемого осадка 0,3 г, то
коэффициент k следует установить
равным 0,1. В таком случае
рациональной будет навеска, равная Ьрт =
= 100-0,1.0,2032 = 2,0320 г. В
таком случае, получив вес осадка,
делят его на величину k и получают
содержание никеля: % Ni = a : 0,1.
Пример 2. Найти рациональную
навеску для гравиметрического
определения кремния в виде двуокиси
кремния. Анализируется сталь,
содержащая примерно 0,2% кремния.
Факторный множитель Ф = 0,4672.
Если k принять равным единице,
то рациональная навеска будет
составлять 46,72 г, что, конечно,
неприемлемо. Чтобы получить вес
осадка равным примерно 20 мг и
устранить неудобства в аналитических
операциях, рационально взять
навеску с учетом коэффициента k —
= 0,01. В этом случае рациональная
навеска составит величину bp3a =
= 100-0,01 -0,4672 = 0,4672 г.
Содержание кремния в процентах находят,
деля вес полученного осадка на 0,01.
Пример 3. Найти рациональный
объем для определении сульфат-иоиа
в электролите для цианистого кадми-
рования. Сульфат-ион осаждается и
взвешивается в виде сернокислого
бария. Содержание сульфат-иона
составляет примерно 10 г/л.
Фактор пересчета веса осадка
сернокислого бария на сульфат-ион
равен Ф = 0,4115. При k = 0,01
рациональный объем составит 4,12 мл,
а при k = 0,1—41,15 мл.
Пример 4. Найти рациональный
объем для определения кальция
в природных водах. Результаты
анализа выразить в мг-экв/л. Осадок
взвешивается в виде окиси кальция.
Фактор пересчета окиси
кальция на искомый кальций Ф =
= 0,7147. Грамм-эквивалент
кальция равен 20,24 г. Рациональный
объем воды, который необходимо
взять для анализа, составит при
коэффициенте k = 0,001
т. 106-0,00! -0,7147 ос сс
VPW = Щ4 = 35,66 МЛ-
16. 2. ТИТРИМЕТРИЧЕСКИЙ
МЕТОД АНАЛИЗА
Рациональные величины в титри-
метрическом методе анализа могут
быть использованы во всех
вариантах этого метода, обусловленных
способами индикации конечной точки
титрования. Рациональные
величины сохраняют постоянство, если титр
раствора не изменяется. Если титр
используемого для титрования
раствора изменился, то следует
произвести расчет новых рациональных
величин.
Рациональная величина
Масса (навеска) анализируемого
вещества при титровании всей
навески, г
Масса (навеска) анализируемого
вещества при титровании аликвотной
части из общего объема раствора, г
Единица
измерения
определяемого
компонента
%
%
Формула для нахождения
рациональной величины
Ьоя„ — lOOkT
. 10Qft7To
°рац — ,,
v a
101
Продолжение
Рациональная величина
Титр раствора при титровании всей
Объем аликвотиой части раствора,
взятый для титрования из общего
объема, в котором растворена наве-
Объем при титровании растворов,
Титр при титровании растворов,
©бъем при титровании растворов, мл
Единица
измерения
определяемого
компонента
%
%
f/л
г/л
г-экв/л
мг-экв/л
моль/л
Формула для нахождения
рациональной величины
т 0,01Ьо
1 Ран - k
l00kTVo
рац h
Урац — lOOOW
ГПя„ —0,001 — V»
„ 10006Г
Ирац ~ гэ
„ ючт
Крац ~ мг-экв
„ 10006Г
Ирац~ моль
Примечание. ЬПаг„ 7' V„.,. — соответственно рациональные навеска, тнтр, объем;
нац. рац рац
V — расход тнтранта, мл; k — коэффициент, имеющий то же значение, что н в рациональных
величинах для гравиметрического метода анализа; Т — титр раствора, используемого для титрования, г/мл;
V — общий объем раствора, в котором растворена навеска, мл; V — аликвотная часть раствора,
взятая для анализа, мл; b — MaGca (навеска) анализируемого вещества (для данной сернн анализов
аадается постоянной), р.
Содержание определяемого
компонента рассчитывают по формуле X =
= Wife.
Пример 1. Вычислить
рациональный титр раствора иода для
определения серы в металлах методом
сожжения в токе кислорода. Содержание
серы в металле колеблется от 0,01
до 0,05%.
Примем навеску, равную 1 г.
Тогда при к—100 рациональный титр
равен Трац — -—^— = 0,0001 г/мл.
В практике обычно при сжигании
серы используют навеску стали 0,5 г.
В таком случае рациональный титр
будет равен 0,00005 г/мл. Тогда при
титровании количество миллилитров
израсходованного раствора,
поделенное на 100, даст искомое содержание
в процентах.
Пример 2. Вычислить
рациональный титр раствора комплексона III
при определении никеля в титановых
сплавах. Содержание никеля в
сплавах до 5%.
Если навеска сплава, взятая для
анализа, равна 1 г и титруется
какая-то часть ее, то достаточную
точность анализа можно достигнуть
при титровании из микробюретки
при расходе титранта более 1 мл.
Например, титруется 1/10 часть
навески. При k — 10 рациональный
титр будет равен 0,001 г/мл.
Пример 3. Вычислить величину
рациональной навески для
определения содержания меди в рудах иодид-
ным методом с использованием
титрованного раствора тиосульфата.
Содержание меди в анализируемом
материале составляет 1—4%.
ьрац = ЮО/гГ. Пусть титр
раствора тиосульфата равен Т =
= 0,0100 г/мл. Для k — 1
рациональная навеска будет составлять
1 г и при содержании меди 1—4%
расход титранта составит 1—4 мл.
При k = 10 рациональная навеска
составит 10 г, а расход титранта
10—40 мл. Следовательно, следует
выбрать коэффициент k = 1 и
рациональную навеску 1 г, а для
обеспечения достаточной точности
анализа раствор титранта отмеривать
из микро- или полумикробюретки.
102
16. 3. ФОТОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА
Рациональная величина
Масса (навеска) анализируемого
вещества, г, при фотометрировании всей
навескн
Объем анализируемого раствора, мл
Объем анализируемого раствора, мл
Масса (навеска) анализируемого
вещества при фотометрировании али-
квотной части, взятой из общего
объема, г
Масса (навеска) анализируемого
вещества при применении стандартного
образца с содержанием (Р, %)
определяемого компонента, г
То же самое, но при анализе из али-
квотной части, взятой из общего
объема, VQ, г
Единица
измерения
определяемого
компонента
%
г/т
(или мкг/г)
г/л
мг/л
мкг/л
моль/л
г-экв/л
мг-экв/л
%
%
%
Формула для нахождения
рациональной величины
и lOO&lcT
°Рац г)
£/Ст
100£Креакц моль
bv™ ~ lOOOel
„ lOOOfaio
*>ц - Dq
Ирац -- Dq
"рац - 0o
„ \000kao
Vpm~ t-o-моль
T/ 1000ftoo
10"too
1 veu- - и0-мг-экв
W0kaoVo
Рац " D0Va.4
PkH„V0
°Pau - .,
,, Pft«ciVo
PaU " U0Va. ч
П р И !
e ч а и и е.
известная масса определяемого вещества, содержащаяся ь
реакционном объеме, г; D , £> — оптическая плотность раствора, содержащего в реакционном объеме
а грамм определяемого вещества: l7D — объем фотометрируемого раствора, мл; е — коэффициент
------ - " -' в ко-
масса
(навеска) стандартного образца, взятая для анализа (определения £>0). г; моль, ГЭ. мг-экв —
соответственно, моль, грамм-эквивалент, миллиграмм-эквивалент искомого вещества.
Содержание определяемого
компонента рассчитывали по формуле X =
= DJk.
Рациональные величины в
фотометрическом анализе вычисляются
перед работой и пригодны только
при работе с данным
спектрофотометром (фотоэлектроколориметром).
Соблюдение закона Бугера—Бера
обязательно. Обязательна
периодическая проверка постоянства
кажущегося коэффициента молярного
погашения. Целесообразно
пользоваться стандартными образцами
ВНИИСО. Формулы для вычисления
рациональных величин справедливы
и для турбидиметрических и экстрак-
ционно-фотометрических
определений.
Пример 1. Вычислить
рациональную навеску стали при определении
в ней п-10~3% кобальта фотометри-
103
ческим методом с нитрозо-Р-солью.
Фотометрируемый объем Vpe^ =
= 25 мл. Используется стандартный
раствор кобальта, содержащий а0 —
= 4,20 мкг/25 мл кобальта. Кювета
с / = 5 см. Оптическая плотность
D0 = 0,210.
Используем формулу Ьрац =
\00kacr
— причем в данном случае
А
экстракта с метиловым фиолетовым.
Содержание сурьмы в образце более
10_4%. Анализируется вся навеска.
Стандартный раствор сурьмы
содержит 4,6 мкг сурьмы в 12 мл экстракта
и имеет оптическую илотносгь в
кювете с / = 3 см D0 = 0,520.
Используя ту же формулу, что
и в примере 1, получаем для: k —
ст
и
100
1-4,2-Ю"6
рац
При к = 1
= 2 • 10~3 г,
0,2 г, при к =
100 Ьп
0,046 г; Dx
0,21
при к — 100 Ьрац
= 200 Ьрац = 0,4 г.
Отсюда следует, что для расчета
результатов анализа при содержании
кобальта 0,001% при навеске 2-10~*
оптическая плотность раствора будет
равна Dx = 0,001, а при навеске
0,2 tDx = 0,1. Так как
определяются содержания п-10-3%, то
целесообразно в качестве рациональной
навески выбрать 0,2 г (к = 100).
При большей навеске величины
оптических плотностей могут получиться
слишком высокими и неточно
измеряются.
Пример 2. Вычислить
рациональную массу (навеску) для определения
сурьмы экстракционно-фотометриче-
ским методом в виде толуольного
%X = ИГ4; k = ЮО0 6рац = 0,46 г;
Dx = 0,1; %X = 10~4; k = 2000
bpau = 0,92 r; Dx = 0,2; %X =
= 10"4.
Отсюда следует, что наиболее
удобной и рациональной является
навеска величиной 0,92 г.
Пример 3. Вычислить
рациональный объем природной воды для
определения в ней содержания меди
в мкг/л (в воде содержится более
100 мкг/л медя) с помощью диэтил-
дитиокарбамината свинца. Толуоль-
ный экстракт объемом 12 мл и при
содержании меди 10,1 мкг в кювете
с / — 3 см имеет оптическую
плотность D0 = 0,500 при 400 нм.
Используется формула Vn
l0akao
Do
Наиболее
рац
удобным
является значение к = 0,002, а
рациональным объем величиной 40,4 мл.
17. РАСТВОРЫ
17. I. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ И ФОРМУЛЫ ПЕРЕСЧЕТА
Основные термины концентрации
Наименование
Грамм-атом
Грамм-ион
Моль (грамм-моль)
Грамм-эквивалент
Краткое
обозначение,
формула
г-атом
г-ион
моль
г-экв
Пояснение
Атомная масса элемента, выраженная в граммах
Масса иона как сумма атомных масс веек соста-
вляющнх ево элементов, выраженная в граммах
Молекулярная пасса соединения, внраженная
в граммах
Эквивалентная масса, выраженная в граммах
Наименование
Растворенное вещество
I раммы растворителя
Граммы растворенного вещества
Миллилитры растворителя
Миллилитры растворенного
вещества
Число молей растворителя
Число молен растворенного
вещества
Число эквивалентов
растворенного вещества
Обозначение
А 1
§р
ША
mlp
пАа
пр \
ПА
Са
Наименование
Миллилитры раствора
Плотность растворителя
Плотность растворенного
вещества
Плотность раствора
Молекулярная масса
растворителя
Молекулярная масса
растворенного вещества
Эквивалентная масса
растворенного вещества
Обозначение
V
£
dA
dR
МВр
MB А
CBA
104
Основные способы выражения концентрации
Наименование
Обозначение
Пояснение
14
Весовое соотношение q .
Весовая часть W'а
Процент (по массе) %
Объемный процент
Молярное соотношение
Молярная доля у.
Молярный, % (мол.)
Молярность Ма
(объемная молярность)
Нормальность Na
Разбавление Va
Моляльность гпа
(весовая молярность)
Весовая нормальность х
1а =■
Ва
W,
%=■
еА
L+gn
Ва
100
Л + Вр
% (объемн.) = —у—
па 100 (или 1000)
А~ nD
У А
ПА
ПА + Яр
% (мол.)
МА =
NA =
Va
__паШ_
па + лр
яд1000
V
С.^ЮОО
v
ллЮОО
v
QdlOOO
X =
у —
л^1000
gp
СлЮОО
gp
8Ат
V
ёА\Ш)
Количество граммов
растворенного вещества Л на 1 г
растворителя
Количество граммов
растворенного вещества в общем весе
смеси
Количество граммов вещества А
в 100 г раствора
Количество миллилитров
растворенного вещества А в 100 мл
раствора (только для смесей
жидкостей или газов)
Число молей растворенного
вещества А, приходящееся на 100
или 1000 молей растворителя
Число молей растворенного
вещества А по отношению к
общему числу молей веществ
в смеси
Число молей растворенного
вещества Л в 100 моля* ияствер;1
Число молей растворенной ье-
щества Л в 1 л раствора
Число эквивалентов,
пйсчкоренного вещества А в i л раствор-.
Число литров раствори, -сдер-
жащих 1 моль или i г--.кг>
растворенного вещества. Пол
разбавлением также понимается
число грамк-растворичел? на 1 i
растворенного вещеовь kj\i-.
число рранш растворителя на
1 моль растворенного вещества
Число молен растворенного ее
ществв А. приходящихся на
1 кг растворителя
Число грамм-экБивьлекюБ
претворенного вещества
приходящихся на ! кг растворителя
Число грамм растворенного ве-
шествя А в 100 м.ч раствор?
Число 1рам;.: инстгоре;.ко;с
вещества А в 1 л раствора
Выражения № 1—3 и 5—7 спра- справедливо только для жидких и
ведливы для жидких, твердых и га- газообразных смесей, но не для твер-
зообразных смесей. Выражение № 4 дых веществ.
105
1аблица :ля пересчета одних способов выражения концентрации на другие
Требуемое выражение
концентрации вещества А
Соотношение масс
Чана
Часть по пассе
«.4
W
*Л + 2р
Процент по массе
Соотношение масс
gA
Чл=-
8р
U- i~wA
Ча 100—%
Часть но массе
ёА
WA =
SA + SP
WA=-
1л
1 + ЯА
WA = -
00
Процент по массе
ёАЮ0
%=■
8 а + ёр
Чл
ЮС
1 + Ял
%=WAW
Объемны! процент
т1АШ)
% (объемн.) = •
% (объемн.) =
ЧА V00
(> + ЧЛ) dA
% (объемн.) =
WAdRlQ0
% (объемн.) =■
dA
Молярное соотношение
м лл100 (или 1000)
а.МВ„ 100 (или 1000)
ША = -^ Е__1 L
л МВА
MVA =
Гл/И5р100(или 1000)
(\—WA)MBA
MVA
%/И5рЮ0(или 1000)
(№-%)МВА
Молярная доля
пА
Уа~ пА + пр
УА =
Чамвр
ддМВ +МВА
WAMBP
ул — мв А (\ — wA) + wambp
Уа =
% мвр
% МВр + Л1ВА100 — % М-ВА
Молярный процент
% (мол.) =■
1.4 + лр
fl .MS 100
% (мол.) = —г^б р
дАмвр + МВа
% (мол.) =
WAMBPW)
MBA(l-WA) + WAMBp
I (МОЛ.) =
%MBplOO
% МВР + МВД If0 — Го МВЛ
Молярность
А V
Л!д =
(1 + ?д)Л1Вд
м,=
Г л^ ЮОО
.VJfl4
Ма~ MB а
Нормальность
Na
С а Ю00
NA =
7A(iR1000
/Ул = -
СВА
Na= /0
о й(«10
св„
^л =
Разбавление
у ,. v
rt^lOOO ^_СлЮ00
VA =
(I + qA) MBл (или С5д)
(/Л^1000
^Л =
МВА (или С5л)
1ГдйК1009
Ил =
MBА (a.in СВА)
% dRl0
Нормальность по массе
СА ЮОО
# =
<?дЮ00
свА
WA1000
(l-WA)Cfl„
% 1000
(100- %)СВА
12
Л00
у = -
1 + Ь)
y = WAiRlQ0
У = % <*R
13
г =
£д
1000
г =
qAdR\0Q0
(1+ЯА)
г = Гл^1000
г = % rfRlO
Продолжение
Требуемое выражение
концентрации вещества А
Объемный процент
% (обьеми.) .-
Молярное соотношение
п^ЮО (или 1000)
MV
Соотношение масс
Ча =
Sa
% (объеми.) dA
qA — d^WO — % (объемн.) dA
a MVAMBA
Ча AlflplOO (или 1000)
Часть по массе
wA= if
еА + 8р
w % (объемн.) dA
А = dRW0
MVAMBA
MVaMBa +МВр100 (или 1000)
Процент по массе
йЛЮ0
% = /*, п
еА + 8р
% (объеми.) dA
dR
оу = МУАМВА№
/0 MVaMBa+MBp№ (или 1000)
Объемный процент
mlл 100
% (объемн.) = ■
0 MVAMBAdR№
/о (ооъемн.) _ dA щуаМва + МВъШ (или 1000)]
Молярное соотношение
М\'я - "-4'00 (ИЛ" 10°0)
% (объемн.) dRMBp 100 (или 1000)
MVa = MBA [dR№ — dA % (объемн.)]
Молярная доля
па
<Ул=-
УА=ТЛ
% (объеми.) dAMBp
"А + «Р
% (объемн.)dAMBp + MBA\dR\O0— % (объемн.)йд]
Уа-
W;
MVA+'100 (или 1000)
% (мол.) =
% (объемнО^М£рН>0.
лЩПЛйТТ^Тоо^ % (°бъемн-) ^
МУд 100
% (мол.) =Л1у^ юо (или 1000)
MVa<jrI№
Мл ~ 'MVAMBA + AlSplOO (или 1000)
?1000
Л'л — САд[МУдМАд + М#р1(Х) (или 1000)]
МУ„М5л + /WSplDO (или 1000) _ г СВа_-\
Va = /ИУ^ЮОО ' L МВА J
ЗДУлМДдЮОО
CBAMBpW (иЛи ЮОО)
/^улМД4а(^100
V~ М^4/Ивл+/ИДРЮ>(или 1000)
,\WaMBaJrIW>
г ~ МУАМВд + МВр100{и™ 10UO)
Продолжение
Требуемое выражение
концентрации вещества А
Молярная доля
Л пА + "р
Молярный процент
{мол.)=
пА+пр
Соотношение масс
8а
4 =
8р
п УАША
«л- (1-Х)МВр
__ % (мол.) МВА
qA [100 -% (мол,)]Л15р
Часть по массе
Вл
WA
8л + Вр
Процент по массе
£л100
% =
ёА + ёр
WA =
уАмвА
уамвд + {1-Уа}мвр
%
V^Alfl^lOO
уАМВД + {1-уА)МВр
Wa =
% (мол.) МВА
% (мол.)Л15л + [100— % (мол.)] МЗр
% (мол.) МВА100
% (мол.) МВА + [ 100 — % (мол.)] МВР
Объемный процент
, , в ч mlA\00
% (объеми.) = —
% (объемн.) •
yAMBAdR 100
lVAMBA+(l-YA)MBp]dA
% (объемн.) =
% (Mon.)MBAdRl00
% (мол.) MBAdA -f [(100 — % (мол.)] MBpdA
Л1оляриое соотношение
му _ «Л Ю0 (или 1000)
Л1КЛ =
уд 100 (или 1000)
Л1ИЛ
% (мол.) 100 (или 1000)
100— % (мол.)
Молярная доля
пА
У а
"А + Пр
% (мол.)
уА— ЮО
Молярный процент
«л LOO
% (мол.) =
Па -Г «1
Г "р
% (МОЛ.) = Уд ЮО
Молярпость
яд W00
Мл=-
ЛЬ =
тА1000
уяА1В/, + (1-Т14)Шр
Мд =
A=jr
% (мол.) <*д 1000
(мол.) УИВд + 1100 — о/„ (мол.)] /ИВР
Нормальность
A'j
С 41000
МВАуАйя\Юл
\4AMBA + (\-yA)MBv]CBA
N.\ =
Мйд% (мол.) <*д 1000
СВл 1% (мол.) MBА + (100 - о/0 (мол.)) Л1ЙР]
in
17л
Разбавление
или 1/д =
«41ооо н Сдюоо;
улМВл + ('-ул)^р г Сил 1
L мвд j
_ % (мол.) МВА + (100 - о/0 (мол.)) /ИВР г СВА 1
А ~ % (мол.) d«1000 ' J. МВЛ j
Нормальность по мае
х =
СА10QQ
X =
Д!ВлулЮ00
сал(1-ул)лшр
МВд о/о (мол.) 1000
СВд [100—% (мол.)]Л4Вр
12
§а[ "
10.-,
</ = ■
vAMB*100
ул(МВл-Л!Вр) + Л1Вр
% (мол.) dRMBAW)
У ~ % (мол.) (МВА — МВр) + Л1ВР100
yAdRMBA\0d0
уА(тА-мва) + мвр
г =
% (мол.) <*д/ИВл1000
'6 (мол.) (МВд — МВР) + Л'ШрЮО
Продолжение
й
<
с
3
4
5
6
Требуемое выражение
концентрацги вещества А
Соотношение масс
14 §р
Часть по массе
" sA + gp
Пропент по мавсе
..„ W100
/0 «„+V
Объемный процен!
«/„(объеми.)-"^100
Молярное соотношение
щ, пА 100 (или 1000)
Молярная доля
Л ПА + »р
8
Молярнооть
лЛООО
/И. =
МАМВА
^А~ dRl000 — MAMBA
WA - М№*
А dRl0C0
*-■*№■
%m^-J!fflL
МАМВplOO (или 1000)
MVa~ dRW00—MAMBA
MAMBV
УА ~ d«!0OO + MA (MBP — MBA)
9
Нормальность
С Л0О0
VA V
NAQeA
^A urIOOO —NAC ВД
A d^lOOO
%-NaC$a
/0 4}10
о,(объемн,=^
#дСА ^ВрЮС (или 1000)
MVA~ MBa (d/?iooo — Л^СВд)
УулС^Л1Вр
УЛ ~ ЫАСВАМВР + Л1В^ (d^lOOO _ NaCBa)
7
h
9
10
11
12
13
Полярный процент
% (мол.) =—2Д»й—
"А + Пр
Молярность
с
Нормальность
СлЮОО.
Na = '—*
V
Разбавление
и v
1а~ пА 1000 ,ип»л-Сл 1000
Нормальность по массе
к=^1(?00.
«Р
§л100
j/=—.*
ёлЮ00
Л^/ИйрКО
,„ ^ол.; - dRim+MA (MBp — MBA)
МАМВА
Na~ сва
ул 1 Г СВА "J
14 Л1л L МВА J
tffti&iiooo
"— Сил №1000— МАМВА)
МАМВА
У ~ in
г = МАМВА
na.cba-mbp.ioo
/0 (»юл.) _ мА.СВА.МВр + MBA(dp.1000-NA.CBA)
м Л^лСВл
17 MB^ . ., 1
А - NACBA ' л NA
мА\т
dRl000 — NACBA
NACBA
y 10
г = NACBA
Продолжение
Требуемое выражение
концентрации вещества Л
Разбавление (молярное или нормальное)
V,=
А пА (или СА) 1000
Нормальность по массе
Соотношение масо
8а
Ч ='
Яр
МВА (или СВА)
Яа ~ Уд*? 1000 — MBA (или СВА)
хСВА
qA~ 1000
Часть по массе
Фл =
8а
&А + 8Р
Wa =
MB а (или СВА)
VAdR\0O0
WA =
хСВА
хСВА + 1000
Процент по массе
£л'00
о? — *А _,
ft» + *P
__Мйд(или Сбд)
K4d*10
98 =
хСВА
хСВА + 1000
Объемный процент
% (объемн.) =
ml A100
% (объемн.)
МДд(или Сбд)
V4d410
% (объемн.) ■
xCBAdR\00
dA(xCBA + ЮОО)
Молярное соотношение
яд 100 (или 1000)
MVA
Л?Др100(или 1000) г СВА 1
' А ** VAdR\000 — MBA (или С5д) [ МВА j
jtMflplOO (или 1000)
MV* Чш
Молярная доля
пА
У А
пА + пр
Уд = Т
[СВА]МВР
А \МВА] VAdR\000+[СВА] (МВр — МВА)
хСВАМВр
уА = хСВАМВр +МВЛ\ 000
%
Молярный процент
% (мол.) = •
"л + пр
% (мол-)-[мВА].Ул-4-Ю00 + !СВА](МВр-МВА)
хСВА МВр 100
% <ыол,) = Icb^mbJ+ЖвмШ
Молярность
ллЮОО
/Ил=-
МА =
ПсвА]
Va [MBA]
Мл =
xCBAdR\000
А хСВАМВр +MB АЮ00
Нормальность
СлЮОО
Л л =
МВА . 1
л/Л =
jct/д 1000
хСВА + 1000
Ю
Разбавление
СлЮОО
Ил (норм.) = V/i (моляр.)-
МВА
[хСВА+1000] МВА г СВА 1
л ~~ xdfilOOOCfiA L МД4 J
II
Нормальность по массе
СлЮОО
*лг =
1000
VAdRl000 — MBA (или СВА) l MBA J
12
У =
§л100
Мйл (или СДЛ)
г/ =
хСВл +1000
13
«л
1000
МДл (или СВА)
VA
xCBAdR\000
' хСВА + 1000
Продолжение
Требуемое выражение
концентрации вещества А
Соотношение масс
8л
Яа=-
Sp
Часть по массе
WA= SA + 8P
Процент по массе
%=—4с
8A + SP
Объемный процент
% (объемн.) = —^
Молярное соотношение
■му _ пл ЮО (или 1000)
Молярная доля
v Па
УА~ йД + Пр
«Л
100
4л" dRl00-y
WA
dRl00
JL
dR
% (объемн.) = ■
dA
МИл--
yMBp№ (или 1000)
MBAdR 100 — у MB a
уМВр
уА ™ уМВр + MBА (drflOO — у)
«А
1000
Qa — dfllOOO — г
d/?1000
%
dR\0
% (объемн.) = ~aJTo"
гМВрЮО (или 1000)
MVA = ~мв&я1Ш — гкоА
гМВр
?Л - - zMBv+MBa (d«1000 - г)
7
8
9
10
11
12
13
Молярный процент
% (мол.) = ——,
ПА+Пр
Молярность
„лЮОО
л v
Нормальность
_ СлШОО
л v
Разбавление
V V
[A~nAiooomuXA~cAiow
Нормальность по массе
х СдЮОО
ёА100
у== —-—
с'
, g^iooo
V
oMflD100
V /мпл ^ i_ . .....
% (мол.) _ уД1йр+ ^ №Ш0 _ у)
^~ ^л
к, У10
Na= сва
Ki4~ jrlO ' ' л~ уЮ
4/Ю00
ж-СЗл(^Ю0-«/)
г = у10
z/Mfip100
% (мол.) _ гД1бр + МВа (dRim_г)
М л Z
Ма~ MBа
Ыл - 2
^~ Сбл
МВА . „ САЛ
кл— г , "л— 2
г 1000
*~ CBA(dR\0Q0-z)
г
17. 2. ПРИГОТОВЛЕНИЕ
СТАНДАРТНЫХ (ЭТАЛОННЫХ)
РАСТВОРОВ (КОНЦЕНТРАЦИЯ >0"2M)
Ag. а. Навеску серебра 1,0787 г
высокой чистоты растворяют в 20 мл
азотной кислоты (1 : 1) при слабом
нагревании. После растворения
вливают 50 мл воды, кипятят до
удаления окислов азота, охлаждают,
переливают в мерную колбу емкостью
1 л, доливают водой до метки.
Раствор содержит 1,0787 мг/мл серебра.
б. Навеску 1,7000 г азотнокислого
серебра растворяют в воде, доливают
до 1 л водой. Содержание серебра
(устанавливают) контролируют
гравиметрически, титриметрически.
Растворы светочувствительны,
хранят в темноте и в склянках из
темного стекла.
А1. а. 0,2698 г алюминия
высокой чистоты растворяют в 20 мл
соляной кислоты (1 : 1), доливают
до 1 л водой. Раствор содержит
0,2698 мг/мл алюминия.
б. 4,7439 или 4,5333 г
соответственно алюмокалиевых или алю-
моаммонийных квасцов растворяют
в воде с добавлением 5 мл
концентрированной серной кислоты,
доливают до 1 л водой. Содержание
алюминия контролируют
гравиметрически.
As. a. 0,7492 г металлического
мышьяка высокой чистоты
растворяют при комнатной температуре
в 10 мл азотной кислоты (1 : 1),
а затем при нагревании до полного
растворения. Разбавляют 50 мл воды,
кипятят до удаления окислов азота,
охлаждают, переливают в мерную
колбу емкостью 1 л, доливают водой
до метки. Раствор содержит ионы
нитрата и 0,7492 мг/мл мышьяка (V).
Для удаления нитратов после
растворения вливают 20 мл серной
кислоты (1 : 1), нагревают дважды до
выделения белых паров. Охлаждают
и доливают до метки водой.
б. 1,98 г KH2As04-H20
растворяют в воде, доливают до 1 л водой.
Содержание мышьяка (V)
устанавливают гравиметрически или
титриметрически.
в. 1,9784 г As203 высокой чистоты
(или возгнанной) растворяют в 10 мл
4 М раствора NaOH, разбавляют
до 1 л водой. Раствор содержит
1,4984 мг/мл мышьяка (III).
г. Раствор мышьяка для
фотометрических определений готовят
следующим образом: 0,660 г As203
растворяют в небольшом объеме 1 М.
едкого натра и нейтрализуют 1 М.
НС1 по лакмусу. Затем разбавляют
водой до 500 мл и еще разбавляют
водой в 50 раз. Раствор содержит
20 мкг/мл мышьяка.
Аи. а. 1,9697 г чистого золота
растворяют в 10 мл азотной и 30 мл
соляной кислот. Удаляют из раствора
газообразные продукты реакции
продуванием через стеклянную
трубочку, погруженную в раствор, сильной
струи очищенного воздуха в
течение 5 мин. Разбавляют водой до 1 л.
б. 4,1186 г Н1АиС14Ь4Н20
растворяют в 0,1 М НС1 в мерной колбе
емкостью 1 л.
В. а. 3,8137 г тетраборнокислого
натрия Na2B4O7-10H2O,
перекристаллизованного из горячей воды
(t = 60° С) и высушенного на
воздухе и над насыщенным раствором
NaBr-2H30, растворяют в воде и
доливают водой до 1 л. Раствор
содержит 0,4324 мг/мл бора.
б. 0,6962 г измельченного борного
ангидрида, полученного
прокаливанием борной кислоты в платиновой
чашке при 800° С до прекращения
выделения пузырьков, растворяют
в воде, доливают водой до 1 л.
Раствор содержит 0,2162 мг/мл бора.
в. 0,6183 г перекристаллизованной
борной кислоты растворяют в воде,
доливают водой до 1 л. Раствор
содержит 0,1081 мг/мл бора.
Приготовленные борсодержащие
растворы недопустимо хранить в
сосудах из борсодержащего стекла.
Лучше хранить в сосудах из
платины, полиэтилена, фторопласта,
кварца.
Ва. 2,4428 г ВаС12-2Н20 или
2,6135 г Ba(N03)2 растворяют в воде,
доливают до 1 л водой. Раствор
содержит 1,3734 мг/мл бария.
Содержание бария в растворах
контролируют гравиметрически.
Be. a. 0,09012 г металлического
бериллия высокой чистоты
растворяют в 20 мл соляной кислоты (1 : 1),
118
раствор переносят в мерную колбу
емкостью I л и доливают водой до
1 л. Раствор содержит 0,09012 мг/мл
бериллия.
б. 1,7714 г BeS04.4H,0 или
1,8707 Be(N08)a-3HaO растворяют
в воде с добавлением 5 мл
концентрированной серной кислоты или
5 мл азотной кислоты в мерной колбе
емкостью 1 л, доливают водой до
метки. Раствор содержит
0,09012 мг/мл бериллия. Содержание
бериллия в растворах контролируют
гравиметрически.
Bi. a. 2,0898 г металлического
висмута растворяют в 100 мл
раствора азотной кислоты (1 : 3), кипятят
до удаления окислов азота,
переносят в мерную колбу емкостью 1 л,
доливают водой до метки. Раствор
содержит 2,0898 мг/мл висмута (III).
б. 4,851 г Bi(N03)3-5H20
растворяют в 100 мл раствора азотной
кислоты (1 + 3), переносят в мерную
колбу емкостью 1 л, доливают до
метки водой. Содержание висмута
в растворе 2,0898 мг/мл, его
контролируют гравиметрически.
Br", a. 1,1901 г КВг высшей
квалификации (для ИК-спектроско-
пии), высушенного при температуре
ШО^ С, растворяют в воде, переносят
в мерную колбу емкостью 1 л,
доливают водой до метки. Раствор
содержит 0,79904 мг/мл бромида.
б. 1,3892 г NaBr-2H20
растворяют в воде, переносят в мерную
колбу емкостью 1 л, доливают водой
до метки. Раствор содержит
0,7990 мг/мл бромида. Содержание
бромида контролируют
гравиметрически или титриметрически.
ВгО". 2,40 г едкого натра
растворяют в 1 л дистиллированной воды,
охлаждают до —4° С. Прибавляют
0,80 г чистого брома, перемешивают,
оставляют раствор при этой
температуре в течение 2 ч. Содержание
ВгО" устанавливают
титриметрически через 12 ч. Растворы необходимо
хранить в темных склянках,
устойчивость их невысокая.
BrOJ. 1,6700 г КВЮ3,
перекристаллизованные из воды и
высушенные при 180° С, растворяют в воде,
переливают в мерную колбу емкостью
1 л, доливают водой до метки.
Раствор содержит 1,2791 мг на 1 мл
бромата. Содержание бромата
контролируют титриметрически.
С. a. COt-1,0599 г Na2C03,
высушенный при температуре 280—
300° С, растворяют в воде,
переливают в мерную колбу емкостью 1 л,
доливают водой до метки. Раствор
содержит 0,6001 мг/мл карбоната;
его содержание контролируют
гравиметрически или
титриметрически.
б. НСО;. 1,0012 г КНС03
растворяют в воде, переливают в мерную
колбу емкостью 1 л, доливают водой
до метки. Раствор содержит
0,6102 мг/мл гидрокарбоната; его
содержание контролируют
титриметрически.
Са. а. В суспензию из 1,0009 г
СаС03, высушенного при 110° С,
вливают 10 мл НС1 (1 : 1), переливают
в мерную колбу емкостью 1 л,
доливают до метки водой. Раствор
содержит 0,4008 мг/мл кальция и избыток
хлорида.
б. 0,5608 г СаО, свежепрокаленной
при температуре 850° С, растворяют
в воде и 2 мл НС1 или HN03,
переливают в мерную колбу 1 л,
доливают водой до метки. Раствор
содержит 0,4008 мг/мл кальция и избыток
хлорида или нитрата.
Cd. a. 1,1240 г кадмия
металлического высокой чистоты растворяют
в 20 мл серной кислоты (1 : 1) при
нагревании или 10 мл
концентрированной кислоты, растворение
ускоряется в присутствии нескольких
капель азотной кислоты, охлаждают,
разбавляют водой до 1 л. Раствор
содержит 1,1240 мг/мл кадмия.
б. 2,5650 г CdS04-8/3 H20
растворяют в воде, доливают водой до 1 л.
Раствор содержит 1,1240 мг/мл
кадмия; его содержание контролируют
гравиметрически или
титриметрически.
Се (III). а. 3,7259 г СеС13-
• 7Н20 растворяют в воде с
добавлением 20 мл соляной кислоты
(1:1) и объем раствора в мерной
колбе 1 л доливают до метки водой.
Раствор содержит 1,4012 мг/мл церия
(III); его содержание контролируют
гравиметрически или
титриметрически.
119
б. 7,1255 г Cea(S04)3 растворяют
в воде с добавлением 10 мл раствора
серной кислоты (1 : 1), объем
раствора в мерной колбе емкостью 1 л
доливают до метки. Раствор содержит
2,8024 мг/мл церия (III).
Се (IV). а. 4,043 г Ce(S04)a-
• 4Н20 растворяют в 0,5 М растворе
серной кислоты, объем раствора
в мерной колбе емкостью 1 л
доливают до метки этой же кислотой.
Раствор содержит 1,401 мг/мл церия
(IV); его содержание контролируют
титриметрически.
б. 5,8426 г (NH4),[Ce(NO,)f].
•2Н20 растворяют в мерной колбе
емкостью 1 л в 0,1 М HN03.
CI", a. 0,5844 г NaCl,
высушенной при 180° С, растворяют в воде,
объем раствора в мерной колбе 1 л
доливают до метки водой. Раствор
содержит 0,3545 мг/мл хлорида.
б. Такой же концентраоии готовят
разбавлением 100 мл 0,1 н. раствора
NaCl, приготовленного из фиксанала,
в мерной колбе емкостью 1 л.
CIO-. а. 7,00 г Са(С10)а-4Н20
растирают в ступке с 25 мл воды,
переносят в бутыль, доливают до
объема 1 л, перемешивают
встряхиванием, дают отстояться,
фильтруют в темную склянку.
Содержание гипохлорита устанавливают
титриметрически. Растворы
неустойчивы.
б. 1,50 г хлорамина Т
Na \
н8с— свн4—so2n/ .знао)
С1 /
растворяют в воде, объем раствора
в мерной колбе емкостью 1 л
доливают водой до метки. Содержание
«активного хлора» устанавливают
титриметрически; растворы
устойчивы при хранении в склянках из
темного стекла. рН растворов более 7.
СЮ~. 1,00 г NaC102 растворяют
в воде, объем раствора в мерной
колбе I л разбавляют до метки водой.
Содержание хлорита устанавливают
титриметрически.
СЮ;. 1,226 г КС103,
перекристаллизованного из воды,
растворяют в воде, объем раствора в мерной
колбе 1 л разбавляют до метки водой.
Раствор содержит 0,8345 мг/мл
хлората; его содержание контролируют
титриметрически.
СЮ;. 1,3855 г КС104,
перекристаллизованного из воды и
высушенного при 110° С, растворяют при
нагревании в воде, объем раствора
й мерной колбе 1 л разбавляют до
метки водой. Раствор содержит
0,9945 мг/мл перхлората; его
содержание контролируют
гравиметрически или титриметрически.
Со (II). а. 0,5893 г
металлического кобальта высокой чистоты
растворяют в 5 мл раствора азотной
кислоты (1 : 1) или в 25 мл серной
кислоты (1:4) при нагревании,
прибавляют 50 мл воды, кипятят
до удаления окислов азота. Объем
раствора в мерной колбе 1 л
разбавляют водой до метки. Раствор
содержит 0,5893 мг/мл кобальта (II)
и соответственно избыток ионов
нитрата или сульфата.
б. 2,82 г CoS04-7HaO растворяют
в воде, объем раствора в мерной
колбе 1 л разбавляют водой до 1 л.
Содержание кобальта устанавливают
гравиметрически или
титриметрически.
Со (III). 2,50 г Со203-ЗНгО
растворяют в 1 л горячей (70° С)
ледяной уксусной кислоты, раствор
фильтруют через пористый стеклянный
фильтр № 3. Фильтрат содержит
около 60% ацетата кобальта (III)
и 40% кобальта (II). Содержание
кобальта (III) в растворе
устанавливают титриметрически.
Сг(П). а. 29.421 г для 0,1 М
раствора КаСг207, высушенного при
150° С, растворяют в 500 мл воды
в конической колбе, приливают
27,8 мл концентрированной H2S04.
В горло колбы вставляют воронку
с длинной трубкой, приливают
небольшими порциями 75 мл 30%-ной
Н2Ог для восстановления Сг (VI)
в Сг (III). Раствор нагревают почти
до кипения до прекращения
выделения 02 (около 20 мин), охлаждают.
Раствор переливают в мерную колбу
емкостью 2 л, разбавляют водой до
метки. Заполняют приготовленным
раствором хрома (III) бутыль с
тубусом у дна, в которой содержится
200 г амальгамированного цинка.
120
Раствор хрома (II) устойчив при
хранении его в атмосфере С02, N2.
Содержание хрома (II) в растворе
устанавливают титриметрически.
б. 4,9941 г КСг (S04)2-12H20
растворяют в 1 л 0,01 М раствора серной
кислоты и пропускают через
редуктор с амальгамированным цинком.
Сг(Ш). а. 4,9941 г KCr(S04)2-
• 12Н20 растворяют в воде с
добавлением 5 мл концентрированной
H2S04, объем раствора в мерной
колбе емкостью 1 л доливают до
метки водой. Раствор содержит
0,5200 мг/мл хрома (III).
б. 1,9419 г КгСг207, высушенного
при 150° С, растворяют в 100 мл
1 М H2S04, вносят 5 мл 30% -ной
перекиси водорода, нагревают почти
до кипения в течение 20—30 мин до
полного разложения перекиси
водорода, охлаждают. Объем раствора
в мерной колбе емкостью 1 л
доливают до метки водой. Раствор
содержит 0,5200 мг/мл хрома (III).
Cr(VI). 1,9419 г К2Сга07,
высушенного при 150° С, растворяют
в воде. Объем раствора в мерной
колбе емкостью 1 л разбавляют водой
до метки. Раствор содержит
0,5200 мг/мл хрома (VI).
Cs. 1,6836 г CsCl,
перекристаллизованного и высушенного при 200° С,
растворяют в воде. Объем раствора
в мерной колбе емкостью 1 л
разбавляют водой до метки. Раствор
содержит 1,3290 мг/мл цезия.
Си (I). а. 1,00 г СиС1 растворяют
в 30 мл концентрированной НС1,
переносят в склянку, заполненную
двуокисью углерода. При
помешивании добавляют небольшими
порциями 600 мл воды, предварительно
прокипяченной, охлажденной в токе
С02. Раствор сохраняют в темной
склянке в атмосфере С02.
Содержание меди (I) устанавливают
титриметрически. Титр сохраняется в
течение 2—3 недель.
б. 2,5000 г CuS04-5H20
растворяют в 1 л 2 М НС1. Раствор
пропускают через серебряный редуктор.
Вытекающий раствор используют
непосредственно для титрования
анализируемых растворов в атмосфере
С02; титр устанавливают
титриметрически,
Си (II). а. 0,6355 г
металлической меди высокой чистоты
растворяют в 5 мл HNOs (1 : 1) при
нагревании, разбавляют водой до
50 мл, кипятят до удаления окислов
азота. Раствор разбавляют водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 0,6355 мг/мл меди
(II). Если присутствие нитрат-ионов
мешает, то после растворения трижды
выпаривают с 5 мл
концентрированной НС1 до влажных солей или с 5 мл
H2S04 (1 : 1) дважды до паров.
б. 2,4969 г CuS04-5H20
растворяют в воде, объем раствора в мерной
колбе емкостью 1 л доливают водой
до метки. Раствор содержит
0,6355 мг/мл меди (II); ее содержание
контролируют гравиметрически,
титриметрически.
в. 2,9565 г Cu(N03)a-6H20
растворяют в воде, объем раствора в
мерной колбе емкостью 1 л доливают
до метки водой. Раствор содержит
0,6355 мг/мл меди (II), ее
содержание контролируют гравиметрически,
титриметрически.
F". 0,5810 г KF или 0,4199 г
NaF, высушенных при температуре
выше 130° С, растворяют в воде,
объем раствора в мерной колбе
емкостью 1 л доливают до метки водой.
Раствор содержит 0,1900 мг/мл
фторида, его содержание контролируют
гравиметрически, титриметрически,
раствор хранят в посуде из
полиэтилена, фторопласта.
Fe (II). а. 0,5585 г
металлического железа высокой чистоты
растворяют в 10 мл НС1 (1 : 1) или
10 мл H2S04 (1:4) при нагревании
в атмосфере С02. Объем раствора
доливают до 1 л охлажденной в токе
СОа свежепрокипяченной водой.
Раствор сохраняют в атмосфере СОа.
Раствор содержит железа (II)
0,5585 мг/мл; его содержание
контролируют титриметрически.
б. 2,80 г FeS04-7H20 растворяют
в 500 мл 1,8 М раствора серной
кислоты, если раствор мутный, то
фильтруют. Фильтрат доливают до
объема 1 л 1,8 М раствором серной
кислоты. Раствор содержит железо
(II) и железо (III); содержание
железа (II) устанавливают
титриметрически.
121
в. 3,921 г (NH4)2Fe(S04)2-GH,0
(соли Л\орп) растворяют в 1 л 1,8 М
серной кислоты. В случае
необходимости раствор фильтруют. Раствор
содержит в качестве примеси железо
(III). Содержание железа (II)
устанавливают титриметрпчески.
Fe (III), a. 0,5585 г
металлического железа высокой чистоты
растворяют в 10 мл смеси соляной и
азотной кислот (3 : 1), разбавляют
водой до 50 мл, кипятят до удаления
окислов азота. Объем раствора в
мерной колбе емкостью 1 л доливают
до метки водой. Раствор содержит
0,5585 мг/мл железа (3-Ь), хлориды,
нитраты.
б. 4,8219 г NI^FefSO^s • 12Н20
растворяют в воде с добавлением 5 мл
концентрированной H„S04 и при
перемешивании разбавляют водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 0,5585 мг/мл
железа (3+); его содержание
контролируют гравиметрически.
в. 2,75 FeCl3-6H20 растворяют
в воде с добавлением 10 мл
концентрированной НС1 и при
перемешивании разбавляют водой до метки
в мерной колбе емкостью 1 л.
Содержание железа (3+) в растворе
устанавливают гравиметрически, титри-
метрически.
Ga (III), a. 0,6972 г
металлического галлия высокой чистоты
растворяют в 20 мл раствора НС1
(1 : 2) или 10 мл смеси НС1 и HNOs
в соотношении (1 : 1) и при
перемешивании разбавляют водой до метки
в мерной колбе емкостью 1 л. Раствор
содержит 0,6972 мг/мл галлия
(3+).
б. 4,00 г Ga(N03)3-8H30
растворяют в воде с добавлением 10 мл
концентрированной HN03 и при
перемешивании разбавляют водой до
метки в мерной колбе емкостью 1 л.
Содержание галлия в растворе
устанавливают гравиметрически.
Gd. a. 1,5725 г металлического
гадолиния высокой чистоты
растворяют в 20 мл разбавленных НС1
(1 + 1) или HN03 (1 : 2), H2S04
(1 : 2), НС104 (1 : 2) при слабом
нагревании и при перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 1,5725 мг/мл гадолиния (III);
его содержание контролируют
гравиметрически.
б. 3,0250 г Gd2Oa высокой
чистоты, предварительно прокаленной,
растворяют в 20 мл
концентрированной HCI и при перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 3,1450 мг/мл гадолиния.
Ge(IV). a. 0,7259 г тонко
измельченного германия высокой
чистоты растворяют в 50 мл 1 М
раствора NaOH, подкисляют раствором
НС1 (1 : 1) [вливают 10 мл] и при
перемешивании разбавляют водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 0,7259 мг/мл
германия (IV).
б. 1,0459 г прокаленной при 900° С
GeOa сплавляют в платиновом тигле
с 5 г Na2C03. Плав растворяют
в воде. Объем раствора доливают
до метки водой в мерной колбе
емкостью 1 л. Раствор содержит
0,7259 мг/мл германия (IV).
Hf (IV). 1,7849 г металлического
гафния высокой чистоты растворяют
в чашке (стакане) из фторопласта,
платины, прибавляя к 10 мл воды
по каплям фтористоводородную
кислоту до растворения; окисляют 1 мл
концентрированной HN03, добавляя
ее по каплям, слабо кипятят до
отгонки окислов азота, охлаждают.
Приливают 20 мл раствора серной
кислоты (1:1), выпаривают до
появления паров серной кислоты,
продолжают выпаривать еще 10 мин,
охлаждают. Приливают 20 мл воды,
50 мл серной кислоты (1 : 1) и при
перемешивании разбавляют водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 1,7849 мг/мл
гафния (IV).
Hg(I). 5,61 г Hg2(N03)2.2H20
растворяют в 500 мл 0,05 М HN03,
разбавляют 0,05 М HN03 до метки
в мерной колбе емкостью 1 л.
Содержание ртути (I) в растворе
устанавливают гравиметрически или титри-
метрически. Раствор сохраняют
в темной склянке в присутствии
2—3 капель ртути . металлической.
Hg (II)- а. 3,426 г Hg(N03)2-
• Н25 растворяют в 50 мл HN03
(1:1) и разбавляют до метки водой
122
при помешивании в мерной колбе
емкостью 1 л. Содержание ртути (II)
устанавливают гравиметрически или
титриметрически. Раствор сохраняют
в склянках из темного стекла.
б. 2,715 г HgCl 2 растворяют в воде
и разбавляют водой до метки в
мерной колбе емкостью 1 л. Раствор
содержит 2,006 мг/мл ртути (II).
в. 2,0059 г металлической ртути
растворяют в 10 мл HN03 (1 : 1)
при слабом нагревании, доливают
воды до метки в мерной колбе
емкостью 1 л. Раствор содержит
2,0059 мг/мл ртути (II) и избыток
HN03.
Но (111). а. 1,6493 г
металлического гольмия высокой чистоты
растворяют в 20 мл раствора НС1
(1 : 1) или HN03 (1 : 2), H2S04 (1 : 2),
НСЮ4 (1:2) при слабом нагревании
и при перемешивании разбавляют
водой до метки в мерной колбе
емкостью 1 л. Раствор содержит
1,6493 мг/мл гольмия (III).
б. 3,7786 г Но203 высокой чистоты
растворяют в 20 мл
концентрированной НС1 и при перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 3,2986 мг/мл гольмия (III).
h. 1,269 г Ь, очищенного
возгонкой, растворяют в растворе,
содержащем 5 г KI в 25 мл Н20.
После растворения разбавляют водой
до объема 1 л. Раствор содержит
1,269 мг/мл иода; его содержание
контролируют титриметрически.
Растворы хранят в темных склянках.
Подобные растворы готовят
разбавлением 100 мл 0,1 н. раствора
иода из фиксанала водой до объема
1 л.
I". 1,6601 г KI,
перекристаллизованного из этанола и высушенного
при 400° С, растворяют в воде и
доливают до метки водой, объем
мерной колбы емкостью 1 л. Раствор
содержит 1,269 мг/мл 1~. Он более
устойчив в склянках из темного
стекла. Содержание контролируют
титриметрически.
10". 2,1400 г КЮ3, высушенного
при 130—150° С, растворяют в воде
и доливают до метки водой, объем
мерной колбы емкостью 1 л. Раствор
содержит 1,7490 мг/мл IO3.
104". 2,3000 г КЮ4 растворяют
в воде и доливают до метки водой,
объем мерной колбы емкостью 1 л.
Раствор содержит 1,9090 мг/мл Ю~;
его содержание контролируют
гравиметрически, титриметрически.
In (111), a. 1,1482 г
металлического индия высокой чистоты
растворяют в 20мл НС1 (1:1) и при
перемешивании доливают водой до метки,
объем мерной колбы емкостью 1 л.
Раствор содержит 1,1482 мг/мл индия
(III).
б. 3,548 г In(N03)3-3H20
растворяют в воде, содержащей 10 мл
HN03, при перемешивании
разбавляют водой до метки в мерной колбе
емкостью 1 л. Содержание индия
контролируют гравиметрически,
титриметрически.
Ir (IV). 4,8312 г К2[1гС1в]
растворяют в 1 М НС1, разбавляют этой же
кислотой до объема 1 л. Раствор
содержит 1,922 мг/мл I г(IV). Его
содержание контролируют гравиметрически.
К. а. 0,7456 г KQ высокой
чистоты (или перекристаллизованного
из воды и высушенного при 120—
130° С) растворяют в воде и доливают
водой до метки объем мерной колбы
емкостью 1 л. Раствор содержит
0,3910 мг/мл калия.
б. 1,0111 г KN03 высокой чистоты
или перекристаллизованного из воды
и высушенного при 120—130° С
растворяют в воде и доливают водой до
метки объем мерной колбы емкостью
1 л. Раствор содержит 0,3910 мг/мл
калия; его содержание контролируют
гравиметрически.
La (III), a. 1,3891 г
металлического лантана высокой чистоты
растворяют в 20 мл разбавленных НС1
(1 : 1) или HN03 (1 : 2), H2S04
(1 : 2), НСЮ4 (1:2) при слабом
нагревании. При перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 1,3891 мг/мл лантана.
б. 3,2582 г La203 высокой
чистоты растворяют в 20 мл
концентрированной НС1 и при
перемешивании разбавляют водой до метки в
мерной колбе емкостью 1 л. Раствор
содержит 2,7782 мг/мл лантана; его
содержание контролируют
гравиметрически, титриметрически.
123
Li. a. 0,7389 г Li2C03,
высушенного при 105° С, всыпают в 50 мл
воды и для растворения постепенно
приливают HQ (1 -j- 1) или HNCX,
(1 + 1), H2S04 (1 + 2) и разбавляют
водой до метки в мерной колбе
емкостью 1 л. Раствор содержит
0,1388 мг/мл лития.
б. 1,300 г Li2S04, прокаленного
при 400—450° С, разбавляют водой
до метки в мерной колбе емкоствао
1 л. Раствор содержит 0,1388 мг/мл
лития; его содержание контролируют
гравиметрически.
Lu (III), a. 1,7497
металлического лутеция высокой чистоты
растворяют в 20 мл разбавленных НС1
(1 + 1) или HN03 (1 + 2), H2SO,
(1 + 2), НСЮ4 (1 -f 2) при слабом
нагревании. При перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 1,7497 мг/мл лутеция (III).
б. 3,9794 г Lu203 высокой чистоты
растворяют в 20 мл
концентрированной НС1 и при перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 3,4994 мг/мл лутеция (III).
Mg. a. 0,4030 г MgO высокой
чистоты (или полученного из
Mg2(OH)2C03), свежепрокаленного
при 700—900° С, всыпают в 10 мл
воды, приливают 10 мл НС1 (1 + 1)
или H2S04 (1 +2), нагревают до
растворения, разбавляют водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 0,2430 мг/мл маг-
пня.
б. 1,2037 г MgS04, прокаленного
при 400—500° С, растворяют в воде
с добавлением 1 мл
концентрированной H2S04, разбавляют водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 0,2430 мг/мл
магния; его содержание контролируют
гравиметрически или титриметри-
чески.
Мп(П). а. 0,5494 г
металлического марганца высокой чистоты
растворяют при нагревании в 5 мл
HN03 (1 + 1), приливают 20 мл
воды, кипятят для удаления окислов
азота. Для получения солей
марганца (II) с другими кислотами после
растворения выпаривают
многократно с НС1 (10 +10+10 мл) до
влажных солей или с 10 мл H2S04
(1:1) дважды до паров серной
кислоты. Доливают раствор до метки
водой в мерной колбе емкостью 1 л.
Раствор содержит 0,5494 мг/мл
марганца (II) и нитраты.
б. 0,5494 г металлического
марганца высокой чистоты растворяют
в 50 мл H2S04 (1 + 4) при
нагревании, охлаждают и разбавляют
водой до 1 л. Раствор содержит
0,5494 мг/мл марганца (II).
в. 1,5804 г КМп04 растворяют
в 50 мл H2S04 (1 : 4), пропускают
SOa до обесцвечивания раствора или
приливают при перемешивании по
каплям 5%-ный раствор сульфита
натрия (пиросульфита) или перекись
водорода (1 : 1). Кипятят для
удаления избытка восстановителей,
доливают до метки водой в мерной
колбе емкостью 1 л. Раствор
содержит 0,5494 мг/мл марганца (II).
Его содержание контролируют
гравиметрически или титриметрически.
Mn(VII). 1,5804 г КМп04
[растворяют в воде и доливают водой до
метки в мерной колбе емкостью 1 л.
Раствор содержит 0,5494 мг/мл
Мп (VII); его содержание
контролируют титриметрически.
Мо (III). Раствор молибдена (VI)
в 4 М НС1, полученный, как описано
ниже, из металлического молибдена,
восстанавливают 100 г амальгамы
цинка. Содержание молибдена
устанавливают титриметрически.
Такой же раствор Мо (III)
получают при пропускании через
редуктор, заполненный
амальгамированным цинком.
Мо (V). Раствор молибдена (VI)
в 2 М НС1, полученный, как описано
ниже, из металлического молибдена,
восстанавливают 100 г амальгамы
висмута или пропусканием через
редуктор с висмутом или серебром.
Мо (VI). а. 0,9592 г
металлического молибдена высокой чистоты
растворяют в 5 мл HN03 (1 + 1)
при нагревании, разбавляют водой
до 50 мл, кипятят для удаления
окислов азота, охлаждают. Для
получения растворов молибдена (VI)
многократно выпаривают до
влажных солей с НС1 (10 +10+10 мл)
или дважды с 10 мл HaS04 (1 + 1)
124
до паров серной кислоты. Доливают
до метки в мерной колбе емкостью
1 л. Раствор содержит 0,9592 мг/мл
молибдена (VI)..
б. 1,4395 г МоО», высушенной при
350° С, растворяют в 10 мл раствора
аммиака (1+5) или Ю мл 10%-ной
NaOH и разбавляют водой до объема
1 л. Раствор содержит 0,9592 мг/мл
молибдена (VI).
в. 1,7655 г (NH4)«Mo£)M-4H/)
растворяют в горячей воде и
доливают раствор до метки водой.
Раствор содержит 0,9592 мг/мл
молибдена (VI); его содержание
контролируют гравиметрически или титри-
метрически.
NH^. 0,53497 г NH4C1,
перекристаллизованного и высушенного при
105—110° С, растворяют в воде и
разбавляют водой до объема 1 л.
Раствор содержит 0,1804 мг/мл
NH|; его содержание контролируют
гравиметрически или титриметри-
чески.
[N2H4 2Н]а+. 1,3013 г N2H4-
• H2S04, перекристаллизованного из
воды и высушенного при 150° С,
растворяют в воде и разбавляют
водой до объема 1 л. Раствор
содержит 0,3205 мг/мл гидразиния; его
содержание контролируют титриме-
трически.
N0". 0,8510 г KN02 или 0,6900 г
NaN02 растворяют в воде и
разбавляют водой до объема 1 л.
Раствор содержит 0,4600 мг/мл NO";
его содержание контролируют
тетраметрически.
N0". 1,0111 г KNOa,
перекристаллизованного из воды и
высушенного при 120° С, растворяют в
воде и разбавляют водой до объема
1 л. Раствор содержит 0,6201 мг/мл
NO"; его содержание контролируют
гравиметрически.
Na. 0,5845 г Nad высокой
чистоты (или перекристаллизованного
и прокаленного при 500—600° С)
растворяют в воде и разбавляют
водой до объема 1 л. Раствор
содержит 0,2299 мг/мл натрия.
Nb (V). К 0,9291 г
металлического ниобия высокой чистоты
в чашке из платины или стакане
из фторопласта приливают 10 мл
концентрированной HF и по
каплям 2 мл HN03 (1 -+- 1), приливают
50 мл H2S04 (l-|-l) и выпаривают
дважды до паров серной кислоты.
Раствор разбавляют до объема 1 л
концентрированной серной кислотой
(или 5%-вгым оксалатом аммония,
10%-ной винной кислотой,
концентрированной НС1). Раствор
содержит 0,9291 мг/мл ниобия (V) и-анионы
SO^~ с комилексантом.
б. 2,6582 г Nb205 высокой
чистоты, свежепрокаленной при 900° С,
сплавляют в платиновом тигле с 20 г
K2S^07. Плав растворяют в 20%-ной
винной кислоте и доливают его до
объема 1 л. Раствор содержит
1^582 мг/мл ниобия (V), анионы
SO^~, винную кислоту; содержание
ниобия контролируют
гравиметрически.
Nd(III). a. 1,4424 г
металлического неодима высокой чистоты
растворяют в 20 мл разбавленных НС1
(1 + 1) или HN03 (1 + 2), H2S04
(1 +2), НСЮ4 (1 + 2) при еяабом
нагревании и при перемешивании
разбавляют водой до метки в мерной
колбе емкостью 1 л. Раствор
содержит 1,4424 мг/мл неодима (III).
б. 3,3648 г Nd203 высокой чистоты
растворяют в 20 мл
концентрированной НС1 и при перемешивании
разбавляют водой до объема 1 л.
Раствор содержит 2,8848 мг/мл неодима;
его содержание контролируют
гравиметрически или титриметрически.
Ni. a. 0,5870 г металлического
никеля высокой чистоты растворяют
в 10 мл HN03 (1 : 1) при нагревании,
разбавляют водой до 50 мл, кипятят
для удаления окислов азота,
охлаждают и разбавляют водой до объема
1 л. Раствор содержит 0,5870 мг/мл
никеля и нитрат-ионы.
б. 2,809 г №S04-7H20 растворяют
в воде и разбавляют водой до объема
1 л. Раствор содержит 0,5870 г
никеля, его контролируют
гравиметрически, титриметрически.
Os(IV). Раствор осмия (IV)
приготовляют, исходя из величины
навески Os04, хранящегося в
стеклянных ампулах. На ампуле делают
несколько царапин напильником,
взвешивают ее, опускают в
стеклянную бутыль с притертой пробкой
емкостью 200 мл, в которую предва-
125
рительно налипают 50 мл волы.
Разбивают ампулу потряхиванием
бутыли и после растворения Os04
декантируют большую часть жидкости
в мерную колбу емкостью 250 мл,
хорошо промывают бутыль
последовательно несколькими порциями
воды, сливая промывные воды в
мерную колбу и следя за тем, чтобы
в нее не попали осколки стекла.
После этого осколки стекла
извлекают, сушат и взвешивают. Титр
раствора можно установить
следующим образом: 10 мл раствора
обрабатывают 15 мл 6 М серной кислоты
и 2 г иодида калия и затем оттитро-
вывают иод 0,025 н. раствором
тиосульфата.
Pb(II). a. 2,0719 г
металлического свиица высокой чистоты
растворяют в 50 мл HN03 (1 : 1) при
нагревании, приливают 50 мл воды,
кипятят для удаления окислов азота.
Для получения раствора хлорида
свинца выпаривают многократно
с концентрированной НС1 (10 + 10+
+ 10 мл) до влажных солей.
Разбавляют водой или 6 М раствором
НО до метки объем 1 л. Раствор
содержит 2,0719 мг/мл свинца.
б. 3,79 г РЬ(ООССН3)2.ЗН20
растворяют в 1 М растворе уксусной
кислоты и доливают до объема 1 л
этим же раствором кислоты.
Содержание свинца в растворе
устанавливают гравиметрически или титриме-
трически.
Pb(IV). a. 4,434 г РЬ(ООССН3)4,
перекристаллизованного из ледяной
уксусной кислоты, растворяют в
ледяной уксусной кислоте и ею же
доливают до метки в мерной колбе
емкостью 1 л. Раствор содержит
2,072 мг/мл РЬ (IV); его содержание
контролируют титриметрически.
Раствор не содержит РЬ (II), устойчив
при хранении в темных склянках.
б. 6,86 г РЬ304 растворяют в
ледяной уксусной кислоте и доливают
ею же до объема 1 л. Содержание
РЬ (IV) устанавливают
титриметрически.
Pd(II). a. 1,064 г
металлического палладия растворяют в 10 мл
царской водки при нагревании,
выпаривают до влажных солей, с
концентрированной НС1 (10 мл + 10 мл)
разбавляют водой до объема 1 л.
Раствор содержит 1,064 мг/мл
Pd (II) в форме PdClf-
б. 2,941 г Na2[PdCl4] растворяют
в 2 М НСГи разбавляют этой
кислотой до объема 1 л. Раствор содержит
1,064 мг/мл Pd (II); его содержание
контролируют гравиметрически.
Н2РО^. 1,041 г КН2Р02
растворяют в воде и разбавляют водой до
объема 1 л. Содержание Н2Р02
устанавливают титриметрически.
Р0~. 1,181 г КР03 растворяют
в воде и разбавляют водой до объема
1 л. Раствор содержит 0,790 мг/мл
РО~; его содержание контролируют
гравиметрически.
POf. a. 1,3609 г КН2Р04
растворяют в воде и разбавляют водой
до объема 1 л. Раствор содержит
0,9498 мг/мл POf.
б. 1,78 г Na2HP04-2H20
растворяют в воде и разбавляют водой
до объема 1 л. Раствор содержит
0,9498 мг/мл POJ"; его содержание
контролируют гравиметрически.
Р20?-. 2,6590 г Na4P,07. свеже-
прокаленной при 800—900° С,
растворяют в воде и доливают водой до
объема 1 л. Раствор содержит
1,739 мг/мл Р20£~; его содержание
контролируют гравиметрически.
Рг(1П). а. 1,4091 г
металлического Рг высокой чистоты
растворяют в 20 мл разбавленных НС1
(1 : 1) или HN03 (1 : 2), H2S04 (1 : 2),
НСЮ4 (1 : 1), при слабом нагревании
и при перемешивании разбавляют
водой до объема 1 л. Раствор
содержит 1,4091 мг/мл празеодима (III).
б. 3,2918 г Рг2Оэ высокой чистоты
растворяют в 20 мл НС1 и при
перемешивании разбавляют водой до
объема 1 л. Раствор содержит
2,8182 мг/мл празеодима.
Pt (IV). 1,9509 г чистой платины
растворяют в царской водке, трижды
выпаривают до влажных солей с НС1
(10 мл -)- Ю мл + 10 мл),
разбавляют 1 М НС1 до объема 1 л.
Rb. a. 1,475 г RbN03
растворяют в воде и доливают водой объем
до 1 л. Раствор содержит
0,8547 мг/мл рубидия; его
содержание контролируют гравиметрически.
б. 1,2193 г RbCl высокой чистоты
(или перекристаллизованного из во-
126
ды) высушивают при 150° С,
растворяют в воде и доливают водой до
объема 1 л. Раствор содержит
0,8547 мг/мл рубидия.
Re (IV). а. 2,893 г KRe04
растворяют в 100 мл НС1 (1 : 1),
раствор восстанавливают 100 г
амальгамы висмута. Раствор,
разбавленный до 1 л, содержит 1,862 мг/мл
рения (IV); его содержание
контролируют титриметрически.
б. 2,893 г KRe04 растворяют
в 500 мл концентрированной НС1,
прибавляют 10 г хлорида гидрази-
ния, кипятят 1 ч, охлаждают,
разбавляют водой до объема 1 л. Раствор
содержит 1,862 мг/мл рения (IV)
в виде [ReCl^f •
Re (V). 2,893 г KRe04
растворяют в 100 мл H2S04 (1 : 2), раствор
восстанавливают 100 г амальгамы
висмута. Этот раствор содержит
1,862 мг/мл рения (V); его
содержание контролируют
титриметрически.
Re (VII). 2,8931 г KRe04,
перекристаллизованного из воды и
высушенного при 180° С, растворяют
при нагревании в воде, охлаждают
и доливают водой до объема 1 л.
Раствор содержит 1,8621 мг/мл
рения (VII).
Rh (III), a. 3,156 г K3[RhCle!
растворяют в 1 М НС1 и разбавляют
ею же до объема 1 л. Раствор
содержит 1,03 мг/мл родия (III).
Содержание родия (III) контролируют
гравиметрически.
б. 1,0291 г металлического родия
тонко измельчают и сплавляют с 5 г
пиросульфата калия в кварцевом
тигле. Плав выщелачивают в 0,5 М
серной кислоте и разбавляют в
мерной колбе емкостью 1 л до метки
той же кислотой.
S0. 0,3206 г серы высокой
чистоты растворяют в бензоле (или
ацетоне, дихлорэтане) при нагревании,
разбавляют растворителем до объема
1 л. Раствор содержит 0,3206 мг/мл
серы.
S2-. 2,50 г Na2S-9H20 в виде
крупных кристаллов, высушенных
между листами фильтровальной
бумаги, растворяют в воде и доливают
водой до объема 1 л. Содержание S2~
устанавливают титриметрически.
S2Of. 2,482 г Na2S,08-5H20,
очищенную перекристаллизацией и
промыванием этанолом, растворяют
в воде, добавляют 0,1 г Na2COs,
доливают водой до метки.
Содержание S20|~ устанавливают
титриметрически.
SOl". 2,25 г K2S2O5 (п-иросуль-
фит, метабисульфит) растворяют в
воде и доливают водой до объема 1 л.
Содержание SOI" устанавливают
титриметрически. Раствор при
хранении неустойчив.
SOl-. a. 1,420 г Na2S04,
прокаленного при 400° С, растворяют в
воде и доливают водой до объема 1 л.
Раствор содержит 0,961 мг/мл SOl",
его содержание устанавливают
гравиметрически.
б. Разбавлением водой 100 мл
раствора фиксанала 0,1 н. серной
кислоты до объема 1 л.
Sb(III). a. 1,2175 г
металлической сурьмы высокой чистоты
растворяют при нагревании в 100 мл
концентрированной H2S04, охлаждают,
при перемешивании разбавляют
водой до объема 1 л. Раствор содержит
1,218 мг/мл сурьмы (III). •
б. 3,339 г K(SbO)C4H4Oe.0,5HaO
растворяют в 2 М растворе серной
кислоты и доливают до объема 1 л
этой же кислотой.
в. Для фотометрических
определений готовят разбавленные растворы
сурьмы (III) следующим образом:
0,1000 г металлической сурьмы
растворяют в 15 мл концентрированной
серной кислоты, охлаждают и
разбавляют водой до 500 мл, а затем
разбавляют также водой в 50 раз.
Раствор содержит 5 мкг/мл сурьмы.
Растворы Sb (V) специально не
готовят. Используют раствор сурьмы
(III), окисляя его в ходе анализа.
Sc. a. 0,4496 г металлического
скандия высокой чистоты
растворяют в 10 мл НС1 (1:2) и
разбавляют водой при перемешивании до
объема .. 1 л. Раствор содержит
0,4490 мг/мл скандия.
б. 1,3792 г Sc203, свежепрокален-
ной при 700—800° С, растворяют
в 10 мл H2S04 (1 : 1) или 20 мл HC1,
концентрированной при нагревании,
охлаждают и разбавляют водой при
помешивании до объема 1 л. Раствор
127
содержит 0,8992 мг/мл скандия; его
содержание контролируют
гравиметрически, титриметрически.
Se (IV). 0,78% г еелена высокой
чистоты растворяют в 50 мл
концентрированной НО, куда до полного
растворения приливают 7—ГО капель
концентрированной азотной
кислоты, затем нагревают на водяной бане
до растворения. Охлаждают,
разбавляют водой при помешивании до
объема 1 л. Раствор содержит
0,7896 мг/мл селена (IV).
Se(VI). 1,889 г Na2Se04
растворяют в воде и доливают водой до
объема 1 л. Раствор содержит
0,7896 мг/мл селена (VI); его
содержание контролируют
гравиметрически, титриметрически.
Si. 0,2809 г прокаленного
порошка Si или 0,6009 г SiOa
сплавляют с 5 г Na2GO& в платиновом
тигле, охлаждают, выщелачивают
0,1 М NaOH и доливают до объема
1 л этим же. раствором. Раствор
содержит 0,2809 мг/мл кремния, его
хранят в посуде из полиэтилена,
фторопласта.
Sn (II). а. 1,187 г
металлического олова высокой чистоты растворяют
при нагревании в 100 мл НС1 (1:1)
в атмосфере СОа. Охлаждают и
разбавляют НС1 (1 : 1) до объема 1 л.
Раствор содержит 1,187 мг/мл олова
(II); его содержание контролируют
титриметрически.
б. 2,256 г SnCl2-2HaO растворяют
в 100 мл НС1 (1 : 1) (старые
препараты растворяются при нагревании
или длительном стоянии) и
разбавляют НС1 (1 : 1) до объема 1 л. Go-
держание олова (II) устанавливают
титриметрически; растворы содержат
в качестве примеси олово (IV),
их хранят в атмосфере инертного
газа.
в. 2,256 г SnCl2>2H20 растворяют
в смеси глицерин + этанол (3 : 1)
и разбавляют до объема 1 л этой же
смесью. Раствор содержит
1,187 мг/мл олова (II).
Sn (IV). К 3,00 г жидкого SnCl4
в колбе осторожно приливают НС1
(1 : 1), разбавляют этим же
раствором до объема 1 л. Содержание
олова (IV) устанавливают
гравиметрически или титриметрически.
Sr. а. 1,036 г свежепрокаленного
SrO высокой чистоты растворяют
в 30 мл растворе НС1 (1:2) (или
HN03) и доливают водой до объема
1 л. Раствор содержит 0,8763 мг/мл
стронция.
б. 1,4764 г SfG03, высушенною
при 200° С, растворяют в 30 мя
НС1 (1:2) и доливают водой до
объема 1 л. Раствор содержит
0,8763 мг/мя етронция.
Та (V). а. К 1,8095 г
металлического тантала высокой чистоты в
платиновой или фторопластовой чашке
приливают 20 мл концентрированной
HF и по каплям до растворения
концентрированную HN03. Вливают
100 мл H2S04 (1 : 1), выпаривают
дважды до паров, охлаждают.
Разбавляют до объема 1 л 15% -ним
раствором винной кислоты или
4%-ным раствором щавелевокислого
аммония. Раствор содержит
1,8095 мг/мл тантала (V).
б. К 3,918 г KaTaF, в чашках из
платины или фторопласта приливают
100 мл HaS04 (1 : 1), выпаривают
дважды до паров и разбавляют до
объема 1 л растворами 15%-ной
винной кислоты или 4%-ного
щавелевокислого аммония. Раствор
содержит 1,8095 мг/мл тантала (V); его
содержание контролируют
гравиметрически.
Те (IV). 1,276 г теллура высокой
чистоты растворяют в 50 мл
концентрированной НС1 при добавлении
10 капель концентрированной HNOa
и нагревании на водяной бане.
Разбавляют при помешивании водой до
объема 1 л. Раствор содержит
1,276 мг/мл теллура (IV), следы
окислов азота, избыток СГ.
Те (VI). 3,598 г К2Те04-5Н20
растворяют в I M H2S04 при
нагревании, разбавляют этим же раствором
до объема 1 л. Раствор содержит
1,276 мг/мл теллура (VI); его
содержание контролируют гравиметрически.
Th (IV). 5,522 г Th(N03)4-4H20
растворяют в 1 М HN03 и доливают
этой же кислотой объем до 1 л.
Раствор содержит 2,32 мг/мл Th (IV);
его содержание контролируют
гравиметрически.
Ti (III), a. 5 мл 15%-ного
раствора Tia(SOJ3 растворяют в 0,5 М
128
H2S04 и доливают до объема 1 л
этим же раствором. Содержание
титана (III) устанавливают титриме-
трически. Растворы хранят в
атмосфере С02, N2.
б. 0,4790 г металлического титана
высокой чистоты растворяют в 50 мл
H2S04 (1 : 4) при нагревании в
атмосфере С02. Разбавляют свежепро-
кипяченной и охлажденной в токе
СО2 водой до объема 1 л. Раствор
содержит 0,4790 мг/мл титана
(Ш).
Ti (IV). а. 0,4790 г
металлического титана высокой чистоты
растворяют в 50 мл .H2S04 (1 : 5), после
растворения для окисления
приливают по каплям HN03 до
обесцвечивания и выпаривают до густых
паров серной кислоты дважды.
Раствор разбавляют до объема 1 л 0,5 М
H2S04. Раствор содержит
0,4790 мг/мл титана (IV).
б. К 2,571 rK2[TiFfi]-H2OB4amKax
из платины или фторопласта
приливают 80 мл концентрированной
H2S04, выпаривают до появления
густых паров H2S04. Операцию
повторяют трижды. Раствор
разбавляют 0,5 М H2S04 до объема I л.
Раствор содержит 0,4790 мг/мл
титана (IV); его содержание
контролируют гравиметрически.
Т1 (I). а. 2,12235 г Т120
растворяют в 50 мл HN03 (1 : 1) при
нагревании, разбавляют водой до
объема 1 л. Раствор содержит
2,044 мг/мл таллия (I).
б. 2,664 г T1N03, высушенного
при 110° С, растворяют в воде с 2 мл
HN03, разбавляют водой до объема
1 л. Раствор содержит 2,044 мг/мл
таллия (I).
Т1(П1). 2,044 г металлического
таллия высокой чистоты растворяют
в 20 мл HN03 (1 : 1), выпаривают
досуха на водяной бане. Остаток
растворяют в НС1 (1 : 1) и доливают
ею же до объема 1 л. Раствор
содержит 2,044 мг/мл таллия (III),
избыток СГ.
U (VI). 5,021 г U02(N03)2-6H20
растворяют в воде и разбавляют
водой до объема 1 л. Раствор
содержит 2,380 мг/мл урана (VI); его
содержание контролируют
гравиметрически.
V (II). а. 0,01 М раствор V (V)
в 0,5 М H2S04 восстанавливают
100 г амальгамы цинка в атмосфере
С02. После фильтрования раствора
устанавливают содержание V (II) ти-
триметрически. Раствор хранят в
атмосфере С02, N2.
б. 0,01 М раствор V (V) в 0,5 М
H2S04 пропускают через редуктор,
заполненный амальгированным Zn.
V(IV). a. 1,65 г VOS04-3H20
растворяют в 0,25 М H2S04 и этим же
раствором доливают до объема 1 л.
Содержание V (IV) устанавливают
титриметрически.
б. В 1 л нагретого до 70° С
раствора 1,170 г NH4V03 в 1 M H2S04
пропускают ток S02 или добавляют
порциями 2 г Na2S205, удаляют
избыток SOa кипячением,
охлаждают. Раствор содержит
0,5094 мг/мл ванадия (IV).
V(V). a. 1,1699 г NH4V03
растворяют в 100 мл H2S04 (1:1) и
при перемешивании доливают водой
до объема 1 л. Раствор содержит
0,5094 мг/мл ванадия (V); его
содержание контролируют
гравиметрически или титриметрически.
б. 1,819 г V205 растворяют пр»
нагревании в 50 мл 1 М КОН или
NaOH, раствор разбавляют водой
до объема 1 л. Раствор содержит
1,0188 мг/мл ванадия (V).
W (VI). а. 3,299 г Na2W04-2HaO
растворяют в воде и разбавляют
до объема 1 л. Раствор содержит
1,838 мг/мл вольфрама (VI); его
содержание контролируют
гравиметрически. (
б. 2,319 W03 растворяют в 0,5 М
NaOH и им же доливают до объема
1 л. Раствор содержит 1,838 мг/мл
вольфрама (VI); его содержание
контролируют гравиметрически.
Y (III), a. 0,8891 г
металлического иттрия высокой чистоты
растворяют в 20 мл разбавленных НС1
(1 : 1) или HN03 (1 : 2), H2S04 (1:2),
HC!04 (1 : 2) при слабом нагревании
и при перемешивании разбавляют
водой до объема 1 л. Раствор
содержит 0,8891 мг/мл иттрия.
б. 2,2582 г Y203 высокой чистоты,
предварительно прокаленной,
растворяют при нагревании в 20 мл
концентрированной НС1 и при пере-
9 А. И. Лазарев и др.
129
мешивании разбавляют водой до
объема 1 л. Раствор содержит
1,7782 мг/мл иттрия (0,02 М); его
содержание контролируют
гравиметрически, титриметрически.
Yb(III). a. 1,730 г
металлического Yb высокой чистоты
растворяют в 20 мл концентрированной
НС1 или других кислотах при слабом
нагревании и при перемешивании
разбавляют водой до объема 1 л.
Раствор содержит 1,730 мг/мл Yb.
б. 3,941 г свежепрокаленной
Yb203 высокой чистоты растворяют
при нагревании в 20 мл НС1
концентрированной и разбавляют водой до
объема 1 л (0,02 М). Раствор
содержит 3,461 мг/мл Yb.
Zn. a. 0,6538 г металлического
цинка растворяют в 10 мл НС1
(1 : 1) или H2S04 (1:2) и
разбавляют водой до объема 1 л. Раствор
содержит 0,6538 мг/мл цинка.
б. 2,88 г ZnS04-7H20 растворяют
в воде и разбавляют до объема 1 л.
Содержание цинка устанавливают
гравиметрически или
титриметрически.
Zr(IV). a. 0,9122 г
металлического циркония высокой чистоты
помещают в чашку из платины или
фторопласта, вливают 10 мл воды,
10 мл HF концентрированной,
растворяют при слабом нагревании,
добавляя по каплям
концентрированную HN03. Вливают 50 мл H2S04
(1 : 1), выпаривают дважды до паров
HaS04, охлаждают, вливают 50 мл
H2S04 (1 : 1), при помешивании
разбавляют водой до объема 1 л. Раствор
содержит 0,9122 мг/мл циркония (IV).
б. 3,222 г ZrOCl2-8H20
растворяют в 100 мл НС1 (1 : 1) и при
помешивании доливают водой до
объема 1 л. Раствор содержит
0,9122 мг/мл циркония (IV). Его
содержание контролируют
гравиметрически и титриметрически.
17.3. СПОСОБЫ ПЕРЕВОДА
МЕТАЛЛОВ И НЕКОТОРЫХ
ИХ СОЕДИНЕНИЙ В РАСТВОР
AI и его сплавы. Хорошо
растворяются в соляной кислоте. Медленно
растворяются в концентрированной
и разбавленной азотной кислоте и
разбавленной серной кислоте.
Хорошо растворяются в
концентрированных растворах щелочей (20—
40%).
А1203. Сплавление со смесью соды
и поташа (1 : 1): анализируемое
вещество сплавляется с 4—6-кратным
избытком безводной смеси соды и
поташа в платиновом, никелевом или
железном тигле. Охлажденный сплав
растворяется в воде, причем в
остатке могут находиться карбонаты,
растворяемые в соляной кислоте. Можно
также сплавить с сульфатом
аммония и плав растворить в воде.
Be. Хорошо растворяется в
растворах соляной, серной и азотной
кислот. Холодная азотная кислота
пассивирует металл; не растворяется
в плавиковой кислоте.
ВеО. Растворим в кислотах при
нагревании или сплавление с бифто-
ридом калия в платиновом тигле и
растворение плава в воде.
В. Растворяется в кислотах,
кроме НС1. Сплавляется с едкими
щелочами, образуя метабораты.
V. Растворяется в азотной
кислоте и смесях ее с соляной кислотой.
При нагревании растворяется в
концентрированной серной кислоте.
Нерастворим в разбавленных
серной и соляной кислотах.
Сплавляется со щелочами.
Bi. Хорошо растворяется в
азотной кислоте, ее смеси с соляной
кислотой, в горячей серной кислоте.
Нерастворим в разбавленных
соляной и серной кислотах.
W. Растворяется в смеси
плавиковой и азотной кислот, в смесях
кислот, содержащих фосфорную
кислоту; в насыщенном растворе
щавелевой кислоты в присутствии
перекиси водорода. Порошкообразный
вольфрам хорошо растворяется в
растворах перекиси водорода.
Сплавляется со щелочами или содой в
присутствии окислителей (например,
КСЮ3) с образованием вольфраматов.
Ga. Хорошо растворяется в
растворах соляной, серной, хлорной и
плавиковой кислот. Слабо
растворяется в растворах азотной кислоты.
Растворим в растворах щелочей.
Hf. Легко растворяется в смеси
соляной, азотной и плавиковой
130
кислот. Нерастворим в соляной и
серной кислотах. Легко переводится
в раствор мокрым сплавлением со
смесью концентрированной серной
кислоты и калия сернокислого кислого.
Ge. Хорошо растворяется в смеси
соляной и азотной кислот, а также
в щелочном растворе перекиси
водорода. При добавке азотной
кислоты образуется гидрат двуокиси
германия.
Fe. Легко растворяется в
разбавленных серной, соляной и азотной
кислотах.
Fe203. Растворяется в серной,
соляной и азотной кислотах. Можно
перевести в раствор сплавлением
с 6-кратным количеством KHS04 и
выщелачиванием сплава в
разбавленной серной кислоте или
сплавлением с солями аммония и
растворением охлажденного сплава или
сублимата в воде.
Аи. Растворяется в смеси
соляной и азотной кислот.
In. Легко растворяется в
растворах соляной, хлорной кислот,
медленно — в серной, с трудом в
концентрированной азотной кислоте.
1г. В мелкодисперсном состоянии
медленно растворяется в смеси
соляной и азотной кислот. Можно
перевести в растворимое соединение
сплавлением с перекисью натрия или
спеканием с перекисью бария.
Y. Растворяется в растворах
соляной, серной и азотной кислот.
Cd. Растворяется в горячей
разбавленной азотной кислоте. Плохо
растворяется в разбавленных
соляной и серной кислотах. Растворение
ускоряется в присутствии перекиси
водорода или азотной кислоты.
Са. Переводят в амальгаму, при
нагревании которой с водой
образуется гидроокись кальция.
CaS04. Сплавление со смесью
соды и поташа (см. п. 2).
CaF2. Обработка смесью серной
и плавиковой кислот для удаления
фтора и последующее сплавление
прокаленной соли со смесью соды и
поташа, как указано в п. 2.
Со. Растворяется в
разбавленной азотной, соляной и серной
кислотах. Концентрированная азотная и
серная кислоты пассивируют металл.
СоО. Сплавление со смесью соды
и поташа, как указано в п. 2.
La (и другие РЗЭ). Легко
растворяются в растворах соляной,
серной и азотной кислот.
Li. Энергично взаимодействует
с разбавленной серной кислотой и
концентрированными соляной и
азотной кислотами.
Mg. Легко растворяется в
кислотах, в том числе и в уксусной кислоте.
Растворяется в концентрированных
растворах солей аммония.
Мп. Растворяется в
разбавленных растворах соляной, серной,
азотной кислот, в
концентрированной серной кислоте.
Си. Растворяется в азотной
кислоте, в концентрированной серной
кислоте при нагревании до ее паров.
Соляная кислота растворяет в
присутствии окислителей (железа (III),
перекиси водорода, азотной кислоты
и др.).
Мо. Легко растворяется в
азотной кислоте, в смеси соляной и
азотной кислот, в концентрированной
серной кислоте при сильном
нагревании. Порошкообразный молибден
растворяется в растворе перекиси
водорода.
As. Растворяется в азотной
кислоте, в смеси соляной и азотной
кислот, в концентрированной серной
кислоте при сильном нагревании.
Сульфиды As. Переводятся в
растворимое состояние окислительным
сплавлением (вещество
смешивается с трехкратным количеством
Na2C03 + KN03 или NaN03 (I : 1),
сплавляется и охлажденный сплав
растворяется в воде).
Na. Действием ртути
превращают в амальгаму, нагревая
которую с водой получают раствор
едкого натра.
Ni. Растворяется в
разбавленных растворах азотной кислоты,
в смеси соляной и азотной кислот.
Nb. Растворяется в смеси
азотной и плавиковой кислот, в смеси
концентрированной серной кислоты
с сульфатом аммония или калия при
сильном нагревании.
SnOa. а. В фарфоровом тигле
сплавляют с шестикратным количеством
смеси поташа с серой (1 : 1).
о*
131
б. Сплавляют cNaOH, KOH,Na2Os,
их смесями в никелевом, железном,
серебряном тигле и выщелачивают
в воде.
Sn. Растворяется в соляной
кислоте, в смеси соляной с азотной
кислотой, в горячей
концентрированной серной кислоте.
Платиновые металлы.
Растворяются в соляной кислоте при
наличии окислителей (HNOs, С12, НСЮ4,
NaC103 и др.). Переходят в
растворимую форму при окислительном
сплавлении или спекании (см. п. 31).
Re. Растворяется в азотной
кислоте с образованием рениевой
кислоты. Порошкообразный рений легко
растворяется в растворах Н202.
Hg. Хорошо растворяется в
азотной кислоте, горячей
концентрированной серной кислоте.
Нерастворима в соляной и разбавленной
серной кислотах.
РЬ. Хорошо растворяется в
разбавленной азотной кислоте, в
уксусной кислоте. Соляная и серная
концентрированные кислоты
растворяют при нагревании.
PbS04. а. Сплавлением со смесью
соды и поташа (см. п. 2).
б. Обработка аммиачным
раствором винной кислоты.
Se. Растворяется в азотной кисло-
тес образованием селенистой кислоты.
Ag. Легко растворяется в
азотной кислоте. При нагревании можно
растворить в концентрированной
серной кислоте.
Sb. Растворяется при
нагревании в концентрированной серной
кислоте, в смесях соляной и азотной
кислот, азотной и винной кислот.
Sr. Хорошо растворяется в
разбавленных серной, соляной и
азотной кислотах.
SrS04. Сплавление со смесью
соды и поташа (см. п. 2).
TI. Легко растворяется в
азотной кислоте, в серной кислоте
труднее, а в соляной кислоте плохо
вследствие образования
малорастворимого хлорида таллия- (1).
Та. Растворяется в смеси
плавиковой и азотной кислот. Сплавляется
со щелочами. Концентрированная
серная кислота действует на металл
при нагревании.
Та205. а. Сплавление со смесью
соды и поташа (см. п. 2).
б. Сплавление с едкими щелочами.
Те. Растворяется в азотной
кислоте, в смеси соляной и азотной
кислот, в концентрированной серной
кислоте.
Ti. Растворяется в разбавленной
соляной (1 : 1) и серной (1:1)
кислотах. Легко растворяется в
разбавленной плавиковой кислоте и ее
смеси с азотной кислотой. Азотная
кислота пассивирует титан.
ТЮ2. а. Растворение в кислотах
при нагревании.
б. Растворение в смеси серной
кислоты с сульфатом натрия при
кипячении.
Th u Тп02. Легко растворяется
в концентрированной соляной
кислоте, в смеси азотной и соляной кислот.
U. Растворяется в разбавленных
серной, соляной, хлорной кислотах.
Сг. Растворяется в соляной и
хлорной кислотах, разбавленной
серной кислоте.
Се. Легко растворяется в
минеральных кислотах с образованием
церия (III).
Zn. Хорошо растворяется в
разбавленных минеральных кислотах и
в концентрированных растворах
щелочей.
Zr02. Растворяется в смеси
соляной и азотной кислот, плавиковой
кислоте, а также смеси плавиковой
и азотной кислот. Растворяется
мокрым сплавлением в смеси серной
кислоты с сульфатом калия или в
расплаве калия сернокислого кислого.
17.4. БУФЕРНЫЕ РАСТВОРЫ
17.4.1. Образцовые
буферные растворы
В соответствии с ГОСТ 10170—62,
ГОСТ 101171—62, принятая в СССР
шкала рН основана на
воспроизводимых значениях рН следующих пяти
образцовых буферных растворов:
I. Раствор, содержащий в 1 л при
20° С 12,70 ± 0,02 г тетраоксалата
калия КНС204-Н2С204-2Н20
(0,05 моль/л).
II. Насыщенный при 25° С
раствор калия виннокислого кислого
КС4НБ06,
132
III. Раствор, содержащий в 1 л
при 20° С 10,21 и= 0,02 г калия фта-
левокислого KCgHgO,, (0,05 моль/л).
IV. Раствор, содержащий в 1 л
при 20° С 3,40 ± 0,01 г калия
фосфорнокислого однозамещенного
КН2Р04 (0,015 моль/л) и 3,55 =£
=t 0,01 г натрия фосфорнокислого
двузамещенного Na2HP04
(0,025 моль/л).
V. Раствор, содержащий в 1 л
при 20° С 3.81 =±= 0,01 г тетра-
борнокислого натрия (буры)
Na2B4O7-10H2O7 (0,01 моль/л).
Реагенты должны быть высушены
до постоянной массы при
следующих условиях: тетраоксалат калия—
при 57 =t 2° С; калий фталевокис-
лый кислый и калий
фосфорнокислый однозамещенный — при
ПО ± 5° С; натрий фосфорнокислый
двузамещенный — при 120 =*= 5° С.
Буру выдерживают до постоянной
массы при комнатной температуре
в эксикаторе над смесью влажного
хлористого натрия и сахара. Калий
виннокислый кислый применяется
без предварительного высушивания.
При хранении буферных
растворов следует предохранять их от
доступа углекислого газа и других
газов из воздуха. Щелочные
растворы следует хранить в
полиэтиленовой посуде. Срок хранения
фосфатных буферных растворов два
месяца, остальных три месяца.
Все соли должны быть
специальной квалификации, для рН-метрии
или марки х. ч., но дважды
перекристаллизованные.
рН образцовых буферных растворов
при температуре 10—60° С
Температура, °С
10
15
20
25
30
35
40
45
50
55
60
Растворы
i
1,67
1,67
1,68
1,69
1,69
1,69
1,70
1,70
1,71
1,72
1,73
11
3,56
3,55
3,55
3,54
3,55
3,55
3,56
3,57
ill
4,0
4,0
4,0
4,01
4,01
4,02
4,03
4,04
4,06
4,08
4,10
IV
6,92
6,90
6,88
6,86
6,84
6,84
6,84
6,83
6,83
6,84
6,84
V
9,33
9,27
9,22
9,18
9,14
9,10
9,07
9,04
9,01
8,99
8,96
Ацетатный буферный раствор по
Михаэлису: рН = 4,618 при 18° С
(50 мл 1 н. раствора NaOH 4-
+ 100 мл 1 н. уксусной кислоты +
4- 350 мл воды).
Буферный раствор по Вейбелю:
рН = 2,038 при 18° С (6,71 г КС1
растворяется в 1000 мл 0,01 н. НС1)
17.4.2. Цитратные буферные
растворы
Исходный раствор: 21,008 г лимонной
кислоты CeH807-H20 -f 200 мл 1 н. раствора
NaOH -)- вода до 1 л
рн
(18° С)
1,2
1,4
1,6
1,8
2,0
2,2
2,4
2,6
2,8
3,0
3,2
3,4
3,6
3,8
4,0
4,2
4,4
4,6
4,8
рН
(18° С)
5,0
5,2
5,4
5,6
5,8
6,0
6,2
6,4
Исходный
цитратиый
раствор, мл
11,0
19,8
24,5
28,2
30,9
32,8
34,8
36,5
38,3
40,4
42,8
45,8
48,4
52,0
56,0
60,8
68,0
76,0
88,0
Исходный
цнтратный
раствор, мл
96,0
85,0
76,5
69,0
64,0
59,5
56,5
54,5
0,1 н. НС1, мл
89,0
80,2
75,5
71,8
69,1
67,2
65,2
63,5
61,7
59,6
57,2
54,2
51,6
48,0
44,0
39,2
32,0
24,0
12,0
0,1 н. NaOH,
мл
4,0
15,0
23,5
31,0
36,0
40,5
43,5
45,5
Примечание. Лимонная кислота
квалификации х. ч., дважды перекрнсталлизован-
ная. При последней кристаллизации раствор не
должен нагреваться выше 60° С. Чистота
проверяется титрованием раствором едкого натра по
фенолфталеину или тимоловому синему
133
17.4.3. Цитратно-фосфатные
буферные растворы
(рН=2,2 ч-8,0)
Исходный цитратный раствор: 21,008 г
лимонной кислоты С6Н807-Н20 в 1000 мл
воды.
Исходный фосфатный раствор: 35,62 г
натрня фосфорнокислого двузамещенного
(Na2HP04-2H20) в 1000 мл воды
РН
(18° С)
2,2
2,4
2,6
2,8
3,0
3,2
3,4
3,6
3,8
4,0
4.2
4,4
4,6
4,8
5,0
5,2
5,4
5.6
5,8
6,0
6,2
6,4
6,6
6,8
7,0
7,2
7,4
7,6
7,8
8,0
Цитратный
раствор, мл
98,0
93,80
89,10
84,15
79,45
75,30
71,50
67,80
64,50
61,45
58,60
55,90
53,25
50,70
48,50
46,40
44,25
42,00
39,55
36,85
33,90
30,75
27,25
22,75
17,65
13,05
9,15
6,35
4,25
2,75
Фосфатный
раствор, мл
2,0
6,20
10,90
15,85
20,55
24,70
28,50
32,20
35,5
38,55
41,40
44,10
46,75
49,30
51,50
53,60
55,75
58,00
60,45
63,15
66,10
69,25
72,75
77,25
82,35
86,95
90,85
93,65
95,75
97,25
Примечание. Na,HP04- 2H20
квалификации х. ч., дважды перекрнсталлизоваиный.
При последней кристаллизации температура
раствора не должна превышать 90* С. Соль
увлажняют водой и высушивают в термостате при 36" С
двое суток.
17.4.4. Фосфатные буферные
растворы (рН=5,4-н8,0)
Исходный раствор однозамещенного
фосфата калня: 9,078 г КН2Р04 в 1000 мл воды.
Исходный раствор двузамещенного
фосфата натрня: 11,876 г Na2HP04-2H20
в 1000 мл воды.
рн
(18° С)
5,4
5,6
5,8
Раствор
КНгР04, мл
96,9
95,0
92,0
Раствор
Na,HP04, мл
3,1
5,0
8,0
Продолжение
р.ч.
(18° С)
6,0
6,2
6,4
6,6
6,8
7,0
7,2
7,4
7,6
7,8
8,0
Раствор KHsP0lf
мл
88,0
81,5
73,8
64,0
50,0
39,0
28,0
19,2
13,0
8,5
5,5
Распор
Na,HPO«, мл
12,0
18,5
26,2
36,0
50,0
61,0
72,0
80,8
87,0
91,5
94,5
Примечание. КН2Р04 квалификация
х. ч. должен быть дважды перекристаллизован н
высушен при ПО* С ^ 5.
17.4.5. Боратные буферные
растворы (7,6 ч-11,0)
Исходный раствор буры: 19,1 г Na2B407X
XlOH20 на 1000 мл воды
рН
(18° С)
7,6
7,8
8,0
8,2
8,4
8,6
8,8
9,0
9,2
РН
(18° С)
9.4
9,6
9,8
10,0
10,2
10,4
10,6
10,8
1Г,0
Раствор буры,
мл
52,2
53,8
55,9
58,5
62,0
67,5
75,0
85,0
96,3
Раствор буры,
мл
87,0
74,0
65,0
59,5
56,0
53,9
52,1
51,0
50,2
0,1 н. HG1, мл
47,8
46,2
44,1
41,5
38,0
32,5
25,0
15,5
3,7
0,1 и. NaOH,
мл
13,0
26,0
35,0
40,5
44,0
46,1
47,9
49,0
49,8
Примечание. Бура квалификации х. ч.
должна быть дважды перекристаллизоваиа,
причем при последней перекристаллизации раствор
ие должен нагреваться выше 55* С. Соль
выдерживается до постоянной массы при комнатной
температуре в эксикаторе над смесью влажного
хлористого натрия и сахара.
134
17.4.6. Фосфатные
буферные растворы
различной концентрации
(по А. Грину)
Буферные растворы, по Грину,
готовятся смешиванием
соответствующих количеств однозамещен-
ного и двузамещенного фосфатов
калия и растворением их в воде.
В таблице содержатся данные о
молярной доле двузамещенного
фосфата калия К2НР04, которая должна
быть взята для приготовления
буферного раствора с определенным
значением рН и соответствующей
концентрации. Например, требуется
изготовить 0,6 М раствор буфера
с рН = 5,8. Из таблицы следует,
что молярная доля для K2HPQ4
равна 0,171. Для приготовления 1 л
требуемого раствора следует
отвесить X г К2НР04 и Г г КН2Р04.
Расчет этих величин производится
по формулам
X = 174,183-0,171-0,8;
Y = 136,089(1 — 0,171)0,8,
где 174,183 — молекулярная масса
К2НР04, а 136,089 —
молекулярная масса КН2Р04.
РН
5,3
5,4
5,5
5,6
5,7
5,8
5,9
6,0
6,1
6,2
6,3
6,4
6,5
6,6
6,7
6,8
6.9
7,0
7,1
7,2
7,3
7,4
7,5
7,6
7,7
Моляриость буферного раствора
0,01
0,065
0,081
0,100
0,122
0,150
0,183
0,222
0,266
0,315
0,369
0,425
0,484
0,544
0,604
0,659
0,710
0,756
0,796
0,831
0,04
0,083
0,103
0,126
0,155
0,190
0,230
0,274
0,325
0,380
0,440
0,498
0,556
0,614
0,670
0,720
0,763
0,805
0,840
0,869
0,1
0,085
0,106
0,132
0,160
0,192
0,232
0,278
0,328
0,381
0,438
0,497
0,557
0,615
0,668
0,717
0,762
0,802
0,837
0,866
0,890
0,2
0,110
0,135
0,163
0,195
0,232
0,276
0,325
0,376
0,429
0,486
0,543
0,598
0,651
0,701
0,747
0,785
0,822
0,854
0,880
0,902
0,3
0,104
0,129
0,155
0,185
0,220
0,261
0,305
0,353
0,403
0,457
0,511
0,565
0,617
0,669
0,716
0,758
0,796
0,829
0,860
0,883
0,905
0,4
0,121
0,146
0,173
0,203
0,239
0,281
0,326
0,373
0,421
0,473
0,526
0,578
0,629
0,677
0,722
0,764
0,801
0,832
0,860
0,884
0,905
0.5
0,109
0,132
0,158
0,186
0,219
0,256
0,298
0,341
0,385
0,435
0,484
0,535
0,586
0,634
0,681
0,724
0,763
0,800
0,832
0,859
0,883
0,904
0,6
0,099
0,121
0,145
0,171
0,200
0,236
0,273
0,312
0,354
0,398
0,444
0.493
0,543
0,590
0,637
0,683
0,725
0,762
0.797
0,828
0,855
0,879
0,901
0.8
0,119
0,141
0,165
0,192
0,224
0,259
0,295
0,333
0,372
0,414
0,458
0,503
0,549
0,594
0,638
0,681
0,721
0,758
0.790
0,821
0,848
0,872
0.894
1,0
0,115
0,134
0,154
0,182
0,212
0,244
0,277
0,312
0,349
0,386
0,424
0,466
0,508
0,551
0,594
0,636
0,676
0.715
0,751
0,784
0,814
0,840
0,864
0,885
1,2
0,110
0,129
0,150
0,172
0,198
0,227
0,259
0,292
0,325
0,360
0,395
0,432
0,471
0,510
0,550
0.590
0,631
0,671
0,707
0,742
0,774
0,803
0,830
0,855
0,876
135
17.5. РАСТВОРИМОСТЬ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В ВОДЕ ПРИ 20°С
Соединение
1
Ag3As04
AgBr
AgCN
Ag2C03
Ag(C2H302)
ацетат
AgCl
AgC103
AgC104
Ag2Cr04
Ag2Cr207
Agl
AgMn04
AgN02
AgN03
Ag20
Ag3P04
Ag2S
AgSCN
Ag2S04
AICI3
Al(NO,)3
A1203
Al(OH)3
A12(S04)3
KA1(S04)2
NH4A1(S04)2
AS2O3
As205
H3As04
As2S3
AS205
AuCl3
H3BO3
Ва(С2Н302)г
ацетат
BaBr»
Ba(C204)
BaC03
BaCl2
Ba(C104)2
ВаСЮ4
BaF2
Bal2
Ba(N03)2
BaO
Ba(OH)2
BaS04
Ba|SiF6]
ВеС1г
Be(N03)2
BeO
BeS04
B|(OH)3
Bi2S3
Br2
HBr
Ca(C2H302)
ацетат
CaBr2
Ca(CA)
CaC03
Растворимость
г/100 г
НгО
2
8,5-10-*
1,3- lO"5
2,2-КГ 5
3,3-10"3
1,04
1,5- Ю-4
14,48
834
2.6-10-3
8,3-Ю-3
3-Ю"7
0,92
0,34
215,5
2,1-КГ3
1.6-1СГ3
1,4-КГ5
1,7-Ю-6
0,8
45,6
73,0
1 -10-*
1-10'4
36,3
6,0
6,59
1,85
65,8
86,3
5-1(Г5
1,4-10"*
68,0
4,9
71
104
8,5-10" 3
2,2-Ю"3
35,7
289,1
3,5-10-*
0,16
577,15
9,03
3,48
3,5
2,3-10-*
2,2-КГ2
238,4
103,3
2-10"5
42,5
1,4-10-*
1,8-10- 5
3,53
198,0
34,7
143
5,1 -КГ4
1,5-КГ»
моль/1000 г
н„о
3 |
1.8-10-6
6,9-10" 7
1,6-10-6
1,2-10-*
6,2-10" 2
1,0 - Ю- й
7,6-Ю"2
40,2
8,0- Ю- 5
1,9-10"*
1,3- Ю- 8
4.0-10-3
2,2-10~2
12,7
9,1 -10- ь
3,8 • 10"5
5,7-10" 7
1,0- Ю- 6
2,6-10-а
3,42
3,42
9,8- lO"6
1,3-КГ5
1,06
0,23
0,278
9,4-10"2
2,9
6,1
2,0-10-6
4,5-10-"
2,2
0,79
2,8
3,5
3,8-10"*
1,1-10-*
1,71
12,2
1,4-КГ6
9,1-10"3
14,8
0,346
0,227
0,20
9,9-10" 6
7,9-10-*
29,8
7,78
8•10"в
4,04
5,4- lO"6
3,5-КГ7
0,221
24,5
2,19
7,15
4,0-10" 5
1,5-КГ4
Соединение
1
СаС12
СаСЮ4
CaF2
Ca(N03)2
CaO
Са(ОН)2
CaHP04
Саз(Р04)2
CaS04
CdBr2 (30° С)
CdCl2
Cdl2
Cd(N03)2
Cd(OH)2
CdS
CdS04
Ce2(S04)3
CI,
HCl
CoC12
Co(N03)2
Co(OH3)
CoS
CoS04
Cr03
Cr(OH)3
KCr(S04)2
CsAl(S04)2
CsCl
CsC104
CsN03
Cs2[PtClJ
Cs,S04
Cufcl
CuCl2
Cu(N03)2
Cu(OH)2
CuS
CuSO„
FeBr2
FeC03
FeCl2
FeCl3
Fe(N03)2
Fe(N03)3
Fe(OH)2
Fe(OH)3
FeS
FeS04
Fe(NH4)2(S04)2
FeNH4(S04)2
Hg
HgBr2
Hg(CN)2
HgCl2
Hg2Cl2
Hgl2
желтая
Hgl2
красная
Hgl
Растворимость
г/100 г
H20
2
74,5
16,6
1,8-10"»
127,0
0,12
0,17
2,0-10" 2
3,6-10-*
0,2
132
134,5
86,2
153,0
2,5-10"4
1,3-10-"
76,9
12,0
1,85
72,1
51,0
100
3,2-Ю"4
4-10-*
36,0
168,0
64
24,4
0,46
186,5
1,6
23,0
8,6-10"3
178,6
1,2-10"2
77,0
121,9
6,7-10-*
3,4-lO"5
20,9
115,1
7,2-10-*
62,6
91,9
209,55
229,7
9,9-10" 5
5-10-"
6,2-10-*
26,6
26,9
124,0
2•10"6
0,62
9,3 (13,5° С)
6,6
2,3-10-*
5-10"3
3-10"5
2-Ю"8
моль/1000 г
нго
3
6,71
1,1
2,3-10"*
7,74
2,1-КГ2
2,31СГа
1,5-10-3
1,2- 1СГ 6
1,5- lO"2
4,85
7,34
2,35
6,48
1,7-10"5
9,0-10-'
3,68
0,211
0,26
19,8
3,93
5,46
2,9-10" 5
4,4-10" 5
2,32
16,8
0,862
1,3-1СГЯ
11,1
6,9-КГ2
1,18
1.3-10-4
4,94
1,2-10"3
5,72
6,50
6,9-10" 5
3,6-10-»
1,31
5,3
6,2 • 10" 5
4,95
5,66
17,7
9,5
1,1-10-»
4,7-10-"
7,1-10" 5
1,75
0,947
4,66
1-10"7
1,7-КГ2
(25° С)
0,37
0,24
9,7- lO"6
1,110-*
6,6-10-'
6,1 -10~1в
136
Продолжение
1
HgO
HgS
Hg2S04
h
hio3
KAl(S04)a
KBr
KBr03
KCN
К(С2Н3Ог)
ацетат
к2со3
КНСОз
КС1
ксюз
ксю4
касю4
К2Сг207
KCr(S04)2
KF
KHF2
K3[Fe(CN)e]
K4[Fe(CN„]
KI
КЮз
KMn04
KN02
KN03
кон
KH„P04
K2[PtCl,]
KRe04
KSCN
K2S03
K2S04
KHS04
K2S208
K2[SiFe]
La(C2H302)
LaCl3
La2(S04)3
LiBr
Li2C03
LiCl
LiF
Lil
LiNOa
LiOH
Li3P04
Li2S04
MgBr2
MgC03
MgCl2
MgF2
Mg(N03)2
MgO
Mg(OH)2
MgNH4P04
MgS04
MnBr2
MnC03
MnCl2
Mn(N03)a
Mn(OH)2
2
5-lO"3
1,3-10-»
6-10-11
2,2-10" 2
269,0
6,0
65,6
6,9
71,6
255,6
111,5
33,3
34,4
7,3
1,7
63,0
12,3
24,4
48,0
39,2
46,0
28,0
144,5
8,1
6,4
298,4
31,5
112,0
22,7
0,77
1,01
218,0
107,0
11,2
51,4
4,7
0,1
22,1
218,3
2,25
177
1,3
82,8
0,27
163
69,5
12,8
3-10"2
34,8
96,5
1,1 -10-2
54,3
8,7-10"3
70,5
6,2-10-*
9-10-*
6,o-10-3
35,6
146,9
4-10"а
73,5
131,5
2-10-*
3
2,3-10-*
5,6-КГ 8
1,2-КГ3
8,7-10-*
15,3
0,23
5,51
0,41
11,0
26
8,06
3,33
4,61
0,6
0,12
3,24
0,418
0,862
8,26
5,02
1,40
0,760
8,71
0,38
0,40
35,0
3,12
20,0
1,67
1.6-10-2
3,49-10- a
22,4
6,76
0,643
3,77
0,17
4,5-10"3
0,64
5,9
3,98-lO"2
20,4
0,18
19,5
0,10
12,2
10,1
5,35
2,6-lO"3
3,17
5,24
1,3-10"3
5,70
1,4-10"3
4,75
1,5-10-*
1,5-10-*
4,4-10-*
2,95
6,84
3,5-lO"3
5,84
7,35
2.2-10-5
1
MnS
MnS04
NH3
NH4Br
(NH4)2C03
NH4HC03
(NH4)2C204
оксалат
NH4C1
NH4F
NH4I
NH4N03
NH4H2P04
(NH4)2HP04
(NH4)2[PtC!e]
NH4SCN
(NH4)2S04
NH4V03
Na2HAs04
Na2B407
NaBr
Na(C2H302)
ацетат
Na3(CeH607)
цитрат
Na2C03
NaHC03
NaCl
NaC103
NaC104
Na2Cr04
Na2Cr207
NaF
Nal
Na2Mo04
NaN02
NaN03
NaOH
NaH2P04
Na2HP04
NaNH4HP04
Na2S
Na2S03
Na2S203
Na2S04
Na2SiF„
NaV03 (25° C)
Na2W04
NiCl2
Ni(N03)2
Ni(OH)2
NiS
NiS04
Ni(NH4)2(S04)2
Os04
PbBr2
Pb(C2H302)2
ацетат
PbC03
PbCl2
PbCr04
PbF2
Pbl2
Pb(NOs)2
PbO
2
6-10"3
62,9
53,1
73,9
100,0
21,7
4,4
37,4
82,6
172,3
178,7
36,8
68,6
0,67
163,0
75,4
0,48
26,5
2,5
90,5
46,2
70,3
21,6
9,6
35,9
96,1
181
90,1
180,1
4,1
179,3
65,0
81,8
88,0
107,0
85,2
7,7
16,7
18,6
26,6
70,0
19,1
0,65
20,7
73,0
55,3
94,1
1.4-10-3
1,5-10-*
37,8
10,4
6,4
0,84
30,6
1 -10-*
0,97
4,3-lO"6
6,6-10"2
6,5-LO"2
52,2
1,7-1(Г3
3
6.9-10-*
4,16
31,2
7,55
10,4
2,74
0,35
7,00
22,3
11,9
22,3
3,20
5,20
1.5-I0-2
21,4
5,70
4.I-10-2
1,43
0,12
8,80
5,63
2,73
2,04
1,1
6,15
9,03
14,8
5,56
6,88
0,98
12,0
3,16
11,9
10,3
26,8
7,10
0,54
1,22
2,66
2,11
4,42
1,34
3,5-10" г
1,70
2,48
4,26
5,15
1,5-10-*
1,7-10-*
2,51
0,362
0,25
3,6-10" a
0,941
3,7-10-»
3,5- lO"2
1,3 -10-'
2,7-10"3
1.4-10-»
1,58
7,6-10-*
10 А, И. Лааары a a». 137
Продолжение
1 I 2 | з || i | 2 | з
Pb(OH)2
PbS
PbS04
RbAl(S04)2
RbCl
RbC104
RbN03
Rb2[PtCl6]
Rb2S04
H2S
SbCl3
Sb2S3
H2SeOs
H2Se04
SnCl2 (15° C)
SnS
SnS2
SrBr2
Sr(C204)
оксалат
SrC03
SrCl2
SrCr04
SrF2
Sr(NO,)2
SrO
2,2-10-*
3•10"8
4,2-IO'3
1,52
91,1
1,0
53,4
2,8-10-*
48,2
0,38
931,5
2-Ю"4
16,8
1329
659
1.3-10-6
l,5-10-s
98
4,6-10" 3
1,1 - Ю-3
53,8
12
1,2-10" a
70,9
0,7
17.6. ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ i ВОДЕ ТРУДНОРАСТВОРИМЫХ
НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
(вычислены на основе концентрации, моль/л)
Соединение
1
AgBr
AgBr03
AgCN
AgCNO
Ag2C03
AgCl
Ag2Cr04
Ag2Cr207
Agl
AglO,
AgOH
Ag3P04
Ag2S
AgSCN
Ag2S04
AgVOs
As3o3
BaCOs
Ba(C204)
BaCr04
BaF2
Ba(IOs)2
Ba(OH)a
BaSO.
Bi(OH)a
Bi2S3
CaCOs
Ca(C„04)
CaCr04
Произведение
растворимости KDp
2
7-10-13
5,8
2
2,3
6,2
1,6
2
2
1
3,2
2
1,8
1
1
8
5
4
7
1,6
2
1.7
6,5
19
1
4,3
1,6
1
2,6
10" 8
10-is
io-7
Ю-12
10-ю
Ю- ia
io-'
Ю- ie
io-8
io-8
10"18
Ю-4»
10- ia
io-B
io-'
Ю-29
io-9
io-7
10-ю
10" •
10-ю
IO"3
10-ю
Ю-31
Ю-72
IO"8
IO"»
2,3-1(Га
Температура, °C
3
25
25
25
18—20
25
25
20
25
25
25
25
18—20
20
25
25
20
16
16
18
18
18
25
25
25
18—20
25
25
25
20
Соединение
1
CaF2
Ca(OH)2
CaS04
CdC03
Cd(C204)
Cd(OH)2
CdS
Ce2(C204)3
CoC03
Co(OH)2
B-CoS
Cr(OH)2
Cr(OH)3
CuC03
Cu(C204)
CuBr
CuCl
Cul
Cu(OH)a
CuS
Cu2S
CuSCN
FeC03
Fe(C204)
Fe(OH)2
Fe(OH)3
FeS
Hg2Br2
Произведение
растворимости К
2
4-1<Ги
5,5
6,1
2,5
1,5
1,2
1
2,6
1
2
2
2
1
1,4
2,9
4,1
1
5
5,6
8,5
2
1,6
2,5
2
3,2
4
3,7
1,3
i0"«
IO"5
10-м
IO"8
io-"
10- a»
10-s»
Ю-12
Ю-ie
Ю-27
Ю-20
Ю-30
10-ю
IO"8
IO"8
IO"'
Ю-12
Ю-20
Ю-45
10-47
10"11
IO""
10"'
Ю-14
Ю-38
10-1»
IO"21
Температура °C
a
25
18
25
25
20
25
25
20
25
25
20
18
25
25
25
18
18
18
25
18
17
18
18
25
18
25
18
25
138
9,1-10-6
1,3 -10-"
1,4-10-*
4,99-10" 2
7,54
5,4-10"2
3,62
4,8-Ю"4
1,80
0,11
40,8
5,9-10" e
1,30
91,7
34,7
8,6-10"8
8.2-10-'
4,0
2,6-10-*
7,5-10-a
3,39
0,59
9,6-IO"4
3,35
6,8-10" 2
Sr(OH)2
SrS04
Te02
H„Te04
Th(N03)4
Th(S04)2
TIBr
T12C03
T1C1
Tl2Cr04
T1I
T1N03
TIOH (30°
Tl2[PtCl„]
T12S
T12S04
U02(N03)2
ZnBra
ZnC03
ZnCl2
Zn(N03)2
ZnO
Zn(OH)2
ZnS04
ZnS
Zr(SQ4)2
C)
0,7
1.1 - IO"3
7-IO"*
33,85
191,0
1,38
2,4-IO" a
3,92
0,32
1,27-10-»
6,4-10-s
9,6
39,9
6,4-10" 3
510-3
4,9
119,3
446,4
2,2-10" a
367,0
117,5
1.6-10"4
5,2-10"*
53,8
6,9-10"*
110,6
5,8-IO" a
6,0-10"*
4,4-10-6
1,75
3,98
3,26-10" a
8,4-10-*
8,36-IO" 2
1.3-10-2
1.8-10-6
1,9-10-*
0,36
1,80
7,8-IO" e
1,1 -IO"3
9,7-10" 2
3,02
19,8
1,8-КГ3
26,9
6,20
2,0-10" 5
5,2-10" 5
3,33
7,1-10" B
3,91
Продолжение
'
HgjCOg
Hg2Cl2
Hg2I2
HgO
Hg(OH),
Hga(OH)2
HgS
Hg2S
Hg,S04
K2[PtCl6]
La2(C204)3
La(OH),
Li,C03
MgCo3
Mg(C204)
MgF2
MgNH4P04
Mg(OH)2
MnC03
Mn(OH)2
MnS
NiC03
Ni(OH)2
P-NiS
PbBr2
PbC03
Pb(C204)
2
9-10"1*
2
1,2-
1,4-
1-
7,8-
4-
1-
4,8-
5-
2-
I-
1,7
2,6
8,6
6
2,5
1,2
1
4
1,4
1,4
2
1
7,4
3,3
IO"18
10-28
10" 2e
10-2в
JO-24
10-53
1Q-4S
10-2
io-5
10-28
10-20
IO"3
10" B
io-B
io-"
io-13
10"u
10-ю
10-14
10"»
io-г
10-ie
Ю-26
•IO"6
IO"14
2,7-lO'11
3
25
25
25
20
18
18
20
25
25
18
25
25
25
12
18
25
25
25
25
18
20
25
25
20
25
18
18
i
PbCl2
PbCr04
PbFa
Pbl2
Pb(OH)2
PbS
PbS04
Sb(OH)s
Sn(OH)2
Sn(OH)4
SnS
SrC03
Sr(C204)
SrCr04
SrF2
SrS04
Th(OH)4
Ti(OH)3
TlBr
T1C1
Til
Tl(OH)|
T12S
ZnC03
Zn(C204)
Zn(OH)2
ZnS
2
2-10"5
1,8-10-"
7.10-0
1,3- IO"8
2-10-1»
1-10-*»
2-Ю"8
4.10-42
5-I0-2»
1.Ю-56
1.Ю-28
1,6-10Г9
5-10-a
3,6-10"5
3-10-»
3,8-10-«
1 • 10- 50
1. 10-40
4-10-»
2-IO"4
2,8-10"8
1. Ю-44
7.Ю-23
6- IO"11
1,4-10-<»
5-10-"
7-10-2«
3
25
18
20
20
25
25
25
25
25
25
25
25
18
18
25
18
25
25
25
25
20
25
18
25
18
25
20
17. 7. ПРОИЗВЕДЕНИЯ РАСТВОРИМОСТИ ГИДРООКИСЕЙ МЕТАЛЛОВ
Значения констант даны для следующих равновесий;
Ме(ОН)п i ^± Меп* + л ОН"; [Ме"+] -(ОН"]" = ПР
Ме(ОН)п \ ^ МЮпНп-1 + Н+; [MeOnHn-i] -[Н+] = ПР*
Элемент
Ag(I)
Al (III)
Au(I)
Au (III)
Ba(II)
Be (II)
Bi (III)
Ca (II)
Cd (II)
Ce (III)
Ce(IV)
Co (II)
Co (III)
Cr(II)
Cr (HI)
Cu(I)
Cu (II)
Fe (II)
Fe(III)
Ga (III)
Hf(IV)
Hg(I)
Hg(II)
U (III)
U (IV)
U(VI)
рПР = — )g
7,6
32,5
19,1
44
2,3
17,7
30,4
5,3
13,5—14,2
22,3
54,8
14,2—15,7
44,5
17,0
30
14,0
19,7
15,1
37,2—38,2
35—36,5
25,4 (20H-)
23—24(20H")
25,5
19
45
22,0 (ЮН")
рПР'=— lp
17,7
11,2—13,9
—
17,2
16,5
—
19,3
—
18,7
—
—
19,1
—
—
14,4
—
19,0
19,1
—
10,6
—
—
16,5
—
17,8
17,6
Элемент
In (III)
La (III)
Li (I)
Mg (II)
Mn (II)
Mn(III)
Mn (IV)
Ni (II)
Pb (II)
Pb (IV)
Pd (II)
Pt (II)
Sb (III)
Sc (III)
Sn (II)
Sn (IV)
Sr (II)
Те (IV)
Th (IV)
Ti (III)
Ti (IV)
TI (I)
TI (III)
V(V)
Zn (II)
Zr (IV)
рПР = -1к
33,2
19,0
1,4
11,0
12,7
36
56
14,7—17,2
14,5—15,6
64
31,0
35
17,1 (OH")
26,3
26,2
56
3,5
57,7
15,5 (OH")
35—40
29 (20H-)
0,2
45,2
14,7 (OH")
16,1—16,9
25,5 (20H-)
рПР' = -)й
16
—
—
—
19,0
—
—
18,2
15—16
32,4 (2H+)
—
—
11,9
—
14,9
32 (2H+)
—
—
19,8
—
—
—
—
—
29,1 (2H+)
18
1G*
17.8. рН ОСАЖДЕНИЯ ГИДРООКИСЕЙ МЕТАЛЛОВ
Гидроокись
Nb(OH)5
Та(ОН)в
Ti(OH)4
H2Si03
H2W04
H,Mo04
Sn(OH)4
Th(OH)4
Tl(OH),
Ce(OH)4
Sn(OH)2
Fe(OH),
HgO
Концентрация
растворов
выпадение
осадка
£
'о
^™
0
0
0.5
0
0
—
0,5
0,5
0
0,8
1,9
2,2
2,3
£
О
0
0
1.2
0
0
—
1
1,2
1
1.5
3,4
3,2
3,8
растворе-
осадка
£
'о
"-*
,_
—
—
И
—
8
14
—
—
—
9,9
14
11,5
£
Ь
_
—
11,5
8
9
15
—
—
—
12,9
—
14,5
Гидроокись
Zr(OH)4
нгио4
А1(ОН)з
Сг(ОН)8
Zn(OH)a
Со(ОН)а
РЬ(ОН)2
Fe(OH)2
РЗЭ(ОН)3
Cd(OH)a
AgaO
Mn(OH)„
Mg(OH)2
Концентрация
растворов
выпадение
осадка
£
Ь
""
2,3
4,0
3,8
4,7
7.0
7,9
7,8
7.4
6.8
7,3
8,4
8,6
9,5
£
О
3
ti.ti
4,8
5,7
8,5
9.4
9,3
8,9
8,5
8,8
11,4
10,1
11,0
растворение
осадка
£
о
""
._
—
6—9
П.4
10,5
14,1
10
13,5
—
—
12,7
14
~
S
Ь
^
._
—
9—12
14,4
13.5
—
13
—
—
—
—
—
17.9. ПРИБЛИЖЕННЫЕ ЗНАЧЕНИЯ рН НЕКОТОРЫХ РАСТВОРОВ
ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ
Вещество
Аммиачная вода
Аммоний
щавелевокислый
Аммоний сернокислый
»
фосфорнокислый однозамещенный
Аммоний
фосфорнокислый двузамещенный
Бура
Кальций гидроокись
)» углекислый
Калий уксуснокислый
» двууглекислый
» углекислый
» аммониевые
квасцы
» гидроокись
»
щавелевокислый кислый
»
фосфорнокислый однозамещенный
Калий цнанибтый .
Кислота бензойная
» борная
» винная
1 лимонная
Молярность
од
0,1
0.1
0,1
0.1
0,1
(насыщенный)
То же
0.1
0.1
0.1
0,1
1.0
0.1
0.1
0.1
(насыщенный)
0.1
0,1
0,1
рН
11,3
6,4
5,5
4,0
7,9
9,2
12,4
9,4
9,7
8,2
11,5
3,2
14,0
2,7
4,7
11,0
2,8
5,3
2,0
2,1
Вещество
Кислотг
»
»
1 молочная
салициловая
серная
Кислота сероводородная
»
»
»
»
»
Натрий
»
»
»
»
»
»
. »
»
»
Магний
соляная
трнхлоруксус-
ная
цианистая
щавелевая
янтарная
уксуснокислый
бензойнокнслый
углекислый
кислый
углекислый
гидроокись
кремневокнслый
сернокислый
кислый
фосфорнокислый
однозамещенный
фосфорнокислый
двузамещенный
фосфорнокислый
трехзамещенный
окнсь
Цннк окись
Молярность
0,1
(насыщенный)
1,0
0,1
0,1
0,1
0.1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
0,1
(насыщенный)
То же
РН
2,4
2,4
0,3
4,1
1,1
1,2
5,1
1,3
2,7
8,9
8,0
8,3
11,5
12,9
12,6
1,4
4,5
9,2
12,0
10,05
5.5
140
17.10. ПЛОТНОСТЬ РАСТВОРОВ КИСЛОТ И ЩЕЛОЧЕЙ
17.10.1. Серная кислота
Плотность
при 20° С
1,0051
1,0118
1,0184
1,0250
1,0317
1,0385
1,0453
1,0522
1,0591
1,0661
1,0731
1,0802
1,0874
1,0947
1,1020
1,1094
1,1168
1,1243
1,1318
1,1394
1,1471
1,1548
1,1626
1,1704
1,1783
1,1862
1,1942
1,2023
1,2104
1,2185
1,2267
1,2349
1,2432
1,2515
1,2599
1,2684
1,2769
1,2855
1,2941
1,3028
1,3116
1,3205
1,3294
1,3384
1,3476
1,3569
1,3663
1,3758
1,3854
1,3951
H2SO,
% |
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
г*л
10,05
20,24
30,55
41,00
51,59
62,31
73,17
84,18
95,32
106,6
118,0
129,6
141,4
153,3
165,3
177,5
189,9
202,4
215,0
227,9
240,9
254,1
267,4
280,9
294,6
308,4
322,4
336,6
351,0
365,6
380,3
395,2
410,3
425,5
441,0
456,6
472,5
488,5
504,7
521,1
537,8
554,6
571,6
588,9
606,4
624,2
642,2
660,4
678,8
697,6
моль/л
0,103
0,206
0,312
0,418
0,526
0,635
0,746
0,858
0,972
1,087
1,203
1,321
1,442
1,563
1,685
1,810
1,936
2,063
2,192
2,324
2,456
2,591
2,726
2,864
3,004
3,144
3,287
3,432
3,579
3,728
3,878
4,029
4,183
4,338
4,496
4,656
4,818
4,981
5,146
5,313
5,483
5,655
5,828
6,004
6,183
6,364
6,548
6,734
6,921
7,113
Плотность
при 20° G
1,4049
1,4148
1,4248
1,4350
1,4453
1,4557
1,4662
1,4768
1,4875
1,4983
1,5091
1,5200
1,5310
1,5421
1,5533
1,5646
1,5760
1,5874
1,5989
1,6105
1,6221
1,6338
1,6456
1,6574
1,6692
1,6810
1,6927
1,7043
1,7158
1,7272
1,7383
1,7491
1,7594
1,7693
1,7786
1,7872
1,7951
1,8022
1,8087
1,8144
1,8195
1,8240
1,8279
1,8312
1,8337
1,8355
1,8364
1,8361
1,8342
1,8305
H,so4
% |
51
52
53
54
55
56 .
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
73
74
75
76
77
78
79
80
81
82
83
84
85
86
87
88'
89
90
91
92
93
94
95
96
97
98
99
100
tin |
716,5
735,7
755,1
774,9
794,9
8115,2
835,7
856,5
877,6
899,0
920,6
942,4
964,5
986,9
1010
1033
1056
1079
1103
1127
1152
1176
1201
1226
1252
1278
1303
1329
1355
1382
1408
1434
1460
1486
1512
1537
1562
1586
1610
1633
1656
1678
1700
1721
1742
1762
1781
1799
1816
1831
моль/л
7,306
7,501
7,699
7,901
8,105
8,312
8,521
8,733
8,948
9,166
9,386
9,609
9,834
10,06
10,30
10,53
10,77
11,00
11,25
11,49
11,75
11,99
12,25
12,50
12,77
13,03
13,29
13,55
13,82
14,09
14,36
14,62
14,89
15,15
15,42
15,67
15,93
16,17
16,42
16,65
16,88
17,11
17,33
17,55
17,76
17,97
18,16
18,34
18,52
18,67
17.10.2. Соляная кислота
Плотность
при 20° С
1
1,0032
1,0082
1,0132
НС1
%
2
1
2
3
т(л
3
10,03
20,16
30,40
моль#л
4
0,2751
0,5529
0,8338
Плотность
при 20° С
1
1,0181
1,0230
1,0279
НС1
%
2
4
5
6
Г^Л
;з
i
40,72
51,15
61,67
моль/л
4
1,117
1,403
1,691
141
Продолжение
1
1,0328
1,0376
1,0425
1,0474
1,0524
1,0574
1,0625
1,0675
1,0726
1,0776
1,0827
1,0878
1,0929
1,0980
1,1032
1,1083
1,1135
2
7
8
9
10
И
12
13
14
15
16
17
18
19
20
21
22
23
3
72,30
83,01
93,83
104,7
115,8
126,9
138,1
149,5
160,9
172,4
184,1
195,8
207,7
219,6
231,7
243,8
256,1
4
1,983
2,277
2,573
2,872
3,176
3,480
3,788
4,100
4,413
4,728
5,049
5,370
5,697
6,023
6,355
6,687
7,024
1
1,1187
1,1239
1,1290
К1341
1,1392
1,1443
1,1493
1,1543
1,1593
1,1642
1,1691
1,1740
1,1789
1,1837
1,1885
1,1933
1,1980
2
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
3
268,5
281,0
293,5
306,2
319,0
331,9
344,8
357,8
371,0
384,2
397,5
410,9
424,4
438,0
451,6
465,4
479,2
4
7,365
7,707
8,050
8,398
8,749
9,103
9,457
9,813
10,18
10,54
10,90
11,27
11,64
12,01
12,39
12,76
13,14
17.10.3. Азотная кислота
Плотность
при 20° С
1
1,0036
1,0091
1,0146
1,0201
1,0256
1,0312
1,0369
1,0427
1,0485
1,0543
1,0602
1,0661
1,0721
1,0781
1,0842
1,0903
1,0964
1,1026
1,1088
1,1150
1,1213
1,1276
1,1340
1,1404
1,1469
1,1534
1,1600
1,1666
1,1733
1,1800
1*1867
1,1934
1,2002
1,2071
. 1,2140
1,2205
1,2270
%
2
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
HNO,
г/л
а
10,04
20,18
30,44
40,80
51,28
61,87
72,58
83,42
94,37
105,4
1Г6.6
127,9
139,4
150,9
162,6
174,4
186,4
198,5
210,7
223,0
235,5
248,1
260,8
273,7
286,7
299,9
313,2
326,6
340,3
354,0
367,9
381,9
396,1
410,4
424,9
439,4
454,0
моль/л
4
0,1593
0,3203
0,4831
0,6475
0,8138
0,9819
1,152
1,324
1,498
1,673
1,850
2,030
2,212
2,395
2,580
2,768
2,958
3,150
3,343
3,539
3,737
3,937
4,139
4,344
4,550
4,758
4,970
5,183
5,401
5,618
5,839
6,061
6,286
6,513
6,743
6,973
7,205
Плотность
при 20° С
1
1,2335
1,2399
1,2463
1,2527
1,2591
1,2655
1,2719
1,2783
1,2847
1,2911
1,2975
1,3040
1,3100
1,3169
1,3219
1,3278
1,3336
1,3393
1,3449
1,3505
1,3560
1,3614
1,3667
■ 1,3719
1,3769
1,3818
1,3866
1,3913
1,3959
1,4004
1,4048
1,4091
1,4134
1,4176
1,4218
1,4258
1,4298
%
2
38
39
40
41
42
43
44
45
46
47
48
49
50
51
52
53
54
55
56
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
73
74
HN03
г(п
3
468,7
483,6
498,5
513,6
528,8
544,2
559,6
575,2
591,0
606,8
622,8
639,0
655,0
671,2
687,4
703,7
720,1
736,6
753,1
769,8
78&£
803,2
820,0
836,9
853,7
870,5
887,4
904,3
921,3
938,3
955,3
972,3
989,4
1006
1024
1041
1058
моль^л
4
7,438
7,675
7,911
8,151
8,392
8,636
8,881
9,128
9,379
9,630
9,884
10,14
10,39
10,65
10,91
11,17
11,43
11,69
11,95
12,22
12,48
12,75
13,01
13,28
13,55
13,81
14,08
14,35
14,62
14,89
15,16
15,43
15,70
15,96
16,25
16,52
16,79
142
Продолжение
1
1,4337
1,4375
1,4413
1,4450
1,4486
1,4521
1,4555
1,4589
1,4622
1,4655
1,4686
1,4716
1,4745
2
75
76
77
78
79
80
81
82
83
84
85
86
87
3
1075
1093
1110
1127
1144
1162
1179
1196
1214
1231
1248
1266
1283
4
17,06
17,35
17,62
17,89
18,16
18,44
18,71
18,98
19,27
19,54
19,81
20,09
29,36
l
1,4773
1,4800
1,4826
1,4850
1,4873
1,4892
1,4912
1,4932
1,4952
1,4974
1,5008
1,5056
1,5129
2
88
89
90
91
92
93
94
95
96
97
98
99
100
3
1300
1317
1334
1351
1368
1385
1402
1419
1435
1452
1471
1491
1513
4
20,63
20,90
21,17
21,44
21,71
21,98
22,24
22,52
22,77
23,04
23,34
23,66
24,01
17.10.4. Фосфорная кислота
Плотность
прн 20° С
1,0038
1,0092
1,0146
1,0200
1,0255
1,0309
1,0365
1,0420
1,0476
1,0532
1,0590
1,0647
1,0705
1,0764
1,0824
1,0884
1,0946
1,1008
1,1071
1,1134
1,1199
1,1263
1,1329
Н8РО«
%
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
г/л
10,038
20,184
30,438
40,800
51,275
61,854
72,555
83,360
92,284
105,32
116,49
127,76
139,17
150,70
162,36
174,14
186,08
198,14
210,35
222,68
235,18
247,79
260,57
моль/л
0,1024
0,2060
0,3106
0,4163
0,5232
0,6312
0,7404
0,8507
0,9621
1,075
1,189
1,304
1,420
1,538
1,657
1,777
1,899
2,022
2,147
2,272
2,400
2,529
2,659
Плотность
при 20° С
1,1395
1,1462
1,1529
1,1597
1,1665
1,1735
1,1805
1,216
1,254
1,293
1,335
1,379
1,426
1,476
1,526
1,579
1,633
1,689
1,746
1,770
1,794
1,819
1,844
1,870
Н„РО,
% |
24
25
26
27
28
29
30
35
40
45
50
55
60
65
70
75
80
85
90
92
94
96
98
100
г/л
273,48
286,55
299,75
313,12
326,62
340,32
354,15
425,6
501,6
581,9
667,5
758,5
855,6
959,4
1068
1184
1306
1436
1571
1628
1686
1746
1807
1870
моль/л
2,791
2,924
3,059
3,195
3,333
3,473
3,614
4,343
5,119
5,938
6,811
7,740
8,731
9,790
10,90
12,08
13,33
14,65
16,03
16,61
17,20
17,82
18,44
19,08
17.10.5. Уксусная кислота
Плотность
при 20° С
1
0,9996
1,0012
1,0025
1,0040
1,0055
1,0069
1,0083
сн,соон
%
2
1
2
3
4
5
6
7
г/л
3
9,996
20,02
30,08
40,16
50,28
60,41
70,58
моль/л
4
0,1665
0,3334
0,5009
0,6687
0,8373
1,006
1,175
Плотность
при 20° С
1
1,0097
1,0111
1,0125
1,0139
1,0154
1,0168
1,0182
сн.соон
%
2
8
9
10
11
12
13
14
г/л
3
80,78
91,0
101,3
111,5
121,8
132,2
142,5
моль/л
4
1,345
1,515
1,687
1,857
2,028
2,201
2,373
143
Продолжение
1
1,0195
1,0209
1,0223
1,0236
1,0250
1,0263
1,0276
1,0288
1,0301
1,0313
1,0326
1,0338
1,0349
1,0361
1,0372
1,0384
1,0395
1,0406
1,0417
1,0428
1,0438
1,0449
1,0459
1,0469
1,0479
1,0488
1,0498
1,0507
1,0516
1,0525
1,0534
1,0542
1,0551
1,0559
1,0567
1,0575
1,0582
1,0590
1,0597
1,0604
1,0611
1,0618
1,0624
2
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42.
43
44
45
46
47
48
49
50
51
52
53
54
55
56
57
3
152,9
163,3
173,8
184,2
194,8
205,3
215,8
226,3
236,9
247,5
258,2
268,8
279,4
290,1
300,8
311,5
322,2
333,0
343,8
354,6
365,3
376,2
387,0
397,8
408,7
419,5
430,4
441,3
452,2
463,1
474,0
484,9
495,9
506,8
517,8
528,8
539,7
550,7
561,6
572,6
583,6
594,6
605,6
4
2,546
2,719
2,894
3,067
3,244
3,419
3,593
3,768
3,945
4,121
4,300
4 4,476
4,653
4,831
5,009
5,187
5,365
5,545
5,725
5,905
6,083
6,264
6,444
6,624
6,806
6,985
7,167
7,349
7,530
7,712
7,893
8,075
8,258
8,439
8,622
8,806
8,987
9,170
9,352
9,535
9,718
9,901
10,08
l
1,0631
1,0637
1,0642
1,0648
1,0653
1,0658
1,0662
1,0666
1,0671
1,0675
1,0678
1,0682
1,0685
1,0687
1,0690
1,0693
1,0694
1,0696
1,0698
1,0699
1,0700
1,0700
1,0700
1,0699
1,0698
1,0696
1,0693
1,0689
1,0685
1,0680
1,0675
1,0668
1,0661
1,0652
1,0643
1,0632
1,0619
1,0605
1,0588
1,0570
1,0549
1,0524
1,0498
2
58
59
60
61
62
63
64
65
66
67
68
69
70
71
72
73
74
75
76
77
78
79
80
81
82
83
84
85
86
87
88
89
90
91
92
93
94
95
96
97
98
99
100
3
616,6
627,6
638,5
649,5
660,5
671,5
682,4
693,3
704,4
715,2
726,1
737,1
748,0
758,8
769,7
780,6
791,4
802,2
813,0
823,8
834,6
845,3
856,0
866,6
877,2
887,8
898,2
908,6
918,9
929,2
939,4
949,5
959,5
969,3
979,2
988,8
998,2
1007
1016
1025
1034
1042
1050
4
10,27
10,45
10,63
10,82
11,00
11,18
11,36
11,54
11,73
11,91
12,09
12,27
12,46
12,64
12,82
13,00
13,18
13,36
13,54
13,72
13,90
14,08
14,25
14,43
14,61
14,78
14,96
15,13
15,30
15,47
15,64
15,81
15,98
16,14
16,31
16,47
16,62
16,77
16,92
17,07
17,22
17,35
17,48
17.10.6. Калия гидроокись
Плотность
при 20° С
1
1,0074
1.0165
1,0257
1,0348
1,0440
1,0531
1,0624
1,0717
1,0811
1,0904
КОН
%
2
1
2
3
4
5
6
7
8
9
10
г^л
3
10,07
20,33
30,77
41,39
52,20
63,19
74,37
85,74
97,30
109,0
моль/л
4
0,1795
0,3623
0,5484
0,7377
0,9303
1,126
1,325
1,528
1,734
1,943
Плотность
при 20° С
1
1,0998
1,1092
1,1187
1,1283
1,1379
1,1475
1,1572
1,1669
1,1766
1,1864
КОН
%
2
11
12
13
14
15
16
17
18
19
20
г/л
3
121,0
133,1
145,4
158,0
170,7
183,6
196,7
210,0
223,6
237,3
моль/л
4
2,157
2,372
2,592
2,816
3,042
3,272
3,506
3,743
3,985
4.229
144
Продолжение
1
1,1963
1,2062
1,2162
1,2263
1,2364
1,2466
1,2567
1,2669
1,2774
1,2879
1,2985
1,3091
1,3197
1,3304
1,3412
2
21
22
23
24
25
26
27
28
29
30
31
32
33
34
35
3
251,2
265,4
279,7
294,3
309,1
324,1
339,3
354,7
370,4
386,4
402,5
418,9
435,5
452,3
469,4
4
4,477
4,730
4,985
5,245
5,509
5,776
6,047
6,322
6,601
6,887
7,174
7,466
7,762
8,061
8,366
1
1,3520
1,3629
1,3738
1,3848
1,3959
1,4071
1,4183
1,4296
1,4409
1,4524
1,4639
1,4755
1,4871
1,4988
1,5106
2
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
3
486,7
504,3
522,0
540,1
558,4
576,9
595,7
614,7
634,0
653,6
673,4
693,5
713,8
734,4
755,3
4
8,674
8,988
9,303
9,626
9,952
10,28
10,62
10,96
11,30
11,65
12,00
12,36
12,72
13,09
13,46
17.10.7. Натрия гидроокись
Плотность
при 20° С
1,0095
1,0207
1,0318
1,0428
1,0538
1,0648
1,0758
1,0869
1,0979
1,1089
1,1199
1,1309
1,1420
1,1530
1,1641
1,1751
1,1862
1,1972
1,2082
1,2191
1,2301
1,2411
1,2520
1,2629
1,2739
NaOH
%
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
25
г/л
10,10
20,41
30,95
41,71
52,69
63,89
75,31
86,95
98,81
110,9
123,2
135,7
148,5
161,4
174,6
188,0
201,7
215,5
229,6
243,8
258,3
273,0
288,0
303,1
318,5
моль/л
0,2525
0,5103
0,7738
1,043
1,317
1,597
1,883
2,174
2,470
2,773
3,080
3,393
3,713
4,035
4,365
4,701
5,040
5,388
5,740
6,095
6,458
6,825
7,201
7,578
7,963
Плотность
при 20° С
1,2848
1,2956
1,3064
1,3172
1,3279
1,3385
1,3490
1,3593
1,3696
1,3798
1,3900
1,4001
1,4101
1,4201
1,4300
1,4397
1,4494
1,4590
1,4685
1,4779
1,4873
1,4969
1,5065
1,5159
1,5253
NaOH
%
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
г/л
334,0
349,8
365,8
382,0
398,4
414,9
431,7
448,6
465,7
482,9
500,4
518,0
535,8
553,8
572,0
590,3
608,7
627,4
646,1
665,1
684,2
703,5
723,1
742,8
762,7
моль/л
8,351
8,746
9,146
9,551
9,960
10,37
10,79
11,22
11,64
12,07
12,51
12,95
13,40
13,85
14,30
14,76
15,22
15,69
16,15
16,63
17,11
17,59
18,08
18,57
19,07
17.10.8. Аммония гидроокись
Плотность
при 20° С
1
0,9939
0,9895
0,9853
0,9811
NH4OH
%
2
1
2
3
4
г/л
3
9,939
19,79
29,56
39,24
моль/л
4
0,5836
1,162
1,736
2,304
Плотность
при 20" С
1
0,9770
0,9730
0,9690
0,9651
NH4OH
%
2
5
6
7
8
г/л
3
48,85
58,38
67,83
77,21
моль/л
4
2,868
3,428
3,983
4,534
145
Продолжение
[1
0,9613
0,9575
0,9538
0,9501
0,9465
0,9430
0,9396
0,9362
0,9328
0,9295
0,9262
2
9
10
11
12
13
14
15
16
17
18
19
3
86,52
95,75
104,9
114,0
123,0
132,0
140,9
149,8
158,6
167,3
175,8
4
5,080
5,622
6,160
6,694
7,222
7,751
8,273
8,796 ■
9,313
9,823
10,32
1
0,9229
0,9196
0,9164
0,9132
0,9101
0,9070
0,9040
0,9010
0,8980
0,8950
0,8920
2
20
21
22
23
24
25
26
27
28
29
30
3
184,6
193,1
201,6
210,0
218,4
226,8
235,0
243,3
251,4
259,6
267,6
4
10,84
11,34
11,84
12,33
12,82
13,32
13,80
14,29
14,76
15,24
15,71
17. 11. ПРИГОТОВЛЕНИЕ РАЗБАВЛЕННЫХ РАСТВОРОВ КИСЛОТ
И ЩЕЛОЧЕЙ
Предлагаемые ниже в таблицах
данные по приготовлению 1 л
разбавленных растворов кислот и
щелочей основаны на расчетах и с
учетом того, что концентрированная
серная кислота является 96%-ной,
соляная 37%-ной, азотная 65%-ной,
раствор аммиака 37%-ным в
расчете на NH,.
Серная
Требуемая
концентрация
25%
10%
5%
2 н.
1 н.
кислота
Количество
концентрированной
кислоты, мл
167,2
60,5
29,3
55,7
27,8
Азотная кислота
Требуемая
концентрация
25%
10%
5%
2 н.
1 н.
Количество
концентрированной
кислоты, мл
317,1
116,2
56,7
139,3
69,6
Соляная кислота
Требуемая
концентрация
25%
10%
5%
2 н.
1 н.
Количество
концентрированной
кислоты, мл
641,5
239,1
116,8
166,5
83,3
Аммония
Требуемая
концентрация
10%
5%
2 н.
1 н.
гидроокись
Количество
концентрированного
раствора, мл
422,3
215,4
150,2
75,1
146
17.12. ПРАВИЛО КРЕСТА
3. Дан водный раствор плотностью
1,57 г/мл. Необходимо приготовить
раствор с плотностью 1,20 г/мл:
1,57 0,20
1,20
1,00 0,37
Следует смешать 20 ч. по массе
раствора с плотностью 1,57 г/мл
с 37 ч по массе воды.
Примечание. Применение правила
креста для растворов с заданной плотностью
допустимо только в том случае, если
плотность растворов линейно изменяется с
изменением концентрации, что не всегда
соблюдается (см., например, раствор аммиака
и уксусной кислоты).
Неточные результаты можно получить
также при расчетах с растворами,
концентрация которых выражена в объемных
процентах в том случае, если не соблюдается
правило аддитивности при смешении (например,
смеси воды и этанола).
17.13. ПЛОТНОСТЬ ВОДЫ ПРИ ТЕМПЕРАТУРАХ ОТ О ДО 50° С
Температура, °С
0
0,5
1.0
1,5
2,0
2,5
3,0
3,5
4,0
4,5
5,0
5,5
6,0
6,5
7,0
7,5
8,0
8,5
9,0
9,5
10,0
10,5
11,0
11,5
12,0
Плотность,
г/мл
0,999868
899
927
950
968
982
992
998
1,000000
0,999998
992
982
968
951
929
904
876
844
808
769
727
681
632
580
525
Температура, °С
12,5
13,0
13,5
14,0
14,5
15,0
15,5
16,0
16,5
17,0
17,5
18,0
18,5
19,0
19,5
20,0
20,5
21,0
21,5
22,0
22,5
23,0
23,5
24,0
24,5
Плотность,
г^мл
466
404
339
271
200
126
050
0,998970
887
801
713
622
0,998528
432
332
230
126
019
0,997909
797
682
565
445
323
198
Температура, °С
25,0
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
44
45
46
47
48
49
50
Плотность,
г/мл
071
0,99681
54
26
0,99571
67
37
05
0,99489
40
03
0,99368
33
0,99296
66
21
0,99183
44
04
0,99063
22
0,98979
37
0,98893
49
04
147
Применение правила креста для
приготовления растворов заданной
концентрации или плотности
поясняется следующими ниже примерами:
1. Даны 90%-ный и 65%-ный
растворы. Необходимо приготовить
70%-ный раствор. Составляем
запись в виде следующей таблички:
90 5
70
65 20
Из этой записи следует, что
необходимо смешать 5 ч. по массе 90%-
ного раствора g 20 ч. по массе 65%-
ного раствора.
2. Даны 90%-ный раствор и
чистый растворитель. Необходимо
приготовить 30%-ный раствор:
90 30
30
^ \
С 60
18. ГАЗЫ И ПАРЫ ЖИДКОСТЕЙ
18.1. СПОСОБЫ ПОЛУЧЕНИЯ ГАЗОВ
Н2. 1. В аппарате Киппа из
металлического цинка, свободного от
мышьяка, при действии соляной
кислоты (1 : 1) или серной (1 : 6).
Если используются очень чистые
реагенты, то добавляют небольшое
количество раствора CuS04 или
одну каплю На [PtCle]. 2. Действием
едкого кали (1 : 3) на чистейший
алюминий (проволока, гранулы или
фольга). 3. Электролизом воды.
В4Н4. Внесение борида магния
в разбавленную соляную кислоту или
ЗМ фосфорную кислоту. Выход
—11,5%. Получают газ,
загрязненный НС1, НаО, Н2.
С02. 1. В аппарате Киппа
действием НС1 (1 ; 1) на возможно
более чистый мрамор в кусках
величиной с орех. 2. Взаимодействием
H2S04 (1:3) с карбонатом
калия — натрия, сплавленного в
стержни. 3. Взаимодействием
насыщенного раствора КНС03 с 50%-ной
H2S04 (1 : 2).
СО. 1. Введением по каплям
муравьиной кислоты в
концентрированную серную кислоту при 70° С.
2. Разложением очень чистого фор-
миата бария концентрированной
серной кислотой. 3. Нагреванием при
температуре свыше 440° С смеси
СаСг04 и СаО.
COS. 1. Взаимодействием
NH4 SCONH2 с 10%-ным раствором
НС1. 2. Смешиванием насыщенного
раствора NH4SCN и 66%-ной H2S04.
СОС1а. Введением по каплям СС14
в раствор H2S04, содержащий 45%
S03 (олеум) и нагретый до 80° С.
СН4. 1. Методом Гриньяра
получают очень чистый газ. 2. Внесением
в теплую воду порций (сильное
разогревание!) А14С3, сплавленного
в кусочки. Получается газ, сильно
загрязненный На, NH3, N2 и др.
CgHj. Действием воды на CaQ
в специальных аппаратах.
N2. 1. Пропусканием NH3
через бромную воду, охлаждаемую
льдом. 2. Осторожное нагревание
концентрированных NO, NH3,
(NH4)2S04 и NaN02 при 60-70° С.
3. Разложение азида бария при
температуре <152° С. Получают очень
чистый газ.
NH3. 1. Добавлением по каплям
60%-ного раствора едкого кали к
твердой соли NH4C1 при нагревании.
2. Легким нагреванием или
отсасыванием из продажного чистого
раствора аммиака (примеси СОа, НаО).
3. Тщательным перемешиванием
смеси чистейшего NH4C1 и гашеной
извести и нагревание ее. 4.
Взаимодействием нитрида магния с водяным
паром при пониженном давлении.
Получается чистый газ, свободный
от примесей органических
азотсодержащих соединений.
NOC1. Смешением (NO) HS04
с NaCl в отсутствие влаги и
нагреванием на водяной бане.
N20. KaS03-2NO, легко
получаемое из компонентов, вносят
в воду, имеющую слабощелочную
реакцию, и добавляют по каплям
разбавленную серную кислоту.
Получают очень чистый газ.
NO. 1. В аппарате Киппа из
NaNOa в виде стержней действием
разбавленной серной кислоты (1 : 3).
2. Действием 50%-ной серной
кислоты на раствор, содержащий KN02
и К1. Получают довольно чистый газ.
3. Раствор NaN02 средней
концентрации добавляют по каплям к
концентрированному раствору FeS04,
который смешивают с равным
объемом НС1 (1 : 1). 4. Добавлением
по каплям 50%-ной серной кислоты
к раствору NaN02. Газ загрязнен
многими примесями. 5.
Нагреванием при 300° С смеси KNOa, KN03
и Сг203 или Fe203.
N02. 1. Азотную кислоту
плотностью 1,38—1,40 при 70° С
медленно по каплям добавляют к As203,
пропуская ток кислорода, или
осторожно нагревают кашеобразную
смесь в токе кислорода. Примесь
кислорода (освобождается
сжижением). 2. Pb (N03)2 разлагают
осторожным нагреванием в токе 02.
HCN. 1. K4Fe(CN)e смешивают
с холодным 36%-ным раствором
серной кислоты и нагревают до
выделения газа. 2. Концентрированный
148
раствор NaCN добавляют по каплям
к теплой серной кислоте (1 : 1),
в которую добавлено немного FeSQ4.
(CN)2. Действием по каплям
концентрированного раствора KCN на
раствор CuS04 при нагревании и
добавлении в конце раствора FeCl3.
02. 1. Добавлением по каплям
15%-ного раствора перекиси
водорода к концентрированному
раствору КМп04 в разбавленной
серной кислоте. 2. Нагреванием
КМп04 до 200—250° С (влага, С02,
следы озона и пыль).
03. 1. В специальных сосудах
с использованием тлеющего разряда.
2. Электролизом H2S04 (плотностью
1,08) на платиновом электроде при
температуре ниже 10° С и очень
высокой плотности тока.
HF. 1. Действием
концентрированной серной кислоты на
плавиковый шпат или криолит.
Получается очень загрязненный продукт.
2. Нагреванием KHF2.
РН3. Желтый фосфор нагревают
с разбавленным едким кали в слабом
токе водорода (следы других
соединений фосфора с водородом и водород).
HaS. 1. В аппарате Киппа
действием соляной кислоты (1 : 1,5)
на FeS. Следы 10—12% водорода,
соединения мышьяка. 2.
Нагреванием смеси парафина, кизельгуро-
вого асбеста и серы (1:1:2) до
60° С.
S02. 1. Нагреванием до 60° С
раствора S02 в абсолютном спирте.
2. Нагреванием концентрированной
серной кислоты с равным весовым
количеством Hg или трехкратным
количеством меди (очень чистый газ).
СаС12. Содержание воды в газе
после осушения 0,2—0,8 мг/л.
Применяют для осушения Cl2, H2S, С2Н2,
(CN)2, HCN, СО и т. д. Нельзя
применять для осушения NH3,
аминов, спиртов, HF. Мало подходит
для осушения НВг, HI, Вг2. Для
газов, разлагающихся на пористых
поверхностях (AsH3, PH3 и др.),
применяют плавленый СаС12.
Силикагель. Неприменим для
осушения HF, мало эффективен для
3. Добавлением по каплям серной
кислоты (1:1) к
концентрированному раствору NaHS03 (небольшое
количество С02).
С12. 1. Добавлением по каплям
концентрированной соляной кислоты
к КМп04 с одновременным
охлаждением водой (02 до 0,5% и окислы
хлора). 2. Действием
концентрированной соляной кислоты на
осажденную чистую Мп02 при небольшом
нагревании ^чистый газ). 3.
Нагреванием смеси К2Сга07 и соляной
кислоты (3 : 1) (0,1% 02).
НС1. 1. В небольшом аппарате
Киппа без нижнего тубуса
действием концентрированной серной
кислоты на кусочки NH4C1. 2. При-
ливанием концентрированной серной
кислоты к концентрированной
соляной кислоте. 3. На холоду
пропускают НС1 в возможно более
концентрированный раствор СаС1а, а
затем нагревают. Получают
безводный газ.
AsH3. Действием разбавленной
серной кислоты на арсенид цинка.
Вга. Нагреванием 1 ч. по массе
КаСг207, 1 ч. по массе КВг и 5 ч.
по массе концентрированной серной
кислоты.
НВг. 1. Добавлением по каплям
сиропообразной фосфорной кислоты
при нагревании к КВг Получают
чистый газ. 2. Действием брома по
каплям на тетралин.
HI. 1. Осторожным нагреванием
KI со стекловидной метафосфорной
кислотой. 2. Нагреванием очень
концентрированного раствора HI
при медленном пропускании тока
водорода.
легко конденсируемых газов (NH3,
Cle, Вг2 и др.). Остаточное
содержание влаги после осушки до 0,02 мг/л.
H2S04. Как осушитель имеет
ограниченное применение. Используют
для осушения НС1,С1а, Br2, CO, N20,
SOa,CH4, 02. Нельзя применять для
осушения NH3, НВг, HI, H2S, PH3,
AsH3, CaHa, HCN, (CN)2, N02. Мало
применим для Н2, NO, HF.
Быстродействующий осушитель. Остаточное
содержание влаги до 3 X Ю-3 мг/л.
18.2. ОСУШИТЕЛИ ГАЗОВ
149
Mg(Cl04)s (ангидрон).
Эффективный осушитель. В проходящем газе
остается менее чем 0,001 мг НгО/л.
Вследствие нейтральной реакции
применим для осушения почти всех
газов. Однако поглощает спирты,
ацетон, пиридин. Следует соблюдать
осторожность при очистке газов,
содержащих органические примеси
(взрывоопасно).
Ра05. Эффективный, часто
используемый осушитель. При длительном
соприкосновении при комнатной
температуре остаточное содержание
влаги составляет менее 2•1О-8 мг/л.
Нельзя применять для осушения
NH3, HF, HC1, НВг. Мало пригоден
для осушения HaS, Cl2, Вг2.
КОН. Остаточное содержание
влаги 0,002—0,007 мг НаО/л, NaOH
менее эффективный осушитель.
Неприменим для газов, реагирующих
со щелочью.
А1а03. Преимуществами этого
осушителя являются его нейтральный
характер и очень быстрое действие.
Однако сорбционная емкость его
невелика, остаточное содержание влаги
при комнатной температуре около
0,004 мг Н20/л.
18.3. ВЕЩЕСТВА ДЛЯ ПОГЛОЩЕНИЯ ГАЗОВ
Поглощаемый
газ
1
на
о2
Поглотитель
2
о2
Вг2
Палладиевая чернь
NaC103
КМпО,
СиО
Пирогаллол (12)
Триацетилоксигидрохи-
нон
СгС12
CrS04-5H20
(5)
Си
Na2S204-2H20
(Ю)
(7)
Р (белый)
Состав поглотителя
3
Избыток кислорода, специальная пипетка
Насыщенный водный раствор
Раствор хлористого палладия в щелочи,
восстановленный этанолом
35 г NaC108 + 5 г NaHCO„ + 0,5 г PdCl2 +
+ 0,02 г OsO, в 250 мл воды (температура
80-90° С)
Водный раствор
Гранулированная окись
1 объемн. ч. 25%-ного водного раствора
пирогаллола + 5—6 объеме, ч. 60%-ного
кон
20 г триацетилоксигидрохинона,
смоченного небольшим количеством воды
+ 40 г КОН в 80 мл воды. Пропустить
водород
20%-ный водный раствор
15 г Cr(S04)-5H20 в 100 мл 30%-ной серной
кислоты
Пропускавие кислорода над нагретой медью
1. 250 мл 20%-ного раствора Na2S20« +
+ 40 мл КОН (5 : 7)
2. 16 г Na2SA-2H20+ 13,3 г NaOH +
+ 4 г натриевой соли антрахинонсульфо-
кнслоты в 100 мл воды
Увлажненный фосфор
150
Продолжение
1
Оз
\Л%з ОГ2» Ig
СО
со2
NH,
N0
H4S
2
KI
FeS04
As203
Гидроокиси щелочных
металлов
CuCl
(16)
(5)
CuaO
КОН (40)
НС1
NaBrO
FeSQ4-7HaO
Бромная вода
CdS04
1 Pb(CH3CO0)a-3Ha0
3
Щелочной раствор KI
Водный раствор
Водный раствор, содержащий NaHC03
Водный раствор
3 объемн. ч. (200 г CuCl+250 г NH„CI
в 750 мл воды) + 1 объемн. ч. раствора
аммиака (пл. 0,91)
15 г CuCl + 200 мл 20%-ной НС1 + 10 г
CuS04-5H20 + 30 г NH2OH-HCl + 40 мл
концентрированного раствора аммиака в
500 мл НаО
35 г CuCl в 250 мл концентрированной НС1,
обесцвечивается металлической медью
5 г Cu20 в 100 мл концентрированной
серной кислоты (суспензия)
30—50%-ный раствор КОН в воде
2 М НС1
Водный раствор
28 г FeS04- 7НгО в 64 мл воды + 8,5 мл
концентрированной серной кислоты
Насыщенный водный раствор брома
50 мл 1 М NH4OH + 50 мл 0,1 М NH4C1 +
+ 50 мл 0,5 н. CdS04-8/3 НгО
0,5 М раствор в воде
so2
S03
HCN
На02
50 мл 3%-ной Н202+ 50 мл 1 М, NaOH
K3Fe(CN)„
15 г K3Fe(CN)e + 18,5 r NaaCO3-10HaO
в 100 мл воды
Мп02
CuS04
\ Гранулы МпОа, пропитанные Н3Р04
Нанесенный на пемзу
NaOH
2 М раствор
Вымор аживан ием
NaaCOs
10%-ный раствор в воде
AgN03
0,1 М раствор в азотнокислой среде или
аммиачный раствор ^
151
Продолжение
1
сгн4
СгН2 (ацетилен)
Бензол и его
гомологи, тяжелые
углеводороды
NH3
2
h2so4
(8)
Бромная вода
CuCl
Вга
h2so4
CuCl
Hgl
H2S04
Вга
Гипобромит натрня
3
Дымящая серная кислота
Насыщенный водный раствор брома
См. поглощение СЮ
Насыщенный водный раствор брома
H2S04 с 25% S03
См. поглощение СО
25 г Hgl-f 30 г KI4- 100 мл 1 М КОН
H2S04 с 20—25% S03
Насыщенный водный раствор брома
Водный раствор
Примечание. Цифры в скобках в графе «Поглотитель» — поглощающая способность,
мл газа на 1 мл поглотителя.
18.4. ГАЗЫ ИЗ БАЛЛОНОВ
Газ
1
Водород
Кислород
Азот
Двуокись углерода
(углекислый газ)
Воздух
Аммиак
Окраска баллона,
маркировка (в СССР)
2
Темно-зеленый цвет,
надпись красная
Голубой цвет, надпись
черная
Черный цвет, надпись
желтая, цвет полосы
под надписью
коричневый
Черный цвет, надпись
желтая
Черный цвет, надпись
белая
Желтый цвет, надпись
черная
Примеси в газах
3
В электролитическом до 0,5% N2 и
0,1% Оа; в полученном методе
глубокого охлаждения коксового газа
0,3—1,0% СО и N2, до 0,003% Оа;
0,001% СОа+ Н2
В полученном по методу Линде до
0,7% Аг и до 0,3% N; в
электролитическом до 1% На + Na Ч- С02; в
медицинском кислороде, получаемом
электролитически, до 0,1% Na и до
0,1% СОа
В обычном азоте до 1% Оа, Ar, Ne;
в особо чистом азоте менее 0,01% Ог
Na, 02, НаО
Пары воды, насыщенного масла
В полученном из элементов следы
воды, СОа; в полученном из угля
вода (0,5%), пиридин, ацетонитрил,
метиламин
1 2
Продолжение
1
Аргон технический
Аргои сырой
Аргои чистый
Ацетилен
Гелий
Хлор
2
Черный цвет, надпись
синяя, полоса синяя
Черный цвет, надпись
черная, полоса белая
Серый цвет, надпись
зеленая, полоса зеленая
Цвет белый, надпись
красная
Цвет коричневый,
надпись белая
Цвет защитный, полоса
зеленая
3
02. N,
Оа, N2
02, N2
Газ грязный, содержит ацетон,
очищать следует пропусканием через слой
гератоля
Оа, N2. Ar
02, N2, Н20, СО, НС1, С02, СОС1,
18.5. РАСТВОРИМОСТЬ ГАЗОВ В ВОДЕ
(выражена в объеме газа, приведенного к нормальным условиям, поглощенного единицей
объема жидкости при парциальном давлении газа, равном 760 мм рт. ст.)
Гаа
Растворимость газов в воде при температуре, °С
10
20
40
60
100
Азот
Ацетилен . . .
Водород . . .
Гелий . . . .
Кислород . . .
Сероводород . .
Углекислый газ
0,0235
1,49
0,0205
0,0429
3,977
1,424
0,0186
1,31
0,0195
0,0099
0,0380
3,399
1,194
0,0154
1,03
0,0182
0,0099
0,0310
2,582
0,878
0,0118
0,0164
0,0102
0.0231
1,660
0,530
0,0102
0,0160
0,0195
1,190
0,359
0,0095
0,0160
0,0172
0,81
18.6. РАСТВОРИМОСТЬ ВОЗДУХА В ВОДЕ
1, "С
0
10
20
30
40
Растворимость воздухз (см*)
в 1 дм* воды при нормальных
условиях
всего
воздуха
28,64
22,37
18,26
15,39
13,15
в том числе
азоха
18,45
14,50
11,91
10,35
8,67
кислорода
10,19
7,87
6,35
5,24
4,48
t, °с
50
60
80
100
Растворимость воздуха (см*)
в 1 дм* воды при нормальных
условиях
всего
воздуха
11,40
9,78
6,00
0,00
в том числе
азота
7,55
6,50
4,03
0,00
киолорода
3,85
3,28
1.97
0.00
11 А. И. Лазарев и др.
153
18.7. РАСТВОРИМОСТЬ ГАЗОВ В ВОДНЫХ РАСТВОРАХ
НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
(выражение концентрации то же, что и в табл. 18.5.)
Газ
Водород
Кислород
Углекислый газ
Растворенное
вещество
НС1
HN03
NaCl
NaOH
NaaS04
KCl
K2COs
HCl
HgS04
HN03
NaCl
NaOH
HCl
HNO3
KCl
KNOs
t. °c
25
25
15
25
15
15
15
15
15
15
15
15
15
15
15
15
Концентрация раствора
0,5 и.
0,0170
0,0172
0,0151
0,0326
0,0320
0,0330
0,0292
0,0273
0,989
1,022
0,925
0,953
1 и.
0,0164
0,0168
0,0148
0,0127
0,0137
0,0150
0,0134
0,0310
0,0302
0,0319
0,0246
0,0219
0,974
1,029
0,850
0,897
2 н.
0,0154
0,0159
0,0114
0,0089
0,0099
0,0122
0.0097
0,0283
0,0299
0,0173
0,0144
0,948
1,043
18.8. ПЛОТНОСТЬ ГАЗОВ
Формула газа
Элементарные газы:
азот Na
аргон Аг
гелий Не
водород Нд
кислород 02
хлор С1г
Неорганические соединения:
NH3
HCl
со
соа
воздух
so2
HtS
N20
Органические соединения:
ацетилен СаН2
этан С2Н,
этилен С.Н4
метай СН4
Плотность, г/л
сухого газа
при нормальных
условиях
1,2505
1,7839
0,1785
0,089870
1,42895
3,220
0,7714
1,6391
1,2500
1,9768
1,2928
2,9263
1,5392
1,9780
1,1709
1,356
1,2605
0.7168
Относительна»
плотность (по
отношению к воздуху)
0,9673
1,3799
0,1381
0,06952
1,1053
2,491
0,5967
1,2679
0,9669
1,5291
1,0000
2,2635
1,1906
1,5300
0,9057
1,049
0,9750
0,5545
154
18.9. НЕСОВМЕСТИМЫЕ ГАЗЫ
Несовместимые газы: азота
окись -J- кислород, азота окись +
-j- хлор, аммиак -j- галогены,
аммиак + галогеноводороды,
аммиак + окислы хлора, ацетон +
хлор.
Реагируют при освещении:
водород + окислы хлора, водород +
+ хлор, окись углерода + хлор,
углеводороды алифатические + хлор,
этилен + хлор.
Реагируют в присутствии воды:
сероводород-f- кислород,
сероводород + сернистый газ, селеново-
дород + кислород, теллуроводо-
род + кислород.
18. 10. ПРИВЕДЕНИЕ ОБЪЕМА ГАЗОВ К НОРМАЛЬНЫМ УСЛОВИЯМ
Для идеального сухого газа
V« =
Vp
р0Т
Vf;
Поправка на показание барометра
для приведения его к 0° С,
вычисленная по формуле
Ро = Р< — тг*\
0 л0 + «0
lgV0 = 1gV + lg/.
где ? •— температура воздуха около
Таблица содержит мантиссы фак- барометра (f = 24° С), составляет
3,0 мм рт. ст.
Вычисляем парциальное давление
газа:
торов
рт0
л<1 + «0 р0т'
Приведение объема газа к
нормальным условиям следует делать так,
как указано в следующем ниже
примере:
Измеренный объем газз V, мл . . . • • 25, И
Температура ><, "С 24,2
Давление р, мм рт. ст 750
Давление паров воды при 20,0° С рв,
мм рт. ст. 17,5
р = 750—17,5 —3,0 =
= 729,5 мм рт. ст.;
]gV = lg25,14 = 1,40035.
По таблице находим
lg/(24°C,730MMpT. ст.) =
V0 = 21,98 мл.
0,95176 ± 1
1,35211
и °с
10
11
12
13
14
18.10.1 Давление насыщенного водяного
Рв
9,2
9,8
10,5
11,2
12,0
t, °С
15
16
17
18
19
Рв
12,8
13,6
14,5
15,5
16,5
и °с
20
21
22
23
24
Рв
17,5
18,6
19,8
21.1
22,4
пара (рв, мм рт. <
и °с
| 25
26
27
28
29
"в
23,8 1
25,2
26,7
28,3
30,0
гг.)
t, "С
30
31
32
33
34
"»
31,8
33,7
35,7
37,7
39,9
18.10.2 Приведение объема газа к нормальным условиям
"С
10
И
12
13
14
15
16
р, Торр (мм рт. ст.)
730
96 687
96 533
96 380
96 228
96 076
95 925
95 774
731
96 747
96 593
96 440
96 288
96 136
95 985
95 834
732
96 806
96 652
96 499
96 347
96 195
96 044
95 893
733
96 865
96 711
96 558
96 406
96 254
96 103
95 952
734
96 925
96 771
96 618
96466
96314
96 163
96 012
735
96 984
96 830
96 677
96 525
96 373
96 222
96 071
t,
°с
17
18
19
20
21
22
23
р, Торр (мм рт. ст.)
730
95 624
95 474
95 325
95 176
95028
94 880
94 733
731
95 684
95 534
95 385
95 236
95088
94 940
94 793
732
95 743
95593
95444
95295
95 147
95 002
94 852
733
95802
95652
95 503
95354
95206
95058
94 911
734
95862
95 712
95563
95414
95266
95118
94 971
735
95 921
95 771
95622
95 473
95 325
95177
95030
п*
155
Продолжение
°с
24
25
26
27
28
29
t
°с
10
11
12
13
14
15
16
17
18
19
20
21
22
t
°С
10
11
12
13
14
15
16
17
18
19
20
21
22
р, Торр (мм рт. ст.)
730
94 586
94 440
94 294
94 149
94 004
93 860
731
94 646
94 500
94 354
94 209
94 064
93 920
732
94 705
94 559
94 413
94 268
94 123
93 979
733
94 764
94 618
94 472
94 327
94 182
94 038
734
94 824
94 678
94 532
94 387
94 242
94 098
735
94 833
94 737
94 591
94 446
94 301
94 157
р, Торр (им рт. ст.)
736
97 043
96 889
96 736
96 584
96 432
96 281
96 130
95 980
95 830
95 681
95 532
95 384
95 236
737
97 102
96 948
96 795
96 643
96 491
96 340
96 189
96 039
95 889
95 740
95 591
95 443
95 295
738
97 161
97 007
96 854
96 702
96 550
96 399
96 248
96 098
95 948
95 799
95 650
95 502
95 354
739
97 219
97 065
96 912
96 760
96608
96457
96 306
96 156
96 006
95 857
95 708
95 560
95 412
740
97 278
97 124
96 971
96 819
96 667
96 516
96 365
96 215
96 065
95 916
95 767
95 619
95 471
741
97 337
97 183
97 030
96 878
96 726
96 575
96 424
96 274
96 124
95 975
95 826
95 678
95 530
р, Торр (ми рт. ст.)
742
97 395
97 241
97 088
96 936
96 784
96 633
96 482
96 332
96 182
96 033
95 884
95 736
95 588
t, °с
10
11
12
13
14
15
16
17
18
19
743
97 454
97 300
97 147
96 995
96 843
96 692
96 541
96 391
96 241
96 092
95 943
95 795
95 647
744
97 512
97 358
97 205
97 053
96 901
96 750
96 599
96 449
96 299
96 150
96 001
95 853
95 705
745
97 571
97 417
97 264
97 112
96 960
96 809
96 658
96 508
96 358
96 209
96 060
95 912
95 764
746
97 629
97 475
97 322
97 170
97 018
96 867
96 716
96 566
96 416
96 267
96 118
95 970
95 822
747
97 687
97 533
97 380
97 228
97 076
96 925
96 774
96 624
96 474
96 325
96 176
96 028
95 880
t.
"С
30
31
32
33
34
t,
°с
23
24
25
26
27
28
29
30
31
32
33
34
t,
°с
23
24
25
26
27
28
29
30
31
32
33
34
р, Торр (мм рт. ст.)
730
93 716
93 573
93 430
93 287
93 145
731
93 776
93 633
93 490
93 347
93 205
732
93 835
93 692
93 549
93 406
93 264
733
93 894
93 751
93 608
93 465
93 323
734
93 954
93 811
93 668
93 525
93 383
735
94 013
93 870
93 727
93 584
93 442
р, Торр (мм рт. ст.)
736
95 089
94 942
94 796
94 650
94 505
94 360
94 216
94 072
93 929
93 786
93 643
93 501
737
95 148
95 001
94 855
94 709
94 564
94 419
94 275
94 131
93 988
93 845
93 702
93 560
738
95 207
95 060
94 914
94 768
94 623
94 478
94 334
94 190
94 047
93 904
93 761
93 619
739
95 265
95 118
94 972
94 826
94 681
94 536
94 392
94 248
94 105
93 962
93 719
93 677
740
95324
95 177
95031
94 885
94 740
94 595
94 451
94 307
94 164
94 021
93 878
93 736
741
95 383
95 236
95 090
94 944
94 799
94 654
94 510
94 366
94 223
94 080
93 937
93 795
р. Торр (мм рт. ст.)
742
95 441
95 294
95 148
95 002
94 857
94 712
94 568
94 424
94 281
94 138
93 995
93 853
743
95 500
95 353
95 207
95 061
94 916
94 771
94 627
94 483
94 340
94 197
94 054
93 912
744
95 558
95 411
95 265
95 119
94 974
94 829
94 685
94 541
94 398
94 255
94 112
93 970
745
95 617
95 470
95 324
95 178
95 033
94 888
94 744
94 600
94 457
94 314
94 171
94 029
746
95 675
95 528
95 382
95 236
95 091
94 946
94 802
94 658
94 515
94 372
94 229
94 087
747
95 733
95 586
95 440
95 294
95 149
95 004
94 860
94 720
94 573
94 430
94 287
94 145
р, Торр (мм рт. ст.)
748
97 745
97 591
97 438
97 286
97 134
96 983
96 832
96 682
96 532
96 383
749
97 803
97 649
97 496
97 344
97 192
97 041
96 890
96 740
96 590
96 441
750
97 861
97 707
97 554
97 402
97 250
97 099
96 948
98 798
96 648
96 499
751
97 919
97 765
97 614
97 460
97 308
97 157
97 006
96 856
96 706
96 557
752
97 977
97 823
97 670
97 518
97 366
97 215
97 064
96 914
96 764
96 615
753
98 043
97 880
97 727
97 575
97 423
97 273
97 121
96 971
96 821
96 672
754
98 092
97 938
97 785
97 633
97 481
97 330
97 179
97 029
96 879
96 730
755
98 150
97 996
97 843
97 691
97 539
97 388
97 237
97 087
96 937
96 788
156
Продолжение
t. °G
20
21
22
23
24
25
26
27
28
29
30
31
32
33
34
t, °C
p, Торр (им рт. ст.)
748
96 234
96 086
95 938
95 791
95 644
95 498
95 352
95 207
95 062
94 918
94 774
94 631
94 488
94 345
94 203
749
96 292
96 144
95 996
95 849
95 702
95 556
95 410
95 265
95 120
94 976
94 832
94 689
94 546
94 403
94 261
750
96 350
96 202
96 054
95 907
95 760
95 614
95 468
95 323
95 178
95 034
94 890
94 747
94 604
94 461
94 319
751
96 408
96 260
96 112
95 965
95 818
95 672
95 526
95 381
95 236
95 092
94 948
94 805
94 662
94 519
94 377
752
96 466
96 318
96 170
96 023
95 876
95 730
95 584
95 439
95 294
95 150
95 006
94 863
94 720
94 577
94 435
753
96 523
96 375
96 227
96 080
95 933
95 787
95 641
95 496
95 351
95 207
95 063
94 920
94 777
94 634
94 492
754
96 581
96 433
96 285
96 138
95 991
95 845
95 699
95 554
95 409
95 265
95 121
94 978
94 835
94 692
94 550
755
96 639
96 491
96 343
96 196
96 049
95 903
95 757
95 612
95 467
95 323
95 179
95 036
94 893
94 750
94 608
p, Торр (мм рт. ст.)
756 757 758 759
10 98 207 98 265 | 98 322 | 98 379
11 98 053
12 97 900
13
14
15
16
17
18
19
20
21
22
23
24
25
26
27
28
29
30
97 748
97 596
97 445
97 294
97 144
96 994
96 845
96 696
96 548
96 400
96 253
96 106
95 960
95 814
95 669
95 524
95 380
95 236
760 761
98 436 98 493
762
98 550
763
98 607
98 111 98 168 98 225 98 282 98 339 | 98 396 | 98 453
97 958 1 98 015 I 98 072 | 98 129 98 186
97 806
97 654
97 503
97 352
97 202
97 052
96 903
97 863
97 711
97 560
97 409
97 259
97 109
96 960
96 754 96 811
96 606 1 96 663
96 458
96 311
96 164
96 018
95 872
95 727
95 582
95 438
96 515
96 368
96 221
96 075
95 929
95 784
95 639
95 495
95 294 95 351
31 95 093 95 151 1 95 208
97 920 | 97 977
97 768
97 617
97 466
97 316
97 166
97 017
96 886
96 720
96 572
96 425
96 278
96 137
95 986
95 841
95 696
95 552
97 825
97 674
97 523
97 373
97 223
97 074
96 925
96 777
96 629
96 482
96 335
96 189
96 043
95 898
95 753
95 609
95 408 95 465
95 265 95 322
98 034
97 882
97 731
97 580
98 243 98 300
98 091 98 148
97 939 97 996
97 788 97 845
97 637 97 694
97 430 | 97 487
97 280
97 131
96 982
96 834
96 686
96 539
96 392
96 246
96 100
95 955
95 810
95 666
95 522
97 337
97 188
97 039
96 891
96 743
96 596
96 449
96 303
96 157
96 012
95 867
95 723
95 579
97 544
97 394
97 245
97 096
96 948
96 800
96 653
96 506
96 360
96 214
96 069
95 924
95 780
95 636
95 379 | 95 436 1 95 493
32 94 950 95008 95065 95 122 95 179 95 236 95 293 95350
33 94807 94865 94 922 94 979 95 036 95 093 95 150 95 207
34 94665 94723 94 780 94 837 94 894 94 951 95 008 95 065
t, °c
1 р, Торр (мм рт. ст.)
1 764 1 765 1 766 | 7(
10 98
11 98
12 98
13 98
14 9c
15 9'
16 9'
17 9
18 9
1 * "- "f ' ""
664 1
510
357
205
S053
Г 902
Г 751
7 601
7 451
98 721
98 567
98 414
98 262
98 НО
97 959
97 808
97 658
97 508
1 98 Tit
98 62'
98 47
98 31
98 16
98 01
97 86
97 7
97 51
1 98
1 98
1 98
9 98
7 9с
6 91
>5 9'
5 9
35 9
>7 1 768 1 769
| |
835
681
528
376
224
3 073
Г 922
7 772
7 622
98 891
98 737
98 584
98 432
98 280
98 129
97 978
97 828
97 678
98 948
98 794
98 641
98 489
98 337
98 186
98 035
97 885
97 735
157
Продолжение
tt °С
19
20
21
22
23
24
25
26.
27
28
29
30
31
32
33
34
р, Торр (мм рт. ст.)
764
97 302
97 153
97 005
96 857
96 710
96 563
96 417
96 271
96 126
95 981
95 837
95 693
95 550
95 407
95 264
95 122
765
97 359
97 210
97 062
96 914
96 767
96 620
96 474
96 328
96 183
96 038
95 894
95 750
95 607
95 464
95 321
95 179
766
97 416
97 267
97 119
96 971
96 824
96 677
96 531
96 385
96 240
96 095
95 951
95 807
95 664
95 521
95 378
95 236
767
97 473
97 324
97 176
97 028
96 881
96 734
96 588
96 442
96 297
96 152
96 008
95 864
95 721
95 578
95 435
95 293
768
97 529
97 380
97 232
97 084
96 937
96 790
96 644
96 498
96 353
96 208
96 064
95 920
95 777
95 634
95 491
95 349
769
97 586
97 437
97 289
97 141
96 994
96 847
96 701
96 555
96 410
96 265
96 121
95 977
95 834
95 691
95 548
95 406
19. РАЗНЫЕ СВЕДЕНИЯ
19.1. ДОПУСКАЕМЫЕ ОТКЛОНЕНИЯ ОТ НОМИНАЛЬНОЙ ВМЕСТИМОСТИ
КАЛИБРОВАННОЙ ПОСУДЫ ТЕХНИЧЕСКОГО КЛАССА ПРИ 20°С
1. Пипетки
Вместимость,
мл
200
100
50
25
20
15
10
5
2
1
0,5
Для пипеток
с одной
класса 1
допускаемое
отклонение.
мл .
±0,10
±0,08
±0,05
±0,04
±0,03
±0,03
±0,02
±0.01
±0,005
±0,005
±0,005
вытекания, с
45—50
35—40
35—40
25—30
25—30
25—35
25—35
15—20
15—25
15—25
15—25
без деления
меткой
класса 2
допускаемое
отклонение.
мл
±0,20
±0,16
±0,10
±0,08
±0,06
±0,06
±0,04
±0,020
±0,010
±0,010
±0,010
вытекания, с
40—50
30—40
30—40
15—25
15—25
15—25
15—25
10—20
10—20
10—20
10—20
Для пипеток
с делениями
и без них с двумя отметками
класса 1
допускаемое
отклонение.
мл
±0,10
±0,08
±0,05
±0,05
±0,05
±0,05
±0,025
±0,010
±0,005
±0,005
вытекания, с
—
—
30—40
30—40
30—40
30—40
15—25
15—25
15—25
15—25
класса 2
допускаемое
отклонение,
мл
±0,20
±0,16
±0,10
±0,10
±0,10
±0,10
±0,050
±0,020
±0,010
±0,010
вытекания, с
—
—
10—35
10-35
10—35
10—35
5—25
3—20
3—20
3—20
2. Цилиндры мерные
Вместимость,
мл
2000
1000
500
250
100
Цена
наименьшего
деления,
мл
20
10
5
5
1
Допускаемое
отклонение, мл,
для цилиндров
наливных J отливных
±5,0
±5,0
±2,5
±1,25
±0,50
±10
±10
±5,0
±2,5
±1,0
Вместимость,
мл
50
25
10
5
Цена
наименьшего
деления,
мл
1
0,5
0,1
0,1
Допускаемое
отклонение, мл,
для цилиндров
.наливных 1 отливных
±0,25
±0,25
±0,10
±0,10
±0;50
±0,50
±0,20
±0,20-
156
3. Мерные колбы
гаость.
Вмест1
мл
2000
1000
500
250
200
Допускаемое отклонение
от номинальной вместимости,
мл, для колб
класса 1
наливных
±0,50
±0,30
±0,15
±0,10
±0,10
отливных
±1,00
±0,60
±0,30
±0,20
±0,20
класса 2
наливных
±1,00
±0,60
±0,30
±0,20
±0,20
отливннх
±2,00
±1,20
±0,60
±0,40
±0,40
Вместимость,
мл
100
50
25
10
5
Допускаемое отклонение
от номииаиьиоя вместимости,
мл, для колб
к лаве а 1
наливных
±0,10
±0,05
±0,03
±0,02
±0,01
отливинх
±0,20
±0,10
±0,06
±0,04
±0,02
класса 2
иаииввых
±0,20
±0,10
±0,06
±0,04
±0,02
отливину
±0,40
±0,20
±0,12
±0,08
±0,04
4. Бюретки
Вместимость, мл
100
50
25
10
Допускаемые отклонения, мл
класса 1
±0,10
±0,05
±0,05
±0,025
класса 2
±0,20
±0,10
±0,10
±0,050
Время вытекания, с
класса 1
50—70
40—55
30—45
20—35
класса 2
35—65
35—50
15—40
10—30
Ми кробюретки
10
5
3
2
1
±0,010
±0,010
±0,005
±0,005
±0,005
±0,020
±0,020
±0,010
±0,010
±0,010
30—45
30—45
30—45
20—35
20—35
20—45
20—45
20—45
15—35
15—35
19.2. ГРАДУИРОВКА СТЕКЛЯННОЙ МЕРНОЙ ПОСУДЫ
ВЗВЕШИВАНИЕМ НАПОЛНЯЮЩЕЙ ВОДЫ
Приводимая ниже таблица
предназначена для облегчения расчетов,
связанных с определением
вместимости при нормальной температуре
20° С стеклянных измерительных
приборов (колб, бюреток, пипеток
и пр.).
Таблицы дают истинный вес
бронзовых или латунных гирь,
уравновешивающих в воздухе дистиллирован-
159
ную воду, наполняющую при
температуре от 10 до 40° С измеряемый
сосуд. Вес этот рассчитан по
формуле
Х = 0,998943- 1000£,|l-f-
+ 0,000026 (t — 20° С)],
где X — истинный вес бронзовых
или латунных гирь,
уравновешивающих дистиллированную воду
в объеме 1 л, заключенного в
стеклянный сосуд при температуре воды
t° С; 0,998943 — постоянный
множитель; Е( — плотность
дистиллированной воды при температуре
ГС (по ОСТ 7283); 0,000026 —
коэффициент кубического
расширения стекла.
Эта формула выведена на
основании следующих соображений: вес
1000 мл дистиллированной воды
в безвоздушном пространстве при
20°С равен 998,229 г,
следовательно, в воздухе этот объем воды
будет весить 998,229 — 0,0012 X
X ЮОО, где 0,0012 —вес, г, 1 мл
воздуха. Вес бронзовых или
латунных гирь, уравновешивающих эту
воду в воздухе, равен
X—gj 0,0012,
где X — истинная масса бронзовых
или латунных гирь; 8,4 — плотность
материала гирь.
Следовательно, мы имеем
X— —0,0012 =998,229 —
— 0,0012-1000;
v/8,4 — 0,0012 \
Х\ М ) =
= 998,229(1-^),
откуда
Х = 998,229 Ц$™*,
или
X =998,229.0,998943
при температуре воды 20 С; при
любой температуре воды t, °C,
будем иметь
X = 0,998943^ • 1000.
Если литр воды помещен в
стеклянный сосуд, коэффициент
кубического расширения которого
0,000026, то получится
вышеприведенная формула:
X = 0,998943-1000£, [1 +
+ 0,000026 (* —20° С)].
Таблицами пользуются в двух
случаях: 1) когда требуется определить
поправку вместимости меры, т. е.
верно ли нанесена черта; 2) когда
требуется определить эту
вместимость, т. е. нанести эту черту.
Для примера разберем оба эти
случая.
1. Дана бюретка с обозначением
50 мл. Ставим эту бюретку и 51 г
из бронзовых гирь на одну чашку
весов, а на другую — тару. Отметив
положение стрелки весов на шкале,
наполняем бюретку до черточки
дистиллированной водой, которая,
например, имеет температуру 21,5° С.
Для восстановления равновесия
взамен 51 г приходится поместить
на чашку 1,058 г., следовательно,
вода уравновешена 51 — 1,058 =
= 49,942.Таблица же указывает,
что 0,05 л воды при * = 21,5° С
должны быть уравновешены 49,844 г,
следовательно, разность 49,942 —
— 49,844 = 0,098 г показывает,
что мера велика на 0,098 г воды,
или, переводя на объем, вместимость
бюретки равна 50,098 мл.
2. Требуется нанести черту на
колбу в 0,2 л, имея в распоряжении
воду с температурой 19,9° С. По
таблицам 0,2 л воды при
температуре 19,9° С должны
уравновешиваться 199,44 г бронзовых гирь,
поэтому мы тарируем пустую колбу +
+ 199,44 г, замечаем положение
стрелки весов, а затем, сняв все
гири, наполним колбу водою в
таком количестве, чтобы стрелка
весов показала то же деление шкалы.
Тогда на уровне воды в горлышке
наносим черту.
ISO
Таблица для определения вместимости при нормальной температуре 20° С стеклянной мерной посулы путем уравновешивания в воздухе
латунными или бронзовыми гирями воды
о
1
10,0
1
2
3
4
5
6
7
8
9
11,0
1
2
3
4
5
6
7
3
9
12,0
1
2
3
4
5
6
7
8
9
10
2
9984,1
0
0
9983,9
9
8
7
6
6
5
9983,4
4
3
2
1
0
0
9982,9
8
7
9982,6
5
4
3
2
1
0
0
9981,9
8
5
3
4992,1
0
0
0
4991,9
9
9
8
8
8
4991,7
7
6
6
6
5
5
4
4
3
4991,3
3
2
2
1
0
0
0
4990,9
9
2
4
1996,8
8
8
8
8
8
7
7
7
7
1996,7
7
7
6
6
6
6
6
6
5
1996,5
5
5
5
4
4
4
4
4
4
1
5
998,41
40
40
40
39
38
37
36
36
35
998,34
34
33
32
31
30
30
29
28
27
998,26
25
24
23
22
21
20
20
19
18
0,5
6
499,21
20
20
20
20
19
19
18
18
18
499,17
17
16
16
16
15
15
14
14
13
499,13
13
12
12
11
10
10
10
09
09
0,25
7
249,60
60
СО
60
60
60
59
59
59
59
249,59
58
58
58
58
58
57
57
57
57
249,56
56
56
56
56
55
55
55
55
54
В м
0,2
8
199,68
68
68
68
68
68
67
67
67
67
199,67
67
67
66
66
66
66
66
66
65
199,65
65
65
65
64
64
64
64
64
64
е с т и м
0,1
9
99,841
841
840
839
839
838
837
836
836
835
99,834
834
833
832
831
830
830
829
828
827
99,826
825
824
823
822
821
820
820
819
818
ость, л
0,05
10
49,921
920
920
920
919
919
919
918
918
918
49,917
917
916
916
916
915
915
914
914
913
49,913
913
912
912
911
910
910
910
909
909
0,02
11
19,968
968
968
968
968
968
967
967
967
967
19,967
967
967
966
966
966
966
966
966
965
19,965
965
965
965
964
964
964
964
964
964
0,01
! 12
9,984
984
984
984
984
984
984
984
984
984
9,983
983
983
983
983
983
983
983
983
983
9,983
983
982
982
982
982
982
982
982
982
0.005
! 13
4,9921
9920
9920
9920
9919
9919
9919
9918
9918
9918
4,9917
9917
9916
9916
9916
9915
9915
9914
9914
9913
4,9913
9913
9912
9912
9911
9910
9910
9910
9909
9909
0,004
14
3,9936
9936
9936
9936
9935
9935
9935
9935
9934
9934
3,9934
9933
9933
9933
9932
9932
9932
9931
9931
9931
3,9930
9930
9930
9929
9929
9928
9928
9928
9927
9927
0,003
15
2,9952
9952
9952
9952
9952
9951
9951
9951
9951
9950
2,9950
9950
9950
9950
9949
9949
9949
9949
9948
9948
2,9948
9948
9947
9947
9947
9946
9946
9946
9946
9946
0,002
16
1,9968
9968
9968
9968
9968
9968
9967
9967
9967
9967
1,9967
9967
9967
9966
9966
9966
9966
9966
9966
9965
1,9965
9965
9965
9965
9964
9964
9964
9964
9964
9964
0,001
17
0,9984
9984
9984
9984
9984
9984
9984
9984
9984
9984
0,9983
9983
9983
9983
9983
9983
9983
9983
9983
9983
0,9983
9983
9982
9982
9982
9982
9982
9982
9982
9982
о
о
18
10,0
i
2
3
4
5
6
7
8
9
11,0
1
2
3
4
5
6
7
8
9
12,0
i
2
3
4
5
6
7
8
9
Продолжение
1
13,0
1
2
3
4
5
6
7
3
9
14,0
1
2
3
4
5
6
7
8
9
15,0
1
2
3
4
5
6
7
8
9
2
9981,7
6
5
4
2
1
0
9980,9
8
7
9980,6
5
4
2
1
0
9979,9
8
6
5
9979,4
3
1
0
9978,9
8
6
5
4
2
3
4990,8
8
7
7
6
6
5
5
4
4
4990,3
2
2
1
1
0
0
4989,9
8
8
4989,7
6
5
5
4
4
3
2
2
1
4
1996,3
3
3
3
2
2
2
2
2
1
1996,1
1
1
0
0
0
0
0
1995,9
9
1995,9
9
8
8
8
8
7
7
7
6
5
998,17
16
15
14
12
11
10
09
08
07
998,06
05
04
02
01
00
997,99
98
96
95
997,94
93
91
90
89
88
86
85
84
82
6
499,08
08
07
07
06
06
05
05
04
04
499,03
02
02
01
01
00
498,99
99
98
98
498,97
96
96
95
94
94
93
92
92
91
7
249,54
54
54
53
53
53
53
52
52
52
249,52
51
51
51
50
50
50
49
49
49
249,48
48
48
48
47
47
46
46
46
46
8
199,63
63
63
63
62
62
62
62
62
61
199,61
61
61
60
. 60
60
60
60
59
59
199,59
58
58
58
58
58
57
57
57
56
9
99,817
816
814
814
812
811
810
809
808
807
99,806
805
804
802
801
800
799
798
796
795
99,794
793
791
790
789
788
786
785
784
782
10
49,908
908
907
907
906
906
905
905
904
904
49,903
902
902
901
901
900
900
899
898
898
49,897
896
896
895
894
894
893
892
892
891
И
19,963
963
963
963
962
962
962
962
962
961
19,961
961
961
960
960
960
960
960
959
959
19,959
959
959
958
958
958
957
957
957
956
12
9,982
982
981
981
981
981
981
981
981
981
9,981
980
980
980
980
980
980
980
980
980
9,979
979
979
979
979
979
979
978
978
978
13
4,9908
9908
9907
9907
9906
9906
9905
9905
9904
9904
4,9903
9902
9902
9901
9901
9900
9900
9899
9898
9898
4,9897
9896
9896
9895
9894
9894
9893
9892
9892
9891
14
3,9927
9926
9926
9925
9925
9925
9924
9924
9923
9923
3,9922
9922
9921
9921
9921
9920
9920
9919
9919
9918
3,9918
9918
9916
9916
9916
9915
9915
9914
9914
9913
15
2,9945
9945
9944
9944
9944
9943
9943
9943
9942
9942
2,9942
9941
9941
9941
9940
9940
9940
9939
9939
9939
2,9938
9938
9937
9937
9937
9936
9936
9936
9935
9935
16
1,9963
9963
9963
9963
9962
9962
9962
9962
9962
9961
1,9961
9961
9961
9960
9960
9960
9960
9960
9959
9959
1,9959
9959
9959
9958
9958
9958
9957
9957
9957
9956
17
0,9982
9982
9981
9981
9981
9981
9981
9981
9981
9981
0,9981
9980
9980
9980
9980
9980
9980
9980
9980
9980
0,9979
9979
9979
9979
9979
9979
9979
9978
9978
9978
18
13,0
1
2
3
4
5
6
7
8
9
14,0
1
2
3
4
5
6
7
8
9
15,0
1
2
3
4
5
6
7
8
9
Продолжение
1
16,0
1
2
3
4
5
6
7
8
9
17,0
1
2
3
4
5
6
7
8
9
18,0
1
2
3
4
5
6
7
8
9
2
9978,1
0
9977,8
7
6
4
3
1
0
9976,8
9976,7
5
4
2
1
9975,9
8
6
4
3
9975,1
0
9974,8
7
5
3
2
0
9973,8
7
3
4989,0
0
4988,9
8
8
7
6
6
5
4
4988,3
3
2
1
0
4987,9
9
8
7
6
4987,6
5
4
4
3
2
1
0
4986,9
8
4
1995,6
6
6
5
5
5
5
4
4
4
1995,3
3
3
2
2
2
2
1
1
1
1995,0
0
0
1994,9
9
9
8
8
8
7
5
997,81
80
78
77
76
74
73
71
70
68
997,67
65
64
62
61
59
58
56
54
53
997,51
50
48
47
45
43
42
40
38
37
6
498,90
90
89
88
88
87
86
86
85
84
498,83
83
82
81
80
80
79
78
77
77
498,76
75
74
74
73
72
71
70
69
68
7
249,45
45
45
44
44
44
43
43
42
42
249,42
41
41
41
40
40
40
39
38
38
249,38
38
37
37
36
36
36
35
35
34
8
199,56
56
56
55
55
55
54
54
54
54
199,53
53
53
52
52
52
52
51
51
51
199,50
50
50
49
49
49
48
48
48
47
9
99,781
780
778
777
776
774
773
771
770
768
99,767
765
764
762
761
759
758
756
754
753
99,751
750
748
747
744
743
742
740
738
737
la
49,890
890
889
888
888
887
886
886
885
884
49,883
883
882
881
880
880
879
878
877
876
49,876
875
874
874
872
872
871
870
869
868
n
19,956
956
956
955
955
955
955
954
954
954
19,953
953
953
952
952
952
952
951
951
951
19,950
950
950
949
949
949
948
948
948
947
12
9,978
978
978
978
978
977
977
977
977
977
9,977
977
976
976
976
976
976
976
975
975
9,975
975
975
975
974
974
974
974
974
974
13
4,9890
9890
9889
9888
9888
9887
9886
9886
9885
9884
4,9883
9883
9882
9881
9880
9880
9879
9878
9877
9876
4,9876
9875
9874
9874
9873
9872
9871
9870
9869
9868
14
3,9912
9912
9911
9911
9910
9910
9909
9908
9908
9908
3,9907
9906
9906
9905
9904
9904
9903
9903
9902
9901
3,9901
9900
9899
9899
9898
9897
9897
9895
9895
9895
15
2,9934
9934
9933
1 9933
i 9933
9932
9932
9931
9931
9930
2,9930
9930
9929
9929
9928
9928
9927
9927
9926
9926
2,9926
9925
9925
9924
9924
9923
9923
9922
9921
9921
16
1,9956
9956
9956
9955
9955
9955
9955
9954
9954
9954
1,9953
9953
9953
9952
9952
9952
9952
9951
9951
9951
1,9950
9950
9950
9949
9949
9949
9948
9948
9948
9947
17
0,9978
9978
9978
9978
9978
9977
9977
9977
9977
9977
0,9977
9976
9976
9976
9976
9976
9976
9976
9975
9975
0,9975
9975
9975
9975
9974
9974
9974
9974
9974
9974
18
16,0
I
2
3
4
5
6
7
8
9
17,0
I
2
3
4
5
6
7
8
9
18,0
1
2
3
4
5
6
7
8
9
Продолжение
1
19,0
1
2
3
4
5
6
7
8
9
20,0
1
2
3
4
5
6
7
8
9
21,0
1
2
3
4
5
6
7
8
9
2
9973,5
4
2
0
9972,8
6
5
3
1
9971,9
9971,7
6
4
2
0
9970,8
6
4
3
1
9969,9
8
5
3
1
9968,9
7
5
3
1
3
4986,8
7
6
5
4
3
3
2
0
0
4985,8
8
7
6
5
4
3
2
2
1
4985,0
4984,9
8
6
6
4
4
2
2
0
4
1994,7
7
6
6
6
5
5
5
4
4
1994,3
3
3
2
2
2
1
1
1
0
1994,0
0
1993,9
9
8
8
7
7
7
6
5
997,35
33
32
30
28
26
25
23
21
19
997,17
16
14
12
10
08
06
04
03
01
996,99
97
95
93
91
89
87
85
83
81
6
498,68
67
66
65
64
63
63
62
60
60
498,58
58
57
56
55
54
53
52
52
51
498,50
49
48
46
46
44
44
42
42
41
7
249,34
33
33
33
32
32
31
31
30
30
249,29
29
29
28
28
27
26
26
26
25
249,25
24
24
23
23
22
22
21
21
20
8
199,47
47
46
46
46
45
45
45
44
44
199,43
43
43
42
42
42
41
41
41
40
199,40
40
39
39
38
38
37
37
37
36
9
99,735
734
732
730
728
727
725
723
721
719
99,717
716
714
712
710
708
706
704
703
701
99,699
698
695
693
691
689
687
685
683
681
10
49,868
866
866
865
864
863
863
862
860
860
49,858
858
857
856
855
854
853
852
852
851
49,850
849
848
846
846
844
844
842
842
841
И
19,947
947
946
946
946
945
945
945
944
944
19,943
943
943
942
942
942
941
941
941
940
19,940
940
939
939
938
938
937
937
937
936
12
9,974
973
973
973
973
973
972
972
972
972
9,972
972
971
971
971
971
971
970
970
970
9,970
970
970
969
969
969
969
969
968
968
13
4,9868
9867
9866
9865
9864
9863
9863
9862
9860
9860
4,9858
9858
9857
9856
9855
9855
9853
9852
9852
9851
4,9850
9849
9848
9846
9846
9844
9844
9843
9842
9841
14
3,9894
9893
9893
9892
9891
9890
9890
9889
9888
9888
3,9887
9886
9886
9885
9884
9883
9882
9882
9881
9880
3,9880
9879
9878
9877
9876
9876
9875
9874
9873
9872
15
2,9921
9920
9920
9919
9919
9918
9918
9917
9916
9916
2,9915
9915
9914
9914
9913
9912
9912
9911
9911
9910
2,9910
9909
9908
9908
9907
9907
9906
9906
9905
9904
16
1,9947
9947
9946
9946
9946
9945
9945
9945
9944
9944
1,9943
9943
9943
9942
9942
9942
9941
9941
9941
9940
1,9940
9940
9939
9939
9938
9938
9937
9937
9937
9936
17
0,9974
9973"
9973
9973
9973
9973
9972
9972
9972
9972
0,9972
9972
9971
9971
9971
9971
9971
9970
9970
9970
0,9970
9970
9970
9969
9969
9969
9969
9969
9968
9968
18
19,0
1
2
3
4
5
6
7
8
9
20,0
1
2
3
4
5
6
7
8
9
21,0
1
2
3
4
5
6
7
8
9
Продолжение
1
22,0
1
2
3
4
5
6
7
8
9
23,0
1
2
3
4
5
6
7
8
9
24,0
1
2
3
4
5
6
7
8
9
2
9967,9
7
5
3
1
9966,9
7
5
3
1
9965,9
7
4
2
0
9964,8
6
4
2
9963,9
9963,7
5
3
0
9962,8
6
4
1
9961,9
7
3
4984,0
4983,9
8
6
6
4
4
2
2
1
4983,0
4982,9
7
6
5
4
3
2
1
0
4981,9
8
7
5
4
3
2
0
0
4980,8
4
1993,6
5
5
5
4
4
3
3
3
2
1993,2
1
1
0
0
0
9
9
8
8
1992,7
7
7
6
6
5
5
4
4
4
5
996,79
77
75
73
71
69
67
65
63
61
966,59
57
54
52
50
48
46
44
42
39
996,37
35
33
30
28
26
24
21
19
17
6
498,40
39
38
36
36
34
34
32
32
31
498,30
29
27
26
25
24
23
22
21
20
498,18
18
17
15
14
13
12
10
10
08
7
249,20
19
19
18
18
17
17
16
16
15
249,15
14
14
13
12
12
12
11
10
10
249,09
09
08
08
07
06
06
05
05
04
8
199,36
35
35
35
34
34
33
33
33
32
199,32
32
31
30
30
30
29
29
28
28
199,27
27
27
26
26
25
25
24
24
24
9
99,679
677
675
673
671
669
667
665
663
661
99,659
657
654
652
650
648
646
644
642
639
99,637
635
633
630
628
626
624
621
619
617
10
49,840
839
838
836
836
834
834
832
832
831
48,830
829
827
826
825
824
823
822
821
820
49,818
817
817
815
814
813
812
810
810
808
П
19,936
935
935
935
934
934
933
933
933
932
19,932
931
931
930
930
930
929
929
928
928
19,927
927
927
926
926
925
925
924
924
924
12
9,968
968
968
967
967
967
967
966
966
966
9,966
966
965
965
965
965
965
964
964
964
9,964
964
963
963
963
963
962
962
962
962
13
4,9840
9839
9838
9836
9836
9834
9834
9832
9832
9831
4,9830
9829
9827
9826
9825
9824
9823
9822
9821
9820
4,9818
9817
9817
9815
9814
9813
9812
9810
9810
9808
14
3,9872
9871
9870
9869
9868
9868
9867
9866
9865
9865
3,9864
9863
9862
9861
9860
9859
9859
9858
9857
9856
3,9855
9854
9853
9852
9851
9850
9850
9848
9848
9847
15
2,9904
9903
9903
9902
9901
9901
9900
9900
9899
9898
2,9898
9897
9896
9896
9895
9894
9894
9893
9893
9892
2,9891
9891
9890
9889
9889
9888
9887
9886
9886
9885
13
1,9936
9935
9935
9935
9934
9934
9933
9933
9933
9932
1,9932
9931
9931
9930
9930
9930
9929
9929
9928
9928
1,9927
9927
9927
9926
9926
9925
9925
9924
9924
9924
17
0,9968
9968
9968
9967
9967
9967
9967
9966
9966
9966
0,9966
9966
9965
9965
9965
9965
9965
9964
9964
9964
0,9964
9964
9963
9963
9963
9963
9962
9962
9962
9962
18
22,0
1
2
3
4
5
6
7
8
9
23,0
1
2
3
4
5
6
7
8
9
24,0
1
2
3
4
5
6
7
8
9
Продолжение
1
25,0
1
2
3
4
$
6
7
8
9
26,0
1
2
3
4
5
6
7
8
9
27,0
1
2
3
4
5
6
7
8
9
2
9961,4
2
0
9960,8
5
3
1
9959,9
6
3
9959,1
9958,8
6
4
1
9957,9
6
4
1
9956,9
9956,6
4
2
9955,9
6
4
2
9954,9
6
4
3
4980,7
6
5
4
2
2
1
4979,9
8
6
4979,5
4
3
2
0
0
4978,8
7
6
4
4978,3
2
1
0
4977,8
7
6
4
3
2
4
1992,3
2
2
2
1
1
0
0
1991,9
9
1991,8
7
7
7
6
6
5
5
4
4
1991,3
3
2
2
1
1
0
0
1990,9
9
5
996,14
12
10
08
05
03
01
995,98
96
93
995,91
88
86
84
81
79
76
74
71
69
995,66
64
62
59
56
54
52
49
46
44
6
498,07
06
05
04
02
02
01
497,99
98
96
497,95
94
93
92
90
90
88
87
86
84
497,83
82
81
80
78
77
76
74
73
72
7
249,04
03
02
02
01
01
00
00
248,99
98
248,98
97
96
96
95
95
94
94
93
92
248,92
91
91
90
89
88
88
87
86
86
s
199,23
22
22
22
21
21
20
20
19
19
199,18
17
17
17
16
16
15
15
14
14
199,13
13
12
12
11
11
10
10
09
09
9
99,614
612
610
608
605
603
601
598
596
593
99,591
588
586
584
581
579
576
574
571
569
99,566
564
562
559
556
554
552
549
546
544
10
49,807
806
805
804
802
802
801
799
798
796
49,795
794
793
792
790
790
788
787
786
784
49,783
782
781
780
779
777
776
774
773
772
11
19,923
922
922
922
921
921
920
920
919
919
19,918
918
917
917
916
916
915
915
914
914
19,913
913
912
912
911
911
910
910
909
909
12
9,961
961
961
961
960
960
960
960
960
959
9,959
959
959
958
958
958
958
957
957
957
9,957
956
956
956
956
955
955
955
955
954
13
4,9807
9806
9805
9804
9802
9802
9801
9799
9798
9796
4,9795
9794
9793
9792
9790
9790
9788
9787
9786
9784
4,9783
9782
9781
9780
9779
9777
9776
9774
9773
9772
14
3,9846
9845
9844
9843
9842
9841
9841
9840
9839
9837
3,9836
9835
9834
9834
9832
9832
9830
9830
9828
9828
3,9826
9826
9825
9824
9822
9822
9821
9820
9818
9818
15
2,9884
9884
9883
9883
9882
9881
9880
9880
9879
9878
2,9877
9876
9876
9875
9874
9874
9873
9872
9871
9871
2,9870
9869
9869
9868
9867
9866
9866
9865
9864
9863
16
1,9923
9922
9922
9922
9921
9921
9920
9920
9919
9919
1,9918
9918
9917
9917
9916
9916
9915
9915
9914
9914
1,9913
9913
9912
9912
9911
9911
9910
9910
9909
9909
17
0,9961
9961
9961
9961
9960
9960
9960
9960
9960
9959
0,9959
9959
9959
9958
9958
9958
9958
9957
9957
9957
0,9957
9956
9956
9956
9956
9955
9955
9955
9955
9954
is
25,0
I
2
3
4
5
6
7
8
9
26,0
1
2
3
4
5
6
7
8
9
27,0
1
2
3
4
5
6
7
3
9
Продолжение
1
28,0
1
2
3
4
5
6
7
8
9
29,0
1
2
3
4
5
6
7
8
9
30,0
1
2
3
4
5
6
7
8
9
2
9954,1
9953,9
6
3
1
9952,8
6
3
0
9951,8
9951,5
2
0
9950,7
4
2
9949,9
6
3
0
9948,8
5
2
0
9947,7
4
1
9946,8
6
3
3
4977,0
0
4976,8
6
6
4
3
2
0
4975,9
4975,8
6
5
4
2
1
0
4974,8
6
5
4974,4
2
1
0
4973,9
7
6
4
3
2
4
1990,8
8
7
7
6
6
5
5
4
4
1990,3
3
2
1
1
0
0
1989,9
9
8
1989,8
7
6
6
5
5
4
4
3
3
5
995,41
39
36
33
31
28
26
23
20
18
995,15
12
10
07
04
02
994,99
96
93
90
994,88
85
82
80
77
74
71
68
66
63
6
497,71
70
68
66
66
64
63
62
60
59
497,58
56
55
54
52
51
50
48
46
45
497,44
42
41
40
39
37
36
34
33
32
7
248,85
85
84
83
83
82
82
81
80
80
248,79
78
78
77
76
76
75
74
73
72
248,72
71
70
70
69
69
68
67
66
66
8
199,08
08
07
07
06
06
05
05
04
04
199,03
03
02
01
01
00
00
198,99
99
98
198,98
97
96
96
96
95
94
94
93
93
9
99,541
539
536
533
531
528
526
523
520
518
99,515
512
510
507
504
502
499
496
493
490
99,488
485
482
480
477
474
471
468
466
463
10 11
49,770
770
768
766
766
764
763
762
760
759
49,758
756
755
754
752
751
750
748
746
745
49,744
742
741
740
739
737
736
734
733
732
19,908
908
907
906
906
906
905
905
904
904
19,903
902
902
901
901
900
900
899
899
898
19,898
897
896
896
896
895
894
894
893
893
12
9,954
954
954
953
953
953
953
952
952
952
9,952
951
951
951
950
950
950
950
949
949
9,949
948
948
948
948
947
947
947
947
946
13
4,9770
9770
9768
9766
9766
9764
9763
9762
9760
9759
4,9758
9756
9755
9754
9752
9751
9750
9748
9746
9745
4,9744
9742
9741
9740
9739
9737
9736
9734
9733
9732
14
3,9816
9816
9814
9813
9813
9811
9811
9809
9808
9807
3,9806
9805
9804
9803
9802
9801
9800
9798
9797
9796
3,9796
9794
9793
9792
9791
9790
9788
9787
9786
9785
15
2,9862
9862
9861
9860
9859
9858
9858
9857
9856
9855
2,9854
9854
9853
9852
9851
9851
9850
9849
9848
9847
2^9847
9846
9845
9844
9843
9842
9841
9840
9840
9839
16
1,9908
9908
9907
9907
9906
9906
9905
9905
9904
9904
1,9903
9902
9902
9901
9901
9900
9900
9899
9899
9898
1,9898
9897
9896
9896
9896
9895
9894
9894
9893
9893
17
0,9954
9954
9954
9953
9953
9953
9953
9952
9952
9952
0,9952
9951
9951
9951
9950
9950
9950
9950
9949
9949
0,9949
9948
9948
9948
9948
9947
9947
9947
9947
9946
18
28,0
1
2
3
4
5
6
7
3
9
29,0
1
2
3
4
5
6
7
8
9
30,0
1
2
3
4
5
6
7
8
9
Продолжение
1
31,0
1
2
3
4
5
6
7
8
9
32,0
1
2
3
4
5
6
7
8
9
33,0
1
2
3
4
5
6
7
8
9
2
9946,0
9945,7
4
1
9944,8
6
3
0
9943,7
4
9943,1
9942,8
5
2
9941,9
6
3
0
9940,7
4
9940,1
9939,8
5
3
9938,9
6
3
0
9937,7
4
3
4973,0
4972,8
7
6
4
3
2
0
4971,9
7
4971,6
4
2
1
0
4970,8
6
5
4
2
4970,0
4969,9
8
6
4
3
2
0
4968,9
7
4
1989,2
1
1
0
0
1988,9
9
8
7
7
1988,6
6
5
4
4
3
3
2
1
1
1988,0
0
1987,9
8
8
7
7
6
6
5
5
994,60
57
54
51
48
46
43
40
37
34
994,31
28
25
22
19
16
13
10
07
04
994,01
993,98
95
92
89
86
83
80
77
74
6
497,30
28
27
26
24
23
22
20
19
17
497,16
14
12
11
10
08
06
05
04
02
497,00
496,99
98
96
94
93
92
90
89
87
7
248,65
64
64
63
62
62
61
60
59
59
248,58
57
56
56
54
54
53
52
52
51
248,50
50
49
48
47
47
46
45
44
44
8
198,92
91
91
90
90
89
89
88
88
87
198,86
86
85
84
84
83
83
82
81
81
198,80
80
79
78
78
77
77
76
76
75
9
99,460
457
454
451
448
446
443
440
437
434
99,431
428
425
422
419
416
413
410
407
404
99,401
398
395
392
389
386
383
380
377
374
10
49,730
728
727
726
724
723
722
720
719
717
49,716
714
712
711
710
708
706
705
704
702
49,700
699
698
696
694
693
692
690
689
687
п
19,892
892
891
890
890
889
889
888
888
887
19,886
886
885
884
884
883
883
882
881
881
19,880
880
878
878
878
877
877
876
876
875
12
9,946
946
945
945
945
945
944
944
944
943
9,943
943
943
942
942
942
941
941
941
940
9,940
940
940
939
939
939
938
938
938
937
13
4,9730
9728
9727
9726
9724
9723
9722
9720
9719
9717
4,9716
9714
9712
9711
9709
9708
9707
9705
9704
9702
4,9700
9699
9698
9696
9694
9693
9692
9690
9689
9687
14
3,9784
9783
9782
9780
9779
9778
9777
9776
9775
9774
3,9773
9771
9770
9769
9767
9766
9765
9764
9763
9762
3,9761
9759
9758
9757
9756
9755
9753
9752
9751
9750
15
2,9838
9837
9836
9835
9834
9834
9833
9832
9831
9830
2,9829
9829
9827
9825
9825
9825
9824
9823
9822
9821
2,9820
9819
9818
9818
9817
9816
9815
9814
9813
9812
16
1,9892
9891
9891
9890
9890
9889
9889
9888
9888
9887
1,9886
9886
9885
9885
9884
9883
9883
9882
9881
9881
1,9880
9880
9879
9878
9878
9877
9877
9876
9876
9875
17
0,9946
9946
9945
9945
9945
9945
9944
9944
9944
9943
0,9943
9943
9942
9942
9942
9942
9941
9941
9941
9940
0,9940
9940
9940
9939
9939
9939
9938
9938
9938
9937
18
31,0
1
2
3
4
5
6
7
8
9
32,0
1
2
3
4
5
6
7
8
9
33,0
1
2
3
4
5
6
7
8
9
Продолжение
1
34,0
1
2
3
4
5
6
7
8
9
35,0
1
2
3
4
5
6
7
8
9
36,0
1
2
3
4
5
6
7
8
9
2
9937,1
9936,8
5
2
9935,8
5
3
9934,9
6
3
9934,0
9933,6
3
0
9932,7
4
0
9931,7
4
1
9930,7
4
1
9929,8
4
1
9928,8
4
1
9927,8
3
4968,6
4
2
1
4967,9
8
6
4967,5
3
1
4967,0
4966,8
7
6
4
2
0
4965,9
7
5
4965,4
2
0
4964,9
7
6
4
2
1
4963,9
4
1987,4
4
3
2
2
1
0
1987,0
1986,9
9
1986,8
7
7
6
5
5
4
3
3
2
1986,1
1
0
0
1985,9
8
8
7
6
6
б
993,71
68
65
62
58
55
52
993,49
46
43
993,40
36
33
30
27
24
20
17
14
11
993,07
04
01
992,98
94
91
88
84
81
78
6
496,86
84
82
81
79
78
76
496,75
73
71
496,70
68
67
65
64
62
60
59
57
55
496,54
52
50
49
47
46
44
42
41
39
7
248,43
42
41
40
40
39
38
248,37
37
36
248,35
34
33
33
32
31
30
29
28
28
248,27
26
25
24
24
23
22
21
20
20
в
198,74
74
73
72
72
71
70
198,70
69
69
198,68
67
67
66
65
65
64
64
63
62
198,61
61
60
60
59
58
58
57
56
56
9
99,371
368
365
362
358
355
352
99,349
346
343
99,340
336
334
330
327
324
320
317
314
311
99,307
304
301
298
294
291
288
284
281
278
10
49,685
684
682
681
679
678
676
49,675
673
671
49,670
668
667
665
664
662
660
659
657
655
49,654
652
650
649
647
646
644
642
641
639
U
19,874
874
873
872
872
871
870
19,870
869
869
19,868
867
867
866
865
865
864
864
863
862
19,861
861
860
860
859
858
858
857
856
856
12
9,937
937
936
936
936
936
935
9,935
935
934
9,934
934
933
933
933
932
932
932
931
931
9,931
930
930
930
929
929
929
928
928
928
13
4,9686
9684
9682
9681
9679
9678
9676
4,9675
9673
9671
4,9670
9668
9667
9665
9664
9662
9660
9659
9657
9655
4,9654
9652
9650
9649
9647
9646
9644
9642
9641
9639
14
3,9748
9747
9746
9745
9743
9742
9741
3,9740
9738
9737
3,9736
9734
9733
9732
9731
9730
9728
9727
9726
9724
3,9723
9722
9720
9719
9718
9716
9715
9714
9712
9711
15
2,9811
9810
9810
9809
9808
9806
9806
2,9805
9804
9803
2,9802
9801
9800
9799
9798
9797
9796
9795
9794
9793
2,9792
9791
9790
9789
9788
9787
9786
9786
9784
9783
16
1,9874
9874
9873
9872
9872
9871
9870
1,9870
9869
9869
1,9868
9867
9867
9866
9865
9865
9864
9864
9863
9862
1,9861
9861
9860
9860
9859
9858
9858
9857
9856
9855
17
0,9937
9937
9936
9936
9936
9936
9935
0,9935
9935
9934
0,9934
9934
9933
9933
9933
9932
9932
9932
9931
9931
0,9931
9930
9930
9930
9929
9929
9929
9928
9928
9928
18
34,0
1
2
3
4
5
6
7
3
9
35,0
1
2
3
4
5
6
7
8
9
26,0
1
2
3
4
5
6
7
8
9
Продолжение
1
37,0
1
2
3
4
5
6
7
8
9
38,0
1
2
3
4
5
6
7
8
9
39,0
1
2
3
4
5
6
7
8
9
40,0
2
9927,4
1
9926,8
4
9926,1
9925,8
4
1
9924,8
4
9924,1
9923,7
4
0
9922,7
4
0
9921,7
3
0
9920,6
3
9919,9
6
2
9918,9
5
2
9917,8
5
9917,1
3
4963,7
6
4
2
4963,1
4962,9
7
6
4
2
4962,1
4961.8
7
5
4
2
0
4960,8
6
5
4960,3
2
0
4959,8
6
5
2
1
4958,9
8
4958,6
4
1985,5
4
4
3
1985,2
2
1
0
0
1984,9
1984,8
7
7
6
5
5
4
3
3
2
1984,1
1
0
1983,9
8
8
7
6
6
5
1983,4
5
992,74
71
68
64
992,61
58
54
51
48
44
992,41
37
34
30
27
24
20
17
13
10
992,06
03
991,99
96
92
89
85
82
78
75
991,71
6
496,37
36
34
32
496,31
29
27
26
24
22
496,21
18
17
15
14
12
10
08
06
05
496,02
02
00
495,98
96
95
92
91
89
88
495,86
7
248,18
18
17
16
248,15
14
14
13
12
11
248,10
09
09
08
07
06
05
04
03
03
248,02
01
00
247,99
98
97
96
96
94
94
247,93
8
198,55
54
54
53
198,52
52
51
50
50
49
198,48
47
47
46
46
45
44
43
43
42
198,41
41
40
39
38
38
37
36
36
35
198,34
9
99,274
271
268
264
99,261
258
254
254
248
244
99,241
237
234
230
227
224
220
217
213
210
99,206
203
199
196
192
189
185
182
178
175
99,171
10
49,637
636
634
632
49,631
629
627
626
624
622
49,621
618
617
615
614
612
610
608
606
605
49,603
602
600
598
596
595
592
591
589
588
49,586
и
19,855
854
854
853
19,852
852
851
850
850
849
19,848
847
847
846
845
845
844
843
843
842
19,841
841
840
839
838
838
837
836
836
835
19,834
12
9,927
927
927
926
9,926
926
925
925
925
924
9,924
924
923
923
923
922
922
922
921
921
9,921
920
920
920
919
919
918
918
918
918
9,917
13
4,9637
9636
9634
9632
4,9631
9629
9627
9626
9624
9622
4,9621
9618
9617
9615
9614
9612
9610
9608
9606
9605
4,9603
9602
9600
9598
9596
9595
9592
9591
9589
9588
4,9586
14
3,9710
9708
9707
9706
3,9704
9703
9702
9700
9699
9698
3,9696
9694
9694
9692
9691
9690
9688
9687
9685
9684
3,9682
9681
9680
9678
9677
9676
9674
9673
9672
9671
3,9668
15
2,9782
9781
9780
9779
2,9778
9777
9776
9775
9774
9773
2,9772
9771
9770
9769
9768
9767
9766
9765
9764
9763
2,9762
9761
9760
9759
9758
9757
9756
9755
9754
9753
2,9751
16
1,9855
9854
9854
9853
1,9852
9852
9851
9850
9850
9849
1,9848
9847
9847
9846
9845
9845
9844
9843
9843
9842
1,9841
9841
9840
9839
9838
9838
9837
9836
9836
9936
1,9834
17
0,9927
9927
9927
9926
0,9926
9926
9925
9925
9925
9924
0,9924
9924
9923
9923
9923
9922
9922
9922
9921
9921
0,9921
9920
9920
9920
9919
9919
9918
9918
9918
9918
0,99 • 7
18
37,0
1
2
3
4
5
6
7
8
9
38,0
I
2
3
4
5
6
7
8
9
39,0
1
2
3
4
5
6
7
8
9
40,0
19.3. ВЯЗКОСТЬ Ti НЕКОТОРЫХ ВЕЩЕСТВ ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ
Вещество
т) (сП или мНс-м 2) при температуре, °С
Ацетон
Ацетонитрнл
Бензол
Бутиловый спирт ....
Вода
Гексан
Гептан
Глицерин
Диэтиловый эфир ....
Изобутиловый спирт . , .
Изопропиловый спирт . .
о-Ксилол
Метиловый спирт ....
Муравьиная кислота . . .
Нитробензол
Октан
Пентан
Пропиловый спирт . . .
Толуол
Уксусная кислота ....
Фенол
Хлороформ
Циклогексан
Четыреххлористый углерод
Этиловый спирт
Этиленгликоль
0,395
0,442
0,910
5,19
1,792
0,381
12 100
0,284
8,30
4,60
1,108
0,817
3,090
0,714
0,283
3,883
0,770
0,700
1,330
1,773
10
0,361
0,396
0,755
3,87
1,308
0,343
3 950
0,258
5,65
3,26
0,939
0,690
2,262
2,483
0,622
0,259
2,897
0,667
1,450
0,630
1,132
1,466
20
30
0,325
0,357
0,652
2,95
1,005
0,307
0,414
1 490
0,233
3,95
2,39
0,809
0,597
1,804
2,034
0,546
0,240
2,234
0,584
1,210
11,6
0,570
0,970
0,969
1,200
19,9
0,296
0,325
0,559
2,28
0,801
0,290
0,373
630
0,213
2,88
1,77
0,708
0,510
1,460
1,682
0,486
0,830
0,517
1,040
7,00
0,514
0,822
0,843
1,003
13,2
40
0,271
50
0,249
0,503
1,78
0,656
0,253
0,338
330
0,197
2,12
1,33
0,625
0,450
1,290
1,438
0,435
0,735
2,400
0,469
0,900
4,77
0,466
0,706
0,739
0,834
9,13
0,436
1,41
0,549
0,248
0,308
180
0,180
1,61
1,03
0,557
0,396
1,025
1,251
0,392
0,651
1,129
0,425
0,790
3,42
0,426
0,610
0,651
0,702
6,65
19.4. ОХЛАЖДАЮЩИЕ СМЕСИ
Состав смеси, г
Падение
температуры, °С
от
до
Состав смесн, г
Падение
температуры, °С
от
До
100 воды + 30 NH4C1 .
100 воды + 25 КС1 . .
100 воды + 30 NH4C1 +
+ 30 NaNOa
100 воды+ 250 СаС12-6Н,
100 воды + 100 NH4NOa
100 воды + 100 NH4C1 +
+ 100 NaNOa
100 воды + 200 KSCN .
О
+ 10
+ 10
+ 10
+ 10
+ 10
+ 10
+ 10
-6
-12
-12
-13
-15
-22
-25
100 льда + 25 NH4Cl . . .
300 льда + 100 NaCl . . .
300 льда + 200 MgCla-6HaO
100 льда + 150 СаС1а-6НаО
200 льда +
концентрированной HNOs
Метанол + твердая СОа . .
Диэтиловый эфир + твердая
СОа
0
0
0
0
0
+ 15
+ 15
19.5. ЭЛЮОТРОПНЫЙ РЯД РАСТВОРИТЕЛЕЙ ДЛЯ ОКИСИ АЛЮМИНИЯ,
КРЕМНИЕВОЙ КИСЛОТЫ И ПОДОБНЫХ ПОЛЯРНЫХ СОРБЕНТОВ (20° С)
Растворители
Диэтиловый эфир
Диэлектрическая
проницаемость
80
32
25
20
21
18
12,5
6,2
4,3
Растворители
Четыреххлористый углерод . .
Диэлектрическая
проницаемость
5,1
10,5
2,3
2,4
3,4
2,2
2,0
1,9
1,9
1,9
12*
ш
19.6. ВЫЧИСЛЕНИЕ И ОБРАБОТКА
РЕЗУЛЬТАТОВ АНАЛИЗА
В практике контроля химического
состава материалов необходимыми
элементами являются вычисление,
обработка и сопоставление
результатов анализа. Это дает четкое
представление о точности выполняемых
анализов, качестве продукции,
необходимости арбитража при спорах
между поставщиком и потребителем.
Здесь приводятся два приема
вычисления и обработки результатов
анализа, однако оба они эффективны
лишь в том случае, если исходные
данные получены с помощью
правильных аналитических методов,
безупречной техники их
выполнения, а именно:
1) пробоотбор их произведен
правильно;
2) первичные данные анализа
получены при отсутствии
преобладания какого-либо случайного
фактора, сильно искажающего все
результаты анализа, имеет место
нормальное распределение отклонений,
т. е. разброс получаемых данных
обусловлен действием многих
случайных факторов;
3) в применяемых методиках
отсутствует систематическая
погрешность;
4) данные, являющиеся
следствием грубых ошибок, исключены
из расчетов.
19.6.1. Вычисление результатов
анализа и его погрешности
при известном коэффициенте
вариации
Вычисление результата
анализа. Оценкой истинной
величины служит среднее арифметическое х
параллельных определений,
вычисляемое по формуле
~ ...■*1 + *И \-*п
Д, ——-—————— .
п
Чем больше число выполненных
определений и меньше их разброс,
тем более точной является эта оценка.
Далее вычисляют погрешность
анализа.
Вычисление погрешности
результата анализа. При
вычислении погрешности результата
анализа используют коэффициент
вариации и, значение которого
должно быть указано в инструкции
по выполнению анализа.
Коэффициент вариации
характеризует воспроизводимость
аналитического метода и представляет
собой относительное квадратичное
отклонение, вычисленное не менее чем
по 20 определениям и выраженное
в процентах к результату анализа.
Если коэффициент вариации
вычислен менее чем по 20 определениям,
то он в аналитической инструкции
обозначается символом vN, где N —
число параллельных определений, по
которым вычислен. Погрешность
анализа в этом случае рекомендуется
вычислять, как указано в
следующем разделе.
Следует иметь в виду, что к
инструкции по выполнению анализа
должен быть приложен график или
таблица, показывающая характер
зависимости значений v от хп.
Пользуясь ими, по результату хп
находят нужное для вычисления
значение v. Если в инструкции указано
только одно значение v, то это
означает, что v не зависит существенно
от концентрации определяемого
элемента.
Для вычисления погрешности
результата анализа сначала находят
квадратичное отклонение S
(выраженное в тех же единицах измерения,
что и результат анализа):
Погрешность результата
обозначается е и вычисляется с
надежностью а = 0,95 по формуле
а с надежностью а = 0,99 — по
формуле
2,58s
е = ч ■?=-.
~ Vn
Результат вычисления означает,
что с надежностью 0,95 (т. е. с
вероятностью 95%) истинное значение
122
определяемой величины лежит в
интервале между значениями
2s - 2s
Vn Vn
Численное значение
результата анализа и
его погрешности.
Значение хп должно содержать
последнюю значащую цифру в том же
разряде, в котором стоит последняя
значащая цифра численного
значения погрешности анализа. После
определения количества значащих
цифр в значении результата
анализа последнюю значащую цифру
можно округлять по общему
правилу. Количество знаков в
численном выражении погрешности
анализа определяют следующим
образом: если первая значащая цифра
погрешности анализа е больше или
равна 3, то е выражают числом с
одной значащей цифрой; если же
первая значащая цифра меньше 3, то е
выражают числом с двумя
значащими цифрами. Так, следует
писать е = ±0,07%, а не ±0,074;
±2,2%, а не ±2,23%; ±14 мг/л,
а не ± 14,4 мг/л и т. д. Отсюда следует,
что численное значение результатов
анализа должно иметь последнюю
значащую цифру в разряде сотых
долей (например, х = 5,48%) в
первом случае, в разряде десятых
долей — во втором случае и в разряде
единиц — в третьем случае
(например, 786 мг/л).
Однако если численное значение
результатов анализа оказалось
равным меньше 1% (например, при
определении примесей), то
погрешность анализа можно выражать
числом с одной значащей цифрой
независимо от значения s. Так при
х„ = 0,3432 и е = ±0,0238 можно
писать е = ±0,02% и соответственно
хп =0,34%. Результаты анализа
с погрешностью записываются так:
10,9 ± 2,2%; 34,28 ± 0,07; 786 ±
± 14 мг/л и т. д.
Проверка годности
результатов двух
параллельных определений.
Вычисляют среднее
арифметическое ха и квадратичное
отклонение S. Затем находят величину
разности | хх — х% | и сопоставляют ее
с величиной 4S Если хх — х2
равно или меньше 4S, то оба
результата параллельных определений
считают годными и принимают в
качестве результата анализа
значение хг. Если | хх — х3 | больше 45,
то выполняют еще два определения
и далее поступают, как указано
выше.
Проверка годности
результатов трех и более
параллельных определений.
Вычисляют среднее
арифметическое всех параллельных
определений и квадратичное отклонение S.
Затем находят абсолютную
величину разностей между средним
арифметическим параллельных
определений и каждым из определений: ах —
= | хп — хх |; аг = | хп — х2 | и т. д.
Каждую из этих величин
сопоставляют с величиной 3S. Если для
каждого из значений соблюдается
условие a, «s 3S, то все значения
параллельных определений
считают пригодными и за результат
анализа принимают полученное
значение среднего арифметического.
Если для одного из значений а(
будет иметь место неравенство а. >
> 35, то соответствующее значение
параллельного определения
считают негодным и отбрасывают.
Если же неравенство at > 3S будет
иметь место для нескольких
значений ait то отбрасывают только
значение xt, для которого а,- оказалось
наибольшим. Из оставшихся
значений вычисляют новые значения хп,
5 и at повторяют проверку годности,
как указано выше. Результат
анализа вычисляют как среднее
арифметическое годных определений.
В результате отбраковки может
быть исключено не более одной трети
всех определений. Если исключению
подлежит большее число
определений, то все полученные
аналитические данные считаются
неудовлетворительными. Анализ повторяют,
тщательно контролируя условия его
выполнения. Если необходимо,
проверяют также однородность
анализируемого материала, используя
173
прием дисперсионного анализа,
описанный в специальных
руководствах.
19.6.2. Вычисление
результатов анализа и его
погрешности в случае, когда
коэффициент вариации неизвестен
В тех случаях, когда в
инструкции по выполнению анализа не
указан коэффициент вариации v,
результат анализа и его погрешность
можно вычислить двумя способами.
Первый способ. Прежде всего
проверяют годность первичных данных,
полученных при анализе всех
параллельных проб. Пусть имеется га
параллельных определений.
Располагаем их в порядке возрастания
численных значений. Сомнение
могут вызвать результаты
определений с номерами 1 и га. Вычисляют
величину Q' •— отношение разности
между сомнительным и соседним
значениями к разности между крайними
значениями (т. е. размаху
варьирования):
Q' =
Хп — Xi
для первого определения н
Q'
хп-
5„ =
/■
(*«-*l)2+(*«-*8)3+
Ч \-(хп — х„)*
и— 1
Таблица 1
Значения Q (для исключения
сомнительных данных) в зависимости
от степени надежности н общего числа
выполненных определении
для последнего определения.
Вычисленную величину Q'
сопоставляют с табличным значением Q
(см. табл. 1) для данного значения га
и а = 0,99. Если Q' > Q, то
сомнительное значение следует исключить.
Если же Q' < Q, то сомнительное
значение следует принять в расчет.
Если сомнение вызывают не одно,
а несколько значений, то сначала
производят указанные выше
расчеты для одного из них (наиболее
отклоняющегося). После его
исключения повторяют расчет для
следующего сомнительного значения.
Однако количество исключаемых
значений должно быть по-прежнему
меньше одной трети.
Вычислив среднее арифметическое
значение, находят среднее
квадратичное отклонение для этих га
годных определений:
3
4
5
!Л
<J>
О
II
8
0,94
0,77
0,64
сп
СИ
о
II
8
0,99
0,89
0,76
л
6
7
8
сп
о
II
в
0,56
0,51
0,48
СП
СП
о
II
8
0,70
0,64
0,58
Полученную величину
квадратичного отклонения Sn используют для
вычисления погрешности анализа
с надежностью а = 0,95 по формуле
8 = -f-
tansn
7Т-
Значение /ап находят по табл. 2
для a = 0,95 и числа годных
определений ft.
Таблица 2
Значения tan для степеней надежности
a = 0,95 и a = 0,99 в зависимости
от числа определений
л
2
3
4
5
6
7
8
9
10
11
О»
О
II
8
12,71
4,30
3,18
2,78
2,57
2,45
2,37
2,31
2,26
2.33
о>
О
II
8 |
63,66
9,93
5,84
4,60
4,03
3,71
3,50
3,36
3,25
3,17
п
12
13
14
15
16
17
18
19
20
21
Ю
Oi
О
II
8
2,20
2,18
2,16
2,15
2,13
2,12
2,11
2,10
2,09
2,09
СП
СП
о
II
8
3,11
3,06
3,01
2,98
2,95
2,92
2,90
2,88
2,86
2,85
Второй способ. Этот способ более
простой, применяется для обработки
выборки с малым числом
наблюдений (измерений). Хотя он и уступает
несколько по точности обычно
рекомендуемым методам, однако
экономит время при вычислениях.
174
Имея п параллельных
определений, вычисляют среднее
арифметическое по обычной формуле. Затем
находят размах варьирования:
/? = хтах Xmin.
Среднее квадратичное отклонение
находят, исходя из размаха
варьирования, по формуле
s = KRR,
значение коэффициента Кц находят
в ниже приведенной табл. 3.
Таблица 3
Значения коэффициентов Кц, tR, Qr
для вычисления погрешности результатов
анализа
Число
определений
п
2
3
4
5
6
7
8
9
10
Коэффициент
для
нахождения
среднего
квадратичного
отклонения
0,89
0,59
0,49
0,43
0,39
0,37
0,35
0,34
0,33
доверительного интервала
иа основе
размаха
варьирования tn
6,4
1,3
0,72
0,51
0,40
0,33
0,29
0,26
0,23
для
проверки
сомнительного
значения
««
0,94
0,78
0,67
0,59
0,55
0,51
0,48
0,46
Погрешность анализа вычисляется
с применением коэффициента
доверительных интервалов tR, значение
которого берется из той же табл. 3:
е = ± tRR.
В предлагаемой для пользования
табл. 3 все необходимые величины
составлены для степени надежности
а = 0,95.
Для проверки сомнительного
значения поступают следующим
образом: вычисляют разность между про-
верямым значением и ближайшим
к нему; делят эту разность на
величину размаха варьирования R.
Если полученный результат
превышает значение, показанное в таблице
для данного числа определений п,
то проверяемое значение можно
отбросить. В противном случае
оснований для его исключения нет.
Пример. При определении хрома
в стали объемным персульфатно-
серебряным методом получены шесть
результатов (%): 10,6; 10,6; 10,9;
11,0; 11,2; 11,7. Среднее
арифметическое равно 11,0. Размах
варьирования R = 11,7— 10,6 = 1,1.
Среднее квадратичное отклонение S —
= 0,39-1,1 = 0,43. Погрешность
анализа е = ^=0,40-1,1 = 0,44.
Таким образом, доверительные
границы результата анализа при
степени надежности 0,95 после
округления будут 10,6 —> 11,4.
Проверим, не является ли
исключительным значение 11,7%. Для
этого вычитаем из него ближайшее
значение 11,2% и делим разность
на величину размаха варьирования.
Имеем ——^—— = 0,45. Из
таблицы следует, что для п = 6
критерий Q для отбрасывания равен
0,59. Поскольку полученное
значение 0,45 намного ниже 0,59, об
исключении проверяемого значения
не может быть и речи. Вместе с тем
погрешность анализа не
укладывается в значение, требуемое
соответствующим ГОСТом на определение
хрома в легированных сталях.
Следует тщательно проверить
исполнение методики анализа лаборантом.
19.6.3. Вычисление количества
параллельных определений,
необходимых для получения
результатов анализа с погрешностью
не выше заданной
Число параллельных
определений п, которое необходимо
выполнить при анализе для получения
результата с погрешностью, не
превышающей —е, определяется по
формуле
/ 2s \2
" = (-)•
Результат вычисления всегда
округляется в большую сторону.
Следует также помнить, что
коэффициент 2 в формуле ставится только
в том случае, если число
параллельных определений при расчете
коэффициента вариации, необходимого
для вычисления квадратичного
отклонения 5, было не менее 20. В
противном случае вместо коэффициента 2
175
в формулу следует подставлять
значение tan, найденное по табл. 2.
Пример. Заказчик требует, чтобы
при определении 4% никеля в стали
погрешность результата не
превышала ±0,1%. Химическая
лаборатория применяет метод,
коэффициент вариации которого при
определении никеля составляет 5%.
Вычисляем квадратичное отклоне-
5 4
ние S = щ = 0,2%. Затем
находим п:
/2-0,2\2
п = Ы-) =16-
Естественно, что руководитель
лаборатории должен принять меры
к замене метода определения
никеля на более точный, с помощью
которого необходимые
доверительные границы погрешности
результатов анализа будут обеспечиваться
при определении из 2—3
параллельных навесок.
19.6.4. Выбор метода анализа,
точность которого позволяет
получить результаты с погрешностью
не выше заданной
Для выбора из нескольких
методов с различными коэффициентами
вариации v такого, который при
заданном количестве параллельных
определений п позволил бы
получить результат с погрешностью,
не превышающей ±е, сначала
вычисляют характеризующее нужный
метод квадратичное отклонение S:
S~ 2 '
Затем находят коэффициент
вариации этого метода по формуле
slOO (1/
X
Не следует забывать о подстановке
в это уравнение соответствующего
коэффициента вместо коэффициента 2,
если число параллельных
определений, по которым вычисляется S,
меньше 20.
Для решения поставленной задачи
пригоден любой метод, коэффициент
вариации которого меньше
вычисленного значения v.
19.6.5. Критерий необходимости
арбитражного анализа
Сравниваются, как правило,
результаты двух анализов одного
продукта, выполненные в двух
лабораториях (поставщика и потребителя)
одним и тем же методом,
коэффициент вариации которого известен
по инструкции. Для этого
вычисляется величина гг и сравнивается
с абсолютным значением разности
средних арифметических
результатов двух лабораторий хх и хг\
fcl _ 100 г щ ^ ге, '
Если | Xj — х2\ *£: 8X|> то считают,
что результаты хх и х2
характеризуют одно и то же истинное
значение содержания определяемого
компонента в пробе, их различие
носит случайный характер и нет
оснований обращаться к
арбитражному анализу. Если | хг — х2\ >
> еь то расхождение хх и хг не
случайно, и необходим
арбитражный анализ.
Однако, если результаты анализа
поставщика и потребителя
оказываются совместимыми, но лежат по
разные стороны браковочного
предела, то следует обратиться к
арбитражному анализу.
19.6.6. Оценка результатов
проверочных анализов
и «шифрованных» проб
Правильность работы
аналитической лаборатории или отдельного
исполнителя контролируется по
результатам анализа проб
аналогичного материала с известным, точно
установленным химическим
составом. При этом учитывается, что
точность, с которой установлен состав
шифрованной пробы, заведомо много
выше точности поверочного анализа,
т. е. для шифрованной пробы с
содержанием определяемого
компонента х0 величина квадратичного
отклонения пренебрежимо мала по
сравнению с квадратичным
отклонением S результата проверочного
анаяиза. В связи с этим выражение
17«
для вычисления максимально
допустимого отклонения ех имеет вид
формулы
3vx 3s
б! = у=. ИЛИ Ъ= -у=..
100 Vn Vn
Анализ считается правильным,
если | х1 — х01 s£ 8Х. Если | хх —
— jc0 | > ех, то проверочный
анализ считается
неудовлетворительным.
Если точность анализа
шифрованной пробы сравнима с точностью
проверочного анализа, то для оценки
результата последнего вычисляют
максимально допустимое
отклонение е х по формуле
в1 = 3 ]/— + — *
где SL и S2— квадратичные
отклонения результатов анализа
шифрованной и поверочной проб, которые
предварительно вычисляются по
формулам с известными
коэффициентами вариации
5l- Too и ^-loo-
При сравнении результатов
анализа следует в этом случае помнить,
что если получаются несовместимые
результаты, то возможно, что оба
они являются грубо ошибочными.
19.6.7. Правила действия
с приближенными числами
В количественном химическом
анализе результаты измерений
выражают приближенным числом,
содержащим не более одной
сомнительной цифры. Полученное число
может содержать значащие и
незначащие цифры. Значащими
являются отличные от нуля цифры 1,
2, 3, 4, 5, 6, 7, 8, 9. Нули значащие
расположены в середине числа или
после значащих цифр. Нули,
расположенные перед цифрами,
отличными от нуля, — незначащие.
Например, при взвешивании тигля на
технохимических весах масса его
оказалась равной 5,25 г, на
аналитических 5,2524 г., а на
микроаналитических 5,252444 г, это обеспечивает
результаты соответственно с тремя,
пятью и семью значащими цифрами.
Раствор содержит вещества
0,0702 г/л; 70,2 мг/л; 70200 мкг/мл.
Нули впереди семерки —
незначащие цифры; нуль между семеркой и
двойкой — значащий; после двойки
нули незначащие, так как они
поставлены взамен неизвестных цифр.
Масса предмета, полученная на
технохимических весах, равна 1,00 г,
на аналитических 1,0000 г.
Полученные величины содержат три и пять
значащих цифр, так как нули в этих
числах значащие, их значность
обеспечена точностью измерения на
используемых приборах (весах).
Чтобы отличить в приближенном
числе значащие нули от
незначащих, целесообразно записывать все
нули в виде 10^ (п — число нулей),
а значащие нули — обычной
цифрой. Например, масса предмета на
технохимических весах равна 1,00 г,
или 1,00-103 мг, или 1,00-10е мкг.
При вычислениях результатов
следует быть внимательным и
пользоваться следующими правилами
действий с приближенными числами:
1. При округлении уменьшают
число значащих цифр. Это всегда
связано с введением некоторой
погрешности от округления.
Округление с поправкой предусматривает
отбрасывание последней цифры,
если она «£Л, и увеличение на одну
единицу предпоследней цифры, если
последняя цифра >5. При
округлении чисел с последней цифрой 5
выгоднее применять правило
четной цифры, ибо результат
округления всегда четный. Округление
в этом случае всегда сводится к
отбрасыванию единственной цифры 5,
если предпоследняя цифра четная,
и увеличение ее на единицу, если она
нечетная. В результате округления
вносится погрешность не более
половины единицы последнего
разряда. Например, округление чисел
217,5 и 218,5 дает цифру 218.
Погрешность в обоих случаях равна
половине цифры последнего разряда.
2. Приближенное число надо
писать так, чтобы все значащие цифры,
кроме последней, были верны и лишь
последняя была сомнительна.
177
3. Операция вычисления
результатов не может повысить точность
анализа. Вычисление результатов
анализа с большим числом цифр,
лишенных реального значения,
является «несчетным» обращением
с цифрами и потерянным трудом.
Поэтому при вычислениях
результатов анализа необходимо
выполнять правила действий с
приближенными числами.
а. При сложении и вычитании
приближенных чисел в результатах
необходимо сохранять столько
значащих цифр десятичных знаков,
сколько содержится в
приближенном числе с наименьшим их числом.
Число слагаемых не более 20.
Пример. Вычисляется вес 1 моля
KRe04. С наибольшей точностью
установлена атомная масса
кислорода — шесть значащих цифр;
атомные массы других элементов
установлены с меньшей точностью.
Произведем следующую запись:
К . . . . 39,102?
Re . . . 186,207?
40 . . . 63,9976
289,306?
Таким образом, цифра 6 является
сомнительной, а последующие за
ней цифры неопределенны. Отсюда
следует, что величина моля перре-
ната калия равна 289,306 г.
б. Вычитание двух малоразня-
щихся друг от друга чисел дает
результат с относительной
погрешностью много большей, чем у
уменьшаемого и вычитаемого в
отдельности. Например, для определения
содержания алюминия в
анализируемый раствор влито 25,00 мл
0,05 М раствора комплексона Ш.
На титрование избытка
комплексона затрачено 24,04 мл 0,05 М
раствора сернокислого цинка (К =
= 1). Абсолютная ошибка
отмеривания объемов на обычной
бюретке равна 0,02 мл, а
относительная ошибка J^-.IOO = 0,08%.
Ошибка же измерения разности
равна Jig-. 100 = 4%,
в. При умножении и делении в
результатах следует сохранять столько
значащих цифр, сколько их
содержит приближенная величина с
наименьшим числом значащих цифр.
Пример. Вычисляется содержание
кремния в стали:
0,5682
Результат вычислений не может
содержать больше трех значащих
цифр, так как масса SiOa (0,0566)
содержит только три значащих
цифры.
г. При возведении в квадрат и
в куб в результатах следует
сохранять столько значащих цифр,
сколько их имеет возводимое в
степень приближенное число.
Последняя цифра квадрата или куба при
этом менее надежна, чем последняя
цифра основания.
д. При извлечении квадратного
или кубического корня в результате
следует брать столько значащих
цифр, сколько их имеет
подкоренное. Последняя цифра полученного
числа более надежна, чем последняя
цифра подкоренного выражения.
е. При вычислениях
промежуточный результат следует брать на
одну цифру больше, чем
рекомендуют правила. В конечном
результате эта цифра округляется.
4. Вычисляя результаты анализа
с помощью таблиц логарифмов,
надо учитывать, что
вычислительная погрешность, вносимая в
результат вследствие применения
таблицы &-значных логарифмов,
делает не вполне надежной ft-тую
значащую его цифру. Для
практически полного устранения
вычислительной погрешности,
обусловленной применением таблиц
логарифмов, надо пользоваться таблицами
логарифмов с одним лишним
(запасным) десятичным знаком. Однако
эта погрешность настолько мала,
что часть запасного десятичного
знака не берут и вычисляют k-
значный результат посредством
таблицы &-значных результатов.
Средняя квадратичная погрешность
не больше единицы разряда послед-
178
ней цифры (число складываемых и
вычитаемых логарифмов не больше
трех).
Целесообразно пользоваться при
вычислении результатов
содержания компонента (х): если х^1%,...
трехзначными таблицами логарифмов
или логарифмической линейкой
длиной 25 см; 1 % < х < 10% — трех-,
четырех- значными таблицами
логарифмов; х 5г 10% —четырех-,
пятизначными таблицами
логарифмов.
Приведенные рекомендации
справедливы и для вычислений с помощью
вычислительных машин.
5. Результаты вычислений
следует всегда подвергать проверке.
Простейшей формой проверки
является грубо приближенная оценка
результата анализа. В этом случае
все цифры округляются до первой
значащей цифры и весь расчет
делается в уме. Результат получается
с одной значащей цифрой, т. е.
устанавливается порядок
результата.
19.7. ОБОЗНАЧЕНИЯ ЕДИНИЦ
(с учетом Международной системы единиц СИ и ГОСТ 9867—61)
Единицы
Метр
Сантиметр
Микрон
Ангстрем
Литр
Миллилитр
Килограмм-
масса
Грамм-масса
Ньютон
Килограмм-
сила
Обозначение
ское
и
>.
о.
М
см
МКМ
А
л
мл
кг
г
н
кгс
ду-
одиое
* о.
4> СО
£ S
m
cm
Ч
А
1
ml
kg
g
N
kgf
Единицы
Грамм-сила
Дииа
Атмосфера
техническая
Бар
(дн-см-2)
Торр
(мм рт. ст.)
Килограмм-
сила-метр
Эрг
Джоуль
Обозначение
ское
и
>.
а.
ГС
ДИН
ат
бар
торр
кгс-м
эрг
Дж
ду- .
одное
* о.
4> СО
£ X
gf
dyn
at
bar
torr
kg-m
erg
J
Единицы
Ватт
Килокалория
Калория
Кулон
Вольт
Ампер
Ом
Час
Минута
Секунда
Обози
ское
о
►.
а
Вт
ккал
кал
Кл
В
А
Ом
ч
мин
с
ачение
4>
о
И а
4> Я
£ Я
W
kcal
cal
С
V
А
Q
Ь
mm
s
19.8. ДЕСЯТИЧНЫЕ ПРИСТАВКИ
К НАЗВАНИЯМ ЕДИНИЦ ГОСТ [7663-55]
Приставка
Атто
Фемто
Пи ко
Нано
Микро
Обозначение
русское
'd
■В-
п
н
мк
международное
а
f
Р
п
И
Множитель
ю-18
Ю-16
Ю-12
10"»
Ю-6
Приставка
Милли
Санти
Деци
Дека
Гекто
Обозначение
руссиое
м
с
д
да
г
международное
m
с
d
da
h
Множитель
10-3
Ю-2
ю-1
10
10а
Приставка
Кило
Мега
Гига
Тер а
Обозначение
русское
к
М
Г
т
международное
к
М
G
Т
л
Множител
10»
10е
10»
1012
12*
179
19.9. ШКАЛЫ ТЕМПЕРАТУР
Температура
*°С (шкала Цельсии)
х °К (шкала Кельвина)
х °R (шкала Реомюра)
х °F (шкала Фаренгейта)
х "Rank (шкала Ренкииа)
Эквивалент по шкале
Цельсня
х°С
(х— 273,15) °С
А*°с
4 * Ь
-!~(х:_32РС
-§-<*— 491'69) °С
Кельвина
(х+ 273,15)К
х°К
(~х + 273,15) К
(— *+255,38) К
А,к
19.10. ЗНАЧЕНИЯ ВАЖНЕЙШИХ УНИВЕРСАЛЬНЫХ ФИЗИЧЕСКИХ КОНСТАНТ:
Скорость света в вакууме, 1010 см/с 2,997928 ± 0,000004
Гравитационная постоянная, 10"8 дин-см2/г2 6,670 ± 0,07
Нормальное ускорение силы тяжести, см/с2 980,665
Объем 1 моля идеального газа при нормальных
условиях *, л 22,4139 ± 0,0011
Универсальная газовая постоянная*, 10' эрг/(моль-К) 8,31467 ± 0,00034
Постоянная Больцмана, Ю"16 эрг/К 1,38044 ± 0,00007
Число Авогадро *, 10аз моль"1 6,02322 ± 0,00016
Число Фарадея, Кл/г-экв 96495,5 ±1,1
Постоянная Планка, Ю-27 эрг/с 6,62517 ± 0,00023
* По кислородной химической шкале атомных масс.
19.11. СВЕДЕНИЯ О ВРЕДНОСТИ И ОПАСНОСТИ ПРИ РАБОТЕ С НЕКОТОРЫМИ
ХИМИЧЕСКИМИ РЕАКТИВАМИ
Азотная кислота. Раздражает
кожу, глаза, дыхательные пути,
токсична и взрывоопасна. Пожар,
возникший от действия азотной
кислоты, тушат распылением воды.
Хранят отдельно, защищают от
механических повреждений.
Ацетон. Температура вспышки
в закрытом тигле —18° С,
температура самовоспламенения 538° С,
температура кипения 56,2° С, пределы
воспламенения 2,6—12,8% (объемн.),
раздражает кожу, глаза,
дыхательные пути, токсичен, в высокой
степени взрывоопасен. При горении
тушат порошковыми составами,
углекислым газом, распылением воды.
Хранят отдельно, защищают от
механических повреждений.
Бензол. Температура вспышки
в закрытом тигле —11° С,
температура самовоспламенения 562° С,
температура кипения 80,Г С,
пределы воспламенения 1,3—7,1 %
(объемн.), раздражает кожу, глаза,
дыхательные пути, очень токсичен,
особенно для женщин, в высокой
степени взрывоопасен. При пожаре
тушат распылением воды, пеной,
углекислым газом, сухими
порошками. При хранении тщательно
изолируют и оберегают от механических
повреждений.
Бром. Температура кипения 58,8°С,
раздражает кожу, глаза,
дыхательные пути, токсичен. При пожаре
тушат водой. Хранят отдельно,
оберегают от механических
повреждений и влаги.
Бутиловый спирт (первичный).
Температура вспышки в закрытом
тигле 29° С, температура
самовоспламенения 363° С, температура
кипения 117,5° С, пределы
воспламенения 1,4—11,2% (объемн.),
раздражает кожу, глаза, токсичен, в
высокой степени взрывоопасен. При
пожаре тушат пенными средствами,
180
углекислым газом. Хранят в обычном
складе, оберегают от механических
повреждений.
Гексан (нормальный). Температура
вспышки в закрытом тнгле —21,6° С,
температура самовоспламенения
261° С, температура кипения 69° С,
пределы воспламенения 1,1—7,5%
(объемн.), раздражает глаза,
токсичен, в высокой степени
взрывоопасен. При пожаре тушат пенами,
углекислым газом, сухими
порошками. Хранят в обычном складе,
предохраняют от механических
повреждений, нагревания и искры.
Гидроокиси калия и натрия.
Раздражает кожу, глаза, дыхательные
пути, токсичны. При пожаре тушат
мешениях, предохраняют от
механических повреждении и влаги.
Метиловый спирт. Температура
вспышки в закрытом тигле 11° С,
температура самовоспламенения
464° С, температура кипения 64,5° С,
пределы воспламенения 7,3—36%
(объемн.), раздражает дыхательные
пути, очень токсичен и
взрывоопасен. При пожаре тушат водой,
углекислым газом, сухими порошками,
хранят в специальных
изолированных помещениях, предохраняют от
механических повреждений и искры.
Натраты аммония и калия.
Раздражают глаза, кожу, токсичны,
взрывоопасны, при пожаре тушат
водой. Хранят в отдельных
помещениях, предохраняют от
механических повреждений и влаги.
Перекись водорода (30—50%-ный
раствор). Раздражает кожу, глаза,
верхние дыхательные пути, токсична,
взрывоопасна, при пожаре тушат
водой. Хранят в изолированном
помещении, предохраняют от
механических повреждений.
Перекись натрия. См. Перекись
водорода.
Серная кислота. Раздражает кожу,
глаза, верхние дыхательные пути, при
пожаре тушат сухими порошками.
Хранят в отдельном помещении,
предохраняют от механических
повреждений и влаги.
Соляная кислота. Раздражает
кожу, глаза, дыхательные пути,
токсична, взрывоопасна, при пожаре
тушат водой и специальными
порошками. Хранят в отдельном
помещении, предохраняют от
механических повреждений.
Толуол. Температура
воспламенения в закрытом тигле 4° С,
температура самовоспламенения 536° С,
температура кипения 110,6° С, пределы
воспламенения 1,4—6,7% (объемн.),
раздражает глаза, дыхательные
пути, токсичен, взрывоопасен.
При пожаре тушат распылением
воды, пеной, углекислым газом,
сухими порошками. Хранят в
отдельных помещениях, предохраняют от
механических повреждений,
нагревания и искры.
Уксусная кислота (ледяная).
Температура встгамжи в аау.ръ\том титле
41° С, температура
самовоспламенения 4Д&° С, температура кипения
118° С, пределы воспламенения 5,4—
16% (объемн.), раздражает кожу,
глаза, дыхательные пути, токсична,
в высокой степени взрывоопасна.
При пожаре тушат распылением
воды, углекислым газом, сухими
порошками. Хранят в отдельных
помещениях, предохраняют от
механических повреждений.
Фтористоводородная кислота.
Температура кипения 19,4° С, разъедает
кожу, раздражает глаза,
дыхательные пути, токсична, взрывоопасна.
При пожаре тушат водой. Хранят
в отдельных помещениях,
предохраняют от механических повреждений.
Хлорная кислота. Раздражает
кожу, глаза, дыхательные пути,
токсична, взрывоопасна. При пожаре
тушат распылением воды. Хранят
в отдельных помещениях,
предохраняют от механических повреждений.
Эфир этиловый. Температура
вспышки в закрытом тигле —45° С,
температура самовоспламенения
186° С, температура кипения 34,5° С,
пределы воспламенения 1,9—48%
(объемн.), раздражает дыхательные
пути, токсичен, взрывоопасен. При
пожаре тушат углекислым газом,
сухими порошками. Нельзя тушить
водой. Хранят в изолированных
помещениях, предохраняют от
механических повреждений, нагревания
и искры.
19.12. СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
Алексеев Р. И., Коровин Ю. И. Руководство
по вычислению и обработке результатов
количественного анализа. М., Атомиздат,
1972. 72 с.
Алимарин И. П., Петракова М. Н.
Неорганический ультрамикроанализ. М., Изд-во
АН СССР, 1960. 152 с.
Алимарин И. П., Фрид Б. И. Количественный
микрохимический анализ минералов и руд.
М., Госхимиздат, 1961. 399 с. с ил.
Бабко А. К., Пилипенко А. Т.
Фотометрический анализ. Общие сведения и
аппаратура. М., «Химия», 1968. 388 с. с ил.
Бабко А. К., Пилипенко А. Т.
Фотометрический анализ. Методы определения
неметаллов. М., «Химия», 1974. 360 с. с ил.
Барковский В. Ф., Ганопольский В. И.
Дифференциальный спектрофотометрический
анализ. М., «Химия», 1969. 168 с. с ил.
Беликов В. Г. Дифференциальная
фотометрия. Ставропольское книжное
издательство, 1970. 136 с. с ил.
I Бейтс Р. Определение рН. Теория и
практика. Л., «Химия», 1972. 400 с. с ил.
Бимиш Ф. Аналитическая химия
благородных металлов. Ч. 1 и ч. 2. М., «Мир»,
1969. 697 с. с ил.
Божевольнов Е. А. Люминесцентный анализ
неорганических веществ. М., «Химия»,
1966. 416 с. с ил.
Буданова Л. М., Володарская Р. С, Ка-
наев Н. А. Анализ алюминиевых и
магниевых сплавов. М., «Металлургия», 1966.
360 с.
Будяк Н. Ф., Зельцер Е. Ю., Шестакова Е. И.
Анализ магнитных сплавов. М.,
«Металлургия», 1971. 240 с. с ил.
Булатов М. И., Калинкин И. П.
Практическое руководство по
фотоколориметрическим и спектрофотометрическим методам
анализа. Л., «Химия», 1972. 408 с. с ил.
Бусев А. И. Синтез новых органических
реагентов для неорганического анализа.
М., Изд-во МГУ, 1972, 247 с.
Бусев А. И., Типцова В. Г., Иванов В. М.
Практическое руководство по
аналитической химии редких элементов. М., «Химия»,
1966. 412 с. с ил.
Гейровский Я., Куша Я. Основы
полярографии. М., «Мир», 1965. 560 с. с ил.
Гиллебранд В., Лендель Г., Б раит Г.,
Гофман Д. Практическое руководство по
неорганическому анализу. М., Госхимиздат,
1957. 1016 с. с ил.
Руководство по химическому анализу
платиновых металлов и золота. М., «Наука»,
1965. 314 с Авт.: С. И. Гинзбург, К. А. Гла-
дышевская, Н. А. Езерская, О. М. Иво-
нииа, И. В. Прокофьева, Н. В. Федоренко,
А. Н. Федорова.
Губен-Вейль. Методы органической химии.
Т. II. Методы анализа. М., «Химия», 1967.
1032 с. с ил.
Денеш И. Титрование в неводных средах.
М., «Мир», 1971. 413 с. с ил.
Дымов А. М. Технический анализ (контроль
химического состава железных сплавов).
М., «Металлургия», 1964. 336 с с ил.
Доерфель К- Статистика в аналитической
химии. М., «Мир», 1969. 247 с. с ил.
Жендарева О. Г., Мухина 3. С. Методы
анализа гальванических вани. М., Оборонгиз,
1963. 270 с.
Золотое Ю. А. Экстракция внутрикомплекс-
ных соединений. М., «Наука», 1968. 314 с.
с ил.
Канаев Н. А. Ускоренное определение
редкоземельных элементов. М., «Металлургия»,
1971. 224 с. с ил.
Карякин Ю. В., Ангелов И. И. Чистые
химические вещества. М., «Химия», 1974. 408 с.
с ил.
Киселева Е. К-, Герасимова Н. И.,
Иванова Л. В., Кондратович Г. А. Анализ
электролитов и растворов. Л., Госхимиздат,
1963. 312 с.
Колориметрические (фотометрические)
методы определения неметаллов. М.,
Издательство иностранной литературы, 1963.
468 с. с ил.
Объемный анализ. Т. III. M., Госхимиздат,
1961. 840 с. Авт.: И. М. Кольтгоф, Р. Бел-
чер, В. А. Стеигер, Дж. Матсуяма.
Коренман И. М. Аналитическая химия
малых концентраций. М., «Химия», 1967.
168 с. с ил.
Коренман И. М. Методы определения
органических соединений. М., «Химия», 1970.
334 с.
Коростылев П. П. Приготовление растворов
для химико-аналитических работ. М.,
Издательство АН СССР, 1962. 312 с. с ил.
Краткая химическая энциклопедия. М.,
«Советская энциклопедия». Т. I, 1961. 1262 с.
с ил.; Т. 2, 1963. 1088 с. с ил.; Т. 3, 1964.
1112 с. с ил.; Т. 4, 1965. 1182 с. с ил.; Т. 5,
1967. 1184 с. с ил.
Краткий справочник физико-химических
величин. Л., «Химия», 1974. 200 с.
Крешков А. П. Основы аналитической
химии. Т. 1—3. М., «Химия», 1965 и 1970.
1346 с с ил.
Кульберг Л. М. Органические реактивы
в аналитической химии. М.—Л.,
Госхимиздат, 1950. 259 с.
Лайтинен Г. А. Химический анализ. М.,
«Химия», 1966. 656 с. с ил.
Лурье Ю. Ю. Справочник по аналитической
химии. М., «Химия», 1971. 456 с.
Лурье А. А. Сорбенты и хроматографические
носители (справочник). М., «Химия», 1972.
320 с.
Мазуренко Е. А. Справочник по экстракции.
Киев, «Техника», 1972. 448 с.
Марченко 3. Фотометрическое определение
металлов. М., «Мир», 1971. 501 с. с ил.
Методы анализа веществ высокой чистоты.
М., «Наука», 1965. 528 с. с ил.
Мусакин А. П. Таблицы и схемы
аналитической химии. Л., «Химия», 1971. 128 с. с ил.
Некрасов Б. В. Основы общей химии. Т. 1—3.
М., «Химия», 1965. 1435 с. с ил.
Немодрук А. А., Беэрогова Е. В.
Фотохимические реакции в аналитической химии. М.,
«Химия», 1972. 168 с. с ил.
182
Анализ электролитов и растворов. Л., Гос-
химиздат, 1963. 312 с. Авт.: Л. И. Никан-
дрова, Н. И. Герасимова, Л. В. Иванова,
Г. А. Кондратович.
Окнина В. А. Методы химического
анализа фосфатных руд. М., Госхимиздат,
1961. 144 с. с ил.
Пешкова В. М., Громова М. И. Практическое
руководство по спектрофотометрии и
колориметрии. М., Изд-во МГУ, 1965. 234 с.
с ил.
Перрин Д. Органические аналитические
реагенты. М., «Мир», 1967. 407 с.
Перегуд Е. А., Быковская Е. С, Гернет Е. В.
Быстрые методы определения вредных
веществ в воздухе. М., «Химия», 1970. 360 с.
с ил.
Реми Г. Курс неорганической химии. Т. 1,2.
М., ИЛ, 1963. 1756 с. с ил.
Риман В., Уолшн Г. Иоиообмеииая
хроматография в аналитической химии. М., «Мир»,
1973. 375 с. с ил.
Самуэльсон О. Ионообменные разделения
в аналитической химии. М., «Химия»,
1966. 416 с. с ил.
Семи шин В. И. Периодическая система
химических элементов Д. И. Менделеева. М.,
«Химия», 1972. 188 с. с ил.
Сендэл Е. Колориметрические методы
определения следов металлов. М., «Мир», 1964.
902 с. с ил.
Сонгина О. А. Амперометрическое
титрование. М., «Химия», 1967. 388 с. с ил.
Справочник химика. Т. 1—5. М., «Химия»,
1962—1967.
Стары И. Экстракция хелатов. М., «Мир»,
1966. 392 с. с ил.
Анализ черных металлов, сплавов и
марганцевых руд. М.,
«Металлургия», 1971. 448 с. с ил. Авт.: В. В. Сте-
пии, В. В. Силаева, В. И. Курбатова,
Н. Д. Федорова, В. И. Поносов.
Анализ цветных металлов и сплавов. М.,
«Металлургия», 1965. 188 с. с ил. Авт.:
В. В. Степин, Е. В. Силаева, В. И.
Курбатова, Т. Ф. Ханова, Т. Л. Барбаш,
В. И. Поносов.
Сусленникова В. М., Киселева Е. К-
Руководство по приготовлению титрованных
растворов. Л., «Химия». 1968. 144 с с ил.
Теплоухов В. И. Экспресс-анализ стали. М.,
«Металлургия», 1971. 352 с. с ил.
Тереншьев А. П., Яновская Л. А.
Химическая литература и пользование ею. М.,
«Химия», 1967. 328 с.
Унифицированные методы анализа вод. М.,
«Химия», 1973. 376 с. с ил.
Файнберг С. Ю, Филиппова Н. А. Анализ руд
цветных металлов. М., Металлургиздат,
1963. 871 с. с ил.
Харламов И. П. Спектрофотометрический
анализ сплавов. М., «Металлургия», 1969.
208 с. с ил.
Химический и спектральный анализ в
металлургии. М., «Наука», 1965. 384 с. с ил.
Шарм Г. Методы аналитической химии.
Ч. 1 и ч. 2. М., «Химия», 1969. 1206 с.
Шварценбах Г., Флашка Г. Комплексен оме-
трическое титрование. М., «Химия», 1970.
360 с. с ил.
Шеллер В. Р., Поузлл А. Р. Анализ
минералов и руд редких элементов. М., Гос-
геологтехиздат, 1962. 448 с.
Шемякин Ф. М., Степин В. В.
Ионообменный хроматографический анализ
металлов. М., «Металлургия», 1970. 392 с.
Шемякин Ф. М., Карпов А. П., Брусне-
цов А. Я. Аналитическая химия. М.,
«Высшая школа», 1973. 559 с. с ил.
Щербов Д. П. Флуориметрия в химическом
анализе минерального сырья. М., «Недра»,
1965. 260 с. с ил.
Элвелл В. Т., Вуд Д. Ф. Анализ новых
металлов (титаи, цирконий, гафний, ниобий,
тантал, вольфрам и их сплавы). М.,
«Химия», 1970. 220 с. с ил.
Яковлев П. Я-, Яковлева Е. Ф. Технический
анализ в металлургии. Справочное
руководство для лаборантов. М.,
Металлургиздат, 1963. 288 с с ил.
Яковлев П. Я-, Федоров А. А., Буянов Н. В.
Анализ материалов металлургического
производства. М., Металлургиздат, 1961. 316 с.
с ил.
Яковлев П. Я-, Яковлева Е. Ф., Оржехов-
екая А. И. Определение углерода в
металлах. М., «Металлургия», 1972. 228 с.
с ил.
Яцимирский К- Б. Кинетические методы
анализа. М., «Химия», 1967. 200 с с ил.