Текст
химия
жизнь
Научно-популярный журнал Академии наук СССР
1967
Революционер Лев Карпов
Элемент № 4: бериллий
Эмбрион и организм
Фантастическая повесть
Шоколадный набор
Из писем в редакцию...
РОС ЙНСКА8$ШМТЙВ8*1
Г9ШС*М МШ1Ш1
»*лИ Cent SiHiiir* UMlmt
ОТДЕЛ
**v*4ee*«ofi промышленности
N*
^/<
Москве,
У
ЯсМ* Оихдбрд «/
Р %л /»/ 8
УДОСТОВЕРЕН II
о
о
а?
Наотоящнмъ Отд!уоеъ Хшотеокой Пролшшденноотй
B.C^Hju удоотовЪдеетгдео означенный »ъ семг
каъксЪй Николаевич* Ш&дсдкь одагицМая ученый»
приглашена ОтдЬломъ Химической *1ро*шщвшооти
«ѫͻл»яавЪднвать Jkdopatopiefi такового охд%яа*
ЧЛЕНЪ ПРЕЗВД1УЩ
^дьашущм овдмокь <^/Ж^^/
!рАаа.1ыщ1и д-мми отдш ^>
Зто удостоверение было
и о создании первой советской
получено А. Я. Бахом в октябре лаборатории открывается этот
1918 года—в дни, номер журнала.
когда создавалось первое новое
научное учреждение молодой
Советской республики
лаборатория, положившая начало Фи-
зико-х им ическому институт у
имени Л. Я. Карпова.
Воспоминаниями о Л. Я. Карпове
На обложке: рододепдроп даурский.
Фото Г. П. ТАФИНЦЕВА
1967 февраль № 2 ХИМИЯ И ЖИЗНЬ
ГОД ИЗДАНИЯ 3-И
1917—1967
Элемент №...
.Проблемы и методы
современной науки
Наш календарь
Обыкновенное
вещество
Фантастика
Что мы едим
Фотолаборатория
"Учитесь переводить
"Живые лаборатории
Клуб Юный химик
Научный фольклор
Сказка
г
7
17
25
27
28
31
34
39
40
43
50
51
55
56
57
61
63
66
74
76
77
80
82
89
91
93
94
96
Революционер Карпов
Бериллий
Строительная площадка организма —
эмбрион
Предводитель русской «химической
дружины»
По поводу одной забытой фотографии
Письма Циолковского к Менделееву
Чернила
Документ в руках эксперта
Клин — клином
Чернила, которые в то же время не
чернила
Ловушка для простаков
Наш комментарий
Пища богов
Шоколадный набор
Домашнее приготовление шоколада
Как делают шоколад?
Этикетки за 100 лет
Из писем в редакцию
Макрофотосъемка
Немецкий — для химиков
Советуемся с читателями
Снежинка на память
Рододендрон даурский
Что это такое? Викторина. Хотите
подготовиться к экзаменам получше?
Химический сторож
«Учение, на опытах основанное»
Вопросы для самоподготовки
Приготовление кофе в
научно-исследовательских институтах
Что больше всего нравилось морскому
волку
Необычные портреты
К. А. Капустинская
В. М. Кроль
Н. А. Фигуровский
A. Шамшурин
B. Голоушкин
Г. К. Фаизова
В. Станцо
Г. Семиверстова
А. Азимов
И. В. Петрянов
И. Вольпер
О. М. Либкин
В. Овчаров
Л. Я. Крауш
Ю. В. Таранович
Г. П. Тафинцев
А. М. Скундин
Л. Солодкин
Редакционная коллегия:
И. В. Петрянов-Соколов (главный редактор), П. Ф. Ба-
денков, Н. М. Жаворонков, С. В. Кафтанов, Л. И. Ма-
зур, Б. Д. Мельник, В. И. Рабинович (ответственный
секретарь), П. А. Ребиндер, М. И. Рохлин (зам.
главного редактора), С. С. Скороходов, Б. И. Степанов,
А. С. Хохлов, М. Б. Черненко (зам. главного
редактора), Н. М. Эмануэль
Редакция:
Б. Г. Володин, В. Е. Жвирблис, А. Д. Иорданский,
О. И. Коломийцева, О. М. Либкин, В. В. Станцо,
Т. А. Сулаева, И. М. Чаплина, В. К. Черникова
Художественный редактор С. Верховский
Технический редактор Э. Язловская
Корректоры И. К. Шатуновская, Е. И. Сорокина,
Ю. И. Глазунова
При перепечатке ссылка на журнал «Химия и
жизнь» обязательна
Адрес редакции: Москва В-333, Ленинский проспект,
61/1. Телефоны АВ 7-72-64 и АВ 7-66-23
Подписано к печати 17/1 1967 г. Т00931. Бумага 84\108I/l6.
Печ. л. 6,0. Усл. печ. л. 10,08+1 вкл. Уч.-изд. л. 10,7.
Тираж 126 000 экз. Зак. 1521. Цена 30 коп.
Московская типография № 2 Главполиграфпрома Комитета
по печати при Совете Министров СССР. Москва, проспект
Мира, 105.
Печать обложки и цветной вклейки выполнена во 2-й
типографии издательства «Наука». Москва, Шубинский
пер., 10.
1917— 1967
РЕВОЛЮЦИОНЕР
КАРПОВ
БОНДЮЖСКИЙ ХИМИЧЕСКИЙ ЗАВОД И
ФИЗИКО-ХИМИЧЕСКИЙ ИНСТИТУТ (ПЕРВОЕ НАУЧНО-ИССЛЕДОВАТЕЛЬСКОЕ
УЧРЕЖДЕНИЕ, СОЗДАННОЕ МОЛОДОЙ СОВЕТСКОЙ
РЕСПУБЛИКОЙ) НОСЯТ ИМЯ ЛЬВА ЯКОВЛЕВИЧА КАРПОВА.
В 1898 году девятнадцатилетний студент
химического факультета Высшего технического
училища Лев Карпов был арестован охранкой за
участие в создании «Московского союза борьбы за
освобождение рабочего класса». После
многомесячного одиночного заключения он был выслан
из Москвы сначала в Курск, а затем в Воронеж
под гласный полицейский надзор.
Из письма Л. Я. КАРПОВА, написанного
в 1902 году из ссылки отцу, жившему в Киеве
«Воронеж, 18 января.
Дорогой папа! Меня удивляет в твоих
письмах, что ты постоянно жалуешься на
страданья, которыя я тебе причиняю.
Я этого совершенно не понимаю... Что
касается лично меня, то я несмотря на то,
что состою под надзором (в этом я не вижу
для себя ничего позорящаго), чувствую
себя превосходно... и жизнь меня в общем
удовлетворяет. Не нужно забывать, что
тысячи и миллионы людей живут в
стократ хуже моего...»
31 марта 1902 года в Воронеже Л. Я. Карпов
был вновь арестован вместе с другими социал-
демократами за участие в организации
«Северно-русского социал-демократического союза».
После восьмимесячного одиночного заключения
в московской Таганской тюрьме он был снова
выслан в Воронеж, но скрылся из-под надзора
и перешел на нелегальное положение.
Из воспоминаний Л. Б. КРАСИНА
«Тов. Карпов был членом ЦК...
Я припоминаю период работы 1904—
1905 гг., когда находившийся в России ЦК
был только частью всего ЦК и был связан
с центром нашей партии, находившимся в
Женеве, с тов. Лениным и другими
товарищами лишь посылкою случайных
курьеров, которым нелегально, с величайшими
трудностями удавалось пробираться за
границу, когда всю работу в России
приходилось вести в подполье, когда мы могли
собираться один раз в течение месяца или
двух — сегодня в Смоленске, завтра в
Москве, послезавтра в другом городе...».
10 февраля 1905 года жандармы ворвались в
квартиру писателя Леонида Андреева, где
происходило нелегальное заседание ЦК
большевиков. Вместе с другими членами ЦК Карпов снова
арестован и снова брошен в одиночку Таганской
тюрьмы. Но восемь месяцев спустя — в октябре,
в дни всеобщей стачки, народ освободил
заключенных.
Из воспоминаний
старого большевика В. А. НЕВСКОГО
«Подталкиваемый толпой, я неожиданно
очутился у самых ворот «Таганки»,
которые вдруг отворились, и каково же было
мое удивление, когда я увидел... Льва,
который, улыбаясь и прищуривая глаза,
смотрел на меня.
— Лев Яковлевич!
— А, вот встреча! Я же вам говорил,
что мы обязательно встретимся либо на
баррикадах, либо у виселицы^.
Из воспоминаний А. П. ГОЛУБКОВ А,
бывшего секретаря редакции большевистской га-
зеты «Вперед»
«...Увидел я его снова уже после
октябрьских дней 1905 г. в Москве. Л. Я. принимал
участие в организации и ведении
издававшейся в Москве накануне декабрьского
вооруженного восстания газеты
Московского Комитета «Вперед». Это были дни
подготовки восстания, и помещение
редакции (на Никитской) было одним из
штабов... Приносилось туда огромное
количество оружия: револьверов, маузеров,
винчестеров. Из редакции мы, сотрудники,
работавшие в ней, разносили оружие по
районам. То же делал и Левушка: надевал
под пальто винчестеры, запихивал в
карманы и сапоги револьверы... В 1906—
1907 гг. он был секретарем Московского
комитета и вслед за тем в качестве
нелегального студента, без права жительства
в Москве, он учился в Высшем
техническом училище...».
Он был снова арестован в 1907 году на
общегородской рабочей маевке в Сокольниках. Но
жандармам не удалось обнаружить никаких
улик — Карпов был уже опытным
конспиратором. Снова одиночка. Снова высылка — в Тверь.
В Тверь Карпов не прибыл. Он жил в Москве
по паспорту Н. В. Луначарского (брата А. В.
Луначарского). А в списках студентов ВТУ он
числился под собственной фамилией. И директор
училища А. П. Гавриленко, и учителя Карпова —
профессора Л. А. Чугаев и С. П. Ланговой знали,
что Карпов — высланный
революционер-подпольщик. Ничего не ведала только охранка...
Он стал, как и хотел, химиком. Провел
самостоятельную научную работу, спроектировал и
построил скипидарно-канифольный завод с
совершенно новой технологией. Его работа сразу
обратила на себя внимание предпринимателей —
и российских, и зарубежных. Разумеется, они не
имели ни малейшего понятия о том, что
блестящий инженер — это большевик-подпольщик.
Первая мировая война застала Карпова на
строительстве нового завода на Севере, в
Финляндии. Из-за войны работы
приостанавливаются, и Карпов принимает пост директора Бондюж-
ского химического завода.
Но и сделавшись директором, он по-прежнему
остается революционером.
Из очерка О. И. ПИСАРЖЕВСКОГО
«Страницы жизни большевика-ученого»
«В 1914 году, когда уже началась
империалистическая война, воспользовавшись
одной из поездок «по делам службы», Карпов
устанавливает связь с московской
партийной организацией. Вместе с Г. М.
Кржижановским, М. С. Ольминским и другими
большевиками он принимает участие в
одном из совещаний, на котором обсуждался
вопрос об отношении к войне. И Карпов
решительно отстаивает точку зрения
Л. Я. Карпов A879—1921)
В. И. Ленина, сформулированную в
известных «Тезисах о войне».
«Он смотрел на начавшуюся войну, как
на предтечу грядущей революции... Он не
делал разницы между
империалистическими тенденциями Германии и Антанты
и противопоставлял тому и другому
только последовательную классовую борьбу
революционного марксизма, отвергавшую
всякую поддержку какой-либо из сторон
в этой войне»,—вспоминал П. А. Богданов.
Из воспоминаний А. С. КАРПОВОЙ
«...Мы приехали на завод в 1915 году,
поздней осенью, примерно в октябре
месяце. Первая же весна показала нам все
прелести казарменной жизни рабочих. Уже в
1915 году, несмотря на то, что шла война,
Льву Яковлевичу удалось добиться
разрешения на постройку двухэтажного дома
для рабочих. Это не было уже общежитие-
казарма. В этом доме каждая семья имела
отдельную комнату и кухню.
A. H. Бах A857—1949)
На заводе была резкая грань между
рабочими и так называемой «конторой».
В конторе работали старые, преданные
Ушкову (владельцу завода. — Ред.) слуги.
Большинство из них косо смотрело на
порядки, которые завел новый директор.
...С приездом на Бондюжский завод
Я. И. Збарского, Михайлова и Сармановой,
при наличии нас, С. Н. Гассара и рабочих
Климова, Ветлугина и Мартынова,
создались условия для организации у нас
партийной группы *. Мы регулярно получали
из Москвы все, что выходило легально из
марксистской литературы, и журналы.
Изредка получали от товарищей из Москвы
центральный орган партии
«Социал-демократ», вклеенный в переплеты легальных
книг. Значение нашей партийной группы,
ее влияние на рабочих завода полностью
* Большевик С. Н. Гассар был выслан на
Бондюжский завод из Казани; В. Г. Михайлов,
3. И. Сарманова и Я. И. Збарский были известны
Л. Я. Карпову по подпольной работе и
специально приглашены им на завод.
сказалось после Февральской, а еще
больше— после Октябрьской революции.
Это сказалось в большевистской линии
наших депутатов в Елабужском совете
рабочих, крестьянских и солдатских
депутатов, и в поведении рабочих завода в
период гражданской войны. Все годы
гражданской войны Бондюжский завод боролся
на стороне большевиков: при наступлении
белых пожилые мастера снимали и
эвакуировали все главные части машин.
Молодежь вливалась в Красную Армию.
В апреле 1917 г. в Бондюгу приехал
Алексей Николаевич Бах. Алексей
Николаевич в 1881 г., вернувшись из ссылки,
вступил в партию «Народная воля».
В 1883 году он написал книгу
«Царь-голод», которая пользовалась большой
популярностью среди рабочих. После убийства
Александра II (в 1881 г.), когда «Народная
воля» была разгромлена, А. Н. Бах
эмигрировал в Швейцарию и здесь начал
заниматься химией, стал крупным ученым-
биохимиком. Его научные открытия
получили мировое признание. Он жил и работал
в Женеве. При первом же известии о
революции в России А. Н. Бах оставил
Швейцарию, где он прожил 35 лет, свою работу,
детей — и с женой и старшей дочерью
приехал в Россию. Он приехал в Бондюгу к
своему ученику Б. И. Збарскому, который
у него учился и работал в его лаборатории
в Женеве.
Здесь в Бондюге он и познакомился с
Львом Яковлевичем. Алексей Николаевич,
человек с ясным и проницательным умом,
умудренный своим большим и богатым
жизненным и революционным опытом, в
беседах с Львом Яковлевичем укрепился
в своем решении остаться в России. Он
хорошо принял не только Февральскую, но
и Великую Октябрьскую
социалистическую революцию и решил работать с
большевиками, с Советской властью...
В декабре 1917 года Лев Яковлевич
поехал с группой рабочих в Петроград,
чтобы договориться о будущем завода, о
его работе как государственного
национализированного предприятия. И тогда —
в феврале 1918 г.— Владимир Ильич Ленин
предложил Льву Яковлевичу возглавить
химическую промышленность.»
Октябрь был рубежом.
Он разделил всю жизнь на то, что было «до»
и на то, что стало «после», то есть теперь.
Для Карпова он был итогом девятнадцати лет,
отданных революционной борьбе, беспокойной
жизни подпольщика — с оружием, спрятанным
в сапоги, — тогда, в 1905 году на Пресне; с
арестами, тюрьмами, ссылками.
То, о чем он мечтал, свершилось!
Из воспоминаний Л. Б. КРАСИНА
«...Я видел его в 1917 г., после Октябрьской
революции, ...когда рабочие и крестьяне
брались уже за руль советского корабля,
когда возникали величайшие вопросы
организации советской власти, и в первую
очередь — задачи построения нашего
хозяйства на новых, социалистических
началах...
Лев Яковлевич уже тогда
высказывался, что нет возможности с его стажем, с его
взглядами, остаться сейчас техником на
заводе, концентрировать внимание
исключительно на технической деятельности.
Уже в первые недели после Октябрьского
переворота он говорил о необходимости
немедленно взяться за организационную
работу, за построение того хозяйственного
аппарата, тех руководящих органов,
которые отныне должны регулировать
промышленность, перешедшую целиком в
собственность самих производителей, в
собственность рабочего класса.»
На плечи коммуниста и инженера Карпова
легла задача неимоверной трудности. Советская
Республика сражалась с врагами, с голодом, с
разрухой; многие химические продукты, остро
необходимые стране, в России вообще не
производились. И Карпов приступил к налаживанию
старых и созданию новых производств.
Ленин знал, что он вверяет важнейшую
отрасль народного хозяйства не только
закаленному в революционной борьбе коммунисту, но и
крупному инженеру, ученому, талантливому
организатору, умеющему смотреть далеко вперед.
И в те тяжелые годы Карпов сумел собрать
силы и средства для работы не только ради
сегодняшних и завтрашних насущных
хозяйственных нужд, но и — для будущего страны.
Поначалу все выглядело скромно — при
отделе химической промышленности ВСНХ была
создана центральная химическая лаборатория —
фундамент Физико-химического института. «Эта
лаборатория,— писал один из руководителей
ВСНХ П. А. Богданов,— важна тем, что она
задумана и осуществлена полностью в условиях
революционного творчества и при участии
людей, которые полностью отдавали свои силы на
укрепление советского строя».
В личном архиве первого директора института
имени Карпова — академика Алексея
Николаевича Баха сохранилась стенографическая запись
его выступления, в котором он рассказывал о
событиях того времени *.
Из выступления А. Н. БАХА A935 год)
«...Нас было очень мало — всего 8
человек. Правда, Лев Яковлевич настаивал на
том, чтобы сразу создать большое
учреждение, поставить дело широко, и я,
признаться, боялся этого, потому что неясно
было, как все наладится.
...Сначала нам отвели 5-й этаж жилого
дома в Армянском переулке, но очень
скоро лаборатории пришлось расшириться.
Мы перешли в 4-й и 3-й этаж, и нас стало
работать уже около 40 человек.
Промышленность внимательно
отнеслась к лаборатории, внимательнее, чем
теперь. К нам присылали работников с
заводов с определенными заданиями, мы
вместе работали, нам помогали...
Первоначально лаборатория выполняла все
задания, какие были, какие ставились жизнью:
производство суррогата касторового масла,
топлива для моторов и т. д. Но по мере
того, как жизнь стала
дифференцироваться, по мере того, как возникли другие
лаборатории и институты, Центральная
лаборатория стала специализироваться в
области физической химии.
Я долго жил за границей и знал
значение физической химии, и, хотя я сам не
физико-химик по специальности, работа
пошла все-таки в этом направлении.
Вскоре мы оказались в таком
положении, что не могли уже удовлетворять
требования, которые к нам предъявляла
промышленность, так как мы были очень
плохо оборудованы. И тогда у Льва
Яковлевича возникла идея построить
лабораторию (ныне существующий корпус
института.— Ред.). Это было в 1920 году. Коллегия
химического отдела ВСНХ тогда
поддержала идею с энтузиазмом и вынесла
соответствующее постановление...
Очень много труда и хлопот было
положено на то, чтобы создать институт.
Начали его строить в 20-м году. В 1922
году здание было закончено и передано нам.»
Тяжело заболев осенью 1920 года,
руководитель химического отдела Высшего Совета Народ-
* Материалы предоставлены редакции
Н. А. Бах.
л
,y£ff
3 «су пределу И,Й»С Й К О К*
ЗА&ачва Химического Йлс*«*ута 8СЙХ
4ызлн Л.Я,К«р£о«а ладлетса лАуч*э~зе*жмчесте
о 6 ал ужклвим© х*м»ч^о«о* крошолвляссти Р«е*уй**
к*.
По э^ааил*. соо*ш ехать *;**«* органов Уярдед*
ккя «л» во о »бств-вщ>Л *я*щга*ив« ok рвэр»3«*»~
влет полые мэходы ером.* годе* а а «ли *? решится
/лучат** су^еетяуик*©, арлашоди* экспорт1*м»
«weet свае Аналитические Огделодяе* xotopwv о$-
одулл* аисл гоеударст■?»**« у^эвдл»ж*д# * с »в«
Д«М1ЮМ Я.Э*И. * КОЛ]ГГРОУДАрС*АвАИЫ€ К Ч*С*1№*
об^е^лие*»!!. В Слжаком С убудем *р* И*сгж*?*»
Cy^yt оргаяизовеяы оя^тиые уо?«ю*хи, которые
лду* возможность пъев*ргву¥» к ро верке * аоау-
«шсдском ы*с«т«Се всякая ярооя*, вшщ«А ка
л асе р вторя* И «at «ту?» «л* л в поотлжл^вх^г в№
czHtyt для щучеввл»
О ходе р*€о* Явс*«/*а • вх сэдешмигчк
ж*Д4ШШ Сад ар*;*сг**лея Ц»Г.>*-РСНХ отчет.
ЯИРККТО*» tfwxmjrs*
Письмо А. Н. Баха о
деятельности и задачах института
им. Л. Я. Карпова
ного Хозяйства коммунист Карпов не
переставал работать. Один из последних документов,
вышедших из-под его руки, — написанная
карандашом записка о любимом его детище, о
лаборатории, о строительстве на Воронцовом поле
нынешнего здания института (это была самая
первая в Москве стройка после гражданской войны) *.
«20 декабря 1920 г.
т. Свердлову
Дорогой товарищ, очень Вас прошу,
ввиду того, что строит, работ по постройке
хим. лаборатории осталось совершенные
пустяки, сделать распоряжение по
Комгосору о разрешении химотделу его
средствами и его аппаратом окончить это дело.
Тем более, что главная часть работы вся
состоит из специального оборудования, в
котором Комгосору будет весьма трудно
разобраться.
т. Збарский дополнит необходимыми
объяснениями. Я чувствую себя лучше и
пожалуй проваляюсь недолго.
Цривет
Лев».
Из выступления академика А.
в 1935 г.
Н. БАХА
«...В наши лаборатории были привлечены
молодые силы. Эти силы оказались
довольно крупными.
...Именно с тех пор и стала развиваться:
работа в направлении физической химии.
Нам казалось, что все-таки под наше
производство надо подвести серьезную
научную базу. Мы считали, что физическая
химия это единственное средство овладеть
механикой химических производств. Надо
знать механизм химической реакции для
того, чтобы управлять им. В этом
направлении и велась наша работа. Институт
им. Карпова... несомненно стал одним из
ведущих институтов физической химии в
международном масштабе.
Мы не могли ограничиться тем, чтобы
взять две — три физико-химические
проблемы и разрабатывать их. Нам надо было
разрабатывать физическую химию во всех
ее отраслях.
И при этом мы, конечно, отдавали
много времени и требованиям
промышленности, требованиям прикладной химии.
...Мы с самого начала в полном согласии
с Львом Яковлевичем Карповым считали,
что наука едина. Ведь тогда не делили
науки на теоретическую и прикладную, а
считали, что есть наука и ее приложения...»
22 декабря 1922 года А. Н. БАХ
говорил на митинге, посвященном
основанию института:
«День открытия этого института для нас,
сотрудников его, является днем
чествования памяти его основателя Л. Я.
Карпова — одного из лучших людей, каких я
когда-либо встречал на своем жизненном
пути».
6
* Письма Л. Я. Карпова предоставлены
редакции А. С. Карповой. Записка адресована
В. М. Свердлову — руководителю
научно-технического отдела ВСНХ. «Комгосор» — Комитет
государственных сооружений.
За полвека своего существования Институт
сделал неоценимый вклад в советскую науку, в
строительство нового общества. О сегодняшнем
дне института журнал расскажет в одном из
следующих номеров.
ЭЛЕМЕНТ №
К А. КАПУСТИНСКАЯ,
научный сотрудник
Института минералогии,
геохимии и
кристаллохимии
редких элементов
БЕРИЛЛИЙ
Прежде всего — несколько (их может быть
гораздо больше!) ответов на вопрос: «Что
может нам дать бериллий?»
...Самолет, вес которого вдвое меньше
обычного;
...ракетное топливо с наивысшим
удельным импульсом (мощность на единицу
веса);
...пружины, способные выдержать до
20 миллиардов (!) циклов нагрузки —
пружины, не знающие усталости, практически
вечные.
А еще в начале нашего века в
справочниках и энциклопедиях о бериллии
говорилось: «Практического применения не
имеет». Открытый еще в конце XVIII века
бериллий сто с лишним лет оставался
«безработным» элементом, хотя химикам уже
были известны его уникальные и очень
полезные свойства. Для того, чтобы эти
свойства перестали быть «вещью в себе»,
требовался определенный уровень развития
науки и техники. В тридцатых годах
академик А. Е. Ферсман называл бериллий
металлом будущего. Сейчас о бериллии
можно и должно говорить как о металле
настоящего.
НЕДОРАЗУМЕНИЕ С ПЕРИОДИЧЕСКОЙ
СИСТЕМОЙ
История элемента № 4 началась с того, что
его долго не могли открыть. Многие
химики XVIII века анализировали берилл
(основной минерал бериллия), но никто из
них не смог обнаружить в этом минерале
нового элемента.
Даже современному химику,
вооруженному фотометрическим,
полярографическим, радиохимическим, спектральным,
радиоактивационным и флуориметриче-
ским методами анализа, нелегко выявить
Французский химик Луи
Никола Воклен A763—1829) —
первооткрыватель бериллия и
хрома
этот элемент, словно прячущийся за спину
алюминия и его соединений,— настолько
похожи их признаки. Первым
исследователям бериллия приходилось, разумеется,
гораздо труднее.
Но вот в 1798 году французский химик
Луи Никола Воклен, занимаясь
сравнительным анализом берилла и изумруда,
открыл в них неизвестный окисел —
«землю». Она была очень похожа на окись
алюминия (глинозем), однако Воклен
заметил и отличия. Окисел растворялся в
углекислом аммонии (а окись алюминия не
растворяется); сернокислая соль нового
элемента не образовывала квасцов с
сернокислым калием (а сернокислая соль
алюминия такие квасцы образует). Именно
этой разницей в свойствах Воклен и
воспользовался для разделения окислов
алюминия и неизвестного элемента.
Редакция журнала «Annales de chimie»,
опубликовавшего работу Воклена, предложила
для открытой им «земли» название
«глицина» (от греческого tvuxus — сладкий) из-
за сладкого вкуса ее солей. Однако
известные химики М. Клапрот и А. Экеберг сочли
это название неудачным, так как соли
иттрия также имеют сладковатый вкус. В их
работах «земля», открытая Вокленом,
называется берилловой. Тем не менее, в
научной литературе XIX века, вплоть до
шестидесятых годов, элемент № 4 сплошь и
рядом называется «глицием», «глицинием»
или «глюцинием». Ныне это название
сохранилось только во Франции. Интересно
отметить, что с предложением
называть элемент № 4 бериллием еще в
1814 году выступал харьковский
профессор Ф. И. Гизе.
Окисел был получен, но еще долгое
время никому не удавалось выделить
бериллий в чистом виде. Только через
тридцать лет Ф. Велер и А. Бюсси получили
немного порошкообразного металла
действием металлического калия на хлористый
бериллий, но металл этот содержал много
примесей. Прошло еще почти семьдесят
лет, прежде чем П. Лебо смог получить
(в 1898 г.) чистый бериллий электролизом
бериллиевофтористого натрия.
Сходство бериллия с алюминием
принесло немало хлопот и автору
Периодического закона Д. И. Менделееву. Именно
из-за этого сходства в середине прошлого
века бериллий считали трехвалентным
элементом с атомным весом 13,5. Но,
будучи помещен в таблице между углеродом и
азотом, как того требовал его атомный вес,
бериллий вносил полную путаницу в
закономерное изменение свойств элементов-
Это было серьезной угрозой
Периодическому закону. Однако Д. И. Менделеев
был уверен в правильности открытой им
закономерности и доказывал, что атомный
вес бериллия определен неверно, что
бериллий должен быть не трехвалентным, а
двухвалентным элементом «с
магнезиальными свойствами». Исходя из этого,
Менделеев поместил бериллий во вторую
группу Периодической системы вместе с
двухвалентными щелочноземельными
металлами, исправив его атомный вес на 9.
Первое подтверждение своих взглядов
Менделеев нашел в одной из
малоизвестных работ русского химика И. В. Авдеева,
который считал, что окись бериллия
химически подобна окиси магния. А в конце
семидесятых годов прошлого века шведские
химики Ларе Фредерик Нильсон и Отто
Петерсон (некогда бывшие самыми ярыми
сторонниками мнения о трехвалентном бе-
8
риллии), повторно определив атомный вес
бериллия, нашли его равным 9,1*.
Так бериллий, бывший первым камнем
преткновения на пути Периодического
закона, только подтвердил его всеобщность.
Благодаря Периодическому закону, стало
более четким понятие о физической и
химической сущности бериллия. Образно
говоря, бериллий получил, наконец, свой
«паспорт».
Сейчас бериллием интересуются люди
многих профессий. В каждой из них —
свой подход к элементу № 4, своя «берил-
лиевая» проблематика.
БЕРИЛЛИЙ С ТОЧКИ ЗРЕНИЯ
ГЕОЛОГА
Типично редкий элемент. На тонну
земного вещества в среднем приходится лишь
3,5 грамма бериллия. Это, конечно, очень
немного, но и не так уж мало, если
вспомнить, например, что такого известного
элемента, как свинец, на Земле вдвое меньше
бериллия. Обычно бериллий встречается
как незначительная примесь в различных
минералах земной коры. И лишь
ничтожная часть земного бериллия
сконцентрирована в собственных бериллиевых
минералах. Их известно более 30, но только шесть
из них считаются более или менее
распространенными (берилл, хризоберилл, берт-
рандит, фенакит, гельвин, даналит).
А серьезное промышленное значение
приобрел пока только один берилл, известный
человеку с глубокой древности.
Бериллы встречаются в гранитных
пегматитах, имеющихся почти во всех
странах земного шара. Это красивые
зеленоватые кристаллы, достигающие иногда
очень больших размеров; известны
бериллы-гиганты весом до тонны и длиной до
9 метров.
К сожалению, пегматитовые
месторождения очень малы, и добывать там берилл
в широких промышленных масштабах не
удается. Однако есть и другие источники
бериллия, в которых его концентрация
гораздо выше. Это так называемые пневма-
* В «Химии и жизни» A965, № 7—8, стр. 155)
опубликовано письмо Л. Ф. Нильсона Д. И.
Менделееву от 17 апреля 1884 года, в котором
шведский ученый сообщает об экспериментальном
подтверждении предсказанного Менделеевым
атомного веса бериллия.
то-гидротермальные месторождения (т. e.j
месторождения, образовавшиеся в
результате взаимодействия
высокотемпературных паров и растворов с определенными
типами горных пород).
Природный бериллий состоит из
единственного устойчивого изотопа Be9.
Интересно, что бериллий — единственный
элемент периодической системы, имеющий
при четном номере всего один стабильный
изотоп. Известны еще несколько
нестабильных, радиоактивных изотопов
бериллия. (О двух из них — Be10 и Be7 — будет
сказано ниже.)
БЕРИЛЛИЙ С ТОЧКИ ЗРЕНИЯ
МЕТАЛЛУРГА
Свойства бериллия чаще всего именуются
«удивительными», «чудесными» и т. п.
Отчасти это справедливо, причем главная
«удивительность» заключается в
сочетании противоположных, иногда, казалось
бы, взаимоисключающих свойств.
Бериллий обладает одновременно и легкостью,
и прочностью, и теплостойкостью. Этот
металл серебристо-серого цвета в полтора
раза легче алюминия и в то же время
прочнее специальных сталей. Особенно
важно, что бериллий и многие его сплавы
не утрачивают полезных свойств при
температуре 700—800° С и могут работать в
таких условиях.
Чистый бериллий очень тверд — им
можно резать стекло. К сожалению,
твердости сопутствует хрупкость.
Бериллий очень устойчив против
коррозии. Как и алюминий, он покрывается
при взаимодействии с воздухом тонкой
окисной пленкой, защищающей металл от
действия кислорода даже при высоких
температурах. Лишь за порогом 800°С идет
окисление бериллия в массе, а при
температуре 1200°С металлический бериллий
сгорает, превращаясь в белый порошок
ВеО.
Бериллий легко образует сплавы со
многими металлами, придавая им
большую твердость, прочность, жаростойкость
и коррозионную стойкость. Один из его
сплавов — бериллиевая бронза — это
материал, позволивший решить многие
сложные технические задачи.
Бериллиевыми бронзами называют
сплавы меди с 1—3% бериллия. В отличие
от чистого бериллия они хорошо поддают-
2 Химия и Жизнь, № 2
ся механической обработке, из них можно,
например, изготовить ленты толщиной
всего 0,1 мм. Разрывная прочность этих
бронз больше, чем у многих легированных
сталей. Еще одна примечательная деталь:
с течением времени большинство
материалов, в том числе и металлы, «уетают» и
теряют прочность. Бериллиевые бронзы —
наоборот. При старении их прочность
возрастает! Они немагнитны. Кроме того, они
не искрят при ударе. Из них делают
пружины, рессоры, амортизаторы,
подшипники, шестерни и многие другие изделия, от
которых требуются большая прочность,
хорошая сопротивляемость усталости и
коррозии, сохранение упругости в
широком интервале температур, высокие
электро- и теплопроводные характеристики.
Одним из потребителей этого сплава стала
авиационная промышленность:
утверждают, что в современном тяжелом самолете
насчитывается больше тысячи деталей из
бериллиевой бронзы.
Добавки бериллия облагораживают
сплавы на основе алюминия и магния. Это
понятно: удельный вес бериллия всего
1,82 г/см3, а температура плавления —
вдвое выше, чем у этих металлов. Самые
небольшие количества бериллия
(достаточно 0,005%) намного уменьшают потери
магниевых сплавов от горения и окисления
при плавке и литье. Одновременно
улучшается качество отливок, значительно
упрощается технология.
Выяснилось, что с помощью бериллия
можно увеличивать прочность, жесткость
и жаростойкость других металлов, не
только вводя его в те или иные сплавы. Чтобы
предотвратить быстрый износ стальных
деталей, их иногда бериллизуют —
насыщают их поверхность бериллием путем
диффузии. Делается это так: стальную
деталь опускают в бериллиевый порошок и
выдерживают в нем при 900—1100°С в
течение Ю—15 часов. Поверхность детали
покрывается твердым химическим
соединением бериллия с железом и углеродом.
Этот прочный панцирь толщиной всего
0,15—0,4 мм придает деталям
жаростойкость и устойчивость к морской воде и
азотной кислоте.
Интересными свойствами отличаются и
бериллиды — интерметаллические
соединения бериллия с танталом, ниобием,
цирконием и другими тугоплавкими
металлами. Бериллиды обладают исключительной
твердостью и стойкостью против
окисления. Лучшей технической
характеристикой бериллидов служит тот факт, что они
могут проработать более 10 часов при
температуре 1650°С.
БЕРИЛЛИЙ С ТОЧКИ ЗРЕНИЯ
ФИЗИКА
В истории многих элементов есть особые
вехи — открытия, после которых значение
этих элементов неизмеримо возрастает.
В истории бериллия таким событием стало
открытие нейтрона.
В начале 30-х годов немецкие физики
В. Боте и Г. Беккер, бомбардируя
бериллий альфа-частицами, заметили так
называемое «бериллиевое излучение» — очень
слабое, но чрезвычайно проникающее.
Оно, как было доказано позже, оказалось
потоком нейтронов. А еще позже это
свойство бериллия легло в основу «нейтронных
пушек» — источников нейтронов,
применяемых в разных областях науки и
техники.
Так было положено начало изучению
атомной структуры бериллия.
Выяснилось, что его отличают малое сечение
захвата нейтронов и большое сечение их
рассеяния. Иными словами, бериллий (а
также его окись) рассеивает нейтроны,
изменяет направление их движения и
замедляет их скорость до таких величин, при
которых цепная реакция может протекать
более эффективно. Из всех твердых
материалов бериллий считается лучшим
замедлителем нейтронов.
Кроме того, бериллий может выполнять
роль отражателя нейтронов: менять их
направление, возвращать нейтроны в
активную зону реактора, противодействовать
их утечке. Бериллию свойственна также
значительная радиационная стойкость,
сохраняющаяся и при очень высокой
температуре.
На всех этих свойствах основано
применение бериллия в атомной технике — он
один из самых необходимых ей элементов.
Замедлители и отражатели из бериллия
и его окиси позволяют намного уменьшить
размеры активной зоны реакторов,
увеличить рабочую температуру и эффективнее
использовать ядерное топливо. Поэтому,
несмотря на высокую стоимость бериллия,
его использование считают экономически
оправданным, особенно в небольших
энергетических реакторах для самолетов и
морских судов.
Окись бериллия стала основным
материалом для оболочек тепловыделяющих
элементов (твэлов) атомных реакторов.
В твэлах особенно велика плотность
нейтронного потока, самая высокая
температура, самые большие напряжения и
коррозионная активность. Поскольку уран
коррозионно неустойчив и недостаточно
прочен, его приходится защищать
специальными оболочками, как правило,— из
ВеО.
Большая теплопроводность (в 7 раз
выше, чем у стали), большая теплоемкость
и жаропрочность позволяют использовать
бериллий и его соединения в
теплозащитных конструкциях космических кораблей.
Из бериллия была сделана внешняя
тепловая защита капсулы космического
корабля «Фрэндшип-7», на котором Джон
Гленн первым из американских
космонавтов совершил (после Юрия Гагарина и
Германа Титова) орбитальный полет.
1. Установка для получения
металлического бериллия
электролизом ВеС12: 1 —
графитовый анод, 2 — отверстие для
удаления расплавленных
хлоридов, 3 — асбестовая
прокладка, 4 — никелевый
тигель, 5 — электрическая
печь, 6 — изолятор
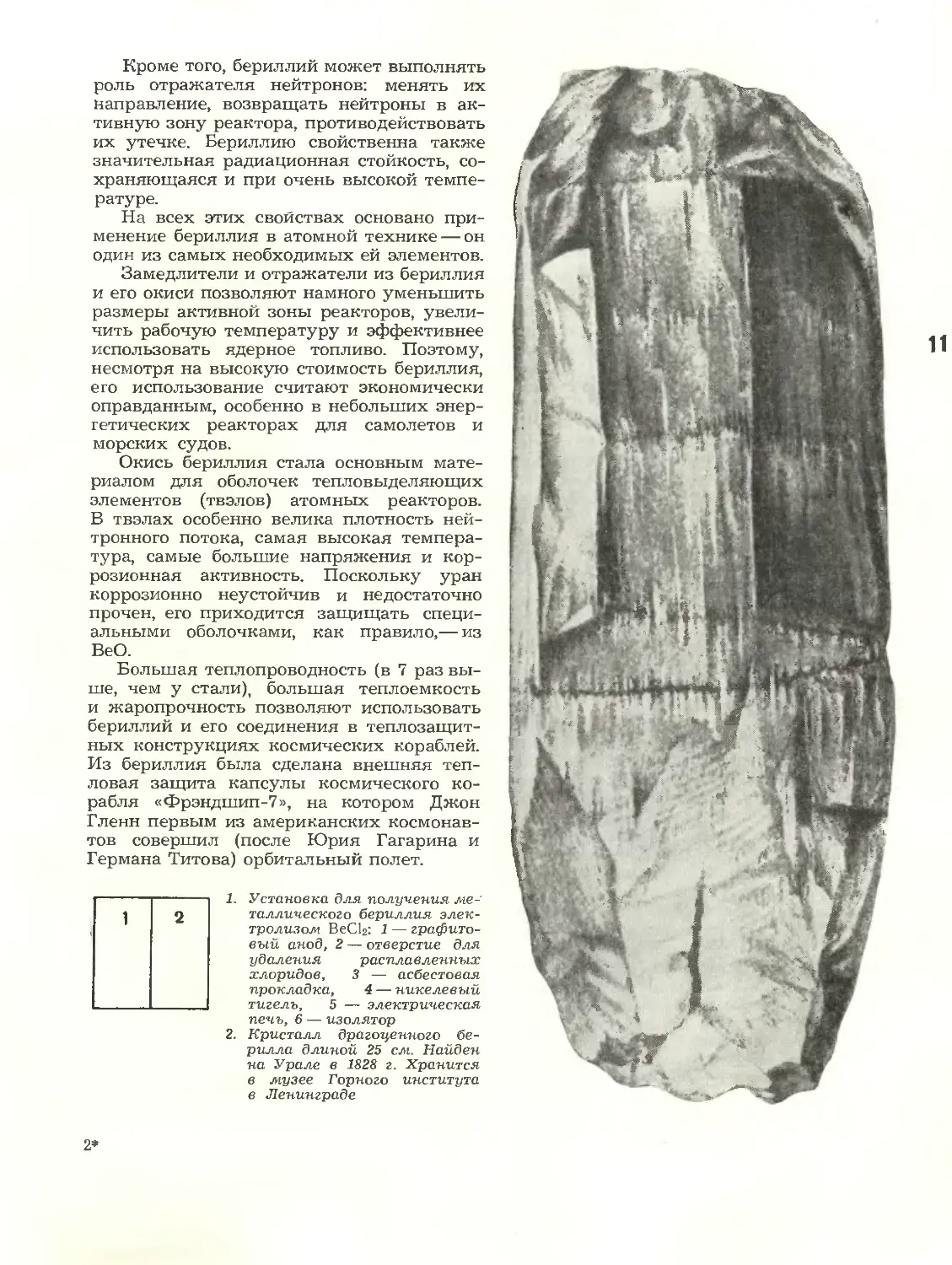
2. Кристалл драгоценного
берилла длиной 25 см. Найден
на Урале в 1828 г. Хранится
в музее Горного института
в Ленинграде
1
2
2*
В еще большей мере космическую
технику привлекают в бериллии легкость,
прочность, жесткость, и особенно —
необыкновенно высокое отношение
прочности к весу. Благодаря способности
сохранять высокую точность и стабильность
размеров, бериллиевые детали
используют в гироскопах — приборах, входящих в
систему ориентации и стабилизации ракет,
космических кораблей и искусственных
спутников Земли.
Элемент № 4 применяется и в других
областях современной техники, в том
числе в радиоэлектронике. В частности,
керамика на основе окиси бериллия стала
материалом корпусов так называемых «ламп
бегущей волны» ■— очень эффективных
радиоламп, не утративших своего значения
под натиском полупроводников.
Рентгенотехнике металлический
бериллий дал прекрасные окна для
рентгеновских трубок: благодаря малому атомному
весу, он пропускает в 17 раз больше
мягких рентгеновских лучей, чем алюминий
такой же толщины.
БЕРИЛЛИИ С ТОЧКИ ЗРЕНИЯ
ХИМИКА
Типично амфотерен, т. е. обладает
свойствами и металла, и неметалла. Однако
металлические свойства все же преобладают.
С водородом бериллий не реагирует
даже при нагревании до 1000°С, зато он
легко соединяется с галогенами, серой и
углеродом. Из галогенидов бериллия
наибольшее значение имеют его фторид и
хлорид, используемые в процессе
переработки бериллиевых руд.
Бериллий хорошо растворяется во всех
минеральных кислотах, кроме, как это
ни странно, азотной. От нее, как и от
кислорода, бериллий защищен окисной
пленкой.
Окись бериллия (ВеО) обладает
ценными свойствами и в некоторых случаях
конкурирует с самим бериллием.
Высокая тугоплавкость (температура
плавления 2570°С), малая упругость паров
при температуре плавления, значительная
химическая стойкость и большая
теплопроводность позволяют применять окись
бериллия во многих отраслях техники, в
частности, для футеровки бессердечнико-
вых индукционных печей и тиглей для
плавки различных металлов и сплавов.
Интересно, что окись бериллия
совершенно инертна по отношению к
металлическому бериллию. Это единственный
материал, из которого изготовляют тигли для
плавки бериллия в вакууме.
Сравнительно давно используют окись
бериллия в производстве стекла. Добавки
ее увеличивают плотность, твердость,
показатель преломления и химическую
стойкость стекол. С помощью окиси бериллия
создают специальные стекла, обладающие
большой прозрачностью для
ультрафиолетовых и инфракрасных лучей.
Стекловолокно, в состав которого
входит окись бериллия, может найти
применение в конструкциях ракет и подводных
лодок.
При горении бериллия выделяется
много тепла — 15 000 ккал на килограмм.
Поэтому бериллий может быть
компонентом высокоэнергетического ракетного
горючего. В частности, топливо с присадкой
бериллия предполагали применить для
посадки на Луну аппарата «Сервейор».
Некоторые соединения бериллия
служат катализаторами химических
процессов. С щелочами бериллий реагирует,
образуя соли-бериллаты, подобные
алюминатам. Многие из них имеют сладковатый
вкус, но пробовать на язык их не стоит —
почти все бериллаты ядовиты.
Многие ученые считают, что изотопы
бериллия Be10 и Be7 образуются не в
недрах земли, а в атмосфере — в результате
воздействия космических лучей на ядра
азота и кислорода. Незначительные
примеси этих изотопов обнаружены в дожде,
снеге, воздухе, в метеоритах и морских
отложениях.
Однако, если собрать воедино весь Be10,
находящийся в атмосфере, водных
бассейнах, почве и на дне океана, то получится
довольно внушительная цифра — около
800 тонн.
Изотоп Be10 (период полураспада
2,5-106 лет) представляет исключительный
интерес для геохимии и ядерной
метеорологии. Рождаясь в атмосфере, на высоте
примерно 25 км, атомы Be10 вместе с
осадками попадают в океан и оседают на дне.
Зная концентрацию Be10 во взятой со дна
пробе и период полураспада этого изотопа,
можно вычислить возраст любого слоя на
дне океана.
Бериллий-10 аккумулируется также в
морских илах и ископаемых костях (кости
сорбируют бериллий из природных вод).
В связи с этим возникло предположение
о возможности определения возраста
органических остатков по Be10. Дело в том, что
довольно широко освоенный
радиоуглеродный метод непригоден для определения
возраста образцов в интервале 105—108 лет
(из-за большой разницы между периодами
полураспада С14 и долгоживущих
изотопов (К40, Rb82, Th232, U235 и U238). Изотоп
Be10 как раз «заполняет» этот разрыв.
Жизнь другого радиоизотопа — берил-
лия-7 значительно короче: период его
полураспада равен всего 53 дням. Поэтому
неудивительно, что количество его на
Земле измеряется граммами. Изотоп Be7
может быть получен и в циклотроне, но это
дорого обойдется. Поэтому широкого
применения этот изотоп не получил. Его
используют иногда для прогнозирования
погоды. Он выполняет роль своеобразной
«метки» воздушных слоев: наблюдая
изменение концентрации Be7, можно
определить промежуток времени от начала
движения воздушных масс. Еще реже
применяют Be7 в других исследованиях:
химики — в качестве радиоактивного
индикатора, биологи — для изучения
возможностей борьбы с токсичностью самого
бериллия.
БЕРИЛЛИЙ С ТОЧКИ ЗРЕНИЯ
БИОЛОГА И МЕДИКА
Бериллий обнаружен в растениях,
произрастающих на бериллийсодержащих
почвах, а также в тканях и костях животных.
Но если для растения бериллий безвреден,
то у животных он вызывает так
называемый «бериллиевый рахит». Повышенное
содержание солей бериллия в пище
способствует образованию в организме
растворимого фосфата бериллия. Постоянно
«похищая» фосфаты, бериллий тем самым
способствует ослаблению костной ткани —
это и есть причина болезни.
Многие соединения бериллия ядовиты.
Они могут стать причиной
воспалительных процессов на коже и бериллиоза —
специфического заболевания, вызываемого
вдыханием бериллия и его соединений.
При кратковременном вдыхании больших
концентраций растворимых соединений
бериллия возникает острый бериллиоз,
представляющий собой раздражение
дыхательных путей, иногда сопровождающееся
отеком легких и удушьем. Есть и
хроническая разновидность бериллиоза. Для нее
характерны менее резкие симптомы, но
большие нарушения в функциях всего
организма.
Допустимые пределы содержания
бериллия в воздухе очень малы — всего
одна тысячная доля микрограмма на
кубический метр. Это значительно меньше
допустимых норм для большинства
металлов, даже таких токсичных, как свинец.
Для лечения бериллиоза применяют
чаще всего химические соединения,
связывающие ионы бериллия и способствующие
их выведению из организма.
ТРИ «НО» БЕРИЛЛИЯ
Эта глава не означает, что все
предыдущее — только «теория». Но, к сожалению,
факторы, ограничивающие применение
бериллия, вполне реальны, и не учитывать
их нельзя.
Это, прежде всего, хрупкость металла.
Она намного усложняет процесс его
механической обработки, затрудняет получение
больших листов бериллия и сложных
профилей, необходимых в тех или иных
конструкциях. Предпринимаются упорные
попытки устранить этот недостаток. Но,
несмотря на некоторые успехи (изготовление
металла высокой чистоты, различные
технологические усовершенствования),
получение пластичного бериллия продолжает
оставаться трудной проблемой.
Второе — токсичность бериллия.
Тщательный контроль за чистотой
воздуха, особые системы вентиляции,
возможно большая автоматизация производства —
все это позволяет успешно бороться с
токсичностью элемента № 4 и его соединений.
И, наконец, третье и очень важное «но»
бериллия — его высокая стоимость. Цена
одного килограмма бериллия в США
сейчас равняется 136 долларам, то есть
бериллий в несколько раз дороже титана.
Однако рост потребления всегда
приводит к технологическим
усовершенствованиям, которые, в свою очередь,
способствуют уменьшению издержек
производства и цены. За последние пятнадцать лет
в связи с развитием атомной, авиационной
и ракетной техники цены на бериллий
значительно снизились. В будущем спрос на
бериллий возрастет еще больше: ведь этот
металл человечество начало применять
лишь тридцать пять лет назад. И,
конечно, достоинства элемента № 4 возьмут
верх над его недостатками.
3SSX ТОЛЬКО ФАКТЫ
ДРАГОЦЕННЫЕ
БЕРИЛЛЫ
Основной минерал бериллия —
берилл относится, как известно, к
полудрагоценным камням. Но
когда говорят о четырех его
разновидностях — изумруде,
аквамарине, воробьевите и гелиодоре,
то приставку «полу» отбрасывают.
Изумруды, особенно весом
больше пяти каратов, ценятся дороже
бриллиантов.
Чем отличаются эти камни от
обычного берилла? Ведь
формула их та же — А12Ве3 (SieOis). Но
эта формула не учитывает
примесей, которые, собственно, и
превращают полудрагоценные
камни в драгоценные. Аквамарин
окрашен ионами двухвалентного
железа, в изумруде (он же
смарагд), кроме Fe2+, есть
незначительная примесь окиси хрома.
Розовый цвет воробьевита
объясняется примесью соединений
цезия, рубидия и двухвалентного
марганца, а золотисто-желтый
гелиодор окрашен ионами
трехвалентного железа.
ДРАГОЦЕННЫЙ МЕТАЛЛ
ИЗ ПОЛУДРАГОЦЕННОГО
КАМНЯ
Высокая стоимость бериллия
объясняется не только
ограниченностью сырьевых ресурсов, но
и сложностями технологии
получения чистого металла. Основной
метод производства бериллия —
восстановление его фторида
металлическим магнием. Фторид
получают из гидроокиси, а
гидроокись из бериллового
концентрата. Уже первый прогон этой
технологической лестницы состоит
из нескольких ступеней:
концентрат подвергают термообработке,
измельчению, затем на него
последовательно действуют серной
кислотой, водой, растворами
аммиака и едкого натра,
специальными комплексообразова-
телями.
Получившийся бериллат натрия
гидролизуют, и на центрифуге
отделяют гидроокись.
Гидроокись превращается во
фторид тоже лишь после
нескольких операций, каждая из
которых достаточна сложна и
трудоемка. Восстановление
магнием идет при температуре 900°С,
ход процесса тщательно
контролируется. Важная деталь: тепло,
выделяющееся в реакции,
поглощается с той же скоростью, что
и выделяется. Полученный
жидкий металл выливают в
графитовые изложницы, но он
загрязнен шлаком, и поэтому его еще
раз переплавляют в вакууме.
БЕРИЛЛИЙ В БЫТУ
Сферы применения бериллия не
ограничиваются «высокой»
техникой. С изделиями из никель-бе-
риллиевых сплавов (содержание
Be не превышает 1,5%) можно
встретиться и в повседневной
жизни. Из этих сплавов
изготавливают хирургические инструменты,
иглы для подкожных инъекций,
литые металлические зубы. Из
сплава «Элинвар» (никель,
бериллий, вольфрам) в Швейцарии
делают пружины для часов.
ИСКУССТВЕННЫЕ
ИЗУМРУДЫ
Получить изумруды
искусственным путем гораздо труднее, чем
большинство других драгоценных
камней. Главная причина в том,
что берилл — сложное
комплексное соединение. Однако ученые
смогли имитировать природные
условия, в которых происходило
образование минерала: изумруды
«рождаются» при очень высоком
давлении A50 000 атм) и высокой
температуре A550°С).
Искусственные изумруды могут использо^
ваться в электронике.
БЕРИЛЛИЙ
И СВЕРХПРОВОДИМОСТЬ
Сейчас известно более тысячи
материалов, приобретающих при
температуре, близкой к
абсолютному нулю, свойство
сверхпроводимости. В их числе —
металлический бериллий. Будучи
сконденсирован в виде тонкой пленки
на холодную подложку, бериллий
становится сверхпроводником при
температуре около 8°
абсолютной шкалы.
БЕРИЛЛИЙ
В ЦЕЛЕБНОМ БАЛЬЗАМЕ
В 1964 году группа советских
химиков во главе с
вице-президентом Академии наук Таджикской
ССР, доктором химических наук
К. Т. Порошиным провела
химический анализ древнего
целебного бальзама мумие. Оказалось,
что это вещество — сложного
состава, причем в числе многих
элементов, содержащихся в
мумие, есть и бериллий *.
ГЕОГРАФИЯ
МЕСТОРОЖДЕНИЙ
БЕРИЛЛИЯ
Бериллиевое сырье имеется во
многих странах мира. Наиболее
крупные месторождения его на-
* Подробнее о мумие см.
«Химия и жизнь», 1965, № 9.
ходятся в Бразилии и Аргентине.
На их долю приходится
примерно 60% запасов берилловых руд
в капиталистических странах.
Значительные запасы бериллиевых
руд имеются также в США, ЮАР,
Южной Родезии, Индии, Маль-
гашской республике и Австралии.
Вплоть до последнего
времени крупнозернистый берилл
добывали вручную. В Бразилии
таким кустарным способом и
сейчас ежегодно добывается до
3 000 тонн концентрата.
Лишь недавно были
предложены новые методы флотации,
позволяющие использовать
нерентабельные ранее
месторождения мелкозернистого берилла.
КЕРАМИКА «БЕРИСЕР»
По сообщению французской
печати, фирма «Электрокерамик»
изготовила керамический
материал «берисер» путем обжига при
высокой температуре окиси
сверхчистого бериллия.
«Берисер» обладает
прекрасными электроизоляционными
свойствами, но проводит тепло
почти так же хорошо, как
серебро.
По мнению авторов открытия,
полученный ими материал найдет
широкое применение в специаль-
Восьмидесятые годы прошлого
века — время оживленных
научных споров об атомном весе
бериллия.
Д. И. Менделеев писал по
этому поводу:
«Недоразумение длилось
несколько лет. Не раз мне
приходилось слышать о том, что
вопрос об атомном весе бериллия
грозит поколебать общность
периодического закона, может
потребовать глубоких в нем
преобразований. В научном
ной теплорассеивающей
изоляции, в производстве
полупроводников и миниатюрных
электронных приборов. А благодаря
высокой огнеупорности и
химической инертности «берисер»
сможет быть использован для
изготовления тиглей для плавки урана,
тория и бериллия.
БЕРИЛЛИЙ
И «АТОМНАЯ ИГЛА»
Теплоизоляционные свойства
окиси бериллия могут пригодиться и
при исследовании земных глубин.
Так, существует проект взятия
разноречии, касающемся
бериллия, приняли участие
многие силы, конечно, потому
именно, что дело шло о
предмете более многозначительном,
чем атомность сравнительно
редкого элемента;
периодический закон разъяснялся в этих
разноречиях, и взаимная связь
элементов разных групп стала
более очевидной, чем было
когда-либо».
Долгое время главными
противниками двухвалентности
проб из мантии Земли с глубин
до 32 километров с помощью так
называемой «атомной иглы». Это
миниатюрный атомный реактор
диаметром всего 60 см. Реактор
должен быть заключен в
теплоизолирующий футляр из окиси
бериллия с тяжелым вольфрамовым
наконечником.
Принцип действия «атомной
иглы» заключается в следующем:
высокие температуры,
создаваемые в реакторе (свыше 1100°С),
вызовут плавление скальных
пород и продвижение реактора к
центру Земли. На глубине
примерно 32 км тяжелое
вольфрамовое острие должно отделиться, а
реактор, став более легким, чем
окружающие его породы, взяв
пробы с недостижимых пока
глубин, «всплывет» на
поверхность.
БЕРИЛЛИЙ —
ЛИТЕРАТУРНЫЙ ПЕРСОНАЖ
О бериллии написано много
научных трудов, как и о
большинстве других элементов. Но
элементу № 4 посвящено еще и
литературное произведение
«Ловушка для простаков», с
отрывками из которого можно
познакомиться в этом номере.
бериллия были шведские
химики профессора Л. Ф. Ниль-
сон и О. Петерсон. В 1878 году
они опубликовали статью
«О получении и валентности
ИЗ ДОКУМЕНТОВ ПРОШЛОГО
бериллия», в конце которой
были такие слова:
«...наше мнение об истинном
атомном весе и химической
природе этого металла
противоречит так называемому
периодическому закону, который
Менделеев предначертал для
всех элементов, а именно не
только потому, что при
бериллии, равном 13,8, металл этот
едва ли может быть помещен в
менделеевскую систему, но и
потому, что тогда элемент с
атомным весом 9,2, как это
требует периодический закон, в
системе отсутствовал бы и, по-
видимому, еще должен быть
открыт».
В защиту Периодического
закона выступил чешский
химик Богуслав Браунер,
считавший, что известный закон Дю-
лонга и Пти, которым пользо-
ТЕХНОЛОГИ, ВНИМАНИЕ!
МОЖНО
И БЕЗ ХОЛОДИЛЬНИКА
В последнее время стало
популярным глубокое анодирование
алюминиевых сплавов. Этот
способ дает возможность наносить
толстые пленки окиси, которые
хорошо полируются, плохо
проводят тепло и электричество,
устойчивы к коррозии. Вся беда
в том, что сейчас этот процесс
ведут при низкой температуре
и малых плотностях тока; значит,
скорость процесса невелика.
В Харьковском
политехническом институте им. В. И. Ленина
проведены опыты по глубокому
анодированию при температуре
15—20°С и более высоких
плотностях тока. Испытанию подверглись
алюминий и его сплавы —
литейные и ковочные. Результаты —
положительные: удалось,
например, упрочнить поверхность
поршней двигателей внутреннего
сгорания, и механический к.п.д.
двигателя увеличился на 4%.
Повались шведские химики,
имеет некоторые отступления
в области малых атомных
весов, к которой собственно и
относится бериллий. Кроме
того, Браунер советовал Нильсо-
ну и Петерсону определить
плотность паров хлористого
бериллия, считая, что
количественное определение этой
характеристики поможет точно
установить принадлежность
элемента к той или иной
группе Периодической системы.
Когда шведские химики
повторили свои опыты и проделали
то, что советовал им Браунер,
они убедились в правоте
Менделеева. В статье, отражавшей
результаты зтой работы, Ниль-
сон и Петерсон написали: «...мы
должны отказаться от ранее
защищавшегося нами мнения
о том, что бериллий трехва-
ТЕХНОЛОГИ, ВНИМАНИЕ!
лученную на детали пленку
пропитывали масляным коллоидным
графитом.
(«Журнал прикладной химии»,
1966, № 7)
КАК РЕЗАТЬ РЕАКТОР
При высоких температурах и
давлениях водород разрушает
стенки стальных реакторов. Он
обезуглероживает и разрыхляет
материал. Как проверить состояние
реактора? Твердость
поверхностных слоев ни о чем не говорит —
под ними могут быть рыхлые
слои. Можно вырезать сквозное
отверстие в стенке реактора; но
есть и более простой путь.
Достаточно вырезать конус глубиной
15 мм — а эту операцию можно
проделать ручной
электродрелью — и исследовать его на
прочность. Если все в порядке, —
углубление можно заварить и
продолжать работу. Если же
появляются какие-либо сомнения, то
лентный элемент...
Одновременно мы признаем правильность
периодического закона и в
этом важном случае».
В 1884 году Нильсон писал
Менделееву: «...не могу не
выразить Вам моего сердечного
поздравления по поводу того,
что и в этом случае, как и во
многих других, система
оправдала себя».
Позднее в «Основах химии»
Д. И. Менделеев сказал:
«Нильсон и Петерсон — одни из
главных защитников трехатомно-
сти бериллия... доставили
опытные доказательства в пользу
двухатомности бериллия и,
громко высказав это, показали,
что в науке истина, даже при
разноречиях, одинаково дорога
всем, хотя бы сперва и
отрицалась теми, кто ее утвердил».
ТЕХНОЛОГИ, ВНИМАНИЕ!
для проверки придется вырезать
образец по всей глубине стенки.
Такой способ контроля реакторов
предложили сотрудники ВНИИ
нефтехимических процессов.
(«Защита металлов», 1966, № 3)
НОВЫЙ КЕРАМИЧЕСКИЙ
МАТЕРИАЛ
Создан новый керамический
материал на основе окиси циркония.
Он получил название цирколит.
Это белый полупрозрачный
материал, похожий на матовое стекло,
но обладающий большой
термостойкостью. Образцы его
выдержали 260-часовые испытания при
температуре 2200°С.
Пока из цирколита
изготовляют детали размером не более
пяти сантиметров.
Незначительные отклонения в
технологическом процессе приводят к
значительному ухудшению
характеристик получаемого материала.
(«Science News», 1966, № 3)
В. М. КРОЛЬ,
Институт автоматики
и телемеханики АН СССР
ПРОБЛЕМЫ
И
МЕТОДЫ
СОВРЕМЕННОЙ
НАУКИ
СТРОИТЕЛЬНАЯ
ПЛОЩАДКА
ОРГАНИЗМА—
ЭМБРИОН
Одна из наиболее интригующих загадок
природы, с которой когда-либо
сталкивался человек,— развитие живого организма.
Мы как-то привыкли к тому, что живой
организм, обладающий огромным
количеством различных тканей и органов,
развивается из одной единственной клетки. Но
попробуйте представить эту проблему, так
сказать, заново.
Организм, где каждый орган находится
на строго предназначенном для него месте,
где многочисленные типы клеток,
организуясь вместе, создают самые различные
ткани; организм с его многообразной
деятельностью, от самовоспроизведения до
мыслительных процессов, сложнейший
живой организм — и одна клетка!
Другая сторона той же загадки
развития: как получается, что из поколения в
поколение у животных, принадлежащих
к одному и тому же виду, сохраняется
одинаковое строение тела? Почему,
например, животные, существующие сейчас,
мало чем отличаются от своих предков,
живших много веков назад? Почему
найденные при раскопках семена древних
растений — пшеницы, ячменя — очень
похожи на современные?
Яйцеклетки, принадлежащие
животным различных типов, на первый взгляд,
совершенно неотличимы одна от другой.
Тем не менее, в каждой из них
содержатся не только различные наборы
наследственных качеств, зашифрованных в моле-
О Химия и Жизнь. № 2
кулах ДНК хромосом *. Кроме этого в
яйцеклетке хранится огромное количество
«документации» о том, как эти качества
должны развиваться, по каким схемам и
правилам организм должен строить сам
себя, какие процессы должны произойти
раньше, а какие позже. Другими словами,
в яйцеклетке заключены сведения о всех
этапах развития организма. Как же это
развитие происходит?
ЯЙЦЕКЛЕТКА, ЕЕ СТРОЕНИЕ
И РАЗВИТИЕ
Проследим за изменениями (пока еще
далеко не все они известны науке), которые
претерпевает яйцеклетка в процессе
своего длительного роста и развития.
Как и всякая другая клетка, яйцеклетка
состоит из оболочки, ядра с набором
хромосом и окружающей его жидкой среды —
цитоплазмы. Размеры яйцеклеток, если
учитывать ту роль, которая возложена на
них природой, удивительно невелики. Так,
до начала своего развития диаметр
яйцеклетки лягушки — икринки — всего
17 микрон. Яйцеклетки млекопитающих
немного больше — 80—120 микрон.
* Эта сторона проблемы, вероятно, известна
читателю по многочисленным статьям и книгам
о генетике, появившимся в последние годы.
В «Химии и жизни», например, печатались
статьи «Наследственная информация: эстафета
жизни» A965, № 7—8), «Человек: генетика и
эволюция» A966, № 7).
Первые важные события происходят в
клетке, когда она еще не оплодотворена
и, так сказать, далека от мысли о делении.
Созревание начинается с синтеза в
различных частях яйцеклетки белков, жиров,
нуклеиновых кислот. Увеличивается
кислородный обмен. Яйцеклетка усиленно
поглощает из окружающей среды сложные
молекулы, синтезируемые в других частях
организма. Все это приводит к тому, что
размеры ее гигантски растут. Объем
яйцеклетки лягушки увеличивается, например,
в 1 600 000 раз — зрелая икринка достигает
2000 микрон, т. е. 2 мм в диаметре.
Но самое важное событие,
происходящее во время созревания яйцеклетки,—
очень точное и упорядоченное
перераспределение вещества в ней, появление ярко
выраженной полярности. Ядро
передвигается к так называемому верхнему полю-
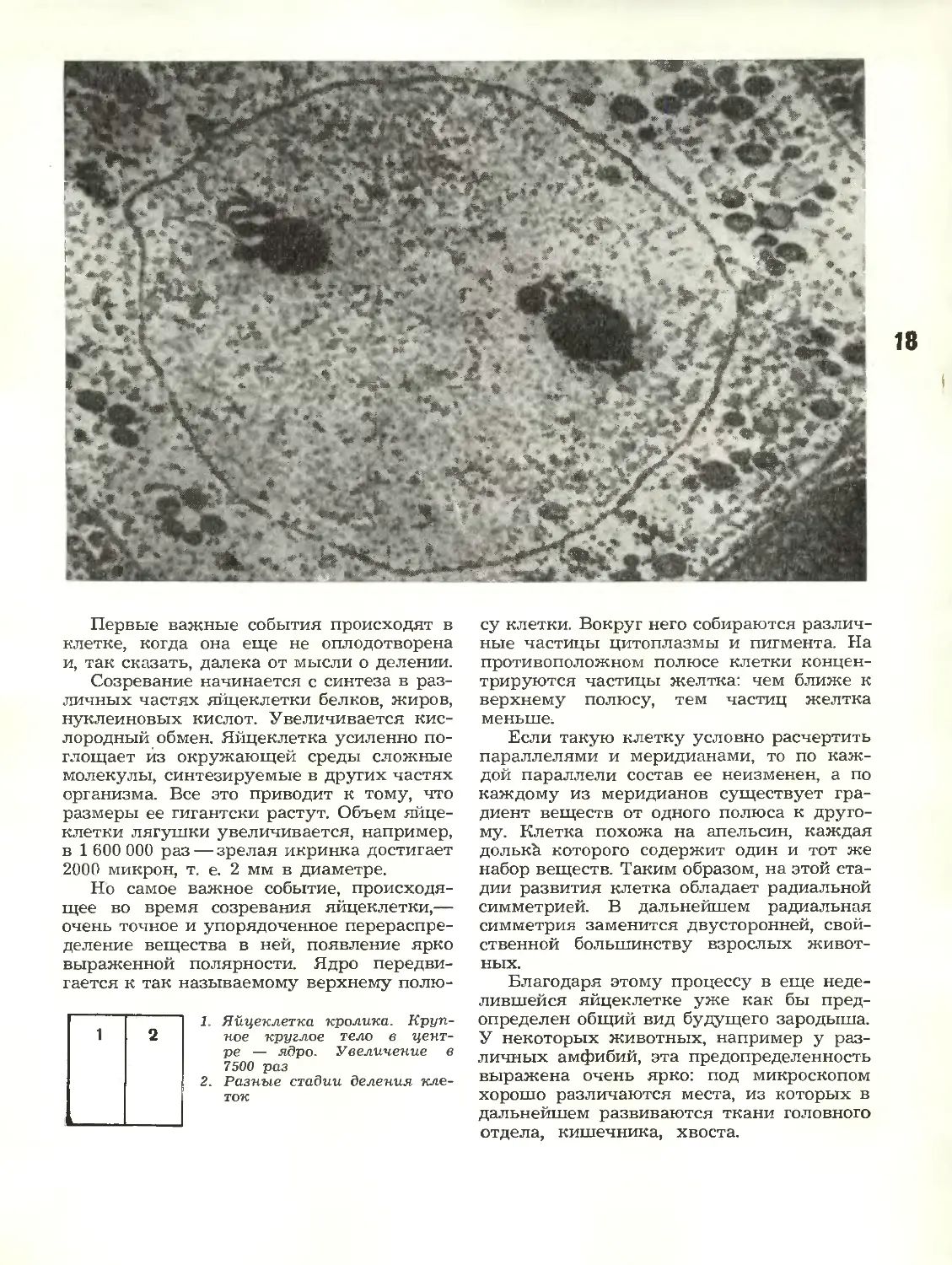
1. Яйцеклетка кролика.
Крупное круглое тело в
центре — ядро. Увеличение в
7500 раз
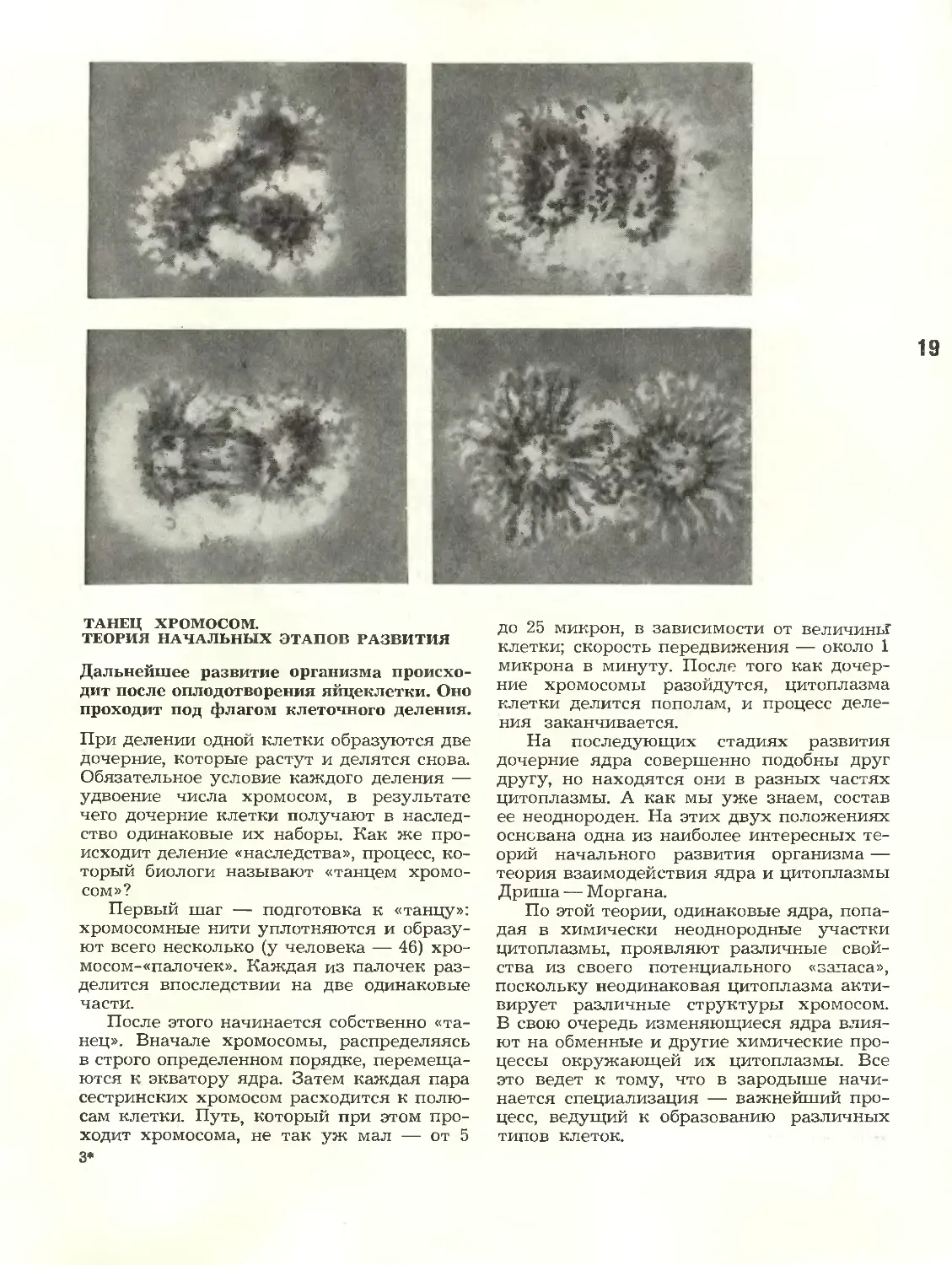
2. Разные стадии деления
клеток
1
1
2
су клетки. Вокруг него собираются
различные частицы цитоплазмы и пигмента. На
противоположном полюсе клетки
концентрируются частицы желтка: чем ближе к
верхнему полюсу, тем частиц желтка
меньше.
Если такую клетку условно расчертить
параллелями и меридианами, то по
каждой параллели состав ее неизменен, а по
каждому из меридианов существует
градиент веществ от одного полюса к
другому. Клетка похожа на апельсин, каждая
долька которого содержит один и тот же
набор веществ. Таким образом, на этой
стадии развития клетка обладает радиальной
симметрией. В дальнейшем радиальная
симметрия заменится двусторонней,
свойственной большинству взрослых
животных.
Благодаря этому процессу в еще неде-
лившейся яйцеклетке уже как бы
предопределен общий вид будущего зародыша.
У некоторых животных, например у
различных амфибий, эта предопределенность
выражена очень ярко: под микроскопом
хорошо различаются места, из которых в
дальнейшем развиваются ткани головного
отдела, кишечника, хвоста.
*UI,"^'( .'^
ТАНЕЦ ХРОМОСОМ.
ТЕОРИЯ НАЧАЛЬНЫХ ЭТАПОВ РАЗВИТИЯ
Дальнейшее развитие организма
происходит после оплодотворения яйцеклетки. Оно
проходит под флагом клеточного деления.
При делении одной клетки образуются две
дочерние, которые растут и делятся снова.
Обязательное условие каждого деления —
удвоение числа хромосом, в результате
чего дочерние клетки получают в
наследство одинаковые их наборы. Как же
происходит деление «наследства», процесс,
который биологи называют «танцем
хромосом»?
Первый шаг — подготовка к «танцу»:
хромосомные нити уплотняются и
образуют всего несколько (у человека — 46) хро-
мосом-«палочек». Каждая из палочек
разделится впоследствии на две одинаковые
части.
После этого начинается собственно
«танец». Вначале хромосомы, распределяясь
в строго определенном порядке,
перемещаются к экватору ядра. Затем каждая пара
сестринских хромосом расходится к
полюсам клетки. Путь, который при этом
проходит хромосома, не так уж мал — от 5
3*
до 25 микрон, в зависимости от величиньГ
клетки; скорость передвижения — около 1
микрона в минуту. После того как
дочерние хромосомы разойдутся, цитоплазма
клетки делится пополам, и процесс
деления заканчивается.
На последующих стадиях развития
дочерние ядра совершенно подобны друг
другу, но находятся они в разных частях
цитоплазмы. А как мы уже знаем, состав
ее неоднороден. На этих двух положениях
основана одна из наиболее интересных
теорий начального развития организма —
теория взаимодействия ядра и цитоплазмы
Дриша — Моргана.
По этой теории, одинаковые ядра,
попадая в химически неоднородные участки
цитоплазмы, проявляют различные
свойства из своего потенциального «запаса»,
поскольку неодинаковая цитоплазма
активирует различные структуры хромосом.
В свою очередь изменяющиеся ядра
влияют на обменные и другие химические
процессы окружающей их цитоплазмы. Все
это ведет к тому, что в зародыше
начинается специализация — важнейший
процесс, ведущий к образованию различных
типов клеток.
Теорию Дриша — Моргана
подтверждают изящные опыты с хромосомами
развивающихся личинок насекомых. На нитях
хромосом, в структуре которых, как
известно, и зашифрована вся наследственная
информация организма, через
определенные интервалы сидят
утолщения—«бусинки», так называемые хромомеры.
Число хромомеров примерно равно количеству
предполагаемых генов клетки. (Напомним,
что геном называют наследственную
структуру, определяющую в общих чертах
развитие какого-то определенного признака
организма.)
Когда личинка развивается, «бусинки»-
^сромомеры ведут себя по-разному. На
одних этапах развития начинают свою
деятельность одни из них, на других —
другие. Порядок, по которому хромомеры
включаются в работу, строго определен и
зависит только от стадии развития. Как
только хромомер начинает «работать»,
меняется его внешний вид: активные
хромомеры похожи не на «бусинки», а скорее
на огромные кольца или вздутия.
Оказалось, что если ядра из клеток уже
развитых личинок осторожно перенести в
клетки более молодых зародышей, т. е.
окружить эти ядра другой цитоплазмой, то
прежние вздутия хромомеров исчезают.
Появляются новые, соответствующие тому
этапу развития, на котором находится
второй, более молодой, зародыш. Но другой
опыт показывает, что влияние цитоплазмы
на ядро в целом необратимо, особенно на
поздних стадиях развития. Если ядро из
клетки зародыша лягушки (на ранней
стадии развития) перенести в клетку совсем
другого зародыша, находящегося тоже в
самом начале своего развития, то
вырастает нормальный головастик. Но если ядро
из клетки зародыша, уже прошедшего
сравнительно долгий путь развития, пере-
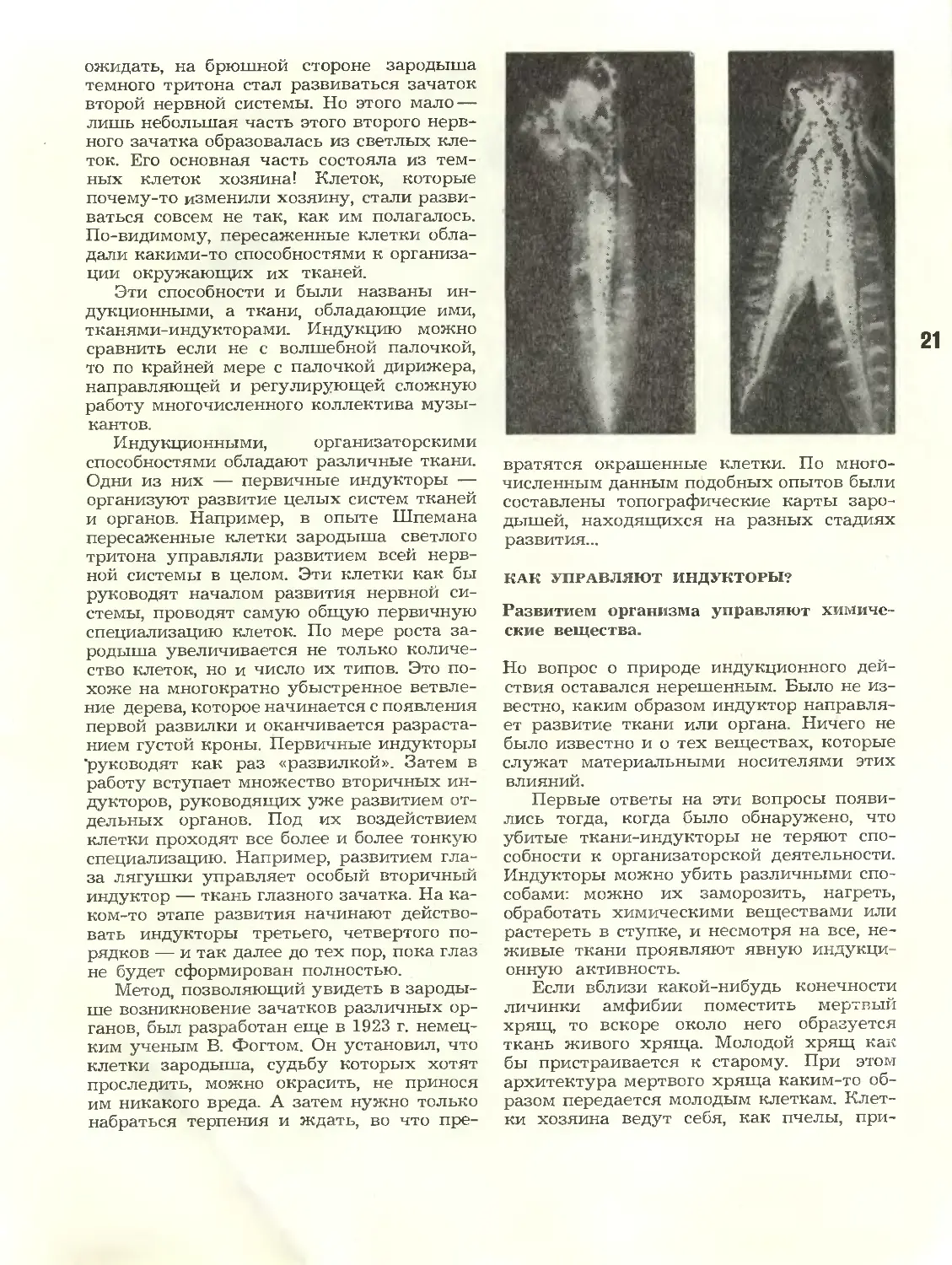
Разные стадии развития
зародыша
Слева — развитие второй
головы у зародыша тритона;
справа — развитие второго
хвоста у зародыша тритона
1
L
2
садить в клетку другого зародыша, то
головастик погибнет.
Ядра изменяют свои свойства в
зависимости от того, в каком месте цитоплазмы
они находятся. А как будут вести себя
одни и те же клетки, если помещать их в
различных местах зародыша?
Природа, естественно, таких
экспериментов не ставила. У нормальных
зародышей каждая группа клеток находится
всегда на одном и том же «своем» месте и
развивается по своему нормальному пути.
Оказалось, что если перенести клетки со
«своего» места на чужое на ранних
стадиях, то клетки будут развиваться в ту или
иную ткань только в зависимости от того,
в какой части зародыша они находятся.
Так, можно заставить клетки зародыша
лягушки, из которых в будущем должны
были возникнуть кожные покровы,
образовать глазной бокал. Для этого нужно
только одно — пересадить их на те места
зародыша, из которых впоследствии
должны развиться глаза. Но такие результаты
получаются только на самых первых
стадиях жизни зародыша.
ЧТО ТАКОЕ ИНДУКЦИЯ?
Развитием организма управляют ткани-
индукторы (ткани-организаторы).
Пересадка клеток, находящихся на более
поздних стадиях развития, приводит к
другим, совершенно противоположным и,
пожалуй, еще более поразительным
результатам. Пересаженные клетки
развиваются на новом месте так, будто с ними
ничего не произошло; дают те самые
структуры, которые они образовали бы,
оставаясь на своем старом месте: у
зародыша где-нибудь на животе может
возникнуть зачаток третьего глаза или второй
головы.
Иногда при таких пересадках
результаты еще более удивительные. Весной
1921 года немецкий ученый Г. Шпеман
пересадил несколько клеток зародыша
светлого тритона на брюшную часть зародыша
другого, темного тритона. Как и следовало
ожидать, на брюшной стороне зародыша
темного тритона стал развиваться зачаток
второй нервной системы. Но этого мало —
лишь небольшая часть этого второго
нервного зачатка образовалась из светлых
клеток. Его основная часть состояла из
темных клеток хозяина! Клеток, которые
почему-то изменили хозяину, стали
развиваться совсем не так, как им полагалось.
По-видимому, пересаженные клетки
обладали какими-то способностями к
организации окружающих их тканей.
Эти способности и были названы
индукционными, а ткани, обладающие ими,
тканями-индукторами. Индукцию можно
сравнить если не с волшебной палочкой,
то по крайней мере с палочкой дирижера,
направляющей и регулирующей сложную
работу многочисленного коллектива
музыкантов.
Индукционными, организаторскими
способностями обладают различные ткани.
Одни из них — первичные индукторы —
организуют развитие целых систем тканей
и органов. Например, в опыте Шпемана
пересаженные клетки зародыша светлого
тритона управляли развитием всей
нервной системы в целом. Эти клетки как бы
руководят началом развития нервной
системы, проводят самую общую первичную
специализацию клеток. По мере роста
зародыша увеличивается не только
количество клеток, но и число их типов. Это
похоже на многократно убыстренное
ветвление дерева, которое начинается с появления
первой развилки и оканчивается
разрастанием густой кроны. Первичные индукторы
"руководят как раз «развилкой». Затем в
работу вступает множество вторичных
индукторов, руководящих уже развитием
отдельных органов. Под их воздействием
клетки проходят все более и более тонкую
специализацию. Например, развитием
глаза лягушки управляет особый вторичный
индуктор — ткань глазного зачатка. На
каком-то этапе развития начинают
действовать индукторы третьего, четвертого
порядков — и так далее до тех пор, пока глаз
не будет сформирован полностью.
Метод, позволяющий увидеть в
зародыше возникновение зачатков различных
органов, был разработан еще в 1923 г.
немецким ученым В. Фогтом. Он установил, что
клетки зародыша, судьбу которых хотят
проследить, можно окрасить, не принося
им никакого вреда. А затем нужно только
набраться терпения и ждать, во что
превратятся окрашенные клетки. По
многочисленным данным подобных опытов были
составлены топографические карты
зародышей, находящихся на разных стадиях
развития...
КАК УПРАВЛЯЮТ ИНДУКТОРЫ?
Развитием организма управляют
химические вещества.
Но вопрос о природе индукционного
действия оставался нерешенным. Было не
известно, каким образом индуктор
направляет развитие ткани или органа. Ничего не
было известно и о тех веществах, которые
служат материальными носителями этих
влияний.
Первые ответы на эти вопросы
появились тогда, когда было обнаружено, что
убитые ткани-индукторы не теряют
способности к организаторской деятельности.
Индукторы можно убить различными
способами: можно их заморозить, нагреть,
обработать химическими веществами или
растереть в ступке, и несмотря на все,
неживые ткани проявляют явную индукци
онную активность.
Если вблизи какой-нибудь конечности
личинки амфибии поместить мертвый
хрящ, то вскоре около него образуется
ткань живого хряща. Молодой хрящ как
бы пристраивается к старому. При этом
архитектура мертвого хряща каким-то
образом передается молодым клеткам.
Клетки хозяина ведут себя, как пчелы, при-
страивающие новые соты к
искусственным.
Потом выяснилось, что способность к
индукции присуща не только тканям
зародыша. Эта способность обнаружилась у
многих других тканей, даже
принадлежащих животным совсем других видов.
Ткани печени, надпочечников и жировой
клетчатки мыши, мышцы амфибий или
зачатки сетчатки тритона оказываются
способными к индукции, если их пересадить в
зародыш, находящийся на ранних стадиях
развития. Причем одни ткани
способствуют развитию одних структур зародыша,
другие — других. Например, почки мыши
преимущественно индуцируют развитие
тканей головы, а печень тритона —
мощный «хвостовой» индуктор... Все это,
естественно, наводило на мысль, что
существуют какие-то химические вещества,
благодаря которым совершаются
индукционные процессы.
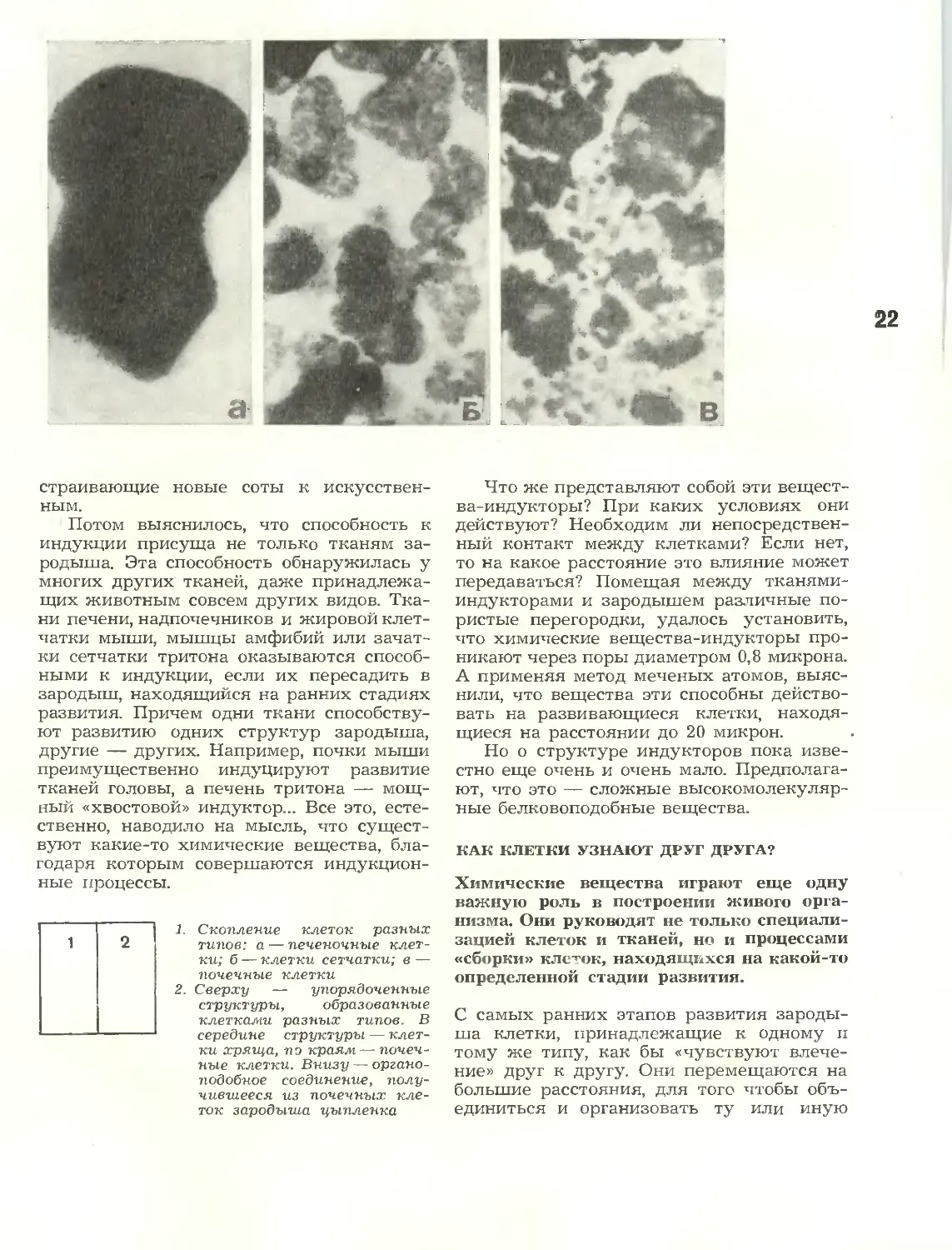
Скопление клеток разных
типов: а — печеночные
клетки; б — клетки сетчатки; в —
почечные клетки
Сверху — упорядоченные
структуры, образованные
клеткалш разных типов. В
середине структуры —
клетки хряща, по краям —
почечные клетки. Внизу — органо-
подобное соединение,
получившееся из почечных
клеток зародыша цыпленка
1
2
Что же представляют собой эти
вещества-индукторы? При каких условиях они
действуют? Необходим ли
непосредственный контакт между клетками? Если нет,
то на какое расстояние это влияние может
передаваться? Помещая между тканями-
индукторами и зародышем различные
пористые перегородки, удалось установить,
что химические вещества-индукторы
проникают через поры диаметром 0,8 микрона.
А применяя метод меченых атомов,
выяснили, что вещества эти способны
действовать на развивающиеся клетки,
находящиеся на расстоянии до 20 микрон.
Но о структуре индукторов пока
известно еще очень и очень мало.
Предполагают, что это — сложные
высокомолекулярные белковоподобные вещества.
КАК КЛЕТКИ УЗНАЮТ ДРУГ ДРУГА?
Химические вещества играют еще одну
важную роль в построении живого
организма. Они руководят не только
специализацией клеток и тканей, но и процессами
«сборки» клеток, находящихся на какой-то
определенной стадии развития.
С самых ранних этапов развития
зародыша клетки, принадлежащие к одному и
тому же типу, как бы «чувствуют
влечение» друг к другу. Они перемещаются на
большие расстояния, для того чтобы
объединиться и организовать ту или иную
ткань. Объединившиеся печеночные
клетки, например, образуют доли печени,
почечные клетки — почечные канальцы и
клубочки, клетки сердца —
сокращающуюся сердечную ткань и т. д. Клетки
одного и того же типа обладают каким-то
высокоизбирательным средством, благодаря
которому они способны «узнавать» друг
друга.
Предположив, что и в «узнавании»
основная роль принадлежит химическим
веществам, исследователи прежде всего
попытались выяснить, в каких частях
клеток они содержатся. Клетки одной и той
же ткани выдерживали в течение
нескольких дней отдельно друг от друга, т. е. как
бы промывали их поверхность. Не
соприкасаясь, клетки постепенно утрачивали
свою способность распознавать «своих-» и
«чужих». Так появилось предположение,
что узнаванием ведают вещества,
находящиеся на поверхностях клеток.
Это подтвердилось, когда сближение и
взаимодействие клеток удалось снять на
кинопленку. Клетки, принадлежащие к
одному и тому же типу, не расходятся при
столкновении, а образуют агрегаты.
Причем это не постоянные, неподвижные
структуры: контакты между клетками в
таких группах динамичны, клетки
двигаются, перегруппировываясь, но не
нарушая своей взаимосвязи.
Клетки же, принадлежащие к разным
тканям, встречаясь друг с другом, тут же
расходятся. Процесс расхождения внешне
похож на рефлекторную реакцию.
Длительность такого «рефлекса» — примерно
10^3 сек., она изменяется в зависимости от
подвижности клеток и от степени их
«чуждости».
Динамичность связей между клетками
и способность их к «самосортировке»
подтверждает давно известный опыт с
обычной пресноводной гидрой. Это животное
можно вывернуть наизнанку, как
перчатку, так что ее внутренние и наружные
ткани поменяются местами. Но спустя
некоторое время, благодаря миграции
клеток, ткани гидры снова возвращаются на
свои привычные места!
ПОВЕДЕНИЕ КЛЕТОК
В ИСКУССТВЕННОЙ СРЕДЕ
Исследовать процессы объединения клеток
в ткани в живом организме очень трудно.
Поведение клеток изучают в
искусственных средах.
Чтобы иметь возможность изменять и
регулировать условия различных процессов
взаимодействия между клетками, в
последнее время «сборку» тканей стали изучать
в искусственных средах. Вначале
экспериментировали с тканями низших
организмов. Если морскую губку осторожно
продавить сквозь тонкое сито, она распадается
на отдельные клетки. Эти клетки
помещали в сосуд с морской водой. При
определенных условиях клетки образуют
скопления, которые в конце концов
превращаются в маленькие губки. Если смешать
клетки, принадлежащие нескольким по-
разному окрашенным губкам, то при
восстановлении клетки каждого цвета
объединяются только друг с другом.
Затем опыты по ресинтезу тканей в
искусственных средах стали делать и с
зародышами млекопитающих. Такие ткани
можно разделить на клетки, обрабатывая
их, например, пищеварительным
ферментом трипсином. При этом разрушаются
только связи между клетками, а сами
клетки остаются неповрежденными. Смеси
таких клеток помещают тоже на
искусственные среды. На основании этих опытов
сейчас уже накоплено много интересных
фактов. Во-первых, оказалось, что из
клеток каждой ткани образуются скопления
строго определенной формы. Если
подсадить такие искусственно созданные
скопления в зародыш, то они срастаются с его
тканями и развиваются впоследствии
именно в те органы, из которых были
взяты.
Во-вторых, если выращивать на
искусственных средах смеси из клеток двух
разных типов, то образуются сложные
упорядоченные агрегаты. На фотографии
показана такая структура из клеток хряща и
почек. В середине ее (при каких бы
условиях она не выращивалась) находятся
хрящевые клетки, а вокруг них
располагаются почечные.
Размер искусственных клеточных
скоплений зависит от возраста зародыша.
Чем старше зародыш, тем мельче
скопления. Искусственно разделенные клетки
зародыша, находящегося на последних
стадиях развития, вообще не способны к
организации ткани.
Кроме того, размер клеточных
скоплений зависит от температз'ры среды. Самые
крупные возникают при температуре
около 38° С, а при 16° С агрегаты клеток не
создаются вовсе. И еще один интересный
факт: клетки зародышей разных
животных, но принадлежащие к тканям одних
и тех же органов, не отталкиваются друг
от друга, а образуют ткань-химеру.
Например, в смеси почечных клеток,
принадлежащих зародышам цыпленка и мыши,
из всех клеток создается единая ткань
почечных канальцев. По-видимому, факторы
распознавания оказываются более
сильными, чем межвидовые различия.
Изучение законов развития клеточных
сообществ только началось. Сделаны
первые шаги. Поняв законы развития на
молекулярном уровне, человек в будущем
получит мощное оружие управления
живым организмом, сможет активно
вмешаться в неподвластные ему пока дела
природы.
1
2
4
3
5
На вклейке: образование
клеточных скоплений из
клеток губок, принадлежащих
к двум разным видам. 1 —
сосуды с клетками губок вида
Щсгосюпа оранжевого цвета
и с клетками вида С Но па
желтого цвета; 2 — клетки обоих
видов слиты в одну плоскую
чашку; 3 и 4 — клетки
перемещаются по дну чашки, в
которую их поместили, и образуют
скопления, причем клетки
одного вида соединяются только
с себе подобпъши; 5 — через
двенадцать часов образуются
маленькие оранжевые и
желтые губки
На обороте вклейки:
иллюстрация к заметке «Этикетки
за 100 лет», напечатанной на
стр. 61
Обертка шоколада или
конфеты — это исторический
документ, оригинальная «визитная
карточка» своего времени.
v Шоквишнл кгшн
LMfiflEHbKlft АРХИТЕКТОРА ~*^
r tif&4r*ct**4 ( torn.
^5
Л967%
ПРЕДВОДИТЕЛЬ
РУССКОЙ „ХИМИЧЕСКОЙ
ДРУЖИНЫ"
2 февраля B0 января по
старому стилю) 1907 года умер
Дмитрий Иванович Менделеев,
общепризнанный глава русской
науки, предводитель нашей
«химической дружины».
Еще в 1889 году
современник Менделеева историк химии
Т. Е. Торпе так писал в
журнале «Nature»: «Ни один русский
не оказал более важного, более
длительного влияния на
развитие физических знаний, чем
Менделеев. Способ работы и
мышления у него настолько
самобытен, его метод
преподавания и чтения лекций так
оригинален, а успех великого
обобщения, с которым связаны
его имя и слава, так
поразительно полон, что в глазах
ученого мира Европы и Америки
он стал для России тем, чем
Берцелиус был для Швеции,
Либих — для Германии, Дюма —
для Франции».
Менделеев отдал служению
русской науке более 50 лет
жизни. Начав свою деятельность со
скромной должности учителя в
Одесской гимназии, он уже
через 10 лет после окончания
Главного педагогического института
становится профессором
столичного университета, а два года
спустя, в 1867 году занимает
там ведущую кафедру химии.
Петербургскому
университету Менделеев отдает лучшие
годы жизни. Здесь им созданы
знаменитые «Основы химии»
и открыт периодический закон,
ставший прочным фундамен-
4 Химия и Жизнь, J\T° 2
том всего дальнейшего
развития химии и физики. В
лаборатории университета
Менделеев выполнил много
исследований, в том числе по
упругости газов, по растворам,
нефти, бездымному пороху.
Д. И. Менделеев в последние
годы жизни. Кабинет в Палате
мер и весов
CsmtcfsAJt^ Q^^^/^7*^"
Записка Д. И. Менделеева в
Комитет по празднованию
40-летнего юбилея его научной
деятельности
В 1890 году Менделеев
покинул Петербургский
университет, «защищая его авторитет
и студенчество». Дальнейшая
деятельность его посвящена
«практике экономической
жизни России». На посту
управляющего Главной палаты мер
и весов Менделеев вел
обширную литературную работу,
отстаивал необходимость
быстрого научного и технического
развития России.
«Ограниченный рост промышленности, —
писал он, — совершенно не
пригоден нашему краю и не
приличен нашему народу,
привыкшему шагать так уж
шагать... Это потому, что народ
смутно, но решительно, по
здравому инстинкту сознает,
что идя помаленьку, мы
никогда не догоним соседей, а надо
не только догнать, но и
перегнать». Менделеев ратовал за
организованную подготовку
научных кадров в России,
указывая, что такую подготовку
«нельзя предоставить
случайности».
В условиях царского
режима многие мысли и
предложения Менделеева оставались
лишь мечтами. Только Великая
Октябрьская революция
широко открыла шлюзы народной
инициативы и свободного
труда. Через 10 лет после смерти
Менделеева началась новая
эпоха в истории человечества —
эпоха социализма. Мечты
великого ученого стали реальностью.
Его передовые идеи и в наши
дни живут в среде советских
ученых и
производственников — достойных
продолжателей его научного творчества.
Доктор химических наук
Н. А. ФИГУРОВСКИЙ
УЧЕНЫЕ ЗВАНИЯ
И НАГРАДЫ
Д. И. МЕНДЕЛЕЕВА
В кабинете-музее Д. И.
Менделеева при Ленинградском
университете хранятся
многочисленные дипломы, где
засвидетельствовано присуждение
великому химику различных
званий отечественными и
зарубежными научными организациями.
Первое звание Менделеев
получил в августе 1855 года —
звание «старшего учителя
гимназии» (по окончании Главного
педагогического института в
Петербурге). Одновременно ему
присуждена золотая медаль «За
отменные успехи в учебе».
9 сентября 1856 года
Петербургский университет
присваивает ему звание магистра,
а через 10 дней —
приват-доцента по кафедре химии.
Начиная примерно с 1875
года, многие отечественные ака-
дем ии, университеты,
институты, общества удостаивают
Менделеева самых разных титулов.
Он становится почетным членом
Медико-хирургической
академии, Киевского
фармацевтического общества, Московского
технического училища,
Общества русских врачей, Общества
естествоиспытателей при
Казанском университете,
Петербургского собрания сельских
хозяев, Петровской
земледельческой и лесной академии,
Общества врачей города Вятки,
Совета торговли и мануфактур
Министерства финансов,
Петербургского минералогического
общества, Российского общества
содействия промышленности и
торговле, Русского
астрономического общества, Русского
физико-химического общества,
Общества содействия
мореходству, Полтавского кружка
любителей
физико-математических наук...
Академия художеств
избирает его действительным
членом и членом своего совета;
Русское физико-химическое
общество — почетным
председателем; Петербургский
университет — заслуженным
профессором, город Тобольск —
почетным гражданином.
Среди зарубежных научных
учреждений Парижская
Академия наук оказалась первой,
которая присвоила Д. И. Менде-
лееву звание своего члена; зто
произошло 5 февраля 1871 года.
Через 22 дня ее примеру
следует Немецкое химическое
общество.
В начале 1900-х годов
основатель периодической системы
был членом Парижской,
Ирландской, Датской, Чешской,
Венгерской, Краковской,
Римской, Туринской, Бельгийской,
Прусской, Итальянской,
Сербской, Шведской, Болонской
академий. Звание доктора
присвоили ему университеты
Эдинбурга, Геттингена, Оксфорда,
Кембриджа, Принстона, Глазго.
Он — член Физического
общества Франкфурта-на-Майне,
Французского общества
навигации и воздухоплавания,
Дублинского королевского
общества, Великобританского
фармацевтического общества,
Национальной академии наук в
Вашингтоне, Манчестерского
литературного и философского
общества, Международного
комитета мер и весов в Париже,
Кембриджского философского
общества.
Парижское центральное
общество спасения на водах
избрало его членом-основателем.
Химическое общество в
Лондоне — «Фарадеевским чтецом»,
Королевское общество наук в
Геттингене — корреспондентом,
Всемирная Парижская
выставка 1899 года — членом жюри.
Менделееву присуждались
почетные награды: в 1872
году — диплом и медаль
Международной выставки в Лондоне;
в 1875 году — диплом и медаль
Международного конгресса
географических наук в Париже; в
1882 году — медаль Дэви от
лондонского Королевского
института; в 1891 году — медаль
Фарадея от Лондонского
химического общества; в 1904 году —
адрес «Философу химии» от
Лондонского королевского
общества; от этого же общества
в 1905 году — медаль Коплея.
Всего Дмитрий Иванович
Менделеев имел около 130
научных званий и наград.
Кандидат химических наук flQ ПОВОЛУ ОЛНОЙ
А. ШАМШУРИН о v#-***w*
ЗАБЫТОЙ ФОТОГРАФИИ
В петербургской квартире
Д. И. Менделеева (он жил при
университете) на известных
менделеевских «средах» среди
других разнообразных гостей
часто бывали
художники-передвижники Крамской, Репин,
Мясоедов, Куинджи. Дмитрий
Иванович был большим
ценителем живописи. Он всегда
откликался на события
художественной жизни — выставки,
появление новых произведений.
13 ноября 1880 го'да в
петербургской газете «Голос»
появилась заметка Менделеева о
только что выставленной в
картинной галерее картине
Куинджи «Лунная ночь на Днепре».
В этой заметке он писал:
«Перед Днепровской ночью
А. И. Куинджи, как я думаю,
забудется мечтатель, у
художника явится невольно своя
новая мысль об искусстве, поэт
заговорит стихами, в мыслителе
же родятся новые понятия —
всякому она дает свое».
4*
*« £
if* **
<*ч*
На фотографии, сделанной с
рисунка Анны Ивановны
Менделеевой, жены ученого, —
Д. И. Менделеев, играющий в
шахматы с Архипом
Ивановичем Куинджи. В глубине
комнаты сидит А. И. Менделеева.
Кандидат
физико-математических
наук
В. ГОЛОУШКИН
ПИСЬМА ЦИОЛКОВСКОГО
К МЕНДЕЛЕЕВУ
Менделеев записал однажды: «Сам
удивляюсь, чего только я ни делывал на своей
научной жизни»...
В круг его интересов входило и
воздухоплавание. В 1875 г. Дмитрий Иванович
публикует исследование «Об упругости
газов». Его интересуют процессы,
протекающие в верхних слоях атмосферы — этой
«великой лаборатории погоды», как
называл ее Менделеев.
В 1880 г. он пишет книгу «О
сопротивлении жидкостей и воздухоплавании».
В 1887 г. в Клину, во время солнечного
затмения Менделеев совершил полет на
воздушном шаре, описанный им в журнале
«Северный вестник».
В доме-музее Циолковского в Калуге
хранится книга Д. И. Менделеева «Основы
химии» с надписью Константина
Эдуардовича: «Этим я доволен, куплена в
сентябре 1879».
В «Основах химии» напечатан также
список некоторых других сочинений
Менделеева с примечанием: «Суммы, которые могут
быть выручены (до 1880 г.) от продажи...
книг, назначаются на устройство большого
аэростата».
В 1887 году в Москве Циолковский
сделал первое публичное сообщение о проекте
металлического аэростата. После этого он
долго работал над своим проектом. В итоге
появился труд «О возможности построения
металлического аэростата». И Циолковский
посылает свою работу Менделееву в
сопровождении следующего письма.
«Милостивый государь Дмитрий
Иванович!
Я тот самый учитель из г. Боровска,
Калужской губ., работы которого в сентябре
1882 и 1883 года были доставлены г.
Лавровым (кандидатом химии — Вашим
учеником) в «Физико-химическое общество»,
отнесшееся к ним весьма сочувственно.
С тех пор прошло восемь лет, в течение
которых я особенно настойчиво занимался
вопросами воздухоплавания, всегда меня
интересовавшими, и успел накопить
значительные материалы и прийти к некоторым
положительным выводам.
Важнейший из этих выводов — о
возможности построения металлического
корабля, подобного аэростату, выяснен и
формулирован мною только недавно.
Придавая ему (простите за
откровенность — может быть я ошибаюсь)
громадную важность, посылаю Вам статью об
этом, где все выводы и формулы
многократно и тщательно проверены, и прошу
покорнейше Вас прочесть и оценить ее и,
по мере этой оценки, посодействовать
моему труду.
Значение работы, о которой я говорю,
сделалось бы очевидным, если бы мне
удалось построить модель металлического
аэростата, на которую, по ее немалым
размерам, требуется некоторая сумма
(рублей 300).
Научите, где мне достать эту сумму и
куда обратиться с работой. Не может ли
мне помочь какое-нибудь состоятельное
лицо или ученое общество, может быть, то
самое, которое рассматривало мои работы?
В настоящее время я занят устройством
бумажной модели аэростата, которую я
надеюсь выслать Вам, если она окажется
удачной и не будет черезчур велика.
Еще раз прошу Вас, Дмитрий Иванович,
взять мой труд под свое покровительство.
Гнет обстоятельств, глухота с
десятилетнего возраста, проистекающее отсюда
незнание жизни и людей и другие
неблагоприятные условия, надеюсь, извинят в Ваших
глазах мою слабость.
У меня имеется еще четыре экземпляра
моего труда, относительно их
употребления жду Ваших указаний.
Всегда уважающий Вас
Константин Эдуардович Циолковский
Адрес: Боровск, Калужской губ.,
учителю уездного училища К. Э. Циолковскому.
30 августа 1890 г.»
Письмо было получено Дмитрием
Ивановичем 13 сентября 1890 г. На нем
сохранилась его пометка: «14-го сентября
ответил * и стал временно заниматься этим».
* Ответ, к сожалению, не сохранился.
18 сентября Циолковский послал
Менделееву еще одно письмо **:
«Милостивый государь Дмитрий
Иванович!
Посылаю Вам модель аэростата,
которая хотя ничего серьезного не говорит,
кроме верности формул, на основании
которых она построена, однако служит
полезной иллюстрацией к присланному
мною труду. Раздувать ее можно
посредством мехов, ртом же очень трудно, так
как коленкоровые складки сильно
пропускают воздух.
Эта модель есть только грубое
изображение аэростата; так, число складок
должно быть по крайней мере в 10 раз больше,
относительная величина полных конусов
также неверна и должна быть раза в два
меньше, притом она изображает аэростат
со складками, модель же аэростата с
волнистой поверхностью требует для своего
устройства некоторых аппаратов, которых
у меня пока нет. Желал бы получить пока,
Дмитрий Иванович, хоть уведомление о
получении Вами модели и тетради.
Всегда искренне уважавший Вас
Конст. Циолковский
Калуж. губ., гор. Боровск.
18 сентября 1890 года»
26 сентября Менделеев отправил все
присланное Циолковским члену Русского
технического общества В. И. Срезневскому
со следующей запиской:
«Согласно с желанием г. Циолковского
(оч[ень] талантливого господина)
препровождаю в Техническое Общество 1) его
письмо, 2) тетрадь его исследования о
форме складного металлического аэростата и
3) бумажную модель к проекту г.
Циолковского.
С почтением, готовый к услугам
Д. Менделеев»
А Техническое общество, рассмотрев
расчеты и модель, отметило, что ошибок в
проекте нет, но из-за того, что К. Э.
Циолковский не обратил внимания «на
конструктивную сторону дела», просьбу о пособии на
опыты отклонило...
** Право первой публикации обоих писем
принадлежит А. И. Дубравину, научному сотруднику
Музея-архива Д. И. Менделеева при
Ленинградском государственном университете. См. журнал
«Авиация и космонавтика», 1967, № 2.—
Редакция.
t ^■utA&crfi*&г<.b */*e-&yJ*t/Ф-S
*tfty#-t
/C&fjb* &£*р*-€б4£.*К, f*<& -& £*?■** J* *****
fc^fe/^*6*^ /P/C&- -Z€<f>*Z0*<Z^C^ < t?t?/f*
£f< &У S'Y *1Г0$^О&Л 4^Л -Хк*уг f**s ,. V^^c^ /*Г
f&W£ £*?S 2jt.*>Y.
, / Or
4s* К Л ft r£,'%s&
UtZ£ U*S ^0 -t4 & ty4*s/f£*w fSrffc/бы
4ЛЛ fS< f€f *€* 'ft <S tffjftx S f C*
юег*<^12л wflf^Ji*
НАШИ КОНСУЛЬТАЦИИ
Мы получили письмо от
читательницы Л. ИВЛЕВОЙ из города Но-
вошахтинска. Вот что она нам
пишет:
«Уважаемая редакция!
Некоторые мои знакомые, ремонтируя
квартиры, употребили для
побелки в качестве красителя
парижскую зелень. Ее же добавляли в
масляную краску, чтобы
получить красивый зеленый цвет.
Так как парижская зелень
является мышьяксодержащим
ядохимикатом, прошу вас
ответить на следующие вопросы:
1. Какой вред принесет
здоровью людей, проживающих в
этих квартирах, названный
ядохимикат!
2. Каким образом будет
действовать на организм человека
As (реакции)!
3. Что надо сделать в этих
квартирах, чтобы избежать
вредного действия мышьяка на
организм человека!»
Парижская (или «швейнфуртская»)
зелень — это двойная соль
состава Си(ОСОСН3J • Cu(As02J.
В справочниках о парижской
зелени сообщается, что она
отличается ярко-зеленым цветом, не
выгорает на свету, но крайне
ядовита; именно поэтому ее
обычно используют для борьбы
с сельскохозяйственными
вредителями, а как пигмент применяют
чрезвычайно редко — и то лишь
для окраски заборов, крыш
и т. д., но никак не жилых
помещений.
Мышьяк и его соединения —
сильнейшие яды, они инактиви-
руют некоторые ферменты,
связываясь с имеющимися в них
группировками атомов SH.
Поэтому, хотя парижская зелень и
нелетуча, ее лучше не
использовать для побелки и окраски
жилых помещений: побелка может
осыпаться и попасть в пищу, дети
могут испачкать в ней руки и
затем облизать их и т. д.
Одним словом — лучше не
рисковать своим здоровьем и
здоровьем близких, соскоблить
побелку (смыть ее полностью
вряд ли удастся) и побелить
квартиры заново, пользуясь в качестве
пигмента обычными
применяемыми для этой цели красителями, а
не ядохимикатами.
«Дорогие товарищи!
Убедительно прошу сообщить мне о
наилучшем способе (в домашних
условиях) удаления накипи из
чайников. Жду ответа.
С уважением Я. ВЕРЬЯНЕН-
КОВ, Волгоградская область, ст.
Панфилово».
Чтобы удалить накипь из
чайника, можно воспользоваться
одним из приведенных ниже
способов.
Если накипи не очень много,
годится пятипроцентный раствор
гексаметафосфата натрия (он
продается в хозяйственных
магазинах). Чтобы приготовить такой
раствор, нужно взять
приблизительно 50 граммов соли на литр
воды; этот раствор следует
налить в чайник и оставить на
ночь при комнатной температуре,
или же некоторое время
прокипятить. Накипь раскрошится и
кусками отвалится от стенок.
Если же стенки чайника
покрылись очень толстым (или
плотным) слоем накипи, то ее можно
удалить с помощью соляной (или
какой-либо иной — НО НЕ
СЕРНОЙ!) кислоты. Этот раствор
должен иметь концентрацию от 0,1
до 0,5 процента; приготовить его
можно так: на 1 литр воды
добавляют от 2,5 до 12,5
миллилитров сорокапроцентной
(концентрированной) или от 5 до 25
миллилитров двадцатипроцентной
(разбавленной) соляной кислоты.
Так же, как и в предыдущем
случае, чайник с раствором можно
или оставить на длительное
время при комнатной температуре,
или же недолго прокипятить.
Если внутренняя поверхность
чайника не покрыта эмалью, то
для того, чтобы кислота не
затрагивала металл, имеет смысл
добавить к раствору 1—2 таблетки
гексаметилентетрамина
(уротропина), замедляющего этот
процесс; можно воспользоваться и
так называемой «ингибированной»
соляной кислотой, которая
продается в магазинах.
После того, как накипь
удалена, чайник надо тщательно
промыть водой, а если была
использована кислота — то слабым
раствором питьевой соды.
Г. К. ФАИЗОВА
ОБЫКНОВЕННОЕ
ВЕЩЕСТВО
ЧЕРНИЛА
В 1925 году в печати появилась заметка
о том, что некоторым рукописям
Владимира Ильича Ленина грозит гибель:
написанное быстро тускнело, а местами
полностью исчезало; реставраторам стоило
немалого труда спасти бесценное наследство.
Первое, что приходит в голову, когда
знакомишься с этим сообщением,— это
невольное сравнение судьбы рукописей
Ленина с судьбами рукописей
тысячелетней давности, написанных чернилами,
которые не только не выцвели от времени,
но и по сей день сохранили удивительный
блеск и яркость.
Имя изобретателя чернил, естественно,
осталось неизвестным. Мы знаем только,
что в Древнем Египте (то есть еще задолго
до нашей эры) писали чернилами,
изготовленными из сажи, смешанной с раствором
камеди *.
Очень давно были известны чернила и
в Китае. Так же как и египетские, они
отличались чрезвычайной устойчивостью к
действию света, поскольку представляли
* Камедь — клейкие густые соки некоторых
деревьев (акации, вишни и др.), выступающие из
надрезов коры. — Ред.
собой смесь сажи со смолами,
растворенными в щелочах.
Строго говоря, это были не чернила, а
тушь, которая, как известно, обладает
одним очень существенным недостатком:
высохнув, она становится ломкой и на
сгибах отскакивает от бумаги. Кроме того,
тушь очень густа и поэтому плохо стекает
с пера.
В Европе чернила появились
значительно позже. В I веке нашей эры это
были чернила примерно того же типа, что
и в Египте и в Китае — так называемые
«угольные» чернила, состоящие на три
четверти из сажи и на одну четверть из
смолы.
Плиний оставил нам рецепт
приготовления таких чернил: «...Приготовляют
черную краску многими способами
посредством копоти, получаемой сжиганием
древесной смолы. Черная краска более
ценная делается таким путем и употребляется
для писания книг с прибавлением клея».
Но такие чернила давно уже стали
историей. На смену им пришли
железо-дубильные (или железо-галловые) чернила,
содержащие дубильные вещества и соли
железа.
Каждый из вас, обращал, наверное,
внимание на орешки, обычно в изобилии
покрывающие листья дуба. Эти орешки —
галлы — образуются на листьях дуба от
укуса особой мушки. Вытяжка орешков,
содержащая много дубильных веществ (и,
в частности, галловой кислоты), и
послужила основой для создания новых чернил.
Дело в том, что галловая кислота
образует с ионами трехвалентного (окисного)
железа чрезвычайно устойчивые к
действию света черные комплексные соли; но
таких солей не дают ионы двухвалентного
(закисного) железа. Это и определило
способ изготовления и применения
железо-дубильных чернил: к вытяжке, содержащей
галловую кислоту, добавляли соли
закисного железа. Полученная жидкость
наносилась на бумагу — чернила стекали с пера
в виде мутной, почти бесцветной жидкости,
но затем под влиянием света и воздуха
происходило окисление закисного железа
в окисное и, в результате образования
комплексной соли галловой кислоты с
окисным железом, написанное приобретало
глубокий черный тон.
Затем к таким чернилам стали
добавлять камедь, в результате чего жидкость
стала гуще, лучше держалась на пере, а
написанное приобретало красивый блеск;
железо-галловые чернила стали
повсеместно вытеснять угольные чернила и тушь,
слишком густые и не очень-то удобные
для письма.
Итальянские и испанские галловые
чернила XVI—XVII веков были уже очень
хорошими. Сохранившиеся рукописи этой
эпохи — например, автографы папы Льва X
имеют такой вид, как будто только что
написаны. Вот один из рецептов того
времени:
камеди .3 части,
железного купороса . . 2 части,
чернильных орешков . . 3 части,
воды ... 30 частей.
Химические процессы, происходящие в
вытяжке из галлов при добавлении солей
железа, были тогда неизвестны. Поэтому
довольно долго не знали, как
предотвратить выпадение осадка в чернилах. Лишь
позднее стали добавлять в чернила
кислоту — серную или соляную,— чтобы не дать
двухвалентному железу окислиться до
трехвалентного. На бумаге кислота
нейтрализовалась частицами золы и
окислению ионов закисного железа после этого
уже ничто не препятствовало. Надо
сказать, что это усовершенствование
оказалось роковым для некоторых рукописей:
порой чернила подкисляли так сильно, что
кислота разрушала бумагу.
Но у галловых чернил был и другой
недостаток: написанное можно было
прочитать только спустя 10—12 часов, до
этого текст был почти бесцветным. Это
свойство галловых чернил затрудняло и сам
процесс письма.
Но в том же XVI столетии появились
яркоокрашенные кампешевые чернила.
Краситель кампеш получался из
кампешевого дерева, произрастающего на
островах Кубе, Ямайке, он появился в Европе
после открытия Америки. Первыми с этим
деревом познакомились испанцы, они
назвали его по имени залива Кампече в
Мексике.
Кампеш (или гематоксилин) быстро
завоевал популярность как краситель. В
соединении с различными протравами
кампеш дает ряд тонов:
с оловянными . . . фиолетовый,
с глиноземом .... синий,
с хромом сине-черный,
с медью сине-зеленый.
С хромпиком кампеш дает жидкость,
которая при нанесении на бумагу сразу же
окрашивается в черный цвет. Это и были
чернила, названные кампешевыми.
Но, увы, эти чернила оказались
далекими от совершенства: они недостаточно
устойчивы к действию света, с течением
времени сгущаются и, наконец,
написанный ими текст мог быть легко вытравлен.
Не удивительно поэтому, что довольно
скоро пришлось снова вернуться к
забытым было железо-галловым чернилам.
Однако необходимость избавиться от их
основного недостатка — отсутствия
первоначальной окраски — стала еще
настоятельнее.
И вот в 1855 году (этот год считают
годом переворота в производстве чернил)
саксонский учитель Христиан Август Ле-
онгарди взял патент на изобретенные им
чернила, которые он назвал
«ализариновыми». Это были галловые чернила, но не
бесцветно-мутные, а интенсивно
окрашенные в сине-зеленый цвет, который на
бумаге переходил в глубоко черный тон.
Леонгарди добился этого, применив
краситель индигокармин в сочетании с
голландским краппом. Крапп — продукт особой
обработки корней марены, известной еще
с незапамятных времен египтянам, персам
и индусам; с Востока марена продвинулась
в Италию, где она получила название
«ализари».
Вот рецепт, который предложил Леон-
гарди:
42 части алеппских чернильных
орешков (это один из самых известных тогда
сортов, содержащий до 70 процентов
дубильной кислоты) и 2 части голландского
краппа заливают водой, чтобы всего
получить 120 частей, затем прибавляют 1,2
части индигокармина, 5,2 части железного
купороса и 2 части уксуса.
В наше время дорогостоящий крапп
заменяют синтетическими красителями, а
чернильные орешки — танином и
галловой кислотой. Эти чернила, отличающиеся
исключительной устойчивостью к
действию света и химических реактивов, не
дающие с течением времени осадка, хорошо
стекающие с пера и яркоокрашенные, и
поныне остаются непревзойденными.
Правда, позже у ализариновых чернил
появился конкурент: широкое
распространение получили анилиновые чернила,
например фиолетовые, представляющие
собой разведенный в воде синтетический
краситель — метилвиолет. Любопытно, что
из всех синтетических красителей самое
широкое распространение получил легко
смывающийся, наименее светопрочный,
наименее устойчивый, разлагающийся даже
под действием следов хлора, остающегося
в бумаге после ее отбеливания. Но,
несмотря на это, фиолетовыми чернилами
пользуются до сих пор и в школах и в
учреждениях. В этом есть свой резон: они не
только чрезвычайно дешевы, но и удобны
для повседневного применения. Разве
приятно было бы испачкать руки или одежду
несмываемыми чернилами?
Однако естественно, что такими
чернилами нельзя вести архивные записи или
заполнять документы; для этого нужны
специальные долговечные чернила.
Кстати, во многих странах мира существуют
специальные правила, в которых
оговаривается— какими чернилами в каких
случаях следует писать.
Технический прогресс нашел свое
отражение и в технике письма: сейчас даже
школьники пишут авторучками.
Естественно, что к чернилам стали предъявлять
требования иные, чем в те времена, когда
в ходу были гусиные перья.
Чернила для авторучек не должны
разрушать металлических и пластмассовых
деталей, они не должны содержать
твердых частиц, способных забить капилляры
механизма, дсЗлжны, наконец, легко
стекать с пера, но не слишком — в ином
случае при письме все время будут
получаться кляксы. И еще — применяемый
краситель не должен кристаллизоваться на пере
по мере высыхания раствора, а
закристаллизовавшись — легко растворяться
последующей порцией чернил.
В общем-то, состав чернил для
авторучек довольно прост. Берут какой-нибудь
краситель, растворяют его в воде,
добавляют загуститель (например, глицерин) и
антисептик — обычно фенол. Загуститель
выполняет двоякую функцию: во-первых,
он делает чернила более вязкими, но
такими, чтобы они не только хорошо
удерживались на пере, но и легко с него стекали,
а во-вторых, он гигроскопичен и поэтому
препятствует быстрому высыханию
чернил и кристаллизации красителя.
Все это значит, что качества чернил
определяются, в первую очередь,
качеством использованного красителя: он должен
иметь яркий насыщенный цвет, быть
устойчивым к выцветанию и действию
различных химических реагентов (некоторые
красители обладают еще одним ценным
свойством — они прочно соединяются с
волокнами целлюлозы и с наполнителями,
содержащимися в бумаге, и после
высыхания уже больше не смываются). Кроме
того, растворы различных красителей не
должны давать осадка при смешивании.
До сих пор в нашей стране последнее
требование не соблюдалось: например, для
изготовления черных, красных и зеленых
чернил применялись кислотные красители,
а синих и фиолетовых — основные. Если
не промыть как следует авторучку,
заполненную, скажем, черными чернилами и
набрать в нее синих, то ручка перестанет
писать. С нового, 1967 года, начинается
производство так называемых
совместимых чернил — фиолетовых, синих, черных,
голубых, зеленых и красных,— которые не
обладают этим неприятным свойством.
Новым чернилам присвоено название
«Радуга»; будут выпускаться и
специальные черные несмываемые чернила,
пригодные для заполнения важных
документов.
Рисунок
С. БАРХИНА
5 Химия и Жизнь, № 2
ДОКУМЕНТ
В РУКАХ ЭКСПЕРТА
ОПРЕДЕЛЕНИЕ
21 мая 1966 г. народный судья
Фрунзенского района г.
Москвы Езин В. Ф., ознакомившись
с заявлением Морозовой Анны
Григорьевны об установлении
юридического факта
регистрации рождения,
НАШЕЛ,
что до внесения дела к
слушанию в судебное заседание
необходимо произвести
предусмотренные ст. 141 ГПК РСФСР
действия по предварительной
подготовке дела, а потому,
руководствуясь ст. 141-6 ГПК РСФСР,
ОПРЕДЕЛИЛ:
Поручить Центральному
научно-исследовательскому
институту судебной экспертизы
произвести криминалистическую
экспертизу выписки из
метрической книги и поставить на
разрешение эксперта
следующие вопросы:
1. Какой текст содержится в
метрической записи?
На чье имя, фамилию и
отчество выдана
метрическая запись?
В каком году и месяце
родилось лицо, указанное
в метрической записи?
2. Ке содержится ли в данном
документе подчисток и
исправлений?
Приложение: Заявление
Морозовой и метрическое
свидетельство.
Печать.
Подпись народного судьи Езина.
Как выглядел документ,
направленный в Институт
судебной экспертизы, видно на фото
вверху: различимы лишь
фрагменты некоторых слов. Время,
свет и влага почти полностью
уничтожили текст. Такие
записи эксперты называют
«угасшими».
Но вот прошло около трех
недель, и на стол руководителя
лаборатории технических
экспертиз документов А. А.
Гусева легло заключение, сделанное
экспертом В. А. Семеновой.
Теперь уже не составляло
труда прочитать и, для большей
ясности, обвести востановлен-
ный текст (фото внизу): в
«счете родившихся женска
пола» священник Дмитрий
Покровский записал, что 23 июля
1911 года у супругов Морозовых
родилась дочь, названная
Анной.
Анна Григорьевна Морозова
обратилась в народный суд
потому, что когда-то была
допущена досадная ошибка: в ее
документах, в графе «год
рождения», последнюю единицу
случайно заменили на двойку.
Сначала это показалось
несущественным. Какая разница —
одним годом больше или
меньше? Но сейчас, когда пришло
время идти на пенсию, ошибка
стала ощутимой, и ее удалось
исправить только благодаря
искусству экспертов.
Но все-таки, как удалось
восстановить «угасшую»
запись? По остаткам слов и фраз
можно было заключить, что
чернила, которыми она
сделана, когда-то были черными. Но
в начале нашего столетия были
распространены черные
чернила двух сортов:
железо-галловые и кампешевые. Первые
содержали соли железа, вторые —
хрома. Начать реставрацию не
теми реактивами значит почти
наверняка окончательно
погубить документ. Поэтому
реставрации всегда предшествует
анализ, цель которого — точно
установить тип чернил.
Делается это так. Прежде
всего, документ
фотографируют. Затем с сохранившихся
участков записи аккуратно
соскабливают немного высохших
чернил; зтот соскоб растворяют
в воде или спирте, раствор
фильтруют, выпаривают, а
остаток (можете представить
сколько его получается') делят
на несколько порций.
Итак, подготовка закончена,
можно приступать к анализу.
Первую порцию порошка
обработали каплей соляной
кислоты — проба дала желтое окра-
шивание. Вторая и третья
пробы обесцветились, когда на
них подействовали азотной и
щавелевой кислотами. А вот
проба с 5%-ным раствором
едкого натра приобрела красную
окраску. Еще несколько
подобных «цветных» реакций и
эксперт сделал первое
заключение: текст написан
железо-галловыми чернилами.
В распоряжении эксперта
довольно богатый арсенал
физических и химических
методов «проявления» угасших
записей. В нашем случае было
решено обработать документ
слабым раствором 8-оксихино-
лина в уксусной кислоте. И
хотя этот реактив не вернул
чернилам первоначальной яркой
окраски, запись стала
достаточно четкой, чтобы ее можно
было прочитать. Неясными
остались лишь несколько букв,
которые нетрудно восстановить
логически или по архивным
данным.
Фотокопии метрического
свидетельства Л. Г. Морозовой
до того, как оно побывало па
экспертизе, и после
окончания экспертизы
^JVtf"^%
5*
^
ъ& U*
A^JLfrj^V<
ПРОПИСИ
\2h
T^>&
V
1 1
2
1 Страница паспорта, залитого
черными чернилами. Вии-
зу — фото того же
документа в инфракрасных лучах
2 Страница трудовой книжки.
Текст в 4-й графе эксперт
прочел после обработки
документа щелочным
раствором гидросульфита натрия
Судебным экспертам
приходится иметь дело и с
материалами иного рода: подчистками,
приписками, умышленно
залитыми или вытравленными
записями. Когда знакомишься с
такими документами после
того, как они побывали в руках
экспертов, хочешь не хочешь,
а вспоминаешь известную
пословицу: «Что написано пером,
не вырубишь топором».
Два примера.
Первый: паспорт, записи в
котором сделаны тушью, залит
черными чернилами.
Второй: документ,
заполненный черными чернилами,
нацело залит черной же тушью.
Попробуй, прочти.1
И та, и другая задачи
вполне разрешимы с помощью
методов технической экспертизы.
Задача с паспортом, пожалуй,
проще. Анилиновые красители,
входящие в состав чернил,
прозрачны для инфракрасных
лучей, а тушь — нет. Запись,
которая кажется безвозвратно
утраченной, фотографируется в
инфракрасных лучах; снимок
восстанавливает
первоначальную картину (фото на этой
странице. Тот же метод
помогает разоблачать приписки,
сделанные тушью, если
основная запись сделана чернилами,
и наоборот.
А вот вторая задача долгое
время считалась
трудноразрешимой. Только в 1956 году
советский криминалист С. Ш.
Касимова предложила новый
метод исследования документов,
получивший название диффуз-
но-копировального. За десять
лет этот метод значительно
усовершенствовался, и теперь
с его помощью не составит
тРУДа прочитать залитый
тушью чернильный текст.
Вот вкратце сущность этого
метода. К обратной стороне
документа прикладывают лист
увлажненной фотобумаги.
Набухший в воде желатиновый
слой эмульсии «вытягивает»
молекулы красителя, которые
реагируют с мельчайшими
кристалликами галоидов серебра и
меняют их чувствительность к
лучам определенной части
спектра. Если краситель,
например, повышает
чувствительность к желтым лучам, то
бумагу экспонируют и проявляют
при желтом освещении, затем
обрабатывают закрепителем, и
вскоре фотография позволяет
установить истину: на белом
фоне явственно проступает
темная запись.
Усовершенствованный диф-
фузно-копировальный метод
позволяет решать и более
сложные задачи. Как бы
профессионально ни подчищал
преступник запись, в порах
бумаги обязательно останутся
следы чернил. Более того, диф-
фузно-копировальный метод
позволяет восстановить не
только подчищенные или
залитые записи, но и записи,
сделанные чернилами,
разбавленными почти в 1000 раз
(фактически — бесцветными).
В наиболее сложных
случаях возможности этого метода
усиливаются действием
специальных реактивов.
Некоторые из них, например,
щелочной раствор гидросульфита
натрия, используются и
самостоятельно.
С разными красителями
гидросульфит натрия реагирует
по-разному: обесцвечивает
одни, изменяет окраску других,
третьи делает темнее, а на
четвертые совсем не влияет.
Однажды научному
сотруднику Института судебной
экспертизы Л. Г. Никаноровой
поручили исследовать трудовую
книжку. Ее владелец
утверждал, что огромная синяя клякса,
скрывшая часть записей на
одной из страниц (фото на стр.
37), — не что иное, как
результат неосторожных
манипуляций кадровиков с чернилами и
чернильницей. Он ссылался на
свидетелей, которые могут
подтвердить, что под пятном
именно такой текст, как он
утверждает.
Но книжку направили на
экспертизу.
Пятно было синее, записи —
тоже. Проанализировав те и
другие чернила, Никанорова
пришла к выводу, что это —
именно тот случай, когда
обработка гидросульфитом поможет
установить истину. Под
действием раствора пятно сильно
поблекло, и эксперт увидела,
что смысл записанного под
«случайной кляксой»
диаметрально противоположен тому,
что утверждал владелец
трудовой книжки.
Иногда раствор
гидросульфита играет с преступниками
злые шутки. Гидросульфит —
сильный восстановитель.
Некоторые анилиновые красители
под его действием
обесцвечиваются, а затем вскоре вновь
окисляются кислородом
воздуха и принимают
первоначальный цвет. В «минуты
просветления » текст фотографируют.
А теперь представьте
очередной допрос. Преступник
знает, что документ побывал на
экспертизе. Следователь ему
этот документ показывает.
Спасительное пятно на месте!
Преступник уже готов
вздохнуть с облегчением, и вдруг
рядом с документом ложится
фотокопия. Чистенькая, без
единого пятнышка...
Одна из самых сложных
задач судебной экспертизы —
прочитать текст сожженного
или обожженного документа.
Но если испепеленные листки
доставлены на стол эксперта с
соблюдением всех правил,
специально разработанных для
таких случаев, то нередко текст,
подобно сказочной птице
Феникс, восстает из пепла.
При сжигании бумага
проходит три стадии разрушения.
Первая — высушивание.
Бумага теряет влагу, желтеет,
сморщивается.
Вторая — обугливание.
Бумага приобретает
темно-коричневый, затем черный цвет,
прочность ее становится
ничтожной.
Третья стадия —
испепеление. Уголь сгорает, от бумаги
остается одна зола.
Однако в большинство бумаг
входят термостойкие
минеральные наполнители — каолин,
мел, гипс. Благодаря им, даже
на последней стадии бумага
может частично сохранить свою
структуру. Характерно, что при
температуре 300—500°С
испепеленная бумага снова становится
белой, вернее почти белой.
Иногда удается прочесть, что
написано на пепле и без
специальных приспособлений или
химической обработки текста.
Особенно устойчивы к огню
типографские краски и
карандашные записи. Иногда
обуглившиеся бумаги обрабатывают
флуоресцирующими составами,
и в ультрафиолетовых лучах
проявляется запись.
Естественно, что в какой бы
стадии разрушения не
находился документ, побывавший в
огне, его прежде всего
закрепляют. Сильно покоробленные
бумаги наклеивают на
прозрачную полимерную пленку, а
потом хранят между двумя
стеклами...
Конечно, все, о чем вы узнали
из этих заметок, — только
малая доля арсенала
химических средств, которым
располагают
эксперты-исследователи. Их наборы реактивов и
методы исследования достаточно
совершенны, чтобы
разоблачить любого рода
фальсификацию. Методы, о которых здесь
рассказано, — хорошие,
надежные, но не самые новые и не
самые филигранные. Новейшие
методы — профессиональное
достояние экспертов. Я в них
не посвящен.
В. СТАНЦО
клин—клином...
Чем только ни занимался за свою долгую жизнь
Менделеев — создатель периодического закона! Круг его
интересов выходил далеко за рамки «чистой» науки:
достаточно вспомнить его работы по воздухоплаванию,
созданию бездымного пороха, или хотя бы, его энергичную
борьбу со спиритизмом...
Предлагаемая читателям заметка открывает еще одну
страницу в бурной и многогранной деятельности великого
русского ученого.
В марте 1870 года Дмитрий
Иванович Менделеев получил
письмо от управляющего
Российским государственным
банком с просьбой принять
участие в деятельности комиссии,
которая должна была
разработать меры по защите-
денежных чеков от подчисток и
подделок.
Менделеев, всегда
интересовавшийся вопросами
писчебумажного производства (этой
отрасли промышленности он
посвятил даже отдельный том
выпущенной им химической
энциклопедии), охотно
откликнулся на это предложение. Он
тщательнейшим образом
изучил все, что имело отношение
к проблеме изготовления
чернил, и вскоре стал подлинным
знатоком в этой области.
В 1871 году при активном
участии Д. И. Менделеева
комиссия закончила работу и
предложила проект новых
денежных чеков, таких, что
подчистки и подделки на них
можно было легко обнаружить.
Самое интересное, что
рекомендации комиссии не
предусматривали каких-либо химических
«хитростей»: они представляли
собой остроумную комбинацию
технологических приемов,
причем, как ни парадоксально, в
основу был положен
недостаток обычно применяемых
чернил — их нестойкость к
действию различных реагентов.
Вот некоторые из этих
рекомендаций.
Бумага должна быть тонкой
и слабо проклеенной, чтобы
чернила глубоко в нее
проникали — это исключало
возможность выскабливания
написанного; в бумажную массу при ее
изготовлении следует добавлять
обыкновенные чернила, чтобы
равномерно окрасить ее в
сероватый цвет и придать
чувствительность к различным
химическим реактивам; наконец,
печатать текст следует
типографской краской, в которую
добавлен все тот же нестойкий
чернильный порошок. (В наше
время нестойкий краситель
наносят на поверхность бумаги в
виде мелкой сетки.)
Совокупность этих мер
должна была сделать
невозможным любой вид подделок.
В самом деле, попытка
вытравить часть чека неизбежно
повлечет за собой порчу фона и
заметное изменение
напечатанного текста; при попытке же
вытравить весь чек исчезнет
подпись выдавшего, изменится
все напечатанное, а
первоначальный цвет бумаги не
удастся восстановить, так как
поверхностным окрашиванием
невозможно придать тону
прежнюю однородность.
Остается добавить, что все
предложения комиссии были
приняты и с успехом
применены на практике.
И еще раз обращались
криминалисты за помощью к
Д. И. Менделееву — на этот раз
по вопросу о знаках почтовой
оплаты. Дело в том, что
катастрофически участились
случаи вытравливания штемпелей
и вторичного гашения марок.
И снова Менделеев охотно
принялся за работу, и по его
предложению рисунок на марках
стали печатать двумя
красками, каждая из которых была
чувствительна к действию
химических реактивов,
применяемых для вытравливания
штемпелей.
Г. СЕМИВЕРСТОВА
4EFF* ..л, , ВТОРЫЕ
В ТС <KF " >tM
НЕ lEPrk^iA.
В конце сороковых годов нашего века мир
увлекло новомодное изобретение —
шариковая авторучка. Изобретение это и впрямь
подкупало простотой и остроумием:
вместо непрочного пера новая ручка писала
миниатюрным стальным шариком,
вделанным в конический латунный наконечник, а
вместо резервуара, наполненного жидкими
чернилами, в ней была всего-навсего
трубочка, наполненная густой и клейкой
пастой. При письме шарик катился по
бумаге, непрерывно («другим боком»)
смазываясь пастой. В результате на бумаге
оставался тонкий и ровный след.
Но это увлечение быстро прошло. И
виной тому была не сама шариковая ручка,
а чернильная паста, свойства которой
оставляли желать много лучшего. Эту
пасту готовили на основе касторового масла;
оставленный ею след чрезвычайно
медленно высыхал и легко смазывался. Более
того, написанное можно было без особого
труда вытравить, подпись на документе
ничего не стоило перенести на новый лист
бумаги — одним словом, доверять
шариковой ручке было нельзя.
Но в 1951 году шариковая ручка была
спасена. В этом году была изобретена так
называемая «сухая» паста, изготовленная
на основе синтетической смолы. Эта паста
уже не обладала недостатками своей
предшественницы — написанное не
смазывалось, не вытравливалось, не копировалось.
И шариковые ручки новой волной
хлынули на прилавки магазинов, тесня
заслуженные «вечные перья». Появились и
другие новинки — многоцветные шариковые
ручки и шариковые ручки с
увеличенными резервуарами, такими, что одной
заправки хватало чуть ли не на целый год.
Последнее новшество потребовало
усовершенствования и самого пишущего узла:
дело в том, что обычный стальной шарик
быстро истирается при письме, его форма
меняется, зазор увеличивается — ручка
начинает наносить на бумагу прерывистую
линию переменной толщины, а паста по
каплям вытекает через зазор и пачкает
руки и бумагу. Поэтому в ручках с большим
резервуаром стали использовать шарики,
изготовленные из какого-нибудь твердого
сплава (например, карбида вольфрама), а
наконечники начали делать из
нержавеющей стали.
Но тут же возникла новая проблема
паста хотя и медленно, но высыхала, и
поэтому не всегда удавалось ее использовать
до конца. Значит, надо было снова работать
над ее качеством. В конце концов удалось
создать пасты, которые не засыхают
внутри ручки почти два года.
В состав современных паст для
шариковых ручек входят следующие
компоненты:
синтетический краситель (растворимый
в органическом растворителе);
синтетическая смола (алкидная или
полиэфирная);
пластификатор (олеиновая или рицино-
левая кислота);
растворитель (гликоли, полигликоли,
эфиры гликолей и полигликолей,
бензил овый спирт).
Казалось бы, что стоит изготовить
пасту для шариковой ручки? Достань все
необходимые вещества, смешай их в
необходимой пропорции — и паста готова. Но
почему-то даже паста, изготовленная на
специальных предприятиях, далеко не
всегда бывает удовлетворительного
качества... Скажем прямо — часто только что
заправленная ручка сразу же отказывает.
В прошлом году в ноябрьском номере
журнала «Химия и жизнь» был
опубликован ответ на письма читателей, которые
просили рассказать о том, как сделать
высококачественную пасту для шариковой
ручки в домашних условиях. В ответе
было честно сказано, что сделать это
невозможно по нескольким причинам.
Во-первых, к перечисленному выше
сырью предъявляется очень серьезное
требование: все компоненты должны быть
тщательнейшим образом очищены от
механических примесей. (Ведь зазор между
шариком и конусом измеряется
микронами! Можно только удивляться, как после
варварской операции извлечения шарика,
которой ручку подвергают на заправочном
пункте, она еще продолжает писать. На
худой конец при так называемой
«перезарядке» следовало бы вынимать весь конус,
в котором держится шарик, заполнять
трубочку, снова надевать ее на конус и
подводить пасту к шарику, поддавливая ее,
например, сжатым воздухом. Не вынимая
шарика! Но почему-то этого нигде не
делают...)
Во-вторых, технологический режим для
каждой партии сырья должен быть
отрегулирован таким образом, чтобы
величина вязкости полученной пасты была
строго определенной и совершенно
постоянной — в ином случае заправленная такой
пастой ручка просто не будет писать.
Но после опубликования этого ответа
редакция получила письма, в которых
утверждалось, что изготовить пасту для
шариковой ручки в домашних условиях все-
таки можно. Авторы писем ссылались на
советы, приведенные в «Неделе» от 2—
8 октября (№ 41) прошлого года. Вот эти
советы
СОВЕТ № 1
«Читательница Э. Папасова из Ростова-на-
Дону предлагает за основу пасты взять мед
E0 процентов), добавить к нему 48 процен-
6 Химия и Жизнь, № 2
тов красителя (метиленовая синь, которая
продается в аптеках) и как
антизагуститель — 2 процента лимонной кислоты. Эта
смесь тщательно растирается в
фарфоровой ступке.»
СОВЕТ № 2
«Харьковчанин А. Добров считает, что для
изготовления пасты необходимы:
чернильный порошок любого цвета, карболовая
кислота и машинное масло. 0,5
кубического сантиметра порошка надо растереть в
ступке с эфиром. Эфир нужен лишь для
более тщательного растирания. Когда он
испарится, залить 10—13 капель спирта.
Он тоже должен испариться. Затем по
каплям вливать карболовую кислоту. Смесь
растирается пестиком до густоты меда.
После этого добавляется 1—2 капли
машинного масла. Смесь готова.»
СОВЕТ № 3
«Читатель В. Зарытовский из Зеленоград-
ска Калининградской области прислал
вырезку из польского журнала (название его
он, к сожалению, не написал). В ней
говорится:
«Паста хорошего качества
приготовляется из окисленного касторового масла и
синтетических смол.
Как окислить касторовое масло?
Заливаем его в пробирку и опускаем в сосуд с
водой. Нагреваем до 25 градусов, а затем
постепенно пропускаем через слой
касторового масла пузырьки воздуха. Окисление
при этой температуре продолжается в
течение двух часов. В окисленное касторовое
масло добавляем двухпроцентный раствор
гликолевой поливинилацетатной смолы;
20-процентную суспензию красителя,
растворенного в касторовом масле.
Поливинилацетатную смолу можно
получить из поливинилацетатной эмульсии
ПВА-Э (ее продают в хозяйственных
магазинах в отделе бытовой химии), в которой
эта смола является основным
компонентом. Кроме нее в эмульсии имеются
растворители. Их следует выпарить. Смолу
надо растворить в этиленгликоле (этилен-
гликолем обычно заливают радиаторы
автомобилей в зимнее время).
В качестве красителей можно
использовать ультрамарин, нигрозин, кадмиевый
красный краситель. Красители надо
смешать с окисленным касторовым маслом и
тщательно растереть в ступке. Только эту
смесь можно добавлять к маслу и смоле».
Там же сказано о том, как заправлять
шариковую ручку:
«Для этого нужно иметь кусок упругой
стальной проволоки толщиной 0,5
миллиметра, длиной сантиметров 20 и
медицинский шприц.
Заостренным концом проволоки
изнутри осторожно выдавливается шарик.
Наконечник медицинского шприца
подводится к стержню в том месте, где был шарик.
Паста вдавливается в стержень. Затем
шарик вставляется на место.»
Мы надеемся, что читатели, которые
испытывают эти советы на практике,
пришлют нам свои отзывы, ответив на еле-»
дующие вопросы:
1. Что побудило вас заняться
изготовлением пасты?
2. Каким (или какими) советом вы
решили воспользоваться и почему?
3. Все ли необходимые компоненты вам
удалось найти? Если да, то сколько вы на
это потратили времени?
4. Опишите подробно, как вы делали
пасту (если вас постигали неудачи —
расскажите и о них). Сколько времени вы
потратили на работу?
5. Писала ли ручка, заправленная
изготовленной вами пастой? Если да, то как
долго? Отказывала ли она при письме?
Если да, то как часто? Легко ли она
«расписывалась» после перерыва?
6. Удовлетворены ли вы качеством
письма? Не смазывается ли написанное?
7. Если вы изменили состав или способ
приготовления пасты, подробно опишите
свою методику.
8. Удобно ли в домашних условиях
готовить пасту для шариковых ручек?
Сделайте общий вывод из ваших опытов.
Отзыв нужно снабдить образцом
текста, написанного изготовленной пастой.
Если будут фотографии, иллюстрирующие
процесс изготовления, — это тоже хорошо.
Срок представления отзывов —15 мая.
Самые интересные будут опубликованы в
«Химии и жизни», а их авторы —
премированы набором стержней, заправленных
отличной пастой разных цветов.
Рисунок
Ю. КУПЕРМАНА
ФАНТАСТИКА
А A3SoB« ЛОВУШКА
Д. АНИКЕЕВА
ДЛЯ ПРОСТАКОВ
...Самым великолепным зрелище было
тогда, когда Малышка находилась еще
довольно далеко, и всю ее можно было
окинуть взглядом.
На севере и на юге треть планеты
покрывали ледяные шапки, только
начавшие свое тысячелетнее
отступление.
Посадочная спираль корабля была
проложена с севера на юг, специально,
чтобы можно было разглядеть полярные
области, хоть это была и не самая
безопасная траектория. Поэтому внизу под
кораблем видна была то одна, то другая
ледяная шапка. Обе они одинаково сияли
в солнечных лучах: ось Малышки не
имела наклона. И каждая шапка была
разделена на секторы, как торт,
разрезанный радужным ножом. Одна
треть была освещена сразу обоими
солнцами и сверкала ослепительно белым
светом, который понемногу желтел
к западу и зеленел к востоку. Восточнее
белого сектора лежал следующий, вдвое
уже его, освещенный только зеленым
солнцем Лагранж-I, и здесь снег горел
Отрывки из фантастической повести.
6*
изумрудными отблесками. К западу еще
полсектора, доступные только лучам
красного солнца Лагранж-П, светились
теплыми оранжево-красными тонами
земного заката. Цвета полосами
переходили друг в друга, отчего сходство
с радугой еще усиливалось. И, наконец,
последняя треть казалась сравнительно
темной, хотя можно было разглядеть, что
и она поделена на неравные части.
Меньшая была в самом деле черной,
большая — чуть молочного оттенка.
Спираль спуска изогнулась, изменив свое
направление на юго-западное, а потом на
западное, обещавшее меньше всего риска
при посадке. В рубку проник глухой рев
прорезаемой атмосферы — сначала резкий
и высокий, он становился все ниже и
глуше. Поверхность планеты как будто
бросилась навстречу кораблю. Ледяные
шапки исчезли из виду, сменившись
равномерным чередованием суши и воды.
Под кораблем все реже и реже проносился
материк с гористыми окраинами и равниной
посередине, как суповая миска с двумя
ледяными ручками. Материк занимал
половину планеты — остальное было
покрыто водой. В свете Лагранжа-П вода
казалась тускло-пурпурной. Там и сям
виднелись багровые точки, к северу и к
югу их становилось больше. Айсберги!
Корабль быстро замедлял полет. Он
в последний раз пронесся над океаном.
Началась посадка.
...Малышка казалась настоящим
двойником Земли. Все отличия были
только в ее пользу. Насколько было
известно до сих пор, на этой планете ничто
не угрожало человеку. Никто и не подумал
бы, что здесь может таиться какая-то
опасность. Если бы только не то
обстоятельство, что первая колония людей
на Малышке погибла до последнего
человека. И что хуже всего,— это
произошло таким образом, что все
сохранившиеся сведения ничего не могли
объяснить.
...Только в последние двадцать лет,
столкнувшись с проблемой растущего
перенаселения старых планет,
Конфедерация приступила к
систематическому обследованию
Галактики. До этого человечество заселяло
новые миры наугад. В поисках земли и
лучших условий жизни мужчины и
женщины отправлялись туда, где могли
находиться пригодные для жизни планеты,
или посылали туда разведочные партии
добровольцев.
ПО лет назад одна такая партия
обнаружила Малышку. Они не сделали
официального объявления об открытии:
не хотели, чтобы за ними последовали
полчища предпринимателей,
горнопромышленников и всякого другого
сброда. Спустя несколько месяцев часть
холостых мужчин добилась, чтобы на
Малышку были доставлены женщины,
и некоторое время колония процветала.
Только через год, когда часть поселенцев
уже умерла, а большинство остальных
были больны или при смерти, они дали
сигнал бедствия на ближайшую населенную
планету. Ее правительство, которое в этот
момент переживало очередное кризис,
переслало весть о несчастье правительству
галактического сектора и сочло себя
вправе забыть об этом.
Правительство сектора сразу же выслало
на Малышку санитарный корабль. Он
сбросил на планету сыворотку и разные
другие медикаменты. Садиться корабль
не стал, потому что находившийся на
борту врач заочно поставил диагноз
гриппа и в своем докладе сильно
преуменьшил опасность. По его словам,
сброшенные медикаменты позволяли
прекрасно справиться с эпидемией.
Вполне возможно, что сесть на планету
не захотел боявшийся заразы экипаж;
впрочем, в официальном докладе об этом
ничего не говорилось.
Три месяца спустя с Малышки пришло
последнее сообщение, гласившее, что в
живых осталось всего десять человек, и те
уже умирают. Они умоляли о помощи. Это
сообщение было переправлено на Землю
вместе с докладом санитарной экспедиции.
Но Центральное правительство
представляло собой гигантский лабиринт,
где бумаги то и дело терялись, если не
находилось какого-нибудь лично
заинтересованного человека, достаточно
влиятельного, чтобы довести
дело до конца. А людей, заинтересованных
в судьбе далекой неизвестной планеты,
где умирали десять мужчин и женщин, не
нашлось. Поэтому сообщение было
зарегистрировано и забыто. И в течение
столетия человеческая нога не ступала на
поверхность Малышки.
Потом, когда поднялась новая шумиха
вокруг галактических исследований, сотни
кораблей начали там и сям бороздить
огромные просторы Галактики. Сообщения
об открытии планет потекли тонкой
струйкой, а потом хлынули потоком.
Год назад все накопившиеся сведения
о планетах, разбираться с которыми было
уже никому не под силу, ввели в
перегруженную Большую
вычислительную машину. Этому
придавалось такое значение, что ждать
очереди пришлось всего пять месяцев.
Машине был задан вопрос о планетах,
пригодных для жизни. Машина ответила,
выдав список, и Малышка возглавила
его.
Планета была разрекламирована на всю
Галактику. Преимущества Малышки были
стократно преувеличены. О ее плодородии,
климате и великом будущем шумели
повсюду. Это должно было стать
успешным началом правительственной
программы колонизации новых планет.
И тут кто-то наткнулся на давнишний
доклад одной санитарной экспедиции,
посвященный одной планете в одной
звездной системе, местонахождение и
описание которой в точности совпадало
с местонахождением и описанием
Малышки...
Положение решили спасать. На
Малышку направлена
экспедиция, в состав которой
вошли самые видные ученые
Земли, представители
различных научных
специальностей. Лишь один
участник экспедиции не был
ученым. Это был Марк
Аннунчио — юноша с
феноменальной памятью, один
из работников Мнемонической
службы, призванием которых
было накапливать и
запоминать самые
разнообразные сведения,
факты, числа. Не изучая ничего
всерьез, мнемонисты могли
делать то, что уже было не под
силу ученым, ушедшим в дебри
своих глубоко
специализированных наук.—
сопоставляя разнородные
факты, обобщать, питать
других оригинальными идеями.
Перед экспедицией была
поставлена задача: во что бы
то ни стало обнаружить
источник смертельной
опасности, затаившийся где-то
на планете двух солнц...
Экспедиция прибыла на
Малышку.
Геохимик Вернадский, что-то ворча, не
отрывался от газового анализатора.
— По-моему, мы находимся примерно на
уровне моря,— сказал он.— Судя по
величине 7- То есть гравитационной
постоянной,— добавил он. Большинство
присутствовавших все равно ничего не
поняло, но он продолжал:
— Атмосферное давление — около
800 миллиметров ртутного столба, значит,
процентов на пять выше, чем на Земле.
И из них 240 миллиметров — кислород,
а на Земле только 150. Неплохо.
Он как будто ожидал одобрительных
откликов, но ученые предпочитали как
можно меньше высказываться о чем-либо
из чужой области. Вернадский
продолжал:
— Ну, конечно, азот. Скучно — природа
Повторяется, как трехлетний ребенок,
который выучил только три урока.
Теряешь всякий интерес, когда видишь,
что планета, где есть вода, всегда имеет
кислородно-азотную атмосферу.
— Что еще есть в атмосфере? — спросил
астрофизик и начальник экспедиции
Саймон. Не заглядывая в свои записи,
Вернадский перечислил:
— От одной сотой процента до одного
процента водорода, гелия и двуокиси
углерода. От десятитысячной
до сотой процента метана,
аргона и неона. От миллионной до
статысячной процента радона, криптона
и ксенона. Все, что я могу из этих цифр
извлечь,— это то, что Малышка окажется
богатой ураном, бедной калием, и
неудивительно, что у нее такие
симпатичные ледяные шапки.
Это было сказано в расчете на то, что
кто-нибудь удивленно спросит, откуда он
знает, и кто-то, конечно, спросил.
Довольный Вернадский
покровительственно улыбнулся и
объяснил:
— Радона в атмосфере в 10—100 раз
больше, чем на Земле. Гелия тоже. Радон
и гелий образуются при радиоактивном
распаде урана и тория. Вывод: урановых
и ториевых минералов в коре Малышки
в 10—100 раз больше, чем в земной.
С другой стороны, аргона в сто с лишним
раз меньше, чем на Земле. Скорее всего,
первоначального аргона на Малышке
не осталось вовсе. А новый аргон на
планетах такого типа может образоваться
только из калия-40. Мало аргона — значит,
мало калия. Проще пареной репы.
— А насчет ледяных шапок? — спросил
кто-то.
— Двуокиси углерода примерно вдвое
меньше, чем на Земле, а она дает
парниковый эффект: пропускает к
поверхности коротковолновую
часть солнечного излучения, но не
выпускает наружу длинноволновое
тепловое излучение планеты. Когда
в результате вулканической деятельности
содержание углекислого газа повышается,
планета нагревается, и начинается
каменноугольный период с высоким
уровнем океанов и минимальной
поверхностью суши. А когда
растительность начинает поглощать
бедную двуокись углерода и поправляться
за ее счет, температура падает,
образуются ледники...
...Микробиолог Родригес-и-Лопес со
своей обычной тщательностью и
аккуратностью вырастил культуры
микроорганизмов из пыли, уловленной
газовым анализатором Вернадского,
— Ничего,— сказал он в конце концов.—
Те культуры, которые размножились,
выглядят совершенно безобидными.
Ему возразили, что бактерии Малышки
могут только казаться безобидными и что
токсины и метаболические процессы
нельзя изучить на глазок, даже
вооружившись микроскопом. Но Родригес
возмутился и, подняв бровь, заявил:
— У меня на это чутье. Кто с мое
поработает с микромиром, тот начинает
чуять, где опасность есть, а где — нет.
Это было, конечно, чистейшее хвастовство,
но Родригес доказал, что прав: он
тщательно перенес пробы из различных
колоний микробов в буферные
изотонические растворы и ввел их
концентрат привезенным с Земли
хомякам, что не произвело на них
никакого впечатления...
Первые следы погибшего поселения
обнаружил ботаник Фоукс, облетевший
планету на атмосферной ракете.
Вернувшись, он рассказывал:
— Обе большие реки текут в
меридианальном направлении: та, что
побольше, вытекает из северной полярной
шапки, поменьше — из южной. Они
сливаются в сотне миль южнее экватора
и текут в море, прорезая горный хребет.
Отсюда до берега около восьмидесяти
миль. Устье рек — идеальное место для
поселения. Даже если бы мы не знали
широты и долготы, я искал бы его именно
там. А поселенцы думали о будущем.
Именно там они и устроились.
— Во всяком случае, им казалось, что они
думают о будущем,— тихо заметил
психолог экспедиции Шеффилд.— От них,
наверное, немного осталось?
Фоукс постарался ответить как можно
спокойнее:
— Прошло больше ста лет, чего же вы
хотите? Дома были в основном сборными.
Они обрушились, и местность заросла.
Правда, из-за ледникового климата
деревья невелики и, очевидно, растут
медленно. Но все равно место поселения
заросло. С воздуха его можно узнать
только потому, что молодая поросль
окрашена иначе, чем окружающий лес.
Он показал привезенную
фотографию.
— Вот просто куча лома. Может быть,
здесь когда-то стояли механизмы. А это,
по-моему, кладбище...
— А останки? Кости? — спросил кто-то.
Фоукс покачал головой.
— Но не могли же последние, кто остался
в живых, сами себя похоронить?
— Вероятно, это сделали животные,—
ответил Фоукс. Он встал и отвернулся.
— Когда я пробирался там, шел дождь.
Он падал на плоские листья над головой,
а под ногами была мягкая, мокрая земля.
Было темно и мрачно. Дул холодный
ветер. На снимках это не чувствуется.
Но мне казалось, что вокруг — тысяча
призраков, которые чего-то ждут...
Тайна оставалась нераскрытой.
Родригес продолжал
утверждать, что ни микробы,
ни вирусы, живущие на
Малышке, не представляют
никакой опасности для
человека. Тогда было решено
перейти к следующему этапу
и высадить на место погибшего
поселения группу ученых,
которые продолжат изучение
планеты...
...Врач экспедиции Нови с
профессиональным хладнокровием
исследовал раскопанные останки десятка
поселенцев. Но это были всего лишь
рассыпавшиеся кости, по которым ничего
нельзя было сказать.
— Кажется, есть какие-то ненормальности
в костной ткани, — сказал он, но после
допроса с пристрастием признал, что это
могло быть и результатом столетнего
пребывания костей во влажной почве.
Перед глазами ученых снова и снова
вставала картина, преследовавшая их
даже наяву. Им виделась неуловимая
раса разумных обитателей планеты,
которые, затаившись в подземных
убежищах, выращивали грибки и споры
в поисках разновидности, губительной
для человека. Может быть, для своих
экспериментов они похищали детей.
А когда они нашли то, что искали, споры
ядовитыми тучами поплыли над
поселением...
Все знали, что это — плод фантазии. Но,
оставаясь один в лесу, каждый то и дело
резко оборачивался в ужасе, чувствуя на
себе пристальный взгляд чьих-то глаз,
скрывающихся в сумрачной тени
деревьев...
...Однажды вся группа сильно
встревожилась, хомяки и белые мыши
неожиданно отказались есть новые виды
травы, принесенной ботаником. А когда
эту траву стали подмешивать- в их
обычную пищу, животные погибли.
Занявшийся этими растениями
Вернадский скоро объявил:
— Медь, свинец, ртуть. Растения
содержат много тяжелых металлов.
Возможно, это эволюционное защитное
приспособление, чтобы их не ели.
— Значит, первые поселенцы...— начал
Саймон.
— Нет, это исключено. Эти растения
никто есть не станет.
— Откуда вы знаете?
Только этого Вернадский и ждал. Он
торжественно провозгласил:
— Вы видите перед собой скромного
мученика науки. Я их попробовал.
— Что?—вскричал Нови.
— Не беспокойтесь, Нови, я только
лизнул разочек. Я — из осторожных
мучеников. В общем, они горькие, как
стрихнин.
— А кроме того,— добавил Нови,
подумав,— поселенцы погибли не от
отравления тяжелыми металлами.
Симптомы были совсем другие.
Эти симптомы прекрасно знали все.
Затрудненное, болезненное дыхание,
и чем дальше — тем хуже. Вот и все...
...Приближался вечер. Лагранж-I стоял
уже низко над горизонтом. День выдался
ясный, теплый, и Вернадский был им
доволен.
Сейчас от него падала длинная красная
тень, и только нижняя ее треть,
совпадавшая с тенью от Лагранжа-П,
была серой. Он протянул руку, и она
отбросила две тени: нечеткую оранжевую
футах в 15 от него и более густую голубую
в той же стороне, но футах в пяти.
Поодаль появился Марк Аннунчио.
Вернадский отставил в сторону свой
нуклеометр и помахал рукой.
— Иди сюда!
Юноша робко приблизился.
— Тебе чего-нибудь надо?
— Я... я просто смотрел.
— Знаешь, что я делал?
Марк замотал головой.
— Это нуклеометр. Его втыкают в землю,
вот так. У него наверху — генератор
силового поля, так что его можно
воткнуть в любой камень.
Продолжая говорить, он нажал на
нуклеометр, и тот на два фута погрузился
в скальную породу.
— По бокам стержня есть
микроскопические устройства, каждое из
которых испаряет около миллиона
молекул окружающей породы и разлагает;
их на атомы. Потом атомы разделяются
по заряду ядер и массе, и результаты
можно прямо считывать вот с этих шкал^
Получается содержание различных
элементов в коре. На Малышке они
распределены очень равномерно.
Кислорода мало — в среднем каких-
нибудь 42,113%. Кремния тоже мало —
22,722%. Зато тяжелых металлов в
10—100 раз больше, чем на Земле.
Вернадский и сам не знал, зачем он все
это говорит мальчишке. Отчасти потому,
что всегда приятно иметь внимательного
слушателя. Когда не с кем поговорить
о своей профессии, иногда становится
одиноко и грустно. И он продолжал:
— Легкие элементы распределены
равномернее, чем на Земле. В океанах
здесь не преобладает хлористый натрий,
а довольно много солей магния. А литий,
бериллий и бор? Они легче углерода, но
на Земле и на других планетах
встречаются очень редко. А тут их многа,
Почти 0,4% коры, а на Земле — только
0,004%.
— А есть у вас цифры содержания в коре
всех элементов?
— Пожалуйста.
Вернадский вынул из заднего кармана
брюк сложенную бумажку и показал ее
Марку. Тот просмотрел цифры,
повернулся и зашагал прочь, не
попрощавшись.
Вернадский поглядел ему
вслед, пожал плечами, вытащил из земли
нуклеометр и тоже пошел в лагерь.
А на следующий день Марка
Аннунчио застали в тот момент,
когда сн подстрекал экипаж
корабля немедленно, сию
минуту покинуть планету.
Капитану с трудом удалось
уговорить людей подождать с
отлетом хоть немного — чтобы
только захватить и ученых.
По космическим законам
подстрекательство к мятежу
каралось смертью. На второй
день после того, как корабль
оторвался от поверхности
Малышки, состоялся суд над
Марком Аннунчио.
— Марк, зачем ты это сделал? —
спросил психолог доктор Шеффилд.
— Потому что нам всем нужно было
убраться с Малышки, не теряя ни
минуты. Это был самый быстрый способ.
— А почему нам так важно было
покинуть Малышку?
Марк, не колеблясь, посмотрел прямо
в глаза сидевшим против него ученым
и ответил:
— Потому что мы погибли бы от того же,
отчего погибла первая экспедиция. Это
был только вопрос времени. Может быть,
и сейчас уже поздно. Может, мы уже
умираем. И умрем все до единого.
— Почему же ты не рассказал все нам,
Марк?
— Потому что никто мне не поверил бы.
— От чего же, по-твоему, они умерли?
Все затихли. Марк огляделся вокруг
и ответил:
— От пыли.
Раздался общий хохот, и щеки Марка
вспыхнули.
— Что ты хочешь сказать? — спросил
Шеффилд.
— От пыли! Пыли, которая в воздухе!
В ней — бериллий. Спросите у доктора
Вернадского!
Вернадский встал и протолкался вперед.
— Причем тут я?
— Ну, конечно же,— продолжал Марк.—
Это было в тех листках, которые вы мне
показывали. Бериллия очень много в коре,
значит, он должен быть с пылью в воздухе.
— А что если там есть бериллий?
— Отравление бериллием, вот что! Когда
вы дышите бериллиевой пылью, в легких
образуются незаживающие грануломы.
Я не знаю, что это такое, но во всяком
случае, становится все труднее дышать,
и в конце концов вы умираете.
К всеобщему шуму прибавился еще один
возбужденный голос. Это был Нови:
— О чем ты говоришь? Ты же не врач!
— Знаю,— серьезно ответил Марк,-—но я
как-то прочитал очень старинную книгу
о ядах. Такую старинную, что она была
напечатана на настоящей бумаге.
— Ну и что ты прочел? — с недоверием
спросил Нови.— Ты можешь рассказать?
Марк гордо поднял голову.
— Могу сказать напамять. Слово в слово.
«Любой из двухвалентных металлических
ионов одинакового радиуса может
активировать в организме поразительное
разнообразие ферментативных реакций.
Это могут быть ионы магния, марганца,
цинка, железа, кобальта, никеля и другие.
Во всех этих случаях ион бериллия, у
которого такие же размеры и заряд,
действует как ингибитор. Поэтому он и
тормозит многие реакции, катализируемые
ферментами. Поскольку бериллий,
по-видимому, никак не выводится из
легких, вдыхание пыли, содержащей
бериллий, вызывает различные
метаболические расстройства, серьезные
заболевания и смерть. Известны случаи,
когда к летальному исходу приводило
однократное действие бериллия.
Первичные симптомы незаметны, и
признаки заболевания появляются
иногда через три года после контакта
с бериллием. Прогноз тяжелый».
Капитан в волнении наклонился вперед.
— Что он говорит, Нови? Есть в этом
какой-нибудь смысл?
— Не знаю, прав он или нет, — ответил
Нови, — но в том, что он говорит, нет
ничего невероятного.
— Вы хотите сказать, что не знаете,
ядовит бериллий или нет?
— Не знаю. Никогда об этом не читал.
Мне не попадалось ни единого случая.
Шеффилд повернулся к Вернадскому:
— Где-нибудь бериллий применяется?
Не скрывая своего изумления,
Вернадский ответил:
— Нет. Черт возьми, не могу припомнить,
чтобы он где-нибудь применялся.
Впрочем, вот что. В начале атомной
эпохи его использовали в примитивных
атомных реакторах как замедлитель
нейтронов, вместе с парафином и
графитом. В этом я почти уверен.
— Значит, сейчас он не применяется? —
настаивал Шеффилд.
— Нет.
Тут вмешался электронщик:
— По-моему, в первых люминесцентных
лампах использовались цинк-бериллиевые
покрытия. Кажется, где-то я об этом
слышал.
— И все? — спросил психолог.
— Все.
— Так вот, слушайте. Во-первых, все, что
цитирует Марк, точно. Значит, так и было
написано в той книге. Значит, бериллий
ядовит. В обычных условиях это неважно,
потому что его содержание в почвах
ничтожно. Когда же человек
концентрирует бериллий, чтобы
применять его в реакторах или лампах,
или даже в виде сплавов, он сталкивается
с его ядовитыми свойствами и ищет ему
заменителей. Он их находит, забывает
о бериллии, а потом забывает и о том,
что бериллий ядовит. А потом мы
попадаем на планету, необычно богатую
бериллием, вроде Малышки, и не можем
понять, что с нами происходит.
Астрофизик Саймон тихо спросил:
— А что значит «прогноз тяжелый»?
Нови рассеянно ответил:
— Это значит, что если вы отравились
бериллием, вам не вылечиться.
Саймон закусил губу и откинулся
в кресло.
Нови вздохнул и сказал:
— Предлагаю как можно скорее вернуться
на Землю и пройти медицинское
обследование.
— Но если мы все равно не
вылечимся, — слабым голосом возразил
Саймон, — то что толку?
— Медицина сильно продвинулась
вперед с тех пор, как книги печатали на
бумаге, — ответил Нови. — Кроме того,
мы могли получить не смертельную дозу.
Первые поселенцы больше года прожили
под постоянным воздействием бериллия.
Мы же подвергались ему только месяц —
благодаря быстрым и решительным
действиям Марка Аннунчио...
Система Лагранжа превратилась
в звездочку, затерянную
в оставшемся позади скоплении
звезд.
Шеффилд поглядел на это пятнышко
света и со вздохом произнес:
— А такая красивая планета... Ну что ж,
будем надеяться, что останемся в живых.
Во всяком случае, на будущее
человечество будет остерегаться планет
с высоким содержанием бериллия.
В эту разновидность ловушки для
простаков оно больше не попадет...
Перевод с английского
А. ИОРДАНСКОГО
НАШ КОММЕНТАРИЙ
В этой фантастической повести
содержится суровое
предупреждение ученого: космонавты
будущего на вымышленной
планете встретились со страшной,
но вполне реальной угрозой.
Аэрозоли бериллия в ее
атмосфере делают эту планету
неотвратимо гибельной для
каждого, кто ступит на ее
поверхность.
Это совсем не фантастика.
Азимов не преувеличил
токсичность бериллиевой пыли. Но
бериллий не исключение —
современная промышленность
выбрасывает в атмосферу
Земли бесчисленное множество
загрязнений, подчас не менее
страшных, чем аэрозоли
бериллия.
Уже теперь воздушные
бассейны больших промышленных
районов часто становятся почти
столь же гибельными, как
атмосфера на придуманной планете.
Известны страшные
катастрофы (в Лондоне, Нью-Йорке,
Лос-Анжелосе), когда погибали
сотни и тысячи людей,
отравленные загрязненным
промышленными выбросами
воздухом.
Забота о чистоте воздуха на
своем предприятии — долг
каждого химика, технолога и
инженера. Люди на прекрасной
планете Земля повсюду должны
дышать чистым воздухом. В
этом смысл фантастической
повести «Ловушка для
простаков». Это — предупреждение.
Академик
И. В. ПЕТРЯНОВ
И. ВОЛЬПЕР
Рисунки
Д. ЛИОНА
ЧТО
мы
ЕДИМ
ПИЩА БОГОВ
В ноябре 1519 года испанские
конкистадоры под водительством Эрнана Кортеса
ворвались в древнюю столицу Мексики город
Теночтитлан и захватили его. Легенда
утверждает, что, разграбив дворец
императора ацтеков Монтесумы, испанцы
обнаружили в дворцовых кладовых большие
запасы каких-то сушеных бобов. Кортес и
его спутники вскоре узнали, что ацтеки, во-
первых, использовали эти бобы вместо
монет, а во-вторых, готовили из них
своеобразный, острый напиток, который они
называли «чоколатль».
Среди множества легенд существовала
у ацтеков и легенда о дереве, дававшем им
плоды для чоколатля. Жил когда-то в
далекие времена волшебник-садовод Квет-
цалькоатль, у которого был замечательный
сад. Среди многих деревьев росло в этом
саду и какао-дерево, из плодов которого
люди готовили чоколатль. Но Кветцалько-
атль возгордился, возомнил себя
бессмертным, за что был наказан богами — лишен
разума. В безумии садовник разрушил сад,
уцелело только одно дерево — дерево
какао, оставшись на земле единственным
представителем волшебных деревьев.
Напиток чоколатль ацтеки готовили
так: разводили в горячей воде растертые
бобы какао и добавляли в этот раствор...
кайенский перец. Этот демократический
напиток Кортесу не понравился. Зато ему
пришлось по вкусу другое питье из какао,
которое готовилось специально для царя
Монтесумы. Жареные бобы какао
растирали вместе с зернами молодой кукурузы, к
этой смеси добавляли мед и уваренный
сладкий сок агавы, а все вместе сдабривали
ванилью. Считалось, что этот напиток Мон-
тесума пил только из золотой чаши.
Вернувшись в Испанию, Кортес привез
королю бобы какао и рецепты
приготовления чоколатля (европейцы произносили это
слово несколько иначе — шоколад).
Первое время новый продукт был известен
только при испанском королевском дворе,
через несколько десятилетий о какао
узнали во Франции. Но и там до середины
семнадцатого века никто, кроме королевы, не
пил шоколада. Только в середине XVIII
столетия напиток получил широкое
распространение. Судя по картине
французского художника XVIII века Лиотара,
появилась даже специальная профессия —
шоколадница.
Итак, родина шоколада или точнее де-
чегс:? несколько десятилетий о клкао у?на-
-м* и во Франции, но итим до серваины
семИМЧагОГО веМ никто, кроме кШаеш,
нёпил шокодлдл
^
\1Л *Ш%- Цуг
Мишка на Cefiene
рева какао — Южная Америка, Мексика.
Со временем это дерево перекочевало и в
Африку, и ныне «черный континент» —
основной производитель бобов какао. Более
половины всех какао-бобов в мире
поставляет Гана.
Историю культуры какао в Африке
связывают с именем кузнеца Тетте Куарши
из города Мампонг, который в 1876 году
побывал на острове Фернандо-По.
Вернувшись на Золотой берег (старое название
Ганы), Куарши привез с собой мешочек
бобов какао. Он посеял их на родной земле
и через четыре года собрал первый
урожай.
Предприимчивый кузнец продал
семена своим соседям, и те тоже заложили
«шоколадные плантации».
Плоды какао похожи на большие
заостренные на концах огурцы. Они достигают
тридцати сантиметров в длину, десяти-
двенадцати сантиметров в диаметре и
весят от трехсот до шестисот граммов. У
плодов какао желтая, оранжевая или
буро-красная плотная кожица и белая или
розовая мякоть, в которой пятью рядами
располагаются от двадцати пяти до
сорока семян. Это и есть какао-бобы —
сырье для изготовления какао-порошка и
шоколада. С одного дерева снимают от
пятисот граммов до двух килограммов бобов,
урожай с одного гектара — от пятисот
килограммов до тонны. Вынутые из плодов
какао-бобы ссыпают в кучи или
деревянные ящики. Сверху бобы укрывают
банановыми листьями. Температура в кучах
достигает 40—50°С. За неделю под
влиянием микроорганизмов сахаристые вещества
бобов превращаются в спирт и углекислый
газ. Из части спирта образуется уксусная
кислота, которая пропитывает бобы. Они
теряют способность прорастать. За это
время их цвет становится шоколадным.
Кроме того, расщепляется входящий в состав
бобов глюкозид какомин, благодаря чему
горечь их становится меньше.
После ферментации бобы сушат на
солнце или обжаривают на огне. Во время
этой операции заканчиваются все
биохимические процессы. Дальнейшее
приготовление какао-порошка и шоколада связано в
основном с процессами механическими
(хотя, конечно, каждая механическая
операция сопровождается химическими
изменениями, создающими в совокупности
структуру, цвет и аромат какао и
шоколада).
Бобы какао очищают от примесей, с
них снимают оболочку — какаовелу, затем
их измельчают и на гидравлических
прессах под давлением в 400 атмосфер
отжимают какао-масло. Жмых какао
размалывают и просеивают — так получается какао-
порошок. Величина частиц порошка
(отдельных пылинок) должна быть не
больше 10 микрон. Такой тонкий размол нужен
для того, чтобы при приготовлении
напитка порошок какао дольше не оседал на дно
чашки. Хорошее какао образует
суспензию, которая остается стойкой, по крайней
мере в течение десяти минут.
Из бобов, которые идут на изготовление
шоколада, какао-масло не отжимают. Их
дробят в крупку, а затем размалывают на
жерновах в жидкую массу тертого какао.
Тертое какао смешивается дополнительно
с какао-маслом, сахарной пудрой (сахар,
как правило, добавляют в соотношении
2: 1), добавляют немного ванилина и
других ароматических веществ, и вся смесь
тщательно размалывается — размер
твердых частиц шоколадной смеси не должен
превышать пятнадцати—двадцати микрон.
Из этой тонкодисперсной массы и
формуют шоколад.
По питательной ценности шоколад и
какао занимают первое место среди всех
пищевых продуктов. Из чего же
складываются высокие питательные качества
какао и шоколада, в чем их ценность? Бобы
какао примерно наполовину состоят из
жира — какао-масла, в них содержится до
15 процентов белковых веществ и от 6 до
10 процентов углеводов. Масло какао
плавится при сравнительно низкой
температуре C3—36°С), близкой к температуре
человеческого тела. Поэтому твердая
плитка шоколада приятно тает во рту. Оно
состоит из различных глицеридов. Самые
важные из них, составляющие более
70%, — олео-пальмито-стеарин и олео-ди-
стеарин. Какао-порошок богат солями
фосфора и калия.
Кроме того, в состав какао входит от
0,85 до 2,85 процентов физиологически
активного вещества — теобромина.
Теобромин — алкалоид, и в малой дозе он,
подобно кофеину, действует возбуждающе
на сердечно-сосудистую и нервную
системы. Теобромин — сильно действующее
средство: десять граммов его —
смертельная доза для человека. В шоколаде
содержится обычно около 0,4 процента
теобромина, доза совершенно безопасная, но
достаточная, чтобы придать шоколаду
тонизирующие свойства, способность снимать
усталость, повышать работоспособность.
Кроме теобромина, в какао-бобах
содержится 0,05—0,1 процент кофеина,
красный какао-пигмент, а также вещества,
создающие приятный тонкий аромат
шоколада и какао. Установлено, что
специфический запах какао обуславливают по
крайней мере 40 летучих соединений. Наиболее
важный из них терпеновый спирт — лина-
лоол. В ароматической смеси содержатся
также низшие жирные кислоты и их эфи-
ры — амилацетат, амилбутират, бутил-
ацетат.
При приготовлении шоколада и какао
в них добавляют сахар и молоко — и
содержание углеводов достигает сорока
процентов. Калорийность хорошего
шоколада — 600 килокалорий на сто граммов.
Желая подчеркнуть превосходные
качества какао, шведский натуралист Карл
Линней дал дереву какао ботаническое
название — «Какао теоброма» (Cacao the-
obroma). Слово «какао» Линней
позаимствовал у индейцев племени майя, а от себя
добавил два греческих слова «теос» (бог)
и «брома» (пища). Стало быть, шоколад —
это пища богов.
ШОКОЛАДНЫЙ НАБОР
Тонизирующее вещество какао-
бобов— теобромин было впервые
выделено из какао-бобов и
изучено 125 лет назад русским
химиком А. А. Воскресенским.
Сейчас теобромин
О
HN С—N—СН3
i if i °
о=с с сн
N N7
СН3
получают синтетически и широко
используют в приготовлении
лекарств.
Бобы какао отличаются
между собой по вкусу, аромату,
цвету.
Благородные сорта бобов:
«Криоло», «Криоло-Форастеро» и
«Тринитарио-Тип». Деревья этих
сортов очень чувствительны,
плодоносят поздно, урожай
небольшой. Чистое «Криоло»
встречается чрезвычайно редко. У бобов
«Криоло» необыкновенный вкус,
нежный цветочный аромат.
Самый распространенный
неблагородный сорт — «Форасте-
ро» (Чужеземец). Бобы «Форасте-
ро» терпкие, с сильным ароматом.
Деревья дают богатый урожай.
Кроме этих основных сортов,
есть еще множество других.
Чтобы различать их, нужен
многолетний опыт.
Фигурный шоколад обычно
завертывают в фольгу. Чтобы она
плотно облегала шоколад,
поступают так: неплотно завернутые в
фольгу конфеты загружают на
три минуты в специальный
вращающийся барабан, заполненный
мелкими без острых краев
зернышками — семенами люпина.
Зернышки, как маленькие
молоточки, стучат по фольге и
приминают ее в соответствии с формой
шоколадных фигурок.
Многие сорта шоколада
содержат поваренную соль — ведь она
входит в состав сливок и молока.
А иногда в молочный шоколад
даже вводят немного соли
дополнительно — как ни странно,
она улучшает вкус шоколада.
При формовке шоколада часть
плиток деформируется и
ломается. Их, конечно, не выбрасывают,
а разогревают, фильтруют
полученную массу и формуют ее
вторично. Но еще чаще
шоколадный лом используют для
приготовления начинок.
Если шоколад горчит, значит, в
нем мало сахара. А так как сахар
намного дешевле какао, то, есте-
ственно, горький шоколад —
самый дорогой.
ДОМАШНЕЕ ПРИГОТОВЛЕНИЕ
ШОКОЛАДА
В наши дни городскому, да и не
только городскому жителю,
трудно представить себе, что
дома можно испечь хлеб, сбить
масло, закоптить окорок или
изготовить шоколад.
Но каких-нибудь пятьдесят
лет назад это было самым
обычным делом. Прочитав старый
рецепт домашнего изготовления
шоколада, вы убедитесь, что
располагая большим запасом
времени и небольшим запасом
какао-масла (оно сейчас,
правда, продается только в аптеках),
не так уж трудно сделать
шоколад дома.
«Взять 1 фунт сладкого
миндаля, ошпарить крутым кипятком,
вычистить кожу, промыть
миндаль в холодной воде, сложить
на решето и поставить сушить.
Так же ошпарить '/2 фунта
чищенной фисташки, промыть в
воде и сложить на решето,
поставить сушить. Затем взять
7г фунта орехов полуфундуков
(без скорлупы), сложить на
сковородку, поставить в духовую
печь и хорошенько пожарить
(но не пожечь), вынуть,
высыпать на редкое решето и
просеять сквозь него, чтобы
очистились орехи от кожи.
Затем сложить отдельно на
сковородке миндаль и
фисташку и прожарить. Как немного
зарумянится, сейчас же вынуть,
соединить вместе, мелко
изрубить, затем сложить в ступку
(если есть ступка каменная или
мраморная, то можно толочь
сразу, а если нет, то толочь
понемногу в медной ступке).
Между тем взять 5 фунтов
сахарного песку, выложить его
в кастрюльку, налить 2 бутылки
воды, размешать, поставить на
плиту, дать чтобы вскипело,
снять, процедить сквозь чистое
сито, вылить в ту же
кастрюльку, положить 3 палочки
ванилина, поставить на плиту и
варить до такой поры, что когда
сахар прокипит не менее 7г
часа, то взять чайной ложкой на
кснчике немного кипящего
сахару и сейчас же опустить
ложку в холодную воду, если же
оставшийся на ложке сахар
будет густой и крепкий, то
значит варить довольно. Тогда
снять его с плиты и выливать
понемногу в массу, которую в
ступке и толочь, как можно
меньше.
Затем взять 3 фунта какао,
сложить в кастрюлю, налить
в сотейник кипятку, поставить
кастрюлю с какао в нее и греть
на пару, мешая лопаткой. Как
какао разойдется и не будет
кусочков, то сейчас же вылить его
в приготовленную массу,
хорошенько размешать, взять
Vs фунта масла какаового,
разогреть его и вылить туда же.
Приготовить какой-нибудь
поднос, предварительно тщательно
вымытый и насухо вытертый,
а если есть небольшие
формочки, то лучше выложить в них,
вынести на ледник, обложить
льдом и как застынет, стукнуть
об стол каждую формочку и
вынимать.
Примечание:
Приготовленный таким способом
шоколад выходит гораздо вкуснее
покупного и обходится дешевле.
(Библиотека журнала «Домашний
ремесленвик», № 21, 1913. СПб.)
Инженер
О. М. ЛИБКИН
КАК ДЕЛАЮТ ШОКОЛАД?
Не сомневаемся — вопрос этот интересовал и интересует
очень многих. Сразу же должны извиниться перед
читателем: ответ на него не будет сопровождаться снимками.
Все операции при изготовлении шоколада идут в
закрытых машинах, но дело не только в этом. В цехи очень
неохотно пускают фоторепортеров: все-таки стекло... И
посылая на Московскую фабрику «Красный Октябрь»
сотрудника редакции, мы решили руководствоваться
известной пословицей о монастыре и уставе.
Все начинается с сортировки и очистки.
Бобы просеивают через сита, чистят
щетками и обдувают воздухом (конечно, в
машине). Сильным магнитом проверяют, не
попала ли в них чудом хоть соринка
железа. После этого бобы направляют на
термическую обработку или, проще, — на
обжарку.
Запах в тех отделениях, где
обрабатывают бобы, отнюдь не благовонный. Но
цель обработки в том и состоит, чтобы
избавиться от этого запаха, удалить из
бобов какао примеси, прежде всего —
дубильные вещества и летучие органические
кислоты.
В весьма внушительной сушилке бобы
обдувают горячим (до 180°С) воздухом. Из
них удаляется влага — значит, их легче
будет дробить. Одновременно с этим
удаляются и органические кислоты,
например, уксусная (сырые бобы имеют слабый
уксусный запах, а кто будет есть шоколад
с уксусом?). Уменьшается количество
водорастворимых дубильных веществ, и
вяжущий вкус, свойственный сырым бобам
какао, смягчается. Кроме того, при сушке
погибают все микроорганизмы.
Охлажденные бобы идут в дробилку —
вполне современную машину, с одной
стороны которой выходит крупка какао, а с
другой — оболочка, какаовелла. Чем
мельче крупка, тем больше в ней
непитательной и безвкусной какаовеллы. Поэтому
самую крупную крупку берут для
приготовления высших сортов шоколада (скажем,
«Золотого ярлыка»), а ту, что помельче, —
для глазури и начинок.
У каждого шоколада — своя рецептура,
и в нее входит несколько сортов
какао-бобов. Крупку разных сортов можно уже
смешивать. Можно смешивать какао и
после дальнейших операций, а вот неразмо-
лотые бобы — нельзя: у разных сортов
разные размеры, и обжарятся бобы
неравномерно. Названия этих сортов
таинственны и звучат, как заклинания: Тринидад,
Пуэрто-Кабелло, Ариба, Аккра...
После дробления наступает время
измельчать крупку, растереть ее настолько,
чтобы разрушились клеточные стенки
бобов и освободилось масло какао. Из
мельниц (например, дисковых) вытекает густая
горячая масса — тертое какао. Из него
можно выжать на прессе масло. Остаток,
весьма непоэтично называемый жмыхом,
снова мелют, и он получает изящное и
знакомое всем имя — порошок какао. А
масло потом прибавят к тертому какао, чтобы
получился нежный, жирный шоколад.
Кроме масла, добавят еще и сахарную
пудру. Этих трех компонентов уже достаточно,
но во многие сорта шоколада добавляют
еще сухие или сгущенные сливки (или
молоко), орехи, кофе, ванилин, эссенции. Все
это дозируется и смешивается на рецеп-
турно-смесительной станции с
автоматическим электронным управлением.
Прежде чем тертое какао попадет в
смеситель, оно подвергается еще одной
обработке, на этот раз — сугубо химической.
К нему добавляют небольшое количество
углекислых солей, чаще всего — питьевой
соды. От этого вкус шоколада становится
намного приятнее. Улучшение вкуса
объясняют тем, что такие соли нейтрализуют
остатки кислот и способствуют лучшему
окислению дубильных веществ. Кроме
того, в присутствии этих солей образуются
высокомолекулярные соединения,
придающие шоколаду яркую окраску.
Шоколадная масса, вышедшая из
смесителя, уже съедобна, но это еще не
шоколад. Ее нужно снова измельчать, и эту
работу выполняют валковые машины.
Пластичную шоколадную массу
пропускают между валками, которые вращаются
навстречу друг другу с разной скоростью,
и перетирают все мало-мальски крупные
частицы (те, размер которых больше
30 микронов). Если читатель видел, как
вальцуют резину или полимерные пленки,
то он вправе утверждать, что знает, как
вальцуют шоколад, — настолько похожи
эти операции. Только вместо черного
резинового листа с валковой машины сходит
порошок приятного шоколадного цвета.
Порошок получается потому, что размер
частиц уменьшился, а значит, их
поверхность увеличилась, — и жира уже
недостаточно, чтобы смочить все частицы.
Поэтому шоколадную массу вымешивают
опять, добавляя к ней масло какао, и
разводят тем же маслом с добавкой разжижи-
теля.
О разжижителях стоит сказать
несколько слов. По сути дела — это
эмульгаторы, которые помогают равномерно
распределить жир в шоколадной массе.
Они должны быть гидрофильными
(хорошо набухать в воде) и липофильными
(хорошо соединяться с жирами). Этими
свойствами обладает лецитин, представитель
группы фосфатидов. Его получают из сои
или подсолнечника, но предпочитают
соевый лецитин, так как подсолнечный имеет
неприятный привкус. Разжижителя
добавляют всего три килограмма на тонну, и это
дает возможность сэкономить сорок
килограммов куда более дорогого масла какао.
Теперь можно уже формовать
шоколад — «Аленку» или «Чайку». Но дорогие,
десертные сорта шоколада проходят еще
одну стадию обработки — отделку.
Представьте себе огромное, килограммов на
тысячу, корыто, заполненное горячим
жидким шоколадом, который находится
все время в движении, подгоняемый
валиками. Частицы тертого какао и сахара
ударяются друг о друга, о стенки и валики;;
естественно, что они округляются и
уменьшаются в размере. После трех суток (!)
отделки шоколад выгружают, и теперь он в
самом деле тает во рту. К тому же масло
очень равномерно распределяется в массе
шоколада, а остатки дубильных веществ
переходят в нерастворимую форму.
Шоколад — продукт капризный. Если
сразу после отделки (или разводки) его
охладить, то вкус у него будет грубый.
Твердые частицы соберутся в крупные
агрегаты, сцементированные маслом. А на
поверхности шоколада выступит серый
налет, который специалисты именуют
жировым поседением. Масло какао полиморфно
и кристаллизуется в четырех формах, но
только одна из них — стабильная. И если
перед формовкой шоколад нагреть выше
31°С, то масло будет кристаллизоваться в
неустойчивой форме и «поседеет». А если
температура упадет ниже 29°С, то шоколад
не вынуть из формочки. Выход есть
только один: перед разливкой в формы
температура шоколада должна быть точно
между 29 и 31°С. Такую температуру
поддерживают в специальных темперирующих
машинах^
Наступает пора весьма ответственной и
самой наглядной операции — формования
шоколада. Там, где эта операция
совершается, никаких посторонних запахов уже
нет, все идеально чисто (как, в впрочем, и
на всей фабрике). Разливка шоколада
происходит автоматически и выглядит весьма
прозаично. Формочки движутся на
конвейере, из воронки в них льется точно
отмеренная доза шоколада, и наполненные
формы поступают на вибротранспортер,
который «вытряхивает» из шоколада
воздушные пузырьки. Затем шоколад быстро
охлаждают, чтобы не образовались
крупные кристаллы, формочки переворачивают,
и из них выпадают готовые плитки. Если
же делают шоколад с начинкой, то после
заливки формочку переворачивают вверх
дном; шоколад стекает в поддон, а на
формочке остается лишь тонкий его- слой.
Потом формочка принимает нормальное
положение и заполняется сначала начинкой,
а затем еще одним слоем шоколада.
Осталось совсем немного: завернуть
шоколад в фольгу и красивую этикетку,
уложить в картонные футляры и отправить в
магазин. Потом эта плитка попадет к
ребятам, которые будут мечтать попасть
когда-нибудь туда, где делают шоколад:
во-первых, интересно, как это его делают,
а во-вторых, говорят, там его можно есть
сколько хочешь...
ТРИ ВОПРОСА
ЗАМЕСТИТЕЛЮ НАЧАЛЬНИКА
ТЕХНИЧЕСКОГО ОТДЕЛА
ФАБРИКИ «КРАСНЫЙ ОКТЯБРЬ» В. М. ТА-
РАТУНИНОИ
1. Ваша фабрика выпускает
пористый шоколад. Чем он
отличается от обычного!
Он нежнее и приятнее на вкус и,
конечно, легче. А по рецептуре —
ничем не отличается.
Шоколадная масса готовится точно так же,
как и для десертного шоколада.
Только при разливке форма
заполняется не доверху, а на %
высоты. Форму ставят в
вакуум-камеру, и при разрежении
пузырьки воздуха, которые попали в
массу во время отделки,
увеличиваются в объеме. Воздушные
поры, пронизывающие шоколад,
придают ему своеобразную, очень
приятную консистенцию.
2. В магазинах продают шоколад
в блоках, без завертки. Из чего
его делают!
Из тех же продуктов, что и
любой шоколад без добавлений, —
из тертого какао, сахарной пудры
и какао-масла. Шоколад в
блоках — это шоколадная глазурь,
точно такая же, какой покрывают
конфеты. И предназначен этот
шоколад для кулинарных целей.
Это, конечно, не означает, что его
нельзя есть просто так. Может
быть, он недостаточно красив, но
это — натуральный шоколад.
3. Почему в магазинах не
продают шоколад в порошке для
приготовления напитка! Нельзя
ли с этой целью размолоть
обычный шоколад!
У шоколада в порошке — своя
рецептура. В порошке
содержится меньше масла какао. Поэтому
и нельзя для приготовления
жидкого шоколада использовать
шоколад в плитках — жир будет
просто плавать в чашке. Наша
фабрика выпускает шоколадный
порошок, но пока — только в
крупной расфасовке. Насыпать
шоколад в банки приходится
вручную: шоколадный порошок
жирнее порошка какао, поэтому
он легко собирается в комки. Все
же мы предполагаем выпускать
его и в маленьких баночках, для
розничной продажи.
НАЧАЛЬНИКУ ЦЕНТРАЛЬНОЙ
ЛАБОРАТОРИИ ФАБРИКИ Л. П
ДМИТРИЕВОЙ
1. Какие анализы делает
лаборатория!
Мы определяем содержание
жира и сахара, влажность шоколада,
степень измельчения. В цехе все
анализы выполнять нельзя:
степень измельчения, например,
определяют, растворяя шоколад
в керосине. Естественно, керосин
в цех вносить запрещается...
2. Почему шоколад обязательно
заворачивают в
парафинированную бумагу и фольгу!
Чтобы сохранить его «товарный
вид». Если шоколад
увлажнится, то на его поверхности может
выступить сероватый налет. Дело
в том, что влага растворяет сахар
на поверхности шоколада, и
сахар выделяется из раствора в
виде крупных кристаллов. Поэтому
мы твердо оговариваем, при
какой температуре и влажности
нужно хранить шоколад, —
может случиться так, что и фольга
не спасет.
3. Вы входите в дегустационный
совет фабрики. Чем вы
руководствуетесь при оценке новых
сортов шоколада!
Это настолько субъективно...
Впрочем, каким объективным
методом можно определить,
достаточно ли эссенции? Мы
оцениваем и аромат, и консистенцию
шоколада. А критерий один:
вкусно — невкусно.
«В трюмо испаряется
чашка какао...»
Б. Пастернак
В окнах и полированных досках
столов испаряется множество
чашек с горячим шоколадом:
недавно в Москве открылось кафе
«Шоколадница», где горячий
шоколад •— самый главный напиток.
А все остальные блюда в этом
кафе приготовлены обязательно
с добавлением шоколада.
Но и те, кто живет далеко от
«Шоколадницы», смогут
испробовать божественный напиток —
кондитерские фабрики обещают
начать выпуск шоколадного
порошка, из которого варят
шоколадный напиток, в мелкой
расфасовке.
А рецепты, которыми
пользуются повара кафе
«Шоколадница», мы печатаем сейчас.
ШОКОЛАДНЫЙ НАПИТОК
Тщательно растереть
шоколадный порошок, залить его крутым
кипятком и, чтобы напиток стал
однородным, поставить на один
час на горячую плиту. Пьют
шоколад горячим (хорошо, если
температура напитка градусов
пятьдесят). К горячему шоколаду
подают сбитые сливки.
Шоколадного порошка — 33
грамма, воды — 67 граммов,
сливок — 50 граммов.
ШОКОЛАДНЫЙ СОУС
Растереть шоколадный порошок,
смешать его со сгущенным
молоком и залить водой. Вскипятить
помешивая, а затем поставить на
горячую плиту на один час (не
мешать).
Соус подается к рисовым и
творожным пудингам, вареникам,
оладьям, омлетам.
Шоколадного порошка — 35
граммов, сгущенного молока —
110 граммов, воды — 60 граммов.
в. овчаров ЭТИКЕТКИ ЗА 100 ЛЕТ
У конфетной обертки есть своя
история, наверное, не менее
увлекательная, чем у почтовой
марки. Слово «наверное»
пришлось вставить потому, что
среди множества
коллекционеров собиратели «фантиков» —
редкость. А ведь конфетная или
шоколадная этикетка — это
интереснейший исторический
документ, одна из
многочисленных «визитных карточек»
своего времени.
Сто лет назад на набережной
Москва-реки, неподалеку от
Кремля выросло кирпичное
здание, увенчанное огромной по
тем временам трубой. В том же
году труба задымила, а в
кондитерских магазинах на
Петровке и Арбате, у Ильинских
и Мясницких ворот впервые
появились изделия «Паровой
бисквитной фабрики
товарищества Эйнем». Это та самая
фабрика, из которой выросло одно
из крупнейших кондитерских
предприятий — «Красный
Октябрь».
Немец Эйнем создал
«собственное дело», когда в Москве
был уже добрый десяток
подобных фабрик и более опытные
конкуренты выпускали
шоколад и конфеты, которые
пользовались большим спросом. Но
не потому, что были слаще или
вкуснее. Шоколад «Зоология
рыб», который выпускало
«Товарищество Абрикосова», не
залеживался на прилавках
магазинов явно благодаря
этикеткам — на их оборотной
стороне покупатель мог прочесть
описание «любимых мест ше-
респера и способов его ловли».
Не менее популярным был и
«Этнографический» шоколад, на
этикетке которого было
изображение какой-либо
национальной одежды.
Не отставали и другие
фабриканты. Фабрика Сиу
продавала шоколад с баснями и
целую серию «Новый век» с
наивными, а иногда просто
вульгарными стихами.
Например:
Циклисты наши на Луне
За самоваром отдыхают,
Забывши о стальном коне,
О новом веке рассуждают
«Товарищество Эйнем»
пытается обойти соперников. Оно
выпускает шоколад с
загадочными картинками. Появляются
призывы: «Новость! Интересный
подарок для детей.
Шоколадные кубики «Маленький
архитектор». И тому подобное.,.
Среди множества
дореволюционных этикеток редко
встретишь сделанную со вкусом.
Ярких — сколько угодно,
красивых — мало. Сладкое
предпочитали завертывать в слащавое.
После революции облик
шоколадной обертки изменился.
На место двуглавого орла встал
герб молодой республики — его
можно видеть на многих
этикетках первых лет Советской
власти. Государственная
кондитерская фабрика «Красный
Октябрь» помещает герб в центре
этикетки.
Для конфетных оберток
двадцатых годов характерен
злободневный рисунок и текст,
написанный плакатным
языком. «Законодатель» этого
направления — Маяковский. Он
не только пишет рекламы для
Моссельпрома («Где конфеты
дешевле и лучше? Убедись сам!
Беги по этим адресам»), но и
создает этикетки. Маяковский
прославляет Красную Армию и
пропагандирует вводимые в то
время метрические меры
(«...чтоб каждый запомнить мог.
Четыре сантиметра — один
вершок»). Лучшие конфетные
этикетки Маяковского (созданные
с художником А. Родченко),
например, «Наша индустрия»,
вместе с рекламными
плакатами экспонировались в 1925 году
на Парижской художественно-
промышленной выставке и
были удостоены дипломов и
серебряных медалей.
В тридцатых годах в
кондитерских магазинах можно было
купить... азбуку. Азбука из
«фантиков» рассказывала о
советском Аэроплане, о
непривычном еще Метро и подвигах
Челюскинцев. В те же годы на
конфетах появились
изображения автомобилей и тракторов,
дирижаблей и парашютов.
Строгий милиционер с этикетки
стал учить школьника правилам
уличного движения.
Об этикетках последних лет
мы не рассказываем —
читатель хорошо знаком с ними.
У ребят всегда было в моде
собирать «фантики». Не все
родители одобрительно относятся
к этому занятию, да и сами
юные коллекционеры
постепенно остывают к нему. Жаль!
Много лет спустя эти фантики
могли бы рассказать в весьма
оригинальной форме о нашем
времени. Ведь интересно же нам
разглядывать обертки столетней
давности, которые
воспроизведены здесь в журнале.
КО
ИЗ ПИСЕМ В РЕДАКЦИЮ
«Вы пишите, что разработан
метод уничтожения в озерах
«сорной рыбы», и, мол, уже через
два года все будут кушать из
этих озер разных сигов, форелей
и прочих. А на деле? Такие
«опыты» уже были устроены в
Псковской области. Сейчас эти озера
превратились в вонючие
водоемы, на берегах которых гниет
рыба. Лисы и птицы, хватая
рыбешку, отравляются также. Местность
вокруг озер стала прямо-таки
«зоной пустыни».
Это письмо пришло в редакцию
через несколько дней после
выхода в свет октябрьского номера
нашего журнала, где была
опубликована статья А. Г. Гусева
«Химия и рыба» с упоминанием о
химическом методе уничтожения
«сорной рыбы» в озерах. Мы
позвонили в Ленинград, в
Государственный институт озерного и
речного рыбного хозяйства. И вот
что рассказал нам сотрудник
института профессор Е. В. БУРМА-
КИН:
— Да, мы действительно
разработали химический метод рыбо-
хозяйственного преобразования
озер. Этот простой, удобный и
дешевый метод позволяет
«облагораживать» рыбное население
закрытых водоемов. Мелкая
сорная рыба, против которой он
направлен, не имеет никакого
рыбохозяйственного значения, а
только конкурирует с ценными
породами, уничтожая их
кормовую базу. Отловить ее всю
невозможно: какая-то часть —
несколько килограммов на
гектар — обязательно избежит
сетей. Тут-то и добавляют в воду
озера (не всякого, а только
изолированного от рек и других
озер) ядовитое для рыб
вещество — полихлорпинен. Для
теплокровных животных этот препарат
в применяемых концентрациях
не опасен. Оставшаяся в озере
рыба погибает и, действительно,
на первых порах попадает на
берега, ложится на дно. Но бить
тревогу рано: пройдет год — и
вода в озере, казалось бы,
безнадежно отравленном,
превращается из «мертвой» в «живую»
в нее можно запускать рыбу
ценных пород, которой уже не
грозит конкуренция со стороны
прожорливой мелочи.
Преобразовывать таким
способом рыбохозяйственные водоемы
в десятки раз выгоднее, чем рыть
специальные пруды.
С 1959 года наш институт, а
также и другие организации
в широких масштабах применяют
этот метод в водоемах страны, в
частности, — ив Псковской
области. Здесь обработанные по
нашему методу озера дают в
среднем за год по 100—150, а
иногда и до 400 кг ценной рыбы
с гектара вместо 5—15 кг сорной
рыбы до обработки. К
сожалению, автор письма не указывает,
какие именно озера он имеет в
виду, так что конкретных
результатов проведенных там работ я
сообщить не могу. Можно
сказать лишь одно: такого случая,
чтобы использование нашего
метода превращало озера и их
окрестности в «зону пустыни»,
еще не было и, при правильном
применении метода, не должно
быть. В этом убеждают
многочисленные опыты, проведенные за
последние 8 лет. Не возникает
угрозы и для здоровья людей:
население широко оповещается
о том, что погибшую рыбу есть
не рекомендуется. За все время
применения нашего метода
случаев отравления
зарегистрировано не было.
Конечно, используя любые
химические средства, нужно делать
это разумно, соблюдая все
инструкции и указания. Только при
этом условии мы можем
гарантировать безопасность нашего
метода для окружающей
природы.
Мы обратились также к
начальнику отдела науки Министерства
рыбного хозяйства РСФСР В. В.
ЛАВРОВСКОМУ. Он сказал:
— Известно, что «химия» —
вернее, те разнообразные
химические вещества, что попадают в
реки и озера со сточными водами
промышленных предприятий,
наносят исключительно большой
ущерб нашему рыбному
хозяйству. Тем более важно, продолжая
и усиливая борьбу с загрязнением
природных водоемов,
использовать то полезное, что может нам
дать настоящая химия.
Возможности ее огромны. Одним из
примеров может служить и метод
преобразования озер,
разработанный ГосНИОРХом. Он уже
приносит большую пользу
рыбному хозяйству, дает серьезный
экономический эффект.
Конечно, нельзя считать этот
метод в его нынешнем виде
верхом совершенства. Сейчас перед
учеными поставлена задача
сократить сроки детоксикации
водоемов — сделать так, чтобы
после обработки они становились
пригодными для рыбы не через
один-два года, а спустя считанные
дни. И здесь мы опять-таки
надеемся на помощь химиков. Вот,
например, сахарные заводы
сбрасывают в реки и озера в составе
своих сточных вод большие
количества сапонинов. Эти сложные
органические вещества из группы
глюкозидов — сильнейший яд для
рыбы. Но именно это их свойство
можно обратить на пользу
рыбному хозяйству. Сапонины
быстро разлагаются в воде, и если
обрабатывать озера ими вместо
полихлорпинена, то сроки
детоксикации можно было бы намного
сократить. Мы надеемся, что
химики-органики разработают
способ извлекать сапонины из
сточных вод в чистом виде и
превратят эти вещества из врага
рыбоводов в их союзника.
НОВОСТИ ОТОВСЮДУ
НОВОСТИ ОТОВСЮДУ
НОВОСТИ ОТОВСЮДУ
ОБУВНЫЕ КОНСЕРВЫ
Сколько времени можно хранить
обувь? Сколько угодно — если
законсервировать. О том, как это
делается, рассказал немецкий
журнал «Schuh—Technik» A966,
№ 8).
Оказывается, делается это
очень просто. Обувь помещают
в жестяную коробку с
прокладками (чтобы не болтались при
транспортировке) и закрывают
герметичной крышкой на винтах.
Когда коробку раскупоривают,
обувь выглядит совсем новой —
ни краска, ни кожа не портятся.
Для этого внутрь коробки перед
упаковкой вводят
дезинфицирующие препараты. Некоторые
фирмы уже приступили к выпуску
«консервных банок» для
башмаков.
ВИТАМИН ПРОТИВ СТОЛБНЯКА!
В августе прошлого года журнал
«Science News» сообщил, что
сотрудник Калькуттского
университета доктор П. К. Дей
разрабатывает новый способ лечения
столбняка. Это тяжелое
заболевание вызывается проникновением
в нервные ткани токсинов,
выделяемых столбнячной палочкой,
в результате чего у больного
начинаются сильнейшие судороги.
Примерно такая же картина
наблюдается и при отравлении
стрихнином. Ранние опыты
доктора Дея показали, что действие
стрихнина на организм можно
нейтрализовать инъекциями
витамина С — аскорбиновой кислоты.
Как оказалось в дальнейшем,
точно так же можно предотвратить
конвульсии и при столбняке.
Будет ли применено открытие
доктора Дея в медицинской
практике, сказать трудно: опыты
проводились пока еще только на
крысах.
ЕЩЕ ОДНА ЧАСТИЦА!
В результате совместного
эксперимента, проведенного
несколькими европейскими
лабораториями, обнаружена новая
элементарная частица — 1-мезон с массой,
почти равной двум массам
протона. Частица была получена при
бомбардировке ядер водорода
к-мезонами.
Время жизни 1-мезона
невелико: через 10~22 секунды он,
минуя несколько промежуточных
стадий, распадается на k-мезон и
два-три ^ -мезона, которые в
свою очередь менее чем
через 10~6 секунды тоже
распадаются.
Для того чтобы сделать это
открытие, понадобилось
проанализировать 200 000
стереофотографий. Обработка полученных
данных на быстродействующей
электронной вычислительной
машине заняла несколько сот часов.
ЛАКОВОЕ ЗЕРКАЛО
Как заставить обычное лаковое
покрытие отражать свет, подобно
зеркалу? Оказывается, для этого
достаточно ввести в лак на
основе летучего растворителя
стеклянные бусинки диаметром
около 50 микронов и тонкие
металлические чешуйки. Бусинки
образуют двояковыпуклый монослой
на лаковой поверхности и как бы
проецируют свет на
металлический «отражатель». Такой
сверкающий лак запатентован
недавно в США.
Не следует, однако, думать,
что из любого лака, любых бусин
и чешуек можно приготовить
такое блестящее покрытие. Лак
должен иметь строго
определенную вязкость, твердые частицы —
строго определенные размеры;
кроме того, необходимо, чтобы
показатель преломления бусинок
был равен примерно 1,8.
В3 И ШИЗОФРЕНИЯ
Американские психиатры Ос-
монд и Хаффнер предложили
новый способ лечения
шизофрении. Они установили, что в мозгу
у предрасположенных к этому
заболеванию людей
накапливается большое количество адрено-
лютина — вещества,
образующегося при разложении адреналина.
Это, по их мнению, препятствует
нормальному ходу химических
процессов в мозгу и составляет
одну из причин болезни.
Оказалось, что адреналютин
разрушается под действием больших
доз витамина Вз — ниацина.
В своей книге, вышедшей
недавно в Соединенных Штатах,
авторы утверждают, что из 1 000
больных шизофренией, подвергнутых
лечению витамином Вз,
выздоровели 750.
ЦЕНА ДРАГОЦЕННЫХ
МЕТАЛЛОВ
Американский журнал «СпегшсаГ
and Engineering News» A966,
№ 41) опубликовал материалы,
свидетельствующие о
значительном росте спроса на драгоценные
металлы платиновой группы.
Главными потребителями этих
металлов стали химическая, нефтяная
и электротехническая
промышленность. По сравнению с ними
доля ювелирного дела совсем не
велика.
Одновременно журнал
опубликовал нынешние американские
цены на эти металлы. Самый
дешевый из них — палладий, его
цена — 1,16—1,23 доллара за
грамм. Вторым идет рутений,
грамм которого стоит около 2
долларов. Платина на третьем
месте — 4,8 доллара за грамм.
Далее идут иридий E,82—6,00) и
родий F,95—7,05). Самый
дорогой металл платиновой группы —
НОВОСТИ ОТОВСЮДУ
новости отовсюду
новости отовсюду
осмий. Грамм его стоит 8,12—
8,80 доллара.
В сведениях о потреблении
обратная картина. В 1965 году в
США было использовано всего
46,2 килограмма осмия, а
палладия — свыше 20 тонн. Годовой
расход платины составил 11,6
тонны.
БАКТЕРИИ ПРОТИВ
ВЫХЛОПНЫХ ГАЗОВ
Журнал «New Scientist» A966,
№ 513) сообщил, что в Японии, в
лаборатории «Хоко сайенс»,
открыто вещество бактериального
происхождения, позволяющее
уменьшить загрязнение воздуха
выхлопными газами. Это
вещество обладает сильным
окислительным действием, оно эффективно
нейтрализует вредные сернистые
соединения. Своеобразный
окислитель получен из микробов
шестнадцати типов. Химический
состав его пока неизвестен.
СУХОЙ СОК
В стакан кладут 30 граммов сухих,
неаппетитных на вид хлопьев,
доливают холодной водой —
и спустя минуту можно пить
яблочный сок...
Технология приготовления
хлопьев такова. Обычный
яблочный сок испаряют на барабанах,
нагреваемых изнутри паром. На
их поверхности образуется
пленка, которую охлаждают сухим
холодным воздухом и
соскребают с барабанов. Получаются
хлопья, которые могут
храниться, не слипаясь, в герметической
таре при температуре до 30°С.
ЕЩЕ ВОСЕМНАДЦАТЬ
СВЕРХПРОВОДЯЩИХ
Английский журнал «New
Scientist» A966, № 512) сообщил о
получении еще восемнадцати
сверхпроводящих сплавов с общей
формулой АзВ, где А — хром,
ванадий, титан, ниобий или
молибден, а В — осмий, иридий,
платина, родий или золото.
Некоторые из этих сплавов становятся
сверхпроводниками уже при 15°
абсолютной шкалы. Наиболее
подробно описан сплав хрома и
ниобия, обладающий характерной
кристаллической структурой. Он
переходит в состояние
сверхпроводимости при 4,03° абсолютной
шкалы. Получают этот сплав
расплавлением смеси хрома с
99,999%-ным ниобием в среде
аргона и гелия. После
затвердевания сплав подвергается
дополнительной термообработке.
УРАНА МОЖЕТ
НЕ ХВАТИТЬ
Американский журнал «Chemical
and Engineering News» A966,
№ 39) опубликовал заметку о
настоящем и будущем атомной
энергетики в США. Сейчас
атомные электростанции дают лишь
0,3% электроэнергии,
вырабатываемой в этой стране. Однако к
1980 году их доля достигнет 25%,
а мощность будет равняться
80—110 миллионам киловатт. Это
увеличит дефицит уранового
сырья, который Соединенные
Штаты испытывают уже теперь.
МИКРОБЫ
В АТОМНОМ РЕАКТОРЕ
Специалисты Японского научно-
исследовательского института
атомной энергии обнаружили
колонии микробов в радиоактивных
теплоносителях ядерных
реакторов.
Присутствие микробов в
теплоносителе — не только
интересный феномен, но и серьезная
помеха в работе реактора.
Микроорганизмы, отлагаясь на стенках,
ухудшают циркуляцию воды,
охлаждающей реактор. Для
ликвидации этой помехи японские
ученые рекомендуют регулярно
прогонять через всю систему
растворы химических моющих
средств.
ТЫСЯЧЕЛЕТНЯЯ ПЫЛЬ
Примерно семьсот лет назад на
Землю выпадало втрое меньше
космической пыли, чем сейчас.
Нынешний климат Земли
почти не отличается от климата
нашей планеты тысячу лет назад.
К таким выводам пришли
американские сейсмологи,
пробурившие во льдах Гренландии
скважины полуторакилометровой
глубины. Слои льда на севере
Гренландии постоянно нарастают и,
подобно годичным кольцам
деревьев, содержат сведения о
прошлом. Ученым удалось
проанализировать пыль, находящуюся
во льду в воздушных пузырях
многовековой давности. Кроме
того, выяснено, что возраст
нижних слоев ледяного покрова
Гренландии—примерно 10 000 лет.
Рисунки
В. ЗУЙКОВА
66
ФОТОЛАБОРАТОРИЯ
Кандидат технических наук
Л. Я. КРАУШ,
кафедра научной
фотографии МГУ
МАКРОФОТОСЪЕМКА
Снимать животных, растения, минералы нужно прежде;
всего научным работникам. Но в последнее время охота
с фотоаппаратом стала популярной и среди любителей.
Особенно интересны и неожиданны снимки насекомых.
Макроснимки растений, цветов, плодов и насекомых
могут послужить отличным наглядным пособием на
уроках биологии, особенно, если сделать их цветными.*
Макрофотосъемкой называют
фотографирование мелких
предметов. Причем такое, когда
изображение на негативе
получается либо в натуральную
величину, либо с небольшим
уменьшением или небольшим
увеличением. Более точное
определение: макрофотосъемка — зто
фотографирование в масштабе
от 1: 5 до 5: 1 (масштабом в
фотографии принято считать
отношение линейных размеров
изображения к линейным
размерам объекта).
Пользуясь фотоаппаратами
с раздвижным мехом (старые
аппараты типа «Фотокор»,
современные камеры «ФК»,
работающие на фотопластинках),
при полном растяжении меха
* О цветной фотографии
будет рассказано в следующем
номере журнала.
Лист папоротника. Снято
фотоаппаратом «Зенит» с кольцом
18 мм на пленке 90 ед. ГОСТ.
Освещение двумя лампами по
100 ватт на расстоянии 50 см от
столика с объектом.
Диафрагма 16, выдержка 7?сек.
можно «уместить» на
пластинке размером 9X12 см или
13X18 см в натуральную
величину изображения предметов,
размеры которых не больше
размеров пластинки, например,
яблока, образца горной породы,
лягушки и т. п.
Если нужно
сфотографировать более мелкие объекты —
насекомых, цветы, зерна, то
масштаб изображения 1: 1
оказывается недостаточным и для
такой съемки приходиться
применять специальные
приспособления.
Малоформатные аппараты,
в которые заряжается пленка
шириной 35 мм (размер кадра
в этом случае 24X36 мм),
рассчитаны на фотографирование
объектов, которые находятся от
фотоаппарата на расстоянии не
ближе, чем в один метр.
Фотоаппараты «Зенит-С», «Зенит-3»,
«Зенит-ЗМ» позволяют снимать
с расстояния не больше 0,65
метра.
При съемке с расстояния
в 1 метр нормальным
объективом с фокусным расстоянием
5 см (напомним, что фокусное
расстояние объектива всегда
указывается на его оправе) изо^
бражение на негативе полу^
чается в масштабе 1: 20; зто
значит, что на пленке в кадре
размером 24X36 мм строится
изображение предметов,
расположенных в натуре на площади
48X72 см.
Чтобы получить на пленке
изображение в более крупном
масштабе, например, в
масштабе 1:3, 1:2 или в натуральную
величину — в масштабе 1:1,
нужно было бы объект съемки
приблизить к фотоаппарату на
расстояние до 20—10 см.
(С уменьшением расстояния
между аппаратом и объектом
съемки масштаб изображения
увеличивается.) Однако при
таком малом расстоянии до объ-г
екта съемки обычный пленоч-i
ный аппарат нельзя навести на
резкость. Чем меньше
расстояние до объекта, тем больше
должно быть расстояние между
объективом и пленкой, а в
обычных малоформатных
аппаратах винтовая оправа
объектива, с помощью которой он
перемещается вдоль оптической
оси, не позволяет выдвинуть
объектив сильнее, чем это тре-
1
2
3
4
5
6 J
буется для съемки с
расстояния 65—100 см. Для
макрофотосъемки такими
аппаратами нужны специальные
удлинительные кольца.
УДЛИНИТЕЛЬНЫЕ
КОЛЬЦА
Удлинительные кольца
(фото 1) — это цилиндрические
трубки различной длины,
внутренним диаметром 3,5 см.
С обеих сторон у каждого
кольца винтовая нарезка. На одном
конце нарезка располагается
внутри кольца, а на другом —
с поверхности.
Объектив аппарата
осторожно вывинчивается и на его
место ввинчивается
удлинительное кольцо или несколько
колец, соединенных в одну
трубку. Затем объектив
ввинчивается в свободный конец
последнего кольца, и получается
удлиненная фотокамера (фото 2).
Чем больше длина (принято
говорить «высота») вставленных
в аппарат колец, тем крупнее
получается изображение.
В таблице показано, как
масштаб съемки зависит от высоты
кольца для объектива «Инду-
стар-22» и «Индустар-50».
На фото 3, 4, 5, 6 вы видите
снимки одного и того же
объекта, сделанные без
удлинительных колец с расстояния
1 метр; с кольцом высотой 5 мм;
с кольцом высотой 18 мм;
с кольцом высотой 52 мм.
We
8
9
10
U
12
13
Зависимость масштаба изображения и выдержки от высоты удлинительного кольца
Масштаб
Высота колец, мм
Коэффициент
увеличения выдер-
1:20
—
1
1:10
4
1
1:5
7
1
1:4
И
1,4
1:3
18
1,8
1:2
20
2,2
1:1,3
35
2,8
1:1,2
44
3,3
1:1
52
4
1,2:1
62
4,8
1,5:]
80
6,2
2:1
104
У
4:1
156
16
РАЗДВИЖНЫЕ ОБЪЕКТИВЫ
Вместо удлинительных колец
разной высоты можно
применять специальный объектив,
оправа которого раздвигается.
На фото 7 показан раздвижной
объектив в укороченном и в
удлиненном положении.
Раздвижной объектив вставляется
в аппарат вместо обычного
объектива и выдвигается на
определенную длину в
зависимости от того, какой масштаб
изображения нужен (фото 8).
Величина удлинения
измеряется от плоского кольца на
неподвижной части оправы,
прилегающего к камере, до
ближайшего края
выдвигающейся вперед части оправы
(фото 7).
НАВОДКА НА РЕЗКОСТЬ
Снимая аппаратом с
зеркальным видоискателем (типа
«Зенит»), наводить на резкость
легко. Это значительно
сложнее для аппаратов с оптическим
дальномером (типа «ФЭД»,
«Зоркий», «Киев»).
Снимая аппаратом с
зеркальным видоискателем, нужно,
непрерывно глядя в линзу
видоискателя, постепенно
приблизить аппарат к объекту съемки
и нажать спусковую кнопку
в тот момент, когда резкость
изображения окажется
наилучшей (9). Выдвигать или
укорачивать объектив, наводя на
резкость, совсем не требуется.
В лабораторных условиях
аппарат укрепляется на
штативе: объектив аппарата
направлен вертикально вниз A0).
Расстояние от аппарата до объекта
съемки меняют, либо
перемещая аппарат вверх и вниз по
штанге штатива A1), либо
поднимая и опуская столик, на
котором расположен объект
съемки. Когда изображение на
матовом стекле аппарата станет
максимально резким, аппарат
или столик закрепляют и
снимают.
Конструкция аппаратов с
оптическим дальномером
(«Зоркий», «ФЭД») не позволяет
непосредственно наблюдать за
качеством изображения.
Расстояние до объекта,
нужное для того, чтобы
изображение было резким, приходится
вычислять и затем отмерять
линейкой. Аппараты без
зеркального видоискателя для
макросъемки обычно не
используются, но при желании фотограф
может сам изготовить
несложные приспособления для
макросъемки аппаратами «ФЭД» или
«Зоркий».
Это прежде всего
макровизир, с помощью которого легко
находят нужное расстояние до
объекта. Макровизир — зто
раздвижная рейка, которую
укрепляют на нижней крышке
фотоаппарата специальным винтом
(этот винт входит в гнездо
винта для штатива A2). Рейку
вытягивают в направлении
оптической оси объектива и
раздвигают таким образом, чтобы
расстояние от задней стенки до
выдвинутого вперед конца
рейки точно равнялось
расстоянию, высчитанному для
данного удлинительного кольца.
Отметки на шкале рейки
удобно делать цветными.
В комплект макровизира,
кроме рейки и винта, входят
рамки, определяющие размер и
границы участка, который
нужно сфотографировать A2).
Рамку укрепляют на двух
штырьках в отверстиях на
переднем конце рейки A3). Рамку
надо отметить тем же цветом,
что и кольцо и деления на
шкале рейки.
Аппарат устанавливают так,
чтобы объект съемки оказался
в пределах рамки, и передняя
плоскость объекта совместилась
с плоскостью рамки. В этом по-
1. Гусеница. Снято с рук
фотоаппаратом «Зенит» с
кольцом 18 мм на пленке 90 ед.
ГОСТ. Диафрагма 11,
выдержка 7зо сек. при ярком
солнце.
2. Цееток растения «Иван да
Марья». Лабораторная
макросъемка аппаратом «Зенит»
с кольцом 35 мм на пленке
90 ед. ГОСТ. Освещение
двумя лампами по 100 ватт на
расстоянии 50 см от
объекта, диафрагма 16, выдержка
1 сек.
71
Зависимость глубины резкости изображения от масштаба съемки
и относительного отверстия (диафрагмы)
Г"^*^^-^_ Масштаб 1:М
^^^^-^^^
Диафрагма *--*^^^
2,8
4
5,6
8
И
16
1:20
50
i 120
180
230
330
1 550
1:3
40
5
7
11
15
20
1:2
1,8
i 2,5
3,5
5
7
! 10
1:1,5
1,0
1,5
2
3
4
fi
1:1,2
0,8
1,1
J,6
2,2
3,4
5
1:1
0,6
0,8
1,2
1,6
2,3
3,5
1.2:1
0,45
0,6
ол>
1,2
1,15
2,5
1.5.1
0.3
0.45
0.0
1
1,1
1.8
2:1
0,25
0,35
0,50
0,80
1,00
1,40
\
3:1 1
0,2
0,32
0,4
0,6
0,9
1,25
ложении и снимают.
Макровизир и рамки легко сделать
самим. Рейку нужно размечать
очень тщательно и затем
проверить разметку на практике *.
ГЛУБИНА РЕЗКОСТИ
И ВЫБОР МАСШТАБА
СЪЕМКИ
Глубина резкости оптического
изображения тем меньше, чем
больше масштаб этого
изображения (при прочих равных
условиях). Увеличить глубину
резкости можно, уменьшая
отверстие, изменяя диафрагмы
объектива. В таблице показана
зависимость глубины резкости
от масштаба съемки и от
диафрагмы для объективов «Инду-
стар-22» и «Индустар-50».
Величина глубины резкости дана
в миллиметрах. Пользоваться
таблицей нужно следующим
образом. Например, вы хотите
сфотографировать пчелу. По
своим размерам изображение
пчелы может уместиться в
кадре 24X36 мм в натуральную
величину, однако максимальная
глубина резкости для этого
масштаба (при диафрагме 16)
всего лишь 3,5 мм, а этого явно
недостаточно, потому что пчела
толще. Необходимую глубину
* Формулу для расчета
расстояния до объекта и размер
рамок можно найти в книге
И. Б. Минсынова
«Макрофотосъемка» серии «Библиотека
фотолюбителя» издательства
«Наука»,
резкости 5—6 мм можно
получить, как следует из таблицы,
если снимать в масштабе 1:1,2
или 1:1,5 при диафрагме 16.
Если же из-за того, что
отверстие объектива очень мало,
потребуется слишком большая
выдержка, а снимая с рук, такую
выдержку дать невозможно, то
придется снимать в масштабе
1:2 с диафрагмой 11 или 8.
В лабораторных условиях,
когда аппарат укреплен на
штативе, всегда выгоднее
диафрагмировать объектив до предела
(обычно до 16) и снимать с
более длительной выдержкой. В
этом случае обязательно нужно
применять тросик. Снимая
аппаратом «Зенит», укрепленным
в штативе, нужно наводить на
резкость при полном отверстии
объектива (диафрагма 3,5);
после наведения на резкость перед
съемкой объектив
диафрагмируется. При съемке с рук
нужно сначала установить
выбранную диафрагму, а затем
навести на резкость.
ОСВЕЩЕНИЕ ОБЪЕКТА
И ВЫБОР ПЛЕНКИ
При съемке на натуре
выбирают хорошо освещенный
объект. Нужно стараться
снимать по возможности под углом
к направлению падения света:
при косом освещении тени от
выпуклых мест объекта
подчеркивают рельеф поверхности,
и предмет на снимке кажется
объемным. Тени не должны
быть слишком темными, иначе
детали в тенях объекта не
воспроизведутся на снимке.
Особенно темные места объекта
можно подсветить зеркалом или
каким-либо белым экраном,
отражающим свет.
В лабораторных условиях
предмет, который нужно снять,
помещают на чистое стекло
(стеклянный столик) и
освещают с двух сторон. Свет обоих
источников должен падать под
большим углом F0—70°) к
оптической оси объектива; очень
мелкие объекты освещают
узким пучком сильного света,
скользящего вдоль предметного
столика. Одна сторона объекта
должна освещаться более
сильным светом («основной свет»);
с другой стороны свет должен
быть слабее («подсветка
теней»). Выбирая направление
съемки, столик с объектом
поворачивают относительно
источников света до тех пор, пока
не находят наиболее выгодное
освещение.
Правильную выдержку
выбирают либо на основании
пробной съемки, либо
определяют по фотоэлектрическому
экспонометру с поправкой на
высоту кольца.
Для макросъемки хорош
равномерный черный фон.
В тех случаях, когда сам
объект съемки очень темный,
фон должен быть светлее
объекта. Пестрый фон
ухудшает качество снимка, детали
в этом случае передаются
менее отчетливо,
731
Муха. Снято с рук
фотоаппаратом «Зенит» с кольцом 26 мм
на пленке 130 ед. ГОСТ с
диафрагмой 8, выдержка 7зо сек.
Освещение — облака, 5 ч. дня.
ЧЕТЫРЕ СОВЕТА
Объект макрофотосъемки
удобно закрепить на стеклянном
столике маленьким кусочком
пластилина. Пластилин лучше брать
темный, чтобы он сливался по
цвету с черной бумагой, лежащей
под стеклом столика. Насекомые
из коллекций, засушенные на
булавках, также укрепляются при
помощи пластилина: маленький
комочек пластилина приклеивают
к стеклу, и в него вводят острый
конец булавки. Живых насекомых
можно на время усыпить
хлороформом.
Снимать в поле травы и злаки,
которые по цвету сливаются с
окружающими их предметами, удобно
на фоне неба. Располагать объект
и аппарат надо при этом так,
чтобы в объектив не попадал
прямой солнечный свет.
В аппаратах с зеркальным
видоискателем затвор иногда не
срабатывает и зеркало не опускается
(в видоискателе не видно
изображения). Чаще всего это
происходит из-за того, что механизм
заведен не полностью: нужно
доводить заводную ручку или
заводной рычаг сильным движением
до упора. Иногда во время
съемки отключается механизм затвора,
так как спусковую кнопку
нажимают неаккуратно: спуская
затвор, следует нажимать на
центральный столбик спусковой
кнопки, не задевая по возможности
кольцо, которое выключает
механизм.
Для макрофотосъемки с рук в
лесу и в поле лучше выбирать
высокочувствительную пленку A30-
180 единиц ГОСТ), чтобы можно
было снимать с короткими
выдержками: 1/100—1/50 секунды
при диафрагме 11. Такое
диафрагмирование дает
необходимую глубину резкости при
съемке цветков и насекомых.
Старший преподаватель
кафедры иностранных
языков АН СССР
Ю. В. ТАРАНОВИЧ
УЧИТЕСЬ
ПЕРЕВОДИТЬ
НЕМЕЦКИЙ
ДЛЯ ХИМИКОВ
Современный ученый вынужден быть полиглотом.
Наверное, этим и объясняется множество писем, в которых
читатели требуют продолжать публикации материалов в
помощь изучающим иностранные языки. Выполняя эти
требования, мы с этого номера начинаем серию статей,
которые помогут вам разобраться в трудных для перевода
химических текстах на немецком языке.
Начну с небольшой, но весьма поучительной
истории — для тех, кто уверен в том, что перевод
немецкой научной и технической литературы не
таит в себе никаких трудностей. Эту историю
рассказал мне один аспирант. Он собирался
сдавать кандидатский минимум по языку и пришел
на кафедру посоветоваться — сдавать ли ему
немецкий или английский. И тот, и другой он знал
не блестяще. Заведующий кафедрой выслушал
его и посоветовал: «Готовьте немецкий. В нем все
ясней и проще, и вы потратите меньше времени
на подготовку». Аспирант внял совету и... с
треском провалился на экзамене. Как выяснилось
потом, уважаемый профессор был специалистом
по английскому языку...
Для перевода научной и технической
литературы (в том числе — и с немецкого) необходим
своеобразный синтез знаний и навыков в
области иностранного языка, русского языка и
своей специальности. Полагая, что два последних
условия читателями журнала выполнены,
приступим к восполнению пробелов двух остальных:
в знании немецкого языка и в навыках перевода
с него.
Необходимость переводить научные и
технические тексты с немецкого не всегда согласуется
с возможностями специалистов-химиков (в
особенности — молодых специалистов). Для
примера предложим читателю перевести три
предложения:
1. Erst die Aufgabe der alten Vorstellung von
dem Bau der Materic ormogliclite die Erforschung
der inneren Zu sain men ban ge der Natur.
2. YVollen wir einige Beispiel nehmen.
3. Wir wollen uns zunachst auf Losungeii nicht
fliichtiger Stoffe beschranken.
Сам собой напрашивается такой перевод:
1. Сначала задача старого представления о
строении материи дала возможность
исследования внутренних взаимосвязей природы.
2. Мы хотим взять некоторые примеры.
3. Мы хотим сначала ограничиться
растворами нелетучих веществ *.
Первое предложение в переводе совершенно
бессмысленно, а перевод двух других
предложений тоже неверен, хотя неправильность и не
столь очевидна.
Эти предложения следует переводить так:
1. Только отказ от прежнего представления о
строении материи дал возможность исследовать
внутренние взаимосвязи природы.
2. Приведем (рассмотрим) несколько
примеров.
3. Прежде всего, мы ограничимся растворами
нелетучих веществ.
Рассмотрим сначала некоторые
отличительные признаки немецкой научной и технической
литературы по химии, бросающиеся в глаза
даже мало знакомому с языком
специалисту-химику. Вот зти признаки.
Научная и техническая
терминология. Поскольку термин — это слово (или
группа слов), служащие для точного обозначения
специального понятия, то такие слова, как die
Wertigkeit (валентность), die Reduktion
(восстановление), das Nichtmetall (металлоид), gesattigt
(насыщенный), — безусловно, химические термины.
* Все примеры будут даны в этой и
последующих публикациях со сквозной нумерацией.
Переводы даются под теми же номерами, что и
примеры — Ред.
Сокращения терминологического
и общенаучного характера. Несколько
примеров: Е — Erstarrungspunkt (точка
затвердевания), G — Gewicht (вес), Schmp — Schmelzpunkt
(точка плавления), v. Н. — vom Hundert
(процентов).
Обозначения химических
элементов и химических соединений.
Это вряд ли требует долгих пояснений:
Al (Aluminium), Fe (Eisen), H20 (Wasser).
Но помимо внешних отличительных
признаков, научная и техническая литература, и в
частности — химическая литература, имеет более
глубокие внутренние особенности. Тематика и
задачи научной и технической литературы
требуют логической строгости и последовательности
изложения, краткости, точности и ясности стиля.
Эмоционально окрашенные слова, выражения и
грамматические конструкции, как правило,
отсутствуют. Такие особенности стиля не исключают в
некоторых случаях оттенков
предположительности, вероятности, неуверенности, условности,
нереальности, отрицательных суждений и
отрицательных оценок. Все это достигается
определенными грамматическими и лексическими
средствами, которые, не являясь исключительной
принадлежностью стиля научной и технической
литературы, в известной мере типичны для него.
ЛЕКСИЧЕСКИЙ СОСТАВ СТИЛЯ НАУЧНОЙ
ПРОЗЫ. К более специальным и менее
заметным некомпетентному человеку внутренним
признакам, характеризующим стиль научной и
технической литературы, относятся:
а) Употребление слов с
общенаучным или специальным значением
или вариантами значений. Например:
des Verfahren — способ, метод, процесс;
festlegen — устанавливать, определять, выяснять,
фиксировать, констатировать, назначать,
утверждать;
kunstlich — искусственный, синтетический.
Более сложны случаи, когда общенаучное или
терминологическое значение слова отличается от
обычного, общеупотребительного. Например:
die Losung — решение, в химии — раствор;
der Anteil — участие, сочувствие, в научной
литературе — доля, часть, компонент,
составляющая;
fassen — хватать, ловить, поймать, а в науке —
формулировать, понимать, вмещать,
охватывать.
б) Употребление иностранных и
интернациональных слов с
общенаучным или специальным значением. Например:
die Konvergenz — конвергенция, сходимость;
reversibel — обратимый;
definieren — определять, толковать, трактовать.
в) Употребление слов, словосочетаний и
оборотов, выражающих отношение автора к
высказыванию. Несколько примеров:
anscheinend — по-видимому, по всей вероятности;
mit Sicherheit — без сомнения, с уверенностью;
wohl — пожалуй, кажется, конечно, по-видимому,
может быть, должно быть.
г) Часто встречаются предлоги, союзы,
вводные слова и обороты, служащие для указания на
связь с предыдущим и последующим
изложением. Например:
eingangs — вначале;
im Nachfolgenden, nachstehend — ниже, в
последующем изложении;
infolgedessen — вследствие этого.
д) Использование множества
фразеологических оборотов, готовых шаблонов,
стандартных фраз и сочетаний слов. Например:
vor allem — в первую очередь, прежде всего;
nach wie vor — по-прежнему;
es ist der Fall — это имеет место, бывает,
случается.
ГРАММАТИКА. В научной и технической
литературе сплошь и рядом встречаются сложные
предложения, в том числе и смешанного типа —
сложно-сочиненные с одним или несколькими
придаточными, с инфинитивными и
причастными оборотами.
Широко применяются предложные
конструкции, эквивалентные предлогам:
auf Grund — на основе (чего-либо);
mit Hilfe von — с помощью (чего-либо);
im Hinblick auf — ввиду (чего-либо), принимая во
внимание (что-либо), в расчете на (что-либо).
Для выражения логических связей
используются такие союзы, как einmal... zum anderen — во-
первых... во-вторых; demzufolge — вследствие
этого; demgegenuber — в противоположность этому.
В описании процессов, явлений, принципов
действия и конструкций механизмов в центре
внимания обычно находится не действующее
лицо — субъект, а объект воздействия или само
действие. Такое содержание требует применения
пассивных, безличных или
неопределенно-личных конструкций.
4. Auf dem Gebiet der Katalyse wird we iter in-
tensiv gearbeitet (безличный пассив, презенс).
«В области катализа продолжается
дальнейшая интенсивная работа».
Закончив это краткое вступление, перейдем к
практической работе над химическими текстами.
Попытайтесь перевести одно предложение и
небольшой отрывок из книги. Ваши затруднения
и сомнения будут разрешены в следующем
номере журнала, где будет помещена статья о
псевдопростых словах. В начале статьи будут
разобраны приведенные ниже примеры.
5. ДШ dem Nam en Katalyse bezeichnet man den
Vorgang der Beschleunigung gewisser chemisclier
Reaktioneii durch tlie Gegcnwarl von Substaiizen, die
Scheinbar keinen Anteil an denselben haben.
6. Diesc experimentell gefundene Tatsache fur-
to zu dem SchluS, da? eine Verbindung sich in der
Weise vollzieht. daB einzelne Individuen (Atome)
sich in bestiniinter Gruppienuig zu Molekeln zusam-
monschliefien. Man versteht das Gesetz der konstan-
ten Proportionen sofort, wenn man annimmt, daB
alle Sauerstofi'atomo unter sich ebenfalls gleiche
Masse haben, wobei die oben angegebenen Zahlen
fur die relativen Verbindungsgewichte dann heraus-
k о in men, wenn man annimmt, dafi das Sauerstoff-
atom U gerade sechzehnmal so schwer ist wie das
Wasserstoffatom H. Man hal auf Grund dieser
Uberlegung den Begriff des Atomgewicbts einge-
fiihrt, der ursprunglich angeben sollte, um wieviel
das Atom irgendeines Elementes schwercr ist als
das leichteste unter ihnen, nahmlich jenes des Was-
aerstoffs. Exaktere Messungen haben spater gezeigt,
da В unter Benutzung dieser Einheit das Atomge-
wicht des VVassersstoffs sclbst nicht genau gleich 1
ist, sondern 1,008. Daruber spater mehr.
СОВЕТУЕМСЯ
С ЧИТАТЕЛЯМИ
Правление Менделеевского
общества в Ленинграде устроило
обсуждение журнала «Химия и
жизнь», пригласив на него
сотрудников редакции.
Ленинградские химики высказали
интересные пожелания. Мы хотим
познакомить читателей с
некоторыми из них.
Профессор К. П. МИЩЕНКО,
председатель правления
Ленинградского отделения
Всесоюзного химического общества имени
Менделеева:
Я знаю многих людей
гуманитарных профессий, которые
выписывают «Химию и жизнь» или
берут почитать журнал у нас. Но
мне кажется, что технологи,
инженеры проявляют такой интерес
еще далеко недостаточно. И это
прямо подсказывает редакции
один из путей в ее работе.
П. К. ГРИГОРИАДИ, учитель
химии 38-й школы:
Хотелось бы видеть в журнале
фотографии и рисунки такие,
чтобы их можно было класть
прямо под эпидиаскоп.
Член-корреспондент Академии
наук СССР М. В. ВОЛЬКЕНШТЕЙН*
Институт высокомолекулярных
соединений:
Напоминаю об исторических
редкостях, о первоисточниках! В
частности, о том, что даже «Химик-
скептик» Роберта Бой ля не
издавался на русском языке никогда
и, значит, известен в основном по
отдельным цитатам да
извлечениям!
Ю. ГЕНДЕЛЕВ, ученик 81-й школы:
Пишите о том, как строить
приборы; обязательно печатайте
практикумы — это интересно.
Профессор Е. И. АХУМОВ,
Ленинградский технологический
институт целлюлозно-бумажной
промышленности:
Редакция должна принимать во
внимание то, что можно назвать
психологией чтения. Когда, где,
что мы читаем. Разницу между
чтением дома, за рабочим
столом и в автобусе. В журнале
должна быть пища и для первого,
и для второго, и для третьего —
все в свое время и на своем
месте. Заказывайте статьи не только
нашим, но и зарубежным ученым.
Введите раздел специально для
вузов, как вы это сделали с
«Клубом Юный химик» для школы.
Профессор В. В. РАЗУМОВСКИЙ,
Ленинградский
электротехнический институт связи:
Учебники и монографии не могут
поспеть за развитием знаний,
особенно это относится к теории.
И научно-популярный журнал
мог бы во многом просто помочь
студентам и преподавателям
высшей школы. Специальный раздел,
может быть «Высшая школа
химии», просто необходим!
В обсуждении, на нотором
председательствовал профессор
С. А. ЩУКАРЕВ (ЛГУ),
участвовали также кандидат химических
наук А. А. МАКАРЕНЯ (директор
Музея-квартиры Д. И.
Менделеева), доцент Г. П. УГРЮМОВ
(Педагогический институт им.
Герцена), школьник С. КУЛИКОВ (81-я
школа).
Главный редактор журнала
академик И. В. ПЕТРЯНОВ заверил
участников обсуждения, что
редакция постарается реализовать
их предложения на страницах
журнала. Ожидаем
соответствующей инициативы и от самих
ученых — наших авторов,
независимо от того, носят они высокие
научные звания или нет.
СНЕЖИНКА НА ПАМЯТЬ
В тихий безветренный день,
когда валит крупный
пушистый снег, у вас наверняка
возникало желание сохранить на
память хотя бы одну
снежинку — столь неповторима и
изящна форма каждой из них.
К сожалению, кристаллы
снега столь же эфемерны, сколь
и прекрасны. Обычно они тают
или сублимируют (испаряются
без таяния), едва достигают
земли.
Многие годы специалисты и
любители были вынуждены
довольствоваться поспешными
зарисовками; более
радикальное решение проблемы
принесла микрофотография.
В 1885 году этим делом
занялся один рьяный
фотолюбитель, Вильсон Бентли, который
опубликовал книгу с 5000
изображениями снежинок. Однако
подлинный переворот в этой
области произошел в 1940 году,
когда снежинки стали
копировать в пластмассе. Вот что
пишет изобретатель метода
Винсент Шефер:
«Однажды, лет двадцать
пять тому назад, когда я ждал
автобуса, повалил снег.
Снежинки были необыкновенно
красивы, и я подумал — нельзя
ли найти способ сохранить их?
Добравшись до дома, я
растворил 1 грамм поливинил-
формаля * в 100 миллилитрах
дихлорэтана и поставил раствор
в морозильник. Когда раствор
охладился до температуры
ниже 0°С, я налил его на
охлажденное до той же температуры
стеклышко — ровно столько,
чтобы образовалась тонкая
пленка — затем соскреб со
стенки морозильника немного
снега, положил его на
полученную пленку и поставил
стеклышко снова в морозильник.
* Поливинилформаль — это
продукт взаимодействия
поливинилового спирта с
формальдегидом.
Через несколько часов, когда
растворитель испарился и
стекло высохло, я стал
рассматривать полученные отпечатки
кристаллов снега через
увеличительное стекло. Они не
исчезли и после того, как
нагрелись до комнатной
температуры.
Всю зиму я увлекался
заготовкой снежинок. Не все мои
первые отпечатки были
удачными, но спустя некоторое
время я приобрел сноровку.
Изготовление копий снежинок
в пластмассе — дело не очень
сложное».
Начинающий может
столкнуться с некоторыми
затруднениями: иногда при испарении
растворителя кристаллы льда
сублимируют и отпечатки
получаются недостаточно
четкими; иногда же на поверхности
пленки образуется белый
налет. Этот налет появляется в
том случае, если при испарении
растворителя поверхность плен-
кп очень сильно охладилась и
на ней в виде мельчайших
капелек (или кристалликов) осела
влага. Чтобы избежать этого,
следует не очень сильно
охлаждать раствор, уменьшить
скорость испарения
растворителя (например, поместив
пластинку в атмосферу с высоким
содержанием его паров) или
снизить относительную
влажность атмосферы^
Чтобы получить хорошие
отпечатки, концентрацию
раствора следует подбирать в
соответствии с размером кристаллов.
Для так называемой «алмазной
пыли» — кристаллов льда ди-а-
метром не более 0,2
миллиметра — концентрация раствора
должна быть от 0,1 до 0,5
процента, для обычного снега и
ледяного налета она должна быть
выше — до 1 процента, а при
снятии отпечатков со снега с
земли, а также с изморози и
крупы, концентрацию раствора
следует повысить до 2
процентов и более.
Поливинилформаль — самый
удачный материал для
получения нетающих снежинок.
Однако могут быть использованы и
другие вещества, растворенные
в дихлорэтане. И растворитель
может быть другой: например,
если требуется ускоренное
испарение, годится хлороформ;
однако следует иметь в виду,
что в этом случае пленка
сильнее охлаждается, что, в свою
очередь, вызывает
конденсацию влаги и появление белого
налета. Следует избегать и
таких растворителей, как ацетон
и спирт, так как они
растворимы в воде (и вода растворяется
в них). Непригоден также
бензол, поскольку он затвердевает
при температуре выше 0°С.
Вместо поливинилформаля
можно использовать
полистирол и полиметилметакрилат
(плексиглас); обе пластмассы
растворяются как в
дихлорэтане, так и в хлороформе
Нежные снежинки можно
ловить куском черного бархата,
отбирать наиболее интересные
экземпляры и делать с них
отпечатки. Снежинки можно
снимать с бархата спичкой, на
кончике которой находится
капелька раствора пластмассы;
для этого нижней частью
капельки надо слегка коснуться
снежинки и затем перенести ее
на стекло. Действуйте
осторожно, не раздавите снежинку
спичкой.
На одном куске стекла
можно разместить довольно много
снежинок; готовые отпечатки
следует накрыть еще одним
куском стекла и после этого
скрепить края липкой лентой.
Теперь снежинки можно
рассматривать под микроскопом,
проецировать на экран или
фотографировать. Вместо
стекла в качестве подложки можно
использовать и черный картон:
на нем отпечатки выглядят
особенно эффектно; годится
также пленка из полиэтилена.
Очень удобно пользоваться
таким способом: покрыть
стекло пленкой раствора, высушить
его, а затем наносить снежинки
вместе с капелькой
растворителя. Вблизи снежинок покрытие
растворяется, излишек
растворителя поглощается
окружающими участками покрытия, а
каждая мельчайшая деталь
кристалла покрывается тонкой
пленкой пластмассы. Самые
удачные отпечатки обычно
получаются именно таким
способом.
Мелкие ледяные кристаллы
копируются лучше всего
видоизмененным способом
предварительного покрытия. Поместив
ледяной кристаллик на
предварительно нанесенный и
высушенный слой пластмассы,
стеклышко надо внести в
атмосферу паров растворителя;
испарительную камеру можно
сделать в виде небольшого
деревянного ящичка с
герметически закрывающейся крышкой.
На дно ящичка надо поставить
блюдце с растворителем: пары
растворителя конденсируются в
виде тонкой пленки (в основном
около кристаллов) и растворяют
пластмассу. Благодаря
поверхностному натяжению и
капиллярному эффекту кристаллы
льда покрываются слоем
полимера.
Еще один удобный способ
заключается в том, что на
расположенные на подложке
снежинки набрызгивается раствор
прозрачного лака. Этот метод
особенно удобен для получения
копий с рисунков мороза на
стекле. Распылитель следует
держать подальше от стекла,
чтобы лак был уже почти
сухим, когда он коснется
кристаллов. Наилучшие
результаты дают лаки-аэрозоли.
Красивые кристаллы льда
можно вырастить искусственно.
Для этого следует растворить
желатин A—3 грамма
желатина на 100 миллилитров
дистиллированной воды), тонким
слоем этого раствора покрыть
кусок стекла, поместить его на
холод и подождать, пока
пленка не переохладится, то есть
не охладится ниже обычной
температуры замерзания воды.
Если теперь на пленку
поместить мельчайший кристалл
льда или создать какой-либо
другой центр кристаллизации,
то мгновенно вырастут
красивые кристаллы; по мере их
роста желатин будет
осаждаться из раствора, подчеркивая
контуры кристаллов. Через
несколько дней (при температуре
ниже 0СС) лед испарится и
останется красивый отпечаток.
Сокращенный перевод с
английского
Ф. БУШАНСКОГО
Рисунок КХ ВАЩЕНКО
От редакции. Мы
надеемся, что читатели
заинтересуются этим способом
изготовления изображений снежинок.
Оригиналы или фотографии
можно присылать по адресу:
Москва В-333, Ленинский
проспект, 61, редакция журнала
«Химия и жизнь».
Самые интересные
отпечатки будут опубликованы.
ПОПРАВКА
В заметке «Рижские моды: товары одеваются по-новому»,
напечатанной в № 11 A966 г.), допущены серьезные неточности.
Неверно указано, что завод «Сподриба» находится в Риге. Ошибочно
утверждается, что в полиэтиленовые тубы, изготовленные на этом
заводе, упаковывают пищевые продукты. Серийно такие тубы не
изготовляются. Горловина от полиэтиленовых туб-пакетов не
отрезается, отрезается только уголок пакета, торчащий из
горловины.
ЖИВЫЕ
ЛАБОРАТОРИИ
РОДОДЕНДРОН
ДАУРСКИЙ
Г. П. ТАФИНЦЕВ,
Главный ботанический сад
АН СССР
Rhododendron
dahuricuni
«Туртыгин сел около одного
куста и стал закуривать
трубку. Едва он чиркнул спичку,
как окружающие куст эфирные
масла вспыхнули с шумом
бесцветным пламенем. Это
понравилось стрелкам, и они стали
устраивать такие фейерверки
около каждого куста. Наконец,
я остановил их, прося поберечь
спички. Если непривычный
человек в безветренный жаркий
день попадет в заросли этого
растения, с ним может
сделаться дурно: так много оно
выделяет из себя эфирного масла»,—
рассказывает в своей книге
«В дебрях Уссурийского края»
известный русский
путешественник В. К. Арсеньев.
Что же это был за куст, так
поразивший его спутников?
Вряд ли найдется в Сибири
растение, по красоте равное
даурскому рододендрону (по-
бурятски — «морольчи»). Его
цветение знаменует начало
весны, когда на деревьях едва
пробиваются почки, а земля
еще не покрылась травой. В зто
время склоны прибайкальских
сопок сплошь окрашиваются в
яркий сиренево-розовый цвет—
это цветет рододендрон,
название которого в переводе на
русский язык и означает «розовое
дерево». Крупнейший
ученый, исследователь Сибири
П. С. Паллас так описывает в
своем дневнике глубокое
впечатление, произведенное на
него цветущим рододендроном:
«17 мая. Между тем луга от
часу более и более расцветали.
Я не знаю, можно ли
что-нибудь великолепнее представить,
как сии крутые по Ононю и
безлесные склоны, коих
полуденная сторона цветами
сибирского черносливу (Prunus Sibiri—
са), а полунощная же
цветущими Rhododendron dahuricum с
верху до подошвы вишнево-
пурпуровым цветом одевались.
Во всю мою дорогу я подобного
сему, будто вымышленного,
места не видывал...»
Сибиряки называют
рододендрон багульником. Это
неверно: хотя рододендрон и
багульник и относятся к одному
и тому же семейству
вересковых и оба содержат в своих
листьях эфирные масла,
обладающие специфическим
запахом, но это совершенно
разные растения.
Зачем же рододендрону
окутывающее его облачко
эфирного масла?
Еще в 1867 г. английский
физик Дж. Тиндаль высказал
мысль, что выделяемые
некоторыми растениями эфирные
масла, испаряясь, окутывают
их невидимой «шубой»,
которая, уменьшая прозрачность
воздуха для теплового
излучения, предохраняет растение от
чрезмерного нагревания днем и
от переохлаждения ночью.
Видимо, так обстоит дело и с
рододендроном.
Это не единственная его
любопытная особенность. В
народной медицине даурский
рододендрон издавна применялся
как целебное средство против
ревматизма и
желудочно-кишечных заболеваний.
Старинные тибетские рецепты
особенно рекомендуют его листья
(«да-ли-маг-бо») и цветки («да-
ли-муг-бо»).
В наше время целебные
свойства рододендрона вызвали
интерес ученых. Опыты
подтвердили, что сок, выжатый из
его листьев и корней,
действительно, губительно действует
на простейшие
микроорганизмы, к которым относятся и
возбудители многих
заболеваний.
Серьезные исследования
состава и бактерицидных свойств
даурского рододендрона были
недавно проведены
сотрудниками Иркутского противочумного
института Р. Г. Медведевой и
Э. И. Клец. Им удалось
установить, что листья
рододендрона содержат большое
количество (до 5,5 %) дубильных
веществ пирокатехиновой
группы. Соединения аналогичного
строения давно известны своей
физиологической активностью и
используются при изготовлении
многих лекарственных средств.
Исследователи испытали
действие спирто-водной
вытяжки из листьев рододендрона
на микробов — возбудителей
таких тяжелых и особо
опасных заболеваний, как брюшной
тиф, дизентерия, чума,
бруцеллез, холера. Оказалось, что
после пятичасового пребывания
в 8—10%-ной вытяжке
микроорганизмы теряют способность
к размножению, а через сутки
полностью погибают.
Можно надеяться, что
дальнейшее исследование сибирских
рододендронов позволит
получить препараты, которые
смогут быть применены во
врачебной практике. Но пока что
ближайшая перспектива
использования рододендрона
человеком связана с декоративным
садоводством и озеленением.
В декабрьском номере журнала
«Химия и жизнь» было
опубликовано письмо читателя А. ЛЕЕН-
СОНА, в котором рассказывалось
об интересном факте —
скисании молока во время грозы.
В примечании от редакции
говорилось, что сотрудники
Всесоюзного научно-исследовательского
института молочной
промышленности знакомы с этим явлением,
но причин его не знают и
изучением его не занимаются.
На эту публикацию мы
получили отклик читателя С. ИВАНОВА
из Москвы. Приводим выдержки
из его письма:
«...Молоко представляет собой
эмульсию, весьма
высокодисперсную эмульсию жира в воде. Как
и всякая коллоидная система,
молоко имеет заряд. Все шарики
эмульсии заряжены одноименно,
этим и объясняется состояние
равномерного (более или менее]
распределения дисперсной фазы...
Если заряд удалить, то частички
эмульсии будут агрегировать, а
затем и коагулировать — молоко
створожится. При близком
разряде атмосферного электричества
(если заряды разноименны] будет
обязательно коагуляция молока...»
Цветущий рододендрон,
действительно, необыкновенно
красив. Важно и то, что цветет он
очень рано, во второй половине
мая, еще до того, как на нем
появятся листья. Его цветы,
сначала темно-вишневые,
понемногу светлеют — как бы
выгорают. И только когда
осыплются их лепестки, куст
покрывается светло-зелеными
овальными листочками,
которые постепенно темнеют.
Цветение рододендрона
продолжается около месяца. У
него есть и еще одно
замечательное свойство, особенно ценное в
Это письмо мы попросили
прокомментировать старшего
научного сотрудника Института
физической химии АН СССР
кандидата химических наук И. Н. ВЛО-
ДАВЦА
Существует превеликое
множество теорий, каждая из которых
более или менее правдоподобно
объясняет, почему молоко
скисает во время грозы. Более того,
иногда даже предлагают
использовать это явление для того,
чтобы с помощью искусственных
электрических разрядов ускорить
производство различных
кисломолочных продуктов в
промышленном масштабе. Почти каждая
из этих работ начинается словами:
«Как известно, во время грозы
молоко скисает...».
Но самое печальное в этой
истории состоит в том, что
буквально нигде в научной
литературе сам этот факт не
зарегистрирован... Иначе говоря — скисание
молока во время грозы не
столько явление, сколько суеверие.
Более того. Невозможно
представить себе никаких — ни
физических, ни физико-химических —
причин, благодаря которым во
условиях Сибири, —
способность к выгонке. Зимой, в
морозы, когда еще ничто в
природе не говорит о приближении
весны, срезанная ветка
рододендрона расцветает в теплой
комнате через 11 суток.
К сожалению, этот красивый
и полезный кустарник до сих
пор редко выращивают в на-,
ших городах, хотя его
исключительная красота и
морозостойкость делают рододендрон
особенно ценным для городского
озеленения. 81
время грозы скорость развития
микроорганизмов могла бы
увеличиться (автор последнего
письма заблуждается: молоко не
имеет заряда, оно
электронейтрально. Молоко не коагулирует
потому, что каждая капелька
жира окружена структурированной
белковой оболочкой).
Разумеется, сснет дыма без
огня»: что-то, но все же
послужило причиной разнообразных
толков, какая-то связь между
грозой и скисанием молока,
по-видимому, все же имеется. Но эта
связь совершенно иного рода:
ведь перед грозой температура
воздуха обычно повышается,
микроорганизмы начинают
размножаться более интенсивно...
Читатели могут проверить это на
простом эксперименте: достаточно
посмотреть, скиснет ли во время
грозы свежее молоко,
находящееся в холодильнике...
ИЗ ПИСЕМ В РЕДАКЦИЮ
КЛУБ
ЮНЫЙ
ХИМИК
Устав клуба состоит всего из двух пунктов.
Пункт первый. Членом клуба может быть каждый
школьник.
Пункт второй. Ответы на вопросы викторины клуба
Юный химик нужно высылать в редакцию до выхода в
свет следующего номера журнала (потому что в этом
следующем номере ответы будут уже опубликованы).
Десять школьников, которые пришлют лучшие ответы в
течение учебного года, будут премированы подпиской на
наш журнал на следующий год.
82
ЧТО ЭТО ТАКОЕ?
(Ответ на стр. 90)
ВИКТОРИНА
ИСПРАВЬТЕ ОШИБКУ...
...В ПРИБОРЕ. Внимательно рассмотрев
рисунок, вы, конечно, поймете, что на нем
изображен газогенератор. Принцип действия
его прост: если открыт зажим 3, то раствор
кислоты из сосуда 1 начнет перетекать в
сосуд 2, на дне которого находится мрамор
или цинк. При этом выделяется газ
(двуокись углерода или водород), который по
газоотводной трубке попадает в приемник 4.
Если закрыть зажим, то газ будет
собираться в сосуде 2 и вытеснит кислоту
обратно в сосуд 1. Реакция прекратится.
В ЭТОМ ПРИБОРЕ ЕСТЬ ОДИН ДЕФЕКТ,
который не сразу бросается в глаза. Что
это за дефект? Как его устранить?
...В РЕАКЦИИ. В дистиллированной воде,
насыщенной хлором, растворили при
непрерывном помешивании 1 моль тонкоизмель-
ченной пятихлористой сурьмы. В
результате, реакции образовался 1 моль
сурьмяной кислоты Нз5Ь04 и 5 молей хлористого
водорода НС1.
В ОПИСАНИИ ДОПУЩЕНА ОШИБКА.
Попытайтесь найти ее.
83
ХОТИТЕ ПОДГОТОВИТЬСЯ
К ЭКЗАМЕНАМ ПОЛУЧШЕ?
На приемных экзаменах по химии в"
билетах обычно даются два вопроса (один
по курсу неорганической химии, а
другой — по курсу органической химии).
Кроме того, абитуриентам предлагаются
расчетные или качественные задачи.
Расчетные задачи в вузах с химическим
уклоном достаточно сложны. Чтобы
решить такие задачи, нужно не только
хорошо знать химию, но и иметь определенные
навыки.
Клуб Юный химик предлагает
выпускникам средней школы серию расчетных
задач повышенной трудности. Такие
задачи предлагались поступающим в
медицинские и педагогические вузы. Задачи
подготовлены старшим преподавателем
Московского государственного заочного
педагогического института Д. В.
ПАЛЬЧИКОВЫМ.
ЗАДАЧА № 1.
При восстановлении магнитного
железняка водородом получили 14 кг железа.
Сколько водорода вступило в реакцию
и сколько воды образовалось? Сколько
литров серной кислоты 17%-ной концентрации
с плотностью 1,2 г/мл было израсходовано
для получения нужного количества
водорода?
ЗАДАЧА № 2.
Определить процентное содержание
железа в техническом препарате, если при
обработке 8,5 г этого препарата соляной
кислотой выделилось 2,8 л газа при
нормальных условиях.
Сколько миллилитров 20%-ного
раствора соляной кислоты с плотностью 1,1 г/мл
вступило в реакцию?
(Г. И. Хомченко «Пособие по химии
для поступающих в вузы», 1966)
ЗАДАЧА № 3.
При разложении известняка,
содержащего 10% примесей, было получено 11,2 л
углекислого газа.
Сколько граммов воды необходимо
взять, чтобы получить гашеную известь из
образовавшейся окиси кальция?
Определите вес взятого известняка. Какой объем
10%-ного раствора соляной кислоты с
d = 1,05 г/мл потребуется для
нейтрализации полученного гидрата окиси кальция?
ЗАДАЧА № 4.
Имеется 20 г смеси кальция и окиси
кальция. Один грамм этой смеси с водой
образует 224 мл водорода.
Определите количество кальция в этой
смеси. Сколько граммов гашеной извести
образуется при взаимодействии 20 г смеси
с водой?
ЗАДАЧА № 5.
Сколько граммов масляной кислоты
и бутилового спирта потребуется для
получения 61,2 г маслянобутилового эфира,
если выход — 85% от теоретического?
ЗАДАЧА № 6.
При нагревании 23 г спирта с
концентрированной серной кислотой было получено
8,96 л непредельного углеводорода с одной
двойной связью. Определите формулу
спирта, если выход углеводорода
составляет 80%. Какой углеводород образовался
в реакции?
ЗАДАЧА № 7.
К смеси 10 л этана и пропилена
прибавили 10 л водорода. Смесь пропустили над
нагретым катализатором из платины. При
этом объем смеси уменьшился до 16 л.
Определите процентное содержание
этана и пропилена в смеси газов.
(РЕШЕНИЕ ЗАДАЧ —на стр. 87)
опыты
БЕЗ
ВЗРЫВОВ
ХИМИЧЕСКИЙ СТОРОЖ
Вам, наверное, приходилось слышать о хе-
мотронике — новой отрасли науки, совсем
недавно возникшей на стыке химии,
электроники и электротехники. В ведении хе-
мотроники — приборы и элементы для
электронных схем, основанные на химических
процессах в жидкости (статья о хемотро-
нике будет напечатана в одном из номеров
журнала в этом году).
Вы можете попробовать сделать сами
модель хемотронного прибора — датчика.
Корпус датчика лучше всего выточить на
токарном станке из оргстекла. Все размеры
корпуса даны на рисунке. Можно обойтись
и без токарного станка, но тогда корпус
придется склеивать из отдельных пластинок
дихлорэтановым клеем. Его приготовляют,
растворяя 10—15 г стружки оргстекла
в 100 мл дихлорэтана. (ОСТОРОЖНО!
ДИХЛОРЭТАН ЯДОВИТ!) Разумеется, в этом
случае корпус будет не круглым, а
прямоугольным.
Просверлите в корпусе четыре
отверстия. В три отверстия (на рисунке — справа)
вставьте графитовые стержни (толстые
грифели для цанговых карандашей). Это —
электроды. Места выхода электродов из
корпуса смажьте дихлорэтановым клеем,
а когда он засохнет, осторожно высверлите
небольшое, диаметром 0,3—0,5 мм,
центральное отверстие в корпусе датчика. Это
отверстие обязательно должно пройти
через средний электрод. Затем приклейте
к корпусу сверху и снизу две мембраны,
заранее вырезанные из тонкого оргстекла
толщиной 0,3—0,5 мм.
А пока клей сохнет, приготовьте
электролит. Растворите в половине стакана
дистиллированной воды 20—30 г йодистого
калия. Слегка подогревая раствор,
добавьте 0,5—1 г иода. Электролит можно залить
в датчик медицинским шприцем. При этом
следите, чтобы под мембранами не
осталось пузырьков воздуха.
Остается загерметизировать датчик.
Закройте отверстие заранее приготовленной
пробкой из оргстекла, осушите поверхность
корпуса около пробки фильтровальной
бумагой и залейте пробку дихлорэтановым
клеем.
Электрическая схема датчика показана
на рисунке и не требует пояснений.
Включите ток, с помощью реостата установите
напряжение между электродами 0,8—0,9 в.
Микроамперметр, включенный в цепь
центрального электрода — катода, покажет ток
100—200 мка. Если оставить схему
включенной на 10—15 часов, ток понизится до 10—
20 мка. В таком состоянии датчик готов к
работе.
Проверить его очень просто: слегка
подуйте на одну из мембран или коснитесь ее
кончиком отточенного карандаша. Стрелка
микроамперметра резко отклонится вправо.
Так чутко датчик реагирует на незаметное
глазу смещение мембраны.
Объясняется это так. Сила тока зависит
от количества иода около катода. Под
действием постоянного электрического тока на
катоде иод восстанавливается:
J2 + 2е -> 2J-.
А на аноде иод вновь образуется:
2J- -> J3 + 2e.
Иод как бы «перекачивается» к аноду.
Поэтому-то после зарядки датчика ток
падает. Сдвигая мембраны с места, мы
«толкаем» к катоду молекулы иода, и ток вновь
увеличивается.
Такие приборы настолько
чувствительны, что могут «зарегистрировать» даже
несколько молекул. Это свойство датчиков
используют там, где нужно почувствовать
очень слабый механический сигнал: при под-
86
счете мелких деталей на конвейере, для
измерения частоты пульса.
Если поставить датчик в дверях
квартиры, он сообщит вам о приходе гостя.
Конечно, для этого придется смотреть на
микроамперметр не отрываясь. Но если вы
сумеете сделать систему сигнализации,
использовав в ней хемотронный датчик, то
такая система может отреагировать на
приход гостя звонком или вспышкой лампочки.
Кстати, это используется при охране
важных объектов, например банков. Правда,
в этом случае датчик отнюдь не
гостеприимен: его задача — сигналом
предупредить охрану об опасности.
РЕШЕНИЕ ЗАДАЧ
(см. стр. 84)
ЗАДАЧА № 1.
1. Запишем уравнение реакции и
найдем объем водорода, вступившего в
реакцию, и количество образовавшейся воды»
хм3 14 кг у кг
Fe304 + 4Н2 = 3Fe j- 4H2G.
89,6 мз 168 кг 72 кг
89,6-14
168
7,47 мз; у
14-72
168
С кг.
2. Определим, сколько 100%-ной
серной кислоты необходимо для получения
7,47 м3 водорода.
х кг 7,47 м3
H,S04 Me — MeS04 \- H2.
98 кг 22,4 м3
Me — двухвалентный металл.
__ 98.7,47 = 32,67 кг.
х ~~ 22,4
3. Произведем пересчет 100%-ной
серной кислоты на 17%-ную:
192 кг.
100 кг — 17 кг х = 100-32,67
х кг — 32,67 кг 17
4. Найдем, наконец, искомый объем
кислоты:
т 192
1,2
160 л.
ЗАДАЧА № 2.
1. Напишем уравнение реакции между
железом и соляной кислотой, и по объему
выделившегося водорода определим
количество железа в препарате:
х г v г 2,8 л
Fe + 2НС1 = FeCl2 + Н2
56 г
73 г
22,4 л
56-2,8
22,4
= 7 г.
Значит, в препарате содержится
g~ 100% =82,35% железа.
2. Определим количество 100%-ной
соляной кислоты, необходимое для получения
2,8 л водорода:
73-2,8
& =
22.4
9,12 г.
3. Пересчитаем 100%-ную соляную
кислоту на 20%-ную:
9,12-100
20
= 45,6 г.
Это количество соляной кислоты имеет
объем:
45,6
1,1
= 41,46 mjt.
ЗАДАЧА № 3.
1. Из уравнения реакции найдем вес
чистого известняка, который необходимо
взять для получения 11,2 л СОг-
х г у г 11,2 л
СаС03 __ СаО , СОо.
100 г ~ 56 г ^ 22,4 л
х --= 50 г.
2. В известняке содержится 10%
примесей. На долю СаСОз приходится 90%.
Общий вес известняка будет равен
so
~- 100 = 55,56 г.
3. Из уравнения реакции найдем вес
окиси кальция:
56-11,2
У
22,4
. — 28 г.
4. Запишем уравнение реакции
получения гидрата окиси кальция из окиси
кальция. Из уравнения определим, сколько
воды затрачено на гашение извести и сколько
образовалось Са(ОНJ-
28 г х г у г
СаО -, Н20 = Са(ОНJ.
56 г 18 г 74 г
56 У 56
5. Определим количество 100%-ной
соляной кислоты, которое потребуется для
нейтрализации 37 г гидрата окиси кальция:
х г 37 г
2НС1 Са(ОНJ = СаС12 + 2Н20
73 г
74 г
73-37
74
=- 36,5 г.
Значит, 10%-ной кислоты потребуется
100.36,5 ,-_
10 =365 Г"
6. Найдем объем 365 г соляной кислоты:
m 365 п/гу а В1тт
v = — = 347,6 мл.
d 1,05
ЗАДАЧА № 4.
1. Водород образуется при реакции
кальция с водой. Поэтому сначала
определим количество кальция в смеси.
х г 224 мл
Са ± 2Н20 = Са (ОНJ +
40 г
22400 мл
40-224 п,
х = — 0,4 г.
22400
2. В одном грамме смеси содержится
0,4 г Са, а в 20 г смеси 0,4 • 20 = 8 г. На долю
окиси кальция остается 20—8=12 г.
3. Узнаем теперь, сколько гашеной
извести образуется при взаимодействии 8 г
кальция с водой:
8 г ' х г
Са + 2НоО = Са @НJ -\ Н2.
40 г 74 г
8-74
40
. = 14,8 г.
4. При взаимодействии СаО с водой
тоже образуется гашеная известь.
Определим ее количество:
12 г у г
СаО -f н20 = Са @НJ.
56 г 74 г
S - i*« = 15.8 г.
56
5. При реакции заданной смеси с водой
образовалось всего
14,8 - 15,8 - 30,6 г Са @НJ.
ЗАДАЧА № 5
1. Найдем теоретический выход масля-
нобутилового эфира:
61,2-100
85
. = 72 г.
2. Напишем уравнение реакции
получения маслянобутилового эфира.
х г у г 72 г
С3Н-С0ОН + С4Н90Н -> С3Н7 С00С4Н9 + Н20,
88 г 74 г 144 г
3. Определим количества исходных
веществ:
88-72
144
74-72
= 44 г масляной кислоты;
= 37 г бутилового спирта.
у - 144
ЗАДАЧА № 6
1. Теоретический выход непредельного
углеводорода составит
8,96-100
80
11,2 л.
2. Напишем уравнение химической
реакции получения непредельного углеводорода
из спирта и определим вес г-м спирта.
23 г H2S04 11,2 л
R — ОН > R2— СН = СН2 + Н20.
х г нагрев 22,4 л
_ 23-22,4
11,2
= 46 г.
3. Подберем формулу спирта с
молекулярным весом 46.
R — ОН
29 17
Единственный радикал с молекулярным
весом 29 — этил. Значит, спирт—этиловый.
Непредельный углеводород,
образующийся при нагревании этилового спирта
с концентрированной серной кислотой, —
это этилен С2Н4. Вот как выглядит
уравнение реакции:
H2S04
СоН50Н —--► С2Н4 4 Н20-
нагрев
ЗАДАЧА № 7
1. Общий объем смеси газов равен 20 л.
В результате химической реакции объем
уменьшился на 20—16 = 4 л.
2. Запишем уравнение реакции
взаимодействия пропилена с водородом (этан —
предельный углеводород, с водородом он
не взаимодействует).
СзН6 + Н2 —> С3Н8.
3. Как следует из уравнения реакции, из
двух объемов исходных газов образуется
один объем пропана. Объем смеси газов
уменьшился на 4 л, следовательно, в 10 л
смеси содержится 4 л пропилена.
4
Значит, в смеси содержится -ттг- 100% =
= 40% пропилена и 60% этана.
10
СТРАНИЦЫ
ИСТОРИИ
а мскундин „УЧЕНИЕ, НА ОПЫТАХ
ОСНОВАННОЕ"
Первый русский учебник
химии увидел свет в 1808 году.
Это было время бурного
развития химии — в первое
десятилетие XIX века были открыты
великие законы — закон
эквивалентов, закон постоянства
состава, закон простых кратных
отношений.
На титульном листе
учебника написано: «Руководство
к преподаванию химии,
сочиненное Александром Шерером,
Надворным Советником,
Императорской Академии наук
Экстраординарным
Академиком, Медико-Хирургической
Академии, Педагогического
Института и Горного Кадетского
Корпуса профессором химии, и
членом Академий наук
Копенгагенской и Эрфуртской,
Обществ Естествоиспытателей
Берлинского, Московского, Гет-
тингского, Эрфуртского, Гар-
лемского, Иенского,
Соревнования Врачебных и Физических
наук Парижского, Монтпельер-
ского, Брюссельского и
Московского, Минералогического
Иенского и Экономических
Императорского Санктпетербург-
ского и Лейпцигского».
Учебники химии выходили
на русском языке и раньше, но
все они были переводными.
Александр Иванович Шерер в
«предуведомлении» к книге
пишет, что настала пора
создать оригинальный русский
учебник. Автор ставит перед
собой задачу — «...преподавать
учение, более на опытах
основанное, нежели как
обыкновенно преподавали оное; и
следственно, лаборатории, смотря
по обширности опытной части
Химии в новейшие времена,
устроить приличнейшим или
вовсе другим образом... Доселе
по худому вкравшемуся
обычаю преподавали учение по
рукописным тетрадям, которые
учащиеся, списывая с
погрешностями, сообщали один
другому». Списывание с чужих
тетрадей во все времена не
поощрялось. Но что оставалось
делать учащимся в те годы —
стабильных учебников-то не было!
Отметим кстати, что слово
Химия в учебнике всегда
пишется с заглавной буквы.
ЧТО ТАКОЕ ХИМИЯ?
Учебник А. И. Шерера,
несмотря на полуторавековую
разницу в возрасте, очень схож
с современными учебниками.
Это не относится, конечно,
к стилю изложения. В первом
томе учебника — семь крупных
разделов («отделений»). В двух
первых разделах
рассказывается о химических
закономерностях, в остальных — описаны
свойства отдельных веществ.
Второй том посвящен
химическим соединениям.
В первом же параграфе
учебника дано определение
науки химии. Вот оно: «Химия
есть наука, которая показывает
действие простых веществ в
природе, составление тел из
оных по их различным
содержаниям, и купно же способ
разлагать или паки составлять
новые тела». В современном
учебнике сказано то же самое, но
несколько короче: химия —
это наука о веществах и их
превращениях.
Описание свойств многих
веществ в учебнике А. И.
Шерера находится почти на
«современном уровне». Вот как,
например, описаны свойства
«кислотворного газа»
(кислорода):
«1. Кислотворный газ
несколько тяжелее атмосферного
воздуха.
2. Он не имеет ни запаха,
ни вкуса и не показывает ни
малейших следов кислоты.
3. С водою, лишенною
воздуха через варение, столь слабо
смешивается, что при одном
уже болтании и согревании
отделяется от оной.
4. С атмосферным воздухом
смешивается без малейшей
перемены.
5. Наиболее к дыханию
способен.
6. Все явления окисления
особливо приметны в оном.»
«ОБОЗРЕНИЕ НАЧАЛ»
Так называется один из
параграфов «Руководства». Это —
систематизация элементов
(«начал» или «неразложных
веществ»). Вспомните: система
предложена за 62 года до
открытия периодического закона.
Поэтому пусть она не
покажется вам наивной и запутанной *.
«Начала» бывают:
I. Неопределяемые весом,
или необъемлемые: светотвор,
теплотвор.
II. Определяемые весом.
А. В свободном состоянии
токмо в воздушном виде
представляемые (выражаясь
современным языком — газы) —■
кислотвор (кислород), селитро-
твор (азот), водотвор (водород);
Б. В свободном плотнейшем
состоянии представляемые
(иными словами, твердые тела).
1. Нерастворяемые в воде.
Среди них — в огне
непостоянные, но удобосгораемые: угле-
твор (углерод), сера, фосфор —
и неудобосгораемые, металлы:
платина, золото, серебро, ртуть,
свинец, висмут, никель, медь,
мышьяк, железо, кобальт,
олово, цинк, сурьма, марганец,
молибден, вольфрам, уран, титан,
теллур, хром, тантал, колумб
(ниобий), церий, никколан,
новый металл, открытый в
платине (иридий, осмий, палладий
или родий).
Есть «элементы» и огнепо-
стоянные, земли (окислы):
голыш (двуокись кремния), глина
(окись алюминия), тальк (окись
магния), циркон (двуокись
циркония), глицин (окись
бериллия), иттрия (окись иттрия).
2. Растворяемые в воде —
* Мы позволим себе
несколько упростить систему
А. И. Шерера и дать ее в
кратком изложении, сохранив при
зтом терминологию автора.
В скобках даются современные
названия элементов и
веществ. — А. С.
кислоты (соляная, борная,
плавиковая); щелочные вещества:
кали (едкое кали), натр (едкий
натр), известь (гидроокись
кальция), барит (гидроокись бария),
стронтит (гидроокись стронция).
Как видите, к «неразлож-
ным веществам» — элементам
относятся и многие соединения:
окислы, щелочи, некоторые
кислоты. Сложное строение зтих
веществ было установлено
лишь позднее. С другой
стороны, в этом списке нет,
например, элемента хлора, хотя он
был известен химикам еще
с 1774 года. Дело в том, что хлор
во времена А. И. Шерера
считался сложным веществом —
окислом соляной кислоты.
УГЛЯКИ И УКСУСНЯКИ
За полтора века, прошедшие
после издания «Руководства»
А. И. Шерера, было открыто
множество новых элементов.
А вот «закрыто» совсем
немного. В книге упоминаются
только три элемента, которых
нет в современных учебниках
(если не считать, конечно,
элементами окислы, кислоты и
основания). Закрытые элементы —
зто теплотвор, светотвор и
никколан. Что же зто такое? По
определению автора
«теплотвор... почитается существом
особенного рода, производящим
чувствие теплоты». «Светотвор
есть подлежательная причина
чувства, именуемого зрением».
Что же касается никколана,
то, судя по описанию его
свойств и методу получения,
зто скорее всего сплав никеля
с кобальтом.
9 декабря 1807 года
Александр Иванович Шерер
выступил в Петербургской Академии
наук с докладом «Опыт
методического определения
химических наименований для
Российского языка». Этот доклад
вошел в его руководство в
качестве приложения. По сути
дела, зто была первая научная
работа по составлению русской
химической номенклатуры.
Как видно уже из «Обозрения
начал», многие названия,
употребляемые Шерером,
сохранились до сих пор. Именно
А. И. Шереру принадлежат
такие, например, названия
кислот, как угольная, лимонная,
яблочная, янтарная,
мышьяковая.
А многие другие термины,
введенные А. И. Шерером,
теперь вызывают только
улыбку. В стремлении
русифицировать всю химическую
номенклатуру, А. И. Шерер
предлагает называть соли угольной
кислоты «угляками», а соли
уксусной кислоты — «уксусня-
ками». Нитраты и нитриты он
именует, соответственно, «сели-
тряками» и «селитриками», ар-
сенаты и арсениты — «мышья-
ковяками» и «мышьяковика-
ми». Щавелевую кислоту он
называет «сахарной», а ее соли
(оксалаты) — «сахарняками».
Галловая кислота получила
в «Руководстве» имя
«чернильной кислоты», а производные
камфоры называются «камфор-
няками». Несмотря на
непривычные для нашего уха
названия, нужно воздать должное
такой последовательности в
разработке русской номенклатуры.
ЧТО ЭТО ТАКОЕ?
(СМ. СТР. 82)
Снятый с близкого расстояния поролон. У этого
популярного материала есть и более строгое имя —
пенополиуретан.
ВОПРОСЫ
ДЛЯ САМОПОДГОТОВКИ
13
КАКИЕ СУЩЕСТВУЮТ ТИПЫ
ОКИСЛОВ!
14
КАКИЕ СУЩЕСТВУЮТ
ОСНОВНЫЕ СПОСОБЫ ПОЛУЧЕНИЯ
ОКИСЛОВ!
15
ЧТО ТАКОЕ ОСНОВАНИЕ!
91
16
КАКИЕ СУЩЕСТВУЮТ
СПОСОБЫ ПОЛУЧЕНИЯ
ОСНОВАНИЙ!
17
ЧТО ТАКОЕ КИСЛОТА!
18
КАКИЕ СУЩЕСТВУЮТ ТИПЫ
КИСЛОТ!
19
КАКИЕ СУЩЕСТВУЮТ
СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОТ!
20
КАКИЕ СУЩЕСТВУЮТ ТИПЫ
СОЛЕЙ!
21
КАКИЕ СУЩЕСТВУЮТ
СПОСОБЫ ПОЛУЧЕНИЯ СОЛЕЙ!
22
В КАКИХ
СЛУЧАЯХ
ИДУТ ДО КОНЦА!
1
РЕАКЦИИ
1
23
ЧТО ТАКОЕ
ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ!
24
ЧТО ТАКОЕ ИОННЫЕ
УРАВНЕНИЯ!
Основания - это вещества,
диссоциирующие в растворе с
образованием ионов гидрокспла
ОН- (NaOH ;t Na+ -J- OH-), или
вещества , присоединяющие ионы
водорода Н+, образующиеся при
I диссоциации воды (NHs +Н+-|-
-J- ОН- ^ NHj+ -f OH-).
Кислоты бывают кислородные
(H2S04) н бескислородные (НС1).
Соли ооразуютгя при реакциях
нейтрализации BNaOH-|-HcSOj=
=NaeSQ,-J-2HX))t при реакциях
замещения (Fe -f Си SO, = Си + FeSOj),
а также лри реакциях обмена
(Na-SO, -f BaCl2 = BaS04 + 2NaCl).
В растворах электролитов реакции
происходят не между молекулами,
а между ионами, на которые они
распадаются.
Например, уравнение реакции
нейтрализации NaOH-J-HCl—NaCl+H20
в ионной форме запишется так:
Na* 4- ОН- + Н+ + Cl-=Na+4-CI- +
-| НоО, или окончательно в общем
виде так: ОН" 4- Н* = Н20.
Окислы образуются при
взаимодействии некоторых элементов или их
соединений с кислородом (S 4- 02 =
= S02, 2H.S 4- 303 = 2H20 4-2S02), a
также при обезвоживании
(дегидратации) некоторых кислот и
оснований (H«Si0.=H904-Si02, Cu(OHJ=
= CuO 4- ВД))-
Кислоты — это вещества,
диссоциирующие в растворе с
образованием ионов водорода Н*\ но не
дающие никаких других
положительно заряженных ионов (срашш:
НС1 ^t Н- 4- С1-, но KHSO» ^K 4
4- Н+ 4- S'V").
Соли бывают кислые и средние.
Кислые соли — зто продукты
неполной нейтрализации многооенов-
ных кислот (NaOH -J- H2SO» =
= NaHS04 4- НоО), а средние —
полной BNaOHV H,S04 = Ка,й04 4-
4- l!ELO). Кислоты с основностью
больше двух могут давать
несколько кислых солей (КаНЛЮ4,
Na,HPG4).
Явление электролитической
диссоциации состоит d том, что
молекулы электролитов (веществ,
растворы которых проводят
электрический ток) при растворении
распадаются на ионы — положительно
заряженные катионы и отрицательно
заряженные анионы. Сумма
положительных зарядов равна сумме
отрицательных зарядов. Свойства
ионов отличаются от свойств
нейтральных атомов и молекул, на
которых эти ионы образовались.
Окислы делятся на солеобразу-
ющпе и несолеобразующие. Соле-
образующне окислы делятся на
основные (Na20, CuO), кислотные
(SO.) и амфотерные (А1202);
несолеобразующие окислы составляют
отдельную группу веществ (СО, NO).
Основания образуются при
взаимодействии некоторых металлов с
водой BNa 4- 2H.O=2NaOH4-H2), при
взаимодействии некоторых
основных окислов с водой (CaO -J- Н*0 =
=Са(ОНM), при взаимодействии
некоторых солей с сильными
основаниями (CuS04 4- 2КаОН=Си(ОНM 4-
4- Na?SCL), а также при
взаимодействии некоторых солен слабых
кислот с водой гидролине (Na*S -\-
4- НоО ^t NaOH -J- NaHS).
Кислородные кислоты образуются
при взаимодействии некоторых
кислотных окислов с водой (SOj-J-
h HX) = H.S04), а также при
действии кислот на соли (NaN034-
4-H2S04=HN04+NaHS01, Na„S iO,4-
4-2HC1 = H,SiOa 4- 2NaCD-
Бескислородные кислоты ооразуются при
взаимодействии некоторых
элементов с водородом (Но 4 Cls = 2HC1),
а также при действии кислот на
соли (NaC! — H3S04=HCl-j-NaHS04).
Реакции идут до конца в тех
случаях, когда образуется летучий
продукт реакции (NaC! -j- H^SO» =
= НС1 4 NaHS04), когда выпадает
малорастнорпмый осадок (CuSOj-f-
4 2NaOH = Си(ОНJ 4- Na5S04), или
когда продукт реакции злабо
диссоциирован BNaOH |-H,SOe—
=Na,rfOs 4- 2Н,0).
НАУЧНЫЙ
ФОЛЬКЛОР
ПРИГОТОВЛЕНИЕ КОФЕ
В НАУЧНО-
ИССЛЕДОВАТЕЛЬСКИХ
ИНСТИТУТАХ
В своих лабораториях и
кабинетах ученые существенную
часть времени посвящают
приготовлению и потреблению
кофе.
Необходимость упорядочить
зту деятельность чувствуется
очень остро. Настоящая
заметка — скромная попытка
обобщить богатый опыт.
МАТЕРИАЛЫ И МЕТОДЫ
Используются все имеющиеся
в продаже сорта кофе, берутся
порошки различного помола.
Варка осуществляется в
сосудах из стекла, алюминия или
нержавеющей стали (включая
и лабораторные стаканы,
огнеупорные мензурки, цедилки,
автоклавы, а также перегонные
кубы). В крайнем случае
используется обычное
коммерческое оборудование.
Источниками энергии для повышения
температуры экстрагирующей
воды могут служить: пламя
газовой горелки, электрический
ток. перегретый пар,
выхлопные газы двигателей
внутреннего сгорания. Летом
используются охлаждающие системы:
холодильники, морозильники,
ледяные кубики, сухой лед и
жидкий воздух.
Существуют следующие
способы варки кофе:
«Любительский», «Профессиональный»,
«Экспресс» и «Экспрессо»,
1. «Любительски й»:
кофе грубого помола высыпается
в холодную воду, затем вода
доводится до кипения. Осадок
тщательно взбалтывается,
полученная суспензия
разливается по чашкам. В том что
получающийся продукт —
действительно кофе, можно
убедиться, пожалуй, лишь с помощью
фотометрических измерений.
2.
«Профессиональный» способ. Вода нагревается
до 99°С. В нее добавляется
кофе тонкого помола (примерно
12 г на чашку). Жидкость
доводится до кипения и снимается
с огня. Полученный продукт
имеет тонкий вкус, который
удается отбить, добавляя
молоко.
3. «Экспресс» — метод,
котрый следует отличать от
описываемого ниже «Экспрес-
со». Он состоит в
использовании быстрорастворимого кофе
в сочетании с кипящей или
горячей водой, в соответствии
с инструкциями, написанными
на жестянке. Способ имеет два
преимущества перед всеми
другими. Первое — быстрота.
Второе — в этом случае
отсутствует пресловутый «чудный
аромат свежего кофе», что
позволяет избежать нашествия
жаждущих соседей.
4. «Экспрессо». Это
название стало нарицательным
для паровой экстракции.
Перегретый пар пропускается через
спрессованный кофейный
порошок, а затем охлаждается.
Полученный конденсат обладает
цветом и запахом кофе. Этот
способ слишком трудоемок и
может быть рекомендован лишь
для тех случаев, когда вы
страдаете из-за избытка
технического персонала и недостатка
идей, которые позволили бы
вам занять их на более
производительной работе.
РЕЗУЛЬТАТЫ
В лабораторных условиях
результаты варки и питья кофе
в чрезвычайной степени
зависят от времени, потраченного
на зти процедуры.
Мы не будем
останавливаться на совершенно непривив-
шемся способе употребления
кофе в одиночку и сбсудим
результаты, к которым
приводит коллективное кофепитие.
Эти результаты можно кратко
представить в виде следующей
эмпирической формулы:
п Ст. Сп. Нн.Ст. р
Здесь П — продуктивность или
количество человеко-часов,
потраченное на достижение
результатов, ожидаемых от
лаборатории дирекцией; Тн— время,
затраченное на питье кофе; Ст.
Сп. — степень спаянности
коллектива, возникающей в
результате группового кофепи-
тия, Ин. Ст. — интенсивность
интеллектуального
стимулирования, появляющаяся в
результате употребления кофе и
проходящих в это время
различных обсуждений; Р —
константа «трепа», зависящая от
числа сотрудников
лаборатории, принимающих участие в
кофепитии.
Продуктивность П обратно
пропорциональна Т —времени
кофепития; зто справедливо
лишь в определенных
пределах, не нашедших отражения в
приведенной формуле.
Действительно, если Т{. = 0 (то есть на
питье и приготовление кофе не
потрачено и секунды), значит
П=оо, чего, очевидно, не
бывает. С другой стороны, в
пределе Тн _>эс продуктивность
неизбежно упадет до нуля,
несмотря на то, что «спаивание»
коллектива и стимулирование
интеллектуальных усилий
путем непрерывного потребления
кофе имеет тенденцию
возрастать вместе с ростом Т .
Если вспомнить, что сумма
Т и Р обычно не превышает
7—16 часов, то оптимальная
интеллектуальная стимуляция
получится лишь в том случае,
если время, потраченное на
употребление кофе, и
продуктивное время окажутся
равными. В этом случае Р = Т и,
следовательно, (Ст. Сп. + Ин.
Ст.) ■ Р = 1, максимально
возможному значению этой
величины.
Обсуждение результатов и
выводы читатели могут сделать
сами.
Сокращенный перевод
с английского
СКАЗКА
ЧТО БОЛЬШЕ ВСЕГО
НРАВИЛОСЬ
МОРСКОМУ ВОЛКУ
Однажды мы увидели, что множество
людей направляется в сторону пристани. Мы
поинтересовались, что там случилось.
— Морской Волк приехал! —
объяснили нам.
Мы тоже поспешили к пристани, и еще
издали увидели перед старым трактиром
огромную толпу. Нам удалось
пробраться внутрь. У большого стола стоял
Морской Волк в синей фуражке с якорем. Он
курил трубку, а вокруг толпились
фотографы и журналисты с блокнотами. Все
просили Волка рассказать что-нибудь
такое...
— Ну ладно, — сказал наконец
Морской Волк. — Спрашивайте!
— Уважаемый Морской Волк, —
спросил первый журналист. — Где вы плавали?
— Я плавал всюду, — сказал Волк. —
Везде. Вчера был на Луне, — добавил он
скромно.
Все бросились записывать, а пока
фотографы щелкали своими аппаратами,
второй журналист протискался поближе и
спросил:
— Очень интересно узнать, на каких
судах вы туда плавали?
— На всех, — ответил Волк. — На
самых больших. На одном мне даже
пришлось ездить по палубе на самокате. С
одного конца в другой — четырнадцать дней!
— Благодарим вас, уважаемый
Морской Волк, — закричали вокруг. — Вы
совершили так много героических подвигов.
Расскажите пожалуйста...
— Я совершаю ежедневно по тридцать
подвигов, — строго сказал Морской Волк.
А иногда и по пятьдесят. Вот вчера
вечером, когда мы везли орехи с Луны, нам
повстречалось стадо крокодиловых китов,
и все перепугались, потому что один такой
кит может сожрать сразу три корабля.
Тогда я бросился в воду и откусил всем
крокодиловым китам головы!
Все вокруг замерли от восторга, и нам
удалось ввернуть свой вопрос: какое
место на свете больше всего нравится
отважному путешественнику?
— Все места, — сказал Морской
Волк. — А больше всего — трактир.
Потому что здесь бальзам продают...
— Еще бы, ему здесь не нравилось, —
тихо сказал трактирщик, оказавшийся
возле нас. — Он отсюда уже который год не
выходит.
ЧТО ЖЕ ЭТО ЗА ТАКОЙ
БАЛЬЗАМ?
Его изобрел в середине XVIII века
рижский купец Абрахам Кунцен и в 1789 году
получил специальную привилегию,
запрещающую подделку бальзама. Кунцен
готовил свой напиток из спирта, настоянного
на травах и черных кореньях, собранных
местными крестьянами. А некоторые
специи покупал даже за границей...
Сохраняется ли в точности рецептура
XVIII века, сказать затруднительно. Но во
есяком случае и сейчас Рижский ликеро-
водочный завод выпускает такой крепкий
алкогольный напиток — «Рижский черный
бальзам». Входит в него великое
множество специй, в том числе — довольно
необычных для спиртного. Вот некоторые из
них: померанцевая корка, перец черный,
малина свежая, бальзамное перуанское
масло, дубовая кора, аирный корень,
арниковый цвет...
Этот напиток необычного черного цвета
и почтенного возраста пользуется
репутацией, которую можно было бы назвать,
употребив научный термин, полярной.
Один полюс — мнение Морского Волка
(как никак, крепость бальзама — 45°).
Другой — убеждение, что «Бальзам»
обладает целебными свойствами.
Врачи, а также журнал «Здоровье»
этого второго мнения не разделяют, не
закрывая, впрочем, глаза на то, что чайная
С тех пор, как алхимики намеревались обогатить
человечество, превратив неблагородные металлы в
золото, и до сегодняшнего дня, когда химики вот-
вот накормят нас синтетической черной икрой, их
загадочная работа, победы и неудачи вызывают
живейший интерес и внимание.
Но слава создается не только научными
публикациями и парадными портретами знаменитых ученых.
Говорят, что об успехе литературного произведения
лучше всего свидетельствует количество написанных
на него пародий. И рассказы о тиотимолине («Химия
и жизнь», № 9 за 1965 год) говорят о популярности
химии, пожалуй, не меньше, чем солидный том
«Справочника химика».
На третьей странице обложки помещено
несколько шаржей прошлого века на знаменитых
химиков.
1. Август Фридрих Кекуле A829—1896),
открывший структуру бензола. Шарж 1860 года.
2. Жан Батист Дюма A800—1896) — член
Парижской академии наук, член Лондонского
королевского общества, член Петербургской академии наук.
Впервые определял атомные веса по плотности
паров, разработал теорию замещения органических
соединений, открыл гомологические ряды и многое
другое, т. е. вполне достоин шаржа. Но кроме того,
Дюма был еще и политическим деятелем, что, разу-
ложка спиртного на стакан горячего
крепкого чая — не самое опасное средство для
взрослого человека, почувствовавшего
признаки простуды.
Химикам какое-либо особое действие
входящих в бальзам веществ не
известно.
Бот, пожалуй, и все о «Рижском черном
бальзаме».
А сказку о Морском Волке
чешского писателя И. Климы пересказала
Е. АНИКСТ
меется, отрывало его от научной работы. На
рисунке он изображен в химической лаборатории, это
должно было лишний раз напомнить ему, что его
главное занятие — наука. Рисунок О. Домье.
3. Мишель Эжен Шеврель A786—1889) — член
Парижской академии наук. Знаменит не только
работами по растительным и животным жирам и
технологии мыловарения, но и тем, что прожил 103 го-»
да, до последних дней печатая свои работы.
Рисунок П. Ренуара.
4. Встреча знаменитого Джона Дальтона A766—
1844) с профессором натурфилософии Утрехтского
университета Герритом Моллом A785—1838)
произошла в Эдинбурге на съезде Лондонского
королевского общества. Маленький великий Дальтон и
длинный Молл — подходящие объекты для
художника. Рисунок 1834 года.
5. Майкл Фарадей и некий отец Темзы.
Нетрудно понять, о чем они разговаривали между собой.
Карикатура из журнала «Панч» от 21 июля 1855 года.
6. В 1880 году виднейшие русские ученые
выдвинули Д. И. Менделеева в члены Петербургской
академии наук, но его кандидатура была отвергнута
реакционным большинством академии. Журнал
«Стрекоза» в декабре 1880 года откликнулся на это
событие карикатурой.
Л. СОЛОДКИН
1 2 3|
45
6 ! НЕОБЫЧНЫЕ ПОРТРЕТЫ
l«*.
•^^^„ гаялрау givim his <-«hi> tt> глтнгк Tuva»
Цена 30 коп.
Индекс 71050
Издательство «Наука»
3
химия
жизнь
1917 — 1967. Первый
в мире синтетический
каучук
Элемент № 102
Завод, который работал
без промышленных стоков
Что такое химический
лазер
Страницы истории:
как была встречена
«новая алхимия»
Грибы-диверсанты
Как «лечат» книгу
Настоящие водовидцы
Заочная конференция
наших читателей
Что вы знаете и чего не
знаете о минеральных
водах
Мимоза или акация?
Клуб Юный химик:
викторина, как продлить
жизнь батарейки, задачи
с решениями,
универсальная марганцовка,
вопросы для
самоподготовки
Наши консультации: еще
раз о пиротехнике
Из писем в редакцию
Книжная полка
Новости отовсюду
Фотолаборатория
Что могут и чего не
могут катализаторы