Похожие
Текст
химия
жизнь
с;
(С
X
а
•3
2
Z
CL
к
с:
>
с
о
с
I
о
Z
У
>
(В
Z
(О
X
а
9
1966
В ЭТОМ НОМЕРЕ:
Экономическая реформа
в действии
Существует ли вещество
памяти?
Вспышка гения
Элемент № 7: азот
Погоня за нейтрино
Как сделать значок
Полезные советы парфюмера
а
2
х
а
ос
с:
>
с
о
с
I
о
X
У
>
CD
X
Среди победителей конкурса клуба Юный химик за 1965 год были 32 львовских
школьника — они занимаются в химическом кружке областной станции юных техников. Участники
кружка ставят «яркие» опыты: получают светящиеся красители и пробуют писать ими
пейзажи, делают легкоплавкое окрашенное стекло. Девятиклассник Николай Тормахов
занимается усовершенствованием состава стекла. Он пытается найти такие рецепты, чтобы
стекло могло имитировать драгоценные камни — рубин и изумруд.
2* сн%£№
химия
жизнь
В НОМЕРЕ:
Экономика и производство. БОЛЬШЕ ПЛАТИТЬ — ЧТОБЫ БОЛЬШЕ
ПРОИЗВОДИТЬ. БОЛЬШЕ ПРОИЗВОДИТЬ — ЧТОБЫ БОЛЬШЕ ПЛАТИТЬ. Очерк М.
Черненко 2
ЭЛЕМЕНТ № 7: АЗОТ. СИНТЕЗ АММИАКА — инженер П. А. Гинзбург. КАК
СВЯЗАТЬ АЗОТ—И. Луначарская. БЕЗЖИЗНЕННЫЙ ЭЛЕМЕНТ — И. В о п ь-
пер я 9
ПЛАСТМАССОВАЯ СКУЛЬПТУРА 17
ОТ КИЖЕЙ К АЭРОПОРТУ. Очерк инженера В. Цукермана 18
ПРОИСХОЖДЕНИЕ ЖИЗНИ. Окончание статьи Джорджа Уолда . . . . 23
Страница интервью. КАК СОЗДАВАЛОСЬ «СЕРДЦЕ» ПРОТИВОГАЗА .... 30
ОТ ДО Н20. Рассказывает кандидат химических наук Е. И. Г у р о в и ч . . . 32
Наш календарь. КАК БЫЛА ОТКРЫТА РАДИОАКТИВНОСТЬ. Заметки С.
Владимирова 34
ПОГОНЯ ЗА НЕЙТРИНО. Статья Ж. Л е в и-Л е 6 л о н а с комментарием
кандидата физико-математических наук А. Т. Филиппова 36
Страницы разных мнений. СУЩЕСТВУЕТ ЛИ ВЕЩЕСТВО ПАМЯТИ! На вопрос
отвечает доктор химических наук В. С. Т о н г у р 44
Словарь науки. И ВЫ МОЖЕТЕ ГОВОРИТЬ ПО-ГЭЛЬСКИ. Очерк А. Азимова . 49
ИСКУССТВО ПАРФЮМЕРА. Рассказывает Р. А. Ф р и д м а н 54
ЧТО ВЫ ЗНАЕТЕ И ЧЕГО НЕ ЗНАЕТЕ О ПАРФЮМЕРИИ. Рассказывает Я. Ф. П е ш-
ковский 59
КРАСКИ ТУРКМЕНСКОГО КОВРА. Статья кандидата химических наук В. И. К р и-
венцова 62
КАК ОБРАЗУЮТСЯ СИТАЛЛЫ 65
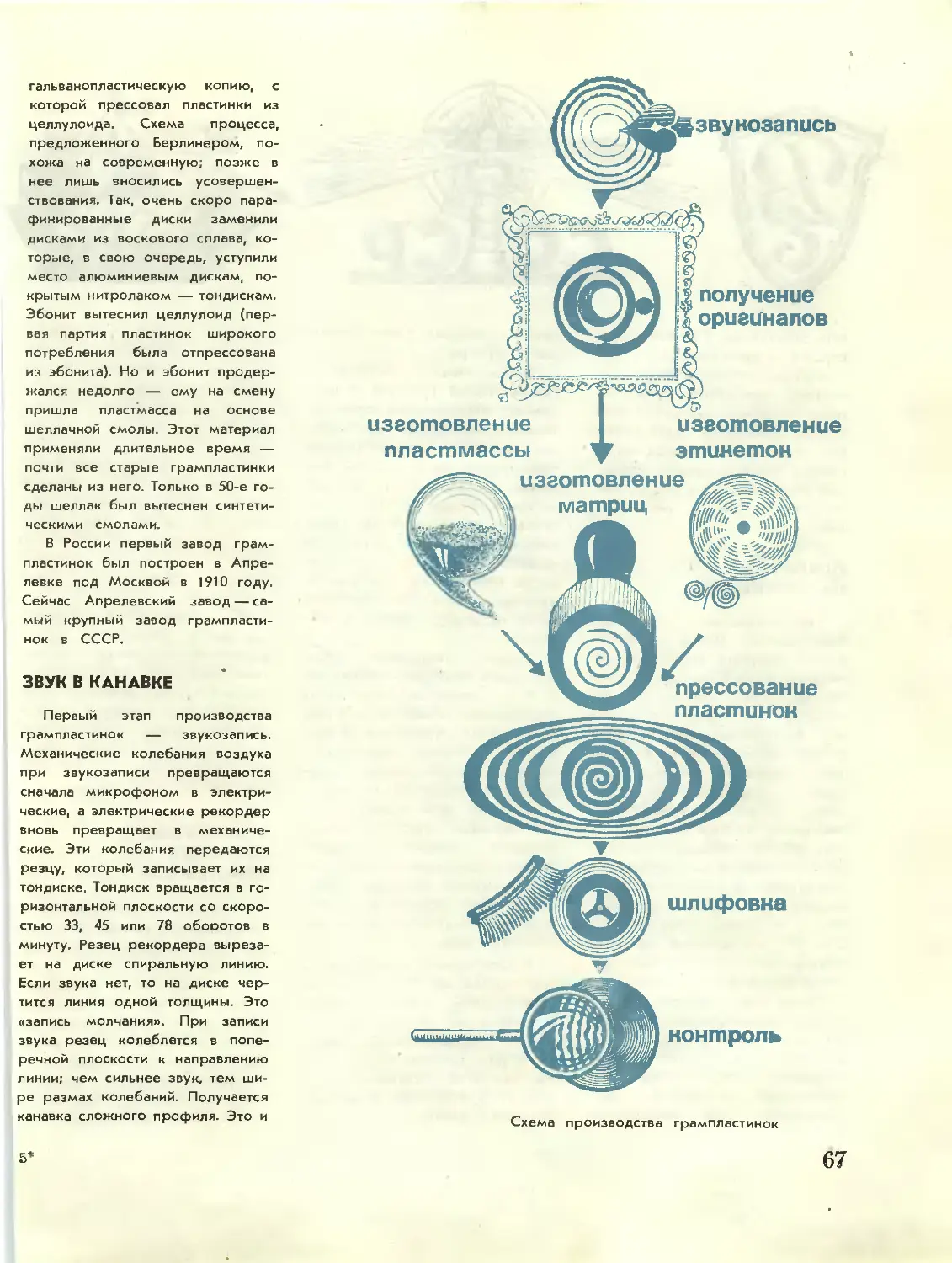
ГРАММОФОННАЯ ПЛАСТИНКА. Рассказывает кандидат химических наук
М. Л. Е з е р с к и й 66
ВСПЫШКА ГЕНИЯ. Перевод с английского 71
Клуб Юный химик. ХОТИТЕ ПОДГОТОВИТЬСЯ К ЭКЗАМЕНАМ ПОЛУЧШЕ!
ВИКТОРИНА. ВОПРОСЫ ДЛЯ САМОПОДГОТОВКИ. ПОЛ-ЛИТРА ЭЛЕКТРИЧЕСТВА.
РАССКАЗ-ЗАГАДКА «ПОРОШОК ПРАЙСА» 74
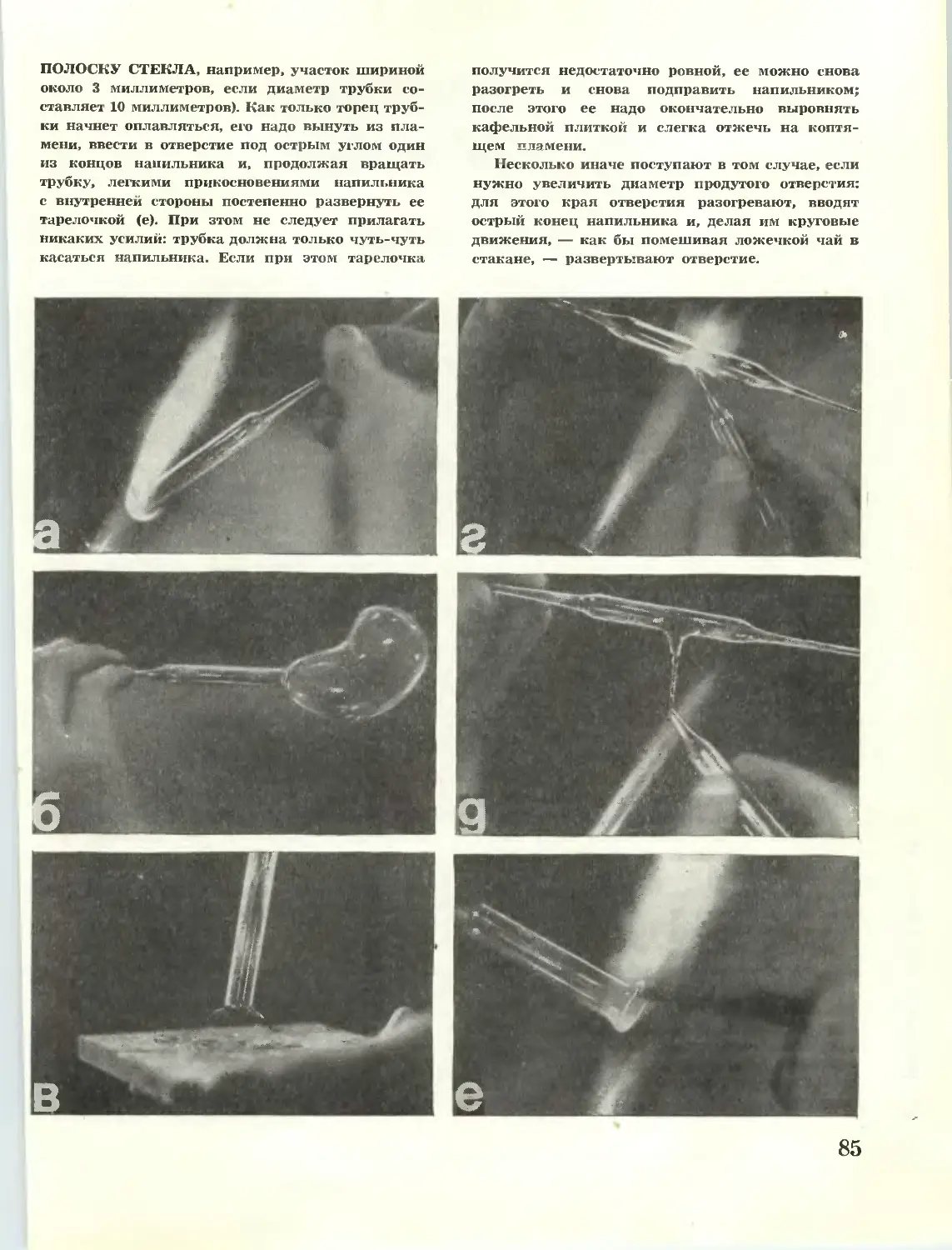
Наш практикум. СТЕКЛОДУВНАЯ МАСТЕРСКАЯ 84
УЧИТЕСЬ ПЕРЕВОДИТЬ. Английский — для химиков 86
Книжная полка. ЧИТАТЕЛЬ — СОРАТНИК ИССЛЕДОВАТЕЛЯ. Рецензия
члена-корреспондента АН СССР В. И. Гопьданского 89
Уголок фотолюбителя. ПРОЯВЛЯЮЩИЕ РАСТВОРЫ С ФЕНИДОНОМ. Заметки
кандидата технических наук Е. А. И о ф и с а 90
Страница садовода и огородника. ИЗВЕСТКОВАНИЕ: КОГДА ОНО НУЖНО!
Советы агрохимика Ф, П. Кащенко 91
НАШИ КОНСУЛЬТАЦИИ 94
ЗНАЧОК, КОТОРОГО НИ У КОГО НЕТ 95
НАУЧНО-ПОПУЛЯРНЫЙ сентябрь 19 6 6
ЖУРНАЛ М2 9
АКАДЕМИИ НАУК СССР год издания 2-й
больше платить—
чтобы больше производить,
больше производить—
чтобы больше платить
заметки о переходе
рязанского комбината химического волокна
на новую хозяйственную систему
М. ЧЕРНЕНКО,
специальный корреспондент «Химии и жизни»
О
ю
О
ЕЕ
О
ю
X
О
а
с
<
ас
О
х
О
ас
m
Цель этих заметок — не разъяснять
задачи новой системы планирования и
материального стимулирования (об этом
написано достаточно много), а показать ее
«механизм» в действии — на примере одного
предприятия.
ЧТО ПРЕДСТАВЛЯЕТ СОБОЙ
КОМБИНАТ
Новое предприятие; он пущен в
эксплуатацию в 1960 году.
Основное сырье — листовая целлюлоза.
Ее поставляют главным образом из
Архангельской и Калининградской областей.
Основная продукция — штапельное
волокно.
Технология производства в общих чертах
такова. Подготовка и машинная резка
листовой целлюлозы, подача ее
пневмотранспортом в бункера химического цеха.
Приготовление вискозного раствора, фильтрация,
обезвоздушивание, автоматическое
дозирование. На этом заканчивается химический
цех и начинается прядильно-отделочный,
находящийся с ним под одной крышей.
Здесь происходит формование нитей. Часть
волокна (в зависимости от требований
заказчиков) окрашивают. Далее волокно
вытягивается, упрочняется и режется на
прядки длиной несколько сантиметров. Затем
следуют отделочные операции и, наконец,—
сушка и упаковка.
Разумеется, существуют еще
вспомогательные цехи, в том числе приготовляющие
химические вещества, используемые в
основном производстве.
Штапельное волокно потребляют
многочисленные фабрики легкой
промышленности, изготовляющие самые
разнообразные ткани. География потребителей: от
Карелии до Грузии и от Белоруссии до
Забайкалья.
С ЧЕГО НАЧИНАЕТСЯ ПЕРЕХОД
НА НОВУЮ СИСТЕМУ
С нового плана. Вот как выглядит этот
документ (здесь и далее приводим только
самое основное).
«...В связи с переходом предприятия с 1 апреля
1966 г. на новую систему планирования и
экономического стимулирования Главное управление
промышленности химических волокон устанавливает вам
следующий план производства:
1 Показатели,
1 в тысячах рублей
[Сумма балансовой |
III лита за фонды . .
II
квартал
4249 !
580
Ш
квартал
5036
580
IV 1
квартал 1
5016
580
Есть в плане и строки «Объем
реализуемой продукции», «Рентабельность»,
«Фонд заработной платы», и строка
«Наиболее важные виды продукции в натураль-
2
ном выражении», в которой сказано, сколько
именно тонн штапельного волокна должен
выпустить комбинат в каждом квартале (и
какого сорта).
Квартальная и месячная отчетность
построены на тех же основных показателях.
Приведенные выше строки плана ясно
говорят о том, что в этих документах
главное. Но существует также и документ,
которым предприятие сообщает
(подчеркиваю — не отчитывается, а сообщает)
статистическому управлению и своему
министерству о цифрах, характеризующих валовую
продукцию. Пока экономическая реформа
проведена не везде, упразднение «вала»
в статистических сводках дезорганизовало
бы государственный учет.
КАКИЕ СРЕДСТВА И ОТКУДА ПОЛУЧАЕТ
ПРЕДПРИЯТИЕ В СВОИ РУКИ
Это, прежде всего, отчисления за счет
собственной прибыли. (Кроме того, в
поощрительные фонды на 1966 г. вошли,
естественно, средства из «директорского
фонда» и премиальные для ИТР и служащих,
запланированные раньше в фонде
зарплаты). Нормативы отчислений утверждены
приказом Министерства на основании
расчетов, сделанных работниками самого
комбината, и выглядят так:
1 Фонды
1 Фонд материального
1 поощрения (it про цен-
1 тах к фонду зарпла-
1 ты производственного
1 Фонд социально-куль-
1 турных мероприятий
1 и жилищного строи!
1 тельства (в процентах
1 к общему фонду зар-
1 Фонд развития произ-
1 водства (в процентах
1 к стоимости производ-
1 ственных основных
1 Нормативы 1
За каждый 1%
увеличения
прибыли*
0,91
0,38
0,014
За каждый 1
1% рента- 1
бельностн 1
0,22 1
0,094 1
0,0037 1
* По сравнению с отчетной за 1965 год. —
М. Ч.
Из этой очень короткой таблицы
однозначно следует, что именно нужно делать
предприятию. Чтобы увеличить свои
средства, нужно увеличивать прибыль.
К таблице есть такие примечания:
«1. За перевыполнение плана по показателю
роста прибыли дополнительные начисления в
каждый из фондов производятся в пониженном размере
с применением коэффициента 0,7 к указанным в
таблице размерам отчислений.
2. При невыполнении плана прибыли и плана
реализации продукции в установленной
номенклатуре отчисления от прибыли в эти фонды
производятся с понижением на 3% за каждый 1%
недовыполнения...»
Связь между этими словами и
заинтересованностью предприятия в том, чтобы как
можно больше был план, а не
перевыполнение плана, — очевидна.
Необходимое пояснение. Предприятиям,
переходящим в этом году на новую систему,
было дано право выбрать в качестве
одного из двух основных показателей или
увеличение реализации или рост
прибыли.
Руководители комбината химического
волокна выбрали второе — прибыль.
Почему? Привожу мнение главного экономиста
комбината Анатолия Антоновича Касель-
ского:
— Прибыль — более гибкий,
всеобъемлющий показатель. Особенно там, где
немалое значение имеют цены на сырье.
Можно продать волокна сегодня на десять
тысяч рублей, а завтра на десять с
половиной. Но если сырье для этого завтрашнего
волокна обойдется нам в полтора раза
дороже, то от такого увеличения
«доходов» на пятьсот рублей выгоды будет,
мягко говоря, мало. Скорее — наоборот.
Итак, главным источником
поощрительных фондов должна была стать прибыль.
Надо было решать главную, в конечном
счете, задачу материального
стимулирования: больше платить, чтобы больше и
эффективнее производить.
КАКАЯ РАЗНИЦА МЕЖДУ ЗАРПЛАТОЙ
РАБОЧИХ РАНЬШЕ И ТЕПЕРЬ
Действующая система заработной платы
рабочих — фонд зарплаты, тарифные ставки,
надбавки за работу в ночное время и в
праздничные дни, премии за качество
остаются в силе, их никто не отменял. И тем
не менее, во многих вещах понадобилось
разобраться заново.
з
Вот типичный пример — условия
премирования аппаратчиков содовой станции:
Показатели и условия
премирования
Выдерживание параметров но
концентрации рабочего
раствора на 100% с первого
предъявления
, Выдерживание параметров по
отстою рабочего раствора
щелочи на 100% с первого
предъявления
Правильное ведение
технологического журнала
Чистота рабочего места и
оборудования
Итого . . .
Премия {и
процентах тарифной
ставки)
5
2
5
20
Многочисленность этих условий способна
поставить в тупик даже счетовода, а
содержание некоторых из них не может не
вызвать улыбки. Руководители комбината и его
цехов, пользуясь предоставленными им
теперь правами, отменили многие
«условия», сократив их число почти вдвое. Для
аппаратчиков содовой станции из четырех
оставлены два — первое и второе, за
каждое по 10 процентов тарифной ставки. А,
скажем, для дежурных слесарей — вообще
одно и единственное условие: отсутствие
простоев, зависящих от слесаря.
Разумеется, никакое упрощение само по
себе не могло бы изменить существа дела.
Доказательством этому может служить
параграф из «Сборника руководящих
материалов по вопросам труда и заработной
платы в химической промышленности»:
«17. Выплата премии рабочим за выполнение
и перевыполнение плана, а также за качественные
показатели производится за счет фонда заработной
платы.
Премиальные системы должны быть
разработаны таким образом, чтобы их применение не
вызывало перерасхода фондов заработной платы и
увеличения себестоимости продукции.»
В чем дело? Ведь само собой очевидно,
что никакая разумная система поощрения
не может увеличить истинную
себестоимость продукции. Загвоздка, известная всем
производственникам, кроется в словах
«фонд заработной платы». Этот фонд никак
не зависит от результатов труда в каждом
данном месяце, автоматически сокращаясь,
как только в цеху становится хоть одним
рабочим меньше, ровно на столько, сколько
получал этот рабочий. Участок, цех, завод
теряют всякий интерес к тому, чтобы двое
управлялись за троих, потому что
разложить на них существенную часть
заработка этого третьего все равно нельзя...
Порочный замкнутый круг: большая
производительность не влечет за собой
большего вознаграждения. Точнее —
вознаграждение может расти только в пределах
небольшого увеличения производительности,
дальнейшее же ничего самому работнику
уже не давало. Дальнейшего увеличения
производительности в последние годы и не
происходило...
Хозяйственная реформа разрывает
порочный круг. Разрывает тем, что фонд
зарплаты (а он пока ограничен по-прежнему —
ведь в государственной казне есть только
то, что уже создано трудом) перестает
быть единственным источником
вознаграждения; причем размеры второго
источника— фонда материального поощрения,
который создается за счет своей прибыли,
своей экономии, не ограничиваются
в принципе. Например:
ПОЛОЖЕНИЕ
О ПРЕМИРОВАНИИ РАБОЧИХ ХИМИЧЕСКОГО
ЦЕХА ИЗ ФОНДА МАТЕРИАЛЬНОГО ПООЩРЕНИЯ
ЗА СНИЖЕНИЕ УДЕЛЬНЫХ НОРМ РАСХОДА
СЫРЬЯ
Вводится с 1 апреля 1966 г.
Показатели
премирования
Снижение
удельных
норм расхода
каустика на
0,1\
Размер премии
(в процентах
к сдельном>
заработку пли
тарифной ставке)
1,5
Профессии
Старшие
сливщики
каустика,
сливщики каустика,
аппаратчики
содовой
станции, слесари
по ремонту
оборудования
содовой
станции
Снижение
удельной
нормы
расхода
целлюлозы на 0,1%
Загрузчики ап-
паратов«ВА»,
старшие
аппаратчики
«ВА'>,
аппаратчики
«ВА»,
дежурные слесари
Размер премии за улучшение предусмотренных
по каждой профессии показателей не
ограничивается . . .
4
Как это «Положение» (и подобные ему —
в других цехах) претворяется в жизнь, как
оно «работает»?
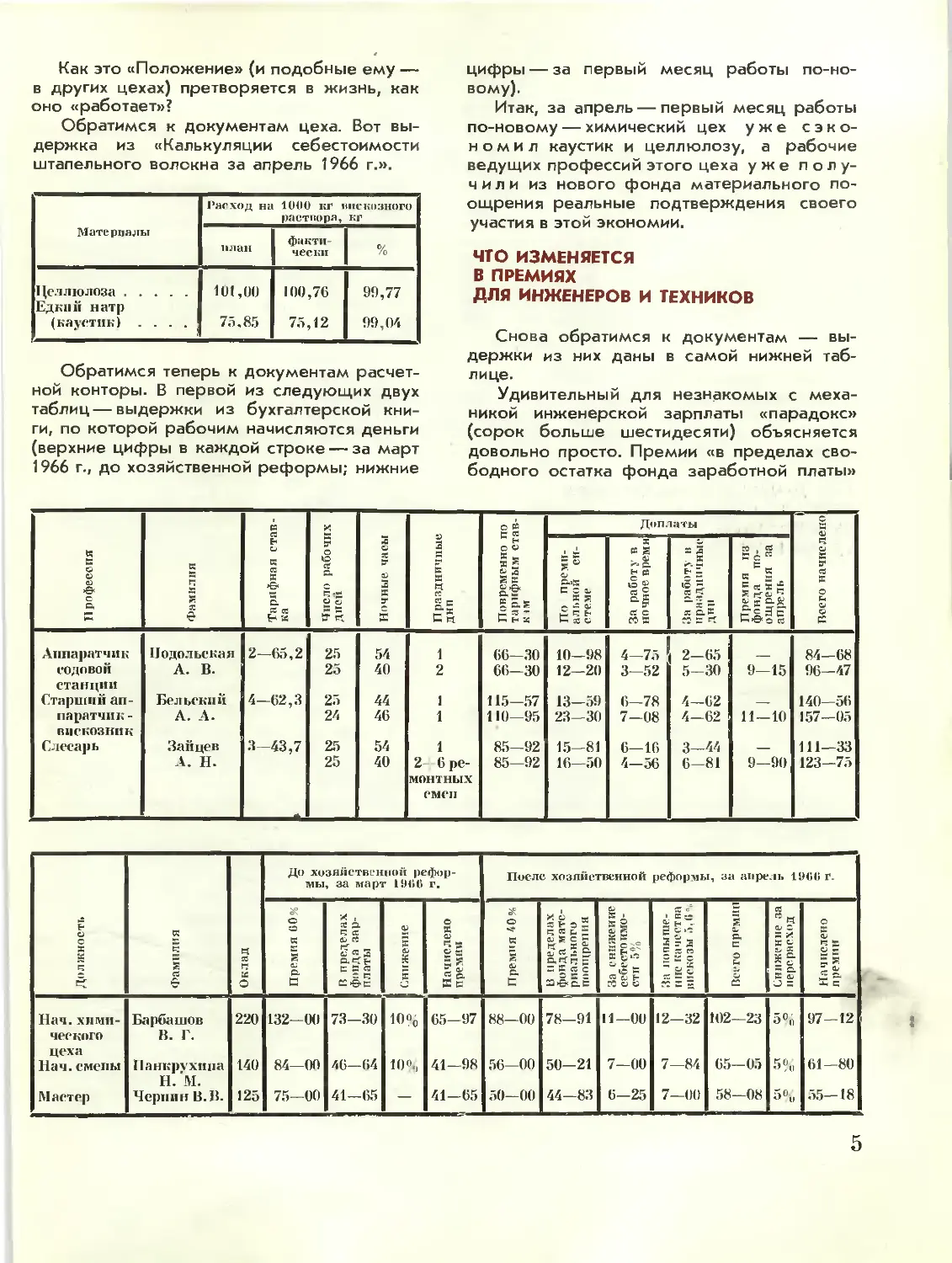
Обратимся к документам цеха. Вот
выдержка из «Калькуляции себестоимости
штапельного волокна за апрель 1966 г.».
1 Мате риалы
[Едкий натр
1 (каустик) . . . . |
Расход на 1000 кг вискозного 1
раствора, кг |
план
101,00
75,85
фактически
100,76
75,12
%
99,77
99,04
Обратимся теперь к документам
расчетной конторы. В первой из следующих двух
таблиц—выдержки из бухгалтерской
книги, по которой рабочим начисляются деньги
(верхние цифры в каждой строке — за март
1966 г., до хозяйственной реформы; нижние
цифры — за первый месяц работы
по-новому).
Итак, за апрель — первый месяц работы
по-новому — химический цех уже
сэкономил каустик и целлюлозу, а рабочие
ведущих профессий этого цеха уже
получили из нового фонда материального
поощрения реальные подтверждения своего
участия в этой экономии.
ЧТО ИЗМЕНЯЕТСЯ
В ПРЕМИЯХ
ДЛЯ ИНЖЕНЕРОВ И ТЕХНИКОВ
Снова обратимся к документам —
выдержки из них даны в самой нижней
таблице.
Удивительный для незнакомых с
механикой инженерской зарплаты «парадокс»
(сорок больше шестидесяти) объясняется
довольно просто. Премии «в пределах
свободного остатка фонда заработной платы»
| Профессия
1 Аппаратчик
1 содовой
1 станции
1 Старший ап-
1 паратчик-
1 вискозник
1 Слесарь
Фамилия
Подольская
А. В.
Вельский
А. А.
| Зайцев
А. Н.
8 |
ка
2—65,2
4—62,3
3-43,7
* *
и
Число рабоч!
дней
25
25
25
24
25
25
Ночные часы
54
40
44
46
54
40
Праздничньи
Дни
1
2
1
1
1
2 6
ремонтных
смен
ов 1
Повременно i
тарифным ст
к ш
66—30
66—30
115—57
110—95
85—92
85—92
По
премиальной
системе
10—98
12—20
13—59
23—30
15-81
16—50
Доплаты
За работу в
ночное время
4—75 1
3-52
6-78
7-08
6—16
4-56
Зн работу в
дни
| 2—65 i
5-30
4-62
4—62
1 3~44
6-81
Премия из
фонда
поощрения за
апрель
9—15
—
11 — 10
—
9—90
ei ol
84—68
96—47
140—56
157—05
111—33
123—75
Должность 1
1 Нач. хими-
1 ческого
1 цеха
|Нач. смены
1 Мастер
Фамилия 1
Барбашов
В. Г.
Панкрухипа
н. 'м.
Чериин В. В.
220
140
125
До хозяйственной
реформы, за март 19til> г.
о
о
я
&
132-00
84—00
75-00
В пределах
! платы
73—30
46—64
41—65
-
-
Ю°с
10%
—
Начислено
премии
65—97
41—98
41—65
После хозяйственной реформы, за апрель 19GC г. 1
88—00
56—00
50—00
В пределах
фонда
материального
поощрения
78—91
50-21
44-83
За снижение
стн 5%
11—00
7—00
6—25
В Чг^ \
£?3
к хм
~ Tj 5
~ я -
1 '■*' "^
12-32
7—84
7—00
Всего премии
102—23
65—05
58—08
1 Снижение за
перерасход
5°°
5%
5%
Начислено
премии
97—12!
61— 801
55—181
не могли не уменьшаться сразу же:
источниками этого «свободного остатка»
могли служить только вакантные должности
(незанятые, но существующие по штатному
расписанию рабочие места), заболевания
(во время болезни трудящийся получает не
зарплату, а деньги из профсоюзных
средств), да отпуска за свой счет...
И еще одно немаловажное
обстоятельство, прямо касающееся всех
работников предприятия — и
инженерно-технических, и рабочих, и служащих. Это
вознаграждение в конце года — по итогам работы за
весь год, от 25 до 55% среднемесячного
заработка (в зависимости от трудового
вклада и от стажа работы).
Та истина, что такая доплата за весь
год усиливает сочетание «я и мое
предприятие», в доказательствах не нуждается.
И что это будет способствовать
закреплению постоянных кадров — тоже.
КАК ДОЛЖНЫ ПОЛЬЗОВАТЬСЯ
СВОИМИ ПРАВАМИ
РУКОВОДИТЕЛИ
ЦЕХОВ И УЧАСТКОВ
Им приходится становиться
исследователями, находить экономические
зависимости между своими распоряжениями,
действиями своих подчиненных и
результатами работы.
Экономическая реформа меняет в
условиях оплаты труда главное: ограничения
накладываются не бумажным запретом, а
результатами труда. Это вовсе не просто —
при научно обоснованных нормах, на
химическом оборудовании, работающем в
фиксированных технологических режимах,
находить те условия, которые надо заложить
в систему поощрений.
Работники комбината не считают
принимаемые ими решения (не подлежащие
теперь никаким утверждениям свыше)
окончательными или бесповоротными.
Некоторое представление об этом может дать
разговор между экономистом одного из
вспомогательных цехов (условия премирования
по новой системе еще не были
распространены на этот цех) и исполняющей
обязанности начальника отдела труда и
заработной платы Валентиной Андреевной Теренть-
евской.
Н. (экономист цеха): А нам какой взять
показатель премирования?
Терентьевская: Подумайте,
посоветуйтесь в цеху и сами решайте — что
выгоднее цеху и рабочим, то и выбирайте.
Н.: А если мы не знаем или неверно
выберем?
Т.: Попробуйте месяц, другой. Не
подойдет— будете искать новый. Это в ваших
интересах.
...Им приходится по-новому относиться
к находящимся в их распоряжении
материальным ценностям, потому что плата
за фонды (см. главу «С чего начинается
переход на новую систему») тоже имеет
прямое отношение к денежным делам
цеха.
КТО И ПОЧЕМУ СТАНОВИТСЯ
«ЦЕНТРАЛЬНОЙ ФИГУРОЙ»,
ЧТО И ПОЧЕМУ —
«ГЛАВНЫМ ДОКУМЕНТОМ»
Как и везде, на Рязанском комбинате
такими фигурами всегда были начальники
цехов. Их первыми слушали на
«оперативках» и на всех прочих совещаниях и
заседаниях, «с них» первых, как говорится, и
спрашивали.
Многое изменилось само собой
немедленно после введения новой системы. Не то
чтобы начальники цехов потеряли
значение, но первое слово в кабинете директора
держит теперь начальник отдела сбыта
Федор Егорович Шарапов. Потому что первый
вопрос, интересующий теперь
руководителей производства, заключается не в том,
сколько выработал продукции тот или иной
цех, выполнил ли он план, — это
подразумевается очевидным. Первый вопрос в
другом: сколько продукции отправлено
потребителям.
Ответ на него—необходимый шаг к
выяснению следующего, самого главного
вопроса: на какую сумму получены
банковские документы об оплате. Об этом
докладывает начальник финансового отдела
Лариса Ивановна Понукалина, которая перед
тем должна еще сообщить, — на какую
сумму и в какие сроки переданы в банк
документы на оплату продукции комбината.
Это выдвижение вперед финансистов
и сбытовиков никем не декретировалось.
Чтобы уяснить себе существо и
необходимость этого естественным образом
происшедшего изменения, попытаемся вникнуть
в его причины.
6
Основа любого хозяйства — учет. Но что
считали раньше? Раньше считали «план» —
кипы штапельного волокна на собственном
складе. Зададимся вопросом — совершенно
отвлеченным и не имеющим никакого
отношения к комбинату и его работникам. Если
у вас к концу последней смены последнего
дня месяца не хватает на складе нескольких
единиц готовой продукции, будь то те же
кипы волокна или кубометры дров —
безразлично, то станете ли вы записывать в
отчет невыполнение месячного плана?
Пойдете на все вытекающие из этой записи
последствия? Ведь через каких-нибудь
несколько часов недостающие кипы
(кубометры, тонны и т. д.) непременно
появятся— производство-то работает.
Когда и куда ваша продукция попадет —
это было, естественно, делом десятым.
Сведения о том, как реализованы
произведенные материальные ценности, относились
к категории «держать дела в порядке», а эта
категория, как известно, в большом почете
у людей педантичных, но — в отличие от
сведений о выполнении плана! — не служит
основанием ни для бухгалтерии, ни для
Госплана.
Что считают теперь? «Отгрузку» волокна
потребителям и «реализацию» —
поступление документов об оплате потребителями
счетов. «Отгрузка» 100 тонн — это не
100 тонн волокна, погруженных в вагоны на
складе готовой продукции комбината. Это —
сданные в банк квитанции железной дороги
на 100 тонн волокна.
По правилам полагается сдать
платежные документы в банк не позже, чем через
72 часа после их оформления на железной
дороге. Раньше еле-еле укладывались в этот
срок. Кого особенно интересовало, сдали
или не сдали в банк какие-то там квитанции?
Днем позже, днем раньше. Какая разница?
Теперь комбинат учитывает, сколько
часов уходит на сдачу квитанций. За май
получилось: в среднем 15 часов. Решили, что
это много, что надо довести до 12 часов.
Ведут переговоры с железной дорогой —
чтобы товарный кассир работал прямо на
подъездных путях комбината (станция — за
полтора километра). Чтобы он прямо здесь,
у рампы склада, выписывал квитанцию.
Банк принимает платежные документы
вообще-то до часу дня. Теперь комбинату
пришлось специально просить, чтобы
«отгрузку» принимали и позже — до четырех
дня. Ведь комбинат работает, вагоны
грузятся,— и финотдел спешит предъявить по-
лучителям счета на оплату как можно
скорее.
Раньше, как и на других заводах,
«глазным документом» текущего учета был
диспетчерский план-график, отвечающий по
существу на единственный вопрос:
сколько произведено.
Теперь же самый главный документ
находится не у диспетчера, не у главного
технолога и не в производственно-техническом
отделе. Этот совершенно новый документ
называется «Сведения о выполнении плана
реализации, прибыли, отгрузки (по
документам, сданным в банк)». Он лежит на столе
у Понукалиной в специально заведенной
для него ярко-красной папке — чтобы
всегда был на виду, потому что именно этот
документ чаще всего нужен теперь
директору комбината Василию Ивановичу
Воробьеву.
«Сведения» — это таблица, которая
пополняется каждый день и ведется
нарастающим итогом, чтобы в любой момент можно
было сразу увидеть всю динамику
денежных дел комбината.
Вот выдержка из «самого главного
документа» (за третью декаду апреля):
1 Дни
1 На 22.IV
1 На 23.IV
1 На 24.IV
1 На 25.IV
1 На 26.IV
Прибыль, 1
тысяч рублей 1
план
1111,8
1184,0
1256,1
1328,3
1400,5 |
факт 1
1233 Л 1
1290,2 1
1363,4 1
1363,4 1
1526,9 1
НЕКОТОРЫЕ ЦИФРЫ, ПО КОТОРЫМ
МОЖНО СУДИТЬ О РАБОТЕ
ВСЕГО КОМБИНАТА
ДО И ПОСЛЕ РЕФОРМЫ
За первый квартал (три месяца до
хозяйственной реформ ы):
Прибыль от реализации товарной продукции
план 4 669 тысяч рублей
фактически 4 926 тысяч рублей
7
За второй квартал (три месяца после
форм ы):
ре-
Прибыль от реализации товарной продукции
план 13 037 тысяч рублей
фактически 13 267 тысяч рублей
Результат — увеличение прибыли почти
втрое — говорит сам за себя.
И еще одно сопоставление цифр — на
этот раз последнее. В марте (до реформы)
план выпуска штапельного волокна был
выполнен на 107,2 процента. В апреле (после
реформы) — только на 101,6 процента. Но
волокна в этих меньших процентах было на
несколько десятков тонн больше!
Проценты уменьшились, но продукции стало
больше! Больше, потому что начала
действовать заинтересованность в увеличенном
плане.
(Окончание в следующем номере)
ТЕХНОЛОГИ — ВНИМАНИЕ!
КЛЕЙ ХРАНИТСЯ ДОЛЬШЕ
МЕТАЛЛ КЛЕИТ МЕТАЛЛ
МАШИНА В ТРУБЕ
Какой резиновый клей известен
больше других! Конечно,
восемьдесят восьмой. Пожалуй, индекс
«88» знаком не только
специалистам по резине.
Клей 88 готовят из хлоропре-
нового каучука — найрита. Новый
хлоропреновый каучук найрит
НП тоже имеет высокую
клейкость.
Клей на его основе получил
название 88 НП. В нормальных
условиях этот каучук кристалпичен,
поэтому перед приготовлением
клея его греют. В остальном
технология остается прежней.
В отличие от клея 88 новый
клей стабилен — он не меняет
вязкости при хранении. У него
несколько выше теплостойкость и
морозостойкость. Этот клей (как,
впрочем, и все другие клеи] не
универсален. Если в резине есть
пластификатор, то прочность
склеивания снижается.
Это, пожалуй, единственное
ограничение для применения клея
88 НП.
(«Каучук и резина», 1966, № 4)
Металлические клеи еще мало
известны. Но, по-видимому, у них
большое будущее. Ими можно
соединять детали без нагрева ипи
с небольшим нагревом (до 100° С).
Образовавшееся клеевое
соединение выдерживает температуру
до 700—800С и прекрасно
проводит электрический ток.
В Институте машиноведения
разработан ряд металлических
клеев. По внешнему виду это
пасты. Они состоят из смеси
жидкого металла (ртути, галлия] с
металлическим порошком. Клей
наносят на детали и сжимают их.
Происходит взаимная диффузия
металлов и образуются сплавы
с достаточно высокой
температурой плавления. Как видите,
сходство с обычным клеем лишь
внешнее.
Металлическими клеями можно
клеить детали под водой. Они
дают герметический шов. Эти клеи
можно использовать для
соединения металла с керамикой и
полимерами.
(«Приборостроение». 1966. № ft)
Покрыть футеровкой
внутреннюю сторону трубы дело
сложное, но во многих случаях без
этого нельзя обойтись. Сейчас
футеровку труб чаще всего
производят, много раз нанося тонкие
слои, которые затвердевают
только после тепловой обработки.
В Англии сконструирована
машина, которая производит футеровку
труб за один проход. Она
работает в трубах диаметром от 7 до
70 см. Небольшие изменения
позволяют использовать ее в трубах
диаметром до 1,2 м.
Процесс начинается с того, что
резервуар с жидким
покрывающим материалом проходит через
трубу, оставляя полосу
материала. Затем резервуар заменяется
промазывающей головкой,
которая равномерно распределяет
материал по стенкам трубы, а
щетки заглаживают нанесенный слой.
Вращаясь вокруг оси трубы,
головка завершает обработку при
обратном ходе.
(«Technik unci Forschimg», 1966,
AS '.)-
ТЕХНОЛОГИ — ВНИМАНИЕ!
8
АЗОТ
Д. И. МЕНДЕЛЕЕВ
«Хотя деятельнейшую, т. е. наиболее легко и часто химически действую"
щую часть окружающего нас воздуха составляет кислород, но
наибольшую массу его, судя как по объему, так и по весу, образует азот, а
именно газообразный азот составляет более 3/4, хотя и менее 4/б объема
воздуха. А так как азот лишь немногим легче кислорода, то весовое
содержание азота в воздухе составляет около 3/4 всей его массы. Входя
в таком значительном количестве в состав воздуха, азот, по-видимому,
не играет особо видной роли в атмосфере, химическое действие которой
определяется преимущественно содержанием в ней кислорода. Но
правильное представление об азоте получается только тогда, когда узнаем,
что в чистом кислороде животные не могут долго жить, даже умирают,
и что азот воздуха, хотя лишь медленно и мало-помалу, образует
разнообразные соединения, часть которых играет важнейшую роль в природе,
особенно в жизни организмов. Растения, а особенно животные, нуждаясь
в свободном, газообразном кислороде, немыслимы без питания
азотистыми соединениями, потому что в их теле азотистые соединения
составляют самую деятельную, в химическом смысле, составную часть. Однако
ни растения (говоря вообще), ни животные прямо не поглощают
газообразного азота воздуха, а берут его из готовых азотистых соединений,
притом растения питаются азотистыми веществами почвы и воды, а
животные азотистыми веществами, содержащимися в растениях или в
других животных. Атмосферное электричество способно содействовать
переходу газообразного азота в азотистые соединения, как увидим далее,
а происшедшие вещества с дождями вносятся в почву, служа для
питания растений. Обильная жатва, хороший укос и сильный прирост дерев,
при прочих равных условиях, наблюдаются только тогда, когда в почве
уже есть готовые азотистые соединения, состоящие или из тех, которые
находятся в воздухе и в воде, или из остатков разрушения других
растений или животных (напр., в навозе]. Азотистые вещества, заключающиеся
в животных, ведут свое начало от тех веществ, которые образовались в
растениях. Таким образом, началом для всех азотистых веществ,
находящихся в животных и растениях, служит азот воздуха, но не прямо, а пере"
шедши предварительно в соединение с другими элементами воздуха.
Азотные же соединения, входящие в состав растений и животных, имеют
в них первостепенное значение: ни одной растительной или животной
клетки, т. е. элементарной формы организма, не существует без
содержания в ней азотистого вещества; жизнь организма прежде всего
проявляется в этих азотистых веществах. В зародыше, в семенах и в тех
частях, которыми клетки размножаются, изобилуют азотистые вещества:
совокупность явлений, которые свойственны организмам, очень явно и
тесно связана с химическими свойствами легко изменяющихся сложных
(белковых) азотистых веществ, которые входят в их состав».
«Основы химии», глава пятая,
изд. VIII, 1906 г.
9
СИНТЕЗ АММИАКА
Инженер П. А. ГИНЗБУРГ,
Государственный институт
азотной промышленности
(ГИАП)
природный воздух
саз "^ —
водяной'
лар
ш
VL
[г
и
X.
ЗНо
NB^2NIIa.
конвертированный
ваз
Основной продукт азотной промышленности —■
аммиак. Его используют для производства азотной
кислоты, аммиачной селитры, мочевины, аммиачной
воды и многих других продуктов. Получают аммиак
из смеси водорода и азота в присутствии
катализатора при температуре около 500°С и
давлении 300—800 атм:
Катализатором служит железо с активирующими
добавками. Азот получают из воздуха. Источником
водорода служат природные или другие газы, а
также жидкие топлива.
Предварительно подогретая до 400°С смесь
природного газа и водяного пара поступает под
давлением около 30 атм в трубчатую печь A), где
проходит по трубам, заполненным никелевым
катализатором. Здесь метан взаимодействует с водяным паром.
Образуется смесь Н2, СО, С02, СН4 и остатка
избыточного водяного пара; ее называют
«конвертированным газом».
Реакция взаимодействия метана с водяным
паром идет при 750—800°С с поглощением тепла.
Поэтому трубы обогревают снаружи газовыми
форсунками. Конвертированный газ, содержащий около
8% метана направляется в шахтный конвертор B).
Здесь, в присутствии никелевого катализатора при
температуре около 1000°С газовая смесь реагирует
с воздухом; содержание метана снижается до 0,5%.
Газовая смесь, которая кроме Н2 и N2 содержит
довольно много СО и С02, поступает в
конвертор C). Здесь окись углерода в присутствии
различных катализаторов реагирует с водяным паром:
со + н2о^п2 : со2.
Затем газовую смесь очищают от С02 в абсорбере
D) с помощью поглотительного раствора.
<?
Т\
1_Г
<5
8
^J
NH3
газ
[FI
10
Гк
NH ;
H4U£ В
1 — трубчатая печь
2 — шахтный конвертор СН4
3 — конвертор СО
4 — абсорбер С02
5 — регенератор
6 — метанатор
7 — газовый компрессор
8 — колонна синтеза аммиака
9 — конденсатор аммиака
10 — сепаратор
11 — циркуляционный компрессор
Отработанный поглотительный раствор,
содержащий С02, направляется в регенератор E), где
выделяется углекислота, используемая для синтеза
мочевины, получения сухого льда и других целей.
Промытый газ необходимо еще окончательно
очистить от остатков СО и С02. Дело в том, что
железный катализатор в условиях реакции синтеза
аммиака легко реагирует с соединениями,
содержащими кислород, и «отравляется» — теряет свою
активность. Очистка происходит в метанаторе F), где
СО и С02 в присутствии катализатора
восстанавливаются до метана, который потом возвращается
в конвертор B):
со + зн2 7t сн4 -; н2о
С02 + 4Н2 -> СН4 -f 2Н20.
Газовый компрессор G) сжимает азото-водород-
ную смесь до давления 300—800 атм. Сжатая смесь
поступает в агрегат синтеза. В колонне (8) 20—30%
смеси превращается в аммиак. В конденсаторе (9)
образовавшийся аммиак конденсируется, а в
сепараторе A0) отделяется от непрореагировавшего
газа, который компрессором A1) снова подается в
колонну синтеза (8). Из сепаратора A0) жидкий
аммиак по трубопроводам подается на склад.
10
КАК СВЯЗАТЬ АЗОТ
И. ЛУНАЧАРСКАЯ,
научный обозреватель АПН
ПРОШЛОЕ И НАСТОЯЩЕЕ
В атмосфере Земли почти 80 % азота, в
земной коре — всего 0,04%. Проблема —
как связать азот — старая, она — ровесник
агрохимии.
В прошлом веке довольно богатый
источник связанного азота был обнаружен
в природе. Это — чилийская селитра,
натриевая соль азотной кислоты. Ее
месторождение в Южной Америке уникально,
практически оно единственное в мире. И не
удивительно, что в 1879 году за обладание
богатой селитрой пограничной провинцией
Тарапака вспыхнула война между Перу,
Боливией и Чили. Победителем оказалось
Чили. Однако удовлетворить мировую
потребность в азотных удобрениях чилийское
месторождение, конечно, не могло.
Конец XIX века ознаменовался
изобретением, потребовавшим громадных
количеств связанного азота: для производства
бездымного пороха нужна азотная кислота.
Опять-таки связанный азот.
Возможность связывания азота воздуха
с кислородом в электрическом разряде
первым увидел англичанин Генри Кавендиш.
Это было еще в XVIII веке. Но осуществить
процесс управляемого синтеза окислов
азота удалось лишь в 1904 году.
Норвежцы Христиан Биркеланд и
Самюэль Эйде пропускали струю воздуха
через мощную электрическую дугу, и при
температуре 3000 С азот соединялся с
кислородом воздуха, образуя окись азота NO.
Однако огромный расход электроэнергии
делал этот процесс чрезвычайно
дорогостоящим.
Поэтому, когда в 1914 году немцы Фриц
Габер и Карл Бош предложили аммиачный
метод связывания азота, который был
сложнее, но дешевле, он быстро вытеснил метод
Биркеланда — Эйде.
Сейчас, пользуясь принципами,
разработанными 50 лет назад, сотни заводов всех
континентов вырабатывают из воздуха
более 20 миллионов тонн связанного азота в
год. Три четверти его идет на производство
азотных удобрений.
Ежегодно из почвы с урожаем уносится
около 100 миллионов тонн связанного
азота, а восполняется — меньше 12 миллионов
тонн. Дефицит азота на посевных площадях
земного шара составляет около 88
миллионов тонн в год.
Азотная промышленность, развиваясь,
использует высокие температуры и
давления, сложные, многостадийные процессы,
дорогостоящие катализаторы. Все это
требует огромных капиталовложений,
дефицитных материалов, дорогостоящего
оборудования.
Поэтому поиски новых, более
эффективных и экономичных методов фиксации
атмосферного азота продолжаются.
«ХОЛОДНАЯ» ПЛАЗМА
Плазма — четвертое качественное
состояние вещества, в которое оно переходит
при температуре в тысячи и миллионы
градусов. В последние годы химики и
инженеры начали получать и изучать
низкотемпературную, «холодную» плазму. «Холодной»
ее называют потому, что температура ее не
превышает нескольких десятков тысяч
градусов.
В плазме, даже «холодной», химические
реакции идут с громадной скоростью.
Сущность плазмохимического процесса
заключается в том, что в плазменной струе
происходит распад молекул исходного
вещества, в частности воздуха, на осколки —
ионы, атомы, радикалы, — обладающие
очень высокой реакционной способностью.
Взаимодействуя между собой, они
образуют соединения, в том числе и такие,
которые при обычных температурах получить
невозможно. В плазменную струю,
состоящую из осколков молекул одного вещества,
можно ввести осколки другого, перемешать
11
их и тем самым намного увеличить
«ассортимент» активных частиц и их возможные
комбинации. Отсюда — неисчерпаемые
возможности плазмохимии для синтеза.
Применением низкотемпературной
плазмы для химических реакций в нашей стране
занимаются многие научные учреждения, в
том числе лаборатория института
нефтехимического синтеза АН СССР, которой
руководит доктор физико-математических наук,
профессор Л. С. Полак.
Сотрудник этой лаборатории В. С. Щипа-
чев исследовал возможности плазмохимии
для получения окиси азота из воздуха.
Оказалось, что возможности эти велики.
Уже при температуре в 5000 С в
воздухе происходит распад газовых молекул на
более активные одиночные атомы.
Атомарный азот несравненно активнее химически,
чем молекулярный (N2). Атомарный
кислород — тоже.
Процесс идет по чрезвычайно простой, в
принципе схеме. В цилиндр-реактор
плазмотрона поступает струя воздуха, нагретого
до температуры 5000 С. (Здесь «воздух» —
термин условный, — так как это уже не
смесь газов, а смесь беспорядочно
движущихся ионов, атомов, радикалов, на
которые распались газы, составляющие воздух).
В этой смеси и происходят столкновения
атомов азота и кислорода, их соединение
в окись азота.
Особенность плазмохимического
процесса — бурная динамика: все реакции —
распад, столкновения и соединения
происходят вдоль плазменной струи в
определенные промежутки времени. Промежутки эти
очень невелики, весь процесс происходит за
одну десятитысячную секунды. По выходе
из плазмотрона смесь охлаждается.
Здесь-то и встретилась основная
трудность. Оказалось, что окись азота,
образовавшаяся в плазме, при медленном
охлаждении вновь разлагается на азот и кислород.
Удержать ее от этой обратной реакции
можно только при очень быстром
охлаждении. Этот процесс, по аналогии с
металлургическим, назвали «закалкой». Удалось
рассчитать, что для этого надо охлаждать
струю на 1000 С за одну
десятитысячную секунды (!) и делать это надо в
строго определенном месте плазменной
струи, там, где количество образовавшейся
окиси азота будет наибольшим. Нужно ли
разъяснять, насколько трудна технически
эта задача. Но в значительной мере она
решена. Удалось достичь выхода
«плазменной» окиси азота, приближающегося к
выходу в общепринятом аммиачном процессе.
Кроме простоты и быстроты, для
плазменного метода связывания азота
характерно и то, что для изготовления плазмотрона
не требуется никаких специальных
дорогостоящих материалов. Реакция идет с такой
быстротой, что время взаимодействия
плазмы со стенками плазмотрона очень
невелико. И кроме того, плазма «отжимается» от
стенок струей холодного газа.
Казалось бы, теперь проблема
получения связанного азота решена. Но в
действительности из-за огромного расхода
электроэнергии на создание плазмы новый метод
пока не имеет экономических преимуществ
по сравнению с аммиачным. Повышая
температуру плазмы и ведя процесс под
давлением, можно увеличить выход окиси
азота. Однако это потребует еще большего
расхода энергии.
Но вряд ли кто-нибудь решится назвать
плазмохимический метод
бесперспективным. Тенденция мирового экономического
развития такова, что химические источники
сырья становятся все дороже, а энергия —
дешевле. Поэтому явление,
представляющее сейчас, в основном, теоретический
интерес, завтра может стать важным
практически.
Это подтверждается работами, которые
ведутся в секторе связанного азота
Государственного института азотной
промышленности.
ВАРИАЦИИ ГИАП
В Институте азотной промышленности
по проблеме фиксации атмосферного
азота работы ведутся в нескольких
направлениях. Одно из них — получение окислов
азота в низкотемпературной плазме.
Однако ГИАП как отраслевой институт, теснее
связанный с промышленностью, уделяет
больше внимания вопросам
рентабельности процесса. Поэтому здесь
разрабатываются технологические схемы с
использованием тепла плазмы для попутного
получения пара, найдена также возможность
утилизовать воду, охлаждающую плазмотрон.
Полученный пар можно использовать
для вращения турбины, то есть для
получения электроэнергии, питающей тот же плаз-
12
мотрон. Это частичное «самообслуживание»
сделает процесс использования
низкотемпературной плазмы для фиксации азота
значительно дешевле. Для дальнейшего
уменьшения расхода электроэнергии можно
использовать магнитогидродинамический
(МГД) генератор, поставленный в месте
«закалки», а также ввести в плазмотрон
некоторое количество горючего газа.
Таким образом можно вернуть до
60 процентов электроэнергии, затраченной
на получение ллазмы. А это уже серьезная
цифра!
АЗОТ ПОД ПУЧКОМ ЭЛЕКТРОНОВ
В Сибирском отделении Академии наук
СССР совместно с ГИАП начаты поисковые
работы по связыванию азота в ускорителях
электронов высоких энергий.
Пучок электронов с кинетической
энергией в 1—2 миллиона электрон-вольт,
направленный на азотокислородную смесь,
превращает ее в холодную плазму. Но эта
холодная ллазма отличается от той, которая
создается в плазмотронах. Там ее называют
так лишь условно, потому что температура
ее составляет несколько тысяч, а то и
десятков тысяч градусов. Плазма,
образующаяся в ускорителях электронов высоких
энергий, — холодная в полном смысле
этого слова. Она может образоваться без
нагрева, при нормальной температуре.
Энергия при этом будет расходоваться на
расщепление молекул на атомы и их
ионизацию.
Процесс образования окислов азота в
такой плазме идет не с поглощением, а с
выделением тепла. Однако выход окиси
азота в этом процессе пока очень невелик.
Оптимальные условия образования
окиси азота в ускорителях пока не найдены.
ХИМИЧЕСКАЯ ФИКСАЦИЯ АЗОТ/
Исследования возможности получения
соединений азота с помощью холодной
плазмы не исключают поисков новых
методов химического связывания азота. Один
из них разработан в Институте элементо-
органических соединений АН СССР.
Сотрудники лаборатории, которую возглавляет
доктор химических наук, лауреат Ленинской
премии М. Е. Вольпин, заинтересовались
биологическими процессами,
позволяющими некоторым микроорганизмам связывать
молекулярный азот в обычных, мягких
условиях—без повышения температуры и
давления.
До последнего времени биохимики
почти не знали природы этого превращения.
Лишь недавно удалось выяснить, что
биологическая фиксация азота — с точки зрения
химической — процесс восстановительный,
то есть идущий с присоединением
электронов. Бактерии связывают азот с водородом
и превращают его в аммиак. Но для того,
чтобы эта реакция произошла, и азот, и
водород должны быть предварительно
активированы. Химическая природа активного
центра и механизм активизации азота
микроорганизмами пока не ясны. Однако стало
известно, что существенную роль в этом
процессе играют соединения переходных
металлов, в частности железа, хрома,
молибдена. Известно, что, если в почве нет
молибдена, процесс фиксации азота
микроорганизмами полностью прекращается.
Исследователи предположили, что азот
активируется, образуя комплексные
соединения с ионами переходных металлов,
входящих в состав ферментов — белков,
ускоряющих химические взаимодействия в
клетках. Весьма вероятно, что процесс
связывания азота в биологических системах
происходит так: молекула азота, образуя
комплекс с металлом фермента,
активируется; другой фермент «подает» активный
водород; начинается взаимодействие, в
результате которого получается аммиак.
Теоретические представления о
механизме активации азота в живой природе
получили экспериментальное подтверждение.
Удалось осуществить фиксацию азота чисто
химическим путем при комнатной
температуре и нормальном давлении. Струю
газообразного азота пропускали через
каталитические системы, содержащие соединения
переходных металлов. В результате были
получены соединения азота, которые
можно превратить в аммиак. Но пока
химическое связывание азота проходит лишь
однократно: один атом металла связывает
не более одной молекулы азота. А ведь в
природе этот процесс идет непрерывно, там
активный центр действует как катализатор,
не погибающий в результате реакции.
Сейчас идет совместная работа ученых
ИНЭОС и отдела химической кинетики
Института химической физики АН СССР по
13
подбору и испытанию других
каталитических систем.
Ведется исследование структур
комплексных соединений, содержащих
различные переходные металлы. Эти работы
помогут найти новые соединения такого рода,
которые могут оказаться более
эффективными катализаторами процесса фиксации
молекулярного азота.
Найдено несколько способов связывания
молекулярного азота в комплексы. В
частности, карбен — частица двухвалентного уг-
леродаг легко реагирует непосредственно
с азотом, образуя диазосоединения.
Говорить о создании промышленного
процесса связывания азота методом,
предложенным М. Е. Вольпиным и его
сотрудниками, можно будет только после того, как
удастся получить соединения,
активирующие молекулы азота и при этом не
разрушающиеся.
Трудно предсказать, кто «одержит
победу» в этом интереснейшем соревновании:
те, кто идет по пути «насилия» над
природой — искусственного дробления и
последующего соединения молекул, или те, кто
воспроизводит естественный природный
процесс.
Возможно, что оба эти процесса,
построенные на столь различных принципах,
войдут в промышленность и помогут
насытить землю азотом.
ЧТО ВЫ ЗНАЕТЕ
И ЧЕГО НЕ ЗНАЕТЕ
ОБ АЗОТЕ
и ЕГО СОЕДИНЕНИЯХ
ОТКРЫТИЕ АЗОТА
Возможно, что азот, как и
кислород, был открыт Карлом Шеепе в
начале семидесятых годов XVIII в.,
но первым, кто более или менее
основательно изучил азот, был
англичанин Даниэль Резерфорд.
Его учитель Блэк установил, что
часть воздуха, остающегося в
закрытом сосуде после того, как в
нем гибло от удушья подопытное
животное, поглощается
растворами щелочей. (Это была
общеизвестная теперь реакция
взаимодействия щелочей с углекислым
газом). Ученик исследовал непо-
гпощенную часть и дал ей
такую характеристику:
«Остающаяся часть, хотя и не вызывает
осадка с раствором гашеной извести,
гасит пламя и губит жизнь». Это
первое описание свойств азота.
Имя «азот», принятое до сих
пор в нашей стране и во
Франции, новому элементу дал
выдающийся французский химик Ан-
туан Лоран Лавуазье.
ГДЕ ПРИМЕНЯЮТ АЗОТ
Азот — самый дешевый из всех
газов, химически инертных в
обычных условиях. Его широко
применяют в химической
технологии для создания неокислительных
сред. В атмосфере азота хранят
в лабораториях легко
окисляющиеся соединения. Выдающиеся
произведения живописи иногда (в
хранилищах или при
транспортировке! помещают в герметические
футляры, заполненные азотом,—
чтобы предохранить краски от
влаги и химически активных
компонентов воздуха.
Значительной бывает роль
азота в металлургии и при
металлообработке. Различные металлы в
расплавленном состоянии
реагируют на присутствие азота по-
разному. Медь, например,
абсолютно инертна по отношению к
азоту, поэтому изделия из меди
часто сваривают в струе этого
газа. Магний, напротив, при
горении на воздухе дает соединения
не только с кислородом, но и с
азотом. Так что для работы с
изделиями из магния при высоких
температурах, азотная среда
неприменима. Насыщение азотом
поверхности титана придает
металлу большую прочность и
износостойкость — на ней образуется
очень прочный и химически
инертный нитрид титана. Эта
реакция идет только при высоких
температурах.
При обыкновенной
температуре азот активно реагирует только
с одним металлом — литием.
Наибольшее количество азота
идет на производство аммиака.
АЗОТНЫЙ НАРКОЗ
Распространенное мнение о
физиологической инертности
азота не совсем правильно. Азот
физиологически инертен при
обычных условиях.
При повышенном давлении,
например при погружении
водолазов, растет концентрация
растворенного азота в белковых и
особенно жировых тканях
организма. Это приводит к так
называемому азотному наркозу.
Водолаз словно пьянеет: нарушается
координация движений, мутится
сознание. В том, что причина
этого — азот, ученые окончательно
убедились после проведения
экспериментов, в которых вместо
обычного воздуха в скафандр
водолаза подавалась гелио-кисло-
родная смесь. При этом симптомы
наркоза исчезли.
ОТКРЫТИЕ АММИАКА
«Летучая щелочь» впервые
описана немецким химиком
Иоганном Кункепем в конце
XVII века. Он получил аммиак,
нагревая нашатырь с «фиксируе-
14
мой щелочью» — негашеной
известью. Кункель называл аммиак не
только «летучей щелочью», но и
«щелочным воздухом».
КОСМИЧЕСКИЙ АММИАК
Большие планеты солнечной
системы Сатурн и Юлитер
состоят, как полагают астрономы,
частично из твердого аммиака.
Аммиак замерзает при -78СС, а на
поверхности Юпитера, например,
средняя температура — минус
138Х.
ВЕСЕЛЯЩИЙ ГАЗ
Из пяти окислов азота два —
окись (N0) и двуокись (N02) —
нашли широкое промышленное
применение. Два других — азотистый
ангидрид (N203| и азотный
ангидрид |N205J — не часто
встретишь и в лабораториях. Пятый —
закись азота (N20). Она обладает
весьма своеобразным
физиологическим действием, за которое ее
часто называют веселящим газом.
Выдающийся английский химик
Гэмфри Дэви с помощью этого
газа устраивал специальные
сеансы. Вот как описывал действие
закиси азота один из
современников Дэви: «Одни джентльмены
прыгали по столам и стульям, у
других развязались языки, третьи
обнаружили чрезвычайную
склонность к потасовке».
СВИФТ СМЕЯЛСЯ
НАПРАСНО
Выдающийся писатель-сатирик
Джонатан Свифт охотно
издевался над бесплодием современной
ему науки. В «Путешествиях
Гулливера», в описании академии
Лага до, есть такое место: «В его
распоряжении были две большие
комнаты, загроможденные
самыми удивительными диковинами;
пятьдесят помощников работали
под его руководством. Одни
сгущали воздух в сухое плотное
вещество, извлекая из него
селитру...»
Сейчас селитра из воздуха —
вещь абсолютно реальная.
Аммиачную селитру NH4N03
действительно делают из воздуха и воды.
БАКТЕРИИ СВЯЗЫВАЮТ
АЗОТ
Идею о том, что некоторые
микроорганизмы могут связывать
азот воздуха, первым высказал
русский физик П. Коссович.
Русскому биохимику С. Н. Виноград-
скому первому удалось выделить
из почвы один вид бактерий,
связывающих азот.
РАСТЕНИЯ РАЗБОРЧИВЫ
Дмитрий Николаевич
Прянишников установил, что растение,
если ему предоставлена
возможность выбора, предпочитает
аммиачный азот нитратному.
(Нитраты — соли азотной кислоты).
ГЛАВНЫЙ ОКИСЛИТЕЛЬ
Азотная кислота НЖК — один
из самых главных окислителей,
применяемых в химической
промышленности. Первым ее
приготовил, действуя серной кислотой
на селитру, один из крупнейших
химиков XVII века Глаубер.
Среди соединений, получаемых
сейчас с помощью азотной
кислоты, многие совершенно
необходимые вещества: удобрения,
красители, полимерные материалы,
взрывчатые вещества.
ДВОЙНАЯ РОЛЬ
Некоторые азотсодержащие
соединения, применяемые в
агрохимии, выполняют двоякие
функции. Например, цианамид кальция
хлопкоробы применяют как
дефолиант — вещество, вызывающее
опадение листьев перед уборкой
урожая. Но это соединение
одновременно служит и удобрением.
АЗОТ В ЯДОХИМИКАТАХ
Далеко не все вещества, в
состав которых входит азот,
способствуют развитию любых растений.
Аминные соли феноксиуксусной и
трихлорфеноксиуксусной кислот —
гербициды. Первая подавляет
рост сорняков на полях злаковых
культур, вторая применяется для
очистки земель под пашни —
уничтожает мелкие деревья и
кустарники.
ПОЛИМЕРЫ:
ОТ БИОЛОГИЧЕСКИХ
ДО НЕОРГАНИЧЕСКИХ
Атомы азота входят в состав
многих природных и синтетических
полимеров — от белка до
капрона. Кроме того, азот —
важнейший элемент безуглеродных,
неорганических полимеров.
Молекулы неорганического каучука —
полифосфонитрилхлорида — это
замкнутые циклы, составленные из
чередующихся атомов азота и
фосфора, в окружении ионов
хлора.
К неорганическим полимерам
относятся и нитриды некоторых
металлов, в том числе и самое
твердое из всех веществ — бора-
зон.
безжизненный
СКОЛЬКО ИМЕН У АЗОТА!
Азоту «не везло» с
названием. Пять знаменитых
химиков XVIII века дали ему пять
различных имен.
элемент
и. вольпер
Честь открытия азота
принадлежит английскому химику
Даниэлю Резерфорду. 17
сентября 1772 года он представил
в Эдинбургский университет
диссертацию под названием
«О постоянном, или удушливом
воздухе».
В том же году другой
английский ученый — Джозеф
Пристли пришел к выводу, что
воздух состоит из двух разных
<
X
о.
<
CQ
О
с;
о
15
-веществ. Одно из них —
кислород: он необходим для жизни и
горения; другое, наоборот, не
поддерживает ни горения, ни
жизни. Это второе вещество
Пристли назвал «флогистиро-
ванным воздухом».
Третий английский
ученый — Генри Кавендиш (тоже
в 1772 году!) выделил из
воздуха газ и назвал его «удушливым
воздухом».
Примерно в те же годы
молодой аптекарь из шведского
города Упсалы Карл Вильгельм
Шееле независимо повторил эти
открытия. Газ,
поддерживающий горение, он назвал
«огневым», а другой газ (это был
азот) — «дурным воздухом».
Итак, «постоянный» воздух,
«удушливый», «флогистиро-
ванный», «дурной» — а почему
же «азот»? Это слово придумал
французский химик Антуан
Лоран Лавуазье. Когда он
установил, что после удаления
кислорода мышь задыхается в
оставшейся части воздуха, он назвал
этот оставшийся газ
«безжизненным». Вскоре он предложил
новое название
«безжизненному» газу — азот (ft
по-гречески — отрицание, зое — жизнь).
Но слово «азот» отнюдь не
было неологизмом в химии. Еще
в средневековых рукописях
встречается «azot philosopho-
rum» — азот философов. Этот
алхимический азот мог
превращать медь в золото, возвращать
больным здоровье, старикам —
молодость. Алхимики создали
это слово так. Они взяли
первую букву всех алфавитов {о ) и
последние буквы трех древних
алфавитов: «зет» латинского,
*омега» греческого и «тов»
древнееврейского. Слово а + з +
~\ о + т как бы вобрало в себя
,«все начала и концы».
Но вернемся к настоящему
азоту. В свое время его можно
было назвать безжизненным. Но
сейчас это вызывает улыбку.
Разве азотные удобрения не
способствуют жизни растений?
Мало того — азот входит в
состав всех белковых веществ.
Материальная основа жизни —
и «безжизненный» элемент!
Как бы то ни было, но,
написав латинскую букву N, мы
автоматически произносим: азот.
Но позвольте, почему же
химический символ азота — N? Дело
в том, что слово азот
укоренилось только в русском и
французском языках. Англичанин,
увидев символ N, скажет
другое слово — nitrogen, а немец
скажет еще иначе — Stickstoff.
Английское nitrogen
происходит от латинского слова nitroge-
nium, которое в 1790 году
предложил французский химик
Шапталь для обозначения
азота. Первая буква этого слова
стала химическим символом
элемента.
Nitrogenium— словесвый
гибрид. Оно образовано от латин-
слого слова nitrum — селитра, и
греческого генос — рождение.
Значит — рождающий селитру.
Это название и вошло почти без
изменений в английский язык.
В свое время пытались
перевести это слово на русский
язык и называть азот селитро-
твором. Однако это
искусственное слово было
неудобопроизносимым, и в русском языке не
удержалось. Перепробовали еще
несколько названий:
«удушливый газ», «удушающее
вещество». Но в 1824 году по
предложению химика М. Ф.
Соловьева вернулись к термину «азот».
А вот у немцев удержалось
слово Stickstoff — удушающее
вещество.
ДУША НАШАТЫРЯ
В большой семье азота есть
странное соединение — аммоний
NH4. В свободном виде он нигде
не встречается, а в солях играет
роль щелочного металла.
Название «аммоний» предложил в
1808 году знаменитый
английский химик Гемфри Дэви,
Латинское слово ammonium когда-
то означало: соль из Аммонии.
Аммония — область в Ливии.
Там находился храм
египетского бога Аммона, по имени
которого и называли всю область.
В Аммонии издавна получали
аммонийные соли (в первую
очередь — нашатырь), сжигая
верблюжий навоз. При распаде
солей получался газ, который
сейчас называют аммиаком.
В 1787 году (в том самом
году, когда был принят термин
«азот») комиссия по химической
номенклатуре дала этому газу
имя ammoniaque (аммониак).
Русскому химику Я. Д.
Захарову это название показалось
слишком длинным, и в 1801
году он исключил из него две
буквы. Так получился аммиак.
Раствор аммиака в воде
зовут нашатырным спиртом.
Нашатырный — потому что он
может быть получен из
нашатыря NH4CI. Но почему спирт?
Ведь NH4OH ничего общего со
спиртами не имеет. Обратимся
к этимологии слова «спирт».
Химики заимствовали это
слово из английского языка.
Английское spirit восходит к
латинскому spiritus, что значит —
дух, душа. Еще алхимики, не
зная природы того или иного
вещества, но отдавая ему
предпочтение, называли его
спиртом. Винный спирт (по-латыни
spiritus vini) означает — душа
вина.
Именно поэтому алхимики
Валентин и Андрей Либавий
соляную кислоту называли
«кислым спиртом», а немецкий
ученый Глаубер — «соляным
спиртом». Очевидно,
неизвестный нам химик, растворивший
в воде полученный из
нашатыря аммиак, назвал остро
пахнущую жидкость «душой
нашатыря» — нашатырным спиртом.
16
Киев. Памятник Николаю Островскому
СТОЙ НС СГМ
Севастополь- Памятник героям-комсомольцам
ПЛАСТМАССОВАЯ
СКУЛЬПТУРА
Полимер-мономерные композиции — вот название
материала, из которого созданы показанные здесь
скульптуры.
Киевский изобретатель, заслуженный мастер
народного творчества УССР О. К. Кошевой задался
целью найти замену традиционным и дорогим
материалам монументальной скульптуры — камню и
дереву.
Работа продолжалась более 15 лет.
И вот материал найден. Наиболее часто
употребляемая смесь содержит 60% поливинилхлоридной
смолы, 30% метилового эфира метакриловой
кислоты (мономера оргстекла) и 10%
гранулированного полиметилметакрилата. Сверх 100% основных
компонентов в смесь вводятся катализатор
полимеризации — 0,1 % перекиси бензоила,
пластификатор — 3,6% дибутилфталата и краситель.
Из этой смеси делают как небольшие
художественные изделия, так и монументальные скульптуры,
установленные уже в Киеве, Херсоне, Севастополе,
Николаеве. Из этого же материала сделан
центральный свод станции московского метро «Спортивная», а
также многочисленные бюсты, светильники и
красочные панно станции метро «Университет» в Киеве.
^ Химия и Жизнь, № 9
17
от
кижей
к
аэропорту
поиски
формулы
Инженер
В. ЦУКЕРМАН
^л**И>
Люди находят какую-то
особую прелесть в том, чтобы
бежать из городов, из своего дома,
бродить по лесам, ночевать
в палатке, а то и просто под
открытым небом, или
переплывать океан на бревенчатом
плоту. Но покинуть свой дом
насовсем человек не может, как
не может черепаха сбросить
свой панцирь, хотя
физиологически человек с домом и не
связан.
Человек живет в доме.
Можно даже историю
материальной культуры
рассматривать как историю жилища.
Ведь дом концентрирует в себе
главные стороны процесса
развития общества: экономический
и материально - технический
уровень эпохи,
непосредственно влияющие на конструкцию
дома, на выбор материала, на
технологию строительства *;
общественные отношения,
отражающиеся в структуре и
планировке помещения;
эстетический идеал эпохи. Не случайно
даже термины, вначале бывшие
лишь названиями
архитектурных стилей, такие, как
«готика», «барокко», впоследствии
стали обозначать стили в жи -
вописи, литературе, театре,
музыке. Они стали
определениями целых эпох. В здании
находят отражение различные
стороны
общественно-исторического процесса, которые,
сливаясь в одно органичное целое,
собираются в нем, как в
фокусе.
Почему же, размышляя
о себе, о жизни, о смысле эпохи
и ее культуры, мы редко
вспоминаем о домах, в которых и
среди которых проходит почти
вся наша жизнь? Ведь столько
интересного открывается при
рассмотрении любой из частич-
* Интересно, что и само
слово — «экономика» произошло
от древнегреческого «oixec»,
означающего «дом», «жилище».
2*
ных проблем, связанных со
зданием!
В этой статье мы расскажем
об истории строительных
материалов. Мы проследим, как
возникали материалы, из
которых сложены наши дома, и в
процессе их развития
попытаемся найти свои, на первый
взгляд незаметные
закономерности.
Что нам даст знание этих
закономерностей?
Дело в том, что среди
множества причин, влияющих на
эволюцию архитектурных форм,
изменение материалов — одна
из важнейших. Зная закон
этого изменения, мы сможем
предсказать состав
строительных материалов будущего, а
следовательно, сможем
представить себе, как будут
выглядеть дома будущего. Для того
чтобы хотя бы мельком
заглянуть в город 2000 года, нужно
знать «формулу», по которой
изменяются строительные
материалы. Давайте попробуем ее
отыскать.
КАК ВОЗНИКЛИ
МАТЕРИАЛЫ
Как только человек вышел
из пещеры и начал строить
себе жилище, началось
непрерывное, продолжающееся и
поныне, совершенствование
строительного материала. Сначала
человек брал материал у
природы в его естественном,
природой созданном виде и
употреблял в дело, почти не
изменяя ни формы его, ни
структуры. Затем он начал
обрабатывать то, что давала ему
природа, — материал в здании
все более и более терял
внешнее сходство с естественным.
Наконец начали создавать
искусственные материалы, уже
совсем не похожие на сырье, из
которого они созданы.
«Материалы движутся от
естественности к
искусственности» — это уже тенденция,
почти «формула». Для
«формулы» здесь недостает
конкретности. Присмотримся к процессу
развития материала
поподробнее.
Строя, человек укладывал
крупные каменные глыбы друг
на друга, так же складывали
срубы из стволов деревьев. Они
сохраняли устойчивость под
действием тяжести.
Постепенно камни, из
которых складывали здание, стали
уменьшать и, чтобы удержать
их в стене, понадобился
скрепляющий материал — раствор.
Современный строительный
раствор — двухкомпонентный:
вяжущее вещество и
заполнитель. Древнейший раствор
состоял только из вяжущего
вещества, которое употребляли в
необработанном природном
виде — из глины. Затем к ней
стали добавлять такой же
природный заполнитель —
рубленую солому или тростник.
ПЕРВЫЕ ИСКУССТВЕННЫЕ
Первым искусственным
строительным материалом был,
очевидно, кирпич-сырец,
слепленный иэ глины, но не обож-
Церковь в Кижах (фрагмент)
19
женный. Его, правда, можно
еще считать естественным
материалом, поскольку глина пока
не изменила свою внутреннюю
структуру.
По-настоящему
искусственным материалом кирпич стал,
когда его начали обжигать. По
внешнему виду и по составу он
сильно отличается от
исходного продукта. Глина — это
продукт выветривания полево-
шпатных пород, и состоит она
в основном из алюмосиликатов
(типичнейший из них —
каолинит А1 ;03 - Si02 • 2Н20) и
множества примесей. При обжиге
алюмосиликаты, подобные
каолиниту, теряют химически
связанную воду и преобразуются
в новые, безводные
алюмосиликаты.
Одновременно с обжигом
кирпича был открыт новый
скрепляющий раствор —
известковый. Вяжущее здесь —
известь, заполнитель — песок.
Известковый раствор, как и
кирпич-сырец, — переходная
форма между естественными и
искусственными материалами.
Его можно назвать
искусственным, потому что получается он
в результате довольно сложного
химического процесса *. Но
исходный и конечный продукт
в нем один и тот Же — углекис-
* Этот процесс таков: изве^
стняк обжигают, под влиянием
высокой температуры он
разлагается на окись кальция и
углекислый газ СаСОз ^ СаО +
+ С02. Полученную окись
кальция называют негашеной изве-
стью. Ее «гасят», заливая водой:
СаО + Н20 = Са(ОНJ.
Полученную гидроокись кальция
называют известью-пушонкой. Она
и есть вяжущий материал.
В строительном растворе она
соединяется с углекислым
газом яоздуха и превращается в
карбонат кальция: Са(ОНJ +
+ С02 = СаСОз + Н2О.Круг
замкнулся — углекислый кальций
вновь стал углекислым
кальцием.
лый кальций, поэтому
раствор — материал естественный.
В XIX веке появляется
цементный раствор — материал
вне всяких сомнений
искусственный.
Смесь глины и известняка
(в состав современных
цементов входят еще различные
добавки) обжигают до спекания,
затем перемалывают. Порошок,
содержащий окись кальция
СаО, кремнезем Si02, глинозем
А1203 и окись железа Fe203, и
есть цемент. Если его смешать
с водой, происходит сложная
цепь превращений одних
кальциевых силикатов и
алюминатов в другие, образование золя,
и, наконец — твердение,
образование твердого цементного
камня.
Так все строительные
материалы — и камень, и вяжущее
вещество становятся
искусственными, совершенно
изменяя при этом свою структуру.
РЕВОЛЮЦИЯ
В МИРЕ
МАТЕРИАЛОВ
Мы говорили пока только
о тех материалах, из которых
складывают стены. Но
строители использовали и другие
материалы: этажи перекрывали
деревянными и стальными
балками, кровли покрывали тесом,
черепицей, железом. Такое
^разделение труда» было
вызвано различными
механическими свойствами материалов,
неодинаковой способностью
воспринимать различные
напряжения: сжимающие,
растягивающие, изгибающие. Стальной
трос приспособлен только для
работы на растяжение, кирпич
же хорошо работает на сжатие,
но плохо — на растяжение, а
следовательно, и на изгиб.
Поэтому из кирпича можно делать
стены и колонны, но нельзя
делать балки. Зато стальные
балки великолепно
воспринимают растягивающие и
изгибающие напряжения.
Дерево — универсально
работающий материал, дающий
необыкновенный простор
архитектурному творчеству. Целые
здания строили только из
дерева, не употребляя других
материалов. Деревянная церковь
в Кижах — слава и гордость
строительного искусства
России — была возведена без
единого гвоздя!
Но необходимость в большей
прочности, долговечности,
огнестойкости материалов для здэ-
ний вынудили человека искать
дереву замену. В наше время
начали соединять воедино
разные строительные материалы,
получая при этом качественно
новые м атериа л ы, способ ные
с одинаковым успехом
образовывать и стены, и перекрытия,
и кровли зданий.
Одним из них был
железобетон — искусственный
материал, синтезировавший в себе
старые материалы, и почти
такой же универсальный, как
естественный материал —
дерево.
Теперь «формула» как будто
у нас в руках: «от
естественного — к искусственному, от
универсальности, через
временное разделение функц-ий, к
новой, высшей универсальности,
к синтезу».
Но является ли железобетон
таким синтезом? Может ли он
стать материалом будущего?
ЧТО ЭТО —
ЖЕЛЕЗОБЕТОН!
Бетон, как и все стеновые
материалы, очень хорошо
работает на сжатие, но плохо на
растяжение. В конце прошлого
века инженерам невольно
пришла мысль соединить бетон с
20
материалами, хорошо работаю-
щими на растяжение.
В 1885 году на выставке
в Париже демонстрировалась
лодка с металлическим
сетчатым каркасом, обмазанным
цементным раствором. А еще
раньше — в 1867 году были
цветочные кадки садовника
Ж. Менье.
Строители обнаружили, что
соединение хорошо
сжимающегося бетона и хорошо
растягивающейся стали открывает
перед ними огромные
возможности. Из железобетона можно
изготовлять изделия любой
формы, закладывая стальную
арматуру в те места бетонного
монолита, где по расчетам
ожидаются растягивающие
напряжения. Совместная работа
стали и бетона в железобетонном
элементе похожа на симбиоз
в мире животных и растений.
Действительно: сталь помогает
бетону выдержать недоступные
ему растягивающие нагрузки,
бетон же защищает стальную
арматуру от коррозии.
Железобетонная конструкция обладает
прочностью, недоступной
одному бетону без стали, и
долговечностью, недоступной стали без
бетона.
Современный аэропорт
СИМБИОЗ СТАЛИ
И БЕТОНА
НЕ УНИВЕРСАЛЕН
Но железобетон
неоднороден. Арматура расположена в
бетонной массе неравномерно, и
поэтому каждый
железобетонный элемент способен
воспринимать нагрузки только в
одном направлении. Сталь и
бетон, находясь в одном элементе,
работают раздельно — сталь на
растяжение, а бетон на сжатие.
Железобетон еще не стал
синтезом различных материалов, а
явился только их
механическим соединением.
Железобетон, как будто, —
универсальный материал. Из
него одного можно построить
дом так же, как и из дерева. Но
каждый элемент такого здания
сможет работать только в этом
здании или в аналогичных
условиях другой конструкции.
Б этом его отличие от дерева:
деревянную балку можно с
таким же успехом употребить как
колонну, железобетонную —
нельзя.
Искусственный материал —
железобетон еще не достиг
универсальности
естественного — дерева.
ЗАВЕРШЕНИЕ РЕВОЛЮЦИИ
БЛИЗКО
Строители давно заметили,
что в железобетонном
элементе, вблизи от арматуры, бетон
меняет свои свойства: он
начинает работать на растяжение
так же хорошо, как и на
сжатие. Причина этого явления
известна: вблизи стальной
арматуры у бетона меняются
условия твердения. Силикаты, из
которых состоит бетон,
сцепляясь с кристаллами стали,
образуют направленную
кристаллическую структуру.
Это явление заставило
итальянского инженера Пьеро
Луиджи Нерви вспомнить о самых
первых железобетонных
конструкциях — лодках и кадках
со стальными сетками. Нерви
уменьшил ячейки сеток,
превратив их в стальную паутину.
Бетон находится в близком
соседстве со сталью, и поэтому
хорошо работает на
растяжение. Так получился новый,
однородный строительный
материал — армоцемент. В 1946
году первые армоцементные
лодки Нерви начали плавать вдоль
берегов Италии, а сейчас
конструкции из армоцемента при-
21
меняют на стройках всего
мира.
Армоцементные листы
тонки, поэтому для прочности
элементам из армоцемента
придают сложную
пространственную форму складок, оболочек,
или корыт. Сталь и бетон
работают вместе, но
универсальность материала еще не
достигнута, потому что элементы
работают только в специально
для них предназначенных
местах.
Лрмоцемент — следующий
после бетона шаг к созданию
универсального материала.
ПОЛНАЯ
УНИВЕРСАЛЬНОСТЬ
ПЛАСТМАСС
Мы называли дерево
материалом однородным и
универсальным. Это не совсем точно,
волокнистая структура дерева
делает его не полностью
однородным материалом,
механические свойства которого вдоль
и поперек волокон различны.
Структура многих
современных материалов, стремящихся
к универсальности —
железобетона, и особенно армоцемента,
похожа на волокнистую
структуру дерева. Но односторонняя
направленность волокон
приводит неизбежно к
неоднородности материала, тем более, что
«волокна» армоцемента более
крупные, чем у дерева.
Но вот в строительстве
появились пластмассы,
армированные стеклянным волокном.
Волокна арматуры в них не
ТЕХНОЛОГИ —ВНИМАНИЕ! 1
КАКАЯ НУЖНА ТЕМПЕРАТУРА!
Пасты из поливинипхлорида с
пластификатором — пластизоли —
в последние годы приобрели
отличную репутацию. Они очень
легко перерабатываются в
изделия. Но для каждого способа
переработки нужен пластизоль с
определенными свойствами. Осо-
ориентированы, и поэтому
свойства такой пластмассы во всех
направлениях однородны.
Но нужно ли вообще
армировать пластмассу? Ведь она
уже имеет своеобразную
волокнистую структуру — длинные
цепи молекул, более мелкую,
чем у дерева.
Армировать пластмассу
стеклянными волокнами
приходится пока только потому,
что ее собственные
молекулярные волокна недостаточно
прочны. Но получение прочной
пластмассы — вопрос времени,
причем не столь уж далекого.
Появление такой
пластмассы — материала, прочного, как
сталь, легкого, как дерево,
прозрачного, как стекло, дешевого,
как бетон, не подверженного
коррозии, не боящегося огня,
долговечного, абсолютно
однородного, означало бы
величайшую революцию в архитектуре.
ФАНТАСТИЧЕСКИЕ
ЗДАНИЯ
Универсальный материал —
дерево вызвал необыкновенный
расцвет архитектуры. Мы не
видели древнегреческих
деревянных сооружений, но даже
построенные по их образцу
каменные здания (античные
храмы подражают в мраморе и
известняке деревянным формам)
великолепны. Сейчас в
строительство пришли железобетон
и армо цемент, материалы не
полностью однородные, только
предвестники будущего синте-
бенно важно точно знать
температуру желатинизации. Например,
для ротационного литья гель не
должен образовываться слишком
быстро — нужно время, чтобы он
затек во все уголки формы. Л при
макании скорость желатинизации
должна быть как можно большей.
Недавно был предложен новый
прибор для определения темпе-
за, но какое богатство новых
форм, какие открытия они
принесли!
Старые материалы
связывали архитектора. Тяжелые,
неповоротливые, вышедшие из
земли, связанные с ней, они
тяготели к земле, заставляли
зодчего кружиться в лабиринте
одних и тех же форм:
прямоугольных коробок, колонн,
куполов, прямоугольных
отверстий в стенах — окон и дверей.
Уже железобетон позволил
отказаться от этих форм, поднять
здание на легких опорах в
воздух, заменить тяжелые несущие
стены с прорезями окон
гигантскими стеклянными
витражами, висящими в воздухе.
Раньше, как бы ни менялась форма
здания, вертикаль в нем
оставалась незыблемой — камень
давил на камень, и стена была
обязательно прямолинейной и
направленной вниз.
Железобетон дал бесконечное
разнообразие форм, органичных и точно
соответствующих
распределению напряжений в материале.
Но железобетон еще не
окончательно универсален, он тяжел,
еще связан с землей.
Когда в строительство
придет пластмасса, архитекторам
станут доступны любые
криволинейные формы, появятся
здания фантастических очертаний.
Тяжесть, приземленность,
сырость и темнота — эти понятия
навсегда исчезнут в городах
будущего. И день, когда
появятся эти города, уже близок.
Дело за химиками.
ратуры желатинизации. Прибор
довольно прост. Его основная
деталь — трубка, в которую
наливают пластизоль. Трубка погружена
в расплавленный парафин.
Термометр, опущенный в пластизоль,
служит также и мешалкой. Для
определения скорости
желатинизации достаточно 7 мл материала.
(«British Plastics»», 1966, № 2)
22
ПРОИСХОЖДЕНИЕ
ЖИЗНИ
ДЖОРДЖ УОЛД
ИЗ ВСЕХ ЭЛЕМЕНТОВ во Вселенной
шире всего распространен водород; водород
и кислород составляют также
значительную долю A5,4 и 55,19 процентов
соответственно) общего числа атомов биосферы
Земли.
Но вот углерод живые существа
должны были накопить за счет только 0,44
процента всех доступных атомов, азот — за
счет 0,16 процента, а фосфор и серу — за
счет 0,23 и 0,12 процента атомов,
имеющихся в биосфере.
Иначе говоря, далеко не все органогены
принадлежат к широко распространенным
элементам. Их особое положение
определяется пригодностью по существу: среди
элементов только они обладают теми
критическими свойствами, которыми
повсеместно во Вселенной должна определяться
возможность жизни. (Меня не раз
спрашивали, можно ли уверенно сказать, что где-
нибудь во Вселенной не встречаются
элементы, отличающиеся от элементов
Периодической системы. В ответ я ссылался на
то, что это все равно что спрашивать, не
существует ли где-нибудь во Вселенной
еще какое-то целое число, стоящее между
4 и 5. К сожалению, есть люди, которые
находят и этот вопрос резонным...)
ВПОЛНЕ ЕСТЕСТВЕННО, что
закономерности Периодической системы
производят на нас столь большое впечатление,
что мы иногда преувеличиваем их
значение. Но самые легкие элементы
действительно обладают особыми свойствами, не
повторяющимися в следующих периодах.
Существенное отличие водорода,
кислорода, азота и углерода от их аналогов
состоит прежде всего в том, что это первые
четыре элемента Периодической системы,
способные присоединять соответственно
1, 2, 3 или 4 электрона, образуя
устойчивые электронные конфигурации. Как из-
Окончание. Начало в прошлом номере.
вестно, это свойство лежит в основе
образования химических связей и,
следовательно, построения молекул. Особое
значение имеет тот факт, что эти легкие
элементы образуют самые крепкие (притом
углерод, азот и кислород — также двойные
и тройные) связи.
Нередко высказывают предположение,
что на других космических телах кремний
может замещать в живых организмах
углерод. В пользу такой возможности
приводят следующие доводы: кремний
располагается в Периодической системе
непосредственно под углеродом; подобно
углероду он способен соединяться с самим
собой, образуя длинные цепи и тем
самым— очень сложные молекулы; у нас
на Земле в доступных для жизни областях
кремния примерно в 35 раз больше, чем
углерода.
И все же кремний не может служить
заменой углероду в живых существах. Во-
первых, он образует менее компактные и
менее прочные соединения:
УГЛЕРОДНЫЕ И КРЕМНИЕВЫЕ ЦЕПИ
С С
ХС С С/
Расстояние С — С 1,54 А (энергия связи.
83,1 к кал моль)
Si Si
xSi Si SK
Расстояние Si — Si 2,34 А (энергия евязи
42,5 ккал/моль)
Во-вторых, кремниевые цепи легко
доступны атаке молекулами, имеющими не-
поделенные электронные пары (кислорода,
аммиака, воды), и не способны к
длительному существованию в их присутствии.
Я полагаю, что одно это заставляет
исключить кремний как возможную основу
жизни.
2
О
со
з:
<
ас
<
z
23
Помимо этого у кремния еще один
фатальный недостаток: он не способен давать
кратные (двойные, тройные) связи.
Значение этого фактора становится понятным
при сопоставлении двуокиси углерода с
двуокисью кремния:
ДВУОКИСЬ УГЛЕРОДА II ДВУОКИСЬ
КРЕМНИЯ
Двуокись углерода: С02
0 = С = 0
Двуокись кремния: (Si02)n
I I
О — Si — О
I I
О — Si — О
I I
В СС>2 валентное сродство атомов
углерода и кислорода полностью
насыщается образующимися между ними
двойными связями. Поэтому молекулы
двуокиси углерода свободно выделяются в виде
газа, растворяются в воде и, значит,
доступны для усвоения живыми
организмами. А вот в двуокиси кремния все связи
простые, и поэтому у молекулы остаются
четыре неспаренных электрона. Последние
тотчас же образуют связи с соседними
молекулами. В результате этого получается
полимерная «сверхмолекула» типа кварца,
которая, естественно, практически
нерастворима в воде.
Несколько менее непреложны доводы,
касающиеся благоприятных свойств серы
и фосфора. В организме эти элементы
наряду с другими функциями выполняют
специальную роль, входя в состав реак-
ционноспособных соединений,
участвующих в переносе энергии и органических
групп в клетках.
Как уже отмечалось, живые существа
возникли (и, вероятно, могли бы
существовать неопределенно долго) в отсутствие
молекулярного кислорода. Однако
кислород сделал возможным развитие
клеточного дыхания, и это открыло организмам
доступ к наиболее эффективному
химическому способу добывания энергии,
основанному на окислении водорода —
горючего с наибольшим энергетическим
потенциалом. Более того, жизнь, по-видимому,
оставалась подводной и не могла породить
высших наземных форм до тех пор, пока
в атмосфере Земли, в верхних ее слоях, не
появился кислород: под действием
радиации из него образовался озон,
поглощающий смертельное для организмов жесткое
ультрафиолетовое излучение.
ИТАК, ГЛАВНЫЕ БИОЭЛЕМЕНТЫ
обладают уникальными свойствами,
позволившими живым существам возникнуть и
функционировать; из этих же элементов
построены и многие уникальные,
абсолютно необходимые для жизни вещества.
Главное из этих соединений — вода,
которая, я полагаю, совершенно незаменима.
Не раз высказывалась мысль, что на
других космических телах средой для
жизни вместо воды мог бы служить
жидкий аммиак. В ряде важных отношений
аммиак, однако, значительно уступает
воде.
Во-первых, аммиак остается жидким в
гораздо более узком температурном
интервале, нежели вода:
СВОЙСТВА АММИАКА
Точка кипения: —33,35°С (при давлении J ат)
Точка замерзания: — 77,7ГС (при давлении 1 ат)
Плотность при —79СС:
/кпдкого аммика 0,7354 г см3
твердого аммиака 0,817 г/см3
Во-вторых, в этом интервале (т. е.
ниже минус 40°С) все реакции протекали
бы значительно медленнее, чем на Земле.
Если считать, что скорости реакций
уменьшаются в среднем в два раза при
понижении температуры на каждые 10°С, то при
температуре жидкого аммиака химические
процессы происходили бы в 26 (то есть в
64) раза медленнее, чем на Земле. Иначе
говоря, процесс, который привел к
возникновению жизни на нашей планете
примерно за миллиард лет, требовал бы в среде
жидкого аммиака около 64 миллиардов
лет. Этот срок намного превышает все
современные оценки возраста нашей
Галактики.
И, наконец, решающее значение для
живых организмов имеет еще одно
своеобразное свойство воды, а именно —
плавучесть льда. Если бы лед не всплывал, то
земные воды уже давно целиком
промерзли; они не оттаивали бы даже за
длительные периоды теплой погоды. Естественно,
что в таких условиях возникновение или
поддержание жизни оказалось бы
практически невозможным.
Этим странным свойством вода
обязана тому обстоятельству, что, хотя подобно
24
другим добропорядочным веществам она
при охлаждении испытывает сжатие, ниже
4СС она расширяется. Причина этого
явления состоит в том, что ниже 4°С молекулы
воды в возрастающей мере соединяются
друг с другом водородными связями, так
что при точке замерзания они образуют
более жесткую, но менее плотную
структуру- В противоположность этому,
аммиачный лед быстро тонет в жидком
аммиаке, с отчетливым стуком падая на дно
сосуда. Такую особенность нужно
причислить к недостаткам аммиака, не
позволяющим ему служить в качестве среды для
жизни.
Но есть и другие возражения.
Разложение воды при фотосинтезе высших
растений дает в качестве побочного продукта
молекулярный кислород, который сделал
возможным развитие клеточного дыхания.
Аналогичный процесс с участием аммиака
мог бы вместо этого дать азот —
удручающе инертный газ.
Я ГОТОВ УТВЕРЖДАТЬ, что когда
организмы поставлены перед
необходимостью «разработать» вещество,
предназначенное для выполнения какой-либо
фундаментальной клеточной функции, то
они крайне ограничены в выборе структур.
Хлорофиллы для фотосинтеза, гемсодер-
жащие пигменты для клеточного дыхания,
каротиноиды и витамин А для
фоторецепции — все эти вещества представляют
собой итог происходивших на нашей
планете длительных и строгих процессов
отбора, неизменно идущих к достижению
оптимального решения. Все эти молекулы
обладают свойствами, которые делают их
особо пригодными для выполнения
присущих им биохимических функций. Я не
сомневаюсь, что, чем лучше мы в каждом
отдельном случае станем понимать
существо процесса, тем будет яснее, почему
природа отбирала именно эти, а не другие
молекулы.
Иногда такие молекулы представляют
собой странное смешение удачных и
отрицательных качеств; так, у всех хлорофил-
лов имеется странное свойство — они хуже
scero поглощают свет при тех длинах волн,
при которых солнечный свет на
поверхности Земли или под водой наиболее
интенсивен. Очевидно, хлорофиллы
должны представлять для фотосинтеза другие
преимущества, перевешивающие этот
недостаток. А поскольку благодаря этим
преимуществам хлорофиллы играют
уникальную роль в фотосинтезе на Земле,
эти же свойства могли бы в равной мере
способствовать селекции тех же структур
и в других местах.
Возьмем другой пример. Три отряда
животных * на Земле, создав совершенно
независимо один от другого три
существенно различающихся типа глаз, пришли
к одному и тому же хромофору
зрительных пигментов — 11-цис-ретинену. Между
тем 11-цис-изомер ** представляет собой
особенно нестойкую модификацию.
Почему же именно он был повторно
отобран для данной функции? Оказалось*
что при зрительном акте действие света
сводится единственно к изменению формы
этой молекулы, а 11-цис-ретинен
образцово выполняет свою роль, так как свет с
высокой степенью эффективности
превращает его изогнутую и скрученную цис-
конформацию в относительно
спрямленную полностью транс-конформацию.
Естественно поэтому предположить, что силы,
трижды «выбравшие» именно эту
молекулу на нашей планете, могли бы и в иных
местах привести к тому же (или
аналогичному) решению.
Подведем итог. Поставленные почти
перед универсальными задачами, организмы
могут повсеместно тяготеть к отбору типов
молекул, которые в рамках возможностей
органической химии представляют
оптимальные решения или близки к таковым.
Я говорю «типов», а не «индивидуальных
видов молекул», так как в каждом из
упомянутых случаев мы и на Земле видим за
работой не один вид молекул, а целую
категорию их: по меньшей мере пять
различных хлорофиллов, разнообразные гемы,
несколько активных каротиноидов, два
витамина А.
ЭТИМ ПРОЦЕССОМ должен
повсеместно управлять естественный отбор,
описанный сто лет назад Дарвином и
Уоллесом. Это в одно и то же время и фор-
* Речь идет, по-видимому, о позвоночных,
насекомых и ракообразных. — Ред.
** Цис-транс-изомерия присуща органическим
соединениям, имеющим двойные связи. У цис-
изомера однотипные заместители расположены
«по одну сторону» от двойной связи, а у
трансизомера заместители находятся «с разных
сторон». — Ред.
25
мирующии, и консервативный принцип в
эволюции живых объектов.
Он складывается из трех компонентов:
1) механизма наследования, без
которого жизнь не может существовать где бы
то ни было;
2) непрерывно вторгающегося в
генетическую информацию «шума», который
проявляется в потомстве в виде
унаследованных случайных вариаций (мутаций);
3) борьбы за существование —
конкуренции за все необходимое для жизни.
Таковы универсальные факторы,
которые едва ли могут быть обойдены какой-
либо популяцией живых объектов. И если
в целом процесс естественного отбора
приводит к выживанию всего наиболее
приспособленного, то и на молекулярном
уровне естественный отбор находит
выражение в непрестанной оптимизации
структур.
Иногда утверждают, что естественного
отбора «недостаточно» — недостаточно,
чтобы объяснить эволюцию глаза, или
крыла, или, например, столь
совершенного механизма развития эмбриона. Но
нельзя же отрицать естественный отбор лишь
потому, что он действует лучше, чем мы
склонны этого ожидать!
Более того. Иногда высказываются
соображения вроде того, что «с точки
зрения физика представляется чудом
существование структур, которые воспроизводят
идентичные им структуры». В
подтверждение этого приводятся расчеты, имеющие
целью доказать к вантово-механическую
невозможность предохранения
закодированной в генах информации от
возрастающей неупорядочности по мере ее передачи.
К счастью, никакого чуда как раз и не
происходит. Если бы воспроизведение
происходило абсолютно точно, то
наследственность работала как будто лучше, но
естественный отбор совсем не мог бы
действовать. Мутации действительно непрерывно
вносят беспорядок в генетическую
информацию, но процесс отбора столь же
непрерывно ведет отсев, обеспечивая
упорядоченную и, мало того, направленную на
совершенствование преемственность.
Из расчетов, доказывающих
невозможность точной передачи наследственной
информации, можно извлечь некоторую
пользу: они вселяют уверенность в том,
что любой молекулярный генетический
код должен непрестанно давать начало
случайным вариациям, каких требует
естественный отбор. Иначе говоря,
порядок не внесен в живые организмы заранее,
по предумышленному плану; он создается
post factum, вслед за случайными
мутациями. Так что можно сказать, что мы
являемся продуктами скорее
редактирования, чем авторского творчества...
Я как-то подумал, что было бы
интересно создать экспериментальную модель,
воспроизводящую некоторые черты этого
процесса. Допустим, что на ленту
выписываются произвольные слова и что
полдюжины людей последовательно, но
независимо друг от друга выписывают
некоторые из них с тем, чтобы составить сперва
осмысленную фразу, а затем — связное
повествование. Вероятно, каждый
оператор избрал бы свое начало; но даже
первые — особенно последующие — слова все
в возрастающей мере станут влиять на
дальнейший выбор. В сравнении с
естественным отбором эта модель имеет,
конечно, существенный порок, поскольку в ней
фигурирует наделенный волей оператор,
предыстория и намерения которого
неизбежно должны повлиять на конечный
результат. Но столь же очевидно, что итог
будет существенно отклоняться от любого
задуманного оператором плана. В большой
мере он окажется результатом
диалектического взаимодействия между
предварительным замыслом и тем, что внушают
возникающие на ленте слова. Мне кажется,
что такой опыт стоит провести, если не
как научный, то хотя бы как
литературный эксперимент...
В ЭТОЙ СТАТЬЕ я пытался кратко
разобрать некоторые из условий,
сформировавших жизнь на этой планете, и
изложил причины, дающие основания верить,
что те же условия повсюду привели бы к
формированию жизни. Эти рассуждения
позволяют рассматривать развитие жизни
как упорядоченный процесс, повсеместно
дающий полный простор проявлениям
случая, но не представляющий в сколько-
нибудь существенной мере итог
случайности.
Мы, живые существа, представляем
собой поздний продукт развития нашей
Галактики.
Углерод, занимающий столь важное
место в составе наших тел, был выпечен
26
в отдаленном прошлом на умирающей
звезде. Из него при более низких
температурах образовались азот и кислород. Эти
незаменимые элементы были выброшены
в пространство при извержениях на
красных гигантах (или при таких звездных
катастрофах, как рождение сверхновых),
смешались здесь с водородом и образовали
в конечном итоге материю Солнца, планет
и живых существ. Воды первобытного
океана задали ионный состав нашей крови.
Первобытные атмосферы сформировали
наш метаболизм.
Как часто, с каким подавляющим
авторитетом нам говорили, будто сущность
вещей должна навсегда остаться скрытой от
нас, будто мы должны стоять вне природы,
подобно детям, прижавшим носы к окну и
способным заглянуть, но не войти внутрь.
Изложенные выше представления о
нашем происхождении подкрепляют другой
В первом номере журнала «Химия и жизнь» за
1966 год автором статьи «Реакция идет в
кристалле — твердофазная полимеризация» кандидатом
химических наук И. М. Баркаловым допущена
грубая ошибка. Структуры изотактических и синдио-
н н
: :
'СНг—С СН2— С —■ СН^—
6 6
Изотактический полистирол
На приведенных здесь рисунках пунктирные
линии показывают, что заместители находятся за
плоскостью, в которой лежит основная цепочка
атомов; жирные линии показывают, что заместители
выступают из этой плоскости.
Та структура, которую автор изобразил под
названием синдиотактической, в химии полимеров
взгляд на вещи. Мы не глядим на
Вселенную извне, мы видим ее изнутри- Ее
история — это наша история, ее вещество —
наше вещество- Сознание этого дает нам
уверенность в реальности того, что мы
видим.
Подобная цепь событий, начинающаяся
от элементарных частиц, в итоге приводит
(возможно, с неизбежностью) к странному
движущемуся продукту — к существу,
которое мыслит и знает, к животному,
творящему науку и оглядывающемуся на
процесс, который его породил.
Большая доля нашего человеческого
достоинства, пожалуй, в том и состоит, что
мы способны познавать и что через нас
материя познает себя...
Сокращенный перевод с английского
ствдемика А. Е. БРАУНШТЕЙНА
тактических полимеров отличаются
пространственным расположением заместителей и в случае
полистролов, о которых говорится в статье, должны
быть изображены так:
. о
—сн2—с сн5— с сн2—
I I
О "
Синдиотактический полистирол
называется типом присоединения «голова к голове».
К проблеме стереорегулярности и к катализаторам
Циглера — Натта она отношения не имеет. Эта
ошибка повторяется и в изображении спирали,
сопровождающем текст.
Редакция приносит читателям извинения за
допущенную ошибку.
поправка
27
НОВОСТИ ОТОВСЮДУ
УПРОЧНЕННЫЕ СТЕБЛИ
В Чехословакии на заводе
«Синтезия» началось производство
так называемого морфорегупи-
рующего раствора — нового
средства против полегания пшеницы.
Им опрыскивают растения,
достигшие 10—20 см в длину. Такая
обработка на некоторое время
замедляет рост стеблей, но делает
их более прочными и устойчивыми
против полегания. Затем
упрочненные стебли вновь начинают
расти. При обработке посевов мор-
форегулирующим раствором
урожай увеличивается на 30 7 .
СЛЕДЫ СВИНЦА ВО ЛЬДАХ
Массовое применение тетра-
этилсвинца дпя повышения
октанового числа бензина приводит к
загрязнению свинцом воздуха в
городах и вдоль автомагистралей.
Изучение льдов полярных и
приполярных областей заставило
ученых снова обратить на это
внимание. Исследуя льды
Гренландии, они обнаружили, что
содержание в них свинца за последнее
десятилетие катастрофически
возросло. Ученые предполагают, что
такой рост концентрации свинца
во льдах вызван увеличением
количества его в атмосферных
осадках.
Вероятно, изучение
химического состава различных слоев льда
и снегов Антарктиды представит
большой научный интерес. По
анализу, например, содержания
свинца в этих слоях можно
регистрировать отклонения от средних
значений, связанные с атомными
взрывами, с началом массовых
плавок свинца человеком и с
широким применением соединений
свинца в бензине.
НОВЫЕ ДАННЫЕ
ОБ ИСКУССТВЕННЫХ ДОЖДЯХ
До последнего времени
считалось, что распыление в атмосфере
веществ типа йодистого серебра
всегда приводит к образованию
туч и к дождю. Кроме того,
опыты, проводившиеся в течение семи
лет в Швейцарии, давали
основания считать, что таким же
способом можно предотвратить
образование и выпадение града.
Недавно доктор Нейман,
директор статистической
лаборатории Калифорнийского
университета, сообщил о четырех больших
опытах, показавших, что массовое
распыление химикалиев в
атмосфере может привести к
совершенно противоположным
результатам.
В трех таких опытах число
осадков уменьшилось. В
четвертом получены противоречивые
данные.
Что касается града, то
статистическая обработка результатов
этих опытов показала, что
применение йодистого серебра в
основном приводит к выпадению
сильных градов, а не к их
предотвращению, как считалось
раньше.
КОСМИЧЕСКИЙ ПАРАШЮТ
Обычные парашюты
раскрываются только в сравнительно
плотных слоях атмосферы.
Журнал «Plastics Week», 1965, № 29
сообщает о новом парашюте,
который срабатывает в сильно
разреженном воздухе верхних слоев
стратосферы. Парашют
изготовлен из металлизированной
полиэфирной ппенки и дакроновой
полиэфирной ткани.
ТРУБЫ УСТОЙЧИВЫЕ
К КОРРОЗИИ
Металлические трубы,
покрытые изнутри слоем пластмассы,
широко распространены в
технике. Металл придает трубе
необходимую механическую
прочность, а пластмасса — химическую
стойкость.
В ФРГ для особо агрессивных
сред разработаны трубы, в
которых пластмасса и металл
поменялись ролями. Наружный слой
этих труб сделан из
стеклопластика и несет механическую
нагрузку, а внутренний слой — из
листового тантала — металла,
отличающегося исключительной
устойчивостью к коррозии.
НОВЫЕ
МЕТАЛЛСОДЕРЖАЩИЕ
ПОКРЫТИЯ
Японские ученые получают из
соединений алюминия и жирных
кислот льняного масла новые
виды смол, пригодные для
применения в лакокрасочной
промышленности. Технологический
процесс получения смол занимает
2 часа, максимальная
температура — 200 С. Пленка,
приготовленная из раствора такой смолы
в ксилоле, быстро высыхает. Она
отличается высокой твердостью,
ярким блеском, хорошей
эластичностью, не коробится и не
размокает в воде.
ТЕПЛОЧУВСТВИТЕЛЬНАЯ
КРАСКА
В одной американской научно-
исследовательской лаборатории
краски, меняющие цвет под
действием тепла, используются при
испытаниях новых типов
высокоскоростных самолетов. С
увеличением скорости движения
самолета отдельные детали сильнее или
слабее нагреваются. Теплочувст-
вительные краски помогают
контролировать эти температурные
изменения.
Чтобы предотвратить утечку
тепла, модели для испытаний
изготовляют из керамических
материалов, обладающих низкой
теплопроводностью.
Каждое испытание длится 30
или более секунд, при скорости
10—21 000 км/ч. Сейчас ведутся
работы по получению красок,
цвет которых будет меняться за
несколько миллисекунд.
28
СОЛНЦЕ РАЗРУШАЕТ,
СОЛНЦЕ ЛЕЧИТ
ФОТОЭЛЕМЕНТЫ
Искусственные спутники Земпи
и автоматические межпланетные
станции часть электроэнергии
получают от установленных на
борту батарей фотоэлементов,
преобразующих энергию солнечного
излучения в электрическую. Но
одновременно частицы высоких
энергий солнечного и
космического излучений вызывают
постепенное снижение мощности
солнечных батарей и в конце концов
выводят их из строя. За несколько
месяцев мощность
фотоэлементов, установленных на спутнике,
может уменьшиться вдвое.
Происходит это потому, что при
бомбардировке частицами высокой
энергии нарушается структура
кремниевых полупроводников,
из которых изготовлены
фотоэлементы, и фототок
уменьшается.
Опыты, поставленные фирмой
«Вестингауз», показали, что если
прогреть фотоэлементы при 500 С
в течение нескольких минут, то их
мощность восстанавливается почти
до первоначальной величины.
Но как нагреть фотобатареи,
установленные на борту спутника,
летящего в космическом
пространстве!
Инженеры фирмы собираются
сделать это с помощью того же
Солнца. Для этого
предполагается использовать специальные
линзы, фокусирующие солнечные
лучи и по команде с Земли
направляющие световой пучок на
солнечную батарею.
Пока на Земле проводятся
предварительные опыты. В этих
опытах вместо космического
пространства — вакуумная камера,
вместо космических лучей —
ускоренные электроны, и только
солнечные лучи — естественные.
После двухминутного прогрева
сфокусированными солнечными
лучами мощность пострадавшего
фотоэлемента восстанавливается
почти до первоначальной.
КАУЧУКОВЫЕ
КАЧЕЛИ
Такие качели очень популярны
сейчас в Швейцарии. Конечно, они
сделаны не целиком из каучука —
рама, сиденье и ручка у них
металлические. Но «раскачивающая»
деталь — рессора сделана из
резины на основе натурального
каучука. По конструкции она очень
похожа на резиновые
амортизаторы, которые гасят колебания.
Кстати, это важно и для качелей —
вовремя прекратить раскачивание.
Дети довольны новыми
качелями. Размах у качелей большой,
а ход — гладкий и плавный.
Родители тоже довольны: качели с
резиновой рессорой можно
собрать за несколько минут и
поставить в любом месте.
ТЕРМОМЕТР ДЛЯ ПЛАСТИКОВ
Американской фирмой «Дю-
лон» разработаны термометры
для бесконтактного измерения
температуры пластиков.
Температура определяется по
интенсивности инфракрасного излучения
расплавов термопластов, в
частности полиэтилена.
Датчик, улавливающий
инфракрасные лучи, снабжен фильтром,
который пропускает лишь узкую
полосу частот, присущих тому или
другому виду веществ. В этой
ограниченной области частот
чувствительный элемент
воспринимает излучение пластмассы как
почти абсолютно черного тела.
Поэтому источники теппа,
находящиеся под изделием, не влияют
на показания прибора. Новый
термометр позволяет замерять
температуру пластмассовых изделий
непосредственно в процессе их
формирования.
КОПИРКА ИЗ ПЛАСТМАССОВОЙ
ПЛЕНКИ
Журнал «Plastverarbeiter» 1965,
№ 5 сообщает о высокопрочной
копирке из пластмассы.
Прочность такой копирки всего в три
раз меньше прочности стали.
Даже при самом сильном ударе по
клавише пишущей машинки на
пленке не остается никакого
следа. Одну колирку можно
употреблять до 30 раз. Копирка
очень тонка. Используя ее, можно
сделать сразу десять копий.
Кроме того, пленка имеет еще одно
хорошее свойство — она не
свертывается в трубочку, как это
часто случается с копировальной
бумагой.
ОКРАШЕННЫЙ
СИНТЕТИЧЕСКИЙ КВАРЦ
В Японии ученые исследуют
возможность окрашивать
синтетический кварц, вводя в его состав
гидроокиси, карбонаты или
окислы различных металлов в виде
растворов или взвесей в
растворителях.
Кристаллы кварца легко
окрашиваются при введении в его
состав железа, никеля, кобальта,
марганца и селена и слабо — при
добавках меди и ванадия.
НЕ ТОЛЬКО ДЛЯ НАРКОМАНОВ
Как блокировать действие
наркотиков! Это важно не только для
лечения наркоманов. Ведь в
клинической практике нередко
используются наркотические
средства (морфин, к примеру],
которые могут вызвать нежелательный
побочный эффект. И пациент
рискует поневоле впасть в
наркотическое состояние.
Журнал «Chemistry and
Engineering News» A966, № 8)
сообщает о новом препарате —
циклоазоцине, который подавляет
действие таких наркотиков, как
морфин и героин. Настоящее имя
препарата довольно сложно —
2-циклопропилметип - 2'-окси-5,9 -
ди мети л-6,7-морфа н.
Новое лекарство было
испытано в клиниках на наркоманах,
которые пожелали избавиться от
вредной привычки.
НОВОСТИ ОТОВСЮДУ
как создавалось
„сердце" противогаза
Пятьдесят лет назад известный русский ученый
Николай Дмитриевич Зелинский предложил
использовать активированный уголь в качестве поглотителя
отравляющих газов, применявшихся кайзеровской
Германией против союзников во время первой
мировой войны; с тех пор противогаз Н. Д. Зелинского
был значительно усовершенствован, однако принцип
его действия практически не изменился.
О том, как создавалось «сердце» первого
русского противогаза, рассказал корреспонденту
«Химии и жизни» В. Батракову бывший сотрудник
Н. Д. Зелинского, ныне чпен-корреспондент АН СССР
А. П. Терентьев. Он же любезно разрешил
опубликовать уникальную фотографию Николая
Дмитриевича Зелинского, сделанную им в 1918 году.
Да, так вот, насчет этой фотографии. Она была
сделана в кабинете Николая Дмитриевича, тогда еще
профессора Московского университета. Зелинский
сидел тогда возле прибора для микроопределения
азота по Дюма. Это очень характерно для Николая
Дмитриевича — он пюбил работать руками и сам
делал много анализов. Помню, однажды обратился
к нему за помощью один пчеловод:
— Николай Дмитриевич,— говорит,— не
поможете пи мне узнать, как у пчел образуются белки!
В белках есть азот, а азот можно определить по
Дюма. Николай Дмитриевич взял целую пчелу,
положил ее в лодочку, засыпал окисью меди и, как
положено, провел сожжение. А прибор после этого не
разобрал, а оставил до следующего утра. На
следующий день смотрит он — в лодочке лежит медная
пчела. Самая настоящая такая пчела,— в лупу даже
все подробности было видно,— но только покрытая
медью. Впрочем, ничего в этом странного не было.
Судите сами: медь — окислитель, а пчела —
восстановитель. Пчела восстановила медь, и та покрыла ее
тонким слоем. Я работап вместе с Николаем
Дмитриевичем, рядом с его кабинетом в старом здании
Московского университета. Засиживались мы оба
допоздна; а когда устаешь, то хочется, что называется,
поболтать. Вот как-то поздно вечером, часов в
десять, зашеп я к кему и спрашиваю:
— Николай Дмитриевич, расскажите, как это вы
изобрели угопь для противогаза!
Он мне и рассказал эту историю. Вы знаете,
конечно, в шестнадцатом году немцы начали первые
газовые атаки. Тогда с фронта приезжало много
раненых, они всем рассказывали, какой это ужас. Надо
сказать, что в то время Николай Дмитриевич
работал в Петрограде, а не в Москве. Дело в том, что
в одиннадцатом году он ушеп из Московского
университета. Это была та самая история, когда царское
правительство ввело в университет полицию. Ректор
и оба проректора в знак протеста подали тогда в
отставку. А отставку взяли да и приняли. Тогда
преподаватели тоже стали уходить — каждый день
целые списки вывешивали, кто ушел. В их числе был
и Николай Дмитриевич. Бросил он свою школу,
переехал в Петроград и поступил на работу в
лабораторию Министерства финансов. А работа у него была —
очищать винно-водочные изделия. Но не чем-нибудь,
а активированным углем. Самым обычным
березовым углем. Вот это его и натолкнуло на мысль. Тогда
были химические противогазы — может быть, вы
видели их на картинках — мордочки такие. Но оки
почти не защищали от газов. Николай Дмитриевич
и подумал: если углем можно очищать водку, то
почему нельзя очищать воздух! Ведь хлор и фосген
должны тоже поглощаться! Взял он носовой ппаток,
насыпал на него угля и сделал такую простенькую
повязку. Потом в большом эксикаторе приготовил
хлор, приложил повязку к носу и стал дышать. И
оказалось, что хлор не действует! Оставалось только
сделать коробку. Для этого пригласили инженера
Куманта: поэтому те противогазы и стали называться
противогазами Куманта-Зелинского (Хотя непонятно,
почему не Зелинского-Куманта, ведь главным в них
был уголь.) Об этом противогазе сразу же
рассказали союзникам. Николай Дмитриевич показывал мне
протоколы — в них описывалось, как союзники
анализировали уголь. Подумайте, они не верили, что в
нем ничего больше нет! А потом были назначены
специальные испытания. Под Петроградом на одну
из станций пригнали несколько специальных вагонов.
Их наполнили хлором и по команде стали загонять
туда солдат в противогазах разных конструкций. По
условию солдаты должны были, не двигаясь,
пробыть в вагонах целый час. Прошло минут десять —
из вагона выскакивает один солдат — не может, зна-
30
читг больше терпеть. Николай Дмитриевич очень
волновался, сразу бросился к нему — посмотреть, чей
противогаз. Оказался — не его. Еще немного
времени прошло — еще один солдат выскакивает, и опять
в чужом противогазе. И еще, и еще... Вдруг смотрит
Николай Дмитриевич — и его противогаз не
выдержал. Бросился он к солдату, спрашивает, в чем дело.
А тот говорит,— глаза болят, сил нету. Николай
Дмитриевич заволновался, взял этот противогаз, на-
Профессор Московского университета Н. Д. Зелинский в
дел его сам — ив вагон. И правда, больно глазам.
Конкуренты сразу же обрадовались — вот, говорят,
пожалуйста, и у Зелинского тоже плохой противогаз.
А оказалось, что противогаз тут не при чем. Просто
стекло было плохо приклеено. Так в протоколе и
записали.
Да, кстати, вместе с солдатами в вагон вошел
препаратор Зелинского — Сергей Степанов. Так вот
прошел час, все уже вышли, а Степанов кричит из
вагона:
— Николай Дмитриевич, я еще могу!
Но больше-то было и не нужно. Другие
противогазы и этого не выдержали... Потом было еще одно
испытание: в том же вагоне солдаты должны были
всякие свои артикулы делать. Так тут только
противогаз Николая Дмитриевича и смог работать. На этих
испытаниях присутствовал царь — Николай П. Он
поблагодарил Зелинского и руку ему пожал. Да и толь-.
ко. Ничего за это Николай Дмитриевич не получил*
Впрочем, он всегда больше не для себя, а для сво-
й в своей лаборатории 24 апреля 1918 года
ей лаборатории старался. Вот, например, уже после
Революции пришли к нему с Дулевского
фарфорового завода за консультацией. Николай Дмитриевич
объяснил все, что было нужно. Спрашивают его
потом, а как вам заплатить! Николай Дмитриевич и
говорит:
— У нас в лаборатории нет фарфоровой посуды,
Сделайте нам ее, вот и вся плата.
Эту посуду дулевцы действительно сделали —
много посуды! — и мы очень долго потом с ней
работали...
31
от Vgo H20
В древности было известно
немного элементов. В основном
это были металлы. Их
называли полным именем, без всяких
символов.
Впрочем, понятие «элемент»
было тогда своеобразным. Так,
по Аристотелю, существует
лишь четыре элемента — огонь,
вода, земля и воздух, которые
в различных сочетаниях
образуют все вещества. Алхимики,
следовавшие учению
Аристотеля, обозначали эти элементы
так:
^ Воздух
Земля
V Вода
/\ Огонь
Отдавая дань цифровой
мистике (семь — счастливое число),
алхимики считали, что
существует только семь металлов.
Русский ученый, народоволец
Н. А. Морозов изложил эту
«теорию» в стихах.
Семь металлов создал свет,
По числу семи планет.
Дал нам космос на добро
Медь, железо, серебро,
Злато, олово, свинец...
Сын мой! Сера их отец!
И спеши, мой сын, узнать:
Всем им ртуть родная мать!
Для большинства металлов
алхимики использовали
астрономические символы,
характеризующие небесные светила.
(£ Серебро
\^J Золото
Q Ртуть
ии Олово
у Свинец
Qf Железо
Q Медь
Q Сурьма
X Мышьяк
Для сурьмы и мышьяка
сопоставлений со светилами не
делалось — может быть потому,
что долгое время они были
известны лишь в виде
соединений с серой.
Алхимики не делали
различия между простым веществом
и сложным, и сталь обозначали
тем же значком, что и железо.
В сочинениях алхимиков
часто попадаются символы не
только элементов, но и
соединений, сплавов, природных
веществ.
jfc Зола
.А. Бура
Т Известь
© Киноварь
у* Азотная кислота
Серная кислота
Царская водка
\U Селитра
j*1-^ Амальгама
\^ Винный спирт
V* Воск
н^1 Масло
V Мыло
Q Поваренная соль
^Х! Тальк
LpJ Винный камень
32
«-£-» Уксус
|T] Моча
Ш, Песок
Единой номенклатуры у
алхимиков не было, и некоторые
вещества получали по
несколько обозначений.
Если внимательно
рассмотреть алхимические символы, то
можно заметить между ними
некоторую связь. Например,
схожи значки воды и азотной
кислоты (aqua Fort is — «крепкая
вода»), воды и царской водки.
Квасцы, селитра и поваренная
соль тоже обозначаются
похожими рисунками.
Не только элементы и
химические вещества получили у
алхимиков символы.
Обозначения имели и многие предметы
алхимической лаборатории,
абстрактные и мистические
понятия. Иногда для них
использовались те же символы, что и
для некоторых веществ.
Jv\ ПеРегч>нный куб
JVp Водяная баня
\£5 Паровая баня
Т7* Тигель
^j Реторта
^2 Возгон
О Приемник
Г^ Бальзам
О Химия и Жизнь, № 9
Q2 Квинтэссенция
«Близнец» — сосуд
для нагревания
1807
Символика алхимиков была
в употреблении много веков, и
даже М. В. Ломоносов
пользовался ей. В его трудах мы еще
встречаем и обозначение
металлов символами небесных
светил, и некоторые другие
алхимические обозначения.
4Д Сера
Q£) Мышьяк
О Сурьма
"\д/г Висмут
У Поташ
Qj Квасцы
(jj Селитра
^3 Соль
ф Купорос
0|0
oio
о1о Уксус
о
ОО Масло
^О Спирт ректификат
\У Окалина и известь
1-Н Тигель
В начале XIX века делаются
первые попытки изображать
элементы более рационально.
Так, Джон Дальтон, профессор
Механического института в
Манчестере, в 1807 году
предложил новую химическую
символику. Вот примеры знаков
Дальтона:
(•) Водород
QJ Кислород
(J) Азот
@ Хлор
^Ь Углерод
^^ Фосфор
0 Сера
(^) Свинец
(Z) Цинк
(J) Железо
(Т) Олово
® Медь
Символы Дальтона
несколько напоминают значки
алхимиков — это еще рисунки, но здесь
есть и элементы современной
символики. В кружочке для
цинка стоит буква Z —
начальная буква слова «цинк» (Zinc),
в кружочке для железа стоит
буква ! (! гоп — по-английски
железо), для свинца — буква L
(Lead), для меди — С (Copper),
зз
\
для олова — Т (Tin). Правда,
большинство металлоидов
получили у Дальтона
обозначения, не связанные с алфавитом.
Особая заслуга Дальтона в
том, что он изображает своими
символами химические
соединения, хотя и без учета
валентности. Он полагал, что вода
состоит из 1 атома водорода и 1
атома кислорода, а аммиак —
из 1 атома водорода и 1 атома
азота. Вот как выглядят по
Дальтону некоторые
соединения:
©О Вода
0Ф Аммиак
®Ф Сульфид железа
©О Окись железа
©О Окись свинца
j
©Ф Сульфид меди
В 1814 году шведский химик
Е. Берцелиус предложил
значительно более простую и
удобную систему химических
символов. Берцелиус, как и
Дальтон, каждому элементу дал свой
символ, но не графический, а
буквенный. Каждый знак — это
сокращенное латинское
название элемента. Такие
обозначения элементов легко
запомнить, и они стали
международными.
Эту символику не надо
пояснять рисунком. Каждый
школьник знает ее — мы пользуемся
этими символами и поныне.
Дальтон до самой смерти
был противником системы Бер-
целиуса. В 1837 году он писал:
«Знаки Берцелиуса ужасны.
Они представляются хаосом
атомов... Ничто меня не
удивляет больше, чем то, что такая
система знаков получила
распространение...»
В России первое сообщение
о символах Берцелиуса сделал
московский врач И. Я. Зацепин.
В журнале «Новый магазин
естественной истории, физики,
химии и сведений
экономических» он поместил сообщение
под названием «О Берцелиевых.
законах химического сродства*
A824 г., ч. 2, стр. 85—103).
В 1819 году Берцелиус ввел
символы для органических
кислот. Кислоту он обозначал
первой буквой ее латинского
названия с черточкой наверху:
лимонная кислота — С (acidum
citricum), уксусная — A (acidum
aceticum). Берцелиус предложил
также символы для алкалоидов,
отмечая их сверху значком
« 4-»: М — морфин, В г — бру-
цин.
Эти сокращения уже в
середине прошлого века вышли
из употребления.
Все элементы, которые были
открыты после Берцелиуса,
получили символы из латинских
букв — вплоть до Lr — лоурен-
сия, элемента № 103. А скоро мы
узнаем и символ элемента
№ Ю4 — курчатовия.
Кандидат химических наук
Е. И. ГУРОВИЧ
' Рисунки Л. КУЛАГИНА
\1966£
*але^
/18961
%
как была открыта
РАДИОАКТИВНОСТЬ
С. ВЛАДИМИРОВ
В 1896 г. французский 1 физик
А при Беккерель в возрасте
44 лет открыл явление радио-
активвости.
Теперь атомная физика
представляется нам цельным
зданием, каждый этаж
которого возведен по заранее
намеченному плану — так стройно,
последовательно
выстраиваются исследования нескольких
поколений ученых, изучавших
строение и свойства атомного
ядра.
Но в первые годы после
открытия Беккереля в умах
естествоиспытателей царило
смятение. Только за год до открытия
радиоактивности немецкий
исследователь Вильгельм Конрад
Рентген обнаружил невидимые
лучи, проникающие сквозь
плотные тела. Это было
крупным научным событием. О
природе рентгеновых лучей
высказывались разные
предположения. Французский математик
34
Апри Пуанкаре выдвинул
гипотезу, говорящую, что
испускание лучей Рентгена связано с
флюоресценцией стекла в
трубке Крукса. Лнри Беккерель
занялся проверкой этой идеи.
И пришел к неожиданным
результатам...
Произошло это так. У Беккс-
реля хранилась собранная еще
его отцом большая коллекция
флюоресцирующих веществ.
Среди них — и урановая соль.
Ее-то Беккерель взял для
опыта. Сначала он держал урановую
соль на ярком солнечном свете,
затем подносил к ней
фотографическую пластинку,
завернутую в черную бумагу. Если при
флюоресценции кроме лучей
обычного света выделяются и
невидимые лучи, то для них,
как и для лучей Рентгена,
бумага будет прозрачна. Если
пластинка при проявлении
останется светлой, рассуждал
Беккерель, значит, невидимых лучей
нет, и Пуанкаре ошибочно
связал х-лучи Рентгена с
флюоресценцией.
Пластинка почернела. Бек -
керель был готов заявить о
подтверждении гипотезы
математика, но, повторив опыт,
заметил, что вблизи урановой
соли пластинка чернеет даже в
том случае, если уран хранился
в полной темноте и не
подвергался освещению. Значит,
урановая соль выделяла какие-то
другие лучи... Так Беккерель
задал физикам и химикам
новую загадку.
Даже ученые, имена
которых навеки вписаны в историю
1зучения радиоактивности, не
•разу освоились с представле-
шем, что атомы могут само-
[роизвольно распадаться, выде-
шя при этом огромное количе-
тво энергии; начались споры.
Прежде всего надо обнару-
сить источник энергии. Может
ыть, радиоактивные вещества
*
заимствуют ее из воздуха?
Например, они могут улавливать
из воздуха молекулы,
движущиеся с огромной скоростью, и
излучать энергию захваченных
молекул в виде коротких
лучей, — так рассуждал о
природе радиоактивности
английский физик и химик Уильям
Крукс.
Крупнейший французский
ученый Пьер Кюри, вместе со
своей женой Марией Склодов-
ской-Кюри открывший в
урановой руде новый элемент
радий, думал так: «Существует
некоторый род лучей, не
доступных нашим чувствам;
радий способен поглощать часть
этих лучей и превращать их в
энергию радиоактивных тел».
Кюри считал, что
радиоактивность все-таки можно
объяснить флюоресценцией; она
вызывалась, по его мнению,
какими-то невидимыми, не
доступными наблюдению лучами,
пронизывающими весь мир.
Немецкий химик Август
Нернст предложил еще одну
теорию. Существуют
спаренные электрические частицы, —
утверждал он, — которые
состоят из положительно и
отрицательно заряженных
электронов. Эти частицы невесомы,
они заполняют все
пространство. Попадая в атомы радия,
частицы расщепляются. При этом
из радия вылетают электроны
и выделяется тепло.
Русский естествоиспытатель
професор Н. Умов сравнил
атомы радия с крохотными
светилами: Солнце,— говорил он, —
обладает запасом энергии,
благодаря которому оно светит
миллиарды лет*; в атомах
радиоактивных веществ запасена
энергия, питающая их
излучение тысячи лет.
Свою гипотезу о природе
радиоактивности предложил и
знаменитый английский физик
лорд Кельвин. Вот как
излагалась его гипотеза в
журнале «Вопросы физики» в
1908 г.: «...Пушка заряжается и
разряжается, но из этого не
следует, что ее состав или
устройство изменились. Все дело
сводится к более или менее
значительной перестройке частей.
Так точно и в радии атом то
разряжается, то есть
выбрасывает электрон, то снова
заряжается. Но состав его остается
неизменным: никакой
эволюции материи не происходит».
Были и другие гипотезы,
объясняющие явление
радиоактивности. Лишь постепенно
вырисовывалась действительная
картина: Беккерель первым
обнаружил распад атомов,
сопровождающийся возникновением
новых элементов с появлением
излучений.
Дальнейшие события
известны. После открытия Беккере-
ля в разных странах мира
физиками и химиками были
сделаны важнейшие исследования
атомного ядра. Была
установлена сложная природа
радиоизлучения, открыты альфа-,
бета- и гамма-лучи, радий и
целое семейство радиоактивных
элементов; альфа-лучи были
использованы для изучения
строения, а затем и для
расщепления атомов; наконец,
была раскрыта тайна управления
внутриядерной энергией.
Новые факты привели к
появлению новых теорий. Но
нельзя думать, что ошибочные
гипотезы не имели никакого
значения для развития науки.
Только убедившись в
бесплодности старых научных
представлений для объяснения
радиоактивности, ученые
приступили к созданию новых,
казавшихся вначале невероятными,,
опрокидывавшими многие
утвердившиеся понятия. В
естествознании началась
революция, послужившая истоком
наших знаний о природе.
35
ПОГОНЯ ЗА НЕЙТРИНО
Ж. ЛЕВИ-ЛЕБЛОН
Нейтрино, одна из самых замечательных и
распространенных во Вселенной элементарных частиц,
очень похожа на частицы света — фотоны. Но если
свет, играющий в нашей жизни колоссальную роль,
можно видеть и глазом и приборами, то для
нейтринного «света» мы сейчас абсолютно слепы. А если
бы прозрели, то смогли бы беспрепятственно
разглядывать глубины Земли, Солнца и даже далекие
области Вселенной. За последние четыре года в
разных странах были проведены эксперименты, ставшие
первым шагом к овладению нейтринным «зрением».
По сложности и масштабам (первая группа опытов
велась на самых мощных ускорителях, а вторая —
на дне самых глубоких в мире шахт) эти
исследования занимают особое место в современной ядерной
физике*. Эксперименты такого рода готовятся и в
Советском Союзе; наши ученые внесли
выдающийся вклад в разработку теоретических проблем
нейтринной физики.
Q необычных свойствах нейтрино, об истории
изучения этой частицы рассказал недавно в журнале
«Science Progres la Nature» французский физик
Ж. Леви-Леблон. Мы печатаем реферат его статьи,
сделанный В. И. Манько.
Большая и непрерывно пополняющаяся
семья частиц, называемых элементарными,
включает «личности» с крайне разными
характерами. Некоторые из них — такие, как
нуклоны или к -мезоны, не упустят случая
выставить себя напоказ, реагируя
практически со всем, что встречается на их пути.
Другие, наоборот, бесконечно скромны и
незаметны. К ним как раз и относится
нейтрино, о котором пойдет дальше речь. Эта
частица, которую называют иногда «прохо-
дя-щей сквозь стены», могла бы
беспрепятственно пересечь свинцовую плиту
толщиной в 50 световых лет, но во всей В.селенной
не найти твердого тела подобных размеров.
Эта частица почти неуловима и в
течение почти двадцати лет была лишь чисто
теоретической величиной, призраком,
измучившим ученых-физиков. Однако им все же
удалось заставить его себя обнаружить.
ЗАГАДКА ^-РАДИОАКТИВНОСТИ
Чтобы хорошо понять историю открытия
нейтрино, вспомним далекие события,
положившие начало всей ядерной физике.
В 1896 г. А. Беккерель обнаружил
казавшееся необычайно странным явление: какие-то
таинственные лучи, испускавшиеся солями
урана, сообщали воздуху
электропроводность и засвечивали фотопластинку,
обернутую черной бумагой. Лучи испускались
урановыми солями в любых условиях, вне
зависимости от давления воздуха и
температуры. Еще через два года Пьеру Кюри и
Марии Склодовской-Кюри удалось выделить
из урановой руды гораздо более сильные
источники тех же лучей — новые химические
элементы радий и полоний. Эти элементы
(а вслед за ними — и другие с такими же
свойствами} были названы радиоактивными.
Довольно быстро было установлено, что
встречаются радиоактивные излучения трех
видов: а (альфа), Р (бета) и у (гамма).
Альфа-лучи— это атомные ядра самого легкого
благородного газа — гелия (ядра гелия
называют также а-частицами); бета-излучение
состоит из обычных электронов или из их
античастиц — позитронов; а
гамма-излучение— это просто частицы света, фотоны,
только очень энергичные. Все три вида
лучей были подвергнуты детальному
исследованию. И тут оказалось, что ^-излучению
свойственны некоторые странности.
Известно, что когда ядро урана теряет
ос -частицу (ядро гелия), то оно
превращается в ядро другого элемента — тория:
ipse _^ TV34 |_не4.
Ядра гелия и тория разлетаются, как
проверено экспериментально, в противоположных
направлениях — в соответствии с законом
сохранения количества движения. Этот
распад ядра урана на две части полностью
идентичен вылету снаряда из пушки: снаряд
(ядро гелия) улетает, а пушка (ядро тория)
откатывается назад. Обратим внимание —
именно назад, а не вбок! Казалось бы, так
же должен выглядеть и р-распад, например,
радиоактивного изотопа меди Си64:
Си64-> Ni64 + e+
медь никель позитрон
36
Тонкие и сложные эксперименты (их
сложность прежде всего заключалась в том,
что разница в массах ядер и позитронов
очень велика: ядро никеля, например, в
1 СО 000 раз тяжелее позитрона) показали —
в случае р-распада ядра отскакивают в
основном именно вбок.
Кроме того, если при распаде урана все
ядра гелия имели одну, строго
фиксированную энергию, то позитроны при распаде
меди наделены самыми разными энергиями —
от нулевой до некоторой максимальной.
Причем именно эту максимальную энергию
должны были бы иметь по элементарному
расчету, основанному на законе сохранения
энергии, все позитроны. Получалось, что в
ходе эксперимента часть энергии куда-то
исчезала: ядра никеля и позитроны имели в
сумме меньше энергии, чем ее было
вначале у ядер меди.
Такие странности обнаруживали £-лучи,
испускаемые любыми радиоактивными
источниками.
Сначала физики не особенно
тревожились, считая, что часть энергии теряется при
столкновении 3-лучей с атомами
окружающей среды. Но если это так, то вблизи
источника излучения должна была бы
повышаться температура, а точные
колориметрические измерения показали, что тепла
выделяется недостаточно, чтобы можно было
объяснить наблюдаемый эффект. Тогда
предположили, что в распаде участвует
третья частица — фотон, который и уносит
недостающую энергию. Но фотон был бы
заметен, а его, сколько ни искали, так и не
обнаружили. В отчаянии стали сомневаться
в самом законе сохранения энергии! Но это
было уже настоящим святотатством, и
физики почувствовали, что почва колеблется
у них под ногами. Ни один из случаев альфа-
или гамма-радиоактивности таких
сюрпризов ученым не преподносил.
«ИЗОБРЕТЕНИЕ» НЕЙТРИНО
Вот тут-то в 1931 г. швейцарский физик
В. Паули и предложил решить все
наблюдаемые парадоксы, приняв, что недостающую
энергию уносит какая-то неизвестная
частица, которая в эксперименте просто не была
замечена. В этом случае было понятно,
почему ядра никеля отскакивают под углом к
направлению полета позитрона и почему
сами позитроны имеют неодинаковую
энергию. Действительно, при распаде ядра на
три частицы энергия может неравномерно
распределяться между продуктами распада,
а направление их вылета тоже может быть
разным. Гипотетическую частицу быстро
окрестили «нейтрино», так как она
обязательно должна была быть нейтральной,
чтобы в реакции, как это и наблюдалось,
сохранялся электрический заряд. Точные
измерения энергии продуктов р-распада
показали, что масса нейтрино, как и масса фотона,
равна нулю, но от частицы света нейтрино
отличается спином — величиной,
определяющей некоторое внутреннее свойство
частиц, от которого зависит, в частности, их
взаимодействие с магнитным полем: у
фотона он равен единице, а у нейтрино—'/г-
Но главная отличительная черта новой
частицы заключалась в том, как она
взаимодействует с другими обитателями
микромира.
Хорошо известно, что в микромире
действуют три рода сил или взаимодействий:
сильные, управляющие я-распадами;
электромагнитные, вызывающие у
-радиоактивность и слабые, отвечающие как раз за
Р -распады. Реакции, обусловленные
сильными и электромагнитными
взаимодействиями, протекают во много раз быстрее тех,
которые вызваны слабыми силами.
Например, гамма-радиоактивное ядро живет
всего 10 16 секунд, а бета-распад нейтрона на
протон и электрон продолжается целых
10 минут. Так вот, для нейтрино оказалось
характерным то, что оно не участвует ни
в сильных, ни в электромагнитных
взаимодействиях, а проявляет себя только в
слабых. Именно потому эта частица
совершенно свободно проникает сквозь любые
преграды, просто не успевая прореагировать
со встречными атомами. Десять тысяч
миллиардов раз может пройти нейтрино через
ядро свинца и только в одном случае
оставит след, вызвав ядерную реакцию. Мы уже
говорили, что понадобилась бы броня
свинца, толщиной в десятки световых лет, чтобы
остановить поток этих частиц. Сквозь тело
каждого из нас в течение жизни проходят
десятки тысяч миллиардов нейтрино
солнечного происхождения, и мы этого
совершенно не замечаем.
Слабость взаимодействия нейтрино с
веществом делает вещество практически
прозрачным для него. Легко понять, как трудно
непосредственно обнаружить нейтрино —
37
ведь для этого нужно обязательно
наблюдать реакцию, вызванную им! Поэтому
казалось, что гипотеза Паули практически не
поддается прямой экспериментальной
проверке. Однако уже спустя год Э. Ферми
удалось объяснить, исходя из свойств
гипотетического нейтрино, многие
закономерности, наблюдающиеся в экспериментах при
Р -радиоактивности, а главное, была
выведена формула, по которой совершенно точно
рассчитывались энергии позитронов или
электронов в любом р-распаде.
Наконец, появилась еще одна интересная
идея. Как мы знаем, в микромире наряду
с частицами существуют и их античастицы.
Почему же было не предположить, что есть
античастица и у нейтрино? Это антинейтрино
могло встречаться в тех случаях Ь-распада,
при которых из радиоактивного ядра
вылетает не позитрон, а его античастица —
электрон. Например:
и -*• р е~ "v
нейтрон протон электрон антинейтрино
А если все сказанное верно, то физикам все
равно было, что искать: реакцию,
вызванную нейтрино или антинейтрино. И та, и
другая в одинаковой мере служила бы прямым
подтверждением существования этой
загадочной частицы.
ЭКСПЕРИМЕНТ ГОВОРИТ: ДА
Из всех трудновоспроизводимых и
редких реакций, вызываемых нейтрино или
антинейтрино, самой подходящей для
наблюдения оказалась реакция соединения
антинейтрино с протоном с последующим
распадом на нейтрон и позитрон:
р \ - > II е~"
(Формула этой реакции легко выводится из
уравнения Р -распада нейтрона, о котором
мы только что говорили). Уже примерно лет
двадцать физики располагают достаточно
мощными источниками антинейтрино, так
как в «начинке» ядерных реакторов очень
важную роль играют именно нейтроны,
которые, как мы уже видели, испускают при
распаде потоки антинейтрино.
Остановив выбор на какой-то реакции,
нужно было решить не менее важную
задачу— как будут детектированы, то есть
пойманы и опознаны конечные продукты этой
реакции — нейтрон и позитрон. И эта
проблема была решена. Позитрон выдает себя
Т-излучением, которое возникает при
неизбежной аннигиляции этой частицы с первым
же встречным электроном. Что же касается
нейтронов, то решено было использовать
свойство кадмия жадно поглощать их с
одновременным испусканием фотонов.
Обнаружить гамма-кванты сравнительно
нетрудно: эти лучи вызывают в особых
жидкостях, называемых сцинтилляционными,
вспышки видимого света, которые
фиксируются специальными приборами —
фотоумножителями. Сложность заключается только
в том, что необходимо отличать вспышки,
вызываемые реакцией соединения протонов
с антинейтрино, от вспышек, вызванных
иными причинами. Поэтому понадобилось
защищать приборы от всех других частиц,
которые могли присутствовать в окружающей
среде — в так называемом фоне. Лишь в
1956 году американским физикам Ф.
Райнису и С. Коуну удался этот ювелирный
эксперимент. Через двадцать пять лет после того,
как Паули «изобрел» нейтрино, эта частица
обрела, наконец, осязаемую реальность.
...И ДРУГИЕ ЧАСТИЦЫ
Период между 1950 и 1960 годами
оказался весьма «урожайным» для физики
элементарных частиц. В это десятилетие было
открыто много новых обитателей
микромира. Но все вновь открытые частицы
оказались нестабильными. В некоторых случаях их
распад сопровождался испусканием
электрона и демонстрировал тот же кажущийся
парадокс — исчезающую энергию, которой
прославилась р -радиоактивность атомных
ядер. Естественно, это наводило на мысль,
что в таких реакциях может быть замешано
нейтрино. К ^-распаду нейтрона оказались
очень близки реакции распада А- и
^-гиперонов, и их результат представлялся
физикам так:
Л -•> |) е- v
2+ ->ЛП -| е>- v.
гс- и К-мезоны могут дать:
К > к'1 е" v.
Фигурирующие в этих реакциях нейтрино
имеют чисто гипотетический характер,
прямо их еще никто не наблюдал, так как
получить достаточно интенсивные пучки частиц
А, Е или К пока невозможно. Впрочем,
дальше мы увидим, что некоторые нейтрино,
38
«спускаемые в реакциях этого типа, все-таки
были обнаружены.
ДВА ТИПА НЕЙТРИНО
Для исследований, о которых пойдет
теперь речь, наиболее важным оказался факт
существования частицы, пока нами не
упомянутой. Это мюон р., примерно в 100 раз
более тяжелый, чем электрон. Раньше его
смешивали с я -мезоном, отсюда и
происходит еще употребляющееся название мю-
мезон. Между тем, это наименование
глубоко ошибочно, так как мюон не участвует в
сильных взаимодействиях и ничем не похож
на --мезон. С другой стороны, ничто, за
исключением массы, не отличает его от
электрона. Как и электрон, мюон
подчиняется только слабым и электромагнитным
взаимодействиям. Это настоящий тяжелый
электрон. Он появляется в тех же реакциях, что
и обычный электрон, если для его рождения
достаточно энергии. Например, наблюдают
такой процесс, обусловленный слабыми
силами:
т.~ — > \ь~ v
Пи-мезон мюон антинейтрино
Давайте сравним эту реакцию с
процессом ^-распада нейтрона, вызванного теми
же слабыми силами:
п —> р -j e -! v.
Здесь антинейтрино ( v) образуется вместе
с электроном. В случае же распада
"-мезона антинейтрино находится в паре с мюоном.
Этот снимок
фиксирует
процесс
распада
л-мезона
Сравнение этих двух весьма сходных
процессов наводит на интересную мысль.
Мюон, как известно, называют тяжелым
электроном, но все же мюон и электрон —
частицы разные. Не может ли быть так, что и те
«ейтрино, которые возникают в паре с
мюоном, тоже не совсем идентичны нейтрино,
образующимся в паре с электроном? Иными
словами, может быть, в природе существует
не один сорт нейтрино и антинейтрино, а
два?
Сама постановка этого вопроса казалась
сначала странной, так как в течение многих
лет у всех нейтрино, которые удалось
наблюдать, отмечались одинаковые спины,
нулевая масса, неизменное отсутствие
электрического заряда, наконец, участие только
в слабых взаимодействиях. Что же все-таки
могло отличать один тип нейтрино от
другого, если допустить существование обоих?
Предположили, что существует какой-то
особый заряд, который назвали мюонным,
так как им обладает мюон — в отличие от
электрона, который его лишен. Мюонный
заряд, подобно электрическому,
сохраняется во всех реакциях (иными словами,
суммарный заряд частиц до реакции равен
суммарному заряду продуктов реакции).
Гипотезу о существовании двух типов
нейтрино, отличающихся мюонным зарядом,
одними из первых выдвинули советские
ученые академики М. А. Марков и Б. М.
Понтекорво. Прямая проверка этой гипотезы
заключалась бы в следующем.
Предположим, у нас есть чистый пучок нейтрино, и
мы точно знаем, что все частицы родились
в паре с мюоном. Подставим под этот пучок
какую-либо мишень, в которой могут
происходить реакции мюонного нейтрино с
нейтроном такого типа:
мюонное
нейтрино
|%|
мюон же
нейтрино
нейтрон протон мюон
п -* Р -+- е~
нейтрон протон электрон
Одинаково ли вероятны обе реакции?
Ответ на этот вопрос и будет проверкой
гипотезы. И вот почему. Если мюонный заряд
в природе существует, то первая реакция
разрешена, так как в ней заряд слева равен
заряду справа. Вторая же реакция будет
запрещена, так как слева заряд в ней есть, а
справа его нет. (В формулах присутствие или
отсутствие зарядов не отмечено.) Значит,
если в продуктах реакции будут
обнаружены электроны — гипотеза неверна, и
наоборот, отсутствие электронов докажет
правоту ученых.
Схема проверки была ясна. Оставалось
только найти подходящие источники
нейтрино.
39
Ф|*Ц4
■iH^iibh "ii
\r\\ ИНН
it |ЫЬш
hiin -I
В искровой камере легко
отличить электрон от мюона. На
этой фотографии
многочисленные вспышки и протяженная
траектория отмечают путь
электрона, входящего в
камеру справа (сравните с нижним
снимком)
На этом снимке
зафиксирована траектория мюона,
входящего в искровую камеру
слева. Она чиста и четко
выражена, в отличие от следов,
оставленных электроном на верхнем
снимке
В 1960 году Т. Ли и Ч. Янг заметили, что
самые мощные в мире ускорители в Брук-
хейвене (США) и Церне (Швейцария)
позволяют получить пучки нейтрино такой
интенсивности, что их можно детектировать
(В 1967 г. под Серпуховом вступит в строй
протонный ускоритель на 70 миллиардов
электрон-вольт, который будет самым
мощным в мире. На нем, в частности,
планируется провести и опыты с нейтрино.— Ред.).
Эксперименты, поставленные для проверки
новой гипотезы, должны были быть
чрезвычайно тонкими. Требовалось получить
возможно более интенсивный и узкий пучок
т:-мезонов, затем устранить из него те
частицы, которые не успели распасться, и
только при этом условии исследователи могли
располагать чистым пучком нейтрино.
Условия опыта делали необходимой особую
защиту приборов, защиту, которую могли
преодолеть только нейтрино. Нужен был и
•детектор, который позволил бы с полной
уверенностью отличать ядерные реакции с
участием нейтрино от фоновых реакций,
вызванных, например, космическими лучами...
Первый эксперимент такого типа был
поставлен в 1962 году в Брукхейвене. Чтобы
дать представление о его масштабах,
скажем, что искровая камера, в которой шла
реакция, была защищена от всех частиц.
40
кроме нейтрино, броней из стали толщиной
13,5 метров. В ходе эксперимента камеру
пересекли почти 100000 миллиардов
нейтрино и громадное большинство из них не
оставило вообще никакого следа. Приборы
зарегистрировали только 5 000 ядерных реакций.
И большая их часть оказалась неинтересной,
вызванной фоновыми событиями. После
скрупулезного исследования полученных
снимков экспериментаторы оставили всего
50 более или менее интересных
фотографий. И все они, за исключением одного или
двух снимков, интерпретация которых была
сомнительна, показали следы мюонов,
рожденных нейтрино, и не обнаружили никаких
следов электрона. Выводы были ясными: в
природе существует действительно два типа
нейтрино!
Эксперимент того же типа, только более
усовершенствованный и точный, был
проведен затем и в Церне. Он полностью
подтвердил полученные результаты и принес
другие драгоценные сведения для физики
слабых взаимодействий. Было уточнено, в
частности, что если нейтрино ve, связанное
с электроном, имеет нулевую массу, то
сведения о массе мюонного нейтрино v^
(иногда называемого нейтретто) далеко
не точны: известно только, что она меньше
пяти электронных масс.
НА ПУТИ К НЕЙТРИННОМУ
ЗРЕНИЮ
Нейтрино, которые исследовались в
экспериментах, — искусственного
происхождения. Однако сама природа производит эти
частицы в невиданных масштабах.
Громадное число вторичных нейтрино присутствует,
например, в космических лучах, которые
постоянно бомбардируют Землю. Мощные
потоки мюонных нейтрино рождаются при
распаде в земной атмосфере вторичных
^-мезонов. Чтобы напасть на следы этих потоков,
нужна колоссальная защита, способная
задержать все другие частицы. Самый
простой вариант — спуститься для наблюдений
в глубокую шахту и использовать несколько
тысяч метров скальной породы над головой
как естественную защиту от помех. Среди
множества нейтрино, ежесекундно
пронизывающих землю, какое-то малое число
прореагирует с протоном встречного ядра,
рождая мюон, согласно уже описанной
реакции. Попытки «поймать» нейтрино из
космоса и сводятся, в конце концов, к
регистрации именно этих мюонов с помощью
сложного ансамбля счетчиков,
расположенных на дне шахты. Чем большую площадь
охватывают счетчики, тем больше шансов
обнаружить нейтрино.
Теорию экспериментов с космическими
нейтрино разработали еще в 50-х годах
академик М. А. Марков и его сотрудники.
А совсем недавно такие эксперименты были
проведены на самых глубоких в мире
шахтах на территории Южной Африки и Индии.
(Аналогичные эксперименты готовятся и в
СССР. — Ред.).
В первом случае детектор счетчиков
покрывал поверхность в 175 м2 и примерно за
сто дней зарегистрировал 7 ядерных
реакций, которые недвусмысленно можно
интерпретировать как прохождение мюона,
рожденного нейтрино.
Помимо вторичных нейтрино,
космические лучи несут с собой (в пропорции
слишком малой, чтобы их детектировать в
настоящее время) нейтрино внеземного
происхождения. Известно, что энергия звезд
рождается в сложных циклах ядерных
реакций. Среди них фигурируют различные типы
$ -распада и другие слабые реакции, в
процессе которых появляются нейтрино. При
этом звезды теряют часть своей энергии в
виде «нейтринного дыма», вырывающегося
из этих исполинских ядерных печей.
Считается, например, что нейтрино, рожденные
Солнцем, уносят несколько процентов
энергии нашего светила. А остальная ее часть
испускается в хорошо известных нам
формах— фотонов и другого
электромагнитного излучения. Объем любого вещества на
Земле, равный объему коробки спичек,
каждый момент пронизывается примерно
двадцатью нейтрино солнечного
происхождения.
Астрофизики проявляют в последнее
время все больший интерес к нейтрино: они
предполагают, что это излучение становится
чрезвычайно важным на некоторых стадиях
звездной эволюции и составляет один из
критических факторов, приводящих к таким
гигантским катаклизмам, как взрыв
сверхновых звезд. Не исключается также
возможность, что большая часть полной энергии
Вселенной приходится на кинетическую
энергию невидимого, но присутствующего
повсюду нейтринного газа. Интересно, что
советский ученый академик Я. Б. Зельдович
предложил модель возникновения Вселен-
41
ной, в которой главную роль играют
нейтрино.
По сегодняшний день мы исследуем
Вселенную с помощью телескопов и
радиотелескопов. Но сколько ни усовершенствуй эти
приборы, они могут дать информацию лишь
о тех явлениях, которые происходят в
тонких поверхностных слоях звезд, так как
фотоны из более глубоких областей этих
объектов Вселенной не доходят даже до их
поверхности, и с сегодняшней техникой мы
никогда не сможем увидеть эти глубинные
процессы, даже разместив приборы на
высочайших горных вершинах или на Луне.
Прогресс в детектировании нейтрино из
космоса открывает новые захватывающие
возможности в этом направлении. Ведь
потоки этих частиц доходят к нам без помех
из всех уголков Вселенной, из любых глубин
звезд — надо только уметь «увидеть» этих
космических посланцев. Нейтринная
астрофизика возьмет на вооружение не те
телескопы, которые мы стремимся поднять все
выше и выше, а приборы, которые нужно
опускать как можно глубже в землю. По
существу, детектор, использованный в шахтах
Африки и Индии и есть очень примитивный
нейтринный телескоп будущего. Так
проявляется связь физики бесконечно малого И
бесконечно большого, которая уже сама па
себе подчеркивает важность изучения
неосязаемого нейтрино.
НАШ КОММЕНТАРИИ
Статья французского физика
Ж. Леви-Лебпона посвящена
одной из наиболее загадочных
элементарных (точнее их называть
фундаментальными) частиц. Сама
история теоретического
«изобретения» и экспериментального
открытия этой частицы, ласково
названной физиками «нейтрино»
(по-русски это звучало бы
примерно как «нейтральненькая»|г
похожа на увлекательный
детектив, и с ней интересно
познакомиться всем, кого интересует,
какими путями приходит
человеческая мысль к пониманию явлений,
стоящих далеко вне границ
нашего обычного, повседневного
опыта и находящихся на пределе
возможностей современной науки.
Нейтрино играет заметную
роль не только в элементарных
процессах взаимодействий и
взаимных превращений
фундаментальных частиц и атомных ядерг
но и в сложнейших, мапо
изученных процессах, протекающих в
звездах и в межзвездном
пространстве. Наконец, невероятная
способность нейтрино
беспрепятственно проходить через любые
преграды, непроницаемые дпя
всех остальных частиц, супит им
в будущем роль важнейшего
инструмента дпя исследования
небесных теп и глубин Космоса.
Статья Леви-Лебпона написана
живог увлекательно и
основательно; но, конечно, популярная
статья, к тому же ограниченного
объема, не может охватить всех
вопросов, относящихся к физике
нейтрино. Стараясь не выходить
из круга вопросов и понятий,
затронутых в статье, ограничимся
несколькими комментариями к
ней.
Современному читателю,
слышавшему о том, что
элементарных частиц не меньше, а, может
быть, даже и больше, чем
химических элементов, трудно
представить себе всю смелость
гипотезы Паули, объяснившего в
конце 1930 года загадку
бета-распада ядер существованием новой,
дотоле неизвестной и неуловимой
частицы. Только став на точку
зрения физиков тех пет, поняв, что
тогда быпо известно, а что — нет,
какие тогда господствовали идеи,
можно в полной мере оценить
фантазию этого выдающегося
теоретика. Во-первых, знания о
строении и свойствах ядер были в то
время крайне скудными. Только в
1932 году бып открыт нейтрон и
к 1933 году разработано
представление о том, что ядра состоят из
протонов и нейтронов. Во-вторых,
не быпо известно, что существует
максимальная энергия
бета-электронов. И наконец, популярной и
авторитетной была радикальная
гипотеза знаменитого Нипьса Бора
о нарушении закона сохранения
энергии в отдельных актах бета-
распада ядер (закон сохранения
энергии при этом должен бып
выполняться лишь в среднем, для
большого числа актов). Вот тогда
и появилась гипотеза Паули. Она
смогла вытеснить гипотезу Бора
только поспе экспериментального
опредепення максимальной
энергии бета-эпектрона и
установления протонно-нейтронной
структуры ядра.
Важнейшей характеристикой
пюбой фундаментальной частицы
служит ее масса. Уже в 1933 г.
французский физик Ф. Перрен,
исследуя распределение энергии
бета-электронов, показал, что
масса нейтрино очень мапа или
равна нулю, о чем и пишет Леви-
Лебпон. С теоретической точки
зрени я считать массу нейтрино
строго равной нулю очень
привлекательно, однако, до сих пор
прямого экспериментального
подтверждения этой гипотезы нет.
Сейчас можно утверждать только
одно с достаточной
уверенностью: масса нейтрино не
превышает 1/2500 массы электрона.
В статье Леви-Лебпона
несколько неточно рассказана
интереснейшая история открытия мю-
онкого нейтрино. Трудно
согласиться с утверждением автора,
что постановка вопроса о мюон-
ном нейтрино сначала казалась
странной. Напротив, это
представлялось самым вероятным. Сразу
поспе открытия мюона (в конце
тридцатых годов) быпо введено
42
второе нейтрино, появляющееся
в результате распада мюона.
Тогда же эта частица была названа
нейтретто. Но так как не
было ясно, чем именно отличается
нейтретто от нейтрино, физики-
теоретики постепенно склонялись
к мысли, что существует один-
едннственный тип нейтрино, т. е.
что нейтрино, возникающие в
различных реакциях, тождественны.
Впоследствии это предположение
приобрело силу предрассудка, так
чтог когда в конце пятидесятых
годов три теоретика (советский
физик М. А. Марков, японский физик
К. Нишиджима и американский
физик Ю. Швингер) вновь
вернулись к идее о двух разных
нейтрино, то их работы были
встречены без всякого энтузиазма.
Первоначально они исходили из
чисто теоретической возможности
существования двух нейтрино,
однако, позже выяснилось, что
существуют довольно веские
экспериментальные основания для
введения понятия мюонного заряда
и двух типов нейтрино. Тогда-то
известный советский физик
новости отовсюду т
УДОБРЕНИЯ
ХВАТАЕТ НАДОЛГО
Государственный
научно-исследовательский и проектный
институт азотной промышленности
разрабатывает технологию
промышленного производства медленно
действующих мочевино-формаль-
дегидных удобрений (МФУ|.
Такие удобрения уже испытаны на
сероземных и луговых почвах под
хлопчатник. Разового внесения
годовой нормы МФУ пока еще
недостаточно: его эффективность
оказывается меньше, чем при
обычном неоднократном внесении
аммиачной селитры и мочевины.
Но если внести при посеве в
виде МФУ основную часть годовой
нормы азота A00 кг на гектар| и
провести лишь одну подкормку
.мочевиной или аммиачной
селитрой в период цветения или
бутонизации (из расчета 50 кг азота на
гектар), то урожай хлопка-сырца
получается выше, чем обычный, а
созревание хлопка ускоряется на
2 недели. Таким образом,
применение МФУ позволяет исключить
Б. М. Понтекорво и предложил
реальный способ проверки этой
гипотезы, который привел к
окончательному выяснению вопроса.
В заключение — несколько
слов о роли нейтрино в
космологии и астрофизике. Космология
пока еще во многом похожа на
научную фантастику — в ней
мирно сосуществуют конкурирующие
и часто взаимно исключающие
ДРУГ Друга гипотезы. Во многих
из них нейтрино играет если не
главную, то очень существенную
роль. Это в первую очередь,
относится к гипотезам о
происхождении Вселенной, высказанным в
1961—1963 гг. советскими
учеными Б. М, Понтекорво, Я. А. Смо-
родинскнм и Я. Б. Зельдовичем.
Чтобы проверить их идеи, очень
важно измерить плотность
нейтрино и антинейтрино во
Вселенной; работы в этом направлении
сейчас ведутся.
Возможно, испускание
нейтрино важно для отвода энергии
звезд. Это впервые отметили
американские ученые Г. Гамов и
М. Шенберг. Эти ученые
предложили механизм образования
нейтрино, — это захват электрона
ядром, после которого происходит
бета-распад и образуется
нейтрино. Следующий важный шаг
сделал Б. М. Понтекорво. Он
показал, что в определенных условиях
более существенно
непосредственное образование нейтринно-
антинейтринных пар при
столкновении электронов с ядрами. Эти
идеи разрабатываются сейчас
многими советскими и
зарубежными физиками, но с
окончательными выводами пока не следует
спешить.
Нейтринная астрофизика
переживает свой младенческий
возраст и пока трудно судить, во что
она вырастет.
Кандидат
физико-математических
наук
А. Т. ФИЛИППОВ,
Объединенный институт
ядерных исследований
три подкормки азотными
удобрениями, что для условий Средней
Азии дает экономию до 2 млн.
рублей.
ВЫХЛОПНЫЕ ГАЗЫ
СТАНУТ ЧИЩЕ
Выхлопные газы двигателей
внутреннего сгорания давно
вызывают беспокойство у гигиенистов:
в них содержатся разнообразные
вредные вещества, от окиси
углерода до канцерогенных
углеводородов. Особенно велики
связанные с этим неудобства при
подземных работах.
В Институте химических наук
АН Казахской ССР разработан
жидкий катализатор, который при
температуре 10—40 С полностью
окисляет окись углерода,
содержащуюся в количестве 0,01 —
3,00% в выхлопных газах
подземного самоходного оборудования.
Катализатор состоит из солей
палладия, меди и железа. Ученые
предложили также способ
регенерации катализатора, позволяющий
непрерывно использовать его в
течение длительного времени.
Сейчас проводятся
опытно-дорожные испытания палладиевого
катализатора на 1000 двигателей.
И СНОВА — ТИТАН
В одном из предыдущих
номеров журнала мы рассказывали о
перспективах применения титана
как конструкционного материала
для сверхзвуковых самолетов. А в
одном из американских научно-
исследовательских институтов
изучают возможности изготовления
из титана двухслойных баков для
ракетного топлива и окислителя,
диаметром больше 3 метров.
Гофрированный внутренний лист
титана предполагается сваривать
с гладким наружным листом
методом горячей прокатки. Чтобы
сохранить форму ребер и
избежать прогиба листов, между ними
вкладывают железные
прокладки, которые потом растворяют
химическим путем.
43
ВЫ ПОМНИТЕ?
ВЫ ВСЕ, КОНЕЧНО,
ПОМНИТЕ...
А почему, собственно, мы хорошо помним одно,
хуже — другое и можем совсем забыть третье! Как
работает невидимая картотена нашего мозга,
хранящая такое огромное количество сведений, какое
даже трудно себе представить! Эта проблема лишь
недавно стала по ппечу науке и сейчас привлекает
все больше ученых самых разных специальностей —
от химиков до кибернетиков.
Еще не так давно природа памяти
оставалась нам полностью неизвестной. Это было
одно из немногих белых пятен науки, куда
нога ученого не ступала, и мы бы сказали,
даже не знала, как ступить.
Экспериментаторы не располагали методами, которые
позволили бы подойти к изучению природы
памяти. Дух, мысль, память — это были
понятия одной категории, сущность которых
почти не поддавалась точному
исследованию. И только недавно начался штурм этой
труднейшей загадки природы.
В настоящее время считается, что
существует два вида памяти — «короткая» и
«длинная». Пример первой: студент тут же
в коридоре, ожидая очереди на экзамен,
«выучил» предмет и сдал его. Но как только
дверь экзаменационной комнаты
захлопнулась за ним, все вылетело из головы. Еще
пример: вам говорят номер телефона, вы
набрали его — занято и... второй раз набрать
его без ошибки вы не можете. Вероятно, эта
«короткая» память, бесследно исчезающая
из сознания, имеет биоэлектрическую
природу.
Но существует и «длинная» память — на
всю жизнь или во всяком случае на очень
длительный срок. В самое последнее время
стало ясно, что гипотеза о ее электрической
В редакцию поступили две статьи, посвященные
современным исследованиям памяти. Автор первой
из них, доктор химических наук В. С Тонгур, —
сторонник «химической» гипотезы памяти. Автор
второй статьи (она будет напечатана в следующем
номере) доктор химических наук В. А. Кухтин,
относится к этой гипотезе скептически.
Научный спор продолжается.
природе не выдерживает проверки
экспериментом и жизнью. Многочисленные
наблюдения показали, что в мозгу людей,
находящихся в состоянии шока, контузии, как
правило, происходят глубочайшие
биоэлектрические изменения. Но потеря памяти в
таких случаях распространяется только на
события, случившиеся непосредственно перед
катастрофой: эти люди продолжают хорошо
помнить всю свою предыдущую жизнь.
Если бы память имела электрическую
природу, то на протяжении человеческой
жизни, по мере увеличения объема памяти
(а он до какого-то возраста увеличивается)
должен был бы увеличиваться и
электрический потенциал мозга. Но самые
тщательные измерения дали отрицательные
результаты: никакого существенного увеличения
потенциала с возрастом наблюдать не
удается.
Можно еще указать на опыты, в которых
поверхность мозга животных рассекали
множеством разрезов, которые, конечно,
должны были бы разрушить электрические цепи
запоминания, если бы они существовали, и
таким образом нарушить память. Но
сколько-нибудь существенного нарушения памяти
в таких экспериментах не происходило. Эти
и другие факты (о всех писать невозможно)
привели к тому, что большинство ученых
СУЩЕСТВУЕТ ЛИ
ВЕЩЕСТВО ПАМЯТИ?
Доктор химических наук В. С. ТОНГУР
Рисунок Д. АНИКЕЕВА
44
сейчас не поддерживает точку зрения об
электрической природе «длинной» памяти.
Но какова же тогда материальная
сущность памяти? Лет 15—16 назад было
высказано предположение, что материальным
субстратом — носителем памяти могут быть
высокомолекулярные соединения —
нуклеиновые кислоты или белки. Как известно, эти
соединения могут хранить большое
количество информации, кодируемой различной
последоветельностью мономеров
(аминокислот в белке и нуклеотидов в нуклеиновой
кислоте). Подсчитано, что если молекула
содержит всего тысячу мономеров (что не так
уж много, особенно для РНК), то число
возможных их комбинаций достигает фантасти-
20!
для белков и 41000 для
ческих величин:
РНК.
Конечно, количество информации,
перерабатываемой и усваиваемой человеком за
всю жизнь, подсчитать довольно труднсч
Однако, по-видимому, гигантские молекулы
белков и нуклеиновых кислот имеют
достаточную емкость, чтобы хранить всю эту
информацию.
Гипотеза о «молекулах памяти»
показалась поначалу многим довольно
фантастической (таковой она, впрочем, многим
кажется и до сих пор), и поэтому
экспериментов для ее проверки, особенно в первое
время после выдвижения, было поставлено
очень мало, И только в последние годы
интерес к этой идее резко возрос.
Мы не будем подробно останавливаться
на ранних этапах изучения этого вопроса:
они довольно широко освещались нашей
популярной печатью. Напомним только
коротко об основных полученных фактах.
Шведский исследователь X. Хиден
разработал ювелирную микрометодику
определения состава нуклеиновых кислот и
установил нуклеотидный состав РНК одной
нервной клетки. Заметим, что в клетке
содержится всего несколько десятков пикограм-
45
мов РНК (пикограмм равен одной
тысячемиллиардной части — 10 ~12 грамма). Трудно
даже представить себе эту исчезающе
малую величину. Но Хидену удалось
обнаружить, что состав РНК нервных клеток мозга
крысы после тренировки отличается от
начального. Это явно указывало на какую-то
связь РНК с процессом обучения. Следует
отметить, однако, что до сих пор данным
Хидена верят не все ученые.
Широко известны и опыты с червями,
обладающими способностью к регенерации,—
планариями. Планарий «обучали»
сжиматься в ответ на действие света и затем
разрезали их. Если регенерация происходила в
обычных условиях, то планарий «помнили»
то, чему их обучили, и после регенерации.
Но если регенерация хвостов шла в слабом
растворе рибонуклеазы — фермента,
разрушающего РНК, то планария,
регенерировавшая из хвоста, все «забывала». Эти опыты
были проведены в США и с успехом
воспроизведены в Советском Союзе. Они
опять-таки указывают на причастность РНК
к памяти.
Любопытные эксперименты были
поставлены лет пять назад американцами В. Динг-
маном и М. Спорном. Они обучали крыс
ориентироваться в лабиринте. Но
предварительно опытной группе крыс был введен 8-
азогуанин — вещество, родственное
входящему в состав РНК гуанину. Исследователи
предполагали, что 8-азогуанин, конкурируя
с гуанином, будет включен вместо него в
РНК и таким образом получится РНК
необычного состава.
Такое изменение состава РНК,
оказывается, отражается на способности
животного к обучению: подопытные крысы при
обучении делали в два раза больше
ошибок, чем контрольные.
Эти эксперименты снова позволяли как-
то связать РНК и процессы запоминания и
обучения.
В 1963—1964 гг. мы вместе с О. А.
Крыловым и Р. А. Даниловой поставили опыты,
в которых мышам после их обучения (они
были обучены находить безопасное место в
лабиринте, пол которого находился под
током) вводилась рибонуклеаза. После этого
мыши забывали все то, чему их обучали.
Но, может быть, они забудут все и под
влиянием других веществ, разрушающих,
скажем, ДНК или белок, которые так же,
как и РНК, потенциально могут быть
отнесены к веществам-носителям памяти? Ответ
на этот вопрос дали опыты, в которых
мышам вводились дезоксирибонуклеаза —
фермент, разрушающий ДНК, и трипсин —
фермент, переваривающий белки. Ни в
одном из этих случаев мыши ничего не забыли.
Более того, были поставлены опыты, в
которых с помощью фермента
дезоксирибонуклеазы и антибиотика актиномицина
затруднялся синтез РНК в теле животного. Как
известно, РНК синтезируется на ДНК, как на
матрице. Поэтому если разрушить ДНК с
помощью дезоксирибонуклеазы, то синтез
РНК прекратится. Актиномицин также
блокирует синтез РНК (этим, кстати говоря, и
объясняется его губительное действие на
микроорганизмы).
Эксперименты показали, что если
вводить дезоксирибонуклеазу или актиномицин
до обучения, способность мышей к
обучению резко ухудшается. Введение же этих
препаратов после обучения потери памяти
не вызывало. Это и понятно: в таком случае
в мозгу уже появлялась синтезированная во
время обучения РНК, которую
дезоксирибонуклеаза и актиномицин не разрушают.
Описанные опыты вновь и еще более
четко говорили в пользу специфической роли
в процессах памяти именно РНК, а не белка
и не ДНК.
Но вот в 1965 году почти одновременно
датские ученые Е. Фердингстат, Т. Ниссен и
X. Ричаард-Петерсон и американцы А. Дже-
кобсон, Р. Бабич и С. Бубеч провели
сенсационные эксперименты, давшие солидное
подтверждение макромолекулярной
гипотезе памяти.
Крыс обучали доставать пищу по звонку
определенной частоты. Затем животных
убивали, и из их мозга выделяли РНК,
которую вводили внутрибрюшинно новым,
необученным крысам. Другой партии крыс,
контрольной, вводили РНК, выделенную из
мозга необученных крыс. И что бы вы
думали? В первом случае крысы как будто
оказались более способными к обучению,
чем во втором.
Опыты были продолжены. РНК выделили
из мозга уже не крыс, а обученных тем же
способом хомяков, и вводили эту РНК
крысам. После этого каждую из 16 взятых в
эксперимент крыс (8 из них была введена РНК
от обученных, а 8 — от необученных
животных) 25 раз подвергали испытанию: звенел
звонок, и двое наблюдателей отмечали,
46
найдет животное пищу или нет. Для того
чтобы данные были вполне объективными,
«судьи» не знали, какая крыса перед
ними— опытная или контрольная; кроме того,
для Верности очко засчитывалось только в
тех случаях, когда мнения обоих
наблюдателей совпадали.
О результатах можете судить сами.
В верхней строке цифры означают
количество «очков», набранных за 25 проб каждой
из крыс, которым была введена РНК от
обученных хомяков. В нижней строке — очки,
набранные каждой из контрольных крыс.
Опыт 4578991011
Контроль 100201 0 1
Таким образом, опытные крысы находили
пищу в среднем 7,9 раза из 25, а
контрольные — всего 0,6 раза!
Однако скептики (в науке их всегда
много, и это очень хорошо) подвергли
сомнению выводы исследователей. «Позвольте,—
говорили они,— а почему вы думаете, что
в ваших опытах происходила именно
передача памяти? Ведь РНК — весьма важное для
организма вещество, и ваши результаты
можно объяснить просто ее общим
стимулирующим действием. Кроме того,
введенная вами внутрибрюшинно РНК должна
разрушиться в организме и никоим образом не
может дойти целиком до мозга. Наконец,
уверены ли вы, что введенный вами
препарат действительно представляет собой
чистую РНК и не содержит примесей каких-либо
других веществ, извлеченных из мозга
хомяков вместе с РНК и как раз являющихся
переносчиками памяти?»
Блестящий ответ на первое возражение
был дан в опытах, проведенных в конце
1965 — начале 1966 года той же группой
американских ученых во главе с А. Джекобсо-
ном на червях планариях и крысах.
Исследователи разделили планарий на три группы.
У одной вырабатывался рефлекс (сжатие)
на вспышку света, которая сопровождалась
удгром электрического тока. Для второй
группы вспышки света не связывались с
ударами тока, а давались беспорядочно;
конечно, при этом никакого рефлекса на свет у
пленарий не вырабатывалось. Наконец,
третья группа червей была контрольной, то
есть оставалась в покое. РНК выделяли из
всех трех групп животных и вводили
необученным планаоиям, после чего испытывали,
будут ли они сжиматься под действием
света или нет.
Результаты были четкими. Планарий,
получившие РНК, выделенную из обученных
животных, давали значительно большее
количество ответов на свет, чем остальные две
группы: получившие РНК из планарий,
подвергавшихся беспорядочному раздражению,
и из необученных планарий.
Однако Джекобсон на этом не
успокоился. Он задал себе такой вопрос: если
исходить из того, что РНК кодирует память, то
что произойдет с ней при угасании
условного рефлекса, выработанного у планарий?
Погасить выработанный условный рефлекс
у животного вообще несложно. Если,
например, мышь приучена к тому, что при
вспышке света она получает удар током и поэтому
должна искать безопасное место, то первое
время она делает это и тогда, когда удара
током не происходит. Но с каждой такой
ложной тревогой рефлекс угасает, и в
конце концов сколько бы вы ни давали
вспышек, мышь не двинется с места.
Примерно то же самое Джекобсон
делал и с планариями. Давая вспышку света и
удар током, он добился того, что черви
сжимались только при вспышке. Затем он
продолжал давать свет, не подкрепляя
рефлекса током. Планарий, естественно, перестали
реагировать на вспышки. Но изменилась ли
за это время РНК, кодировавшая угасший
условный рефлекс?
Джекобсон выделил РНК из обученных
планарий, а также из червей, имевших
рефлекс и забывших его, и ввел ту и другую
РНК необучавшимся планариям. Оказалось,
что в обоих случаях планарий дали
одинаковое количество правильных ответов при
воздействии света. Значит, несмотря на то что
животное забыло условный рефлекс,
кодирующая его РНК осталась в организме.
На крысах те же исследователи провели
несколько иные, но не менее изящные
эксперименты. Одну группу животных они
обучали искать пищу под влиянием звука, а
другую— при вспышке света. Затем крыс
убивали и из их мозга выделяли РНК, которую
вводили необученным крысам. Проверка
показала, что животные, которым была
введена РНК от крыс первой группы, находили
пищу при световом сигнале значительно
лучше, чем контрольные. Если же их
способности испытывались при звуковом
сигнале, то они ничем не отличались от обычных.
С другой стороны, крысы, получившие РНК
из мозга животных второй группы, лучше
47
обучались реагировать именно на звуковой
сигнал, а при световом вели себя точно так
же, как контрольные.
Эти опыты дают полное основание
говорить о специфическом действии РНК (или
какого-то другого вещества,
извлекающегося вместе с ней из мозга) и показали, что
именно она (или оно) является
переносчиком памяти.
Как только результаты этих
экспериментов были опубликованы, их попытались
повторить и воспроизвести во многих
лабораториях. Пока что счет 5:2 в пользу опытов
по перенесению памяти: в пяти
лабораториях показано, что оно происходит, в двух же
его обнаружить не удалось (животные,
которым вводился экстракт из мозга
обученных, вели себя так же, как и контрольные) *.
Чем же можно объяснить такие
противоречия? Это сказать пока трудно. Весьма
возможно, что не совпадали методы работы
исследователей, а значит, и результаты
должны были получиться разные.
Вы, наверное, заметили, что, рассказывая
о переносчике памяти, мы вместо «РНК»
начали говорить «оно», «какое-то другое
вещество», «экстракт». Дело в том, что все
описанные эксперименты опровергают
только одно из возражений, о которых мы
говорили выше. Они показывают, что речь
идет не об общестимулирующем влиянии
РНК на организм, а о специфическом
воздействии именно на процессы запоминания
и обучения (иначе животные, получавшие
РНК от необученных крыс или планарий,
добивались бы точно таких же успехов, как и
получавшие РНК от обученных).
Два других возражения пока остаются в
силе. В самом деле, когда РНК вводят
животному внутрибрюшинно, она не должна
доходить в неповрежденном виде до
головного мозга: ее должны разрушить
ферменты, всегда присутствующие в организме.
* Об одном из таких экспериментов, давших
отрицательный результат, мы сообщали в заметке
«Открытие не подтверждается?» в N9 7 журнала. Ред.
Правда, можно предположить, что в мозг
попадают какие-то фрагменты — участки
молекул РНК, как раз и кодирующие память.
Но это еще нужно доказать.
С другой стороны, анализ полученньЛ из
мозга экстрактов, действительно, показал,
что они содержат кроме РНК довольно
большое количество белка. Если на такой
экстракт подействовать рибонуклеазой,
которая разрушит находящуюся в нем РНК,
экстракт, несмотря на это, остается
активным. На этом основании можно сделать два
предположения: либо в самом деле память
переносят отдельные (и притом не очень
большие) куски молекулы РНК, которые
остаются в экстракте и после обработки
рибонуклеазой, либо в передаче памяти
принимает участие и белок.
На последнюю возможность указывают
и некоторые другие эксперименты. Были
опубликованы сообщения о том, что водные
экстракты мозга обученных крыс также
способны стимулировать обучение при
введении их необученным крысам. Эта
способность исчезает при обработке экстрактов
трипсином — ферментом, переваривающим
белок. В ряде экспериментов было
обнаружено, что блокировка синтеза белка
(например, антибиотиком пуромицином)
затрудняет обучение животного и ускоряет
забывание им выученного. Вероятно, белок и в
самом деле тоже может иметь какое-то
отношение к памяти.
Что же все-таки является носителем
памяти: РНК, белок или оба эти вещества? Как
они взаимодействуют? Связаны ли с
памятью какие-то не только молекулярные, но
и надмолекулярные, субклеточные
структуры? Эти вопросы еще не решены. Здесь все
в движении: каждый эксперимент, каждая
публикация может дать какие-то новые,
неожиданные результаты, может подтвердить
или опровергнуть нынешние представления.
Это самый передний край науки. Но в том,
что память связана с какой-то химической
макромолекулярной структурой, у многих
ученых уже нет сомнения.
48
и вы можете говорить
по-гэльски
А. АЗИМОВ
ДЕ-ПЦ 'ПЛ-ГА-ДМ-МЕЬМ-А-МИ
Заставить неискушенного
человека поверить, что вы химик,
нелегко. Когда мне предлагают
определить, что за пятно на
ткани из неизвестного
материала, я ничего не могу сказать.
Более того, понюхав пасту не-
Гэльский — язык кельтов,
жителей Ирландии и Шотландии.
— Прим. пере в.
известного состава, я не берусь
определить, на что она годится.
Л название патентованного
средства ничего не говорит мне
о том, что в нем содержится.
Так что, как видите, я не
проявляю способностей в
химической практике, но зато на
химическом языке говорю бегло.
Говорить на химическом
языке не так трудно, как
кажется. Вся загвоздка в том, что
в XIX веке органическая химия
была монополией немцев. Л
немцы вообще почему-то любят
соединять слова вместе,
тщательно маскируя стык между
ними. Именно такая судьба и
постигла названия
органических соединений, а потом почти
без изменений их рабски
переняли другие языки.
Таким образом, вы легко
можете столкнуться с вполне без-
4 Химия и Жизнь, №9
49
обидным соединением, и вдруг
выясняется, что его название —
что-нибудь вроде пара-диметил-
аминобензальдегид.
Для простого человека этот
набор букв не имеет смысла и
даже вызывает раздражение.
Но это несправедливо. Если
взяться за дело энергично и
прочитать это слово с начала
до конца, то получится не так
уж плохо. Попробуйте сказать
его так: ПА-ра-ДИ-мет-ИЛ-а-
МИ-но-БЕН-заль-де-ГИД. Если
произносить написанное
заглавными буквами с ударением, то
вы сможете проговорить это
слово настолько быстро, что
удивлению ваших друзей не
будет конца.
Я познакомился с этим
веществом впервые несколько лет
назад. Его раствор в соляной
кислоте химики используют
как индикатор на вещество под
названием «глюкозамин». Я
подошел к шкафу с реактивами и
спросил кого-то:«У нас есть
пара - диметиламинобензальде-
гид?» Этот кто-то ответил: «А
что, по-вашему, такое ПА-ра-
ДИ - мет - ИЛ - а-МИ-но-БЕН-
заль-де-ГИД?», и запел это на
мотив «Ирландской прачки».
«Ирландская прачка» — это
джиг с однообразным мотивом,
который звучит примерно так:
«ТАМ - ти - ТАМ-ти-ТАМ-ти-
ТАМ-ти-ТАМ» и дальше так же
монотонно.
Несколько недель меня
преследовал этот барабанный ритм.
ПА - ра-ДИ-мет-ИЛ-а-МИ-но-
БЕН - заль-де-ГИД-ПА-ра-ДИ-
мет-ИЛ-а-МИ-но-БЕН - заль —
прочно засело у меня в голове.
Однажды я сидел в какой-то
приемной. Секретарша была
привлекательной ирландкой, а
я не спешил и терпеливо ждал,
поглядывая на нее. Ее типично
ирландская внешность
пробудила во мне воспоминания об
ирландской музыке иг сам того не
замечая, я тихо пропел
несколько раз «ПА-ра-ДИ-мет-ИЛ-а-
МИ-но-БЕН-заль-де-ГИД».
Секретарша с восторгом
захлопала в ладоши и
воскликнула: «О, Вы говорите на
настоящем гэльском!» Мне оставалось
только смущенно улыбнуться —
по-гзльски я не знал ни
единого слова.
Но что же означает это
слово, которое звучит так по-гэль-
ски? Давайте разберемся.
Может быть, и вы сможете
объясняться на языке кельтов.
На юго-востоке Азии, на
островах Ява и Суматра растет
дерево, кора которого выделяет
красно-коричневую смолу.
Когда зта смола горит, она издает
приятный запах. В средние века
арабские торговцы проникли на
берега Индийского океана и
вывезли оттуда смолу с приятным
запахом. Они называли ее
яванским ладаном. По-арабски
зто звучало как «лубан джави».
Европейцы покупали зтУ
смолу у арабских торговцев. Ее
арабское название они
воспринимали как набор
бессмысленных звуков. Но первый слог
«лу» напоминал определенный
артикуль в некоторых
европейский языках — «1о» в
итальянском или «1е» и «1а» во
французском. Поэтому европейцы
стали называть это вещество
«лу банджави», а потом,
отбросив артикль, «банджави».
Позднее это слово претерпело
различные искажения. Его
произносили и как «бенджамин», и
как «бенджоин» и, наконец,
примерно года с 1650 как
«бензоин». Теперь зто вещество
называют бензойной смолой.
Около 1608 года из
бензойной смолы выделили кислоту,
которая в конце концов
получила название бензойной.
В 1834 году немецкий химик
Митчерлих превратил
бензойную кислоту в вещество,
состоящее только из углерода и
водорода и не содержащее
кислорода. Митчерлих назвал его
ЛУ БАНДЖАВИ
50
БАНДЖАВИ
БЕНДЖАМИН
БЕНЗОИН
бензином (benzin), подчеркнув
тем самым его происхождение.
Но другой немецкий химик
Либих вполне обоснованно
возражал. Он утверждал, что
суффикс «ин» (in) химики
применяют для обозначения веществ,
содержащих атом азота, а
бензин Митчерлиха его не
содержит. Он предложил заменить
суффикс «ин» на «ол» —
вещество растворялось в маслах
лучше, чем в воде, а слово «01»
по-немецки означает масло. Но
зто тоже было ничуть не
лучше, потому что суффикс «ол»
химики обычно используют в
названиях совершенно других
веществ. Однако в Германии
слово привилось, и это
вещество там называют бензолом.
Молекула бензола состоит
из шести атомов углерода,
расположенных по вершинам
правильного шестиугольника. К
каждому из них присоединено
по одному атому водорода.
Запомнив истинное расположение
атомов в молекуле бензола, его
суммарную формулу можно
записать как ССН6.
И Бензол
Так на долгом и извилистом
пути от Явы к молекуле
бензола мы растеряли все буквы
из названия острова. Но мы
кое-что приобрели на этом
пути. Пара-диметиламинобен-
зальдегид содержит сочетание
«бенз», а мы теперь знаем,
откуда оно взялось.
Много веков женщины
красят брови и ресницы. В давние
времена они пользовались для
этого темной краской (обычно
4*
АЛ — КУЛ
это были соединения сурьмы),
растертой в очень тонкий
порошок. Арабы так просто и
называли зту косметическую
краску «тонко измельченным
порошком», а по-арабски зто
звучит «ал-кул».
Арабы — величайшие
алхимики раннего средневековья.
Европейцы алхимию переняли
у них вместе со всеми
терминами. Арабы стали называть
словом «ал-кул» любые
порошки независимо от того,
применялись они в косметике или
нет, и европейцы поступили
так же. Но они произносили и
писали это слово на свой лад
и в конце концов арабское «ал-
кул» превратилось в
«алкоголь».
Алхимики не понимали, что
представляют собой пары или
газы. Они считали, что пар, в
отличие от жидкости или
твердого тела, нематериален и
называли пар духом или
спиритом. Вещества, способные
превращаться в пар даже при
комнатной температуре,
поражали их воображение. В
средние века самым известным из
таких веществ было вино.
Поэтому летучую часть вина
алхимики называли винным
духом, или винным спиртом.
Когда жидкость испаряется,
то кажется, что она
размельчается в ничто. Поэтому пар, как
и тонко размельченный
порошок, стали называть алкоголем,
появилось выражение винный
алкоголь. К XVII веку слово
«алкоголь» стало обозначать
только винные пары. В начале
XIX века определили
структуру винных паров. Оказалось,
что их молекула содержит два
атома углерода и один атом
кислорода. К первому
углеродному атому присоединено три
атома водорода, а ко второму
только два. С атомом
кислорода связан один атом водорода.
\ у
н—с с—н
/}/7ногаль
Кислородно -
водородную группу -ОН называют гид-
роксильной (от латинских слов
«гидрогениум» — водород и
«оксигениум» — кислород).
Химики открыли много веществ,
в которых гидроксильная
группа присоединена к атому
углерода, так же как в молекуле
винного алкоголя. Все эти
вещества получили общее назва-
АЛКОГОЛЬ
51
ние «алкоголи» или «спирты»,
но конечно, у каждого из них
есть еще и свое название.
Винный алкоголь, кроме
гидроксильной группы,
содержит два атома углерода и
пять атомов водорода.
Подобная комбинация атомов
существует еще в одном веществе.
Его впервые получили в 1540
году. Оно испарялось еще
быстрее, чем алкоголь. Казалось,
будто оно, исчезая на глазах,
непреодолимо стремится на
небеса. А вещество, из которого
состоят небеса, Аристотель
называл эфиром. Поэтому в
1730 году это легко
испаряющееся вещество получило
название «эфирного духа» —
«эфирного спирта». Позднее оно
превратилось в более краткое
слово «эфир».
9fup
Группа из двух атомов
углерода и пяти атомов водорода,
типичная для молекулы эфира,
естественно стала называться
этильной *, а винный алкоголь,
содержащий ее, около 1850
года превратился в этиловый
алкоголь, или этиловый спирт.
Позже химики сочли
достаточным вводить в названия
веществ суффикс «ол», чтобы
показать, что они содержат
гидроксильную группу,
связанную с углеродом, и
принадлежат к классу алкоголей.
Именно поэтому название «бензол»
не годится для вещества с
формулой С6Нк, не содержащего
гидроксильной группы.
Если из молекулы
этилового спирта СН3СН2ОН удалить
два атома водорода, один из
которых соединен с кислоро-
* В английском языке слова
«ether» — «эфир» и «ethyl group»—
«этильная группа» имеют общий
корень. — Прим. пере в.
дом, а другой — с
примыкающим к кислороду атомом
углерода, то образуется молекула
СН3СНО.
Эту реакцию впервые
осуществил Либих в 1835 году.
Поскольку отщепление атомов
водорода (водород по-латыни
«гидрогениум») естественно
называется процессом
дегидрирования, то Либих получил
дегидрированный алкоголь. По-
латыни зто звучало как
«алкоголь дегидрогенатус».
Но это слишком длинное
название для такого простого
соединения, и химики вскоре
сократили его. Взяли первый
слог из слова алкоголь и два
слога из слова
дегидрогенатус и получили название
альдегид. Комбинацию атомов
углерода, водорода и кислорода
(-СНО) стали называть
альдегидной группой, а любое
вещество, содержащее такую
группу — альдегидом.
Например, если один из
атомов водорода в молекуле
бензола С6Н6 заменить на
группу — СНО, то получится новое
вещество С6Н5СНО — альдегид
бензола или короче бензальде-
гид.
Теперь поговорим о древних
египтянах.
Богом-покровителем египетского города Фивы
на Верхнем Ниле был Амен
или Амон. При царствовании
XVIII или XIX династии Фивы
добились господства над всем
Египтом, и Амен стал главным
богом египтян. В честь него
египтяне воздвигали храмы,
один из которых на севере
Африки был известен древним
грекам, а позднее и римлянам.
Римляне называли бога
египтян Аммоном.
В пустыне всегда не хватает
топлива. На севере Африки
самым доступным топливом
был верблюжий помет. Копоть
от сгоревшего помета
покрывала потолки и стены храма бога
Аммона. Среди черной копоти
поблескивали белые, похожие
на соль кристаллы, о которых
римляне говорили, что зто соль
Аммона. Сейчас мы называем
это в ещество хл ори до м
аммония.
В 1774 году английский
химик Пристли обнаружил, что
при нагревании соли Аммона
выделяется белый едкий газ,
а в 1782 году шведский химик
Бергман предложил называть
этот газ аммонниаком**. Тремя
годами позже французский
химик Бертоле определил его
формулу. Молекула этого
вещества состоит из атома азота
и трех атомов водорода — так
что ее формулу можно
записать как NH3.
Со временем
химики-органики открыли много веществ,
в которых группа из атома
азота и двух атомов водорода
( —NH2) присоединяется к
одному из углеродных атомов
органической молекулы. Сходство
группы — NH2 с аммиаком было
очевидно и, чтобы подчеркнуть
его, с 1860 года ее стали
называть аминогруппой.
Если мы теперь вернемся к
бензальдегиду С6Н5СНО и
представим себе, что в
молекуле исходного бензола один
атом водорода замещен
аминогруппой, то получим вещество
С6Н4(СНО) (NH2) — аминобенз-
альдегид.
Винный спирт иногда
называют хлебным спиртом, потому
что его можно получить при
брожении зерна. Но
существуют и другие алкоголи. Еще
в 1661 году английский химик
Р. Бойль заметил, что при
нагревании древесины без
доступа воздуха образуются пары,
часть которых конденсируется в
прозрачную жидкость, напоми-
** В русском языке это
вещество называется аммиаком.
— Прим. пере в.
52
нающую винный спирт. Эта
жидкость оказалась ядовитой и
испарялась быстрее, чем
винный спирт. Вещество получило
название древесного спирта.
В те времена, чтобы название
выглядело научным, нужно
было перевести его на греческий
или латынь. Вино по-гречески
«мети», а дерево — «или». Из
этих двух слов в 1835 году
шведский химик Берцелиус
образовал название древесного
спирта — метиловый, которым
до настоящего времени
пользуются все химики.
Формулу этого вещества
нашел в 1834 году французский
химик Дюма. Метиловый спирт
проще этилового, он содержит
только один атом углерода, его
формула будет СН3ОН. Атом
углерода с тремя атомами
водорода (-СНз) стали называть ме-
тильной группой. В 1849 году
французский химик Вюрц
заместил один из двух
водородных атомов аминогруппы на
метильную группу и получил
группу—NHCH3, которая,
естественно, называется, метил-
а мин о вой. Если на метильные
группы заместить оба атома
водорода аминогруппы,
образуется диметиламинная группа —
(CH3JN — (приставка «ди» от
греческого «дис» — дважды).
Метильная группа
присоединена к аминогруппе дважды.
Теперь мы можем вернуться
к нашему аминобензальдегиду
C6H4(CHO)(NH2). Если
аминогруппу заместить диметиламин-
ной группой, то формула примет
такой вид —С6Н4(СНО) [N(CH3J]
и называться это вещество
будет диметиламинооензальдегид.
Молекула бензола — это
правильный шестиугольник с
атомами углерода на вершинах. К
каждому атому углерода
присоединен атом водорода. В нашем
соединении один из атомов
водорода замещен на альдегидную
группу, а другой — на диметил-
аминную группу. Но какие же
именно из шести атомов
водорода замещены?
Молекула бензола —
шестиугольник совершенно
симметричный. Поэтому для любых
двух атомов водорода может
быть только три комбинации.
Во-первых, два атома водорода
могут располагаться рядом, во-
вторых— через один и,
наконец,— у двух противоположных
атомов углерода.
Если пронумеровать атомы
углерода в шестиугольнике
молекулы бензола от 1 до 6, то
комбинации, о которых мы
рассказали, можно обозначить как
1, 2; 1,3 и 1,4 соответственно. На
рисунке видно, что других
комбинаций быть не может.
Каждой комбинации химики
дали название. Комбинация 1,2
называется «орто». «Орто» по-
гречески означает правильный.
Эта комбинация простейшая, а
все, что просто — то правильно.
«Мета» переводится с
греческого как «средний» или
«находящийся через одного». Это как
раз подходит для комбинации
1,3. Мы замещаем первый атом
водорода, второй оставляем
нетронутым, и замещаем
следующий после него.
«Пара» в переводе с
греческого означает «рядом» или
«один за другим». Если
повернуть шестиугольник молекулы
так, что 1-й атом пойдет
направо, то 4-й атом пойдет
налево. Создается впечатление, что
атомы движутся один за
другим. Приставка «пара»
применяется для обозначения
комбинации 1,4.
I f j Тметил
&ензоаьнсе
кс/тьцо
^ л^~ aj1t^eitJ^
ПАРА-ДИМЕТИЛАМИНОБЕН-
ЗАЛЬДЕГИД
После введения этих
обозначений название точно
определяет соединение, и ошибки быть
не может. Если мы говорим
«нара - диметиламинобензаль-
дегид», зто значит, что
диметиламинная и альдегидная группы
находятся в положении 1,4 друг
к другу, т. е. располагаются
напротив друг друга в бензольном
кольце и формула соединения
записывается (CH3JNC6H4CHO.
А теперь, когда вы уже
легко говорите по-гэльски, как вы
думаете, что означают слова:
^-D-глюкопиранозил- |^-D-
фруктофуранозид;
Д4-прегнендиол-17а, 21-трион-З,
11, 20;
хлоргидрат 4 -метил-5 - В -ок-
сиэтил- N- B'-метил-4'-аминопи-
римидил-5'-метил) - тиааолий-
хлорида.
Если вы еще не совсем
овладели гэльским, я помогу вам —
зто сахар, кортизон и
витамин В].
Перевод А. СОЛОДКИНА
Рисунки В. ЗУЙКОВА
53
ИСКУССТВО ПАРФЮМЕРА
Все знают, что парфюмерия — это духи, одеколоны,
лосьоны, туалетная вода. В этом номере журнала в разделе
«Обыкновенное вещество», рассказывается о том, чего
многие не знают. Иэ чего делаются духи? Как работает
парфюмер? Где синтезируются искусственные душистые
вещества? Как возникло древнейшее искусство
парфюмерии?
О
CQ
I-
U
ш
Э"
ш
CQ
CQ
О
X
ас
.о
ш
О
Некоторые люди недоумевают,
когда слышат, что
парфюмерия — это искусство. Правда,
для них оно почти неизвестно,
деятельность парфюмера
относится к редким профессиям.
Подобно тому, как художник
с помощью палитры красок
создает картину, а композитор
«в музыку преобразует шум»,
разрозненные, а иногда и не
существующие в природе —
«фантазийные» композиции запахов
парфюмер превращает в
стройное гармоническое целое —
изящные и тонкие духи и
одеколоны.
ПАРФЮМЕРНЫЕ
КОМПОЗИЦИИ
Парфюмерные
композиции — зто сложное сочетание
различных душистых веществ,
как естественных, так и
синтетических.
Природа создала свои
многочисленные запахи из довольно
ограниченного количества
элементов, но все многообразие
запахов зависит от их
сочетаний. Как из букв алфавита
слагается все многообразие слов и
предложений, так из основных
запахов складываются все
оттенки природных ароматов.
Общеизвестны такие
определения характеров запаха, как
тонкий, изящный, богатый,
бедный» тусклый, легкий, сухой,
влажный (не говоря уже о
просто приятном или неприятном).
Парфюмер, выбирая
ассортимент и весовые отношения
душистых веществ, казалось бы,
совершенно свободен в своем
творчестве. Однако это далеко
не так. К запахам естественных
душистых растений он
добавляет другие, в природе не
встречающиеся, но дающие с ними
гармоническое сочетание.
Найти основное звучание и
правильную окраску запаха —
ее тембр — и есть самая
трудная задача для парфюмера. Он
вводит в композицию душистые
вещества, сопровождающие
основной элемент; эти
сопровождающие вещества составляют
иногда 70—80 весовых
процентов состава композиции, они
подчеркивают характер и
окраску ведущего запаха.
Как объяснить понятие
«тембр запаха»? Его можно
уловить, если сравнить, например,
запахи розы и герани,
апельсина и мандарина, чай грузинский
и цейлонский, различные сорта
кофе, особенно при добавлении
в него цикория.
В композициях парфюмера
иногда сочетаются запахи, по
тону и окраске совершенно
противоположные; например,
такие светлые, как ваниль, и
темные, как деготь или
пачули *; влажные, как роза, и
яркие, как амбра; звучные, как
лимон, апельсин и бергамот,
и глухие, как дубовый мох;
теплые и сладкие плодовые
запахи жасмина парфюмер
соединяет с грубыми запахами
индола и скатола. Из одних и тех
же веществ, в зависимости от
их соотношения, могут быть
созданы и новые запахи, такие,
которые напоминают
зеркальное отображение известных —
например, запахи амбровая
роза и розовая амбра.
Чтобы из различных
душистых веществ получить удачную
новую композицию, парфюмеру
приходится немало
экспериментировать. В основе всякой
композиции лежит какая-то идея —
основа будущего запаха,
которая зародилась у парфюмера.
Она может относиться и к ка-
* Подобные сочетания были
модными в духах, завоевавших
популярность еще в начале
века — «Жокей-клуб» и «Русская
кожа». Сейчас на этой основе
разработаны новые прекрасные
советские духи — «Маскарад»,
«Русь» и другие.
кому-либо одному душистому
веществу, и к сочетанию
нескольких. Это сочетание будет
служить как бы наброском
будущей композиции и нередко
определяет ее конечный тип и
характер. Именно поэтому духи
одних и тех же цветочных
наименований созданные
различными парфюмерами, имеют
различные оттенки ароматов,
зависящие от вкуса и личности
парфюмера.
В готовых композициях
парфюмер ярче и полнее
подчеркивает специфические запахи.
Можно даже сказать, что
хорошие духи «Сирень» или
«Ландыш» больше пахнут сиренью
или ландышем, чем их
естественные прототипы.
Парфюмеру, помимо
отличного знания характера и
свойств запахов, требуется большое
художественное чутье и вкус.
Только тогда он может создать
настоящее произведение своего
искусства.
НОСИТЕЛИ ЗАПАХОВ —
ЭФИРНЫЕ МАСЛА
Дочь известного
естествоиспытателя Карла Линнея
заметила однажды душным летним
вечером в саду странное
свечение цветов настурции. Над
лепестками появлялись как будто
искры или легкое пламя. Она
зажгла свечу и поднесла ее
к цветку. Яркое пламя
охватило все растение, по стеблям
побежали огоньки. Но оно
осталось целым и свежим...
Такое же свечение
наблюдается над красными цветами
пеларгонии. Многие дети любят
сжимать кожицу мандарина и
апельсина перед горящей
спичкой или свечой; из кожицы при
этом выдавливаются струйки
масла, которое с треском
вспыхивает. Это светятся и
вспыхивают пары эфирных масел,
сообщающие растениям свой-
55
ственный им запах. Их роль
в жизни растений очень велика:
пары эфирных масел,
выделяемые листьями и цветами,
окутывая их со всех сторон,
предохраняют растения от слишком
сильного нагревания
солнечными лучами днем и от
охлаждения ночью. Вспомните, как
сильно пахнут по вечерам
цветы душистого табака, метиолы,
ночной фиалки-любки.
Из чего же состоят эфирные
масла? До начала XIX века
считалось, что эфирные масла
представляют собой однородное
по составу вещество, более или
менее загрязненное какими-
либо примесями. Позже химики
доказали, что эфирные масла,
В рабочей комнате парфюмера
нет химической аппаратуры. Это
кабинет с шкафами, в которых
стоят флаконы, содержащие
образцы душистых веществ.
Центральное место занимает
парфюмерный стол. К столу приделаны
полки, на которых расставлены
пробирки с образцами, и
баночки с полосками плотной бумаги
для «разнюхивания». Вот и вся
техника, с помощью которой
осуществляется фантазия
парфюмера
содержащиеся в душистых
растениях, — зто сочетание
большого числа химически
индивидуальных веществ, каждое из
которых обладает собственным
запахом.
Эти масла летучи. Они, в
отличие от жирных масел, не
оставляют на ткани или бумаге
жирных пятен. В смеси
эфирных масел, содержащихся
в каждом растении, есть масла
и с приятными, и с
неприятными (иногда даже
отталкивающими) запахами. Например,
натуральное масло жасмина
содержит около 2,5% индола —
вещества с отвратительным
фекальным запахом. Но в этой
дозе оно сообщает запаху
жасмина особый (и очень
приятный) оттенок. В лимонном
масле — около 90% терпенов, тоже
обладающих очень неприятным
запахом.
Содержатся в эфирных
маслах м нелетучие душистые
вещества — воски, смолы и
другие. Они понижают летучесть
м асел, зам едляют их порчу.
При перегонке масел они боль-
тлей частью остаются в осадке.
Поэтому запах масел, не
извлеченных из растений, более
стоек, несравненно медленнее
улетучивается и очень долго не
портится. Например, если
корицу или гвоздику хранить
даже при доступе воздуха, они
сохравяют свой запах много
лет, в то время как коричное
или гвоздичное масло
улетучивается и портится довольно
быстро.
Многие знают китайские и
индийские веера, сделанные из
сандалового дерева. Они в
течение десятилетий сохраняют
свой особый аромат, а носитель
этого запаха — сандаловое
масло, нанесенное на какую-либо
поверхность, улетучивается за
несколько дней.
Парфюмеры используют
природное душистое сырье в
огромном ассортименте — в их
распоряжении около пяти тысяч
названий. Это сырье поступает
Отделочный зал духов и одеколонов одной из первых русских
парфюмерных фабрик
56
из всех теплых и жарких зон
земного шара. В СССР
душистые растения разводят на
Кавказе, в Крыму, в Молдавии,
в Средней Азии, в
Центральночерноземной зоне, на Украине.
Это роза, кориандр, тмин,
мускатный шалфей, герань, мята,
лаванда, анис, жасмин, дубовый
мох, азалия, ладанник и
другие. Извлеченные из них
различными способами эфирные
масла растворяют в зтиловом
спирте; так получаются
одеколоны и духи. В одеколоны идет
меньше душистого сырья, и
раствор спирта в них не тако и
крепкий, как в духах.
Большое значение в
парфюмерии имеют смолистые
вещества, которые добывают из
деревьев, надрезая их кору и
ствол: бензойная смола, ладан,
толуанский бальзам, стиракс.
Эти вещества обладают
собственным приятным запахом,
они способны повышать
стойкость других ароматов и, кроме
того, принадлежат к сильней-
ши м фитонцидам. Последнее
означает, что их можно
использовать также для очищения и
дезинфекции воздуха.
Огромное значение в
парфюмерии имеют душистые
вещества животного
происхождения — высушенные железы
мускусного быка, бобра,
ондатры, а также амбра и цибет*.
Но естественные душистые
вещества и животного, и
растительного происхождения очень
дороги. Эфироносные культуры
требуют больших площадей
под посевы, большого труда для
извлечения масел из сырья.
РОЖДЕНИЕ ЗАПАХОВ
В ЛАБОРАТОРИИ
Еще в конце XIX века в
результате исследований хими-
* О применении в
парфюмерии душистых веществ
животного происхождения см. «Химия
и жизнь», 1966, № 2, статья
«Звериные духи».
Здесь на московской парфюмерной фабрике «Новая заря» разливают
готовую продукцию
ков-органиков были выделены
в чистом виде составные части
многих зфирных масел.
Началось изучение их химического
состава, а зто, естественно,
привело к синтезу многих
душистых веществ.
Массовое, промышленное
производство этих веществ
стало возможным только
благодаря высокому развитию
химической науки и техники: такой
синтез относится к области
тонкой и весьма сложной
химической технологии. Даже
незначительные примеси, которые
трудно определить обычными
химическими или физическими
методами, становятся
препятствием к применению в
парфюмерии всего продукта.
В СССР производство синте-
В этих огромных баллонах
созревают духи. Создание
парфюмерной композиции — только первая
стадия работы. На парфюмерных
фабриках и заводах носители
запаха проходят долгую обработку:
растворение в спирте,
выстаивание, вызревание. Во время
вызревания исчезает запах
растворителя, сглаживаются неровности
ароматов, букет становится
«стройнее»
Ч**Г!
ь
57
тических душистых вещестя
бурно развивается.
Синтезированы, в частности, совершенно
новые душистые вещества (ти-
бетолид, мустен, сан та л и до л,
мирценоль и многие другие). Из
широко применяемых
синтетических душистых веществ
назовем бензилацетат, ванилин,
гераниол, фенилэтиловый спирт
и цитронеллол, цитраль,
цитроне л л ал ь, линалоол, терпинеол,
гелиотропин» ионон, жасмина л ь-
дегид, кумарин.
■ Работы, связанные с изучением
ароматических продуктов, были
начаты еще в первой половине
XIX в. Немецкий ученый Дюмас
впервые разделил вещества,
входящие в состав эфирных масел,
на содержащие кислород и
свободные от кислорода; при
дальнейшем изучении эти группы
веществ были определены как
терпены и камфора. Позднее О.
Баллах установил, что большинство
терпенов, встречающихся в
разных эфирных маслах, идентичны.
Они представляют собой
углеводороды с общей формулой
C]0Hic.
Эфирные масла из химически
чистых соединений выделяли
сначала чисто физическими
методами. Но изучение их химических
свойств помогло разработать для
этой же цели методы
химические — выделение из естественных
эфирных масеп первичных
спиртов при помощи кислых эфиров
фталевой кислоты, выделение
гераниола с помощью СаС12г
выделение альдегидов и кетонов с
помощью бисульфатных соединений.
Естественно задать
парфюмеру вопрос: могут ли
синтетические дуплистые вещества
полностью заменить естественные?
Постараюсь ответить.
Синтетические душистые
вещества (цветочного характера)
определяют лишь основную
черту запаха растений, и то не
полностью; они лишь
напоминают запах того или много
растительного вещества, но не
воспроизводят его. Они лишены
окраски, звучности, бархатисто-
■ Изучение состава цветочных
эфирных масел показало, что
некоторые их компоненты —
известные органические соединения,
возможность использования кото-_
рых как душистых веществ было
трудно раньше предположить.
К ним относятся, например,
азотсодержащие соединения индол и
скатол, продукты распада
животного организма. До того, как они
были обнаружены в эфирном
масле жасмина, их присутствие в
растительном мире учеными не
допускалось.
■ Создание А. М. Бутлеровым
теории строения химических
соединений оказало, в частности,
сильное влияние нэ работы по
использованию в парфюмерии
синтезированных эфирных
масел.
Появилась новая отрасль
химического производства — синтез
душистых веществ на базе
простейших продуктов
коксохимической промышленности.
сти, я бы сказал —
«оркестровки» запаха, которые присущи
натуральным душистым
веществам.
По моему мнению, полностью
заменить естественные
душистые вещества синтетическими
невозможно.
Только сочетание тех и
других дает возможность создать
действительно полноценные
парфюмерные композиции.
Р. А. ФРИДМАН
■ Изучение химического состава
эфирных масеп дало
возможность выделить в чистом виде
основные душистые вещества,
входящие в их состав. От
использования масел в чистом виде
химики перешли к выделению и
использованию их отдельных
компонентов, фракций.
■ В химической промышленности
применяется, например, способ
переработки составных частей
эфирных масел в более ценные
душистые вещества,
предложенный группой советских химиков во
главе с академиком С. С.
Наметкиным. Из кориандрового масла,
которое само по себе имеет
ограниченное применение в
парфюмерии, но обеспечено отличной
сырьевой базой (культура
кориандра легко возделывается),
удалось путем химической
переработки получить до 12 различных
душистых веществ. И в их числе —
такие ценные, как линапилаце-
тат, цитраль, гидроксицитронел-
лаль.
ПРОСТО ХИМИЧЕСКИЙ
ПРОДУКТ
58
ЧТО ВЫ ЗНАЕТЕ И ЧЕГО НЕ ЗНАЕТЕ
О ПАРФЮМЕРИИ
■ Чисто химическим путем
синтезированы важнейшие для
парфюмерии вещества: нитросоеди-
нения с мускусным запахом;
иононные препараты, имеющие
в разбавленном виде запах
цветов фиалки; гидроксицитронеп-
паль, обладающий нежным
запахом ландыша; метиловый эфир
гептинкарбоноаой кислоты —
вещество с тонким запахом свежей
зелени, и многие другие,
■ Выбор производственного
способа получения того или иного
душистого вещества определяется
сейчас технико-экономическими
^соображениями^ Практически
любой компонент природных
эфирных масел может быть получен
путем синтеза,
■ Основные методы выделения
эфирных масел из растительного
сырья а наше время те же, что
и в древности: отгонка с водяным
паром и перегонка под
уменьшенным давлением.
■ При промышленном получении
искусственных душистых веществ
применяют различные методы
органического синтеза: реакции
конденсации, апкилирования, эте-
рификации, окисления,
восстановления, нитрования, синтезы с ме-
таллоорганическими
соединениями и другие.-
■ Исследования по синтезу
новых душистых веществ и
изучению свойств природных эфирных
масел ведутся в нашей стране во
Всесоюзном
научно-исследовательском институте синтетических
и натуральных душистых веществ.
Степень «готовности» духов и
одеколонов, правильность
производственной технологии и
соответствие состава продукции
рецептуре определяют
химики-технологи на парфюмерных
фабриках и заводах.
СИМВОЛ ОЧИЩЕНИЯ
Древнеримский историк и
писатель Плиний Старший
свидетельствует, что
ароматические вещества впервые стали
применять в странах Востока.
Так произошло видимо потому,
что именно здесь росли в
изобилии сандал и камфора,
мускатный орех и ладан, аппокакс,
нард и ароматический
тростник...
Вначале душистые вещества
воскуривали лишь во время
религиозных церемоний. Они
были своего рода символом
очищения. Как известно, душистые
бальзамы и смолы обладают
антисептическими свойствами.
В Древнем Египте их
использовали при бальзамировании тел
умерших,
БЛАГОВОНИЯ
ВХОДЯТ В БЫТ
В эпоху Птоломеев C30—
30 гг. до н. э.) в Египте
употребление благовоний
распространяется шире, особенно
среди богатых женщин. Настои
ароматных растений и
душистые смолы употребляют и с
гигиенической целью, и как
косметику. Египтяне достигли
больших успехов в
производстве душистых веществ.
Найденные в гробницах флаконы
с духами двухтысячелетней
давности до сих пор источают
приятный аромат.
АРОМАТИЧЕСКИЕ БАНИ
Арабские женщины не
довольствовались тем, что
обрызгивались душистыми
жидкостями и носили ладанки. Они
предпочитали пропитывать
ароматическими веществами все
тело. Для этой цели
существовали особые бани. В
специальном углублении в полу
разжигали уголь; в пламя
бросали благовония.
Поднимавшийся дым вскоре наполнял
все помещение. Женщины
раздевались и наклонялись над
огнем.
Под действием горячих
паров тело начинало потеть, поры
раскрывались и впитывали
драгоценные ароматы.
ИЗОБРЕТЕНИЕ
БЕССМЕРТНЫХ БОГОВ!
Древние греки
познакомились с ароматическими
веществами после битвы при Гавга-
меле в 331 году до н. э.
Захватив персидского царя Дария,
воины Александра
Македонского нашли среди его вещей
небольшие сосуды и коробочки
с благовониями. Сначала это
вызвало у греков только
насмешки. Но прошло несколько
лет... и победители тоже
пристрастились к душистым
веществам. Они даже приписали их
«изобретение» бессмертным
богам. Ароматические
жидкости и мази сделались в Элладе
необходимой
принадлежностью.
Душили мебель, кушанья,
залы для пиршеств,
опрыскивали розовой водой гостей.
Наиболее рьяные поклонники
благовоний пускали в залы, где
находились гости, голубей с
надушенными крыльями. Птицы
окропляли присутствовавших
падавшими с крыльев каплями
душистых веществ.
59
Египетский жрец воскуривает
ароматы (рисунок на камне)
С ТОЧКИ ЗРЕНИЯ
МУДРЕЦОВ
Многие выдающиеся деятели
древней Греции видели в
увлечении парфюмерией большое
зло и старались бороться с ним.
Например, Солон предписывал
афинянам не употреблять
благовоний. Сократ утверждал, что
надушившись, все приобретают
одинаковый запах — и
достойные, и недостойные; а это
плохо. В Спарте всех торговцев
косметикой изгоняли из города,
чтобы они не переводили зря
масло. Конечно, все эти
запреты и ограничения не достигали
цели.
ДУХИ И ПИРОГИ
От греков обычай
пользоваться ароматическими
веществами перешел к римлянам.
Потребление духов достигло
здесь поразительных размеров.
Их добавляли в воду для
купания, обрызгивали постели,
подмешивали ароматические
жидкости в вина и другие
напитки.
Даже пироги пекли так, что
из них при малейшем
прикосновении струилось пахучее
вещество — вероятно,
растворенный в вине шафран.
Только перечисление
парфюмерных и косметических
средств занимает в сочинениях
Плиния несколько страниц. А
древнеримский поэт Овидии
Назоы написал целое сочинение,
называвшееся «Косметики».
К сожалению, от него
сохранился только небольшой
отрывок.
МОНАХ ИЗОБРЕЛ
ТУАЛЕТНЫЙ УКСУС
В средние века нравы были
более суровыми. Теперь только
во время церковных служб
священники курили фимиам и
помазывали молящихся душистой
миррой.
В 1608 году в одном из
монастырей Флоренции появилась
парфюмерная фабрика,
основанная
монахами-доминиканцами. Знать
покровительствовала хозяевам фабрики и делала
щедрые взносы для ее
расширения. В 1659 году один из
монахов изобрел, в числе других
косметических средств,
туалетный уксус, который вскоре
приобрел большую популярность.
В туалетный уксус, кроме
спирта и душистых веществ,
входит около 3% уксусной
кислоты. Процветающая фабрика
стала известна во всей Европе.
МУЖЧИНЫ ЗАЩИЩАЮТСЯ
В Англии парфюмерия
достигла расцвета во времена
королевы Елизаветы. Духи и
всевозможные косметические
средства употреблялись в огромных
количествах. В XVIII веке
англичанки стали настолько
злоупотреблять притираниями,
что в 1770 году парламент (в
нем заседали, конечно, только
мужчины) единогласно принял
билль, в котором говорилось:
«Всякая женщина, какого бы
она ни была возраста,
положения или профессии; девица,
замужняя или вдова, которая
с помощью косметики, румян,
помад и проч. соблазнит к
браку мужчину, наказу ется, как
обмаящица, а самый брак
считается недействительным, если
обманутый муж этого
пожелает».
Билль был отменен совсем
недавно...
О ПРОИСХОЖДЕНИИ
ТРОЙНОГО
ОДЕКОЛОНА
Наполеон I не любил духов.
Это вскоре сказалось на нравах
французского двора. В моду
вошел одеколон, который
производил в Кельне итальянский
химик и предприниматель
Жан-Мари Фарина, — так
называемая «Кельнская вода», не
только освежающая, но и
укрепляющая кожу.
Это была одна из первых
парфюмерных композиций,
ставших классическими. И
сейчас этот одеколон (с несколько
измененной рецептурой)
распространен повсеместно под
названием «Тройной одеколон».
Основой одеколона служит 60—
80-процентный раствор
этилового спирта с добавлением
цветочных композиций.
РАЗНООБРАЗИЕ
И ТРАДИЦИИ
Несмотря на то, что
современный человек далек от того,
чтобы втирать себе в кожу
душистые мази, опрыскивать
духами стены комнат и
добавлять ароматические вещества
в еду, общее потребление духов
по сравнению с древностью
и даже с эпохой Возрождения
нам япго возросло. Объясняется
это просто: раньше
парфюмерия была доступна только
богатым людям, а теперь ею поль- |
зуется большинство населения.
Разнообразие ассортимента
позволяет каждому выбрать
себе духи или одеколон по вку-
60
Древнеегипетский сосуд для
благовоний
су. Некоторые употребляют
одни и те же составы на
протяжении всей жизни. Особенно
это принято в Англии, где такое
постоянство считается шиком.
Многие известные исторические
лица (например Гладстон, Чем-
берлен) всегда пользовались
только «своими» духами. Этот
аромат служил как бы
предвестником появления их
владельца.
ПАРФЮМЕРИЯ
В РОССИИ
Русская парфюмерная
промышленность возникла в
середине XIX века. Это были
фабрики Брокара, Остроумова, Рал-
ле и другие — всего около
20 предприятий. Работали они
на импортном сырье. Несмотря
на то, что русские
парфюмерные изделия отличались
высоким качеством, убеждение, что
французские духи все-таки
лучше, давало знать. Однажды
владелец фабрики Брокар
проделал такой опыт. Выпустив
в продажу новый сорт духов, он
разлил в такие же флаконы со
своими этикетками
французские духи, пометив эти
флаконы особым знаком. Затем он
обратился к покупателям
с просьбой прислать отзывы.
Покупатели единодушно
одобрили новинку;
немногочисленные претензии относились
только к флаконам, в которых
были французские духи...
СОВЕТСКАЯ
ПАРФЮМЕРНАЯ
ПРОМЫШЛЕННОСТЬ
За годы советской власти в
СССР, кроме крупнейших
парфюмерных фабрик в Москве,
Ленинграде и Риге, построены
новые предприятия в Харькове,
Николаеве, Казани,
Свердловске, Львове, Краснодаре,
Ташкенте. Они работают на
первоклассном отечественном сырье.
По количеству выпускаемой
продукции парфюмерно-кос-
метическая промышленность
СССР прочно занимает первое
место в мире. А о качестве
советской парфюмерии
свидетельствует тот факт, что мы
экспортируем духи и одеколон в
десятки стран, в том числе
в США, Канаду, Англию, ФРГ.
Высокий показатель
отличного качества наших духов —
присуждение Ленинградской
фабрике «Северное сияние»
золотой медали на Парижской
выставке 1937 года и
Московской фабрике «Новая заря» —
золотой медали на Всемирной
выставке 1958 года в Брюсселе.
Я. Ф. ПЕШКОВСКИЙ
ЗАПАХИ
ИЗМЕНЯЮТСЯ
Часто, находясь в
общественном месте, поражаешься
смешению запахов, которое там
царит... Поистине, многие
любители парфюмерии не знают меры
в своем увлечении!
Запах духов не бывает
всегда однородным. Различают три
основные стадии запаха духов,
переходящие одна в другую:
начальный запах, основной
(серединный) и остаточный.
Наиболее характерные свойства
запаха проявляются только через
15—20 минут после нанесения
духов на ткань или волосы.
Обычно через 20—25 часов
основной запах духов начинает
затухать, а остающийся
остаточный запах может держаться
на надушенной поверхности
еще часов 10—15.
Такие изменения в оттенках
запаха духов происходят
вследствие различной испаряемости
веществ, входящих в
парфюмерные композиции.
Качество духов
характеризует основной, серединный
запах. Чем он продолжительнее,
тем более стойкими считаются
духи.
ВРЕМЯ И ЗАПАХ
Некоторые считают, что
старые духи или остатки духов во
флаконе, который долго стоял,
лучше пахнут и более стойки.
Это верно. Закрепителем духов
оказалось время. В духах все
время происходят сложные
химические и физические
процессы — идут реакции, в которые
вступают компоненты,
входящие в композицию и
принадлежащие к разным классам
химических соединений.
Но существует предел, когда
желательный процесс —
созревание переходит в
нежелательное явление — старость.
Установить здесь границу очень
трудно^ каждые духи ведут себя
по-своему. У хороших сортов
духов и одеколонов
выдерживание (как и для лучших марок
вин и коньяков) только
улучшает качества.
А. ФЕДОРОВ
61
Немало чудес повидал
знаменитый итальянский
путешественник и купец Марко Поло на
пути в Китай через
Центральную Азию семь столетий назад.
Среди вещей, поразивших его
больше всего, были
туркменские ковры, которые он назвал
самыми тонкими и красивыми
в мире. Уже в средние века
туркменские орнаментальные
ковры были гордостью многих
коллекций Европы.
В Туркмении издавна
сложились благоприятные условия
для развития самобытного
искусства — ковроделия.
Ковровые изделия не только
украшали жилище: они служили
материалом для дверных
занавесей, мешков, заменявших
сундуки, перекидных сумок — хур-
джумов и многих других
вещей, необходимых в
полукочевом быту туркмен. По
многовековой традиции, каждая
туркменка к свадьбе ткала ковер
себе в приданое. За сырьем для
ковроделия — шерстью не надо
было далеко ходить:
овцеводство было главной отраслью
натурального хозяйства
туркменских племен. Шерстяную
пряжу окрашивали корнями
марены, кожурой гранатов и
незрелых грецких орехов,
листьями айвы, инжира, солодки,
цветами шафрана, корой
яблони и крушины. Не особенно
Ковер «Долой калым», вытканный
в 1927 г. туркменской
ковровщицей Биби Ахмедовой
КРАСКИ
ТУРКМЕНСКОГО
КОВРА
Кандидат химических наук В. И. КРИВЕНЦОВ
Институт химии АН Туркменской ССР
Ь ^h)$P:b^~^Xmz
62
широка была палитра древних
мастеров — всего из 7—10
цветов состоит красочная гамма
туркменских ковров. Но зато в
гармоничном сочетании этих
цветов — красного, оранжевого,
а также желтого, зеленого,
синего, черного — проявлялось
высокое искусство
туркменских ковровщиц.
До сих пор орнаментальные
туркменские ковры ручной
выработки ценятся наравне с
лучшими произведениями
искусства. Академик А. Е. Ферсман
писал, что старинный
туркменский ковер представляется ему
законченной и четкой картиной
художника. Такое совершенство
достигается благодаря мягким
сочетаниям красных тонов
фона и разноцветных «гелей» —
восьмиугольных
орнаментальных фигур. Это придает ковру
радостный, торжественный и в
то же время сдержанный,
благородный характер.
Спрос на туркменские ковры
в нашей стране и за рубежом
не ослабевает. Им
присуждаются почетные дипломы и медали
на международных выставках
в Париже, Нью-Йорке,
Брюсселе. Почти на каждой
международной ярмарке отмечается
высокая художественная ценность
наших ковров.
Не зря изображение
орнамента ковра украшает герб
Туркменской ССР. Ковры —
национальная гордость
республики.
ДРАГОЦЕННАЯ МАРЕНА
Для производства ковров,
предназначенных служить не
одному поколению людей,
нужны гораздо более прочные
красители, чем для крашения,
например, текстильных изделий,
которые изнашиваются
быстрее, чем успеет выгореть их
окраска.
В народном производстве
ковров издавна употреблялись
природные красители. Их
красящее начало — это чаще всего
производные ароматических и
гетероциклических
соединений — нафтахинона, антрахино-
на, хромона и индола. Наибо-
сф dp
о о
Нафтахинон Антрахинон
О
СО СИ
Индол Хромон
лее светопрочные из них —
производные антрахинона.
Основным природным источником
красителей на их основе с
незапамятных времен служили
корни распространенного в
Средней Азии и на Ближнем
Востоке растения марены,
которую так и называют —
марена красильная.
Красящее начало марены —
это соединения антрахинона, у
которых два или три атома
водорода в одном из колец заме-
о он
о
Ализарин
A, 2-диоксиантрахинон)
О ОН
dpr
о он
Пурпурин
A, 2, 4-триокСиантрахинон)
щены на гид рок с ильные
группы. Главные из них — ализарин
и пурпурин. Ализарин (его
название и происходит от древнего
имени марены — «ализари»)
находится в растении в виде
соединения с углеводом —
гликозида, который называется рубе-
ритриновой кислотой. Как и
большинство гликозидов, она
обладает некоторой
растворимостью в воде и спирте.
При нагревании раствора
гликозида, особенно в
присутствии кислоты, он гидролизует-
ся на ализарин и углевод. Сам
ализарин хуже растворим в
воде, но зато растворяется во
многих органических
растворителях.
Из-за растворимости чистого
ализарина и его гликозида они
не годятся для крашения
тканей: окраска будет бледная и
непрочная — до первой стирки.
По тем же причинам нельзя
окрасить ткань и пурпурином.
Поэтому для крашения
тканей используют свойство
ализарина и пурпурина
образовывать так называемые лаки —
внутрикомплексные соединения
с некоторыми металлами.
В общих чертах процесс ла-
кообразования происходит так.
Окраска антрахинона и его
производных зависит от
электронной плотности входящей в
их состав хиноидной группы
(=/ \—). Присоединенные
к ней в молекулах ализарина
и пурпурина атомы кислорода
имеют достаточно подвижную
пару электронов, благодаря
которой образуют связь с
металлом. В результате окраска
соединения становится более
глубокой.
При образовании
алюминиевого лака ализарина атом
алюминия, помимо такой связи с
кислородом хиноидной
группировки, замещает водород в
ближайшей к ней ОН-группс.
63
Образование алюминиевого лака
ализарина
Таким же образом атом
алюминия может связываться и
еще с одной молекулой
ализарина. Образуются новые шести -
членные кольца, обладающие
большой прочностью. Новое
соединение уже нерастворимо ни
в воде, ни в спирте, ни в
бензоле, ни в хлороформе, ни во
многих других растворителях.
В то же время оно имеет ярко-
красную окраску, не
выцветающую под действием света.
Разные металлы дают лаки
разного цвета: это объясняется
различием их зарядов и
характера электронной оболочки.
Хром дает с ализарином
коричневый лак, а трехвалентное
железо — фиолетовый.
При крашении тканей
подобными красителями и
происходит образование лаков.
Шерстяную пряжу сначала
помещают в раствор солей
металлов. В зависимости от того,
какой цвет нужно получить,
применяют алюмокалиевые
квасцы, двухромовокислый калий,
молибдат аммония, хлористое
олово, добавляют соли кальция.
При этом атомы металла
связываются с содержащимся в
шерсти белком — кератином,
обладающим способностью к
ионному обмену. Такой
процесс закрепления металла на
пряже или ткани называется
протравливанием.
Теперь остается поместить
протравленную пряжу в
раствор красителя, чтобы на ней
образовались прочные,
несмываемые лаки.
Как показывают
археологические находки, так красили
ткани мареной еще в древнем
Египте, Сирии, Персии,
Монголии, Парфянском государстве,
столица которого находилась
недалеко от Ашхабада. В
Европе марена появилась сначала
в Испании, Италии, а затем
распространилась в Германию,
Францию, Голландию и другие
страны.
Из марены делали и
масляные художественные краски,
отличающиеся высокой
светостойкостью, богатством и
теплотой оттенков, — баканы,
широко известные под их
старинными названиями: «лак
Рембрандта», «красная Ван-Дейка»,
«Рубенс-лак», крапп лак (от
древнегерманского слова «Кгар-
so» — крючок, как называли
марену за колючки на ее
стеблях и листьях). Получаемый
синтетическим путем
алюминиевый лак ализарина и теперь
называется крапплаком.
Лаки из марены считались
более прочными, чем даже
драгоценный кармин,
добывавшийся из кошенили — черве-
цов, обитающих на кактусах.
Особенно большое
распространение получили краски из
марены в миниатюрной живописи.
Марена славилась и как
лечебное средство. Начиная с
Гиппократа и Галена, ее
применяли для лечения рахита,
заболеваний почек, печени и других
болезней. Шерстяные ткани,
окрашенные мареной,
считались целебными при подагре и
ломоте в костях.
В средние века марена
разводилась повсеместно. В 1720
году в Москве появился завод по
размолу ее корней. Марена
считалась лучшим красителем
в ситцепечатании, и к 1869
году годовое потребление ее
сухих корней достигло 4,5 млн.
пудов!
МАРЕНА УСТУПАЕТ
ПОЗИЦИИ
Однако дни преуспевания
марены были сочтены.
Первый тяжелый удар по
этой культуре нанесло
открытие 18-летнего англичанина
Вильяма Генри Перки на.
В 1856 г., пытаясь в своей
домашней лаборатории
синтезировать хинин путем окисления
анилина, он получил первый в
истории синтетический
краситель мовеин, и уже на
следующий год основанная им
фабрика выпустила мовеин в
продажу. В 1869 году К. Гребе и
К. Либерман впервые в истории
синтезировали природный
краситель ализарин — основное
красящее вещество марены.
Вскоре были получены и
другие синтетические
красители — пурпурный фуксин и
голубой трифенилрозанилин.
Родилась анилино-красочная
промышленность,
теоретические основы которой заложил
еще в 1842 году русский химик
Н. Н. Зинин, открывший способ
получения анилина из
нитробензола. С тех пор
производство марены быстро пошло на
убыль.
Современная
анилино-красочная промышленность
производит огромные количества
красителей сотен
наименований. И все-таки... Многие
любители и знатоки ковров ценят
старые туркменские ковры,
пряжа для которых
окрашивалась естественными
растительными красителями и прежде
всего мареной, выше новых.
Опытные товароведы с
первого взгляда отличают такие
ковры. Некоторые специалисты
считают, что большинство
синтетических красителей не всег-
64
t
<$
^s
да удовлетворяет требованиям
ковроделия и что необходимо
вернуться к растительным
красителям, отличающимся
богатством и теплотой оттенков. Еще
в 1930-х годах в Иране и
некоторых других странах были
даже приняты законы,
запрещавшие применение синтетических
красителей в ковроделии и
производстве гобеленовых изделий.
Все это заставило ученых
снова заняться изучением
растений-красителей, чтобы
понять причину их преимущества
перед синтетическими
красками.
ПСЕВДОПУРПУРИН
ОТКРЫВАЕТ
НОВЫЕ ПЕРСПЕКТИВЫ
Долгое время считалось, что
красящие начала марены
хорошо известны. Это были
ализарин и пурпурин. И тот и другой
краситель были давно
синтезированы, но окрашенная ими
пряжа по цвету и стойкости все
равно значительно уступала
пряже, окрашенной
природными красителями.
Только в 1936 году Хилл и
Рихтер выделили из корней
марены еще одно красящее
вещество — псевдопурпурин,
также представляющий собой
производное антрахинона. Он
отличается от пурпурина только
тем, что вместо незамещенного
водорода в его правом кольце
стоит группа — СООН. Он-то и
О
он
он
СООН
он
Псевдопурпурин A, 2, 4-триок-
сиантрахинонкарбоновая-3
кислота)
оказался главным красителем
марены. Лаки
псевдопурпурина отличаются яркостью,
необыкновенно прозрачны и
превосходят по прочности лаки
ализарина и пурпурина. Теперь
именно присутствием
псевдопурпурина объясняют
преимущество мареновых лаков перед
синтетическими красителями.
Несмотря на столь высокое
качество псевдопурпурина как
красителя, он до сих пор нигде
не выпускается в
промышленных масштабах. Хотя лаки
псевдопурпурина отличаются
прочностью, само это вещество
очень нестойко, и
синтезировать его крайне трудно. При
нагревании с водой уже при
температуре 70° С
псевдопурпурин начинает отщеплять
углекислый газ и переходит в
обычный пурпурин.
(Окончание на стр. 88)
КАК
ОБРАЗУЮТСЯ
СИТАЛЛЫ?
1
2|
3
4
5
6
1 1
Кино все шире используется как инструмент научного
исследования.
На вклейке — снятый через микроскоп процесс
кристаллизации стекла — образование нового материала ситал-
ла, очень твердого, прочного, термостойкого. Ситаллы
находят все большее применение в промышленности как
конструкционный материал.
К микроскопу (фото 1) крепится высокотемпературная
печь. Это очень маленькая платиновая петелька (для
сравнения на фото 6 она снята рядом с игольным ушком), через
которую пропущен ток. По изменению цвета раскаленной
платины можно судить о температуре в момент съемки.
На фото 2 и 3 — расплавленное стекло при температуре
1560° С — самой высокой температуре, при которой вели
съемку. Затем платиновую печь охлаждали, и при
температуре 900° С наблюдали кристаллизацию стекла (фото 4). На
фото 5 — кристаллизованное стекло — ситалл.
Киносъемка дает возможность определить начало,
скорость и характер кристаллизации, вид преобладающей
кристаллической фазы, т. е. все характеристики процесса,
определяющие термостойкость, механическую прочность и
электроизоляционные свойства полученного ситалла.
Киносъемка, микроскоп и высокая температура,
примененные одновременно, позволили впервые в нашей стране
наблюдать динамику кристаллизации стекла — процесс
возникновения ситаллов.
5 Химия и Жизнь, № 9
65
ГРАММОФОННАЯ
ПЛАСТИНКА
Кандидат химических наук
М. Л. ЕЗЕРСКИЙ
Рисунки Е. ДАНИЛЬЦЕВА
Начнем с утверждения:
грампластинка — уникальное изделие.
Уникальность ее состоит в том,
что при огромных тиражах (сотни
миллионов штук в год) каждую
пластинку изготовляют с очень
высокой точностью. Звуковые
канавки имеют глубину 70 микронов
для обычных пластинок и 30
микронов для долгоиграющих. И в
такой канавке записана вся
«звуковая информация». Как достичь
такой точности при массовом
выпуске? Для этого нужно
комплексное производство, в значительной
мере — химическое. Без
гальванотехники и полимерных
материалов промышленное изготовление
граммофонных пластинок было бы
невозможным.
СПОСОБ ШАРЛЯ КРО
Пословица «Слово — не
воробей...» до поры до времени была
справедливой. И все же кое-кто
верил, что слово можно поймать
и услышать вновь. Слышал же
барон Мюнхгаузен замороженные
звуки...
Звуковые колебания воздуха,
воздействуя на легкий острый
предмет (например," иглу),
заставляют его колебаться. Колебания
иглы могут оставить след на
какой-нибудь поверхности. Этот
след и есть запись звука.
Звуковая запись обратима — ее можно
воспроизвести. Эта мысль
впервые была высказана французским
ученым Шарлем Кро в 1877 году.
Он писал: «...Мой способ состоит
в получении следа переменного
движения вибрирующей
мембраны, так чтобы можно было
воспользоваться тем же следом для
воспроизведения первоначальных
вибраций... Прибор,
застенографировавший ваши слова, пение,
игру, сохранит их в виде клише,
которое может быть сделано
металлическим с помощью
гальванопластики и которое при
воспроизведении повторит ваш голос,
произношение, тембр...» Этот
принцип размножения
звукозаписи остался в силе и в наши дни.
Кро не удалось воплотить свои
идеи в жизнь. Первый прибор,
воспроизводящий звук, изготовил
Т. А. Эдисон. Он назвал его
фонографом. В фонографе звук
записывался на барабан, покрытый
оловянной фольгой, в которую
вдавливалось стальное острие.
Фонограф произвел впечатление
на современников, однако
широкого применения не получил.
Каждая запись была уникальной,
и размножить ее было нельзя.
Это был только шаг к прибору, о
котором говорил Кро.
Первый патент на
грампластинку, близкую к современной,
получил в США Е. Берлинер в 1888
году. Он записывал звук на
стеклянный диск, покрытый парафином.
С этого диска Берлинер получал
66
гальванопластическую копию, с
которой прессовал пластинки из
целлулоида. Схема процесса,
предложенного Берлинером,
похожа на современную; позже в
нее лишь вносились
усовершенствования. Так, очень скоро
парафинированные диски заменили
дисками из воскового сплава,
которые, в свою очередь, уступили
место алюминиевым дискам,
покрытым нитролаком — тондискам.
Эбонит вытеснил целлулоид
(первая партия пластинок широкого
потребления была отпрессована
из эбонита). Но и эбонит
продержался недолго — ему на смену
пришла пластмасса на основе
шеллачной смолы. Этот материал
применяли длительное время —
почти все старые грампластинки
сделаны из него. Только в 50-е
годы шеллак был вытеснен
синтетическими смолами.
В России первый завод
грампластинок был построен в Апре-
левке под Москвой в 1910 году.
Сейчас Апрелевский завод —
самый крупный завод
грампластинок в СССР.
ЗВУК В КАНАВКЕ
Первый этап производства
грампластинок — звукозапись.
Механические колебания воздуха
при звукозаписи превращаются
сначала микрофоном в
электрические, а электрические рекордер
вновь превращает в
механические. Эти колебания передаются
резцу, который записывает их на
тондиске. Тондиск вращается в
горизонтальной плоскости со
скоростью 33, 45 или 78 обооотов в
минуту. Резец рекордера
вырезает на диске спиральную линию.
Если звука нет, то на диске
чертится линия одной толщины. Это
«запись молчания». При записи
звука резец колеблется в
поперечной плоскости к направлению
линии; чем сильнее звук, тем
шире размах колебаний. Получается
канавка сложного профиля. Это и
^звукозапись
получение
оригиналов
изготовление | изготовление
пластмассы у этинетон
изготовление
\ матриц
прессование
пластиной
шлифовна
*11тц.|.,.,и«ч.....ц.с
нонтроль
Схема производства грампластинок
67
есть звукозапись. Ее можно
прослушать на проигрывателе.
Однако этот единственный
экземпляр звукозаписи нужно
беречь. И прежде чем делать
пластинки, необходимо иметь
солидный запас копий тондиска —
оригиналов. Такие оригиналы,
сделанные из металла, будут
инструментом для прессования
грампластинок.
ОРИГИНАЛ
НА ОРИГИНАЛЕ
Гальванопластика, пожалуй,
единственный метод, которым
можно получить точную копию
тондиска — со всеми тончайшими
изгибами стенок канавки. Металл,
осажденный в гальванической
ванне, безупречно воспроизводит
рельеф той поверхности, на
которую он осажден. Но тондиск не
проводит электричества, и для
снятия гальванопластической
копии его приходится
металлизировать. Обычно используют
химическое серебрение —
восстановление серебра из раствора его соли
каким-нибудь жидким
восстановителем, например, формалином.
Эта реакция известна каждому
старшекласснику под именем
реакции «серебряного зеркала».
Смесь двух растворов
напыляется пневматическим
пистолетом на поверхность тондиска. Тон-
диск при этом вращается в
вертикальной плоскости, и растворы
равномерно растекаются по его
поверхности. Она покрывается
тонким сплошным слоем
блестящего серебра.
Теперь тондиск поступает в
гальванический цех, где с него
снимают металлические копии,
которые и называются
оригиналами. На посеребренный тондиск
гальванически наносят тонкий слой
никеля, а поверх него — слой
меди или еще один слой никеля. Их
отделяют от тондиска. Так
получается «негативный отпечаток»
звукозаписи: углублениям на тон-
диске соответствуют выступы на
никелевом слое. Эта негативная
копия называется первым
оригиналом.
Первым оригиналом можно
прессовать пластинки—на них
получится правильное (позитивное)
изображение записи, как и на тон-
диске. Этого, однако, не делают
по двум причинам. Во-первых, с
одного оригинала можно отпре-
совать не больше 500 пластинок.
А во-вторых, если первый
оригинал случайно испортится, запись
придется повторять — тондиск
нельзя использовать дважды.
Поэтому первый оригинал имеет
только одно назначение: с него
получают следующие
металлические оригиналы.
Второй оригинал копируют с
первого так же, как с тондиска.
Правда, чтобы никель не сросся
с никелем, на первый оригинал
наносят разделительный слой —
сотые доли микрона окисла
никеля. Для этого достаточно
погрузить диск оригинала в раствор
бихромата калия.
Второй оригинал — это уже
позитивное изображение записи.
Его можно проиграть, но им
нельзя прессовать пластинки, так
как на пластинке получится запись
«наоборот». Обычно с одного
первого оригинала можно снять
десять вторых оригиналов
хорошего качества. Соответственно с
десяти вторых оригиналов
получают сто третьих. Ими можно
прессовать пластинки, что часто и
делают. Но если тираж пластинок
большой, готовят тысячу пятых
оригиналов.
Когда третий или пятый
оригинал идет в производство, то его
дополнительно хромируют в
гальванической ванне. Хром — очень
твердый металл. Он меньше
изнашивается, чем никель, а тем
более медь. После покрытия
хромом оригинал получает новое
имя. Его называют матрицей. Это
уже термин прессовщиков.
КОМПОНЕНТЫ
ЗВУЧАЩЕЙ
ПЛАСТМАССЫ
Прежде чем знакомиться с
прессованием грампластинок,
давайте посмотрим, из чего их
прессуют.
Пластмасса, из которой
сделана пластинка,— не индивидуальное
вещество, а смесь многих
веществ. Обычно ее называют более
благозвучно — композиция.
Главный компонент
композиции — связующее. Это всегда
смола. Только прежде она была
68
4S& m
ТА XrLU fZZS S^ Рч *bos £*
природной: шеллак — смола
животного происхождения. Теперь
используют только синтетические
смолы, большей частью поливи-
нилхлорид (ПВХ) и поливинилаце-
тат. ПВХ применяют вместе с
пластификатором, который
облегчает формование материала.
Сополимер винилхлорида и винилаце-
тата — винилит — достаточно
пластичен и легко формуется без
пластификатора. Он применяется
для изготовления долгоиграющих
пластинок.
Наполнитель — это обычно
минеральный порошок, который
придает пластинке твердость. Чаще
всего берут измельченные
природные минералы: шифер
(глинистый сланец) или маршалит
(пылевидный кварц). Чтобы окрасить
пластинку в черный цвет,
прибавляют еще сажу.
Для уменьшения трения между
иглой и пластинкой вводят
смазки. Они особенно важны для
обычных пластинок. Такими
смазками служат различные воска,
чаще всего — синтетические.
Смазка удлиняет жизнь
пластинки — поверхность меньше
изнашивается
Наконец, чтобы удешевить
композицию, в нее вводят
готовую измельченную пластмассу —
из бракованных пластинок или тех,
которые сдают в утиль.
Содержание боя в различных
композициях довольно велико — от 20
до 40%.
Материалы очень тонко
измельчают, затем смешивают
точно по рецепту и направляют в ма-
стикатор. Эта машина
перемешивает массу и нагревает ее.
Получается тестообразная масса,
которая после остывания
становится твердой.
После варки в мастикаторе
массу пропускают через вальцы и
полученное «полотно» подают к
каландрам. Вращаясь навстречу
друг другу, валки каландра
раскатывают массу в лист толщиной
около 3 мм. Лист пропускают
через систему ножей, которые
режут из него четырехугольники —
таблетки. Из них-то и прессуют
пластинку.
Так готовят пластмассу для
обычных пластинок. Для
долгоиграющих пластинок, требующих
особой точности, наполнитель
слишком груб. Приходится
обходиться без него. Массу без
наполнителя готовят на
специальных вальцах, или же не делают
таблеток вообще, а выдавливают
гранулы на черзячной машине —
экструдере.
Пластмасса для пластинок
(таблетки или гранулы) проходит
специальный контроль: на опытном
прессе из нее делают пробные
пластинки, определяют их
прочность и другие характеристики.
Если все в порядке, то
пластмасса идет в прессовый цех.
ОТ ТАБЛЕТКИ
К ПЛАСТИНКЕ
Прессование — самый старый
и самый распространенный
способ изготовления грампластинок.
Он держится так долго потому,
что при всей своей простоте,
прессование позволяет получить
пластинки отличного качества. Вот
как прессуют пластинки.
Прессформа для пластинок —
это две металлические пластины,
соединенные шарнирно. Они
могут закрываться и раскрываться,
как книга. Прессформу сначала
заряжают — укладывают в
«книгу» две матрицы, которые и
печатают звуковую канавку на
обеих сторонах пластинки. В стенках
преесформы есть каналы — по
ним подают водяной пар. Рядом,
на нагревательном столе,
разогревают и размягчают таблетку
или гранулы. В горячую пресс-
форму кладут сначала этикетки,
потом пластмассу; «книгу»
захлопывают и передвигают под пресс.
Раскрытая «книжка»
преесформы, в которую вставлены две
матрицы, оформляющие
пластинку
Как только она встала на место,
подается высокое давление A00—
150 ат). Нескольких секунд
достаточно, чтобы под таким
давлением разогретая тестообразная
пластмасса заполнила все
углубления и приняла форму
пластинки. Затем прессформа с
пластинкой охлаждается — вместо пара
пускают холодную воду — и
давление сбрасывается. Холодная
прессформа с пластинкой
автоматически выкатывается из пресса и
раскрывается: пластинка готова.
Один цикл закончен, можно
начинать следующий. Все это длилось
30—60 секунд.
Пластмасса, даже звучащая, —
это все же обычная пластмасса.
А прессование — не самый
быстрый способ переработки
пластмасс. Поэтому в последнее время
стали применять более
производительный способ — литье под
давлением. Для литья чаще
используют полистирольную
пластмассу — она легче льется. Звучат
такие пластинки хуже, чем вини-
При литье под давлением
расплавленная масса выдавливается
поршнем в форму, и пластичный
материал заполняет полость
между матрицами
литовые. Однако высокая
производительность (на одну пластинку
тратится всего 20 секунд)
привлекает внимание к этому способу.
Кроме того, с одной матрицы
вместо 500 можно сделать 15
тысяч отпечатков. При литье
матрица меньше изнашивается.
Еще быстрее можно сделать
грампластинку штамповкой.
Штампуют листовой материал,
например, ацетилцеллюлозную
пленку.
Пленка с рулона проходит
через камеру нагрева, в которой
она размягчается, и поступает в
штамповальную машину.
Специальный механизм прекращает
движение пленки на несколько
секунд, и в это время пресс резко
прижимает матрицы к пленке.
Затем матрицы возвращаются в
исходное положение, пленка вновь
перемещается, и процесс
повторяется. Производительность — 5—
8 тысяч пластинок в час. Однако
пока что штампованные
пластинки хуже не только
отпрессованных, но и литых, поэтому этим
способом делают не музыкальные
пластинки, а записи уроков,
лекций, выступлений. »
МАГНИТОФОН
ИЛИ
ПРОИГРЫВАТЕЛЬ!
Этот вопрос сводится к
следующему: вытеснит ли
магнитофонная запись граммофонную?
Каждый из вас может привести
немало доводов в пользу
магнитофона, и в то же время
статистика каждый год утверждает: спрос
на грампластинки неуклонно
растет. Соответственно растет и
выпуск пластинок.
Пожалуй, дело в том, что
противопоставлять пластинку
магнитной ленте неверно. Магнитофон и
проигрыватель не исключают, а
дополняют друг друга. У
грампластинки есть важное
преимущество — если вам нужна
какая-нибудь запись, вы идете в магазин
и покупаете пластинку. Кусочек
ленты с одной песней не купишь.
Размножать пластинки на заводе
намного легче, чем магнитофиль-
мы. Многие владельцы
магнитофонов делают записи с пластинок.
Качество записи на пластинке
намного выше, чем на бытовом
магнитофоне.
Кстати, теперь в производстве
грампластинок используют магни- I
тофоны — только, конечно, не
бытовые, а студийные — сложные
и дорогие.
При записи на тондиск нужно
сделать хоть одну пластинку,
чтобы узнать, хороша ли запись.
А вдруг певец взял фальшивую
ноту? Поэтому звук записывают
сначала на магнитофон и сразу
прослушивают запись. Если
нужно, повторяют запись — до тех
пор, пока все будет безупречно.
И тогда уже с ленты звук
записывают на тондиск.
Долго ли еще будут
существовать граммофонные пластинки?
Пока на этот вопрос ответить
трудно. Ясно одно: магнитная
запись в ее современном виде не
вытеснит механическую — на
пластинке. И еще одно
обстоятельство: граммофонную запись
можно хранить неограниченно долго —
в виде металлических оригиналов.
Это особенно ценно для
уникальных, неповторимых записей.
Граммофонную пластинку рано еще
списывать в архив.
70
ВСПЫШКА
ГЕНИЯ
«Как зарождается новая идея? Что приводит
к вспышке гения, к решающему этапу
научного открытия, к завершающему моменту
в творческом процессе?»
Профессор Колумбийского университета
А. Гаррет — составитель сборника
«Вспышка гения» — пытается ответить на этот
вопрос, найти ключ к разгадке.
В сборнике — описания многих открытий
из разных областей науки. Составитель
стремился рассказать о ключевом эксперименте
словами самого первооткрывателя, а если
это оказывалось невозможным, то словами
свидетелей открытия.
А. Гаррет отдавал предпочтение не
ценности открытия, а скорее «способу, при
помощи которого оно совершилось».
Сопоставляя обстоятельства,
сопутствующие тому или иному открытию, Гаррет
приходит к выводу, что все их
многообразие можно разделить на три группы:
открытия, сделанные методом проб и ошибок,
методом запланированного, заранее
намеченного исследования и случайные.
А. Гаррет считает, что вероятность
открытия, сделанного методом проб и
ошибок, зависит в основном от того, достаточно
ли число проведенных экспериментов.
При запланированном, преднамеренном
исследовании открытие зависит, конечно, от
основной идеи, которая подтверждается или
СТРОЕНИЕ АТОМА —ЭРНЕСТ РЕЗЕРФОРД
В 1896 г. Мария Кюри-Склодовская и Пьер Кюри
открыли радиоактивность и впервые выделили
соединения радия.
В 1911 году Эрнест Резерфорд, использовав новое
орудие в атомных исследованиях — бомбардировку
различных элементов а -частицами, — получил
необходимые данные и блестяще разрешил проблему
строения атома.
Вот как описывает Резерфорд в лекции,
прочитанной им в Кэмбридже в 1936 году, каким образом
родилась у него идея о строении атома.
«...Сегодня мы будет говорить о
структуре атомного ядра.
отвергается в результате накопления
данных. Труднее и интереснее всего объяснить,
как совершается случайное открытие.
Прежде всего «случайность
благосклонна к прилежному уму» — известные слова
Пастера. Кроме того, общий и, вероятно,
существенный для многих случайных
открытий признак — элемент «серендипити».
Термин «серендипити» ввел Хорее Велпоуль в
1754 году. Термин родился из старой
легенды о принцах Цейлона (Серендипа).
Легенда рассказывает, что у принцев
Серендипа была способность совершать
совсем случайно счастливые и неожиданные
открытия. Они, например, находили не те
вещи, которые упорно искали, а совсем другие
и часто более нужные.
Термин «серендипити» применяют, когда
хотят сказать о счастливых совпадениях,
случайностях. В современном понимании он
означает умение выделять из ряда
привычных фактов интересное и необычное.
Конечно, ни одно из открытий нельзя
строго подвести под одну из этих категорий,
чаще всего в каждом есть элементы всех
трех. Но все же какой-нибудь метод
оказывается главным, и выявление этого помогает
приблизиться к пониманию процесса
научного творчества.
Мы печатаем несколько отрывков из
сборника А. Гаррета «Вспышка гения».
В 1895 г. О. Ленард провел свой
знаменитый эксперимент: пучок электронов,
полученный в разрядной трубке, он пропустил
через отверстие в ней и впервые наблюдал
электроны вне такой трубки. Так как
электроны легко проникали через отверстие,
Ленард сделал вывод, что у атомов,
расположенных в пространстве окна, структура
неплотная, и что они находятся на большом
расстоянии друг от друга. Тогда Ленард
предположил, что в атомах существуют
положительно заряженные образования,
связанные каким-то образом с отрицательными
71
зарядами. Эту идею подхватил Томсон. Он
рассчитал, каким образом отрицательно
заряженные электроны могли бы
распределяться по шару положительного заряда и
таким образом впервые смог объяснить
основную природу периодического закона.
Теперь я перехожу к следующей стадии
исследований — они представляют для меня
огромный интерес, и о них я хочу
рассказать вам во всех подробностях. На этом
примере мне хотелось бы показать, как часто
на важнейшие открытия мы натыкаемся
совершенно случайно.
В то далекое время я занимался
рассеянием а-частиц. Подробно это рассеяние в
моей лаборатории изучал Гейгер. Он
обнаружил, что в тонких листах тяжелых
металлов это рассеяние чрезвычайно мало,
порядка 10" \ Однажды Гейгер спросил меня: «Не
думаете ли вы, что молодому Марсдену
пора поручить небольшую самостоятельную
работу? Он уже давно работает у меня с
радиоактивными веществами». Я согласился и
предложил: «Почему бы не дать ему
проверить, могут ли а -частицы рассеиваться под
большими углами?»
Теперь я могу сказать вам по секрету,
что в такую возможность я совершенно не
верил. Ведь мы хорошо знали, что
а-частицы— это очень массивные быстрые частицы
с большим запасом энергии. Вы сами легко
могли бы показать, что если наблюдаемое
рассеяние складывается из суммарного
эффекта нескольких малых рассеяний, то
вероятность того, что а-частица может
отлететь назад, очень мала. Я помню, как дня
через два или три после нашего разговора
ко мне пришел Гейгер. Он был очень
взволнован: «Частицы отлетают назад!» Ничего
более неправдоподобного в моей жизни не
случалось. Это было почти также
неправдоподобно, как если бы вы выстрелили 15-
дюймовым снарядом по листу папиросной
бумаги, а снаряд отскочил бы от этого листа
и убил вас.
Размышляя над этим невероятным
фактом, я пришел к выводу, что такое
рассеяние могло быть только результатом
единичного столкновения. Но когда я проделал
расчеты, то увидел, что получить что-либо
похожее на тот порядок величин, которые
давал опыт, невозможно, если не принять
предположение — большая часть массы
атома сконцентрирована в каком-то очень
маленьком объеме. И тогда у меня родилась
идея об атоме с чрезвычайно малым
ядром огромной массы, заряженном
положительно.
Основываясь на этом предположении, я
сделал математические расчеты и нашел,
что число частиц, рассеянных под
определенным углом, должно быть
пропорционально толщине рассеивающей фольги,
квадрату заряда ядра и обратно
пропорционально четвертой степени скорости. Гейгер
и Марсден подтвердили эти расчеты серией
блестящих экспериментов.
Какие же следствия вытекали из этой
идеи? Я смог показать, что размер ядра
должен быть очень мал. Я смог оценить
величину заряда ядра и нашел, что в наших
опытах она примерно в 100 раз больше, чем
заряд электрона. Точный расчет тогда
сделать было невозможно, но из общих
соображений было ясно, что заряд ядра
водорода + 1, гелия (-2 и т. д. Гейгер и
Марсден проверили рассеяние на многих
элементах и нашли, что вероятность рассеяния
изменяется пропорционально квадрату
атомного веса. Результат этот был весьма
грубым, но все же вполне достаточным, чтобы
прийти к выводу, что заряд ядра грубо про-*
порционален атомному весу элемента».
ОТКРЫТИЕ ТЕФЛОНА —РОЙ ПЛАНКЕТТ
В 1938 году был открыт полимерный материал,
термо- и коррозионная устойчивость которого не
знает равных среди пластмасс.
Доктор Рой Дж. Планкетт так описывает
открытие полимера, широко известного в наше время под
названием «тефлон».
«...После получения докторской степени
я работал химиком-исследователем в
лаборатории Джексона в Нью-Джерси. Летом
1938 года я занимался изучением
хлорированных и фторированных углеводородов.
В лабораторию привозили очень мало
четырехфтористого этилена, а для одного
из опытов мне понадобилось его довольно
много, и я решил синтезировать его сам.
Полученный сначала на лабораторной, а
потом на опытной установке четырехфтори-
стый этилен собирали в цилиндр, который
охлаждался твердой двуокисью углерода.
Тем временем я пытался получать новые
соединения реакцией четырехфтористого
этилена с другими веществами.
Однажды вместе со своим ассистентом
Джеком Ребока я проводил такой опыт. Че-
72
тырехфтористый этилен испарялся из
небольшого цилиндра (в цилиндре было
приблизительно два фунта четырехфтористого
этилена), установленного на платформу
весов. Газообразный четырехфтористый
этилен, выходящий из цилиндра, пропускали
через прибор для измерения скорости
потока газа и вводили в реакционные сосуды,
где он вступал в реакцию с другими
веществами. В тот день вскоре после начала
эксперимента ассистент заметил, что поток
четырехфтористого этилена уменьшился и
затем прекратился вовсе. Я проверил вес
цилиндра и убедился, что в нем все еще
большое количество вещества, которое, как я
думал, было четырехфтористым этиленом.
Я открыл кран полностью и прочистил
проволокой дырку, но газ не выходил. Тогда я
встряхнул цилиндр и почувствовал, что
внутри цилиндра — какое-то твердое вещество.
Наконец, я открыл ножом цилиндр и
высыпал белый порошок. Я сразу понял,
что четырехфтористый этилен заполимери-
зовался, и белый порошок — это полимер
четырехфтористого этилена. Я тут же
принялся определять свойства белого порошка
и способ его получения.»
МЕТАЛЛУРГИЯ АЛЮМИНИЯ —
ЧАРЛЬЗ М. ХОЛЛ
В 1825 году алюминий стоил в 1500 раз дороже
железа, а сегодня всего лишь втрое. Тому, что
алюминий стал промышленным металлом, мы обязаны
электролизному способу получения его из руд.
Этот способ разработал в 1886 г. Чарльз М. Холл.
Вот что рассказывает учитель Холла —
профессор Иветт, преподававший в то время в колледже в
городе Оберлине химию, о Холле и его открытии.
«...Я считаю, что сделал открытие:
открыл человека. В 1880 г. вскоре после моего
возвращения из Японии, где я преподавал
четыре года химию, я обратил внимание на
шестнадцатилетнего паренька. Этот юноша
приходил в лабораторию, чтобы за
несколько центов купить стеклянные трубки,
пробирки или еще что-нибудь в этом роде.
Я ничего не знал об этом мальчике, но часто
думал, что, возможно, он станет ученым —
ведь он занимается исследованиями в те
годы, когда другие подростки проводят
время только в играх и развлечениях. Этот
подросток и был Чарльз М. Холл, человек,
в 21 год открывший метод выделения
алюминия из руд.
Чарльз поступил в колледж, и после того
как он прошел часть обязательного курса,
я забрал его к себе в лабораторию. Как-то,
беседуя со студентами, я сказал:
«Изобретатель, которому удастся разработать
дешевый способ получения алюминия и сделать
алюминий металлом массового
потребления, окажет большую услугу человечеству и
заслужит славу выдающегося ученого».
Я услышал, как, обернувшись к одному
из своих сокурсников, Чарльз сказал: «Я
займусь этим металлом». И он принялся за
работу. Он испробовал множество методов,
но все безуспешно. Наконец, Холл
остановился на электролизе. Я отдал ему старые,
ненужные приборы и батареи. Те из вас,
кто видел электрические батареи,
рассмеялись бы при виде того, что смог соорудить
Холл из разных чашек с кусками угля. Но
ток мы получили такой, какой нам был
нужен.
Вскоре после этого Холл закончил
колледж и забрал это сооружение к себе. Он
устроил свою лабораторию в лесу
неподалеку от дома, упорно продолжал свои
опыты и часто рассказывал мне о результатах.
Нужно было найти растворитель для
двуокиси алюминия — основного алюминиевого
сырья. И через шесть месяцев Холл
установил, что окисел хорошо растворим в
расплаве фтористого алюмината натрия (NasAlF6).
Однажды утром Холл вбежал ко мне с
радостным возгласом: «Профессор, я
получил его!» На протянутой ладони лежало
двенадцать маленьких шариков алюминия,
самого первого алюминия, полученного
электролизом. Это произошло 23 февраля
1886 года.я
Перевод с английского
Р. ДАШЕВСКОЙ
Рисунок В. ЗУЙКОВА.
КЛУБ
юный
химик
ВНИМАНИЮ
новичков
Устав клуба состоит всего из двух пунктов.
Пункт первый. Членом клуба может быть каждый школьник.
Пункт второй. Ответы на вопросы викторины клуба Юный химик
нужно высылать в редакцию до выхода в свет следующего номера
журнала (потому что в этом следующем номере ответы будут уже
опубликованы).
Десять школьников, которые пришлют лучшие ответы в течение
учебного года, будут премированы подпиской на наш журнал на следующий
год.
ХОТИТЕ ПОДГОТОВИТЬСЯ
К ЭКЗАМЕНАМ ПОЛУЧШЕ?
Окислительно-восстановительным реакциям в школьной программе уделено много
внимания. Это закономерно — такие реакции встречаются очень часто.
Если вы хорошо усвоили сущность процессов окисления-восстановления и умеете
составлять уравнения несложных реакций, попытайтесь ответить на восемь вопросов,
которые подготовил для вас Г. Б. Вольеров.
1. Существуют ли химические реакции, в которых:
а) кислород окисляется;
б) водород восстанавливается;
в) кислород окисляется, и одновременно водород восстанавливается!
2. Может ли элемент окислить сам себя!
3. Хлор — более сильный окислитель, чем кислород. Но хлор вытесняется из
соляной кислоты при реакции с двуокисью марганца и другими веществами,
содержащими много кислорода. Как это объяснить!
4. При взаимодействии иода с хлорной кислотой иод замещает хлор. Согласуется
ли этот факт с положением галогенов в периодической системе!
5. Может пи протекать окислительно-восстановительная реакция без
непосредственного контакта окислителя с восстановителем!
6. Как будет взаимодействовать в растворе азотнокислое серебро с хлорным
железом и с хлористым железом! Если есть возможность, проверьте эти реакции
на опыте и объясните наблюдаемые явления.
7. Какие процессы будут происходить при действии хлора на бромистое железо
и при действии брома на хлористое железо!
8. Знаете ли вы, как изготовляют печатные радиосхемы! На пластмассовую плату
наклеивают пластинку медной фольги. На фольге нитрокраской рисуют схему. Затем
пластинку погружают в раствор хлорного железа. Через несколько минут все
оголенные участки медной фольги вытравляются. Достаточно промыть пластинку и снять
нитрокраску — и радиосхема готова.
Как объяснить разрушение меди в растворе хлорного железа!
(Ответы на вопросы — на стр. 82)
74
ВИКТОРИНА
Закончилась викторина 1966 г. Ее итоги мы сообщаем на стр. 96. А
сейчас начинается викторина 1966/67 учебного года. Она закончится в мае,
до начала экзаменов. После этого будут подведены итоги и названы
имена десяти победителей. Итак, начинается первый тур викторины.
двойка по химии
Коллекции бывают разные. Одни собирают
редкие книги, другие — марки, третьи —
спичечные этикетки. Профессор П. Р. Таубе
коллекционирует... химические ошибки,
обнаруженные в художественной литературе,
кинофильмах, газетных статьях.
Предлагаем вам найти ошибки в
отрывках из трех известных романов.
А. Н. Толстой
«ГИПЕРБОЛОИД ИНЖЕНЕРА ГАРИНА»
«Это же золото! — крикнул он хохоча.
Мы просто бараньи головы... Золото и ртуть
кипят рядом... Что получается! Ртутное
золото!
Глядите же! — он разжал ладонь, на
которой лежали жидкие дробинки.— В
ртути золотистый оттенок. Здесь девяносто
процентов червонного золота!»
Р. А. Штильмарк
«НАСЛЕДНИК ИЗ КАЛЬКУТТЫ»
«Крыша в хижине была худая, с потолка
падали дождевые капли, но в очаге слабо
мерцало голубоватое пламя... концы
хвороста тлели голубоватым огнем.
О фосфоре, воспламеняющемся от
воды, они не вспомнили, им было не до
химии...»
Жюль Берн
«ДВАДЦАТЬ ТЫСЯЧ ЛЬЕ ПОД ВОДОЙ»
«— Вы знаете состав морской воды!., в
ней хлористый натрий. Далее, в ней
содержатся в небольшом количестве хлористый
магний и хлористый кальций, бромистый
магний, сернокислый магний, серная кислота
и углекальциевая соль...»
вопросы для самоподготовки
Начиная с первого номера 1967 года, клуб Юный
химик будет помещать не только задачи. Чтобы
успешно сдать экзамен по химии (на аттестат
зрелости или при поступлении в вуз), нужно
систематически повторять и теорию. Поэтому на страницах
клуба из номера в номер будут печататься контрольные
вопросы (разумеется, с ответами) по основным
разделам программы по химии.
Здесь помещен образец такой таблицы (в
дальнейшем она будет занимать целую страницу). На
одной стороне листа помещены вопросы, а на
другой— соответствующие ответы. Вы можете вырезать
из листа карточки, на каждой из которых помещены
вопрос и ответ на него. Прочитав вопрос,
попытайтесь на него ответить, а потом сравните свой ответ
с тем, который напечатан на обратной стороне
карточки. Если вы предпочитаете заниматься вдвоем
с товарищем, то удобнее задавать друг другу
вопросы, а потом сверять по карточке ответь1. Все
карточки будут пронумерованы.
ЧТО ТАКОЕ
НОРМАЛЬНОСТЬ
РАСТВОРА!
ЧТО ТАКОЕ МЫЛО
И КАК ЕГО
ПОЛУЧАЮТ!
КАК МЕНЯЮТСЯ
МЕТАЛЛИЧЕСКИЕ
И МЕТАЛЛОИДНЫЕ
СВОЙСТВА ЭЛЕМЕНТОВ
В РЯДАХ И ГРУППАХ
ПЕРИОДИЧЕСКОЙ
СИСТЕМЫ
Д. И. МЕНДЕЛЕЕВА!
75
л
мммя
а
опыты
О
ш
3
а.
ш
ш
ю
ПОЛ-ЛИТРА
ЭЛЕКТРИЧЕСТВА
Когда говорят об энергетике завтрашнего
дняг обязательно упоминают топливные
элементы *.
Напомним вкратце, как работает
топливный элемент или, как его еще называют,
электрохимический генератор.
В принципе — это гальванический
элемент. Но в отличие от батареек и
аккумуляторов в топливном элементе активные
вещества хранятся отдельно. Они подаются на
электроды постепенно, по мере
использования.
На топливном, отрицательном электроде
окисляется («горит») природное топливо или
какое-нибудь вещество, которое легко
получить из природного топлива. Оно может
быть газообразным (окись углерода,
водород) или жидким (например, спирты). А на
положительном электроде топливного
элемента обычно реагирует кислород.
Как видите, принцип действия прост.
Однако воплотить его в реальной конструкции
значительно труднее. Предстоит решить
немало сложных задач, прежде чем будут
созданы надежные и мощные топливные
элементы.
* О топливных элементах рассказывается в
статье Ю. Б. Васильева («Химия и Жизнь», f 966, № 4).
А вот сделать действующий макет
топливного элемента малой мощности можно
даже в школьной химической лаборатории.
Для этого потребуются несколько кусков
оргстекла (плексигласа), старый противогаз,
щелочь и... бутылка водки. Не удивляйтесь:
водка — это водный раствор этилового
спирта, отличного «горючего» для топливного
элемента.
Прежде всего сделайте корпус
топливного элемента — коробочку, которая
показана на рисунке. Лучше всего сделать
корпус из оргстекла. Наружные стенки должны
быть толстыми (примерно по 5 мм), а внут^
ренние перегородки можно сделать потоны
ше (около 3 мм). Корпус из оргстекла
можно склеить из отдельных пластинок таким'
клеем: на 100 мл дихлорэтана или
хлороформа 5—6 г стружки оргстекла
(ОСТОРОЖНО! РАБОТАТЬ ПОД ТЯГОЙ!). Можно
сделать корпус и из других материалов.
Важно только, чтобы он не протекал и не
проводил электричества.
В одной из наружних стенок просверлите
отверстие, в которое через резиновую
пробку введите стеклянную сливную трубку.
На внутренних перегородках насверлите по
нескольку отверстий диаметром 5—6 мм
(расстояние между отверстиями также
5—6 мм).
Наиболее активные металлы
находятся в нижнем левом углу
периодической системы; наиболее
активные металлоиды — в правом
верхнем углу. Способность
отдавать электроны растет по мере
уменьшения числа валентных
электронов и увеличения общего
числа электронных слоев;
поэтому металлические свойства
элементов усиливаются справа налево
и сверху вниз. В центре таблицы
находятся элементы, способные
проявлять как металлические, так
и металлоидные свойства.
Мыло — это соль (натриевая
или калиевая) какой-нибудь
высшей жирной кислоты, например,
стеариновой (CiyH^COOH).
Натриевые мыла — твердые;
калиевые — жидкие. Кальциевые и
магниевые мыла нерастворимы в
воде. Мыла получают гидролизом
(ссомылением») жиров — сложны)
эфиров высших жирных кислот и
глицерина.
Нормальность характеризует
концентрацию раствора. Она
показывает, сколько
грамм-эквивалентов данного вещества
содержится в 1 л раствора.
Например, запись 1,5 н. NaOH (или
1,5 N NaOH) означает, что в 1 л
такого раствора содержится
1,5 грамм-эквивалентов NaOH (то
есть 60 г). Равные объемы
растворов с одинаковой
нормальностью реагируют полностью, так
как содержат равное число
грамм-эквивалентов.
76
Теперь посмотрите на соседний
рисунок. На нем показан готовый элемент. Вот в
какой последовательности его нужно
делать.
В отделения II и IV (между первой и
второй, третьей и четвертой перегородками)
насыпьте активированный уголь из старого
противогаза. Это — электроды. Чтобы
крупинки угпя не высыпались через отверстия,
предварительно положите на перегородки
куски капроновой ткани (можно взять
старые чупки].
В камере I будет циркулировать
топливо, в камере V должен быть воздух —
поставщик кислорода. Между эпектродами
должен быть, конечно, электролит. Чтобы
электролит не просачивался в воздушную
камеру, уголь для воздушного электрода
(в камере IV) перед засыпкой пропитайте
раствором 2 г парафина в половине стакана
бензина. Такой пропитанный электрод не
пропускает жидкость и свободно пропускает
газ.
На спой активированного угпя положите
медные планки с припаянными проводами и
осторожно вдавите их. Через ппанки ток
будет отводиться от электродов.
Элемент готов, но его нужно еще
зарядить. Вот как готовится топливо. Разбавьте
водку водой (на 0,5 п водки 0,5 л воды).
В полученной смеси растворите 300—350 г
едкого капи (ОСТОРОЖНО?). Электролит
приготовить еще проще: 60—70 г едкого ка-
78
ли растворить в 200 мл воды. РАБОТАЙТЕ
СО ЩЕЛОЧЬЮ В РЕЗИНОВЫХ ПЕРЧАТКАХ
И ОЧКАХ. ПОМНИТЕ, ЧТО ПОПАДАНИЕ
ЩЕЛОЧИ НА КОЖУ, И, ОСОБЕННО, В
ГЛАЗА ОЧЕНЬ ОПАСНО.
Теперь топливный элемент можно
испытать. Одновременно напейте в корпус
топливо (в камеру I) и электролит (в камеру III).
Вольтметр, присоединенный к электродам,
покажет напряжение 0,7—0,9 вольт.
Чтобы элемент проработал некоторое
время, использованное топливо нужно
отводить, а свежее — постоянно подливать.
Свежее топливо подается из бутылки через
резиновую трубку (как показано на
рисунке). Скорость подачи можно регулировать,
сжимая трубку. Использованное топливо
спивается в стакан.
Отсоедините вольтметр и соберите цепь
с ключом, миллиамперметром и реостатом
с сопротивлением около 1000 ом (если нет
реостата, можно взять
радиосопротивление). Замкните ключ — стрелка
миллиамперметра откпонится. Уменьшая сопротивление
цепи, понаблюдайте за величиной тока.
К сожалению, мощность элемента
невелика. Чтобы загорелась лампочка для
карманного фонарика или завертелся ротор
микродвигателя, нужно соединить
последовательно два таких элемента.
Какие же реакции идут на электродах
нашего элемента! На левом электроде
окисляется топливо: молекула спирта теряет
два электрона и превращается в молекулу
уксусного альдегида:
G.H-OH — 2е > СН3СН0 | 2Н
А на правом электроде, воздушном,
расходуется кислород воздуха:
О. 2Н.0 + 4е > 40Н-
Наш топливный элемент имеет очень
малую мощность и работает сравнительно
недолго. А как сделать мощную батарею
элементов с длительным сроком службы!
Над этим и работают ученые и
инженеры во многих странах мира.
М ЧТО ЭТО ТАКОЕ!
ПОРОШОК ПРАЙСА
РЛССКЛЗ-ЗЛГАДКА
Рисунок Д. ЛИОНА
На протяжении одиннадцати с
лишним столетий алхимия
считалась вполне респектабельным
занятием во всей Европе. В
средневековые времена сотни искателей
«философского камня» повсюду
находили поддержку. Однако
никому из них не удавалось достичь
успеха. И лишь в 1782 году —
спустя столетие после того, как
миновало всеобщее увлечение
алхимией, — появились сообщения о
триумфальных экспериментах
англичанина Джеймса Прайса.
Эти опыты
демонстрировались десяткам свидетелей. Король
Георг III осмотрел и одобрил
образцы «искусственного золота»,
изготовленного Прайсом. Во
время каждой демонстрации
производилась дотошная проверка,
исключавшая всякую возможность
обмана. Но никто так и не смог
найти объяснение загадки
«волшебного порошка» Прайса...
В тридцать лет Прайса считали
одним из самых
многообещающих молодых ученых Англии. Он
был удостоен высоких почестей:
его избрали членом
Королевского общества—самого известного
научного учреждения страны, ему
присудили почетную степень в
Оксфорде.
Весной 1782 года Прайс купил
небольшое поместье неподалеку
от Гилфорда. Оно раньше
принадлежало старому доктору Айри-
шу, который жил уединенно и
умер, как поговаривали соседи,
при странных обстоятельствах в
комнате, которая была им
переоборудована в лабораторию.
Прайс приехал со своей
невестой осмотреть их будущий
дом. Они обследовали старинное
здание, в котором оставалась еще
обстановка доктора Айриша. По
документам, дошедшим до нас,
можно воспроизвести события в
тот день, который закончился
открытием, бесповоротно
изменившим все...
Разбирая ящик письменного
стола, они обнаружили
пожелтевшую от времени рукопись. Имени
автора нигде не было. Но
сомнений быть не могло — ее написал
доктор Айриш.
— Джеймс, что за человек
был этот доктор? — спросила
девушка, перелистывая мятые
страницы.
— Мы никогда не встречались.
Говорят его обуревали странные
идеи, и он беспрестанно
занимался экспериментами. Его не
удовлетворяла химия, и он увлекся
другими вещами...
Склонившись над рукописью,
они внимательно прочли
несколько страниц, заполненных
расчетами и формулами, а потом
обнаружили документ, озаглавленный
«Как я нашел секрет
всемогущества».
Прайс рассмеялся. «Бедный
старик. Он, наверное, совсем
выжил из ума».
К рукописи был приколот
небольшой запечатанный конверт.
Прайс взял его и небрежно
распечатал: внутри был какой-то
порошок.
— Наверное, средство от его
подагры, — сказал он и, отложив
конверт, снова занялся
рукописью. Но смешливое настроение
как рукой сняло, когда он
прочитал первые фразы.
«Однажды вечером, 6
сентября 1753 года ко мне пришел
незнакомый человек. Он произвел
на меня хорошее впечатление.
После приятной беседы, он
спросил меня, видел ли я когда-нибудь
«философский камень», знаю ли
я вещество, из которого он
состоит. Когда я ответил, что ни
разу не видел этого камня,
пришелец достал шкатулку из черного
дерева. В ней лежали четыре
больших куска вещества,
похожего на стекло, но красного, как
рубин. Я уговорил его дать мне
немного этого драгоценного
вещества. Затем он покинул мой
дом, и я больше не встречал
его...»
В рукописи сообщалось, как
доктор решил испробовать
порошок. Дальше шло описание
эксперимента — «вылил настойку в
воск... шесть драхм ртути...
шипящий звук... газы... через
пятнадцать минут ртуть превратилась...
в чистое золото!»
«Я был богат... но настойка
кончилась... построил
лабораторию... пытался получить подобное
вещество... Наконец удалось... но
слишком дорогой ценой. Моя
жизнь в опасности... Я слишком
стар, чтобы продолжать!»
На этом повествование
заканчивалось. Прайс взял конверт,
который перед этим отложил в
сторону. Открыв его, он обнаружил
внутри около унции красного
порошка.
Прайс высыпал на ладонь
немного порошка и понюхал его
Потом направился к двери,
которая вела в лабораторию.
— Я должен удостовериться в
том, что это самая обыкновенная
аптечная смесь. Всего несколько
несложных опытов. Я ненадол-
79
«tB порыве отчаяния Прайс схватил бутылку с синильной кислотой...»
го — в рукописи сказано
«пятнадцать минут».
— Но ведь там ни одному
слову нельзя верить — все это
богохульный вздор!
Прайс укоризненно взглянул
на невесту.
— Дорогая, — сказал он, —
приговор выносит лаборатория
ученого, а не его ум.
Эксперимент занял намного
больше, чем пятнадцать минут.
Наконец, раствор в тигле начал
шипеть и пениться, выделяя
газы — точь-в-точь, как описывал
доктор Айриш.
Прайс вернулся в комнату. Он
держал щипцами дымящийся
тигель.
— Посмотри — это уже не
ртуть. Это золото!
Девушка с недоверием
заглянула в тигель и отпрянула. И
голос и выражение лица жениха
испугали ее. Его глаза горели
фанатичным огнем. Возбужденно
шагая по кабинету, Прайс с
восторгом говорил: «Изумительное
открытие! Ключ к утраченному
искусству превращения
элементов!» Сомнений быть не могло —
азотная кислота не оставила ни
малейшего следа на ярко-желтом
осадке. Это было золото.
— Джеймс, дай мне слово,
что ты никогда больше не
вернешься к этой работе. Это магия!
— Это наука, — резко
возразил он. — И мой долг —
продолжать, пока я не выясню все, что
возможно.
Она помолчала немного, потом
взяла свой плащ и направилась
к выходу.
— Тогда ты должен делать
свои опыты без меня, Джеймс! —
сказала она твердо.
Прайс сделал необратимый
выбор: он перестал быть химиком
и стал алхимиком. Он не только
порвал с невестой, но и поставил
на карту свою профессиональную
репутацию, все свое будущее.
Прошел год. Все это время
Прайс без устали работал один в
старом доме. Потом он начал
демонстрировать плоды своего
труда. Сначала к нему приходили
соседи, затем сенсационные
слухи дошли до Лондона, и к нему
стали приезжать ученые,
писатели, политические деятели.
Есть достоверные
свидетельства того, что во время публичных
демонстраций опытов Прайс часто
предлагал добровольцам
провести весь эксперимент самим.
А он сам стоял в стороне и лишь
подсказывал, что и как нужно
делать. Опытные химики каждый
раз обследовали всю
лабораторию, но специалисты не могли
обнаружить ни малейшего следа
какой-либо подтасовки.
Образцы «самодельного»
золота Прайса были исследованы
крупнейшими специалистами
Англии. Они признали, что это
«чистейшее настоящее золото».
Сенсационные заявления
Прайса привели в замешательство
Королевское общество. Прайсу
предложили изложить ученым
сущность его открытия, которое
сулило великолепное будущее
Британской империи.
Прайсу было уготовано
почетное место на страницах
истории— ему надо было только
передать Королевскому обществу
запас красного порошка вместе
с описанием всего процесса. Но
именно этот последний шаг
Прайс не хотел — или не мог —
сделать.
Шли месяцы. Прайс не
предпринимал никаких действий для
того, чтобы обессмертить свое
имя. Шумные восторги сменились
презрением. У Прайса
потребовали объяснений. Он заявил, что
израсходовал весь запас
красного порошка и не хочет больше
заниматься его изготовлением,
так как этот процесс не только
труден, но и опасен для здоровья.
Действительно, за последний год
здоровье Прайса резко
ухудшилось. Он сильно постарел, у него
были явные признаки нервного
расстройства.
В августе 17ВЗ года двое
ученых, сэр Филипп Кларк и доктор
Спенс отправились к Прайсу,
чтобы предъявить ему ультиматум:
либо он доказывает свою
правоту и передает им порошок, либо
его ждет изгнание из общества
и, возможно, судебное
преследование.
К удивлению ученых оказалось,
что молодой химик, несмотря на
крайнее переутомление, снова
был полон энергии. Он заявил,
что приготовил немного порошка
и готов немедленно приступить
к опыту. Прайс вместе с учеными
вошел в лабораторию»
А через три часа он лежал
мертвым около рабочего стола.
Мы не знаем точно, что
произошло в последние минуты его
жизни. Известно лишь, что
эксперимент закончился полным
провалом. В порыве отчаяния Прайс
схватил бутылку с синильной
кислотой и прежде, чем ему смогли
помешать, выпил смертельный яд.
Научные доклады и протоколы
Королевского общества и
письма Прайса помогли воссоздать
эту историю. Однако самое
важное звено утрачено навсегда.
Секрет красного порошка умер
вместе с Прайсом. Во время
неудачной демонстрации был
израсходован весь запас порошка,
и хотя впоследствии весь дом
перевернули вверх дном, записей
с формулами найти не удалось.
Перед современным
исследователем этой загадочной истории
встает множество вопросов.
Был ли красный порошок
эквивалентом философского
камня? Почему ртуть превращалась в
золото? Каков был состав
порошка? Почему Прайс не хотел
поделиться своим секретом с
Королевским обществом? Что
подорвало его здоровье?
Как бы вы ответили на эти
вопросы?
6 Химия и Жизнь, № 9
81
ОТВЕТЫ НА ВОПРОСЫ
(см. стр. 74)
1.
а. С такими реакциями вам приходилось нередко встречаться. Вспомните
различные способы лабораторного получения кислорода:
2+ 2—0 0
2HgO = 2Hg 02;
l+5-г 2- 1+ 1- 0
2К С1 03 = 2КС1 + 302;
1 + 7+2— 1+ 6+ 2- 4-1-2— 0
2К Мп04 = К2 Мп 04 ^ Мп 02 + 02.
Во всех этих случаях отрицательно заряженные атомы кислорода теряют
электроны, то есть окисляются, а ртути, хлора, марганца — восстанавливаются. Часто думают,
что восстановленный элемент обязательно выделяется в свободном виде, а
окисленный — обязательно связывается. Такое понимание процесса
окисления-восстановления ошибочно.
Кислород может окиспяться не только в реакциях разложения, но и в реакциях
замещения, например при вытеснении его галогенами:
2+2 0 2+1—0
2CuO 2C12= 2CuCI2 +02.
б. Образование гидридов — единственный случай восстановления свободного
водорода:
0 0 1+1—
2Na + Н2 = 2Na H
гидрид натрия
Восстановление связанного водорода (например, при вытеснении его из воды
и кислот) встречается довольно часто.
в. Кислород окисляется, а водород одновременно восстанавливается при
разложении воды (термическим или электролитическим способом):
1+2- 0 0
2Н20 = 2Н2ф02.
2. «Сам себя окислить» и, следовательно, «сам себя восстановить» может элемент
в виде простого вещества
0 1~ 5+
ЗС12 + 6КОН нагрев 5КС1 -f КСЮ3 + ЗН20,
и в составе сложного вещества
умеренный
5+ нагрев 1— 7 J-
4КСЮ3 - КС1-|-ЗКСЮ4,
и в составе двух веществ, в которых валентность его различна
■ ' 1— 1~о
КСЮ3 - 0НС1 -- КС1 - ЗС12 У ЗНйО.
В последнем примере хлор бертолетовой соли восстанавливается от валентности
5+ до 1—, а хлор соляной кислоты окисляется от валентности 1— до 0.
Попробуйте сами подобрать подобные примеры для серы.
3. Многие сложные вещества-окислители богаты кислородом — Мп02, КМп04г
КСЮзг К2Сг207 и т. д. Однако не кислород этих веществ является
элементом-окислителем. Ведь кислород в них предельно восстановлен (валентность 2 —]. Здесь
окислители — это элементы с высокой положительной валентностью: марганец, хлор, хром.
Пример — в ответе на предыдущий вопрос (реакция между бертолетовой солью и
соляной кислотой).
4. Рассмотрим реакцию с точки зрения окисления-восстановления:
7+0 7+0
2НСЮ4 ! J2 = 2HJ04 Ь С12.
Обычно, когда говорят, что хлор активнее иода, мысль не доводят до конца: хлор
активнее иода как окислитель. Значит, иод активнее хлора как восстановитель! А в
нашем примере иод выступает как раз в роли восстановителя.
5. В химических источниках электрического тока процессы окисления протекают на
катоде, а процессы восстановления — на аноде. Таким образом, окисление и
восстановление разделены в пространстве.
6. При взаимодействии растворов азотнокислого серебра и хлорного железа
образуется белый осадок хлористого серебра:
3AgN03 H FeCI3 = Fe (N03K + 3AgCl I.
Или в сокращенной ионной форме:
1+ 1- i+ J-
Ag ; О = AgCI |.
Это реакция обмена, идущая без изменения валентности.
При реакции нитрата серебра с хлористым железом образуется черный осадок
металлического серебра:
1+ 2+ 3+ Я+ 0
3AgNO, H 3FeCl2 = Fe(N03K ! 2FeCI3 H 3Ag I .
Или в ионной форме:
1+ 2+ 0 3 +
Ag-|-Fe = Ag-| Fe.
В этом случае ионы серебра восстанавливаются двухвалентными ионами железа.
7. При действии хлора на бромистое железо происходит окисление как железа, так
и брома:
2 + 1- 0 3+1-0
2Fe Вг2 Н ЗС12 = 2Fe Cl3 + 2Вг2.
Ером не может окислить ионы хлора, но он способен окислить железо:
2+ 1- 0 3+ 1— 3+ 1 —
6Fe Cl2 H ЗВг2 -= 4Fe Cl3 + 2Fe Вг3.
8. Медь окисляется ионами трехвалентного железа:
0 3+ 2ь 2+
Си Ь 2FeCI, = CuCI2 + 2FeCl2
о з+ 2: 2+
Си 1 2Те = СиН 2Fe.
Медь малоактивный восстановитель, и восстановить железо до свободного
металла она не может.
СТЕКЛОДУВНАЯ
МАСТЕРСКАЯ
В. ЖВИРБЛИС
КАК ПРОДУВАТЬ ОТВЕРСТИЯ
Проще всего научиться продувать отверстия
в круглом дне. Для этого сначала надо сделать,
как обычно, заготовку, отпаять одну из оттяжек,
выбрать лишнее стекло, выровнять дно легким
поддуванием и после этого снова нагреть его до
рабочей температуры. ОБРАТИТЕ ВНИМАНИЕ:
НАГРЕВАТЬ СЛЕДУЕТ ТОЛЬКО
ЗАКРУГЛЕННУЮ ЧАСТЬ ДНА, не затрагивая
цилиндрических стенок! Это делают так: заготовку держат
в правой руке, повернув ее дном «на себя» (ось
трубки составляет с осью горелки угол около
45°), и нагревают, непрерывно вращая, самым
краем пламени (а). В этом случае нагреваться
будет только центр дна, а плечики заготовки
останутся сравнительно холодными.
После того как стекло достаточно
размягчится, заготовку надо вынуть из пламени и, не
прекращая вращать, сильно подуть через
оставшуюся оттяжку: на месте дна вырастет тончайший
стеклянный пузырь причудливой формы,
переливающийся всеми цветами радуги (б). Этот
пузырь можно смахнуть напильником или
кафельной плиткой (в). Отверстие готово. Выполняя эту
операцию, имейте в виду еще следующее:
1) дно, которое вы продуваете, должно быть
не слишком толстым, но и не слишком тонким;
2) стекло нельзя перегревать, но и нельзя
вынимать из пламени холодным — в последнем
случае отверстие просто не «продуется»;
3) дно надо обогревать очень равномерно по
окружности;
4) дуть в этом случае надо легкими (а не
щеками, как при изготовлении дна), делая один
сильный и плавный выдох — не слишком
быстрый, но и не слишком медленный.
Если вы научитесь соблюдать все эти правила,
у вас будут получаться отверстия, пригодные для
дальнейшей работы. Это значит, что плоскость
«среза» будет строго перпендикулярной оси
трубки, а сам пузырь — очень тонким. Описывать все
возможные ошибки было бы очень долго и
утомительно; заметим только, что не надо пугаться,
если при продувании отверстия раздастся
оглушительный хлопок. Это значит, что вы просто
очень сильно нагрели стекло и слишком резко
дунули.
Диаметр продутого таким способом отверстия
равен диаметру трубки.
А как быть, если в круглом дне надо сделать
маленькое отверстие или если это отверстие
надо сделать в боковой, цилиндрической стенке
трубки?
В этом случае придется воспользоваться
маленькой хитростью. Возьмите в одну руку
заготовку, а в другую — тонкую стеклянную
палочку. Нагрейте стенку заготовки до начала
размягчения стекла и прикоснитесь кончиком горячей
(но не размягченной!) палочки к центру
разогретого участка трубки — точно там, где должно
быть отверстие (г). После зтого выньте из пламени
заготовку вместе с прилипшей к ней палочкой и
с ее помощью оттяните маленький отросток (д).
Теперь, нагревая отросток у самого основания,
отделите палочку вместе с прилипшим к ней
стеклом, нагрейте как следует (причем
равномерно со всех сторон!) самый кончик отростка и
продуйте отверстие, как это описывалось выше.
КАК РАЗВЕРТЫВАТЬ ОТВЕРСТИЯ
Иногда отверстия продувают для того, чтобы
на месте дна сделать горло — небольшую
плоскую «тарелочку» с утолщенными краями (В
некоторых простейших случаях — например, при
изготовлении пробирок — отверстие можно не
продувать, а просто сделать обычный срез.) При
выполнении ответственных стеклодувных
операций продутые отверстия развертывают
специальным инструментом — разверткой,
представляющей собой деревянный или графитовый
конус, или же сужающуюся к концу латунную
пластинку с рукояткой. Но не менее удобно
вместо развертки пользоваться обыкновенным
трехгранным напильником (тем самым, которым вы
режете стеклянные трубки).
Возьмите в одну руку отрезок стеклянной
трубки, конец которой надо развернуть, а в другую —
напильник. Начните вращать трубку
(перекатывая ее в пальцах туда — обратно) и внесите ее
торец в пламя горелки (ОЧЕНЬ ВАЖНО:
РАЗОГРЕВАТЬ НАДО ТОЛЬКО ОЧЕНЬ УЗКУЮ
84
ПОЛОСКУ СТЕКЛА, например, участок шириной
около 3 миллиметров, если диаметр трубки
составляет 10 миллиметров). Как только торец
трубки начнет оплавляться, его надо вынуть из
пламени, ввести в отверстие под острым углом один
из концов напильника и, продолжая вращать
трубку, легкими прикосновениями напильника
с внутренней стороны постепенно развернуть ее
тарелочкой (е). При зтом не следует прилагать
никаких усилий: трубка должна только чуть-чуть
касаться напильника. Если при этом тарелочка
получится недостаточно ровной, ее можно снова
разогреть и снова подправить напильником;
после этого ее надо окончательно выровнять
кафельной плиткой и слегка отжечь на
коптящем пламени.
Несколько иначе поступают в том случае, если
нужно увеличить диаметр продутого отверстия:
для этого края отверстия разогревают, вводят
острый конец напильника и, делая им круговые
движения, — как бы помешивая ложечкой чай в
стакане, — развертывают отверстие.
85
/£ju АНГЛИЙСКИЙ-
W для химиков
РОЛЬ СОЮЗОВ and, or, but
При анализе и переводе английских
предложений следует уделять особое внимание
сочинительным союзам and, or, и противительному союзу
but.
Дело в том, что эти союзы (а также запятая)
ставятся между однородными членами предложения.
При этом отдельные элементы предложения обычно
подразумеваются и требуют соответствующего
выявления. Например, когда используется глагол to be,
он обычно не повторяется, несмотря на то, что
подчас выполняет совершенно различные
грамматические функции; при повторном введении инфинитива
часто не повторяется частица to; при повторении
герундия, стоящего после предлога, предлог обычно
опускается и т. д.
Следовательно, обнаружив and, or, but (или
запятую), надо помнить об их «коварстве» и
обязательно посмотреть, что стоит до них — это позволит
обнаружить отсутствующие лексические и
грамматические элементы и выявить логическое развитие
мысли, изложенной в предложении. Делается это
следующим образом.
The regular method for cyclizing the keto
ester YT consists in removing the ester group
by hydrolysis, reducing the ketone and
effecting a cyclodehydration of the alcohol.
На первый взгляд может показаться, что инго-
вые формы — reducing и effecting — надо
переводить деепричастиями «восстанавливая» и
«осуществляя». Это не так. По запятой и союзу and выясняем,
что это не инговые формы, а герундий после
предлога in, no аналогии с in removing. Предлог in в
обоих случаях подразумевается. Теперь легко
сделать правильный перевод:
«Обычный метод циклизации кетоэфира VI
заключается в удалении эфирной группы гидролизом,
(в) восстановлении кетона и (в) осуществлении цик-
лодегидратации спирта».
The second class gives dimolecular and
polymolecular products but no monomolecular
products.
Обратите внимание, после союза and перед
существительным стоит отрицательная частица по.
Поскольку в английском предложении может быть
только одно отрицание (см. № В, 32), то в этом
случае надо найти глагол-сказуемое и перевести его
отрицательной формой. Но где же в этом
предложении глагол? Мы ведь уже выяснили, что сказуемое
находится в начале предложения; зная это,
переводим:
«Второй класс дает бимолекулярные и
полимолекулярные продукты, но не дает мономолекулярных
продуктов».
The hydrocarbon n-heptacontane has been
synthesized and found to have the melting
point 105° and to be distillableinhigh vacuum.
Это предложение интересно тем, что мы
встречаемся дважды с союзом and. После первого and
опущено подлежащее и часть сказуемого — has
been, а после второго — has been found. Теперь ясно,
что to be distillable — это инфинитив в обороте
«подлежащее с инфинитивом» (см. № 6), поскольку
он сочетается с глаголом-характеристикой
«находить». Отсюда перевод:
«Был синтезирован углеводород н-гептаконтан
и найдено, что он имеет точку плавления 105° и
способен перегоняться в высоком вакууме».
Compared with succinic and glutaric
anhydrides this compound showed a diminished
solubility and ability to cristallise.
He зная роли союзов and, or, but, можно прийти
к ошибочному выводу, что «это соединение легко
кристаллизуется». Но, восстановив перед ability
прилагательное diminished, мы переведем
правильно:
«По сравнению с янтарным и глутаровым
ангидридами это соединение имело пониженную
растворимость и пониженную способность
кристаллизоваться».
Активное владение правилом анализа and, or,
but оказывает большую помощь при переводе
характерных для английского языка предложений, в
которых одновременно встречаются страдательный
и действительный залоги.
Например:
The trisaccharide fraction was partly
hydrolyzed with acid and gave rise to
five disaccharide compounds.
86
«Трисахаридную фракцию частично гидролизо-
вали кислотой и эта фракция дала пять дисахаридных
соединений».
В английском языке часто употребляются
существительные в общем падеже в качестве
определения других существительных. Это явление необычно
для русского языка и поэтому вызывает трудности
при переводе. Запомните следующее: если после
артикля стоит ряд существительных, то только
последнее будет тем существительным, к которому
относится артикль (определяемым словом) и
перевод надо начинать с него. Все остальные слова,
стоящие перед ним, будут определениями и
переводятся после него.
Например:
An integrated absorption area value
based on all methyl groups is reasonably good,
«Величина общей площади поглощения всех ме-
тильных групп является достаточно точной».
Перевод становится еще сложнее, когда между
отдельными определениями стоят союзы and, or,
but (или запятая), поскольку в таком случае эти
определения часто воспринимаются как
существительные в общем падеже.
Например, предложение:
We use oxygen, hydrogen, and nitrogen
reactions
означает не «Мы применяем кислородные,
водородные и азотные реакции», а «Мы применяем реакции
кислорода, водорода и азота».
А теперь рассмотрим специфику перевода
предложений, в состав которых входит
наречие-характеристика и существительное-характеристика.
НАРЕЧИЕ-ХАРАКТЕРИСТИКА
Как и соответствующие им
глаголы-характеристики, эти наречия только характеризуют отношение
автора к описываемому факту или событию и могут
употребляться в предложениях, аналогичных
безличным предложениям с глаголом-характеристикой или
их эквивалентам в обороте «подлежащее с
инфинитивом» (см. № 6).
34. These interpretations are admittedly
conjectural.
«Считают, что эти толкования являются
предположительными».
35. This is, announcedly, a very powerful
reagent.
«Как сообщают, это очень сильный реагент».
36. Dibromohydrin VI conceivably could
be produced as an intermediate.
«Можно предположить, что в качестве
промежуточного соединения образовался дибромгид-
рин VI» (см. также № 2, 3).
37. Silica hydrogel, reportedly, was
prepared by combination of dilute sodium
silicate and sulfuric acid in wooden tanks.
«Как сообщалось, силикагель готовили,
смешивая в деревянных емкостях разбавленный силикат
натрия и серную кислоту».
СУЩЕСТВИТЕЛЬНОЕ-ХАРАКТЕРИСТИКА
По аналогии с глаголами-характеристиками и
наречиями-характеристиками в английской научной и
технической литературе можно также встретить
существительные-характеристики с последующими
as + инговая форма, или с as и пропущенными
being (сравните № 8, 33).
Например:
38. The most which can be derived from
the infra-red spectrum is theidentifica-
tiоn of the skeleton X-C-X as being
correlated with the appearance of a medium
intensity absorption band near 1950 cm.
Поскольку между
существительным-характеристикой identification и as H- инговая форма стоит
существительное the skeleton X-C-X, такое сочетание
можно четко перевести по аналогии с переводом
оборота «дополнение с as + инговая форма»,
формула которого, как известно, близка к данному
сочетанию, а именно: «глагол-характеристика +
дополнение (существительное или местоимение) -f- as +
+ инговая форма» (см. № 6). Отсюда получаем
перевод:
«Самое большое, о чем можно судить по
инфракрасному спектру, это указание на то, что
скелет Х-С-Х связан с появлением полосы
поглощения средней интенсивности около 1950 cm~j».
39. The recent recognition of phos-
phonitrilic compounds as (being) «aromatic»
systems has stimulated research.
В примерах такого типа нередко опускается
being. Наличие существительного-характеристики и
as позволяет восстановить опущенную форму и
дать правильный перевод:
«Недавно установленный факт, что фосфонит-
рильные соединения являются «ароматическими»
системами, стимулировал исследования».
В следующей статье мы познакомимся с тем, как
надо находить и переводить абсолютные причастные
обороты, а также рассмотрим специфику перевода
следующих предложений:
87
40. The equilibrium initial stress is seen
to be markedly affected.
41. The new procedure enabled us to
overcome the above difficulties. Again there
took place an unexpected drop in the demand
for this product.
42. We obtained a complex product which
was to be expected.
43. Polyesters and polyamides are spin-
ned from melts. The latter are more
polar.
44. The reaction started at a temperature
over 100—150.
45. These compounds were previously
assigned the following structure.
Кандидат филологических наук
А. Л. ПУМПЯНСКИЙ
краски туркменского ковра
Отщепление С02 особенно
легко происходит в щелочной
среде и в растворах
минеральных кислот. Надо полагать, что
именно поэтому в марене
долгое время находили только
ализарин, пурпурин и другие менее
пенные красители.
Правда, у псевдопурпурина
есть еще одна особенность:
в 4—5-летних корнях марены,
особенно после нескольких лет
хранения, он исчезает, тогда как
количество пурпурина
соответственно возрастает. Очевидно,
псевдопурпурин разрушается в
результате ферментативных
процессов. А в свежевыкопан-
ных корнях марены
псевдопурпурин составляет большую
часть красящих веществ, а
ализарин — только одну треть.
Недавно проведенные нами
исследования показали, что
псевдопурпурин накапливается
не только в корнях, но и почти
в таких же количествах в
корневищах и стеблях растений.
Поэтому для крашения пряжи
можно использовать как
собственно корни, так и стебли
Окончание. Начало на стр. 65
и корневища марены,
измельченные до пылевидного
состояния.
В пользу марены говорит и
экономика. Это
высокоурожайная культура: сбор только
корней ее достигает 100 ц с гектара
(в пересчете на сухой вес). При
содержании 4—5,5% красящих
веществ их себестоимость
оказывается даже несколько ниже,
чем лучших синтетических
красителей.
Технология применения
псевдопурпурина также
разработана. Он обладает очень высокой
соле- и комплексообразующей
способностью. Поэтому при
крашении нельзя применять
жесткую воду, как это
рекомендовали делать старые рецепты
красок на основе марены, когда
стремились использовать в
основном ализарин и пурпурин.
А сам процесс крашения
следует вести при температуре не
выше 60—65°С до тех пор, пока
весь псевдопурпурин не
превратится в стойкие лаки.
Используя для протравы
пряжи соли алюминия, хрома,
молибдена, олова, железа и
кальция, можно получить почти
все основные цвета
знаменитых туркменских ковров. При
этом окраска получается
красивой и очень прочной.
Наконец, нельзя забывать и
о целебных свойствах марены
красильной. Сок, отжатый из ее
корней (а они очень сочны — их
влажность достигает 75—80 % )>
содержит большое количество
гликозидов, которые и теперь
считаются действующим
лечебным началом, способствующим
растворению почечных камней.
Экстракты из марены входят
в состав лекарственного
препарата «Цистенал», выпускаемого
в Чехословакии. В Советском
Союзе также начато
производство сухого экстракта марены.
Ее выращивают кое-где в
Грузии и Дагестане, а сейчас ее
начали возделывать в одном из
совхозов недалеко от Ашхабада.
Вероятно, наиболее
рентабельным окажется именно
комплексное использование
марены, при котором найдут
применение и ее лечебные свойства,
и содержащийся в ней
замечательный краситель —
псевдопурпурин.
Марена еще послужит
людям!
88
Ш11ШЩШ
Читатель—
соратник исследователя
Можно назвать немного областей
науки, которые вызывали бы у
широкого читателя столь же
большой интерес, как молекулярная
генетика. Это объяснянется
многими причинами: и тем, что
генетика помогает нам познавать
самих себя, и тем, что она
рождается буквально на наших
глазах, и тем, что в ее
достижениях сконцентрировано все
лучшее, чем располагает наука, —
остроумие гилотез, мастерство
эксперимента, неустанность
поиска. И еще тем, что о ней у нас
пока почти нет книг. Насколько
я знаю, книга В. Азерникова
«Тайнопись жизни» — первое
наше обстоятельное популярное
издание, посвященное химическим
основам наследственности.
Научное исследование, как
каждое творчество, интересно не
только своими конечными
результатами, но и своей технологией.
В этом смысле новая книга
несомненно интересна: наука предстает
в ней не просто суммой
накопленных знаний, но в первую оче-
В. Азерников. Тайнолись
жизни. М., издательство «Советская
Россия», 1966.
редь историей их кропотливого,
по крохам, добывания. Конечно
история, как бы ни была она
увлекательна, требует опытного
проводника, эрудированного гида,
знающего истинную цену каждой
находке.
Автор сумел стать таким гидом
для читателя. Это заметно и в
четкой, логичной композиции
книги, и б конструировании глав.
Это, несомненно, помогает
читателю в его увлекательном
путешествии от открытия к открытию.
При этом читатель не остается
равнодушным свидетелем
рождения новой науки, он становится
как бы соратником ученых. Ко
многим находкам он прикасается
первым после исследователя —
эти находки еще не успели даже
войти в учебники и монографии.
Молекулярная генетика,
родившаяся совсем недавно на
стыке биологии, химии и физики,
очень трудна для популяризации.
И тем не менее книга читается с
увлечением. Это связано в
значительной мере с тем, что многие
ее главы, как это ни необычно
для научной публицистики, —
имеют сюжет, причем иногда
довольно острый*
В книге, рассказывающей о
захватывающих, драматических
событиях, не трудно сбиться на
дешевую патетику, на ложную
занимательность. Автор
«Тайнописи жизни» счастливо избежал
этой опасности. Его книга
написана строго и просто. Лишь один
раз он позволяет себе отступить
от строго фактической основы,
когда в последней главе пытается
заглянуть за горизонт
сегодняшних достижений и рассказать о
том, что может дать сугубо
теоретическая наука медицине,
сельскому хозяйству, химии, биологии.
Мне кажется, это оправданная
концовка.
Можно было бы упрекнуть
автора в некотором схематизме
изложения отдельных частных
проблем, но вероятно, это
вызвано недостатком места.
Мне думается, что новая
работа В. Азерникова, которого
широкий читатель знает как
серьезного и широко образованного
популяризатора науки, может быть
признана весьма удачной и
своевременной.
Член-корреспондент
АН СССР
В. И. ГОЛЬДАНСКИЙ
89
о
ПРОЯВЛЯЮЩИЕ РАСТВОРЫ
С ФЕНИДОНОМ
Фотографическое изображение
получается в два этапа.
Во время экспонирования
фотоматериала (съемка или
печатание] под действием лучистой
энергии в эмульсионном слое в
микрокристаллах галогенида
серебра возникают ничтожно малые
вкрапления металлического
серебра. Они образуют скрытое
фотографическое изображение
объекта съемки. Затем эти вкрапления
в результате химической
обработки фотоматериала разрастаются,
образуя зерна металлического
серебра, которые и создают
видимое фотографическое
изображение.
Природа образования
скрытого фотографического
изображения и переход его в видимое
очень сложны и до конца не
изучены.
Скрытое фотографическое
изображение возникает при действии
очень малого количества лучистой
энергии (при очень коротких
выдержках или небольшой
освещенности]. Чтобы получить видимое
изображение, воздействуя на
фотографический материал только
лучистой энергией, потребовалось
бы увеличить эту энергию в сотни
миллионов и миллиарды раз.
Такую огромную затрату
лучистой энергии заменяет
химический процесс — проявление,
превращение микрокристалла
галогенида серебра в металлическое
серебро, начинающееся с
вкраплений — центров проявления.
Металлическое серебро выделяется в
виде тонких нитей, которые
растут от этих центров в разные
стороны за пределы микрокристалла
галогенида серебра. Благодаря
сращиванию соседних серебряных
частиц образовавшееся зврно из
металлического серебра обычно
больше первоначального
микрокристалла. Форма зерна зависит
от природы микрокристаллов и
свойств проявляющего раствора.
В последнее время появились
новые проявители. Один из самых
известных из них — фенидон, о
котором мы уже упоминали в
статье «Фотография: далекое —
близкое» (№ 3 за 1966 г.).
Проявляющий раствор из
одного фенидона действует очень
медленно, изображение получается
вялое, с вуалью. Но в сочетании
с каким-пибо другим
проявляющим веществом, например
гидрохиноном, он работает быстро и
энергично. Обычно фенидоном
заменяют метол в метоло-гидрохи-
ноновых проявителях, причем
фенидона нужно гораздо меньше, чем
метола. Например, на киностудии
«Ленфильм» 1 л проявляющего
раствора содержат только 0,05 г
фенидона.
Малое содержание фенидона
в растворе позволяет изготовлять
концентрированные проявители,
которые перед использованием
разбавляют водой. Фенидон
ускоряет действие многих
проявляющих веществ и поэтому применим
дпя быстрой и сверхбыстрой
обработки фотоматериалов.
Самое важное свойство
фенидона — способность повышать
светочувствительность
фотоматериалов. Светочувствительность
увеличивается по-разному в
зависимости от свойств
фотоматериала, состава проявляющего
раствора, режима проявления. Для
одних фотоматериалов она
увеличивается более, чем втрое, для
других никакого повышения не
происходит. Важно отметить, что
светочувствительность
фотоматериала под действием фенидона
растет, если оценивать ее по
проработке темных деталей объекта
съемки. Если же действие
фенидона в проявителе оценивать ло
проработке ярких деталей в
изображении, то
светочувствительность даже снижается.
Это объясняется разным
характером изображения,
получающегося в различных по составу
проявляющих растворах. В фени-
доно-гидрохиноновых растворах
изображение проявляют до
малого контраста, оно кажется
сероватым и имеет повышенную вуаль.
Проявление до малого контраста
ведет к увеличению практической
фотографической широты, а
следовательно, и к повышению
светочувствительности. Правда, из-за
малой контрастности печатать это
изображение сложнее, чем
проявленное в метоло-гидрохиноновом
растворе.
Другое важное свойство фени-
донового проявителя —
сохранение первоначальной концентрации
фенидона в процессе проявления.
Дело в том, что гидрохинон
регенерирует образующиеся
продукты окисления фенидона и таким
образом поддерживает его
первоначальную концентрацию до
тех лор, пока в растворе
достаточно много самого
гидрохинона.
Еще одно положительное
свойство фенидона — его способность
сопротивляться действию
бромидов, которые накапливаются в
растворе в процессе проявления,
сохранять свои свойства даже при
концентрации их 1,5—2,0 г на 1 л.
Это позволяет обработать в фе-
нидоно-гидрохиноновых
проявителях гораздо больше
фотоматериала, чем в
метоло-гидрохиноновом.
Кроме того растворы с
фенидоном в процессе проявления
почти не окрашиваются, поэтому
в них можно обрабатывать
фотобумагу и обращаемые
фотоматериалы.
На то, как влияет фенидон на
зернистость изображения, единой
точки зрения пока нет. Одни
исследователи утверждают, что в
фенидоно-гидрохиноновых
растворах получается мелкозернистое
изображение, другие считают, что
фенидоно-гидрохиноновые
растворы вообще не влияют на
зернистость.
У фенидона есть ряд
недостатков. Во-первых, он
разлагается в растворах с высокой
концентрацией щелочи. Кроме того, если
при комнатной температуре
раствор сохраняется от 18 до 24
месяцев, то при температуре выше
30° С время хранения его
уменьшается до 6 месяцев. Фенидон
растворяется хуже, чем другие
90
проявляющие вещества. Это очень
важно, потому что концентрация
-его в проявляющем растворе
очень мала, и неполное
растворение фенидона может сильно
сказаться на свойствах проявителя.
Поэтому фенидон обычно
растворяют последним в небольшом
количестве проявителя, нагревая его
до 50—60° С.
Рецептура фенидоно-гидрохи-
ноновых проявляющих растворов
весьма обширна и рассчитана на
все виды обработки
фотоматериалов. Вот пример универсального
раствора, который рекомендует
фирма «Ильфорд»:
Фенидона 0,5 г
Гидрохинона . ... 12,0 г
Сульфита натрия
безводного .... 50,0 г
Соды безводной . . . 60,0 г
Бромистого калия . . 2,0 г
Бензотриазола .... 0,2 г
Воды до 1,0 л
Для проявления фотопленок
этот концентрированный раствор
разбавляют водой в отношении
1 : 7. Продолжительность
проявления 4—8 минут при температуре
раствора 20° С. Для обработки
фотобумаг концентрированный
раствор разбавляют водой в
отношении 1:1. Продолжительность
проявления 45—75 секунд при
температуре раствора 20° С.
Из растворов для
одноразового использования распространен
такой:
Фенидона
Гидрохинона
Сульфита натрия
безводного
Соды безводной
Бромистого калия
Бензотриазола
Воды ....
Для проявления
1,0 г
16,0 г
125,0 г
60,0 г
9,0 г
3,0 г
. до 1,0 л
фотопленок
средней светочувствительности
концентрированный раствор
разбавляют водой в отношении 1 :20.
Продолжительность проявления
6—8 минут при температуре
раствора 20 С.
Высокочувствительные фотопленки в этом же
растворе нужно обрабатывать 8—10
минут.
При разбавлении
концентрированного раствора в отношении
1 : 50 продолжительность
проявления фотопленок увеличивается
вдвое.
Научно-исследовательский
кино-фотоинститут для обработки
фотопленок рекомендует такой
рецепт:
Фенидона 0,15 г
Гидрохинона .... 3,0 г
Сульфита натрия
безводного .... 100,0 г
Буры 2,0 г
Борной кислоты ... 4,0 г
Бромистого калия 1,0 г
Воды до 1,0 л
В этом растворе фотопленку
следует проявлять 12—16 минут
при температуре раствора 20° С.
Обрабатывать фотобумагу
можно в растворе, составленном
по такому рецепту:
Фенидона 0,1 г
Гидрохинона .... 2,2 г
Сульфита натрия
безводного .... 16,0 г
Соды безводной . . . 22,0 г
Бромистого калия . . 4,0 г
Воды до 1,0 л
Фенидоно - гидрохиноновые
проявляющие растворы
применяют для обработки черно-белых
обращаемых кинопленок и для
первого проявления цветных
обращаемых кинопленок.
Пользуясь фенидоном, нужно
помнить, что для каждого
фотоматериала требуется подбор
особого режима проявления. Этот
режим обычно устанавливают с
помощью специальной
аппаратуры. В любительских условиях его
подбирают по проявленным экс-
понограммам, сделанным на
фотоматериале, который в
дальнейшем собираются обрабатывать.
Кандидат технических наук
Е. А. ИОФИС,
Всесоюзный
государственный институт
кинематографии
ИЗВЕСТКОВАНИЕ:
ногда оно нужно?
Правильное внесение
удобрений — главное условие
нормального развития растений и
хорошего урожая. Вреден не только
недостаток, но и избыток
удобрений, и этот вред не всегда удается
исправить. Например, был случай,
когда некоторые хозяйства, не
утруждая себя анализом почвы,
за несколько лет внесли столько
суперфосфата, что его хватило бы
почти на 80 лет. Пользы это
никакой не принесло, хотя и стоило
очень дорого; кроме того,
кислотность почвы резко повысилась,
что потребовало новых затрат на
ее нейтрализацию.
Садовод должен заранее, еще
до закладки сада, узнать
особенности почвы на своем участке.
чтобы улучшить ее. Поэтому одно
из важнейших и первоочередных
мероприятий при выращивании
сада — анализ почвы. Прежде
всего надо определить степень
кислотности или щелочности
почвенного раствора —
концентрацию в нем водородных ионов,
которую выражают отрицательным
логарифмом — величиной рН.
Знать кислотность почвы очень
важно: при повышенной
кислотности эффективность удобрений
значительно снижается.
Чтобы определить кислотность,
не нужны какие-либо специальные
агрохимические знания: такой
простейший анализ может
самостоятельно выполнить каждый
садовод-любитель.
Для этого прежде всего нужно
правильно взять средние образцы
почвы. Если исследуемый участок
однороден по рельефу и
почвенному покрову, то для одного
анализа необходимо сделать, по
крайней мере, три прикопки (ямы),
расположенные треугольником в
2—3 м одна от другой. Прикопку
делают шириной 18—20 см и
глубиной 30—40 см, так, чтобы одна
из ее стенок была отвесной.
Очистив прикопку от земли,
срезают с отвесной стенки слой
толщиной 5—7 см во всю ее высоту.
Обрушенную землю собирают в
ведро или ящик. В то же ведро
собирают землю из других
прикопок и тщательно перемешивают,
после чего из разных мест ведра
91
НОРМЫ ИЗВЕСТКОВЫХ УДОБРЕНИЙ, Г/М*
1 Виды удобрений .
1 Известняк молотый (мел)
1 Известь гашеная
1 Известняк доломитовый
1 Известняк доломитовый
1 гашеный
1 Доломитовая мука
рН солевой вытяжки почвы 1
менее 4,5
500/600/800
375/450/600
1 465/560/740
330/400/530
240/290/380
1 4'5
450/550/750
340/410/560
420/510/700
300/360/500
220/260/360
5,0
350/450/550
260/340/410
330/420/510
230/300/360
170/220/260
5f4—5f5
250/350/450
190/260/340
230/330/420
165/230/300
120/170/220
Примечание. Первая цифра — для супесчаных почв и легких суглинков;
вторая— для средних и третья — для тяжелых суглинков.
набирают в банку или коробку
емкостью 0,5—1 л среднюю пробу.
Перед анализом почву нужно
просушить. Для этого ее
рассыпают на чистой бумаге слоем
толщиной 1—2 см и оставляют на
2—3 дня в хорошо
проветриваемом помещении (но не на
солнце!]. Просушенную почву
растирают и просеивают через сито
с отверстиями диаметром 1 мм.
Теперь можно приступить
к анализу. Самый быстрый и
простой способ определения
кислотности — способ Н. И. Алямов-
ского. Существует специальный
набор, в который входят все
принадлежности и реактивы,
необходимые для определения
кислотности по методу Алямовского.
Но анализ можно проделать и не
пользуясь этим набором.
В колбочку емкостью 100 мл
насыпают 20 г высушенной и
растертой почвы, заливают 50 мл
раствора хлористого калия G5 г
KCI в 1 л раствора] и, тщательно
перемешав, оставляют на сутки.
Пипетку и пробирку, которыми
будут пользоваться при
определении кислотности, осторожно
ополаскивают отстоявшимся
прозрачным раствором. С помощью
пипетки в пробирку наливают
2,5 мл раствора и приливают
к нему чистой пипеткой 0,15 мл
(около 4 капель]
комбинированного индикатора, состоящего из
2 частей бромтимолового синего и
1 части метилового красного (эти
индикаторы можно купить в
любом магазине химреактивов
или достать в химической
лаборатории]. Пробирку осторожно
встряхивают, чтобы перемешать
ее содержимое. Первоначальный
зеленоватый цвет индикатора
изменится.
Собственно говоря, на этом
анализ закончен. Остается только
найти на специальной шкале цвет,
соответствующий окраске
получившейся смеси, и вы узнаете
величину рН почвенной вытяжки.
Если раствор окрасился в сине-
зеленый цвет, то величина рН
составляет около 7—8, в зеленый —
примерно 6,5, оранжевый или
желтый — от 5,5 до 6, желтовато-
розовый — 5, розовый — от 4 до 5.
Почвы, имеющие рН солевой
вытяжки от 6 до 7, считаются
нейтральными, более 7 —
щелочными, менее 6 — кислыми. Если рН
почвы ниже 4,5, то ее считают
сильно кислой.
Если анализ показал, что почва
вашего участка кислая, ее нужно
нейтрализовать лутем
известкования. Внесение извести устраняет
избыточную, вредную для
большинства растений кислотность и
создает благоприятные условия
для нормальной
жизнедеятельности полезных микроорганизмов,
с помощью которых растения
усваивают органические
вещества.
Кроме того, известкование
улучшает физические свойства
почвы (механический состав,
структуру, влагоемкость] и
повышает эффективность органических
и минеральных удобрений.
Наконец, с известью в почву вносится
один из необходимых растению
элементов — кальций, а если
вносить доломитовый известняк или
доломитовую муку, — то и
магний.
Дозы внесения извести зависят
от степени кислотности почвы и от
ее механического состава. Они
приведены в таблице.
Наибольший эффект дает вне*
сение извести с осени. Ее
заделывают в почву при перекопке или
перед закладкой сада.
Впоследствии известковые материалы
нужно вносить в почву сада один
раз в 3—4 года.
Размолотая известь должна
быть возможно более
равномерно распределена по поверхности
почвы и хорошо перемешана со
всем пахотным слоем. Для более
полного взаимодействия извести
с почвой желательно, чтобы
между внесением извести и
посевом сельскохозяйственных
культур или посадкой деревьев
прошло несколько дней.
Консультацию по производству
анализов, инструктаж и
необходимые для анализов реактивы
садоводы-любители Москвы и
Московской области могут получить
в агрохимической лаборатории
Московского городского
отделения Общества озеленил и охраны
природы (Москва, ул. Б.
Хмельницкого, д. 6]. Лаборатория
делает и более сложные анализы
почв, на основании которых
может дать совет, в каких
удобрениях нуждается исследованная
почва, в каких дозах, когда и
каким способом должны быть
внесены эти удобрения.
Ф. П. КАЩЕНКО,
Агрохимическая
лаборатория
Московского отделения
Общества озеленения
и охраны природы
92
4Ш
НОВОСТИ ОТОВСЮДУ
КОМФОРТ В НОРЕ
Микроклимат в норах
животных — это одна из
неразрешенных еще загадок природы. В норе
большой песчанки (грызуна,
обитающего в зоне пустынь]
температура воздуха не опускается
ниже -Ь5°С зимой и не
поднимается выше +23 С летом. Этот факт
тем более удивителен, что в
периоды, когда проводились
замеры, температура приземного слоя
воздуха зимой была —20°С и
летом + 48 С, причем
поверхностный слой земли иногда
прогревался до +68°. Температура
воздуха в норе регулируется каким-
то, пока еще не разгаданным
способом (кстати, в мае, когда
животное начинает выходить из
норы, температура поднимается
сразу на 10° хотя в остальные
месяцы колебания не превышают 2—
УС].
Конечно, было бы весьма
занятно представить дело так,
будто песчанка сама регулирует
температуру воздуха. Но в
действительности зверек просто инстик-
тивно использует какие-то
природные особенности почвы,
благодаря чему добивается столь
удивительных результатов.
ЧЕРЕЗ ТРИ СТРАНЫ
Подходит к концу разработка
проекта газопровода Копер —
Грац — Требич. Первый город
находится в Югославии, второй —
в Австрии, третий — в
Чехословакии.
На восточном побережье
Алжира запроектирована станция
сжижения газа. В порту Копер
будет построена пристань для
разгрузки судов со сжиженным
газом из Алжира. Она сможет
принимать суда с грузоподъемностью
до 100000 тонн. Для хранения
газа предусматриваются огромные
подводные резервуары.
Каждый год по трубопроводу
будет транспортироваться 1
миллиарда кубометров
высококачественного газа без серы, который
необходим для черной
металлургии.
Трасса газопровода проходит
возле венгерской границы, и,
возможно, Венгрия станет одним из
потребителей газа. Это не
уменьшит «доли» остальных стран —
пропускную способность
газопровода можно будет увеличить в
три с лишним раза.
ЛУННЫЕ ЗАВОДЫ
Отсутствие воздуха на Луне
может послужить развитию
«лунной промышленности» — такое
предположение высказывает
американская газета «Чикаго три-
бюн». В самом деле,
производство некоторых изделий требует
глубокого вакуума, а на Луне для
этого — идеальные условия. К
таким изделиям относятся,
например, микроэлектронные схемы,
электронно-лучевые трубки,
некоторые лекарства. Их производство
на Луне может оказаться
выгодным и с технологической, и с
экономической точек зрения.
Правда, экономические
выгоды пока что сомнительны — очень
уж велики расходы по доставке
на лунную поверхность сырья и
машин. Но специалисты полагают,
что это вопрос времени. Газета
утверждает, что в 1965 году
стоимость доставки груза с Земли на
Луну составляла 5000 долларов за
фунт; к 1980 году эта сумма
уменьшится, возможно, до 30
долларов.
ЛАМПА РАБОТАЕТ ДОЛЬШЕ
Йодные лампы накаливания,
появившиеся в последнее время,
служат намного дольше
обычных — небольшая добавка
газообразного иода уменьшает
испарение вольфрамовой нити.
Английский журнал «New Scientist»
A966, № 482] сообщает о еще
более совершенных лампах, в
которых вместо иода используется
фтор.
В чем же преимущества
фтора перед иодом! Фтор —
единственный элемент,
вступающий в реакцию с вольфрамом
при комнатной температуре.
Образовавшийся шестифтористый
вольфрам во время горения
лампы попадает на раскаленную нить
и разлагается. Вольфрам оседает
на нити, а фтор возвращается в
«атмосферу» лампы. Так как
вольфрам все время оседает на нити,
то он не попадает на стекло
лампы и не затемняет его.
ШИВОРОТ — НАВЫВОРОТ
Связанный азот — это
удобрения, а удобрения — это хлеб,
жизнь. Но процесс связывания
атмосферного азота имеет и свои
отрицательные стороны.
Например, при производстве азотной
кислоты вместе с дымом в
атмосферу выбрасывается много
ядовитых окислов. Следовательно,
азот надо уметь не только
«связывать», но и «развязывать»...
Как сообщает американский
журнал «Chemical Week» A9
февраля 1966 г.], сейчас разработан
новый способ очистки газов,
образующихся при производстве
азотной кислоты. Он основан на
том, что в специальных камерах,
содержащих катализатор, окислы
азота восстанавливаются до
азота; благодаря этому количество
вредных примесей удается
снизить до 50 частей на миллион.
НОВЫЙ
СВЕРХПРОВОДНИК
Используя сверхпроводимость
различных материалов при
температурах, приближающихся к
абсолютному нулю, можно создавать
мощные магниты весьма
небольших размеров, конструировать
радиоэлектронные устройства с
очень низким уровнем помех,
работающие с малой затратой
электроэнергии.
Но создание таких приборов
связано с большими трудностями,
так как получение и поддержание
низкой температуры (обычно
требуется температура около 0,3 К]
очень сложно. В связи с этим
большой интерес представляет
открытие сверхпроводящих свойств
теллурида свинца при 5К.
Разница температур кажется
небольшой, но технически достичь
температуры 5°К несравненно
легче, чем 0,3°К.
НОВОСТИ ОТОВСЮДУ
93
ПАШИ КОНСУЛЬТАЦИИ
Первого мая этого года на праздничном
телевизионном «Огоньке» выступали сотрудники журнала
«Химия и Жизнь». Многие читатели, видевшие эту
передачу, заинтересовались показанным там
опытом — «химическими часами» и просили рассказать,
как сделать такой опыт, а также в чем состоит его
«секрет».
Опыт «химические часы» делается так.
Предварительно готовят два раствора:
Раствор № 1
Йодата калия (КЛОз) 3,9 г
Воды 1л
Раствор № 2
Сульфита натрия (ЫагБОз) 1 г
Серной кислоты (концентрированной) . . . 0,94 мл
Воды 1л
Крахмального клейстера несколько
миллилитров
Оба раствора прозрачны и бесцветны. Для
первого опыта берут 100 миллилитров раствора № 2,
быстро (лучше при перемешивании) приливают его
к 100 миллилитрам раствора № 1 и сразу же
начинают отсчет времени. Через 6—8 секунд (точное
время зависит от температуры) жидкость
мгновенно окрасится по всему объему в темно-синий, почти
черный цвет.
Для второго опыта берут 100 миллилитров
раствора № 2, а 50 миллилитров раствора № 1
разбавляют чистой водой ровно вдвое. В этом случае
время, прошедшее с момента сливания растворов
до их окрашивания, увеличится в два раза.
И, наконец, если смешать 100 миллилитров
раствора № 2 с 25 миллилитрами раствора № 1,
разбавленного 75 миллилитрами чистой воды, то
«часы» будут работать в четыре раза дольше, чем в
первом опыте.
Этот эксперимент наглядно демонстрирует один
из фундаментальных химических законов — закон
действия масс. Согласно этому закону
скорость реакции пропорциональна концентрациям
реагирующих веществ.
Но у всех, кто когда-либо видел этот опыт,
возникает вопрос: почему растворы окрашиваются
мгновенно, как по мановению волшебной палочки,
а не постепенно, как этого следовало бы ожидать?
Посмотрим, какие при этом происходят реакции.
Поскольку в растворе есть серная кислота, то она
вытесняет йодноватую и сернистую кислоты из их
солей:
2KJ03 -f H2S04 = 2HJ03 + K2S04,
Na2S03 + H2S04 = H2S03 4- Na2S04.
Затем эти две кислоты взаимодействуют между
собой по уравнению:
HJ03 + 3H2S03 = Ш + 3H2S04.
Но это — лишь суммарная запись процессов,
происходящих в демонстрационном сосуде. В
действительности же образующаяся йодистоводородная
кислота немедленно вступает во взаимодействие
с йодноватой кислотой:
5HJ + HJ03 = 3J2 + 3H20.
Если бы все ограничилось только этими
реакциями, то присутствующий в растворе крахмал темнел
бы постепенно, по мере выделения йода. Почему
же этого не происходит? Потому что в сосуде идет
еще один процесс:
H2S03 + J2 h H20 = 2HJ + H2S04.
Эта реакция протекает значительно быстрее
предыдущей, и поэтому йод как бы «не успеваете окрасить
крахмал, а тут же снова восстанавливается до йодис-
товодородной кислоты.
Но обратите внима; »е: в ходе этой реакции
непрерывно расходуется сернистая кислота. И как
только она вся превратится в серную, немедленно
произойдет выделение йода и раствор мгновенно
окрасится по всему объему.
Разбавляя раствор № 1 в два и четыре раза, мы
соответственно уменьшали концентрацию йодата
калия (ведь общий объем смеси оставался
постоянным), в результате чего скорость основной реакции
пропорционально уменьшалась.
Всем читателям, заинтересовавшимся статьей
«Информация на спице» («Химия и Жизнь», 1966 г.,
№ 5} и приславшим письма в редакцию,
сообщаем дополнительные сведения о перфокарто-
теках.
Заявки на перфокатры принимаются Бюро
технической информации Эстонской ССР по адресу:
г. Таллин, ул. Ломоносова, 29. Обращаем внимание
читателей на то, что перфокарты выпускаются трех
размеров: карты формата К-4 B91 X 207 мм),
К-5 B07X147 мм) и К-6 A47X105 мм). Выбрав
какой-либо один формат, его следует постоянно
придерживаться, иначе будет невозможна
сплошная сортировка картотеки. В описанной нами карто-
94
теке были использованы карты К-5, которые
кажутся нам наиболее подходящими для подобной
цели.
Кроме самих перфокарт, полезно приобрести
комплект оборудования, состоящий из щипцов для
прорезывания перфораций, сортировальных спиц,
селектора и кодирующей линейки. Заказы на такие
комплекты принимает «Союзглавприбор» по адресу:
Москва, площадь Ногина, 5/2. Попутно заметим, что
приобретение комплекта оборудования желательно,
но не обязательно. В картотеках малого объема (до
500 карт в год) энтузиасты с успехом используют
ножницы для прорезания перфорации и
обыкновенную упругую вязальную спицу для сортировки
перфокарт.
Самый ответственный этап работы — составление
списка кодируемых признаков, который должен
отразить весь круг интересов создателя картотеки.
Прежде чем приступить к кодированию, необходимо
ознакомиться с элементарными основами теории
кодирования и типами различных кодов. Помните:
ПОСЛЕ ТОГО КАК НАЧАТО КОДИРОВАНИЕ, ДАЖЕ
САМОЕ НЕЗНАЧИТЕЛЬНОЕ ИЗМЕНЕНИЕ СИСТЕМЫ
ПРИЗНАКОВ ПОТРЕБУЕТ СПЛОШНОГО ПРОСМОТРА
ВСЕЙ КАРТОТЕКИ И ИСПРАВЛЕНИЯ МНОГИХ КАР-
Если вы увлекаетесь коллекционированием значков
и вам хочется иметь в коллекции уникальный
значок — сделайте его сами.
Конечно, это предложение — не только для
коллекционеров. Очень приятно иметь собственный
значок, который будет напоминать о пионерском
лагере, спортивных соревнованиях, туристских
походах. Сделать двадцать—тридцать таких сувениров в
школьной мастерской или даже дома не так уж
сложно.
Прежде всего хорошо продумайте форму значка,
его внешний вид, надписи. Нарисуйте эскиз в
натуральную величину. Не увлекайтесь сложным
контуром: чем проще значок, тем он лучше смотрится,
да и делать его легче. Когда эскиз готов, вырежьте
из картона шаблон значка. Из тонкой медной или
латунной фольги нарежьте по шаблону заготовки,
повторяющие контуры будущих значков.
ТОЧЕК. Превосходные рекомендации по составлению
списков признаков, а также по принципам
кодирования можно найти в монографии «Перфокарты и их
применение в науке и технике» (сборник под ред.
Р. С. Кейси, Дж. Перри, У. Берри и А. Кента,
Москва, Машгиз, 1963) и книге С. Я. Роометса
«Перфокарты и их применение» (Таллин, БТИ СНХ ЭССР,
1963).
Для некоторых областей химии уже существуют
детально разработанные списки признаков, которые
могут оказаться полезными для будущих
составителей перфокартотек. Такие списки, а также опыт
ведения картотек регулярно описываются в
периодических изданиях, например, в ежемесячном
сборнике ВИНИТИ «Научно-техническая информация» и
в журнале «Journal of Chemical Education»
(США).
Из последних литературных новинок можно
рекомендовать вышедшую в издательстве «Наука» книгу
«Кибернетика и документалистика», подготовленную
Научным советом по комплексной проблеме
«Кибернетика». В этом году то же издательство выпустит
книгу С. А. Пищальникова «Перфокарты—ученому.
Механический поиск информации — новое средство
организации труда ученого».
Теперь заготовку надо сделать жесткой. Для
этого ее придется покрыть слоем меди в
гальванической ванне. Начните с того, что у края каждой
заготовки иголкой проткните по отверстию. В отверстия
пропустите тонкие медные проволочки. Заготовки
тщательно промойте, обезжирьте бензином,
протрите зубным порошком и промойте в проточной воде.
Затем пинцетом опустите их на полминуты в раствор
азотной кислоты E—10 мл HN03 на 100 мл воды;
ОБРАЩАТЬСЯ С ОСТОРОЖНОСТЬЮ!) и снова
промойте в проточной воде.
Теперь на проволочках подвесьте заготовки на
металлический стержень — катодную штангу (см. 3-ю
стр. обложки]. Листки фольги не должны
закрывать друг друга. Опустите подвеску в химический
стакан с медными пластинками — анодами и
электролитом для меднения B5 г медного купороса и
*,5 £Ш верной кислоты на 100 мл воды, лучше дис-
Ш
ЗНАЧОК,
которого
ни у кого нет
95
тиллированной]. Раствор должен полностью
покрывать заготовки. Ток в цепи установите из расчета
100 ма на 10 см2 покрываемой поверхности.
Источник тока — аккумулятор (если есть выпрямитель, то
можно питаться от сети). Каждые два часа вынимайте
заготовки и измеряйте их толщину (она должна
быть в пределах 0,5—0,8 мм]. После меднения
детали промойте.
Если вы хотите дать рельефные детали или
надписи, наметьте их иголкой на поверхности. Ту часть
поверхности, которую покрывать не нужно,
изолируйте — нанесите на нее кисточкой клей БФ или
расплавленный парафин. После этого значки вновь
опустите в электролит и включите ток. Открытые
участки покроются медью — получатся значки с
рельефным изображением. Снимите слой лака или
парафина.
На значке можно выгравировать рисунок или
надпись — но это не обязательно. Аккуратно
припаяйте к оборотной стороне значка булавку. Теперь
нужно придать значку нарядный вид. Можно
прибегнуть к химической окраске или никелированию *.
Но особенно хорошо выглядят значки,
обработанные лод старое серебро.
Приготовьте раствор азотнокислого серебра:
2—3 г AgNQ3 (ОСТОРОЖНО!) на 100 мл воды. Коли-
* О химической окраске клуб Юный химик
сообщал в № 8 за этот год, о никелировании — в № 7.
чество раствора — то же, что и для меднения.
В этот раствор небольшими порциями приливайте
соляную кислоту C—4 объема HCI на 1 объем
раствора]. На дно стакана выпадет белый осадок
хлористого серебра. Раствор над осадком слейте, а
осадок 5—6 раз промойте дистиллированной водой.
Воду каждый раз аккуратно сливайте так, чтобы не
потерять хлористое серебро. К отмытому осадку
добавляйте понемногу раствор йодистого калия
C0—40 г. KJ на 100 мл воды] до полного
растворения хлористого серебра. Доливая воду, доведите
объем раствора до первоначального. Электролит
для серебрения готов.
В этом электролите значки нужно выдерживать
около часа. Ток— 10 ма на каждые 10 см2
поверхности. Аноды — серебряные или (что проще)
угольные. Их можно сделать из электродов, которыми
пользуются сварщики, либо, в крайнем случае, из
карандашных стержней, хорошо скрепленных
медной проволочкой. Общая площадь электродов
должна быть немного больше площади значков.
Посеребренные значки можно почернить. Для
этого приготовьте водный раствор сульфида калия
@,5—1 г K2S на 100 мл воды] и нагрейте его до
50°С В раствор опустите значки, и металл станет
сначала серым, потом синим и, наконец, черным.
Вымойте значки и потрите их поверхность суконкой.
Все выпуклые детали приобретут серебристый
светлый оттенок, остальная поверхность останется
черной. Значки готовы.
ПОБЕДИТЕЛИ КОНКУРСА КЛУБА ЮНЫЙ ХИМИК
Андрей ЗАХАРОВ (рудник Жолымбет
Целиноградской обл., школа № 1), Виктор СЛОНИМ
(Ленинград, школа № 76), Виталий СМИРНОВ
(село Шихазаны Чувашской АССР), Николай
СМИРНОВ (Ленинград, школа № 318), Геннадий
ТОДРАМОВИЧ (г. Единцы Молдавской ССР,
школа № 1), Кристьян X АЛЛ ЕР (г. Тарту,
школа № 5).
Победители конкурса награждаются годовой
подпиской на журнал «Химия и жизнь».
Редакция от души поздравляет победителей и
благодарит всех ребят, принявших участие в конкурсе.
На обложке: 1-я стр. — рисунок Л. Кулагина к статье Е. И. Гуровича «От V Д° НгО». 3-я стр. — рисунок
Е. Данильцева к заметке «Значок, которого ни у кого нет».
На вклейке: 1-я стр. — рисунок В. Колтунова по мотивам туркменских ковров к статье В. И. Кривенцова
«Краски туркменского ковра». 2-я стр. — кадры киносъемки процесса образования ситаллов
Редакционная коллегия:
Главный редактор И. В. Петрянов-Соколов
П. Ф. Баденков, В. И. Гольданский, Н. М. Жаворонков, С. В. Кафтанов, Л. И. Мазур,
Б. Д. Мельник, М. И. Рохлин (зам. главного редактора), П. А. Ребиндер, С. С. Скороходов,
Б. И. Степанов, А. С. Хохлов, М. Б. Черненко (зам. главного редактора), Н. М. Эмануэль
Рукописи не возвращаются. При перепечатке ссылка на журнал «Химия и Жизнь» обязательна.
Оформление С. Верховского Технический редактор Э. Язловская
Адрес редакции: Москва, В-333, Ленинский проспект, 61/1. Телефоны АВ 7-72-64 и АВ 7-66-23
Т 11649. Подп. к печ. 13/VIII 1966 г. Бумага 84 X 108Vi6- Бум. л. 3,0. Печ. л. 6,0. Усл. п. л. 10,08 + 1 вкл. Уч.-иэд. л. И,4. Тираж 77 000.
Зак. № 1231. Цена 30 коп. Набор и печать выполнены в Московской типографии № 2 Главполиграфпрома Комитета по печати при Совете
Министров СССР. Москва, Проспект Мира, 105. Печать обложки и цветной вклейки и брошюровочные работы выполнены во 2-й
типографии издательства «Наука». Москва, Шубинский пер., 10.
96
I Без полимерных матери- ►
| алов и гальванотехники
(промышленное
изготовление граммофонных
пластинок было бы
невозможным
i
JMAGNJFJCAT
В 243
Сократ утверждал, что
духи — это зло, поскольку,
надушившись, все
приобретают одинаковый
запах— и достойные, и
недостойные
Желающие постичь азы
стеклодувного мастерства
найдут в этом номере
советы о том, как продувать
отверстия