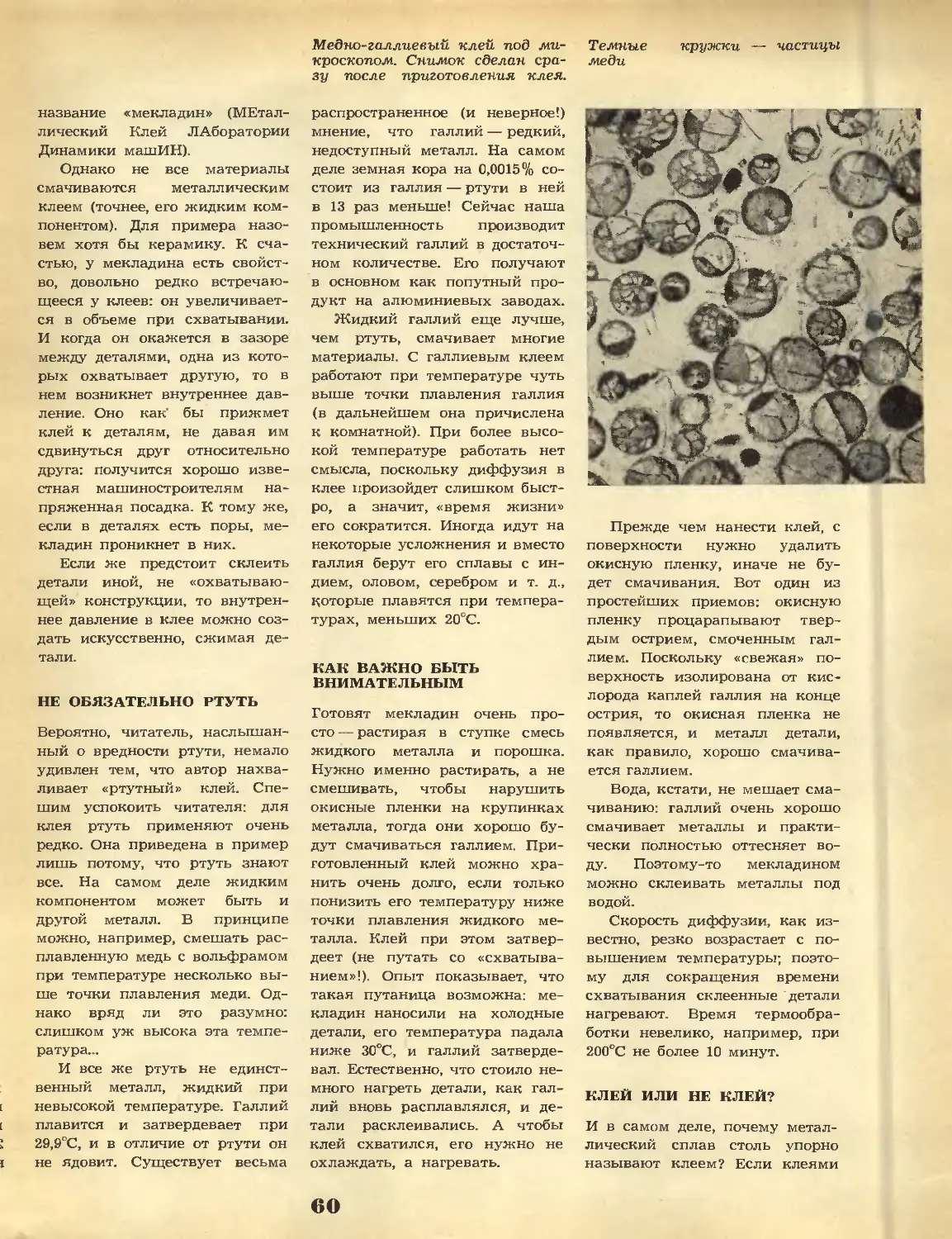
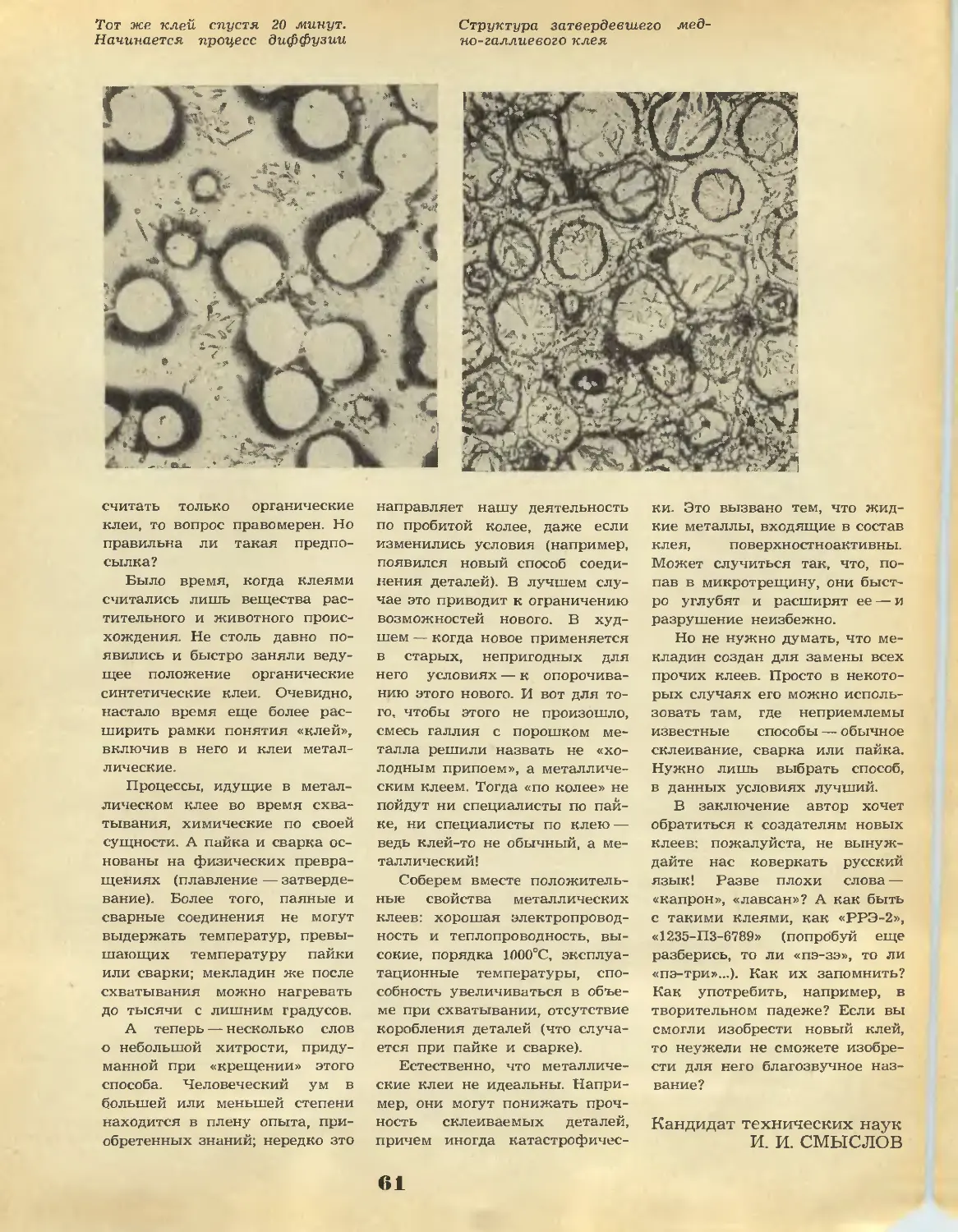
Текст
химия и жизнь
Научно-популярный журнал Академии наук VVCP 1У6Н
12
вакщша предотвращает резус-конфликт.»
Мальчик, вынимающий занозу.
V в. до н. э. Рим, Палаццо Кон-
серватори.
Прогулки босиком по
скользкой, колючей, острой,
занозистой поверхности нашей
планеты не всегда заканчиваются
удачно. Обувь — непременный
атрибут цивилизации. «Между
нами и землей» — так
называется помещенная в этом
номере статья о материалах
для подошв.
1-я страница обложки.
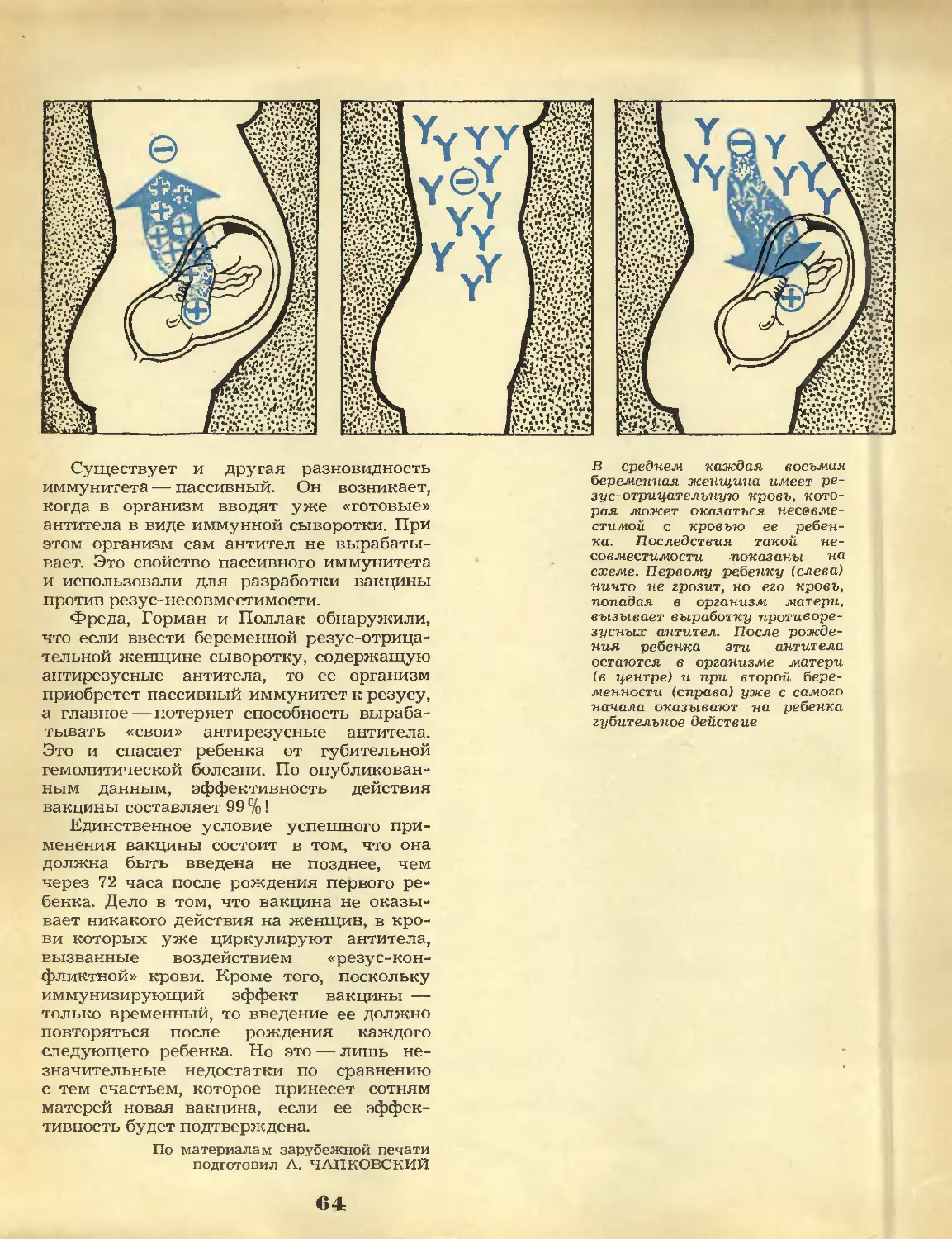
У каждой восьмой женщины —
отрицательный резус-фактор.
О том, чем это грозит и как
можно предотвратить резус-
конфликт, рассказывает статья
«Вакцина против резуса» в
Э1 ом номере.
ЕЖЕМЕСЯЧНЫЙ
НАУЧНО-
ПОПУЛЯРНЫЙ
ЖУРНАЛ
АКАДЕМИИ
НАУК СССР
ХИМИЯ И ЖИЗНЬ
Л 12
ГОД ИЗДАНИЯ 4-й
ДЕКАБРЬ 1968
Редакционная коллегия:
И. В. Петрянов-Соколов
(главный редактор),
П. Ф. Баденков,
Н. М. Жаворонков,
B. А. Каргин,
C. В. Кафтанов,
Н. К. Кочетков,
Л. И. Мазур,
Б. Д. Мельник,
В. И. Рабинович
(ответственный секретарь),
П. А. Ребиндер,
М. И. Рохлин
(зам. главного редактора),
> С. С. Скороходов,
! Б. И. Степанов,
. А. С. Хохлов,
'. М. Б. Черненко
(зам. главного редактора),
[ Н. М. Эмануэль
[Редакция:
[Б. Г. Володин,
[В. Е. Жвирблис,
lA. Д. Иорданский,
H. И. Коломийцева,
H. М. Либкин,
;Э. И. Михлин,
Ш. В. Станцо,
ГТ. А. Сулаева,
IB. К. Черникова
I Художественный редактор
)С. С. Верховский
Г Технический редактор
>Э. С. Язловская
I Корректоры:
1Ю. И. Глазунова,
ЗЕ. И. Сорокина
Шри перепечатке ссылка на журнал
»«Химия и жизнь» обязательна.
\Адрес редакции:
Шосква В-333,
{.Ленинский проспект, 61.
ГТелефоны:
1135-52-29,
1135-32-41,
1135-63-91.
[[Подписано к печати 6/XI 1968 г. Т 16615. Бумага 84 X
< X108'/ie. Печ. л. 6,0. Усл. печ. л. 10,08. Уч.-изд. л. 11,1 +
f +1 вкл. Тираж 135 000. Зак. 2787. Цена 30 коп.
/[Московская типография № 2 Главполиграфпрома
И Комитета по печати при Совете Министров СССР.
Л Москва, проспект Мира, 105.
13
15
19
22
25
29
34
36
38
41
44
47
51
56
59
62
63
65
66
70
74
77
79
81
83
91
Мастерские науки
Психофармакология сегодня —
О короткой истории
психофармакологии
Изгнание максвеллова демона
Страницы истории
Сто лет завода
Продолжая читать
Элемент №...
Калий
классиков
Что вы знаете и чего не знаете
о калии и его соединениях
«Не для того учреждаются
университеты...»
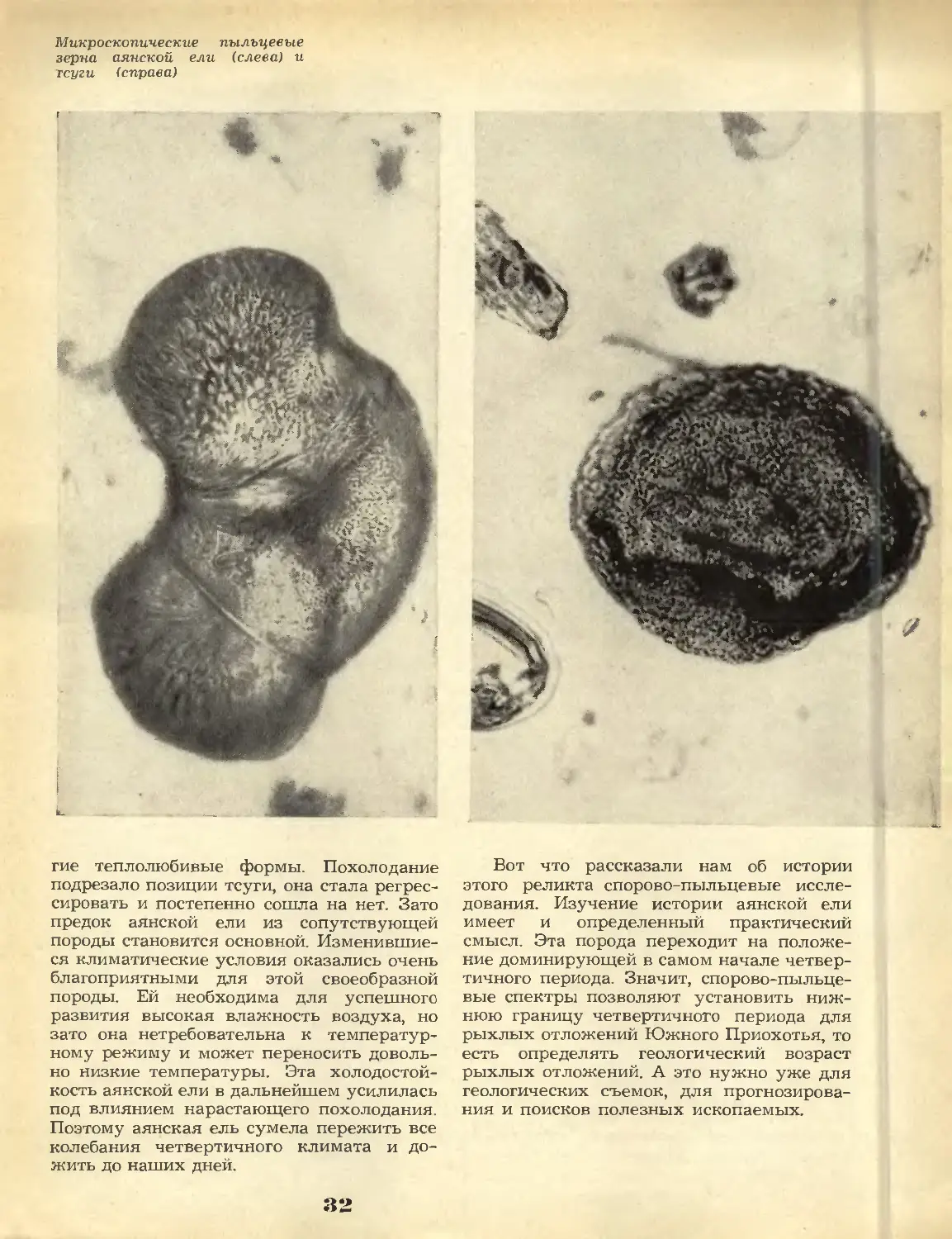
История одного реликта
Наш календарь
Борис Николаевич Меншуткин
«Незримые нити,
связывающие нас с прошлым...»
Наука о живом
По сигналу красного света .
Наш календарь
Август Вильгельм Гофман
Что вы знаете и чего не знаете
о красителях
Конкурс 1969 года
«Любимое дитя мое, мой образ,
мой опыт...»
Новости отовсюду
Наука — производству
Может ли металл быть клеем?
Информация
В лабораториях зарубежных ученых
Вакцина против резуса?
Комментирует врач-иммунолог
Сказка
Не нашей работы
Между нами и землей
Полезные советы и пояснения к ним
Не бойтесь мороза!
Как обращаться с
искусственным мехом -— _
Библиотека
«Воспитай ученика...»
Учитесь переводить
Немецкий — для химиков
Клуб Юный химик
Что это такое? Задачи о
кристаллах. Как различить пере-
И. П. Лапин
М. В. Волькенштейн
П. М. Лукьянов
И. Вольпер
П. П. Иванов
Т. А. Абрамова
С. А. Погодин
А. Г. Ломагин
Ю. С. Мусабеков
А. А. Макареня
И. И. Смыслов
А. Чапковский
Л. И. Привалова
Д. Плектей
Г. Филановский
А. А. Крейнин
Л. Ольгин
О. Коломийцева
Р. Г. Синев
путанные лекарства. Пять
вопросов о солях. Решения задач
Статьи, опубликованные в
журнале «Химия и жизнь» в
1968 году
МАСТЕРСКИЕ
НАУКИ
ПСИХОФАРМАКОЛОГИЯ
СЕГОДНЯ
Рассказывает Изяслав Петрович ЛАПИН —
руководитель отдела психофармакологии
Ленинградского психоневрологического
института им. В. М. Бехтерева
ЧТО УЖЕ ЕСТЬ
Сейчас мы располагаем тремя большими
группами лекарств, многие из которых
применяют. Нейролептиками — сильными
успокаивающими препаратами лечат
различные психозы и такой тяжкий недуг, как
шизофрению. В этой группе лекарств —
аминазин, резерпин, стелазин, мажептил,
галоперидол. Кроме сильнодействующих
средств, есть еще вторая группа — как их
называют, малые транквилизаторы: ме-
пробамат (он же — андаксин), триоксазин,
либрий (иначе — элениум), валий
(седуксен). Эти транквилизаторы помогают при
неврастении, истерии, психастении. Третья
большая группа лекарств —
антидепрессанты: имипрамин (другие названия —
имизин, мелипрамин, тофранил), амитрип-
тилин (то же — дамилен, триптизол), про-
триптилин и другие. Эти вещества
применяют против различных форм депрессий,
патологически сниженного настроения,
тоски, меланхолии.
Есть еще целый ряд соединений, с
которыми приходится иметь дело, но
лекарствами их назвать нельзя — это
галлюциногены (вызывающие галлюцинации), или
психозомиметики (то есть вызывающие
состояния, подобные психозам). Такие
вещества используют, правда, очень редко —
при исследовании некоторых психических
функций.
Необходимость в психотропных
медикаментах растет год от года. В некоторых
странах Европы потребление
нейролептиков за 10 лет увеличилось в 25 раз,
транквилизаторов за 8 лет — в 30 раз,
антидепрессантов за 7 лет — в 15 раз. Множество»
самых разных обстоятельств, среди
которых и ускорение ритма жизни, и
напряженная работа, и, как ни странно, успехи
медицины (она справилась со многими
заболеваниями, которые раньше как бы
маскировали различные психозы), привело к
тому, что половина всех больничных коек
мира сейчас — психиатрические.
КАК ПОЯВЛЯЮТСЯ НОВЫЕ ПРЕПАРАТЫ
Прежде чем создать новое лекарство, мы
с химиками подолгу изучаем формулы
уже известных соединений, пытаемся
установить, есть ли связь между строением
этих веществ и их фармакологическим
действием, сопоставляем лабораторные-
результаты с клиническими данными.
Только после такого тщательного
исследования мы можем «заказать» химикам
новый препарат.
Фармацевтические фирмы обычно
синтезируют много различных препаратов.
Мы же стараемся заниматься этим, если
так можно выразиться, более прицельно.
Лекарство, которое мы ждем, должно от—
личаться от существующих либо силой
действия, либо механизмом воздействия
на больных с разными психическими
заболеваниями, должно обладать какими-либо
преимуществами по сравнению с уже
известными препаратами. Иначе зачем
добавлять еще один, скажем, антидепрессант
к десяткам, которые уже применяют, если
его не отличает что-либо новое?
По нашему заказу лекарства
синтезируют в Технологическом институте
им. Ленсовета (на кафедре технологии
красителей), на кафедре органической химигг
Ленинградского педагогического
института им. Герцена и в других лабораториях.
А затем препараты попадают к нам, в от-
2
1 хотропных препаратов; это — 2
Сейчас психофармакология рас- антидепрессанты, пейролеп- ГАМ К — аминокислота, обра-
полагает тремя группами пси- тики и транквилизаторы зующаяся в мозгу
дел психофармакологии. Мы должны с
помощью простых, экономных и
обязательно быстрых методик (тестов) сравнить
новые соединения с так называемыми
эталонными: для нейролептиков такой
эталон — аминазин, для транквилизаторов —
мепробамат, для антидепрессантов — ими-
прамин.
Испытания, с помощью которых мы
проверяем новые препараты, называются
довольно метко — «просеивание». Надо
как бы насыпать их на «сито», «потрясти^
фармакологическими методами и
«высеять» лекарства, которые могут оказаться
наиболее эффективными для лечения тех
или иных психических или нервных
заболеваний.
Отбор таким способом любых новых
лекарств — процесс довольно сложный, но
особенно трудно «просеивать»
психотропные препараты. И прежде всего потому,
что оценивать такие вещества приходится
с помощью опытов на животных.
Психические расстройства человека и нарушение
поведения животного вызываются какими-
то общими биохимическими процессами, в4
которых принимают участие глубокие
мозговые структуры. Именно на эти мозговые
структуры животных и человека и
действуют современные психотропные
препараты.
Часто одни лекарства помогают нам
проверять другие. Антидепрессанты, к
примеру, не действуют на здоровых людей
и нормальных животных. Такие вещества
проявляют свою специфическую
активность только на фоне психической
заторможенности, депрессии, тоски. Как это
смоделировать на животных?
Еще раньше врачи заметили, что люди,
которые на протяжении длительного
времени принимают излишне большие дозы
резерпина (обычно это больные
гипертонической болезнью), постепенно
становятся вялыми, апатичными, у них часто
плохое настроение. Иногда дело заходит так
далеко, что даже опытный психиатр не
может отличить «резерпиновую
депрессию» от психической. Оба состояния
поддаются лечению антидепрессантами.
Не попробовать ли резерпин на
животных?
Мыши и крысы, которым давали
резерпин, переставали бегать, забивались в
угол клетки и сидели там, закрыв глаза;
температура тела у них была ниже
нормальной — получалось тоже что-то вроде
1*
3
«резерпиновой депрессии». Когда же такие
животные получали антидепрессанты, их
состояние значительно улучшалось.
Теперь почти во всех лабораториях, в том
числе и в нашей, испытывают новые
антидепрессанты, пользуясь «резерпиновой
моделью».
Для проверки других лекарств создают
другие модели: нейролептики, например,
иногда проходят испытание с помощью
« фенаминовой стереотипии » —
возбужденного состояния у животных, которым дали
стимулятор (фенамин).
ФЕНИГАМА — НОВЫЙ ТРАНКВИЛИЗАТОР
В процессе жизнедеятельности организма
участвуют разные аминокислоты. Среди
них есть одна, которая образуется только
в мозгу — это гамма-аминомасляная
кислота (ГАМК). Не так давно установили,
что ГАМК связана с процессами
торможения в головном мозгу. Мы и другие
психофармакологи сразу же заинтересовались
ГАМК, так как с помощью подобного
вещества можно было бы попытаться
регулировать некоторые функции мозга.
У ГАМК есть два огромных
достоинства. Во-первых, ГАМК находят только в
некоторых участках мозга. Значит, если
использовать ее как психотропное
средство, она будет, по-видимому, действовать
избирательно на мозг, не влияя на сердце,
печень и другие органы. Кроме того,
почти все психофармакологические
лекарства — эмпирически найденные
химические структуры, они не похожи на те
соединения, которые есть в организме, и
поэтому чужды ему. Как чужаки, эти
вещества оказывают иногда побочное
вредное действие. А гамма-аминомасляная
кислота — естественный продукт обмена
веществ, такой же, как, например,
витамины или гормоны; поэтому ГАМК не
токсична.
Применили ГАМК и ее оксиформу
ГАМК-ОН (которая активнее ГАМК и
тоже есть только в мозгу) впервые в Японии
для лечения эпилепсии (з виде препаратов
«Гам а л он» и «Гамибетал»). Эти вещества
ослабляли или даже полностью
прекращали судороги примерно у половины
больных. Но не было известно, почему такое
происходит.
Тем временем биохимики натолкнулись
на интересный факт: если ввести здоровым
животным даже очень большие дозы
ГАМК и ГАМК-ОН, количество этих
соединений в мозгу не изменится. Значит в
мозг они не проникают. Но как же
лекарства могут вылечивать эпилепсию, не
попадая в мозг?
Можно было предположить две
возможности. Либо ГАМК и ГАМК-ОН
оказывают противосудорожное действие не на
мозг, а на кровеносные сосуды, печень и
другие органы, связанные с обменом
веществ. Либо, что вероятнее, — у больных
эпилепсией проницаемость барьера между
кровью и мозгом (гемато-энцефалический
барьер) выше, чем у здоровых людей;
поэтому ГАМК и ее оксиформа могут
проникнуть в мозг больного...
Вскоре установили, что судороги,
искусственно вызванные у животных,
действительно увеличивают проницаемость ге-
мато-энцефалического барьера. Однако
введенная таким животным ГАМК все
равно не попадает в мозг — это проверено
опытами.
Нам тоже не удалось узнать, почему
ГАМК лечит эпилепсию; опыты на
животных ничего не дали. Тогда мы изменили
план действий: решили заставить ГАМК
проходить в мозг.
Известно, что для того, чтобы вещество
проникало в мозг, оно должно легко
растворяться в липидах (жирах), так как
мозговая ткань состоит в основном из липи-
дов. Известно и то, что легче всего
растворяются в липидах те препараты, в
молекулах которых есть фенильный
радикал (шестичленное углеводородное
кольцо). Химики-органики из Ленинградского
педагогического института такое вещество
получили. Это «фенигама», или «фенибут».
А в нашем отделе его предстояло
испытать Р. А. Хауниной и И. В. Прахье.
Когда давали фенигаму животным, они
вели себя так, как будто получили
успокаивающие препараты (транквилизаторы
или нейролептики). Животные
успокаивались, условные рефлексы у них
затормаживались, энцефалограмма
свидетельствовала, что биотоки мозга замедлились.
И еще: после приема фенигамы
усиливалось действие различных снотворных и
других успокаивающих веществ. Кроме
того, новое лекарство было действительно
нетоксично.
Прежде чем перейти к клиническим
испытаниям, исследователи обычно
проверяют препарат на себе. Все мы в нашей
лаборатории, да и не только мы, но и наши
4
друзья из других лабораторий изучали
действие фенигамы на себе. Мы
принимали этот препарат, затем следили за
изменением кровяного давления, пульса,
дыхания, записывали свои ощущения. Решали
простые арифметические задачи или
выполняли сложные задания перед пультом,
где проходят испытания летчики и моряки.
Оказалось, что фенигама в обычных
условиях на здоровых людей почти не
действует (вызывает лишь некоторое
успокоение). Но все испытуемые в один голос
утверждали, что сон в дни этих опытов
(несмотря на то, что принимали препарат
днем, а не перед сном) был глубоким и
приносил отдых. Причем испытуемые
засыпали почти мгновенно после того, как
ложились в постель, и так же мгновенно
утром наступало пробуждение.
Клиническая проверка показала, что
никаких побочных эффектов фенигама не
вызывала (в отличие от многих
психотропных препаратов) и в то же время обладала
отчетливым успокаивающим действием.
Кроме того, клиническое испытание
выявило, что фенигама ослабляет маниакальное
возбуждение — это было для нас приятной
неожиданностью. Какую бы ценную
информацию ни давал тщательный и
разносторонний фармакологический
эксперимент, не всегда можно полностью
предусмотреть и предсказать, как лекарство в
действительности повлияет на больного.
Так появился еще Один транквилизатор.
Наверное, каждый препарат имеет свою
историю — короткую или длинную,
завершенную или еще не законченную. Мы
рассказали только об одной, чтобы в общих
чертах показать, как создаются в
лаборатории новые лекарства.
О КОРОТКОЙ ИСТОРИИ
ПСИХОФАРМАКОЛОГИИ
Коротка ли на самом деле
история психофармакологии?
Если вести счет с тех
далеких времен, когда люди начали
замечать, что перебродивший
виноградный сок (возможно,
первое психотропное —
избирательно действующее на
психику средство) улучшает
настроение, создает иллюзию
благополучия, или с того момента,
когда индусы впервые
обнаружили, что настои раувольфии
лечат некоторые психические
недуги, то назвать короткой
историю психофармакологии
нельзя никак. Более 1000 лет
назад человеку уже было
известно действие опия, кокаина и
кофеина; издавна на Руси
исцеляли больных лечебными
травами, например кузьмичевой
травой, из которой позднее был
выделен алкалоид эфедрин. За
это время народная медицина
и наука накопили массу
сведений о всевозможных растениях,
содержащих сильные средства
воздействия на психику.
Однако серьезные
исследования в этой области начались
совсем недавно, поэтому сами
медики считают
психофармакологию молодой наукой.
В начале пятидесятых годов
французская
фармацевтическая фирма «Рон-Пуленк»
предложила
врачам-анестезиологам препарат, который
числился в каталогах фирмы как
«4560 R.P.». Предполагалось, что
он будет усиливать действие
анестезирующих веществ,
таких как хлороформ и закись
азота, и вместе с тем подавлять
защитную реакцию организма,
возникающую при наркозе:
понижать кровяное давление,
температуру, ослаблять мышечный
тонус и напряжение
симпатической нервной системы.
Зачастую случайное стечение
обстоятельств ускоряет ход тех
или иных событий. Так было и
на этот раз. Среди хирургов,
успешно применивших «4560 R. Р.»
в нескольких операциях, был
А. Лабори. Он заметил, что с
хирургическими больными,
которые принимали «4560 R. Р.»,
происходила психическая
метаморфоза: у них начисто исчезал
страх перед операцией. Хирург .
рассказал о необычных
свойствах препарата своему
родственнику — известному
парижскому психиатру П. Деникеру, и
тот вместе с Ж. Делеем
проверил действие этого вещества на
больных — пациентах
парижских психиатрических клиник.
О своих первых наблюдениях
П. Деникер и Ж. Делей
сообщили в мае 1952 года. «4560 R. Р.»
оказался отличным
успокаивающим средством. Вместо
безликого номера лекарству сразу
дали имя «ларгактил» (от
французского «large» — «широкий»,
то есть препарат широкого
действия), позднее его стали
называть «хлорпромазин», или
«аминазин».
Окончание на стр. 28.
5
a
ИЗГНАНИЕ
МАКСВЕЛЛОВА
ДЕМОНА
Член-корреспондент АН СССР
М. В. ВОЛЬКЕНШТЕЙН
«Полно, бес, мучить ея!»
„..Итак, «демон», наделенный Максвеллом
«сверхизощренной способностью следить за
молекулами, сидел в сосуде, разгорожен-
■ном на два отсека, и нарушал второе
начало термодинамики. То открывая, то
.закрывая отверстие в перегородке, демон
пропускал более быстрые молекулы из
отсека А в отсек Б, а более медленные из Б
ъ А и таким образом повышал
температуру в отсеке Б и понижал ее в отсеке А,
ле затрачивая работы.
Физики этого демона истребили.
Заметим, что изгнание демонов и бесов
/было весьма важным занятием еще в
средние века. Вот как описал его протопоп Ав-
ъакум: «И нападе на нея бес..., учала
кричать и вопить, собакою лаять, и козою
клекотать, и кокушкою коковать. Аз же
.зжалился об ней: покиня херувимскую
петь, взяше от престола крест, и на крылос
ъзошед, закричал: «Запрещаю ти именем
господня; полно, бес, мучить ея!»... Бес же
изыде от нея».
Для термодинамического демона одних
заклинаний мало. Поэтому сначала
польский физик Мариан Смолуховский указал,
-что само тепловое движение молекул
должно нарушать управляемое демоном
закрывание и открывание дверцы между
отсеками, но это убедило еще не всех.
Далее были предприняты новые шаги, и
особенно наглядно изгнание демона было
произведено с помощью теории информации.
ИНФОРМАЦИЯ
Она — всюду.
В быту под информацией разумеется
сообщение сведений о каких-либо явле-
Юкончание. Начало см. в № 11.
ниях. Без передачи и получения
информации жизнь невозможна. И потому
телеграфные агентства, газеты, журналы,
радио, телевидение ежедневно информируют
нас о событиях, происходящих в мире,
а институты научной и технической
информации — о событиях в науке и технике,
а некий аноним информирует редакцию
газеты о личной жизни соседей...
Науке было необходимо сделать
понятие информации строгим, дать ей
количественную меру. Действительно важно
определить количество информации,
содержащейся в передаваемой телеграмме,
важно уметь оценивать эффективность
кодирующих устройств. Решение этого
вопроса— одно из крупнейших достижений
современной науки. Оно радикально
повлияло на все ее развитие.
Современная теория информации —
часть кибернетики, общей науки об
управлении. Никакое управляющее устройство
не может работать без наличия каналов
связи, по которым информация передается.
Наука дает информации вероятностное,
статистическое определение. Информация,
заключающаяся в каком-либо сообщении,
есть количественная мера сведений,
которые такое сообщение содержит. Пока
игральная кость не брошена, нет события
и нет сообщения о событии. Все шесть
исходов равновероятны, информация
отсутствует— она равна нулю. После того,
как кость брошена и выпало, допустим,
четыре очка — опыт сделан, определенное
событие осуществилось и получена
отличная от нуля информация.
Как ее измерить?
НЕМНОГО МАТЕМАТИКИ
Бросим одновременно две кости. Получим,
например, на первой кости четыре очка,
7
на второй — пять. В этом сообщении
содержится вдвое больше сведений, чем в
сообщении о том, что на одной кости —
четыре очка. Информации складываются.
А число равновероятных событий?
Вероятность выпадения четырех очков на
первой кости равна Уб, пяти очков на
второй кости — тоже равна Уб. Вероятность
того, что эти два независимых события
произошли одновременно, равна Узб, то
есть число равновероятных событий
равно 36. Вероятности и числа
равновероятных событий перемножаются.
Если мы хотим связать информацию
о событии с вероятностью события, то
зависимость между этими двумя
величинами должна быть логарифмической. Когда
две величины перемножаются, их
логарифмы складываются. Итак, напишем:
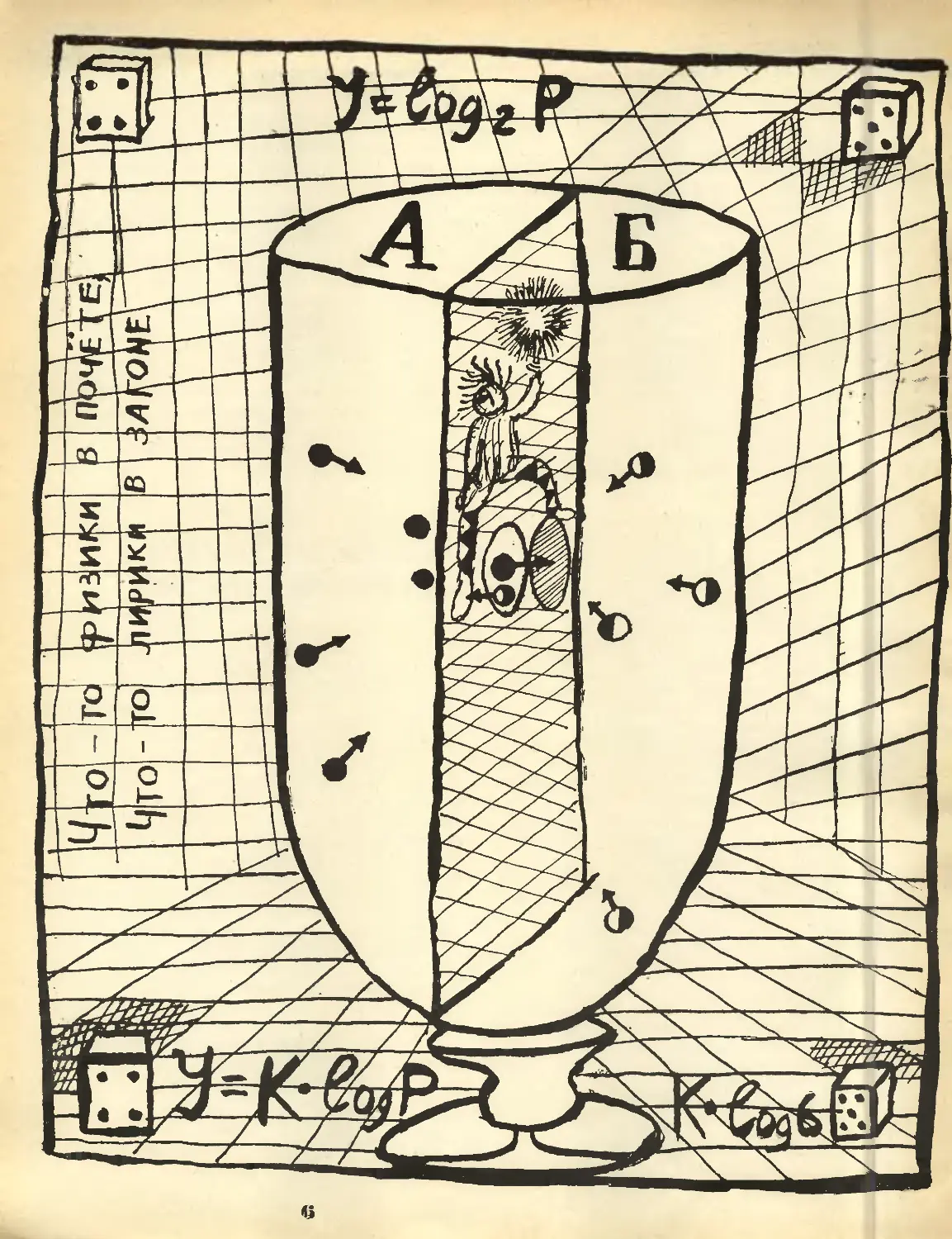
информация J = К • log P.
Р — число возможных событий до их
осуществления, К — некий коэффициент
пропорциональности. В нашем примере
Р = 6. Бросив кость, мы реализовали одно
событие из 6 возможных и получили
информацию, равную К • log 6.
Для простоты примем, что К равно
единице, и возьмем в качестве основания
логарифмов двойку:
J = log2P.
Такое определение соответствует
задачам, в которых возможны лишь два
события, то есть на вопрос о результате
отдельного опыта возможны только два ответа —
«да» или «нет». Допустим, что в родильном
доме за какое-то время появилось на свет
пять младенцев. Вероятность того, что
рождается мальчик или девочка,
одинакова: она равна 1/2. До того как младенцы
родились, нет никакой информации об их
рождении и возможно 25 различных
событий (первый ребенок — мальчик, четверо
остальных — девочки, первый — девочка,
остальные мальчики и т. д.).
Вероятность рождения пяти детей
определенного пола в определенной
последовательности равна 1/25 = 1/128. Сообщение
о результате всех рождений содержит
информацию, равную
J = log2128 = log225=5,
то есть при таком определении
информация просто равна числу выборов с двойной
альтернативой — «да» или «нет».
Соответствующая единица информации
называется бит. В нашем примере мы получили
5 битов информации.
Очевидно, что описанная
количественная мера информации совершенно не
связана с ее ценностью для человека. На
вопрос о результате бросания монеты можно
дать два ответа — «орел» или «решка».
Соответственно информация о результате
такого бросания равна одному биту.
Столько же информации мы получим при ответе
на любой вопрос, поставленный в форме
«да или нет?», —например на вопрос:
«подчиняется ли живой организм второму
началу термодинамики,—да или нет?»
Но в этой статье мы говорим только
о количестве информации, а не об ее
ценности.
Строгое определение количества
информации чрезвычайно важно, и то, что
оно не связано с вопросом о ее ценности,
следует считать его большим
достоинством. Это позволяет дать полную теорию
связи, не осложненную никакими субъек^
тивными элементами.
ИНФОРМАЦИЯ, ПОЭЗИЯ И ПЕРЕВОД
С легкой руки автора интересной книги
«Сигнал» И. А. Полетаева, сейчас стало
модным противопоставлять физику лирике.
Об этом писал в шутливом стихотворении
Борис Слуцкий: «что-то физики в почете,
что-то лирики в загоне».
Но поэзия и наука — явления единой
культуры, находящиеся во
взаимодействии. Поэтическое восприятие науки и
научный анализ поэзии обогащают и науку
и искусство. Существует перекресток и
этих путей.
Поэт несет в мир гармонию, то есть
информацию. Перевод его стихотворения на
другой язык можно рассматривать как
передачу информации.
Поэт-переводчик ставит перед собой
различные задачи. Он может
воспользоваться информацией, содержащейся в
иноязычном стихотворении, для создания-
оригинального произведения. Так поступил:
Тютчев, писавший на мотив Гейне:
Если смерть есть ночь, если жизнь есть день:
Ах умаял он, пестрый день меня...
Это «умаял», этот «пестрый день» звучат
настолько по-русски, по-тютчевски, что*
здесь приходится говорить о создании
новой поэтической информации, а не о
перекодировке, переводе информации,
содержащейся в стихотворении Гейне.
Не менее достойна задача передать ино-
8
язычную поэтическую информацию.
Литературовед Е. Г. Эткинд посвятил этой
проблеме талантливую книгу «Поэзия и
перевод». В ней тонко и точно
проанализирована природа поэтического перевода
и показано, что оптимальная передача
информации достигается разными
средствами, в зависимости от ее характера в
оригинале. Дело это трудное. Автор
сопоставляет десять различных русских переводов
стихотворения Гете «Близость любимого»
{«Nahe des Geliebten»), Переводы
различаются сильнейшим образом. Например,
в четырех переводах из десяти стихи
обращены не женщиной к мужчине, как у Гете,
а мужчиной к женщине. Передача
оказывается сугубо неоднозначной.
Полная, лишенная каких бы то ни было
искажений, передача поэтической
информации на другом языке принципиально
невозможна, так как языки различны,
а поэтическая информация, в отличие от
научной, содержится во всем — в каждом
слове и в каждом звуке.
Поэту-переводчику приходится решать задачу
оптимального донесения информации, неизбежно
чем-то поступаясь. Талант
поэта-переводчика и состоит в способности такой
оптимум найти. Поэтический перевод — работа
творческая, художественная. Естественно,
что ею занимались величайшие русские
поэты — и Пушкин, и Лермонтов, и
Тютчев, и Блок...
Но пора оставить лирику и вернуться
к физике как таковой.
ОПЯТЬ ЭНТРОПИЯ
Из сказанного об информации явствует,
что это научное понятие имеет много
общего с энтропией.
Напомним: энтропия есть мера
вероятности состояния физической системы. Она
потому и возрастает с уменьшением
порядка, что неупорядоченное состояние
более вероятно, чем упорядоченное.
Теоретический анализ показывает, что энтропия
выражается формулой
S = k-lnP,
где к = 1.38 • 106эрг на градус —
постоянная Больцмана, а Р — число способов
осуществления данного состояния, его
статистический вес, который можно приравнять
числу равновероятных событий в системе,
находящейся в данном состоянии.
Логарифм в приведенной формуле
натуральный, то есть он взят при основании
е = 2,78... Переходя к двоичной системе,
которой мы пользовались для вычисления
информации, получаем
S = k In 2 .log2 P = 0,693 к J,
то есть энтропия отличается от
информации лишь множителем к • In 2.
Аналогия эта не формальна.
Информация передается и воспринимается в
реальных физических процессах, протекающих
в соответствии со вторым началом
термодинамики. За получение информации
нужно платить увеличением энтропии.
Рассмотрим это на примере
кристаллизации жидкости.
Жидкость обладает большей энтропией,
чем кристалл, так как ее состояние можно
реализовать большим числом способов
распределения молекул, чем состояние
кристалла. Ведь кристалл упорядочен:
молекулы в нем расположены строго
регулярно. Значит, при кристаллизации
энтропия уменьшается. Однако в то же время
возрастает информация, так как
расположение молекул в кристалле известно, а в
жидкости оно неизвестно.
Закристаллизовав жидкость, мы
получим новую информацию, равную
уменьшению энтропии с точностью до
множителя 0,693 к. Одному биту информации
при этом соответствует очень малая
величина энтропии, так как очень мала
постоянная Больцмана. На один бит
приходится около Ю-16 эрг/градус, т. е. примерно
2,5 ■ 10 ~2А кал/градус.
Где же плата за полученную
информацию? Она отдана при кристаллизации
жидкости. Для того чтобы закристаллизовать
жидкость, ее нужно охладить.
Холодильник при этом нагреется. Его энтропия
повысится — ведь при повышении
температуры движение молекул становится все
более беспорядочным. При этом
увеличение энтропии холодильника больше, чем
уменьшение энтропии кристаллизующейся
жидкости. Так говорит второе начало.
Значит, информация получается из
понижения энтропии, из энтропии с
отрицательным знаком, «негэнтропии». А платить
за нее нужно энтропией.
ИЗГНАНИЕ ДЕМОНА
Демон Максвелла был изгнан
французским физиком Леоном Бриллюэном.
Последуем за его рассуждениями.
- Химия и Жизнь, № 12 !?
Для того чтобы максвеллов демон смог
увидеть и сортировать молекулы, ему
нужно их осветить. Поэтому демона
следует снабдить фонарем. Фонарь, то есть
батарея с электрической лампочкой,
должен быть источником неравновесного
излучения. Иными словами, температура
нити электрической лампочки должна быть
выше температуры газа в сосуде. Излучая
свет, лампочка отдает энергию и теряет
энтропию. Без вмешательства демона
энергия поглощается газом, находящимся при
более низкой температуре, чем
температура нити, и поэтому энтропия газа
возрастает на величину, большую, чем ее
уменьшение у лампочки. В целом
энтропия увеличивается.
Демон может обнаружить молекулу
только в том случае, если она рассеяла по
меньшей мере один квант света, который
поглотится в глазу демона. При этом опять-
таки происходит возрастание энтропии, за
счет которого демон и получил
информацию о молекуле.
Но раз информация получена, она
может быть использована для уменьшения
энтропии всей системы. Это и делает
демон, открывая дверцу перед быстрой
молекулой (или не открывая ее перед
медленной молекулой).
Однако расчеты, проделанные Брил-
люэном, показали, что в целом энтропия
системы возрастает в полном согласии со
вторым началом. Поглощение кванта света
вызывает увеличение энтропии (то есть
повышение температуры), перекрывающее
то ее уменьшение, которое связано с
внесением порядка в систему. Температура
обязательно выравнивается.
Таким образом, демон Максвелла не
может нарушить второе начало. Ни в
неживой системе, ни в клетке.
Следовательно, и делать ему в них нечего.
Но, может быть, живой организм
спасается от второго начала иным способом?
ПОЧЕМУ АТОМЫ МАЛЫ?
Как уже было сказано, второе начало
является вполне строгим для системы,
состоящей из очень большого числа частиц,
но для немногих атомов оно не
обязательно. Именно в связи с этим в блестящей
книге крупнейшего физика Эрвина Шре-
дингера «Что такое жизнь с точки зрения
физики?» поставлен вопрос: почему
атомы малы?
Но что значит — малы? Почему мы
считаем атомы маленькими? Потому что
они малы по сравнению с нашими
размерами. Живой организм, начиная с
наименьшей бактериальной клетки, во много
раз больше атома. Диаметр самой
маленькой бактерии Mycoplasma laidlawii в
тысячу раз больше диаметра атома, а ее
объем соответственно в миллиард раз больше
объема атома.
Очевидно, что вопрос нужно
переформулировать. Его смысл состоит в
следующем: почему живая клетка состоит из
очень большого числа атомов?
Именно потому — отвечает Шредин-
гер,— что при малом числе атомов жизнь
невозможна. Всякий атомный порядок,
диктуемый первым и вторым началом,
при малом числе атомов нарушался бы
флуктуациями, случайными отклонениями
от наиболее вероятного состояния.
Отсутствовала бы как раз та самая
специфическая способность организма творить и
воспроизводить порядок, которая нас
занимает.
Следовательно, и флуктуационными
нарушениями тоже нельзя объяснить
антиэнтропийные свойства живого
организма. Никуда от второго начала не
денешься.
В чем все-таки дело?
В действительности ларчик открывался
достаточно просто. Я не совсем честно
поступил с читателем. Вместо того чтобы
сразу ответить на вопрос, поставленный
в начале этого рассказа, я повел читателя
окольными путями — то в один тупик, то
в другой.- Но мне должно послужить
извинением то, что это позволило рассказать
о многих интересных вещах.
Мы ведь совершенно забыли (и это,
очевидно, входило в мои намерения) о
точной формулировке второго начала. Второе
начало, как и первое, справедливо лишь
для системы изолированной, не
подвергающейся внешним воздействиям.
Никакое физическое тело нельзя
полностью изолировать от внешнего мира.
Однако можно его изолировать
практически, то есть так, чтобы утечка или приток
вещества и энергии были относительно
малыми.
Термодинамика различает
изолированные, замкнутые и открытые системы.
Изолированные не обмениваются с
окружающим миром ни веществом, ни энергией —
для них-то и справедливы первое и второе
10
начала. Замкнутые не обмениваются
с внешней средой веществом, но
энергообмен происходит. Наконец, открытые
системы обмениваются с окружающей
средой и веществом, и энергией.
Живой организм •— система
принципиально открытая. Жизнь существует
благодаря метаболизму — обмену веществ
с окружающей средой. Живое существо
дышит и питается, выделяет ряд веществ,
получает и отдает тепловую энергию.
Однако, констатировав это очевидное
положение, мы еще не преодолели всех
трудностей, ибо нам нужно объяснить, за
счет чего создается упорядоченность
живого организма, чем она поддерживается
и оплачивается.
КОСМОНАВТ В КАБИНЕ
КОСМИЧЕСКОГО КОРАБЛЯ
Для этого придется рассмотреть живой
организм вместе со всем, что его окружает.
В самом деле, если жизнь существует
именно в результате обмена веществом
и энергией с окружающей средой, то это
означает, что и интересующая нас
особенность жизни — упорядоченность —
возникает и существует именно в результате
такого обмена; стоит лишить живое
существо обмена — пищи, воды и воздуха — и
оно умрет, обратится в прах, и
упорядоченность исчезнет.
Так как оба начала термодинамики
справедливы лишь для изолированных
систем, то для физического анализа
вопроса следует изолировать — мысленно или
фактически — живое существо вместе с
запасом пищи, воды и воздуха и
исследовать энтропийный баланс такой системы.
Космический корабль с находящимся
в нем космонавтом — хороший образчик
изолированной системы. Космонавт дышит
и питается, работают его выделительные
органы. Пищевой рацион подобран таким
образом, что космонавт не теряет и не
прибавляет в весе, он остается в стационарном
состоянии. Иными словами,
упорядоченность его молекул и клеток непрерывно
поддерживается. Но что же происходит
с энтропией?
Внутри тела космонавта энтропия все
время производится, ибо биохимические
реакции протекают в соответствии с
законом ее возрастания.
Однако, если бы дело этим
ограничивалось, то стационарное состояние,
постоянная упорядоченность, то есть постоянное
значение энтропии космонавта
поддерживаться бы не могло.
Следовательно, избыток энтропии
должен из тела космонавта удаляться. Это и
происходит в результате обмена веществ
и теплообмена. Иными словами, космонавт
потребляет вещества с меньшей энтропией
и выделяет вещества с большей энтропией.
Можно сказать, что через его тело
проходит поток отрицательной энтропии или,
словами Шредингера, что он «питается
отрицательной энтропией».
Энтропия космонавта слагается из
энтропии, производимой внутри его
организма в результате биохимических процессов,
и из энтропии, поступающей извне — с
пищей, с воздухом. Первое слагаемое
обязательно положительно, в силу второго
начала. В то же время организм выделяет
энтропию — выделяет тепло, выдыхает
углекислоту и воду, выделяет отбросы. Для
того чтобы его состояние оставалось
стационарным, то есть чтобы его суммарная
энтропия не изменялась, необходимо,
очевидно, чтобы выделяемая энтропия была
больше поступающей в организм извне.
Так оно и есть. Энтропия выделяемых
веществ больше энтропии веществ,
которыми питается и дышит космонавт. Куда же
девается выделяемая энтропия? Она
остается в корабле. Энтропия среды,
непосредственно окружающей космонавта, все
время возрастает и именно это обстоятельство
позволяет ему сохранять свое
стационарное состояние, свою упорядоченность.
Все сказанное относится не только
к космонавту, но и к любому другому
живому существу, остающемуся на Земле.
Жизнь поддерживается потоком
отрицательной энтропии.
Но, как мы видели, отрицательная
энтропия эквивалентна информации. Живой
организм непрерывно получает
упорядочивающую информацию из окружающей
среды и платит за это выделяемой
энтропией. Это относится и к информации в ее
научном значении, то есть к информации,
приносимой молекулами, содержащимися
в пище, и к информации в обычном
смысле слова.
Читая эту статью, вы получаете
некоторую информацию. Какова ее ценность —
судить вам, а не мне. Но количество этой
информации можно измерить в битах. При
этом вы совершаете умственную работу
и выделяете больше тепла, больше энтро-
2*
11
пии в окружающую среду, чем при полном
безделье! В энтропийных единицах плата
за полученные сведения не велика — ведь
каждый бит стоит всего 2,5 • 10~24 калорий
на градус. В этом смысле написание всех
книг, когда-либо созданных человечеством,
увеличило энтропию вселенной меньше,
чем один вскипевший чайник с водой.
Однако измерять человеческую культуру
в калориях на градус бессмысленно.
Говоря о стационарном состоянии
космонавта, мы имели в виду только
постоянство энтропии, выраженной в этих самых
калориях на градус. В битах его состояние
не стационарно. Ведь космонавт получает
информацию о внеземном пространстве.
Ценность информации, полученной
космонавтом и сообщенной им человечеству,
огромна, хотя в энтропийных единицах
космическая информация очень мала.
Может ли организм полностью
избавиться от своей энтропии, выделяя ее
наружу? Нет — все, на что он способен,
будучи открытой системой, это достичь
некоторого стационарного состояния с
определенным уровнем энтропии. В таком
состоянии производство энтропии в
организме минимально.
Посмотрим, что означало бы
противоположное утверждение (с ним иногда
приходится встречаться). Допустим, что можно
уменьшать энтропию тела неограниченно.
Энтропия уходит во вне. Информация
организма увеличивается, а в окружающей
среде она, очевидно, уменьшается. Иными
словами, чем больше я скажу (или
опубликую в печатной форме) глупостей, тем я
стану умнее, ибо я избавился от излишка
глупости...
Если бы это было так! В
действительности человек, говорящий или пишущий
глупости, никак от этого не умнеет. Скорее —
наоборот.
ЗАЧЕМ КОРМЯТ ДЕТЕЙ
Организм возник из одной
оплодотворенной яйцеклетки. Эта первая клетка
разделилась на две, потом на четыре и т. д.,
потом образовался зародыш, потом ребенок
появился на свет и стал расти.
Что происходило в это время с
энтропией и информацией?
Очевидно, что упорядоченность
организма все время возрастала,
увеличивалась его информация и уменьшалась
энтропия. Соответственно возрастала
энтропия окружающей среды — и в
значительно большей степени, чем после
достижения стационарного состояния. Обмен
веществ у развивающегося организма
происходит гораздо интенсивнее, чем у
взрослого. Детей нужно хорошо кормить.
Процесс развития живого организма
поистине чудесен. И удивление при виде
этого чуда может сбить с толку даже
солидного ученого.
Физик В. Эльзассер написал книгу с
громким названием «Физические основы
биологии». К сожалению, она не
увеличивает объема информации у читателя.
Эльзассер утверждает, что способность
растущего организма «высасывать» информацию
из окружающей среды не может быть
объяснена физикой. В сущности, он
считает организм вечным двигателем второго
рода.
Между тем термодинамических
трудностей при объяснении развития
организма на самом деле нет. Растущий организм
можно уподобить кристаллу, растущему
из жидкости при ее охлаждении.
Изолированную жидкость закристаллизовать
нельзя — от нее нужно отводить тепло.
Увеличение в кристалле порядка (то есть
информации) оплачивается увеличением
энтропии нагревающегося холодильника.
Рост организма оплачивается увеличением
энтропии окружающей среды.
Жизнь полностью согласуется с
законами термодинамики. Однако признание
этого положения еще не означает понимания
сущности жизни.
Современная теоретическая биология
объединяется с физикой и химией во
многих областях. Одной термодинамикой
здесь не обойдешься.
И об этом нужен особый рассказ.
12
Лаборатория Бондюжского
завода, в которой в 1893 году
работал Д. И. Менделеев
Г
В конце сороковых годов
прошлого века выходец из
крестьян села Бондюги * Вятской
губернии Капитон Ушков начал
строить завод по производству
хромпика, широко
применявшегося тогда в текстильной
промышленности. Завод строился
на принадлежавшей Ушкову
земле Кокшанской лесной дачи,
примерно в 25 верстах от Камы.
В 1850 году Кокшанскии
завод дал первую продукцию, а
Ныне — город Менделеевск.
СТРАНИЦЫ ИСТОРИИ
СТО ЛЕТ
ЗАВОДА
Профессор
П. М. ЛУКЬЯНОВ
через 10 лет его годовая
выработка достигла 12 тысяч пудов.
Кокшанскии хромпик оказался
значительно дешевле
английского, его стали продавать в
Германию, Голландию и даже
в Англию.
Вскоре на заводе появился
цех серной кислоты. Сырьем
для нее служил уральский
серный колчедан, содержащий
медь. Из отхода
сернокислотного производства — колчеданного
огарка — стали изготовлять
медный и железный купорос.
Потом построили цех стеклянной
тары и листового стекла, еще
позже — керамический цех,
выпускавший кислотоупорную
аппаратуру для химических
предприятий. Дело давало хорошую
прибыль. И Ушков начал
строить близ села Бондюги
второй химический завод. В
1868 году новый завод начал
выпускать серную кислоту,
купоросное масло, медь,
извлеченную из колчеданного
огарка, сернокислый глинозем,
квасцы.
А производство хромпика на
Кокшанской лесной даче стало
13
Город Менделеевск. 1968
филиалом Бондюжского завода.
После смерти Ушкова дело
взял в свои руки его сын. При
нем на заводе стали
производить соляную кислоту, сульфат
натрия. Хлорной известью
Бондюжского завода пользовались
все текстильные фабрики
Центральной России. Многие
важные химические производства
были организованы на Бондюж-
ском заводе впервые в нашей
стране.
В конце прошлого века на
заводе два раза был Д. И.
Менделеев. Под его наблюдением
там изготовили опытную
партию пироколлодия,
необходимого в производстве бездымного
пороха. В 1908 году на заводе
была выпущена партия
порошковидного суперфосфата. В этой
работе принимал участие
выдающийся агрохимик академик
Д. Н. Прянишников.
В первые годы Советской
власти, в условиях разрухи на
транспорте и постоянной
нехватки топлива и сырья, Бон-
дюжский завод обеспечивал
промышленность страны
квасцами, соляной кислотой,
сернистым натрием, хлороформом,
соединениями хрома и другими
важными химическими
продуктами.
В 1920 году, по указанию
В. И. Ленина, там было
организовано производство солей
радия из отечественного сырья.
На Бондюжском заводе
начинали свою деятельность многие
выдающиеся русские и
советские химики: академик В. Г.
Хлопин, член-корреспондент
Академии наук П. П. Федотьев,
профессора К. Г. Дементьев,
И. Я. Башилов, И. Н.
Кузьминых. В 1915—1917 годах
директором завода был видный
революционер Л. Я. Карпов. Теперь
Бондюжский химический завод
носит имя Карпова; на
территории завода установлен
памятник ученому-революционеру.
Сейчас старейшее русское
химическое предприятие
специализируется на выпуске
дорогих высококачественных
реактивов. Это — бариевые
присадки к смазочным маслам и
топливу (хлористый барий и
гидроокись бария), карбонат
бария для стекольной
промышленности и радиоэлектроники,
гипосульфит, хлористый
кальций- Продукцию Бондюжского
химического завода имени Л. Я.
Карпова хорошо знают в
фармацевтической
промышленности, в исследовательских
лабораториях. Ее потребители —
около 2000 предприятий 200
городов Советского Союза, страны
социалистического содружества,
Ирак, Алжир.
Завод имени Л. Я. Карпова —
одно из передовых предприятий
химической промышленности
страны. Семилетний план
выполнен им за четыре с
половиной года. Так старейшее
химическое предприятие страны
встречает второй век своего
существования.
1
УКАЗ ПРРЗИМИУЦД
ВеРХОВМОГО СОВЕТА СССР
О *т. раждекмм *цмнчес*ого эаяода
нм^нм Я> Я Карпов А
Министерства химической
прэмышя<е*тост* СССР орденом
Тру#и»о*ч> Красного Знамени
За &о#ьш«£ закупа ш развит* ка~
**ич*с*Ы1 прлмырзлениости * » смзм со
ИИМетме» со дня основания наградить
хдоическлй зздод имени Й. Я* К«рпо*а
Министерств химической
промышленности СССР ардеяом Трудового
Красного Зйане**,
Председатель Президиума
Верховного Сшет* СССР
Н. ПОДГОРНЫЙ,
Секретарь Лррэкдздод
Вг-рэшвяого Совета СССР
М. ГЕОРГАДЗЕ,
Моск&з. Кремль, 2d августа 1968 г.
14
В майском номере "Химии и жизни" была напечатана статья
"Перечитывая классиков", автор которой И.Г.Жирнаускас познано-
мил читателей с несколькими отрывками из художественных
произведений, посвященными химии.
€амо собой разумеется, что тема эта не может быть исчерпана
одной публикацией. Мы хотим напомнить еще несколько
"химических" эпизодов, заимствованных из литературных
произведений.
ПРОДОЛЖАЯ
ЧИТАТЬ
КЛАССИКОВ...
Есть у замечательного датского
сказочника Ганса Христиана Андерсена одна
любопытная история («Ветер рассказывает
о Вальдемаре До и его дочерях»), целиком
посвященная алхимии. Вот что
рассказывал ветер о герое истории и его жилище:
— Огонь пылал в его комнате даже
летом, все об этом шептались, а дверь всегда
была на замке; он работал там дни и ночи,
но не любил разговаривать о своей работе:
силы природы нужно испытывать в тиши;
скоро, скоро он найдет самое лучшее,
самое драгоценное на свете — красное
золото!
Ветер сам помогал алхимику раздувать
огонь в камине, а неутомимый Вальдемар
До ставил один опыт за другим,
добиваясь своей цели. Все свое богатство-
истратил До на бесконечные опыты, но
когда, казалось, получил долгожданное
золото, его ждало горькое разочарование:
это было лишь окрашенное стекло...
Закончив свой грустный рассказ, ветер
заключил:
— ...И я унесся из дома алхимика...
Н. В. Гоголь в одной статье из «Арабесок»
тоже описал занятия средневекового
алхимика. Алхимия, по словам Гоголя,
считалась ключом ко всем познаниям, венцом
учености средних веков, а ее заветной
целью было «детское желание открыть
совершеннейший металл, который доставил
бы человеку все!».
А вот и описание самого жилища и
лаборатории алхимика: «...Ветхий, почти
валящийся, считаемый необитаемым [домик],
по растреснувшимся стенам которого
лепится мох и старость, окна глухо
заколочены — это жилище алхимика. Ничто не
говорит в нем о присутствии живущего, но
в глухую ночь голубоватый дым, вылетая
из трубы, докладывает о неусыпном
бодрствовании старца, уже поседевшего в своих
исканиях, но все еще неразлучного с
надеждою...»
Гоголь замечает далее, что алхимия
была первоначальной стихией всего
европейского духа.
В отличие от Андерсена и Гоголя,
нарисовавших тип абстрактного алхимика,
А. С. Пушкин собирался показать
реальную историческую личность — монаха
Бертольда Шварца, изобретателя пороха.
Сохранился план незаконченного
произведения Пушкина («Сцены из рыцарских
времен»), в котором автор прямо говорит,
что Ъертольд в тюрьме «открывает
порох — и взрывается». Впоследствии, однако
Пушкин несколько отошел от намеченного
плана. В опубликованном после его смерти
отрывке купец Мартын обращается к
ученому монаху:
— Эх, отец Бертольд! Коли бы ты не
побросал в алхимический огонь всех денег,
которые прошли через твои руки, ты был
бы богат.
В ответ на это Бертольд заявляет, что
цель его — не открытие способа получения
золота, а познание одной лишь истины.
На замечание того же Мартына; «А если
15
опыт не удастся?», он отвечает: «Нечего
будет делать. Если и этот не удастся, то
алхимия вздор».
И Гоголь, и Пушкин писали об
алхимиках Западной Европы, так как в России
своих алхимиков никогда не было. Лишь
как о забавном курьезе рассказывают
о предложении некоего иностранного
барона превращать свинец в золото. В обмен
за это барон требовал произвести его в
графы и кавалеры андреевского ордена и
назначить российским посланником при
французском дворе...
Как, наверное, помнят читатели, барон
д'Астарак из романа Анатоля Франса
«Харчевня королевы Гусиные Лапы» был
куда скромнее. Он не претендовал на титул
графа и не пытался превращать свинец
в золото. Его интересовало другое —
химическая пища; мсье д'Астарак мечтал о том
времени, когда пища будет вариться
и жариться в ретортах и перегонных кубах,
а место поваров займут химики...
Анатоль Франс закончил свой роман
в конце 1892 года. А через 12 лет в
социально-философском романе «На белом
камне», посвященном коммунистическому
обществу XXIII века, Франс снова
вспоминает о химической пище, но на этот раз —
увы — в плане отрицания.
Когда Дюфрен, французский буржуа,
прибывший из XX века в далекое будущее,
спрашивает об усовершенствовании
процесса питания, ему отвечают: «Ты,
вероятно, имеешь в виду химическую пищу,
товарищ. Здесь мы еще не достигли
заметных успехов. Тщетно мы направляли
наших химиков на кухни... Их пилюли
ничего не стоят».
Все дело, как мы видим, в пилюлях,
о которых много и назойливо писали
фантасты в конце XIX и начале XX веков.
Теперь мы знаем, что химическая пища
будущего не будет ни пилюлями, ни
таблетками. Как говорит академик А. Н.
Несмеянов, синтетические продукты питания
не должны отличаться от природных не
только по вкусу и запаху, но и по своей
форме и консистенции.
Итак, Франс в конце концов отозвался
о химической пище отрицательно.
Противоположную точку зрения на этот счет
высказал замечательный русский писатель
А. И. Куприн. В повести «Жидкое солнце»
Куприн устами одного из героев говорит
16
\
?±^£j(-%>
о важнейшей проблеме — «из простых
элементов, входящих в воздух, составить
вкусное, питательное и съедобное, почти
бесплатное вещество».
Писатель приводит в своей повести ряд
имен знаменитых физиков (Ньютона,
Френеля, Гука и других), но не называет ни
одного химика. Знал ли Куприн, что его
слова — это по существу перефразировка
известной мысли нашего великого химика
Д. И. Менделеева? Ведь еще в своих
«Заветных мыслях» Менделеев писал:
«Как химик я убежден в возможности
получения питательных веществ из
сочетания элементов воздуха, воды и земли...»
Целые страницы, посвященные химии и
химической технологии, найдем мы в
произведениях Жюля Верна и в особенности
в романе «Таинственный остров». По сути
дела, вся XVII глава первой части
является «химической». Из нее мы узнаем, как
инженер Сайрус Смит получил из серного
колчедана сернистое железо, из него —
железный купорос и наконец — серную
кислоту. При этом Жюль Берн справедливо
замечает: «Серная кислота нашла широкое
применение во всем мире; ее потребление
для нужд производства является
показателем промышленного развития любой
страны».
Далее путешественники под
руководством Смита добыли из жира глицерин, из
селитры — азотную кислоту, а из азотной
кислоты и глицерина изготовили
нитроглицерин! Попутно Жюль Верн рассказывает
более или менее подробно о жирах, о
мыле, об азотной кислоте, допуская лишь
отдельные неточности.
В главе XV этой же части изложены
элементы химии металлургического
процесса (выплавки железа из руды). «Под
действием воздуха, нагнетаемого
мехами,— пишет Жюль Верн,— уголь в этой
руде превращался в двуокись, а затем
в окись углерода, которая, воздействуя на
окись железа, отнимала от нее кислород».
Большой интерес представляет и
XI глава второй части, в которой
разбирается вопрос о «горючем грядущих
веков». Герой романа заявляет, что вода —
это уголь грядущих веков. Не будем в
претензии к Жюлю Верну и к Сайрусу Смиту
за то, что они смогли предвидеть лишь
использование водорода и кислорода,
полученных при электрохимическом
разложении воды. И в заключение несколько
3 Химия и Жизнь, № 12
17
слов о «химических» высказываниях
А. М. Горького.
В серии горьковских «литературных
портретов» есть очень интересный рассказ
о фабриканте Савве Морозове, который был
по образованию химиком. Горький
вспоминает восторженный отзыв Морозова о
химической науке. «Химия,— говорил Савва
Морозов,— это область чудес, в ней скрыто
счастье человечества, величайшие
завоевания разума будут сделаны именно в этой
области».
Но еще большим пафосом проникнуты
слова главного героя пьесы «Дети солнца»
Протасова о значении химии и ее будущем.
Вот что он говорит: «Но прежде всего и
внимательнее всего изучайте химию,
химию! Это изумительная наука, знаете! Она
еще мало развита, сравнительно с
другими, но уже и теперь она представляется
мне каким-то всевидящим оком. Ее зоркий,
смелый взгляд проникает и в огненную
массу солнца, и во тьму земной коры, в
невидимые частицы вашего сердца, в тайны
строения камня и в безмолвную жизнь
дерева. Она смотрит всюду и, везде открывая
гармонию, упорно ищет начало жизни...
И она найдет его, она найдет! Изучив
тайны строения материи, она создаст в
стеклянной колбе живое вещество...»
Пусть далеко еще до создания живого
вещества, но вдохновенные слова горьков-
ского героя и в наши дни, спустя шесть
с лишним десятилетий, звучат подлинным
гимном в честь химической науки...
И. ВОЛЬПЕР
Рисунки
Д. ЛИОНА
НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ
ЕЩЕ О ЗАГРЯЗНЕННОМ ВОЗДУХЕ
В Англии проведено важное
обследование: врачи попытались
выяснить количественную
зависимость между заболеваниями детей
и условиями воздушного бассейна.
Были проанализированы сведения
о загрязненности воздуха в
населенных пунктах» в которых когда-
либо жили охваченные
обследованием почти 4000 детей,
родившихся 15 лет назад в первой неделе
марта.
Были выделены четыре
статистические группы: деревенская
местность или маленькие городки,
города с населением до 200 000,
большие города с населением до
500 000, густонаселенные
промышленные районы. Вот цифры по
первой и последней названным
группам (из журнала «Wissenschaft
und Fortschritt», 1968, № 7):
Важность этого впечатляющего
сравнения, конечно, в том, что оно
основано на достоверном
статистическом материале.
НА ПУТИ К ИСКУССТВЕННЫМ
ГЕНАМ
Можно ли синтезировать
«настоящую» молекулу ДНК чисто
химическим путем? До последнего
времени это вызывало большие
сомнения: молекулярный вес
ДНК огромен (по разным
данным — от 106 до Ю9), и
синтезировать такие грандиозные
молекулы еще никто не умеет. Но путь
чисто химического синтеза — не
единственный. По сообщению
журнала «New Scientist» A968,
№ 606) другую заманчивую
возможность открывают
исследования профессора X. Хорана, о ко-
В деревне В промышленных
районах
Пребывание в больнице из-за
бронхита или пневмонии в возрасте
До 5 лет, % 1,1
Заболевания верхних дыхательных
путей, % 7,2
Заболевания в течение первых двух
лет жизни, % 19,4
Повторные заболевания в течение
того же времени, % .... 4,3
3,1
17,1
34,1
12,9
торых он докладывал на V
Международном симпозиуме по химии
природных соединений,
проходившем в Лондоне в июле 1968 г.
Еще в 1967 г. был открыт
фермент, способный «стыковать»
между собой короткие нуклеотид-
ные цепочки. В клетке он
выполняет роль ремонтной бригады:
если одна из двух цепей ДНК
разорвана, он соединяет ее концы,
пользуясь при этом второй цепью,
как матрицей. Это свойство
фермента и использовал X. Хорана. Он
заставляет фермент сшивать два
коротких отрезка цепи ДНК на
третьем отрезке-матрице таким
образом, что новый полинуклео-
тид оказывается длиннее матрицы
на несколько нуклеотидов. Этот
«хвост», выходящий за пределы
третьего отрезка ДНК, в свою
очередь становится матрицей, на
которой к третьему отрезку
присоединяется четвертый,
образующий новый «хвост», и цепь
продолжает расти. Профессор Хорана
считает, что таким путем можно в
конце концов получить
«полнометражную» молекулу ДНК — ген
с заданной последовательностью
нуклеотидов.
За свои исследования
профессор Хар Гобинд Хорана удостоен
Нобелевской премии 1968 года по
медицине, которую он разделил
с американскими биохимиками
Р. Холли и М. Ниренбергом.
18
19
Атомный вес —
39,102
Число электронов
в застраивающейся оболочке -
4 s'
Массовые числа изотопов:
стабильных- 39 и 41
нестабильного (природного)- 40
самого распространенного-39
Число электронов
в слоях:
ЭЛЕМЕНТ №.
КАЛИЙ
Кандидат педагогических наук
П. П. ИВАНОВ
Человечество знакомо с калием больше
полутора веков. В лекции, прочитанной в
Лондоне 20 ноября 1807 года, Гемфри Дэви
сообщил, что при электролизе едкого кали
он получил «маленькие шарики с сильным
металлическим блеском... Некоторые из
них сейчас же после своего образования
сгорали со взрывом». Это и был калий.
Калий — замечательный металл.
Замечателен он не только потому, что режется
ножом, плавает на воде, вспыхивает на ней
со взрывом и горит, окрашивая пламя
в фиолетовый цвет. И не только потому,
что этот элемент — один из самых
активных химически. Все это можно считать
естественным, потому что соответствует
положению щелочного металла калия
в таблице Менделеева. Калий замечателен
своей незаменимостью для всего живого
и примечателен как всесторонне
«нечетный» металл.
Обратите внимание: его атомный
номер— 19, атомная масса — 39, во внешнем
электронном слое — один электрон,
валентность —1+. Как считают химики, именно
этим объясняется исключительная
подвижность калия в природе. Он входит
в состав нескольких сотен минералов. Он
находится в почве, в растениях, в
организмах людей и животных. Он — как
классический Фигаро: здесь — там — повсюду.
КАЛИЙ И ПОЧВА
Вряд ли можно объяснить случайностью
или прихотью лингвистов тот факт, что
в русском языке одним словом
обозначаются и сама наша планета, и ее верхний
слой — почва. «Земля-матушка», «земля-
кормилица» — это, скорее, о почве, чем
о планете в целом...
Но что такое почва?
3*
19
Самостоятельное и весьма своеобразное
природное тело. Оно образуется из
поверхностных слоев разнообразных горных
пород под действием воздуха, воды,
температурных перепадов, жизнедеятельности
всевозможных обитателей Земли. Ниже,
под почвой, скрыты так называемые
материнские горные породы, сложенные из
различных минералов. Они постепенно
разрушаются и пополняют «запасы» почвы.
А в почве, помимо чисто механического,
постоянно происходит и другое
разрушение. Его называют химическим
выветриванием. Вода и углекислый газ (в меньшей
мере другие вещества) постепенно
разрушают минералы.
Почти 18% веса земной коры
приходится на долю калийсодержащего
минерала— ортоклаза. Это двойная соль
кремневой кислоты—K2AbSi60i6 или КгО-АЬОз*
•бБЮг. Вот что происходит с ортоклазом
в результате химического выветривания:
К20-А1203-6Si02 ф 2Н20 + С02 -> К2С03 4*
-f Al2<V2Si02-2H20 + 4Si02.
Ортоклаз превращается в каолин
(разновидность глины), песок и поташ. Песок и
глина идут на построение минерального
костяка почвы, а калий, перешедший из
ортоклаза в поташ, «раскрепощается»,
становится доступным для растений. Но не
вось сразу.
В почвенных водах молекулы К2СО3
диссоциируют: КгСОэ^К+ 4- КСОз"^2К+ 4-
4- СОз2-. Часть ионов калия остается в
почвенном растворе, который для растений
служит источником питания. Но большая
часть ионов калия поглощается
коллоидными дастицами почвы, откуда корням
растений извлечь их довольно трудно. Вот
и получается, что, хотя калия в земле
ь:ного, часто растениям его не хватает.
Из-за того, что комочки почвы
«запирают» большую часть калия, содержание
этого элемента в морской воде почти
в 50 раз меньше, чем натрия. Подсчитано,
что из тысячи атомов калия,
освобождающихся при химическом выветривании,
только два достигают морских бассейнов,
а 998 остаются в почве. «Почва поглощает
калий, и в этом ее чудодейственная
сила»,— писал академик А. Е. Ферсман.
КАЛИЙ И РАСТЕНИЕ
Калий содержится во всех растениях.
Отсутствие калия приводит растение к
гибели. Почти весь калий находится в
растениях в ионной форме — К+. Часть ионов
находится в клеточном соке, другая часть
поглощена структурными элементами
клетки.
Ионы калия участвуют во многих
биохимических процессах, происходящих в
растении. Установлено, что в клетках
растений эти ионы находятся главным образом
в протоплазме. В клеточном ядре они не
обнаружены. Следовательно, в процессах
размножения и в передаче наследственных
признаков калий не участвует. Но и без
этого роль калия в жизни растения велика
и многообразна.
Калий входит и в плоды, и в корни, и в
стебли, и в листья, причем в вегетативных
органах его, как правило, больше, чем
в плодах. Еще одна характерная
особенность: в молодых растениях больше калия,
чем в старых. Замечено также, что по
мере старения отдельных органов растений
ионы калия перемещаются в точки
наиболее интенсивного роста.
При недостатке калия растения
медленнее растут, их листья, особенно старые,
желтеют и буреют по краям, стебель
становится тонким и непрочным, а семена
теряют всхожесть.
Установлено, что ионы калия
активизируют синтез органических веществ в
растительных клетках. Особенно сильно
влияют они на процессы образования
углеводов. Если калия не хватает, растение
хуже усваивает углекислый газ, и для
синтеза новых молекул углеводов ему
недостает углеродного «сырья». Одновременно
усиливаются процессы дыхания, и сахара,
содержащиеся в клеточном соке,
окисляются. Таким образом, запасы углеводов в
растениях, оказавшихся на голодом пайке
(по калию), не пополняются, а расходуются.
Плоды такого растения — это особенно
заметно на фруктах — будут менее
сладкими, чем у растений, получивших
нормальную дозу калия. Крахмал — тоже углевод,
поэтому и на его содержание в плодах
сильно влияет калий.
Но и это не все. Растения, получившие
достаточно калия, легче переносят засуху
и морозные зимы. Это объясняется тем, что
калий влияет на способность коллоидных
веществ растительных клеток поглощать
воду и набухать. Не хватает калия —
клетки хуже усваивают и удерживают влагу,
сжимаются, отмирают.
Ионы калия влияют и на азотный
20
обмен растений. При недостатке калия
в клетках накапливается избыток аммиака.
Это может привести к отравлению и гибели
растения.
Уже упоминалось, что калий влияет
и на дыхание растений, а усиление
дыхания сказывается не только на содержании
углеводов. Чем интенсивнее дыхание, тем
активнее идут все окислительные
процессы, и многие органические вещества
превращаются в органические кислоты.
Избыток кислот может вызвать распад белков.
Продукты этого распада — весьма
благоприятная среда для грибков и бактерий.
Вот почему при калийном голодании
растения намного чаще поражаются болезнями
и вредителями. Фрукты и овощи,
содержащие продукты распада белков, плохо
переносят транспортировку, их нельзя долго
хранить.
Одним словом, хочешь получать
вкусные и хорошо сохраняющиеся плоды —
корми растение калием вволю. А для
зерновых калий важен еще по одной причине:
он увеличивает прочность соломы и тем
самым предупреждает полегание хлебов...
КАЛИЙНЫЕ УДОБРЕНИЯ
Растения ежегодно извлекают из почвы
большое количество калия. Обедненная
калием почва нуждается в удобрении.
Самое дешевое (фактически даровое)
и в то же время прекрасное по качеству
калийное удобрение — печная зола. В ней
калий находится в виде поташа К2СО3.
Состав золы различных растений далеко не
одинаков. Больше всего калия в золе
подсолнечника— 36,3% КгО (содержание калия
в калийных удобрениях принято
пересчитывать на КгО). В золе дров окиси калия
значительно меньше — от 3,2% (еловые
дрова) до 13,8% (березовые дрова). Еще
меньше калия в золе торфа.
Конечно, одной золой калийный голод
растений не утолить. Самым важным
калийным удобрением стали природные
калийные соли, в первую очередь
сильвинит и каинит. Сильвинит — очень
распространенный минерал. Его состав
обозначают формулой mKCl-nNaCl. Кроме
хлоридов натрия и калия, в нем есть примеси
солей кальция, магния и других элементов.
Обычно в сильвините 14—18% КгО. В
каините КС1 'MgS04" ЗНгО окиси калия
меньше—10—12%.
Значительную часть природных
калийных солей перерабатывают в технический
продукт — хлористый калий с
содержанием КгО 50—62%.
Из сильвинита хлористый калий
получают методами галургии или флотации.
Первый основан на различной
растворимости КС1 и NaCl в воде при повышенных
температурах. Второй — на разной
смачиваемости этих веществ.
Первый метод используется шире. При
нормальной температуре растворимость
хлоратов калия и натрия почти одинакова.
С повышением температуры растворимость
NaCl почти не меняется, а растворимость
КС1 сильно возрастает. На холоду готовят
насыщенный раствор обеих солей, затем
его нагревают и обрабатывают им
сильвинит. При этом раствор дополнительно
насыщается хлористым калием, а часть
поваренной соли вытесняется из раствора,
выпадает в осадок и отделяется
фильтрованием. Раствор охлаждают, и из него
выкристаллизовывается избыточный
хлористый калий. Кристаллы отделяют на
центрифугах и сушат, а маточный раствор идет
на обработку новой порции сильвинита.
Технический хлористый калий
применяют и самостоятельно и в смеси с
природными калийными солями.
В качестве удобрения используется
также более дорогой, но не гигроскопичный и
не слеживающийся сульфат калия K2SO4.
Это удобрение можно применять на любых
почвах. А ионы хлора, вносимые
хлористым калием, для некоторых почв явно
нежелательны. Противопоказаны они и
некоторым растениям. Избыток ионов С1~
снижает содержание крахмала в клубнях
картофеля, ухудшает качество льняных
волокон, а персики, виноград и цитрусовые
делает более кислыми.
Таким образом, удобряя землю
хлористым калием, мы одновременно делаем все,
чтобы улучшить и... ухудшить качество
будущих плодов. Последнего можно
избежать, если применять наиболее
рациональные, химически обоснованные способы
внесения калийных солей.
Ионы хлора, в отличие от ионов калия,
почвой не поглощаются: они легко
вымываются грунтовыми водами и уносятся
в нижние горизонты. Поэтому, чтобы
сохранить в почве калий, но убрать из нее
хлор, нужно хлорсодержащие калийные
удобрения вносить в почву осенью. Пока
семена прорастут и корневая система
начнет усваивать ионы из почвы, осенние
21
дожди и талые воды успеют унести ионы
хлора вглубь.
Кстати, любое калийное удобрение
нужно не просто разбрасывать равномерно
по полю, а заделывать его плугом на
глубину пахоты — тогда оно будет намного
эффективнее.
В сельскохозяйственной практике
принято вносить от 30 до 90 кг К2О на гектар
посева. Но эти дозы весьма условны,
поскольку потребность в калийных
удобрениях определяется не только составом
почвы, но и тем, какая культура на этом
поле посеяна. Свекле, картофелю, бобовым
культурам, подсолнечнику, гречихе нужно
больше калия, нежели пшенице, ржи,
ячменю.
Агрономы считают, что при
благоприятных условиях один килограмм Кг О в
среднем дает такие прибавки урожая: зерна —
от 3 до 8 КГ, картофеля — 35 кг, сахарной
свеклы — 40 кг.
В нашей стране находятся самые
богатые в мире месторождения калийных
солей (район Соликамска — Березняков).
В 1965 году было получено около 5
миллионов тонн калийных удобрений. Это
в 170 раз больше, чем в 1913 году, и в
5 раз больше, чем в 1950 году.
КАЛИЙ — ЧЕЛОВЕКУ
Собственно, все, о чем рассказано выше,—
тоже на тему «калий — человеку». А здесь
коротко — о биологической роли элемента
№ 19 в жизни наиболее сложного из
живых организмов Земли.
Установлено, что соли калия не могут
быть заменены в организме человека
никакими другими солями. В основном калий
содержится в крови и протоплазме клеток.
Богаты калием печень и селезенка.
Значительна роль этого элемента в
регулировании деятельности ферментов.
Нельзя забывать еще об одной роли
калия в нашей жизни. Природный калий
состоит из трех изотопов: двух
стабильных— К39 и К41 и одного радиоактивного —
К40 с периодом полураспада около 13
миллиардов лет. Этот изотоп содержится в
живых организмах и своим излучением
вносит значительный вклад в общую сумму
естественного (фонового) облучения...
Организм ребенка, как и молодое
растение, требует больше калия, чем организм
взрослого человека. Суточная потребность
в калии у ребенка составляет 12—13 мг на
один килограмм веса, а у взрослого — 2 —
3 мг, то есть в 4—6 раз меньше.
Большую часть необходимого ему
калия человек получает из пищи
растительного происхождения. Недостаток калия
сказывается на разных системах и органах,
а также на обмене веществ.
Видимо, не очень преувеличивал
Александр Евгеньевич Ферсман, написавший
в одной из своих книг: «калий — основа
жизни».
Что вы знаете
и чего не знаете о калии
и его соединениях
ВСТРЕЧА С КАЛИЕМ?
Если на складе или на товарной
станции вы увидите стальные
ящики с надписями:
«Огнеопасно!», «От воды взрывается!», то
весьма вероятно, что вы
встретились с калием.
Много предосторожностей
предпринимают при перевозке
этого металла. Поэтому, вскрыв
стальной ящик, вы не увидите
калия, а увидите тщательно
запаянные стальные банки. В них —
калии и инертный газ —
единственная безопасная для калия среда.
Большие партии калия перевозят
в герметических контейнерах под
давлением инертного газа,
равным полутора атмосферам.
ЗАЧЕМ НУЖЕН
МЕТАЛЛИЧЕСКИЙ КАЛИЙ?
Металлический калий используют
как катализатор в производстве
некоторых видов синтетического
каучука, а также в лабораторной
практике. В последнее время
основным применением этого
металла стало производство перекиси
калия К2О4, используемой для
регенерации кислорода. Сплав калия
с натрием служит теплоносителем
в атомных реакторах, а в
производстве титана — восстановителем.
ИЗ СОЛИ И ЩЕЛОЧИ
Получают калий чаще всего в
обменной реакции расплавленных
едкого кали и металлического на-
22
трия: КОН + Na = NaOH + К.
Процесс идет в
ректификационной колонне из никеля при
температуре 380—440°С. Подобным
образом получают элемент № 19
и из хлористого калия, только в
этом случае температура
процесса выше — 760—800°С. При такой
температуре и натрий, и калий
превращаются в пар, а хлористый
калий (с добавками) плавится.
Пары натрия пропускают через
расплавленную соль и конденсируют
полученные пары калия. Этим же
способом получают и сплавы
натрия с калием. Состав сплава в
большой мере зависит от условий
процесса.
КАК БЫТЬ, ЕСЛИ...
...если вы впервые имеете дело с
металлическим калием?
Необходимо помнить о
высочайшей реакционной способности
этого металла, о том, что калий
воспламеняется от малейших
следов воды. Работать с калием
обязательно в резиновых перчатках
и защитных очках, а лучше — в
маске, закрывающей все лицо.
С большими количествами калия
работают в специальных камерах,
заполненных азотом или аргоном.
(Разумеется, в специальных
скафандрах.)
...если калий все-таки
воспламенился?
Горящий калий тушат не водой,
а содой или поваренной солью.
ЕСТЬ ЛИ В РАСТВОРЕ
ИОНЫ КАЛИЯ?
Выяснить это несложно.
Проволочное колечко опустите в
раствор, а затем внесите в пламя
газовой горелки. Если калий есть,
пламя окрасится в фиолетовый
цвет, правда, не в такой яркий,
как желтый цвет, придаваемый
пламени соединениями натрия.
Сложнее определить
количество калия в растворе.
Нерастворимых в воде соединений у этого
металла немного. Обычно калий
осаждают в виде перхлората —
соли очень сильной хлорной
кислоты НСЮ4. Кстати, перхлорат
калия — очень сильный
окислитель и в этом качестве
применяется в производстве некоторых
взрывчатых веществ и ракетных
топлив.
ДЛЯ ЧЕГО НУЖЕН
ЦИАНИСТЫЙ КАЛИЙ?
Для извлечения золота и серебра
из руд. Для гальванического золо-
23
чения и серебрения
неблагородных металлов. Для получения
многих органических веществ. Для
азотирования стали — это
придает ее поверхности большую
прочность.
К сожалению, это очень
нужное вещество чрезвычайно
ядовито. А выглядит KCN вполне
безобидно: мелкие кристаллы белого
цвета с коричневатым или серым
оттенком.
ЧТО ТАКОЕ ХРОМПИК?
Точнее — хромпик калиевый. Это
оранжевые кристаллы состава
К2СГ2О7. Хромпик используют в
производстве красителей, а его
растворы — для «хромового»
дубления кож, а также в качестве
протравы при окраске и
печатании тканей. Раствор хромпика в
серной кислоте — хромовая смесь,
которую во всех лабораториях
применяют для мытья стеклянной
посуды.
ЗАЧЕМ НУЖНО
ЕДКОЕ КАЛИ?
В самом деле, зачем? Ведь
свойства этой щелочи и более
дешевого едкого натра практически
одинаковы. Разницу между этими
веществами химики обнаружили
лишь в XVIII веке. Самое заметное
различие между NaOH и КОН в
том, что едкое кали в воде
растворяется еще лучше, чем едкий
натр. КОН получают
электролизом растворов хлористого калия.
Чтобы примесь хлоридов была
минимальной, используют ртутные
катоды. А нужно это вещество
прежде всего как исходный
продукт для получения различных
солей калия. Кроме того, без
едкого кали не обойтись в
производстве жидких мыл, некоторых
красителей и органических
соединений. Раствор едкого кали
используется в качестве электролита в
щелочных аккумуляторах.
ЧТО ТАКОЕ МАРГАНЦОВКА?
Это калиевая соль КМгЮ4
марганцовой кислоты, широко
применяемая в медицине и ветеринарии, в
органическом синтезе (как
окислитель) и лабораторной практике
(как реактив). Темно-фиолетовые
кристаллы марганцовокислого
калия получают, сплавляя на
воздухе пиролюзит МпОг с КОН.
СЕЛИТРА ИЛИ СЕЛИТРЫ?
Правильнее — селитры. Это
общее название азотнокислых солей
щелочных и щелочноземельных
металлов. Если же говорят просто
«селитра» (не «натриевая» или
«кальциевая» или «аммиачная», а
просто — «селитра»), то имеют в
виду иитрат калия. Этим
веществом человечество пользуется уже
больше тысячи лет — для
получения черного пороха. Кроме того,
селитра — первое двойное
удобрение: из трех важнейших для
растений элементов в ней есть
два — азот и калий. Вот как
описал селитру Д. И. Менделеев в
«Основах химии»:
«Селитра представляет
бесцветную соль, имеющую особый
прохладительный вкус. Она легко
кристаллизуется длинными, по
бокам бороздчатыми, ромбическими,
шестигранными призмами,
оканчивающимися такими же
пирамидами. Ее кристаллы (уд. вес 1,93) не
содержат воды. При слабом
накаливании C39°) селитра плавится в
совершенно бесцветную
жидкость. При обыкновенной
температуре в твердом виде KN03
малодеятельна и неизменна, но при
возвышенной температуре она
действует, как весьма сильное
окисляющее средство, потому что
может отдать смешанным с нею
веществам значительное
количество кислорода. Брошенная на
раскаленный уголь селитра
производит быстрое его горение, а
механическая смесь ее с измельченным
углем загорается от
прикосновения с накаленным телом и
продолжает сама собою гореть. При
этом выделяется азот, а
кислород селитры идет на окисление
угля, вследствие чего и
получаются углекалиевая соль * и
углекислый газ...
В химической практике и
технике селитра употребляется во
многих случаях как окислительное
средство, действующее при
высокой температуре. На этом же
основано применение ее для
обыкновенного пороха, который есть
механическая смесь мелко
измельченных: серы, селитры и угля».
ГДЕ И ДЛЯ ЧЕГО
ПРИМЕНЯЮТСЯ
ПРОЧИЕ СОЛИ КАЛИЯ?
Бромистый калий КВг — в
фотографии, чтобы предохранить
негатив или отпечаток от
вуали.
Йодистый калий KJ — в медицине
и как химический реактив.
Фтористый калий KF — в составе
металлургических флюсов и для
введения фтора в органические
соединения.
Углекислый калий (поташ) К2СО3—
в стекольном и мыловаренном
производствах, а также как
удобрение.
* Имеется в виду поташ.
Фосфаты кол и я, в частности
К4Р2О7 и КбРзОю, — как
компоненты моющих средств.
Хлорат калия (бертолетова соль)
КС103 — в спичечном
производстве и пиротехнике.
Кремнефтористый калий K^SiFe —
как добавка к шихте при
извлечении редкоземельных
элементов из минералов.
Железистосинеродистый калий
(желтая кровяная соль)
K4Fe(CNN • ЗН2О — как
протрава при крашении тканей и в
фотографии.
ПОЧЕМУ КАЛИИ
НАЗВАЛИ КАЛИЕМ?
Слово это арабского
происхождения. По-арабски, «аль-кали» —
зола растений. Впервые калий
получен из едкого кали, а едкое
кали — из поташа, выделенного из
золы растений... Впрочем, в
английском и других европейских
языках сохранилось название
potassium, данное калию его
первооткрывателем Г. Дэви. Как
нетрудно догадаться, это слово берет
начало от слова «поташ». А
называть элемент № 19 калием
предложил в 1831 году русский химик
Г. И. Гесс.
Рисунки Е. ГОЛЬДИНА
24
«НЕ ДЛЯ ТОГО
УЧРЕЖДАЮТСЯ
УНИВЕРСИТЕТЫ...»
Страницы
жизни
Менделеева
к Менделееву с полным беспристрастием.
Однажды он показал мне только что
полученную им книгу английского химика
Рейнольдса, присланную ему автором, и
сказал: «Рейнольде оспаривает первенство
Менделеева в открытии им периодической
системы элементов, но ведь Менделеев
один предсказывает новые элементы...»
В начале осени 1880 года он [А. М.
Бутлеров — Ред.] написал, что, делая
представление в Академию о замещении вакантной
кафедры химии, он, согласно §2
действовавшего тогда устава Академии, должен
будет представить Д. И. Менделеева. Стало
известным, что президент Академии Литке,
непременный секретарь Веселовский и
большинство академиков являются
решительными противниками кандидатуры
Менделеева, противопоставляя ему
профессора Технологического института Бель-
штейна. Менделеев был забаллотирован.
После этого профессора Университета в
виде протеста устроили обед в честь
Менделеева, во время которого говорены были
соответствующие речи; полемика в газетах,
которая началась еще раньше, оживилась
особенно теперь. Статьи против
Менделеева появились преимущественно в «St. Ре-
tersburger Zeitung». Вопрос перешел на
национальную почву и обострился еще
более... На другой день после заседания
Академии, на котором была решена судьба
Менделеева, мне случилось зайти в
академическую библиотеку и при мне шел
разговор между академиком и лицом из штата
библиотеки; академик говорил, что
Менделеева невозможно было допустить в
Академию из-за его тяжелого характера;
других причин неизбрания Менделеева в
члены Академии он не приводил.
С. Ф. ГЛИНКА *
.осле кончины
Н. Н. Зинина (в феврале 1880 года) в
Академии освободилась кафедра химии и
возник вопрос о замещении ее. А. М.
Бутлеров был всегда высокого мнения о
Д. И. Менделееве как о выдающемся
русском химике и, конечно, прежде всего
вспомнил о нем. В это время отношения
между Бутлеровым и Менделеевым были
несколько испорчены. Менделеев
незадолго перед этим повел систематическую
борьбу со спиритизмом, которым усердно
занимался Бутлеров, прочитал лекцию и
напечатал книгу против спиритизма;
кроме того, он отрицательно отнесся к учению
о структуре органических соединений,
которое развивал Бутлеров... Несмотря на
все это, Бутлеров продолжал относиться
Продолжение публикации отрывков из
воспоминаний современников о Д. И. Менделееве
(начало в № 11). Публикация подготовлена
кандидатом химических наук А. А. Макареней и
И. Н. Филимоновой.
* С. Ф. Глинка A855—1927?) — минералог,
профессор Московского университета, а затем —
Института инженеров путей сообщения.
4 Химия и Жизнь» № 12
25
Е. А. РОГОВСКИЙ
Академик А. А. БАЙКОВ '
усское
физико-химическое общество снарядило... две
экспедиции для наблюдения полного
солнечного затмения 7 августа 1887 г. Одна
экспедиция была отправлена в Красноярск,
другая близ станции Подсолнечной
Николаевской дороги...
И вот дня за два до затмения в
Никольское прискакал на тройке, загнав одну
лошадь, Дмитрий Иванович, весь
забрызганный грязью. Не надеясь увидеть корону
солнца на земле, он решил взлететь на
воздушном шаре выше облаков... Помню
одну фразу, сказанную им при прощаньи:
«я не боюсь лететь, а боюсь того, что при
спуске мужики примут меня за черта и
изобьют».Рассказывают, что сев в Клину
перед затмением в корзину воздушного
шара вместе с Кованько, начальником
воздухоплавательного парка, Дмитрий
Иванович заметил, что шар, веревочные сети
которого намокли от дождя, не в
состоянии поднять двух наблюдателей, и
обратился к г. Кованько с требованием выйти
из корзины. Так как шар был военного
ведомства и г. Кованько был его
начальником, то он отказался первоначально выйти
из корзины, но Д. И. Менделеев пригрозил
выкинуть его из нее, если он не сойдет
добровольно. Г-ну Кованько ничего
другого не оставалось делать, как исполнить
это требование, так энергично выраженное,
и Дмитрий Иванович полетел один и
поднялся выше облаков и, таким образом, мог
наблюдать корону. Дмитрий Иванович
совершал полет впервые.
* Е. А. Роговский A849—1919) русский физик;
преподавал физику в различных учебных
заведениях Петербурга, позднее работал вместе с
Менделеевым в палате мер и весов.
марта 1890 г_
в Петербургском университете начались
студенческие волнения. Они приняли
крупные размеры. Студенты устраивали
сходки для обсуждения требований к
правительству и составления петиций, и когда
все было подготовлено, на сходку были
приглашены професора.
На эту сходку в числе других
профессоров явился Д. И. Менделеев, который
пользовался необычайной популярностью,
любовью и уважением всего студенчества.
Речь шла о том, чтобы подать
правительству выработанную петицию и просить это
сделать Менделеева, который это
предложение принял и обещал исполнить.
Петиция, которая была составлена
с этой целью и которая была затем
вручена Д. И. Менделееву для передачи
правительству, содержала явно политические
требования, например, свободы слова,
свободы печати, равноправия мужчин и
женщин и пр. Я это подчеркиваю потому,
что и здесь проявилось исключительное
мужество Менделеева, который не
побоялся в это смутное, мрачное время русской
истории взять на себя такое поручение,
которое, конечно, являлось в политическом
отношении чрезвычайно опасным.
Это были годы самого черного
мракобесия, годы, когда царствовал
Александр III, когда все живое душилось,
притеснялось, угнеталось...
И здесь сказывается величие
Менделеева не только как ученого, но как
человека и гражданина.
Я хорошо помню ту лекцию, на
которой Менделеев эту петицию принял. Это
было 14 марта 1890 г. Собралось на эту
* А А. Байков A870—1946), выдающийся
советский физико-химик и металловед.
26
лекцию-сходку громадное количество
студентов.
Когда Менделеев появился, его
встретили громом аплодисментов,
рукоплесканий, восторженными криками. Он махал
руками, хмурился, просил успокоиться.
Наконец, когда все затихло, он свой
хмурый вид изменил и улыбнулся. Опять
взрыв аплодисментов. Он более уже не
махал руками, стоял, молчал, ждал, когда
все окончится, и приступил к лекции. Все
ожидали от него сильных выступлений,
выражений, а он ее начал так: «Марганец
встречается в природе главным образом в
виде кислородных соединений». Это было
начало, а затем он стал развивать те
глубокие мысли и идеи широкого общественно-
политического характера о необходимости
развития промышленности и связи ее
с наукой, которые составили главное
содержание лекции. После этой лекции
Менделееву была передана петиция для
вручения министру народного просвещения
Делянову.
16 марта петиция, переданная
Менделееву, была им отвезена Делянову,
который возвратил ее Менделееву с надписью:
«По приказанию Министра Народного
Просвещения прилагаемая бумага
возвращается Действ. Стат. Сов. профессору
Менделееву, так как ни министр и никто
из состоящих на службе Его
Императорского Величества лиц не имеет права
принимать подобные бумаги. Его пр-ву
Д. И. Менделееву 16 марта 1890 г.». Не
считая возможным после этого оставаться
в Университете, Менделеев подал
прошение об отставке и летом выехал из
квартиры в Университете на новую квартиру.
Когда стало известно, что министр Де-
лянов отказался принять петицию и
Менделеев ушел в отставку, в Университете
снова вспыхнули волнения.
Университетская администрация ввела полицию в
Университет. Было произведено много арестов,
протест был подавлен.
При таких обстоятельствах Менделеев
прочел свою последнюю лекцию. Это было
22 марта 1890 г. На этой лекции студентов
было уже мало, многие были арестованы,
многие были в угнетенном состоянии.
Аудитория была немногочисленна. Но тем
не менее Менделеева слушали с большим
вниманием. Менделеев читал последнюю
заключительную главу курса
неорганической химии. Он говорил о важных,
крупных вопросах, о роли науки в жизни
государства и народа, о значении науки для
промышленности, он призывал заниматься
этими вопросами — сближать
промышленность и науку. Таким образом он излагал
свою идею о более близкой связи между
наукой и промышленностью, о поднятии
техники для индустриализации страны. Эти
идеи всегда проводил в своих
выступлениях.
И закончил он эту свою лекцию такими
словами: «Покорнейше прошу не
сопровождать моего ухода аплодисментами по
множеству различных причин».
Эти слова были так выразительны, что
не раздалось ни одного возгласа, ни одного
хлопка, и среди этой мертвой тишины он
оставил аудиторию, оставил ее навсегда.
Б. П. ВЕЙНБЕРГ *
; от какой
последний завет дал он нам — последний
потому, что эта была последняя лекция его
как профессора С.-Петербургского
университета студентам.
«Но не для того мы здесь и не для того
учреждаются университеты, чтобы
получились только дипломы и чтобы
получалось знакомство с предметом, с его... как
сказать... в его прошлом. Это—одна
сторона, это — неизбежно, это — сторона,
можно сказать, первичная, но есть и другая
высшая сторона, которая и дает то...,
дает тот оттенок университетскому
знанию, который должен быть назван духом
университета.
Вы знаете сказки, в которых говорится
* Б. П. Вейнберг A871—1942) геофизик, в 1889—
1893 гг. студент Петербургского университета.
22 марта 1890 г. застенографировал последнюю
лекцию Менделеева. Впоследствии был
профессором Томского университета, директором
Главной геофизической обсерватории.
4*
27
о том, что приходит кто-то и говорит: «Фу,
русским духом пахнет!» — Вам это
непонятно, вам это в детстве кажется чем-то
даже смешным.
Когда поживете, тогда увидите, что есть
во всем, что сложилось, что образовалось,
что имеет влияние, что имеет значение —
есть во всем нечто неуловимое, что люди
в первичном образе всегда изображали
в виде духа..., т. е. воздуха. Вы в курсах
философии узнаете, что первые учения
философские старались весь мир... понять...
при помощи представлений... о воздухе или
духе... проникающем все. ...Это самое
первоначальное представление у всех народов
так или иначе сказалось даже в словах...
между воздухом и духом есть всегда, во
всех... у всех... первичных понятий —
а следовательно, и в языке, ибо он тогда
слагается, когда еще первичные понятия
слагаются — есть, как сказать, единение.
Так есть и в университетах свой дух...
Этот дух состоит исключительно и всецело,
в существе только в одном: в стремлении
достигнуть истину во что бы то ни стало —
не практическую пользу, не личное
улучшение, не каких бы то ни было этих
политических или экономических улучшений —
все это сбоку, все это придатки, все это есть
не что иное, как атрибуты, члены
основного, одного, исключительного
стремления, это — достижения истины во что бы
то ни стало и как бы то ни было — но
только истины в том виде, в каком она... ее
можно достигнуть. Не в том, чтобы,
отпирая храм ключом, прямо пойти
сдернуть завесу сокрытой истины, — ничего
нету, сказки, пустое! Ничего такого нету,
никакой такой завесы нет: истина не
спрятана от людей, она среди нас, во всем мире
рассеяна. Ее везде искать можно: и в
химии, и в математике, и в физике, и в
истории, и в языкознании — во всем том, что
направлено к отысканию истины, —
оттого-то это все и соединяется в
университете»...
«Наука бесконечна, — говорил он, —
в ней являются с каждым днем новые и
новые задачи, и университетское
образование должно стараться возбудить желание
внести свою лепту в сокровищницу науки».
Рисунки И. БЕЛЬМ АН А
О КОРОТКОМ ИСТОРИИ
ПСИХОФАРМАКОЛОГИИ
Окончание. Начало на стр. 5.
Вслед за аминазином было
синтезировано несколько его
производных, и все они в
большей7 или меньшей степени
обладали психотропными
свойствами. В университетах, в
медицинских институтах и кли^
никах открывались
психофармакологические лаборатории.
В 1957 году в них уже
испытывали 15 производных
аминазина, в 1964 году — 75. Через
десять лет после сообщения П. Де-
никера число работ,
посвященных аминазину, перевалило за
10 000. В 1963 году пятьдесят
миллионов больных лечили
этим медикаментом.
Количество психотропных
средств росло, характер
лекарств становился
разнообразнее. В том же 1952 году химики
швейца рекой фирмы «Сиба»
выделили из кустарника рау-
вольфии кристаллический
алкалоид — резерпин.
Американский психиатр Н. Клайн
испытал резерпин на больных — по
своему действию препарат
оказался похожим на аминазин.
Доктор Р. Каун получил от
фармацевтической фирмы
«Гаити» в Базеле еще одно
вещество — «тофранил». Действие его
оказалось противоположным
действию аминазина. Больные,
страдающие тяжелой формой
депрессии, после приема
лекарства преображались: от
депрессии оставались лишь слабые
следы. Тофранил положил
начало еще одной группе
лекарств — антидепрессантов.
Сейчас известно более 400
психофармакологических
препаратов. Каждый год химики
синтезируют тысячи, а
фармакологи испытывают сотни
новых соединений; правда, в
клинику из этих сотен и тысяч
попадают только единицы.
28
Дикий виноград на березе...
Такое можно увидеть только
на Дальнем Востоке
ИСТОРИЯ
одного
РЕЛИКТА
Т. А. АБРАМОВА,
Географический факультет МГУ
Фото
А. СОКОЛЬСКОГО
и автора
Даже те, кому не доводилось бывать на
Дальнем Востоке, много слышали о его
своеобразной растительности, о
легендарной Уссурийской тайге, об удивительных
лесах Приморья. Здесь можно встретить
кедр и монгольский дуб, амурскую пихту
и маньчжурскую липу, черную березу и
амурскую сирень. Здесь шумят деревья
амурского бархата и маньчжурского ореха,
зреют гроздья дикого винограда и цветут
рододендроны. В лесах густо разрослись
лианы, а в тенистых таежных уголках
притаился женьшень со своими
напоминающими человеческие фигуры корнями...
Юг Дальнего Востока — настоящий
заповедник древней растительности. Здесь
остались так называемые третичные леса,
более миллиона лет назад покрывавшие
обширные пространства нашей Земли.
В бурное четвертичное время, пришедшее
на смену третичному, многократные
оледенения изменили облик растительного
покрова, местами стерли с лица земли,
местами оттеснили и изменили древние
растения. Здесь же не было сплошных
оледенений, да и климат остался достаточно
мягким и влажным.
Но перенесемся на несколько сотен
29
Всего несколько сотен
километров разделяют места
распространения охотской (слева)
и маньчжурской (справа) флор
километров к северу — и как же резко
изменится пейзаж! Посмотрите на эти две
фотографии. На одной из них — хвойно-
широколиственные леса Приморья. На
другой — ландшафты м атерикового
побережья Сахалинского залива. Здесь
растительность бедна и однообразна. Повсюду
бесконечные «мари» — болота, местами
поросшие редким лиственничником, а
большей частью безлесные. Остальные
деревья— сосна, береза, ольха — под влиянием
суровых условий превратились здесь в
карликов, распластались, ища приют на
неласковой земле. Такие унылые безлесные
ландшафты тянутся на многие сотни
километров. Но эти две совершенно разные
флоры, которые так и называют — «охотская»
и «маньчжурская», — имеют и много общих
форм, дошедших до наших дней из
отдаленных геологических эпох. Один из таких
своеобразных реликтов — аянская ель.
Удивительное это дерево! Проникая до
высоких широт на севере Приохотья, оно
существует там в самых неблагоприятных
для древесных пород условиях. По своей
природе аянская ель — горное дерево, но
местами она, особенно на севере,
спускается до уровня моря. В то же время она
прекрасно развивается и в смешанных
маньчжурских лесах, а в Японии растет вместе
с представителями субтропической флоры.
На острове Иезо в лесах из аянской ели
можно встретить магнолии, лианы и
бамбук.
Как удалось аянской ели завоевать
такие прочные позиции в суровых условиях
Приохотья?
Историю вида, связанную со сменами
растительного покрова, могут рассказать
нам свидетельства отдаленных эпох —
древние растительные остатки, изучением
которых занимается палеоботаника.
Окаменевшие шишки, хвою, кору,
древесину предка аянской ели (ее предложено
было назвать «проаянской») находят на
еще более обширных площадях, чем те,
которые занимает сейчас аянская ель. Но
по макроостаткам трудно судить о месте
этой ели в растительном покрове прошлого.
Дело в том, что обычно древесина и другие
остатки хвойных пород, содержащие
смолистые вещества, сохраняются лучше, чем
остатки пород лиственных.
Гораздо больше сведений могут дать
нам микроскопические остатки — пыльца
и споры, сохранившиеся в рыхлых отло-
30
ткениях. Оболочка пыльцевых зерен и спор
содержит обладающие исключительным
запасом прочности высокомолекулярные
вещества типа полимерных терпенов —
спорополленины. Благодаря им оболочки
сохраняют свои характерные структурные
особенности и после длительного
пребывания во вмещающей породе, и при
химической обработке. Состав и изменение этих
спорово-пыльцевых спектров и могут
ловедать нам о ходе развития и сменах
растительного покрова за то время, когда
отлагались осадки.
Выделить пыльцу и споры,
составляющие лишь ничтожнейшую часть
содержащей их породы,— не такая простая задача.
В процессе обработки образец породы
прежде всего подвергают обогащению. Для
этого его нагревают до кипения со
щелочью — она размягчает цементирующие
вещества породы, и пыльца легче
выделяется из образца. После этого образец
центрифугируют с тяжелыми жидкостями,
удельный вес которых выше удельного
веса пыльцы и спор, но меньше удельного
веса самых легких минеральных
компонентов породы. Для этого применяют так
называемую «жидкость Туле» (раствор
смеси йодистого калия и двуиодистои
ртути), кадмиевую жидкость (раствор смеси
йодистого кадмия и йодистого калия),
а также жидкости ПД-1, ПД-2 и ПД-3
(смесь концентрированных растворов
йодистого и бромистого цинка). При
центрифугировании с такой жидкостью порода
разделяется: органические остатки, в том
числе пыльца и споры, всплывают наверх,
а минеральные частицы оседают на дно.
Что же рассказали анализы рыхлых
отложений Приохотья?
Оказывается, там, где теперь
растительный покров так скуден и однообразен,
более миллиона лет назад была
распространена иная, теплолюбивая
растительность. Здесь, в хвойно-широколиственных
лесах, произрастали такие экзотические
виды, как лапина, гикори, таксодиевые,
гинкго, тсуга и другие. В числе хвойных
пород была и аянская ель. Но тогда она не
играла существенной роли в растительном
покрове. Доминирующей породой
третичных лесов была тсуга, характерное древнее
хвойное дерево.
Однако в начале четвертичного периода
климат здесь стал значительно более
холодным и влажным. Стали исчезать мно-
31
Микроскопические пыльцевые
зерна аянскои ели (слева) и
тсуги (справа)
Шш
гие теплолюбивые формы. Похолодание
подрезало позиции тсуги, она стала
регрессировать и постепенно сошла на нет. Зато
предок аянскои ели из сопутствующей
породы становится основной.
Изменившиеся климатические условия оказались очень
благоприятными для этой своеобразной
породы. Ей необходима для успешного
развития высокая влажность воздуха, но
зато она нетребовательна к
температурному режиму и может переносить
довольно низкие температуры. Эта
холодостойкость аянскои ели в дальнейшем усилилась
под влиянием нарастающего похолодания.
Поэтому аянская ель сумела пережить все
колебания четвертичного климата и
дожить до наших дней.
Вот что рассказали нам об истории
этого реликта спорово-пыльцевые
исследования. Изучение истории аянскои ели
имеет и определенный практический
смысл. Эта порода переходит на
положение доминирующей в самом начале
четвертичного периода. Значит,
спорово-пыльцевые спектры позволяют установить
нижнюю границу четвертичного периода для
рыхлых отложений Южного Приохотья, то
есть определять геологический возраст
рыхлых отложений. А это нужно уже для
геологических съемок, для
прогнозирования и поисков полезных ископаемых.
32
НАШИ КОНСУЛЬТАЦИИ НАШИ КОНСУЛЬТАЦИИ НАШИ КОНСУЛЬТАЦИИ НАШИ КОНСУЛЬТАЦИИ
■ КАК ПОДСЧИТЫВАЮТ
УДОБРЕНИЯ?
Б сообщениях ЦСУ СССР цифры
производства минеральных
удобрений приводятся в пересчете на
100% -ное содержание
питательных веществ и в условных
единицах. Хотелось бы знать
подробнее, что это значит. И второе: в
какой мере это удовлетворяет
потребность страны!
Л. Г. БЕСПАЛОВ, Минск
По просьбе редакции, на вопрос
читателя отвечает агроном О. Н.
КОРЧАГИНА.
всякое минеральное удобрение
содержит действующее начало —
ту составную часть, которая
усваивается растением, полезна для
него. Например, в калийном
удобрении это калий, в азотном —
азот и т. д. Действующее начало
еходит в состав химических
соединений, остальная часть которых
растением не усваивается и
является, по существу, балластом.
Чтобы определить, сколько
нужно вносить того или иного
удобрения, надо учитывать
содержание в нем действующего
вещества. Например, вам надо внести
азотное удобрение из расчета
12 г азота на 1 м2. В вашем
распоряжении два сорта удобрения:
сернокислый аммоний B1 %
действующего вещества) и аммиачная
селитра C5% действующего
вещества). Доза сернокислого
аммония на 1 м2 должна составлять
12X100
21
^ 57 г, а аммиачной се-
12x100 ,.. u л
литры - ^ 34 г. Чем ооль-
ше действующего вещества
содержит удобрение, тем меньшие
его дозы надо вносить.
В сводках же ЦСУ количество
минеральных удобрений,
производимых в СССР, исчисляется в
тоннах «стандартного продукта»:
азотные удобрения
пересчитывают на сульфат аммония (то есть
на содержание азота 20,5—21%),
фосфорные — на суперфосфат
A8,7 Р2О5), калийные — на
калийную соль B5%, КС1).
Несмотря на то, что
производство минеральных удобрений в
нашей стране за последние годы
значительно увеличилось оно еще
не может полностью
удовлетворить потребность сельского
хозяйства. Поэтому пятилетним
планом предусмотрен дальнейший
рост промышленности
минеральных удобрений.
■ КАКИЕ ГАЗЫ?
Какие газы и в каких условиях
выделяются при реакциях
металлов с азотной кислотой! Может ли
лри этом выделиться водород!
Г. ПЕТРОВА
Отвечает А. А. БАГАТУРЬЯНЦ.
Заметим сразу же, что водород
при реакциях металлов с азотной
кислотой не выделяется. Дело в
том, что анион NO^ — сильный
окислитель. В присутствии веществ,
способных окисляться, ион NO "^
восстанавливается в зависимости
от условий реакции до: NO <Г,
N02, NO, N2Of N2 или NH3. Ион
NO3 в кислой среде, то есть и в
виде азотной кислоты, особенно
сильно проявляет свои
окислительные свойства.
Как известно, азотная кислота
растворяет очень многие металлы,
стоящие в ряду напряжений за
водородом, в том числе и
металлы, обычно не растворяющиеся в
кислотах. При взаимодействии
азотной кислоты с металлами,
стоящими в ряду напряжений до
водорода, могут образовываться
любые продукты восстановления
вплоть до NH3. На холоду, в
разбавленной кислоте увеличивается
доля выделяющегося аммиака, а
в жестких условиях — при
повышенной температуре в
концентрированной кислоте увеличивается
вероятность образования NO и
N02. Остальные продукты
образуются реже и в меньших
количествах. Однако при всех
обстоятельствах выделяется смесь газов.
Металлы, стоящие в ряду
напряжений после водорода, при
любых условиях восстанавливают
HNOs лишь до NO и N02. При
меньшей концентрации кислоты и
в реакциях, проводимых без
нагрева, выделяется главным
образом NO.
5 Химия и Жизнь, № 12
33
Борис Николаевич Меншуткин
A874—1938)
БОРИС
НИКОЛАЕВИЧ
МЕНШУТКИН
Случается иногда, что один, казалось бы,
и не такой уж значительный факт меняет
всю жизнь человека. Так произошло и с
известным русским историком химии,
профессором, доктором химических наук
Борисом Николаевичем Меншуткиным.
Он родился 17 апреля 1874 года в
Петербурге. Отец его — профессор химии
Петербургского университета Николай
Александрович Меншуткин был широко
известен в научном мире. Он был одним
из сподвижников Менделеева, одним из
основателей Русского химического
общества.
i Казалось, жизненный путь сына
определен. Он учится в Петербургском
университете — и тоже изучает химию. После
окончания курса остается работать на
кафедре отца, в университете, а в 1902
году вместе с отцом переходит в только что
основанный Петербургский политехниче-^
ский институт. В 1907 году Борис
Николаевич защищает магистерскую
диссертацию о взаимодействии бромистого и
йодистого магния с органическими
соединениями — спиртами, эфирами,
альдегидами. После смерти отца он в 1907 году
избран профессором аналитической и
органической химии в Петербургском
политехническом институте...
Борис Николаевич продолжил дело
своего отца. Он сохранил методику
преподавания Николая Александровича Мен-
шуткина, опубликовал (под своей
редакцией) семь изданий его классического
руководства по аналитической химии. Но
не меньше его привлекали научные
архивы, старые, забытые книги.
Работая в химическом обществе, он, к
удивлению своему, обнаружил, что
русская общественность почти ничего не
знает о химических трудах М. В.
Ломоносова. Собрать и популяризировать это
ценнейшее достояние русской науки стало
делом жизни Бориса Николаевича Мен-
шуткина.
Никто из его ученых коллег не мог
ответить ничего определенного на его
расспросы. Сведений о Ломоносове-химике
не было ни в одной истории химии... Лишь
французский историк Ф. Гефер упоминает
«о руском химике Ломоносове», которого
он просит не путать с однофамильцем
Ломоносова — поэтом!
В 1902 году Борис Николаевич
приступает к тщательнейшему разбору,
изучению и переводу на русский язык химиче-
ских трудов Ломоносова (многие из них
были написаны по-латыни, как это было
принято в середине XVIII века). Скоро
выходит капитальный труд Б. Н. Меншут-
кина «Ломоносов как физико-химик». Это
была первая из 31 работы ломоносовской
серии.
Благодаря изысканиям Б. Н. Меншут-
кина, нам стали известны забытые
рукописи Ломоносова: «Элементы
математической химии», его диссертация «О
нечувствительных физических частичках »,
«Рассуждение о селитре», «Курс истинной
физической химии», программы физико-
химических исследований великого
ученого, письмо к Эйлеру от 5 июля 1748 года,
документы о постройке и оборудовании
химической лаборатории Академии наук
и многое другое. Меншуткин первый в
истории науки дал подробный историко-
критический анализ всей совокупности
работ Ломоносова по физике и химии и на
основании бесспорных документальных
данных охарактеризовал его как физико-
химика, предвосхитившего на многие
десятилетия развитие науки.
Исторические работы Меншуткина
были представлены на соискание премии «За
ученое жизнеописание Ломоносова». Эта
премия была учреждена Петербургской
академией наук еще в 1868 году, но около
сорока лет ни разу не присуждалась —
ведь не было выпущено ни одной работы...
В 1907 году ее получил Меншуткин —
правда, в половинном размере (согласно
положению, полностью премия могла
быть выдана только за сочинение,
охватывающее все стороны многогранной
деятельности Ломоносова).
В 1911 году Борис Николаевич
Меншуткин опубликовал первую научную
биографию Ломоносова. Книга была
издана неслыханным для того времени
тиражом: 80 тысяч экземпляров! После
революции она была переиздана дважды — в
1937 и 1947 годах. Английский перевод
второго издания вышел в 1952 году в США.
В 1936 году Меншуткин выпустил
монографию «Труды Ломоносова по физике
и химии». Здесь подведены итоги более
чем тридцатилетней неустанной и
кропотливой работы. Многие результаты своих
поисков Меншуткин публиковал за
границей, благодаря чему имя и научные
заслуги Ломоносова стали широко известны и в
других странах. Появились интересные
отклики. В конце 1911 года известный
химик профессор А. Смит, вступая в
должность президента Американского
химического общества, произнес речь.
«Ломоносов — один из первых физико-химиков, —
говорил он, — открытие Ломоносова
прибавило химика первой величины и
личность удивительной силы к ограниченному
ряду величайших людей мира». В 1912
году знаменитый историк естествознания
Ж. Сартон назвал Ломоносова «славой
международной науки, отцом физической
химии». Были, конечно, и другие мнения,
принижавшие и даже отрицавшие значение
работ Ломоносова. Этим скептикам дал
отповедь немецкий ученый профессор Г. Рин-
кер, писавший уже в 1951 году: «Люди
обедняют самих себя, когда они избегают
встречаться с великими умами; изучение
физико-химических работ Ломоносова
доставляет наслаждение и в наше время, а
также содействует знакомству с
творческой личностью, которой можно только
удивляться».
Кроме классических работ о
Ломоносове, Борис Николаевич Меншуткин
написал немало статей и книг по истории
химии. Среди них — биография его отца,
Н. А. Меншуткина (СПб., 1908) и книга
«Химия и пути ее развития» (М. — Л.,
1937), предназначенная для учащейся
молодежи.
В 1912 году Меншуткин защитил
докторскую диссертацию о взаимодействии
органических соединений с
неорганическими, но после этого не возвращается к
экспериментальной работе. Он продолжает
чтение лекций, организует практические
занятия студентов, пишет учебники и
главное — исторические труды.
Характерно, что при переиздании его «Курса
общей химии» (а он издавался четыре
раза —в 1924, 1929, 1930 и 1933 годах)
Борис Николаевич отказывался от
авторского гонорара, чтобы сделать свою книгу
более дешевой и доступной для студентов.
Борис Николаевич Меншуткин
скончался 15 сентября 1938 года. Он похоронен
в Ленинграде, на Смоленском кладбище.
5*
35
«НЕЗРИМЫЕ
НИТИ,
СВЯЗЫВАЮЩИЕ НАС
С
ПРОШЛЫМ...»
В октябре 1912 года Борис
Николаевич Меншуткин делал
доклад по случаю десятилетия
Петербургского
политехнического института о его истории.
Мне, студенту первого курса,
было очень интересно
услышать, как был основан и
развивался институт — лучшее тогда
высшее техническое учебное
заведение России. Лучшее и по
помещениям, и по богатству
оборудования, и по методике
преподавания, и по
первоклассному составу профессоров и
преподавателей. Назову лишь
несколько имен ученых, чьи
лекции я имел счастье слушать:
Н. С. Курнаков, В. А. Кистяков-
ский, А. Ф. Иоффе, Ф. Ю. Ле-
винсон-Лессинг, В. Л. Кирпичев,
A. А. Байков, М. А. Павлов,
B. Е. Грум-Гржимайло. Имена,
не требующие пояснений...
Борис Николаевич
Меншуткин с 1907 года заведовал в
Институте кафедрой
аналитической и органической химии, а с
1922 года кафедрой общей хи-
Объ эф^ратахъ
бпмшо я щмт итк
«имгефнри V. V *■"--<!»:■:*. !■>*»-<. i л, W ft.
193? I
мии. Его лекции посещались
очень усердно (при
существовавшей тогда предметной
системе посещение лекций было
необязательным). Студентов
привлекало спокойное,
неторопливое изложение, позволявшее
вести запись лекций, простота и
ясность объяснений. Лектор
имел обыкновение сообщать
студентам о новых открытиях,
еще не вошедших ни в один
учебник. Меншуткин обладал
обширной эрудицией и
превосходной памятью. Тем не менее
он тщательно готовился к
лекциям, составлял к ним
конспекты. Он дополнил рядом новых
опытов великолепный подбор
лекционных опытов по общей
химии, сделанный Н. С. Курна-
ковым. Благодаря стараниям
Меншуткина, были
изготовлены многочисленные стенные
таблицы и чертежи,
иллюстрирующие новейшие теории
строения материи, периодический
закон, новые производства. На
эту работу часто не хватало
Б. Н* Меншуткин*..
•' - ' чтщягк** '""—с—
0 1ШЯНШ ЗАМЗДТЛТШЙ
DA НЪКОТШШ РВАЮЦИ
БЕНЗО/ТА
И [ГО ЗШЩЕНШ ЯГОШДМУХЪ
*%*-
mz ]
средств, и тогда Борис
Николаевич собственноручно исправлял
таблицы и делал новые.
Он приходил в аудиторию
за 15—20 минут до звонка,
осматривал выставленные
приборы, препараты и чертежи,
заглядывая в свой конспект.
Лекции читал спокойно, не
торопясь, не прибегая к каким-либо
театральным приемам. Много
внимания он уделял истории
основных понятий и законов
химии, излагал науку в ее
развитии, а не как окаменелую
догму.
Борис Николаевич был
человеком высокой культуры —
свободно владел французским,
немецким, английским
языками, хорошо знал латинский и
древнегреческий, был прекрасно
знаком с отечественной и с
западной литературой и, конечно,
особенно с историей.
В кругах ленинградских
химиков Меншуткин слыл
отшельником и даже
«подвижником». Действительно, он вел
36
Б. И. Меншутктгь.
м. в. ломоносовъ
КАКЪ ФИЗИКО-ХИКИКЪ.
иъ истоми
ХИМШ въ РОСС1И.
Отд»д»мгЯ «туи***.
шъ.ИдеЬстЮ С.-П««р^Грг«)(вго Политехнически-* И«:т*пут««-
~<*2Ш--
С-ПСТЕРВУРГ-К
? Мнхайло ВасилЬевичЪ
• ЛОМОНОСОНЪ.
АКАДЕМИЯ Н A v а СССР
Б.Н. МЕНШУТКИН
ЖИЗНЕОПИСАНИЕ
МИХАИЛА ВАСИЛЬЕВИЧА
ЛОМОНОСОВА
»9» I-
акадским наук ссСр
носкви — ажяинград
(«О
строго размеренный,
уединенный образ жизни, вставал в
шесть часов утра и сразу же
садился за работу. Лекции он
обычно читал с 9 до 11 часов, а
остальное время дня проводил
частью дома за письменным
столом, частью за исполнением
обязанностей по кафедре. В
десять часов вечера он ложился
спать. Своей семьи у него
никогда не было.
Борис Николаевич —
человек удивительно сдержанный и
деликатный — не переносил
небрежности в терминологии. За
правильность и чистоту
научного языка он боролся неустанно.
Он доказывал ошибочность
таких распространенных
терминов, как «галоид», «металлоид»
и предлагал другие
определения: «галоген» и «неметалл».
Его буквально выводили из
себя некоторые выражения,
каким-то образом укоренившиеся
в учебной и научной
литературе. Он не мог понять, почему
стали говорить и даже писать
«замещение водорода на хлор»
вместо «замещение водорода
хлором», как всегда писали
Менделеев и Бутлеров.
Неизменно он поправлял тех, кто
называл «число молекул»
«количеством молекул» или
употреблял слово «цифра» вместо
«число». Он протестовал против
смешения терминов «натр»
(окись натрия) и «натрий»
(металл), «кали» (окись калия) и
«калий» (металл) и всегда
подчеркивал, что надо говорить
«едкий натр», «едкое кали», а
не «едкий натрий» и «едкий
калий», так как металлы
едкими не бывают.
Моя судьба сложилась так,
что в молодые годы я работал
сначала лекционным
ассистентом у Н. С. Курнакова, а потом,
когда Курнаков отказался от
чтения лекций по общей
химии, я в течение восьми лет
ассистировал на лекциях Б. Н.
Меншуткина. И у своих
сотрудников он тоже старался
выработать придирчивое и строгое
отношение к литературному и
научному языку, развивал
наше историческое чувство. Борис
Николаевич живо ощущал
незримые нити, связывающие нас
с прошлым.
Однажды в беседе со мной
он сказал: «До чего коротка
человеческая жизнь! Ведь нас
отделяют от Лавуазье всего
несколько поколений, и мы с
вами его прямые потомки, как
химики». Он пояснил свою
мысль: «Вы учились у меня, я
учился у моего отца, ученика
Воскресенского, который был
учеником Либиха. Либих
учился у Гей-Люссака, ученика Бер-
толле, который был одним из
соратников Лавуазье».
Так вечно вьется нить
жизни, так от поколения к
поколению передается эстафета
научной мысли.
С. А. ПОГОДИН
37
НАУКА О ЖИВОМ
ПО СИГНАЛУ
КРАСНОГО СВЕТА
Кандидат биологических наук
А. Г. ЛОМАГИН
Ботанический институт АН СССР
Видимый спектр солнечного
света охватывает длины волн
от 400 до 700 миллимикронов.
400 миллимикронов — это
пограничная линия между
невидимыми ультрафиолетовыми
лучами и видимыми —
фиолетовыми и синими, 700
миллимикронов — граница между
видимыми красными и
невидимыми инфракрасными. Лучи
этих пограничных областей
спектра, как бы соревнуясь
между собой, оказывают на
живые организмы сильное и
часто прямо противоположное
влияние.
СИНИЕ — ПРОТИВ
УЛЬТРАФИОЛЕТОВЫХ
Уже давно известно, что
ультрафиолетовые лучи в больших
дозах оказывают губительное
действие на все живое.
Солнечные ожоги на спине
неосторожного курортника и
обеззараживание хирургических
инструментов ультрафиолетовыми
светильниками — вот разные
проявления этого действия. Точно
так же влияет ультрафиолет и
на растения. Но недавно было
обнаружено, что это вредное
действие ультрафиолетовых
лучей можно полностью
предотвратить, если после облучения
ими осветить организм синим
светом.
Правда, большинство живых
организмов, поврежденных
ультрафиолетом, синие лучи могут
спасти только в том случае,
если будут даны не позднее чем
через 1—2 часа после
ультрафиолетового облучения.
Единственное исключение
составляют растения: они сохраняют
способность вылечиваться
синим светом от
«ультрафиолетовой болезни» по крайней мере
в течение суток.
Оказалось, что
ультрафиолетовое облучение вызывает в
веществах живой клетки
образование новых химических
связей. В частности, такие связи
появляются и в молекуле
«вещества жизни» — ДНК: они
«сшивают» между собой
молекулы одного из нуклеотидов
ДНК тимина. Такие молекулы
ДНК с «пришитыми» друг к
другу нуклеотидами не могут
больше нормально
функционировать, и клетка гибнет. Но если
вовремя успеть облучить ее
синим светом, то под его
влиянием, как выяснилось,
образуется особый фермент, который
разрывает лишние связи между
парами тиминов, освобождает
«скованные» ультрафиолетом
молекулы ДНК и возвращает
клетке жизнь.
КРАСНЫЕ — ПРОТИВ
ИНФРАКРАСНЫХ
Если теперь обратиться к
другому концу видимого спектра —
длинноволновому, то и здесь мы
обнаружим конфликт между
видимыми и невидимыми
лучами — на этот раз между
красными и инфракрасными.
Около 15 лет назад группа
американских ученых детально
исследовала влияние красных и
инфракрасных лучей на
растения.
Было известно, что семена
некоторых видов растений
(табака, наперстянки, салата)
лучше прорастают на свету.
Ученые установили, что дружнее
всего такие семена прорастают,
если их осветить красным
светом с длиной волны около
650 миллимикронов. Реакция
семян на красный свет оказалась
поразительно быстрой:
вспышка продолжительностью всего
0,001 секунды уже резко
увеличивает процент проросших
семян. Но самым интересным
оказалось то, что невидимые
соседи красных лучей из
инфракрасной области спектра
сводят на нет их чудесное
действие: если семена салата
облучить сначала красными, а затем
инфракрасными лучами с
длиной волны около 730
миллимикронов, то семена прорастать не
будут. Но они все-таки
прорастут, если их еще раз осветить
красным светом. Облучение
красными и инфракрасными
лучами можно чередовать много
раз — результат будет зависеть
лишь от того, какой свет был
последним.
38
КРАСНЫЕ ЛУЧИ 654VtMK
ШШ ^4 Ши U |4-И
i(H4>PAкрасные луги730*»к
гшгтШлтгш
КРАСНЫЕ АУЧИ
UHlHWUiUUUT
^
•^2?
ИНФРАКРАСНЫЕ ЛУЧИ
Красные и ближние
инфракрасные лучи по-разному
действуют не только на
прорастающие семена. Давно известно,
что существуют две группы
растений: короткодневные и
длиннодневные. Первые
(например, соя, просо, молочай) могут
цвести только при коротком
дне и длинной ночи; вторые
(клевер, белена, подорожник),
наоборот, зацветают только при
длинном дне. Одно из самых
удобных для исследования ко-
роткодневных растений — так
называемый дурнишник
пенсильванский: ему для начала
цветения достаточно всего
одного 12-часового дня и одной
12-часовой ночи. И вот когда
ученые исследовали условия
зацветания дурнишника, снова
обнаружилось магическое
действие красного света с той же
длиной волны — 650
миллимикронов. Если темный период
суток прерывался всего
двухминутным освещением красным
светом, то дурнишник
отказывался цвести, как будто
длинной ночи и не было.
И снова ближние
инфракрасные лучи оказались
способными полностью
ликвидировать действие своих
видимых соседей по спектру:
дурнишник, получавший ночью
вслед за красным
двухминутное инфракрасное облучение,
совершенно «забывал» о
красном сигнале и цвел как ни в
чем не бывало. И вновь было
установлено, что при
многократном чередовании красных
и инфракрасных лучей
дурнишник слушается лишь
последнего «приказания».
Получается, что
кратковременное освещение красным
светом превращает для коротко-
дневных растений ночь в день
и тормозит их цветение. Для
длиннодневных растений
красный свет, наоборот,
способствует зацветанию, если, конечно,
за ним по пятам не следуют
инфракрасные лучи.
Удивительные превращения,
вызываемые красными и
ближними инфракрасными лучами,
заинтересовали многих
исследователей из разных стран.
Сейчас почти в каждом научном
журнале по физиологии
растений, на каком бы языке он ни
издавался, можно найти статьи
на эту тему. Сообщаются все
новые и новые данные о
влиянии красных и инфракрасных
лучей на самые различные
жизненные процессы у
растений — и почти всегда
обнаруживается непримиримая
конкуренция между ними. Красный
свет ускоряет рост листьев,
вызывает движение хлоропластов
в клетках по направлению к
источнику света, способствует
образованию красящего
вещества — антоциана в листьях
красной капусты. Во всех этих
случаях последующее
облучение инфракрасными лучами
бесследно уничтожает влияние
красных.
В свою очередь
инфракрасные лучи способствуют росту
стеблей у некоторых растений,
а красные лучи, не оставаясь в
долгу, ликвидируют действие
инфракрасных. И длины
конкурирующих волн всегда
составляют примерно 650 и
730 миллимикронов. Чем же
объяснить это поразительное
явление?
ОТКРЫТИЕ ФИТОХРОМА
В 1956 г. биологи С. Хендрикс,
Г. Бортвик и Р. Дауне
предположили, что в растительных
клетках содержится особое
вещество, которое может
существовать в двух формах —А и Б.
Форма А поглощает красные
лучи и при освещении ими
переходит в форму Б, а та в свою
очередь поглощает
инфракрасный свет и под его влиянием
может снова перейти в
форму А.
Если такие вещества
существуют, то загадочное влияние
30
^рлскмЛ сев^
красного и инфракрасного
света на прорастающие семена
можно объяснить так.
Вещество А как бы запирает на ключ
первое звено процессов,
ведущих к прорастанию. Если же
облучить семена красным
светом, то вещество А переходит
в вещество Б, и «замок»,
мешающий прорастанию,
отпирается. А облучение
инфракрасным светом снова запирает
этот «замок», так как вновь
образуется вещество А. Правда,
это возможно лишь до тех пор,
пока начавшийся процесс
прорастания не успеет зайти
слишком далеко. В самом деле:
эксперименты показали, что
инфракрасный свет может
ликвидировать действие красного
лишь в том случае, если
облучение им следует не позже чем
через 30 минут.
Совершенно так же
объясняются и все остальные случаи
противоположного влияния
красных и ближних инфракрас~
ных лучей на растения.
Гипотеза Хендрикса, Борт-
вика и Даунса блестяще
подтвердилась. Наличие вещества,
меняющего свой спектр
поглощения после облучения
красным или инфракрасным
светом, — его назвали фитохро-
мом — было констатировано в
тканях различных растений.
Спектр поглощения фитохрома
менялся именно так, как того
требовала гипотеза. Наконец, в
1959 г. фитохром был впервые
выделен из растений, а в самое
последнее время удалось
тщательно очистить его и изучить
ряд его особенностей.
Способность менять свой
спектр поглощения под
влиянием красных и инфракрасных
лучей фитохром сохраняет и в
пробирке. Но при изменении
спектра поглощения должен
меняться и цвет раствора
фитохрома. Так и происходит в
действительности: после
освещения инфракрасным светом
раствор фитохрома
зелено-голубой, а после освещения
красным светом — светло-зеленый.
Фитохром оказался белком.
В форма А он значительно
устойчивее к высокой
температуре и другим физическим и
химическим агентам,
разрушающим с* руктуру белков, чем в
форме Б. Это обстоятельство
очень важно: оно говорит о том,
что при превращениях,
вызываемых красными и
инфракрасными лучами,
конфигурация молекул фитохрома
существенно изменяется. Возможно,
именно этими изменениями и
объясняется различное влияние
форм А и Б на процессы роста
и развития растений.
Многое еще предстоит
выяснить. Неизвестно, как
фитохром взаимодействует с
ростовыми гормонами; неясно,
какова природа реакций,
вызываемых им... Однако то, что уже
сделано, заставляет думать, что
в недалеком будущем и эта до
сих пор загадочная сторона
жизни растений попадет под
контроль человека.
Рисунки и вклейка
КХ ВАЩЕНКО
40
"■650ммк
730 ммк
^ Ь50нм*» —
400 ммк
>45
' k Л » ■ * ft
400 ммк
., верным садовником, лелеявшим и
растившим могучее дерево красочной промышленности.
1\Квро
/1968%
АВГУСТ
ВИЛЬГЕЛЬМ
ГОФМАН
Член-корреспондент
Международной Академии
истории наук
Ю. С. МУСАБЕКОВ
Немецкий химик Август Вильгельм
Гофман родился 8 апреля 1818 года в Гиссене,
в семье архитектора. В детстве он много
разъезжал с отцом по Франции и Италии;
в 1836 году поступил на факультет права
в Гиссенский университет. Его привлекали
и естественные науки, но только
прослушав курс лекций прославленного химика
Юстуса Либиха, он понял, что посвятит
себя химии. Первое самостоятельное
исследование Гофмана посвящено анилину.
В 1841 году он защищает докторскую
диссертацию, через два года она выходит в
«Анналах», редактируемых Ю. Либихом,
под названием «Химическое исследование
оснований каменноугольной смолы».
В 1843 году Гофман становится
ассистентом Либиха, а еще через два года его
утверждают приват-доцентом Боннского
университета. Но неожиданно
обстоятельства резко меняются... Молодой ученый
получает приглашение от английского
принца Альберта (учившегося в молодости
в Гиссене) переехать в Лондон, чтобы
наладить там преподавание химии в духе
либиховских методов (лабораторно-иссле-
довательской системы преподавания).
Гофман соглашается приехать на два года;
в Лондоне он становится главой
Лондонского Королевского химического
колледжа. Вокруг него создается большая
научная школа. В числе учеников Гофмана -
известные химики Ф. Абель, Ч. Манс-
фельд, У. Крукс, П. Грисс.
Пребывание в .Англии затянулось:
Гофман прожил там двадцать лет. К нему
часто приезжали на консультации химики
из разных стран. В этот период выходит
из печати капитальная работа Гофмана —
«Вклад в познание летучих органических
оснований». Он продолжает свои
исследования аммиака и аминов. В 1858 году
действием четыреххлористого углерода на
анилин он получает красный краситель
(за два года до этого впервые полученный
польским ученым Я. Натансоном, а годом
позже повторно синтезированный
французом Э. Бергеном и названный им
фуксином). Он выясняет природу «парижской
сини», синтезирует «фиолетовую
Гофмана» и целый ряд этил- и метилпроизвод-
ных розанилина, поражающих красотой и
разнообразием оттенков — от
красноватого до сине-фиолетового. Затем он
устанавливает состав «голубых анилинов».
Уже на Лондонской выставке 1862 года
синтетические красители, найденные
Гофманом, вызывают всеобщий восторг.
Благодаря его работам химия синтетических
красителей, окрещенных анилиновыми,
находит широкую дорогу в
промышленность.
6 Химия и Жизнь, № 12
-И
А. В. Гофман в двадцатиеось- Справа — созданная Гофманом Внизу — молекулярные модели.
милетнем возрасте химическая лаборатория Вер- простейших органических ее-
линского университета в год ее ществ, изготовленные Гофма-
открытия A869) ном в Англии
% I
bfr IWt«fbrn $brm\$rhtn i*
Метан
Хлористый
метил
Метанол
Метиламин Этан
42
Гофман в своей лаборатории в
Берлине в 1870 году
В 1864 году Гофман возвращается в
Германию. Он получает кафедру химии
в Боннском университете, создает
собственную лабораторию и работает здесь весь
последний период своей жизни. По
отзывам современников, Гофман был
превосходным педагогом, его лекции были
безукоризненны по содержанию и форме; он
сопровождал их оригинальными опытами,
которые придумывал сам. Он создал
несколько удобных установок, которые
охотно используются в химических
лабораториях и сейчас: так называемый
«аппарат Гофмана» для демонстрации
объемных соотношений в реакциях газов,
прибор для определения плотностей паров
и другие.
В 1868 году Гофман вместе с Байером
и Мартиусом основал Немецкое
химическое общество. Его четырнадцать раз
избирали президентом общества; им же
был основан журнал «Berichte der deut-
schen chemischen Gesellschaft» — и сейчас
одно из авторитетнейших изданий по
химии. Всего им было опубликовано около
трехсот оригинальных статей и докладов,
а также несколько книг, в их числе
знаменитое «Введение к изучению современной
химии», а также интересные труды по
истории науки. Гофман выпустил книгу
очерков «Берлинские алхимики и
химики», собрание воспоминаний (в трех томах)
«Памяти ушедших друзей»,
жизнеописания Иоганна Кункеля, открывшего способ
изготовления рубинового стекла,
Фридриха Гофмана, изобретшего «гофмановские
капли» и первую искусственную
минеральную воду, медика И. Эллера,
керамиста И. Лотта и многих других.
Исторические этюды для Гофмана были одним
из средств самовыражения. Историю
науки он «пропускал через биографии»,
одновременно приобщая читателей к научным
спорам.
Но, конечно, создание промышленности
искусственных красителей было главным
делом его жизни. В 1871 году Гофман
вместе с К. Мартиусом открыл
интересную реакцию перегруппировки жирно-
ароматических аминов: из метиланилина
был получен изомерный ему толуидин.
Гофман показал, что при действии на
первичные амины хлороформа и щелочи
образуются изонитрилы, которые он
считал производными синильной
кислоты. «Получаясь путем чрезвычайно
своеобразного процесса образования, — писал
Гофман, — обладая совершенно
неожиданными свойствами, стабильные при одних
условиях, изменчивые при других,
отличаясь такой многообразной способностью
к реакциям, о которых нельзя было и
думать, — эти тела соединяют в себе все
условия, которые влекут к широкой
работе».
По выражению современника ученого,
Генриха Каро, Гофман был «верным
садовником, лелеявшим и растившим
могучее дерево красочной промышленности,
пока оно было еще слабым и хрупким
ростком».
Фотографии из фондов Сенатской комиссии по
изучению истории Берлинского университета
им. Гумбольдта присланы ассистентом Института
истории медицины и естествознания (ГДР)
К. ХАЙНИГОМ
6*
4:3
Что вы знаете
и чего не знаете
о красителях
Красители растительного и
животного происхождения испокон века
использовались человеком.
«Король красителей» — синее
индиго — был весьма популярен еще
в древности. Индиго добывали из
кустарника индигоноска (Indigofe-
га), распространенного в Индии, на
острове Ява и в Натале (Южная
Африка). Ализарин вырабатывали
из марены; с его помощью
окрашивали ткани в различнее
цвета — цвет зависел от
использованной протравы (средства для
укрепления красителя на волокне). Из
кошенили — высушенных
насекомых — делали кармин. Но более
всех из античных красок славился
пурпур, который добывали из
мельчайших моллюсков —
багрянок. Багрянки обитают в теплых
морях. Чтобы добыть один грамм
пурпура, приходилось
перерабатывать до восьми тысяч
моллюсков. Стоил пурпур дороже
золота... В древнем Риме плебея,
осмелившегося надеть платье,
окрашенное в пурпурный цвет, за
дерзость казнили. В виде особого
отличия знаменитому оратору
древности Цицерону было
разрешено облачаться в тогу, дважды
выкрашенную в пурпуре.
До конца 80-х годов XIX века
ученые разных стран тщетно пытались
найти искусственный заменитель
индиго. Император Наполеон
объявил даже конкурс на
удачный заменитель, обещав
победителю премию в размере
миллиона франков... Но конкурс не дал
результатов: природа красителей
была еще не познана, не было
предпосылок и для химического
синтеза.
В 1845 году Август Вильгельм
Гофман обнаружил в каменноугольной
смоле бензол — бесцветную
жидкость с характерным запахом,
удельным весом 0,88 и
температурой кипения 80,1 СС. Открыт был
бензол в 1825 году известным
английским физиком Майклом Фа-
радеем, который обнаружил эту
летучую жидкость среди
продуктов конденсации в газовых
баллонах, использовавшихся в Лондоне
для газового освещения.
Ученик Гофмана Ч. Мансфельд в
1854 году приступил к
технической выработке бензола как
продукта коксохимии. По несчастью
ом стал первой жертвой новой
отрасли техники: приготовляя
большее, чем обычно, количество
бензола — для Промышленной
выставки в Париже — он случайно
перегрел реторту при перегонке.
Вырвалась струя жидкости,
мгновенно воспламенившаяся. Ученый
получил сильные ожоги и через
несколько дней скончался в
больнице.
Немецкий ученый А. Кекуле в
1865 году установил формулу
строения бензола и других
ароматических соединений. Это был
очень важный этап в биографии
бензола: предложенные Кекуле
формулы легли в основу
дальнейших разработок. Выглядели они
так:
сн»
СН3
I
сн3
/\ /Ч
II I II I II
бензол толуол орто-ксилол
СН*
сня
II )
сн3
мета-ксилол
и
I
пара-ксилол
В 1840 году русский химик
Ю. Ф. Фрицше выделил из
продуктов разложения индиго амино-
бензол, или анилин, — почти
бесцветную, темнеющую на воздухе
жидкость с неприятным запахом,
кипящую при температуре 184°С.
44
Он и дал открытому им веществу
название «анилин» (от арабского
«анил» — ссиндиго»). Двумя
годами позже известный русский
химик Н. Н. Зинин получил это же
вещество, названное им «бензида-
мом», при восстановлении
нитробензола. Гофман писал позже:
«Если бы Зинин не сделал ничего
более, кроме превращения
нитробензола в анилин, то и тогда бы
его имя осталось записанным
золотыми буквами в историю
химии!»
Анилин и его гомологи —
ароматические амины — стали
исходными продуктами в производстве
многочисленных искусственных
красителей, а также лекарственных
соединений и некоторых
химически активных веществ для
полимеров.
Вот формулы наиболее широко
применяемых ароматических
аминов:
NH,
I
/X
II I
анилин
СН3 СИ,
I NH8 |
/N/ /\
II I II I
толундшии
N (СН,),
I
"Л
II I
Ч/
ДИМСТИЛсШИЛНН
СН3
I
/ч
II I
i
NH,
I
II I
NH„
NH2
I
II I
NH.
NH2
A
I
NH,
фенилендпампны
H=N-\_/
бензидин
—NH»
В 1842 году Н. К. Зинин нашел
важнейшую общую реакцию
восстановления ароматических нитросое-
динений в амины:
CeH5NOa + «Ш -> C6H5NII2 4 Urf).
Эта реакция указала путь к
дешевому получению анилина и его
аналогов — основного сырья, из
которого синтезируют
многочисленные красители. Гофман — об
открытии Зинина: «Никто не мог
представить себе и во сне, что
новому методу амидирования
суждено будет послужить
основою могучей заводской
промышленности, которая в свою очередь
даст совершенно неожиданный и
плодотворный толчок науке».
Усовершенствование метода
Зинина шло преимущественно в
направлении выбора все более
целесообразных и дешевых
восстановителей.
В 1850 году А. В. Гофман
открыл универсальную реакцию
получения первичных, вторичных и
третичных аминов и четвертичных
аммониевых производных
последовательным замещением водо-
родов аммиака алкильными или
арильными радикалами. Схему
реакции можно изобразить так:
получает мовеин — краситель
красновато-фиолетового цвета.
Оба открытия сделаны без
предварительного знакомства с
теорией, «в темную».
В 1861 году замечательный
русский химик А. М. Бутлеров создал
теорию строения органических
соединений, ставшую основой
всей органической химии. Новая
теория позволила превратить хи-
NH3 f CH3J -> [CH3NH3] J
NH,
— NH,J
CH3J + -
>CH3NH2—-> [(CH3JNH2]J->
NIL
CHJ
первичный амин
NH;i
+-
Z^T-y (CH3JNH > [(CH3KNH] J __*-> (CH3KN --> (CH3LN J
вторичный амин третичный амин
В 1856 году получены два первых
синтетических красителя.
Польский химик Я. Натансон,
работавший в то время в Юрьеве (ныне
Тарту Эстонской ССР), нагревая
анилин и дихлорэтан, получает
красный краситель, хорошо
окрашивающий шелк и шерсть. Позже
этот краситель стал известен под
названием фуксина. Английский
химик У. Перкин, окисляя анилин,
мию красителей и их синтез в
планомерно развивающуюся
область науки и производства.
Рисунки и вклейка
Р. ВАРШАМОВА
45
ИЗ ПИСЕМ В РЕДАКЦИЮ ИЗ ПИСЕМ В РЕДАКЦИЮ ИЗ ПИСЕМ В РЕДАКЦИЮ ИЗ ПИСЕМ
■ ПОЧЕМУ ЧИТАЮТ
«химию и жизнь»
В сентябрьском номере журнала
«Химия и жизнь» были
опубликованы итоги заочной читательской
конференции 1968 года. Конечно,
приятно, что редакция идет в
ногу со временем и пользуется в
своей работе не только пером,
клеем и ножницами, но и
вычислительной техникой.
Однако меня (да, наверное, и
не только меня) удивило, что
сводная таблица не была
сопровождена никакими
комментариями. Поэтому я взял на себя
смелость эту таблицу
проанализировать.
Тематику журнала в целом
можно разбить на три большие
части. Первая — это чисто
практические сведения (помощь в
работе, помощь в учебе, полезные
сведения для дома); вторая —
информирующая (удовлетворение
любознательности); третья —
развлекательная (занимательный
досуг). В соответствии с этим ваша
анкета показала, что в журнале
должно быть 56,1 % материалов
полезных, 27,8% — интересных и
16,1 % — развлекательных. Иначе
говоря, читатели журнала «Химия
и жизнь» ждут от него в первую
очередь не развлекательных, а
деловых сведений.
Чем это можно объяснить?
Ответ на этот вопрос дает, мне
кажется, графа «образование». Дпя
наглядности я составил график,
на котором по оси абсцисс
отложил условный возраст читателей
соответствующей группы
(школьники -~14 лет, лица со средним
образованием ^ 18 лет,
студенты .—'20 лет, лица с высшим
образованием -—' 23 года,
аспиранты .—< 25 лет, лица с ученой
степенью^—'30 лет; за крайние точки
приняты новорожденные и
академики — они ведь, наверное,
совсем не читают
научно-популярных журналов).
В целом получилась кривая
нормального распределения — от
новорожденного (разумеется,
кривая на участке 0—14 лет не
реализуется: химию начинают
изучать лишь после седьмого класса)
до академика с максимумом на
чгЛ
читателях, имеющих высшее
образование. Но если отделить
химиков от нехимиков, то получатся
две кривые: с одним и с двумя
максимумами соответственно.
Теперь видно, что число читателей-
химиков изменяется закономерно
и достигает максимума для лиц
с высшим образованием; а вот
почему другая кривая
двугорбая, — вроде бы непонятно.
Мне кажется, что вторая
кривая характеризует изменение
интересов человека по мере его
продвижения по жизненному
пути. Совершенно понятно
обостренное внимание к журналу у
читателей со средним
образованием, собирающихся поступать в
нехимический институт: они не
пренебрегают никакой
информацией, которая им могла бы в этом
помочь. Но добившись своего,
читатель-нехимик перестает
интересоваться €<пустяками» и с
головой уходит в учебу. Окончив же
институт, он вновь оказывается на
перепутье: ограничиться
достигнутым или учиться дальше? И вновь
резкое повышение внимания к
журналу. А вот, поступив в
аспирантуру и защитив кандидатскую
диссертацию, человек уже стойко
теряет интерес к популярной
литературе. (Эту же мысль
подтверждает и плавный характер первой
кривой: для студента-химика
важно все время интересоваться
избранной специальностью.)
Все это, по-моему, и
объясняет преимущественно утилитарные
устремления читателей,
приславших в редакцию ответы на
вопросы анкеты.
Е. В.
SO J4*r\
-и;
Победительнице «Конкурса на
конкурс» ученице X класса
школы JVo 5 города Шауляй —
Мейлуте НИСТЕЛИТЕ вручен
приз — портативная пишущая
машинка. Пока Мейлуте
печатает, конечно, только одним
пальцем. Ничего, все еще
впереди...
А условия нового конкурса,
предложенного
победительницей, публикуются на этой же
^странице.
Фото Д. РУЧИНСКАСА
КОНКУРС 1969 ГОДА
«Если бы я был редактором
журнала «Химия и жизнь»
КАЖДЫЙ УЧАСТНИК КОНКУРСА должен
составить макет номера журнала «Химия и
жизнь» из опубликованных в нем в 1968 году
очерков, статей, корреспонденции и
заметок, которые он считает лучшими.
Следует помнить, что у каждого номера
:журнала есть иллюстрированная обложка
из четырех страниц; участник конкурса
должен выбрать лучшие четыре страницы
обложек, опубликованных в 1968 году. Текст
статей и заметок, рисунки и фотографии,
которые печатаются в журнале, должны
занимать в составляемом номере 96
страниц— столько, сколько содержится в
каждом номере «Химии и жизни». Одну из
страниц журнала следует отвести для
оглавления. При составлении номера желательно
не забывать, что его читают люди разного
возраста, разных интересов. Чтобы читатель
мог легче найти материал на интересующую
его тему, статьи и иллюстрации желательно
группировать по рубрикам. Можно
использовать традиционные рубрики журнала,
либо придумать новые.
КАК ДЕЛАЮТ МАКЕТ ЖУРНАЛА? В конце
этого номера «Химии и жизни», как и всегда
в последнем номере года, опубликован
перечень всех материалов, напечатанных в
журнале в 1968 году. На этот раз перед
каждым названием стоит порядковый номер —
его-то и можно использовать при
составлении макета. Сам макет тоже напечатан —
на следующих двух полосах журнала. Его
нужно вынуть из номера и заполнить,
указав для всех полос (так в полиграфии
называется каждая страница готовящегося
издания) порядковый номер помещаемых вами
статей и заметок.
ПОМНИТЕ: НИКАКОЕ ТВОРЧЕСТВО НЕ
ВОЗБРАНЯЕТСЯ! Редакция будет рада
получить не только заполненные таблицы, но
и познакомиться с макетами, которые
участники конкурса изготовят в натуральную
величину журнала, а также с любыми
мнениями, пожеланиями, предложениями.
Словом, с тем, «что бы вы сделали, если
бы были редактором журнала «Химия и
жизнь»...
КТО ПОБЕДИТ? Читатель, составивший
самый интересный по содержанию и
оформлению макет номера.
Трем победителям конкурса будут
присуждены ТРИ ПРИЗА — ТВОРЧЕСКИЕ
КОМАНДИРОВКИ за счет журнала.
Все материалы на конкурс надо выслать
в редакцию НЕ ПОЗДНЕЕ 30 АПРЕЛЯ
1969 года.
Результаты конкурса будут
опубликованы в № 9 «Химии и жизни» 1969 года.
Редакция
47
обложка
и
4j
обложка
|_2
з|
вклейка
[1
2\
1
2
7
8
13
14
19
20
25
26
31
32
37 .
38
[43
44
3
4
9
10
15
16
21
22
27
28
33
34
39
40
[45
46
5
6 1
11
12 |
17
18 |
23
24 J
29
30 J
35
36 |
^^■^^*^~^^^^^^^^ / 1
41
1 42
|_47
48J
49
50
| 55
56
1 61
62
67
68
73
74
79
80
85
86
1 91
| 92_
51
52
57
58
63
64
6b
70
75
76
81
82
87
88
93
9^
53
54 J
59
60 1
65
66 J
71
72 1
77
78 J
83
84 1
89
90 1
95
96 1
Место склейки
Место
ДЛЯ
марки
МОСКВА, В-333,
ЛЕНИНСКИЙ ПРОСПЕКТ, ДОМ 61
Редакция журнала «ХИМИЯ И ЖИЗНЬ»
На конкурс 1969 года
Отправитель:
фамилия, имя, отчество
профессия
адрес
Место сгиба ■
► Страницы макета нужно
► аккуратно вынуть
[ из номера журнала.
\ Заполненный макет
► сложить и отправить в редакцию.
эМ Место склейки
Б статье М.В.Волькен1тейна иНе нуждаясь в мистичесних
санкциях" , опубликованной в К» 9 нашего журнала," было рассназано' о'
квартире Д.И.Менделеева, сохраненной по сей день в старинном
здании Ленинградского университета. Сейчас там находятся
музей и архив замечательного ученого.
Предлагаем нашим читателям совершить маленьную энсвурсию в
архив Менделеева. С некоторыми хранящимися в нем довументами
вас познакомит директор музея-архива, кандидат химических
наук Александр Александрович МАКАРЕНЯ.
«ЛЮБИМОЕ ДИТЯ МОЕ,
МОЙ ОБРАЗ,
МОИ ОПЫТ...»
Маленькая экскурсия
в Менделеевский архив
— Среди многих материалов, которые
хранятся в нашем архиве, есть связка
документов. На первом листе этой связки
рукой Дмитрия Ивановича Менделеева
написано: «Счеты Общественной] Пользы
и вообще бумаги 1-го издания Основы
химии. Спря[тал] Сентяб[ре] 1872».
— «Общественная польза» — акционерное
издательство, которое в 60—70 годах
прошлого века выпускало в Петербурге
научную и учебную литературу (в его
типографии печатался, например, «Журнал
Русского физико-химического общества»).
Здесь были впервые изданы многие труды
Д. И. Менделеева, и с 1868 года в
«Общественной пользе» отдельными выпусками
стали выходить в свет знаменитые
«Основы химии».
«Эти Основы химии — любимое дитя
мое. В них мой образ, мой опыт педагога
и мои задушевные научные мысли», — так
писал о книге ее великий автор.
— Вот еще один документ из этой
связки — письмо А. М. Бутлерова:
«Казань. Октябрь, 10, 1868.
Милостивый Государь Дмитрий Иванович!
На днях получил письмо Ваше, а
сегодня принесли и объявление о книгах.
Сейчас посылаю на почту и с особенным
интересом приступлю к чтению, а между
тем спешу поблагодарить вас очень. Что
касается распространения Вашей книги
в здешнем Университете, то не
сомневаюсь, что с особенной пользой могу
рекомендовать ее слушателям, и постараюсь
сделать в этом отношении все зависящее
от меня...»
51
Записка Д. И. Менделеева на
связке материалов,
относящихся к «Основам химии»
Титульный лист первого
издания «Основ химии»
основы
CD- «Л^епЭеииг&е1?а,
профессора Я. Cat». Уткчусвти*.
о***£с^
ЧАСТЬ ПЕРВАЯ,
съ ?.51~всъ псмгатиявлекъ.
Вы, наверное, обратили внимание на слова
Бутлерова: «Что касается распространения
Вашей книги в здешнем Университете,..».
В те времена распространять книгу
должен был сам ученый — тираж просто
зависел от числа подписчиков. По просьбе
Менделеева его коллеги А. М. Бутлеров в
Казани, П. П. Алексеев — в Киеве,
А. Н. Попов—в Варшаве, Н. К Яцуко-
вич — в Харькове, Н. Э. Лясковский и
П. А. Григорьев — в Москве проводили
среди химиков и студентов подписку на
«Основы химии».
— Книгу Менделеева соотечественники
приняли с восторгом:
«Основы химии совершенно не похожи
на другие учебники. Подобного им
сочинения я не знаю за границей ни одного.
ч Замечательна, так сказать, целостность
изложения; переход от одного соединения
к другому совершенно естественный, а не
искусственный, как в большинстве
учебников, чрез что весьма облегчается чтение.
Кроме того, изложение не догматическое;
автор постоянно старается дать
объяснение, постоянно обращает внимание на ана-
52
Фотокопия письма Бутлерова
Пометки Менделеева на
титульном листе 4-го издания
~s0Ajj>Jfc /сН Яг*#
(hcsi^ ь^^/2^ии 'tisCvL^t^L* 'у&сшл*-., сО
*^ Itb-ts-Obt*' , **\ *-*<AJh&<s sTbiSA^ £фи*Г1ъ<*£
основы
X И M I II
/" U } &л
Д. М^НЛЕЛ-ЬЕВЛ,
&/*Ls
4-Е И8ДАЙ11
ГЛ
^IIETEFI
7,o
логии и т. п. Вообще в своем сочинении
Менделеев постоянно знакомит читателя
с научными приемами представляющихся
вопросов, научает думать, обсуждать, а не
принимать на веру, старается
заинтересовать наукой, выказать привлекательные
ее стороны», — так писал о книге
профессор П. П. Алексеев, возглавлявший
кафедру химии в Киевском
университете.
А десять лет спустя, в 1879 году,
представляя Менделеева в адъюнкты
Петербургской академии наук, академики
Н. Н. Зинин, О. И. Сомов, А. Н. Савич и
А. М. Бутлеров заявили:
«Можно утверждать, что «Основы
химии» представляют курс, подобного
которому не отыщется в заграничной
химической литературе».
— «Основам химии» наша экскурсия
посвящена не случайно. Первый выпуск
вышел в свет ровно сто лет назад — в
1868 году.
В 1869 году был издан второй выпуск,
содержавший знаменитый «Опыт систе-
53
вММШЕЛ Ш ft,
VOJ,
D- Mendeleje/r,
: are f-RpMiATA *£ acaoemia rohaka
CURS tXEMENTAR
V-y xi x i V JL J J—•
PESTRl) ' M : -И А-ГМ .МЖЁАТ
0* С Г 1STRATI
НАЧАЛЬНЫЙ МГСЪ
x и м ilI
/V []от«лииынА
«мдамю* л*»*
JuitM^^i^4^
'яЬлЛьЛг *Ж*£е^
и*'
~<^,
APHNTES
С CHEMISTRY
^oco»»|MOf
ОIT 1 М 1 С А. да°«с lAW
Dieter PEDP ч#* ^
**>
<**
fr*
^
**.
^
*<£-
^
^4
rV?
e^
GxV г
•*•
t#
><
ih " «^d£LeE№
V
*fA>ft-
A.fi,^.'
л'£^ш,
'aeriw«*«*4„
УЧЕБНИКЪ
flllECMf 11Щ
Wfe^«c
новъй&изгъ %'^^ншмъ,
и J**** ткра,
<?*Л
*€*#i4
■*-*£?'
ШЕСТОЕ, ИСПРАВЛЕНИЕ Я ДЭДО*Н£Ш>€ ИЗДАЙ*,
ti№
мы» — изложение великого открытия,
сделанного Менделеевым 1 марта 1869 года.
Эти два выпуска составили первый том.
У «Основ химии» была на редкость
счастливая судьба. Книга буквально
завладела умами естествоиспытателей. При
жизни Менделеева она выдержала восемь
изданий на русском языке. Дмитрий
Иванович тщательно работал над подготовкой
каждого издания. Сохранился том 4-го
издания «Основ» с любопытными
пометками Менделеева —это мысли,
касающиеся разных волновавших его вопросов:
«У нас главное—работа, а не знание,
не труд...
Нуж[на] эпоха — статистики, изучения,
исслед [ов аний].
Образование] долж[но] показать, что
же сделать из материала...»
Менделеева всегда очень волновали
проблемы отношения к исследовательской
работе, к накапливаемым фактам,
организации науки, положения ученого в царской
России. Именно осмыслению всех
накопленных химией знаний он посвятил свой
замечательный труд.
На этом же титульном листе есть и
заметка чисто химического плана:
«Соединения] С, N, Au, Ag, Hg непроч[ны],
а они сами очень»...
— «Основы химии» завоевали не
только Россию, но и весь ученый мир. Они
были переведены на английский,
немецкий и французский языки. В Англии
их издавали три раза еще при жизни
Менделеева. Отзывы английских химиков
полны восхищения.
Уильям Рамзай писал Менделееву
6 января 1892 года, тотчас после выхода
английского перевода «Основ химии»:
«Наконец-то я имею удовольствие прочесть
Вашу большую книгу («большую» во всех
отношениях), которую Вы любезно
прислали мне несколько лет назад на русском
языке. Я пытался время от времени читать
ее в оригинале, но, право, это было свыше
моих возможностей. Но превосходный
английский перевод, который только что
вышел, дает мне возможность отметить
то, что я уже знал, — Вашу и Ваших
сотрудников работу относительно объема —
упругости газов при очень малых
давлениях, опубликованную ранее...»
Джон Кнотт опубликовал в журнале
«Science and Art» рецензию:
«Мы не читали другой такой работы по
химии, которая бы давала столь четкое
представление о внутреннем строении
материи... Мы хотим выразить
благодарность... выдающемуся ученому, который,
вероятно, сделал больше, чем любой
человек его положения, для расширения
границ философии этой области физических
исследований, которым он посвятил всю
замечательную энергию своей жизни».
А чешский химик Богуслав Браунер
написал в 1902 году:
«На эту книгу я всегда смотрел как на
библию неорганических химиков».
— Когда говорят о той роли, которую
играли «Основы химии» в жизни мировой
науки, обычно упоминают только о том,
что книга издавалась и читалась на
разных языках во многих странах. А ведь
«Основы» сделались для химиков всего
мира эталоном при создании учебников и
руководств.
В 1874 году ученик Дмитрия
Ивановича В. Ю. Рихтер выпустил свой «Учебник
неорганической химии». Эта книга была
пронизана «менделеевским духом»,
насыщена идеями «Основ». Учебник Рихтера
выдержал 13 изданий на русском языке.
Столько же раз его издавали в
Германии— перевод на немецкий язык был
сделан самим автором. В 1883 году он был
переведен на английский язык, а еще год
спустя — на итальянский.
«Основы химии» были образцом, по
которому создавались учебники и
руководства А. Л. Потылицына, С. И.
Ковалевского, хорошо известный учебник для
средней школы В. Н. Верховского,
венгерский учебник Т. Кароли, румынский
К. Истрати, американские учебники
A. Ремзена, Ф. Венейбла и Л. Хоу.
И, наконец, последнее: замечательный
русский ученый академик А. А. Байков
писал в воспоминаниях, что он избрал
химию делом своей жизни именно под
влиянием менделеевских «Основ». Об этом же
рассказывали многие другие
известнейшие ученые. По этой книге учились
B. И. Вернадский, И. П. Павлов, В. Л.
Комаров, Н. Д. Зелинский, Н. Н. Семенов.
Книга, которой исполнилось сто лет,
по сей день освещает химикам путь, как
говорил Менделеев, «искания истины».
55
НОВОСТИ ОТОВСЮДУ НОВОСХИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ
НЕБЕСНЫЕ ДВОЙНИКИ
Согласно теории относительности,
луч света, пропутешествовав по
Вселенной миллиарды лет,
должен вернуться в исходную точку.
Это значит, что в принципе
каждое небесное тело мы должны
видеть дважды, в двух
противоположных точках небосвода...
Правда, излучение, обежав всю
Вселенную, должно стать крайне
слабым. Но можно надеяться, что
«двойников» наиболее ярких
радиозвезд все же удастся
обнаружить с помощью современных
радиотелескопов. Как пишет
журнал «New Scientist» A968, № 590),
изучение звездных каталогов
показало, что почти у каждой яркой
радиозвезды действительно есть
очень слабый «двойник». Остается
проверить, не простое ли это
совпадение...
СТАТИСТИКА И ПРОГНОЗЫ
Западногерманский журнал «Che-
mische Industrie» A968, № 3)
опубликовал статистические данные о
мировом потреблении каучука в
1967 году и прогнозы на будущее.
Предполагается, что к 1975 году
мировое потребление
синтетического каучука по сравнению с
1966 годом возрастет на 52—80%
и достигнет 6,5—7,7 миллиардов
тонн. Потребность в натуральном
каучуке возрастет на 7—30% и
достигнет 2,7—3,3 миллиардов
тонн. При этом использование
натурального каучука для шинной
промышленности будет
сокращаться почти повсеместно. Однако
за 10 месяцев 1967 года мировое
потребление каучука осталось на
уровне 1966 г. и составило около
6 миллиардов тонн. Стабильный
уровень потребления каучука в
капиталистическом мире
обусловлен экономическим спадом в
США, Великобритании, ФРГ и
повышенным спросом на каучук в
Японии, Италии, Франции и
некоторых других странах.
АМИНОКИСЛОТЫ,
КОТОРЫЕ БЫЛИ
ЕЩЕ В ДОКЕМБРИИ
Они обнаружены в погибших
микроорганизмах, сохранившихся в
образце докембрийской
осадочной породы, возраст которой —
больше трех миллиардов лет!
Возраст породы был определен
стронций-рубидиевым методом,
сами докембрийские
аминокислоты идентифицированы способом
газовой хроматографии.
Структура древних аминокислот
представляется исследователям
совершенно такой же, как обычно.
КОФЕ В ЗЕРНАХ НАДО
ПОДЖАРИВАТЬ ТАК...
Вывод венгерских исследователей,
задавшихся целью выяснить, как
влияет способ поджаривания
зерен на свойства будущего напитка,
неутешителен для любителей,
предпочитающих жарить кофе
дома. Дело в том, что специалисты
рекомендуют, как об этом пишет
журнал ciWissenschaft und Fortsch-
ritt» A96B, № 7), инфракрасный
прогрев. Его преимущества: лучше
сохраняются экстрактивные
вещества, крепче аромат...
Итак, для поджаривания
кофе— инфракрасные лучи (частота
6- 105 — 3 ■ 109 Мгц, длина волны
0,001—0,5 мм)!
И КЕРОСИН — НЕ ПОСЛЕДНЕЕ
СЛОВО ТЕХНИКИ...
До сих пор считалось, что все
реактивные самолеты летают и
будут летать на керосине, как и
нынешние «Ту», «Каравеллы» и
прочие.
Издающийся в ГДР журнал
ccWissenschaft und Fortschritt»
A968, № 7) сообщает о другой
возможности: горючим для
проектируемых сверхзвуковых
пассажирских самолетов может стать
более экономичный метан —
болотный газ (разумеется,
сжиженный). Дело в том, что благодаря
лучшим тепловым свойствам
жидкий метан может служить
одновременно для охлаждения
двигателя. Отсюда — возможность
повышения температуры топлива на
входе и, следовательно, меньший
расход горючего. А значит,
больше (на 25—30%!) полезный груз,
дешевле перевозки. А может
быть, даже билеты...
ЛОЛИМИКРОУДОБРЕНИЯ
Журнал «Сельское хозяйство
Молдавии» A968, № 2) сообщил, что
научные работники Молдавского
института орошаемого земледелия
применили отходы Тираспольско-
го химического завода как поли-
микроудобрения (ПМУ-Т).
Препарат ПМУ-Т — серый порошок,
нерастворимый в воде и неслежи-
вающийся при хранении, —
получают при размоле отходов
цинкобелильного производства.
В его состав входит от 8 до 30%
цинка, небольшое количество
меди, марганца, магния и никеля.
Вместе с другими удобрениями
препарат вносился в почву, на
которой рос картофель.
НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ
В результате применения этих
полимикроудобрений с каждого
гектара стали собирать на 32,5 ц
картофеля больше, чем раньше.
Каждый гектар принес чистый
доход — 244 рубля. Химический
анализ клубней показал, что
никаких существенных перемен в их
качестве не произошло, только
несколько увеличилось
содержание крахмала. Ученые
рекомендуют вносить удобрения на
весенние и летние посадки по 50 кг
на гектар.
ПЛАЩИ
ДЛЯ ОВЕЦ
Около миллиона овец гибнет
ежегодно в Австралии от простуды
вскоре после стрижки.
Исследования ветеринаров показали, что
причина этого — не просто
охлаждение: особенно губительным для
стриженых овец (как и для людей)
оказалось сочетание холода с
дождем и ветром. Чтобы остаться
сухим и защититься от ветра,
человек надевает плащ. То же самое
средство предложено и для овец:
на них надевают «плащи» из
дешевой полиэтиленовой пленки
толщиной 0,05 мм. К тому времени,
когда овца снова обрастает
шерстью и перестает бояться
простуды, пленка изнашивается, рвется и
теряется — снимать плащ с овцы
не приходится. Такие овечьи
плащи сокращают потерю тепла
животными настолько, что это
соответствует повышению температуры
воздуха на 9°С. В эксперименте, о
котором сообщил журнал «New
Scientist» A968, № 606), падеж
овец снизился благодаря этому с
55 до 5%,
СОЛЬ ПРОТИВ СЛОНОВОСТИ
В тропических и субтропических
странах широко распространена
тяжелая болезнь — слоновость,
или элефантиаз, — стойкое
увеличение размеров отдельных частей
тела. Чаще всего виновники
слоновости — паразитические черви
филярии. В некоторых странах,
например, на тихоокеанских
островах Самоа или на Гаити, ими
поражена половина взрослых
обитателей.
Средство лечения этой
болезни известно уже 15 лет — это ди-
этилкарбамазин. Однако
широкому применению его мешает то, что
люди, не замечающие у себя
признаков заболевания, не хотят
принимать таблетки, иногда
вызывающие незначительное ухудшение
общего самочувствия. Оставалось
одно: подмешивать лекарство в
какой-нибудь распространенный
пищевой продукт. Выбор пал на
соль. Как сообщает журнал «New
Scientist» A968, № 606), недавно
в Бразилии был проведен
массовый эксперимент, в котором
тысяча взрослых людей получала в
пищу в течение 40 дней соль с
добавкой 0,5%, а затем, в течение
года, — с добавкой 0,1 % диэтил-
карбамазина. На вкус соли это не
повлияло. Зато уже шесть недель
спустя 70% испытуемых, в крови
которых были найдены зародыши
филярий, освободились от
паразита. Всемирная организация
здравоохранения рекомендовала этот
метод другим странам, где
распространена слоновость.
БЫСТРОТВЕРДЕЮЩИЙ КЛЕЙ
Обычно затвердевание клея
длится гораздо дольше, чем само
склеивание. Это неудобство
особенно заметно в промышленности,
потому что мешает
автоматизировать процессы склеивания.
Но существуют и клеи
(конечно, синтетические), которые
затвердевают за несколько секунд.
Например, японский клей «арона-
руфа», которым можно соединять
детали из пластмассы (шов
выдерживает нагрузку 176 кг/см2),
меди B70 кг/см2) и некоторых
других материалов.
ГЛИНА В ПЛАСТМАССЕ
О новом материале,
представляющем собой композицию из
пластмассы и керамики, сообщил
журнал «Modern Plastics» A968,
№ 5). В расплавленный полимер
(например, полиэтилен) вводят
недорогие неорганические
наполнители: порошки каолиновой глины,
карбоната кальция, асбеста. У ди-
лоя (так называется новый
материал) модуль упругости при
растяжении почти вдвое больше, чем у
чистого полиэтилена, а
устойчивость к растрескиванию — в 10 раз
выше.
ХИМИЧЕСКИЙ ДОЗИМЕТР
Кислые спиртовые растворы
бесцветного молибдата аммония под
действием ультрафиолетового
излучения приобретают синевато-
зеленую окраску. Японские
ученые справедливо предположили,
что подобные превращения
должны происходить и при облучении
этих растворов гамма-лучами и
создали простой химический
дозиметр гамма-излучения. Главная
деталь такого дозиметра
—прозрачный сосуд с раствором, в
котором на 1000 мл воды
приходится 5 г мол иб дата аммония и 25 мл
концентрированной соляной
кислоты. Перед употреблением к
100 мл этого раствора прибавляют
20 мл спирта. После облучения,
например радиоактивным
кобальтом, химическим или спектрофо-
тометрическим путем определяют
количество образовавшегося
окрашенного вещества и по
результатам анализа легко определяют
дозу облучения.
Рисунки С ДОНСКОЙ
57
ИЗ ПИСЕМ Б РЕДАКЦИЮ
ИЗ ПИСЕМ В РЕДАКЦИЮ
ИЗ ПИСЕМ Б РЕДАКЦИЮ
■ русский —
для химиков
Инициатива журнала «Химия и
жизнь», поднявшего вопрос о
русском языке для химиков,
заслуживает всяческого одобрения.
Действительно, правильное
произношение и написание химических
терминов и понятий — дело не
только филологов. Ведь
неправильное применение этих
терминов приводит только к путанице и
невероятно осложняет работу
библиографов и переводчиков.
Мне хочется остановиться на
некоторых из таких случаев.
Большинство химиков говорит
«песчаная баня». Но «баня», в
которой передатчиком тепла или
теплоносителем служит песок,
никак не может быть «песчаной». По
этому вопросу, после спора со
своими коллегами, я в свое время
обратился в Институт русского
языка АН СССР. И мне ответили,
что слово «песчаный» следует
относить только к природным
скоплениям песка (песчаный берег,
песчаная отмель, песчаные
наносы); во всех же случаях
применения песка следует пользоваться
термином «песочный» (песочные
часы, песочная баня). Я с этим
совершенно согласен и уже 36 лет,
со времени первого издания моей
книги «Техника лабораторных
работ», стремлюсь привить
правильный термин.
От многих химиков часто
слышишь, даже с кафедр высших
учебных заведений, неправильное
произношение названий физико-
химических методов:
полярография, колориметрия и прочие
«графин» и «метрии». Я нередко
спрашиваю таких химиков, что они
учили в средней школе:
геометрию или геометрию? Географию
или географию? В
орфографическом словаре указаны
правильные произношения. Но спросите
химиков, особенно тех, кто читает
лекции, часто ли они обращаются
к нему? И есть ли у них этот
словарь?
Хочется отметить еще одну
несуразность. По радио мы часто
слышим слово «металлургия»
вместо «металлургия». Интересно
следующее: для радио и
телевидения выпущен " специальный
словарь с ударениями. Казалось бы,
он не должен отличаться от
академического орфографического
словаря. Но — ничего подобного.
Видимо, составители словаря для
радио считают себя более
компетентными в русском языке, чем
специальный институт АН СССР, в
чем у меня, например, большое
сомнение. Поэтому радио, по
которому мы должны были бы
слышать только безукоризненно
правильную русскую речь, нередко
вносит путаницу в химическую
терминологию своей далеко не
художественной
«самодеятельностью».
Не без греха в части узакони-
вания неправильных терминов и
«Химическая энциклопедия». В т. 5
в статье В. И. Кузнецова
неправильно применяется термин
«твердофазные реакции». Обычно под
этим понимают реакции между
твердыми фазами. А тут
образование окрашенных осадков с
неорганическими ионами также
названо «твердофазными
реакциями»... К сожалению, «Химическая
энциклопедия» не учла
возражений против неправильного
толкования этого термина и узаконила
его. В результате я уже встречал
научные статьи, в которых в
термин «твердофазные реакции»
вкладывается этот совершенно
неверный смысл.
Одним словом, мы еще
слишком небрежно относимся к
родному языку. А где, как не в науке,
четкость и однозначность
выражения мыслей должна быть
доведена до совершенства?
а в.
■ ВЕСЬМА
СПЕЦИФИЧЕСКАЯ
ОБЛАСТЬ...
В журнале «Химия и жизнь» № 5
за 1968 год помещена статья
А. Т. Склярова «Коварство
микромира», посвященная некоторым
проблемам коррозии и катализа.
К сожалению, в статье
встречаются неточности, которые могут
повести к искажению смысла,
особенно для читателей, мало
знакомых с электрохимией. Так, автор
пишет: «Электроэнергия,
вырабатываемая в гальваническом
элементе воздушной деполяризации,
выделяется при коррозии
цинка». Это неверно. По-видимому,
автор хотел сказать, что
механизм растворения цинка в
элементе и при электрохимической
коррозии один и тот же. В
гальваническом элементе с воздушной
деполяризацией (как и в других
элементах с цинковым анодом)
коррозия цинка происходит лишь
при хранении элемента. При этом
электрическая энергия не
выделяется, а емкость элемента
бесполезно теряется.
В гальванических ваннах с
помощью коррозии металлы не
обрабатывают. Хочу подчеркнуть:
нельзя отождествлять процесс
растворения металла при
прохождении тока с электрохимической
коррозией.
В статье высказана правильная
мысль о том, что коррозионное
выделение водорода (как и
любая другая газовая
электрохимическая реакция) — каталитический
процесс. Но в то же время
неправильно отождествлять
электрохимический катализ с катализом
химических реакций. Полагаю, что
автору следовало подчеркнуть,
что речь идет лишь об одной,
весьма специфической области
катализа.
Кандидат химических наук
М. ЕЗЕРСКИЙ
58
t
****
E§
•'Mi" фЩг/Л
■ • :■■ ■ ■'■->'»'.^ lit *.«•■ '
НАУКА —
ПРОИЗВОДСТВУ
МОЖЕТ ЛИ
МЕТАЛЛ
БЫТЬ
КЛЕЕМ?
ЧЕТЫРЕ ВОПРОСА
И ОДИН ОТВЕТ
...Археолог задумчиво
рассматривал извлеченное из
захоронения золотое украшение:
«Изделие, по-видимому, литое, но как
древний мастер смог отлить
украшение такой сложной
формы?»
«...Этот зуб не причинит вам
неприятностей, он еще вас
переживет», — оптимистически
заметил зубной врач, поставив
мне пломбу лет двадцать тому
назад. Я не особенно сожалею
о том, что мне не удалось
проверить справедливость второй
части его утверждения; меня
вполне удовлетворяет
правдивость первой части... Но что же
сделал врач с моим зубом?
И еще два вопроса — из
области современной техники.
Как быстрее и проще всего
соединить порванный кабель,
проходящий по морскому дну?
Как присоединить выводы к
электронным микросхемам, если
нагрев до температуры пайки
выводит их из строя?
Как следует из названия
этой главы, решения столь
разнообразных задач основаны на
одном и том же явлении. А
заключается оно в следующем:
если смешать какой-либо
жидкий при комнатной
температуре металл (очевидный
пример — ртуть) с порошком более
тугоплавкого металла, скажем
меди, то получится
пастообразная, однородная на вид масса —
амальгама. Ей, естественно,
легко придать некую форму.
А дальше происходит самое
интересное: пастообразная масса
сама собой переходит в твердое
состояние.
Причина — во взаимной
диффузии: медь растворяется в
ртути, атомы ртути проникают
между атомами меди. Более
того, ртуть химически
связывается с медью, образуя различные
сплавы. А плавятся они при
значительно большей
температуре, чем ртуть, потому-то
паста и затвердевает,
«схватывается».
Теперь не сложно ответить
на вопрос археолога: пасту из
ртути и золота (которое тоже
хорошо растворяется в ртути)
можно залить в любую форму.
И врач, запломбировав зуб,
защитил пломбу медной
амальгамой.
Вполне понятно, что такие
самотвердеющие при комнатной
температуре пасты заманчиво
применять для соединения токо-
проводящих деталей, особенно
в тех случаях, когда не
подходят пайка или сварка. Однако
«схватывания» для этого
недостаточно. Нужно еще
прилипание, или адгезия, пасты к
поверхностям соединяемых
деталей. Поскольку ртуть довольно
хорошо смачивает многие
металлы, особенно если на них
нет окисной пленки, то можно
ожидать хорошей адгезии.
В нашей стране такой
способ соединения
электропроводящих деталей впервые был
применен в лаборатории динамики
машин Института
машиноведения АН СССР. Пастообразная
смесь жидкого металла с
металлическим порошком получила
59
Медно-галлиевый клей под ми- Темные
кроскопом. Снимок сделан ера- меди
зу после приготовления клея.
кружки
частицы
название «мекладин» (МЕтал-
лический Клей ЛАборатории
Динамики машИН).
Однако не все материалы
смачиваются металлическим
клеем (точнее, его жидким
компонентом). Для примера
назовем хотя бы керамику. К
счастью, у мекладина есть
свойство, довольно редко
встречающееся у клеев: он
увеличивается в объеме при схватывании.
И когда он окажется в зазоре
между деталями, одна из
которых охватывает другую, то в
нем возникнет внутреннее
давление. Оно как" бы прижмет
клей к деталям, не давая им
сдвинуться друг относительно
друга: получится хорошо
известная машиностроителям
напряженная посадка. К тому же,
если в деталях есть поры,
мекладин проникнет в них.
Если же предстоит склеить
детали иной, не
«охватывающей» конструкции, то
внутреннее давление в клее можно
создать искусственно, сжимая
детали.
НЕ ОБЯЗАТЕЛЬНО РТУТЬ
Вероятно, читатель, наслышан-
ный о вредности ртути, немало
удивлен тем, что автор
нахваливает «ртутный» клей.
Спешим успокоить читателя: для
клея ртуть применяют очень
редко. Она приведена в пример
лишь потому, что ртуть знают
все. На самом деле жидким
компонентом может быть и
другой металл. В принципе
можно, например, смешать
расплавленную медь с вольфрамом
при температуре несколько
выше точки плавления меди.
Однако вряд ли это разумно:
слишком уж высока эта
температура...
И все же ртуть не
единственный металл, жидкий при
невысокой температуре. Галлий
плавится и затвердевает при
29,9°С, и в отличие от ртути он
не ядовит. Существует весьма
распространенное (и неверное!)
мнение, что галлий — редкий,
недоступный металл. На самом
деле земная кора на 0,0015%
состоит из галлия — ртути в ней
в 13 раз меньше! Сейчас наша
промышленность производит
технический галлий в
достаточном количестве. Его получают
в основном как попутный
продукт на алюминиевых заводах.
Жидкий галлий еще лучше,
чем ртуть, смачивает многие
материалы. С галлиевым клеем
работают при температуре чуть
выше точки плавления галлия
(в дальнейшем она причислена
к комнатной). При более
высокой температуре работать нет
смысла, поскольку диффузия в
клее произойдет слишком
быстро, а значит, «время жизни»
его сократится. Иногда идут на
некоторые усложнения и вместо
галлия берут его сплавы с
индием, оловом, серебром и т. д.,
которые плавятся при
температурах, меньших 20°С.
КАК ВАЖНО БЫТЬ
ВНИМАТЕЛЬНЫМ
Готовят мекладин очень
просто — растирая в ступке смесь
жидкого металла и порошка.
Нужно именно растирать, а не
смешивать, чтобы нарушить
окисные пленки на крупинках
металла, тогда они хорошо
будут смачиваться галлием.
Приготовленный клей можно
хранить очень долго, если только
понизить его температуру ниже
точки плавления жидкого
металла. Клей при этом
затвердеет (не путать со
«схватыванием»!). Опыт показывает, что
такая путаница возможна:
мекладин наносили на холодные
детали, его температура падала
ниже 30°С, и галлий
затвердевал. Естественно, что стоило
немного нагреть детали, как
галлий вновь расплавлялся, и
детали расклеивались. А чтобы
клей схватился, его нужно не
охлаждать, а нагревать.
Прежде чем нанести клей, с
поверхности нужно удалить
окисную пленку, иначе не
будет смачивания. Вот один из
простейших приемов: окисную
пленку процарапывают
твердым острием, смоченным гал-
лием. Поскольку «свежая»
поверхность изолирована от
кислорода каплей галлия на конце
острия, то окисная пленка не
появляется, и металл детали,
как правило, хорошо
смачивается галлием.
Вода, кстати, не мешает
смачиванию: галлий очень хорошо
смачивает металлы и
практически полностью оттесняет
воду. Поэтому-то мекладином
можно склеивать металлы под
водой.
Скорость диффузии, как
известно, резко возрастает с
повышением температуры;
поэтому для сокращения времени
схватывания склеенные "детали
нагревают. Время
термообработки невелико, например, при
200°С не более 10 минут.
КЛЕЙ ИЛИ НЕ КЛЕЙ?
И в самом деле, почему
металлический сплав столь упорно
называют клеем? Если клеями
во
Тот же клей спустя 20 минут.
Начинается процесс диффузии
Структура затвердевшего мед-
но-галлиевого клея
считать только органические
клеи, то вопрос правомерен. Но
правильна ли такая
предпосылка?
Было время, когда клеями
считались лишь вещества
растительного и животного
происхождения. Не столь давно
появились и быстро заняли
ведущее положение органические
синтетические клеи. Очевидно,
настало время еще более
расширить рамки понятия «клей»,
включив в него и клеи
металлические.
Процессы, идущие в
металлическом клее во время
схватывания, химические по своей
сущности. А пайка и сварка
основаны на физических
превращениях (плавление —
затвердевание). Более того, паяные и
сварные соединения не могут
выдержать температур,
превышающих температуру пайки
или сварки; мекладин же после
схватывания можно нагревать
до тысячи с лишним градусов.
А теперь — несколько слов
о небольшой хитрости,
придуманной при «крещении» этого
способа. Человеческий ум в
большей или меньшей степени
находится в плену опыта,
приобретенных знаний; нередко зто
направляет нашу деятельность
по пробитой колее, даже если
изменились условия (например,
появился новый способ
соединения деталей). В лучшем
случае это приводит к ограничению
возможностей нового. В
худшем — когда новое применяется
в старых, непригодных для
него условиях — к
опорочиванию этого нового. И вот для
того, чтобы этого не произошло,
смесь галлия с порошком
металла решили назвать не
«холодным припоем», а
металлическим клеем. Тогда «по колее» не
пойдут ни специалисты по
пайке, ни специалисты по клею —
ведь клей-то не обычный, а
металлический!
Соберем вместе
положительные свойства металлических
клеев: хорошая
электропроводность и теплопроводность,
высокие, порядка 1000°С,
эксплуатационные температуры,
способность увеличиваться в
объеме при схватывании, отсутствие
коробления деталей (что
случается при пайке и сварке).
Естественно, что
металлические клеи не идеальны.
Например, они могут понижать
прочность склеиваемых деталей,
причем иногда
катастрофически. Это вызвано тем, что
жидкие металлы, входящие в состав
клея, поверхностноактивны.
Может случиться так, что,
попав в микротрещину, они
быстро углубят и расширят ее — и
разрушение неизбежно.
Но не нужно думать, что
мекладин создан для замены всех
прочих клеев. Просто в
некоторых случаях его можно
использовать там, где неприемлемы
известные способы — обычное
склеивание, сварка или пайка.
Нужно лишь выбрать способ,
в данных условиях лучший.
В заключение автор хочет
обратиться к создателям новых
клеев: пожалуйста, не
вынуждайте нас коверкать русский
язык! Разве плохи слова —
«капрон», «лавсан»? А как быть
с такими клеями, как «РРЭ-2»,
«1235-ПЗ-6789» (попробуй еще
разберись, то ли «пэ-зэ», то ли
«пэ-три»...). Как их запомнить?
Как употребить, например, в
творительном падеже? Если вы
смогли изобрести новый клей,
то неужели не сможете
изобрести для него благозвучное
название?
Кандидат технических наук
И. И. СМЫСЛОВ
61
ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ ИНФОРМАЦИЯ
осх
II
шл
в"
О*
их
17-я конференция по
высокомолекулярным соединениям.
Январь—февраль. Москва. (Научный
совет по высокомолекулярным
соединениям АН СССР)
2-я конференция «Физиология,
биохимия, фармакология и
клиническое применение гепарина».
Январь. Москва. (Научный совет
по физиологии висцеральных
систем АН СССР)
Школа «Передовые методы
работы на поточно-автоматической
линии вулканизации покрышек на
шинных заводах». Январь. Москва.
(Московский опытный шинный
завод)
X
ч:
о
о.
<
ш *^
2и
Симпозиум по передаче тепла
при изготовлении стекла. Январь.
Великобритания, Ормскерк.
Международный симпозиум по
смазке в неблагоприятной среде.
Январь. Великобритания, Лондон.
5-й химический симпозиум стран
Карибского бассейна. Январь.
Остров Барбадос.,
Симпозиум по проблемам
надежности. Январь. США, Чикаго.
Сессия комиссии ООН по
наркотикам. Январь — февраль.
Швейцария, Женева.
X
В ближайшее время выходят в
издательствах
«Наук а»:
Г. Т. АФАНАСЬЕВ, В. К. БОБОЛЕВ.
Инициирование твердых
взрывчатых веществ ударом. 65 к.
Н. Д. ЗЕЛИНСКИЙ. Избранные
труды. 2 р. 85 к.
3. Н. ПАРНЕС, Д. Н. КУРСАНОВ.
Реакции гидридного
перемещения в органической химии. 50 к.
«м и р»:
Исследования с молекулярными
пучками. Под ред. Дж. Росса.
2 р. 22 к.
Р. КЕЙДЛ. Твердые частицы в
атмосфере и космосе. 1 р. 30 к.
Л. ЛИТТЛ. Инфракрасные спектры
адсорбированных молекул. 2 р.
72 к.
Новое в переработке полимеров.
Сборник статей. 1 р. 28 к.
Новые поликонденсационные
полимеры. Сборник статей. 1 р. 28 к.
Новые проблемы физической
органической химии. 2 р. 72 к.
Химические и физические
свойства углерода. Под ред. Ф. Уокера.
Том 1.2р.
ДЖ. ЭМСЛИ и др. Спектроскопия
ядерного магнитного резонанса
высокого разрешения. Том 2.
4 р. 26 к.
Д. ЯНГ. Кинетика разложения
твердых веществ. 1 р. 64 к.
«X и м и я»:
Ароматические углеводороды из
продуктов нефтепереработки и
синтезы на их основе. 1 р. 38 к.
Кинетика каталитических
процессов. 1 р. 15 к.
Г. М. ПАНЧЕНКОВ, Л. К. ЦАБЕК.
Поведение эмульсий во внешнем
электрическом поле. 83 к.
Справочник азотчика. Том 2.
2 р. 37 к.
в
О
X
В ближайшее время поступят в
прокат фильмы
киностудии «Центрнаучфильм»:
«За чистоту наших вод» B части,
черно-белый) — о новых методах
очистки сточных вод
нефтеперерабатывающих предприятий.
«Снова в дорогу» B части, черно-
белый) — о восстановлении шин.
Свердловской киностудии:
«Салаватский нефтехимический
комбинат» B части,
черно-белый) о городе Салавате и
работе комбината.
Киевской киностудии
научно-популярных фильмов:
«Производство парафинов и де-
парафинизация масел» B части,
черно-белый).
О
О
С
Н. С. ХОМЯКОВ, Москва: В
разделе «Информация» вы постоянно
пишете о Выставке достижений
народного хозяйства. Какие
новинки химии можно будет увидеть
на ВДНХ в будущем году!
В 1969 году экспозиция павильона
«Химическая промышленность»
полностью обновляется.
Основные темы новой экспозиции: пути
использования химических
продуктов в промышленности и
сельском хозяйстве; передовые
методы переработки химических
материалов в изделия; новые
химические продукты.
В общей экспозиции будет
освещена тема «Мероприятия по
охране поверхностных и
подземных вод от загрязнения». Кроме
того, организуются специальные
экспозиции, одна из которых
посвящена современным
материалам для живописи и
флуоресцентным краскам, а другая —
химическим волокнам, их крашению в
массе, тканям и изделиям из
химических волокон.
К СВЕДЕНИЮ ОРГАНИЗАЦИЙ!
Если вы хотите, чтобы информация о проводимых вами мероприятиях своевременно публиковалась в «Химии и жизни»,
присылайте ее в редакцию заранее — не позднее, чем за три месяца до намеченного мероприятия.
Редакция
В ЛАБОРАТОРИЯХ
ЗАРУБЕЖНЫХ УЧЕНЫХ
ВАКЦИНА
ПРОТИВ
РЕЗУСА?
Больше 90 лет известно медицине
тяжелое заболевание новорожденных —
гемолитическая болезнь. И долгое время она
оставалась загадкой. Лишь в 1940 г. была
открыта истинная причина заболевания —
несовместимость крови ребенка и матери.
Сейчас, вероятно, каждый знает, что
такое группы крови. Если перелить
больному кровь не той группы, то у него
возникает реакция несовместимости —
антитела, вырабатываемые организмом,
разрушают «чужие» эритроциты.
Заканчивается это обычно печально.
Примерно такая же реакция
несовместимости и составляет сущность
гемолитической болезни. Но вызывает ее не
групповая несовместимость, а
резус-фактор — вещество, впервые обнаруженное в
крови макак породы резус и
присутствующее, как выяснилось позднее, в крови 85%
людей (таких людей называют
резус-положительными). Если
резус-положительная кровь попадает в организм
резус-отрицательного человека, то происходит
примерно то же, что и при переливании крови
«не своей» группы — организм начинает
вырабатывать антирезусные антитела.
Если отец ребенка резус-положителен,
а мать — резус-отрицательна, то ребенок
может унаследовать или резус-фактор от
отца, или его отсутствие от матери. В
последнем случае ничего не произойдет: и у
ребенка, и у матери кровь окажется
одинаковой. Но кровь резус-положительного
ребенка чужеродна для
резус-отрицательной матери, и ее организм, повинуясь
слепым законам природы, обязательно
начнет вырабатывать антитела против
крови ребенка.
К счастью, для первого ребенка это
серьезной опасности не представляет: его
система кровообращения отделена от
кровяного русла матери плацентой, и кровь
ребенка начинает попадать в организм
матери только во второй половине
беременности, а особенно — в момент родов. К тому
времени, когда в крови матери появятся
антитела против крови ребенка, он
оказывается уже вне пределов их досягаемости.
Но антитела остаются в организме матери.
И если при следующей беременности
кровь ребенка снова будет
резус-положительной, то его организм будет
атакован этими антителами. Возникнет
гемолитическая болезнь.
Как предотвратить
резус-несовместимость? Единственный совет, который до
последнего времени мог дать врач резус-
отрицательной женщине, — выходить
замуж только за резус-отрицательного
мужчину: только это гарантировало
отрицательный резус-фактор у ребенка. Если же
рождался ребенок, пораженный
гемолитической болезнью, то единственным
средством его спасения было полное переливание
крови. Но и оно не могло вылечить от
врожденных дефектов, вызванных
проникновением антител в кровь ребенка до
рождения.
Недавно появились сообщения, что
американским ученым — Д-ру В. Фреда, д-ру
Дж. Горману и д-ру У. Поллаку удалось
разработать совершенно новое средство
борьбы с гемолитической болезнью —
вакцину против резус-несовместимости,
способную противодействовать образованию
антител в организме матери.
Принцип действия обычных вакцин
состоит в том, что организм заражают
безопасной дозой бактерий или вирусов,
которые не вызывают заболевания, но
заставляют организм вырабатывать нужные
антитела. Такой активный иммунитет
позволяет организму при встрече с
«настоящим» болезнетворным началом вовремя
распознать его и обезвредить.,
6S
Р§Щ Vy РЩ
!.'■.•. ■•»■"* •«*-?.'
кнЕ&евд
i'.'ji .* »*^l|
YYY
y Y
YT
•W'V
Существует и другая разновидность
иммунитета — пассивный. Он возникает,
когда в организм вводят уже «готовые»
антитела в виде иммунной сыворотки. При
этом организм сам антител не
вырабатывает. Это свойство пассивного иммунитета
и использовали для разработки вакцины
против резус-несовместимости.
Фреда, Горман и Поллак обнаружили,
что если ввести беременной
резус-отрицательной женщине сыворотку, содержащую
антирезусные антитела, то ее организм
приобретет пассивный иммунитет к резусу,
а главное — потеряет способность
вырабатывать «свои» антирезусные антитела.
Это и спасает ребенка от губительной
гемолитической болезни. По
опубликованным данным, эффективность действия
вакцины составляет 99 %!
Единственное условие успешного
применения вакцины состоит в том, что она
должна быть введена не позднее, чем
через 72 часа после рождения первого
ребенка. Дело в том, что вакцина не
оказывает никакого действия на женщин, в
крови которых уже циркулируют антитела,
вызванные воздействием
«резус-конфликтной» крови. Кроме того, поскольку
иммунизирующий эффект вакцины —
только временный, то введение ее должно
повторяться после рождения каждого
следующего ребенка. Но это — лишь
незначительные недостатки по сравнению
с тем счастьем, которое принесет сотням
матерей новая вакцина, если ее
эффективность будет подтверждена.
По материалам зарубежной печати
подготовил А. ЧАПКОВСКИЙ
В среднем каждая восьмая
беремегтая женщина имеет
резус-отрицательную кровь,
которая может оказаться
несовместимой с кровью ее
ребенка. Последствия такой
несовместимости показаны па
схеме. Первому ребенку (слева)
ничто не грозит, но его кровь,
попадая в организм матери,
вызывает выработку противоре-
зусных антител. После
рождения ребенка эти антитела
остаются в организме матери
(в центре) и при второй
беременности (справа) уже с самого
начала оказывают на ребенка
губительное действие
G4
Комментирует врач-иммунолог,
кандидат медицинских наук
Л. И. ПРИВАЛОВА
Гемолитическая болезнь
новорожденных — весьма тяжелое
заболевание. 10—14%
пораженных им детей погибают еще в
утробе матери, а оставшиеся
в живых страдают
малокровием, отеками, желтухой, часто
нуждаются в длительном
лечении, которое не всегда
оказывается эффективным. А
профилактики болезни до недавнего
времени вообще не
существовало.
Чаще всего гемолитическая
болезнь новорожденных
вызвана резус-конфликтом между
кровью матери и плода. Это
явление, однако, типично в
основном для европейцев, 15%
которых резус-отрицательны. В
Африке же, например, и в
большинстве стран Азии население
почти полностью
резус-положительно, и проблемы
резус-конфликта там просто не
существует.
К счастью, далеко не все
резус-отрицательные женщины,
родившие
резус-положительного ребенка, вырабатывают
антитела. По данным разных
авторов, доля таких женщин
колеблется от 20 до 30%. При
этом здесь подмечена
интересная закономерность: антитела
появляются у
резус-отрицательной матери чаще всего
тогда, когда ее кровь совместима
с кровью ее
резус-положительного ребенка по обычным
групповым признакам (или, как это
принято называть в научной
литературе, по системе АВО).
Объяснить эту закономерность
пока еще не удалось.
В 1961—1962 годах несколько
английских и американских
ученых высказали
предположение о том, что можно
предупреждать выработку антител
у резус-отрицательных женщин
путем пассивной иммунизации
их резусными антителами.
Авторы этой идеи основывались на
том, что быстро разрушенные
этими антителами
резус-положительные эритроциты плода
во время родов не смогут
поступить в кровообращение матери;
ее организм, можно сказать,
«не узнает» о наличии резус-
конфликта и при следующей
беременности не начнет
вырабатывать собственные антитела.
С этой целью было
предложено вводить беременным
резус-отрицательным женщина м
плазму доноров, в крови
которых заведомо содержатся
резус-антитела. Результаты
оказались ободряющими. К марту
1967 года был собран материал
о 900 женщинах, половина
которых получала такое
профилактическое лечение, а вторая
половина служила контролем.
Прошло 6 месяцев, и ни одна из
женщин, которых лечили анти-
резусной плазмой, не
выработала антител. Больше того, 40 из
них впоследствии забеременели
вторично, и тем не менее резус-
конфликта у них не возникло.
В контрольной же группе
у 60 женщин антитела
появились в большом количестве.
Защитное действие антирезусного
гамма-глобулина было
доказано.
Но для широкого внедрения
нового метода в практику
предстоит еще решить много
важнейших вопросов. Прежде всего
неясен сам механизм действия
этого препарата. Твердо
установлено, что в присутствии
введенных в организм резусных
антител эритроциты плода
действительно быстро исчезают из
кровяного русла матери.
Однако в эту стройную теорию
вклинивается наблюдение
американского ученого Кларка,
говорящее о том, что антиген в
некоторых случаях после введения
резусных антител плода не
тормозит, а, наоборот, стимулирует
иммунизацию матери. Феномен.
Кларка еще полностью не
разгадан и требует тщательного
изучения. Кроме того, при
объяснении механизма действия
антирезусного
гамма-глобулина нельзя не учитывать и
других факторов, в частности,
различной биологической
активности исходной плазмы доноров-
Существуют и другие
нерешенные задачи. Например,
неизвестна минимальная доза
гамма-глобулина. Оптимальная
дозировка также не отработана:
английские ученые вводят 5 мг
препарата, а американцы
снизили эту дозу до 0,1 мг.
Разница, как видите, немалая!
Неясно, как можно сохранять га м-
ма-глобулин в жидком и
высушенном состояниях, чтобы
обеспечить его стабильность.
Предстоит срочно разработать
национальные и
международные стандарты антирезусного
гамма-глобулина, с которыми
можно было бы сравнивать-
плазму потенциальных доноров.
и «фабричный» препарат.
В заключение следует
сказать, что лечебный эффект
антирезусного гамма-глобулина
бесспорен. Работы по его
получению и изучению ведутся в
СССР, США, Англии,
Швейцарии, Голландии и других
странах. Окончательное его
освоение —по-видимому, вопрос
ближайшего будущего.
G5
СКАЗКА
НЕ НАШЕП РАБОТЫ
Дэнни ПЛЕКТЕЙ
ПАТРУЛЬНЫЙ КОРАБЛЬ «Солнечный
океан» был всего в миллиарде миль за
орбитой Плутона, когда в капитанской
каюте зазвучал сигнал вызова. Капитан
мгновенно проснулся и нащупал в
темноте на ночном столике тумблер
видеофона.
— Капитан слушает. Доброе утро.
—Докладывает штурман, сэр. Сообщаю
показания радара.
— Что у вас там?—спросил капитан.
— Большой выброс, сэр. Препятствие
по курсу примерно в ста тысячах миль.
Теперь уже в сорока тысячах... Какое-то
тело большой плотности, сэр.
Капитан снова пошарил на ночном
столике, зажмурился от яркого света и
вскочил с постели.
— Продолжайте следить. Сейчас
оденусь и приду.
И пяти минут не прошло, а он уже
стоял рядом с штурманом и разглядывал
на экране локатора неяркое пятнышко
света, окруженное своим особым
мирком — подобием крохотных звездочек и
смутно светящихся облачков газа.
— Что-то большое и плотное, — с
опаской заметил штурман.
— Очень большое и очень плотное, —
спокойно поправил капитан.
— Уник говорит, до него уже всего
около двадцати тысяч миль, капитан, —
сказал программист, сидевший у
вычислителя.
Как и все новые патрульные суда,
«Солнечный океан» был оснащен элект-
GG
ронно-счетной машиной самой последней
марки — Сверхэкономичным
Малогабаритным Универсальным Вычислителем.
Экипаж называл его любовно — Уник, и в
обиход вошла неизменная присказка «Уник
его знает!»
— Скомандуйте Унику замедлить ход
на три четверти и готовиться к полной
остановке, — распорядился капитан, не
отрываясь от радара.
— Есть, сэр, слушаю, — отозвался
программист.
Корабль содрогнулся от резкого
торможения. Капитан ухватился за поручни,
окружавшие радарную установку. Потом
с усилием прошел четыре шага, которые
отделяли его от программиста.
— Уник исследует его, сэр, — сказал
программист. — Пока ничего не известно.
Истекли две долгие минуты
торможения, и на панели вычислителя мигнул
зеленый огонек.
—Вот данные, капитан, — сказал
программист. — Уник говорит: «Строение —
сплав»... сплав, капитан!.. «Действующего
источника энергии не обнаружено»...
Какая-то штука не нашей работы!..
— Велите Унику удирать ко всем
чертям! Полный ход, общая тревога!
Капитан ухватился за поручни.
Корабль снова тряхнуло.
...ПЫТАЯСЬ СВЯЗАТЬСЯ с чужим
кораблем на расстоянии, они перепробовали
все средства и способы. Ни ответа, ни хотя
бы малейшего признака, что их призывы
замечены.
Вспышки осветительных атомных
ракет — и те не вызвали отклика.
Непрерывные наблюдения Уника тоже ничего
не давали. «Никаких сигналов не
обнаружено...— сообщал он снова и снова.—
Курс без изменений... общее состояние без
перемен».
Тогда капитан с десятком
добровольцев сел в космоскаф, и маленькое
суденышко, описав длинную кривую, начало
приближаться к чужаку.
— Если с нами или даже с
«Солнечным океаном» что-нибудь стрясется,—
рассуждал капитан, —что ж, во всяком
случае, все показания Уника будут
переданы на базу. И телепередатчики у нас
с собой. Все, что мы узнаем, станет
известно и там.
Они снова попытались связаться с
чужаком, обходя его по малой орбите, но
безуспешно, — и тогда крохотная ракетка
подошла вплотную к исполинскому
чужому кораблю. Пилот остался у штурвала,
капитан и все прочие надели скафандры
и вышли.
Они долго простукивали безответный
корпус корабля, и наконец капитан решил,
что уже хватит канителиться и надо
проникнуть внутрь, без зазрения совести
пустив в ход маленькую бомбочку.
— По крайней мере они заметят наше
присутствие, — сказал он.
— Еще вскроем эту коробку
где-нибудь не в том месте, — заметил кто-то из
команды.
— Ну, в дамскую уборную, может, и не
вломимся, — сострил еще кто-то позади.
— Скафандров ни в коем случае не
снимать, — распорядился капитан. —
Держаться поближе друг к другу,
телепередатчики — на максимальный обзор.
И он нырнул в отверстие, проделанное
в обшивке молчаливого корабля.
Остальные поспешили за ним. Тот, кто шел
последним, прощально помахал рукой
плывущему невдалеке космоскафу.
ЧУЖОЙ КОРАБЛЬ и вправду был
огромен, и все каюты тоже. Люди бродили по
нему, ни на минуту нигде не задерживаясь,
и все же потратили несколько часов, пока
■обошли его весь. Наконец, они вновь
очутились близ отверстия, через которое
проникли внутрь. Картограф — он на
ходу все время делал пометки и
зарисовки— доложил об этом капитану. Здесь они
остановились и начали совещаться.
— Каюты прямо как ангары, тут нигде
не спрячешься, — сказал кто-то. — Разве
что сами они совсем крохотные.
— Ну, какое-то соответствие должно
быть, — возразил капитан, быстро глянув
по сторонам. — На такой махине вряд ли
могли летать существа мельче нас с вами.
Судя по всему, на борту, кроме нас, ни
души. Подозреваю, что команда давным-
давно покинула корабль.
И он приказал всем отправиться в отсек,
где, как уверял картограф, находился
жизненный центр корабля. Во всяком
случае, он был еще больше других, и
капитан считал, что его-то и надо первым
делом тщательно обследовать. Они
принялись дотошно осматривать каждый уголок
и каждую мелочь, и тут к капитану
подошел один из команды.
— Я так думаю, сэр, на борту никогда
i
1
07
никого и не было, — сказал он. — Может,
это просто такая огромная станция-робот.
Но эта гипотеза рухнула уже через
минуту, потому что несколько человек
наткнулись на большие листы какого-то
материала вроде пластика. Тысячи таких
листов были сложены в ящиках вдоль
стен — что-то вроде огромной картотеки.
И в этих листах они сразу узнали на
удивленье подробные маршруты... или, скорее,
карты целых солнечных систем и
отдельных звезд, и планет, больших и малых.
— Смотрите-ка, а ведь это, по-моему,
наша солнечная система, — сказал
капитан. — А вот и наша Земля!
Люди с изумлением разглядывали
тонкие листы. Они подносили телекамеры
поближе к сложной сети значков и
пометок, чтобы на корабле увидели все
подробности.
— Пускай Уник все как следует
разглядит, — сказал капитан. — Может, он
разберется в их надписях.
— Наверно, тут у них была
штурманская рубка, -— догадался кто-то, и все с
ним согласились.
— Право, они неплохо ориентировались
в пространстве, — заключил
бираясь в обратный путь.
капитан, со-
...НАКОНЕЦ-ТО ОН СНОВА У СЕБЯ
в каюте, в носовой части «Солнечного
океана». Он сидит на краю постели,
которую всегда называл по-морскому
«койкой», и обстоятельно описывает в дневнике
(«вахтенном журнале», как он
предпочитал выражаться) удивительные события
последних часов. Он остановился,
обдумывая какую-то особенно цветистую
фразу, но вдруг зазвонил сигнал вызова и он
протянул руку к видеофону.
— Капитан слушает. Что у вас там?
— Докладываю данные вычислителя,
сэр.
— Ну как, удалось нашему Унику
расшифровать надписи на картах?
— Пока есть только предварительные
результаты, сэр. И вот что, капитан: Уник
говорит, это не карты...
...Это — рабочие чертежи!..
Перевела с английского
Нора ГАЛЬ
Рисунки Ю. ВАЩЕНКО
ИЗ ПИСЕМ В;РЕДАКЦИЮ ИЗ ПИСЕМ Б РЕДАКЦИЮ ИЗ ПИСЕМ В РЕДАКЦИЮ ИЗ ПИСЕМ
■ КАК ПРИКЛЕИТЬ
ПОЛИСТИРОЛЬНУЮ
ПЛИТКУ
(По поводу заметки
«О пластмассовом кафеле»
в № 5 за 1968 г.)
...Строительная практика показала,
что различные мастики,
содержащие толуол, бензол, сольвент-
нафту и другие органические
растворители, непригодны для
наклейки полистирольных плиток,
так как растворители с течением
времени (по мере испарения из
мастики) вызывают коробление
плиток и дальнейшее их
отслаивание от поверхности.
В Центральной строительной
лаборатории Главюжуралстроя
было получено подтверждение
хороших клеящих свойств полимерце-
ментных мастик (на поливинил-
ацетатной эмульсии или латексе).
Использовался бутадиен-стироль-
ный латекс СКС-65, значительно
более дешевый материал, чем по-
ливинилацетатная эмульсия. К
тому же у латекса есть еще одно
немаловажное преимущество: он
недефицитен...
Нами рекомендуются
следующие составы полимерцементных
мастик для наклейки
полистирольных плиток
1. Цемент М-300 или М-400 —
100 весовых частей, молотый
песок или маршалит — 300—500
частей, латекс СКС-65 или поливи-
нилацетатная эмульсия — 60—
20 частей, вода — до рабочей
консистенции.
2. Цемент М-300 или М-400 —
29,2 весовых части, мел
тонкомолотый — 29,2 части, асбест № 7 —
29,2 части, сухой казеиновый
клей — 3,5 части, поливинилаце-
татная эмульсия — 8,9 части,
вода — до рабочей консистенции.
На наш взгляд, ВНИИ новых
строительных материалов или
другому институту необходимо
провести тщательные исследования
мастик для полистирольных плиток
(в том числе и указанных выше) и
выдать строителям научно
обоснованные рекомендации.
Инженер ЦСЛ Главюжуралстроя
Е. ЛАГУТКИН, Челябинск
69
«
I
1,
МЕЖДУ НАМИ
И ЗЕМЛЕЙ
Г. ФИЛАНОВСКИЙ
Робинзон пришел в ужас,
обнаружив на своем острове след
босой ступни. Такой след мог
оставить только дикарь, потому
что обувь — непременный
атрибут цивилизации.
Когда-то первобытный
человек приладил к ступне
звериную шкурку, или, может быть,
пальмовый лист — это уже
обувь. Сегодня в магазинах
продают пинетки, туфли,
ботинки, сапоги, пуанты, бутсы,
кеды, босоножки, тапочки... Одна
обувь не похожа на другую —
разные конструкции, фасоны,
расцветки, размеры. Но есть и
общий элемент, который
непременно присутствует в каждой
из трех миллиардов пар обуви,
ежегодно выпускаемых в мире.
Это — подошва.
Слов нет, приятно походить
босиком по траве или по
прибрежному песку. Но вряд ли
можно считать удовольствием
прогулку по стерне, по острым
камням или снегу. Отдадим же
должное подошве — этим
считанным миллиметрам вещества,
возвышающим нас над землей!
Она отделяет человека от
жаркой или холодной, жесткой или
вязкой, скользкой, колючей,
занозистой поверхности планеты.
Она охраняет нас на каждом
шагу.
КАК ДОСТИЧЬ ИДЕАЛА?
Юноша теряет возлюбленную —
сообщает сказка. И пешком
(поскольку дело происходит в
далекие времена) отправляете»
на поиски, куда-то за тридевять,
земель. Волшебник выдает
герою в дорогу железные
башмаки. Бедный юноша! Опыты,,
проведенные в XX веке,
показали, что если подошва весит
всего четыреста граммов, то
человек утомляется так, словно»
несет на плечах
двухкилограммовый груз...
Правда, волшебник
остановил свой выбор на железе из
лучших побуждений. Отправь
он юношу в тридесятое царство
в лаптях -— не хватило бы и
сотни пар. Вот и первое
противоречие в требованиях к
подошве: она должна долго служить,
и в то же время быть легкой..
70
Раскроенные особым образом и
завязанные тесемками куски
кожи служили одновременно и
подошвой, и верхом обуви.
Такая обувь была найдена в гроб-
ницах X века в Швабии
Основной деталью
древнеегипетской обуви была подошва
Железо не годится. Нужен
компромиссный материал. Может
быть, дерево — легкое, прочное
и недорогое?
У разных народов была в
ХОДУ деревянная подошва или
обувь целиком из дерева. Но —
не от хорошей жизни.
Достаточно походить час-другой в
ботинках на деревянной подошве,
чтобы оценить справедливость
выражения «гудят ноги».
Дело в том, что при ходьбе
форма ступни изменяется,
сокращаются мышцы. А жесткий
материал подошвы мешает
мышцам работать естественным
образом, они напрягаются — и
ноги устают. Значит, еще одно
требование — гибкость. Пробка
в этом смысле лучше дерева,
но разве мыслимо достать
столько пробки?
Материал, будто бы самой
природой предназначенный для
подошвы, — это кожа. Она и
прочна, и легка, и эластична. Но
если дерево можно
использовать в первозданном виде, то
шкуру нужно еще превратить
в кожу. Раньше на это уходили
годы, теперь — месяцы; и все
равно выделка кожи — едва ли
не самый длительный
технологический процесс. Да к тому же
сложный, нестабильный,
требующий громоздкой
аппаратуры и растительных или
синтетических дубителей *.
* Об этом можно прочитать
в статье «Советские синтаны»
(«Химия и жизнь», 1968, № 6).
В этом году в мире будет
произведено примерно 25
миллионов тонн подошвенной
кожи. Этого хватит не более чем
на треть всей обуви.
Подсчитано, что лет через пятнадцать
обуви будут выпускать вдвое
больше. А поголовье крупного
рогатого скота увеличится
процентов на тридцать.
Это противоречие между
потребностью- в обуви и сырьевой
базой было замечено в
прошлом веке. Тогда же появился
заменитель подошвенной
кожи — резина.
Люди старшего поколения
помнят массовое
распространение обуви «на резиновом ходу».
Распространение, связанное
скорее с ценой, чем с
качеством. Обуви на коже отдавали
предпочтение — и не без
оснований. У кожи пористая
структура, и поэтому нога в кожаной
обуви «дышит». Монолитная
резина воздух не пропускает.
Впрочем, кожаная подошва
тоже не идеальна. В самом
деле, сырой лондонской осенью
она промокает за час. А если
герой современной сказки
вздумает пешком искать свою
возлюбленную, ему придется
менять обувь на кожаной подошве
каждые три месяца. Какой уж
тут идеал! Еще хуже, когда
кожаными подошвами ступают в
бензиновые лужи или
пролитую кислоту — тут и три
месяца не проходишь...
Просуммируем требования к
материалу подошвы. Он должен
быть: а) прочным, б) легким,
в) эластичным, г) пористым,
д) водостойким, е)
фрикционным, ж) несъедобным для
бактерий и грибков, з) дешевым...
В алфавите еще достаточно
букв; требований, наверное, не
меньше (огнестойкость,
теплостойкость, морозостойкость,
устойчивость к действию
кислот, щелочей, нефтепродуктов
и т. д.). Искомый материал по
универсальности уступает разве
философскому камню.
71
ВЫДАЕТСЯ РЕЦЕПТ
Если внимательно перечитать
список требований, можно
сделать вывод, что резина все же
наиболее приемлема. Впрочем,
далеко не всякая резина.
Рецепт «теста» обувных ре*
зин включает в себя не меньше
компонентов, чем рецепт
изысканного торта. Главное — это,
безусловно, каучук. Читатель,
предположивший, что речь
пойдет о туфлях «на каучуке»,
будет прав, только не на сто, а на
40, 60 или 80 процентов — в
зависимости от того, сколько
каучука в смеси.
Много зависит от выбора
каучука. Бутадиен-стирол ьный
придает подошве стойкость к
истиранию и повышенную
диэлектрическую прочность (что
очень важно для монтеров).
Найрит (продукт
полимеризации хлоропрена) повышает
стойкость подошвы к
растворителям, нефтепродуктам, огню.
Резина на бутилкаучуке не
боится кислот и щелочей,
прекрасно сопротивляется
многократному изгибу. В последние
годы для подошвенных смесей
применяют новые каучуки, в
частности стереорегулярные, и
такие известные полимерные
материалы, как полистирол или
полиэтилен.
Полагая, что читатель зна-
Ли и/
&.
ЛИП
ИЛТК£
^ I *, J -ч* < ЛЛ
,-*f а Ш уЩг« "SX'^i-'vJ^
r\i «'ЛЛ* '\
150 1604 Г
к
72
ком в общих чертах с
производством резиновых изделий *,
не будем останавливаться на
технологических подробностях.
Заметим лишь, что в последнее
время вместо «неактивных
наполнителей» (увеличивающих
объем смеси и удешевляющих
резину, — например, мела)
стали применять «активные»,
усиливающие наполнители, в
частности фенольные смолы,
алюмосиликаты. В рецепты
термостойких подошв входит
асбестовое волокно, кварц. По-
лиизобутилен и полипропилен
вводят для придания кислото-
стойкости. В условиях
тропического климата важна
устойчивость к грибкам; для этого в
смесь добавляют фунгициды.
Волокнистые наполнители
придают резине «кожеподобность».
НЕЛЬЗЯ ЛИ
ПОЛЕГЧЕ?
Вес подошвы находится в
прямой зависимости от пористости.
Достаточно ввести в резиновую
смесь вещество, выделяющее
при нагревании газ (например,
питьевую соду), чтобы в толще
материала появились закрытые
или сквозные поры.
Долгое время никак не
удавалось преодолеть «барь-
* См., например, статью
«Галоши шагают по свету» в № 4
«Химии и жизни» за 1966 г.
Материал
Кожа подошвенная
натуральная
Резина непористая
Резина пористая
Облегченная гористая типа А
Пористая экстра типа Б . . .
«Прогресс)) В
«Победа»
«Особая»
Средняя
плотность,
г/см3
1,10
1,55
1,10
0,92
0,60
0,40
0,25
0,15
Вес одной
пары, г
320
520
360
316
270
210
128
70
Срок воски,
месяцы
4
3 — 4
5 — 6
7 — 9
7 — 9
8 — 12
7 — 12
ер 0,5» — то есть создать
прочный подошвенный материал с
плотностью ниже 0,5 г/см3. Тут
все зависело от технологии
производства. Обычно сырую
заготовку закладывали в гнездо
прессформы, и при
температуре 150—160°С под давлением эта
заготовка, содержащая порооб-
разователь, начинала расти. Но
воздух в прессформе неизбежно
ограничивал ее рост, и
соответственно не позволял снижаться
удельному весу.
Теперь рост заготовки
регулируют сменой давлений —
низкого A—2 атмосферы) и
высокого B5—30 атмосфер).
Комбинируя выдержку под низким
и высоким давлением, удается
получить изделие с удельным
весом до 0,15 г/см3. Так были
получены новые марки
пористых подошв: «Прогресс»,
«Победа», «Особая». Чем они
замечательны, явствует из таблицы,
которая не нуждается в
комментариях (она заимствована
из книги Б. А. Сафрая
«Синтетические материалы для низа
обуви»).
Кстати, гигиенические
свойства новых подошв прекрасны.
При опытной носке было
установлено, что в обуви на
кожаной подошве можно пройти без
устали десять километров, на
непористой резиновой — всего
лишь пять, зато на подошве
облегченного типа — все
пятнадцать.
До сих пор всегда было так,
что у башмаков в первую
очередь снашивалась подошва.
Теперь дело идет к тому, что
подошва может «пережить» верх
обуви. Тогда возможен (и уже
существует в виде
эксперимента) оригинальный вариант
крепления подошвы — с помощью
декоративных винтов. Обувь
продается комплектом: подошва
и набор сменных элементов
верха — различных фасонов и
расцветки. Такие туфли без
труда «подстраиваются» под
погоду и костюм владельца.
Рисунки С. ЮКИНА
73
ПОЛЕЗНЫЕ СОВЕТЫ
И ПОЯСНЕНИЯ К НИМ
НЕ БОИТЕСЬ
МОРОЗА!
Инженер
А. А. КРЕЙНИН
В былые времена приближение холодов
определяли по улетающим к югу птицам.
Современному городскому жителю
незачем смотреть на небо, чтобы понять,
что зима на носу. Есть верная
примета— на улицах остается меньше
автомобилей...
Любому школьнику знаком такой
нехитрый опыт: в сосуд с узким горлом
(скажем, бутылку) наливают воду и
выставляют на мороз. И вода, расширяясь
при замерзании, разрывает сосуд. То же
случается с двигателем автомобиля, если
зимой забывают слить воду из системы
охлаждения.
Можно, правда, построить для
автомобилей с водяным охлаждением (а таких
большинство) сложные установки для
подогрева и циркуляции воды в системе
охлаждения; можно периодически
прогревать двигатель, чтоб вода не замерзала.
Но все это приемлемо для автобаз и
автопарков. А что делать автолюбителям,
которые хотят ездить в любое время года?
Ответ, вероятно, может быть один —
заменить воду!
Незамерзающие жидкости для
охлаждения получили название антифризов.
Действие большинства из них основано на
том, что при растворении в воде
органических или минеральных веществ
температура ее замерзания снижается.
Антифризом может быть любая жидкость со
следующими свойствами: высокой
теплоемкостью, теплопроводностью и
температурой кипения, низкой температурой
замерзания; жидкость не должна
вызывать коррозии, должна быть негорючей,
неядовитой, дешевой, распространенной.
Как видите, определение «любая»
значительно сузилось...
Наиболее подходящими оказались
жидкости с этиленгликолем. Их очень
много; расскажем лишь о некоторых.
Антифриз «В-2» желтоватого цвета: он
состоит из 55% этиленгликоля и 45%
воды. Его температура кипения и
теплоемкость существенно не отличаются от
соответствующих показателей воды и
поэтому, заменяя им воду, никаких
изменений в системе охлаждения делать не
нужно. Замерзает «В-2» при минус 40°С.
Антифриз «40» состоит из 47% воды и
537о технического этиленгликоля. Этот
антифриз тоже желтоватый, но слегка
мутный из-за присутствия небольшого
количества декстрина. Температура
замерзания — около минус 40°С.
Антифриз «65» составлен из 34%) воды
и 66 % технического этиленгликоля. Он
специально окрашен в оранжевый цвет —
так, не зная марки антифриза, можно
опознать его. Температура замерзания —
около минус 65° С.
Если вам придется работать с
антифризом «40к» (концентрированным), то на
74
I ю zc so Ao ы to 7o *o 50 'QO
I ЭТИЛЕНГЛИКОЛЬ, % *-
* ■ ■ ' 1 1 ^ * 1 и \ j
\0Q 30 tfP ft IQ SQ 4o 30 Zo 10 О
каждый литр его нужно добавить 700 г
дистиллированной воды — получится
обычный антифриз «40».
Имея технический этиленгликоль и
дистиллированную воду, можно
приготовить антифриз самим. Смешав
компоненты, в смесь добавляют динатрийфосфат
Na2HP04 B,5—3,5 г/л) и декстрин A г/л).
Динатрийфосфат защищает от коррозии
чугунные, стальные, медные и латунные
детали, а декстрин — свинцово-оловяни-
стые припои, алюминий, а также медь.
Смешивая этиленгликоль с водой в
разных соотношениях, получают смеси
с различной температурой замерзания —
от —10 до —75° С (см. таблицу).
Помните, что этиленгликоль
гигроскопичен, и чтобы при хранении он не набрал
воды, держите его в плотно закрытой
посуде!
Состав смеси, %
этиленгликоль
100
90
80
70
66,7
60
50
1 40
I 20
вода
0
10
20
30
33,3
40
50
60
80
Температура замер- 1
зания смеси, °С 1
—И
—30
-48
-07
—75
i —55
1 —34
—25
—10
75
На диаграмме — зависимость
температуры замерзания
раствора этиленгликоля в воде
(или, если хотите, — воды в эти-
ленгликоле) от состава смеси.
Если в растворе содержится от
0 до 33,3% воды, при
замерзании образуются кристаллы
этиленгликоля; при более высоком
содержании воды она
кристаллизуется, а этиленгликоль
остается в растворе. В точке
пересечения двух ветвей кривой
кристаллизуются оба вещества
одновременно
Может показаться странным, что
этиленгликоль, замерзающий при минус 11°С,
и вода, замерзающая при 0°С, образуют
растворы с температурой замерзания ниже
минус 70°С. Дело в том, что жидкость
начинает замерзать при той температуре,
при которой давление ее паров в точности
равно давлению паров над ее
кристаллами. А при растворении одного вещества
в другом давление паров растворителя
обязательно снижается, вне зависимости
от температуры. Совершенно безразлично,
что считать растворителем — воду или
этиленгликоль. Важно лишь, что давление
паров становится меньше, а насколько
именно, зависит от того, какой
концентрации раствор.
Равновесное давление паров воды при
нуле градусов около 4,6 мм ртутного
столба. Когда в воде растворяют любое
вещество, в том числе и этиленгликоль,
равновесное давление уменьшается, и этому
новому давлению соответствует более
низкая температура замерзания. При этой
температуре начинает выделяться твердая
фаза — кристаллы льда или
этиленгликоля.
Конечно, антифризы можно готовить
не только с этиленгликолем. Одно время
применяли водные растворы спиртов
(чаще всего наиболее дешевого этилового).
Смешивая 60% этилового спирта и 40%
воды, получают смесь, замерзающую при-
мерно при минус 40°С. Но спирт легко
испаряется, его приходится часто
добавлять.
Водно-глицериновая смесь, в которой
67% глицерина, легко вспенивается; у нее
повышенная вязкость, а это ухудшает
условия теплоотдачи. Температура
замерзания — минус 47°С.
Иногда составляют тройные смеси —
водно-спирто-глицериновые. Например,
смесь 42% этилового спирта, 15%
глицерина и 43% воды замерзает при —32°С.
Есть и солевые антифризы. Один из
них (с температурой замерзания минус
45°С) состоит из хлористого кальция C2%),
хлористого натрия G%), воды F1%). Но
у таких антифризов высокая
коррозионная активность, они образуют накипь,
а при испарении воды выпадают
кристаллы.
Все перечисленные антифризы пока не
очень дешевы, да и не всегда их можно
достать. В таких случаях можно
использовать в качестве охлаждающей жидкости
зимнее дизельное топливо. Оно замерзает
при минус 35°С, не образует накипи, мало
испаряется. Но использовать его без
предварительной обработки нельзя — из
зимнего дизельного топлива выделяется
слишком много смол, а
вещества-окислители в топливе разрушают дюритовые
шланги.
Чтобы уменьшить содержание
окислителей, дизельное топливо нагревают до
120—130°С, опустив в него немного медной
или латунной стружки. Затем для
разрушения смол добавляют 4—5% серной
кислоты (ОСТОРОЖНО!) и греют еще два
часа. Потом к топливу прибавляют 10%
кальцинированной соды и трижды
промывают его горячей водой (ведь топливо
легко отделяется от воды). Наконец,
заканчивая обработку, нагревают топливо
до 100°С, чтобы удалить остатки воды.
У обработанного таким образом
дизельного топлива значительно снижена
окислительная активность, смол оно выделяет
в два раза меньше. И теперь его можно
смело заливать в систему охлаждения.
ПЯТЬ СОВЕТОВ
Автолюбителю, решившему
воспользоваться антифризом,
необходимо:
БЫТЬ
ПРЕДУСМОТРИТЕЛЬНЫМ!
Проверьте, нет ли в системе
охлаждения (в соединительных
шлангах, радиаторе, сальниках
водяного насоса и т. д.) течи; если есть—
устраните eel Иначе все ваши
труды пропадут — антифриз
попросту вытечет.
БЫТЬ ТЕРПЕЛИВЫМ!
Перед заливкой промойте
систему охлаждения чистой горячей
водой (желательно под давлением).
После этого обязательно
проверьте, не осталась ли в системе вода.
Смешавшись с антифризом, она
изменит температуру его
замерзания. <
БЫТЬ АККУРАТНЫМ!
Заливайте антифриз на 20—
30 мм ниже горловины радиатора.
Нагреваясь, антифриз
расширяется больше, чем вода, и может
переполнить систему охлаждения.
БЫТЬ ВНИМАТЕЛЬНЫМ!
Следите за уровнем антифриза, и
когда часть его испарится, долейте
в радиатор чистую кипяченую
воду (потому что испаряется
главным образом вода). Количество
воды определяйте по плотности
антифриза. Лучше всего
пользоваться денсиметром —
гидрометром, шкала которого
градуирована в процентах. Так можно быстро
узнать и содержание гликоля, и
температуру замерзания смеси.
БЫТЬ ОСТОРОЖНЫМ!
При использовании антифризов не
забывайте, что почти все они в
большей или меньшей степени
токсичны. Правда, в отличие от
легких нефтепродуктов, они
вызывают отравление, только попадая
внутрь организма. В пожарном
отношении антифризы безопасны
(за исключением зимнего
дизельного топлива).
76
КАК
ОБРАЩАТЬСЯ
С
ИСКУССТВЕННЫМ
МЕХОМ
Хотя создатели искусственного
меха прилагают все усилия,
чтобы он был точь-в-точь как
натуральный, вряд ли это
осуществимо, по крайней мере, в
ближайшие годы. И пока они
разные, за ними, естественно, и
ухаживать надо по-разному. Но
если у человечества за многие
века выработались приемы
обращения с «настоящим»,
звериным мехом, то о мехе
искусственном этого сказать нельзя.
Вернее говоря, навыки уже
есть, — но у специалистов, а не
у большинства потребителей...
Искусственного меха сейчас
выпускают очень много *.
Нельзя сказать, что он теснит
натуральный, они мирно уживаются
друг с другом; но в
производстве искусственного меха
прогресс более ощутим: все-таки
«нейлоновый век»! Вот пример:
всего несколько лет назад у нас
начали выпускать тканый мех с
ворсом из грубоволокнистого
вискозного шелка. В этом году
только Московский шелковый
комбинат им. П. П. Щербакова
(кстати, пионер этого
производства) выпустит миллион метров
такого меха.
Если бы весь мех делали из
вискозного волокна на ткацких
станках, было бы, вероятно,
нетрудно объяснить, как же с ним
обращаться. Но дело
осложняется тем, что искусственный мех
изготовляют различными спосо-
* О том, как делают
искусственный мех, было рассказано
в N° 12 нашего журнала за 1967 г.
бами, да к тому же из десятков
различных волокон — тут и
ацетатный шелк, и капрон, и
полиэфирные волокна, и акриловые.
Более того, мех нередко
делают не из какого-то
определенного волокна, а из смеси
различных волокон. Тут и специалист
может запутаться.
Итак, первый полезный
совет: не пытайтесь с помощью
простейших средств (скажем,
спички) определить, из какого
материала сделана ваша шуба.
Наверняка ошибетесь.
Но независимо от того, из
какого волокна изготовлен
искусственный мех, с шубами надо
обращаться аккуратно. Это
означает — хранить их не в
свернутом или скомканном виде, а
развешенными на «плечиках».
При долгом хранении — лучше
в бумажном или
полиэтиленовом мешке, чтобы не попадали
пыль и влага. И уж по меньшей
мере — в закрытом шкафу.
Одно преимущество
искусственного меха перед
натуральным неоспоримо:
искусственный мех не боится ни моли, ни
микроорганизмов. Поэтому не
стоит прибегать к помощи
испытанного нафталина или более
современных средств. В
некоторых случаях они могут лишь
испортить волокно, и уж во
всяком случае от них не будет
никакой пользы.
Искусственный мех часто
бывает подвержен пилингу —
явлению, которое в быту
называют обычно «сваливанием».
Волоконца сбиваются,
спутываются, на концах пучков
образуются маленькие плотные
шарики. К сожалению, зто —
свойство самого волокна, и
избавиться от пилинга трудно. Но
его можно предупредить. Для
этого нужно время от времени
расчесывать ворс
искусственного меха металлической
расческой или жесткой массажной
щеткой.
Теперь о самом сложном —
о чистке искусственного меха.
По правде говоря, лучше
всего отдать шубу или шапку в
химчистку. И не только
потому, что это сбережет вам
время и труд. Искусственный мех
обязательно покрывают тонким
слоем поверхностноактивных
веществ. Это делают для того,
чтобы мех не намокал и не
электризовался. Последнее
довольно часто случается, когда
от долгой носки с шубы слезает
покрытие. И к тому же шуба
без такого покрытия имеет
невзрачный, тусклый вид.
Так вот, при чистке или
стирке эти защитные вещества
удаляются. И в химчистке на
изделия обязательно наносят
кремнийорганические эмульсии.
Тогда шуба вновь приобретает
водоотталкивающие свойства и
блеск.
Прежде чем чистить
искусственный мех, приемщик
обязательно посмотрит, на какой
он основе. Если на тканой, то
его можно чистить так
называемым «сухим способом» — в
77
растворителях. А трикотажный
мех погружать в растворитель
нельзя. Дело в том, что ворс не
вплетают в трикотажную
основу, а лишь продергивают сквозь
нее; для прочности ворс
закрепляют с изнанки
синтетическим латексом. И этот латекс
при «сухой чистке»
растворится, а сам мех в скором времени
расползется. Мех на
трикотажной основе можно чистить лишь
в водных моющих растворах.
Это же относится и к меху «на
клею», например,
искусственному каракулю. Сейчас на
фабриках химчистки используют
обычно синтетические моющие
средства или препарат ПАСТ-7,
на калийном мыле.
Вообще-то и дома можно
отличить при некотором навыке
трикотажный мех от тканого.
Для этого достаточно
посмотреть на изнанку: если там есть
тонкая пленка латекса, значит,
основа трикотажная. Но это
делать вовсе необязательно,
потому что дома лучше всего
чистить искусственный мех не
растворителями, а моющими
средствами. А они годятся для
любого искусственного меха.
Промышленность выпускает
препарат под названием «Ме-
хочистка» — специально для
искусственного меха. В коробке
«Мехочистки» два флакона.
В первом — обычная моющая
смесь для синтетики: поверх-
ностноактивные вещества, три-
полифосфат натрия, оптический
отбеливатель — на тот случай,
если мех белый. В другом
флаконе — кремнийорганическая
эмульсия для опрыскивания
меха после стирки. Из-за этого
второго флакона и стоит купить
«Мехочистку», потому что
моющему средству можно найти
замену, а вот средств для
отделки меха отдельно не
продают.
После чистки шубы не
забудьте хорошенько промыть ее
водой и отжать, проводя рукой
по ворсу. Иначе грязь, которая
могла пробраться в ватин,
вылезет на подкладку. А затем,
пока шуба еще влажная,
нужно опрыскать ее эмульсией.
Если все же вам по каким-
либо причинам не удастся
отдать шубу в химчистку, а
«Мехочистки» в магазине не
окажется, можно постирать шубу и
синтетическими моющими
средствами, предназначенными для
синтетики, например
«Новостью» или «Лотосом». Только
ни в коем случае не
препаратами для стирки белого белья —
так вы можете испортить
искусственный мех.
Перед стиркой желательно
отпороть ватин с подкладкой,
иначе шуба будет очень долго
сохнуть. В крайнем случае
можно стирать и нераспоротую
шубу, но тогда ее обязательно
нужно сушить поочередно с
двух сторон. И только при
комнатной температуре, так как
печка, батарея, рефлектор (не
говоря уже об открытом огне)
могут повредить ворс меха.
После сушки не забудьте
расчесать мех расческой или
жесткой щеткой «по ворсу».
И все-таки рекомендовать
домашнюю стирку
искусственного меха, если поблизости есть
химчистка, нельзя. Если после
стирки не обработать
поверхность меха специальными
эмульсиями, о которых здесь
уже говорилось, то шуба или
шапка загрязнятся слишком
быстро —намного быстрее, чем
новая вещь. И все из-за той же
склонности к электризации. При
трении на волокнах образуются
статические электрические
заряды. А пылинки в воздухе
тоже заряжены. Разноименные
заряды притягиваются друг к
другу, и шуба будет
вылавливать из воздуха пылинки.
Впрочем, отдельные части
шубы, которые загрязняются
сильнее других, можно без
особых опасений почистить
мягкой щеткой, смоченной в
растворе «Новости» или «Лотоса».
78
Это относится, в частности, к
воротнику и манжетам. Если
они после такой местной чистки
скоро опять загрязнятся, то
операцию несложно повторить.
Отдельные пятна на тканом
искусственном мехе можно
удалять обычными
пятновыводителями для тканей — к
каждому из них приложена
инструкция. Для проклеенного меха
пятновыводители применять не
следует — растворители,
входящие в их состав, могут
разрушить клеевую пленку. Впрочем,
некоторые растворители все же
можно использовать. Так, для
выведения жировых пятен
рекомендуют смесь 93% изопро-
пилового спирта и 7% цикло-
гексанола.
Так как антистатик
понемногу смывается водой,
искусственный мех не рекомендуют
носить в дождь. Но если уж вы
попали под дождь или мокрый
снег, то прежде чем войти в
помещение, хорошенько
встряхните шубу или шапку, а потом
аккуратно развесьте шубу на
«плечиках».
И последний совет: отдавайте
шубу в химчистку или
стирайте ее сами «Мехочисткой»
почаще. Чем меньше на мехе грязи,
тем легче его очистить.
Л. ОЛЬГИН
БИБЛИОТЕКА
«ВОСПИТАЙ
УЧЕНИКА...»
■■ :%■ и 91
В этом году продолжается
перестройка учебных планов и
программ советской средней
школы. К началу занятий
выпущено несколько новых стабильных
учебников, в том числе и
«Органическая химия» для
десятого класса. Но если по
некоторым другим предметам —
общей биологии, анатомии,
физиологии и гигиене человека,
зарубежной литературе —
учебники удовлетворяют самым
высоким требованиям, то новый
курс химии — это по существу
лишь слегка подреставрирован-
ный вариант старого учебника.
Директор издательства
«Просвещение» И. М. Терехов в
своем интервью в газете
«Правда» сообщил, что в создании
новых учебников для средней
школы участвуют многие
виднейшие деятели советской
науки; он назвал имена академика
А. Н. Колмогорова и
действительного члена Академии
педагогических наук СССР А. И.
Маркушевича, которые состоят
в авторских коллективах,
создающих ученические пособия
по алгебре, академика И. К.
Кикоина, под руководством
которого вышла книга по физике
для шестиклассников и
готовится учебник для 8—10-х
классов. После открытого
обсуждения утвержден, как
стабильный, новый учебник зоологии
под редакцией академика Б. Е.
Быховского.
Но, к сожалению, даже в
перспективный план
издательства «Просвещение» не входит
новое учебное пособие для
школьников по химии, среди
авторов которого стояли бы
имена наших крупнейших
специалистов. Почему-то наши
академики,
члены-корреспонденты, лауреаты отечественных
и международных премий по
химии не считают нужным
участвовать непосредственно в
этой важнейшей работе.
А между тем об этой
проблеме пишут, и много. Строки
из стихотворения Евгения
Винокурова «Художник, воспитай
ученика...» стали крылатыми.
Все понимают, что новые
Ландау, Капицы, Семеновы
начинают формироваться еще за
школьной партой, в
лабораторном кабинете, во время чтения
умной, нестандартной книги,
которая неожиданно
пробуждает интерес к казавшейся
скучной науке.
И тут мне хочется привести
одну цитату.
«Кульминацией
исследования окружающего нас мира
является постановка вопроса:
«Почему происходит зто явление?»
Мы ищем объяснение.
Например, мы видим, что объяснение
сводится к открытию общих
черт, связывающих непонятное
нам явление с явлениями,
которые мы понимаем. Это вид
наиболее плодотворной научной
деятельности, который ведет к
изучению явления. Научитесь
задавать себе вопрос: «Почему»,
когда вы наблюдаете за чем-
либо в стенах ли химической
лаборатории или в
повседневной жизни. Это ценная
привычка, которая часто делает нашу
жизнь более полной и
интересной... Возможно, на некоторые
из этих вопросов мы все же не
получим удовлетворительных
ответов. Эти вопросы наиболее
интересны, так как нацелены в
будущее — ваше будущее...».
Это пишет, обращаясь к
школьникам, известный
ученый, лауреат Нобелевской
премии и член многих академий
мира Глен Т. Сиборг. Он
обращается к своим юным
читателям от имени группы ученых,
принимавших участие в состав-
79
лении школьного учебника по
химии, который был издан в
1963 году в Лондоне и Сан-
Франциско. В конце 1967 года
перевод зтой книги появился и
в наших книжных магазинах *.
Учебник по химии,
составленный под редакцией Сиборга,
написан просто и строго. План
его своеобразен и интересен, он
в точности соответствует
периодическому закону Менделеева.
Вообще Глен Т. Сиборг — один
из наиболее последовательных
продолжателей идей создателя
периодического закона.
Написан учебник очень современно.
В нем разъяснены новейшие
приложения химии в биологии,
физике, геологии и других
науках. Понятия и законы химии
изложены очень логично. Как
пишет академик О. А. Реутов в
предисловии, «впервые в
истории учебной литературы
нелегкие для понимания
представления кинетики и термодинамики
изложены столь просто и
образно благодаря использованию
модельных образцов и
превосходно выполненных иллюстра-
* «Химия. Курс для средней
школы». Под общей редакцией
Г. Т. Сиборга. Москва,
Издательство «Мир», 1967.
ФЕРМЕНТ СИНТЕЗИРОВАН
В ПРОБИРКЕ
Один из самых перспективных
методов изучения механизма
белкового синтеза в живом
организме — попытки воспроизвести
процесс или отдельные его этапы
вне организма, в бесклеточной
системе, — попросту говоря, в
пробирке с набором нужных
веществ (аминокислот,
информационных РНК, рибосом и др.).
Но синтезируемые в пробирке
белки, в частности ферменты,
обычно обладают в тысячи раз
меньшей биологической активно-
ций». Все эти иллюстрации
повторены в русском тексте.
Конечно, хорошо, что
издательство «Мир» выпустило это
учебное пособие: оно полезно и
учащимся, и учителям. Новая
методология, непривычный
подбор задач и контрольных
упражнений заставят задуматься
там, где раньше ученик
оперировал лишь готовыми
представлениями. Появятся элементы
творчества, пробудится
самостоятельная мысль, пусть еще
робкая в начале. А это
главное...
Но появление зтой — пусть и
превосходной — книги никак не
может заменить нового
отечественного стабильного учебника:
во-первых, книга иностранных
специалистов составлена
совсем по иному учебному плану;
во-вторых... Тут возникает еще
один вопрос, сразу ко многим
инстанциям.
Курс химии Сиборга — для
наших учащихся не учебник,
всего лишь учебное пособие. Но
можно ли было выпустить его
по цене три рубля пятнадцать
копеек? Ведь школьнику такую
книгу не поднять...
Мне легко возразят, что у
издательства «Мир» высокая
стью, чем натуральные — натив-
ные. И только недавно первого
успеха в этом направлении достиг
биохимик, д-р Солсер,
работающий в Женевском университете.
Ему удалось синтезировать
фермент лизоцим, биологическая
активность которого сравнима с
активностью нативного фермента.
Лизоцим нередко вырабатывается
бактериальными клетками в
результате их заражения вирусом.
Д-р Солсер выделил из таких
зараженных бактерий
информационную РНК, несущую в себе
«приказ» синтезировать лизоцим, и,
поместив ее в бесклеточную си-
себестоимость изданий, что у
него — маленькие тиражи и
большие накладные расходы,
поэтому книги так и дороги...
А что «Просвещение», наоборот,
выпускает учебники по
чрезвычайно низким, доступным
ценам...
Это так. И тем не менее,
наши школьники все ждут
новый хороший учебник по
химии. И переходят из класса в
класс.
Из этого положения надо,
наконец, найти выход.
О. КОЛОМИЙЦЕВА
стему, вскоре обнаружил там
активный лизоцим.
ПЛАСТМАССОВАЯ ПУШКА
Журнал «Chemische Rundschau»
A967f № 15) сообщил, что в США
проведены испытания
81-миллиметровой пушки, ствол которой
изготовлен из стеклопластика. При
испытаниях на ствол пушки деист*
вовало давление в 35 тонн, при
этом внутренняя стенка ствола
разогревалась до 3500°С.
Стеклопластик выдержал эти нагрузки.
НШОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ НОВОСТИ ОТОВСЮДУ
80
УЧИТЕСЬ
ПЕРЕВОДИТЬ
НЕМЕЦКИЙ-
ДЛЯ ХИМИКОВ
ПРЕДЛОГИ
Часто бывает так: запомнив какое-либо одно,
обычно пространственное значение немецкого
предлога, начинающий переводчик пользуется им
всякий раз при встрече с этим предлогом. Так,
auf всегда переводят «на», in — «в», zu — «к»
и т. д. Иными словами, предполагается, что
немецкие и соответствующие им русские предлоги
употребляются в одних и тех же случаях.
К сожалению, это не так.
Если мы говорим по-русски «на столе», «на
5%», «на работу», «на запад», то это вовсе не
означает, что по-немецки здесь непременно будет
стоять auf. Обратный пример: по-немецки
говорят auf der Krim, auf diese Weise, auf deutsch, auf
dem Tisch, а на русский язык переводят — «в
Крыму», «таким образом», «по-немецки», «на столе»...
Насколько легко впасть в ошибку при
прямолинейном подходе к переводу предлогов,
покажем на примерах, казалось бы, легких и ясных.
105. Das Wasserbad wird auf 52CC geheizt.
На первый взгляд, предложение простое, и
перевести его следует так: «Водяная баня
подогревается на 52°С». Однако auf означает в этом
предложении не «на», а «до». Правильный
перевод: «Водяная баня подогревается до 52°С».
Источником ошибки может быть и предлог
um:
106. Der Gefrierpunkt des Benzols wird durch
Zusatz von 2,47g Athylbenzoat auf 100 ml Losungs-
mittel um 0,8400° erniedrigt.
Основное значение um—«вокруг»; поэтому
напрашивается перевод его словом «около».
(Действительно, такое значение предлога um
встречается часто. Например, в предложении:
«Um 700° schmolz das Eisenchlorur...» — «Около 700°
расплавилось хлористое железо...».) Но в нашем
примере um означает «на», и правильный
перевод выглядит так: «Точка замерзания бензола
Предыдущая статья из цикла «Немецкий —
для химиков» напечатана в № 8 за этот год.
в результате добавки 2,47 г этилбензоата на
100 мл растворителя понижается на 0,8400°».
Возникает довольно противоречивая картина:
um и auf переводятся то одинаково, то различно.
На самом деле никакого противоречия нет.
Запомните: с глаголами, означающими рост,
увеличение (erhohen, steigern, wachsen и т. п.) или
падение, понижение (fallen, erniedrigen и т. п.),
auf означает «до» (достижение уровня), a um —
«на» (доля, на которую растет или падает какая-
либо величина).
Таким образом, предлог auf в отличие от
русского «на» указывает на уровень, а не на долю.
Зная это, легко понять следующее предложение:
107. Die Beobachtungsfehler sind an If 0,0002 zu
schatzen.
«Ошибки наблюдения можно оценить в (на
уровне) 0,0002».
Не менее коварен предлог zu. Обычно он
известен в значениях «к», «до». Поэтому
предложение
108. Das verwendete Material besteht zu 99.7%
aus Aluminiumoxid, - -
переводят иногда так: «Применяемый материал
состоит до 99,7% из окиси алюминия». Этот
перевод неверен! Русский предлог «до» указывает
на интервал значений (до 99,7 % означает — от
некоторой величины до 99,7%). Немецкий же
предлог zu указывает на вполне определенное
значение. Правильный перевод: «Применяемый
материал состоит на 99,7% из окиси алюминия».
Значение же русского предлога «до»
передается сочетанием bis zu:
109. Hartgummi enthalt bis zu 30% Schwei'el.
«Эбонит содержит до 30% серы».
С глаголами, обозначающими процессы, zu
указывает на конечный результат этих
процессов. Перевод этого предлога зависит от
соответствующего русского глагола.
ПО. Atome vereinigen sich zu Molekeln.
«Атомы объединяются в молекулы».
111. Mit Dikarbonsauren setzt sich Glyzerin zu
raumlich vernetzten Polyestern um.
81
«Взаимодействуя с дикарбоновыми кислотами,
глицерин образует сложные полиэфиры с
сетчатой структурой».
Перед формулами zu переводится как «в
(виде)», «по формуле».
112. Das Eigenpotcnzial des Molekiils erhalt man
<lurch Summation zu <pM ^- 2rf\.
«Собственный потенциал молекулы получают
суммированием по формуле 'pM—^Pi»-
Предлог mit, помимо основных значений
совместности («с») и инстру мента льности («с» или
творительный падеж), может указывать на
абсолютную величину чего-либо В этом значении он
близок к предлогам von (пример 106) и zu
(пример 108). Mit в таких случаях переводится как
«на (уровне)», «в (размере)».
113. Die Temperatur wurde mit 25 bis 3(Г sta-
bil gehalten.
«Температура поддерживалась постоянной на
уровне 25 — 30°».
В следующем предложении mit имеет
значение, которое в словарях пока не указывается:
114. Mit S:iN2F2 ist das Fluoranalogon dcs Chlorids
S3N2CI2 aui'gehjnden worden.
«Когда было открыто соединение S3 N2 F2,
оказалось, что оно является фтористым аналогом
хлорида S3 N2 Cl2».
Следует знать, что mit употребляется не
только как предлог и глагольная приставка, но и как
наречие в значении «также», «заодно», «и», «со
своей стороны». Например:
115. Die Reaktionsgeschwindigkeit bestimmt
mit die Geschwindigkeit des Stoffumsatzes.
«Скорость реакции также определяет
скорость обмена веществ».
Следующий «хитрый» предлог — von — хорошо
известен в значении «из», «от», в пассивных
конструкциях (der von uns angestellte Versuch —
«поставленный нами эксперимент»), с дополнениями
при глаголах речи («о»). Помимо этого, он может
обозначать принадлежность. Именно такое
значение имеет часто встречающийся оборот,
состоящий из глагола sein + von +
существительное.
116. Perlon ist von gelbliehweifter Farbe.
«Перлон имеет желтовато-белый цвет».
Вот пример посложнее:
117. Die kernmagnetische Resonanzfrequenz ist
in Magnetfeldern von etwa 10 000 Gauft von der
Groftenordnung 10<; bis 108 Umdreliungen pro Sekunde.
Интересующий нас здесь оборот — не ist von
etwa 10 000 Gau ft, a ist von der GrSBenordnimg;
сочетание von der GroRenordnung является
именной частью сказуемого и должно стоять на
последнем месте в предложении (определения,
естественно, в расчет не принимаются). Перевод:
«Ядерная резонансная частота в магнитных
полях около 10 000 гаусс имеет порядок 106 —
108 колебаний в секунду».
Чаще всего употребляются следующие
обороты такого типа:
von Bedeutung sein — иметь значение,
von Interesse sein — представлять интерес,
von Betrag sein — иметь величину,
von Struktur sein — иметь структуру,
von Beschaffenheit sein — иметь свойство.
Предлоги durch и iiber известны прежде всего
в значении «через». Но русский предлог «через»
может означать и «поверх», и «сквозь»; для
правильного перевода это бывает иногда очень
важно. Вот пример:
118. Die zu verbessernde Erdolfraktion wird iiber
einen Katalysator geleitet.
Как перевести iiber einen Katalysator? «Через
катализатор» или «над катализатором»? Перевод
«по смыслу» вряд ли возможен, так как в
принципе допустимо и то, и другое. Очевидно, здесь
нужно точно, однозначно перевести iiber. В
отличие от durch предлог iiber означает не «через» =
«сквозь», а «через» = «над», «поверх».
Правильный перевод: «Обогащаемая нефтяная фракция
пропускается над катализатором».
Предлог durch в современном немецком языке
широко используется для указания на деятеля
(причем не только в пассивных конструкциях).
119. Die erste Indigo-Synthese gelang nach jah-
relanger Arbeit 1879 durch A. von Baeyer.
Перевод durch предлогами «через» или «сквозь»
в этом случае выглядел бы комично. Уместнее
всего переводить, ставя существительное в
творительный падеж: «Синтез индиго был впервые
осуществлен после многолетней работы в 1879
году А. фон Байером».
Связь предлога с глаголом может стать
настолько тесной, что значение всего сочетания не
будет равно сумме значений глагола и предлога.
Так, zuriickfiihren («вести назад») в сочетании с
предлогом auf означает «объяснять (чем-либо)»,
«сводить (к чему-либо)»; eingehen («входить») с
предлогом auf получает значение «рассматривать
(что-либо)», «останавливаться (на чем-либо)»;
bestehen («существовать») с предлогом auf
означает «настаивать», а с предлогом aus «состоять»;
liegen («лежать») с предлогом an означает
«объясняться (чем-либо)», «зависеть». Эти примеры еще
раз подтверждают известное правило: предлоги
обязательно следует переводить в связи с
глаголом, от которого они зависят. (См. также
примеры 3, 5, 6, 8, 12, 26, 27, 32, 40, 42, 43, 44, 50, 55, 67,
71, 72, 75, 76, 78, 80, 83 в предыдущих номерах.)
Старший преподаватель Кафедры
иностранных языков АН СССР
Р. Г. СИНЕВ
82
КЛУБ
ЮНЫЙ
ХИМИК
] ЧТО
J5^-f*«! ЭТО
ТАКОЕ?
(Ответ на стр. 85)
83
ХОТИТЕ ПОДГОТОВИТЬСЯ
К ЭКЗАМЕНАМ ПОЛУЧШЕ!
ЗАДАЧИ О КРИСТАЛЛАХ
Химикам далеко не всегда приходится
решать задачи, связанные с превращением
веществ; очень часто возникает
необходимость просто рассчитать какие-нибудь их
характеристики.
Примером могут служить задачи о
кристаллах, которые иногда предлагаются
абитуриентам и участникам химических
олимпиад. Мы приводим типичные задачи такого
рода; эти задачи подготовлены старшим
преподавателем Челябинского
педагогического института Г. Б. ВОЛЬЕРОВЫМ.
ЗАДАЧА 1
В кристаллах металлической меди объем,
занимаемый атомами, составляет 74
процента общего объема кристаллов.
Рассчитайте удельный вес меди, зная, что ее атом
имеет pa;yiyc 1,28 • 10~8 сантиметра (форма
атома понимается за шарообразную).
ЗАДАЧ Л 2
Какую часть объема металлического
алюминия занимают его атомы?
Эта задача обратна предыдущей. Но
в ней отсутствуют числовые данные; их
вам придется найти самостоятельно.
Можно воспользоваться, например,
«Справочником по химии для средней школы» (Изд.
«Просвещение», М., 1964).
(Решения — на стр. 90)
ОТВЕТ НА ВОПРОС
ПРЕДЫДУЩЕГО НОМЕРА
Решим Колину задачу сначала в общем
виде, введя следующие обозначения:
нн—начальная нормальность раствора,
нк—конечная нормальность раствора,
V —общий объем раствора,
AV — объем отливаемой части раствора,
п —число разбавлений.
Концентрация раствора понижается на
столько, на сколько разбавляют раствор.
Разбавление раствора выразится
отношением «А V» к «V». Следовательно, после
первого разбавления концентрация
понизится на
AV
и составит
ду
V
= нн (l - ^J
После второго разбавления
концентрация понизится на
/ ДУ \
ДУ
У
84
и составит
/ AV\ / AV\ AV
нн- ^ - —) - нн. ^1 - — j . — =
Продолжая и далее рассуждать
подобным же образом, мы можем убедиться, что
в найденной формуле показатель степени
есть не что иное, как число разбавлений п.
Следовательно, формула имеет общий
вид:
( AV\n
Конечную нормальность раствора
найдем из результатов титрования.
V щелочи : ^кислоты = нкислоты • нщелочи
_ 20-J_ _
нщелочи ~ 28,7 ~ Н"
Выпишем теперь числовые данные:
нн — 2 н.
нк = 0,7 н.
У=3л
ДУ =0,3 л
п = ?
Сравнивая данные с выведенной
ранее формулой, видим, что искомая
величина представляет собой показатель
степени.
Следовательно, нам предстоит решить
показательное уравнение относительно п;
(<-^г-г-
Подставим числовые значения:
0,7
2
п =
n-lg 0.9 = lg 0.35,
lg 0,35 _ Г,5441 _ —0,4559
lg0,9 ^1,9542 ~ — 0,0458
10.
Как видим, Коля применил
разработанный им «метод» 10 раз!
ЧТО ЭТО ТАКОЕ?
(См. стр. 83)
Вы, конечно, догадались, что на снимке—•
кора березы, береста. В древней Руси на
бересте писали, сухой перегонкой из нее
добывали деготь, из бересты делали
домашнюю утварь.
Сейчас мы пишем на бумаге,
смазываем машины минеральными и
синтетическими маслами, пользуемся посудой,
сделанной из металла, пластмассы,
керамики... И потому нет ничего удивительного
в том, что сегодня живая природа
интересует человека прежде всего как объект
внимательного изучения, а не
использования.
85
i
Первую карманную
аналитическую лабораторию изготовил
известный русский химик
Ф. Ы. Флавицкий в конце
прошлого века
86
ОПЫТЫ БЕЗ ВЗРЫВОВ
КАК РАЗЛИЧИТЬ
ПЕРЕПУТАННЫЕ
ЛЕКАРСТВА
Для многих часто употребляемых
лекарств известны характерные химические
реакции. Чтобы сделать простейший
анализ, достаточно небольшого количества
лекарства (на кончике ножа). Понадобятся
также реактивы, которые есть во многих
стандартных наборах, в том числе в
карманных аналитических лабораториях
геологов.
Такая лаборатория — железная
коробка, которая умещается даже в кармане.
В ней — набор сухих реактивов,
маленькая спиртовка, тигли, фильтровальная
бумага, пинцет, несколько стеклянных
палочек. С помощью карманной
лаборатории можно анализировать минералы,
удобрения, демонстрировать интересные
химические опыты *.
Она же годится и для того, чтобы
отличить, например, аспирин от кальцекса,
хотя почти все порошки и таблетки
одинакового белого цвета.
АЦЕТИЛСАЛИЦИЛОВАЯ КИСЛОТА
(аспирин). На листке белой бумаги смешайте
тщательно растертые порошки соли
бериллия (например, BeS04) и едкого натра.
Таблетку аспирина разотрите ложкой.
Полученный порошок добавьте в смесь и
хорошо перемешайте ее спичкой. При
реакции сернокислого бериллия со щелочью
образуются сернокислый натрий и
гидроокись бериллия:
BeS04 H 2NaOH -~ Be (OHJ + Na2S04.
Молекулы гидроокиси бериллия и
ацетилсалициловой кислоты образуют
сложное комплексное соединение
желто-оранжевого цвета.
АНТИПИРИН. Жаропонижающее и
средство от головной боли; органическое
вещество, представляющее собой
метилированный фенил метилпиразол он.
* О качественном анализе минералов и руд в
походных условиях было рассказано в клубе
«Юный химик» в № 7 за 1967 г. — Ред.
Это — «ППХЛ», или походная
полевая химическая
лаборатория, которую скоро начнет
выпускать промышленность. Она
предназначена для анализа
минералов и руд в полевых
условиях, рассчитана на 10—
12 элементов. С помощью такой
лаборатории можно делать и
простейшие анализы лекарств.
В карманной лаборатории есть
складная спиртовка. На ней
можно плавить образцы руд,
упаривать растворы. Топливо
для нее — таблетка уротропина.
Лабораторию ППХЛ можно
использовать и в сельском
хозяйстве — для анализа
минеральных удобрений и почв
87
Растертую таблетку антипирина
смешайте с кристаллами соли кобальта
(например СоС12). После перемешивания
смесь окрасится в ярко-синий цвет. Для
определения антипирина известна и другая
реакция: при взаимодействии с хлорным
железом появляется красная окраска.
Продукты этих реакций — сложные
комплексные соединения, состав которых
до сих пор точно не выяснен.
КАЛЬЦЕКС. Смесь хлористого кальция
и органического вещества уротропина
(гексаметилентетрамина) применяется для
предупреждения и лечения гриппа.
Если растертую таблетку кальцекса
смешать с едким натром и органическим
реактивом мурексидом (пурпурат
аммония С8Н80б1М6 • Н20), то порошок
окрасится в красно-фиолетовый цвет. Состав
сложного комплексного соединения,
придающего порошку эту окраску, точно не
известен.
ХИНИН. Природное противомалярийное
лекарство, алкалоид, получаемый
экстракцией из коры хинного дерева.
Для аналитического определения
хинина нужно сначала приготовить
индикатор. Смешайте порошки соли висмута,
например Bi(N03K и йодистого калия,
причем йодистого калия возьмите в 4—5 раз
больше. Разотрите смесь спичкой. В
результате реакции образуется желтоватая
масса:
Bi (N03K 4- 5KJ -> K2(BiJ5) -f 3KN03.
Если к ней добавить порошок хинина,
перемешать смесь, затем добавить
немного едкого натра и еще раз перемешать, то
появится темно-розовая окраска.
БОРНАЯ КИСЛОТА Н3В03 — хорошее
дезинфицирующее средство. Ее применяют
для полоскания и обработки ран. Борная
кислота обладает слабыми кислотными
свойствами, поэтому обнаружить ее
обычными индикаторами, например
метилоранжем, нельзя. Если же смешать порошок
борной кислоты с природным
шестиатомным спиртом маннитом (C6Hi406), который
содержится в соке деревьев, грибах,
цветах жасмина, образуется комплексное
соединение с сильно выраженными
кислотными свойствами. Стоит добавить к
тщательно перемешанной смеси порошков
борной кислоты и маннита кристаллик
метилоранжа, как смесь окрасится в
красный цвет.
ГИДРОПЕРИТ. Перекись водорода —
сильное дезинфицирующее средство, ее
слабые растворы применяют для
обработки ран. Но кристаллическая перекись
водорода взрывоопасна. Поэтому ее
связывают в комплексное соединение с
мочевиной— НоОг • CO(NH2J. Это и есть
гидроперит.
Если смешать порошок гидроперита
с едким натром и сернокислым хромом
и растирать эту смесь, то образуется
хромовокислый натрий — соль ярко-желтого
цвета:
2NaOH + Н202 -> Na202 + 2Н20,
5Na2G2 + Сг2 (S04K -> 2Na2Cr04 -f- 3Na2S04 + 02.
НО ЛУЧШЕ ВСЕГО лекарства хранить
так (даже в походе), чтобы все
рассказанное здесь пригодилось вам только для
демонстрации опытов. Химия — химией,
но так надежнее...
Доцент П. И. ВОСКРЕСЕНСКИЙ
88
ВИКТОРИНА
ПЯТЬ
ВОПРОСОВ
о
солях
1. Много ли
соленых
солей?
%
Какими
солями вы
пользуетесь
поутру,
еще
не успев
сесть
за завтрак?
♦♦♦♦♦++♦♦+♦+++++♦++++4
Знаете ли
вы соли
сладкие,
кислые,
горькие,
безвкусные?
»»»»»»++++++++»+»»+++ 5 Как
получить
раствор
соли,
не используя
никаких
растворителей?
4- + + +++*4**i^M» + + 4-* + + + +
Существуют ли
жидкие
при обычных
условиях
соли?
» •#*+•••<
Рисунки
М. РЕБИНДЕР
80
РЕШЕНИЯ ЗАДАЧ
(См. стр. 84)
ЗАДАЧА 1
Вы решите эту задачу, если сообразите,
что расчет нужно вести на грамм-атом:
ведь мы знаем атомный вес элемента и
число содержащихся в нем атомов (число
Авогадро N).
Объем одного атома (Va) определим,
используя известную из курса геометрии
формулу для объема шара:
4
Так как в одном грамм-атоме содержится
N атомов, то суммарный объем атомов
меди (Vn) составит
\N = Va-N =-3- rr3N.
По условию объем атомов составляет
74 процента (или 0,74) от общего объема
кристаллов; следовательно, мы можем
определить и общий объем одного грамм-
атома меди (Vr-a):
Vn \_
: 0,74 — 0,74
VP
3
Но масса грамм-атома (т г-а) меди
известна F3,54 г), и поэтому удельный вес (d)
меди мы узнаем, разделив тг-а на Vr-a^
тг-а 3
Остается только подставить
соответствующие числовые значения и проделать
вычисления:
3
d = 63,54.0,74-
4-ЗД4-A,28-10"8)з.6,02-1023
чем3 /
Сверьтесь с таблицей удельных весов
металлов — и вы убедитесь в
правильности полученного ответа.
радиус атома алюминия (г) —1,43 ■
• 10 8 см.
Определим суммарный объем атомов,
содержащихся в одном грамм-атоме
алюминия:
VN = — -r*N.
С другой стороны, объем одного грамм-
атома:
и часть объема кристаллов, занятая
атомами:
Vn
= ~з" ™щ'
Подставим соответствующие числовые
данные и проделаем вычисления:
-д- -3,14-A,43-10"8)8-6,02-1023- ^jyf ^0,74.
Сравнивая, какую часть объема
занимают атомы в кристаллах меди (см.
предыдущую задачу) и алюминия, мы видим,
что она выражается одним и тем же
числом. Случайное ли это совпадение? Или
же для всех металлов эта величина
действительно одинакова?
Проверьте это, сделав такие же
расчеты и для других металлов, и объясните
полученные результаты.
ЗАДАЧА 2
Выпишем из справочника необходимые
данные:
масса грамм-атома алюминия (тг_а)—
26,97 г;
удельный вес алюминия (d) — 2,7 —3 '
90
СТАТЬИ, ОПУБЛИКОВАННЫЕ
В ЖУРНАЛЕ «ХИМИЯ И ЖИЗНЬ»
в 1968 году
I. К 98-ЛЕТИЮ СО ДНЯ РОЖДЕНИЯ 5. ДЕРЯГИН Б. В. «Вода, вода, кругом вода...»—
ВЛАДИМИРА ИЛЬИЧА ЛЕНИНА № 5f стр. 14—23.
6, ЕЗЕРСКИЙ М. Л. Твердые электролиты. — № Ю,
Два документа с двумя комментариями, 1. ВОЛ- стр. 23—27.
КОВ В. А. Первый комментарий: это было в ты- 7. КАЦ М., КОПРОВСКИ X. Искоренение инфекций:
сяча девятьсот девятнадцатом. — № 4, стр. 2—6; точка зрения биолога. — № 4, стр. 54—59;
2. ФАЙНБЕРГ В. С. Второй комментарий: горю- 8. Комментирует директор Института эпидемио-
чие сланцы — значение и перспективы. — № 4, логии и микробиологии им. Н. Ф. Гамалея, дей-
стр. 6—9; 3. Что вы знаете и чего не знаете о го- ствительный член Академии медицинских наук
рючих сланцах. — № 4, стр. 9. СССР О. В. БАРОЯН. — № 4, стр. 59—60.
9. СТРИЖЕВСКИЙ И. В., ГУРЕВИЧ М. А. Хемотрони-
II. К 150-ЛЕТИЮ СО ДНЯ РОЖДЕНИЯ ка- это электроника жидкости. - № 7, стр. 4Г-
КАРЛА МАРКСА ' ° сег°Дня «умеют» хемотроны. — № 7
стр. 45.
1- Имя его и дело переживут века... — № 5,
стр. 2—3. |у ОБзоРЫ. КЛАССИКА НАУКИ
III. ПРОБЛЕМЫ И МЕТОДЫ СОВРЕМЕННОЙ НАУКИ 1" "МЯНИТОВ И. М., ТИХИЙ Д. Я Шаровая мол-
" ния: сто теории и гипотез. — № 2, стр. 6—13
1. БАЕВ А. А. Разрезанные молекулы. — № 4, 2. Шаровая молния о себе. — № 2, стр. 14—15
стр. 19—26. 3. Объявляется розыск. — № 2, стр. 15—16
ВОЛЬКЕНШТЕЙН М. В. Изгнание максвеллова демо- 4. Как делали искусственные шаровые молнии. —
на. 1. — № 11, стр. 8—13; 3. —№ 12 стр. 6—12. № 2, стр. 16.
4. ГОЛЬДАНСКИЙ В. И. Восьмой период — каким 5. КРОНГАУЗ В. А. Как толковать законы. — № 7,
он будет? — № 8, стр. 2—7. стр. 11—16.
rj?SUE5H5H5c^5H5HSHSMHSZSH5c^SZ5MZ5Z5HSMH5HSE5HSH ESUBSH5Z52SZSHSHSUE5H5Z5H5Z52SUE5HS2U
К
G
я
я
я
Вниманию участников конкурса! я
и
S В этом указателе статей, опубликованных в 1968 году, рубрики ^
д журнала пронумерованы римскими цифрами, а каждая статья— Й
G арабскими цифрами. В макете номера, который составляет участ- Щ
Я ник конкурса, нужно указывать номер рубрики и номер статьи— ц
о} например, статья Л. Пономарева «Атомы, лучи, кванты», публи- Й
G ковавшаяся с продолжением, должна быть обозначена шифром й
G «IV-8», «IV-9», «IV-10», «IV-11», а фантастический рассказ «Об- g
Й лы» — шифром «XVIII-2», и так далее. Й
Й Обложки (Об) и вклейки (Вк) шифруются номером журнала, из Й
К которого они взяты. Например: «Об-8-З» (обложка восьмого но- Ц
мера журнала, третья страница), «Вк-1-2» (цветная вклейка пер
Я ллера .жугнала, i pci dx *_ i рапица/, \\ит\- i-*.« \l^d^i п«л вгл.л^пгл.« ■ n-j-r- pj
Cj вого номера журнала, вторая страница). Н
гЗ
я
я
я
nJ
я
я
0aszsHszsc^asa5c^E5HsasEsasasHSE5EnsasEc^SHsaFHsaEHSHsasHSc^z5Hszsc^i5S5asc^c^r^zsEsasaszsa
91
6. НАЗИРОВ М. Погода и организм. — № 4, стр.
37—40.
7. Океан и человек. — № 9, стр. 41—45.
ПОНОМАРЕВ Л. И. Атомы, лучи, кванты. 8.— № 1,
стр. 12—23; 9. —№ 2, стр. 41—49; 10. —№ 4f
стр. 27—36; 11. —№ 5, стр. 27—38.
12. ТРАВКИН М. П. Жизнь в магнитном поле. — № 9,
стр. 22—25.
13. ФРЕНКЕЛЬ А. И. ...Порождающие рак.— № 3,
стр. 26—31.
V. НАУКА —ПРОИЗВОДСТВУ.
ЭКОНОМИКА И ПРОИЗВОДСТВО
1. АВРЕХ Г. Л. Исследователь на перепутье. — № 6,
стр. 28—32.
2. АВРЕХ Г. Л., МАКАРОВ О. В. Линия жизни
этилового спирта. — № 11, стр. 20—23.
3. БЛОХИНА С. Н. Что дешевле сжечь. — № 4, стр.
10—11.
4. ВИНИЦКИЙ Л. Е. Ни километра без резины. —
№ 4, стр. 61—66.
5. ВОЙТОВИЧ В. А. Пластмассы на обеденном
столе. — № 11, стр. 78—80.
6. ГИНЕР П. Г. Рыцари консервной банки. — № 7,
стр. 36—39; 7. ИОРДАНСКИЙ А. Д.
Бронированные помидоры. — № 7, стр. 40.
8. ГУРЕВИЧ М. А., КЛЯЦКИН В. Б. Пластмассовые
автомобили, игрушечные и настоящие. — № 6,
стр. 88—90; 9. КРЕЙНИН А. А. В единственном
экземпляре.— № 6, стр. 90—93.
10. ДОЦЕНКО Б. Н. Осторожно —пузырьки.— № 8f
стр. 23.
11. ПЕРЕПЕЛКИН К. Е. Растворимые волокна.—
№ 11, стр. 58—60.
12. СКЛЯРОВ А. Т. Коварство микромира. — № 5,
стр. 11—13.
13. СМЫСЛОВ И. И. Может ли металл быть
клеем.— № 12, стр. 59—61.
14. СУЛИМЕНКО Л. М. Как лечат бетон. — № 9,
стр. 35—39; 15. Что вы знаете и чего не знаете
о бетоне. — № 9, стр. 39—40.
16. ТУРОВСКИЙ В. В. Мягкие цистерны. — № 8,
стр. 70.
17. Успехи химии. — № 7, стр. 33—34.
18. ФИЛАНОВСКИЙ Г. Ю. Между нами и землей.—
№ 12, стр. 70—73.
19. ШУТЕР Л. М. Советские синтаны. — № 6, стр. 9—
14; 20. Несколько маленьких фактов из истории
кожевенного дела. — № 6, стр. 14—16.
21. ЯРОВ Р. Универсальный двигатель или
универсальное топливо? — № 10, стр. 2—4.
VI. ЭЛЕМЕНТ №...
1. ДИОГЕНОВ Г. Г. Фосфор. — № 2, стр. 17—23;
2. Что вы знаете и чего не знаете о фосфоре и
его соединениях. — № 2, стр. 24—25.
3. ИВАНОВ П. П. Калий. — № 12, стр. 19—22; 4. Что
вы знаете и чего не знаете о калии и его
соединениях.— № 12, стр. 22—24.
5. КАЗАКОВ Б. И. Ртуть. — № 6, стр. 33—37; 6. Что
вы знаете и чего не знаете о ртути и ее
соединениях. — № 6, стр. 37—40.
7. КИПНИС А. Я. Никель. —№ 1, стр. 26—35;
8. Еще о никеле. —№ 1, стр. 34—37; 9.
ЯКОВЛЕВ А. Карбонил никеля — одно из самых
интересных соединений элемента № 28. — № 1,
стр. 38—39.
10. КУЗНЕЦОВ В. И. Плутоний. —№ 5, стр. 41—52.
11. МОЛДАВЕР Т. И., ЛЕВИН И. С. Индий. — № 10,
стр. 17—21; 12. Менделеев об индии. — № 10,
стр. 21—22.
13. ПОЛЕЖАЕВ Ю. М. Гафний. — № 8, стр. 12—18;
14. Что вы знаете и чего не знаете о гафнии и
его соединениях. — № 8, стр. 1В.
15. ФИНКЕЛЬШТЕЙН Д. Н. Аргон. — № 11, стр.
24—29.
16. ШЕСТИТКО В. С. Сурьма. —№ 9, стр. 15—19;
17. Что вы знаете и чего не знаете о сурьме и
ее соединениях. — № 9, стр. 20.
18. ЭЛЬКИНД Л. М., ЛОБАНОВА Т. С. Ниобий.—
№ 3, стр. 4—10; 19. Что вы знаете и чего не
знаете о ниобии и его соединениях. — № 3,
стр. 10—11.
VII. ОБЫКНОВЕННОЕ ВЕЩЕСТВО.
КАК ДЕЛАЮТ ВЕЩИ И ВЕЩЕСТВА
1. ГУРОВИЧ Р. Э. Синтетический спирт. — № 10,
стр. 49—51.
2. ГУРЕВИЧ М., КРЕЙНИН А. Соперница спички.—
№ 8, стр. 60—64; 3. Что вы знаете и чего не
знаете о зажигалках. — № 8, стр. 64—65.
4. ДМИТРИЕВ В. Б., ТРУНОВА Т. К. Стекло. — № 4,
стр. 41—52.
5. СКУНДИН А. М. Соляная кислота. — № 9, стр.
30—34.
6. СТАНИЦЫН В. В. Керосин. —№ В, стр. 24—29.
VIII. НАУКА О ЖИВОМ
1. Ваша жизнь во сне. — № 6, стр. 17—21; 2.
Осторожно— сны! — № 6, стр. 20—21; 3. Наш
комментарий.— № 6, стр. 22—24.
ГРИГОРЬЕВ Г. Гены и гении. 4. — № 2, стр. 62—68;
5. — № 3, стр. 44—47; 6. Ум и тесты. — № 2,
стр. 69—73.
7. ГРУНТЕНКО Е. В. Зачем человеку тимус? — № 7,
стр. 51—55.
8. ДЕМЬЯНОВ В. П. Человек в отсеке. — № 5,
стр. 5—10.
9. КОНОВАЛОВ Б. Хлорелла — космическая
водоросль.— № 8, стр. 8—11.
10. КОРЖУЕВ П. А. Гравитация, скелет,
гемоглобин... — № 5, стр. 24—26.
11. ЛЕВИТЕС Э. П. Искусственное
кровообращение. — № 6, стр. 41—44; 12. КАРА-МУРЗА С. Г.
Химия против тромбоза. — № 6, стр. 45—46.
13. ЛОМАГИН А. Г. По сигналу красного света.—
№ 12, стр. 38—40.
14. МАКСИМОВСКИИ Л. Ф. Клетка на операционном
столе биохимика. — № 10, стр. 35—39.
15- ОБУХ И. Б. Вирусы и рак. — № 11, стр. 34—40.
16. |ТРНГУР В. С| Два открытия. — № 1, стр. 67—70.
17. ФАИЗОВА Г. К. Наши друзья микробы. — № 5,
стр. 53—57; 18. Только факты. — № 5, стр. 58.
IX. РАССКАЗЫ О БОЛЕЗНЯХ И ЛЕКАРСТВАХ
1. ГУБЕРМАН И. Борьба с безумием. — № 2, стр.
34—40.
2. КИСИН И. Е. Избавляющие от страха. — № 10,
стр. 52—55.
3. КИСИН И. Е. Таблетки, о которых спорят
газеты.— № 5, стр. 59—61; 4. Комментирует главный
акушер-гинеколог Москвы, кандидат
медицинских наук Ю. М. БЛОШАНСКИЙ. — № 5, стр.
61—63.
5. ЛИТВИНОВ В. В. В поисках «магической пули». —
№ 3, стр. 31—36.
02
6. МАРТЫНОВ С. Жаба-фармацевт. — № 11, стр.
68—71; 7. Что вы знаете и чего не знаете о
жабах и жабьем яде. — № 11, стр. 72—73.
8. ФИЛИМОНОВА М. Люди и звери. — № 2, стр.
94—96.
X. И ХИМИЯ — И ЖИЗНЬ!
1. БРОЙТМАН А. Я. О веществах — мутагенах и те-
ратогенах. — № В, стр. 19—22.
2. ЖОЛОНДКОВСКИЙ О. Воздух над заводами.—
№ 7, стр. 17—22.
3. ПЛАХОТНИК А. Ф. Океан должен быть
чистым. — № 9, стр. 2—7.
4. ТРОФИМЕНКО П. П. Закурим и подумаем...—
№ 1, стр. 39—40.
5. УИЛЬЯМС М. Третье поколение ядохимикатов. —
№ 3f стр. 15—18;
6. Комментирует доктор К. СЛАМА. — № 3,
стр. 19—20.
7. ХОНИКЕВИЧ А. А. Атомная техника — джин,
выпущенный из бутылки? — № 5, стр. 84—87.
XI. ЧТО МЫ ЕДИМ, ЧТО МЫ ПЬЕМ
1. ВАСИЛЬЕВА О., ГЛАДКИЙ И.г ДЖУРИНСКИЙ Б.г
КРЫЛОВ А. Пуд соли. —№ 2, стр. 52—61.
2. ИОРДАНСКИЙ А. Грузинский чай. — № 1, стр.
44—50; 3. Что вы знаете и чего не знаете
о чае. — № 1, стр. 51—55.
4. ЛИБКИН О. Вы любите ли сыр? — № 6, стр. 47—
54; 5. Что вы знаете и чего не знаете о сыре. —
№ 6, стр. 54—56; 6. Немного истории. — № 6,
стр. 56—57; 7. МАРЬИНСКИЙ А., РАЗБЕГАЕВ А.
Приглашение к столу. — № 9, стр. 55—57.
8. СОКОЛОВ И. Душа рябины. —№ 10, стр. 88—89.
ТРОФИМЕНКО П. П. Химия в кастрюле. 9.—
№ 10, стр. 68—70; 10. —№ 11, стр. 51—54.
XII. МАСТЕРСКИЕ НАУКИ
1. ЛАПИН И. П. Психофармакология сегодня.—
№ 12, стр. 2—5; 2. О короткой истории
психофармакологии. — № 12, стр. 5, 28.
3. ЛИФШИЦ Л. Институт, в котором создаются
лекарства. — № 10, стр. 5—10.
4. СТАНЦО В. Институт стабильных изотопов.—
№ 11г стр. 2—6.
XIII. СТРАНИЦА ИНТЕРВЬЮ.
ИЗ ДАЛЬНИХ ПОЕЗДОК.
В ЛАБОРАТОРИЯХ ЗАРУБЕЖНЫХ УЧЕНЫХ.
ЗАГЛЯДЫВАЯ В БУДУЩЕЕ
1. Вакцина против резуса? — № 12, стр. 63—64;
2. Комментирует врач Л. И. ПРИВАЛОВА. —
№ 12, стр. 65.
3. ГНИДЕК Я. Будущее полимеров. — № 6, стр.
25—26.
4. ГОЛЛАНЕК А. Заметки о полюсе холода,
о его прошлом, настоящем и будущем. — № 10,
стр. 28—31; 5. Польша — СССР: сотрудничество
и успехи. — № 10, стр. 31—33.
6. МАККЬЮЗИК В. А., РИМОЙН Д. Л. Могут ли
расти лилипуты. — № 3, стр. 50—59; 7.
ЗАРУБИНА Н. А. К сожалению, это не так просто. — № 3,
стр. 59.
8. МУСЛИН Е. Жабры для нас с вами. — № 11, стр.
41—43.
9. ОСТАПОВ Л. В Западной Германии. — № 3,
стр. 65—68.
10- ПЕРУТЦ М. Молекулярная биология: настоящее
и будущее. — № 3, стр. 72—75.
11. ЧЕРНИХОВ А. В Италии, в институте у Джулио
Натта. —№ 7, стр. 57—61.
12. ЧУБУКОВ В. Соленая земля. — № 7, стр. 7—10.
XIV. НАШ КАЛЕНДАРЬ. СТРАНИЦЫ ИСТОРИИ.
ЖИЗНЬ ЗАМЕЧАТЕЛЬНЫХ УЧЕНЫХ.
ИСТОРИЯ ЗАВОДОВ
1. АНТОНОВ А. С. «Omnis molecula ex mole-
cula...». — № 7, стр. 46—50.
2. БАТАЛИИ А. X. Письмо А. М. Горького
М. А. Блоху. — № 11, стр. 32—33.
3. ВЛАДИМИРОВ С. Желтая линия солнечного
спектра. — № 7, стр. 23—25.
4. ВОЛКОВ В. А. «Химия» начиналась так... — № 11,
стр. 30—32.
5. ВОЛЬКЕНШТЕЙН М. В. «Не нуждаясь в
мистических санкциях...». — № 9, стр. 8—14.
6. ДУБРАВИН А. И. «...Если не теперь, то в
будущее время». — № 11, стр. 14—18.
7. КОЗЛОВ В. В., БЕЛОВ Б. И. Менделеевские
чаепития.— № 10, стр. 12—16.
8. КОЛОМИЙЦЕВА О. Песня, которой более
500 лет. —№ 1, стр. 95—96; 9. ПЫШНЫЙ М.
«Gaudeamus», еще один текст. — № 8, стр. 93.
10. КОЛОМИЙЦЕВА О. Что такое Нобелевская
премия.— № 4, стр. 86—87; 11. Лауреаты
Нобелевской премии по химии. — № 4, стр. 88—91.
12. ЛУКЬЯНОВ П. М. Сто лет заводу. — № 12, стр.
13—14.
13. МАКСИМЕНКО А. М., МУСАБЕКОВ Ю. С,
КУЗНЕЦОВ В. И. В. Н. Ипатьев. —№ 1, стр. 76—77.
14. МАРКОВНИКОВ В. В. Московская речь о
Бутлерове. — № 8, стр. 42—47.
15. МУСАБЕКОВ Ю. Август Вильгельм Гофман.—
№ 12, стр. 41—43; 16. Что вы знаете и чего не
знаете о красителях. — № 12, стр. 44—45.
17. МУСАБЕКОВ Ю. Байер. — № 6, стр. 58—61.
18. МУСАБЕКОВ Ю. С. Гавриил Гавриилович Густав-
сон.— № 11, стр. 46—49; 19. Воспоминания
современников. — № 11, стр. 49.
20. МУСАБЕКОВ Ю. С. Первые русские женщины-
химики.— № 3, стр. 12—14.
21. «На букву «К» экзаменую завтра...» — № 11,
стр. 55—57.
22. Научные открытия — № 5, стр. 76; 23.
ПОГОДИН С. А. Годовщины жизни. — № 5, стр. 76—77.
24. «Не для того учреждаются университеты...» —
№ 12, стр. 25—28.
25. Первый советский химический. — № 11, стр.
62—65.
26. ПОГОДИН С. А. Борис Николаевич Меншут-
кин. — № 12, стр. 34—35; 27. «Незримые нити,
связывающие нас с прошлым...» — № 12,
стр. 36—37.
28. ПОГОДИН С. А. Иене Якоб Берцелиус. — № 10,
стр. 44—48.
29. ПОГОДИН С. А. Открытие нулевой группы
элементов. — № 7, стр. 26—27; 30. РАМЗАЙ У.
Благородные газы. — № 7, стр. 27—32.
31. ПОГОДИН С А. Э. Ф. Жоффруа. —№ 9, стр.
51—53.
32. ФИЛИМОНОВА М. Патент Леблана. — № 8, стр.
48—51.
XV. СПОРТПЛОЩАДКА
1. АРКИН Я. Г. Мячи—похожие и разные.— № 7,
стр. 66—70; 2. Немного истории. — № 7, стр.
93
70—72; 3, ЛИБКИН О. Вокруг мяча. —№ 7f стр.
73—74.
4. ГУРЕВИЧ М. Опираясь на стеклопластик... — № 9,
стр. 78—82.
5. ГУРЕВИЧ М., СТЕПАНОВ Ю. Из чего сделан
хоккей. — № 1, стр. 56—65.
XYI. ЖИВЫЕ ЛАБОРАТОРИИ.
ВООРУЖЕННЫМ ГЛАЗОМ
1. ЗЕЛЕПУХА С. И. Плоды против микробов. —
№ 6, стр. 71—73.
2. ЗЛОТИН А. 3. Химическое оружие насекомых.—
№ 10, стр. 40.
3. ИВАШИН М. В. Лаборатория в кашалоте. — № 2,
стр. 26—29.
4. КНУНЯНЦ И. Л., ЛОШАДКИН Н. А. Яд лягушки
кокой — самый сильный небелковый яд. — № 4,
стр. 74—76; 5. ЛЭТАМ М. За ядовитыми
лягушками в джунгли Колумбии. — № 4, стр. 77—79.
6. МАЗУРЕНКО М. Т. Василек.—№ 8f стр. 40.
7. МАЗУРЕНКО М. Волчье лыко. — № 4, стр. 66—67.
8. МОСОЛОВ А. Клетки без присмотра. — № 3f стр.
22—24.
9. МЮЛЛЕР К. Фитоалексины — антибиотики
растений. — № 11, стр. 74—76.
10. ФУРМАН Ф. Тетродотоксин. — № 8, стр. 68—69.
11. ХОХРЯКОВ А. П. Безвременник. — № 9, стр.
68—70.
12. ХОХРЯКОВ А. П. Вороний глаз. — № 5, стр.
74—75.
13. ХОХРЯКОВ А. П. Наперстянка. — № 7, стр.
62—63.
14. ХОХРЯКОВ А. П. Подснежники. — № 3f стр. 2—3.
15. ЧАПЛЫГИН Б. К. Чудо-дерево. — № 1, стр.
72—74.
XVII. ИСКУССТВО. АРХЕОЛОГИЯ.
ИСТОРИЯ
1. БАЛУЕВА Г. А. Золото без золота. — № 2, стр.
30—33.
2. ДВОРЯШИН В. М. Возрождение. — № 5f стр.
39—40.
3. ДМИТРИЕВА Е. Перегонный куб из лаборатории
М. В. Ломоносова. — № 9, стр. 47—48.
4. ЧЕРНЫХ Е. Н. Запечатленное в металле. — № 3,
стр. 37—40.
5. ШАМШУРИН А. А. Волконскоит — зеленый
камень.— № 1, стр. 41—43.
6. ЯБЛОНСКАЯ Н. Испытание светом. — № 6, стр.
95—96.
XVIII, ЛИТЕРАТУРНЫЕ СТРАНИЦЫ.
ФАНТАСТИКА. СКАЗКА
1. АЙЗЕНБЕРГ Л. Эффект Пирокина. — № 6, стр.
66—69.
2. ВАРЛАМОВ B.f СТАРИКОВИЧ С. Облы. — № 5,
стр. 80—84.
3. ВОЛЬПЕР И. М. Продолжая читать классиков. —
№ 12, стр. 15—18.
4. ГУМИЛЕВСКИЙ Л. Как ученый приходит к
открытию. — № 1, стр. 7—11.
5. ЖИРНАУСКАС И. Г. Перечитывая классиков... —
_ № 5Г стр. 68—72.
ЛЕЙНСТЕР М. Этические уравнения. 6. — № 9, стр.
72—77; 7.— № 10, стр. 71—76. 8. Наш
комментарий. — № 10, стр. 76—77.
9. НУРС А. Эликсир Коффина. — № 8, стр. 54—59.
10. ПЛЕКТЕЙ Д. Не нашей работы. — № 12, стр.
66—69.
УОТСОН Дж. Д. Двойная спираль. 11.— № 7, стр.
77—В5; 12. —№ 8, стр. 71—78; 13. —№ 9, стр.
60—66; 14. — № 10, стр. 62—67; 15. Академик
В. А. ЭНГЕЛЬГАРДТ о книге Дж. Д. Уотсона
«Двойная спираль». — № 7, стр. 76.
16. ЭИДЕЛЬМАН Н. Я «О, сколько нам открытий
чудных...» — № 6, стр. 2—8.
17. ЯРОВ Р. Горькие слезы. — № 3, стр. 62—64.
XIX. СТРАНИЦЫ РАЗНЫХ МНЕНИЙ
1. АЛЬФВЕН X. Антимиры — наши соседи? — № 8Г
стр. 30—38; 2. ДАВЫДОВ А. С. Интересная
гипотеза. — № 8, стр. 38; 3. ПИКЕЛЬНЕР С. Б.
Некоторые доводы против. — № 8, стр. 39.
4. ЗВЕРЕВ В. Л. «Х-трансуран». — № 7, стр. 2—5;
5. Комментирует проф. В. В. ЧЕРДЫНЦЕВ. — № 7,
стр. 5; 6. ДОНЕЦ Е. Д. Доказательств
недостаточно. — № 7, стр. 5—6.
7. РАССОХИН В. П. Защищать или не защищать. —
№ 1, стр. 2—5.
8. РАССОХИН В. П. Непременно заявлять! — № 9,
стр. 26—28.
9. РАССОХИН В. П. Что есть изобретение? — № 11,
стр. 44—45.
XX. НАБЛЮДЕНИЯ
1. АБРАМОВА Т. А. История одного реликта. —
№ 12, стр. 29—32.
2. ЕРОФЕЕВ Б. В. Необычные реакции. — № 3, стр.
24—25.
3. Загадка скрапи. — № 8, стр. 41.
4. Как закручена молекула? — № 9, стр. 49—50.
5. КРАСОВСКИЙ А. И. В мире металла. — № 5, стр.
78—79.
6. МАРТЫНЮК М. М., ВОРОНКОВ М. Г. Эта
дурацкая замазка... — № 6, стр. 74—76.
XXI. А ПОЧЕМУ БЫ И НЕТ!
1. ГЕРДОВ А. Эволюция, информация... — № 8, стр..
94—96.
2. ГРИДНЕВА А. С. Утешение подагрикам. — № 5Г
стр. 95—96.
3. ЛЕБЕДЕВ А. Д. «Алфизхимия». — № 3, стр.
48—49.
4. ЛУКНИЦКИЙ А. Н. Кларки и цены. — № 10, стр.
90—91.
XXII. БИБЛИОТЕКА
1. ГУБЕРМАН И. Подлинное путешествие. — № 11 г
стр. 91.
2. КОЛОМИЙЦЕВА О. «Воспитай ученика...» — № 12,
стр. 79—80.
3. МАКАРЕНЯ А. А. «Любимое дитя мое, мой
образ, мой опыт»... Маленькая экскурсия в
Менделеевский архив. — № 12, стр. 51—55.
4. ПЛАТЭ Н. А. Для тех, чьи наклонности еще не
определились. — № 10, стр. 85.
Страницы из летописи атомного века. 5. ФЕРМИ Э.
Как мы пытались осуществить ядерную цепную
реакцию. —№ 1, стр. 78—81; 6. РЕВИЧ В.
Свидетель защиты. — № 1, стр. 81—82; 7. Здравый-
смысл восторжествует. — № 1, стр. 83—84.
XXIII. МАТЕМАТИКА —ДЛЯ ХИМИКОВ
1. НАЛИМОВ В. В. Планирование эксперимента. —
№ 10, стр. 92—94.
9±
XXIV. УЧИТЕСЬ ПЕРЕВОДИТЬ.
СЛОВАРЬ НАУКИ
КОМРОВСКАЯ Т. Н. Французский — для химиков.
1, —№ 3, стр. 70—71; 2. — № 4, стр. 93—95; 3.—
№ 5, стр. 72—74; 4. — № 6, стр. 86—87; 5. — № 8,
стр. 92; 6. — № 11, стр. 85—86.
ПУМПЯНСКИЙ А. Л. Английский — для химиков. 7.—
№ 1, стр. 70—71; 8. —№ 9, стр. 66—68; 9.—
№ 10, стр. 86—87.
СИЛКИН Б. И. Человек —мера вещей. 10. — № 3f
стр. 78—79; 11.— № 9, стр. 90—91.
СИНЕВ Р. Г. Немецкий — для химиков. 12. — № 2,
стр. 88—89; 13. —№ 12, стр. 81—82.
14. СУПЕРАНСКАЯ А. В. Русский — для химиков.—
№ 6, стр. 64—65.
15. ТАРАНОВИЧ Ю. В. Немецкий — для химиков.—
№ 8, стр. 90—91.
XXY. КЛУБ ЮНЫЙ ХИМИК
1. БОЙС Ч. Мыльные пузыри. — № 7, стр. 88—96;
2. Комментирует академик П. А. РЕБИНДЕР. —
№ 7, стр. 89—91, 94—96.
Викторина. 3. — № 1, стр. 87—88; 4. — № 2, стр. 76;
5. — № 3, стр. 84—86; 6. — № 4, стр. 80; 7. —
№ 5, стр. 92—93; 8. — № 9, стр. 83; 9. — № 10,
стр. 82; 10. —№ 11, стр. 88; 11. —№ 12, стр. 89.
12. Впереди — олимпиада! — № 10, стр. 84.
13. Игра. — № 4, стр. 72—73, 92.
14. Итоги викторины. — № 9, стр. 87.
15. Можно ли стать невидимым? — № 11, стр. 93.
16. Мысли по поводу. — № 9, стр. 89.
Опыты без взрывов. 17. — № 3, стр. 80—82; 18.—
№ 9, стр. 85—86; 19. —№ 12г стр. 86^88.
20. СЕВАСТЬЯНОВА К. И. Какие книги читать к
экзаменам. — № 6, стр. 80—81.
Сделай, посмотри и подумай. 21. — № 7, стр. 87;
22. —№ 8, стр. 80—82; 23. ФЕДОСЕЕВ П. К,
ЛАГОШНАЯ Р. М. А можно сделать и так. —
№ 8, стр. 82—83.
24. Химические профессии. — № 2, стр. 81—82.
Хотите подготовиться к экзаменам получше? 25. —
N2 1, стр. 85—86, 89—91; 26. — № 2, стр. 75,
79—81; 27. — № 3, стр. 86—87, 89—90; 28. — № 4,
стр. 81, 84—85; 29. — № 5, стр. 89, 91—92; 30.—
№ 6, стр. 78, 82—84; 31. —№ 9, стр. 84—85;
88—89; 32. —№ 10, стр. 79, 83—84; 33. — № 11г
стр. 89, 94—95; 34. — № 12, стр. 84, 90.
XXVI. ПОЛЕЗНЫЕ СОВЕТЫ
И ПОЯСНЕНИЯ К НИМ.
1001-я МЕЛОЧЬ
1. БУЧИН В. М. Четыре совета автомобилистам. —
№ 3, стр. 76—77.
2. ВОЙТОВИЧ В. А. Материал тысячи
возможностей.— № 4, стр. 12—14; 3. Пять из тысячи.—
№ 4, стр. 14—15.
4. ГОНЧАРОВ В. В. Как зимуют автомобили. — № 11,
стр. 82—84.
5. ГОНЧАРОВ В. В. Как смазывать автомобиль. —
№ 8, стр. 84—86; 6. Советы знатока. — № 8, стр.
86—87.
7. ГРИКИТИС Э. Я., МОРДЕЛЬ Г. И. Казалось бы,
простое дело: лак для волос. — № 3, стр. 41—43.
8. ДЯТЛОВ П. П. О забытых рецептах. — № 4, стр.
70—71.
9. ЖВИРБЛИС В. Перегонка-чемпионка. — № 6, стр.
84—85.
10. Как обращаться с искусственным мехом. — № 12,
стр. 77—78.
11. КАЩЕНКО Ф. П. Органика в почве. — № 1f стр.
74—75.
12. КРЕЙНИН А. А. Не бойтесь мороза! — № 12, стр.
74—76; 13. Пять советов. — № 12, стр. 76.
14. РОЗЕН Я. И. €(Спортивный» — крем для
спортивной обуви. — № 1, стр. 65—66.
15. СТАНЦО В. В. «Дорогой, многоуважаемый
шкаф!..» —№ 2, стр. 83—87; 16. И. В. ПЕТРЯНОВ.
Наш комментарий. — № 2, стр. 87.
17. УШАКОВА М. И. О плащах «болонья». — № 4,
стр. 15—16.
18. ФЕДОСЕЕВ П. Н. Как усовершенствовать
горелку.—№ !, стр. 92—93.
19. ШАЛКАУСКАС М. Не все то золото. — № 10, стр.
41—43.
XXVII. НАШ ПРАКТИКУМ
1. ...Из полиэтилена. — № 11, стр. 96.
2. Профильтруйте каплю. — № 3, стр. 91—94.
3. Секреты сплавов. — № 4, стр. 82—84.
4. Энтальпиметрия. — № 10, стр. 57—59; 5.
Комментирует Е. В. КИСЕЛЕВА, доцент Московского
химико-технологического института им. Д. И.
Менделеева.— № 10, стр. 59.
XXVIII. ЧТО ЕСТЬ ЧТО
1. —№ 6, стр. 93—94; 2. — № 7, стр. 86; 3. — № 9,
стр. 92—93; 4. — № 10, стр. 95—96; 5. — № 11, стр.
80—81.
XXIX. ИНФОРМАЦИЯ
1. —№ 4, стр. 53; 2. — № 5, стр. 66—67; 3._№ 6,
стр. 69—70; 4. —№ 7, стр. 55—56; 5. — № 8, стр.
87—88; 6. —№ 9, стр. 71, 77; 7. — № 10, стр. 56; 8.—
№ 11, стр. 76—77; 9. — № 12, стр. 62.
XXX. НАШИ КОНСУЛЬТАЦИИ
1. Валентность азота. — № 11, стр. 19; 2. Всегда
прозрачное стекло. — № 7, стр. 16; 3. В чем ошибка.—
№ 11, стр. 18—19; 4. Две воды одного названия.—
№ 1, стр. 43; 5. Золото и стекло. — № 9, стр. 21;
6. Как бороться с древесным грибком. — № 11,
стр. 50; 7. Как восстановить ленту и «копирку». —
№ 11, стр. 87; 8. Какие газы? — № 12, стр. 33;
9. Калий закаливает. — № 4, стр. 18; 10. Можно ли
синтезировать соединения дейтерия? — № 11, стр.
49—50; 11. Можно ли склеить полиэтиленовую
пленку?— № 10, стр. 11; 12. Не обязательно синтетика.—
№ 8, стр. 52; 13. О пластмассовом кафеле. — № 5,
стр. 94; 14. Опреснение морской воды. — № 1, стр.
43; 15. О силикатах. — № Ю, стр. 34, 59; 16. О
сплавах золота. — № 10, стр. 33—34; 17. Осторожно —
яд! — № 5, стр. 23; 18. Почему идет процесс. — № 8,
стр. 52—53; 19. Правило Марковникова. — № 9, стр.
54; 20. Разрезанная подошва. — № 5, стр. 94;
21. Сверху вниз — и снизу вверх. — № 8, стр. 52;
22. Скачущие песчинки. — № 9, стр. 21; 23. Снова
о меле, который не пачкает. — № 5, стр. 63; 24. Сок
здоровья. — № 3, стр. 95; 25. Спасительный мох. —
№ 7, стр. 75; 26. ...С поля вон. — № 8, стр. 53; 27. То-
копроводящая паста. — № 9, стр. 94; 28. Три вопроса.—
№ 10, стр. 77; 29. Уж эта кока-кола! — № 3, стр. 68—
69; 30. Ученики, отметки, способности. — № 1, стр.
5—6; 31. Хлористый кальций не при чем. — № 8, стр.
47; 32. Хотим подготовиться получше! — № 4, стр. 18;
33. Чем заменить бруснику. — № 7, стр. 75; 34. Чем
красить кофту из синтетики. — № 8, стр. 47; 35. Что
\
95
делать с колорадским жуком? — № 5, стр. 88; 36. Что
окисляется? Что восстанавливается? — 3f стр. 21;
37. Это варенье не вредно для здоровья? — № 5,
стр. 63; 38. Белки и ревматизм. — № 11, стр. 87;
39. Как подсчитывают удобрения. — № 12, стр. 33.
читают «Химию и жизнь». — № 12, стр. 46; 19. «Путь
к бессмертию». — № 4, стр. 16—17; 20. Русский —
для химиков.— № 12, стр. 58; 21. Точка зрения
рецензента и мнение издательства «Просвещение». —
№ 10, стр. 22; 22. Что такое «тиноль»? — № 9, стр. 29.
XXXI. ИЗ ПИСЕМ В РЕДАКЦИЮ
1. А клей все-таки есть! — № 9, стр. 29; 2.
Безграмотное пособие.—№ 2, стр. 91—93; 3. Бывает и
так. — № 7, стр. 86; . Весьма специфическая
область... — № 12, стр. 58; 5. Где купить реактивы и по-
СУДУ- — № 10, стр. 94—95; 6. Да, вредных животных
в природе нет! — № 6, стр. 27; 7. Еретическая
гипотеза.— № 1, стр. 94; 8. Еще об эпоксидных клеях.—
№ 2, стр. 33; 9. Еще раз про чернила, которые не
совсем чернила. — № 6, стр. 26—27; 10. Как
закончилась одна дуэль. — № 4, стр. 17; 11. Как
приклеить полистирольную плитку. — № 12, стр. 69;
12. Какому автору верить? — № 11, стр. 7; 13. Когда
же родился Бутлеров? — № 11, стр. 7; 14. Мел,
который не пачкает. — № 1, стр. 94; 15. Накипь можно
снимать и магнитом. — № 6, стр. 32; 16. Отчего
сломался телевизор. — № 9, стр. 28—29; 17.
Поправляем консультанта. — № 7, стр. 34—35; 18. Почему
XXXII. ЧТО ЭТО ТАКОЕ!
1. — № 2, стр. 74; 2. — № 3, стр. 83; 3. — № 6, стр. 77;
4, —№ 7, стр. 87; 5. — № 8, стр. 79; 6. —№ 9, стр. 84;
7,—№ 10, стр. 78; 8. — № 11, стр. 90; 9.—№ 12,
стр. 83.
ТЕХНОЛОГИ, ВНИМАНИЕ! ТЕХНОЛОГИ, ВНИМАНИЕ! ТЕХНОЛОГИ, ВНИМАНИЕ!
МЕТАЛЛИЗАЦИЯ ПО-НОВОМУ
Фирма «General Electric»
разработала новый способ, позволяющий
наносить тонкий слой материала
на важнейшие металлы, сплавы,
керамические материалы.
Покрытия, наносимые новым способом,
повышают механическую
прочность, твердость, упругость,
устойчивость к окислению и
коррозионную стойкость материалов.
Например, вольфрамовая проволока,
сгорающая при температуре
700° С в течение нескольких
минут, после покрытия ее слоем
кремния по новой технологии
выдерживает вдвое большие
температуры в течение нескольких
сотен часов.
Новый способ
электролитической металлизации основан на
электролизе при высокой
температуре. В качестве электролита
используют расплав фторидов, в котором
растворяют вещества, которые
нужно нанести на поверхность
детали. Метод позволяет также
накосить последовательно два
различных покрытия на одну и ту же
поверхность.
Фирма продолжает
исследования по получению коррозионно-
и виброустойчивых сталей с
покрытиями из бора или кремния.
Делается это в расчете на то, что
благодаря этим покрытиям
удастся заменить дорогие
высококачественные стали более дешевыми
марками.
«Chemische Rundschau» A967,№ 32)
ОСТОРОЖНО С ФРЕОНОМ!
Фреоны — фтор- и хлорпроиз-
водные различных углеводородов
жирного ряда — широко
применяются в современной технике
(например, в качестве рабочих
жидкостей в системах
охлаждения). Обычно считается, что они в
химическом отношении довольно
инертны. Однако в октябре 1967 г.
в одной из американских
лабораторий произошел взрыв, в
результате которого два человека
погибли и 11 были ранены.
Комиссия, расследовавшая причины
взрыва, установила, что его
виновником были несколько сот
кубических сантиметров смеси одного
из фреонов — трихлортрифтор-
этана с бариевой пылью.
Оказалось, что фреоны бурно
реагируют с металлами, особенно
щелочными и щелочноземельными в
мелкодисперсном состоянии.
Комиссия обратила внимание на то,
что в нескольких других
подобных случаях причиной взрыва
были смеси алюминия с
полимерами трифторхлорэтилена, магния с
тефлоном и даже бария с четы-
реххлористым углеродом.
«New Scientist», 1968, № 607.
НОВЫЙ УПЛОТНИТЕЛЬНЫЙ
МАТЕРИАЛ
Для уплотнения насосов и
вентилей, которые соприкасаются с
кислотами и агрессивными
жидкостями, предлагается новый уп-
лотнительный материал,
изготовленный на основе
длинноволокнистого асбеста, пропитанного
жидким фторопластом. Материал
отличается хорошей вязкостью и
прост в употреблении. Чтобы
изготовить прокладку для вентиля,
уплотнительную массу
накладывают на металлическую поверхность
и затем устанавливают вентиль.
При этом не нужно удалять старые
прокладки и уплотнители, так как
новый материал надежно
заполняет все пустоты. Большое
преимущество его также в том, что
он рассчитан на применение в
широком диапазоне температур: от
—180 до +260° С.
«Chemiker-Zeitung», 1967, № 8
ъ j%&<mso£ <&@Шо///
Издательство
мНаука"
Цена 30 кои.
Индекс 71050